Заявляемое изобретение относится к области биологически активных соединений, предназначенных для лечения и профилактики заболеваний, вызываемых патогенными для человека и животных вирусами, в том числе новой коронавирусной инфекции COVID-19.
Из предшествующего уровня техники известна натриевая соль 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата (1), способ получения которой включает этап конденсации соли диазония (3), который выполняют путем диазотирования 3-амино-5-метилтио-1,2,4-триазола (2), с этилнитроацетатом в щелочной среде.
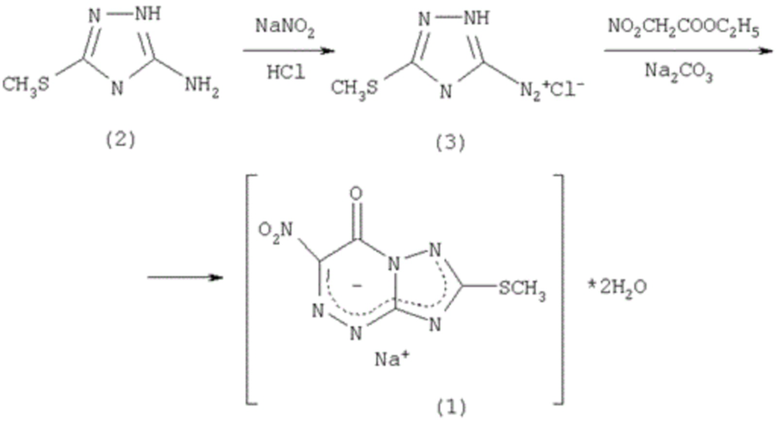
На последней стадии образуется натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат, которую далее отделяют от раствора и примесей. В реакционной смеси остается в нерастворенном виде только натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат [патент РФ № 2294936 на изобретение «Натриевая соль 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрат», дата подачи 29.06.2005, опубликовано 10.03.2007, Бюл. № 7; статья V.L. Rusinov, E.N. Ulomskii, O.N. Chupakhin, V.N. Charushin. Azolo[5,1-c]-1,2,4-triazines as a new class of antiviral compounds//Russian Chemical Bulletin, Int. – 2008-Vol.57- No.5-P.985-1014].
Известное соединение эффективно в отношении определенного списка инфекций, в частности, вызываемых вирусами лихорадки долины Рифт, вирусами ЗЭЛ, парагриппа, респираторно-синцитиального вируса, вируса болезни Ауески, инфекционного ларинготрахеита птиц, вируса гриппа птиц, всего более 10 РНК и ДНК содержащих вирусов Рифт. Соединение активно при лечебной схеме применения.
Техническим результатом, на достижение которого направлено предлагаемое к защите изобретение, является расширение области применения натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрата при лечении и профилактике заболеваний, вызываемых патогенными для человека и животных вирусами, в частности, новой коронавирусной инфекцией COVID-19.
Указанный технический результат достигается применением натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, обладающей противовирусной активностью, для лечения новой коронавирусной инфекции COVID-19.
При этом лечение проводят путем приема капсул с содержанием натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, 250 мг.
Прием капсул осуществляют 3 раза в сутки по одной капсуле.
Заявляемое изобретение осуществляется следующим образом.
Натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат является основным компонентом (активным веществом) лекарственного средства - препарата риамиловир (торговое наименование «Триазавирин»), которое промышленно выпускается с содержанием по 250 мг в капсуле.
В результате проведенных исследований было установлено, что вещество (препарат) обладает высокой эффективностью в отношении новой коронавирусной инфекцией COVID-19, вызванной штаммом SARS-CoV-2.
Исследования клинической эффективности и безопасности применения противовирусного препарата риамиловир были проведены у группы пациентов старше 18 лет с подтвержденным диагнозом COVID-19 средней степени тяжести.
Лечение и наблюдение пациентов проводилось на нескольких крупных клинических базах, включая ФГБУ «Поликлиника №3» Управления делами Президента Российской Федерации (Москва), муниципального автономного учреждения здравоохранения «Городская клиническая больница № 40» (Екатеринбург), КГБУЗ «Красноярская межрайонная клиническая больница скорой медицинской помощи имени Н.С. Карповича» (Красноярск).
Оценка тяжести заболевания была проведена на основании критериев, изложенных во временных рекомендациях Министерства здравоохранения Российской Федерации «Профилактика, диагностика и лечение новой коронавирусной инфекции Covid-19».
Лабораторная верификация диагноза проводилась методами полимеразной цепной реакции (ПЦР) мазков из носо- и ротоглотки.
Пациенты получали препарат риамиловир в качестве противовирусной монотерапии в дозировке 250 мг 3 раза в сутки.
Длительность курса лечения составила 10 дней.
Назначение препарата осуществлялось в соответствии с Постановлением Правительства Российской Федерации № 441 «Об особенностях обращения лекарственных препаратов для медицинского применения, которые предназначены для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайной ситуации и для организации оказания медицинской помощи лицам, пострадавшим в результате чрезвычайных ситуаций, предупреждения чрезвычайных ситуаций, профилактики и лечения заболеваний, представляющих опасность для окружающих, заболеваний и поражений, полученных в результате воздействия неблагоприятных химических, биологических, радиационных факторов».
Одновременно пациенту назначалась патогенетическая и симптоматическая терапия.
Измерение температуры тела пациентов проводили ежедневно. Основные контрольные точки для оценки динамики изменения температуры у пациента были определены на 3 и 7 дни наблюдения. При этом отдельно выделяли и фиксировали день проведения терапии, на который температура тела пациента достигала уровня нормализации. Под нормализацией температуры тела следует иметь в виду значение температуры <37°С.
Для оценки эффективности и безопасности лечения использовались следующие параметры:
- количество дней до получения двух подряд отрицательных результатов ПЦР анализа;
- количество дней до наступления улучшения состояния пациента (на основании отсутствия жалоб от пациента);
- количество дней до наступления нормализации температуры у пациента;
- количество дней до наступления улучшения результатов компьютерной томографии (КТ) легких пациентов;
- изменение результатов анализа на C-реактивный белок;
- переносимость препарата пациентом.
В результате проведенных исследований установлено, что среднее время наступления улучшения состояния пациентов на фоне лечения препаратом риамиловир (натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат) в форме капсул, каждая из которых содержит 250 активного вещества, составило 6-7 дней.
Первый отрицательный результат ПЦР-анализа на вирус SARS-CoV-2 зафиксирован на 10-11 день лечения. Два подряд отрицательных результата ПЦР - к 14-19 дням лечения у 63±4,28% пациентов.
Температура большей части пациентов (75%) нормализовалась к 4-му дню лечения.
Отмечено улучшение результатов КТ легких пациентов: после прохождения терапии повторный результат КТ, выполненной в среднем на 19 день от начала терапии показал отсутствие поражения легких у 10±3,0% пациентов, либо было отмечено отсутствие прогрессирования. При проведении КТ легких через 1-2 месяца после выписки число пациентов с отсутствием признаков поражения возросло до 27±4,44%.
В результате лечения у пациентов, находящихся под наблюдением, было зафиксировано снижение показателя С-реактивного белка.
Переносимость препарата оценена как хорошая: не было выявлено нежелательных явлений или значимых отклонений лабораторных показателей анализов.
В исследование методом случайной выборки было включено 214 пациентов со среднетяжелой формой заболевания, подтверждённого методом ПЦР диагнозом COVID-19. Средний возраст 52,69±1,29 ДИ [50,13-55,25] лет. Большая часть пациентов (67±4,7%) не имела сопутствующих заболеваний.
Для остальной части пациентов были зафиксированы следующие сопутствующие заболевания, в частности,
- заболевания органов дыхания (хроническая инструктивная болезнь легких, бронхиальная астма) - 11±3,13%;
- заболевания эндокринной системы, расстройства питания и нарушения обмена веществ (сахарный диабет и ожирение) - 17±3,76%;
- заболевания органов дыхания и заболевания эндокринной системы, расстройства питания и нарушения обмена веществ одновременно - 5±2,18%.
К концу первой недели лечения (на 6-7-й день) улучшение общего состояния было отмечено у 57±4,95% пациентов. При этом согласно некоторым исследованиям, состояние пациентов, не принимавших специфическую противовирусную терапию, в среднем улучшалось только к 12-14 дню терапии, а в некоторых случаях к 21 дня проведения терапии [Tang W, Cao Z, Han M, et al. Hydroxychloroquine in patients with mainly mild to moderate coronavirus disease 2019: open label, randomised controlled trial. BMJ. 2020;369:m1849. DOI:10.1136/bmj.m1849 ; Mitjà O, Corbacho-Monné M, Ubals M, et al. Hydroxychloroquine for Early Treatment of Adults with Mild Covid-19: A Randomized-Controlled Trial. ClinInfectDis. 2020;ciaa1009. doi:10.1093/cid/ciaa1009 ; Skipper CP, Pastick KA, Engen NW, et al. Hydroxychloroquine in Nonhospitalized Adults With Early COVID-19: A Randomized Trial. Ann Intern Med. 2020; M20-4207. DOI:10.7326/M20-4207].
Первый отрицательный результат ПЦР-анализ на вирус SARS-CoV-2 у большинства наблюдаемых пациентов был получен до 13-го дня лечения - улучшение составило у 59±4,92% пациентов. Точный критерий Фишера р=0,00001, по сравнению с первым результатом ПЦР. Наибольшее количество пациентов с первым отрицательным результатом ПЦР было на 10-й (42,37±3,8% пациентов) и 11-й (35,59±3,68% пациентов) дни наблюдения.
В процессе проведения наблюдения установлено, что два подряд отрицательных результата ПЦР на вирус SARS-CoV-2 было зарегистрировано у большинства пациентов (63±4,28%) к 14-19 дням лечения.
Динамика температурной реакции с учетом контрольных точек была следующей:
- при поступлении 100% пациентов имели температуру тела выше нормы (Т>37°С);
- на третий день терапии 18±3,84% пациентов имели нормальную температуру тела (точный критерий Фишера р=0,00001);
- на 7-й день терапии температура нормализовалась у 100% пациентов (точный критерий Фишера р=0,00001).
При этом у 75±4,33% пациентов температура нормализовалась к 4-ому дню лечения.
В ходе наблюдения отмечено улучшение результатов КТ легких пациентов. При поступлении 69±4,63% пациентов имели процент поражения легких от 25 до 50%, 29,0±4,54% пациентов имели процент поражения легких до 25% и 2,0±1,4% пациентов имели степень поражения легких свыше 50%. Пациентов без поражения легких не было.
После прохождения терапии повторный результат КТ (выполненной в среднем на 19-й день от начала терапии) показал, что у 10±3,0% пациентов не было поражения легких (р=0,0008).
Третий результат КТ, проведенный через 1-2 месяца после выписки пациента, показал, что число пациентов с отсутствием поражения легких возросло до 27±4,44% (χ²=9,58, р=0,002).
При этом в отдельных зарубежных исследованиях показано, что при отсутствии специфической терапии, состояние пациентов может ухудшаться [Ye XT, Luo YL, Xia SC, et al. Clinical efficacy of lopinavir/ritonavir in the treatment of Coronavirus disease 2019. EurRevMedPharmacolSci. 2020;24(6):3390-3396. DOI:10.26355/eurrev_202003_20706].
Результаты анализа С-реактивного белка у пациентов на начало исследования были менее 10 мг/л - у 33±4,7% пациентов, более 10 мг/л - у 67±4,7% пациентов.
В результате терапии на 14-й день наблюдения у большинства пациентов (90±3,0%, χ²=68,61 р=0,00001) уровень С-реактивного белка был менее 10 мг/л.
При этом в исследованиях, где пациенты не применяли специфическую противовирусную терапию, число пациентов с показателем за пределами нормы в течение времени терапии росло [Ye XT, Luo YL, Xia SC, et al. Clinical efficacy of lopinavir/ritonavir in the treatment of Coronavirus disease 2019. EurRevMed Pharmacol Sci. 2020;24(6):3390-3396. DOI:10.26355/eurrev_202003_20706].
В ходе наблюдения у пациентов не было выявлено каких-либо нежелательных проявляющихся клинически явлений или значимыми отклонениями лабораторных показателей, что свидетельствует о хорошей переносимости препарата. Отсутствие возникновения нежелательных явлений сравнимо с данными о количестве нежелательных явлений у пациентов, не получавших специфическую противовирусную терапию, при других проведенных исследованиях [Tang W, Cao Z, Han M, et al. Hydroxychloroquine in patients with mainly mild to moderate coronavirus disease 2019: open label, randomised controlled trial. BMJ. 2020;369:m1849. DOI:10.1136/bmj.m1849 ; Ye XT, Luo YL, Xia SC, et al. Clinical efficacy of lopinavir/ritonavir in the treatment of Coronavirus disease 2019. EurRevMedPharmacolSci. 2020;24(6):3390-3396. DOI:10.26355/eurrev_202003_20706 ; Li Y, Xie Z, Lin W, Zhang F, Deng X, Li L, et al. Efficacy and safety of lopinavir/ritonavir or arbidol in adult patients with mild/moderate COVID-19: an exploratory randomized controlled trial. Cellpress.2020. DOI: 10.1016/j.medj.2020.04.001]
Обсуждение результатов.
В ходе наблюдения за пациентами со среднетяжелой формой Covid-19, в лечении которых в качестве этиотропной монотерапии был использован противовирусный препарат риамиловир (натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она), полученная заявляемым способом, эмпирическим путем были получены результаты, доказывающие высокую эффективность данного вещества/ лекарственного средства в проведении терапии новой коронавирусной инфекции COVID-19.
Подавлением вирусной активности можно объяснить полученный клинический эффект в виде сроков исчезновения общих симптомов заболевания, включая купирование лихорадки, и лабораторных признаков системного воспаления, отсутствие прогрессирования заболевания и обратное развитие пневмонии, подтвержденное данными КТ, при этом отрицательные результаты ПЦР получены на 10, 11, 14-й дни проведения терапии. При этом в ранее проведенных зарубежных исследованиях было показано, что отрицательный результат ПЦР анализа у пациентов был получен только к 23-му дню наблюдения [Tang W, Cao Z, Han M, et al. Hydroxychloroquine in patients with mainly mild to moderate coronavirus disease 2019: open label, randomised controlled trial. BMJ. 2020;369:m1849. DOI:10.1136/bmj.m1849].
Таким образом, получены клинические, лабораторные, рентгенологические данные об эффективности применения противовирусного препарата риамиловир, полученного предлагаемым к защите способом, в лечении новой коронавирусной инфекции COVID-19. Результаты исследования подтвердили гипотезу об отсутствии нежелательных побочных явлений при лечении риамиловиром пациентов с Covid-19, что свидетельствует о хорошей переносимости препарата.
Применение натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, обладающей противовирусной активностью, полученной заявляемым способом, эффективно при лечении новой коронавирусной инфекции COVID-19, при этом сроки лечения сокращены.
| название | год | авторы | номер документа |
|---|---|---|---|
| Применение способа введения натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, обладающей противовирусной активностью, для лечения коронавирусной инфекции COVID-19 | 2021 |
|
RU2754532C1 |
| Применение способа введения натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, обладающей противовирусной активностью, для профилактики коронавирусной инфекции COVID-19 | 2021 |
|
RU2754531C1 |
| Способ получения натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, обладающей противовирусной активностью | 2020 |
|
RU2741502C1 |
| НАТРИЕВАЯ СОЛЬ 2-МЕТИЛТИО-6-НИТРО-1,2-4-ТРИАЗОЛО[5,1-C]-1,2,4-ТРИАЗИН-7(4H)-ОНА, ДИГИДРАТ, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2294936C1 |
| 2-МЕТИЛСУЛЬФАНИЛ-6-НИТРО-7-ОКСО-1,2,4-ТРИАЗОЛО[5,1-c] [1,2,4]ТРИАЗИНИД L-АРГИНИНИЯ ДИГИДРАТ, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЛИХОРАДКИ ЗАПАДНОГО НИЛА | 2013 |
|
RU2536874C1 |
| 3-Бензил-5-метил-6-(фенилтио)-[1,2,4]триазоло[1,5-a]пиримидин-7(3H)-он, обладающий противовирусной активностью в отношении коронавируса SARS-CoV2 | 2022 |
|
RU2808622C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ | 2010 |
|
RU2457844C2 |
| 3-Нитро-4-гидрокси-7-пропаргилтио-[1,2,4]триазоло[5,1c][1,2,4]триазин и 3-нитро-4-гидрокси-7-этилтио-[1,2,4]триазоло[5,1c][1,2,4]триазин, обладающие противовирусной активностью | 2019 |
|
RU2775551C2 |
| НАТРИЕВАЯ СОЛЬ 2-МЕТИЛТИО-6-ЦИАНО-1,2,4-ТРИАЗОЛО[5,1-с]-1,2,4-ТРИАЗИН-7(4Н)-ОНА, ТРИГИДРАТ | 2015 |
|
RU2607628C1 |
| ИНЪЕКЦИОННЫЙ ИЛИ ИНФУЗИОННЫЙ РАСТВОР L-АРГИНИНИЕВОЙ СОЛИ 5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-а]ПИРИМИДИН-7-ОНА МОНОГИДРАТА ДЛЯ ТЕРАПИИ ГРИППА И ДРУГИХ ВИРУСНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2586283C1 |
Изобретение относится к области медицины, а именно к инфектологии, и предназначено для лечения новой коронавирусной инфекции COVID-19. Для лечения новой коронавирусной инфекции COVID-19 применяют способ введения натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, обладающей противовирусной активностью, заключающийся в приеме по одной капсуле препарата риамиловир с содержанием натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, в количестве 250 мг три раза в сутки в течение 10 дней. Использование изобретения обеспечивает лечение COVID-19.
Применение способа введения натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, обладающей противовирусной активностью путем приема по одной капсуле препарата риамиловир с содержанием натриевой соли 2-метилтио-6-нитро-1,2-4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата, в количестве 250 мг три раза в сутки в течение 10 дней для лечения новой коронавирусной инфекции COVID-19.
| US 2020237689 A1 (BLUEWILLOW BIOLOGICS INC), 30.07.2020 | |||
| PANDA KP et al | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Trials, 2020 Oct 20;21(1):866 | |||
| НОВИКОВА Н.А | |||
| и | |||
Авторы
Даты
2022-06-23—Публикация
2020-11-06—Подача