Перекрестная ссылка на родственные заявки
[0001] По настоящей заявке испрашивается приоритет предварительных патентных заявок США: 62/464371, поданной 27 февраля 2017 г., озаглавленной «COMPOSITIONS, ARTICLES OF MANUFACTURE AND METHODS RELATED TO DOSING IN CELL THERAPY»; 62/465817, поданной 1 марта 2017 г., озаглавленной «COMPOSITIONS, ARTICLES OF MANUFACTURE AND METHODS RELATED TO DOSING IN CELL THERAPY»; 62/470180, поданной 10 марта 2017 г., озаглавленной «COMPOSITIONS, ARTICLES OF MANUFACTURE AND METHODS RELATED TO DOSING IN CELL THERAPY»; 62/527002, поданной 29 июня 2017 г., озаглавленной «COMPOSITIONS, ARTICLES OF MANUFACTURE AND METHODS RELATED TO DOSING IN CELL THERAPY»; 62/580416, поданной 1 ноября 2017 г., озаглавленной «COMPOSITIONS, ARTICLES OF MANUFACTURE AND METHODS RELATED TO DOSING IN CELL THERAPY»; 62/584740, поданной 10 ноября 2017 г., озаглавленной «COMPOSITIONS, ARTICLES OF MANUFACTURE AND METHODS RELATED TO DOSING IN CELL THERAPY»; и 62/596703, поданной 8 декабря, озаглавленной «COMPOSITIONS, ARTICLES OF MANUFACTURE AND METHODS RELATED TO DOSING IN CELL THERAPY», полное содержание которых, приведено в настоящем описании в качестве ссылки для всех целей.
Включение списка последовательностей в качестве ссылки
[0002] Настоящая заявка подана вместе со списком последовательностей в электронном формате. Список последовательностей представлен в форме файла, озаглавленного 735042009340SeqList.TXT, созданного 27 февраля 2018 г., имеющего размер 37444 байт. Полная информация в электронном формате из списка последовательностей приведена в качестве ссылки.
Область изобретения
[0003] Настоящее изобретение относится к клеточной терапии, включающей введение одной или нескольких доз терапевтической композиции T–клеток, и к способам, композициям и изделиям для применения в ней. Клетки из композиции T–клеток экспрессируют рекомбинантные рецепторы, такие как химерные рецепторы, например, химерные рецепторы антигенов (CAR) или другие трансгенные рецепторы, такие как T–клеточные рецепторы (TCR). Признаки вариантов осуществления по настоящему описанию, включая вводимое количество клеток или единиц клеток и/или активность введенных клеток, обеспечивают различные преимущества, такие как более низкий риск токсичности у индивидов, которым вводили композиции T–клеток.
Уровень техники
[0004] Различные способы клеточной терапии доступны для лечения заболеваний и состояний. Необходимы улучшенные способы, например, для уменьшения риска токсичности таких способов. Например, необходимы улучшенные способы для уменьшения риска токсичности способов клеточной терапии, с сохранением в то же время эффективности введенных клеток у индивида. Настоящее изобретение относится к композициям, изделиям, способам и применениям, удовлетворяющим такую необходимость.
Сущность изобретения
[0005] Настоящее изобретение относится к вариантам осуществления, относящимся к способам клеточной терапии, таким как способы адоптивной клеточной терапии, включая способы, которые можно использовать для прогнозирования, уменьшения, предотвращения, облегчения одного или нескольких нежелательных или неблагоприятных эффектов или видов токсичности, или их риска, которые могут быть ассоциированы с такими видами терапии, таких как виды токсичности, включающие виды тяжелой токсичности, включая тяжелую или летальную нейротоксичность, включая виды токсичности, ассоциированные с отеком головного мозга или включающие отек головного мозга. Среди таких представленных вариантов осуществления присутствуют изделия, композиции, такие как композиции, содержащие одну или несколько единичных доз клеток, и способы и применения, такие как способы и применения, относящиеся к способам или предназначенные для способов адоптивной клеточной иммунотерапии, таких как способы терапии с использованием сконструированных T–клеток, включая способы CAR–T–клеточной терапии.
[0006] Среди представленных вариантов осуществления присутствуют изделия, такие как изделия, содержащие: (a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, который, необязательно представляет собой химерный антигенный рецептор (CAR), который специфически связывается с антигеном, где единичная доза содержит целевое количество эталонных единиц (RU) в пределах данного диапазона, где RU в данной композиции определяют по формуле RU=A x B, где: A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его долю, или кратное, или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и (b) инструкции для введения композиции, необязательно, одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
[0007] Настоящее изобретение относится также к изделию, содержащему: (a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, необязательно, представляющий собой химерный антигенный рецептор (CAR), который специфически связывается с антигеном, где: единичная доза содержит или содержит приблизительно (i) целевое количество тотальных экспрессирующих рекомбинантный рецептор клеток или целевое количество тотальных экспрессирующих рекомбинантный рецептор CD3+ клеток, или целевое количество тотальных экспрессирующих рекомбинантный рецептор CD8+ клеток, или (ii) целевое количество эталонных единиц (RU) в пределах данного диапазона, которое равно или меньше порогового количества RU, где единичная доза не содержит больше порогового значения RU, где количество RU в данной композиции определяют по формуле: RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции T–клеток; и (b) инструкции для введения композиции, необязательно одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
[0008] Настоящее изобретение относится также к изделию, содержащему: (a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие химерный антигенный рецептор (CAR), который специфически связывается с антигеном, где единичная доза содержит целевую дозу терапевтической композиции T–клеток, где: (i) если значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности композиции, равно или больше порогового значения, целевая доза представляет собой первое количество (или лежит в первом диапазоне количеств) клеток данного фенотипа из композиции; (ii) если значение параметра меньше порогового значения, целевая доза представляет собой второе количество (или лежит во втором диапазоне количеств) клеток данного фенотипа из композиции, где первое количество (или первый диапазон) ниже, чем второе количество (или второй диапазон); и (b) инструкции для введения композиции, необязательно одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
[0009] Настоящее изобретение относится также к изделию, содержащему: (a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, необязательно, представляющий собой химерный антигенный рецептор (CAR), который специфически связывается с антигеном, где: единичная доза содержит целевую дозу терапевтической композиции T–клеток; и терапевтическая композиция T–клеток находится выше нижнего установленного предела (LSL) и ниже верхнего установленного предела (USL) для B, где B представляет собой значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности композиции; и (b) инструкции для введения композиции, необязательно одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
[0010] Настоящее изобретение относится к способу лечения, включающему введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащих клетки, содержащие рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит целевое количество эталонных единиц (RU) в пределах данного диапазона, где RU в данной композиции определяют по формуле RU=A x B, где: A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции.
[0011] Настоящее изобретение относится также к способу лечения, включающему введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащих клетки, содержащие рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит или содержит приблизительно (i) целевое количество тотальных экспрессирующих рекомбинантный рецептор клеток или целевое количество тотальных экспрессирующих рекомбинантный рецептор CD8+ клеток или (ii) целевое количество эталонных единиц (RU) в пределах данного диапазона, которое равно или меньше порогового количества RU, где единичная доза не содержит больше порогового значения RU, где количество RU в данной композиции определяют по формуле: RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции T–клеток.
[0012] В конкретных вариантах осуществления, A представляет собой общее количество T–клеток, общее количество CD3+ клеток, общее количество CD4+ или CD8+ клеток, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, общее количество CD4+ CAR+, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение. В некоторых вариантах осуществления, A представляет собой общее количество CD3+ клеток, общее количество CD8+, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение. В конкретных вариантах осуществления, A представляет собой общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD3+ CAR+ клетки, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD4+ CAR+, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD8+ CAR+ клетки, или его кратное или преобразованное значение, где маркер апоптоза представляет собой аннексин V или активную каспазу 3. В конкретных вариантах осуществления, A представляет собой общее количество маркер апоптоза– CD3+ CAR+ клеток или общее количество маркер апоптоза– CD8+ CAR+ клеток, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0013] Настоящее изобретение относится также к способу лечения, включающему введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащих клетки, содержащие рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит целевую дозу терапевтической композиции T–клеток: (i) если значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности композиции, равно или больше порогового значения, целевая доза представляет собой первое количество (или лежит в первом диапазоне количеств) клеток данного фенотипа из композиции; (ii) если значение параметра меньше порогового значения, целевая доза представляет собой второе количество (или лежит во втором диапазоне количеств) клеток данного фенотипа из композиции, где первое количество (или первый диапазон) ниже, чем второе количество (или второй диапазон).
[0014] Настоящее изобретение относится также к способу анализа терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающему: (a) анализ образца из композиции T–клеток, содержащей T–клетки, происходящие от индивида, имеющего заболевание или состояние, и трансдуцированные нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где анализ определяет B для композиции клеток, где B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции; и (b) оценку активности композиции клеток на основании B, и/или оценку того, находится ли композиция выше нижнего установленного предела (LSL) для B или ниже верхнего установленного предела (USL) для B.
[0015] Настоящее изобретение относится также к способу оценки терапевтической композиции T–клеток, включающему оценку образца из композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, по активности композиции клеток на основании B, и/или оценку того, находится ли композиция выше нижнего установленного предела (LSL) для B или ниже верхнего установленного предела (USL) для B.
[0016] Настоящее изобретение относится также к способу оценки риска токсичности терапевтической композиции T–клеток, включающему: (a) оценку образца из композиции T–клеток, введенной индивиду, по количеству эталонных единиц (RU) в пределах данного диапазона, где композиция T–клеток содержит T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где RU в данной композиции определяют по формуле: RU=A x B, где: A представляет собой количество клеток, или его кратное, долю или преобразование, клеток некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его долю, или кратное, или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и (b) сравнение количеств RU с эталонными безопасными количествами RU, где сравнение показывает, подвержен или нет индивид риску возникновения неблагоприятного события, необязательно, серьезного неблагоприятного события, необязательно, тяжелой нейротоксичности, степени, равной или выше степени 4 или степени 5, или по меньшей мере, длительной нейротоксичности степени 3.
[0017] Настоящее изобретение относится также к способу получения терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающему: (a) анализ композиции T–клеток, содержащей T–клетки, происходящие от индивида, имеющего заболевание или состояние, и трансдуцированные нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где анализ определяет B для композиции клеток, где B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и (b) заполнение контейнера всей или частью композиции и необязательно, другим раствором для получения единичной дозы композиции T–клеток, где единичная доза содержит целевое количество эталонных единиц (RU) из композиции T–клеток, где RU в данной композиции определяют по формуле: RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
[0018] Настоящее изобретение относится также к способу получения терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающему заполнение контейнера всей или частью композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, и необязательно, другим раствором, для получения единичной дозы композиции T–клеток, где единичная доза содержит целевое количество эталонных единиц (RU) композиции T–клеток, где RU в данной композиции определяют по формуле: RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции.
[0019] Настоящее изобретение относится также к способу получения терапевтической композиции T–клеток для клеточной терапии, включающему заполнение контейнера всей или частью композиции, содержащей T–клетки, до концентрации между приблизительно 10 миллионов клеток и приблизительно 70 миллионов клеток на мл, включительно, и необязательно, другим раствором.
[0020] Настоящее изобретение относится к единичной дозе терапевтической композиции T–клеток, содержащих некоторое количество клеток, содержащих рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), специфический для антигена, ассоциированного с заболеванием или состоянием, или экспрессируемого при заболевании или состоянии, где количество клеток составляет между и между приблизительно 5,0×106 и 2,25×107, 5,0×106 и 2,0×107, 5,0×106 и 1,5×107, 5,0×106 и 1,0×107, 5,0×106 и 7,5×106, 7,5×106 и 2,25×107, 7,5×106 и 2,0×107, 7,5×106 и 1,5×107, 7,5×106 и 1,0×107, 1,0×107 и 2,25×107, 1,0×107 и 2,0×107, 1,0×107 и 1,5×107, 1,5×107 и 2,25×107, 1,5×107 и 2,0×107, 2,0×107 и 2,25×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0021] Настоящее изобретение относится к способу определения того, подвержен ли индивид риску токсичности, включающему анализ количества экспрессирующих рекомбинантный рецептор клеток в крови индивида, где указанному индивиду ранее вводили дозу экспрессирующих рекомбинантный рецептор клеток, где индивид подвержен риску развития токсичности, если: (i) не более чем через четверо суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 2 экспрессирующие рекомбинантный рецептор клетки на микролитр; (ii) не более чем через пять или шесть суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 5 экспрессирующих рекомбинантный рецептор клеток на микролитр или составляет по меньшей мере или приблизительно 10 экспрессирующих рекомбинантный рецептор клеток на микролитр; или (iii) не более чем через семь суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 15 экспрессирующих рекомбинантный рецептор клеток на микролитр.
[0022] Настоящее изобретение относится также к способу определения того, подвержен ли индивид риску токсичности, включающему: (a) введение индивиду, страдающему заболеванием или состоянием, дозы экспрессирующих рекомбинантный рецептор клеток; и (b) после введения клеток, анализ количества экспрессирующих рекомбинантный рецептор клеток в крови индивида, где индивид подвержен риску развития токсичности, если: (i) не более чем через четверо суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 2 экспрессирующие рекомбинантный рецептор клетки на микролитр; (ii) не более чем через пять или шесть суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 5 экспрессирующих рекомбинантный рецептор клеток на микролитр, или составляет по меньшей мере или приблизительно 10 экспрессирующих рекомбинантный рецептор клеток на микролитр; или (iii) не более чем через семь суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 15 экспрессирующих рекомбинантный рецептор клеток на микролитр.
[0023] Настоящее изобретение относится также к способу оценки стимулирующего реагента для использования в получении терапевтической композиции T–клеток, включающему: (i) оценку композиции T–клеток, полученной с использованием стимулирующего реагента, по зависимым от рекомбинантного рецептора активности или фенотипу; и (ii) сравнение зависимых от рекомбинантного рецептора активности или фенотипа, с такими же активностью или фенотипом, полученными для контрольной композиции, или сравнение со стандартной единицей зависимых от рекомбинантного рецептора активности или фенотипа, где стимулирующее средство определяют как пригодное для выпуска для использования в способе получения терапевтической композиции T–клеток, если зависимые от рекомбинантного рецептора активность или фенотип композиции клеток, полученной с использованием стимулирующего реагента, отличаются не более чем на 40% или не более чем на 30%, или не более чем на 20% или не более чем на 10%, или не более чем на 5% от такой же активности, полученной для контрольной композиции, или от стандартной единицы.
[0024] В некоторых из любых таких вариантов осуществления, степень или уровень зависимых от рекомбинантного рецептора активности или фенотипа терапевтической композиции T–клеток, в конкретных аспектах, представляет признаки или свойства, специфические для терапевтической композиции и/или ее продукции, ассоциированные с риском возникновения неблагоприятного побочного эффекта после введения терапевтической композиции T–клеток индивиду. В некоторых аспектах, такие риски выше или возникают с более высокой частотой у конкретных индивидов, имеющих один или несколько факторов риска, например, у (i) индивидов, которых подвергали меньшему количеству циклов предшествующей терапии, необязательно, менее чем двум циклам предшествующей терапии, до начала введения терапевтической композиции T–клеток, (ii) индивидов молодого возраста, необязательно, менее чем 30 лет, (iii) индивидов, у которых соотношение CD4:CD8 в образце после афереза от индивида ниже определенного порога, необязательно, ниже 1:1 или ниже 1,5:1 или ниже 0,5:1 или ниже, например, когда вводимая доза основана на общем количестве T–клеток или общем количестве T–клеток, экспрессирующих сконструированный или рекомбинантный рецептор, такой как CAR, например, без указания количества или соотношения CD4+ или CD8+ T–клеток в дозе; (iv) индивидов, имеющих массу, превышающую среднюю массу среди группы индивидов, подвергаемых лечению; (v) индивидов с количеством тромбоцитов менее чем или приблизительно менее чем 120000; (vi) индивидов, имеющих B–клеточный лейкоз, необязательно острый лимфоцитарный лейкоз (ALL); (vii) индивидов, имеющих высокую нагрузку заболевания перед, например, непосредственно перед или в пределах одного месяца перед началом введения терапевтической композиции T–клеток, необязательно, как определено на основании процента бластных клеток костного мозга, большего или равного 5%, суммы произведений диаметров (SPD), или уровней лактатдегидрогеназы; или (viii) индивидов, не имеющих молекулярного подтипа острого лимфобластного лейкоза (ALL) с филадельфийской хромосомой (Ph+) и/или подобного подтипу с Ph–хромосомой (Ph–подобного); (ix) индивидов, подвергнутых переходной химиотерапии до начала введения терапевтической композиции T–клеток; (x) индивидов, подвергнутых предварительной подготовке с использованием противолимфоцитарной терапии, необязательно включающей введение флударабина и/или циклофосфамида, до начала введения терапевтической композиции T–клеток; и/или (xi) индивидов, у которых уровень, количество или концентрация интерлейкина–15 (IL–15) в образце крови до начала введения терапевтической композиции T–клеток выше порогового значения. В некоторых вариантах осуществления, настоящее изобретение относится к вариантам осуществления, например, относится к способам, изделиям, композициям, дозам и способам дозирования, ответственным за такие признаки или свойства, например, в связи с дозированием у индивида, и таким образом, за предотвращение, облегчениe или уменьшение риска или вероятности возникновения у индивида неблагоприятного события или токсичности, такой как тяжелая нейротоксичность или нейротоксичность степени 3 или выше, или длительная нейротоксичность степени 3, степени 4 или степени 5, после введения терапевтической композиции T–клеток.
[0025] В некоторых из любых таких вариантов осуществления, иллюстративные признаки включают количество или частоту (или количество/кг) жизнеспособных клеток, и/или клеток различных фенотипов, в индивидуальных дозах, вводимых индивидуальным индивидам. Иллюстративные такие фенотипы включают экспрессию одного или нескольких поверхностных маркеров, как оценено посредством проточной цитометрии. Например, в некоторых аспектах, фенотипы включают CD3+, CD8+, CD4+ и/или CAR+. Среди фенотипов присутствует также жизнеспособность и фенотипы, ассоциированные с функциональными, здоровыми или биологически активными клетками, или показательные для них, или, как считают, показательные для них. В конкретных аспектах, такие фенотипы включают отсутствие или небольшие присутствие или экспрессию маркеров, показательных для апоптоза, апоптотических клеток или различных, например, ранних или поздних, стадий одного или нескольких из гибели или входа в апоптотический путь (например, аннексина V, каспазы 3). В конкретных аспектах, такие маркеры включают способность клеток продуцировать цитокины или другие факторы не специфическим для антигена CAR образом, например, при окрашивании внутриклеточных цитокинов (ICS) в ответ на PMA/иономицин и/или FOXP3. В некоторых аспектах, маркеры и фенотипы включают маркеры и фенотипы, ассоциированные с одним или несколькими из активации T–клеток, истощения, подобных стволовым клеткам свойств, наивных T–клеток, продолжительность жизни, подгрупп T–клеток, фенотипа(фенотипов) памяти и фенотипов одной или нескольких подгрупп T–клеток памяти, таких как один или несколько из TCM, TEM и TSCM.
[0026] В некоторых из любых таких вариантов осуществления, относящиеся к терапевтической композиции клеток признаки включают общее количество CD8+CAR+ T–клеток в вводимой дозе, общее количество или частоту (например, среди CD8+CAR+ T–клеток) CD8+CAR+ T–клеток в вводимой дозе, как наблюдают, отрицательных по фактору, показательному для апоптоза, такому как поверхностное окрашивание аннексина V (аннексин V–) или расщепление каспазой 3 (что указывает на неапоптотические клетки). Конкретные примеры относящихся к терапевтической композиции клеток признаков включают общее количество CD3+CAR+ T–клеток в вводимой дозе, общее количество или частоту (например, среди CD3+CAR+ T–клеток) CD3+CAR+ T–клеток в вводимой дозе, как наблюдают, отрицательных по фактору, показательному для апоптоза, такому как поверхностное окрашивание аннексина V (аннексин V–) или расщепление каспазой 3 (что указывает на неапоптотические клетки).
[0027] В некоторых из любых таких вариантов осуществления, иллюстративные параметры представляют собой свойства, специфические для терапевтических композиций и/или для их получения, включая концентрацию жизнеспособных клеток (VCC), кратность размножения клеток между инокуляцией и сбором продукта лекарственного средства; и количество копий вектора (VCN) в введенной дозе. Среди иллюстративных параметров присутствуют также параметры, в общем ассоциированные или показательные для функции или активности или других признаков или возможностей клеток в композициях. Среди них присутствуют различные признаки, ассоциированные с исходами стимуляции клеток, включая различные показатели пролиферации и активации или активности, включая индуцированные способом, индуцированным или зависимым от TCR и/или CAR. Иллюстративными такими параметрами, относящимися к функции или активности, являлись показатели или уровни (такие как их количество или концентрация, или уровень на клетку) продукции одного или нескольких факторов (таких как различные цитокины) клетками в композиции, в ответ на специфическую для антигена CAR или другую стимуляцию.
[0028] В некоторых из любых таких вариантов осуществления, параметры, показательные для направляемых CAR видов антигенспецифической активности и функций (таких как зависимая от антигена CAR секреция цитокинов и цитотоксичность) композиций оценивают в анализах совместного культивирования. Клетки из оцениваемой терапевтической композиции инкубируют в присутствии экспрессирующих CD19 клеток–мишеней. Для анализов цитокинов, накопленные количества (пг/мл) цитокина(цитокинов) (например, IL–2, IFN–гамма, TNF–альфа, IL–6, sCD137, MIP1b, MIP1a, IL–10, IL–4, IL–13, IL–5 или GM–CSF) можно оценивать после инкубации клеток–мишеней и количества различных композиций, включающего одинаковое количество трансдуцированных или CAR+ клеток, в одинаковом объеме, например, в течение периода приблизительно 22–24 часов. Такие анализы предоставляют показатель антигенспецифической секреции цитокинов на CAR+ клетку в дозе. В других анализах, цитолитическую активность против экспрессирующих CD19 клеток–мишеней оценивали после инкубации с T–клетками.
[0029] В некоторых из любых таких вариантов осуществления, оценивают показатели активности или функционального эффекта в ответ на не специфический для антигена CAR стимул, такие как продукция цитокина или другого фактора после стимуляции с использованием антитела против CD3/против CD28, например, в форме покрытия магнитных бусин. В таких анализах, культуры, содержащие меньшее количество CAR+ клеток среди T–клеток в культуре, могут иметь более высокий относительный уровень показателя.
[0030] В некоторых из любых таких вариантов осуществления, взаимосвязи применительно к количеству копий вектора (на клетку или на геном) считают суррогатными показателями выносливости клеток и/или множества переменных, ассоциированных с относительной представленностью модифицированных или немодифицированных клеток в композиции и/или общей плотностью клеток в композиции. Например, в некоторых вариантах осуществления, клетки из образцов крови, которые в общем являются менее здоровыми в начале процесса, имеют более низкую вероятность выживания во время фазы трансдукции, и/или гибель клеток во время трансдукции могла увеличивать эффективность трансдукции. Таким образом, в конкретных случаях, более высокое количество копий вирусного вектора на композицию, например, введенное посредством трансдукции лентивирусным или гамма–ретровирусным вектором, может указывать на композицию, в которой больший процент клеток являлись нездоровыми в начале процесса и, в конкретных аспектах, могут иметь свойства, коррелирующие, например, обратно, с нейротоксичностью. В некоторых вариантах осуществления, более высокая частота трансдукции может приводить к получению композиции, имеющей более высокую частоту модифицированных (например, CAR+) клеток во время криоконсервации, хранения и размораживания. В конкретных аспектах, когда доза основана на количествах модифицированных клеток (или их подтипов, например, CAR+CD3+), такие композиции с более высокой частотой модифицированных клеток могут иметь более низкую общую плотность клеток, что, в конкретных вариантах осуществления, коррелирует с уменьшением уровня или частоты биологически активных или неапоптотических клеток.
[0031] В некоторых из любых таких вариантов осуществления, различные показатели количества(количеств) или нормализованных количеств клеток, отрицательных по поверхностному окрашиванию маркеров апоптоза (включая аннексин V), в дозах, вводимых индивиду (или частота таких отрицательных по маркеру апоптоза клеток среди клеток продукта, например, среди CAR+CD3+ или CAR+CD8+) коррелируют или ассоциированы с неблагоприятным событием, таким как токсичность, например, нейротоксичность. В некоторых аспектах, наблюдают, что аннексин V и каспаза–3 являются в общем сходными. В то время как такие параметры можно также считать связанными с функцией или активностью композиции CAR–T–клеток, и таким образом, можно ожидать, что они связаны с эффективностью, эти переменные, как правило, значимо не коррелируют с исходом ответа на лечение, например, достигнет или нет индивид полного ответа или отсутствия ответа.
[0032] В некоторых из любых таких вариантов осуществления, комбинация признаков или параметров терапевтической композиции CAR–T–клеток (например, антигенспецифической активности и/или жизнеспособности), признаков и/или характеристик индивида (например, возраста, массы и/или заболевания), и других видов лечения (например, количество предшествующих циклов лечения) ассоциирована с риском развития летальной нейротоксичности, например, после лечения с использованием композиции CAR–T–клеток.
[0033] В некоторых из любых таких вариантов осуществления, отек головного мозга коррелирует и/или ассоциирован с ранним и быстрым размножением CAR–T–клеток и/или с увеличением уровня IL–15, биомаркера воспаления и фактора роста CAR–T. В некоторых аспектах, доза и функция CD8+ CAR+ клеток, вместе с характеристиками и/или признаками индивида, управляют, коррелируют с, и/или ассоциированы с ранним и/или быстрым размножением CAR–T–клеток.
[0034] В некоторых из любых таких вариантов осуществления, характеристики и/или признаки индивида представляют собой или включают молодой возраст (например, возраст менее чем 30 лет), предшествующее лечение (например, с двумя или менее предшествующими режимами), интенсивную переходную химиотерапию, и/или высоко интенсивное использование флударабина и/или циклофосфамида, например, для противолимфоцитарной терапии.
[0035] В некоторых из любых таких вариантов осуществления, отек головного мозга, например, отек головного мозга, ассоциированный с и/или следующий за CAR–T–клеточной терапией, ассоциирован с повреждением эндотелия и полным разрушением гематоэнцефалического барьера (BBB). В конкретных аспектах, отек головного мозга не ассоциирован с инфильтрацией CAR–T–клетками головного мозга, лейкозом центральной нервной системы (ЦНС) или предшествующими циклами терапии лейкоза ЦНС.
[0036] В некоторых из любых таких вариантов осуществления, идентификация пациентов с высоким риском до лечения или перед лечением, например, с использованием CAR–T–клеточной терапии, является ключевой для потенциального управления течением и смягчения риска, например, риска или вероятности токсичности, такой как нейротоксичность или отек головного мозга. В конкретных аспектах, риск летальной нейротоксичности можно смягчать, уменьшать и/или снижать посредством минимизации изменчивости композиций CAR–T–клеток, например, минимизации изменчивости среди композиций клеток по такому параметру, как жизнеспособность, соотношение CD4+/CD8+ и активность. В конкретных аспектах, использование определенного продукта композиции, например, композиции CAR–T–клеток с определенными параметрами, может уменьшать изменчивость дозы и функции.
[0037] В некоторых из любых таких вариантов осуществления, представленные способы, изделия, композиции, дозы и способы дозирования обеспечивают преимущества в том, что они принимают во внимание и, в соответствующих случаях, регулируют или корректируют, потенциальные источники изменчивости, включая изменчивость, возникающую из–за смены реагентов, и/или изменчивость от пациента к пациенту. Например, в конкретных вариантах осуществления, может обеспечивать преимущества получение модифицированных T–клеток способом, включающим использование реагента для стимуляции/размножения T–клеток (или множества реагентов), с подтверждением посредством анализа высвобождения нахождения ниже или в пределах приемлемого диапазона переменной, по сравнению с пороговым уровнем параметра, например, специфической активности по отношению к такому параметру терапевтической композиции (такой как показатель количества или относительного количества реагента, необходимого для индукции конкретной степени антигенспецифической активности в конечной композиции T–клеток, полученной способом модификации T–клеток, например, по сравнению с контрольным реагентом или стандартной единицей, применительно к такому анализу). В конкретных вариантах осуществления, представленные варианты осуществления включают дозы клеток, в которых клетки получены способом, включающим анализ высвобождения для подтверждения того, что любая изменчивость такого специфического параметра активности (например, антигенспецифический уровень провоспалительного цитокина) находится в пределах приемлемого диапазона и/или ниже верхнего установленного предела. В некоторых вариантах осуществления, приведенные способы включают такой анализ высвобождения. В конкретных вариантах осуществления, получение композиций клеток проводят с использованием реагентов и/или способов, для которых изменчивость таких параметров находится в пределах приемлемого диапазона. В конкретных вариантах осуществления, представленные способы, композиции и изделия обеспечивают преимущества в том, что для них используют способы дозирования и/или получения клеток, которые смягчают риск, ассоциированный с потенциальной изменчивостью таких специфических параметров активности, например, посредством минимизации изменчивости второго параметра, который, вместе со специфическим параметром активности, коррелирует с риском токсичности. Например, посредством минимизации изменчивости частоты биологически активных или здоровых клеток (например, неапоптотических клеток), полученных способом, можно минимизировать влияние изменений специфических связанных с активностью параметров на безопасность. В некоторых вариантах осуществления, доза или способ дозирования, включающие признак(и), связанные с количеством или частотой биологически активных или неапоптотических клеток, таких как биологически активные или неапоптотические модифицированные клетки, или модифицированные CD8+ клетки, уменьшают риск, ассоциированный с изменчивостью параметров антигенспецифической активности. В конкретных аспектах, этого достигают посредством дозирования, включающего верхний предел для таких клеток и/или определяющего дозу на основании эталонных единиц, например, на основании формулы, принимающей во внимание количество биологически активных клеток.
[0038] В конкретных вариантах осуществления, использование способа с уменьшенной изменчивостью частоты таких биологически активных клеток среди модифицированных клеток, уменьшает риск того, что конкретным пациентам (например, пациентам, имеющим клетки, менее склонные к апоптозу или более здоровые) могут непреднамеренно вводить более высокую дозу биологически активных клеток, чем намеревались, при дозировании на основании количества модифицированных T–клеток в целом. Кроме того, наблюдали, что способы, такие как этот способ с большей степенью контроля фенотипа и функции, уменьшает степень изменчивости для способности клеток, полученных этим способом, продуцировать провоспалительные цитокины антигенспецифическим образом. Результаты вышеописанного исследования согласуются с интерпретацией, что, в частности, в сочетании с количествами биологически активных модифицированных клеток, способ дозирования, принимающий во внимание такие специфические для клеток параметры активности (например, таким образом, что конкретный целевой диапазон такой активности – или не более порогового значения – представлены в данной дозе), можно использовать для предоставления дозы, способной обеспечивать желательный клинический или терапевтический исход, в то же время все еще оставаясь в границах безопасности или уменьшая риск нежелательной токсичности, например, нейротоксичности.
[0039] В некоторых вариантах осуществления, использование способа, в котором постоянно получают более высокие частоты биологически активных модифицированных клеток, позволяет использование доз клеток, намного более низких (с позиции количеств модифицированных, например, CAR+, клеток), по сравнению с другими способами дозирования, в которых с большей частотой модифицированные клетки являются положительными по апоптотическим маркерам или являются в ином отношении менее здоровыми. Например, на основании наблюдений в настоящем описании, и принимая во внимание то наблюдение, что в доступных способах дозирования, как правило, не принимают во внимание частоту апоптотических клеток, в конкретных вариантах осуществления, количества модифицированных (например, CAR+) T–клеток (например, модифицированных CD8+ и/или CD4+ клеток), являются настолько низкими, как 5, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 30, 40 или 50 миллионов клеток.
[0040] В некоторых из любых таких вариантов осуществления, представленный вариант осуществления включает оценку или определение количества клеток или его кратного или доли, или преобразования, данного фенотипа, присутствующих в данной композиции. В некоторых вариантах осуществления, A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции. В конкретных вариантах осуществления, целевое количество единиц составляет менее, чем пороговое количество единиц, необязательно, представляющее собой безопасное количество эталонных единиц, где безопасное количество эталонных единиц составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события. В конкретных вариантах осуществления, неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность, необязательно, степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
[0041] В некоторых вариантах осуществления, целевое количество эталонных единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, и/или на количество в диапазоне от 1,5– до 3–кратного, необязательно, приблизительно 2–кратное, или на количество, кратное стандартному отклонению в группе индивидов, у которых не возникло неблагоприятного события, необязательно, нейротоксичности степени 0–2, необязательно, где кратное лежит в диапазоне от 1,5– до 3–кратного. В конкретных вариантах осуществления, целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, для которой показан желательный терапевтический исход, необязательно, частичный ответ или полный ответ (CR).
[0042] В конкретных вариантах осуществления, A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции. В некоторых вариантах осуществления: целевое количество представляет собой целевое количество экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD3+, которые являются отрицательными(–) по маркеру апоптоза и CD3+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; или целевое количество представляет собой целевое количество экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0043] В конкретных вариантах осуществления, целевое количество клеток в (i) составляет: между и между приблизительно 5,0×106 и 2,25×107, 5,0×106 и 2,0×107, 5,0×106 и 1,5×107, 5,0×106 и 1,0×107, 5,0×106 и 7,5×106, 7,5×106 и 2,25×107, 7,5×106 и 2,0×107, 7,5×106 и 1,5×107, 7,5×106 и 1,0×107, 1,0×107 и 2,25×107, 1,0×107 и 2,0×107, 1,0×107 и 1,5×107, 1,5×107 и 2,25×107, 1,5×107 и 2,0×107, 2,0×107 и 2,25×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD3+ или CD8+ или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0044] В конкретных вариантах осуществления, целевое количество клеток в (i) составляет: между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; между по меньшей мере или по меньшей мере приблизительно 5,55×106, 6,66×106, 7,77×106, 8,99×106, 1,0×107, 1,1×107 и приблизительно 1,67×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; между по меньшей мере или по меньшей мере приблизительно 7,14×106, 8,5×106, 1,0×107, 1,14×107, 1,29×107, 1,42×107 и приблизительно 2,14×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0045] В некоторых вариантах осуществления, целевое количество клеток в (i) составляет между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, которые являются отрицательными(–) по маркеру апоптоза и CD8+, включая каждое, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3. В конкретных вариантах осуществления, целевое количество клеток в (i) составляет между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, включая каждое.
[0046] В конкретных вариантах осуществления, целевое эталонное количество RU составляет менее, чем пороговое количество единиц или составляет менее, чем эталонное безопасное количество RU, где эталонное безопасное количество RU составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
[0047] В некоторых вариантах осуществления, A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции. В конкретных вариантах осуществления, A и/или B представляет собой преобразование количества или значения, соответственно, где преобразование включает логарифмическое преобразование, степенное преобразование или логит–преобразование. В конкретных вариантах осуществления, A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой кратное или преобразование значения параметра, указывающего на степень или коррелирующего со степенью зависимой от CAR активности в данной композиции T–клеток, необязательно, где B представляет собой логарифмическое преобразование значения.
[0048] В некоторых вариантах осуществления, логарифмическое преобразование представляет собой десятичный log (log10(x)), натуральный log (ln(x)) или двоичный log (log2(x)). В конкретных вариантах осуществления, представляет собой количество жизнеспособных клеток в композиции и/или представляет собой количество клеток, которые не являются апоптотическими, не имеют фактора, показательного для раннего апоптоза или апоптоза, не находятся на ранних стадиях апоптоза, или не находятся на поздних стадиях апоптоза, и/или представляет собой количество клеток в определенном состоянии дифференцировки, и/или представляет собой количество клеток, имеющих признак клеток памяти/стволовых клеток, или представляет собой его кратное или преобразование.
[0049] В конкретных вариантах осуществления, фенотип включает положительную экспрессию поверхностного маркера, представляющего собой один или несколько из CD3, CD4 или CD8, и/или включает положительную экспрессию рекомбинантного рецептора, необязательно, CAR, или суррогатный маркер экспрессии рекомбинантного рецептора. В некоторых вариантах осуществления, фенотип представляет собой CD3+ CAR, CD4+/CAR+, CD8+/CAR+. В конкретных вариантах осуществления, фенотип включает отсутствие фактора, показательного для апоптоза или одной или нескольких стадий апоптотического каскада или пути, необязательно, экспрессии маркера апоптоза. В конкретных вариантах осуществления, фенотип включает отрицательную экспрессию маркера апоптоза, необязательно, маркера раннего апоптоза или позднего апоптоза. В некоторых вариантах осуществления, маркер апоптоза представляет собой поверхностный фосфатидилсерин и/или детектирован с использованием аннексина V, или представляет собой активную каспазу или проформу каспазы, необязательно, активную каспазу 3 или проформу каспазы 3. В конкретных вариантах осуществления, фенотип включает аннексин–.
[0050] В конкретных вариантах осуществления, фенотип включает показатель продукции одного или комбинации цитокинов, необязательно, не специфической для антигена или рекомбинантного рецептора и/или поликлональной продукции, где один или несколько цитокинов представляет собой IL–2, IL–13, IL–17, IFN–гамма или TNF–альфа. В некоторых вариантах осуществления, показатель продукции измеряют в анализе, необязательно, анализе окрашивания внутриклеточных цитокинов, включающем инкубацию образца из композиции T–клеток с поликлональным средством, антигенспецифическим средством или средством, связывающим рекомбинантный рецептор, необязательно CAR. В конкретных вариантах осуществления, средство представляет собой или содержит PMA и иономицин, или представляет собой или содержит T–клеточный рецептор или агонист комплекса T–клеточного рецептора. В конкретных вариантах осуществления, фенотип включает отрицательную экспрессию маркера активации, где маркер активации выбран из CD25, CD127, LAG3, Ki67 и их комбинаций.
[051] В некоторых вариантах осуществления, фенотип включает отрицательную экспрессию маркера истощения, где маркер истощения представляет собой продукт гена PD1 или FOXP3, или их комбинацию. В конкретных вариантах осуществления, фенотип включает наивный фенотип или фенотип клеток памяти, необязательно, где фенотип клеток памяти включает фенотип эффекторных T–клеток памяти, фенотип центральных T–клеток памяти, или фенотип эффекторных T–клеток памяти, экспрессирующих CD45RA (Temra).
[0052] В некоторых вариантах осуществления, пороговое значение зависимой от рекомбинантного рецептора активности менее, чем эталонный уровень безопасности, где эталонный уровень безопасности составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наиболее низкий уровень зависимой от CAR активности терапевтической композиции, введенной индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события. В конкретных вариантах осуществления, показатель определяют в анализе, включающем культивирование или инкубацию в течение фиксированного времени, необязательно 24 часов, данной композиции или образца из нее в присутствии антигена, клеток, экспрессирующих антиген, и/или средства, специфически связывающегося с рекомбинантным рецептором, необязательно, CAR. В конкретных вариантах осуществления, анализ представляет собой ELISA.
[0053] В некоторых вариантах осуществления, показатель фактора представляет собой: (i) концентрацию, относительную концентрацию, количество или относительное количество фактора; или (ii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции, или (iii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции в единицу времени, необязательно, один час; или (iv) уровень, показательный для любого из (i)–(iii). В конкретных вариантах осуществления, один или несколько факторов представляет собой один или комбинацию из растворимых факторов, необязательно, один или комбинацию из цитокинов, хемокинов или растворимых рецепторов, необязательно, растворимых костимулирующих рецепторов. В конкретных вариантах осуществления, один или несколько факторов представляет собой один или комбинацию из провоспалительных цитокинов, Th2–цитокинов и Th17–цитокинов. В некоторых вариантах осуществления, один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа, IL4, IL–5, IL–10, IL–13, GM–CSF, sCD137, MIP1a и M1Pb. В конкретных вариантах осуществления, один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа и IL–10. В конкретных вариантах осуществления, один или несколько факторов представляет собой комбинацию любых двух или более из вышеуказанных растворимых факторов, и параметр представляет собой среднее арифметическое или среднее геометрическое из показателей для двух или более факторов.
[0054] В некоторых вариантах осуществления, параметр представляет собой среднее арифметическое или среднее геометрическое показателя, необязательно, количества или концентрации, для по меньшей мере двух из TNF–альфа, IFN–гамма и IL–2 или из TNF–альфа, IFN–гамма и IL–2. В конкретных вариантах осуществления, параметр представляет собой нормализованное значение показателя, где нормализация проведена по сравнению с эталонным показателем фактора. В конкретных вариантах осуществления, эталонный показатель представляет собой среднее из показателей среди множества, необязательно, по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, эталонных терапевтических композиций T–клеток, содержащих химерный антигенный рецептор (CAR), в которых: (i) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате приемлемый профиль безопасности после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном; и/или (ii) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате желательную эффективность после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном. В некоторых вариантах осуществления, приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 2 или выше, или отсутствие нейротоксичности степени 3 или выше. В конкретных вариантах осуществления, приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 3 или выше.
[0055] В конкретных вариантах осуществления, эффективность представляет собой частичный ответ или полный ответ (CR). В некоторых вариантах осуществления, эталонный показатель представляет собой показатель, в таком же анализе, фактора в эталонной композиции T–клеток, которая получена таким же способом, как терапевтическая композиция T–клеток, но не экспрессирует рекомбинантный рецептор, необязательно, CAR, не узнает специфически антиген и/или не экспрессирует никакого рекомбинантного рецептора, необязательно, никакого CAR. В конкретных вариантах осуществления, этот параметр нормализуют для контроля специфической для пациента изменчивости показателя одного или нескольких факторов.
[0056] В конкретных вариантах осуществления, параметр представляет собой нормализованное значение показателя фактора, по сравнению с таким же показателем в таком же анализе, для контрольного фактора, где для уровня контрольного фактора в терапевтической композиции T–клеток известно отсутствие или наблюдали отсутствие признака или корреляции, или значимой корреляции с исходом неблагоприятного события или токсичности, или их вероятностью или риском, где исход неблагоприятного события или токсичности, необязательно, представляет собой тяжелую нейротоксичность. В некоторых вариантах осуществления, контрольный фактор представляет собой фактор, который статистически не коррелирует и/или не коррелирует с возникновением неблагоприятного события среди множества индивидов, у которых продолжалось развитие неблагоприятного события, после введения композиции T–клеток, необязательно, контрольный фактор представляет собой или содержит один из или комбинацию из IL–5, IL–13, GM–CSF и IL–6, необязательно, где показатель контрольного фактора представляет собой среднее арифметическое или среднее геометрическое из двух или более из вышеуказанного.
[0057] В конкретных вариантах осуществления, параметр не включает цитолитическую активность или ее показатель. В конкретных вариантах осуществления, параметр не включает зависимую от рекомбинантного рецептора или антигенспецифическую цитолитическую активность или ее показатель. В некоторых вариантах осуществления, фенотип представляет собой CD8+ CAR+ клетки или маркер апоптоза– CD8+ CAR+ клетки, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; и параметр представляет собой показатель для провоспалительного цитокина, который, необязательно, представляет собой один из или комбинацию из TNF–альфа, IL–2 и IFN–гамма, или представляет собой его нормализованное значение.
[0058] В конкретных вариантах осуществления, неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и пороговое количество единиц: составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,0×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,5×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0059] В конкретных вариантах осуществления, неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и данный диапазон целевых эталонных единиц: составляет между или приблизительно между 2,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 4×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 5×106 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 2,0×105 и 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 2,0×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 2,5×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0060] В некоторых вариантах осуществления, неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и пороговое количество единиц: составляет или составляет приблизительно 1,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 1,25×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,88×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,12×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2; или его нормализованное значение составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+ и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0061] В конкретных вариантах осуществления, неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и данный диапазон целевых эталонных единиц: составляет между или приблизительно между 3,0×105 и 1,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,25×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 4×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 5×106 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 2,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 1,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,88×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 2,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 3,12×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105, включительно, и 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0062] В конкретных вариантах осуществления, терапевтическая композиция T–клеток содержит между приблизительно 10 миллионов клеток на мл и приблизительно 70 миллионов клеток на мл или между приблизительно 10 миллионов жизнеспособных клеток на мл и приблизительно 70 миллионов жизнеспособных клеток на мл, включая каждое. В некоторых вариантах осуществления, терапевтическая композиция T–клеток содержит между приблизительно 15 миллионов клеток или жизнеспособных клеток на мл и приблизительно 60 миллионов клеток или жизнеспособных клеток на мл, включая каждое. В конкретных вариантах осуществления, композиция T–клеток содержит более чем 10 миллионов клеток или жизнеспособных клеток на мл. В конкретных вариантах осуществления, терапевтическая композиция T–клеток содержит более чем 15 миллионов клеток или более чем 15 миллионов клеток на мл. В некоторых вариантах осуществления, композиция дополнительно содержит криопротектор и/или изделие дополнительно содержит инструкции для размораживания композиции перед введением индивиду.
[0063] В конкретных вариантах осуществления, заболевание или состояние представляет собой злокачественную опухоль, необязательно, миелому, лимфому или лейкоз. В конкретных вариантах осуществления, заболевание или состояние представляет собой злокачественное новообразование из B–клеток, необязательно, злокачественное новообразование из B–клеток, выбранное из группы, состоящей из острого лимфобластного лейкоза (ALL), ALL взрослых, хронического лимфобластного лейкоза (CLL), неходжскинской лимфомы (NHL) и диффузной крупноклеточной B–клеточной лимфомы (DLBCL). В некоторых вариантах осуществления, антиген представляет собой интегрин αvβ6 (интегрин avb6), антиген созревания B–клеток (BCMA), B7–H3, B7–H6, карбоангидразу 9 (CA9, также известную как CAIX или G250), раково–тестикулярный антиген, раково–тестикулярный антиген 1B (CTAG, также известный как NY–ESO–1 и LAGE–2), карциноэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокинов с мотивом C–C (CCL–1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, белок эпидермальный фактор роста (EGFR), укороченный белок эпидермальный фактор роста (tEGFR), рецептор эпидермального фактора роста с мутацией типа III (EGFR vIII), эпителиальный гликопротеин 2 (EPG–2), эпителиальный гликопротеин 40 (EPG–40), эфрин B2, рецептор эфрина A2 (EPHa2), рецептор эстрогена, подобный рецептору Fc белок 5 (FCRL5; также известный как гомолог 5 рецептора Fc или FCRH5), фетальный рецептор ацетилхолина (фетальный AchR), связывающий фолат белок (FBP), рецептор фолата альфа, ганглиозид GD2, O–ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), сопряженный с G белком рецептор 5D (GPCR5D), Her2/neu (рецепторную тирозинкиназу erb–B2), Her3 (erb–B3), Her4 (erb–B4), димеры erbB, ассоциированный с меланомой высокомолекулярный антиген человека (HMW–MAA), поверхностный антиген вируса гепатита B, человеческий лейкоцитарный антиген A1 (HLA–A1), человеческий лейкоцитарный антиген A2 (HLA–A2), рецептор IL–22 альфа (IL–22Ra), рецептор IL–13 альфа 2 (IL–13Ra2), рецептор, содержащий домен вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1–CAM), эпитоп CE7 из L1–CAM, член A семейства 8, содержащего богатые лейцином повторы (LRRC8A), Lewis Y, ассоциированный с меланомой антиген (MAGE)–A1, MAGE–A3, MAGE–A6, мезотелин, c–Met, мышиный цитомегаловирус (CMV), муцин 1 (MUC1), MUC16, лиганды члена D группы 2 естественных киллеров (NKG2D), мелан A (MART–1), молекулу адгезии нервных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простатспецифический антиген, антиген стволовых клеток предстательной железы (PSCA), простатспецифический мембранный антиген (PSMA), подобный рецепторной тирозинкиназе орфанный рецептор 1 (ROR1), сурвивин, гликопротеин трофобластных клеток (TPBG, также известный как 5T4), опухолеассоциированный гликопротеин 72 (TAG72), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор фактора роста эндотелия сосудов 2 (VEGFR2), антиген опухоли Вильмса 1 (WT–1), специфический для патогена антиген или антиген, ассоциированный с универсальной меткой, и/или биотинилированные молекулы, и/или молекулы, экспрессированные HIV, HCV, HBV или другими патогенами. Антигены, на которые нацелены рецепторы в некоторых вариантах осуществления, включают антигены, ассоциированные с злокачественным новообразованием из B–клеток, такие как любой из ряда известных маркеров B–клеток. В некоторых вариантах осуществления, антиген представляет собой или включает CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig–каппа, Ig–лямбда, CD79a, CD79b или CD30.
[0064] В конкретных вариантах осуществления, изделие дополнительно содержит информацию, указывающую, что контейнер содержит целевое количество единиц. В некоторых вариантах осуществления, контейнер представляет собой первый контейнер, и изделие, кроме того, содержит дополнительные контейнеры, где каждый из дополнительных контейнеров содержит единичную дозу, содержащую целевое количество единиц композиции T–клеток. В конкретных вариантах осуществления, дополнительные контейнеры содержат между приблизительно 10 миллионов клеток или жизнеспособных клеток на мл и приблизительно 70 миллионов клеток или жизнеспособных клеток на мл, между приблизительно 15 миллионов клеток или жизнеспособных клеток и приблизительно 60 миллионов клеток или жизнеспособных клеток на мл, включая каждое, более чем 10 миллионов клеток или жизнеспособных клеток на мл, более чем 15 миллионов клеток или жизнеспособных клеток на мл, или их комбинацию. В конкретных вариантах осуществления, единичная доза содержит количество не более, чем 15×106 CD8+CAR+ клеток, которые являются отрицательными по детекции с использованием аннексина V или по активной каспазе 3 или проформе каспазы 3. В некоторых вариантах осуществления, единичная доза дополнительно содержит некоторое количество CD4+ клеток, положительных по CAR, где количество находится в соотношении или приблизительно в соотношении 1:1 с CD8+CAR+ клетками.
[0065] В конкретных вариантах осуществления, композицию T–клеток получают способом, в котором: частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции, и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на признаки биологически активных клеток и/или отсутствие апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, от среднего указанной частоты во множестве композиций T–клеток, полученных этим способом, и/или отличается от такого среднего не более чем на одно стандартное отклонение; или частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции, и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на отсутствие апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 20%, или не более чем на 10%, среди множества композиций T–клеток, полученных этим способом.
[0066] В конкретных вариантах осуществления, способ включает: (a) инкубацию популяции клеток, содержащей T–клетки, со средством, содержащим молекулу нуклеиновой кислоты, кодирующую рекомбинантный рецептор, в условиях для введения нуклеиновой кислоты, кодирующей рекомбинантный рецептор, в клетки в популяции; и (b) стимуляцию клеток, до, во время и/или после указанной инкубации, где стимуляция включает инкубацию клеток при наличии стимулирующего условия, индуцирующего первичный сигнал, передачу сигналов, стимуляцию, активацию и/или размножение клеток. В некоторых вариантах осуществления, способ дополнительно включает, перед (a), выделение популяции клеток из биологического образца. В конкретных вариантах осуществления, выделение включает отбор клеток на основании поверхностной экспрессии CD3 или на основании поверхностной экспрессии одного или обоих из CD4 и CD8, необязательно, посредством положительного или отрицательного отбора.
[0067] В некоторых вариантах осуществления, биологический образец представляет собой или содержит образец цельной крови, образец лейкоцитарной пленки, образец мононуклеарных клеток периферической крови (PBMC), образец нефракционированных T–клеток, образец лимфоцитов, образец лейкоцитов, продукт афереза или продукт лейкафереза.
[0068] В конкретных вариантах осуществления, стимулирующее условие включает инкубацию со стимулирующим реагентом, способным активировать один или несколько внутриклеточных доменов передачи сигналов одного или нескольких компонентов комплекса TCR, и/или один или несколько внутриклеточных доменов передачи сигналов одной или нескольких костимулирующих молекул.
[0069] В конкретных вариантах осуществления, стимулирующий реагент содержит первичное средство, которое специфически связывается с членом комплекса TCR, и вторичное средство, которое специфически связывается с костимулирующей молекулой T–клетки. В некоторых вариантах осуществления, первичное средство специфически связывается с CD3 и/или костимулирующей молекулой, выбранной из группы, состоящей из CD28, CD137 (4–1–BB), OX40 или ICOS. В конкретных вариантах осуществления, первичное и вторичное средства содержат антитела и/или присутствуют на поверхности твердой подложки, необязательно, бусины.
[0070] В конкретных вариантах осуществления: стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, от среднего показателя продукции или накопления провоспалительного цитокина среди множества композиций T–клеток, полученных этим способом с использованием стимулирующего реагента, и/или отличается от такого среднего не более чем на одно стандартное отклонение; и/или стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, среди множества композиций T–клеток, полученных этим способом; и/или стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, для композиции клеток, полученной с использованием стимулирующего реагента, отличается не более чем на 40%, не более чем 30%, не более чем 20% или не более чем на 10%, или не более чем на 5% от контрольной композиции, где контрольная композиция и композиция клеток получены с использованием одинакового способа, включая получение из такой же популяции клеток, за исключением того, что контрольная композиция реализована в присутствии контрольного стимулирующего реагента, или стандартного количества единиц зависимой от рекомбинантного рецептора активности. В некоторых вариантах осуществления, известно, что контрольный стимулирующий реагент, при использовании в способе, приводит к получению композиции T–клеток, в которой зависимая от рекомбинантного рецептора активность или антигенспецифическая активность находится в пределах приемлемого диапазона изменчивости.
[0071] В конкретных вариантах осуществления, контейнер заполняют всей или частью композиции T–клеток, и необязательно, другим раствором, до концентрации между приблизительно 10 миллионов клеток и приблизительно 70 миллионов клеток на мл, включительно. В конкретных вариантах осуществления, контейнер заполняют другим раствором, и раствор содержит криопротектор, необязательно, DMSO. В некоторых вариантах осуществления, концентрация составляет между приблизительно 15 и приблизительно 60 миллионов клеток на мл, включительно. В конкретных вариантах осуществления, концентрация составляет более чем 10 миллионов клеток на мл. В конкретных вариантах осуществления, концентрация составляет более чем 15 миллионов клеток на мл. В некоторых вариантах осуществления, концентрация DMSO составляет или составляет приблизительно, или не превышает 7,5%. В конкретных вариантах осуществления, концентрация составляет более чем 60 миллионов клеток на мл. В конкретных вариантах осуществления, концентрация DMSO составляет более чем 7,5%, необязательно, между или приблизительно между 7,5% и 9,0%, включительно.
[0072] В некоторых вариантах осуществления, заполнение осуществляют автоматическим способом, необязательно, в закрытой системе. В конкретных вариантах осуществления, корректированная единичная доза составляет менее чем, необязательно, менее чем 1,5–кратную, менее чем 2–кратную, менее чем 3–кратную, менее чем 4–кратную среднюю единичную дозу для группы индивидов, подвергнутых лечению с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR. В конкретных вариантах осуществления, образец из композиции T–клеток, необязательно, криоконсервированный образец, оценивают после введения композиции T–клеток индивиду. В некоторых вариантах осуществления, если B превышает USL, определяют, что индивид подвержен риску токсичности. В конкретных вариантах осуществления, если B превышает USL, индивида, которому вводили композицию, подвергают мониторированию и/или лечению с использованием средства для облегчения или уменьшения вероятности исхода токсичности или синдрома высвобождения цитокинов после введения композиции клеток и необязательно, до возникновения признака или симптома исхода токсичности.
Краткое описание чертежей
[0073] На ФИГ. 1 показан график, отображающий концентрации CAR+ клеток/мкл крови в различных временных точках после введения композиций T–клеток, содержащих экспрессирующие CAR против CD19 клетки. Данные показаны для индивидов, у которых возникла нейротоксичность степени 3 или менее (звезды), степени 4 (пятиугольники) или степени 5 (круги).
[0074] На ФИГ. 2 показан график, отображающий концентрации CAR+ клеток/мкл крови в различных временных точках после введения композиций T–клеток, содержащих экспрессирующие CAR против CD19 клетки. Данные показаны для индивидов, у которых возникла нейротоксичность степени 2 или менее (квадраты), степени 3 (звезды), длительная нейротоксичность степени 3 (ромб), нейротоксичность степени 4 (пятиугольник) или степени 5 (круги со стрелками).
[0075] На ФИГ. 3A – 3V показаны блочные диаграммы, количественно оценивающие различные параметры композиций клеток, содержащих клетки, экспрессирующие CAR против CD19. Блочные диаграммы слева сравнивают измерения для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 4 или менее, с измерениями для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 5. Блочные диаграммы справа сравнивают измерения для композиций клеток, происходящих от индивидов, которые испытали полный ответ (CR), с измерениями для композиций клеток, происходящих от индивидов, которые не испытали ответа (NR). Измерения для композиций клеток, происходящих от индивидов, ответ которых недоступен, также показаны на этой диаграмме (NA).
[0076] Блочные диаграммы из ФИГ. 3A показывают показатели общего количества CD8+CAR+отрицательных по маркеру апоптоза клеток, введенных индивидам.
[0077] Блочные диаграммы из ФИГ. 3B показывают процент CD8+CAR+ клеток, положительных по IL–13, после PMA/иономицина, посредством внутреннего окрашивания цитокинов (ICS), в введенных дозах.
[0078] Блочные диаграммы из ФИГ. 3C показывают количество/кг введенных CD8+CAR+ отрицательных по маркеру апоптоза (аннексин V–) клеток.
[0079] Блочные диаграммы из ФИГ. 3D показывают процент CD4+CAR+ клеток, положительных по CD127+.
[0080] Блочные диаграммы из ФИГ. 3E показывают общее количество введенных посредством инфузии клеток/кг.
[0081] Блочные диаграммы из ФИГ. 3F показывают процент CD4+CAR+ клеток, положительных по IL–13 после PMA/иономицина, по ICS.
[0082] Блочные диаграммы из ФИГ. 3G показывают частоту положительных по маркеру апоптоза (аннексину V) клеток среди введенных CD8+CAR+ клеток.
[083] Блочные диаграммы из ФИГ. 3H показывают уровни FOXP3 по QПЦР.
[084] Блочные диаграммы из ФИГ. 3I показывают общее количество введенных CD3+CAR+ отрицательных по маркеру апоптоза (аннексину V) клеток.
[0085] Блочные диаграммы из ФИГ. 3J показывают количество/кг введенных CD3+CAR+ отрицательных по маркеру апоптоза (аннексин V–) клеток.
[0086] Блочные диаграммы из ФИГ. 3K показывают концентрацию жизнеспособных клеток для криоконсервированного продукта лекарственного средства (CDP).
[0087] Блочные диаграммы из ФИГ. 3L показывают общее количество введенных посредством инфузии клеток.
[0088] Блочные диаграммы из ФИГ. 3M показывают ICS IL2 в CD4+CAR+ клетках.
[0089] Блочные диаграммы из ФИГ. 3N показывают частоту положительных по маркеру апоптоза (аннексину V) клеток среди введенных CD3+CAR+ клеток.
[0090] Блочные диаграммы из ФИГ. 3O показывают частоту FOXP3+ клеток среди CD4+ клеток.
[0091] Блочные диаграммы из ФИГ. 3P показывают частоту CD3+ клеток.
[0092] Блочные диаграммы из ФИГ. 3Q показывают количество/кг введенных CD8+CAR+ клеток.
[0093] Блочные диаграммы из ФИГ. 3R показывают не специфическую для антигена/CAR продукцию IL–10 на общее количество клеток (стимулированных CD3/28).
[0094] Блочные диаграммы из ФИГ. 3S показывают ICS TNF–альфа для CD4+CAR+ клеток.
[0095] Блочные диаграммы из ФИГ. 3T показывают ICS для TNF–альфа CD8+CAR+ клеток.
[0096] Блочные диаграммы из ФИГ. 3U показывают не специфическую для антигена/CAR продукцию IL–6 на общее количество клеток (стимулированных CD3/28).
[0097] Блочные диаграммы из ФИГ. 3V показывают количество введенных CD3+CAR+ клеток/кг.
[0098] На ФИГ. 4 показаны блочные диаграммы, количественно оценивающие продукцию TNF–альфа после стимуляции с использованием CD19 композициями клеток, содержащими клетки, экспрессирующие CAR против CD19. Блочная диаграмма слева сравнивает измерения для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 4 или менее с измерениями для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 5. Блочные диаграммы справа сравнивают измерения для композиций клеток, происходящих от индивидов, которые испытали CR, с измерениями для композиций клеток, происходящих от индивидов, которые испытали NR. Измерения для композиций клеток, происходящих от индивидов, ответ которых недоступен, также показаны на этой диаграмме (NA).
[0099] На ФИГ. 5A–B показаны блочные диаграммы, количественно оценивающие продукцию цитокинов после стимуляции с использованием CD19 композициями клеток, содержащими клетки, экспрессирующие CAR против CD19. Блочная диаграмма слева сравнивает измерения для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 4 или менее, с измерениями для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 5. Блочные диаграммы справа сравнивают измерения для композиций клеток, происходящих от индивидов, которые испытали CR, с измерениями для композиций клеток, происходящих от индивидов, которые испытали NR. Измерения для композиций клеток, происходящих от индивидов, ответ которых недоступен, также показаны на этой диаграмме (NA).
[0100] Блочные диаграммы из ФИГ. 5A показывают стимулированную антигеном продукцию IL–2.
[0101] Блочные диаграммы из ФИГ. 5B показывают стимулированную антигеном продукцию IFN–гамма.
[0102] На ФИГ. 6A и 6B показаны двумерные диаграммы рассеяния количества маркер апоптоза– (аннексин V–) CD8+CAR+ клеток в введенной дозе и стимулированной антигеном продукции TNF–альфа. Точки данных для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 4 или менее (круги) или степени 5 (треугольники), показаны на ФИГ. 6A. Точки данных для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 0–2, 3, длительная нейротоксичность степени 3 (3p), нейротоксичность степени 4 и 5, показаны на ФИГ. 6B. На ФИГ. 6B показаны точки данных, ассоциированные с индивидами, у которых возникла нейротоксичность степени 5, и которых подвергали противолимфоцитарной химиотерапии с использованием циклофосфамида (CY) или флударабина и циклофосфамида (Flu/CY). Овалом обозначен диапазон этих параметров для большинства из 11 иллюстративных композиций клеток, оцененных в клиническом исследовании, в котором ни у одного из индивидов не показана нейротоксичность степени 5 или отек головного мозга.
[0103] На ФИГ. 7 показана двумерная диаграмма рассеяния количества маркер апоптоза–(аннексин V–) CD8+CAR+ клеток в введенной дозе и стимулированной антигеном продукции TNF–альфа. Показаны точки данных для композиций клеток, происходящих от индивидов, у которых возникла нейротоксичность степени 4 или менее (квадраты и круги), или степени 5 (треугольники). Показаны композиции клеток, происходящих от индивидов из дополнительного клинического исследования (квадраты).
[0104] На ФИГ. 8 показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза (аннексин V)– CD8+CAR+ клеток x продукции TNF–альфа для индивидов, у которых возникла нейротоксичность различной степени.
[0105] На ФИГ. 9 показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток x продукции TNF–альфа для индивидов с различными ответами.
[0106] На ФИГ. 10 показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток x продукции IFN–гамма для индивидов, у которых возникла нейротоксичность различной степени.
[0107] На ФИГ. 11 показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток x продукции IFN–гамма для индивидов с различными клиническими ответами.
[0108] На ФИГ. 12 показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток x продукции IL–2 для индивидов, у которых возникла нейротоксичность различной степени.
[0109] На ФИГ. 13 показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток x продукции IL–2 для индивидов с различными клиническими ответами.
[0110] На ФИГ. 14A и 14B показаны графики, отображающие индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток (A) x нормализованной продукции TNF–альфа (B) для индивидов, у которых возникла нейротоксичность различной степени (ФИГ. 14A), или для индивидов с различными ответами (ФИГ. 14B).
[0111] На ФИГ. 15A и 15B показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток (A) x нормализованной продукции IFN–гамма (B) для индивидов, у которых возникла нейротоксичность различной степени (ФИГ. 15A), или для индивидов с различными ответами (ФИГ. 15B).
[0112] На ФИГ. 16A и 16B показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток (A) x нормализованной продукции IL–2 (B) для индивидов, у которых возникла нейротоксичность различной степени (ФИГ. 16A), или для индивидов с различными ответами (ФИГ. 16B).
[0113] На ФИГ. 17A и 17B показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V)– CD8+CAR+ клеток (A) x нормализованной продукции TNF–альфа и IFN–гамма (B) для индивидов, у которых возникла нейротоксичность различной степени (ФИГ. 17A), или для индивидов с различными ответами (ФИГ. 17B).
[0114] На ФИГ. 18A и 18B показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин V–) CD8+CAR+ клеток (A) x нормализованной продукции TNF–альфа и IL–2 (B) для индивидов, у которых возникла нейротоксичность различной степени (ФИГ. 18A), или для индивидов с различными ответами (ФИГ. 18B).
[0115] На ФИГ. 19A и 19B показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин–) CD8+CAR+ клеток (A) x нормализованной продукции IFN–гамма и IL–2 (B) для индивидов, у которых возникла нейротоксичность различной степени (ФИГ. 19A), или для индивидов с различными ответами (ФИГ. 19B).
[0116] На ФИГ. 20A и 20B показан график, отображающий индивидуальные точки данных для количества введенных маркер апоптоза– (аннексин–) CD8+CAR+ клеток (A) x нормализованной продукции TNF–альфа, IFN–гамма, и продукция IL–2 (B) для индивидов, у которых возникла нейротоксичность различной степени (ФИГ. 20A), или для индивидов с различными ответами (ФИГ. 20B).
[0117] На ФИГ. 21A и 21B показаны графики, отображающие фенотипы клеток из композиций, содержащих CAR против CD19+ клетки, полученные способом, описанным в примере 1 (A), и альтернативным способом, описанным в примере 2 (B). На ФИГ. 21A показана блочная диаграмма, отображающая процент маркер апоптоза– (аннексин V–) клеток среди CD8+CAR+ клеток. На ФИГ. 21B показан график, отображающий значения для индивидуальных композиций клеток для дозированных отрицательных по аннексину CD8+CAR+ клеток и продукции цитокинов, для композиций клеток, полученных иллюстративным способом A и иллюстративным способом B. Заштрихованными рамками показаны наблюдаемые распределения.
[0118] На ФИГ. 22 показаны индивидуальные точки данных для количества/кг CD3+CAR+ клеток (x106 клеток/кг), введенных индивидам, у которых возникла нейротоксичность степени 0–2 или степени 3–5.
[0119] На ФИГ. 23A–C показаны блочные диаграммы, сравнивающие композиции T–клеток, содержащие клетки, экспрессирующие CAR против CD19. На ФИГ. 23A и 23B показаны блочные диаграммы, сравнивающие композиции T–клеток, содержащие клетки, обработанные одинаковым реагентом из различных партий в ходе получения. ФИГ. 23A количественно оценивает продукцию TNF–альфа клеткой после стимуляции посредством CD19. На ФИГ. 23B показана частота CD27+/CD28+ клеток среди CD8+CAR+ клеток. Показаны точки данных для композиций T–клеток, ассоциированных с нейротоксичностью степени 0–2 (квадраты), 3 (звезды со стрелками), длительной нейротоксичностью степени 3 (3p; ромбы), нейротоксичностью степени 4 (пятиугольники со стрелками) и 5 (круги). На ФИГ. 23C показана продукция TNF–альфа после стимуляции с использованием экспрессирующих CD19 клеток в композициях T–клеток, содержащих клетки, экспрессирующие CAR против CD19, полученные с использованием одинаковых сред, которые хранили в различных условиях.
[0120] На ФИГ. 24 показаны блочные диаграммы, отображающие частоту T–клеток в композициях T–клеток, обогащенных по CD4+ и CD8+ клеткам, на различных стадиях способа получения композиций модифицированных клеток, содержащих CAR–T–клетки, описанные в примере 8. Показана частота (% от общего количества лейкоцитов) CD4+ и CD8+ клеток в композициях.
[0121] На ФИГ. 25 показан график, показывающий уровни CD3+ T–клеток в индивидуальных дозах при уровне дозы 1 (DL1) и уровне дозы 2 (DL2).
[0122] На ФИГ. 26 показаны блочные диаграммы, отображающие концентрацию, жизнеспособность и частоту отрицательных по каспазе–3 CD4+ и CD8+ T–клеток в терапевтических композициях клеток, содержащих CAR–T–клетки, в высоком или низком объеме состава.
[0123] На ФИГ. 27 показаны графики, отображающие контролируемую дозу, фенотипы T–клеток и специфическую для клеток функцию индивидуальной композиции клеток, содержащей CAR–T–клетки, которые вводили посредством инфузии. Показаны точки данных для количеств CD4+CAR+, CD8+CAR+, CD4+CAR+TNF–α, CD8+CAR+TNF–α, CD4+CAR+CCR7+, CD8+CAR+CCR7+, введенных посредством инфузии индивидуальным индивидам.
[0124] На ФИГ. 28 показан график, отображающий (i) для каждого из ряда индивидуальных индивидов, индивидуальные не заключенные в рамки точки показывают максимальный показатель PK (количество CAR+ T–клеток/мкл крови (показатель PK) на пике (в индивидуальном порядке, временная точка, в которой измерено наивысшее количество CAR+ T–клеток, среди временных точек, в которых количество CAR+ T–клеток оценивали после лечения индивида с использованием композиций экспрессирующих CAR против CD19 T–клеток) (где точки показывают также наивысшую степень нейротоксичности, наблюдаемую для каждого индивида: нейротоксичность степени 0–2 (квадраты), степени 3 (звезды), длительная нейротоксичность степени 3 (ромбы), нейротоксичность степени 4 (пятиугольники со стрелками) или степени 5 (круги), и (ii) медианные уровни, для тех из таких пациентов, которые, по–видимому, имели ранний или поздний пик CAR+ T–клеток (показанный верхними и нижними линиями с заключенными в рамку точками с планками диапазонов, соответственно) IL–15 (пикограмм/мл) в сыворотке в различных указанных временных точках до и после введения таких композиций T–клеток. Овал показывает индивидов, у которых наблюдали раннее, быстрое размножение CAR–T–клеток, по сравнению с другими индивидами.
Подробное описание
[0125] Полное содержание всех публикаций, включая патентные документы, научные статьи и базы данных, на которые ссылаются в этой заявке, приведено в качестве ссылки для всех целей в такой же степени, как если бы содержание каждой индивидуальной публикации было индивидуально приведено в качестве ссылки. Если определение, приведенное в настоящем описании, противоречит или иным образом не соответствует определению, приведенному в патентах, заявках, опубликованных заявках и других публикациях, приведенных в настоящем описании в качестве ссылки, определение, приведенное в настоящем описании, имеет преимущество перед определением, приведенным в настоящем описании в качестве ссылки.
[0126] Заголовки разделов, используемые в настоящем описании, приведены только с целью организации, и их не следует рассматривать как ограничивающие описанный объект.
I. ДОЗЫ И ОПРЕДЕЛЕНИЕ ДОЗЫ ТЕРАПЕВТИЧЕСКИХ КОМПОЗИЦИЙ T–КЛЕТОК ДЛЯ УМЕНЬШЕНИЯ РИСКА ТОКСИЧНОСТИ
[0127] Настоящее изобретение относится к способам, композициям и изделиям для использования применительно к клеточной терапии, такой как терапия с использованием модифицированных T–клеток, для лечения заболеваний и состояний, включая различные опухоли. Представленные варианты осуществления относятся к терапевтическим композициям T–клеток, содержащим модифицированные T–клетки, такие как клетки, модифицированные для экспрессии рекомбинантных белков, такие как клетки, экспрессирующие рекомбинантные рецепторы, сконструированные, чтобы узнавать и/или специфически связывать молекулы, ассоциированные с заболеванием или состоянием, и приводящие к ответу, такому как иммунный ответ против таких молекул, после связывания с такими молекулами. Рецепторы могут включать химерные рецепторы, например, химерные рецепторы антигенов (CAR), и другие трансгенные рецепторы антигенов, включая трансгенные T–клеточные рецепторы (TCR).
[0128] Представленные варианты осуществления, в некоторых аспектах, относятся к аспектам, в которых определенные параметры, связанные с функцией или активностью терапевтической композиции T–клеток, например, антигенспецифической или зависимой от рекомбинантного рецептора активности, могут прогнозировать риск вероятности возникновения неблагоприятного события или токсичности, такой как тяжелая нейротоксичность, у индивида, подвергнутого введению композиции T–клеток, и/или могут предоставлять информацию об активности терапевтической композиции T–клеток. Аспекты представленных вариантов осуществления относятся также к введению или предоставлению единичной дозы, содержащей некоторое количество единиц, такое как целевое количество единиц, являющееся функцией от количества клеток конкретного фенотипа, такого как фенотип, показательный для биологически активных клеток или популяции клеток, и функции или активности клеток, присутствующих в терапевтической композиции T–клеток, например, антигенспецифической или зависимой от рекомбинантного рецептора активности, включая количество для использования применительно к дозированию терапевтической композиции T–клеток. В некоторых аспектах, представленные способы могут облегчать или уменьшать риск токсичности у индивида, подвергнутого введению дозы терапевтической композиции T–клеток, в то же время обеспечивая активность композиции T–клеток. Настоящее изобретение относится также к изделиям, содержащим клетки и разработанным для введения, следующего таким режимам дозирования.
[0129] В некоторых вариантах осуществления, представленные способы, дозы, единичные дозы, композиции и изделия основаны на наблюдениях, что может обеспечивать преимущества принятие во внимание определенных параметров и их комбинаций при определении подходящей дозы для клеточной терапии и/или выпуске композиций клеток для терапии. В конкретных доступных способах, дозы основаны на количествах клеток конкретных типов, таких как клетки, модифицированные для обладания конкретной активностью, таких как клетки, положительные по модифицированному рецептору. Например, в конкретных доступных способах и дозах, доза основана на наблюдаемой или предполагаемой взаимосвязи между количеством (или количеством на массу пациента) жизнеспособных модифицированных T–клеток, или их подгруппы, такой как жизнеспособные, цитотоксические (например, CD8+) модифицированные T–клетки. В различных контекстах, такие количества могут иметь взаимосвязь с исходами эффективности и/или безопасности, такими как ответ и/или риск видов токсичности, таких как нейротоксичность (NTx), отек головного мозга и CRS. Настоящее изобретение относится к вариантам осуществления, основанным на наблюдении, что несмотря на это, такие показатели, в некоторых контекстах, не обеспечивают согласованного адекватного прогнозирования риска видов токсичности, например, тяжелой нейротоксичности или отека головного мозга, в частности, без принятия во внимание других переменных. Соответственно, способы определения дозы и оценки продукта для выпуска, основанные только на таких показателях, могут являться не полностью удовлетворительными. Например, такие способы могут, в некоторых контекстах, не справляться с определением соответствующей границы безопасности и/или терапевтического окна, для безопасной и эффективной клеточной терапии. Настоящее изобретение относится к способам (включая способы лечения, дозирования, определения дозы и анализ высвобождения) и дозам, и терапевтическим композициям, направленным на преодоление таких недостатков.
[0130] В некоторых аспектах, в настоящей работе обнаружено, что определенные специфические для продукта признаки и клинические или специфические для пациента факторы могут влиять на риск, относительный риск или вероятность возникновения токсичности после проведения клеточной терапии. В некоторых случаях, изменчивость таких специфических для продукта и/или специфических для пациента признаков может приводить к изменчивости признаков доз терапевтических композиций клеток, введенных различным индивидуумам внутри группы индивидов, и/или исходов, наблюдаемых у таких различных индивидуумов после такого введения. В некоторых аспектах, такую изменчивость наблюдают, несмотря на определенное сходство доз, вводимых различным индивидуальным индивидам, например, когда введенная доза или композиция содержит клетки, модифицированные для экспрессии одинакового модифицированного рецептора, такого как химерный антигенный рецептор, содержащие одинаковый вектор, или трансдуцированные или трансфицированные с использованием одинакового вектора; в некоторых аспектах, различные дозы или композиции, введенные различным индивидам, включают или содержат, или состоят из одинакового количества (или количества на массу или другую характеристику индивида) клеток (или клеток конкретного фенотипа). В некоторых аспектах, контроль изменчивости одного или нескольких признаков композиций клеток может минимизировать такие риски и/или минимизировать такую изменчивость признаков доз или исходов. В некоторых аспектах, минимизация или контроль изменчивости, такой как степень изменчивости (или увеличение единообразия), одного или нескольких признаков продукта или композиции среди индивидов, которых подвергают конкретной терапии, может минимизировать влияние изменчивости на признаки исхода или дозы среди пациентов с изменчивостью специфических для пациента факторов или клинических факторов, которые в ином случае могут влиять на такие признаки исхода или дозы. Например, в некоторых аспектах, уменьшение изменчивости признака(признаков) продукта или композиции может уменьшать изменчивость риска или вероятности, или может уменьшать риск или вероятность развития у индивида или в популяции индивидов связанной с лечением токсичности, такой как нейротоксичность или отек головного мозга, или их степень, например, без уменьшения или значительного уменьшения вероятности достижения конкретного ответа или клинического исхода. В некоторых случаях, уменьшение изменчивости, объясняемой клиническими или специфическими для пациента факторами, может минимизировать риск возникновения токсичности, такой как нейротоксичность или отек головного мозга, после проведения клеточной терапии.
[0131] В некоторых аспектах, изменчивость среди единичных доз композиции клеток может быть обусловлена одним или несколькими аспектами производственных процессов, используемых в получении или изготовлении терапевтического средства на основе модифицированных клеток. В некоторых случаях, изменения сырья или манипуляций с ним, или его хранения, могут влиять на переменные, как наблюдали в этой работе, влияющие на риск токсичности и/или исходы. В некоторых аспектах, изменчивость от партии к партии или при хранении/манипуляциях с сырьем, и/или использование различных видов сырья среди способов, осуществляемых для ряда индивидов, может влиять, например, посредством увеличения изменчивости, или увеличения или уменьшения определенных аспектов полученных композиций клеток, таких как аспекты, которые, если меняются, могут приводить к изменчивости риска токсичности или клинических исходов среди индивидов, подвергаемых способам клеточной терапии, в частности, среди таких индивидов, отличающихся определенными специфическими для пациента признаками. В некоторых вариантах осуществления, настоящее изобретение относится к способам, включающим оценку, тестирование и/или контроль потенциального влияния или изменчивости для одного или нескольких таких признаков продукта или рисков, или вероятности, из–за (например, одного или всех из) сырья (нескольких видов сырья), партии(ий), реагента(ов) или их хранения или манипуляций с ними, или их изменения. В некоторых вариантах осуществления, такие способы включают анализы, такие как анализы, проводимые до использования таких сырья, партии, хранения или манипуляций, при получении композиции клеток, подлежащих введению индивиду, или перед таким введением. В некоторых аспектах, анализы оценивают влияние сырья, партии, изменения, или способа манипуляций или хранения, на один или несколько признаков композиции клеток, таких как признаки, которые, как наблюдали в этой работе, влияют на риск токсичности или исход, или отягощают влияние изменчивости от пациента к пациенту таких исходов. В некоторых аспектах, анализы оценивают, является ли приемлемо низкой степень изменчивости, по сравнению с другим материалом, партией, или способом хранения или манипуляций, или приемлемо низким влияние на такие один или несколько признаков. В некоторых аспектах, сырье, партию или способ хранения или манипуляций, выпускают для изготовления терапевтического средства на основе клеток, подлежащего введению пациенту, – или пациента подвергают такой клеточной терапии, – если, например, только если, или только после того как анализ подтверждает, что такие изменчивость или влияние находятся в пределах приемлемого диапазона или значения, или предела. В некоторых из любых таких вариантов осуществления, такие оцененные параметры могут включать количество или процент биологически активных клеток, неапоптотических клеток, здоровых клеток, клеток с определенной активностью (или количество или процент биологически активных, неапоптотических или здоровых, или активных клеток данного фенотипа), и/или показатель, показательный для активности, такой как активность на клетку, композиции. В некоторых вариантах осуществления, определение того, что изменчивость одного или нескольких таких признаков ниже определенного уровня с использованием нового сырья или партии, или способа хранения или манипуляций, может уменьшать риск токсичности или уменьшение ответа после внедрения такого нового сырья или партии, или способа хранения или манипуляций. В некоторых вариантах осуществления, среди таких способов, к которым относится настоящее изобретение, присутствуют способы, анализирующие композицию перед выпуском продукта и/или корректирующие стратегию дозирования на основании таких параметров.
[0132] В некоторых вариантах осуществления, один или несколько рисков или исходов, таких как риск токсичности, или подходящая доза могут зависеть от или изменяться с одной или несколькими специфическими для лечения или для пациента переменными. Например, среди иллюстративных клинических признаков и признаков пациента, которые могут коррелировать, в некоторых вариантах осуществления, с риском определенных видов токсичности, включая нейротоксичность или отек головного мозга, или их степени, включены общее состояние здоровья или возраст пациента (например, является ли возраст пациента более чем или менее чем, или равным 30 лет), до анамнеза лечения, включая количество предшествующих циклов лечения и/или то, подвергали ли пациента противолимфоцитарной и/или поддерживающей химиотерапии до лечения, такого как лечение, включающее флударабин. В частности, среди тех признаков пациента или клинических признаков, которые могут увеличивать риск, относительный риск и/или вероятность возникновения токсичности после введения дозы клеток при клеточной терапии (например, CAR–T–клеточной терапии), включены, например, меньшее количество циклов предшествующей терапии, например, два или менее циклов предшествующей терапии, молодой возраст, например, возраст младше, чем 30 лет, соотношение CD4+ и CD8+ T–клеток в образце от пациента после афереза или количество клеток, введенных индивиду, обусловленное дозированием клеток на основании массы, например, где больше клеток вводят индивидам с большей массой. Такие признаки могут влиять на полученные признаки модифицированных композиций клеток, полученных от индивида, и/или влиять на признаки пациента при инфузии, которые могут вносить вклад в риск возникновения токсичности после проведения клеточной терапии (например, с использованием CAR–T–клеток). Настоящее изобретение относится к способам, уменьшающим изменчивость исходов и/или риска токсичности среди пациентов с изменчивостью одного или нескольких таких специфических для пациента или лечения признаков. Настоящее изобретение относится также к способам, принимающим во внимание такие специфические для пациента или лечения признаки при определении или составлении или введении дозы терапевтического средства на основе клеток для пациента или пациентов.
[0133] В некоторых вариантах осуществления, представленные способы, такие как способы введения, и дозы включают (или включают введение) меньшего количества клеток или меньшего количества биологически активных или активных клеток (или модифицированных клеток) в вводимой дозе индивиду, который является более здоровым, является более молодым, например, имеет возраст менее 30 лет, меньшее количество циклов предшествующей терапии, например, два или менее циклов предшествующей терапии, или имел определенную предшествующую терапию, такую как противолимфоцитарная терапия или химиотерапия, такая как включающая флударабин, и/или трансплантат. В других вариантах осуществления, признаки процесса или способа дозирования вносят вклад в изменчивость таких специфических для пациента факторов, например, таким образом, что такие специфические для пациента факторы не приводят к изменчивости или не приводят к значительной изменчивости токсичности или другого риска. В некоторых вариантах осуществления, представленные способы включают использование фиксированной дозы, например, общего количества CAR+ клеток, общего количества CAR+CD8+ T–клеток и/или CAR+/CD4+ T–клеток, таким образом, чтобы вводить точную или фиксированную дозу такого типа(типов) клеток в каждой из групп подвергаемых лечению индивидов, включая индивидов изменчивой массы. В некоторых аспектах, специфические для пациента переменные являются важными для дозирования, если терапия является аутологичной, так что свойства клеток пациента могут являться важными для состояния здоровья или функции, или выносливости клеток в композиции.
[0134] В некоторых аспектах, определенные признаки пациента или клинические факторы могут усиливать размножение введенных при клеточной терапии клеток у индивида, которого подвергали терапии, что, в некоторых случаях, может вносить вклад, такой как увеличение, или может являться ассоциированным с риском или ассоциированным с увеличенным риском, относительным риском или вероятностью возникновения токсичности, например, нейротоксичности, после проведения клеточной терапии. В некоторых вариантах осуществления, признаки пациента или клинические факторы, ассоциированные с риском возникновения токсичности, такой как нейротоксичность или отек головного мозга, включают тип заболевания (например, ALL); нагрузку заболевания (например, как определено по измерению объема или присутствию маркера воспаления); подвергали ли индивида предшествующей переходной химиотерапии или противолимфоцитарной терапии, такой как включающая флударабин (Flu), или циклофосфамида и флударабина (CY/Flu); пик раннего размножения T–клеток с рекомбинантным рецептором (например, CAR) в крови, например, в пределах 2, 3, 4, 5, 6 или 7 суток после начала проведения клеточной терапии; и/или присутствие пиковых уровней IL–15, например, больше или равно 30 пг/мл, в крови или сыворотке, например, в пределах 2, 3, 4, 5, 6 или 7 суток после начала проведения клеточной терапии. В некоторых вариантах осуществления, представленные способы, такие как представленные способы и/или способы дозирования, такие как способы контроля дозы и/или изменчивости, могут минимизировать или уменьшать такие риски, и/или минимизировать влияние признаков пациента или клинических факторов на такие риски или исход. Среди этих способов присутствуют способы, в которых такие факторы принимают во внимание при коррекции или определении дозы для таких индивидов, и способы, в которых используют признаки процесса или дозирования, которые минимизируют влияние таких факторов на риск токсичности или исход.
[0135] В некоторых вариантах осуществления, представленные композиции, дозы и способы обеспечивают преимущества в том, что они могут ограничивать изменчивость дозы клеток, вводимой индивидуальным индивидам, факторов, как наблюдали, коррелирующих с неблагоприятными событиями, например, видами токсичности, такими как виды нейротоксичности, включая тяжелые формы нейротоксичности и/или отек головного мозга. Такую изменчивость ограничивают или уменьшают, в некоторых аспектах, посредством дозы или способа определения дозы, которые принимают во внимание или корректируют такую изменчивость, например, дозирования на основании количества клеток или фенотипа клеток, которые имеют свойство, как известно, коррелирующее с неблагоприятным событием. В некоторых аспектах, изменчивость ограничивают посредством использования анализа высвобождения, учитывающего такую изменчивость. В некоторых вариантах осуществления, в дополнение к количествам модифицированных T–клеток, доза и/или выпуск продукта кроме того, основан на одном или нескольких из комбинации важных показателей. Такие показатели, в некоторых аспектах, включают параметры, показательные для степени, в которой жизнеспособные клетки являются биологически активными или здоровыми (например, не запрограммированными для гибели), что, в некоторых аспектах, определяют на основании отсутствия поддающегося детекции апоптотического маркера и/или на основании относительно низких уровней внутриклеточной продукции конкретных факторов, по сравнению с умирающими или апоптотическими клетками. В некоторых аспектах, показатели включают частоту модифицированных CD8+ клеток, в отличие от принятия во внимание только количества модифицированных T–клеток в целом и/или соотношение CD4:CD8 клеток среди модифицированных клеток. В некоторых аспектах, показатели включают параметры, показательные для степени специфической для антигена или клеток активности, присутствующей в композиции, такие как показатели степени, в которой клетки в композиции способны проявлять конкретные виды активности или функции, такие как секреция конкретных факторов (таких как провоспалительные цитокины) в ответ на специфическую для антигена или клеток стимуляцию.
[0136] В некоторых вариантах осуществления, доза основана на количестве биологически активных модифицированных T–клеток; в некоторых аспектах, биологически активный относится к свойству клеток, не запрограммированных, чтобы подвергаться клеточной смерти, например, к свойству неапоптотических клеток или клеток, не имеющих признаков входа в апоптотический путь. В некоторых аспектах, доза основана на количестве биологически активных модифицированных CD8+ T–клеток, и/или, когда доза основана на общем количестве биологически активных модифицированных T–клеток, верхний предел или пороговое количество биологически активных модифицированных CD8+ T–клеток также указаны.
[0137] В некоторых вариантах осуществления, обеспечения того, что единичная доза содержит относительно постоянное количество биологически активных модифицированных клеток, частично достигают посредством способа получения клеток, проявляющего изменчивость в такой биологически активной популяции, которая является низкой, или ниже приемлемой или пороговой изменчивости, среди композиций, полученных этим способом, включая композиции, полученные из образцов от ряда различных индивидов, например, индивидов, имеющих различные характеристики, таких как индивиды различного возраста, с различным количеством циклов и/или типами предшествующей терапии, и показаниями и их подтипами или тяжестью, или степенью. В некоторых аспектах, таким способом получают частоту такой биологически активной популяции, которая отличается не более чем на 20% или не более чем на 10%, или не более чем на 5%, от среднего указанной частоты во множестве композиций T–клеток, полученных этим способом, и/или отличается от такого среднего не более чем на одно стандартное отклонение, или отличается не более чем на 20%, или не более чем на 10%, или не более чем на 5%, среди множества композиций T–клеток, полученных этим способом, среди таких различных образцов и пациентов. В некоторых таких аспектах, доза основана на количестве (или количестве на массу или рост, или объем крови пациента) модифицированных T–клеток или модифицированных CD8+ T–клеток, принимая во внимание ожидаемую частоту биологически активных или неапоптотических клеток среди таких клеток, и/или изменчивость такой частоты среди композиций клеток, модифицированных из репрезентативных популяций индивидов. В некоторых аспектах, численность популяции клеток в дозе выбирают для обеспечения адекватной границы безопасности, например, ниже порогового значения, принимая во внимание такую изменчивость и частоту.
[0138] В некоторых вариантах осуществления, доза и/или выпуск продукта, кроме того, основаны на показателе, показательном для активности, например, конкретном показателе специфической для антигена или клетки активности, предоставляющий информацию относительно риска неблагоприятного события или токсичности. В некоторых аспектах, такой показатель представляет собой или включает параметр, как наблюдали или как описано в настоящем описании, коррелирующий с риском неблагоприятного события, таким как тяжелая нейротоксичность или нейротоксичность конкретной степени (например, степени 3, длительная нейротоксичность степени 3, нейротоксичность степени 4 и/или степени 5), или отек головного мозга. В некоторых аспектах, параметр является показательным для специфического для модифицированной клетки или антигена высвобождения провоспалительного цитокина и/или одного или комбинации из TNFa, IFNg, IL–2 и IL–10.
[0139] В некоторых вариантах осуществления, способ, кроме того, учитывает изменчивость (например, среди клеток, модифицированных от различных индивидов и/или для использования различных видов сырья, таких как реагенты для активации, в способе). Например, в некоторых вариантах осуществления, параметр, показательный для специфической для клетки активности или удельной активности, нормализуют по сходному показателю, который может меняться среди таких индивидов или способов, но не прогнозирует неблагоприятный исход. Например, параметр, показательный для специфической для клетки активности (например, показатель антигенспецифической секреции провоспалительного цитокина), может быть в некоторых аспектах нормализован против или относительно другого параметра, такого как специфическое для антигена или клетки высвобождение фактора, который не коррелирует с нежелательным исходом или не прогнозирует нежелательный исход, такой как тяжелая нейротоксичность или нейротоксичность некоторой степени (например, степени 3, длительная степени 3, степени 4 и/или степени 5), или отек головного мозга. Например, наблюдали, что, в некоторых вариантах осуществления, секреция цитокинов, таких как IL–5, IL–13, GM–CSF и IL–6 не коррелирует с нежелательным исходом или не прогнозирует нежелательный исход. В ответ на специфический для клетки антиген, в то время как он может меняться среди клеток, модифицированных от различных индивидов (например, изменчивость от пациента к пациенту), изменчивость этого параметра в общем не коррелирует с риском или не прогнозирует риск нежелательного исхода, такого как тяжелая нейротоксичность или нейротоксичность некоторой степени (например, степени 3, длительная нейротоксичность степени 3, нейротоксичность степени 4 и/или степени 5), или отек головного мозга. В некоторых вариантах осуществления, секреция одного или нескольких из таких цитокинов может служить контрольным фактором, например, среднее арифметическое или среднее геометрическое показателя для двух или более из IL–5, IL–13, GM–CSF и IL–6.
[0140] В некоторых аспектах, доступные в настоящее время способы не являются удовлетворительными для характеризации как безопасности, так и эффективности терапевтической композиции T–клеток. Например, в некоторых случаях, в современных способах используют более низкий пороговый параметр высвобождения (например, показатель высвобождения интерферона–гамма для терапевтической композиции T–клеток), который не включает верхний предел безопасности. В некоторых случаях, терапевтическую композицию T–клеток не выпускают для дальнейшего использования в качестве терапевтического средства, если нет соответствия нижнему порогу; например, если терапевтическая композиция T–клеток не высвобождает выше порогового количества цитокина в определенном анализе, композицию не выпускают для инфузии пациенту. В некоторых аспектах, такие параметры могут включать высвобождение цитокина, высвобождение цитотоксических гранул и определение состояния активации T–клетки (например, конкретный процент клеток, экспрессирующих один или несколько маркеров активации). В некоторых аспектах, используемые в настоящее время параметры включают нижние пределы процентов CAR+ клеток и/или клеток, имеющих специфический фенотип. В некоторых способах, возможно то, что в то время как эффективность можно контролировать посредством обеспечения того, что терапевтическая композиция T–клеток имеет минимальную активность (т.е. высвобождает минимальное количество цитокина и/или проявляет определенный уровень активности в анализе цитотоксичности) или фенотип, является или нет композиция безопасной для введения, не определяют с использованием верхнего предела сходных параметров.
[0141] Представленные варианты осуществления основаны на обнаружениях того, что конкретные фенотипы и/или параметры, ассоциированные с функцией или активностью терапевтической композиции T–клеток, ассоциированы с риском возникновения токсичности, например, тяжелой нейротоксичности, у индивида, подвергнутого введению композиции T–клеток. В некоторых аспектах, обнаружено, что выносливость введенных клеток является признаком, коррелирующим с риском токсичности. В некоторых вариантах осуществления, количество или доза клеток, введенных индивиду, имеющих фенотип, указывающий на биологическую активность, таких как клетки, не имеющие апоптотического фенотипа, и/или имеющие фенотип, не проявляющий параметра, показательного для апоптоза (например, параметра, показательного для раннего или позднего апоптоза, такого как детектированный посредством аннексина V) и/или продуцирующие конкретные цитокины (например, провоспалительные цитокины), могут коррелировать с риском токсичности. В некоторых аспектах, индивиды, которым вводят большее общее количество клеток, такое как основанное на общем количестве CD3+CAR+ клеток или CD8+CAR+ клеток, или их подгруппы, могут быть подвержены более высокому риску развития тяжелой токсичности, чем индивид, которому вводят меньшее общее количество таких клеток. В некоторых случаях, конкретные режимы дозирования, которые не принимают во внимание общее количество клеток с такими признаками, и/или в которых присутствует высокая степень изменчивости фенотипа или функции введенных клеток среди группы подвергнутых лечению индивидов, могут, в конкретных аспектах, приводить к общему риску возникновения токсичности у подвергнутых лечению индивидов.
[0142] В некоторых аспектах, обнаружено, что более низкая общая доза введенных клеток, проявляющих такой фенотип, может являться желательной, например, для облегчения или минимизации риска токсичности. Тем не менее, несмотря на то, что такие признаки клеток могут влиять на риск токсичности у индивида, подвергнутого введению клеток, введение слишком небольшого количества таких клеток может уменьшать эффективность терапевтической композиции. Для учета эффективности, для способов дозирования является общепринятым устанавливать нижний предел активности композиции клеток, например, на основании цитолитической активности, продукции цитокина или другого фактора, ассоциированного с терапевтической композицией T–клеток, например, для обеспечения того, что достаточно клеток вводят индивиду для достижения эффекта. Исследования, описанные в настоящем описании, однако, показывают, что способы дозирования, в которых вводят дозу клеток, включая фиксированную дозу клеток, которая соответствует только нижнему уровню активности или функции, могут подвергать индивида риску токсичности, если такие клетки имеют высокий уровень антигенспецифической активности или функции.
[0143] На основании обнаружений в настоящем описании, настоящее изобретение относится к способам, композициям и изделиям, в которых единичная доза клеток основана на двух функциях, (A) количестве клеток конкретного фенотипа, такого как фенотип, показательный для биологической активности, и (B) значении параметра, которое показывает или коррелирует с зависимой от рекомбинантного рецептора активностью и/или антигенспецифической активностью в композиции. Иллюстративные переменные, которые, как обнаружено в этой работе, являются индикатором A или B, описаны в другом месте в настоящем описании, включая примеры. В некоторых вариантах осуществления, функция B, такая как продукция или накопление антигенспецифического цитокина, например, провоспалительного цитокина, является функцией, которая часто может отличаться и/или может являться изменчивой среди композиций T–клеток, полученных из клеток, происходящих от индивидов, включая специфические для пациента факторы риска, например, обусловленные конкретным заболеванием или состоянием индивида, возрастом индивида, массой индивида, предшествующим лечением, и другие факторы, которые могут менять или вносить вклад в один или несколько функциональных признаков T–клеток.
[0144] В некоторых вариантах осуществления, обнаружено, что B представляет собой индикатор безопасности терапевтической композиции T–клеток. В некоторых случаях, если B является слишком высоким, более низкую дозу клеток следует вводить для уменьшения или минимизации риска токсичности, такой как тяжелая нейротоксичность. В некоторых случаях, если B находится ниже порогового уровня или предела, может присутствовать большее окно для дозы, которую можно вводить, так что целевую дозу клеток можно вводить индивиду без известного риска возникновения токсичности или неблагоприятного события, например, тяжелой токсичности. В некоторых аспектах, контроль или коррекция общего количества клеток или общего количества клеток конкретного фенотипа (например, CD3+CAR+ или CD8+CAR+ или аннексин V–CD8+CAR+) в терапевтической композиции T–клеток, которую вводят, может стандартизировать или регулировать общее количество единиц активности вводимых композиций T–клеток среди подвергаемых лечению индивидов, таким образом, учитывая функциональные различия или различия активности из B в T–клетках среди композиций T–клеток, происходящих от группы индивидов, которые могли в ином случае привести к риску возникновения токсичности, например, тяжелой токсичности, у некоторых индивидов.
[0145] В некоторых вариантах осуществления, B, представляющее собой значение параметра зависимой от рекомбинантного рецептора (например, зависимой от CAR), например, антигенспецифической активности, может обеспечивать контроль активности для композиции T–клеток. В некоторых аспектах, анализ активности на основании функции T–клеток из B может обеспечивать преимущества по сравнению с существующими способами. Во–первых, в некоторых аспектах, существующие анализы активности для композиций клеток основаны на признаках, которые коррелируют с эффективностью клеток, например, цитолитической активностью и/или продукцией IFN–гамма, в отличие от безопасности. Кроме того, такие анализы активности часто имеют только нижний предел или уровень активности в рамках анализа.
[0146] На основании обнаружений в настоящем описании, среди представленных вариантов осуществления присутствуют анализы активности, такие как анализы, в которых существует нижний установленный предел (LSL) и/или верхний установленный предел (USL). В некоторых аспектах, USL основан на параметре B. В некоторых аспектах, USL представлен для проверки безопасности композиции T–клеток, например, в сочетании с анализом высвобождения перед введением композиции индивиду. Как указано выше, различные клинические критерии и другие специфические для пациента признаки могут влиять на уровень или степень функции модифицированных клеток. Подобным образом, в некоторых случаях, способ в целом, включая реагенты, используемые в сочетании с изготовлением или модификацией композиции клеток и/или при замораживании клеток, полученных способом для клеток, также может приводить к изменчивости B среди множества композиций T–клеток, полученных с использованием одинакового способа. В некоторых случаях, обнаружено, что замораживание клеток ниже плотности менее чем 15×106 клеток/мл может приводить к увеличению изменчивости и/или уменьшению активности композиции T–клеток. В некоторых вариантах осуществления, представленные способы являются особенно преимущественными для оценки композиций клеток, в которых изменчивость клеток, имеющих конкретный фенотип, такой как фенотип A, описанный ниже, включая фенотип, показательный для биологической активности, например, аннексин V–CD8+CAR+, отличается или, вероятно, отличается более чем на 20%, более чем на 30%, более чем на 40%, более чем на 50% или более, среди множества композиций T–клеток, полученных этим способом, или от среднего частоты фенотипа во множестве композиций T–клеток, полученных этим способом, и/или отличается или, вероятно, отличается от такого среднего не более чем на одно стандартное отклонение.
[0147] В некоторых вариантах осуществления представленных способов и доз, клетки получают способом, разработанным для минимизации изменчивости факторов, таких как факторы, как наблюдали в этой работе, коррелирующие (отдельно или в комбинации) с риском нейротоксичности. В некоторых аспектах таких вариантов осуществления, дозирование может быть основано на общем количестве или относительном количестве модифицированных клеток или модифицированных T–клеток, или популяции T–клеток, без увеличения риска токсичности, который может присутствовать, когда клетки получают с использованием способа, в котором такие параметры являются более изменчивыми. В некоторых аспектах, такие способы включают использование лентивирусных векторов, определенных соотношений подгрупп T–клеток, таких как CD4 и/или CD8 клетки. В некоторых аспектах, они включают конструирование клеток, включающих CAR с происходящим из 41BB костимулирующим доменом, в отличие от домена CD28. В некоторых аспектах, способ включает контролируемые соотношения подгрупп T–клеток, цитокинов и реагентов, чтобы обеспечивать контроль фенотипа, функции и состояние метаболизма) и/или контролируемую и относительно более высокую общую плотность клеток во время криоконсервации (например, между 10 и между 60 или между 15 и 60 миллионов клеток на мл, включая каждое), хранения и/или размораживания образца перед введением. В некоторых аспектах используют способ, в котором метаболические и функциональные свойства T–клеток легче контролировать. В некоторых вариантах осуществления, такие способы используют для предоставления единообразных доз биологически активных клеток, даже в контексте специфических для пациента переменных, которые могут влиять на здоровье клеток.
[0148] Среди вариантов осуществления присутствуют варианты, в которых в способах получают более высокую частоту биологически активных или здоровых клеток среди CD8+CAR+ клеток, как измерено по отрицательности различных апоптотических маркеров среди образцов, полученных с использованием этого способа. В некоторых аспектах, присутствует более низкая степень изменчивости этого параметра среди образцов, полученных этим способом от различных индивидов. Как наблюдали в этой работе, количество таких клеток может коррелировать с нейротоксичностью степени 5 и отеком головного мозга, в то время как CD3+CAR+ жизнеспособные клетки (без учета апоптотического состояния по сравнению с биологически активными клетками) могут не всегда прогнозировать токсичность или ясно определять границу безопасности применительно к этому риску.
[0149] В некоторых вариантах осуществления, использование способа с уменьшенной изменчивостью частоты таких биологически активных клеток среди модифицированных клеток, уменьшает риск того, что конкретным пациентам, таким как пациенты, имеющие конкретные специфические для пациента факторы риска, как описано (например, пациенты, имеющие клетки, которые менее склонны к апоптозу или которые являются более здоровыми), могут непреднамеренно вводить более высокую дозу, чем намеревались, биологически активных клеток, при дозировании на основании количества модифицированных T–клеток в целом. Кроме того, наблюдали, что способы с большей степенью контроля фенотипа и функции уменьшают степень изменчивости для способности клеток, полученных этим способом, продуцировать провоспалительные цитокины антигенспецифическим образом. Результаты в настоящем описании согласуются с интерпретацией, что, в частности, в сочетании с количествами биологически активных модифицированных клеток, способ дозирования, принимающий во внимание такие специфические для клеток параметры активности (например, таким образом, что конкретный целевой диапазон такой активности – или не более порогового значения – представлены в данной дозе), можно использовать для предоставления дозы, способной обеспечивать желательный клинический или терапевтический исход, в то же время все еще оставаясь в границах безопасности или уменьшая риск нежелательной токсичности, например, нейротоксичности.
[0150] В некоторых вариантах осуществления, использование способа, в котором постоянно получают более высокие частоты биологически активных модифицированных клеток, позволяет использование доз клеток, намного более низких (с позиции количеств модифицированных, например, CAR+, клеток), по сравнению с другими способами дозирования, в которых с большей частотой модифицированные клетки являются положительными по апоптотическим маркерам или являются в ином отношении менее здоровыми. Например, на основании наблюдений в настоящем описании, и принимая во внимание то наблюдение, что в доступных способах дозирования, как правило, не принимают во внимание частоту апоптотических клеток, в некоторых вариантах осуществления, количества модифицированных (например, CAR+) T–клеток (например, модифицированных CD8+ и/или CD4+ клеток), являются настолько низкими, как 5, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 30, 40 или 50 миллионов клеток.
[0151] Представленные способы предоставляют анализ высвобождения, который может мониторировать или оценивать композиции клеток для определения, если композицию вводят индивиду, может ли она, вероятно, коррелировать с риском возникновения токсичности, такой как тяжелая нейротоксичность. В некоторых вариантах осуществления, композицию T–клеток не рекомендуют вводить индивиду, и/или единичную дозу, подлежащую введению индивиду, изменяют или корректируют, если B превышает USL. Если B ниже USL, продукт можно выпускать для лечения. В некоторых вариантах осуществления, оценка того, находится ли B выше LSL и/или ниже USL, также может обеспечивать информацию о том, подвержен ли индивид, которому ранее вводили композицию T–клеток, риску развития токсичности, такой как тяжелая токсичность. В некоторых вариантах осуществления, оценку образца композиции T–клеток, введенной индивиду, по B проводят после введения. В некоторых вариантах осуществления, определяют, что индивид, которому вводили композицию T–клеток, подвержен риску возникновения токсичности, такой как тяжелая нейротоксичность, если B составляет или превышает USL. В таких вариантах осуществления, индивида, которому вводили композицию, подвергают мониторированию и/или лечению с использованием средства для уменьшения или снижения вероятности исхода токсичности, такого как нейротоксичность или синдром высвобождения цитокинов, после введения композиции клеток и необязательно, до возникновения признака или симптома исхода токсичности.
[0152] В некоторых аспектах, представленные варианты осуществления основаны на наблюдениях, что эффективность адоптивной клеточной терапии может быть ограничена из–за возникновения токсичности у индивида, которому вводят такие клетки, где токсичность, в некоторых случаях, может являться тяжелой. Например, в некоторых случаях, введение дозы клеток, экспрессирующих рекомбинантный рецептор, например, CAR, может приводить к токсичности или ее риску, например, CRS или нейротоксичности. В некоторых случаях, в то время как более высокая доза таких клеток может увеличивать эффективность лечения, например, посредством увеличения воздействия клеток, например, посредством стимуляции размножения и/или персистенции, они могут также приводить к даже более высокому риску возникновения токсичности или более тяжелой токсичности. А также, в некоторых случаях, индивиды с более высокой нагрузкой заболевания также могут быть подвержены более высокому риску возникновения токсичности или более тяжелой токсичности.
[0153] Конкретные доступные способы лечения или облегчения токсичности могут не всегда являться полностью удовлетворительными. Множество таких способов сфокусированы, например, на нацеливании на нижестоящие эффекты токсичности, например, посредством блокирования цитокинов, и/или доставки таких средств, как высокая доза стероидов, которые также могут прекращать или нарушать функцию введенных клеток. Кроме того, такие способы часто включают проведение таких вмешательств только при детекции физических признаков или симптомов токсичности, которые, как правило, включают признаки или симптомы умеренной или тяжелой токсичности (например, умеренной или тяжелой CRS). Многие из этих других способов также не предотвращают другие формы токсичности, такие как нейротоксичность, которые могут быть ассоциированы с адоптивной клеточной терапией. В некоторых случаях, это происходит в то время, когда такие симптомы являются тяжелыми, и это, таким образом, может требовать даже более жестких или более экстремальных видов лечения (например, более высоких доз или увеличенной частоты введения) для облегчения или лечения токсичности.
[0154] Использование конкретных альтернативных способов не обеспечивает удовлетворительных решений таких проблем. В некоторых случаях, такие средства и виды терапии (например, стероиды) сами являются ассоциированными с токсичными побочными эффектами. Такие побочные эффекты могут быть даже больше при более высокой дозе или частоте, при которых их необходимо вводить или проводить лечение с использованием средства или терапии, для лечения или облегчения тяжести токсичности, которая может возникать в результате клеточной терапии. Кроме того, в некоторых случаях, считают, что средство или терапия для лечения токсичности могут ограничивать эффективность клеточной терапии, например, эффективность химерного рецептора (например, CAR), экспрессированного на клетках, предоставленных в качестве части клеточной терапии (Sentman (2013) Immunotherapy, 5:10).
[0155] Представленные варианты осуществления обеспечивают преимущества в том, что направлены или нацелены на риск токсичности, такой как тяжелая нейротоксичность, у индивидов, которым вводили терапевтическую композицию T–клеток. В некоторых вариантах осуществления, вероятность возникновения у индивида токсичности, такой как тяжелая нейротоксичность, уменьшают или предотвращают посредством представленных вариантов осуществления, в которых признаки безопасности композиции оценивают и/или корректируют посредством дозирования у индивида. В некоторых вариантах осуществления, вероятность возникновения у индивида токсичности, такой как тяжелая токсичность, уменьшают или предотвращают посредством мониторирования или оценки безопасности терапевтической композиции T–клеток перед выпуском для введения индивиду и/или посредством введения единичной дозы клеток, содержащей не более целевой дозы клеток или содержащей или не превышающей целевое количество эталонных единиц (RU) клеток.
[0156] В некоторых вариантах осуществления, представленные варианты осуществления разработаны, чтобы включать, или включают признаки, приводящие к более низкой степени или к более низкой степени риска токсичности, исхода или симптома токсичности, способствующего токсичности профиля, фактора или свойства, например, симптома или исхода, ассоциированного с или показательного для синдрома высвобождения цитокинов (CRS) или нейротоксичности, например, по сравнению с другими способами, в которых терапевтическую композицию T–клеток не оценивали в анализе для контроля безопасности, и/или в которых терапевтическую композицию T–клеток не вводили индивиду в соответствии с представленной формулой дозирования, принимая во внимание A и B, и/или не дозировали при целевом количестве RU, таком как меньшее, чем пороговое количество RU, или не дозировали при целевом количестве клеток или количестве клеток в пределах данного целевого диапазона, в терапевтической композиции T–клеток.
Токсичность и исход токсичности
[0157] В некоторых аспектах, исход токсичности терапии, такой как клеточная терапия, представляет собой или ассоциирован с, или является показательным для синдрома высвобождения цитокинов (CRS) или тяжелого CRS (sCRS). CRS, например, sCRS, может возникать, в некоторых случаях, после адоптивной T–клеточной терапии и введения индивидам других биологических продуктов. См. Davila et al., Sci Transl Med 6, 224ra25 (2014); Brentjens et al., Sci. Transl. Med. 5, 177ra38 (2013); Grupp et al., N. Engl. J. Med. 368, 1509–1518 (2013); и Kochenderfer et al., Blood 119, 2709–2720 (2012); Xu et al., Cancer Letters 343 (2014) 172–78.
[0158] Как правило, CRS вызван избыточным системным иммунным ответом, опосредованным, например, T–клетками, B–клетками, NK–клетками, моноцитами и/или макрофагами. Такие клетки могут высвобождать большое количество медиаторов воспаления, таких как цитокины и хемокины. Цитокины могут запускать острый воспалительный ответ и/или индуцировать повреждение эндотелия органов, что может приводить к просачиванию микрососудов, сердечной недостаточности или смерти. Тяжелый, опасный для жизни CRS может приводить к инфильтрации легких и повреждению легких, почечной недостаточности или диссеминированному внутрисосудистому свертыванию. Другие виды тяжелой, опасной для жизни токсичности могут включать кардиологическую токсичность, респираторный дистресс, неврологическую токсичность и/или печеночную недостаточность.
[0159] Исходы, признаки и симптомы CRS известны и включают описанные в настоящем описании. В некоторых вариантах осуществления, где конкретный режим дозирования или введение вызывает или не вызывает данный ассоциированный с CRS исход, признак или симптом, конкретные исходы, признаки и симптомы, и/или их уровни или степени могут быть указаны.
[0160] В контексте введения экспрессирующих CAR клеток, CRS, такой как тяжелый CRS, как правило, возникает через 6–20 суток после инфузии клеток, экспрессирующих CAR. См. Xu et al., Cancer Letters 343 (2014) 172–78. В некоторых случаях, CRS возникает менее чем через 6 суток или более чем через 20 суток после инфузии CAR–T–клеток. Частота возникновения и временные рамки CRS могут быть связаны с фоновыми уровнями цитокинов или опухолевой нагрузкой на время инфузии. Обычно, CRS включает увеличенные уровни в сыворотке интерферона (IFN)–γ, фактора некроза опухоли (TNF)–α и/или интерлейкина (IL)–2. Другие цитокины, которые могут быть быстро индуцированы при CRS, представляют собой IL–1β, IL–6, IL–8 и IL–10.
[0161] Разработаны критерии CRS, которые, по–видимому, коррелируют с началом CRS, для прогнозирования того, какие пациенты, более вероятно, подвержены риску возникновения CRS (см. Davilla et al. Science translational medicine. 2014;6(224):224ra25). Факторы включают лихорадку, гипоксию, гипотензию, неврологические изменения, увеличенные уровни в сыворотке провоспалительных цитокинов, например, набора из семи цитокинов (IFNγ, IL–5, IL–6, IL–10, Flt–3L, фракталкина и GM–CSF), индуцированное лечением увеличение уровня которых может хорошо коррелировать как с опухолевой нагрузкой до лечения, так и с симптомами sCRS. Известны другие руководства по диагностике и управлению течением CRS (см., например, Lee et al, Blood. 2014;124(2):188–95). В некоторых вариантах осуществления, критерии, отражающие степени CRS, представляют собой критерии, подробно описанные в таблице 1 ниже.
Мягкая
Умеренная
• Потребность в кислороде < 40%, или
• Гипотензия, отвечающая на жидкости или низкую дозу одиночного сосудосуживающего средства или
• Токсичность для органа степени 2 (по CTCAE v4.0)
Тяжелая
• Потребность в кислороде ≥ 40%, или
• Гипотензия, требующая высокой дозы одиночного сосудосуживающего средства (например, норадреналина ≥ 20 мкг/кг/мин, дофамина ≥ 10 мкг/кг/мин, фенилэфрина ≥ 200 мкг/кг/мин или адреналина ≥ 10 мкг/кг/мин), или
• Гипотензия, требующая множества сосудосуживающих средств (например, вазопрессин+одно из вышеуказанных средств, или комбинация сосудосуживающих средств, эквивалентная ≥ 20 мкг/кг/мин норадреналина), или
• Токсичность для органа степени 3 или степени 4 трансаминит (по CTCAE v4.0)
Опасная для жизни
• Требует искусственной вентиляции, или
• Токсичность для органа степени 4 (исключая трансаминит)
Летальная
[0162] В некоторых вариантах осуществления, у индивида, по видимому, развивается «тяжелый CRS» («sCRS») в ответ на или вследствие проведения клеточной терапии или введения дозы клеток для нее, если, после введения, у индивида показано: (1) лихорадка по меньшей мере при 38 градусов Цельсия в течение по меньшей мере трех суток; (2) увеличение уровня цитокина, включающее либо (a) максимальную кратность изменения по меньшей мере 75 по меньшей мере для двух из следующей группы из семи цитокинов, по сравнению с уровнем непосредственно после введения: интерферон гамма (IFNγ), GM–CSF, IL–6, IL–10, Flt–3L, фракталкин и IL–5, и/или (b) максимальную кратность изменения по меньшей мере 250 по меньшей мере для одного из следующей группы из семи цитокинов, по сравнению с уровнем непосредственно после введения: интерферон гамма (IFNγ), GM–CSF, IL–6, IL–10, Flt–3L, фракталкин и IL–5; и (c) по меньшей мере один клинический признак токсичности, такой как гипотензия (требующая по меньшей мере одного внутривенного сосудосуживающего средства) или гипоксия (PO2<90%) или одно или несколько неврологическое нарушение(нарушения) (включая изменения психического состояния, притупление чувствительности и/или судороги). В некоторых вариантах осуществления, тяжелый CRS включает CRS степени 3 или выше, например, как указано в таблице 1.
[0163] В некоторых вариантах осуществления, исходы, ассоциированы с тяжелым CRS или CRS степени 3 или выше, например, степени 4 или выше, например, как указано в таблице 1. В некоторых вариантах осуществления, они включают одно или несколько из: персистентной лихорадки, например, лихорадки при указанной температуре, например, более или приблизительно 38 градусов Цельсия, в течение двух или более, например, трех или более, например, четырех или более суток или в течение по меньшей мере трех последовательных суток; лихорадки более чем при или приблизительно при 38 градусов Цельсия; увеличения уровня цитокинов, такого как максимальная кратность изменения, например, по меньшей мере или приблизительно 75, по сравнению с уровнями до лечения, по меньшей мере для двух цитокинов (например, по меньшей мере двух из группы, состоящей из интерферона гамма (IFNγ), GM–CSF, IL–6, IL–10, Flt–3L, фракталкина и IL–5, и/или фактора некроза опухоли альфа (TNFα)), или максимальная кратность изменения, например, по меньшей мере или приблизительно 250 по меньшей мере для одного из таких цитокинов; и/или по меньшей мере одного клинического признака токсичности, такого как гипотензия (например, как измерено посредством по меньшей мере одного внутривенного сосудосуживающего средства); гипоксии (например, уровней кислорода (PO2) в плазме менее или приблизительно 90%); и/или одного или нескольких неврологических нарушений (включая изменения психического состояния, притупление чувствительности и судороги). В некоторых вариантах осуществления, тяжелый CRS включает CRS, требующий управления течением или лечения в отделении реанимации (ICU).
[0164] В некоторых вариантах осуществления, тяжелый CRS включает комбинацию (1) персистентной лихорадки (лихорадки по меньшей мере при 38 градусов Цельсия в течение по меньшей мере трех суток) и (2) уровня CRP в сыворотке по меньшей мере или приблизительно 20 мг/дл. В некоторых вариантах осуществления, тяжелый CRS включает гипотензию, требующую использования двух или более сосудосуживающих средств, или дыхательную недостаточность, требующую искусственной вентиляции. В некоторых вариантах осуществления, дозу сосудосуживающих средств увеличивают при втором или последующем введении.
[0165] В некоторых вариантах осуществления, тяжелый CRS или CRS степени 3 включает увеличение уровня аланинаминотрансферазы, увеличение уровня аспартатаминотрансферазы, озноб, фебрильную нейтропению, головную боль, дисфункцию левого желудочка, энцефалопатию, гидроцефалию и/или тремор.
[0166] В некоторых аспектах, исход токсичности терапии, такой как клеточная терапия, представляет собой или ассоциирован с, или является показателем нейротоксичности или тяжелой нейротоксичности. В некоторых вариантах осуществления, симптомы, ассоциированные с клиническим риском нейротоксичности, включают спутанность, бред, экспрессивную афазию, притупление чувствительности, миоклонию, летаргию, изменение психического состояния, конвульсии, подобную судорогам активность, судороги (необязательно, как подтверждено посредством электроэнцефалограммы [EEG]), увеличенные уровни бета–амилоида (Aβ), увеличенные уровни глутамата и увеличенные уровни кислородных радикалов. В некоторых вариантах осуществления, нейротоксичность разделяют на степени на основании тяжести (например, с использованием шкалы степени 1–5 (см., например, Guido Cavaletti & Paola Marmiroli Nature Reviews Neurology 6, 657–666 (December 2010); Национальный институт онкологии США – Общие критерии токсичности версии 4.03 (NCI–CTCAE v4.03).
[0167] В некоторых случаях, неврологические симптомы могут являться наиболее ранними симптомами sCRS. В некоторых вариантах осуществления, наблюдают, что неврологические симптомы начинаются через 5–7 суток после инфузии клеточной терапии. В некоторых вариантах осуществления, длительность неврологических изменений может лежать в диапазоне от 3 до 19 суток. В некоторых случаях, восстановление неврологических изменений происходит после разрешения других симптомов sCRS. В некоторых вариантах осуществления, время или степень разрешения неврологических изменений не ускоряется в результате лечения с использованием антител против IL–6 и/или стероида(стероидов).
[0168] В некоторых вариантах осуществления, у индивида, по видимому, развивается «тяжелая нейротоксичность» в ответ на или вследствие проведения клеточной терапии или введения дозы клеток для нее, если, после введения, у индивида показаны симптомы, ограничивающие самообслуживание (например, мытье, одевание и раздевание, питание, использование туалета, прием лекарств) среди: 1) симптомов периферической моторной нейропатии, включая воспаление или дегенерацию периферических моторных нервов; 2) симптомов периферической сенсорной невропатии, включая воспаление или дегенерацию периферических сенсорных нервов, дизестезию, такую как искажение сенсорного восприятия, приводящее к аномальному и неприятному ощущению, невралгию, такую как интенсивное болезненное ощущение на протяжении нерва или группы нервов, и/или парестезию, такую как функциональные раздражения сенсорных нейронов, приводящие к аномальным кожным ощущениям покалывания, онемения, давления, холода и тепла в отсутствие стимула. В некоторых вариантах осуществления, тяжелая нейротоксичность включает нейротоксичность степени 3 или более, например, как указано в таблице 2. В некоторых вариантах осуществления, тяжелую нейротоксичность рассматривают как длительную нейротоксичность степени 3, если симптомы нейротоксичности степени 3 продолжаются 10 суток или дольше. В некоторых вариантах осуществления, токсичность, такую как нейротоксичность, например, нейротоксичность степени 3 или 4, рассматривают как длительную нейротоксичность (например, длительную нейротоксичности степени 3), если симптомы нейротоксичности данной степени, например, степени 3 или выше, присутствуют или присутствовали в течение по меньшей мере 10 суток или по меньшей мере приблизительно 10 суток, или по меньшей мере 11 суток, или по меньшей мере приблизительно 11 суток, или по меньшей мере 10–11 суток, или приблизительно 10–11 суток. Длительная нейротоксичность степени 3, как правило, ассоциирована с нейротоксичностью степени 3, персистирующей в течение более чем или в среднем, более чем 9 суток, 8 суток, или 1 недели. В некоторых аспектах, не длительная нейротоксичность степени 3, как правило, ассоциирована с симптомами нейротоксичности степени 3, не персистирующей в течение более чем или в среднем, более чем 9 суток, 8 суток или 1 недели, или, в некоторых случаях, менее чем 6, 5, 4 или 3 суток.
Бессимптомная или мягкая
Умеренная
Тяжелая
Опасная для жизни
Летальная
[0169] В некоторых вариантах осуществления, представленные варианты осуществления, включая способы лечения, применения, изделия, единичные дозы, приводят к уменьшению симптомов, ассоциированных с нейротоксичностью после клеточной терапии, по сравнению с другими вариантами осуществления или способами. Например, индивиды, которых лечили в соответствии с представленными способами, могут иметь уменьшенные симптомы нейротоксичности, такие как слабость или онемение конечностей, потеря памяти, зрения и/или интеллекта, неконтролируемое обсессивное и/или компульсивное поведение, галлюцинации, головная боль, когнитивные и поведенческие расстройства, включая потерю моторного контроля, нарушение когнитивных функций и дисфункцию автономной нервной системы и половую дисфункцию, по сравнению с индивидами, которых лечили другими способами. В некоторых вариантах осуществления, индивиды, которых лечили в соответствии с представленными способами, могут иметь уменьшенные симптомы, ассоциированные с периферической моторной нейропатией, периферической сенсорной невропатией, дизестезией, невралгией или парестезией.
[0170] В некоторых вариантах осуществления, способы уменьшают исходы, ассоциированные с нейротоксичностью, включая повреждение нервной системы и/или головного мозга, такое как гибель нейронов. В некоторых аспектах, способы уменьшают уровень факторов, ассоциированных с нейротоксичностью, таких как бета–амилоид (Aβ), глутамат и кислородные радикалы.
[0171] В некоторых вариантах осуществления, индивиды, которым вводят одну или несколько единичных доз представленной терапевтической композиции T–клеток или терапевтической композиции T–клеток, выпущенной для введения в соответствии с представленными способами, и/или которых подвергают дозированию в соответствии с представленными способами, имеют уменьшенную вероятность возникновения серьезного неблагоприятного события, такого как длительная нейротоксичность по меньшей мере степени 3, например, нейротоксичность степени 4 или степени 5. В некоторых аспектах, у индивидов, которых лечили в соответствии с представленными вариантами осуществления, не возникает нейротоксичность или возникает нейротоксичность степени, которая является менее тяжелой, чем если бы индивида лечили другими способами или с использованием других терапевтических композиций T–клеток, включая терапевтические композиции T–клеток, не оцененные в соответствии с представленными способами.
II. ПРИЗНАКИ КОМПОЗИЦИЙ КЛЕТОК
[0172] Представленные в настоящем описании способы относятся к признакам клеток в терапевтической композиции T–клеток. В некоторых вариантах осуществления, признаки, отдельно или в комбинации, коррелируют с риском возникновения неблагоприятного события или токсичности, такой как тяжелая токсичность, например, длительная токсичность по меньшей мере степени 3 или токсичность степени 4, или степени 5. В некоторых вариантах осуществления, признак представляет собой фенотип клеток в композиции, также обозначенный как «A» в настоящем описании, включая фенотип, показательный для биологической активности клеток или популяции клеток. В некоторых вариантах осуществления, признак представляет собой зависимую от рекомбинантного рецептора активность, такую как антигенспецифическая активность, также обозначенную как «B» в настоящем описании. В некоторых вариантах осуществления, признак A и/или B клеток в композиции T–клеток рассматривают в сочетании с представленными способами. В некоторых аспектах, функцию признака A и B рассматривают в сочетании с определением целевого количества эталонных единиц (RU), например, в сочетании с предоставлением или введением единичной дозы терапевтической композиции T–клеток. В некоторых аспектах, пороговое значение признака B, или нижний установленный предел (LSL) и верхний установленный предел (USL) B, используют для оценки или определения безопасности или вероятности безопасности терапевтической композиции T–клеток, например, в сочетании с анализом активности или анализом высвобождения. Представлены различные иллюстративные способы, в которых признаки A и/B принимают во внимание или оценивают.
A. Фенотипы композиций клеток
[0173] В некоторых вариантах осуществления, фенотип «A» представляет собой присутствие или отсутствие одной или нескольких специфических молекул, включая поверхностные молекулы и/или молекулы, которые могут накапливаться или могут быть продуцированы клетками или субпопуляцией клеток в композиции T–клеток. В некоторых вариантах осуществления, фенотип, напрямую или обратным образом, показывает или является показательным для биологической активности клеток или популяции клеток в композиции T–клеток. В некоторых вариантах осуществления, фенотип может включать активность клеток, такую как продукция фактора в ответ на стимул. В конкретных вариантах осуществления, оценку композиции клеток проводят для идентификации, детекции или количественной оценки фенотипа композиции клеток. В конкретных вариантах осуществления, измерение композиции клеток проводят для идентификации, детекции или количественной оценки присутствия, отсутствия, степени экспрессии или уровня специфической молекулы
[0174] В некоторых вариантах осуществления, фенотип является показателем жизнеспособности клетки. В некоторых вариантах осуществления, фенотип является показателем отсутствия апоптоза, отсутствия ранних стадий апоптоза или отсутствия поздних стадий апоптоза. В некоторых вариантах осуществления, фенотип представляет собой отсутствие фактора, показательного для отсутствия апоптоза, раннего апоптоза или поздних стадий апоптоза. В некоторых вариантах осуществления, фенотип представляет собой фенотип субпопуляции или подгруппы T–клеток, такой как экспрессирующие рекомбинантный рецептор T–клетки (например, CAR+ T–клетки) или CD8+ T–клетки, наивные T–клетки или конкретная субпопуляция T–клеток памяти, или T–клетки, имеющие признаки, подобные стволовым клеткам памяти. В некоторых вариантах осуществления, фенотип представляет собой фенотип клеток, которые не являются активированными и/или в которых отсутствует или уменьшена, или является низкой экспрессия одного или нескольких маркеров активации. В некоторых вариантах осуществления, фенотип представляет собой фенотип клеток, которые не являются истощенными и/или в которых отсутствует или уменьшена, или является низкой экспрессия одного или нескольких маркеров истощения.
[0175] В некоторых вариантах осуществления, на фенотип указывает присутствие, отсутствие или уровень экспрессии в клетке одной или нескольких специфических молекул, таких как определенные поверхностные маркеры, показательные для фенотипа, например, поверхностные белки, внутриклеточные маркеры, показательные для фенотипа, или нуклеиновые кислоты показательные для фенотипа, или другие молекулы или факторы, показательные для фенотипа. В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию одной или нескольких специфических молекул. В некоторых вариантах осуществления, специфические молекулы включают, но без ограничения, поверхностный маркер, например, мембранный гликопротеин или рецептор, маркер, ассоциированный с апоптозом или жизнеспособностью, или специфическую молекулу, показывающую статус иммуноцитов, например, маркер, ассоциированный с активацией, истощением или зрелым или наивным фенотипом. В некоторых вариантах осуществления, любой известный способ оценки или измерения, подсчета и/или количественной оценки клеток на основании специфических молекул можно использовать для определения количества клеток этого фенотипа.
[0176] В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию одной или нескольких специфических молекул в клетке. В некоторых вариантах осуществления, положительную экспрессию показывают по поддающемуся детекции количеству специфической молекулы в клетке. В конкретных вариантах осуществления, поддающееся детекции количество представляет собой любое детектированное количество специфической молекулы в клетке. В конкретных вариантах осуществления, поддающееся детекции количество представляет собой количество, превышающее фон, например, фоновое окрашивание, сигнал и т.д., в клетке. В конкретных вариантах осуществления, положительная экспрессия представляет собой количество специфической молекулы, не превышающее порог, например, предопределенный порог. Подобным образом, в конкретных вариантах осуществления, клетка с отрицательной экспрессией специфической молекулы может представлять собой любую клетку, не определенную как имеющая положительную экспрессию, или представляет собой клетку, в которой отсутствует поддающееся детекции количество специфической молекулы или поддающееся детекции количество специфической молекулы выше фона. В некоторых вариантах осуществления, клетка имеет отрицательную экспрессию специфической молекулы, если количество специфической молекулы ниже порога. Специалисту в данной области понятно, как определять порог для определения положительной и/или отрицательной экспрессии специфической молекулы общепринятым образом, и то, что пороги можно определять в соответствии со специфическими параметрами, например, но без ограничения, анализа или способа детекции, идентичности специфической молекулы, реагентов, используемых для детекции, и оборудования.
[0177] Примеры способов, которые можно использовать для детекции специфической молекулы и/или анализа фенотипа клеток, включают, но без ограничения, биохимический анализ; иммунохимический анализ; анализ визуализации; цитоморфологический анализ; молекулярный анализ, такой как ПЦР, секвенирование, определение метилирования ДНК; протеомный анализ, такой как определение паттерна гликозилирования и/или фосфорилирования белка; геномный анализ; эпигеномный анализ; транскриптомный анализ; и любую их комбинацию. В некоторых вариантах осуществления, молекулярные характеристики фенотипа анализируют посредством анализа визуализации, ПЦР (включая стандартную и все варианты ПЦР), микромассива (включая, но без ограничения, микромассив ДНК, MMchips для микро–РНК, микромассив белков, клеточный микромассив, микромассив антител и углеводный массив), секвенирования, детекции биомаркера или способов определения паттерна метилирования ДНК или гликозилирования белка. В конкретных вариантах осуществления, специфическая молекула представляет собой полипептид, т.е. белок. В некоторых вариантах осуществления, специфическая молекула представляет собой полинуклеотид.
[0178] В некоторых вариантах осуществления, положительную или отрицательную экспрессию специфической молекулы определяют посредством инкубации клеток с одним или несколькими антителами или другими связующими средствами, которые специфически связываются с одним или несколькими поверхностными маркерами, экспрессированными или экспрессированными (маркер+) на относительно более высоком уровне (маркервысокий) на положительно или отрицательно отобранных клетках, соответственно. В конкретных вариантах осуществления, положительную или отрицательную экспрессию определяют посредством проточной цитометрии, иммуногистохимии или любого другого пригодного способа детекции специфических маркеров.
[0179] В конкретных вариантах осуществления, экспрессию специфической молекулы оценивают с использованием проточной цитометрии. Проточная цитометрия представляет собой биофизическую технологию на основе лазера или сопротивления, используемую при подсчете клеток, сортировке клеток, детекции биомаркера и белковой инженерии, посредством суспендирования клеток в потоке жидкости и их пропускания через электронное устройство для детекции. Она позволяет одновременный многопараметрический анализ физических и химических характеристик вплоть до тысяч частиц в секунду.
[0180] Данные, полученные посредством проточных цитометров, можно наносить на график в одном измерении, для получения гистограммы, или на двумерные точечные диаграммы, или даже в трех измерениях. Области на этих графиках можно затем разделять, на основании интенсивности флуоресценции, посредством получения серий вычитаний подгрупп, называемых «отборами». Существуют способы специфического отбора для диагностических и клинических целей, особенно применительно к иммунологии. Графики часто получают в логарифмических шкалах. Поскольку спектры излучения различных флуоресцентных красителей перекрываются, сигналы на детекторах необходимо компенсировать электронным, так же как вычислительным способом. Данные, собранные с использованием проточного цитометра, можно анализировать с использованием программного обеспечения, например, JMP (статистического программного обеспечения), WinMDI, [10] программного обеспечения Flowing, [11] и доступного через интернет Cytobank[12]), Cellcion, FCS Express, FlowJo, FACSDiva, CytoPaint (также известный как Paint–A–Gate), [13] VenturiOne, CellQuest Pro, Infinicyt или Cytospec.
[0181] Проточная цитометрия является стандартным способом в данной области, и специалисту в данной области хорошо понятно, каким образом разрабатывать или подгонять способы для детекции одной или нескольких специфических молекул и анализировать данные для определения экспрессии одной или нескольких специфических молекул в популяции клеток. Стандартные протоколы и способы проточной цитометрии обнаружены в Loyd «Flow Cytometry in Microbiology; Practical Flow Cytometry by Howard M. Shapiro; Flow Cytometry for Biotechnology by Larry A. Sklar, Handbook of Flow Cytometry Methods by J. Paul Robinson, et al., Current Protocols in Cytometry, Wiley–Liss Pub, Flow Cytometry in Clinical Diagnosis, v4, (Carey, McCoy, and Keren, eds), ASCP Press, 2007, Ormerod, M.G. (ed.) (2000) Flow Cytometry –A practical approach. 3rd edition. Oxford University Press, Oxford, UK, Ormerod, M.G. (1999) Flow Cytometry. 2nd edition. BIOS Scientific Publishers, Oxford., и Flow Cytometry –A basic introduction. Michael G. Ormerod, 2008.
[0182] В некоторых вариантах осуществления, клетки сортируют по фенотипу для дальнейшего анализа. В некоторых вариантах осуществления, клетки различных фенотипов внутри одной и той же композиции клеток сортируют посредством активированной флуоресценцией сортировки клеток (FACS). FACS представляет собой специализированный тип проточной цитометрии, позволяющий сортировку гетерогенной смеси клеток в два или более контейнера, по одной клетке, на основании специфического рассеяния света и флуоресцентных характеристик каждой клетки. Она является полезным научным инструментом, поскольку обеспечивает быструю, объективную и количественную регистрацию флуоресцентных сигналов от индивидуальных клеток, так же как физическое выделение представляющих особенный интерес клеток.
[0183] В некоторых вариантах осуществления, фенотип включает общее количество T–клеток или общее количество CD3+ T–клеток. В конкретных вариантах осуществления, композиция T–клеток, например, терапевтическая композиция T–клеток, содержащая клетки, экспрессирующие рекомбинантный рецептор или CAR, может включать один или несколько различных подтипов T–клеток. В некоторых вариантах осуществления, фенотип представляет собой или включает идентичность подтипа T–клеток. Различные популяции или подтипы T–клеток включают, но без ограничения, эффекторные T–клетки, T–клетки–помощники, T–клетки памяти, регуляторные T–клетки, CD4+ T–клетки, и CD8+ T–клетки. В конкретных вариантах осуществления, подтип T–клеток можно идентифицировать посредством детекции присутствия или отсутствия специфической молекулы. В конкретных вариантах осуществления, специфическая молекула представляет собой поверхностный маркер, который можно использовать для идентификации подтипа T–клеток.
[0184] В некоторых вариантах осуществления, фенотип представляет собой положительный или высокий уровень экспрессии одной или нескольких специфических молекул, которые являются поверхностными маркерами, например, CD3, CD4, CD8, CD28, CD62L, CCR7, CD27, CD127, CD45RA, и/или CD45RO. В конкретных вариантах осуществления, фенотип представляет собой поверхностный маркер T–клеток или субпопуляции, или подгруппы T–клеток, например, на основании положительной экспрессии поверхностного маркера для одного или нескольких поверхностных маркеров, например, CD3+, CD4+, CD8+, CD28+, CD62L+, CCR7+, CD27+, CD127+, CD4+, CD8+, CD45RA+ и/или CD45RO+.
[0185] В конкретных вариантах осуществления, поверхностный маркер показывает экспрессию рекомбинантного рецептора, например, CAR. В конкретных вариантах осуществления, поверхностный маркер представляет собой экспрессию рекомбинантного рецептора, например, CAR, которую, в некоторых аспектах, можно определять с использованием антитела, такого как антиидиотипическое антитело. В некоторых вариантах осуществления, поверхностный маркер, указывающий на экспрессию рекомбинантного рецептора, представляет собой суррогатный маркер. В некоторых вариантах осуществления, суррогатный маркер представляет собой белок, полученный для совместной экспрессии на клеточной поверхности с рекомбинантным рецептором, например, CAR. В конкретных вариантах осуществления, такой суррогатный маркер представляет собой поверхностный белок, модифицированный, чтобы иметь небольшую активность или не иметь активности. В конкретных вариантах осуществления, суррогатный маркер кодирован тем же полинуклеотидом, который кодирует рекомбинантный рецептор, используемым для трансдукции. Неограничивающие примеры суррогатного маркера включают, но без ограничения, укороченный EGFR (EGFRt), укороченный HER2 (tHER2) или простатспецифический мембранный антиген (PSMA), или их модифицированную форму. В некоторых аспектах, маркер, например, суррогатный маркер, включает весь или часть (например, укороченную форму) CD34, NGFR, CD19 или укороченный CD19, например, укороченный не относящийся к человеку CD19, или эпидермальный фактор роста рецептор (например, tEGFR). В конкретных вариантах осуществления, клетка, имеющая поддающееся детекции количество CAR, имеет фенотип, который представляет собой или включает CAR+. В конкретных вариантах осуществления, клетка, имеющая поддающееся детекции количество суррогатного маркера, имеет фенотип, который представляет собой или включает CAR+.
[0186] В конкретных вариантах осуществления, фенотип включает экспрессию, например, поверхностную экспрессию, одного или нескольких из поверхностных маркеров CD3, CD4, CD8 и/или рекомбинантного рецептора (например, CAR) или его суррогатного маркера, показывающего или коррелирующего с экспрессией рекомбинантного рецептора (например, CAR).
[0187] В конкретных вариантах осуществления, фенотип идентифицируют по экспрессии одной или нескольких специфических молекул, которые являются поверхностными маркерами. В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию CD3, CD4, CD8 и/или рекомбинантного рецептора, например, CAR. В конкретных вариантах осуществления, рекомбинантный рецептор представляет собой CAR. В конкретных вариантах осуществления фенотип включает CD3+/CAR+, CD4+/CAR+ и/или CD8+/CAR+.
[0188] В некоторых вариантах осуществления, фенотип представляет собой жизнеспособность. В конкретных вариантах осуществления, фенотип представляет собой положительную экспрессию маркера, показывающую, что клетка подвергается нормальным функциональным клеточным процессам и/или не подвергалась или не подвергается процессу некроза или программируемой гибели клетки. В некоторых вариантах осуществления, жизнеспособность можно оценивать по окислительно–восстановительному потенциалу клетки, целостности мембраны клетки или активности или функции митохондрий. В некоторых вариантах осуществления, жизнеспособность представляет собой отсутствие специфической молекулы, ассоциированной с гибелью клетки, или отсутствие признака гибели клетки в анализе.
[0189] В некоторых вариантах осуществления, фенотип представляет собой или включает жизнеспособность клетки. В конкретных вариантах осуществления, жизнеспособность клеток можно детектировать, измерять и/или оценивать рядом способов, которые являются общепринятыми в данной области. Неограничивающие примеры таких анализов жизнеспособности включают, но без ограничения, анализы поглощения красителя (например, анализы кальцеина AM), анализы жизнеспособности клетки XTT и анализы исключения красителя (например, анализы исключения красителя трипанового синего, эозина или пропидия). Анализы жизнеспособности можно использовать для определения количества или процента (например, частоты) жизнеспособных клеток в дозе клеток, композиции клеток и/или образце клеток. В конкретных вариантах осуществления, фенотип включает жизнеспособность клетки, наряду с другими признаками, например, экспрессией рекомбинантного рецептора.
[0190] В конкретных вариантах осуществления, фенотип представляет собой или включает жизнеспособность клетки, жизнеспособные CD3+, жизнеспособные CD4+, жизнеспособные CD8+, жизнеспособные CD3+/CAR+, жизнеспособные CD4+/CAR+, жизнеспособные CD8+/CAR+ или их комбинацию.
[0191] В конкретных вариантах осуществления, фенотип представляет собой или включает отсутствие апоптоза и/или признака того, что клетка подвергается апоптотическому процессу. Апоптоз представляет собой процесс программируемой гибели клетки, включающий серии стереотипных морфологических и биохимических событий, приводящих к характерным изменениям клетки и гибели. Эти изменения включают пузырение, уменьшение размера клетки, фрагментацию ядра, конденсацию хроматина, фрагментацию хромосомной ДНК и глобальное расщепление мРНК. Апоптоз является хорошо охарактеризованным процессом, и специфические молекулы, ассоциированные с различными стадиями, хорошо известны в данной области.
[0192] В некоторых вариантах осуществления, фенотип представляет собой отсутствие ранней стадии апоптоза, и/или отсутствие индикатора и/или специфической молекулы, ассоциированной с ранней стадией апоптоза. На ранних стадиях апоптоза, изменения клеточной и митохондриальной мембраны становятся очевидными. Биохимические изменения также являются очевидными в цитоплазме и ядре клетки. Например, ранние стадии апоптоза можно показать по активации конкретных каспаз, например, 2, 8, 9 и 10. В конкретных вариантах осуществления, фенотип представляет собой отсутствие поздней стадии апоптоза, и/или отсутствие индикатора и/или специфической молекулы, ассоциированной с поздней стадией апоптоза. Стадии апоптоза от средней до поздней характеризуются дальнейшей потерей целостности мембраны, конденсацией хроматина и фрагментацией ДНК, включают такие биохимические события, как активация каспаз 3, 6 и 7.
[0193] В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию одного или нескольких факторов, ассоциированных с программируемой гибелью клетки. В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию одного или нескольких факторов, ассоциированных с апоптозом, включая проапоптотические факторы, как известно, инициирующие апоптоз, например, члены пути рецептора смерти, активированные члены митохондриального (внутреннего) пути, такие как члены семейства Bcl–2, например, Bax, Bad и Bid, и каспазы. В некоторых вариантах осуществления, фенотип представляет собой отсутствие или низкое количество маркера апоптоза. В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию маркера апоптоза. В конкретных вариантах осуществления, фенотип представляет собой отсутствие индикатора, например, молекулы аннексина V, который предпочтительно связывается с клетками, подвергающимися апоптозу, при инкубации или контакте с композицией клеток. В некоторых вариантах осуществления, фенотип представляет собой или включает экспрессию одного или нескольких маркеров, которые являются показательными для апоптотического состояния в клетке.
[0194] В некоторых вариантах осуществления, фенотип представляет собой отрицательную (или низкую) экспрессию специфической молекулы, являющейся маркером апоптоза. Различные маркеры апоптоза известны специалисту в данной области и включают, но без ограничения, увеличение активности одной или нескольких каспаз, т.е. активированной каспазы, увеличение расщепления PARP, активацию и/или транслокацию белков семейства Bcl–2, члены пути гибели клетки, например, Fas и FADD, присутствие уменьшения размера ядра (например, мониторируемое посредством микроскопа) и присутствие фрагментации хромосомной ДНК (например, присутствие лестницы хромосомной ДНК) или анализы апоптоза, включающие окрашивание TUNEL и окрашивание аннексина V.
[0195] Каспазы представляют собой ферменты, расщепляющие белки после остатка аспарагиновой кислоты, термин происходит от «цистеиновые–аспарагиновокислые протеазы». Каспазы вовлечены в апоптоз, таким образом, активация каспаз, таких как каспаза–3, является показательной для увеличения или возобновления апоптоза. В конкретных вариантах осуществления, активацию каспазы можно детектировать способами, известными специалисту в данной области. В некоторых вариантах осуществления, антитело, которое специфически связывается с активированной каспазой (т.е., специфически связывается с расщепленным полипептидом), можно использовать для детекции активации каспазы. В другом примере, анализ флуорохромного ингибитора активности каспазы (FLICA) можно использовать для детекции активации каспазы–3 посредством детекции гидролиза ацетил–Asp–Glu–Val–Asp–7–амидо–4–метилкумарина (Ac–DEVD–AMC) посредством каспазы–3 (т.е., детекции высвобождения флуоресцентного 7–амино–4–метилкумарина (AMC)). Анализы FLICA можно использовать для определения активации каспазы посредством детекции продукта субстрата, процессируемого множеством каспаз (например, FAM–VAD–FMK FLICA). Другие способы включают анализы каспазы CASPASE–GLO® (PROMEGA), в которых используют люминогенный тетрапептидный субстрат каспазы–8 (Z–LETD–аминолюциферин), тетрапептидный субстрат каспазы–9 (Z–LEHD–аминолюциферин), субстрат каспазы–3/7 (Z–DEVD–аминолюциферин), субстрат каспазы–6 (Z–VEID–аминолюциферин) или субстрат каспазы–2 (Z–VDVAD–аминолюциферин).
[0196] В конкретных вариантах осуществления, фенотип представляет собой или включает отрицательную экспрессию активной каспазы–1, активной каспазы–2, активной каспазы–3, активной каспазы–7, активной каспазы–8, активной каспазы–9, активной каспазы–10 и/или активной каспазы–13 в клетке. В конкретных вариантах осуществления, фенотип представляет собой или включает активная каспаза–3–. В некоторых вариантах осуществления, проформа (расщепляемая зимогеном) форма каспазы, такой как любая из вышеуказанных, также является маркером, показывающим присутствие апоптоза. В некоторых вариантах осуществления, фенотип представляет собой или включает отсутствие или отрицательную экспрессию проформы каспазы, такой как проформа каспазы–3.
[0197] В некоторых вариантах осуществления, маркер апоптоза расщепляет полимеразу 1 поли(АДФ–рибозы) (PARP). PARP расщепляется посредством каспазы в ходе ранних стадий апоптоза. Таким образом, детекция расщепленного пептида PARP является маркером апоптоза. В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию расщепленного PARP.
[0198] В некоторых вариантах осуществления, маркер апоптоза представляет собой реагент, детектирующий признак клетки, ассоциированный с апоптозом. В конкретных вариантах осуществления, реагент представляет собой молекулу аннексина V. В ходе ранних стадий апоптоза липид фосфатидилсерин (PS) транслоцируется от внутреннего к наружному слою плазматической мембраны. PS в норме ограничен внутренней мембраной в здоровых и/или неапоптотических клетках. Аннексин V представляет собой белок, предпочтительно связывающий фосфатидилсерин (PS) с высокой аффинностью. После конъюгации с флуоресцентной меткой или другим репортером, аннексин V можно использовать для быстрой детекции этого раннего индикатора апоптоза на клеточной поверхности. В некоторых вариантах осуществления, присутствие PS на наружной мембране может персистировать на поздних стадиях апоптоза. Таким образом, в некоторых вариантах осуществления, окрашивание аннексина V является показателем как ранних, так и поздних стадий апоптоза. В конкретных вариантах осуществления, аннексин, например, аннексин V, помечают поддающейся детекции меткой и инкубируют с клетками, подвергают воздействию клеток и/или приводят в контакт с клетками из композиции клеток для детекции клеток, которые подвергаются апоптозу, например, посредством проточной цитометрии. В некоторых вариантах осуществления, флуоресцентно меченные аннексины, например, аннексин V, используют для окрашивания клеток для анализа проточной цитометрии, например, с использованием анализа аннексина–V/7–AAD. Альтернативные способы, пригодные для детекции апоптоза с использованием аннексина, включают способы и анализы, в которых используют радиоактивно меченный аннексин V. В конкретных вариантах осуществления, фенотип представляет собой или включает отрицательное окрашивание по аннексину, например, аннексин V–. В конкретных вариантах осуществления, фенотип представляет собой или включает отсутствие PS на наружной плазматической мембране. В конкретных вариантах осуществления, фенотип представляет собой или включает клетки, которые не связываются с аннексином, например, аннексином V. В конкретных вариантах осуществления, клетка, лишенная поддающегося детекции PS на наружной мембране, является аннексин V–. В конкретных вариантах осуществления, клетка, которая не связывается с аннексином V– в анализе, например, проточной цитометрии, после инкубации с меченым аннексином V, является аннексин V–.
[0199] В конкретных вариантах осуществления, фенотип представляет собой аннексин V–, аннексин V– CD3+, аннексин V–CD4+, аннексин V– CD8+, аннексин V–CD3+/CAR+, аннексин V– CD4+/CAR+, аннексин V– CD8+/CAR+, активированная каспаза–3–, активированная каспаза–3–/CD3+, активированная каспаза–3–/CD4+, активированная каспаза–3– /CD8+, активированная каспаза–3–/CD3+/CAR+, активированная каспаза–3–/ CD4+/CAR+, активированная каспаза–3–/CD8+/CAR+ или их комбинацию.
[0200] Конкретные варианты осуществления предусматривают, что клетки, положительные по экспрессии маркера апоптоза, подвергаются программируемой гибели клетки, имеют уменьшенную или отсутствующую иммунную функцию, и если имеют, имеют уменьшенную способность подвергаться активации, размножению, и/или связываться с антигеном для инициации, осуществления или внесения вклада в иммунный ответ или активность. В конкретных вариантах осуществления, фенотип определяют по отрицательной экспрессии активированной каспазы и/или отрицательному окрашиванию по аннексину V.
[0201] В конкретных вариантах осуществления, фенотип представляет собой или включает активированная каспаза–3– (каспаза–3–) и/или аннексин V–.
[0202] В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию одного или нескольких факторов, ассоциированных с воспалительной гибелью клетки. В некоторых вариантах осуществления, воспалительная гибель клетки представляет собой пироптоз. В конкретных вариантах осуществления, пироптоз возникает или потенциально может возникать в инфицированных вирусом и/или трансдуцированных клетках, например, инфицированных вирусом и/или трансдуцированных CD4+ и/или CD8+ T–клетках. В некоторых вариантах осуществления, пироптоз ассоциирован или может быть ассоциирован с одним или несколькими из лизиса клетки, разбухания клетки, формирования пор, фрагментации ДНК и/или активации каспазы–1. В конкретных вариантах осуществления, пироптоз не приводит к пузырению мембраны, активации каспазы–3 и/или высвобождению цитохрома–C.
[0203] В некоторых вариантах осуществления, один или несколько факторов, ассоциированных с пироптозом, представляет собой или включает узнающие паттерн рецепторы, инфламмасомы, активную каспазу–1, активный IL–1b и/или активный IL–18. В некоторых вариантах осуществления, один или несколько факторов представляет собой или включает активированные и/или лигированные рецепторы паттерна. В конкретных вариантах осуществления, один или несколько факторов представляет собой или включает активированные и/или лигированные TLR, NOD–подобные рецепторы, RIG–I, MDA5 и/или STING. В некоторых вариантах осуществления, один или несколько факторов представляет собой или включает активный IL–1b. В конкретных вариантах осуществления, один или несколько факторов представляет собой или включает активный IL–18. В конкретных вариантах осуществления, один или несколько факторов представляет собой или включает активную каспазу–1.
[0204] В конкретных вариантах осуществления, фенотип представляет собой или включает активированная каспаза–1– (каспаза–1–). В некоторых вариантах осуществления, фенотип представляет собой или включает активный IL–1b–. В конкретных вариантах осуществления, фенотип представляет собой или включает активный IL–18–.
[0205] В конкретных вариантах осуществления, воспалительная гибель клетки представляет собой или включает некроптоз. В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию одного или нескольких факторов, ассоциированных с некроптозом. В некоторых вариантах осуществления, некроптоз представляет собой программируемую некротическую гибель клетки, управляемую активацией семейства киназ RIP. В некоторых вариантах осуществления, некроптоз возникает или может возникать после связывания и/или активации семейства рецепторов TNF, и/или после привлечения узнающих паттерн рецепторов (т.е. связывания вирусных компонентов с RIG–I/MDA5 или в родственных путях). В некоторых вариантах осуществления, продукция TNFα в ходе вирусной инфекции приводит к стимуляции его рецептора TNFR1, активации ассоциированного с TNFR белка смерти TRADD, который, в свою очередь, активирует RIPK1 для привлечения RIPK3 для формирования некросомы. В некоторых вариантах осуществления, формирование некросомы приводит к фосфорилированию MLKL и олигомеризации MLKL, позволяющие MLKL встраиваться и проникать в плазматические мембраны и органеллы. В некоторых вариантах осуществления, интеграция MLKL приводит к воспалительному фенотипу и высвобождению ассоциированных с повреждением молекулярных паттернов (DAMP), вызывающих иммунные ответы.
[0206] В некоторых вариантах осуществления, один или несколько факторов, ассоциированных с некроптозом, представляет собой активированные и/или лигированные узнающие паттерн рецепторы, например, активированные и/или лигированные RIG–I/MDA5, активированный TNFR1, TRADD, некросому и/или фосфорилированный и/или олигомеризованный MLKL. В некоторых вариантах осуществления, один или несколько факторов, ассоциированных с некроптозом, представляет собой или включает активированную киназу RIP, например, RIPK1, RIPK2, RIPK3, RIPK4 и/или RIPK5. В некоторых вариантах осуществления, один или несколько факторов представляет собой активированный RIPK1 и/или RIPK3. В некоторых вариантах осуществления, фенотип представляет собой или включает активированный RIPK1–, активированный RIPK3–, фосфорилированный MLKL– и/или олигомеризованный MLKL–.
[0207] В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию одного или нескольких факторов, ассоциированных с аутофагией. В некоторых вариантах осуществления, аутофагия представляет собой или включает свойственный клеткам катаболический механизм, который возникает и/или может возникать в определенных условиях культивирования клеток, например, в условиях, когда критические питательные вещества ограничены, и/или в ответ на определенные цитокины. В некоторых вариантах осуществления, аутофагия возникает независимо от активности каспазы.
[0208] В некоторых вариантах осуществления, аутофагия представляет собой макро–аутофагию, микро–аутофагию и/или опосредованную шаперонами аутофагию. В некоторых вариантах осуществления, один или несколько факторов, ассоциированных с маркером аутофагии, включают AMPK, ULK1, ULK2 и/или другие члены семейства Atg (например, ATG16L), PIK3C3, BECN1, Vps34, Beclin–1, MAP1LC3A, B,C, GABARAP, GABARAPL1, GABARAPL2, UVRAG, IRGM, CLN3, Parkin, p62 и LAMP2, и/или другие известные факторы, такие как описано в Behrends, Nature. 2010 Jul l;466(7302):68–76 и Glick et al. J Pathol. 2010 May;221(l):3–12. В некоторых вариантах осуществления, фенотип представляет собой AMPK–, ULK1–, ULK2–, PIK3C3–, BECN1–, Vps34–, Beclin–1–, MAP1LC3A–, MAP1LC3B–, MAP1LC3C–, GABARAP–, GABARAPL1–, GABARAPL2–, UVRAG–, IRGM–, CLN3–, Parkin–, p62– и/или LAMP2–.
[0209] Среди фенотипов присутствуют экспрессия или поверхностная экспрессия одного или нескольких маркеров, как правило, ассоциированных с одним или несколькими подтипами или субпопуляциями T–клеток или их фенотипами. Подтипы и субпопуляции T–клеток могут включать CD4+ и/или CD8+ T–клетки и их подтипы, которые могут включать наивные T–клетки (TN), эффекторные T–клетки (TЭФФ), T–клетки памяти и их подтипы, такие как стволовые T–клетки памяти (TSCM), T–клетки памяти (TCM), эффекторные T–клетки памяти (TEM), клетки TEMRA или терминально дифференцированные эффекторные T–клетки памяти, инфильтрующие опухоль лимфоциты (TIL), незрелые T–клетки, зрелые T–клетки, T–клетки–помощники, цитотоксические T–клетки, ассоциированные со слизистыми оболочками инвариантные T–клетки (MAIT), природные и адаптивные регуляторные T–клетки (T–рег), T–клетки–помощники, такие как TH1–клетки, TH2–клетки, TH3–клетки, TH17–клетки, TH9–клетки, TH22–клетки, фолликулярные T–клетки–помощники, альфа/бета–T–клетки и дельта/гамма T–клетки.
[0210] В некоторых вариантах осуществления, фенотип представляет собой или включает фенотип T–клеток памяти или подгруппы T–клеток памяти. T–клетки памяти представляют собой антигенспецифические T–клетки, ранее подвергнутые воздействию родственного им антигена. T–клетки памяти длительно персистируют после разрешения инфекции. T–клетки памяти быстро размножаются до больших количеств эффекторных T–клеток после повторного воздействия родственного им антигена, таким образом, обеспечивая иммунную систему «памятью» против прошедших инфекций. T–клетки памяти содержат три подтипа: центральные T–клетки памяти (TCM–клетки) и два типа эффекторных T–клеток памяти (TEM–клетки и TEMRA–клетки). В некоторых вариантах осуществления фенотип представляет собой или включает фенотип T–клетки памяти (или один или несколько ассоциированных с ним маркеров), такой как TCM–клетка, TEM–клетка или TEMRA–клетка, стволовая T клетка памяти (TSCM) или их комбинацию. В конкретных вариантах осуществления, фенотип представляет собой или включает экспрессию одной или нескольких специфических молекул, являющихся маркером T–клеток памяти и/или T–клеток памяти, или их подтипов.
[0211] В конкретных вариантах осуществления, фенотип представляет собой или включает экспрессию одной или нескольких специфических молекул, являющихся маркером наивных T–клеток. Наивные T–клеток включают свежие T–клетки, которые образованы в костном мозге и являются способными отвечать на новые встретившиеся патогены, содержащие антигены, ранее не процессированные иммунной системой. После стимуляции родственным им антигеном, часть активированных наивных T–клеток развивается в клетки памяти.
[0212] В некоторых вариантах осуществления, фенотип представляет собой или включает T–клетку памяти или наивную T–клетку. В конкретных вариантах осуществления, фенотип представляет собой положительную или отрицательную экспрессию одной или нескольких специфических молекул, которые являются маркерами памяти. В некоторых вариантах осуществления, маркер памяти представляет собой специфическую молекулу, которую можно использовать для определения популяция T–клеток памяти.
[0213] В некоторых вариантах осуществления, фенотип представляет собой или включает фенотип одного или нескольких маркеров, ассоциированных с T–клеткой, не относящейся к T–клетке памяти или ее подтипу; в некоторых аспектах, он представляет собой или включает фенотип или маркер(ы), ассоциированные с наивной клеткой. В некоторых вариантах осуществления, фенотип представляет собой CCR7+/CD27+/CD28+/CD45RA+. В конкретных вариантах осуществления, фенотип представляет собой или включает CCR7+/CD45RA+. В некоторых вариантах осуществления, фенотип представляет собой или включает фенотип T–клетки памяти. В конкретных вариантах осуществления, фенотип представляет собой или включает CCR7+/CD27+/CD28+/CD45RA−. В некоторых вариантах осуществления, фенотип представляет собой или включает эффекторную клетку памяти. В некоторых вариантах осуществления, фенотип представляет собой или включает CCR7−/CD27+/CD28+/CD45RA−. В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип TEMRA–клетки или TSCM–клетки. В конкретных вариантах осуществления, фенотип представляет собой или включает CD45RA+. В конкретных вариантах осуществления, фенотип представляет собой или включает CCR7−/CD27−/CD28−/CD45RA+. В некоторых вариантах осуществления, фенотип представляет собой или включает один из CD27+/CD28+, CD27−/CD28+, CD27+/CD28− или CD27−/CD28−.
[0214] В некоторых вариантах осуществления фенотип представляет собой или включает любое из предшествующих фенотипических свойств и дополнительно включает экспрессию рекомбинантного рецептора, например, фенотип, который ассоциирован с T–клеткой памяти или подтипом T–клетки памяти и который экспрессирует CAR, или фенотип, ассоциированный с наивной клеткой, которая экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип T–клетки памяти или стволовой T–клетки памяти, которая экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип эффекторной клетки памяти, которая экспрессирует CAR. В некоторых вариантах осуществления, фенотип представляет собой или включает фенотип клетки TEMRA, которая экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает CAR+/CCR7+/CD27+/CD28+/CD45RA−; CAR+/CCR7−/CD27+/CD28+/CD45RA−; CAR+/CCR7−/CD27−/CD28−/CD45RA+; CAR+/CD27+/CD28+; CAR+/CD27−/CD28+; CAR+/CD27+/CD28−; или CAR+/CD27−/CD28−.
[0215] В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип T–клетки, которая является отрицательной по маркеру апоптоза. В конкретных вариантах осуществления, фенотип представляет собой или включает наивную клетку, которая является отрицательной по маркеру апоптоза. В некоторых вариантах осуществления, маркер апоптоза представляет собой активированную каспазу–3. В некоторых вариантах осуществления, маркер апоптоза представляет собой положительное окрашивание по аннексину V.
[0216] В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип T–клетки памяти или ее подтипа, отрицательного по маркеру апоптоза, который экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип T–клетки памяти или конкретного подтипа, отрицательного по маркеру апоптоза, который экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает наивную клетку, которая является отрицательной по маркеру апоптоза, которая экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип T–клетки памяти или TSCM–клетки, или наивной клетки, которая является отрицательной по маркеру апоптоза, которая экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает фенотип эффекторной клетки памяти, которая является отрицательной по маркеру апоптоза, которая экспрессирует CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает аннексин V−/CAR+/CCR7+/CD27+/CD28+/CD45RA−; аннексин V− /CAR+/CCR7−/CD27+/CD28+/CD45RA−; аннексин V−/CAR+/CCR7−/CD27−/CD28−/CD45RA+; аннексин V− /CAR+/CD27+/CD28+; аннексин V−/CAR+/CD27−/CD28+; аннексин V−/CAR+/CD27+/CD28−; или аннексин V−/CAR+/CD27−/CD28−. В конкретных вариантах осуществления, фенотип представляет собой или включает активированная каспаза–3−/CAR+/CCR7+/CD27+/CD28+/CD45RA−; активированная каспаза–3−/CAR+/CCR7−/CD27+/CD28+/CD45RA−; активированная каспаза–3−/CAR+/CCR7−/CD27−/CD28−/CD45RA+; активированная каспаза–3−/CAR+/CD27+/CD28+; активированная каспаза–3−/CAR+/CD27−/CD28+; активированная каспаза–3−/CAR+/CD27+/CD28−; или активированная каспаза–3−/CAR+/CD27−/CD28−.
[0217] В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера истощения. Истощение T–клетки представляет собой состояние дисфункции T–клетки, которое возникает во время множества хронических инфекций и злокачественных опухолей. Его определяют по плохой эффекторной функции, длительной экспрессии ингибирующих рецепторов и состоянию транскрипции, отличному от состояния функциональных эффекторных T–клеток или T–клеток памяти. Истощение предотвращает оптимальный контроль инфекции и опухолей. В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию специфической молекулы, ассоциированной с истощением. В конкретных вариантах осуществления, специфическая молекула представляет собой любую молекулу, ассоциированную с истощением, или количество, ассоциированное с истощением, например, плохой эффекторной функцией или экспрессией ингибирующего рецептора. В конкретных вариантах осуществления, фенотип представляет собой положительную или отрицательную экспрессию ингибитора иммунной контрольной точки. В конкретных вариантах осуществления, маркер истощения представляет собой CTLA–4, FOXP3, PD–1, TIGIT, LAB–3, 2B4, BTLA, TIM3, VISTA или CD96, или их комбинацию. В конкретных вариантах осуществления, фенотип представляет собой положительную или отрицательную экспрессию CTLA–4, FOXP3, PD–1, TIGIT, LAB–3, 2B4, BTLA, TIM3, VISTA или CD96, или их комбинацию. В конкретных вариантах осуществления, фенотип представляет собой положительную или отрицательную экспрессию PD1 и/или FOXP3.
[0218] В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию специфической молекулы, ассоциированной с активацией T–клетки. В некоторых вариантах осуществления, фенотип представляет собой или включает отрицательную экспрессию одной или нескольких из специфических молекул, являющихся маркером активации. Активация T–клетки относится к стимуляции иммунного ответа T–клетки, после стимуляции последней посредством антигенпредставляющей клетки (APC). Этот основанный на взаимодействии путь объясняет основные стимулирующие сигналы, запускающие активацию T–клетки, так же как ее нижестоящие пути. Как правило, активация T–клетки требует двух одновременных сигналов. Первый представляет собой связывание комплекса T–клеточного рецептора (TCR) с молекулой главного комплекса гистосовместимости (MHC), несущей пептидный антиген. Второй обеспечивается связыванием костимулирующего рецептора CD28 с белками на поверхности APC, такими как B7–2 или B7–1. В конкретных вариантах осуществления, специфическая молекула ассоциирована с активацией TCR, например, активируется, изменяется или экспрессируется в результате активации T–клетки. В некоторых вариантах осуществления, специфическая молекула ассоциирована с активацией рецептора CD28, например, молекула, которая активируется, изменяется или экспрессируется в результате активации T–клетки.
[0219] В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера истощения. Истощение T–клетки представляет собой состояние дисфункции T–клетки, которое возникает во время множества хронических инфекций и злокачественных опухолей. Его определяют по плохой эффекторной функции, длительной экспрессии ингибирующих рецепторов и состоянию транскрипции, отличному от состояния функциональных эффекторных T–клеток или T–клеток памяти. Истощение предотвращает оптимальный контроль инфекции и опухолей. В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию специфической молекулы, ассоциированной с истощением. В конкретных вариантах осуществления, специфическая молекула представляет собой любую молекулу, ассоциированную с истощением, или количество, ассоциированное с истощением, например, плохой эффекторной функцией или экспрессией ингибирующего рецептора. В конкретных вариантах осуществления, фенотип представляет собой положительную или отрицательную экспрессию ингибитора иммунной контрольной точки. В конкретных вариантах осуществления, маркер истощения представляет собой CTLA–4, FOXP3, PD–1, TIGIT, LAB–3, 2B4, BTLA, TIM3, VISTA или CD96, или их комбинацию. В конкретных вариантах осуществления, фенотип представляет собой положительную или отрицательную экспрессию CTLA–4, FOXP3, PD–1, TIGIT, LAB–3, 2B4, BTLA, TIM3, VISTA или CD96, или их комбинацию. В конкретных вариантах осуществления, фенотип представляет собой положительную или отрицательную экспрессию PD1 и/или FOXP3.
[0220] В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера истощения в CD3+ клетке, которая экспрессирует рекомбинантный рецептор или CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера истощения в CD4+ клетке, которая экспрессирует рекомбинантный рецептор или CAR. В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера истощения и CD3+, и положительную экспрессию рекомбинантного рецептора или CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера истощения в CD4+ клетке, которая экспрессирует рекомбинантный рецептор или CAR. В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера истощения в CD8+ клетке, которая экспрессирует рекомбинантный рецептор или CAR. В конкретных вариантах осуществления, маркер истощения представляет собой один или несколько из CTLA–4, FOXP3, PD–1, TIGIT, LAB–3, 2B4, BTLA, TIM3, VISTA или CD96. В конкретных вариантах осуществления, маркер истощения представляет собой PD1 и/или FOXP3.
[0221] В конкретных вариантах осуществления, фенотип представляет собой или включает PD1–/CD3+, PD1–/CD4+, PD1–/CD8+, PD1–/CD3+/CAR+, PD1–/CD4+/CAR+, PD1–/CD8+/CAR+, PD1–/аннексин V–, PD1–/аннексин V–/CD3+, PD1–/аннексин V–/CD4+, PD1–/аннексин V–/CD8+, PD1–/аннексин V/–CD3+/CAR+, PD1–/аннексин V–/ CD4+/CAR+, PD1–/аннексин V–/CD8+/CAR+, PD1–/активированная каспаза–3–, PD1–/активированная каспаза–3–/CD3+, PD1–/активированная каспаза–3–/CD4+, PD1–/активированная каспаза–3– /CD8+, PD1–/активированная каспаза–3–/CD3+/CAR+, PD1–/активированная каспаза–3–/ CD4+/CAR+, PD1–/активированная каспаза–3–/CD8+/CAR+ или их комбинацию.
[0222] В конкретных вариантах осуществления, фенотип представляет собой или включает FOXP3–/CD3+, FOXP3–CD4+, FOXP3–/CD8+, FOXP3–/CD3+/CAR+, FOXP3–/CD4+/CAR+, FOXP3–/CD8+/CAR+, FOXP3–/аннексин V–, FOXP3–/аннексин V–/CD3+, FOXP3–/аннексин V–/CD4+, FOXP3–/аннексин V–/CD8+, FOXP3–/аннексин V/–CD3+/CAR+, FOXP3–/аннексин V–/ CD4+/CAR+, FOXP3–/аннексин V–/CD8+/CAR+, FOXP3–/активированная каспаза–3–, FOXP3–/активированная каспаза–3–/CD3+, FOXP3–/активированная каспаза–3–/CD4+, FOXP3–/активированная каспаза–3– /CD8+, FOXP3–/активированная каспаза–3–/CD3+/CAR+, FOXP3–/активированная каспаза–3–/ CD4+/CAR+, FOXP3–/активированная каспаза–3–/CD8+/CAR+ или их комбинацию.
[0223] В конкретных вариантах осуществления, фенотип представляет собой отрицательную экспрессию специфической молекулы, ассоциированной с активацией T–клетки. В некоторых вариантах осуществления, фенотип представляет собой или включает отрицательную экспрессию одной или нескольких из специфических молекул, являющихся маркером активации. Активация T–клетки относится к стимуляции иммунного ответа T–клетки, после стимуляции последней посредством антигенпредставляющей клетки (APC). Этот основанный на взаимодействии путь объясняет основные стимулирующие сигналы, запускающие активацию T–клетки, так же как ее нижестоящие пути. Как правило, активация T–клетки требует двух одновременных сигналов. Первый представляет собой связывание комплекса T–клеточного рецептора (TCR) с молекулой главного комплекса гистосовместимости (MHC), несущей пептидный антиген. Второй обеспечивается связыванием костимулирующего рецептора CD28 с белками на поверхности APC, такими как B7–2 или B7–1. В конкретных вариантах осуществления, специфическая молекула, ассоциированная с активацией TCR, например, активируется, изменяется или экспрессируется в результате активации T–клетки. В некоторых вариантах осуществления, специфическая молекула, ассоциированная с активацией рецептора CD28, например, молекула, которая активируется, изменяется или экспрессируется в результате активации T–клетки.
[0224] В конкретных вариантах осуществления, фенотип представляет собой или включает отрицательную экспрессию одной или нескольких из специфических молекул, являющихся маркером активации. В конкретных вариантах осуществления, маркер активации представляет собой один или несколько из CD25, CD26, CD27, CD28, CD30, CD71, CD154, CD40L, CD127, LAG3, Ki67, или их комбинацию. В конкретных вариантах осуществления, фенотип представляет собой отрицательную или положительную экспрессию одного или нескольких из CD25, CD26, CD27, CD28, CD30, CD71, CD154, CD40L, CD127, LAG3 или Ki67. В конкретных вариантах осуществления, фенотип представляет собой или включает экспрессию CD25, CD127, LAG3, Ki67 или их комбинацию.
[0225] В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера активации в CD3+ клетке, которая экспрессирует рекомбинантный рецептор или CAR. В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера активации в CD4+ клетке, которая экспрессирует рекомбинантный рецептор или CAR. В некоторых вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера активации в CD8+ клетке, которая экспрессирует рекомбинантный рецептор или CAR. В конкретных вариантах осуществления, маркер активации представляет собой один или несколько из CD25, CD26, CD27, CD28, CD30, CD71, CD154, CD40L, CD127, LAG3 или Ki67. В конкретных вариантах осуществления, маркер активации представляет собой CD25, CD127, LAG3, Ki67 или их комбинацию.
[0226] В конкретных вариантах осуществления, фенотип представляет собой или включает положительную или отрицательную экспрессию маркера активации и CD3+, CD4+, CD8+, CD3+/CAR+, CD4+/CAR+, CD8+/CAR+, аннексин V–, аннексин V–/CD3+, аннексин V–/CD4+, аннексин V–/CD8+, аннексин V/–CD3+/CAR+, аннексин V–/ CD4+/CAR+, аннексин V–/CD8+/CAR+, активированная каспаза–3–, активированная каспаза–3–/CD3+, активированная каспаза–3–/CD4+, активированная каспаза–3– /CD8+, активированная каспаза–3–/CD3+/CAR+, активированная каспаза–3–/ CD4+/CAR+, активированная каспаза–3–/CD8+/CAR+ или их комбинацию.
[0227] В некоторых вариантах осуществления, фенотип оценивают по ответу на стимул, например, стимул, который стимулирует, запускает, индуцирует, стимулирует или продлевает функцию иммуноцита. В конкретных вариантах осуществления, клетки инкубируют в присутствии стимулирующих условий или стимулирующего средства, фенотип представляет собой или включает ответ на стимуляцию. В конкретных вариантах осуществления, фенотип представляет собой или включает продукцию или секрецию растворимого фактора в ответ на одну или несколько стимуляций. В некоторых вариантах осуществления, фенотип представляет собой или включает отсутствие продукции или секреции растворимого фактора в ответ на одну или несколько стимуляций. В конкретных вариантах осуществления, растворимый фактор представляет собой цитокин.
[0228] В некоторых вариантах осуществления, стимулирующие условия могут включать одно или несколько из конкретных сред, температуры, содержания кислорода, содержания диоксида углерода, времени, средств, например, питательных веществ, аминокислот, антибиотиков, ионов и/или стимулирующих факторов, таких как цитокины, хемокины, антигены, связывающие паттерны, слитые белки, рекомбинантные растворимые рецепторы и любые другие средства, разработанные для активации клеток. В некоторых вариантах осуществления, клетки стимулируют, и фенотип определяют по тому, продуцируется ли или секретируется ли, или нет, растворимый фактор, например, цитокин или хемокин. В некоторых вариантах осуществления, стимуляция является неспецифической, т.е., не является антигенспецифической стимуляцией. В некоторых вариантах осуществления, клетки инкубируют в присутствии стимулирующих условий или стимулирующего средства в течение приблизительно 1 часа, приблизительно 2 часов, приблизительно 3 часов, приблизительно 4 часов, приблизительно 5 часов, приблизительно 6 часов, приблизительно 7 часов, приблизительно 8 часов, приблизительно 9 часов, приблизительно 10 часов, приблизительно 11 часов, приблизительно 12 часов, приблизительно 18 часов, приблизительно 24 часов, приблизительно 48 часов, или в течение периода времени между 1 часом и 4 часами, между 1 часом и 12 часами, между 12 часами и 24 часами, включая каждое, или в течение более чем 24 часов.
[0229] В некоторых вариантах осуществления, клетки стимулируют с использованием средства, представляющего собой антиген или его эпитоп, который является специфическим для рекомбинантного рецептора, или представляющего собой антитело или его фрагмент, которые связывают и/или узнают рекомбинантный рецептор, или их комбинацию. В некоторых вариантах осуществления, рекомбинантный рецептор представляет собой CAR, и средство представляет собой антиген или его эпитоп, которые являются специфическими для CAR, или представляет собой антитело или его фрагмент, которые связывают и/или узнают CAR, или их комбинацию. В конкретных вариантах осуществления, клетки стимулируют посредством инкубации клеток в присутствии клеток–мишеней с поверхностной экспрессией антигена, узнаваемого CAR. В конкретных вариантах осуществления, рекомбинантный рецептор представляет собой CAR, и средство представляет собой антитело или его активный фрагмент, вариант или их часть, которые связывают CAR. В конкретных вариантах осуществления, антитело или его активный фрагмент, вариант или их часть, которые связывают CAR, представляют собой антиидиотипическое (анти–ID) антитело.
[0230] В некоторых вариантах осуществления, стимулирующие условия или средства включают одно или несколько средств, например, лиганд, способный активировать внутриклеточный передающий сигналы домен комплекса TCR. В некоторых аспектах, средство запускает или инициирует внутриклеточный каскад передачи сигналов TCR/CD3 в T–клетке. Такие средства могут включать антитела, такие как антитела, специфические для компонента TCR и/или костимулирующего рецептора, например, антитело против CD3, антитело против CD28, например, связанное с твердой подложкой, такой как бусина, и/или один или несколько цитокины. В некоторых вариантах осуществления одно или несколько средствs представляют собой PMA и иономицин.
[0231] В конкретных вариантах осуществления, фенотип представляет собой или включает продукцию или секрецию цитокина в ответ на одну или несколько стимуляций. Продукция и/или секреция цитокинов вносит вклад иммунные ответы и вовлечена в различные процессы, включая индукцию противовируснных белков и индукцию пролиферации T–клетки. Цитокины не являются предварительно образованными факторами, но быстро продуцируются и секретируются в ответ на клеточную активацию. The продукцию или секрецию цитокинов можно измерять, детектировать и/или количественно оценивать любым пригодным способом, известным в данной области.
[0232] В конкретных вариантах осуществления, фенотип представляет собой продукцию одного или нескольких цитокинов. В конкретных вариантах осуществления, продукцию одного или нескольких цитокинов измеряют, детектируют и/или количественно оценивают посредством окрашивания внутриклеточных цитокинов. Окрашивание внутриклеточных цитокинов (ICS) посредством проточной цитометрии является способом, хорошо подходящим для исследования продукции цитокина на уровне отдельной клетки. Оно детектирует продукцию и накопление цитокинов в эндоплазматическом ретикулуме после стимуляции клетки, позволяя идентификацию популяций клеток, которые являются положительными или отрицательными по продукции конкретного цитокина, или разделение клеток с высокой продукцией и низкой продукцией на основании порога. ICS также можно использовать в комбинации с другими способами проточной цитометрии для иммунофенотипирования с использованием поверхностных маркеров клетки или с использованием мультимеров MHC для оценки продукции цитокинов в конкретной подгруппе клеток, что делает его необычайно гибким и многофункциональным способом. Другие способы на основе отдельных клеток для измерения или детекции продукции цитокинов включают, но без ограничения, ELISPOT, предельное разведение и клонирование T–клеток.
[0233] В некоторых вариантах осуществления, фенотип представляет собой продукцию цитокина. В конкретных вариантах осуществления, фенотип представляет собой отсутствие продукции цитокина. В конкретных вариантах осуществления, фенотип представляет собой положительный по продукции или представляет собой высокий уровень продукции цитокина. В конкретных вариантах осуществления, фенотип представляет собой отрицательный по продукции или представляет собой низкий уровень продукции цитокина. Цитокины могут включать, но без ограничения, IL–1, IL–1β, IL–2, sIL–2Ra, IL–3, IL–5, IL–6, IL–7, IL–8, IL–10, IL–12, IL–13, IL 27, IL–33, IL–35, TNF, TNF–альфа, CXCL2, CCL2, CCL3, CCL5, CCL17, CCL24, PGD2, LTB4, интерферон гамма (IFN–γ), гранулоцитарно–макрофагальный колониестимулирующий фактор (GM–CSF), воспалительный белок макрофагов (MIP)–1a, MIP–1b, Flt–3L, фракталкин и/или IL–5.
[0234] В некоторых вариантах осуществления, фенотип представляет собой или включает продукцию цитокина. В конкретных вариантах осуществления, фенотип представляет собой или включает продукцию более чем одного цитокина. В конкретных вариантах осуществления, фенотип представляет собой или включает отсутствие продукции одного или нескольких цитокинов. В конкретных вариантах осуществления, фенотип представляет собой или включает продукцию или ее отсутствие, для одного или нескольких из IL–2, IL–13, IFN–гамма, или TNF–альфа. В некоторых вариантах осуществления, фенотип представляет собой присутствие продукции, и/или присутствие высокого уровня продукции цитокина. В некоторых вариантах осуществления, фенотип представляет собой низкую, уменьшенную или отсутствующую продукцию цитокина.
[0235] В некоторых вариантах осуществления, фенотип представляет собой или включает внутреннюю (внутриклеточную) продукцию цитокина, например, как оценено в присутствии стимулирующего средства или в стимулирующих условиях, когда секрецию предотвращают или ингибируют. В конкретных вариантах осуществления, фенотип представляет собой или включает лишение или отсутствие внутренней продукции цитокина. В конкретных вариантах осуществления, фенотип представляет собой или включает внутреннее количество одного или нескольких цитокинов, когда продукцию более чем одного цитокина оценивают с использованием анализа ICS. В конкретных вариантах осуществления, фенотип представляет собой или включает внутренний уровень одного или нескольких из IL–2, IL–13, IFN–гамма или TNF–альфа, как оценено с использованием анализа ICS. В некоторых вариантах осуществления, фенотип представляет собой или включает низкий внутренний уровень или отсутствие поддающегося детекции количества одного или нескольких цитокинов, как оценено с использованием анализа ICS. В конкретных вариантах осуществления, фенотип представляет собой или включает низкий внутренний уровень или отсутствие поддающегося детекции количества IL–2, IL–13, IFN–гамма или TNF–альфа, как оценено с использованием анализа ICS.
[0236] Конкретные варианты осуществления предусматривают, что фенотип может включать продукцию цитокина или отсутствие или низкий уровень продукции цитокина. Это может зависеть от нескольких факторов, которые включают, но без ограничения, идентичность цитокина, анализ, проведенный для детекции цитокина, и стимулирующее средство или условие, используемое в сочетании с анализом. Например, в некоторых вариантах осуществления предусматривают, что фенотип представляет собой или включает отсутствие или низкий уровень продукции IL–13, как показано посредством ICS, в то время как, в некоторых вариантах осуществления, фенотип представляет собой или включает продукцию IFN–гамма, как показано посредством ICS.
[0237] В некоторых вариантах осуществления, фенотип представляет собой или включает продукцию одного или нескольких цитокинов и любой из CD3+, CD4+, CD8+, CD3+/CAR+, CD4+/CAR+, CD8+/CAR+, аннексин V–, аннексин V– CD3+, аннексин V–CD4+, аннексин V– CD8+, аннексин V–CD3+/CAR+, аннексин V– CD4+/CAR+, аннексин V– CD8+/CAR+, активированная каспаза–3–, активированная каспаза–3–/CD3+, активированная каспаза–3–/CD4+, активированная каспаза–3– /CD8+, активированная каспаза–3–/CD3+/CAR+, активированная каспаза–3–/ CD4+/CAR+ или активированная каспаза–3–/CD8+/CAR+ или их комбинацию. В конкретных вариантах осуществления, фенотип представляет собой или включает продукцию одного или нескольких цитокинов в CD4+/CAR+ и/или CD8+/CAR+.
[0238] В некоторых вариантах осуществления, фенотип представляет собой или включает отсутствие продукции одного или нескольких цитокинов. В конкретных вариантах осуществления, фенотип представляет собой или включает отсутствие продукции одного или нескольких цитокинов и любой из CD3+, CD4+, CD8+, CD3+/CAR+, CD4+/CAR+, CD8+/CAR+, аннексин V–, аннексин V– CD3+, аннексин V–CD4+, аннексин V– CD8+, аннексин V–CD3+/CAR+, аннексин V– CD4+/CAR+, аннексин V– CD8+/CAR+, активированная каспаза–3–, активированная каспаза–3–/CD3+, активированная каспаза–3–/CD4+, активированная каспаза–3– /CD8+, активированная каспаза–3–/CD3+/CAR+, активированная каспаза–3–/ CD4+/CAR+ или активированная каспаза–3–/CD8+/CAR+, или их комбинацию.
[0239] В конкретных вариантах осуществления, фенотип представляет собой или включает присутствие или отсутствие внутреннего уровня одного или нескольких из IL–2, IL–13, IFN–гамма или TNF–альфа, как оценено с использованием анализа ICS, и одного или нескольких специфических маркеров для подгруппы клеток или клеток конкретного типа клеток. В некоторых вариантах осуществления, фенотип представляет собой или включает продукцию или ее отсутствие для одного или нескольких из IL–2, IL–13, IFN–гамма или TNF–альфа и CD4+/CAR+ и/или CD8+/CAR+. В конкретных вариантах осуществления, фенотип представляет собой или включает продукцию IL–2 и CD4+/CAR+ и/или CD8+/CAR+. В некоторых вариантах осуществления, фенотип представляет собой или включает отсутствие или низкую продукцию IL–2 и CD4+/CAR+, и/или CD8+/CAR+. В некоторых вариантах осуществления, фенотип представляет собой или включает продукцию IL–13 и CD4+/CAR+ и/или CD8+/CAR+. В некоторых вариантах осуществления, фенотип представляет собой или включает продукцию IL–13 и CD4+/CAR+ и/или CD8+/CAR+. В конкретных вариантах осуществления, фенотип представляет собой или включает отсутствие или низкую продукцию IL–13 и CD4+/CAR+ и/или CD8+/CAR+. В некоторых вариантах осуществления, фенотип представляет собой или включает продукцию IFN–гамма и CD4+/CAR+ и/или CD8+/CAR+. В конкретных вариантах осуществления, фенотип представляет собой или включает продукцию TNF–альфа и CD4+/CAR+ и/или CD8+/CAR+. В конкретных вариантах осуществления, фенотип представляет собой или включает отсутствие или низкую продукцию TNF–альфа и CD4+/CAR+ и/или CD8+/CAR+.
[0240] Любой один или несколько фенотипов, отдельно или в комбинации, можно оценивать или определять в соответствии с представленными способами. В некоторых вариантах осуществления, фенотип представляет собой CD3+, CD3+/CAR+, CD4+/CAR+, CD8+/CAR+ или их комбинацию.
[0241] В конкретных вариантах осуществления, фенотип представляет собой или включает CD3+. В конкретных вариантах осуществления, фенотип представляет собой или включает CD3+/CAR+. В некоторых вариантах осуществления, фенотип представляет собой или включает CD8+/CAR+. В конкретных вариантах осуществления, фенотип представляет собой или включает
[0242] В конкретных вариантах осуществления, фенотип представляет собой или включает аннексин–/CD3+/ CAR+. В некоторых вариантах осуществления, фенотип представляет собой или включает аннексин–/CD4+/CAR+ В конкретных вариантах осуществления, фенотип представляет собой аннексин–/CD8+/CAR.
[0243] В конкретных вариантах осуществления, фенотип представляет собой или включает отсутствие или низкий уровень внутриклеточного IL–2 и CD4+/CAR+. В конкретных вариантах осуществления, фенотип представляет собой отсутствие или низкий уровень внутриклеточного IL–13 и CD4+/CAR+. В некоторых вариантах осуществления, фенотип представляет собой отсутствие или низкий уровень внутриклеточной экспрессии IL–13 и CD8+/CAR+ клетки. В конкретных вариантах осуществления, фенотип представляет собой отсутствие или низкий уровень внутриклеточного TNF–альфа CD4+/CAR+.
[0244] В конкретных вариантах осуществления, фенотип представляет собой или включает CD8+/CAR+. В конкретных вариантах осуществления, фенотип представляет собой или включает аннексин–/CD8+/CAR+.
[0245] В конкретных вариантах осуществления, количество, кратное или фракцию клеток конкретного фенотипа из композиции клеток определяют, измеряют, получают, детектируют, наблюдают и/или идентифицируют. В некоторых вариантах осуществления, композиция клеток представляет собой композицию T–клеток. В конкретных вариантах осуществления, композиция клеток содержит клетки, экспрессирующие рекомбинантный рецептор, например, CAR. В конкретных вариантах осуществления, композиция клеток представляет собой терапевтическую композицию T–клеток, содержащую клетки, экспрессирующие рекомбинантный рецептор, которую можно вводить индивиду для лечения заболевания или состояния. В конкретных вариантах осуществления, количество клеток фенотипа представляет собой общее количество клеток фенотипа в композиции клеток. В конкретных вариантах осуществления, количество клеток фенотипа представляет собой общее количество клеток этого фенотипа, присутствующее в дозе композиции клеток. В конкретных вариантах осуществления, количество клеток этого фенотипа представляет собой количество клеток этого фенотипа, присутствующее в образце композиции клеток. В некоторых вариантах осуществления, количество клеток фенотипа можно выражать как частоту, соотношение и/или процент клеток фенотипа, присутствующие в композиции клеток или в дозе или образце из нее.
[0246] В некоторых вариантах осуществления, композицию клеток получают от индивида, и количество, кратное или фракция клеток фенотипа представляет собой количество клеток этого фенотипа, присутствующее в композиции клеток, нормализованное по массе тела индивида. В конкретных вариантах осуществления, показатель фенотипа представляет собой количество клеток этого фенотипа на фунт массы тела индивида. В конкретных вариантах осуществления, показатель фенотипа представляет собой количество клеток этого фенотипа на 1 фунт (0,4 кг), 2 фунта (0,8 кг), 3 фунта (1,2 кг), 4 фунта (1,6 кг), 5 фунтов (2,0 кг), 10 фунтов (4,1 кг) или 20 фунтов (8,2 кг) массы тела индивида. В некоторых вариантах осуществления, показатель фенотипа представляет собой количество клеток этого фенотипа на кг массы тела индивида. В конкретных вариантах осуществления, показатель фенотипа представляет собой количество клеток этого фенотипа на 1 кг, 2 кг, 3 кг, 4 кг, 5 кг, 10 кг или 20 кг массы тела индивида.
[0247] В конкретных вариантах осуществления, количество, кратное или фракцию клеток фенотипа преобразуют, например, для сужения диапазона соответствующих значений количества, кратного или фракции. В некоторых вариантах осуществления, преобразование представляет собой любое приложение детерминистской математической функции к каждой точке набора данных, таким образом, что каждую точку данных x заменяют преобразованным значением y=f(x), где f представляет собой функцию. Как правило, преобразования можно прилагать таким образом, чтобы данные выглядели более близко соответствующими допущениям способа статистического исследования, подлежащего использованию, или улучшения интерпретируемости или внешнего вида графиков. В большинстве случаев функция, которую используют для преобразования данных, является обратимой, и, как правило, является непрерывной. Преобразование обычно прилагают к набору поддающихся сравнению измерений. Примеры пригодных преобразований включают, но без ограничения, логарифмическое преобразование и преобразование квадратного корня, обратные преобразования и степенные преобразования. В конкретных вариантах осуществления, количество, кратное или долю клеток фенотипа преобразуют посредством логарифмического преобразования. В конкретных вариантах осуществления, логарифмическое преобразование представляет собой десятичный log (log10(x)), натуральный log (ln(x)) или двоичный log (log2(x)).
B. Антигенспецифическая или зависимая от рекомбинантного рецептора активность
[0248] Конкретные варианты осуществления предусматривают, что зависимая от рекомбинантного рецептора активность, например, зависимая от CAR активность или «B», представляет собой активность, которая возникает в клетке, экспрессирующей рекомбинантный рецептор, которая не возникает и/или не может возникать в клетке, не экспрессирующей рекомбинантный рецептор. В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность представляет собой активность, которая зависит от активности или присутствия рекомбинантного рецептора. Зависимая от рекомбинантного рецептора активность может представлять собой любой клеточный процесс, на который напрямую или опосредованно влияет экспрессия и/или присутствие рекомбинантного рецептора или изменение активности, такое как стимуляция рецептора, для рекомбинантного рецептора. В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность может включать, но без ограничения, такие клеточные процессы, как деление клетки, репликация ДНК, транскрипция, синтез белка, транспорт через мембрану, транслокация белка и/или секреция, или она может представлять собой функцию иммуноцита, например, цитолитическую активность. В конкретных вариантах осуществления, зависимую от рекомбинантного рецептора активность можно измерять по изменению конформации рецептор CAR, фосфорилированию внутриклеточной передающей сигналы молекулы, деградации белка, транскрипции, трансляции, транслокации белка, и/или продукции и секреции такого фактора, как белок или фактор роста, цитокин. В конкретных вариантах осуществления, рекомбинантный рецептор представляет собой CAR.
[0249] В конкретных вариантах осуществления, зависимая от рекомбинантного рецептора активность, например, зависимая от CAR активность, представляет собой показатель фактора, например, количество или концентрацию, или изменение количества или концентрации после стимуляции композиции клеток. В конкретных вариантах осуществления, фактор может представлять собой белок, фосфорилированный белок, расщепленный белок, транслоцированный белок, белок в активной конформации, полинуклеотид, РНК–полинуклеотид, мРНК и/или кшРНК. В конкретных вариантах осуществления, показатель может включать, но без ограничения, увеличение или уменьшение активности киназы, активности протеазы, активности фосфатазы, продукции цАМФ, метаболизма АТФ, транслокацию, например, ядерную локализацию белка, увеличение активности транскрипции, увеличение активности трансляции, продукцию и/или секрецию растворимого фактора, клеточное поглощение, убиквитинилирование и/или деградацию белка.
[0250] В конкретных вариантах осуществления, фактор представляет собой растворимый фактор, который секретируется, такой как гормон, фактор роста, хемокин и/или цитокин.
[0251] В некоторых вариантах осуществления, активность рекомбинантного рецептора, например, зависимая от CAR активность, представляет собой ответ на стимуляцию. В конкретных вариантах осуществления, клетки инкубируют в присутствии стимулирующих условий или стимулирующего средства, и активность представляет собой или включает по меньшей мере один аспект ответа на стимуляцию. Ответ может включать, но без ограничения, событие внутриклеточной передачи сигнала, например, увеличенную активность молекулы рецептора, увеличенную активность киназы для одной или нескольких киназ, увеличение транскрипции одного или нескольких генов, увеличенный синтез белка для одного или нескольких белков, и/или молекулу внутриклеточной передачи сигналов, например, увеличенную активность протеинкиназы. В некоторых вариантах осуществления, ответ или активность ассоциированы с иммунной активностью, и могут включать, но без ограничения, продукцию и/или секрецию растворимого фактора, например, цитокина, увеличение продукции антитела, и/или увеличение цитолитической активности.
[0252] В конкретных вариантах осуществления, ответ на стимуляцию из композиции клеток оценивают посредством измерения, детекции или количественной оценки ответа на стимул, т.е., по меньшей мере одной активности, инициированной, запущенной, поддерживаемой, продленной и/или вызванной стимулом. В конкретных вариантах осуществления, клетки стимулируют, и ответ на стимуляцию представляет собой активность, которая является специфической для клеток, экспрессирующих рекомбинантный рецептор. В конкретных вариантах осуществления, активность представляет собой специфическую для рекомбинантного рецептора активность, и активность возникает в клетках, экспрессирующих рекомбинантный рецептор, но не возникает, или только минимально возникает, в клетках, не экспрессирующих рецептор. В конкретных вариантах осуществления, рекомбинантный рецептор представляет собой CAR. В некоторых вариантах осуществления, активность представляет собой зависимую от CAR активность.
[0253] Условия, используемые для стимуляции клеток, например, иммуноцитов или T–клеток, могут включать одно или несколько из конкретных сред, температуры, содержания кислорода, содержания диоксида углерода, времени, средств, например, питательных веществ, аминокислот, антибиотиков, ионов и/или стимулирующих факторов, таких как цитокины, хемокины, антигены, связывающие паттерны, слитые белки, рекомбинантные растворимые рецепторы, и любые другие средства, разработанные для активации клеток. В некоторых вариантах осуществления, клетки стимулируют, и активность определяют по тому, продуцируется ли или секретируется ли, или нет, растворимый фактор, например, цитокин или хемокин. В некоторых вариантах осуществления, стимуляция является неспецифической, т.е., не является антигенспецифической стимуляцией.
[0254] В некоторых вариантах осуществления, активность является специфической для клеток, экспрессирующих рекомбинантный рецептор. В некоторых вариантах осуществления, активность, которая является специфической для клеток, экспрессирующих рекомбинантный рецептор, не возникает в клетках, в которых отсутствует экспрессия рекомбинантного рецептора. В конкретных вариантах осуществления, рекомбинантный рецептор представляет собой CAR, и активность представляет собой зависимую от CAR активность. В конкретных вариантах осуществления, активность не присутствует в клетках, в которых отсутствует экспрессия рекомбинантного рецептора в таких же условиях, в которых активность присутствует в клетках, экспрессирующих рекомбинантный рецептор. В конкретных вариантах осуществления, зависимая от CAR активность составляет приблизительно на 10%, приблизительно на 20%, приблизительно на 30%, приблизительно на 40%, приблизительно на 50%, приблизительно на 60% приблизительно на 70%, приблизительно на 75%, приблизительно на 80%, приблизительно на 85%, приблизительно на 90%, приблизительно на 95%, приблизительно на 97%, приблизительно на 98%, приблизительно на 99% или приблизительно на 99% меньше, чем зависимая от CAR активность, в CAR– клетках в таких же условиях.
[0255] В некоторых вариантах осуществления, активность является специфической для клеток, экспрессирующих рекомбинантный рецептор, например, CAR, и активность получают посредством стимуляции с использованием средства или в стимулирующих условиях, которые являются специфическими для клеток, экспрессирующих рекомбинантный рецептор. В некоторых вариантах осуществления, рекомбинантный рецептор представляет собой CAR, и специфическая для CAR стимуляция стимулирует, запускает, инициирует и/или продлевает активность в CAR+ клетках, но не стимулирует, не запускает, не инициирует и/или не продлевает активность в CAR– клетках. В некоторых вариантах осуществления, зависимая от CAR активность составляет приблизительно на 10%, приблизительно на 20%, приблизительно на 30%, приблизительно на 40%, приблизительно на 50%, приблизительно на 60% приблизительно на 70%, приблизительно на 75%, приблизительно на 80%, приблизительно на 85%, приблизительно на 90%, приблизительно на 95%, приблизительно на 97%, приблизительно на 98%, приблизительно на 99% или приблизительно на 99% меньше в CAR– клетках, чем в CAR+ клетках, после стимуляции посредством специфического для CAR стимула.
[0256] В конкретных вариантах осуществления, активность представляет собой зависимую от рекомбинантного рецептора, например, зависимую от CAR активность, стимулируемую средством, которое является специфическим для рекомбинантного рецептора. В некоторых вариантах осуществления, специфическое для рекомбинантного рецептора средство, например, специфическое для CAR средство, представляет собой антиген или его эпитоп, связываемый и/или узнаваемый рекомбинантным рецептором, например, CAR. В некоторых вариантах осуществления, специфическое для рекомбинантного рецептора средство представляет собой антитело или его активный фрагмент, связывающие и/или узнающие рекомбинантный рецептор. В некоторых вариантах осуществления, средство представляет собой антиидиотипическое антитело или его активный фрагмент, вариант или часть (анти–ID), связывающие рекомбинантный рецептор. В конкретных вариантах осуществления, специфическое для рекомбинантного рецептора средство представляет собой клетку, которая экспрессирует антиген на своей поверхности. В некоторых вариантах осуществления, зависимую от рекомбинантного рецептора активность стимулируют посредством антигена или его эпитопа, связываемый и/или узнаваемый рекомбинантным рецептором. В конкретных вариантах осуществления, зависимую от рекомбинантного рецептора активность стимулируют посредством антитела или его активного фрагмента, связывающие и/или узнающие рекомбинантный рецептор. В конкретных вариантах осуществления, зависимую от рекомбинантного рецептора активность стимулируют посредством анти–ID.
[0257] В некоторых вариантах осуществления, активность измеряют в композиции клеток, содержащей клетки, экспрессирующие рекомбинантный рецептор, например, CAR, и измерение сравнивают с одним или несколькими контролями. В конкретных вариантах осуществления, контроль представляет собой сходную или идентичную композицию клеток, которую не стимулировали. Например, в некоторых вариантах осуществления, активность измеряют в композиции клеток после или во время инкубации со средством, и полученное измерение сравнивают с контрольным измерением активности для сходной или идентичной композиции клеток, которую не инкубировали со средством. В некоторых вариантах осуществления, активность представляет собой зависимую от рекомбинантного рецептора активность, и как композиция клеток, так и контрольная композиция клеток содержит клетки, экспрессирующие рекомбинантный рецептор. В некоторых вариантах осуществления, активность представляет собой зависимую от рекомбинантного рецептора активность, и контроль отбирают из сходной композиции клеток, которая не содержит клеток, экспрессирующих рекомбинантный рецептор, например, CAR+ клеток. Таким образом в некоторых вариантах осуществления, композицию клеток, которая содержит экспрессирующие рекомбинантный рецептор клетки, и контрольную композицию клеток, которая не содержит экспрессирующие рекомбинантный рецептор клетки, приводят в контакт с стимулирующим рекомбинантный рецептор специфическим средством. В конкретных вариантах осуществления, контроль представляет собой показатель для такой же композиции клеток, которая экспрессирует рекомбинантный рецептор, который получают перед какой–либо стимуляцией. В конкретных вариантах осуществления, контрольный показатель получают для определения фонового сигнала, и контрольный показатель вычитают из показателя активности. В некоторых вариантах осуществления, показатель активности в композиции клеток делят на контрольный показатель, для получения значения, представляющего собой соотношение активности и контрольного уровня.
[0258] В конкретных вариантах осуществления, активность представляет собой или включает продукцию и/или секрецию растворимого фактора. В некоторых вариантах осуществления, активность представляет собой зависимую от рекомбинантного рецептора, например, CAR, активность, которая представляет собой или включает продукцию и/или секрецию растворимого фактора. В конкретных вариантах осуществления, растворимый фактор представляет собой цитокин или хемокин.
[0259] Пригодные способы измерения продукции или секреции растворимого фактора известны в данной области. Продукцию и/или секрецию растворимого фактора можно измерять посредством определения концентрации или количества внеклеточного уровня фактора, или определения уровня активности транскрипции гена, кодирующего фактор. Пригодные способы включают, но без ограничения, анализы, такие как иммуноанализ, анализ на основе аптамеров, гистологический или цитологический анализ, анализ уровня экспрессии мРНК, твердофазный иммуноферментный анализ (ELISA), иммуноблоттинг, иммунопреципитацию, радиоиммунный анализ (RIA), иммуноокрашивание, анализ проточной цитометрии, поверхностный плазмонный резонанс (SPR), анализ хемилюминесценции, проточный иммуноанализ, анализ ингибирования или анализ авидност, анализ микромассивов белков, высокоэффективную жидкостную хроматографию (HPLC), электрохемилюминесценцию способом Meso Scale Discovery (MSD) и мультиплексные иммуноанализы на основе бусин (MIA). В некоторых вариантах осуществления, в пригодном способе можно использовать поддающийся детекции связывающий реагент, который специфически связывает растворимый фактор.
[0260] В конкретных вариантах осуществления, измерение растворимого фактора представляет собой измерение посредством ELISA (твердофазный иммуноферментный анализ). ELISA представляет собой способ анализа с использованием планшетов, разработанный для детекции и количественной оценки веществ, таких как пептиды, цитокины, антитела и гормоны. В ELISA, растворимый фактор должен является иммобилизованным на твердой поверхности и затем образовывать комплексы с антителом, связанным с ферментом. Детекцию осуществляют посредством оценки активности конъюгированного фермента посредством инкубации с субстратом для получения поддающегося детекции сигнала. В некоторых вариантах осуществления, зависимую от CAR активность измеряют с использованием анализ ELISA.
[0261] В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность представляет собой секрецию или продукцию растворимого фактора. В конкретных вариантах осуществления, продукцию или секрецию стимулируют в композиции клеток, содержащей экспрессирующие рекомбинантный рецептор клетки, например, экспрессирующие CAR клетки, посредством специфического для рекомбинантного рецептора средства, например, специфического для CAR+ средства. В некоторых вариантах осуществления, специфическое для рекомбинантного рецептора средство представляет собой антиген или его эпитоп, которые являются специфическими для рекомбинантного рецептора; клетку, например, клетку–мишень, которая экспрессирует антиген; или антитело или его часть или вариант, связывающие и/или узнающие рекомбинантный рецептор; или их комбинацию. В конкретных вариантах осуществления, специфическое для рекомбинантного рецептора средство представляет собой рекомбинантный белок, содержащий антиген или его эпитоп, связываемые или узнаваемые рекомбинантным рецептором.
[0262] В конкретных вариантах осуществления, зависимую от рекомбинантного рецептора продукцию и/или секрецию растворимого фактора измеряют посредством инкубации композиции клеток, содержащей клетки, экспрессирующие рекомбинантный рецептор, например, CAR, со специфическим для рекомбинантного рецептора средством, например, специфическим для CAR+ средством. В конкретных вариантах осуществления, растворимый фактор представляет собой цитокин или хемокин. В некоторых вариантах осуществления, клетки из композиции клеток, содержащей экспрессирующие рекомбинантный рецептор клетки, инкубируют в присутствии специфического для рекомбинантного рецептора средства в течение некоторого периода времени, и продукцию и/или секрецию растворимого фактора измеряют в одной или нескольких временных точках в ходе инкубации. В некоторых вариантах осуществления, клетки инкубируют со специфическим для CAR средством в течение вплоть до или приблизительно 1 часа, приблизительно 2 часов, приблизительно 3 часов, приблизительно 4 часов, приблизительно 5 часов, приблизительно 6 часов, приблизительно 7 часов, приблизительно 8 часов, приблизительно 9 часов, приблизительно 10 часов, приблизительно 11 часов, приблизительно 12 часов, приблизительно 18 часов, приблизительно 19 часов, приблизительно 20 часов, приблизительно 21 часа, приблизительно 22 часов, приблизительно 23 часов, приблизительно 24 часов, приблизительно 48 часов, или в течение периода времени между 1 часом и 4 часами, между 1 часом и 12 часами, между 12 часами и 24 часами, включая каждое, или в течение более чем 24 часов, и количество растворимого фактора, например, цитокина, детектируют.
[0263] В некоторых вариантах осуществления, специфическое для рекомбинантного рецептора средство представляет собой клетку–мишень, которая экспрессирует антиген, узнаваемый рекомбинантным рецептором. В некоторых вариантах осуществления, рекомбинантный рецептор представляет собой CAR, и клетки композиции клеток инкубируют с клетками–мишенями в соотношении общего количества клеток, CAR+ клеток, CAR+/CD8+ клеток или аннексин–/CAR+/CD8+ клеток из композиции клеток к клеткам–мишеням приблизительно 10:1, приблизительно 5:1, приблизительно 4:1, приблизительно 3:1, приблизительно 2:1, приблизительно 1:1, приблизительно 1:2, приблизительно 1:3, приблизительно 1:4, приблизительно 1:5, приблизительно 1:6, приблизительно 1:7, приблизительно 1:8, приблизительно 1:9 или приблизительно 1:10, или в диапазоне между любыми из вышеуказанных, например, в соотношении между 10:1 и 1:1, 3:1 и 1:3, или 1:1 и 1:10, включая каждое.
[0264] В некоторых вариантах осуществления, между приблизительно 1×102 и приблизительно 1×104, между приблизительно 1×103 и приблизительно 1×105, между приблизительно 1×104 и приблизительно 1×106, между приблизительно 1×105 и приблизительно 1×107, между приблизительно 1×106 и приблизительно 1×108, между приблизительно 1×107 и приблизительно 1×109, или между приблизительно 1×108 и приблизительно 1×1010 клеток из композиции клеток, включая каждое, инкубируют со специфическим для рекомбинантного рецептора средством, например, специфическим для CAR+ реагентом. В некоторых вариантах осуществления, между приблизительно 1×106 и приблизительно 1×107 клетки композиции клеток, включительно, инкубируют со специфическим для рекомбинантного рецептора средством, например, специфическим для CAR+ реагентом. В конкретных вариантах осуществления, приблизительно 2,5×106 клеток из композиции инкубируют со специфическим для рекомбинантного рецептора средством. В конкретных вариантах осуществления, между приблизительно 1×102 и приблизительно 1×104, между приблизительно 1×103 и приблизительно 1×105, между приблизительно 1×104 и приблизительно 1×106, между приблизительно 1×105 и приблизительно 1×107, между приблизительно 1×106 и приблизительно 1×108, между приблизительно 1×107 и приблизительно 1×109, или между приблизительно 1×108 и приблизительно 1×1010 экспрессирующих рекомбинантный рецептор клеток, CAR+ клеток, CAR+/CD8+ клеток, или аннексин–/CAR+/CD8+ клеток из композиции клеток, включая каждое, инкубируют со специфическим для CAR+ средством.
[0265] В некоторых вариантах осуществления, клетки из композиции клеток инкубируют со специфическим для рекомбинантного рецептора средством, например, специфическим для CAR+ средством, в некотором объеме среды для клеток. В конкретных вариантах осуществления, клетки инкубируют со специфическим для рекомбинантного рецептора средством в объеме по меньшей мере или приблизительно 1 мкл, по меньшей мере или приблизительно 10 мкл, по меньшей мере или приблизительно 25 мкл, по меньшей мере или приблизительно 50 мкл, по меньшей мере или приблизительно 100 мкл, по меньшей мере или приблизительно 500 мкл, по меньшей мере или приблизительно 1 мл, по меньшей мере или приблизительно 1,5 мл, по меньшей мере или приблизительно 2 мл, по меньшей мере или приблизительно 2,5 мл, по меньшей мере или приблизительно 5 мл, по меньшей мере или приблизительно 10 мл, по меньшей мере или приблизительно 20 мл, по меньшей мере или приблизительно 25 мл, по меньшей мере или приблизительно 50 мл, по меньшей мере или приблизительно 100 мл, или более чем 100 мл. В конкретных вариантах осуществления, клетки инкубируют со специфическим для CAR+ средством в объеме, лежащем в диапазоне между приблизительно 1 мкл и приблизительно 100 мкл, между приблизительно 100 мкл и приблизительно 500 мкл, между приблизительно 500 мкл и приблизительно 1 мл, между приблизительно 500 мкл и приблизительно 1 мл, между приблизительно 1 мл и приблизительно 10 мл, между приблизительно 10 мл и приблизительно 50 мл, или между приблизительно 10 мл и приблизительно 100 мл, включая каждое. В конкретных вариантах осуществления, клетки инкубируют со специфическим для рекомбинантного рецептора средством в объеме между приблизительно 100 мкл и приблизительно 1 мл, включительно. В конкретных вариантах осуществления, клетки инкубируют со специфическим для рекомбинантного рецептора средством в объеме приблизительно 500 мкл.
[0266] В некоторых вариантах осуществления, клетки из композиции клеток инкубируют со специфическим для CAR+ средством в количестве между приблизительно 1 фмоль и приблизительно 1 пмоль, между приблизительно 1 пмоль и приблизительно 1 нмоль, между приблизительно 1 нмоль и приблизительно 1 мкмоль, между приблизительно 1 мкмоль и приблизительно 1 ммоль, или между приблизительно 1 ммоль и 1 моль, включая каждое. В конкретных вариантах осуществления, клетки композиции клеток инкубируют со специфическим для CAR+ средством в концентрации между приблизительно 1 фМ и приблизительно 1 пМ, между приблизительно 1 пМ и приблизительно 1нМ, между приблизительно 1 нМ и приблизительно 1 мкМ, между приблизительно 1 мкМ и приблизительно 1 мМ, или между приблизительно 1 мМ и 1 М, включая каждое. Иллюстративные единицы включают, но без ограничения, пг/мл, пг/(мл/час), пг(мл x клетка), пг/(мл x час x клетка), и пг/(мл x час x 106 клеток).
[0267] В конкретных вариантах осуществления, показатель специфическая для рекомбинантного рецептора активность, например, специфическая для CAR+ активность представляет собой количество или концентрацию, или относительное количество или концентрацию, растворимого фактора в композиции T–клеток во временной точке в ходе или по окончанию инкубации. В конкретных вариантах осуществления, из показателя вычитают контрольный показатель, или показатель нормализуют по контрольному показателю. В некоторых вариантах осуществления, контрольный показатель представляет собой показатель для той же самой композиции клеток, полученный до инкубации. В конкретных вариантах осуществления контрольный показатель представляет собой показатель, полученный для идентичной контрольной композиции клеток, которую не инкубировали со специфическим для рекомбинантного рецептора стимулирующим средством. В конкретных вариантах осуществления, контроль представляет собой показатель, полученный в идентичной временной точке в ходе инкубации со специфическим для рекомбинантного рецептора средством для композиции клеток, не содержащей положительные по рекомбинантному рецептору клетки.
[0268] В некоторых вариантах осуществления, показатель представляет собой нормализованное соотношение количества или концентрации по сравнению с контролем. В конкретных вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на количество времени, например, в минуту или в час. В некоторых вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на клетку или на группу или эталонное количество клеток, например, на 100 клеток, на 103 клеток, на 104 клеток, на 105 клеток, на 106 клеток и т.д. В конкретных вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на количество времени, на клетку или на эталонное количество клеток. В некоторых вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на клетку, которая экспрессирует рекомбинантный рецептор, CAR+ клетку, CAR+/CD8+ клетку или аннексин–/CAR+/CD8+ клетку из композиции клеток. В конкретных вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на количество времени (например, в минуту или в час) на клетку, которая экспрессирует рекомбинантный рецептор, CAR+ клетку, CAR+/CD8+ клетку или аннексин–/CAR+/CD8+ клетку из композиции клеток. В некоторых вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на количество времени на количество или концентрацию специфического для рекомбинантного рецептора или CAR+ средства. В некоторых вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на клетку или на группу или эталонное количество клеток на количество или концентрацию специфического для CAR+ средства. В конкретных вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на количество времени, на количество или концентрацию специфического для рекомбинантного рецептора или CAR+ средства, на клетку или на эталонное количество клеток. В некоторых вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на количество или концентрацию специфического для рекомбинантного рецептора или CAR+ средства, на клетку, которая экспрессирует рекомбинантный рецептор, CAR+ клетку, CAR+/CD8+ клетку, или аннексин–/CAR+/CD8+ клетку из композиции клеток. В конкретных вариантах осуществления, показатель представляет собой количество или концентрацию растворимого фактора на количество времени, на количество или концентрацию специфического для рекомбинантного рецептора или CAR+ средства, на количество CAR+ клеток, CAR+/CD8+ клеток или аннексин–/CAR+/CD8+ клеток из композиции клеток.
[0269] В конкретных вариантах осуществления, зависимая от рекомбинантного рецептора или CAR активность представляет собой продукцию или секрецию двух или более растворимых факторов. В конкретных вариантах осуществления, зависимая от рекомбинантного рецептора или CAR активность представляет собой продукцию или секрецию двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти или более чем десяти растворимых факторов. В некоторых вариантах осуществления, показатели для двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, или более чем десяти растворимых факторов объединяют в среднее арифметическое или среднее геометрическое. В конкретных измерениях, показатель активности рекомбинантного рецептора представляет собой составную секрецию двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, или более чем десяти растворимых факторов.
[0270] В конкретных вариантах осуществления, показатель зависимой от рекомбинантного рецептора активности преобразуют, например, посредством логарифмического преобразования. В конкретных вариантах осуществления, показатель активности рекомбинантного рецептора преобразуют посредством десятичного log (log10(x)), натурального log (ln(x)) или двоичного log (log2(x)). В некоторых вариантах осуществления, показатель зависимой от рекомбинантного рецептора активности представляет собой составной показатель продукции или секреции двух или более растворимых факторов. В некоторых вариантах осуществления, два или более показателя продукции или секреции растворимых факторов преобразуют до комбинации в составной показатель. В конкретных вариантах осуществления, показатель зависимой от рекомбинантного рецептора активности преобразуют для нормализации по эталонному показателю. В конкретных вариантах осуществления, показатель зависимой от рекомбинантного рецептора активности преобразуют для нормализации по эталонному показателю.
[0271] В конкретных вариантах осуществления, растворимый фактор представляет собой цитокин. Цитокины представляют собой большую группу малых передающих сигналы молекул, которые интенсивно функционируют при клеточной коммуникации. Цитокины наиболее часто ассоциированы с различными иммуномодулирующими молекулами, включающими интерлейкины, хемокины и интерфероны. Альтернативно, цитокины можно характеризовать по их структуре, которая классифицирует их на четыре семейства, семейство с четырьмя альфа–спиралями, включающее подсемейство IL–2, подсемейство IFN и подсемейство IL–10; семейство IL–1, семейство IL–17 и цитокины с цистеиновыми узлами, включающие члены семейства трансформирующего фактора роста бета. В некоторых вариантах осуществления, зависимая от CAR активность представляет собой продукцию или секрецию одного или нескольких растворимых факторов, включающих интерлейкины, интерфероны и хемокины. В конкретных вариантах осуществления, зависимая от CAR активность представляет собой продукцию или секрецию одного или нескольких из члена семейства IL–2, члена подсемейства IFN, члена подсемейства IL–10; члена семейства IL–1, члена семейства IL–17, цитокина с цистеиновыми узлами и/или члена семейства трансформирующего фактора роста бета.
[0272] В конкретных вариантах осуществления, зависимая от рекомбинантного рецептора или CAR активность представляет собой продукцию и/или секрецию одного или нескольких из IL–1, IL–1β, IL–2, sIL–2Ra, IL–3, IL–5, IL–6, IL–7, IL–8, IL–10, IL–12, IL–13, IL 27, IL–33, IL–35, TNF, TNF–альфа, CXCL2, CCL2, CCL3, CCL5, CCL17, CCL24, PGD2, LTB4, интерферона гамма (IFN–γ), гранулоцитарно–макрофагального колониестимулирующего фактора (GM–CSF), воспалительного белка макрофагов (MIP)–1a, MIP–1b, Flt–3L, фракталкина и/или IL–5. В конкретных вариантах осуществления, зависимая от CAR активность представляет собой продукцию или секрецию Th17–цитокина. В некоторых вариантах осуществления, Th17–цитокин представляет собой GMCSF. В некоторых вариантах осуществления, зависимая от CAR активность включает продукцию или секрецию Th2–цитокина, где Th2–цитокин представляет собой IL–4, IL–5, IL–10 или IL–13.
[0273] В конкретных вариантах осуществления, зависимая от рекомбинантного рецептора или CAR активность представляет собой продукцию или секрецию провоспалительного цитокина. Провоспалительные цитокины играют роль в инициации воспалительного ответа и в регуляции защиты хозяина против патогенов, опосредованной врожденным иммунным ответом. Провоспалительные цитокины включают, но без ограничения, интерлейкины (IL), интерлейкин–1–бета (IL–1), интерлейкин–3 (IL–3), интерлейкин–5 (IL– 5), интерлейкин–6 (IL–6), интерлейкин–13 (IL–13), фактор некроза опухоли (TNF), лиганд 2 CXC–хемокинов (CXCL2), лиганд 2 CC–хемокинов (CCL2), лиганд 3 CC–хемокинов (CCL3), лиганд 5 CC–хемокинов (CCL5), лиганд 17 CC–хемокинов (CCL17), лиганд 24 CC–хемокинов (CCL24), простагландин D2 (PGD2) и лейкотриен B4 (LTB4), так же как IL–33.). В некоторых вариантах осуществления, зависимая от CAR активность представляет собой продукцию и или секрецию члена семейства интерлейкина и/или TNF. В конкретных вариантах осуществления, зависимая от CAR активность представляет собой продукцию и/или секрецию IL–1, IL–6, IL–8, и IL–18, TNF–альфа или их комбинацию.
[0274] В конкретных вариантах осуществления специфическая для CAR активность представляет собой секрецию IL–2, IFN–гамма, TNF–альфа или их комбинацию.
[0275] В конкретных вариантах осуществления, активность представляет собой цитолитическую (цитотоксическую) активность композиции T–клеток. В конкретных вариантах осуществления, активность представляет собой зависимую от рекомбинантного рецептора, например, CAR, цитолитическую активность. В некоторых вариантах осуществления, зависимую от рекомбинантного рецептора цитолитическую активность оценивают посредством подвергания воздействию, инкубации и/или приведения в контакт клеток, экспрессирующих рекомбинантный рецептор, или композиции клеток, содержащей клетки, экспрессирующие рекомбинантный рецептор, с клеткой–мишенью, которая экспрессирует антиген и/или эпитоп, связываемый и/или узнаваемый рекомбинантным рецептором. Цитолитическую активность можно измерять посредством прямого или непрямого измерения количества клеток–мишеней с течением времени. Например, клетки–мишени можно инкубировать с поддающимся детекции маркером до инкубации с экспрессирующими рекомбинантный рецептор клетками, например, с маркером, который поддается детекции, когда клетка–мишень лизирована, или поддающимся детекции маркером, который поддается детекции в жизнеспособных клетках–мишенях. Эти считывания предоставляют прямое или непрямое количество клеток–мишеней и/или гибель клеток–мишеней, и их можно измерять в различных временных точках в ходе анализа. Уменьшение количества клеток–мишеней и/или увеличение гибели клеток–мишеней показывает цитолитическую активность клеток. Пригодные способы проведения цитолитических анализов известны в данной области, и включают, но без ограничения, анализы высвобождения хрома–51, анализы с использованием нерадиоактивного хрома, анализы проточной цитометрии, в которых используют флуоресцентные красители, такие как сукцинимидильный сложный эфир карбоксифлуоресцеина (CFSE), PKH–2 и PKH–26.
[0276] В конкретных вариантах осуществления, зависимую от рекомбинантного рецептора, например, CAR, цитолитическую активность измеряют посредством инкубации композиции клеток, содержащей клетки, экспрессирующие рекомбинантный рецептор, с клетками–мишенями, экспрессирующими антиген или его эпитоп, связываемый или узнаваемый рекомбинантным рецептором. В конкретных вариантах осуществления, рекомбинантный рецептор представляет собой CAR. В некоторых вариантах осуществления, клетки из композиции клеток инкубируют с клетками–мишенями в соотношении of приблизительно 10:1, приблизительно 5:1, приблизительно 4:1, приблизительно 3:1, приблизительно 2:1, приблизительно 1:1, приблизительно 1:2, приблизительно 1:3, приблизительно 1:4, приблизительно 1:5, приблизительно 1:6, приблизительно 1:7, приблизительно 1:8, приблизительно 1:9 или приблизительно 1:10, или в соотношении между 10:1 и 1:1, 3:1 и 1:3 или 1:1 и 1:10, включая каждое. В некоторых вариантах осуществления, клетки из композиции клеток инкубируют с клетками–мишенями в соотношении CAR+ клеток, CAR+/CD8+ клеток, или аннексин–/CAR+/CD8+ клеток из композиции клеток к клеткам–мишеням приблизительно 10:1, приблизительно 5:1, приблизительно 4:1, приблизительно 3:1, приблизительно 2:1, приблизительно 1:1, приблизительно 1:2, приблизительно 1:3, приблизительно 1:4, приблизительно 1:5, приблизительно 1:6, приблизительно 1:7, приблизительно 1:8, приблизительно 1:9 или приблизительно 1:10, или в соотношении между 10:1 и 1:1, 3:1 и 1:3 или 1:1 и 1:10, включая каждое.
[0277] В конкретных вариантах осуществления, клетки композиции клеток инкубируют с клетками–мишенями в течение вплоть до или приблизительно 1 часа, приблизительно 2 часов, приблизительно 3 часов, приблизительно 4 часов, приблизительно 5 часов, приблизительно 6 часов, приблизительно 8 часов, приблизительно 12 часов, приблизительно 18 часов, приблизительно 24 часов, приблизительно 48 часов или более чем 48 часов. В некоторых вариантах осуществления, композиции клеток инкубируют в течение приблизительно 18 часов, 19 часов, 20 часов, 21 часа, 22 часов, 23 часов или 24 часов. В некоторых вариантах осуществления, между приблизительно 1×102 и приблизительно 1×104, между приблизительно 1×103 и приблизительно 1×105, между приблизительно 1×104 и приблизительно 1×106, между приблизительно 1×105 и приблизительно 1×107, между приблизительно 1×106 и приблизительно 1×108, между приблизительно 1×107 и приблизительно 1×109, или между приблизительно 1×108 и приблизительно 1×1010 клеток из композиции клеток, включая каждое, инкубируют с клетками–мишенями. В конкретных вариантах осуществления, между приблизительно 1×102 и приблизительно 1×104, между приблизительно 1×103 и приблизительно 1×105, между приблизительно 1×104 и приблизительно 1×106, между приблизительно 1×105 и приблизительно 1×107, между приблизительно 1×106 и приблизительно 1×108, между приблизительно 1×107 и приблизительно 1×109, или между приблизительно 1×108 и приблизительно 1×1010 CAR+ клеток, CAR+/CD8+ клеток или аннексин–/CAR+/CD8+ клеток из композиции клеток, включая каждое, инкубируют с клетками–мишенями.
[0278] В некоторых вариантах осуществления, показатель активности сравнивают с контролем. В конкретных вариантах осуществления, контроль представляет собой культуру клеток–мишеней, которую не инкубировали с композицией клеток. В некоторых вариантах осуществления, контроль представляет собой показатель для контрольной композиции клеток, не содержащей CAR+ клетки, которую инкубируют с клетками–мишенями в таком же соотношении.
[0279] В конкретных вариантах осуществления, показатель в анализе цитолитической активности представляет собой количество клеток–мишеней, которые являются жизнеспособными, во временной точке в ходе или по окончанию инкубации. В конкретных вариантах осуществления, показатель представляет собой количество маркера гибели клеток–мишеней, например, хрома–51, высвобожденное в ходе инкубации. В некоторых вариантах осуществления, показатель представляет собой уровень гибели клеток–мишеней, который определяют посредством вычитания количества клеток–мишеней при совместной инкубации, в данной временной точке, из количества клеток–мишеней в контроле, который инкубировали отдельно. В некоторых вариантах осуществления, показатель представляет собой процент клеток–мишеней, оставшихся во временной точке, по сравнению с исходным количеством клеток–мишеней. В конкретных вариантах осуществления, показатель представляет собой количество клеток, уничтоженных в течение некоторого периода времени. В конкретных вариантах осуществления, показатель представляет собой количество уничтоженных клеток, на каждую клетку из композиции клеток. В некоторых вариантах осуществления, показатель представляет собой количество уничтоженных клеток на клетку, или количество уничтоженных клеток на установленное или эталонное количество клеток, например, но без ограничения, количество уничтоженных клеток–мишеней на 100 клеток, на 103 клеток, на 104 клеток, на 105 клеток, на 106 клеток, на 107 клеток, на 108 клеток, на 109 клеток или на 1010 клеток из композиции. В конкретных вариантах осуществления, показатель представляет собой количество уничтоженных клеток на каждую CAR+ клетку, CAR+/CD8+ клетку или аннексин–/CAR+/CD8+ клетку, или их эталонное или установленное количество, из композиции клеток. В конкретных вариантах осуществления, показатель представляет собой количество клеток, уничтоженных в течение некоторого периода времени, на клетку из композиции клеток. В конкретных вариантах осуществления, показатель представляет собой количество клеток, уничтоженных в течение некоторого периода времени, на CAR+ клетки, CAR+/CD8+ клетки или аннексин–/CAR+/CD8+ клетки из композиции клеток.
[0280] В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность не является цитолитической активностью. В конкретных вариантах осуществления, зависимая от CAR+ активность не является цитолитической активностью.
Эталонные стандарты
[0281] Конкретные варианты осуществления предусматривают, что зависимую от рекомбинантного рецептора активность и/или зависимую от CAR+ активность можно нормализовать по эталонному измерению, (т.е. эталонному показателю). В конкретных вариантах осуществления, эталонный показатель представляет собой предопределенный показатель, или его значение, для активности. В некоторых вариантах осуществления, эталонный показатель представляет собой среднее или моду для множества композиции клеток, происходящих от различных индивидов. В некоторых вариантах осуществления, композиции клеток из множества происходят от различных индивидов и содержат клетки, экспрессирующие одинаковый рекомбинантный рецептор. В конкретных вариантах осуществления, эталонный стандарт выводят из показателей, нормализованных или подвергнутых вычитанию, для контрольных групп, таким же способом, как показатель зависимой от рекомбинантного рецептора активности. В конкретных вариантах осуществления, эталонный показатель выводят из показателей, полученных для различных композиций клеток, полученных в таких же условиях анализа, что и показатель активности рекомбинантного рецептора. В конкретных вариантах осуществления, показатель зависимой от рекомбинантного рецептора активности нормализуют по эталонному показателю.
[0282] В конкретных вариантах осуществления эталонный показатель представляет собой среднее или моду показателей для множества композиции клеток. В конкретных вариантах осуществления, эталонный показатель получают для композиции клеток, которая содержит клетки, экспрессирующие такой же CAR, какой экспрессирует по меньшей мере часть клеток в композициях клеток из множества. В конкретных вариантах осуществления, эталонный показатель представляет собой среднее или медиану измерений, полученных для двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати, тринадцати, четырнадцати, пятнадцати, шестнадцати, семнадцати, восемнадцати, девятнадцати, двадцати, двадцати одного, двадцати двух, двадцати трех, двадцати четырех, двадцати пяти, более чем двадцати пяти, более чем тридцати, более чем сорока или более чем пятидесяти композиций клеток.
[0283] В конкретных вариантах осуществления, показатель специфической для рекомбинантного рецептора или специфической для CAR активности получают для композиции клеток, происходящей от индивида–человека с заболеванием или состоянием, и сравнивают по эталонному показателю. В конкретных вариантах осуществления, эталонный показатель получают для композиций клеток, представляющих собой терапевтические композиции T–клеток. В конкретных вариантах осуществления, терапевтические композиции T–клеток представляют собой композиции клеток, которые вводят терапевтически индивидам–людям, например, в клинических исследованиях. В некоторых вариантах осуществления, исходы безопасности и эффективности после введения эталонных композиций T–клеток известны. В конкретных вариантах осуществления, индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном.
[0284] В некоторых вариантах осуществления, каждую из эталонных композиций T–клеток вводили индивиду. В конкретных вариантах осуществления, введение эталонных композиций T–клеток индивидам наблюдали и определяли для получения приемлемого профиля безопасности после введения индивиду. В конкретных вариантах осуществления, введение эталонных композиций T–клеток не приводило к какой–либо тяжелой токсичности. В конкретных вариантах осуществления, введение эталонных композиций T–клеток не приводило к какой–либо тяжелой нейротоксичности. В конкретных вариантах осуществления, эталонные композиции T–клеток все представляют собой композиции, ассоциированные с баллом нейротоксичности степени 4 или ниже, степени 3 или ниже, степени 2 или ниже, степени 1 или ниже, или степени 0. В некоторых вариантах осуществления, эталонные композиции клеток ассоциированы с приемлемыми профилями безопасности. В конкретных вариантах осуществления, приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 1 или выше, наблюдаемой нейротоксичности степени 2 или выше, наблюдаемой нейротоксичности степени 3 или выше, или степени 4 или выше. В конкретных вариантах осуществления, эталонные композиции T–клеток ассоциированы с приемлемыми профилями безопасности с отсутствием наблюдаемой нейротоксичности степени 3 или выше. В конкретных вариантах осуществления, эталонные композиции T–клеток ассоциированы с приемлемыми профилями безопасности с отсутствием наблюдаемой нейротоксичности степени 3 или выше.
[0285] В конкретных вариантах осуществления, для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате желательную эффективность после введения индивиду. В конкретных вариантах осуществления, индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном, как индивиды, которым вводили эталонные композиции T–клеток. В конкретных вариантах осуществления, для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате полный ответ (CR).
[0286] В некоторых вариантах осуществления, показатель зависимой от рекомбинантного рецептора активности представляет собой показатель продукции или секреции одного или нескольких растворимых факторов. В конкретных вариантах осуществления, растворимые факторы представляют собой один или несколько цитокинов. В конкретных вариантах осуществления, специфическая для CAR активность представляет собой секрецию двух или более цитокинов. В конкретных вариантах осуществления, показатель зависимой от рекомбинантного рецептора секреции двух или более цитокинов получают для композиции клеток и нормализуют по эталонным показателям для соответствующих цитокинов. В некоторых вариантах осуществления, два или более нормализованных измерения нормализуют по эталонным показателям. В некоторых вариантах осуществления, нормализованные показатели комбинируют в одно составное значение.
[0287] В конкретных вариантах осуществления, специфическая для CAR активность представляет собой секрецию IL–2, IFN–гамма, TNF–альфа или их комбинации. В конкретных вариантах осуществления, показатель зависимой от CAR секреции IL–2, IFN–гамма, TNF–альфа или их комбинации, получают для композиции клеток и нормализуют по эталонным показателям для соответствующих цитокинов. В некоторых вариантах осуществления, показатели для двух или более из IL–2, IFN–гамма, и TNF–альфа нормализуют по эталонным показателям. В некоторых вариантах осуществления, нормализованные показатели комбинируют в одно значение.
[0288] Конкретные варианты осуществления предусматривают, что когда эталонный показатель получают для эталонных композиций, ассоциированных с приемлемыми профилями безопасности и/или желательной эффективностью, нормализованный показатель, близкий к 1, имеет высокую вероятность также являться ассоциированным с приемлемыми профилями безопасности и/или желательной эффективностью. Конкретные варианты осуществления предусматривают, что показатель для композиции T–клеток имеет высокую вероятность являться ассоциированным с приемлемыми профилями безопасности и/или желательной эффективностью, если соотношение показателя к эталонному показателю составляет около или приблизительно 1:1.
[0289] Конкретные варианты осуществления предусматривают, что наблюдаемая зависимая от CAR+ секреция конкретных цитокинов не указывает на исход или вероятность, или не коррелирует с исходом или вероятностью, или значимо не коррелирует с исходом или вероятностью неблагоприятного события или токсичности. Для этих цитокинов, показатель зависимой от CAR секреции не прогнозируют безопасность или эффективность терапевтического введения композиции T–клеток. В некоторых вариантах осуществления, показатели зависимой от CAR секреции цитокинов, которые не коррелируют с безопасностью или эффективностью, или не указывают на безопасность или эффективность, измеряют и сравнивают с эталонным показателем или нормализуют по эталонному показателю, выведенному из измерений соответствующих цитокинов, полученных для композиций клеток, происходящих от других индивидов. В некоторых вариантах осуществления, показатели зависимой от CAR секреции цитокинов для цитокинов, которые не коррелируют с безопасностью или эффективностью, или не указывают на безопасность или эффективность, сравнивают с соответствующими эталонными показателями для определения того, вызывает ли композиция клеток различные ответы на зависимую от CAR стимуляцию. В некоторых вариантах осуществления, секрецию не считают коррелирующей с безопасностью или эффективностью или указывающей на безопасность или эффективность. Конкретные варианты осуществления предусматривают, что нормализацию одного или нескольких показателей зависимой от CAR секреции цитокинов для IL–4, IL–5, IL–10 или IL–13, или их составное значение можно использовать для определения или подтверждения изменчивости и надежности показателей, полученных для композиции клеток.
III. СПОСОБЫ ОЦЕНКИ ТЕРАПЕВТИЧЕСКОЙ КОМПОЗИЦИИ T–КЛЕТОК
[0290] Настоящее изобретение относится к способам, включающим характеризацию или оценку удельной активности и/или безопасности, и/или активности и/или эффективности терапевтической композиции, в некоторых вариантах осуществления, и терапевтической композиции T–клеток до или во время, или после введения одной или нескольких единичных доз терапевтической композиции T–клеток индивиду, страдающему заболеванием или состоянием. В некоторых вариантах осуществления, представленные способы оценивают риск возникновения неблагоприятного события после введения композиции T–клеток, описанной в настоящем описании. В некоторых вариантах осуществления, композицию T–клеток не выпускают для последующего введения индивиду, если определяют, что композиция находится вне определенного диапазона безопасности. В некоторых аспектах, представленные способы включают анализ высвобождения, который может оценивать композиции клеток для определения, среди других аспектов, если композицию вводят индивиду, имеет ли она вероятность коррелировать с риском возникновения токсичности, такой как тяжелая нейротоксичность, и/или имеет ли она вероятность являться эффективной. В некоторых вариантах осуществления, композицию T–клеток не рекомендуют для введения индивиду, и/или единичную дозу, подлежащую введению индивиду, изменяют или корректируют, если B превышает USL. Если B составляет ниже USL, продукт можно выпускать для лечения.
[0291] В некоторых вариантах осуществления, образец, подлежащий оценке с использованием способов, описанных в настоящем описании отбирают или получают из композиции T–клеток, содержащей T–клетки, происходящие от индивида, имеющего заболевание или состояние, и трансдуцированные нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием. В некоторых аспектах, анализы, описанные в настоящем описании, определяют B для композиции клеток, где B представляет собой значение параметра, или его кратное или преобразование, которое указывает на степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции. Настоящее изобретение относится также к способом анализа терапевтической композиции T–клеток, включающим оценку образца из композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, по активности композиции клеток на основании B, где B представляет собой значение параметра, или его кратное или преобразование, которое указывает на степень или коррелирует со степенью активности в данной композиции. В некоторых вариантах осуществления, представленные способы дополнительно оценивают активность композиции клеток на основании B и/или оценивают, находится ли композиция выше LSL и/или ниже USL для B.
[0292] В некоторых вариантах осуществления, если B превышает USL, единичную дозу подлежащую введению индивиду изменяют или корректируют, где корректированная единичная доза содержит целевое количество клеток или целевое количество эталонных единиц (RU) из композиции T–клеток, где RU в данной композиции определяют по формуле: RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, клеток некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его долю, или кратное, или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции.
[0293] В некоторых вариантах осуществления, параметр представляет собой показатель одного или нескольких факторов или его нормализованное значение. В некоторых вариантах осуществления, индикатор продукции измеряют в анализе окрашивания внутриклеточных цитокинов, включающем инкубацию образца из композиции T–клеток с поликлональным средством, антигенспецифическим средством или средством, связывающим рекомбинантный рецептор. В некоторых вариантах осуществления, показатель определяют в анализе, включающем культивирование или инкубацию в течение фиксированного времени, необязательно, 24 часов, данной композиции или образца из нее в присутствии антигена, клеток, экспрессирующих антиген, и/или средства, специфически связывающегося с рекомбинантным рецептором, необязательно, CAR. В некоторых аспектах, анализ представляет собой ELISA.
[0294] В некоторых вариантах осуществления, показатель фактора представляет собой показатель или уровень, показательный для концентрации, относительной концентрации, количества или относительного количества фактора, количества или относительного количества фактора на единицу вводимых клеток из данной композиции, количества или относительного количества фактора на единицу вводимых клеток из данной композиции в единицу времени, необязательно, один час. В некоторых вариантах осуществления, один или несколько факторов представляет собой один или комбинацию из растворимых факторов, необязательно, один или комбинацию из цитокинов, хемокинов или растворимых рецепторов, необязательно, растворимых костимулирующих рецепторов.
[0295] В некоторых вариантах осуществления, параметр представляет собой показатель для одного или нескольких факторов или его нормализованное значение. В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления одного или нескольких из IL–1, IL–1β, IL–2, sIL–2Ra, IL–3, IL–5, IL–6, IL–7, IL–8, IL–10, IL–12, IL–13, IL 27, IL–33, IL–35, TNF, TNF–альфа, CXCL2, CCL2, CCL3, CCL5, CCL17, CCL24, PGD2, LTB4, интерферона гамма (IFN–γ), гранулоцитарно–макрофагального колониестимулирующего фактора (GM–CSF), воспалительного белка макрофагов (MIP)–1a, MIP–1b, Flt–3L, фракталкина и/или IL–5. В конкретных вариантах осуществления, зависимая от CAR активность представляет собой продукцию или секрецию Th17–цитокина. В некоторых вариантах осуществления, Th17–цитокин представляет собой GMCSF. В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления Th2–цитокина, где Th2–цитокин представляет собой IL–4, IL–5, IL–10 или IL–13. В конкретных вариантах осуществления, B является показателем продукции и/или секреции провоспалительного цитокина, такого как интерлейкины (IL), интерлейкин–1–бета (IL–1), интерлейкин–3 (IL–3), интерлейкин–5 (IL–5), интерлейкин–6 (IL–6), интерлейкин–13 (IL–13), фактор некроза опухоли (TNF), лиганд 2 CXC–хемокинов (CXCL2), лиганд 2 CC–хемокинов (CCL2), лиганд 3 CC–хемокинов (CCL3), лиганд 5 CC–хемокинов (CCL5), лиганд 17 CC–хемокинов (CCL17), лиганд 24 CC–хемокинов (CCL24), простагландин D2 (PGD2) и лейкотриен B4 (LTB4), так же как IL–33. В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления интерлейкина и/или члена семейства TNF, такого как IL–1, IL–6, IL–8 и IL–18, TNF–альфа, или их комбинации. В конкретных вариантах осуществления, зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления IL–2, IFN–гамма, TNF–альфа или их комбинации. В некоторых вариантах осуществления, один или несколько факторов представляют собой один или комбинацию из провоспалительных цитокинов, Th2–цитокинов и Th17–цитокинов. В некоторых вариантах осуществления, один или несколько факторов представляют собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа, IL4, IL–5, IL–10, IL–13, GM–CSF, sCD137, MIP1a и M1Pb. В некоторых вариантах осуществления, один или несколько факторов представляют собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа и IL–10.
[0296] В некоторых вариантах осуществления, один или несколько факторов представляет собой один или комбинацию из растворимых факторов, необязательно, один, или один или комбинацию из цитокинов, хемокинов или растворимых рецепторов, необязательно, растворимых костимулирующих рецепторов. В некоторых вариантах осуществления, параметр представляет собой среднее арифметическое или среднее геометрическое из показателей для двух или более факторов. В некоторых вариантах осуществления, параметр представляет собой среднее арифметическое или среднее геометрическое показателя, необязательно, количества или концентрации, для по меньшей мере двух из TNF–альфа, IFN–гамма и IL–2 или TNF–альфа, IFN–гамма и IL–2. В некоторых вариантах осуществления, параметр представляет собой нормализованное значение показателя, где нормализация проведена по сравнению с эталонным показателем фактора.
[0297] В некоторых вариантах осуществления, A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции. В некоторых аспектах, A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции, где, необязательно два или более фенотипов включают первый фенотип, включающий CD8+ и второй фенотип, включающий CD4+.
[0298] В некоторых вариантах осуществления, целевое количество эталонных RU равно или меньше порогового количества RU, где корректированная единичная доза не содержит больше порогового значения RU. В некоторых аспектах, целевое количество единиц составляет менее, чем пороговое количество единиц, необязательно, представляющее собой безопасное количество эталонных единиц, где безопасное количество эталонных единиц составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события. В некоторых аспектах, неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность, необязательно, степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичности степени 3. В некоторых аспектах, целевое количество эталонных единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, и/или на количество в диапазоне от 1,5– до 3–кратного, необязательно, приблизительно 2–кратное, или на количество, кратное стандартному отклонению в группе индивидов, у которых не возникло неблагоприятного события, необязательно, нейротоксичности степени 0–2, необязательно, где кратное лежит в диапазоне от 1,5– до 3–кратного. В некоторых вариантах осуществления, целевое количество эталонных единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности. В конкретных вариантах осуществления, коэффициент запаса безопасности лежит в диапазоне от 0,5–кратного до 10–кратного, 1,0–5,0–кратного или от 1,5– до 3–кратного, и/или составляет, приблизительно, или по меньшей мере, 1–кратное, 1,5–кратное, 2–кратное, 2,5–кратное или 3–кратное безопасное количество. В конкретных вариантах осуществления, коэффициент запаса безопасности составляет менее, чем безопасное количество. В некоторых вариантах осуществления, коэффициент запаса безопасности составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, такой как CAR, кратное стандартному отклонению от среднего, например, среднего дозы эталонных единиц, введенной индивидам в группе, в которой не возникло неблагоприятного события, например, индивидам в группе, испытавшим нейротоксичность степени 2 или менее. В некоторых вариантах осуществления, коэффициент запаса безопасности лежит в диапазоне от 0,5–кратного до 10– кратного, 1,0–5,0–кратного, или от 1,5– до 3– кратного, и/или является приблизительно, или по меньшей мере, 1–кратным, 1,5–кратным, 2–кратным, 2,5–кратным или 3–кратным стандартному отклонению. В некоторых вариантах осуществления, количество или доза эталонных единиц, которые ниже безопасного количества на количество, соответствующее коэффициенту запаса безопасности, включают количества или дозы эталонных единиц, которые ассоциированы с ответом, например, CR, например, применительно к группе индивидов, у которых продолжалось развитие ответа, например, a CR.
[0299] В некоторых аспектах, целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество единиц лекарственного средства, введенных одному или нескольким индивидам в группе, для которой показан желательный терапевтический исход, необязательно, частичный ответ или полный ответ (CR).
[0300] В некоторых аспектах, корректированная единичная доза составляет менее чем, необязательно, менее чем 1,5–кратную, менее чем 2–кратную, менее чем 3–кратную, менее чем 4–кратную, среднюю единичную дозу для группы индивидов, подвергнутых лечению с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR.
[0301] В некоторых вариантах осуществления, образец из композиции T–клеток, необязательно, криоконсервированный образец, оценивают после введения композиции T–клеток индивиду. В некоторых вариантах осуществления, если B превышает USL, определяют, что индивид подвержен риску токсичности. В некоторых вариантах осуществления, если B превышает USL, индивида, которому вводили композицию, подвергают мониторированию и/или лечению с использованием средства для облегчения или уменьшения вероятности исхода токсичности или синдрома высвобождения цитокинов после введения композиции клеток и необязательно, до возникновения признака или симптома исхода токсичности.
[0302] Настоящее изобретение относится также к способу оценки риска токсичности терапевтической композиции T–клеток, включающему: (a) оценку образца из композиции T–клеток, введенной индивиду, по количеству эталонных единиц (RU) в пределах данного диапазона, где композиция T–клеток содержит T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где RU в данной композиции определяют по формуле: RU=A x B, где: A представляет собой количество клеток, или его кратное, долю или преобразование, клеток некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его долю, или кратное, или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и (b) сравнение количеств RU с эталонными безопасными количествами RU, где сравнение показывает, подвержен или нет индивид риску возникновения неблагоприятного события, необязательно, серьезного неблагоприятного события, необязательно, тяжелой нейротоксичности степени, равной или выше степени 4 или степени 5, или по меньшей мере длительной нейротоксичности степени 3. В некоторых аспектах, A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции. В некоторых аспектах, A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции, где, необязательно, два или более фенотипов включают первый фенотип, включающий CD8+, и второй фенотип, включающий CD4+. В некоторых аспектах, эталонное безопасное количество RU составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события. В некоторых аспектах, если сравнение показывает количество RU выше эталонного безопасного количества RU, индивида, которому вводили композицию, подвергают мониторированию и/или лечению с использованием средства для облегчения или уменьшения вероятности исхода токсичности, или синдрома высвобождения цитокинов после введения композиции клеток и необязательно, до возникновения признака или симптома исхода токсичности.
[0303] Настоящее изобретение относится также к способу получения терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающему: (a) анализ композиции T–клеток, содержащей T–клетки, происходящие от индивида, имеющего заболевание или состояние, и трансдуцированные нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где анализ определяет B для композиции клеток, где B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и (b) заполнение контейнера, например, ампулы, всей или частью композиции и необязательно, другим раствором для получения единичной дозы композиции T–клеток, где единичная доза содержит целевое количество эталонных единиц (RU) из композиции T–клеток, где RU в данной композиции определяют по формуле: RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, клеток некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции;.
[0304] Настоящее изобретение относится также к способу получения терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающему заполнение контейнера, например, ампулы, всей или частью композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, и необязательно, другим раствором, для получения единичной дозы композиции T–клеток, где единичная доза содержит целевое количество эталонных единиц (RU) из композиции T–клеток, где RU в данной композиции определяют по формуле: RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции. В некоторых аспектах, A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции. В некоторых аспектах, A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции, где, необязательно, два или более фенотипов включают первый фенотип, включающий CD8+, и второй фенотип, включающий CD4+.
[0305] В некоторых вариантах осуществления, A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции. В некоторых вариантах осуществления, A и/или B представляет собой преобразование количества или значения, соответственно, где преобразование включает логарифмическое преобразование, степенное преобразование или логит–преобразование. В некоторых вариантах осуществления, A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой кратное или преобразование значения параметра, указывающего на степень или коррелирующего со степенью зависимой от CAR активности в данной композиции T–клеток, необязательно, где B представляет собой логарифмическое преобразование значения. В некоторых вариантах осуществления, логарифмическое преобразование представляет собой десятичный log (log10(x)), натуральный log (ln(x)) или двоичный log (log2(x)).
[0306] В некоторых вариантах осуществления, A представляет собой количество жизнеспособных клеток в композиции и/или представляет собой количество клеток, которые не являются апоптотическими, не имеют фактора, показательного для раннего апоптоза или апоптоза, не находятся на ранних стадиях апоптоза, или не находятся на поздних стадиях апоптоза, и/или представляет собой количество клеток в определенном состоянии дифференцировки, и/или представляет собой количество клеток, имеющих признак клеток памяти/стволовых клеток, или представляет собой его кратное или преобразование. В некоторых вариантах осуществления, фенотип включает отсутствие фактора, показательного для апоптоза или одной или нескольких стадий апоптотического каскада или пути, необязательно, экспрессии маркера апоптоза. В некоторых вариантах осуществления, фенотип включает отрицательную экспрессию маркера апоптоза, необязательно, маркера раннего апоптоза или позднего апоптоза. В некоторых вариантах осуществления, маркер апоптоза представляет собой поверхностный фосфатидилсерин и/или детектирован с использованием аннексина V, или представляет собой активную каспазу или проформу каспазы, необязательно активную каспазу 3 или проформу каспазы 3. В некоторых вариантах осуществления, фенотип включает аннексин–. В некоторых вариантах осуществления, A представляет собой общее количество T–клеток, общее количество CD3+ клеток, общее количество CD4+ или CD8+ клеток, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, общее количество CD4+ CAR+, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение. В некоторых вариантах осуществления, A представляет собой общее количество CD3+ клеток, общее количество CD8+, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение. В некоторых вариантах осуществления, A представляет собой общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD3+ CAR+ клетками, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD4+ CAR+, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD8+ CAR+ клетки, или его кратное или преобразованное значение, где маркер апоптоза представляет собой аннексин V или каспазу. A представляет собой общее количество аннексин– CD3+ CAR+ клеток, общее количество аннексин– CD4+ CAR+, общее количество аннексин– CD8+ CAR+ клеток, или его кратное или преобразованное значение. В некоторых вариантах осуществления, A представляет собой общее количество аннексин– CD3+ CAR+ клеток или общее количество аннексин– CD8+ CAR+ клеток.
[0307] В некоторых вариантах осуществления, фенотип включает положительную экспрессию поверхностного маркера, представляющего собой один или несколько из CD3, CD4 или CD8, и/или включает положительную экспрессию рекомбинантного рецептора, необязательно, CAR, или суррогатный маркер экспрессии рекомбинантного рецептора. В некоторых аспектах, фенотип представляет собой CD3+ CAR, CD4+/CAR+, CD8+/CAR+. В некоторых вариантах осуществления, фенотип включает показатель продукции одного или комбинации цитокинов, необязательно, не специфической для антигена или рекомбинантного рецептора и/или поликлональной продукции, где один или несколько цитокинов представляет собой IL–2, IL–13, IL–17, IFN–гамма или TNF–альфа. В некоторых вариантах осуществления, показатель продукции измеряют в анализе, необязательно, в анализе окрашивания внутриклеточных цитокинов, включающем инкубацию образца из композиции T–клеток с поликлональным средством, антигенспецифическим средством или средством, связывающим рекомбинантный рецептор, необязательно CAR. В некоторых вариантах осуществления, средство представляет собой или содержит PMA и иономицин, или представляет собой или содержит T–клеточный рецептор или агонист комплекса T–клеточного рецептора. В некоторых вариантах осуществления, фенотип включает отрицательную экспрессию маркера активации, где маркер активации выбран среди CD25, CD127, LAG3, Ki67 и их комбинаций. В некоторых вариантах осуществления, фенотип включает отрицательную экспрессию маркера истощения, где маркер истощения представляет собой продукт гена PD1 или FOXP3, или их комбинацию. В некоторых вариантах осуществления, фенотип включает наивный фенотип или фенотип клеток памяти, необязательно, где фенотип клеток памяти включает фенотип эффекторных T–клеток памяти, фенотип центральных T–клеток памяти, или фенотип эффекторных T–клеток памяти, экспрессирующих CD45RA (Temra).
[0308] В некоторых вариантах осуществления, зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления провоспалительного цитокина, необязательно, одного или комбинации из TNF–альфа, IFN–гамма, IL–2 и IL–10. В некоторых вариантах осуществления, эталонный показатель представляет собой среднее из показателей среди множества, необязательно, по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, из эталонных терапевтических композиций T–клеток, содержащих химерный антигенный рецептор (CAR), в которых: (i) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате приемлемый профиль безопасности после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном; и/или (ii) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате желательную эффективность после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном.
[0309] В некоторых конкретных вариантах осуществления, параметр представляет собой нормализованное значение показателя, где нормализация проведена по сравнению с эталонным показателем фактора. В некоторых вариантах осуществления, эталонный показатель представляет собой среднее из показателей среди множества, необязательно по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, из эталонных терапевтических композиций T–клеток, содержащих химерный антигенный рецептор (CAR), в которых: (i) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате приемлемый профиль безопасности после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном; и/или (ii) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате желательную эффективность после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном. В некоторых вариантах осуществления, приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 2 или выше, или отсутствие нейротоксичности степени 3 или выше.
[0310] В некоторых вариантах осуществления, приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 3 или выше. В некоторых вариантах осуществления, эффективность представляет собой частичный ответ или представляет собой полный ответ (CR). В некоторых вариантах осуществления, эталонный показатель представляет собой показатель, в таком же анализе, фактора в эталонной композиции T–клеток, которая получена таким же способом, как терапевтическая композиция T–клеток, но не экспрессирует рекомбинантного рецептора, необязательно, CAR, не узнает специфически антиген и/или не экспрессирует никакого рекомбинантного рецептора, необязательно, никакого CAR. В некоторых вариантах осуществления, этот параметр нормализуют для контроля специфической для пациента изменчивости показателя одного или нескольких факторов. В некоторых вариантах осуществления, параметр представляет собой нормализованное значение показателя фактора, по сравнению с таким же показателем в таком же анализе, для контрольного фактора, где для уровня контрольного фактора в терапевтической композиции T–клеток известно отсутствие или наблюдали отсутствие признака или корреляции, или значимой корреляции с исходом неблагоприятного события или токсичности, или их вероятностью или риском, где исход неблагоприятного события или токсичности необязательно, представляет собой тяжелую нейротоксичность. В некоторых вариантах осуществления, контрольный фактор представляет собой или содержит фактор, который статистически не коррелирует и/или не коррелирует с возникновением неблагоприятного события среди множества индивидов, у которых продолжалось развитие неблагоприятного события, после введения композиции T–клеток, необязательно, контрольный фактор представляет собой один из или комбинацию из IL–5, IL–13, GM–CSF и IL–6, необязательно, где показатель контрольного фактора представляет собой среднее арифметическое или среднее геометрическое из двух или более из вышеуказанного.
[0311] В некоторых вариантах осуществления, параметр не включает цитолитическую активность или ее показатель. В некоторых вариантах осуществления, параметр не включает зависимую от рекомбинантного рецептора или антигенспецифическую цитолитическую активность или ее показатель.
[0312] В некоторых конкретных вариантах осуществления, фенотип представляет собой CD8+ CAR+ клетки или аннексин– CD8+ CAR+ клетки; и параметр представляет собой показатель для провоспалительного цитокина, который, необязательно, представляет собой один из или комбинацию из TNF–альфа, IL–2 и IFN–гамма, или представляет собой его нормализованное значение.
[0313] В некоторых вариантах осуществления, неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и пороговое значение: составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+ и если B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+ и B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+ и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,0×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,5×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0314] В некоторых вариантах осуществления, неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и данный диапазон целевых эталонных единиц: составляет между или приблизительно между 2,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 4×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 5×106 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 2,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 2,0×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 2,5×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+ и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0315] В некоторых вариантах осуществления, неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и пороговое значение: составляет или составляет приблизительно 1,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 1,25×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+ и если B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+ и B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,88×106, если A представляет собой CD8+CAR+ и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,12×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2; или его нормализованное значение составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0316] В некоторых вариантах осуществления, неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и данный диапазон целевых эталонных единиц: составляет между или приблизительно между 3,0×105 и 1,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,25×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 4×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+ и если B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 5×106 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 2,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 1,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,88×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 2,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 3,12×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0317] В некоторых вариантах осуществления, которые можно комбинировать с любым другим вариантом осуществления, описанным в настоящем описании, рекомбинантный рецептор представляет собой CAR. В некоторых вариантах осуществления, CAR содержит внеклеточный узнающий антиген домен, который специфически связывается с антигеном, и внутриклеточный передающий сигналы домен, содержащий ITAM, где необязательно, внутриклеточный передающий сигналы домен содержит внутриклеточный домен из цепи CD3–зета (CD3ζ); и/или где CAR дополнительно содержит область передачи костимулирующих сигналов, которая, необязательно, содержит передающий сигналы домен из CD28 или 4–1BB. В некоторых вариантах осуществления, которые можно комбинировать с любым другим вариантом осуществления, T–клетки являются CD4+ или CD8+. В некоторых вариантах осуществления, T–клетки представляют собой первичные T–клетки, необязательно, аутологичные или аллогенные для индивида.
IV. СПОСОБЫ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ ТЕРАПЕВТИЧЕСКОЙ КОМПОЗИЦИИ T–КЛЕТОК
[0318] Настоящее изобретение относится к способам, включающим введение индивиду, страдающему заболеванием или состоянием, одной или нескольких единичных доз терапевтической композиции T–клеток. В некоторых вариантах осуществления, одна или несколько единичных доз содержит целевое эталонное количество единиц композиции клеток, основанное на A (количестве клеток некоторого фенотипа) и/или B (значении параметра, ассоциированном со степенью зависимой от рекомбинантного рецептора активности, такой как зависимая от CAR активность, например, антигенспецифическая активность).
A. Заболевания и состояния, и способы введения
[0319] В некоторых вариантах осуществления, дозу экспрессирующих рекомбинантный рецептор клеток вводят индивиду для лечения или предотвращения заболеваний, состояний и нарушений, включая злокачественные опухоли. В некоторых вариантах осуществления, клетки, популяции и композиции вводят индивиду или пациенту, имеющему конкретное заболевание или состояние, подлежащее лечению, например, посредством адоптивной клеточной терапии, такой как адоптивная T клеточная терапия. В некоторых вариантах осуществления, клетки и композиции, такие как модифицированные композиции и композиции на конечном этапе производственного цикла после инкубации и/или других стадий переработки, вводят индивиду, такому как индивид, имеющий заболевание или состояние, или подверженный риску заболевания или состояния. В некоторых аспектах, способы таким образом, обеспечивают лечение, например, облегчение одного или нескольких симптомов заболевания или состояния, например, посредством уменьшения опухолевой нагрузки при злокачественной опухоли, экспрессирующий антиген, узнаваемый модифицированной T–клеткой.
[0320] Способы введения клеток для адоптивной клеточной терапии известны и могут быть использованы в сочетании с представленными способами и композиции. Например, способы адоптивной T–клеточной терапии описаны, например, в Публикации патентной заявки США No. 2003/0170238 от Gruenberg et al; Патенте США No. 4690915 от Rosenberg; Rosenberg (2011) Nat Rev Clin Oncol. 8(10):577–85). См., например, Themeli et al. (2013) Nat Biotechnol. 31(10): 928–933; Tsukahara et al. (2013) Biochem Biophys Res Commun 438(1): 84–9; Davila et al. (2013) PLoS ONE 8(4): e61338.
[0321] Заболевание или состояние, которое подвергают лечению, может представлять собой любое заболевание или состояние, при котором экспрессия антигена ассоциирована с этиологией и/или вовлечена в этиологию заболевания, состояния или нарушения, например, вызывает, отягощает или иным образом вовлечена в такое заболевание, состояние или нарушение. Иллюстративные заболевания и состояния могут включать заболевания или состояния, ассоциированные с злокачественным развитием или трансформацией клеток (например, злокачественную опухоль), аутоиммунное или воспалительное заболевание, или инфекционное заболевание, например, вызванное бактериальным, вирусным или другим патогеном. Иллюстративные антигены, включающие антигены, ассоциированные с различными заболеваниями и состояниями, которые можно лечить, описаны выше. В конкретных вариантах осуществления, химерный антигенный рецептор или трансгенный TCR специфически связывается с антигеном, ассоциированным с заболеванием или состоянием.
[0322] Среди заболеваний, состояний и нарушений присутствуют опухоли, включая солидные опухоли, гематологические злокачественные новообразования и меланомы, и включая локализованные и метастазирующие опухоли, инфекционные заболевания, такие как инфекция вирусом или другим патогеном, например, HIV, HCV, HBV, CMV, и паразитарное заболевание, и аутоиммунные и воспалительные заболевания. В некоторых вариантах осуществления, заболевание или состояние представляет собой опухоль, злокачественную опухоль, злокачественное новообразование, неоплазию или другое пролиферативное заболевание или нарушение. Такие заболевания включают, но без ограничения, лейкоз, лимфому, например, хронический лимфоцитарный лейкоз (CLL), острый лимфобластный лейкоз (ALL), неходжскинскую лимфому, острый миелоидный лейкоз, множественную миелому, невосприимчивую фолликулярную лимфому, лимфому из клеток мантийной зоны, индолентную B–клеточную лимфому, злокачественные новообразования B–клеток, злокачественные опухоли ободочной кишки, легкого, печени, молочной железы, предстательной железы, яичников, кожи, меланому, злокачественные опухоли кости и злокачественную опухоль мозга, рак яичника, эпителиальные злокачественные опухоли, почечноклеточный рак, аденокарциному поджелудочной железы, лимфому Ходжкина, карциному шейки матки, колоректальный рак, глиобластому, нейробластому, саркому Юинга, медуллобластому, остеосаркому, синовиальную саркому и/или мезотелиому. В некоторых вариантах осуществления, индивид имеет острый лимфобластный лейкоз (ALL). В некоторых вариантах осуществления, индивид имеет неходжскинскую лимфому.
[0323] В некоторых вариантах осуществления, заболевание или состояние представляет собой инфекционное заболевание или состояние, такое как, но без ограничения, вирусные, ретровирусные, бактериальные и протозойные инфекции, иммунодефицит, инфекции цитомегаловируса (CMV), вируса Эпштейна–Барр (EBV), аденовируса, полиомавируса BK. В некоторых вариантах осуществления, заболевание или состояние представляет собой аутоиммунное или воспалительное заболевание или состояние, такое как артрит, например, ревматоидный артрит (RA), диабет типа I, системная красная волчанка (SLE), воспалительное заболевание кишечника, псориаз, склеродермия, аутоимунный тиреоидит, болезнь Грэйва, болезнь Крона, рассеянный склероз, астма и/или заболевание или состояние, ассоциированное с трансплантацией.
[0324] В некоторых вариантах осуществления, антиген, ассоциированный с заболеванием или нарушением, выбран из группы, состоящей из орфанного тирозинкиназного рецептора RORl, tEGFR, Her2, Ll–CAM, CD19, CD20, CD22, мезотелина, CEA и поверхностного антигена вируса гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, EGP–2, EGP–4, 0EPHa2, ErbB2, 3, или 4, FBP, фетального рецептора ацетилхолина, GD2, GD3, HMW–MAA, IL–22R–альфа, IL–13R–альфа2, kdr, легкой цепи каппа, Lewis Y, молекулы клеточной адгезии L1, MAGE–A1, мезотелина, MUC1, MUC16, PSCA, лигандов NKG2D, NY–ESO–1, MART–1, gp100, онкофетального антигена, ROR1, TAG72, VEGF–R2, карциноэмбрионального антигена (CEA), простатспецифического антигена, PSMA, Her2/neu, рецептора эстрогенов, рецептора прогестерона, эфрина B2, CD123, CS–1, c–Met, GD–2, и MAGE A3, CE7, антигена опухоли Вильмса 1 (WT–1), циклина, такого как циклин A1 (CCNA1), и/или биотинилированных молекул, и/или молекул, экспрессированных HIV, HCV, HBV или другими патогенами.
[0325] В некоторых вариантах осуществления, антиген представляет собой или включает интегрин αvβ6 (интегрин avb6), антиген созревания B–клеток (BCMA), B7–H3, B7–H6, карбоангидраза 9 (CA9, также известный как CAIX или G250), раково–тестикулярный антиген, раково–тестикулярный антиген 1B (CTAG, также известный как NY–ESO–1 и LAGE–2), карциноэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокинов с мотивом C–C (CCL–1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, белок эпидермальный фактор роста (EGFR), укороченный белок эпидермальный фактор роста (tEGFR), рецептор эпидермального фактора роста с мутацией типа III (EGFR vIII), эпителиальный гликопротеин 2 (EPG–2), эпителиальный гликопротеин 40 (EPG–40), эфрин B2, рецептор эфрина A2 (EPHa2), рецептор эстрогена, подобный рецептору Fc белок 5 (FCRL5; также известный как гомолог 5 рецептора Fc или FCRH5), фетальный рецептор ацетилхолина (фетальный AchR), связывающий фолат белок (FBP), рецептор фолата альфа, ганглиозид GD2, O–ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), сопряженный с G белком рецептор 5D (GPCR5D), Her2/neu (рецепторную тирозинкиназу erb–B2), Her3 (erb–B3), Her4 (erb–B4), димеры erbB, ассоциированный с меланомой высокомолекулярный антиген человека (HMW–MAA), поверхностный антиген вируса гепатита B, человеческий лейкоцитарный антиген A1 (HLA–A1), человеческий лейкоцитарный антиген A2 (HLA–A2), рецептор IL–22 альфа(IL–22Ra), рецептор IL–13 альфа 2 (IL–13Ra2), рецептор, содержащий домен вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1–CAM), эпитоп CE7 из L1–CAM, член A семейства 8, содержащего богатые лейцином повторы (LRRC8A), Lewis Y, ассоциированный с меланомой антиген (MAGE)–A1, MAGE–A3, MAGE–A6, мезотелин, c–Met, мышиный цитомегаловирус (CMV), муцин 1 (MUC1), MUC16, лиганды члена D группы 2 естественных киллеров (NKG2D), мелан A (MART–1), молекулу адгезии нервных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простатспецифический антиген, антиген стволовых клеток предстательной железы (PSCA), простатспецифический мембранный антиген (PSMA), подобный рецепторной тирозинкиназе орфанный рецептор 1 (ROR1), сурвивин, гликопротеин трофобластных клеток (TPBG также известный как 5T4), опухолеассоциированный гликопротеин 72 (TAG72), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор фактора роста эндотелия сосудов 2 (VEGFR2), антиген опухоли Вильмса 1 (WT–1), специфический для патогена антиген, или антиген, ассоциированный с универсальной меткой, и/или биотинилированные молекулы, и/или молекулы, экспрессированные HIV, HCV, HBV или другими патогенами. Антигены, на которые нацелены рецепторы, в некоторых вариантах осуществления включают антигены, ассоциированные с злокачественным новообразованием из B–клеток, такие как любой из ряда известных маркеров B–клеток. В некоторых вариантах осуществления, антиген представляет собой или включает CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig–каппа, Ig–лямбда, CD79a, CD79b или CD30.
[0326] В некоторых вариантах осуществления, клеточную терапию, например, адоптивную T–клеточную терапию, осуществляют посредством аутологичного переноса, при котором клетки выделяют и/или иным образом получают от индивида, подлежащего проведению клеточной терапии, или из образца, полученного от такого индивида. Таким образом, в некоторых аспектах, клетки получают от индивида, например, пациента, нуждающегося в лечении, и клетки, после выделения и переработки, вводят тому же самому индивиду.
[0327] В некоторых вариантах осуществления, клеточную терапию, например, адоптивную T–клеточную терапию, осуществляют посредством аллогенного переноса, при котором клетки выделяют и/или иным образом получают от индивида, отличного от индивида, подлежащего проведению клеточной терапии или в конечном счете подлежащего проведению клеточной терапии, например, первого индивида. В таких вариантах осуществления, клетки затем вводят другому индивиду, например, второму индивиду, того же вида. В некоторых вариантах осуществления, первый и второй индивиды являются генетически идентичными. В некоторых вариантах осуществления, первый и второй индивиды являются генетически сходными. В некоторых вариантах осуществления, второй индивид экспрессирует HLA такого же класса или супертипа, что и первый индивид.
[0328] Клетки можно вводить любыми пригодными способами, например, посредством болюсной инфузии, посредством инъекции, например, внутривенной или подкожной инъекций, внутриглазной инъекции, периокулярной инъекции, субретинальной инъекции, инъекции в стекловидное тело, инъекции посредством прокола перегородки, субсклеральной инъекции, интрахороидальной инъекции, интракамеральной инъекции, субконъюнктивальной инъекции, инъекции в субтеноново пространство, ретробульбарной инъекции, перибульбарной инъекции или задней околосклеральной доставки. В некоторых вариантах осуществления, их вводят посредством парентерального, внутрилегочного и интраназального, и, если желательно для местного лечения, внутриочагового введения. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. В некоторых вариантах осуществления, данную дозу вводят посредством однократного болюсного введения клеток. В некоторых вариантах осуществления, ее вводят посредством множества болюсных введений клеток, например, в течение периода не более чем 3 суток, или посредством введения клеток непрерывной инфузией.
[0329] Для предотвращения или лечения заболеваний, соответствующая доза может зависеть от типа заболеваний, подлежащих лечению, типа клеток или рекомбинантных рецепторов, тяжести и течения заболевания, того, вводят ли клетки для профилактических или терапевтических целей, предшествующей терапии, анамнеза индивида и ответа на клетки, и решения лечащего терапевта. Композиции и клетки, в некоторых вариантах осуществления, подходящим образом вводят индивиду за один раз или на протяжении серий обработок.
[0330] В некоторых вариантах осуществления, клетки вводят в качестве части комбинированного лечения, например, одновременно или последовательно, в любом порядке, с другим терапевтическим вмешательством, например, с антителом или модифицированной клеткой или рецептором, или средством, таким как цитотоксическое или лекарственное средство. Клетки, в некоторых вариантах осуществления, вводят совместно с одним или несколькими дополнительными лекарственными средствами или в сочетании с другим терапевтическим вмешательством, либо одновременно, либо последовательно, в любом порядке. В некоторых контекстах, клетки вводят совместно с другой терапией достаточно близко по времени, таким образом, что популяции клеток усиливают эффект одного или нескольких дополнительных лекарственных средств, или наоборот. В некоторых вариантах осуществления, клетки вводят перед одним или несколькими дополнительными лекарственными средствами. В некоторых вариантах осуществления, клетки вводят после одного или нескольких дополнительных лекарственных средств. В некоторых вариантах осуществления, одно или несколько дополнительных средств включают цитокин, такой IL–2, например, для улучшения персистенции. В некоторых вариантах осуществления, способы включают введение химиотерапевтического средства.
[0331] В некоторых вариантах осуществления, способы включают введение химиотерапевтического средства, например, подготовительного химиотерапевтического средства, например, для уменьшения опухолевой нагрузки перед введением.
[0332] Предварительная подготовка индивидов с использованием видов иммуноистощающей (например, противолимфоцитарной) терапии в некоторых аспектах может улучшать эффекты адоптивной клеточной терапии (ACT).
[0333] Таким образом, в некоторых вариантах осуществления, способы включают введение средства для предварительной подготовки, такого как противолимфоцитарное или химиотерапевтическое средство, например, циклофосфамида, флударабина или их комбинаций, индивиду перед началом клеточной терапии. Например, индивиду можно вводить средство для предварительной подготовки по меньшей мере за 2 суток до, например, по меньшей мере за 3, 4, 5, 6 или 7 суток до начала клеточной терапии. В некоторых вариантах осуществления, индивиду вводят средство для предварительной подготовки не более чем за 7 суток до, например, не более чем за 6, 5, 4, 3 или 2 суток до начала клеточной терапии. Иллюстративные режимы дозирования для предварительной подготовки описаны в Международной патентной заявке No. WO2016/191756.
[0334] В некоторых вариантах осуществления, индивида подвергают предварительной подготовке с использованием циклофосфамида в дозе между или между приблизительно 20 мг/кг и 120 мг/кг, например, между или между приблизительно 40 мг/кг и 80 мг/кг, включая каждое. В некоторых аспектах, индивида подвергают предварительной подготовке с использованием или с использованием приблизительно 60 мг/кг циклофосфамида. В некоторых вариантах осуществления, индивида подвергают предварительной подготовке с использованием циклофосфамида в дозе между или между приблизительно 200 мг/м2 и 4440 мг/м2, например, между или между приблизительно 200 мг/м2 и 500 мг/м2, включая каждое. В некоторых случаях, индивида подвергают предварительной подготовке с использованием 300 мг/м2 циклофосфамида, в некоторых случаях ежесуточно, например, 300 мг/м2/сутки. В некоторых случаях, индивида подвергают предварительной подготовке с использованием или с использованием приблизительно 500 мг/м2 циклофосфамида, в некоторых случаях ежесуточно, например, 500 мг/м2/сутки. В некоторых случаях, индивида подвергают предварительной подготовке с использованием или с использованием приблизительно 2220–4440 мг/м2 циклофосфамида. В некоторых аспектах, индивида подвергают предварительной подготовке с использованием или с использованием приблизительно 200 мг/м2/сутки, приблизительно 250 мг/м2/сутки приблизительно 300 мг/м2/сутки, приблизительно 350 мг/м2/сутки, приблизительно 400 мг/м2/сутки, приблизительно 450 мг/м2/сутки, приблизительно 500 мг/м2/сутки, приблизительно 550 мг/м2/сутки, приблизительно 600 мг/м2/сутки, приблизительно 650 мг/м2/сутки, приблизительно 700 мг/м2/сутки, приблизительно 800 мг/м2/сутки, приблизительно 900 мг/м2/сутки, или приблизительно 1000 мг/м2/сутки. В некоторых вариантах осуществления, циклофосфамид можно вводить в однократной дозе или можно вводить в множестве доз, например, вводимых ежесуточно, на каждые вторые сутки или на каждые третьи сутки. В некоторых вариантах осуществления, циклофосфамид вводят один раз в сутки в течение одних или двух, или трех или более суток. В некоторых вариантах осуществления, дозы, описанные в настоящем описании, представляют собой ежесуточные дозы, например, мг/м2/сутки, вводимые ежесуточно в течение трех последовательных суток.
[0335] В некоторых вариантах осуществления, где противолимфоцитарное средство содержит флударабин, индивиду вводят флударабин в дозе между или между приблизительно 1 мг/м2 и 100 мг/м2, например, между или между приблизительно 10 мг/м2 и 75 мг/м2, 15 мг/м2 и 50 мг/м2, 20 мг/м2 и 30 мг/м2, или 24 мг/м2 и 26 мг/м2, включая каждое. В некоторых случаях, индивида подвергают предварительной подготовке с использованием или с использованием приблизительно 10 мг/м2/сутки, приблизительно 15 мг/м2/сутки, приблизительно 20 мг/м2/сутки, приблизительно 25 мг/м2/сутки, приблизительно 30 мг/м2/сутки, приблизительно 35 мг/м2/сутки, приблизительно 40 мг/м2/сутки, приблизительно 45 мг/м2/сутки, приблизительно 50 мг/м2/сутки, приблизительно 55 мг/м2/сутки, приблизительно 60 мг/м2/сутки, приблизительно 65 мг/м2/сутки, приблизительно 70 мг/м2/сутки, приблизительно 75 мг/м2/сутки, приблизительно 80 мг/м2/сутки, приблизительно 85 мг/м2/сутки, приблизительно 90 мг/м2/сутки, приблизительно 95 мг/м2/сутки, приблизительно 100 мг/м2/сутки, приблизительно 200 мг/м2/сутки, или приблизительно 300 мг/м2/сутки. В некоторых случаях, индивиду вводят 25 мг/м2 флударабина. В некоторых случаях, индивиду вводят 30 мг/м2 флударабина. В некоторых вариантах осуществления, флударабин можно вводить в однократной дозе или можно вводить в множестве доз, например, вводимых ежесуточно, на каждые вторые сутки или на каждые третьи сутки. В некоторых вариантах осуществления, флударабин вводят ежесуточно, например, в течение 1–5 суток, например, от 3 до 5 суток. В некоторых вариантах осуществления, дозы, описанные в настоящем описании, представляют собой ежесуточные дозы, например, мг/м2/сутки, вводимые ежесуточно в течение трех последовательных суток.
[0336] В некоторых вариантах осуществления, противолимфоцитарное средство содержит комбинацию средств, например, комбинацию циклофосфамида и флударабина. Таким образом, комбинация средств может включать циклофосфамид в любой дозе или с любым расписанием введения, такими как описанные выше, и флударабин в любой дозе или с любым расписанием введения, такими как описанные выше. Например, в некоторых аспектах, индивиду вводят 60 мг/кг (~2 г/м2) циклофосфамида и 3–5 доз по 25 мг/м2 флударабина перед первой или последующей дозой. Dosing
[0337] Фармацевтическая композиция, в некоторых вариантах осуществления, содержит клетки в количествах, эффективных для лечения или предотвращения заболевания или состояния, таких как терапевтически эффективное или профилактически эффективное количество. В некоторых вариантах осуществления, композиция содержит клетки в количестве, эффективном для уменьшения нагрузки заболевания или состояния.
[0338] В некоторых вариантах осуществления, настоящее изобретение относится к способам, включающим введение индивиду одной или нескольких единичных доз терапевтической композиции T–клеток, в которой каждая единичная доза содержит либо (i) целевое количество тотальных экспрессирующих рекомбинантный рецептор (например, экспрессирующих CAR) клеток или целевое количество или общее количество экспрессирующих рекомбинантный рецептор (например, экспрессирующих CAR) клеток конкретного фенотипа; либо (ii) целевое количество эталонных единиц (RU) из композиции T–клеток, находящееся в пределах данного или целевого диапазона RU. В некоторых вариантах осуществления, единичная доза не содержит больше порогового значения RU, например, больше безопасного количества эталонных единиц.
[0339] В некоторых вариантах осуществления, настоящее изобретение относится к способам лечения, включающим введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащих клетки, содержащие рекомбинантный рецептор, такой как химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит целевое количество эталонных единиц (RU) в пределах данного диапазона. RU в данной композиции определяют по формуле RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции. Иллюстративные признаки, ассоциированные с A и B, описаны в настоящем описании вместе с эталоном для определения или предоставления единичной дозы клеток для введения.
[0340] В некоторых вариантах осуществления, A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции, такого как фенотип, который представляет собой или включает CD8+ клетки, или другого фенотипа, как описано в настоящем описании. В некоторых вариантах осуществления, A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции. В одном примере, два или более фенотипов включают первый фенотип, включающий CD8+ и второй фенотип, включающий CD4+.
[0341] В некоторых вариантах осуществления, целевое количество единиц, содержащихся в единичной дозе для введения, которое составляет менее, чем пороговое количество эталонных единиц, например, предопределенный порог, как идентифицировано или как известно, указывающий на риск неблагоприятного события, такого как тяжелая токсичность, такая как по меньшей мере длительная токсичность степени 3 или выше, или токсичность степени 4 или степени 5. В некоторых вариантах осуществления, пороговое количество RU представляет собой безопасное количество эталонных единиц, которое можно определять для группы или множества индивидов, которых сходным образом лечили с использованием терапевтической композиции T–клеток, и как правило, терапевтической композиции T–клеток, полученной, например, модифицированной, поддерживаемой в культуре, культивированной, активированной, криоконсервированной, с использованием одинаковых или сходных способов. В некоторых вариантах осуществления, множество индивидов включает по меньшей мере 10 индивидов, например, по меньшей мере 15, по меньшей мере 20, по меньшей мере 25, по меньшей мере 30, по меньшей мере 40, по меньшей мере 50, по меньшей мере 60, по меньшей мере 70, по меньшей мере 80, по меньшей мере 90, по меньшей мере 100 или более индивидов.
[0342] В некоторых вариантах осуществления, безопасное количество эталонных единиц составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, такой как CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события. В некоторых вариантах осуществления, неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность, необязательно, степени, равной или выше степени 4 или степени 5, или по меньшей мере длительной нейротоксичности степени 3.
[0343] В некоторых вариантах осуществления, целевое количество эталонных единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, и/или на количество в диапазоне от 1,5– до 3–кратного, необязательно, приблизительно 2–кратное, или на количество, кратное стандартному отклонению в группе индивидов, у которых не возникло неблагоприятного события, необязательно, нейротоксичности степени 0–2, необязательно, где кратное лежит в диапазоне от 1,5– до 3–кратного.
[0344] В некоторых вариантах осуществления, целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, которое можно определять для группы или множества индивидов, которых сходным образом лечили с использованием терапевтической композиции T–клеток, и как правило, терапевтической композиции T–клеток, полученной, например, модифицированной, поддерживаемой в культуре, культивированной, активированной, криоконсервированной, с использованием одинаковых или сходных способов. В некоторых вариантах осуществления, множество индивидов включает по меньшей мере 10 индивидов, например, по меньшей мере 15, по меньшей мере 20, по меньшей мере 25, по меньшей мере 30, по меньшей мере 40, по меньшей мере 50, по меньшей мере 60, по меньшей мере 70, по меньшей мере 80, по меньшей мере 90, по меньшей мере 100 или более индивидов. В некоторых вариантах осуществления, эффективное количество эталонных единиц составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, в которой показан желательный терапевтический исход, необязательно, частичный ответ или полный ответ (CR).
[0345] В некоторых вариантах осуществления, настоящее изобретение относится к способам, включающим введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащих клетки, содержащие рекомбинантный рецептор, такой как химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где или вводят целевое количество тотальных CD8+ клеток, экспрессирующих рекомбинантный рецептор, из терапевтической композиции, и/или вводят единичную дозу таких клеток, в которых вводят целевое количество эталонных единиц в пределах данного диапазона, как описано выше. В некоторых случаях, целевое количество эталонных единиц, которое вводят, равно или меньше порогового количества RU, таким образом, что единичная доза не содержит больше порогового значения RU. В некоторых аспектах, целевое количество тотальных CD8+ клеток с рекомбинантным рецептором, которое вводят, представляют собой CD8+, которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0346] В некоторых вариантах осуществления, представленные способы включают введение дозы, содержащей некоторое количество клеток, например, дозы, предоставляющей целевое количество клеток. В некоторых вариантах осуществления, доза, такая как целевое количество клеток, составляет между или между приблизительно 5,0×106 и 2,25×107, 5,0×106 и 2,0×107, 5,0×106 и 1,5×107, 5,0×106 и 1,0×107, 5,0×106 и 7,5×106, 7,5×106 и 2,25×107, 7,5×106 и 2,0×107, 7,5×106 и 1,5×107, 7,5×106 и 1,0×107, 1,0×107 и 2,25×107, 1,0×107 и 2,0×107, 1,0×107 и 1,5×107, 1,5×107 и 2,25×107, 1,5×107 и 2,0×107, 2,0×107 и 2,25×107, включая каждое. В некоторых вариантах осуществления, такая доза, например, такое целевое количество клеток, относится к общему количеству экспрессирующих рекомбинантный рецептор клеток в вводимой композиции. В некоторых вариантах осуществления, такая доза, например, такое целевое количество клеток, относится к общему количеству экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+. В некоторых вариантах осуществления, маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0347] В некоторых вариантах осуществления, доза клеток из единичной дозы содержит количество клеток, такое как целевое количество клеток, между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15 x106 экспрессирующих рекомбинантный рецептор клеток, таких как экспрессирующие рекомбинантный рецептор клетки, которые представляют собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0348] В некоторых вариантах осуществления, доза клеток из единичной дозы содержит количество клеток, такое как целевое количество клеток, между по меньшей мере или по меньшей мере приблизительно 5,55×106, 6,66×106, 7,77×106, 8,99×106, 1,0×107, 1,1×107 и приблизительно 1,67×107 экспрессирующих рекомбинантный рецептор клеток, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, например, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0349] В некоторых вариантах осуществления, доза клеток из единичной дозы содержит количество клеток, такое как целевое количество клеток, между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, например, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0350] В некоторых вариантах осуществления, доза клеток из единичной дозы содержит количество клеток, такое как целевое количество клеток, между по меньшей мере или по меньшей мере приблизительно между по меньшей мере или по меньшей мере приблизительно 7,14×106, 8,5×106, 1,0×107, 1,14×107, 1,29×107, 1,42×107 и приблизительно 2,14×107 экспрессирующих рекомбинантный рецептор клеток, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0351] В некоторых вариантах осуществления, доза клеток из единичной дозы содержит количество клеток, такое как целевое количество клеток, между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0352] В некоторых вариантах осуществления, доза клеток из единичной дозы содержит количество клеток, такое как целевое количество клеток, между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+.
[0353] В некоторых вариантах осуществления, способ включает введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащих клетки, содержащие рекомбинантный рецептор, такой как химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит целевое количество эталонных единиц (RU) в пределах данного диапазона. В некоторых вариантах осуществления, целевое количество эталонных единиц составляет менее, чем пороговое значение, например, менее, чем эталонный уровень безопасности. В некоторых аспектах, неблагоприятное событие представляет собой серьезное неблагоприятное событие, такое как тяжелая нейротоксичность степени, равной или выше степени 4 или степени 5, или по меньшей мере длительная нейротоксичность степени 3. В некоторых вариантах осуществления, пороговое значение составляет менее, чем эталонный уровень безопасности, на количество, соответствующее коэффициенту запаса безопасности, или по меньшей мере в 2 раза.
[0354] В некоторых вариантах осуществления, неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и пороговое значение: составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,0×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,5×107, если A представляет собой CD8+CAR+ и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение. В некоторых вариантах осуществления, маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0355] В некоторых вариантах осуществления, неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и данный диапазон целевых эталонных единиц: составляет между или приблизительно между 2,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 4×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 5×106 и 1,56×107 включительно, если A представляет собой CD8+CAR+ и B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 2,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 2,0×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 2,5×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+ и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение. В некоторых вариантах осуществления, маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0356] В некоторых вариантах осуществления, неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и пороговое значение: составляет или составляет приблизительно 1,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 1,25×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение; составляет или составляет приблизительно 1,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 1,88×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,12×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2; или его нормализованное значение; составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+ и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+ и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение. В некоторых вариантах осуществления, маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0357] В некоторых вариантах осуществления, неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и данный диапазон целевых эталонных единиц: составляет между или приблизительно между 3,0×105 и 1,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,25×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение; составляет между или приблизительно между 4×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 5×106 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение; составляет между или приблизительно между 2,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 2,5×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+ и B представляет собой IL–2 или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 1,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 1,88×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение; составляет между или приблизительно между 3,0×105 и 2,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 3,75×105 и 3,12×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 4,0×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение; составляет между или приблизительно между 5,0×105 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение. В некоторых вариантах осуществления, маркер апоптоза представляет собой аннексин V или активную каспазу 3.
[0358] В конкретных вариантах осуществления, клетки, или индивидуальные популяции подтипов клеток, вводят индивиду в диапазоне от приблизительно одного миллиона до приблизительно 100 миллиардов клеток и/или в количестве клеток на килограмм массы тела, например, таком как от 1 миллиона до приблизительно 50 миллиардов клеток (например, приблизительно 5 миллионов клеток, приблизительно 25 миллионов клеток, приблизительно 500 миллионов клеток, приблизительно 1 миллиард клеток, приблизительно 5 миллиардов клеток, приблизительно 20 миллиардов клеток, приблизительно 30 миллиардов клеток, приблизительно 40 миллиардов клеток, или в диапазоне, определяемом любыми двумя из предшествующих значений), например, от приблизительно 10 миллионов до приблизительно 100 миллиардов клеток (например, приблизительно 20 миллионов клеток, приблизительно 30 миллионов клеток, приблизительно 40 миллионов клеток, приблизительно 60 миллионов клеток, приблизительно 70 миллионов клеток, приблизительно 80 миллионов клеток, приблизительно 90 миллионов клеток, приблизительно 10 миллиардов клеток, приблизительно 25 миллиардов клеток, приблизительно 50 миллиардов клеток, приблизительно 75 миллиардов клеток, приблизительно 90 миллиардов клеток, или в диапазоне, определяемом любыми двумя из предшествующих значений), и, в некоторых случаях, приблизительно 100 миллионов клеток до приблизительно 50 миллиардов клеток (например, приблизительно 120 миллионов клеток, приблизительно 250 миллионов клеток, приблизительно 350 миллионов клеток, приблизительно 450 миллионов клеток, приблизительно 650 миллионов клеток, приблизительно 800 миллионов клеток, приблизительно 900 миллионов клеток, приблизительно 3 миллиарда клеток, приблизительно 30 миллиардов клеток, приблизительно 45 миллиардов клеток) или в любом количестве в пределах этих диапазонов и/или на килограмм массы тела. Дозы можно менять в зависимости от признаков, специфических для заболевания или нарушения, и/или пациента и/или другого лечения.
[0359] В некоторых вариантах осуществления, например, когда индивид представляет собой человека, доза включает менее, чем приблизительно 5×108 тотальных экспрессирующих рекомбинантный рецептор (например, CAR) клеток, T–клеток или мононуклеарных клеток периферической крови (PBMC), например, в диапазоне от приблизительно 1×106 до 5×108 таких клеток, например, 2×106, 5×106, 1×107, 5×107, 1×108, или 5×108 таких тотальных клеток, или в диапазоне между любыми двумя из предшествующих значений.
[0360] В некоторых вариантах осуществления, доза генетически модифицированных клеток содержит от или приблизительно от 1×105 до 5×108 тотальных экспрессирующих CAR T–клеток, 1×105 до 2,5×108 тотальных экспрессирующих CAR T–клеток, 1×105 до 1×108 тотальных экспрессирующих CAR T–клеток, 1×105 до 5×107 тотальных экспрессирующих CAR T–клеток, 1×105 до 2,5×107 тотальных экспрессирующих CAR T–клеток, 1×105 до 1×107 тотальных экспрессирующих CAR T–клеток, 1×105 до 5×106 тотальных экспрессирующих CAR T–клеток, 1×105 до 2,5×106 тотальных экспрессирующих CAR T–клеток, 1×105 до 1×106 тотальных экспрессирующих CAR T–клеток, 1×106 до 5×108 тотальных экспрессирующих CAR T–клеток, 1×106 до 2,5×108 тотальных экспрессирующих CAR T–клеток, 1×106 до 1×108 тотальных экспрессирующих CAR T–клеток, 1×106 до 5×107 тотальных экспрессирующих CAR T–клеток, 1×106 до 2,5×107 тотальных экспрессирующих CAR T–клеток, 1×106 до 1×107 тотальных экспрессирующих CAR T–клеток, 1×106 до 5×106 тотальных экспрессирующих CAR T–клеток, 1×106 до 2,5×106 тотальных экспрессирующих CAR T–клеток, 2,5×106 до 5×108 тотальных экспрессирующих CAR T–клеток, 2,5×106 до 2,5×108 тотальных экспрессирующих CAR T–клеток, 2,5×106 до 1×108 тотальных экспрессирующих CAR T–клеток, 2,5×106 до 5×107 тотальных экспрессирующих CAR T–клеток, 2,5×106 до 2,5×107 тотальных экспрессирующих CAR T–клеток, 2,5×106 до 1×107 тотальных экспрессирующих CAR T–клеток, 2,5×106 до 5×106 тотальных экспрессирующих CAR T–клеток, 5×106 до 5×108 тотальных экспрессирующих CAR T–клеток, 5×106 до 2,5×108 тотальных экспрессирующих CAR T–клеток, 5×106 до 1×108 тотальных экспрессирующих CAR T–клеток, 5×106 до 5×107 тотальных экспрессирующих CAR T–клеток, 5×106 до 2,5×107 тотальных экспрессирующих CAR T–клеток, 5×106 до 1×107 тотальных экспрессирующих CAR T–клеток, 1×107 до 5×108 тотальных экспрессирующих CAR T–клеток, 1×107 до 2,5×108 тотальных экспрессирующих CAR T–клеток, 1×107 до 1×108 тотальных экспрессирующих CAR T–клеток, 1×107 до 5×107 тотальных экспрессирующих CAR T–клеток, 1×107 до 2,5×107 тотальных экспрессирующих CAR T–клеток, 2,5×107 до 5×108 тотальных экспрессирующих CAR T–клеток, 2,5×107 до 2,5×108 тотальных экспрессирующих CAR T–клеток, 2,5×107 до 1×108 тотальных экспрессирующих CAR T–клеток, 2,5×107 до 5×107 тотальных экспрессирующих CAR T–клеток, 5×107 до 5×108 тотальных экспрессирующих CAR T–клеток, 5×107 до 2,5×108 тотальных экспрессирующих CAR T–клеток, 5×107 до 1×108 тотальных экспрессирующих CAR T–клеток, 1×108 до 5×108 тотальных экспрессирующих CAR T–клеток, 1×108 до 2,5×108 тотальных экспрессирующих CAR T–клеток, или 2,5×108 до 5×108 тотальных экспрессирующих CAR T–клеток.
[0361] В некоторых вариантах осуществления, доза генетически модифицированных клеток содержит по меньшей мере или по меньшей мере приблизительно 1×105 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 2,5×105 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 5×105 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 1×106 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 2,5×106 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 5×106 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 1×107 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 2,5×107 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 5×107 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 1×108 экспрессирующих CAR клеток, по меньшей мере или по меньшей мере приблизительно 2,5×108 экспрессирующих CAR клеток, или по меньшей мере или по меньшей мере приблизительно 5×108 экспрессирующих CAR клеток.
[0362] В некоторых вариантах осуществления, клеточная терапия включает введение дозы, содержащей количество клеток, от или приблизительно от 1×105 до 5×108 тотальных экспрессирующих рекомбинантный рецептор клеток, тотальных T–клеток или тотальных мононуклеарных клеток периферической крови (PBMC), от или приблизительно от 5×105 до 1×107 тотальных экспрессирующих рекомбинантный рецептор клеток, тотальных T–клеток, или тотальных мононуклеарных клеток периферической крови (PBMC), или от или приблизительно от 1×106 до 1×107 тотальных экспрессирующих рекомбинантный рецептор клеток, тотальных T–клеток, или тотальных мононуклеарных клеток периферической крови (PBMC), включая каждое. В некоторых вариантах осуществления, клеточная терапия включает введение дозы клеток, содержащей количество клеток по меньшей мере или приблизительно по меньшей мере 1×105 тотальных экспрессирующих рекомбинантный рецептор клеток, тотальных T–клеток, или тотальных мононуклеарных клеток периферической крови (PBMC), например, по меньшей мере или по меньшей мере 1×106, по меньшей мере или приблизительно по меньшей мере 1×107, по меньшей мере или приблизительно по меньшей мере 1×108 таких клеток. В некоторых вариантах осуществления, количество присутствует применительно к общему количеству CD3+ или CD8+, в некоторых случаях, также экспрессирующих рекомбинантный рецептор (например, CAR+) клеток. В некоторых вариантах осуществления, клеточная терапия включает введение дозы, содержащей количество клеток от или приблизительно от 1×105 до 5×108 CD3+ или CD8+ тотальных T–клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, от или приблизительно от 5×105 до 1×107 CD3+ или CD8+ тотальных T–клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, или от или приблизительно от 1×106 до 1×107 CD3+ или CD8+ тотальных T–клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, включая каждое. В некоторых вариантах осуществления, клеточная терапия включает введение дозы, содержащей количество клеток от или приблизительно от 1×105 до 5×108 тотальных CD3+/CAR+ или CD8+/CAR+ клеток, от или приблизительно от 5×105 до 1×107 тотальных CD3+/CAR+ или CD8+/CAR+ клетки, или от или приблизительно от 1×106 до 1×107 тотальных CD3+/CAR+ или CD8+/CAR+ клетки, включая каждое.
[0363] В некоторых вариантах осуществления, T–клетки из дозы включают CD4+ T–клетки, CD8+ T–клетки или CD4+ и CD8+ T–клетки.
[0364] В некоторых вариантах осуществления, например, когда индивид представляет собой человека, CD8+ T–клетки в дозе, включая дозу, включающую CD4+ и CD8+ T–клетки, включает между приблизительно 1×106 и 5×108, включительно, тотальных экспрессирующих рекомбинантный рецептор (например, CAR) CD8+клеток, например, в диапазоне от приблизительно 5×106 до 1×108 таких клеток, 1×107, 2,5×107, 5×107, 7,5×107, 1×108 или 5×108 тотальных таких клеток, или в диапазоне между любыми двумя из предшествующих значений. В некоторых вариантах осуществления, пациенту вводят множество доз, и каждая из доз или суммарная доза может находиться между любыми из предшествующих значений. В некоторых вариантах осуществления, доза клеток включает введение от или приблизительно от 1×107 до 0,75×108 тотальных экспрессирующих рекомбинантный рецептор CD8+ T–клеток, 1×107 до 2,5×107 тотальных экспрессирующих рекомбинантный рецептор CD8+ T–клеток, от или приблизительно от 1×107 до 0,75×108 тотальных экспрессирующих рекомбинантный рецептор CD8+ T–клеток, включая каждое. В некоторых вариантах осуществления, доза клеток включает введение или введение приблизительно 1×107, 2,5×107, 5×107 7,5×107, 1×108, или 5×108 тотальных экспрессирующих рекомбинантный рецептор CD8+ T–клеток.
[0365] В некоторых вариантах осуществления, дозу клеток, например, экспрессирующих рекомбинантный рецептор T–клеток, вводят индивиду в форме однократной дозы или вводят только один раз в пределах периода двух недель, одного месяца, трех месяцев, шести месяцев, 1 года или более.
[0366] В контексте адоптивной клеточной терапии, введение данной «дозы» включает введение данного количества или количества клеток в форме одиночной композиции и/или однократного непрерывного введения, например, в форме однократной инъекции или непрерывной инфузии, а также включает введение данного количества или количества клеток в форме дробной дозы, представленной во множестве индивидуальных композиций или инфузий, на протяжении указанного периода времени, который составляет не более 3 суток. Таким образом, в некоторых контекстах, доза представляет собой однократное или непрерывное введение указанного количества клеток, проведенное или начатое в отдельной временной точке. В некоторых контекстах, однако, дозу вводят во множестве инъекций или инфузий на протяжении периода не более трех суток, например, один раз в сутки в течение трех суток или в течение двух суток или посредством множества инфузий на протяжении периода одних суток.
[0367] Таким образом, в некоторых аспектах, клетки из дозы вводят в одной фармацевтической композиции. В некоторых вариантах осуществления, клетки из дозы вводят во множестве композиций, совместно содержащих клетки из первой дозы.
[0368] Термин «дробной дозы» относится к дозе, которая разделена таким образом, что ее вводят на протяжении более чем одних суток. Этот тип дозирования включают в настоящие способы и считают представляющим собой однократную дозу.
[0369] Таким образом, дозу, в некоторых аспектах, можно вводить в форме дробной дозы. Например, в некоторых вариантах осуществления, дозу можно вводить индивиду в течение 2 суток или в течение 3 суток. Иллюстративные способы дробного дозирования включают введение 25% дозы на первые сутки и введение оставшихся 75% дозы на вторые сутки. В других вариантах осуществления, 33% из первой дозы можно вводить на первые сутки и оставшиеся 67% вводить на вторые сутки. В некоторых аспектах, 10% дозы вводят на первые сутки, 30% дозы вводят на вторые сутки и 60% дозы вводят на третьи сутки. В некоторых вариантах осуществления, дробную дозу не распределяют более чем на 3 суток.
[0370] В некоторых вариантах осуществления, клетки вводят в желательной дозе, которая, в некоторых аспектах, включает желательные дозу или количество клеток или типа(типов) клеток и/или желательное соотношение типов клеток. Таким образом, дозирование клеток в некоторых вариантах осуществления основано на целевом количестве тотальных клеток или целевом эталонном количестве единиц и желательном соотношении индивидуальных популяций или подтипов, таком как соотношение CD4+ и CD8+. В некоторых вариантах осуществления, дозирование клеток основано на желательном целевом количестве тотальных клеток или целевом эталонном количестве единиц в индивидуальных популяциях или для индивидуальных типов клеток. В некоторых вариантах осуществления, дозирование основано на комбинации таких признаков, например, желательного общего количества клеток, целевого количества эталонных единиц, желательного соотношения и желательного общего количества клеток в индивидуальных популяциях.
[0371] В некоторых вариантах осуществления, популяции или подтипы клеток, таких как CD8+ и CD4+ T–клетки, вводят в желательной дозе или в пределах переносимых различий желательной дозы общего количества клеток, например, желательной дозы T–клеток. В некоторых аспектах, желательная доза представляет собой желательное количество клеток или желательное количество клеток на единицу массы тела индивида, которому вводят клетки, например, клеток/кг. В некоторых аспектах, желательная доза представляет собой или превышает минимальное количество клеток или минимальное количество клеток на единицу массы тела. В некоторых аспектах, среди тотальных клеток, введенных в желательной дозе, индивидуальные популяции или подтипы присутствуют в желательном соотношении или приблизительно в желательном соотношении на выходе (таком как соотношение CD4+ и CD8+), например, в пределах определенных переносимых различий или ошибки такого соотношения.
[0372] В некоторых вариантах осуществления, клетки вводят в желательной дозе или в пределах переносимых различий желательной дозы одного или нескольких из индивидуальных популяций или подтипов клеток, таких как желательная доза CD4+ клеток и/или желательная доза CD8+ клеток. В некоторых аспектах, желательная доза представляет собой желательное количество клеток из подтипа или популяции, или желательное количество таких клеток на единицу массы тела индивида, которому вводят клетки, например, клеток/кг. В некоторых аспектах, желательная доза представляет собой или превышает минимальное количество клеток из популяции или подтипа, или минимальное количество клеток из популяции или подтипа на единицу массы тела.
[0373] Таким образом, в некоторых вариантах осуществления, дозирование основано на желательной фиксированной дозе общего количества клеток и желательном соотношении, и/или основано на желательной фиксированной дозе одного или нескольких, например, каждого, из индивидуальных подтипов или субпопуляций. Таким образом, в некоторых вариантах осуществления, дозирование основано на желательной фиксированной дозе, которая может представлять собой или превышать минимальную дозу T–клеток и/или представлять собой или превышать максимальную дозу, и в некоторых аспектах, желательное соотношение CD4+ и CD8+ клеток, и/или основано на желательной фиксированной дозе CD4+ и/или CD8+ клеток.
[0374] В некоторых вариантах осуществления, целевая доза или доза включает или включает приблизительно, или составляет менее чем или приблизительно 5×106 CD8+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 7×106 CD8+ CAR+ клеток или CD3+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 8×106 CD8+ CAR+ клеток или CD3+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 8×106CD8+ CAR+ клеток или CD3+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 9×106 CD8+ CAR+ клеток или CD3+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 10×106 CD8+ CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 11×106 CD8+ CAR+ клеток или CD3+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 12×106 CD8+ CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 13×106 CD8+ CAR+ клеток или CD3+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 14×106 CD8+ CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 15×106 CD8+ CAR+ клеток или CD3+CAR+ клеток, включает или включает приблизительно, или составляет менее чем или приблизительно 20×106 или 30×106 или 40×106 или 50×106 CD8+ CAR+ клеток или CD3+CAR+ клеток. В некоторых аспектах таких вариантов осуществления, для или приблизительно для, или по меньшей мере для или приблизительно для 70, 75, 80, 85 или 90% CD8+CAR+ клеток из такой дозы показаны одно или несколько свойств или фенотипов, показательных для здоровья клеток или биологически активной клетки с CAR, таких как отсутствие маркера апоптоза, и/или в способе, использованном для получения клеток, достигают процента таких клеток среди CD8+CAR+ клеток в дозе в пределах 70–90% или в среднем, 80% кратности. В некоторых аспектах, изменчивость частоты биологически активных или функциональных, или неапоптотических клеток среди дозы составляет менее, чем пороговое значение, и/или частота не является изменчивой за пределами диапазона 70–80% более чем на 1, 5, 10 или 20% кратности.
[0375] В некоторых вариантах осуществления, клетки вводят в желательном соотношении на выходе или в пределах переносимого диапазона желательного соотношения на выходе множества популяций или подтипов клеток, таких как клетки или подтипы CD4+ и CD8+. В некоторых аспектах, желательное соотношение может представлять собой конкретное соотношение или может представлять собой диапазон соотношений. например, в некоторых вариантах осуществления, желательное соотношение (например, соотношение CD4+ и CD8+ клеток) составляет между 1:5 или приблизительно 1:5 и 5:1 или приблизительно 5:1 (или более чем приблизительно 1:5 и менее чем приблизительно 5:1), или между 1:3 или приблизительно 1:3 и 3:1 или приблизительно 3:1 (или более чем приблизительно 1:3 и менее чем приблизительно 3:1), например, между 2:1 или приблизительно 2:1 и 1:5 или приблизительно 1:5 (или более чем приблизительно 1:5 и менее чем приблизительно 2:1, включая каждое, или например, составляет или составляет приблизительно 5:1, 4,5:1, 4:1, 3,5:1, 3:1, 2,5:1, 2:1, 1,9:1, 1,8:1, 1,7:1, 1,6:1, 1,5:1, 1,4:1, 1,3:1, 1,2:1, 1,1:1, 1:1, 1:1,1, 1:1,2, 1:1,3, 1:1,4, 1:1,5, 1:1,6, 1:1,7, 1:1,8, 1:1,9: 1:2, 1:2,5, 1:3, 1:3,5, 1:4, 1:4,5, или 1:5. В некоторых аспектах, переносимое различие находится в пределах приблизительно 1%, приблизительно 2%, приблизительно 3%, приблизительно 4% приблизительно 5%, приблизительно 10%, приблизительно 15%, приблизительно 20%, приблизительно 25%, приблизительно 30%, приблизительно 35%, приблизительно 40%, приблизительно 45%, приблизительно 50% от желательного соотношения, включая любое количестве в пределах этих диапазонов.
B. Специфические для пациента и/или клинические факторы
[0376] В некоторых из представленных вариантов осуществления, дозу клеток в соответствии со способами, представленными в настоящем описании, можно вводить индивиду со специфическим для пациента и/или клиническим фактором риска, таким как любой, описанный в настоящем описании. В некоторых вариантах осуществления, среди таких подвергнутых лечению индивидов, способ не приводит к существенному различию, не приводит к значимому различию или не приводит к различию выше порогового уровня или степени, частоты возникновения или риска токсичности, например, тяжелого неблагоприятного побочного эффекта, CRS и/или нейротоксичности, или их степени, по сравнению с общей группой подвергнутых лечению индивидов, в соответствии с этим способом, или индивидами, не имеющими такого специфического для пациента или клинического фактора риска. В конкретных вариантах осуществления, различие для индивидов, имеющих такой фактор риска, по сравнению с общим количеством индивидов или индивидами без фактора риска, составляет не более чем 1%, 5%, 10%, 15%, 20%, 25% или 30%, 35% или 40%. В некоторых вариантах осуществления, токсичность представляет собой CRS. В конкретных вариантах осуществления, токсичность представляет собой CRS степени 2 или выше, степени 3 или выше, степени 4 или выше, или степени 5. В конкретных вариантах осуществления, токсичность представляет собой нейротоксичность. В конкретных вариантах осуществления, токсичность представляет собой нейротоксичность степени 2 или выше, степени 3 или выше, степени 4 или выше, или степени 5. В некоторых вариантах осуществления, токсичность представляет собой или ассоциирована с отеком головного мозга.
[0377] В конкретных вариантах осуществления, дозу клеток в соответствии со способами, представленными в настоящем описании, вводят индивиду без специфического для пациента и/или клинического фактора, такого как любой, описанный в настоящем описании. В некоторых вариантах осуществления, уменьшенную и/или более низкую дозу клеток вводят индивиду со специфическим для пациента и/или клиническим фактором. В конкретных вариантах осуществления, уменьшенная и/или более низкая доза составляет или составляет по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 95% менее, чем доза, которую вводят индивиду без специфического для пациента и/или клинического фактора. В конкретных вариантах осуществления, не присутствует значимого различия частоты возникновения токсичности, например, тяжелого неблагоприятного побочного эффекта, CRS и/или нейротоксичности, между индивидами без специфического для пациента и/или клинического фактора, которым вводят дозу клеток, и индивидами со специфическим для пациента и/или клиническим фактором, которым вводят более низкую дозу клеток.
[0378] В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой количество предшествующих циклов терапии, например, один или несколько циклов терапии до начала введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, предшествующие циклы терапии проводили для лечения того же заболевания и/или состояния, что и в случае терапевтической композиция T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой менее, чем десять предшествующих циклов терапии, девять предшествующих циклов терапии, восемь предшествующих циклов терапии, семь предшествующих циклов терапии, шесть предшествующих циклов терапии, пять предшествующих циклов терапии, четыре предшествующих цикла терапии, три предшествующих цикла терапии, два предшествующих цикла терапии или менее, чем один предшествующий цикл терапии. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой менее, чем три предшествующих цикла терапии. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой два или менее циклов предшествующей терапии.
[0379] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой возраст, например, возраст индивида на начало введения терапевтической композиции T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой молодой и/или относительно молодой возраст. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой возраст менее чем 65 лет, 60 лет, 55 лет, 50 лет, 45 лет, 40 лет, 35 лет, 30 лет, 25 лет, или 20 лет. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой возраст менее чем 30 лет.
[0380] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой соотношение CD4:CD8 T–клеток в образце после афереза от индивида. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой соотношение CD4:CD8 T–клеток в образце после афереза ниже определенного порога. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой соотношение CD4:CD8 T–клеток ниже 3:1, 2:1, 1,5:1, 1:1, 0,9:1, 0,8:1, 0,7:1, 0,6:1, 0,5:1, 0,4:1, 0,3:1, 0,2:1 или 0,1:1. В конкретных вариантах осуществления, соотношение CD4:CD8 T–клеток в образце после афереза представляет собой специфический для пациента и/или клинический фактор, когда вводимая доза основана на общем количестве T–клеток или общем количестве T–клеток, экспрессирующих рекомбинантный рецептор. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой соотношение CD4:CD8 T–клеток в образце после афереза ниже 1:5, ниже 1:1 или ниже 0,5:1.
[0381] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой массу индивида, например, массу тела. В конкретных вариантах осуществления, масса индивида представляет собой массу индивида на время введения терапевтической композиции T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой массу более 100 фунтов (41,0 кг), более 125 фунтов (51,2 кг), более 150 фунтов (61,4 кг), более 175 фунтов (71,7 кг), более 200 фунтов (81,9 кг), более 225 фунтов (92,1 кг), более 250 фунтов (102,4 кг), более 275 фунтов (112,6 кг), более 300 фунтов (122,9 кг), более 350 фунтов (143,3 кг) или более 400 фунтов (163,8 кг) В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой массу более 50 кг, 60 кг, 70 кг, 80 кг, 90 кг, 100 кг, 125 кг, 150 кг, 175 кг, или 200 кг. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой массу, превышающую среднюю массу среди группы индивидов. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой массу, превышающую среднее, медиану и/или моду массы среди группы индивидов. В некоторых вариантах осуществления, группу индивидов подвергают лечению с использованием такой же терапевтической композиции клеток.
[0382] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой количество тромбоцитов. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой количество тромбоцитов менее чем или приблизительно менее чем 500000, менее чем 450000, менее чем 400000, менее чем 350000, менее чем 300000, менее чем 250000, менее чем 200000, менее чем 180000, менее чем 160000, менее чем 140000, менее чем 120000, менее чем 100000, менее чем 75000, менее чем 50000 или менее чем 25000. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой количество тромбоцитов менее чем 120000.
[0383] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой наличие лейкоза. В некоторых вариантах осуществления, специфический для пациента или клинический фактор представляет собой наличие B–клеточного лейкоза. В конкретных вариантах осуществления, лейкоз представляет собой острый лимфобластный лейкоз (ALL), неходжскинскую лимфому (NHL), хронический лимфоцитарный лейкоз (CLL), диффузную крупноклеточную B–клеточную лимфому (DLBCL), или острый миелоидный лейкоз (AML). В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой наличие острого лимфоцитарного лейкоза (ALL).
[0384] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой высокую нагрузку заболевания, например, высокую нагрузку заболевания до начала введения терапевтической композиции T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой высокую нагрузку заболевания непосредственно до, или в пределах 1 недели, 2 недель, 3 недель, 4 недель, 5 недель, 6 недель, 7 недель, 8 недель, 9 недель, одного месяца, двух месяцев, трех месяцев, четырех месяцев, пяти месяцев, шести месяцев, или более чем шести месяцев до начала введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, высокую нагрузку заболевания определяют на основании процента бластных клеток костного мозга. В конкретных вариантах осуществления, высокая нагрузка заболевания представляет собой больше или равно 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, или 10% бластных клеток. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой нагрузку заболевания более чем 5% бластных клеток непосредственно до, или в пределах одного месяца до начала введения терапевтической композиции T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой высокую нагрузку заболевания, такую как сумма произведений диаметров (SPD) или уровни лактатдегидрогеназы.
[0385] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой высокую опухолевую нагрузку, например, a высокую нагрузку заболевания до начала введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, фактор, показательный для опухолевой нагрузки представляет собой показатель объема опухоли(опухолей). В некоторых вариантах осуществления, показатель объема представляет собой показатель очага(очагов), такой как размер опухоли, диаметр опухоли, объем опухоли, масса опухоли, нагрузка или основной объем опухоли, связанный с опухолью отек, связанный с опухолью некроз, и/или количество или степень метастазов. В некоторых вариантах осуществления, показатель объема опухоли представляет собой двумерное измерение. Например, в некоторых вариантах осуществления, площадь очага(очагов) рассчитывают как произведение наиболее длинного диаметра и наиболее длинного перпендикулярного диаметра для всех поддающихся измерению опухолей. В некоторых случаях, показатель объема опухоли представляет собой одномерное измерение. В некоторых случаях, размер поддающихся измерению очагов оценивают как наиболее длинный диаметр. В некоторых вариантах осуществления, измеряют сумму произведений диаметров (SPD), наиболее длинный диаметр опухолей (LD), сумму наиболее длинных диаметров опухолей (SLD), некроз, объем опухоли, объем некроза, соотношение некроза–опухоли (NTR), перитуморальный отек (PTE), и соотношение отека–опухоли (ETR).
[0386] Иллюстративные способы измерения и оценки опухолевой нагрузки включают способы, описанные, например, в Carceller et al., Pediatr Blood Cancer. (2016) 63(8):1400–1406 и Eisenhauer et al., Eur J Cancer. (2009) 45(2):228–247. В некоторых вариантах осуществления, волюметрический показатель представляет собой сумму произведений диаметров (SPD), измеренную посредством определения суммы произведений наибольших перпендикулярных диаметров для всех поддающихся измерению опухолей. В некоторых аспектах, опухоль или очаг измеряют в одном направлении с использованием наиболее длинного диаметра (LD) и/или посредством определения суммы наиболее длинных диаметров опухолей (SLD) для всех поддающихся измерению очагов. В некоторых вариантах осуществления, показатель объема опухоли представляет собой волюметрическую количественную оценку некроза опухоли, такую как объем некроза и/или соотношение некроза–опухоли (NTR), см. Monsky et al., Anticancer Res. (2012) 32(11): 4951–4961. В некоторых аспектах, показатель объема опухоли представляет собой волюметрическую количественную оценку связанного с опухолью отека, такую как перитуморальный отек (PTE) и/или соотношение отека–опухоли (ETR). В некоторых вариантах осуществления, измерение можно проводить с использованием способов визуализации, таких как компьютерная томография (КТ), позитронная эмиссионная томография (PET), и/или магнитно–резонансная томография (МРТ) индивида.
[0387] В некоторых вариантах осуществления, показатель объема представляет собой SPD и в некоторых случаях, возникновение токсичности, например, CRS или NT, коррелирует с значением SPD, превышающим пороговое значение. В некоторых вариантах осуществления, показатель объема представляет собой SPD, и пороговое значение составляет или составляет приблизительно 30 на см2, составляет или составляет приблизительно 40 на см2, составляет или составляет приблизительно 50 на см2, составляет или составляет приблизительно 60 на см2, или составляет или составляет приблизительно 70 на см2. В некоторых вариантах осуществления, показатель объема представляет собой SPD, и пороговое значение составляет или составляет приблизительно 30 на см2, составляет или составляет приблизительно 40 на см2, составляет или составляет приблизительно 50 на см2, составляет или составляет приблизительно 60 на см2, или составляет или составляет приблизительно 70 на см2. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой SPD более чем 30 на см2, более чем 40 на см2, более чем 50 на см2, более чем 60 на см2, или более чем 70 на см2.
[0388] В некоторых вариантах осуществления, показатель объема опухоли определяют на стадии скрининга, такой как общепринятая оценка или отбор крови для подтверждения и/или идентификации состояния или заболевания у индивида.
[0389] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой уровень, количество и/или концентрацию маркера воспаления. В некоторых вариантах осуществления, маркер воспаления представляет собой или включает уровень или присутствие C–реактивного белка (CRP), скорость оседания эритроцитов (ESR), альбумин, ферритин, β2–микроглобулин (β2–M) или лактат–дегидрогеназу (LDH), детектированные и оцененные. В некоторых вариантах осуществления, маркер воспаления оценивают с использованием иммуноанализа. Например, твердофазный иммуноферментный анализ (ELISA), ферментный иммуноанализ (EIA), радиоиммунный анализ (RIA), поверхностный плазмонный резонанс (SPR), Вестерн–блоттинг, горизонтальный проточный анализ, иммуногистохимию, массив белков или иммуно–ПЦР (iPCR) можно использовать для детекции маркера воспаления. В некоторых вариантах осуществления, присутствие, уровень, количество, и/или концентрация маркера воспаления являются показательными для опухолевой нагрузки, например, высокой опухолевой нагрузки. В некоторых случаях, анализ или оценку маркера воспаления проводят с использованием проточной цитометрии. В некоторых случаях, реагент представляет собой растворимый белок который связывается с маркером воспаления. В некоторых примерах, реагент представляет собой белок, который связан с C–реактивным белком (CRP), скоростью оседания эритроцитов (ESR), альбумином, ферритином, β2–микроглобулином (β2–M) или лактат–дегидрогеназой (LDH).
[0390] В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой уровень, количество или концентрацию маркера воспаления, составляющие более чем или составляющие более чем приблизительно, или составляющие 5%, 10%, 15%, 20%, 25%, 30%, 40%, 50%, 75%, 100%, 150%, 1–кратное, 2–кратное, 3–кратное, 4–кратное, 5–кратное от усредненного, медианы или среднего, и/или на 3, 2,5, 2, 1,5, 1, 0,8, 0,6, 0,5, 0,4, 0,3, 0,2, или 0,1 стандартных отклонения превышающие медиану или среднее уровня, количества или концентрации маркера воспаления, измеренных в образцах, полученных от группы индивидов до введения терапевтической композиции T–клеток, где у каждого индивида из группы не продолжалось развитие токсичности степени 2 или выше, степени 3 или выше, длительная токсичность степени 3 или выше, степени 4 или выше, или токсичность степени 5 после введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, токсичность представляет собой нейротоксичность.
[0391] В некоторых вариантах осуществления, биомаркер, например, маркер воспаления представляет собой или включает C–реактивный белок (CRP). В некоторых вариантах осуществления, CRP оценивают с использованием твердофазного иммуноферментного анализа in vitro для получения количественного показателя CRP человека для образца, такого как сыворотка, плазма или кровь. В некоторых примерах, CRP детектируют с использованием твердофазного иммуноферментного анализа (ELISA) для человека. В некоторых вариантах осуществления, биомаркер, например, маркер воспаления, представляет собой или включает скорость оседания эритроцитов (ESR). В некоторых вариантах осуществления, ESR оценивают посредством измерения расстояния (в миллиметрах в час), на которое падают красные клетки после отделения от плазмы в вертикальной пипетке или пробирке. В некоторых вариантах осуществления биомаркер представляет собой или включает альбумин. В некоторых аспектах, альбумин оценивают с использованием колориметрического теста или твердофазного иммуноферментного анализа in vitro. В некоторых примерах, альбумин детектируют с использованием твердофазного иммуноферментного анализа (ELISA) для человека. В некоторых вариантах осуществления, биомаркер, например, маркер воспаления, представляет собой или включает ферритин или β2–микроглобулин. В некоторых вариантах осуществления, ферритин или β2–микроглобулин оценивают с использованием иммуноанализа или детектируют с использованием ELISA. В некоторых аспектах, биомаркер, например, маркер воспаления, представляет собой или включает лактат–дегидрогеназу (LDH), и LDH оценивают с использованием колориметрического теста или твердофазного иммуноферментного анализа in vitro.
[0392] В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой уровень, концентрацию и/или количество LDH. В некоторых вариантах осуществления, возникновение токсичности, например, CRS или NT, коррелирует с значением LDH, превышающим пороговое значение. В некоторых вариантах осуществления, маркер воспаления представляет собой LDH, и пороговое значение составляет или составляет приблизительно 300 единиц на литр, составляет или составляет приблизительно 400 единиц на литр, составляет или составляет приблизительно 500 единиц на литр или составляет или составляет приблизительно 600 единиц на литр. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор риска составляет по меньшей мере 300 единиц на литр, по меньшей мере 400 единиц на литр, по меньшей мере 500 единиц на литр или по меньшей мере 600 единиц на литр.
[0393] В некоторых вариантах осуществления, уровень, концентрация и/или количество LDH представляет собой суррогат для нагрузки заболевания, например, для опухолей или злокачественных опухолей, и может быть полезным для оценки потенциального риска нейротоксичности и/или адаптированного с учетом риска дозирования, или коррекции лечения конкретных индивидов. В некоторых аспектах, уровни LDH можно оценивать отдельно и/или в комбинации с другим параметром до лечения, таким как другой показатель или индикатор нагрузки заболевания, например, волюметрический показатель опухоли, такой как сумма произведений измерений (SPD) или другой основанный на КТ или основанный на МРТ волюметрический показатель нагрузки заболевания, такой как любой, описанный в настоящем описании. В некоторых аспектах, оценивают один или несколько параметров, которые являются показательными для нагрузки заболевания, и в некоторых контекстах, могут указывать на присутствие, отсутствие или степень риска возникновения нейротоксичности после T–клеточной терапии. В некоторых аспектах, один или несколько параметров включают LDH и/или a волюметрический показатель опухоли. В некоторых вариантах осуществления, параметр представляет собой SPD и/или LDH.
[0394] В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой подвергание переходной химиотерапии до начала введения терапевтической композиции T–клеток.
[0395] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой предварительную подготовка с использованием противолимфоцитарной терапии, например, до начала введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, противолимфоцитарная терапия представляет собой или включает проведение химиотерапии. В конкретных вариантах осуществления, противолимфоцитарная терапия представляет собой или включает введение. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой предварительную подготовку с использованием флударабина и/или циклофосфамида до начала введения терапевтической композиции T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой предварительную подготовку с использованием циклофосфамида до начала введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой предварительную подготовку с использованием флударабина и циклофосфамида до начала введения терапевтической композиции T–клеток.
[0396] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой молекулярный подтип заболевания. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой молекулярный подтип лейкоза. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой молекулярный подтип ALL. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой молекулярный подтип ALL, не являющийся положительным по филадельфийской хромосоме (Ph+) или подобным подтипу с филадельфийской хромосомой (Ph) молекулярным подтипом ALL, такой как не–Ph молекулярный подтип. В конкретных вариантах осуществления, не–Ph молекулярные подтипы ALL включают, но без ограничения, подтипы, ассоциированные с слиянием TCF3–PBX1, слиянием ETV6–RUNX1, слиянием EP300–ZNF384, слиянием KMT2A–AFF1, гиперплоидией или хромосомной аномалией dic(9;20), например, dic(9;20)(p13,2;q11,2).
[0397] В конкретных вариантах осуществления, филадельфийская хромосома содержит транслокацию, t(9;22)(q34;ql 1), приводящую к образованию новго химерного гена и белка, со слиянием гена BCR на хромосоме 22 с геном, кодирующим тирозинкиназу Абельсона (ABL1), на хромосоме 9. В конкретных вариантах осуществления, подобный подтипу с филадельфийской хромосомой (Ph–подобный) подтип ALL характеризуется связанными профилями экспрессии генов, различным образом обозначаемыми как профиль «группы кластера R8», «подобный подтипу с филадельфийской хромосомой (Ph)», «Ph–подобный», «BCR–ABLl–подобный» профиль или «профиль экспрессии гена активированной тирозинкиназы». Для этих профилей экспрессии генов показано высокое сходство с профилями экспрессии генов, измеренными для Ph+ индивидов с ALL, несмотря на тот факт, что, в некоторых вариантах осуществления, Ph–подобные индивиды не имеют транслокации филадельфийской хромосомы или слитого транскрипта BCR–ABLl. Методы и способы идентификации и/или определения Ph+ и/или a Ph–подобного подтипов ALL описаны (см., например, Roberts et al., N Engl J Med (2014) 371(11): 1005–1015; Roberts et al. Cancer Cell (2012) 14;22(2):153–66; Perez–Andreu et al. Nature Genetics (2013) 45(12): 1494–1498; Yap et al. Leuk Lymphoma (2017) 58(4): 950–958; Roberts et al. J Clin Oncol (2017) 35(4): 394–401; Harvey et al. Blood (2013) 122:826; Harvey et al., Blood (2010) 116(23): 4874–4884; и заявку Pct No. WO 2013/090419, полное содержание которых, таким образом, приведено в качестве ссылки).
[0398] В некоторых вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой уровень, количество или концентрацию цитокина в образце крови, сыворотки или плазмы до начала введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, цитокин представляет собой интерлейкин, например, интерлейкин–15 (IL–15). В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой увеличенные уровень, количество или концентрацию IL–15 в образце крови до начала введения терапевтической композиции T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой уровень, количество или концентрацию IL–15, составляющие больше или равно 1 пг/мл, 5 пг/мл, 10 пг/мл, 15 пг/мл, 20 пг/мл, 25 пг/мл, 30 пг/мл, 35 пг/мл, 40 пг/мл, 45 пг/мл, 50 пг/мл, 100 пг/мл, 150 пг/мл, 200 пг/мл, 250 пг/мл, или 300 пг/мл в образце крови, сыворотки или плазмы до начала введения терапевтической композиции T–клеток. В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой уровень, количество или концентрацию IL–15, составляющие больше или равно 30 пг/мл в образце крови, сыворотки или плазмы до начала введения терапевтической композиции T–клеток.
[0399] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой уровень, количество или концентрацию IL–15, составляющие более чем или составляющие более чем приблизительно, или составляющие 5%, 10%, 15%, 20%, 25%, 30%, 40%, 50%, 75%, 100%, 150%, 1–кратное, 2–кратное, 3–кратное, 4–кратное, 5–кратное от усредненного, медианы или среднего, и/или на 3, 2,5, 2, 1,5, 1, 0,8, 0,6, 0,5, 0,4, 0,3, 0,2, или 0,1 стандартных отклонения превышающие медиану или среднее уровня, количества или концентрации IL–15 в образцах крови, полученных от группы индивидов до введения терапевтической композиции T–клеток, содержащих дозу клеток, модифицированных с использованием рекомбинантного рецептора, где у каждого индивида из группы не продолжалось развитие токсичности степени 2 или выше, степени 3 или выше, длительная токсичность степени 3 или выше, степени 4 или выше, или токсичность степени 5 после введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, токсичность представляет собой нейротоксичность.
[0400] В конкретных вариантах осуществления, специфический для пациента и/или клинический фактор представляет собой фармакокинетическое свойство композиции клеток после ее введения индивиду, например, представляет собой размножение in vivo экспрессирующих рекомбинантный рецептор клеток, например, CAR–T–клеток. В некоторых вариантах осуществления, фармакокинетический параметр может включать воздействие, количество, концентрацию, персистенция и пролиферация. В некоторых случаях, фармакокинетику можно оценивать посредством измерения таких параметров, как максимальная (пиковая) концентрация в плазме (Cмакс.), пиковое время (т.е. когда возникает максимальная концентрация в плазме (Cмакс.); Tмакс.), минимальная концентрация в плазме (т.е. минимальная концентрация в плазме между дозами лекарственного средства, например, CAR+ T–клеток; Cмин.), время полувыведения (T1/2) и площадь под кривой (т.е. площадь под кривой, полученной при нанесении на график времени против концентрации в плазме лекарственного средства CAR+ T–клеток; AUC), после введения. Концентрацию конкретного лекарственного средства, например, CAR+ T–клеток, в плазме после введения можно измерять с использованием любого способа, известного в данной области, пригодного для оценки концентраций лекарственных средств, например, CAR+ T–клеток, в образцах крови, или любых способов, описанных в настоящем описании. Например, можно использовать способы на основе нуклеиновой кислоты, такие как способы на основе количественной ПЦР (QПЦР) или проточной цитометрии, или других анализов, таких как иммуноанализ, ELISA, или анализы на основе хроматографии/масс–спектрометрии.
[0401] В некоторых вариантах осуществления, фармакокинетику (PK) введенных клеток, например, композиции CAR+ T–клеток, определяют для оценки доступности, например, биодоступности, веденных клеток. В некоторых вариантах осуществления, определяемые фармакокинетические параметры веденных клеток включают максимальные (пиковые) концентрации в плазме (Cмакс.), такие как Cмакс. CD3+ CAR+ клеток, CD4+ CAR+ клеток и или CD8+ CAR+ T–клеток; временную точку, в которой достигают Cмакс. (Tмакс.), такую как Tмакс. CD3+ CAR+ клеток, CD4+ CAR+ клеток и или CD8+ CAR+ T–клеток, и/или площадь под кривой (AUC), такую как AUC0–28, CD3+ CAR+ клеток, CD4+ CAR+ клеток и или CD8+ CAR+ T–клетки. В некоторых вариантах осуществления, фармакокинетический параметр представляет собой пиковую концентрацию CD3+ CAR+ T–клеток (Cмакс. CD3+ CAR+ T–клеток) или концентрацию CD8+ CAR+ T–клеток (Cмакс. CD8+ CAR+ T–клеток). В некоторых вариантах осуществления, фармакокинетический параметр представляет собой AUC0–28, CD3+ CAR+ T–клеток, (AUC0–28 CD3+ CAR+ T–клеток) или AUC0–28, CD8+ CAR+ T–клеток, (AUC0–28 CD8+ CAR+ T–клеток).
[0402] Воздействие, например, количество или концентрацию клеток, например, T–клеток, введенных для T–клеточной терапии, показательные для размножения и/или персистенции, можно указывать применительно к максимальным количествам или концентрациям клеток, воздействию которых подвергают индивида, длительности присутствия поддающихся детекции клеток или клеток выше определенного количества или процента, площади под кривой (AUC) количества или концентрации клеток в зависимости от времени, и/или к их комбинациям и индикаторам. Такие исходы можно оценивать с использованием известных способов, таких как QПЦР для детекции количества копий нуклеиновой кислоты, кодирующей рекомбинантный рецептор, по сравнению с общим количеством нуклеиновой кислоты или ДНК в конкретном образце, например, крови, сыворотки, плазмы или ткани, таком как образец ткани, и/или анализы проточной цитометрии, детектирующие клетки, экспрессирующие рецептор, как правило, с использованием антител, специфических для рецепторов. Анализы на основе клеток также можно использовать для детекции количества или процента, или концентрации функциональных клеток, таких как клетки, способные к связыванию и/или нейтрализации и/или индукции ответов, например, цитотоксических ответов, против клеток, связанных с заболеванием или состоянием, или экспрессирующих антиген, узнаваемый рецептором.
[0403] В некоторых вариантах осуществления воздействие можно указывать, как площадь под кривой зависимости концентрации лекарственного средства от времени (AUC), как определено посредством фармакокинетического анализа после введения дозы лекарственного средства, например, CAR+ T–клеток. В некоторых случаях, AUC выражают в клетках*сутки/мкл, для клеток, вводимых в клеточной терапии, или в соответствующих им единицах. В некоторых вариантах осуществления, AUC измеряют как среднюю AUC в популяции пациентов, такой как выборка популяции пациентов, например, среднюю AUC для одного или нескольких пациента(пациентов). В некоторых вариантах осуществления, системное воздействие относится к площади под кривой (AUC) в пределах определенного периода времени, например, от суток 0 до суток 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 21, 28 суток или более, или недели 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или более, или месяца 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 18, 24, 48 или более. В некоторых вариантах осуществления, AUC измеряют как AUC от суток 0 до суток 28 (AUC0–28) после введения лекарственного средства, например, CAR+ T–клетки, включая все измеренные данные и данные, экстраполированные из измеренных фармакокинетических (PK) параметров, таких как средняя AUC для популяции пациентов, такой как выборка популяции пациентов. В некоторых вариантах осуществления, для определения воздействия с течением времени, например, AUC для определенного периода времени, например, AUC0–28, получают кривую зависимости концентрации лекарственного средства от времени, с использованием множества измерений или оценки параметров, например, концентраций клеток, с течением времени, например, измерений, полученных каждые 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 21 или 28 суток, или более.
[0404] В некоторых вариантах осуществления, определяют присутствие и/или количество клеток, экспрессирующих рекомбинантный рецептор (например, экспрессирующих CAR клеток, введенных для терапии на основе T–клеток) у индивида после введения T–клеток. В некоторых аспектах, способы на основе нуклеиновой кислоты, такие как количественная ПЦР (QПЦР), используют для оценки количества клеток, экспрессирующих рекомбинантный рецептор (например, экспрессирующих CAR клеток, введенных для терапии на основе T–клеток) в образце крови или сыворотки, или органа, или ткани (например, из участка заболевания, например, в образце опухоли) индивида. В некоторых аспектах, персистенцию количественно оценивают как количество копий ДНК или плазмиды, кодирующей рецептор, например, CAR, на микрограмм ДНК, или как количество экспрессирующих рецептор, например, экспрессирующих CAR, клеток на микролитр образца, например, крови или сыворотки, или на общее количество мононуклеарных клеток периферической крови (PBMC) или лейкоцитов или T–клеток на микролитр образца. В некоторых вариантах осуществления, праймеры или зонд, используемые для QПЦР или других способов на основе нуклеиновой кислоты, являются специфическими для связывания, узнавания и/или амплификации нуклеиновых кислот, кодирующих рекомбинантный рецептор, и/или других компонентов или элементов плазмиды и/или вектора, включая регуляторные элементы, например, промоторы, транскрипционные и/или пост–транскрипционные регуляторные элементы или отвечающие элементы, или маркеры, например, суррогатные маркеры. В некоторых вариантах осуществления, праймеры могут являться специфическими для регуляторных элементов, таких как пост–транскрипционный регуляторный элемент вируса гепатита лесного североамериканского сурка (WPRE).
[0405] В некоторых вариантах осуществления, клетки детектируют у индивида через или по меньшей мере через 2, 3, 4, 5, 6, 7, 14, 15, 27, или 28 суток после введения T–клеток, например, экспрессирующих CAR T–клетки. В некоторых аспектах, клетки детектируют через или по меньшей мере через 2, 4 или 6 недель после, или через 3, 6, или 12, 18, или 24 или 30, или 36 месяцев, или 1, 2, 3, 4, 5, или более лет, после введения T–клеток, например, экспрессирующих CAR T–клеток. В некоторых вариантах осуществления, клетки, экспрессирующие рецептор поддаются детекции в сыворотке, плазме, крови или ткани, например, в образце опухоли, индивида, например, посредством указанного способа, такого как способ детекции на основе QПЦР или проточной цитометрии.
[0406] В некоторых вариантах осуществления, экспрессирующие рецептор клетки, например, экспрессирующие CAR клетки, размножаются у индивида после введения T–клеток, например, экспрессирующих CAR T–клеток. В некоторых аспектах, увеличенное воздействие клеток на индивида включает увеличенное размножение клеток. Как показано в настоящем описании, увеличенное размножение, которое происходит рано, например, в пределах 7 суток, например, 4–7 суток, после проведения клеточной терапии ассоциировано с, коррелирует с и/или может являться показателем риска или вероятного риска возникновения токсичности. В некоторых вариантах осуществления, настоящее изобретение относится к способам, в которых у индивидов мониторируют фармакокинетические свойства введенных экспрессирующих рекомбинантный рецептор клеток и, если детектируют раннее или быстрое размножение, одно или несколько средств для облегчения токсичности, или уменьшения риска или вероятного риска токсичности можно вводить индивиду. Иллюстративные средства для облегчения токсичности известны и описаны, например, в разделе IV.E.
[0407] В конкретных вариантах осуществления, фармакокинетический параметр представляет собой количество экспрессирующих рекомбинантный рецептор клеток, которое является показательным для раннего или быстрого размножение клеток у индивида. В некоторых вариантах осуществления, такое поддающееся детекции размножение можно показать, если по меньшей мере или приблизительно 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 125, 150, или 200 экспрессирующих рекомбинантный рецептор клеток на микролитр детектируют в образце крови или сыворотки, собранном в пределах четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати, тринадцати или четырнадцати, или более чем четырнадцати суток после начала проведения клеточной терапии. В некоторых вариантах осуществления, фармакокинетический параметр представляет собой количество экспрессирующих рекомбинантный рецептор клеток, составляющее по меньшей мере, составляющее или составляющее приблизительно 2 экспрессирующие рекомбинантный рецептор клетки на микролитр в образце крови или сыворотки, собранном в пределах четверо суток после начала введения. В конкретных вариантах осуществления, фармакокинетический параметр представляет собой количество экспрессирующих рекомбинантный рецептор клеток, составляющее по меньшей мере, составляющее или составляющее приблизительно 5 экспрессирующих рекомбинантный рецептор клеток на микролитр в образце крови или сыворотки, собранном в пределах пять или шесть суток после начала введения. В некоторых вариантах осуществления, фармакокинетический параметр представляет собой количество экспрессирующих рекомбинантный рецептор клеток, составляющее по меньшей мере, составляющее или составляющее приблизительно 10 экспрессирующих рекомбинантный рецептор клеток на микролитр в образце крови или сыворотки, собранном в пределах пять или шесть суток после начала введения. В конкретных вариантах осуществления, фармакокинетический параметр представляет собой количество экспрессирующих рекомбинантный рецептор клеток, составляющее по меньшей мере, составляющее или составляющее приблизительно 15 экспрессирующих рекомбинантный рецептор клеток на микролитр в образце крови или сыворотки, собранном в пределах семь суток после начала введения.
[0408] В конкретных вариантах осуществления, настоящее изобретение относится к способам планирования исследования для введения терапевтической композиции T–клеток. В некоторых вариантах осуществления, способы включают распределение индивида для режима лечения на основании присутствия или отсутствия одного или нескольких специфических для пациента и/или клинических факторов риска, таких как любой из описанных. В некоторых вариантах осуществления, индивид не имеет или не идентифицирован как имеющий, или не считается имеющим специфический для пациента и/или клинический фактор, и его распределяют для введения дозы терапевтической композиции T–клеток. В конкретных вариантах осуществления, индивид имеет или идентифицирован как имеющий, или считается имеющим, специфический для пациента и/или клинический фактор, и его распределяют для введения уменьшенной и/или более низкой дозы клеток. В конкретных вариантах осуществления, уменьшенная и/или более низкая доза составляет или составляет по меньшей мере на 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 95% менее, чем доза, которую вводят индивиду без специфического для пациента и/или клинического фактора. В конкретных вариантах осуществления, не присутствует существенного различия в частоте возникновения токсичности, например, тяжелых неблагоприятных побочных эффектов, CRS и/или нейротоксичности, между индивидами без специфического для пациента и/или клинического фактора, которым вводят дозу клеток, и индивидами со специфическим для пациента и/или клиническим фактором, которым вводят более низкую дозу клеток.
[0409] В конкретных вариантах осуществления, индивида распределяют для введения низкой или уменьшенной дозы, если индивид имеет один или несколько специфических для пациента и/или клинических факторов, которые могут включать, но без ограничения, (i) индивидов, подвергнутых меньшему количеству циклов предшествующей терапии, необязательно, менее чем двум предшествующим циклам терапии, до начала введения терапевтической композиции T–клеток, (ii) индивидов молодого возраста, необязательно, менее чем 30 лет, (iii) индивидов, у которых соотношение CD4:CD8 в образце после афереза от индивида ниже определенного порога, необязательно ниже 1:1 или ниже 1,5:1, или ниже 0,5:1, или ниже, необязательно, где введенная доза основана на общем количестве T–клеток или общем количестве T–клеток, экспрессирующих рекомбинантный рецептор; (iv) индивидов, имеющих массу, превышающую среднюю массу среди группы подвергнутых лечению индивидов; (v) индивидов с количеством тромбоцитов менее чем или приблизительно менее чем 120000; (vi) индивидов, имеющих B–клеточный лейкоз, необязательно, острый лимфоцитарный лейкоз (ALL); (vii) индивидов, имеющих высокую нагрузку заболевания перед, например, непосредственно перед или в пределах одного месяца перед началом введения терапевтической композиции T–клеток, необязательно, как определено на основании процента бластных клеток костного мозга, большего или равного 5%, суммы произведений диаметров (SPD), или уровней лактатдегидрогеназы; (ix) индивидов, подвергнутых переходной химиотерапии до начала введения терапевтической композиции T–клеток; (x) индивидов, подвергнутых предварительной подготовке с использованием противолимфоцитарной терапии, необязательно, включающей введение флударабина и/или циклофосфамида, до начала введения терапевтической композиции T–клеток; (xi) индивидов, у которых уровень, количество или концентрация интерлейкина–15 (IL–15) в образце крови до начала введения терапевтической композиции T–клеток больше или равно пороговому значению, необязательно, где пороговое значение составляет 30 пг/мл плазмы, (xii) быстрое размножение in vivo клеток, экспрессирующих рекомбинантный рецепторы, (xiii) индивидов, не имеющих молекулярного подтипа с филадельфийской хромосомой (Ph+) и/или подобного подтипу с Ph–хромосомой (Ph–подобного) молекулярного подтипа острого лимфобластного лейкоза (ALL).
C. Исход ответа
[0410] В некоторых вариантах осуществления, исход ответа у индивида после введения композиции T–клеток можно мониторировать или оценивать. В некоторых вариантах осуществления, исход ответа представляет собой отсутствие ответа. В некоторых вариантах осуществления, исход ответа представляет собой частичный ответ. В некоторых вариантах осуществления, исход ответа представляет собой полный ответ (CR). В некоторых вариантах осуществления, исход ответа оценивают посредством мониторирования нагрузки заболевания у индивида. В некоторых вариантах осуществления, можно оценивать отсутствие ответа, присутствие частичного ответа, или клинического или полного ответа.
[0411] В некоторых вариантах осуществления, частичный ответ или полный ответ представляет собой ответ, при котором лекарственное средство уменьшает или предотвращает усиление или нагрузку заболевание или состояния у индивида. Например, когда заболевание или состояние представляет собой опухоль, уменьшение нагрузки заболевания существует или присутствует, если присутствует уменьшение размера опухоли, основного объема, метастазирования, процента бластных клеток в костном мозге или поддающейся детекции на молекулярном уровне злокачественной опухоли и/или улучшение прогноза или выживамости, или другого симптома, ассоциированного с опухолевой нагрузкой, по сравниваю с состоянием до лечения с использованием лекарственного средства (например, CAR–T–клеток).
[0412] В некоторых вариантах осуществления, заболевание или состояние представляет собой опухоль и уменьшение нагрузки заболевания представляет собой уменьшение размера опухоли. В некоторых вариантах осуществления, уменьшение нагрузки заболевания показывают по уменьшению одного или нескольких факторов, таких как нагрузка или количество пораженных заболеванием клеток у индивида или в его жидкости организма или органе, или ткани, масса или объем опухоли, или количество или степень метастазов. В некоторых вариантах осуществления, нагрузку заболевания, например, опухолевую нагрузка, можно оценивать или мониторировать по степени морфологически подтвержденного заболевания и/или минимального остаточного заболевания.
[0413] В некоторых вариантах осуществления, нагрузку заболевания или состояния у индивида детектируют, оценивают или измеряют. Нагрузку заболевания можно детектировать, в некоторых аспектах, посредством детекции общего количества пораженных заболеванием или ассоциированных с заболеванием клеток, например, клеток опухолей, у индивида, или в органе, ткани или физиологической жидкости индивида, такой как кровь или сыворотка. В некоторых вариантах осуществления, нагрузку заболевания, например, опухолевую нагрузку, оценивают посредством измерения массы солидной опухоли и/или количества или степень метастазов. В некоторых аспектах, оценивают выживаемость индивида, выживаемость в пределах определенного периода времени, степень выживаемости, присутствие или длительность присутствия выживаемости в отсутствие неблагоприятного события или симптома, или безрецидивную выживаемость. В некоторых вариантах осуществления, оценивают любой симптом заболевания или состояния. В некоторых вариантах осуществления, показатель нагрузки заболевания или состояния указан.
[0414] В некоторых вариантах осуществления, нагрузка заболевания может включать общее количество пораженных заболеванием клеток у индивида или в органе, ткани или физиологической жидкости индивида, таком как орган или ткань в локализации опухоли или другой локализации, например, которое может указывать на метастаз. Например, клетки опухолей можно детектировать и/или количественно оценивать в крови или в костном мозге в контексте определенных гематологических злокачественных новообразований. Нагрузка заболевания может включать, в некоторых вариантах осуществления, массу опухоли, количество или степень метастазов, и/или процент бластных клеток, присутствующих в костном мозге.
[0415] В некоторых вариантах осуществления, индивид имеет лейкоз. Степень нагрузки заболевания можно определять посредством оценки остаточного лейкоза в крови или в костном мозге.
[0416] В некоторых вариантах осуществления, исход ответа существует, если присутствует уменьшение процента бластных клеток в костном мозге, по сравнению с процентом бластных клеток в костном мозге до лечения с использованием лекарственного средства. В некоторых вариантах осуществления, уменьшение нагрузки заболевания существует, если присутствует уменьшение или снижение по меньшей мере на или по меньшей мере приблизительно на 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или более количества или процента бластных клеток в костном мозге, по сравнению с количеством или процентом бластных клеток в костном мозге до лечения.
[0417] В некоторых вариантах осуществления, для индивида показан ответ, если для индивида не показано морфологически подтвержденного заболевания (морфологически не подтвержденное заболевания) или не показано существенного морфологически подтвержденного заболевания. В некоторых вариантах осуществления, для индивида показано морфологически подтвержденное заболевание, если присутствует больше или равно 5% бластных клеток в костном мозге, например, как детектировано посредством световой микроскопии. В некоторых вариантах осуществления, для индивида показана полная или клиническая ремиссия, если присутствует менее чем 5% бластных клеток в костном мозге.
[0418] В некоторых вариантах осуществления, для индивида показано уменьшение или снижение нагрузки заболевания, если для него показано морфологически подтвержденное заболевание до лечения и показана полная ремиссия (например, менее чем 5% бластных клеток в костном мозге) в присутствии или в отсутствие поддающегося детекции на молекулярном уровне заболевания (например, минимального остаточного заболевания (MRD), которое поддается детекции на молекулярном уровне, например, как детектировано посредством проточной цитометрии или количественной ПЦР) после лечения. В некоторых вариантах осуществления, для индивида показано уменьшение или снижение нагрузки заболевания, если для него показано поддающееся детекции на молекулярном уровне заболевание до лечения и не показано поддающегося детекции на молекулярном уровне заболевания после лечения.
[0419] В некоторых вариантах осуществления, для индивида может быть показана полная ремиссия, но присутствует небольшая доля не поддающихся морфологической детекции (способами световой микроскопии) остаточных лейкозных клеток. Считают, что для индивида показано минимальное остаточное заболевание (MRD), если для индивида показано менее чем 5% бластных клеток в костном мозге и показана поддающаяся детекции на молекулярном уровне злокачественная опухоль. В некоторых вариантах осуществления, поддающуюся детекции на молекулярном уровне злокачественную опухоли можно оценивать с использованием любого из множества молекулярных способов, позволяющих чувствительную детекцию небольшого количества клеток. В некоторых аспектах, такие способы включают анализы ПЦР, которые могут определять уникальные реаранжировки генов Ig/T–клеточного рецептора или слитые транскрипты, полученные посредством хромосомных транслокаций. В некоторых вариантах осуществления, проточная цитометрия можно использовать для идентификации клеток злокачественных опухолей на основании специфических для лейкоза иммунофенотипов. В некоторых вариантах осуществления, молекулярная детекция злокачественной опухоли может детектировать настолько мало, как 1 лейкозную или бластную клетку, среди 100000 нормальных клеток или 1 лейкозную или бластную клетку среди 10000 нормальных клеток. В некоторых вариантах осуществления, для индивида показано MRD, которое поддается детекции на молекулярном уровне, если детектируют по меньшей мере или более чем 1 лейкозную клетку среди 100000 клеток, например, посредством ПЦР или проточной цитометрии.
[0420] В некоторых вариантах осуществления, нагрузка заболевания у индивида не поддается детекции на молекулярном уровне, или MRD–, так что, в некоторых случаях, невозможно детектировать лейкозные клетки у индивида с использованием способов ПЦР или проточной цитометрии.
[0421] В некоторых вариантах осуществления исход ответа представляет собой отсутствие CR или присутствие полного ответа, при котором для индивида достигнут или показан статус минимального остаточного заболевания или поддающегося детекции на молекулярном уровне заболевания. В некоторых вариантах осуществления, исход ответа представляет собой присутствие CR с наличием поддающегося детекции на молекулярном уровне заболевания или присутствие CR без поддающегося детекции на молекулярном уровне заболевания. В некоторых вариантах осуществления, у индивидов оценивают нагрузку заболевания с использованием способов, как описано в настоящем описании, таких как способы, оценивающие бластные клетки в костном мозге или поддающееся детекции на молекулярном уровне заболевание посредством проточной цитометрии или способов QПЦР.
[0422] После введения клеток, биологическую активность модифицированных популяций клеток в некоторых вариантах осуществления измеряют, например, посредством любого из ряда известных способов. Параметры для оценки включают специфическое связывание модифицированной или природной T–клетки или другого иммуноцита с антигеном, in vivo, например, посредством визуализации, или ex vivo, например, посредством ELISA или проточной цитометрии. В конкретных вариантах осуществления, способность модифицированных клеток разрушать клетки–мишени можно измерять с использованием любого пригодного способа, известного в данной области, такого как анализы цитотоксичности, описанные, например, в Kochenderfer et al., J. Immunotherapy, 32(7): 689–702 (2009), и Herman et al. J. Immunological Methods, 285(1): 25–40 (2004). В конкретных вариантах осуществления, биологическую активность клеток измеряют посредством анализа экспрессии и/или секреции одного или нескольких цитокинов, таких как CD 107a, IFNγ, IL–2 и TNF. В некоторых аспектах биологическую активность измеряют посредством оценки клинического исхода, такого как уменьшение опухолевая нагрузка или массы.
D. Средство для облегчения или лечения токсичности
[0423] В некоторых вариантах осуществления, способы, представленные в настоящем описании, относятся к мониторированию индивидов по риску или вероятному риску токсичности, и/или идентификации индивидов, подверженных риску или вероятному риску возникновения токсичности, например, тяжелой токсичности, такой как тяжелый CRS или тяжелая нейротоксичность, после проведения клеточной терапии, включающей клетки, экспрессирующие рекомбинантный рецептор (например, CAR). В некоторых вариантах осуществления, способы включают введение одного или нескольких средств или видов терапии, осуществляющих лечение токсичности клеточной терапии, такой как CRS или нейротоксичность, например, тяжелый CRS или тяжелая нейротоксичность). В некоторых вариантах осуществления, средство вводят в то время, в которое определили, что индивид подвержен риску возникновения токсичности, такой как тяжелая токсичность, и/или в то время, в которое проявились один или несколько признаков или симптомов токсичности.
[0424] В некоторых вариантах осуществления, средство представляет собой стероид. В некоторых вариантах осуществления, средство представляет собой антагонист или ингибитор рецептора цитокина, такого как рецептор IL–6, рецептор CD122 (рецептор IL–2R–бета) или CCR2, или представляет собой ингибитор цитокина, такого как IL–6, MCP–1, IL–10, IFN–γ, IL–8, или IL–18. В некоторых вариантах осуществления, средство представляет собой агонист рецептора цитокина и/или цитокина, такого как TGF–β. В некоторых вариантах осуществления, средство, например, агонист, антагонист или ингибитор, представляет собой антитело или антигенсвязывающий фрагмент, малую молекулу, белок или пептид, или нуклеиновую кислоту.
[0425] В некоторых вариантах осуществления, жидкий болюс можно использовать в качестве вмешательства, например, для лечения гипотензии, ассоциированной с CRS. В некоторых вариантах осуществления, целевые гематокритные числа составляют >24%. В некоторых вариантах осуществления, вмешательство включает использование технология абсорбирующей смолы вместе с фильтрацией крови или плазмы. В некоторых случаях, вмешательство включает диализ, плазмаферез или сходные технологии. В некоторых вариантах осуществления, можно использовать сосудосуживающие средства или ацетаминофен.
1. Стероид
[0426] В некоторых вариантах осуществления, средство, осуществляющее лечение и/или предотвращение, задержку или ослабление развития или риска возникновения токсичности клеточной терапии, такой как CRS или нейротоксичность степени 2 или выше, или тяжелые CRS или нейротоксичность, представляет собой стероид, например, кортикостероид. Кортикостероиды, как правило, включают глюкокортикоиды и минералокортикоиды.
[0427] Любой кортикостероид, например, глюкокортикоид, можно использовать в способах, представленных в настоящем описании. В некоторых вариантах осуществления, глюкокортикоиды включают синтетические и несинтетические глюкокортикоиды. Иллюстративные глюкокортикоиды включают, но без ограничения,: аклометазоны, альгестоны, беклометазоны (например, дипропионат беклометазона), бетаметазоны (например, 17–валерат бетаметазона, ацетат бетаметазона натрия, фосфат бетаметазона натрия, валерат бетаметазона), будезониды, клобетазолы (например, пропионат клобетазола), клобетазоны, клокортолоны (например, пивалат клокортолона), клопреднолы, кортикостероны, кортизоны и гидрокортизоны (например, гидроацетат кортизона), кортивазолы, дефлазакорты, дезониды, дезоксиметазоны, дексаметазоны (например, фосфат дексаметазона–21, ацетат дексаметазона, фосфат дексаметазона натрия), дифлоразоны (например, диацетат дифлоразона), дифторкортолоны, дифлупреднаты, эноксолоны, флуазакорты, флуклорониды, флудрокортизоны (например, флудроацетат кортизона), флуметазоны (например, пивалат флуметазона), флунизолиды, флуоцинолоны (например, ацетонид флуоцинолона), флуоциониды, флуокортины, флуокортолоны, фторметолоны (например, ацетат фторметолона), флуперолоны (например, ацетат флуперолона), флупреднидены, флупреднизолоны, флурандренолиды, флуказоны (например, пропионат флуказона), формокорталы, галцинониды, галобетазолы, галометазоны, галопредоны, гидрокортаматы, гидрокортизоны (например, бутират гидрокортизона–21, ацепонат гидрокортизона, гидроацетат кортизона, бутепрат гидрокортизона, бутират гидрокортизона, ципионата гидрокортизона, гемисукцинат гидрокортизона, пробутат гидрокортизона, фосфат гидрокортизона натрия, сукцинат гидрокортизона натрия, валерат гидрокортизона), этабонат лотепреднола, мазипредоны, медризоны, мепреднизоны, метилпреднизолоны (ацепонат метилпреднизолона, ацетат метилпреднизолона, гемисукцинат метилпреднизолона, сукцинат метилпреднизолона натрия), мометазоны (например, фуроат мометазона), параметазоны (например, ацетат параметазона), предникарбаты, преднизолоны (например, диэтиламиноацетат преднизолона–25, фосфат преднизолона натрия, гемисукцинат преднизолона–21, ацетат преднизолона; фарнезилат преднизолона, гемисукцинат преднизолона, преднизолон–21 (бета–D–глюкуронид), метасульфобензоат преднизолона, стеаглат преднизолона, тебутат преднизолона, тетрагидрофталат преднизолона), преднизоны, преднивалы, преднилидены, римексолоны, тиксокортолы, триамцинолоны (например, ацетонид триамцинолона, бенетонид триамцинолона, гексацетонид триамцинолона, триамцинолона ацетонида 21–пальмитат, диацетат триамцинолона). Эти глюкокортикоиды и их соли подробно обсуждают, например, в Remington's Pharmaceutical Sciences, A. Osol, ed., Mack Pub. Co., Easton, Pa. (16th ed. 1980).
[0428] В некоторых примерах, глюкокортикоид выбран из кортизонов, дексаметазонов, гидрокортизонов, метилпреднизолонов, преднизолонов и преднизонов. В конкретном примере, глюкокортикоид представляет собой дексаметазон.
[0429] В некоторых вариантах осуществления, средство представляет собой кортикостероид, и его вводят в количестве, которое является терапевтически эффективным для лечения, облегчения или уменьшения одного или нескольких симптомов токсичности клеточной терапии, такой как CRS или нейротоксичность. В некоторых вариантах осуществления, индикаторы улучшения или успешного лечения включают определение отсутствия проявления соответствующего показателя по шкале градации токсичности (например, по шкале градации CRS или нейротоксичности), например, балл менее чем 3, или изменение степени или тяжести по шкале градации, как обсуждаемый в настоящем описании, например, изменение от балла 4 до балла 3.
[0430] В некоторых аспектах, кортикостероид предоставляют в терапевтически эффективной дозе. Терапевтически эффективную концентрацию можно определять эмпирически посредством тестирования в известных системах in vitro или in vivo (например, модель на животных). Например, количество выбранного кортикостероида, подлежащее введению для облегчения симптомов или неблагоприятных эффектов токсичности клеточной терапии, такой как CRS или нейротоксичность, можно определять посредством стандартных клинических способов. Кроме того, модели на животных можно использовать, чтобы способствовать идентификации оптимальных диапазонов дозирования. Точная доза, которую можно определять эмпирически, может зависеть от конкретного терапевтического препарата, режима и расписания дозирования, способа введения и тяжесть заболевания.
[0431] Кортикостероид можно вводить в любом количестве, которое является эффективным для облегчения одного или нескольких симптомов, ассоциированных с токсичностью, например, с CRS или нейротоксичностью. Кортикостероид, например, глюкокортикоид, можно вводить, например, в количестве между или приблизительно между 0,1 и 100 мг, на дозу, 0,1 и 80 мг, 0,1 и 60 мг, 0,1 и 40 мг, 0,1 и 30 мг, 0,1 и 20 мг, 0,1 и 15 мг, 0,1 и 10 мг, 0,1 и 5 мг, 0,2 и 40 мг, 0,2 и 30 мг, 0,2 и 20 мг, 0,2 и 15 мг, 0,2 и 10 мг, 0,2 и 5 мг, 0,4 и 40 мг, 0,4 и 30 мг, 0,4 и 20 мг, 0,4 и 15 мг, 0,4 и 10 мг, 0,4 и 5 мг, 0,4 и 4 мг, 1 и 20 мг, 1 и 15 мг или 1 и 10 мг, включая каждое, для взрослого индивида–человека массой 70 кг. Как правило, кортикостероид, такой как глюкокортикоид, вводят в количестве между или приблизительно между 0,4 и 20 мг, например, при или приблизительно при 0,4 мг, 0,5 мг, 0,6 мг, 0,7 мг, 0,75 мг, 0,8 мг, 0,9 мг, 1 мг, 2 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 11 мг, 12 мг, 13 мг, 14 мг, 15 мг, 16 мг, 17 мг, 18 мг, 19 мг или 20 мг на дозу, для среднего взрослого индивида–человека.
[0432] В некоторых вариантах осуществления, кортикостероид можно вводить, например, посредством дозирования при или приблизительно при 0,001 мг/кг (массы тела индивида), 0,002 мг/кг, 0,003 мг/кг, 0,004 мг/кг, 0,005 мг/кг, 0,006 мг/кг, 0,007 мг/кг, 0,008 мг/кг, 0,009 мг/кг, 0,01 мг/кг, 0,015 мг/кг, 0,02 мг/кг, 0,025 мг/кг, 0,03 мг/кг, 0,035 мг/кг, 0,04 мг/кг, 0,045 мг/кг, 0,05 мг/кг, 0,055 мг/кг, 0,06 мг/кг, 0,065 мг/кг, 0,07 мг/кг, 0,075 мг/кг, 0,08 мг/кг, 0,085 мг/кг, 0,09 мг/кг, 0,095 мг/кг, 0,1 мг/кг, 0,15 мг/кг, 0,2 мг/кг, 0,25 мг/кг, 0,30 мг/кг, 0,35 мг/кг, 0,40 мг/кг, 0,45 мг/кг, 0,50 мг/кг, 0,55 мг/кг, 0,60 мг/кг, 0,65 мг/кг, 0,70 мг/кг, 0,75 мг/кг, 0,80 мг/кг, 0,85 мг/кг, 0,90 мг/кг, 0,95 мг/кг, 1 мг/кг, 1,05 мг/кг, 1,1 мг/кг, 1,15 мг/кг, 1,20 мг/кг, 1,25 мг/кг, 1,3 мг/кг, 1,35 мг/кг или 1,4 мг/кг, для среднего взрослого индивида–человека, как правило, массой приблизительно 70 кг – 75 кг.
[0433] Кортикостероид, или глюкокортикоид, например, дексаметазон, можно вводить перорально (таблетки, жидкость или жидкий концентрат), PO, внутривенно (IV), внутримышечно или посредством любого другого известного способа или способа, описанного в настоящем описании (например, применительно к фармацевтическим составам). В некоторых аспектах, кортикостероид вводят в форме болюса, и в других аспектах, его можно вводить в течение некоторого периода времени.
[0434] В некоторых аспектах, глюкокортикоид можно вводить в течение периода более чем одни сутки, например, более двух суток, в течение 3 суток, или в течение 4 или более суток. В некоторых вариантах осуществления, кортикостероид можно вводить один раз в сутки, два раза в сутки, или три раза или более в сутки. Например, кортикостероид, например, дексаметазон, можно, в некоторых примерах, вводить при 10 мг (или эквивалентно) IV два раза в сутки в течение трех суток.
[0435] В некоторых вариантах осуществления, дозирование кортикостероида, например, глюкокортикоида, вводят в последовательно уменьшающихся дозах на цикл лечения. Таким образом, в некоторых таких режимах лечения, дозу кортикостероида сводят на нет. Например, кортикостероид можно вводить в начальной дозе (или эквивалентной дозе, например, применительно к дексаметазону) 4 мг, и при каждом последующем введении дозу можно уменьшать, так что доза составляет 3 мг для следующего введения, 2 мг для следующего введения, и 1 мг для следующего введения
[0436] Как правило, вводимая доза кортикостероида зависит от конкретного кортикостероида, поскольку существует различие активности между различными кортикостероидами. Как правило, понятно, что лекарственные средства изменчивы по активности, и что дозы можно, таким образом, менять, для получения эквивалентных эффектов. В таблице 4 показана эквивалентность применительно к активности для различных глюкокортикоидов и способов введения. Эквивалентная активность для клинического дозирования хорошо известна. Информацию относительно эквивалентного дозирования стероидов (не на хронотерапевтической основе) можно обнаружить в British National Formulary (BNF), 37 March 1999.
[0437] Таким образом, в некоторых вариантах осуществления, стероид вводят в количестве, эквивалентном дозированию от или приблизительно от 1,0 мг до 20 мг дексаметазона в сутки, например, от 1,0 мг до 15 мг дексаметазона в сутки, от 1,0 мг до 10 мг дексаметазона в сутки, от 2,0 мг до 8 мг дексаметазона в сутки или от 2,0 мг до 6,0 мг дексаметазона в сутки, включая каждое. В некоторых случаях, стероид вводят в дозе, эквивалентной или приблизительно эквивалентной 4 мг, или эквивалентной или приблизительно эквивалентной 8 мг дексаметазона в сутки.
[0438] В некоторых вариантах осуществления, стероид вводят, если лихорадка персистирует после лечения тоцилизумабом. Например, в некоторых вариантах осуществления, дексаметазон вводят перорально или внутривенно в дозе 5–10 мг вплоть до каждых 6–12 часов при продолжающейся лихорадке. В некоторых вариантах осуществления, тоцилизумаб вводят одновременно или после дополнительного кислорода.
2. Другие средства
[0439] В некоторых вариантах осуществления, средство, осуществляющее лечение или облегчение симптомов токсичности клеточной терапии, например, CRS или нейротоксичности, представляет собой средство, нацеленное на цитокин, например, представляет собой антагонист или ингибитор цитокина, такого как трансформирующий фактор роста бета (TGF–бета), интерлейкин 6 (IL–6), интерлейкин 10 (IL–10), IL–2, MIP1β (CCL4), TNF–альфа, IL–1, интерферон гамма (IFN–гамма), или моноцитарный хемотаксический белок–1 (MCP–1). В некоторых вариантах осуществления, средство, осуществляющее лечение или облегчение симптомов токсичности клеточной терапии, например, CRS или нейротоксичности, представляет собой средство, нацеленное на (например, ингибитор или антагонист) рецептор цитокина, такой как рецептор IL–6 (IL–6R), рецептор IL–2 (IL–2R/CD25), рецептор MCP–1 (CCL2) (CCR2 или CCR4), рецептор TGF–бета (TGF–бета I, II или III), рецептор IFN–гамма (IFNGR), рецептор MIP1β (например, CCR5), рецептор TNF–альфа (например, TNFR1), рецептор IL–1 (IL1–Rα/IL–1Rβ) или рецептор IL–10 (IL–10R).
[0440] Количество выбранного средства, осуществляющего лечение или облегчение симптомов токсичности клеточной терапии, например, CRS или нейротоксичности, подлежащее введению для облегчения симптомов или неблагоприятных эффектов токсичности клеточной терапии, например, CRS или нейротоксичности, можно определять посредством стандартных клинических способов. Иллюстративные неблагоприятные события включают, но без ограничения, увеличение уровня аланинаминотрансферазы, увеличение уровня аспартатаминотрансферазы, озноб, фебрильную нейтропению, головную боль, гипотензию, дисфункцию левого желудочка, энцефалопатию, гидроцефалию, судороги и/или тремор.
[0441] В некоторых вариантах осуществления, средство вводят при уровне дозы от или приблизительно от 30 мг до 5000 мг, например, от 50 мг до 1000 мг, 50 мг до 500 мг, 50 мг до 200 мг, 50 мг до 100 мг, 100 мг до 1000 мг, 100 мг до 500 мг, 100 мг до 200 мг, 200 мг до 1000 мг, 200 мг до 500 мг или 500 мг до 1000 мг.
[0442] В некоторых вариантах осуществления, средство вводят при от или приблизительно от 0,5 мг/кг до 100 мг/кг, например, от или приблизительно от 1 мг/кг до 50 мг/кг, 1 мг/кг до 25 мг/кг, 1 мг/кг до 10 мг/кг, 1 мг/кг до 5 мг/кг, 5 мг/кг до 100 мг/кг, 5 мг/кг до 50 мг/кг, 5 мг/кг до 25 мг/кг, 5 мг/кг до 10 мг/кг, 10 мг/кг до 100 мг/кг, 10 мг/кг до 50 мг/кг, 10 мг/кг до 25 мг/кг, 25 мг/кг до 100 мг/кг, 25 мг/кг до 50 мг/кг до 50 мг/кг до 100 мг/кг. В некоторых вариантах осуществления, средство вводят при уровне дозы от или приблизительно от 1 мг/кг до 10 мг/кг, 2 мг/кг до 8 мг/кг, 2 мг/кг до 6 мг/кг, 2 мг/кг до 4 мг/кг или 6 мг/кг до 8 мг/кг, включая каждое. В некоторых аспектах, средство вводят при уровне дозы по меньшей мере или по меньшей мере приблизительно, или приблизительно 1 мг/кг, 2 мг/кг, 4 мг/кг, 6 мг/кг, 8 мг/кг, 10 мг/кг или более. В некоторых вариантах осуществления, средство вводят в дозе 4 мг/кг или 8 мг/кг.
[0443] В некоторых вариантах осуществления, средство вводят посредством инъекции, например, внутривенной или подкожной инъекций, внутриглазной инъекции, периокулярной инъекции, субретинальной инъекции, инъекции в стекловидное тело, инъекции посредством прокола перегородки, субсклеральной инъекции, интрахороидальной инъекции, интракамеральной инъекции, субконъюнктивальной инъекции, инъекции в субтеноново пространство, ретробульбарной инъекции, перибульбарной инъекции, или задней околосклеральной доставки. В некоторых вариантах осуществления, его вводят посредством парентерального, внутрилегочного и интраназального, и, если желательно для местного лечения, внутриочагового введения. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение.
[0444] В некоторых вариантах осуществления, это количество средства вводят приблизительно или приблизительно два раза в сутки, один раз в сутки, на каждые вторые сутки, три раза в неделю, один раз в неделю, один раз в две недели или один раз в месяц.
[0445] В некоторых вариантах осуществления, средство вводят в качестве части композиции или состава, например, фармацевтической композиции или состава, как описано ниже. Таким образом, в некоторых случаях, композицию, содержащую средство, вводят, как описано ниже. В других аспектах, средство вводят отдельно, и его можно вводить посредством любого известного пригодного способа введения или посредством способа, описанного в настоящем описании, например, применительно к композициям и фармацевтическим составам.
[0446] В некоторых вариантах осуществления, средство, осуществляющее лечение или облегчение симптомов токсичности клеточной терапии, например, CRS или нейротоксичности, представляет собой антитело или антигенсвязывающий фрагмент. В некоторых вариантах осуществления, средство представляет собой тоцилизумаб, силтуксимаб, сарилумаб, олокизумаб (CDP6038), элсилимомаб, ALD518/BMS–945429, сирукумаб (CNTO 136), CPSI–2634, ARGX–109, FE301 или FM101.
[0447] В некоторых вариантах осуществления, средство представляет собой антагонист или ингибитор IL–6 или рецептора IL–6 (IL–6R). В некоторых аспектах, средство представляет собой антитело, нейтрализующее активность IL–6, например, антитело или антигенсвязывающий фрагмент, которые связываются с IL–6 или IL–6R. Например, в некоторых вариантах осуществления, средство представляет собой или содержит тоцилизумаб (атлизумаб) или сарилумаб, антитела против IL–6R. В некоторых вариантах осуществления, средство представляет собой антитело против IL–6R, описанное в Патенте США No: 8562991. В некоторых случаях, средство, нацеленное на IL–6, представляет собой антитело против IL–6, такое как силтуксимаб, элсилимомаб, ALD518/BMS–945429, сирукумаб (CNTO 136), CPSI–2634, ARGX–109, FE301, FM101 или олокизумаб (CDP6038). В некоторых аспектах, средство может осуществлять нейтрализацию активности IL–6 посредством ингибирования взаимодействия лиганд–рецептор. Целесообразность этого общего типа способов продемонстрирована с использованием природного антагониста рецептора интерлейкина–1. См. Harmurn, C. H. et al., Nature (1990) 343:336–340. В некоторых аспектах, антагонист или ингибитор IL–6/IL–6R представляет собой мутеин IL–6, такой как описан в Патенте США No. 5591827. В некоторых вариантах осуществления, средство, являющееся антагонистом или ингибитором IL–6/IL–6R, представляет собой малую молекулу, белок или пептид, или нуклеиновую кислоту.
[0448] В некоторых вариантах осуществления, средство представляет собой тоцилизумаб. В некоторых вариантах осуществления, тоцилизумаб вводят в качестве раннего вмешательства в соответствии с представленными способами дозирования от или приблизительно от 1 мг/кг до 12 мг/кг, например, при или приблизительно при 4 мг/кг, 8 мг/кг, или 10 мг/кг. В некоторых вариантах осуществления, тоцилизумаб вводят посредством внутривенной инфузии. В некоторых вариантах осуществления, тоцилизумаб вводят при персистентной лихорадке при более чем 39°C, длящейся 10 часов, которая не отвечает на ацетаминофен. В некоторых вариантах осуществления, второе введение тоцилизумаба проводят, если симптомы рецидивируют через 48 часов после начальной дозы.
[0449] В некоторых вариантах осуществления, средство представляет собой агонист или стимулятор TGF–β или рецептора TGF–β (например, рецептора TGF–β I, II, или III). В некоторых аспектах, средство представляет собой антитело, увеличивающее активность TGF–β, например, антитело или антигенсвязывающий фрагмент, которые связываются с TGF–β или с одним из его рецепторов. В некоторых вариантах осуществления, средство, являющееся агонистом или стимулятором TGF–β и/или его рецептора, представляет собой малую молекулу, белок или пептид, или нуклеиновую кислоту.
[0450] В некоторых вариантах осуществления, средство представляет собой антагонист или ингибитор MCP–1 (CCL2) или рецептора MCP–1 (например, рецептора MCP–1 CCR2 или CCR4). В некоторых аспектах, средство представляет собой антитело, нейтрализующее активность MCP–1, например, антитело или антигенсвязывающий фрагмент, которые связываются с MCP–1 или с одним из его рецепторов (CCR2 или CCR4). В некоторых вариантах осуществления, антагонист или ингибитор MCP–1 представляет собой любой, описанный в Gong et al. J Exp Med. 1997 Jul 7; 186(1): 131–137 или Shahrara et al. J Immunol 2008; 180:3447–3456. В некоторых вариантах осуществления, средство, являющееся антагонистом или ингибитором MCP–1 и/или его рецептора (CCR2 или CCR4), представляет собой малую молекулу, белок или пептид, или нуклеиновую кислоту.
[0451] В некоторых вариантах осуществления, средство представляет собой антагонист или ингибитор IFN–γ или рецептора IFN–γ (IFNGR). В некоторых аспектах, средство представляет собой антитело, нейтрализующее активность IFN–γ, например, антитело или антигенсвязывающий фрагмент, которые связываются с IFN–γ или его рецептором (IFNGR). В некоторых аспектах, антитело, нейтрализующее IFN–гамма, представляет собой любое антитело, описанное в Dobber et al. Cell Immunol. 1995 Feb;160(2):185–92 или Ozmen et al. J Immunol. 1993 Apr 1;150(7):2698–705. В некоторых вариантах осуществления, средство, являющееся антагонистом или ингибитором IFN–γ/IFNGR, представляет собой малую молекулу, белок или пептид, или нуклеиновую кислоту.
[0452] В некоторых вариантах осуществления, средство представляет собой антагонист или ингибитор IL–10 или рецептора IL–10 (IL–10R). В некоторых аспектах, средство представляет собой антитело, нейтрализующее активность IL–10, например, антитело или антигенсвязывающий фрагмент, которые связываются с IL–10 или IL–10R. В некоторых аспектах, антитело, нейтрализующее IL–10, представляет собой любое антитело, описанное в Dobber et al. Cell Immunol. 1995 Feb;160(2):185–92 или Hunter et al. J Immunol. 2005 Jun 1;174(11):7368–75. В некоторых вариантах осуществления, средство, являющееся антагонистом или ингибитором IL–10/IL–10R, представляет собой малую молекулу, белок или пептид, или нуклеиновую кислоту.
V. МОДИФИЦИРОВАННЫЕ КЛЕТКИ
[0453] Настоящее изобретение относится к модифицированным клеткам, которые экспрессируют один или несколько рекомбинантных рецепторов антигенов. В некоторых вариантах осуществления, клетки могут включать клетки, генетически модифицированные с использованием рекомбинантного рецептора, такого как химерный антигенный рецептор.
A. Рекомбинантные рецепторы антигенов
[0454] Настоящее изобретение относится к модифицированным клеткам, таким как T–клетки, которые экспрессируют рекомбинантный рецептор, включая химерные рецепторы, содержащие связывающие лиганд домены или их связывающие фрагменты, такие как функциональные не относящиеся к TCR рецепторы антигенов, такие как химерные рецепторы антигенов (CAR), а также включая T–клеточные рецепторы (TCR), такие как трансгенные TCR, и их компоненты. Химерный рецептор, такой как CAR, как правило, включает внеклеточный связывающий антиген (или лиганд) домен, связанный с одним или несколькими компоненты для передачи внутриклеточных сигналов, в некоторых аспектах, посредством линкеров и/или трансмембранный домен(s).
1. Химерные рецепторы антигенов
[0455] Иллюстративные рецепторы антигенов, включая CAR, и способы конструирования и введения таких рецепторов в клетки, включают способы, описанные, например, в публикациях международных патентных заявок номер WO200014257, WO2013126726, WO2012/129514, WO2014031687, WO2013/166321, WO2013/071154, WO2013/123061, в публикациях Патентных заявок США номер US2002131960, US2013287748, US20130149337, в Патентах США No.: 6451995, 7446190, 8252592, 8339645, 8398282, 7446179, 6410319, 7070995, 7265209, 7354762, 7446191, 8324353 и 8479118, и в Европейской патентной заявке номер EP2537416, и/или способы, описанные в Sadelain et al., Cancer Discov., 3(4): 388–398 (2013); Davila et al. PLoS ONE 8(4): e61338 (2013); Turtle et al., Curr. Opin. Immunol., 24(5): 633–39 (2012); Wu et al., Cancer, 18(2): 160–75 (2012). В некоторых аспектах, рецепторы антигенов включают CAR, как описано в Патенте США No.: 7446190, и рецепторы, описанные в Публикации международной патентной заявки No.: WO/2014055668 A1. Примеры CAR включают CAR как описано в любой из вышеупомянутых публикаций, таких как WO2014031687, US 8339645, US 7446179, US 2013/0149337, Патент США No.: 7446190, Патент США No.: 8389282, Kochenderfer et al., Nature Reviews Clinical Oncology, 10, 267–276 (2013); Wang et al., J. Immunother. 35(9): 689–701 (2012); и Brentjens et al., Sci Transl Med,. 5(177) (2013). См. также WO2014031687, US 8339645, US 7446179, US 2013/0149337, Патент США No.: 7446190, и Патент США No.: 8389282. Химерные рецепторы, такие как CAR, как правило, включают внеклеточный антигенсвязывающий домен, такой как часть молекулы антитела, как правило, вариабельную область тяжелой (VH) цепи и/или вариабельную область легкой (VL) цепи антитела, например, фрагмент scFv антитела.
[0456] В некоторых вариантах осуществления, рекомбинантный рецептор, например, рецептор антигена содержит внеклеточный связывающий антиген или лиганд домен, который связывается, например, специфически связывается, с антигеном, лигандом и/или маркером. Среди рецепторов антигенов присутствуют функциональные не относящиеся к TCR рецепторы антигенов, такие как химерные рецепторы антигенов (CAR). В некоторых вариантах осуществления, рецептор антигена представляет собой CAR, содержащий внеклеточный узнающий антиген домен, который специфически связывается с антигеном. В некоторых вариантах осуществления, CAR сконструирован со специфичностью для конкретного антигена, маркера или лиганда, такого как антиген, экспрессирующийся в клетках конкретного типа, подлежащих нацеливанию посредством адоптивной терапии, например, маркера злокачественной опухоли, и/или антигена, предназначенного для индукции ослабления ответа, например, антигена, экспрессирующегося в клетках нормального или не пораженного заболеванием типа. Таким образом, CAR, как правило, включает, в своей внеклеточной части, один или несколько связывающих лиганд (например, антиген) молекул, таких как один или несколько антигенсвязывающих фрагментов, доменов или частей, или один или несколько вариабельных доменов антител, и/или молекул антител. В некоторых вариантах осуществления, CAR включает антигенсвязывающую часть или части молекулы антитела, такую как одноцепочечный фрагмент антитела (scFv), происходящий из вариабельной тяжелой (VH) и вариабельной легкой (VL) цепей моноклонального антитела (mAb), или однодоменного антитела (sdAb), такого как sdFv, нанотело, VHH и VNAR. В некоторых вариантах осуществления, антигенсвязывающий фрагмент содержит вариабельные области антитела, соединенные гибким линкером.
[0457] В некоторых вариантах осуществления, среди антигенов, на которые нацелены химерные рецепторы, присутствуют антигены, экспрессирующиеся в контексте заболевания, состояния или типа клеток, подлежащих нацеливанию посредством адоптивной клеточной терапии. Среди заболеваний и состояний присутствуют пролиферативные, неопластические и злокачественные заболевания и нарушения, включая злокачественные опухоли и опухоли, включая гематологические злокачественные опухоли, злокачественные опухоли иммунной системы, такие как лимфомы, лейкозы и/или миеломы, такие как B–, T– и миелоидные лейкозы, лимфомы, и множественные миеломы. В некоторых вариантах осуществления, антиген, на который нацелен рецептор, представляет собой полипептид. В некоторых вариантах осуществления, он представляет собой углевод или другую молекулу. В некоторых вариантах осуществления, антиген является избирательно экспрессированным или сверхэкспрессированным на клетках, пораженных заболеванием или состоянием, например, клетках опухоли или патогенных клетках, по сравнению с нормальными или не являющимися объектом нацеливания клетками или тканями, например, в здоровых клетках или тканях. В других вариантах осуществления, антиген является экспрессированным на нормальных клетках и/или является экспрессированным на модифицированных клетках.
[0458] Антигены, на которые нацелены рецепторы, в некоторых вариантах осуществления, включают орфанный тирозинкиназный рецептор ROR1, tEGFR, Her2, Ll–CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген вируса гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, EGP–2, EGP–4, 0EPHa2, ErbB2, 3, или 4, FBP, фетальный рецептор ацетилхолина, GD2, GD3, HMW–MAA, IL–22R–альфа, IL–13R–альфа2, kdr, легкую цепь каппа, Lewis Y, молекулы клеточной адгезии L1, MAGE–A1, мезотелин, MUC1, MUC16, PSCA, лиганды NKG2D, NY–ESO–1, MART–1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF–R2, карциноэмбриональный антиген (CEA), простатспецифический антиген, PSMA, Her2/neu, рецептор эстрогенов, рецептор прогестерона, эфрин B2, CD123, c–Met, GD–2, и MAGE A3, CE7, антиген опухоли Вильмса 1 (WT–1), циклин, такой как циклин A1 (CCNA1) и/или биотинилированные молекулы, и/или молекулы, экспрессированные HIV, HCV, HBV или другими патогенами.
[0459] В некоторых вариантах осуществления, антиген, на который нацелен рецепторы, включает интегрин αvβ6 (интегрин avb6), антиген созревания B–клеток (BCMA), B7–H3, B7–H6, карбоангидраза 9 (CA9, также известный как CAIX или G250), раково–тестикулярный антиген, раково–тестикулярный антиген 1B (CTAG, также известный как NY–ESO–1 и LAGE–2), карциноэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокинов с мотивом C–C (CCL–1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, эпидермальный фактор роста белок (EGFR), укороченный эпидермальный фактор роста белок (tEGFR), рецептор эпидермального фактора роста с мутацией типа III (EGFR vIII), эпителиальный гликопротеин 2 (EPG–2), эпителиальный гликопротеин 40 (EPG–40), эфрин B2, рецептор эфрина A2 (EPHa2), рецептор эстрогенов, подобный рецептору Fc белок 5 (FCRL5; также известный как гомолог 5 рецептора Fc или FCRH5), фетальный рецептор ацетилхолина (фетальный AchR), связывающий фолат белок (FBP), рецептор фолата альфа, фетальный рецептор ацетилхолина, ганглиозид GD2, O–ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), сопряженный с G белком рецептор 5D (GPCR5D ), Her2/neu (рецепторную тирозинкиназу erb–B2), Her3 (erb–B3), Her4 (erb–B4), димеры erbB, ассоциированный с меланомой высокомолекулярный антиген человека (HMW–MAA), поверхностный антиген вируса гепатита B, человеческий лейкоцитарный антиген A1 (HLA–AIA1), человеческий лейкоцитарный антиген A2 (HLA–A2), рецептор IL–22 альфа(IL–22Ra), рецептор IL–13 альфа 2 (IL–13Ra2), рецептор, содержащий домен вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1–CAM), эпитоп CE7 из L1–CAM, член A семейства 8, содержащего богатые лейцином повторы (LRRC8A), Lewis Y, ассоциированный с меланомой антиген (MAGE)–A1, MAGE–A3, MAGE–A6, мезотелин, c–Met, мышиный цитомегаловирус (CMV), муцин 1 (MUC1), MUC16, лиганды члена D группы 2 естественных киллеров (NKG2D), мелан A (MART–1), молекулу адгезии нервных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простатспецифический антиген, антиген стволовых клеток предстательной железы (PSCA), простатспецифический мембранный антиген (PSMA), подобный рецепторной тирозинкиназе орфанный рецептор 1 (ROR1), сурвивин, гликопротеин трофобластных клеток (TPBG также известный как 5T4), опухолеассоциированный гликопротеин 72 (TAG72), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор фактора роста эндотелия сосудов 2 (VEGFR2), антиген опухоли Вильмса 1 (WT–1), специфический для патогена антиген, или антиген, ассоциированный с универсальной меткой, и/или биотинилированные молекулы, и/или молекулы, экспрессированные HIV, HCV, HBV или другими патогенами. Антигены, на который нацелены рецепторы, в некоторых вариантах осуществления, включает антигены, ассоциированные с злокачественным новообразованием из B–клеток, такие как любой из ряда известных маркеров B–клеток. В некоторых вариантах осуществления, антиген, на который нацелен рецептор, представляет собой или включает CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig–каппа, Ig–лямбда, CD79a, CD79b или CD30.
[0460] В некоторых вариантах осуществления, CAR связывает специфический для патогена антиген. В некоторых вариантах осуществления, CAR является специфическим для вирусных антигенов (таких как вирусный антиген из HIV, HCV, HBV и т.д.), бактериальных антигенов и/или паразитарных антигенов.
[0461] В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент (например, scFv или домен VH) специфически узнает антиген, такой как CD19. В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент происходит из или представляет собой вариант антитела или антигенсвязывающий фрагмент, который специфически связывается с CD19.
[0462] В некоторых вариантах осуществления, домены scFv и/или VH происходят из FMC63. FMC63 в общем относится к мышиному моноклональному антителу IgG1, полученному против клеток Nalm–1 и –16, экспрессирующих CD19 человеческого происхождения (Ling, N. R., et al. (1987). Leucocyte typing III. 302). Антитело FMC63 содержит CDR H1, указанную в SEQ ID NO: 38; CDR H2, указанную в SEQ ID NO:39; CDR H3, указанную в SEQ ID NO: 40 или 54; и CDR L1, указанную в SEQ ID NO: 35; CDR L2, указанную в SEQ ID NO:36 или 55; и CDR L3, указанную в SEQ ID NO:37 или 56. Антитело FMC63 содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность из SEQ ID NO: 41, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность из SEQ ID NO: 42. В некоторых вариантах осуществления, scFv содержит вариабельную легкую цепь, содержащую последовательность CDR L1 из SEQ ID NO:35, последовательность CDR L2 из SEQ ID NO:36 и последовательность CDR L3 из SEQ ID NO:37, и/или вариабельную тяжелую цепь, содержащую последовательность CDR H1 из SEQ ID NO:38, последовательность CDR H2 из SEQ ID NO:39 и последовательность CDR H3 из SEQ ID NO:40, или вариант из любого из вышеуказанных, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними. В некоторых вариантах осуществления, scFv содержит вариабельную область тяжелой цепи из FMC63, указанную в SEQ ID NO:41 и вариабельную область легкой цепи из FMC63, указанную в SEQ ID NO:42, или вариант любого из вышеуказанных, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними. В некоторых вариантах осуществления, вариабельная тяжелая и вариабельная легкая цепи соединены посредством линкера. В некоторых вариантах осуществления, линкер указан в SEQ ID NO:58. В некоторых вариантах осуществления, scFv содержит, в следующем порядке, VH, линкер и VL. В некоторых вариантах осуществления, scFv содержит, в следующем порядке, VL, линкер и VH. В некоторых вариантах осуществления, scFv кодирован последовательностью нуклеотидов, указанной в SEQ ID NO:57, или последовательностью, имеющей по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO:57. В некоторых вариантах осуществления, scFv содержит последовательность аминокислот, указанную в SEQ ID NO:43, или последовательность, имеющей по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO:43.
[0463] В некоторых вариантах осуществления, домен scFv и/или VH происходит из SJ25C1. SJ25C1 представляет собой мышиное моноклональное антитело IgG1, полученное против клеток Nalm–1 и –16, экспрессирующих CD19 человеческого происхождения (Ling, N. R., et al. (1987). Leucocyte typing III. 302). The антитело SJ25C1 содержит CDR H1, H2 и H3, указанную в SEQ ID NO: 47–49, соответственно, и CDR L1, L2 и L3 последовательности, указанную в SEQ ID NO: 44–46, соответственно. Антитело SJ25C1 содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность из SEQ ID NO: 50 и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность из SEQ ID NO: 51. В некоторых вариантах осуществления, svFv содержит вариабельную легкую цепь, содержащую CDR L1 последовательность, указанную в SEQ ID NO:44; CDR L2, указанную в SEQ ID NO: 45; и CDR L3, указанную в SEQ ID NO:46; и/или вариабельную тяжелую цепь, содержащую CDR H1, указанную в SEQ ID NO:47, CDR H2, указанную в SEQ ID NO:48, и CDR H3, указанную в SEQ ID NO:49, или вариант из любого из вышеуказанных, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними. В некоторых вариантах осуществления, scFv содержит вариабельную область тяжелой цепи из SJ25C1, указанную в SEQ ID NO:50 и вариабельную область тяжелой цепи из SJ25C1, указанную в SEQ ID NO:51, или вариант из любого из вышеуказанных, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними. В некоторых вариантах осуществления, вариабельная тяжелая и вариабельная легкая цепи соединены посредством линкера. В некоторых вариантах осуществления, линкер указан в SEQ ID NO:52. В некоторых вариантах осуществления, scFv содержит, в следующем порядке, VH, линкер, и VL. В некоторых вариантах осуществления, scFv содержит, в следующем порядке, VL, линкер и VH. В некоторых вариантах осуществления, scFv содержит последовательность аминокислот, указанную в SEQ ID NO:53, или последовательность, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO:53.
[0464] В некоторых аспектах, CAR содержит связывающий лиганд (например, антиген) домен который связывает или узнает, например, специфически связывает, универсальную метку или универсальный эпитоп. В некоторых аспектах, связывающий домен может связывать молекулу, метку, полипептид и/или эпитоп, которые могут быть соединены с другой связывающей молекулой (например, антителом или антигенсвязывающим фрагментом), узнающий антиген, ассоциированный с заболеванием или нарушением. Иллюстративные метка или эпитоп включают краситель (например, флуоресцеинизотиоцианат) или биотин. В некоторых аспектах, связывающая молекула (например, антитело или антигенсвязывающий фрагмент) соединена с меткой, которая узнает антиген, ассоциированный с заболеванием или нарушением, например, антиген опухоли, вместе с модифицированной клеткой, экспрессирующей CAR, специфический для метки, чтобы вызывать цитотоксичность или другие эффекторные функции модифицированной клетки. В некоторых аспектах, специфичность CAR для антигена, ассоциированного с заболеванием или нарушением, обеспечивают посредством снабженной меткой связывающей молекулы (например, антитела), и различные снабженные метками связывающие молекулы можно использовать для нацеливания на различные антигены. Иллюстративные CAR, специфические для универсальной метки или универсального эпитопа, включают CAR, описанные, например, в U.S. 9233125, WO 2016/030414, Urbanska et al., (2012) Cancer Res 72: 1844–1852, и Tamada et al., (2012). Clin Cancer Res 18:6436–6445.
[0465] В некоторых вариантах осуществления, CAR содержит a подобное TCR антитело, такое как антитело или антигенсвязывающий фрагмент (например, scFv), которое специфически узнает внутриклеточный антиген, такой как опухолеассоциированный антиген, представленный на поверхности клетки в форме комплекса главный комплекс гистосовместимости (MHC)–пептид. В некоторых вариантах осуществления, антитело или его антигенсвязывающую часть, узнающие комплекс MHC–пептид, можно экспрессировать на клетках как часть рекомбинантного рецептора, такого как рецептор антигена. Среди рецепторов антигенов присутствуют функциональные не относящиеся к T–клеточному рецептору (TCR) рецепторы антигенов, такие как химерные рецепторы антигенов (CAR). В некоторых вариантах осуществления, CAR, содержащий антитело или антигенсвязывающий фрагмент, имеющие подобную TCR специфичность, направленную против комплексов пептид–MHC, также может быть обозначен как подобный TCR CAR. В некоторых вариантах осуществления, CAR представляет собой подобный TCR CAR, и антиген представляет собой процессированный пептидный антиген, такой как пептидный антиген из внутриклеточного белка, который, подобно TCR, осуществляет узнавание на поверхности клетки в контексте молекулы MHC. В некоторых вариантах осуществления, внеклеточный антигенсвязывающий домен, специфический для комплекса MHC–пептид, из подобного TCR CAR, соединен с одним или нескольким компонентами для передачи внутриклеточных сигналов, в некоторых аспектах, посредством линкеров и/или трансмембранного домена(доменов). В некоторых вариантах осуществления, такие молекулы могут, как правило, имитировать или приблизительно воспроизводить сигнал через природный рецептор антигена, такой как TCR, и, необязательно, сигнал через такой рецептор в комбинации с костимулирующим рецептором.
[0466] Ссылка на «главный комплекс гистосовместимости» (MHC) относится к белку, как правило, гликопротеину, который содержит полиморфный участок связывания пептида или связывающую бороздку, который может, в некоторых случаях, образовывать комплекс с пептидными антигенами из полипептидов, включая пептидные антигены, процессированные клеточным аппаратом. В некоторых случаях, молекулы MHC могут быть экспонированы или экспрессированы на поверхности клетки, включая форму комплекса с пептидом, т.е. комплекса MHC–пептид, для представления антигена в конформации, узнаваемой рецептором антигена на T–клетках, таким как TCR или подобное TCR антитело. Как правило, молекулы MHC класса I представляют собой гетеродимеры, имеющие трансмембранную α–цепь, в некоторых случаях, с тремя α–доменами, и нековалентно связанный β2–микроглобулин. Как прравило, молекулы MHC класса II состоят из двух трансмембранных гликопротеинов, α и β, оба из которых, как правило, пересекают мембрану. Молекула MHC может включать эффективный участок MHC, который содержит антигенсвязывающий участок или участки для связывания пептида, и последовательности, необходимые для узнавания соответствующим рецептором антигена. В некоторых вариантах осуществления, молекулы MHC класса I доставляют пептиды, образованные в цитозоле, к поверхности клетки, где комплекс MHC–пептид узнают T–клетки, как правило, такие как CD8+ T–клетки, но, в некоторых случаях, CD4+ T–клетки. В некоторых вариантах осуществления, молекулы MHC класса II доставляют пептиды, образованные в везикулярной системе, к поверхности клетки, где их, как правило, узнают CD4+ T–клетки. Как правило, молекулы MHC кодированы группой сцепленных локусов, совместно называемых H–2 у мыши и человеческими лейкоцитарными антигенами (HLA) у человека. Таким образом, как правило, MHC человека может быть также обозначен, как человеческий лейкоцитарный антиген (HLA).
[0467] Термин «комплекс MHC–пептид» или «комплекс пептид–MHC», или его варианты, относится к комплексу или ассоциации пептидного антигена и молекулы MHC, например, как правило, посредством нековалентных взаимодействий пептида в связывающей бороздке или щели молекулы MHC. В некоторых вариантах осуществления, комплекс MHC–пептид представлен или экспонирован на поверхности клеток. В некоторых вариантах осуществления, комплекс MHC–пептид может быть специфически узнан рецептором антигена, таким как TCR, подобным TCR CAR или их антигенсвязывающими фрагментами.
[0468] В некоторых вариантах осуществления, пептид, такой как пептидный антиген или эпитоп из полипептида, может связываться с молекулой MHC, например, для узнавания рецептором антигена. Как правило, пептид происходит из или образован на основе фрагмента более длинной биологической молекулы, такой как полипептид или белок. В некоторых вариантах осуществления, пептид, как правило, имеет длину от приблизительно 8 до приблизительно 24 аминокислот. В некоторых вариантах осуществления, пептид имеет длину от или приблизительно от 9 до 22 аминокислот для узнавания в комплексе с MHC класса II. В некоторых вариантах осуществления, a пептид имеет длину от или приблизительно от 8 до 13 аминокислот для узнавания в комплексе с MHC класса I. В некоторых вариантах осуществления, после узнавания пептида в контексте молекулы MHC, например, в комплексе MHC–пептид, рецептор антигена, такой как TCR или подобный TCR CAR, подает или запускает сигнал активации для T–клетки, который индуцирует ответ T–клетки, такой как пролиферация T–клетки, продукция цитокинов, ответ цитотоксической T–клетки или другой ответ.
[0469] В некоторых вариантах осуществления, подобное TCR антитело или антигенсвязывающий фрагмент, известны или могут быть получены известными способами (см., например, Публикации патентных заявок США No. US 2002/0150914; US 2003/0223994; US 2004/0191260; US 2006/0034850; US 2007/00992530; US20090226474; US20090304679; и Публикацию международной патентной заявки No. WO 03/068201).
[0470] В некоторых вариантах осуществления, антитело или его антигенсвязывающую часть, которые специфически связываются с комплексом MHC–пептид, можно получать посредством иммунизации хозяина с использованием эффективного количества иммуногена, содержащего специфический комплекс MHC–пептид. В некоторых случаях, пептид из комплекса MHC–пептид представляет собой эпитоп антигена, способного связываться с MHC, такого как антиген опухоли, например, универсальный антиген опухоли, антиген миеломы или другой антиген, как описано ниже. В некоторых вариантах осуществления, эффективное количество иммуногена затем вводят хозяину для вызова иммунного ответа, где иммуноген сохраняет свою трехмерную форму в течение периода времени, достаточного для вызова иммунного ответа против трехмерного представления пептида в связывающей бороздке молекулы MHC. Сыворотку, собранную от хозяина, затем анализируют для определения того, продуцированы ли желательные антитела, узнающие трехмерное представление пептида в связывающей бороздке молекулы MHC. В некоторых вариантах осуществления, продуцированные антитела можно оценивать для подтверждения того, что антитело может отличать комплекс MHC–пептид от отдельной молекулы MHC, отдельного представляющего интерес пептида, и комплекса MHC и не относящегося к делу пептида. Затем желательные антитела можно выделять.
[0471] В некоторых вариантах осуществления, антитело или его антигенсвязывающую часть, которые специфически связываются с комплексом MHC–пептид, можно получать с использованием способов дисплея библиотек антител, таких как фаговые библиотеки антител. В некоторых вариантах осуществления, можно получать библиотеки фагового дисплея для мутантного Fab, scFv или других форм антитела, например, в которых члены библиотеки мутированы в одном или нескольких остатках CDR или нескольких CDR. См., например, Публикации патентных заявок США No. US20020150914, US20140294841; и Cohen CJ. et al. (2003) J Mol. Recogn. 16:324–332.
[0472] Термин «антитело» использован в настоящем описании в самом широком смысле и включает поликлональные и моноклональные антитела, включая интактные антитела и функциональные (антигенсвязывающие) фрагменты антител, включая фрагменты антигенсвязывающих (Fab) фрагментов, фрагменты F(ab’)2, фрагменты Fab’, фрагменты Fv, фрагменты рекомбинантного IgG (rIgG), вариабельные области тяжелой цепи (VH), способные специфически связывать антиген, одноцепочечные фрагменты антител, включая одноцепочечные вариабельные фрагменты (scFv), и однодоменные антитела (например, sdAb, sdFv, нанотело, VHH или VNAR) или фрагменты. Термин включает генетически модифицированные и/или иным образом модифицированные формы иммуноглобулинов, такие как интраантитела, пептидные антитела, химерные антитела, полностью человеческие антитела, гуманизированные антитела, и гетероконъюгированные антитела, мультиспецифические, например, биспецифические, антитела, диатела, триатела и тетратела, тандемный ди–scFv, тандемный три–scFv. Если не указано иначе, термин «антитело» следует понимать как включающий их функциональные фрагменты антител. Термин включает также интактные или полноразмерные антитела, включая антитела любого класса или подкласса, включая IgG и его подклассы, IgM, IgE, IgA и IgD. В некоторых аспектах, CAR представляет собой биспецифический CAR, например, содержащий два антигенсвязывающих домена с различными специфичностями.
[0473] В некоторых вариантах осуществления, антигенсвязывающие белки, антитела и их антигенсвязывающие фрагменты специфически узнают антиген полноразмерного антитела. В некоторых вариантах осуществления, тяжелая и легкая цепи антитела могут являться полноразмерными или могут представляет собой антигенсвязывающий фрагмент (a Fab, F(ab’)2, Fv или одноцепочечный фрагмент Fv (scFv)). В других вариантах осуществления, константная область тяжелой цепи антитела выбрана, например, из IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD, и IgE, в частности выбрана, например, из IgG1, IgG2, IgG3, и IgG4, более конкретно, IgG1 (например, IgG1 человека). В другом варианте осуществления, константная область легкой цепи антитела выбрана, например, из каппа или лямбда, в частности каппа.
[0474] Среди представленных антител присутствуют фрагменты антител. «Фрагмент антитела» относится к молекуле, отличной от интактного антитела, которая содержит часть интактного антитела, который связывается с антигеном, с которым связывается интактное антитело. Примеры фрагментов антител включают, но без ограничения, Fv, Fab, Fab’, Fab’–SH, F(ab’)2; диатела; линейные антитела; вариабельные области тяжелой цепи (VH), одноцепочечные молекулы антител, такие как scFv и однодоменные антитела VH; и мультиспецифические антитела, сформированные из фрагментов антител. В конкретных вариантах осуществления, антитела представляют собой одноцепочечное фрагменты антител, содержащие вариабельную область тяжелой цепи и/или вариабельную область легкой цепи, например, scFv.
[0475] Термин «вариабельная область» или «вариабельный домен» относится к домену тяжелой или легкой цепи антитела, вовлеченному в связывание антитела с антигеном. Вариабельные домены тяжелой цепи и легкой цепи (VH и VL, соответственно) нативного антитела, как правило, имеют сходные сруктуры, где каждый домен содержит четыре консервативные каркасные области (FR) и три CDR. (См., например, Kindt et al. Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007). Один домен VH или VL может являться достаточным для обеспечения специфичности связывания антигена. Кроме того, антитела, связывающие конкретный антиген, можно выделять с использованием домена VH или VL из антитела, который связывается с антигеном, для скрининга библиотеки комплементарных домены VL или VH, соответственно. См., например, Portolano et al., J. Immunol. 150:880–887 (1993); Clarkson et al., Nature 352:624–628 (1991).
[0476] Однодоменные антитела (sdAb) представляют собой фрагменты антител, содержащие весь или часть вариабельного домена тяжелой цепи, или весь или часть вариабельного домена легкой цепи антитела. В конкретных вариантах осуществления, однодоменное антитело представляет собой человеческое однодоменное антитело. В некоторых вариантах осуществления, CAR содержит домен тяжелой цепи антитела, который специфически связывается с антигеном, таким как маркер злокачественной опухоли или антиген клеточной поверхности для клетки или заболевания, подлежащих нацеливанию, например, клетки опухоли или клетки злокачественной опухоли, таким как любой из антигенов–мишеней, описанных в настоящем описании или известных. Иллюстративные однодоменные антитела включают sdFv, нанотело, VHH или VNAR.
[0477] Фрагменты антител можно получать различными способами, включая, но без ограничения, протеолитическое расщепление интактного антитела, так же как продукцию рекомбинантными клетками–хозяевами. В некоторых вариантах осуществления, антитела представляют собой рекомбинантно полученные фрагменты, такие как фрагменты, содержащие аранжировки, не встречающиеся в природе, такие как фрагменты с двумя или более областями или цепями антитела, соединенными посредством синтетических линкеров, например, пептидных линкеров, и/или которые невозможно получить посредством ферментного расщепления природного интактного антитела. В некоторых вариантах осуществления, фрагменты антител представляют собой scFv.
[0478] «Гуманизированное» антитело представляет собой антитело, в котором все или в основном все аминокислотные остатки CDR происходят из не относящихся к человеку CDR, и все или в основном все аминокислотные остатки FR происходят из человеческих FR. Гуманизированное антитело, необязательно, может включать по меньшей мере часть константной области антитела, происходящую из человеческого антитела. «Гуманизированная форма» не относящегося к человеку антитела относится к варианту не относящегося к человеку антитела, подвергнутому гуманизации, как правило, для уменьшения иммуногенности для человека, с сохранением в то же время специфичности и аффинности исходного не относящегося к человеку антитела. В некоторых вариантах осуществления, некоторые остатки FR в гуманизированном антителе заменены на соответствующие остатки из не относящегося к человеку антитела (например, антитела, из которого происходят остатки CDR), например, для сохранения или улучшения специфичности или аффинности антитела.
[0479] Таким образом, в некоторых вариантах осуществления, химерный антигенный рецептор, включая подобные TCR CAR, включает внеклеточный фрагмент, содержащий антитело или фрагмент антитела. В некоторых вариантах осуществления, антитело или фрагмент включает scFv. В некоторых аспектах, антитело или антигенсвязывающий фрагмент можно получать посредством скрининга множества, например, библиотеки, антигенсвязывающих фрагментов или молекул, например, посредством скрининга библиотеки scFv по связыванию со специфическим антигеном или лигандом.
[0480] В некоторых аспектах, рекомбинантный рецептор, например, химерный антигенный рецептор, включает внеклеточный фрагмент, содержащий один или несколько связывающих лиганд (например, антиген) доменов, таких как антитело или его фрагмент, и одну или несколько внутриклеточных передающих сигнал областей или доменов (также взаимозаменяемо называемых цитоплазматическими передающими сигнал доменами или областями). В некоторых аспектах, рекомбинантный рецептор, например, CAR, дополнительно включает спейсер и/или трансмембранный домен, или фрагмент. В некоторых аспектах, спейсер и/или трансмембранный домен может соединять внеклеточный фрагмент, содержащий связывающий лиганд (например, антиген) домен, и внутриклеточные передающие сигнал область(области) или домен(ы).
[0481] В некоторых вариантах осуществления, часть антитела рекомбинантного рецептора, например, CAR, дополнительно включает по меньшей мере часть константной области иммуноглобулина, такую как шарнирная область, например, шарнирная область IgG4 и/или CH1/CL, и/или область Fc. В некоторых вариантах осуществления, константная область или фрагмент происходит из IgG человека, такого как IgG4 или IgG1. В некоторых аспектах, часть константной области служит спейсерной областью между узнающим антиген компонентом, например, scFv, и трансмембранным доменом. Спейсер может иметь длину, обеспечивающую увеличенную способность клетки отвечать после связывания антигена, по сравнению с отсутствием спейсера. Иллюстративные спейсеры, например, шарнирные области, включают спейсеры, описанные в публикации международной патентной заявки номер WO2014031687. В некоторых примерах, спейсер составляет или составляет приблизительно 12 аминокислот в длину, или составляет не более чем 12 аминокислот в длину. Иллюстративные спейсеры включают спейсеры, имеющие по меньшей мере приблизительно от 10 до 229 аминокислот, приблизительно от 10 до 200 аминокислот, приблизительно от 10 до 175 аминокислот, приблизительно от 10 до 150 аминокислот, приблизительно от 10 до 125 аминокислот, приблизительно от 10 до 100 аминокислот, приблизительно от 10 до 75 аминокислот, приблизительно от 10 до 50 аминокислот, приблизительно от 10 до 40 аминокислот, приблизительно от 10 до 30 аминокислот, приблизительно от 10 до 20 аминокислот или приблизительно от 10 до 15 аминокислот, и включает любое целое число между конечными точками любого из перечисленных диапазонов. В некоторых вариантах осуществления, область спейсера имеет приблизительно 12 аминокислот или менее, приблизительно 119 аминокислот или менее, или приблизительно 229 аминокислот или менее. В некоторых вариантах осуществления, спейсер составляет менее чем 250 аминокислот в длину, менее чем 200 аминокислот в длину, менее чем 150 аминокислот в длину, менее чем 100 аминокислот в длину, менее чем 75 аминокислот в длину, менее чем 50 аминокислот в длину, менее чем 25 аминокислот в длину, менее чем 20 аминокислот в длину, менее чем 15 аминокислот в длину, менее чем 12 аминокислот в длину, или менее чем 10 аминокислот в длину. В некоторых вариантах осуществления, спейсер составляет от или приблизительно от 10 до 250 аминокислот в длину, от 10 до 150 аминокислот в длину, от 10 до 100 аминокислот в длину, от 10 до 50 аминокислот в длину, от 10 до 25 аминокислот в длину, от 10 до 15 аминокислот в длину, 15 до 250 аминокислот в длину, от 15 до 150 аминокислот в длину, от 15 до 100 аминокислот в длину, от 15 до 50 аминокислот в длину, 15 до 25 аминокислот в длину, от 25 до 250 аминокислот в длину, от 25 до 100 аминокислот в длину, от 25 до 50 аминокислот в длину, от 50 до 250 аминокислот в длину, от 50 до 150 аминокислот в длину, от 50 до 100 аминокислот в длину, от 100 до 250 аминокислот в длину, от 100 до 150 аминокислот в длину или от 150 до 250 аминокислот в длину. Иллюстративные спейсеры включают шарнир IgG4 отдельно, шарнир IgG4, связанный с доменами CH2 и CH3, или шарнир IgG4, связанный с доменом CH3. Иллюстративные спейсеры включают, но без ограничения, спейсеры, описанные в Hudecek et al. Clin. Cancer Res., 19:3153 (2013), публикации международной патентной заявки номер WO2014031687, Патент США No. 8822647 или публикации патентной заявки No. US2014/0271635.
[0482] В некоторых вариантах осуществления, константная область или фрагмент происходит из IgG человека, такого как IgG4 или IgG1. В некоторых аспектах, спейсер представляет собой полипептидный спейсер, такой как один или несколько, выбранных из того, который: (a) содержит или состоит из всего или части шарнира иммуноглобулина или его модифицированного варианта, или содержит приблизительно 15 аминокислот или менее, и не содержит внеклеточную область CD28 или внеклеточную область CD8, (b) содержит или состоит из всего или части шарнира иммуноглобулина, необязательно, шарнира IgG4 или его модифицированного варианта, и/или содержит приблизительно 15 аминокислот или менее, и не содержит внеклеточную область CD28 или внеклеточную область CD8, или (c) имеет или имеет приблизительно 12 аминокислот в длину и/или содержит или состоит из всего или части шарнира иммуноглобулина, необязательно, IgG4, или его модифицированного варианта; или (d) содержит или состоит из формулы X1PPX2P (SEQ ID NO: 31), где X1 представляет собой глицин, цистеин или аргинин, и X2 представляет собой цистеин или треонин. В некоторых вариантах осуществления, спейсер имеет последовательность ESKYGPPCPPCP (указанную в SEQ ID NO: 1), и кодирован последовательностью, указанной в SEQ ID NO: 2. В некоторых вариантах осуществления, спейсер имеет последовательность, указанную в SEQ ID NO: 3. В некоторых вариантах осуществления, спейсер имеет последовательность, указанную в SEQ ID NO: 4. В некоторых вариантах осуществления, константная область или фрагмент происходит из IgD. В некоторых вариантах осуществления, спейсер имеет последовательность, указанную в SEQ ID NO: 5. В некоторых вариантах осуществления, спейсер имеет последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с любой из SEQ ID NO: 1, 3, 4 или 5 или 27–34.
[0483] Этот узнающий антиген домен, как правило, является связанным с одним или несколькими компонентами для передачи внутриклеточных сигналов, такими как передающие сигналы компоненты, имитирующие активацию через комплекс рецептора антигена, такой как комплекс TCR, в случае CAR, и/или передачу сигнала посредством другого рецептора поверхности клетки. Таким образом, в некоторых вариантах осуществления, антигенсвязывающ компонент (например, антитело) является связанным с одним или несколькими трансмембранными и внутриклеточными доменами передачи сигналов. В некоторых вариантах осуществления, трансмембранный домен слит с внеклеточным доменом. В одном варианте осуществления, используют трансмембранный домен, естественным образом ассоциированный с одним из доменов в рецепторе, например, CAR. В некоторых случаях, трансмембранный домен отбирают или модифицируют посредством замены аминокислот, для исключения связывания таких доменов с трансмембранными доменами одинаковых или различных поверхностных мембранных белков для минимизации взаимодействий с другими членами комплекса рецептора.
[0484] Трансмембранный домен, в некоторых вариантах осуществления, происходит либо из природного, либо из синтетического источника. Когда источник является природным, домен, в некоторых аспектах, происходит из любого связанного с мембраной или трансмембранного белка. Трансмембранные области включают области, происходящие из (т.е., содержащие по меньшей мере трансмембранную область(области) из) цепи альфа, бета или зета T–клеточного рецептора, CD28, CD3–эпсилон, CD45, CD4, CD5, CD8, CD9, CD 16, CD22, CD33, CD37, CD64, CD80, CD86, CD 134, CD137(4–1BB), CD 154. Альтернативно, трансмембранный домен, в некоторых вариантах осуществления, является синтетическим. В некоторых аспектах, синтетический трансмембранный домен содержит преимущественно гидрофобные остатки, такие как лейцин и валин. В некоторых аспектах, триплет из фенилаланина, триптофана и валина можно обнаружить на каждом конце синтетического трансмембранного домена. В некоторых вариантах осуществления, связывание осуществляют посредством линкеров, спейсеров и/или трансмембранного домена(доменов). В некоторых аспектах, трансмембранный домен содержит трансмембранный фрагмент из CD28 или его варианта. Внеклеточный и трансмембранный домен могут быть связаны напрямую или опосредованно. В некоторых вариантах осуществления, внеклеточный и трансмембранный домен связаны посредством спейсера, такого как любой, описанный в настоящем описании.
[0485] Среди внутриклеточных доменов передачи сигналов присутствуют домены, имитирующие или приблизительно воспроизводящие сигнал через природный рецептор антигена, сигнал через такой рецептор в комбинации с костимулирующим рецептором, и/или сигнал через костимулирующий рецептор отдельно. В некоторых вариантах осуществления, короткий олиго– или полипептидный линкер, например, линкер между 2 и 10 аминокислот в длину, такой как линкер, содержащий остатки глицина и серина, например, дуплет глицин–серин, присутствует и формирует связь между трансмембранным доменом и цитоплазматическим передающим сигналы доменом CAR.
[0486] Рецептор, например, CAR, как правило, включает по меньшей мере один внутриклеточный передающий сигналы компонент или компонентов. В некоторых вариантах осуществления, рецептор включает внутриклеточный компонент комплекса TCR, такой как цепь CD3 TCR, опосредующая активацию T–клетки и цитотоксичность, например, цепь CD3–зета. Таким образом, в некоторых аспектах, антигенсвязывающий фрагмент является связанным с одним или несколькими модули передачи сигналов. В некоторых вариантах осуществления, модули передачи сигналов включают трансмембранный домен CD3, внутриклеточные передающие сигналы домены CD3 и/или другие трансмембранные домены CD. В некоторых вариантах осуществления, рецептор, например, CAR, дополнительно включает часть одной или нескольких дополнительных молекул, таких как рецептор Fc γ, CD8, CD4, CD25 или CD16. Например, в некоторых аспектах, CAR или другой химерный рецептор включает химерную молекулу между CD3–зета (CD3–ζ) или рецептором Fc γ и CD8, CD4, CD25 или CD16.
[0487] В некоторых вариантах осуществления, при связывании CAR или другого химерного рецептора, цитоплазматический домен или внутриклеточный передающий сигналы домен рецептора активирует по меньшей мере одно из нормальных эффекторных функций или ответов иммуноцита, например, T–клетки, модифицированной для экспрессии CAR. Например, в некоторых контекстах, CAR индуцирует функцию T–клетки, такую как цитолитическая активность или активность T–клетки–помощника, например, секрецию цитокинов или другие факторы. В некоторых вариантах осуществления, укороченный фрагмент внутриклеточного домена передачи сигналов компонента рецептора антигена или костимулирующей молекулы используют вместо интактной иммуностимулирующей цепи, например, если он передает сигнал эффекторной функции. В некоторых вариантах осуществления, внутриклеточный домен или передающие сигналы домены включают цитоплазматические последовательности T–клеточного рецептора (TCR), и в некоторых аспектах, также цитоплазматические последовательности корецепторов, которые в природном контексте действуют во взаимодействии с такими рецепторами для инициации передачи сигналов после привлечения рецептора антигена.
[0488] В контексте природного TCR, полная активация, как правило, требует не только передачи сигналов через TCR, но также костимулирующего сигнала.
[0489] Таким образом, в некоторых вариантах осуществления, для стимуляции полной активации, компонент для образования вторичного или костимулирующего сигнала также включают в CAR. В других вариантах осуществления, CAR не включает компонент для образования костимулирующего сигнала. В некоторых аспектах, дополнительный CAR является экспрессированным на той же клетке и обеспечивает компонент для образования вторичного или костимулирующего сигнала.
[0490] Активацию T–клетки в некоторых аспектах описывают как опосредованную двумя классами цитоплазматических последовательностей для передачи сигналов: последовательностями, инициирующими зависимая от антигена первичная активация через TCR (первичные цитоплазматические передающие сигналы последовательности), и последовательностями, которые действуют независимым от антигена образом для образования вторичного или костимулирующего сигнала (вторичные цитоплазматические передающие сигналы последовательности). В некоторых аспектах, CAR включает один или оба из таких передающих сигналы компонентов.
[0491] В некоторых аспектах, CAR включает первичную цитоплазматическую передающую сигналы последовательность, которая регулирует первичную активацию комплекса TCR. Первичные цитоплазматические передающие сигналы последовательности, которые действуют стимулирующим образом, могут содержать передачи сигналов, известные как иммунорецепторные тирозиновые активирующие мотивы или ITAM. Примеры ITAM, содержащих первичные цитоплазматические передающие сигналы последовательности, включают ITAM, происходящие из TCR–зета, FcR–гамма, FcR–бета, CD3–гамма, CD3–дельта, CD3–эпсилон, CD8, CD22, CD79a, CD79b, и CD66d. В некоторых вариантах осуществления, цитоплазматические молекула(молекулы) передачи сигналов в CAR содержит(содержат) цитоплазматический передающий сигналы домен, его часть, или последовательность, происходящую из CD3–зета.
[0492] В некоторых вариантах осуществления, CAR включает передающий сигналы домен и/или трансмембранный фрагмент костимулирующего рецептора, такого как CD28, 4–1BB, OX40, DAP10 и ICOS. В некоторых аспектах, один и тот же CAR включает как активирующий, так и костимулирующий компоненты.
[0493] В некоторых вариантах осуществления, активирующий домен включен в один CAR, в то время как костимулирующий компонент предоставлен другим CAR, узнающим другой антиген. В некоторых вариантах осуществления, CAR включают активирующие или стимулирующие CAR, костимулирующие CAR, оба экспрессированнные на одной и той же клетке (см. WO2014/055668). В некоторых аспектах, клетки включают один или несколько стимулирующих или активирующих CAR и/или a костимулирующих CAR. В некоторых вариантах осуществления, клетки дополнительно включают ингибирующие CAR (iCAR, см. Fedorov et al., Sci. Transl. Medicine, 5(215) (2013), такие как CAR, узнающие антиген, отличный от антигена, ассоциированного с и/или специфического для заболевания или состояния, посредством чего активирующий сигнал, подаваемый через нацеленный на заболевание CAR уменьшают или ингибируют посредством связывания ингибирующего CAR с его лигандом, например, для уменьшения неспецифические эффекты.
[0494] В конкретных вариантах осуществления, внутриклеточный передающий сигналы домен содержит трансмембранный и передающий сигналы домен CD28, связанный с внутриклеточным доменом CD3 (например, CD3–зета). В некоторых вариантах осуществления, внутриклеточный передающий сигналы домен содержит химерные из CD28 и CD137 (4–1BB, TNFRSF9) костимулирующие домены, связанные с внутриклеточным доменом CD3–зета.
[0495] В некоторых вариантах осуществления, CAR включает один или несколько, например, два или более, костимулирующих домена и активирующий домен, например, первичный активирующий домен, в цитоплазматической части. Иллюстративные CAR включают внутриклеточные компоненты CD3–зета, CD28 и 4–1BB.
[0496] В некоторых вариантах осуществления, CAR или другой рецептор антигена дополнительно включает маркер, такой как поверхностный маркер клетки, который можно использовать для подтверждения трансдукции или модификации клетки для экспрессии рецептора, такой как укороченный вариант рецептора поверхности клетки, такой как укороченный EGFR (tEGFR). В некоторых аспектах, маркер включает весь или часть (например, укороченную форму) CD34, NGFR, или рецептора эпидермального фактора роста (например, tEGFR). В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая маркер, является функционально связанной с полинуклеотидом, кодирующим линкерную последовательность, такую как расщепляемая линкерная последовательность, например, T2A. Например, маркер, и необязательно, линкерная последовательность, могут представлять собой любые, как описано в опубликованной патентной заявке No. WO2014031687. Например, маркер может представлять собой укороченный EGFR (tEGFR), необязательно, связанный с линкерной последовательностью, такой как расщепляемая линкерная последовательность T2A. Иллюстративный полипептид для укороченного EGFR (например, tEGFR) содержит последовательность аминокислот, указанную в SEQ ID NO: 7 или 23, или последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 7 или 23. Иллюстративная линкерная последовательность T2A содержит последовательность аминокислот, указанную в SEQ ID NO: 6 или последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 6.
[0497] В некоторых вариантах осуществления, маркер представляет собой молекулу, например, поверхностный белок клетки, не обнаруженный в природе на T–клетках или не обнаруженный в природе на поверхности T–клеток, или его фрагмент. В некоторых вариантах осуществления, молекула представляет собой не собственную молекулу, например, не собственный белок, т.е., белок, не узнаваемый как «собственный» иммунной системой хозяина, которому будут адоптивно переносить клетки.
[0498] В некоторых вариантах осуществления, маркер не выполняет терапевтической функции и/или не оказывает эффекта, отличного от использования в качестве маркера для генетической модификации, например, для отбора успешно модифицированных клеток. В других вариантах осуществления, маркер может представлять собой терапевтическую молекулу или молекулу, иным образом оказывающую некоторый желательный эффект, такой как лиганд для клетки которая может быть встречена in vivo, например, костимулирующую молекулу или молекулу иммунной контрольной точки для усиления и/или ослабления ответов клеток после адоптивного переноса и встречи с лигандом.
[0499] В некоторых случаях, CAR обозначают как CAR первого, второго, третьего или четвертого поколения. В некоторых аспектах, CAR первого поколения представляет собой CAR, обеспечивающий единственно первичны стимулирующий или активирующий сигнал, например, через индуцированный CD3–цепью сигнал после связывания антигена; в некоторых аспектах, CAR второго поколения представляет собой CAR, обеспечивающий такой сигнал и костимулирующий сигнал, такой как CAR, включающий внутриклеточные передающие сигналы область(области) или домен(ы) из одного или нескольких костимулирующих рецепторов, таких как CD28, CD137 (4–1BB), OX40 (CD134), CD27, DAP10, DAP12, NKG2D, ICOS и/или другие костимулирующий рецепторы; в некоторых аспектах, CAR третьего поколения представляет собой CAR, включающий множество костимулирующих доменов из различных костимулирующих рецепторов, например, выбранных из CD28, CD137 (4–1BB), OX40 (CD134), CD27, DAP10, DAP12, NKG2D, ICOS и/или других костимулирующих рецепторов; в некоторых аспектах, CAR четвертого поколения представляет собой CAR, включающий три или более костимулирующих домена из различных костимулирующий рецепторы, например, выбранных из CD28, CD137 (4–1BB), OX40 (CD134), CD27, DAP10, DAP12, NKG2D, ICOS и/или других костимулирующих рецепторов.
[0500] В некоторых вариантах осуществления, химерный антигенный рецептор включает внеклеточный фрагмент, содержащий антитело или фрагмент антитела. В некоторых аспектах, химерный антигенный рецептор включает внеклеточный фрагмент, содержащий антитело или фрагмент, и внутриклеточный передающий сигналы домен. В некоторых вариантах осуществления, антитело или фрагмент включает scFv, и внутриклеточный домен содержит ITAM. В некоторых аспектах, внутриклеточный передающий сигналы домен включает передающий сигналы домен зета–цепи из зета–цепи CD3 (CD3ζ). В некоторых вариантах осуществления, химерный антигенный рецептор включает трансмембранный домен, связывающий внеклеточный домен и внутриклеточный передающий сигналы домен. В некоторых аспектах, трансмембранный домен содержит трансмембранный фрагмент CD28. В некоторых вариантах осуществления, химерный антигенный рецептор содержит внутриклеточный домен из костимулирующей молекулы T–клетки. Антигенсвязывающий фрагмент внеклеточного домена и трансмембранный домен могут быть связаны напрямую или опосредованно. В некоторых вариантах осуществления, антигенсвязывающий фрагмент внеклеточного домена и трансмембранный домен связаны посредством спейсера, такого как любой из описанных в настоящем описании. В некоторых вариантах осуществления, рецептор содержит внеклеточный фрагмент молекулы, из которой происходит трансмембранный домен, например, внеклеточный фрагмент CD28. В некоторых вариантах осуществления, химерный антигенный рецептор содержит внутриклеточный домен, происходящий из костимулирующей молекулы T–клетки, или его функциональный вариант, например, химерный между трансмембранным доменом и содержащим ITAM, например, происходящим из CD3–зета, передающим сигналы доменом. В некоторых аспектах, костимулирующая молекула T–клетки представляет собой CD28 или 41BB.
[0501] Например, в некоторых вариантах осуществления, CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранный фрагмент CD28 или его функциональный вариант, и внутриклеточный передающий сигналы домен, содержащий передающий сигналы фрагмент CD28 или его функциональный вариант и передающий сигналы фрагмент CD3–зета или его функциональный вариант. В некоторых вариантах осуществления, CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранный фрагмент CD28 или его функциональный вариант, и внутриклеточный передающий сигналы домен, содержащий передающий сигналы фрагмент 4–1BB или его функциональный вариант, и передающий сигналы фрагмент CD3–зета или его функциональный вариант. В некоторых таких вариантах осуществления, рецептор дополнительно включает спейсер, содержащий фрагмент молекулы Ig, например, молекулы Ig человека, такой как шарнир Ig или его вариант, например, шарнир IgG4 или его вариант, например, содержащий только шарнир спейсер.
[0502] В некоторых вариантах осуществления, трансмембранный домен рекомбинантного рецептора, например, CAR, представляет собой или включает трансмембранный домен CD28 человека (например, No. доступа P10747.1) или его вариант, такой как трансмембранный домен, содержащий последовательность аминокислот, указанную в SEQ ID NO: 8, или последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 8; в некоторых вариантах осуществления, содержащий трансмембранный домен фрагмент рекомбинантного рецептора содержит последовательность аминокислот, указанную в SEQ ID NO: 9, или последовательность аминокислот, имеющую по меньшей мере или приблизительно 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней.
[0503] В некоторых вариантах осуществления, внутриклеточный передающий сигналы компонент(ы) рекомбинантного рецептора, например, CAR, содержит внутриклеточный передающий костимулирующие сигналы домен из CD28 человека, или его функциональный вариант или фрагмент, такой как домен с заменой LL на GG в положениях 186–187 нативного белка CD28. Например, внутриклеточный передающий сигналы домен может содержать последовательность аминокислот, указанную в SEQ ID NO: 10 или 11 или последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 10 или 11. В некоторых вариантах осуществления, внутриклеточный домен содержит внутриклеточный передающий костимулирующие сигналы домен из 4–1BB (например, (No. доступа Q07011.1) или его функциональный вариант или фрагмент, такой как последовательность аминокислот, указанная в SEQ ID NO: 12, или последовательность аминокислот, имеющая по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 12.
[0504] В некоторых вариантах осуществления, внутриклеточный передающий сигналы домен рекомбинантного рецептора, например, CAR, содержит стимулирующий передающий сигналы домен CD3–зета человека или его функциональный вариант, такой как 112 AA цитоплазматический домен из изоформы 3 CD3ζ человека (No. доступа: P20963.2), или передающий сигналы домен CD3–зета, как описано в Патенте США No.: 7446190 или Патенте США No. 8911993. Например, в некоторых вариантах осуществления, внутриклеточный передающий сигналы домен содержит последовательность аминокислот, как указано в SEQ ID NO: 13, 14 или 15, или последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 13, 14 или 15.
[0505] В некоторых аспектах, спейсер содержит только шарнирную область IgG, например, только шарнир из IgG4 или IgG1, такой как содержащий только шарнир спейсер, указанный в SEQ ID NO: 1. В других вариантах осуществления, спейсер представляет собой или содержит шарнир Ig, например, происходящий из IgG4 шарнир, необязательно, связанный с доменами CH2 и/или CH3. В некоторых вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный с доменами CH2 и CH3, такой, как указано в SEQ ID NO: 4. В некоторых вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный только с доменом CH3, такой, как указано в SEQ ID NO: 3. В некоторых вариантах осуществления, спейсер представляет собой или содержит богатую глицином–серином последовательность или другой гибкий линкер, такой как известные гибкие линкеры.
[0506] Например, в некоторых вариантах осуществления, CAR включает антитело, например, фрагмент антитела, включая scFv, спейсер, такой как спейсер, содержащий фрагмент молекулы иммуноглобулина, такой как шарнирная область и/или одна или несколько константных областей из молекулы тяжелой цепи, например, содержащий шарнир Ig спейсер, трансмембранный домен, содержащий весь или часть происходящего из CD28 трансмембранного домена, происходящий из CD28 внутриклеточный передающий сигналы домен и передающий сигналы домен CD3–зета. В некоторых вариантах осуществления, CAR включает антитело или фрагмент, такой как scFv, спейсер, такой как любой из содержащих шарнир Ig спейсеров, происходящий из CD28 трансмембранный домен, происходящий из 4–1BB внутриклеточный передающий сигналы домен и происходящий из CD3–зета передающий сигналы домен.
[0507] В некоторых вариантах осуществления, молекулы нуклеиновой кислоты, кодирующие такие конструкции CAR, дополнительно включают последовательность, кодирующую элемент проскальзывания рибосомы T2A, и/или последовательность tEGFR, например, ниже последовательности, кодирующей CAR. В некоторых вариантах осуществления, последовательность кодирует элемент проскальзывания рибосомы T2A, указанный в SEQ ID NO: 6, или последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 6. В некоторых вариантах осуществления, T–клетки, экспрессирующие рецептор антигена (например, CAR), можно также получать для экспрессии укороченного EGFR (EGFRt) в качестве неиммуногенного эпитопа для отбора (например, посредством введения конструкции, кодирующей CAR и EGFRt, разделенные посредством переключателя рибосомы T2A, для экспрессии двух белков с одной и той же конструкции), который затем можно использовать в качестве маркера для детекции таких клеток (см., например, Патент США No. 8802374). В некоторых вариантах осуществления, последовательность кодирует последовательность tEGFR, указанную в SEQ ID NO: 7 или 23, или последовательность аминокислот, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 7 или 23.
[0508] Рекомбинантные рецепторы, такие как CAR, экспрессированные клетками, введенными индивиду, как правило, узнают или специфически связывают молекулу, которая является экспрессированной при, ассоциированной с и/или специфической для заболевания или состояния, подвергаемого лечению, или ассоциированных с ними клеток. После специфического связывания с молекулой, например, антигеном, рецептор, как правило, подает иммуностимулирующий сигнал, такой как передаваемый ITAM сигнал, клетке, таким образом, стимулируя иммунный ответ, нацеленный на заболевание или состояние. Например, в некоторых вариантах осуществления, клетки экспрессируют CAR, который специфически связывается с антигеном, экспрессированным клеткой или тканью, пораженными заболеванием или состоянием, или ассоциированными с заболеванием или состоянием.
B. TCR
[0509] В некоторых вариантах осуществления, настоящее изобретение относится к модифицированным клеткам, таким как T–клетки, которые экспрессируют T–клеточный рецептор (TCR) или его антигенсвязывающий фрагмент, которые узнают пептидный эпитоп или T–клеточный эпитоп полипептида–мишени, такого как антиген опухоли, вирусный или аутоиммунный белок.
[0510] В некоторых вариантах осуществления, «T–клеточный рецептор» или «TCR» представляет собой молекулу, которая содержит вариабельные цепи α и β (также известные как TCRα и TCRβ, соответственно) или вариабельные цепи γ и δ (также известные как TCRα и TCRβ, соответственно), или их антигенсвязывающие фрагменты, и которая является способной специфически связывать пептид, связанный с молекулой MHC. В некоторых вариантах осуществления, TCR находится в форме αβ. Как правило, TCR, существующие в формах αβ и γδ, как правило, являются структурно сходными, но экспрессирующие их T–клетки могут иметь отличные анатомические локализации или функции. TCR можно обнаруживать на поверхности клетки или в растворимой форме. Как правило, TCR обнаруживают на поверхности T–клеток (или T–лимфоцитов), где он, как правило, является ответственным за узнавание антигенов, связанных с молекулами главного комплекса гистосовместимости (MHC).
[0511] Если не указано иначе, термин «TCR» следует понимать как включающий полноразмерные TCR, так же как их антигенсвязывающие части или антигенсвязывающие фрагменты. В некоторых вариантах осуществления, TCR представляет собой интактный или полноразмерный TCR, включая TCR в форме αβ или в форме γδ. В некоторых вариантах осуществления, TCR представляет собой антигенсвязывающий фрагмент, который меньше полноразмерного TCR, но который связывается со специфическим пептидом, вязанным с молекулой MHC, например, связывается с комплексом MHC–пептид. В некоторых случаях, антигенсвязывающие часть или фрагмент TCR могут содержать только часть структурных доменов полноразмерного или интактного TCR, но все еще являются способными связывать пептидный эпитоп, такой как комплекс MHC–пептид, с которым связывается полноразмерный TCR. В некоторых случаях, антигенсвязывающий фрагмент содержит вариабельные домены TCR, такие как вариабельная α–цепь и вариабельная β–цепь TCR, достаточные для формирования участка связывания для связывания со специфическим комплексом MHC–пептид. Как правило, вариабельные цепи TCR содержат определяющие комплементарность области, вовлеченные в узнавание пептида, MHC и/или комплекса MHC–пептид.
[0512] В некоторых вариантах осуществления, вариабельные домены TCR содержат гипервариабельные петли, или определяющие комплементарность области (CDR), которые, как правило, вносят первичный вклад в способность узнавания и связывания антигена, и в специфичность. В некоторых вариантах осуществления, CDR из TCR или их комбинация формирует весь или по существу весь антигенсвязывающий участок данной молекулы TCR. Различные CDR в вариабельной области TCR, как правило, разделены каркасными областями (FR), которые, как правило, имеют меньшую изменчивость среди молекул TCR, по сравнению с CDR (см., например, Jores et al., Proc. Nat'l Acad. Sci. U.S.A. 87:9138, 1990; Chothia et al., EMBO J. 7:3745, 1988; см. также Lefranc et al., Dev. Comp. Immunol. 27:55, 2003). В некоторых вариантах осуществления, CDR3 является главной CDR, ответственной за связывание с антигеном или специфичность, или является наиболее важной среди трех CDR в данной вариабельной области TCR для узнавания антигена, и/или для взаимодействия с частью процессированного пептида комплекса пептид–MHC. В некоторых контекстах, CDR1 альфа–цепи может взаимодействовать с N–концевой частью определенных антигенных пептидов. В некоторых контекстах, CDR1 бета–цепи может взаимодействовать с C– концевой частью пептида. В некоторых контекстах, CDR2 оказывает наиболее сильное влияние или является первичной CDR, ответственной за взаимодействие с частью MHC или узнавание части MHC из комплекса MHC–пептид. В некоторых вариантах осуществления, вариабельная область β–цепи может содержать дополнительную гипервариабельную область (CDR4 или HVR4), которая, как правило, вовлечена в связывание суперантигена, а не в узнавание антигена (Kotb (1995) Clinical Microbiology Reviews, 8:411–426).
[0513] В некоторых вариантах осуществления, TCR может также содержать константный домен, трансмембранный домен и/или короткий цитоплазматический хвост (см., например, Janeway et al., Immunobiology: The Immune System in Health and Disease, 3rd Ed., Current Biology Publications, p. 4:33, 1997). В некоторых аспектах, каждая цепь TCR может иметь один N–концевой иммуноглобулин вариабельный домен, один константный домен иммуноглобулина, трансмембранную область и короткий цитоплазматический хвост на C–конце. В некоторых вариантах осуществления, TCR ассоциирован с инвариантыми белками из комплекса CD3, вовлеченными в опосредование передачи сигнала.
[0514] В некоторых вариантах осуществления, цепь TCR содержит один или несколько константных доменов. Например, внеклеточный фрагмент данной цепи TCR (например, α–цепь или β–цепь) может содержать два иммуноглобулиноподобных домена, таких как вариабельный домен (например, Vα или Vβ; как правило, аминокислоты 1–116, на основании нумерации Kabat, Kabat et al., «Sequences of Proteins of Immunological Interest, US Dept. Health и Human Services, Public Health Service National Institutes of Health, 1991, 5th ed.), и константный домен (например, константный домен α–цепи или Cα, как правило, положения 117–259 цепи на основании нумерации Kabat или константный домен β цепи, или Cβ, как правило, положения 117–295 цепи на основании Kabat), прилежащий к клеточной мембране. Например, в некоторых случаях, внеклеточный фрагмент TCR, сформированный двумя цепями, содержит два ближайших к мембране константных домена и два отдаленных от мембраны вариабельных домена, где каждый из вариабельных доменов содержит CDR. Константный домен TCR может содержать короткие связывающие последовательности в которых остаток цистеина формирует дисульфидную связь, таким образом, связывая две цепи TCR. В некоторых вариантах осуществления, TCR может иметь дополнительный остаток цистеина на каждой из α и β цепей, так что TCR содержит две дисульфидные связи в константных доменах.
[0515] В некоторых вариантах осуществления, цепи TCR содержат трансмембранный домен. В некоторых вариантах осуществления, трансмембранный домен является положительно заряженным. В некоторых случаях, цепь TCR содержит цитоплазматический хвост. В некоторых случаях, структура позволяет TCR вступать в ассоциацию с другими молекулами, подобными CD3 и его субъединицам. Например, TCR, содержащий константные домены с трансмембранной областью, может заякоривать белок в мембране клетки и вступать в ассоциацию с инвариантыми субъединицами аппарата или комплекса передачи сигналов CD3. Внутриклеточные хвосты передающих сигналы субъединиц CD3 (например, цепей CD3γ, CD3δ, CD3ε и CD3ζ) содержат один или несколько иммунорецепторных тирозиновых активирующих мотивов или ITAM, которые вовлечены в способность комплекса TCR передавать сигналы.
[0516] В некоторых вариантах осуществления, TCR может представлять собой гетеродимер из двух цепей α и β (или необязательно, γ и δ) или он может представлять собой одноцепочечную конструкцию TCR. В некоторых вариантах осуществления, TCR представляет собой гетеродимер, содержащий две отдельные цепи (цепи α и β или цепи γ и δ), которые являются связанными, например, посредством дисульфидной связи или дисульфидных связей.
[0517] В некоторых вариантах осуществления, TCR можно получать из известной последовательности(последовательностей) TCR, таких как последовательности цепей Vα,β, для которых по существу полноразмерная кодирующая последовательность является легко доступной. Способы получения полноразмерных последовательностей TCR, включая последовательности V–цепи, из клеточных источников, хорошо известны. В некоторых вариантах осуществления, нуклеиновые кислоты, кодирующие TCR, можно получать из множества источников, например, посредством полимеразной цепной реакции (ПЦР) амплификации кодирующих TCR нуклеиновых кислот внутри или после выделения из данной клетки или клеток, или синтеза публично доступной последовательности ДНК TCR.
[0518] В некоторых вариантах осуществления, TCR получают из биологического источника, например, из клеток, например, из T–клетки (например, цитотоксической T–клетки), T–клеточной гибридомы или другого публично доступного источника. В некоторых вариантах осуществления, T–клетки можно получать из выделенных in vivo клетки. В некоторых вариантах осуществления, TCR is a прошедший отбор в тимусе TCR. В некоторых вариантах осуществления, TCR представляет собой рестрицированный по неоэпитопу TCR. В некоторых вариантах осуществления, T–клетки могут представлять собой культивированные гибридому или клон T–клеток. В некоторых вариантах осуществления, TCR или его антигенсвязывающую часть можно получать синтетически, зная последовательность TCR.
[0519] В некоторых вариантах осуществления, TCR получают из TCR, идентифицированного или отобранного при скрининге библиотеки TCR–кандидатов против полипептидного антигена–мишени, или T–клеточного эпитопа–мишени из него. Библиотеки TCR можно получать посредством амплификации репертуара Vα и Vβ из T–клеток, выделенных от индивида, включая клетки, присутствующие в PBMC, селезенке или другом лимфоидном органе. В некоторых случаях, T–клетки можно амплифицировать из инфильтрующих опухоль лимфоцитов (TIL). В некоторых вариантах осуществления, библиотеки TCR можно получать из CD4+ или CD8+ клеток. В некоторых вариантах осуществления, TCR можно амплифицировать из T–клеточного источника от нормального или здорового индивида, т.е. библиотеки нормальных TCR. В некоторых вариантах осуществления, TCR можно амплифицировать из T–клеточного источника от пораженного заболеванием индивида, т.е. библиотеки ассоциированных с заболеванием TCR. В некоторых вариантах осуществления, вырожденные праймеры используют для амплификации репертуара генов Vα и Vβ, например, посредством RT–ПЦР, в образцах, таких как T–клетки, полученные от людей. В некоторых вариантах осуществления, библиотеки scTv можно собирать из библиотек наивных Vα и Vβ, в которых амплифицированные продукты клонируют или собирают, с разделением посредством линкера. В зависимости от источника индивида и клеток, библиотеки могут являться специфическими для аллеля HLA. Альтернативно, в некоторых вариантах осуществления, библиотеки TCR можно получать посредством мутагенеза или внесения разнообразия в исходной или каркасной молекулы TCR. В некоторых аспектах, TCR подвергают направленной эволюции, например, посредством мутагенеза, например, цепи α или β. В некоторых аспектах, конкретные остатки в пределах CDR TCR изменяют. В некоторых вариантах осуществления, отобранные TCR можно модифицировать посредством аффинного созревания. В некоторых вариантах осуществления, можно отбирать антигенспецифические T–клетки, например, посредством скрининга для оценки активности CTL против пептида. В некоторых аспектах, можно отбирать TCR, например, присутствующие на антигенспецифических T–клетках, например, по активности связывания, например, конкретной аффинности или авидности для антигена.
[0520] В некоторых вариантах осуществления, TCR или его антигенсвязывающая часть являются модифицированными или сконструированными. В некоторых вариантах осуществления, способы направленной эволюции используют для получения TCR с измененными свойствами, например, с более высокой аффинностью для специфического комплекса MHC–пептид. В некоторых вариантах осуществления, направленную эволюцию осуществляют способами дисплея включая, но без ограничения, дрожжевой дисплей (Holler et al. (2003) Nat Immunol, 4, 55–62; Holler et al. (2000) Proc Natl Acad Sci U S A, 97, 5387–92), фаговый дисплей (Li et al. (2005) Nat Biotechnol, 23, 349–54), или T–клеточный дисплей (Chervin et al. (2008) J Immunol Methods, 339, 175–84). В некоторых вариантах осуществления, способы дисплея включают конструирование или модификацию известного, исходного или эталонного TCR. Например, в некоторых случаях, TCR дикого типа можно использовать в качестве матрицы для получения подвергнутых мутагенезу TCR, в которых один или несколько остатков CDR мутированы, и отбирают мутанты с желательным измененным свойством, таким как более высокая аффинность для желательного антигена–мишени.
[0521] В некоторых вариантах осуществления, пептиды полипептида–мишени для использования для продукции или получения представляющих интерес TCR известны или могут быть легко идентифицированы специалистом в данной области. В некоторых вариантах осуществления, пептиды, пригодные для использования для получения TCR или антигенсвязывающих фрагментов, можно определять на основании присутствия рестрицированного по HLA мотива в представляющем интерес полипептиде–мишени, таком как полипептид–мишень, описанный ниже. В некоторых вариантах осуществления, пептиды идентифицируют с использованием компьютерных прогностических моделей, известных специалистам в данной области. В некоторых вариантах осуществления, прогнозирования участков связывания MHC класса I, такие модели включают, но без ограничения, ProPred1 (Singh and Raghava (2001) Bioinformatics 17(12):1236–1237, и SYFPEITHI (см. Schuler et al. (2007) Immunoinformatics Methods in Molecular Biology, 409(1): 75–93 2007). В некоторых вариантах осуществления, рестрицированный по MHC эпитоп представляет собой HLA–A0201, который является экспрессированным приблизительно у 39–46% из всех европеоидов и таким образом, представляет собой подходящий выбор антигена MHC для использования для получения TCR или другой связывающей MHC–пептид молекулы.
[0522] Мотивы, связывающие HLA–A0201, и участки расщепления для протеасом и иммунопротеасом, с использованием компьютерных прогностических моделей, известны специалистам в данной области. Для прогнозирования участков связывания MHC класса I, такие модели включают, но без ограничения, ProPred1 (описанные более подробно в Singh and Raghava, ProPred: prediction of HLA–DR binding sites. BIOINFORMATICS 17(12):1236–1237 2001), и SYFPEITHI (см. Schuler et al. SYFPEITHI, Database for Searching and T–Cell Epitope Prediction. in Immunoinformatics Methods in Molecular Biology, vol 409(1): 75–93 2007)
[0523] В некоторых вариантах осуществления, TCR или его антигенсвязывающий фрагмент может представлять собой полученный рекомбинантным способом природный белок или его мутантную форму, в которой изменены одно или несколько свойств, таких как характеристики связывания. В некоторых вариантах осуществления, TCR может происходить из одного из различных видов животных, таких как человек, мышь, крыса или другое млекопитающее. TCR может находиться в связанной с клеткой или в растворимой форме. В некоторых вариантах осуществления, для целей представленных способов, TCR находится в связанной с клеткой форме, экспрессированной на поверхности клетки.
[0524] В некоторых вариантах осуществления, TCR представляет собой полноразмерный TCR. В некоторых вариантах осуществления, TCR представляет собой антигенсвязывающий фрагмент. В некоторых вариантах осуществления, TCR представляет собой димерный TCR (dTCR). В некоторых вариантах осуществления, TCR представляет собой одноцепочечный TCR (sc–TCR). В некоторых вариантах осуществления, dTCR или scTCR имеют структуры, как описано в WO 03/020763, WO 04/033685, WO2011/044186.
[0525] В некоторых вариантах осуществления, TCR содержит последовательность, соответствующую трансмембранной последовательности. В некоторых вариантах осуществления, TCR содержит последовательность, соответствующую цитоплазматической последовательности. В некоторых вариантах осуществления, TCR является способным формировать комплекс TCR с CD3. В некоторых вариантах осуществления, любые из TCR, включая dTCR или scTCR, могут быть связаны с передающими сигналы доменами, что приводит к образованию активного TCR на поверхности T–клетки. В некоторых вариантах осуществления, TCR является экспрессированным на поверхности клеток.
[0526] В некоторых вариантах осуществления dTCR содержит первый полипептид, где последовательность, соответствующая последовательности вариабельной области α–цепи TCR, слита с N–концом последовательности, соответствующей внеклеточной последовательности константной области α–цепи TCR, и второй полипептид, где последовательность, соответствующая последовательности вариабельной области β–цепи TCR, слита с N–концом последовательности, соответствующей внеклеточной последовательности константной области β–цепи TCR, где первый и вторый полипептиды связаны посредством дисульфидной связи. В некоторых вариантах осуществления, связь может соответствовать природной межцепьевой дисульфидной связи, присутствующей в природных димерных TCR αβ. В некоторых вариантах осуществления, межцепьевые дисульфидные связи не присутствуют в природном TCR. Например, в некоторых вариантах осуществления, один или несколько остатков цистеина можно включать в внеклеточные последовательности константной области пары полипептидов dTCR. В некоторых случаях, как природная, так и неприродная дисульфидная связь может являться желательной. В некоторых вариантах осуществления, TCR содержит трансмембранную последовательность для заякоривания в мембране.
[0527] В некоторых вариантах осуществления, dTCR содержит α–цепь TCR, содержащую вариабельный домен α, a константный домен α и первый мотив для димеризации, присоединенный к C–концу константного домена α, и β–цепь TCR, содержащую вариабельный домен β, константный домен β и первый мотив для димеризации, присоединенный к C–концу константного домена β, где первый и второй мотивы для димеризации легко взаимодействуют с образованием ковалентной связи между аминокислотой в первом мотиве для димеризации и аминокислотой во втором мотиве для димеризации, связывая вместе α–цепь TCR и β–цепь TCR.
[0528] В некоторых вариантах осуществления, TCR представляет собой scTCR. Как правило, scTCR можно получать с использованием способов, известных специалистам в данной области, См., например, Soo Hoo, W. F. et al. PNAS (USA) 89, 4759 (1992); Wülfing, C. and Plückthun, A., J. Mol. Biol. 242, 655 (1994); Kurucz, I. et al. PNAS (USA) 90 3830 (1993); Публикации международных PCT No. WO 96/13593, WO 96/18105, WO99/60120, WO99/18129, WO 03/020763, WO2011/044186; и Schlueter, C. J. et al. J. Mol. Biol. 256, 859 (1996). В некоторых вариантах осуществления, scTCR содержит введенные неприродные дисульфидные межцепьевые связи для облегчения ассоциации цепей TCR (см., например, Публикацию международной PCT No. WO 03/020763). В некоторых вариантах осуществления, scTCR представляет собой не связанный дисульфидной связью укороченный TCR, в котором гетерологичные лейциновые молнии, слитые с его C–концов, облегчают ассоциацию цепей (см., например, Публикацию международной PCT No. WO99/60120). В некоторых вариантах осуществления, scTCR содержит вариабельный домен TCRα, ковалентно связанный с вариабельным доменом TCRβ посредством пептидного линкера (см., например, Публикацию международной PCT No. WO99/18129).
[0529] В некоторых вариантах осуществления, scTCR содержит первый фрагмент, состоящий из аминокислотной последовательности, соответствующей вариабельной области α–цепи TCR, второй фрагмент, состоящий из аминокислотной последовательности, соответствующей последовательности вариабельной области β–цепи TCR, слитые с N–концом аминокислотной последовательности, соответствующей внеклеточной последовательности константного домена β–цепи TCR, и линкерную последовательность, связывающую C–конец первого фрагмента с N–концом второго фрагмента.
[0530] В некоторых вариантах осуществления, scTCR содержит первый фрагмент, состоящий из последовательности вариабельной области α–цепи, слитые с N–концом внеклеточной последовательности константного домена α–цепи, и второй фрагмент, состоящий из последовательности вариабельной области β–цепи, слитые с N–концом последовательности внеклеточной константной и трансмембранной последовательности β–цепи, и, необязательно, линкерную последовательность, связывающую C–конец первого фрагмента с N–концом второго фрагмента.
[0531] В некоторых вариантах осуществления, scTCR содержит первый фрагмент, состоящий из последовательности вариабельной области β–цепи TCR, слитой с N–концом внеклеточной последовательности константного домена β–цепи, и второй фрагмент, состоящий из последовательности вариабельной области α–цепи, слитый с N–концом последовательности внеклеточной константной и трансмембранной последовательности α–цепи, и, необязательно, линкерную последовательность, связывающую C–конец первого фрагмента с N–концом второго фрагмента.
[0532] В некоторых вариантах осуществления, линкер из scTCR, связывающий первый и второй фрагменты TCR, может представлять собой любой линкер, способный формировать одиночную полипептидную цепь, с сохранением в то же время специфичности связывания TCR. В некоторых вариантах осуществления, линкерная последовательность может, например, иметь формулу –P–AA–P–, где P представляет собой пролин, и AA представляет собой аминокислотную последовательность, где аминокислоты представляют собой глицин и серин. В некоторых вариантах осуществления, первый и второй фрагменты образуют пару таким образом, что последовательности их вариабельных областьей ориентированы для такого связывания. Таким образом, в некоторых случаях, линкер имеет достаточную длину для перекрывания расстояния между C–концом первого фрагмента и N–концом второго фрагмента, или наоборот, но является не слишком длинным для блокирования или уменьшения связывания scTCR с его лигандом–мишенью. В некоторых вариантах осуществления, линкер может содержать от или приблизительно от 10 до 45 аминокислот, например, от 10 до 30 аминокислот или от 26 до 41 аминокислотных остатков, например, 29, 30, 31 или 32 аминокислоты. В некоторых вариантах осуществления, линкер имеет формулу –PGGG–(SGGGG)5–P–, где P представляет собой пролин, G представляет собой глицин, и S представляет собой серин (SEQ ID NO: 16). В некоторых вариантах осуществления, линкер имеет последовательность GSADDAKKDAAKKDGKS (SEQ ID NO: 17)
[0533] В некоторых вариантах осуществления, scTCR содержит ковалентную дисульфидную связь, связывающую остаток из иммуноглобулиновой области константного домена α–цепи с остатком из иммуноглобулиновой области константного домена β–цепи. В некоторых вариантах осуществления, межцепьевая дисульфидная связь в природном TCR не присутствует. Например, в некоторых вариантах осуществления, один или несколько остатков цистеина можно включать в внеклеточные последовательности константной области первого и второго фрагментов полипептида scTCR. В некоторых случаях, как природная, так и неприродная дисульфидная связь может являться желательной.
[0534] В некоторых вариантах осуществления dTCR или scTCR, содержащего введенные межцепьевые дисульфидные связи, природные дисульфидные связи не присутствуют. В некоторых вариантах осуществления, один или несколько из природных остатков цистеина, формирующих природные межцепьевые дисульфидные связи, заменены на другой остаток, например, на серин или аланин. В некоторых вариантах осуществления, введенная дисульфидная связь может быть сформирована посредством мутагенеза не относящихся к цистеину остатков в первом и втором фрагментах на цистеин. Иллюстративные неприродные дисульфидные связи TCR описаны в Публикации международной PCT No. WO2006/000830.
[0535] В некоторых вариантах осуществления, TCR или его антигенсвязывающий фрагмент имеет аффинность с равновесной константой связывания для антигена–мишени между или между приблизительно 10–5 и 10–12 M, и всеми ее инивидуальными значениями и диапазонами. В некоторых вариантах осуществления, антиген–мишень представляет собой комплекс MHC–пептид или лиганд.
[0536] В некоторых вариантах осуществления, нуклеиновую кислоту или нуклеиновые кислоты, кодирующие TCR, например, цепи α и β, можно амплифицировать посредством ПЦР, клонирования или других пригодных способов и клонировать в пригодные экспрессирующие вектор или векторы. Экспрессирующий вектор может представлять собой любой пригодный рекомбинантный экспрессирующий вектор, и может быть использован для трансформации или трансфекции любого пригодного хозяина. Пригодные векторы включают векторы, разработанные для размножения и распространения или для экспрессии, или для того и другого, такие как плазмиды и вирусы.
[0537] В некоторых вариантах осуществления, вектор может представлять собой вектор из серий pUC (Fermentas Life Sciences), серий pBluescript (Stratagene, LaJolla, Calif.), серий pET (Novagen, Madison, Wis.), серий pGEX (Pharmacia Biotech, Uppsala, Sweden) или серий pEX (Clontech, Palo Alto, Calif.). В некоторых случаях, бактериофаговые векторы, такие как λG10, λGT11, λZapII (Stratagene), λEMBL4 и λNM1149, также можно использовать. В некоторых вариантах осуществления, можно использовать экспрессирующие векторы для растений, и они включают pBI01, pBI101.2, pBI101.3, pBI121 и pBIN19 (Clontech). В некоторых вариантах осуществления, экспрессирующие векторы для животных включают pEUK–Cl, pMAM и pMAMneo (Clontech). В некоторых вариантах осуществления, используют вирусный вектор, такой как ретровирусный вектор.
[0538] В некоторых вариантах осуществления, рекомбинантные экспрессирующие векторы можно получать с использованием стандартных способов рекомбинантной ДНК. В некоторых вариантах осуществления, векторы могут содержать регуляторные последовательности, такие как кодоны инициации и терминации транскрипции и трансляции, которые являются специфическими для типа хозяина (например, бактерии, гриба, растения или животного), для введения которому предназначен вектор, в соответствующих случаях и принимая во внимание, основан ли вектор на ДНК или РНК. В некоторых вариантах осуществления, вектор может содержать неприродный промотор, функционально связанный с нуклеотидной последовательностью, кодирующей TCR или антигенсвязывающий фрагмент (или другую связывающую MHC–пептид молекулу). В некоторых вариантах осуществления, промотор может представлять собой невирусный промотор или вирусный промотор, такой как промотор цитомегаловируса (CMV), промотор SV40, промотор RSV и промотор, обнаруженный в длинном концевом повторе вируса стволовых клеток мыши. Предусмотрены также другие промоторы, известные специалисту в данной области.
[0539] В некоторых вариантах осуществления, для получения вектора, кодирующего TCR, цепи α и β амплифицируют посредством ПЦР с тотальной кДНК, выделенной из клона T–клеток, экспрессирующего представляющий интерес TCR, и клонируют в экспрессирующий вектор. В некоторых вариантах осуществления, цепи α и β клонируют в один и тот же вектор. В некоторых вариантах осуществления, цепи α и β клонируют в различные векторы. В некоторых вариантах осуществления, полученные цепи α и β вставляют в ретровирусный, например, лентивирусный, вектор.
C. Множественное нацеливание
[0540] В некоторых вариантах осуществления, клетки и способы включены в стратегии множественного нацеливания, такие как экспрессия двух или более генетически модифицированных рецепторов на клетке, где каждый узнает одинаковый или различный антиген и как правило, каждый включает различный внутриклеточный передающий сигналы компонент. Такие способы множественного нацеливания описаны, например, в Публикации международной патентной заявки No.: WO 2014055668 A1 (описывающей комбинации активирующих и костимулирующих CAR, например, нацеленных на два различных антигена, присутствующих индивидуально на нецелевых, например, нормальных, клетках, но присутствующих совместно только на клетках, пораженных заболеванием или состоянием, подлежащим лечению) и Fedorov et al., Sci. Transl. Medicine, 5(215) (2013) (описывающей клетки, экспрессирующие активирующий и ингибирующий CAR, такие как CAR, в которых активирующий CAR связывается с одним антигеном, экспрессированным как на нормальных или не пораженных заболеванием клетках, так и на клетках, пораженных заболеванием или состоянием, подлежащим лечению, и ингибирующий CAR связывается с другим антигеном, экспрессированным только на нормальных клетках или клетках, которые нежелательно подвергать лечению).
[0541] Например, в некоторых вариантах осуществления, клетки включают рецептор, экспрессирующий первый генетически модифицированный рецептор антигена (например, CAR или TCR), который является способным индуцировать активирующий сигнал для клетки, как правило, после специфического связывания с антигеном, узнаваемым первым рецептором, например, первым антигеном. В некоторых вариантах осуществления, клетка дополнительно включает второй генетически модифицированный рецептор антигена (например, CAR или TCR), например, химерный костимулирующий рецептор, который является способным индуцировать костимулирующий сигнал для иммуноцита, как правило, после специфического связывания с вторым антигеном, узнаваемым вторым рецептором. В некоторых вариантах осуществления, первый антиген и второй антиген являются одинаковыми. В некоторых вариантах осуществления, первый антиген и второй антиген являются различными.
[0542] В некоторых вариантах осуществления, первый и/или второй генетически модифицированный рецептор антигена (например, CAR или TCR) является способным индуцировать активирующий сигнал для клетки. В некоторых вариантах осуществления, рецептор включает внутриклеточный передающий сигналы компонент, содержащий ITAM или подобный ITAM мотивы. В некоторых вариантах осуществления, активация, индуцированная первым рецептором, включает передачу сигнала или изменение экспрессии белка в клетке, приводящие к инициации иммунного ответа, такого как фосфорилирование ITAM, и/или к инициации каскада опосредованной ITAM передачи сигналов, к формированию иммунологического синапса и/или кластеризации молекулы около связанного рецептора (например, CD4 или CD8 и т.д.), активации одного или нескольких факторов транскрипции, таких как NF–κB и/или AP–1, и/или индукцию экспрессии генов таких факторов, как цитокины, пролиферация, и/или выживаемость.
[0543] В некоторых вариантах осуществления, первый и/или второй рецептор включает внутриклеточные передающие сигналы домены костимулирующих рецепторов, таких как CD28, CD137 (4–1 BB), OX40, CD27, DAP10, DAP12, NKG2D, ICOS и/или другие костимулирующие рецепторы. В некоторых вариантах осуществления, первый и второй рецептор включают внутриклеточные передающие сигналы домены костимулирующих рецепторов, которые являются различными. В одном варианте осуществления, первый рецептор содержит передающую костимулирующие сигналы область CD28, и второй рецептор содержит передающую костимулирующие сигналы область 4–1BB, или наоборот.
[0544] В некоторых вариантах осуществления, первый и/или второй рецептор включает как внутриклеточный передающий сигналы домен, содержащий ITAM или подобный ITAM мотивы, так и внутриклеточный передающий сигналы домен костимулирующего рецептора.
[0545] В некоторых вариантах осуществления, первый рецептор содержит внутриклеточный передающий сигналы домен, содержащий ITAM или подобный ITAM мотивы, и второй рецептор содержит внутриклеточный передающий сигналы домен костимулирующего рецептора. Костимулирующий сигнал в комбинации с активирующим сигналом, индуцированные в одной и той же клетке, представляют собой то, что приводит к иммунному ответу, такому как надежный и длительный иммунный ответ, такой как увеличенная экспрессия генов, секреция цитокинов и другие факторы, и опосредованные T–клеткой эффекторные функции, такие как уничтожение клеток.
[0546] В некоторых вариантах осуществления, ни связывание первого рецептора отдельно, ни связывание второго рецептора отдельно, не индуцирует надежный иммунный ответ. В некоторых аспектах, если только один рецептор является связанным, клетка приобретает толерантность или не отвечает на антиген, или подвергается ингибированию, и/или не подвергается индукции для пролиферации или секреции факторов, или выполнения эффекторных функций. В некоторых таких вариантах осуществления, однако, когда множество рецепторов являются связанными, например, при встрече с клеткой, экспрессирующей первый и второй антигены, достигают желательного ответа, такого как полная иммунная активация или стимуляция, например, как показано посредством секреции одного или нескольких цитокинов, пролиферации, персистенции и/или выполнения иммуноэффекторной функции, такой как цитотоксическое уничтожение клетки–мишени.
[0547] В некоторых вариантах осуществления, два рецептора индуцируют, соответственно, активирующий и ингибирующий сигнал для клетки, таким образом, что связывание одного рецептора с его антигеном активирует клетку или индуцирует ответ, однако, связывание второго ингибирующего рецептора с его антигеном индуцирует сигнал, который супрессирует или ослабляет такой ответ. Примеры представляют собой комбинации активирующих CAR и ингибирующих CAR, или iCAR. Можно использовать, например, такой способ, в котором активирующий CAR связывается с антигеном, который экспрессируется при заболевании или состоянии, но который также экспрессируется на нормальных клетках, и ингибирующий рецептор связывается с отдельным антигеном, который экспрессируется на нормальных клетках, но не на пораженных заболеванием или состоянием клетках.
[0548] В некоторых вариантах осуществления, способ множественного нацеливания используют в случае, когда антиген, ассоциированный с конкретным заболеванием или состоянием экспрессируется на не пораженной заболеванием клетке и/или экспрессируется на собственно модифицированной клетке, либо временно (например, при стимуляции в сочетании с генетической модификацией), либо постоянно. В таких случаях, посредством необходимости связывания двух отдельных и имеющих индивидуальную специфичность рецепторов антигенов, можно улучшать специфичность, избирательность и/или эффективность.
[0549] В некоторых вариантах осуществления, множество антигенов, например, первый и второй антигены, экспрессируются на клетке, ткани, или при заболевании или состояния, подвергаемых нацеливанию, например, на клетке злокачественной опухоли. В некоторых аспектах, клетка, ткань, заболевание или состояние представляет собой множественную миелому или клетка множественной миеломы. В некоторых вариантах осуществления, один или несколько из множества антигенов, как правило, также экспрессируются на клетке, на которую нежелательно нацеливаться при клеточной терапии, такой как нормальная или не пораженная заболеванием клетка или ткань, и/или собственно модифицированные клетки. В таких вариантах осуществления, посредством необходимости связывания множества рецепторов для достижения ответа клетки, достигают специфичности и/или эффективности.
D. Клетки и подготовка клеток для модификации
[0550] Настоящее изобретение относится также к клеткам, таким как клетки, содержащие модифицированный рекомбинантный рецептор, такой, как описано в настоящем описании. Настоящее изобретение относится также к популяциям таких клеток, композициям, содержащим такие клетки и/или обогащенным по таким клеткам, например, к тем, в которых клетки, экспрессирующие рекомбинантный рецептор, например, химерный рецептор, составляют по меньшей мере 50, 60, 70, 80, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, или более процентов от общего количества клеток в композиции или клеток конкретного типа, таких как T–клетки или CD8+, или CD4+ клетки. Среди композиций присутствуют фармацевтические композиции и составы для введения, например, для адоптивной клеточной терапии. Настоящее изобретение относится также к терапевтическим способам для введения клеток и композиций индивидам, например, пациентам, например, в соответствии с представленными способами.
[0551] Таким образом, настоящее изобретение относится также к генетически модифицированным клеткам, экспрессирующим рекомбинантные рецепторы например, CAR. Клетки, как правило, представляют собой эукариотические клетки, такие как клетки млекопитающих, и как правило, представляют собой клетки человека. В некоторых вариантах осуществления, клетки происходят из крови, костного мозга, лимфы или лимфоидных органов, представляют собой клетки иммунной системы, такие как клетки врожденного или адаптивного иммунитета, например, миелоидные или лимфоидные клетки, включая лимфоциты, как правило, T–клетки и/или клетки NK. Другие иллюстративные клетки включают стволовые клетки, такие как мультипотентые и плюрипотентные стволовые клетки, включая индуцированные плюрипотентные стволовые клетки (iPSC). Клетки, как правило, представляют собой первичные клетки, такие как клетки, выделенные непосредственно от индивида и/или выделенные от индивида и замороженные. В некоторых вариантах осуществления, клетки включают одну или несколько подгрупп T–клеток или другие типы клеток, такие как полные популяции T–клеток, CD4+ клеток, CD8+ клеток и их субпопуляции, такие как субпопуляции, определяемые по функции, состоянию активации, зрелости, потенциалу дифференцировки, размножению, рециркуляции, локализации и/или способности к персистенции, антигенной специфичности, типу рецептора антигена, присутствию в конкретном органе или компартменте, маркеру или профилю секреции цитокинов, и/или степени дифференцировки. Применительно к индивиду, подлежащему лечению, клетки могут являться аллогенными и/или аутологичными. Среди способов включены способы применения готового к немедленному использованию продукта. В некоторых аспектах, например, для технологий применения готового к немедленному использованию продукта, клетки представляют собой плюрипотентные и/или мультипотентые, например, стволовые клетки, такие как индуцированные плюрипотентные стволовые клетки (iPSC). В некоторых вариантах осуществления, способы включают выделение клеток от индивида, их подготовку, переработку, культивирование и/или модификацию, как описано в настоящем описании, и их повторное введение тому же самому пациенту, до или после криоконсервации.
[0552] Среди подтипов и субпопуляций T–клеток и/или CD4+ и/или CD8+ T–клеток, присутствуют наивные T–клетки (TN), эффекторные T–клетки (TЭФФ), T–клетки памяти и их подтипы, такие как стволовые T–клетки памяти (TSCM), T–клетки памяти (TCM), эффекторные T–клетки памяти (TEM), или терминально дифференцированные эффекторные T–клетки памяти, инфильтрующие опухоль лимфоциты (TIL), незрелые T–клетки, зрелые T–клетки, T–клетки–помощники, цитотоксические T–клетки, ассоциированные со слизистыми оболочками инвариантные T–клетки (MAIT) клетки, природные и адаптивные регуляторные T–клетки (T–рег) клетки, T–клетки–помощники, такие как TH1 клетки, TH2 клетки, TH3–клетки, TH17–клетки, TH9–клетки, TH22–клетки, фолликулярные T–клетки–помощники, альфа/бета–T–клетки, и дельта/гамма–T–клетки.
[0553] В некоторых вариантах осуществления, клетки представляют собой клетки естественные киллеры (NK). В некоторых вариантах осуществления, клетки представляют собой моноциты или гранулоциты, например, миелоидные клетки, макрофаги, нейтрофилы, дендритные клетки, тучные клетки, эозинофилы и/или базофилы.
[0554] В некоторых вариантах осуществления, клетки включают одну или несколько нуклеиновых кислот, введенных посредством генетической модификации, и таким образом, экспрессируют рекомбинантные или генетически модифицированные продукты таких нуклеиновых кислот. В некоторых вариантах осуществления, нуклеиновые кислоты являются гетерологичными, т.е., в норме не присутствующими в клетке или образце, полученном из клетки, такими как полученные из другого организма или клетки, которые например, обычно не обнаруживают в клетке, подвергаемой модификации, и/или в организме, из которого происходит такая клетка. В некоторых вариантах осуществления, нуклеиновые кислоты являются неприродными, такими как нуклеиновая кислота, не обнаруженная в природе, включая нуклеиновую кислоту, содержащую химерные комбинации нуклеиновых кислот, кодирующих различные домены из множества различных типов клеток.
[0555] В некоторых вариантах осуществления, изготовление, образование или получение средства для клеточной терапии, например, терапевтических композиций клеток, содержащих клетки, экспрессирующие рекомбинантный рецептор, можно проводить способом, который включает одну или несколько дополнительных стадий переработки, таких как стадии для активации или стимуляции, трансдукции, культивирования, размножения, промывки, суспендирования, разведения, концентрирования и/или получения состава клеток. В некоторых вариантах осуществления, способы образования или получения средства для клеточной терапии включают выделение клеток от индивида, подготовку, переработку, культивирование при одном или нескольких стимулирующих условий. В некоторых вариантах осуществления, способ включает стадии переработки, проводимые в порядке, при котором: клетки, например, первичные клетки, сначала выделяют, например, отбирают или отделяют, из биологического образца; отобранные клетки инкубируют с частицами вирусного вектора для трансдукции, необязательно, после стадии стимуляции выделенных клеток в присутствии стимулирующего реагента; культивирования трансдуцированных клеток, например, для размножения клеток; составление трансдуцированных клетках в композицию и введение композиции в предоставленный сосуд из биомедицинского материала. В некоторых вариантах осуществления, полученные модифицированные клетки повторно вводят тому же индивиду, до или после криоконсервации.
[0556] В некоторых вариантах осуществления, одна или несколько стадии переработки может включать одно или несколько из (a) промывки биологического образца, содержащего клетки (например, образца цельной крови, образца лейкоцитарной пленки, образца мононуклеарных клеток периферической крови (PBMC), образца нефракционированных T–клеток, образца лимфоцитов, образца лейкоцитов, продукта афереза или продукта лейкафереза), (b) выделения, например, отбора, из образца желательной подгруппы или популяции клеток (например, CD4+ и/или CD8+ T–клеток), например, посредством инкубации клеток с селективным или иммуноаффинным реагентом для разделения на основании иммуноаффинности; (c) активации и/или стимуляции клеток посредством подвергания клеток воздействию стимулирующих условий и/или стимулирующих реагентов, которые можно осуществлять до, во время и/или после инкубации клеток с частицами вирусного вектора, (d) инкубации выделенных, например, отобранных клеток, с частицами вирусного вектора, например, трансдукции клеток, (e) культивирования, культивации или размножения клеток, например, с использованием способов, как описано, и (f) получения состава трансдуцированных клеток, например, в фармацевтически приемлемом буфере, криоконсерванте или другой пригодной среде. В некоторых вариантах осуществления, клетки из образца PBMC, нефракционированного образца T–клеток, образца лимфоцитов, образца белых кровяных клеток, продукта афереза или продукта лейкафереза подвергают криозамораживанию и затем размораживают перед любыми стадиями для выделения, отбора, инкубации, трансдукции, трансфекции, культивации, размножения и/или получения состава клеток.
[0557] В некоторых вариантах осуществления, одну или несколько дополнительных стадий промывки или стадий суспендирования, например, для разведения, концентрирования и/или замены буфера клеток, также можно проводить до или после любой из вышеуказанных стадий. В некоторых аспектах, полученную модифицированную композицию клеток вводят в один или несколько предоставленных биомедицинских культуральных сосудов.
[0558] В некоторых вариантах осуществления, одну, несколько или все стадии при подготовке клеток для клинического использования, например, в адоптивной клеточной терапии, осуществляют без подвергания клеток воздействию нестерильных условий и без необходимости использования стерильного помещения или шкафа. В некоторых вариантах осуществления такого способа, клетки выделяют, отделяют или отбирают, трансдуцируют, промывают, необязательно, активируют или стимулируют и составляют, все в пределах закрытой системы. В некоторых аспектах такого способа, клетки извлекают из закрытой системы и вводят в один или несколько сосудов для биологического материала. В некоторых вариантах осуществления, способы проводят в автоматическом режиме. В некоторых вариантах осуществления, одну или несколько стадий проводят вне закрытой системы или устройство.
[0559] В некоторых вариантах осуществления, закрытую систему используют для проведения одной или нескольких из других стадий переработки способа для изготовления, образования или получения средства для клеточной терапии. В некоторых вариантах осуществления, одну или несколько, или все стадии переработки, например, выделение, отбор и/или обогащение, переработка, инкубация в сочетании со стадиями трансдукции и модификации, и получения состава проводят с использованием системы, устройства, или аппарата в интегрированной или автономной системе, и/или в автоматизированном или программируемом режиме. В некоторых аспектах, система или аппарат включает компьютер и/или компьютерную программу в коммуникации с системой или аппаратом, позволяющими пользователю программировать, контролировать, оценивать исход и/или корректировать различные аспекты стадий переработки, выделения, модификации и получения состава. В одном примере, система представляет собой систему, как описано в Международной патентной заявке, публикация номер WO2009/072003, или US 20110003380 A1. В одном примере, система представляет собой систему, как описано в Международной публикации номер WO2016/073602.
[0560] В некоторых вариантах осуществления, получение модифицированных клеток включает одну или несколько стадий культивирования и/или получения. Клетки для введения рекомбинантного рецептора, например, CAR, можно выделять из образца, такого как биологический образец, например, образец, полученный из или происходящий от индивида. В некоторых вариантах осуществления, индивид, из которого выделяют клетку, представляет собой индивида, который имеет заболевание или состояние или который нуждается в клеточной терапии, или которого будут подвергать клеточной терапии. Индивид, в некоторых вариантах осуществления, представляет собой человека, нуждающегося в конкретном терапевтическом вмешательстве, таком как адоптивная клеточная терапия, для которой клетки выделяют, перерабатывают и/или модифицируют.
[0561] Соответственно, клетки в некоторых вариантах осуществления представляют собой первичные клетки, например, первичные клетки человека. Образцы включают ткань, жидкость, и другие образцы, взятые напрямую от индивида, так же как образцы, полученные в результате одной или нескольких стадий переработки, таких как разделение, центрифугирование, генетическая модификация (например, трансдукция вирусным вектором), промывка и/или инкубация. Биологический образец может представлять собой образец, полученный напрямую из биологического источника, или образец, который является переработанным. Биологические образцы включают, но без ограничения, образцы жидкостей организма, таких как кровь, плазма, сыворотка, спинномозговая жидкость, синовиальная жидкость, моча и пот, тканей и органов, включая полученные из них переработанные образцы.
[0562] В некоторых аспектах, образец, из которого получают или выделяют клетки, представляет собой кровь или происходящий из крови образец, или представляет собой продукт афереза или лейкафереза, или происходит из него. Иллюстративные образцы включают цельную кровь, мононуклеарные клетки периферической крови (PBMC), лейкоциты, костный мозг, тимус, биопсию ткани, опухоль, лейкоз, лимфому, лимфатический узел, ассоциированную с кишечником лимфоидную ткань, ассоциированную со слизистой оболочкой лимфоидную ткань, селезенку, другие лимфоидные ткани, печень, легкое, желудок, кишечник, ободочную кишку, почку, поджелудочную железу, молочную железу, кость, предстательную железу, шейку матки, яички, яичники, миндалину или другой орган, и/или происходящие из него клетки. Образцы включают, в контексте клеточной терапии, например, адоптивной клеточной терапии, образцы из аутологичных и аллогенных источников.
[0563] В некоторых вариантах осуществления, клетки происходят из линий клеток, например, линий T–клеток. Клетки, в некоторых вариантах осуществления получены из ксеногенного источника, например, из мыши, крысы, нечеловекообразного примата или свиньи.
[0564] В некоторых вариантах осуществления, выделение клеток включает одну или несколько стадий получения и/или не основанного на аффинности разделения клеток. В некоторых примерах, клетки промывают, центрифугируют и/или инкубируют в присутствии одного или нескольких реагенты, например, для удаления нежелательных компонентов, обогащения желательных компонентов, лизиса или удаления клеток, чувствительных к конкретным реагентам. В некоторых примерах, клетки отделяют на основании одного или нескольких свойств, таких как плотность, адгерентные свойства, размер, чувствительность и/или устойчивость к конкретным компонентам.
[0565] В некоторых примерах, клетки из циркулирующей крови индивида получены, например, посредством афереза или лейкафереза. Образцы, в некоторых аспектах, содержат лимфоциты, включая T–клетки, моноциты, гранулоциты, B клетки, другие ядросодержащие лейкоциты, эритроциты и/или тромбоциты, и в некоторых аспектах, содержит клетки, отличные от эритроцитов и тромбоцитов.
[0566] В некоторых вариантах осуществления, клетки крови, собранные от индивида промывают, например, для удаления фракции плазмы и для помещения клеток в подходящий буфер или среды для последующих стадий переработки. В некоторых вариантах осуществления, клетки промывают фосфатно–солевым буфером (PBS). В некоторых вариантах осуществления, в растворе для промывки отсутствует кальций и/или магний, и/или многие или все двухвалентные катионы. В некоторых аспектах, стадию промывки осуществляют с использованием полуавтоматизированной «проточной» центрифуги (например, устройства для переработки клеток Cobe 2991, Baxter), в соответствии с инструкциями производителя. В некоторых аспектах, стадию промывки проводят в камере для центрифугирования, например, производимой и продаваемой в Biosafe SA, включая камеры для использования с системой Sepax® и Sepax® 2, включая камеры для центрифугирования A–200/F и A–200, в соответствии с инструкциями производителя. В некоторых аспектах, стадию промывки осуществляют посредством проточной фильтрации вдоль потока (TFF) в соответствии с инструкциями производителя. В некоторых вариантах осуществления, клетки ресуспендируют во множестве биосовместимых буферов после промывки, например, таком как не содержащий Ca++/Mg++ PBS. В конкретных вариантах осуществления, компоненты образца клеток крови удаляют и клетки напрямую ресуспедируют в культуральной среде.
[0567] В некоторых вариантах осуществления, способы включают способы разделения клеток на основании плотности, такие как получение лейкоцитов из периферической крови посредством лизиса эритроцитов и центрифугирования в градиенте перколла или фиколла.
[0568] В некоторых вариантах осуществления, способы выделения включают разделение различных типов клеток на основании экспрессии или присутствия в клетке одной или нескольких специфических молекул, таких как поверхностные маркеры, например, поверхностные белки, внутриклеточные маркеры или нуклеиновая кислота. В некоторых вариантах осуществления, можно использовать любой известный способ разделения на основании таких маркеров. В некоторых вариантах осуществления, разделение представляет собой разделение на основании аффинности или иммуноаффинности. Например, выделение, в некоторых аспектах, включает разделение клеток и популяций клеток на основании экспрессии или уровня экспрессии в клетках одного или нескольких маркеров, как правило, поверхностных маркеров клеток, например, посредством инкубации с антителом или партнером по связыванию, которые специфически связываются с такими маркерами, за которыми, как правило, следуют стадии промывки и отделения клеток, связавшихся с антителом или партнером по связыванию, от клеток, не связавшихся с антителом или партнером по связыванию.
[0569] Такие стадии разделения могут быть основаны на положительном отборе, в котором клетки, связавшиеся с реагентами, сохраняют для дальнейшего использования, и/или отрицательный отбор, в котором клетки, не связавшихся с антителом или партнером по связыванию сохраняют. В некоторых примерах, обе фракции сохраняют для дальнейшего использования. В некоторых аспектах, отрицательный отбор может являться особенно полезным, когда недоступно антитело, которое специфически идентифицирует тип клеток в гетерогенной популяции, так что разделение наилучшим образом проводят на основании маркеров экспрессированных клетками, отличными от желательной популяции.
[0570] Разделение не обязательно должно приводить к 100% обогащению или удалению конкретной популяции клеток или клеток, экспрессирующих конкретный маркер. Например, положительный отбор или обогащение клеток конкретного типа, таких как клетки, экспрессирующие маркер, относится к увеличению количества или процента таких клеток, но не должны приводить к полному отсутствию клеток, не экспрессирующих маркер. Подобным образом, отрицательный отбор, удаление или истощение клеток конкретного типа, таких как клетки, экспрессирующие маркер, относится к уменьшению количества или процента таких клеток, но не должно приводить к полному удалению всех таких клеток.
[0571] В некоторых примерах, проводят множество циклов стадий разделения, где положительно или отрицательно отобранную фракцию с одной стадии подвергают другой стадии разделения, например, последующему положительному или отрицательному отбору. В некоторых примерах, на одной стадии разделения можно истощать клетки, экспрессирующие множество маркеров, одновременно, например, посредством инкубации клеток с множеством антител или связывающих паттернов, каждое специфическое для маркера, на который нацеливаются для отрицательного отбора. Подобным образом, множество типов клеток можно одновременно положительно отбирать посредством инкубации клеток с множеством антител или связывающих паттернов, экспрессированных на различных типах клеток.
[0572] Например, в некоторых аспектах, специфические субпопуляции T–клеток, такие как клетки, положительные для или экспрессирующие высокие уровни одного или нескольких поверхностных маркеров, например, CD28+, CD62L+, CCR7+, CD27+, CD127+, CD4+, CD8+, CD45RA+, и/или CD45RO+ T–клеток, выделяют посредством способов положительного или отрицательного отбора.
[0573] Например, CD3+, CD28+ T–клетки можно положительно отбирать с использованием конъюгированных с CD3/CD28 магнитных бусин (например, DYNABEADS® M–450 CD3/CD28 T Cell Expander).
[0574] В некоторых вариантах осуществления, выделение проводят посредством обогащения конкретной популяции клеток посредством положительного отбора, или истощения конкретной популяции клеток, посредством отрицательного отбора. В некоторых вариантах осуществления, положительный или отрицательный отбор осуществляют посредством инкубации клеток с одним или несколькими антителами или другими связывающими веществами, которые специфически связываются с одним или несколькими поверхностными маркерами, экспрессированными или экспрессированными (маркер+) на относительно более высоком уровне (маркервысокий) на положительно или отрицательно отобранных клетках, соответственно.
[0575] В некоторых вариантах осуществления, T–клетки отделяют от образца PBMC посредством отрицательного отбора по маркерам, экспрессированным на клетках, не относящихся к T–клеткам, таких как B клетки, моноциты, или другие лейкоциты, такие как CD14. В некоторых аспектах, стадию отбора CD4+ или CD8+ используют для разделения CD4+ T–клеток–помощников и CD8+ цитотоксических T–клеток. Такие популяции CD4+ и CD8+ можно далее сортировать на субпопуляции посредством положительного или отрицательного отбора по маркерам, экспрессированным или экспрессированным в относительно более высокой степени на одной или нескольких субпопуляциях наивных T–клеток, T–клеток памяти и/или эффекторных T–клеток.
[0576] В некоторых вариантах осуществления, CD8+ клетки дополнительно обогащают или истощают по наивным клеткам, центральным клеткам памяти, эффекторным клеткам памяти и/или центральным стволовым клеткам памяти, например, посредством положительного или отрицательного отбора на основании поверхностных антигенов, ассоциированных с соответствующей субпопуляцией. В некоторых вариантах осуществления, обогащение по центральным T–клеткам памяти (TCM) проводят для увеличения эффективности, например, для улучшения длительной выживаемости, размножения и/или приживления после введения, которые, в некоторых аспектах, являются особенно сильными в таких субпопуляциях. См. Terakuraet al. (2012) Blood.1:72–82; Wang et al. (2012) J Immunother. 35(9):689–701. В некоторых вариантах осуществления, комбинация обогащенных TCM CD8+ T–клеток и CD4+ T–клеток дополнительно улучшает эффективность.
[0577] В некоторых вариантах осуществления, T–клетки памяти присутствуют в обеих CD62L+ и CD62L– подгруппах CD8+ лимфоцитов периферической крови. PBMC можно обогащать или истощать по CD62L–CD8+ и/или CD62L+CD8+ фракциям, например, с использованием антител против CD8 и против CD62L.
[0578] В некоторых вариантах осуществления, обогащение по центральным T–клеткам памяти (TCM) основано на положительной или высокой поверхностной экспрессии CD45RO, CD62L, CCR7, CD28, CD3 и/или CD127; в некоторых аспектах, оно основано на отрицательном отборе клеток, экспрессирующих или высоко экспрессирующих CD45RA и/или гранзим B. В некоторых аспектах, выделение CD8+ популяции, обогащенной по клеткам TCM, проводят посредством истощения клеток, экспрессирующих CD4, CD14, CD45RA, и положительного отбора или обогащения клеток, экспрессирующих CD62L. В одном аспекте обогащение по центральным T–клеткам памяти (TCM) проводят, начиная с отрицательной фракции клеток, отобранной на основании экспрессии CD4, которую подвергают отрицательному отбору на основании экспрессии CD14 и CD45RA, и положительному отбору на основании CD62L. Такие отбор, в некоторых аспектах, проводят одновременно, и в других аспектах проводят последовательно, в любом порядке. В некоторых аспектах, такую же стадию отбора на основании экспрессии CD4 используют для получения популяции или субпопуляции CD8+ клеток, используют также для получения популяции или субпопуляции CD4+ клеток, таким образом, что как положительную, так и отрицательную фракции после разделения на основании CD4 сохраняют и используют в последующих стадиях способов, необязательно, после одной или нескольких дополнительных стадий положительного или отрицательного отбора.
[0579] В конкретном примере, образец PBMC или образец других белых кровяных клеток подвергают отбору CD4+ клеток, при котором как отрицательную, так и положительную фракции сохраняют. Отрицательную фракцию затем подвергают отрицательному отбору на основании экспрессии CD14 и CD45RA или ROR1, и положительному отбору на основании маркера, характерного для центральных T–клеток памяти, такого как CD62L или CCR7, где положительный и отрицательный отборы проводят в любом порядке.
[0580] CD4+ T–клетки–помощники сортируют на наивные клетки, центральные клетки памяти и эффекторные клетки посредством идентификации популяций клеток, имеющих антигены клеточной поверхности. CD4+ лимфоциты можно получать посредством стандартных способов. В некоторых вариантах осуществления, наивные CD4+ T–лимфоциты представляют собой CD45RO–, CD45RA+, CD62L+, CD4+ T–клетки. В некоторых вариантах осуществления, центральные CD4+ клетки памяти представляют собой CD62L+ и CD45RO+. В некоторых вариантах осуществления, эффекторные CD4+ клетки представляют собой CD62L– и CD45RO–.
[0581] В одном примере, для обогащения CD4+ клеток посредством отрицательного отбора, коктейль моноклональных антител, как правило, включает антитела против CD14, CD20, CD11b, CD16, HLA–DR и CD8. В некоторых вариантах осуществления, антитело или партнер по связыванию связаны с твердой подложкой или матриксом, такими как магнитная бусина или парамагнитная бусина, для обеспечения разделения клеток для положительного и/или отрицательного отбора. Например, в некоторых вариантах осуществления, клетки и популяции клеток are отделяют или выделяют с использованием иммуномагнитных (или аффинномагнитных) способов разделения (обзор которых приведен в Methods in Molecular Medicine, vol. 58: Metastasis Research Protocols, Vol. 2: Cell Behavior In vitro and In vivo, p 17–25 Edited by: S. A. Brooks и U. Schumacher © Humana Press Inc., Totowa, NJ).
[0582] В некоторых аспектах, две или более стадии отбора можно проводить последовательно. Например, образец или композицию клеток, подлежащие разделению, подвергают отбору CD8+ клеток, при котором как отрицательную, так и положительную фракции сохраняют. Отрицательную по CD8 фракцию можно далее подвергать отбору CD4+ клеток. В некоторых аспектах, образец или композицию клеток, подлежащие разделению, подвергают отбору CD4+ клеток, при котором как отрицательную, так и положительную фракции сохраняют, и отрицательную по CD4 фракцию можно подвергать отбору CD8+ клеток. Иллюстративные способы отбора клеток описаны в Публикациях международных патентных заявок номер WO2015157384 и/или WO 2015/164675, полное содержание которых приведено в качестве ссылки, и все или часть из них можно использовать в сочетании со способами, описанными в настоящем описании.
[0583] В некоторых аспектах, образец или композицию клеток, подлежащие разделению, инкубируют с небольшим, поддающимся намагничиванию или способным отвечать на магнитное воздействие материалом, таким как способные отвечать на магнитное воздействие частицы или микрочастицы, такие как парамагнитные бусины (например, такие как бусины Dynalbeads или MACS). Способный отвечать на магнитное воздействие материал, например, частица, как правило, напрямую или опосредованно прикреплен к партнеру по связыванию, например, антителу, который специфически связывается с молекулой, например, поверхностным маркером, присутствующим на клетке, клетках или популяции клеток, которые желательно отделить, например, которые желательно отрицательно или положительно отобрать.
[0584] В некоторых вариантах осуществления, магнитная частица или бусина содержит способный отвечать на магнитное воздействие материал, связанный с участником специфического связывания, таким как антитело или другой партнер по связыванию. Существует множество хорошо известных способных отвечать на магнитное воздействие материалов, используемых в способах магнитного разделения. Пригодные магнитные частицы включают частицы, описанные в Molday, Патент США No. 4452773, и в описании Европейской патентной заявки EP 452342 B, содержание которых, таким образом, приведено в качестве ссылки. Другие примеры представляют собой частицы коллоидного размера, такие как частицы, описанные в Owen, Патент США No. 4795698, и Liberti et al., Патент США No. 5200084.
[0585] Инкубацию, как правило, проводят в условиях, в которых антитела или связывающие паттерны, или молекулы, такие как вторичные антитела или другие реагенты, которые специфически связываются с такими антителами или связывающими паттернами, которые присоединены к магнитной частице или бусине, специфически связываются с поверхностными молекулами клетки, если они присутствуют на клетках в образце.
[0586] В некоторых аспектах, образец помещают в магнитное поле, и клетки, имеющие связанные с ними способные отвечать на магнитное воздействие или поддающиеся намагничиванию частицы, можно связывать с магнитом и отделять от немеченых клеток. Для положительного отбора, клетки, которые являются связанными с магнитом, сохраняют; для отрицательного отбора, клетки, которые не являются связанными (немеченые клетки), сохраняют. В некоторых аспектах, комбинацию положительного и отрицательного отбора осуществляют в ходе одной и той же стадии отбора, где положительную и отрицательную фракции сохраняют и далее перерабатывают или подвергают дальнейшим стадиям разделения.
[0587] В конкретных вариантах осуществления, способные отвечать на магнитное воздействие частицы покрывают первичными антителами или другими связывающими паттернами, вторичными антителами, лектинами, ферментами или стрептавидином. В конкретных вариантах осуществления, магнитные частицы присоединяют к клеткам посредством покрытия первичными антителами, специфическими для одного или нескольких маркеров. В конкретных вариантах осуществления, клетки, а не бусины, метят первичным антителом или партнером по связыванию, и затем добавляют покрытые специфическим для типа клеток вторичным антителом или другим партнером по связыванию (например, стрептавидином) магнитные частицы. В конкретных вариантах осуществления, покрытые стрептавидином магнитные частицы используют в сочетании с биотинилированными первичными или вторичными антителами.
[0588] В некоторых вариантах осуществления, способные отвечать на магнитное воздействие частицы остаются присоединенными к клеткам, которые подлежат последующим инкубации, культивированию и/или модификации; в некоторых аспектах, частицы остаются присоединенными к клеткам для введения пациенту. В некоторых вариантах осуществления, поддающиеся намагничиванию или способные отвечать на магнитное воздействие частицы удаляют от клеток. Способы удаления поддающихся намагничиванию частиц от клеток известны и включают, например, использование конкурентных немеченых антител, поддающихся намагничиванию частиц или антител, конъюгированных с расщепляемыми линкерами и т.д. В некоторых вариантах осуществления, поддающиеся намагничиванию частицы являются биоразлагаемыми.
[0589] В некоторых вариантах осуществления, отбор на основании аффинности проводят посредством магнитная сортировка активированных клеток (MACS) (Miltenyi Biotec, Auburn, CA). Системы магнитной сортировки активированных клеток (MACS) способны осуществлять с высокой частотой отбор клеток, имеющих присоединенные к ним намагниченные частицы. В конкретных вариантах осуществления, MACS функционирует в режиме, где не целевые и целевые молекулы последовательно элюируют после приложения внешнего магнитного поля. То есть, клетки, присоединенные к намагниченным частицам, удерживают на месте, в то время как не присоединенные молекулы элюируют. Затем, по завершению первой стадии элюции, молекулы, захваченные в магнитном поле и защищенные от элюции, высвобождают каким–либо способом, таким образом, что их можно элюировать и выделять. В конкретных вариантах осуществления, не целевые клетки метят и истощают из гетерогенной популяции клеток.
[0590] В конкретных вариантах осуществления, выделение или разделение проводят с использованием системы, устройства или аппарата, осуществляющего одно или несколько из стадий способов выделения, получения клеток, разделения, переработки, инкубации, культивирования и/или получения состава. В некоторых аспектах, систему используют для проведения каждой из этих стадий в закрытом или стерильном окружении, например, для минимизации ошибки, манипуляций пользователя и/или контаминации. В одном примере, система представляет собой систему как описано в Международной патентной заявке, публикация номер WO2009/072003, или US 20110003380 A1. В некоторых аспектах, продукт афереза или лейкафереза, или происходящий из него образец, перерабатывают и/или проводят выделение или отбор с использованием системы, устройства, аппарата и/или способа, как описано в Публикации международной патентной заявки номер WO2016/073602 или US 2016/0122782, полное содержание которых приведено в качестве ссылки. В некоторых вариантах осуществления, выделение или разделение проводят в соответствии со способами, описанными в Публикации международной патентной заявки номер WO 2015/164675, полное содержание которой приведено в качестве ссылки.
[0591] В некоторых вариантах осуществления, система или аппарат осуществляет одну или несколько, например, все, из стадий выделения, переработки, модификации и получения состава в интегрированной или автономной системе, и/или в автоматизированном или программируемом режиме. В некоторых аспектах, система или аппарат включает компьютер и/или компьютерную программу в коммуникации с системой или аппаратом, позволяющими пользователю программировать, контролировать, оценивать исход и/или корректировать различные аспекты стадий переработки, выделения, модификации и получения состава.
[0592] В некоторых аспектах, разделение и/или другие стадии проводят с использованием системы CliniMACS (Miltenyi Biotic), например, для автоматизированного разделения клеток на уровне клинического масштаба в закрытой и стерильной системе. Компоненты могут включать интегрированный микрокомпьютер, магнитный сепаратор, перистальтический насос, и различные запорные клапаны. Интегрированный компьютер в некоторых аспектах контролирует все компоненты устройства и управляет системой для проведения повторных процедур в стандартизированной последовательности. Магнитный сепаратор в некоторых аспектах включает подвижный постоянный магнит и держатель для отбирающей колонки. Перистальтический насос контролирует скорость потока через комплект трубок и, вместе с запорными клапанами, обеспечивает контролируемый поток буфера через систему и непрерывную суспензию клеток.
[0593] В системе CliniMACS в некоторых аспектах используют связанные с антителом поддающиеся намагничиванию частицы, которые поставляют в стерильном, апирогенном растворе. В некоторых вариантах осуществления, после мечения клеток с использованием магнитных частиц, клетки промывают для удаления избытка частиц. Затем пакет для препарата клеток соединяют с комплектом трубок, который, в свою очередь, соединяют с пакетом, содержащим буфер, и пакетом для сбора клеток. Комплект трубок состоит из предварительно собранных стерильных трубок, включающих предколонку и разделяющую колонку, и предназначен только для однократного использования. После запуска программы разделения, система автоматически наносит образец клеток на разделяющую колонку. Меченные клетки остаются в колонке, в то время как немеченые клетки удаляют посредством серий стадий промывки. В некоторых вариантах осуществления, популяции клеток для использования в способах, описанных в настоящем описании, не являются мечеными и не остаются в колонке. В некоторых вариантах осуществления, популяции клеток для использования в способах, описанных в настоящем описании являются мечеными и остаются в колонке. В некоторых вариантах осуществления, популяции клеток для использования в способах, описанных в настоящем описании, элюируют с колонки после удаления магнитного поля, и собирают в пакет для сбора клеток.
[0594] В конкретных вариантах осуществления, разделение и/или другие стадии проводят с использованием системы CliniMACS Prodigy (Miltenyi Biotec). Система CliniMACS Prodigy в некоторых аспектах оборудована единицей для переработки клеток, позволяющей автоматизированную промывку и фракционирование клеток посредством центрифугирования. Система CliniMACS Prodigy может также включать встроенную камеру и программное обеспечение для распознавания изображений, которое определяет оптимальную конечную точку фракционирования клеток посредством различения макроскопических слоев источника продукта клеток. Например, периферическую кровь можно автоматически разделять на слои эритроцитов, лейкоцитов и плазмы. Система CliniMACS Prodigy может также включать интегрированную камеру для культивирования клеток, осуществляющую способы культивирования клеток, например, такие как дифференцировка и размножение клеток, нагрузка антигеном и длительное культивирование клеток. Входные отверстия могут позволять стерильное удаление и пополнение сред, и клетки можно мониторировать с использованием интегрированного микроскоп. См., например, Klebanoff et al. (2012) J Immunother. 35(9): 651–660, Terakuraet al. (2012) Blood.1:72–82, и Wang et al. (2012) J Immunother. 35(9):689–701.
[0595] В некоторых вариантах осуществления, популяцию клеток, описанную в настоящем описании, собирают и обогащают (или истощают) посредством проточной цитометрии, при которой клетки, окрашенные по множеству маркеров поверхности клетки, переносят в потоке жидкости. В некоторых вариантах осуществления, популяцию клеток, описанную в настоящем описании, собирают и обогащают (или истощают) посредством сортировки (FACS) в препаративном масштабе. В конкретных вариантах осуществления, популяцию клеток, описанную в настоящем описании собирают и обогащают (или истощают) с использованием чипов микроэлектромеханических систем (MEMS) в комбинации с системой детекции на основе FACS (см., например, WO 2010/033140, Cho et al. (2010) Lab Chip 10, 1567–1573; и Godin et al. (2008) J Biophoton. 1(5):355–376. В обоих случаях, клетки можно метить с использованием множества маркеров, позволяющих выделение хорошо определенных подгрупп T–клеток с высокой чистотой.
[0596] В некоторых вариантах осуществления, антитела или связывающие паттерны метят с использованием одного или нескольких поддающихся детекции маркеров, для облегчения разделения для положительного и/или отрицательного отбора. Например, разделение может быть основано на связывании флуоресцентно меченных антител. В некоторых примерах, разделение клеток на основании связывания антител или других связывающих паттернов, специфических для одного или нескольких поверхностных маркеров клетки проводят в потоке жидкости, например, посредством активированной флуоресценцией сортировки клеток (FACS), включая сортировку в препаративном масштабе (FACS) и/или чипы микроэлектромеханических систем (MEMS), например, в комбинации с системой проточно–цитометрической детекции. Такие способы позволяют положительный и отрицательный отбор на основании множества маркеров одновременно.
[0597] В некоторых вариантах осуществления, способы получения включают стадии замораживания, например, криоконсервации, клеток, либо до, либо после выделения, инкубации и/или модификации. В некоторых вариантах осуществления, на стадии замораживания и последующего размораживания удаляют гранулоциты и, до некоторой степени, моноциты в популяции клеток. В некоторых вариантах осуществления, клетки суспендируют в растворе для замораживания, например, после стадии промывки для удаления плазмы и тромбоцитов. В некоторых аспектах, можно использовать любой из множества известных растворов и параметров для замораживания. Один пример включает использование PBS, содержащего 20% DMSO и 8% человеческий сывороточный альбумин (HSA), или других пригодных сред для замораживания клеток. Затем это разводят 1:1 средой, так чтобы конечные концентрации DMSO и HSA составляли 10% и 4%, соответственно. В некоторых вариантах осуществления, клетки замораживают любым способом, и/или с использованием любых реагентов, контейнеров, растворов для замораживания, и/или криопротекторов, описанных в настоящем описании. В некоторых вариантах осуществления, клетки затем замораживают до −80°C со скоростью или со скоростью приблизительно 1° в минуту и сохраняют в паровой фазе в сосуде для хранения с жидким азотом.
[0598] В некоторых вариантах осуществления, представленные способы включают стадии культивирования, инкубации, культивации и/или генетической модификации. Например, в некоторых вариантах осуществления, настоящее изобретение относится к способам инкубации и/или модификации истощенных популяций клеток и композициям для начала культивирования.
[0599] Таким образом, в некоторых вариантах осуществления, популяции клеток инкубируют в композиции для начала культивирования. Инкубацию и/или модификацию можно проводить в культуральном сосуде, таком как единица, камера, лунка, колонка, пробирка, комплект трубок, клапан, флакон, культуральная чашка, пакет или другой контейнер для культивирования или культивации клеток.
[0600] В некоторых вариантах осуществления, клетки инкубируют и/или культивируют перед или в сочетании с генетической модификацией. Стадии инкубации могут включать культивирование, культивацию, стимуляцию, активацию и/или размножение. В некоторых вариантах осуществления, композиции или клетки инкубируют в присутствии стимулирующих условий или стимулирующего средства. Такие условия включают условия, разработанные для индукции пролиферации, размножения, активации и/или выживаемости клеток в популяции, для имитации воздействия антигена и/или для примирования клеток для генетической модификации, например, для введения рекомбинантного рецептора антигена.
[0601] Условия могут включать одно или несколько из конкретных сред, температуры, содержания кислорода, содержания диоксида углерода, времени, средств, например, питательных веществ, аминокислот, антибиотиков, ионов и/или стимулирующих факторов, таких как цитокины, хемокины, антигены, связывающие паттерны, слитые белки, рекомбинантные растворимые рецепторы, и любые другие средства, разработанные для активации клеток. В некоторых аспектах, клетки инкубируют в присутствии одного или нескольких цитокинов и в некоторых вариантах осуществления коктейль цитокинов можно использовать, например, как описано в Публикации международной патентной заявки номер WO2015157384. В некоторых вариантах осуществления, клетки инкубируют с одним или несколькими цитокинами и/или коктейлем цитокинов до, во время или после трансдукции.
[0602] В некоторых вариантах осуществления, стимулирующие условия или средства включают одно или несколько средств, например, лиганд, способный активировать внутриклеточный передающий сигналы домен комплекса TCR. В некоторых аспектах, средство запускает или инициирует внутриклеточный каскад передачи сигналов TCR/CD3 в T–клетке. Такие средства могут включать антитела, такие как антитела, специфические для TCR, например, антитело против CD3. В некоторых вариантах осуществления, стимулирующие условия включают одно или несколько средств, например, лиганд, способный стимулировать a костимулирующий рецептор, например, антитело против CD28. В некоторых вариантах осуществления, такие средства и/или лиганды могут быть связаны с твердой подложкой, такой как бусина, и/или с одним или несколькими цитокинами. Иллюстративные стимулирующие реагенты описаны в настоящем описании, например, в разделе V–D–1. Необязательно, способ размножения может дополнительно включать стадию добавления антитела против CD3 и/или антитело против CD28 в культуральную среду (например, в концентрации по меньшей мере приблизительно 0,5 нг/мл). В некоторых вариантах осуществления, стимулирующие средства включают IL–2, IL–15 и/или IL–7. В некоторых аспектах, концентрация IL–2 составляет по меньшей мере приблизительно 10 единиц/мл. В некоторых вариантах осуществления, стимулирующие средства включают IL–2, IL–7 и/или IL–15, например, в концентрациях, в концентрациях по меньшей мере или в концентрациях приблизительно 10 единиц/мл, 20 единиц/мл, 50 единиц/мл, 100 единиц/мл, 250 единиц/мл, 500 единиц/мл, 600 единиц/мл, 700 единиц/мл, 800 единиц/мл, 900 единиц/мл или 1000 единиц/мл.
[0603] В некоторых аспектах, инкубацию проводят в соответствии с такими способами, как описано в Патенте США No. 6.040.1 77 от Riddell et al., Klebanoff et al.(2012) J Immunother. 35(9): 651–660, Terakuraet al. (2012) Blood.1:72–82, и/или Wang et al. (2012) J Immunother. 35(9):689–701. В некоторых аспектах, инкубацию проводят с использованием системы, устройства, аппарата и/или способа, как описано в Публикации международной патентной заявки номер WO2016/073602 или US 2016/0122782, полное содержание которых приведено в качестве ссылки. В некоторых вариантах осуществления, инкубацию и/или культивирование проводят в соответствии со способами, описанными в Публикации международной патентной заявки номер WO 2015/164675, полное содержание которых приведено в качестве ссылки. В некоторых вариантах осуществления, по меньшей мере часть инкубации, проводимой в камере для центрифугирования, включает смешивание с реагентом или реагентами для индукции стимуляции и/или активации. В некоторых вариантах осуществления, клетки, такие как отобранные клетки, объединяют со стимулирующим условием или стимулирующем средством в камере для центрифугирования. В некоторых аспектах таких способов, объем клеток объединяют с уровнем одного или нескольких стимулирующих условий или с количеством средств, намного меньшее чем используют в норме при проведении сходных стимуляций в культуральном планшете или другой системе.
[0604] В некоторых вариантах осуществления, стимулирующее средство добавляют к клеткам в полости камеры в количестве, значительно меньшем чем (например, составляющем не более чем 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70% или 80% количества), по сравнению с количеством стимулирующего средства, которое как правило, используют или необходимо использовать для достижения приблизительно такой же или сходной эффективности отбора для такого же количества клеток или такого же объема клеток when отбор проводят без смешивания в камере для центрифугирования, например, в пробирке или пакете с периодическим встряхиванием или качанием. В некоторых вариантах осуществления, инкубацию проводят с добавлением буфера для инкубации к клеткам и стимулирующего средства для достижения целевого объема при инкубация реагента, например, от 10 мл до 200 мл, например, по меньшей мере или приблизительно по меньшей мере, или приблизительно, или 10 мл, 20 мл, 30 мл, 40 мл, 50 мл, 60 мл, 70 мл, 80 мл, 90 мл, 100 мл, 150 мл или 200 мл. В некоторых вариантах осуществления, буфер для инкубации и стимулирующее средство предварительно смешивают перед добавлением к клеткам. В некоторых вариантах осуществления, буфер для инкубации и стимулирующее средство по отдельности добавляют к клеткам. В некоторых вариантах осуществления, стимулирующую инкубацию проводят в условиях периодического осторожного перемешивания, которое может способствовать стимуляции энергетически выгодных взаимодействий и, таким образом, позволяет использование меньшего общего количества стимулирующего средства, с достижением в то же время стимуляции и активации клеток.
[0605] В некоторых вариантах осуществления, инкубацию, как правило, проводят в условиях перемешивания, например, в присутствии вращения, как правило, при относительно низких ускорении или скорости, такой как скорость ниже, чем используют для осаждения клеток, например, от или приблизительно от 600 об./мин до 1700 об./мин (например, при или приблизительно при, или по меньшей мере при 600 об./мин, 1000 об./мин или 1500 об./мин, или 1700 об./мин), например, при RCF для образца или стенки камеры или другого контейнера от или приблизительно от 80 g до 100 g (например, при или приблизительно при, или по меньшей мере при 80 g, 85 g, 90 g, 95 g или 100 g). В некоторых вариантах осуществления, вращение проводят с использованием повторяющихся интервалов вращения при такой низкой скорости с последующим периодом покоя, например, вращение и/или покой в течение 1, 2, 3, 4, 5, 6, 7, 8, 9, или 10 секунд, например, вращение в течение приблизительно 1 или 2 секунд с последующим покоем в течение приблизительно 5, 6, 7 или 8 секунд.
[0606] В некоторых вариантах осуществления, общая длительность инкубации, например, со стимулирующим средством, составляет между или между приблизительно 1 часом и 96 часами, 1 часом и 72 часами, 1 часом и 48 часами, 4 часами и 36 часами, 8 часами и 30 часами или 12 часами и 24 часами, например, по меньшей мере или приблизительно по меньшей мере 6 часов, 12 часов, 18 часов, 24 часа, 36 часов или 72 часа, включая каждое. В некоторых вариантах осуществления, дополнительную инкубацию проводят в течение времени между или приблизительно между 1 часом и 48 часами, 4 часами и 36 часами, 8 часами и 30 часами или 12 часами и 24 часами, включая каждое.
[0607] В некоторых вариантах осуществления, стадии переработки включают введение молекулы нуклеиновой кислоты, кодирующей рекомбинантный белок. Среди таких рекомбинантных белков присутствуют рекомбинантные рецепторы, такие как любые, описанные в разделе V. Введение молекул нуклеиновой кислоты, кодирующих рекомбинантный белок, такой как рекомбинантный рецептор, в клетке можно проводить с использованием любого из ряда известных векторов. Такие векторы включают вирусные и невирусные системы, включая лентивирусные и гаммаретровирусные системы, так же как системы на основе транспозонов, такие как системы переноса генов на основе PiggyBac или Sleeping Beauty. Иллюстративный способы включают способы переноса нуклеиновых кислот, кодирующих рецепторы, включая способы посредством вирусной, например, ретровирусной или лентивирусной трансдукции, транспозонов и электропорации.
[0608] В некоторых вариантах осуществления, перенос генов осуществляют посредством сначала стимуляции клетки, например, посредством ее объединения со стимулом, который индуцирует ответ, такой как пролиферация, выживаемость, и/или активация, например, как измерено по экспрессии цитокина или маркера активации, с последующей трансдукцией активированных клеток, и размножением в культуре до количеств, достаточных для клинических применений.
[0609] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносят в клетки с использованием рекомбинантных инфекционных вирусных частиц, например, такой как, векторы, происходящие из вируса обезьян 40 (SV40), аденовирусов, аденоассоциированный вирус (AAV), и вирус иммунодефицита человека (HIV). В некоторых вариантах осуществления, рекомбинантный нуклеиновые кислоты переносят в T–клетки с использованием рекомбинантных лентивирусных векторов или ретровирусных векторов, таких как гамма–ретровирусные векторы.
[0610] Способы вирусной трансдукции, например, лентивирусной трансдукции, известны. Иллюстративные способы описаны, например, в Wang et al. (2012) J. Immunother. 35(9): 689–701; Cooper et al. (2003) Blood. 101:1637–1644; Verhoeyen et al. (2009) Methods Mol Biol. 506: 97–114; и Cavalieri et al. (2003) Blood. 102(2): 497–505.
[0611] В некоторых вариантах осуществления, введение проводят посредством приведения одной или нескольких клеток из композиции в контакт с молекулой нуклеиновой кислоты, кодирующей рекомбинантный белок, например, рекомбинантный рецептор. В некоторых вариантах осуществления, приведение в контакт можно осуществлять с использованием центрифугирования, такого как спинокуляция (например, центрифужная инокуляция). Такие способы включают любые из способов, как описано в Международной публикации номер WO2016/073602. Иллюстративные камеры для центрифугирования включают камеры, производимые и продаваемые в Biosafe SA, включая камеры для использования с системой Sepax® и Sepax® 2, включая камеры для центрифугирования A–200/F и A–200 и различные наборы для использования с такими системами. Иллюстративные камеры, системы, и оборудование и шкафы для переработки описаны, например, в Патенте США No. 6123655, Патент США No. 6733433 и опубликованной Патентной заявке США, Публикация No.: US 2008/0171951, и опубликованной международной патентной заявке, публикация no. WO 00/38762, полное содержание каждого из которых приведено в настоящем описании в качестве ссылки. Иллюстративные наборы для использования с такими системами включают, но без ограничения, одноразовые наборы, продаваемые BioSafe SA под наименованиями продуктов CS–430.1, CS–490.1, CS–600.1 или CS–900.2.
[0612] В некоторых вариантах осуществления, в систему включают и/или систему помещают во взаимодействие с другим оборудованием, включая оборудование для выполнения, автоматизации, контроля и/или мониторирования аспектов стадии трансдукции и одной или нескольких различных других стадий переработки, осуществляемых в системе, например, одной или нескольких стадий переработки, которые можно проводить с или в сочетании с системой камеры для центрифугирования как описано в настоящем описании или в Международной публикации номер WO2016/073602. Это оборудование, в некоторых вариантах осуществления, содержат внутри шкафа. В некоторых вариантах осуществления, оборудование включает шкаф, включающий корпус, содержащий контрольные схемы, центрифугу, крышку, моторы, насосы, сенсоры, дисплеи и пользовательский интерфейс. Иллюстративные устройства описаны в Патенте США No. 6123655, Патент США No. 6733433 и US 2008/0171951.
[0613] В некоторых вариантах осуществления, система содержит серии контейнеров, например, пакетов, трубок, электронных схем, зажимов, коннекторов и камеру для центрифугирования. В некоторых вариантах осуществления, контейнеры, такие как пакеты, включают один или несколько контейнеров, таких как пакеты, содержащие клетки, подлежащие трансдукции, и частицы вирусного вектора, в одном и том же контейнере или в отдельных контейнерах, таких как один и тот же пакет или отдельные пакеты. В некоторых вариантах осуществления, система дополнительно включает один или несколько контейнеров, таких как пакеты, содержащие среду, такую как разбавитель и/или раствор для промывки, которые входят в состав камеры и/или других компонентов для разведения, ресуспендирования и/или промывки компонентов и/или композиций в ходе способов. Контейнеры можно присоединять в одном или нескольких положениях в системе, например, в положении, соответствующем линии входа, линии разведения, линии промывки, линии отходов и/или линии выхода.
[0614] В некоторых вариантах осуществления, камера взаимодействует с центрифугой, способной осуществлять вращение камеры, например, вокруг ее оси вращения. Вращение может происходить до, во время и/или после инкубации в сочетании с трансдукцией клеток, и/или на одной или нескольких из других стадий переработки. Таким образом, в некоторых вариантах осуществления, одну или несколько из различных стадий переработки проводят при вращении, например, с определенным ускорением. Камера, как правило, является способной к вертикальному или в основном вертикальному вращению, таким образом, что камера находится вертикально во время центрифугирования, и боковая стенка и ось являются вертикальными или в основном вертикальными, где торцевая стенка(стенки) являются горизонтальными или в основном горизонтальными.
[0615] В некоторых вариантах осуществления, композицию, содержащую клетки, вирусные частицы и реагент, можно подвергать вращению, как правило, при относительно низких ускорении или скорости, такой как скорость ниже, чем используют для осаждения клеток, например, от или приблизительно от 600 об./мин до 1700 об./мин (например, от или приблизительно от, или по меньшей мере 600 об./мин 1000 об./мин, или 1500 об./мин, или 1700 об./мин). В некоторых вариантах осуществления, вращение осуществляют при ускорении, например, относительном центробежном ускорении, от или приблизительно от 100 g до 3200 g (например, при или приблизительно при, или по меньшей мере при или приблизительно при 100 g, 200 g, 300 g, 400 g, 500 g, 1000 g, 1500 g, 2000 g, 2500 g, 3000 g или 3200 g), как измерено, например, у внутренней или внешней стенке камеры или полость. Термин «относительное центробежное ускорение» или RCF, как правило, понимают как эффективное ускорение, придаваемое объекту или веществу (такому как клетка, образец или осадок, и/или точка в камере или другом контейнере, подвергаемом вращению), относительно гравитационной силы Земли, в конкретной точке пространства, по сравнению с осью вращения. Это значение можно определять с использованием хорошо известных формул, принимая во внимание гравитационную силу, скорость вращения и радиус вращения (расстояние от оси вращения и объекта, вещества или частицы, для которых измеряют RCF).
[0616] В некоторых вариантах осуществления, в ходе по меньшей мере части генетической модификации, например, трансдукции, и/или после генетической модификации, клетки переносят в контейнер, такой как пакет для культуры генетически модифицированных клеток, например, для культивирования или размножения клеток, как описано выше. В некоторых вариантах осуществления, контейнер для культивирования или размножения клеток представляет собой пакет для биореактора, такой как пакет для перфузии.
[0617] В некоторых вариантах осуществления, представленные способы включают одну или несколько стадий культивирования модифицированных клеток, например, культивирования клеток в условиях, стимулирующих пролиферацию и/или размножение. В некоторых вариантах осуществления, модифицированные клетки культивируют в условиях, стимулирующих пролиферацию и/или размножение, после стадии генетической модификации, например, введение рекомбинантного полипептида в клетки посредством трансдукции или трансфекции. В конкретных вариантах осуществления, клетки культивируют после инкубации клеток в стимулирующих условиях и трансдукции или трансфекции с использованием рекомбинантного полинуклеотида, например, полинуклеотида, кодирующего рекомбинантный рецептор. В некоторых вариантах осуществления, в результате культивирования получают одну или несколько культивированных композиций обогащенных T–клеток.
[0618] В некоторых аспектах, культуральная среда представляет собой адаптированную культуральную среду, поддерживающую рост, культивирование, размножение или пролиферацию клеток, таких как T–клетки. В некоторых аспектах, среда может представлять собой жидкость, содержащую смесь солей, аминокислот, витаминов, сахаров или любой их комбинации. В некоторых вариантах осуществления, культуральная среда дополнительно включает одно или несколько стимулирующих условий или средств, например, для стимуляции культивирования, размножения или пролиферации клеток в ходе инкубации. В некоторых вариантах осуществления, стимулирующее условие представляет собой или включает один или несколько цитокинов, выбранных из IL–2, IL–7 или IL–15. В некоторых вариантах осуществления, цитокин представляет собой рекомбинантный цитокин. В некоторых вариантах осуществления, концентрация одного или нескольких цитокинов в культуральной среде во время культивирования или инкубации, независимо составляет от или приблизительно от 1 МЕ/мл до 1500 МЕ/мл, например, от или приблизительно от 1 МЕ/мл до 100 МЕ/мл, от 2 МЕ/мл до 50 МЕ/мл, от 5 МЕ/мл до 10 МЕ/мл, от 10 МЕ/мл до 500 МЕ/мл, от 50 МЕ/мл до 250 МЕ/мл или от 100 МЕ/мл до 200 МЕ/мл, от 50 МЕ/мл до 1500 МЕ/мл, от 100 МЕ/мл до 1000 МЕ/мл или от 200 МЕ/мл до 600 МЕ/мл. В некоторых вариантах осуществления, концентрация одного или нескольких цитокинов, независимо составляет по меньшей мере или по меньшей мере приблизительно 1 МЕ/мл, 5 МЕ/мл, 10 МЕ/мл, 50 МЕ/мл, 100 МЕ/мл, 200 МЕ/мл, 500 МЕ/мл, 1000 МЕ/мл или 1500 МЕ/мл.
[0619] В некоторых аспектах, клетки инкубируют в течение по меньшей мере части времени после переноса модифицированных клеток и культуральной среды. В некоторых вариантах осуществления, стимулирующие условия, как правило, включают температура пригодную для роста первичных иммуноцитов, таких как T–лимфоциты человека, например, по меньшей мере приблизительно 25 градусов Цельсия, как правило, по меньшей мере приблизительно 30 градусов, и, как правило, при или приблизительно при 37 градусов Цельсия. В некоторых вариантах осуществления, клетки инкубируют при температуре от 25 до 38 градусов Цельсия, например, при 30–37 градусов Цельсия, например, при или приблизительно при 37 градусов Цельсия±2 градуса Цельсия. В некоторых вариантах осуществления, инкубацию проводят в течение периода времени пока культивирование, например, культивация или размножение, не приведетт к желательным или пороговым плотности, количеству или дозе клеток. В некоторых вариантах осуществления, инкубация составляет более чем или более чем приблизительно, или составляет приблизительно или составляет 24 часа, 48 часов, 72 часа, 96 часов, 5 суток, 6 суток, 7 суток, 8 суток, 9 суток или более.
[0620] В некоторых вариантах осуществления, клетки инкубируют в условиях для поддержания целевого количества диоксида углерода в культуре клеток. В некоторых аспектах, это обеспечивает оптимальные культивирование, размножение и пролиферацию клеток в ходе роста. В некоторых аспектах, количество диоксида углерода (CO2) составляет между 10% и 0% (об./об.) указанного газа, например, между 8% и 2% (об./об.) указанного газа, например, количество, равное или приблизительно равное 5% (об./об.) CO2.
[0621] В некоторых вариантах осуществления, клетки инкубируют с использованием контейнеров, например, пакетов, которые используют в сочетании с биореактором. В некоторых случаях, биореактор можно подвергать движению или качанию, что, в некоторых аспектах, может увеличивать перенос кислорода. Движение биореактора может включать, но без ограничения, вращение относительно горизонтальной оси, вращение относительно вертикальной оси, качательное движение относительно наклонной или расположенной под углом горизонтальной оси биореактора или любую их комбинацию. В некоторых вариантах осуществления, по меньшей мере часть инкубации проводят с качанием. Скорость качания и угол качания можно корректировать для достижения желательного встряхивания. В некоторых вариантах осуществления, угол качания составляет или составляет приблизительно 20°, 19°, 18°, 17°, 16°, 15°, 14°, 13°, 12°, 11°, 10°, 9°, 8°, 7°, 6°, 5°, 4°, 3°, 2° или 1°. В конкретных вариантах осуществления, угол качания составляет между 6–16°, включительно. В других вариантах осуществления, угол качания составляет между 7–16°. В других вариантах осуществления, угол качания составляет между 8–12°, включительно. В некоторых вариантах осуществления, скорость качания составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 1 12, 13, 14 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40 об./мин. В некоторых вариантах осуществления, скорость качания составляет между 4 и 12 об./мин, например, между 4 и 6 об./мин, включительно. По меньшей мере часть размножения культуры клеток проводят с качательным движением, например, с углом между 5° и 10°, включительно, таким как 6°, при постоянной скорости качания, такой как скорость между 5 и 15 об./мин, включительно, например, 6 RMP или 10 об./мин. Каждые из CD4+ и CD8+ клеток отдельно размножают, пока каждые из них не достигнут порогового количества или плотности клеток.
[0622] В некоторых вариантах осуществления, по меньшей мере a часть инкубации is проводят в статических условиях. В некоторых вариантах осуществления, по меньшей мере часть инкубации проводят с перфузией, чтобы выводить посредством перфузии использованную среду и вводить посредством перфузии свежую среду в ходе культивирования. В некоторых вариантах осуществления, способ включает стадию перфузии свежей культуральной среды в культуру клеток, например, через загрузочное отверстие. В некоторых вариантах осуществления, культуральная среда, добавленная в ходе перфузии, содержит одно или несколько стимулирующих средств, например, один или несколько рекомбинантных цитокинов, таких как IL–2, IL–7 и/или IL–15. В некоторых вариантах осуществления, культуральная среда, добавленная в ходе перфузии, представляет собой такую же культуральную среду, используемую в ходе статической инкубации.
[0623] В некоторых вариантах осуществления, после инкубации, контейнер, например, пакет, повторно присоединяют к системе для проведения одной или несколько другие стадии переработки для изготовления, образования или получения средства для клеточной терапии, например, повторно присоединяют к системе, содержащей камеру для центрифугирования. В некоторых аспектах, культивированные клетки переносят из пакета во внутреннюю полость камеры для получения состава культивированных клеток .
[0624] В некоторых вариантах осуществления, T–клетки размножают посредством добавления в композицию для начала культивирования фидерных клеток, таких как не делящиеся мононуклеарные клетки периферической крови (PBMC), (например, таким образом, что полученная популяция клеток содержит по меньшей мере приблизительно 5, 10, 20 или 40 или более фидерных клеток PBMC для каждого T–лимфоцита в исходной популяции, подлежащей размножению); и инкубации культуры (например, в течение времени, достаточного для размножения этих количеств T–клеток). В некоторых аспектах, не делящиеся фидерные клетки могут содержать облученные гамма–излучением фидерные клетки PBMC. В некоторых вариантах осуществления, PBMC облучают с использованием гамма–излучения в диапазоне от приблизительно 3000 до 3600 рад для предотвращения деления клеток. В некоторых аспектах, фидерные клетки добавляют в культуральную среду перед добавлением популяций T–клеток.
[0625] В некоторых вариантах осуществления, стимулирующие условия включают температуру, пригодную для роста T–лимфоцитов человека, например, по меньшей мере приблизительно 25 градусов Цельсия, как правило, по меньшей мере приблизительно 30 градусов, и, как правило, при или приблизительно при 37 градусов Цельсия. Необязательно, инкубация может дополнительно включать добавление не делящихся трансформированных EBV лимфобластоидных клеток (LCL) в качестве фидерных клеток. LCL можно облучать с использованием гамма–излучения в диапазоне от приблизительно 6000 до 10000 рад. Фидерные клетки LCL, в некоторых аспектах, предоставляют в любом пригодном количестве, например, в соотношении фидерных клеток LCL к исходным T–лимфоцитам по меньшей мере приблизительно 10:1.
[0626] В некоторых вариантах осуществления, антигенспецифические T–клетки, такие как антигенспецифические CD4+ и/или CD8+ T–клетки, получают посредством стимуляции антигеном наивных или антигенспецифических T–лимфоцитов. Например, антигенспецифические линии или клоны T–клеток можно получать против антигенов цитомегаловируса посредством выделения T–клеток от инфицированных индивидов и стимуляции клеток in vitro с использованием того же самого антигена.
[0627] В некоторых вариантах осуществления, модифицированные клетки накапливают, например, собирают, для получения состава после того как клетки трансдуцировали, трансфицировали, культивировали и/или размножали. В некоторых вариантах осуществления, клетки собирают в пределах некоторого количества времени, например, в течение или в пределах 2 суток, 3 суток, 4 суток, 5 суток, 6 суток, 7 суток, 8 суток, 9 суток, 10 суток, 11 суток, 12 суток, 13 суток или 14 суток, после начала и/или инициации, или окончания и/или завершения стадии переработки, такой как стадии выделения, отбора, инкубации, стимуляции, активации, трансдукции, трансфекции, культивирования и/или размножения. В конкретных вариантах осуществления, модифицированные клетки собирают после культивирования, например, в течение или в пределах 1 суток, 2 суток, 3 суток, 4 суток, 5 суток, 6 суток, 7 суток, 8 суток, 9 суток или 10 суток культивирования и/или после того, как модифицированные клетки и/или композиции клеток, включающие модифицированные клетки, размножены до пороговых плотности клеток, количества клеток, и/или уровня размножения. В некоторых вариантах осуществления, собранные клетки составляют любым способом, описанным в настоящем описании, например, таким, как описано в разделе VI.
1. Стимулирующие реагенты
[0628] В некоторых вариантах осуществления, клетки можно инкубировать и/или приводить в контакт со стимулирующим реагентом, способным к активации и/или размножению T–клеток. В конкретных вариантах осуществления, стимулирующий реагент содержит частицу, например, бусину, которая является конъюгированной или связанной с одним или несколькими средствами, например, биомолекулами, которые являются способным к активации и/или размножению клеток, например, T–клеток. В некоторых вариантах осуществления, одно или несколько средств являются связанными с бусиной. В некоторых вариантах осуществления, бусина является биосовместимой, т.е., состоит из материала, пригодного для биологического применения. В некоторых вариантах осуществления, бусины являются нетоксичными для культивированных клеток, например, культивированных T–клеток. В некоторых вариантах осуществления, бусины могут представлять собой любые частицы, способные к присоединению средств способом, позволяющим взаимодействие между средством и клеткой.
[0629] В некоторых вариантах осуществления, стимулирующий реагент содержит одно или несколько средств, которые являются способным к активации и/или размножению клеток, например, T–клетки, которые являются связанными с бусиной или иным образом прикрепленными к бусине, например, к поверхности бусины. В конкретных вариантах осуществления, бусина представляет собой не относящуюся к клетке частицу. В конкретных вариантах осуществления, бусина может включать коллоидную частицу, микросферу, наночастицу, магнитную бусину или т.п. В некоторых вариантах осуществления бусины представляют собой агарозные бусины. В конкретных вариантах осуществления, бусины представляют собой сефарозные бусины.
[0630] В конкретных вариантах осуществления, стимулирующий реагент содержит бусины, которые являются монодисперсными. В конкретных вариантах осуществления, бусины, которые являются монодисперсными, имеют дисперсию размеров со стандартным отклонением диаметров менее чем 5% друг от друга.
[0631] В некоторых вариантах осуществления, бусина содержит одно или несколько средств, таких как средство, соединенное, конъюгированное или связанно (напрямую или опосредованно) с поверхностью бусины. В некоторых вариантах осуществления, средство, как предусмотрено в настоящем описании, может включать, но без ограничения, РНК, ДНК, белки (например, ферменты), антигены, поликлональные антитела, моноклональные антитела, фрагменты антител, углеводы, липиды лектины или любую другую биомолекулу с аффинностью для желательной мишени. В некоторых вариантах осуществления, желательная мишень представляет собой T–клеточный рецептор и/или компонент T–клеточного рецептора. В конкретных вариантах осуществления, желательная мишень представляет собой CD3. В конкретном варианте осуществления, желательная мишень представляет собой костимулирующую молекулу, например, CD28. Одно или несколько средств можно присоединять напрямую или опосредованно к бусине посредством множества способов, известных и доступных в данной области. Соединение может являться ковалентным, нековалентным, электростатическим или гидрофобным, и его можно осуществлять посредством множества способов присоединения, включая например, химические способы, механические способы или ферментные способы. В некоторых вариантах осуществления, биомолекулу (например, a биотинилированное антитело против CD3 антитело) можно присоединять опосредованно к бусине посредством другой биомолекулы (например, антитела против биотина), напрямую присоединенной к бусине.
[0632] В некоторых вариантах осуществления, одно или несколько средств, присоединенных к бусине, представляет собой антитело. Антитело может включать поликлональное антитело, моноклональное антитело (включая полноразмерные антитела, имеющие область Fc иммуноглобулина), композиции антител с полиэпитопной специфичностью, мультиспецифические антитела (например, биспецифические антитела, диатела и одноцепочечные молекулы, так же как фрагменты антител (например, Fab, F(ab')2 и Fv). В некоторых вариантах осуществления, стимулирующий реагент представляет собой фрагмент антитела (включая антигенсвязывающий фрагмент), например, фрагмент Fab, Fab′–SH, Fv, scFv или (Fab′)2. Понятно, что константные области любого изотипа можно использовать для антител, предусмотренных в настоящем описании, включая константные области IgG, IgM, IgA, IgD и IgE, и что такие константные области можно получать из любых видов человека или животного (например, видов мышей). В некоторых вариантах осуществления, средство представляет собой антитело, которое связывает и/или узнает один или несколько компонентов T–клеточного рецептора. В конкретных вариантах осуществления, средство представляет собой антитело против CD3. В конкретных вариантах осуществления, средство представляет собой антитело, которое связывает и/или узнает a корецептор. В некоторых вариантах осуществления, стимулирующий реагент содержит антитело против CD28.
[0633] В некоторых вариантах осуществления, бусина имеет диаметр более чем приблизительно 0,001 мкм, более чем приблизительно 0,01 мкм, более чем приблизительно 0,1 мкм, более чем приблизительно 1,0 мкм, более чем приблизительно 10 мкм, более чем приблизительно 50 мкм, более чем приблизительно 100 мкм или более чем приблизительно 1000 мкм и не более чем приблизительно 1500 мкм. В некоторых вариантах осуществления, бусина имеет диаметр от приблизительно 1,0 мкм до приблизительно 500 мкм, от приблизительно 1,0 мкм до приблизительно 150 мкм, от приблизительно 1,0 мкм до приблизительно 30 мкм, от приблизительно 1,0 мкм до приблизительно 10 мкм, от приблизительно 1,0 мкм до приблизительно 5,0 мкм, от приблизительно 2,0 мкм до приблизительно 5,0 мкм или от приблизительно 3,0 мкм до приблизительно 5,0 мкм. В некоторых вариантах осуществления, бусина имеет диаметр от приблизительно 3 мкм до приблизительно 5 мкм. В некоторых вариантах осуществления, бусина имеет диаметр по меньшей мере или по меньшей мере приблизительно, или приблизительно 0,001 мкм, 0,01 мкм, 0,1мкм, 0,5мкм, 1,0 мкм, 1,5 мкм, 2,0 мкм, 2,5 мкм, 3,0 мкм, 3,5 мкм, 4,0 мкм, 4,5 мкм, 5,0 мкм, 5,5 мкм, 6,0 мкм, 6,5 мкм, 7,0 мкм, 7,5 мкм, 8,0 мкм, 8,5 мкм, 9,0 мкм, 9,5 мкм, 10 мкм, 12 мкм, 14 мкм, 16 мкм, 18 мкм или 20 мкм. В конкретных вариантах осуществления, бусина имеет диаметр или имеет диаметр приблизительно 4,5 мкм. В конкретных вариантах осуществления, бусина имеет диаметр или имеет диаметр приблизительно 2,8 мкм.
[0634] В некоторых вариантах осуществления, бусины имеют плотность более чем 0,001 г/см3, более чем 0,01 г/см3, более чем 0,05 г/см3, более чем 0,1 г/см3, более чем 0,5 г/см3, более чем 0,6 г/см3, более чем 0,7 г/см3, более чем 0,8 г/см3, более чем 0,9 г/см3, более чем 1 г/см3, более чем 1,1 г/см3, более чем 1,2 г/см3, более чем 1,3 г/см3, более чем 1,4 г/см3, более чем 1,5 г/см3, более чем 2 г/см3, более чем 3 г/см3, более чем 4 г/см3 или более чем 5 г/см3. В некоторых вариантах осуществления, бусины имеют плотность между приблизительно 0,001 г/см3 и приблизительно 100 г/см3, приблизительно 0,01 г/см3 и приблизительно 50 г/см3, приблизительно 0,1 г/см3 и приблизительно 10 г/см3, приблизительно 0,1 г/см3 и приблизительно 0,5 г/см3, приблизительно 0,5 г/см3 и приблизительно 1 г/см3, приблизительно 0,5 г/см3 и приблизительно 1,5 г/см3, приблизительно 1 г/см3 и приблизительно 1,5 г/см3, приблизительно 1 г/см3 и приблизительно 2 г/см3, или приблизительно 1 г/см3 и приблизительно 5 г/см3, включая каждое. В некоторых вариантах осуществления, бусины имеют плотность приблизительно 0,5 г/см3, приблизительно 0,5 г/см3, приблизительно 0,6 г/см3, приблизительно 0,7 г/см3, приблизительно 0,8 г/см3, приблизительно 0,9 г/см3, приблизительно 1,0 г/см3, приблизительно 1,1 г/см3, приблизительно 1,2 г/см3, приблизительно 1,3 г/см3, приблизительно 1,4 г/см3, приблизительно 1,5 г/см3, приблизительно 1,6 г/см3, приблизительно 1,7 г/см3, приблизительно 1,8 г/см3, приблизительно 1,9 г/см3, или приблизительно 2,0 г/см3. В конкретных вариантах осуществления, бусины имеют плотность приблизительно 1,6 г/см3. В конкретных вариантах осуществления, бусины или частицы имеют плотность приблизительно 1,5 г/см3. В конкретных вариантах осуществления, частицы имеют плотность приблизительно 1,3 г/см3.
[0635] В конкретных вариантах осуществления, множество бусин имеют однородную плотность. В конкретных вариантах осуществления, однородная плотность имеет стандартное отклонение плотности менее чем 10%, менее чем 5%, или менее чем 1% от средней плотности бусин.
[0636] В некоторых вариантах осуществления, бусины имеют площадь поверхности между приблизительно 0,001 м2 на каждый грамм частиц (м2/г) и приблизительно 1000 м2/г, приблизительно 0,010 м2/г и приблизительно 100 м2/г, приблизительно 0,1 м2/г и приблизительно 10 м2/г, приблизительно 0,1 м2/г и приблизительно 1 м2/г, приблизительно 1 м2/г и приблизительно 10 м2/г, приблизительно 10 м2/г и приблизительно 100 м2/г, приблизительно 0,5 м2/г и приблизительно 20 м2/г, приблизительно 0,5 м2/г и приблизительно 5 м2/г, или приблизительно 1 м2/г и приблизительно 4 м2/г, включая каждое. В некоторых вариантах осуществления, частицы или бусины имеют площадь поверхности от приблизительно 1 м2/г до приблизительно 4 м2/г.
[0637] В некоторых вариантах осуществления, бусина содержит по меньшей мере один материал на или около поверхности бусины, который можно соединять, связывать или конъюгировать с средством. В некоторых вариантах осуществления, бусина имеет функционализированную поверхность, т.е. содержит функциональные группы, которые являются способными формировать ковалентную связь со связывающей молекулой, например, полинуклеотидом или полипептидом. В конкретных вариантах осуществления, бусина содержит экспонированные на поверхности карбоксильные, амино, гидроксильные, тозильные, эпокси и/или хлорметильные группы. В конкретных вариантах осуществления, бусины содержат экспонированные на поверхности агарозу и/или сефарозу. В конкретных вариантах осуществления, поверхность бусины содержит присоединенные стимулирующие реагенты, которые могут связывать или присоединять связывающие молекулы. В конкретных вариантах осуществления, биомолекулы представляют собой полипептиды. В некоторых вариантах осуществления, бусины содержат экспонированные на поверхности белок A, белок G или биотин.
[0638] В некоторых вариантах осуществления, бусина вступает в реакцию в магнитном поле. В некоторых вариантах осуществления, бусина представляет собой магнитную бусину. В некоторых вариантах осуществления, магнитных бусина является парамагнитной. В конкретных вариантах осуществления, магнитная бусина является суперпарамагнитной. В конкретных вариантах осуществления, бусины не проявляют никаких магнитных свойств, пока не подвергнуты воздействию магнитного поля.
[0639] В конкретных вариантах осуществления, бусина содержит магнитный кор, парамагнитный кор или суперпарамагнитный кор. В некоторых вариантах осуществления, магнитный кор содержит металл. В некоторых вариантах осуществления, металл может представлять собой, но без ограничения, железо, никель, медь, кобальт, галолиний, марганец, тантал, цинк, цирконий или любые их комбинации. В конкретных вариантах осуществления, магнитный кор содержит оксиды металла (например, оксиды железа), ферриты (например, ферриты марганца, ферриты кобальта, ферриты никеля и т.д.), гематит и сплавы металлов (например, CoTaZn). В некоторых вариантах осуществления, магнитный кор содержит один или несколько из феррита, металла, сплава металлов, оксида железа, или диоксида хрома. В некоторых вариантах осуществления, магнитный кор содержит элементарное железо или его соединение. В некоторых вариантах осуществления, магнитный кор содержит один или несколько из магнетита (Fe3O4), маггемита (γFe2O3) или грейгита (Fe3S4). В некоторых вариантах осуществления, внутренний кор содержит оксид железа (например, Fe3O4).
[0640] В конкретных вариантах осуществления, бусина содержит магнитный, парамагнитный и/или суперпарамагнитный кор, покрытый оболочкой или покрытием с функционализированной поверхностью. В некоторых вариантах осуществления, оболочка может содержать материал, который может включать, но без ограничения, полимер, полисахарид, диоксид кремния, жирную кислоту, белок, углерод, агарозу, сефарозу или их комбинацию. В некоторых вариантах осуществления, полимер может представлять собой полиэтиленгликоль, сополимер (молочной–гликолевой кислоты), полиглутаральдегид, полиуретан, полистирол или поливиниловый спирт. В конкретных вариантах осуществления, внешняя оболочка или покрытие содержит полистирол. В конкретных вариантах осуществления, поверхность внешнего покрытия является функционализированной.
[0641] В некоторых вариантах осуществления, стимулирующий реагент содержит бусину, содержащую кор из оксида металла (например, кор из оксида железа), и оболочку, где кор из оксида металла содержит по меньшей мере один полисахарид (например, декстран), и где оболочка содержит по меньшей мере один полисахарид (например, аминодекстран), по меньшей мере один полимер (например, полиуретан) и диоксид кремния. В некоторых вариантах осуществления кор из оксида металла представляет собой коллоидный кор из оксида железа. В конкретных вариантах осуществления, одно или несколько средств включают антитело или его антигенсвязывающий фрагмент. В конкретных вариантах осуществления, одно или несколько средств включают антитело против CD3 антитело и антитело против CD28. В некоторых вариантах осуществления, стимулирующий реагент содержит антитело против CD3, антитело против CD28 и антитело против биотина. В некоторых вариантах осуществления, стимулирующий реагент содержит антитело против биотина. В некоторых вариантах осуществления, бусина имеет диаметр от приблизительно 3 мкм до приблизительно 10 мкм. В некоторых вариантах осуществления, бусина имеет диаметр от приблизительно 3 мкм до приблизительно 5 мкм. В конкретных вариантах осуществления, бусина имеет диаметр приблизительно 3,5 мкм.
[0642] В некоторых вариантах осуществления, стимулирующий реагент содержит одно или несколько средств, которые являются присоединенными к бусине, содержащей кор из оксида металла (например, внутренний кор из оксида железа) и оболочку (например, защитную оболочку), где оболочка содержит полистирол. В конкретных вариантах осуществления, бусины представляют собой монодисперсные, суперпарамагнитные бусины, содержащие суперпарамагнитный кор из железа, например, кор, содержащий магнетит (Fe3O4) и/или маггемит (γFe2O3), и полистирольную оболочку или покрытие. В некоторых вариантах осуществления, бусина является непористой. В некоторых вариантах осуществления, бусины содержат функционализированную поверхность, к которой присоединены одно или несколько средств. В конкретных вариантах осуществления, одно или несколько средств являются ковалентно связанными с бусинами на поверхности. В некоторых вариантах осуществления, одно или несколько средств включают антитело или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления, одно или несколько средств включают антитело против CD3 и антитело против CD28. В конкретных вариантах осуществления, бусины имеют плотность приблизительно 1,5 г/см3 и площадь поверхности от приблизительно 1 м2/г до приблизительно 4 м2/г. В конкретных вариантах осуществления; бусины представляют собой монодисперсные суперпарамагнитные бусины, имеющие диаметр приблизительно 4,5 мкм и плотность приблизительно 1,5 г/см3. В некоторых вариантах осуществления, бусины представляют собой монодисперсные суперпарамагнитные бусины, имеющие средний диаметр приблизительно 2,8 мкм и плотность приблизительно 1,3 г/см3.
E. Векторы и способы для генной инженерии
[0643] Полинуклеотиды (молекулы нуклеиновой кислоты), кодирующие рекомбинантные рецепторы, можно включать в векторы для генетической модификации клеток для экспрессии таких рецепторов. В некоторых вариантах осуществления, векторы или конструкции содержат один или несколько промоторов, функционально связанных с нуклеотидом, кодирующим полипептид или рецептор, для управления его экспрессией. В некоторых вариантах осуществления, промотор функционально связан с одной или несколькими молекулами нуклеиновой кислоты.
[0644] В некоторых случаях, вектор представляет собой вирусный вектор, такой как ретровирусный вектор, например, лентивирусный вектор или гаммаретровирусный вектор. В некоторых вариантах осуществления, полинуклеотид, такой как вектор, кодирующий рекомбинантный рецептор, вводят в композицию, содержащую культивированные клетки, например, посредством ретровирусной трансдукции, трансфекции или трансформации.
[0645] Различные способы введения генетически модифицированных компонентов, например, рекомбинантных рецепторов, например, CAR или TCR, хорошо известны и могут быть использованы с представленными способами и композициями. Иллюстративные способы включают способы переноса нуклеиновых кислот, кодирующих полипептиды или рецепторы, например, посредством вирусны векторов, например, ретровирусных или лентивирусных, невирусных векторов или транспозонов, например, системы транспозона Sleeping Beauty. Способы переноса генов могут включать трансдукцию, электропорацию или другой способ, осуществляющий перенос генов в клетку.
[0646] В некоторых вариантах осуществления, перенос генов осуществляют сначала посредством стимуляции клетки, например, посредством ее объединения со стимулом, который индуцирует ответ, такой как пролиферация, выживаемость и/или активация, например, как измерено по экспрессии цитокина или маркера активации, с последующей трансдукцией активированных клеток, и размножения в культуре до количеств, достаточных для клинических применений.
[0647] В некоторых контекстах, может являться желательной предосторожность против возможности того, что сверхэкспрессия стимулирующего фактора (например, лимфокина или цитокина) может потенциально приводить к нежелательному исходу или более низкой эффективности у индивида, например, фактора, ассоциированные с токсичностью у индивида. Таким образом, в некоторых контекстах, модифицированные клетки включают фрагменты генов, которые делают клетки чувствительными к отрицательному отбору in vivo, например, при введении в адоптивной иммунотерапии. Например, в некоторых аспектах, клетки модифицируют таким образом, что их можно уничтожать в результате изменения условия in vivo для пациента, которому их вводят. Поддающийся отрицательному отбору фенотип может возникать в результате вставки гена, придающего чувствительность к введенному средству, например, соединению. Поддающиеся отрицательному отбору гены включают ген тимидинкиназы вируса простого герпеса типа I (HSV–I TK) (Wigler et al., Cell II:223, I977), придающий чувствительность к ганцикловиру; ген клеточной гипоксантин–фосфорибозилтрансферазы (HPRT), ген клеточной аденин–фосфорибозилтрансфераза (APRT), ген бактериальной цитозиндезаминазы, (Mullen et al., Proc. Natl. Acad. Sci. USA. 89:33 (1992)).
[0648] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносят в клетки с использованием рекомбинантных инфекционных вирусных частиц, например, таких как векторы, происходящие из вируса обезьян 40 (SV40), аденовирусов, аденоассоциированного вируса (AAV). В некоторых вариантах осуществления, рекомбинантный нуклеиновые кислоты переносят в T–клетки с использованием рекомбинантных лентивирусных векторов или ретровирусных векторов, таких как гамма–ретровирусные векторы (см., например, Koste et al. (2014) Gene Therapy 2014 Apr 3. doi: 10.1038/gt.2014,25; Carlens et al. (2000) Exp Hematol 28(10): 1137–46; Alonso–Camino et al. (2013) Mol Ther Nucl Acids 2, e93; Park et al., Trends Biotechnol. 2011 November 29(11): 550–557.
[0649] В некоторых вариантах осуществления, полинуклеотид, кодирующий рекомбинантный рецептор и/или дополнительный полипептид, содержатся в векторе или могут быть клонированы в один или несколько вектор(ов). В некоторых вариантах осуществления, один или несколько вектор(ов) можно использовать для трансформации или трансфекции клетки–хозяина, например, клетки для модификации. Иллюстративные векторы включают векторы, разработанные для введения, размножения и распространения или для экспрессии, или для того и другого, такие как плазмиды и вирусные векторы. В некоторых аспектах, вектор представляет собой экспрессирующий вектор, например, рекомбинантный экспрессирующий вектор. В некоторых вариантах осуществления, рекомбинантные экспрессирующие векторы можно получать с использованием стандартных способов рекомбинантной ДНК.
[0650] В некоторых вариантах осуществления, вектор может представлять собой вектор из серий pUC (Fermentas Life Sciences), серий pBluescript (Stratagene, LaJolla, Calif.), серий pET (Novagen, Madison, Wis.), серий pGEX (Pharmacia Biotech, Uppsala, Sweden), или серий pEX (Clontech, Palo Alto, Calif.). В некоторых случаях, бактериофаговые векторы, такие как λG10, λGT11, λZapII (Stratagene), λEMBL4 и λNM1149, также можно использовать. В некоторых вариантах осуществления, можно использовать экспрессирующие векторы для растений, и они включают pBI01, pBI101.2, pBI101.3, pBI121 и pBIN19 (Clontech). В некоторых вариантах осуществления, экспрессирующие векторы для животных включают pEUK–Cl, pMAM и pMAMneo (Clontech).
[0651] В некоторых вариантах осуществления, вектор представляет собой вирусный вектор, такой как ретровирусный вектор. В некоторых вариантах осуществления, полинуклеотид, кодирующий рекомбинантный рецептор и/или дополнительный полипептид(ы), вводят в клетку посредством ретровирусных или лентивирусных векторов, или посредством транспозонов (см., например, Baum et al. (2006) Molecular Therapy: The Journal of the American Society of Gene Therapy. 13:1050–1063; Frecha et al. (2010) Molecular Therapy 18:1748–1757; и Hackett et al. (2010) Molecular Therapy 18:674–683).
[0652] В некоторых вариантах осуществления, транскрипционные единицы могут являться модифицированными в форме бицистронной единицы, содержащей IRES, что позволяет совместную экспрессию продуктов генов (например, кодирующих рекомбинантный рецептор и дополнительный полипептид) посредством матричной РНК с одного промотора. Альтернативно, в некоторых случаях, один промотор может управлять экспрессией РНК, содержащей, в одной открытой рамке считывания (ORF), два или три гена (например, кодирующий маркер и кодирующий рекомбинантный рецептор), отделенные друг от друга последовательностями, кодирующими саморасщепляющийся пептид (например, последовательностями 2A) или участок узнавания протеазы (например, фурина). ORF, таким образом, кодирует один полипептид, который, либо в ходе (в случае 2A), либо после трансляции, подвергается процессингу до индивидуальных белков. В некоторых случаях, пептид, такой как T2A, может заставлять рибосому пропускать (проскальзывание рибосомы) синтез пептидной связи на C–конце элемента 2A, что приводит к разделению между концом последовательности 2A и следующим ниже пептидом (см., например, de Felipe, Genetic Vaccines and Ther. 2:13 (2004) и de Felipe et al. Traffic 5:616–626 (2004)). Известны различные элементы 2A. Примеры последовательностей 2A, котрые можно использовать в способах и системе, описанных в настоящем описании, включают, без ограничения, последовательности 2A из вируса ящура (F2A, например, SEQ ID NO: 21), вируса ринита лошадей A (E2A, например, SEQ ID NO: 20), вируса Thosea asigna (T2A, например, SEQ ID NO: 6 или 17) и тешовируса–1 свиней (P2A, например, SEQ ID NO: 18 или 19), как описано в Публикации Патента США No. 20070116690.
[0653] В некоторых вариантах осуществления, рекомбинантный рецептор, например, CAR, находится под контролем промотора. В некоторых вариантах осуществления, вектор включает промотор. В некоторых вариантах осуществления, промотор представляет собой или содержит конститутивный промотор. Иллюстративные конститутивные промоторы включают, например, ранний промотор вируса обезьян 40 (SV40), немедленный ранний промотор цитомегаловируса (CMV), промотор убиквитина C человека (UBC), промотор фактора элонгации 1α человека (EF1α), промотор фосфоглицераткиназы 1 мыши (PGK) и промотор β–актина курицы в сочетании с ранним энхансером CMV (CAGG). В некоторых вариантах осуществления, конститутивный промотор представляет собой синтетический или модифицированный промотор. В некоторых вариантах осуществления, промотор представляет собой или содержит промотор MND, синтетический промотор содержащий область U3 из модифицированного LTR MoMuLV с энхансером вируса миелопролиферативной саркомы (см. Challita et al. (1995) J. Virol. 69(2):748–755). В некоторых вариантах осуществления, промотор представляет собой тканеспецифический промотор. В другом варианте осуществления, промотор представляет собой вирусный промотор. В другом варианте осуществления, промотор представляет собой невирусный промотор. В некоторых вариантах осуществления, иллюстративные промоторы могут включать, но без ограничения, промотор фактора элонгации 1 альфа человека (EF1α) или его модифицированную форму, или промотор MND.
[0654] В некоторых вариантах осуществления, промотор представляет собой регулируемый промотор (например, индуцируемый промотор). В некоторых вариантах осуществления, промотор представляет собой индуцируемый промотор или репрессируемый промотор. В некоторых вариантах осуществления, промотор содержит последовательность оператора Lac, последовательность тетрациклинового оператора, последовательность галактозного оператора или последовательность доксицилинового оператора, или представляет собой их аналог, или является способным к связыванию или узнаванию репрессором Lac или тетрациклиновым репрессор, или их аналогом. В некоторых вариантах осуществления, полинуклеотид не включает регуляторный элемент, например, промотор.
[0655] В некоторых случаях, последовательность нуклеиновой кислоты, кодирующая рекомбинантный рецептор, содержит сигнальную последовательность, кодирующую сигнальный пептид. В некоторых аспектах, сигнальная последовательность может кодировать сигнальный пептид, происходящий из нативного полипептида. В других аспектах, сигнальная последовательность может кодировать гетерологичный или неприродный сигнальный пептид, такой как иллюстративный сигнальный пептид из альфа–цепи GMCSFR, указанный в SEQ ID NO:25 и кодируемый нуклеотидной последовательностью, указанной в SEQ ID NO:24. В некоторых случаях, последовательность нуклеиновой кислоты, кодирующая рекомбинантный рецептор, например, химерный антигенный рецептор (CAR), содержит сигнальную последовательность, кодирующую сигнальный пептид. Неограничивающие иллюстративные сигнальные пептиды включают, например, сигнальный пептид альфа–цепи GMCSFR, указанный в SEQ ID NO: 25 и кодируемый нуклеотидной последовательностью, указанной в SEQ ID NO:24, или сигнальный пептид CD8–альфа, указанный в SEQ ID NO:26.
[0656] В некоторых вариантах осуществления, полинуклеотид содержит последовательность нуклеиновой кислоты, кодирующую один или несколько дополнительных полипептидов, например, один или несколько маркер(ов) и/или одну или несколько эффекторных молекул. В некоторых вариантах осуществления, один или несколько маркер(ов) включает маркер трансдукции, суррогатный маркер и/или маркер для отбора. Среди введенных дополнительных последовательностей нуклеиновой кислоты, например, кодирующих один или несколько дополнительный полипептид(ов), включены последовательности нуклеиновой кислоты, которые могут улучшать эффективность терапии, например, посредством стимуляции жизнеспособности и/или функции перенесенных клеток; последовательности нуклеиновой кислоты для предоставления генетического маркера для отбора и/или оценки клеток, например, для оценки выживаемости или локализации in vivo; последовательности нуклеиновой кислоты для улучшения безопасности, например, посредством придания клетки чувствительности к отрицательному отбору in vivo, как описано в Lupton S. D. et al., Mol. and Cell Biol., 11:6 (1991); и Riddell et al., Human Gene Therapy 3:319–338 (1992); см. также WO 1992008796 и WO 1994028143, описывающие использование бифункциональных поддающихся отбору слитых генов, полученных в результате слияния доминтантного положительного селективного маркера с отрицательным селективным маркером, и Патент США No. 6040177.
[0657] В некоторых вариантах осуществления, один промотор может управлять экспрессией РНК, содержащей, в одной открытой рамке считывания (ORF), два или три гена (например, кодирующий молекулу, вовлеченную в модуляцию метаболического пути, и кодирующий рекомбинантный рецептор), отделенные друг от друга последовательностями, кодирующими саморасщепляющийся пептид (например, последовательностями 2A) или участок узнавания протеазы (например, фурина). ORF, таким образом, кодирует один полипептид, который, либо в ходе (в случае 2A), либо после трансляции, подвергается процессингу до индивидуальных белков. В некоторых случаях, пептид, такой как T2A, может заставлять рибосому пропускать (проскальзывание рибосомы) синтез пептидной связи на C–конце элемента 2A, что приводит к разделению между концом последовательности 2A и следующим ниже пептидом (см., например, de Felipe. Genetic Vaccines and Ther. 2:13 (2004) и deFelipe et al. Traffic 5:616–626 (2004)). Известно множество элементов 2A. Примеры последовательностей 2A, котрые можно использовать в способах и нуклеиновых кислотах, описанных в настоящем описании, включают, без ограничения, последовательности 2A из вируса ящура (F2A, например, SEQ ID NO: 22), вируса ринита лошадей A (E2A, например, SEQ ID NO: 21), вируса Thosea asigna (T2A, например, SEQ ID NO: 6 или 18), и тешовируса–1 свиней (P2A, например, SEQ ID NO: 19 или 20), как описано в Публикации Патента США No. 20070116690.
[0658] В некоторых вариантах осуществления, вектор содержит последовательность нуклеиновой кислоты, кодирующую один или несколько маркер(ов). В некоторых вариантах осуществления, один или несколько маркер(ов) представляет собой маркер трансдукции, суррогатный маркер и/или маркер для отбора.
[0659] В некоторых вариантах осуществления, маркер представляет собой маркер трансдукции или суррогатный маркер. Маркер трансдукции или a суррогатный маркер можно использовать для детекции клеток, в которые введен полинуклеотид, например, a полинуклеотид, кодирующий рекомбинантный рецептор. В некоторых вариантах осуществления, маркер трансдукции может показвать или подтверждать модификацию клетки. В некоторых вариантах осуществления, суррогатный маркер представляет собой белок, который подвергают совместной экспрессии на поверхности клетки с рекомбинантным рецептором, например, CAR. В конкретных вариантах осуществления, такой суррогатный маркер представляет собой поверхностный белок, модифицированный, чтобы иметь небольшую активность или не иметь активности. В конкретных вариантах осуществления, суррогатный маркер кодирован тем же полинуклеотидом, который кодирует рекомбинантный рецептор. В некоторых вариантах осуществления, последовательность нуклеиновой кислоты, кодирующая рекомбинантный рецептор, является функционально связанной с последовательностью нуклеиновой кислоты, кодирующей маркер, необязательно, отделенной внутренним участком связывания рибосомы (IRES), или нуклеиновой кислотой, кодирующей саморасщепляющийся пептид или пептид, который вызывает проскальзывание рибосомы, такой как последовательность 2A, например, T2A, P2A, E2A или F2A. Внешние маркерные гены можно, в некоторых случаях, использовать в сочетании с модифицированной клеткой, чтобы позволять детекцию или отбор клеток и, в некоторых случаях, также стимулировать самоубийство клетки.
[0660] Иллюстративные суррогатные маркеры могут включать укороченные формы полипептидов поверхности клетки, такие как укороченные формы, которые являются нефункциональными и не передают или являются неспособными передавать сигнал, или сигнал, обычно передаваемый полноразмерной формой полипептида поверхности клетки, и/или которые не подвергаются или являются неспособными подвергаться интернализации. Иллюстративные укороченные полипептиды поверхности клетки включают укороченные формы факторов роста или других рецепторов, такие как укороченный рецептор 2 эпидермального фактора роста человека (tHER2), укороченный рецептор эпидермального фактора роста (tEGFR, иллюстративная последовательность tEGFR, указанная в SEQ ID NO:7 или 23) или простатспецифический мембранный антиген (PSMA) или их модифицированную форму. tEGFR может содержать эпитоп, узнаваемый антителом цетуксимабом (эрбитуксом®) или другим терапевтическим антителом против EGFR или связывающей молекулой, который можно использовать для идентификации или отбора клеток, модифицированных с использованием конструкции tEGFR и кодируемого экзогенного белка, и/или для исключения или отделения клеток, экспрессирующих кодируемый экзогенный белок. См. Патент США No. 8802374 и Liu et al., Nature Biotech. 2016 April; 34(4): 430–434). В некоторых аспектах, маркер, например, суррогатный маркер, включает весь или часть (например, укороченную форму) CD34, NGFR, CD19 или укороченный CD19, например, укороченный не относящийся к человеку CD19, или рецептор эпидермального фактора роста (например, tEGFR).
[0661] В некоторых вариантах осуществления, маркер представляет собой или содержит флуоресцентный белок, такой как зеленый флуоресцентный белок (GFP), улучшенный зеленый флуоресцентный белок (EGFP), такой как суперсвернутый GFP (sfGFP), красный флуоресцентный белок (RFP), такой как tdTomato, mCherry, mStrawberry, AsRed2, DsRed или DsRed2, голубой флуоресцентный белок (CFP), сине–зеленый флуоресцентный белок (BFP), улучшенный синий флуоресцентный белок (EBFP) и желтый флуоресцентный белок (YFP), и их варианты, включая видовые варианты, мономерные варианты и подвергнутые оптимизации кодонного состава и/или улучшенные варианты флуоресцентных белков. В некоторых вариантах осуществления, маркер представляет собой или содержит фермент, такой как люцифераза, ген lacZ из E. coli, щелочная фосфатаза, секретируемая эмбриональная щелочная фосфатаза (SEAP), хлорамфениколацетилтрансфераза (CAT). Иллюстративные гены светоиспускающих репортеров включают гены люциферазы (luc), β–галактозидазы, хлорамфениколацетилтрансферазы (CAT), β–глюкуронидазы (GUS) или их варианты.
[0662] В некоторых вариантах осуществления, маркер представляет собой маркер для отбора. В некоторых вариантах осуществления, маркер для отбора представляет собой или содержит a полипептид, придающий устойчивость к экзогенным средствам или лекарственным средствам. В некоторых вариантах осуществления, маркер для отбора представляет собой ген устойчивости к антибиотику. В некоторых вариантах осуществления, маркер для отбора представляет собой ген устойчивости к антибиотику, придающий устойчивость к антибиотику клетке млекопитающего. В некоторых вариантах осуществления, маркер для отбора представляет собой или содержит ген устойчивости к пуромицину, ген устойчивости к гигромицину, ген устойчивости к бластицидину, ген устойчивости к неомицину, ген устойчивости к генетицину или ген устойчивости к зеоцину или их модифицированную форму.
[0663] В некоторых вариантах осуществления, ретровирусный вектор имеет последовательность длинного концевого повтора (LTR), например, из ретровирусного вектора, происходящую из вируса лейкоза мышей Молони (MoMLV), вируса миелопролиферативной саркомы (MPSV), вируса эмбриональных стволовых клеток мыши (MESV), вируса стволовых клеток мыши (MSCV), вируса, образующего очаги в селезенке (SFFV), или аденоассоциированного вируса (AAV). Большинство ретровирусных векторов происходят из ретровирусов мышей. В некоторых вариантах осуществления, ретровирусы включают ретровирусы, происходящие из любого источника среди клеток птиц или млекопитающиих. Ретровирусы, как правило, являются амфотропными, что означает, что они являются способными инфицировать клетки–хозяева из нескольких видов, включая человека. В одном варианте осуществления, геном, подлежащим экспрессии, заменяют ретровирусные последовательности gag, pol и/или env. Описан ряд иллюстративных ретровирусных систем (например, Патенты США No. 5219740; 6207453; 5219740; Miller and Rosman (1989) BioTechniques 7:980–990; Miller, A. D. (1990) Human Gene Therapy 1:5–14; Scarpa et al. (1991) Virology 180:849–852; Burns et al. (1993) Proc. Natl. Acad. Sci. USA 90:8033–8037; и Boris–Lawrie и Temin (1993) Cur. Opin. Genet. Develop. 3:102–109.
[0664] Способы лентивирусной трансдукции известны. Иллюстративный способы описаны, например, в Wang et al. (2012) J. Immunother. 35(9): 689–701; Cooper et al. (2003) Blood. 101:1637–1644; Verhoeyen et al. (2009) Methods Mol Biol. 506: 97–114; и Cavalieri et al. (2003) Blood. 102(2): 497–505. В некоторых вариантах осуществления, полинуклеотид, кодирующий рекомбинантный рецептор и/или один или несколько дополнительный полипептид(ов), вводят в композицию, содержащую культивированные клетки, например, посредством ретровирусной трансдукции, трансфекции или трансформации.
[0665] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносят в T–клетки посредством электропорации (см., например, Chicaybam et al, (2013) PLoS ONE 8(3): e60298 и Van Tedeloo et al. (2000) Gene Therapy 7(16): 1431–1437). В некоторых вариантах осуществления, рекомбинантный нуклеиновые кислоты переносят в T–клетки посредством транспозиции (см., например, Manuri et al. (2010) Hum Gene Ther 21(4): 427–437; Sharma et al. (2013) Molec Ther Nucl Acids 2, e74; и Huang et al. (2009) Methods Mol Biol 506: 115–126). Другие способы введения и экспрессии генетического материала в иммуноциты включают трансфекцию с использованием фосфата кальция (например, как описано в Current Protocols in Molecular Biology, John Wiley & Sons, New York. N.Y.), слияние протопластов, опосредованную катионными липосомами трансфекцию; бомбардировку микрочастицами с использованием частиц вольфрама (Johnston, Nature, 346: 776–777 (1990)); и копреципитацию фосфата стронция и ДНК (Brash et al., Mol. Cell Biol., 7: 2031–2034 (1987)). В некоторых аспектах, a стадия промывки проводят в камере для центрифугирования, например, those производимые и продаваемые by Biosafe SA, включая камеры для использования с системой Sepax® и Sepax® 2, включая камеры для центрифугирования A–200/F и A–200 в соответствии с инструкциями производителя.
[0666] Другие способы и векторы для переноса нуклеиновых кислот, кодирующих рекомбинантные продукты, представляют собой способы, описанные, например, в Публикации международной патентной заявки No.: WO2014055668, и Патент США No. 7446190.
[0667] В некоторых вариантах осуществления, клетки, например, T–клетки, можно трансфицировать либо во время, либо после размножения, например, с использованием T–клеточного рецептора (TCR), или химерного рецептора антигена (CAR). Эту трансфекцию для введения гена желательного полипептида или рецептора можно проводить, например, с использованием любого пригодного ретровирусного вектора. Генетически модифицированную популяцию клеток можно затем освобождать от исходного стимула (например, стимула CD3/CD28) и затем стимулировать с использованием второго типа стимула например, с использованием нового введенного рецептора). Этот второй тип стимула может включать антигенный стимул в форме пептида/молекулы MHC, родственный (перекрестно сшивающий) лиганд для генетически введенного рецептора (например, природный лиганд CAR) или любой лиганд (такой как антитело), который напрямую связывается в пределах каркаса нового рецептора (например, узнающий константные области в рецепторе). См., например, Cheadle et al, «Chimeric antigen receptors for T–cell based therapy» Methods Mol Biol. 2012; 907:645–66 или Barrett et al., Chimeric Antigen Receptor Therapy for Cancer Annual Review of Medicine Vol. 65: 333–347 (2014).
[0668] Среди введенных дополнительных нуклеиновых кислот, например, генов для введения, включены нуклеиновые кислоты, которые могут улучшать эффективность терапии, например, посредством стимуляции жизнеспособности и/или функции перенесенных клеток; гены для предоставления генетического маркера для отбора и/или оценки клеток, например, для оценки выживаемости или локализации in vivo; гены для улучшения безопасности, например, посредством придания клетки чувствительности к отрицательному отбору in vivo, как описано в Lupton S. D. et al., Mol. and Cell Biol., 11:6 (1991); и Riddell et al., Human Gene Therapy 3:319–338 (1992); см. также публикации PCT/US91/08442 и PCT/US94/05601 от Lupton et al., описывающие использование бифункциональных поддающихся отбору слитых генов, полученных в результате слияния доминантного положительного селективного маркера с отрицательным селективным маркером. См., например, Riddell et al., Патент США No. 6040177, в колонках 14–17.
[0669] В некоторых вариантах осуществления, клетки инкубируют и/или культивируют до или в сочетании с генетической модификацией. Стадии инкубации могут включать культивацию, культивирование, стимуляцию, активацию и/или размножение. Инкубацию и/или модификацию можно проводить в культуральном сосуде, таком как единица, камера, лунка, колонка, пробирка, комплект трубок, клапан, флакон, культуральная чашка, пакет или другой контейнер для культивирования или культивации клеток. В некоторых вариантах осуществления, композиции или клетки инкубируют в присутствии стимулирующих условий или стимулирующего средства. Такие условия включают условия, разработанные для индукции пролиферации, размножения, активации и/или выживаемости клеток в популяции, для имитации воздействия антигена и/или для примирования клеток для генетической модификации, например, для введения рекомбинантного рецептора антигена. В некоторых вариантах осуществления, одну или несколько из стадий инкубации можно проводить с использованием биореактора с качанием, такого как биореактор WAVE™ (GE Healthcare) или BIOSTAT® RM (Sartorius). В некоторых вариантах осуществления, одну или несколько из стадий инкубации можно проводить с использованием статического биореактора или камеры дл инкубации. В конкретных вариантах осуществления, средство, уменьшающее усилие сдвига, например, полоксамер, можно добавлять в композицию, если биореактор с качанием используют для одной или нескольких стадий инкубации.
[0670] В некоторых случаях, можно использовать вектор, не требующий, чтобы клетки, например, T–клетки, являлись активированными. В некоторых таких случаях, клетки можно отбирать и/или трансдуцировать до активации. Таким образом, клетки можно модифицировать до или после культивирования клеток, и, в некоторых случаях, во время или в ходе по меньшей мере части культивирования.
[0671] Условия могут включать одно или несколько из конкретных сред, температуры, содержания кислорода, содержания диоксида углерода, времени, средств, например, питательных веществ, аминокислот, антибиотиков, ионов и/или стимулирующих факторов, таких как цитокины, хемокины, антигены, связывающие паттерны, слитые белки, рекомбинантные растворимые рецепторы, и любые другие средства, разработанные для активации клеток. В некоторых аспектах, клетки инкубируют в присутствии одного или нескольких цитокинов, и в некоторых вариантах осуществления, можно использовать коктейль цитокинов, например, как описано в Публикации международной патентной заявки номер WO2015157384. В некоторых вариантах осуществления, клетки инкубируют с одним или несколькими цитокинами и/или с коктейлем цитокинов до, во время или после трансдукции.
[0672] В некоторых вариантах осуществления, стимулирующие условия или средства включают одно или несколько средств, например, лиганд, способный активировать внутриклеточный передающий сигналы домен комплекса TCR. В некоторых аспектах, средство запускает или инициирует внутриклеточный каскад передачи сигналов TCR/CD3 в T–клетке. Такие средства могут включать антитела, такие как антитела, специфические для компонента TCR, например, антитело против CD3. В некоторых вариантах осуществления, стимулирующие условия включают одно или несколько средств, например, лиганд, способный стимулировать костимулирующий рецептор, например, антитело против CD28. В некоторых вариантах осуществления, такие средства и/или лиганды могут быть связаны с твердой подложкой, такой как бусина, и/или с одним или несколькими цитокинами. Необязательно, способ размножения может дополнительно включать стадию добавления антитела против CD3 и/или антитела против CD28 в культуральную среду (например, в концентрации по меньшей мере приблизительно 0,5 нг/мл). В некоторых вариантах осуществления, стимулирующие средства включают IL–2, и/или IL–15, например, в концентрации IL–2 по меньшей мере приблизительно 10 единиц/мл. В конкретных вариантах осуществления, стимулирующие условия включают инкубацию с любыми стимулирующими реагентами, описанными в настоящем описании, такими как описанные в разделе V–D–1.
[0673] В некоторых аспектах, инкубацию проводят в соответствии с такими способами, как описано в Патенте США No. 60401 77 от Riddell et al., Klebanoff et al.(2012) J Immunother. 35(9): 651–660, Terakuraet al. (2012) Blood.1:72–82, и/или Wang et al. (2012) J Immunother. 35(9):689–701. В некоторых аспектах, трансдукцию проводят с использованием системы, устройства, аппарата и/или способа, как описано в Публикации международной патентной заявки номер WO2016/073602 или US 2016/0122782, полное содержание которых приведено в качестве ссылки. В некоторых вариантах осуществления, трансдукцию проводят, в соответствии со способами, описанными в Публикации международной патентной заявки номер WO 2015/164675, полное содержание которой приведено в качестве ссылки.
[0674] В некоторых вариантах осуществления, T–клетки размножают посредством добавления в композицию для начала культивирования фидерных клеток, таких как не делящиеся мононуклеарные клетки периферической крови (PBMC), (например, таким образом, что полученная популяция клеток содержит по меньшей мере приблизительно 5, 10, 20 или 40 или более фидерных клеток PBMC для каждого T–лимфоцита в исходной популяции, подлежащей размножению); и инкубации культуры (например, в течение времени, достаточного для размножения этих количеств T–клеток). В некоторых аспектах, не делящиеся фидерные клетки могут содержать облученные гамма–излучением фидерные клетки PBMC. В некоторых вариантах осуществления, PBMC облучают с использованием гамма–излучения в диапазоне от приблизительно 3000 до 3600 рад для предотвращения деления клеток. В некоторых аспектах, фидерные клетки добавляют в культуральную среду перед добавлением популяций T–клеток.
[0675] В некоторых вариантах осуществления, стимулирующие условия включают температуру, пригодную для роста T–лимфоцитов человека, например, по меньшей мере приблизительно 25 градусов Цельсия, как правило, по меньшей мере приблизительно 30 градусов, и, как правило, при или приблизительно при 37 градусов Цельсия.. Необязательно, инкубация может дополнительно включать добавление не делящиеся трансформированных EBV лимфобластоидных клеток (LCL) в качестве фидерных клеток. LCL можно облучать с использованием гамма–излучения в диапазоне от приблизительно 6000 до 10000 рад. Фидерные клетки LCL, в некоторых аспектах, предоставляют в любом пригодном количестве, например, в соотношении фидерных клеток LCL к исходным T–лимфоцитам по меньшей мере приблизительно 10:1.
[0676] В некоторых вариантах осуществления, способы получения включают стадии замораживания, например, криоконсервации, клеток, либо до, либо после выделения, инкубации и/или модификации. В некоторых вариантах осуществления, на стадии замораживания и последующего размораживания удаляют гранулоциты и, до некоторой степени, моноциты в популяции клеток. В некоторых вариантах осуществления, клетки суспендируют в растворе для замораживания, например, после стадии промывки для удаления плазмы и тромбоцитов. В некоторых аспектах, можно использовать любой из множества известных растворов и параметров для замораживания. Один пример включает использование PBS, содержащего 20% DMSO и 8% сывороточный альбумин человека (HSA), или других пригодных сред для замораживания клеток. Затем это разводят 1:1 средой, так чтобы конечные концентрации DMSO и HSA составляли 10% и 4%, соответственно. Затем клетки, как правило, замораживают до −80°C со скоростью 1° в минуту и сохраняют в паровой фазе в сосуде для хранения с жидким азотом. В некоторых вариантах осуществления, композицию заключают в пакет, пригодный для криоконсервации (например, пакеты для замораживания CryoMacs®, Miltenyi Biotec). В некоторых вариантах осуществления, композицию заключают в ампулу, пригодную для криоконсервации (например, ампулы CellSeal®, Cook Regentec). В некоторых вариантах осуществления, стадии и/или реагенты для замораживания представляют собой или включают любые из стадий и/или реагентов для замораживания, которые являются описанными в настоящем описании.
[0677] В конкретных вариантах осуществления, клетки замораживают, например, после стадии промывки, например, для удаления плазмы и тромбоцитов. В некоторых вариантах осуществления, клетки замораживают до, после и/или во время любой из стадий, ассоциированных с изготовлением и/или получением клеток, например, CD4+ и/или CD8+ T–клеток, которые экспрессируют рекомбинантный рецептор, например, CAR. В конкретных вариантах осуществления, такие стадии могут включать любые стадии, ассоциированные с получением модифицированных клеток, включая, но без ограничения, отбор и/или выделение подгруппы клеток, например, CD4+ и/или CD8+ T–клеток, стимуляцию и/или размножение клеток, например, T–клеток или их подгруппы, или трансфекцию или трансдукцию клеток. В некоторых вариантах осуществления, клетки представляют собой клетки из образца после афереза, отобранного у индивида, до отбора и/или выделения клеток, стимуляции и/или размножения клеток, или трансфекции или трансдукции клеток. В конкретных вариантах осуществления, клетки замораживают после завершения процесса модификации, например, после процесса, включающего одну или несколько стадий выделения, отборов, стимуляции, активации, трансдукции, трансфекции и/или размножения.
[0678] В некоторых вариантах осуществления, клетки суспендируют в растворе для замораживания, например, в криопротекторе и/или в растворе, содержащем криопротектор. В некоторых аспектах, можно использовать любой из множества известных растворов и параметров для замораживания, включая растворы для замораживания, содержащие среды или растворы для криоконсервации или перехода в стекловидное состояние, содержащие криопротектор. Пригодные криопротекторы включают, но без ограничения, диметилсульфоксид (DMSO), глицерин, гликоль, пропиленгликоль, этиленгликоль, пропандиол, полиэтиленгликоль (PEG), 1,2–пропандиол (PROH) или их смесь. В некоторых примерах, раствор для криоконсервации может содержать один или несколько не проникающих в клетку криоконсервантов, включая, но без ограничения, поливинилпирролидон, гидроксиэтилкрахмал, полисахарид, моносахарид, альгинат, трегалозу, раффинозу, декстран, человеческий сывороточный альбумин, фиколл, липопротеины, поливинилпирролидон, гидроксиэтил крахмал, аутологичную плазму или их смесь. В некоторых вариантах осуществления, клетки суспендируют в растворе для замораживания с конечной концентрацией криопротектора между приблизительно 1% и приблизительно 20%, между приблизительно 3% и приблизительно 9%, или между приблизительно 6% и приблизительно 9% по объему, включая каждое. В конкретных вариантах осуществления, конечная концентрация криопротектора в растворе для замораживания составляет приблизительно 3%, приблизительно 4%, приблизительно 5%, приблизительно 5,5%, приблизительно 6%, приблизительно 6,5%, приблизительно 7%, приблизительно 7,5%, приблизительно 8%, приблизительно 8,5%, приблизительно 9%, приблизительно 9,5%, или приблизительно 10% по объему.
[0679] В некоторых вариантах осуществления, клетки, например, замораживают при конкретной плотности клеток, например, известной или контролируемой плотности клеток. В конкретных вариантах осуществления, плотность клеток в ходе процесса замораживания может влиять на гибель клеток и/или повреждение клеток, возникающие во время и/или в результате процесса замораживания.
[0680] Например, в конкретных вариантах осуществления, плотность клеток влияет на равновесие, например, осмотическое равновесие, с окружающей средой в ходе процесса замораживания. В некоторых вариантах осуществления, это равновесие представляет собой, включает и/или приводит к дегидратации. В конкретных вариантах осуществления, дегидратация представляет собой или включает клеточную дегидратацию, которая возникает по мере контакта, объединения и/или инкубации с раствором для замораживания, например, DMSO и/или содержащим DMSO раствором. В конкретных вариантах осуществления, дегидратация представляет собой или включает дегидратацию, возникающую в результате нуклеации и увеличения кристаллов льда во внеклеточном пространстве, например, посредством уменьшения эффективной концентрации жидкой воды, воздействующей на клетки. В некоторых вариантах осуществления, клетки замораживают при плотности клеток, приводящей к более медленной и/или менее быстрой дегидратации, чем для клеток, которые замораживают при другой, например, более высокой или низкой, плотности клеток. В некоторых вариантах осуществления, клетки замораживают при плотности клеток, приводящей приблизительно к, по меньшей мере к или к на 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 125%, 150%, 175%, 200%, в 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 10 раз, 50 раз или 100 раз более медленной дегидратации, чем для клеток, замороженных при другой плотности клеток, например, более высокой или низкой, в таких же или сходных условиях.
[0681] В некоторых вариантах осуществления, криопротектор представляет собой DMSO. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания с конечной концентрацией DMSO между приблизительно 1% и приблизительно 20%, между приблизительно 3% и приблизительно 9%, или между приблизительно 6% и приблизительно 9% по объему, включая каждое. В конкретных вариантах осуществления, конечная концентрация DMSO в растворе для замораживания составляет приблизительно 3%, приблизительно 4%, приблизительно 5%, приблизительно 5,5%, приблизительно 6%, приблизительно 6,5%, приблизительно 7%, приблизительно 7,5%, приблизительно 8%, приблизительно 8,5%, приблизительно 9%, приблизительно 9,5% или приблизительно 10% по объему.
[0682] В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности между или между приблизительно 0,1×106 клеток/мл и приблизительно 5,000×106 клеток/мл, между или между приблизительно 1×106 клеток/мл и приблизительно 500×106 клеток/мл, между или между приблизительно 5×106 клеток/мл и приблизительно 150×106 клеток/мл, между или между приблизительно 10×106 клеток/мл и приблизительно 70×106 клеток/мл, или между или между приблизительно 15×106 клеток/мл и приблизительно 60×106 клеток/мл, включая каждое. В некоторых вариантах осуществления, клетки представляют собой жизнеспособные клетки.
[0683] В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности между или между приблизительно 1×106 клеток/мл и приблизительно 1×108 клеток/мл, между приблизительно 1×106 клеток/мл и приблизительно 2×107 клеток/мл, между приблизительно 1×107 клеток/мл и приблизительно 5 ×107 клеток/мл, или между приблизительно 1×107 клеток/мл и 5×107 клеток/мл, включая каждое. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности приблизительно 1×106 клеток/мл, приблизительно 2×106 клеток/мл, приблизительно 5×106 клеток/мл, приблизительно 1×107 клеток/мл, приблизительно 1,5×107 клеток/мл, приблизительно 2×107 клеток/мл, приблизительно 2,5×107 клеток/мл, приблизительно 2,5×107 клеток/мл, приблизительно 2,5×107 клеток/мл, приблизительно 3×107 клеток/мл, приблизительно 3,5×107 клеток/мл, приблизительно 4×107 клеток/мл, приблизительно 4,5×107 клеток/мл, или приблизительно 5×107 клеток/мл, включая каждое. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности между приблизительно 1,5×107 клеток/мл и приблизительно 6×107 клеток/мл, включительно. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности по меньшей мере приблизительно 1×107 клеток/мл. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности по меньшей мере приблизительно 1,5×107 клеток/мл. В некоторых вариантах осуществления, клетки представляют собой жизнеспособные клетки.
[0684] В некоторых вариантах осуществления, клетки замораживают в контейнере. В конкретных вариантах осуществления, контейнер представляет собой контейнер для замораживания и/или контейнер для криопротекции. Контейнеры, пригодные для криозамораживания, включают, но без ограничения, ампулы, пакеты, например, пластиковые пакеты и трубки. В конкретных вариантах осуществления, клетки, например, клетки из одной и той же композиции клеток, такой как композиция клеток, содержащая экспрессирующие CAR клетки, замораживают в 1, 2, 3, 4, 5, 6, 7, 8, 9 10 или более чем 10 отдельных контейнерах. Например, в некоторых вариантах осуществления, клетки и/или композицию клеток суспендируют в некотором объеме, например, в объеме раствора, раствора для замораживания и/или криопротектора, и он превышает объем, подходящий для контейнера, и таким образом, объем помещают в два или более контейнера. В некоторых вариантах осуществления, объем составляет, составляет приблизительно или составляет менее чем 100 мл, 50 мл, 25 мл, 20 мл, 15 мл, 10 мл, 5 мл или менее чем 5 мл, и клетки замораживают в двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти или более десяти отдельных ампул. В конкретных вариантах осуществления, одинаковый объем клеток помещают в каждую ампулу. В некоторых вариантах осуществления, ампулы представляют собой идентичные ампулы, например, ампулы из одного и того же цикла, модели и/или партии изготовления. В конкретных вариантах осуществления, объем составляет, составляет приблизительно или составляет более чем 10 мл, 15 мл, 20 мл, 25 мл, 30 мл, 40 мл, 50 мл, 60 мл, 70 мл, 80 мл, 90 мл, 100 мл, 120 мл, 150 мл, 200 мл или более чем 200 мл, и клетки замораживают в двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти или более десяти отдельных пакетов. В конкретных вариантах осуществления, одинаковый объем клеток помещают в каждый пакет. В некоторых вариантах осуществления, пакеты представляют собой идентичные пакеты, например, пакеты из одного и того же цикла, модели и/или партии изготовления.
[0685] В некоторых вариантах осуществления, контейнер представляет собой ампулу. В конкретных вариантах осуществления, контейнер представляет собой ампулу с объемом заполнения, составляющим, составляющим, приблизительно или составляющим по меньшей мере 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл, 5 мл, 6 мл, 7 мл, 8 мл, 9 мл, 10 мл, 11 мл, 12 мл, 13 мл, 14 мл, 15 мл, 16 мл, 17 мл, 18 мл, 19 мл, 20 мл, 25 мл, 30 мл, 35 мл, 40 мл, 45 мл или 50 мл. В некоторых вариантах осуществления, ампула имеет объем заполнения между 1 мл и 120 мл, 1 мл и 20 мл, 1 мл и 5 мл, 1 мл и 10 мл, 1 мл и 40 мл, или 20 мл и 40 мл, включая каждое. В некоторых вариантах осуществления, ампула представляет собой ампулу для замораживания, ампулу для криопротекции и/или крио ампулу. Пригодные ампулы известны, и включают, но без ограничения, ампулы CellSeal® (Cook Regentec), и ампулы описанное в Патентах США No: US 8936905, US 9565854 и US 8709797, полное содержание которых, таким образом, приведено в качестве ссылки.
[0686] В конкретных вариантах осуществления, контейнер представляет собой пакет. В конкретных вариантах осуществления, контейнер представляет собой пакет с объемом заполнения, составляющим, составляющим приблизительно или составляющим по меньшей мере 0,5 мл, 1 мл, 2 мл, 3 мл, 4 мл, 5 мл, 6 мл, 7 мл, 8 мл, 9 мл, 10 мл, 11 мл, 12 мл, 13 мл, 14 мл, 15 мл, 16 мл, 17 мл, 18 мл, 19 мл, 20 мл, 25 мл, 30 мл, 35 мл, 40 мл, 45 мл или 50 мл. В некоторых вариантах осуществления, пакет имеет объем заполнения между 1 мл и 120 мл, 1 мл и 20 мл, 1 мл и 5 мл, 1 мл и 40 мл, 20 мл и 40 мл, 1 мл и 70 мл, или 50 мл и 70 мл, включая каждое. В некоторых вариантах осуществления, пакет заполняют объемом, составляющим, составляющим приблизительно или составляющим менее чем 100 мл, 75 мл, 70 мл, 50 мл, 25 мл, 20 мл, или 10 мл. Пригодные пакеты известны, и включают, но без ограничения, пакеты для замораживания CryoMacs® (Miltenyi Biotec). В конкретных вариантах осуществления, объем представляет собой объем при комнатной температуре. В некоторых вариантах осуществления, объем представляет собой объем при между 37°C и 4°C, 16°C и 27°C, включительно, или при, при приблизительно, или при по меньшей мере 16°C, 17°C, 18°C, 19°C, 20°C, 21°C, 22°C, 23°C, 24°C, 25°C, 26°C, 27°C, 28°C, 29°C, 30°C, 31°C, 32°C, 33°C, 34°C, 35°C, 36°C или 37°C. В некоторых вариантах осуществления, объем представляет собой объем при 25°C.
[0687] В некоторых вариантах осуществления, клетки в объеме среды или раствора, например, раствора для замораживания, между 1 мл и 20 мл, замораживают в одной или нескольких ампулах, включительно. В некоторых вариантах осуществления, одна или несколько ампул имеют объем заполнения между 1 мл и 5 мл, включительно. В конкретных вариантах осуществления, клетки в объеме среды или раствора, например, раствора для замораживания, между 20 мл и 120 мл, включительно, замораживают в одном или нескольких пакетах. В конкретных вариантах осуществления, один или несколько пакетов имеют объем заполнения между 20 мл и 40 мл, включительно. В некоторых вариантах осуществления, клетки в объеме среды или раствора, например, раствора для замораживания, 120 мл или более, замораживают в одном или нескольких пакетах. В конкретных вариантах осуществления, один или несколько пакетов имеют объем заполнения между 50 мл и 70 мл, включительно.
[0688] В конкретных вариантах осуществления, клетки замораживают в растворе, например, растворе для замораживания, помещенном в контейнер, например, пакет или флакон, при некотором соотношении площади поверхности к объему. В конкретных вариантах осуществления, соотношение площади поверхности к объему составляет от или приблизительно от 0,1 см–1 до 100 см–1; от 1 см–1 до 50 см–1, от 1 см–1 до 20 см–1, от 1 см–1 до 10 см–1, от 2 см–1 до 10 см–1, от 3 см–1 до 7 см–1 или от 3 см–1 до 6 см–1, включая каждое. В конкретных вариантах осуществления, соотношение площади поверхности к объему составляет между или между приблизительно 3 см–1 и 6 см–1. В некоторых вариантах осуществления, соотношение площади поверхности к объему составляет, составляет приблизительно или составляет по меньшей мере 3 см–1, 4 см–1, 5 см–1, 6 см–1 или 7 см–1.
[0689] В некоторых вариантах осуществления, перенос в среду для криоконсервации ассоциирован с одной или несколькими стадиями переработки, которые могут включать промывку образца, например, модифицированной композиции клеток, например, для удаления среды и/или замены среды для клеток подходящим буфером для криоконсервации или средой для последующего замораживания. В конкретных вариантах осуществления, перенос в среду для криоконсервации является полностью автоматизированным на уровне клинического масштаба в закрытой и стерильной системе. В конкретных вариантах осуществления перенос в среду для криоконсервации проводят с использованием системы CliniMACS (Miltenyi Biotec).
[0690] В некоторых вариантах осуществления, клетки размораживают. В конкретных вариантах осуществления, клетки размораживают быстро, например, настолько быстро, насколько возможно, без перегрева клеток или подвергания клеток воздействию высоких температур, например, выше 37°C. В некоторых вариантах осуществления, быстрое размораживание уменьшает и/или предотвращает подвергание клеток воздействию клеток высоких концентраций криопротектора и/или DMSO. В конкретных вариантах осуществления, на скорость, с которой происходит размораживание, могут влиять свойства контейнера, например, ампулы и/или пакета, в котором клетки замораживают и размораживают. В конкретных вариантах осуществления, клетки размораживают при температуре, составляющей, составляющей приблизительно или составляющей менее чем 37°C, 35°C, 32°C, 30°C, 29°C, 28°C, 27°C, 26°C, 25°C, 24°C, 23°C, 22°C, 21°C, 20°C или 15°C, или между 15°C и 30°C, между 23°C и 28°C или между 24°C и 26°C, включая каждое. В некоторых вариантах осуществления, клетки размораживают в термоблоке или на водяной бане. В конкретных вариантах осуществления, клетки не размораживают в термоблоке или на водяной бане. В некоторых вариантах осуществления, клетки размораживают при комнатной температуре. В некоторых вариантах осуществления, толщина стенок контейнера влияет на скорость размораживания клеток, таким образом, например, что клетки в контейнерах с толстыми стенками размораживаются при более низкой скорости, чем в контейнерах с более тонкими стенками. В некоторых вариантах осуществления, контейнеры, имеющие низкое соотношение площади поверхности к объему, имеют медленную и/или неравномерную скорость размораживания. В некоторых вариантах осуществления, подвергнутые криозамораживанию клетки быстро размораживают в контейнере, имеющем соотношение площади поверхности к объему, составляющее, составляющее приблизительно или составляющее по меньшей мере 1 см–1, 2 см–1, 3 см–1, 4 см–1, 5 см–1, 6 см–1 или 7 см–1, 8 см–1, 9 см–1, или 10 см–1. В конкретных вариантах осуществления, клетки размораживают за, приблизительно за или менее чем за 120 минут, 90 минут, 60 минут, 45 минут, 30 минут, 25 минут, 20 минут, 15 минут или десять минут. В некоторых вариантах осуществления, клетки размораживают в течение между 10 минут и 60 минут, 15 минут и 45 минут, или 15 минут и 25 минут, включая каждое. В конкретных вариантах осуществления, клетки размораживают за, приблизительно за или менее чем за 20 минут.
[0691] В конкретных вариантах осуществления, размороженным клеткам обеспечивают период покоя, например, инкубации или культивирования, перед введением или перед любыми последующими стадиями модификация и/или переработки. В некоторых вариантах осуществления, клеткам обеспечивают период покоя при низких и/или не поддающихся детекции количествах криопротектора, или в отсутствие криопротектора, например, DMSO. В конкретных вариантах осуществления, размороженным клетки клеткам обеспечивают период покоя после или непосредственно после стадий промывки, например, для удаления криопротектора и/или DMSO. В некоторых вариантах осуществления, период покоя представляет собой или включает культивирование и/или инкубацию при или приблизительно при 37°C. В некоторых вариантах осуществления, период покоя проводят в отсутствие любых реагентов, например, стимулирующих реагенты, реагентов на бусинах или рекомбинантных цитокинов, используемых для и/или ассоциированных с любой стадией переработки или модификации. В некоторых вариантах осуществления, клеткам обеспечивают период покоя в течение приблизительно или в течение по меньшей мере 5 минут, 10 минут, 15 минут, 30 минут, 1 часа, 2 часов, 3 часов, 4 часов, 5 часов, 6 часов, 8 часов, 12 часов, 18 часов или 24 часов. В конкретных вариантах осуществления, клеткам обеспечивают период покоя в течение приблизительно, или в течение по меньшей мере 2 часов.
[0692] В некоторых вариантах осуществления, клетки замораживают, например, подвергают криоконсервации, до, во время или после указанных способов переработки и/или модификации клеток. В некоторых вариантах осуществления, на стадии замораживания и последующего размораживания удаляют гранулоциты и, до некоторой степени, моноциты в популяции клеток. Затем клетки, как правило, замораживают до −80°C со скоростью 1° в минуту и сохраняют в паровой фазе в сосуде для хранения с жидким азотом. В некоторых вариантах осуществления, клетки активно и/или эффективно охлаждают со скоростью, составляющей или составляющей приблизительно 1° в минуту, с использованием устройства для замораживания с контролируемой скоростью. В некоторых вариантах осуществления, клетки можно замораживать с использованием устройства для замораживания с контролируемой скоростью. В некоторых аспектах, устройства для замораживания с контролируемой скоростью используют для замораживания клеток с программируемыми профилями охлаждения, например, профилями с множеством скоростей охлаждения и/или нагревания. Такие профили замораживания можно программировать для контроля нуклеации, например, образования льда, например, для уменьшения внутриклеточного образования льда.
[0693] В некоторых вариантах осуществления, признаки замороженных клеток, включая любые клетки и композиции, как описано, такие как композиции клеток с конкретной концентрацией или плотностью клеток, замораживают в присутствии криопротектора и/или заполняют ими контейнер с конкретным объемом или соотношением поверхности к объему, включают улучшенное, увеличенное и/или ускоренное размножение; улучшенную, увеличенную и/или усиленную выживаемость клеток и уменьшение количества случаев гибели клеток, например, некроза, программируемой гибели клеток и/или апоптоза; улучшенную, усиленную и/или увеличенную активность, например, цитолитическую активность; и/или уменьшение количества случаев старения или латентности после размораживания, по сравнению с клетками, замороженными альтернативными способами.
[0694] В конкретных вариантах осуществления, клетки замораживают при плотности клеток и/или соотношении площади поверхности к объему, представленных в настоящем описании, и они имеют уменьшенную гибель клеток, например, некроз и/или апоптоз, в ходе и/или в результате замораживания, криозамораживания и/или криоконсервации, по сравнению с клетками, замороженными при другой плотности клеток и/или другом соотношении площади поверхности к объему, в таких же или сходных условиях. В конкретных вариантах осуществления, клетки замораживают при плотности клеток и/или соотношении площади поверхности к объему, представленных в настоящем описании, и они имеют уменьшенную отсроченную гибель клеток, например, уменьшенное количество клеток, которые погибают, например, из–за некроза, программируемой гибели клеток или апоптоза, в пределах 48 часов после замораживания, криозамораживания и/или криоконсервации, например, после размораживания замороженных клеток. В конкретных вариантах осуществления, по меньшей мере на или приблизительно на 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 99% меньше клеток погибают в ходе и/или в результате замораживания и/или криоконсервации по сравнению с клетками, замороженными при другой плотности клеток и/или другом соотношении площади поверхности к объему, в таких же или сходных условиях. В конкретных вариантах осуществления, менее чем 40%, 30%, 25%, 20%, 15%, 10%, 5%, 1%, 0,1% или 0,01% клеток, замороженных при представленной плотности клеток и/или соотношении площади поверхности к объему, погибают в ходе или в результате замораживания, криозамораживания и/или криоконсервации.
[0695] В некоторых вариантах осуществления, клетки замораживают при плотности клеток и/или соотношении площади поверхности к объему, представленных в настоящем описании, и они имеют уменьшенное количество случаев старения или латентности в ходе и/или в результате замораживания, криозамораживания и/или криоконсервации, по сравнению с клетками, замороженными при другой плотности клеток и/или другом соотношении площади поверхности к объему, в таких же или сходных условиях. В конкретных вариантах осуществления, по меньшей мере на или приблизительно на 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 99% меньше клеток представляют собой стареющие и/или латентные клетки, по сравнению с клетками, замороженными при другой плотности клеток и/или другом соотношении площади поверхности к объему, в таких же или сходных условиях. В конкретных вариантах осуществления, клетки замораживают при представленной плотности клеток и/или соотношении площади поверхности к объему, и менее чем 40%, 30%, 25%, 20%, 15%, 10%, 5%, 1%, 0,1% или 0,01% клеток становятся стареющими и/или латентными в результате замораживания, криозамораживания и/или криоконсервации.
[0696] В конкретных вариантах осуществления, клетки замораживают, например, подвергают криозамораживанию, при плотности клеток и/или соотношении площади поверхности к объему, представленных в настоящем описании, и они имеют улучшенное, ускоренное и/или более быстрое размножение, например, в стимулирующих условиях, таких как инкубация со стимулирующим реагентом, описанным в настоящем описании, после размораживания клеток, по сравнению с клетками, замороженными при другой плотности клеток и/или другом соотношении площади поверхности к объему, в таких же или сходных условиях. В конкретных вариантах осуществления, клетки размножаются при скорости, которая является ускоренной и/или более быстрой на, приблизительно на или по меньшей мере на 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 150%, 200%, в 1 раз, 1,5 раза, 2 раза, 3 раза, 4 раза, 5 раз или 10 раз, по сравнению с клетками, замороженными при другой плотности клеток и/или другом соотношении площади поверхности к объему, в таких же или сходных условиях. Например, в некоторых вариантах осуществления, размороженные клетки достигают порога размножение, например, предопределенных количества, плотности клеток, или фактора, такого как 2–кратное размножение, в течение на, в течение приблизительно на или в течение по меньшей мере на 5% 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 99% меньшего времени, чем размороженные клетки, которые замораживали при другой плотности клеток и/или другом соотношении площади поверхности к объему, в таких же или сходных условиях.
[0697] В некоторых вариантах осуществления, клетки замораживают, например, подвергают криозамораживанию, при определенной плотности клеток, и они имеют улучшенную, увеличенную, и/или большую цитолитическую активность, например, такую, как измерено посредством любого анализа для измерения цитолитической активности, описанного в настоящем описании, после размораживания клеток, по сравнению с клетками, замороженными при другой плотности клеток, например, более высокой или более низкой плотность, в таких же или сходных условиях. В конкретных вариантах осуществления, цитолитическая активность увеличена на, приблизительно на или по меньшей мере на 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, 150%, 200%, в 1 раз, 1,5 раза, 2 раза, 3 раза, 4 раза, 5 раз или 10 раз, по сравнению с клетками, замороженными при другой плотности, в таких же или сходных условиях.
VI. КОМПОЗИЦИИ И СОСТАВЫ
[0698] Настоящее изобретение относится также к композициям, включающим клетки, включая фармацевтические композиции и составы, например, единичную дозированную форму композиций, включающую количество клеток для введения в данной дозе или ее доле. Фармацевтические композиции и составы, как правило, включают один или несколько необязательных фармацевтически приемлемых носителей или наполнителей. В некоторых вариантах осуществления, композиция включает по меньшей мере одно дополнительное лекарственное средство.
[0699] Термин «фармацевтический состав» относится к препарату, который находится в такой форме, чтобы обеспечивать эффективность биологической активности содержащегося в нем активного ингредиента, и который не содержит дополнительных компонентов, неприемлемо токсичных для индивида, которому будут вводить состав.
[0700] «Фармацевтически приемлемый носитель» относится к ингредиенту в фармацевтическом составе, отличному от активного ингредиента, который является нетоксичным для индивида. Фармацевтически приемлемый носитель включает, но без ограничения, буфер, наполнитель, стабилизатор или консервант.
[0701] В некоторых аспектах, выбор носителя частично определяется конкретной клеткой и/или способом введения. Соответственно, существует множество пригодных составов. Например, фармацевтическая композиция может содержать консерванты. Пригодные консерванты могут включать, например, метилпарабен, пропилпарабен, бензоат натрия и хлорид бензалкония. В некоторых аспектах, используют смесь из двух или более консервантов. Консерванты или их смеси, как правило, присутствуют в количестве приблизительно от 0,0001% до приблизительно 2% по массе от суммарной композиции. Носители описаны, например, в Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980). Фармацевтически приемлемые носители являются, как правило, нетоксичными для реципиентов в применяемых дозах и концентрациях, и включают, но без ограничения: буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как хлорид октадецилдиметилбензиламмония; хлорид гексаметэтония; хлорид бензалкония, хлорид бензэтония; фенол, бутил или бензиловый спирт; алкилпарабены, такие как метил– или пропилпарабен; катехол; резорцинол; циклогексанол; 3–пентанол; и м–крезол); полипептиды с низкой молекулярной массой (менее приблизительно 10 остатков); белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин, или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТА; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексы с металлом (например, комплексы Zn–белок); и/или неионные поверхностно–активные вещества, такие как полиэтиленгликоль (PEG).
[0702] Забуферивающие средства в некоторых аспектах включают в композиции. Пригодные забуферивающие средства включают, например, лимонную кислоту, цитрат натрия, фосфорную кислоту, фосфат калия, и различные другие кислоты и соли. В некоторых аспектах, используют смесь из двух или более забуферивающих средств. Забуферивающие средства или их смеси, как правило, присутствуют в количестве от приблизительно 0,001% до приблизительно 4% по массе от суммарной композиции. Способы получения пригодных для введения фармацевтические композиции известны. Иллюстративные способы описаны более подробно, например, в Remington: The Science and Practice of Pharmacy, Lippincott Williams & Wilkins; 21st ed. (May 1, 2005).
[0703] Составы могут включать водные растворы. Состав или композиция могут также содержать более одного активного ингредиента, которые можно использовать для конкретного признака, заболевания или состояния, подвергаемых лечению с использованием клеток, предпочтительно, ингредиенты с активностью, дополняющей активность клеток, где соответствующие активности не оказывают неблагоприятного влияния друг на друга. Такие активные ингредиенты подходящим образом присутствуют в комбинации в количествах, которые являются эффективными для намеченной цели. Таким образом, в некоторых вариантах осуществления, фармацевтическая композиция дополнительно включает другие фармацевтически активные вещества или лекарственные средства, такие как химиотерапевтические средства, например, аспарагиназа, бусульфан, карбоплатин, цисплатин, даунорубицин, доксорубицин, фторурацил, гемцитабин, гидроксимочевина, метотрексат, паклитаксел, ритуксимаб, винбластин и/или винкристин.
[0704] В некоторых вариантах осуществления, композиция включает клетки в количестве, эффективном для уменьшения нагрузки заболевания или состояния, и/или в количестве, которое не приводит к CRS или тяжелому CRS у индивида, и/или не вызывает никакого из других исходов для способов, как описано в настоящем описании.
[0705] Фармацевтическая композиция, в некоторых вариантах осуществления, содержит клетки в количествах, эффективных для лечения или предотвращения заболевания или состояния, таких как терапевтически эффективное или профилактически эффективное количество. Терапевтическую или профилактическую эффективность, в некоторых вариантах осуществления, мониторируют посредством периодической оценки подвергаемых лечению индивидов. Желательную дозу можно доставлять посредством однократного болюсного введения клеток, посредством множества болюсных введений клеток, или посредством введения клеток непрерывной инфузией.
[0706] Клетки и композиции можно вводить с использованием стандартных способов, составов и/или устройств для введения. Введение клеток может являться аутологичным или гетерологичным. Например, иммунореактивные клетки или предшественники можно получать от одного индивида и вводить тому же самому индивиду или другому, совместимому индивиду. Полученные из периферической крови иммунореактивные клетки или их потомство (например, полученное in vivo, ex vivo или in vitro) можно вводить посредством локализованной инъекции, включая введение через катетер, системной инъекции, местной инъекции, внутривенной инъекции или парентерального введения. При введении терапевтической композиции (например, фармацевтической композиции, содержащей генетически модифицированные иммунореактивные клетки), ее, как правило, составляют в единичной дозированной пригодной для инъекции форме (растворе, суспензии, эмульсии).
[0707] Составы включают составы для перорального, внутривенного, внутрибрюшинного, подкожного, внутрилегочного, чрескожного, внутримышечного, интраназального, трансбуккального, подъязычного введения, или введения с использованием суппозитория. В некоторых вариантах осуществления, популяции клеток вводят парентерально. Термин «парентеральное», в рамках изобретения, включает внутривенное, внутримышечное, подкожное, ректальное, вагинальное и внутрибрюшинное введение. В некоторых вариантах осуществления, клетки вводят индивиду с использованием периферической системной доставки посредством внутривенной, внутрибрюшинной или подкожной инъекции.
[0708] Композиции, в некоторых вариантах осуществления, представлены в форме стерильных жидких препаратов, например, изотонических водных растворов, суспензий, эмульсий, дисперсий или вязких композиций, которые можно, в некоторых аспектах, забуферивать до выбранного pH. Жидкие препараты обычно проще получать, чем гели, другие вязкие композиции и твердые композиции. Кроме того, жидкие композиции несколько более удобны для введения, особенно посредством инъекции. Вязкие композиции, с другой стороны, можно составлять в пределах соответствующего диапазона вязкости для обеспечения более длительных периодов контакта со специфическими тканями. Жидкие или вязкие композиции могут содержать носители, которые могут представлять собой растворитель или диспергирующую среду, содержащие, например, воду, солевой раствор, фосфатно–солевой буфер, полиол (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль) и их пригодные смеси.
[0709] Стерильные пригодные для инъекции растворы можно получать посредством включения клеток в растворитель, например, в смеси с пригодным носителем, разбавителем или наполнителем, таким как стерильная вода, физиологический солевой раствор, глюкоза, декстроза или т.п. Композиции могут содержать вспомогательные вещества, такие как смачивающие, диспергирующие вещества или эмульгаторы (например, метилцеллюлозу), забуферивающие pH средства, гелеобразующие или повышающие вязкость добавки, консерванты, ароматизаторы и/или окрашивающие средства, в зависимости от желательного способа введения и получения. В некоторых аспектах, можно консультироваться со стандартными руководствами для получения пригодных препаратов.
[0710] Различные добавки, которые повышают стабильность и стерильность композиции, включая противомикробные консерванты, антиоксиданты, хелатирующие агенты и буферы, можно добавлять. Предотвращение действия микроорганизмов можно обеспечивать посредством различных антибактериальных и противогрибковых средств, например, парабенов, хлорбутанола, фенола и сорбиновой кислоты. Длительную абсорбцию пригодной для инъекции фармацевтической формы можно получать с использованием средств, замедляющих абсорбцию, например, моностеарата алюминия и желатина.
[0711] Составы, подлежащие использованию для введения in vivo, как правило, являются стерильными. Стерильность можно легко обеспечивать, например, посредством фильтрации через мембраны для стерилизации фильтрацией.
[0712] В некоторых вариантах осуществления, терапевтическая композиция T–клеток содержит между приблизительно 10 миллионов клеток на мл и приблизительно 70 миллионов клеток на мл или между приблизительно 10 миллионов жизнеспособных клеток на мл и приблизительно 70 миллионов жизнеспособных клеток на мл, включая каждое. В некоторых вариантах осуществления, терапевтическая композиция T–клеток содержит между приблизительно 15 миллионов клеток или жизнеспособных клеток на мл и приблизительно 60 миллионов клеток или жизнеспособных клеток на мл, включая каждое. В некоторых вариантах осуществления, композиция T–клеток содержит более чем 10 миллионов клеток или жизнеспособных клеток на мл. В некоторых вариантах осуществления, терапевтическая композиция T–клеток содержит более чем 15 миллионов клеток или более чем 15 миллионов клеток на мл.
[0713] В некоторых вариантах осуществления, изделие дополнительно содержит информацию, указывающую, что контейнер, например, флакон или пакет, такой как IV пакет, или шприц, содержит целевое количество единиц.
[0714] В некоторых вариантах осуществления изделия, контейнер представляет собой первый контейнер и изделие, кроме того, содержит дополнительные контейнеры, где каждый из дополнительных контейнеров содержит единичную дозу, содержащую целевое количество единиц композиции T–клеток. В некоторых вариантах осуществления, дополнительные контейнеры содержат между приблизительно 10 миллионов клеток или жизнеспособных клеток на мл и приблизительно 70 миллионов клеток или жизнеспособных клеток на мл, между приблизительно 15 миллионов клеток или жизнеспособных клеток и приблизительно 60 миллионов клеток или жизнеспособных клеток на мл, более чем 10 миллионов клеток или жизнеспособных клеток на мл, более чем 15 миллионов клеток или жизнеспособных клеток на мл, включая каждое, или их комбинацию. В некоторых вариантах осуществления, композиция дополнительно содержит криопротектор, и/или изделие дополнительно содержит инструкции для размораживания композиции перед введением индивиду.
[0715] В некоторых вариантах осуществления, клетки суспендируют в растворе для замораживания, например, после стадии промывки для удаления плазмы и тромбоцитов. В некоторых аспектах, можно использовать любой из множества известных растворов и параметров для замораживания. Один из примеров включает использование PBS, содержащего 20% DMSO и 8% человеческий сывороточный альбумин (HSA), или других пригодных сред для замораживания клеток. Затем их разводят средой 1:1, таким образом, чтобы конечная концентрация DMSO и HSA составляли 10% и 4%, соответственно.
[0716] В некоторых аспектах, можно использовать любой из множества известных растворов и параметров для замораживания. В некоторых вариантах осуществления, образец клеток может содержать среду или раствор для криоконсервации или перехода в стекловидное состояние, содержащие криопротектор. Пригодные криопротекторы включают, но без ограничения, диметилсульфоксид (DMSO), глицерин, гликоль, пропиленгликоль, этиленгликоль, пропандиол, полиэтиленгликоль (PEG), 1,2–пропандиол (PROH) или их смесь. В некоторых примерах, раствор для криоконсервации может содержать один или несколько не проникающих в клетку криоконсервантов, включая, но без ограничения, поливинилпирролидон, гидроксиэтилкрахмал, полисахарид, моносахарид, альгинат, трегалозу, раффинозу, декстран, человеческий сывороточный альбумин, фиколл, липопротеины, поливинилпирролидон, гидроксиэтилкрахмал, аутологичную плазму или их смесь. В некоторых вариантах осуществления, клетки суспендируют в растворе для замораживания с конечной концентрацией криопротектора между приблизительно 1% и приблизительно 20%, между приблизительно 3% и приблизительно 9%, или между приблизительно 6% и приблизительно 9% по объему, включая каждое. В конкретных вариантах осуществления, конечная концентрация криопротектора в растворе для замораживания составляет приблизительно 3%, приблизительно 4%, приблизительно 5%, приблизительно 5,5%, приблизительно 6%, приблизительно 6,5%, приблизительно 7%, приблизительно 7,5%, приблизительно 8%, приблизительно 8,5%, приблизительно 9%, приблизительно 9,5% или приблизительно 10% по объему.
[0717] В некоторых вариантах осуществления, криопротектор представляет собой DMSO. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания с конечной концентрацией DMSO между приблизительно 1% и приблизительно 20%, между приблизительно 3% и приблизительно 9%, или между приблизительно 6% и приблизительно 9% по объему, включая каждое. В конкретных вариантах осуществления, конечная концентрация DMSO в растворе для замораживания составляет приблизительно 3%, приблизительно 4%, приблизительно 5%, приблизительно 5,5%, приблизительно 6%, приблизительно 6,5%, приблизительно 7%, приблизительно 7,5%, приблизительно 8%, приблизительно 8,5%, приблизительно 9%, приблизительно 9,5% или приблизительно 10% по объему.
[0718] В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности между приблизительно 1×106 клеток/мл и приблизительно 1×108 клеток/мл, между приблизительно 1×106 клеток/мл и приблизительно 2×107 клеток/мл, между приблизительно 1×107 клеток/мл и приблизительно 5 ×107 клеток/мл, или между приблизительно 1×107 клеток/мл до 5×107 клеток/мл, включая каждое. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности приблизительно 1×106 клеток/мл, приблизительно 2×106 клеток/мл, приблизительно 5×106 клеток/мл, приблизительно 1×107 клеток/мл, приблизительно 1,5×107 клеток/мл, приблизительно 2×107 клеток/мл, приблизительно 2,5×107 клеток/мл, приблизительно 2,5×107 клеток/мл, приблизительно 2,5×107 клеток/мл, приблизительно 3×107 клеток/мл, приблизительно 3,5×107 клеток/мл, приблизительно 4×107 клеток/мл, приблизительно 4,5×107 клеток/мл, или приблизительно 5×107 клеток/мл. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности между приблизительно 1,5×107 клеток/мл и приблизительно 6×107 клеток/мл, включительно. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности по меньшей мере приблизительно 1×107 клеток/мл. В конкретных вариантах осуществления, клетки суспендируют в растворе для замораживания при плотности по меньшей мере приблизительно 1,5×107 клеток/мл. В некоторых вариантах осуществления, клетки представляют собой жизнеспособные клетки.
[0719] В некоторых вариантах осуществления, перенос в среду для криоконсервации ассоциирован с одной или несколькими стадиями переработки, которые могут включать промывку образца, например, модифицированной композиции клеток, например, для удаления среды и/или замены среды для клеток подходящим буфером для криоконсервации или средой для последующего замораживания. В конкретных вариантах осуществления, перенос в среду для криоконсервации является полностью автоматизированным на уровне клинического масштаба в закрытой и стерильной системе. В конкретных вариантах осуществления перенос в среду для криоконсервации проводят с использованием системы CliniMACS (Miltenyi Biotec).
[0720] В некоторых вариантах осуществления, клетки замораживают, например, криоконсервируют, до, во время или после указанных способов для переработки и/или модификации клеток. В некоторых вариантах осуществления, на стадии замораживания и последующего размораживания удаляют гранулоциты и, до некоторой степени, моноциты в популяции клеток. Затем клетки, как правило, замораживают до −80°C со скоростью 1° в минуту и сохраняют в паровой фазе в сосуде для хранения с жидким азотом.
[0721] В некоторых вариантах осуществления, композицию заключают в пакет, пригодный для криоконсервации (например, пакеты для замораживания CryoMacs®, Miltenyi Biotec). В некоторых вариантах осуществления, композицию заключают в ампулу, пригодную для криоконсервации (например, ампулы CellSeal®, Cook Regentec).
VII. ИЗДЕЛИЯ
[0722] Настоящее изобретение относится также к изделиям, таким как наборы и устройства, для введения клеток индивидам в соответствии с представленными способами адоптивной клеточной терапии, и для хранения и введения клеток и композиций.
[0723] Изделия включают один или несколько контейнеров, как правило, множество контейнеров, упаковочный материал, и этикетку или вкладыш в упаковку на контейнере или ассоциированные с контейнером или контейнерами и/или упаковкой, как правило, включающие инструкции для введения клеток индивиду.
[0724] Контейнеры, как правило, содержат клетки, подлежащие введению, например, одну или несколько их единичных доз. Изделие как правило, включает множество контейнеров, где каждый содержит однократную единичную дозу клеток. Единичная доза может представлять собой количество или число клеток, подлежащее введению индивиду в первой дозе, или двойное количество (или более) клеток, подлежащее введению в первой или любой одной или нескольких последовательной дозе(дозах). Она может представлять собой низшую дозу или низшую возможную дозу клеток, которую вводят индивиду в сочетании со способом введения. В некоторых вариантах осуществления, единичная доза представляет собой минимальное количество клеток или количество клеток, или минимальное количество эталонных единиц, или целевое количество эталонных единиц, или эталонных единиц в пределах целевого диапазона, которое можно вводить в однократной дозе любому индивиду, имеющему конкретное заболевание или состояние, или любому индивиду, в соответствии со способами в настоящем описании. В некоторых вариантах осуществления, количество клеток в единичной дозе представляет собой количество клеток или количество экспрессирующих рекомбинантный рецептор или экспрессирующих CAR клеток, или количество таких клеток конкретного фенотипа, например, CD8+, маркер апоптоза отрицательный (например, аннексин V– или каспаза 3–) и CD8+, которое желательно вводить конкретному индивиду в дозе, например, индивиду, от которого происходят клетки. В некоторых вариантах осуществления, целевое количество эталонных единиц или эталонных единиц в целевом диапазоне в единичной дозе представляет собой количество эталонных единиц из композиции как функцию от количества клеток или количества экспрессирующих рекомбинантный рецептор или экспрессирующих CAR клеток, или количества таких клеток конкретного фенотипа, например, CD8+, маркер апоптоза отрицательный (например, аннексин V– или каспаза 3–) и CD8+, и зависимой от рекомбинантного рецептора активности (например, антигенспецифической активности) композиции, и его желательно вводить конкретному индивиду в дозе, например, индивиду, от которого происходят клетки. В некоторых вариантах осуществления, клетки получают от индивида, подлежащего лечению, посредством способов, как представлено в настоящем описании, или нуждающегося в нем.
[0725] В некоторых вариантах осуществления, изделие содержит единичную дозу клеток, содержащей целевое количество эталонных единиц (RU) в пределах данного диапазона, например, в соответствии с формулой, как описано в другом месте в настоящем описании. Иллюстративные единичные дозы целевого количества эталонных единиц (RU) или целевого количества тотальных клеток включают любое, как описано на протяжении этого описания.
[0726] В некоторых вариантах осуществления, каждый из контейнеров индивидуально содержит единичную дозу клеток, например, включающие одинаковое или по существу одинаковое количество клеток, или количество экспрессирующих рекомбинантный рецептор или экспрессирующих CAR клеток, или количество таких клеток конкретного фенотипа, например, CD8+, маркер апоптоза отрицательный (например, аннексин V– или каспаза 3–). В некоторых вариантах осуществления, каждый из контейнеров индивидуально содержит единичную дозу клеток, например, включающие одинаковое или по существу одинаковое количество целевых эталонных единиц или количество эталонных единиц в пределах целевого диапазона.
[0727] Пригодные контейнеры включают, например, бутыли, флаконы, шприцы и гибкие пакеты, такие как пакеты для инфузии. В конкретных вариантах осуществления, контейнеры представляют собой пакеты, например, гибкие пакеты, такие как пакеты, пригодные для инфузии клеток индивидам, например, гибкие пакеты из пластика или PVC, и/или пакеты для IV раствора. Пакеты, в некоторых вариантах осуществления, можно герметично закрывать и/или можно стерилизовать, так чтобы обеспечивать стерильность раствора и доставки клеток и композиций. В некоторых вариантах осуществления, контейнеры, например, пакеты, имеют емкость, составляющую или составляющую приблизительно, или составляющую по меньшей мере или приблизительно 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, или 1000 мл, например, составляющую емкость между 10 или приблизительно между 10 и 100 или приблизительно 100, или между 10 или приблизительно между 10 и 500 или приблизительно 500 мл, включая каждое. В некоторых вариантах осуществления, контейнеры, например, пакеты, состоят и/или изготовлены из материала, который является стабильным и/или обеспечивает стабильное хранение и/или поддержание клеток при одной или нескольких из различных температур, таких как низкие температуры, например, составляющие ниже или приблизительно, или составляющие или приблизительно составляющие –20°C, –80°C, –120°C, 135°C и/или температуры, пригодные для криоконсервации, и/или другие температуры, такие как температуры, пригодные для размораживания клеток, и температура тела, такая как составляющая или приблизительно составляющая 37°C, например, чтобы позволять размораживание, например, в месте расположения индивида или проведения лечения, например, на месте, непосредственно перед лечением.
[0728] Контейнеры можно изготавливать из множества материалов, таких как стекло или пластик. В некоторых вариантах осуществления, контейнер имеет одно или несколько отверстий, например, отверстий для стерильного доступа, например, для присоединения трубок или канюляции с одной или несколькими трубками, например, для внутривенной или другой инфузии, и/или для соединения с целью переноса в другие контейнеры и из других контейнеров, таких как пакеты для культивирования и/или хранения клеток, или другие контейнеры. Иллюстративные контейнеры включают пакеты для инфузии, пакеты для внутривенного раствора, флаконы, включая флаконы с пробками, которые можно прокалывать иглой для инъекции.
[0729] Изделие может дополнительно включать вкладыш в упаковку или этикетку с одним или несколькими разделами идентификационной информации и/или инструкциями для использования. В некоторых вариантах осуществления, информация или инструкции указывают, что содержимое можно или необходимо использовать для лечения конкретного состояния или заболевания, и/или предоставляют инструкции для этого. На этикетке или во вкладыш в упаковку может быть указано, что содержимое изделия предназначено для лечения заболевания или состояния. В некоторых вариантах осуществления, на этикетке или во вкладыше в упаковку представлены инструкции для лечения индивида, например, индивида, от которого происходят клетки, способом, включающим введение первой и одной или нескольких последующих доз клеток, например, в соответствии с любым из вариантов осуществления представленных способов. В некоторых вариантах осуществления, в инструкциях указано введение, в первой дозе, одной единичной дозы, например, содержимого одного индивидуального контейнера из изделия, за которым следуют одна или несколько последовательных доз в указанной временной точке или в пределах указанного временного окна, и/или после детекции присутствия или отсутствия, или количества, или уровня одного или нескольких факторов, или исходов у индивида.
[0730] В некоторых вариантах осуществления, в инструкциях указано введение одной или нескольких единичных доз индивиду.
[0731] В некоторых вариантах осуществления, этикетка или вкладыш в упаковку, или упаковка содержит идентификатор для указания специфической идентичности индивида, от которого происходят клетки, и/или для введения которому предназначены клетки. В случае аутологичного переноса, идентичность индивида, от которого происходят клетки, является такой же, как идентичность индивида, для введения которому предназначены клетки. Таким образом, идентификационная информация может указывать, что клетки предназначены для введения конкретному пациенту, например, тому, от которого исходно получены клетки. Такая информация может присутствовать на упаковочном материале и/или этикетке в форме штрих–кода или другого закодированного идентификатора, или может указывать имя и/или другие идентификационные характеристики индивида.
[0732] Изделие, в некоторых вариантах осуществления, включает один или несколько, как правило, множество, контейнеров, содержащих композиции, содержащие клетки, например, в форме их индивидуальных единичных доз, и дополнительно включает один или несколько дополнительных контейнеров с содержащейся в них композицией, включающей дополнитльное средство, такое как цитотоксическое или иное лекарственное средство, например, предназначенное для введения в комбинации, например, одновременно или последовательно, в любом порядке, с клетками. Альтернативно или дополнительно, изделие может дополнительно содержать другой или такой же контейнер, содержащий фармацевтически приемлемый буфер. Оно может дополнительно включать другие материалы, такие как другие буферы, разбавители, фильтры, трубки, иглы и/или шприцы.
[0733] Термин «вкладыш в упаковку» используют для обозначения инструкций, обычно включенных в коммерческие упаковки терапевтических продуктов, которые содержат информацию относительно показаний, применения, дозирования, введения, комбинированной терапии, противопоказаний и/или предостережений, касающихся использования таких терапевтических продуктов.
VIII. ОПРЕДЕЛЕНИЯ
[0734] Если не определено иное, все специальные термины, номенклатура и другие технические и научные термины или терминология, в рамках изобретения, предназначены, чтобы иметь такое же значение, какое является общепринятым для специалиста в области, к которой относится заявленный объект изобретения. В некоторых случаях, термины с общеизвестными значениями определены в настоящем описании для ясности и/или для справки, и включение таких определений в настоящем описании не обязательно следует рассматривать как представление значительных отличий от того, что является общеизвестным в данной области.
[0735] В рамках изобретения, формы единственного числа включают объекты ссылки множественного числа, если контекст явно не требует иного. Например, форма единственного числа обозначает «по меньшей мере один», или «один или несколько». Понятно, что аспекты и варианты, описанные в настоящем описании, включают «состоящие» и/или «в основном состоящие из» аспектов и вариантов.
[0736] На протяжении этого описания, различные аспекты заявленного объекта изобретения представлены в формате диапазона. Следует понимать, что описание в формате диапазона присутствует просто для удобства и краткости, и его не следует рассматривать как жесткое ограничения объема заявленного объекта изобретения. Соответственно, описание диапазона следует рассматривать как конкретно описывающее все возможные поддиапазоны, так же как индивидуальные числовые значения внутри этого диапазона. Например, когда представлен диапазон значений, понятно, что каждое промежуточное значение, между верхним и нижним пределами этого диапазона, и любым другим указанным или промежуточным значением в этом указанном диапазоне включено в заявленный объект изобретения. Верхний и нижний пределы этих меньших диапазонов могут быть независимо включены в меньшие диапазоны, а также включены в заявленный объект изобретения, ограниченный любым конкретно исключенным пределом в указанном диапазоне. Когда указанный диапазон включает один или оба предела, диапазоны, исключающие любой или оба из этих включенных пределов, также включены в описанный или заявленный объект изобретения. Это применимо вне зависимости от ширины диапазона.
[0737] Термин «приблизительно», в рамках изобретения, относится к обычному диапазону ошибки для соответствующего значения, уже известному специалисту в данной области. Ссылка на «приблизительное» значение или параметр в настоящем описании включает (и описывает) варианты осуществления, которые относятся к этому значению или параметру по существу. Например, описание, относящееся к «приблизительно X», включает описание «X».
[0738] В рамках изобретения, композиция относится к любой смеси из двух или более продуктов, веществ или соединений, включая клетки. Она может представлять собой раствор, суспензию, жидкость, порошок, пасту, водную, неводную или любую их комбинацию.
[0739] В рамках изобретения, утверждение, что клетка или популяция клеток является «положительной» по конкретному маркеру, относится к поддающемуся детекции присутствию на или в клетке конкретного маркера, как правило, поверхностного маркера. Применительно к поверхностному маркеру, термин относится к присутствию поверхностной экспрессии, как детектировано посредством проточной цитометрии, например, посредством окрашивания с использованием антитела, которое специфически связывается с маркером, и детекции указанного антитела, где окрашивание поддается детекции посредством проточной цитометрии на уровне значительно выше окрашивания, детектированного при осуществлении такого же способа для совпадающего по изотипу контроля, в идентичных в ином отношении условиях, и/или на уровне, по существу сходным с уровнем для клетки, как известно, положительной по этому маркеру, и/или на уровне значительно выше уровня для клетки, как известно, отрицательной по этому маркеру.
[0740] В рамках изобретения, утверждение, что клетка или популяция клеток является «отрицательной» по конкретному маркеру, относится к отсутствию значительного поддающегося детекции присутствия на или в клетке конкретного маркера, как правило, поверхностного маркера. Применительно к поверхностному маркеру, термин относится к отсутствию поверхностной экспрессии, как детектировано посредством проточной цитометрии, например, посредством окрашивания с использованием антитела, которое специфически связывается с маркером, и детекции указанного антитела, где окрашивание не детектировано посредством проточной цитометрии на уровне значительно выше окрашивания, детектированного при осуществлении такого же способа для совпадающего по изотипу контроля, в идентичных в ином отношении условиях, и/или на уровне значительно ниже уровня для клетки, как известно, положительной по этому маркеру, и/или на уровне, по существу сходным с уровнем для клетки, как известно, отрицательной по этому маркеру.
[0741] Термин «вектор», в рамках изобретения, относится к молекуле нуклеиновой кислоты, способной к размножению другой нуклеиновой кислоты, с которой она связана. Термин включает вектор как самореплицирующуюся структуру нуклеиновой кислоты, так же как вектор, встроенный в геном клетки–хозяина, в которую он введен. Определенные векторы являются способными управлять экспрессией нуклеиновых кислот, с которыми они функционально связаны. Такие векторы обозначены в настоящем описании как «экспрессирующие векторы».
IX. ИЛЛЮСТРАТИВНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
1. Изделие, содержащее:
(a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, необязательно, представляющий собой химерный антигенный рецептор (CAR), который специфически связывается с антигеном, где единичная доза содержит целевое количество эталонных единиц (RU) в пределах данного диапазона, где RU в данной композиции определяют по формуле
RU=A x B, где:
A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его долю, или кратное, или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и
(b) инструкции для введения композиции, необязательно одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
2. Изделие из варианта осуществления 1, где A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции.
3. Изделие из варианта осуществления 1, где A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
4. Изделие из любого из вариантов осуществления 1–3, где целевое количество единиц составляет менее, чем пороговое количество единиц, необязательно, представляющее собой безопасное количество эталонных единиц, где безопасное количество эталонных единиц представляет собой, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
5. Изделие из варианта осуществления 4, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность, необязательно, степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
6. Изделие из варианта осуществления 4 или варианта осуществления 5, где целевое количество эталонных единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, и/или на количество в диапазоне от 1,5– до 3–кратного, необязательно, приблизительно 2–кратное, или на количество, кратное стандартному отклонению в группе индивидов, у которых не возникло неблагоприятного события, необязательно, нейротоксичности степени 0–2, необязательно, где кратное лежит в диапазоне от 1,5– до 3–кратного.
7. Изделие из любого из вариантов осуществления 1–6, где целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, для которой показан желательный терапевтический исход, необязательно, частичный ответ или полный ответ (CR).
8. Изделие, содержащее:
(a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, необязательно, представляющий собой химерный антигенный рецептор (CAR), который специфически связывается с антигеном, где:
единичная доза содержит или содержит приблизительно (i) целевое количество тотальных экспрессирующих рекомбинантный рецептор клеток или целевое количество тотальных CD3+ экспрессирующих рекомбинантный рецептор клеток, или целевое количество тотальных CD8+ экспрессирующих рекомбинантный рецептор клеток, или (ii) целевое количество эталонных единиц (RU) в пределах данного диапазона, где целевое количество эталонных RU равно или меньше порогового количества RU, где единичная доза не содержит больше порогового значения RU,
где количество RU в данной композиции определяют по формуле:
RU=A x B, где
A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции T–клеток; и
(b) инструкции для введения композиции, необязательно одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
9. Изделие из варианта осуществления 8, где A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции.
10. Изделие из варианта осуществления 8, где A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
11. Изделие из любого из вариантов осуществления 8–10, где:
целевое количество представляет собой целевое количество экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD3+, которые являются отрицательными(–) по маркеру апоптоза и CD3+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; или
целевое количество представляет собой целевое количество экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
12. Изделие из любого из вариантов осуществления 1–11, где целевое количество клеток в (i) составляет: между и между приблизительно 5,0×106 и 2,25×107, 5,0×106 и 2,0×107, 5,0×106 и 1,5×107, 5,0×106 и 1,0×107, 5,0×106 и 7,5×106, 7,5×106 и 2,25×107, 7,5×106 и 2,0×107, 7,5×106 и 1,5×107, 7,5×106 и 1,0×107, 1,0×107 и 2,25×107, 1,0×107 и 2,0×107, 1,0×107 и 1,5×107, 1,5×107 и 2,25×107, 1,5×107 и 2,0×107, 2,0×107 и 2,25×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD3+ или CD8+ или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
13. Изделие из любого из вариантов осуществления 1–12, где целевое количество клеток в (i) составляет:
между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 5,55×106, 6,66×106, 7,77×106, 8,99×106, 1,0×107, 1,1×107 и приблизительно 1,67×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 7,14×106, 8,5×106, 1,0×107, 1,14×107, 1,29×107, 1,42×107 и приблизительно 2,14×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
14. Изделие из любого из вариантов осуществления 1–13, где целевое количество клеток в (i) составляет между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, которые являются отрицательными(–) по маркеру апоптоза и CD8+, включая каждое, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
15. Изделие из любого из вариантов осуществления 1–13, где целевое количество клеток в (i) составляет между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, включая каждое.
16. Изделие из любого из вариантов осуществления 8–15, где целевое эталонное количество RU составляет менее, чем пороговое количество единиц или составляет менее, чем эталонное безопасное количество RU, где эталонное безопасное количество RU составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
17. Изделие из варианта осуществления 16, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
18. Изделие из варианта осуществления 16 или вариант осуществления 17, где целевое эталонное количество RU составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, или по меньшей мере в 2 раза.
19. Изделие из любого из вариантов осуществления 8–18, где целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество эталонных единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, для которой показан желательный терапевтический исход, необязательно, полный ответ (CR).
20. Изделие из любого из вариантов осуществления 1–19, где A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции.
21. Изделие из любого из вариантов осуществления 1–20, где A и/или B представляет собой преобразование количества или значения, соответственно, где преобразование включает логарифмическое преобразование, степенное преобразование или логит–преобразование.
22. Изделие из любого из вариантов осуществления 1–21, где A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой кратное или преобразование значения параметра, указывающего на степень или коррелирующего со степенью зависимой от CAR активности в данной композиции T–клеток, необязательно, где B представляет собой логарифмическое преобразование значения.
23. Изделие из варианта осуществления 21 или варианта осуществления 22, где логарифмическое преобразование представляет собой десятичный log (log10(x)), натуральный log (ln(x)) или двоичный log (log2(x)).
24. Изделие из любого из вариантов осуществления 1–23, где A представляет собой количество жизнеспособных клеток в композиции и/или представляет собой количество клеток, которые не являются апоптотическими, не имеют фактора, показательного для раннего апоптоза или апоптоза, не находятся на ранних стадиях апоптоза, или не находятся на поздних стадиях апоптоза, и/или представляет собой количество клеток в определенном состоянии дифференцировки, и/или представляет собой количество клеток, имеющих признак клеток памяти/стволовых клеток, или представляет собой его кратное или преобразование.
25. Изделие из любого из вариантов осуществления 1–24, где фенотип включает положительную экспрессию поверхностного маркера, представляющего собой один или несколько из CD3, CD4 или CD8, и/или включает положительную экспрессию рекомбинантного рецептора, необязательно, CAR, или суррогатный маркер экспрессии рекомбинантного рецептора.
26. Изделие из варианта осуществления 25, где фенотип представляет собой CD3+ CAR, CD4+/CAR+, CD8+/CAR+.
27. Изделие из любого из вариантов осуществления 1–26, где фенотип включает отсутствие фактора, показательного для апоптоза или одной или нескольких стадий апоптотического каскада или пути, необязательно, экспрессии маркера апоптоза.
28. Изделие из любого из вариантов осуществления 1–27, где фенотип включает отрицательную экспрессию маркера апоптоза, необязательно, маркера раннего апоптоза или позднего апоптоза.
29. Изделие из варианта осуществления 28, где маркер апоптоза представляет собой поверхностный фосфатидилсерин и/или детектирован с использованием аннексина V, или представляет собой активную каспазу или проформу каспазы, необязательно, активную каспазу 3 или проформу каспазы 3.
30. Изделие из любого из вариантов осуществления 1–29, где фенотип включает аннексин–.
31. Изделие из любого из вариантов осуществления 1–30, где фенотип включает показатель продукции одного или комбинации цитокинов, необязательно, не специфической для антигена или рекомбинантного рецептора и/или поликлональной продукции, где один или несколько цитокинов представляет собой IL–2, IL–13, IL–17, IFN–гамма или TNF–альфа.
32. Изделие из варианта осуществления 31, где показатель продукции измеряют в анализе, необязательно, анализе окрашивания внутриклеточных цитокинов, включающем инкубацию образца из композиции T–клеток с поликлональным средством, антигенспецифическим средством или средством, связывающим рекомбинантный рецептор, необязательно CAR.
33. Изделие из варианта осуществления 31 или варианта осуществления 32, где средство представляет собой или содержит PMA и иономицин, или представляет собой или содержит T–клеточный рецептор или агонист комплекса T–клеточного рецептора.
34. Изделие из любого из вариантов осуществления 1–33, где фенотип включает отрицательную экспрессию маркера активации, где маркер активации выбран среди CD25, CD127, LAG3, Ki67 и их комбинаций.
35. Изделие из любого из вариантов осуществления 1–34, где фенотип включает отрицательную экспрессию маркера истощения, где маркер истощения представляет собой продукт гена PD1 или FOXP3, или их комбинацию.
36. Изделие из любого из вариантов осуществления 1–35, где фенотип включает наивный фенотип или фенотип клеток памяти, необязательно, где фенотип клеток памяти включает фенотип эффекторных T–клеток памяти, фенотип центральных T–клеток памяти, или фенотип эффекторных T–клеток памяти, экспрессирующих CD45RA (Temra).
37. Изделие из любого из вариантов осуществления 1–36, где A представляет собой общее количество T–клеток, общее количество CD3+ клеток, общее количество CD4+ или CD8+ клеток, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, общее количество CD4+ CAR+, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение.
38. Изделие из любого из вариантов осуществления 1–37, где A представляет собой общее количество CD3+ клеток, общее количество CD8+, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение.
39. Изделие из любого из вариантов осуществления 1–38, где A представляет собой общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD3+ CAR+ клетки, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD4+ CAR+, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD8+ CAR+ клетки, или его кратное или преобразованное значение, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
40. Изделие из любого из вариантов осуществления 1–39, где A представляет собой общее количество маркер апоптоза– CD3+ CAR+ клеток или общее количество маркер апоптоза– CD8+ CAR+ клеток, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
41. Изделие, содержащее:
(a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие химерный антигенный рецептор (CAR) который специфически связывается с антигеном, где единичная доза содержит целевую дозу терапевтической композиции T–клеток, где:
(i) если значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности композиции, равно или больше порогового значения, целевая доза представляет собой первое количество (или лежит в первом диапазоне количеств) клеток данного фенотипа из композиции;
(ii) если значение параметра меньше порогового значения, целевая доза представляет собой второе количество (или лежит во втором диапазоне количеств) клеток данного фенотипа из композиции
где первое количество (или первый диапазон) ниже, чем второе количество (или второй диапазон); и
(b) инструкции для введения композиции, необязательно одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
42. Изделие из варианта осуществления 41, где пороговое значение зависимой от рекомбинантного рецептора активности менее, чем эталонный уровень безопасности, где эталонный уровень безопасности составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наиболее низкий уровень зависимой от CAR активности терапевтической композиции, введенной индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
43. Изделие из варианта осуществления 42, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
44. Изделие из варианта осуществления 42 или варианта осуществления 43, где пороговое значение составляет менее, чем эталонный уровень безопасности, на количество, соответствующее коэффициенту запаса безопасности, или по меньшей мере в 2 раза.
45. Изделие из любого из вариантов осуществления 41–44, где первое количество ниже, чем второе количество, более чем в или более чем приблизительно в 1,5 раза, 2,0 раза, 3,0 раза, 4,0 раза, 5,0 раз, 6,0 раз, 7,0 раз, 8,0 раз, 9,0 раз, 10,0 раз или более.
46. Изделие, содержащее:
(a) контейнер, содержащий единичную дозу терапевтической композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, необязательно, представляющий собой химерный антигенный рецептор (CAR), который специфически связывается с антигеном, где:
единичная доза содержит целевую дозу терапевтической композиции T–клеток; и
терапевтическая композиция T–клеток находится выше нижнего установленного предела (LSL) и ниже верхнего установленного предела (USL) для B, где B представляет собой значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности композиции; и
(b) инструкции для введения композиции, необязательно одной или нескольких ее единичных доз, индивиду, необязательно, индивиду, имеющему или, как подозревают, имеющему заболевание или состояние.
47. Изделие из варианта осуществления 46, где продукт выпускают для лечения индивида, только если композиция находится ниже USL для B.
48. Изделие из любого из вариантов осуществления 41–47, где зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления провоспалительного цитокина, необязательно, одного или комбинации из TNF–альфа, IFN–гамма, IL–2 и IL–10.
49. Изделие из любого из вариантов осуществления 1–48, где параметр представляет собой показатель одного или нескольких факторов или его нормализованное значение.
50. Изделие из варианта осуществления 49, где показатель определяют в анализе, включающем культивирование или инкубацию в течение фиксированного времени, необязательно, 24 часов, данной композиции или образца из нее в присутствии антигена, клеток, экспрессирующих антиген, и/или средства, специфически связывающегося с рекомбинантным рецептором, необязательно, CAR.
51. Изделие из варианта осуществления 50, где анализ представляет собой ELISA.
52. Изделие из любого из вариантов осуществления 49–51, где показатель фактора представляет собой:
(i) концентрацию, относительную концентрацию, количество или относительное количество фактора; или
(ii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции, или
(iii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции в единицу времени, необязательно, один час; или
(iv) уровень, показательный для любого из (i)–(iii).
53. Изделие из любого из вариантов осуществления 49–52, где один или несколько факторов представляет собой один или комбинацию из растворимых факторов, необязательно, один или комбинацию из цитокинов, хемокинов или растворимых рецепторов, необязательно, растворимых костимулирующих рецепторов.
54. Изделие из любого из вариантов осуществления 49–53, где один или несколько факторов представляет собой один или комбинацию из провоспалительных цитокинов, Th2–цитокинов и Th17–цитокинов.
55. Изделие из любого из вариантов осуществления 49–54, где один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа, IL4, IL–5, IL–10, IL–13, GM–CSF, sCD137, MIP1a и M1Pb.
56. Изделие из любого из вариантов осуществления 49–55, где один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа и IL–10.
57. Изделие из любого из вариантов осуществления 53–56, где один или несколько факторов представляет собой комбинацию любых двух или более из вышеуказанных растворимых факторов, и параметр представляет собой среднее арифметическое или среднее геометрическое из показателей для двух или более факторов.
58. Изделие из любого из вариантов осуществления 49–57, где параметр представляет собой среднее арифметическое или среднее геометрическое показателя, необязательно, количества или концентрации, для по меньшей мере двух из TNF–альфа, IFN–гамма и IL–2 или из TNF–альфа, IFN–гамма и IL–2.
59. Изделие из любого из вариантов осуществления 49–58, где параметр представляет собой нормализованное значение показателя, где нормализация проведена по сравнению с эталонным показателем фактора.
60. Изделие из варианта осуществления 59, где эталонный показатель представляет собой среднее из показателей среди множества, необязательно по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, из эталонных терапевтических композиций T–клеток, содержащих химерный антигенный рецептор (CAR), в которых:
(i) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате приемлемый профиль безопасности после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном; и/или
(ii) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате желательную эффективность после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном.
61. Изделие из варианта осуществления 60, где приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 2 или выше, или отсутствие нейротоксичности степени 3 или выше.
62. Изделие из варианта осуществления 60 или вариант осуществления 61, где приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 3 или выше.
63. Изделие из любого из вариантов осуществления 60–62, где эффективность представляет собой частичный ответ или представляет собой полный ответ (CR).
64. Изделие из варианта осуществления 59, где эталонный показатель представляет собой показатель, в таком же анализе, фактора в эталонной композиции T–клеток, которая получена таким же способом, как терапевтическая композиция T–клеток, но не экспрессирует рекомбинантный рецептор, необязательно, CAR, не узнает специфически антиген и/или не экспрессирует никакого рекомбинантного рецептора, необязательно, никакого CAR.
65. Изделие из варианта осуществления 64, где этот параметр нормализуют для контроля специфической для пациента изменчивости показателя одного или нескольких факторов.
66. Изделие из варианта осуществления 64 или вариант осуществления 65, где параметр представляет собой нормализованное значение показателя фактора, по сравнению с таким же показателем в таком же анализе, для контрольного фактора, где для уровня контрольного фактора в терапевтической композиции T–клеток известно отсутствие или наблюдали отсутствие признака или корреляции, или значимой корреляции с исходом неблагоприятного события или токсичности, или их вероятностью или риском, где исход неблагоприятного события или токсичности необязательно, представляет собой тяжелую нейротоксичность.
67. Изделие из варианта осуществления 66, где контрольный фактор представляет собой фактор, который статистически не коррелирует и/или не коррелирует с возникновением неблагоприятного события среди множества индивидов, у которых продолжалось развитие неблагоприятного события, после введения композиции T–клеток, необязательно контрольный фактор представляет собой или содержит один из или комбинацию из IL–5, IL–13, GM–CSF и IL–6, необязательно, где показатель контрольного фактора представляет собой среднее арифметическое или среднее геометрическое из двух или более из вышеуказанного.
68. Изделие из любого из вариантов осуществления 1–67, где параметр не включает цитолитическую активность или ее показатель.
69. Изделие из любого из вариантов осуществления 1–68, где параметр не включает зависимую от рекомбинантного рецептора или антигенспецифическую цитолитическую активность или ее показатель.
70. Изделие из любого из вариантов осуществления 1–40 и 49–69, где:
фенотип представляет собой CD8+ CAR+ клетки или маркер апоптоза – CD8+ CAR+ клетки, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; и
параметр представляет собой показатель для провоспалительного цитокина, который, необязательно, представляет собой один из или комбинацию из TNF–альфа, IL–2 и IFN–гамма, или представляет собой его нормализованное значение.
71. Изделие из любого из вариантов осуществления 1–70, где неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и пороговое количество единиц:
составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+ и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,0×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,5×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
72. Изделие из любого из вариантов осуществления 1–71, где неблагоприятное событие представляет собой нейротоксичность степени 4 или 5 и данный диапазон целевых эталонных единиц:
составляет между или приблизительно между 2,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 4×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 5×106 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 2,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 2,0×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 2,5×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
73. Изделие из любого из вариантов осуществления 1–70, где неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и пороговое количество единиц:
составляет или составляет приблизительно 1,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 1,25×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,88×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,12×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2; или его нормализованное значение
составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+ и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
74. Изделие из любого из вариантов осуществления 1–70 и 73, где неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и данный диапазон целевых эталонных единиц:
составляет между или приблизительно между 3,0×105 и 1,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,25×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 4×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 5×106 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 2,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 1,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,88×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 2,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 3,12×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
75. Изделие из любого из вариантов осуществления 1–74, где терапевтическая композиция T–клеток содержит между приблизительно 10 миллионов клеток на мл и приблизительно 70 миллионов клеток на мл или между приблизительно 10 миллионов жизнеспособных клеток на мл и приблизительно 70 миллионов жизнеспособных клеток на мл, включая каждое.
76. Изделие из любого из вариантов осуществления 1–75, где терапевтическая композиция T–клеток содержит между приблизительно 15 миллионов клеток или жизнеспособных клеток на мл и приблизительно 60 миллионов клеток или жизнеспособных клеток на мл, включительно.
77. Изделие из любого из вариантов осуществления 1–76, где композиция T–клеток содержит более чем 10 миллионов клеток или жизнеспособных клеток на мл.
78. Изделие из любого из вариантов осуществления 1–77, где терапевтическая композиция T–клеток содержит более чем 15 миллионов клеток или более чем 15 миллионов клеток на мл.
79. Изделие из любого из вариантов осуществления 1–78, где композиция дополнительно содержит криопротектор, и/или изделие дополнительно содержит инструкции для размораживания композиции перед введением индивиду.
80. Изделие из любого из вариантов осуществления 1–79, где заболевание или состояние представляет собой злокачественную опухоль, необязательно, миелому, лимфому или лейкоз.
81. Изделие из варианта осуществления 80, где заболевание или состояние представляет собой злокачественное новообразование из B–клеток, необязательно, злокачественное новообразование из B–клеток, выбранное из группы, состоящей из острого лимфобластного лейкоза (ALL), ALL взрослых, хронического лимфобластного лейкоза (CLL), неходжскинской лимфомы (NHL) и диффузной крупноклеточной B–клеточной лимфомы (DLBCL).
82. Изделие из любого из вариантов осуществления 1–81, где антиген представляет собой CD19, CD22, ROR1, Ig–каппа, Her2, L1–CAM, CD20, мезотелин, CEA, поверхностный антиген вируса гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, EGP–2, EGP–4, EPHa2, ErbB2, ErbB3, ErbB4, FBP, фетальный рецептор ацетилхолина, GD2, GD3, HMW–MAA, IL–22R–альфа, IL–13R–альфа2, kdr, легкую цепь каппа, Lewis Y, молекулы клеточной адгезии L1, MAGE–A1, мезотелин, MUC1, MUC16, PSCA, лиганды NKG2D, NY–ESO–1, MART–1, gp100, онкофетальный антиген, TAG72, VEGF–R2, карциноэмбриональный антиген (CEA), простатспецифического антигена, PSMA, рецептор эстрогенов, рецептор прогестерона, эфринB2, CD123, CS–1, c–Met, GD–2, MAGE A3, CE7, антиген опухоли Вильмса 1 (WT–1) и циклин A1 (CCNA1).
83. Изделие из любого из вариантов осуществления 1–82, где рекомбинантный рецептор представляет собой CAR.
84. Изделие из варианта осуществления 83, где CAR содержит внеклеточный узнающий антиген домен, который специфически связывается с антигеном, и внутриклеточный передающий сигналы домен, содержащий ITAM, где необязательно, внутриклеточный передающий сигналы домен содержит внутриклеточный домен из цепи CD3–зета (CD3ζ); и/или где CAR дополнительно содержит область передачи костимулирующих сигналов, которая, необязательно, содержит передающий сигналы домен из CD28 или 4–1BB.
85. Изделие из любого из вариантов осуществления 1–84, где T–клетки представляют собой CD4+ или CD8+.
86. Изделие из любого из вариантов осуществления 1–85, где T–клетки представляют собой первичные T–клетки, полученные от индивида.
87. Изделие из любого из вариантов осуществления 1–86, где изделие дополнительно содержит информацию, указывающую, что контейнер содержит целевое количество единиц.
88. Изделие из любого из вариантов осуществления 1–87, где контейнер представляет собой первый контейнер, и изделие, кроме того, содержит дополнительные контейнеры, где каждый из дополнительных контейнеров содержит единичную дозу, содержащую целевое количество единиц из композиции T–клеток.
89. Изделие из варианта осуществления 88, где дополнительные контейнеры содержат между приблизительно 10 миллионов клеток или жизнеспособных клеток на мл и приблизительно 70 миллионов клеток или жизнеспособных клеток на мл, между приблизительно 15 миллионов клеток или жизнеспособных клеток и приблизительно 60 миллионов клеток или жизнеспособных клеток на мл, включая каждое, или более чем 10 миллионов клеток или жизнеспособных клеток на мл, более чем 15 миллионов клеток или жизнеспособных клеток на мл, или их комбинацию.
90. Изделие из любого из вариантов осуществления 1–89, где единичная доза содержит количество не более чем 15×106 CD8+CAR+ клеток, которые являются отрицательными при детекции по аннексину V или по активной каспазе 3 или проформе каспазы 3.
91. Изделие из любого из вариантов осуществления 1–90, где единичная доза дополнительно содержит количество CD4+ клеток, положительных по CAR, где количество находится в соотношении или приблизительно в соотношении CD8+CAR+ клеток 1:1.
92. Композиция из изделия из любого из вариантов осуществления 1–91, где композицию T–клеток получают способом, в котором:
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции, и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на признаки биологически активных клеток и/или отсутствия апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем 5% от среднего указанной частоты во множестве композиций T–клеток, полученных этим способом, и/или отличается от такого среднего не более чем на одно стандартное отклонение; или
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции, и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на отсутствие апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 20%, или не более чем на 10%, среди множества композиций T–клеток, полученных этим способом
93. Изделие из варианта осуществления 92, где способ включает:
(a) инкубацию популяции клеток, содержащей T–клетки, со средством, содержащим молекулу нуклеиновой кислоты, кодирующую рекомбинантный рецептор, в условиях для введения нуклеиновой кислоты, кодирующей рекомбинантный рецептор, в клетки в популяции; и
(b) стимуляцию клеток, до, во время и/или после указанной инкубации, где стимуляция включает инкубацию клеток при наличии стимулирующего условия, индуцирующего первичный сигнал, передачу сигналов, стимуляцию, активацию и/или размножение клеток.
94. Изделие из варианта осуществления 93, где способ дополнительно включает, перед (a), выделение популяции клеток из биологического образца.
95. Изделие из варианта осуществления 94, где выделение включает отбор клеток на основании поверхностной экспрессии CD3 или на основании поверхностной экспрессии одного или обоих из CD4 и CD8, необязательно, посредством положительного или отрицательного отбора.
96. Изделие из варианта осуществления 94 или варианта осуществления 95, где выделение включает проведение иммуноотбора на основании аффинности.
97. Изделие из варианта осуществления 94–96, где биологический образец представляет собой или содержит образец цельной крови, образец лейкоцитарной пленки, образец мононуклеарных клеток периферической крови (PBMC), образец нефракционированных T–клеток, образец лимфоцитов, образец лейкоцитов, продукт афереза или продукт лейкафереза.
98. Изделие из любого из вариантов осуществления 93–97, где стимулирующее условие включает инкубацию со стимулирующим реагентом, способным активировать один или несколько внутриклеточных доменов передачи сигналов одного или нескольких компонентов комплекса TCR, и/или один или несколько внутриклеточных доменов передачи сигналов одной или нескольких костимулирующих молекул.
99. Изделие из варианта осуществления 98, где стимулирующий реагент содержит первичное средство, которое специфически связывается с членом комплекса TCR, и вторичное средство, которое специфически связывается с костимулирующей молекулой T–клетки.
100. Изделие из варианта осуществления 98 или вариант осуществления 99, где первичное средство специфически связывается с CD3 и/или костимулирующей молекулой, выбранной из группы, состоящей из CD28, CD137 (4–1–BB), OX40 или ICOS.
101. Изделие из варианта осуществления 99 или варианта осуществления 100, где первичное и вторичное средства содержат антитела и/или присутствуют на поверхности твердой подложки, необязательно, бусины.
102. Изделие из любого из вариантов осуществления 98–101, где:
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, от среднего показателя продукции или накопления провоспалительного цитокина среди множества композиций T–клеток, полученных этим способом с использованием стимулирующего реагента, и/или отличается от такого среднего не более чем на одно стандартное отклонение; и/или
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10% или не более чем на 5%, среди множества композиций T–клеток, полученных этим способом; и/или
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, для композиции клеток, полученной с использованием стимулирующего реагента, отличается не более чем на 40%, не более чем на 30%, не более чем на 20% или не более чем на 10% или не более чем на 5% от контрольной композиции, где контрольная композиция и композиция клеток получены с использованием одинакового способа, включая получение из такой же популяции клеток, за исключением того, что контрольная композиция реализована в присутствии контрольного стимулирующего реагента, или стандартного количества единиц зависимой от рекомбинантного рецептора активности.
103. Изделие из варианта осуществления 102, где контрольный стимулирующий реагент, при использовании в способе, приводит к получению композиции T–клеток, в которой зависимая от рекомбинантного рецептора активность или антигенспецифическая активность находится в пределах приемлемого диапазона изменчивости.
104. Изделие из любого из вариантов осуществления 93–103, где стимуляцию клеток проводят или инициируют до инкубации, необязательно, в течение 18–24 часов при или приблизительно при 37 градусов.
105. Изделие из любого из вариантов осуществления 93–104, где стимулирующее условие включает цитокин, выбранный среди IL–2, IL–15 и IL–7.
106. Изделие из любого из вариантов осуществления 93–105, где стимуляцию клеток проводят после инкубации, необязательно, в течение периода времени для достижения пороговой концентрации.
107. Изделие из любого из вариантов осуществления 93–106, дополнительно включающее (c) заполнение контейнера всей или частью композиции T–клеток, и необязательно, другим раствором, до концентрации между приблизительно 10 миллионов клеток и приблизительно 70 миллионов клеток на мл, включительно.
108. Изделие из варианта осуществления 107, где контейнер заполняют другим раствором, и раствор содержит криопротектор, необязательно DMSO.
109. Изделие из варианта осуществления 107 или варианта осуществления 108, где концентрация составляет между приблизительно 15 и приблизительно 60 миллионов клеток на мл, включительно.
110. Изделие из любого из вариантов осуществления 107–109, где концентрация составляет более чем 10 миллионов клеток на мл.
111. Изделие из любого из вариантов осуществления 107–110, где концентрация составляет более чем 15 миллионов клеток на мл.
112. Изделие из любого из вариантов осуществления 107–111, где концентрация DMSO составляет или составляет приблизительно, или не превышает 7,5%.
113. Изделие из варианта осуществления 107 или варианта осуществления 108, где концентрация составляет более чем 60 миллионов клеток на мл.
114. Изделие из любого из вариантов осуществления 107–108 и 113, где концентрация DMSO составляет более чем 7,5%, необязательно, между или приблизительно между 7,5% и 9,0%, включительно.
115. Изделие из любого из вариантов осуществления 93–114, где средство, содержащее молекулу нуклеиновой кислоты, кодирующую рекомбинантный рецептор, представляет собой вирусный вектор, необязательно, лентивирусный вектор или гамма–ретровирусный вектор.
116. Изделие из любого из вариантов осуществления 107–115, где заполнение проводят в автоматическом режиме, необязательно, в закрытой системе.
117. Изделие из любого из вариантов осуществления 93–116, дополнительно включающее замораживание клеток в контейнере или хранение контейнера при температуре менее чем или приблизительно менее чем 80ºC.
118. Способ лечения, включающий введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащей клетки, содержащие рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит целевое количество эталонных единиц (RU) в пределах данного диапазона, где RU в данной композиции определяют по формуле
RU=A x B, где:
A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции.
119. Способ из варианта осуществления 118, где A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции.
120. Способ из варианта осуществления 118, где A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
121. Способ из любого из вариантов осуществления 118–120, где целевое количество единиц составляет менее, чем пороговое количество RU, необязательно, представляющее собой безопасное количество эталонных единиц, где безопасное количество эталонных единиц представляет собой, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
122. Способ из варианта осуществления 121, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность, необязательно степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
123. Способ из варианта осуществления 121 или варианта осуществления 122, где целевое количество эталонных единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, и/или на количество в диапазоне от 1,5– до 3–кратного, необязательно, приблизительно 2–кратное, или на количество, кратное стандартному отклонению в группе индивидов, у которых не возникло неблагоприятного события, необязательно, нейротоксичности степени 0–2, необязательно, где кратное лежит в диапазоне от 1,5– до 3–кратного.
124. Способ из любого из вариантов осуществления 118–123, где целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, для которой показан желательный терапевтический исход, необязательно, частичный ответ или полный ответ (CR).
125. Способ лечения, включающий введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащей клетки, содержащие рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит или содержит приблизительно (i) целевое количество тотальных экспрессирующих рекомбинантный рецептор клеток или целевое количество тотальных CD8+ экспрессирующих рекомбинантный рецептор клеток или (ii) целевое количество эталонных единиц (RU) в пределах данного диапазона, где целевое количество равно или меньше порогового количества RU, где единичная доза не содержит больше порогового значения RU,
где количество RU в данной композиции определяют по формуле:
RU=A x B, где
A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции T–клеток.
126. Способ из варианта осуществления 125, где A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции.
127. Способ из варианта осуществления 125, где A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
128. Способ из любого из вариантов осуществления 118–127, где целевое количество представляет собой целевое количество экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD3+ или CD8+, которые являются отрицательными(–) по маркеру апоптоза и CD3+ или CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
129. Способ из любого из вариантов осуществления 125–128, где целевое количество клеток в (i) составляет: между и между приблизительно 5,0×106 и 2,25×107, 5,0×106 и 2,0×107, 5,0×106 и 1,5×107, 5,0×106 и 1,0×107, 5,0×106 и 7,5×106, 7,5×106 и 2,25×107, 7,5×106 и 2,0×107, 7,5×106 и 1,5×107, 7,5×106 и 1,0×107, 1,0×107 и 2,25×107, 1,0×107 и 2,0×107, 1,0×107 и 1,5×107, 1,5×107 и 2,25×107, 1,5×107 и 2,0×107, 2,0×107 и 2,25×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
130. Способ из любого из вариантов осуществления 125–129, где целевое количество клеток в (i) составляет:
между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными (–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 5,55×106, 6,66×106, 7,77×106, 8,99×106, 1,0×107, 1,1×107 и приблизительно 1,67×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 7,14×106, 8,5×106, 1,0×107, 1,14×107, 1,29×107, 1,42×107 и приблизительно 2,14×107 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
131. Способ из любого из вариантов осуществления 125–130, где целевое количество клеток в (i) составляет между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, которые являются отрицательными(–) по маркеру апоптоза и CD8+, включая каждое, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
132. Способ из любого из вариантов осуществления 125–130, где целевое количество клеток в (i) составляет между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, включая каждое.
133. Способ из любого из вариантов осуществления 118–132, где целевое эталонное количество RU составляет менее, чем эталонное безопасное количество RU, где эталонное безопасное количество RU составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
134. Способ из варианта осуществления 133, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
135. Способ из варианта осуществления 133 или варианта осуществления 134, где целевое эталонное количество RU составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, или по меньшей мере в 2 раза.
136. Способ из любого из вариантов осуществления 118–135, где целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество эталонных единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, для которой показан желательный терапевтический исход, необязательно, полный ответ (CR).
137. Способ из любого из вариантов осуществления 118–136, где A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции.
138. Способ из любого из вариантов осуществления 118–137, где A и/или B представляет собой преобразование количества или значения, соответственно, где преобразование включает логарифмическое преобразование, степенное преобразование или логит–преобразование.
139. Способ из любого из вариантов осуществления 118–138, где A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой кратное или преобразование значения параметра, указывающего на степень или коррелирующего со степенью зависимой от CAR активности в данной композиции T–клеток, необязательно, где B представляет собой логарифмическое преобразование значения.
140. Способ из варианта осуществления 138 или варианта осуществления 139, где логарифмическое преобразование представляет собой десятичный log (log10(x)), натуральный log (ln(x)) или двоичный log (log2(x)).
141. Способ из любого из вариантов осуществления 118–140, где A представляет собой количество жизнеспособных клеток в композиции и/или представляет собой количество клеток, которые не являются апоптотическими, не имеют фактора, показательного для раннего апоптоза или апоптоза, не находятся на ранних стадиях апоптоза, или не находятся на поздних стадиях апоптоза, и/или представляет собой количество клеток в определенном состоянии дифференцировки, и/или представляет собой количество клеток, имеющих признак клеток памяти/стволовых клеток, или представляет собой его кратное или преобразование.
142. Способ из любого из вариантов осуществления 118–141, где фенотип включает положительную экспрессию поверхностного маркера, представляющего собой один или несколько из CD3, CD4 или CD8, и/или включает положительную экспрессию рекомбинантного рецептора, необязательно, CAR, или суррогатный маркер экспрессии рекомбинантного рецептора.
143. Способ из варианта осуществления 142, где фенотип представляет собой CD3+ CAR, CD4+/CAR+, CD8+/CAR+.
144. Способ из любого из вариантов осуществления 118–143, где фенотип включает отсутствие фактора, показательного для апоптоза или одной или нескольких стадий апоптотического каскада или пути, необязательно, экспрессии маркера апоптоза.
145. Способ из любого из вариантов осуществления 118–144, где фенотип включает отрицательную экспрессию маркера апоптоза, необязательно, маркера раннего апоптоза или позднего апоптоза.
146. Способ из варианта осуществления 145, где маркер апоптоза представляет собой поверхностный фосфатидилсерин и/или детектирован с использованием аннексина V, или представляет собой активную каспазу или проформу каспазы, необязательно, активную каспазу 3 или проформу каспазы 3.
147. Способ из любого из вариантов осуществления 118–146, где фенотип включает аннексин–.
148. Способ из любого из вариантов осуществления 118–147, где фенотип включает показатель продукции одного или комбинации цитокинов, необязательно, не специфической для антигена или рекомбинантного рецептора и/или поликлональной продукции, где один или несколько цитокинов представляет собой IL–2, IL–13, IL–17, IFN–гамма или TNF–альфа.
149. Способ из варианта осуществления 148, где показатель продукции измеряют в анализе, необязательно, анализе окрашивания внутриклеточных цитокинов, включающем инкубацию образца из композиции T–клеток с поликлональным средством, антигенспецифическим средством или средством, связывающим рекомбинантный рецептор, необязательно CAR.
150. Способ из варианта осуществления 148 или варианта осуществления 149, где средство представляет собой или содержит PMA и иономицин, или представляет собой или содержит T–клеточный рецептор или агонист комплекса T–клеточного рецептора.
151. Способ из любого из вариантов осуществления 118–150, где фенотип включает отрицательную экспрессию маркера активации, где маркер активации выбран среди CD25, CD127, LAG3, Ki67 и их комбинаций.
152. Способ из любого из вариантов осуществления 118–151, где фенотип включает отрицательную экспрессию маркера истощения, где маркер истощения представляет собой продукт гена PD1 или FOXP3, или их комбинацию.
153. Способ из любого из вариантов осуществления 118–152, где фенотип включает наивный фенотип или фенотип клеток памяти, необязательно, где фенотип клеток памяти включает фенотип эффекторных T–клеток памяти, фенотип центральных T–клеток памяти, или фенотип эффекторных T–клеток памяти, экспрессирующих CD45RA (Temra).
154. Способ из любого из вариантов осуществления 118–153, где A представляет собой общее количество T–клеток, общее количество CD3+ клеток, общее количество CD4+ или CD8+ клеток, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, общее количество CD4+ CAR+, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение.
155. Способ из любого из вариантов осуществления 118–154, где A представляет собой общее количество CD3+ клеток, общее количество CD8+, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение.
156. Способ из любого из вариантов осуществления 118–155, где A представляет собой общее количество отрицательных (–) по маркеру апоптоза клеток, которые являются CD3+ CAR+ клетки, общее количество отрицательных (–) по маркеру апоптоза клеток, которые являются CD4+ CAR+, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD8+ CAR+ клетки, или его кратное или преобразованное значение, где маркер апоптоза представляет собой аннексин V или каспазу.
157. Способ из любого из вариантов осуществления 118–156, где A представляет собой общее количество маркер апоптоза– CD3+ CAR+ клеток или общее количество маркер апоптоза– CD8+ CAR+ клеток, где маркер апоптоза представляет собой аннексин V или каспазу 3
158. Способ лечения, включающий введение индивиду, страдающему заболеванием или состоянием, единичной дозы композиции T–клеток, содержащей клетки, содержащие рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где единичная доза содержит целевую дозу терапевтической композиции T–клеток:
(i) если значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности композиции, равно или больше порогового значения, целевая доза представляет собой первое количество (или лежит в первом диапазоне количеств) клеток данного фенотипа из композиции;
(ii) если значение параметра меньше порогового значения, целевая доза представляет собой второе количество (или лежит во втором диапазоне количеств) клеток данного фенотипа из композиции
где первое количество (или первый диапазон) ниже, чем второе количество (или второй диапазон).
159. Способ из варианта осуществления 158, где пороговое значение зависимой от рекомбинантного рецептора активности менее, чем эталонный уровень безопасности, где эталонный уровень безопасности составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наиболее низкий уровень зависимой от CAR активности терапевтической композиции, введенной индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
160. Способ из варианта осуществления 159, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
161. Способ из варианта осуществления 159 или вариант осуществления 160, где пороговое значение составляет менее, чем эталонный уровень безопасности, на количество, соответствующее коэффициенту запаса безопасности, или по меньшей мере в 2 раза.
162. Способ из любого из вариантов осуществления 159–161, где первое количество ниже, чем второе количество, более чем в или более чем приблизительно в 1,5 раза, 2,0 раза, 3,0 раза, 4,0 раза, 5,0 раз, 6,0 раз, 7,0 раз, 8,0 раз, 9,0 раз, 10,0 раз или более.
163. Способ из любого из вариантов осуществления 118–162 где зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления провоспалительного цитокина, необязательно, одного или комбинации из TNF–альфа, IFN–гамма, IL–2 и IL–10.
164. Способ из любого из вариантов осуществления 118–163, где параметр представляет собой показатель одного или нескольких факторов или его нормализованное значение.
165. Способ из варианта осуществления 164, где показатель определяют в анализе, включающем культивирование или инкубацию в течение фиксированного времени, необязательно, 24 часов, данной композиции или образца из нее в присутствии антигена, клеток, экспрессирующих антиген, и/или средства, специфически связывающегося с рекомбинантным рецептором, необязательно, CAR.
166. Способ из варианта осуществления 165, где анализ представляет собой ELISA.
167. Способ из любого из вариантов осуществления 164–166, где показатель фактора представляет собой:
(i) концентрацию, относительную концентрацию, количество или относительное количество фактора; или
(ii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции, или
(iii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции в единицу времени, необязательно, один час; или
(iv) уровень, показательный для любого из (i)–(iii).
168. Способ из любого из вариантов осуществления 164–167, где один или несколько факторов представляет собой один или комбинацию из растворимых факторов, необязательно, один или комбинацию из цитокинов, хемокинов или растворимых рецепторов, необязательно, растворимых костимулирующих рецепторов.
169. Способ из любого из вариантов осуществления 164–168, где один или несколько факторов представляет собой один или комбинацию из провоспалительных цитокинов, Th2–цитокинов и Th17–цитокинов.
170. Способ из любого из вариантов осуществления 164–169, где один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа, IL4, IL–5, IL–10, IL–13, GM–CSF, sCD137, MIP1a и M1Pb.
171. Способ из любого из вариантов осуществления 164–170, где один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа и IL–10.
172. Способ из любого из вариантов осуществления 168–171, где один или несколько факторов представляет собой комбинацию любых двух или более из вышеуказанных растворимых факторов, и параметр представляет собой среднее арифметическое или среднее геометрическое из показателей для двух или более факторов.
173. Способ из любого из вариантов осуществления 168–172, где параметр представляет собой среднее арифметическое или среднее геометрическое показателя, необязательно, количества или концентрации, для по меньшей мере двух из TNF–альфа, IFN–гамма и IL–2 или из TNF–альфа, IFN–гамма и IL–2.
174. Способ из любого из вариантов осуществления 164–173, где параметр представляет собой нормализованное значение показателя, где нормализация проведена по сравнению с эталонным показателем фактора.
175. Изделие из варианта осуществления 174, где эталонный показатель представляет собой среднее из показателей среди множества, необязательно по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, из эталонных терапевтических композиций T–клеток, содержащих химерный антигенный рецептор (CAR), в которых:
(i) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате приемлемый профиль безопасности после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном; и/или
(ii) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате желательную эффективность после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном.
176. Способ из варианта осуществления 175, где приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 2 или выше, или отсутствие нейротоксичности степени 3 или выше.
177. Способ из варианта осуществления 175 или варианта осуществления 176, где приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 3 или выше.
178. Способ из варианта осуществления 177, где эффективность представляет собой частичный ответ или представляет собой полный ответ (CR).
179. Способ из варианта осуществления 178, где эталонный показатель представляет собой показатель, в таком же анализе, фактора в эталонной композиции T–клеток, которая получена таким же способом, как терапевтическая композиция T–клеток, но не экспрессирует рекомбинантный рецептор, необязательно, CAR, не узнает специфически антиген и/или не экспрессирует никакого рекомбинантного рецептора, необязательно, никакого CAR.
180. Способ из варианта осуществления 179, где этот параметр нормализуют для контроля специфической для пациента изменчивости показателя одного или нескольких факторов.
181. Способ из варианта осуществления 179 или вариант осуществления 180, где параметр представляет собой нормализованное значение показателя фактора, по сравнению с таким же показателем в таком же анализе, для контрольного фактора, где для уровня контрольного фактора в терапевтической композиции T–клеток известно отсутствие или наблюдали отсутствие признака или корреляции, или значимой корреляции с исходом неблагоприятного события или токсичности, или их вероятностью или риском, где исход неблагоприятного события или токсичности необязательно, представляет собой тяжелую нейротоксичность.
182. Способ из варианта осуществления 181, где контрольный фактор представляет собой или содержит фактор, который статистически не коррелирует и/или не коррелирует с возникновением неблагоприятного события среди множества индивидов, у которых продолжалось развитие неблагоприятного события, после введения композиции T–клеток, необязательно, контрольный фактор представляет собой один из или комбинацию из IL–5, IL–13, GM–CSF, и IL–6, необязательно, где показатель контрольного фактора представляет собой среднее арифметическое или среднее геометрическое из двух или более из вышеуказанного.
183. Способ из любого из вариантов осуществления 118–182, где параметр не включает цитолитическую активность или ее показатель.
184. Способ из любого из вариантов осуществления 118–183, где параметр не включает зависимую от рекомбинантного рецептора или антигенспецифическую цитолитическую активность или ее показатель.
185. Способ из любого из вариантов осуществления 118–184, где:
фенотип представляет собой CD8+ CAR+ клетки или маркер апоптоза – CD8+ CAR+ клетки, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; и
параметр представляет собой показатель для провоспалительного цитокина, который, необязательно, представляет собой один из или комбинацию из TNF–альфа, IL–2 и IFN–гамма, или представляет собой его нормализованное значение.
186. Способ из любого из вариантов осуществления 118–185, где неблагоприятное событие представляет собой нейротоксичность степени 4 или 5 и пороговое значение:
составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,0×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,5×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
187. Способ из любого из вариантов осуществления 118–186, где неблагоприятное событие представляет собой нейротоксичность степени 4 или 5 и данный диапазон целевых эталонных единиц:
составляет между или приблизительно между 2,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 4×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 5×106 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 2,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 2,0×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 2,5×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
188. Способ из любого из вариантов осуществления 118–185, где неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и пороговое значение:
составляет или составляет приблизительно 1,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 1,25×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,88×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,12×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2; или его нормализованное значение
составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
189. Способ из любого из вариантов осуществления 118–185 и 188, где неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и данный диапазон целевых эталонных единиц:
составляет между или приблизительно между 3,0×105 и 1,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,25×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 4×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 5×106 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 2,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 1,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,88×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 2,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 3,12×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
190. Способ из любого из вариантов осуществления 118–189, где терапевтическая композиция T–клеток содержит между приблизительно 10 миллионов клеток на мл и приблизительно 70 миллионов клеток на мл или между приблизительно 10 миллионов жизнеспособных клеток на мл и приблизительно 70 миллионов жизнеспособных клеток на мл, включая каждое.
191. Способ из любого из вариантов осуществления 118–190, где терапевтическая композиция T–клеток содержит между приблизительно 15 миллионов клеток или жизнеспособных клеток на мл и приблизительно 60 миллионов клеток или жизнеспособных клеток на мл, включая каждое.
192. Способ из любого из вариантов осуществления 118–191, где композиция T–клеток содержит более чем 10 миллионов клеток или жизнеспособных клеток на мл.
193. Способ из любого из вариантов осуществления 118–192, где терапевтическая композиция T–клеток содержит более чем 15 миллионов клеток или более чем 15 миллионов клеток на мл.
194. Способ из любого из вариантов осуществления 118–193, где заболевание или состояние представляет собой злокачественную опухоль, необязательно, миелому, лимфому или лейкоз.
195. Способ из варианта осуществления 194, где заболевание или состояние представляет собой злокачественное новообразование из B–клеток, необязательно, злокачественное новообразование из B–клеток, выбранное из группы, состоящей из острого лимфобластного лейкоза (ALL), ALL взрослых, хронического лимфобластного лейкоза (CLL), неходжскинской лимфомы (NHL) и диффузной крупноклеточной B–клеточной лимфомы (DLBCL).
196. Способ из любого из вариантов осуществления 118–195, где антиген представляет собой CD19, CD22, ROR1, Ig–каппа, Her2, L1–CAM, CD20, мезотелин, CEA, поверхностный антиген вируса гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, EGP–2, EGP–4, EPHa2, ErbB2, ErbB3, ErbB4, FBP, фетальный рецептор ацетилхолина, GD2, GD3, HMW–MAA, IL–22R–альфа, IL–13R–альфа2, kdr, легкую цепь каппа, Lewis Y, молекулы клеточной адгезии L1, MAGE–A1, мезотелин, MUC1, MUC16, PSCA, лиганды NKG2D, NY–ESO–1, MART–1, gp100, онкофетальный антиген, TAG72, VEGF–R2, карциноэмбриональный антиген (CEA), простатспецифического антигена, PSMA, рецептор эстрогенов, рецептор прогестерона, эфрин B2, CD123, CS–1, c–Met, GD–2, MAGE A3, CE7, антиген опухоли Вильмса 1 (WT–1) и циклин A1 (CCNA1).
197. Способ из любого из вариантов осуществления 118–196, где рекомбинантный рецептор представляет собой CAR.
198. Способ из варианта осуществления 197, где CAR содержит внеклеточный узнающий антиген домен, который специфически связывается с антигеном, и внутриклеточный передающий сигналы домен, содержащий ITAM, где необязательно, внутриклеточный передающий сигналы домен содержит внутриклеточный домен из цепи CD3–зета (CD3ζ); и/или где CAR дополнительно содержит область передачи костимулирующих сигналов, которая, необязательно, содержит передающий сигналы домен из CD28 или 4–1BB.
199. Способ из любого из вариантов осуществления 118–198, где T–клетки представляют собой CD4+ или CD8+.
200. Способ из любого из вариантов осуществления 118–199, где T–клетки представляют собой первичные T–клетки, необязательно, где T–клетки являются аутологичными для индивида или аллогенными для индивида.
201. Способ из любого из вариантов осуществления 118–200, где единичная доза содержит количество не более, чем 15×106 CD8+CAR+ клеток, которые являются отрицательными при детекции по аннексину V или по активной каспазе 3 или проформе каспазы 3.
202. Способ из любого из вариантов осуществления 118–201, где единичная доза дополнительно содержит количество CD4+ клеток, положительных по CAR, где количество находится в соотношении, по меньшей мере, или находится в соотношении CD8+CAR+ клеток 1:1 или приблизительно 1:1.
203. Способ из любого из вариантов осуществления 118–202, где способ дополнительно включает проведение противолимфоцитарной химиотерапии перед введением композиции T–клеток, и/или где индивида подвергают противолимфоцитарной химиотерапии перед введением композиции T–клеток.
204. Способ из варианта осуществления 203, где противолимфоцитарная химиотерапия включает введение флударабина и/или циклофосфамида индивиду.
205. Способ из варианта осуществления 204, где циклофосфамид вводят в количестве от или приблизительно от 30 мг/кг до 60 мг/кг, и/или флударабин вводят в количестве от или приблизительно от 25 мг/м2 до 30 мг/м2.
206. Способ из варианта осуществления 204, где:
циклофосфамид вводят в количестве от или приблизительно от 900 до 1000 мг, и/или флударабин вводят в количестве от или приблизительно от 25 мг/м2 до 30 мг/м2; или
циклофосфамид вводят в количестве от или приблизительно от 300 мг/м2, и/или флударабин вводят в количестве от или приблизительно от 30 мг/м2.
207. Способ из варианта осуществления 204, где циклофосфамид вводят в количестве от или приблизительно от 500 мг/м2, и/или флударабин вводят в количестве от или приблизительно от 30 мг/м2.
208. Способ из варианта осуществления 204, где циклофосфамид вводят в количестве от или приблизительно от 500 мг/м2, и/или флударабин вводят в количестве от или приблизительно от 60 мг/м2.
209. Способ из любого из вариантов осуществления 203–208, где противолимфоцитарное лекарственное средство вводят один раз в сутки в течение трех последовательных суток.
210. Способ из любого из вариантов осуществления 203–209, где противолимфоцитарное лекарственное средство вводят на 5–е сутки перед, на 4–е сутки перед и на 3–е сутки перед введением композиции T–клеток.
211. Способ из любого из вариантов осуществления 203–210, где противолимфоцитарное лекарственное средство вводят один раз в сутки в течение 3–5 суток, необязательно, один раз в сутки в течение 3 суток.
212. Способ из любого из вариантов осуществления 204–211, где флударабин и циклофосфамид вводят последовательно.
213. Способ из любого из вариантов осуществления 204–211, где флударабин и циклофосфамид вводят одновременно.
214. Способ анализа терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающий:
(a) анализ образца из композиции T–клеток, содержащей T–клетки, происходящие от индивида, имеющего заболевание или состояние, и трансдуцированные нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где анализ определяет B для композиции клеток, где B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции; и
(b) оценку активности композиции клеток на основании B и/или оценку того, находится ли композиция выше нижнего установленного предела (LSL) для B или ниже верхнего установленного предела (USL) для B.
215. Способ оценки терапевтической композиции T–клеток, включающий оценку образца из композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, по активности композиции клеток на основании B, и/или оценку того, находится ли композиция выше нижнего установленного предела (LSL) для B или ниже верхнего установленного предела (USL) для B.
216. Способ из варианта осуществления 214 или вариант осуществления 215, где продукт выпускают для лечения индивида, только если композиция находится ниже USL для B.
217. Способ из варианта осуществления 214 или варианта осуществления 215, где если B превышает USL, рекомендуют не вводить композицию индивиду или изменить количество клеток, вводимых индивиду, до корректированной единичной дозы, где корректированная единичная доза доза содержит целевое количество клеток или целевое количество эталонных единиц (RU) из композиции T–клеток, где RU в данной композиции определяют по формуле
RU=A x B, где:
A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его долю, или кратное, или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции.
218. Способ из любого из вариантов осуществления 214–217, где A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции.
219. Способ из любого из вариантов осуществления 214–217, где A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
220. Способ из любого из вариантов осуществления 214–219, где целевое количество единиц составляет менее, чем пороговое количество единиц, необязательно, представляющее собой безопасное количество эталонных единиц, где безопасное количество эталонных единиц представляет собой, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
221. Способ из варианта осуществления 220, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность, необязательно степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
222. Способ из варианта осуществления 220 или варианта осуществления 221, где целевое количество эталонных единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, и/или на количество в диапазоне от 1,5– до 3–кратного, необязательно, приблизительно 2–кратное, или на количество, кратное стандартному отклонению в группе индивидов, у которых не возникло неблагоприятного события, необязательно, нейротоксичности степени 0–2, необязательно, где кратное лежит в диапазоне от 1,5– до 3–кратного.
223. Способ из любого из вариантов осуществления 217–222, где целевое количество эталонных единиц составляет или превышает эталонное эффективное количество эталонных единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, для которой показан желательный терапевтический исход, необязательно, частичный ответ или полный ответ (CR).
224. Способ из любого из вариантов осуществления 217–223, где корректированная единичная доза составляет менее чем, необязательно, менее чем 1,5–кратную, менее чем 2–кратную, менее чем 3–кратную, менее чем 4–кратную среднюю единичную дозу для группы индивидов, подвергнутых лечению с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR.
225. Способ из любого из вариантов осуществления 214–224, где образец из композиции T–клеток, необязательно, криоконсервированный образец, оценивают после введения композиции T–клеток индивиду.
226. Способ из любого из вариантов осуществления 214–225, где если B превышает USL, определяют, что индивид подвержен риску токсичности.
227. Способ из любого из вариантов осуществления 214–225, где если B превышает USL, индивида, которому вводили композицию, подвергают мониторированию и/или лечению с использованием средства для облегчения или уменьшения вероятности исхода токсичности или синдрома высвобождения цитокинов, после введения композиции клеток и, необязательно, до возникновения признака или симптома исхода токсичности.
228. Способ оценки риска токсичности терапевтической композиции T–клеток, включающий:
(a) оценку образца из композиции T–клеток, введенной индивиду, по количеству эталонных единиц (RU) в пределах данного диапазона, где композиция T–клеток содержит T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где RU в данной композиции определяют по формуле:
RU=A x B, где:
A представляет собой количество клеток, или его кратное, долю или преобразование, клеток некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его долю, или кратное, или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и
(b) сравнение количеств RU с эталонными безопасными количествами RU, где сравнение показывает, подвержен или нет индивид риску возникновения неблагоприятного события, необязательно, серьезного неблагоприятного события, необязательно тяжелой нейротоксичности степени, равной или выше степени 4 или степени 5 или по меньшей мере длительной нейротоксичности степени 3.
229. Способ из варианта осуществления 228, где A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции.
230. Способ из варианта осуществления 229, где A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
231. Способ из любого из вариантов осуществления 228–230, где эталонное безопасное количество RU составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество эталонных единиц лекарственного средства, введенное индивиду, среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
232. Способ из любого из вариантов осуществления 228–231, где если сравнение показывает, что RU выше эталонного безопасного RU, индивида, которому вводили композицию, подвергают мониторированию и/или лечению с использованием средства для облегчения или уменьшения вероятности исхода токсичности или синдрома высвобождения цитокинов, после введения композиции клеток и, необязательно, до возникновения признака или симптома исхода токсичности.
233. Способ получения терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающий:
(a) анализ композиции T–клеток, содержащей T–клетки, происходящие от индивида, имеющего заболевание или состояние, и трансдуцированные нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, где анализ определяет B для композиции клеток, где B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции; и
(b) заполнение контейнера всей или частью композиции и необязательно, другим раствором для получения единичной дозы композиции T–клеток, где единичная доза содержит целевое количество эталонных единиц (RU) из композиции T–клеток, где RU в данной композиции определяют по формуле:
RU=A x B, где A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
234. Способ получения терапевтической композиции, содержащей единичную дозу композиции T–клеток, включающий заполнение контейнера всей или частью композиции T–клеток, содержащей T–клетки, содержащие рекомбинантный рецептор, который специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, и необязательно, другим раствором, для получения единичной дозы композиции T–клеток, где единичная доза содержит целевое количество эталонных единиц (RU) из композиции T–клеток, где RU в данной композиции определяют по формуле:
RU=A x B, где
A представляет собой количество клеток, или его кратное, долю или преобразование, некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции.
235. Способ из варианта осуществления 233 или вариант осуществления 234, где A представляет собой количество клеток, или его кратное или долю, или преобразование, данного фенотипа, присутствующих в данной композиции.
236. Способ из варианта осуществления 233 или вариант осуществления 234, где A представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции.
237. Способ из любого из вариантов осуществления 217–236, где A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой значение параметра, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора активности в данной композиции.
238. Способ из любого из вариантов осуществления 217–237, где A и/или B представляет собой преобразование количества или значения, соответственно, где преобразование включает логарифмическое преобразование, степенное преобразование или логит–преобразование.
239. Способ из любого из вариантов осуществления 217–238, где A представляет собой количество клеток некоторого фенотипа, присутствующих в данной композиции, и B представляет собой кратное или преобразование значения параметра, указывающего на степень или коррелирующего со степенью зависимой от CAR активности в данной композиции T–клеток, необязательно, где B представляет собой логарифмическое преобразование значения.
240. Способ из варианта осуществления 238 или вариант осуществления 239, где логарифмическое преобразование представляет собой десятичный log (log10(x)), натуральный log (ln(x)) или двоичный log (log2(x)).
241. Способ из любого из вариантов осуществления 217–240, где A представляет собой количество жизнеспособных клеток в композиции и/или представляет собой количество клеток, которые не являются апоптотическими, не имеют фактора, показательного для раннего апоптоза или апоптоза, не находятся на ранних стадиях апоптоза, или не находятся на поздних стадиях апоптоза, и/или представляет собой количество клеток в определенном состоянии дифференцировки, и/или представляет собой количество клеток, имеющих признак клеток памяти/стволовых клеток, или представляет собой его кратное или преобразование.
242. Способ из любого из вариантов осуществления 217–241, где фенотип включает положительную экспрессию поверхностного маркера, представляющего собой один или несколько из CD3, CD4 или CD8, и/или включает положительную экспрессию рекомбинантного рецептора, необязательно, CAR, или суррогатный маркер экспрессии рекомбинантного рецептора.
243. Способ из варианта осуществления 242, где фенотип представляет собой CD3+ CAR, CD4+/CAR+, CD8+/CAR+.
244. Способ из любого из вариантов осуществления 217–243, где фенотип включает отсутствие фактора, показательного для апоптоза или одной или нескольких стадий апоптотического каскада или пути, необязательно, экспрессии маркера апоптоза.
245. Способ из любого из вариантов осуществления 217–244, где фенотип включает отрицательную экспрессию маркера апоптоза, необязательно, маркера раннего апоптоза или позднего апоптоза.
246. Способ из варианта осуществления 245, где маркер апоптоза представляет собой поверхностный фосфатидилсерин и/или детектирован с использованием аннексина V, или представляет собой активную каспазу или проформу каспазы, необязательно, активную каспазу 3 или проформу каспазы 3.
247. Способ из любого из вариантов осуществления217–246, где фенотип включает аннексин–.
248. Способ из любого из вариантов осуществления 217–247, где фенотип включает показатель продукции одного или комбинации цитокинов, необязательно, не специфической для антигена или рекомбинантного рецептора и/или поликлональной продукции, где один или несколько цитокинов представляет собой IL–2, IL–13, IL–17, IFN–гамма или TNF–альфа.
249. Способ из варианта осуществления 248, где показатель продукции измеряют в анализе, необязательно, анализе окрашивания внутриклеточных цитокинов, включающем инкубацию образца из композиции T–клеток с поликлональным средством, антигенспецифическим средством или средством, связывающим рекомбинантный рецептор, необязательно CAR.
250. Способ из варианта осуществления 248 или варианта осуществления 249, где средство представляет собой или содержит PMA и иономицин, или представляет собой или содержит T–клеточный рецептор или агонист комплекса T–клеточного рецептора.
251. Способ из любого из вариантов осуществления 217–250, где фенотип включает отрицательную экспрессию маркера активации, где маркер активации выбран среди CD25, CD127, LAG3, Ki67 и их комбинаций.
252. Способ из любого из вариантов осуществления 217–251, где фенотип включает отрицательную экспрессию маркера истощения, где маркер истощения представляет собой продукт гена PD1 или FOXP3, или их комбинацию.
253. Способ из любого из вариантов осуществления 217–252, где фенотип включает наивный фенотип или фенотип клеток памяти, необязательно, где фенотип клеток памяти включает фенотип эффекторных T–клеток памяти, фенотип центральных T–клеток памяти, или фенотип эффекторных T–клеток памяти, экспрессирующих CD45RA (Temra).
254. Способ из любого из вариантов осуществления 217–253, где A представляет собой общее количество T–клеток, общее количество CD3+ клеток, общее количество CD4+ или CD8+ клеток, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, общее количество CD4+ CAR+, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение.
255. Способ из любого из вариантов осуществления 217–253, где A представляет собой общее количество CD3+ клеток, общее количество CD8+, общее количество CD3+CAR+ клеток, общее количество CD8+CAR+ клеток, или общее количество живых или жизнеспособных клеток из любого из вышеуказанных, или его кратное или преобразованное значение.
256. Способ из любого из вариантов осуществления 217–253, где A представляет собой общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD3+ CAR+ клетки, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD4+ CAR+, общее количество отрицательных (–) по маркеру апоптоза клеток, представляющих собой CD8+ CAR+ клетки, или его кратное или преобразованное значение, где маркер апоптоза представляет собой аннексин V или каспазу.
257. Способ из любого из вариантов осуществления 217–256, где A представляет собой общее количество аннексин– CD3+ CAR+ клеток или общее количество аннексин– CD8+ CAR+ клеток.
258. Способ из любого из вариантов осуществления 214–257, где зависимая от рекомбинантного рецептора активность представляет собой показатель продукции или накопления провоспалительного цитокина, необязательно, одного или комбинации из TNF–альфа, IFN–гамма, IL–2 и IL–10.
259. Способ из любого из вариантов осуществления 214–258, где параметр представляет собой показатель одного или нескольких факторов или его нормализованное значение.
260. Способ из варианта осуществления 259, где показатель определяют в анализе, включающем культивирование или инкубацию в течение фиксированного времени, необязательно, 24 часов, данной композиции или образца из нее в присутствии антигена, клеток, экспрессирующих антиген, и/или средства, специфически связывающегося с рекомбинантным рецептором, необязательно, CAR.
261. Способ из варианта осуществления 260, где анализ представляет собой ELISA.
262. Способ из любого из вариантов осуществления 259–261, где показатель фактора представляет собой:
(i) концентрацию, относительную концентрацию, количество или относительное количество фактора; или
(ii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции, или
(iii) количество или относительное количество фактора на единицу вводимых клеток из данной композиции в единицу времени, необязательно, один час; или
(iv) уровень, показательный для любого из (i)–(iii).
263. Способ из любого из вариантов осуществления 259–262, где один или несколько факторов представляет собой один или комбинацию из растворимых факторов, необязательно, один или комбинацию из цитокинов, хемокинов или растворимых рецепторов, необязательно, растворимых костимулирующих рецепторов.
264. Способ из любого из вариантов осуществления 259–263, где один или несколько факторов представляет собой один или комбинацию из провоспалительных цитокинов, Th2–цитокинов и Th17–цитокинов.
265. Способ из любого из вариантов осуществления 259–264, где один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа, IL4, IL–5, IL–10, IL–13, GM–CSF, sCD137, MIP1a и M1Pb.
266. Способ из любого из вариантов осуществления 259–265, где один или несколько факторов представляет собой один или комбинацию из IL–2, IFN–гамма, TNF–альфа и IL–10.
267. Способ из любого из вариантов осуществления 259–266, где один или несколько факторов представляет собой комбинацию любых двух или более из вышеуказанных растворимых факторов, и параметр представляет собой среднее арифметическое или среднее геометрическое из показателей для двух или более факторов.
268. Способ из любого из вариантов осуществления 259–267, где параметр представляет собой среднее арифметическое или среднее геометрическое показателя, необязательно, количества или концентрации, для по меньшей мере двух из TNF–альфа, IFN–гамма и IL–2 или из TNF–альфа, IFN–гамма и IL–2.
269. Способ из любого из вариантов осуществления 259–268, где параметр представляет собой нормализованное значение показателя, где нормализация проведена по сравнению с эталонным показателем фактора.
270. Способ из варианта осуществления 269, где эталонный показатель представляет собой среднее из показателей среди множества, необязательно по меньшей мере 10, по меньшей мере 15, по меньшей мере 20, из эталонных терапевтических композиций T–клеток, содержащих химерный антигенный рецептор (CAR), в которых:
(i) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате приемлемый профиль безопасности после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном; и/или
(ii) для каждой из эталонных терапевтических композиций T–клеток наблюдали или определяли в результате желательную эффективность после введения индивиду, необязательно, где индивид имеет заболевание или состояние с экспрессией антигена или с ассоциацией с антигеном.
271. Способ из варианта осуществления 270, где приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 2 или выше, или отсутствие нейротоксичности степени 3 или выше.
272. Способ из варианта осуществления 270 или варианта осуществления 271, где приемлемый профиль безопасности представляет собой отсутствие наблюдаемой нейротоксичности степени 3 или выше.
273. Способ из любого из вариантов осуществления 270–272, где эффективность представляет собой частичный ответ или представляет собой полный ответ (CR).
274. Способ из варианта осуществления 269, где эталонный показатель представляет собой показатель, в таком же анализе, фактора в эталонной композиции T–клеток, которая получена таким же способом, как терапевтическая композиция T–клеток, но не экспрессирует рекомбинантный рецептор, необязательно, CAR, не узнает специфически антиген и/или не экспрессирует никакого рекомбинантного рецептора, необязательно, никакого CAR.
275. Способ из варианта осуществления 274, где этот параметр нормализуют для контроля специфической для пациента изменчивости показателя одного или нескольких факторов.
276. Способ из варианта осуществления 274 или варианта осуществления 275, где параметр представляет собой нормализованное значение показателя фактора, по сравнению с таким же показателем в таком же анализе, для контрольного фактора, где для уровня контрольного фактора в терапевтической композиции T–клеток известно отсутствие или наблюдали отсутствие признака или корреляции, или значимой корреляции с исходом неблагоприятного события или токсичности, или их вероятностью или риском, где исход неблагоприятного события или токсичности необязательно, представляет собой тяжелую нейротоксичность.
277. Способ из варианта осуществления 276, где контрольный фактор представляет собой или содержит фактор, который статистически не коррелирует и/или не коррелирует с возникновением неблагоприятного события среди множества индивидов, у которых продолжалось развитие неблагоприятного события, после введения композиции T–клеток, необязательно, контрольный фактор представляет собой один из или комбинацию из IL–5, IL–13, GM–CSF и IL–6, необязательно, где показатель контрольного фактора представляет собой среднее арифметическое или среднее геометрическое из двух или более из вышеуказанного.
278. Способ из любого из вариантов осуществления 214–277, где параметр не включает цитолитическую активность или ее показатель.
279. Способ из любого из вариантов осуществления 214–278, где параметр не включает зависимую от рекомбинантного рецептора или антигенспецифическую цитолитическую активность или ее показатель.
280. Способ из любого из вариантов осуществления 217–279, где:
фенотип представляет собой CD8+ CAR+ клетки или маркер апоптоза– CD8+ CAR+ клетки, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3; и
параметр представляет собой показатель для провоспалительного цитокина, который, необязательно, представляет собой один из или комбинацию из TNF–альфа, IL–2 и IFN–гамма, или представляет собой его нормализованное значение.
281. Способ из любого из вариантов осуществления 217–280, где:
неблагоприятное событие представляет собой нейротоксичность степени 4 или 5 и пороговое значение:
составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,5×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,88×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,0×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,5×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,25×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,56×107, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,75×107, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,19×107, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
282. Способ из любого из вариантов осуществления 217–281, где неблагоприятное событие представляет собой нейротоксичность степени 4 или 5, и данный диапазон целевых эталонных единиц:
составляет между или приблизительно между 2,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 4×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 5×106 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 2,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 1,5×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,88×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 2,0×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 2,5×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 1,25×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 1,56×107, включительно, если A представляет собой CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 1,75×107, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 2,19×107, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
283. Способ из любого из вариантов осуществления 217–280, где неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3 и пороговое значение:
составляет или составляет приблизительно 1,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 1,25×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет или составляет приблизительно 1,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 1,88×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,12×106, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2; или его нормализованное значение
составляет или составляет приблизительно 3,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 3,75×106, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,0×106, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет или составляет приблизительно 2,5×106, если A представляет собой CD8+CAR+ и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
284. Способ из любого из вариантов осуществления 217–280 и 283, где неблагоприятное событие представляет собой по меньшей мере длительную нейротоксичность степени 3, и данный диапазон целевых эталонных единиц:
составляет между или приблизительно между 3,0×105 и 1,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза и CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,25×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа или его нормализованное значение;
составляет между или приблизительно между 4×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 5×106 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 2,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 2,5×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 1,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 1,88×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IFN–гамма или его нормализованное значение;
составляет между или приблизительно между 3,0×105 и 2,5×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 3,75×105 и 3,12×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 3,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 3,75×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 4,0×105 и 2,0×106, включительно, если A представляет собой отрицательные (–) по маркеру апоптоза CD8+CAR+, и если B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение;
составляет между или приблизительно между 5,0×105 и 2,5×106, включительно, если A представляет собой CD8+CAR+, и B представляет собой TNF–альфа, IFN–гамма и IL–2 или его нормализованное значение,
необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
285. Способ из любого из вариантов осуществления 214–284, где рекомбинантный рецептор представляет собой CAR.
286. Способ из варианта осуществления 285, где CAR содержит внеклеточный узнающий антиген домен, который специфически связывается с антигеном, и внутриклеточный передающий сигналы домен, содержащий ITAM, где необязательно, внутриклеточный передающий сигналы домен содержит внутриклеточный домен из цепи CD3–зета (CD3ζ); и/или где CAR дополнительно содержит область передачи костимулирующих сигналов, которая, необязательно, содержит передающий сигналы домен из CD28 или 4–1BB.
287. Способ из любого из вариантов осуществления 214–286, где T–клетки представляют собой CD4+ или CD8+.
288. Способ из любого из вариантов осуществления 214–287, где T–клетки представляют собой первичные T–клетки, необязательно, аутологичные или аллогенные для индивида.
289. Способ получения терапевтической композиции T–клеток для клеточной терапии, включающий заполнение контейнера всей или частью композиции, содержащей T–клетки, до концентрации между приблизительно 10 миллионов клеток и приблизительно 70 миллионов клеток на мл, включительно, и необязательно, другим раствором.
290. Способ из варианта осуществления 289, где T–клетки получают от индивида, имеющего заболевание или состояние, и трансдуцируют нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), специфический для антигена, ассоциированного с заболеванием или состоянием, или экспрессируемого при заболевании или состоянии, и/или T–клетки содержат рекомбинантный рецептор, необязательно, CAR.
291. Способ из любого из вариантов осуществления 233–290, где контейнер заполняют с использованием между приблизительно 15 и приблизительно 60 миллионов клеток на мл, включительно.
292. Способ из любого из вариантов осуществления 233–291, где контейнер заполняют с использованием более чем 10 миллионов клеток на мл.
293. Способ из любого из вариантов осуществления 233–292, где контейнер заполняют с использованием более чем 15 миллионов клеток на мл.
294. Способ из любого из вариантов осуществления 233–293, где заполнение проводят в автоматическом режиме.
295. Способ из любого из вариантов осуществления 233–295, где заполнение проводят в закрытой системе.
296. Способ из любого из вариантов осуществления 233–295, где контейнер заполняют другим раствором, и раствор содержит криопротектор, необязательно DMSO.
297. Способ из любого из вариантов осуществления 233–295, дополнительно включающий замораживание клеток в контейнере или хранение контейнера при температуре менее чем или приблизительно менее чем 80º C.
298. Способ из любого из вариантов осуществления 233–298, где рекомбинантный рецептор представляет собой CAR.
299. Способ из варианта осуществления 298, где CAR содержит внеклеточный узнающий антиген домен, который специфически связывается с антигеном, и внутриклеточный передающий сигналы домен, содержащий ITAM, где необязательно, внутриклеточный передающий сигналы домен содержит внутриклеточный домен из цепи CD3–зета (CD3ζ); и/или где CAR дополнительно содержит область передачи костимулирующих сигналов, которая, необязательно, содержит передающий сигналы домен из CD28 или 4–1BB.
300. Способ из любого из вариантов осуществления 233–299, где T–клетки представляют собой CD4+ или CD8+.
301. Способ из любого из вариантов осуществления 233–301, где T–клетки представляют собой первичные T–клетки, необязательно, аутологичные или аллогенные для индивида.
302. Способ из любого из вариантов осуществления 118–301, где композицию T–клеток получают способом, в котором:
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции, и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на признаки биологически активных клеток и/или отсутствия апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10% или не более чем на 5%, от среднего указанной частоты во множестве композиций T–клеток, полученных этим способом, и/или отличается от такого среднего не более чем на одно стандартное отклонение; или
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на отсутствие апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 20%, или не более чем на 10%, среди множества композиций T–клеток, полученных этим способом
303. Способ из варианта осуществления 302, включающий:
(a) инкубацию популяции клеток, содержащей T–клетки, со средством, содержащим молекулу нуклеиновой кислоты, кодирующую рекомбинантный рецептор, в условиях для введения нуклеиновой кислоты, кодирующей рекомбинантный рецептор, в клетки в популяции; и
(b) стимуляцию клеток, до, во время и/или после указанной инкубации, где стимуляция включает инкубацию клеток при наличии стимулирующего условия, индуцирующего первичный сигнал, передачу сигналов, стимуляцию, активацию и/или размножение клеток.
304. Способ из варианта осуществления 303, дополнительно включающий, перед (a), выделение популяции клеток из биологического образца.
305. Способ из варианта осуществления 304, где выделение включает отбор клеток на основании поверхностной экспрессии CD3 или на основании поверхностной экспрессии одного или обоих из CD4 и CD8, необязательно, посредством положительного или отрицательного отбора.
306. Способ из варианта осуществления 304 или варианта осуществления 305, где выделение включает проведение иммуноотбора на основании аффинности.
307. Способ из варианта осуществления 304–306, где биологический образец представляет собой или содержит образец цельной крови, образец лейкоцитарной пленки, образец мононуклеарных клеток периферической крови (PBMC), образец нефракционированных T–клеток, образец лимфоцитов, образец лейкоцитов, продукт афереза или продукт лейкафереза.
308. Способ из любого из вариантов осуществления 303–307, где стимулирующее условие включает инкубацию со стимулирующим реагентом, способным активировать один или несколько внутриклеточных доменов передачи сигналов одного или нескольких компонентов комплекса TCR и/или один или несколько внутриклеточных доменов передачи сигналов одной или нескольких костимулирующих молекул.
309. Способ из варианта осуществления 308, где стимулирующий реагент содержит первичное средство, которое специфически связывается с членом комплекса TCR, и вторичное средство, которое специфически связывается с костимулирующей молекулой T–клетки.
310. Способ из варианта осуществления 308 или варианта осуществления 309, где первичное средство специфически связывается с CD3 и/или костимулирующей молекулой, выбранной из группы, состоящей из CD28, CD137 (4–1–BB), OX40 или ICOS.
311. Способ из варианта осуществления 306 или варианта осуществления 310, где первичное и вторичное средства содержат антитела и/или присутствуют на поверхности твердой подложки, необязательно, бусины.
312. Способ из любого из вариантов осуществления 308–311, где:
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, от среднего показателя продукции или накопления провоспалительного цитокина среди множества композиций T–клеток, полученных этим способом с использованием стимулирующего реагента, и/или отличается от такого среднего не более чем на одно стандартное отклонение; и/или
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20% или не более чем на 10%, или не более чем на 5%, среди множества композиций T–клеток, полученных этим способом; и/или
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, of для композиции клеток, полученной с использованием стимулирующего реагента, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20% или не более чем на 10%, или не более чем на 5% от контрольной композиции, где контрольная композиция и композиция клеток получены с использованием одинакового способа, включая получение из такой же популяции клеток, за исключением того, что контрольная композиция реализована в присутствии контрольного стимулирующего реагента, или стандартного количества единиц зависимой от рекомбинантного рецептора активности.
313. Способ из варианта осуществления 312, где контрольный стимулирующий реагент, при использовании в способе, приводит к получению композиции T–клеток, в которой зависимая от рекомбинантного рецептора активность или антигенспецифическая активность находится в пределах приемлемого диапазона изменчивости.
314. Способ из любого из вариантов осуществления 303–313, где стимуляцию клеток проводят или инициируют до инкубации, необязательно, в течение 18–24 часов при или приблизительно при 37 градусов
315. Способ из любого из вариантов осуществления 303–314, где стимулирующее условие включает включает цитокин, выбранный среди IL–2, IL–15 и IL–7.
316. Способ из любого из вариантов осуществления 303–315, где стимуляцию клеток проводят после инкубации, необязательно, в течение периода времени для достижения пороговой концентрации.
317. Способ из любого из вариантов осуществления 303–316, дополнительно включающий (c) заполнение контейнера всей или частью композиции T–клеток, и необязательно, другим раствором, до концентрации между приблизительно 10 миллионов клеток и приблизительно 70 миллионов клеток на мл, включительно.
318. Способ из варианта осуществления 317, где контейнер заполняют другим раствором, и раствор содержит криопротектор, необязательно DMSO.
319. Способ из варианта осуществления 317 или вариант осуществления 318, где концентрация составляет между приблизительно 15 и приблизительно 60 миллионов клеток на мл, включительно.
320. Способ из любого из вариантов осуществления 317–319, где концентрация составляет более чем 10 миллионов клеток на мл.
321. Способ из любого из вариантов осуществления 317–320, где концентрация составляет более чем 15 миллионов клеток на мл.
322. Способ из любого из вариантов осуществления 317–321, где концентрация DMSO составляет или составляет приблизительно, или не превышает 7,5%.
323. Способ из варианта осуществления 317 или варианта осуществления 318, где концентрация составляет более чем 60 миллионов клеток на мл.
324. Способ из любого из вариантов осуществления 317–320 и 323, где концентрация DMSO составляет более чем 7,5%, необязательно, между или приблизительно между 7,5% и 9,0%, включительно.
325. Способ из любого из вариантов осуществления 303–324, где средство, содержащее молекулу нуклеиновой кислоты, кодирующую рекомбинантный рецептор, представляет собой вирусный вектор, необязательно, лентивирусный вектор или гамма–ретровирусный вектор.
326. Способ из любого из вариантов осуществления 317–325, где заполнение проводят в автоматическом режиме, необязательно, в закрытой системе.
327. Способ из любого из вариантов осуществления 303–326, дополнительно включающий замораживание клеток в контейнере или хранение контейнера при температуре менее чем или приблизительно менее чем 80º C.
328. Единичная доза терапевтической композиции T–клеток, содержащая количество клеток, содержащих рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), специфический для антигена, ассоциированного с заболеванием или состоянием, или экспрессируемого при заболевании или состоянии, где количество клеток составляет между и между приблизительно 5,0×106 и 2,25×107, 5,0×106 и 2,0×107, 5,0×106 и 1,5×107, 5,0×106 и 1,0×107, 5,0×106 и 7,5×106, 7,5×106 и 2,25×107, 7,5×106 и 2,0×107, 7,5×106 и 1,5×107, 7,5×106 и 1,0×107, 1,0×107 и 2,25×107, 1,0×107 и 2,0×107, 1,0×107 и 1,5×107, 1,5×107 и 2,25×107, 1,5×107 и 2,0×107, 2,0×107 и 2,25×107 экспрессирующих рекомбинантный рецептор клеток, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, включая каждое, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
329. Единичная доза из варианта осуществления 328, где количество клеток составляет:
между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, включая каждое, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 5,55×106, 6,66×106, 7,77×106, 8,99×106, 1,0×107, 1,1×107 и приблизительно 1,67×107 экспрессирующих рекомбинантный рецептор клеток, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, включая каждое, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, включая каждое, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3;
между по меньшей мере или по меньшей мере приблизительно 7,14×106, 8,5×106, 1,0×107, 1,14×107, 1,29×107, 1,42×107 и приблизительно 2,14×107 экспрессирующих рекомбинантный рецептор клеток, необязательно, экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, или которые являются отрицательными(–) по маркеру апоптоза и CD8+, включая каждое, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3.
330. Единичная доза из варианта осуществления 328 или вариант осуществления 329, где количество клеток составляет между по меньшей мере или по меньшей мере приблизительно 5×106, 6×106, 7×106, 8×106, 9×106, 10×106 и приблизительно 15×106 экспрессирующих рекомбинантный рецептор клеток, представляющих собой CD8+, включая каждое.
331. Единичная доза из варианта осуществления 328 или вариант осуществления 329, где количество клеток составляет между по меньшей мере или по меньшей мере приблизительно 6,25×106, 7,5×106, 8,75×106, 1,0×107, 1,13×107, 1,25×107 и приблизительно 1,9×107 экспрессирующих рекомбинантный рецептор клеток, которые являются отрицательными(–) по маркеру апоптоза и CD8+, необязательно, где маркер апоптоза представляет собой аннексин V или активную каспазу 3 включая каждое.
332. Единичная доза из любого из вариантов осуществления 328–332, не содержащая более порогового количества эталонных единиц (RU), где количество RU в данной композиции определяют по формуле:
RU=A x B, где
A представляет собой количество клеток, или его кратное или преобразование, клеток некоторого фенотипа, присутствующих в данной композиции, или представляет собой среднее или взвешенное среднее количества клеток, или его кратное, долю или преобразование, двух или более фенотипов в данной композиции; и
B представляет собой значение параметра, или его кратное или преобразование, которое показывает степень или коррелирует со степенью зависимой от рекомбинантного рецептора, необязательно, зависимой от CAR, активности в данной композиции T–клеток.
333. Единичная доза из варианта осуществления 332, где пороговое количество эталонных единиц составляет менее, чем эталонное безопасное количество единиц, где эталонное безопасное количество единиц составляет, применительно к группе индивидов, анализированных после лечения с использованием терапевтической композиции T–клеток, содержащей T–клетки, экспрессирующие рекомбинантный рецептор, необязательно, CAR, наименьшее количество единиц лекарственного средства, введенное индивиду среди тех индивидов в группе, у которых продолжалось развитие неблагоприятного события.
334. Единичная доза из варианта осуществления 333, где неблагоприятное событие представляет собой серьезное неблагоприятное событие, необязательно, тяжелую нейротоксичность степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность степени 3.
335. Единичная доза из варианта осуществления 333 или варианта осуществления 334, где пороговое количество единиц составляет менее, чем безопасное количество эталонных единиц, на количество, соответствующее коэффициенту запаса безопасности, или по меньшей мере в 2 раза.
336. Единичная доза из любого из вариантов осуществления 332–335, где пороговое количество единиц составляет или превышает эталонное эффективное количество единиц, где эталонное эффективное количество составляет, применительно к группе индивидов, анализированных после лечения с использованием композиции T–клеток, содержащих рекомбинантный рецептор, необязательно, CAR, количество единиц лекарственного средства, введенное одному или нескольким индивидам среди группы, для которой показан желательный терапевтический исход, необязательно, полный ответ (CR).
337. Единичная доза из любого из вариантов осуществления 121–127, где по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 75%, по меньшей мере 80%, или по меньшей мере 90% CD8+ клеток и/или CD8+CAR+ клеток в композиции не являются положительными по маркеру апоптоза, не являются апоптотическими или не находятся на ранних стадиях апоптоза, или не находятся на поздних стадиях апоптоза.
338. Единичная доза из любого из вариантов осуществления 328–337, содержащая не более чем 1,88×107 CD8+ CAR+ T–клеток, необязательно, CD8+CAR+ T–клеток, которые не являются апоптотическими или не находятся на ранних стадиях апоптоза, или не находятся на поздних стадиях апоптоза.
339. Единичная доза композиции из любого из вариантов осуществления 328–338, содержащая по меньшей мере 5×106 аннексин– CD8+ CAR+ клеток, но не более чем 1,5×107 аннексин– CD8+CAR+ клеток.
340. Единичная доза композиции из любого из вариантов осуществления 328–339, где композицию T–клеток получают способом, в котором:
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции, и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на признаки биологически активных клеток и/или отсутствия апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, от среднего указанной частоты во множестве композиций T–клеток, полученных этим способом, и/или отличается от такого среднего не более чем на одно стандартное отклонение; или
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции, и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на отсутствие апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 20%, или не более чем на 10%, среди множества композиций T–клеток, полученных этим способом.
341. Единичная доза из варианта осуществления 340, где способ включает:
(a) инкубацию популяции клеток, содержащей T–клетки, со средством, содержащим молекулу нуклеиновой кислоты, кодирующую рекомбинантный рецептор, в условиях для введения нуклеиновой кислоты, кодирующей рекомбинантный рецептор, в клетки в популяции; и
(b) стимуляцию клеток, до, во время и/или после указанной инкубации, где стимуляция включает инкубацию клеток при наличии стимулирующего условия, индуцирующего первичный сигнал, передачу сигналов, стимуляцию, активацию и/или размножение клеток.
342. Единичная доза из варианта осуществления 341, где способ дополнительно включает, перед (a), выделение популяции клеток из биологического образца.
343. Единичная доза из варианта осуществления 342, где выделение включает отбор клеток на основании поверхностной экспрессии CD3 или на основании поверхностной экспрессии одного или обоих из CD4 и CD8, необязательно, посредством положительного или отрицательного отбора.
344. Единичная доза из варианта осуществления 342 или варианта осуществления 343, где выделение включает проведение иммуноотбора на основании аффинности.
345. Единичная доза из варианта осуществления 342–344, где биологический образец представляет собой или содержит образец цельной крови, образец лейкоцитарной пленки, образец мононуклеарных клеток периферической крови (PBMC), образец нефракционированных T–клеток, образец лимфоцитов, образец лейкоцитов, продукт афереза, или продукт лейкафереза.
346. Единичная доза из любого из вариантов осуществления 341–345, где стимулирующее условие включает инкубацию со стимулирующим реагентом, способным активировать один или несколько внутриклеточных доменов передачи сигналов одного или нескольких компонентов комплекса TCR и/или один или несколько внутриклеточных доменов передачи сигналов одной или нескольких костимулирующих молекул.
347. Единичная доза из варианта осуществления 346, где стимулирующий реагент содержит первичное средство, которое специфически связывается с членом комплекса TCR, и вторичное средство, которое специфически связывается с костимулирующей молекулой T–клетки.
348. Единичная доза из варианта осуществления 346 или варианта осуществления 347, где первичное средство специфически связывается с CD3 и/или костимулирующей молекулой, выбранной из группы, состоящей из CD28, CD137 (4–1–BB), OX40 или ICOS.
349. Единичная доза из варианта осуществления 347 или варианта осуществления 348, где первичное и вторичное средства содержат антитела и/или присутствуют на поверхности твердой подложки, необязательно, бусины.
350. Единичная доза из любого из вариантов осуществления 346–349, где:
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, от среднего показателя продукции или накопления провоспалительного цитокина среди множества композиций T–клеток, полученных этим способом с использованием стимулирующего реагента, и/или отличается от такого среднего не более чем на одно стандартное отклонение; и/или
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5%, среди множества композиций T–клеток, полученных этим способом; и/или
стимулирующий реагент представляет собой реагент, для которого определено, что зависимая от рекомбинантного рецептора активность или антигенспецифическая активность, необязательно, зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина, для композиции клеток, полученной с использованием стимулирующего реагента, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20% или не более чем на 10%, или не более чем на 5% от контрольной композиции, где контрольная композиция и композиция клеток получены с использованием одинакового способа, включая получение из такой же популяции клеток, за исключением того, что контрольная композиция реализована в присутствии контрольного стимулирующего реагента, или стандартного количества единиц зависимой от рекомбинантного рецептора активности.
351. Единичная доза из варианта осуществления 350, где контрольный стимулирующий реагент, при использовании в способе, приводит к получению композиции T–клеток, в которой зависимая от рекомбинантного рецептора активность или антигенспецифическая активность находится в пределах приемлемого диапазона изменчивости.
352. Единичная доза из любого из вариантов осуществления 341–351, где стимуляцию клеток проводят или инициируют до инкубации, необязательно, в течение 18–24 часов при или приблизительно при 37 градусов
353. Единичная доза из любого из вариантов осуществления 341–352, где стимулирующее условие включает включает цитокин, выбранный среди IL–2, IL–15 и IL–7.
354. Единичная доза из любого из вариантов осуществления 341–353, где стимуляцию клеток проводят после инкубации, необязательно, в течение периода времени для достижения пороговой концентрации.
355. Единичная доза из любого из вариантов осуществления 341–354, дополнительно включающая (c) заполнение контейнера всей или частью композиции T–клеток, и необязательно, другим раствором, до концентрации между приблизительно 10 миллионов клеток и приблизительно 70 миллионов клеток на мл, включительно.
356. Единичная доза из варианта осуществления 355, где контейнер заполняют другим раствором, и раствор содержит криопротектор, необязательно DMSO.
357. Единичная доза из варианта осуществления 355 или варианта осуществления 356, где концентрация составляет между приблизительно 15 и приблизительно 60 миллионов клеток на мл, включительно.
358. Единичная доза из любого из вариантов осуществления 355–357, где концентрация составляет более чем 10 миллионов клеток на мл.
359. Единичная доза из любого из вариантов осуществления 355–358, где концентрация составляет более чем 15 миллионов клеток на мл.
360. Единичная доза из любого из вариантов осуществления 355–359, где концентрация DMSO составляет или составляет приблизительно, или не превышает 7,5%.
361. Единичная доза из варианта осуществления 355 или варианта осуществления 356, где концентрация составляет более чем 60 миллионов клеток на мл.
362. Единичная доза из любого из вариантов осуществления 355–358 и 361, где концентрация DMSO составляет более чем 7,5%, необязательно, между или приблизительно между 7,5% и 9,0%, включительно.
363. Единичная доза из любого из вариантов осуществления 341–362, где средство, содержащее молекулу нуклеиновой кислоты, кодирующую рекомбинантный рецептор, представляет собой вирусный вектор, необязательно, лентивирусный вектор или гамма–ретровирусный вектор.
364. Единичная доза из любого из вариантов осуществления 355–363, где заполнение проводят в автоматическом режиме, необязательно, в закрытой системе.
365. Единичная доза из любого из вариантов осуществления 341–364, дополнительно включающая замораживание клеток в контейнере или хранение контейнера при температуре менее чем или приблизительно менее чем 80º C.
366. Способ определения того, подвержен ли индивид риску токсичности, включающий анализ количества экспрессирующих рекомбинантный рецептор клеток в крови индивида, где указанному индивиду ранее вводили дозу экспрессирующих рекомбинантный рецептор клеток, где индивид подвержен риску развития токсичности, если:
(i) не более чем через четверо суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 2 экспрессирующие рекомбинантный рецептор клетки на микролитр;
(ii) не более чем через пять или шесть суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 5 экспрессирующих рекомбинантный рецептор клеток на микролитр или составляет по меньшей мере или приблизительно 10 экспрессирующих рекомбинантный рецептор клеток на микролитр; или
(iii) не более чем через семь суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 15 экспрессирующих рекомбинантный рецептор клеток на микролитр.
367. Способ определения того, подвержен ли индивид риску токсичности, включающий:
(a) введение индивиду, страдающему заболеванием или состоянием, дозы экспрессирующих рекомбинантный рецептор клеток; и
(b) после введения клеток, анализ количества экспрессирующих рекомбинантный рецептор клеток в крови индивида, где индивид подвержен риску развития токсичности, если:
(i) не более чем через четверо суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 2 экспрессирующие рекомбинантный рецептор клетки на микролитр;
(ii) не более чем через пять или шесть суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 5 экспрессирующих рекомбинантный рецептор клеток на микролитр, или составляет по меньшей мере или приблизительно 10 экспрессирующих рекомбинантный рецептор клеток на микролитр; или
(iii) не более чем через семь суток после начала введения, количество экспрессирующих рекомбинантный рецептор клеток в крови индивида составляет по меньшей мере или приблизительно 15 экспрессирующих рекомбинантный рецептор клеток на микролитр.
368. Способ из варианта осуществления 366 или варианта осуществления 367, где если определяют, что индивид подвержен риску возникновения токсичности; прекращают введение экспрессирующих рекомбинантный рецептор клеток, вводят индивиду более низкую дозу экспрессирующих рекомбинантный рецептор клеток; вводят индивиду клетки, экспрессирующие другой рекомбинантный рецептор; и/или вводят индивиду средство, способное лечить, предотвращать, замедлять или ослаблять развитие токсичности.
369. Способ из любого из вариантов осуществления 366–368, где если определяют, что индивид подвержен риску возникновения токсичности, вводят индивиду средство, способное лечить, предотвращать, замедлять или ослаблять развитие токсичности.
370. Способ оценки стимулирующего реагента для использования в получении терапевтической композиции T–клеток, включающий:
(i) оценку композиции T–клеток, полученной с использованием стимулирующего реагента, по зависимым от рекомбинантного рецептора активности или фенотипу; и
(ii) сравнение зависимых от рекомбинантного рецептора активности или фенотипа, с такими же активностью или фенотипом, полученными для контрольной композиции, или сравнение со стандартной единицей для зависимых от рекомбинантного рецептора активности или фенотипа,
где стимулирующее средство определяют как пригодное для выпуска для использования в способе получения терапевтической композиции T–клеток, если зависимые от рекомбинантного рецептора активность или фенотип композиции клеток, полученной с использованием стимулирующего реагента отличаются не более чем на 40% или не более чем на 30%, или не более чем на 20%, или не более чем на 10%, или не более чем на 5% от такой же активности, полученной для контрольной композиции, или от стандартной единицы.
371. Способ из варианта осуществления 370, где зависимая от рекомбинантного рецептора активность представляет собой антигенспецифическую активность.
372. Способ из варианта осуществления 370 или варианта осуществления 371, где контрольная композиция и композиция T–клеток получены с использованием одинакового способа, включая получение из такой же популяции клеток, за исключением того, что контрольная композиция реализована в присутствии контрольного стимулирующего реагента.
373. Способ из любого из вариантов осуществления 370–372, где зависимую от рекомбинантного рецептора активность оценивают и сравнивают с такой же активностью, полученной для контрольной композиции, или сравнивают со стандартным количеством единиц зависимой от рекомбинантного рецептора активности.
374. Способ из любого из вариантов осуществления 370–373, где зависимая от рекомбинантного рецептора активность представляет собой зависимые от рекомбинантного рецептора или зависимые от антигенной специфичности продукция или накопление провоспалительного цитокина.
375. Способ из варианта осуществления 364, где провоспалительный цитокин представляет собой IL–2, TNF–альфа, IFN–гамма или IL–10.
376. Способ из любого из вариантов осуществления 370–372, где фенотип оценивают и сравнивают с таким же фенотипом, полученным для контрольной композиции, или сравнивают со стандартной единицей для фенотипа.
377. Способ из любого из вариантов осуществления 370–372 и 376, где фенотип включает конкретное состояние дифференцировки и/или фенотип, подобный клеткам памяти/стволовым клеткам.
378. Способ из любого из вариантов осуществления 370–372, 376 и 377, где фенотип включает положительную экспрессию поверхностного маркера, представляющего собой CD3, CD8, CD27, CD28, и/или включает положительную экспрессию рекомбинантного рецептора, необязательно, CAR, или суррогатный маркер экспрессии рекомбинантного рецептора.
379. Способ из любого из вариантов осуществления 370–372 и 376–378, где фенотип включает CD27+/CD28+/CD8+.
380. Способ из любого из вариантов осуществления 370–379, где стимулирующий реагент является способным активировать один или несколько внутриклеточных доменов передачи сигналов одного или нескольких компонентов комплекса TCR и/или один или несколько внутриклеточных доменов передачи сигналов одной или нескольких костимулирующих молекул.
381. Способ из любого из вариантов осуществления 370–380, где стимулирующий реагент содержит первичное средство, которое специфически связывается с членом комплекса TCR, и вторичное средство, которое специфически связывается с костимулирующей молекулой T–клетки.
382. Способ из варианта осуществления 380 или вариант осуществления 381, где первичное средство специфически связывается с CD3 и/или костимулирующей молекулой, выбранной из группы, состоящей из CD28, CD137 (4–1–BB), OX40 или ICOS.
383. Способ из варианта осуществления 381 или варианта осуществления 382, где первичное и вторичное средства содержат антитела и/или присутствуют на поверхности твердой подложки, необязательно, бусины.
384. Контейнер, содержащий терапевтическую композицию T–клеток в концентрации между приблизительно 10 миллионов клеток и приблизительно 70 миллионов клеток на мл, и необязательно, другой раствор, где терапевтическая композиция T–клеток содержит T–клетки, содержащие рекомбинантный рецептор.
385. Контейнер из варианта осуществления 384, где концентрация составляет между приблизительно 15 и приблизительно 60 миллионов клеток на мл.
386. Контейнер из варианта осуществления 384 или 385, где концентрация составляет или составляет приблизительно 15 миллионов клеток на мл.
387. Контейнер из варианта осуществления 384 или 385 где контейнер заполняют другим раствором, и раствор содержит криопротектор, необязательно DMSO.
388. Контейнер из любого из вариантов осуществления 384–386, где контейнер представляет собой ампулу или представляет собой пакет.
389. Контейнер из любого из вариантов осуществления 384–387, где контейнер представляет собой ампулу, необязательно, криогенную ампулу, и объем композиции составляет не более чем 20 мл, необязательно, 1 мл – 20 мл, 1 мл – 15 мл, 1 мл – 10 мл, 1 мл – 5 мл, 1 мл – 2,5 мл, 2,5 мл – 20 мл, 2,5 мл – 15 мл, 2,5 мл – 10 мл, 2,5 мл – 5 мл, 5 мл – 20 мл, 5 мл – 15 мл, 5 мл – 10 мл, 10 мл – 20 мл, 10 мл – 15 мл или 15 мл – 20 мл.
390. Контейнер из любого из вариантов осуществления 384–388, где контейнер представляет собой пакет, необязательно, пакет для замораживания, и объем композиции:
составляет между или между приблизительно 15 мл и 150 мл, 20 мл и 100 мл, 20 мл и 80 мл, 20 мл и 60 мл, 20 мл и 40 мл, 40 мл и 100 мл, 40 мл и 80 мл, 40 мл и 60 мл, 60 мл и 100 мл, 60 мл и 80 мл или 80 мл и 100 мл, включая каждое; или
составляет по меньшей мере или по меньшей мере приблизительно 15 мл, по меньшей мере или по меньшей мере приблизительно 20 мл, по меньшей мере или по меньшей мере приблизительно 30 мл, по меньшей мере или по меньшей мере приблизительно 40 мл, по меньшей мере или по меньшей мере приблизительно 50 мл, по меньшей мере или по меньшей мере приблизительно 60 мл, по меньшей мере или по меньшей мере приблизительно 70 мл, по меньшей мере или по меньшей мере приблизительно 80 мл или по меньшей мере или по меньшей мере приблизительно 90 мл; и/или
составляет не более чем 100 мл.
391. Контейнер из любого из вариантов осуществления 384–390, где соотношение площади поверхности к объему композиции в контейнере:
составляет между или между приблизительно 0,1 см–1 и 100 см–1; 1 см–1 и 50 см–1, 1 см–1 и 20 см–1, 1 см–1 и 10 см–1, 1 см–1 и 7 см–1, 1 см–1 и 6 см–1, 1 см–1 и 3 см–1, 1 см–1 и 2 см–1, 2 см–1 и 20 см–1, 2 см–1 и 10 см–1, 2 см–1 и 7 см–1, 2 см–1 и 6 см–1, 2 см–1 и 3 см–1, 3 см–1 и 20 см–1, 3 см–1 и 10 см–1, 3 см–1 и 7 см–1, 3 см–1 и 6 см–1, 6 см–1 и 20 см–1, 6 см–1 и 10 см–1, 6 см–1 и 7 см–1, 7 см–1 и 20 см–1, 7 см–1 и 10 см–1 или 7 см–1 и 20 см–1, включая каждое; или
составляет, составляет приблизительно или составляет по меньшей мере 3 см–1, 4 см–1, 5 см–1, 6 см–1, 7 см–1, 10 см–1, 15 см–1 или 20 см–1.
392. Контейнер из любого из вариантов осуществления 384–3391, где T–клетки получают от индивида, имеющего заболевание или состояние, и трансдуцируют нуклеиновой кислотой, кодирующей рекомбинантный рецептор, необязательно, химерный антигенный рецептор (CAR), специфический для антигена, ассоциированного с заболеванием или состоянием, или экспрессируемого при заболевании или состоянии, и/или T–клетки содержат рекомбинантный рецептор, необязательно, CAR.
393. Контейнер из любого из вариантов осуществления 97–105, где рекомбинантный рецептор представляет собой CAR.
394. Контейнер из варианта осуществления 106, где CAR содержит внеклеточный узнающий антиген домен, который специфически связывается с антигеном, и внутриклеточный передающий сигналы домен, содержащий ITAM, где необязательно, внутриклеточный передающий сигналы домен содержит внутриклеточный домен из цепи CD3–зета (CD3ζ); и/или где CAR дополнительно содержит область передачи костимулирующих сигналов, которая, необязательно, содержит передающий сигналы домен из 4–1BB.
395. Контейнер из любого из вариантов осуществления 97–107, где T–клетки представляют собой CD4+ или CD8+.
396. Способ из любого из вариантов осуществления 97–108, где T–клетки представляют собой первичные T–клетки.
397. Контейнер из любого из вариантов осуществления 97–109, где композицию T–клеток получают способом, в котором:
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на признаки биологически активных клеток и/или отсутствия апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 30%, или не более чем на 20% или не более чем на 10%, или не более чем на 5%, от среднего указанной частоты во множестве композиций T–клеток, полученных этим способом, и/или отличается от такого среднего не более чем на одно стандартное отклонение; или
частота, (1) среди CAR+ клеток в композиции, (2) среди CAR+CD3+ клеток в композиции и/или (3) среди CAR+CD8+ клеток в композиции, клеток фенотипа, указывающего на отсутствие апоптоза, или ранних или поздних стадий апоптоза, отличается не более чем на 40% или не более чем на 20%, или не более чем на 10%, среди множества композиций T–клеток, полученных этим способом.
X. ПРИМЕРЫ
[0742] Следующие примеры включены только для иллюстративных целей и не предназначены для ограничения объема изобретения.
Пример 1: Определение параметров композиций CAR+ T–клеток, которые являются прогностическими для тяжелой нейротоксичности
[0743] Различные параметры оценивали после лечения индивидов, имеющих рецидивирующий или невосприимчивый острый лимфобластный лейкоз (ALL), с использованием терапевтических композиций, содержащих аутологичные T–клетки, модифицированные для экспрессии химерного рецептора антигена (CAR) против CD19. Оцененные параметры включали параметры терапевтических композиций клеток и дозы (включая функциональные признаки и количества, и частоты клеток различных фенотипов), характеристики пациента, и клинические параметры и параметры лечения, включая параметры, показательные для связанных с ответом и токсичностью исходов.
[0744] Параметры анализировали для индивидуальных индивидов, после введения, и сравнивали среди индивидов с использованием ряда статистических анализов, включая описательные, графические, непараметрические и основанные на моделях анализы. Оценивали взаимосвязи между различными параметрами. В частности, в этом исследовании оценивали степень, в которой различные параметры индивидуальных пациентов и композиций клеток или доз, коррелировали (напрямую или обратным образом) с вероятностью проявления терапевтического ответа и/или с риском неблагоприятного исхода, такого как нейротоксичность, например, тяжелая нейротоксичность или нейротоксичность степени 5 и отек головного мозга.
A. CAR+ T–клеточная терапия
[0745] Оцениваемым индивидам (N=38) вводили композицию T–клеток, содержащую аутологичные T–клетки, экспрессирующие химерный антигенный рецептор (CAR) против CD19, для лечения ALL взрослых. На начало лечения, из 38 индивидов, для тридцати двух (32) показано морфологическое доказательство заболевания в костном мозге (по меньшей мере 5% бластных клеток), и для шести (6) показано поддающееся детекции на молекулярном уровне заболевание посредством ПЦР. Индивиды имели возраст 18 лет или старше, с рецидивирующим или невосприимчивым морфологически положительным по CD19 заболеванием (как определено по более чем 5% бластных клеток в костном мозге) включая экстрамедуллярное и положительное по филадельфийской хромосоме (Ph+) заболевание, с предшествующими одним или более циклами терапии спасения (включая индивидов после лечения аллогенными гематопоэтическими стволовыми клетками), и имели оценки в баллах 0–2 согласно Восточной объединенной онкологической группе США (ECOG). Индивиды имели адекватную функцию органов, как показано посредством уровней креатинина в сыворотке < 1,5 x верхний предел нормы [0ULN] или выведения креатинина > 30 мл/мин/1,73м2, аланинаминотрансферазы < 5 x ULN, билирубина < 2,0 мг/дл, диспноэ степени < 1 и насыщения кислородом > 92% при дыхании комнатным воздухом, и фракции выброса левого желудочка of > 40%. Индивиды включали индивидов с предшествующим лечением блинатумомабом. Критерии исключения включали изолированное экстрамедуллярное заболевание или болезнь Беркитта, активное вовлечение ЦНС в заболевание (ЦНС3) или патологию ЦНС, активную острую (степени II–IV) или обширную хроническую реакцию трансплантат против хозяина (GvHD), активную инфекцию и предшествующую генотерапию. Индивидов, включающих индивидов, подвергавшихся лечению с использованием алемтузумаба в пределах прошедших 6 месяцев, клофарабина или кладрибина в прошедшие 3 месяца, лекарственных средств GvHD в прошедшие 4 недели, или химиотерапии спасения и терапевтических кортикостероидов в пределах прошедшей недели, также исключали.
[0746] Демографические и исходные характеристики индивидов, включенных в исследование, показаны в таблице E1A.
Таблица E1–A: Демографические и исходные характеристики
(0,5–21,5)
(0,5–10,6)
(0,6–21,5)
IT, интратекальный; LD, противолимфоцитарная терапия.
aHyper CVAD части A или B, режимы, включающие флударабин и/или цитарабин.
[0747] Введенные терапевтические композиции T–клеток получены способом, включающим основанный на иммуноаффинности отбор T–клеток (включая CD4+ и CD8+ клетки) из образцов после лейкафереза от индивидуальных индивидов, с последующей активацией и трансдукцией вирусным вектором, кодирующим CAR против CD19, размножением и криоконсервацией. CAR содержал scFv против CD19, происходящий из мышиного антитела, область CD28, включающую внеклеточную область, трансмембранный домен и костимулирующую область, и внутриклеточный передающий сигналы домен CD3–зета. Криоконсервированные композиции клеток размораживали на месте перед внутривенным введением. Вводили полные объемы композиций клеток, которые были заполнены и криоконсервированы.
[0748] Клетки вводили в первой целевой дозе приблизительно 1×106 CD3+CAR+ клеток/кг (массы тела индивида). Целевую дозу и диапазон доз для введения оценивали частично на основании сравнения исходов токсичности для группы индивидов с морфологически подтвержденным заболеванием, которым вводили сходные композиции, в диапазоне различных количеств CD3+CAR+ клеток на введенную дозу. В частности, оценивали взаимосвязь дозы CD3+CAR+/кг и того, что присутствовало или нет, включая то, продолжалось ли или нет у индивида развитие нейротоксичности степени 3, и были или нет целевая доза и диапазон доз ниже наименьшего количества CD3+CAR+ клеток/кг, введенных любому из таких индивидов, для которых показана нейротоксичность степени 3 или выше, меньше границы безопасности по меньшей мере 1,5×106 CD3+CAR+ клеток/кг. См. фигуру 22. Доза не учитывала количества или частоты CD4+ клеток по сравнению с CD8+ клетками, или количества или частоты других подгрупп T–клеток. Цитотоксическую активность против антиген CAR+ клеток оценивали в качестве показателя активности. Некоторым индивидам вводили вторую дозу, приблизительно между 14 и 28 сутками после начальной дозы. Перед введением аутологичных экспрессирующих CAR клеток, индивидов подвергали подготовительной противолимфоцитарной химиотерапии, включающей однократную дозу либо только циклофосфамида (приблизительно 1–3 г/м2), либо циклофосфамида (30–60 мг/кг) и флударабина (25 мг/м 2–30 мг/м2, вводимую один раз в сутки в течение трех суток).
[0749] У индивидов мониторировали ответ и другие исходы, включая исследование костного мозга, периферической крови и спинномозговой жидкости (CSF). У индивидов также оценивали и мониторировали нейротоксичность (неврологические осложнения включая симптомы спутанности, афазии, энцефалопатии, миоклонических судорог, конвульсий, летаргии и/или изменения психического состояния), разделенную на степени по шкале 1–5, в соответствии с разработанной Национальным институтом онкологии США – Шкалой общих критериев токсичности (CTCAE), версии 4.03 (NCI–CTCAE v4.03). Common Toxicity Criteria (CTCAE) scale, version 4.03 (NCI–CTCAE v4.03). См. Common Terminology for Adverse Events (CTCAE) Version 4, U.S. Department of Health and Human Services, Published: May 28, 2009 (v4.03: June 14, 2010); и Guido Cavaletti & Paola Marmiroli Nature Reviews Neurology 6, 657–666 (December 2010). Синдром высвобождения цитокинов (CRS) также определяли и мониторировали, разделяя на степени на основании тяжести.
[0750] Исходы ответа (процент индивидов, для которых показан полный ответ (CR) или полный ответ с неполным восстановлением мозга (CRi) (соотношение CR/CRi) (с медианой отслеживания 4 месяцев)), и токсичности обобщены в таблице E1–B и E1–C для индивидов, для которых показано морфологически подтвержденное заболевание на начало лечения. (NE=не поддается оценке). Как показано, у 56% индивидов возникла нейротоксичность степени 3–5. У пяти (5) индивидов возникла нейротоксичность степени 5 и, в частности, отек головного мозга степени 5.
Таблица E1–B: Обобщение подвергнутых лечению индивидов
Таблица E1–C: Исходы для 32 индивидов, подвергнутых лечению, с морфологически подтвержденным заболеванием
(всего подвергнуто лечению=38 индивидов)
# не поддается оценке
(all NTX events)
(оба события NTX)
Дополнительные 6 подвергнутых лечению индивидов являлись положительными по минимальному остаточному заболеванию (MRD+) на время лечения.
[0751] По меньшей мере 15 случаев нейротоксичности степени 5 и по меньшей мере 13 случаев отека головного мозга, ассоциированных с CAR–T–клеточной терапией, опубликовано в нескольких различных клинических исследованиях, как сообщено в публично доступной информации, включая исследования, включающие CAR–T–клетки, экспрессирующие различные CAR с различными антигенсвязывающими доменами и различными костимулирующими доменами, полученные с использованием различных способов изготовления, и для лечения различных заболеваний или показаний.
B. Фармакокинетика (PK) CAR+ T–клеток в крови
[0752] Анализ проводили для образцов, полученных из крови индивидов в различные временные точки после введения первой и, где это применимо, второй дозы композиций клеток. Образцы анализировали посредством проточной цитометрии по присутствию и количеству экспрессирующих CAR клеток в крови.
[0753] Как показано на ФИГ. 1 и 2, более быстрые пики размножения экспрессирующих CAR T–клеток наблюдали в крови индивидов, у которых продолжалось развитие более тяжелой нейротоксичности, и в частности, тех, у которых возникла нейротоксичность степени 5 и отек головного мозга. Например, результаты показали, что эти индивиды имели поддающийся детекции уровень CAR+ клеток на мкл крови в пределах 4–7 суток после первой дозы клеток, с более чем 20 CAR+ клетками на мкл крови, наблюдаемыми в крови всех таких индивидов в пределах семи суток после введения клеток. У индивидов с нейротоксичностью степени 3 или 4, пик размножения CAR+ T–клеток, как правило, наблюдали позже и с более низким максимальным количеством CAR+ T–клеток на микролитр (ФИГ. 2).
C. Оценка и сравнение клинических параметров, параметров пациентов, трансляции и CMC у различных индивидов
[0754] Различные параметры оценивали для различных групп пациентов, в соответствии с тяжестью заболевания на начало лечения и исходами лечения или возникновением токсичности, включая различные степени нейротоксичности. Присутствие или отсутствие корреляций и значимость оценивали посредством описательных, графических, непараметрических и основанных на моделях анализов, как описано в этом примере и в примере 2. Приблизительно 500 клинических параметров и параметров трансляции анализировали с использованием однофакторной и многофакторной логистической регрессии. Приблизительно 140 параметров химических свойств, процесса производства и контроля качества (CMC) исследовали в однофакторных и многофакторных анализов с использованием непараметрических тестов и способов на основе разбиения на части (дерева решений).
[0755] Различные признаки CMC оценивали в образцах из композиций T–клеток, которые вводили индивидам (размороженных из образцов криоконсервированных терапевтических композиций, которые вводили индивидам (CDP)). Образцы анализировали по присутствию, отсутствию, уровню, нормализованному уровню, количеству и/или нормализованному количеству для различных параметров. Среди иллюстративных оцененных клинических признаков и признаков пациента присутствовали возраст пациента, анамнез предшествующего лечения и то, подвергали ли пациента противолимфоцитарной и/или поддерживающей химиотерапии до лечения, возникновение и степень нейротоксичности, и другие исходы токсичности. Специфические для композиции клеток и/или связанные с дозой параметры включали количества и частоты (или их нормализованные значения) для различных популяций клеток (в вводимой дозе и/или введенных на массу индивида), продукцию цитокинов, цитотоксическую активность в ответ на стимуляцию антигеном CAR, и другие параметры, показательные для функции, такой как активация или стимуляция, и/или эффекторная функция, в ответ на различные условия. Оценивали степень корреляции различных параметров (индивидуально и, в некоторых случаях, их комбинаций) терапевтических композиций с нейротоксичностью и другими исходами, наблюдаемыми у индивидуальных индивидов после инфузии CAR+ T–клеток.
[0756] Результаты иллюстративных статистических анализов конкретных параметров для подгруппы индивидов, имеющих морфологически подтвержденное заболевание на начало лечения, согласовывались с обнаружением, что возраст пациента, анамнез предшествующего лечения и противолимфоцитарная и/или поддерживающая химиотерапия коррелировали (напрямую или обратным образом) с возникновением нейротоксичности степени 5. Например, в этой группе индивидов, более молодые пациенты в возрасте менее чем 30 лет, пациенты, которых подвергали более низкому количеству (равному двум или менее) циклов предшествующей терапии, и пациенты, которым вводили флударабин в пределах 3 месяцев или которых подвергали агрессивной поддерживающей химиотерапии, имели большую вероятность возникновения нейротоксичности степени 5 в этом исследовании. Рассчитанные отношения шансов, оцененные для испытывающих отек головного мозга после лечения с использованием клеточной терапии, для иллюстративных клинических факторов, показаны в таблице E1–D. Отношение шансов рассчитывали посредством деления шансов возникновения нейротоксичности степени 5, ассоциированных с демографическим признаком или анамнезом лечения, на шансы, ассоциированные с отсутствием демографического признака или лечения в анамнезе. Отношение шансов выше 1 указывает на увеличенные вероятность или правдоподобие возникновения нейротоксичности степени 5.
Таблица E1–D: Иллюстративные клинические Факторы, ассоциированные с отеком головного мозга
[0757] Не наблюдали ассоциации с более высоким риском для предшествующего радиоактивного облучения ЦНС, предшествующего лечения с использованием интратекальной (IT) химиотерапии, предшествующего заболевания ЦНС, предшествующей аллогенной клеточной терапии, более высокого функционального статуса по ECOG или предшествующего лечения с использованием блинатумомаба.
[0758] В этом исследовании также наблюдали, что определенные такие параметры (например, молодой (< 30 лет) возраст пациента и меньшее количество циклов предшествующего лечения) коррелируют с определенными специфическими для терапевтической композиции или связанными с дозой признаками (включая общее количество CD8+CAR+AnnV отрицательных клеток, введенных индивиду на дозу клеток, и уровень антигенспецифического накопления провоспалительного цитокина, IL–2, как измерено в культурах размороженной терапевтической композиции клеток в присутствии клеток, экспрессирующих CD19, антиген CAR, показательный для индуцированной CAR активности клетки). Также среди иллюстративных оцененных признаков присутствовали количества или частоты (или количество/кг) жизнеспособных клеток, и/или клеток различных фенотипов, в индивидуальных дозах, вводимых индивидуальным индивидам. Иллюстративные такие фенотипы включали экспрессию одного или нескольких поверхностных маркеров, как оценено посредством проточной цитометрии. Например, фенотипы включали CD3+, CD8+, CD4+ и/или CAR+. Также среди фенотипов присутствовали жизнеспособность, и фенотипы, ассоциированные с или показательные для, или, как считают, показательные для функциональных, здоровых или биологически активных клеток. В некоторых аспектах, такие фенотипы включали отсутствие или небольшие присутствие или экспрессию маркеров, показательных для апоптоза, апоптотических клеток или различных, например, ранних или поздних, стадий одного или нескольких из гибели или входа в апоптотический путь (например, аннексина V, каспазы 3). В некоторых аспектах, такие маркеры включают способность клеток продуцировать цитокины или другие факторы не специфическим для антигена CAR образом, например, при окрашивании внутриклеточных цитокинов (ICS) в ответ на PMA/иономицин и/или FOXP3. В некоторых аспектах, маркеры и фенотипы включали маркеры и фенотипы ассоциированные с активацией T–клеток, истощением, подобными стволовым клеткам свойствами, наивными T–клетками, продолжительностью жизни, подгруппами T–клеток, фенотипом(фенотипами) памяти и фенотипами подгрупп T–клеток памяти, такими как TCM, TEM, TSCM.
[0759] Например, относящиеся к терапевтической композиции клеток признаки включали общее количество CD8+CAR+ T–клеток в вводимой дозе, общее количество или частоту (например, среди CD8+CAR+ T–клеток) CD8+CAR+ T–клеток в вводимой дозе, как наблюдают, отрицательных по фактору, показательному для апоптоза, такому как поверхностное окрашивание аннексина V (аннексин V–) или расщепление каспазой 3 (что указывает на неапоптотические клетки). В некоторых примерах, относящиеся к терапевтической композиции клеток признаки включали общее количество CD3+CAR+ T–клеток в вводимой дозе, общее количество или частоту (например, среди CD3+CAR+ T–клеток) CD3+CAR+ T–клеток в вводимой дозе, как наблюдают, отрицательных по фактору, показательному для апоптоза, такому как поверхностное окрашивание аннексина V (аннексин V–) или расщепление каспазой 3 (что указывает на неапоптотические клетки).
[0760] Также среди иллюстративных параметров присутствовали свойства, специфические для терапевтических композиций и/или их получения, включая концентрацию жизнеспособных клеток (VCC), кратность размножения клеток между инокуляцией и сбором продукта лекарственного средства; и количество копий вектора (VCN) в введенной дозе.
[0761] Также среди иллюстративных параметров присутствовали параметры, как правило, ассоциированные с или показательные для функции или активности, или других признаков или способностей клеток в композициях. Среди них присутствовали различные признаки, ассоциированные с исходами стимуляции клеток, включая различные показатели пролиферации и активации или активности, включая индуцированные зависимым от TCR и/или CAR, или индуцированным TCR и/или CAR образом. Иллюстративными такими параметрами, связанными с функцией или активностью, являлись показатели или уровни (такие как количество или концентрация, или уровень на клетку) продукции одного или нескольких факторов (таких как различные цитокины) клетками в композиции, в ответ на специфическую для антигена CAR или другую стимуляцию.
[0762] В анализах окрашивания внутриклеточных цитокинов (ICS), проточные способы использовали для оценки способности клеток в композиции продуцировать различные цитокины в ответ на не специфический для антигена стимул. Клетки стимулировали с использованием PMA/иономицина в присутствии ингибитора аппарата Гольджи. Экспрессию FoxP3 оценивали посредством анализа QПЦР, нацеленного на специфическую для T–рег область деметилирования (TSDR) в гене FOXP3. Уровней FOXP3, показательных для фенотипа T–рег, не наблюдали.
[0763] Несколько параметров, показательных для направляемых CAR видов антигенспецифической активности и функций (таких как зависимая от антигена CAR секреция цитокинов и цитотоксичность) композиций, оценивали в анализах совместного культивирования. Клетки оцениваемой терапевтической композиции инкубировали в присутствии экспрессирующих CD19 клеток–мишеней. Для анализов цитокинов, накопленные количества (пг/мл) цитокина(цитокинов) (например, IL–2, IFN–гамма, TNF–альфа, IL–6, sCD137, MIP1b, MIP1a, IL–10, IL–4, IL–13, IL–5 или GM–CSF) оценивали после инкубации клеток–мишеней и количества различных композиций, включающего одинаковое количество трансдуцированных или CAR+ клеток, в одинаковом объеме, в течение периода приблизительно 22–24 часа. Такие анализы предоставляют показатель антигенспецифической секреции цитокинов на CAR+ клетку в дозе. В других анализах, цитолитическую активность против экспрессирующих CD19 клеток–мишеней оценивали после инкубации с T–клетками.
[0764] В некоторых случаях, оценивали показатели активности или функционального эффекта в ответ на не специфический для антигена CAR стимул, такие как продукция цитокина или другого фактора после стимуляции с использованием антитела против CD3/против CD28, например, в форме покрытия магнитных бусин. В таких анализах, культуры, содержащие меньшее количество CAR+ клеток среди T–клеток в культуре, могут иметь более высокий относительный уровень показателя.
[0765] В таблице E2 приведен список множества признаков, выбранных несмещенным образом среди признаков, которые оценивали для терапевтических композиций клеток и/или их доз, введенных индивидам, в исследованиях. Эти признаки оценивали посредством однофакторного анализа для подгруппы (22) индивидов, для которых показано морфологически подтвержденное заболевание на начало лечения. В таблице E2 перечислены значения p, показывающие степень, в которой каждый признак, как наблюдали, коррелировал (напрямую (+) или обратным образом (–)), на основании однофакторного анализа, с нейротоксичностью степени и/или отеком головного мозга (при сравнении индивидов с нейротоксичностью степени 5/отеком головного мозга с другими индивидами). Среди 15 индивидов, степень, в которой каждый признак коррелировал или не коррелировал с исходом ответа (как оценено посредством сравнения индивидов, достигших полного ответа (CR) или в отсутствие ответа (NR)), также оценивали; В таблице E2 перечислены также значения p для этого сравнения.
[0766] Параметры, перечисленные в таблице E2, расположены от самого низкого значения p до самого высокого значения p, в порядке убывания, на основании однофакторного статистического сравнения между данным признаком и нейротоксичностью/отеком головного мозга (нейротоксичность степени 5/CE, по сравнению с нейротоксичностью степени 4 или ниже). Для параметров, для которых значения p, применительно к степени нейротоксичности, составляли меньше или равно 0,2, в таблице E2 дополнительно указано, являлась ли наблюдаемая взаимосвязь с нейротоксичностью прямой ((+), показывающей, что наблюдали, что средний уровень или показатель параметра был больше у индивидов с нейротоксичностью степени 5 и отеком головного мозга, по сравнению с индивидами с нейротоксичностью степени 4 или ниже), или являлась обратной ((–), показывающей, что наблюдали, что средний уровень или показатель параметра был ниже у индивидов со степенью 5).
[0767] На ФИГ. 3A – ФИГ. 3U показаны графики для подгруппы параметров, для которых наблюдали взаимосвязи (прямые или обратные) между параметром и нейротоксичностью степени 5, показывающие результаты для индивидуальных индивидов в группах различных нейротоксичности или ответа. Наблюдаемые значения p для этих графиков, применительно к нейротоксичности, составляли 0,05 или ниже.
[0768] На ФИГ. 3V показан график, сравнивающий показатель количества CD3+CAR+ клеток/кг (дозу), введенных индивидам, и то, развилась ли у индивида нейротоксичность степени 5 (с правой стороны) и/или достигнут ли полный ответ (с левой стороны). В то время как наблюдали взаимосвязь между двумя переменными, CD3+CAR+ клеток/кг не являлся сильным прогностическим фактором нейротоксичности степени 5, и не наблюдали четкой границы безопасности. Эти результаты согласуются с интерпретацией, что определение дозы на основании только количеств или частот CD3+CAR+ в дозе, не принимая во внимание других параметров, таких как представленность биологически активных (например, неапоптотических) клеток и/или CD8 по сравнению с CD4 клетками, может не являться адекватным для предотвращения риска тяжелой нейротоксичности, и что имеет преимущество разработка способов дозирования, принимающих во внимание один или несколько прогностических параметров, как наблюдали в настоящем описании.
[0769] На ФИГ. 4, 5A и 5B показаны графики и значения p для показателей антигенспецифической секреции индивидуальных цитокинов (TNF–альфа, IFN–гамма, IL–2), для индивидуальных индивидов в группах различных нейротоксичности или ответа.
[0770] Как показано, наблюдали, что ряд параметров, оцененных для терапевтических композиций клеток и доз, значимо коррелировали (напрямую или обратным образом) с развитием нейротоксичности степени 5 после введения композиции индивиду.
Таблица E2: Оценка параметров терапевтических композиций клеток и/или дозы, и корреляция с исходами нейротоксичности и ответа
[0771] Наблюдали, что взаимосвязи, наблюдаемые в этом исследовании применительно к количеству копий вектора (на клетку или на геном), рассматривали как суррогатные индикаторы выносливости клеток и/или множества переменных, ассоциированных с относительной представленностью модифицированных или немодифицированных клеток в композиции и/или общей плотностью клеток в композиции. Например, в некоторых вариантах осуществления, клетки из образцов крови, которые в общем являлись менее здоровыми в начале процесса, имели более низкую вероятность выживания во время фазы трансдукции, и/или гибель клеток во время трансдукции могла увеличивать эффективность трансдукции. Таким образом, в некоторых аспектах, в некоторых случаях, более высокие количества копий вирусного вектора на композицию, например, введенные посредством трансдукции лентивирусным или гамма–ретровирусным вектором, могут указывать на композиции, в которых больший процент клеток являлись нездоровыми в начале процесса и, в конкретных аспектах, могут иметь свойства, коррелирующие, например, обратно, с нейротоксичностью, например, обратно, с нейротоксичностью. В некоторых вариантах осуществления, более высокая частота трансдукции может приводить к получению композиции, имеющей более высокую частоту модифицированных (например, CAR+) клеток во время криоконсервации, хранения и размораживания. В некоторых аспектах, когда доза основана на количествах модифицированных клеток (или их подтипов, например, CAR+CD3+), такие композиции с более высокой частотой модифицированных клеток могут иметь более низкую общую плотность клеток, что, в конкретных вариантах осуществления, коррелирует с уменьшением уровня или частоты биологически активных или неапоптотических клеток.
[0772] Результаты этого однофакторного анализа идентифицировали несколько параметров дозы и/или терапевтической композиции клеток, которые, как наблюдали, значимо коррелировали (напрямую или обратным образом) с возникновением нейротоксичности степени 5/отека головного мозга. Среди этих параметров присутствовали параметры, показательные для количества, количества на массу пациента и/или частоты клеток, имеющих фенотип, как правило, показательный для биологически активных клеток, таких как неапоптотические CAR+ T–клетки или неапоптотические CAR+CD8+ T–клетки, введенные в дозе. Наблюдали, что ряд параметров, коррелирующих с нейротоксичностью степени 5, значимо не коррелируют с исходом ответа на лечение (в настоящем описании, с тем, достигает ли или нет индивид полного ответа или отсутствия ответа). В различных случаях, наблюдали, что ряд индивидов, достигающих CR, имеют уровни этих параметров, более низкие (в случае прямой корреляции), чем пороговый уровень, соответствующий наименьшему количеству (в случае прямой корреляции), наблюдаемому среди индивидов, у которых развился нежелательный эффект, такой как нейротоксичность степени 5. Например, результаты показали, что количества биологически активных или неапоптотических CD3+ и/или CD8+ клеток, экспрессирующих CAR, можно использовать для определения дозы в пределах границ безопасности и эффективности, чтобы уменьшать риск нейротоксичности и находиться в пределах диапазона, при котором наблюдают ответы. Не идентифицировано ассоциации между летальной нейротоксичностью и состоянием дифференцировки T–клеток или другими фенотипами.
[0773] Наблюдали, что различные показатели количества(количеств) или нормализованных количеств клеток, являвшихся отрицательными по поверхностному окрашиванию для маркеров апоптоза (включая аннексин V), в дозах, вводимых индивиду (или частота таких отрицательных по маркеру апоптоза клеток среди клеток продукта, например, среди CAR+CD3+ или CAR+CD8+), коррелируют с нейротоксичностью. Как правило, наблюдали, что результаты для аннексина V и каспазы–3 являются сходными. В то время как такие параметры также можно считать связанными с функцией или активностью композиции CAR–T–клеток, и таким образом, можно ожидать, что они связаны с эффективностью, как правило, не наблюдали, что эти переменные значимо коррелируют с исходом ответа на лечение, в этом случае, с тем, достигает ли или нет индивид полного ответа или отсутствия ответа (см., например, ФИГ. 2–5).
[0774] Результаты являлись единообразными при использовании частоты или количества неапоптотических (и/или биологически активных) T–клеток или CAR+ клеток, или их подгруппы(подгрупп) (как показано по различным показателям) в качестве параметра для прогнозирования нейротоксичности степени 5 или отека головного мозга, и/или тяжести нейротоксичности, и при использовании такого параметра(параметров) для определения подходящей дозы и/или подходящих пределов безопасности для CAR–T–терапии.
Пример 2: Многофакторный анализ параметров CAR+ композиций T–клеток, которые являются прогностическими для тяжелой нейротоксичности и/или отека головного мозга
[0775] Однофакторные анализы, как правило, учитывают одну ковариацию за один раз. Многофакторные анализы учитывают множество ковариаций за один раз и/или в комбинации, и, как правило, могут принимать во внимание ковариантность, т.е. взаимодействие между ковариациями.
[0776] Многофакторные анализы проводили для идентификации комбинаций параметров (среди параметров, индивидуально оцененных в однофакторном анализе), которые сильно коррелировали с и/или имели высокую прогностическую ценность для клинических исходов и/или исходов токсичности.
[0777] Рекурсивный анализ дерева, с разбиением факторов на две части, проводили для анализа различных комбинаций признаков. Конкретно, объединенный набор данных из однофакторного анализа, включая приблизительно 250 ковариаций (параметров), исследовали с использованием способа на основе разбиения (алгоритмически, с использованием дерева решений) для бинарной классификации. Обычно, с использованием классических способов регрессии получают функциональные (линейные и нелинейные) взаимосвязи, как правило, более пригодные для физико–химических данных и/или тестирования гипотез. С использованием способов разбиения, как правило, получают алгоритмические модели («дерева»), которые могут, в некоторых вариантах осуществления, являться более пригодными для биологических данных и разведочного анализа. По сравнению с такими способами сбора данных, как способ опорных векторов (SVM) и искусственные нейронные сети (ANN), модели разбиения могут обеспечивать преимущества простоты интерпретации.
[0778] Модели разбиения как правило, включают вложенные контейнеры/корзины условных операторов «если–то–иначе», например, прогнозирующие средние ответы. В некоторых вариантах осуществления, поскольку в способах разбиения не принимают предварительную модель, они являются более полезными при оценке измерений с большим шумом или индивидивных измерений, нелинейных данных и наборов данных со смешанными типами данных (т.е. переменными прогностического фактора и ответа, которые являются категорийными и/или непрерывными).
[0779] Как правило, способы на основе деревьев являются непараметрическими и, по сравнению с другими многофакторными способами, лучше оснащенными для манипуляций с измерениями с большим шумом и индивидивными измерениями, комбинацией непрерывных и категорийных переменных и нелинейными взаимосвязями.
[0780] В способе в этом исследовании, учитывали данные для общей группы из 38 индивидов и, отдельно, для группы из 24 индивидов с морфологически подтвержденным заболеванием. Корреляции с нейротоксичностью оценивали посредством группировки пациентов тремя различными способами: в соответствии с тем, возникла или нет у индивидов нейротоксичность степени 5, возникла или нет у них нейротоксичность степени 4 или 5, и возникла или нет у них нейротоксичность степени 4, 5 или длительная (10 суток или больше) нейротоксичность степени 3 (3p). Сложность модели минимизировали посредством использования комбинаций из, самое большее, двух ковариаций (одного первичного прогностического фактора и одного вторичного прогностического фактора) за один раз и поддерживая размер разделенных групп минимум для пяти наблюдений.
[0781] Проводили итеративный поиск, в котором несколько альтернативных моделей получали с использованием (одного и того же) наилучшего первичного прогностического фактора и нескольких вторичных прогностических факторов, при условии, что количество ложноположительных и ложноотрицательных результатов являлось удовлетворительно малым. Затем проводили поиск с учетом следующего наилучшего первичного прогностического фактора, и стадии повторяли. Оценивали несколько альтернативных моделей и обнаружили, что в лучших моделях (моделях с наименьшим количеством ложноположительных и ложноотрицательных) единообразно использованы сходные ковариации.
[0782] С использованием этого способа наблюдали, что конкретные пары параметров имеют большую прогностическую мощность для тяжести нейротоксичности (например, нейротоксичности степени 5). Среди таких пар присутствовали комбинации количеств, или нормализованных количеств, конкретных популяций клеток (таких как CAR+CD3+ неапоптотических или CAR+CD8+ неапоптотических) в вводимой дозе и индикатора специфической для антигена CAR активности в терапевтической композиции, такого как провоспалительные цитокины. Среди таких пар присутствовала комбинация количества отрицательных по маркеру апоптоза CD8+ экспрессирующих CAR клеток, введенных индивиду, в комбинации с параметром, показательным для продукции TNF–альфа, как измерено по накоплению в супернатанте после 18–частового совместного культивирования образца терапевтической композиции клеток, содержащей 0,25×106 CD3+CAR+ клетки, в совместной культуре с экспрессирующими CD19 клетками в соотношении 1:1 (см. фигуры 6A и 6B). Сходные обнаружения получали для других провоспалительных цитокинов, таких как IFN–гамма и IL–2 вместо TNF–альфа.
[0783] В этом исследовании, для этих комбинаций переменных не наблюдали сильного прогнозирования ответа (как измерено по CR по сравнению с отсутствием CR), обратного или прямого (см., например, фигуры 9, 11, 13). Кроме того, нескольким индивидам, достигшим CR или CRi в исследовании, описанном в примере 1, вводили дозы продукта клеток, содержащие количества (или нормализованные количества) маркер апоптоза–CD8+CAR+ клеток, которые были ниже наименьшего количества (или нормализованного количества) в любой дозе, введенной среди индивидов, у которых продолжалось развитие нейротоксичности степени 5/отек головного мозга. Подобным образом, нескольким индивидам, которые продолжали достигать CR, вводили композиции клеток, как определено в анализе, имеющие уровни продукции специфического для антигена CAR цитокина (например, TNF–a, IFN–g, IL–2), которые были ниже, чем наименьшие, наблюдаемые среди композиций, введенных любым индивидам, у которых возникла нейротоксичность степени 5/отек головного мозга (см., например, фигуры 4 и 5).
[0784] Результаты анализа после другого исследования согласовывались с полезностью идентифицированных пар ковариаций для определения дозы и прогнозирования нейротоксичности. Результаты отслеживания сходных композиций экспрессирующих CAR против CD19 клеток, введенных в другом клиническом исследовании в подгруппе (11 из 31) индивидов (отобранных по представленности ряда различных ответов), с рецидивирующим или невосприимчивым ALL взрослых, анализировали по показателям определенных параметров, по–видимому, коррелирующих или обратным образом коррелирующих с исходами нейротоксичности в вышеуказанном исследовании. Из 31 индивида, 77% испытали CR или CRi, с частотами 61% для рецидива и 27% для трансплантата стволовых клеток = (SCT) среди индивидов с CR/CRi. 42% испытали CRS степени 3 или выше, и для 35% показана нейротоксичность степени 3 или 4; ни один из 31 индивидов не испытал нейротоксичности степени 5 или отека головного мозга.
[0785] Определенные параметры оценивали и сравнивали для индивидов и композиций клеток в этом другом исследовании, как правило, как описано выше, включая количество введенных отрицательных по маркеру апоптоза CD8+ экспрессирующих CAR клеток и такой же параметр антигенспецифической активности (такой же показатель накопления TNF–альфа в анализе, включающем совместное культивирование с экспрессирующими CD19 клетками, как использовали выше). Результаты показаны на ФИГ. 7 и ФИГ. 6B. Для дозы, введенной каждому из 11 индивидов, оцененных для другого сходного клинического исследования – из которых ни для одного не показана нейротоксичность степени 5 или отек головного мозга – : (i) количество отрицательных по маркеру апоптоза, экспрессирующих CAR CD8+ клеток было ниже наименьшего количества таких клеток в дозе, введенной любому индивиду с нейротоксичностью степени 5 в вышеуказанном исследовании и/или (ii) уровень параметра, показательного для индуцированной CAR активности (например, показатель продукции TNF–альфа) (B) был ниже самого низкого уровня, наблюдаемого в дозах для индивидов со степенью 5 в вышеуказанном исследовании. Как показано на ФИГ. 6B, общий диапазон профиля продукта для этого анализа среди большинства индивидов в другом оцененном исследовании, был ниже такого уровня, показательного для индуцированной CAR активности, как показано посредством заштрихованного овала.
[0786] Таким образом, среди индивидов в другом исследовании с использованием сходной композиции экспрессирующих CAR клеток, ни у одного из которых не возникла нейротоксичность степени 5, одна или обе из ковариаций в паре, прогностической для нейротоксичности, были ниже уровня, наблюдаемого для любого пациента, испытывающего токсичность. Сходные результаты наблюдали, когда IFNg или IL–2 оценивали вместо TNF–альфа. Результаты согласовывались с интерпретацией использования комбинации функционального признака (степени специфической для антигена CAR активности, как оценено по секреции провоспалительных цитокинов после совместного культивирования с экспрессирующими антиген клетками) и количества (или количества на массу) неапоптотических CAR+CD8+ клеток для определения или оценки подходящей дозы для минимизации риска или тяжести нейротоксичности.
[0787] Результаты этих исследований согласовывались с преимуществами использования составного способа для определения подходящей единичной дозы для введения композиций CAR–T. Например, результаты согласуются с полезностью способа, в котором единичная доза основана на двух или более параметрах, и/или в котором выпуск единичной дозы, подлежащей введению, происходит только после учета любой изменчивости, которая потенциально может вносить вклад в каждый из таких двух или более параметров. Например, результаты согласуются с преимуществами введения единичной дозы и/или идентификации подходящей дозы, в которых (A) относится к количеству или числу клеток конкретного фенотипа (таких как CD3+CAR+, CD8+CAR+, или CD8+CAR+ отрицательный по маркеру апоптоза) и других, или составному количеству клеток множества фенотипов, в которых (B) показывает индуцированную CAR/зависимую от CAR и/или антигенспецифическую активность, такую как индуцированная CAR продукция провоспалительного цитокина. Результаты согласовывались с полезностью составного способа, в котором (1) целевое количество клеток (A) вводят, при условии, что показатель активности (B) ниже определенного порогового количества (на основании корреляций с токсичностью), (2) различную целевую дозу (A) вводят, в зависимости от того, составляет ли B выше или ниже данного одного или нескольких пороговых значений (и необязательно, где клетки не вводят, если B превышает верхний предел порога безопасности) и/или (3) дозу определяют как целевое количество эталонных единиц, где количество эталонных единиц определяют на основании функции A и B (например, A x B, или функции преобразованного значения(значений) или кратного(кратных) A и B).
[0788] Кроме того, наблюдали, что, в некоторых случаях, изменение условий хранения или манипуляций, или партии вида(видов) сырья или реагента(реагентов), используемых в способе получения композиции модифицированных T–клеток – в сходном в ином отношении способе модификации клеток – по–видимому, коррелирует, в конечной терапевтической композиции, с определенными параметрами, которые, как наблюдали в настоящем описании, имеют взаимосвязь с тяжестью нейротоксичности и/или отеком головного мозга, например, в исследовании, описанном выше, например, в комбинации с другой ковариацией. Например, наблюдали, что изменение таких условий хранения или манипуляций, или партий таких материалов или реагентов коррелирует с изменениями конкретных показателей антигенспецифической активности в терапевтической композиции, полученной этими способами, например, таких как показатель продукции провоспалительного цитокина (например, TNF–альфа) в ответ на совместное культивирование с клетками, экспрессирующими антиген CAR.
[0789] Уровни, наблюдаемые для показателей иллюстративных параметров (показателя специфической для антигена CAR продукции TNF–альфа и частоты CD27+/CD28+ фенотипа среди CAR+ клеток) сравнивали для двух групп терапевтических композиций клеток, полученных способом с использованием двух различных партий сырья.
[0790] Результаты показаны на фигурах 23A и 23B. Как показано, уровни этих параметров были изменчивыми среди образцов. Более высокий средний уровень каждого параметра наблюдали в композициях клеток, полученных с использованием способа с использованием одной партии (партии 2) сырья, по сравнению с композициями клеток, полученными с использованием сравнимого способа с использованием другой партии (партии 1) того же реагента (TNFa: p=0,066); (CD27+/CD28+ частота: p=0,018). На фигуре 23B, кроме того, показаны степени нейротоксичности/отека головного мозга, развившихся у индивидов, которым вводили каждую индивидуальную композицию клеток. Среди 15 индивидов, более высокие степени нейротоксичности/отека головного мозга наблюдали среди индивидов, которым вводили композиции клеток, полученные с использованием партии 2 реагента.
[0791] В другом примере, наблюдали также, что хранение реагентов и/или манипуляции с реагентами влияют на параметры среди двух групп терапевтических композиций клеток, полученных посредством способа с использованием одинаковой культуральной среды, с использованием двух различных условий хранения и/или манипуляций, в сходном в ином отношении способе модификации клеток. Две группы терапевтических композиций клеток, полученных из одинаковой среды, сохраняемых в каждых условиях, оценивали по продукции TNF–альфа в ответ на совместное культивирование с клетками, экспрессирующими антиген CAR. Как показано на фигуре 23C, уровни продукции TNF–альфа были изменчивыми среди образцов. Тенденцию к более низкой продукции TNF–альфа наблюдали в композициях клеток, полученных с использованием сред, сохраняемых в первых условиях хранения, по сравнению с композициями, полученными с использованием таких же сред, сохраняемых во вторых условиях хранения.
[0792] Наблюдения согласовывались с интерпретацией того, что может обеспечивать преимущества – например, при идентификации безопасной и эффективной дозы композиции клеток – учет (например, анализ перед выпуском продукта и/или для фактора в способе дозирования) степени изменчивости факторов, которые могут вносить вклад в виды специфической для конкретной клетки/антигена активности в композиции, с позиции композиций, полученных из клеток, происходящих от различных индивидов, и/или в присутствии одного или нескольких различных условий хранения, видов сырья или реагентов, или манипуляций с ними, например, при использовании различных партий реагентов или других видов сырья. Результаты подчеркивают определенные преимущества вариантов осуществления, представленных в настоящем описании. В некоторых аспектах, обеспечивает преимущества уменьшение изменчивости таких параметров и/или подтверждение приемлемого диапазона изменчивости среди таких различных условий/партий, например, при введении новой партии или реагента, подвергнутых хранению или манипуляциям в различных условиях, например, с использованием анализа высвобождения, тестирующего один или несколько параметров композиций клеток, полученных с использованием способа, включающего такие изменения, таких как параметры, как наблюдали в настоящем описании, ассоциированные с риском нейротоксичности, таким образом, чтобы исключать изменчивость таких параметров, например, в различных дозах или продуктах клеток.
[0793] В некоторых вариантах осуществления, представленные способы, изделия, композиции, дозы и способы дозирования обеспечивают преимущества в том, что для них принимают во внимание и, в соответствующих случаях, регулируют или корректируют, потенциальные источники изменчивости, включая изменчивость, полученную из–за изменения реагентов, и/или изменчивость от пациента к пациенту. Например, в некоторых вариантах осуществления, может обеспечивать преимущества получение модифицированных T–клеток способом, включающим использование реагента для стимуляции/размножения T–клеток (или его партии), который, как подтверждено в анализе высвобождения, находится ниже или в пределах приемлемого диапазона изменчивости, по сравнению с пороговым уровнем параметра, например, специфической активности применительно к такому параметру терапевтической композиции (такому как показатель количества или относительного количества реагента, необходимого для индукции определенной степени антигенспецифической активности в конечной композиции T–клеток, полученной способом модификации T–клеток, например, по сравнению с контрольным реагентом или стандартной единицей, применительно к такому анализу). В некоторых вариантах осуществления, представленные варианты осуществления включают дозы клеток, в которых клетки получены способом, включающим анализ высвобождения для подтверждения того, что любая изменчивость таких специфических параметров активности (например, антигенспецифического уровня провоспалительного цитокина) находится в пределах приемлемого диапазона и/или ниже верхнего установленного предела. В некоторых вариантах осуществления, представленные способы включают такой анализ высвобождения. В некоторых вариантах осуществления, получение композиций клеток проводят с использованием реагентов и/или способов, для которых изменчивость таких параметров находится в пределах приемлемого диапазона. В некоторых вариантах осуществления, представленные способы, композиции и изделия обеспечивают преимущества в том, что для них используют способы дозирования и/или получения клеток, уменьшающие риск, ассоциированный с потенциальной изменчивостью таких специфических параметров активности, например, посредством минимизации изменчивости второго параметра, который, вместе со специфическим параметром активности, коррелирует с риском токсичности. Например, посредством минимизации изменчивости частоты биологически активных или здоровых клеток (например, неапоптотических клеток), полученных способом, можно минимизировать влияние изменений специфических связанных с активностью параметров на безопасность. В некоторых вариантах осуществления, доза или способ дозирования, включающие признак(и), связанные с количеством или частотой биологически активных или неапоптотических клеток, таких как биологически активные или неапоптотические модифицированные клетки, или модифицированные CD8+ клетки, уменьшают риск, ассоциированный с изменчивостью параметров антигенспецифической активности. В конкретных аспектах, этого достигают посредством дозирования, включающего верхний предел для таких клеток и/или определяющего дозу на основании эталонных единиц, например, на основании формулы, принимающей во внимание количество биологически активных клеток.
[0794] Композиции, введенные индивидам в исследовании в примере 1, сравнивали с композициями, полученными альтернативным способом получения модифицированных T–клеток из образцов крови, происходящих от индивидов, имеющих рецидивирующую или невосприимчивую NHL. Способ включает отдельное получение и затем смешивание, приблизительно в целевом соотношении, CD4+ и CD8+ популяций модифицированных T–клеток, происходящих из одного и того же индивида. Каждую популяцию получали сходным способом, включающим использование различных факторов и реагентов, включая цитокины, например, в ходе активации, трансдукции (включающей использование лентивирусного вектора) и/или размножения клеток. Способ дополнительно включал заполнение продуктом контейнеров, криоконсервацию и размораживание клеток при плотности клеток, которая являлась сравнительно более высокой, чем плотности, используемые в способе в вышеуказанном исследовании, и являлась единообразной среди образцов (см. пример 4). В общем, способ обеспечивал повышенную степень контроля фенотипа, функции и метаболического профиля модифицированных клеток в конечной композиции. CAR включал происходящий из 41BB костимулирующий домен, в отличие от домена CD28.
[0795] Наблюдали, что среди образцов, полученных с использованием этого способа (например, способа с использованием контролируемых соотношений подгрупп T–клеток, цитокинов и реагентов для обеспечения контроля фенотипа, функции и состояния метаболизма) и контролируемой и более высокой плотности клеток в ходе криоконсервации), присутствовала меньшая изменчивость от индивида к индивиду, по сравнению с изменчивостью среди образцов, анализированных в примере 1, для признаков терапевтических композиций клеток, как наблюдали в настоящем описании, являющихся высоко прогностическими (отдельно и/или в комбинации) для риска тяжелой нейротоксичности.
[0796] Например, альтернативный способ (B) приводил к более высоким частотам биологически активных или здоровых клеток среди CD8+CAR+ клеток, как измерено по отрицательности по различным маркерам апоптоза среди образцов, полученных с использованием этого способа, по сравнению с образцами после введения, как описано в примере 1 (см., например, ФИГ. 21A). Кроме того, присутствовала более низкая степень изменчивости этого параметра среди образцов, полученных этим способом от различных индивидов. Как наблюдали в настоящем описании, количество таких клеток, как наблюдали, коррелировало с нейротоксичностью степени 5 и отеком головного мозга, в то время как количество CD3+CAR+ жизнеспособных клеток (без учета апоптотического состояния, по сравнению с биологически активными клетками), являлось худшим прогностическим фактором и не определяло четко границу безопасности. В некоторых вариантах осуществления, использование способа с уменьшенной изменчивостью частоты таких биологически активных клеток среди модифицированных клеток, уменьшает риск того, что конкретным пациентам (например, пациентам, имеющим клетки, которые менее склонны к апоптозу или которые являются более здоровыми), могут непреднамеренно вводить более высокую дозу, чем намеревались, биологически активных клеток, при дозировании на основании количества модифицированных T–клеток в целом. Кроме того, наблюдали, что способы с большей степенью контроля фенотипа и функции уменьшают степень изменчивости для способности клеток, полученных этим способом, продуцировать провоспалительные цитокины антигенспецифическим образом (см., например, ФИГ. 21B). Результаты в вышеуказанном исследовании согласуются с интерпретацией, что, в частности, в сочетании с количествами биологически активных модифицированных клеток, способ дозирования, принимающий во внимание такие специфические для клеток параметры активности (например, таким образом, что конкретный целевой диапазон такой активности – или не более порогового значения – представлены в данной дозе), можно использовать для предоставления дозы, способной обеспечивать желательный клинический или терапевтический исход, в то же время все еще оставаясь в границах безопасности или уменьшая риск нежелательной токсичности, например, нейротоксичности.
[0797] В некоторых вариантах осуществления, использование способа, в котором постоянно получают более высокие частоты биологически активных модифицированных клеток, позволяет использование доз клеток, намного более низких (с позиции количеств модифицированных, например, CAR+, клеток), по сравнению с другими способами дозирования, в которых с большей частотой модифицированные клетки являются положительными по апоптотическим маркерам или являются в ином отношении менее здоровыми. Например, на основании наблюдений в настоящем описании, и принимая во внимание то наблюдение, что в доступных способах дозирования, как правило, не принимают во внимание частоту апоптотических клеток, в некоторых вариантах осуществления, количества модифицированных (например, CAR+) T–клеток (например, модифицированных CD8+ и/или CD4+ клеток), являются настолько низкими, как 5, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 30, 40 или 50 миллионов клеток.
Пример 3: Определение и формула для целевой единичной дозы
[0798] Иллюстративные дозы, диапазоны доз, и способы и формулы для дозирования и определения дозы, идентифицировали и разрабатывали на основании комбинаций параметров, идентифицированных в многофакторных анализах, по–видимому, являющихся прогностическими для степени нейротоксичности.
[0799] Оценивали данные для всех тридцати восьми индивидов или только для индивидов с морфологически подтвержденным заболеванием. Данные дозирования являлись доступными для 37/38 индивидов; корреляцию с ответом (CR по сравнению с отсутствием CR) учитывали только для пациентов с морфологической нагрузкой заболевания, и не учитывали для индивидов, у которых развилась нейротоксичность степени 5, и которые на поддавались оценке CR. Для индивидуальных индивидов, определяли количество эталонных единиц (RU) в вводимой дозе, где:
[0800] RU=A x B,
[0801] A являлось равным количеству отрицательных по маркеру апоптоза, CD8+, экспрессирующих CAR клеток, и
[0802] B представлял собой параметр, показательный для специфической для антигена CAR активности среди клеток в композиции. В некоторых анализах (см. фиг. 8–13), B представлял собой показатель, показательный для уровня антигенспецифической продукции индивидуального цитокина (например, концентрацию в час на количество введенных клеток), или среднее геометрическое или среднее арифметическое такого показателя, для множества цитокинов.
[0803] В других анализах (см. ФИГ. 14–20), B представляло собой корректированное значение, показательное для уровней одного или нескольких цитокинов, основанное на таком показателе или составном показателе, нормализованном по центральной тенденции такого показателя среди индивидов с нейротоксичностью степени 0–2.
[0804] Результаты нанесены на график в логарифмической шкале для подгрупп индивидов, сгруппированных в соответствии со степенью нейротоксичности (где индивиды сгруппированы по тому, возникла или нет у них нейротоксичность степени 4 или 5, или возникла или нет у них длительная нейротоксичность степени 3 (3p), 4 или 5 нейротоксичность) и/или по частоте ответа (CR/отсутствие CR).
[0805] Результаты показаны на ФИГ. 8–20. Конкретно, на фигурах 8–13 показаны результаты среди 38 индивидов.
[0806] На фигурах 14, 15 и 16 показаны результаты RU среди 32 индивидов с морфологически подтвержденным заболеванием, где A являлось равным количеству отрицательных по маркеру апоптоза, CD8+, экспрессирующих CAR клеток, B представлял собой корректированный показатель антигенспецифической продукции индивидуального цитокина (TNF–альфа, IFN–гамма, и IL–2, соответственно) нормализованный по центральной тенденции показателя для индивидуального цитокина среди индивидов с нейротоксичностью степени 0–2 (где на фигурах 14A, 15A, и 16A показаны результаты для индивидов, сгруппированных в соответствии со степенью нейротоксичности, и на фигурах 14B, 15B и 16B показаны результаты для индивидов, сгруппированных в соответствии с ответом (CR по сравнению с отсутствием ответа CR)).
[0807] Разделение по различным количествам RU наблюдали между группировками индивидов, имеющих различные степени видов токсичности. Результаты использовали для идентификации иллюстративных верхних или пороговых количеств эталонных единиц (на основании формулы RU=A x B), и иллюстративных целевых количеств RU и целевых доз. В некоторых примерах, идентифицировано, что пороговое или целевое количество RU ниже, чем количество RU, определенное среди индивидов, у которых развилась конкретная степень нейротоксичности, в некоторых аспектах, ниже, чем количество RU, соответствующее окну безопасности, например, приводя к 1,5–кратному или 2–кратному уменьшению количества RU. Графики, группирующие пациентов в соответствии с ответом, согласовывались с обнаружением, что целевые значения RU и целевые дозы должны находиться в пределах приемлемых окон ответа.
Пример 4: Коррелляция общей плотности клеток в криоконсервироваанной композиции и параметры композиции, показательные для функции клеток и других признаков
[0808] Исследовали вклад плотности клеток, например, концентрации жизнеспособных клеток (VCC), в ходе криоконсервации и хранения терапевтических композиций T–клеток. Известно, что увеличение плотности клеток в конкретных композициях уменьшает выживаемость клеток. В настоящем описании наблюдали, однако, что для некоторых криоконсервированных композиций клеток для терапевтического использования, в частности, тех, которые являются криоконсервированными при относительно низких плотностях клеток (например, ниже 10% объема клеток от общего замораживаемого объема), увеличение плотности клеток в ходе криоконсервации, хранения и/или размораживания композиции, например, терапевтического продукта, может обеспечивать преимущества, например, применительно к состоянию здоровья и/или биологической активности и/или функции клеток.
[0809] Криоконсервированные терапевтические композиции клеток, введенные индивидам в клиническом исследовании, описанном в примере 1, подвергали криогенному замораживанию при различных плотностях приблизительно ниже 1% (объем клеток как процент от общего замораживаемого объема), с использованием DMSO. В исследованиях, оценивающих различные параметры выше, образцы из композиций клеток подвергали криоконсервации, хранению и размораживанию в условиях, имитирующих условия, в которых введенные композиции клеток хранили, транспортировали и размораживали, включая сходные периоды времени.
[0810] Для оценки вклада плотности клеток в ходе криоконсервации, хранения и размораживания, оценивали композиции клеток от различных индивидов, подвергнутые криогенному замораживанию при различных плотностях клеток (1×106 клеток на мл, 8×106 клеток на мл и 15×106 клеток на мл) и с использованием различных концентраций DMSO (между приблизительно 3% и 9% DMSO по объему). Затем криоконсервированные композиции клеток размораживали, и оценивали активность клеток (как оценено по показателю антигенспецифической цитотоксичности) в композициях.
[0811] Результаты показали наблюдение, что увеличение клеточной активности, как правило, было ассоциировано с более высокими концентрациями клеток и/или концентрациями DMSO в ходе криоконсервации. Результаты согласовывались с интерпретацией, что условия криоконсервации могут влиять на биологическую активность терапевтических композиций T–клеток.
[0812] В дополнительном исследовании, композиции клеток, содержащие клетки, экспрессирующие CAR против CD19, подвергали криогенному замораживанию при различных концентрациях (например, 1×106 клеток/мл, 2×106 клеток/мл, 5×106 клеток/мл 10×106 клеток/мл, 20×106 клеток/мл, 50×106 клеток/мл и 100×106 клеток/мл) и 7,5% DMSO и хранили при 80 градусов в течение приблизительно 15 часов, размораживали, и затем анализировали по жизнеспособности (концентрации и диаметру жизнеспособных клеток (VCC), и по маркерам апоптоза (например, аннексину V и активированной каспазе–3) посредством проточной цитометрии.
[0813] Наблюдаемая потеря концентрации жизнеспособных клеток (% различия VCC), в этом исследовании, на протяжении периода криогенного замораживания и размораживания, лежала в диапазоне 10–45%. Не наблюдали общей тенденции среди концентраций для этих признаков.
[0814] Результаты оценки маркеров апоптоза показали общую тенденцию как для CD4+ экспрессирующих CAR клеток, так и для CD8+ экспрессирующих CAR клеток, к более высоким уровням маркеры апоптоза клеток+ клеток, наблюдаемым после размораживания, для композиций, в которых клетки замораживали и хранили при более низких концентрациях клеток. В частности, результаты показали, что в тестируемом диапазоне концентраций DMSO, например, при 7,5% DMSO, в некоторых вариантах осуществления, общие плотности клеток между 10 или приблизительно между 10 и 60 или приблизительно 60 миллионов, или при или приблизительно при 15 и при или приблизительно при 60 или 70 миллионов клеток на мл в ходе криоконсервации, хранения и размораживания, являлись особенно предпочтительными для улучшения здоровья клеток и/или увеличения частоты биологически активных клеток в композиции после криоконсервации и размораживания.
[0815] Результаты согласуются с полезностью более высоких плотностей клеток или концентраций клеток для CD8+ клеток и/или CD4+ клеток при криоконсервации терапевтических продуктов T–клеток.
Пример 5: Оценка и сравнение невропатологии у различных индивидов
[0816] Оценки невропатологии при аутопсии проводили для четырех индивидов, имеющих острый лимфобластный лейкоз (ALL), у которых возникла тяжелая нейротоксичность, включая нейротоксичность степени 4 или 5, и/или отек головного мозга после лечения с использованием терапевтических композиций, содержащих T–клетки, модифицированные для экспрессии химерного рецептора антигена (CAR). Конкретно, исследования аутопсии проводили для 2 индивидов, которые испытали отек головного мозга степени 5 (n=2), и для 2 индивидов, которые испытали тяжелую нейротоксичность в отсутствие отека головного мозга (n=2). Результаты, в общем, поддерживают заключение, что не наблюдали, что затрагивание головного мозга B–ALL является фактором отека головного мозга. У двух индивидов с отеком головного мозга, в ЦНС не наблюдали ни врожденных иммуноцитов, ни клеток злокачественной опухоли B–ALL и ни CD19+ клеток злокачественных опухолей. Кроме того, наблюдали, что у пациентов с отеком головного мозга, отек имел тенденцию являться вазогенным, не цитотоксическим. У пациентов с отеком головного мозга, просачивание периваскулярного фибрина и красных кровяных клеток позволяли предполагать полное повреждение гематоэнцефалического барьера (BBB). BBB исследовали у этих индивидов. Наблюдали также повреждение эндотелия. По–видимому, однако, отсутствовала какая–либо заметная инфильтрация T–клеток, что согласуется с заключением, что отек головного мозга не развивался в результате инфильтрации и/или активации CAR–T–клеток в головном мозге или ЦНС.
[0817] Кроме того, в головном мозге индивидов, у которых возник отек головного мозга, наблюдали периваскулярные и более диффузные паттерны повреждения/активации астроцитов и микроглии, показательные для BBB. Наблюдение согласовывалось с заключением, что активация микроглии вносила вклад в развитие отека головного мозга у индивидов, подвергнутых CAR–T–клеточной терапии. Кроме того, необратимое повреждение астроцитов (клазматодендроз) наблюдали у индивидов, у которых возник отек головного мозга, на фоне пролиферации астроцитов, наблюдаемой у индивидов, у которых возникла нейротоксичность степени 4. У индивидов, для которых показан отек головного мозга, не наблюдали значительного отека в периферических тканях, таких как легкое, печень или почка. Полного повреждения BBB и возникшего в результате вазогенного отека не наблюдали у индивидов, у которых возникла нейротоксичность степени 4.
[0818] При аутопсии для индивидов, у которых не возник отек головного мозга (n=2), наблюдали диффузную инфильтрацию CD8+ T–клеток, не согласующуюся с простой реакцией на очаговое повреждение. T–клетки присутствовали в ЦНС у этих индивидов. Не наблюдали доказательств патологии гематоэнцефалического барьера у этих индивидов в отсутствие отека головного мозга.
Пример 6: Введение клеток, экспрессирующих CAR против CD19, индивидам с рецидивирующей и невосприимчивой неходжскинской лимфомой (NHL)
[0819] Терапевтические композиции CAR+ T–клеток, содержащие аутологичные T–клетки, экспрессирующие химерный антигенный рецептор (CAR), специфический для CD19, вводили индивидам со злокачественными новообразованиями B–клеток. Вводимые терапевтические композиции T–клеток получали способом, включающим основанное на иммуноаффинности обогащение CD4+ и CD8+ клеток из образцов после лейкафереза от индивидуальных индивидов, подлежащих лечению. Выделенные CD4+ и CD8+ T–клетки по отдельности активировали и независимо трансдуцировали лентивирусным вектором, кодирующим CAR против CD19. Модифицированные CD4+ и CD8+ T–клетки независимо размножали в присутствии цитокинов до порогового количества клеток. После размножения, клетки вводили в состав и подвергали криоконсервации в низком объеме. CAR содержал scFv против CD19, происходящий из мышиного антитела, происходящий из иммуноглобулина спейсер, трансмембранный домен, происходящий из CD28, костимулирующую область, происходящую из 4–1BB, и внутриклеточный передающий сигналы домен из CD3–зета. Криоконсервированные композиции клеток размораживали перед внутривенным введением. Терапевтическую дозу T–клеток вводили в форме определенной композиции клеток посредством введения включенной в состав CD4+ CAR+ популяции клеток и включенной в состав CD8+ CAR+ популяции, введенных в целевом соотношении приблизительно 1:1.
A. Индивиды и лечение
Пример 6.A.1
[0820] Исследования, описанные в этом примере 6.A.1, описывают лечение и оценку индивидов в конкретной временной точке (6.A.1) продолжающегося в настоящее время клинического исследования проведения такой терапии для пациентов с злокачественными новообразованиями B–клеток. Конкретно, когорта (полная когорта) (в этой временной точке, пятьдесят пять (55)) взрослых индивидов–людей с рецидивирующей или невосприимчивой (R/R) агрессивной неходжскинской лимфомой (NHL), включая диффузную крупноклеточную B–клеточную лимфому (DLBCL), вновь возникшую или трансформированную из индолентной лимфомы (NOS), первичной медиастинальной крупноклеточной B–клеточной лимфомой (PMBCL) и фолликулярной лимфомой степени 3b (FLG3B) после неудачи 2 линий терапии. Среди подвергнутых лечению индивидов присутствовали индивиды, имеющие оценку в баллах по шкале Восточной объединенной онкологической группы США (ECOG) между 0 и 2 (медиана отслеживания 3,2 месяцев). Полная когорта не включала индивидов с лимфомой из клеток мантийной зоны (MCL). Ни одного индивида не исключали на основании предшествующей аллогенной трансплантации стволовых клеток (SCT), вторичного затрагивания центральной нервной системы (ЦНС) или балла по ECOG 2, и не присутствовало требования минимального абсолютного количества лимфоцитов (ALC) для афереза.
[0821] Исходы отдельно оценивали для коровой подгруппы индивидов в пределах полной когорты (индивидов в пределах полной когорты, за исключением индивидов с плохим функциональным статусом (ECOG 2), DLBCL, трансформированной из лимфом из клеток маргинальной зоны (MZL) и/или хронического лимфоцитарного лейкоза (CLL, трансформация Рихтера) (коровая когорта)). В этой временной точке, в примере 1.A.1, оценивали исходы для 44 индивидов в пределах этой коровой когорты.
[0822] Демографические и фоновые характеристики индивидов из полной и коровой когорты в этой временной точке в примере 6.A.1 указаны в таблице E3.
[0823] Как показано в таблице E4, индивидам вводили однократную или двойную дозу экспрессирующих CAR T–клеток (каждую однократную дозу посредством отдельных инфузий CD4+ экспрессирующих CAR T–клеток и CD8+ экспрессирующих CAR T–клеток, соответственно) следующим образом: однократную дозу с уровнем дозы 1 (DL–1), содержащую 5×107 тотальных экспрессирующих CAR T–клеток (n=30 для индивидов, оцененных в примере 6.A.1), двойную дозу DL1, в которой каждую дозу вводили с интервалом приблизительно четырнадцать (14) суток (n=6 для индивидов, оцененных в примере 6.A.1, включая одного индивида, которому непреднамеренно ввели две дозы DL2 в расписании с двумя дозами, из–за ошибки дозирования), или однократную дозу с уровнем дозы 2 (DL–2), содержащую 1×108 (DL–2) тотальных экспрессирующих CAR T–клеток (n=18 для индивидов, оцененных в примере 6.A.1). Начиная с трех (3) суток до инфузии CAR+ T–клеток, индивидов подвергали противолимфоцитарной химиотерапии с использованием флударабина (flu, 30 мг/м2 ) и циклофосфамида (Cy, 300 мг/м2).
Таблица E4: Уровни дозирования и количество подгрупп T–клеток для композиции клеток, содержащих T–клетки с CAR против CD19
Пример 6.A.2
[0824] Для примера 6.A.2, в последующей временной точке в клиническом исследовании, описанном в этом примере выше, результаты анализировали во второй временной точке. В этой временной точке анализа в примере 6.A.2, 74 пациентов подвергали лечению (51 мужчин, 23 женщин). Индивиды включали шестьдесят девять (69) индивидов в полной когорте DLBCL (включая 67 DLBCL NOS (45 вновь возникших, 14 трансформированных из FL, 8 трансформированных из CLL или MZL), 1 FL степени 3B, и 1 PMBCL), и 5 индивидов в когорте MCL. Среди индивидов в полной (DLBCL) когорте, медиана возраста составляла 61 лет (диапазон 26, 82), медиана предшествующих циклов терапии составляла 3 (диапазон 1, 12), 46 (67%) являлись невосприимчивыми к химиотерапии, 32 (46%) имели какую–либо предшествующую трансплантацию, и по меньшей мере 16 (23%) пациентов имели лимфому с двойной/тройной перестройкой генов. Сорок девять (49) индивидов в коровой когорте оценивали в этой временной точке in 6.A.2.
B. Безопасность
[0825] Оценивали присутствие или отсутствие вызванных терапией неблагоприятных событий (TEAE) после проведения CAR–T–клеточной терапии. Индивидов также оценивали и мониторировали по нейротоксичности (неврологическим осложнениям, включая симптомы спутанности, афазии, энцефалопатии, миоклонических судорог, конвульсий, летаргии и/или изменения психического состояния), разделенной на степени по шкале 1–5, в соответствии с разработанной Национальным институтом онкологии США – Шкалой общих критериев токсичности (CTCAE), версии 4.03 (NCI–CTCAE v4.03). Common Toxicity Criteria (CTCAE) scale, version 4.03 (NCI–CTCAE v4.03). См. Common Terminology for Adverse Events (CTCAE) Version 4, U.S. Department of Health and Human Services, Published: May 28, 2009 (v4.03: June 14, 2010); и Guido Cavaletti & Paola Marmiroli Nature Reviews Neurology 6, 657–666 (December 2010). Синдром высвобождения цитокинов (CRS) также определяли и мониторировали, разделяя на степени на основании тяжести. См. Lee et al, Blood. 2014;124(2):188–95.
Пример 6.B.1
[0826] В примере 6.B.1 описаны результаты на основании анализа временной точки в примере 6.B.1.
[0827] У 84% индивидов из полной когорты в анализе в примере 6.B.1, тяжелого (степени 3 или выше) синдрома высвобождения цитокинов (CRS) и тяжелой нейротоксичности не наблюдали. Кроме того, наблюдали, что у 60% индивидов из полной когорты не возникло никакой степени CRS или нейротоксичности. Не наблюдали различий в частоте возникновения CRS, нейротоксичности (NT), sCRS, или тяжелой нейротоксичности (sNT) между уровнями дозы. В таблице E5 обобщена частота возникновения неблагоприятных событий синдрома высвобождения цитокинов (CRS) и нейротоксичности у пациентов через 28 суток после введения по меньшей мере одной дозы CAR–T–клеток. Как показано в таблице E5, sCRS (степени 3–4) не наблюдали у каких–либо индивидов, которым вводили однократную дозу DL2 или двойную дозу DL1. Тяжелую нейротоксичность или тяжелый CRS (степени 3–4) наблюдали у 16% (9/55) индивидов из полной когорты и у 18% (8/44) индивидов в коровой подгруппе. 11% (n=6) индивидов вводили тоцилизумаб, 24% (n=13) индивидов вводили дексаметазон. Среди индивидов с ECOG2 в полной когорте, наблюдаемые частоты CRS и нейротоксичности составляли 71% и 29%, соответственно.
Пример 6.B.2
[0828] В примере 6.B.2 описана оценка во временной точке в примере 6.B.2. Вплоть до этой временной точки, данные о неблагоприятных событиях (AE) собирали для противолимфоцитарной терапии (LD) до 90 суток после введения экспрессирующих CAR T–клеток. Во второй временной точке, 69 индивидов в когорте DLBCL (полной когорте) оценивали по безопасности, где 38 имели расписание с введением однократной дозы DL1, 25 имели расписание с введением однократной дозы DL2, и 6 имели расписание с введением двойной дозы DL1. Наиболее частые TEAE, отличные от CRS или NT, включали нейтропению (41%, 28/69), утомляемость (30%, 21/69), тромбоцитопению (30%, 21/69) и анемию (26%, 18/69). Наблюдали одно TEAE диффузное альвеолярное повреждение степени 5.
[0829] Не наблюдали острой инфузионной токсичности, и наблюдали, что большинство индивидов в полной когорте, 64% (44/69), не имели CRS или NT, что показывает, что амбулаторная доставка экспрессирующих CAR T–клеток может являться возможной. Частоты ассоциированных с CAR–T–клетками видов токсичности, включая CRS и NT, не отличались между уровнями дозирования. Наблюдали, что профиль безопасности является сходным среди когорт и уровней дозирования. Среди 25 индивидов в полной когорте (36%), которые испытали CRS или NT любой степени, 21 (30%) имели CRS, и 14 (20%) имели NT. Ни один из индивидов не имел CRS степени 3, и только один (1%, 1/69) имел CRS степени 4 и требовал лечения в ICU; другие 29% (20/69) имели CRS степени 1–2. Из 20% индивидов с NT, 6% (4/69) имели NT степени 1–2 и 14% (10/69) имели NT степени 3–4; 2 (3%) имели судороги. Не наблюдали CRS степени 5 или NT степени 5. Не наблюдали случаев возникновения отека головного мозга. Все события CRS и NT разрешились, за исключением одного случая тремора степени 1, который продолжался на время анализа. Медиана времени до начала первого CRS и NT составляла 5 суток (диапазон 2, 12) и 10 суток (диапазон 5, 23), соответственно. В первые 72 часа после инфузии, ни у одного из индивидов не наблюдали наличия NT, и только у 10% (7/69) наблюдали наличие CRS (все степени 1); NT предшествовал CRS у >70% индивидов. Всего, тринадцати (13) индивидам (19%) требовалось вмешательство из–за CRS или NT с использованием терапии против цитокинов (тоцилизумаба отдельно для 1 (1%), дексаметазона отдельно для 6 (9%) или обоих для 6 (9%)), и только одному требовалась поддержка любого сосудосуживающего средства. Медианы дозы тоцилизумаба и дексаметазона составляли 1 и 6, соответственно. Медиана длительности присутствия CRS и NT составляла 5 суток и 11 суток, соответственно. Анализ коровой когорты (n=49) также показал сходные частоты CRS и NT.
[0830] В этой оценке, наблюдали низкие частоты возникновения и позднее начало CRS и/или NT при дозировании, что поддерживает целесообразность амбулаторной инфузии, например, с госпитализацией при первых признаках лихорадки, или при лихорадке, продолжающейся дольше определенного периода времени, вследствие нее. На время оценки в 6.B.2, четырех индивидов подвергали лечению в амбулаторных условиях.
C. Исходы ответа после лечения
[0831] Индивидов мониторировали по ответу, включая оценку опухолевой нагрузки через 1, 3, 6, 7, 12, 18 и 24 месяцев после введения CAR+ T–клеток.
Пример 6.C.1
[0832] В примере 6.C.1 описаны результаты на основании анализа временной точки в примере 6.A.1 и 6.B.1.
[0833] Частоты ответов перечислены в таблице E6. Частоты ответов с высокой длительностью наблюдали в когорте индивидов, которая включала индивидов с серьезным предшествующим лечением или с плохим прогнозом, и/или с рецидивирующим или невосприимчивым заболеванием. Для индивидов среди всех доз в коровой (n=44) когорте, наблюдаемая общая частота ответа (ORR) составляла 86% и наблюдаемая частота полного ответа (CR) составляла 59%. Через три месяца для коровой когорты, общая частота ответа (ORR) составляла 66%; частота CR через три месяца составляла 50% среди коровой когорты. В коровой когорте, ORR через 3 месяца составляла 58% (11/19) при уровне дозы 1 и 78% при уровне дозы 2; частота CR через 3 месяца составляла 42% (8/19) для уровня дозы 1 и 56% (5/9) для уровня дозы 2, что согласовывалось с предполагаемым эффектом ответа в зависимости от дозы на исход лечения. Кроме того, результаты согласовывались с взаимосвязью между дозой и длительностью ответа.
a Включены пациенты с событиями PD, смерти, или повторным определением стадий в течение 28 суток. Пациентов, подвергнутых лечению за <28 суток до получения точки данных, не включали.
b Знаменатель представляет собой количество пациентов, которых подвергали CAR–T–клеточной терапии ≥ 3 месяцев назад, до получения точки данных, с оценкой эффективности в месяц 3 или до оценки PD или смерти.
c Включая одного пациента, подвергнутого лечению с расписанием дозирования DL2 2–из–за ошибки дозирования
[0834] Среди индивидов, подвергнутых лечению за шесть месяцев или больше до конкретной временной точки оценки, из десяти (10) пациентов, имеющих ответ через три месяца, у 9 (90%) сохранялся ответ через шесть месяцев. В этой временной точке оценки, 97% индивидов в коровой подгруппе, имевших ответ, являлись живыми и при отслеживании, с медианой времени отслеживания 3,2 месяцев. Длительную выживаемость наблюдали у отвечающих, с увеличенной длительностью ответа у индивидов с CR. Все пациенты с ответом через три месяца оставались живыми на время оценки, хотя для 5/6 индивидов с плохим функциональным статусом (ECOG 2) исследование прекратили.
Пример 6.C.2
[0835] В примере 6.C.2 описаны результаты на основании анализа временной точки в примере 6.A.2 и 6.B.2.
[0836] Вплоть до временной точки в примере 6.C.2, 68 индивидов в полной когорте DLBCL оценивали по ответу. Для общего или объективного ответа (OR), 3–месячная, и 6–месячная частоты объективных ответов составляли 75% (51/68), 49% (27/55) и 40% (14/35), соответственно. Частота полного ответа (CR), 3–месячная частота CR и 6–месячная частота CR составляли 56% (38/68), 40% (22/55) и 37% (13/35), соответственно. Тенденцию к улучшению частоты ответа через 3 месяца наблюдали у индивидов, подвергнутых лечению при DL2, по сравнению с DL1: 63% (12/19; 95% CI 38, 84) по сравнению с 40% (12/30; 95% CI 23, 59) для ORR с p=0,148, и 58% (11/19; 95% CI 34, 80) по сравнению с 27% (8/30; 95% CI: 12, 46) для CR с p=0,0385. Среди 16 индивидов с лимфомой с двойной/тройной перестройкой генов, ORR составляла 81%, и 3–месячная частота CR составляла 60%.
[0837] В коровой когорте (n=49 для временной точки в примере 1.C.2), для OR, 3–месячная и 6–месячная частоты OR составляли 84% (41/49), 65% (26/40) и 57% (13/23), соответственно. Частота CR, 3–месячная частота CR и 6–месячная частота CR составляли 61% (30/49), 53% (21/40) и 52% (12/23), соответственно. Наблюдали сходную тенденцию к улучшению длительного ORR и CR через 3 месяца при более высоких дозах. Конкретно, для пациентов в коровой когорте, подвергнутых введению DL2, 3–месячная ORR составляла 80% (12/15; 95% CI 52, 96) и 3–месячная CR составляла 73% (11/15; 95% CI 45, 92), по сравнению с 3–месячной частотой ORR и частотой CR 52% (11/21; 95% CI 30, 74) и 33% (7/21; 95% CI 15, 57) у индивидов в коровой когорте, подвергнутых введению DL1, с p=0,159 и p=0,0409 соответственно. Среди индивидов в коровой когорте, подвергнутых введению DL2 и с 3–месячным отслеживанием (n=15), 3–месячная ORR составлял 80%, и 3–месячный CR составлял 73%.
[0838] Медиана DOR в полной когорте и коровой когорте в этой временной точке в 1.C.2 составляла 5,0 и 9,2 месяцев, соответственно; медиана длительности присутствия CR составляла 9,2 месяцев в полной когорте. Медиана длительности присутствия CR не была достигнута в коровой когорте. Медиана общей выживаемости (OS) составляла 13,7 месяцев в полной когорте и не была достигнута в коровой когорте. 6–месячная OS составляла 75% в полной когорте, с медианой отслеживания 5,8 месяцев. 6–месячная OS составляла 88% в коровой когорте, с медианой отслеживания 5,6 месяцев.
D. Оценка CAR+ T–клеток в крови
[0839] На основании данных из временной точки, описанной в примере 6.A.1, 6.B.1 и 6.C.1, проводили фармакокинетический анализ для оценки количеств CAR+ T–клеток в периферической крови в различных временных точках после лечения. Анализировали результаты для пятидесяти пяти (55) индивидов, оцененных во временной точке в примере 6.A.1 в когорте DLBCL, и четырех (4) индивидов (оцененных в той же самой временной точке) в когорте лимфомы из клеток мантийной зоны (MCL), как описано в примере 7 ниже. Фармакокинетические (PK) измерения проводили с использованием подтвержденной проточной цитометрии для детекции маркера, экспрессированного в конструкции CAR и анализов на основе количественной ПЦР для детекции интеграции конструкции CAR. Аплазию B–клеток оценивали посредством проточной цитометрии с использованием антитела против CD19. CD4+ и CD8+ экспрессирующие CAR клетки, как измерено по количеству клеток/мкл крови (медиана±квартили), нанесенных на график в логарифмической шкале, детектировали в ходе оценки при обоих уровнях введенной дозы. Индивиды, которых подвергали введению DL2, по сравнению с DL1, имели более высокую медиану Cмакс. и медиану AUC0–28 для подгрупп CD3+/CAR+, CD4+/CAR+ и CD8+/CAR+ T–клеток в периферической крови (AUC0–28: DL2 по сравнению с DL1 составляла 1836 по сравнению с 461, 350 по сравнению с 182 и 1628 по сравнению с 114, для CD3+, CD4+ и CD8+, соответственно; p < 0,05 для CD8+; Cмакс.: DL2 по сравнению с DL1 составляла 99,8 по сравнению с 27,9, 15,1 по сравнению с 5,2, и 73,1 по сравнению с 5,5 клеток/мкл, соответственно). Медиана времени до максимального размножения CD3+ CAR+ T–клеток составляла 15 суток (диапазон 8–29) и не отличалась между уровнями дозирования. CD4+ и CD8+ экспрессирующие CAR T–клетки подвергались хомингу в костном мозге при относительно сходных уровнях.
[0840] Увеличенную медианную площадь под кривой (AUC) (количеств CD8+ CAR+ T–клеток в зависимости от времени в крови) наблюдали среди индивидов, которым вводили более высокий уровень дозы, по сравнению с более низким уровнем дозы, без наблюдаемого увеличения токсичности. Более высокое максимальное воздействие CD8+/CAR+ T–клеток наблюдали у отвечающих (CR/PR), чем у не отвечающих (PD); персистенцию клеток в течение времени оценки, включая 3 и 6 месяцев, наблюдали даже у индивидов, заболевание которых прогрессировало. Медиана Cмакс. и медиана AUC0–28 CD8+ CAR+ T–клеток были более высокими у отвечающих индивидов и с длительным ответом на месяц 3 (CD8+ Cмакс. медиана=20,8 по сравнению с 5,5; CD8+ AUC0–28 медиана=235 по сравнению с 55 для CR/PR на месяц 3 по сравнению с PD на месяц 3). Среди индивидов, которых оценивали по персистенции CAR–T–клеток, 90% и 93% из 29 индивидов имели поддающиеся детекции CD8+ и CD4+ CAR+ T–клетки, соответственно, на месяц 3; 63% и 58% из 19 индивидов имели поддающиеся детекции CD8+ и CD4+ CAR+ T–клетки, соответственно, на месяц 6. На месяцы 3 и 6, статистически значимых различий в персистенции CAR+ T–клеток не наблюдали между индивидами с длительным ответом или рецидивом. CAR+ T–клетки поддавались детекции на время рецидива в 89% из 11 индивидов с PK, даже несмотря на то, что аплазия B–клеток (<1 клетка/мкл) показана почти у всех индивидов, 97% (34/35) на месяц 3 и 100% (24/24) на месяц 6.
[0841] Не наблюдали, что более высокие Cмакс. и AUC0–28 для DL2, по сравнению с DL1, ассоциированы с увеличением CRS или NT. Для любой NT или для CRS > степени 2, медианы AUC для CD4+/CAR+ и CD8+/CAR+ T–клеток были в 5–10 раз и в 3–5 раз более высокими, соответственно, чем медиана AUC для DL2. Наблюдали, что более высокая нагрузка заболевания и исходные уровни провоспалительных цитокинов ассоциированы с более высокими максимальными уровнями CAR+ T–клеток, более высокими максимальными уровнями цитокинов, и более высокой частотой возникновения CRS и NT. Результаты согласовывались с заключением, что более высокие Cмакс. и медиана AUC0–28 для DL2 не увеличивали CRS или NT.
Пример 7: Введение экспрессирующих CAR против CD19 клеток индивидам с лимфомой из клеток мантийной зоны (MCL)
[0842] Терапевтические композиции CAR+ T–клеток, содержащие аутологичные T–клетки, экспрессирующие химерный антигенный рецептор (CAR), специфический для CD19, полученные, как описано в примере 1, вводили четырем (4) индивидам–людям с лимфомой из клеток мантийной зоны (MCL), имевшим неудачную терапию 1 линии. Криоконсервированные композиции клеток размораживали перед внутривенным введением. Терапевтическую композицию T–клеток вводили в форме определенной композиции продукта клеток с использованием составов CD4+ и CD8+ популяций модифицированных CAR+ T–клеток, происходящих из того же самого индивида, введенных в целевом соотношении приблизительно 1:1. Индивидам вводили дозы экспрессирующих CAR T–клеток (в форме дробной дозы CD4+ и CD8+ экспрессирующих CAR T–клетки) в однократной дозе с уровнем дозы 1 (DL1), содержащий 5×107 экспрессирующих CAR T–клеток. Начиная с трех (3) суток перед инфузией CAR+ T–клеток, индивидов подвергали противолимфоцитарной химиотерапии с использованием флударабина (flu, 30 мг/м2) и циклофосфамида (Cy, 300 мг/м2).
[0843] Индивидов мониторировали по ответу и видам токсичности, как описано в примере 1. CRS или нейротоксичности не наблюдали ни у одного из индивидов. Из 4 индивидов, подвергнутых лечению, два (2) индивида достигли PR (не длительного) и два (2) пациента имели прогрессирующее заболевание.
Пример 8: Признаки терапевтической композиции T–клеток для введения и способ получения композиции
[0844] Иллюстративные терапевтические композиции T–клеток, содержащие аутологичные T–клетки, экспрессирующие химерный антигенный рецептор (CAR), специфический для CD19, используемые для введения в примере 2 выше, оценивали по более чем ста фенотипических, функциональных и связанных со здоровьем клеток признаков, с использованием проточной цитометрии и анализов in vitro. Оценивали терапевтические композиции клеток, полученные от индивидов, зарегистрированных в клиническом исследовании, оценивающем терапию с использованием T–клеток с CAR против CD19 для лечения рецидивирующей/невосприимчивой B–клеточной неходжскинской лимфомы (N=63; коровая когорта). Клетки оценивали до и после модификации, по различным признакам. Признаки, которые оценивали, включают признаки, описанные в примере 1, и иллюстративные оцененные признаки указаны в таблице E7. Фенотипические маркеры, ассоциированные с здоровьем клеток и фенотипом клеток памяти и другими фенотипами продуктов клеток, исследовали с использованием проточной цитометрии. Функциональность T–клеток оценивали с использованием антигенспецифических биологических анализов in vitro. Характеризацию и тестирование для выпуска проводили для образцов из составленных терапевтических композиций T–клеток, которые подвергали репрезентативному количеству циклов замораживания–размораживания, соответствующему циклам для вводимых композиций клеток.
[0845] Для получения композиций клеток для введения, аутологичные клетки выделяли от индивидов посредством лейкафереза. Образцы после лейкафереза подвергали способу получения экспрессирующих CAR клеток. Способ включал промывку клеток с использованием автоматизированной промывки и отбора на основании иммуноаффинности для очистки CD4+ и CD8+ T–клеток, с получением в результате двух композиций, обогащенных по CD8+ (в которой при медиане 99%, интерквартильной широте (IQR) 98–100%, клеток представляли собой CD8+) и CD4+ (в которой при медиане 99%, IQR 99–100%, клеток представляли собой CD4+) клеткам, соответственно.
[0846] Как показано на ФИГ. 24 и обобщено в таблице E8, при автоматизированной очистке T–клеток получали в результате указанную чистоту CD8+ и CD4+ популяций T–клеток. В некоторых вариантах осуществления, такие аспекты очистки могут уменьшать вероятность трансдукции клеток, не относящихся к T–клеткам, на стадиях трансдукции в способе и/или приводить к высокой чистоте T–клеток в терапевтической композиции клеток, образом, независимым от длительности размножения или других аспектов размножения или инкубации со специфическими для T–клеток реагентами.
[0847] Клетки из обогащенных CD4+ и CD8+ композиций по отдельности подвергали лентивирусной трансдукции с использованием вектора, кодирующего CAR против CD19 с костимулирующим доменом 41BB. Затем трансдуцированные популяции по отдельности инкубировали в присутствии стимулирующих реагентов для размножения клеток. Размноженные CD8+ и CD4+ клетки составляли и подвергали криоконсервации по отдельности и сохраняли перед введением. Для минимизации изменчивости между партиями и/или композициями клеток, происходящих из различных пациентов, таких как пациенты, имеющие различные признаки пациентов, по параметрам, показательным для здоровья клеток, клетки поддерживали постоянные объемы среди партий. Для продуктов клеток показан узкий диапазон жизнеспособных клеток (на основании оценки композиции клеток для одной группы индивидов, CD8+: медиана 31×106 клеток/мл, IQR 28–40×106 клеток/мл, N=38; CD4+: медиана 35×106 клеток/мл, IQR 31–40×106, N=36).
[0848] На месте введения, клетки размораживали и вводили, в соответствии с целевым объемом каждой композиции, соответствующим количеству CD8+CAR+ и CD4+CAR+ клеток в соответствующей дозе (например, для DL1 или DL2). Для минимизации изменчивости состояния здоровья клеток между партиями, для получения составов, криоконсервации и хранения поддерживали при постоянном объеме, с узким диапазоном концентраций жизнеспособных клеток (CD8+: медиана 31×106 клеток/мл, IQR 28–40×106 клеток/мл, N=38; CD4+: медиана 35×106 клеток/мл, IQR 31–40×106, N=36).
[0849] В ходе клинических исследований присутствовало изменение в способе от высокого объема состава до низкого объема состава. После изменения терапевтическую композицию клеток составляли при постоянном низкой объеме, со строго контролируемым диапазоном концентраций жизнеспособных клеток. В некоторых случаях, состав низкого объема использовали вместо состава высокого объема. Оценивали параметры, показательные для состояния здоровья экспрессирующих CAR T–клеток в композициях для введения, например, посредством измерения, после размораживания, жизнеспособности, экспрессии на поверхности клетки аннексина V и уровней активной внутриклеточной каспазы 3. Сравнивали композиции клеток, составленные с высоким объемом и композиции, составленные с низким объемом.
[0850] Изменение в способе от высокого объема состава до низкого объема состава приводило к увеличению надежности способа и уменьшению изменчивости признаков здоровья клеток. Значения концентрации, процента жизнеспособных клеток и процента отрицательных по активной каспазе–3 клеток среди CD4+ и CD8+ T–клеток из индивидуальных композиций клеток показаны на ФИГ. 25 и обобщены в таблице E9. Медиана процента экспрессирующих аннексин V клеток составляла 11% (IQR 9–18%; N=33) CD8+CAR+ T–клеток и 10% (IQR 8–17%; N=31) CD4+CAR+ T–клеток. Наблюдали, что экспрессия каспазы 3 являлась сходной с экспрессией аннексина V. Переход к составу низкого объема приводил к увеличению надежности способа и уменьшению изменчивости признаков здоровья клеток.
• Количества CAR+CD4+ и CAR+CD8+ T–клеток в композиции для введения точно контролировали. Наблюдали, что количество клеток, фактически введенное в иллюстративной группе индивидов, находилось в пределах 8% или менее от целевого количества клеток для данной дозы: 2,4–2,7×107 (целевое ±8%) CD4+CAR+ T–клеток и 2,4–2,7×107 (целевое ±8%) CD8+CAR+ T–клеток для индивидов, которым вводили клетки при DL1 (n=48)
• 4,6–5,1×107 (целевое ±8%) CD4+CAR+ T–клеток или 4,6–5,1×107 (целевое ±8%) CD8+CAR+ T–клеток для индивидов, которым вводили клетки при DL2 (n=20).
[0851] Обнаружили, что диапазон введенной дозы имел низкую изменчивость в различных иллюстративных группах индивидов:
– 48–52 ×106 CD3+CAR+T–клеток при DL1 (n =34)
– 96–101×106 CD3+CAR+T–клеток при DL2 (n=29)
– 24–27×106 CD4+CAR+ или CD8+CAR+ T–клеток при DL1 (n=34)
– 46–51×106 CD4+CAR+ или CD8+CAR+ T–клеток при DL2 (n=29).
[0852] Как показано на ФИГ. 26, наблюдали, что для экспрессирующих CAR композиций T–клеток, введенных индивидам, показана высокая чистота T–клеток и низкая изменчивость между партиями. С использованием контроля способа и продукта получены терапевтические композиции клеток, содержащие CAR–T–клетки с низкой изменчивостью между партиями специфических для клетки функций T–клеток.
[0853] Для антигенспецифического накопления цитокинов и окрашивания внутриклеточных цитокинов (ICS) in vitro показана сходная низкая изменчивость между партиями продукции цитокинов для множества цитокинов (IL–2, TNF–α и IFN–γ). В иллюстративном эксперименте ICS, клетки из композиций стимулировали с использованием CD19, окрашивали по цитокинам, включая TNF–α, и поверхностным белкам, включая рецептор C–C хемокинов типа 7 (CCR7) в качестве маркера фенотипа клеток памяти, и анализировали посредством проточной цитометрии. Определяли количество клеток в композиции для введения, которые являлись положительными по цитокинам или поверхностным белкам. На ФИГ. 27 показано количество CD4+CAR+ и CD8+CAR+ клеток, CD4+CAR+TNF–α+ и CD8+CAR+TNF–α+ клеток, CD4+CAR+CCR7+ и CD8+CAR+CCR7+, и представлены композиции CAR–T–клеток для введения при DL1 и DL2. Эти результаты обобщены в таблице E10. Результаты показывают низкую изменчивость количества CD4+CAR+ и CD8+CAR+ клеток, CD4+CAR+TNF–α+ и CD8+CAR+TNF–α+ клеток, CD4+CAR+CCR7+ и CD8+CAR+CCR7+ клеток. Например, наблюдали узкий диапазон для количества клеток, положительных по продукции TNF–α (n=61).
TNF–α+
TNF–α+
CCR7+
CCR7+
[0854] Для параметра, показательного для продукции CAR+ клетками фактора некроза опухоли альфа (TNFα) после стимуляции с использованием CD19, показан узкий диапазон среди различных партий, с относительным стандартным отклонением (RSD) 37% для CD4+CAR+ T–клеток (N=59) и 51% для CD8+CAR+ T–клеток (N=61).
[0855] Результаты согласовывались с наблюдением, что композиция, содержащая точную и единообразную дозу CD4+ и CD8+ CAR–T–клеток, контроль и оптимизация условий культивирования CD4+ и CD8+ T–клеток, низкая изменчивость продукции цитокинов и/или постоянный состав и объем композиции для введения могут приводить к единообразному состоянию здоровья клеток в композиции. В представленных вариантах осуществления, аспекты такого изготовления и контроля процесса вносят вклад в низкую изменчивость признаков таких композиций клеток, сконструированных с использованием клеток от ряда различных индивидов и полученных для введения ряду различных индивидов. Такие аспекты, в некоторых аспектах, включают использование точной, единообразной фиксированной дозы вводимых CD4+ и CD8+ клеток среди индивидов; контроль и оптимизацию условий культивирования CD4+ и CD8+ T–клеток, таких как условия, приводящие к низкой изменчивости между партиями продукта лекарственного средства фенотипов (например, CCR7) и функции in vitro (например, продукции IL–2, TNF–α и IFN–γ после стимуляции антигеном) например, среди различных индивидов; и использование постоянного состава и объема продукта лекарственного средства, что может приводить к единообразию или вносить вклад в единообразие среди терапевтических композиций клеток, полученных этим способом, для признаков, показательных для состояния здоровья клеток.
Пример 9: Дополнительные фоновые факторы, ассоциированные с развитием нейротоксичности после CAR+ T–клеточной терапии
[0856] Различные фоновые факторы, измеренные до лечения с использованием композиций CAR–T–клеток в ряде различных клинических исследований для злокачественных новообразований из B–клеток, таких как ALL и NHL, оценивали и сравнивали среди индивидов, у которых возникла и у которых не возникла нейротоксичность степени 3 или выше. Анализировали данные из 3 клинических исследований (включая исследование, описанное в примере 1, включающее лечение с использованием T–клеток с CAR против CD19 у индивидов с ALL (исследование 1), клиническое исследование, описанное в примере 2, включающее сходное лечение с использованием CAR против CD19, проведенное для индивидов с рецидивирующим или невосприимчивым ALL взрослых (исследование 2), и дополнительные клинические исследования, в которых индивидов с злокачественными новообразованиями из B–клеток, включая ALL и неходжскинскую лимфому (NHL), подвергали лечению с использованием клеток, экспрессирующих различные CAR против CD19 (исследование 3)). Индивидам вводили композиции T–клеток с CAR против CD19 и мониторировали по клиническому ответу и неблагоприятным исходам. Нейротоксичность разделяли на степени по шкале 0–5, как описано в примере 1.
[0857] Фоновые факторы анализировали, после лечения и сравнивали среди индивидов с использованием ряда статистических анализов. Иллюстративные фоновые факторы, как наблюдали, ассоциированные с нейротоксичностью степени 3 или выше у индивидов, перечислены в таблицах E11–A и E11–B ниже, включая уровни IL–15 в сыворотке и количество клеток тромбоцитов перед введением CAR–T–клеток, тип заболевания (неходжскинская лимфома (NHL) по сравнению с ALL) и нагрузку заболевания, как определено по процентам бластных клеток в костном мозге. Профили экспрессии генов также присутствовали среди идентифицированных параметров: индивиды, положительные по филадельфийской хромосоме (Ph+) или имеющие профиль экспрессии генов, напоминающий Ph+ профиль экспрессии генов (Ph–подобный), имели значимо меньшее количество случаев нейротоксичности степени 3 или выше, чем не положительные индивиды (не–Ph). Иллюстративные фоновые факторы, ассоциированные с нейротоксичностью степени 3 или выше в исследовании 1, показаны в таблице E11–A. Иллюстративные фоновые факторы, ассоциированные с нейротоксичностью степени 3 или выше, среди трех клинических исследований, показаны в таблице E11–B.
Таблица E11–A: Иллюстративные фоновые параметры, ассоциированные с нейротоксичностью степени 3 или выше в исследовании 1
Таблица E11–B: Иллюстративные фоновые параметры, ассоциированные с нейротоксичностью степени 3 или выше
aДвусторонний точный тест Фишера
bHigh IL–15 > 30 пг/мл.
[0858] Образцы крови, собранные от индивидов в различных временных точках после введения CAR–T–клеток в исследовании 1, анализировали по количеству CAR+–T–клеток. Уровни цитокинов, например, IL–15, в сыворотке от индивидов, оценивали перед лечением (скрининг) и в различных временных точках после лечения (сутки 2, сутки 4 и сутки 7). Результаты показали, что длительная и летальная нейротоксичность коррелировали с ранним и быстрым увеличением уровней IL–15, стимулирующего T–клетки цитокина, и с размножением CAR–T–клеток.
[0859] Как обсуждали в примере 1, более быстрое размножение CAR–T–клеток и более ранний максимум размножения экспрессирующих CAR T–клеток наблюдали в крови индивидов, у которых продолжалось развитие более тяжелой нейротоксичности, и в частности, тех, у которых возникла нейротоксичность степени 5 и отек головного мозга. Например, результаты показали, что эти индивиды имели поддающийся детекции уровень CAR+ клеток на мкл крови в пределах 4–7 суток после первой дозы клеток, с более чем 20 CAR+ клеток на мкл крови, наблюдаемыми в крови всех таких индивидов в пределах семи суток после введения клеток (см. ФИГ. 1 и 2). У индивидов с менее тяжелой нейротоксичностью, максимальное размножение CAR+ T–клеток, как правило, наблюдали позже и с более низким максимальным количеством CAR+ T–клеток на микролитр (ФИГ. 2, 28).
[0860] Среди цитокинов, медианные уровни которых увеличивались в несколько раз, по сравнению с фоновыми уровнями, после инфузии CAR–T–клеток, присутствовали IL–2 (14 раз), IL–6 (2,7 раза), IL–10 (3,5 раза), IL–15 (2,5 раза) и IFN–гамма (3,3 раза). Для группы индивидов, испытавших более раннее максимальное размножение CAR–T–клеток (максимальные количества CAR+–T–клеток к суткам 7), наблюдали более высокие средние фоновые уровни IL–15 в сыворотке и повышенное увеличение в сыворотке через 4 суток после введения, по сравнению с индивидами с более поздним максимальным размножением CAR–T–клеток (ФИГ. 28). К следующей временной точке (сутки 7), в которой измеряли уровни IL–15 в сыворотке, уровни IL–15 в сыворотке у этих индивидов с быстрым максимальным размножением, уменьшались и являлись приблизительно сравнимыми или более низкими, чем уровни у индивидов с более поздним максимальным размножением. Результаты согласовывались с заключением, что фоновые уровни IL–15 в сыворотке и/или более высокое или быстрое увеличение уровней IL–15, может показывать или коррелировать с потенциальным риском нейротоксичности или отека головного мозга, или с их тяжестью, после лечения с использованием CAR–T–клеток. Наблюдали также, что циклы противолимфоцитарной и переходной химиотерапии также являлись ассоциированными с увеличением уровня стимулирующих пролиферацию T–клеток цитокинов, таких как IL–15.
[0861] Настоящее изобретение не ограничено по объему конкретными описанными вариантами осуществления, которые представлены, например, для иллюстрации различных аспектов изобретения. Различные модификации описанных композиций и способов очевидны из описания и объяснений в настоящем описании. Такие варианты могут быть осуществлены на практике без отклонения от объема и содержания описания, и включены в объем настоящего описания.
ПОСЛЕДОВАТЕЛЬНОСТИ
X1 представляет собой глицин, цистеин или аргинин
X2 представляет собой цистеин или треонин
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ДЖУНО ТЕРАПЬЮТИКС, ИНК.
КОВИНГТОН, Майкл, Джерард
ДЕЙВ, Кедар, Химаншу
ГЕТТО, Ричард, Джеймс, Мл.
КОВСКИ, Том
ЛАРСОН, Райан, П.
РАМСБОРГ, Кристофер, Глен
ТРЕДЕ, Николаус, Себастьян
ВЕБЕР, Клинтон
УИТМОР, Джеймс, Бойд
ЙИ, Нейтан
БОШЕН, Паскаль
БЕКЕТТ, Трэвис
БЛЭКМАН, Сэмюэл, Чарльз
ШАРТРАН, Натаниэль
ДЭВИС-ПИКЕТТ, Мэл
ГИЛБЕРТ, Марк
ЛАМБЕРТ, Натаниэль
ЛИ, Хе
МЭЛЛЭНИ, Мэри
ПОЛЛОК, Кэтрин, Линдси
ОДЕГАРД, Валери
СМИТ, Джефф
САЗЕРЛЭНД, Клэр
УОКЕР, Эндрю, В.
<120> КОМПОЗИЦИИ, ИЗДЕЛИЯ И СПОСОБЫ, СВЯЗАННЫЕ С ДОЗИРОВАНИЕМ
В КЛЕТОЧНОЙ ТЕРАПИИ
<130> 735042009340
<150> 62/464371
<151> 2017-02-27
<150> 62/465817
<151> 2017-03-01
<150> 62/470180
<151> 2017-03-10
<150> 62/527002
<151> 2017-06-29
<150> 62/580416
<151> 2017-11-01
<150> 62/584740
<151> 2017-11-10
<150> 62/596703
<151> 2017-12-08
<160> 58
<170> PatentIn версии 3.5
<210> 1
<211> 12
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> спейсер (шарнир IgG4)
<400> 1
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 2
<211> 36
<212> ДНК
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> спейсер (шарнир IgG4)
<400> 2
gaatctaagt acggaccgcc ctgcccccct tgccct 36
<210> 3
<211> 119
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> Спейсер шарнир-CH3
<400> 3
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Gly Gln Pro Arg
1 5 10 15
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
20 25 30
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
35 40 45
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
50 55 60
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
65 70 75 80
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
85 90 95
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
100 105 110
Leu Ser Leu Ser Leu Gly Lys
115
<210> 4
<211> 229
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> Спейсер шарнир-CH2-CH3
<400> 4
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys
225
<210> 5
<211> 282
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> IgD-шарнир-Fc
<400> 5
Arg Trp Pro Glu Ser Pro Lys Ala Gln Ala Ser Ser Val Pro Thr Ala
1 5 10 15
Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala
20 25 30
Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys
35 40 45
Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
50 55 60
Ser His Thr Gln Pro Leu Gly Val Tyr Leu Leu Thr Pro Ala Val Gln
65 70 75 80
Asp Leu Trp Leu Arg Asp Lys Ala Thr Phe Thr Cys Phe Val Val Gly
85 90 95
Ser Asp Leu Lys Asp Ala His Leu Thr Trp Glu Val Ala Gly Lys Val
100 105 110
Pro Thr Gly Gly Val Glu Glu Gly Leu Leu Glu Arg His Ser Asn Gly
115 120 125
Ser Gln Ser Gln His Ser Arg Leu Thr Leu Pro Arg Ser Leu Trp Asn
130 135 140
Ala Gly Thr Ser Val Thr Cys Thr Leu Asn His Pro Ser Leu Pro Pro
145 150 155 160
Gln Arg Leu Met Ala Leu Arg Glu Pro Ala Ala Gln Ala Pro Val Lys
165 170 175
Leu Ser Leu Asn Leu Leu Ala Ser Ser Asp Pro Pro Glu Ala Ala Ser
180 185 190
Trp Leu Leu Cys Glu Val Ser Gly Phe Ser Pro Pro Asn Ile Leu Leu
195 200 205
Met Trp Leu Glu Asp Gln Arg Glu Val Asn Thr Ser Gly Phe Ala Pro
210 215 220
Ala Arg Pro Pro Pro Gln Pro Gly Ser Thr Thr Phe Trp Ala Trp Ser
225 230 235 240
Val Leu Arg Val Pro Ala Pro Pro Ser Pro Gln Pro Ala Thr Tyr Thr
245 250 255
Cys Val Val Ser His Glu Asp Ser Arg Thr Leu Leu Asn Ala Ser Arg
260 265 270
Ser Leu Glu Val Ser Tyr Val Thr Asp His
275 280
<210> 6
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<223> T2A
<400> 6
Leu Glu Gly Gly Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp
1 5 10 15
Val Glu Glu Asn Pro Gly Pro Arg
20
<210> 7
<211> 335
<212> Белок
<213> Искусственная последовательность
<220>
<223> tEGFR
<400> 7
Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp Ser Leu
1 5 10 15
Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn Cys Thr Ser Ile
20 25 30
Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg Gly Asp Ser Phe
35 40 45
Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp Ile Leu Lys Thr
50 55 60
Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala Trp Pro Glu Asn
65 70 75 80
Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile Ile Arg Gly Arg
85 90 95
Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val Ser Leu Asn Ile
100 105 110
Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser Asp Gly Asp Val
115 120 125
Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn Thr Ile Asn Trp
130 135 140
Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys Ile Ile Ser Asn
145 150 155 160
Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val Cys His Ala Leu
165 170 175
Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg Asp Cys Val Ser
180 185 190
Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp Lys Cys Asn Leu
195 200 205
Leu Glu Gly Glu Pro Arg Glu Phe Val Glu Asn Ser Glu Cys Ile Gln
210 215 220
Cys His Pro Glu Cys Leu Pro Gln Ala Met Asn Ile Thr Cys Thr Gly
225 230 235 240
Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile Asp Gly Pro
245 250 255
His Cys Val Lys Thr Cys Pro Ala Gly Val Met Gly Glu Asn Asn Thr
260 265 270
Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His Leu Cys His
275 280 285
Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro Gly Leu Glu Gly Cys Pro
290 295 300
Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala Thr Gly Met Val Gly Ala
305 310 315 320
Leu Leu Leu Leu Leu Val Val Ala Leu Gly Ile Gly Leu Phe Met
325 330 335
<210> 8
<211> 27
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> CD28
<400> 8
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 9
<211> 66
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> CD28
<400> 9
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
1 5 10 15
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
20 25 30
Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly Gly
35 40 45
Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe
50 55 60
Trp Val
65
<210> 10
<211> 41
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> CD28
<400> 10
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 11
<211> 41
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> CD28
<400> 11
Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 12
<211> 42
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> 4-1BB
<400> 12
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 13
<211> 112
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> CD3-зета
<400> 13
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 14
<211> 112
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> CD3-зета
<400> 14
Arg Val Lys Phe Ser Arg Ser Ala Glu Pro Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 15
<211> 112
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> CD3-зета
<400> 15
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 16
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<223> Линкерная последовательность
<400> 16
Pro Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Pro
20 25 30
<210> 17
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> линкерная последовательность
<400> 17
Gly Ser Ala Asp Asp Ala Lys Lys Asp Ala Ala Lys Lys Asp Gly Lys
1 5 10 15
Ser
<210> 18
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> T2A
<400> 18
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
1 5 10 15
Gly Pro
<210> 19
<211> 22
<212> Белок
<213> Искусственная последовательность
<220>
<223> P2A
<400> 19
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 20
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> P2A
<400> 20
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 21
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> E2A
<400> 21
Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp Val Glu Ser
1 5 10 15
Asn Pro Gly Pro
20
<210> 22
<211> 22
<212> Белок
<213> Искусственная последовательность
<220>
<223> F2A
<400> 22
Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala Gly Asp Val
1 5 10 15
Glu Ser Asn Pro Gly Pro
20
<210> 23
<211> 357
<212> Белок
<213> Искусственная последовательность
<220>
<223> tEGFR
<400> 23
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro Arg Lys Val Cys Asn Gly Ile Gly Ile Gly
20 25 30
Glu Phe Lys Asp Ser Leu Ser Ile Asn Ala Thr Asn Ile Lys His Phe
35 40 45
Lys Asn Cys Thr Ser Ile Ser Gly Asp Leu His Ile Leu Pro Val Ala
50 55 60
Phe Arg Gly Asp Ser Phe Thr His Thr Pro Pro Leu Asp Pro Gln Glu
65 70 75 80
Leu Asp Ile Leu Lys Thr Val Lys Glu Ile Thr Gly Phe Leu Leu Ile
85 90 95
Gln Ala Trp Pro Glu Asn Arg Thr Asp Leu His Ala Phe Glu Asn Leu
100 105 110
Glu Ile Ile Arg Gly Arg Thr Lys Gln His Gly Gln Phe Ser Leu Ala
115 120 125
Val Val Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu
130 135 140
Ile Ser Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr
145 150 155 160
Ala Asn Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys
165 170 175
Thr Lys Ile Ile Ser Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly
180 185 190
Gln Val Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu
195 200 205
Pro Arg Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys
210 215 220
Val Asp Lys Cys Asn Leu Leu Glu Gly Glu Pro Arg Glu Phe Val Glu
225 230 235 240
Asn Ser Glu Cys Ile Gln Cys His Pro Glu Cys Leu Pro Gln Ala Met
245 250 255
Asn Ile Thr Cys Thr Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala
260 265 270
His Tyr Ile Asp Gly Pro His Cys Val Lys Thr Cys Pro Ala Gly Val
275 280 285
Met Gly Glu Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His
290 295 300
Val Cys His Leu Cys His Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro
305 310 315 320
Gly Leu Glu Gly Cys Pro Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala
325 330 335
Thr Gly Met Val Gly Ala Leu Leu Leu Leu Leu Val Val Ala Leu Gly
340 345 350
Ile Gly Leu Phe Met
355
<210> 24
<211> 66
<212> ДНК
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> сигнальная последовательность альфа-цепи GMCSFR
<400> 24
atgcttctcc tggtgacaag ccttctgctc tgtgagttac cacacccagc attcctcctg 60
atccca 66
<210> 25
<211> 22
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> сигнальная последовательность альфа-цепи GMCSFR
<400> 25
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro
20
<210> 26
<211> 18
<212> Белок
<213> Homo sapiens
<220>
<221> неопределенный признак
<223> сигнальный пептид CD8-альфа
<400> 26
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala
<210> 27
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<400> 27
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 28
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<400> 28
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 29
<211> 61
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<400> 29
Glu Leu Lys Thr Pro Leu Gly Asp Thr His Thr Cys Pro Arg Cys Pro
1 5 10 15
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
20 25 30
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro
35 40 45
Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 30
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<400> 30
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro
1 5 10
<210> 31
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<220>
<221> неопределенный признак
<222> (1)..(1)
<223> глицин, цистеин или аргинин
<220>
<221> неопределенный признак
<222> (4)..(4)
<223> Xaa представляет собой цистеин или треонин
<400> 31
Xaa Pro Pro Xaa Pro
1 5
<210> 32
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<400> 32
Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5
<210> 33
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<400> 33
Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 34
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирная последовательность
<400> 34
Glu Val Val Val Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 35
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L1
<400> 35
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
1 5 10
<210> 36
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L2
<400> 36
Ser Arg Leu His Ser Gly Val
1 5
<210> 37
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L3
<400> 37
Gly Asn Thr Leu Pro Tyr Thr Phe Gly
1 5
<210> 38
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR H1
<400> 38
Asp Tyr Gly Val Ser
1 5
<210> 39
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR H2
<400> 39
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 40
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR H3
<400> 40
Tyr Ala Met Asp Tyr Trp Gly
1 5
<210> 41
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 VH
<400> 41
Glu Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 42
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 VL
<400> 42
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
100 105
<210> 43
<211> 245
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 scFv
<400> 43
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser
245
<210> 44
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR L1
<400> 44
Lys Ala Ser Gln Asn Val Gly Thr Asn Val Ala
1 5 10
<210> 45
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR L2
<400> 45
Ser Ala Thr Tyr Arg Asn Ser
1 5
<210> 46
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR L3
<400> 46
Gln Gln Tyr Asn Arg Tyr Pro Tyr Thr
1 5
<210> 47
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR H1
<400> 47
Ser Tyr Trp Met Asn
1 5
<210> 48
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR H2
<400> 48
Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe Lys
1 5 10 15
Gly
<210> 49
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR H3
<400> 49
Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr
1 5 10
<210> 50
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 VH
<400> 50
Glu Val Lys Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 51
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 VL
<400> 51
Asp Ile Glu Leu Thr Gln Ser Pro Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Pro Leu Ile
35 40 45
Tyr Ser Ala Thr Tyr Arg Asn Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Lys Asp Leu Ala Asp Tyr Phe Cys Gln Gln Tyr Asn Arg Tyr Pro Tyr
85 90 95
Thr Ser Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 52
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Линкерная последовательность
<400> 52
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 53
<211> 245
<212> Белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 scFv
<400> 53
Glu Val Lys Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Lys Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val Thr Cys
145 150 155 160
Lys Ala Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr Arg Asn
180 185 190
Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp Tyr Phe
210 215 220
Cys Gln Gln Tyr Asn Arg Tyr Pro Tyr Thr Ser Gly Gly Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys Arg
245
<210> 54
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 HC-CDR3
<400> 54
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
1 5 10
<210> 55
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 LC-CDR2
<400> 55
His Thr Ser Arg Leu His Ser
1 5
<210> 56
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> FMC63 LC-CDR3
<400> 56
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 57
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность, кодирующая scFv
<400> 57
gacatccaga tgacccagac cacctccagc ctgagcgcca gcctgggcga ccgggtgacc 60
atcagctgcc gggccagcca ggacatcagc aagtacctga actggtatca gcagaagccc 120
gacggcaccg tcaagctgct gatctaccac accagccggc tgcacagcgg cgtgcccagc 180
cggtttagcg gcagcggctc cggcaccgac tacagcctga ccatctccaa cctggaacag 240
gaagatatcg ccacctactt ttgccagcag ggcaacacac tgccctacac ctttggcggc 300
ggaacaaagc tggaaatcac cggcagcacc tccggcagcg gcaagcctgg cagcggcgag 360
ggcagcacca agggcgaggt gaagctgcag gaaagcggcc ctggcctggt ggcccccagc 420
cagagcctga gcgtgacctg caccgtgagc ggcgtgagcc tgcccgacta cggcgtgagc 480
tggatccggc agccccccag gaagggcctg gaatggctgg gcgtgatctg gggcagcgag 540
accacctact acaacagcgc cctgaagagc cggctgacca tcatcaagga caacagcaag 600
agccaggtgt tcctgaagat gaacagcctg cagaccgacg acaccgccat ctactactgc 660
gccaagcact actactacgg cggcagctac gccatggact actggggcca gggcaccagc 720
gtgaccgtga gcagc 735
<210> 58
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Линкерная последовательность
<400> 58
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ | 2018 |
|
RU2795984C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ ГЕННО-ИНЖЕНЕРНЫХ КЛЕТОК И РОДСТВЕННЫХ КОМПОЗИЦИЙ | 2018 |
|
RU2790444C2 |
| ХИМЕРНЫЕ РЕЦЕПТОРЫ, СОДЕРЖАЩИЕ TRAF-6-ИНДУЦИРУЮЩИЕ ДОМЕНЫ, И СВЯЗАННЫЕ С НИМИ КОМПОЗИЦИИ И СПОСОБЫ | 2016 |
|
RU2773159C2 |
| СПОСОБЫ МОДУЛИРОВАНИЯ CART-КЛЕТОК | 2017 |
|
RU2774232C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПОЛУЧЕНИЯ ГЕННО-ИНЖЕНЕРНЫХ КЛЕТОК | 2018 |
|
RU2795454C2 |
| ПРОДУЦИРОВАНИЕ СКОНСТРУИРОВАННЫХ КЛЕТОК ДЛЯ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ | 2017 |
|
RU2780156C2 |
| СОЧЕТАНИЕ КЛЕТОЧНОЙ ТЕРАПИИ И ИММУНОМОДУЛЯТОРНОГО СОЕДИНЕНИЯ | 2018 |
|
RU2777911C2 |
| СПОСОБЫ ПРОВЕДЕНИЯ ИММУНОТЕРАПИИ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА В КОМБИНАЦИИ С АГОНИСТОМ 4-1BB | 2019 |
|
RU2788524C2 |
| СПОСОБЫ ВЫДЕЛЕНИЯ, КУЛЬТИВИРОВАНИЯ И ГЕНЕТИЧЕСКОЙ ИНЖЕНЕРИИ ПОПУЛЯЦИЙ КЛЕТОК ИММУННОЙ СИСТЕМЫ ДЛЯ АДОПТИВНОЙ ТЕРАПИИ | 2015 |
|
RU2763795C2 |
| РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ | 2018 |
|
RU2783956C2 |
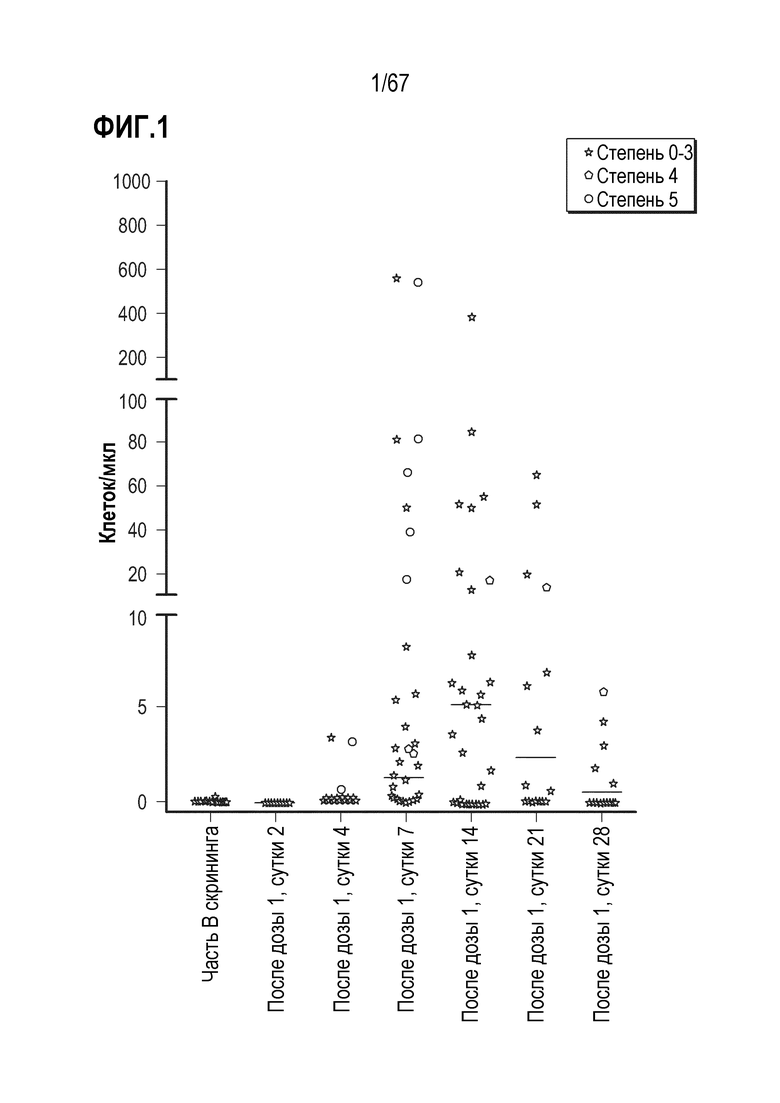


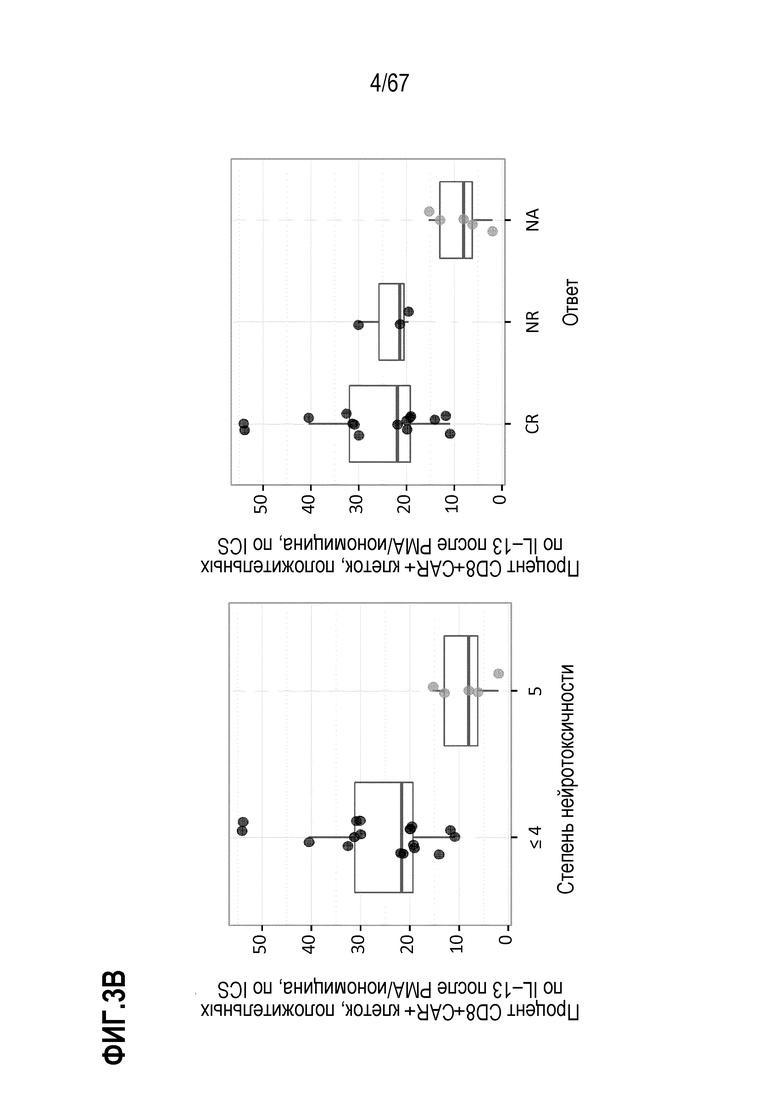
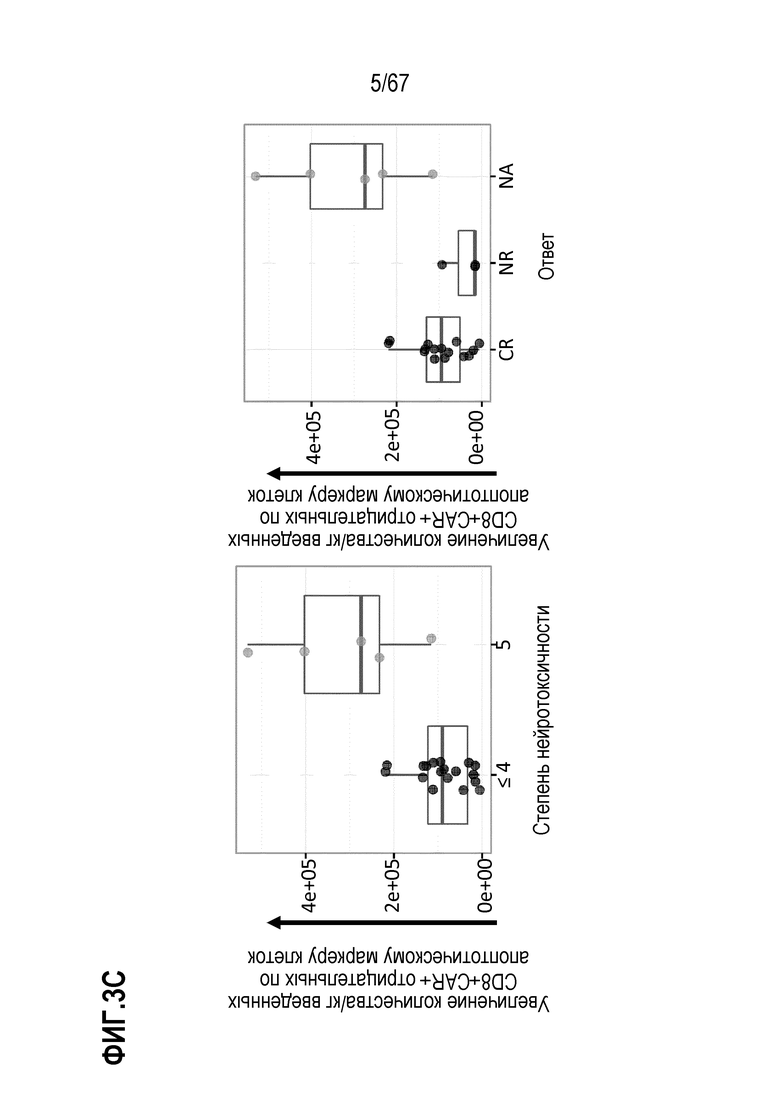
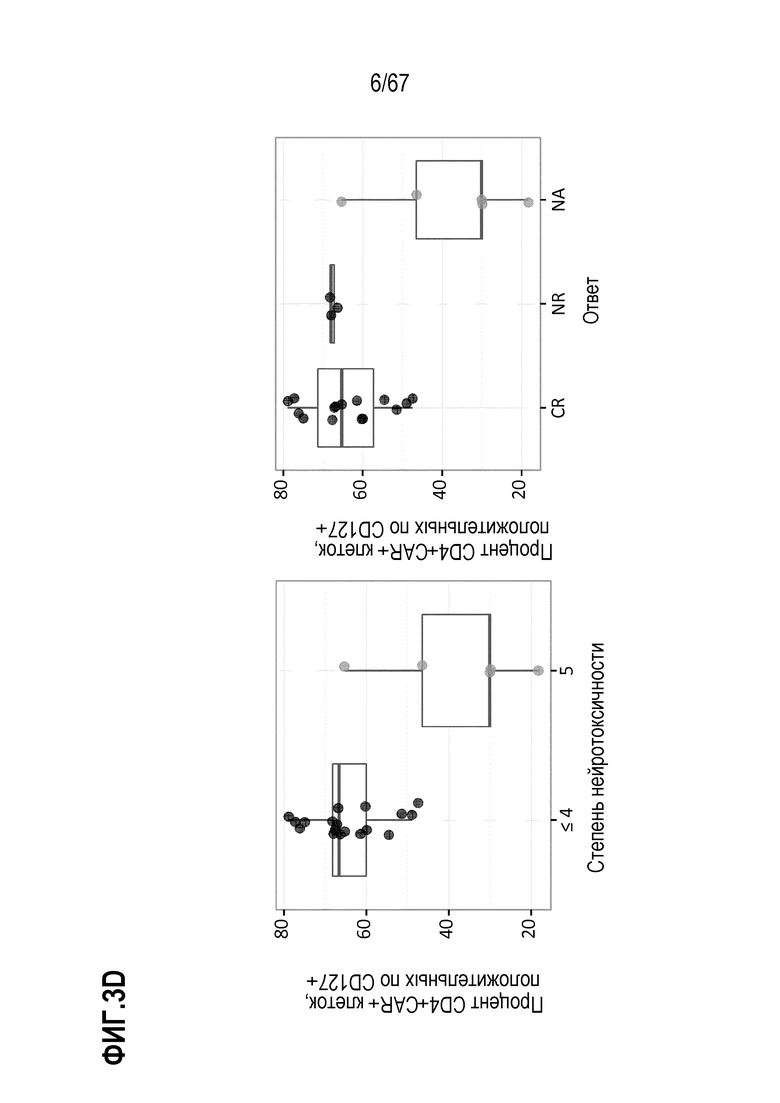
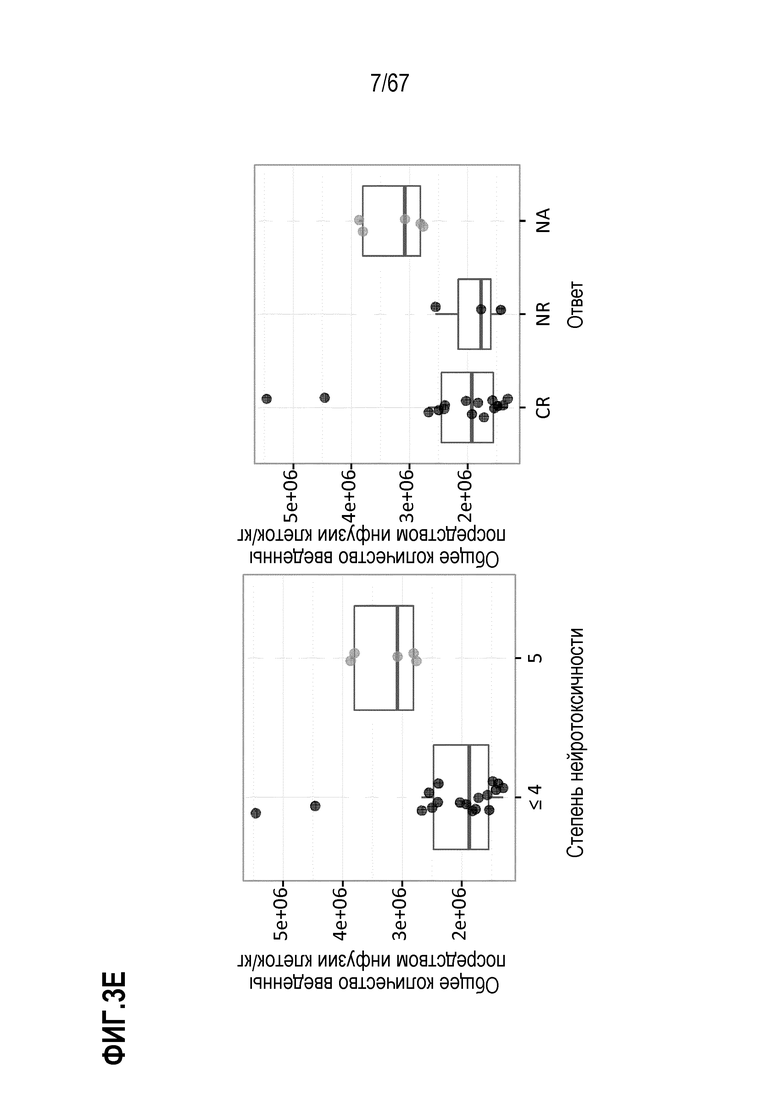


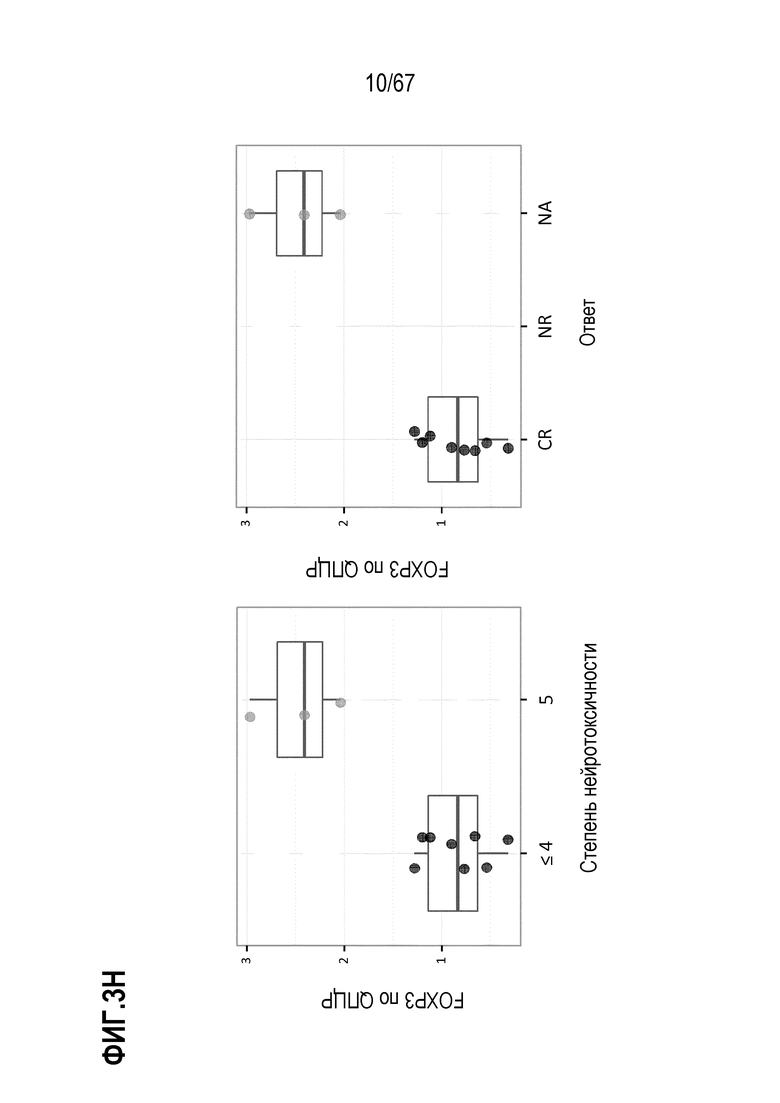

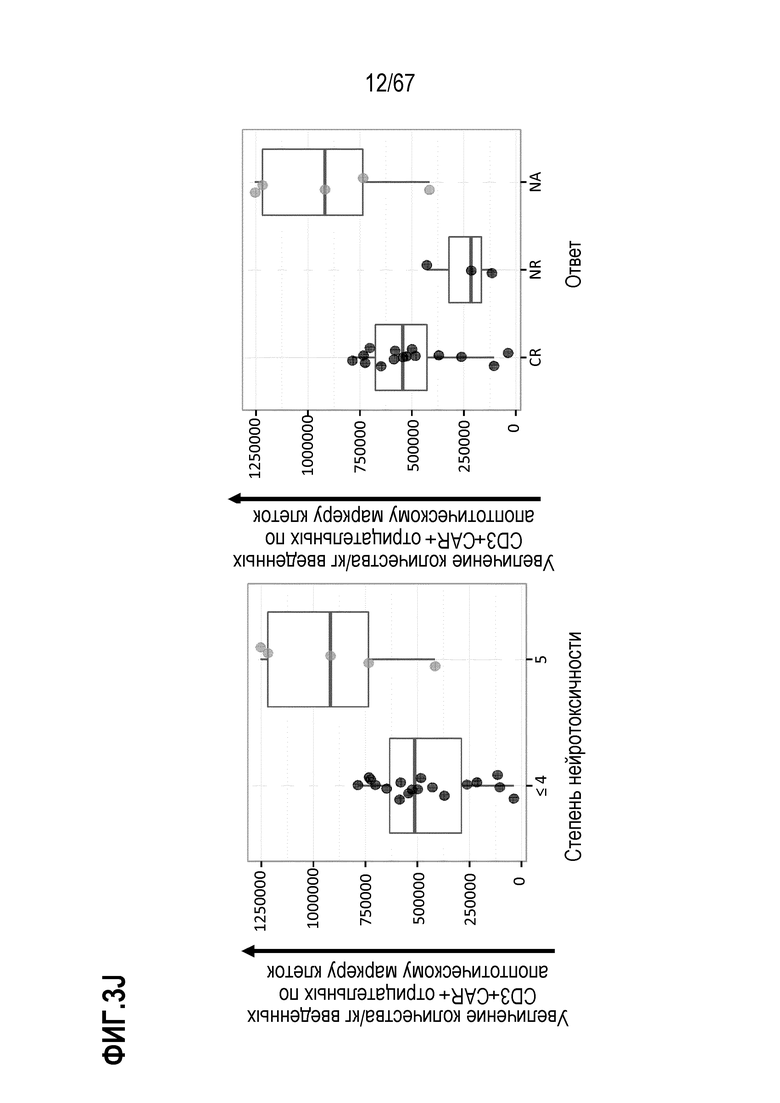



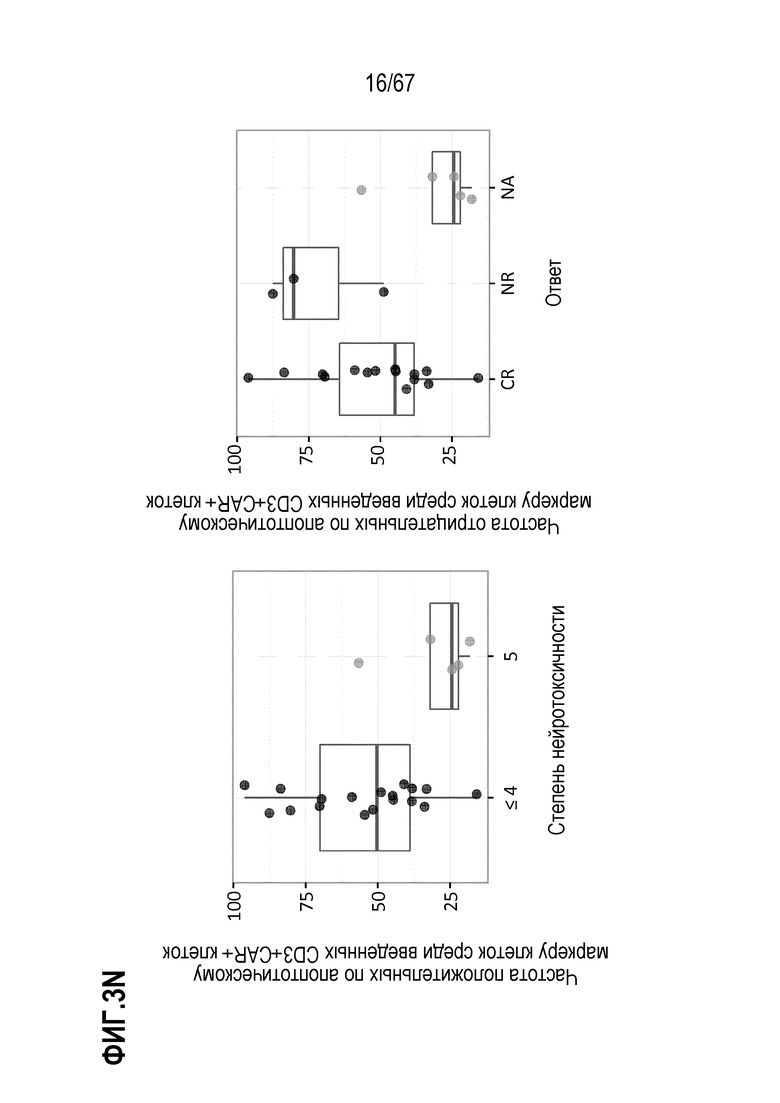

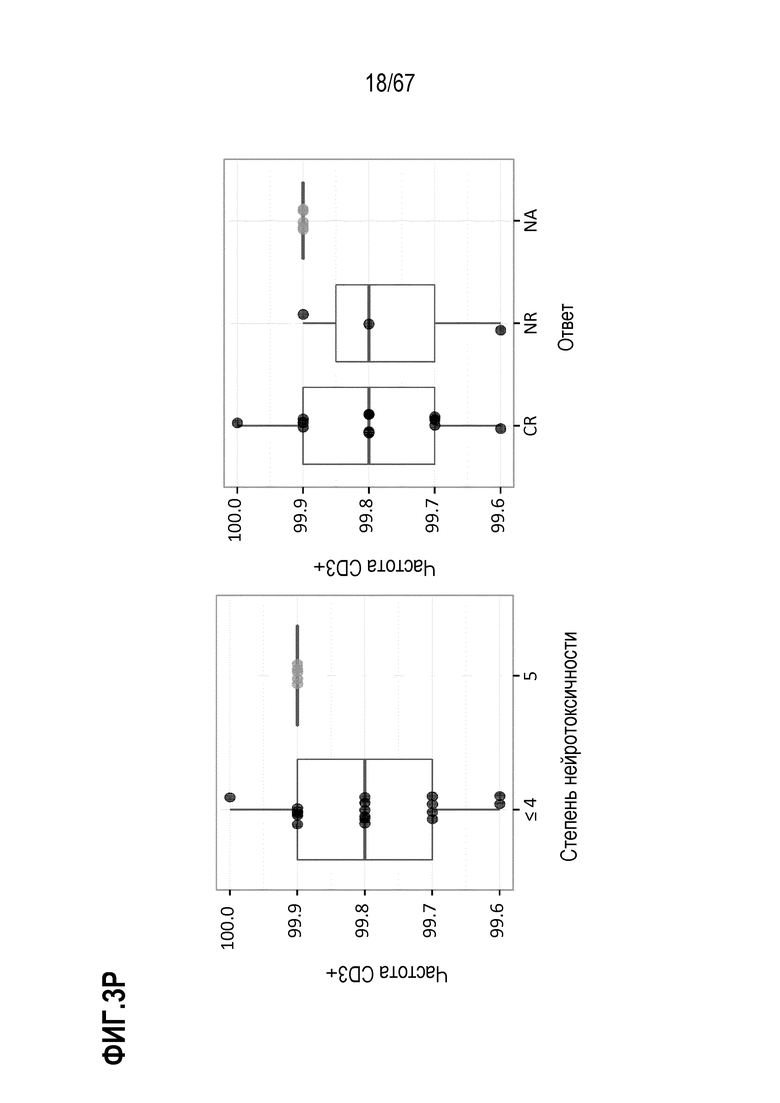


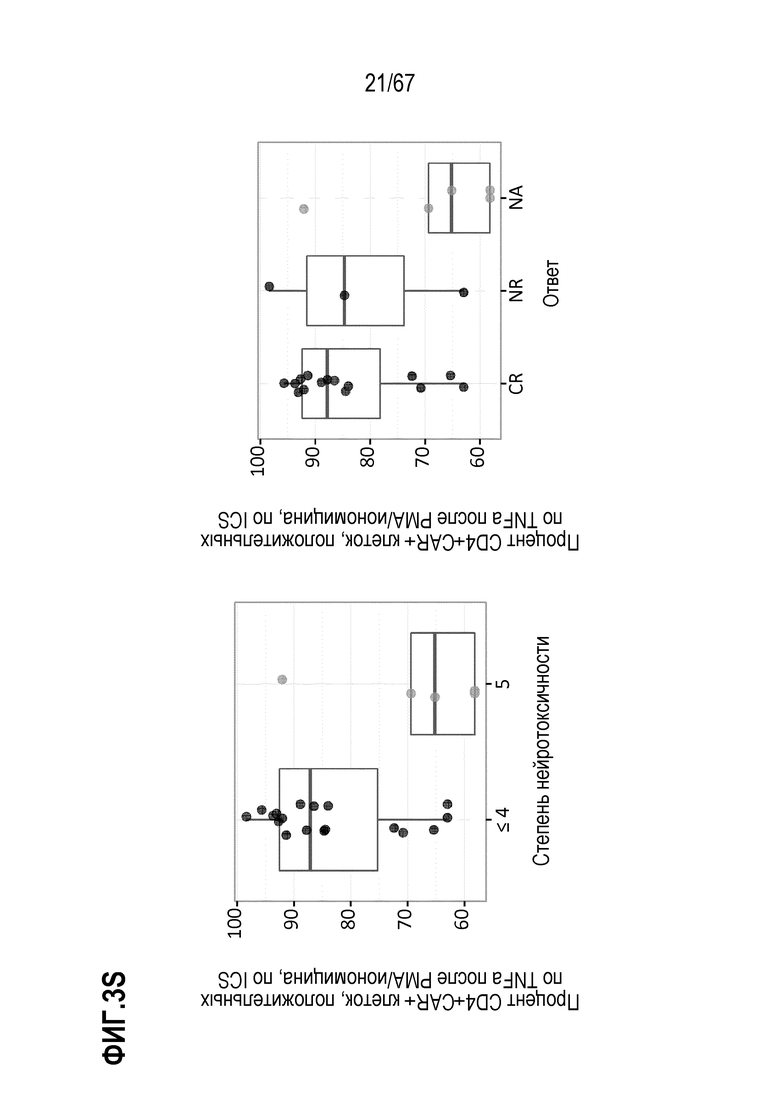
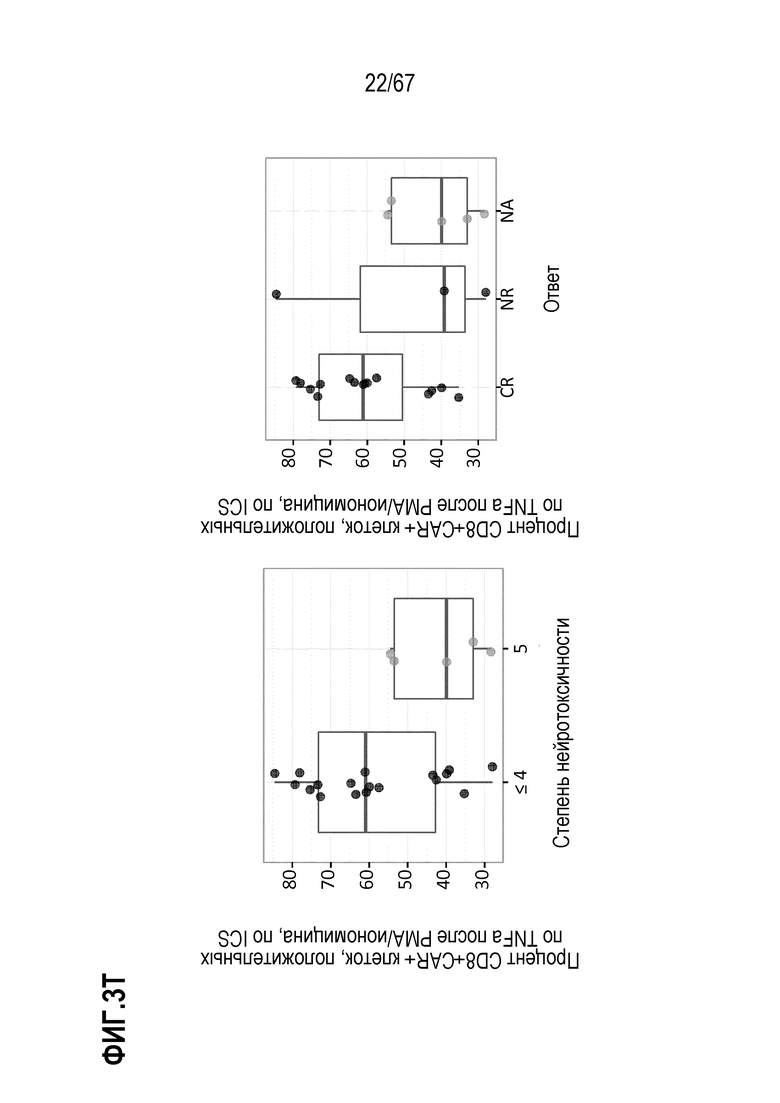






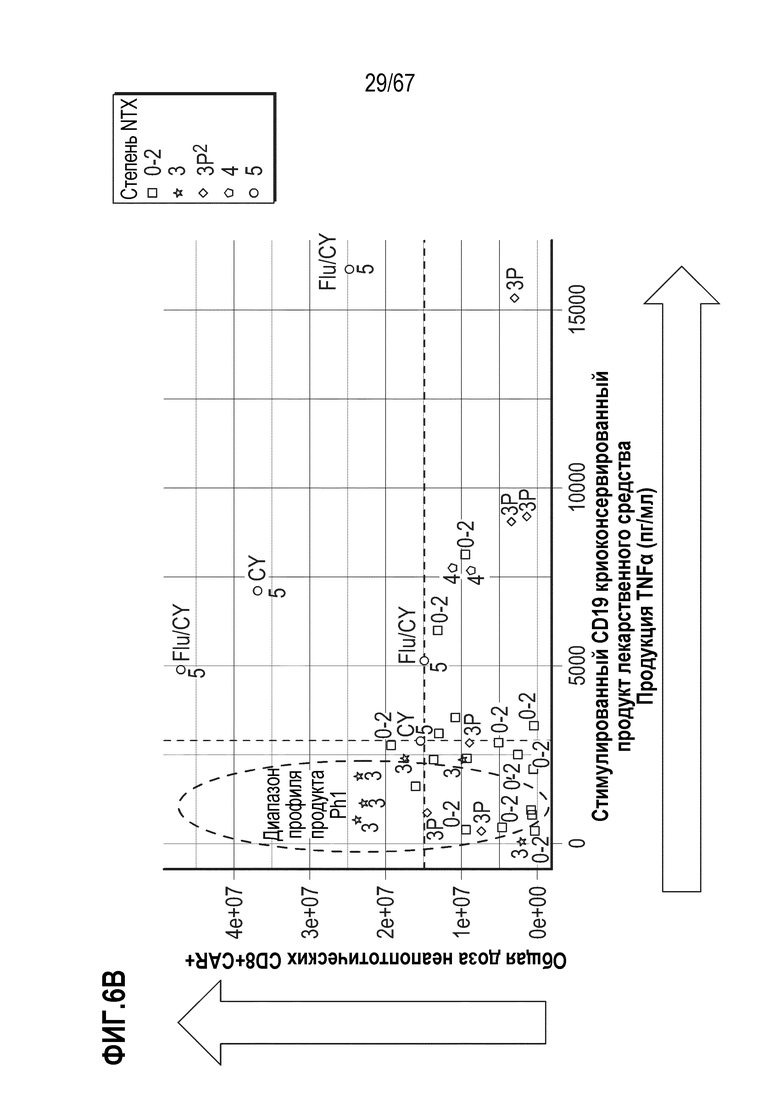



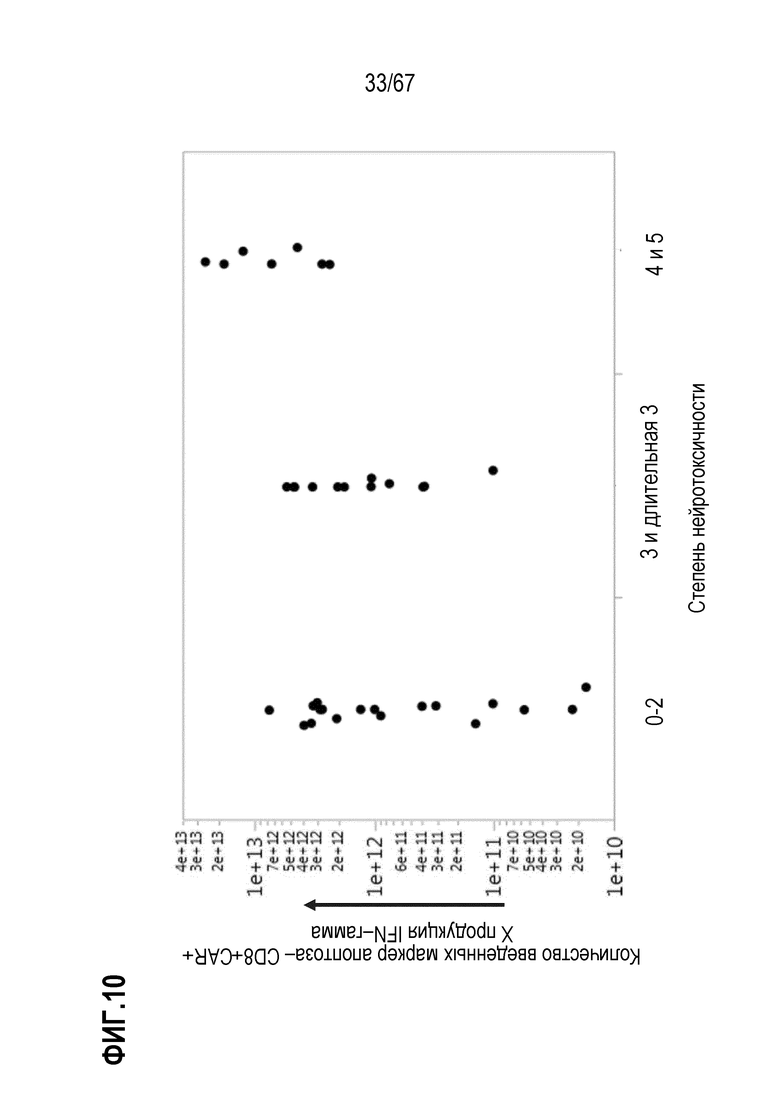

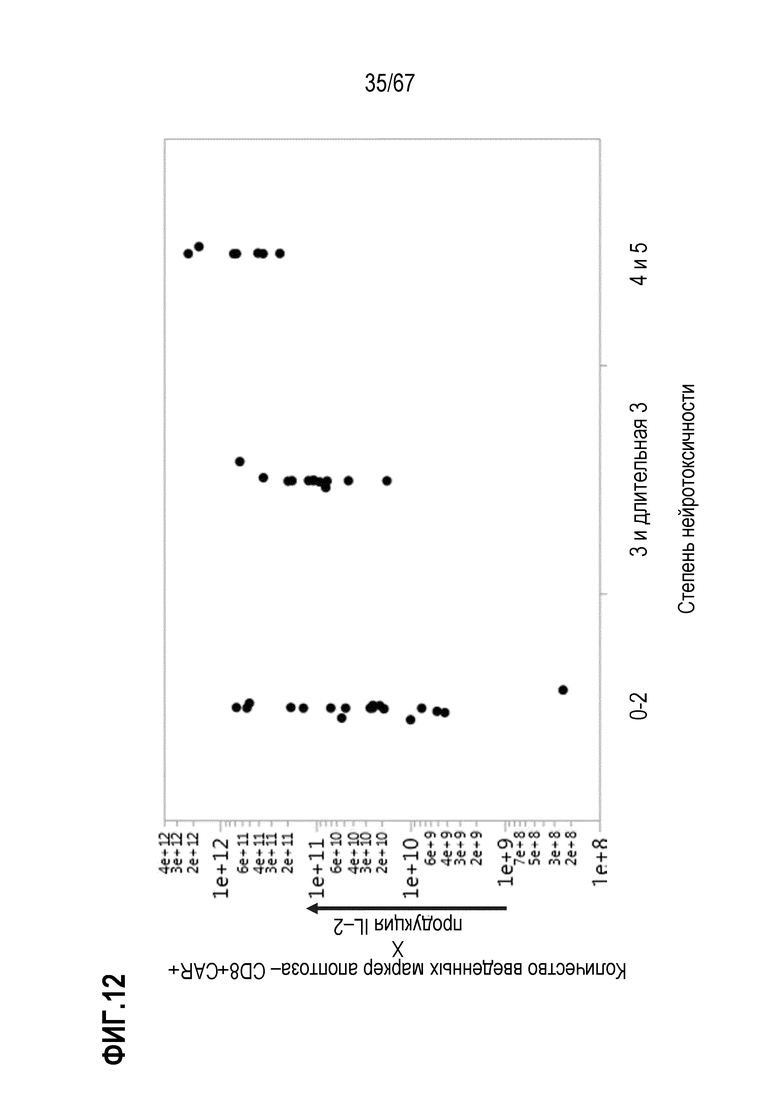
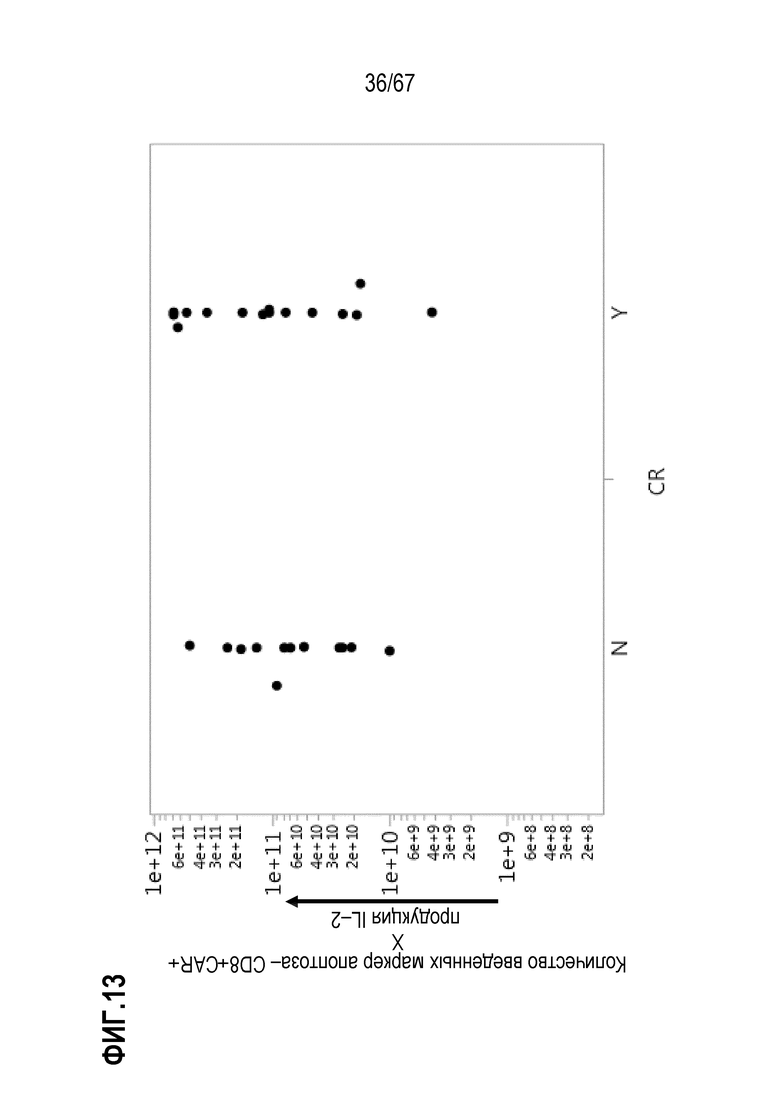

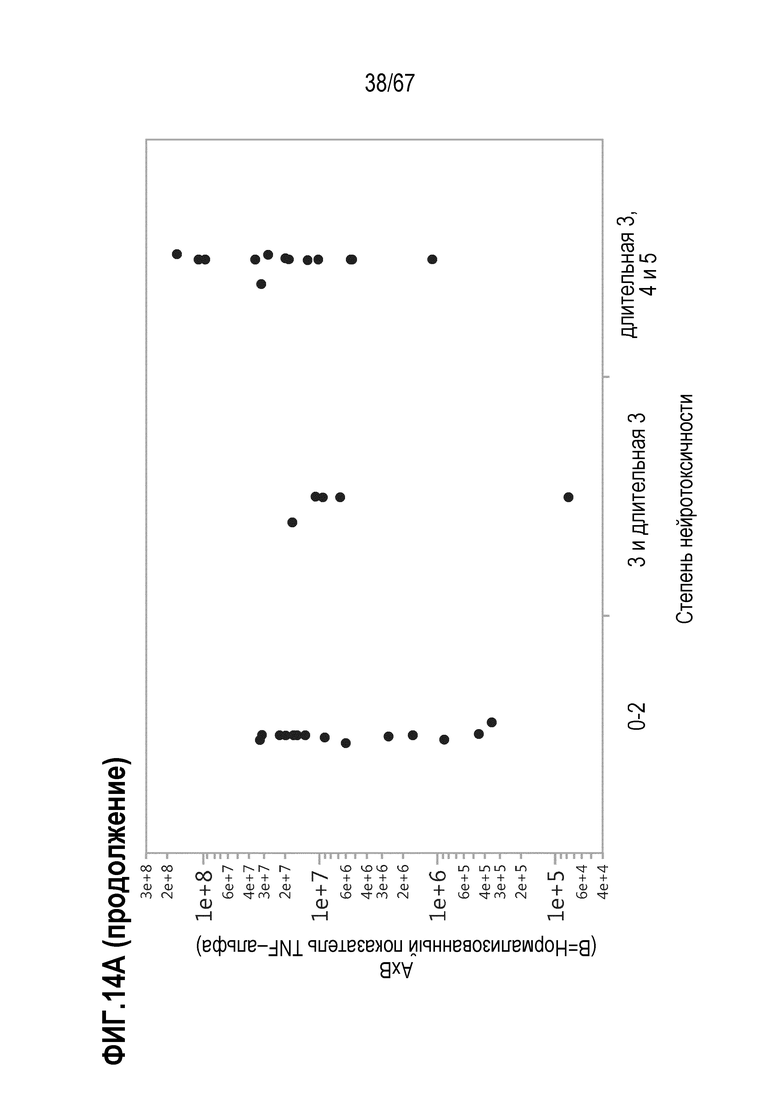

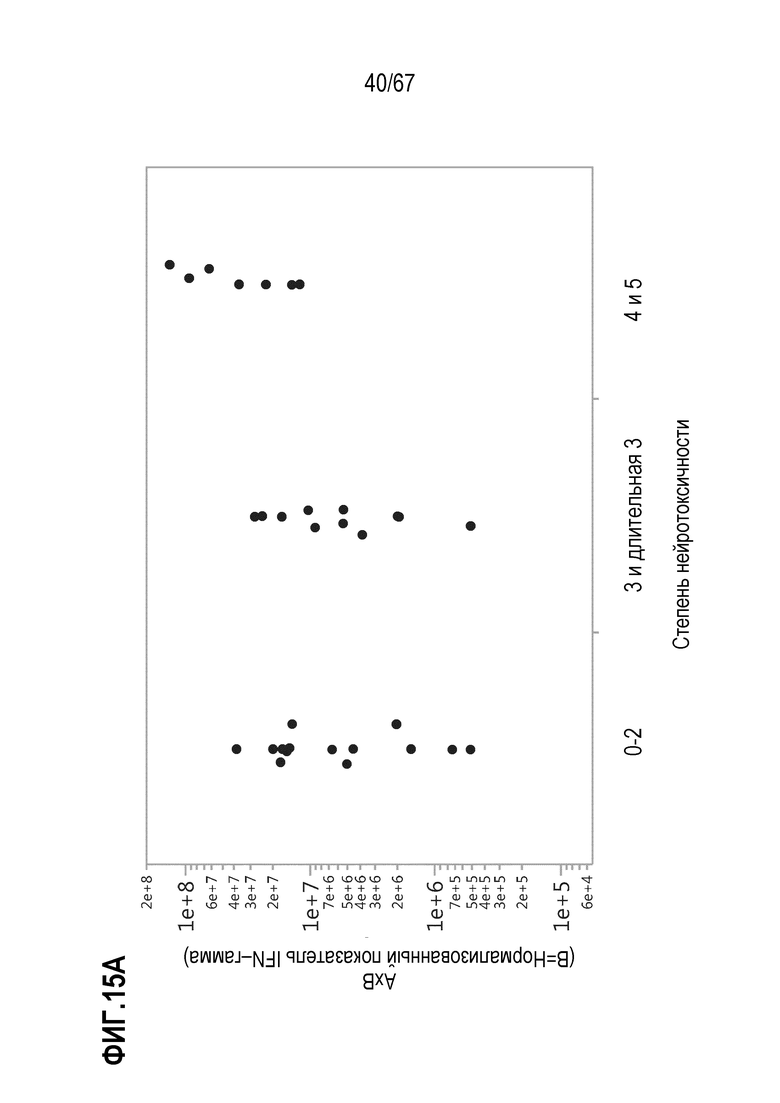
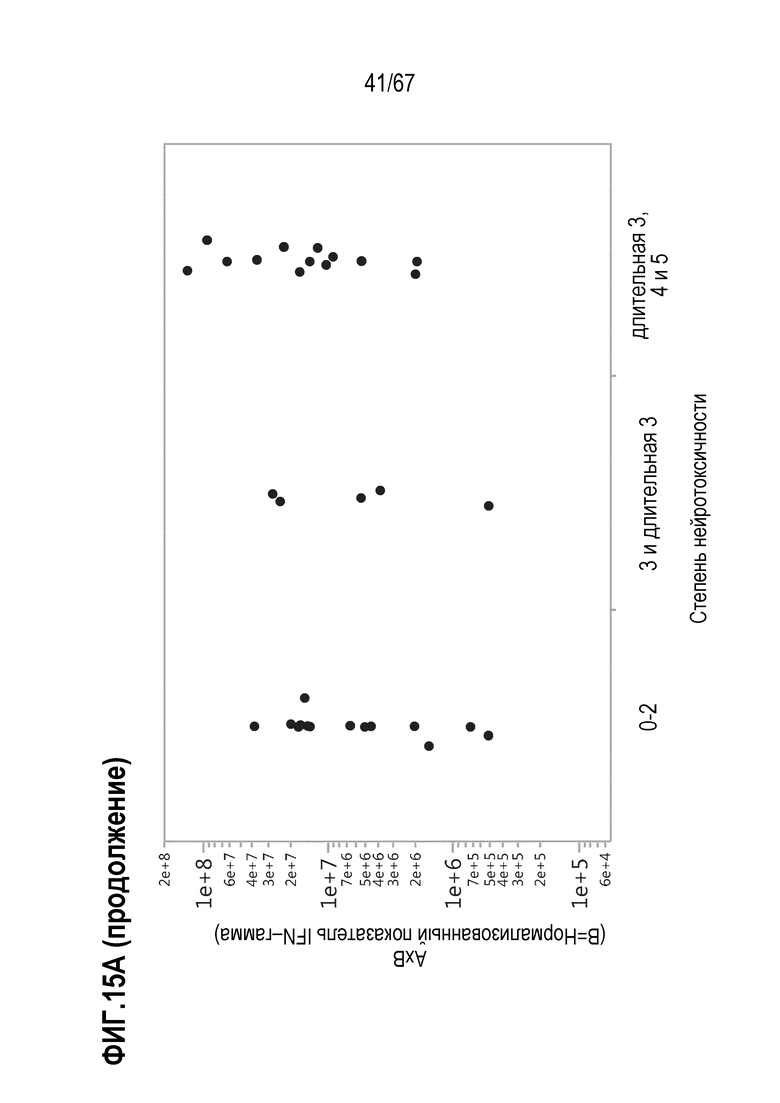
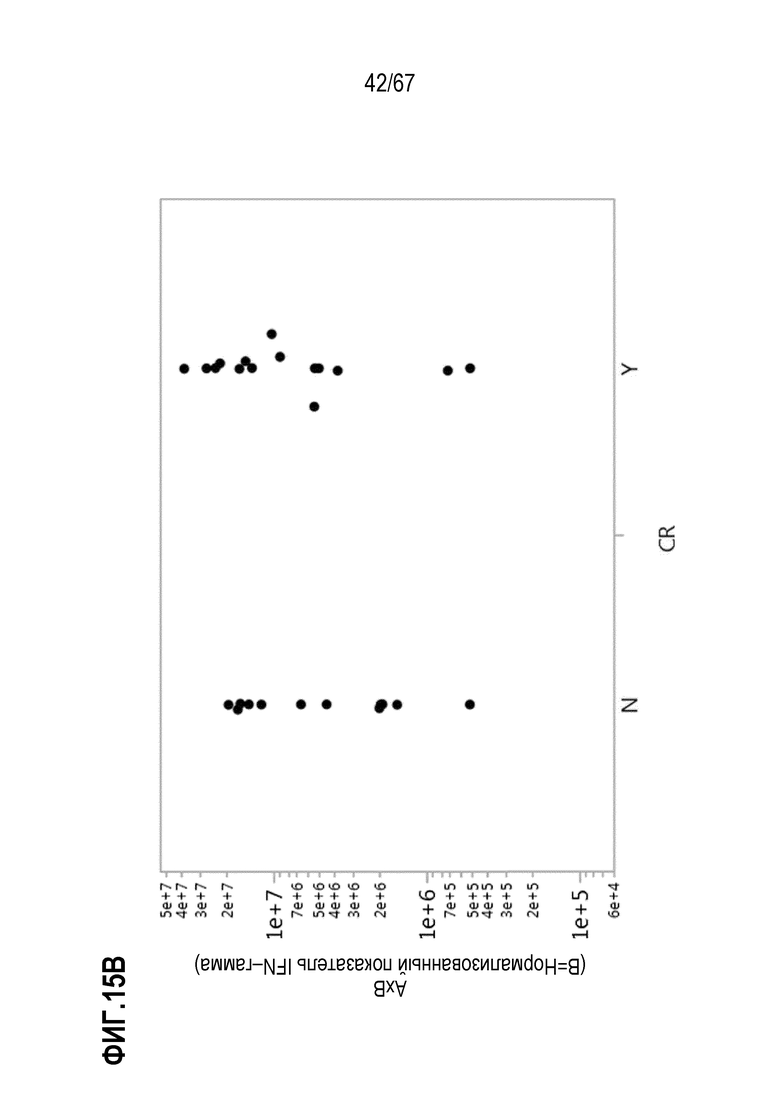
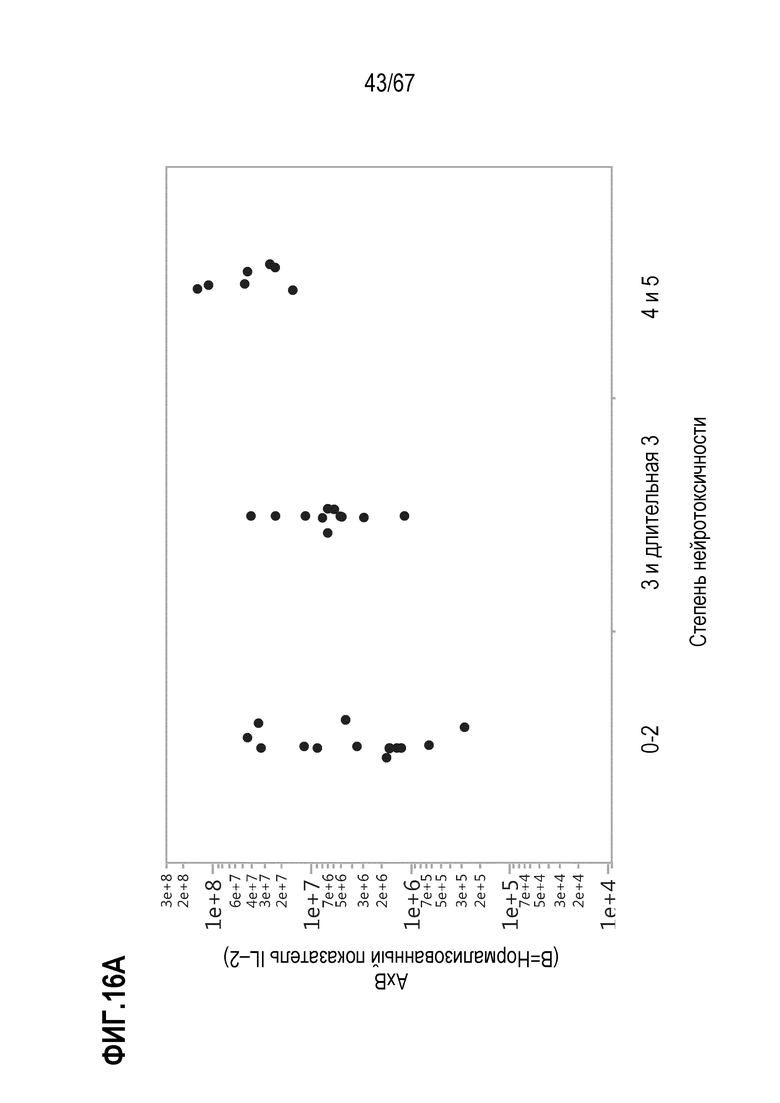



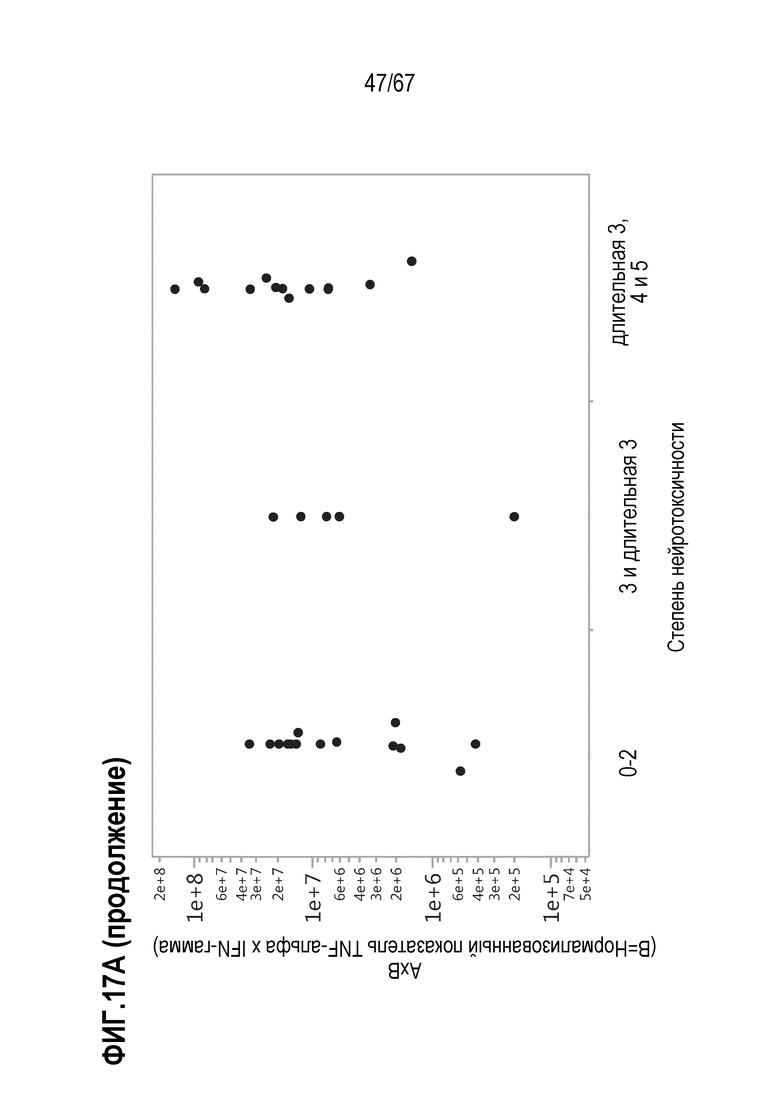
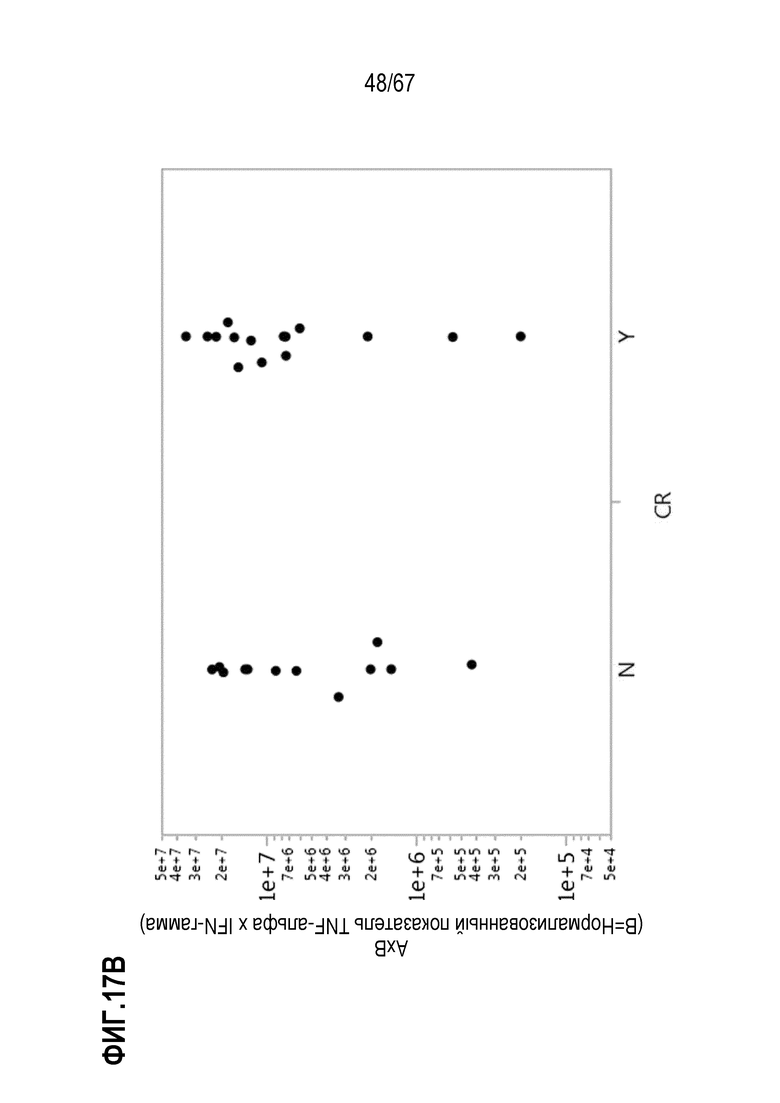
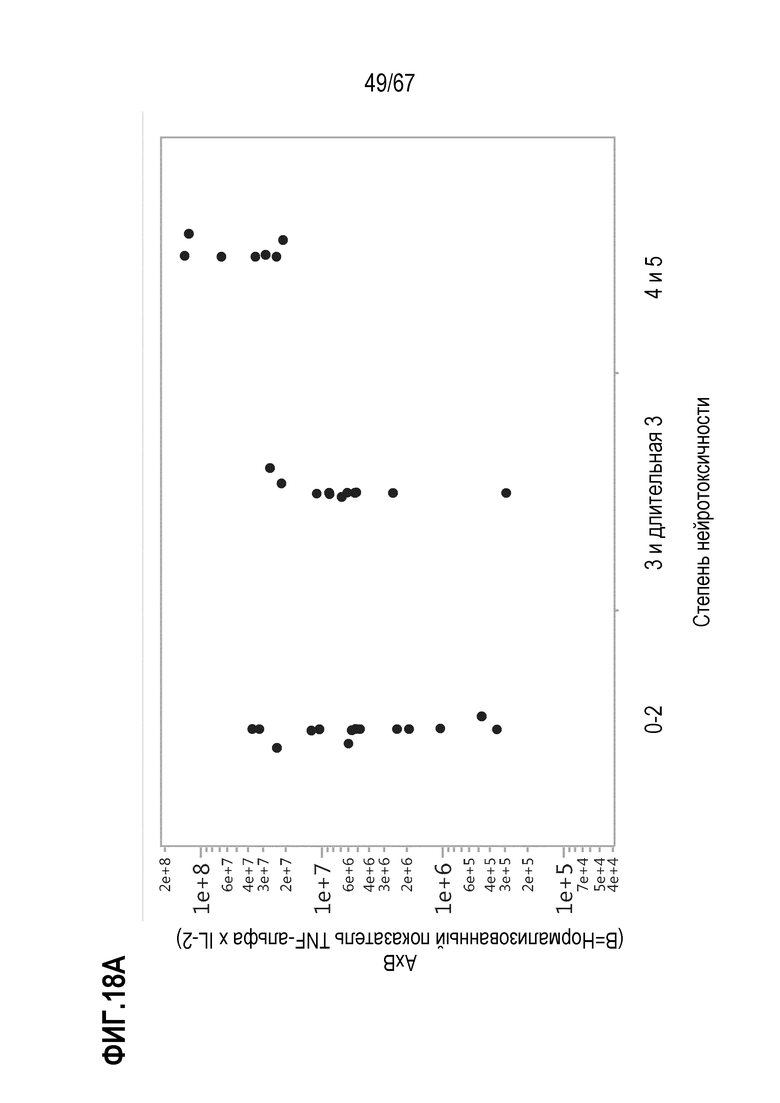
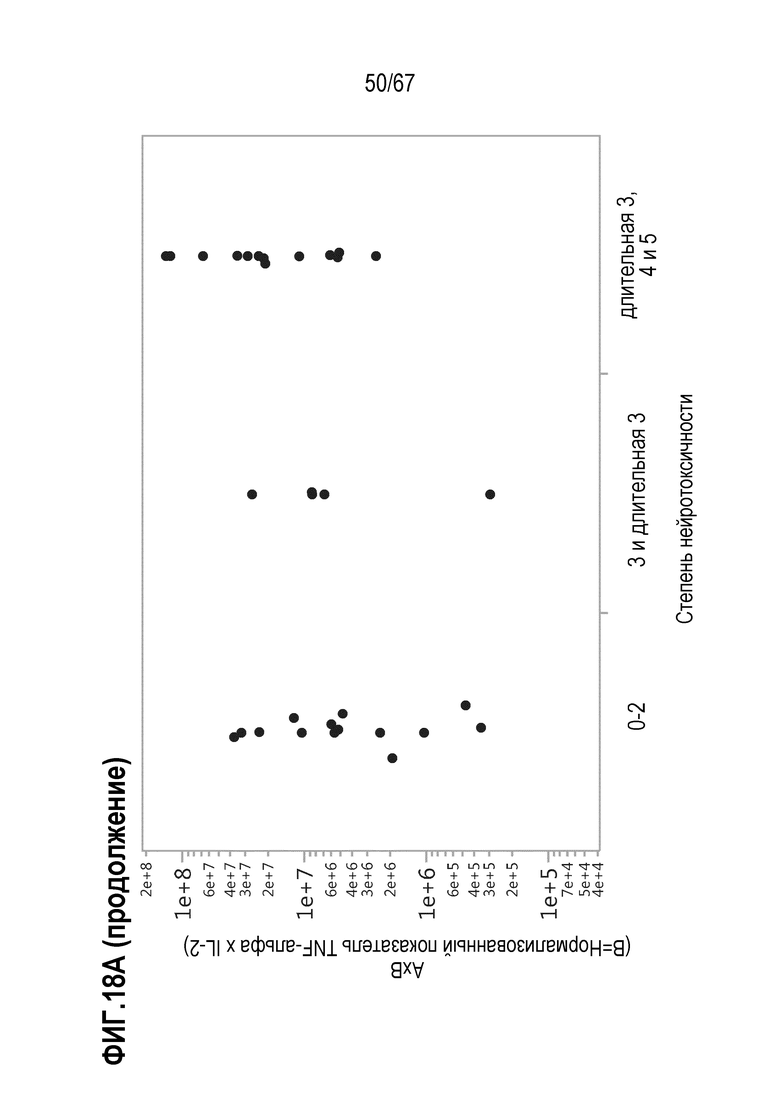
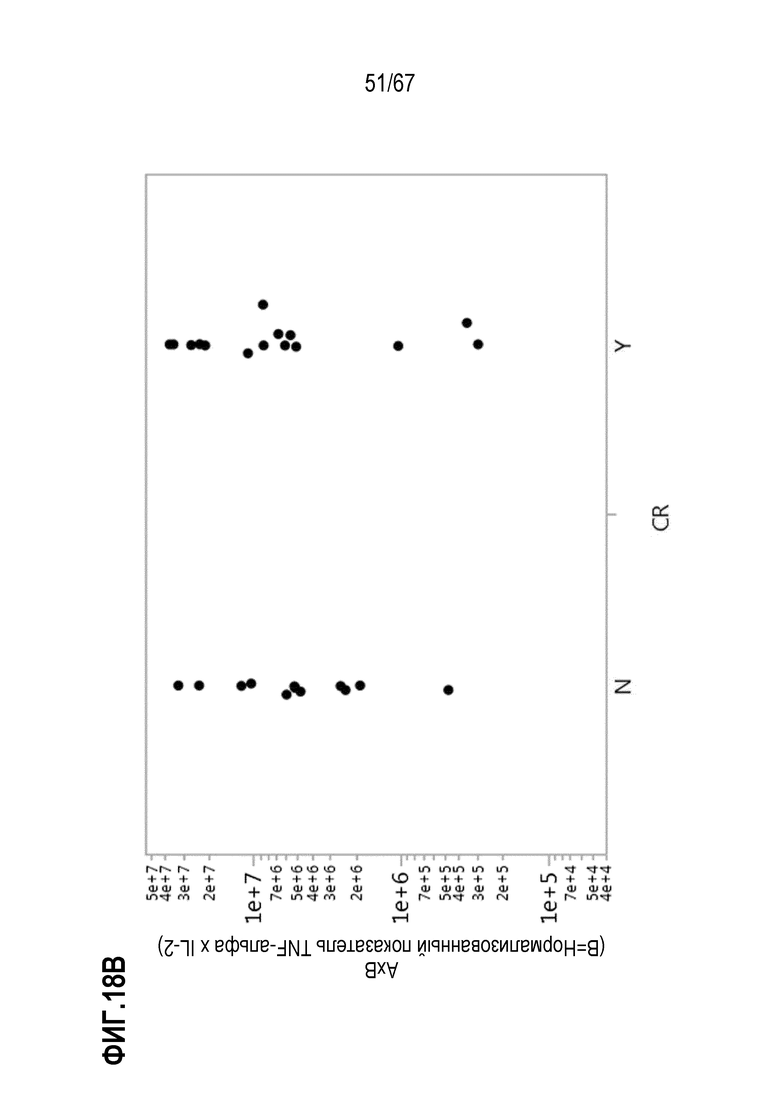
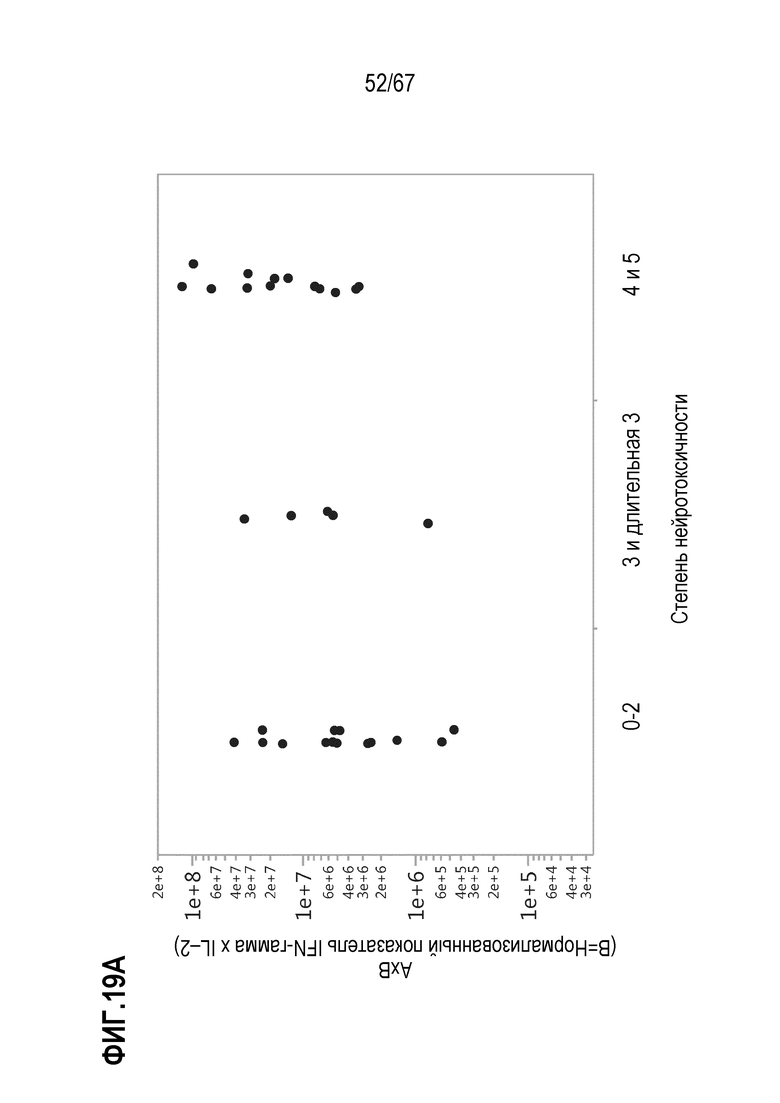



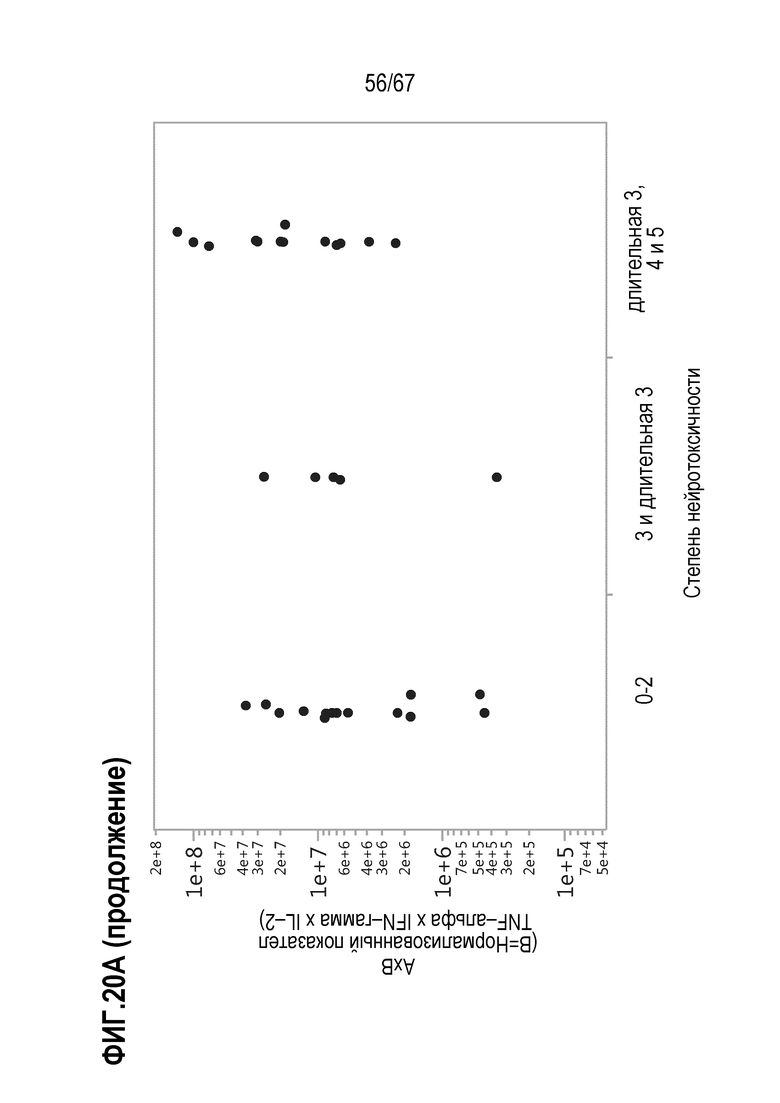

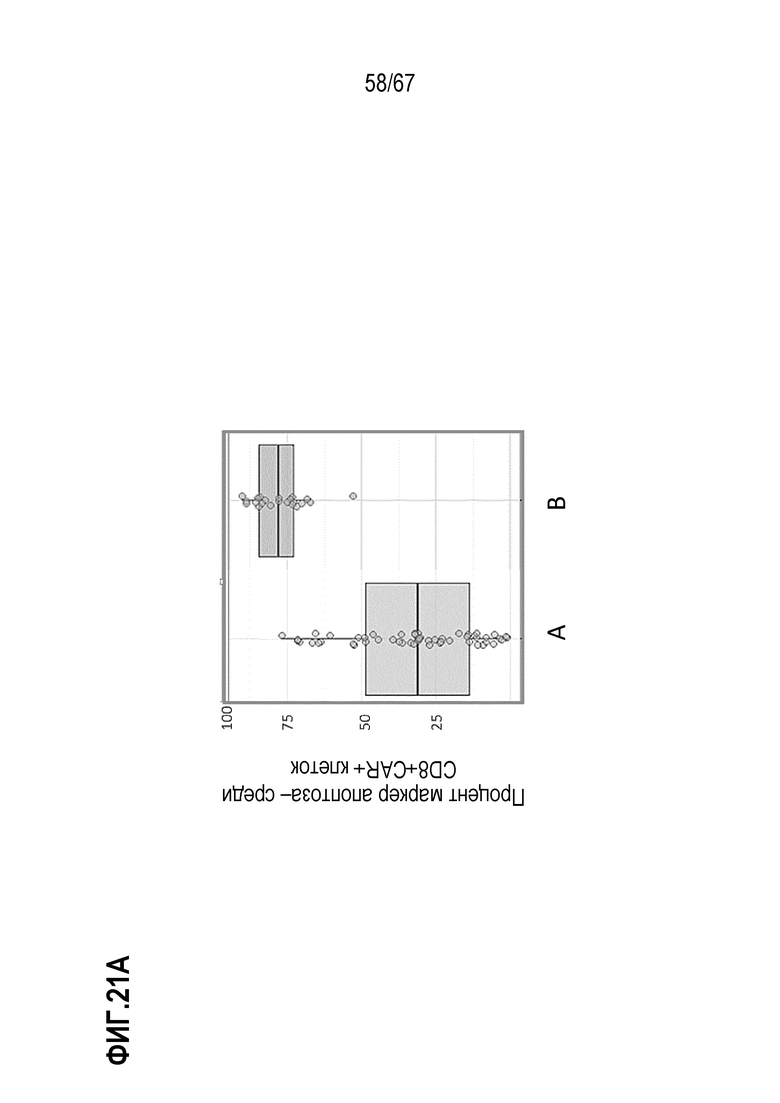





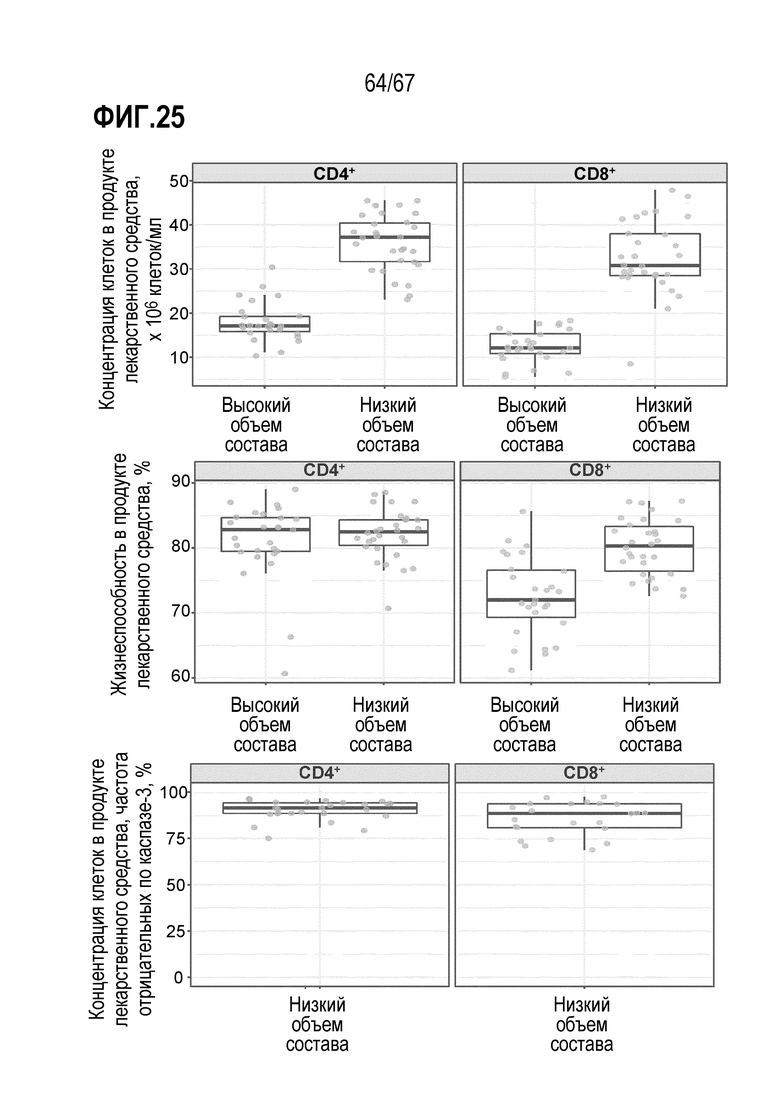


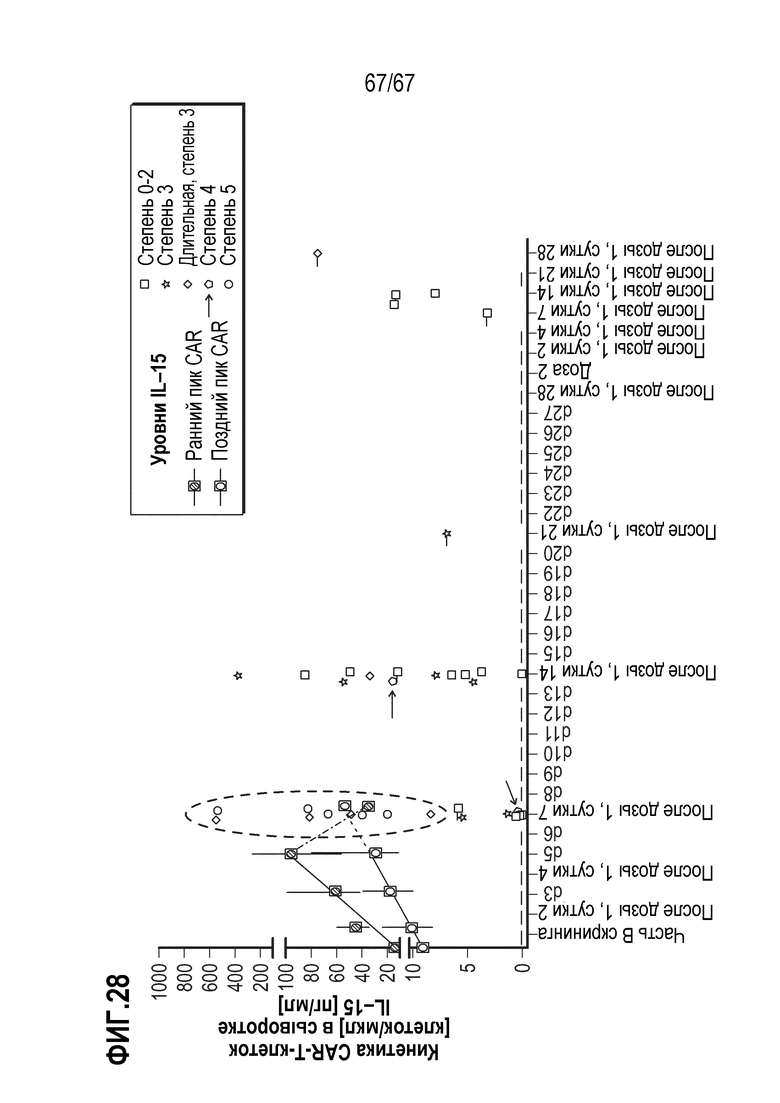
Изобретение относится к области биотехнологии. Предложены варианты способа определения риска развития токсичности у индивида, включающие анализ количества экспрессирующих рекомбинантный рецептор клеток в образце крови индивида, которому ранее вводили дозу экспрессирующих рекомбинантный рецептор клеток. У индивида имеется риск развития токсичности, если не более чем через четверо суток после начала введения количество указанных клеток в образце крови составляет по меньшей мере около 2 клеток на микролитр. Также у индивида имеется риск развития токсичности, если не более чем через пять или шесть суток после начала введения количество указанных клеток в образце крови составляет по меньшей мере около 5 или 10 клеток на микролитр. Также у индивида имеется риск развития токсичности, если не более чем через семь суток после начала введения количество указанных клеток в образце крови составляет по меньшей мере около 15 клеток на микролитр. Изобретение обеспечивает возможность уменьшения риска токсичности способов Т-клеточной терапии с сохранением эффективности введенных клеток у индивида. 2 н. и 22 з.п. ф-лы, 62 ил., 18 табл., 9 пр.
1. Способ определения риска развития токсичности у индивида, включающий анализ количества экспрессирующих рекомбинантный рецептор клеток в образце крови индивида,
где указанному индивиду ранее вводили дозу экспрессирующих рекомбинантный рецептор клеток,
где у индивида имеется риск развития токсичности, если:
(i) не более чем через четверо суток после начала введения количество экспрессирующих рекомбинантный рецептор клеток в образце крови индивида составляет по меньшей мере около 2 экспрессирующих рекомбинантный рецептор клеток на микролитр;
(ii) не более чем через пять или шесть суток после начала введения количество экспрессирующих рекомбинантный рецептор клеток в образце крови индивида составляет по меньшей мере около 5 экспрессирующих рекомбинантный рецептор клеток на микролитр или составляет по меньшей мере 10 экспрессирующих рекомбинантный рецептор клеток на микролитр; или
(iii) не более чем через семь суток после начала введения количество экспрессирующих рекомбинантный рецептор клеток в образце крови индивида составляет по меньшей мере около 15 экспрессирующих рекомбинантный рецептор клеток на микролитр.
2. Способ по п.1, где индивиду ранее вводили дозу экспрессирующих рекомбинантный рецептор клеток в связи с осуществлением способа лечения заболевания или состояния.
3. Способ определения риска развития токсичности у индивида, включающий:
(a) введение индивиду, страдающему заболеванием или состоянием, дозы экспрессирующих рекомбинантный рецептор клеток; и
(b) после введения клеток проведение анализа количества экспрессирующих рекомбинантный рецептор клеток в образце крови индивида,
где у индивида имеется риск развития токсичности, если:
(i) не более чем через четверо суток после начала введения количество экспрессирующих рекомбинантный рецептор клеток в образце крови индивида составляет по меньшей мере около 2 экспрессирующих рекомбинантный рецептор клеток на микролитр;
(ii) не более чем через пять или шесть суток после начала введения количество экспрессирующих рекомбинантный рецептор клеток в образце крови индивида составляет по меньшей мере около 5 экспрессирующих рекомбинантный рецептор клеток на микролитр или составляет по меньшей мере около 10 экспрессирующих рекомбинантный рецептор клеток на микролитр; или
(iii) не более чем через семь суток после начала введения количество экспрессирующих рекомбинантный рецептор клеток в образце крови индивида составляет по меньшей мере около 15 экспрессирующих рекомбинантный рецептор клеток на микролитр.
4. Способ по любому из пп.1-3, где проведение анализа включает применение способа детекции на основе нуклеиновой кислоты или проточной цитометрии.
5. Способ по любому из пп.1-4, где анализ включает применение способа детекции на основе количественной полимеразной цепной реакции (qПЦР).
6. Способ по любому из пп.1-5, где у индивида есть риск развития токсичности, если, кроме того, уровень, количество или концентрация интерлейкина–15 (IL–15), детектированные в образце крови или сыворотке индивида, составляет или превышает 30 пг/мл.
7. Способ по п.6, где образец взят у индивида не более чем через около 1 суток, 2 суток, 3 суток, 4 суток или 5 суток после начала введения дозы экспрессирующих рекомбинантный рецептор клеток.
8. Способ по любому из пп.1–7, где токсичность представляет собой нейротоксичность в степени, равной или выше степени 4 или степени 5, или по меньшей мере длительную нейротоксичность в степени 3.
9. Способ по любому из пп.1-7, где токсичность вызвана или связана с отеком мозга.
10. Способ по любому из пп.1-9, где рекомбинантный рецептор представляет собой химерный антигенный рецептор (CAR).
11. Способ по любому из пп.2-10, где заболевание или состояние представляет собой злокачественную опухоль.
12. Способ по любому из пп.2-11, где заболевание или состояние представляет собой миелому, лимфому или лейкоз.
13. Способ по любому из пп.2-12, где заболевание или состояние представляет собой В-клеточную злокачественную опухоль.
14. Способ по п.13, где В-клеточная злокачественная опухоль выбрана из группы, состоящей из острого лимфобластного лейкоза (ALL), ALL взрослых, хронического лимфобластного лейкоза (CLL), неходжскинской лимфомы (NHL) и диффузной крупноклеточной B–клеточной лимфомы (DLBCL).
15. Способ по любому из пп.1-14, где рекомбинантный рецептор нацелен на антиген, связанный с В-клеточной злокачественной опухолью.
16. Способ по любому из пп.1-15, где рекомбинантный рецептор нацелен на антиген, который представляет собой или включает CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig каппа, Ig лямбда, CD79a, CD79b или CD30.
17. Способ по любому из пп.1-16, где, если определено, что у индивида имеется риск возникновения токсичности, способ дополнительно включает прекращение введения экспрессирующих рекомбинантный рецептор клеток, введение индивиду более низкой дозы экспрессирующих рекомбинантный рецептор клеток, введение индивиду клеток, экспрессирующих другой рекомбинантный рецептор, и/или введение индивиду средства, способного лечить, предотвращать, замедлять или ослаблять развитие токсичности.
18. Способ по п.17, где средство представляет собой стероид, антагонист или ингибитор рецептора цитокина или ингибитор цитокина.
19. Способ по п.18, где рецептор цитокина представляет собой рецептор IL-6, рецептор CD122 (рецептор IL-2Rбета) или CCR2.
20. Способ по п.18 или 19, где цитокин представляет собой IL-6, СР-1, IL-10, IFN-γ, IL-8 или IL-18.
21. Способ по п.18, где стероид представляет собой кортикостероид.
22. Способ по п.21, где кортикостероид представляет собой глюкокортикоид.
23. Способ по п.22, где глюкокортикоид представляет собой дексаметазон.
24. Способ по любому из пп.17-20, где средство представляет собой тоцилизумаб, силтуксимаб, сарилумаб, олокизумаб (CDP6038), элсилимомаб, ALD518/BMS-945429, сирукумаб (CNTO 136), CPSI-2634, ARGX-109, FE301 или FM101.
| WO 2016064929 A1, 28.04.2016 | |||
| KLAVER YARNE et al | |||
| Adoptive T-cell therapy: a need for standard immune monitoring, IMMUNOTHERAPY, 2015,Vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| BRUDNO J.N., KOCHENDERFER J.N | |||
| Toxicities of chimeric antigen receptor T cells: recognition and management, BLOOD, 2016, Vol.127, No.26, pp.3321-3330 | |||
| МОРОЗОВА О.Л | |||
| и др | |||
| Перспективы | |||
Авторы
Даты
2022-07-27—Публикация
2018-02-27—Подача