Перекрестная ссылка на родственные заявки
[0001] По этой заявке испрашивается приоритет временной заявки на патент США No. 62/514,774, поданной 2 июня 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/515,530, поданной 5 июня 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/521,366, поданной 16 июня 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/527,000, поданной 29 июня 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/549,938, поданной 24 августа 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/580,425, поданной 1 ноября 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/593,871, поданной 1 декабря 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/596,764, поданной 8 декабря 2017, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, временной заявки на патент США No. 62/614,957, поданной 8 января 2018, озаглавленной “ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ”, содержание которых полностью включено посредством ссылок.
Включение списка последовательностей путем ссылки
[0002] Настоящая заявка подается вместе со Списком последовательностей в электронном формате. Список последовательностей представлен как файл, названный 735042012140SeqList.txt, созданный 1 июня 2018, который составляет в размере 35306 байтов. Информация в электронном формате Списка последовательностей полностью включена посредством ссылок.
Область, к которой относится изобретение
[0003] Настоящее раскрытие относится в некоторых аспектах к адоптивной клеточной терапии, включающей введение доз клеток для лечения пациентов с заболеванием и состояниями, такими как некоторые В-клеточные злокачественные опухоли, и к связанным способам, композициям, применениям и изделиям. Клетки обычно экспрессируют рекомбинантные рецепторы, такие как химерные антигенные рецепторы (CAR). В некоторых вариантах осуществления, заболевание или состояние представляет собой неходжкинскую лимфому (NHL), такую как рецидивирующая или рефрактерная NHL или специфический подтип NHL; в некоторых вариантах осуществления пациент относится к специфической группе или субпопуляции пациентов NHL, таких как пациенты, подвергавшиеся предварительной интенсивной терапии, или пациенты с неблагоприятным прогнозом.
Уровень техники
[0004] Различные способы иммунотерапия и/или клеточной терапии доступны для лечения заболеваний и состояний. Например, адоптивные клеточные терапии (включая те, которые включают введение клеток, экспрессирующих химерные рецепторы, специфичные для заболевания или нарушения, представляющего интерес, такие как химерные антигенные рецепторы (CAR) и/или другие рекомбинантные антигенные рецепторы, а также другие адоптивные иммунотерапии и адоптивные Т-клеточные терапии), могут быть использованы в лечении рака или других заболеваний или нарушений. Необходимы улучшенные подходы. Изобретение относится к способам и применениям, удовлетворяющим таким потребностям.
Сущность изобретения
[0005] Изобретение относится к способам, применениям, композициям, составам и изделиям для лечения пациентов, имеющих или подозреваемых в наличии заболевания или состояния, такого как рак или опухоль, необязательно В-клеточная злокачественная опухоль, такая как NHL или ALL, или CLL или их подтип. Способы и другие варианты осуществления обычно относятся к введению пациенту Т-клеткок, обычно генно-инженерных Т-клеткок, таких как клетки, которые экспрессируют или которые содержат рекомбинантный рецептор, такой как химерный антигенный рецептор (CAR) или TCR.
[0006] В некоторых вариантах осуществления доза клеток или клетки, введенные в связи с любыми вариантами осуществления способов, композиций, изделий и применений по изобретению, содержит CD4+ Т-клетки или их подтип или фенотип (такой как генно-инженерные или рекомбинантные экспрессирующие рецептор CD4+ Т-клетки) и/или CD8+ Т-клетки или их подтип (такой как генно-инженерные или рекомбинантные экспрессирующие рецептор CD4+ клетки). В некоторых вариантах осуществления, CD8+ клетки или подтип или фенотип присутствуют в определенной дозе или количестве или числе; в некоторых вариантах осуществления CD4+ клетки или их подтип или фенотип присутствуют в определенной дозе или количестве, или числе. В некоторых вариантах осуществления, CD8+ клетки или их подтип или фенотип этого и CD4+ клетки или подтип или фенотип присутствуют в изделии или композиции, или комбинации, или используются в способах, в определенном отношении, таком как, или приблизительно, 1:1, или от или от приблизительно 1:3 и до или до приблизительно 3:1. В некоторых вариантах осуществления, доза или введение содержит или состоит из определенного количества или числа одной популяции клеток, и отношение является определенным отношением или является естественным отношением, таким как отношение в крови пациента, от которого клетки получены, или отношение, имеющее место без выбора или контроля определенного отношения.
[0007] В некоторых вариантах осуществления, CD4+ Т-клетки (или их субпопуляция) и CD8+ Т-клетки (или их субпопуляция) индивидуально содержат рецептор, специфично связывающийся с антигеном-мишенью, экспрессируемым заболеванием или состоянием, или клеткой или тканью, и/или который ассоциирован с этим заболеванием или состоянием.
[0008] В некоторых вариантах осуществления, CD4+ и CD8+ клетки вводят и/или составляют вместе, например, в единственном составе и/или из единственного контейнера.
[0009] В некоторых вариантах осуществления отдельные введения несут CD4+ и CD8+ клетки в дозе, и/или включены отдельные составы или контейнеры, каждый из которых индивидуально обогащен CD4+ клетками или CD4+ генно-инженерными клетками (такой как состав, содержащий по меньшей мере определенный процент, например, по меньшей мере 80%, 85%, 90% или 95% или более CD4+ клеток и/или не включающий более чем 10% или более чем 5% CD8+ Т-клеток) и CD8+ клетками или CD8+ генно-инженерными клетками (такой как состав, содержащий по меньшей мере определенный процент, например, по меньшей мере 80%, 85%, 90% или 95% или более CD8+ клеток и/или не включающий более чем 10% или более чем 5% CD4+ Т-клеток).
[0010] В некоторых аспектах введение включает введение множества отдельных композиций, причем указанное множество отдельных композиций включает первую композицию, включающую что-либо одно из CD4+ Т-клеток и CD8+ Т-клеток, и вторую композицию, включающая другое из CD4+ Т-клеток и CD8+ Т-клеток. В некоторых вариантах осуществления любого из способов по изобретению рецептор, содержащийся в CD4+ Т-клетках, и/или рецептор, содержащийся в CD8+ Т-клетках, включает Т-клеточный рекомбинантный рецептор, и/или причем CD4+ Т-клетки и/или CD8+ Т-клетки генетически сконструированы для экспрессии этого рецептора.
[0011] В некоторых вариантах осуществления любого из вариантов осуществления изобретения, введение первой композиции и введение второй композиции осуществляют в тот же день, осуществляют с интервалом от приблизительно 0 и до приблизительно 12 часов, с интервалом от приблизительно 0 и до приблизительно 6 часов или с интервалом от приблизительно 0 и до 2 часов; и/или инициацию введения первой композиции и инициацию введения второй композиции осуществляют с интервалом от приблизительно 1 минуты и до приблизительно 1 часа или с интервалом от 5 минут и до приблизительно 30 минут. В некоторых вариантах осуществления любого из способов по изобретению первую композицию и вторую композицию вводят с интервалом от не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут.
[0012] В некоторых вариантах осуществления любого из вариантов осуществления изобретения первая композиция включает CD4+ Т-клетки. В некоторых вариантах осуществления любого из способов по изобретению первая композиция включает CD8+ Т-клетки. В некоторых вариантах осуществления любого из способов по изобретению инициацию введения первой композиции осуществляют до инициации введения второй композиции. В некоторых вариантах осуществления любого из способов по изобретению доза клеток включает определенное отношение CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет или приблизительно составляет 1:1 или от приблизительно 1:3 до приблизительно 3:1; и/или CD4+ Т-клетки, включающие рецептор в одной из первой и второй композиций, и CD8+ Т-клетки, включающие рецептор в другой из первой и второй композиций, присутствуют в определенном отношении, причем это отношение необязательно составляет или приблизительно составляет 1:1 или от приблизительно 1:3 до приблизительно 3:1; и/или CD4+ Т-клетки, включающие рецептор, и CD8+ Т-клетки, включающие рецептор, вводимые в первой и второй композициях, присутствуют в определенном отношении, причем это отношение необязательно составляет или приблизительно составляет 1:1 или от приблизительно 1:3 до приблизительно 3:1. В некоторых вариантах осуществления любого из способов по изобретению определенное отношение составляет или приблизительно составляет 1:1. В некоторых вариантах осуществления любого из способов по изобретению дозу Т-клеток вводят пациенту в виде единственной дозы или вводят только один раз за период двух недель, одного месяца, трех месяцев, шести месяцев, 1 года или более. В некоторых вариантах осуществления любого из способов по изобретению дозу Т-клеток вводят в виде двойной дозы, включающей первую дозу Т-клеток и последующую дозу Т-клеток, причем одна или обе из первой дозы и второй дозы включает введение множества композиций Т-клеток. В некоторых вариантах осуществления любого из способов по изобретению последующую дозу вводят в момент времени по меньшей мере или более чем приблизительно 7 дней или 14 дней после и менее чем приблизительно 28 дней после инициации введения первой дозы клеток.
[0013] В некоторых вариантах осуществления любого из способов по изобретению или вариантов осуществления, доза клеток включает от или от приблизительно 1 x 105 и до или до приблизительно 5 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 1 x 105 и до или до приблизительно 1 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 5 x 105 и до или до приблизительно 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, или от или от приблизительно 1 x 106 до 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, включительно. В некоторых вариантах осуществления любого из способов по изобретению доза Т-клеток включает введение не более чем 1 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1 x 106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5 x 106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток. В некоторых вариантах осуществления любого из способов по изобретению доза Т-клеток включает от или от приблизительно 5 x 107 экспрессирующих рекомбинантный рецептор Т-клеток до 1 x 108 экспрессирующих рекомбинантный рецептор Т-клеток, включительно.
[0014] В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор специфически связывается с антигеном, ассоциированным с заболеванием или состоянием, или экспрессируемым в клетках среды поражения, связанной с заболеванием или состоянием. В некоторых вариантах осуществления любого из способов по изобретению, заболевание или состояние представляет собой рак. В некоторых вариантах осуществления любого из способов по изобретению, заболевание или состояние представляет собой миелому, лейкоз или лимфому. В некоторых вариантах осуществления любого из способов по изобретению антиген представляет собой ROR1, антиген созревания В-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторная тирозинкиназа erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолта-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор области вставки киназы (kdr), легкую каппа-цепь, антиген Ley, молекулу L1-клеточной адгезии, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, альфа-рецептор 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D), или патоген-специфичный антиген. В некоторых вариантах осуществления любого из способов по изобретению антиген представляет собой CD19.
[0015] В некоторых вариантах осуществления любого из способов по изобретению, заболевание или состояние представляет собой В-клеточную злокачественную опухоль и/или острый лимфообластный лейкоз (ALL), ALL взрослых, хронический лимфообластный лейкоз (CLL), неходжкинскую лимфому (NHL) и диффузную крупноклеточную В-клеточную лимфому (DLBCL). В некоторых вариантах осуществления любого из способов по изобретению, заболевание или состояние представляет собой NHL, и NHL выбрана из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (неуточненной) (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), Т-клеточной/гистоцитарной крупноклеточной В-клеточной лимфомы (TCHRBCL), лимфомы Беркитта, мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B).
[0016] В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор включает внеклеточный домен, содержащый антигенсвязывающий домен. В некоторых вариантах осуществления антигенсвязывающий домен представляет собой или включает антитело или фрагмент антитела, который необязательно является фрагментом одиночной цепи. В некоторых вариантах осуществления любого из способов по изобретению фрагмент включает вариабельные участки антитела, к которым присоединен гибкий линкер. В некоторых вариантах осуществления фрагмент включает scFv. В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор также включает спейсер и/или шарнирную область.
[0017] В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор включает внутриклеточную сигнальную область. В некоторых вариантах осуществления любого из способов по изобретению внутриклеточная сигнальная область включает внутриклеточный сигнальный домен. В некоторых вариантах осуществления любого из способов по изобретению внутриклеточный сигнальный домен представляет собой или включает первичный сигнальный домен, сигнальный домен, который способен индуцировать сигнал первичной активации в Т-клетке, сигнальный домен компонента Т-клеточного рецептора (TCR) и/или сигнальный домен, содержащей иммунорецепторный тирозиновый активирующий мотив (ITAM). В некоторых вариантах осуществления внутриклеточный сигнальный домен представляет собой или включает внутриклеточный сигнальный домен цепи CD3, необязательно CD3-дзэта (CD3ζ) цепи, или его сигнальную часть.
[0018] В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор также включает трансмембранный домен, расположенный между внеклеточным доменом и внутриклеточной сигнальной областью.
[0019] В некоторых вариантах осуществления любого из способов по изобретению внутриклеточный сигнальный домен также включает костимулирующий сигнальный домен. В некоторых вариантах осуществления костимулирующая сигнальная область включает внутриклеточный сигнальный домен костимулирующей Т-клетки молекулы или его сигнальную часть. В некоторых вариантах осуществления любого из способов по изобретению костимулирующая сигнальная область включает внутриклеточный сигнальный домен CD28, 4-1BB или ICOS или его сигнальную часть. В некоторых вариантах осуществления костимулирующая сигнальная область расположена между трансмембранным доменом и внутриклеточной сигнальной областью.
[0020] В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор является химерным антигенным рецептором (CAR), причем необязательно рекомбинантный рецептор является химерным антигенным рецептором (CAR), причем необязательно CAR включает внеклеточный антигенраспознающий домен, специфически связывающийся с антигеном, и внутриклеточный сигнальный домен, включающий ITAM, причем необязательно внутриклеточный сигнальный домен включает внутриклеточный домен CD3-дзэта (CD3ζ) цепи; и/или причем CAR дополнительно включает костимулирующий сигнальный домен, необязательно включающую сигнальный домен CD28 или 4-1BB.
[0021] В некоторых вариантах осуществления изделия включают контейнер, такой как флакон, включающий композицию, включающую CD4+ Т-клетки, экспрессирующие рекомбинантный рецептор, и инструкции по введению пациенту, имеющему заболевание или состояние, композиции CD4+ Т-клеток в виде множества композиций с композицией, включающей CD8+ Т-клетки, экспрессирующие рекомбинантный рецептор, или разовую дозу клеток, включающих все или часть множества CD4+ Т-клеток, и композицией, включающей CD8+ Т-клетки, экспрессирующие рекомбинантный рецептор. В некоторых вариантах осуществления изделие включает контейнер, такой как флакон, включающий композицию, включающую CD8+ Т-клетки, экспрессирующие рекомбинантный рецептор, и инструкции по введению пациенту, имеющему заболевание или состояние, композиции CD8+ Т-клеток в виде множества композиций с композицией, включающей CD4+ Т-клетки, экспрессирующие рекомбинантный рецептор, или разовую дозу клеток, включающих все или часть множества CD4+ Т-клеток, и композицией, включающей CD8+ Т-клетки, экспрессирующие рекомбинантный рецептор.
[0022] В некоторых из вариантов осуществления CAR включает, в указанном порядке, CAR включает scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, которая необязательно представляет собой или включает 4-1BB, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, которая необязательно представляет собой или включает CD3дзета сигнальный домен и необязательно дополнительно включает спейсер между трансмембранным доменом и scFv;
[0023] В некоторых из вариантов осуществления CAR включает, в указанном порядке, scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, которая необязательно представляет собой или включает 4-1BB сигнальный домен, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, которая необязательно представляет собой CD3дзета сигнальный домен.
[0024] В некоторых из вариантов осуществления CAR включает, или состоит из них, в указанном порядке, scFv, специфичный для антигена, спейсер, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, которая необязательно представляет собой 4-1BB сигнальный домен, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, которая необязательно представляет собой или включает CD3дзета сигнальный домен.
[0025] В некоторых аспектах спейсер является полипептидным спейсером, который (a) включает или состоит из всего или части шарнирного участка иммуноглобулина или его модифицированной версии или включает приблизительно 15 аминокислот или менее и не включает внеклеточную область CD28 или внеклеточную область CD8, (b) включает или состоит из всего или части шарнирного участка иммуноглобулина, необязательно стержня IgG4 или его модифицированной версии, и/или включает приблизительно 15 аминокислот или менее и не включает внеклеточную область CD28 или внеклеточную область CD8, или (c) имеет длину 12 или приблизительно 12 аминокислот и/или включает или состоит из всего или части шарнирного участка иммуноглобулина, необязательно IgG4 или его модифицированной версии; или (d) имеет или состоит из последовательности SEQ ID NO: 1, последовательности, кодируемая SEQ ID NO: 2, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34 или вариантом любой из вышеназванных, имеющим по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с указанной, или (e) включает или состоит из формулы X1PPX2P, где X1 является глицином, цистеином или аргинином, и X2 является цистеином или треонином; и/или костимулирующая область включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней; и/или первичный сигнальный домен включает SEQ ID NO: 13 или 14, или 15, или их вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними; и/или scFv включает последовательность CDRL1 RASQDISKYLN (SEQ ID NO: 35), последовательность CDRL2 SRLHSGV (SEQ ID NO: 36) и/или последовательность CDRL3 GNTLPYTFG (SEQ ID NO: 37), и/или последовательность CDRH1 DYGVS (SEQ ID NO: 38), последовательность CDRH2 VIWGSETTYYNSALKS (SEQ ID NO: 39) и/или последовательность CDRH3 YAMDYWG (SEQ ID NO: 40), или причем scFv включает вариабельную область тяжелой цепи FMC63 и вариабельную область легкой цепи FMC63 и/или последовательность CDRL1 FMC63, последовательность CDRL2 FMC63, последовательность CDRL3 FMC63, последовательность CDRH1 FMC63, последовательность CDRH2 FMC63 и последовательность CDRH3 FMC63, или связывается с тем же эпитопом или конкурирует за связывание с любым из указанных, и причем необязательно scFv включает, в указанном порядке, VH, линкер, необязательно включающий SEQ ID NO: 24, и VL и/или scFv включает гибкий линкер и/или включает последовательность аминокислот, представленную как SEQ ID NO: 24.
[0026] В некоторых вариантах осуществления спейсер включает или состоит из SEQ ID NO: 1, костимулирующая область включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, трансмембранный домен имеет CD28 или включает SEQ ID NO: 9 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, scFv содержит связывающий домен или CDR, или VH и VL FMC63, первичный сигнальный домен содержит SEQ ID NO: 13, 14 или 15 и/или их вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними.
[0027] В некоторых вариантах осуществления спейсер включает или состоит из SEQ ID NO: 30, костимулирующая область включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, трансмембранный домен имеет CD28 или включает SEQ ID NO: 9 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, scFv содержит связывающий домен или CDR, или VH и VL FMC63, первичный сигнальный домен содержит SEQ ID NO: 13, 14 или 15 и/или их вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними.
[0028] В некоторых вариантах осуществления спейсер включает или состоит из SEQ ID NO: 31, костимулирующая область включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, трансмембранный домен имеет CD28 или включает SEQ ID NO: 9 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, scFv содержит связывающий домен или CDR, или VH и VL FMC63, первичный сигнальный домен содержит SEQ ID NO: 13, 14 или 15 и/или их вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними.
[0029] В некоторых вариантах осуществления спейсер включает или состоит из SEQ ID NO: 33, костимулирующая область включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, трансмембранный домен имеет CD28 или включает SEQ ID NO: 9 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, scFv содержит связывающий домен или CDR, или VH и VL FMC63, первичный сигнальный домен содержит SEQ ID NO: 13, 14 или 15 и/или их вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними.
[0030] В некоторых вариантах осуществления спейсер включает или состоит из SEQ ID NO: 34, костимулирующая область включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, трансмембранный домен имеет CD28 или включает SEQ ID NO: 9 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, scFv содержит связывающий домен или CDR, или VH и VL FMC63, первичный сигнальный домен содержит SEQ ID NO: 13, 14 или 15 и/или их вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ними.
[0031] В некоторых вариантах осуществления любого из изделий по изобретению рекомбинантный рецептор, экспрессируемый CD4+ клетками, и рекомбинантный рецептор, экспрессируемый CD8+ Т-клетками, являются одинаковыми или разными. В некоторых вариантах осуществления любого из изделий по изобретению флакон включает более чем или более чем приблизительно 10 x 106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток, более чем или более чем приблизительно 15 x 106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток, более чем или более чем приблизительно 25 x 106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток.
[0032] В некоторых вариантах осуществления любого из изделий по изобретению флакон включает от приблизительно 10 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 25 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 15 миллионов клеток на мл, от 15 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 15 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл, от приблизительно 15 миллионов клеток на мл до приблизительно 25 миллионов клеток на мл, от приблизительно 25 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 25 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл и от приблизительно 50 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл. В некоторых вариантах осуществления любого из изделий по изобретению композиция дополнительно включает криопротектор, и/или изделие дополнительно включает инструкции для оттаиванию композиции до введения пациенту.
[0033] В некоторых вариантах осуществления любого из изделий по изобретению композиция или множество композиций включает дозу клеток, включающую от или от приблизительно 2 x 107 до приблизительно 4 x 107 CD8+ клеток, например, приблизительно 2 x 107, 2,5 x 107, 3 x 107, 3,5 x 107 или 4 x 107 CD8+ клеток, и от или от приблизительно 2 x 107 до приблизительно 4 x 107 CD4+ клеток, например, приблизительно 2 x 107, 2,5 x 107, 3 x 107, 3,5 x 107 или 4 x 107 CD4+ клеток, включительно. В некоторых вариантах осуществления композиция или множество композиций включает дозу клеток, включающую приблизительно 3 x 107 CD8+ клеток и 3,5 x 107 CD4+ клеток.
[0034] В некоторых вариантах осуществления любого из изделий по изобретению множество композиций клеток включает определенное отношение CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет приблизительно 1:1 или от приблизительно 1:3 до приблизительно 3:1. В некоторых вариантах осуществления любого из изделий по изобретению определенное отношение составляет или приблизительно составляет 1:1. В некоторых вариантах осуществления любого из изделий по изобретению множество композиций, коллективно, включает дозу клеток, включающую от или от приблизительно 1 x 105 до 5 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от 1 x 105 до 1 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 5 x 105 до 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток или от или от приблизительно 1 x 106 до 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, включительно. В некоторых вариантах осуществления любого из изделий по изобретению множество композиций, коллективно, включает дозу клеток, включающую не более чем 1 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1 x 106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5 x 106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток. В некоторых вариантах осуществления любого из изделий по изобретению множество композиций, коллективно, включает дозу клеток, включающую от или от приблизительно 5 x 107 экспрессирующих рекомбинантный рецептор Т-клеток и 1 x 108 экспрессирующих рекомбинантный рецептор Т-клеток, включительно.
[0035] В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD4+ Т-клетки, и композиции, включающей CD8+ Т-клетки с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часов. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD4+ Т-клетки, и композиции, включающей CD8+ Т-клетки с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD4+ Т-клетки, до введения композиции, включающей CD8+ клетки. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD8+ Т-клетки, до введения композиции, включающей CD4+ клетки.
[0036] В некоторых вариантах осуществления любого из изделий по изобретению рекомбинантный рецептор специфично связывается с антигеном, ассоциированным с заболеванием или состоянием, или экспрессируемым в клетках среды поражения, ассоциированного с заболеванием или состоянием. В некоторых вариантах осуществления любого из изделий по изобретению, заболевание или состояние представляет собой рак. В некоторых вариантах осуществления любого из изделий по изобретению, заболевание или состояние представляет собой миелому, лейкоз или лимфому.
[0037] В некоторых вариантах осуществления любого из изделий по изобретению антиген представляет собой ROR1, антиген созревания В-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторная тирозинкиназа erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолта-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор области вставки киназы (kdr), легкую каппа-цепь, антиген Ley, молекулу L1-клеточной адгезии, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, альфа-рецептор 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D), или патоген-специфичный антиген. В некоторых вариантах осуществления любого из изделий по изобретению антиген представляет собой CD19.
[0038] В некоторых вариантах осуществления любого из изделий по изобретению заболевание или состояние представляет собой В-клеточную злокачественную опухоль и/или острый лимфообластный лейкоз (ALL), ALL взрослых, хронический лимфообластный лейкоз (CLL), неходжкинскую лимфому (NHL) и диффузную крупноклеточную В-клеточную лимфому (DLBCL). В некоторых вариантах осуществления любого из способов по изобретению, заболевание или состояние представляет собой NHL, и NHL выбрана из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (неуточненной) (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), Т-клеточной/гистоцитарной крупноклеточной В-клеточной лимфомы (TCHRBCL), лимфомы Беркитта, мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B).
[0039] В некоторых вариантах осуществления любого из изделий по изобретению Т-клетки представляют собой первичные Т-клетки, полученные от пациента. В некоторых вариантах осуществления любого из изделий по изобретению Т-клетки являются аутологичными для пациента. В некоторых вариантах осуществления любого из изделий по изобретению Т-клетки являются аллогенными для пациента.
[0040] В некоторых вариантах осуществления любого из изделий по изобретению рекомбинантный рецептор представляет собой или включает функциональный не-TCR антигенный рецептор или TCR или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления рекомбинантный рецептор является химерным антигенным рецептором (CAR).
[0041] В некоторых вариантах осуществления любого из изделий по изобретению рекомбинантный рецептор включает внеклеточный домен, содержащий антигенсвязывающий домен. В некоторых вариантах осуществления антигенсвязывающий домен представляет собой или включает антитело или фрагмент антитела, который необязательно является фрагментом одиночной цепи. В некоторых вариантах осуществления фрагмент включает вариабельные участки антитела, к которым присоединен гибкий линкер. В некоторых вариантах осуществления фрагмент включает scFv.
[0042] В некоторых вариантах осуществления любого из изделий или способов по изобретению рекомбинантный рецептор также включает спейсер и/или шарнирную область.
[0043] В некоторых вариантах осуществления любого из изделий или способов по изобретению рекомбинантный рецептор включает внутриклеточную сигнальную область. В некоторых вариантах осуществления внутриклеточная сигнальная область включает внутриклеточный сигнальный домен. В некоторых вариантах осуществления любого из изделий по изобретению внутриклеточный сигнальный домен представляет собой или включает первичный сигнальный домен, сигнальный домен, который способен индуцировать сигнал первичной активации в Т-клетке, сигнальный домен компонента T-клеточного рецептора (TCR) и/или сигнальный домен, содержащий иммунорецепторный тирозиновый активирующий мотив (ITAM). В некоторых вариантах осуществления внутриклеточный сигнальный домен представляет собой или включает внутриклеточный сигнальный домен цепи CD3, необязательно CD3-дзэта (CD3ζ) цепи, или его сигнальную часть.
[0044] В некоторых вариантах осуществления любого из изделий или способов по изобретению рекомбинантный рецептор также включает трансмембранный домен, расположенный между внеклеточным доменом и внутриклеточной сигнальной областью.
[0045] В некоторых вариантах осуществления любого из изделий или способов по изобретению внутриклеточный сигнальный домен также включает костимулирующий сигнальный домен. В некоторых вариантах осуществления костимулирующая сигнальная область включает внутриклеточный сигнальный домен костимулирующей Т-клетки молекулы или его сигнальную часть. В некоторых вариантах осуществления любого из изделий по изобретению костимулирующая сигнальная область включает внутриклеточный сигнальный домен CD28, 4-1BB или ICOS или их сигнальную часть. В некоторых вариантах осуществления костимулирующая сигнальная область расположена между трансмембранным доменом и внутриклеточной сигнальной областью.
[0046] В некоторых вариантах осуществления способы и изделия предназначены для или способны к лечению пациента, имеющего неходжкинскую лимфому (NHL). В некоторых аспектах способ включает, и/или изделие определяет или включает составы, способные к введению пациенту дозы или множества Т-клеток. В некоторых аспектах, Т-клетки, включая такие Т-клетки, как CD8+ Т-клетки и/или CD4+ Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым NHL.
[0047] В некоторых вариантах осуществления доза Т-клеток включает от или от приблизительно 5 x 107 CAR-экспрессирующих Т-клеток и 1 x 108 CAR-экспрессирующих Т-клеток, включительно; и NHL включает диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B, и причем пациент является или был идентифицирован как имеющий статус 0 или 1 согласно Eastern Cooperative Oncology Group Performance Status (ECOG).
[0048] В некоторых вариантах осуществления любого из вариантов осуществления изобретения способы дополнительно включают идентификацию, или изделие включает информационное определение, лечение пациента, имеющего диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B, имеющего статус ECOG 0 или 1. В некоторых вариантах осуществления любого из вариантов осуществления изобретения доза Т-клеток и/или введенных клеток включает определенное отношение CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет приблизительно 1:1 или от приблизительно 1:3 до приблизительно 3:1.
[0049] В некоторых аспектах варианты осуществления предназначены для лечения пациента, имеющего неходжкинскую лимфому (NHL), и включают введение пациенту дозы Т-клеток, включающей Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым NHL. В некоторых аспектах доза Т-клеток включает определенное отношение CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение в некоторых аспектах приблизительно составляет или составляет 1:1. В некоторых аспектах NHL включает диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (неуточненную) (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B.
[0050] В некоторых вариантах осуществления любого из вариантов осуществления изобретения пациент является или был идентифицирован как, или определен как имеющий статус 0, 1 или 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG). В некоторых вариантах осуществления любого из вариантов осуществления изобретения пациент является или был идентифицирован как, или определен как имеющий статус ECOG 0 или 1.
[0051] В некоторых вариантах осуществления любого из вариантов осуществления изобретения, способы и/или применения и/или введение клеток согласно изделиям достигают определенных результатов и/или связаны с определенным сниженным риском токсичности, например, в популяции пациентов, получающих лечение согласно способам или согласно информации, предоставленной в изделии. В некоторых аспектах по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полного ответа (CR) и/или длительного CR; и/или по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR) и/или длительного OR. В некоторых вариантах осуществления любого из способов по изобретению ответ длится более чем 3 месяца или более чем 6 месяцев. В некоторых вариантах осуществления, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70% пациентов, которые в момент введения или до введения дозы клеток имели или были идентифицированы как имеющие лимфому double/triple hit или рецидив, необязательно рецидив в течение 12 месяцев, после введения трансплантата аутогенных стволовых клеток (ASCT) достигли OR, причем необязательно OR длился в течение или более чем 3 месяцев или в течение 6 месяцев или более. В некоторых вариантах осуществления любого из способов по изобретению, более чем или более чем приблизительно 50% пациентов, получающих лечение согласно способу, не демонстрируют степень 3 или выше синдрома высвобождения цитокинов (CRS) или степень 3 или выше нейротоксичности. В некоторых вариантах осуществления такие пациенты не демонстрируют раннее начало CRS и/или нейротоксичности.
[0052] Изобретение относится к способам оценки вероятности ответа на клеточную терапию, включающим: оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбран из ферритина, LDH, CXCL10, G-CSF и IL-10, причем: биологический образец происходит от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением, с определением, таким образом, вероятности, что пациент достигнет ответа на клеточную терапию. В некоторых вариантах осуществления способы также включают применение клеточной терапии к пациенту, если для пациента определена вероятность достижения ответа.
[0053] Изобретение относится к способам отбора пациента для лечения, включающим: оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбран из ферритина, LDH, CXCL10, G-CSF и IL-10, причем: биологический образец происходит от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен из пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и отбор пациента, для которого определена вероятность ответа на лечение на основе результатов определения вероятности, что пациент достигнет ответа на клеточную терапию путем сравнения, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением. В некоторых вариантах осуществления способы также включают применение клеточной терапии к пациенту, выбранному для лечения.
[0054] Изобретение относится к способам лечения, включающим: отбор пациента, для которого определена вероятность ответа на лечение клеточной терапией на основе результатов определения вероятности, что пациент достигнет ответа на клеточную терапию, путем сравнения, индивидуально, уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбран из ферритина, LDH, CXCL10, G-CSF и IL-10, с пороговым значением, причем: биологический образец происходит от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и применение клеточной терапии к пациенту, выбранному для лечения.
[0055] В некоторых вариантах осуществления для пациента определяют вероятность достижения ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения, и пациент вряд ли достигнет ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения.
[0056] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации, или равно или приблизительно равно медиане или среднему уровню, количеству или концентрации аналита в биологическом образце, полученном от группы пациентов до получения ими клеточной терапии, причем каждый из пациентов группы продолжал достигать ответа после введения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0057] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения ими клеточной терапии, причем каждый из пациентов группы продолжал показывать стабильное заболевание (SD) и/или прогрессирующее заболевание (PD) после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0058] В некоторых вариантах осуществления ответ включает объективный ответ. В некоторых вариантах осуществления объективный ответ включает полный ответ (CR) или частичный ответ (PR).
[0059] Изобретение относится к способам оценки вероятности длительного ответа на клеточную терапию, включающим: оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбран из LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β, причем: биологический образец происходит от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением, с определением, таким образом, вероятности, что пациент достигнет длительного ответа на клеточную терапию.
[0060] В некоторых вариантах осуществления способы также включают применение клеточной терапии к пациенту, если для пациента показана вероятность достижения ответа.
[0061] Изобретение относится к способам отбора пациента для лечения, включающим: оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбран из LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β, причем: биологический образец происходит от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и отбор пациента, для которого определена вероятность ответа на лечение на основе результатов определения вероятности, что пациент достигнет длительного ответа на клеточную терапию, путем сравнения, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением. В некоторых вариантах осуществления способы также включают применение клеточной терапии к пациенту, выбранному для лечения.
[0062] Изобретение относится к способам лечения, включающим: отбор пациента, для которого определена вероятность ответа на лечение клеточной терапией на основе результатов определения вероятности, что пациент достигнет длительного ответа на клеточную терапию, путем сравнения, индивидуально, уровня, количества или концентрации одного или более аналитов в биологическом образце с пороговым значением, причем один или более аналитов выбран из LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β, причем: биологический образец происходит от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и применение клеточной терапии к пациенту, выбранному для лечения.
[0063] В некоторых вариантах осуществления пациент, вероятно, достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения, и пациент вряд ли достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения.
[0064] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации, или равно или приблизительно равно медиане или среднему уровню, количеству или концентрации аналита в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал достигать длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0065] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы не достигал длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0066] В некоторых вариантах осуществления длительный ответ включает полный ответ (CR) или частичный ответ (PR), который длится в течение 3 месяцев или более, 4 месяца, 5 месяцев или 6 месяцев.
[0067] В некоторых вариантах осуществления длительный ответ включает CR или PR, который длится в течение по меньшей мере 3 месяцев.
[0068] Изобретение относится к способам оценки риска развития токсичности после введения клеточной терапии, включающим оценку уровня, количества или концентрации одного или более аналитов в биологическом образце от пациента или объемного параметра опухолевой массы у пациента, причем один или более аналитов выбраны из LDH, Ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-8, IL-10, IL-15, IL-16 TNF-α, IFN-α2, MCP-1, MIP-1α и MIP-1β, причем: пациентом является кандидат на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и сравнение, индивидуально, уровня, количества или концентрации аналита в образце или объемного параметра опухолевой массы с пороговым значением с определением, таким образом, риска развития токсичности после введения клеточной терапии.
[0069] Изобретение относится к способам идентификации пациента, включающим оценку уровня, количества или концентрации одного или более аналитов в биологическом образце от пациента или объемного параметра опухолевой массы у пациента, причем один или более аналитов выбраны из LDH, Ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-8, IL-10, IL-15, IL-16 TNF-α, IFN-α2, MCP-1, MIP-1α и MIP-1β, причем: пациентом является кандидат на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и идентификацию пациента, у которого имеется риск развития токсичности после введения клеточной терапии, на основании сравнения, индивидуально, уровня, количества или концентрации аналита в образце или объемного параметра опухолевой массы с пороговым значением.
[0070] Изобретение относится к способам лечения, включающим оценку уровня, количества или концентрации одного или более аналитов в биологическом образце от пациента или объемного параметра опухолевой массы у пациента, причем один или более аналитов выбраны из LDH, Ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-8, IL-10, IL-15, IL-16 TNF-α, IFN-α2, MCP-1, MIP-1α и MIP-1β, причем: пациентом является кандидат на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и сравнение, индивидуально, уровня, количества или концентрации аналита в образце или объемного параметра опухолевой массы с пороговым значением с определением, таким образом, риска развития токсичности после введения клеточной терапии; и последующее или на основе результатов оценки применение к пациенту клеточной терапии, и, необязательно, агента или другого лечения, способное к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности.
[0071] В некоторых вариантах осуществления биологический образец является образцом крови или плазмы.
[0072] В некоторых вариантах осуществления объемный параметр опухолевой массы является суммой габаритов продукта (SPD) или является объемным измерением на основе отображения CT и/или MRI или другого отображения тела. В некоторых вариантах осуществления объемный параметр опухолевой массы определяют до лечения, до афереза или до производства клеточного продукта.
[0073] В некоторых вариантах осуществления способы также включают контроль пациента в отношении симптомов токсичности, если пациенту вводят клеточную терапию и идентифицируют его как имеющего риск развития токсичности.
[0074] В некоторых вариантах осуществления пациент имеет риск развития токсичности, если уровень, количество или концентрация одного или более аналитов или объемный параметр опухолевой массы выше порогового значения, и пациент имеет низкий риск развития токсичности, если уровень, количество или концентрация одного или более аналитов или объемный параметр опухолевой массы ниже порогового значения.
[0075] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации, или равно или приблизительно равно медиане или среднему уровню, количеству или концентрации аналита или объемного параметра опухолевой массы в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы продолжает не развиваться какая-либо токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0076] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации аналита или объемного параметра опухолевой массы в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0077] В некоторых вариантах осуществления токсичность является нейротоксичностью или CRS.
[0078] В некоторых вариантах осуществления токсичность является нейротоксичностью или CRS степени 1 или более высокой.
[0079] В некоторых вариантах осуществления токсичность является тяжелой нейротоксичностью или является нейротоксичностью степени 2 или выше, нейротоксичностью степени 3 или более высокой, по меньшей мере пролонгированной нейротоксичностью степени 3 или степени 4 или выше, или нейротоксичностью степени 5; или токсичность является тяжелым CRS или включает CRS степени 2 или выше или степени 3 или выше.
[0080] В некоторых вариантах осуществления токсичность является нейротоксичностью, и объемный параметр опухолевой массы представляет собой SPD, и один или более аналитов выбраны из LDH, IL-10, IL-15, IL-16, TNF-α и MIP-1β.
[0081] В некоторых вариантах осуществления токсичность является нейротоксичностью, и оценивают один или более аналитов, и аналиты выбраны из LDH, Ферритина, CRP, IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β.
[0082] В некоторых вариантах осуществления токсичность является нейротоксичностью, и оценивают один или более аналитов, и аналиты выбраны из IL-8, IL-10 и CXCL10.
[0083] В некоторых вариантах осуществления нейротоксичность является тяжелой нейротоксичностью или нейротоксичностью степени 3 или более высокой.
[0084] В некоторых вариантах осуществления токсичность является CRS и один или более аналитов или объемный параметр опухолевой массы выбраны из LDH, SPD, CRP, d-димера, IL-6, IL-15, TNF-α и MIP-1α.
[0085] В некоторых вариантах осуществления CRS является тяжелым CRS или CRS степени 3 или выше.
[0086] В некоторых вариантах осуществления, если пациент идентифицируется как имеющий риск развития токсичности, введение пациенту: (1) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности и (2) клеточной терапии, причем введение агента должно быть введено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или клеточная терапия в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или которое подозревается у него, после введения клеточной терапии; и/или ввдения пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0087] В некоторых вариантах осуществления, агент или другое средство для лечения представляет собой анти-IL-6 антитело или антитело к рецептору IL6.
[0088] В некоторых вариантах осуществления, агент или другое средство для лечения представляет собой или включает средство, выбранное из числа тоцилизумаба, силтуксимаба, клазакизумаба, сарилумаба, олокизумаба (CDP6038), элсилимомаба, ALD518/BMS-945429, сирукумаба (CNTO 136), CPSI-2634, ARGX-109, FE301 и FM101.
[0089] В некоторых вариантах осуществления, агент или другое средство для лечения представляет собой или включает стероид, необязательно дексаметазон.
[0090] В некоторых вариантах осуществления оценивают объемный параметр, и объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 30 см2, или приблизительно 40 см2, или приблизительно 50 см2, или приблизительно 60 см2, или составляет или приблизительно составляет 70 см2. В некоторых вариантах осуществления объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 50 см2.
[0091] В некоторых вариантах осуществления, один или более аналитов представляет собой или включает LDH, и пороговое значение составляет или приблизительно составляет 300 единиц на литр, или составляет приблизительно 400 единиц на литр, или составляет приблизительно 500 единиц на литр или составляет или приблизительно составляет 600 единиц на литр. В некоторых вариантах осуществления аналит представляет собой LDH, и пороговое значение составляет или приблизительно составляет 500 единиц на литр.
[0092] В некоторых вариантах осуществления рекомбинантный рецептор специфично связывается с антигеном, ассоциированным с заболеванием или состоянием или экспрессируемым в клетках среды поражения, ассоциированного с заболеванием или состоянием. В некоторых вариантах осуществления, заболевание или состояние представляет собой рак. В некоторых вариантах осуществления, заболевание или состояние представляет собой миелому, лейкоз или лимфому. В некоторых вариантах осуществления, заболевание или состояние представляет собой В-клеточную злокачественную опухоль и/или острый лимфообластный лейкоз (ALL), ALL взрослых, хронический лимфообластный лейкоз (CLL), неходжкинскую лимфому (NHL) и диффузную крупноклеточную В-клеточную лимфому (DLBCL).
[0093] В некоторых вариантах осуществления рекомбинантный рецептор является химерным антигенным рецептором (CAR). В некоторых вариантах осуществления генно-инженерные клетки включают Т-клетки, необязательно CD4+ и/или CD8+. В некоторых вариантах осуществления Т-клетки являются первичными Т-клетками, полученными от пациента, или являются аутологичными для пациента.
[0094] Изобретение относится к способам лечения пациента, имеющего неходжкинскую лимфому (NHL), включающим введение пациенту дозы Т-клеток, включающей Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым NHL, причем: доза Т-клеток включает от или от приблизительно 5 x 107 экспрессирующих рекомбинантный рецептор Т-клеток до 1 x 108 экспрессирующих рекомбинантный рецептор Т-клеток, включительно, причем указанная доза включает определенное отношение CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор и/или CD4+ клеток к CD8+ клеткам, причем это отношение приблизительно составляет или составляет 1:1; и способ приводит к (1) полному ответу (CR) у по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% получающих лечение пациентов и/или объективному ответу (OR) у по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% получающих лечение пациентов, и приводит к (2) тому, что у не более чем 50% пациентов развивается синдром высвобождения цитокинов (CRS) выше, чем в степени 2 и/или нейротоксичность выше, чем в степени 2.
[0095] В некоторых вариантах осуществления любого из способов по изобретению, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70% пациентов, у которых, в момент или до введения дозы клеток имелась или была идентифицирована лимфома double/triple hit (или высокодифференцированная В-клеточная лимфома с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit)) или рецидив после введения трансплантата аутологичных стволовых клеток (ASCT), достигли OR, причем необязательно OR длился в течение 3 месяцев или более или в течение 6 месяцев или более.
[0096] В некоторых вариантах осуществления любого из способов по изобретению, CR или OR длился в течение более чем 3 месяцев или более чем 6 месяцев. В некоторых вариантах осуществления любого из способов по изобретению, более чем или приблизительно более чем 50% пациентов, получающих лечение согласно способу, не показывают синдрома высвобождения цитокина (CRS) или нейротоксичности какой-либо степени.
[0097] В некоторых вариантах осуществления, CR или OR длился в течение более чем 3 месяцев или более чем 6 месяцев; по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают CR, который является длительным; по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом и которые достигали CR, остаются в состоянии ответа или остается в состоянии CR, или остаются в живых в течение или более чем 3 месяцем или в течение 6 месяцев или более или в течение или более чем 9 месяцев; и/или причем по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом, которые достигали CR за один месяц и/или за три месяца, остаются в состоянии ответа, остается в состоянии CR и/или остаются в живых или остаются в живых без прогрессии в течение или более чем 3 месяцев и/или в течение 6 месяцев или более и/или в течение более чем девяти месяцев; и/или по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR), причем необязательно OR является длительным, или длительным у по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR, в течение или более чем 3 месяцев или в течение 6 месяцев или более; и/или причем по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом и достигающих OR, остаются в состоянии ответа или остаются в живых в течение или более чем 3 месяцев и/или в течение 6 месяцев или более.
[0098] В некоторых вариантах осуществления, в момент или до введения дозы клеток, пациент имеет или был идентифицирован как имеющий лимфому, ассоциированную с или включающую участие центральной нервной системы (ЦНС); и/или по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% пациентов, получающих лечение согласно способу, у которых, в момент или до введения дозы клеток была показана или которые были идентифицированы как демонстрирующие лимфому с участием ЦНС, достигли устранения заболевания ЦНС.
[0099] Изобретение относится к способам лечения пациента, включающим введение пациенту, имеющему лимфому, дозы Т-клеток, включающей Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым лимфомой, причем лимфома у пациента ассоциирована с или включает участие центральной нервной системы (ЦНС). В некоторых аспектах, в момент или до введения дозы клеток, пациент имеет поражение мозга, необязательно поражение височной доли мозга. В некоторых примерах лимфома является В-клеточной злокачественной опухолью. В некоторых вариантах осуществления лимфома является неходжкинской лимфомой (NHL).
[0100] В некоторых из любых таких вариантов осуществления по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полного ответа (CR) или ремиссии заболевания ЦНС и/или достигают сокращения или клиренса заболевания ЦНС, причем необязательно CR или ремиссия или сокращение или клиренс заболевания ЦНС являются длительными или длятся у по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR, в течение или более чем 3 месяцев или в течение 6 месяцев или более; и/или по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR или ремиссии или другого сокращения заболевания ЦНС за один месяц и/или за три месяца, остаются в состоянии ответа, остаются в состоянии ремиссии, например, в CR, или продолжают показывать признаки сокращения или ремиссии, и/или остаются в живых или остаются в живых без прогрессии в течение или более чем 3 месяцев и/или в течение 6 месяцев или более и/или более чем девять месяцев; и/или по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR) или ремиссии заболевания ЦНС, причем необязательно OR или ремиссия заболевания ЦНС являются длительными или длятся у по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR, в течение или более чем 3 месяцем или в течение 6 месяцев или более; и/или по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR или ремиссии заболевания ЦНС, остаются в состоянии ответа или остаются в живых в течение или более чем 3 месяцев и/или в течение 6 месяцев или более; и/или поражение мозга уменьшается в размере или объеме, необязательно более чем или более чем приблизительно на 25%, 50%, 75% или более. В некоторых аспектах сокращение или ремиссия, или клиренс заболевания ЦНС достигается без или без существенных признаков или симптомов токсичности, такой как нейротоксичность, такая как тяжелая нейротоксичность, например, нейротоксичность более чем степени 2 или более, чем степени 3, и/или без токсичности, вызванной активацией или присутствием клеток клеточной терапии в мозге пациента, и/или достигается без увеличенного уровня токсичности по сравнению с пациентом, у которого заболевание ЦНС сохраняется, и/или получающего лечение терапией, но не демонстрирующего заболевание ЦНС.
[0101] В некоторых вариантах осуществления любого из способов по изобретению, более чем или более, чем приблизительно 30%, 35%, 40% или 50% пациентов, получающих лечение согласно способу, не показывают синдрома высвобождения цитокинов (CRS) или нейротоксичности какой-либо степени. В некоторых вариантах осуществления любого из способов по изобретению, по меньшей мере у или приблизительно у 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% пациентов, получающих лечение согласно способу, не показано раннего начала CRS или нейротоксичности и/или не показано начала CRS ранее, чем через 3 дня после инициации введения и/или не показано начала нейротоксичности ранее, чем через 5 дней после инициации введения, и/или причем среднее начало нейротоксичности среди пациентов, получающих лечение согласно способу, имеет место в момент или после среднего пика, или среднее время устранения CRS у пациентов, получающих лечение согласно способу, и/или среднего начала нейротоксичности среди пациентов, получающих лечение согласно способу, составляет более чем или приблизительно 8, 9, 10 или 11 дней.
[0102] В некоторых вариантах осуществления любого из способов по изобретению, до инициации введения дозы клеток пациенту не вводили агент или средство для лечения, способное к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности. В некоторых вариантах осуществления любого из способов по изобретению пациенту не вводили агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого, в течение промежутка времени после введения дозы, причем промежуток времени необязательно составляет или приблизительно составляет 1, 2, 3, 4, 5 дней или необязательно составляет или приблизительно составляет 6, 7, 8, 9, 10, 11 дней или необязательно составляет 1, 2, 3 или 4 недели. В некоторых вариантах осуществления любого из способов по изобретению пациенту не вводили агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого, после введения дозы, до того как или если пациент не показывает признак или симптом токсичности и/или до того как или если пациент не показывает признак или симптом токсичности кроме повышения температуры, причем необязательно повышение температуры не является длительным повышением температуры, или повышение температуры было уменьшено или снижено более чем на 1°C после лечения жаропонижающим средством. В некоторых вариантах осуществления любого из способов по изобретению, введение и любое наблюдение осуществляют на амбулаторной основе и/или без допуска пациента в больницу и/или без оставления на ночь в больнице и/или не требуя допуска или оставления на ночь в больнице, необязательно если или пока пациент не показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на на 1°C после лечения жаропонижающим средством.
[0103] В некоторых вариантах осуществления любого из способов по изобретению, до инициации введения дозы клеток пациенту не вводили анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или ситуксимаб, и/или не вводили стероид, необязательно дексаметазон. В некоторых вариантах осуществления любого из способов по изобретению пациенту не вводили анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб, и/или не вводили стероид, необязательно дексаметазон, в течение промежутка времени после введения дозы, причем промежуток времени необязательно составляет или приблизительно составляет 1, 2, 3, 4, 5 дней или необязательно составляет или приблизительно составляет 6, 7, 8, 9, 10, 11 дней, или необязательно составляет 1, 2, 3 или 4 недели. В некоторых вариантах осуществления любого из способов по изобретению пациенту не вводили анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб, и/или не вводили стероид, необязательно дексаметазон, после введения дозы клеток, до того как, или если, пациент не показывает признак или симптом токсичности, необязательно нейротоксичности или CRS, и/или до того как, или если, пациент не показывает признак или симптом токсичности, необязательно нейротоксичности или CRS, кроме повышения температуры, причем необязательно повышение температуры не является длительным повышением температуры, или повышение температуры является или было уменьшено или снижено более чем на 1°C после лечения жаропонижающим средством. В некоторых вариантах осуществления любого из способов по изобретению, введение и любое наблюдение осуществляют на амбулаторной основе и/или без допуска пациента в больницу и/или без оставления на ночь в больнице и/или не требуя допуска или оставления на ночь в больнице, необязательно если или пока пациент не показывает длительное повышение температуры или повышение температуры, которое является или не было уменьшено или не уменьшено более чем на 1°C после лечения жаропонижающим средством.
[0104] В некоторых вариантах осуществления любого из способов по изобретению введение осуществляют на амбулаторной основе и/или не требуя допуска или оставления на ночь в больнице. В некоторых вариантах осуществления какого-либо из способов по изобретению, если пациент, который получает или получал лечение на амбулаторной основе, показывает длительное повышение температуры или повышение температуры, которое является или не было уменьшено или не уменьшено более чем на 1°C после лечения жаропонижающим средством, пациента госпитализируют или оставляют на ночь в больнице и/или ему вводят агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого.
[0105] В некоторых вариантах осуществления любого из способов по изобретению NHL выбрана из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B). В некоторых вариантах осуществления любого из способов по изобретению NHL включает диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B. В некоторых примерах NHL включает DLBCL. В некоторых вариантах осуществления любого из способов по изобретению DLBCL является таковой de novo или трансформированной из фолликулярной лимфомы (FL) и/или не включает DLBCL, трансформированной из MZL и CLL (Рихтера).
[0106] В некоторых вариантах осуществления любого из способов по изобретению пациент является или был идентифицирован как имеющий статус 0, 1 или 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG). В некоторых вариантах осуществления любого из способов по изобретению пациент является или был идентифицирован как имеющий статуса ECOG 0 или 1. В некоторых вариантах осуществления любого из способов по изобретению, в момент или непосредственно перед введением дозы клеток у пациента наблюдался рецидив после ремиссии после лечения с, или рефрактерность к, одной или более предшествующих терапий NHL, необязательно одной, двум или трем предшествующим терапиям, отличным от другой дозы CAR-экспрессирующих клеток.
[0107] В некоторых вариантах осуществления любого из способов по изобретению, в момент или до введения дозы клеток пациент является или был идентифицирован как имеющий лимфому, ассоциированную с или включающую участие центральной нервной системы (ЦНС). В некоторых вариантах осуществления любого из способов по изобретению по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% пациентов, получающих лечение согласно способу, у которых, в момент или до введения дозы клеток, была показана или была идентифицирована лимфома с участием ЦНС, достигли устранения заболевания ЦНС.
[0108] В некоторых вариантах осуществления любого из способов по изобретению, в момент или до введения дозы клеток: пациент является или был идентифицирован как имеющий лимфому double/triple hit (или высокодифференцированную В-клеточную лимфому с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit)); пациент является или был идентифицирован как имеющий хеморефрактерную лимфому, необязательно хеморефрактерную DLBCL; пациент не достиг полной ремиссии (CR) в ответ на предшествующую терапию; и/или пациент имел рецидив в течение 1 года или спустя меньше чем 1 год после получения трансплантата аутологичных стволовых клеток (ASCT).
[0109] В некоторых вариантах осуществления любого из способов по изобретению способ включает, до введения дозы клеток, идентификацию или выбор пациента для введения дозы клеток, имеющего лимфому double/triple hit (или высокодифференцированную В-клеточную лимфому, с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit)), хеморефрактерную лимфому, необязательно хеморефрактерную DLBCL, не достиг полной ремиссии (CR) в ответ на предшествующую терапию для лечения злокачественной опухоли, необязательно NHL; и/или имел рецидив в течение 1 года или спустя меньше чем 1 год после получения трансплантата аутологичных стволовых клеток (ASCT); и/или имеет лимфому, ассоциированную с или включающую участие центральной нервной системы (ЦНС).
[0110] В некоторых вариантах осуществления любого из способов по изобретению способ дополнительно включает введение дополнительного терапевтического агента или терапии, необязательно отличной от клеточной терапии, необязательно отличной от CAR+ Т-клеточной терапии. В некоторых вариантах осуществления, дополнительный терапевтический агент или терапия предназначены для лечения NHL или злокачественной опухоли и/или увеличивает персистирование, активность и/или эффективность дозы клеток. В некоторых вариантах осуществления дополнительный терапевтический агент или терапию вводят, если пациент не демонстрирует ответ, необязательно не демонстрирует CR или OR, на клеточную терапию в течение 1 месяца, в течение 2 месяцев или в течение 3 месяцев после введения дозы клеток. В некоторых вариантах осуществления дополнительный терапевтический агент или терапию вводят пациенту: который является или был идентифицирован как имеющий стабильное или прогрессирующее заболевание (SD/PD) после лечения предшествующей терапией, необязательно предшествующей терапией химиотерапевтическим агентом, который является или был идентифицирован как имеющий статус 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG), который является или был идентифицирован как имеющий трансформированную фолликулярную лимфому (tFL) и/или который является или был идентифицирован как имеющий DLBCL, трансформированную из MZL и CLL. В некоторых вариантах осуществления, до введения дозы клеток или дополнительного терапевтического агента или терапии, способ включает идентификацию или отбор пациента для введения дозы клеток, имеющего стабильное или прогрессирующее заболевание (SD/PD) после лечения предшествующей терапией, необязательно предшествующей терапией химиотерапевтическим агентом, статус 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG), трансформированную фолликулярную лимфому (tFL) и/или DLBCL, трансформированную из MZL и CLL. В некоторых из таких вариантов осуществления, дополнительный терапевтический агент или терапию вводят до, с или одновременно и/или после инициации введения дозы клеток.
[0111] В некоторых вариантах осуществления любого из способов по изобретению CAR включает scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно представляет собой 4-1BB, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно представляет собой CD3дзета. В некоторых вариантах осуществления любого из способов по изобретению антиген является В-клеточным антигеном, который необязательно представляет собой CD19.
[0112] В некоторых вариантах осуществления любого из способов по изобретению, до введения пациент предварительно получал противолимфоцитарную терапию, включающую введение флударабина и/или циклофосфамида. Некоторые варианты осуществления любого из способов по изобретению дополнительно включают, непосредственно перед введением, применение к пациенту противолимфоцитарной терапии, включающей введение флударабина и/или циклофосфамида. В некоторых вариантах осуществления любого из способов по изобретению противолимфоцитарная терапия включает введение циклофосфамида приблизительно в количестве 200-400 мг/м2, необязательно в количестве или приблизительно в количестве 300 мг/м2, включительно, и/или флударабина приблизительно в количестве 20-40 мг/м2, необязательно 30 мг/м2, ежедневно в течение 2-4 дней, необязательно в течение 3 дней. В некоторых вариантах осуществления любого из способов по изобретению противолимфоцитарная терапия включает введение циклофосфамида в количестве или приблизительно в количестве 300 мг/м2 и флударабина приблизительно в количестве 30 мг/м2 ежедневно в течение 3 дней.
[0113] В некоторых вариантах осуществления любого из способов по изобретению введение дозы клеток и/или противолимфоцитарную терапию осуществляют в амбулаторном режиме. В некоторых вариантах осуществления любого из способов по изобретению дозу клеток вводят парентерально, необязательно внутривенно.
[0114] В некоторых вариантах осуществления любого из способов по изобретению: по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полной ремиссии (CR), демонстрируют выживание без прогрессий (PFS) и/или полное выживание (OS) в течение более чем или приблизительно 3 месяцев, 6 месяцев или 12 месяцев; в среднем пациенты, получающие лечение согласно способу, показывают в среднем PFS или OS в течение более чем или приблизительно 6 месяцев, 12 месяцев или 18 месяцев; и/или пациент показывает PFS или OS после терапии по меньшей мере в течение или приблизительно 6, 12, 18 или более месяцев. В некоторых вариантах осуществления любого из способов по изобретению, в момент или спустя приблизительно 14 или 28 дней после инициации введения дозы клеток, число CAR+ Т-клеток, необязательно CAR+ CD8+ Т-клеток и/или CAR+ CD4+ Т-клеток, поддающихся обнаружению в крови пациента, или у большинства пациентов, получающих лечение согласно способу, составляет более 1 клетки на мкл, более 5 клеток на мкл или более 10 клеток на мкл.
[0115] В некоторых вариантах осуществления любого из способов по изобретению Т-клетками являются первичные Т-клетки, полученные от пациента. В некоторых вариантах осуществления любого из способов по изобретению Т-клетки являются аутологичными для пациента. В некоторых вариантах осуществления любого из способов по изобретению Т-клетки являются аллогенными для пациента. В некоторых вариантах осуществления любого из способов по изобретению Т-клетки включают CD4+ и CD8+ Т-клетки, вводимые как множество композиций, причем указанное множество композиций включает введение первой композиции, включающей CD4+ Т-клетки или CD8+ Т-клетки, и введение второй композиции, включающей другие из числа CD4+ Т-клеток или CD8+ Т-клеток.
[0116] В некоторых вариантах осуществления любого из способов по изобретению первую композицию и вторую композицию вводят с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часов. В некоторых вариантах осуществления любого из способов по изобретению первую композицию и вторую композицию вводят с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут. В некоторых вариантах осуществления любого из способов по изобретению первая композиция включает CD4+ Т-клетки. В некоторых вариантах осуществления любого из способов по изобретению первая композиция включает CD8+ Т-клетки. В некоторых вариантах осуществления любого из способов по изобретению первую композицию вводят до второй композиции.
[0117] В некоторых вариантах осуществления любого из способов по изобретению дозу Т-клеток вводят пациенту как единственную дозу или вводят только один раз за период двух недель, одного месяца, трех месяцев, шести месяцев, 1 года или более. В некоторых вариантах осуществления любого из способов по изобретению дозу Т-клеток вводят как двойную дозу, включающую первую дозу Т-клеток и последующую дозу Т-клеток, причем одна или обе из первой дозы и второй дозы включает введение множества композиций Т-клеток. В некоторых вариантах осуществления любого из способов по изобретению последующую дозу вводят в момент времени по меньшей мере или более чем приблизительно 7 дней или 14 дней и менее чем приблизительно 28 дней после инициации введения первой дозы клеток.
[0118] Изобретение относится к изделию, включающему клеточную терапию, включающую дозу или композицию генно-инженерных клеток, экспрессирующих химерный антигенный рецептор (CAR), и инструкции по введению клеточной терапии, причем инструкции определяют: доза клеток предназначена для введения пациенту, имеющему или идентифицированному как имеющий неходжкинскую лимфому (NHL), причем NHL выбрана из диффузной крупноклеточной В-клеточной лимфомы (DLBCL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), NOS (de novo или трансформированной из вялотекущей лимфомы) или фолликулярной лимфомы стадии 3B, причем пациент является или был идентифицирован как имеющий статус 0 или 1 согласно Eastern Cooperative Oncology Group Performance Status (ECOG); и доза Т-клеток для введения включает от или от приблизительно 5 x 107 CAR-экспрессирующих Т-клеток до 1 x 108 CAR-экспрессирующих Т-клеток, включительно. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение дозы Т-клеток в определенном отношении CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно приблизительно составляет 1:1 или от приблизительно 1:3 до приблизительно 3:1.
[0119] Изобретение относится к изделию, включающему клеточную терапию, включающую дозу или композицию генно-инженерных клеток, экспрессирующих химерный антигенный рецептор (CAR), и инструкции по введению клеточной терапии, причем инструкции определяют: доза Т-клеток предназначена для введения в определенном отношении CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение приблизительно составляет или составляет 1:1; и доза клеток предназначена для введения пациенту, имеющему или идентифицированному как имеющий неходжкинскую лимфому (NHL), причем NHL выбрана из диффузной крупноклеточной В-клеточной лимфомы (DLBCL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), NOS (de novo или трансформированной из вялотекущей лимфомы) или фолликулярной лимфомы стадии 3B.
[0120] Изобретение относится к изделие, включающему клеточную терапию, включающую дозу или композицию генно-инженерных клеток, экспрессирующих химерный антигенный рецептор (CAR), и инструкции по введению клеточной терапии, причем инструкции определяют: доза клеток предназначена для введения пациенту, имеющему или идентифицированному как имеющий неходжкинскую лимфому (NHL), необязательно NHL, выбранную из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B), доза Т-клеток для введения включает от или от приблизительно 5 x 107 CAR-экспрессирующих Т-клеток до 1 x 108 CAR-экспрессирующих Т-клеток, включительно; и доза Т-клеток предназначена для введения в определенном отношении CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение приблизительно составляет или составляет 1:1.
[0121] В некоторых вариантах осуществления любого из изделий по изобретению инструкции дополнительно определяют, что доза клеток предназначена для введения пациенту, который является или был идентифицирован как имеющий статус 0, 1 или 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG), необязательно статус ECOG 0 или 1. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют, что введение осуществляют пациенту, не получавшему, непосредственно перед введением дозы клеток или до или до приблизительно 1 месяц до введения дозы клеток, агент или средство для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности. В некоторых вариантах осуществления любого из изделий по изобретению агент представляет собой или включает анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб и/или стероид, необязательно дексаметазон. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют, что доза клеток не предназначена для введения пациенту, имеющему DLBCL, трансформированную из MZL и CLL (Рихтера), и/или пациенту, имеющему DLBCL, которая является таковой de novo или трансформированной из вялотекущего заболевания. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют, что пациент не имеет DLBCL, трансформированную из MZL и CLL (Рихтера).
[0122] В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют, что введение клеточной терапии осуществляют пациенту, который является или был идентифицирован как имеющий лимфому double/triple hit (или высокодифференцированную В-клеточную лимфому с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit)), является или был идентифицирован как имеющий хеморефрактерную лимфому, необязательно хеморефрактерную DLBCL; и/или не достиг полной ремиссии (CR) в ответ на предшествующую терапию. В некоторых вариантах осуществления любого из изделий по изобретению CAR включает scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно представляет собой 4-1BB, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно представляет собой CD3дзета. В некоторых вариантах осуществления любого из изделий по изобретению антиген является В-клеточным антигеном, который необязательно представляет собой CD19.
[0123] Некоторые варианты осуществления любого из изделий по изобретению дополнительно включают инструкции для использования с, после или в связи с противолимфоцитарной терапией, причем противолимфоцитарная терапия необязательно включает флударабин и/или циклофосфамид. В некоторых вариантах осуществления любого из изделий по изобретению противолимфоцитарная терапия включает введение циклофосфамида приблизительно в количестве 200-400 мг/м2, необязательно в количестве или приблизительно в количестве 300 мг/м2, включительно, и/или флударабина приблизительно в количестве 20-40 мг/м2, необязательно 30 мг/м2, ежедневно в течение 2-4 дней, необязательно в течение 3 дней. В некоторых вариантах осуществления любого из изделий по изобретению противолимфоцитарная терапия включает введение циклофосфамида в количестве или приблизительно в количестве 300 мг/м2 и флударабина приблизительно в количестве 30 мг/м2 ежедневно в течение 3 дней.
[0124] В некоторых вариантах осуществления любого из изделий по изобретению инструкции дополнительно определяют, что введение клеточной терапии должно быть или может быть осуществлено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней. В некоторых вариантах осуществления любого из изделий по изобретению инструкции дополнительно определяют, что клеточная терапия предназначена для парентерального введения, необязательно внутривенного введения. В некоторых вариантах осуществления любого из изделий по изобретению клеточная терапия включает первичные Т-клетки, полученные от пациента. В некоторых вариантах осуществления любого из изделий по изобретению Т-клетки являются аутологичными для пациента. В некоторых вариантах осуществления любого из изделий по изобретению Т-клетки являются аллогенными для пациента.
[0125] В некоторых вариантах осуществления любого из изделий по изобретению изделие включает множество композиций клеточной терапии, причем это множество композиций включает первую композицию генно-инженерных клеток, включающих CD4+ Т-клетки или CD8+ Т-клетки, причем инструкции определяют, что первая композиция предназначена для использования со второй композицией, включающей другие из CD4+ Т-клеток или CD8+ Т-клеток, причем необязательно клетки первой композиции и клетки той же композиции получены от того же пациента.
[0126] В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют, что первая композиция и вторая композиция предназначены для введения при определенном отношении CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор и/или CD4+ клеток к CD8+ клеткам, причем это отношение отношение необязательно составляет приблизительно 1:1 или от приблизительно 1:3 до приблизительно 3:1. В некоторых вариантах осуществления любого из изделий по изобретению определенное отношение составляет или приблизительно составляет 1:1. В некоторых вариантах осуществления любого из изделий по изобретению композиция дополнительно включает криопротектор, и/или изделие дополнительно включает инструкции по размораживанию композиции до введения пациенту.
[0127] В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD4+ Т-клетки, и композиции, включающей CD8+ Т-клетки, с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часов. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD4+ Т-клетки, и композиции, включающей CD8+ Т-клетки, с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD4+ Т-клетки, до введения композиции, включающей CD8+ клетки. В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют введение композиции, включающей CD8+ Т-клетки, до введения композиции, включающей CD4+ клетки.
[0128] Изобретение относится к изделиям, включающим один или более реагентов, способных к детекции одного или более аналитов, и инструкции по использованию реагента для тестирования биологического образца от пациента, который является кандидатом на лечение, необязательно клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
[0129] Некоторые варианты осуществления любого из изделий по изобретению дополнительно включают клеточную терапию и/или дополнительно включают инструкции по использованию с, до и/или в связи с лечением клеточной терапией. Некоторые варианты осуществления любого из изделий по изобретению дополнительно включают один или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности и/или инструкции по введению одного или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности у пациента.
[0130] В некоторых вариантах осуществления любого из изделий по изобретению инструкции дополнительно определяют, если уровень, количество или концентрация аналита в образце равны или выше порогового значения для аналита: введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или у которого подозревается его наличие, после введения клеточной терапии; и/или введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0131] В некоторых вариантах осуществления любого из изделий по изобретению инструкции дополнительно определяют, если уровень, количество или концентрация аналита ниже порогового значения для аналита, введение пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0132] В некоторых вариантах осуществления любого из изделий по изобретению инструкции дополнительно определяют введение клеточной терапии пациенту, и причем инструкции дополнительно определяют, если уровень, количество или концентрация аналита ниже порогового значения: введение клеточной терапии не включает введение, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или введение клеточной терапии должно быть или может быть осуществлено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0133] В некоторых вариантах осуществления любого из изделий по изобретению пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации, и/или в пределах стандартного отклонения среднего уровня, количества или концентрации, аналита в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния. Изобретение относится к изделию, включающему клеточную терапию, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор, и инструкции по введению клеточной терапии после или на основе результатов оценки, в биологическом образце, уровня или количества, или концентрации одного или более аналитов в биологическом образце, причем указанный биологический образец получен от пациента до применения клеточной терапии, и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
[0134] В некоторых вариантах осуществления любого из изделий по изобретению указанная оценка включает детекцию, необязательно включающую контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом и определение уровня, количества или концентрации аналита в биологическом образце. Некоторые варианты осуществления любого из изделий по изобретению дополнительно включают реагент и/или дополнительно включают инструкции по использованию с, до и/или в связи с реагентом для детекции аналита. Некоторые варианты осуществления любого из изделий по изобретению дополнительно включают один или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности и/или инструкции по введению одного или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности у пациента.
[0135] В некоторых вариантах осуществления любого из изделий по изобретению инструкции по введению клеточной терапии определяют, если уровень, количество или концентрация аналита в образце равны или выше порогового значения: введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения терапевтической композиции клеток или генно-инженерных клеток; и/или введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или подозревается в его наличии, после введения клеточной терапии; и/или введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0136] В некоторых вариантах осуществления любого из изделий по изобретению инструкции по введению клеточной терапии определяют, если уровень, количество или концентрация аналита в образце ниже порогового значения, введение пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней. В некоторых вариантах осуществления любого из изделий по изобретению инструкции дополнительно определяют введение клеточной терапии пациенту, и причем инструкции дополнительно определяют, если уровень, количество или концентрация аналита ниже порогового значения: не введение, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или введение клеточной терапии должно быть или может быть осуществлено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0137] В некоторых вариантах осуществления любого из изделий по изобретению пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации, и/или в пределах стандартного отклонения от среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0138] Изобретение относится к изделию, включающему агент, способный к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности и инструкции по введению агента после или на основе результатов оценки в биологическом образце уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина). В некоторых вариантах осуществления любого из изделий по изобретению, указанная оценка включает детекцию, необязательно включающую контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом и определение уровня, количества или концентрации аналита в биологическом образце.
[0139] В некоторых вариантах осуществления любого из изделий по изобретению инструкции определяют, что агент предназначен для введения i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту и/или дополнительно включает инструкции по использованию с, до и/или в связи с лечением клеточной терапией. В некоторых вариантах осуществления любого из изделий по изобретению, указанный биологический образец получен от пациента до введения клеточной терапии или агента. В некоторых вариантах осуществления любого из изделий по изобретению реагент является связывающей молекулой, специфично связывающейся с маркером или клетками популяции миелоидных клеток. В некоторых вариантах осуществления любого из изделий по изобретению реагент является антителом или его антигенсвязывающим фрагментом. В некоторых вариантах осуществления любого из изделий по изобретению биологический образец представляет собой или получен из образца крови, плазмы или сыворотки. В некоторых вариантах осуществления любого из изделий по изобретению, включающих реагент для детекции аналита и/или дополнительно включающих инструкции по использованию с, до и/или в связи с реагентом для детекции аналита. Некоторые варианты осуществления любого из изделий по изобретению дополнительно включают клеточную терапию и/или дополнительно включают инструкции по использованию с, до и/или в связи с лечением клеточной терапией.
[0140] В некоторых вариантах осуществления любого из изделий по изобретению инструкции по введению агента определяют, если уровень, количество или концентрация аналита в образце равны или выше порогового значения, введение пациенту агента. В некоторых вариантах осуществления любого из изделий по изобретению инструкция дополнительно определяет введение пациенту клеточной терапии, причем введение агента должно быть осуществлено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту. В некоторых вариантах осуществления любого из изделий по изобретению инструкции по введению агента определяют, если уровень, количество или концентрация ниже порогового значения, введение пациенту клеточной терапии, причем необязательно инструкции определяют, что клеточная терапия должна быть или может быть введена пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0141] В некоторых вариантах осуществления любого из изделий по изобретению пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации, и/или в пределах стандартного отклонения от среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния. В некоторых вариантах осуществления любого из изделий по изобретению, тестирование или оценку клетки для аналита проводят иммунологическим анализом.
[0142] В некоторых вариантах осуществления любого из изделий по изобретению токсичность включает нейротоксичность или синдром высвобождения цитокинов (CRS), необязательно нейротоксичность или CRS степени 1 или более высокой. В некоторых вариантах осуществления любого из изделий по изобретению: токсичность включает тяжелую нейротоксичность и/или включает нейротоксичность степени 2 или более высокой, нейротоксичность степени 3 или более высокой, по меньшей мере пролонгированную нейротоксичность степени 3 или нейротоксичность степени 4 или степени 5 или выше; и/или токсичность включает тяжелый CRS и/или включает CRS степени 2 или выше или степени 3 или выше. В некоторых вариантах осуществления любого из изделий по изобретению токсичность связана с отеком мозга.
[0143] В некоторых вариантах осуществления любого из изделий по изобретению, агент или другое средство для лечения представляет собой или включает один или более стероидов; антагонист или ингибитор рецептора цитокина или цитокина, выбранного из числа IL-10, IL-10R, IL-6, рецептора IL-6, IFNγ, IFNGR, IL-2, IL-2R/CD25, MCP-1, CCR2, CCR4, MIP1β, CCR5, TNFальфа, TNFR1, IL-1, и IL-1Rальфа/IL-1бета; или агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток. В некоторых вариантах осуществления любого из изделий по изобретению, антагонист или ингибитор представляет собой или включает агент, выбранный из числа антитела или антигенсвязывающего фрагмента, малой молекулы, белка или пептида и нуклеиновой кислоты. В некоторых вариантах осуществления любого из изделий по изобретению, агент или другое средство для лечения представляет собой анти-IL-6 антитело или антитело к рецептору IL6.
[0144] В некоторых вариантах осуществления любого из изделий по изобретению, агент или другое средство для лечения представляет собой или включает агент, выбранный из числа тоцилизумаба, силтуксимаба, клазакизумаба, сарилумаба, олокизумаба (CDP6038), элсилимомаба, ALD518/BMS-945429, сирукумаба (CNTO 136), CPSI-2634, ARGX-109, FE301 и FM101. В некоторых вариантах осуществления любого из изделий по изобретению, агент или другое средство для лечения представляет собой или включает тоцилизумаб. В некоторых вариантах осуществления любого из изделий по изобретению, агент или другое средство для лечения представляет собой или включает силтуксимаб. В некоторых вариантах осуществления любого из изделий по изобретению стероид представляет собой или включает дексаметазон.
[0145] В некоторых вариантах осуществления любого из изделий по изобретению агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток, выбран из противовоспалительного средства, ингибитора NADPH оксидазы (NOX2), блокатора кальциевых каналов, блокатора натриевых каналов, ингибирует GM-CSF, ингибирует CSF1R, специфично связывается с CSF-1, специфично связывается с IL-34, ингибирует активацию ядерного фактора каппа-B (NF-κB), активирует рецептор CB2 и/или является агонистом CB2, ингибитором фосфодиэстеразы, ингибирует микроРНК-155 ((miR-155) или повышающе регулирует микроРНК-124 ((miR-124). В некоторых вариантах осуществления любого из изделий по изобретению агент, способный к предотвращению, блокированию или ослаблению активации или функции микроглиальных клеток, является малой молекулой, пептидом, белком, антителом или его антигенсвязывающим фрагментом, миметиком антитела, аптамером или молекулой нуклеиновой кислоты.
[0146] В некоторых вариантах осуществления любого из изделий по изобретению агент выбран из миноциклина, налоксона, нимодипина, Рилузола, MOR103, леналидомида, каннабиноида (необязательно WIN55 или 212-2), внутривенного иммуноглобулина (IVIg), ибудиласта, анти-miR-155 закрытой нуклеиновой кислоты (LNA), MCS110, PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945, эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003. В некоторых вариантах осуществления любого из изделий по изобретению агент является ингибитором рецептора колониестимулирующего фактора 1 (CSF1R). В некоторых вариантах осуществления любого из изделий по изобретению ингибитор выбран из: PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945 или их фармацевтической соли или пролекарства; эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003 или является его антигенсвязывающим фрагментом; или комбинации любого из предшествующих. В некоторых вариантах осуществления любого из изделий по изобретению ингибитор представляет собой PLX-3397.
[0147] В некоторых вариантах осуществления любого из изделий по изобретению, заболевание или состояние представляет собой рак. В некоторых вариантах осуществления любого из изделий по изобретению, заболевание или состояние представляет собой миелому, лейкоз или лимфому. В некоторых вариантах осуществления любого из изделий по изобретению, заболевание или состояние представляет собой В-клеточную злокачественную опухоль и/или острый лимфообластный лейкоз (ALL), ALL взрослых, хронический лимфообластный лейкоз (CLL), неходжкинскую лимфому (NHL) и диффузную крупноклеточную В-клеточную лимфому (DLBCL).
[0148] В некоторых вариантах осуществления любого из изделий по изобретению антиген представляет собой ROR1, Антиген созревания B-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторная тирозинкиназа erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолат-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор, содержащий домен вставки киназы (kdr), легкую каппа-цепь, Антиген Ley, молекулу адгезии L1-клеток, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, рецептор альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D), или патоген-специфический антиген.
[0149] В некоторых вариантах осуществления любого из изделий по изобретению рекомбинантный рецептор является Т-клеточным рецептором или функциональным не Т-клеточным рецептором. В некоторых вариантах осуществления любого из изделий по изобретению рекомбинантный рецептор является химерным антигенным рецептором (CAR). В некоторых вариантах осуществления любого из изделий по изобретению CAR включает внеклеточный антигенраспознающий домен, специфично связывающийся с антигеном, и внутриклеточный сигнальный домен, включающей ITAM, причем необязательно внутриклеточный сигнальный домен включает внутриклеточный домен CD3-дзэта (CD3ζ) цепи; и/или причем CAR дополнительно включает костимулирующий сигнальный домен, необязательно включающую сигнальный домен CD28 или 4-1BB.
[0150] В некоторых вариантах осуществления любого из изделий по изобретению генно-инженерные клетки включают Т-клетки, необязательно CD4+ и/или CD8+. В некоторых вариантах осуществления любого из изделий по изобретению Т-клетками являются первичные Т-клетки, полученные от пациента. В некоторых вариантах осуществления любого из изделий по изобретению доза, не связанная с риском развития токсичности или тяжелой токсичности, представляет собой или включает менее чем или менее чем приблизительно 5 x 107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, менее чем или менее чем приблизительно 2,5 x 107, менее чем или менее чем приблизительно 1,0 x 107, менее чем или менее чем приблизительно 5,0 x 106, менее чем или менее чем приблизительно 1,0 x 106, менее чем или менее чем приблизительно 5,0 x 105, или менее чем или менее чем приблизительно 1 x 105 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерны клеток периферической крови (PBMC). В некоторых вариантах осуществления любого из изделий по изобретению доза, не связанная с риском развития токсичности или тяжелой токсичности, составляет или включает от или от приблизительно 1 x 105 до 5 x 107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, от 1 x 105 до 2,5 x 107, от 1 x 105 до 1,0 x 107, от 1 x 105 до 5,0 x 106, от 1 x 105 до 1,0 x 106, от 1,0 x 105 до 5,0 x 105, от 5,0 x 105 до 5 x 107, от 5 x 105 до 2,5 x 107, от 5 x 105 до 1,0 x 107, от 5 x 105 до 5,0 x 106, от 5 x 105 до 1,0 x 106, от 1,0 x 106 до 5 x 107, от 1 x 106 до 2,5 x 107, от 1 x 106 до 1,0 x 107, от 1 x 106 до 5,0 x 106, от 5,0 x 106 до 5 x 107, от 5 x 106 до 2,5 x 107, от 5 x 106 до 1,0 x 107, от 1,0 x 107 до 5 x 107, от 1 x 107 до 2,5 x 107 или от 2,5 x 107 до 5 x 107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
[0151] В некоторых вариантах осуществления любого из изделий по изобретению, реагент мечен таким образом, чтобы его можно было детектировать, необязательно флуоресцентно мечен. В некоторых вариантах осуществления любого из изделий по изобретению один или более аналитов представляет собой LDH, ферритин, CRP, IL-6, IL-8, IL-10, TNF-альфа, IFN-альфа2, MCP-1 и MCP-1бета. В некоторых вариантах осуществления любого из изделий по изобретению один или более аналитов представляет собой или включает LDH.
[0152] Изобретение относится к способы отбора пациента для лечения, включающим: (a) контактирование биологического образца с одним или более реагентами, которые могут быть детектированы или которые являются специфичными для одного или более аналитов, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина), причем: биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и (b) отбор пациента, у которого: (i) уровень, количество или концентрация аналита в образцах равны или выше порогового значения, таким образом идентифицируя пациента, подверженного риску развития токсичности к клеточной терапии; или (ii) уровень, количество или концентрация аналита ниже порогового значения.
[0153] В некоторых вариантах осуществления любого из способов по изобретению: (a) пациент в (i) выбран для введения пациенту (1) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности и (2) клеточной терапии, причем введение агента должно быть осуществлено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или (c) пациент в (i) выбран для введения пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии; и/или (b) пациент в (i) выбран для введения пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0154] В некоторых вариантах осуществления любого из способов по изобретению пациент в (i) выбран, и способ дополнительно включает: (a) введение пациенту (1) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, и (2) клеточной терапии, причем введение агента осуществляют (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или (b) введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии; и/или (c) введение пациенту клеточной терапии или дозы генно-инженерных клеток клеточной терапии, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии; и/или (d) введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0155] В некоторых вариантах осуществления любого из способов по изобретению: (a) пациент в (ii) выбран для введения пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней; (b) пациент в (ii) выбран для введения пациенту клеточной терапии, причем клеточная терапия не включает введение, до или одновременно с применением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или пациент в (ii) выбран для введения клеточной терапии в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0156] В некоторых вариантах осуществления любого из способов по изобретению пациент в (ii) выбран, и способ дополнительно включает введение пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней. В некоторых вариантах осуществления любого из способов по изобретению пациент в (ii) выбран, и способ дополнительно включает введение пациенту клеточной терапии, причем: введение клеточной терапии не включает введение, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или введение клеточной терапии пациенту должно быть или может быть осуществлено в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0157] Изобретение относится к способу лечения, включающему: (a) тестирование биологического образца в отношении уровня, количества или концентрации одного или более аналитов, причем биологический образец происходит от пациента, который является кандидатом на лечение, необязательно клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор для лечения заболевания или состояния, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина); и (b) после или на основе результатов теста, введение пациенту клеточной терапии, и, необязательно, агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности.
[0158] Изобретение относится к способу лечения, включающему, после или на основе результатов тестирования биологического образца от пациента в отношении уровня, количества или концентрации одного или более аналитов, введение пациенту (i) клеточной терапии, необязательно включающей дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор, для лечения заболевания или состояния, и, необязательно, (ii) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, причем: биологический образец получен от пациента до применения клеточной терапии; и один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
[0159] В некоторых вариантах осуществления любого из способов по изобретению указанное тестирование включает детекцию, необязательно включающую контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом, и определение уровня, количества или концентрации аналита в биологическом образце. В некоторых вариантах осуществления любого из способов по изобретению, если уровень, количество или концентрация аналита в образце равны или выше порогового значения: введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или подозревается в его наличии, после введения клеточной терапии; и/или введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0160] В некоторых вариантах осуществления любого из способов по изобретению, если уровень, количество или концентрация аналита равны или выше порогового значения: введение клеточной терапии не включает введение, до или одновременно с применением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или введение пациенту клеточной терапии должно быть или может быть осуществлено в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0161] В некоторых вариантах осуществления любого из способов по изобретению введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, причем: пациентом является кандидат на лечение необязательно клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор для лечения заболевания или состояния; и пациент был идентифицирован как подверженный риску развития токсичности после или на основе результатов тестирования биологического образца от пациента в отношении уровня, количества или концентрации одного или более аналитов, причем указанный биологический образец получен от пациента до применения клеточной терапии, и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
[0162] В некоторых вариантах осуществления любого из способов по изобретению указанное тестирование включает детекцию, необязательно включающую контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом и определение уровня, количества или концентрации аналита в биологическом образце. В некоторых вариантах осуществления любого из способов по изобретению агент вводят пациенту, если уровень, количество или концентрация аналита в образце равны или выше порогового значения.
[0163] В некоторых вариантах осуществления любого из способов по изобретению агент вводят (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту. В некоторых вариантах осуществления любого из способов по изобретению пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего процента или числа, и/или в пределах стандартного отклонения от среднего процента или числа клеток с поверхностью, положительной в отношении миелоидного маркера в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0164] В некоторых вариантах осуществления любого из способов по изобретению пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации, и/или в пределах стандартного отклонения от среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния. В некоторых вариантах осуществления любого из способов по изобретению реагент является связывающей молекулой, специфично связывающейся с маркером или клетками популяции миелоидных клеток. В некоторых вариантах осуществления любого из способов по изобретению реагент является антителом или его антигенсвязывающим фрагментом. В некоторых вариантах осуществления любого из способов по изобретению биологический образец представляет собой или получен из образца крови, плазмы или сыворотки. В некоторых вариантах осуществления любого из способов по изобретению тестирование или оценка клетки аналита включает иммунологический анализ.
[0165] В некоторых вариантах осуществления любого из способов по изобретению токсичность включает нейротоксичность или синдром высвобождения цитокинов (CRS), необязательно нейротоксичность или CRS степени 1 или более высокой. В некоторых вариантах осуществления любого из способов по изобретению: токсичность включает тяжелую нейротоксичность и/или включает нейротоксичность степени 2 или более высокой, нейротоксичность степени 3 или более высокой, по меньшей мере пролонгированную нейротоксичность степени 3 или нейротоксичность степени 4 или степени 5 или выше; и/или токсичность включает тяжелый CRS и/или включает CRS степени 2 или выше или степени 3 или выше. В некоторых вариантах осуществления любого из способов по изобретению токсичность связана с отеком мозга.
[0166] В некоторых вариантах осуществления любого из способов по изобретению, агент или другое средство для лечения представляет собой или включает один или более стероидов; антагонистов или ингибиторов рецептора цитокина или цитокина, выбранных из числа IL-10, IL-10R, IL-6, рецептора IL-6, IFNγ, IFNGR, IL-2, IL-2R/CD25, MCP-1, CCR2, CCR4, MIP1β, CCR5, TNFальфа, TNFR1, IL-1, и IL-1Rальфа/IL-1бета; или агентов, способных к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток. В некоторых вариантах осуществления любого из способов по изобретению, антагонист или ингибитор представляет собой или включает агент, выбранный из числа антитела или антигенсвязывающего фрагмента, малой молекулы, белка или пептида и нуклеиновой кислоты.
[0167] В некоторых вариантах осуществления любого из способов по изобретению, агент или другое средство для лечения представляет собой анти-IL-6 антитело или антитело к рецептору IL6. В некоторых вариантах осуществления любого из способов по изобретению, агент или другое средство для лечения представляет собой или включает агент, выбранный из числа тоцилизумаба, силтуксимаба, клазакизумаба, сарилумаба, олокизумаба (CDP6038), элсилимомаба, ALD518/BMS-945429, сирукумаба (CNTO 136), CPSI-2634, ARGX-109, FE301 и FM101. В некоторых вариантах осуществления любого из способов по изобретению агент или другое средство для лечения представляет собой или включает тоцилизумаб. В некоторых вариантах осуществления любого из способов по изобретению агент или другое средство для лечения представляет собой или включает силтуксимаб.
[0168] В некоторых вариантах осуществления любого из способов по изобретению стероид представляет собой или включает дексаметазон. В некоторых вариантах осуществления любого из способов по изобретению агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток, выбран из противовоспалительного средства, ингибитора NADPH оксидазы (NOX2), блокатора кальциевых каналов, блокатора натриевых каналов, ингибирует GM-CSF, ингибирует CSF1R, специфично связывается с CSF-1, специфично связывается с IL-34, ингибирует активацию ядерного фактора каппа-B (NF-κB), активирует рецептор CB2 и/или является агонистом CB2, ингибитором фосфодиэстеразы, ингибирует микроРНК-155 ((miR-155) или повышающе регулирует микроРНК-124 ((miR-124).
[0169] В некоторых вариантах осуществления любого из способов по изобретению агент, способный к предотвращению, блокированию или ослаблению активации или функции микроглиальных клеток, является малой молекулой, пептидом, белком, антителом или его антигенсвязывающим фрагментом, миметиком антитела, аптамером или молекулой нуклеиновой кислоты. В некоторых вариантах осуществления любого из способов по изобретению агент выбран из миноциклина, налоксона, нимодипина, Рилузола, MOR103, леналидомида, каннабиноида (необязательно WIN55 или 212-2), внутривенного иммуноглобулина (IVIg), ибудиласта, анти-miR-155 закрытой нуклеиновой кислоты (LNA), MCS110, PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945, эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003.
[0170] В некоторых вариантах осуществления любого из способов по изобретению агент является ингибитором рецептора колониестимулирующего фактора 1 (CSF1R). В некоторых вариантах осуществления любого из способов по изобретению ингибитор выбран из: PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945 или их фармацевтической соли или пролекарства; эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003 или является его антигенсвязывающим фрагментом; или комбинации любого из предшествующих.
[0171] В некоторых вариантах осуществления любого из способов по изобретению ингибитор представляет собой PLX-3397. В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор специфично связывается с антигеном, ассоциированным с заболеванием или состоянием или экспрессируемым в клетках среды поражения, ассоциированного с заболеванием или состоянием. В некоторых вариантах осуществления любого из способов по изобретению заболевание или состояние представляет собой рак. В некоторых вариантах осуществления любого из способов по изобретению заболевание или состояние представляет собой миелому, лейкоз или лимфому. В некоторых вариантах осуществления любого из способов по изобретению заболевание или состояние представляет собой В-клеточную злокачественную опухоль и/или острый лимфообластный лейкоз (ALL), ALL взрослых, хронический лимфообластный лейкоз (CLL), неходжкинскую лимфома (NHL) и диффузную крупноклеточную В-клеточную лимфому (DLBCL).
[0172] В некоторых вариантах осуществления любого из способов по изобретению антиген представляет собой ROR1, Антиген созревания B-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторная тирозинкиназа erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA, и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолат-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор, содержащий домен вставки киназы (kdr), легкую каппа-цепь, Антиген Ley, молекулу L1-клеточной адгезии, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, рецептор альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, Эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D), или патоген-специфический антиген.
[0173] В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор является Т-клеточным рецептором или функциональным не Т-клеточным рецептором. В некоторых вариантах осуществления любого из способов по изобретению рекомбинантный рецептор является химерным антигенным рецептором (CAR). В некоторых вариантах осуществления любого из способов по изобретению CAR включает внеклеточный антигенраспознающий домен, специфично связывающийся с антигеном, и внутриклеточный сигнальный домен, включающей ITAM, причем необязательно внутриклеточный сигнальный домен включает внутриклеточный домен CD3-дзэта (CD3ζ) цепи; и/или причем CAR дополнительно включает костимулирующий сигнальный домен, необязательно включающую сигнальный домен CD28 или 4-1BB.
[0174] В некоторых вариантах осуществления любого из способов по изобретению генно-инженерные клетки включают Т-клетки, необязательно CD4+ и/или CD8+. В некоторых вариантах осуществления любого из способов по изобретению Т-клетками являются первичные Т-клетки, полученные от пациента. В некоторых вариантах осуществления любого из способов по изобретению клеточная терапия включает введение от или от приблизительно 1 x 105 до 1 x 108 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), от или от приблизительно 5 x 105 до 1 x 107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC) или от или от приблизительно 1 x 106 до 1 x 107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), включительно.
[0175] В некоторых вариантах осуществления любого из способов по изобретению клеточная терапия включает введение не более чем 1 x 108 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 1 x 107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 0,5 x 107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 1 x 106 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 0,5 x 106 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
[0176] В некоторых вариантах осуществления любого из способов по изобретению доза, не связанная с риском развития токсичности или тяжелой токсичности, представляет собой или включает менее чем или менее чем приблизительно 5 x 107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, менее чем или менее чем приблизительно 2,5 x 107, менее чем или менее чем приблизительно 1,0 x 107, менее чем или менее чем приблизительно 5,0 x 106, менее чем или менее чем приблизительно 1,0 x 106, менее чем или менее чем приблизительно 5,0 x 105, или менее чем или менее чем приблизительно 1 x 105 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
[0177] В некоторых вариантах осуществления любого из способов по изобретению доза, не связанная с риском развития токсичности или тяжелой токсичности, составляет или включает от или от приблизительно 1 x 105 до 5 x 107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, от 1 x 105 до 2,5 x 107, от 1 x 105 до 1,0 x 107, от 1 x 105 до 5,0 x 106, от 1 x 105 до 1,0 x 106, от 1,0 x 105 до 5,0 x 105, от 5,0 x 105 до 5 x 107, от 5 x 105 до 2,5 x 107, от 5 x 105 до 1,0 x 107, от 5 x 105 до 5,0 x 106, от 5 x 105 до 1,0 x 106, от 1,0 x 106 до 5 x 107, от 1 x 106 до 2,5 x 107, от 1 x 106 до 1,0 x 107, от 1 x 106 до 5,0 x 106, от 5,0 x 106 до 5 x 107, от 5 x 106 до 2,5 x 107, от 5 x 106 до 1,0 x 107, от 1,0 x 107 до 5 x 107, от 1 x 107 до 2,5 x 107 или от 2,5 x 107 до 5 x 107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC). В некоторых вариантах осуществления любого из способов по изобретению генно-инженерные клетки являются аутологичными для пациента. В некоторых вариантах осуществления любого из способов по изобретению генно-инженерные клетки являются аллогенными для пациента. В некоторых вариантах осуществления любого из способов по изобретению, реагент мечен таким образом, чтобы его можно было детектировать, необязательно флуоресцентно мечен.
[0178] В некоторых вариантах осуществления инструкции предоставляют информацию о пороговом значении, индивидуально для каждого одного или более аналитов, которое является индикатором вероятности того, продемонстрирует ли пациент ответ на лечение клеточной терапией. В некоторых вариантах осуществления инструкции предоставляют информацию о пороговом значении, индивидуально для каждого одного или более аналитов, которое является индикатором вероятности того, продемонстрирует ли пациент длительный ответ после введения клеточной терапии. В некоторых вариантах осуществления инструкции предоставляют информацию о пороговом значении, индивидуально для каждого одного или более аналитов, которое является индикатором вероятности того, продемонстрирует ли пациент токсичность после введения клеточной терапии.
Краткое описание чертежей
[0179] ФИГ. 1 показывает процент пациентов, демонстрирующих отклонения лабораторных показателей от нормы и нежелательные явления, возникшие в ходе лечения (TEAE), имеющие место у ≥20% пациентов. *: Одно AE Степени 5 в форме полиорганной недостаточности, не связанной с исследуемым лечением и являющейся следствием развития лимфомы; †: Одно AE Степени 5 в форме диффузного альвеолярного повреждения, по оценке исследователя, связанное с флударабином, циклофосфамидом и CAR Т-клеточной терапией, произошедшее в день 23 у пациента, который отказался от искусственной вентиляции для прогрессивного нарушения дыхания, демонстрируя нейтропению на факторах роста и антибиотиках широкого спектра действия и противогрибковых средствах.
[0180] ФИГ. 2 является кривой Каплана-Мейера, изображающей наблюдаемое время к началу CRS и нейротоксичности.
[0181] ФИГ. 3A и ФИГ. 3B изображают частоту объективных ответов (ORR) за 3-месячный период среди подгрупп получающих лечение пациентов.
[0182] ФИГ. 4A и ФИГ. 4B показывают продолжительность ответа (CR/PR, CR или PR) и полное выживание в полном и основном контингенте пациентов.
[0183] ФИГ. 5A показывает фармакокинетику CAR+ Т-клеток в периферической крови в разные моментов времени после лечения при разных уровнях дозы. ФИГ. 5B показывает фармакокинетику CAR+ Т-клеток в периферической крови в разные моментов времени после лечения между отвечающими пациентами и неотвечающими пациентами. ФИГ. 5C показывает фармакокинетику CAR+ Т-клеток в периферической крови в разные моментов времени после лечения у пациентов, у которых развивалась или не развивалась нейротоксичность.
[0184] ФИГ. 6A показывает число CD3+/CAR+, CD4+/CAR+, CD8+/CAR+ T-клеток в периферической крови пациента с хеморефрактерно трансформированной DLBCL, измеренное в определенные моменты времени. ФИГ. 6B изображает осевое изображение PET-CT после предварительной обработки, показывающее внутричерепную патологию в правой средней черепной ямке и обширную патологию в подкожных тканях в правой задней ушной области. ФИГ. 6C является изображением PET-CT после лечения патологии на ФИГ. 2B после лечения анти-CD19 CAR+ Т-клетками. ФИГ. 6D является MRI мозга после предварительной обработки (T1-взвешенное изображение с высокой разрешающей способностью с использованием контраста; осевое представление), показывающим гомогенно увеличенную массу в правой средней черепной ямке. ФИГ. 6E является изображением MRI после лечения, показывающим почти полное устранение увеличенной массы. ФИГ. 6F является осевым изображением PET-CT в правой задней ушной области, показывающим рецидив опухоли, связанный с интенсивным накоплением 18F-фтордезоксиглюкозы (стрелка). ФИГ. 6G является отображением PET-CT, показывающим устранение задней ушной опухоли после инцизионной биопсии и повторной экспансии CAR+ Т-клеток.
[0185] ФИГ. 7 показывает уровни аналитов, измеренных в сыворотке пациентов до введения CAR+ Т-клеток, и корреляцию с развитием нейротоксичности.
[0186] ФИГ. 8 показывает график, на котором показано время без прогрессий (месяцы) и лучший полный ответ и длительность ответа, и индивибивалентные клинические результаты, наблюдаемые в течение времени у индивидуальных пациентов в Полном контингенте и Основном контингенте пациентов с NHL, получающих лечение анти-CD19 клеточной терапией, содержащей CAR-T-экспрессирующие CD4+ и CD8+ Т-клетки. a: Пациенты достигли BOR в месяц 1, кроме случаев, где указано иное; b: Полное устранение участия ЦНС в лимфоме, наблюдаемое у 2 пациентов; c: Один пациент с повторной экспансией после биопсии после прогрессии заболевания
[0187] ФИГ. 9A изображает медианное (±квартили) число CAR-экспрессирующих CD3+ клеток/мкл крови, оцененное потоковой цитометрией с использованием антитела, специфичного для усеченного рецептора (CD3, круг; N=87); или медианное (±квартили) число копий интегрированного CAR трансгена/мг геномной ДНК, оцененное количественной полимеразной цепной реакцией (кПЦР) с использованием праймеров, специфичных для посттранскрипционного регуляторного элемента вируса гепатита сурков (WPRE), присутствующего в векторе, кодирующем CAR (кПЦР, квадрат; N=85) в образцах крови от 87 пациентов, которым вводили CAR-экспрессирующие клетки анти-CD19. Отсечка для детекции CAR+ клеток в потоковой цитометрии была установлена на ≥ 25 событий в CAR+ воротах, и предел детекции для кПЦР составлял ≥ 12,5 копий трансгенных CAR на мкг геномной ДНК.
[0188] ФИГ. 9B изображает относительные числа CD4+ и CD8+CAR-экспрессирующих клеток/мкл в образцах крови и костного мозга от 67 пациентов, которым вводили CAR-экспрессирующие клетки анти-CD19 в день 11 ± 3 дня. Линия представляет линию единства и не является линией регрессии.
[0189] ФИГ. 10А и 10B изображают медианную (±квартили) область под кривой между днями 0 и 28 (AUC0-28; ФИГ. 10A) и максимальную концентрацию в сыворотке (AUC0-28; CAR+ клеток/мкл крови; ФИГ. 10B) CD4+ и CD8+ CAR+ клеток в подгруппах пациентов с диффузной крупноклеточной В-клеточной лимфомой de novo или трансформированной из вялотекущей лимфомы (DLBCL, NOS; N=27), трансформированной фолликулярной лимфомой (tFL; N=10), DLBCL, трансформированной из лимфомы маргинальной зоны или хронического лимфолейкоза (tMZL/tCLL; N=4), или мантийноклеточной лимфомы (MCL; N-5), которые получали CAR-экспрессирующие Т-клетки в DL1.
[0190] ФИГ. 11А и 11B изображают медианную (±квартили) область под кривой между днями 0 и 28 (AUC0-28; ФИГ. 11A) и максимальную концентрацию в сыворотке (AUC0-28; CAR+ клеток/мкл крови; ФИГ. 11B) CD3+, CD4+ и CD8+ CAR+ клетки у пациентов, которые получали CAR+ клетки в DL1 или DL2.
[0191] ФИГ. 12A-12D изображают медианное (±квартили) число CAR-экспрессирующих CD4+ и CD8+ CAR+ клеток/мкл крови в течение времени у пациентов, у которых развился синдром высвобождения цитокинов (любой CRS), по сравнению с пациентами, у которых не развился CRS (никакого CRS) (CD4+: ФИГ. 12A; CD8+: ФИГ. 12B), или у пациентов, у которых развилась нейротоксичность (любая NT) по сравнению с пациентами, у которых не развилась NT (никакая NT) (CD4+: ФИГ. 12C; CD8+: ФИГ. 12D).
[0192] ФИГ. 13А и 13B изображают число пиковых CD3+ CAR+ клеток/мкл (CD3+ AUC0-28) у пациентов, распределенных в группы пациентов, у которых был лучший полный ответ (BOR) CR, PR или PD или 3-месячный длительный ответ (M3) CR, PR или PD.
[0193] ФИГ. 14A изображает уровни аналита в крови перед лимфодеплецией в образцах сыворотки от пациентов, показавших высокую экспансию CAR+ клеток (CD3+ AUC0-28 >500), и пациентов, показавших низкую экспансию CAR+ клеток (CD3+ AUC0-28 <500).
[0194] ФИГ. 14B изображает пиковые уровни аналита крови в образцах сыворотки от пациентов, показавших высокую экспансию CAR+ клеток (CD3+ AUC0-28 >500), и пациентов, показавших низкую экспансию CAR+ клеток (CD3+ AUC0-28 <500).
[0195] ФИГ. 15 изображает участок, изображающий SPD перед лимфодеплецией (см2) против AUC0-28 (клеток*день/мкл) CD3+ CAR+ клеток для индивидуальных пациентов, которым вводили DL1 или DL2 CAR+ клеток.
[0196] ФИГ. 16А и 16B изображают уровни аналита в крови перед лимфодеплецией в образцах сыворотки от пациентов, у которых развился синдром высвобождения цитокинов (CRS степени 1-4), по сравнению с пациентами, у которых не развился CRS (CRS степени 0) (ФИГ. 16A), или у пациентов, у которых развилась нейротоксичность (NT степени 0), по сравнению с пациентами, у которых не развилась NT (NT степени 1-4) (ФИГ. 16B). Единицы были следующими: Ферритин и D-димер (мкг/л); CRP (мг/л) и цитокины (пг/мл).
[0197] ФИГ. 17 изображает оценку перед лимфодеплецией параметра пациента в виде суммы габаритов продукта (SPD; см2), показывающего опухолевую массу и уровень лактатдегидрогеназы (LDH; Ед/л) у пациентов, у которых развился синдром высвобождения цитокинов (любой CRS) по сравнению с пациентами, у которых не развился CRS (никакой CRS), или у пациентов, у которых развилась нейротоксичность (любой NT), по сравнению с пациентами, у которых не развилась NT (никакой NT).
[0198] ФИГ. 18A является графиком, изображающим SPD (см2) перед лимфодеплецией против уровней LDH (Ед/л) перед лимфодеплецией у лиц, у которых развилась нейротоксичность (NT степени 1-4), или пациентов, у которых не развилась NT (NT степени 0) (левая группа), и у лиц, у которых развился CRS (CRS степени 1-4), или пациентов, у которых не развился CRS (CRS степени 0) (правая группа). Пунктиры представляют уровни SPD (50 см2 или выше) или LDH (500 Ед/л или выше), которые связаны с более высокими показателями CRS или NT. ФИГ. 18B изображает оценки вероятности развития CRS или NT на основе уровней SPD (50 см2 или выше) или LDH (500 Ед/л или выше), с 95%-ми доверительными интервалами (CI). ФИГ. 18C изображает оценки вероятности развития CRS или NT на основе уровней SPD или LDH, включая оценки вероятности для значений ниже пороговых, с 95%-ми доверительными интервалами (CI).
[0199] ФИГ. 19 изображает параметр опухолевой массы (SPD) перед лимфодеплецией и уровни аналита крови для пациентов, имевших длительный ответ в 3 месяца по сравнению с пациентами, не имевшими ответа в 3 месяца. Единицы были следующими: Ферритин и D-димер (мкг/л); CRP и SAA-1 (мг/л) и цитокины (пг/мл).
[0200] ФИГ. 20А и 20B изображают пиковые уровни аналита в крови в образцах сыворотки от пациентов, у которых развился синдром высвобождения цитокинов (любой CRS), по сравнению с пациентами, у которых не развился CRS (никакой CRS) (ФИГ. 20A), или у пациентов, у которых развилась нейротоксичность (любая NT), по сравнению с пациентами, у которых не развилась NT (никакая NT) (ФИГ. 20B). Единицы были следующими: CRP (мг/л), SAA-1 (мг/л) и цитокины (пг/мл).
[0201] ФИГ. 21A изображает пиковые уровни аналита крови в образцах сыворотки от пациентов, имевших лучший общий ответ (BOR) в форме полного ответа (CR) или частичного ответа (PR) (N=57) по сравнению с уровнями у пациентов, имевших стабильное заболевание (SD) или прогрессирующее заболевание (PD) (N=17). ФИГ. 21B изображает пиковые уровни аналита крови в образцах сыворотки от пациентов, имевших 3-месячный ответ SD/PD (N=31), по сравнению с пациентами, у которых был 3-месячный ответ CR/PR (N=35). Единицы были следующими: CRP (мг/л), SAA-1 (мг/л) и цитокины (пг/мл).
[0202] ФИГ. 22 изображает частоту объективных ответов (ORR) в месяц 3 среди подгрупп получающих лечение пациентов с 95%-м доверительным интервалом.
[0203] ФИГ. 23А и 23B изображают продолжительность ответа (DOR) для полного контингента (ФИГ. 23A) и основного контингента (ФИГ. 23B) и ФИГ. 23C и 23D изображают полное выживание для полного контингента (ФИГ. 23C) и основного контингента (23D ФИГ.), пациентов, которые достигли CR, PR, всех пациентов, показавших ответ, неотвечающих пациентов и все получающих лечение пациентов. Медианный F/U составлял 6,3 месяцев в течение ответа.
[0204] ФИГ. 24 показывает процент пациентов, испытавших нежелательные явления, возникшие в процессе лечения (TEAE) в контингенте FULL DLBCL, имевшие место у ≥20% пациентов. Данные для 5 пациентов с MCL, получавшие лечение продуктом в DL1 по меньшей мере с 28 днями наблюдения, не были включены. b: Одно AE Степени 5 в форме септического шока, не связанного с введением CAR+ Т-клеток. c: Одно AE Степени 5 в форме диффузного альвеолярного повреждения, по оценке исследователя, связанного с флударабином, циклофосфамидом и CAR+ Т-клетками, произошло в день 23 у пациента, отказавшегося от искусственной вентиляции для прогрессивного нарушения дыхания, демонстрирующего нейтропению на факторах роста и антибиотиках широкого спектра действия и противогрибковых средствах. d: Лабораторные аномалии.
[0205] ФИГ. 25 показывает процент пациентов, у которых развились CRS или нейротоксичность в течение времени в полном контингенте.
[0206] ФИГ. 26 показывает диаграммы, показывающие чистоту Т-клеток композиций Т-клеток, обогащенных CD4+ и CD8+ клетками на различных стадиях процесса генерации композиций генно-инженерных клеток, содержащих CAR Т-клетки, которые описаны в Примере 8. Показана частота (% общих лейкоцитов) CD4+ и CD8+ клеток в композициях.
[0207] ФИГ. 27A-27C показывают диаграммы, показывающие концентрацию (ФИГ. 27A), жизнеспособность (ФИГ. 27B) и частоту каспаза-3 негативных (ФИГ. 27C) CD4+ и CD8+ CAR+ Т-клеток в составах композиций терапевтических клеток высокого или низкого объема.
[0208] ФИГ. 28A показывает число CD3+ CAR+ Т-клеток, присутствующих в композициях CAR Т-клеток для введения в DL1 и DL2. ФИГ. 28B показывает число CD4+CAR+ и CD8+CAR+ клеток и CD4+CAR+TNF-α+ клеток и CD8+CAR+TNF-α+ клеток, присутствующих в композициях CAR Т-клеток для введения в DL1 и DL2.
[0209] ФИГ. 29 показывает процент пациентов, испытавших нежелательные явления в процессе лечения (TEAE) в контингенте FULL DLBCL, имевшие место у ≥20% пациентов в момент времени, описанный в Примере 6. Данные для 6 пациентов с MCL, получавших лечение продуктом в DL1 по меньшей мере с 28 днями наблюдения, не были включены. b: Одно AE Степени 5 в форме септического шока, не связанного с введением CAR+ Т-клеток, произошло при прогрессии заболевания. c: Одно AE Степени 5 в форме диффузного альвеолярного повреждения, по оценке исследователя, связанное с флударабином, циклофосфамидом и CAR+ Т-клетками, произошло в день 23 у пациента, отказавшегося от искусственной вентиляции для прогрессивного нарушения дыхания, демонстрирующего нейтропению на факторах роста и антибиотиках широкого спектра действия и противогрибковых средствах. d: Лабораторные аномалии.
[0210] ФИГ. 30 изображает частоту объективных ответов (ORR) за шесть (6) месяцев среди подгрупп получающих лечение пациентов с 95%-м доверительным интервалом. аВключает всех пациентов с DLBCL, получавших лечение со всеми уровнями дозы в основном контингенте.
[0211] ФИГ. 31А и 31B изображает продолжительность ответа (DOR) для полного контингента (ФИГ. 31A) и основного контингента (ФИГ. 31B), и ФИГ. 31C и 31D изображают полное выживание для полного контингента (ФИГ. 31C) и основного контингента (ФИГ. 31D), для пациентов, которые достигли CR, PR, всех пациентов, показавших ответ, неотвечающих пациентов и всех получающих лечение пациентов. NE, не поддается оценке.
Подробное описание
I. Способы и применения клеточной терапии с генно-инженерными клетками
[0212] Изобретение относится к способам и применениям генно-инженерных клеток (например, Т-клеток) и/или их композиции для лечения пациентов, имеющих заболевание или состояние, которое обычно представляет собой или включает рак или опухоль, такую как лейкоз или лимфома, в частности, неходжкинская лимфома (NHL). В некоторых аспектах способы и применения обеспечивают или достигают улучшенного ответа и/или более длительных ответов или эффективности и/или сниженного риска токсичности или других побочных эффектов, например, в определенных группах получающих лечение пациентов по сравнению с некоторыми альтернативными методами. В некоторых вариантах осуществления способы являются выгодными на основании введения конкретных чисел или относительных количеств генно-инженерных клеток, введения определенных отношений определенных типов клеток, лечения определенной популяции пациентов, таких как те, которые имеют определенный профиль риска, стадию и/или предшествующую историю лечения и/или комбинации этого. Изобретение также относится к способам, включающим оценку определенных параметров, например, экспрессии определенных биомаркеров или аналитов, которые могут коррелировать с развитием токсичности, и способам лечения, например, интервенционной терапии, для предотвращения и/или облегчения токсичности. Изобретение также относится к способам, включающим оценку определенных параметров, например, экспрессии определенных биомаркеров или аналитов, которые могут коррелировать с результатом, таким как терапевтический результат, включая ответ, такой как полный ответ (CR) или частичный ответ (PR), необязательно длительный ответ, такой как ответ, который длится в течение по меньшей мере 3 месяцев, 6 месяцев или более; или результат в отношении безопасности, такой как развитие токсичности, например, нейротоксичности или CRS, после введения иммунотерапии и/или клеточной терапии. Изобретение также относится к способам оценки вероятности ответа и/или вероятности риска токсичности, на основе оценки параметров, таких как экспрессия биомаркеров или аналитов. Изобретение также относится к композициям для использования в клеточной терапии. Изобретение также относится к изделиям и наборам, например, для использования в способах по изобретению. В некоторых вариантах осуществления изделия и наборы необязательно содержат инструкции по применению согласно способам по изобретению.
[0213] В некоторых вариантах осуществления способы и применения включают введение пациенту клеток, экспрессирующих генно-инженерные (рекомбинантные) рецепторы поверхности клеток в адоптивной клеточной терапии, которые обычно являются химерными рецепторами такими как химерные антигенные рецепторы (CAR), распознающими антиген, экспрессируемый, связанный с и/или специфичный для лейкоза или лимфомы и/или типа клетки, из которого он(а) происходит. Клетки обычно вводят в композиции, составленной для введения; способы обычно включают введение одной или более доз клеток пациенту, причем доза(ы) может включать определенное число или относительное число клеток или генно-инженерных клеток, и/или определенное отношение или композиции двух или более подтипов в композиции, например, CD4 по отношению к CD8 Т-клеткам.
[0214] В некоторых вариантах осуществления клетки, популяции и композиции вводят пациенту, имеющему определенное заболевание или состояние, подлежащее лечению, например, путем адоптивной клеточной терапии, такой как адоптивная T-клеточная терапия. В некоторых вариантах осуществления способы включают лечение пациента, имеющего лимфому или лейкоз, такую как неходжкинская лимфома (NHL), дозой клеток, экспрессирующих рецептор антигена (например, CAR-экспрессирующих клеток).
[0215] В некоторых вариантах осуществления способы по изобретению включают лечение определенной группы или субпопуляции пациентов, например, пациентов, идентифицированных как имеющие высокий риск заболевания, например, высокий риск NHL. В некоторых аспектах способы используют для лечения пациентов, имеющих агрессивную и/или с неблагоприятным прогнозом форму В-клеточной неходжкинской лимфомы (NHL), такой как NHL, которая является рецидивирующей или рефрактерной (R/R) к стандартной терапии, имеет неблагоприятный прогноз. В некоторых случаях, частота общего ответа (ОРР; также известный в некоторых случаях как частота объективного ответа) на доступные терапии, стандартные способы или эталонные терапии для заболевания и/или популяции пациентов, для которых эта терапия показана, составляет менее 40% и/или полный ответ (CR; также известный в некоторых случаях как полная ремиссия) составляет менее 20%. В некоторых вариантах осуществления, в случае хеморефрактерной DLBCL, ОРР эталонным или доступным лечением или стандартной терапией составляет приблизительно 26%, и уровень CR составляет приблизительно 8% (Crump et al. Outomes in refractory aggressive diffuse large B-cell lymphoma (DLBCL): Results from the international SCHOLAR study. ASCO 2016 [Реферат 7516]). В некоторых аспектах способы по изобретению, композиции, применения и изделия достигают улучшенных и превосходящих ответов по сравнению с доступными терапиями.
[0216] В некоторых вариантах осуществления способы, применения и изделия включают или используются для лечения пациентов, включая отбор или идентификацию определенной группы или субпопуляции пациентов, например, на основе определенных типов заболевания, диагностических критериев, предшествующих лечений и/или реакции на предшествующие лечения. В некоторых вариантах осуществления способы включают лечение пациента с рецидивом после ремиссии после лечения с, или ставшего рефраткерным к ним, одной или более предшествующих методов лечения; или пациент, который рецидивирующая или является невосприимчивым (R/R) к одному или более предшествующих терапий, например, одной или более линиям стандартной терапии. В некоторых вариантах осуществления способы включают лечение пациентов, имеющих диффузную крупноклеточную В-клеточную лимфому (DLBCL), неуточненную (NOS; de novo и трансформированную из вялотекущей), первичную медиастинальную В-клеточную лимфому (PMBCL) или фолликулярную лимфому, такую как фолликулярная лимфома стадии 3B (FL3B). В некоторых вариантах осуществления способы включают лечение пациента, имеющего Eastern Cooperative Oncology Group Performance Status (ECOG) 0-1 или 0-2. В некоторых вариантах осуществления способы используются для лечения популяций с неблагоприятным прогнозом или пациентов с DLBCL, или пациентов, которые обычно плохо отвечают на терапии или определенные эталонные терапии, таких как имеющие одну или более, например, две или тре хромосомных транслокаций (таких как так называемая лимфома «double-hit» или «triple-hit»; имеющих транслокации локусов MYC/8q24, обычно в комбинации с t(14; 18) (q32; q21)bcl-2 геном или/и хромосомной транслокацией BCL6/3q27; см., например, Xu et al. (2013) Int J Clin Exp Pathol. 6(4): 788-794), и/или пациентов с рецидивом, необязательно рецидивом в течение 12 месяцев, после введения трансплантата аутологичных стволовых клеток (ASCT), и/или пациентов, определенных как хеморефрактерные.
[0217] В некоторых аспектах варианты осуществления изобретения основываются на наблюдениях, что способы по изобретению могут использоваться для достижения высокой частоты ответов с высокой длительностью по сравнению с некоторыми доступными способами клеточной терапии, без повышенного риска токсичности. В некоторых вариантах осуществления способы по изобретению обеспечивают пролонгированную персистенцию адоптивно перенесенных клеток для клеточной терапии и/или низкий процент развития токсичности у пациента. В некоторых вариантах осуществления способы могут использоваться для отбора для лечения клеточной терапией пациентов, которые, вероятно или более вероятно, ответят на терапию и/или определения подходящих доз или режима дозирования для более высокой частоты ответа и/или более длительного ответа при уменьшении риска токсичности. Такие способы могут обеспечить рациональные стратегии для облегчения безопасного и эффективного клинического применения адоптивной клеточной терапии, такой как CAR-T-клеточная терапия.
[0218] В некоторых вариантах осуществления антигенный рецептор (например, CAR) специфично связывается с антигеном-мишенью, ассоциированным с заболеванием или состоянием, таким как ассоциированный с NHL. В некоторых вариантах осуществления антиген, ассоциированный с заболеванием или нарушением, выбирают из CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Igкаппа, Igлямбда, CD79a, CD79b или CD30.
[0219] В некоторых вариантах осуществления способы включают введение клеток или композиции, содержащей клетки, пациенту, в ткань или клетку, такому как имеющий, подвергающийся риску или подозреваемый в наличии заболевания, состояния или нарушения. В некоторых вариантах осуществления пациентом является взрослый пациент. В некоторых вариантах осуществления пациент имеет возраст приблизительно 30, 40, 50, 60 или 70 лет или выше.
[0220] В некоторых вариантах осуществления способы включают введение клеток пациенту, выбранному или идентифицированному как имеющий определенный прогноз или риск NHL. Неходжкинская лимфома (NHL) может быть вариативным заболеванием. Некоторые пациенты с NHL могут оставаться в живых без лечения, в то время как другие могут потребовать немедленного вмешательства. В некоторых случаях пациенты с NHL могут быть классифицированы в группы, которые могут сообщить прогноз заболевания и/или рекомендуемую стратегию лечения. В некоторых случаях эти группы могут быть группами «низкого риска», “промежуточного риска”, «высокого риска» и/или «очень высокого риска», и пациенты могут быть классифицированы в них в зависимости от многих факторов, включая, но не ограничиваясь этим, генетические аномалии и/или морфологические или физические свойства. В некоторых вариантах осуществления пациентов, получающих лечение в соответствии со способами и/или с изделиями или композициями, классифицироуют или идентифицируют на основе риска NHL. В некоторых вариантах осуществления пациентом является пациент, имеющий высокий риск NHL.
[0221] В некоторых вариантах осуществления пациент ранее проходил лечение терапией или терапевтическим агентом, нацеливаемым на заболевание или состояние, например, NHL, до введения клеток, экспрессирующих рекомбинантный рецептор. В некоторых вариантах осуществления пациент ранее проходил лечение трансплантацией гематопоэтических стволовых клеток (HSCT), например, аллогенных HSCT или аутогенных HSCT. В некоторых вариантах осуществления пациент имел неблагоприятный прогноз после лечения стандартной терапией и/или не имел положительного результата после одной или более линий предыдущей терапии. В некоторых вариантах осуществления пациент проходил лечение или ранее получал по меньшей мере или приблизительно по меньшей мере или приблизительно 1, 2, 3 или 4 других терапий для лечения NHL кроме противолимфоцитарной терапии и/или дозы клеток, экспрессирующих антигенный рецептор. В некоторых вариантах осуществления пациент ранее проходил лечение радиационной терапией или химиотерапией. В некоторых аспектах пациент является рефрактерным или нечувствительным к другой терапии или терапевтическому агенту. В некоторых вариантах осуществления пациент имеет постоянное или рецидивирующее заболевание, например, после лечения другой терапией или терапевтическим вмешательством, включая химиотерапию или радиацию.
[0222] В некоторых вариантах осуществления пациентом является пациент, имеющий право на трансплантацию, такой как имеющий право на трансплантацию гематопоэтических стволовых клеток (HSCT), например, аллогенных HSCT. В некоторых таких вариантах осуществления пациент ранее не получал трансплантацию, несмотря на то, что имел на это право, до введения генно-инженерных клеток (например, клеток CAR-T) или композиции, содержащей клетки, пациенту, как предусмотрено в настоящем изобретении.
[0223] В некоторых вариантах осуществления пациентом является пациент, который не имеет право на трансплантацию, является таким как не имеющий право на трансплантацию гематопоэтических стволовых клеток (HSCT), например, аллогенных HSCT. В некоторых вариантах осуществления такому пациенту вводят генно-инженерные клетки (например, клетки CAR-T) или композицию, содержащую клетки согласно вариантам осуществления изобретения.
[0224] В некоторых вариантах осуществления способы включают введение клеток пациенту, выбранному или идентифицированному как имеющий высокий риск NHL. В некоторых вариантах осуществления пациент показывает одну или более цитогенетических патологий, таких как связанная с высоким риском NHL. В некоторых вариантах осуществления пациент выбран или идентифицирован на основе наличия заболевания или состояния, характеризуемого как или определенного как агрессивная NHL, диффузная крупноклеточная В-клеточная лимфома (DLBCL), первичная медиастинальная крупноклеточная В-клеточная лимфома (PMBCL), Т-клеточная/гистоцит-обогащенная крупноклеточная В-клеточная лимфома (TCHRBCL), лимфома Беркитта, мантийноклеточная лимфома (MCL) и/или фолликулярная лимфома (FL). В некоторых вариантах осуществления пациент, который может подвергаться лечению с помощью способов по изобретению, включают пациентов с агрессивной NHL, в частности с диффузной крупноклеточной В-клеточной лимфомой (DLBCL), неуточненной (NOS; de novo и трансформированной из вялотекущей), первичной медиастинальной В-клеточной лимфомой (PMBCL) или фолликулярной лимфомой стадии 3B (FL3B). В некоторых вариантах осуществления пациент имеет статус неудовлетворительного лечения. В некоторых аспектах популяция, которую подвергают лечению, включает пациентов, имеющих Eastern Cooperative Oncology Group Performance Status (ECOG), который составляет от 0-2. В других аспектах любого из вариантов осуществления, пациенты, которых подвергают лечению, включают пациентов с ECOG 0-1 или не включают пациентов с ECOG 2. В некоторых аспектах любого из вариантов осуществления пациенты, которых подвергают лечению, не добились положительных результатов после двух или более предшествующих терапий. В некоторых вариантах осуществления пациент не имеет DLBCL, трансформированной из лимфомы маргинальной зоны (MZL) и хронического лимфолейкоза (CLL; Рихтер). В некоторых вариантах осуществления пациент с CLL может демонстрировать синдром Рихтера (RS), определяемый как трансформация CLL в агрессивную лимфому, обычно диффузную крупноклеточную В-клеточную лимфому (DLBCL) (см., например, Parikh et al. Blood 2014 123:1647-1657). В некоторых вариантах осуществления пациент имеет мантийноклеточную лимфому (MCL). В некоторых вариантах осуществления пациент имеет признаки, коррелирующие с низкой общей выживаемостью. В некоторых вариантах осуществления пациент никогда не достигал полного ответа (CR), никогда не получал трансплантацию аутогенных стволовых клеток (ASCT), является рефрактерным к 1 или более терапиям второй линии, имеет первичное рефрактерное заболевание и/или имеет индекс состояния ECOG 2.
[0225] В некоторых вариантах осуществления пациент, которого подвергают лечению, включает группу пациентов с диффузной крупноклеточной В-клеточной лимфомой (DLBCL), de novo или трансформированной из вялотекущей лимфомы (NOS), первичной медиастинальной крупноклеточной В-клеточной лимфомой (PMBCL) и фолликулярной лимфомой стадии 3B (FL3B) после неудачи 2 линий терапии и оценку ECOG 0-2, и пациент мог необязательно ранее получать трансплантацию алогенных стволовых клеток (SCT). В некоторых вариантах осуществления такая группа пациентов может упоминаться как “полный контингент”. В некоторых вариантах осуществления пациент выбран для лечения адоптивной клеточной терапией, если пациент соответствует указанным критериям. В некоторых вариантах осуществления в указанной группе (“полный контингент”) пациент не выбран для лечения или исключен из лечения, если пациент имеет неудовлетворительный статус (например, ECOG 2) и/или имеет DLBCL, трансформированную из лимфом маргинальной зоны (MZL) и хронического лимфолейкоза (CLL, Рихтер). Таким образом, в некоторых вариантах осуществления, пациент выбран для лечения, если пациент имеет пациентов с диффузной крупноклеточной В-клеточной лимфомой (DLBCL), de novo или трансформированной из вялотекущей лимфомы (NOS), первичной медиастинальной крупноклеточной В-клеточной лимфомой (PMBCL) и фолликулярной лимфомой стадии 3B (FL3B) после неудачи 2 линий терапии и с оценкой ECOG 0 или 1, и пациент мог необязательно ранее получать трансплантацию алогенных стволовых клеток (SCT), но не имеет DLBCL, трансформированной из лимфом маргинальной зоны (MZL) и хронического лимфолейкоза (CLL, Рихтер). В некоторых вариантах осуществления такая группа пациентов может упоминаться как “основной контингент”. В некоторых вариантах осуществления пациентом, получающим лечение, являются пациенты в “основном контингенте”.
[0226] В некоторых аспектах варианты осуществления изобретения основываются на наблюдениях, что некоторые популяции пациентов, например, паиценты “основного контингента”, которым вводят определенную дозу клеточной терапии, демонстрируют частоту общего ответа (ORR) более 80%, причем частота полного ответа (CR) составляет более 55%, с высокой длительностью, например, ответ, сохраняющийся в течение более длительного промежутка времени, например, более чем 3 месяца, с 3-месячным ОРР более 65% и 3-месячным уровнем CR приблизительно 50%. В частности, наблюдения показали, что 3-месячный ОРР был высок у пациентов с двумя или тремя хромосомными транслокациями («double-hit» или «triple-hit» лимфома; имеющих транслокации в локусах MYC/8q24, обычно в комбинации с t(14; 18)(q32; q21)bcl-2 геном или/и хромосомной транслокацией BCL6/3q27; см., например, Xu et al. (2013) Int J Clin Exp Pathol. 6(4): 788-794), первично рефрактерные лимфомы, хеморефрактерную DLBCL, и пациенты, которые ранее никогда не достигали CR.
[0227] В некоторых аспектах изобретение относится к композициям, способам и применениям для введения определенной композиции клеточной терапии, в определенных дозах, связанных с высокой частотой ответа и/или высокой длительностью ответа и низкими уровнями и/или частотой токсичности. В некоторых вариантах осуществления введенная композиция или доза представляют собой плоскую и/или фиксированную дозу, такую как точная плоская доза, клеток и/или одной или более клеток, имеющих определенный фенотип, такая как определенное число таких клеток или число, которое находится в определенном диапазоне и/или степени вариабельности или различия по сравнению с целевым числом. В некоторых вариантах осуществления, введенная композиция или доза содержит определенное отношение CD4+ и CD8+ клеток (например, отношение 1:1 CD4+: CD8+ CAR+ Т-клетки), и/или содержит отношение, которое находится в определенной степени вариабельности от такого отношения, такой как не более чем+10%, такой как не более чем+8%, такой как степень вариабельности или различие не более чем+10%, такой как не более чем+8%. В некоторых вариантах осуществления, CD4+ и CD8+ клетки индивидуально составляют и вводят. В некоторых вариантах осуществления вводимые клетки показывают согласующуюся активность и/или функцию, например, продукции цитокинов, апоптоза и/или роста. В некоторых вариантах осуществления композиции по изобретению показывают очень согласующуюся и определенную активность и низкую вариабельность между клетками, например, с точки зрения числа клеток, функции клеток и/или активности клеток, в композиции или между препаратами. В некоторых вариантах осуществления соглсованность в активности и/или функции, например, низкая вариабельность между препаратами композиций, позволяет усилить эффективность и/или безопасность. В некоторых вариантах осуществления введение определенных композиций приводит к низкой вариабельности продукта и низкой токсичности, например, CRS или нейротоксичности, по сравнению с введением композиций клеток с высокой гетерогенностью. В некоторых вариантах осуществления определенная согласующаяся композиция также показывает согласующийся рост клеток. Такая согласованность может облегчить идентификацию дозы, терапевтического окна, оценки доза-ответ и идентификации факторов пациента, которые могут коррелировать с результатами безопасности или токсичности.
[0228] В некоторых вариантах осуществления, в определенном контингенте пациентов, получающих единственное вливание определенного уровня дозы, может быть достигнута частота длительных ответов через 6 месяцев более 60%. В некоторых вариантах осуществления пациенты в некоторых контингентах могут достигать общей частоты ответов (ОРР, в некоторых случаях также известная как частота объективного ответа) более 80%, частоты полного ответа (CR) более 60% и/или высокого длительного уровня CR в 6 месяцев. В некоторых вариантах осуществления пациенты, получающие определенную дозу, показывают улучшенные результаты безопасности, например, более двух третей пациентов не показывают CRS или NT. В некоторых аспектах уровень тяжелого CRS или тяжелой NT является низким. В некоторых вариантах осуществления, более высокая экспозиция (например, AUC0-28 и AUC0-28), наблюдаемая с особой определенной дозой, не ассоциируется с увеличенной токсичностью, например, CRS или NT. В некоторых вариантах осуществления особые факторы пациента, например, некоторые биомаркеры, могут использоваться для предсказания риска токсичности. В некоторых вариантах осуществления варианты осуществления изобретения могут использоваться для достижения высокой частоты ответа с низким риском токсичности.
[0229] В некоторых вариантах осуществления, не более чем 25%, не более чем 20%, не более чем 15%, не более чем 10% или не более чем 5% пациентов, получающих лечение с помощью композиций, изделий, наборов, способов и применений по изобретению, вводят агент (например, тоцилизумаб и/или дексаметазон), чтобы облегчить, вылечить или предотвратить токсичность как до, так и после введения клеточной терапии. В некоторых вариантах осуществления пациенту не назначают никакого профилактического лечения до получения генно-инженерных клеток (например, клеток CAR-T).
[0230] В некоторых вариантах осуществления варианты осуществления изобретения обеспечивают преимущество, например, позволяя проводить клеточную терапию на амбулаторной основе. В некоторых вариантах осуществления введение клеточной терапии, например, дозы Т-клеток в соответствии с вариантами осуществления изобретения, может быть осуществлено на амбулаторной основе или не требует допуска пациента в больницу, такого как допуск в больницу, требующую ночного пребывания. В некоторых вариантах осуществления такое амбулаторное введение может обеспечить увеличенный доступ и уменьшенные затраты при поддержании высокой длительной частоты ответа с низкой токсичностью. В некоторых аспектах амбулаторное лечение может быть выгодным для пациентов, которые уже имеют ослабленный предшествующими лечениями иммунитет, например, после лимфодеплеции, и подвергаются большему риску инфицирования при пребывании в больнице или в режиме стационара. В некоторых аспектах амбулаторные лечения также увеличивают возможности для лечения пациентов, которые могут не иметь доступа к стационару, стационарному режиму или центрам трансплантации, таким образом расширяя доступ к лечению. В некоторых вариантах осуществления пациенты, получающие лечение на амбулаторной основе с помощью композиций, изделий, наборов, способов и применений по изобретению, остаются на амбулаторном режиме в течение по меньшей мере 3 дней, или определенный процент пациентов, например, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% паицентов остаются на амбулаторном режиме в течение по меньшей мере 3 дней. В некоторых аспектах пациенты остаются на амбулаторном режиме в течение по меньшей мере 4 дней, 5 дней, 6 дней, 7 дней, 8 дней или более. В некоторых вариантах осуществления пациентов, получающие лечение с использованием композиций, изделий, наборов, способов и применений по изобретению, показывают уменьшение продолжительности пребывания в больнице, например, на по меньшей мере 10%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 30%, по меньшей мере 35% или по меньшей мере 40%, по сравнению с пациентами, получающими лечение другими композициями, изделиями, наборами, способами и применениями.
[0231] В некоторых вариантах осуществления способы, клетки и композиции могут обеспечить пациенту высокий показатель длительного ответа через ряд характеристик пациента и/или опухолевой массы. В некоторых вариантах осуществления способы, клетки и композиции могут обеспечить высокий показатель длительного ответа для пациента с высоким риском с неблагоприятным прогнозом, со сниженным риском неблагоприятных эффектов или токсичности. В некоторых вариантах осуществления способы и применения обеспечивают или достигают более высокой частоты ответа и/или более длительных ответов или эффективности и/или сниженного риска токсичности или других побочных эффектов, которые могут быть связаны с клеточной терапией, таких как нейротоксичность (NT) или синдром высвобождения цитокинов (CRS). В некоторых аспектах наблюдения показали низкий процент тяжелой NT (sNT) или тяжелого CRS (sCRS), и высокий показатель пациентов без какой-либо токсичности, например, NT или CRS.
[0232] В некоторых вариантах осуществления по меньшей мере 35%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70% или по меньшей мере 75% или более пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, достигают полного ответа (CR). В некоторых вариантах осуществления по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90% пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, достигают объективного ответа (OR). В некоторых вариантах осуществления по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или более пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, достигают CR или OR в течение одного месяца, двух месяцев или трех месяцев.
[0233] В некоторых вариантах осуществления, в течение трех месяцев, четырех месяцев, пяти месяцев, шести месяцев или более после инициации введения клеточной терапии, у по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или более пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, сохраняется ответ, такой как CR или OR. В некоторых вариантах осуществления такой ответ, такой как CR или OR, длится в течение по меньшей мере трех месяцев, четырех месяцев, пяти месяцев, шести месяцев, семи месяцев, восьми месяцев или девяти месяцев, например, у по меньшей мере или приблизительно по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или более пациентов, получающих лечение согласно способам по изобретению, или у таких пациентов, которые достигают CR за один месяц или за три месяца. В некоторых вариантах осуществления по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или более пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, или таких пациентов, которые достигают CR за один месяц или за три месяца, остаются в живых или остаются в живых без прогрессии в течение более чем или более чем приблизительно три месяца, четыре месяца, пять месяцев, шесть месяцев, семь месяцев, восемь месяцев или девять месяцев.
[0234] В некоторых вариантах осуществления полученный ответ, наблюдаемый у таких пациентов при лечении в соответствии со способами по изобретению, и/или с использованием изделий или композиций по изобретению, связан с или приводит к низкому риску какой-либо токсичности или низкому риску тяжелой токсичности у большинства получающих лечение пациентов. В некоторых вариантах осуществления, более чем или более чем приблизительно 30%, 35%, 40%, 50%, 55%, 60% или более пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, не показывают какой либо степени CRS или какой либо степени нейротоксичности (NT). В некоторых вариантах осуществления, более чем или более чем приблизительно 50%, 60%, 70%, 80% или более пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, не показывают тяжелого CRS или CRS степени 3 или выше. В некоторых вариантах осуществления, более чем или более чем приблизительно 50%, 60%, 70%, 80% или более пациентов, получающих лечение согласно способам по изобретению и/или с использованием изделий или композиций по изобретению, не показывают тяжелую нейротоксичность или нейротоксичность степени 3 или более высокой, такой как нейротоксичности степени 4 или 5.
[0235] В некоторых вариантах осуществления, по меньшей мере или приблизительно 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% пациентов, получающих лечение согласно способу и/или с использованием изделий или композиций по изобретению, не показывают раннее начало CRS или нейротоксичности и/или не показывают начало CRS ранее, чем через 1 день, 2 дня, 3 дня или 4 дня после инициации введения. В некоторых вариантах осуществления, по меньшей мере или приблизительно 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% пациентов, получающих лечение согласно способам и/или с использованием изделий или композиций по изобретению, не показывают начало нейротоксичности ранее, чем через 3 дня, 4 дня, 5 дней, шесть дней или 7 дней после инициации введения. В некоторых аспектах среднее начало нейротоксичности среди пациентов, получающих лечение согласно способам и/или с использованием изделий или композиций по изобретению, имеет место в момент или после медианного пика или медианного времениустранения CRS у пациентов, получающих лечение согласно способу. В некоторых случаях среднее начало нейротоксичности среди пациентов, получающих лечение согласно способу, имеет место через более чем или приблизительно 8, 9, 10 или 11 дней.
[0236] В некоторых вариантах осуществления такие результаты наблюдаются после введения от или от приблизительно 5 x 107 до 1,5 x 108, например, от 5 x 107 до 1 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток, таких как доза Т-клеток, включающих CD4+ и CD8+ Т-клетки, вводимые в определенном отношении, как описано здесь, например, в или приблизительно в отношении 1:1, и/или в точном или плоском, или постоянном числе CAR+ Т-клеток, или точном или плоском, или постоянном числе определенного типа CAR+ Т-клеток, таких как CD4+CAR+ Т-клетки и/или CD8+CAR+ Т-клетки, и/или числе любых из таких клеток, которое находится в указанной степени вариативности, например, не более чем+или - (плюс или минус, в некоторых случаях обозначено как ±) 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15% по сравнению с таким точным или плоским или постоянным числом. В некоторых вариантах осуществления такое плоское или постоянное число клеток составляет или приблизительно составляет 2,5 x 107, 5×107, 10 x 107, 15 x 107 или 20 x 107, например, общих CAR+ Т-клеток или CD8+ и/или CD4+ CAR+ Т-клеток. В некоторых вариантах осуществления число клеток в дозе включает или состоит из или состоит по существу из 5 x 107 CD4+CAR+ Т-клеток (необязательно 2,5 x 107 CD4+CAR+ Т-клеток и 2,5 x 107 CD8+CAR+ Т-клеток); в некоторых вариантах осуществления это число включает или состоит из или состоит по существу из 10 x 107 CAR+ Т-клеток (необязательно 5 x 107 CD4+CAR+ Т-клеток и 5 x 107 CD8+CAR+ Т-клеток). В некоторых аспектах число введенных клеток находится в определенной степени вариативности таких чисел в вышеупомянутых вариантах осуществления, например, в плюс или минус (±) 5, 6, 7, 8, 9 или 10%, например, в плюс или минус 8%, по сравнению с таким числом(лами) клеток. В некоторых аспектах доза находится в диапазоне, в котором наблюдается корреляция (необязательно линейное соотношение) между числом таких клеток (например, общих CAR+ Т-клеток или CD8+ и/или CD4+ CAR+ Т-клеток) и одним или более результатов, показательных для терапевтического ответа или его продолжительности (например, вероятность достижения ремиссии, полной ремиссии и/или определенной продолжительности ремиссии) и/или продолжительности любого из предшествующих. В некоторых аспектах обнаружено, что более высокая доза введенных клеток может приводить к более сильному ответу без или без существенного влияния или оказания влияния на уровень или риск токсичности (например, CRS или нейротоксичности) или степень уровня или риск токсичности у пациента, например, тяжелого CRS или тяжелой нейротоксичности.
[0237] В некоторых аспектах способы по изобретению могут достигать высокой или определенной частоты ответа (такого как частота ответа среди популяции, оцениваемая через определенный период после ведения, например, три месяца или шесть месяцев), например, ОРР (такого как 6-месячный или 3-месячный ОРР) 40% или более, 45% или более, 50% или более, 55% или более, 60% или более, 65% или более, 70% или более, 75% или 80% или 81%, 82%, 83%, 84% или 85% или более и уровень CR (такого как 6-месячный или 3-месячный уровень CR) 30% или более, 35% или более, 40% или более, 45% или более, 50% или более, 55% или более, 60% или более, 65% или более, 70% или более, 71%, 72%, 73% или более или приблизительно 75% или более, который также является длительным, например, в течение определенного промежутка времени или по меньшей мере определенного промежутка времени, например, длится в течение более чем 1, 3 или 6 месяцев или более или 9 месяцев или более после инициации терапии. В некоторых вариантах осуществления такие частота и длительность ответа получены после только единственного введения или дозы такой терапии. Лечение таких пациентов способами по изобретению и/или с использованием изделий или композиций по изобретению, в некоторых вариантах осуществления, также приводит к тому, что пациенты достигают высокой частоты ответа, не показывая при этом более высокий уровень развития токсичности, такой как нейротоксичность или CRS, даже при более высокой дозировке клеток. В некоторых вариантах осуществления, у приблизительно или более чем 50%, 55% или 60% пациентов, достигающих таких ответов, не развиваются степени токсичности, например, какой-либо степени CRS и/или нейротоксичности.
[0238] Таким образом, в некоторых вариантах осуществления, способы, изделия и/или композиции по изобретению могут обеспечить преимущества перед другими доступными способами или решениями, или подходами к лечению, такому как адоптивная клеточная терапия. В частности, среди вариантов осуществления изобретения можно назвать те, которые обеспечивают преимущество для пациентов с риском NHL, путем достижения длительного ответа с высокой частотой, со сниженным уровнем токсичности или побочных эффектов.
A. Способ лечения
[0239] Изобретение относится к способам лечения, включающим введение генно-инженерных клеток, или композициям, содержащим генно-инженерные клетки, такие как генно-инженерные Т-клетки. Изобретение также относится к способам и применениям генно-инженерных клеток (например, Т-клетки) и/или их композиций, включая способы лечения пациентов, имеющих заболевание или состояние, такое как лейкоз или лимфома, например, неходжкинская лимфома (NHL), включающие введение генно-инженерных клеток и/или их композиций. В некоторых вариантах осуществления способы и применения по изобретению могут достигать улучшенного ответа и/или более длительных ответов или эффективности, и/или сниженного риска токсичности или других побочных эффектов, например, в определенных группах получающих лечение пациентов, по сравнению с некоторыми альтернативными методами. В некоторых аспектах, изобретение также относится к способам введения генно-инженерных клеток или композиций, содержащих генно-инженерные клетки, такие как генно-инженерные Т-клетки, пациенту, такому как пациент, имеющий заболевание или нарушение. В некоторых аспектах изобретение также относится к использование генно-инженерных клеток или композиций, содержащих генно-инженерные клетки, такие как генно-инженерные Т-клетки для лечения заболевания или нарушения. В некоторых аспектах изобретение также относится к применениям генно-инженерных клеток или композиций, содержащих генно-инженерные клетки, такие как генно-инженерные Т-клетки, для получения лекарственного средства для лечения заболевания или нарушения. В некоторых аспектах изобретение также относится к способам введения генно-инженерных клеток или композиций, содержащих генно-инженерные клетки, такие как генно-инженерные Т-клетки, для применения в лечении заболевания или нарушения, или для введения пациенту, имеющему заболевание или нарушение. В некоторых аспектах, применения генно-инженерных клеток или композиций, содержащих генно-инженерные клетки, такие как генно-инженерные Т-клетки, находится в соответствии с любым из способов, описанных здесь.
[0240] Обычные способы для введения клеток для адоптивной клеточной терапии известны и могут использоваться в связи со способами и композициями по изобретению. Например, способы адоптивной T-клеточной терапии описаны, например, в Публикации No. 2003/0170238 Заявки на патент США на имя Gruenberg et al; Патенте США No. 4,690,915 на имя Rosenberg; Rosenberg (2011) Nat Rev Clin Oncol. 8(10):577-85). См., например, Themeli et al. (2013) Nat Biotechnol. 31(10): 928-933; Tsukahara et al. (2013) Biochem Biophys Res Commun 438(1): 84-9; Davila et al. (2013) PLoS ONE 8(4): e61338.
[0241] Подвергаемое лечениею заболевание или состояние могут быть любым, в котором экспрессия антигена связана с и/или участвует в этиологии болезненного состояния или нарушения, например, вызывает, усиливает или иным образом участвует в таком заболевании, состоянии или нарушении. Примеры заболеваний и состояний могут включать заболевания или состояния, связанные со злокачественной опухолью или трансформацией клеток (например, рак), аутоиммунное заболевание или воспалительное заболевание, или инфекционное заболевание, например, вызванное бактериальным, вирусным или другим патогеном. Примеры антигенов, включающие антигены, связанные с различными заболеваниями и состояниями, которые могут быть подвергнуты лечению, описаны выше. В некоторых вариантах осуществления, химерный антигенный рецептор или трансгенный TCR специфично связывается с антигеном, связанным с заболеванием или состоянием.
[0242] Среди заболеваний, состояний и нарушений можно назвать опухоли, включая солидные опухоли, гематологические злокачественные опухоли и меланомы, и включая локализованные и метастатические опухоли, инфекционные заболевания, такие как инфекция вируса или другого патогена, например, HIV, HCV, HBV, CMV, HPV, и паразитарное заболевание, и аутоиммунные заболевания и воспалительные заболевания. В некоторых вариантах осуществления, заболевание, нарушение или состояние представляет собой опухоль, рак, злокачественную опухоль, новообразование или другое пролиферативное заболевание или нарушение. Такие заболевания включают, но не ограничены ими, лейкоз, лимфому, например, острый миелоидный (или миелогенный) лейкоз (AML), хронический миелоидный (или миелогенный) лейкоз (CML), острый лимфоцитарный (или лимфообластный) лейкоз (ALL), хронический лимфолейкоз (CLL), волосатоклеточный лейкоз (HCL), лимфому из малых лимфоцитов (SLL), мантийноклеточную лимфому (MCL), лимфому маргинальной зоны, лимфому Беркитта, лимфому Ходжкина (HL), неходжкинскую лимфому (NHL), анапластическую крупноклеточную лимфому (ALCL), фолликулярную лимфому, рефрактерную фолликулярную лимфому, диффузную крупноклеточную В-клеточную лимфому (DLBCL) и множественную миелому (MM). В некоторых вариантах осуществления, заболевание или состояние представляет собой В-клеточную злокачественную опухоль, выбранную из числа острого лимфообластного лейкоза (ALL), ALL взрослых, хронического лимфообластного лейкоза (CLL), неходжкинской лимфомы (NHL) и диффузной крупноклеточной В-клеточной лимфомы (DLBCL). В некоторых вариантах осуществления, заболевание или состояние представляет собой NHL, и NHL выбрана из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), Т-клеточной/гистоцит-обогащенной крупноклеточной В-клеточной лимфомы (TCHRBCL), лимфомы Беркитта, мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B).
[0243] В некоторых вариантах осуществления NHL может быть подразделена на стадии на основе классификации Лугано (см., например, Cheson et al., (2014) JCO 32(27):3059-3067; Cheson, B.D. (2015) Chin Clin Oncol 4(1):5). В некоторых случаях стадии описываются Римскими цифрами I - IV (1-4), и лимфомы ограниченной стадии (I или II), поражающие орган вне лимфатической системы (экстранодальный орган) обозначены буквой E. Стадия I означает участие в одном узле или группе смежных узлов, или единственное экстранодальное поражение без центрального участия (IE). Стадия 2 означает участие в двух или более центральных группах на той же стороне диафрагмы или стадии I или II центральной степени с ограниченным смежным экстранодальным участием (IIE). Стадия III означает участие в узлах с обеих сторон диафрагмы или узлах выше диафрагмы с участием селезенки. Стадия IV означает участие в дополнительном экстралимфатическом участии состоящем из нескольких несмежных участков. Кроме того, “массивная лимфаденопатия” может использоваться для описания больших опухолей в груди, в частности, стадии II. Степень заболевания определяют эмиссионной позитронной томографией (PET) - компьютерной томографией (CT) для специфичных лимфом и CT для неспецифичных гистологий.
[0244] В некоторых вариантах осуществления индикатор Eastern Cooperative Oncology Group Performance Status (ECOG) может использоваться для оценки или выбора пациентов для лечения, например, пациентов, у которых был неудовлетворительный результат предшествующих терапий (см., например, Oken et al. (1982) Am J Clin Oncol. 5:649-655). Шкала ECOG Статуса производительности описывает уровень функционирования пациентов с точки зрения их способности заботиться о себе, ежедневной активности и физических способностей (например, ходьба, работа и т.д.). В некоторых вариантах осуществления статус производительности ECOG 0 указывает, что пациент может осуществлять нормальную активность. В некоторых аспектах пациенты со статусом производительности ECOG 1 демонстрируют некоторое ограничение в физической активности, но пациент является полностью амбулаторным. В некоторых аспектах пациенты со статусом производительности ECOG 2 являются более чем на 50% амбулаторными. В некоторых случаях пациент со статусом производительности ECOG 2 может также быть способен к уходу за собой; см., например, Sørensen et al., (1993) Br J Cancer 67(4) 773-775. Критерии, отражающие статус производительности ECOG, описаны в Таблице 1 ниже:
Таблица 1. Критерии статуса производительности ECOG
[0245] В некоторых вариантах осуществления пациент имеет или был идентифицирован как имеющий лимфому double/triple hit или лимфому молекулярных подтипов double/triple-hit. В некоторых вариантах осуществления лимфома является лимфомой double-hit, характеризуемой наличием генных перестановок (например, транслокаций) MYC (онкоген миелоцитоматоза), BCL2 (В-клеточная лимфома 2) и/или BCL6 (В-клеточная лимфома 6). В некоторых вариантах осуществления генная перестановка оказывает влияние на локус MYC/8q24 в комбинации с другой генной перестановкой. Например, другая генная перестановка включает t(14; 18)(q32; q21), включающий BCL2. В некоторых вариантах осуществления генные перестановки оказывают влияние на локус MYC/8q24 в комбинации с BCL6/3q27. В некоторых вариантах осуществления лимфома является лимфомой triple-hit, характеризуемой наличием генных перестановок MYC, BCL2 и BCL6; см., например, Aukema et al., (2011) Blood 117:2319-2331. В некоторых аспектах таких вариантов осуществления пациент является ECOG 0-1 или не имеет или не подозревается или не характеризуется как имеющий DLBCL, трансформированную из MZL или CLL. В некоторых аспектах терапия показана для таких пациентов, и/или инструкции указывают введение пациенту из такой популяции. В некоторых вариантах осуществления, на основе критериев 2016 WHO (Swerdlow et al., (2016) Blood 127 (20):2375-2390), лимфому double/triple hit можно считать высокодифференцированной В-клеточной лимфомой с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit).
[0246] В некоторых вариантах осуществления, заболевание или состояние представляет собой инфекционное заболевание или состояние, такое как, но не ограничиваясь ими, вирусные, ретровирусные, бактериальные и протозойные инфекции, иммуннодефицит, Цитомегаловируса (CMV), Вирус Эпштейна-Барр (EBV), аденовирус, полиомавирус BK. В некоторых вариантах осуществления, заболевание или состояние представляет собой аутоиммунное заболевание или воспалительное заболевание или состояние, такое как артрит, например, ревматоидный артрит (RA), диабет типа 1, системную красную волчанку (SLE), воспалительное заболевание кишечника, псориаз, склеродермию, аутоиммунное заболевание щитовидной железы, диффузный токсический зоб, болезнь Крона, рассеянный склероз, астму и/или заболевание или состояние, связанное с трансплантацией.
[0247] В некоторых вариантах осуществления антиген, связанный с заболеванием или нарушением, выбран из числа αvβ6 интегрина (avb6 интегрин), антигена созревания В-клеток (BCMA), B7-H3, B7-H6, карбоангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, антигена рака яичек 1B (CTAG, также известного как NY-ESO-1 и LAGE-2), карциноэмбрионального антигена (CEA), циклина, циклина A2, Лиганда 1 Хемокина Мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, хондроитин сульфат протеогликана 4 (CSPG4), белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфрина B2, рецептора эфрина A2 (EPHa2), эстрогенового рецептора, Fc-подобного рецептора 5 (FCRL5; также известного как гомолог Fc-рецептора 5 или FCRH5), эмбрионального рецептора ацетилхолина (эмбриональный AchR), фолат-связывающего белка (FBP), фолатного альфа-рецептора, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), глипикана-3 (GPC3), 5D рецептора, связанного с G-белком (GPCR5D), Her2/neu (рецепторной тирозинкиназы erb-B2), Her3 (erb-B3), HeR4 (erb-B4), димеров erbB, человеческого высокомолекулярного меланомаассоциированного антигена (HMW-MAA), поверхностного антигена гепатита B, антигена A1 лейкоцитов человека (HLA-A1), антигена A2 лейкоцитов человека (HLA-A2), альфа рецептора IL-22 (IL-22Rα), альфа рецептора IL-13 2 (IL-13Rα2), рецептора, содержащего домен вставки киназы (kdr), легкой каппа-цепи, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, содержащего богатые лейцином повторы члена А семейства 8 (LRRC8A), антигена Ley, меланома-ассоциированного антигена (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелина (MSLN), c-Met, мышиного цитомегаловируса (CMV), муцина 1 (MUC1), MUC16, лиганда члена D группы 2 естественных киллеров (NKG2D), мелана А (MART-1), молекулы адгезии нервных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простатоспецифического антигена, антигена стволовых клеток предстательной железы (PSCA), простатоспецифического мембранного антигена (PSMA), подобного рецепторной тирозинкиназе орфанного рецептора 1 (ROR1), сурвивина, трофобластного гликопротеина (TPBG, также известного как 5T4), опухолеассоциированного гликопротеина 72 (TAG72), Тирозиназа, отнесся белок 1 (TRP1, также известный как TYRP1 или gp75), тирозиназа-зависимого белка 2 (TRP2, также известного как допахром таутомераза, допахром дельта-изомераза или DCT), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора фактора роста эндотелия сосудов 2 (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфического или экспрессируемого патогеном антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекул и/или молекул, экспрессируемых HIV, HCV, HBV или другими патогенами. Антигены, на которые нацеливаются рецепторы в некоторых вариантах осуществления, включают антигены, ассоциированные с В-клеточной злокачественной опухолью, такие как любой из множества известных В-клеточных маркеров. В некоторых вариантах осуществления антиген представляет собой или включает CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Igкаппа, Igлямбда, CD79a, CD79b или CD30.
[0248] В некоторых вариантах осуществления антиген представляет собой или включает патоген-специфический или экспрессируемый патогеном антиген. В некоторых вариантах осуществления антиген является вирусным антигеном (таким как вирусный антиген из HIV, HCV, HBV и т.д.), бактериальными антигенами и/или паразитарными антигенами.
[0249] В некоторых вариантах осуществления клеточную терапию, например, адоптивную T-клеточную терапию, осуществляют аутологическим переносом, при котором клетки выделяют и/или иным образом получают от пациента, который должен получить клеточную терапию, или из образца, полученного из такого пациента. Таким образом, в некоторых аспектах, клетки получают от пациента, например, пациента, нуждающегося в лечении, и клетки после выделения и обработки вводят тому же пациенту.
[0250] В некоторых вариантах осуществления клеточную терапию, например, адоптивную T-клеточную терапию, осуществляют аллогенным переносом, при котором клетки выделяют и/или иным образом получают от пациента, отличного от пациента, который должен получить или который в конечном счете получает клеточную терапию, например, первого пациента. В таких вариантах осуществления клетки затем вводят другому пациенту, например, второму пациенту, того же вида. В некоторых вариантах осуществления первые и вторые пациенты генетически идентичны. В некоторых вариантах осуществления первые и вторые пациенты генетически подобны. В некоторых вариантах осуществления второй пациент экспрессирует тот же класс или супертип HLA, что и первый пациент.
[0251] Клетки могут быть введены любыми подходящими средствами, например, болюсным вливанием, инъекцией, например, внутривенными или подкожными инъекциями, внутриглазной инъекцией, периокулярной инъекцией, подсетчаточной инъекцией, интравитреальной инъекцией, транссептальной инъекцией, подсклеральной инъекцией, внутрихориоидальной инъекцией, внутрикамеральной инъекцией, субконъюнктивальной инъекцией, подконъюнктивальной инъекцией, субтеноновой инъекцией, ретробульбарной инъекцией, перибульбарной инъекцией или задней околосклеральной доставкой. В некоторых вариантах осуществления их вводят парентеральным, интрапульмонарным и интраназальным, и, если требуется местное лечение, внутриочаговым введением. Парентеральные вливания включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. В некоторых вариантах осуществления вводимую дозу вводят единственным болюсным введением клеток. В некоторых вариантах осуществления ее вводят многократными болюсными введениями клеток, например, в течение не более чем 3 дней, или непрерывным инфузионным введением клеток. В некоторых вариантах осуществления, введение дозы клеток или любых дополнительных терапий, например, противолимфоцитарной терапии, интервенционной терапии и/или комбинированной терапии, осуществляют амбулаторной доставкой.
[0252] Для профилактики или лечения заболевания подходящая дозировка может зависеть от типа заболевания, которое подвергают лечению, типа клеток или рекомбинантных рецепторов, серьезности и течения заболевания, того, вводят ли клетки в профилактических или терапевтических целях, предыдущей терапии, истории болезни пациента и ответа на клетки, и усмотрения лечащего врача. Композиции и клетки в некоторых вариантах осуществления предпочтительно вводят пациенту однократно или серией лечений.
[0253] В некоторых вариантах осуществления клетки вводят как часть комбинированного лечения, такого как одновременно с или последовательно с, в любом порядке, другим или дополнительным терапевтическим вмешательством, таким как антитело или генно-инженерная клетка или рецептор, или агент, такой как цитотоксический или терапевтический агент. Клетками в некоторых вариантах осуществления вводят совместно с одним или более дополнительными терапевтическими агентами или в связи с другим терапевтическим вмешательством, одновременно или последовательно в любом порядке. В некоторых вариантах осуществления дополнительный терапевтический агент является любыми вмешательствами или агентами, описанными здесь, такими как любые описанные вмешательства или агенты, которые могут облегчить симптомы токсичности, описанные здесь, например, в Разделе II. В некоторых контекстах клетки вводят совместно с другой терапией с достаточно малыми интервалами таким образом, что популяция клеток усиливает эффект одного или более дополнительных терапевтических агентов, или наоборот. В некоторых вариантах осуществления клетки вводят до одного или более дополнительных терапевтических агентов. В некоторых вариантах осуществления клетки вводят после одного или более дополнительных терапевтических агентов. В некоторых вариантах осуществления один или более дополнительных агентов включают цитокин, такой как IL-2, например, для улучшения персистирования. В некоторых вариантах осуществления способы включают введение химиотерапевтического агента.
[0254] В некоторых вариантах осуществления способы включают введение химиотерапевтического агента, например, кондиционирующего химиотерапевтического агента, например, для уменьшения опухолевой массы до введения.
[0255] Предварительное кондиционирование пациентов иммунодеплецирующей (например, лимфодеплецирующей) терапией в некоторых аспектах может усилить эффекты адоптивной клеточной терапии (ACT).
[0256] Таким образом, в некоторых вариантах осуществления, способы включают введение агента для предварительного кондиционирования, такого как агент для лимфодеплеции, или химиотерапевтического агента, такого как циклофосфамид, флударабин, или их комбинаций, пациенту до инициации клеточной терапии. Например, пациенту может быть введен агент для предварительного кондиционирования по меньшей мере за 2 дня, например, по меньшей мере 3, 4, 5, 6 или 7 дней, предшествующих инициации клеточной терапии. В некоторых вариантах осуществления пациенту вводят агент для предварительного кондиционирования не более чем за 7 дней, например, не более чем 6, 5, 4, 3 или 2 дней, предшествующие инициации клеточной терапии.
[0257] В некоторых вариантах осуществления пациента предварительно кондиционируют циклофосфамидом в дозе от или от приблизительно 20 мг/кг до 100 мг/кг, например, от или от приблизительно 40 мг/кг до 80 мг/кг. В некоторых аспектах пациента предварительно кондиционируют с или приблизительно с 60 мг/кг циклофосфамида. В некоторых вариантах осуществления циклофосфамид может быть введен в единственной дозе или может быть введен во множестве доз, например, вводимых ежедневно, через день или каждые три дня. В некоторых вариантах осуществления циклофосфамид вводят один раз в сутки в течение одного или двух дней. В некоторых вариантах осуществления, где агент для лимфодеплеции включает циклофосфамид, пациенту вводят циклофосфамид в дозе от или от приблизительно 100 мг/м2 до 500 мг/м2, например, от или от приблизительно 200 мг/м2 до 400 мг/м2, или от 250 мг/м2 до 350 мг/м2, включительно. В некоторых случаях пациенту вводят приблизительно 300 мг/м2 циклофосфамида. В некоторых вариантах осуществления циклофосфамид может быть введен в единственной дозе или может быть введен во множестве доз, таких как вводимые ежедневно, через день или каждые три дня. В некоторых вариантах осуществления циклофосфамид вводят ежедневно, например, в течение 1-5 дней, например, в течение 3-5 дней. В некоторых случаях пациенту вводят приблизительно 300 мг/м2 циклофосфамида ежедневно в течение 3 дней до инициации клеточной терапии.
[0258] В некоторых вариантах осуществления, где агент для лимфодеплеции включает флударабин, пациенту вводят флударабин в дозе от или от приблизительно 1 мг/м2 до 100 мг/м2, такой как от или от приблизительно 10 мг/м2 до 75 мг/м2, от 15 мг/м2 до 50 мг/м2, от 20 мг/м2 до 40 мг/м2 или от 24 мг/м2 до 35 мг/м2, включительно. В некоторых случаях пациенту вводят приблизительно 30 мг/м2 флударабина. В некоторых вариантах осуществления флударабин может быть введен в единственной дозе или может быть введен во множестве доз, таких как вводимые ежедневно, через день или каждые три дня. В некоторых вариантах осуществления флударабин вводят ежедневно, например, в течение 1-5 дней, например, в течение 3-5 дней. В некоторых случаях пациенту вводят приблизительно 30 мг/м2 флударабина ежедневно в течение 3 дней до инициации клеточной терапии.
[0259] В некоторых вариантах осуществления агент для лимфодеплеции включает комбинацию агентов, такую как комбинация циклофосфамида и флударабина. Таким образом, комбинация агентов может включать циклофосфамид в любой дозе или при схеме введения, такой как описанные выше, и флударабин в любой дозе или при схеме введения, такой как описанные выше. Например, в некоторых аспектах, пациенту вводят 60 мг/кг (~2 гр/м2) циклофосфамида и от 3 до 5 доз 25 мг/м2 флударабина перед первой или последующей дозой.
[0260] После введения клеток в некоторых вариантах осуществления измеряют биологическую активность популяции генно-инженерных клеток, например, любым из многих известных способов. Параметры для оценки включают специфическое связывание генно-инженерных или естественных Т-клеток или другой иммунной клетки с антигеном in vivo, например, путем визуализации, или ex vivo, например, потоковой цитометрией или ELISA. В некоторых вариантах осуществления способность генно-инженерных клеток разрушать клетки-мишени может быть измерена с помощью любых подходящих известных способов, таких как тесты цитотоксичности, описанные в, например, Kochenderfer et al., J. Immunotherapy, 32(7): 689-702 (2009), и Herman et al. J. Immunological Methods, 285(1): 25-40 (2004). В некоторых вариантах осуществления биологическую активность клеток измеряют анализом экспрессии и/или секреции одного или более цитокинов, таких как CD107a, IFNγ, IL-2 и TNF. В некоторых аспектах биологическую активность измеряют путем оценки исхода заболевания, такого как сокращение опухолевой массы или нагрузки.
[0261] В некоторых вариантах осуществления генно-инженерные клетки дополнительно модифицируют любым числом путей, так, что их терапевтическая или профилактическая эффективность увеличивается. Например, генно-инженерные CAR или TCR, экспрессируемые популяцией, могут быть конъюгированы, прямо или косвенно через линкер, с нацеливающей группой. Практика конъюгации соединений, например, CAR или TCR, с нацеливающими группами является известной. См., например, Wadwa et al., J. Drug Targeting 3: 1 1 1 (1995), и патент США 5,087,616. В некоторых вариантах осуществления клетки вводят как часть комбинированного лечения, например, одновременно с или последовательно с, в любом порядке, другим терапевтическим вмешательством, таким как антитело или генно-инженерная клетка или рецептор, или агент, такой как цитотоксический или терапевтический агент. Клетки в некоторых вариантах осуществления вводят совместно с одним или более дополнительными терапевтическими агентами или в связи с другим терапевтическим вмешательством, одновременно или последовательно в любом порядке. В некоторых контекстах клетки вводят совместно с другой терапией, с достаточно малыми интервалами таким образом, что популяция клеток усиливает эффект одного или более дополнительных терапевтических агентов, или наоборот. В некоторых вариантах осуществления клетки вводят до одного или более дополнительных терапевтических агентов. В некоторых вариантах осуществления клетки вводят после одного или более дополнительных терапевтических агентов. В некоторых вариантах осуществления, один или более дополнительных агентов включают цитокин, такой как IL-2, например, для улучшения персистирования.
B. Дозирование
[0262] В некоторых вариантах осуществления дозу клеток вводят пациентам в соответствии со способами по изобретению, и/или с использованием изделий или композиций по изобретению. В некоторых вариантах осуществления, выбор размера или времени введения доз определяют в зависимости от конкретного заболевания или состояния у пациента. В некоторых случаях выбор размера или времени введения доз для конкретного заболевания ввиду представленного описания могут быть определены эмпирически.
[0263] В некоторых вариантах осуществления доза клеток включает от или от приблизительно 2 x 105 клеток/кг и до или до приблизительно 2 x 106 клеток/кг, например, от или от приблизительно 4 x 105 клеток/кг и до или до приблизительно 1 x 106 клеток/кг или от или от приблизительно 6 x 105 клеток/кг и до или до приблизительно 8 x 105 клеток/кг. В некоторых вариантах осуществления доза клеток включает не более чем 2 x 105 клеток (например, антиген-экспрессирующих, таких как CAR-экспрессирующие клетки) на килограмм массы тела пациента (клеток/кг), например, не более чем или приблизительно 3 x 105 клеток/кг, не более чем или приблизительно 4 x 105 клеток/кг, не более чем или приблизительно 5 x 105 клеток/кг, не более чем или приблизительно 6 x 105 клеток/кг, не более чем или приблизительно 7 x 105 клеток/кг, не более чем или приблизительно 8 x 105 клеток/кг, не более чем или приблизительно 9 x 105 клеток/кг, не более чем или приблизительно 1 x 106 клеток/кг или не более чем или приблизительно 2 x 106 клеток/кг. В некоторых вариантах осуществления доза клеток включает по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 2 x 105 клеток (например, антиген-экспрессирующих, таких как CAR-экспрессирующие клетки) на килограмм массы тела пациента (клеток/кг), например, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 3 x 105 клеток/кг, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 4 x 105 клеток/кг, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 5 x 105 клеток/кг, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 6 x 105 клеток/кг, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 7 x 105 клеток/кг, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 8 x 105 клеток/кг, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 9 x 105 клеток/кг, по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 1 x 106 клеток/кг или по меньшей мере или по меньшей мере приблизительно или до или до приблизительно 2 x 106 клеток/кг.
[0264] В некоторых вариантах осуществления клетки или отдельную популяцию подтипов клето вводят пациенту в диапазоне от приблизительно одного миллиона до приблизительно 100 миллиардов клеток и/или такое количество клеток на килограмм массы тела, как, например, от 1 миллиона до приблизительно 50 миллиардов клеток (например, приблизительно 5 миллионов клеток, приблизительно 25 миллионов клеток, приблизительно 500 миллионов клеток, приблизительно 1 миллиард клеток, приблизительно 5 миллиардов клеток, приблизительно 20 миллиардов клеток, приблизительно 30 миллиардов клеток, приблизительно 40 миллиардов клеток или диапазон, определяемый любыми двумя из предшествующих значений), такое как от приблизительно 10 миллионов до приблизительно 100 миллиардов клеток (например, приблизительно 20 миллионов клеток, приблизительно 30 миллионов клеток, приблизительно 40 миллионов клеток, приблизительно 60 миллионов клеток, приблизительно 70 миллионов клеток, приблизительно 80 миллионов клеток, приблизительно 90 миллионов клеток, приблизительно 10 миллиардов клеток, приблизительно 25 миллиардов клеток, приблизительно 50 миллиардов клеток, приблизительно 75 миллиардов клеток, приблизительно 90 миллиардов клеток, или диапазон, определяемый любыми двумя из предшествующих значений), и в некоторых случаях от приблизительно 100 миллионов клеток до приблизительно 50 миллиардов клеток (например, приблизительно 120 миллионов клеток, приблизительно 250 миллионов клеток, приблизительно 350 миллионов клеток, приблизительно 450 миллионов клеток, приблизительно 650 миллионов клеток, приблизительно 800 миллионов клеток, приблизительно 900 миллионов клеток, приблизительно 3 миллиардов клеток, приблизительно 30 миллиардов клеток, приблизительно 45 миллиардов клеток) или любое промежуточное значение из этих диапазонов и/или на килограмм массы тела. Дозировки могут варьировать в зависимости от признаков, присущих заболеванию или нарушению и/или пациенту и/или другим лечениям.
[0265] В некоторых вариантах осуществления доза клеток является плоской дозой клеток или фиксированной дозой клеток, таким образом, что доза клеток не привязана к или не основана на площади поверхности или массе тела пациента.
[0266] В некоторых вариантах осуществления доза генно-инженерных клеток включает от или от приблизительно 1 x 105 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 1 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 5 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 2,5 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 1 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 5 x 106 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 2,5 x 106 общих CAR-экспрессирующих Т-клеток, от 1 x 105 до 1 x 106 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 1 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 5 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 2,5 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 1 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 5 x 106 общих CAR-экспрессирующих Т-клеток, от 1 x 106 до 2,5 x 106 общих CAR-экспрессирующих Т-клеток, от 2,5 x 106 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 2,5 x 106 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток, от 2,5 x 106 до 1 x 108 общих CAR-экспрессирующих Т-клеток, от 2,5 x 106 до 5 x 107 общих CAR-экспрессирующих Т-клеток, от 2,5 x 106 до 2,5 x 107 общих CAR-экспрессирующих Т-клеток, от 2,5 x 106 до 1 x 107 общих CAR-экспрессирующих Т-клеток, от 2,5 x 106 до 5 x 106 общих CAR-экспрессирующих Т-клеток, от 5 x 106 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 5 x 106 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток, от 5 x 106 до 1 x 108 общих CAR-экспрессирующих Т-клеток, от 5 x 106 до 5 x 107 общих CAR-экспрессирующих Т-клеток, от 5 x 106 до 2,5 x 107 общих CAR-экспрессирующих Т-клеток, от 5 x 106 до 1 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 107 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 107 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 107 до 1 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 107 до 5 x 107 общих CAR-экспрессирующих Т-клеток, от 1 x 107 до 2,5 x 107 общих CAR-экспрессирующих Т-клеток, от 2,5 x 107 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 2,5 x 107 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток, от 2,5 x 107 до 1 x 108 общих CAR-экспрессирующих Т-клеток, от 2,5 x 107 до 5 x 107 общих CAR-экспрессирующих Т-клеток, от 5 x 107 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 5 x 107 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток, от 5 x 107 до 1 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 108 до 5 x 108 общих CAR-экспрессирующих Т-клеток, от 1 x 108 до 2,5 x 108 общих CAR-экспрессирующих Т-клеток или от 2,5 x 108 до 5 x 108 общих CAR-экспрессирующих Т-клеток.
[0267] В некоторых вариантах осуществления доза генно-инженерных клеток включает по меньшей мере или по меньшей мере приблизительно 1 x 105 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5 x 105 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 5 x 105 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 1 x 106 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5 x 106 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 5 x 106 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 1 x 107 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5 x 107 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 5 x 107 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 1 x 108 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5 x 108 CAR-экспрессирующих клеток или по меньшей мере или по меньшей мере приблизительно 5 x 108 CAR-экспрессирующих клеток.
[0268] В некоторых вариантах осуществления клеточная терапия включает введение дозы, включающей число клеток от или от приблизительно 1 x 105 до 5 x 108 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), от или от приблизительно 5 x 105 до 1 x 107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC) или от или от приблизительно 1 x 106 до 1 x 107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), включительно. В некоторых вариантах осуществления клеточная терапия включает введение дозы клеток, включающих число клеток по меньшей мере или по меньшей мере приблизительно 1 x 105 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, по меньшей мере или по меньшей мере приблизительно 1 x 106, по меньшей мере или по меньшей мере приблизительно 1 x 107, по меньшей мере или по меньшей мере приблизительно 1 x 108 таких клеток. В некоторых вариантах осуществления это число относится к общему количеству CD3+ или CD8+, в некоторых случаях также экспрессирующих рекомбинантный рецептор (например, CAR+) клеток. В некоторых вариантах осуществления клеточная терапия включает введение дозы, включающей число клеток от или от приблизительно 1 x 105 до 5 x 108 CD3+ или CD8+ общих Т-клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, от или от приблизительно 5 x 105 до 1 x 107 CD3+ или CD8+ общих Т-клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, или от или от приблизительно 1 x 106 до 1 x 107 CD3+ или CD8+ общих Т-клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, включительно. В некоторых вариантах осуществления клеточная терапия включает введение дозы, включающей число клеток от или от приблизительно 1 x 105 до 5 x 108 общих CD3+/CAR+ или CD8+/CAR+ клеток, от или от приблизительно 5 x 105 до 1 x 107 общих CD3+/CAR+ или CD8+/CAR+ клеток, или от или от приблизительно 1 x 106 до 1 x 107 общих CD3+/CAR+ или CD8+/CAR+ клеток, включительно.
[0269] В некоторых вариантах осуществления доза Т-клеток включает: 5 x 107 или приблизительно 5 x 107 экспрессирующих рекомбинантный рецептор Т-клеток или 2,5 x 107 или до приблизительно 2,5 x 107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток. В некоторых вариантах осуществления доза Т-клеток включает: 1 x 108 или приблизительно 1 x 108 экспрессирующих рекомбинантный рецептор Т-клеток или 5 x 107или до приблизительно 5 x 107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток. В некоторых вариантах осуществления доза Т-клеток включает: 1,5 x 108 или приблизительно 1,5 x 108 экспрессирующих рекомбинантный рецептор Т-клеток или 0,75 x 108 или до приблизительно 0,75 x 108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток.
[0270] В некоторых вариантах осуществления Т-клетки дозы включают CD4+ Т-клетки, CD8+ Т-клетки или CD4+ и CD8+ Т-клетки.
[0271] В некоторых вариантах осуществления, например, где пациент является человеком, CD8+ Т-клетки дозы, включая в дозе, включающей CD4+ и CD8+ Т-клетки, включают от приблизительно 1 x 106 до 5 x 108 общих экспрессирующих рекомбинантный рецептор (например, CAR) CD8+ клеток, например, в диапазоне приблизительно от 5 x 106 до 1 x 108 таких клеток, 1 x 107, 2,5 x 107, 5 x 107, 7,5 x 107, 1 x 108 или 5 x 108 таких общих клеток или диапазон между любыми двумя из предшествующих значений. В некоторых вариантах осуществления пациенту вводят многократные дозы, и каждая из доз или общая доза может составлять любое из предшествующих значений. В некоторых вариантах осуществления доза клеток включает введение от или от приблизительно 1 x 107 до 0,75 x 108 общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, от 1 x 107 до 2,5 x 107 общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, от или от приблизительно 1 x 107 до 0,75 x 108 общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, включительно. В некоторых вариантах осуществления доза клеток включает введение 1 x 107, 2,5 x 107, 5 x 107 7,5 x 107, 1 x 108 или 5 x 108 или приблизительно этого количества общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток.
[0272] В некоторых вариантах осуществления, например, где пациентом является человек, доза включает менее чем приблизительно 2 x 108 1 x 108 общих экспрессирующих рекомбинантный рецептор (например, CAR) клеток, Т-клеток или одноядерных клеток периферической крови (PBMC), например, в диапазоне приблизительно от 1 x 106 до 2 x 108 или от 1 x 106 до 1 x 108 таких клеток, например, 2 x 106, 5 x 106, 1 x 107, 5 x 107, 1 x 108 или 1,5 x 108 таких общих клеток или диапазон между любыми двумя из предшествующих значений. В некоторых вариантах осуществления, где пациентом является человек, доза включает от приблизительно 1 x 106 до 3 x 108 общих экспрессирующих рекомбинантный рецептор (например, CAR) клеток, например, в диапазоне приблизительно от 1 x 107 до 2 x 108 таких клеток, например, 1 x 107, 5 x 107, 1 x 108 или 1,5 x 108 таких общих клеток или диапазон между любыми двумя из предшествующих значений. В некоторых вариантах осуществления пациенту вводят многократные дозы, и каждая из доз или общая доза может составлять любое из предшествующих значений. В некоторых вариантах осуществления доза клеток включает введение от или от приблизительно 1 x 105 до 5 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от 1 x 105 до 1,5 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от 1 x 105 до 1 x 108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 5 x 105 до 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, или от или от приблизительно 1 x 106 до 1 x 107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, включительно.
[0273] В некоторых вариантах осуществления Т-клетки дозы включают CD4+ Т-клетки, CD8+ Т-клетки или CD4+ и CD8+ Т-клетки.
[0274] В некоторых вариантах осуществления, например, где пациент является человеком, CD8+ Т-клетки дозы, включая в дозе, включающей CD4+ и CD8+ Т-клетки, включает от приблизительно 1 x 106 до 1 x 108 общих экспрессирующих рекомбинантный рецептор (например, CAR) CD8+ клеток, например, в диапазоне приблизительно от 5 x 106 до 1 x 108 таких клеток, 1 x 107, 2,5 x 107, 5 x 107, 7,5 x 107 или 1 x 108 таких общих клеток или диапазон между любыми двумя из предшествующих значений. В некоторых вариантах осуществления пациенту вводят многократные дозы, и каждая из доз или общая доза может составлять любое из предшествующих значений. В некоторых вариантах осуществления доза клеток включает введение от или от приблизительно 1 x 107 до 0,75 x 108 общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, от 1 x 107 до 2,5 x 107 общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, от или от приблизительно 1 x 107 до 0,75x108x 108 общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, включительно. В некоторых вариантах осуществления доза клеток включает введение 1x107, 2,5x107, 5x107 7,5x107 или 1x108 или приблизительно этого количества общих экспрессирующих рекомбинантный рецептор CD8+ Т-клеток.
[0275] В некоторых вариантах осуществления дозу клеток, например, экспрессирующих рекомбинантный рецептор Т-клеток, вводят пациенту в виде единственной дозы или вводят только один раз за период двух недель, одного месяца, трех месяцев, шести месяцев, 1 года или более.
[0276] В контексте адоптивной клеточной терапии введение данной «дозы» охватывает введение данного количества или числа клеток в форме единственной композиции и/или единственного непрерывного введения, например, в форме единственной инъекции или непрерывного вливания, и также охватывает введение данного количества или числа клеток в форме раздельных доз или в форме множества композиций, поставляемых в множественных отдельных композициях или вливаниях, за установленный период времени, такой как не более 3 дней. Таким образом, в некоторых контекстах, доза является единственным или непрерывным введением конкретного количества клеток, данным или инициированным в единственный момент времени. В некоторых контекстах, однако, дозу вводят в многократных инъекциях или вливаниях в течение не более трех дней, например, один раз в день в течение трех дней или в течение двух дней или многократными вливаниями за период в один день.
[0277] Таким образом, в некоторых аспектах, клетки дозы вводят в единственной фармацевтической композиции. В некоторых вариантах осуществления клетки дозы вводят во множестве композиций, коллективно содержащих клетки дозы.
[0278] В некоторых вариантах осуществления термин “разделенная доза” относится к дозе, разделенной так, чтобы она была введена более чем за один день. Этот тип дозирования охватывается способами по изобретению и считается единственной дозой.
[0279] Таким образом, доза клеток может быть введена как разделенная доза, например, разделенная доза, вводимая в течение времени. Например, в некоторых вариантах осуществления, доза может быть введена пациенту в течение 2 дней или в течение 3 дней. Примеры способов разделенного введения включают введение 25% дозы в первый день и введение остаьных 75% дозы во второй день. В других вариантах осуществления 33% дозы могут быть введены в первый день и остальные 67% введены во второй день. В некоторых аспектах 10% дозы вводят в первый день, 30% дозы вводят во второй день, и 60% дозы вводят в третий день. В некоторых вариантах осуществления разделенную дозу не растягивают более чем на 3 дня.
[0280] В некоторых вариантах осуществления клетки дозы могут быть введены путем введения множества композиций, или растворов, таких как первая и вторая, необязательно больше, каждая из которых содержит некоторые клетки дозы. В некоторых аспектах множество композиций, каждая из которых содержит различные популяции и/или подтипы клеток, вводят отдельно или независимо, необязательно за определенный период времени. Например, популяции или подтипы клеток могут включать CD8+ и CD4+ Т-клетки, соответственно, и/или CD8+- и CD4+-обогащенные популяции, соответственно, например, CD4+ и/или CD8+ Т-клетки, причем каждая индивидуально включает клетки, генетически измененные для экспрессии рекомбинантного рецептора. В некоторых вариантах осуществления введение дозы включает введение первой композиции, включающей дозу CD8+ Т-клеток или доза CD4+ Т-клеток, и введение второй композиции, включающей другую дозу CD4+ Т-клеток и CD8+ Т-клеток.
[0281] В некоторых вариантах осуществления введение композиции или дозы, например, введение множества композиций клеток, включает раздельное введение композиций клеток. В некоторых аспектах раздельные введения осуществляют одновременно или последовательно, в любом порядке. В некоторых вариантах осуществления доза включает первую композицию и вторую композицию, и первую композицию и вторую композицию вводят с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часа. В некоторых вариантах осуществления инициацию введения первой композиции и инициацию введения второй композиции осуществляют с интервалом не более чем 2 часа, не более чем 1 час, или не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут. В некоторых вариантах осуществления инициацию и/или завершение введения первой композиции и завершение и/или инициацию введения второй композиции осуществляют с интервалом не более чем 2 часа, не более чем 1 час или не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут.
[0282] В некоторых композициях первая композиция, например, первая композиция дозы, включает CD4+ Т-клетки. В некоторых композициях первая композиция, например, первая композиция дозы, включает CD8+ Т-клетки. В некоторых вариантах осуществления первую композицию вводят до второй композиции.
[0283] В некоторых вариантах осуществления доза или композиция клеток включает определенное или целевое отношение CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет приблизительно 1:1 или от приблизительно 1:3 до приблизительно 3:1, например, приблизительно 1:1. В некоторых аспектах введение композиции или дозы с целевым или желаемым отношением различных популяций клеток (таким как отношение CD4+: CD8+ или отношение CAR+CD4+: CAR+CD8+, например, 1:1) включает введение композиции клетки, содержащей одну из популяций, и затем введение отдельной композиции клеток, включающей другую популяции, где введение осуществляют в или приблизительно в целевом или желаемом отношении. В некоторых аспектах введение дозы или композиции клеток в определенном отношении приводит к улучшенному росту, пресистированию и/или противоопухолевой активности Т-клеточной терапии.
[0284] В некоторых вариантах осуществления пациент получает многократные дозы, например, две или более доз, или многократные последовательные дозы клеток. В некоторых вариантах осуществления пациенту вводят две дозы. В некоторых вариантах осуществления пациент получает последующую дозу, например, вторую дозу, которую вводят приблизительно через 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 день после первой дозы. В некоторых вариантах осуществления многократные последующие дозы вводят после первой дозы, так, что дополнительная доза или дозы вводят после введения последующей дозы. В некоторых аспектах число клеток, вводимых пациенту в дополнительной дозе, совпадает с или подобно первой дозе и/или последующей дозе. В некоторых вариантах осуществления дополнительная доза или дозы превышают предшествующие дозы.
[0285] В некоторых аспектах размер первой и/или последующей дозы определяют на основе одного или более критериев, таких как ответ пациента на предшествующее лечение, например, химиотерапию, тяжести заболевания у пациента, такой как опухолевая нагрузка, масся, размер или степень, степень или типе метастаза, стадия и/или вероятность, или частота развития у пациента токсичности, например, CRS, синдрома активации макрофагов, синдрома лизиса опухоли, нейротоксичности и/или иммунного ответа хозяина на вводимые клетки и/или рекомбинантные рецепторы.
[0286] В некоторых аспектах время между введением первой дозы и введением последующей дозы составляет от приблизительно 9 до приблизительно 35 дней, от приблизительно 14 до приблизительно 28 дней или от 15 до 27 дней. В некоторых вариантах осуществления введение последующей дозы осуществляют в момент времени более чем приблизительно 14 дней после и менее чем приблизительно 28 дней после введения первой дозы. В некоторых аспектах время между первой и последующей дозой составляет приблизительно 21 день. В некоторых вариантах осуществления дополнительная доза или дозы, например, последующие дозы, вводят после введения последующей дозы. В некоторых аспектах дополнительная последовательная доза или дозы вводят по меньшей мере приблизительно 14 и менее чем приблизительно 28 дней после введения предшествующей дозы. В некоторых вариантах осуществления дополнительную дозу введена менее чем приблизительно 14 дней после предшествующей дозы, например, спустя 4, 5, 6, 7, 8, 9, 10, 11, 12 или 13 дней после предшествующей дозы. В некоторых вариантах осуществления никакую дозу не вводят через менее чем приблизительно 14 дней после предшествующей дозы и/или никакую дозу не вводят через более чем приблизительно 28 дней после предшествующей дозы.
[0287] В некоторых вариантах осуществления доза клеток, например, экспрессирующих рекомбинантный рецептор клеток, включает две дозы (например, двойную дозу), включая первую дозу Т-клеток и последующую дозу Т-клеток, причем одна или обе из первой дозы и второй дозы включает введение разделенной дозы Т-клеток.
[0288] В некоторых вариантах осуществления доза клеток обычно является достаточно большой, чтобы быть эффективной в уменьшении серьезности заболевания.
[0289] В некоторых вариантах осуществления клетки вводят в желаемой дозировке, в некоторых аспектах включающей желаемую дозу или число клеток или тип(ы) клеток и/или желаемое отношение типов клеток. Таким образом, дозировка клеток в некоторых вариантах осуществления основывается на общем количестве клеток (или числе на кг массы тела) и желаемое отношение отдельных популяций или подтипов, такое как отношение CD4+ к CD8+. В некоторых вариантах осуществления дозировка клеток основывается на желаемом общем количестве (или числе на кг массы тела) клеток в отдельных популяциях или отдельных типах клеток. В некоторых вариантах осуществления дозировка основывается на комбинации таких признаков, таких как желаемое число общих клеток, желаемое отношение и желаемое общее количество клеток в отдельных популяциях.
[0290] В некоторых вариантах осуществления, популяции или подтипы клеток, таких как CD8+ и CD4+ Т-клетки, вводят в или в пределах переносимого отличия от желаемой дозы общих клеток, такой как желаемая доза Т-клеток. В некоторых аспектах желаемая доза является желаемым числом клеток или желаемым числом клеток на единицу массы тела пациента, которому эти клетки вводят, например, клеток/кг. В некоторых аспектах желаемая доза составляет или выше минимального числа клеток или минимального числа клеток на единицу массы тела. В некоторых аспектах, среди общих клеток, вводимых в желаемой дозе, отдельные популяции или подтипы присутствуют в или около желаемой выходной величины отношения (такого как отношение CD4+ к CD8+), например, в определенном переносимом отличии или ошибке такого отношения.
[0291] В некоторых вариантах осуществления клетки вводят в или в переносимом отличии желаемой дозы одной или более отдельных популяций или подтипов клеток, такой как желаемая доза CD4+ клеток и/или желаемая доза CD8+ клеток. В некоторых аспектах желаемая доза является желаемым числом клеток подтипа или популяции, или желаемым числом таких клеток на единицу массы тела пациента, которому эти клетки вводят, например, клеток/кг. В некоторых аспектах желаемая доза составляет или выше минимального числа клеток популяции или подтипа, или минимального числа клеток популяции или подтипа на единицу массы тела.
[0292] Таким образом, в некоторых вариантах осуществления, дозировка основывается на желаемой фиксированной дозе общих клеток и желаемом отношении, и/или на основе желаемой фиксированной дозы одного или более, например, каждого, отдельных подтипов или субпопуляций. Таким образом, в некоторых вариантах осуществления, дозировка основывается на желаемой фиксированной или минимальной дозе Т-клеток и желаемом отношении CD4+ к CD8+ клеткам, и/или основывается на желаемой фиксированной или минимальной дозе CD4+ и/или CD8+ клеток.
[0293] В некоторых вариантах осуществления клетки вводят в или в пределах переносимого диапазона желаемого выходного отношения множественных популяций или подтипов клеток, таких как CD4+ и CD8+ клетки или подтипы. В некоторых аспектах желаемое отношение может быть определенным отношением или может быть диапазоном отношений. Например, в некоторых вариантах осуществления, желаемое отношение (например, отношение CD4+ к CD8+ клеткам) составляет от или от приблизительно 5:1 и до или до приблизительно 5:1 (или более чем приблизительно 1:5 и менее чем приблизительно 5:1), или от или от приблизительно 1:3 и до или до приблизительно 3:1 (или более чем приблизительно 1:3 и менее чем приблизительно 3:1), например, от или от приблизительно 2:1 и до или до приблизительно 1:5 (или более чем приблизительно 1:5 и менее чем приблизительно 2:1, например, в отношении или приблизительно в отношении 5:1, 4,5:1, 4:1, 3,5:1, 3:1, 2,5:1, 2:1, 1,9:1, 1,8:1, 1,7:1, 1,6:1, 1,5:1, 1,4:1, 1,3:1, 1,2:1, 1,1:1, 1:1, 1:1,1, 1:1,2, 1:1,3, 1:1,4, 1:1,5, 1:1,6, 1:1,7, 1:1,8, 1:1,9: 1:2, 1:2,5, 1:3, 1:3,5, 1:4, 1:4,5 или 1:5. В некоторых аспектах переносимое отличие составляет приблизительно 1%, приблизительно 2%, приблизительно 3%, приблизительно 4% приблизительно 5%, приблизительно 10%, приблизительно 15%, приблизительно 20%, приблизительно 25%, приблизительно 30%, приблизительно 35%, приблизительно 40%, приблизительно 45%, приблизительно 50% желаемого отношения, включая любое промежуточное значение этих диапазонов.
[0294] В некоторых вариантах осуществления числа и/или концентрации клеток относятся к числу экспрессирующих рекомбинантный рецептор (например, CAR) клеток. В других вариантах осуществления числа и/или концентрации клеток относятся к числу или концентрации всех вводимых клеток, Т-клеток или одноядерных клеток периферической крови (PBMC).
[0295] В некоторых аспектах размер дозы определяют на основе одного или более критериев, таких как ответ пациента на предшествующее лечение, например, химиотерапию, серьезность заболевания у пациента, такая как опухолевая нагрузка, масся, размер или степень, степень или тип метастаза, стадия и/или вероятность или частота развития у пациента токсичности, например, CRS, синдрома активации макрофагов, синдрома лизиса опухоли, нейротоксичности и/или иммунного ответа хозяина на вводимые клетки и/или рекомбинантные рецепторы.
[0296] В некоторых вариантах осуществления способы также включают введение одной или более дополнительных доз клеток, экспрессирующих химерный антигенный рецептор (CAR), и/или противолимфоцитарной терапии, и/или одну или более стадий способов повторяют. В некоторых вариантах осуществления, одна или более дополнительных доз совпадают с начальной дозой. В некоторых вариантах осуществления, одна или более дополнительных доз отличается от начальной дозы, например, являются более высокими, такими как 2-кратная, 3-кратная, 4-кратная, 5-кратная, 6-кратная, 7-кратная, 8-кратная, 9-кратная или 10-кратная или еще более высокой, чем начальная доза, или более низкими, такими как, например, более высокие, такие как 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно или 10-кратно или еще более низкими, чем начальная доза. В некоторых вариантах осуществления введение одной или более дополнительных доз определяется на основании ответа пациента на начальное лечение или любое предшествующее лечение, серьезности заболевания у пациента, такой как опухолевая нагрузка, масса, размер или степень, степень или тип метастаза, стадия и/или вероятность, или частота развития у пациента токсичности, например, CRS, синдрома активации макрофагов, синдрома лизиса опухоли, нейротоксичности и/или иммунного ответа хозяина на вводимые клетки и/или рекомбинантные рецепторы.
C. Ответ, эффективность и выживание
[0297] В некоторых вариантах осуществления введение эффективно лечит пациента, несмотря на то, что пациент резистентен к другой терапии. В некоторых вариантах осуществления по меньшей мере 30%, по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полной ремиссии (CR); и/или по меньшей мере приблизительно 40%, по меньшей мере приблизительно 50%, по меньшей мере приблизительно 60% или по меньшей мере приблизительно 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR). В некоторых вариантах осуществления по меньшей мере или приблизительно по меньшей мере 50% пациентов, по меньшей мере или приблизительно по меньшей мере 60% пациентов, по меньшей мере или приблизительно по меньшей мере 70% пациентов, по меньшей мере или приблизительно по меньшей мере 80% пациентов или по меньшей мере или приблизительно по меньшей мере 90% пациентов, получающих лечение согласно способу, достигают CR и/или достигают объективного ответа (OR). В некоторых вариантах осуществления критерии, оцениваемые для эффективного лечения, включают частоту общего ответа (ОРР; также известную в некоторых случаях как частота объективного ответа), полный ответ (CR; также известный в некоторых случаях как полный ответ), продолжительность ответа (DOR), выживаемость без прогрессий (PFS) и/или полная выживаемость (OS).
[0298] В некоторых вариантах осуществления по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способам, достигают полной ремиссии (CR; также известной в некоторых случаях как полный ответ), демонстрируют выживаемость без прогрессии (PFS) и/или полную выживаемость (OS) более чем или приблизительно 3 месяца, 6 месяцев или 12 месяцев или более чем 13 месяцев или приблизительно 14 месяцев; в среднем, пациенты, получающие лечение согласно способу, показывают в среднем PFS или OS более чем или приблизительно 6 месяцев, 12 месяцев или 18 месяцев; и/или пациент показывает PFS или OS после терапии в течение по меньшей мере или приблизительно 6, 12, 18 или более месяцев или дольше.
[0299] В некоторых аспектах частоты ответа у пациентов, таких как пациенты с NHL, основываются на критериях Лугано. (Cheson et al., (2014) JCO 32(27):3059-3067; Johnson et al., (2015) Radiology 2:323-338; Cheson, B.D. (2015) Chin Clin Oncol 4(1):5). В некоторых аспектах в оценке ответа используют любой из клинических, гематологических и/или молекулярных способов. В некоторых аспектах ответ, оцениваемый с использованием критериев Лугано, включает использование позитронной эмиссионной томографии (PET) - компьютерной томографии (CT) и/или CT, в зависимости от ситуации. Оценки PET-CT могут дополнительно включать использование фтордеоксиглюкозы (FDG) для лимфом с повышенным накоплением FDG. В некоторых аспектах, где PET-CT используется для оценки ответа в гистологиях с повышенным накоплением FDG, может использоваться 5-балльная шкала. В некотором отношении 5-балльная шкала включает следующие критерии: 1, отсутствие накопления выше фона; 2, накопление ≤ средостение; 3, накопление > средостение, но ≤ печень; 4, накопление умеренно > печень; 5, накопление заметно выше, чем печень и/или новые поражения; X, новые области накопления, вероятно не связанные с лимфомой.
[0300] В некоторых аспектах полный ответ, как описано с использованием критериев Лугано, включает полный метаболический ответ и полный рентгенологический ответ на различных измеримых участках. В некоторых аспектах эти участки включают лимфатические узлы и экстралимфатические участки, в которых CR описан как балл 1, 2, или 3 с или без остаточной массы по 5-балльной шкале, когда используется PET-CT. В некоторых аспектах, в кольце Вальдейера или экстранодальных участках с высоким физиологическим накоплением или с активацией в селезенке или костном мозге (например, с химиотерапией или миелоидными колониестимулирующими факторами), накопление может быть больше, чем в нормальном средостении и/или печени. При этом обстоятельстве может быть выведен полный метаболический ответ, если накопление в участках начального участия не больше, чем в окружающей нормальной ткани, даже если ткань имеет высокое физиологическое накопление. В некоторых аспектах ответ оценивают в лимфатических узлах с помощью CT, причем CR описан как если никакие экстралимфатические участки заболевания и целевые узлы/центральные массы не должны регрессировать до ≤ 1,5 см в самом длинном поперечном диаметре поражения (LDi). Дальнейшие места оценки включают костный мозг, в котором оценка на основании PET-CT должна показать отсутствие признаков заболевания с повышенным накоплением FDG в костном мозге, и оценка на основании CT должна показать нормальную морфологию, которая, если оказывается неопределенной, должна быть расценена как IHC-негативная. Дальнейшие участки могут включать оценку увеличения органа, которое должно регрессировать до нормы. В некоторых аспектах оценивают неизмеренные поражения и новые поражения, которые в случае CR должны отсутствовать (Cheson et al., (2014) JCO 32(27):3059-3067; Johnson et al., (2015) Radiology 2:323-338; Cheson, B.D. (2015) Chin Clin Oncol 4(1):5).
[0301] В некоторых аспектах, частичный ответ (PR; также известный в некоторых случаях как частичная ремиссия), как описано с использованием критериев Лугано, включает частичный метаболический и/или радиологический ответ в различных измеримых участках. В некоторых аспектах эти участки включают лимфатические узлы и экстралимфатические участки, в которых PR описан как балл 4 или 5 со сниженным накоплением по сравнению с начальной и остаточной массой(ами) любого размера, когда используется PET-CT. В промежуточном периоде такие результаты исследования могут указывать отвечающее заболевание. В конце лечения такие результаты исследования могут указывать остаточное заболевание. В некоторых аспектах ответ оценивают в лимфатических узлах с помощью CT, причем PR описан как уменьшение на ≥50% в SPD до 6 целевых измеримых узлов и экстранодальных участков. Если поражение является слишком маленьким для измерения с помощью CT, 5 мм х 5 мм назначают в качестве значения по умолчанию; если поражение больше не видимо, значение составляет 0 мм х 0 мм; для узла > 5 мм х 5 мм, но меньше, чем нормальное, фактические измерения используются для вычисления. Другие места для оценки включают костный мозг, причем оценка на основании PET-CT должна показать остаточное накопление выше, чем накопление в нормальном костном мозге, но уменьшенное по сравнению с базовым (диффузное накопление, совместимое с реактивными изменениями от химиотерапии). В некоторых аспектах, если существуют персистирующие очаговые изменения в костном мозге в контексте узлового ответа, внимание должно быть уделено дальнейшей оценке с использованием MRI или биопсии, или интервального сканирования. В некоторых аспектах другие места могут включать оценку увеличения органа, где селезенка должна регрессировать на > 50% в длину за пределами нормальной. В некоторых аспектах оценивают неизмеренные поражения и новые поражения, которые в случае PR должны быть отсутствующими/нормальными, регрессировать, но не увеличиваться. Отсутствие ответа/стабильное заболевание (SD) или прогрессирующее заболевание (PD) может также быть измерено с помощью оценки на основании PET-CT и/или CT. (Cheson et al., (2014) JCO 32(27):3059-3067; Johnson et al., (2015) Radiology 2:323-338; Cheson, B.D. (2015) Chin Clin Oncol 4(1):5).
[0302] В некотором отношении выживаемость без прогрессий (PFS) описывается как отрезок времени в течение и после лечения заболевания, такого как рак, в течение которого пациент живет с заболеванием, но оно не усугубляется. В некоторых аспектах объективный ответ (OR) описывается как измеримый ответ. В некоторых аспектах частота объективного ответа (ОРР; также известная в некоторых случаях как частота общего ответа) описывается как пропорция пациентов, достигнувших CR или PR. В некоторых аспектах полную выживаемость (OS) описывают как отрезок времени либо с даты постановки диагноза, либо с начала лечения заболевания, такого как рак, в течение которого пациент, у которого диагностировано это заболевание, все еще жив. В некоторых аспектах выживаемость без событий (EFS) описывается как отрезок времени после окончания лечения рака, в течение которого пациент не имеет определенных осложнений или событий, предотвратить или задержать которые было предназначением лечения. Эти события могут включать рецидив рака или начало определенных симптомов, таких как боль в костях по причине распространения рака в костную ткань, или смерть.
[0303] В некоторых вариантах осуществления измерение продолжительности ответа (DOR) включает время от документации ответа опухоли до прогрессии заболевания. В некоторых вариантах осуществления параметр для оценки ответа может включать длительный ответ, например, ответ, сохраняющийся после промежутка времени от инициации терапии. В некоторых вариантах осуществления длительный ответ обозначается продолжительностью ответа приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 18 или 24 месяца после инициации терапии. В некоторых вариантах осуществления ответ длится в течение более чем 3 месяца или более чем 6 месяцев.
[0304] В некоторых аспектах критерии RECIST используются для определения объективного канцерогенного эффекта; в некоторых аспектах, при солидных опухолях. (Eisenhauer et al., European Journal of Cancer 45 (2009) 228-247). В некоторых аспектах критерии RECIST используются для определения объективного канцерогенного эффекта для поражений органов-мишеней. В некотором отношении полный ответ, как определено с использованием критериев RECIST, описан как исчезновение всех поражений органов-мишеней, и любые патологические лимфатические узлы (или цель или нецель) должны иметь уменьшение короткой оси до < 10 мм. В других аспектах частичный ответ, как определено с использованием критерией RECIST, описывают как по меньшей мере 30%-е уменьшение суммы диаметров поражений органов-мишеней, принимая за референсное значение сумму начальных диаметров. В других аспектах прогрессирующее заболевание (PD) описывают как по меньшей мере 20%-е увеличение суммы диаметров поражений органов-мишеней, принимая за референсное значение самую маленькую сумму на протяжении исследования (это включает начальную сумму, если она является самой маленькой на протяжении исследования). В дополнение к относительному увеличению на 20%, сумма должна также продемонстрировать абсолютный прирост по меньшей мере 5 мм (в некоторых аспектах, появление одного или более новых поражений также считают прогрессией). В других аспектах стабильное заболевание (SD) описывают как не демонстрирующее ни достаточного уменьшения для приобретения статуса PR, ни достаточного увеличения для приобретения статуса PD, принимая за референсное значение самые маленькие суммы диаметров на протяжении исследования.
[0305] В некоторых аспектах введение в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению обычно уменьшает или предотвращает увеличение или серьезность заболевания или состояния у пациента. Например, если заболевание или состояние являются опухолью, способы обычно уменьшают размер, массу опухоли, метастазирование, процент бластов в костном мозге или поддающейся обнаружению на молекулярном уровне злокачественной опухоли и/или улучшают прогноз или выживаемость или другой симптом, связанный с опухолевой нагрузкой.
[0306] Серьезность заболевания может охватывать общее число клеток заболевания у пациента или в органе, ткани или физической жидкости пациента, таком как орган или ткань опухоли или другого местоположения, например, которое указывает на метастаз. Например, опухолевые клетки могут быть обнаружены и/или определены количественно в крови или костном мозге в контексте некоторых гематологических злокачественных опухолей. Серьезность заболевания может включать, в некоторых вариантах осуществления, массу опухоли, число или степень метастазов и/или процент бластных клеток, пристутствующих в костном мозге.
[0307] В некоторых вариантах осуществления пациент имеет лейкоз. Степень серьезности заболевания может быть определена оценкой остаточного лейкоза в крови или костном мозге.
[0308] В некоторых аспектах частоты ответа у пациентов, таких как пациенты с CLL, основываются на критериях ответа, определенных на Международном семинаре по Хроническому Лимфолейкозу (IWCLL) (Hallek, et al., Blood 2008, Jun 15; 111(12): 5446-5456). В некоторых аспектах эти критерии описаны следующим образом: полная ремиссия (CR; также известная в некоторых случаях как полный ответ), которая в некоторых аспектах требует отсутствия клональных лимфоцитов периферической крови при иммунофенотипировании, отсутствие лимфаденопатии, отсутствие гепатомегалии или спленомегалии, отсутствие симптомов, свидетельствующих о генерализации процесса и удовлетворительных анализов крови; полная ремиссия с неполным восстановлением костного мозга (CRi), в некоторых аспектах описанная как CR выше, но без нормальных анализов крови; частичная ремиссия (PR; также известная в некоторых случаях как частичный ответ), которая в некоторых аспектах описана как ≥ 50%-е падение количества лимфоцитов, ≥ 50%-е сокращение лимфаденопатии или ≥ 50%-е сокращение печени или селезенки, вместе с улучшением количества периферической крови; прогрессирующее заболевание (PD), в некоторых аспектах описанное как ≥ 50%-е повышение количества лимфоцитов до > 5 х 109/л, ≥ 50%-е увеличение лимфаденопатии, ≥ 50%-е увеличение размера печени или селезенки, трансформация Рихтера или новые цитопении вследствие CLL; и стабильное заболевание, в некоторых аспектах описанное как не соответствующее критериям для CR, CRi, PR или PD.
[0309] В некоторых вариантах осуществления пациенты показывают CR или OR, если в течение 1 месяца после введения дозы клеток лимфатические узлы у пациента имеют размер менее чем или приблизительно 20 мм, размер менее чем или приблизительно 10 мм или размер менее чем или приблизительно 10 мм.
[0310] В некоторых вариантах осуществления клон индекса CLL не обнаружен в костном мозге пациента (или в костном мозге более чем 50%, 60%, 70%, 80%, 90% или более пациентов, получающих лечение согласно способам). В некоторых вариантах осуществления клон индекса CLL оценивают шлубоким секвенированием IgH. В некоторых вариантах осуществления клон индекса не детектируется в момент времени, который составляет или приблизительно или по меньшей мере составляет или приблизительно 1, 2, 3, 4, 5, 6, 12, 18 или 24 месяца после введения клеток.
[0311] В некоторых вариантах осуществления пациент показывает морфологическое заболевание, если число бластов в костном мозге превышает или равно 5%, например, как в случае детекции световой микроскопией, например, число бластов в костном мозге более или равно 10%, число бластов в костном мозге более или равно 20%, число бластов в костном мозге более или равно 30%, число бластов в костном мозге более или равно 40%, число бластов в костном мозге более или равно 50%. В некоторых вариантах осуществления пациент показывает полную или клиническую ремиссию, если имеется менее 5% бластов в костном мозге.
[0312] В некоторых вариантах осуществления пациент имеет лейкоз. Степень серьезности заболевания может быть определена оценкой остаточного лейкоза в крови или костном мозге.
[0313] В некоторых вариантах осуществления пациент показывает морфологическое заболевание, если число бластов в костном мозге превышает или равно 5%, например, как в случае детекции световой микроскопией, например, число бластов в костном мозге более или равно 10%, число бластов в костном мозге более или равно 20%, число бластов в костном мозге более или равно 30%, число бластов в костном мозге более или равно 40%, число бластов в костном мозге более или равно 50%. В некоторых вариантах осуществления пациент показывает полную или клиническую ремиссию, если имеется менее 5% бластов в костном мозге.
[0314] В некоторых вариантах осуществления пациент может показывать полную ремиссию, но маленькая пропорция морфологически невыявляемых (методами световой микроскопии) остаточных лейкозных клеток присутствует. Пациент, как говорят, показывает минимальное остаточное заболевание (MRD), если пациент показывает менее 5% бластов в костном мозге и показывает поддающийся обнаружению на молекулярном уровне рак. В некоторых вариантах осуществления поддающийся обнаружению на молекулярном уровне рак может быть оценен с помощью любого множества молекулярных методов, обеспечивающих чувствительное обнаружение небольшого количества клеток. В некоторых аспектах такие методы включают тесты ПЦР, которые могут определить уникальные перестановки рецепторного гена Ig/T-cell или транскрипты слияния, произведенные транслокациями хромосомы. В некоторых вариантах осуществления потоковая цитометрия может использоваться для идентификации раковых клеток на основе специфических для лейкоза иммунофенотипов. В некоторых вариантах осуществления молекулярная диагностика рака может обнаружить только 1 лейкозную клетку на 100000 нормальных клеток. В некоторых вариантах осуществления пациент показывает MRD, который является поддающимся обнаружению на молекулярном уровне, если по меньшей мере или более чем 1 лейкозная клетка на 100000 обнаруживается, например, потоковой цитометрией или ПЦР. В некоторых вариантах осуществления серьезность заболевания пациента на молекулярном уровне недетектируется или MRD-, так что в некоторых случаях никаких лейкозных клеток не может быть обнаружено у пациента с помощью ПЦР или методов потоковой цитометрии.
[0315] В некоторых вариантах осуществления клон индекса лейкоза, например, CLL, не обнаружен в костном мозге пациента (или в костном мозге более чем 50%, 60%, 70%, 80%, 90% или более пациентов, получающих лечение согласно способам). В некоторых вариантах осуществления клон индекса лейкоза, например, CLL, оценивают глубоки секвенированием IGH. В некоторых вариантах осуществления клон индекса не детектируется в момент времени, который составляет или приблизительно или по меньшей мере составляет или приблизительно 1, 2, 3, 4, 5, 6, 12, 18 или 24 месяца после введения клеток.
[0316] В некоторых аспектах MRD детектируется потоковой цитометрией. Потоковая цитометрия может использоваться для мониторинга костного мозга и образцов периферической крови в отношении раковых клеток. В определенных аспектах потоковая цитометрия используется для детекции или мониторинга присутствия раковых клеток в костном мозге. В некоторых аспектах многопараметрическая иммунологическая детекция методом потоковой цитометрии используется для детекции раковых клеток (см., например, Coustan-Smith et al., (1998) Lancet 351:550-554). В некоторых аспектах многопараметрическая иммунологическая детекция методом массовой цитометрии используется для детекции раковых клеток. В некоторых примерах 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 20, 25, 30, 35, 40, 45 или 50 параметров могут использоваться для детекции раковых клеток. Антигены, используемые для детекции, выбирают в зависимости от диагностируемого рака (Foon and Todd (1986) Blood 68:1-31).
[0317] В некоторых примерах костный мозг получают аспиратами костного мозга или биопсиями костного мозга, и лимфоциты выделяют для анализа. Моноклональные и/или поликлональные антитела, конъюгированные с флуорохромом (например, флуоресцеин изотиоцианатом (FITC), фикоэритрином, белком перидинин хлорофилла или биотином), могут использоваться для детекции эпитопов, таких как терминальная деоксинуклеотидил трансфераза (TdT), CD3, CD10, CD11c, CD13, CD14, CD33, CD19, CD20, CD21, CD22, CD23, CD34, CD45, CD56, CD79b, IgM и/или KORSA3544, на изолированных лимфоцитах. Меченные клетки могут быть обнаружены с помощью потоковой цитометрии, такой как многопараметрическая потоковая цитометрия, или массовой цитометрии, для детекции множественных эпитопов.
[0318] Лимфоидные клетки могут быть идентифицированы и сгруппированы на основании точечной диаграммы рассеяния света и затем во вторую очередь сгруппированы на основе идентификации популяции клеток, экспрессирующих представляющие интерес иммунофенотипические признаки. Примеры эпитопов представлены в Таблице 2 ниже. Другая иммунологическая классификация лейкозов и лимфом приведена Foon and Todd (Blood (1986) 68(1): 1-31). В некоторых аспектах оценка потоковой цитометрией MRD может быть осуществлена путем определения количества живых лимфоцитов, имеющих один или более иммунофенотипов CLL (например, низко расположенное вперед-направленное/боковое рассеяние; CD3neg; CD5+; CD14neg; CD19+; CD23+; CD45+; CD56neg).
del(13)(q14,3)
del 11q22-q23
del 17p13 (p53)
t(11;14)(q13;q32) BCL1/IgH перегруппировка
t(14;19)(q32;q13)
IgH делеция (14q32)
del(6q)
+8q24
+3
+18
del 6q21
t(3;V)(q27;V)/ BCL6 Rearr
варианты c-MYC Rearr
t(8;14)+ t(14;18)
t(1;14)(p21;q32): экстранодальная лимфома MALT-типа
del(7)(q22-31): MZBCL селезенки
/+3q: MZBCL нодальная, экстранодальная и селезенки
+/-: положительный в более чем 50% случаев
-/+: положительный в менее чем 50% случаев
-: положительный в <10% случаев
Pan-B маркеры: напр., CD19, CD20, CD79a
sIG: поверхностные иммуноглобулины
cyIg: цитоплазматические иммуноглобулины
[0319] В некоторых аспектах глубокое секвенирование локуса тяжелой цепи иммуноглобулина (IGH) собранных В-клеток может использоваться для детекции минимального остаточного заболевания (MRD). Клональное присутствие особой перестановки IgG может обеспечить маркер детекции присутствия В-клеточных злокачественных опухолей, таких как CLL или NHL, и/или остаточного присутствия злокачественных клеток этих опухолей. В некоторых аспектах клетки, такие как популяция, содержащая или подозреваемая в содержании В-клеток, получают и выделяют из крови. В некоторых аспектах клетки получают и выделяют из костного мозга, например, из аспиратов костного мозга или биопсий костного мозга и/или из других биологических образцов. В некоторых аспектах амплификацию методом полимеразной цепной реакции (ПЦР) определяющей комплементарность области 3 (CDR3) осуществляют с использованием праймеров для высококонсервативных последовательностей в областях V и J локуса гена, который может использоваться для идентификации клональных популяций клеток в целях оценить минимальное остаточное заболевание. Другие способы детекции клональных популяций, такие как подходы секвенирования одиночных клеток, включая предоставляющие информацию относительно числа клеток определенной линии, и/или экспрессия определенной вариабельной цепи, такой как вариабельная область тяжелой цепи или ее связывающий участок, такой как клональная популяция, могут использоваться. В некоторых аспектах ДНК IGH амплифицируют с использованием вырожденных праймеров или праймеров, распознающих вариабельные области цепей, общие для различных клонов клеток, таких как те, которые распознают консенсусные V и вырожденные консенсусные J области последовательности IGH. Примером последовательность вариабельной области является ACACGGCCTCGTGTATTACTGT (SEQ ID NO: 57). Примером вырожденной последовательность консенсусной области J является ACCTGAGGAGACGGTGACC (SEQ ID NO: 58).
[0320] Продукт ПЦР или результат секвенирования в некоторых аспектах являются специфичными для перестроенного аллельного сегмента и служат клональным маркером для детекции MRD. После амплификации ПЦР области CDR3 продукты ПЦР могут быть секвенированы для получения специфических для пациента олигонуклеотидов, сконструированных как зонды для аллель-специфической ПЦР для чувствительной детекции MRD после лечения В-клеточных злокачественных опухолей CAR-T-клеточной терапией, например, CD19 CAR-T-клеточной терапией. В примерах, где продукт ПЦР не генерируют с использованием консенсусных праймеров, вместо этого могут использоваться праймеры, специфичные для семейства V-области для области рамки считывания 1.
[0321] В некоторых аспектах персистирование ПЦР-детектируемых опухолевых клеток, таких как клетки В-клеточной злокачественной опухоли, такой как NHL или CLL, такие как детектируемые последовательности IGH, соответствующие злокачественным или клональным последовательностям IGH, после лечения связано с повышенным риском рецидива. В некоторых аспектах пациенты, которые являются негативными в отношении злокачественных последовательностей IGH после лечения (в некоторых аспектах, даже в контексте других критериев, указывающих прогрессирующее заболевание или только частичный ответ, таких как постоянное увеличение лимфатических узлов или другие критерии, которые могут в некоторых контекстах быть связанными с заболеванием или отсутствием полного ответа), как можно считать, имеют увеличенную вероятность PFS или вступили в CR или длительный CR или пролонгированную выживаемость, по сравнению с пациентами с постоянными злокачественными последовательностями IGH. В некоторых вариантах осуществления такие прогностические и определяющие стадию определения особенно важны для лечений, при которых клиренс злокачественных клеток наблюдается в короткий период времени после введения терапии, например, по сравнению с устранением других клинических симптомов, таких как размер лимфатических узлов или другие определяющие стадию критерии. Например, в некоторых таких аспектах, отсутствие детектируемого IGH или минимальное остаточное заболевание в образце, таком как костный мозг, может быть предпочтительным считыванием ответа или вероятности ответа, или его длительности, по сравнению с другими доступными определениями стадийности или прогностическими подходами. В некоторых аспектах результаты MRD, например, информация глубокого секвенирования IGH, могут дать информацию по дальнейшему вмешательству или его отсутствию. Например, согласно способам и другим вариантам осуществления по изобретению, в некоторых контекстах пациент, который считается негативным в отношении злокачественного IGH, может в некоторых аспектах не получать доплнительного лечения или введения дозы терапии, или пациенту может быть введена более низкая или уменьшенная доза. С другой стороны, может быть установлено или определено, что пациент, показывающий MRD через глубокое секвенирование IGH, может получать дополнительное лечение, например, терапией, первоначально вводимой в подобной или более высокой дозе, или другое средство для лечения. В некоторых аспектах, заболевание или состояние персистирует после введения первой дозы, и/или введение первой дозы не достаточно для устранения заболевания или состояния у пациента.
[0322] В некоторых вариантах осуществления способ уменьшает серьезность заболевания или состояния, например, число опухолевых клеток, размер опухоли, продолжительность выживания пациента или выживания без событий, в большей степени и/или в течение большего промежутка времени по сравнению с уменьшением, которое наблюдалось бы с сопоставимым способом с помощью альтернативного режима дозирования, такого как тот, в котором пациент принимает один или более альтернативных терапевтических агентов, и/или того, в котором пациент не получает дозу клеток и/или агента для лимфодеплеции в соответствии со способами по изобретению, и/или с использованием изделий или композиций по изобретению. В некоторых вариантах осуществления серьезность заболевания или состояния у пациента обнаруживают, оценивают или измеряют. Серьезность заболевания может быть обнаружена в некоторых аспектах путем детекции общего количества клеток заболевания или клеток, ассоциируемых с заболеванием, например, опухолевых клеток, у пациента, или в органе, ткани или физиолоческой жидкости пациента, такой как кровь или сыворотка. В некоторых аспектах оценивают выживаемость пациента, выживаемость в определенном интервале времени, степень выживаемости, наличие или продолжительность выживания без событий, бессимптомного выживания или выживания без рецидивов. В некоторых вариантах осуществления оценивают любой симптом заболевания или состояния. В некоторых вариантах осуществления определяют степень заболевания или серьезность состояния.
[0323] В некоторых вариантах осуществления, выживаемость без событий или полная выживаемость пациента улучшают способами, по сравнению с другими способами, например, способами, в которых пациент принимает один или более альтернативных терапевтических агентов, и/или способом, в котором пациент не получает дозу клеток и/или агента для лимфодеплеции в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению. Например, в некоторых вариантах осуществления, частота или вероятность выживаемости без событий для пациентов, получающих лечение способами, через 6 месяцев после введения составляет более чем приблизительно 40%, более чем приблизительно 50%, более чем приблизительно 60%, более чем приблизительно 70%, более чем приблизительно 80%, более чем приблизительно 90% или более чем приблизительно 95%. В некоторых аспектах полная выживаемость составляет более чем приблизительно 40%, более чем приблизительно 50%, более чем приблизительно 60%, более чем приблизительно 70%, более чем приблизительно 80%, более чем приблизительно 90% или более чем приблизительно 95%. В некоторых вариантах осуществления пациент, получающий лечение способами, демонстрирует выживаемость без событий, выживаемость без рецидивов или выживаемость по меньшей мере 6 месяцев или по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 лет. В некоторых вариантах осуществления, время до прогрессирования усиливается, например, время до прогрессирования составляет более чем или приблизительно 6 месяцев или по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 лет.
[0324] В некоторых вариантах осуществления, после лечения способом, вероятность рецидива уменьшается по сравнению с другими способами, например, способами, в которых пациент принимает один или более альтернативных терапевтических агентов, и/или способом, в котором пациент не получает дозу клеток и/или агента для лимфодеплеции в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению. Например, в некоторых вариантах осуществления, вероятность рецидива в 6 месяцев после первой дозы составляет менее чем приблизительно 80%, менее чем приблизительно 70%, менее чем приблизительно 60%, менее чем приблизительно 50%, менее чем приблизительно 40%, менее чем приблизительно 30%, менее чем приблизительно 20% или менее чем приблизительно 10%.
[0325] В некоторых случаях фармакокинетику вводимых клеток, например, адоптивно переносимых клеток, определяют для оценки доступности, например, биодоступности вводимых клеток. Способы определения фармакокинетики адоптивно переносимых клеток могут включать отбор периферической крови от пациентов, которым вводят генно-инженерные клетки, и определение числа или отношения генно-инженерных клеток в периферической крови. Подходы для отбора и/или выделения клеток могут включать использование специфических к химерному антигенному рецептору (CAR) антител (например, Brentjens et al., Sci. Transl. Med. 2013 Mar; 5(177): 177ra38) Protein L (Zheng et al., J. Transl. Med. 2012 Feb; 10:29), эпитопных меток, таких как последовательности Strep-Tag, введенные непосредственно в активные центры в CAR, посредством чего связывающие реагенты для Strep-Tag используются для прямой оценки CAR (Liu et al. (2016) Nature Biotechnology, 34:430; Публикация международной заявки на патент No. WO2015095895) и моноклональные антитела, специфично связывающиеся с полипептидом CAR (см. Публикация международной заявки на патент No. WO2014190273). Внешние маркерные гены могут в некоторых случаях быть использованы в связи с терапиями генно-инженерными клетками, чтобы обеспечить детекцию или выбор клеток и, в некоторых случаях, также промотировать самоубийство клеток. Усеченный рецептор эпидермального фактора роста (EGFRt) в некоторых случаях может быть коэкспрессирован с представляющим интерес трансгеном (CAR или TCR) в трансдуцированных клетках (см., например, Патент США No. 8,802,374). EGFRt может содержать эпитоп, распознаваемый антителом цетуксимабом (Erbitux®) или другим терапевтическим анти-EGFR антителом, или связывающей молекулой, которая может использоваться для идентификации или выбора клеток, подвергнутых генно-инженерным методам с конструкцией EGFRt и другим рекомбинантным рецептором, таким как химерный антигенный рецептор (CAR), и/или для устранения или отделения клеток, экспрессирующих рецептор. См. патент США No. 8,802,374 и Liu et al., Nature Biotech. 2016 April; 34(4): 430-434.
[0326] В некоторых вариантах осуществления число CAR+ Т-клеток в биологическом образце, полученном от пациента, например, крови, может быть определено в промежуток времени после введения клеточной терапии, например, для определения фармакокинетики клеток. В некоторых вариантах осуществления число CAR+ Т-клеток, необязательно CAR+ CD8+ Т-клеток и/или CAR+ CD4+ Т-клеток, детектируемых в крови пациента или у большинства пациентов, получающих лечение способом, составляет более 1 клетки на мкл, более 5 клеток на мкл или более 10 клеток на мкл.
D. Токсичность
[0327] В некоторых вариантах осуществления способы по изобретению разработаны для или включают признаки, приводящие к более низкой частоте и/или более низкой степени токсичности, токсичного результата или симптома, вызывающего токсичность профиля, фактора или свойства, такого как симптом или результат, ассоциируемый с или показательный для синдрома высвобождения цитокинов (CRS) или нейротоксичности, например, по сравнению с введением альтернативной клеточной терапии, такой как альтернативная композиция CAR+ Т-клеток, и/или альтернативным введением клеток, например, введением клеток, не вводимых в определенном отношении.
[0328] В некоторых вариантах осуществления способы по изобретению не приводят к высокой частоте или вероятности токсичности или токсичных результатов, или уменьшают частоту или вероятность токсичности или токсичных результатов, такой как нейротоксичность (NT), синдром высвобождения цитокинов (CRS), по сравнению с некоторыми другими клеточными терапиями. В некоторых вариантах осуществления способы не приводят к или не увеличивают риск тяжелой NT (sNT), тяжелого CRS (sCRS), синдрома активации макрофагов, синдрома лизиса опухоли, повышения температуры по меньшей мере до или приблизительно до 38 градусов Цельсия в течение трех или более дней и плазменного уровня CRP по меньшей мере до или приблизительно до 20 мг/дл. В некоторых вариантах осуществления, более чем или более чем приблизительно 30%, 35%, 40%, 50%, 55%, 60% или более пациентов, получающих лечение согласно способам по изобретению, не показывают какой-либо степени CRS или какой-либо степени нейротоксичности. В некоторых вариантах осуществления, не более чем 50% получающих лечение пациентов (например, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или более получающих лечение пациентов) демонстрируют синдром высвобождения цитокинов (CRS) выше, чем степени 2, и/или нейротоксичность выше, чем степени 2. В некоторых вариантах осуществления по меньшей мере 50% пациентов, получающих лечение согласно способу (например, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или более получающих лечение пациентов) не показывают тяжелый токсичный результат (например, тяжелый CRS или тяжелую нейротоксичность), такой как нейротоксичность степени 3 или более высокой, и/или не демонстрируют тяжелый CRS или не демонстрируют его в течение определенного периода времени после лечения, например, в течение недели, двух недель или одного месяца после введения клеток. В некоторых вариантах осуществления параметры, оцениваемые для определения определенной токсичности, включают побочные явления (AEs), ограничивающую дозу токсичность (DLTs), CRS и NT.
[0329] Введение адоптивной T-клеточной терапии, такое как лечение Т-клетками, экспрессирующими химерные антигенные рецепторы, может вызвать токсичные эффекты или результаты, такие как синдром высвобождения цитокинов и нейротоксичность. В некоторых примерах такие эффекты или результаты соответствуют высоким уровням циркулирующих цитокинов, которые могут лежать в основе наблюдаемой токсичности.
[0330] В некоторых аспектах токсичный результат представляет собой или ассоциирован с или является показательным для синдрома высвобождения цитокинов (CRS) или тяжелого CRS (sCRS). CRS, например, sCRS, может произойти в некоторых случаях после адоптивной T-клеточной терапии и введения пациентам других биологических продуктов. См. Davila et al., Sci Transl Med 6, 224ra25 (2014); Brentjens et al., Sci. Transl. Med. 5, 177ra38 (2013); Grupp et al., N. Engl. J. Med. 368, 1509-1518 (2013); and Kochenderfer et al., Blood 119, 2709-2720 (2012); Xu et al., Cancer Letters 343 (2014) 172-78.
[0331] Как правило, CRS вызывается чрезмерным системным иммунным ответом, опосредуемым, например, Т-клетками, В-клетками, NK клетками, моноцитами и/или макрофагами. Такие клетки могут высвобождать большую количество воспалительных медиаторов, таких как цитокины и хемокины. Цитокины могут вызывать острый воспалительный ответ и/или вызывать эндотелиальное повреждение органа, которое может приводить к проницаемости капилляров, сердечной недостаточности или смерти. Тяжелый опасный для жизни CRS может привести к легочной инфильтрации и повреждению легкого, почечной недостаточности или диссеминированному внутрисосудистому свертыванию. Другая тяжелая опасная для жизни токсичность может включать кардиальную токсичность, респираторный дистресс-синдром, неврологическую токсичность и/или отказ печени.
[0332] CRS может быть подвергнут лечению с помощью противовоспалительной терапии, такой как анти-IL-6 терапия, например, анти-IL-6 антитело, например, тоцилизумаб, или антибиотики или другие вещества, как описано. Результаты, признаки и симптомы CRS известны и включают описанные здесь. В некоторых вариантах осуществления, в которых определенный режим дозировки или введения оказывает или не оказывает эффект на данный CRS-ассоциированный результат, признак или симптом, определенные результаты, признаки и симптомы и/или их количества или степени могут быть определены.
[0333] В контексте введения CAR-экспрессирующих клеток CRS, как правило, наступает спустя 6-20 дней после вливания клеток, экспрессирующих CAR. См. Xu et al., Cancer Letters 343 (2014) 172-78. В некоторых случаях CRS наступает спустя менее чем 6 дней или более чем 20 дней после вливания CAR Т-клеток. Уровень и время наступления CRS могут быть связаны с начальными уровнями цитокинов или опухолевой нагрузкой во время вливания. Обычно CRS включает увеличенные сывороточные уровни интерферона (IFN)-γ, фактора некроза опухоли (TNF)-α и/или интерлейкина (IL)-2. Другими цитокинами, которые могут быть быстро индуцированы в CRS, являются IL-1β, IL-6, IL-8 и IL-10.
[0334] Примеры результатов, связанные с CRS, включают повышение температуры, дрожь, озноб, гипотензию, одышку, острый респираторный дистресс-синдром (ARDS), энцефалопатию, повышение ALT/AST, почечную недостаточность, сердечно-сосудистые нарушения, гипоксию, неврологические нарушения и смерть. Неврологические осложнения включают делирий, приступоподобную активность, спутанность сознания, затруднения с подбором слов, афазию и/или заторможенность. Другие CRS-связанные результаты включают усталость, тошноту, головную боль, судороги, тахикардию, миалгии, высыпание, острый синдром проницаемости сосудов, ухудшение функции печени и почечную недостаточность. В некоторых аспектах CRS связан с увеличением одного или более факторов, таких как сывороточный ферритин, d-димер, аминотрансферазы, лактатдегидрогеназа и триглицериды, или с гипофибриногенемией или гепатоспленомегалией. Другие примеры признаков или симптомов, связанных с CRS, включают гемодинамическую нестабильность, лихорадочную нейтропению, увеличение сывороточного С-реактивного белка (CRP), изменения параметров коагуляции (например, международного коэффициента нормализации (INR), протромбинового индекса (PTI) и/или фибриногена), изменения функции сердца и другого органа и/или абсолютное число нейтрофилаов(ANC).
[0335] В некоторых вариантах осуществления результаты, связанные с CRS, включают один или более из следующего: персистирующая лихорадка, например, лихорадка с повышением температуры, например, до более чем или приблизительно 38 градусов Цельсия, в течение двух или более, например, трех или более, например, четырех или более дней или в течение по меньшей мере трех дней подряд; повышение температуры до более чем или приблизительно 38 градусов Цельсия; повышение цитокинов, такое как максимальное кратное изменение, например, по меньшей мере или приблизительно 75, по сравнению с уровнями перед лечением, по меньшей мере двух цитокинов (например, по меньшей мере двух из группы, состоящей из интерферона (IFNγ), GM-CSF, IL-6, IL-10, Flt-3L, фракталкина и IL-5 и/или альфа фактора некроза опухоли (TNFα)), или максимальное кратное изменение, например, по меньшей мере или приблизительно 250, по меньшей мере одного из таких цитокинов; и/или по меньшей мере один клинический признак токсичности, такой как гипотензия (например, при измерении по меньшей мере одним внутривенным вазоактивным вазопрессорным средством); гипоксия (например, плазменные уровни кислорода (PO2) менее чем или приблизительно 90%); и/или одно или более неврологических нарушений (включая изменения психического статуса, оглушенное состояние и судороги).
[0336] Примеры CRS-ассоциированных результатов включают увеличенные или высокие сывороточные уровни одного или более факторов, включая цитокины и хемокины и другие факторы, ассоциированные с CRS. Примеры результатов дополнительно включают увеличения синтеза или секреции одного или более таких факторов. Такой синтез или секреция могут осуществляться Т-клеткой или клеткой, взаимодействующей с Т-клеткой, такой как клетка врожденной иммунной системы или В-клетка.
[0337] В некоторых вариантах осуществления CRS-ассоциированные сывороточные факторы или CRS-ассоциированные результаты включают воспалительные цитокины и/или хемокины, включая интерферон (IFN-γ), TNF-a, IL-1β, IL-2, IL-6, IL-7, IL-8, IL-10, IL-12, sIL-2Ra, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), макрофагальный воспалительный белок (MIP)-1, альфа фактор некроза опухоли (TNFα), IL-6 и IL-10, IL-1β, IL-8, IL-2, MIP-1, Flt-3L, фракталкин и/или IL-5. В некоторых вариантах осуществления фактор или результат включает C-реактивный белок (CRP). В дополнение к тому, что он является ранним и легко измеримым фактором риска CRS, CRP также является маркером роста клеток. В некоторых вариантах осуществления пациенты, у которых измерены высокие уровни CRP, такие как ≥ 15 мг/дл, имеют CRS. В некоторых вариантах осуществления пациенты, у которых измерены высокие уровни CRP, не имеют CRS. В некоторых вариантах осуществления измерение CRS включает измерение CRP и другого фактора, являющегося показательным для CRS.
[0338] В некоторых вариантах осуществления один или более воспалительных цитокинов или хемокинов мониторят до, во время или после лечения CAR. В некоторых аспектах один или более цитокинов или хемокинов включают IFN-γ, TNF-α, IL-2, IL-1β, IL-6, IL-7, IL-8, IL-10, IL-12, sIL-2Rα, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) или макрофагальный воспалительный белок (MIP). В некоторых вариантах осуществления осуществляют мониторинг IFN-γ, TNF-α и IL-6.
[0339] Были разработаны критерии CRS, которые, по-видимому, коррелируют с началом CRS для предсказания того, какие пациенты, более вероятно, имеют риск развития sCRS (см. Davilla et al. Science translational medicine. 2014;6(224):224ra25). Факторы включают повышение температуры, гипоксию, гипотензию, неврологические изменения, увеличенные сывороточные уровни воспалительных цитокинов, таких как ряд семи цитокинов (IFNγ, IL-5, IL-6, IL-10, Flt-3L, фракталкин и GM-CSF), чье вызванное лечением увеличение может хорошо коррелировать как с опухолевой нагрузкой перед лечением, так и с sCRS симптомами. Другие рекомендации по диагностике и контролю CRS известны (см., например, Lee et al, Blood. 2014;124(2):188-95). В некоторых вариантах осуществления критерии, отражающие степень CRS, представлены в Таблице 3 ниже.
Слабая
Умеренная
Потребность в кислороде <40%, или
Гипотензия, чувствительная к жидкостям или низкой дозе единственного вазопрессорного средства, или
Степень 2 органотоксичности (CTCAE v4,0)
Тяжелая
Потребность в кислороде ≥ 40%, или
Гипотензия, требующая большей дозы единственного вазопрессорного средства (например, норэпинефрин ≥ 20 мг/кг/мин, допамин ≥ 10 мг/кг/мин, фенилэфрин ≥ 200 мг/кг/мин или адреналин ≥ 10 мг/кг/мин), или
Гипотензия, требующая множественных вазопрессорных средств (например, вазопрессин+один из вышеупомянутых агентов или комбинация вазопрессорных средств, эквивалентная ≥ 20 мг/кг/мин норэпинефрина), или
Степень 3 органотоксичности или Степень 4 трансаминита (CTCAE v4,0)
Опасная для жизни
Требует ИВЛ, или
Степень 4 органотоксичности (исключая трансаминит)
Летальная
[0340] В некоторых вариантах осуществления у пациента, как считается, развивается “тяжелый CRS” («sCRS») в ответ на или после введения клеточной терапии или дозы клеток, если после введения пациент демонстрирует: (1) повышение температуры по меньшей мере до 38 градусов Цельсия в течение по меньшей мере трех дней; (2) повышение цитокинов, включающее либо (a) максимальное кратное изменение по меньшей мере 75 для по меньшей мере двух из следующей группы из семи цитокинов по сравнению с уровнем непосредственно после введения: интерферон (IFNγ), GM-CSF, IL-6, IL-10, Flt-3L, фракталкин и IL-5 и/или (b) максимальное кратное изменение по меньшей мере 250 для по меньшей мере одного из следующей группы из семи цитокинов по сравнению с уровнем непосредственно после введения: интерферон (IFNγ), GM-CSF, IL-6, IL-10, Flt-3L, фракталкин и IL-5; и (c) по меньшей мере один клинический признак токсичности, такой как гипотензия (требующая по меньшей мере одного внутривенного вазоактивного вазопрессорного средства) или гипоксия (PO2 <90%), или одно или более неврологических нарушений (включая изменения психического статуса, оглушенное состояние и/или судороги). В некоторых вариантах осуществления тяжелый CRS включает CRS степени 3 или более, такой как сформулированный в Таблице 3.
[0341] В некоторых вариантах осуществления результаты, ассоциированные с тяжелым CRS или CRS степени 3 или более, такой как степени 4 или более, включают один или более из следующих: персистирующая лихорадка, например, лихорадка с указанной температурой, например, более чем или приблизительно 38 градусов Цельсия, в течение двух или более, например, трех или более, например, четырех или более дней или в течение по меньшей мере трех дней подряд; повышение температуры до более чем или приблизительно 38 градусов Цельсия; повышение цитокинов, такое как максимальное кратное изменение, например по меньшей мере или приблизительно 75, по сравнению с уровнями перед лечением по меньшей мере двух цитокинов (например, по меньшей мере двух из группы, состоящей из интерферона (IFNγ), GM-CSF, IL-6, IL-10, Flt-3L, фракталкина и IL-5 и/или альфа фактора некроза опухоли (TNFα)), или максимальное кратное изменение, например, по меньшей мере или приблизительно 250 по меньшей мере одного из таких цитокинов; и/или по меньшей мере один клинический признак токсичности, такой как гипотензия (например, при измерении по меньшей мере одним внутривенным вазоактивным вазопрессорным средством); гипоксия (например, плазменные уровни кислорода (PO2) менее чем или приблизительно 90%); и/или одно или более неврологических нарушений (включая изменения психического статуса, оглушенное состояние и судороги). В некоторых вариантах осуществления тяжелый CRS включает CRS, требующий контроля или лечения в палате интенсивной терапии (ICU).
[0342] В некоторых вариантах осуществления CRS, такой как тяжелый CRS, охватывает комбинацию (1) персистирующей лихорадки (повышение температуры до по меньшей мере 38 градусов Цельсия в течение по меньшей мере трех дней) и (2) сывороточного уровня CRP по меньшей мере по или приблизительно 20 мг/дл. В некоторых вариантах осуществления CRS охватывает гипотензию, требующую использования двух или более вазопрессорных средств, или нарушение дыхания, требующее искусственной вентиляции. В некоторых вариантах осуществления дозировку вазопрессорных средств увеличена при втором или последующем введении.
[0343] В некоторых вариантах осуществления тяжелый CRS или CRS степени 3 охватывает увеличение аланинаминотрансферазы, увеличение аспартатаминотрансферазы, озноб, фебрильную нейтропению, головную боль, левожелудочковую дисфункцию, энцефалопатию, гидроцефалию и/или тремор.
[0344] Способ измерения или детекции различных результатов может быть определен.
[0345] В некоторых аспектах токсичный результат представляет собой или связан с нейротоксичностью. В некоторых вариантах осуществления симптомы, связанные с клиническим риском нейротоксичности, включают спутанное состояние сознания, делирий, афазию, экспрессивную афазию, оглушенное состояние, миоклонус, летаргию, измененный психический статус, конвульсии, приступоподобную активность, судороги (необязательно подтвержденные электроэнцефалограммой [ЭЭГ]), повышенные уровни бета амилоида (Aβ), повышенные уровни глутамата и повышенные уровни радикалов кислорода. В некоторых вариантах осуществления нейротоксичность классифицирована на основе серьезности (например, с использованием шкалы 1-5 (см., например, Guido Cavaletti & Paola Marmiroli Nature Reviews Neurology 6, 657-666 (December 2010); National Cancer Institute-Common Toxicity Criteria version 4,03 (NCI-CTCAE v4,03).
[0346] В некоторых случаях неврологические симптомы могут быть самыми ранними симптомами sCRS. В некоторых вариантах осуществления неврологические симптомы, по наблюдениям, начинаются спустя 5-7 дней после вливания клеточной терапии. В некоторых вариантах осуществления продолжительность неврологических изменений может составлять от 3 до 19 дней. В некоторых случаях восстановление неврологических изменений происходит после того, как устранены другие симптомы sCRS. В некоторых вариантах осуществления, время или степень устранения неврологических изменений не ускоряется лечением анти-IL-6 и/или стероидом(ами).
[0347] В некоторых вариантах осуществления у пациента, как считается, развивается “тяжелая нейротоксичность” в ответ на или после введения клеточной терапии или дозы клеток, если после введения пациент демонстрирует симптомы, ограничивающие самопомощь (например, купание, перевязывание и разбинтовывание, кормление, пользование туалетом, прием лекарств) из числа: 1) симптомы периферической моторной невропатии, включая воспаление или дегенерацию периферических двигательных нервов; 2) симптомы периферической сенсорной невропатии, включая воспаление или дегенерацию периферических чувствительных нервов, дисестезии, такие как искажение сенсорного восприятия, приводящее к аномальным и неприятным ощущениям, невралгию, такую как интенсивные болезненные ощущения вдоль нерва или группы нервов, и/или парестезии, такие как функциональные нарушения сенсорных нейронов, приводящие к патологическим кожным ощущениям покалывания, онемения, давления, холода и тепла в отсутствие стимула. В некоторых вариантах осуществления тяжелая нейротоксичность включает нейротоксичность степени 3 или более, такой как сформулировано в Таблице 4.
Бессимптомная или слабая
Умеренная
Тяжелая
Опасная для жизни
летальная
[0348] В некоторых вариантах осуществления способы уменьшают симптомы, ассоциированные с CRS или нейротоксичностью, по сравнению с другими способами. В некоторых аспектах способы по изобретению уменьшают симптомы, результаты или факторы, ассоциированные с CRS, включая симптомы, результаты или факторы, ассоциированные с тяжелым CRS или CRS степени 3 или выше, по сравнению с другими способами. Например, пациенты, получающие лечение согласно способам по изобретению, могут не иметь детектируемых симптомов, результатов или факторов CRS и/или иметь уменьшенные симптомы, результаты или факторы CRS, например, тяжелый CRS или CRS степени 3 или выше, такой как любой описанный, например, сформулированный в Таблице 3. В некоторых вариантах осуществления пациенты, получающие лечение согласно способам по изобретению, могут иметь уменьшенные симптомы нейротоксичности, такие как слабость или онемение в конечностях, снижение памяти, зрения и/или интеллекта, обсессивное и/или компульсивное поведение, не поддающееся контролю, галлюцинации, головную боль, когнитивные и поведенческие проблемы, включая потерю регуляции моторики, ухудшение когнитивной функции и дисфункцию автономной нервной системы и сексуальную дисфункцию, по сравнению с пациентами, получающими лечение другими способами. В некоторых вариантах осуществления пациенты, получающие лечение согласно способам по изобретению, могут иметь уменьшенные симптомы, связанные с периферической моторной невропатией, периферической сенсорной невропатией, дизэстезией, невралгией или парестезией.
[0349] В некоторых вариантах осуществления способы уменьшают результаты, связанные с нейротоксичностью, включая повреждения нервной системы и/или мозга, такие как гибель нейронов. В некоторых аспектах способы уменьшают уровень факторов, связанных с нейротоксичностью, такие как бета амилоид (Aβ), глутамат и радикалы кислорода.
[0350] В некоторых вариантах осуществления результатом токсичности является ограничивающая дозу токсичность (DLT). В некоторых вариантах осуществления токсичным результатом является ограничивающая дозу токсичность. В некоторых вариантах осуществления токсичным результатом является отсутствие ограничивающей дозу токсичности. В некоторых вариантах осуществления ограничивающая дозу токсичность (DLT) определяется как токсичность степени 3 или более высокой, по оцененке любыми известными или опубликованными рекомендациями для оценки определенной токсичности, такими как любая из описанных выше и включая Common Terminology Criteria for Adverse Events (CTCAE) version 4,0, опубликованные National Cancer Institute (NCI).
[0351] В некоторых вариантах осуществления низкая частота, риск или вероятность развития токсичности, например, CRS или нейротоксичности или тяжелого CRS или нейротоксичности, например, CRS или нейротоксичности стадии 3 или выше, наблюдаемая с введением дозы Т-клеток в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, позволяет осуществлять введение клеточной терапии на амбулаторной основе. В некоторых вариантах осуществления введение клеточной терапии, например, дозы Т-клеток (например, CAR+ Т-клеток) в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, осуществляется на амбулаторной основе или не требует допуска пациента в больницу, такого как допуск в больницу, требующий оставления на ночь.
[0352] В некоторых аспектах пациентам, которым вводят клеточную терапию, например, дозу Т-клеток (например, CAR+ Т-клеток) в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, включая пациентов, получающих лечение на амбулаторной основе, не вводят вмешательство для лечения какой-либо токсичности до или с введением дозы клеток, если или пока пациент не демонстрирует признак или симптом токсичности, такой как нейротоксичность или CRS. Примеры агентов для лечения, задержки, уменьшения или облегчения токсичности описаны в Разделе II.
[0353] В некоторых вариантах осуществления, если пациент, которому вводят клеточную терапию, например, дозу Т-клеток (например, CAR+ Т-клеток), включая пациентов, получающих лечение на амбулаторной основе, показывает повышение температуры, пациенту предписывают или назначают лечение для снижения температуры. В некоторых вариантах осуществления повышение температуры у пациента характеризуется как температура тела пациента, которая составляет (или измерена как таковая) температуру на уровне или выше температуры определенного порога или уровня. В некоторых аспектах пороговая температура представляет собой температуру, который ассоциирована с по меньшей мере субфебрильным повышением температуры, с по меньшей мере умеренной повышением температуры и/или с по меньшей мере сильным повышением температуры. В некоторых вариантах осуществления пороговая температура является определенной температурой или диапазоном. Например, пороговая температура может составлять или приблизительно составлять, или по меньшей мере приблизительно составлять или приблизительно приблизительно составлять 38, 39, 40, 41 или 42 градуса Цельсия, и/или может быть находиться в диапазоне от или от приблизительно 38 градусов Цельсия до или до приблизительно 39 градусов Цельсия, в диапазоне от или от приблизительно 39 градусов Цельсия до или до приблизительно 40 градусов Цельсия, в диапазоне от или от приблизительно 40 градусов Цельсия до или до приблизительно 41 градусов или в диапазоне от или от приблизительно 41 градуса Цельсия до или до приблизительно 42 градусов Цельсия.
[0354] В некоторых вариантах осуществления лечение, разработанное для снижения температуры, включает лечение жаропонижающим средством. Жаропонижающее средство может включать любой агент, например, соединение, композицию или ингредиент, снижающий температуру, такой как любое число агентов, которые известны как имеющие жаропонижающие эффекты, таких как NSAID (такие как ибупрофен, напроксен, кетопрофен и нимесулид), салицилаты, такие как аспирин, холин салицилат, салицилат магния и салицилат натрия, парацетамол, ацетоаминофен, метамизол, набуметон, фенаксон, антипирин, антипиретики. В некоторых вариантах осуществления жаропонижающее средство является ацетоаминофеном. В некоторых вариантах осуществления ацетоаминофен может быть введен в дозе 12,5 мг/кг перорально или внутривенно с частотой до одного раза в четыре часа. В некоторых вариантах осуществления жаропонижающее средство представляет собой или включает ибупрофен или аспирин.
[0355] В некоторых вариантах осуществления, если повышение температуры является длительным повышением температуры, пациенту вводят альтернативное лечение для лечения токсичности, такое как любое описанный в Разделе II ниже. Для пациентов, получающих лечение на амбулаторной основе, пациенту предписывают возвратиться в больницу, если пациент имеет и/или для него установлено или имеет длительное повышение температуры. В некоторых вариантах осуществления пациент имеет и/или для него установлено или, как считается, имеет, длительное повышение температуры, если он или она показывает повышение температуры на уровне или выше соответствующей пороговой температуры, и где повышение температуры или температура тела пациента не уменьшается, или не уменьшается на или более, чем на указанную величину (например, более чем на 1 °C, и обычно не колеблется приблизительно или более чем приблизительно на 0,5 °C, 0,4 °C, 0,3°C или 0,2 °C) после указанного лечения, такого как лечение, разработанное для уменьшение температуры, такое как лечение жаропонижающим средством, например, NSAID или салицилатами, например, ибупрофеном, ацетоаминофеном или аспирином. Например, считается, что пациент имеет длительное повышение температуры, если он или она показывает или для него определено повышение температуры по меньшей мере до или приблизительно до 38 или 39 градусов Цельсия, которое не уменьшается или не уменьшается более чем на или приблизительно на 0,5 °C, 0,4 °C, 0,3°C или 0,2 °C, или на или приблизительно на 1%, 2%, 3%, 4% или 5%, в течение 6 часов, в течение 8 часов или в течение 12 часов, или в течение 24 часов, даже после лечения жаропонижающим, таким как ацетоаминофен. В некоторых вариантах осуществления дозировка жаропонижающего средства является дозировкой, обычно эффективной для такого пациента для уменьшения температуры или уменьшения повышения температуры определенного типа, такого как повышение температуры, связанное с бактериальной или вирусной инфекцией, например, локализованной или общей инфекцией.
[0356] В некоторых вариантах осуществления пациент имеет, и/или для него определено или считается, что он имеет длительное повышение температуры, если он или она показывает повышение температуры до или выше соответствующей пороговой температуры, и где повышение температуры или температура тела пациента не колеблются приблизительно или более, чем приблизительно на 1 °C, и обычно не колеблются приблизительно, или более, чем приблизительно на 0,5 °C, 0,4 °C, 0,3°C или 0,2 °C. Такое отсутствие колебания выше или на определенную величину обычно измеряют за установленный период времени (например, за 24-часовой, 12-часовой, 8-часовой, 6-часовой, 3-часовой или 1-часовой промежуток времени, который может быть измерен от первого симптома повышения температуры или первой температуры выше обозначенного порога). Например, в некоторых вариантах осуществления, считается, что пациент показывает, или для него определено, что он показывает пролонгированное повышение температуры, если он или она показывает повышение температуры по меньшей мере до или приблизительно или по меньшей мере до или приблизительно 38 или 39 градусов Цельсия, которая не колеблется на более чем или приблизительно 0,5°C, 0,4 °C, 0,3°C или 0,2°C в течение 6 часов, в течение 8 часов или в течение 12 часов, или в течение 24 часов.
[0357] В некоторых вариантах осуществления повышение температуры является длительным повышением температуры; в некоторых аспектах пациент получает лечение в момент времени, в который для пациента было определено длительное повышение температуры, такой как в один, два, три, четыре, пять, шесть или менее часов от такого определения или первого такого определения после начальной терапии, имеющей потенциал для стимуляции токсичности, такой как клеточная терапия, такая как доза Т-клеток, например, CAR+ Т-клеток.
[0358] В некоторых вариантах осуществления одно или более вмешательств или агентов для лечения токсичности, таких как направленные на токсичность терапии, вводят в момент времени, в который или непосредственно после которого для пациента определено или подтверждено (например, сначала определено или подтверждено), длительное повышение температуры, например, при измерении согласно любому из вышеупомянутых вариантов осуществления. В некоторых вариантах осуществления одну или более направленных на токсичность терапий вводят в определенный период времени после такого подтверждения или определения, такой как в течение 30 минут, 1 часа, 2 часов, 3 часов, 4 часов, 6 часов или 8 часов.
E. Биомаркеры, аналиты или параметры
[0359] Среди способов по изобретению можно назвать способы оценки риска развития токсичности, связанной с клеточной терапией у пациента, включающие оценку или обнаружение биомаркеров (например, аналитов) или параметров, связанных с токсичностью, например, нейротоксичностью, такой как тяжелая нейротоксичность, и/или CRS, такой как тяжелый CRS. Также среди способов по изобретению можно назвать способы оценки вероятности ответа на клеточную терапию у пациента, включающие оценку или обнаружение биомаркеров (например, аналитов) или параметров, связанных с результатом ответа, такого как объективный ответ (OR), включая полный ответ (CR) и частичный ответ (PR). В некоторых вариантах осуществления ассоциированный результат ответа включает длительный ответ, такой как ответ, который длится в течение 3 месяцев, 6 месяцев, 9 месяцев 12 месяцев или более после начального ответа.
[0360] В некоторых вариантах осуществления способы включают оценку или обнаружение наличия или отсутствия одного или группы биомаркеров (например, аналитов) и/или параметров (например, концентрации, количества, уровня или активности), связанных с одним или группой биомаркеров (например, аналитов). В некоторых случаях способы могут включать сравнение одного или более параметров с определенным референсным значением, таким как пороговое значение (также называемое здесь «пороговым значением»), например, связанным с риском развития токсичности или связанным с определенным ответом, таким как OR, CR или PR, или длительным ответом, таким как ответ, который длится в течение 3 месяцев, 6 месяцев, 9 месяцев, 12 месяцев или более после начального ответа. В некоторых вариантах осуществления способы также включают выбор пациентов для лечения клеточной терапией на основе оценки наличия или отсутствия биомаркера и/или сравнения биомаркеров с референсным значением или пороговым значением биомаркера. В некоторых вариантах осуществления способы также включают введение агента или терапии, которая может обработать, предотвратить, задержать и/или уменьшить развитие токсичности, например, на основе оценки наличия или отсутствия биомаркера и/или сравнения биомаркеров с референсным значением или пороговым значением биомаркера.
[0361] В некоторых вариантах осуществления способы включают оценку вероятности ответа пациента или риска развития токсичности после введения клеточной терапии. В некоторых вариантах осуществления способы включают оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем биологический образец происходит от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и биологический образец получен от пациента до применения клеточной терапии, и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки. В некоторых аспектах способы включают сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением, с определением, таким образом, риска развития токсичности после введения клеточной терапии. В некоторых аспектах сравнения могут использоваться для определения вероятности ответа пациента или риска развития токсичности после введения клеточной терапии.
[0362] В некоторых вариантах осуществления способы также включают выбор пациентов для лечения клеточной терапией, такой как определенная доза клеточной терапии, включая введение определенной дозы клеточной терапии, такой как описанные здесь, например, в Разделе I.A и I.B, на основе оценки наличия или отсутствия биомаркера и/или сравнения биомаркеров с референсным значением или пороговым значением биомаркера. В некоторых вариантах осуществления способы также включают выбор пациентов для лечения дополнительным агентом, таким как агент или другое средство для лечения, способное к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, на основе оценки наличия или отсутствия биомаркера и/или сравнения биомаркеров с референсным значением или пороговым значением биомаркера.
[0363] В некоторых вариантах осуществления параметр представляет собой или включает признаки, факторы, характеристику пациента и/или заболевания или состояния. В некоторых вариантах осуществления параметр является параметром, относящимся к опухолевой нагрузке, например, измерением опухолевой массы. В некоторых аспектах способы также включают дальнейший контроль пациента на возможные симптомы токсичности на основе риска токсичности, определенного оценкой наличия или отсутствия биомаркера и/или сравнением биомаркеров с референсным значением или пороговым значением биомаркера. В некоторых аспектах биологический образец, например, образец крови или образец ткани от пациента, может быть получен для детекции наличия или отсутствия биомаркера (например, аналита), например, для детекции или измерения параметра (например, концентрации, количества, уровня или активности) биомаркера и/или оценки наличия биомаркера, для анализа, корреляции и/или обнаружения определенных результатов и/или токсичности. В некоторых вариантах осуществления определенные физиологические или биологические параметры, связанные с биомаркером, включая экспрессию биомаркеров, и/или клинические и лабораторные параметры, могут быть оценены в биологическом образце, например, крови, от пациентов до или после введения клеточной терапии. В некоторых вариантах осуществления биомаркеры экспрессии или аналиты и/или клинические и лабораторные параметры могут быть оценены в биологическом образце, например, крови, от пациентов перед введением клеточной терапии (предварительное оечение). В некоторых вариантах осуществления биомаркеры экспрессии или аналиты и/или клинические и лабораторные параметры могут быть оценены в биологическом образце, например, крови, от пациентов после введения клеточной терапии (последующее лечение). В некоторых вариантах осуществления концентрация, количество, уровень или активность биомаркеров (например, аналитов) и/или клинические и лабораторные параметры могут быть оценены в один или более моментов времени до или после введения клеточной терапии. В некоторых вариантах осуществления могут также быть определены пиковая концентрация, количество, уровень или активность биомаркеров (например, аналитов) и/или клинические и лабораторные параметры в течение установленного периода времени.
[0364] В некоторых вариантах осуществления биомаркер или аналит представляет собой объективно измеримую характеристику или молекулу, экспрессируемую биологическим образцом или в биологическом образце, включая клетки, которые могут быть индикативными или связанными с определенным состоянием или явлением, такими как биологический процесс, терапевтический результат, фенотип клеток или болезненный статус. В некоторых аспектах биомаркер или аналит или параметры, связанные с биомаркером или аналитом, могут быть измерены или обнаружены. Например, может быть обнаружено наличие или отсутствие экспрессии биомаркера или аналита. В некоторых аспектах могут быть измерены или обнаружены такие параметры, как концентрация, количество, уровень или активность биомаркера или аналита. В некоторых вариантах осуществления наличие, отсутствие, экспрессия, концентрация, количество, уровень и/или активность биомаркера могут быть связаны с, коррелировать с, быть показательными для и/или прогностическими для определенных состояний, таких как определенные терапевтические результаты или состояния пациента. В некоторых аспектах наличие, отсутствие, экспрессия, концентрация, количество, уровень и/или активность биомаркера или аналита, такого как любой описанный здесь, может использоваться для оценки вероятности определенного результата или состояния, такого как определенный терапевтический результат, включая результат ответа или результат токсичности. В некоторых вариантах осуществления примеры биомаркеров включают цитокины, молекулы поверхности клеток, хемокины, рецепторы, растворимые рецепторы, растворимые сывороточные белки и/или продукты расщепления. В некоторых вариантах осуществления биомаркеры или аналиты могут также включать определенные признаки, факторы, характеристики пациента и/или заболевания или состояния или факторы, показательные для состояния пациента и/или заболевания или состояния пациента (включая серьезность заболевания), и/или клинические или лабораторные параметры.
[0365] В некоторых вариантах осуществления биомаркеры могут использоваться отдельно или в комбинации с другими биомаркерами, например, в панели биомаркеров. В некоторых вариантах осуществления экспрессия определенных биомаркеров может коррелировать с определенными результатами или токсичностью, например, развитием нейротоксичности. В некоторых вариантах осуществления, биомаркеры (например, аналиты), включая их параметры, которые могут быть оценены, включают лактатдегидрогеназу (LDH), ферритин, C-реактивный белок (CRP), Интерлейкин-6 (IL-6), IL-7, IL-8, IL-10, IL-15, IL-16, альфа фактор некроза опухоли (TNF-α), интерферон альфа 2 (IFN-α2), моноцитарный хемоаттрактантный белок-1 (MCP-1), макрофагальный воспалительный белок 1 альфа (MIP-1α), макрофагальный воспалительный белок 1 бета (MIP-1β), эотаксин, гранулоцитарный колониестимулирующий фактор (G-CSF), альфа рецептор IL-1 (IL-1Rα), IL-1β, IFN-γ-индуцируемый белок 10 (IP-10), перфорин и D-димер (продукт распада фибрина). В некоторых вариантах осуществления биомаркеры (например, аналиты), включая их параметры, включают LDH, ферритин, CRP, IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β. В некоторых вариантах осуществления, биомаркеры (например, аналиты), включая их параметры, включают ферритин, CRP, D-димер, IL-6, IL-15, TNF-α и MIP-1α. В некоторых вариантах осуществления биомаркеры (например, аналиты), включая их параметры, включают ферритин, CRP, IL-10, IL-15, IL-16, TNF-α или MIP-1β.
[0366] В некоторых вариантах осуществления способы включают обнаружение наличия или отсутствия одного или более биомаркеров, таких как параметр (например, концентрация, количество, уровень или активность), связанный с одним или более биомаркерами, в которых один или более биомаркеров выбраны из числа Лактатдегидрогеназы (LDH), ферритина, С-реактивного белка (CRP), Интерлейкина-6 (IL-6), IL-7, IL-8, IL-10, IL-15, IL-16, альфа фактора некроза опухоли (TNF-α), интерферона альфа 2 (IFN-α2), моноцитарного хемоаттрактантного белка-1 (MCP-1), макрофагального воспалительного белка 1 альфа (MIP-1α), макрофагального воспалительного белка 1 бета (MIP-1β), эотаксина, гранулоцитарного колониестимулирующего фактора (G-CSF), альфа рецептора IL-1 (IL-1Rα), IL-1β, IFN-γ-индуцибельного Белка 10 (IP-10), перфорина и D-димера (продукт распада фибрина).
[0367] В некоторых вариантах осуществления оцениваемый параметр представляет собой или включает признаки, факторы, характеристику пациента и/или заболевания или состояния и/или экспрессии биомаркеров. В некоторых вариантах осуществления параметр представляет собой или включает один или более факторов, показательных для статуса пациента и/или заболевания или состояния пациента. В некоторых вариантах осуществления параметр показателен для опухолевой массы. В некоторых вариантах осуществления фактор, показательный для опухолевой массы, представляет собой объемный параметр опухоли(ей). В некоторых вариантах осуществления объемный параметр представляет собой размер поражения(й), такой как размер опухоли, диаметр опухоли, объем опухоли, масса опухоли, опухолевая нагрузка, связанный с опухолью отек, связанный с опухолью некроз и/или число или степень метастазов. В некоторых вариантах осуществления объемный параметр опухоли представляет собой двухмерный размер. Например, в некоторых вариантах осуществления, область поражения(й) вычисляют как продукт самого длинного диаметра и самого длинного перпендикулярного диаметра всех измеримых опухолей. В некоторых случаях объемный параметр опухоли представляет собой одномерный размер. В некоторых случаях размер измеримых поражений оценивают как самый длинный диаметр. В некоторых вариантах осуществления измеряют сумму продуктов диаметров (SPD), самые длинные диаметры опухоли (LD), сумму самых длинных диаметров опухоли (SLD), некроз, объем опухоли, объем некроза, отношение некроза к опухоли (NTR), околоопухолевый отек (PTE) и отношение отека к опухоли (ETR).
[0368] Примеры способов измерения и оценки опухолевой массы включают описанные в, например, Carceller et al., Pediatr Blood Cancer. (2016) 63(8):1400-1406 and Eisenhauer et al., Eur J Cancer. (2009) 45(2):228-247. В некоторых вариантах осуществления объемный параметр представляет собой сумму продуктов диаметров (SPD), измеренную путем определения суммы продуктов самых больших перпендикулярных диаметров всех измеримых опухолей. В некоторых аспектах опухоль или поражение измеряют в одном измерении с самым длинным диаметром (LD) и/или путем определения суммы самых длинных диаметров опухоли (SLD) всех измеримых поражений. В некоторых вариантах осуществления объемный параметр опухоли представляет собой объемное определение количества некроза опухоли, такого как объем некроза и/или отношения некроза к опухоли (NTR), см. Monsky et al., Антирак Res. (2012) 32 (11): 4951-4961. В некоторых аспектах объемный параметр опухоли представляет собой объемное определение количества связанного с опухолью отека, такого как околоопухолевый отек (PTE), и/или отношения отека к опухоли (ETR). В некоторых вариантах осуществления измерение может быть осуществлено с помощью методов отображения, таких как компьютерная томография (CT), эмиссионная позитронная томография (PET) и/или магнитно-резонансная томография (MRI) пациента.
[0369] В некоторых вариантах осуществления объемный параметр опухоли определяют в процедуре скрининга, такой как обычная оценка или взятие крови, чтобы подтвердить и/или идентифицировать состояние или заболевание у пациента.
[0370] В некоторых вариантах осуществления наличие или отсутствие и/или параметр одного или более биомаркеров (например, аналитов) оценивают в биологическом образце. В некоторых аспектах биологический образец является физической жидкостью или тканью. В некоторых таких вариантах осуществления биологический образец, например, физическая жидкость, представляет собой или содержит цельную кровь, сыворотку или плазму.
[0371] В некоторых вариантах осуществления, наличие или отсутствие и/или параметр одного или более биомаркеров (например, аналитов) оценивают до введения клеточной терапии (например, предварительного вливания), например, полученной до 2 дней, до 7 дней, до 14 дней, до 21 дня, до 28 дней, до 35 дней или до 40 дней до инициации введения генно-инженерных клеток. В некоторых вариантах осуществления биологический образец получен от пациента до введения клеточной терапии (например, предварительного вливания), например, получен до 2 дней, до 7 дней, до 14 дней, до 21 дня, до 28 дней, до 35 дней или до 40 дней до инициации введения генно-инженерных клеток.
[0372] В некоторых вариантах осуществления биологический образец является образцом афереза или лейкафереза. В некоторых вариантах осуществления оценивают присутствие или отсутствие и/или параметр одного или более биомаркеров (например, аналитов), или биологический образец получен после введения клеточной терапии. В некоторых вариантах осуществления реагенты могут использоваться до введения клеточной терапии или после введения клеточной терапии, в диагностических целях, чтобы идентифицировать пациентов и/или оценить способы лечения и/или токсичность.
[0373] В некоторых вариантах осуществления, измерение значения одного или более биомаркеров включает осуществление теста in vitro. В некоторых аспектах тест in vitro является иммунологическим тестом, основанным на аптамере тестом, гистологическим или цитологическим тестом или тестом уровня экспрессии мРНК. В некоторых вариантах осуществления значения одного или более биомаркеров измеряют твердофазным иммуноферментным анализом (ELISA), иммуноблоттингом, иммунопреципитацией, радиоиммуноанализом (RIA), иммунным окрашиванием, тестом потоковой цитометрии, поверхностным плазмонным резонансом (SPR), тестом хемилюминесценции, иммунохроматографическим анализом, тестом ингибирования или тестом авидности. В некоторых случаях значение по меньшей мере одного из одного или более биомаркеров определяют с помощью связывающего реагента, специфично связывающегося с по меньшей мере одним биомаркером. В некоторых аспектах связывающий реагент является антителом или его антигенсвязывающим фрагментом, аптамером или зондом нуклеиновой кислоты.
[0374] В некоторых вариантах осуществления измерение значения одного или более биомаркеров (например, аналитов) включает контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом и определение наличия или отсутствия, уровня, количества или концентрации аналита в биологическом образце. В некоторых вариантах осуществления один или более биомаркеров (например, аналит) представляет собой лактатдегидрогеназу (LDH), ферритин, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксин, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорин и D-димер (продукт распада фибрина). В некоторых вариантах осуществления, один или более биомаркеров (например, аналит) представляет собой LDH, ферритин, CRP, IL-6, IL-8, IL-10, TNF-альфа, IFN-альфа2, MCP-1 и MIP-1бета. В некоторых вариантах осуществления один или более биомаркеров (например, аналит) представляет собой или включает LDH.
[0375] В некоторых аспектах реагент является связывающей молекулой, специфично связывающейся с аналитом. Например, в некоторых вариантах осуществления, реагент является антителом или его антигенсвязывающим фрагментом. В некоторых вариантах осуществления реагент представляет собой или включает субстрат или связывающий партнер аналита.
[0376] В некоторых вариантах осуществления наличие, отсутствие или параметр (например, уровень, количество, концентрацию и/или другую величину) LDH детектируют или определяют в образце. Известны различные способы обнаружения или определения LDH. Например, тест, измеряющий преобразование LDH лактата в пируват через восстановление NAD+ до NADH, может использоваться для детекции LDH в образце. В некоторых вариантах осуществления образец приводят в контакт с лактатом в присутствии коэнзима NAD, который, как мера LDH в образце, приводит к NADH, который затем окисляют в присутствии агента переноса электронов. В некоторых вариантах осуществления NADH взаимодействует с зондом или предшественником красителя, который может быть детектирован путем измерения поглощения в видимом диапазоне света. В некоторых примерах диафораза использует NADH для восстановления соли тетразолия (INT) до продукта красного формазана, и продукт измеряют. Поэтому в некоторых вариантах осуществления количество сформированного цветного продукта непосредственно пропорционально активности LDH в образце.
[0377] В некоторых вариантах осуществления способы включают сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением, с определением, таким образом, риска развития токсичности после введения клеточной терапии или определения таким образом вероятности, что пациент достигнет ответа на клеточную терапию. В некоторых аспектах примеры пороговых значений могут быть определены на основе средних или медианных значений и значений в диапазоне или среднеквадратичном отклонении от средних или медианных значений уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал показывать определенный результат, такой как определенный терапевтический результат, или включая представление ответа или включая не представление ответа; или или развитие токсичности или не развитие токсичности. В некоторых вариантах осуществления определенные аспекты определения пороговых значений включают описанные ниже в Разделах I.E,1 и I.E,2.
1. Примеры биомаркеров, аналитов или параметров, связанных с результатами ответа
[0378] В некоторых вариантах осуществления аналит или биомаркер связан с, коррелирует с, является показательным для и/или прогностическим для определенного результата, такого как определенный результат ответа, такого как объективный ответ (OR) полный ответ (CR) или частичный ответ (PR) или длительный ответ, такой как OR или CR или PR, который длится 3, 6, 9 месяцев или более. В некоторых вариантах осуществления сниженные или уменьшенные уровни или увеличенные уровни одного или более таких биомаркеров (например, аналитов), например, по сравнению с референсным значением или пороговым значением, могут быть связаны с ответом, таким как OR, CR или PR, или любыми результатами ответа, описанными здесь, например, в Разделе I.C, необязательно длительным ответом, таким как ответ, который длится в течение по меньшей мере 3 месяцев, 6 месяцев или более.
[0379] В некоторых вариантах осуществления аналит или биомаркер связан с, коррелирует с, является показательным для и/или прогностическим для определенного результата, такого как результат определенного ответа или длительного ответа, у пациента, которому вводят клеточную терапию, такую как терапия композицией, содержащей генетически измененные клетки. В некоторых вариантах осуществления наличие, экспрессия, уровень, количество или концентрация одного или более аналитов в биологическом образце, полученном от пациента до введения клеточной терапии, может быть связан с, коррелировать с, быть показательным для и/или прогностическим для определенного результата, такого как результат определенного ответа или длительного ответа. В некоторых вариантах осуществления наличие, экспрессия, уровень, количество или концентрация определенных биомаркеров могут коррелировать с результатом определенного ответа или длительного ответа. В некоторых вариантах осуществления результатом ответа могут быть любые результаты ответа, описанные здесь, например, в Разделе I.C.
[0380] В некоторых вариантах осуществления способы включают сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением с определением, таким образом, вероятности, что пациент достигнет ответа на клеточную терапию. В некоторых вариантах осуществления способы включают отбор пациента, для которого определена вероятность ответа на лечение на основе результатов определения вероятности, что пациент достигнет ответа на клеточную терапию путем сравнения, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением. В некоторых вариантах осуществления способы также включают введение клеточной терапии пациенту, выбранному для лечения. В некоторых вариантах осуществления, если для пациент определено, что он вряд ли достигнет ответа или длительного ответа, способ дополнительно включает введение пациенту дополнительного терапевтического агента.
[0381] В некоторых вариантах осуществления биомаркеры (например, аналиты) включают связанные с результатом ответа и/или длительного ответа. В некоторых вариантах осуществления биомаркеры (например, аналиты), включая их параметры, включают LDH, ферритин, CRP, D-димер, амилоид сыворотки A1 (SAA-1), IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α и хемокин мотива C-X-C 10 (CXCL10).
[0382] В некоторых аспектах примеры аналитов или биомаркеров, которые могут быть оценены или проанализированы относительно оценки вероятности ответа после введения клеточной терапии, включают один или более аналитов, выбранных из ферритина, LDH, CXCL10, G-CSF и IL-10. В некоторых вариантах осуществления, для любого из вышеуказанных аналитов или биомаркеров, пациент, вероятно, достигнет ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения, и пациент вряд ли достигнет ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения. В некоторых вариантах осуществления ответ представляет собой или включает объективный ответ. В некоторых вариантах осуществления объективный ответ представляет собой или включает полный ответ (CR) или частичный ответ (PR). В некоторых аспектах уменьшенные уровни ферритина, LDH, CXCL10, G-CSF и IL-10, в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть связаны с достижением объективного ответа, включая полный ответ (CR) или частичный ответ (PR).
[0383] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации ферритина, LDH, CXCL10, G-CSF или IL-10 в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал достигать ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния. В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации ферритина, LDH, CXCL10, G-CSF или IL-10 в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал показывать стабильное заболевание (SD) и/или прогрессирующее заболевание (PD) после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0384] В некоторых аспектах примеры аналитов или биомаркеров, которые могут быть оценены или проанализированы относительно оценки вероятности длительного ответа после введения клеточной терапии, включают один или более аналитов, выбранных из LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β. В некоторых вариантах осуществления для любого из вышеуказанных аналитов или биомаркеров, пациент, вероятно, достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения, и пациент вряд ли достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения. В некоторых вариантах осуществления длительный ответ представляет собой или включает полный ответ (CR) или частичный ответ (PR), который длится в течение или более чем 3 месяцев, 4 месяцев, 5 месяцев или 6 месяцев. В некоторых вариантах осуществления длительный ответ представляет собой или включает CR или PR, который длится в течение по меньшей мере 3 месяцев. В некоторых аспектах уменьшенные уровни LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть связаны с достижением длительного ответа, такого как CR или PR, который длится в течение по меньшей мере 3 месяцев.
[0385] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 или MIP-1β в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал достигать длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0386] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 или MIP-1β в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы не достигал длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0387] В некоторых вариантах осуществления ответ является длительным ответом, таким как CR или PR, который длится в течение по меньшей мере 3 месяцев.
[0388] В некоторых вариантах осуществления пороговое значение для LDH составляет или приблизительно составляет или ниже или приблизительно ниже 600 Ед/л, 500 Ед/л, 400 Ед/л, 300 Ед/л или 200 Ед/л.
[0389] В некоторых вариантах осуществления пример порогового значения для ферритина составляет или приблизительно составляет или ниже или приблизительно ниже 1000 мг/л, 900 мг/л, 800 мг/л, 700 мг/л, 600 мг/л, 500 мг/л, 400 мг/л, 300 мг/л или 200 мг/л.
[0390] В некоторых вариантах осуществления пример порогового значения для CRP составляет или приблизительно составляет или ниже или приблизительно ниже 20 мг/л, 19 мг/л, 18 мг/л, 17 мг/л, 16 мг/л, 15 мг/л, 14 мг/л, 13 мг/л, 12 мг/л, 11 мг/л, 10 мг/л, 9 мг/л, 8 мг/л, 7 мг/л, 6 мг/л или 5 мг/л.
[0391] В некоторых вариантах осуществления пример порогового значения для D-димера составляет или приблизительно составляет или ниже или приблизительно ниже 1000 мг/л, 900 мг/л, 800 мг/л, 700 мг/л, 600 мг/л, 500 мг/л, 400 мг/л, 300 мг/л или 200 мг/л.
[0392] В некоторых вариантах осуществления пример порогового значения для SAA-1 составляет или приблизительно составляет или ниже или приблизительно ниже 100 мг/л, 90 мг/л, 80 мг/л, 70 мг/л, 60 мг/л, 50 мг/л, 40 мг/л, 30 мг/л или 20 мг/л.
[0393] В некоторых вариантах осуществления пример порогового значения для IL-6 составляет или приблизительно составляет или ниже или приблизительно ниже 6 пг/мл, 5 пг/мл, 4 пг/мл, 3 пг/мл или 2 пг/мл.
[0394] В некоторых вариантах осуществления пример порогового значения для IL-10 составляет или приблизительно составляет или ниже или приблизительно ниже 2 пг/мл, 1 пг/мл, 0,9 пг/мл, 0,8 пг/мл, 0,7 пг/мл, 0,6 пг/мл или 0,5 пг/мл.
[0395] В некоторых вариантах осуществления пример порогового значения для IL-15 составляет или приблизительно составляет или ниже или приблизительно ниже 7 пг/мл, 6 пг/мл, 5 пг/мл, 4 пг/мл или 3 пг/мл.
[0396] В некоторых вариантах осуществления пример порогового значения для IL-16 составляет или приблизительно составляет или ниже или приблизительно ниже 1000 пг/мл, 900 пг/мл, 800 пг/мл, 700 пг/мл или 600 пг/мл.
[0397] В некоторых вариантах осуществления пример порогового значения для TNF-α составляет или приблизительно составляет или ниже или приблизительно ниже 10 пг/мл, 9 пг/мл, 8 пг/мл, 7 пг/мл или 6 пг/мл.
[0398] В некоторых вариантах осуществления пример порогового значения для IFN-γ составляет или приблизительно составляет или ниже или приблизительно ниже 30 пг/мл, 20 пг/мл, 10 пг/мл, 9 пг/мл, 8 пг/мл или 7 пг/мл;
[0399] В некоторых вариантах осуществления пример порогового значения для MIP-1α составляет или приблизительно составляет или ниже или приблизительно ниже 40 пг/мл, 30 пг/мл или 20 пг/мл; и/или
[0400] В некоторых вариантах осуществления пример порогового значения для CXCL-10 составляет или приблизительно составляет или ниже или приблизительно ниже 1500 пг/мл, 1000 пг/мл, 900 пг/мл, 800 пг/мл, 700 пг/мл, 600 пг/мл или 500 пг/мл.
[0401] В некоторых аспектах примеры аналитов или биомаркеров, которые могут быть оценены или проанализированы в отношении оценки вероятности длительного ответа после введения клеточной терапии, включают один или более аналитов, выбранных из ферритина, CRP, LDH, CXCL10, IL-8, IL-10, IL-15, MCP-1, MIP-1β и TNF-α. В некоторых вариантах осуществления для любого из указанных выше аналитов или биомаркеров, пациент, вероятно, достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения, и пациент вряд ли достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения. В некоторых вариантах осуществления длительный ответ представляет собой или включает полный ответ (CR) или частичный ответ (PR), который длится в течение или более 3 месяцев, 4 месяцев, 5 месяцев или 6 месяцев. В некоторых вариантах осуществления длительный ответ представляет собой или включает CR или PR, который длится в течение по меньшей мере 3 месяцев. В некоторых аспектах уменьшенные уровни ферритина, CRP, LDH, CXCL10, IL-8, IL-10, IL-15, MCP-1, MIP-1β и TNF-α в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть связаны с достижением длительного ответа, такого как CR или PR, который длится в течение по меньшей мере 3 месяцев.
[0402] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации ферритина, CRP, LDH, CXCL10, IL-8, IL-10, IL-15, MCP-1, MIP-1β или TNF-α в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал достигать длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0403] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации ферритина, CRP, LDH, CXCL10, IL-8, IL-10, IL-15, MCP-1, MIP-1β или TNF-α в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы не достигал длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0404] В некоторых аспектах примеры аналитов или биомаркеров, которые могут быть оценены или проанализированы в отношении оценки вероятности длительного ответа после введения клеточной терапии, включают один или более аналитов, выбранных из гемоглобина и белка. В некоторых вариантах осуществления для любого из указанных выше аналитов или биомаркеров, пациент, вероятно, достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения, и пациент вряд ли достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения. В некоторых вариантах осуществления длительный ответ представляет собой или включает полный ответ (CR) или частичный ответ (PR), который длится в течение или более 3 месяцев, 4 месяцев, 5 месяцев или 6 месяцев. В некоторых вариантах осуществления длительный ответ представляет собой или включает CR или PR, который длится в течение по меньшей мере 3 месяцев. В некоторых аспектах повышенные уровни гемоглобина и белка в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть связаны с достижением длительного ответа, такого как CR или PR, который длится в течение по меньшей мере 3 месяцев.
[0405] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации гемоглобина или белка в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал достигать длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0406] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации гемоглобина или белка в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы не достигал длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
2. Примеры биомаркеров, аналитов или параметров, ассоциированных с результатами токсичности
[0407] В некоторых вариантах осуществления аналит или биомаркер ассоциирован с, коррелирует с, является показательным для и/или прогностическим для определенного результата, такого как развитие токсичности, у пациента, которому вводят клеточную терапию, такую как терапия композицией, содержащей генно-инженерные клетки. В некоторых вариантах осуществления наличие, экспрессия, уровень, количество или концентрация одного или более аналитов в биологическом образце, полученном от пациента до введения клеточной терапии, может быть ассоциирован с, коррелировать с, быть показательным для и/или прогностическим для определенного результата, такого как развитие токсичности, такой как любые результаты токсичности, описанные здесь, например, в Разделе I.D. В некоторых вариантах осуществления наличие, экспрессия, уровень, количество или концентрация определенных биомаркеров могут коррелировать с определенными результатами токсичности, например, развитием NT или CRS. В некоторых вариантах осуществления токсичность является токсичностью, потенциально ассоциированной с клеточной терапией, такой как любая описанная здесь, например, в Разделе I.D. В некоторых вариантах осуществления токсичность является нейротоксичностью (NT) или синдромом высвобождения цитокинов (CRS). В некоторых вариантах осуществления токсичность является тяжелой NT или тяжелым CRS. В некоторых вариантах осуществления токсичность является NT степени 2 или выше или CRS степени 2 или выше. В некоторых вариантах осуществления токсичность является NT степени 3 или выше или CRS степени 3 или выше.
[0408] В некоторых вариантах осуществления способы включают сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением с определением, таким образом, риска развития токсичности после введения клеточной терапии. В некоторых вариантах осуществления способы включают идентификацию пациента, у которого имеется риск развития токсичности после введения клеточной терапии, на основании сравнения, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением. В некоторых вариантах осуществления способы также включают, после или на основе результатов оценки, введение пациенту клеточной терапии, и, необязательно, агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности. В некоторых вариантах осуществления способы также включают контроль пациента в отношении симптомов токсичности, если пациенту вводят клеточную терапию, и он идентифицируется как имеющий риск развития токсичности.
[0409] В некоторых вариантах осуществления, если пациент идентифицируется как имеющий риск развития токсичности, одна или более следующих стадий может быть осуществлена с введением пациенту: (a) (1) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, и (2) клеточной терапии, причем введение агента должно быть осуществлено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или (b) введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или у большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии; и/или (c) введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0410] В некоторых вариантах осуществления биомаркеры или аналиты, включая их параметры, которые могут быть оценены, включают Лактатдегидрогеназу (LDH), ферритин, C-реактивный белок (CRP), Интерлейкин-6 (IL-6), IL-7, IL-8, IL-10, IL-15, IL-16, альфа фактора некроза опухоли (TNF-α), интерферон альфа 2 (IFN-α2), моноцитарный хемоаттрактантный белок-1 (MCP-1), макрофагальный воспалительный белок 1 альфа (MIP-1α), макрофагальный воспалительный белок 1 бета (MIP-1β), Эотаксин, гранулоцитарный колониестимулирующий фактор (G-CSF), альфа рецептор IL-1 (IL-1Rα), IL-1β, IFN-γ-индуцируемый белок 10 (IP-10), перфорин и D-димер (продукт распада фибрина). В некоторых вариантах осуществления биомаркеры (например, аналиты), включая их параметры, включают LDH, ферритин, CRP, IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β. В некоторых вариантах осуществления, биомаркеры (например, аналиты), включая их параметры, включают ферритин, CRP, D-димер, IL-6, IL-15, TNF-α и MIP-1α. В некоторых вариантах осуществления биомаркеры (например, аналиты), включая их параметры, включают ферритин, CRP, IL-10, IL-15, IL-16, TNF-α или MIP-1β. В некоторых вариантах осуществления повышенные уровни или увеличенные уровни одного или более таких биомаркеров (например, биомаркеров), например, по сравнению с референсным значением или пороговым значением, могут быть ассоциированы с развитием нейротоксичности, например, тяжелой нейротоксичностью или нейротоксичности степени 3 или выше или степени 4 или 5. В некоторых вариантах осуществления повышенные уровни или увеличенные уровни одного или более таких биомаркеров (например, аналитов), например, по сравнению с референсным значением или пороговым значением, могут быть ассоциированы с развитием нейротоксичности, например, тяжелой нейротоксичности или нейротоксичности степени 3 или выше или степени 4 или 5.
[0411] В некоторых аспектах примеры аналитов или биомаркеров, которые могут быть оценены или проанализированы в отношении оценки риска развития токсичности после введения клеточной терапии, включает один или более аналитов, выбранных из LDH, Ферритина, С-реактивного белка (CRP), IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β. В некоторых вариантах осуществления, для любого из вышеуказанных аналитов или биомаркеров, пациент имеет риск развития токсичности, если уровень, количество или концентрация одного или более аналитов выше порогового значения, и пациент имеет низкий риск развития токсичности, если уровень, количество или концентрация одного или более аналитов ниже порогового значения. В некоторых вариантах осуществления токсичность является нейротоксичностью. В некоторых аспектах повышенные уровни LDH, Ферритина, С-реактивного белка (CRP), IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β, в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть связаны с более высоким риском развития нейротоксичности.
[0412] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 30% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации LDH, Ферритина, С-реактивного белка (CRP), IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 или MIP-1β в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы по-прежнему не развивается какая-либо токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0413] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 30% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации LDH, Ферритина, С-реактивного белка (CRP), IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 или MIP-1β в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0414] В некоторых вариантах осуществления токсичность является нейротоксичностью.
[0415] В некоторых вариантах осуществления пример порогового значения для LDH составляет или приблизительно составляет или выше или выше приблизительно 300 Ед/л, 400 Ед/л, 500 Ед/л, 600 Ед/л или 700 Ед/л.
[0416] В некоторых вариантах осуществления пример порогового значения для Ферритина составляет или приблизительно составляет или выше или выше приблизительно 500 нг/мл, 600 нг/мл, 700 нг/мл, 800 нг/мл, 900 нг/мл, 1000 нг/мл или 1500 нг/мл.
[0417] В некоторых вариантах осуществления пример порогового значения для CRP составляет или приблизительно составляет или выше или выше приблизительно 20 мг/л, 30 мг/л, 40 мг/л, 50 мг/л, 60 мг/л, 70 мг/л или 80 мг/л.
[0418] В некоторых вариантах осуществления пример порогового значения для IL-6 составляет или приблизительно составляет или выше или выше приблизительно 5 пг/мл, 6 пг/мл, 7 пг/мл, 8 пг/мл, 9 пг/мл, 10 пг/мл, 20 пг/мл или 30 пг/мл.
[0419] В некоторых вариантах осуществления пример порогового значения для IL-8 составляет или приблизительно составляет или выше или выше приблизительно 8 пг/мл, 9 пг/мл, 10 пг/мл, 20 пг/мл или 30 пг/мл.
[0420] В некоторых вариантах осуществления пример порогового значения для IL-10 составляет или приблизительно составляет или выше или выше приблизительно 20 пг/мл, 30 пг/мл, 40 пг/мл, 50 пг/мл, 60 пг/мл или 70 пг/мл.
[0421] В некоторых вариантах осуществления пример порогового значения для TNF-α составляет или приблизительно составляет или выше или выше приблизительно 20 пг/мл или 30 пг/мл.
[0422] В некоторых вариантах осуществления пример порогового значения для IFN-α2 составляет или приблизительно составляет или выше или выше приблизительно 40 пг/мл, 50 пг/мл, 60 пг/мл, 70 пг/мл или 80 пг/мл.
[0423] В некоторых вариантах осуществления пример порогового значения для MCP-1; и/или составляет или приблизительно составляет или выше или выше приблизительно 200 пг/мл или 300 пг/мл.
[0424] В некоторых вариантах осуществления пример порогового значения для MIP-1β составляет или приблизительно составляет или выше или выше приблизительно 40 пг/мл, 50 пг/мл, 60 пг/мл, 70 пг/мл или 80 пг/мл.
[0425] В некоторых аспектах примеры аналитов или биомаркеров, которые могут быть оценены или проанализированы в отношении оценки риска развития токсичности после введения клеточной терапии включает один или более аналитов, выбранных из IL-8, IL-10 и CXCL10. В некоторых вариантах осуществления для любого из вышеуказанных аналитов или биомаркеров пациент имеет риск развития токсичности, если уровень, количество или концентрация одного или более аналитов выше порогового значения, и пациент имеет низкий риск развития токсичности, если уровень, количество или концентрация одного или более аналитов ниже порогового значения. В некоторых вариантах осуществления токсичность является нейротоксичностью. В некоторых вариантах осуществления токсичность является тяжелой нейротоксичностью или нейротоксичностью степени 3 или более высокой. В некоторых аспектах повышенные уровни IL-8, IL-10 и CXCL10 в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть ассоциированы с более высоким риском развития нейротоксичности или тяжелой нейротоксичности, или нейротоксичности степени 3 или более высокой.
[0426] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 30% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации IL-8, IL-10 или CXCL10 в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы по-прежнему не развивается какая-либо токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0427] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 30% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации IL-8, IL-10 или CXCL10 в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0428] В некоторых аспектах примеры аналитов или биомаркеров, или объемного параметра опухолевой массы, которое может быть оценено или проанализировано в отношении оценки риска развития токсичности после введения клеточной терапии включает один или более аналитов или объемную меру опухолевой массы, выбранных из количества продуктов диаметров (SPD), LDH, Ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-10, IL-15, IL-16 TNF-α, MIP-1α и MIP-1β. В некоторых вариантах осуществления для любого из вышеуказанных аналитов или биомаркеров или объемного параметра опухолевой массы пациент имеет риск развития токсичности, если уровень, количество или концентрация одного или более аналитов или объемный параметр опухолевой массы выше порогового значения, и пациент имеет низкий риск развития токсичности, если уровень, количество или концентрация одного или более аналитов или объемный параметр опухолевой массы ниже порогового значения. В некоторых вариантах осуществления токсичность является нейротоксичностью. В некоторых аспектах повышенные уровни или измерение количества продуктов диаметров (SPD), LDH, Ферритина, С-реактивного белка (CRP), D-димер (продукт распада фибрина), IL-6, IL-10, IL-15, IL-16 TNF-α, MIP-1α и MIP-1β в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть ассоциированы с более высоким риском развития нейротоксичности (NT) или синдрома высвобождения цитокинов (CRS).
[0429] В некоторых вариантах осуществления один или более аналитов или объемный параметр опухолевой массы, выбранные из LDH, SPD, IL-10, IL-15, IL-16, TNF-α и MIP-1β, и токсичность представляет собой нейротоксичность. В некоторых вариантах осуществления один или более аналитов или объемный параметр опухолевой массы, выбранные из LDH, SPD, CRP, d-димера, IL-6, IL-15, TNF-α и MIP-1α, и токсичность является CRS. В некоторых аспектах повышенные уровни или величина LDH, SPD, IL-10, IL-15, IL-16, TNF-α и MIP-1β в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть ассоциированы с более высоким риском развития нейротоксичности (NT). В некоторых аспектах повышенные уровни или величина LDH, SPD, CRP, d-димера, IL-6, IL-15, TNF-α и MIP-1α в биологическом образце от пациента, полученном до введения клеточной терапии (предварительное лечение), могут быть ассоциированы с более высоким риском развития синдрома высвобождения цитокинов (CRS).
[0430] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 32% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации LDH, Ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-10, IL-15, IL-16 TNF-α, MIP-1α или MIP-1β, или медианы или среднего объемного параметра опухолевой массы количества продуктов диаметров (SPD) в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы по-прежнему не развивается какая-либо токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0431] В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 32% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации LDH, Ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-10, IL-15, IL-16 TNF-α, MIP-1α или MIP-1β, или медианы или среднего объемного параметра опухолевой массы количества продуктов диаметров (SPD) в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0432] В некоторых вариантах осуществления токсичность является нейротоксичностью, и пример порогового значения для LDH составляет или приблизительно составляет или выше или выше приблизительно 300 Ед/л, 400 Ед/л, 500 Ед/л или 600 Ед/л.
[0433] В некоторых вариантах осуществления токсичность является нейротоксичностью, и пример порогового значения для SPD составляет или приблизительно составляет или выше или выше приблизительно 30 см2, 40 см2, 50 см2, 60 см2, 70 см2, 80 см2 или 90 см2.
[0434] В некоторых вариантах осуществления токсичность является нейротоксичностью, и пример порогового значения для IL-10 составляет или приблизительно составляет или выше или выше приблизительно 0,8 пг/мл, 0,9 пг/мл, 1 пг/мл, 2 пг/мл, 3 пг/мл или 4 пг/мл.
[0435] В некоторых вариантах осуществления токсичность является нейротоксичностью, и пример порогового значения для IL-15 составляет или приблизительно составляет или выше или выше приблизительно 3 пг/мл, 4 пг/мл, 5 пг/мл, 6 пг/мл или 7 пг/мл.
[0436] В некоторых вариантах осуществления токсичность является нейротоксичностью, и пример порогового значения для IL-16 составляет или приблизительно составляет или выше или выше приблизительно 600 пг/мл, 700 пг/мл, 800 пг/мл, 900 пг/мл или 1000 пг/мл.
[0437] В некоторых вариантах осуществления токсичность является нейротоксичностью, и пример порогового значения для TNF-α составляет или приблизительно составляет или выше или выше приблизительно 6 пг/мл, 7 пг/мл, 8 пг/мл, 9 пг/мл или 10 пг/мл.
[0438] В некоторых вариантах осуществления токсичность является нейротоксичностью, и пример порогового значения для MIP-1β составляет или приблизительно составляет или выше или выше приблизительно 70 пг/мл, 80 пг/мл, 90 пг/мл или 100 пг/мл.
[0439] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для LDH составляет или приблизительно составляет или выше или выше приблизительно 300 Ед/л, 400 Ед/л, 500 Ед/л или 600 Ед/л.
[0440] В некоторых вариантах осуществления токсичность является CRS, и пороговое значение для SPD составляет или приблизительно составляет или выше или выше приблизительно 20 см2, 30 см2, 40 см2 или 50 см2.
[0441] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для ферритина составляет или приблизительно составляет или выше или выше приблизительно 300 нг/мл, 400 нг/мл, 500 нг/мл, 600 нг/мл, 700 нг/мл, 800 нг/мл, 900 нг/мл или 1000 нг/мл.
[0442] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для CRP составляет или приблизительно составляет или выше или выше приблизительно 20 мг/л, 30 мг/л или 40 мг/л.
[0443] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для d-димера составляет или приблизительно составляет или выше или выше приблизительно 300 пг/мл, 400 пг/мл, 500 пг/мл, 600 пг/мл, 700 пг/мл, 800 пг/мл, 900 пг/мл или 1000 пг/мл.
[0444] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для IL-6 составляет или приблизительно составляет или выше или выше приблизительно 2 пг/мл, 3 пг/мл, 4 пг/мл, 5 пг/мл, 6 пг/мл, 7 пг/мл, 8 пг/мл или 9 пг/мл.
[0445] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для IL-15 составляет или приблизительно составляет или выше или выше приблизительно 3 пг/мл, 4 пг/мл, 5 пг/мл, 6 пг/мл, 7 пг/мл, 8 пг/мл, 9 пг/мл или 10 пг/мл.
[0446] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для TNF-α составляет или приблизительно составляет или выше или выше приблизительно 7 пг/мл, 8 пг/мл, 9 пг/мл, 10 пг/мл или 15 пг/мл.
[0447] В некоторых вариантах осуществления токсичность является CRS, и пример порогового значения для MIP-1α составляет или приблизительно составляет или выше или выше приблизительно 20 пг/мл, 30 пг/мл или 40 пг/мл.
[0448] В некоторых вариантах осуществления биомаркер является LDH, и в некоторых случаях развитие токсичности, например, CRS или NT, коррелирует со значением LDH, которое выше порогового значения. В некоторых вариантах осуществления воспалительный маркер является LDH, и пороговое значение составляет или приблизительно составляет 300 единиц на литр, составляет или приблизительно составляет 400 единиц на литр, составляет или приблизительно составляет 500 единиц на литр или составляет или приблизительно составляет 600 единиц на литр.
[0449] В некоторых вариантах осуществления, если уровень, количество или концентрация биомаркера (например, аналита) в образце равно или выше порогового значения аналита, вещества или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, вводят пациенту до, в течение одного, двух или трех дней, одновременно с и/или при первом повышении температуры после инициации введения клеточной терапии к пациенту. Примеры агентов или вмешательств для использования в связи со способами по изобретению для лечения, предотвращения, задержки, уменьшения или смягчения риска развития токсичности, описаны в Разделе II.
[0450] В некоторых случаях, если уровень, количество концентрации биомаркера в образце равно или выше порогового значения, кеточную терапию вводят пациенту в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или у большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии. В некоторых случаях, если уровень, количество концентрации биомаркера в образце равно или выше порогового значения, клеточную терапию вводят пациенту в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0451] В некоторых вариантах осуществления, если уровень, количество или концентрация биомаркера (например, аналита) ниже порогового значения для аналита, клеточную терапию вводят пациенту, необязательно в несниженной дозе. В некоторых случаях клеточную терапию необязательно вводят на амбулаторной основе или без допуска в больницу в течение одного или более дней. В некоторых вариантах осуществления, если уровень, количество или концентрация аналита ниже порогового значения, введение клеточной терапии не включает введение, до или одновременно с применением клеточной терапии и/или до развития признака симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или введение клеточной терапии должно быть или может быть введено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0452] В некоторых аспектах способов по изобретению пациент определен как подверающийся риску развития токсичности (например, нейротоксичности, такой как тяжелая нейротоксичность или нейротоксичность степени 3 или выше, например, нейротоксичности степени 4 или 5, и/или CRS, такой как тяжелый CRS или CRS степени 3 или выше) путем сравнения параметра (например, концентрации, количества, уровня или активности) биомаркера (например, аналита) или, индивидуально, каждого из биомаркеров (например, аналитов) с референсным значением, таким как пороговое значение, соответствующего параметра для биомаркера или каждого биомаркера. В некоторых вариантах осуществления сравнение указывает, является ли пациент или находится ли он в опасности развития токсичности, например, нейротоксичности, такой как тяжелая нейротоксичность или нейротоксичность степени 3 или выше, например, нейротоксичность степени 4 или 5 и/или CRS, такой как тяжелый CRS или CRS степени 3 или выше, и/или указывает уровень риска для развития сказанной токсичности. В некоторых вариантах осуществления референсное значение является значением, которое является пороговым значением или отсечением, при котором наблюдается хорошее прогностическое значение (например, точность, чувствительность и/или специфичность), что такая токсичность будет иметь место или, вероятно, будет иметь место, индивидуально или в комбинации с одним или более биомаркерами в группе. В некоторых случаях такое референсное значение, например, пороговое значение, может быть предопределено или известно до осуществления способа, например, от множества пациентов, ранее получавших лечение клеточной терапией и оцениваемых для корреляции параметра биомаркера или, индивидуально, каждого из биомаркеров в группе с наличием токсичного результата (например, наличием нейротоксичности, такой как тяжелая нейротоксичность или нейротоксичность степени 3 или выше, например, нейротоксичность степени 4 или 5 и/или CRS, такой как тяжелый CRS Или CRS степени 3 или выше).
[0453] В некоторых вариантах осуществления параметр биомаркера (например, LDH, ферритин, CRP, IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β), который выше или больше, чем референсное значение, например, пороговое значение, соответствующего параметра ассоциирован с положительным прогнозом риска токсичности (индивидуально или в комбинации с оценкой других биомаркеров в группе). В некоторых вариантах осуществления параметр биомаркера, который равен или ниже, чем референсное значение, например, пороговое значение, соответствующего параметра ассоциирован с отрицательным прогнозом риска токсичности (индивидуально или в комбинации с оценкой других биомаркеров в группе).
[0454] В некоторых вариантах осуществления пороговое значение определяется на основе уровня, количества, концентрации или другой величины биомаркера (например, аналита) в образце, положительном для биомаркера. В некоторых аспектах пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации или величины, и/или в пределах стандартного отклонения среднего уровня, количества или концентрации или величины, аналита или параметра в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность, например, нейротоксичность, такая как тяжелая нейротоксичность или нейротоксичность степени 3 или выше, например, нейротоксичность степени 4 или 5 и/или CRS, такой как тяжелый CRS или CRS степени 3 или выше, после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0455] В некоторых вариантах осуществления любого из способов по изобретению биомаркер (например, аналит) коррелирует с и/или является прогностическим для риска развития тяжелой нейротоксичности, такой как тяжелая нейротоксичность или нейротоксичность степени 3 или выше, например, нейротоксичность степени 4 или 5 и/или тяжелый CRS или CRS степени 3 или выше. В некоторых вариантах осуществления пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации или величины, и/или в пределах стандартного отклонения среднего уровня, количества или концентрации или величины, аналита или параметра в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться тяжелая нейротоксичность или нейротоксичность степени 3 или выше, например, нейротоксичность степени 4 или 5 и/или тяжелый CRS или CRS степени 3 или выше, после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
[0456] В некоторых вариантах осуществления объемный параметр представляет собой SPD, и в некоторых случаях развитие токсичности, например, CRS или NT, коррелирует со значением SPD, которое выше порогового значения. В некоторых вариантах осуществления объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 30 см2, составляет или приблизительно 40 см2, составляет или приблизительно 50 см2, составляет или приблизительно 60 см2, или составляет или приблизительно составляет 70 см2. В некоторых вариантах осуществления объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 30 см2, составляет или приблизительно 40 см2, составляет или приблизительно 50 см2, составляет или приблизительно 60 см2 или составляет или приблизительно составляет 70 см2.
[0457] В некоторых вариантах осуществления параметр, включая объемные измерения опухоли, ассоциирован с ответом на клеточную терапию и/или риском развития токсичности, например, CRS или нейротоксичности (NT).
[0458] В некоторых вариантах осуществления объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 30 см2, составляет или приблизительно 40 см2, составляет или приблизительно 50 см2, составляет или приблизительно 60 см2 или составляет или приблизительно составляет 70 см2. В некоторых вариантах осуществления объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 50 см2.
[0459] В некоторых вариантах осуществления аналит представляет собой LDH, и пороговое значение составляет или приблизительно составляет 300 единиц на литр (Ед/л), составляет или приблизительно составляет 400 Ед/л, составляет или приблизительно составляет 500 Ед/л или составляет или приблизительно составляет 600 Ед/л. В некоторых вариантах осуществления аналит представляет собой LDH, и пороговое значение составляет или приблизительно составляет 500 Ед/л.
[0460] В некоторых вариантах осуществления параметр или биомаркер представляет собой LDH. В некоторых вариантах осуществления биомаркер представляет собой LDH, и пороговое значение составляет 500 Ед/л или выше. В некоторых вариантах осуществления параметр или биомаркер представляет собой SPD. В некоторых вариантах осуществления параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 50 см2 или выше. В некоторых вариантах осуществления биомаркер или параметры представляют собой SPD и LDH, и пороговые значения составляют SPD 50 см2 или выше и LDH 500 Ед/л или выше. В некоторых вариантах осуществления биомаркеры или параметры ассоциированы с повышенным риском развития CRS или NT.
[0461] В некоторых вариантах осуществления измерение параметра или маркера, который выше порогового значения, например, SPD 50 см2 или выше и LDH 500 Ед/л или выше, ассоциированы с приблизительно 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9-, 10-кратным или более повышенным риском развития CRS или NT, таких как CRS или NT любой степени. В некоторых вариантах осуществления измерение параметра или маркера, который ниже порогового значения, например, SPD ниже, чем 500 см2 и LDH ниже, чем 500 Ед/л, ассоциированы с приблизительно 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9-, 10-кратным или более сниженным риском развития CRS или NT, таких как CRS или NT любой степени.
[0462] В некоторых вариантах осуществления биомаркеры (например, аналиты) включают ассоцированные с увеличенными фармакокинетическими параметрами (PK) клетки, например, увеличенной максимальной концентрацией в сыворотке клетки (AUC0-28) или увеличенной экспозицией (например, область под кривой (AUC)). В некоторых вариантах осуществления биомаркеры (например, аналиты), включая их параметры, включают IL-7, IL-15, MIP-1α и TNF-α.
[0463] В некоторых вариантах осуществления параметр является параметром, относящимся к опухолевой нагрузке, например, измерением опухолевой массы. В некоторых аспектах способы также включают дальнейший контроль пациента в отношении возможных симптомов токсичности на основе риска токсичности, определенной оценкой наличия или отсутствия биомаркера и/или сравнением биомаркеров с референсным значением или пороговым значением биомаркера.
II. АГЕНТЫ ИЛИ ВМЕШАТЕЛЬСТВА, ЛЕЧАЩИЕ ИЛИ ОБЛЕГЧАЮЩИЕ СИМПТОМЫ ТОКСИЧНОСТИ
[0464] В некоторых вариантах осуществления способы и изделия по изобретению могут использоваться в связи с или включать или задействовать, один или более агентов или средств для лечения, предотвращения, задержки или уменьшения развития токсичности. В некоторых примерах агент или другое средство для лечения, способное к лечению, предотвращению, задержке или уменьшению развития токсичности, вводят до и/или одновременно с введением терапевтической композиции клеток, включающей генно-инженерные клетки.
[0465] В некоторых вариантах осуществления агент, например, нацеливаемый на токсичность агент или средство для лечения, способное к лечению, предотвращению, задержке или уменьшению развития токсичности, представляет собой стероид, антагонист или ингибитор рецептора цитокина, такого как рецептор IL-6, рецептор CD122 (рецептор IL-2Rбета) или CCR2, или ингибитор цитокина, такого как IL-6, MCP-1, IL-10, IFN-γ, IL-8 или IL-18. В некоторых вариантах осуществления агент является агонистом рецептора цитокина и/или цитокина, такого как TGF-β. В некоторых вариантах осуществления, агент, например, агонист, антагонист или ингибитор, является антителом или антигенсвязывающим фрагментом, малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0466] В некоторых вариантах осуществления жидкий болюс может использоваться в качестве вмешательства, такого как для лечения гипотензии, связанной с CRS. В некоторых вариантах осуществления целевые уровни гематокрита составляют > 24%. В некоторых вариантах осуществления вмешательство включает использование технологии абсорбирующей смолы с фильтрацией крови или плазмы. В некоторых случаях вмешательство включает диализ, плазмоферез или подобные технологии. В некоторых вариантах осуществления может использоваться вазопрессоры или ацетоаминофен.
[0467] В некоторых вариантах осуществления агент может быть введен последовательно, периодически или в то же время, что и, или в той же композиции, что и терапия, такая как клетки для адоптивной клеточной терапии. Например, агент может быть введен до, во время, одновременно с или после введения клеточной терапии и/или иммунотерапии.
[0468] В некоторых вариантах осуществления агент вводят в момент времени, как описано здесь, и в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению. В некоторых вариантах осуществления нацеливаемый на токсичность агент вводят в момент времени, такой как менее чем или не более чем через 3, 4, 5, 6, 7, 8, 9 или 10 дней после инициации клеточной терапии и/или иммунотерапии. В некоторых вариантах осуществления нацеливаемый на токсичность агент вводят через или в течение приблизительно 1 дня, 2 дней или 3 дней после инициации введения клеточной терапии и/или иммунотерапии.
[0469] В некоторых вариантах осуществления агент, например, нацеливаемый на токсичность агент, вводят пациенту после инициации введения иммунотерапии и/или клеточной терапии в момент времени, в который пациент не показывает CRS степени 2 или выше или нейротоксичность степени 2 или более высокой. В некоторых аспектах нацеливаемый на токсичность агент вводят после инициации введения иммунотерапии и/или клеточной терапии в момент времени, в которой пациент не показывает тяжелый CRS или тяжелую нейротоксичность. Таким образом, между инициацией введения иммунотерапии и/или клеточной терапии и нацеливаемого на токсичность агента, пациентом является пациент, не показывающий CRS степени 2 или выше, такого как тяжелый CRS, и/или не показывающий нейротоксичность степени 2 или более высокой, такой как тяжелая нейротоксичность.
[0470] Неограничивающие примеры вмешательств для лечения или облегчения токсичности, такой как тяжелый CRS (sCRS), описаны в Таблице 5. В некоторых вариантах осуществления вмешательство включает тоцилизумаб или другой нацеливаемый на токсичность агент, как описано, который может быть в момент времени, в котором имеет место длительное или персистирующее повышение температуры до более чем или приблизительно 38°C или более чем или более чем приблизительно 39°C у пациента. В некоторых вариантах осуществления повышение температуры длится у пациента более 10 часов, более 12 часов, более 16 часов или более 24 часов до вмешательства.
[0471] В некоторых случаях агент или терапия или вмешательство, например, нацеливаемый на токсичность агент, вводят индивидуально или вводят как часть композиции или состава, такой как фармацевтическая композиция или состав, как описано здесь. Таким образом, агент индивидуально или как часть фармацевтической композиции может быть введен внутривенно или перорально, или любым другим приемлемым известным путем введения, или как описано здесь.
[0472] В некоторых вариантах осуществления дозировка агента или частота введения агента в режиме дозировки уменьшены по сравнению с дозировкой агента или ее частотой в способе, в котором пациента лечат агентом после того, как развились или были диагностированы CRS или нейротоксичности степени 2 или выше, например, после тяжелого CRS, например, степени 3 или выше, или после тяжелой нейротоксичности, например, степени 3 или более высокой (например, после проявления физических признаков или симптомов CRS или нейротоксичности степени 3 или выше). В некоторых вариантах осуществления дозировка агента или частота введения агента в режиме дозировки уменьшены по сравнению с дозировкой агента или ее частотой в способе, в котором пациента лечат от CRS или нейротоксичности через более чем 3 дня, 4 дня, 5 дней, 6 дней, 1 неделю, 2 недели три недели или более после введения клеточной терапии и/или иммунотерапии. В некоторых вариантах осуществления дозировка уменьшена более чем или более чем приблизительно 1,2-кратно, 1,5-кратно, 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно или более. В некоторых вариантах осуществления дозировка уменьшена более чем или приблизительно на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более. В некоторых вариантах осуществления, частота дозирования уменьшена, например, сокращено количество суточных доз или сокращено количество дней дозирования.
A. Стероид
[0473] В некоторых вариантах осуществления агент, например, нацеливаемый на токсичность агент, который лечит и/или который предотвращает, задерживает или уменьшает развитие или риск развития токсичности на иммунотерапию и/или клеточную терапию, представляет собой стероид, например, кортикостероид. Кортикостероиды, как правило, включают глюкокортикоиды и минералокортикоиды.
[0474] Любой кортикостероид, например, глюкокортикоид, может использоваться в способах по изобретению. В некоторых вариантах осуществления глюкокортикоиды включают синтетические и несинтетические глюкокортикоиды. Примеры глюкокортикоидов включают, но не ограничены ими: алклометазоны, алгестоны, беклометазоны (например, беклометазон дипропионат), бетаметазоны (например, бетаметазон 17-валерат, бетаметазон натрий ацетат, бетаметазон натрий фосфат, бетаметазон валерат), будесонид, клобетазолы (например, клобетазол пропионат), клобетазоны, клокортолоны (например, клокортолон пивалат), клопреднолы, кортикостероны, кортизоны и гидрокортизоны (например, гидрокортизон ацетат), кортивазолы, дефлазакорты, десониды, дезоксиметазоны, дексаметазоны (например, дексаметазон 21-фосфат, дексаметазон ацетат, дексаметазон натрий фосфат), дифлоразоны (например, дифлоразон диацетат), дифлукортолоны, дифлупреднаты, эноксолоны, флуазакорты, флуклорониды, флудрокортизоны (например, флудрокортизон ацетат), флуметазоны (например, флуметазон пивалат), флунисолиды, флуоцинолоны (например, флуоцинолон ацетонид), флуоцинониды, флуокортины, флуокортолоны, флуорометолоны (например, флуорометолон ацетат), флуперолоны (например, флуперолон ацетат), флупреднидены, флупреднизолоны, флурандренолиды, флутиказоны (например, флутиказон пропионат), формокорталы, галцинониды, галобетазолы, галометазоны, галопредоны, гидрокортаматы, гидрокортизоны (например, гидрокортизон 21-бутират, гидрокортизон ацепонат, гидрокортизон ацетат, гидрокортизон бутепрат, гидрокортизон бутират, гидрокортизон ципионат, гидрокортизон гемисукцинат, гидрокортизон пробутат, гидрокортизон натрий фосфат, гидрокортизон натрий сукцинат, гидрокортизон валерат), лотепреднол этабонат, мазипредоны, медризоны, мепреднизоны, метилпреднизолоны (метилпреднизолон ацепонат, метилпреднизолон ацетат, метилпреднизолон гемисукцинат, метилпреднизолон натрий сукцинат), мометазоны (например, мометазонфуроат), параметазоны (например, параметазон ацетат), предникарбаты, преднизолоны (например, преднизолон 25-диэтиламиноацетат, преднизолон натрий фосфат, преднизолон 21-гемисукцинат, преднизолон ацетат; преднизолон фарнезилат, преднизолон гемисукцинат, преднизолон-21(бета-D-глюкуронид), преднизолон метасульфобензоат, преднизолон стеаглат, преднизолон тебутат, преднизолон тетрагидрофталат), преднизоны, преднивалы, преднилидены, римексолоны, тиксокортолы, триамцинолоны (например, триамцинолон ацетонид, триамцинолон бенетонид, триамцинолон гексацетонид, триамцинолон ацетонид 21-пальмитат, триамцинолон диацетат). Эти глюкокортикоиды и их соли обсуждаются подробно, например, в Remington’s Pharmaceutical Sciences, A. Osol, ed., Mack Pub. Co., Easton, Pa. (16th ed. 1980).
[0475] В некоторых примерах глюкокортикоид выбран из числа кортизонов, дексаметазонов, гидрокортизонов, метилпреднизолонов, преднизолонов и преднизонов. В частном примере глюкокортикоид является дексаметазоном.
[0476] В некоторых вариантах осуществления агент является кортикостероидом, и его вводят в количестве, которое является терапевтически эффективным для лечения, облегчения или уменьшения одого или более симптомов токсичности в ответ на иммунотерапию и/или клеточную терапию, такой как CRS или нейротоксичности. В некоторых вариантах осуществления индикаторы улучшения или успешного лечения включают определение отсутствия проявления соответствующего балла в масштабе оценки токсичности (например, масштабе оценки CRS или нейротоксичности), такого как балл менее 3 или изменение в оценке или серьезности в масштабе оценки, как обсуждается здесь, такой как изменение от балла 4 до балла 3 или изменение от балла 4 до балла 2, 1 или 0.
[0477] В некоторых аспектах кортикостероид вводят в терапевтически эффективной дозе. Терапевтически эффективная концентрация может быть определена эмпирически путем тестирования в известных системах in vitro или in vivo (например, на модели животных). Например, количество выбранного кортикостероида, который вводят для облегчения симптомов или неблагоприятных эффектов токсичности в ответ на иммунотерапию и/или клеточную терапию, такой как CRS или нейротоксичности, может быть определена стандартными клиническими методами. Кроме того, модели животных могут использоваться для того, чтобы помочь идентифицировать оптимальные диапазоны дозировки. Точная дозировка, которая может быть определена эмпирически, может зависеть от конкретного терапевтического препарата, режима и схемы дозирования, пути введения и серьезности заболевания.
[0478] Кортикостероид может быть введен в любом количестве, которое является эффективным для облегчения одного или более симптомов, связанных с токсичностью, такой как CRS или нейротоксичность. Кортикостероид, например, глюкокортикоид, может быть введен, например, в количестве от или от приблизительно 0,1 до 100 мг, на дозу, от 0,1 до 80 мг, от 0,1 до 60 мг, от 0,1 до 40 мг, от 0,1 до 30 мг, от 0,1 до 20 мг, от 0,1 до 15 мг, от 0,1 до 10 мг, от 0,1 до 5 мг, от 0,2 до 40 мг, от 0,2 до 30 мг, от 0,2 до 20 мг,от 0,2 до 15 мг, от 0,2 до 10 мг, от 0,2 до 5 мг, от 0,4 до 40 мг, от 0,4 до 30 мг, от 0,4 до 20 мг, от 0,4 до 15 мг, от 0,4 до 10 мг, от 0,4 до 5 мг, от 0,4 до 4 мг, от 1 до 20 мг, от 1 до 15 мг или от 1 до 10 мг на 70 кг взрослого человека. Как правило, кортикостероид, такой как, глюкокортикоид, вводят в количестве от или от приблизительно 0,4 до 20 мг, например, составляющем или приблизительно составляющем 0,4 мг, 0,5 мг, 0,6 мг, 0,7 мг, 0,75 мг, 0,8 мг, 0,9 мг, 1 мг, 2 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 11 мг, 12 мг, 13 мг, 14 мг, 15 мг, 16 мг, 17 мг, 18 мг, 19 мг или 20 мг на дозу, среднему взрослому человеку.
[0479] В некоторых вариантах осуществления кортикостероид может быть введен, например, в дозировке, составляющей или приблизительно составляющей 0,001 мг/кг (пациента), 0,002 мг/кг, 0,003 мг/кг, 0,004 мг/кг, 0,005 мг/кг, 0,006 мг/кг, 0,007 мг/кг, 0,008 мг/кг, 0,009 мг/кг, 0,01 мг/кг, 0,015 мг/кг, 0,02 мг/кг, 0,025 мг/кг, 0,03 мг/кг, 0,035 мг/кг, 0,04 мг/кг, 0,045 мг/кг, 0,05 мг/кг, 0,055 мг/кг, 0,06 мг/кг, 0,065 мг/кг, 0,07 мг/кг, 0,075 мг/кг, 0,08 мг/кг, 0,085 мг/кг, 0,09 мг/кг, 0,095 мг/кг, 0,1 мг/кг, 0,15 мг/кг, 0,2 мг/кг, 0,25 мг/кг, 0,30 мг/кг, 0,35 мг/кг, 0,40 мг/кг, 0,45 мг/кг, 0,50 мг/кг, 0,55 мг/кг, 0,60 мг/кг, 0,65 мг/кг, 0,70 мг/кг, 0,75 мг/кг, 0,80 мг/кг, 0,85 мг/кг, 0,90 мг/кг, 0,95 мг/кг, 1 мг/кг, 1,05 мг/кг, 1,1 мг/кг, 1,15 мг/кг, 1,20 мг/кг, 1,25 мг/кг, 1,3 мг/кг, 1,35 мг/кг или 1,4 мг/кг, среднему взрослому человеку, как правило, имеющему массу тела от приблизительно 70 кг до 75 кг.
[0480] Кортикостероид или глюкокортикоид, например, дексаметазон, может быть введен перорально (таблетки, жидкость или жидкий концентрат), РО, внутривенно (IV), внутримышечно или любым другим известным путем или путем, описанным здесь (например, относительно фармацевтических составов). В некоторых аспектах кортикостероид вводят как болюс, и в других аспектах он может быть введен в течение периода времени.
[0481] В некоторых аспектах глюкокортикоид может быть введен в течение периода, составляющего более одного дня, например, более чем два дня, более чем 3 дня или более чем 4 или более дней. В некоторых вариантах осуществления кортикостероид может быть введен один раз в сутки, два раза в сутки или три или более раз в сутки. Например, кортикостероид, например, дексаметазон, может, в некоторых примерах, быть введен в количестве 10 мг (или эквивалентном) IV два раза в день в течение трех дней.
[0482] В некоторых вариантах осуществления дозировку кортикостероида, например, глюкокортикоида, вводят в последовательно более низких дозировках в течение лечения. Следовательно, в некоторых таких режимах лечения, доза кортикостероида сужается. Например, кортикостероид может быть введен в начальной дозе (или эквивалентной дозе, например, в пересчете на дексаметазон) 4 мг, и в каждое последующее введение доза может быть понижена, так, что доза составляет 3 мг для следующего введения, 2 мг для следующего введения и 1 мг для следующего введения
[0483] Обычно доза вводимого кортикостероида зависит от конкретного кортикостероида, поскольку между различными кортикостероидами существует различие в активности. Как правило, понятно, что препараты варьируют в отношении активности, и что дозы могут поэтому варьировать для получения эквивалентных эффектов. Таблица 6 показывает эквивалентность с точки зрения активности для различных глюкокортикоидов и путей введения. Эквивалентная активность в клиническом дозировании известна. Информация, касающаяся эквивалентного дозирования стероидов (в нехронотерапевтической манере) может быть найдена в British National Formulary (BNF) 37, March 1999.
[0484] Таким образом, в некоторых вариантах осуществления, стероид вводят в эквивалентном количестве дозировки от или от приблизительно 1,0 мг до 20 мг дексаметазона в сутки, например, от 1,0 мг до 15 мг дексаметазона в сутки, от 1,0 мг до дексаметазона на 10 мг в сутки, от 2,0 мг до 8 мг дексаметазона в сутки или от 2,0 мг до 6,0 мг дексаметазона в сутки, включительно. В некоторых случаях стероид вводят в эквивалентной дозе, составляющей или приблизительно составляющей 4 мг или составляющей или приблизительно составляющей 8 мг дексаметазона в сутки.
[0485] В некоторых вариантах осуществления стероид вводят, если повышение температуры сохраняется после лечения тоцилизумабом. Например, в некоторых вариантах осуществления, дексаметазон вводят перорально или внутривенно в дозировке 5-10 мг вплоть до каждые 6-12 часов при продолжительном повышении температуры. В некоторых вариантах осуществления тоцилизумаб вводят одновременно с или после добавления кислорода.
B. Ингибитор микроглиальных клеток
[0486] В некоторых вариантах осуществления ингибитор в комбинированной терапии является ингибитором активности микроглиальных клеток. В некоторых вариантах осуществления введение ингибитора модулирует активность микроглии. В некоторых вариантах осуществления ингибитор является антагонистом, ингибирующим активность сигнального пути в микроглии. В некоторых вариантах осуществления ингибитор микроглии оказывает влияние на микроглиальный гомеостаз, выживаемость и/или пролиферацию. В некоторых вариантах осуществления ингибитор нацеливается на CSF1R сигнальный путь. В некоторых вариантах осуществления ингибитор является ингибитором CSF1R. В некоторых вариантах осуществления ингибитор является малой молекулой. В некоторых случаях ингибитор является антителом.
[0487] В некоторых аспектах введение ингибитора приводит к одному или более эффектов, выбранных из альтерации микроглиального гомеостаза и жизнеспособности, уменьшения или блокады пролиферации микроглиальных клеток, сокращения или устранения микроглиальных клеток, сокращения микроглиальной активации, сокращения продукции оксида азота в микроглии, сокращения активности синтазы оксида азота в микроглии или защиты мотонейронов, вызванных микроглиальной активацией. В некоторых вариантах осуществления агент изменяет уровень биомаркера ингибирования CSF1R в сыворотке или крови или уменьшения уровня поперечно сшитого N-телопептида (NTX) коллагена мочи типа 1 по сравнению с моментом времени до инициации введения ингибитора. В некоторых вариантах осуществления введение агента временно ингибирует активность активности микроглии и/или причем ингибирование активности микроглии не является постоянным. В некоторых вариантах осуществления введение агента временно ингибирует активность CSF1R и/или причем ингибирование активности CSF1R не является постоянным.
[0488] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, является малой молекулой, пептидом, белком, антителом или его антигенсвязывающим фрагментом, миметиком антитела, аптамером или молекулой нуклеиновой кислоты. В некоторых вариантах осуществления способ включает введение ингибитора активности микроглии. В некоторых вариантах осуществления агент является антагонистом, ингибирующим активность сигнального пути в микроглии. В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, оказывает влияние на микроглиальный гомеостаз, выживаемость и/или пролиферацию.
[0489] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, выбран из противовоспалительного средства, ингибитора NADPH оксидазы (NOX2), блокатора кальциевых каналов, блокатора натриевых каналов, ингибирует GM-CSF, ингибирует CSF1R, специфично связывается с CSF-1, специфично связывается с IL-34, ингибирует активацию ядерного фактора каппа-B (NF-κB), активирует рецептор CB2 и/или является агонистом CB2, ингибитором фосфодиэстеразы, ингибирует микроРНК-155 ((miR-155), повышающе регулирует микроРНК-124 ((miR-124), ингибирует продукцию оксида азота в микроглии, ингибирует синтазу оксида азота или активирует транскрипционный фактор NRF2 (также названный подобным ядерному фактору(полученному из эритроида-2)-, или NFE2L2).
[0490] В некоторых вариантах осуществления, агент, уменьшающий активность микроглиальных клеток, нацеливается на CSF1 (также названный макрофагальным колониестимулирующим фактором MCSF). В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, оказывает влияние на MCSF-стимулированное фосфорилирование рецептора M-CSF (Pryer et al. Proc Am Assoc Cancer Res, AACR Abstract nr DDT02-2 (2009)). В некоторых случаях агент, уменьшающий активность микроглиальных клеток, представляет собой MCS110 (международная публикация заявки на патент номер WO2014001802; Clinical Trial Study Record Nos.:A1 NCT00757757; NCT02807844; NCT02435680; NCT01643850).
[0491] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, является малой молекулой, нацеливаемой на путь CSF1. В некоторых вариантах осуществления агент является малой молекулой, связывающейся с CSF1R. В некоторых вариантах осуществления агент является малой молекулой, ингибирующей активность киназы CSF1R путем конкуренции с ATФ, связывающимся с киназой CSF1R. В некоторых вариантах осуществления агент является малой молекулой, ингибирующей активацию рецептора CFS1R. В некоторых случаях ингибируется связывание лиганда CSF-1 с CSF1R. В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, является любым из ингибиторов, описанных в Публикации заявки на патент США номер US20160032248.
[0492] В некоторых вариантах осуществления агент является ингибитором, представляющим собой малую молекулу, выбранным из PLX-3397, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, PLX73086 (AC-708), DCC-3014, AZD6495, GW2580, Ki20227, BLZ945, PLX647, PLX5622. В некоторых вариантах осуществления агент является любым из ингибиторов, описанных в Conway et al., Proc Natl Acad Sci U S A, 102(44):16078-83 (2005); Dagher et al., Journal of Neuroinflammation, 12:139 (2015); Ohno et al., Mol Cancer Ther. 5(11):2634-43 (2006); von Tresckow et al. Clin Cancer Res.,21(8) (2015); Manthey et al. Mol Cancer Ther. (8(11):3151-61 (2009); Pyonteck et al., Nat Med. 19(10): 1264-1272 (2013); Haegel et al., Cancer Res AACR Abstract nr 288 (2015); Smith et al., Cancer Res AACR Abstract nr 4889 (2016); Clinical Trial Study Record Nos.: NCT01525602; NCT02734433; NCT02777710; NCT01804530; NCT01597739; NCT01572519; NCT01054014; NCT01316822; NCT02880371; NCT02673736; международных публикациях заявок на патенты номера WO2008063888A2, WO2006009755A2, публикации заявки на патент США номер US20110044998, US 2014/0065141 и US 2015/0119267.
[0493] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, представляет собой 4-((2-(((1R,2R)-2-гидроксициклогексил)амино)бензо[d]тиазол-6-ил)окси)-N-метилпиколинамид (BLZ945) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является следующим соединением:

в котором R1 обозначает алкилпиразол или алкилкарбоксамид, и R2 обозначает гидроксициклоалкил
или его фармацевтически приемлемой солью.
[0494] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, представляет собой 5-((5-хлор-1H-пирроло[2,3-b]пиридин-3-ил)метил)-N-((6-(трифторметил)пиридин-3-ил)метил)пиридин-2-амин, N-[5-[(5-хлор-1H-пирроло[2,3-b]пиридин-3-ил)метил]-2-пиридинил]-6-(трифторметил)-3-пиридинeметанамин) (PLX 3397) или их фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент представляет собой 5-(1H-пирроло[2,3-b]пиридин-3-илметил)-N-[[4-(трифторметил)фенил]метил]-2-пиридинамин дигидрохлорид (PLX647) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, является следующим соединением:
или его фармацевтически приемлемой солью. В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, является следующим соединением:
или его фармацевтически приемлемой солью. В некоторых вариантах осуществления агент является любым из ингибиторов, описанных в патенте США номер US7893075.
[0495] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, представляет собой 4-циано-N-[2-(1-циклогексен-1-ил)-4-[1-[(диметиламино)ацетил]-4-пиперидинил]фенил]-1H-имидазол-2-карбоксамид гидрохлорид (JNJ28312141) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является следующим соединением:

или его фармацевтически приемлемой солью. В некоторых вариантах осуществления агент является любым из ингибиторов, описанных в патенте США номер US7645755.
[0496] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, представляет собой 1H-имидазол-2-карбоксамид, N-(2-(4,4-диметилциклогекс-1-енил)-6-(2,2,6,6-тетраметилтетрагидропиран-4-ил)пиридин-3-ил)амид 5-циано-N-(2-(4,4-диметил-1-циклогексен-1-ил)-6-(тетрагидро-2,2,6,6-тетраметил-2H-пиран-4-ил)-3-пиридинил)-4-циано-1H-имидазол-2-карбоновой кислоты, 4-Циано-N-(2-(4,4-диметилциклогекс-1-ен-1-ил)-6-(2,2,6,6-тетраметил-тетрагидро-2H-пиран-4-ил)пиридин-3-ил)-1H-имидазол-2-карбоксамид (JNJ-40346527) или их фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является следующим соединением:

или его фармацевтически приемлемой солью.
[0497] В другом варианте осуществления агент, уменьшающий активность микроглиальных клеток, представляет собой 5-(3-Метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамин (GW2580) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является следующим соединением:
или его фармацевтически приемлемую соль (международная публикация заявки на патент номер WO2009099553).
[0498] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, представляет собой 4-(2,4-дифторанилина)-7-этокси-6-(4-метилпиперазин-1-ил)хинолин-3-карбоксамид (AZD6495) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является следующим соединением:
или его фармацевтически приемлемую соль.
[0499] В некоторых вариантах осуществления агент, уменьшающий активность микроглиальных клеток, представляет собой N-{4-[(6,7-диметокси-4-хинолил)окси]-2-метоксифенил}-N0-[1-(1,3-тиазол-2-ил)этил]карбамид (Ki20227) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является следующим соединением:

или его фармацевтически приемлемой солью.
[0500] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, является антителом, нацеливаемым на путь CSF1. В некоторых вариантах осуществления агент является антителом, связывающимся с CSF1R. В некоторых вариантах осуществления анти-CSF1R антитело блокирует димеризацию CSF1R. В некоторых вариантах осуществления анти-CSF1R антитело блокирует внутреннюю поверхность димеризации CSF1R, сформированную областями D4 и D5 (Ries et al. Cancer Cell 25(6):846-59 (2014)). В некоторых случаях агент выбран из эмактузумаба (RG7155; RO5509554), кабирализумаба (FPA 008), LY-3022855 (IMC-CS4), AMG-820, TG-3003, MCS110, H27K15, 12-2D6, 2-4A5 (Rovida and Sbarba, J Clin Cell Immunol,6:6 (2015); Clinical Trial Study Record Nos.: NCT02760797; NCT01494688; NCT02323191; NCT01962337; NCT02471716; NCT02526017; NCT01346358; NCT02265536; NCT01444404; NCT02713529, NCT00757757; NCT02807844; NCT02435680; NCT01643850).
[0501] В некоторых вариантах осуществления вещество, уменьшающее активацию микроглиальных клеток, является антибиотиком тетрациклинового ряда. Например, агент оказывает влияние на концентрацию IL-1b, IL-6, TNF-α или iNOS в клетках микроглии (Yrjänheikki et al. PNAS 95(26): 15769-15774 (1998); Clinical Trial Study Record No: NCT01120899). В некоторых вариантах осуществления агент является антагонистом опиоида (Younger et al. Pain Med. 10(4):663-672 (2009). В некоторых вариантах осуществления агент уменьшает глутаматергическую передачу нервного импульса (Патент США Номер 5,527,814). В некоторых вариантах осуществления агент модулирует сигнальный путь NFkB (Valera et al J. Neuroinflammation 12:93 (2015); Clinical Trial Study Record No: NCT00231140). В некоторых вариантах осуществления агент нацеливается на каннабиноидные рецепторы (Ramírez et al. J. Neurosci 25(8):1904-13(2005)). В некоторых вариантах осуществления агент выбран из миноциклина, налоксона, рилузола, леналидомида и каннабиноида (необязательно WIN55 или 212-2).
[0502] Считается, что продукция оксида азота в микроглии в некоторых случаях приводит к нейротоксичности или увеличивает ее. В некоторых вариантах осуществления агент модулирует или ингибирует продукцию оксида азота в микроглии. В некоторых вариантах осуществления агент ингибирует синтазу оксида азота (NOS). В некоторых вариантах осуществления ингибитором NOS является роноптерин (VAS 203), также известный как 4-амино-тетрагидробиоптерин (4-ABH4). В некоторых вариантах осуществления ингибитором NOS является циндунистат, A-84643, ONO-1714, L-NOARG, NCX-456, VAS 2381, GW-273629, NXN-462, CKD-712, KD-7040 или гуанидиноэтилдисульфид. В некоторых вариантах осуществления агент является любым из ингибиторов, описанных в Höing et al., Cell Stem Cell. 2012 Nov 2;11(5):620-32.
[0503] В некоторых вариантах осуществления агент блокирует трафик Т-клеткок, такой как направленный к центральной нервной системе. В некоторых вариантах осуществления, блокировка трафика Т-клеток может уменьшить или устранить проход иммунных клеток через стенки кровеносных сосудов в центральную нервную систему, включая пересечение гематоэнцефалического барьера. В некоторых случаях активированные антиген-специфические Т-клетки продуцируют провоспалительные цитокины, включая IFN-γ и TNF, после реактивации в ЦНС, приводя к активации резидентских клеток, таких как микроглия и астроциты. См. Kivisäkk et al., Neurology. 2009 Jun 2; 72(22): 1922-1930. Таким образом, в некоторых вариантах осуществления, изоляция активированных Т-клеток от микроглиальных клеток, например, путем блокировки трафика и/или ингибирования способности таких клеток пересекать гематоэнцефалический барьер, может уменьшить или устранить микроглиальную активацию. В некоторых вариантах осуществления агент ингибирует молекулы адгезии на иммунных клетках, включая Т-клетки. В некоторых вариантах осуществления агент ингибирует интегрин. В некоторых вариантах осуществления интегрин является альфа-4 интегринами. В некоторых вариантах осуществления агент представляет собой натализумаб (Tysabri®). В некоторых вариантах осуществления агент модулирует рецептор поверхности клеток. В некоторых вариантах осуществления агент модулирует рецептор сфингозин-1-фосфата (S1P), такой как S1PR1 или S1PR5. В некоторых вариантах осуществления агент вызывает интернализацию клеточного рецептора, такого как рецептор сфингозин-1-фосфата (S1P), такой как S1PR1 или S1PR5. В некоторых вариантах осуществления агент представляет собой финголимод (Gilenya®) или озанимод (RPC-1063).
[0504] Считается, что транскрипционный фактор NRF2 регулирует антиоксидантный ответ, например, путем включения генов, содержащих действующий в цис-положении элемент в их промоторной области. Пример такого элемента включает элемент антиоксидантного ответа (ARE). В некоторых вариантах осуществления агент активирует NRF2. В некоторых вариантах осуществления активация NRF2 в микроглиальных клетках уменьшает реактивность микроглиальных клеток в ответ на IFN и LPS. В некоторых вариантах осуществления активация ингибирования NRF2 замедляет или уменьшает демиелинизацию, утерю аксонов, гибель нейронов и/или гибель олигодендроцитов. В некоторых вариантах осуществления агент повышающе регулирует клеточный цитопротекторный путь, регулируемый NRF2. В некоторых вариантах осуществления вещество, активирующее NRF2, является диметилфумаратом (Tecfidera®). В некоторых вариантах осуществления агент является любым из ингибиторов, описанных в патенте США номер 8,399,514. В некоторых вариантах осуществления агент является любым из ингибиторов, описанных в Höing et al., Cell Stem Cell. 2012 Nov 2;11(5):620-32.
[0505] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, представляет собой (4S,4aS,5aR,12aS)-4,7-бис(диметиламино)-3,10,12,12a-тетрагидрокси-1,11-диоксо-1,4,4a,5,5a,6,11,12a-октагидротетрацен-2-карбоксамид (Миноциклин) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является любым из соединений, описанных в публикации заявки на патент США номер US20100190755. В некоторых вариантах осуществления агент является следующим соединением:
или его фармацевтически приемлемой солью.
[0506] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, представляет собой 3-(7-амино-3-оксо-1H-изоиндол-2-ил)пиперидин-2,6-дион (леналидомид) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является следующим соединением:
или его фармацевтически приемлемой солью.
[0507] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, представляет собой (4R,4aS,7aR,12bS)-4a,9-дигидрокси-3-проп-2-енил-2,4,5,6,7a,13-гексагидро-1H-4,12-метанoбензофуро[3,2-e]изохинолин-7-он (налоксон) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является любым из соединений, описанных в патенте США номер US8247425. В некоторых вариантах осуществления агент является следующим соединением:

или его фармацевтически приемлемой солью.
[0508] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, представляет собой 2-амино-6-(трифторметокси)бензотиазол, 6-(трифторметокси)бензо[d]тиазол-2-амин или 6-(трифторметокси)-1,3-бензотиазол-2-амин (рилузол) или их фармацевтически приемлемую соль или производные, как описано в патенте США номер US5527814. В некоторых вариантах осуществления агент является следующим соединением:

или его фармацевтически приемлемой солью.
[0509] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, является модулятором сигнального пути в микроглии. В некоторых случаях агент уменьшает сигнальный путь микроглии. В некоторых вариантах осуществления агентом является ингибитор GM-CSF (CSF2). В других вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, является блокатором ионных каналов. В некоторых определенных вариантах осуществления агент является блокатором кальциевых каналов. Например, в некоторых определенных примерах, агент является блокатором дигидропиридин кальциевых каналов. В некоторых вариантах осуществления агент является ингибитором микроРНК. Например, агент нацеливается на miR-155. В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, выбран из MOR103, Нимодипина, IVIg и LNA-анти-miR-155 (Butoxsky et al. Ann Neurol., 77(1):75-99 (2015) and Sanz et al., Br J Pharmacol. 167(8): 1702-1711 (2012); Winter et al., Ann Clin and Transl Neurol. 2328-9503 (2016); Clinical Trial Study Record Nos.: NCT01517282, NCT00750867).
[0510] В некоторых вариантах осуществления агент, уменьшающий активацию микроглиальных клеток, представляет собой 3-(2-метоксиэтил)5-пропан-2-ил-2,6-диметил-4-(3-нитрофенил)-1,4-дигидропиридин-3,5-дикарбоксилат (нимодипин) или его фармацевтически приемлемую соль или производные. В некоторых вариантах осуществления агент является любым из ингибиторов, описанных в патенте США номер US3799934. В некоторых вариантах осуществления агент является следующим соединением:

или его фармацевтически приемлемую соль.
[0511] В некоторых случаях агент, уменьшающий активацию микроглиальных клеток, вводят в форме, оказывающей влияние только на центральную нервную систему и/или не оказывающей влияние на связанные с опухолью макрофаги. В некоторых вариантах осуществления агент промотирует неактивное состояние микроглии, но не устраняет или сокращает количество микроглии. В некоторых вариантах осуществления способ включает ингибирование активности микроглии специфично в мозге, такое как описанное в Ponomarev et al., Nature Medicine, (1):64-70 (2011).
[0512] Примеры веществ, уменьшающих активацию микроглиальных клеток, и примеры режимов дозирования для введения таких агентов, представлены в Таблице 7 ниже.
(IMC-CS4)
(например, WIN55,212-2)
C. Другие Агенты (например, агенты нацеливания цитокина)
[0513] В некоторых вариантах осуществления, агент, например, нацеливаемый на токсичность агент, который лечит или облегчает симптомы токсичности иммунотерапии и/или клеточной терапии, такой как CRS или нейротоксичность, является таким, который нацеливается на цитокин, например, является антагонистом или ингибитором цитокина, таким как трансформирующий фактор роста бета (TGF-бета), интерлейкин 6 (IL-6), интерлейкин 10 (IL-10), IL-2, MIP1β (CCL4), TNF-альфа, IL-1, интерферон (IFN-гамма) или моноцитарный хемоаттрактантный белок-1 (MCP-1). В некоторых вариантах осуществления агент, который лечит или облегчает симптомы токсичности иммунотерапии и/или клеточной терапии, такой как CRS или нейротоксичность, является таким, который нацеливается (например, ингибирует или является антагонистом) на рецептор цитокина, такой как рецептор IL-6 (IL-6R), рецептор IL-2 (IL-2R/CD25), MCP-1 (CCL2) рецептор (CCR2 или CCR4), TGF-бета рецептор (TGF-бета I, II, или III), IFN-гамма рецептор (IFNGR), рецептор MIP1β (например, CCR5), TNF-альфа рецептор (например, TNFR1), рецептор IL-1 (IL1-Rα/IL-1Rβ) или рецептор IL-10 (IL-10R).
[0514] Количество выбранного агента, который лечит или облегчает симптомы токсичности иммунотерапии и/или клеточной терапии, такой как CRS или нейротоксичность, который вводят для облегчения симптомов или неблагоприятных эффектов токсичности в ответ на иммунотерапию и/или клеточную терапию, такой как CRS или нейротоксичность, может быть определено стандартными клиническими методами. Примеры нежелательных явлений включают, но не ограничены ими, увеличение аланин аминотрансферазы, увеличение аспартатаминотрансферазы, озноб, лихорадочную нейтропению, головную боль, гипотензию, левожелудочковую дисфункцию, энцефалопатию, гидроцефалию, судороги и/или тремор.
[0515] В некоторых вариантах осуществления агент вводят в количестве дозировки от или от приблизительно 30 мг до 5000 мг, например, от 50 мг до 1000 мг, от 50 мг до 500 мг, от 50 мг до 200 мг, от 50 мг до 100 мг, от 100 мг до 1000 мг, от 100 мг до 500 мг, от 100 мг до 200 мг, от 200 мг до 1000 мг, от 200 мг до 500 мг или от 500 мг до 1000 мг.
[0516] В некоторых вариантах осуществления агент вводят от или от приблизительно 0,5 мг/кг до 100 мг/кг, например, от или от приблизительно 1 мг/кг до 50 мг/кг, от 1 мг/кг до 25 мг/кг, от 1 мг/кг до 10 мг/кг, от 1 мг/кг до 5 мг/кг, от 5 мг/кг до 100 мг/кг, от 5 мг/кг до 50 мг/кг, от 5 мг/кг до 25 мг/кг, от 5 мг/кг до 10 мг/кг, от 10 мг/кг до 100 мг/кг, от 10 мг/кг до 50 мг/кг, от 10 мг/кг до 25 мг/кг, от 25 мг/кг до 100 мг/кг, от 25 мг/кг до 50 мг/кг до 50 мг/кг до 100 мг/кг. В некоторых вариантах осуществления агент вводят в количестве дозировки от или от приблизительно 1 мг/кг до 10 мг/кг, от 2 мг/кг до 8 мг/кг, от 2 мг/кг до 6 мг/кг, от 2 мг/кг до 4 мг/кг или от 6 мг/кг до 8 мг/кг, включительно. В некоторых аспектах агент вводят в количестве дозировки по меньшей мере или по меньшей мере приблизительно или приблизительно 1 мг/кг, 2 мг/кг, 4 мг/кг, 6 мг/кг, 8 мг/кг, 10 мг/кг или более. В некоторых вариантах осуществления агент вводят в дозе 4 мг/кг или 8 мг/кг.
[0517] В некоторых вариантах осуществления агент вводят инъекцией, например, внутривенными или подкожными инъекциями, внутриглазной инъекцией, периокулярной инъекция, подсетчаточной инъекцией, интравитреальной инъекцией, транссептальной инъекцией, подсклеральной инъекцией, внутрихориоидальной инъекцией, внутрикамеральной инъекцией, субконъюнктивальной инъекцией, подконъюнктивальной инъекция, субтеноновой инъекцией, ретробульбарной инъекцией, перибульбарной инъекцией или задней околосклеральной доставкой. В некоторых вариантах осуществления его вводят парентеральным, интрапульмонарным и внутриносовым путем, и, если желательно местное лечение, внутриочаговым введением. Парентеральные вливания включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение.
[0518] В некоторых вариантах осуществления количество агента вводят примерно или приблизительно два раза в день, один раз в день, через день, три раза в неделю, один раз в неделю, один раз в две недели или один раз в месяц.
[0519] В некоторых вариантах осуществления агент вводят как часть композиции или состава, такого как фармацевтическая композиция или состав, как описано ниже. Таким образом, в некоторых случаях, композицию, включающую агент, вводят, как описано ниже. В других аспектах агент вводят индивидуально, и он может быть введен любым известным приемлемым путем введения или путем, описанным здесь, таким как описаны в отношении композиций и фармацевтических составов.
[0520] В некоторых вариантах осуществления агент, который лечит или облегчает симптомы токсичности иммунотерапии и/или клеточной терапии, такой как CRS или нейротоксичность, является антителом или антигентсвязывающим фрагментом. В некоторых вариантах осуществления агент представляет собой тоцилизумаб, силтуксимаб, сарилумаб, олокизумаб (CDP6038), элсилимомаб, ALD518/BMS-945429, сирукумаб (CNTO 136), CPSI-2634, ARGX-109, FE301 или FM101.
[0521] В некоторых вариантах осуществления агент является антагонистом или ингибитором IL-6 или рецептора IL-6 (IL-6R). В некоторых аспектах агент является антителом, нейтрализующим активность IL-6, таким как антитело или антигентсвязывающий фрагмент, связывающийся с IL-6 или IL-6R. Например, в некоторых вариантах осуществления, агент представляет собой или включает тоцилизумаб (атлизумаб) или сарилумаб, анти-IL-6R антитело. В некоторых вариантах осуществления агент является анти-IL-6R антителом, описанным в Патенте США номер: 8,562,991. В некоторых случаях агент, нацеливающийся на IL-6, является анти-IL-6 антителом, таким как силтуксимаб, элсилимомаб, ALD518/BMS-945429, сирукумаб (CNTO 136), CPSI-2634, ARGX-109, FE301, FM101 или олокизумаб (CDP6038). В некоторых аспектах агент может нейтрализовать активность IL-6 путем ингибирования взаимодействий лиганд-рецептор. Выполнимость этого общего типа подхода была продемонстрирована с антагонистом рецептора интерлейкина-1 натурального происхождения. См. Harmurn, C. H. et al., Nature (1990) 343:336-340. В некоторых аспектах IL-6/IL-6R антагонист или ингибитор являются мутеином IL-6, таким как описанный в Патенте США No. 5591827. В некоторых вариантах осуществления агент, который является антагонистом или ингибитором IL-6/IL-6R, является малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0522] В некоторых вариантах осуществления агент является тоцилизумабом. В некоторых вариантах осуществления тоцилизумаб вводят как вмешательство на ранней стадии в соответствии со способами по изобретению и/или с применением изделий или композиций по изобретению, в дозировке от или от приблизительно 1 мг/кг до 12 мг/кг, например, составляющей или приблизительно составляющей 4 мг/кг, 8 мг/кг или 10 мг/кг. В некоторых вариантах осуществления тоцилизумаб вводят внутривенным вливанием. В некоторых вариантах осуществления тоцилизумаб вводят в случае непроходящего повышения температуры до более чем 39°C длительность 10 часов, которое резистентно к ацетоаминофену. В некоторых вариантах осуществления второе введение тоцилизумаба проводят, если симптомы рецидивируют через 48 часов после начальной дозы.
[0523] В некоторых вариантах осуществления агент является агонистом или стимулятором TGF-β или TGF-β рецептора (например, TGF-β рецептора I, II, или III). В некоторых аспектах агент является антителом, увеличивающим активность TGF-β, таким как антитело или антигентсвязывающий фрагмент, связывающийся с TGF-β или одним из его рецепторов. В некоторых вариантах осуществления агент, который является агонистом или стимулятором TGF-β и/или его рецептора, является малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0524] В некоторых вариантах осуществления агент является антагонистом или ингибитором MCP-1 (CCL2) или рецептора MCP-1 (например, рецептора MCP-1 CCR2 или CCR4). В некоторых аспектах агент является антителом, нейтрализующим активность MCP-1, таким как антитело или антигентсвязывающий фрагмент, связывающийся с MCP-1 или одним из его рецепторов (CCR2 или CCR4). В некоторых вариантах осуществления антагонист MCP-1 или ингибитор являются такими, как описано в Gong et al. J Exp Med. 1997 Jul 7; 186(1): 131-137 или Shahrara et al. J Immunol 2008; 180:3447-3456. В некоторых вариантах осуществления агент, который является антагонистом или ингибитором MCP-1 и/или его рецептора (CCR2 или CCR4), является малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0525] В некоторых вариантах осуществления агент является антагонистом или ингибитором IFN-γ или IFN-γ рецептора (IFNGR). В некоторых аспектах агент является антителом, нейтрализующим активность IFN-γ, таким как антитело или антигентсвязывающий фрагмент, связывающийся с IFN-γ или его рецептором (IFNGR). В некоторых аспектах IFN-гамма нейтрализирующее антитело представляет собой любое описанное в Dobber et al. Cell Immunol. 1995 Feb;160(2):185-92 или Ozmen et al. J Immunol. 1993 Apr 1;150(7):2698-705. В некоторых вариантах осуществления агент, который является антагонистом или ингибитором IFN-γ/IFNGR, является малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0526] В некоторых вариантах осуществления агент является антагонистом или ингибитором IL-10 или рецептора IL-10 (IL-10R). В некоторых аспектах агент является антителом, нейтрализующим активность IL-10, таким как антитело или антигентсвязывающий фрагмент, связывающийся с IL-10 или IL-10R. В некоторых аспектах IL-10 нейтрализирующее антитело представляет собой любое описанное в Dobber et al. Cell Immunol. 1995 Feb;160(2):185-92 или Hunter et al. J Immunol. 2005 Jun 1;174(11):7368-75. В некоторых вариантах осуществления агент, который является антагонистом или ингибитором IL-10/IL-10R, является малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0527] В некоторых вариантах осуществления агент является антагонистом или ингибитором IL-1 или рецептора IL-1 (IL-1R). В некоторых аспектах агент является антагонистом рецептора IL-1, который является модифицированной формой IL-1R, такой как анакинра (см., например, Fleischmann et al., (2006) Annals of the rheumatic diseases. 65(8):1006-12). В некоторых аспектах агент является антителом, нейтрализующим активность IL-1, таким как антитело или антигентсвязывающий фрагмент, связывающийся с IL-1 или IL-1R, таким как канакинумаб (см. также EP 2277543). В некоторых вариантах осуществления агент, который является антагонистом или ингибитором IL-1/IL-1R, является малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0528] В некоторых вариантах осуществления агент является антагонистом или ингибитором фактора некроза опухоли (TNF) или рецептора фактора некроза опухоли (TNFR). В некоторых аспектах агент является антителом, блокирующим активность TNF, таким как антитело или антигентсвязывающий фрагмент, связывающийся с TNF, таким как TNFα или его рецептор (TNFR, например, TNFRp55 или TNFRp75). В некоторых аспектах агент выбран из числа инфликсимаба, адалимумаба, цертолизумаба пегола, голимумаба и этанерцепта. В некоторых вариантах осуществления агент, который является антагонистом или ингибитором TNF/TNFR, является малой молекулой, белком или пептидом или нуклеиновой кислотой. В некоторых вариантах осуществления агент является малой молекулой, оказывающей влияние на TNF, такой как леналидомид (см., например, Muller et al. (1999) Bioorganic & Medicinal Chemistry Letters. 9 (11):1625).
[0529] В некоторых вариантах осуществления агент является антагонистом или ингибитором трансдукции сигналов через Янус-киназу (JAK) и каскад трансдукции сигналов из двух элементов: переносчика сигнала и активаторова транскрипции (STAT). Белки JAK/STAT являются общими компонентами трансдукции сигналов цитокина и рецептора цитокина. В некоторых вариантах осуществления, агент, который является антагонистом или ингибитором JAK/STAT, таким как руксолитиниб (см., например, Mesa et al. (2012) Nature Reviews Drug Discovery. 11(2):103-104), тофацитиниб (также известный как Xeljanz, Jakvinus тасоцитиниб и CP 690550), барицитиниб (также известный как LY-3009104, INCB 28050), филготиниб (G-146034, GLPG-0634), гандотиниб (LY-2784544), лестауртиниб (CEP 701), момелотиниб (GS-0387, CYT-387), пакритиниб (SB1518) и упадацитиниб (ABT 494). В некоторых вариантах осуществления агент является малой молекулой, белком или пептидом или нуклеиновой кислотой.
[0530] В некоторых вариантах осуществления агент является ингибитором киназы. В некоторых вариантах осуществления агент является ингибитором тирозинкиназы Брутона (BTK). В некоторых вариантах осуществления ингибитор представляет собой или включает ибрутиниб или акалабрутиниб (см., например, Barrett et al., ASH 58th Annual Meeting San Diego, CA December 3-6, 2016, Abstract 654; Ruella et al., ASH 58th Annual Meeting San Diego, CA December 3-6, 2016, Abstract 2159). В некоторых вариантах осуществления агент является ингибитором, как описано в Патентах США No. 7,514,444; 8,008,309; 8,476,284; 8,497,277; 8,697,711; 8,703,780; 8,735,403; 8,754,090; 8,754,091; 8,957,079; 8,999,999; 9,125,889; 9,181,257; или 9,296,753.
[0531] В некоторых вариантах осуществления устройство, такое как технология абсорбирующей смолы с фильтрацией крови или плазмы, может использоваться для уменьшения уровней цитокина. В некоторых вариантах осуществления устройство, используемое для уменьшения уровней цитокина, является физическим абсорбером цитокина, таким как экстракорпоральный абсорбер цитокина. В некоторых вариантах осуществления физический абсорбер цитокина может использоваться для устранения цитокинов из кровотока ex vivo экстракорпоральным образом. В некоторых вариантах осуществления вещество является пористым полимером. В некоторых вариантах осуществления агентом является CytoSorb (см., например, Basu et al. Indian J Crit Care Med. (2014) 18(12): 822-824).
III. РЕКОМБИНАНТНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, ЭКСПРЕССИРУЕМЫЕ КЛЕТКАМИ
[0532] В некоторых вариантах осуществления клетки для использования в или вводимые в связи со способами по изобретению содержат или спроектированы так, чтобы содержать генно-инженерный рецептор, например, генно-инженерный антигенный рецептор, такой как химерный антигенный рецептор (CAR) или Т-клеточный рецептор (TCR). Изобретение также относится к популяции таких клеток, композициям, содержащим такие клетки и/или обогащенным такими клетками, таким как в которых клетки определенного типа, такие как Т-клетки или CD8+ или CD4+ клетки, обогащены или выбраны. Среди композиций можно назвать фармацевтические композиции и составы для введения, такого как для адоптивной клеточной терапии. Изобретение также относится к терапевтическим способам введения клеток и композиций лицам, например, пациентам, в соответствии со способами по изобретению, и/или с использованием изделий или композиций по изобретению.
[0533] В некоторых вариантах осуществления клетки включают одну или более нуклеиновых кислот, введенных путем генной инженерии, и таким образом, экспрессируют рекомбинантный ген или генно-инженерные продукты таких нуклеиновых кислот. В некоторых вариантах осуществления перенос генов осуществляют сначала стимуляцией клеток, например, путем их комбинации со стимулом, вызывающим ответ, такой как пролиферация, выживаемость и/или активация, например, при измерении экспрессией цитокина или маркера активации, с последующей трансдукцией активированных клеток и ростом в культуре до чисел, достаточных для клинических применений.
[0534] Клетки обычно экспрессируют рекомбинантные рецепторы, такие как антигенные рецепторы, включая функциональные не-TCR антигенные рецепторы, например, химерные антигенные рецепторы (CAR) и другие антигенсвязывающие рецепторы, такие как трансгенные Т-клеточные рецепторы (TCRs). Также среди рецепторов можно назвать другие химерные рецепторы.
A. Химерные антигенные рецепторы (CAR)
В некоторых вариантах осуществления способов и применений по изобретению, химерные рецепторы, такие как химерные антигенные рецепторы, содержат один или более доменов, объединяющих лигандсвязывающий домен (например, антитело или фрагмент антитела), который обеспечивает специфичность к желаемому антигену (например, антигену опухоли), с внутриклеточными сигнальными доменами. В некоторых вариантах осуществления внутриклеточный сигнальный домен является стимулирующей или активирующей частью внутриклеточного домена, такого как стимулирующий или активирующий Т-клетки домен, обеспечивая первичный сигнал активации или первичный сигнал. В некоторых вариантах осуществления внутриклеточный сигнальный домен содержит или дополнительно содержит костимулирующий сигнальный домен для облегчения эффекторных функций. В некоторых вариантах осуществления химерные рецепторы, когда они введены путем генной инженерии в иммунные клетки, могут модулировать активность Т-клеток и, в некоторых случаях, могут модулировать дифференцировку или гомеостаз Т-клеток, таким образом приводя к генно-инженерным клеткам с улучшенной продолжительностью жизни, выживаемостью и/или персистированием in vivo, например, для использования в способах адоптивной клеточной терапии.
[0535] Примеры антигенных рецепторов, включая CAR, и способов для разработки и введения таких рецепторов в клетки включают описанные, например, в публикациях международных заявок на патенты WO200014257, WO2013126726, WO2012/129514, WO2014031687, WO2013/166321, WO2013/071154, WO2013/123061, публикациях заявок на патенты США US2002131960, US2013287748, US20130149337, Патентах США: 6,451,995, 7,446,190, 8,252,592, 8,339,645, 8,398,282, 7,446,179, 6,410,319, 7,070,995, 7,265,209, 7,354,762, 7,446,191, 8,324,353 и 8,479,118, и европейской заявке на патент EP2537416 и/или описанные Sadelain et al., Cancer Discov. 2013 April; 3(4): 388-398; Davila et al. (2013) PLoS ONE 8(4): e61338; Turtle et al., Curr. Opin. Immunol., 2012 October; 24(5): 633-39; Wu et al., Cancer, 2012 March 18(2): 160-75. В некоторых аспектах антигенные рецепторы включают CAR, как описано в Патенте США: 7,446,190, и описанные в Публикации Международной Заявки на патент: WO/2014055668 A1. Примеры CAR включают CAR, как раскрыто в любой из вышеупомянутых публикаций, таких как WO2014031687, US 8,339,645, US 7,446,179, US 2013/0149337, Патенте США: 7,446,190, Патенте США: 8,389,282, Kochenderfer et al., 2013, Nature Reviews Clinical Oncology, 10, 267-276 (2013); Wang et al. (2012) J. Immunother. 35(9): 689-701; и Brentjens et al., Sci Transl Med. 2013 5(177). См. также WO2014031687, US 8,339,645, US 7,446,179, US 2013/0149337, Патент США: 7,446,190 и Патент США: 8,389,282.
[0536] Химерные рецепторы, такие как CAR, обычно включают внеклеточный антигенсвязывающий домен, такой как часть молекулы антитела, обычно вариабельную область тяжелой цепи (VH) и/или вариабельную область легкой цепи (VL) антитела, например, фрагмент scFv антитела.
[0537] В некоторых вариантах осуществления антиген, нацеливаемый рецептором, является полипептидом. В некоторых вариантах осуществления он представляет собой углевод или другую молекулу. В некоторых вариантах осуществления антиген селективно экспрессируется или суперэкспрессируется на клетках заболевания или состояния, например, опухоли или патогенных клетках, по сравнению с нормальными или не являющимися мишенями клетками или тканями. В других вариантах осуществления антиген экспрессируется на нормальных клетках и/или экспрессируется на генно-инженерных клетках.
[0538] В некоторых вариантах осуществления антиген, нацеливаемый рецептором, представляет собой или включает выбранный из числа αvβ6 интегрина (avb6 интегрина), В-клеточный антиген созревания (BCMA), B7-H3, B7-H6, карбоангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, антигена рака/яичка 1B (CTAG, также известного как NY-ESO-1 и LAGE-2), карциноэмбрионального антигена (CEA), циклина, циклина A2, Лиганда Хемокина Мотива C-C 1 (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, протеогликана 4 с хондроитинсульфатами (CSPG4), белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфринаB2, рецептора эфрина A2 (EPHa2), эстрогенового рецептора, Fc-подобного рецептора 5 (FCRL5; также известного как гомолог рецептора Fc 5 или FCRH5), эмбрионального рецептора ацетилхолина (эмбрионального AchR), фолат-связывающего белка (FBP), альфа рецептора фолата, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), глипикана-3 (GPC3), 5D рецептора, связанного с G-белком (GPCR5D), Her2/neu (рецепторной тирозинкиназы erb-B2), Her3 (erb-B3), HeR4 (erb-B4), димеров erbB, высокомолекулярного меланома-ассоциированного антигена человека (HMW-MAA), поверхностного антигена гепатита B, человеческого лейкоцитарного антиген A1 (HLA-A1), человеческого лейкоцитарного антиген A2 (HLA-A2), альфа рецептора IL-22 (IL-22Rα), альфа рецептора IL-13 2 (IL-13Rα2), рецептора, содержащего домен вставки киназы (kdr), легкой каппа-цепи, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, члена А семейства 8, содержащего богатые лейцином повторы (LRRC8A), антигена Ley, меланома-ассоциированного антигена (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелина (MSLN), c-Met, мышиного цитомегаловируса (CMV), муцина 1 (MUC1), MUC16, лигандов члена D группы 2 естественных клеток-киллеров (NKG2D), мелана (MART-1), молекулы адгезии нервных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простатоспецифического антигена, антигена стволовых клеток предстательной железы (PSCA), простатоспецифического мембранного антигена (PSMA), подобного рецепторной тирозинкиназе орфанного рецептора 1 (ROR1), сурвивина, трофобластного гликопротеина (TPBG, также известного как 5T4), опухолеассоциированного гликопротеина 72 (TAG72), Тирозиназа-зависимого белка 1 (TRP1, также известного как TYRP1 или gp75), Тирозиназа-зависимого белка 2 (TRP2, также известного как допахром таутомераза, допахром дельта-изомераза или DCT), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора фактора роста эндотелия сосудов 2 (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфического или патоген-экспрессируемого антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекул и/или молекул, экспрессируемых HIV, HCV, HBV или другими патогенами. Антигены, нацеливаемые рецепторами, в некоторых вариантах осуществления включают антигены, ассоциированные с В-клеточной злокачественной опухолью, такие как любой из многих известных В-клеточных маркеров. В некоторых вариантах осуществления антиген, нацеливаемый рецептором, представляет собой CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Igкаппа, Igлямбда, CD79a, CD79b или CD30.
[0539] В некоторых вариантах осуществления домены scFv и/или VH получены из FMC63. FMC63 обычно относится к моноклональному мышиному антителу IgG1, продуцируемому против Nalm-1 и -16 клеток, экспрессирующих CD19 человеческого происхождения (Ling, N. R., et al. (1987). Leucocyte typing III. 302). Антитело FMC63 включает CDRH1 и H2, представленные в SEQ ID NOS: 38, 39, соответственно, и CDRH3, представленный в SEQ ID NOS: 40 или 54, и CDRL1, представленный в SEQ ID NOS: 35 и CDR L2 36 или 55 и CDR L3 последовательности 37 или 56. Антитело FMC63 включает вариабельную область тяжелой цепи (VH), включающую аминокислотную последовательность SEQ ID NO: 41, и вариабельную область легкой цепи (VL), включающую аминокислотную последовательность SEQ ID NO: 42. В некоторых вариантах осуществления svFv включает вариабельную легкую цепь, содержащую последовательность CDRL1 SEQ ID NO:35, последовательность CDRL2 SEQ ID NO:36 и последовательность CDRL3 SEQ ID NO:37 и/или вариабельную тяжелую цепь, содержащую последовательность CDRH1 SEQ ID NO:38, последовательность CDRH2 SEQ ID NO:39 и последовательность CDRH3 SEQ ID NO:40. В некоторых вариантах осуществления scFv включает вариабельную область тяжелой цепи FMC63, представленную в SEQ ID NO:41, и вариабельную область легкой цепи FMC63, представленную в SEQ ID NO:42. В некоторых вариантах осуществления вариабельная тяжелая и вариабельная легкая цепь связаны линкером. В некоторых вариантах осуществления линкер представлен в SEQ ID NO:24. В некоторых вариантах осуществления scFv включает, в указанном порядке, VH, линкер и VL. В некоторых вариантах осуществления scFv включает, в указанном порядке, VL, линкер и VH. В некоторых вариантах осуществления svFc кодируется последовательностью нуклеотидов, представленной в SEQ ID NO:25, или последовательностью, показывающей по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности последовательности с SEQ ID NO:25. В некоторых вариантах осуществления scFv включает аминокислотную последовательность, представленную в SEQ ID NO:43, или последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности последовательности с SEQ ID NO:43.
[0540] В некоторых вариантах осуществления scFv получен из SJ25C1. SJ25C1 является моноклональным мышиным антителом IgG1, продуцируемым против Nalm-1 и -16 клеток, экспрессирующих CD19 человеческого происхождения (Ling, N. R., et al. (1987). Leucocyte typing III. 302). Антитело SJ25C1 включает CDRH1, H2 и H3, представленные в SEQ ID NOS: 47-49, соответственно, и CDRL1, последовательности L2 и L3, представленные в SEQ ID NOS: 44-46, соответственно. Антитело SJ25C1 включает вариабельную область тяжелой цепи (VH), включающую аминокислотную последовательность SEQ ID NO: 50, и вариабельную область легкой цепи (VL), включающую аминокислотную последовательность SEQ ID NO: 51. В некоторых вариантах осуществления svFv включает вариабельную легкую цепь, содержащую последовательность CDRL1 SEQ ID NO:44, последовательность CDRL2 SEQ ID NO: 45 и последовательность CDRL3 SEQ ID NO:46 и/или вариабельную тяжелую цепь, содержащую последовательность CDRH1 SEQ ID NO:47, последовательность CDRH2 SEQ ID NO:48 и последовательность CDRH3 SEQ ID NO:49. В некоторых вариантах осуществления scFv включает вариабельную область тяжелой цепи SJ25C1, представленную в SEQ ID NO:50, и вариабельную область легкой цепи SJ25C1, представленную в SEQ ID NO:51. В некоторых вариантах осуществления вариабельная тяжелая и вариабельная легкая цепь связаны линкером. В некоторых вариантах осуществления линкер представлен в SEQ ID NO:52. В некоторых вариантах осуществления scFv включает, в указанном порядке, VH, линкер и VL. В некоторых вариантах осуществления scFv включает, в указанном порядке, VL, линкер и VH. В некоторых вариантах осуществления scFv включает аминокислотную последовательность, представленную в SEQ ID NO:53, или последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности последовательности с SEQ ID NO:53.
[0541] В некоторых вариантах осуществления химерный антигенный рецептор включает внеклеточную часть, содержащую фрагмент антитела или антитело. В некоторых аспектах химерный антигенный рецептор включает внеклеточную часть, содержащую антитело или фрагмент и внутриклеточный сигнальный домен. В некоторых вариантах осуществления антитело или фрагмент включает scFv.
[0542] В некоторых вариантах осуществления часть антитела рекомбинантного рецептора, например, CAR, дополнительно включает по меньшей мере часть константной области иммуноглобулина, такой как шарнирная область, например, шарнирная область IgG4, и/или область Fc и/или CH1/CL. В некоторых вариантах осуществления, константная область или часть происходит от человеческого IgG, такого как IgG4 или IgG1. В некоторых аспектах часть константной области служит областью спейсера между компонентом узнавания антигена, например, scFv, и трансмембранным доменом. Спейсер может иметь длину, обеспечивающую увеличенную реактивность клетки после связывания антигена по сравнению с отсутствием спейсера. Примеры спейсеров включают, но не ограничены ими, описанные в Hudecek et al. (2013) Clin. Cancer Res., 19:3153, публикации международной заявки на патент WO2014031687, Патенте США No. 8,822,647 или опубликованной заявке No. US2014/0271635.
[0543] В некоторых вариантах осуществления константная область или часть происходит от человеческого IgG, такого как IgG4 или IgG1. В некоторых вариантах осуществления спейсер имеет последовательность ESKYGPPCPPCP (представленную в SEQ ID NO: 1), и кодируется последовательностью, представленной в SEQ ID NO: 2. В некоторых вариантах осуществления спейсер имеет последовательность, представленную в SEQ ID NO: 3. В некоторых вариантах осуществления спейсер имеет последовательность, представленную в SEQ ID NO: 4. В некоторых вариантах осуществления константная область или часть происходит от IgD. В некоторых вариантах осуществления спейсер имеет последовательность, представленную в SEQ ID NO: 5. В некоторых вариантах осуществления спейсер имеет аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с любой SEQ ID NOS: 1, 3, 4 или 5. В некоторых вариантах осуществления спейсер имеет последовательность, представленную в SEQ ID NOS: 26-34. В некоторых вариантах осуществления спейсер имеет аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с любой SEQ ID NOS: 26-34.
[0544] В некоторых вариантах осуществления антигенный рецептор включает внутриклеточный домен, связанный прямо или косвенно с внеклеточным доменом. В некоторых вариантах осуществления химерный антигенный рецептор включает трансмембранный домен, связывающий внеклеточный домен и внутриклеточный сигнальный домен. В некоторых вариантах осуществления внутриклеточный сигнальный домен включает ITAM. Например, в некоторых аспектах, антигенраспознающий домен (например, внеклеточный домен) обычно связан с одним или более внутриклеточными сигнальными компонентами, такими как сигнальные компоненты, являющиеся миметиками активации через комплекс антигенного рецептора, такой как комплекс TCR, в случае CAR и/или сигнала через другой рецептор поверхности клеток. В некоторых вариантах осуществления химерный рецептор включает трансмембранный домен, связанный или слитый между внеклеточным доменом (например, scFv) и внутриклеточным сигнальным доменом. Таким образом, в некоторых вариантах осуществления, антигенсвязывающий компонент (например, антитело) связан с одним или более трансмембранными и внутриклеточными сигнальными доменами.
[0545] В одном варианте осуществления используется трансмембранный домен, естественно связанный с одним из доменов в рецепторе, например, CAR. В некоторых случаях трансмембранный домен выбран или модифицирован замещением аминокислоты, чтобы избежать связывания таких доменов с трансмембранными доменами тех же или других поверхностных мембранных белков для уменьшения взаимодействий с другими членами комплекса рецептора.
[0546] Трансмембранный домен в некоторых вариантах осуществления получен из естественного или из синтетического источника. Когда источник является естественным, домен в некоторых аспектах получен из любого мембраносвязанного или трансмембранного белка. Трансмембранные области включают полученные из (т.е., включают по меньшей мере трансмембранную область(и)), альфа, бета или дзэта цепи Т-клеточного рецептора, CD28, эпсилон CD3, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, CD154. Альтернативно трансмембранный домен в некоторых вариантах осуществления является синтетическим продуктом. В некоторых аспектах синтетический трансмембранный домен включает преимущественно гидрофобные остатки, такие как лейцин и валин. В некоторых аспектах триплет фенилаланина, триптофана и валина обнаруживается на каждом конце синтетического трансмембранного домена. В некоторых вариантах осуществления связь осуществляется линкерами, спейсерами и/или трансмембранным доменом(ами). В некоторых аспектах трансмембранный домен содержит трансмембранную часть CD28.
[0547] В некоторых вариантах осуществления внеклеточный домен и трансмембранный домен могут быть связаны прямо или косвенно. В некоторых вариантах осуществления внеклеточный домен и трансмембранный связаны спейсером, таким как любой описанный здесь. В некоторых вариантах осуществления рецептор содержит внеклеточную часть молекулы, из которой трансмембранный домен получен, такую как внеклеточная часть CD28.
[0548] Среди внутриклеточных сигнальных доменов можно назвать такие, которые являются миметиками или аппроксиматорами сигнала через природный антигенный рецептор, сигнала через такой рецептор в сочетании с костимулирующим рецептором и/или сигнала через один только костимулирующий рецептор. В некоторых вариантах осуществления, короткий олиго- или полипептидный линкер, например, линкер длиной от 2 до 10 аминокислот, такой как линкер, содержащий глицины и серины, например, дублет глицин-серин, присутствует и формирует связь между трансмембранным доменом и цитоплазматическим сигнальным доменом CAR.
[0549] Активация Т-клеток в некоторых аспектах описывается как опосредуемая двумя классами цитоплазматических сигнальных последовательностей: теми, которые инициируют антигензависимую первичную активацию через TCR (первичные цитоплазматические сигнальные последовательности), и теми, которые действуют независимым от антигена образом для обеспечения вторичного или костимулирующего сигнала (вторичные цитоплазматические сигнальные последовательности). В некоторых аспектах CAR включает один или оба из таких сигнальных компонентов.
[0550] Рецептор, например, CAR, обычно включает по меньшей мере один внутриклеточный сигнальный компонент или компоненты. В некоторых аспектах CAR включает первичную цитоплазматическую сигнальную последовательность, регулирующую первичную активацию комплекса TCR. Первичные цитоплазматические сигнальные последовательности, действующие стимулирующим образом, могут содержать сигнальные мотивы, которые известны как иммунорецепторные тирозиновые активирующие мотивы, или ITAM. Примеры ITAM, содержащих первичные цитоплазматические сигнальные последовательности, включают полученные из CD3 дзэта цепи, FcR гамма, CD3 гамма, CD3 дельта и CD3 эпсилон. В некоторых вариантах осуществления цитоплазматическая сигнальная молекула(ы) в CAR содержит цитоплазматический сигнальный домен, его часть или последовательность, полученную из CD3 дзэта.
[0551] В некоторых вариантах осуществления рецептор включает внутриклеточный компонент комплекса TCR, такой как цепь CD3 TCR, которая опосредует Т-клеточную активацию и цитотоксичность, например, цепь CD3 дзэта. Таким образом, в некоторых аспектах, антигенсвязывающая часть связана с одной или более модулями клеточных сигналов. В некоторых вариантах осуществления модули клеточных сигналов включают трансмембранный домен CD3, внутриклеточные сигнальные области CD3 и/или другие трансмембранные области CD. В некоторых вариантах осуществления рецептор, например, CAR, дополнительно включает часть одной или более дополнительных молекул, таких как рецептор Fc γ, CD8, CD4, CD25 или CD16. Например, в некоторых аспектах, CAR или другой химерный рецептор включает химерную молекулу между CD3-дзэта (CD3-ζ) или рецептором Fc γ и CD8, CD4, CD25 или CD16.
[0552] В некоторых вариантах осуществления после лигирования CAR или другого химерного рецептора, цитоплазматический домен или внутриклеточный сигнальный домен рецептора активирует по меньшей мере одну из нормальных эффекторных функций или ответов иммунной клетки, например, Т-клеток, модифицированных так, чтобы экспрессировать CAR. Например, в некоторых контекстах, CAR индуцирует функцию Т-клетки, такую как цитолитическая активность или T-хелперная активность, такая как секреция цитокинов или других факторов. В некоторых вариантах осуществления обрезанная часть внутриклеточного сигнального домена компонента антигенного рецептора или костимулирующей молекулы используется вместо интактной иммуностимулирующей цепи, например, если она трансдуцирует сигнал эффекторной функции. В некоторых вариантах осуществления внутриклеточный сигнальный домен или домены включают цитоплазматические последовательности T-клеточного рецептора (TCR), и в некоторых аспектах также те из корецепторов, в естественном контексте действующих совместно с такими рецепторами для инициации трансдукции сигналов после задействования антигенного рецептора.
[0553] В контексте естественного TCR полная активация обычно требует не только трансдукции сигналов через TCR, но также и костимулирующего сигнала. Таким образом, в некоторых вариантах осуществления, для промотирования полной активации компонент для генерации вторичного или костимулирующего сигнала также включен в CAR. В других вариантах осуществления CAR не включает компонент для генерации костимулирующего сигнала. В некоторых аспектах дополнительный CAR экспрессируется в той же клетке и обеспечивает компонент для генерации вторичного или костимулирующего сигнала.
[0554] В некоторых вариантах осуществления химерный антигенный рецептор содержит внутриклеточный домен костимулирующей молекулы Т-клетки. В некоторых вариантах осуществления CAR включает сигнальный домен и/или трансмембранную часть костимулирующего рецептора, такого как CD28, 4-1BB, OX40, DAP10 и ICOS. В некоторых аспектах тот же CAR включает как активирующие, так и костимулирующие компоненты. В некоторых вариантах осуществления химерный антигенный рецептор содержит внутриклеточный домен, полученный из костимулирующей молекулы Т-клетки, или его функциональный вариант, такой как между трансмембранным доменом и внутриклеточным сигнальным доменом. В некоторых аспектах костимулирующая молекула Т-клеток представляет собой CD28 или 41BB.
[0555] В некоторых вариантах осуществления активирующий домен включен в один CAR, тогда как костимулирующий компонент обеспечивается другим CAR, распознающим другой антиген. В некоторых вариантах осуществления CAR включает активирующий или стимулирующий CAR, костимулирующий CAR, которые оба экспрессируются на той же клетке (см. WO2014/055668). В некоторых аспектах клетки включают один или более стимулирующих или активирующих CAR и/или костимулирующих CAR. В некоторых вариантах осуществления клетки дополнительно включают ингибирующие CAR (iCAR, см. Fedorov et al., Sci. Transl. Medicine, 5(215) (December, 2013), такой как CAR, распознающий антиген, отличный от ассоциированного с и/или специфического для заболевания или состояния, посредством чего активирующий сигнал, доставляемый через нацеливающийся на заболевание CAR, уменьшается или ингибируется путем связывания ингибирующего CAR с его лигандом, например, для ослабления нецелевых эффектов.
[0556] В некоторых вариантах осуществления внутриклеточный сигнальный домен включает трансмембранный и сигнальный домен CD28, связанный с внутриклеточным доменом CD3 (например, CD3-дзэта). В некоторых вариантах осуществления внутриклеточный сигнальный домен включает химерные костимулирующие домены CD28 и CD137 (4-1BB, TNFRSF9), связанные с внутриклеточным доменом CD3 дзэта.
[0557] В некоторых вариантах осуществления CAR охватывает один или более, например, два или более, костимулирующих домена и активирующий домен, например, первичный активирующий домен, в цитоплазматической части. Примеры CAR включают внутриклеточные компоненты CD3-дзэта, CD28 и 4-1BB.
[0558] В некоторых вариантах осуществления антигенный рецептор дополнительно включает маркер и/или клетки, экспрессирующие CAR, или другой антигенный рецептор дополнительно включают суррогатный маркер, такой как маркер поверхности клеток, который может использоваться для подтверждения трансдукции или инжиниринга клетки для экспрессии рецептора. В некоторых аспектах маркер включает все или часть (например, усеченную форму) CD34, NGFR или рецептора эпидермального фактора роста, такого как усеченная версия такого рецептора поверхности клеток (например, tEGFR). В некоторых вариантах осуществления нуклеиновая кислота, кодирующая маркер, функционально связана с полинуклеотидом, кодирующим последовательность линкера, такую как расщепяемая последовательность линкера, например, T2A. Например, маркер и необязательно последовательность линкера могут быть любыми, как раскрыто в опубликованной заявке на патент No. WO2014031687. Например, маркер может быть усеченным EGFR (tEGFR) т.е., необязательно связанным с последовательностью линкера, такой как расщепляемая последовательность линкера T2A.
[0559] Пример полипептида для усеченного EGFR (например, tEGFR) включает аминокислотную последовательность, представленную в SEQ ID NO: 7 или 16, или аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 7 или 16. Пример последовательность линкера T2A включает аминокислотную последовательность, представленную в SEQ ID NO: 6 или 17, или аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 6 или 17.
[0560] В некоторых вариантах осуществления маркер является молекулой, например, белком поверхности клеток, не встречающейся в природе на Т-клетких или не встречающейся в природе на поверхности Т-клеток, или ее частью. В некоторых вариантах осуществления молекула является чужеродной молекулой, например, чужеродным белком, т.е., не распознаваемой как «собственная» иммунной системой хозяина, в которого клетки будут адоптивно переноситься.
[0561] В некоторых вариантах осуществления маркер не служит никакой терапевтической функции и/или не оказывает влияния кроме использования в качестве маркера для генной инженерии, например, для отбора клеток, успешно модифицированных генно-инженерным путем. В других вариантах осуществления маркер может быть терапевтической молекулой или молекулой, иным образом проявляющей некоторый желаемый эффект, такой как лиганд для клетки, с которой будет иметь место взаимодействие in vivo, такой как костимулирующая или иммунная молекула контрольной точки, чтобы усилить и/или ослабить ответ клеток после адоптивного переноса и взаимодействия с лигандом.
[0562] В некоторых случаях CAR упоминается как первое, второе и/или третье поколение CAR. В некоторых аспектах первое поколение CAR является тем, которое исключительно обеспечивает индуцируемый CD3-цепью сигнал после связывания антигена; в некоторых аспектах второе поколение CAR является тем, которое обеспечивает такой сигнал и костимулирующий сигнал, такой как включающий внутриклеточный сигнальный домен от костимулирующего рецептора, такого как CD28 или CD137; в некоторых аспектах третье поколение CAR является тем, которое включает множество костимулирующих доменов различных костимулирующих рецепторов.
[0563] Например, в некоторых вариантах осуществления CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранную часть CD28 или ее функциональный вариант, и внутриклеточный сигнальный домен, содержащей сигнальную часть CD28 или ее функциональный вариант и сигнальную часть CD3 дзэта или ее функциональный вариант. В некоторых вариантах осуществления CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранную часть CD28 или ее функциональный вариант, и внутриклеточный сигнальный домен, содержащей сигнальную часть 4-1BB или ее функциональный вариант, и сигнальную часть CD3 дзэта или ее функциональный вариант. В некоторых таких вариантах осуществления рецептор дополнительно включает спейсер, содержащий часть молекулы Ig, такой как человеческая молекула Ig, такая как шарнир Ig, например, шарнир IgG4, такой как спейсер только для шарнирной области.
[0564] В некоторых вариантах осуществления трансмембранный домен рекомбинантного рецептора, например, CAR, представляет собой или включает трансмембранный домен человеческого CD28 (например, No. доступа P01747,1) или его вариант, такой как трансмембранный домен, включающий аминокислотную последовательность, представленную в SEQ ID NO: 8, или аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 8; в некоторых вариантах осуществления трансмембранный домен, содержащий часть рекомбинантного рецептора, включает аминокислотную последовательность, представленную в SEQ ID NO: 9, или аминокислотную последовательность, имеющую по меньшей мере или приблизительно 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней.
[0565] В некоторых вариантах осуществления внутриклеточный сигнальный компонент(ы) рекомбинантного рецептора, например, CAR, содержит внутриклеточный костимулирующий сигнальный домен человеческого CD28 или его функциональный вариант или часть, такой как домен с заменой LL на GG в положениях 186-187 нативного белка CD28. Например, внутриклеточный сигнальный домен может включать аминокислотную последовательность, представленную в SEQ ID NO: 10 или 11, или аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 10 или 11. В некоторых вариантах осуществления внутриклеточный домен включает внутриклеточный костимулирующий сигнальный домен 4-1BB (например, (No. Доступа Q07011,1) или его функциональный вариант или часть, такой как аминокислотная последовательность, представленная в SEQ ID NO: 12, или аминокислотная последовательность, показывающая по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 12.
[0566] В некоторых вариантах осуществления внутриклеточный сигнальный домен рекомбинантного рецептора, например, CAR, включает стимулирующий сигнальный домен человеческого CD3 дзэта или его функциональный вариант, такой как цитоплазматический домен 112 AA изоформы 3 человеческого CD3ζ (номер доступа: P20963,2) или сигнальный домен CD3 дзэта, как описано в Патенте США: 7,446,190 или Патенте США No. 8,911,993. Например, в некоторых вариантах осуществления, внутриклеточный сигнальный домен включает аминокислотную последовательность, как указано в SEQ ID NO: 13, 14 или 15, или аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 13, 14 или 15.
[0567] В некоторых аспектах спейсер содержит только шарнирную область IgG, такую как только шарнир IgG4 или IgG1, такую как спейсер только для шарнирной области, представленный в SEQ ID NO: 1. В других вариантах осуществления спейсер представляет собой или содержит шарнир Ig, например, IgG4-производный шарнир, необязательно связанный с доменами CH2 и/или CH3. В некоторых вариантах осуществления спейсер является шарниром Ig, например, шарниром IgG4, связанным с доменами CH2 и CH3, таким как представленный в SEQ ID NO: 4. В некоторых вариантах осуществления спейсер является шарниром Ig, например, шарниром IgG4, связанным только с доменом CH3, таким как представленный в SEQ ID NO: 3. В некоторых вариантах осуществления спейсер представляет собой или включает последовательность, богатую глицином-серином, или другой гибкий линкер, такой как известные гибкие линкери.
[0568] Например, в некоторых вариантах осуществления, CAR включает антитело, такое как фрагмент антитела, включая scFvs, спейсер, такой как спейсер, содержащий часть молекулы иммуноглобулина, такую как шарнирная область и/или одна или более константных областей молекулы тяжелой цепи, такая как содержащий Ig-шарнир спейсер, трансмембранный домен, содержащий все или часть CD28-производного трансмембранного домена, CD28-производной внутриклеточный сигнальный домен и CD3 дзэта сигнальный домен. В некоторых вариантах осуществления CAR включает антитело или фрагмент, такой как scFv, спейсер, такой как любой из содержащих Ig-шарнир спейсеров, CD28-производный трансмембранный домен, полученный из 4-1BB внутриклеточный сигнальный домен и полученный из CD3 дзэта сигнальный домен.
[0569] В некоторых вариантах осуществления молекулы нуклеиновой кислоты, кодирующие такие конструкции CAR, дополнительно включают последовательность, кодирующую рибосомный элемент пропуска T2A, и/или последовательность tEGFR, например, даунстрим часть последовательности, кодирующей CAR. В некоторых вариантах осуществления последовательность кодирует рибосомный элемент пропуска T2A, представленный в SEQ ID NO: 6 или 17, или аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 6 или 17. В некоторых вариантах осуществления Т-клетки, экспрессирующие антигенный рецептор (например, CAR), могут также быть сгенерированы для экспрессии усеченного EGFR (EGFRt) как неиммуногенный эпитоп выбора (например, введением конструкции, кодирующей CAR и EGFRt, отделенные рибосомным переключателем T2A, для экспрессии двух белков из одной и той же конструкции), который затем может использоваться в качестве маркера для детекции таких клеток (см., например, Патент США No. 8,802,374). В некоторых вариантах осуществления последовательность кодирует tEGFR последовательность, представленную в SEQ ID NO: 7 или 16, или аминокислотную последовательность, показывающую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с SEQ ID NO: 7 или 16. В некоторых случаях пептид, такой как T2A, может заставить рибосому пропускать (пропуск в рибосоме) синтез пептидной связи на C-конце 2А элемента, приводя к разделению между концом 2А последовательности и следующим даунстрим пептидом (см., например, de Felipe. Genetic Vaccines and Ther. 2:13 (2004) и deFelipe et al. Traffic 5:616-626 (2004)). Известны много 2А элементов. Примеры 2А последовательностей, которые могут использоваться в способах и нуклеиновых кислотах, раскрытых здесь, включают, без ограничения, 2А последовательности вируса ящура (F2A, например, SEQ ID NO: 21), вируса ринита А лошадей (E2A, например, SEQ ID NO: 20), вируса Thosea asigna (T2A, например, SEQ ID NO: 6 или 17) и тешовируса-1 свиней (P2A, например, SEQ ID NO: 18 или 19), как описано в Публикации Патента США No. 20070116690.
[0570] Рекомбинантные рецепторы, такие как CAR, экспрессируемые клетками, вводимыми пациенту, обычно распознают или специфично связываются с молекулой, экспрессирующейся в, ассоциированной с, и/или специфической для заболевания или состояния, подвергаемого лечению, или его клеток. После специфического связывания с молекулой, например, антигена, рецептор обычно поставляет иммуностимулирующий сигнал, такой как ITAM-трансдуцированный сигнал, в клетку, таким образом промотируя иммунный ответ, нацеленный на заболевание или состояние. Например, в некоторых вариантах осуществления, клетки экспрессируют CAR, специфично связывающийся с антигеном, экспрессируемым клеткой или тканью заболевания или состояния или ассоциированный с заболеванием или состоянием.
B. Т-клеточные рецепторы (TCRs)
[0571] В некоторых вариантах осуществления генно-инженерные клетки, такие как Т-клетки, используемые в связи со способами, применениями, изделиями или композициями по изобретению, являются клетками, экспрессирующими Т-клеточный рецептор (TCR) или его антигенсвязывающую часть, распознающую эпитоп пептида или Т-клеточный эпитоп целевого полипептида, такого как антиген опухоли, вирусный или аутоиммунный белок.
[0572] В некоторых вариантах осуществления “Т-клеточный рецептор” или «TCR» представляет собой молекулу, содержащую вариабельную α и β цепи (также известные как TCRα и TCRβ, соответственно) или вариабельную γ и δ цепи (также известные как TCRα и TCRβ, соответственно), или их антигенсвязывающие части, и которая способна к специфическому связыванию с пептидом, связывающимся с молекулой MHC. В некоторых вариантах осуществления TCR находится в форме αβ. Как правило, TCR, существующими в αβ и формах γδ, являются обычно структурно подобными, но Т-клетки, экспрессирующие их, могут иметь различные анатомические местоположения или функции. TCR может быть найден на поверхности клеток или в растворимой форме. Обычно TCR обнаруживается на поверхности Т-клеток (или Т-лимфоцитов), где он обычно ответственен за распознавание антигенов, связанных с молекулами главного комплекса гистосовместимости (MHC).
[0573] Если не указано иное, термин «TCR» должен пониматься как затрагивающий полные TCR, а также их антигенсвязывающие части или антигенсвязывающие фрагменты. В некоторых вариантах осуществления TCR является интактным или полноразмерным TCR, включая TCR в форме αβ или форме γδ. В некоторых вариантах осуществления TCR является антигенсвязывающей частью, которая меньше полноразмерного TCR, но связывается со специфическим пептидом, связанным в молекуле MHC, например, связывается с комплексом MHC-пептид. В некоторых случаях антигенсвязывающая часть или фрагмент TCR может содержать только часть структурных областей полноразмерного или интактного TCR, но в состоянии связываться с эпитопом пептида, такого как комплекс MHC-пептид, с которым связывается полный TCR. В некоторых случаях антигенсвязывающая часть содержит вариабельные области TCR, такие как вариабельная α цепь и вариабельная β цепь TCR, достаточные для формирования связывающего участка для связывания со специфическим комплексом MHC-пептид. Обычно вариабельные цепи TCR содержат определяющие комплементарность области, участвующие в распознавании пептида, MHC и/или комплекса MHC-пептид.
[0574] В некоторых вариантах осуществления вариабельные области TCR содержат гипервариабельные петли, или определяющие комплементарность области (CDR), которые обычно являются первичными компонентами, способствующими распознаванию антигена и связывающим способностям и специфичности. В некоторых вариантах осуществления CDR TCR или их комбинация формируют весь или по существу весь антигенсвязывающий сайт данной молекулы TCR. Различные CDR в вариабельной области цепи TCR обычно отделяются областями рамки считывания (FR), обычно показывающими меньшую вариабельность среди молекул TCR по сравнению с CDR (см., например, Jores et al., Proc. Nat’l Acad. Sci. U.S.A. 87:9138, 1990; Chothia et al., EMBO J. 7:3745, 1988; see also Lefranc et al., Dev. Comp. Immunol. 27:55, 2003). В некоторых вариантах осуществления CDR3 является главным CDR, ответственным за связывание антигена или специфичность, или является самым важным среди трех CDR на данной вариабельной области TCR для распознавания антигена, и/или для взаимодействия с подвергнутой процессингу частью пептида комплекса пептид-MHC. В некоторых контекстах CDR1 альфа-цепи может взаимодействовать с N-концевой частью некоторых антигенных пептидов. В некоторых контекстах CDR1 бета цепи может взаимодействовать с C-концевой частью пептида. В некоторых контекстах CDR2 способствует наиболее сильно или является основным CDR, ответственным за взаимодействие с или распознавание части MHC комплекса MHC-пептид. В некоторых вариантах осуществления вариабельная область β-цепи может содержать дополнительный гипервариабельный участок (CDR4 или HVR4), который обычно участвует в связывании суперантигена, а не распознавании антигена (Kotb (1995) Clinical Microbiology Reviews, 8:411-426).
[0575] В некоторых вариантах осуществления TCR также может содержать константный домен, трансмембранный домен и/или короткий цитоплазматический хвост (см., например, Janeway et al., Immunobiology: The Immune System in Health and Disease, 3rd Ed., Current Biology Publications, p. 4:33, 1997). В некоторых аспектах каждая цепь TCR может иметь один N-концевой вариабельный домен иммуноглобулина, один константный домен иммуноглобулина, трансмембранную область и короткий цитоплазматический хвост на C-конце. В некоторых вариантах осуществления TCR связан с инвариантными белками комплекса CD3, участвующего в опосредовании трансдукции сигналов.
[0576] В некоторых вариантах осуществления цепь TCR содержит один или более константных доменов. Например, внеклеточная часть данной цепи TCR (например, α-цепи или β-цепи) может содержать два подобных иммуноглобулину домена, такие как вариабельный домен (например, Vα или Vb; обычно аминокислоты 1-116 на основе нумерации по Kabat, Kabat et al., Sequences of Proteins of Immunological Interest, US Dept. Health and Human Services, Public Health Service National Institutes of Health, 1991, 5th ed) и константный домен (например, константный домен α-цепи, или Cα, как правило, положения 117-259 цепи на основе нумерации Kabat или константный домен β-цепи или Cβ, как правило, положения 117-295 цепи на основе Kabat) смежный с клеточной мембраной. Например, в некоторых случаях, внеклеточная часть TCR, сформированного этими двумя цепьми, содержит два мембранно-проксимальных константных домена и два мембранно-дистальных вариабельных домена, причем каждый их вариабельных доменов содержит CDR. Константный домен TCR может содержать короткие соединительные последовательности, в которых остаток цистеина формирует дисульфидную связь, таким образом связывая две цепи TCR. В некоторых вариантах осуществления TCR может иметь дополнительный остаток цистеина в каждой из α и β цепей, так, что TCR содержит две дисульфидных связи в константных доменах.
[0577] В некоторых вариантах осуществления цепи TCR содержат трансмембранный домен. В некоторых вариантах осуществления трансмембранный домен имеет положительный заряд. В некоторых случаях цепь TCR содержит цитоплазматический хвост. В некоторых случаях структура позволяет TCR связываться с другими молекулами, такими как CD3 и его субъединицы. Например, TCR, содержащий константные домены с трансмембранной областью, может фиксировать белок в клеточной мембране и ассоциироваться с инвариантными субъединицами сигнального аппарата или комплекса CD3. Внутриклеточные хвосты сигнальных субъединиц CD3 (например, цепи CD3γ, CD3δ, CD3ε и CD3ζ) содержат один или более иммунорецепторных тирозиновых мотивов активации, или ITAM, участвующих в сигнальной способности комплекса TCR.
[0578] В некоторых вариантах осуществления TCR может быть гетеродимером двух цепей α и β (или необязательно γ и δ), или он может быть TCR одноцепочечной конструкции. В некоторых вариантах осуществления TCR является гетеродимером, содержащим две отдельных цепи (α и β цепи или γ и δ цепи), которые связаны, например, дисульфидной связью или дисульфидными связями.
[0579] В некоторых вариантах осуществления TCR может быть сгенерирован из известной последовательности(ей) TCR, такой как последовательности цепей Vα,β, для которых по существу полноразмерная кодирующая последовательность легко доступна. Способы получения полноразмерных последовательностей TCR, включая последовательности V цепей, из источников клеток известны. В некоторых вариантах осуществления нуклеиновые кислоты, кодирующие TCR, могут быть получены из множества источников, например, амплификацией путем полимеразной цепной реакции (ПЦР) TCR-кодирующих нуклеиновых кислот в или выделенных из данной клетки или клеток, или синтез общедоступных последовательностей ДНК TCR.
[0580] В некоторых вариантах осуществления TCR получают из биологического источника, например, из клеток, например, из Т-клеток (например, цитотоксических Т-клеток), Т-клеточных гибридом или другого общедоступного источника. В некоторых вариантах осуществления Т-клетки могут быть получены из выделенных in vivo клеток. В некоторых вариантах осуществления TCR является тимусно выбранным TCR. В некоторых вариантах осуществления TCR является ограниченным неоэпитопом TCR. В некоторых вариантах осуществления клетками T-может быть культивируемая Т-клеточная гибридома или клон. В некоторых вариантах осуществления TCR или его антигенсвязывающая часть или его антигенсвязывающий фрагмент могут быть искусственно сгенерированы из известной последовательности TCR.
[0581] В некоторых вариантах осуществления TCR генерируют из TCR, идентифицированного или выбранного скринингом библиотеки кандидатов TCR против целевого полипептидного антигена или его целевого Т-клеточного эпитопа. Библиотеки TCR могут быть сгенерированы амплификацией репертуара Vα и Vβ из Т-клеток, выделенных от пациента, включая клетки, присутствующие в PBMC, селезенке или другом лимфоидном органе. В некоторых случаях Т-клетки могут быть амплифицированы их инфильтрирующих опухоли лимфоцитов (TIL). В некоторых вариантах осуществления библиотеки TCR могут быть сгенерированы из CD4+ или CD8+ клеток. В некоторых вариантах осуществления TCR могут быть амплифицированы из источника Т-клеток нормального или здорового пациента, т.е., нормальных библиотек TCR. В некоторых вариантах осуществления TCR могут быть амплифицированы из источника Т-клеток больного пациента, т.е., пациентов библиотек TCR. В некоторых вариантах осуществления вырожденные праймеры используются для амплификации генного репертуара Vα и Vβ, такой как RT-ПЦР в образцах, таких как Т-клетки, полученные от человека. В некоторых вариантах осуществления, scTv библиотеки могут быть собраны из библиотек интактных Vα и Vβ, в которых амплифицированные продукты клонированы или собраны, чтобы быть разделенными линкером. В зависимости от источника пациента и клеток, библиотеки могут быть HLA аллель-специфическими. Также в некоторых вариантах осуществления библиотеки TCR могут быть сгенерированы мутагенезом или диверсификацией родительской или каркасной молекулы TCR. В некоторых аспектах TCR подвергнуты направленному развитию, такому как мутагенез, например, α или β цепи. В некоторых аспектах определенные остатки в CDR TCR изменены. В некоторых вариантах осуществления выбранные TCR могут быть изменены созреванием аффинности. В некоторых вариантах осуществления антиген-специфические Т-клетки могут быть выбраны, например, путем скрининга для оценки активности CTL против пептида. В некоторых аспектах TCR, например, присутствующие на антиген-специфических Т-клетках, могут быть выбраны, например, по активности связывания, например, определенной аффинности или авидности для антигена.
[0582] В некоторых вариантах осуществления TCR или его антигенсвязывающая являются модифицированными или подвергнутыми генной инженерии. В некоторых вариантах осуществления способы направленного развития используются для генерации TCR с измененными свойствами, например, с более высоким аффинностью к специфическому комплексу MHC-пептид. В некоторых вариантах осуществления направленное развитие достигают способами дисплея, включая, но не ограничиваясь ими, дрожжевой дисплей (Holler et al. (2003) Nat Immunol, 4, 55-62; Holler et al. (2000) Proc Natl Acad Sci U S A, 97, 5387-92), фаговый дисплей (Li et al. (2005) Nat Biotechnol, 23, 349-54), или Т-клеточный дисплей (Chervin et al. (2008) J Immunol Methods, 339, 175-84). В некоторых вариантах осуществления подходы дисплея включают разработку, или изменение, известного, родительского или референсного TCR. Например, в некоторых случаях, TCR дикого типа может использоваться в качестве шаблона для производства мутагенизированных TCR, в котором CDR видоизменены по одному или более остаткам, и мутанты с желаемым измененным свойством, таким как более высокая аффинность к желаемому антигену-мишени, выбраны.
[0583] В некоторых вариантах осуществления пептиды целевого полипептида для использования в получении или генерации представляющего интерес TCR известны или могут быть легко идентифицированы. В некоторых вариантах осуществления пептиды, подходящие для использования в генерации TCR или антигенсвязывающие частей, могут быть определены на основе присутствия HLA-ограниченного мотива в целевом полипептиде, таком как целевой полипептид, описанный ниже. В некоторых вариантах осуществления пептиды идентифицируют с помощью доступных компьютерных прогностических моделей. В некоторых вариантах осуществления, для предсказания связывающих участков MHC класса I, такие модели включают, но не ограничены ими, ProPred1 (Singh and Raghava (2001) Bioinformatics 17(12):1236-1237, и SYFPEITHI (see Schuler et al. (2007) Immunoinformatics Methods in Molecular Biology, 409(1): 75-93 2007). В некоторых вариантах осуществления MHC-ограниченный эпитоп представляет собой HLA-A0201, экспрессирующийся приблизительно у 39-46% всех европеоидов и поэтому представляющий собой подходящий выбор антигена MHC для использования в получении TCR или другой MHC-пептид-связывающей молекулы.
[0584] HLA-A0201-связывающие мотивы и сайты расщепления протеасомами и иммунными протеасомами с помощью компьютерных прогностических моделей известны. Для предсказания связывающих участков MHC класса I такие модели включают, но не ограничены ими, ProPred1 (описанный более подробно в Singh and Raghava, ProPred: prediction of HLA-DR binding sites. BIOINFORMATICS 17(12):1236-1237 2001), и SYFPEITHI (see Schuler et al. SYFPEITHI, Database for Searching and T-Cell Epitope Prediction. in Immunoinformatics Methods in Molecular Biology, vol 409(1): 75-93 2007).
[0585] В некоторых вариантах осуществления TCR или его антигенсвязывающая часть могут быть рекомбинантно полученным натуральным белком или его мутантной формой, в которой были изменены одно или более свойств, таких как характеристика связывания. В некоторых вариантах осуществления TCR может быть получен из одного из различных видов животных, такого как человек, мышь, крыса или другое млекопитающее. TCR может быть связанным с клеткой или быть в растворимой форме. В некоторых вариантах осуществления в целях способов по изобретению TCR находится в связанной с клеткой форме, экспрессируещейся на поверхности клетки.
[0586] В некоторых вариантах осуществления TCR является полноразмерным TCR. В некоторых вариантах осуществления TCR является антигенсвязывающей частью. В некоторых вариантах осуществления TCR является димерным TCR (dTCR). В некоторых вариантах осуществления TCR является одноцепочечным TCR (sc-TCR). В некоторых вариантах осуществления dTCR или scTCR имеют структуры, как описано в WO 03/020763, WO 04/033685, WO2011/044186.
[0587] В некоторых вариантах осуществления TCR содержит последовательность, соответствующую трансмембранной последовательности. В некоторых вариантах осуществления TCR действительно содержит последовательность, соответствующую цитоплазматическим последовательностям. В некоторых вариантах осуществления TCR способен к формированию комплекса TCR с CD3. В некоторых вариантах осуществления любой из TCR, включая dTCR или scTCR, может быть связан с сигнальными областями, выдающими активный TCR на поверхности Т-клетки. В некоторых вариантах осуществления TCR экспрессируется на поверхности клеток.
[0588] В некоторых вариантах осуществления dTCR содержит первый полипептид, в котором последовательность, соответствующая последовательности вариабельная области α цепи TCR, слита с N-концом последовательности, соответствующей последовательность константной внеклеточной области α цепи TCR, и второй полипептид, в котором последовательность, соответствующая последовательности вариабельная области β цепи TCR, слита с N-концом последовательности, соответствующей последовательность константной внеклеточной области β цепи TCR, причем первый и второй полипептиды связаны дисульфидной связью. В некоторых вариантах осуществления связь может соответствовать нативной межцепочечной дисульфидной связи, присутствующей в нативных димерных αβ TCR. В некоторых вариантах осуществления межцепочечные дисульфидные связи не присутствуют в нативном TCR. Например, в некоторых вариантах осуществления один или более цистеинов могут быть включены в константную область внеклеточных последовательностей dTCR полипептидной пары. В некоторых случаях как нативная, так и не-нативная дисульфидная связь могут быть желательными. В некоторых вариантах осуществления TCR содержит трансмембранную последовательность для фиксации к мембране.
[0589] В некоторых вариантах осуществления dTCR содержит TCR α цепь, содержащую вариабельную α область, константную α область и первый мотив димеризации, присоединенный к C-концу константной α области, и TCR β цепь, включающую вариабельную β область, константную β область и первый мотив димеризации, присоединенный к C-концу константной β области, причем первый и второй мотивы димеризации легко взаимодействуют для создания ковалентной связи между аминокислотой в первом мотиве димеризации и аминокислотой во втором мотиве димеризации, связывающем вместе TCR α цепь и TCR β цепь.
[0590] В некоторых вариантах осуществления TCR представляет собой scTCR. Как правило, scTCR может быть сгенерирован с помощью известных способов, см., например, Soo Hoo, W. F. et al. PNAS (USA) 89, 4759 (1992); Wülfing, C. and Plückthun, A., J. Mol. Biol. 242, 655 (1994); Kurucz, I. et al. PNAS (USA) 90 3830 (1993); Международные публикации PCT WO 96/13593, WO 96/18105, WO99/60120, WO99/18129, WO 03/020763, WO2011/044186; и Schlueter, C. J. et al. J. Mol. Biol. 256, 859 (1996). В некоторых вариантах осуществления scTCR содержит введенную ненативную дисульфидную межцепочечную связь для облегчения ассоциации цепей TCR (см., например, Публикацию международной заявки PCT WO 03/020763). В некоторых вариантах осуществления scTCR является недисульфидно связанным усеченным TCR, в котором гетерологичные лейциновые молнии, слитые с его C-концами, облегчают ассоциацию цепей (см., например, Публикацию международной заявки PCT No. WO99/60120). В некоторых вариантах осуществления scTCR содержит вариабельную область TCRα, соединенную ковалентной связью с вариабельной областью TCRβ через пептидный линкер (см., например, Публикацию международной заявки PCT No. WO99/18129).
[0591] В некоторых вариантах осуществления scTCR содержит первый сегмент, составленный аминокислотной последовательностью, соответствующей вариабельной области α цепи TCR, второй сегмент, составленный аминокислотной последовательностью, соответствующей последовательности вариабельной области β цепи TCR, слитый с N-концом аминокислотной последовательности, соответствующей последовательности внеклеточного константного домена β цепи TCR, и линкерную последовательность, связывающую C-конец первого сегмента с N-концом второго сегмента.
[0592] В некоторых вариантах осуществления scTCR содержит первый сегмент, составленный последовательностью вариабельной области α цепи, слитой с N-концом последовательности внеклеточного константного домена α цепи, и второй сегмент, составленный последовательностью вариабельной области β цепи, слитой с N-концом последовательности внеклеточного константного домена β цепи, и трансмембранную последовательность, и, необязательно, последовательность линкера, связывающую C-конец первого сегмента с N-концом второго сегмента.
[0593] В некоторых вариантах осуществления scTCR содержит первый сегмент, составленный последовательностью вариабельной области β цепи TCR, слитой с N-концом последовательности внеклеточного константного домена β цепи, и второй сегмент, составленный вариабельной последовательностью области α цепи, слитой с N-концом последовательности внеклеточного конктантного домена α цепи, и трансмембранную последовательность, и, необязательно, последовательность линкера, связывающую C-конец первого сегмента с N-концом второго сегмента.
[0594] В некоторых вариантах осуществления линкер scTCR, связывающий первый и второй сегменты TCR, может быть любым линкером, способным образовывать одинарную полипептидную цепь при сохранении TCR связывающей специфичности. В некоторых вариантах осуществления последовательность линкера может, например, иметь формулу -P-AA-P-, в которой P обозначает пролин, и AA обозначает аминокислотную последовательность, в которой аминокислоты являются глицином и серином. В некоторых вариантах осуществления первые и вторые сегменты соединены так, чтобы последовательности вариабельных областей ориентировались для такого связывания. Следовательно, в некоторых случаях, линкер имеет достаточную длину для охвата расстояния между C-концом первого сегмента и N-концом второго сегмента, или наоборот, но не является слишком длинным для блокирования или уменьшения связывания scTCR с целевым лигандом. В некоторых вариантах осуществления линкер может содержать от или от приблизительно 10 до 45 аминокислот, например, от 10 до 30 аминокислот или от 26 до 41 аминокислотных остатков, например, 29, 30, 31 или 32 аминокислот. В некоторых вариантах осуществления линкера имеет формулу -PGGG-(SGGGG)5-P-, в которой P обозначает пролин, G обозначает глицин, и S обозначает серин (SEQ ID NO:28). В некоторых вариантах осуществления линкера имеет последовательность GSADDAKKDAAKKDGKS (SEQ ID NO:29)
[0595] В некоторых вариантах осуществления scTCR содержит ковалентную дисульфидную связь, связывающую остаток области иммуноглобулина константного домена α цепи с остатком области иммуноглобулина константного домена β цепи. В некоторых вариантах осуществления межцепочечная дисульфидная связь в нативном TCR не присутствует. Например, в некоторых вариантах осуществления, один или более цистеинов могут быть включены в последовательности внеклеточной константной области первого и второго сегментов scTCR полипептида. В некоторых случаях как нативная, так и ненативная дисульфидная связь могут быть желательными.
[0596] В некоторых вариантах осуществления dTCR или scTCR, содержащие введенные межцепочечные дисульфидные связи, нативные дисульфидные связи не присутствуют. В некоторых вариантах осуществления один или более нативных цистеинов, формирующих нативные межцепочечные дисульфидные связи, заменены на другой остаток, такой как серин или аланин. В некоторых вариантах осуществления введенная дисульфидная связь может быть сформирована путем замены нецистеиновых остатков на первом и втором сегментах на цистеин. Примеры ненативных дисульфидных связей TCR описаны в Публикации международной заявки PCT No. WO2006/000830.
[0597] В некоторых вариантах осуществления TCR или его антигенсвязывающий фрагмент показывает аффинность с равновесной константой связывания для антигена-мишени, составляющей от или от приблизительно 10-5 до 10-12 М и все отдельные значения и диапазоны в этом интервале. В некоторых вариантах осуществления антиген-мишень является комплексом MHC-пептид или лигандом.
[0598] В некоторых вариантах осуществления нуклеиновая кислота или нуклеиновые кислоты, кодирующие TCR, такой как α и β цепи, могут быть амплифицированы ПЦР, клонированием или другими подходящими средствами и клонированы в подходящий вектор или векторы экспрессии. Вектор экспрессии может быть любым подходящим рекомбинантным вектором экспрессии и может использоваться, чтобы трансформировать или трансфицировать любого подходящего хозяина. Подходящие векторы включают разработанные для размножения и роста или для экспрессии, или для обеих целей, такие как плазмиды и вирусы.
[0599] В некоторых вариантах осуществления вектор может представлять собой вектор ряда pUC (Fermentas Life Sciences), ряда pBluescript (Stratagene, LaJolla, Калифорния), ряда pET (Novagen, Мадисон, Висконсин), ряда pGEX (Pharmacia Biotech, Упсала, Швеция) или ряда pEX (Clontech, Пало-Альто, Калифорния). В некоторых случаях также могут использоваться векторы на основе бактериофага, такие как λG10, λGT11, λZapII (Stratagene), λEMBL4,и λNM1149. В некоторых вариантах осуществления векторы экспрессии для растений могут использоваться и включают pBI01, pBI101,2, pBI101,3, pBI121 и pBIN19 (Clontech). В некоторых вариантах осуществления векторы экспрессии для животных включают pEUK-Cl, pMAM и pMAMneo (Clontech). В некоторых вариантах осуществления используется вирусный вектор, такой как ретровирусный вектор.
[0600] В некоторых вариантах осуществления рекомбинантные векторы экспрессии могут быть получены с помощью стандартных методов рекомбинантных ДНК. В некоторых вариантах осуществления векторы могут содержать регуляторные последовательности, такие как инициаторы транскрипции и трансляции и кодоны завершения, которые являются специфическими для типа хозяина (например, бактерии, гриба, растения или животного), в который вектор должен быть введен, в зависимости от ситуации и с учетом того, является ли вектор ДНК- или РНК-вектором. В некоторых вариантах осуществления вектор может содержать ненативный промотор, функционально связанный с нуклеотидной последовательностью, кодирующей TCR или антигенсвязывающую часть (или другую MHC-пептид-связывающую молекулу). В некоторых вариантах осуществления промотор может быть невирусным промотором или вирусным промотором, таким как промотор цитомегаловируса (CMV), промотор SV40, промотор RSV и промотор, найденный в длинном концевом повторе вируса стволовых клеток мышей. Другие известные промоторы также рассматриваются.
[0601] В некоторых вариантах осуществления для генерации вектора, кодирующего TCR, α и β цепи амплифицируют с помощью ПЦР из общей кДНК, выделенной из клона Т-клеток, экспрессирующего представляющий интерес TCR, и клонируют в вектор экспрессии. В некоторых вариантах осуществления α и β цепи клонируют в один и тот же вектор. В некоторых вариантах осуществления α и β цепи клонируют в разные векторы. В некоторых вариантах осуществления сгенерированные α и β цепи включают в ретровирусный, например, лентивирусный, вектор.
Генно-инженерные клетки и способы получения клеток
[0602] В некоторых вариантах осуществления способы по изобретению включают введение пациенту, имеющему заболевание или состояние, клеток, экспрессирующих рекомбинантный антигенный рецептор. Различные способы введения генно-инженерных компонентов, например, рекомбинантных рецепторов, например, CAR или TCR, известны и могут использоваться со способами и композициями по изобретению. Примеры способы включают таковые для переноса нуклеиновых кислот, кодирующих рецепторы, включая перенос путем вирусной, например, ретровирусной или лентивирусной, трансдукции, транспозонов и электропорации.
[0603] Среди клеток, экспрессирующих рецепторы и вводимых способами по изобретению, можно назвать генно-инженерные клетки. Генная инженерия обычно включает введение нуклеиновой кислоты, кодирующей рекомбинантный или генно-инженерный компонент, в композицию, содержащую клетки, например, ретровирусной трансдукцией, трансфекцией или трансформацией.
C. Химерные рецепторы аутоантитела (CAARs)
[0604] В некоторых вариантах осуществления, среди рекомбинантных рецепторов, экспрессируемых генно-инженерными клетками, используемыми в связи со способами, применениями, изделиями и композициями по изобретению, можно назвать химерный рецептор аутоантитела (CAAR). В некоторых вариантах осуществления CAAR является специфическим для аутоантитела. В некоторых вариантах осуществления клетка, экспрессирующая CAAR, такая как Т-клетка, модифицированная генно-инженерным методом для экспрессии CAAR, может использоваться, чтобы специфично связываться с и уничтожать экспрессирующие аутоантитело клетки, но не экспрессирующее нормальное антитело клетки. В некоторых вариантах осуществления CAAR-экспрессирующие клетки могут использоваться для лечения аутоиммунного заболевания, связанного с экспрессией аутоантигенов, такого как аутоиммунные заболевания. В некоторых вариантах осуществления CAAR-экспрессирующие клетки могут нацеливаться на В-клетки, в конечном счете продуцирующие аутоантитела и показывающие аутоантитела на их поверхности клеток, метить эти В-клетки как специфические для заболевания мишени для терапевтического вмешательства. В некоторых вариантах осуществления CAAR-экспрессирующие клетки могут быть использованы для эффективного нацеливания и уничтожения патогенных В-клеток при аутоиммунных заболеваниях путем нацеливания на вызывающие заболевания В-клетки с помощью антиген-специфического химерного рецептора аутоантитела. В некоторых вариантах осуществления рекомбинантный рецептор представляет собой CAAR, такой как любой описанный в публикации заявки на патент США US 2017/0051035.
[0605] В некоторых вариантах осуществления CAAR включает связывающий аутоантитело домен, трансмембранный домен и внутриклеточный сигнальный домен. В некоторых вариантах осуществления внутриклеточная сигнальная область включает внутриклеточный сигнальный домен. В некоторых вариантах осуществления внутриклеточный сигнальный домен представляет собой или включает первичный сигнальный домен, сигнальный домен, который способен индуцировать сигнал первичной активации в Т-клетке, сигнальный домен компонента T-клеточного рецептора (TCR) и/или сигнальный домен, включающий иммунорецепторный тирозиновый активирующий мотив (ITAM). В некоторых вариантах осуществления внутриклеточный сигнальный домен включает вторичный или костимулирующий сигнальный домен (вторичные внутриклеточные сигнальные области).
[0606] В некоторых вариантах осуществления связывающий аутоантитело домен включает аутоантиген или его фрагмент. Выбор аутоантигена может зависеть от типа нацеливаемого аутоантитела. Например, аутоантиген может быть выбран, потому что он распознает аутоантитело на клетке-мишени, такой как В-клетка, ассоциированное с определенным болезненным состоянием, например, аутоиммунным заболеванием, таким как опосредуемое аутоантителом аутоиммунное заболевание. В некоторых вариантах осуществления аутоиммунное заболевание включает обыкновенную пузырчатку (PV). Примеры аутоантигенов включают десмоглеин 1 (Dsg1) и Dsg3.
D. Мультинацеливание
[0607] В некоторых вариантах осуществления клетки, используемые в связи со способами, применениями, изделиями и композициями по изобретению, включают стратегии мультинацеливания с использованием клеток, таких как экспрессия двух или более генно-инженерных рецепторов на клетке, каждый из которых распознает один и тот же или разные антигены и как правило каждый включает разные внутриклеточные сигнальные компоненты. Такие стратегии мультинацеливания описаны, например, в Публикации Международной Заявки на патент: WO 2014055668 A1 (в которой описана комбинация активирующего и костимулирующего CAR, например, нацеливаемого на двух разчных антигена, индивидуально присутствующих на не являющихся мишенью, например, нормальных клетках, но присутствующих вместе только на клетках заболевания или состояния, которое будет подвергнуто лечению) и Fedorov et al., Sci. Transl. Medicine, 5(215) (2013) (описывающем клетки, экспрессирующие активирующий и ингибирующий CAR, такие как те, в которых активирующий CAR связывается с одним антигеном, экспрессируемым как на нормальных, или не имеющих отношение к заболеванию, клетках и на клетках заболевания или состояния, которое будет подвергнуто лечению, и ингибирующий CAR связывается с другим антигеном, экспрессируемым только на нормальных клетках или клетках, которые не являются желаемыми для лечения).
[0608] Например, в некоторых вариантах осуществления, клетки включают рецептор, экспрессирующий первый генно-инженерные антигенный рецептор (например, CAR или TCR), который способен индуцировать активирующий или стимулирующий сигнал в клетке, обычно после специфического связывания с антигеном, распознаваемым первым рецептором, например, первым антигеном. В некоторых вариантах осуществления клетка дополнительно включает второй генно-инженерные антигенный рецептор (например, CAR или TCR), например, химерный костимулирующий рецептор, который способен индуцировать костимулирующий сигнал в иммунной клетке, обычно после специфического связывания со вторым антигеном, распознаваемым вторым рецептором. В некоторых вариантах осуществления первый антиген и второй антиген являются одним и тем же. В некоторых вариантах осуществления первый антиген и второй антиген различаются.
[0609] В некоторых вариантах осуществления первый и/или второй генно-инженерный антигенный рецептор (например, CAR или TCR) способен индуцировать активирующий сигнал в клетке. В некоторых вариантах осуществления рецептор включает внутриклеточный сигнальный компонент, содержащий ITAM или ITAM-подобные мотивы. В некоторых вариантах осуществления активация, индуцированная первым рецептором, включает сигнальную трансдукцию или изменение экспрессии белка в клетке, приводящей к инициации иммунной ответа, такого как фосфорилирование ITAM и/или инициация ITAM-опосредованного каскада трансдукции сигналов, формирование иммунологического синапса и/или группировка молекул около связанного рецептора (например, CD4 или CD8 и т.д.), активация одного или более транскрипционных факторов, таких как NF-κB и/или AP-1 и/или индукция экспрессии гена факторов, таких как цитокины, пролиферация и/или выживаемость.
[0610] В некоторых вариантах осуществления первый и/или второй рецептор включает внутриклеточные сигнальные домены или области костимулирующих рецепторов, таких как CD28, (4-1BB) CD137, OX40 и/или ICOS. В некоторых вариантах осуществления первый и второй рецептор включает внутриклеточный сигнальный домен костимулирующего рецептора, которые отличаются. В одном варианте осуществления первый рецептор содержит костимулирующий сигнальный домен CD28, и второй рецептор содержит 4-1BB костимулирующий сигнальный домен, или наоборот.
[0611] В некоторых вариантах осуществления первый и/или второй рецептор включает как внутриклеточный сигнальный домен, содержащий ITAM или ITAM-подобные мотивы, так и внутриклеточный сигнальный домен костимулирующего рецептора.
[0612] В некоторых вариантах осуществления первый рецептор содержит внутриклеточный сигнальный домен, содержащий ITAM или ITAM-подобные мотивы, и второй рецептор содержит внутриклеточный сигнальный домен костимулирующего рецептора. Костимулирующий сигнал в сочетании с сигналом активации, индуцированным в той же клетке, является сигналом, который приводит к иммунному ответу, такому как сильный и длительный иммунный ответ, такой как увеличенная экспрессия гена, секреция цитокинов и других факторов и опосредуемые Т-клетками эффекторные функции, такие как уничтожение клеток.
[0613] В некоторых вариантах осуществления ни лигирование одного только первого рецептора, ни лигирование одного только второго рецептора не вызывают сильный иммунный ответ. В некоторых аспектах, если только один рецептор лигирован, клетка становится толерантной или устойчивой к антигену, или ингибированной, и/или не индуцируется к пролиферации или секреции факторов, или осуществлению эффекторных функций. В некоторых таких вариантах осуществления, однако, когда множество рецепторов лигированы, например, после взаимодействия с клеткой, экспрессирующей первый и второй антигены, достигается желаемый ответ, такой как полная иммунная активация или стимуляция, например, на которую указывает секреция одного или более цитокинов, пролиферация, персистирование и/или выполнение иммунной эффекторной функции, такой как цитотоксическое уничтожение клеток-мишеней.
[0614] В некоторых вариантах осуществления эти два рецептора индуцируют, соответственно, активирующий и ингибирующий сигнал к клетке, такой, что связывание одного из рецепторов с его антигеном активирует клетку или индуцирует ответ, но связывание второго ингибирующего рецептора с его антигеном индуцирует сигнал, подавляющий или демпфирующий этот ответ. Примерами являются комбинации активирующих CAR и ингибирующих CAR или iCAR. Такая стратегия может использоваться, например, в котором активирующий CAR связывается с антигеном, экспрессируемым при заболевании или состоянии, но который также экспрессируется в нормальных клетках, и ингибирующий рецептор связывается с отдельным антигеном, экспрессирующимся на нормальных клетках, но не на клетках заболевания или состояния.
[0615] В некоторых вариантах осуществления стратегия мультинацеливания используется в случае, где антиген, ассоциируемый с определенным заболеванием или состоянием, экспрессируется на небольной клетке и/или экспрессируется на самой генно-инженерной клетке, временно (например, после стимуляции в ассоциации с генной инженерией) или постоянно. В таких случаях, путем требования лигирования двух отдельных и индивидуально специфических рецепторов антигена, могут быть улучшены специфичность, селективность и/или эффективность.
[0616] В некоторых вариантах осуществления множество антигенов, например, первых и вторых антигенов, экспрессируется на клетке, ткани или при целевом заболевании или состоянии, например, на раковой клетке. В некоторых аспектах клетка, ткань, заболевание или состояние представляет собой множественную миелому или клетку множественной миеломы. В некоторых вариантах осуществления, один или более из множества антигенов обычно также экспрессируется на клетке, для которой нацеливание клеточной терапией не желательно, такой как нормальная или небольная клетка или ткань и/или сами генно-инженерные клетки. В таких вариантах осуществления, благодаря необходимости лигирования множественных рецепторов для достижения клеточного ответа, достигается специфичность и/или эффективность.
E. Векторы и способы для генной инженерии
[0617] В некоторых вариантах осуществления генно-инженерные клетки, такие как Т-клетки, используемые в связи со способами, применениями, изделиями или композициями по изобретению, являются клетками, которые были генетически модифицированы для экспрессии рекомбинантного рецептора, например, CAR или TCR, описанного здесь. В некоторых вариантах осуществления клетки модифицируют введением, доставкой или переносом последовательностей нуклеиновой кислоты, кодирующих рекомбинантный рецептор и/или другие молекулы.
[0618] В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты переносят в клетки с помощью рекомбинантных инфекционных вирусных частиц, таких как, например, векторы, полученные из вируса обезьян 40 (SV40), аденовирусов, аденоассоциированного вируса (AAV). В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты переносят в Т-клетки с помощью рекомбинантных лентивирусных векторов или ретровирусных векторов, таких как гамма-ретровирусные векторы (см., например, Koste et al. (2014) Gene Therapy 2014 Apr 3. doi: 10,1038/gt,2014,25; Carlens et al. (2000) Exp Hematol 28(10): 1137-46; Alonso-Camino et al. (2013) Mol Ther Nucl Acids 2, e93; Park et al., Trends Biotechnol. 2011 November 29(11): 550-557).
[0619] В некоторых вариантах осуществления ретровирусный вектор имеет последовательность длинного концевого повтора (LTR), например, ретровирусный вектор, полученный из вируса лейкоза мышей Moloney (MoMLV), вируса миелопролиферативной саркомы (MPSV), вируса эмбриональных стволовых клеток мышей (MESV), вируса стволовых клеток мышей (MSCV), вируса некроза селезенки (SFFV) или аденоассоциированного вируса (AAV). Большинство ретровирусных векторов получают из мышиных ретровирусов. В некоторых вариантах осуществления ретровирусы включают полученных из любого источника клеток птиц или млекопитающих. Ретровирусы, как правило, являются амфотропными, что означает, что они способны инфицировать клетки-хозяева нескольких видов, включая человека. В одном варианте осуществления ген, который будет экспрессироваться, заменяет ретровирусный последовательности gag, pol и/или env ретровируса. Множество иллюстративных ретровирусных систем были описаны (например, патенты США 5,219,740; 6,207,453; 5,219,740; Miller and Rosman (1989) BioTechniques 7:980-990; Miller, A. D. (1990) Human Gene Therapy 1:5-14; Scarpa et al. (1991) Virology 180:849-852; Burns et al. (1993) Proc. Natl. Acad. Sci. USA 90:8033-8037; and Boris-Lawrie and Temin (1993) Cur. Opin. Genet. Develop. 3:102-109).
[0620] Способы лентивирусной трансдукции являеются известными. Примеры способов описаны в, например, Wang et al. (2012) J. Immunother. 35(9): 689-701; Cooper et al. (2003) Blood. 101:1637-1644; Verhoeyen et al. (2009) Methods Mol Biol. 506: 97-114; and Cavalieri et al. (2003) Blood. 102(2): 497-505.
[0621] В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты переносят в Т-клетки электропорацией (см., например, Chicaybam et al, (2013) PLoS ONE 8(3): e60298 and Van Tedeloo et al. (2000) Gene Therapy 7(16): 1431-1437). В некоторых вариантах осуществления рекомбинантные нуклеиновые кислоты переносят в Т-клетки транспозицией (см., например, Manuri et al. (2010) Hum Gene Ther 21(4): 427-437; Sharma et al. (2013) Molec Ther Nucl Acids 2, e74; and Huang et al. (2009) Methods Mol Biol 506: 115-126). Другие способы введения и экспрессии генетического материала в иммунных клетках включают трансфекцию фосфатом кальция (например, как описано в Current Protocols in Molecular Biology, John Wiley & Sons, Нью-Йорк. Нью-Йорк), слияние протопластов, катионную опосредуемую липосомами трансфекцию; облегченную частицами вольфрама бомбардировку микрочастиц (Johnston, Nature, 346: 776-777 (1990)); и соосаждение ДНК фосфатом стронция (Brash et al., Mol. Cell Biol., 7: 2031-2034 (1987)).
[0622] Другие подходы и векторы для переноса нуклеиновых кислот, кодирующих рекомбинантные продукты, описаны, например, в Публикации международной заявки на патент: WO2014055668 и Патенте США No. 7,446,190.
[0623] В некоторых вариантах осуществления клетки, например, Т-клетки, могут быть трансфицированы либо во время, либо после роста, например, Т-клеточным рецептором (TCR) или химерным антигенным рецептором (CAR). Эта трансфекция для введения гена желаемого рецептора может быть осуществлена, например, с любым подходящим ретровирусным вектором. Популяция генетически модифицированных клеток может затем освобождаться от начального стимула (анти-CD3/анти-CD28 стимула, например) и затем стимулироваться вторым типом стимула, например, через de novo введенный рецептор). Этот второй тип стимула может включать антигенный стимул в форме пептид/MHC молекула, когнатного (перекрестное сшивание) лиганда генетически введенного рецептора (например, естественного лиганда CAR) или любого лиганда (такого как антитело), который непосредственно связывается в рамках нового рецептора (например, путем распознавания константных областей в рецепторе). См., например, Cheadle et al, “Chimeric antigen receptors for T-cell based therapy” Methods Mol Biol. 2012; 907:645-66 или Barrett et al., Chimeric Antigen Receptor Therapy for Cancer Annual Review of Medicine Vol. 65: 333-347 (2014).
[0624] В некоторых случаях может использоваться вектор, который не требует, чтобы клетки, например, Т-клетки, были активированы. В некоторых таких случаях клетки могут быть выбраны и/или трансдуцированы до активации. Таким образом, клетки могут быть модифицированы до или после культивирования клеток, и в некоторых случаях в то же время, что и или во время по меньшей мере части культивирования.
[0625] Среди дополнительных нуклеиновых кислот, например, гены для введения являются такими, которые улучшают эффективность терапии, например, путем промотирования жизнеспособности и/или функции перенесенных клеток; гены для обеспечения генетического маркера для выбора и/или оценки клеток, например, для оценки in vivo выживания или локализации; гены для повышения уровня безопасности, например, делая клетки способными к отрицательному отбору in vivo, как описано Lupton S. D. et al., Mol. and Cell Biol., 11:6 (1991); и Riddell et al., Human Gene Therapy 3:319-338 (1992); см. также публикации PCT/US91/08442 и PCT/US94/05601, Lupton et al., в которых описано использование бифункциональных селектируемых генов слияния, полученных слиянием доминирующего положительного селектируемого маркера с отрицательным селектируемым маркером. См., например, Riddell et al., Патент США No. 6,040,177, в столбцах 14-17.
F. Клетки и получени клеток для генной инженерии
[0626] В некоторых вариантах осуществления клетки, такие как Т-клетки, используемые в связи со способами, применениями, изделиями или композициями по изобретению, являются клетками, которые были генетически модифицированы для экспрессии рекомбинантного рецептора, например, CAR или TCR, описанного здесь. В некоторых вариантах осуществления генно-инженерные клетки используются в контексте клеточной терапии, например, адоптивной клеточной терапии. В некоторых вариантах осуществления генно-инженерные клетки являются иммунными клетками. В некоторых вариантах осуществления генно-инженерными клетками являются Т-клетки, такие как CD4+ или CD8+ Т-клетки.
[0627] В некоторых вариантах осуществления нуклеиновые кислоты, такие как нуклеиновые кислоты, кодирующие рекомбинантный рецептор, являются гетерологичными, т.е., обычно не присутствуют в клетке или образце, полученном из клетки, такими как полученная из другого организма или клетки, которая, например, обычно не обнаруживается в генно-инженерной клетке и/или организме, из которого получена такая клетка. В некоторых вариантах осуществления нуклеиновые кислоты не являются природными, такими как нуклеиновая кислота, не обнаруживанмая в природе, включая включающие комбинации химерных нуклеиновых кислот, кодирующих различные области от множества различных типов клеток.
[0628] Клетки обычно являются эукариотическими клетками, такими как клетки млекопитающих, и как правило, являются клетками человека. В некоторых вариантах осуществления клетки получены из крови, костного мозга, лимфы или лимфоидных органов, клеток иммунной системы, таких как клетки врожденного или приобретенного иммунитета, например, миелоидные или лимфоидные клетки, включая лимфоциты, обычно Т-клетки и/или клетки NK. Другие примеры клеток включают стволовые клетки, такие как мультипотентные и плюрипотентные стволовые клетки, включая индуцированные плюрипотентные стволовые клетки (iPSCs). Клетки, как правило, являются первичными клетками, такими как выделенные непосредственно из пациента и/или выделенные из пациента и замороженные. В некоторых вариантах осуществления клетки включают одну или более субпопуляций Т-клеток или других типов клеток, таких как полная популяция Т-клеток, CD4+ клетки, CD8+ клетки и их субпопуляции, такие как определяемые функцией, состоянием активации, зрелостью, потенциалом для дифференцировки, роста, рециркуляции, локализации и/или способностью к персистированию, специфичностью для антигена, типом антигенного рецептора, присутствием в определенном органе или компартементе, маркером или профилем секреции цитокинов и/или степенью дифференцировки. В отношении пациента, получающего лечение, клетки могут быть аллогенными и/или аутологичными. Среди способов можно назвать стандартные способы. В некоторых аспектах, таких как для стандартных технологий, клетки являются плюрипотентными и/или мультипотентными, такими как стволовые клетки, такие как индуцированные плюрипотентные стволовые клетки (iPSCs). В некоторых вариантах осуществления способы включают выделение клеток из пациента, их препарирование, обработку, культивирование и/или генетическую модификацию и повторное введение тому же пациенту до или после криоконсервации.
[0629] Среди подтипов и субпопуляций Т-клеток и/или CD4+ и/или CD8+ Т-клеток можно назвать интактные T (TN) клетки, эффекторные Т-клетки (TEFF), Т-клетки памяти и их подтипы, такие как память стволовых клеток T (TSCM), центральная память T (TCM), эффекторная память T (TEM), или терминально-дифференцированные эффекторные Т-клетки памяти, инфильтрирующие опухоли лимфоциты (TIL), незрелые Т-клетки, зрелые Т-клетки, Т-хелперы, цитотоксические Т-клетки, мукозальные инвариантные T (MAIT) клетки, естественные и адаптивные регуляторные T (Treg) клетки, Т-хелперы, такие как клетки TH1, клетки TH2, клетки TH3, клетки TH17, клетки TH9, клетки TH22, фолликулярные Т-хелперы, альфа/бета Т-клетки и дельта/гамма Т-клетки.
[0630] В некоторых вариантах осуществления клетки являются естественными клетками-киллерами (NK). В некоторых вариантах осуществления клетки являются моноцитами или гранулоцитами, например, миелоидными клетками, макрофагами, нейтрофилами, дендритными клетками, тучными клетками, эозинофилами и/или базофилами.
[0631] В некоторых вариантах осуществления клетки включают одну или более нуклеиновых кислот, введенных генной инженерией, и таким образом, экспрессируют рекомбинантные или генно-инженерные продукты таких нуклеиновых кислот. В некоторых вариантах осуществления нуклеиновые кислоты являются гетерологичными, т.е., обычно не присутствуют в клетке или образце, полученном из клетки, такими как полученные из другого организма или клетки, который, например, обычно не находится в генно-инженерной клетке и/или организме, из которого получена такая клетка. В некоторых вариантах осуществления нуклеиновые кислоты не являются натуральными, такими как нуклеиновая кислота, не встречающаяся в природе, включая содержащие химерные комбинации нуклеиновых кислот, кодирующих различные домены от множества различных типов клеток.
[0632] В некоторых вариантах осуществления получение генно-инженерных клеток включает одну или более стадий культивирования и/или получения. Клетки для введения нуклеиновой кислоты, кодирующей трансгенный рецептор, такой как CAR, могут быть выделены от образца, такого как биологический образец, например, полученного от или происходящего от пациента. В некоторых вариантах осуществления пациентом, от которого выделена клетка, является имеющий заболевание или состояние или нуждающийся в клеточной терапии или которому будет введена клеточная терапия. Пациентом в некоторых вариантах осуществления является человек, нуждающийся в определенном терапевтическом вмешательстве, таком как адоптивная клеточная терапия, для которой клетки выделяют, подвергают процессингу и/или инжинирингу.
[0633] Соответственно, клетки в некоторых вариантах осуществления являются первичными клетками, например, первичными клетками человека. Образцы включают ткань, жидкость и другие образцы, взятые непосредственно от пациента, а также образцы, полученные в результате одной или более стадий обработки, таких как разделение, центрифугирование, генная инженерия (например, трансдукция вирусным вектором), промывка и/или инкубация. Биологический образец может быть образцом, полученным непосредственно из биологического источника, или образцом после процессинга. Биологические образцы включают, но не ограничены ими, жидкости организма, такие как кровь, плазма, сыворотка, цереброспинальная жидкость, синовиальная жидкость, моча и пот, образцы ткани и органа, включая процессированные образцы, полученные из них.
[0634] В некоторых аспектах образец, от которого клетки получены или выделены, является кровью или полученным из крови образцом, или представляет собой или получен из продукта лейкафереза или афереза. Примеры образцов включают цельную кровь, одноядерные клетки периферической крови (PBMC), лейкоциты, костный мозг, тимус, биопсию ткани, опухоль, лейкоз, лимфому, лимфатический узел, лимфоидную ткань кишечника, лимфоидную ткань слизистой оболочки, селезенку, другие лимфоидные ткани, печень, легкое, желудок, кишечник, толстую кишку, почку, поджелудочную железу, молочную железу, кость, предстательную железу, шейку, яички, яичники, миндалину или другой орган и/или клетки, полученные из них. Образцы включают, в контексте клеточной терапии, например, адоптивной клеточной терапии, образцы из аутогенных и аллогенных источников.
[0635] В некоторых вариантах осуществления клетки получают из клеточных линий, например, Т-клеточных линий. Клетки в некоторых вариантах осуществления получают из ксеногенного источника, например, из мыши, крысы, примата, отличного от человека, и свиньи.
[0636] В некоторых вариантах осуществления выделение клеток включает одну или более стадий получения и/или разделения клеток не на основе аффинности. В некоторых примерах клетки моют, центрифугируют и/или инкубируют в присутствии одного или более реагентов, например, чтобы удалить нежелательные компоненты, обогатить желаемыми компонентами, разложить или удалить клетки, чувствительные к определенным реагентам. В некоторых примерах клетки разделяют на основе одного или более свойств, таких как плотность, адгезивные свойства, размер, чувствительность и/или резистентность к определенным компонентам.
[0637] В некоторых примерах клетки получают из циркулирующей крови пациента, например, аферезом или лейкаферезом. Образцы в некоторых аспектах содержат лимфоциты, включая Т-клетки, моноциты, гранулоциты, В-клетки, другие ядерные лейкоциты, эритроциты и/или тромбоциты, и в некоторых аспектах содержат клетки, отличные эритроцитов и тромбоцитов.
[0638] В некоторых вариантах осуществления клетки крови, собранные от пациента, промывают, например, чтобы удалить плазменную фракцию, и помещают клетки в подходящий буфер или среду для последующих стадий обработки. В некоторых вариантах осуществления клетки промывают фосфатным буферным солевым раствором (PBS). В некоторых вариантах осуществления раствор для промывки не содержит кальций и/или магний и/или многие или все двухвалентные катионы. В некоторых аспектах достигается моющийся шаг, полуавтоматическое «перекачивает» центрифугу (например, Cobe 2991 cell processor, Baxter) согласно инструкциям производителя. В некоторых аспектах стадию промывки осуществляют тангенциальной фильтрацией потока (TFF) согласно инструкциям производителя. В некоторых вариантах осуществления клетки повторно суспендируют во множестве биологически совместимых буферов после мытья, таких как, например, не содержащий Ca++/Mg++ PBS. В некоторых вариантах осуществления компоненты образца клеток крови удаляют, и клетки непосредственно повторно суспендируют в культуральных средах.
[0639] В некоторых вариантах осуществления способы включают основанные на плотности методы разделения клеток, такие как получение лейкоцитов из периферической крови путем разложения эритроцитов и центрифугирования через градиент Перколла или Фиколла.
[0640] В некоторых вариантах осуществления методы выделения включают разделение различных типов клеток на основе экспрессии или присутствия в клетке одной или более определенных молекул, таких как поверхностные маркеры, например, поверхностные белки, внутриклеточные маркеры или нуклеиновая кислота. В некоторых вариантах осуществления может использоваться любой известный способ разделения на основе таких маркеров. В некоторых вариантах осуществления разделение является афинным или иммуноафинным разделением. Например, выделение в некоторых аспектах включает разделение клеток и популяций клеток на основе экспрессии клеток или уровня экспрессии одного или более маркеров, как правило, маркеров поверхности клеток, например, инкубацией с антителом или партнером связывания, специфично связывающегося к таким маркерам, обычно с последующими стадиями промывки и отделения клеток, связавшихся с антителом или партнером связывания, от клеток, не связавшихся с антителом или партнером связывания.
[0641] Такие стадии разделения могут основываться на положительном выборе, в котором клетки, связавшиеся с реагентами, сохраняют для дальнейшего использования, и/или отрицательном выборе, в котором сохраняют клетки, не связавшиеся с антителом или партнером связывания. В некоторых примерах обе фракции сохраняют для дальнейшего использования. В некоторых аспектах отрицательный выбор может быть особенно полезным, если не доступно антитело, которое специфично идентифицирует тип клетки в гетерогенной популяции, так, что разделение лучше всего осуществляют на основе маркеров, экспрессирующихся клетками, отличными от желаемой популяции.
[0642] Разделение не должно приводить к 100%-му обогащению или удалению определенной популяции клеток или клеток, экспрессирующих определенный маркер. Например, положительный выбор или обогащение клетками определенного типа, такого как те, которые экспрессируют маркер, относятся к увеличению числа или процента таких клеток, но не должны приводить к полному отсутствию клеток, не экспрессирующих этот маркер. Аналогично, отрицательный выбор, удаление или истощение клеток определенного типа, такого как те, которые экспрессируют маркер, относится к сокращению числа или процента таких клеток, но не должны заканчиваться полным удалением всех таких клеток.
[0643] В некоторых примерах осуществляют многократные циклы стадий разделения, где положительно или отрицательно выбранные фракции с одной стадии подвергают другой стадии разделения, такой как последующий положительный или отрицательный выбор. В некоторых примерах единственная стадия разделения может истощить клетки, экспрессирующие одновременно множественные маркеры, например, путем инкубации клеток со множеством антител или партнеров связывания, каждый из которых является специфичным для маркера, предназначенного для отрицательного выбора. Аналогично, множественные типы клеток могут одновременно быть положительно выбраны путем инкубации клеток со множеством антител или партнеров связывания, экспрессируемых на различных типах клеток.
[0644] Например, в некоторых аспектах определенные субпопуляции Т-клеток, такие как клетки положительные или экспрессирующие высокие уровни одного или более поверхностных маркеров, например, CD28+, CD62L+, CCR7+, CD27+, CD127+, CD4+, CD8+, CD45RA+, и/или CD45RO+ Т-клетки, выделяют методами положительного или отрицательного выбора.
[0645] Например, CD3+, CD28+ Т-клетки могут быть положительно выбраны с использованием анти-CD3/анти-CD28 конъюгированных магнитных частиц (например, DYNABEADS® M-450 CD3/CD28 T Cell Expander).
[0646] В некоторых вариантах осуществления выделение осуществляют обогащением определенной популяцией клеток положительным выбором или истощением определенной популяции клеток отрицательным выбором. В некоторых вариантах осуществления положительный или отрицательный выбор осуществляют путем инкубации клеток с одним или более антителами или другим связующим веществом, специфично связывающимися с одним или более поверхностными маркерами, экспрессируемыми (маркер+) или экспрессируемыми на относительно более высоком уровне (маркерhigh) на положительно или отрицательно выбранных клетках, соответственно.
[0647] В некоторых вариантах осуществления Т-клетки отделяют от образца PBMC отрицательным выбором маркеров, экспрессируемых на не-Т-клетких, таких как В-клетки, моноциты, или другие лейкоциты, такие как CD14. В некоторых аспектах стадия выбора CD4+ или CD8+ используется для отделения CD4+ хелпера и CD8+ цитотоксических Т-клеток. Такая популяция CD4+ и CD8+ может быть далее сортирована в субпопуляции положительным или отрицательным выбором для маркеров, экспрессируемых или экспрессируемых до относительно более высокой степени на одной или более субпопуляций интактных, памяти и/или эффекторных Т-клеток.
[0648] В некоторых вариантах осуществления CD8+ клетки далее обогащают или истощают в отношении интактных, центральной памяти, эффекторной памяти и/или центральной памяти стволовых клеток, например, положительным или отрицательным выбором на основе поверхностных антигенов, связанных с соответствующей субпопуляцией. В некоторых вариантах осуществления обогащение в отношении клеток центральной памяти T (TCM) осуществляют для увеличения эффективности, например, для улучшения долгосрочной выживаемости, роста и/или приживления после введения, которое в некоторых аспектах особенно сильным в таких субпопуляциях. См. Terakura et al. (2012) Blood,1:72-82; Wang et al. (2012) J Immunother. 35(9):689-701. В некоторых вариантах осуществления комбинация TCM-обогащенных CD8+ Т-клеток и CD4+ Т-клеток дополнительно усиливает эффективность.
[0649] В вариантах осуществления Т-клетки памяти присутствуют в обеих CD62L+ и CD62L- субпопуляциях CD8+ лимфоцитов периферической крови. PBMC могут быть обогащены или истощены в отношении CD62L-CD8+ и/или CD62L+CD8+ фракций, например, с использованием анти-CD8 и анти-CD62L антитела.
[0650] В некоторых вариантах осуществления обогащение клетками центральной памяти T (TCM) основывается на положительной или высокой поверхностной экспрессии CD45RO, CD62L, CCR7, CD28, CD3 и/или CD127; в некоторых аспектах оно основано на отрицательном выборе для клеток, экспрессирующих или высоко экспрессирующих CD45RA и/или гранзим B. В некоторых аспектах выделение популяции CD8+, обогащенной клетками TCM, осуществляют истощением клеток, экспрессирующих CD4, CD14, CD45RA, и положительным выбором или обогащением клеток, экспрессирующих CD62L. В одном аспекте обогащение клетками центральной памяти T (TCM) осуществляют, исходя из отрицательной фракции клеток, выбранных на основе экспрессии CD4, подвергнутой отрицательному выбору на основе экспрессии CD14 и CD45RA, и положительному выбору на основе CD62L. Такие выборы в некоторых аспектах осуществляют одновременно, и в других аспектах осуществляют последовательно, в любом порядке. В некоторых аспектах, та же основанная на экспрессии стадия выбора CD4, используемая в получении CD8+ популяции или субпопуляции клеток, также используется для генерации CD4+ популяции или субпопуляции клеток, так, что и положительные, и отрицательные фракции от основанного на CD4 разделения сохраняются и используются на последующих стадиях способов, необязательно после одной или более дополнительных стадий положительного или отрицательного выбора.
[0651] В частном примере образец PBMC или другой образец лейкоцитов подвергают выбору CD4+ клетки, где и отрицательные, и положительные фракции сохраняются. Отрицательную фракцию затем подвергают отрицательному выбору на основе экспрессии CD14 и CD45RA или CD19, и положительному выбору на основе характеристики маркера центральных Т-клеток памяти, такого как CD62L или CCR7, где положительные и отрицательные выборы осуществляют в любом порядке.
[0652] CD4+ T хелперные клетки сортируют на интактные, центральной памяти и эффекторные клетки путем идентификации популяции клеток, имеющих антигены поверхности клеток. CD4+ лимфоциты могут быть получены стандартными методами. В некоторых вариантах осуществления интактные CD4+ Т-клетки являются CD45RO-, CD45RA+, CD62L+, CD4+ Т-клетками. В некоторых вариантах осуществления, клетки центральной памяти CD4+ являются CD62L+ и CD45RO+. В некоторых вариантах осуществления эффекторные CD4+ клетки являются CD62L- и CD45RO-.
[0653] В одном примере для обогащения CD4+ клетками отрицательным выбором, коктейль моноклонального антитела, как правило, включает антитела к CD14, CD20, CD11b, CD16, HLA-DR и CD8. В некоторых вариантах осуществления антитело или партнер связывания связывается с твердой подложкой или матрицей, такой как магнитная частица или парамагнитная частица, для обеспечения разделения клеток для положительного и/или отрицательного выбора. Например, в некоторых вариантах осуществления клетки и популяцию клеток отделяют или выделяют с использованием иммуномагнитных (или аффинномагнитных) методов разделения (рассмотренных в Methods in Molecular Medicine, vol. 58: Metastasis Research Protocols, Vol. 2: Cell Behavior In Vitro and In Vivo, p 17-25 Edited by: S. A. Brooks and U. Schumacher © Humana Press Inc., Тотова, Нью-Джерси).
[0654] В некоторых аспектах образец или композицию клеток, которые будут разделены, инкубируют с небольшим намагничиваемым или магнитночувствительным материалом, таким как магнитно чувствительные частицы или микрочастицы, такие как парамагнитные частицы (например, такие как частицы Dynalbeads или MACS). Магнитночувствительный материал, например, частица, обычно непосредственно или опосредованно присоединяют к партнеру связывания, например, антителу, специфично связывающемуся с молекулой, например, поверхностным маркером, присутствующей на клетке, клетках или популяции клеток, которые желают разделить, например, отрицательный или положительный выбор которых желают осуществить.
[0655] В некоторых вариантах осуществления магнитная частица или гранула включает магнитночувствительный материал, связывающийся со специфическим партнером связывания, такому как антитело или другой партнер связывания. Существует много известных магнитночувствительных материалов, используемых в способах магнитного разделения. Подходящие магнитные частицы включают описанные в Molday, патент США 4,452,773, и в описании европейского патента EP 452342 B, которые включены в настоящее описание посредством ссылок. Коллоидные частицы, такие как описанные в Owen, патент США 4,795,698, и Liberti et al., патент США 5,200,084 являются другими примерами.
[0656] Инкубацию обычно осуществляют в условиях, в которых чего антитела или партнеры связывания, или молекулы, такие как вторичные антитела или другие реагенты, специфично связывающиеся с такими антителами или партнерами связывания, которые присоединены к магнитной частице или бусинке, специфично связываются с молекулами поверхности клеток, если они присутствуют на клетках в образце.
[0657] В некоторых аспектах образец помещают в магнитное поле, и клетки, имеющие магнитно чувствительные или намагничиваемые частицы, присоединенные к ним, будут притягиваться к магниту и отделяться от немеченных клеток. Для положительного выбора сохраняют клетки, притянутые к магниту; для отрицательного выбора сохраняют непритянутые клетки (немеченные клетки). В некоторых аспектах комбинацию положительного и отрицательного выбора осуществляют во время той же стадии выбора, где положительные и отрицательные фракции сохраняют и далее обрабатывают или подвергают дальнейшим стадиям разделения.
[0658] В некоторых вариантах осуществления магнитночувствительные частицы покрывают первичными антителами или другими партнерами связывания, вторичными антителами, лектинами, ферментами или стрептавидином. В некоторых вариантах осуществления магнитные частицы присоединены к клеткам через покрытие первичных антител, специфичных для одного или более маркеров. В некоторых вариантах осуществления клетки, а не частицы, мечены первичным антителом или партнером связывания, и затем добавляют покрытые специфичным для типа клеток вторичным антителом или другим партнером связывания (например, стрептавидином) магнитные частицы. В некоторых вариантах осуществления покрытые стрептавидином магнитные частицы используют в комбинации с биотинилированными первичными или вторичными антителами.
[0659] В некоторых вариантах осуществления магнитночувствительные частицы оставляют присоединенными к клеткам, которые должны впоследствии инкубироваться, культивироваться и/или генетически модифицироваться; в некоторых аспектах частицы оставляют присоединенными к клеткам для введения пациенту. В некоторых вариантах осуществления намагничиваемые или магнитночувствительные частицы удаляют из клеток. Способы удаления намагничиваемых частиц из клеток известны и включают, например, использование конкурирующих немеченных антител и намагничиваемых частиц или антител, конъюгированных с расщепляемыми линкерамми. В некоторых вариантах осуществления намагничиваемые частицы являются биоразлагаемыми.
[0660] В некоторых вариантах осуществления основанный на аффинности выбор осуществляют через сортировку магнитноактивированных клеток (MACS) (Miltenyi Biotec, Оберн, Калифорния). Системы сортировки магнитноактивированных клеток (MACS) способны к высокочистому выбору клеток, к которым присоединены намагничивающие частицы. В некоторых вариантах осуществления MACS осуществляют в способе, в котором нецелевые и целевые виды последовательно элюируют после применения внешнего магнитного поля. Т.е., клетки, присоединенные к намагниченным частицам, остаются на месте, в то время как неприсоединенные виды элюируются. Затем, после завершения этой первой стадии элюирования, виды, которые были удержаны в магнитном поле и не были элюированы, выделяют некоторым образом, таким образом, что они могут быть элюированы и восстановлены. В некоторых вариантах осуществления не являющиеся мишенями клетки метят и истощают из гетерогенной популяции клеток.
[0661] В некоторых вариантах осуществления выделение или разделение осуществляют с помощью системы, устройства или аппарата, выполняющего одну или более стадий способов выделения, получения клеток, разделения, обработки, инкубации, культивирования и/или составления. В некоторых аспектах система используется для осуществления каждой из этих стадий в закрытой или стерильной среде, например, для минимизации ошибки, пользовательских настроек и/или загрязнения. В одном примере система является системой, описанной в Публикации Международной Заявки на патент WO2009/072003 или US 20110003380 A1.
[0662] В некоторых вариантах осуществления система или аппарат выполняет одну или более, например, все стадии выделения, процессинга, инжиниринга и составления в интегрированной или отдельной системе, и/или автоматизированным или программируемым способом. В некоторых аспектах система или аппарат включает компьютер и/или компьютерную программу в коммуникации с системой или аппаратом, позволяющим пользователю программировать, контролировать, оценивать результат и/или натсраивать различные аспекты стадий процессинга, выделения, инжиниринга и составления.
[0663] В некоторых аспектах разделение и/или другие стадии осуществляют с помощью системы CliniMACS (Miltenyi Biotec), например, для автоматизированного разделения клеток на уровне клинического масштаба в закрытой и стерильной системе. Компоненты могут включать интегрированный микрокомпьютер, единицу магнитной сепарации, перистальтический насос и различные клапаны повышения. Интегрированный компьютер в некоторых аспектах управляет всеми компонентами инструмента и направляет систему для выполнения повторенных процедур в стандартизированной последовательности. Единица магнитной сепарации в некоторых аспектах включает подвижный постоянный магнит и держатель для столбца выбора. Перистальтический насос управляет скоростью потока по всей системе трубки и, вместе с клапанами повышения, гарантирует контролируемый поток буфера через систему и непрерывное суспендирование клеток.
[0664] Система CliniMACS в некоторых аспектах использует соединенные с антителом намагничиваемые частицы, поставляющиеся в стерильном непирогенном растворе. В некоторых вариантах осуществления после мечения клеток магнитными частицами клетки промывают для удаления избыточных частиц. Мешок для получения клеток затем присоединяют к системе трубок, в свою очередь связанной с мешком, содержащим буфер, и мешком для сбора клеток. Система трубок состоит из заранее смонтированного стерильного набора трубок, включая предварительный столбец и столбец для разделения, и предназначена только для одноразового использования. После инициации программы разделения система автоматически наносит образец клеток на столбец для разделения. Меченные клетки сохраняются в столбце, в то время как немеченные клетки удаляют серией стадий промывки. В некоторых вариантах осуществления популяция клеток для использования со способами, описанными здесь, не мечена и не сохраняется в столбце. В некоторых вариантах осуществления популяция клеток для использования со способами, описанными здесь, мечена и сохраняется в столбце. В некоторых вариантах осуществления популяция клеток для использования со способами, описанными здесь, элюируется из столбца после удаления магнитного поля и собирается в мешке для сбора клеток.
[0665] В некоторых вариантах осуществления разделение и/или другие стадии осуществляют с помощью системы CliniMACS Prodigy (Miltenyi Biotec). Система CliniMACS Prodigy в некоторых аспектах оборудована модулем для процессинга клеток, обеспечивающим автоматизированную промывку и фракционирование клеток центрифугированием. Система CliniMACS Prodigy может также включать бортовую камеру и программное обеспечение узнавания изображения, определяющее оптимальный результат фракционирования клеток путем различения макроскопических слоев исходного клеточного продукта. Например, периферическая кровь автоматически разделяется на эритроциты, лейкоциты и плазменные слои. Система CliniMACS Prodigy может также включать интегрированную камеру культивирования клеток, которая обеспечивает протоколы клеточной культуры, такие как, например, клеточная дифференцировка и рост, загрузка антигена и долгосрочное культивирование клеток. Входные порты могут обеспечивать стерильное удаление и пополнение сред, и клетки могут быть проверены с помощью интегрированного микроскопа. См., например, Klebanoff et al. (2012) J Immunother. 35(9): 651-660, Terakura et al. (2012) Blood,1:72-82, и Wang et al. (2012) J Immunother. 35(9):689-701.
[0666] В некоторых вариантах осуществления популяцию клеток, описанную здесь, собирают и обогащают (или истощают) через потоковую цитометрию, в которой клетки, окрашенные множественными маркерами поверхности клеток, находятся в жидком потоке. В некоторых вариантах осуществления популяцию клеток, описанную здесь, собирают и обогащают (или истощают) через (FACS)-сортировку препаративного масштаба. В некоторых вариантах осуществления популяцию клеток, описанную здесь, собирают и обогащают (или истощают) при помощи чипов микроэлектромеханических систем (MEMS) в комбинации с основанной на FACS системой обнаружения (см., например, WO 2010/033140, Cho et al. (2010) Lab Chip 10, 1567-1573; and Godin et al. (2008) J Biophoton. 1(5):355-376). В обоих случаях клетки могут быть мечены множественными маркерами, обеспечивая выделение четко определенных субпопуляций Т-клеток с высокой чистотой.
[0667] В некоторых вариантах осуществления антитела или партнеры связывания мечены одним или более поддающимися обнаружению маркерами для облегчения разделения для положительного и/или отрицательного выбора. Например, разделение может основываться на связывании с флуоресцентно меченными антителами. В некоторых примерах разделение клеток на основе связывания антител или других партнеров связывания, специфичных для одного или более маркеров поверхности клеток, осуществляют в жидком потоке, например, активированной флуоресценцией сортировкой клеток (FACS), включая (FACS) препаративного масштаба и/или чипы микроэлектромеханических систем (MEMS), например, в комбинации с проточно-цитометрической системой обнаружения. Такие способы обеспечивают положительный и отрицательный выбор на основе множественных маркеров одновременно.
[0668] В некоторых вариантах осуществления способы получения включают стадии замораживания, например, сохранение замораживанием, клеток до или после выделения, инкубации и/или инжиниринга. В некоторых вариантах осуществления замораживание и последующая стадия оттаивания удаляет гранулоциты и, в некоторой степени, моноциты в популяции клеток. В некоторых вариантах осуществления клетки суспендируют в охлаждающем растворе, например, осуществляя стадию промывки для удаления плазмы и тромбоцитов. Любое множество известных охлаждающих растворов и параметров в некоторых аспектах может использоваться. Один пример включает использование PBS, содержащего 20% DMSO и 8% человеческого сывороточного альбумина (HSA) или другие подходящие среды для замораживания клеток. Затем их разбавляют 1:1 средами так, чтобы конечная концентрация DMSO и HSA составила 10% и 4%, соответственно. Клетки обычно затем замораживают до -80°C со скоростью 1°C в минуту и хранят в паровой фазе резервуара для хранения жидкого азота.
[0669] В некоторых вариантах осуществления клетки инкубируют и/или культивируют до или в связи с генной инженерией. Инкубационные стадии могут включать культуру, культивирование, стимуляцию, активацию и/или рост. Инкубация и/или инжиниринг могут быть выполнены в сосуде для культивирования, таком как модуль, камера, лунка, столбец, трубка, система трубок, клапан, флакон, чашка для культивирования, мешок или другой контейнер для культивирования или культуры клеток. В некоторых вариантах осуществления композиции или клетки инкубируют в присутствии условий стимуляции или стимулирующего агента. Такие условия включают разработанные для индукции пролиферации, роста, активации и/или выживаемости клеток в популяции, стимуляции экспозиции антигена и/или примирования клеток для генной инженерии, например, для введения рекомбинантного антигенного рецептора.
[0670] Условия могут включать одну или более специфически сред, температуру, содержание кислорода, содержание углекислого газа, время, агенты, например, питательные вещества, аминокислоты, антибиотики, ионы и/или стимулирующие факторы, такие как цитокины, хемокины, антигены, партнеры связывания, слитые белки, рекомбинантные растворимые рецепторы и любые другие вещества, разработанные для активации клеток.
[0671] В некоторых вариантах осуществления стимулирующие условия или агенты включают один или более агентов, например, лигандов, которые способны к активации внутриклеточного сигнального домена комплекса TCR. В некоторых аспектах агент включает или инициирует внутриклеточный сигнальный каскад TCR/CD3 в Т-клетке. Такие агенты могут включать антитела, такие как специфические для TCR, например, анти-CD3. В некоторых вариантах осуществления стимулирующие условия включают один или более агентов, например, лиганд, который способен к стимуляции костимулирующего рецептора, например, анти-CD28. В некоторых вариантах осуществления такие агенты и/или лиганды могут быть связаны с твердой подложкой, такой как частица и/или один или более цитокинов. Необязательно, способ расширения может дополнительно включать стадию добавления антитела анти-CD3 и/или анти-CD28 к культуральной среде (например, в концентрации по меньшей мере приблизительно 0,5 нг/мл). В некоторых вариантах осуществления стимуляторы включают IL-2, IL-15 и/или IL-7. В некоторых аспектах концентрация IL-2 составляет по меньшей мере приблизительно 10 единица/мл.
[0672] В некоторых аспектах инкубацию осуществляют в соответствии с методами, такими как описанные в Патенте США No. 6,040,177 на имя Riddell et al., Klebanoff et al.(2012) J Immunother. 35(9): 651-660, Terakura et al. (2012) Blood,1:72-82, and/or Wang et al. (2012) J Immunother. 35(9):689-701.
[0673] В некоторых вариантах осуществления Т-клетки выращивают путем добавления к инициирующей культивирование композиции питающих клеток, таких как неделящиеся одноядерные клетки периферической крови (PBMC) (например, такие, что полученная популяция клеток содержит по меньшей мере приблизительно 5, 10, 20 или 40 или более питающих клеток PBMC на каждую Т-клетку в начальной популяции, предназначенной для роста); и инкубацию культуры (например, в течение времени, достаточного для увеличения числа Т-клеток). В некоторых аспектах неделящиеся питающие клетки могут включать облученные гамма-излучением питающие клетки PBMC. В некоторых вариантах осуществления PBMC облучают гамма-лучами в диапазоне приблизительно 3000-3600 рад для предотвращения клеточного деления. В некоторых аспектах питающие клетки добавляют к культуральной среде до добавления популяции Т-клеток.
[0674] В некоторых вариантах осуществления стимулирующие условия включают температуру, подходящую для роста человеческих Т-клеток, например, по меньшей мере приблизительно 25 градусов Цельсия, обычно по меньшей мере приблизительно 30 градусов, и обычно составляющую или приблизительно составляющую 37 градусов Цельсия. Необязательно, инкубация может дополнительно включать добавление неделящихся EBV-трансформированных лимфобластных клеток (LCL) в качестве питающих клеток. LCL могут быть облучены гамма-лучами в диапазоне приблизительно 6000-10000 рад. Питающие клетки LCL в некоторых аспектах используют в любом подходящей количестве, таком как отношение питающих клеток LCL к изначальным Т-лимфоцитам по меньшей мере приблизительно 10:1.
[0675] В вариантах осуществления антигенспецифические Т-клетки, такие как антигенспецифические CD4+ и/или CD8+ Т-клетки, получают путем стимуляции интактных или антигенспецифических Т-клеток антигеном. Например, линии или клоны антиген-специфических Т-клеток могут быть сгенерированы к антигенам цитомегаловируса путем выделения Т-клеток от инфицированных пациентов и стимуляции клеток in vitro тем же антигеном.
IV. КОМПОЗИЦИИ И СОСТАВЫ
[0676] В некоторых вариантах осуществления доза клеток, включающих клетки, генетически модифицированные рекомбинантным антигенным рецептором, например, CAR или TCR, обеспечивается как композиция или состав, такая как фармацевтическая композиция или состав. Такие композиции могут использоваться в соответствии со способами или применениями по изобретению и/или с использованием изделий или композиций по изобретению, например, в профилактике или лечении заболеваний, состояний и нарушений, или в способах детекции, диагностики и прогнозирования.
[0677] Термин «фармацевтический состав» относится к препарату, который находится в такой форме, которая орбеспечивает эффективность биологической активности активного ингредиента, содержащегося в нем, и не содержит дополнительных компонентов, которые неприемлемо токсичны для пациента, которому состав вводят.
[0678] “Фармацевтически приемлемый носитель” относится к ингредиенту в фармацевтическом составе, отличному от активного ингредиента, который нетоксичен для пациента. Фармацевтически приемлемый носитель включает, но не ограничен ими, буфер, эксципиент, стабилизатор или консервант.
[0679] В некоторых аспектах выбор носителя определяется частично определенной клеткой или агентом и/или способом введения. Соответственно, существует множество подходящих составов. Например, фармацевтическая композиция может содержать консерванты. Подходящие консерванты могут включать, например, метилпарабен, пропилпарабен, бензоат натрия и хлорид бензалкония. В некоторых аспектах используется смесь двух или более консервантов. Консервант или их смеси, как правило, присутствуют в количестве от приблизительно 0,0001% до приблизительно 2% от общей массы композиции. Носители описаны, например, в Remington’s Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980). Фармацевтически приемлемые носители обычно нетоксичны для реципиентов в используемых дозировках и концентрациях и включают, но не ограничены ими: буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как октадецилдиметилбензил аммоний хлорид; гексоний хлорид; бензалконий хлорид; бензетоний хлорид; фенол, бутиловый спирт или бензиловый спирт; алкил парабены, такие как метил или пропил парабен; катехол; резорцин; циклогексанол; 3-пентанол; и мета-крезол); низкомолекулярные (менее чем приблизительно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как EDTA; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексные соединения металла (например, комплексы Zn-белок); и/или неионогенные поверхностно-активные вещества, такие как полиэтиленгликоль (ПЭГ).
[0680] Буферные вещества в некоторых аспектах включены в композиции. Подходящие буферные вещества включают, например, лимонную кислоту, цитрат натрия, фосфорную кислоту, фосфат калия и различные другие кислоты и соли. В некоторых аспектах используется смесь двух или более буферных веществ. Буферное вещество или их смеси, как правило, присутствуют в количестве от приблизительно 0,001% до приблизительно 4% от общей массы композиции. Способы получения фармацевтических композиций для введения известны. Примеры способов описаны более подробно в, например, Remington: The Science and Practice of Pharmacy, Lippincott Williams & Wilkins; 21st ed. (1 мая 2005).
[0681] Состав или композиция могут также содержать более чем один активный ингредиент, полезный для определенного показания, заболевания или состояния, предотвращаемого или излечиваемого клетками или агентами, где соответствующие действия не оказывают негативное влияние на друг друга. Такие активные ингредиенты предпочтительно присутствуют в комбинации в количествах, которые являются эффективными для предназначенной цели. Таким образом, в некоторых вариантах осуществления, фармацевтическая композиция дополнительно включает другие фармацевтически активные вещества или лекарственные средства, такие как химиотерапевтические вещества, например, аспарагиназу, бусульфан, карбоплатин, цисплатин, даунорубицин, доксорубицин, фтороурацил, гемцитабин, гидроксимочевину, метотрексат, паклитаксел, ритуксимаб, винбластин, винкристин и т.д. В некоторых вариантах осуществления агенты или клетки вводят в форме соли, например, фармацевтически приемлемой соли. Подходящие фармацевтически приемлемые соли присоединения с кислотой включают полученные из неорганических кислот, таких как соляная, бромистоводородная, фосфорная, метафосфорная, азотная и серная кислоти, и органических кислот, таких как винная, уксусная, лимонная, яблочная, молочная, фумаровая, бензойная, гликолевая, глюконовая, янтарная и арилсульфоновая кислота, например, п-толуолсульфоновая кислота.
[0682] Фармацевтическая композиция в некоторых вариантах осуществления содержит вещества или клетки в количествах, эффективных для лечения или профилактики заболевания или состояния, таких как терапевтически эффективное или профилактически эффективное количество. Терапевтическую или профилактическую эффективность в некоторых вариантах осуществления проверяют периодической оценкой получающих лечение пациентов. Для повторных введений в течение нескольких дней или дольше, в зависимости от состояния, лечение повторяют, пока не произойдет желаемое подавление симптомов заболевания. Однако другие режимы дозировки могут быть полезными и могут быть определены. Желаемая дозировка может быть доставлена единственным болюсным введением композиции, множественными болюсными введениями композиции или непрерывным введением композиции путем вливания.
[0683] Агенты или клетки могут быть введены любыми подходящими средствами, например, болюсным вливанием, инъекцией, например, внутривенными или подкожными инъекциями, внутриглазной инъекцией, периокулярной инъекцией, подсетчаточной инъекцией, интравитреальной инъекцией, транссептальной инъекцией, подсклеральной инъекцией, внутрихориоидальной инъекцией, внутрикамеральной инъекцией, субконъюнктивальной инъекцией, подконъюнктивальной инъекцией, субтеноновой инъекцией, ретробульбарной инъекцией, перибульбарной инъекцией или задней околосклеральной доставкой. В некоторых вариантах осуществления их вводят парентеральным, интрапульмонарным и внутриносовым, и, если желательно для местного лечения, внутриочаговым введением. Парентеральные вливания включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. В некоторых вариантах осуществления введенную дозу вводят единственным болюсным введением клеток или агента. В некоторых вариантах осуществления их вводят многократными болюсными введениями клеток или агента, например, в течение не более чем 3 дней, или непрерывным введением клеток или агента путем вливания.
[0684] Для профилактики или лечения заболевания, подходящая дозировка может зависеть от типа заболевания, которое подвергают лечению, типа агента или агентов, типа клеток или рекомбинантных рецепторов, серьезности и течения заболевания, того, вводят ли агент или клетки в профилактических или терапевтических целях, предыдущей терапии, истории заболевания пациента и ответа на агент или клетки и усмотрение лечащего врача. Композиции в некоторых вариантах осуществления предпочтительно вводят пациенту однократно или в серии лечений.
[0685] Клетки или агенты могут быть введены с использованием стандартных способов введения, составов и/или устройств. Изобретение относится к составам и устройствам, таким как шприцы и пузырьки, для хранения и введения композиций. Относительно клеток введение может быть аутологичным или гетерологичным. Например, иммунореактивные клетки или предшественники могут быть получены от одного пациента и введены тому же пациенту или другому совместимому пациенту. Полученные из периферической крови иммунореактивные клетки или их потомство (например, полученные in vivo, ex vivo или in vitro) могут быть введены локализованной инъекцией, включая введение катетером, системную инъекцию, локализованную инъекцию, внутривенную инъекцию или парентеральное введение. При введении терапевтической композиции (например, фармацевтической композиции, содержащей генетически модифицированную иммунореактивную клетку или агент, который лечит или облегчает симптомы нейротоксичности), ее обычно составляют в инъецируемой стандартной лекарственной форме (раствор, суспензия, эмульсия).
[0686] Составы включают таковые для перорального, внутривенного, внутрибрюшинного, подкожного, легочного, чрескожного, внутримышечного, внутриносового, щечного, подъязычного или введения суппозиторием. В некоторых вариантах осуществления агент или популяцию клеток вводят парентерально. Термин «Парентеральный», в рамках изобретения, включает внутривенное, внутримышечное, подкожное, ректальное, вагинальное и внутрибрюшинное введение. В некоторых вариантах осуществления агент или популяцию клеток вводят пациенту с использованием периферической системной доставки внутривенной, внутрибрюшинной, или подкожной инъекцией.
[0687] Композиции в некоторых вариантах осуществления имеют форму стерильных жидких препаратов, например, изотонических водных растворов, суспензий, эмульсий, дисперсий или вязких композиций, которыу в некоторых аспектах могут быть буферизованными до выбранного pH. Жидкие препараты обычно проще получить, чем гели, другие вязкие композиции и твердые композиции. Кроме того, жидкие композиции несколько более удобны для введения, особенно инъекцией. Вязкие композиции, с другой стороны, могут быть составлены в подходящем диапазоне вязкости для обеспечения более длинных периодов контакта со специфическими тканями. Жидкие или вязкие композиции могут включать носители, которые могут быть растворяющей или диспергирующей средой, содержащей, например, воду, солевой раствор, фосфатный буферный солевой раствор, полиол (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль) и подходящие смеси этого.
[0688] Стерильные инъецируемые растворы могут быть получены путем включения агента или клеток в растворитель, например, в смеси с подходящим носителем, разбавителем или эксципиентом, таким как стерилизованная вода, физиологический солевой раствор, глюкоза, декстроза и т.п.
[0689] Составы, которые используются для введения in vivo, обычно являются стерильными. Стерильность может быть легко достигнута, например, фильтрацией через мембраны для стерилизующей фильтрации.
V. КОМБИНИРОВАННАЯ ТЕРАПИЯ
[0690] В некоторых вариантах осуществления способов, изделий, применений или композиций клеточную терапию, например, дозу Т-клеток (например, CAR+ Т-клеток), вводят пациентам в комбинации с дополнительным терапевтическим агентом или терапией, обычно отличной от клеточной терапии или другой клеточной терапии, такой как отличная от CAR+ Т-клеточной терапии. В некоторых вариантах осуществления клеточную терапию, например, дозу генно-инженерных Т-клеток, таких как CAR+ Т-клетки, в способах или применениях по изобретению и/или с изделиями или композициями, вводят как часть комбинированного лечения или комбинированной терапии, например, одновременно с, последовательно с или периодически с, в любом порядке, одним или более дополнительными терапевтическими вмешательствами. В некоторых вариантах осуществления, одно или более дополнительных терапевтических вмешательств включает любой агент или лечение для лечения или профилактики заболевания или состояния, такого как В-клеточная злокачественная опухоль, например, NHL, и/или любой агент или лечение для увеличения эффективности, персистирования и/или активности генно-инженерной клеточной терапии.
[0691] В некоторых вариантах осуществления дополнительный терапевтический агент или терапию вводят пациентам, которые являются или вероятно являются, или для которых это предсказано, организмами с ослабленным иммунитетом и/или которые не отвечают, вероятно не отвечают и/или для которых предсказано, что они не ответят или не ответят в течение определенного времени и/или до некоторой степени на лечение клеточной терапией, например, дозой Т-клеток (например, CAR+ Т-клеток). В некоторых вариантах осуществления дополнительный терапевтический агент вводят пациентам, которые не дают или для которых маловероятно или не предсказано полного ответа или общего ответа, например, в течение 1 месяца, в течение двух месяцев или в течение трех месяцев после инициации введения клеточной терапии. В некоторых вариантах осуществления дополнительный терапевтический агент вводят пациентам, которые показывают или вероятно покажут или для которых предсказана прогрессия заболевания (PD), например, в течение 1 месяца, двух месяцев или трех месяцев после введения клеточной терапии. В некоторых вариантах осуществления для пациента вероятно или предсказано отсутствие ответа или некоторого ответа на основе множества подобных пациентов, получающих или ранее получавших такую же клеточную терапию.
[0692] В некоторых вариантах осуществления замечено, что пациент, который может показать или более вероятно покажет плохой ответ на клеточную терапию, например, дозу Т-клеток (например, CAR+ Т-клеток), включает пациента с NHL, который является или был идентифицирован как имеющий стабильное или прогрессирующее заболевание (SD/PD) после лечения предшествующей терапией, необязательно предшествующей терапией химиотерапевтическим агентом, который является или был идентифицирован как имеющий статус 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG), который является или был идентифицирован как имеющий трансформированную фолликулярную лимфому (tFL), или который является или был идентифицирован как имеющий DLBCL, трансформированную из MZL и CLL. В некоторых вариантах осуществления способы по изобретению включают отбор пациента, который является или, вероятно, покажет плохой ответ на клеточную терапию, когда клеточную терапию вводят индивидуально, и введение клеточной терапии в комбинации с дополнительным агентом или терапии, такой как любая, как описано. В некоторых вариантах осуществления пациентом для лечения в способах комбинированной терапии по изобретению является пациент, выбранный как имеющий В-клеточную злокачественную опухоль, такую как NHL, и который имеет стабильное или прогрессирующее заболевание (SD/PD) после лечения предшествующей терапией, необязательно предшествующей терапией химиотерапевтическим агентом, имеющий статус 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG), который имеет трансформированную фолликулярную лимфому (tFL), или DLBCL, трансформированную из MZL и CLL. В некоторых вариантах осуществления дополнительный агент или терапия могут быть введены до, сопутствующе с или одновременно и/или после инициации введения клеточной терапии, например, дозы Т-клеток (например, CAR+ Т-клеток).
[0693] В некоторых вариантах осуществления обнаружено, что фармакокинетика (PK) клеточной терапии в крови пациентов после введения клеточной терапии подобна или существенно не отличается между пациентами, отвечающими (например, показывающими CR или OR) по сравнению с не отвечающими (например, показывающими PD) на клеточную терапию. В некоторых вариантах осуществления такие наблюдения показывают, что клеточная терапия имеет или расширяется у пациента, но может не показывать оптимальную эффективность.
[0694] В некоторых контекстах оптимальная эффективность клеточной терапии может зависеть от способности вводимых клеток распознавать и связываться с мишенью, например, антигеном-мишенью, для переноса, локализации и успешного вхождения в адекватные сайты у пациента, в опухолях и их средах. В некоторых контекстах оптимальная эффективность может зависеть от способности вводимых клеток становиться активированными, расти, проявлять различные эффекторные функции, включая цитотоксическое уничтожение и секрецию различных факторов, таких как цитокины, для персистирования, включая долгосрочное, дифференцировки, перехода или участия в перепрограммировании в определенные фенотипические состояния (такие как долговременной памяти, менее дифференцированное и эффекторное состояние), избегать или уменьшать иммунодепрессивные состояния в местной микросреде заболевания, для обеспечения эффективных и сильных вторичных иммунных ответов после клиренса и повторной экспозиции к целевому лиганду или антигену, и избегать или уменьшать истощение, анергию, периферическую толерантность, терминальную дифференцировку и/или дифференцировку в супрессивное состояние.
[0695] В некоторых аспектах эффективность иммунотерапии, например, Т-клеточной терапии, может быть ограничена иммунодепрессивной активностью или факторами, присутствующими в местной микросреде заболевания или нарушения, например, TME. В некоторых аспектах TME содержит или продуцирует факторы или состояния, которые могут подавлять активность, функцию, пролиферацию, выживаемость и/или персистирование Т-клеток, введенных для Т-клеточной терапии.
[0696] В некоторых вариантах осуществления введение дополнительного агента или терапии до, сопутствующе с или одновременно и/или после инициации введения клеточной терапии, например, дозы Т-клеток (например, CAR+ Т-клеток), может приводить к улучшенной активности, эффективности и/или персистированию клеточной терапии и/или улучшению ответа получающего лечение пациента. В некоторых вариантах осуществления дополнительный агент для комбинированное лечение или комбинированная терапия усиливает, повышает и/или промотирует эффективность и/или безопасность терапевтического эффекта клеточной терапии, например, генно-инженерной Т-клеточной терапии, такой как CAR+ Т-клетки. В некоторых вариантах осуществления дополнительный агент усиливает или усиливает эффективность, выживаемость или персистирование введенных клеток, например, клеток, экспрессирующих рекомбинантный рецептор, например, CAR.
[0697] В некоторых вариантах осуществления дополнительный агент терапии является антителом или цитотоксическим или терапевтическим агентом, например, химиотерапевтическим агентом. В некоторых вариантах осуществления один или более дополнительных агентов для лечения или терапии являются иммуномодулирующим агентом, ингибитором иммунной контрольной точки, сигнальным путем аденозина или антагонистом или агонистом рецептора аденозина и ингибиторами киназы. В некоторых вариантах осуществления лечение комбинацией или комбинированная терапия включает последующую обработку, такую как хирургическое лечение, пересадка и/или радиационная терапия.
[0698] В некоторых вариантах осуществления дополнительный агент выбран из числа ингибитора протеинфосфатазы, ингибитора киназы, цитокина, иммуномодулятора или агента, уменьшающего уровень или активность регуляторных T (Treg) клеток. В некоторых вариантах осуществления дополнительный агент усиливает безопасность на основании ослабления или улучшения неблагоприятных эффектов введенной клеточной терапии. В некоторых вариантах осуществления дополнительный агент может лечить то же заболевание, состояние или сопутствующую патологию. В некоторых вариантах осуществления дополнительный агент может облегчать, уменьшать или устранять одну или более токсичностей, неблагоприятные эффекты или побочные эффекты, связанные с введением клеток, например, CAR-экспрессирующих клеток.
[0699] В некоторых вариантах осуществления дополнительная терапия, лечение или агент включает химиотерапию, радиационную терапию, хирургию, трансплантацию, адоптивную клеточную терапию, антитела, цитотоксические агенты, химиотерапевтические агенты, цитокины, подавляющие рост агенты, антигормональные агенты, ингибиторы киназы, антиангиогенные агенты, кардиопротекторы, иммуностимулирующие вещества, иммунодепрессанты, ингибиторы иммунной контрольной точки, антибиотики, ингибиторы ангиогенеза, метаболические модуляторы или другие терапевтические агенты или любую их комбинацию. В некоторых вариантах осуществления дополнительный агент является белком, пептидом, нуклеиновой кислотой, веществом малой молекулы, клеткой, токсином, липидом, углеводом или их комбинациями, или любым другим типом терапевтического агента, например, облучением. В некоторых вариантах осуществления дополнительная терапия, агент или лечение включает хирургию, химиотерапию, радиационную терапию, трансплантацию, введение клеток, экспрессирующих рекомбинантный рецептор, например, CAR, ингибитор киназы, ингибитор иммунной контрольной точки, ингибитор пути mTOR, иммунодепрессанты, иммуномодуляторы, антитела, иммунодеструктивные агенты, антитела и/или их антигенсвязывающие фрагменты, конъюгаты антител, другие способы лечения антителами, цитотоксины, стероиды, цитокины, пептидные вакцины, гормональную терапию, антиметаболиты, метаболические модуляторы, лекарственные средства, ингибирующие либо кальцийзависимую кальциневрин фосфатазу, либо p70S6 киназу FK506, или ингибирующие p70S6 киназу, алкилирующие агенты, антрациклины, алкалоиды барвинка, ингибиторы протеосомы, агонисты GITR, ингибиторы протеинтирозин фосфатазы, ингибиторы протеинкиназы, онколитический вирус и/или другие типы иммунотерапии. В некоторых вариантах осуществления дополнительный агент или лечение представляют собой трансплантацию костного мозга, абляционную Т-клеточную терапию с использованием агентов для химиотерапии, таких как флударабин, наружную дистанционную радиационную терапию (XRT), циклофосфамид и/или антительную терапию.
[0700] В некоторых вариантах осуществления дополнительный агент является ингибитором киназы, например, ингибитором тирозин киназы Брутона (Btk), например, ибрутинибом. В некоторых вариантах осуществления дополнительный агент является антагонистом или агонистом пути аденозина или рецептора аденозина. В некоторых вариантах осуществления дополнительный агент является иммуномодулятором, таким как талидомид или производное талидомида (например, леналидомид). В некоторых вариантах осуществления дополнительная терапия, агент или средство для лечения представляет собой цитотоксический агент или агент для химиотерапии, биологической терапии (например, антитело, например, моноклональное антитело или клеточная терапия) или ингибитор (например, ингибитор киназы).
[0701] В некоторых вариантах осуществления дополнительный агент является химиотерапевтическим агентом. Примеры химиотерапевтических агентов включают антрациклин (например, доксорубицин, такой как липосомальный доксорубицин); алкалоид барвинка (например, винбластин, винкристин, виндезин, винорелбин); алкилирующий агент (например, циклофосфамид, декарбазин, мелфалан, ифосфамид, темозоломид); антитело к иммунной клетке (например, алемтузумаб, гемтузумаб, ритуксимаб, тозитумомаб); антиметаболит (включая, например, антагонисты фолиевой кислоты, аналоги пиримидина, аналоги пурина и ингибиторы аденозин деаминазы, такие как флударабин); агонист TNFR глюкокортикоид-индуцированного TNFR-связанного белка (GITR); ингибитор протеасомы (например, аклациномицин A, глиотоксин или бортезомиб); иммуномодулятор, такой как талидомид или производное талидомида (например, леналидомид).
[0702] В некоторых вариантах осуществления дополнительный агент является иммуномодулирующим агентом. В некоторых вариантах осуществления комбинированная терапия включает иммуномодулирующий агент, который может стимулировать, усиливать и/или иначе улучшать противоопухолевый иммунный ответ, например, противоопухолевый иммунный ответ от введенных генно-инженерных клеток, например, путем ингибирования трансдукции иммунодепрессивных сигналов или улучшения трансдукции иммуностимулирующих сигналов. В некоторых вариантах осуществления иммуномодулирующий агент является пептидом, белком или является малой молекулой. В некоторых вариантах осуществления белок может быть слитым белком или рекомбинантным белком. В некоторых вариантах осуществления иммуномодулирующий агент связывается с иммунологической мишенью, такой как рецептор поверхности клеток, экспрессируемый на иммунных клетках, таких как Т-клетки, В-клетки или антигенпредставляющие клетки. Например, в некоторых вариантах осуществления, иммуномодулирующий агент является антителом или антигенсвязывающим фрагментом антитела, слитым белком, малой молекулой или полипептидом. В некоторых вариантах осуществления связывающие молекулы, рекомбинантные рецепторы, клетки и/или композиции вводят в комбинации с дополнительным агентом, который является антителом или его антигенсвязывающим фрагментом, таким как моноклональное антитело.
[0703] В некоторых вариантах осуществления, иммуномодулирующий агент блокирует, ингибирует или противодействует компоненту пути иммунной контрольной точки. Иммунная система имеет множественные ингибирующие пути, участвующие в поддержание аутотолерантности и в модуляции иммунных ответов. Опухоли могут использовать некоторые пути иммунной контрольной точки в качестве главного механизма иммунитета, особенно против Т-клеток, которые являются специфичными для антигенов опухоли (Pardoll (2012) Nature Reviews Cancer 12:252-264), например, генно-инженерных клеток, таких как CAR-экспрессирующие клетки. Поскольку много таких иммунных контрольных точек инициируются взаимодействиями лиганд-рецептор, они могут быть легко заблокированы антителами к лигандам и/или их рецепторам. В отличие от большинства противораковых агентов, ингибиторы контрольной точки не обязательно нацеливаются непосредственно на опухолевые клетки, а нацеливаются на рецепторы лимфоцита или их лиганды для улучшения эндогенной противоопухолевой активности иммунной системы.
[0704] В некоторых вариантах осуществления дополнительный агент является иммуномодулирующим агентом, который является антагонистической молекулой или является ингибитором иммунной контрольной точки, способным ингибировать или блокировать функцию молекулы или сигнального пути, включая молекулу иммунной контрольной точки. В некоторых вариантах осуществления молекула иммунной контрольной точки или пути представляет собой PD-1, PD-L1, PD-L2, CTLA-4, LAG-3, TIM3, VISTA, рецептор аденозина 2А (A2AR) или аденозин, или путь, включающий любой из перечисленных. В некоторых вариантах осуществления антагонистические молекулы, блокирующие путь иммунной контрольной точки, такие как малые молекулы, ингибиторы нуклеиновой кислоты (например, РНКi) или молекулы антитела, становятся многообещающими средствами для иммунотерапии рака и других заболеваний.
[0705] В некоторых вариантах осуществления ингибитор иммунной контрольной точки является молекулой, полностью или частично уменьшающей, ингибирующей, препятствующей или модулирующей один или более белков контрольной точки. Белки контрольной точки регулируют Т-клеточную активацию или функцию. Эти белки ответственны за костимулирующие или подавляющие взаимодействия Т-клеточных ответов. Белки иммунной контрольной точки регулируют и поддерживают аутотолерантность и продолжительность и амплитуду физиологических иммунных ответов.
[0706] Ингибиторы иммунной контрольной точки включают любой агент, блокирующий или ингибирующий статистически значимым образом ингибирующие пути иммунной системы. Такие ингибиторы могут включать ингибиторы малые молекулы или могут включать антитела или их антигенсвязывающие фрагменты, связывающиеся с и блокирующие или ингибирующие рецепторы иммунной контрольной точки, лиганды и/или взаимодействие рецептор-лиганд. В некоторых вариантах осуществления модуляция, улучшение и/или стимуляция определенных рецепторов могут преодолеть компоненты пути иммунной контрольной точки. Иллюстративные молекулы иммунной контрольной точки, которые могут быть нацелены для блокирования, ингибирования, модуляции, улучшения и/или стимуляции, включают, но не ограничены ими, PD-1 (CD279), PD-L1 (CD274, B7-H1), PDL2 (CD273, B7-DC), CTLA-4, LAG-3 (CD223), TIM-3, 4-1BB (CD137), 4-1BBL (CD137L), GITR (TNFRSF18, AITR), CD40, OX40 (CD134, TNFRSF4), CXCR2, опухоль-ассоциированные антигены (TAA), B7-H3, B7-H4, BTLA, HVEM, GAL9, B7H3, B7H4, VISTA, KIR, 2B4 (принадлежит семейству CD2 молекул и экспрессируется на всех NK, γδ и памяти CD8+ (αβ) Т-клетках), CD160 (также называемый BY55), CGEN-15049, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), TIGIT, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), KIR, A2aR, MHC класса I, MHC класса II, GAL9, аденозин и рецептор трансформирующего фактора роста (TGFR; например, бета TGFR). Ингибиторы иммунной контрольной точки включают антитела или их антигенсвязывающие фрагменты или другие связывающие белки, связывающиеся с и блокирующие или ингибирующие и/или улучшающие или стимулирующие активность одной или более из упомянутых молекул.
[0707] Примеры ингибиторов иммунной контрольной точки включают тремелимумаб (блокирующее антитело CTLA-4, также известное как тицилимумаб, CP-675,206), анти-OX40, моноклональное антитело PD-L1 (Анти-B7-H1; MEDI4736), MK-3475 (блокатор PD-1), ниволумаб (антитело анти-PD-1), CT-011 (антитело анти-PD-1), моноклональное антитело BY55, AMP224 (антитело анти-PD-L1), BMS-936559 (антитело анти-PD-L1), MPLDL3280A (антитело анти-PD-L1), MSB0010718C (антитело анти-PD-L1) и ипилимумаб (анти-CTLA-4 антитело, также известное как Yervoy®, MDX-010 и MDX-101). Примеры иммуномодулирующих антител включают, но не ограничены ими, даклизумаб (Zenapax), бевацизумаб (Avastin ®), базиликсимаб, ипилимумаб, ниволумаб, пембролизумаб, MPDL3280A, пидилизумаб (CT-011), MK-3475, BMS-936559, MPDL3280A (атезолизумаб), тремелимумаб, IMP321, BMS-986016, LAG525, урелумаб, PF-05082566, TRX518, MK-4166, дацетузумаб (SGN-40), лукатумумаб (HCD122), SEA-CD40, CP-870, CP-893, MEDI6469, MEDI6383, MOXR0916, AMP 224, MSB0010718C (Avelumab), MEDI4736, PDR001, rHIgM12B7, улокуплумаб, BKT140, варлилумаб (CDX-1127), ARGX-110, MGA271, лирилумаб (BMS-986015, IPH2101), IPH2201, ARGX-115, эмактузумаб, CC-90002 и MNRP1685A или их антитело-связывающий фрагмент. Другие примеры иммуномодуляторов включают, например, афутузумаб (доступный от Roche®); пегфилграстим (Neulasta®); леналидомид (CC-5013, Revlimid®); талидомид (Thalomid®), актимид (CC4047); и IRX-2 (смесь человеческих цитокинов, включая интерлейкин 1, интерлейкин 2 и интерферон-гамма, CAS 951209-71-5, доступный от IRX Therapeutics).
[0708] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, связывающимся с и/или ингибирующим Запрограмированную гибель клеток 1 (PD-1). PD-1 является белком иммунной контрольной точки, экспрессирующимся в В-клетках, NK клетках и Т-клетких (Shinohara et al., 1995, Genomics 23:704-6; Blank et al., 2007, Cancer Immunol Immunother 56:739-45; Finger et al., 1997, Gene 197:177-87; Pardoll (2012) Nature Reviews Cancer 12:252-264). Главная роль PD-1 заключается в ограничении активности Т-клеток в периферических тканях во время воспаления в ответ на инфекцию, а также в ограничении аутоиммунитета. Экспрессия PD-1 индуцируется в активированных Т-клетких, и связывание PD-1 с одним из его эндогенных лигандов ингибирует Т-клеточную активацию путем ингибирования стимулирующих киназ. PD-1 также ингибирует TCR “стоп-сигнал”. PD-1 высоко экспрессируется на клетках Treg и может увеличить их пролиферацию в присутствии лиганда (Pardoll (2012) Nature Reviews Cancer 12:252-264). АнтиPD-1 антитело использовалось для лечения меланомы, немелкоклеточного рака легких, рака мочевого пузыря, рака предстательной железы, рака ободочной и прямой кишки, рака головы и шеи, трижды негативного рака молочной железы, лейкоза, лимфомы и почечно-клеточного рака (Topalian et al., 2012, N Engl J Med 366:2443-54; Lipson et al., 2013, Clin Cancer Res 19:462-8; Berger et al., 2008, Clin Cancer Res 14:3044-51; Gildener-Leapman et al., 2013, Oral Oncol 49:1089-96; Menzies & Long, 2013, Ther Adv Med Oncol 5:278-85). Примеры антител анти-PD-1 включают ниволумаб (Opdivo, BMS), пембролизумаб (Keytruda, Merck), пидилизумаб (CT-011, Cure Tech), ламбролизумаб (MK-3475, Merck) и AMP 224 (Merck), ниволумаб (также называемый Opdivo, BMS-936558 или MDX1106; Bristol-Myers Squibb), полностью человеческое моноклональное антитело IgG4, специфично блокирующее PD-1. Ниволумаб (клон 5C4) и другие человеческие моноклональные антитела, специфично связывающиеся с PD-1, описаны в US 8,008,449 и WO2006/121168. Пидилизумаб (CT-011; Cure Tech) представляет собой гуманизированное моноклональное антитело IgG1k, связывающееся с PD-1. Пидилизумаб и другие гуманизированные моноклональные антитела анти-PD-1 описаны в WO2009/101611. Пембролизумаб (раньше известный как ламбролизумаб, и также называемый Keytruda, MK03475; Merck) представляет собой гуманизированное моноклональное антитело IgG4, связывающееся с PD-1. Пембролизумаб и другие гуманизированные антитела анти-PD-1 описаны в US 8,354,509 и WO2009/114335. Другие антитела анти-PD-1 включают AMP 514 (Amplimmune), среди прочих, например, антитела анти-PD-1, описанные в US 8,609,089, US 2010028330, US 20120114649 и/или US 20150210769. AMP 224 (B7-DCIg; Amplimmune; например, описанный в WO2010/027827 и WO2011/066342) представляет собой PD-L2 Fc слитый растворимый рецептор, блокирующий взаимодействие между PD-1 и B7-H1.
[0709] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению, и/или с использованием изделий или композиций по изобретению, является агентом, связывающимся с или ингибирующим PD-L1 (также известный как CD274 и B7-H1) и/или PD-L2 (также известный как CD273 и B7-DC). PD-L1 и PD-L2 являются лигандами для PD-1, обнаруживаемыми на активированных Т-клетких, В-клетках, миелоидных клетках, макрофагах и некоторых типах опухолевых клеток. Противоопухолевые терапии сосредоточены на антителах анти-PD-L1. Комплекс PD-1 и PD-L1 ингибирует пролиферацию CD8+ Т-клеток и уменьшают иммунный ответ (Topalian et al., 2012, N Engl J Med 366:2443-54; Brahmer et al., 2012, N Eng J Med 366:2455-65). Антитела анти-PD-L1 использовались для лечения немелкоклеточного рака легких, меланомы, рака ободочной и прямой кишки, почечно-клеточного рака, рака поджелудочной железы, рака желудка, рака яичника, рака молочной железы и гематологических злокачественных опухолей (Brahmer et al., 2012, N Eng J Med 366:2455-65; Ott et al., 2013, Clin Cancer Res 19:5300-9; Radvanyi et al., 2013, Clin Cancer Res 19:5541; Menzies & Long, 2013, Ther Adv Med Oncol 5:278-85; Berger et al., 2008, Clin Cancer Res 14:13044-51). Примеры антител анти-PD-L1 включают MDX-1105 (Medarex), MEDI4736 (Medimmune) MPDL3280A (Genentech), BMS-935559 (Bristol-Myers Squibb) и MSB0010718C. MEDI4736 (Medimmune) является человеческим моноклональным антителом, связывающимся с PD-L1 и ингибирующим взаимодействие лиганда с PD-1. MDPL3280A (Genentech/Roche) является моноклональным человеческим Fc оптимизированным антителом IgG1, связывающимся с PD-L1. MDPL3280A и другие человеческие моноклональные антитела PD-L1 описаны в Публикации Патентов США No. 20120039906 и No. 7,943,743. Другие связывающие вещества анти-PD-L1 включают YW243,55. S70 (см. WO2010/077634), и MDX-1105 (также называемый BMS-936559, и, например, связывающие вещества анти-PD-L1, описанные в WO2007/005874).
[0710] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, который является ингибитором цитотоксического T-лимфоцит-ассоциированного антигена (CTLA-4), также известного как CD152, или связывается с CTLA-4. CTLA-4 является ко-ингибирующей молекулой, которая регулирует Т-клеточную активацию. CTLA-4 является членом суперсемейства иммуноглобулина, экспрессирующегося исключительно на Т-клетких. CTLA-4 ингибирует Т-клеточную активацию, и сообщается, что он ингибирует Т-хелперную активность и усиливает регуляторную Т-клеточную иммунодепрессивную активность. Несмотря на то, что точный механизм действия CTLA-4 остается невыясненным, предполагается, что он ингибирует активацию Т-клеток путем вытеснения CD28 в связывании с CD80 и CD86, а также активно поставляя ингибирующие сигналы в Т-клетку (Pardoll (2012) Nature Reviews Cancer 12:252-264). Антитела анти-CTLA-4 использовались в клинических испытаниях для лечения меланомы, рака предстательной железы, мелкоклеточного рака легких, немелкоклеточного рака легких (Robert & Ghiringhelli, 2009, Oncologist 14:848-61; Ott et al., 2013, Clin Cancer Res 19:5300; Weber, 2007, Oncologist 12:864-72; Wada et al., 2013, J Transl Med 11:89). Существенным признаком анти-CTLA-4 является кинетика противоопухолевого эффекта с периодом задержки до 6 месяцев после начального лечения, которое потребовалось для физиологического ответа. В некоторых случаях опухоли могут фактически увеличиться в размере после инициации лечения, прежде чем будет замечено уменьшение (Pardoll (2012) Nature Reviews Cancer 12:252-264). Примеры анти-CTLA-4 антител включают ипилимумаб (Bristol-Myers Squibb) и тремелимумаб (Pfizer). Ипилимумаб недавно получил апробацию FDA для лечения метастатической меланомы (Wada et al., 2013, J Transl Med 11:89).
[0711] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, который связывается с и/или ингибирует ген активации лимфоцитов 3 (LAG-3), также известный как CD223. LAG-3 является другим белком иммунной контрольной точки. LAG-3 был ассоциирован с ингибированием активности лимфоцитов и в некоторых случаях индукции анергии лимфоцитов. LAG-3 экспрессируется на различных клетках в иммунной системе, включая В-клетки, NK клетках и дендритных клетках. LAG-3 является естественным лигандом для рецептора MHC класса II, по существу экспрессирующегося на инфильтрирующих меланому Т-клетких, включая обеспеченных мощной иммунно-подавляющей активностью. Примеры антител анти-LAG-3 включают BMS-986016 (Bristol-Myers Squib), который является моноклональным антителом, нацеливаемым на LAG-3. IMP701 (Immutep) является антагонистическим антителом LAG-3, и IMP731 (Immutep и GlaxoSmithKline) является антителом, истощающим LAG-3. Другие ингибиторы LAG-3 включают IMP321 (Immutep), который является рекомбинантным слитым белком растворимой части LAG-3 и Ig, связывающимся с молекулами MHC класса II и активирующими антигенпредставляющие клетки (APC). Другие антитела описаны, например, в WO2010/019570 и US 2015/0259420.
[0712] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, который связывается с и/или ингибирует Т-клеточный иммуноглобулиновый домен и муциновый домен-3 (TIM-3). TIM-3 был первоначально идентифицирован на активированных клетках Th1 и, как было показано, был отрицательным регулятором иммунного ответа. Блокада TIM-3 опосредует промотируемый Т-клетками противоопухолевый иммунитет и имеет противоопухолевую активность в различных моделях опухоли мыши. Комбинации блокады TIM-3 с другими иммунотерапевтическими агентами, такими как TSR-042, антитела анти-CD137 и другие, могут аддитивно или синергически усиливать противоопухолевые эффекты. Экспрессия TIM-3 была ассоциирована со многими различными типами опухоли, включая меланому, NSCLC и почечный рак, и дополнительно было показано, что экспрессия внутриопухолевого TIM-3 коррелировала с неблагоприятным прогнозом при различных типах опухоли, включая NSCLC, рак шейки матки и рак желудка. Блокада TIM-3 также представляет интерес в свете промотирования увеличенного иммунитета ко многим хроническим вирусным заболеваниям. Также было показано, что TIM-3 взаимодействовал со многими лигандами, включая галектин-9, фосфатидилсерин и HMGB1, несмотря на то, что в настоящее время не ясно, которые из них, если таковые имеются, релевантны в регуляции антиканцерогенных эффектов. В некоторых вариантах осуществления антитела, фрагменты антител, малые молекулы или пептидные ингибиторы, нацеливающиеся на TIM-3, могут связываться с доменом IgV TIM-3, ингибируя взаимодействия с его лигандами. Примеры антител и пептидов, ингибирующих TIM-3, описаны в US 2015/0218274, WO2013/006490 и US 2010/0247521. Другие анти-TIM-3 антитела включают гуманизированные версии RMT3-23 (Ngiow et al., 2011, Cancer Res, 71:3540-3551), and clone 8B,2C12 (Monney et al., 2002, Nature, 415:536-541). Биспецифические антитела, ингибирующие TIM-3 и PD-1, описаны в US 2013/0156774.
[0713] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, который является ингибитором CEACAM (например, CEACAM-1, CEACAM-3 и/или ингибитор CEACAM-5). В некоторых вариантах осуществления ингибитор CEACAM является молекулой антитела анти-CEACAM. Примеры анти-CEACAM-1 антител описаны в WO 2010/125571, WO 2013/082366, WO 2014/059251 и WO 2014/022332, например, моноклональное антитело 34B1, 26H7 и 5F4; или его рекомбинантная форма, как описано в, например, US 2004/0047858, US 7,132,255 и WO 99/052552. В некоторых вариантах осуществления анти-CEACAM антитело связывается с CEACAM-5, как описано в, например, Zheng et al. PLoS One. (2011) 6(6): e21146), или перекрестно реагирует с CEACAM-1 и CEACAM-5, как описано в, например, WO 2013/054331 и US 2014/0271618.
[0714] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, связывающимся с и/или ингибирующим 4-1BB, также известным как CD137. 4-1BB представляет собой трансмембранный гликопротеин, принадлежащий суперсемейству TNFR. 4-1BB рецепторы присутствуют на активированных Т-клетких и В-клетках и моноцитах. Примером анти-4-1BB антитела является урелумаб (BMS-663513), который имеет потенциальные иммуностимулирующие и противоопухолевые активности.
[0715] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, связывающимся с и/или ингибирующим суперсемейство рецептора фактора некроза опухоли, член 4 (TNFRSF4), также известного как OX40 и CD134. TNFRSF4 является другим членом суперсемейства TNFR. OX40 не экспрессируется конститутивно на интактных Т-клетках в состоянии покоя и действует как вторичная костимулирующая молекула иммунной контрольной точки. Примерами антитела анти-OX40 являются MEDI6469 и MOXR0916 (RG7888, Genentech).
[0716] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом или молекулой, уменьшающей популяцию регуляторных Т-клеток (Treg). Способы, сокращающие число (например, истощающие) клетки Treg, известны в уровне техники и включают, например, истощение CD25, введение циклофосфамида и модуляцию функции глюкокортикоид-индуцированного относящегося к семейтсву TNFR гена (GITR). GITR является членом суперсемейства TNFR, регулирующегося положительно на активированных Т-клетках, который усиливает иммунную систему. Сокращение количества клеток Treg у пациента до афереза или до введения генно-инженерных клеток, например, CAR-экспрессирующих клеток, может сократить количество нежелательных иммунных клеток (например, Tregs) в микросреде опухоли и снижает риск рецидива у пациента. В некоторых вариантах осуществления дополнительный агент включает молекулу, нацеливаемую на GITR и/или модулирующую функции GITR, такую как агонист GITR и/или антитело GITR, истощающее регуляторные Т-клетки (Tregs). В некоторых вариантах осуществления дополнительный агент включает циклофосфамид. В некоторых вариантах осуществления GITR связывающую молекулу и/или молекулу, модулирующую функцию GITR (например, агонист GITR и/или Treg истощающие антитела GITR), вводят до генно-инженерных клеток, например, CAR-экспрессирующих клеток. Например, в некоторых вариантах осуществления, агонист GITR может быть введен до афереза клеток. В некоторых вариантах осуществления циклофосфамид вводят пациенту до введения (например, вливания или повторного вливания) генно-инженерных клеток, например, CAR-экспрессирующих клеток или до афереза клеток. В некоторых вариантах осуществления циклофосфамид и анти-GITR антитело вводят пациенту до введения (например, вливания или повторного вливания) генно-инженерных клеток, например, CAR-экспрессирующих клеток или до афереза клеток.
[0717] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, который является агонистом GITR. Примеры агонистов GITR включают, например, слитые белки GITR и анти-GITR антитела (например, бивалентные анти-GITR антитела), такие как, например, слитый белок GITR, описанный в Патенте США No. 6,111,090, Европейском патенте No. 090505 B1, Патенте США No. 8,586,023, Публикациях PCT: WO 2010/003118 и 2011/090754, или анти-GITR антитело, описанное, например, в Патенте США No. 7,025,962, Европейском патенте No. 1947183 B1, Патенте США No. 7,812,135, Патенте США No. 8,388,967, Патенте США No. 8,591,886, Европейском патенте номер EP 1866339, Публикации PCT WO 2011/028683, Публикации PCT WO 2013/039954, Публикации PCT WO2005/007190, Публикации PCT WO 2007/133822, Публикации PCT WO2005/055808, Публикации PCT WO 99/40196, Публикации PCT WO 2001/03720, Публикации PCT WO99/20758, Публикации PCT WO2006/083289, Публикации PCT WO 2005/115451, Патенте США No. 7,618,632 и Публикации PCT WO 2011/051726. Примером анти-GITR антитела является TRX518.
[0718] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, усиливает инфильтрацию опухоли или миграцию введенных клеток, например, CAR-экспрессирующих клеток. Например, в некоторых вариантах осуществления, дополнительный агент стимулирует CD40, такой как CD40L, например, рекомбинантный человеческий CD40L. Кластер дифференцировки 40 (CD40) является также членом суперсемейства TNFR. CD40 является костимулирующим белком, обнаруживаемым на антигенпредставляющих клетках, и опосредует широкий спектр иммунных и воспалительных ответов. CD40 также экспрессируется на некоторых злокачественных опухолях, где он вызывает пролиферацию. Примерами антитела анти-CD40 являются дацетузумаб (SGN-40), лукатумумаб (Novartis, антагонист), SEA-CD40 (Seattle Genetics) и CP-870,893. В некоторых вариантах осуществления дополнительный агент, улучшающий инфильтрацию опухоли, включает ингибитор тирозинкиназы сунитниб, гепараназу и/или рецепторы хемокина, такие как CCR2, CCR4 и CCR7.
[0719] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является иммуномодулирующим агентом, который является структурным или функциональным аналогом или производным талидомида и/или ингибитором убиквитин лигазы E3. В некоторых вариантах осуществления иммуномодулирующий агент связывается с цереблоном (CRBN). В некоторых вариантах осуществления иммуномодулирующий агент связывается с комплексом убиквитин лигазы CRBN E3. В некоторых вариантах осуществления иммуномодулирующий агент связывается с CRBN и комплексом убиквитин лигазы CRBN E3. В некоторых вариантах осуществления иммуномодулирующий агент повышающе регулирует белок или экспрессию гена CRBN. В некоторых аспектах CRBN является адаптером субстрата для CRL4CRBN E3 убиквитин лигазы и модулирует специфичность фермента. В некоторых вариантах осуществления связывание с CRB или комплексом CRBN E3 убиквитин лигазы ингибирует активность убиквитин лигазы E3. В некоторых вариантах осуществления иммуномодулирующий агент вызывает убиквитинилирование KZF1 (Ikaros) и IKZF3 (Aiolos) и/или вызывает разложение IKZF1 (Ikaros) и IKZF3 (Aiolos). В некоторых вариантах осуществления иммуномодулирующий агент вызывает убиквитинилирование казеин киназы 1A1 (CK1α) CRL4CRBN E3 убиквитин лигазой. В некоторых вариантах осуществления убиквитинилирование CK1α приводит к разложению CK1α.
[0720] В некоторых вариантах осуществления иммуномодулирующий агент является ингибитором транскрипционного фактора Ikaros (IKZF1). В некоторых вариантах осуществления иммуномодулирующий агент усиливает убиквитинилирование Ikaros. В некоторых вариантах осуществления иммуномодулирующий агент усиливает разложение Ikaros. В некоторых вариантах осуществления иммуномодулирующий агент понижающе регулирует белок или экспрессию гена Ikaros. В некоторых вариантах осуществления введение иммуномодулирующего агента вызывает уменьшение содержания белка Ikaros.
[0721] В некоторых вариантах осуществления иммуномодулирующий агент является ингибитором транскрипционного фактора Aiolos (IKZF3). В некоторых вариантах осуществления иммуномодулирующий агент усиливает убиквитинилирование Aiolos. В некоторых вариантах осуществления иммуномодулирующий агент усиливает разложение Aiolos. В некоторых вариантах осуществления иммуномодулирующий агент понижающе регулирует белок или экспрессию гена Aiolos. В некоторых вариантах осуществления введение иммуномодулирующего агента вызывает уменьшение содержания белка Aiolos.
[0722] В некоторых вариантах осуществления иммуномодулирующий агент является ингибитором транскрипционных факторов Ikaros (IKZF1) и Aiolos (IKZF3). В некоторых вариантах осуществления иммуномодулирующий агент усиливает убиквитинилирование как Ikaros, так и Aiolos. В некоторых вариантах осуществления иммуномодулирующий агент усиливает разложение как Ikaros, так и Aiolos. В некоторых вариантах осуществления иммуномодулирующий агент усиливает убиквитинилирование и разложение как Ikaros, так и Aiolos. В некоторых вариантах осуществления введение иммуномодулирующего агента приводит к уменьшению уровней обоих белков Aiolos и Ikaros.
[0723] В некоторых вариантах осуществления иммуномодулирующий агент является селективным цитокин-ингибирующим лекарственным средством (SelCID). В некоторых вариантах осуществления иммуномодулирующий агент ингибирует активность фосфодиэстеразы-4 (PDE4). В некоторых вариантах осуществления иммуномодулирующий агент подавляет ферментативную активность фосфатаз CDC25. В некоторых вариантах осуществления иммуномодулирующий агент изменяет внутриклеточный трафик фосфатаз CDC25.
[0724] В некоторых вариантах осуществления иммуномодулирующий агент является талидомидом (2-(2,6-диоксопиперидин-3-ил)-1H-изоиндол-1,3(2H)-дион) или аналогом или производным талидомида. В некоторых вариантах осуществления производное талидомида включает структурные варианты талидомида, имеющие подобную биологическую активность. Примеры производных талидомида включают, но не ограничены ими, леналидомид (REVLIMMUNOMODULATORY COMPOUND™; Celgene Corporation), помалидомид (также известный как ACTIMMUNOMODULATORY COMPOUND™ или POMALYST™ (Celgene Corporation)), CC-1088, CDC-501 и CDC-801, и соединения, раскрытые в патентах США 5,712,291; 7,320,991; и 8,716,315; заявке на патент США 2016/0313300; и Публ. PCT WO 2002/068414 и WO 2008/154252.
[0725] В некоторых вариантах осуществления иммуномодулирующий агент представляет собой 1-оксо- и 1,3-диоксо-2-(2,6-диоксопиперидин-3-ил)изоиндолины, замещенные амино в бензольном кольце, как описано в патенте США 5,635,517, включенном в настоящее описание ссылкой.
[0726] В некоторых вариантах осуществления иммуномодулирующий агент является соединением следующей формулы:
в которой один из X и Y обозначает -C(O)-, а другой X и Y обозначает -C(O)- или -CH2-, и R5 обозначает водород или низший алкил, или его фармацевтически приемлемой солью. В некоторых вариантах осуществления X обозначает -C(O)-, и Y обозначает -CH2-. В некоторых вариантах осуществления оба X и Y обозначают -C(O)-. В некоторых вариантах осуществления R5 обозначает водород. В других вариантах осуществления R5 обозначает метил.
[0727] В некоторых вариантах осуществления иммуномодулирующее соединение является соединением, принадлежащим к классу замещенных 2-(2,6-диоксопиперидин-3-ил)фталимидомодулирующих соединений и замещенных 2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолов, таких как описанные в патентах США 6,281,230; 6,316,471; 6,335,349; и 6,476,052 и Международной Заявке на патент No. PCT/US97/13375 (Международная Публикация WO 98/03502), каждый из которых включен в настоящее описание ссылкой.
[0728] В некоторых вариантах осуществления иммуномодулирующий агент является соединением следующей формулы:

в которой
один из X и Y обозначает -C(O)- и другой X и Y обозначает -C(O)- или -CH2-;
(1) каждый из R1, R2, R3 и R4 независимо обозначает галоген, алкил из 1-4 атомов углерода или алкокси из 1-4 атомов углерода, или
(2) один из R1, R3, R4 и R5 обозначает –NHRa, и остальные из R1, R2, R3 и R4 обозначают водород, причем Rа обозначает водород или алкил из 1-8 атомов углерода;
R5 обозначает водород или алкил из 1-8 атомов углерода, бензил или галоген;
при условии, что R5 отличается от водорода, если X и Y обозначают -C(O)- и (i) каждый из R1, R2, R3 и R4 обозначает фтор; или (ii) один из R1, R2, R3 и R4 обозначает амино;
или его фармацевтически приемлемой солью.
[0729] В некоторых вариантах осуществления иммуномодулирующий агент является соединением, принадлежащим к классу изоиндол-иммуномодулирующих соединений, раскрытых в патенте США No. 7,091,353, Публикации Патента США No. 2003/0045552 и Международной Заявке No. PCT/USOI/50401 (Международная Публикация No. WO02/059106), каждый из которых включен в настоящее описание ссылкой. Например, в некоторых вариантах осуществления, иммуномодулирующий агент представляет собой [2-(2,6-диоксо-пиперидин-3-ил)-1,3-диоксо-2,3-дигидро-1H-изоиндол-4-илметил]-амид; трет-бутиловый эфир (2-(2,6-диоксо-пиперидин-3-ил)-1,3-диоксо-2,3-дигидро-1H-изоиндол-4-илметил)-карбаминовой кислоты; 4-(аминометил)-2-(2,6-диоксо(3-пиперидил))-изоиндолин-1,3-дион; N-(2-(2,6-диоксо-пиперидин-3-ил)-1,3-диоксо-2,3-дигидро-1H-изоиндол-4-илметил)-ацетамид; N-{(2-(2,6-диоксо(3-пиперидил)-1,3-диоксоизоиндолин-4-ил)метил}циклопропил-карбоксамид; 2-хлор-N-{(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)метил}ацетамид; N-(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)-3-пиридилкарбоксамид; 3-{1-оксо-4-(бензиламино)изоиндолин-2-ил}пиперидин-2,6-дион; 2-(2,6-диоксо(3-пиперидил))-4-(бензиламино)изоиндолин-1,3-дион; N-{(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)метил}пропанамид; N-{(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)метил}-3-пиридилкарбоксамид; N-{(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)метил}гептанамид; N-{(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)метил}-2-фурилкарбоксамид; {N-(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)карбамоил}метилацетат; N-(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)пентанамид; N-(2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил)-2-тиенилкарбоксамид; N-{[2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил]метил}(бутиламино)карбоксамид; N-{[2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил]метил}(октиламино)карбоксамид; или N-{[2-(2,6-диоксо(3-пиперидил))-1,3-диоксоизоиндолин-4-ил]метил}(бензиламино)карбоксамид.
[0730] В некоторых вариантах осуществления иммуномодулирующий агент является соединением, принадлежащим к классу изоиндол-иммуномодулирующих соединений, раскрытых в Публикации Заявки на патент США No. 2002/0045643, Международной Публикации WO 98/54170, и патенте США No. 6,395,754, каждый из которых включен в настоящее описание ссылкой. В некоторых вариантах осуществления иммуномодулирующий агент является тетразамещенными 2-(2,6-диоксопиперидин-3-ил)-1-оксоизоиндолинами, описанными в патенте США No. 5,798,368, включенном в настоящее описание ссылкой. В некоторых вариантах осуществления иммуномодулирующий агент представляет собой 1-оксо и 1,3-диоксо-2-(2,6-диоксопиперидин-3-ил)изоиндолины, раскрытые в патенте США No. 6,403,613, включенном в настоящее описание ссылкой. В некоторых вариантах осуществления иммуномодулирующий агент является 1-оксо или 1,3-диоксоизоиндолином, замещенным в положении 4 или 5 индолинового кольца, как описано в патенте США No. 6,380,239 и патенте США No. 7,244,759, оба из которых включены в настоящее описание ссылкой.
[0731] В некоторых вариантах осуществления иммуномодулирующий агент представляет собой 2-(4-амино-1-оксо-1,3-дигидро-изоиндол-2-ил)-4-карбамоил-масляную кислоту или 4-(4-амино-1-оксо-1,3-дигидро-изоиндол-2-ил)-4-карбамоил-масляную кислоту. В некоторых вариантах осуществления иммуномодулирующее соединение представляет собой 4-карбамоил-4-{4-[(фуран-2-ил-метил)-амино]-1,3-диоксо-1,3-дигидро-изоиндол-2-ил}-масляную кислоту, 4-карбамоил-2-{4-[(фуран-2-ил-метил)-амино]-1,3-диоксо-1,3-дигидро-изоиндол-2-ил}-масляную кислоту, 2-{4-[(фуран-2-ил-метил)-амино]-1,3-диоксо-1,3-дигидро-изоиндол-2-ил}-4-фенилкарбамоил-масляную кислоту или 2-{4-[(фуран-2-ил-метил)-амино]-1,3-диоксо-1,3-дигидро-изоиндол-2-ил}-глутаровую кислоту.
[0732] В некоторых вариантах осуществления иммуномодулирующий агент представляет собой изоиндолин-1-он или изоиндолин-1,3-дион, замещенный в положении 2 2,6-диоксо-3-гидроксипиперидин-5-илом, как описано в патенте США No. 6,458,810, включенном в настоящее описание ссылкой. В некоторых вариантах осуществления иммуномодулирующее соединение представляет собой 3-(5-амино-2-метил-4-оксо-4H-хиназолин-3-ил)-пиперидин-2,6-дион или его энантиомер или смесь энантиомеров; или его фармацевтически приемлемую соль, сольват, гидрат, сокристалл, клатрат или полиморф. В некоторых вариантах осуществления иммуномодулирующее соединение представляет собой 3-[4-(4-морфолин-4-илметил-бензилокси)-1-оксо-1,3-дигидро-изоиндол-2-ил]-пиперидин-2,6-дион.
[0733] В некоторых вариантах осуществления иммуномодулирующий агент является таким, как описано в Oshima, K. et al., Nihon Rinsho., 72(6):1130-5 (2014); Millrine, D. et al., Trends Mol Med., 23(4):348-364 (2017); и Collins, et al., Biochem J., 474(7):1127-1147 (2017).
[0734] В некоторых вариантах осуществления иммуномодулирующий агент является леналидомидом, помалидомидом, авадомидом, стереоизомером леналидомида, помалидомида, авадомида или их фармацевтически приемлемой солью, сольватом, гидратом, сокристаллом, клатратом или полиморфом. В некоторых вариантах осуществления иммуномодулирующее соединение является леналидомидом, стереоизомером леналидомида или его фармацевтически приемлемой солью, сольватом, гидратом, сокристаллом, клатратом или полиморфом. В некоторых вариантах осуществления иммуномодулирующее соединение является леналидомидом или ((RS)-3-(4-Амино-1-оксо-1,3-дигидро-2H-изоиндол-2-ил)пиперидин-2,6-дионом).
[0735] В некоторых вариантах осуществления дополнительный агент включает лекарственные средства на основе талидомида или его аналогов и/или производных, таких как леналидомид, помалидомид или апремиласт. См., например, Bertilaccio et al., Blood (2013) 122:4171, Otahal et al., Oncoimmunology (2016) 5(4):e1115940; Fecteau et al., Blood (2014) 124(10):1637-1644 and Kuramitsu et al., Cancer Gene Therapy (2015) 22:487-495). Леналидомид ((RS)-3-(4-Амино-1-оксо-1,3-дигидро-2H-изоиндол-2-ил)пиперидин-2,6-дион; также известный как ревлимид) представляет собой синтетическое производное талидомида и имеет множественные иммуномодулирующие эффекты, включая осуществление формирования иммунного синапса между Т-клеткой и антигенпредставляющими клетками (APCs). Например, в некоторых случаях, леналидомид модулирует Т-клеточный ответ и приводит к увеличенной продукции интерлейкина (IL)-2 в CD4+ и CD8+ Т-клетках, вызывает изменение T хелперного (Th) ответа от Th2 до Th1, ингибирует увеличение субпопуляции регуляторных Т-клеток (Tregs) и усиливает функционирование иммунологических синапсов при фолликулярной лимфоме и хроническом лимфолейкозе (CLL) (Otahal et al., Oncoimmunology (2016) 5 (4): e1115940). Леналидомид также имеет непосредственную уничтожающую опухолевые клетки активность у пациентов со множественной миеломой (MM) и непосредственно и опосредованно модулирует выживаемость опухолевых клеток CLL путем воздействия на поддерживающие клетки, такие как nurse-like клетки, обнаруживаемые в микросреде лимфоидных тканей. Леналидомид также может усиливать Т-клеточную пролиферацию и продукцию интерферона-γ в ответ на активацию Т-клеток через лигирование CD3 или опосредуемую дендритными клетками активацию. Леналидомид может также побудить злокачественные В-клетки экспрессировать более высокие уровни иммуностимулирующих молекул, таких как CD80, CD86, HLA-DR, CD95 и CD40 (Fecteau et al., Blood (2014) 124(10):1637-1644). В некоторых вариантах осуществления леналидомид вводят в дозировке от приблизительно 1 мг до приблизительно 20 мг в сутки, например, от приблизительно 1 мг до приблизительно 10 мг, от приблизительно 2,5 мг до приблизительно 7,5 мг, от приблизительно 5 мг до приблизительно 15 мг, например, приблизительно 5 мг, 10 мг, 15 мг или 20 мг в сутки. В некоторых вариантах осуществления леналидомид вводят в дозе от приблизительно 10 мкг/кг до 5 мг/кг, например, от приблизительно 100 мкг/кг до приблизительно 2 мг/кг, от приблизительно 200 мкг/кг до приблизительно 1 мг/кг, от приблизительно 400 мкг/кг до приблизительно 600 мкг/кг, например, приблизительно 500 мкг/кг.
[0736] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, представляет собой В-клеточный ингибитор. В некоторых вариантах осуществления дополнительный агент является одним или более В-клеточными ингибиторами, выбранными из числа ингибиторов CD10, CD19, CD20, CD22, CD34, CD123, CD79a, CD79b, CD179b, FLT-3 или ROR1 или их комбинаций. В некоторых вариантах осуществления В-клеточный ингибитор является антителом (например, моно- или биспецифическим антителом) или его антигенсвязывающим фрагментом. В некоторых вариантах осуществления дополнительный агент является генно-инженерной клеткой, экспрессирующей рекомбинантные рецепторы, нацеливаемые на В-клеточные мишени, например, CD10, CD19, CD20, CD22, CD34, CD123, CD79a, CD79b, CD179b, FLT-3 или ROR1.
[0737] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является ингибитором CD20, например, антителом анти-CD20 (например, анти-CD20 моно- или биспецифическое антитело) или его фрагментом. Примеры антител анти-CD20 включают, но не ограничены ими, ритуксимаб, офатумомаб, окрелизумаб (также известный как GA101 или RO5072759), велтузумаб, обинутузумаб, TRU-015 (Trubion Pharmaceuticals), окаратузумаб (также известный как AME-133v или окаратузумаб) и Pro131921 (Genentech). См., например, Lim et al. Haematologica. (2010) 95(1):135-43. В некоторых вариантах осуществления антитело анти-CD20 включает ритуксимаб. Ритуксимаб является химерным моноклональным антителом мыши/человека каппа IgG1, связывающимся с CD20 и вызывающим цитолиз CD20-экспрессирующих клеток. В некоторых вариантах осуществления дополнительный агент включает ритуксимаб. В некоторых вариантах осуществления ингибитор CD20 является малой молекулой.
[0738] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является ингибитором CD22, например, антителом анти-CD22 (например, анти-CD22 моно- или биспецифическое антитело) или его фрагментом. Примеры антител анти-CD22 включают эпратузумаб и RFB4. В некоторых вариантах осуществления ингибитор CD22 является малой молекулой. В некоторых вариантах осуществления антитело является моноспецифическим антителом, необязательно конъюгированным со вторым агентом, таким как химиотерапевтический агент. Например, в некоторых вариантах осуществления, антитело является конъюгатом моноклональное антитело-MMAE анти-CD22 (например, DCDT2980S). В некоторых вариантах осуществления антитело является scFv антитела анти-CD22, например, scFv антитела RFB4. В некоторых вариантах осуществления scFv слит со всем или фрагментом экзотоксина-A Pseudomonas (например, BL22). В некоторых вариантах осуществления scFv слит со всем или фрагментом (например, фрагментом 38 килодальтонов) экзотоксина-A Pseudomonas (например, моксетумомаб пасудотокс). В некоторых вариантах осуществления антитело анти-CD22 представляет собой анти-CD19/CD22 биспецифическое антитело, необязательно конъюгированное с токсином. Например, в некоторых вариантах осуществления, антитело анти-CD22 включает анти-CD19/CD22 биспецифическую часть (например, два scFv лиганда, распознающих человеческий CD19 и CD22), необязательно связанный со всем или частью дифтерийного токсина (DT), например, первыми 389 аминокислотами дифтерийного токсина (DT), DT 390, например, лиганд-направленного токсина, такого как DT2219ARL). В некоторых вариантах осуществления биспецифическая часть (например, антиCD 19/анти-CD22) связана с токсином, таким как дегликозилированная рициновая цепь (например, Combotox).
[0739] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является цитокином или является агентом, вызывающим увеличенную экспрессию цитокинов в микросреде опухоли. Цитокины имеют важные функции, связанные с ростом, дифференцировкой, выживаемостью и гомеостазом Т-клеток. Цитокины, которые могут быть введены пациенту, получающему комбинированную терапию в способах или применениях по изобретению, рекомбинантные рецепторы, клетки и/или композиции, описанные здесь, включают один или более IL-2, IL-4, IL-7, IL-9, IL-15, IL-18 и IL-21. В некоторых вариантах осуществления вводимый цитокин является IL-7, IL-15 или IL-21 или их комбинацией. В некоторых вариантах осуществления введение цитокина пациенту, имеющему субоптимальный ответ на введение генно-инженерных клеток, например, CAR-экспрессирующих клеток, улучшает эффективность и/или противоопухолевую активность введенных клеток, например, CAR-экспрессирующих клеток.
[0740] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является цитокином, таким как белок, которые действуют на другую клетку как межклеточные медиаторы. Примерами таких цитокинов являются лимфокины, монокины и традиционные полипептидные гормоны. Среди цитокинов включены гормоны роста, такие как человеческий гормон роста, N-метионильный гормон роста человека и гормон роста крупного рогатого скота; паратиреоидный гормон; тироксин; инсулин; проинсулин; релаксин; прорелаксин; гликопротеиновые гормоны, такие как фолликулостимулирующий гормон (FSH), стимулирующий щитовидную железу гормон (TSH) и лютеинизирующий гормон (LH); печеночный фактор роста; фактор роста фибробластов; пролактин; плацентарный лактоген; фактор некроза опухоли альфа и бета; мюллеровская ингибирующая субстанция; пептид, ассоциированный с гонадотропином мыши; ингибин; активин; фактор роста сосудистого эндотелия; интегрин; тромбопоэтин (TPO); факторы роста нервов, такие как NGF-бета; фактор роста тромбоцитов; трансформирующие факторы роста (TGF), такие как TGF-альфа и TGF-бета; инсулиноподобный фактор-роста-I и -II; эритропоэтин (EPO); остеоиндуктивные факторы; интерфероны, такие как интерферон альфа, бета и гамма; колониестимулирующие факторы (CSF), такие как CSF макрофагов (M-CSF); CSF гранулоцитов-макрофагов (GM-CSF); и CSF гранулоцитов (G-CSF); интерлейкины (IL), такие как IL-1, IL-1альфа, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12; IL-15, фактор некроза опухоли, такой как TNF-альфа или TNF-бета; и другие полипептидные факторы, включая LIF и kit-лиганд (KL). В рамках изобретения термин цитокин включает белки из естественных источников или из рекомбинантной клеточной культуры и биологически активные эквиваленты нативных последовательностей цитокинов. Например, иммуномодулирующий агент является цитокином, и цитокин является IL-4, TNF-α, GM-CSF или IL-2.
[0741] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, включает полипептид интерлейкина 15 (IL-15), полипептид альфа-рецептора интерлейкина 15 (IL-15Rα) или их комбинацию, например, hetIL-15 (Admune Therapeutics, LLC). hetIL-15 является гетеродимерным нековалентным комплексом IL-15 и IL-15Rα. hetIL-15 описан в, например, US 8,124,084, US 2012/0177598, US 2009/0082299, US 2012/0141413 и US 2011/0081311. В некоторых вариантах осуществления иммуномодулирующий агент может содержать один или более цитокинов. Например, интерлейкин может включать инъекцию интерлейкина лейкоцитов (Multikine), который является комбинацией натуральных цитокинов.
[0742] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является модулятором уровней аденозина и/или компонентом пути аденозина. Аденозин может функционировать как иммуномодулирующий агент в организме. Например, аденозин и некоторые аналоги аденозина, неселективно активирующие подтипы рецептора аденозина, уменьшают продукцию нейтрофилами воспалительных окислительных продуктов (Cronstein et al., Ann. N.Y. Acad. Sci. 451:291, 1985; Roberts et al., Biochem. J., 227:669, 1985; Schrier et al., J. Immunol. 137:3284, 1986; Cronstein et al., Clinical Immunol. Immunopath. 42:76, 1987). В некоторых случаях концентрация внеклеточных аналогов аденозина или аденозина может увеличиться в определенных средах, например, микросреде опухоли (TME). В некоторых случаях сигнализация аналога аденозина или аденозина зависит от гипоксии или факторов, участвующих в гипоксии или ее регуляции, например, гипоксия-индуцируемый фактор (HIF). В некоторых вариантах осуществления увеличение трансдукции сигналов аденозина может увеличиться во внутриклеточном цАМФ и цАМФ-зависимой протеинкиназе, что приводит к ингибированию продукции провоспалительных цитокинов и может привести к синтезу иммунодепрессивных молекул и развитию Tregs (Sitkovsky et al., Cancer Immunol Res (2014) 2(7):598-605). В некоторых вариантах осуществления дополнительный агент может уменьшить или обратить иммунодепрессивные эффекты аденозина, аналогов аденозина и/или сигналов трансдукции аденозина. В некоторых вариантах осуществления дополнительный агент может уменьшить или обратить управляемую гипоксией иммунодепрессию A2-аденозинергических Т-клеток. В некоторых вариантах осуществления дополнительный агент выбран из числа антагонистов рецепторов аденозина, внеклеточных разрушающих аденозин агентов, ингибиторов продукции аденозина CD39/CD73 эктоэнзимами и ингибиторов трансдукции сигналов гипоксия-HIF-1α. В некоторых вариантах осуществления дополнительный агент является антагонистом или агонистом рецептора аденозина.
[0743] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, ингибирующим активность и/или количество рецептора аденозина. В некоторых вариантах осуществления рассматривается, что ингибирование или сокращение внеклеточного аденозина или рецептора аденозина за счет ингибитора внеклеточного аденозина (такого как агент, предотвращающий формирование, разрушающий, инактивирующий и/или уменьшающий внеклеточный аденозин) и/или ингибитора рецептора аденозина (такого как антагонист рецептора аденозина) может усилить иммунный ответ, такой как опосредуемый макрофагом, нейтрофилом, гранулоцитом, дендритной клеткой, T- и/или В-клеткой ответ. Кроме того, ингибиторы опосредуемого Gs белком цАМФ-зависимого внутриклеточного пути и ингибиторы вызываемых рецептором аденозина опосредуемых Gi белком внутриклеточных путей могут также увеличить острое и хроническое воспаление.
[0744] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является антагонистом или агонистом рецептора аденозина, например, антагонистом или агонистом одного или более рецепторов аденозина A2a, A2b, A1 и A3. A1 и A3 ингибируют, и A2a и A2b стимулируют, соответственно, активность аденилатциклазы. Некоторые рецепторы аденозина, такие как A2a, A2b и A3, могут подавлять или уменьшать иммунный ответ во время воспаления. Таким образом противодействие иммунодепрессивным рецепторам аденозина может увеличить, повысить или усилить иммунный ответ, например, иммунный ответ от введенных клеток, например, CAR-экспрессирующих Т-клеток. В некоторых вариантах осуществления дополнительный агент ингибирует продукцию внеклеточного аденозина и вызываемую аденозином трансдукцию сигналов через рецепторы аденозина. Например, усиление иммунного ответа, местного воспаления ткани и направленного разрушения ткани может быть усилено путем ингибирования или ослабления продуцирующей аденозин местной тканевой гипоксии; путем разрушения (или инактивации) аккумулированного внеклеточного аденозина; путем предотвращения или уменьшения экспрессии рецепторов аденозина на иммунных клетках; и/или путем ингибирования/противодействия трансдукции сигналов лигандами аденозина через рецепторы аденозина.
[0745] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является антагонистом рецептора аденозина. В некоторых вариантах осуществления антагонист является малой молекулой или химическим соединением рецептора аденозина, такого как рецептор A2a, A2b или A3. В некоторых вариантах осуществления антагонист является пептидом или пептидомиметиком, связывающимся рецептор аденозина, но не запускающим зависимый от Gi белка внутриклеточный путь. Примеры таких антагонистов описаны в патентах США 5,565,566; 5,545, 627, 5,981,524; 5,861,405; 6,066,642; 6,326,390; 5,670,501; 6,117,998; 6,232,297; 5,786,360; 5,424,297; 6,313,131, 5,504,090; и 6,322,771.
[0746] В некоторых вариантах осуществления дополнительный агент является антагонистом рецептора A2 (A2R), таким как антагонист A2a. Примеры антагониста A2R включают, но не ограничены ими, KW6002 (истрадефилин), SCH58261, кофеин, параксантин, 3,7-диметил-1-пропаргилксантин (DMPX), 8-(м-хлорстирил)кофеин (CSC), MSX-2, MSX-3, MSX-4, CGS-15943, ZM-241385, SCH-442416, преладенант, випаденант (BII014), V2006, ST-1535, SYN-115, PSB-1115, ZM241365, FSPTP и ингибирующую нуклеиновую кислоту, нацеливаемую на экспрессию A2R, например, siРНК или shРНК, или любые антитела или их антигенсвязывающий фрагмент, нацеливаемый на A2R. В некоторых вариантах осуществления дополнительный агент является антагонистом A2R, описанным в, например, Ohta et al., Proc Natl Acad Sci U S A (2006) 103:13132-13137; Jin et al., Cancer Res. (2010) 70(6):2245-2255; Leone et al., Computational and Structural Biotechnology Journal (2015) 13:265-272; Beavis et al., Proc Natl Acad Sci U S A (2013) 110:14711-14716; and Pinna, A., Expert Opin Investig Drugs (2009) 18:1619-1631; Sitkovsky et al., Cancer Immunol Res (2014) 2(7):598-605; US 8,080,554; US 8,716,301; US 20140056922; WO2008/147482; US 8,883,500; US 20140377240; WO02/055083; US 7,141,575; US 7,405,219; US 8,883,500; US 8,450,329 и US 8,987,279).
[0747] В некоторых вариантах осуществления антагонист рецептора аденозина, который является антисмысловой молекулой, молекулой ингибирующей нуклеиновой кислоты (например, малой ингибирующей РНК (siРНК)) или молекулой каталитической нуклеиновой кислоты (например, рибозим), который специфично связывается с мРНК, кодирующей рецептор аденозина. В некоторых вариантах осуществления антисмысловая молекула, молекула ингибирующей нуклеиновой кислоты или молекула каталитической нуклеиновой кислоты связывается с нуклеиновыми кислотами, кодирующими A2a, A2b или A3. В некоторых вариантах осуществления антисмысловая молекула, молекула ингибирующей нуклеиновой кислоты или молекула каталитической нуклеиновой кислоты нацеливается на биохимические пути ниже рецептора аденозина. Например, антисмысловая молекула или каталитическая нуклеиновая кислота могут ингибировать фермент, участвующий в зависимом от Gs белка или Gi белка внутриклеточном пути. В некоторых вариантах осуществления дополнительный агент включает доминирующую отрицательную мутантную форму рецептора аденозина, такого как A2a, A2b или A3.
[0748] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является агентом, ингибирующим внеклеточный аденозин. Агенты, ингибирующие внеклеточный аденозин, включают агенты, делающие внеклеточный аденозин нефункциональным (или уменьшающие такую функцию), такие как вещество, изменяющее структуру аденозина для ингибирования способности аденозина к трансдукции сигналов через рецепторы аденозина. В некоторых вариантах осуществления дополнительный агент является внеклеточным генерирующим аденозин или разрушающим аденозин ферментом, его модифицированной формой или модулятором. Например, в некоторых вариантах осуществления дополнительный агент является ферментом (например, аденозин деаминазой) или другой каталитической молекулой, селективно связывающейся и разрушающей аденозин, таким образом подавляя или значительно уменьшая способность эндогенно сформированного аденозина к трансдукции сигналов через рецепторы аденозина и конечное воспаление.
[0749] В некоторых вариантах осуществления дополнительный агент является аденозин деаминазой (ADA) или ее модифицированной формой, например, рекомбинантной ADA и/или модифицированной полиэтиленгликолем ADA (ADA-PEG), который может ингибировать местное накопление в ткани внеклеточного аденозина. ADA-PEG использовался в лечении пациентов с ADA SCID (Hershfield (1995) Hum Mutat. 5:107). В некоторых вариантах осуществления агент, ингибирующий внеклеточный аденозин, включает агенты, предотвращающие или уменьшающие формирование внеклеточного аденозина и/или предотвращающие или уменьшающие накопление внеклеточного аденозина, таким образом устраняя или существенно уменьшая иммунодепрессивные эффекты аденозина. В некоторых вариантах осуществления дополнительный агент специфично ингибирует ферменты и белки, участвующие в регуляции синтеза и/или секреции провоспалительных молекул, включая модуляторы ядерных транскрипционных факторов. Супрессия экспрессии рецептора аденозина или экспрессии зависимого от Gs белка или Gi белка внутриклеточного пути или цАМФ-зависимого внутриклеточного пути может приводить к увеличению/усилению иммунного ответа.
[0750] В некоторых вариантах осуществления дополнительный агент может нацеливаться на эктоэнзимы, генерирующие или продуцирующие внеклеточный аденозин. В некоторых вариантах осуществления дополнительный агент нацеливается на CD39 и CD73 эктоэнзимы, функционирующие в тандеме для генерации внеклеточного аденозина. CD39 (также названный эктонуклеозид трифосфат дифосфогидролазой) превращает внеклеточный АТФ (или АДФ) в 5’АМФ. Впоследствии CD73 (также названный 5’нуклеотидазой) превращает 5’АМФ в аденозин. Активность CD39 обратима под действиями НДФ киназы и аденилат киназы, тогда как активность CD73 необратима. CD39 и CD73 экспрессируются на клетках стромы опухоли, включая эндотелиальные клетки и Tregs, и также на многих раковых клетках. Например, экспрессия CD39 и CD73 на эндотелиальных клетках увеличивается в гипоксических условиях микросреды опухоли. Гипоксия опухоли может следовать из несоответствующего кровоснабжения и дезорганизованной сосудистой сети опухоли, нарушающей доставку кислорода (Carroll and Ashcroft (2005), Expert. Rev. Mol. Med. 7(6):1-16). Гипоксия также ингибирует аденилат киназу (AK), превращающую аденозин в АМФ, приводя к очень высокой внеклеточной концентрации аденозина. Таким образом аденозин высвобождается в высоких концентрациях в ответ на гипоксию, которая является состоянием, часто происходящим в микросреде опухоли (TME), в или вокруг солидных опухолей. В некоторых вариантах осуществления дополнительный агент представляет собой одно или более из числа антитела анти-CD39 или его антигенсвязывающего фрагмента, антитела анти-CD73 или его антигенсвязывающего фрагмента, например, MEDI9447 или TY/23, α-β-метилен-аденозин дифосфат (АДФ), ARL 67156, POM-3, IPH52 (см, например, Allard et al. Clin Cancer Res (2013) 19(20):5626-5635; Hausler et al., Am J Transl Res (2014) 6(2):129-139; Zhang, B., Cancer Res. (2010) 70(16):6407-6411).
[0751] В некоторых вариантах осуществления дополнительный агент, вводимый в соответствии со способами по изобретению и/или с использованием изделий или композиций по изобретению, является химиотерапевтическим агентом (иногда называемым цитотоксическим агентом). В некоторых вариантах осуществления химиотерапевтический агент является любым агентом, известным специалисту как эффективный для лечения, профилактики или облегчения гиперпролиферативных нарушений, таких как рак. Химиотерапевтические агенты включают, но не ограничены ими, малые молекулы, синтетические лекарственные средства, пептиды, полипептиды, белки, нуклеиновые кислоты (например, ДНК и РНК полинуклеотиды, включая, но не ограничиваясь ими, антисмысловые нуклеотидные последовательности, тройные спирали и нуклеотидные последовательности, кодирующие биологически активные белки, полипептиды или пептиды), антитела, синтетические или натуральные неорганические молекулы, миметики и синтетические или натуральные органические молекулы. В некоторых вариантах осуществления химиотерапевтические лекарственные средства включают алкилирующие агенты, антрациклины, разрушители цитоскелета (таксаны), эпотилоны, ингибиторы гистон деацетилазы, ингибиторы топоизомеразы, ингибиторы топоизомеразы II, ингибиторы киназы, аналоги нуклеотида и аналоги предшественника, пептидные антибиотики, основанные на платине вещества, и алкалоиды барвинка и производные.
[0752] Химиотерапевтические агенты могут включать, но не ограничены ими, абареликс, алдеслейкин, алемтузумаб, алитретиноин, аллопуринол, алтретамин, амифостин, анастрозол, триоксид мышьяка, аспарагиназу, живой BCG, бевацизумаб, бексаротен, блеомицин, бортезомиб, бусульфан, калустерон, камптотецин, капецитабин, карбоплатин, кармустин, целекоксиб, цетуксимаб, хлорамбуцил, цинакальцет, цисплатин, кладрибин, циклофосфамид, цитарабин, дакарбазин, дактиномицин, дарбепоетин альфа, даунорубицин, денилейкин дифтитокс, дексразоксан, доцетаксел, доксорубицин, дромостанолон, раствор Эллиота B, эпирубицин, эпоетин альфа, эстрамустин, этопозид, эксеместан, филграстим, флоксуридин, флударабин, фтороурацил, фулвестрант, гемцитабин, гемтузумаб озогамицин, гефитиниб, госерелин, гидроксимочевину, ибритумомаб тиуксетан, идарубицин, ифосфамид, иматиниб, интерферон альфа-2a, интерферон альфа-2b, иринотекан, летрозол, лейковорин, левамизол, ломустин, меклоретамин, мегестрол, мелфалан, меркаптопурин, месна, метотрексат, метокссален, метилпреднизолон, митомицин C, митотан, митоксантрон, нандролон, нофетумомаб, облимерсен, опрелвекин, оксалиплатин, паклитаксел, памидронат, пегадемазу, пегаспаргазу, пегфлиграстим, пеметрексед, пентостатин, пипоброман, пликамицин, полифепрозан, порфимер, прокарбазин, акрихин, расбуриказу, ритуксимаб, сарграмостим, стрептозоцин, тальк, тамоксифен, тарцева, темозолид, тенипозид, тестолактон, тиогуанин, тиотепа, топотекан, торемифен, тозитумомаб, трастузумаб, третиноин, урамустин, валрубицин, винбластин, винкристин, винорелбин и золедронат.
[0753] В некоторых вариантах осуществления дополнительный агент является ингибитором сигнального пути гипоксия-индуцируемого фактор 1 альфа (HIF-1α). Примеры ингибиторов HIF-1α включают дигоксин, акрифлавин, сиртуин-7 и ганетеспиб.
[0754] В некоторых вариантах осуществления дополнительный агент включает ингибитор протеинтирозин фосфатазы, например, ингибитор протеинтирозин фосфатазы, описанный здесь. В некоторых вариантах осуществления ингибитор протеинтирозин фосфатазы является ингибитором SHP-1, например, ингибитором SHP-1, описанным здесь, таким как, например, натрий стибоглюконат. В некоторых вариантах осуществления ингибитор протеинтирозин фосфатазы является ингибитором SHP-2, например, ингибитором SHP-2, описанным здесь.
[0755] В некоторых вариантах осуществления дополнительный агент является ингибитором киназы. Ингибиторы киназы, такие как ингибитор киназы CDK4, ингибитор киназы BTK, ингибитор киназы MNK или ингибитор киназы DGK, может регулировать конститутивно активные пути выживания, существующие в опухолевых клетках и/или модулирующие функцию иммунных клеток. В некоторых вариантах осуществления ингибитор киназы является ингибитором тирозинкиназы Брутона (BTK), например, ибрутинибом. В некоторых вариантах осуществления ингибитор киназы является ингибитором фосфатидилинозитол-4,5-бифосфат-3-киназы (PI3K). В некоторых вариантах осуществления ингибитор киназы является ингибитором CDK4, например, ингибитором CDK4/6. В некоторых вариантах осуществления ингибитор киназы является ингибитором mTOR, таким как, например, рапамицин, аналог рапамицина, OSI-027. Ингибитор mTOR может быть, например, ингибитором mTORC1 и/или ингибитором mTORC2, например, ингибитором mTORC1 и/или ингибитором mTORC2. В некоторых вариантах осуществления ингибитор киназы является ингибитором MNK или двойным ингибитором PI3K/mTOR. В некоторых вариантах осуществления другие примеры ингибиторов киназы включают ингибитор AKT перифосин, ингибитор mTOR темсиролимус, ингибиторы киназы Src дасатиниб и фостаматиниб, ингибиторы JAK2 пакритиниб и руксолитиниб, ингибиторы PKCβ энзастуаурин и бриостатин и ингибитор AAK алисертиб.
[0756] В некоторых вариантах осуществления ингибитор киназы является ингибитором BTK, выбранным из ибрутиниба (PCI- 32765); GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774; и LFM-A13. В некоторых вариантах осуществления ингибитор BTK не уменьшает или ингибирует активность киназы интерлейкин-2-индуцируемой киназы (ITK) и выбран из GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774; и LFM-A13.
[0757] В некоторых вариантах осуществления ингибитор киназы является ингибитором BTK, например, ибрутинибом (1-[(3R)-3-[4-Амино-3-(4-феноксифенил)-1H-пиразоло[3,4-d]пиримидин-1-ил]пиперидин-1-ил]проп-2-ен-1-он; также известный как PCI-32765). В некоторых вариантах осуществления ингибитор киназы является ингибитором BTK, например, ибрутинибом (PCI-32765), и ибрутиниб вводят в дозе приблизительно 250 мг, 300 мг, 350 мг, 400 мг, 420 мг, 440 мг, 460 мг, 480 мг, 500 мг, 520 мг, 540 мг, 560 мг, 580 мг, 600 мг (например, 250 мг, 420 мг или 560 мг) в сутки в течение времени, например, ежедневно в течение 21-дневного цикла, или ежедневно в течение 28-дневного цикла. В некоторых вариантах осуществления вводят 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов ибрутиниб. В некоторых вариантах осуществления ингибитор BTK является ингибитором BTK, описанным в Международной Заявке WO 2015/079417.
[0758] В некоторых вариантах осуществления ингибитор киназы является ингибитором PI3K. PI3K является центральным в PI3K/Akt/mTOR пути, участвующим в регуляции клеточного цикла и выживаемости лимфомы. Примеры ингибитора PI3K включают иделалисиб (ингибитор PI3Kδ). В некоторых вариантах осуществления дополнительный агент представляет собой иделалисиб и ритуксимаб.
[0759] В некоторых вариантах осуществления дополнительный агент является ингибитором мишени рапамицина в клетках млекопитающих (mTOR). В некоторых вариантах осуществления ингибитор киназы является mTOR ингибитором, выбранным из темсиролимуса; ридафоролимуса (также известного как AP23573 и MK8669); эверолимуса (RAD001); рапамицина (AY22989); симапимода; AZD8055; PF04691502; SF1126; и XL765. В некоторых вариантах осуществления дополнительный агент является ингибитором митоген-активированной протеинкиназы (MAPK), таким как вемурафениб, дабрафениб и траметиниб.
[0760] В некоторых вариантах осуществления дополнительный агент является агентом, регулирующим про- или антиапоптические белки. В некоторых вариантах осуществления дополнительный агент включает ингибитор В-клеточной лимфомы 2 (BCL-2) (например, венетоклакс, также названный ABT-199 или GDC-0199; или ABT-737). Венетоклакс является малой молекулой (4-(4-{[2-(4-хлорофенил)-4,4-диметил-1-циклогексен-1-ил]метил}-1-пиперазинил)-N-({3-нитро-4-[(тетрагидро-2H-пиран-4-илметил)амино]фенил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид), которая ингибирует антиапоптический белок BCL-2. Другие агенты, модулирующие про- или антиапоптический белок, включают BCL-2 ингибитор ABT-737, навитоклакс (ABT-263); Mcl-1 siРНК или Mcl-1 ингибитор ретиноид (4-гидроксифенил)N-ретинамид (4-HPR) для максимальной эффективности. В некоторых вариантах осуществления дополнительный агент обеспечивает проапоптотические стимулы, такие как рекомбинантный связанный с фактором некроза опухоли вызывающий апоптоз лиганд (TRAIL), который может активировать путь апоптоза путем связывания со смертельными рецепторами TRAIL DR-4 и DR-5 на поверхности опухолевой клетки или TRAIL-R2 агонистическими антителами.
[0761] В некоторых вариантах осуществления дополнительный агент включает цитотоксический агент, например, CPX-351 (Cyclacel Pharmaceuticals), цитарабин, даунорубицин, возароксин (Sunesis Pharmaceuticals), сапацитабин (Cyclacel Pharmaceuticals), идарубицин или митоксантрон. В некоторых вариантах осуществления дополнительный агент включает гипометилирующий агент, например, ингибитор ДНК метилтрансферазы, например, азацитидин или децитабин.
[0762] В другом варианте осуществления дополнительная терапия является трансплантацией, например, аллогенным трансплантатом стволовых клеток.
[0763] В некоторых вариантах осуществления дополнительная терапия является противолимфоцитарной терапией. В некоторых вариантах осуществления лимфодеплецию осуществляют на пациенте, например, до введения генно-инженерных клеток, например, CAR-экспрессирующих клеток. В некоторых вариантах осуществления лимфодеплеция включает введение одного или более мелфалана, цитоксана, циклофосфамида и флударабина. В некоторых вариантах осуществления противолимфоцитарную химиотерапию вводят пациенту до, одновременно с или после введения (например, вливания) генно-инженерных клеток, например, CAR-экспрессирующих клеток. В примере противолимфоцитарную химиотерапию вводят пациенту до введения генно-инженерных клеток, например, CAR-экспрессирующих клеток.
[0764] В некоторых вариантах осуществления дополнительный агент является онколитическим вирусом. В некоторых вариантах осуществления онколитические вирусы способны к селективной репликации в и триггерному запуску гибели или замедлению роста раковых клеток. В некоторых случаях онколитические вирусы не имеют никакого эффекта или имеют минимальный эффект на нераковые клетки. Онколитический вирус включает, но не ограничен ими, онколитический аденовирус, онколитические вирусы простого герпеса, онколитические ретровирусы, онколитические парвовирусы, онколитические вирусы коровьей оспы, онколитические вирусы Sinbis, онколитические вирусы гриппа или онколитические РНК вирусы (например, онколитический реовирус, онколитический вирус атипичной чумы (NDV), онколитический вирус кори или онколитический вирус везикулярного стоматита (VSV)).
[0765] Другие примеры комбинированной терапии, лечения и/или агентов включают антиаллергеннные агенты, противорвотные средства, аналгезирующие средства и вспомогательные терапии. В некоторых вариантах осуществления дополнительный агент включает цитопротекторные агенты, такие как нейропротекторы, акцепторы свободных радикалов, кардиопротекторы, антрациклиновые нейтрализаторы транссудации и питательные вещества.
[0766] В некоторых вариантах осуществления антитело, используемое в качестве дополнительного агента, конъюгировано или иначе связано с терапевтическим агентом, например, химиотерапевтическим агентом (например, цитоксаном, флударабином, ингибитором гистон деацетилазы, деметилирующим агентом, пептидной вакциной, противоопухолевым антибиотиком, ингибитором тирозинкиназы, алкилирующим агентом, антимикротрубочковым или антимитотическим агентом), антиаллергическим агентом, агентом против тошноты (или противорвотным средством), обезболивающим средством или цитопротекторным агентом, описанным здесь. В некоторых вариантах осуществления дополнительный агент является конъюгатом антитело-лекарственное средство.
[0767] Любой из дополнительных агентов, описанных здесь, может быть получен и введен как комбинированная терапия, описанная в способах, применениях, изделиях или композициях по изобретению, например, в фармацевтических композициях, включающих один или более агентов комбинированной терапии и фармацевтически приемлемый носитель, такой как любой описанный здесь. В некоторых вариантах осуществления комбинированная терапия в способах, применениях, изделиях или композициях по изобретению может быть введена одновременно, параллельно или последовательно, в любом порядке, с дополнительными агентами, терапией или лечением, причем такое введение обеспечивает терапевтически эффективные уровни каждого из агентов в организме пациента. В некоторых вариантах осуществления дополнительный агент можно использовать совместно с комбинированной терапией в способах, применениях, изделиях или композициях по изобретению, например, как часть той же фармацевтической композиции или использования того же способа доставки. В некоторых вариантах осуществления дополнительный агент вводят одновременно с клеточной терапией, например, дозой генно-инженерных Т-клеток (например, CAR+ Т-клеток), но в отдельных композициях. В некоторых вариантах осуществления дополнительный агент инкубируют с генно-инженерной клеткой, например, CAR-экспрессирующими клетками, до введения клеток.
[0768] В некоторых примерах один или более дополнительных агентов вводят после или до введения клеточной терапии, например, дозы генно-инженерных Т-клеток (например, CAR+ Т-клеток) через выбранный интервал времени. В некоторых примерах интервал времени составляет 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 1 неделю, 2 недели, 3 недели, 1 месяц, 2 месяца или 3 месяца. В некоторых примерах один или более дополнительных агентов вводят многократно. В некоторых вариантах осуществления дополнительный агент вводят до клеточной терапии, например, дозы генно-инженерных Т-клеток (CAR+ Т-клеток) в способах, применениях, изделиях или композициях по изобретению, например, за две недели, 12 дней, 10 дней, 8 дней, одну неделю, 6 дней, 5 дней, 4 дня, 3 дня, 2 дня или 1 день до введения. В некоторых вариантах осуществления дополнительный агент вводят после клеточной терапии, например, дозы генно-инженерных Т-клеток (например, CAR+ Т-клеток) в способах, применениях, изделиях или композициях по изобретению, например, через две недели, 12 дней, 10 дней, 8 дней, одну неделю, 6 дней, 5 дней, 4 дня, 3 дня, 2 дня или 1 день после введения.
[0769] Доза дополнительного агента может быть любым терапевтически эффективной количеством, например, любым количеством дозы, описанной здесь, и подходящая дозировка дополнительного агента может зависеть от типа заболевания, которое будет подвергнуто лечению, типа, дозы и/или частоты связывающей молекулы, рекомбинантного рецептора, клетки и/или вводимой композиции, серьезности и течения заболевания, предыдущей терапии, история болезни пациента и ответа на клеточную терапию, например, дозу генно-инженерных Т-клеток (CAR+ Т-клеток), и остается на усмотрение лечащего врача.
VI. ИЗДЕЛИЯ И НАБОРЫ
[0770] Изобретение также относится к изделиям и наборам, содержащим генно-инженерные клетки, экспрессирующие рекомбинантный рецептор, или их композиции, и необязательно инструкции по применению, например, инструкции по введению, согласно способам по изобретению.
[0771] В некоторых вариантах осуществления изобретение относится к изделиям и/или наборам, включающим композицию, включающую терапевтически эффективное количество любой из генно-инженерных клеток, описанных здесь, и инструкции по введению пациенту для лечения заболевания или состояния. В некоторых вариантах осуществления инструкции могут определять некоторые или все элементы способов по изобретению. В некоторых вариантах осуществления инструкции определяют частные инструкции по введению клеток для клеточной терапии, например, дозу, выбор времени, выбор и/или идентификацию пациентов для введения и условия для введения. В некоторых вариантах осуществления изделия и/или наборы дополнительно включают один или более дополнительных агентов для терапии, например, противолимфоцитарной терапии и/или комбинированной терапии, такой как любая описанная здесь, и необязательно дополнительно включает инструкции по введению дополнительного агента для терапии. В некоторых вариантах осуществления изделия и/или наборы дополнительно включают агент для противолимфоцитарной терапии, и необязательно дополнительно включают инструкции по введению противолимфоцитарной терапии. В некоторых вариантах осуществления инструкции могут быть включены как этикетка или листок-вкладыш, сопровождающая композиции для введения.
[0772] В некоторых вариантах осуществления инструкции определяют критерии выбора или идентификации пациентов для терапии. В некоторых вариантах осуществления такие критерии включают пациентов, имеющих NHL, или выделяют их подтипы и/или высокий риск NHL. В некоторых вариантах осуществления инструкции определяют, что пациенты, которых подвергают лечению, включают пациентов, имеющих заболевание или состояние, характеризуемое или определенное как агрессивная NHL, диффузная крупноклеточная В-клеточная лимфома (DLBCL), первичная медиастинальная крупноклеточная В-клеточная лимфома (PMBCL), Т-клеточная/гистоцит-обогащенная крупноклеточная В-клеточная лимфома (TCHRBCL), лимфома Беркитта, мантийноклеточная лимфома (MCL) и/или фолликулярная лимфома (FL). В некоторых вариантах осуществления пациент, которого подвергают лечению, включает пациентов с агрессивной NHL, в частности,Ю с диффузной крупноклеточной В-клеточной лимфомой (DLBCL), неуточненной (NOS) и в некоторых аспектах включая de novo и трансформированную из вялотекущей). В некоторых аспектах пациент или популяция, которых подвергают лечению, могут включать и/или дополнительно включать пациентов с первичной медиастинальной В-клеточной лимфомой (PMBCL) или фолликулярной лимфомой степени 3B (FL3B). В некоторых вариантах осуществления пациент или популяция, которых подвергают лечению, включают пациентов, имеющих неудовлетворительный статус. В некоторых аспектах популяция, которую подвергают лечению, включает, например, пациентов, имеющих Eastern Cooperative Oncology Group Performance Status (ECOG), который составляет от 0-2. В других аспектах любого из вариантов осуществления пациенты, которых подвергают лечению, включают ECOG 0-1 или не включают пациентов ECOG2. В некоторых вариантах осуществления любого из вариантов осуществления пациенты, которых подвергают лечению, потерпели неудачу в ходе двух или более предшествующих терапий. В некоторых вариантах осуществления пациент не имеет DLBCL, трансформированной из лимфомы маргинальной зоны (MZL) и хронического лимфолейкоза (CLL; Рихтер), и/или имеет DLBCL, характеризуемую как de novo или трансформированную из вялотекущего заболевания. В некоторых вариантах осуществления пациент имеет мантийноклеточную лимфому (MCL). В некоторых вариантах осуществления инструкции определяют, что введение клеточной терапии для пациента, который является или был идентифицирован как имеющий лимфому double/triple hit (или высокодифференцированную В-клеточную лимфому с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL), был идентифицирован как имеющий хеморефрактерную лимфому (например, хеморефрактерную DLBCL) и/или не достиг полной ремиссии (CR) в ответ на предшествующую терапию.
[0773] В некоторых вариантах осуществления инструкции определяют дозу клеток, которую вводят. Например, в некоторых вариантах осуществления, доза, определенная в инструкциях, включает общие экспрессирующие рекомбинантный рецептор (например, CAR) клетки в количестве от приблизительно 1x106 до 3x108, например, в диапазоне от приблизительно 1x107 до 2x108 таких клеток, например, 1x107, 5x107, 1x108 или 1,5x108 таких общих клеток или диапазон между любыми двумя из указанных значений. В некоторых вариантах осуществления пациенту вводят множественные дозы, и каждая из доз или общая доза может составлять любое из указанных значений.
[0774] В некоторых вариантах осуществления изделие или набор включают контейнер, необязательно флакон, включающий множество CD4+ Т-клеток, экспрессирующих рекомбинантный рецептор, и контейнер, необязательно флакон, включающий множество CD8+ Т-клеток, экспрессирующих рекомбинантный рецептор. В некоторых вариантах осуществления изделие или набор включают контейнер, необязательно флакон, включающий множество CD4+ Т-клеток, экспрессирующих рекомбинантный рецептор, и дополнительно включают, в том же контейнере, множество CD8+ Т-клеток, экспрессирующих рекомбинантный рецептор. В некоторых вариантах осуществления криопротектор включен вместе с клетками. В некоторых аспектах контейнер является мешком.
[0775] В некоторых вариантах осуществления контейнер, такой как флакон, включает более чем или более чем приблизительно 10x106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток, более чем или более чем приблизительно 15x106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток, более чем или более чем приблизительно 25x106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток. В некоторых аспектах флакон включает от приблизительно 10 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 25 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 15 миллионов клеток на мл, от 15 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 15 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл, от приблизительно 15 миллионов клеток на мл до приблизительно 25 миллионов клеток на мл, от приблизительно 25 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 25 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл и от приблизительно 50 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл.
[0776] В некоторых вариантах осуществления множество пузырьков или множество клеток или разовых доз клеток, определенных для введения, коллективно включают дозу клеток, включающую от или от приблизительно 1x105 до 5x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от 1x105 до 1x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 5x105 до 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, или от или от приблизительно 1x106 до 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, включительно. В некоторых аспектах изделие включает одну или более унифицированных доз CD4+ и CD8+ клеток или CD4+рецептор+ клеток и CD8+рецептор+ клеток, причем разовая доза включает от или от приблизительно 1x107 и до или до приблизительно 2x108 экспрессирующих рекомбинантный рецептор Т-клеток, от или от приблизительно 5x107 и до или до приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток, составляет или приблизительно составляет 5x107 экспрессирующих рекомбинантный рецептор Т-клеток, составляет или приблизительно составляет 1x108 экспрессирующих рекомбинантный рецептор Т-клеток, или до или до приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток, причем необязательно информация в изделии определяет введение одной или множества разовых доз и/или объема, соответствующего такой дозе или множеству разовых доз. В некоторых случаях изделие включает одну или более разовых доз CD8+ клеток, причем доза включает от или от приблизительно 5x106 и до или до приблизительно 1x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, доза включает от или от приблизительно 1x107 и до или до приблизительно 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, доза составляет или приблизительно составляет 2,5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток или доза составляет или приблизительно составляет 5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток или доза составляет или приблизительно составляет 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, причем необязательно информация в изделии определяет введение одного или множества разовых доз и/или объема, соответствующего такой дозе или множеству разовых доз. В некоторых вариантах осуществления клетки в изделии, коллективно, включают дозу клеток, включающих не более чем 1x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1x106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5x106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток.
[0777] В некоторых вариантах осуществления каждый пузырек или множество пузырьков или множество клеток или разовая доза клеток, определенные для введения, коллективно включают плоскую дозу клеток или фиксированную дозу клеток, таким образом, что доза клеток не привязана к или не рассчитана на основе площади поверхности или массы тела пациента.
[0778] В некоторых вариантах осуществления разовая доза клеток представляет собой или включает число или количество клеток, таких как генно-инженерные Т-клетки, которые могут быть введены лицу или пациенту в единственной дозе.
[0779] В некоторых вариантах осуществления каждый пузырек или множество пузырьков или множество клеток или разовая доза клеток, определенные для введения, коллективно включают дозу, включающую менее чем приблизительно 5x108 общих экспрессирующих рекомбинантный рецептор (например, CAR) клеток, Т-клеток или одноядерных клеток периферической крови (PBMC), например, в диапазоне приблизительно от 1x106 до 5x108 таких клеток, например, 2x106, 5x106, 1x107, 5x107, 1x108 или 5x108 таких общих клеток или диапазон между любыми двумя из указанных значений.
[0780] В некоторых вариантах осуществления каждый пузырек или множество пузырьков или множество клеток или разовая доза клеток, определенные для введения, коллективно включают дозу генно-инженерных клеток, включающую от или от приблизительно 1x105 до 5x108 общих CAR-экспрессирующих Т-клеток, от 1x105 до 2,5x108 общих CAR-экспрессирующих Т-клеток, от 1x105 до 1x108 общих CAR-экспрессирующих Т-клеток, от 1x105 до 5x107 общих CAR-экспрессирующих Т-клеток, от 1x105 до 2,5x107 общих CAR-экспрессирующих Т-клеток, от 1x105 до 1x107 общих CAR-экспрессирующих Т-клеток, от 1x105 до 5x106 общих CAR-экспрессирующих Т-клеток, от 1x105 до 2,5x106 общих CAR-экспрессирующих Т-клеток, от 1x105 до 1x106 общих CAR-экспрессирующих Т-клеток, от 1x106 до 5x108 общих CAR-экспрессирующих Т-клеток, от 1x106 до 2,5x108 общих CAR-экспрессирующих Т-клеток, от 1x106 до 1x108 общих CAR-экспрессирующих Т-клеток, от 1x106 до 5x107 общих CAR-экспрессирующих Т-клеток, от 1x106 до 2,5x107 общих CAR-экспрессирующих Т-клеток, от 1x106 до 1x107 общих CAR-экспрессирующих Т-клеток, от 1x106 до 5x106 общих CAR-экспрессирующих Т-клеток, от 1x106 до 2,5x106 общих CAR-экспрессирующих Т-клеток, от 2,5x106 до 5x108 общих CAR-экспрессирующих Т-клеток, от 2,5x106 до 2,5x108 общих CAR-экспрессирующих Т-клеток, от 2,5x106 до 1x108 общих CAR-экспрессирующих Т-клеток, от 2,5x106 до 5x107 общих CAR-экспрессирующих Т-клеток, от 2,5x106 до 2,5x107 общих CAR-экспрессирующих Т-клеток, от 2,5x106 до 1x107 общих CAR-экспрессирующих Т-клеток, от 2,5x106 до 5x106 общих CAR-экспрессирующих Т-клеток, от 5x106 до 5x108 общих CAR-экспрессирующих Т-клеток, от 5x106 до 2,5x108 общих CAR-экспрессирующих Т-клеток, от 5x106 до 1x108 общих CAR-экспрессирующих Т-клеток, от 5x106 до 5x107 общих CAR-экспрессирующих Т-клеток, от 5x106 до 2,5x107 общих CAR-экспрессирующих Т-клеток, от 5x106 до 1x107 общих CAR-экспрессирующих Т-клеток, от 1x107 до 5x108 общих CAR-экспрессирующих Т-клеток, от 1x107 до 2,5x108 общих CAR-экспрессирующих Т-клеток, от 1x107 до 1x108 общих CAR-экспрессирующих Т-клеток, от 1x107 до 5x107 общих CAR-экспрессирующих Т-клеток, от 1x107 до 2,5x107 общих CAR-экспрессирующих Т-клеток, от 2,5x107 до 5x108 общих CAR-экспрессирующих Т-клеток, от 2,5x107 до 2,5x108 общих CAR-экспрессирующих Т-клеток, от 2,5x107 до 1x108 общих CAR-экспрессирующих Т-клеток, от 2,5x107 до 5x107 общих CAR-экспрессирующих Т-клеток, от 5x107 до 5x108 общих CAR-экспрессирующих Т-клеток, от 5x107 до 2,5x108 общих CAR-экспрессирующих Т-клеток, от 5x107 до 1x108 общих CAR-экспрессирующих Т-клеток, от 1x108 до 5x108 общих CAR-экспрессирующих Т-клеток, от 1x108 до 2,5x108 общих CAR-экспрессирующих Т-клеток или от 2,5x108 до 5x108 общих CAR-экспрессирующих Т-клеток.
[0781] В некоторых вариантах осуществления каждый пузырек или множество пузырьков или множество клеток или разовая доза клеток, определенные для введения, коллективно включают дозу генно-инженерных клеток, включающую по меньшей мере или по меньшей мере приблизительно 1x105 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5x105 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 5x105 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 1x106 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5x106 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 5x106 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 1x107 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5x107 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 5x107 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 1x108 CAR-экспрессирующих клеток, по меньшей мере или по меньшей мере приблизительно 2,5x108 CAR-экспрессирующих клеток или по меньшей мере или по меньшей мере приблизительно 5x108 CAR-экспрессирующих клеток.
[0782] В некоторых вариантах осуществления инструкции по введению дозы генно-инженерных клеток определяют введение числа клеток от или от приблизительно 1x105 до 5x108 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), от или от приблизительно 5x105 до 1x107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC) или от или от приблизительно 1x106 до 1x107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), включительно. В некоторых вариантах осуществления клеточная терапия включает введение дозы клеток, включающих число клеток по меньшей мере или по меньшей мере приблизительно 1x105 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, по меньшей мере или по меньшей мере 1x106, по меньшей мере или по меньшей мере приблизительно 1x107, по меньшей мере или по меньшей мере приблизительно 1x108 из таких клеток. В некоторых вариантах осуществления число в отношении общего количества CD3+ или CD8+, в некоторых случаях также экспрессирующих рекомбинантный рецептор (например, CAR+) клеток. В некоторых вариантах осуществления клеточная терапия включает введение дозы, включающей число клеток от или от приблизительно 1x105 до 5x108 CD3+ или CD8+ общих Т-клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, от или от приблизительно 5x105 до 1x107 CD3+ или CD8+ общих Т-клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, или от или от приблизительно 1x106 до 1x107 CD3+ или CD8+ общих Т-клеток или CD3+ или CD8+ экспрессирующих рекомбинантный рецептор клеток, включительно. В некоторых вариантах осуществления клеточная терапия включает введение дозы, включающей число клеток от или от приблизительно 1x105 до 5x108 общих CD3+/CAR+ или CD8+/CAR+ клеток, от или от приблизительно 5x105 до 1x107 общих CD3+/CAR+ или CD8+/CAR+ клеток или от или от приблизительно 1x106 до 1x107 общих CD3+/CAR+ или CD8+/CAR+ клеток, включительно.
[0783] В некоторых вариантах осуществления инструкции могут определять режим дозировки и выбор времени введения. Например, в некоторых вариантах осуществления инструкции могут определять введение пациенту множества доз, например, двух или более доз клеток. В некоторых вариантах осуществления инструкции определяют выбор времени множественных доз, например, вторая доза, введенная приблизительно через 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 день после первой дозы; и/или количество в каждой дозе.
[0784] В некоторых вариантах осуществления изделие или набор включают множество CD4+ Т-клеток, экспрессирующих рекомбинантный рецептор, и инструкции по введению пациенту, имеющему заболевание или состояние, всех или части множества CD4+ Т-клеток и дополнительное введение CD8+ Т-клеток, экспрессирующих рекомбинантный рецептор. В некоторых вариантах осуществления инструкции определяют введение CD4+ Т-клеток до введения CD8+ клеток. В некоторых случаях инструкции определяют введение CD8+ Т-клеток до введения CD4+ клеток. В некоторых вариантах осуществления изделие или набор включают множество CD8+ Т-клеток, экспрессирующих рекомбинантный рецептор, и инструкции по введению пациенту, имеющему заболевание или состояние, всех или части множества CD8+ Т-клеток и CD4+ Т-клеток, экспрессирующих рекомбинантный рецептор. В некоторых вариантах осуществления инструкции определяют режим введения и выбор времени введения клеток.
[0785] В некоторых аспектах инструкции определяют введение всех или части CD4+ Т-клеток и всех или части CD8+ Т-клеток с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часов. В некоторых случаях инструкции определяют введение CD4+ Т-клеток и CD8+ Т-клеток с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут.
[0786] В некоторых вариантах осуществления инструкции определяют дозу или число клеток или типа(ов) клеток и/или отношения типов клеток, например, отдельных популяций или подтипов, такие как отношение CD4+ к CD8+. В некоторых вариантах осуществления популяции или подтипы клеток, такие как CD8+ и CD4+ Т-клетки. Например, в некоторых вариантах осуществления инструкции определяют, что клетки вводят в или в пределах переносимого диапазона выходного отношения множества популяций или подтипов клеток, таких как CD4+ и CD8+ клетки или подтипы, от или от приблизительно 5:1 до или до приблизительно 5:1 (или более чем приблизительно 1:5 и менее чем приблизительно 5:1), или от или от приблизительно 1:3 до или до приблизительно 3:1 (или более чем приблизительно 1:3 и менее чем приблизительно 3:1), например, от или от приблизительно 2:1 до или до приблизительно 1:5 (или более чем приблизительно 1:5 и менее чем приблизительно 2:1, например в отношении, составляющем или приблизительно составляющем 5:1, 4,5:1, 4:1, 3,5:1, 3:1, 2,5:1, 2:1, 1,9:1, 1,8:1, 1,7:1, 1,6:1, 1,5:1, 1,4:1, 1,3:1, 1,2:1, 1,1:1, 1:1, 1:1,1, 1:1,2, 1:1,3, 1:1,4, 1:1,5, 1:1,6, 1:1,7, 1:1,8, 1:1,9: 1:2, 1:2,5, 1:3, 1:3,5, 1:4, 1:4,5 или 1:5). В некоторых аспектах переносимое различие составляет приблизительно 1%, приблизительно 2%, приблизительно 3%, приблизительно 4% приблизительно 5%, приблизительно 10%, приблизительно 15%, приблизительно 20%, приблизительно 25%, приблизительно 30%, приблизительно 35%, приблизительно 40%, приблизительно 45%, приблизительно 50% желаемого отношения, включая любое промежуточное значение этих диапазонов.
[0787] В некоторых вариантах осуществления изделия и/или наборы дополнительно включают один или более дополнительных агентов для терапии, например, противолимфоцитарной терапии и/или комбинированной терапии, как описано здесь, и необязательно инструкции по введению дополнительных агентов. В некоторых примерах изделия могут дополнительно содержать одно или более терапевтических агентов. В некоторых вариантах осуществления терапевтический агент является иммуномодулирующим агентом, цитотоксическим агентом, противораковым агентом или радиотерапевтическим агентом.
[0788] В некоторых вариантах осуществления изделия и/или наборы дополнительно включают один или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности и/или инструкции по введению одного или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности у пациента. В некоторых вариантах осуществления агент представляет собой или включает анти-IL-6 антитело или рецептор анти-IL-6 антитела. Например, в некоторых вариантах осуществления агент или средство для лечения представляет собой или включает агент, выбранный из числа тоцилизумаба, силтуксимаба, клазакизумаба, сарилумаба, олокизумаба (CDP6038), элсилимомаба, ALD518/BMS-945429, сирукумаба (CNTO 136), CPSI-2634, ARGX-109, FE301 и FM101. Например, в некоторых вариантах осуществления агент или средство для лечения представляет собой или включает один или более стероидов; антагонистов или ингибиторов рецептора цитокина или цитокина, выбранного из числа IL-10, IL-10R, IL-6, рецептора IL-6, IFNγ, IFNGR, IL-2, IL-2R/CD25, MCP-1, CCR2, CCR4, MIP1β, CCR5, TNFальфа, TNFR1, IL-1 и IL-1Rальфа/IL-1бета; или агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток.
[0789] В некоторых вариантах осуществления агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток, выбран из противовоспалительного средства, ингибитора NADPH оксидазы (NOX2), блокатора кальциевых каналов, блокатора натриевых каналов, ингибирует GM-CSF, ингибирует CSF1R, специфично связывается с CSF-1, специфично связывается с IL-34, ингибирует активацию ядерного фактора каппа-B (NF-κB), активирует рецептор CB2 и/или является агонистом CB2, ингибитором фосфодиэстеразы, ингибирует микроРНК-155 ((miR-155) или повышающе регулирует микроРНК-124 ((miR-124). В некоторых случаях агент выбран из миноциклина, налоксона, нимодипина, Рилузола, MOR103, леналидомида, каннабиноида (необязательно WIN55 или 212-2), внутривенного иммуноглобулина (IVIg), ибудиласта, анти-miR-155 закрытой нуклеиновой кислоты (LNA), MCS110, PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945, эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003. В некоторых вариантах осуществления агент является ингибитором рецептора колониестимулирующего фактора 1 (CSF1R). Например, агент представляет собой PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамин (GW2580), AZD6495, Ki20227, BLZ945 или их фармацевтическую соль или пролекарство; эмактузумаб, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003 или является антигенсвязывающим фрагментом или комбинацией любого из предшествующих.
[0790] В некоторых вариантах осуществления изделия и/или наборы дополнительно включают один или более реагентов для тестирования биологических образцов, например, биологических образцов от пациентов, являющихся кандидатами на введение или которым вводили терапию, и необязательно инструкции по использованию реагентов или тестов. В некоторых вариантах осуществления биологический образец представляет собой или получен из образца крови, плазмы или сыворотки. В некоторых вариантах осуществления реагенты могут использоваться до введения клеточной терапии или после введения клеточной терапии, в диагностических целях, для идентификации пациентов и/или оценки способов лечения и/или токсичности. Например, в некоторых вариантах осуществления, изделие и/или наборы дополнительно содержат реагенты для измерения уровня определенных биомаркеров, например, цитокинов или аналитов, ассоциированных с токсичностью, и инструкции по измерению. В некоторых вариантах осуществления реагенты включают компоненты для осуществления in vitro теста для измерения биомаркеров (например, аналитов), такого как иммунологический анализ, основанный на аптамере тест, гистологический или цитологический тест или тест уровня экспрессии мРНК. В некоторых вариантах осуществления in vitro тест выбран из числа твердофазного иммуноферментного анализа (ELISA), иммуноблоттинга, иммунопреципитации, радиоиммуноанализа (RIA), иммунного окрашивания, теста потоковой цитометрии, поверхностного плазмонного резонанса (SPR), теста хемилюминесценции, иммунохроматографического анализа, теста ингибирования и теста авидности. В некоторых аспектах реагент является связывающим реагентом, специфически связывающимся с биомаркерами (например, аналитами). В некоторых случаях связывающий реагент является антителом или его антигенсвязывающим фрагментом, аптамером или зондом на основе нуклеиновой кислоты.
[0791] В некоторых вариантах осуществления изделия и/или наборы включают один или более реагентов, способных к обнаружению одного или более аналитов, и инструкции по использованию реагента для тестирования биологического образца от пациента, который является кандидатом на лечение, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина). В некоторых вариантах осуществления также включены инструкции по тестированию присутствия или отсутствия, уровня, количества или концентрации аналита у пациента по сравнению с пороговым значением аналита.
[0792] В некоторых вариантах осуществления включены инструкции, которые определяют, если уровень, количество или концентрация аналита в образце равны или выше порогового значения для аналита, введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту. В некоторых случаях инструкции определяют, что, если уровень, количество или концентрация аналита в образце равны или выше порогового значения для аналита, клеточную терапию вводят пациенту в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии. В некоторых случаях инструкции определяют, что, если уровень, количество или концентрация аналита в образце равны или выше порогового значения для аналита, клеточную терапию вводят в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
[0793] В некоторых вариантах осуществления инструкции по введению клеточной терапии определяют, если уровень, количество или концентрация аналита в образце ниже порогового значения, введение пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней. В некоторых вариантах осуществления инструкции по введению клеточной терапии определяют, если уровень, количество или концентрация аналита в образце ниже порогового значения, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агент или средство для лечения, способное к лечению, предотвращению, задержке или уменьшение развития токсичности, не вводят пациенту. В некоторых аспектах инструкции по введению клеточной терапии определяют, что, если уровень, количество или концентрация аналита в образце ниже порогового значения, введение клеточной терапии должно быть или может быть введено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
[0794] Изделия и/или наборы могут дополнительно включать клеточную терапию и/или дополнительно включать инструкции по использованию с, до и/или в связи с лечением клеточной терапией. В некоторых вариантах осуществления инструкции включены для введения агента, и инструкции определяют, если уровень, количество или концентрация аналита в образце равны или выше порогового значения, введение агента пациенту. В некоторых аспектах инструкции дополнительно определяют введение клеточной терапии пациенту, причем введение агента должно быть осуществлено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту.
[0795] Изделия и/или наборы могут включать контейнер и этикетку или листок-вкладыш на или связанный с контейнером. Подходящие контейнеры включают, например, бутылки, пузырьки, шприцы, мешки для IV раствора и т.д. Контейнеры могут быть сформированы из множества материалов, таких как стекло или пластмасса. Контейнер в некоторых вариантах осуществления содержит композицию, которая является отдельной или объединена с другой композицией, эффективной для лечения, профилактики и/или диагностирования состояния. В некоторых вариантах осуществления контейнер имеет стерильный порт доступа. Примеры контейнеров включают мешки для внутривенного раствора, пузырьки, включая таковые со стопорами, протыкаемым иглой для инъекции, или бутылки или пузырьки для перорально вводимых агентов. Этикетка или листок-вкладыш может указывать, что композиция используется для лечения заболевания или состояния. Изделие может включать (a) первый контейнер с композицией, содержащейся в нем, причем композиция включает генно-инженерные клетки, экспрессирующие рекомбинантный рецептор; и (b) второй контейнер с композицией, содержащейся в нем, причем композиция включает второй агент. В некоторых вариантах осуществления изделие может включать (a) первый контейнер с первой композицией, содержащейся в нем, причем композиция включает подтип генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и (b) второй контейнер с композицией, содержащейся в нем, причем композиция включает другой подтип генно-инженерных клеток, экспрессирующих рекомбинантный рецептор. Изделие может дополнительно включать листок-вкладыш, указывающий, что композиции могут использоваться для лечения определенного состояния. Также или дополнительно, изделие может дополнительно включать другой или тот же контейнер, включающий фармацевтически приемлемый буфер. Оно может дополнительно включать другие материалы, такие как другие буферы, разбавители, фильтры, иглы и/или шприцы.
VII. ПРИМЕРЫ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0796] Среди вариантов осуществления изобретения:
1. Способ лечения пациента, имеющего или подозреваемого в наличии заболевания или состояния, включающий введение пациенту дозы CD4+ и CD8+ Т-клеток, причем каждая из CD4+ и CD8+ Т-клеток, индивидуально, включает рецептор, специфично связывающийся с антигеном-мишенью, экспрессируемым заболеванием или состоянием, или его клеткой или тканью, и/или который ассоциирован с заболеванием или состоянием, причем введение включает введение множества отдельных композиций, причем множество отдельных композиций включает первую композицию, включающую одни из CD4+ Т-клеток и CD8+ Т-клеток, и введение второй композиции, включающей другие из CD4+ Т-клеток и CD8+ Т-клеток.
2. Способ согласно варианту осуществления 1, в котором рецептор, содержащийся в CD4+ Т-клетках и/или рецептор, содержащийся в CD8+ Т-клетках, включают рекомбинантный рецептор и/или в котором CD4+ Т-клетки и/или CD8+ Т-клетки генетически модифицированы так, чтобы экспрессировать рецептор.
3. Способ согласно варианту осуществления 1 или варианту осуществления 2, в котором:
введение первой композиции и введение второй композиции осуществляют в тот же день, осуществляют с интервалом от приблизительно 0 до приблизительно 12 часов, с интервалом от приблизительно 0 до приблизительно 6 часов или с интервалом от приблизительно 0 до 2 часов; или
инициацию введения первой композиции и инициацию введения второй композиции осуществляют с интервалом от приблизительно 1 минуты до приблизительно 1 часа или с интервалом от приблизительно 5 минут до приблизительно 30 минут.
4. Способ по любому из вариантов осуществления 1-3, в котором первую композицию и вторую композицию вводят с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут.
5. Способ по любому из вариантов осуществления 1-4, в котором первая композиция включает CD4+ Т-клетки.
6. Способ по любому из вариантов осуществления 1-5, в котором первая композиция включает CD8+ Т-клетки.
7. Способ по любому из вариантов осуществления 1-6, в котором инициацию введения первой композиции осуществляют до инициации введения второй композиции.
8. Способ по любому из вариантов осуществления 1-7, в котором:
доза клеток включает определенное отношение CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно или приблизительно составляет 1:1 или от приблизительно 1:3 до приблизительно 3:1; и/или
CD4+ Т-клетки, включающие рецептор в одной из первой и второй композиций, и CD8+ Т-клетки, включающие рецептор в другой из первой и второй композиций, присутствуют в определенном отношении, причем это отношение необязательно составляет или приблизительно составляет 1:1 или от приблизительно 1:3 и приблизительно 3:1; и/или
CD4+ Т-клетки, включающие рецептор, и CD8+ Т-клетки, включающие рецептор, вводимые в первой и второй композициях, присутствуют в определенном отношении, причем это отношение необязательно составляет или приблизительно составляет 1:1 или от приблизительно 1:3 и приблизительно 3:1.
9. Способ согласно варианту осуществления 8, в котором определенное отношение составляет или приблизительно составляет 1:1.
10. Способ по любому из вариантов осуществления 1-9, в котором дозу Т-клеток вводят пациенту как единственную дозу или вводят только в один раз за период двух недель, одного месяца, трех месяцев, шести месяцев, 1 года или более.
11. Способ по любому из вариантов осуществления 1-9, в котором дозу Т-клеток вводят как двойную дозу, включающую первую дозу Т-клеток и последующую дозу Т-клеток, причем одна или обе из первой дозы и второй дозы включает введение множества композиций Т-клеток.
12. Способ согласно варианту осуществления 11, в котором последующую дозу вводят в момент времени по меньшей мере или более чем приблизительно 7 дней или 14 дней после и менее чем приблизительно 28 дней после инициации введения первой дозы клеток.
13. Способ по любому из вариантов осуществления 1-12, в котором:
доза клеток включает от или от приблизительно 1x105 и до или до приблизительно 5x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 1x105 и до или до приблизительно 1x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 5x105 и до или до приблизительно 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, или от или от приблизительно 1x106 и до или до приблизительно 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, включительно.
14. Способ по любому из вариантов осуществления 1-13, в котором доза Т-клеток включает введение не более чем 1x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1x106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5x106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток.
15. Способ по любому из вариантов осуществления 1-14, в котором доза CD4+ и CD8+ Т-клеток включает:
от или от приблизительно 5x107 экспрессирующих рекомбинантный рецептор Т-клеток и до или до приблизительно 1x108 экспрессирующих рекомбинантный рецептор Т-клеток, включительно;
от или от приблизительно 1x107 и до или до приблизительно 2x108 экспрессирующих рекомбинантный рецептор Т-клеток;
от или от приблизительно 5x107 и до или до приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток
5x107 или приблизительно 5x107 экспрессирующих рекомбинантный рецептор Т-клеток; или
1x108 или приблизительно 1x108 экспрессирующих рекомбинантный рецептор Т-клеток; или
доза включает 1,5x108 или приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток;
от или от приблизительно 5x106 и до или до приблизительно 1x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток;
от или от приблизительно 1x107 и до или до приблизительно 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток;
2,5x107 или приблизительно 2,5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток;
5x107 или приблизительно 5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток; и/или
0,75x108 или приблизительно 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток.
16. Способ по любому из вариантов осуществления 1-15, в котором рекомбинантный рецептор специфично связывается с антигеном, ассоциированным с заболеванием или состоянием или экспрессируемым в клетках среды поражения, ассоциированного с заболеванием или состоянием.
17. Способ по любому из вариантов осуществления 1-16, в котором заболевание или состояние представляют собой рак.
18. Способ по любому из вариантов осуществления 1-17, в котором заболевание или состояние являются миеломой, лейкозом или лимфомой.
19. Способ по любому из вариантов осуществления 1-18, в котором антиген представляет собой ROR1, антиген созревания B-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторную тирозинкиназу erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолат-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор, содержащий домен вставки киназы (kdr), легкую каппа-цепь, антиген Ley, молекулу L1-клеточной адгезии, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, рецептор альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D) или патоген-специфический антиген.
20. Способ по любому из вариантов осуществления 1-19, в котором антиген представляет собой CD19.
21. Способ по любому из вариантов осуществления 1-20, в котором заболевание или состояние являются В-клеточной злокачественной опухолью и/или являются острым лимфообластным лейкозом (ALL), ALL взрослых, хроническим лимфообластным лейкозом (CLL), неходжкинской лимфомой (NHL) и диффузной крупноклеточной В-клеточной лимфомой (DLBCL).
22. Способ по любому из вариантов осуществления 1-21, в котором заболеванием или состоянием является NHL, и NHL выбрана из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), Т-клеточной/гистоцит-обогащенной крупноклеточной В-клеточной лимфомы (TCHRBCL), лимфомы Беркитта, мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B).
23. Способ по любому из вариантов осуществления 1-22, в котором рекомбинантный рецептор является химерным антигенным рецептором (CAR), причем необязательно рекомбинантный рецептор является химерным антигенным рецептором (CAR), причем необязательно CAR включает внеклеточный антигенраспознающий домен, специфично связывающуюся с антигеном, и внутриклеточный сигнальный домен, включающей ITAM, причем необязательно внутриклеточный сигнальный домен включает внутриклеточный домен CD3-дзэта (CD3ζ) цепи; и/или причем CAR дополнительно включает костимулирующий сигнальный домен, необязательно включающий сигнальный домен CD28 или 4-1BB.
24. Изделие, включающее (1) флакон, содержащий композицию, включающую множество CD4+ Т-клеток, экспрессирующих рекомбинантный рецептор, и (2) инструкции по введению пациенту, имеющему заболевание или состояние:
разовой дозы клеток композиции, причем разовая доза включает все или часть множества CD4+ Т-клеток, и разовой дозы композиции, включающей CD8+ Т-клетки, экспрессирующие рекомбинантный рецептор, причем флакон не включают разовую дозу композиции, включающей CD8+ Т-клетки, экспрессирующие рекомбинантный рецептор.
25. Изделие, включающее (1) флакон, содержащий композицию, включающую множество CD8+ Т-клеток, экспрессирующих рекомбинантный рецептор, и (2) инструкции по введению пациенту, имеющему заболевание или состояние:
разовой дозы клеток композиции, причем разовая доза включает все или часть множества CD8+ Т-клеток, и разовой дозы композиции, включающей CD4+ Т-клетки, экспрессирующие рекомбинантный рецептор, причем флакон не включают разовую дозу композиции, включающей CD4+ Т-клетки, экспрессирующие рекомбинантный рецептор.
26. Изделие согласно варианту осуществления 24 или варианту осуществления 25, в котором:
рекомбинантный рецептор, экспрессируемый CD4+ клетками, и рекомбинантный рецептор, экспрессируемый CD8+ Т-клетками, является одни и тем же;
рекомбинантный рецептор, экспрессируемый CD4+ клетками, и рекомбинантный экспрессируемый CD8+ Т-клетками, отличаются; или
рекомбинантный рецептор, экспрессируемый CD4+ клетками, и рекомбинантный экспрессируемый CD8+ Т-клетками, связываются с одним и тем же антигеном, экспрессирующимся или ассоциированным с заболеванием или состоянием, или его клеткой или тканью.
27. Изделие по любому из вариантов осуществления 24-26, в котором флакон включает более чем или более чем приблизительно 10x106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток, более чем или более чем приблизительно 15x106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток, более чем или более чем приблизительно 25x106 Т-клеток или экспрессирующих рекомбинантный рецептор Т-клеток.
28. Изделие по любому из вариантов осуществления 24-27, в котором флакон включает от приблизительно 10 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 25 миллионов клеток на мл, от приблизительно 10 миллионов клеток на мл до приблизительно 15 миллионов клеток на мл, от 15 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 15 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл, от приблизительно 15 миллионов клеток на мл до приблизительно 25 миллионов клеток на мл, от приблизительно 25 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл, от приблизительно 25 миллионов клеток на мл до приблизительно 50 миллионов клеток на мл и от приблизительно 50 миллионов клеток на мл до приблизительно 70 миллионов клеток на мл.
29. Изделие по любому из вариантов осуществления 24-28, в котором композиция дополнительно включает криопротектор и/или изделие дополнительно включают инструкции по размораживанию композиции до введения пациенту.
30. Изделие по любому из вариантов осуществления 24-29, в котором:
множество CD4+ клеток, экспрессирующих рекомбинантный рецептор, и множество CD8+ клеток, экспрессирующих рекомбинантный рецептор, в изделии и/или CD4+ клетки и CD8+ клетки в пузырьке, присутствуют в определенном отношении, которое необязательно составляет или приблизительно составляет 1:1 или составляет от приблизительно 1:3 до приблизительно 3:1; и/или
изделие дополнительно включает информацию или инструкции, определяющие введение множества клеток в определенном отношении клеток множества CD4+ клеток, экспрессирующих рекомбинантный рецептор, и клеток множества CD8+ клеток, экспрессирующих рекомбинантный рецептор, и/или CD4+ клеток и CD8+ клеток, причем это отношение необязательно составляет или приблизительно составляет 1:1 или составляет от приблизительно 1:3 до приблизительно 3:1; и/или
изделие дополнительно включает информацию или инструкции, определяющие введение составов в пузырьках в определенном объемном или весовом отношении, которое необязательно составляет или приблизительно составляет 1:1 и/или составляет от или от приблизительно 3:1 и до или до приблизительно 1:3, в объемном или весовом отношении, и/или необязательно соответствует отношению CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет или приблизительно составляет 1:1 или составляет от приблизительно 1:3 до приблизительно 3:1.
31. Изделие согласно варианту осуществления 30, в котором определенное отношение составляет или приблизительно составляет 1:1.
32. Изделие по любому из вариантов осуществления 24-31, в котором множество пузырьков или множество клеток, или разовая доза клеток, определенных для введения, коллективно, включают дозу клеток, включающих от или от приблизительно 1x105 до 5x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от 1x105 до 1x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, от или от приблизительно 5x105 до 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, или от или от приблизительно 1x106 до 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, включительно;
изделие включает одну или более разовых доз CD4+ и CD8+ клеток или CD4+рецептор+ клеток и CD8+рецептор+ клеток, причем разовая доза включает от или от приблизительно 1x107 и до или до приблизительно 2x108 экспрессирующих рекомбинантный рецептор Т-клеток, от или от приблизительно 5x107 и до или до приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток, 5x107 или приблизительно 5x107 экспрессирующих рекомбинантный рецептор Т-клеток, 1x108 или приблизительно 1x108 экспрессирующих рекомбинантный рецептор Т-клеток, или до или до приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток, причем необязательно информация в изделии определяет введение одной или множества разовых доз и/или объема, соответствующего такой одной или множеству разовых доз;
изделие включает одну или более разовых доз CD8+ клеток, причем доза включает от или от приблизительно 5x106 и до или до приблизительно 1x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, доза включает от или от приблизительно 1x107 и до или до приблизительно 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, доза включает 2,5x107 или приблизительно 2,5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, или доза включает 5x107 или приблизительно 5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, или доза включает 0,75x108 или приблизительно 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток, причем необязательно информация в изделии определяет введение одной или множества разовых доз и/или объема, соответствующего такой одной или множеству разовых доз.
33. Изделие по любому из вариантов осуществления 24-32, в котором клетки в изделии, коллективно, включают дозу клеток, включающих не более чем 1x108 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5x107 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 1x106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток, не более чем 0,5x106 общих экспрессирующих рекомбинантный рецептор Т-клеток или общих Т-клеток.
34. Изделие по любому из вариантов осуществления 24-33, в котором множество контейнеров, коллективно, включают дозу клеток, включающих:
от или от приблизительно 5x107 экспрессирующих рекомбинантный рецептор Т-клеток до 1x108 экспрессирующих рекомбинантный рецептор Т-клеток, включительно;
от или от приблизительно 1x107 и до или до приблизительно 2x108 экспрессирующих рекомбинантный рецептор Т-клеток;
от или от приблизительно 5x107 и до или до приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток;
5x107 или приблизительно 5x107 экспрессирующих рекомбинантный рецептор Т-клеток;
1x108 или приблизительно 1x108 экспрессирующих рекомбинантный рецептор Т-клеток;
1,5x108 или приблизительно 1,5x108 экспрессирующих рекомбинантный рецептор Т-клеток;
от или от приблизительно 5x106 и до или до приблизительно 1x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток;
от или от приблизительно 1x107 и до или до приблизительно 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток;
2,5x107 или приблизительно 2,5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток;
5x107 или приблизительно 5x107 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток; или
0,75x108 или приблизительно 0,75x108 экспрессирующих рекомбинантный рецептор CD8+ Т-клеток.
35. Изделие по любому из вариантов осуществления 24-34, в котором инструкции определяют введение всех или части CD4+ Т-клеток и всех или части CD8+ Т-клеток с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часов.
36. Изделие по любому из вариантов осуществления 24-34, в котором инструкции определяют введение CD4+ Т-клеток и CD8+ Т-клеток с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут.
37. Изделие по любому из вариантов осуществления 24-36, в котором инструкции определяют введение CD4+ Т-клеток до введения CD8+ клеток.
38. Изделие по любому из вариантов осуществления 24-36, в котором инструкции определяют введение CD8+ Т-клеток до введения CD4+ клеток.
39. Изделие по любому из вариантов осуществления 24-38, в котором рекомбинантный рецептор специфично связывается с антигеном, ассоциированным с заболеванием или состоянием или экспрессируемым в клетках среды поражения, ассоциированной с заболеванием или состоянием.
40. Изделие по любому из вариантов осуществления 24-39, причем заболевание или состояние представляют собой рак.
41. Изделие по любому из вариантов осуществления 24-40, причем заболевание или состояние являются миеломой, лейкозом или лимфомой.
42. Изделие по любому из вариантов осуществления 24-41, причем антиген представляет собой ROR1, антиген созревания B-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторная тирозинкиназа erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA, и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолат-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор, содержащий домен вставки киназы (kdr), легкую каппа-цепь, антиген Ley, молекулу L1-клеточной адгезии, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, рецептор альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D), или патоген-специфический антиген.
43. Изделие по любому из вариантов осуществления 24-42, причем антиген является CD19.
44. Изделие по любому из вариантов осуществления 24-43, причем заболевание или состояние являются В-клеточной злокачественной опухолью и/или являются острым лимфообластным лейкозом (ALL), ALL взрослых, хроническим лимфообластным лейкозом (CLL), неходжкинской лимфомой (NHL) и диффузной крупноклеточной В-клеточной лимфомой (DLBCL).
45. Изделие по любому из вариантов осуществления 24-44, причем заболевание или состояние представляет собой NHL, и NHL выбрана из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), Т-клеточной/гистоцит-обогащенной крупноклеточной В-клеточной лимфомы (TCHRBCL), лимфомы Беркитта, мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B).
46. Изделие по любому из вариантов осуществления 24-45, причем Т-клетками являются первичные Т-клетки, полученные от пациента.
47. Изделие по любому из вариантов осуществления 24-46, причем Т-клетки являются аутологичными для пациента.
48. Изделие по любому из вариантов осуществления 24-46, причем Т-клетки являются аллогенными для пациента.
49. Способ лечения пациента, имеющего или подозреваемого в наличии В-клеточной злокачественной опухоли, необязательно неходжкинской лимфомы (NHL), включающий введение пациенту дозы Т-клеток, включающих Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым NHL, причем:
доза Т-клеток включает от или от приблизительно 2,5x107 CAR-экспрессирующих Т-клеток до 2x108 CAR-экспрессирующих Т-клеток, включительно, необязательно от или от приблизительно 5x107 CAR-экспрессирующих Т-клеток и до или до приблизительно 1x108 CAR-экспрессирующих Т-клеток, включительно; и
злокачественная опухоль, необязательно NHL, включает диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B, и причем пациент является или был идентифицирован как имеющий статус 0 или 1 согласно Eastern Cooperative Oncology Group Performance Status (ECOG), причем необязательно способ дополнительно включает идентификацию пациента как имеющего диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B, имеющего статус ECOG 0 или 1.
50. Способ согласно варианту осуществления 49, в котором доза Т-клеток включает определенное отношение CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет приблизительно 1:1 или от приблизительно 1:3 до приблизительно 3:1.
51. Способ лечения пациента, имеющего неходжкинскую лимфому (NHL), включающий введение пациенту дозы Т-клеток, включающих Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым NHL, причем доза Т-клеток включает определенное отношение CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение приблизительно составляет или составляет 1:1, причем NHL включает диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B.
52. Способ согласно варианту осуществления 51, в котором пациент является или был идентифицирован как имеющий статус 0, 1 или 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG).
53. Способ согласно варианту осуществления 51 или варианту осуществления 52, в котором пациент является или был идентифицирован как имеющий статус ECOG 0 или 1.
54. Способ по любому из вариантов осуществления 49-53, в котором:
по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полного ответа (CR), причем необязательно CR является длительным или длительным по меньшей мере у 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR, в течение 3 месяцев или более или в течение 6 месяцев или более; и/или
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR за один месяц и/или за три месяца, остаются в состоянии ответа, остаются в состоянии CR и/или остаются в живых или остаются в живых без прогрессии в течение 3 месяцев или более и/или в течение 6 месяцев или более и/или более чем девять месяцев; и/или
по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR), причем необязательно OR является длительным или длительным по меньшей мере у 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR, в течение 3 месяцев или более или в течение 6 месяцев или более; и/или
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR, остаются в состоянии ответа или остатся в живых в течение 3 месяцев или более и/или в течение 6 месяцев или более; и/или
по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70% пациентов, которые, в момент или до введения дозы клеток имели или были идентифицированы как имеющие лимфому double/triple hit или рецидив, необязательно рецидив в течение 12 месяцев, после введения трансплантата аутологичных стволовых клеток (ASCT) достигли OR, причем необязательно OR длится в течение 3 месяцев или более или в течение 6 месяцев или более.
55. Способ по любому из вариантов осуществления 49-54, в котором:
клетки являются аутологичными для пациента, и никакое минимальное абсолютное количество лимфоцитов (ALC) для афереза не требуется и/или определяется для производства терапии; и/или
клетки получают способом, который, по меньшей мере для 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% пациентов, имеющих заболевание или состояние, или выбранной популяции пациентов, способен генерировать клеточный продукт для введения и результатов согласно способу.
56. Способ по любому из вариантов осуществления 49-55, в котором:
более чем или более чем приблизительно 50%, приблизительно 60%, приблизительно 70% или приблизительно 80% пациентов, получающих лечение согласно способу, не показывают синдром высвобождения цитокинов (CRS) степени 3 или большей и/или не показывают нейротоксичность степени 3 или большей и/или более чем 40% или 50% или 55% не показывают нейротоксичности или CRS.
57. Способ лечения пациента, имеющего неходжкинскую лимфому (NHL), включающий введение пациенту дозы Т-клеток, включающих Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым NHL, в котором:
доза Т-клеток включает от или от приблизительно 5x107 экспрессирующих рекомбинантный рецептор Т-клеток до 1x108 экспрессирующих рекомбинантный рецептор Т-клеток, включительно, причем указанная доза включает определенное отношение CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор, и/или CD4+ клеток к CD8+ клеткам, причем это отношение приблизительно составляет или составляет 1:1; и
способ приводит к (1) полному ответу (CR) у по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% получающих лечение пациентов и/или объективному ответу (OR) у по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% получающих лечение пациентов, и (2) приводит к не более чем 50% пациентов, показывающих синдром высвобождения цитокинов (CRS) выше, чем степени 2, и/или нейротоксичность выше, чем степени 2.
58. Способ согласно варианту осуществления 57, в котором по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70% пациентов, которые, в момент или до введения дозы клеток имели или были идентифицированы как имеющие лимфому double/triple hit или рецидив после введения трансплантата аутологичных стволовых клеток (ASCT), достигли OR, причем необязательно OR длится в течение 3 месяцев или более или в течение 6 месяцев или более.
59. Способ согласно варианту осуществления 57, в котором:
CR или OR длится в течение более чем 3 месяца или более чем 6 месяцев; и/или
по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают CR, который является длительным; и/или
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом и которые достигают CR, остается в состоянии CR или остается в состоянии ответа, или остается в живых в течение 3 месяцев или более или в течение 6 месяцев или более, или в течение 9 месяцев или более; и/или
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом, которые достигают CR за один месяц и/или за три месяца, остается в состоянии ответа, остается в состоянии CR и/или остается в живых или остается в живых без прогрессии в течение 3 месяцев или более и/или в течение 6 месяцев или более и/или более чем девять месяцев; и/или
по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR), причем необязательно OR является длительным или длительным у по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR, в течение 3 месяцев или более или в течение 6 месяцев или более; и/или
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом и достигающих OR, остается в состоянии ответа или остается в живых в течение 3 месяцев или более и/или в течение 6 месяцев или более.
60. Способ по любому из вариантов осуществления 49-59, в котором:
в момент или до введения дозы клеток пациент является или был идентифицирован как имеющий лимфому, ассоциированную с или включающую участие центральной нервной системы (ЦНС); и/или
по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% пациентов, получающих лечение согласно способу, которые, в момент или до введения дозы клеток показвали или были идентифицированы как показывающие лимфому с участием ЦНС, достигли устранения заболевания ЦНС.
61. Способ лечения пациента, включающий введение пациенту, имеющему лимфому, дозы Т-клеток, включающих Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфично связывающийся с антигеном-мишенью, экспрессируемым лимфомой, причем лимфома у пациента ассоциирована с или включает участие центральной нервной системы (ЦНС).
62. Способ согласно варианту осуществления 60 или варианту осуществления 61, в котором, в момент или до введения дозы клеток пациент имеет поражение мозга, необязательно поражение височной доли мозга.
63. Способ согласно варианту осуществления 62, в котором лимфома является В-клеточной злокачественной опухолью.
64. Способ согласно варианту осуществления 61 или варианту осуществления 62, в котором лимфома является неходжкинской лимфомой (NHL).
65. Способ по любому из вариантов осуществления 60-64, в котором:
по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полного ответа (CR) или ремиссии заболевания ЦНС, причем необязательно CR или ремиссия заболевания ЦНС являются длительными или длительными у по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR, в течение 3 месяцев или более или в течение 6 месяцев или более; и/или
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR или ремиссии заболевания ЦНС за один месяц и/или за три месяца, остаются в состоянии ответа, остаются в состоянии CR и/или остаются в живых или остаются в живых без прогрессии в течение 3 месяцев или более и/или в течение 6 месяцев или более и/или более чем девять месяцев; и/или
по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR) или ремиссии заболевания ЦНС, причем необязательно OR или ремиссия заболевания ЦНС являются длительными или являются длительными у по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR, в течение 3 месяцев или более или в течение 6 месяцев или более; и/или
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR или ремиссии заболевания ЦНС, остаются в состоянии ответа или остаются в живых в течение 3 месяцев или более и/или в течение 6 месяцев или более; и/или
поражение мозга уменьшается в размере или объеме, необязательно на более чем или более чем приблизительно 25%, 50%, 75% или более; и/или
достигаются сокращение или ремиссия, или клиренс заболевания ЦНС, необязательно достигаются у по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу.
66. Способ по любому из вариантов осуществления 49-65, в котором:
более чем или более чем приблизительно 30%, 35%, 40% или 50% пациентов, получающих лечение согласно способу, не показывают какой-либо степени синдрома высвобождения цитокинов (CRS) или нейротоксичности; и/или
по меньшей мере у или приблизительно у 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% пациентов, получающих лечение согласно способу, не наблюдается раннего начала CRS или нейротоксичности и/или не наблюдается начало CRS ранее, чем через 3 дня после инициации введения, и/или не наблюдается начало нейротоксичности ранее, чем через 5 дней после инициации введения, и/или причем среднее начало нейротоксичности среди пациентов, получающих лечение согласно способу, на блюдается в момент или после среднего пика, или среднее время для устранения CRS у пациентов, получающих лечение согласно способу, и/или среднее начало нейротоксичности среди пациентов, получающих лечение согласно способу, составляет более чем или приблизительно 8, 9, 10 или 11 дней.
67. Способ по любому из вариантов осуществления 49-66, в котором:
до инициации введения дозы клеток пациенту не вводили агент или средство для лечения, способное к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности; и/или
пациенту не вводили агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого, в течение промежутка времени после введения дозы, причем промежуток времени необязательно составляет или приблизительно составляет 1, 2, 3, 4, 5 дней, или необязательно составляет или приблизительно составляет 6, 7, 8, 9, 10, 11 дней, или необязательно составляет 1, 2, 3 или 4 недели; и/или
пациенту не вводили агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого, после введения дозы, до того как или если пациент не показывает признаков или симптомов токсичности и/или до того как или если пациент не показывает признаков или симптомов токсичности кроме повышения температуры, причем необязательно повышение температуры не является длительным повышением температуры, или повышение температуры составляет или было уменьшено на или уменьшено более чем на 1°C после лечения жаропонижающим средством; и/или
введение и любое наблюдение осуществляют на амбулаторной основе и/или без допуска пациента в больницу и/или без оставления на ночь в больнице и/или не требуя допуска или оставления на ночь в больнице, необязательно если или пока пациент не показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством.
68. Способ по любому из вариантов осуществления 49-67, в котором:
до инициации введения дозы клеток пациенту не вводили анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб, и/или не вводили стероид, необязательно дексаметазон; и/или
пациенту не вводили анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб, и/или не вводили стероид, необязательно дексаметазон, в течение промежутка времени после введения дозы, причем промежуток времени необязательно составляет или приблизительно составляет 1, 2, 3, 4, 5 дней, или необязательно составляет или приблизительно составляет 6, 7, 8, 9, 10, 11 дней, или необязательно составляет 1, 2, 3 или 4 недели; и/или
пациенту не вводили анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб, и/или не вводили стероид, необязательно дексаметазон, после введения дозы клеток, до того как или если пациент не показывает признаков или симптомов токсичности, необязательно нейротоксичности или CRS, и/или до того как или если пациент не показывает признаков или симптомов токсичности, необязательно нейротоксичности или CRS, кроме повышения температуры, причем необязательно повышение температуры не является длительным повышением температуры, или повышение температуры составляет или было уменьшено на или уменьшено более чем на 1°C после лечения жаропонижающим средством; и/или
введение и любое наблюдение осуществляют на амбулаторной основе и/или без допуска пациента в больницу и/или без оставления на ночь в больнице и/или не требуя допуска или оставления на ночь в больнице, необязательно если или пока пациент не показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством.
69. Способ по любому из вариантов осуществления 49-67, в котором:
введение осуществляют на амбулаторной основе и/или не требуя допуска или оставления на ночь в больнице; и
если пациент показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством, пациента госпитализируют или оставляют на ночь в больнице и/или вводят агент или лечение для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого.
70. Способ по любому из вариантов осуществления 49-60 и 64-69, в котором NHL выбран из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B).
71. Способ по любому из вариантов осуществления 49-60 и 64-70, в котором NHL включает диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B.
72. Способ по любому из вариантов осуществления 49-60 и 64-71, в котором NHL включает DLBCL.
73. Способ по любому из вариантов осуществления 49-60 и 70-72, в котором DLBCL не включает DLBCL, трансформированную из MZL и CLL (Рихтера), и/или пациент, которому вводят дозу клеток, имеет DLBCL, характеризуемую как de novo или трансформированная из вялотекущей, и/или не включает DLBCL, трансформированную из MZL и CLL.
74. Способ по любому из вариантов осуществления 49-60 и 64-73, в котором NHL не включает PMBCL, и/или пациент, которому вводят дозу клеток, не имеет PMBCL.
75. Способ по любому из вариантов осуществления 57-73, в котором пациент является или был идентифицирован как имеющий статус 0, 1 или 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG).
76. Способ по любому из вариантов осуществления 49-75, в котором пациент является или был идентифицирован как имеющий статус ECOG 0 или 1.
77. Способ по любому из вариантов осуществления 49-76, в котором, в момент или непосредственно перед введением дозы клеток, пациент имеет рецидив после ремиссии после лечения с или стал рефрактерным к одной или более предшествующих терапий NHL, необязательно одной, двум или трем предшествующим терапиям, отличным от другой дозы клеток, экспрессирующих CAR.
78. Способ по любому из вариантов осуществления 49-77, в котором, в момент или до введения дозы клеток:
пациент является или был идентифицирован как имеющий лимфому double/triple hit; и/или
пациент является или был идентифицирован как имеющий хеморефрактерную лимфому, необязательно хеморефрактерную DLBCL; и/или
пациент не достиг полной ремиссии (CR) в ответ на предшествующую терапию; и/или
пациент имеет рецидив в течение 1 года или спустя менее чем 1 год после получения трансплантата аутологичных стволовых клеток (ASCT).
79. Способ по любому из вариантов осуществления 49-78, включающий, до введения дозы клеток, идентификацию или отбор пациента для введения дозы клеток, имеющего:
лимфому double/triple hit;
хеморефрактерную лимфому, необязательно хеморефрактерную DLBCL;
не достиг полной ремиссии (CR) в ответ на предшествующую терапию для лечения злокачественной опухоли, необязательно NHL; и/или
имеет рецидив в течение 1 года или спустя менее чем 1 год после получения трансплантата аутологичных стволовых клеток (ASCT); и/или
имеет лимфому, ассоциированную с или включающую участие центральной нервной системы (ЦНС).
80. Способ по любому из вариантов осуществления 49-79, дополнительно включающий введение дополнительного терапевтического агента или терапии, необязательно отличной от клеточной терапии, необязательно отличной от CAR+ Т-клеточной терапии.
81. Способ согласно варианту осуществления 80, в котором дополнительный терапевтический агент или терапия предназначены для лечения NHL или злокачественной опухоли и/или увеличивают персистирование, активность и/или эффективность дозы клеток.
82. Способ согласно варианту осуществления 80 или варианту осуществления 81, в котором дополнительный терапевтический агент или терапию вводят, если пациент не показывает ответ, необязательно не показывает CR или OR, на клеточную терапию в течение 1 месяца, в течение 2 месяцев или в течение 3 месяцев после введения дозы клеток.
83. Способ согласно варианту осуществления 80 или варианту осуществления 81, в котором дополнительный терапевтический агент или терапию вводят пациенту:
который является или был идентифицирован как имеющий стабильное или прогрессирующее заболевание (SD/PD) после лечения предшествующей терапией, необязательно предшествующей терапией химиотерапевтическим агентом;
который является или был идентифицирован как имеющий статус 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG);
который является или был идентифицирован как имеющий трансформированную фолликулярную лимфому (tFL); или
который является или был идентифицирован как имеющий DLBCL, трансформированную из MZL и CLL.
84. Способ по любому из вариантов осуществления 80-83, включающий, до введения дозы клеток или дополнительного терапевтического агента или терапии, идентификацию или отбор пациента для введения дозы клеток, имеющего:
стабильное или прогрессирующее заболевание (SD/PD) после лечения предшествующей терапией, необязательно предшествующей терапией химиотерапевтическим агентом;
Eastern Cooperative Oncology Group Performance Status (ECOG) статус 2;
трансформированную фолликулярная лимфома (tFL); или
DLBCL, трансформированную из MZL и CLL.
85. Способ по любому из вариантов осуществления 80-84, в котором дополнительный терапевтический агент или терапию вводят до, с или одновременно и/или после инициации введения дозы клеток.
86. Способ по любому из вариантов осуществления 49-85, в котором:
CAR включает scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно представляет собой или включает 4-1BB, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно представляет собой или включает CD3дзета сигнальный домен и необязательно дополнительно включает спейсер между трансмембранным доменом и scFv;
CAR включает, в указанном порядке, scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно представляет собой или включает 4-1BB сигнальный домен, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно является CD3дзета сигнальный домен; или
CAR включает, в указанном порядке, scFv, специфичный для антигена, спейсер, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно является 4-1BB сигнальным доменом, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно представляет собой или включает CD3дзета сигнальный домен; и причем:
спейсер является необязательно полипептидным спейсером, который (a) включает или состоит из всего или части шарнирного участка иммуноглобулина или его модифицированной версии или включает приблизительно 15 аминокислот или менее и не включает внеклеточный домен CD28 или внеклеточный домен CD8, (b) включает или состоит из всего или части шарнирного участка иммуноглобулина, необязательно шарнира IgG4 или его модифицированной версии и/или включает приблизительно 15 аминокислот или менее и не включает внеклеточный домен CD28 или внеклеточный домен CD8, или (c) имеет длину 12 или приблизительно 12 аминокислот и/или включает или состоит из всего или части шарнирного участка иммуноглобулина, необязательно IgG4 или его модифицированной версии; или (d) имеет или состоит из последовательности SEQ ID NO: 1, последовательности, кодируемой SEQ ID NO: 2, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, или варианта любой из указанных, имеющего по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, или (e) включает или состоит из формулы X1PPX2P, где X1 является глицином, цистеином или аргинином, и X2 является цистеином или треонином; и/или
костимулирующий домен включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней; и/или
первичный сигнальный домен включает SEQ ID NO: 13 или 14 или 15, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней; и/или
scFv включает последовательность CDRL1 RASQDISKYLN (SEQ ID NO: 35), последовательность CDRL2 SRLHSGV (SEQ ID NO: 36), и/или последовательность CDRL3 GNTLPYTFG (SEQ ID NO: 37), и/или последовательность CDRH1 DYGVS (SEQ ID NO: 38), последовательность CDRH2 VIWGSETTYYNSALKS (SEQ ID NO: 39) и/или последовательность CDRH3 YAMDYWG (SEQ ID NO: 40), или причем scFv включает вариабельную область тяжелой цепи FMC63 и вариабельную область легкой цепи FMC63 и/или последовательность CDRL1 FMC63, последовательность CDRL2 FMC63, последовательность CDRL3 FMC63, последовательность CDRH1 FMC63, последовательность CDRH2 FMC63 и последовательность CDRH3 FMC63, или связывается с тем же эпитопом, как, или конкурирует за связывание с любым из указанных, и причем необязательно scFv включает, в указанном порядке, VH, линкер, необязательно включающий SEQ ID NO: 24, и VL и/или scFv включает гибкий линкер и/или включает аминокислотную последовательность, представленную как SEQ ID NO: 24.
87. Способ по любому из вариантов осуществления 49-86, в котором антиген является В-клеточной антигеном, который необязательно представляет собой CD19.
88. Способ по любому из вариантов осуществления 1-23 и 49-87, в котором, до введения, пациент был предварительно кондиционирован с использованием противолимфоцитарной терапии, включающей введение флударабина и/или циклофосфамида.
89. Способ по любому из вариантов осуществления 1-23 и 49-88, дополнительно включающий, непосредственно перед введением, введение пациенту противолимфоцитарной терапии, включающей введение флударабина и/или циклофосфамида.
90. Способ согласно варианту осуществления 88 или варианту осуществления 89, в котором противолимфоцитарная терапия включает введение циклофосфамида в количестве приблизительно 200-400 мг/м2, необязательно в количестве, составляющем или приблизительно составляющем 300 мг/м2, включительно, и/или флударабин в количестве приблизительно 20-40 мг/м2, необязательно 30 мг/м2, в сутки в течение 2-4 дней, необязательно в течение 3 дней, или в котором противолимфоцитарная терапия включает введение циклофосфамида в количестве приблизительно 500 мг/м2.
91. Способ согласно варианту осуществления 88 или варианту осуществления 89, в котором:
противолимфоцитарная терапия включает введение циклофосфамида в количестве, составляющем или приблизительно составляющем 300 мг/м2, и флударабина в количестве приблизительно 30 мг/м2 в сутки в течение 3 дней; и/или
противолимфоцитарная терапия включает введение циклофосфамида в количестве, составляющем или приблизительно составляющем 500 мг/м2, и флударабина в количестве приблизительно 30 мг/м2 в сутки в течение 3 дней.
92. Способ по любому из вариантов осуществления 49-91, в котором введение дозы клеток и/или противолимфоцитарной терапии осуществляют через амбулаторную доставку, необязательно если или пока пациент не показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством.
93. Способ согласно варианту осуществления 92, в котором, если пациент показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством, пациента госпитализируют или оставляют на ночь в больнице и/или вводят агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого.
94. Способ по любому из вариантов осуществления 49-92, в котором дозу клеток вводят парентерально, необязательно внутривенно.
95. Способ по любому из вариантов осуществления 49-94, в котором:
по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полной ремиссии (CR), показывают выживаемость без прогрессий (PFS) и/или полную выживаемость (OS) более чем или приблизительно 3 месяца, 6 месяцев или 12 месяцев;
в среднем пациенты, получающие лечение согласно способу, показывают в среднем PFS или OS более чем или приблизительно 6 месяцев, 12 месяцев или 18 месяцев; и/или
пациент показывает PFS или OS после терапии в течение по меньшей мере или приблизительно 6, 12, 18 или более месяцев.
96. Способ по любому из вариантов осуществления 1-23 и 49-95, в котором, в момент или спустя приблизительно 14 или 28 дней после инициации введения дозы клеток, число CAR+ Т-клеток, необязательно CAR+ CD8+ Т-клеток и/или CAR+ CD4+ Т-клеток, детектируемых в крови пациента или большинства пациентов, получающих лечение способом, составляет более чем 1 клетка на мкл, более чем 5 клеток на мкл или более чем 10 клеток на мкл.
97. Способ по любому из вариантов осуществления 1-23 и 49-96, в котором Т-клетками являются первичные Т-клетки, полученные от пациента.
98. Способ по любому из вариантов осуществления 1-23 и 49-97, в котором Т-клетки являются аутологичными для пациента.
99. Способ по любому из вариантов осуществления 1-23 и 49-97, в котором Т-клетки являются аллогенными для пациента.
100. Способ по любому из вариантов осуществления 49-99, в котором Т-клетки включают CD4+ Т-клетки, экспрессирующие CAR, и CD8+ Т-клетки, экспрессирующие CAR, и введение включает введение множества отдельных композиций, причем указанное множество отдельных композиций включает первую композицию, включающую одни из CD4+ Т-клеток и CD8+ Т-клеток, и вторую композицию, включающую другие из CD4+ Т-клеток или CD8+ Т-клеток.
101. Способ согласно варианту осуществления 100, в котором:
первую композицию и вторую композицию вводят с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часа, или в котором введение первой композиции и введение второй композиции осуществляют в тот же день, осуществляют с интервалом от приблизительно 0 до приблизительно 12 часов, с интервалом от приблизительно 0 до приблизительно 6 часов или с интервалом от приблизительно 0 до 2 часов; и/или
инициацию введения первой композиции и инициацию введения второй композиции осуществляют с интервалом от приблизительно 1 минутой до приблизительно 1 часа или с интервалом от приблизительно 5 минут до приблизительно 30 минут.
102. Способ согласно варианту осуществления 100 или варианту осуществления 101, в котором первую композицию и вторую композицию вводят с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут.
103. Способ по любому из вариантов осуществления 100-102, в котором первая композиция включает CD4+ Т-клетки.
104. Способ по любому из вариантов осуществления 100-102, в котором первая композиция включает CD8+ Т-клетки.
105. Способ по любому из вариантов осуществления 100-104, в котором первую композицию вводят до второй композиции.
106. Способ по любому из вариантов осуществления 49-105, в котором дозу Т-клеток вводят пациенту как единственную дозу или вводят только в один раз за период двух недель, одного месяца, трех месяцев, шести месяцев, 1 года или более.
107. Способ по любому из вариантов осуществления 49-106, в котором дозу Т-клеток вводят как двойную дозу, включающая первую дозу Т-клеток и последующую дозу Т-клеток,при чем одна или обе из первой дозы и второй дозы включает введение множества композиций Т-клеток.
108. Способ согласно варианту осуществления 107, в котором последующую дозу вводят в момент времени по меньшей мере или более чем приблизительно 7 дней или 14 дней после и менее чем приблизительно 28 дней после инициации введения первой дозы клеток.
109. Способ оценки вероятности ответа на клеточную терапию, включающий:
(a) оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбраны из ферритина, LDH, CXCL10, G-CSF и IL-10, причем:
биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением, с определением, таким образом, вероятности, что пациент достигнет ответа на клеточную терапию.
110. Способ согласно варианту осуществления 109, дополнительно включающий введение клеточной терапии пациенту, если для пациента показана вероятность достижения ответа.
111. Способ отбора пациента для лечения, включающий:
(a) оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбраны из ферритина, LDH, CXCL10, G-CSF и IL-10, причем:
биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) отбор пациента, для которого определена вероятность ответа на лечение на основе результатов определения вероятности, что пациент достигнет ответа на клеточную терапию, путем сравнения, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением.
112. Способ согласно варианту осуществления 111, дополнительно включающий введение клеточной терапии пациенту, выбранному для лечения.
113. Способ лечения, включающий:
(a) отбор пациента, для которого определена вероятность ответа на лечение клеточной терапией на основе результатов определения вероятности, что пациент достигнет ответа на клеточную терапию, путем сравнения, индивидуально, уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбраны из ферритина, LDH, CXCL10, G-CSF и IL-10, с пороговым значением, причем:
биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) введение клеточной терапии пациенту, выбранному для лечения.
114. Способ по любому из вариантов осуществления 109-113, в котором:
пациент, вероятно, достигнет ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения, и пациент вряд ли достигнет ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения.
115. Способ по любому из вариантов осуществления 109-114, в котором пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации, или равно или приблизительно равно медиане или среднему уровню, количеству или концентрации, аналита в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал достигать ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
116. Способ по любому из вариантов осуществления 109-114, в котором пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал показывать стабильное заболевание (SD) и/или прогрессирующее заболевание (PD) после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
117. Способ по любому из вариантов осуществления 109-116, в котором ответ включает объективный ответ.
118. Способ согласно варианту осуществления 117, в котором объективный ответ включает полный ответ (CR) или частичный ответ (PR).
119. Способ оценки вероятности длительного ответа на клеточную терапию, включающий:
(a) оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбраны из LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β, причем:
биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) сравнение, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением, с определением, таким образом, вероятности, что пациент достигнет длительного ответа на клеточную терапию.
120. Способ согласно варианту осуществления 119, дополнительно включающий введение клеточной терапии пациенту, если для пациента показана вероятность достижения ответа.
121. Способ отбора пациента для лечения, включающий:
(a) оценку уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбраны из LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β, причем:
биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) отбор пациента, для которого определена вероятность ответа на лечение на основе результатов определения вероятности, что пациент достигнет длительного ответа на клеточную терапию, путем сравнения, индивидуально, уровня, количества или концентрации аналита в образце с пороговым значением.
122. Способ согласно варианту осуществления 121, дополнительно включающий введение клеточной терапии пациенту, выбранному для лечения.
123. Способ лечения, включающий:
(a) отбор пациента, для которого определена вероятность ответа на лечение клеточной терапией на основе результатов определения вероятности, что пациент достигнет длительного ответа на клеточную терапию, путем сравнения, индивидуально, уровня, количества или концентрации одного или более аналитов в биологическом образце с пороговым значением, причем один или более аналитов выбраны из LDH, ферритина, CRP, D-димера, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α, CXCL-10, IL-8, MCP-1 и MIP-1β, причем:
биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия включает дозу генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) введение клеточной терапии пациенту, выбранному для лечения.
124. Способ по любому из вариантов осуществления 120-123, в котором:
пациент, вероятно, достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут ниже порогового значения, и пациент вряд ли достигнет длительного ответа, если уровень, количество или концентрация одного или более аналитов будут выше порогового значения.
125. Способ по любому из вариантов осуществления 120-124, в котором пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации, или равно или приблизительно равно медиане или среднему уровню, количеству или концентрации, аналита в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы продолжал достигать длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
126. Способ по любому из вариантов осуществления 120-124, в котором пороговое значение находится в пределах 25%, 20%, 15%, 11% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем каждый из пациентов группы не достигал длительного ответа после введения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
127. Способ по любому из вариантов осуществления 120-126, в котором длительный ответ включает полный ответ (CR) или частичный ответ (PR), который длится в течение 3 месяцев, 4 месяца, 5 месяцев или 6 месяцев или более.
128. Способ по любому из вариантов осуществления 120-127, в котором длительный ответ включает CR или PR, который длится в течение по меньшей мере 3 месяцев.
129. Способ оценки риска развития токсичности после введения клеточной терапии, включающий:
(a) оценку уровня, количества или концентрации одного или более аналитов в биологическом образце от пациента или объемного параметра опухолевой массы у пациента, причем один или более аналитов выбраны из LDH, ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-8, IL-10, IL-15, IL-16 TNF-α, IFN-α2, MCP-1, MIP-1α и MIP-1β, причем:
пациентом является кандидат на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) сравнение, индивидуально, уровня, количества или концентрации аналита в образце или объемного параметра опухолевой массы с пороговым значением с определением, таким образом, риска развития токсичности после введения клеточной терапии.
130. Способ идентификации пациента, включающий:
(a) оценку уровня, количества или концентрации одного или более аналитов в биологическом образце от пациента или объемного параметра опухолевой массы у пациента, причем один или более аналитов выбраны из LDH, ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-8, IL-10, IL-15, IL-16 TNF-α, IFN-α2, MCP-1, MIP-1α и MIP-1β, причем:
пациентом является кандидат на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) идентификацию пациента, у кого есть риск развития токсичности после введения клеточной терапии, на основании сравнения, индивидуально, уровня, количества или концентрации аналита в образце или объемного параметра опухолевой массы с пороговым значением.
131. Способ лечения, включающий:
(a) оценку уровня, количества или концентрации одного или более аналитов в биологическом образце от пациента или объемного параметра опухолевой массы у пациента, причем один или более аналитов выбраны из LDH, ферритина, С-реактивного белка (CRP), D-димер (продукт распада фибрина), IL-6, IL-8, IL-10, IL-15, IL-16 TNF-α, IFN-α2, MCP-1, MIP-1α и MIP-1β, причем:
Пациент является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и; и
(b) сравнение, индивидуально, уровня, количества или концентрации аналита в образце или объемного параметра опухолевой массы с пороговым значением, с определением, таким образом, риска развития токсичности после введения клеточной терапии; и
(c) после или на основе результатов оценки, введение пациенту клеточной терапии, и, необязательно, агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности.
132. Способ по любому из вариантов осуществления 129-131, в котором биологический образец является образцом крови или плазмы.
133. Способ по любому из вариантов осуществления 129-132, в котором объемный параметр опухолевой массы является суммой размеров продукта (SPD) или является объемным измерением на основе CT и/или MRI отображения или другого отображения тела.
134. Способ согласно варианту осуществления 133, в котором измерение объемного параметра опухолевой массы осуществляют до лечения, до афереза или до производства клеточного продукта.
135. Способ по любому из вариантов осуществления 129-134, дополнительно включающий контроль пациента в отношении симптомов токсичности, если пациенту вводят клеточную терапию и он идентифицирован как имеющий риск развития токсичности.
136. Способ по любому из вариантов осуществления 129-135, в котором:
пациент имеет риск развития токсичности, если уровень, количество или концентрация одного или более аналитов или объемный параметр опухолевой массы выше порогового значения, и пациент имеет низкий риск развития токсичности, если уровень, количество или концентрация одного или более аналитов или объемный параметр опухолевой массы ниже порогового значения.
137. Способ по любому из вариантов осуществления 129-136, в котором пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения выше медианы или среднего уровня, количества или концентрации, или равно или приблизительно равно медиане или среднему уровню, количеству или концентрации аналита или объемного параметра опухолевой массы в биологическом образце, полученном от группы пациентов до введения клеточной терапии, причем у каждого из пациентов группы по-прежнему не развивалась какая-либо токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
138. Способ по любому из вариантов осуществления 129-137, в котором пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% и/или в пределах стандартного отклонения ниже медианы или среднего уровня, количества или концентрации аналита или объемного параметра опухолевой массы в биологическом образце, полученном от группы пациентов до получения клеточной терапии, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
139. Способ по любому из вариантов осуществления 129-138, в котором токсичность является нейротоксичностью или CRS.
140. Способ по любому из вариантов осуществления 129-139, в котором токсичность является нейротоксичностью или CRS степени 1 или более высокой.
141. Способ по любому из вариантов осуществления 129-140, в котором:
токсичность является тяжелой нейротоксичностью или является нейротоксичностью степени 2 или выше, нейротоксичностью степени 3 или более высокой, по меньшей мере пролонгированной нейротоксичностью степени 3 или нейротоксичностью сорта 4 или сорта 5 или выше; или
токсичность является тяжелым CRS или включает CRS степени 2 или выше или степени 3 или выше.
142. Способ по любому из вариантов осуществления 129-141, в котором токсичность является нейротоксичностью, и объемный параметр опухолевой массы представляет собой SPD, и один или более аналитов выбраны из LDH, IL-10, IL-15, IL-16, TNF-α и MIP-1β.
143. Способ по любому из вариантов осуществления 129-141, в котором токсичность является нейротоксичностью, и оценивают один или более аналитов, и аналиты выбраны из LDH, ферритина, CRP, IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β.
144. Способ по любому из вариантов осуществления 129-141, в котором токсичность является нейротоксичностью, и оценивают один или более аналитов, и аналиты выбраны из IL-8, IL-10 и CXCL10.
145. Способ согласно варианту осуществления 144, в котором нейротоксичность является тяжелой нейротоксичностью или нейротоксичностью степени 3 или более высокой.
146. Способ по любому из вариантов осуществления 129-141, в котором токсичность представляет собой CRS, и один или более аналитов или объемный параметр опухолевой массы выбраны из LDH, SPD, CRP, d-димера, IL-6, IL-15, TNF-α и MIP-1α.
147. Способ согласно варианту осуществления 146, в котором CRS является тяжелым CRS или CRS степени 3 или выше.
148. Способ по любому из вариантов осуществления 129-147, в котором, если пациент идентифицирован как имеющий риск развития токсичности, введение пациенту:
(a) (1) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, и (2) клеточной терапии, причем введение агента должно быть введено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или
(b) клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или подозревается в его наличии, после введения клеточной терапии; и/или
(c) введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
149. Способ согласно варианту осуществления 148, в котором агент или другое средство для лечения представляет собой анти-IL-6 антитело или антитело к рецептору IL6.
150. Способ согласно варианту осуществления 149, в котором агент или другое средство для лечения представляет собой или включает агент, выбранный из тоцилизумаба, силтуксимаба, клазакизумаба, сарилумаба, олокизумаба (CDP6038), элсилимомаба, ALD518/BMS-945429, сирукумаба (CNTO 136), CPSI-2634, ARGX-109, FE301 и FM101.
151. Способ согласно варианту осуществления 148, в котором вещество или другое средство для лечения являются или включают стероид, необязательно дексаметазон.
152. Способ по любому из вариантов осуществления 129-142 и 148-151, в котором оценивают объемный параметр, и объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 30 см2, или приблизительно 40 см2, или приблизительно 50 см2, или приблизительно 60 см2, или составляет или приблизительно составляет 70 см2.
153. Способ согласно варианту осуществления 152, в котором объемный параметр представляет собой SPD, и пороговое значение составляет или приблизительно составляет 50 см2.
154. Способ по любому из вариантов осуществления 129-151, в котором один или более аналитов являются или включают LDH, и пороговое значение составляет или приблизительно составляет 300 единиц на литр, или приблизительно составляет 400 единиц на литр, или приблизительно составляет 500 единиц на литр или составляет или приблизительно составляет 600 единиц на литр.
155. Способ по любому из вариантов осуществления 154, в котором аналит представляет собой LDH, и пороговое значение составляет или приблизительно составляет 500 единиц на литр.
156. Способ по любому из вариантов осуществления 109-155, в котором рекомбинантный рецептор специфично связывается с антигеном, ассоциированным с заболеванием или состоянием, или экспрессируемым в клетках среды поражения, ассоциированного с заболеванием или состоянием.
157. Способ по любому из вариантов осуществления 109-156, в котором заболевание или состояние представляют собой рак.
158. Способ по любому из вариантов осуществления 109-157, в котором заболевание или состояние являются миеломой, лейкозом или лимфомой.
159. Способ по любому из вариантов осуществления 109-158, в котором заболевание или состояние являются В-клеточной злокачественной опухолью и/или являются острым лимфообластным лейкозом (ALL), ALL взрослых, хроническим лимфообластным лейкозом (CLL), неходжкинской лимфомой (NHL) и диффузной крупноклеточной В-клеточной лимфомой (DLBCL).
160. Способ по любому из вариантов осуществления 109-159, в котором рекомбинантный рецептор является химерным антигенным рецептором (CAR).
161. Способ по любому из вариантов осуществления 109-160, в котором генно-инженерные клетки включают Т-клетки, необязательно CD4+ и/или CD8+.
162. Способ согласно варианту осуществления 161, в котором Т-клетки являются первичными Т-клетками, полученными от пациента, или являются аутологичными для пациента.
163. Способ отбора пациента для лечения, включающий:
(a) контактирование биологического образца с одним или более реагентами, способными к обнаружению или которые являются специфичными для одного или более аналитов, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина),
причем:
биологический образец получен от пациента, который является кандидатом на лечение клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор; и
биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки; и
(b) отбор, пациента, у которого:
(i) уровень, количество или концентрация аналита в образце равны или выше порогового значения, с идентификацией, таким образом, пациента, подверженного риску развития токсичности к клеточной терапии; или
(ii) уровень, количество или концентрация аналита ниже порогового значения.
164. Способ согласно варианту осуществления 163, в котором:
(a) пациент в (i) выбран для введения пациенту (1) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, и (2) клеточной терапии, причем введение агента должно быть введено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии к пациенту; и/или
(b) пациент в (i) выбран для введения пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии; и/или
(c) пациент в (i) выбран для введения пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
165. Способ согласно варианту осуществления 163 или варианту осуществления 164, в котором пациент в (i) выбран, и способ дополнительно включает:
(a) введение пациенту (1) агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, и (2) клеточной терапии, причем введение агента осуществляют (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии к пациенту; и/или
(b) введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии; и/или
(c) введение пациенту клеточной терапии или дозы генно-инженерных клеток клеточной терапии, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии; и/или
(d) введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
166. Способ согласно варианту осуществления 163 или варианту осуществления 164, в котором:
(a) пациент в (ii) выбран для введения пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней;
(b) пациент в (ii) выбран для введения пациенту клеточной терапии, причем клеточная терапия не включает введение, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или
(c) пациент в (ii) выбран для введения клеточной терапии в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
167. Способ согласно варианту осуществления 163, 164 или 166, в котором пациент в (ii) выбран, и способ дополнительно включает введение пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней.
168. Способ по любому из вариантов осуществления 163, 164, 166 и 167, в котором пациент в (ii) выбран, и способ дополнительно включает введение пациенту клеточной терапии, причем:
введение клеточной терапии не включает введение, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или
введение клеточной терапии должно быть или может быть введено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
169. Способ лечения, включающий:
(a) тестирование биологического образца в отношении уровня, количества или концентрации одного или более аналитов, причем биологический образец получен от пациента, который является кандидатом на лечение, необязательно клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор, для лечения заболевания или состояния, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина); и
(b) после или на основе результатов тестирования, введение пациенту клеточной терапии, и, необязательно, агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности.
170. Способ лечения пациента, имеющего или подозреваемого в наличии заболевания или состояния, включающий:
(1) введение пациенту клеточной терапии, включающей дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор, для лечения или который специфично распознает заболевание или состояние, и, необязательно, (2) дополнительное введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, причем:
введение осуществляют после или осуществляют на основе результатов оценки одного или более параметров предварительного лечения, причем:
(a) один или более параметров предварительного лечения включают параметр, ассоциируемый или коррелирующий с или маркерный для серьезности заболевания или состояния у пациента, причем эти параметры необязательно включают один или более аналитов и/или один или более объемных или других измерений тела,
(b) оценка одного или более параметров предварительного лечения включает оценку количества или уровня в биологическом образце, который представляет собой или происходит от образца, полученного от пациента, уровня, количества или концентрации одного или более аналитов, биологический образец получен от пациента до введения клеточной терапии, причем образец получен от пациента до введения клеточной терапии и, необязательно, до афереза или до получения клеток для введения, и/или один или более аналитов ассоциированы с тяжестью заболевания и/или один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина); и/или
(c) оценка одного или более параметров предварительного лечения необязательно включает оценку объемного измерения заболевания или состояния у пациента, которое необязательно является измерением, полученным отображением, необязательно результатом суммы размеров продукта (SPD), или другим объемным измерением(ями), необязательно на основе CT и/или MRI отображения или другого отображения тела, выполненного до лечения и необязательно до афереза или получения клеток.
171. Способ согласно варианту осуществления 170, в котором указанная оценка одного или более параметров предварительного лечения включает тестирование одного или более аналитов, включающее обнаружение, необязательно включающее контактироание реагента, способного к непосредственному или опосредованному обнаружению аналита(ов), с биологическим образцом и определение уровня, количества или концентрации аналита(ов) в биологическом образце.
172. Способ согласно варианту осуществления 170 или варианту осуществления 171, в котором оценка одного или более параметров предварительного лечения включает (A) оценку в биологическом образце, который представляет собой или происходит от образца, полученного от пациента до лечения и/или до афереза или процессинга клеток, уровня, количества или концентрации одного или более аналитов, необязательно ассоциированных с тяжестью заболевания, и (B) оценку объемного параметра серьезности заболевания, причем измерение серьезности заболевания необязательно является результатом суммы размеров продукта (SPD) или другим объемным измерением(ями), необязательно на основе CT и/или MRI отображения или другого отображения тела и/или его осуществляют до лечения, до афереза или до получения клеточного продукта.
173. Способ по любому из вариантов осуществления 169-172, в котором, если уровень, количество или концентрация и/или измерение, или их комбинация этого, являющиеся результатом или полученные через оценку предварительного лечения, равны или выше порогового значения:
введение включает дополнительное введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, причем необязательно указанное дополнительное введение осуществляют (i) до, (ii) в течение одного, двух или трех дней, или в течение четырех, пяти или шести дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или
клеточную терапию, вводимую к пациенту, вводят (A) в сниженной дозе по сравнению с тем, если уровень, количество или концентрация и/или измерение или их комбинация ниже порогового значения, или (B) в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или в наличии которого подозревается, после введения клеточной терапии, или (C) в дозе, уменьшенной по сравнению с максимальной переносимой дозой или апробированной дозой или максимальной апробированной дозой, для использования у пациентов, имеющих заболевание или состояние или для лечения заболевания или состояния; и/или
введение пациенту клеточной терапии осуществляют или определяют как требующее осуществления в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия в ином случае, если уровень, количество, концентрация, измерение или комбинация ниже порога или не оценивались, должна быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней или на ночь.
174. Способ по любому из вариантов осуществления 169-173, в котором, если уровень, количество или концентрация и/или измерение, или их комбинация, являются результатом или получены через оценку предварительного лечения, ниже порогового значения:
введение клеточной терапии не включает введение, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или
введение клеточной терапии должно быть, или может быть, введено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней; и/или
клеточную терапию, вводимую пациенту, вводят (A) в дозе, необязательно количестве Т-клеток или генно-инженерных Т-клеток или Т-клеток указанного фенотипа, которая выше, чем та, которую нужно было бы вводить, если бы уровень, количество или концентрация и/или измерение или их комбинация были равны или выше порогового значения, или (B) в дозе, необязательно количестве Т-клеток или генно-инженерных Т-клеток или Т-клеток указанного фенотипа, которая равна или приблизительно равна максимальной переносимой дозе или максимальной дозе, апробированной для использования для лечения пациентов, имеющих заболевание или состояние.
175. Способ профилактического лечения, включающий введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, причем:
пациентом является кандидат на лечение необязательно клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор для лечения заболевания или состояния; и
пациент был идентифицирован как имеющий риск развития токсичности после или на основе оценки одного или более параметров предварительного лечения, причем:
(a) один или более параметров предварительного лечения включают параметр, связанный или коррелирующий с, или являющийся маркером для серьезности заболевания или состояния у пациента, причем эти параметры необязательно включают один или более аналитов и/или один или более объемных или других измерений тела, или
(b) оценка одного или более параметров предварительного лечения включает оценку количества или уровня в биологическом образце, который представляет собой или происходит от образца, полученного от пациента, уровня, количества или концентрации одного или более аналитов в биологическом образце, полученном из или от образца от пациента, в отношении уровня, количества или концентрации одного или более аналитов, причем указанный биологический образец получен от пациента до введения клеточной терапии и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки, причем:
(i) один или более параметров предварительного лечения включают параметр, связанный или коррелирующий с, или являющийся маркером для, серьезности заболевания или состояния у пациента, причем эти параметры необязательно включают один или более аналитов и/или один или более объемных или других измерений тела,
(ii) оценка одного или более параметров предварительного лечения включает оценку количества или уровня в биологическом образце, который представляет собой или происходит от образца, полученного от пациента, уровня, количества или концентрации одного или более аналитов, биологический образец получен от пациента до введения клеточной терапии, причем образец получен от пациента до введения клеточной терапии и, необязательно, до афереза или до получения клеток для введения, и/или один или более аналитов ассоциированы с тяжестью заболевания и/или один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина); и/или
(ii) оценка одного или более параметров предварительного лечения необязательно включает оценку объемного измерения заболевания или состояния у пациента, которое необязательно является измерением, полученным отображением, необязательно результатом суммы размеров продукта (SPD), или другим объемным измерением(ями), необязательно на основе CT и/или MRI отображения или другого отображения тела, выполненного до лечения и необязательно до афереза или получения клеток; или
причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
176. Способ согласно варианту осуществления 175, в котором указанное тестирование включает детекцию, необязательно включающую контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом, и определение уровня, количества или концентрации аналита в биологическом образце, и/или в котором агент вводят пациенту, если уровень, количество или концентрация аналита в образце равны или выше порогового значения, и причем необязательно агент вводят (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии к пациенту.
177. Способ согласно варианту осуществления 175 или варианту осуществления 176, в котором оценка одного или более параметров предварительного лечения включает (A) оценку в биологическом образце, который представляет собой или происходит от образца, полученного от пациента до лечения и/или до афереза или процессинга клеток, уровня, количества или концентрации одного или более аналитов, необязательно ассоциированных с тяжестью заболевания, и (B) оценку объемного параметра серьезности заболевания, причем оценка серьезности заболевания необязательно является результатом суммы размеров продукта (SPD) или другим объемным измерением(ями), необязательно на основе CT и/или MRI отображения или другого отображения тела, и/или ее осуществляют до лечения, до афереза или до получения клеточного продукта.
178. Способ по любому из вариантов осуществления 169-177, в котором пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации или величины, и/или в пределах стандартного отклонения от среднего уровня, количества или концентрации или величины, аналита или параметра в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
179. Способ по любому из вариантов осуществления 169-178, в котором реагент является связывающей молекулой, специфично связывающейся с аналитом.
180. Способ по любому из вариантов осуществления 169-179, в котором реагент является антителом или его антигенсвязывающим фрагментом.
181. Способ по любому из вариантов осуществления 169-180, в котором биологический образец представляет собой или получен из образца крови, плазмы или сыворотки.
182. Способ по любому из вариантов осуществления 169-181, в котором тестирование или оценка клеток аналит включает иммунологический тест.
183. Способ по любому из вариантов осуществления 169-182, в котором токсичность включает нейротоксичность или синдром высвобождения цитокинов (CRS), необязательно нейротоксичность или CRS степени 1 или более высокой.
184. Способ по любому из вариантов осуществления 169-183, в котором:
токсичность включает тяжелую нейротоксичность и/или включает нейротоксичность степени 2 или более высокой, нейротоксичность степени 3 или более высокой, по меньшей мере пролонгированную нейротоксичность степени 3 или нейротоксичность степени 4 или степени 5 или выше; и/или
токсичность включает тяжелый CRS и/или включает CRS степени 2 или выше или степени 3 или выше.
185. Способ по любому из вариантов осуществления 169-184, в котором токсичность связана с отеком мозга.
186. Способ по любому из вариантов осуществления 169-185, в котором агент или другое средство для лечения представляет собой или включает один или более стероидов; антагонистов или ингибиторов рецептора цитокина или цитокина, выбранных из числа IL-10, IL-10R, IL-6, рецептора IL-6, IFNγ, IFNGR, IL-2, IL-2R/CD25, MCP-1, CCR2, CCR4, MIP1β, CCR5, TNFальфа, TNFR1, IL-1, и IL-1Rальфа/IL-1бета; или агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток.
187. Способ согласно варианту осуществления 186, в котором антагонист или ингибитор представляет собой или включает агент, выбранный из числа антитела или антигенсвязывающего фрагмента, малой молекулы, белка или пептида и нуклеиновой кислоты.
188. Способ по любому из вариантов осуществления 169-187, в котором агент или другое средство для лечения является анти-IL-6 антителом или антителом к рецептору IL6.
189. Способ по любому из вариантов осуществления 169-188, в котором агент или другое средство для лечения представляет собой или включает агент, выбранный из тоцилизумаба, силтуксимаба, клазакизумаба, сарилумаба, олокизумаба (CDP6038), элсилимомаба, ALD518/BMS-945429, сирукумаба (CNTO 136), CPSI-2634, ARGX-109, FE301 и FM101.
190. Способ по любому из вариантов осуществления 169-189, в котором агент или другое средство для лечения представляет собой или включает тоцилизумаб.
191. Способ по любому из вариантов осуществления 169-190, в котором агент или другое средство для лечения представляет собой или включает силтуксимаб.
192. Способ согласно варианту осуществления 186, в котором стероид представляет собой или включает дексаметазон.
193. Способ согласно варианту осуществления 186, в котором агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток, выбран из противовоспалительного средства, ингибитора NADPH оксидазы (NOX2), блокатора кальциевых каналов, блокатора натриевых каналов, ингибирует GM-CSF, ингибирует CSF1R, специфично связывается с CSF-1, специфично связывается с IL-34, ингибирует активацию ядерного фактора каппа-B (NF-κB), активирует рецептор CB2 и/или является агонистом CB2, ингибитором фосфодиэстеразы, ингибирует микроРНК-155 ((miR-155) или повышающе регулирует микроРНК-124 ((miR-124).
194. Способ согласно варианту осуществления 193, в котором агент, способный к предотвращению, блокированию или ослаблению активации или функции микроглиальных клеток, является малой молекулой, пептидом, белком, антителом или его антигенсвязывающим фрагментом, миметиком антитела, аптамером или молекулой нуклеиновой кислоты.
195. Способ согласно варианту осуществления 193 или варианту осуществления 194, в котором агент выбран из миноциклина, налоксона, нимодипина, рилузола, MOR103, леналидомида, каннабиноида (необязательно WIN55 или 212-2), внутривенного иммуноглобулина (IVIg), ибудиласта, анти-miR-155 закрытой нуклеиновой кислоты (LNA), MCS110, PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945, эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003.
196. Способ по любому из вариантов осуществления 193-195, в котором агент является ингибитором рецептора колониестимулирующего фактора 1 (CSF1R).
197. Способ по любому из вариантов осуществления 193-196, в котором агент выбран из:
PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945 или его фармацевтической соли или пролекарства;
эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003 или является его антигенсвязывающим фрагментом; или комбинацией любого из вышеуказанных.
198. Способ по любому из вариантов осуществления 193-197, в котором ингибитор представляет собой PLX-3397.
199. Способ по любому из вариантов осуществления 1-23 и 109-198, в котором рекомбинантный рецептор специфично связывается с антигеном, ассоцируемым с заболеванием или состоянием, или экспрессируемым в клетках среды поражения, ассоциируемой с заболеванием или состоянием.
200. Способ по любому из вариантов осуществления 1-23 и 109-199, в котором заболевание или состояние представляют собой рак.
201. Способ по любому из вариантов осуществления 1-23 и 109-200, в котором заболевание или состояние являются миеломой, лейкозом или лимфомой.
202. Способ по любому из вариантов осуществления 1-23 и 109-201, в котором заболевание или состояние являются В-клеточной злокачественной опухолью и/или являются острым лимфообластным лейкозом (ALL), ALL взрослых, хроническим лимфообластным лейкозом (CLL), неходжкинской лимфомой (NHL) и диффузной крупноклеточной В-клеточной лимфомой (DLBCL).
203. Способ по любому из вариантов осуществления 1-23 и 109-202, в котором антиген представляет собой ROR1, антиген созревания B-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторная тирозинкиназа erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолат-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор, содержащий домен вставки киназы (kdr), легкую каппа-цепь, антиген Ley, молекулу L1-клеточной адгезии, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, рецептор альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D) или патоген-специфический антиген.
204. Способ по любому из вариантов осуществления 1-23 и 109-203, в котором рекомбинантный рецептор является Т-клеточным рецептором или функциональным не Т-клеточным рецептором.
205. Способ по любому из вариантов осуществления 1-23 и 109-204, в котором рекомбинантный рецептор является химерным антигенным рецептором (CAR).
206. Способ согласно варианту осуществления 205, в котором CAR включает внеклеточный антигенраспознающий домен, специфично связывающийся с антигеном, и внутриклеточный сигнальный домен, включающий ITAM, причем необязательно внутриклеточный сигнальный домен включает внутриклеточный домен CD3-дзэта (CD3ζ) цепи; и/или причем CAR дополнительно включает костимулирующий сигнальный домен, необязательно включающий сигнальный домен CD28 или 4-1BB.
207. Способ по любому из вариантов осуществления 1-23 и 109-206, в котором генно-инженерные клетки включают Т-клетки, необязательно CD4+ и/или CD8+.
208. Способ согласно варианту осуществления 207, в котором Т-клетками являются первичные Т-клетки, полученные от пациента.
209. Способ по любому из вариантов осуществления 1-23 и 109-208, в котором клеточная терапия включает введение от или от приблизительно 1x105 до 1x108 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), от или от приблизительно 5x105 до 1x107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC) или от или от приблизительно 1x106 до 1x107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), включительно.
210. Способ по любому из вариантов осуществления 1-23 и 109-209, в котором клеточная терапия включает введение не более чем 1x108 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 1x107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 0,5x107 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 1x106 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), не более чем 0,5x106 общих экспрессирующих рекомбинантный рецептор клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
211. Способ по любому из вариантов осуществления 109-210, в котором доза, не связанная с риском развития токсичности или тяжелой токсичности, представляет собой или включает менее чем или менее чем приблизительно 5x107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, менее чем или менее чем приблизительно 2,5x107, менее чем или менее чем приблизительно 1,0x107, менее чем или менее чем приблизительно 5,0x106, менее чем или менее чем приблизительно 1,0x106, менее чем или менее чем приблизительно 5,0x105, или менее чем или менее чем приблизительно 1x105 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
212. Способ по любому из вариантов осуществления 109-211, в котором доза, не связанная с риском развития токсичности или тяжелой токсичности, составляет или включает от или от приблизительно 1x105 до 5x107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, от 1x105 до 2,5x107,от 1x105 до 1,0x107, от 1x105 до 5,0x106, от 1x105 до 1,0x106, от 1,0x105 до 5,0x105, от 5,0x105 до 5x107, от 5x105 до 2,5x107, от 5x105 до 1,0x107, от 5x105 до 5,0x106, от 5x105 до 1,0x106, от 1,0x106 до 5x107, от 1x106 до 2,5x107, от 1x106 до 1,0x107, от 1x106 до 5,0x106, от 5,0x106 до 5x107, от 5x106 до 2,5x107, от 5x106 до 1,0x107, от 1,0x107 до 5x107, от 1x107 до 2,5x107 или от 2,5x107 до 5x107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
213. Способ по любому из вариантов осуществления 109-212, в котором генно-инженерные клетки являются аутологичными для пациента.
214. Способ по любому из вариантов осуществления 109-213, в котором генно-инженерные клетки являются аллогенными для пациента.
215. Способ по любому из вариантов осуществления 109-214, в котором реагент мечен таким образом, чтобы его можно было детектировать, необязательно флуоресцентно мечен.
216. Способ по любому из вариантов осуществления 163-215, в котором один или более аналитов являются LDH, ферритином, CRP, IL-6, IL-8, IL-10, TNF-альфа, IFN-альфа2, MCP-1 и MCP-1бета.
217. Способ по любому из вариантов осуществления 163-215, в котором один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-8, IL-10, TNF-α, MCP-1 и MIP-1бета, и токсичность является нейротоксичностью.
218. Способ по любому из вариантов осуществления 163-215, в котором один или более аналитов выбраны из IL-8 и IL-10, и токсичность является нейротоксичностью, необязательно тяжелой нейротоксичностью или нейротоксичностью степени 3 или более высокой.
219. Способ по любому из вариантов осуществления 163-215, в котором один или более аналитов выбраны из LDH, ферритина, С-реактивного белка (CRP), D-димера (продукта распада фибрина), IL-6, IL-10, IL-15, IL-16 TNF-α, MIP-1α и MIP-1β, и токсичность является CRS или нейротоксичностью.
220. Способ по любому из вариантов осуществления 109-219, в котором один или более аналитов представляют собой или включают LDH.
221. Изделие, включающее одну или более доз клеточной терапии, причем каждая доза включает клетки, экспрессирующие химерный антигенный рецептор (CAR), и инструкции по введению клеточной терапии, причем инструкции определяют, что:
доза клеток предназначена для введения пациенту, имеющему или идентифицированному как имеющий неходжкинскую лимфому (NHL), NHL, выбранную из диффузной крупноклеточной В-клеточной лимфомы (DLBCL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), NOS (de novo или трансформированной из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B, причем пациент является или был идентифицирован как имеющий статус 0 или 1 согласно Eastern Cooperative Oncology Group Performance Status (ECOG); и
инструкции определяют введение числа Т-клеток или клеток указанного фенотипа или определяют введение количества или объема одного или более составов, соответствующих или содержащих указанное конкретное количество клеток, причем конкретное количество клеток включает от или от приблизительно 5x107 CAR-экспрессирующих Т-клеток до 1x108 CAR-экспрессирующих Т-клеток, включительно, от или от приблизительно 5x107 CAR-экспрессирующих Т-клеток и до или до приблизительно 1,5x108 CAR-экспрессирующих Т-клеток, 5x107 или приблизительно 5x107 CAR-экспрессирующих Т-клеток, 1x108 или приблизительно 1x108 CAR-экспрессирующих Т-клеток, или до или до приблизительно 1,5x108 CAR-экспрессирующих Т-клеток, от или от приблизительно 2,5x107 CD8+CAR-экспрессирующих Т-клеток и до или до приблизительно 5x107 CD8+ CAR-экспрессирующих Т-клеток, включительно, от или от приблизительно 2,5x107 CAR-экспрессирующих Т-клеток и до или до приблизительно 0,75x108 CD8+ CAR-экспрессирующих Т-клеток, или до или до приблизительно 2,5x107 CD8+ CAR-экспрессирующих Т-клеток, 5x107 или приблизительно 5x107 CAR-экспрессирующих Т-клеток, или до или до приблизительно 0,75x108 CD8+CAR-экспрессирующих Т-клеток, или жизнеспособную популяцию любого из указанных.
222. Изделие согласно варианту осуществления 221, в котором инструкции определяют введение клеточной терапии в определенном отношении CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, или определяют введение количества объемов составов, соответствующих такому определенному отношению, или включает состав, имеющий клетки в таком отношении, или включает клетки в таком отношении, экспрессирующие CAR и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет приблизительно 1:1 или от приблизительно 1:3 до приблизительно 3:1.
223. Изделие, включающее клеточную терапию или одну из множества композиций клеточной терапии, включающих дозу или композицию генно-инженерных клеток, экспрессирующих химерный антигенный рецептор (CAR), и инструкции по введению клеточной терапии, причем инструкции определяют:
доза Т-клеток предназначена для введения в определенном отношении CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем отношение приблизительно составляет или составляет 1:1; и
доза клеток предназначена для введения пациенту, имеющему или идентифицированному как имеющий неходжкинскую лимфому (NHL), NHL, выбранную из диффузной крупноклеточной В-клеточной лимфомы (DLBCL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), NOS (de novo или трансформированной из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B.
224. Изделие, включающее клеточную терапию или одну из множества композиций клеточной терапии, включающих дозу или композицию генно-инженерных клеток, экспрессирующих химерный антигенный рецептор (CAR), и инструкции по введению клеточной терапии, причем инструкции определяют:
доза клеток предназначена для введения пациенту, имеющему или идентифицированному как имеющий неходжкинскую лимфому (NHL), необязательно NHL, выбранную из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), мантийноклеточную лимфому (MCL) и/или фолликулярную лимфому (FL), необязательно фолликулярную лимфому стадии 3B (FL3B);
доза Т-клеток для введения включает от или от приблизительно 5x107 CAR-экспрессирующих Т-клеток до 1x108 CAR-экспрессирующих Т-клеток, включительно; и
доза Т-клеток предназначена для введения в определенном отношении CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, и/или CD4+ клеток к CD8+ клеткам, причем это отношение приблизительно составляет или составляет 1:1.
225. Изделие согласно варианту осуществления 222 или варианту осуществления 223, в котором инструкции дополнительно определяют, что клеточная терапия предназначена для введения пациенту, который является или был идентифицирован как имеющий статус 0, 1 или 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG), и/или который является или был идентифицирован как имеющий статус ECOG 0 или 1.
226. Изделие по любому из вариантов осуществления 221-225, в котором:
инструкции определяют, что введение пациенту, не получавшему, непосредственно перед введением дозы клеток или за или приблизительно за 1 месяц до дозы клеток, агент или средство для лечения, способное к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности; и/или
инструкции не определяют, что введение пациенту, которому, до инициации введения дозы клеток, вводили анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб, и/или не вводили стероид, необязательно дексаметазон; и/или
инструкции не определяют введение агента, который является анти-IL-6 или анти-IL-6R антителом, необязательно тоцилизумабом или силтуксимабом, стероидом, необязательно дексаметазоном и/или агентом в целях профилактически снижения риска или лечения CRS или нейротоксичность, и/или не определяют введение указанного агента в течение промежутка времени после введения дозы клеток, причем промежуток времени необязательно составляет или приблизительно составляет 1, 2, 3, 4, 5 дней, или необязательно составляет или приблизительно составляет 6, 7, 8, 9, 10, 11 дней, или необязательно 1, 2, 3 или 4 недели, и/или не определяют введение указанного агента до того, как пациент покажет, или если пациент не показывает, признак или симптом нейротоксичности и/или CRS, необязательно кроме повышения температуры, причем необязательно повышение температуры не является длительным повышением температуры, или повышение температуры составляет или было уменьшено на или уменьшено более чем на 1°C после лечения жаропонижающим средством; и/или
инструкции определяют введение дозы клеток на амбулаторной основе и/или без допуска пациента в больницу и/или без оставления на ночь в больнице и/или не требуя допуска или оставления на ночь в больнице, необязательно если фактор риска, определенный для пациента или клеток пациента, иначе не идентифицируется в инструкциях или информации в изделии или необязательно если или пока пациент не показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством.
227. Изделие согласно варианту осуществления 226, в котором инструкции дополнительно определяют, что, если, после введения дозы клетки на амбулаторной основе, не требуя допуска или оставления на ночь в больнице, пациент показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством, пациент должен быть госпитализирован или оставлен на ночь в больнице и/или ему требуется введение агента или средства для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого.
228. Изделие согласно варианту осуществления 226 или варианту осуществления 227, в котором агент представляет собой или включает анти-IL-6 или анти-IL-6R антитело, необязательно тоцилизумаб или силтуксимаб, и/или стероид, необязательно дексаметазон.
229. Изделие по любому из вариантов осуществления 221-228, в котором инструкции определяют, что пациент имеет DLBCL, характеризуемую как de novo или трансформированную из вялотекущего заболевания, и/или DLBCL, не трансформированную из MZL и CLL (Рихтера).
230. Изделие по любому из вариантов осуществления 221-229, в котором инструкции определяют, что пациент не имеет первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL).
231. Изделие по любому из вариантов осуществления 221-230, в котором инструкция определяет, что введение клеток осуществляют пациенту, который является или был идентифицирован как имеющий лимфому, ассоциированную с или включающую участие центральной нервной системы (ЦНС).
232. Изделие по любому из вариантов осуществления 221-231, в котором инструкции определяют, что введение клеточной терапии осуществляют пациенту, который является или был идентифицирован как имеющий лимфому double/triple hit, является или был идентифицирован как имеющий хеморефрактерную лимфому, необязательно хеморефрактерную DLBCL; не достиг полной ремиссии (CR) в ответ на предшествующую терапию; и/или имел рецидив в течение 1 года или спустя меньше чем 1 год после получения трансплантата аутологичных стволовых клеток (ASCT).
233. Изделие по любому из вариантов осуществления 221-232, в котором инструкции определяют дальнейшее введение пациенту дополнительного терапевтического агента или отличной, необязательно отличной от клеточной терапии, необязательно кроме CAR+ Т-клеточной терапии.
234. Изделие согласно варианту осуществления 233, в котором дополнительный терапевтический агент или терапия являются агентом для лечения NHL или злокачественной опухоли и/или увеличивают персистирование, активность и/или эффективность дозы клеток.
235. Изделие согласно варианту осуществления 233 или варианту осуществления 234, в котором инструкции определяют, что введение дополнительного терапевтического агента или терапии осуществляют пациенту, не показывающему ответ, необязательно не показывающему CR или OR, на клеточную терапию в течение 1 месяца, в течение 2 месяцев или в течение 3 месяцев после введения дозы клеток.
236. Изделие по любому из вариантов осуществления 233-235, в котором инструкции определяют, что введение дополнительного терапевтического агента или терапии осуществляют пациенту:
который является или был идентифицирован как имеющий стабильное или прогрессирующее заболевание (SD/PD) после лечения предшествующей терапией, необязательно предшествующей терапией химиотерапевтическим агентом;
который является или был идентифицирован как имеющий статус 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG);
который является или был идентифицирован как имеющий трансформированную фолликулярную лимфому (tFL); или
который является или был идентифицирован как имеющий DLBCL, трансформированную из MZL и CLL.
237. Изделие по любому из вариантов осуществления 233-236, в котором инструкции определяют, что дополнительный терапевтический агент или терапия предназначены для введения до, с или одновременно и/или после инициации введения дозы клеток.
238. Изделие по любому из вариантов осуществления 221-237, в котором CAR включает scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно представляет собой 4-1BB, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно представляет собой CD3дзета.
239. Изделие по любому из вариантов осуществления 221-238, в котором антиген является В-клеточным антигеном, который необязательно представляет собой CD19.
240. Изделие по любому из вариантов осуществления 221-239, дополнительно включающее инструкции по использованию с, после или в связи с противолимфоцитарной терапией, причем противолимфоцитарная терапия необязательно включает флударабин и/или циклофосфамид.
241. Изделие согласно варианту осуществления 240, причем противолимфоцитарная терапия включает введение циклофосфамида в количестве приблизительно 200-400 мг/м2, необязательно в количестве, которое составляет или приблизительно составляет 300 мг/м2, включительно, и/или флударабин в количестве приблизительно 20-40 мг/м2, необязательно 30 мг/м2, в сутки в течение 2-4 дней, необязательно в течение 3 дней.
242. Изделие согласно варианту осуществления 240 или варианту осуществления 241, причем противолимфоцитарная терапия включает введение циклофосфамида в количестве, составляющем или приблизительно составляющем 300 мг/м2, и флударабина в количестве приблизительно 30 мг/м2 в сутки в течение 3 дней.
243. Изделие по любому из вариантов осуществления 221-242, в котором инструкции дополнительно определяют, что введение клеточной терапии должно быть или может быть введено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней, необязательно если или пока пациент не показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством.
244. Изделие согласно варианту осуществления 243, причем, если пациент показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1°C после лечения жаропонижающим средством, инструкции далее определяют, что пациент должен быть госпитализирован или оставлен на ночь в больнице и/или ему следует ввести агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности и/или синдрома высвобождения цитокинов или риска этого.
245. Изделие по любому из вариантов осуществления 221-244, в котором инструкции дополнительно определяют, что клеточная терапия предназначена для парентерального введения, необязательно внутривенного введения.
246. Изделие по любому из вариантов осуществления 221-245, причем клеточная терапия включает первичные Т-клетки, полученные от пациента.
247. Изделие по любому из вариантов осуществления 221-246, в котором Т-клетки являются аутологичными для пациента.
248. Изделие по любому из вариантов осуществления 221-246, в котором Т-клетки являются аллогенными для пациента.
249. Изделие по любому из вариантов осуществления 221-248, в котором изделие включает одно из множества композиций клеточной терапии, включающей первую композицию генно-инженерных клеток, включающих CD4+ Т-клетки или CD8+ Т-клетки, причем инструкции определяют, что первая композиция предназначена для использования со второй композицией, включающей другие из CD4+ Т-клеток или CD8+ Т-клеток, причем необязательно клетки первой композиции и клетки той же композиции проиходят от того же пациента.
250. Изделие согласно варианту осуществления 249, в котором инструкции определяют, что первая композиция и вторая композиция предназначены для введения в определенном отношении CD4+ клеток, экспрессирующих рекомбинантный рецептор, к CD8+ клеткам, экспрессирующим рекомбинантный рецептор, и/или CD4+ клеток к CD8+ клеткам, причем это отношение необязательно составляет приблизительно 1:1 или от приблизительно 1:3 до приблизительно 3:1.
251. Изделие согласно варианту осуществления 250, в котором определенное отношение составляет или приблизительно составляет 1:1.
252. Изделие по любому из вариантов осуществления 221-251, в котором композиция дополнительно включает криопротектор, и/или изделие дополнительно включает инструкции по размораживанию композиции до введения пациенту.
253. Изделие по любому из вариантов осуществления 249-252, в котором инструкции определяют введение композиции, включающей CD4+ Т-клетки, и композиции, включающей CD8+ Т-клетки, с интервалом от 0 до 12 часов, с интервалом от 0 до 6 часов или с интервалом от 0 до 2 часов.
254. Изделие по любому из вариантов осуществления 249-253, в котором инструкции определяют введение композиции, включающей CD4+ Т-клетки, и композиции, включающей CD8+ Т-клетки с интервалом не более чем 2 часа, не более чем 1 час, не более чем 30 минут, не более чем 15 минут, не более чем 10 минут или не более чем 5 минут.
255. Изделие по любому из вариантов осуществления 249-254, в котором инструкции определяют введение композиции, включающей CD4+ Т-клетки, до введения композиции, включающей CD8+ клетки.
256. Изделие по любому из вариантов осуществления 249-254, в котором инструкции определяют введение композиции, включающей CD8+ Т-клетки, до введения композиции, включающей CD4+ клетки.
257. Изделие, включающее один или более реагентов, способных к обнаружению одного или более аналитов, и инструкции по использованию реагента для тестирования биологического образца от пациента, который является кандидатом на лечение, необязательно клеточной терапией, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
258. Изделие согласно варианту осуществления 257, дополнительно включающее клеточную терапию и/или дополнительно включающее инструкции по использованию с, до и/или в связи с лечением клеточной терапией.
259. Изделие согласно варианту осуществления 257 или варианту осуществления 258, дополнительно включающее один или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности и/или инструкции по введению одного или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности у пациента.
260. Изделие по любому из вариантов осуществления 257-259, в котором инструкции дополнительно определяют, если уровень, количество или концентрация аналита в образце равны или выше порогового значения для аналита:
введение пациенту агента или другого средства для лечения, способное к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту; и/или
введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или подозревается в его наличии, после введения клеточной терапии; и/или
введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
261. Изделие по любому из вариантов осуществления 257-259, в котором инструкции дополнительно определяют, если уровень, количество или концентрация аналита ниже порогового значения для аналита, введение пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней.
262. Изделие по любому из вариантов осуществления 257-261, в котором инструкции дополнительно определяют введение клеточной терапии пациенту, и причем инструкции дополнительно определяют, если уровень, количество или концентрация аналита ниже порогового значения:
введение клеточной терапии не включает введение, до или одновременно с введением клеточной терапии и/или до развития признака симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или
введение клеточной терапии должно быть или может быть введено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
263. Изделие по любому из вариантов осуществления 257-262, причем пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации и/или в пределах стандартного отклонения от среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
264. Изделие, включающее:
клеточную терапию, причем указанная клеточная терапия необязательно включает дозу или композицию генно-инженерных клеток, экспрессирующих рекомбинантный рецептор, и
инструкции по введению клеточной терапии после или на основе результатов оценки в биологическом образце уровня или количества, или концентрации одного или более аналитов в биологическом образце, причем указанный биологический образец получен от пациента до введения клеточной терапии, и/или указанный биологический образец не включает рекомбинантный рецептор и/или указанные генно-инженерные клетки, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
265. Изделие согласно варианту осуществления 264, причем указанная оценка включает детекцию, необязательно включающую контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом и определение уровня, количества или концентрации аналита в биологическом образце.
266. Изделие согласно варианту осуществления 265, дополнительно включающее реагент и/или дополнительно включающее инструкции по использованию с, до и/или в связи с реагентом для детекции аналита.
267. Изделие по любому из вариантов осуществления 264-266, дополнительно включающее один или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности и/или инструкции по введению одного или более агентов или средств для лечения для лечения, предотвращения, задержки, ослабления или уменьшения развития или риска развития токсичности у пациента.
268. Изделие по любому из вариантов осуществления 264-267, в котором инструкции по введению клеточной терапии определяют, если уровень, количество или концентрация аналита в образце, равны или выше порогового значения:
введение пациенту агента или другого средства для лечения, способного к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения введения терапевтической композиции клетки или генно-инженерных клеток; и/или
введение пациенту клеточной терапии в сниженной дозе или в дозе, не связанной с риском развития токсичности или тяжелой токсичности, или не связанной с риском развития токсичности или тяжелой токсичности у большинства пациентов и/или большинства пациентов, имеющих заболевание или состояние, которое пациент имеет или подозревается в его наличии, после введения клеточной терапии; и/или
введение пациенту клеточной терапии в режиме стационара и/или с допуском в больницу в течение одного или более дней, причем необязательно клеточная терапия должна в ином случае быть введена пациентам на амбулаторной основе или без допуска в больницу в течение одного или более дней.
269. Изделие по любому из вариантов осуществления 264-268, в котором инструкции по введению клеточной терапии определяют, если уровень, количество или концентрация аналита в образце ниже порогового значения, введение пациенту клеточной терапии, необязательно в несниженной дозе, необязательно на амбулаторной основе или без допуска в больницу в течение одного или более дней.
270. Изделие по любому из вариантов осуществления 264-269, в котором инструкции дополнительно определяют введение клеточной терапии пациенту, и в котором инструкции дополнительно определяют, если уровень, количество или концентрация аналита ниже порогового значения:
не введение, до или одновременно с введением клеточной терапии и/или до развития признака или симптома токсичности кроме повышения температуры, агента или средства для лечения, способного к лечению, предотвращению, задержке или уменьшению развития токсичности; и/или
введение клеточной терапии должно быть или может быть введено пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
271. Изделие по любому из вариантов осуществления 264-270, причем пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации и/или в пределах стандартного отклонения от среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
272. Изделие, включающее агент, способный к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности, и инструкции по введению агента после или на основе результатов оценки в биологическом образце уровня, количества или концентрации одного или более аналитов в биологическом образце, причем один или более аналитов выбраны из LDH, ферритина, CRP, IL-6, IL-7, IL-8, IL-10, IL-15, IL-16, TNF-альфа, IFN-гамма, MCP-1, MIP-1бета, эотаксина, G-CSF, IL-1Rальфа, IL-1Rбета, IP-10, перфорина и D-димера (продукта распада фибрина).
273. Изделие согласно варианту осуществления 272, причем указанная оценка включает детекцию, необязательно включающую контактирование реагента, способного к непосредственной или опосредованной детекции аналита, с биологическим образцом, и определение уровня, количества или концентрации аналита в биологическом образце.
274. Изделие согласно варианту осуществления 272 или варианту осуществления 273, в котором инструкции определяют, что агент предназначен для введения i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту и/или дополнительно включает инструкции по использованию с, до и/или в связи с лечением клеточной терапией.
275. Изделие по любому из вариантов осуществления 272-274, в котором указанный биологический образец получен от пациента до введения клеточной терапии или агента.
276. Изделие по любому из вариантов осуществления 257-275, в котором реагент является связывающей молекулой, специфично связывающейся с аналитом.
277. Изделие по любому из вариантов осуществления 257-276, в котором реагент является антителом или его антигенсвязывающим фрагментом.
278. Изделие по любому из вариантов осуществления 257-277, в котором биологический образец или получен из образца крови, плазмы или сыворотки.
279. Изделие по любому из вариантов осуществления 272-278, дополнительно включающее реагент для детекции аналита и/или дополнительно включающее инструкции по использованию с, до и/или в связи с реагентом для детекции аналита.
280. Изделие по любому из вариантов осуществления 272-279, дополнительно включающее клеточную терапию и/или дополнительно включающее инструкции по использованию с, до и/или в связи с лечением клеточной терапией.
281. Изделие по любому из вариантов осуществления 272-280, в котором инструкции по введению агента определяют, если уровень, количество или концентрация аналита в образце равны или выше порогового значения, введение пациенту агента.
282. Изделие согласно варианту осуществления 281, в котором инструкция далее определяет введение клеточной терапии пациенту, причем введение агента должно быть осуществлено (i) до, (ii) в течение одного, двух или трех дней, (iii) одновременно с и/или (iv) при первом повышении температуры после инициации введения клеточной терапии пациенту.
283. Изделие по любому из вариантов осуществления 272-282, в котором инструкции по введению агента определяют, если уровень, количество или концентрация ниже порогового значения, введение пациенту клеточной терапии, причем необязательно инструкции определяют, что клеточная терапия должна быть или может быть введена пациенту в амбулаторном режиме и/или без допуска пациента в больницу на ночь или на один или более дней подряд и/или без допуска пациента в больницу в течение одного или более дней.
284. Изделие по любому из вариантов осуществления 272-283, причем пороговое значение находится в пределах 25%, 20%, 15%, 10% или 5% среднего уровня, количества или концентрации и/или в пределах стандартного отклонения от среднего уровня, количества или концентрации аналита в биологическом образце, полученном от группы пациентов до получения терапевтической композиции клеток, экспрессирующих рекомбинантный рецептор, причем у каждого из пациентов группы продолжала развиваться токсичность после получения композиции клеток, экспрессирующих рекомбинантный рецептор, для лечения того же заболевания или состояния.
285. Изделие по любому из вариантов осуществления 257-284, в котором тестирование или оценку клеток в отношении аналита осуществляют иммунологическим анализом.
286. Изделие по любому из вариантов осуществления 257-285, причем токсичность включает нейротоксичность или синдром высвобождения цитокинов (CRS), необязательно нейротоксичность или CRS степени 1 или более высокую.
287. Изделие по любому из вариантов осуществления 257-286, причем:
токсичность включает тяжелую нейротоксичность и/или включает нейротоксичность степени 2 или более высокой, нейротоксичность степени 3 или более высокой, по меньшей мере пролонгированную нейротоксичность степени 3 или нейротоксичность степени 4 или степени 5 или выше; и/или
токсичность включает тяжелый CRS и/или включает CRS степени 2 или выше или степени 3 или выше.
288. Изделие по любому из вариантов осуществления 257-287, причем токсичность связана с отеком мозга.
289. Изделие по любому из вариантов осуществления 257-288, причем агент или другое средства для лечения представляет собой или включает один или более стероидов; антагонистов или ингибиторов рецептора цитокина или цитокина, выбранного из числа IL-10, IL-10R, IL-6, рецептора IL-6, IFNγ, IFNGR, IL-2, IL-2R/CD25, MCP-1, CCR2, CCR4, MIP1β, CCR5, TNFальфа, TNFR1, IL-1, и IL-1Rальфа/IL-1бета; или агентов, способных к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток.
290. Изделие согласно варианту осуществления 289, причем антагонист или ингибитор представляет собой или включает агент, выбранный из антитела или антигенсвязывающего фрагмента, малой молекулы, белка или пептида и нуклеиновой кислоты.
291. Изделие по любому из вариантов осуществления 257-290, причем агент или другое средство для лечения является анти-IL-6 антителом или антителом к рецептору IL6.
292. Изделие по любому из вариантов осуществления 257-291, причем агент или другое средство для лечения представляет собой или включает агент, выбранный из тоцилизумаба, силтуксимаба, клазакизумаба, сарилумаба, олокизумаба (CDP6038), элсилимомаба, ALD518/BMS-945429, сирукумаба (CNTO 136), CPSI-2634, ARGX-109, FE301 и FM101.
293. Изделие по любому из вариантов осуществления 257-292, причем агент или другое средство для лечения представляет собой или включает тоцилизумаб.
294. Изделие по любому из вариантов осуществления 257-293, причем агент или другое средство для лечения представляет собой или включает силтуксимаб.
295. Изделие согласно варианту осуществления 289, причем стероид представляет собой или включает дексаметазон.
296. Изделие согласно варианту осуществления 289, причем агент, способный к предотвращению, блокированию или ослаблению активности или функции микроглиальных клеток, выбран из противовоспалительного средства, ингибитора NADPH оксидазы (NOX2), блокатора кальциевых каналов, блокатора натриевых каналов, ингибирует GM-CSF, ингибирует CSF1R, специфично связывается с CSF-1, специфично связывается с IL-34, ингибирует активацию ядерного фактора каппа-B (NF-κB), активирует рецептор CB2 и/или является агонистом CB2, ингибитором фосфодиэстеразы, ингибирует микроРНК-155 ((miR-155) или повышающе регулирует микроРНК-124 ((miR-124).
297. Изделие согласно варианту осуществления 296, причем агент, способный к предотвращению, блокированию или ослаблению активации или функции микроглиальных клеток, является малой молекулой, пептидом, белком, антителом или его антигенсвязывающим фрагментом, миметиком антитела, аптамером или молекулой нуклеиновой кислоты.
298. Изделие согласно варианту осуществления 296 или варианту осуществления 297, причем агент выбрана из миноциклина, налоксона, нимодипина, Рилузола, MOR103, леналидомида, каннабиноида, необязательно WIN55 или 212-2, внутривенного иммуноглобулина (IVIg), ибудиласта, анти-miR-155 закрытой нуклеиновой кислоты (LNA), MCS110, PLX-3297, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945, эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003.
299. Изделие по любому из вариантов осуществления 296-298, причем агент является ингибитором рецептора колониестимулирующего фактора 1 (CSF1R).
300. Изделие по любому из вариантов осуществления 296-299, причем ингибитор выбран из:
PLX-3397, PLX647, PLX108-D1, PLX7486, JNJ-40346527, JNJ28312141, ARRY-382, AC-708, DCC-3014, 5-(3-метокси-4-(4-метоксибензил)окси)бензил)пиримидин-2,4-диамина (GW2580), AZD6495, Ki20227, BLZ945 или их фармацевтической соли или пролекарства;
эмактузумаба, IMC-CS4, FPA008, LY-3022855, AMG-820 и TG-3003 или является его антигенсвязывающим фрагментом; или комбинацией любого из предшествующих.
301. Изделие по любому из вариантов осуществления 296-300, причем ингибитор представляет собой PLX-3397.
302. Изделие по любому из вариантов осуществления 24-48 и 257-301, причем рекомбинантный рецептор специфично связывается с антигеном, ассоциированным с заболеванием или состоянием, или экспрессируемым в клетках среды поражения, ассоциированного с заболеванием или состоянием.
303. Изделие по любому из вариантов осуществления 24-48 и 257-302, причем заболевание или состояние представляют собой рак.
304. Изделие по любому из вариантов осуществления 24-48 и 257-303, причем заболевание или состояние являются миеломой, лейкозом или лимфомой.
305. Изделие по любому из вариантов осуществления 24-48 и 257-304, причем заболевание или состояние являются В-клеточной злокачественной опухолью и/или являются острым лимфообластным лейкозом (ALL), ALL взрослых, хроническим лимфообластным лейкозом (CLL), неходжкинской лимфомой (NHL) и диффузной крупноклеточной В-клеточной лимфомой (DLBCL).
306. Изделие по любому из вариантов осуществления 302-305, причем антиген представляет собой ROR1, антиген созревания B-клеток (BCMA), карбоангидразу 9 (CAIX), tEGFR, Her2/neu (рецепторная тирозинкиназа erbB2), L1-CAM, CD19, CD20, CD22, мезотелин, CEA, и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолат-связывающий белок (FBP), FCRL5, FCRH5, эмбриональный рецептор ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, рецептор, содержащий домен вставки киназы (kdr), легкую каппа-цепь, антиген Ley, молекулу L1-клеточной адгезии, (L1-CAM), меланома-ассоциированный антиген (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, рецептор альфа 2 IL-13 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, альфа-рецептор фолиевой кислоты, CD44v6, CD44v7/8, avb6 интегрин, 8H9, NCAM, рецепторы VEGF, 5T4, эмбриональный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, мышиный CMV, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, карциноэмбриональный антиген (CEA), Her2/neu, эстрогеновый рецептор, прогестероновый рецептор, эфринB2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138, 5D рецептор, связанный с G-белком (GPCR5D) или патоген-специфический антиген.
307. Изделие по любому из вариантов осуществления 24-48 и 257-306, причем рекомбинантный рецептор является Т-клеточным рецептором или функциональным не Т-клеточным рецептором.
308. Изделие по любому из вариантов осуществления 24-48 и 257-307, причем рекомбинантный рецептор является химерным антигенным рецептором (CAR).
309. Изделие согласно варианту осуществления 308, причем CAR включает внеклеточный антигенраспознающий домен, специфично связывающийся с антигеном, и внутриклеточный сигнальный домен, включающий ITAM, причем необязательно внутриклеточный сигнальный домен включает внутриклеточный домен CD3-дзэта (CD3ζ) цепи; и/или причем CAR дополнительно включает костимулирующий сигнальный домен, необязательно включающий сигнальный домен CD28 или 4-1BB.
310. Изделие по любому из вариантов осуществления 24-48 и 257-309, причем генно-инженерные клетки включают Т-клетки, необязательно CD4+ и/или CD8+.
311. Изделие согласно варианту осуществления 310, причем Т-клетками являются первичные Т-клетки, полученные от пациента.
312. Изделие по любому из вариантов осуществления 257-311, причем доза, не связанная с риском развития токсичности или тяжелой токсичности, представляет собой или включает менее чем или менее чем приблизительно 5x107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, менее чем или менее чем приблизительно 2,5x107, менее чем или менее чем приблизительно 1,0x107, менее чем или менее чем приблизительно 5,0x106, менее чем или менее чем приблизительно 1,0x106, менее чем или менее чем приблизительно 5,0x105 или менее чем или менее чем приблизительно 1x105 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
313. Изделие по любому из вариантов осуществления 257-312, причем доза, не связанная с риском развития токсичности или тяжелой токсичности, составляет или включает от или от приблизительно 1x105 до 5x107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC), например, от 1x105 до 2,5x107, от 1x105 до 1,0x107, от 1x105 до 5,0x106, от 1x105 до 1,0x106, от 1,0x105 до 5,0x105, от 5,0x105 до 5x107, от 5x105 до 2,5x107, от 5x105 до 1,0x107, от 5x105 до 5,0x106, от 5x105 до 1,0x106, от 1,0x106 до 5x107, от 1x106 до 2,5x107, от 1x106 до 1,0x107, от 1x106 до 5,0x106, от 5,0x106 до 5x107, от 5x106 до 2,5x107, от 5x106 до 1,0x107, от 1,0x107 до 5x107, от 1x107 до 2,5x107 или от 2,5x107 до 5x107 общих экспрессирующих рекомбинантный рецептор клеток, необязательно CAR+ клеток, общих Т-клеток или общих одноядерных клеток периферической крови (PBMC).
314. Изделие по любому из вариантов осуществления 257-313, причем реагент мечен таким образом, чтобы его можно было детектировать, необязательно флуоресцентно мечен.
315. Изделие по любому из вариантов осуществления 257-314, причем один или более аналитов представляют собой LDH, ферритин, CRP, IL-6, IL-8, IL-10, TNF-альфа, IFN-альфа2, MCP-1 и MCP-1бета.
316. Изделие по любому из вариантов осуществления 257-315, причем один или более аналитов представляет собой или включает LDH.
317. Изделие по любому из вариантов осуществления 221-316, причем:
CAR включает scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно представляет собой или включает 4-1BB, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно представляет собой или включает CD3дзета сигнальный домен и необязательно дополнительно включает спейсер между трансмембранным доменом и scFv;
CAR включает, в указанном порядке, scFv, специфичный для антигена, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно представляет собой или включает 4-1BB сигнальный домен, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно является CD3дзета сигнальный домен; или
CAR включает, в указанном порядке, scFv, специфичный для антигена, спейсер, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, который необязательно является 4-1BB сигнальным доменом, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы, который необязательно представляет собой или включает CD3дзета сигнальный домен; и причем:
спейсер является необязательно полипептидным спейсером, который (a) включает или состоит из всего или части шарнирного участка иммуноглобулина или его модифицированной версии или включает приблизительно 15 аминокислот или менее и не включает внеклеточный домен CD28 или внеклеточный домен CD8, (b) включает или состоит из всего или части шарнирного участка иммуноглобулина, необязательно шарнира IgG4 или его модифицированной версии и/или включает приблизительно 15 аминокислот или менее и не включает внеклеточный домен CD28 или внеклеточный домен CD8, или (c) имеет длину 12 или приблизительно 12 аминокислот и/или включает или состоит из всего или части шарнирного участка иммуноглобулина, необязательно IgG4 или его модифицированной версии; или (d) имеет или состоит из последовательности SEQ ID NO: 1, последовательности, кодируемой SEQ ID NO: 2, SEQ ID NO: 30, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34 или вариантом любой из предшествующих, имеющим по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней, или (e) включает или состоит из формулы X1PPX2P, где X1 является глицином, цистеином или аргинином, и X2 является цистеином или треонином; и/или
костимулирующая область включает SEQ ID NO: 12 или ее вариант, имеющий по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней; и/или
первичный сигнальный домен включает SEQ ID NO: 13 или 14 или 15, имеющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с ней; и/или
scFv включает последовательность CDRL1 RASQDISKYLN (SEQ ID NO: 35), последовательность CDRL2 SRLHSGV (SEQ ID NO: 36) и/или последовательность CDRL3 GNTLPYTFG (SEQ ID NO: 37), и/или последовательность CDRH1 DYGVS (SEQ ID NO: 38), последовательность CDRH2 VIWGSETTYYNSALKS (SEQ ID NO: 39) и/или последовательность CDRH3 YAMDYWG (SEQ ID NO: 40), или причем scFv включает вариабельную область тяжелой цепи FMC63 и вариабельную область легкой цепи FMC63 и/или последовательность CDRL1 FMC63, последовательность CDRL2 FMC63, последовательность CDRL3 FMC63, последовательность CDRH1 FMC63, последовательность CDRH2 FMC63 и последовательность CDRH3 FMC63 или связывается с тем же эпитопом или конкурирует за связывание с любым из предшествующих, и причем необязательно scFv включает, в указанном порядке, VH, линкер, необязательно включающий SEQ ID NO: 24, и VL, и/или scFv включает гибкий линкер и/или включает аминокислотную последовательность, представленную как SEQ ID NO: 24.
318. Изделие по любому из пп. 221-317, в котором инструкции предоставляют информацию о пороговом значении, индивидуально для каждого одного или более аналитов, которое является индикатором вероятности того, продемонстрирует ли пациент ответ на лечение клеточной терапией.
319. Изделие по любому из пп. 221-317, в котором инструкции предоставляют информацию о пороговом значении, индивидуально для каждого одного или более аналитов, которое является индикатором вероятности того, продемонстрирует ли пациент длительный ответ после введения клеточной терапии.
320. Изделие по любому из пп. 221-317, в котором инструкции предоставляют информацию о пороговом значении, индивидуально для каждого одного или более аналитов, которое является индикатором вероятности того, продемонстрирует ли пациент токсичность после введения клеточной терапии.
VIII. Определения
[0797] Термины «полипептид» и «белок» используются взаимозаменяемо для обозначения полимеру из аминокислотных остатков и не ограничены минимальной длиной. Полипептиды, включая рецепторы по изобретению и другие полипептиды, например, линкеры или пептиды, могут включать аминокислотные остатки включая натуральные и/или ненатуральные аминокислотные остатки. Термины также включают постэкспрессионные модификации полипептида, например, гликозилирования, сиалирования, ацетилирования и фосфорилирования. В некоторых аспектах полипептиды могут содержать модификации относительно нативной или естественной последовательности, при условии, что белок поддерживает желаемую активность. Эти модификации могут быть преднамеренными, как через сайт-направленный мутагенез, или могут быть случайными, такими как через мутации хозяев, продуцирующих белки, или вследствие ошибок при амплификации ПЦР.
[0798] В рамках изобретения «пациент» является млекопитающим, таким как человек или другое животное, и как правило, является человеком. В некоторых вариантах осуществления лицо, например, пациент, которому вводят агент или агенты, клетки, популяции клеток или композиции, является млекопитающим, как правило, приматом, таким как человек. В некоторых вариантах осуществления примат является обезьяной или человекообразной обезьяной. Пациент может быть мужчиной или женщиной и может иметь любой подходящий возраст, включая младенца, подростка, юношу, взрослого и гериатрических пациентов. В некоторых вариантах осуществления пациентом является млекопитающее, не являющееся приматом, такое как грызун.
[0799] В рамках изобретения, «лечение» (и грамматические вариации этого термина, такие как «лечить» или «лечащий») относится к полному или частичному облегчению или уменьшению заболевания или состояния, или нарушения, или симптома, неблагоприятного эффекта или результата или фенотипа, связанного с ними. Желаемые эффекты лечения включают, но не ограничены ими, предотвращение возникновения или рецидива заболевания, облегчение симптомов, уменьшение любых прямых или косвенных патологических последствий заболевания, предотвращение метастазирования, уменьшение скорости прогрессирования заболевания, улучшение или временное облегчение болезненного состояния, и ремиссия или улучшенный прогноз. Термины не подразумевают полное исцеление заболевания или полное устранение любого симптома или эффекта(ов) на все симптомы или результаты.
[0800] В рамках изобретения, “задержка развития заболевания” означает отсрочивать, препятствовать, замедлять, задерживать, стабилизировать, подавлять и/или откладывать развитие заболевания (такого как рак). Эта задержка может иметь вариабельные отрезки времени, в зависимости от истории заболевания и/или получающего лечение человека. В некоторых вариантах осуществления достаточная или значительная задержка может, в действительности, охватывать профилактику, в которой у человека не развивается заболевание. Например, рак поздней стадии, такой как развитие метастаза, может быть задержан.
[0801] «Предотвращение», в рамках изобретения, включает обеспечение профилактики относительно возникновения или рецидива заболевания у пациента, который может быть предрасположен к заболеванию, но у кого еще не было диагностировано это заболевание. В некоторых вариантах осуществления клетки и композиции по изобретению используются для задержки развития заболевания или замедления прогрессии заболевания.
[0802] В рамках изобретения, «подавлять» функцию или активность означает уменьшить функцию или активность по сравнению с теми же состояниями за исключением состояния или параметра интереса, или альтернативно, по сравнению с другим состоянием. Например, клетки, подавляющие рост опухоли, уменьшают скорость роста опухоли по сравнению со скоростью роста опухоли в отсутствие клеток.
[0803] “Эффективное количество” агента, например, фармацевтического состава, клеток или композиции, в контексте введения, относится к эффективному количеству, в дозировках/количествах и в течение промежутков времени, необходимых для достижения желаемого результата, такого как терапевтический или профилактический результат.
[0804] “Терапевтически эффективное количество” агента, например, фармацевтического состава или клеток, относится к эффективному количеству, в дозировках и в течение промежутков времени, необходимых для достижения желаемого терапевтического результата, такого как лечение заболевания, состояния или нарушения, и/или фармакокинетического или фармакодинамического эффекта лечения. Терапевтически эффективное количество может варьировать в зависимости от таких факторов как болезненное состояние, возраст, пол и масса тела пациента, и популяция введенных клеток. В некоторых вариантах осуществления способы по изобретению включают введение клеток и/или композиций в эффективных количествах, например, терапевтически эффективных количествах.
[0805] “Профилактически эффективное количество” относится к эффективному количеству, в дозировках и в течение промежутков времени, необходимых для достижения желаемого профилактического результата. Как правило, но не обязательно, так как профилактическая доза используется у пациентов до или в более ранней стадии заболевания, профилактически эффективное количество будет меньше терапевтически эффективного количества. В контексте более низкой опухолевой массы профилактически эффективное количество в некоторых аспектах будет выше, чем терапевтически эффективное количество.
[0806] Термин «приблизительно», используемый здесь, относится к обычному ошибочному диапазону для соответствующего значения, легко понятному для специалиста в этой технической области. Ссылка на «приблизительное» значение или параметр здесь включает (и описывает) варианты осуществления, направленные на это значение или параметр per se.
[0807] В рамках изобретения формы единственного числа включают формы множественного числа, если из контекста ясно не следует иное. Например, «один» означает «по меньшей мере один» или “один или более”.
[0808] В рамках этого раскрытия различные аспекты заявленного изобретения представлены в формате диапазона. Следует понимать, что описание в формате диапазона дано просто для удобства и краткости и не должно быть истолковано как негибкое ограничение объема заявленного изобретения. Соответственно, описание диапазона, как следует понимать, специфично раскрывает все возможные поддиапазоны, а также отдельные числовые обозначения в этом диапазоне. Например, если приведен диапазон значений, понятно, что каждое значение между верхним и нижним пределом этого диапазона и любое другое установленное или упомянутое значение в этом установленном диапазоне охватывается в заявленном изобретении. Верхние и нижние пределы этих меньших диапазонов могут независимо быть включены в меньшие диапазоны и также охвачены в заявленном изобретении согласно любому специфично исключенному пределу в установленном диапазоне. Если установленный диапазон включает один или оба из предельных значений, диапазоны, исключающие один или оба из этих включенных предельных значений, также включены в рамки заявленного изобретения. Это применимо независимо от ширины диапазона.
[0809] В рамках изобретения композиция относится к любой смеси двух или более продуктов, веществ или соединений, включая клетки. Она может быть раствором, суспензией, жидкостью, порошком, пастой, водной, неводной или любой их комбинацией.
[0810] В рамках изобретения «обогащение» по отношению к одному или более определенных типов клеток или популяций клеток относится к увеличению числа или процента этого типа или популяции клеток, например, по сравнению с общим количеством клеток или объемом композиции, или относительно других типов клеток, таких как выбранные положительным выбором на основе маркеров, экспрессируемых популяцией или клеткой, или отрицательным выбором на основе маркера, не присутствующих на популяции клеток или клетке, которая должна быть деплетирована. Термин не требует полного удаления других клеток, типа или популяции клеток из композиции и не требует, чтобы клетки, таким образом, обогащенные, присутствовали в количестве или даже около 100% в обогащенной композиции.
[0811] В рамках изобретения утверждение, что клетка или популяция клеток являются «положительными» в отношении определенного маркера, относится к поддающемуся обнаружению присутствию на или в клетке определенного маркера, как правило поверхностного маркера. При обращении к поверхностному маркеру термин относится к наличию поверхностной экспрессии, обнаруживаемой потоковой цитометрией, например, путем окрашивания антителом, специфично связывающимся с маркером, и детекции указанного антитела, причем окрашивание является поддающимся обнаружению потоковой цитометрией на уровне существенно выше окрашивания, обнаруживаемого при выполнении той же процедуры с подобранным по изотипу контролем или флуоресценцией минус одной (FMO) gating контроль под иначе идентичными состояниями и/или на уровне, существенно подобном этому для клетки, которая, как известно, была положительной для маркера, и/или на уровне существенно выше, чем это для клетки, которая, как известно, была отрицательна для маркера.
[0812] В рамках изобретения, заявление, что клетка или популяция клеток «отрицательны» для определенного маркера, относится к отсутствию существенного детектируемого наличия на или в клетке определенного маркера, как правило поверхностный маркер. При обращении к поверхностному маркеру термин относится к отсутствию поверхностной экспрессии, как обнаружено потоковой цитометрией, например, путем окрашивания антителом, специфично связывающимся к маркеру и обнаружению указанного антитела, в чем окрашивание не обнаружено потоковой цитометрией на уровне существенно выше окрашивания, обнаруженного, выполнив ту же процедуру с подобранным с изотипом контролем или контролем с помощью флуоресценции с комбинацией детектируемых меток без одной (FMO) в в остальном идентичных условиях, и/или на уровне существенно более низком, чем для клетки, которая, как известно, была положительной в отношении маркера, и/или на уровне, существенно подобном по сравнению с таковым для клетки, которая, как известно, была отрицательной в отношении маркера.
[0813] Термин «вектор», в рамках изобретения, относится к молекуле нуклеиновой кислоты, способной к размножению другой нуклеиновой кислоты, с которой она связана. Термин включает вектор как самореплицирующуюся структуру нуклеиновой кислоты, а также вектор, включенный в геном клетки-хозяина, в которую он был введен. Определенные векторы способны к направлению экспрессии нуклеиновых кислот, с которыми они оперативно связаны. Такие векторы упомянуты здесь как «векторы экспрессии».
[0814] Если не указано иное, все термины из уровня техники, примечания и другие технические и научные термины или терминологии, используемые здесь, имеют то же значение, которое обычно понимается в области, к которому относится заявленное изобретение. В некоторых случаях термины с обычно понимаемыми значениями определяются здесь для ясности и/или для быстрой ссылки, и включение таких определений в настоящее описание не должно обязательно быть истолковано для представления существенных различий с тем, что обычно понимается.
[0815] Все публикации, включая патентные документы, научные статьи и базы данных, упомянутые в этой заявке, полностью включены посредством ссылок во всех целях в той же степени, как если бы каждая отдельная публикация была индивидуально включена посредством ссылок. Если определение, сформулированное здесь, противоречит или иначе не совпадает с определением, сформулированным в патентах, заявках, публикациях заявок и других публикациях, которые включены в настоящее описание посредством ссылок, определение, сформулированное здесь, преобладает над определением, включенным в настоящее описание ссылкой.
[0816] Заголовки разделов, используемые здесь, даны только в организационных целях и не должны быть истолкованы как ограничение описанного изобретения.
IX. Примеры
[0817] Следующие примеры включены только в иллюстративных целях и не предназначены для ограничения объема изобретения.
Пример 1: Введение Анти-CD19 CAR-экспрессирующих клеток пациентам с рецидивирующей и рефрактерной неходжкинской лимфомой (NHL)
A. Пациенты и лечение
[0818] Терапевтические композиции CAR+ Т-клеток, содержащие аутогенные Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфичный для CD19, вводят пациентам с В-клеточными злокачественными опухолями.
Пример 1.А.1
[0819] В этом Примере 1.А.1 описаны результаты оценки через определенный момент времени (1.А.1) в продолжающемся клиническом исследовании, в котором вводили такую терапию пациентам с В-клеточными злокачественными опухолями. В частности, контингент (полный контингент) (в этот момент времени пятьдесят пять (55)) взрослых с рецидивирующей или рефрактерной агрессивной неходжкинской лимфомой (NHL) (R/R), включая диффузную крупноклеточную В-клеточную лимфому (DLBCL), de novo или трансформированную из вялотекущей лимфомы (NOS), высокодифференцированную В-клеточную лимфому, с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit), DLBCL, трансформированную из хронического лимфолейкоза (CLL) или лимфом маргинальной зоны (MZL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL) и фолликулярную лимфому степени 3b (FL3B) после неудачи 2 линий терапии. Среди получающих лечение пациентов были те, которые имеют оценку Eastern Cooperative Oncology Group (ECOG) от 0 до 2 (среднее наблюдение 3,2 месяца). Полный контингент не включал пациентов с мантийноклеточной лимфомой (MCL). Никто из пациентов не были исключены на основе предшествующей аллогенной трансплантации стволовых клеток (SCT), вторичного участия центральной нервной системы (ЦНС) или оценки ECOG 2, и не было никакого минимального абсолютного количества лимфоцитов (ALC) для требуемого афереза.
[0820] Результаты были отдельно оценены для основной субпопуляции пациентов в полном контингенте (пациенты в полном контингенте, исключая пациентов с неудовлетворительным статусом (ECOG 2), DLBCL, трансформированной из лимфом маргинальной зоны (MZL) и/или хронического лимфолейкоза (CLL, Рихтер), и пациентов с первичной медиастинальной крупноклеточной В-клеточной лимфомой (PMBCL) и фолликулярной лимфомой стадии 3B (FL3B) (основной контингент)). Основной контингент включает пациентов с DLBCL, NOS и трансформированной фолликулярной лимфомой (tFL) или В-клеточная лимфомой (double/triple hit) высокой стадии или высокодифференцированной В-клеточной лимфомой, с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit) и с Eastern Cooperative Oncology Group Performance Status (ECOG PS) 0 или 1. В момент времени в Примере 1.А.1 оценивали результаты для 44 пациентов в этом основном контингенте.
[0821] Демографические и базовые характеристики полного и основного контингента пациентов в момент времени в Примере 1.А.1 представлены в Таблице E1.
N=55
N=44
[0822] Вводимые композиции терапевтических Т-клеток были получены способом, включающим иммуноафинное (например, иммуномагнитный выбор) обогащение CD4+ и CD8+ клеток из образцов лейкафереза от пациента, получающего лечение. Выделенные CD4+ и CD8+ Т-клетки были отдельно активированы и независимо трансформированы вирусным вектором (например, лентивирусным вектором), кодирующим анти-CD19 CAR, с последующим отдельным ростом и криоконсервацией популяции генно-инженерных клеток в низком объеме. CAR содержали анти-CD19 scFv, полученный из мышиного антитела (вариабельная область, полученная из FMC63, ориентации VL-линкер-VH), полученный из иммуноглобулина спейсер, трансмембранный домен, полученный из CD28, костимулирующая область, полученная из 4-1BB, и CD3-дзэта внутриклеточный сигнальный домен. Вирусный вектор далее содержал последовательности, кодирующие усеченный рецептор, служивший суррогатным маркером для экспрессии CAR; отделенный от последовательности CAR последовательностью пропуска рибосомы T2A.
[0823] Сохраненные замораживанием композиции клеток оттаивали до внутривенного введения. Терапевтическая доза Т-клеток была введена как определенная композиция клеток путем введения составленной популяции CD4+ CAR+ клеток и составленной популяции CD8+ CAR+ клеток, вводимых в целевом отношении приблизительно 1:1. Пациентам вводили единственную или двойную дозу CAR-экспрессирующих Т-клеток (каждая единственная доза через отдельные вливания CD4+ CAR-экспрессирующих Т-клеток и CD8+ CAR-экспрессирующих Т-клеток, соответственно) следующим образом: единственная доза уровня 1 (DL-1) дозы, содержащей 5x107 общих CAR-экспрессирующих Т-клеток (n=30 для пациентов, оцененных в Примере 1.А.1), двойная доза DL1, в которой каждая доза была введена с интервалом приблизительно в четырнадцать (14) дней (n=6 для пациентов, оцененных в Примере 1.А.1, вводимые в день 1 и день 14, включая одного пациента, непреднамеренно получившего две дозы DL2 через график с двумя дозами вследствие ошибки при введении), или единственная доза уровня 2 (DL-2) дозы, содержащей 1x108 общих CAR-экспрессирующих Т-клеток (n=18 для пациентов, оцененных в Примере 1.А.1). Целевой уровень дозы и число субпопуляций Т-клеток для введенных композиций представлены в Таблице E2.
(CD4+CAR+)
(CD8+CAR+)
(CD3+ CAR+)
[0824] Начиная с момента до вливания CAR+ Т-клеток, пациенты получали противолимфоцитарную химиотерапию с использованием флударабина (flu, 30 мг/м2) и циклофосфамида (Cy, 300 мг/м2) в течение трех (3) дней. Пациенты получали CAR-экспрессирующие Т-клетки спустя 2-7 дней после этой лимфодеплеции.
Пример 1.А.2
[0825] В Примере 1.А.2 в следующий момент времени в клиническом исследовании, описанном в этом Примере 1 выше, анализировали результаты. В этот момент времени в Примере 1.А.2 74 пациента получали лечение (51 мужчина, 23 женщины). Пациенты включали шестьдесят девять (69) пациентов в полном контингенте DLBCL (включая 67 NOS DLBCL (45 de novo, 14 трансформированных из FL, 8 трансформированных из CLL или MZL), 1 FL степени 3B и 1 PMBCL) и 5 пациентов в контингенте MCL. Среди пациентов в полном (DLBCL) контингенте средний возраст составлял 61 год (диапазон 26, 82), среднее число предшествующих терапий составляло 3 (диапазон 1, 12), 46 (67%) были хеморефрактерными, 32 (46%) имели любую предшествующую трансплантацию, и по меньшей мере 16 (23%) пациентов - лимфому double/triple hit. Сорок девять (49) пациентов в основном контингенте были оценены в этот момент времени в 1.А.2.
B. Безопасность
[0826] Были оценены наличие или отсутствие нежелательных явлений, возникших в ходе лечения, (TEAE) после введения клеточной терапии CAR-T. Пациентов также оценивали и контролировали в отношении нейротоксичности (неврологические осложнения, включая симптомы спутанности, афазии, энцефалопатии, миоклонические судороги, конвульсии, летаргия и/или изменение психического статуса), классифицированной на основании масштаба 1-5, согласно шкале National Cancer Institute-Common Toxicity Criteria (CTCAE), Version 4,03 (NCI-CTCAE v4,03). Шкала Common Toxicity Criteria (CTCAE), версия 4,03 (NCI-CTCAE v4,03). См. Common Terminology for Adverse Events (CTCAE) Version 4, U.S.Department of Health and Human Services, опубликовано: 28 мая 2009 (v4,03: 14 июня 2010); и Guido Cavaletti & Paola Marmiroli Nature Reviews Neurology 6, 657-666 (декабрь 2010). Синдром высвобождения цитокинов (CRS) также был определен и проверен, классифицирован на основе серьезности. См. Lee et al, Blood. 2014;124(2):188-95. В некоторых случаях сообщалось о нежелательных явлениях, и данные собирали, начиная с лимфодеплеции до 90 дней после введения CAR+ Т-клеток.
Пример 1.B,1
[0827] Пример 1.B,1 описывает результаты на основе анализа в Примере 1.А.1.
[0828] ФИГ. 1 изображает процент таких пациентов, которые, по наблюдениям, испытывали лабораторные патологии и TEAEs, произошедшие у ≥20% пациентов. В дополнение к TEAEs, показанному на ФИГ. 1, следующие термины событий наблюдались на Уровне 3-4 у ≥5% пациентов: количество лейкоцитов уменьшилось на (13,6%), энцефалопатия (12%), гипертензия (7%). Степень наблюдаемой токсичности соответствовала уровням дозы от 1 до 2.
[0829] У 84% полного контингента пациентов в Примере 1.B,1 тяжелый (степени 3 или выше) синдром высвобождения цитокинов (CRS) и тяжелая нейротоксичность не наблюдались. Кроме того, было замечено, что у 60% пациентов полного контингента не развивалось какого-либо CRS или нейротоксичности. Никаких различий в уровне CRS, нейротоксичности (NT), sCRS или тяжелой нейротоксичности (sNT) не наблюдалось между уровнями дозы. Таблица E3 суммирует уровень нежелательных явлений синдрома высвобождения цитокинов (CRS) и нейротоксичности у пациентов спустя 28 дней после получения по меньшей мере одной дозы клеток CAR-T. Как показано в Таблице E3, никакого sCRS (Степени 3-4) не наблюдалось ни у каких пациентов, получивших единственную дозу DL2 или двойную дозу DL1. Тяжелая нейротоксичность или тяжелый CRS (степени 3-4) наблюдались у 16% (9/55) полного контингента пациентов и у 18% (8/44) пациентов в основной субпопуляции. 11% (n=6) пациентов получили тоцилизумаб, 24% (n=13) пациентов получили дексаметазон. Среди пациентов ECOG2 в полном контингенте наблюдаемая частота CRS и нейротоксичности составляла 71% и 29%, соответственно.
[0830] ФИГ. 2 показывает кривую Каплана-Мейера, изображающую наблюдаемое время к началу CRS и/или нейротоксичности для анализа в 1.B,1. Как показано, наблюдаемые средние времена до начала CRS и до начала нейротоксичности составляли 5 и 11 дней, соответственно, только у 11% пациентов наблюдалось начало CRS спустя меньше чем 72 часа после инициации введения клеточной терапии. Среднее время до устранения CRS и нейротоксичности для Степени 1 или лучшей составляло 5 и 7 дней, соответственно. Среднее время завершения устранения CRS и нейротоксичности составляло 5 и 11 дней, соответственно. Результаты согласовывались с заключением, что наблюдался низкий процент раннего начала CRS или нейротоксичности у пациентов.
Пример 1.B,2
[0831] Пример 1.B,2 описывает оценку в момент времени в Примере 1.B,2. До этого момента времени данные о нежелательных явлениях (AE) были собраны от момента лимфодеплеции (LD) до 90 дней после введения CAR-экспрессирующих Т-клеток. Во второй момент времени 69 пациентов в контингенте DLBCL (полный контингент) были оценены на безопасность, 38 получили единственную дозу DL1, 25 получили единственную дозу DL2, и 6 получили двойную дозу DL1. Наиболее распространенные TEAE кроме CRS или NT включали нейтропению (41%, 28/69), усталость (30%, 21/69), тромбоцитопению (30%, 21/69) и анемию (26%, 18/69). Наблюдался один случай TEAE, представлявший собой диффузное альвеолярное повреждение степени 5.
[0832] Никакой острой инфузионной токсичности не наблюдалось, и у большинства пациентов в полном контингенте, 64% (44/69), по наблюдениям, не было CRS или NT, что указывает, что амбулаторная доставка CAR-экспрессирующих Т-клеток может быть возможна. Частота связанной с CAR Т-клетками токсичности, включая CRS и NT, не различалась между уровнями дозы. Профиль безопасности, по наблюдениям, был сравнимым для разных уровней дозы и контингентов. Среди 25 пациентов в полном контингенте (36%), которые испытывали какую-либо степень CRS или NT, 21 (30%) имели CRS и 14 (20%) имели NT. Никто из пациентов не имел CRS Степени 3, и только один (1%, 1/69) имел CRS Степени 4 и потребовал ICU; другие 29% (20/69) имели CRS Степени 1-2. Из 20% пациентов с NT 6% (4/69) имели Степени 1-2, и 14% (10/69) имели Степени 3-4; 2 (3%) имели судороги. Не наблюдалось никаких CRS Степени 5 или NT степени 5. Не наблюдалось никакой заболеваемости отеком мозга. Все события CRS и NT были устранены, кроме одного случая тремора Степени 1, который продолжался во время анализа. Среднее время к началу первого CRS и NT составляло 5 дней (диапазон 2, 12) и 10 дней (диапазон 5, 23), соответственно. В первые 72 часа после вливания никто из пациентов, по наблюдениям, не имел NT, и только 10% (7/69), по наблюдениям, имели CRS (все Степени 1); NT предшествовала CRS у >70% пациентов. В целом, тринадцать (13) пациентов (19%) потребовали вмешательства для терапии CRS или NT с использованием антицитокина (тоцилизумаб индивидуально 1 (1%), дексаметазон индивидуально 6 (9%) или оба 6 (9%)) и только один потребовал вазопрессорной поддержки. Средние дозы тоцилизумаба и дексаметазона составляли 1 и 6, соответственно. Средняя продолжительность CRS и NT составляла 5 дней и 11 дней, соответственно. Анализ основного контингента (n=49) также показал подобную частоту CRS и NT.
[0833] В этой оценке низкая встречаемость и позднее начало CRS и/или NT наблюдались на обоих уровнях дозы, подтверждая выполнимость амбулаторного вливания, например, с госпитализацией при первом симптоме повышения температуры или повышения температуры, длящегося дольше определенного периода времени. Никакого CRS Степени 5 или NT Степени 5 не наблюдалось, и все тяжелые CRS и тяжелые NT были устранены. Далее, приблизительно 2 из 3 пациентов не имели никакого CRS или NT, что подтверждает, что клетки могут быть введены на амбулаторной основе. Во время оценки в 1.B,2, четыре пациента получали лечение в амбулаторном режиме. Далее, никаких значимых различий в токсичности не наблюдалось у пациентов, получающих DL1 или DL2, что указывает достижение более высокой частоты ответа без риска увеличения проблем токсичности или безопасности.
C. Результаты ответа после лечения
[0834] Пациентов проверяли в отношении ответа, включая оценку опухолевой массы через 1, 3, 6, 7, 12, 18 и 24 месяца после введения CAR+ Т-клеток.
Пример 1.C,1
[0835] Пример 1.C,1 описывает результаты на основе анализа в Примере 1.А.1 и 1.B,1.
[0836] Частоты ответа перечислены в Таблице E4. Высокие длительные частоты ответа наблюдались в контингенте пациентов, включавших пациентов, получавших серьезное предварительное лечение, или пациентов с неблагоприятным прогнозом и/или с рецидивирующим или рефрактерным заболеванием. Для пациентов, получавших все уровни дозы в Основном (n=44) контингенте, наблюдаемая частота общего ответа (ORR) составляла 86%, и наблюдаемая частота полного ответа (CR) составляла 59%. В три месяца для основного контингента частота общего ответа (ORR) составляла 66%; трехмесячный уровень CR составлял 50% среди основного контингента. В основном контингенте 3-месячный ОРР составлял 58% (11/19) на уровне 1 дозы и 78% на уровне 2 дозы; 3-месячный уровень CR составлял 42% (8/19) для уровня 1 дозы и 56% (5/9) для уровня 2 дозы, что соответствовало предложенному эффекту доза ответ на результаты лечения. Кроме того, результаты соответствовали отношению между дозой и длительностью ответа.
(95% CI)
(62, 87)
(61, 92)
(47, 90)
(23, 96)
(73, 95)
(64, 95)
(60, 98)
(40, 100)
(95% CI)
(38, 66)
(34, 72)
(26, 74)
(12, 88)
(43, 74)
(35, 76)
(32, 84)
(19, 99)
(95% CI)
(35, 67)
(26, 67)
(31, 89)
(12, 88)
(47, 81)
(34, 80)
(40, 97)
(19, 99)
(95% CI)
(24, 56)
(16, 55)
(17, 77)
(12, 88)
(32, 68)
(20, 67)
(21, 86)
(19, 99)
a Включая пациентов с событием PD, смерти или 28-дневных повторных исследований. Пациенты, получавшие лечение за 28 дней до снимка данных, не были включены.
b Знаменатель представляет собой число пациентов, получавших CAR
Т-клеточную терапию ≥ 3 месяца назад до даты снимка данных с оценкой
эффективности в Месяц 3 или до оценки PD или смерти.
c Включает одного пациента, получавшего лечение 2 дозами DL2 вследствие ошибки при введении
[0837] Полные частоты ответа среди различных подгрупп пациентов в полных и основных контингентах показаны на ФИГ. 3 А и 3B, соответственно. В подгруппе с низким риском DLBCL частоты ответа были обычно высокими. ОРР более чем 50% наблюдался в 3 месяца у пациентов с молекулярным подтипом double/triple hit, имевших первичную рефрактерную или хеморефрактерную DLBCL или которые никогда ранее не достигали CR. Полное устранение участия ЦНС при лимфоме наблюдалось у 2 пациентов.
[0838] Среди пациентов, получающих лечение шесть месяцев или более до определенного момента времени оценки, десять (10) пациентов, которые были в состоянии ответа в три месяца, 9 (90%) остались в состоянии ответа в шесть месяцев. В момент времени оценки 97% пациентов в основной субпопуляции, которые ответили, были живы и в среднее последующее время наблюдения 3,2 месяца.
[0839] Результаты в отношении длительности ответа и полного выживания (сгруппированные по лучшему полному ответу (не отвечающие, CR/PR, CR и/или PR)) показаны для полного и основного контингентов пациентов на Фиг. 4 А и 4B, соответственно. Как показано, длительная выживаемость наблюдалась у отвечающих пациентов с увеличенной длительностью ответа у пациентов с CRs. Все пациенты в состоянии ответа в три месяца остались живыми во время оценки, несмотря на то, что 5/6 пациентов с неудовлетворительным статусом (ECOG 2) скончались.
[0840] ФИГ. 8 показывает график, демонстрирующий время без прогрессии (месяцы) для отдельных пациентов в полном и основном контингентах. Каждая отметка представляет единственного пациента. Штриховка указывает лучший полный ответ (в каждом случае, если не указано иное, достигнутый в 1 месяц); текстура указывает дозу (сплошное закрашивание = уровень дозы 1, единственная доза; косая штриховка, уровень дозы 2, единственная доза; вертикальная штриховка = уровень дозы 1, две дозы). Горизонтальные стрелки указывают на продолжающийся ответ. Некоторых индивидуальных пациентов первоначально оценивали (например, в 1 месяц) как показывающих стабильное заболевание (SD) или частичный ответ (PR), и они, как позже наблюдалось, достигли PR (например, преобразование SD в PR) или CR. В таких случаях штриховка отметки индивидуального пациента, как отмечено, указывает лучший полный ответ, и точки (то же соответствие штриховки достигнутому ответу) вдоль каждой отметки индивидуального пациента указывают, когда каждый из SD, PR и/или CR, по наблюдениям, произошел у пациента.
[0841] Полное устранение участия ЦНС в лимфоме наблюдалось у двух пациентов. CAR+ клетки у одного пациента, по наблюдениям, показали рост после биопсии после рецидива. Пациент, который показал рост после биопсии, имел хеморефрактерную трансформированную DLBCL (подтип герминативного центра с перестановкой BCL2 и множественными копиями MYC и BCL6). Пациенту вводили CAR+ Т-клетки в DL-1, и числа CD3+/CAR+, CD4+/CAR+, CD8+/CAR+ Т-клеток в периферической крови, измеренные в определенные моменты времени, показаны на ФИГ. 6А. Пациент ранее получал, и оказался рефрактерным к ним, пять предшествующих линий терапии, включая этопозид, доксорубицин и циклофосфамид в индивидуально подобранной дозе с винкристином и преднизоном плюс ритуксимаб (DA-EPOCH-R) и среднеинтенсивную аллогенную трансплантацию стволовых клеток от 8/8 HLA-подобранного неродственного донора. После аллогенной трансплантации стволовых клеток и до получения CAR+ Т-клеток, пациент показал 100% донорский химеризм во всех линиях крови, прекратил получение иммуносупрессивной терапии и не имел ответа «трансплантат против хозяина» (GVHD). До введения CAR+ Т-клеток пациент имел поражение периаурикулярной массы и височной доли, наблюдаемое с использованием эмиссионной позитронной томографии и компьютерной томографии (PET-CT) (ФИГ. 6B) и подтвержденное магнитно-резонансной томографией (MRI) (ФИГ. 6D).
[0842] После получения анти-CD19 лечения клетками CAR-T пациент достиг CR через 28 дней после вливания, как показано PET-CT (ФИГ. 6C) и MRI мозга (ФИГ. 6E), без наблюдаемых признаков нейротоксичности или CRS. Через три месяца после вливания клеток CAR-T, у этого пациента отмечали рецидив периаурикулярной массы (ФИГ. 6F) и проводили инцизионную биопсию. Как показано на ФИГ. 6А, после биопсии видимая опухоль отступила без дальнейшей терапии. Фармакокинетический анализ показал выраженный повторный рост CAR+ Т-клеток в периферической крови (до уровня выше, чем начальный наблюдаемый рост, с пиковыми уровнями, наблюдаемыми приблизительно через 113 дней после вливания), который совпал с регрессом опухоли. Пациент затем достиг второго CR, подтвержденного повторной PET-CT через один месяц после биопсии (ФИГ. 6G), и оставался в CR через 6 месяцев после вливания клеток CAR-T. Дальнейшая оценка пациента показала, что ответ ЦНС был длительным, и пациент оставался в CR в 12 месяцев.
[0843] Результаты у пациента, получавшего биопсию, сопровождаемую наблюдаемым повторным ростом CAR+ Т-клеток, согласовывались с заключением, что повторный рост и активация CAR+T клеток могут инициироваться in vivo после сокращения или потери функциональных или активных CAR+ Т-клеток и/или рецидива после противоопухолевого отета на CAR-T клеточную терапию. Далее, после повторного роста in vivo после начального вливания CAR+ Т-клеток, CAR+ Т-клетки могут повторно проявить противоопухолевую активность. Этот результат подтверждает, что Повторный рост и активация CAR+ Т-клеток могут быть вызваны in vivo и что способы реактивации CAR+ Т-клеток может дополнительно увеличить их эффективность.
[0844] Полные ответы у двух пациентов DLBCL с участием ЦНС наблюдались без развития какой-либо степени нейротоксичности. Эти результаты согласовывались с наблюдением, что CAR+ Т-клетки согласно вариантам осуществления изобретения способны проникать в ЦНС и проявлять эффекторную функцию, чтобы уменьшить или уничтожить опухоли ЦНС, не увеличивая или существенно не увеличивая риск токсичности, такой как нейротоксичность. В других исследованиях, среди пациентов, получающих анти-CD19 лечение CAR Т-клетками, никакой явной корреляции не наблюдалось между уровнем нейротоксичности и наличием лейкоза ЦНС в мозге (который, по наблюдениям, ответил на такую терапию CAR Т-клетками). Таким образом, тогда как нейротоксичность может иметь место в некоторых контекстах после лечения терапиями CAR-T, такая нейротоксичность не обязательно является результатом целевой экспрессии в мозге или активности CAR Т-клеток в ЦНС, и может не быть следствием токсичности «на мишени» CAR+ Т-клеток.
Пример 1.C,2
[0845] Пример 1.C,2 описывает результаты на основе анализа в Примере 1.А.2 и 1.B,2.
[0846] До момента времени в Примере 1.C,2, 68 пациентов в полном контингенте DLBCL были оценены в отношении ответа. Для полного или объективного ответа (OR), 3-месячная и 6-месячная частоты объективного ответа составляли 75% (51/68), 49% (27/55) и 40% (14/35), соответственно. Частота полного ответа (CR), 3-месячный уровень CR и 6-месячный уровень CR, составляли 56% (38/68), 40% (22/55) и 37% (13/35), соответственно. Тенденция к улучшенной частоте ответа в 3 месяца наблюдалась у пациентов, получающих лечение в DL2, по сравнению с DL1: 63% (12/19; 95% CI 38, 84) по сравнению с 40% (12/30; 95% CI 23, 59) для ОРРА с p=0,148, и 58% (11/19; 95% CI 34, 80) по сравнению с 27% (8/30; 95% Ки: 12, 46) для CR с p=0,0385. Среди 16 пациентов с лимфомой double/triple hit ОРР составлял 81%, и 3-месячный уровень CR составлял 60%.
[0847] В основном контингенте (n=49 для момента времени в Примере 1.C,2), OR, 3-месячные и 6-месячные частоты OR составляли 84% (41/49), 65% (26/40) и 57% (13/23), соответственно. Уровень CR, 3-месячный уровень CR и 6-месячный уровень CR составляли 61% (30/49), 53% (21/40) и 52% (12/23), соответственно. Наблюдалась подобная тенденция к улучшенному длительному ОРРЕ и CR в 3 месяца в более высоких дозах. В частности, для пациентов в основном контингенте, которым вводили DL2, 3-месячный ОРР составлял 80% (12/15; 95% CI 52, 96), и 3-месячный CR составлял 73% (11/15; 95% CI 45, 92), по сравнению с 3-месячным ОРР и CR 52% (11/21; 95% CI 30, 74) и 33% (7/21; 95% CI 15, 57) в основном контингенте пациентов, получавших DL1, с p=0,159 и p=0,0409, соответственно. Среди пациентов в основном контингенте, получавших DL2, и с 3-месячным наблюдением (n=15), 3-месячный ОРР составлял 80%, и 3-месячный CR составлял 73%.
[0848] Средний DOR в полном контингенте и основном контингенте в этот момент времени в 1.C,2 составлял 5,0 и 9,2 месяцев, соответственно; средняя продолжительность CR составляла 9,2 месяцев в полном контингенте. Средняя продолжительность CR не была достигнута в основном контингенте. Средняя полная выживаемость (OS) составляла 13,7 месяцев в полном контингенте и не была достигнута в основном контингенте. 6-месячный OS составлял 75% в полном контингенте со средним наблюдением 5,8 месяцев. 6-месячный OS составлял 88% в основном контингенте, с медианным наблюдением в течение 5,6 месяцев.
D. Оценка CAR+ Т-клеток в крови
[0849] На основе данных от момента времени, описанного в Примере 1.А.1, 1.B,1 и 1.C,1, фармакокинетический анализ проводили для оценки чисел CAR+ Т-клеток в периферической крови в различные моменты времени после лечения. Были проанализированы результаты пятидесяти пяти (55) пациентов, оцененных в момент времени в Примере 1.А.1 в контингенте DLBCL, и четырех (4) пациентов (оцененных в тот же самый момент времени) в контингенте мантийноклеточной лимфомы (MCL), как описано в Примере 2 ниже. Фармакокинетические (PK) измерения осуществляли с помощью подтвержденной потоковой цитометрии для детекции маркера, экспрессируемого в конструкции CAR, и количественных тестов, основанных на ПЦР, для детекции интеграции конструкции CAR. В-клеточная аплазия была оценена потоковой цитометрией с помощью антител анти-CD19. Как показано на ФИГ. 5А, CD4+ и CD8+ CAR-экспрессирующие клетки, при измерении числа клеток/мкл крови (средние ± квартили), выстраиваемого по логарифмической шкале, были обнаружены всюду по курсу оценки на обоих введенных уровнях дозы. Пациенты, получающие DL2 относительно DL1, имели более высокую среднюю AUC0-28 и среднюю AUC0-28 для субпопуляций CD3+/CAR+, CD4+/CAR+ и CD8+/CAR+ Т-клеток в периферической крови (AUC0-28: DL2 по сравнению с DL1 составляла 1836 по сравнению с 461, 350 по сравнению с 182, и 1628 по сравнению с 114, для CD3+, CD4+ и CD8+, соответственно; p <0,05 для CD8+; AUC0-28: DL2 по сравнению с DL1 составляла 99,8 по сравнению с 27,9, 15,1 по сравнению с 5,2 и 73,1 по сравнению с 5,5 клеток/мкл, соответственно). Среднее время до максимального роста CD3+ CAR+ Т-клеток составляло 15 дней (диапазон 8-29) и не различалось между уровнями дозы. CD4+ и CD8+ CAR-экспрессирующие Т-клетки, локализованные в костном мозге на относительно схожих уровнях.
[0850] Увеличенная средняя область под кривой (AUC) (числа CD8+ CAR+ Т-клеток в течение времени в крови) наблюдалась среди пациентов, которым вводили более высокий уровень дозы, по сравнению с более низким уровнем дозы, без наблюдаемого увеличения токсичности. Более высокие пики экспозиции CD8+/CAR+ Т-клеток наблюдались у отвечающих пациентов (CR/PR), чем у неотвечающих пациентов (PD); персистирование клеток за время оценки, включая до 3 и 6 месяцев, наблюдалось даже у пациентов, заболевание которых прогрессировало (ФИГ. 5B). Средняя AUC0-28 и средняя AUC0-28 CD8+ CAR+ Т-клеток были выше у отвечающих пациентов и с длительным ответом в месяц 3 (CD8+ Cmax медиана = 20,8 vs. 5,5; CD8+ AUC0-28 медиана = 235 vs. 55 в CR/PR в месяц 3 vs. PD в месяц 3). Среди пациентов, оцениваемых в отношении персистирования CAR Т-клеток, 90% и 93% из 29 пациентов имели поддающиеся обнаружению CD8+ и CD4+ CAR+ Т-клетки, соответственно, в месяц 3; 63% и 58% из 19 пациентов имели поддающиеся обнаружению CD8+ и CD4+ CAR+ Т-клетки, соответственно, в месяц 6. В месяцы 3 и 6 никаких статистически значимых различий в персистировании CAR+ Т-клеток на наблюдалось между пациентами с длительным ответом или рецидивом. CAR+ Т-клетки могли быть детектированы во время рецидива у 89% из 11 пациентов с PK, даже при том, что В-клеточная аплазия (<1 клеток/мкл) была продемонстрирована почти у всех пациентов 97% (34/35) в месяц 3, и 100% (24/24) в месяц 6.
[0851] Более высокие AUC0-28 и AUC0-28 в DL2 по сравнению с DL1, по наблюдениям, не были связаны с увеличенным CRS или NT. Для любого NT или для > Степени 2 CRS, средние AUC CD4+/CAR+ и CD8+/CAR+ Т-клеток были в 5-10 раз и 3-5 раз выше, соответственно, чем средняя AUC для DL2. Более высокая серьезность заболевания и начальные уровни воспалительных цитокинов, по наблюдениям, были связаны с более высокими пиковыми уровнями CAR+ Т-клеток, более высокими пиковыми уровнями цитокина и более высокими уровнями CRS и NT. Результаты согласовывались с заключением, что более высокая AUC0-28 и средняя AUC0-28 в DL2 не увеличивали CRS или NT.
[0852] Результаты согласовывались с заключением, что лечение приводило к длительной экспозиции и персистированию генно-инженерных клеток даже у пациентов с плохими ответами. В некоторых вариантах осуществления используются комбинированные подходы, такие как введение модулятора иммунной контрольной точки или другого иммунного модулирующего агента, например, после рецидива или прогрессии заболевания, в момент времени, в который генно-инженерные клетки сохраняются у пациента, например, при измерении уровней клеток в периферической крови. В некоторых аспектах клетки, персистирующие в течение длительного периода, повторно растут или становятся активированными и/или показывают противоопухолевую функцию, после введения другого агента или средства для лечения. Более высокие средние числа CD4+ и CD8+ CAR+ Т-клеток обычно наблюдались в течение времени в крови пациентов, у которых развилась нейротоксичность (ФИГ. 5C). Результаты показали что CAR+ Т-клетки показали рост и персистирование, длительность ответа в 3 месяца, увеличившиеся на более высоких уровнях дозы без увеличенной токсичности. Наблюдались результаты, которые согласовывались с предположением, что высокие пиковые уровни CAR+ Т-клеток и цитокинов в крови могут быть связаны с NT и CRS и могут быть под влиянием базовых факторов пациента. Наблюдалось, что CAR+ Т-клетки присутствовали во время рецидива, указывая, что комбинированные подходы или повторное лечение могут обеспечить определенные преимущества.
E. Аналиты крови и нейротоксичность, CRS и ответ
[0853] Различные аналиты крови после предварительного лечения, включая цитокины, были измерены в сыворотке пациентов (оцененных в момент времени в Примере 1.А.1) до введения CAR+ Т-клеток. Цитокины были измерены с помощью мультиплексного теста цитокинов. Потенциальные корреляции к риску развития нейротоксичности были оценены с помощью статистического анализа на основе однофакторных непараметрических анализов.
[0854] ФИГ. 7 показывает средние уровни оцененных аналитов в единицах (LDH, Ед/л; ферритин, нг/мл; CRP, мг/л; цитокины, пг/мл) у пациентов, у которых не развивалась нейротоксичность по сравнению с пациентами, у которых развивалась нейротоксичность после терапии CAR+ Т-клетками. Уровни некоторых аналитов крови, включая LDH, Ферритин, CRP, IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β, по наблюдениям, были связаны с уровнем риска развития нейротоксичности (Wilcoxon p значения <0,05 без учета множественности сравнения). В частности, результаты согласовывались с заключением, что уровни LDH после предварительного лечения, который в некоторых вариантах осуществления является суррогатом серьезности заболевания, могут быть полезны для потенциальной оценки степени риска нейротоксичности и/или адаптированного к риску дозирования или регулирования лечения определенных пациентов. Кроме того, опухолевая нагрузка, измеренная перед введением композиции CAR-T клеток, коррелировала (Spearman p значения <0,05) с риском развития нейротоксичности. В некоторых аспектах уровни LDH могут быть оценены индивидуально и/или в сочетании с другим параметром предварительного лечения, таким как другая мера или индикатор серьезности заболевания, такая как объемное измерение опухоли, такое как сумма размеров продукта (SPD) или другое основанное на CT или основанное на MRI объемное измерение серьезности заболевания. В некоторых аспектах оценивали один или более параметров, репрезентативных для серьезности заболевания, и в некоторых контекстах может указать наличие, отсутствие или уровень риска развития нейротоксичности после Т-клеточной терапии. В некоторых аспектах один или более параметров включают LDH и/или объемное измерение опухоли.
[0855] В дополнительном анализе пятьдесят пять (55) пациентов в контингенте DLBCL в момент времени в Примере 1.А.1 и четыре (4) пациента с мантийноклеточной лимфомой (MCL), описанной в Примере 2 ниже, были включены в анализ для корреляции с оценками безопасности. У 59 пациентов, оцененных на безопасность, CRS наблюдался у 32% (30% Степени 1-2, 0% Степени 3, 2% Степени 4); NT наблюдалась у 20% (5% Степени 1-2, 10% Степени 3, 5% Степени 4). Уровень дозы не коррелировал с CRS или NT (p=0,565 и p=1,00, соответственно). Факторы пациента, коррелирующие с любыми степенями CRS и NT, представляли собой плохое общее состояние (например, Статус ECOG 2) (p=0,03) и более высокую серьезность заболевания (p <0,05), при измерении суммы диаметров продуктов (SPD) на основе результатов отображения. Клинические лабораторные параметры до вливания CAR+ Т-клеток и измерения цитокинов до вливания CAR+ Т-клеток, которые, по наблюдениям, были связаны с возникновением любой степени NT, включали более высокий сывороточный LDH, ферритин, и CRP, и более высокий плазменный IL-6, IL-8, IL-10, TNF-α, IFN-α2, MCP-1 и MIP-1β (p <0,05 для каждого). Более высокие плазменные уровни IL-8, IL-10 и CXCL10 до вливания CAR+ Т-клеток были также связаны с NT Степени 3-4 (p <0,05 для каждого).
[0856] Из 54 пациентов в контингенте DLBCL, оцененных в отношении ответа, более высокие оценки ECOG и DLBCL, трансформированные из CLL или MZL, коррелировали с более низкой длительностью ответа в месяц 3 (p=0,02 для обоих). Параметры до вливания CAR+ Т-клеток, связанные с лучшим ОРРОМ, включали нижние значения ферритина, LDH, CXCL10, G-CSF и IL-10, и связанные с длительным ответом в 3 месяца включали более низкий ферритин, CRP, LDH, CXCL10, IL-8, IL-10, IL-15, MCP-1, MIP-1β, TNF-α, и более высокий гемоглобин и альбумин до вливания CAR+ T (p <0,05 для каждого).
[0857] В некоторых случаях образец афереза и композицию CAR+ Т-клеток для введения были оценены и коррелировали с клиническими результатами. Результаты показали, что субпопуляции Т-клеток памяти и функциональность Т-клеток могут коррелировать с определенными клиническими результатами.
[0858] Результаты показали, что некоторые начальные характеристики пациента, включая воспалительное состояние и высокую опухолевую нагрузку до лечения, могут быть полезны для идентификации пациентов с риском увеличенной токсичности после введения CAR-экспрессирующих Т-клеток. Низкая опухолевая нагрузка и низкое воспалительное состояние, по наблюдениям, были связаны с улучшенным профилем токсичности и лучшей длительностью ответа. Эти результаты подтверждают, что лечение пациентов ранее в ходе терапии и/или оценки группы клинических и лабораторных биомаркеров в отношении риска стратифицирует пациентов в отношении потенциального раннего вмешательства, может снизить риск токсичности и усилить длительность ответа.
Пример 2: Введение CAR-экспрессирующих клеток анти-CD19 пациентам с мантийноклеточной лимфомой (MCL)
[0859] Терапевтические композиции CAR+ Т-клеток, содержащие аутогенные Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфичный для CD19, сгенерированные, как описано в Примере 1, вводили четырем (4) индивидуумам с мантийноклеточной лимфомой (MCL), у которых 1 линия терапии оказалась неудачной. Сохраненные замораживанием композиции клеток оттаивали перед внутривенным введением. Терапевтическую композицию Т-клеток вводят как определенный композиционный клеточный продукт с составленными популяциями генно-инженерных CD4+ и CD8+ CAR+ Т-клеток, полученных от того же пациента, вводимый в целевом отношении приблизительно 1:1. Пациентам вводили дозу CAR-экспрессирующих Т-клеток (как разделенная доза CD4+ и CD8+ CAR-экспрессирующих Т-клеток) в единственной дозе уровня 1 дозы (DL1), содержащей 5x107 CAR-экспрессирующих Т-клеток. Начиная в третий (3) день до вливания CAR+ Т-клеток, пациенты получали противолимфоцитарную химиотерапию флударабином (flu, 30 мг/м2) и циклофосфамидом (Cy, 300 мг/м2).
[0860] Пациентов проверяли в отношении ответа и токсичности, как описано в Примере 1. Никакой CRS или нейротоксичность не наблюдалось ни у одного из пациентов. Из 4 пациентов, получающих лечение, два (2) пациента достигли PR (не длительного), и у двух (2) пациентов было прогрессирующее заболевание.
Пример 3: дальнейшая оценка ответа, безопасности, фармакокинетики, фармакодинамики и аналитов крови у пациентов с рецидивирующей и рефрактерной неходжкинской лимфомой (NHL) после введения Анти-CD19 CAR-экспрессирующих клеток
[0861] Результаты ответа, результаты безопасности, фармакокинетические и параметры фармакодинамики и аналиты крови, были оценены у пациентов в последующий момент времени в клиническом исследовании, описанном в Примере 1 выше.
A. Пациенты и лечение
[0862] Анализ в этот момент времени, представленный в этом примере, основывается на оценке в общей сложности 91 пациента в полном контингенте DLBCL (88 (65 от основного контингента), оцененных в отношении ответа, и 91 (67 от основного контингента), оцененных в отношении безопасности), которым вводят анти-CD19 CAR-экспрессирующие клетки. Полный контингент включал DLBCL, NOS de novo и трансформированную из любой вялотекущей лимфомы, ECOG 0-2; основной контингент для анализа включал пациентов, имеющих DLBCL, NOS и трансформированную из фолликулярной лимфомы (tFL) или В-клеточной лимфомы высокой степени зло качественности и с Eastern Cooperative Oncology Group Performance Status (ECOG PS) 0 или 1. Приблизительно 90% получавших лечение пациентов в основном контингенте имели по меньшей мере 1 признак заболевания низкого риска, прогностический для короткого среднего полного выживания (OS) 3-6 месяцев, такой как double/triple-hit экспрессоры, первичное рефрактерное заболевание, рефрактерное к 2 или более линиям терапии, никогда не достигали CR, или никогда не получали трансплантацию аутогенных стволовых клеток (ASCT). В некоторых вариантах осуществления контингенту пациентов, имеющих диффузную крупноклеточную В-клеточную лимфому (DLBCL), не охарактеризованную иным образом (NOS; de novo и трансформированную из фолликулярной лимфомы tFL)), или высокодифференцированную В-клеточную лимфому, с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL, и исключая пациентов с оценкой ECOG 2 или пациентов, которые получили предшествующую трансплантацию гематопоэтических стволовых клеток (HSCT), вводили композиции CAR-T, как описано здесь. В некоторых вариантах осуществления пациентам основного контингента вводили анти-CD19 CAR+ Т-клетки в единственной дозе DL2 (1x108 общих CAR-экспрессирующих Т-клеток).
[0863] В этот момент времени в общей сложности 140 пациентов подвергали лейкаферезу, из которых 10 ждали приготовления композиции, 2 вышли из исследования до готовности композиции, и для 2 композиции были недоступны. Еще из 18 пациентов, продукты которых были доступны, 4 ждали лечения, 4 вышли из исследования, и у 10 развилось прогрессирующее заболевание, или они умерли. В общей сложности 108 пациентам вводили анти-CD19 CAR-экспрессирующие клетки, из которых 6 не были оценены и 11 получали несоответствующие анти-CD19 CAR-экспрессирующие клетки (композиции не всегда соответствовали определенным техническим требованиям, но считались безопасными для введения). Пациенты получали DL1 (n=45), двойную доза DL1 (n=6) или DL2 (n=40). Шести (6) пациентам с мантийноклеточной лимфомой (MCL) вводили CAR+ клетки в DL1 (пять получили соответствующий продукт, один получил несоответствующий продукт), и пять (5) прошел все 28 дней наблюдения. У одного пациента MCL развился CRS, и ни один не получил тоцилизумаб или дексаметазон. Продукт был доступен для 98% пациентов, подвергнутых аферезу (126/128) в контингенте DLBCL.
[0864] Пациенты в этот момент времени включали 5 пациентов, получавших лечение в амбулаторном режиме (включая четырех (4) пациентов, получавших DL1, одного (1), получавшего DL2; четыре (4) из которых были включены в основной контингент). Для пациентов, получающих лечение в амбулаторном режиме, средний возраст составил 57 лет (диапазон 26-61), 3 имел DLBCL, NOS, 1 имел tFL, и 1 имел PMBCL. Все пять (5) пациентов имели оценки ECOG 0 или 1. Данные по амбулаторным результатам включали результаты для трех (3) дополнительных пациентов, получающих лечение в амбулаторном режиме (общее количество восемь (8) пациентов) и чьи данные стали доступными после момента времени для анализа в этом Примере.
[0865] Демографические и базовые характеристики полного и основного контингента пациентов в моменте времени представлены в Таблице E5.
[0866]
(n=91)
(n=67)
a При инициировании испытания, включенная в DLBCL, гистология NOS; на основе новых критериев WHO (Swerdlow et al., (2016) Blood 127(20):2375-2390), теперь считаются “высокодифференцированной В-клеточной лимфомой, с перестановками MYC и BCL2 и/или BCL6 с гистологией DLBCL (double/triple hit)».
b SD или PD для последнего включающего химиотерапию режима или рецидива < спустя 12 месяцев после аутогенных SCT.
B. Результаты Безопасности и Ответа после лечения
[0867] Как показано в Таблице E6, частота объективного ответа (ORR) составляла 74%, включая 52% пациентов, которые показали полный ответ (CR). Уровень любой степени синдрома высвобождения цитокинов (CRS) составлял 35% с 1% тяжелого CRS; и уровень любой степени нейротоксичности (NT) составлял 19% с 1% тяжелой NT.
а Четыре пациента, получавших лечение на DL1D (уровень дозы 1, схема с двумя дозами) с подобными результатами.
b Включает пациентов с событием PD, смерти или 28-дневных повторных исследований. Один пациент не имел повторных исследований.
c Включает всех пациентов, которые получили по меньшей мере одну дозу продукта CAR-экспрессирующих клеток за 28 дней до даты сбора данных или умерли.
[0868] Как показано в Таблице E7, высокие показатели ответа и низкие - тяжелой токсичности наблюдали в полной популяции DLBCL.
а Включает пациентов с событием PD, смерти или 28-дневных повторных исследований. Один пациент не имел повторных исследований.
b Включает всех пациентов, которые получили по меньшей мере одну дозу CAR+ экспрессирующих клеток за 28 дней до даты регистрации данных или умерли.
[0869] Как показано в Таблице E8, высокий показатель ответа и дозозависимого ответа наблюдался в основном контингенте пациентов.
а Четыре пациенты (CORE) получали лечение на DL1D с подобными результатами.
b Включает пациентов с событием PD, смерти или 28-дневных повторных исследований. Один пациент не имел повторных исследований.
c знаменатель представляет собой число пациентов, получивших CAR+ клетки ≥ 3 месяца назад, до даты сбора данных, с оценкой эффективности в месяц 3 или перед оценкой PD или смертью.
d знаменатель представляет собой число пациентов, получивших CAR+ клетки ≥ 6 месяцев назад, до даты снимка данных, с оценкой эффективности в месяц 6 или перд оценкой PD или смертью.
[0870] Трехмесячные частоты объективного ответа (ORR) среди различных подгрупп пациентов в подгруппе высокого риска DLBCL, включавших всех пациентов DLBCL, получавших лечение на всех уровнях доз в основном контингенте, показаны на ФИГ. 22. Результаты показали высокий длительный ОРР в подгруппе высокого риска DLBCL.
[0871] Результаты для продолжительности ответа (DOR) и полного выживания (сгруппированные по лучшему полному ответу (неотвечающие, CR/PR, CR и/или PR)) показаны для полного контингента и основного контингента пациентов на ФИГ. 23A-23D. Результаты также показали, что 80% (16/20) пациентов с CR в 3 месяца остается в состоянии CR в 6 месяцев, и 92% (11/12) пациентов с ответом (CR или PR) в 6 месяцев продолжают показывать ответ в долгосрочной перспективе.
[0872] ФИГ. 24 изображает процент пациентов в этот момент времени, которые, по наблюдениям, испытывали лабораторные патологии и нежелательные явления, возникшие в ходе лечения (TEAEs) (данные для 5 пациентов с MCL, получавшие лечение соответствующим продуктом в DL1 по меньшей мере с 28 дней наблюдения, не включены). В дополнение к TEAE, показанным на ФИГ. 24, следующие термины событий наблюдались на Уровне 3-4 у ≥ 5% пациентов: энцефалопатия (8%), (5%) Панцитопения и Лихорадочная нейтропения (7%). У восьми пациентов (9%) была инфузионная токсичность, определенная как AE в день введения, соответствующий введению CAR+ клеток, включая покраснение лица, головную боль, повышение температуры, гипертермию, озноб, дрожь, рвоту, высыпание, крапивницу, зуд, гипотензию, хрипы, бронхоспазм, одышку, тошноту, рвоту, боль в спине, кашель и связанную с вливанием реакцию. События включали озноб (2), гипертермию (5), покраснение лица (1), головную боль (1), гипотензию (1), связанную с вливанием реакцию (1), высыпание (1), зуд (1) и рвоту (1), с 6 событиями степени 1, 1 степени 2 (озноб) и 1 степени 3 (гипотензия). TEAE в основном контингенте не отличался существенно от такового в полном контингенте. Наиболее распространенные родственные TEAE у пациентов, получающих лечение в группе амбулаторного лечения, представляли собой CRS, гипотензию, рвоту, анемию и одышку.
[0873] Таблица E9 представляет TEAE и нейротоксичность, имеющие место у 25 процентов или более пациентов в полном или основном контингенте пациентов, которые получили DL1S и DL2S. Никакого очевидного отношения доза-токсичность не наблюдалось в популяции DLBCL.
(N=91)
(n=67)
(n=34)
(n=29)
а Включает 4 пациентов, получавших лечение на уровне дозы 1, в режиме с двумя дозами.
b Лабораторные аномалии.
[0874] ФИГ. 25 изображает число и процент пациентов, которые, по наблюдениям, имели CRS и/или NT в различные моменты времени после введения CAR+ клеток. В этой оценке среднее время к началу события CRS или NT, по наблюдениям, составляло 5 (диапазон 1-14) или 10 (диапазон 3-23) дней, соответственно. В течение первых 72 часов после введения CAR+ клеток, у 1 пациента была NT (степени 1), и только 14% (13 из 91) имели CRS (7 степени 1; 6 степени 2). Средняя продолжительность (Q1, Q3) CRS или NT равнялась 5 (4, 8) или 10,5 (7, 19) дней, соответственно. NT предшествовала CRS в 12 из 17 случаев (71%). Все поддающиеся оценке события NT были устранены во время анализа кроме одного тремора степени 1, и 2 пациента умерли от прогрессирующего заболевания с продолжающейся NT (на основе базы данных безопасности событий, включая дополнительных пациентов, проанализированных после момента времени проведения анализа, описанного в этом Примере).
[0875] В полном контингенте (n=91) выбранным пациентам с началом CRS или NT вводили антицитокиновую терапию тоцилизумабом и/или дексаметазоном следующим образом: один только Тоцилизумаб, 4% (n=4); один только Дексаметазон, 9% (n=8); Тоцилизумаб и дексаметазон, 8% (n=7). Среднее число доз дексаметазона составляло 6 (диапазон, 2-99); и среднее число доз тоцилизумаба составляло 1 (диапазон, 1-3).
[0876] Таблица E10 показывает результаты токсичности у пациентов в основном контингенте, получивших единственную дозу в DL1 или DL2. Никакие смертельные случаи не произошли от CRS или NT. Среднее время к началу CRS составляло 5 дней (диапазон, 2-14), и для NT оно составляло 11,5 дней (диапазон, 5-23). В основном контингенте 13% (n=9) получили тоцилизумаб, и 18% (n=12) получили дексаметазон для облегчения токсичности. Восемнадцать процентов пациентов (12 из 67) показали термины нейротоксичности, соответствующие энцефалопатии, включая энцефалопатию (13%), 6% (4 из 67) имели афазию, и 3% (2 из 67) имели приступы. В Таблице E10, число пациентов или % общих пациентов (круглые скобки), показывающие обозначенный результат токсичности, показано на всех уровнях дозы или специфично у пациентов, которым вводили DL1 или DL2. Также показаны в скобках верхний и нижний 95% доверительный интервал.
n=67
n=34
n=29
а Четыре пациента, получающих лечение на DL1D с подобными результатами.
b Включает состояние спутанности сознания, энцефалопатию, афазию, атаксию, мозжечковый синдром, делирий, сниженный уровень сознания, головокружение, уплощение эмоций, ухудшенную зрительно-моторную координацию, ухудшение памяти, тремор, возбуждение, нарушение внимания, дизартрию, изменения психического статуса, мышечную слабость, судороги, сонливость и недержание мочи.
[0877] Среди двенадцати (12) пациентов, получающих несоответствующие продукты, 10 в DL1 и 2 в DL2, все проходили 28-дневное наблюдение. CRS наблюдался у 33% пациентов (4/12), и NT не наблюдалась ни у одного из пациентов. Два пациента получили тоцилизумаб, и 3 пациента получили дексаметазон. Показатели токсичности были сопоставимы с наблюдаемыми у большего контингента пациентов, которым вводили соответствующий продукт. У пациентов, получающих несоответствующие продукты, фармакокинетическая (PK) экспансия была выше у пациентов с CRS/NT, пациентов с высокой опухолевой нагрузкой или уровнями LDH.
C. Оценка амбулаторного введения
[0878] Данные для в общей сложности восьми (8) пациентов были оценены в этот момент времени, когда они получали лечение в амбулаторном режиме (средний возраст 58,5 и ECOG 0 или 1) на множественных клинических базах, включая 3 пациента, данные которых были доступны после момента времени, в который их анализировали в целях этого Примера. Средняя продолжительность госпитализации составляла 15,6 дней для пациентов, получающих лечение в стационарном режиме (SD 9,6, n=86) и 9,3 дней для пациентов, получающих лечение в амбулаторном режиме (SD 11,9, n=8). 40%-е сокращение продолжительности госпитализации наблюдалось у пациентов, получающих лечение в амбулаторном режиме. Среднее число дней до госпитализации после амбулаторного введения CAR+ Т-клеток составило 5 дней (диапазон: 4-22). Ни один не потребовал допуска к палате интенсивной терапии (ICU) после амбулаторного введения.
[0879] Среди тех из 8 пациентов, получающих лечение в амбулаторном режиме, с более чем 28-дневным наблюдением после введения, 1 остался на амбулаторным режиме в течение всей продолжительности ограничивающего дозу периода токсичности. Семь (7) пациентов были допущены с повышением температуры (1 в день исследования 4, остальные в день исследования ≥ 5), 6 пациентов были допущены с CRS (4 степени 1, 2 степени 2) и 2 пациента с NT степени 1. Ни один из пациентов не испытывал тяжелый CRS или NT. Один (1) пациент получал лечение тоцилизумабом без дексаметазона для CRS (степени 2), и никто из пациентов не получал лечение дексаметазоном для CRS или NT. Одного пациента допустили спустя 3 дня после введения CAR+ Т-клетки.
[0880] Среди 91 пациентов, получавших лечение в стационарном и амбулаторном режиме, 11 пациентов (12%) потребовали допуска ICU для контроля токсичности; 8 пациентов (9%) потребовали допуска ICU для контроля CRS или NT; 2 пациента (2%) потребовали допуска ICU для контроля острых респираторных событий (один связанный с введением CAR+ Т-клеток, один несвязанный). Шесть (6) пациентов (6%) были интубированы (на основе базы данных безопасности событий, включая проанализированных после момента времени анализа дополнительных пациентов, описанного в этом Примере; n=94); 7 пациентов (7%) получили вазопрессоры (на основе базы данных безопасности событий, определенных как демонстрирующие гипотензию за первые 28 дней после введения CAR+ Т-клеток, в оценке TEAE); и 2 пациента (2%) перенесли гемофильтрацию (на основе базы данных безопасности событий). Результаты показали, что очень немногие из пациентов потребовали уровня ICU и связанных процедур. Результаты подтверждают выполнимость амбулаторного введения с безопасным контролем токсичности в амбулаторном режиме, подходящем образованием и амбулаторным контролем.
[0881] Оценка амбулаторного введения подтвердила выполнимость безопасного амбулаторного введения. 30% пациентов не были повторно допущены.
D. Фармакокинетическая оценка
[0882] Число CAR+ Т-клеток в периферической крови и костном мозге в моменты времени перед введением (предварительная обработка или предварительная противолимфоцитарная химиотерапия (LDC)) и последующее лечение в различные моменты времени (с днем введения как день 1) у 87 пациентов в контингенте DLBCL с оцениваемой PK, потоковой цитометрией с использованием антитела, специфичного для усеченного рецептора, используемого в качестве суррогатного маркера и количественной полимеразной цепной реакцией (кПЦР) с использованием праймеров, специфичных для посттранскрипционного регуляторного элемента вируса гепатита сурков (WPRE), присутствующего в векторе, кодирующем химерный антигенный рецептор (CAR). Оценивали область под кривой с числами построения на микролитр для обозначенной популяции CAR+ клеток между днями 0 и 28 (AUC0-28) и максимальную или пиковую концентрацию CAR+ клеток в крови (AUC0-28; CAR+ клеток/мкл крови). В-клеточная аплазия была оценена в периферической крови потоковой цитометрией путем окрашивания CD19. Цитокины были измерены с помощью мультиплексного цитокинового теста. Для анализа безопасности были объединены данные от всех пациентов, получающих различные уровни дозы. Для анализа ответа данные были стратифицированы по уровню дозы. Статистический анализ был двухсторонним без учета множественности сравнения.
[0883] ФИГ. 9A показывает обнаруженные числа CAR Т-клеток на микролитр крови в различные обозначенные моменты времени при оценке потоковой цитометрией или кПЦР. ФИГ. 9B показывает CAR+ клетки на микролитр крови по сравнению с микролитром костного мозга в день 11±3. Как показано на ФИГ. 9 А, уровни CAR-экспрессирующих клеток в образцах от пациентов наблюдали как с помощью основанных на потоковой цитометрии тестов, так и с помощью кПЦР тестов. Как показано на ФИГ. 9B, все пациенты (n=86 и 85 для потоковой цитометрии и кПЦР, соответственно, исключая одного пациента, не имевшего в наличии результатов потоковой цитометрии, и 2 пациентов, не имевших в наличии результатов кПЦР) с оцененными результатами PK, показали детектируемые числа CAR-экспрессирующих клеток в крови и костном мозге. Результаты согласовывались с наблюдением, что CAR+ Т-клетки распространялись похожим образом в костным мозге и крови.
[0884] Уровни в течение времени CD4+ и CD8+ CAR-экспрессирующих клеток (при оценке AUC0-28 и AUC0-28) сравнивали в различных подгруппах пациентов, получающих уровень 1 дозы (DL1): диффузная крупноклеточная В-клеточная лимфома de novo (DLBCL, NOS) или трансформированная из фолликулярной лимфомы (tFL) (ОСНОВНОЙ; N=32), DLBCL, трансформированная из лимфомы маргинальной зоны или хронического лимфолейкоза (tMZL/tCLL; N=4), или мантийноклеточная лимфома (MCL; N=5), которые получили CAR-экспрессирующие Т-клетки в DL1. Как показано на ФИГ. 10А и 10B, AUC0-28 и AUC0-28 варьировали среди пациентов в различных подгруппах заболеваний, с ростом CD4+ и CD8+ CAR-экспрессирующих клеток, имевшим тенденцию к понижению в НЕ-ОСНОВНЫХ субпопуляциях. PMBCL (n=2) и FL3B (n=1) не показаны вследствие ограниченного числа пациентов. Рост у пациентов, получающих DL2, был подобным таковому у пациентов, получающих DL1.
E. Фармакокинетическая оценка уровня дозы
[0885] AUC0-28 и AUC0-28 для CD3+, CD4+ и CD8+ CAR-экспрессирующих клеток были также сравнены для пациентов, получавших уровень 1 дозы (DL1; n=32) и тех, которые получают уровень 2 дозы (DL2; n=27), в основном контингенте (пациенты с DLBCL, NOS или В-клеточная лимфомой высокой степени злокачественности (double/triple hit); N=59). Как показано на ФИГ. 11А и 11B и в Таблице E11, более высокая средняя AUC0-28 наблюдалась для CD3+, CD4+ и CD8+ CAR-экспрессирующих клеток наблюдалась у пациентов, получивших DL2, по сравнению с пациентами, которые получили DL1. Точно так же тенденция более высокого роста у пациентов, которые получили DL2, наблюдалась в полном контингенте DLBCL. Более высокая длительность ответа (DOR) в 3 месяца также наблюдалась среди пациентов, которые получили DL2, по сравнению с теми, которые получают DL1, без увеличения токсичности. Среднее время для AUC0-28 (Тмакс) для CD4+ и CD8+ CAR+ клеток было похожим между пациентами, которые получили DL1 и DL2.
[0886] Увеличенное экспонирование CAR+ Т-клеток наблюдалось у DL2 по сравнению с DL1, что соответствует увеличенной длительности ответа без увеличенной токсичности у пациентов DL2.
(n=32)
(n=27)
F. Персистирование
[0887] Персистирование CAR-экспрессирующих клеток и CD19+ В-клеточная аплазия (низкие числа или отсутствие CD19+ В-клеток) были оценены в различные моменты времени у оцениваемых пациентов с DLBCL, которым вводили CAR+ Т-клетки, на основе детектируемых уровней CD3+, CD4+ или CD8+ CAR-экспрессирующих клеток и уровней CD19+ В-клеток, обнаруженных в крови, соответственно. Результаты представлены в Таблице E12. Среди пациентов, оцененных в прогрессии (время прогрессии независимо от BOR; n=37), в среднем 0,17 CD4+ CAR+ клеток/мкл (диапазон, 0-65,5 клеток/мкл) и в среднем 0,15 CD8+ CAR+ клеток/мкл (диапазон, 0-131,8 клеток/мкл) наблюдались в прогрессии. Среди пациентов, оцененных при рецидиве (во время прогрессии после достижения CR) (n=12), в среднем 0,17/мкл (диапазон, 0-35,1 клеток/мкл) CD4+ CAR-экспрессирующие клетки и в среднем 0,20 клеток/мкл (диапазон, 0-131,8 клеток/мкл) CD8+ CAR-экспрессирующих клеток наблюдали при рецидиве. Долгосрочное персистирование CAR-экспрессирующих клеток наблюдалось у 75% оцениваемых пациентов с DLBCL в 12 месяцев. Долгосрочное персистирование В-клеточной аплазии также наблюдалось у 75% пациентов в 12 месяцев, и у пациентов независимо от статуса рецидива. Результаты согласуются с заключением, что анти-CD19 CAR-экспрессирующие клетки показали долгосрочное персистирование у большинства пациентов, и дают основание предложить потенциал для продолжительной борьбы с заболеваниями даже у пациентов с рецидивом.
[0888] Среди пациентов, имевших рецидив, 91,7% (11/12) имели детектируемые CAR-экспрессирующие клетки в крови во время рецидива. Этот результат согласуется с заключением, что комбинированная терапия или другое вмешательство в некоторых вариантах осуществления могут использоваться, чтобы увеличить и/или усилить CAR-экспрессирующие клетки, такие как те, которые могут быть истощены.
(< 1 клеток/мкл),%
G фармакокинетическая оценка и токсичность
[0889] AUC0-28 и AUC0-28 CD4+ и CD8+ CAR-экспрессирующих клеток были также сравнены для пациентов в основном контингенте с любой степенью (в этой оценке, любая из степеней 1-4; никакой степени 5 CRS или NT не наблюдалось) синдрома высвобождения цитокинов (CRS) или нейротоксичности (NT) с пациентами, не оцененными как показывающие степени CRS или NT. Медианная CD4+ CAR+ AUC0-28 (Q1, Q3) равнялась 59 (18, 210) для отсутствия CRS (степени 0; n=43) и 267 (91, 1510) для любого CRS (степени 1-4; n=20) (p=0,001); медианная CD8+ CAR+ AUC0-28 (Q1, Q3) составляла 310 (36, 900) для отсутствия CRS (степени 0; n=43) и 605 (174, 5619) для любого CRS (степени 1-4; n=20) (p=0,021); медианная CD4+ CAR+ AUC0-28 (Q1, Q3) равнялась 71 (23, 244) для отсутствия NT (степени 0; n=50) и 1269 (184, 3057) для любой NT (степени 1-4; n=13) (p=0,003); медианная CD8+ CAR+ AUC0-28 (Q1, Q3) составляла 304 (43, 799) для отсутствия NT (степени 0; n=50) и 2463 (607, 7691) для любой NT (степени 1-4; n=13) (p=0,004). Как описано выше и показано на ФИГ. 12A-12D, более высокие уровни CD4+ и CD8+ CAR-экспрессирующих клеток в течение времени были связаны с CRS и NT.
H. Фармакокинетическая оценка и ответ
[0890] Число пиковых CD3+ CAR+ клеток/мкл (CD3+ AUC0-28), оценивалось в течение времени у пациентов, у которых был лучший полный ответ (BOR) CR, PR или PD. Как показано на ФИГ. 13А и 13B, тенденция к лучшему BOR наблюдалась у пациентов с более высоким ростом с вариабельностью среди пациентов.
I. Фармакокинетическая оценка по аналитам крови и параметрам пациента
[0891] Плазменные уровни цитокинов перед лечением CAR+ Т-клетками (пре-противолимфоцитарная химиотерапия), включая интерлейкин 7 (IL-7), IL-15, макрофагальный воспалительный белок (MIP-1α), были оценены у пациентов, показавших CAR+CD3+ кровь Cmax > 500 CAR+ T клеток/мкл (N=55) по сравнению с пациентами, показавшими CAR+CD3+ кровь Cmax < 500 CAR+ T клеток/мкл (N=7). Как показано на ФИГ. 14А, увеличенные уровни цитокинов плазмы перед лечением CAR+ Т-клетками, по наблюдениям, были связаны с CAR+CD3+ Cmax > 500 CAR+ T клеток/мкл (Р значения Вилкоксона <,05 (без разнообразия регулирования); за исключением IL-7 p=0,07).
[0892] Пиковые плазменные уровни различных цитокинов (IL-6, IL-10, IL-16, интерферон (IFN-γ), альфа фактор некроза опухоли (TNF-α), MIP-1α, MIP-1β, моноцитарный хемоаттрактантный белок-1 (MCP-1) и C-X-C мотив хемокина 10 (CXCL10)) были также оценены у пациентов, показавших CAR+ CD3+ кровь Cmax > 500 CAR+ T клеток/мкл (N=68) по сравнению с пациентами, показавшими CAR+ CD3+ кровь Cmax < 500 CAR+ T клеток/мкл; N=9). Как показано на ФИГ. 14B, более высокие пиковые уровни цитокина, по наблюдениям, были связаны с CAR+CD3+ Cmax > 500 CAR+ T клеток/мкл (Р значения Вилкоксона <0,05; без разнообразия регулирования).
[0893] Оценивали отношение между объемным количеством измерения опухоли размеров продукта перед лечением CAR+ Т-клетками (пре-противолимфоцитарная химиотерапия (LDC)) (SPD), как индикатором опухолевой массы, и AUC0-28 CD3+ CAR+ Т-клеток, представляющее экспонирование CAR+ T в течение времени. Как показано на ФИГ. 15, положительная корреляция наблюдалась между начальным SPD и CD3+ AUC0-28, с корреляцией Spearman 0,32 и p=0,019.
J. Параметры пациента до лечения и результаты ответа и токсичности
[0894] Уровни аналита, включая цитокины и воспалительные маркеры, такие как Ферритин, C-реактивный белок (CRP), D-димер (продукт распада фибрина), IL-6, IL-10, IL-15, IL-16 TNF-α, MIP-1α, и MIP-1β, перед лечением CAR+ Т-клетками (pre-LDC) были сравнены для пациентов с любыми степенями (здесь, степени 1-4) синдрома высвобождения цитокинов (CRS) или нейротоксичности (NT) с пациентами, не имевшими никакого CRS или NT (степени 0). В этом контингенте среди пациентов с CRS степени 1-4, все кроме событий CRS были определены как имеющие степень 1 или 2. Как показано на ФИГ. 16А (CRS) и ФИГ. 16B (NT), более высокие пиковые плазменные уровни цитокинов и уровни воспалительных маркеров, по наблюдениям, были связаны с CRS и NT, на основе однофакторного анализа (Р значения Вилкоксона <0,05 для всех аналитов кроме ферритина для CRS (p=0,14) и CRP для CRS (p=0,09)). Для CRS, после калибровки опухолевой массы в многовариантном анализе, MIP-1β, IL-10 и TNF имели p <0,05; для NT IL-15, IL-6, MIP-1α и TNF имели p <0,05.
[0895] Параметры пациента до лечения (pre-LDC), такие как уровни лактатдегидрогеназы (LDH) и объемное измерение опухоли, такое как сумма размеров продукта (SPD), как индикатор опухолевой массы, сравнивали между пациентами, у которых, по наблюдениям, не развились CRS или нейротоксичность, по сравнению с пациентами, у которых, по наблюдениям, развились CRS или NT. Как показано на ФИГ. 17, пациенты с CRS или NT показали более высокие уровни параметров пациента до лечения, такие как уровни SPD (см2) и LDH (Ед/л); такие уровни, по наблюдениям, коррелировали с CRS или NT с однофакторным статистическим анализом. Другие параметры пациента, которые, по наблюдениям, были связаны с CRS и NT, включают более короткое время, начиная с диагностики (p=0,05 и p=0,09, для CRS и NT, соответственно). Параметры пациента, которые, по наблюдениям, не были связаны с CRS или NT, включали возраст (p=0,19 и p=0,54, соответственно) и предшествующие числа терапий (p=0,67 и p=0,59, соответственно), стадию заболевания 0-2 по сравнению с 3-4 (p=0,79, p=0,51), и массу тела пациента (p=0,35 и p=0,44, соответственно).
[0896] ФИГ. 18A показывает уровни SPD и LDH до лечения среди отдельных пациентов (точки; где штриховка отдельных точек, указывает, показывал ли отдельные пациенты или нет степени нейротоксичности (левая группа) или степени CRS (правая группа). На ФИГ. 18А пунктиры на осях y и X очерчивают ≥50 см SPD2 и LDH ≥500 Ед/л, соответственно. Как показано на ФИГ. 18А, SPD приблизительно 50 см2 или выше, и/или LDH приблизительно 500 Ед/л или выше, по наблюдениям, были связаны с риском NT и CRS. Расчетное отношение неравенства для развития CRS или NT у пациентов выше или ниже уровней SPD и LDH, обозначенных пунктирами на ФИГ. 18А, с 95%-ми доверительными интервалами (CI) изображено на ФИГ. 18B и 18C. Отношение неравенства более чем 1 указывает увеличенную вероятность или вероятность развития CRS или NT. Как показано, SPD 50 см2 или выше, и LDH 500 Ед/л или выше, по наблюдениям, были связаны с повышенным риском развития CRS или NT. SPD 50 см2 или выше и LDH 500 Ед/л или выше, по наблюдениям, были связаны с приблизительно 8-кратным повышенным риском развития любой степени CRS и NT, и SPD ниже, чем 50 см2 и LDH ниже, чем 500 Ед/л показали сниженный риск любой степени CRS и NT. Результаты согласовывались с ассоциацией начальных параметров пациента, включая высокую опухолевую нагрузку и воспалительные биомаркеры, с ростом CAR+ Т-клеток и увеличенной степенью CRS и нейротоксичностью.
[0897] Различные параметры пациента до лечения (pre-LDC), включая маркеры, связанные с опухолевой нагрузкой (SPD), воспалительные цитокины и другие аналиты крови, включая LDH, ферритин, CRP, D-димер, SAA-1, IL-6, IL-10, IL-15, IL-16, TNF-α, IFN-γ, MIP-1α и CXCL10, сравнивали для пациентов с и без длительного ответа в 3 месяца с однофакторным статистическим анализом. Как показано на ФИГ. 19, некоторые маркеры опухолевой массы, маркеры воспаления или воспалительных цитокинов, по наблюдениям, были ниже у пациентов, показавших длительный ответ (p значение <0,05 для всех параметров кроме SPD (p=0,1274)). Подобные результаты наблюдались у пациентов, получающих DL2, когда их анализировали индивидуально. Наблюдалась обратная ассоциация начальных параметров пациента, включая высокую опухолевую нагрузку и воспалительные биомаркеры, с длительным ответом. В некоторых аспектах такая обратная ассоциация может быть следствием более высокого роста и истощения CAR+ Т-клеток.
[0898] Отношения между факторами пациента, клиническими коррелятами и аналитами крови с развитием степеней CRS и NT оценивали с помощью статистического анализа на основе однофакторных непараметрических анализов. В Таблице E13 перечислены результаты однофакторного анализа. В этой оценке возраст <40 лет и отсутствие предшествующего HSCT коррелировали с уровнем CRS или NT. Пациенты с возрастом <40 лет, по наблюдениям, не имели статистически отличных показателей более высокой опухолевой массы от пожилых пациентов. Пациенты с оценкой ECOG 2 не имели статистически отличных показателей более высокой опухолевой массы по сравнению с пациентами с оценкой ECOG 0-1. Пациенты без предшествующего HSCT или double/triple hit или double expressor не были связаны с CRS или NT.
K. Пиковые аналиты крови, ответ и токсичность
[0899] Пиковые уровни плазмы аналитов крови после лечения, включая цитокины и воспалительные маркеры, такие как CRP, Амилоид сыворотки A1 (SAA-1), IL-2, IL-6, IL-10, IL-15, TNF-α, MIP-1α, MIP-1β, MCP-1, CXCL10 и Лиганд Хемокина Мотива C-C 13 (CCL13), сравнивали для пациентов с синдромом высвобождения цитокинов (CRS) или нейротоксичностью (NT) степени 1-4 с пациентам, которые, по наблюдениям, не имели CRS или NT. Как показано на ФИГ. 20А (CRS; степени CRS 0, n=51; степени CRS 1-4, n=28) и ФИГ. 20B (NT; степени NT 0, n=63; степени NT 1-4, n=16), более высокие пиковые плазменные уровни цитокинов и уровни воспалительных маркеров, по наблюдениям, были связаны с CRS и NT (Р значения Вилкоксона <0,001 для отсутствия CRS по сравнению с любым CRS и для отсутствия NT по сравнению с любой NT, кроме IL-15 (P=0,05 и 0,006, соответственно)).
[0900] Пиковые плазменные уровни аналитов крови, включая цитокины и воспалительные маркеры, такие как CRP, SAA-1, IL-5, IL-6, IL-7, IL-8, IL-15, Альфа лимфотоксина (LT-α), TNF-α, IFN-γ, MIP-1α, MIP-1β, MCP-1, CXCL10 и трансформирующий фактор роста бета (TGF-β), оценивали для пациентов с лучшим полным ответом (BOR) полного ответа (CR) или частичного ответа (PR) (N=57) по сравнению с уровнями у пациентов со стабильным заболеванием (SD) или прогрессирующим заболеванием (PD) (N=17); или для пациентов с 3-месячным SD или PD (SD/PD) (N=31) по сравнению с пациентами, который показали CR/PR в 3 месяца (N=35). Как показано на ФИГ. 21А (лучший полный ответ (BOR)) и ФИГ. 21B (месяц 3 ответа), более низкие пиковые плазменные уровни цитокинов и уровни воспалительных маркеров, по наблюдениям, были связаны с лучшим BOR и ответом в месяц 3 (Р значения Вилкоксона <0,05 без разнообразия регулирования).
[0901] В этом исследовании введение композиции анти-CD19 CAR+ клеток вводили пациентам с рецидивирующей/рефрактерной агрессивной неходжкинской лимфомой (NHL), имеющим признаки заболевания высокого риска. Наблюдали ответы, включая длительные ответы, включая 81% ОРР, 63% CR в DL2, причем 80% пациентов с CR в 3 месяца оставались в CR в 6 месяцев на всех уровнях дозы, средний DOR пациентов, получающих лечение на всех уровнях дозы 9,2 месяцев, со средней продолжительностью CR, не достигнутой в этот момент времени анализа в этом примере. Результаты также согласовывались с управляемыми уровнями токсичности и благоприятным профилем безопасности, который в некоторых вариантах осуществления может быть соответствующим амбулаторному введению. Наблюдались низкие проценты тяжелого CRS (1%) и тяжелой нейротоксичности (12%) с немногими событиями через первые 72 часа. Результаты согласовывались с осуществимостью амбулаторного введения.
[0902] Фармакокинетические оценки показали, что более высокий рост CAR+ Т-клеток был обычно связан с увеличенной частотой CRS и NT. Пациенты, получающие DL2, показали более высокое экспонирование CAR T по сравнению с пациентами, получающими DL2, что, в целом, соответствовало увеличенной длительности ответа без увеличенного уровня токсичности. В некоторых аспектах, факторы пациента до лечения, такие как pre-LDC, включая гомеостатические и воспалительные цитокины и опухолевую нагрузку, по наблюдениям, были связаны с и/или стимулировали очень высокий рост и токсичность. Было показано, что введенные CAR+ Т-клетки росли в крови и костном мозге всех пациентов с вариабельностью среди пациентов и между типами заболевания. Введенные CAR+ Т-клетки также показали долгосрочное персистирование, причем 75% (9/12) подлежащих оценке пациентов имели детектируемые CAR Т-клетки в 12 месяцев. CAR Т-клетки и В-клеточная аплазия, по наблюдениям, все еще присутствовали во время рецидива (11/12 и 12/12 пациентов, соответственно), подтверждая, что опухоли могут уклоняться от действия CAR Т-клеток, и что комбинированные стратегии могут быть эффективными, чтобы предотвратить рецидив или увеличение, стимулировать или усиливать исчерпанные CAR Т-клетки. В целом, наблюдалась тенденция более высокого ответа с более высоким ростом с вариабельностью среди пациентов, подтверждая, что другие факторы пациента и/или характеристики заболевания, например, опухолевая нагрузка, могут способствовать определению ответа.
Пример 4: Характеристики терапевтической композиции Т-клеток для введения и способ получения композиции
[0903] Примеры терапевтических композиций Т-клеток, содержащих аутогенные Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфичный для CD19, используемые для введения в Примерах 1 и 2 выше, оцененивали по более чем ста фенотипических, функциональных и связанных со здоровьем клетки признаков с помощью потоковой цитометрии и тестов in vitro. Были исследованы композиции терапевтических клеток, сгенерированные для пациентов, зарегистрированных в клиническом исследовании, в котором оценивали анти-CD19 CAR-T клеточную терапию в отношении лечения рецидивирующей/рефрактерной В-клеточной неходжкинской лимфомы (N=63; основной контингент). Клетки оценивали до и после разработки для различных признаков. Примеры оцениваемых признаков представлены в Таблице E14. Фенотипы памяти и клеточного здоровья CAR Т-клеток были исследованы с помощью потоковой цитометрии. Функциональность Т-клеток была оценена с помощью in vitro антиген-специфических биопроб. Охарактеризовывание и тестирование высвобождения проводили на терапевтических композициях Т-клеток, перенесших репрезентативное число циклов замораживания-оттаивания.
Активная внутриклеточная каспаза 3
Аннексин V
(фактор некроза опухоли α)
[0904] Для получения композиций клеток для введения аутогенные клетки выделяли от пациентов через лейкаферез. Образцы лейкафереза были подвергнуты процессу для генерации CAR-экспрессирующих клеток. Процесс включал промывку клеток с помощью автоматизированного мытья и иммуноафинный отбор для очистки CD4+ и CD8+ Т-клеток, в результате чего получали две композиции, обогащенные CD8+ (в котором в среднем 99%, Inter Quartile Range (IQR) 98-100%, клеток были CD8+) и CD4+ (в котором в среднем 99%, IQR 99-100%, клеток были CD4+) клетками, соответственно.
[0905] Клетки обогащенной CD4+ и CD8+ композиции были отдельно подвергнуты лентивирусной трансдукции вектором, кодирующим анти-CD19 CAR с 41BB костимулирующей областью. Трансдуцированные популяции затем отдельно инкубировали в присутствии стимулирующих реагентов для роста клеток. Выращенные CD8+ и CD4+ клетки составляли и сохраняли замораживанием отдельно и хранили до введения. Для уменьшения вариаций между партиями и/или композициями клеток, полученных от разных пациентов, таких как те, которые имеют различные характеристики пациента, в параметрах, репрезентативных для здоровья клетки, клетки проводили в постоянных объемах от партии к партии. Продукты клеток показали тесный ряд жизнеспособных концентраций клеток (на основе оценки композиций клеток для одной группы пациентов, CD8+: средний 31x106 клеток/мл, IQR 28-40x106 клеток/мл, N=38; CD4+: средний 35x106 клеток/мл, IQR 31-40x106, N=36).
[0906] Как показано на ФИГ. 26 и представлено в Таблице E15, автоматизированная очистка Т-клеток приводила к чистым популяциям CD8+ и CD4+ Т-клеток. Эта стратегия уменьшила вероятность трансдукции не-Т-клеток и приводила к высокой чистоте Т-клеток в композиции терапевтических клеток, независимо от продолжительности роста.
[0907] В месте введения композиции клетки оттаивали и вводили отдельно, согласно целевому объему каждой композиции, соответствующему числу CD8+CAR+ и CD4+CAR+ клеток в подходящей дозе (такой как для DL1, содержащей 5x107 общих CAR-экспрессирующих Т-клеток (2,5x107 каждых из CAR-экспрессирующих CD4+ и CAR-экспрессирующих CD8+ клеток), или DL2, содержащей 1x108 общих CAR-экспрессирующих Т-клеток (5x107 каждый из CAR-экспрессирующих CD4+ и CAR-экспрессирующих CD8+ клеток)).
[0908] Во время клинического испытания было изменение процесса с составов большого объема на составы малого объема. После изменения композицию терапевтических клеток составляли в постоянном низком объеме с плотно контролируемым рядом жизнеспособных концентраций клеток. В некоторых случаях состав малого объема использовался вместо состава большого объема. Были оценены параметры, репрезентативные для здоровья CAR-экспрессирующих Т-клеток в композициях для введения, такие как путем измерения, постоттаивание, жизнеспособность, экспрессия Аннексина V поверхности клеток и уровни активной внутриклеточной Каспазы 3, в композициях клеток, составленных с большим объемом и малым объемом.
[0909] Изменение процесса от составов большого объема до составов малого объема приводило к увеличенной надежности процесса и уменьшало вариабельность признаков здоровья клеток. Значения концентрации, процента жизнеспособных клеток и процента отрицательных в отношении активной каспазы 3 клеток среди CD4+ и CD8+ Т-клеток отдельных композиций клеток показаны в ФИГ. 27A-27C и в Таблице E16. Средний процент клеток, экспрессирующих Аннексин V, составлял 11% (IQR 9-18%; N=33) CD8+CAR+ Т-клеток и 10% (IQR 8-17%; N=31) CD4+CAR+ Т-клеток. Экспрессия Каспаза 3, по наблюдениям, была подобна экспрессии Аннексина V. Изменение на составы малого объема приводило к увеличенной надежности процесса и уменьшало вариабельность признаков здоровья клеток.
x106 клеток/мл
[0910] Количества CAR+CD4+ и CAR+CD8+ Т-клеток в композициях для введения прецизионно контролировали. Число клеток, фактически введенных образцовой группе пациентов, по наблюдениям, составляло 8% или менее целевого числа клеток для введенной дозы:
· 2,4-2,7x107 (целевое ±8%) CD4+CAR+ Т-клеток и 2,4-2,7x107 (целевое ±8%) CD8+CAR+ Т-клеток для пациентов, которым вводили клетки в DL1 (n=48)
· 4,6-5,1x107 (целевое ±8%) CD4+CAR+ Т-клеток или 4,6-5,1x107 (целевое ±8%) CD8+CAR+ Т-клеток для пациентов, которым вводили клетки в DL2 (n=20).
[0911] Было обнаружено, что диапазон введенной дозы имел низкую вариабельность среди различных образцовых групп пациентов:
· 48-52 ×106 CD3+CAR+T клеток в DL1 (n =34)
· 96-101×106 CD3+CAR+T клеток в DL2 (n = 29)
· 24-27 x 106 CD4+CAR+ или CD8+CAR+ T клеток в DL1 (n = 34)
· 46-51 x 106 CD4+CAR+ или CD8+CAR+ T клеток в DL2 (n = 29).
[0912] Как показано на ФИГ. 28А, композиции CAR-экспрессирующих Т-клеток, введенные пациентам, по наблюдениям, показали высокую чистоту Т-клеток и низкое различие между партиями. С точки зрения, например, процесса и средств контроля продукта, композиции терапевтических клеток, содержащие CAR Т-клетки, по наблюдениям, имели низкую вариабельность от партии к партии специфичных для клеток функции Т-клеток.
[0913] In vitro аккумуляция антиген-специфических цитокинов и внутриклеточное окрашивание цитокинов (ICS) показали подобное низкое различие между партиями в отношении продукции цитокинов для множества цитокинов (IL-2, TNF-α и IFN-γ). В образцовом эксперименте ICS клетки композиций стимулировали CD19, окрашивали для цитокинов, включая TNF-α и поверхностные белки, включая тип 7 (CCR7) рецептора хемокина C-C как маркер фенотипа памяти, и анализировали потоковой цитометрией. Определяли число клеток в композиции для введения, которые были положительными в отношении цитокинов или поверхностных белков. ФИГ. 28B показывает число CD4+CAR+ и CD8+CAR+ клеток, CD4+CAR+TNF-α+ и CD8+CAR+TNF-α+ клеток, CD4+CAR+CCR7+ и CD8+CAR+CCR7+ и присутствующих в композициях CAR Т-клеток для введения в DL1 и DL2. Эти результаты представлены в Таблице E17. Результаты показывают низкую вариабельность числа CD4+CAR+ и CD8+CAR+ клеток, CD4+CAR+TNF-α+ и CD8+CAR+TNF-α+ клеток, CD4+CAR+CCR7+ и CD8+CAR+CCR7+ клеток. Например, наблюдался плотный диапазон для числа клеток, положительных в отношении продукции TNF-α (n=61).
TNF-α+
TNF-α+
CCR7+
CCR7+
[0914] Параметр, индикативный в отношении продукции CAR+ клеток фактора некроза опухоли альфа (TNFα) после стимуляции CD19, показал узкий ряд среди различных партий с относительным среднеквадратичным отклонением (RSD) 37% для CD4+CAR+ Т-клеток (N=59) и 51% для CD8+CAR+ Т-клеток (N=61).
[0915] Результаты согласовывались с наблюдением, что композиция, содержащая точную и постоянную дозу CD4+ и CD8+ CAR Т-клеток, условия контроля и оптимизации культивирования CD4+ и CD8+ Т-клеток, низкая вариабельность продукции цитокинов и/или постоянный состав и объем композиции для введения могут привести к стабильному здоровью клеток в композиции. В вариантах осуществления изобретения аспекты такого процесса производства и контроля способствуют низкой вариабельности признаков таких композиций генно-инженерных клеток с использованием клеток от, и сгенерированных для введения им, многих различных пациентов. Такие аспекты в некоторых аспектах включают использование точной, постоянной плоской дозы вводимых CD4+ и CD8+ клеток среди пациентов; условия контроля и оптимизации культивирования CD4+ и CD8+ Т-клеток, такие как те, которые приводят к низкой вариабельности партий между фенотипами фармацевтических продуктов (например, CCR7) и функции in vitro (например, продукция IL-2, TNF-α и IFN-γ после стимуляции антигена), например, среди различных пациентов; и использование постоянного состава и объема фармацевтического продукта, который может приводить к или способствовать постоянству среди композиций терапевтических клеток, сгенерированных способом, в отношении признаков, репрезентативных для здоровья клеток.
Пример 5: Оценка биомаркера до и после введения биопсии опухоли от пациентов с рецидивирующей и рефрактерной неходжкинской лимфомой (NHL) для введения Анти-CD19 CAR-экспрессирующих клеток
[0916] Экспрессию нескольких биомаркеров оценивали в биопсиях опухоли, собранных от пациентов до и/или после введения CAR-экспрессирующих клеток.
A. Образцы биопсии опухоли
[0917] Биопсии опухоли были собраны из выбранных пациентов с рецидивирующей или рефрактерной диффузной крупноклеточной В-клеточной лимфомой (DLBCL) (R/R) или мантийноклеточной лимфомой (MCL), которые прошли лечение композициями терапевтических CAR+ Т-клеток, содержащими аутогенные Т-клетки, экспрессирующие химерный антигенный рецептор (CAR), специфичный для CD19, описанного выше в Примерах 1 и 2 выше, на основе момента времени оценки в Примере 1.А.2. Биопсии опухоли были получены до введения CAR+ Т-клеток (до лечения) и в 7-20 дней после введения (посл лечения). Результаты описаны в этом примере для оценки через момент времени в Примере 1.А.2 в продолжающемся исследовании. Были исследованы результаты 43 биопсий (26 до лечения; 17 после дующего и 15 подобранных пар) от 28 общих пациентов (25 DLBCL и 3 мкл).
B. Оценка биомаркеров, результатов ответа и безопасности
[0918] Инфильтрацию CAR+ Т-клеток в биопсии опухоли определяли количественно с помощью гибридизации in situ (ISH) зондов, специфичных для мРНК, кодирующей анти-CD19 CAR. CAR+ Т-клетки, не-CAR Т-клетки и В-клетки были подсчитаны с помощью тестов мультиплексной иммунофлюоресценции (IF), детектирующих суррогатный маркер поверхности клеток для CAR-экспрессирующих клеток, CD4, CD8, CD19, CD20, CD73, FOXP3, CD163, IDO и PD-L1. Секции биопсии опухоли окрашивали гематоксилином и эозином (Г-Э) и оценивали по качеству ткани и идентификации опухоли. Изображения иммунофлюоресценции были проанализированы с помощью программного обеспечения для анализа изображения. Потенциальные корреляции с результатами ответа оценивали с помощью статистического анализа на основе однофакторных t-анализов, и p-значения были 2-сторонними без учета множественности сравнения.
[0919] Пациентов оценивали в отношении результатов ответа и безопасности, включая оценку опухолевой массы в различные моменты времени после введения CAR+ Т-клеток, включая в 3 месяца после введения, и определение того, имел ли пациент прогрессирующее заболевание (PD), стабильное заболевание (SD), частичный ответ (PR) или полный ответ (CR). Оцениваемые результаты безопасности включали нейротоксичность (неврологические осложнения, включая симптомы спутанности сознания, афазии, энцефалопатии, миоклонические судороги, конвульсии, летаргию и/или изменения психического статуса), классифицированную на основании масштаба 1-5 согласно National Cancer Institute-Common Toxicity Criteria (CTCAE), версия 4.03 (NCI-CTCAE v4.03).
C. Результаты
[0920] Наблюдаемая частота объективного ответа (ОРР; включая CR и PR) составляла 71% (20/28) у пациентов, для которых оценивали биопсии. Степени 1, 2 CRS наблюдали у 36% (10/28; степени 1, 2) пациентов, для которых оценивали биопсии, и Степени 2-4 NT наблюдали у 18% (5/28) пациентов, для которых оценивали биопсии.
[0921] Биопсии опухоли до лечения, по наблюдениям, содержали вариабельные клеточные композиции: опухолевые клетки (медиана: 77%; диапазон 5-96%), CD4+ клетки (0,90%; 0,02-15%) и CD8+ клетки (1,5%; 0-23%). Результаты показали, что пациенты с CR или PR в 3 месяца после введения CAR+ Т-клеток имели более высокий процент эндогенных CD4+ клеток в опухолях до лечения по сравнения с PD (CR, медиана PR: 7,9%; медиана PD: 0,38%; p <0,0001). Проценты CD8+ клеток в опухолях до лечения не различались между группами 3-месячного ответа (CR, медиана PR: 1,9%; медиана PD: 0,47%; p=0,6496).
[0922] В биопсиях после лечения CAR+ Т-клетки, по наблюдениям, инфильтрировали опухоль и составляли до 22% клеток в образце биопсии. Уровень инфильтрации опухоли в образцах после лечения (спустя 7-20 дней после введения), по наблюдениям, был выше у пациентов, продолжавших достигать CR (медиана: 3,9%) или PR (медиана: 1,1%) по сравнению с пациентами, продолжавшими достигать лучшего полного ответа (BOR) SD или PD (медиана: 0,51%). Несмотря на то, что как CD4+, так и CD8+ CAR Т-клетки, по наблюдениям, инфильтрировали область опухоли в момент времени после лечения (спустя 7-20 дней после введения), пациенты, продолжавшие достигать CR, по наблюдениям, имели более высокое отношение CD8+ CAR+ Т-клеток к CD4+ CAR+ Т-клеткам в этот момент времени после лечения по сравнению с пациентами, продолжавшими достигать BOR SD или PD (медиана CR: 0,83; SD, медиана PD: 0,14; p=0,0097).
[0923] Сравнение соответствующих биопсий до и после лечения от отдельных пациентов показало, что пациенты, в конечном счете достигающие BOR CR или PR, имели тенденцию к большему увеличению CD8+ клеток после лечения (CAR+ T и не-CAR T) в опухолях по сравнению с пациентами, в конечном счете достигающими BOR SD или PD (CR, медианное изменение PR: +5,3%; SD, медианное изменение PD: +0,06%; p=0,1225).
[0924] Экспрессия иммунодепрессивных факторов, включая CD73, FOXP3, CD163, IDO и PD-L1, варьировала среди пациентов до лечения (CD73 (медиана: 1,5%; диапазон 0-42%), FOXP3 (0,10%; 0-1,5%), IDO (0,06%; 0-11%), CD163 (1,2%; 0-24%) и PD-L1 (0,16%; 0-56%)) и после лечения (CD73 (1,6%; 0-53%), FOXP3 (0,09%; 0-4,3%), IDO (0,28%; 0-15%), CD163 (3,6%; 0-22%) и PD-L1 (3,3%; 0-65%)). Увеличение CD8+ клеток после лечения в подобранных биопсиях, по наблюдениям, было связано с увеличениями после лечения экспрессии IDO (R2=0,64) и PD-L1 (R2=0,61). Этот результат согласуется с заключением, что инфильтрация CD8+ CAR+ клеток во время оценки может указывать на потенциальную вероятность достижения степени ответа или продолжительности ответа, и что наличие и/или активность таких клеток могут приводить к повышающей регуляцией факторов TME.
D. Заключение
[0925] Длительный ответ в месяц 3 после введения CAR+ Т-клеток, по наблюдениям, был связан с более высокими уровнями CD4+ клеток в опухолях до лечения. В опухолевых клетках после лечения CAR+ Т-клетки, как CD4+, так и CD8+, по наблюдениям, инфильтрировали опухоль и смежную ткань. ОРР был связан с увеличением CAR+ Т-клеток в биопсии опухоли. Увеличение уровней CD8+ в биопсии опухоли после лечения по сравнению с уровнями CD8+ в биопсии опухоли до лечения было связано с увеличенной экспрессией IDO и PD-L1. В некоторых вариантах осуществления терапии, нацеленные на эти пути, такие как вводимые во время или после введения CAR-T клеток, могут усилить один или более терапевтических результатов или их продолжительность после введения CAR+ Т-клеток.
Пример 6: Дальнейшая оценка результатов ответа и безопасности у пациентов с рецидивирующей и рефрактерной неходжкинской лимфомой (NHL) после введения анти-CD19 CAR-экспрессирующих клеток
[0926] Результаты ответа и безопасности оценивали у пациентов в последующий момент времени в клиническом исследовании, описанном в Примерах 1 и 3 выше.
A. Пациенты и лечение
[0927] Анализ в этот момент времени, представленный в этом примере, основывается на оценке в общей сложности 102 пациентов в полном контингенте (73 в основном контингенте), которым вводили анти-CD19CAR-экспрессирующие клетки. Полный контингент включал пациентов, у которых была DLBCL (DLBCL, NOS de novo и трансформированная из фолликулярной лимфомы; В-клеточная лимфома высокой степени злокачественности (double/triple hit); DLBCL, трансформированная из CLL или MZL; PMBCL; и FL3B, ECOG 0-2, после 2 линий терапии; основной контингент для анализа включал пациентов, имеющих DLBCL, NOS и трансформированную из фолликулярной лимфомы (tFL) или В-клеточной лимфомы высокой степени злокачественности (double/triple hit) и с Eastern Cooperative Oncology Group Performance Status (ECOG PS) 0 или 1. Приблизительно у 90% получавших лечение пациентов в полном и основном контингенте был по меньшей мере один признак заболевания высокого риска, прогностический для короткого среднего полного выживания (OS) 3-6 месяцев (см. Crump et al., Blood (2017) 130:1800-1808 and Van de Neste et al., Bone Marrow Transplant. (2016) 51(1):51-7), такой как double/triple hit экспрессоры, первичное рефрактерное заболевание, рефрактерное к 2 или более линиям терапии, никогда не достигали CR, никогда не получали трансплантацию аутогенных стволовых клеток (ASCT) или PS ECOG 2.
[0928] В этот момент времени в общей сложности 134 пациента подвергали лейкаферезу, из которых 2 имел недоступные композиции. Продукт был доступен для 99% пациентов, подвергнутых аферезу, (132/134) в контингенте DLBCL. Еще из 18 пациентов, продукты для которых были доступны, 5 вышли из исследования, и у 13 развилось прогрессирующее заболевание, или они умерли. В общей сложности 114 пациентам вводили анти-CD19 CAR-экспрессирующие клетки, из которых 12 получили несоответствующие анти-CD19 CAR-экспрессирующие клетки (композиции не обязательно соответствовали некоторым техническим требованиям, но считались безопасными для введения). Пациенты получили DL1 (n=45), двойную дозу DL1 (n=6) или DL2 (n=51). Семи (7) пациентам с мантийноклеточной лимфомой (MCL) вводили CAR+ клетки в DL1. В этот момент времени восемь (8) пациентов получали лечение в амбулаторном режиме.
[0929] Демографические и базовые характеристики пациентов полного и основного контингента в момент времени представлены в Таблице E18.
a При инициации испытания, включенная в DLBCL, гистология NOS; на основе новых критериев ВОЗ (Swerdlow et al., (2016) Кровь 127(20):2375-2390), теперь считается высокодифференцированной В-клеточная лимфомой, с myc и bcl2 и/или bcl6 перестановками с гистологией DLBCL (double/triple hit).
b SD или PD для длительности включающего химиотерапию режима или рецидива спустя < 12 месяцев после аутологичных SCT.
B. Результаты безопасности и ответа после лечения
[0930] Таблица E19 показывает результат безопасности основного и полного контингента. Как показано, никаких смертельных случаев от CRS или NT не наблюдалось. В полном контингенте среднее время до начала CRS составляло 5 дней (диапазон, 2-12 дней) и время до NT составляло 10 дней (диапазон, 3-23 дня). В полном контингенте 17% (n=17) получили тоцилизумаб и 21% (n=21) получили кортикостероиды в качестве вмешательства для лечения токсичности. В основном контингенте никакого увеличения CRS или NT не наблюдалось в DL2 по сравнению с DL1.
n=102
n=33
n=37
а Три пациента, получавших лечение на DL1D (уровень дозы 1, режим с двумя дозами) с подобными результатами.
[0931] ФИГ. 29 изображает процент пациентов в полном контингенте в этот момент времени (n=102), которые, по наблюдениям, испытывали лабораторные патологии и нежелательные явления, возникшие в ходе лечения (TEAEs) (данные для 6 пациентов с MCL, получавших лечение соответствующим продуктом в DL1 по меньшей мере с 28 дней наблюдения, не включены; показаны TEAEs и лабораторные патологии, проявляющиеся у 20% или более пациентов).
[0932] Как показано в Таблице E20, высокие показатели ответа наблюдались у пациентов с рецидивирующей или рефрактерной (R/R) DLBCL. Результаты согласовывались с эффектом доза-ответ на результат лечения в основном контингенте. Пациенты с опухолевой нагрузкой выше порога (как обозначено объемным измерением опухоли суммы размеров продукта (SPD) более чем 50 см2) были так же распределены между пациентами, получающими DL1 и DL2 (приблизительно 1/3 пациентов в каждой группе).
а Три пациента, получавших лечение DL1D (уровень дозы 1, режим с двумя дозами) с подобными результатами.
[0933] Частота объективного ответа в шесть месяцев (ORR) среди различных подгрупп пациентов в подгруппе с высоким риском DLBCL, включавшей всех пациентов DLBCL, получавших лечение со всеми уровнями дозы в основном контингенте, показана на ФИГ. 30. Результаты показали высокий длительный ОРР в подгруппе с высоким риском DLBCL на введение анти-CD19 CAR+ Т-клеток.
[0934] Результаты в отношении времени ответа (DOR, со средним наблюдением 8 месяцев) и полной выживаемости (сгруппированной по лучшему полному ответу (не отвечающие, CR/PR, CR и/или PR) со средним наблюдением 12 месяцев) показаны для полного контингента и основного контингента пациентов на ФИГ. 31A-31D. Результаты показали, что в основном контингенте 88% пациентов с CR в 3 месяца продолжали показывать CR в 6 месяцев, и 93% пациентов, которые показали CR в 6 месяцев, продолжали показывать перспективу долгосрочного ответа.
[0935] Результаты согласовывались с наблюдением, что введение композиции анти-CD19 CAR+ клеток, которая содержит точную и стабильную дозу CD4+ и CD8+ CAR+ Т-клеток, приводит к длительному ответу у пациентов с агрессивной R/R NHL с неблагоприятным прогнозом и/или тяжелым предварительным лечением. Результаты показали благоприятную частоту длительного ответа в основном контингенте с уровнями 49% ОРР и 46% CR в 6 месяцев, и 93% пациентов (на всех уровнях дозы) в CR в 6 месяцев остались в состоянии ответа в этот момент времени. Результаты также соответствовали контролируемой токсичности и благоприятному профилю безопасности, включая низкие проценты тяжелого CRS (1%) и тяжелой нейротоксичности (13%), что, в некоторых аспектах, делает возможным амбулаторное введение.
[0936] Настоящее изобретение не предназначено для того, чтобы быть ограниченным в объеме частными раскрытыми вариантами осуществления, приведенными, например, для иллюстрации различных аспектов изобретения. Различные модификации описанных композиций и способов будут очевидны из приведенного описания и раскрытия. Такие модификации могут практиковаться без отхода от истинного объема и духа раскрытия и предназначены для включения в рамки настоящего раскрытия.
ПОСЛЕДОВАТЕЛЬНОСТИ
Homo sapiens
homo sapiens
Homo sapiens
Homo sapiens
Homo sapiens
искусственная
искусственная
Homo sapiens
Homo sapiens
Homo sapiens
Homo sapiens
Homo sapiens
Homo sapiens
Homo sapiens
Homo sapiens
искусственная
X1 обозначает глицин, цистеин или аргинин
X2 обозначает цистеин или треонин
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> JUNO THERAPEUTICS, INC.
ALBERTSON, Tina
<120> ИЗДЕЛИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ С ИСПОЛЬЗОВАНИЕМ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ
<130> 735042012140
<140> Еще не присвоено
<141> Одновременно с этим
<150> 62/514,774
<151> 2017-06-02
<150> 62/515,530
<151> 2017-06-05
<150> 62/521,366
<151> 2017-06-16
<150> 62/527,000
<151> 2017-06-29
<150> 62/549,938
<151> 2017-08-24
<150> 62/580,425
<151> 2017-11-01
<150> 62/593,871
<151> 2017-12-01
<150> 62/596,764
<151> 2017-12-08
<150> 62/614,957
<151> 2018-01-08
<160> 58
<170> FastSEQ для Windows Version 4.0
<210> 1
<211> 12
<212> белок
<213> Homo sapiens
<220>
<223> Спейсер (IgG4шарнир)
<400> 1
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 2
<211> 36
<212> ДНК
<213> Homo sapiens
<220>
<223> Спейсер (IgG4шарнир)
<400> 2
gaatctaagt acggaccgcc ctgcccccct tgccct 36
<210> 3
<211> 119
<212> белок
<213> Homo sapiens
<220>
<223> шарнир-CH3 Спейсер
<400> 3
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Gly Gln Pro Arg
1 5 10 15
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
20 25 30
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
35 40 45
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
50 55 60
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
65 70 75 80
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
85 90 95
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
100 105 110
Leu Ser Leu Ser Leu Gly Lys
115
<210> 4
<211> 229
<212> белок
<213> Homo sapiens
<220>
<223> шарнир-CH2-CH3 Спейсер
<400> 4
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys
225
<210> 5
<211> 282
<212> белок
<213> Homo sapiens
<220>
<223> IgD-шарнир-Fc
<400> 5
Arg Trp Pro Glu Ser Pro Lys Ala Gln Ala Ser Ser Val Pro Thr Ala
1 5 10 15
Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala
20 25 30
Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys
35 40 45
Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
50 55 60
Ser His Thr Gln Pro Leu Gly Val Tyr Leu Leu Thr Pro Ala Val Gln
65 70 75 80
Asp Leu Trp Leu Arg Asp Lys Ala Thr Phe Thr Cys Phe Val Val Gly
85 90 95
Ser Asp Leu Lys Asp Ala His Leu Thr Trp Glu Val Ala Gly Lys Val
100 105 110
Pro Thr Gly Gly Val Glu Glu Gly Leu Leu Glu Arg His Ser Asn Gly
115 120 125
Ser Gln Ser Gln His Ser Arg Leu Thr Leu Pro Arg Ser Leu Trp Asn
130 135 140
Ala Gly Thr Ser Val Thr Cys Thr Leu Asn His Pro Ser Leu Pro Pro
145 150 155 160
Gln Arg Leu Met Ala Leu Arg Glu Pro Ala Ala Gln Ala Pro Val Lys
165 170 175
Leu Ser Leu Asn Leu Leu Ala Ser Ser Asp Pro Pro Glu Ala Ala Ser
180 185 190
Trp Leu Leu Cys Glu Val Ser Gly Phe Ser Pro Pro Asn Ile Leu Leu
195 200 205
Met Trp Leu Glu Asp Gln Arg Glu Val Asn Thr Ser Gly Phe Ala Pro
210 215 220
Ala Arg Pro Pro Pro Gln Pro Gly Ser Thr Thr Phe Trp Ala Trp Ser
225 230 235 240
Val Leu Arg Val Pro Ala Pro Pro Ser Pro Gln Pro Ala Thr Tyr Thr
245 250 255
Cys Val Val Ser His Glu Asp Ser Arg Thr Leu Leu Asn Ala Ser Arg
260 265 270
Ser Leu Glu Val Ser Tyr Val Thr Asp His
275 280
<210> 6
<211> 24
<212> белок
<213> Искусственная последовательность
<220>
<223> T2A
<400> 6
Leu Glu Gly Gly Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp
1 5 10 15
Val Glu Glu Asn Pro Gly Pro Arg
20
<210> 7
<211> 357
<212> белок
<213> Искусственная последовательность
<220>
<223> tEGFR
<400> 7
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro Arg Lys Val Cys Asn Gly Ile Gly Ile Gly
20 25 30
Glu Phe Lys Asp Ser Leu Ser Ile Asn Ala Thr Asn Ile Lys His Phe
35 40 45
Lys Asn Cys Thr Ser Ile Ser Gly Asp Leu His Ile Leu Pro Val Ala
50 55 60
Phe Arg Gly Asp Ser Phe Thr His Thr Pro Pro Leu Asp Pro Gln Glu
65 70 75 80
Leu Asp Ile Leu Lys Thr Val Lys Glu Ile Thr Gly Phe Leu Leu Ile
85 90 95
Gln Ala Trp Pro Glu Asn Arg Thr Asp Leu His Ala Phe Glu Asn Leu
100 105 110
Glu Ile Ile Arg Gly Arg Thr Lys Gln His Gly Gln Phe Ser Leu Ala
115 120 125
Val Val Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu
130 135 140
Ile Ser Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr
145 150 155 160
Ala Asn Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys
165 170 175
Thr Lys Ile Ile Ser Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly
180 185 190
Gln Val Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu
195 200 205
Pro Arg Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys
210 215 220
Val Asp Lys Cys Asn Leu Leu Glu Gly Glu Pro Arg Glu Phe Val Glu
225 230 235 240
Asn Ser Glu Cys Ile Gln Cys His Pro Glu Cys Leu Pro Gln Ala Met
245 250 255
Asn Ile Thr Cys Thr Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala
260 265 270
His Tyr Ile Asp Gly Pro His Cys Val Lys Thr Cys Pro Ala Gly Val
275 280 285
Met Gly Glu Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His
290 295 300
Val Cys His Leu Cys His Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro
305 310 315 320
Gly Leu Glu Gly Cys Pro Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala
325 330 335
Thr Gly Met Val Gly Ala Leu Leu Leu Leu Leu Val Val Ala Leu Gly
340 345 350
Ile Gly Leu Phe Met
355
<210> 8
<211> 27
<212> белок
<213> Homo sapiens
<220>
<223> CD28
<300>
<308> UniProt P10747
<309> 1989-07-01
<400> 8
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 9
<211> 66
<212> белок
<213> Homo sapiens
<220>
<223> CD28
<300>
<308> UniProt P10747
<309> 1989-07-01
<400> 9
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
1 5 10 15
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
20 25 30
Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly Gly
35 40 45
Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe
50 55 60
Trp Val
65
<210> 10
<211> 41
<212> белок
<213> Homo sapiens
<220>
<223> CD28
<300>
<308> UniProt P10747
<309> 1989-07-01
<400> 10
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 11
<211> 41
<212> белок
<213> Homo sapiens
<220>
<223> CD28
<400> 11
Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 12
<211> 42
<212> белок
<213> Homo sapiens
<220>
<223> 4-1BB
<300>
<308> UniProt Q07011.1
<309> 1995-02-01
<400> 12
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 13
<211> 112
<212> белок
<213> Homo sapiens
<220>
<223> CD3 дзета
<400> 13
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 14
<211> 112
<212> белок
<213> Homo sapiens
<220>
<223> CD3 дзета
<400> 14
Arg Val Lys Phe Ser Arg Ser Ala Glu Pro Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 15
<211> 112
<212> белок
<213> Homo sapiens
<220>
<223> CD3 дзета
<400> 15
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 16
<211> 335
<212> белок
<213> Искусственная последовательность
<220>
<223> tEGFR
<400> 16
Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp Ser Leu
1 5 10 15
Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn Cys Thr Ser Ile
20 25 30
Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg Gly Asp Ser Phe
35 40 45
Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp Ile Leu Lys Thr
50 55 60
Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala Trp Pro Glu Asn
65 70 75 80
Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile Ile Arg Gly Arg
85 90 95
Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val Ser Leu Asn Ile
100 105 110
Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser Asp Gly Asp Val
115 120 125
Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn Thr Ile Asn Trp
130 135 140
Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys Ile Ile Ser Asn
145 150 155 160
Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val Cys His Ala Leu
165 170 175
Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg Asp Cys Val Ser
180 185 190
Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp Lys Cys Asn Leu
195 200 205
Leu Glu Gly Glu Pro Arg Glu Phe Val Glu Asn Ser Glu Cys Ile Gln
210 215 220
Cys His Pro Glu Cys Leu Pro Gln Ala Met Asn Ile Thr Cys Thr Gly
225 230 235 240
Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile Asp Gly Pro
245 250 255
His Cys Val Lys Thr Cys Pro Ala Gly Val Met Gly Glu Asn Asn Thr
260 265 270
Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His Leu Cys His
275 280 285
Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro Gly Leu Glu Gly Cys Pro
290 295 300
Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala Thr Gly Met Val Gly Ala
305 310 315 320
Leu Leu Leu Leu Leu Val Val Ala Leu Gly Ile Gly Leu Phe Met
325 330 335
<210> 17
<211> 18
<212> белок
<213> Искусственная последовательность
<220>
<223> T2A
<400> 17
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
1 5 10 15
Gly Pro
<210> 18
<211> 22
<212> белок
<213> Искусственная последовательность
<220>
<223> P2A
<400> 18
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 19
<211> 19
<212> белок
<213> Искусственная последовательность
<220>
<223> P2A
<400> 19
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 20
<211> 20
<212> белок
<213> Искусственная последовательность
<220>
<223> E2A
<400> 20
Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp Val Glu Ser
1 5 10 15
Asn Pro Gly Pro
20
<210> 21
<211> 22
<212> белок
<213> Искусственная последовательность
<220>
<223> F2A
<400> 21
Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala Gly Asp Val
1 5 10 15
Glu Ser Asn Pro Gly Pro
20
<210> 22
<211> 9
<212> белок
<213> Искусственная последовательность
<220>
<223> Линкер
<220>
<221> ПОВТОР
<222> (5)...(9)
<223> SGGGG is ПОВТОР 5 times
<400> 22
Pro Gly Gly Gly Ser Gly Gly Gly Gly
1 5
<210> 23
<211> 17
<212> белок
<213> Искусственная последовательность
<220>
<223> Линкер
<400> 23
Gly Ser Ala Asp Asp Ala Lys Lys Asp Ala Ala Lys Lys Asp Gly Lys
1 5 10 15
Ser
<210> 24
<211> 18
<212> белок
<213> Искусственная последовательность
<220>
<223> Линкер
<400> 24
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 25
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<223> scFv
<400> 25
gacatccaga tgacccagac cacctccagc ctgagcgcca gcctgggcga ccgggtgacc 60
atcagctgcc gggccagcca ggacatcagc aagtacctga actggtatca gcagaagccc 120
gacggcaccg tcaagctgct gatctaccac accagccggc tgcacagcgg cgtgcccagc 180
cggtttagcg gcagcggctc cggcaccgac tacagcctga ccatctccaa cctggaacag 240
gaagatatcg ccacctactt ttgccagcag ggcaacacac tgccctacac ctttggcggc 300
ggaacaaagc tggaaatcac cggcagcacc tccggcagcg gcaagcctgg cagcggcgag 360
ggcagcacca agggcgaggt gaagctgcag gaaagcggcc ctggcctggt ggcccccagc 420
cagagcctga gcgtgacctg caccgtgagc ggcgtgagcc tgcccgacta cggcgtgagc 480
tggatccggc agccccccag gaagggcctg gaatggctgg gcgtgatctg gggcagcgag 540
accacctact acaacagcgc cctgaagagc cggctgacca tcatcaagga caacagcaag 600
agccaggtgt tcctgaagat gaacagcctg cagaccgacg acaccgccat ctactactgc 660
gccaagcact actactacgg cggcagctac gccatggact actggggcca gggcaccagc 720
gtgaccgtga gcagc 735
<210> 26
<211> 5
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<220>
<221> ВАРИАНТ
<222> (1)...(1)
<223> Xaa1 = глицин, цистеин или аргинин
<220>
<221> ВАРИАНТ
<222> (4)...(4)
<223> Xaa4 = цистеин или треонин
<400> 26
Xaa Pro Pro Xaa Pro
1 5
<210> 27
<211> 15
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 27
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 28
<211> 12
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 28
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 29
<211> 61
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 29
Glu Leu Lys Thr Pro Leu Gly Asp Thr His Thr Cys Pro Arg Cys Pro
1 5 10 15
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
20 25 30
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro
35 40 45
Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 30
<211> 12
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 30
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro
1 5 10
<210> 31
<211> 12
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 31
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 32
<211> 9
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 32
Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5
<210> 33
<211> 10
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 33
Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 34
<211> 14
<212> белок
<213> Искусственная последовательность
<220>
<223> шарнир
<400> 34
Glu Val Val Val Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 35
<211> 11
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L1
<400> 35
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
1 5 10
<210> 36
<211> 7
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L2
<400> 36
Ser Arg Leu His Ser Gly Val
1 5
<210> 37
<211> 9
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L3
<400> 37
Gly Asn Thr Leu Pro Tyr Thr Phe Gly
1 5
<210> 38
<211> 5
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR H1
<400> 38
Asp Tyr Gly Val Ser
1 5
<210> 39
<211> 16
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR H2
<400> 39
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 40
<211> 7
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR H3
<400> 40
Tyr Ala Met Asp Tyr Trp Gly
1 5
<210> 41
<211> 120
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 VH
<400> 41
Glu Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 42
<211> 107
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 VL
<400> 42
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
100 105
<210> 43
<211> 245
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 scFv
<400> 43
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser
245
<210> 44
<211> 11
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR L1
<400> 44
Lys Ala Ser Gln Asn Val Gly Thr Asn Val Ala
1 5 10
<210> 45
<211> 7
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR L2
<400> 45
Ser Ala Thr Tyr Arg Asn Ser
1 5
<210> 46
<211> 9
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR L3
<400> 46
Gln Gln Tyr Asn Arg Tyr Pro Tyr Thr
1 5
<210> 47
<211> 5
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR H1
<400> 47
Ser Tyr Trp Met Asn
1 5
<210> 48
<211> 17
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR H2
<400> 48
Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe Lys
1 5 10 15
Gly
<210> 49
<211> 13
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 CDR H3
<400> 49
Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr
1 5 10
<210> 50
<211> 122
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 VH
<400> 50
Glu Val Lys Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 51
<211> 108
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 VL
<400> 51
Asp Ile Glu Leu Thr Gln Ser Pro Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Pro Leu Ile
35 40 45
Tyr Ser Ala Thr Tyr Arg Asn Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Lys Asp Leu Ala Asp Tyr Phe Cys Gln Gln Tyr Asn Arg Tyr Pro Tyr
85 90 95
Thr Ser Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 52
<211> 15
<212> белок
<213> Искусственная последовательность
<220>
<223> Линкер
<400> 52
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 53
<211> 245
<212> белок
<213> Искусственная последовательность
<220>
<223> SJ25C1 scFv
<400> 53
Glu Val Lys Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Lys Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val Thr Cys
145 150 155 160
Lys Ala Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr Arg Asn
180 185 190
Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp Tyr Phe
210 215 220
Cys Gln Gln Tyr Asn Arg Tyr Pro Tyr Thr Ser Gly Gly Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys Arg
245
<210> 54
<211> 12
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR H3
<400> 54
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
1 5 10
<210> 55
<211> 7
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L2
<400> 55
His Thr Ser Arg Leu His Ser
1 5
<210> 56
<211> 9
<212> белок
<213> Искусственная последовательность
<220>
<223> FMC63 CDR L3
<400> 56
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 57
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> IGH праймер
<400> 57
acacggcctc gtgtattact gt 22
<210> 58
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<223> IGH праймер
<400> 58
acctgaggag acggtgacc 19
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ, ИЗДЕЛИЯ И СПОСОБЫ, СВЯЗАННЫЕ С ДОЗИРОВАНИЕМ В КЛЕТОЧНОЙ ТЕРАПИИ | 2018 |
|
RU2776823C2 |
| СПОСОБЫ МОДУЛИРОВАНИЯ CART-КЛЕТОК | 2017 |
|
RU2774232C2 |
| СПОСОБЫ ПРОВЕДЕНИЯ ИММУНОТЕРАПИИ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА В КОМБИНАЦИИ С АГОНИСТОМ 4-1BB | 2019 |
|
RU2788524C2 |
| ПРОДУЦИРОВАНИЕ СКОНСТРУИРОВАННЫХ КЛЕТОК ДЛЯ АДОПТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ | 2017 |
|
RU2780156C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ ГЕННО-ИНЖЕНЕРНЫХ КЛЕТОК И РОДСТВЕННЫХ КОМПОЗИЦИЙ | 2018 |
|
RU2790444C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ СВЯЗАННЫХ С BCMA РАКОВЫХ ЗАБОЛЕВАНИЙ И АУТОИММУННЫХ РАССТРОЙСТВ | 2018 |
|
RU2799762C2 |
| ХИМЕРНЫЕ РЕЦЕПТОРЫ, СОДЕРЖАЩИЕ TRAF-6-ИНДУЦИРУЮЩИЕ ДОМЕНЫ, И СВЯЗАННЫЕ С НИМИ КОМПОЗИЦИИ И СПОСОБЫ | 2016 |
|
RU2773159C2 |
| СОЧЕТАНИЕ КЛЕТОЧНОЙ ТЕРАПИИ И ИММУНОМОДУЛЯТОРНОГО СОЕДИНЕНИЯ | 2018 |
|
RU2777911C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ВВЕДЕНИЯ ДОЗ АЛЛОГЕННЫХ T-КЛЕТОК С ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ | 2018 |
|
RU2776322C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ПОЛУЧЕНИЯ ГЕННО-ИНЖЕНЕРНЫХ КЛЕТОК | 2018 |
|
RU2795454C2 |
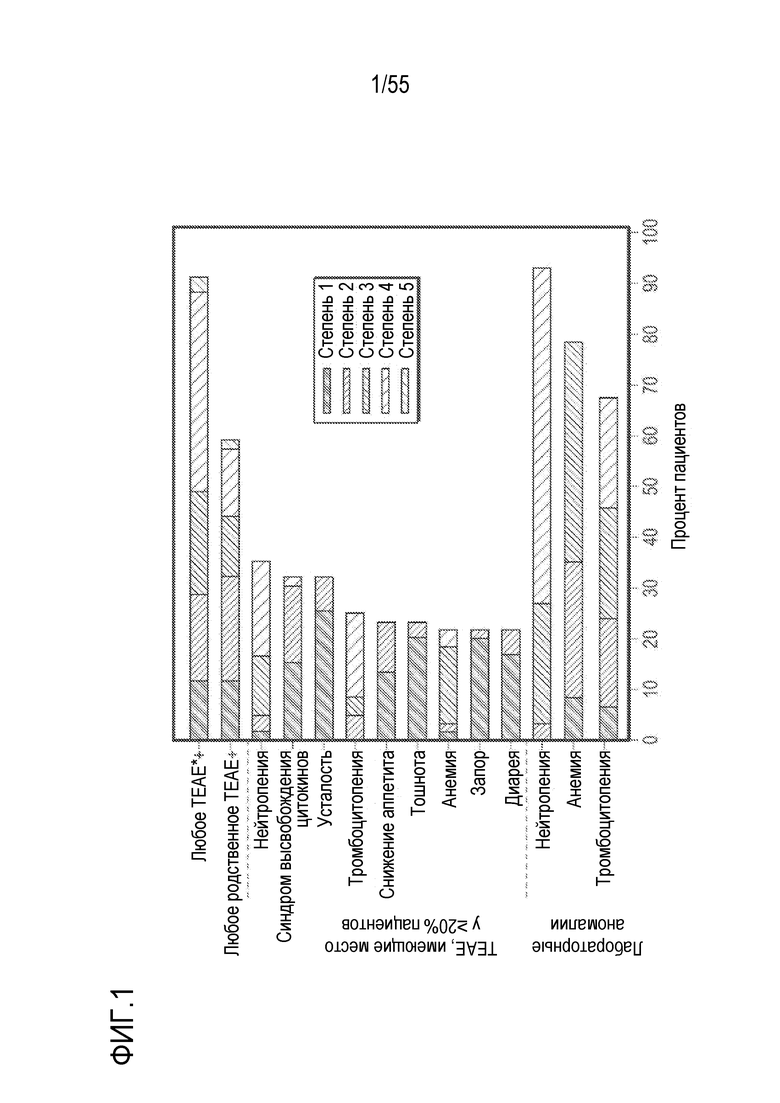



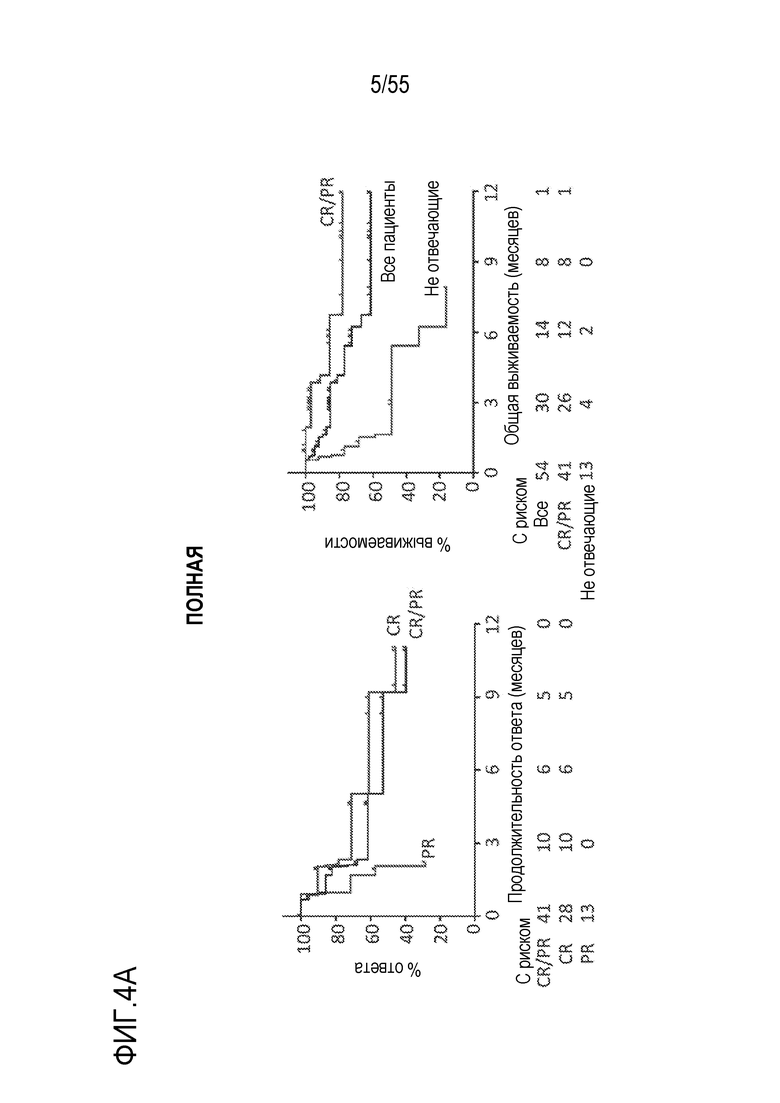


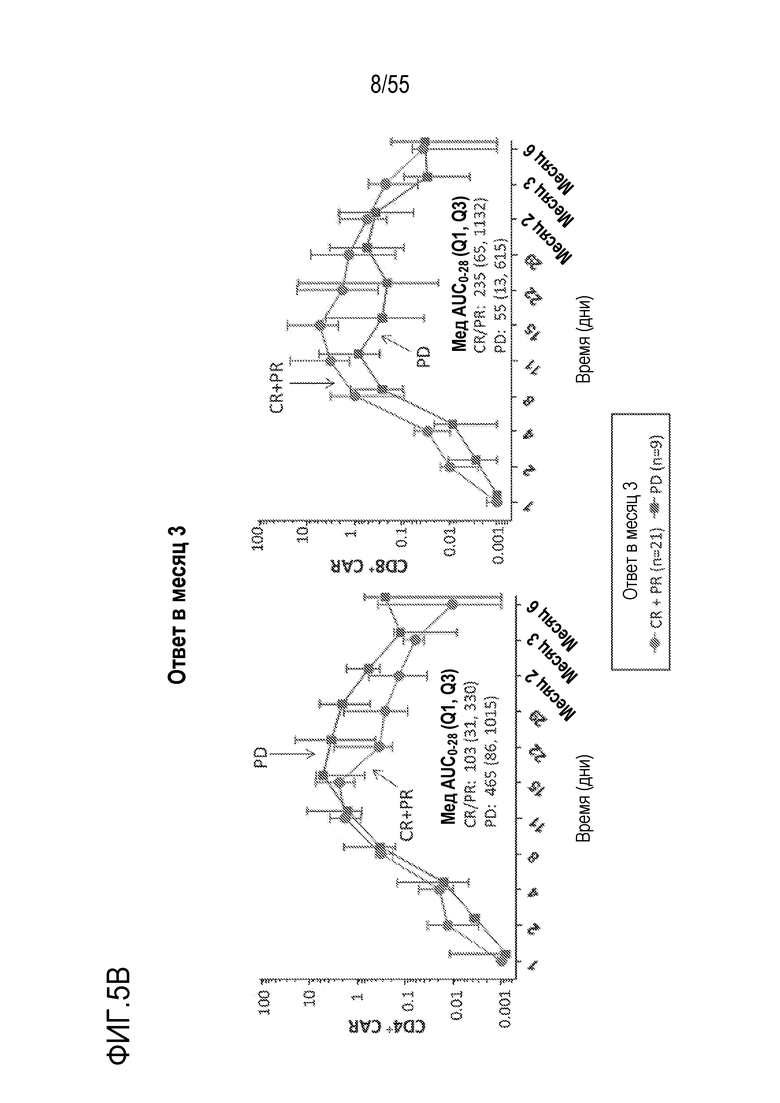


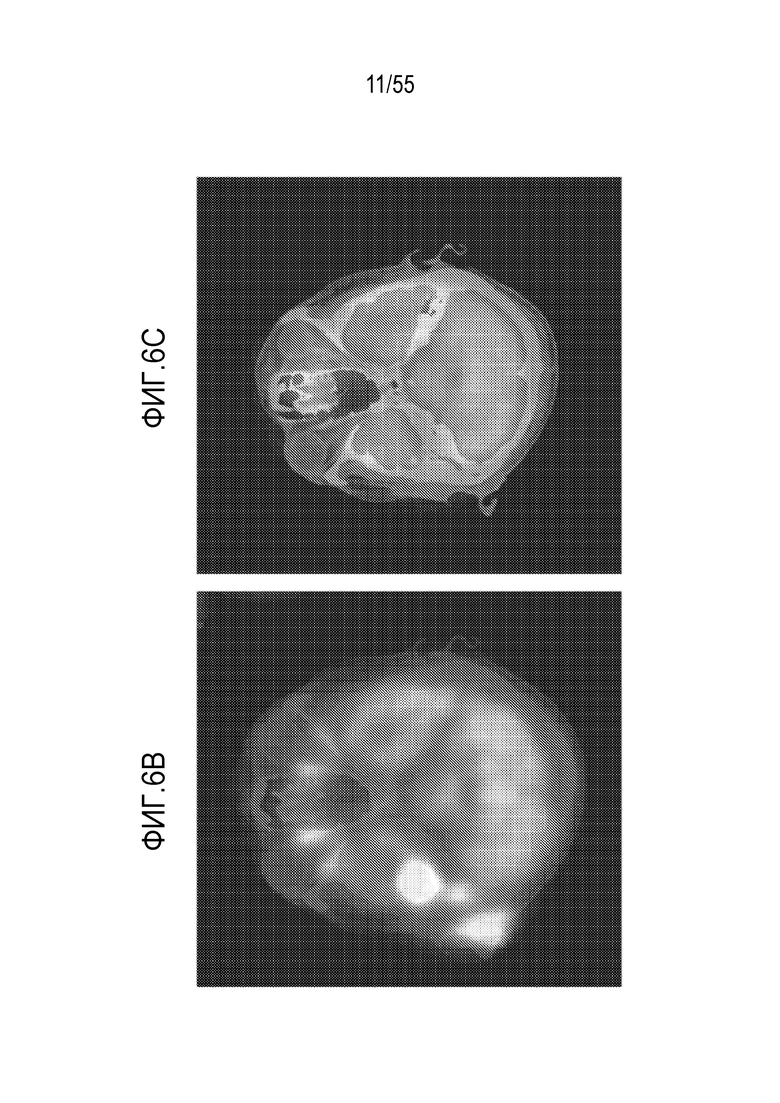




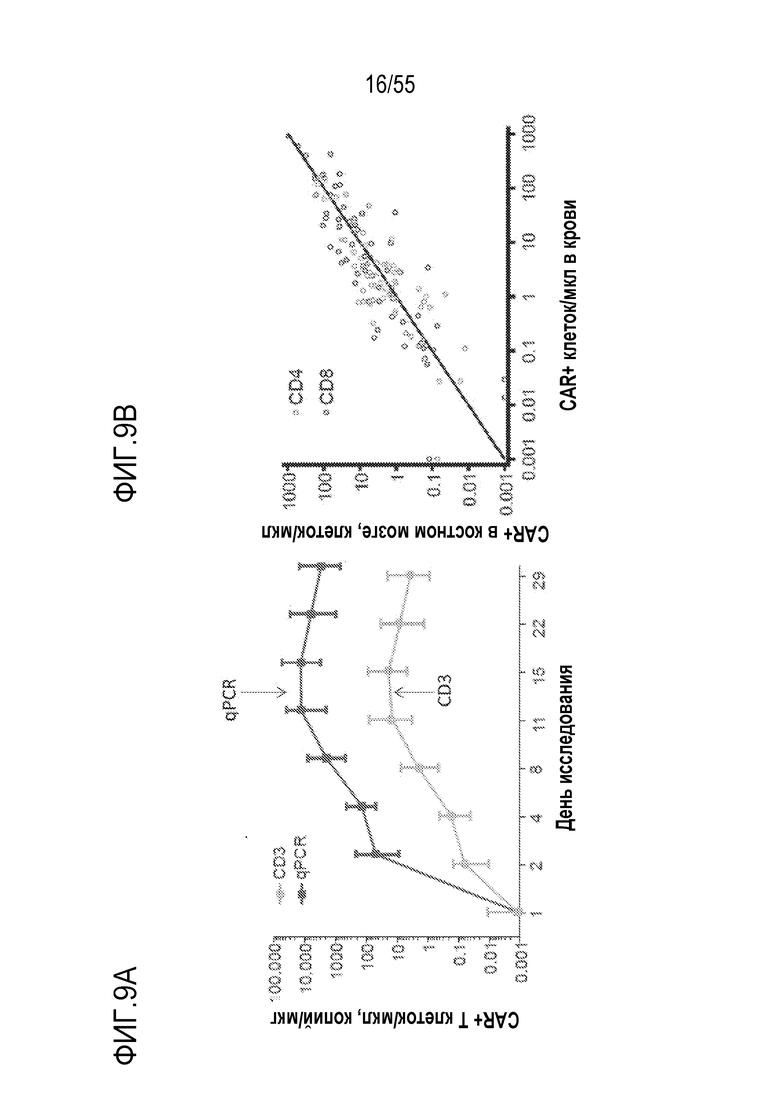


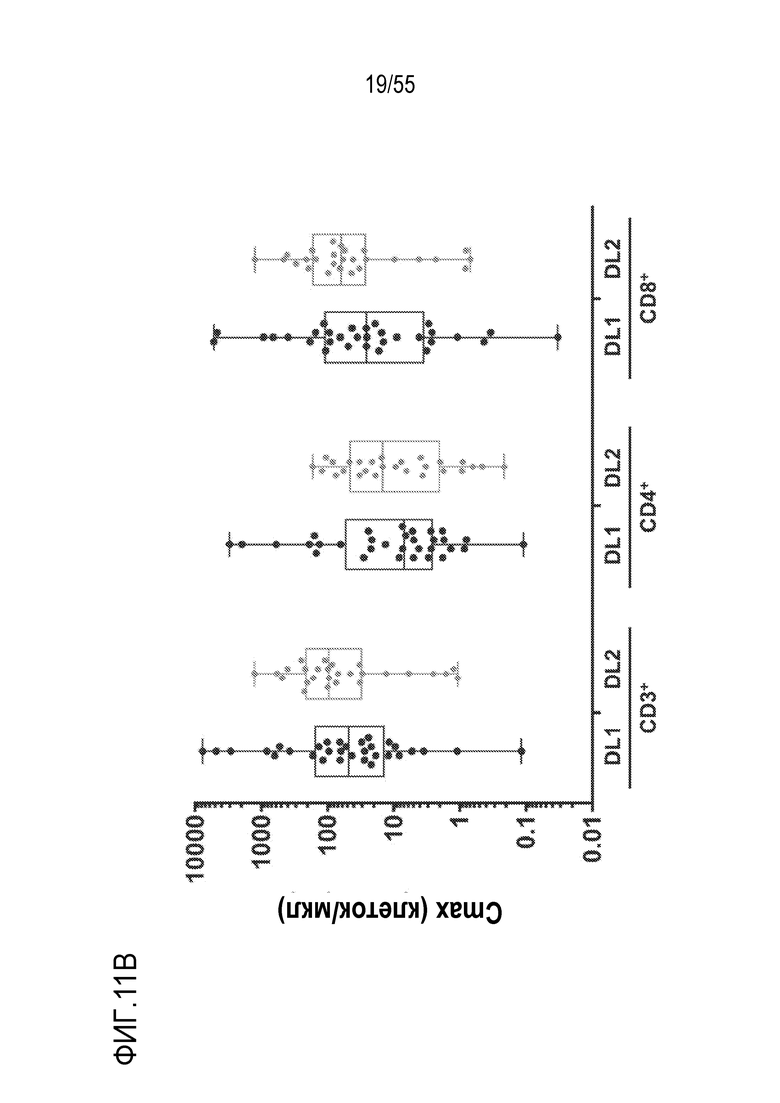


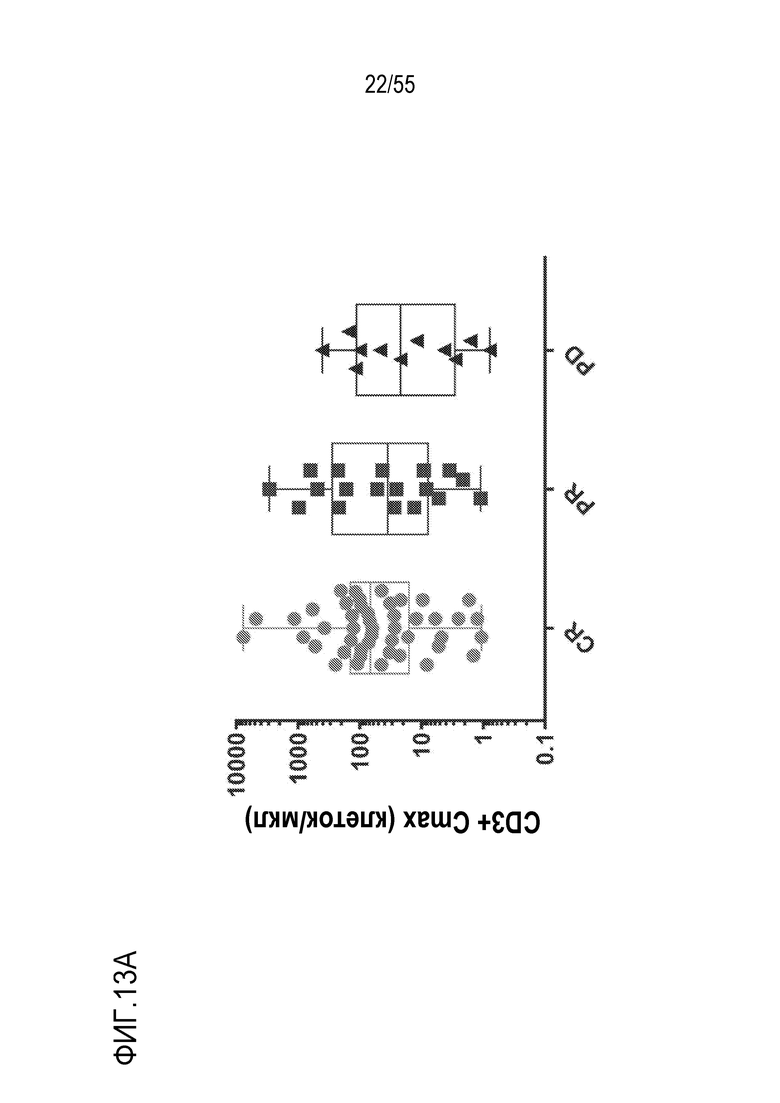
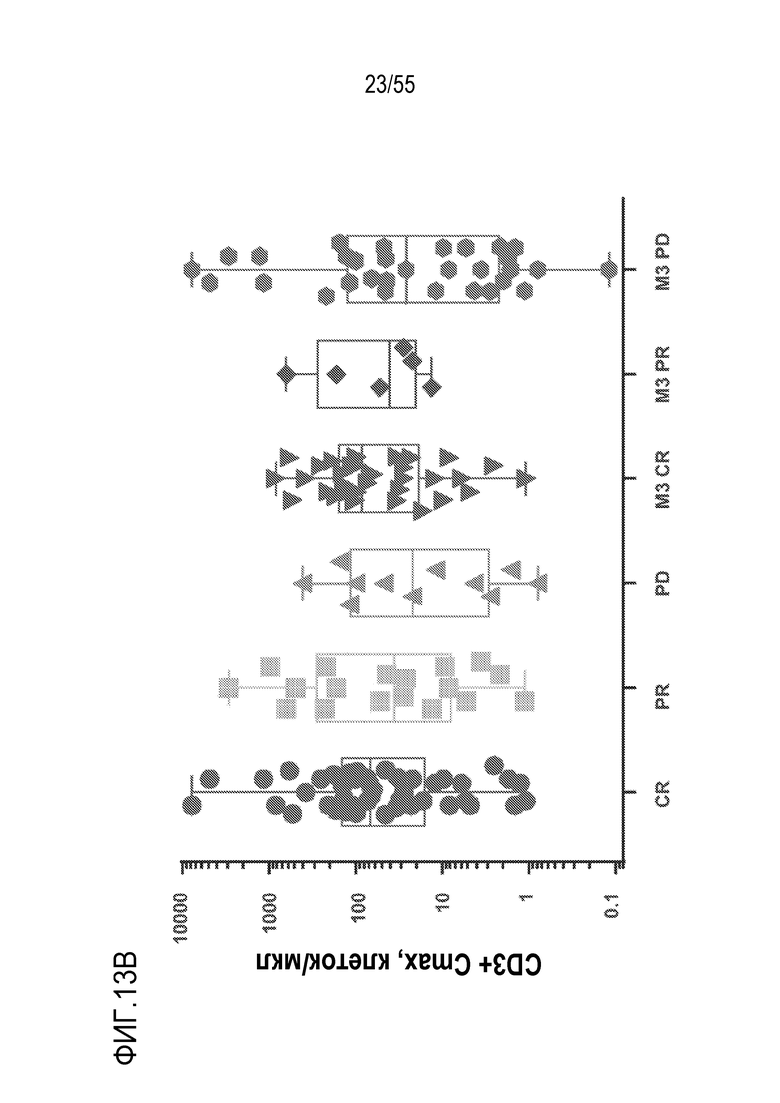
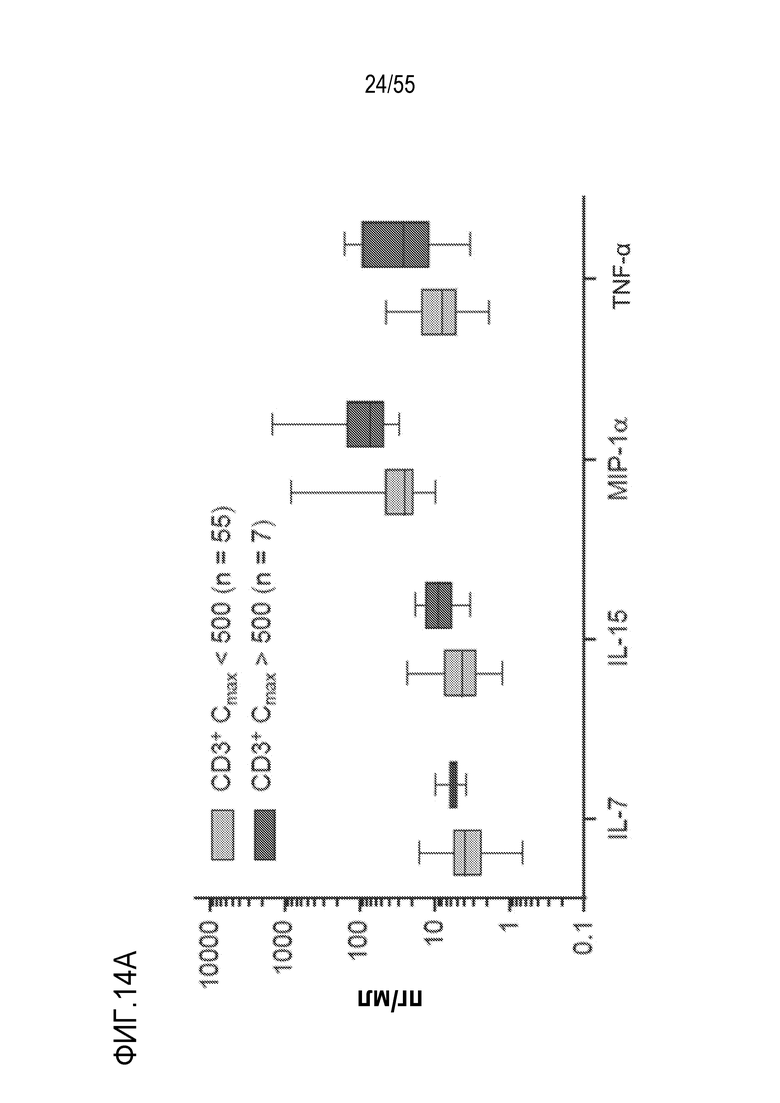



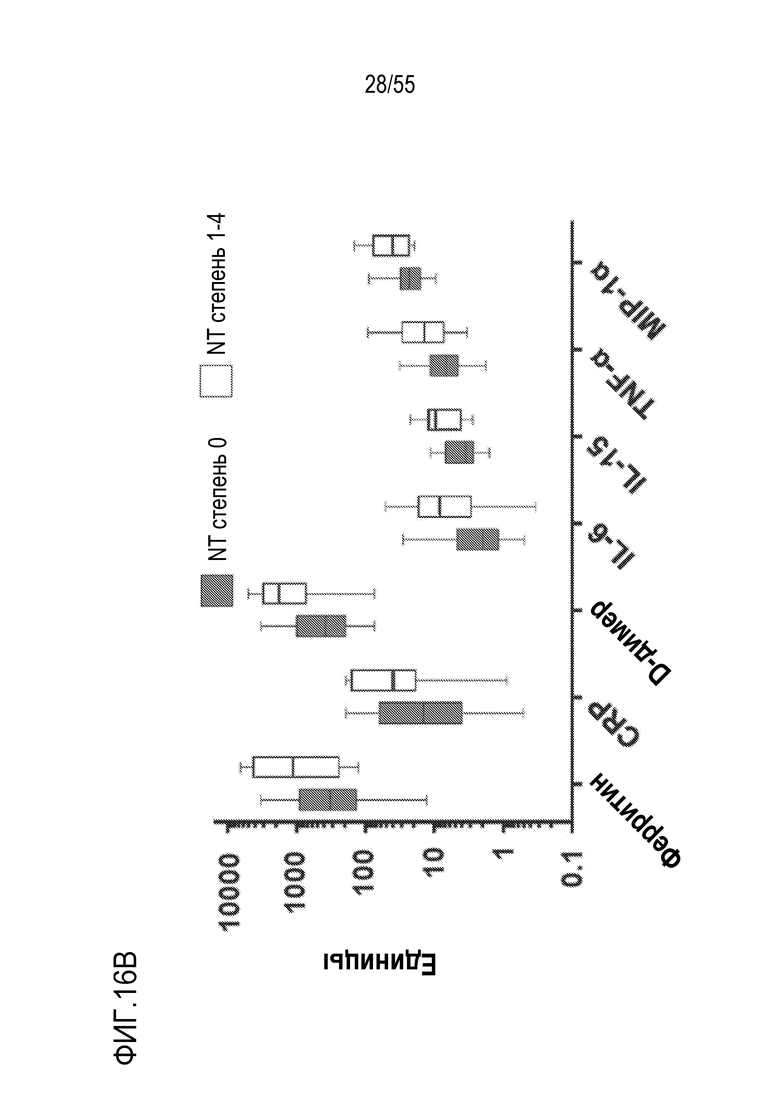
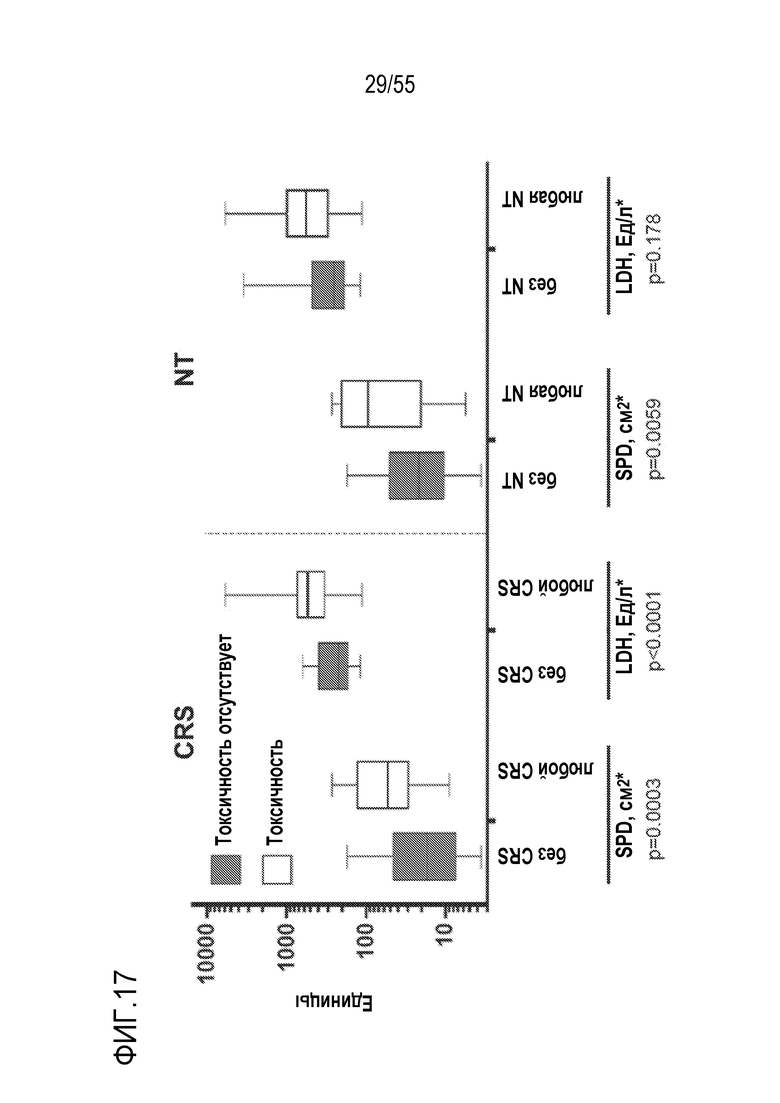

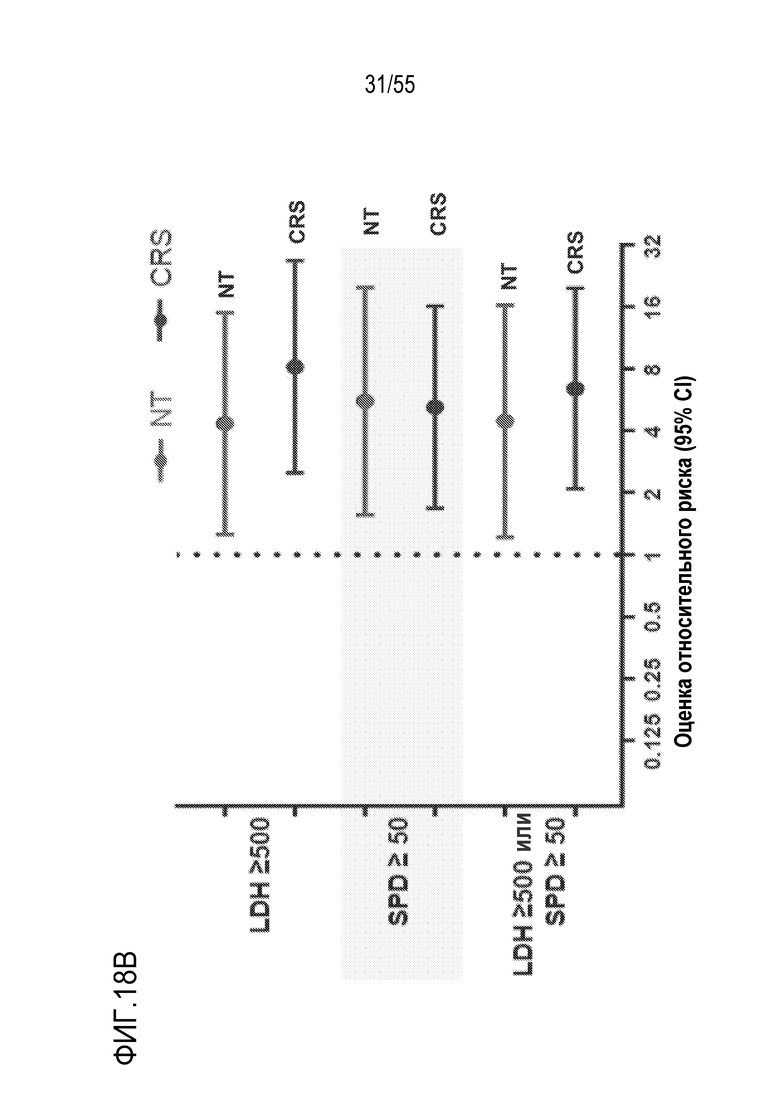





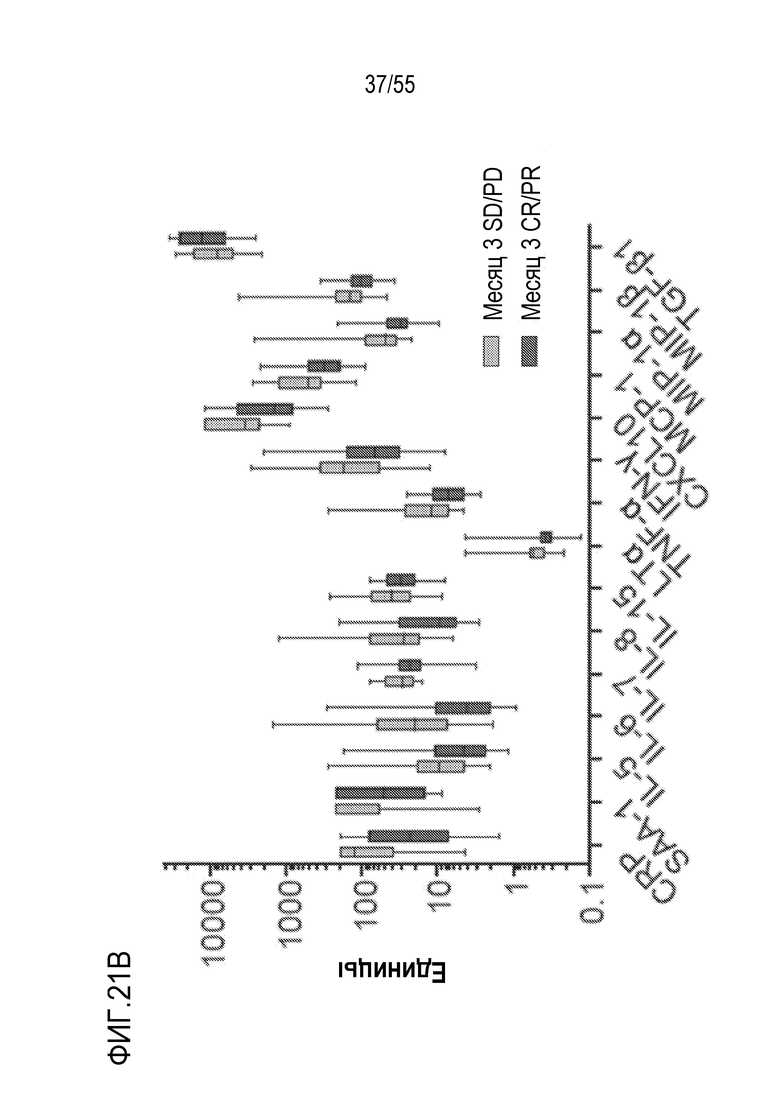
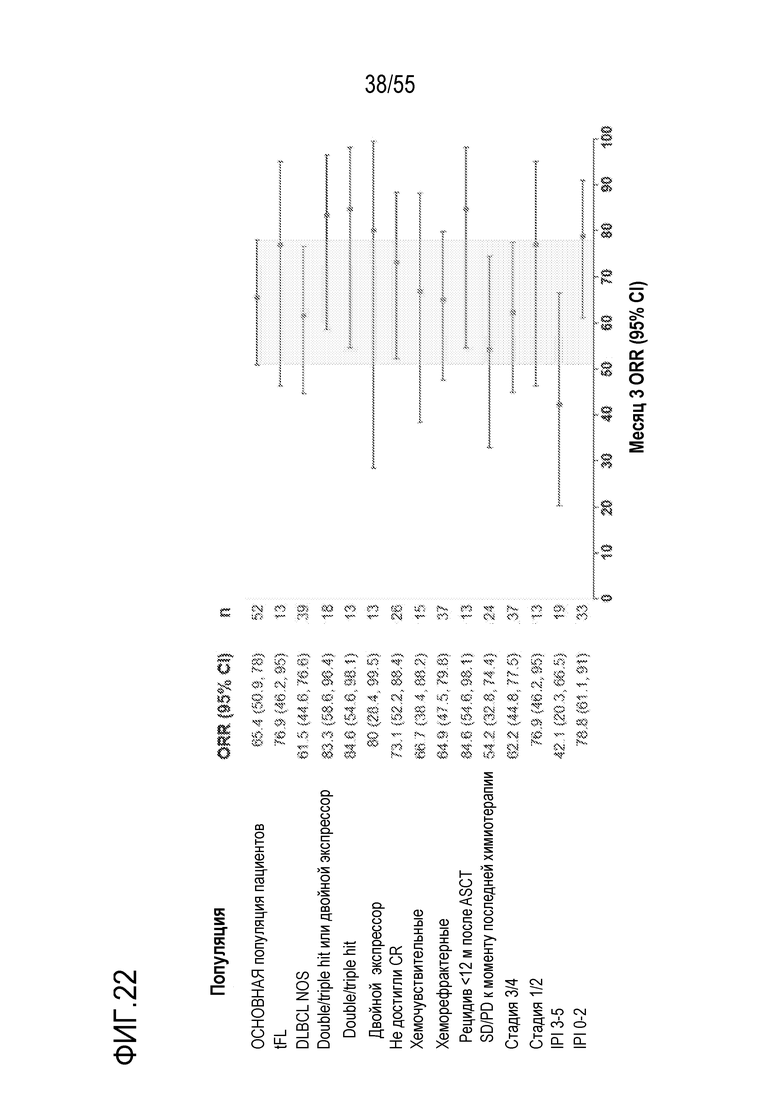
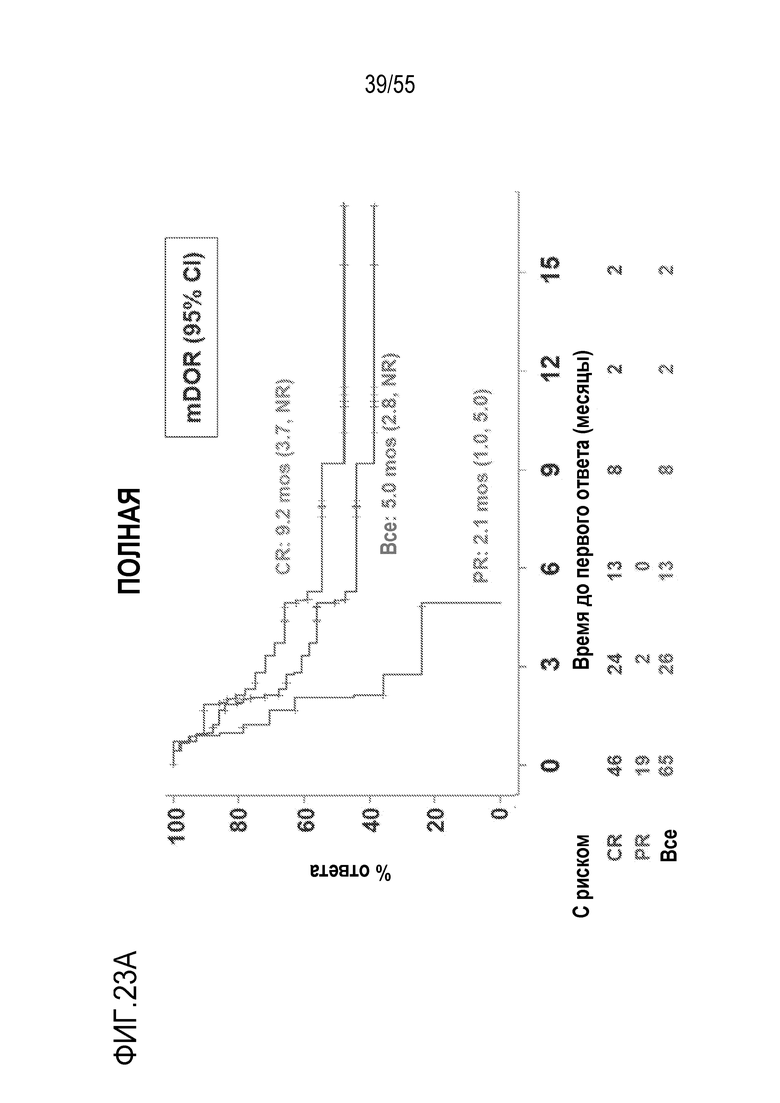

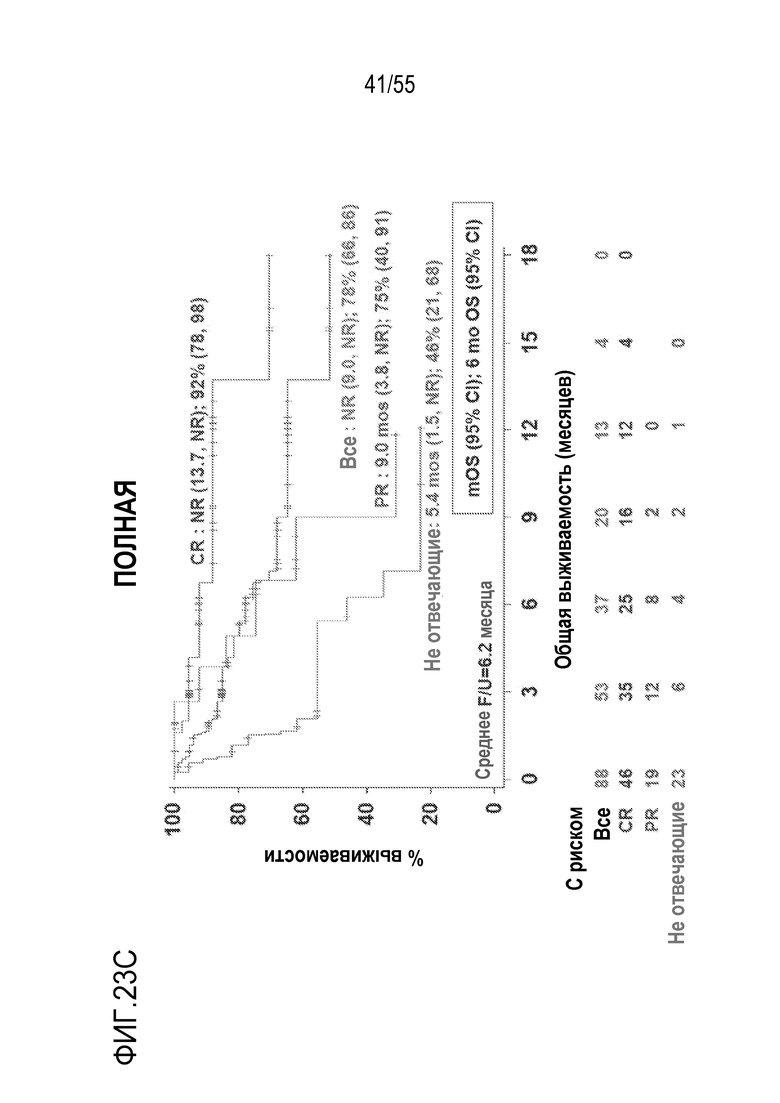






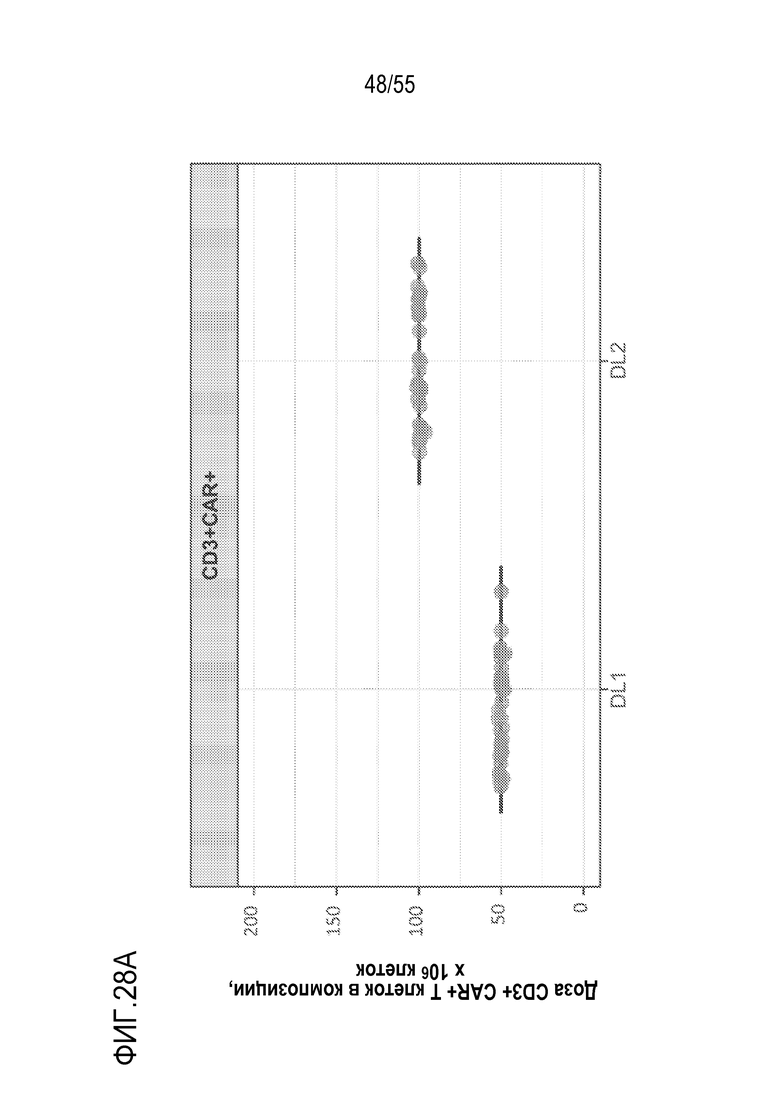


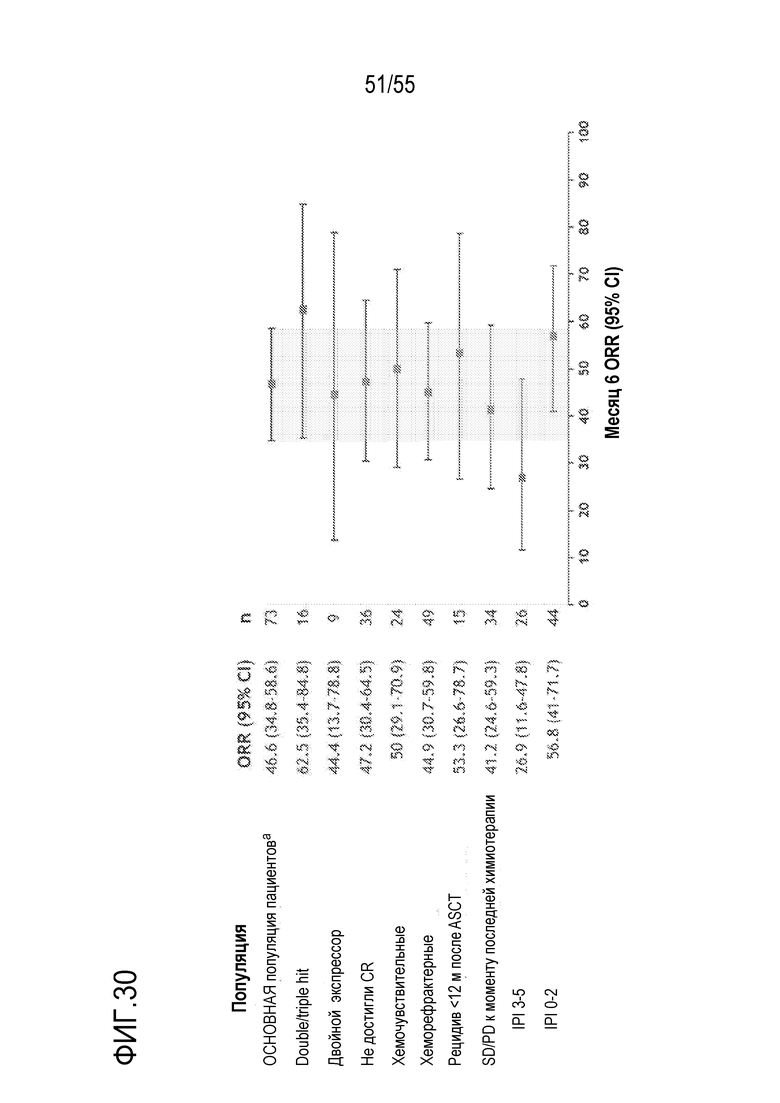




Изобретение относится к биотехнологии, клеточной биологии и медицине, в частности к способу лечения пациента, имеющего или подозреваемого в наличии CD19-экспрессирующей В-клеточной злокачественной опухоли с помощью адоптивной иммунотерапии. Для осуществления указанного способа лечения пациенту вводят дозу CD4+ и CD8+ Т-клеток путём введения множества отдельных композиций, а именно первой композиции, включающей одни из CD4+ Т-клеток и CD8+ Т-клеток, и второй композиции, включающей другие из CD4+ Т-клеток и CD8+ Т-клеток. Каждая из CD4+ и CD8+ Т-клеток, индивидуально, включает химерный антигенный рецептор (CAR), который связывается с CD19. А указанный CAR, содержащийся в CD4+ T-клетках и в CD8+ T-клетках, является одним и тем же. При этом введение первой композиции и второй композиции осуществляют с интервалом от приблизительно 0 до приблизительно 12 часов, с интервалом от приблизительно 0 до приблизительно 6 часов или с интервалом от приблизительно 0 до приблизительно 2 часов. Настоящее изобретение обеспечивает улучшенные подходы для лечения CD19-экспрессирующих В-клеточных злокачественных опухолей. 50 з.п. ф-лы, 63 ил., 27 табл., 6 пр.
1. Способ лечения пациента, имеющего или подозреваемого в наличии CD19-экспрессирующей В-клеточной злокачественной опухоли, включающий введение пациенту дозы CD4+ и CD8+ Т-клеток, причем каждая из CD4+ и CD8+ Т-клеток, индивидуально, включает химерный антигенный рецептор (CAR), который связывается с CD19, причем:
(а) CAR, содержащийся в CD4+ T-клетках и в CD8+ T-клетках является одним и тем же;
(b) введение включает введение множества отдельных композиций, причем множество отдельных композиций включает первую композицию, включающую одни из CD4+ Т-клеток и CD8+ Т-клеток, и вторую композицию, включающую другие из CD4+ Т-клеток и CD8+ Т-клеток; и
(с) введение первой композиции и второй композиции осуществляют с интервалом от приблизительно 0 до приблизительно 12 часов, с интервалом от приблизительно 0 до приблизительно 6 часов или с интервалом от приблизительно 0 до приблизительно 2 часов.
2. Способ по п. 1, в котором введение первой композиции и введение второй композиции осуществляют с интервалом от приблизительно 1 минуты до приблизительно 1 часа.
3. Способ по п. 1 или 2, в котором первую композицию и вторую композицию вводят с интервалом не более чем 2 часа.
4. Способ по любому из пп. 1-3, в котором первая композиция включает CD4+ Т-клетки.
5. Способ по любому из пп. 1-3, в котором первая композиция включает CD8+ Т-клетки.
6. Способ по любому из пп. 1-5, в котором введение первой композиции осуществляют до введения второй композиции.
7. Способ по любому из пп. 1-6, в котором доза CD4+ и CD8+ Т-клеток включает определенное отношение CD4+ клеток, экспрессирующих CAR, к CD8+ клеткам, экспрессирующим CAR, которое составляет от приблизительно 1:3 до приблизительно 3:1.
8. Способ по п. 7, в котором определенное отношение составляет или приблизительно составляет 1:1.
9. Способ по любому из пп. 1-8, в котором доза CD4+ и CD8+ Т-клеток составляет от приблизительно 1х105 общих клеток, экспрессирующих CAR, до приблизительно 5х108 общих клеток, экспрессирующих CAR.
10. Способ по любому из пп. 1-9, в котором доза CD4+ и CD8+ Т-клеток включает от или от приблизительно 1x107 и до или до приблизительно 2x108 общих экспрессирующих рекомбинантный рецептор Т-клеток включительно.
11. Способ по любому из пп. 1-10, в котором доза CD4+ и CD8+ Т-клеток составляет от приблизительно 1х107 общих клеток, экспрессирующих CAR, до приблизительно 1,5х108 общих клеток, экспрессирующих CAR.
12. Способ по любому из пп. 1-11, в котором В-клеточная злокачественная опухоль является миеломой, лейкозом или лимфомой.
13. Способ по любому из пп. 1-12, в котором В-клеточная злокачественная опухоль является острым лимфоцитарным лейкозом (ALL), ALL взрослых, хроническим лимфоцитарным лейкозом (CLL), неходжкинской лимфомой (NHL) или диффузной крупноклеточной В-клеточной лимфомой (DLBCL).
14. Способ по любому из пп. 1-13, в котором В-клеточная злокачественная опухоль представляет собой ALL.
15. Способ по любому из пп. 1-13, в котором В-клеточная злокачественная опухоль представляет собой ALL взрослых.
16. Способ по любому из пп. 1-13, в котором В-клеточная злокачественная опухоль представляет собой CLL.
17. Способ по любому из пп. 1-13, в котором В-клеточная злокачественная опухоль представляет собой NHL.
18. Способ по любому из пп. 1-13, в котором В-клеточная злокачественная опухоль представляет собой DLBCL.
19. Способ по любому из пп. 1-18, в котором CAR включает внеклеточный антигенраспознающий домен, специфично связывающийся с антигеном, и внутриклеточный сигнальный домен, включающий CD3-дзэта (CD3ζ) цепь и костимулирующую сигнальную область, которая является сигнальным доменом CD28 или 4-1BB.
20. Способ по любому из пп. 1-19, в котором Т-клетками являются первичные Т-клетки, полученные от пациента.
21. Способ по любому из пп. 1-20, в котором Т-клетки являются аутологичными для пациента.
22. Способ по любому из пп. 1-21, в котором пациент является или был идентифицирован как имеющий статус ECOG 0 или 1.
23. Способ по любому из пп. 1-22, в котором:
по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полного ответа (CR);
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR, показывают CR, который длится в течение 3 месяцев или более;
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR за один месяц и/или за три месяца, остается в состоянии ответа, остается в состоянии CR и/или остаются в живых или остаются в живых без прогрессии в течение 3 месяцев или более после достижения CR;
по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR);
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR, показывают OR, который длится в течение 3 месяцев или более;
по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, достигающих OR, остается в состоянии ответа или остаются в живых в течение 3 месяцев или более после достижения OR; или
по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70% пациентов, которые в момент или до введения дозы клеток имели или были идентифицированы как имеющие лимфому double/triple hit или рецидив после введения трансплантата аутологичных стволовых клеток (ASCT), достигли OR или OR, который длится в течение 3 месяцев или более.
24. Способ по любому из пп. 1-23, в котором более чем или более чем приблизительно 50%, приблизительно 60%, приблизительно 70% или приблизительно 80% пациентов, получающих лечение согласно способу, не показывают синдром высвобождения цитокинов (CRS) степени 3 или большей, не показывают нейротоксичность степени 3 или большей или более чем 40%, или 50%, или 55% не показывают нейротоксичности или CRS.
25. Способ по любому из пп. 1-24, в котором по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70% пациентов, которые в момент или до введения дозы клеток имели или были идентифицированы как имеющие лимфому double/triple hit или рецидив после введения трансплантата аутологичных стволовых клеток (ASCT), достигли OR или OR, который длится в течение 3 месяцев или более.
26. Способ по п. 25, в котором:
CR или OR длятся в течение более чем 3 месяца;
по меньшей мере 20%, по меньшей мере 25%, по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают CR, который длится в течение более чем 3 месяца;
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом и которые достигают CR, остаются в CR, или остаются в состоянии ответа, или остаются в живых в течение 3 месяцев или более;
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, получающих лечение в соответствии со способом, которые достигают CR за один месяц или за три месяца остаются в состоянии ответа, остаются в состоянии CR, остаются в живых или остаются в живых без прогрессии в течение 3 месяцев или более;
по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR);
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов достигают OR, который длится в течение 3 месяцев или более; или
по меньшей мере по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение в соответствии со способом и достигающих OR, остаются в состоянии ответа или остаются в живых в течение 3 месяцев или более.
27. Способ по любому из пп. 1-26, в котором:
в момент или до введения дозы клеток пациент является или был идентифицирован как имеющий лимфому, ассоциированную с или включающую участие центральной нервной системы (ЦНС); или
по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% пациентов, получающих лечение согласно способу, которые в момент или до введения дозы клеток показывали или были идентифицированы как имеющие лимфому с участием ЦНС, достигли устранения заболевания ЦНС.
28. Способ по любому из пп. 1-27, в котором в момент или до введения дозы клеток пациент имеет поражение мозга, необязательно поражение височной доли мозга.
29. Способ по любому из пп. 1-28, в котором:
по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу, достигают полного ответа (CR) или ремиссии заболевания ЦНС;
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, которые достигают CR, остаются в состоянии CR в течение 3 месяцев или более;
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих CR или ремиссии заболевания ЦНС за один месяц или за три месяца, остаются в состоянии ответа, остаются в состоянии CR, остаются в живых или остаются в живых без прогрессии в течение 3 месяцев или более;
по меньшей мере 50%, по меньшей мере 60% или по меньшей мере 70% пациентов, получающих лечение согласно способу, достигают объективного ответа (OR) или ремиссии заболевания ЦНС;
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов достигают OR, в течение 3 месяцев или более или в течение 6 месяцев или более;
по меньшей мере 60%, 70%, 80%, 90% или 95% пациентов, достигающих OR или ремиссии заболевания ЦНС, остаются в состоянии ответа или остаются в живых в течение 3 месяцев или более и/или в течение 6 месяцев или более;
поражение мозга уменьшается в размере или объеме более чем или более чем приблизительно на 25%, 50%, 75% или более; или
сокращение, или ремиссия, или клиренс заболевания ЦНС достигаются у по меньшей мере 35%, по меньшей мере 40% или по меньшей мере 50% пациентов, получающих лечение согласно способу.
30. Способ по любому из пп. 1-29, в котором:
более чем или более чем приблизительно 30%, 35%, 40% или 50% пациентов, получающих лечение согласно способу, не показывают синдрома высвобождения цитокинов (CRS) или нейротоксичности какой-либо степени;
по меньшей мере или приблизительно 45%, 50%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% пациентов, получающих лечение согласно способу, не показывают начало CRS ранее чем через 3 дня после введения или не показывают начало нейротоксичности ранее чем через 5 дней после введения; или
среднее начало нейротоксичности среди пациентов, получающих лечение согласно способу, происходит в момент или после среднего пика, или среднее время устранения CRS у пациентов, получающих лечение согласно способу, и/или среднее начало нейротоксичности среди пациентов, получающих лечение согласно способу, составляет более чем или приблизительно 8, 9, 10 или 11 дней.
31. Способ по любому из пп. 1-30, в котором до введения дозы клеток пациенту не вводили агент или средство для лечения, способное к лечению, предотвращению, задержке, ослаблению или уменьшению развития или риска развития токсичности после введения дозы клеток.
32. Способ по п. 28, в котором агент представляет собой или включает анти-IL-6 антитело, анти-IL-6R антитело или стероид.
33. Способ по п. 28 или 29, в котором агент представляет собой или включает стероид.
34. Способ по любому из пп. 31-33, в котором агент представляет собой или включает тоцилизумаб, силтуксимаб или дексаметазон.
35. Способ по любому из пп. 1-34, в котором:
введение и любой мониторинг осуществляют на амбулаторной основе или не требуя допуска или оставления на ночь в больнице; и
если пациент показывает длительное повышение температуры или повышение температуры, которое составляет или не было уменьшено на или не уменьшено более чем на 1ºC после лечения жаропонижающим средством, пациента госпитализируют или оставляют на ночь в больнице или вводят агент или средство для лечения для лечения или профилактики или сокращения или ослабления нейротоксичности или синдрома высвобождения цитокинов или риска этого.
36. Способ по любому из пп. 13, 17 и 19-35, в котором NHL выбрана из группы, состоящей из агрессивной NHL, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), NOS (de novo и трансформированной из вялотекущей), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), мантийноклеточной лимфомы (MCL) и/или фолликулярной лимфомы (FL), необязательно фолликулярной лимфомы стадии 3B (FL3B).
37. Способ по любому из пп. 13, 17 и 19-36, в котором NHL включает диффузную крупноклеточную В-клеточную лимфому (DLBCL), первичную медиастинальную крупноклеточную В-клеточную лимфому (PMBCL), NOS (de novo или трансформированную из вялотекущей лимфомы) или фолликулярную лимфому стадии 3B (FL3B).
38. Способ по любому из пп. 13, 17 и 19-37, в котором NHL включает DLBCL.
39. Способ по п. 38, в котором DLBCL не включает DLBCL, трансформированную из MZL и CLL (Рихтера), или пациент, которому вводят дозу клеток, имеет DLBCL, характеризуемую как de novo или трансформированную из вялотекущей, и/или не имеет DLBCL, трансформированную из MZL и CLL.
40. Способ по любому из пп. 13, 17 и 19-37, в котором NHL включает PMBCL.
41. Способ по любому из пп. 13, 17 и 19-37, в котором NHL включает NOS.
42. Способ по любому из пп. 13, 17 и 19-37, в котором NHL включает FL.
43. Способ по любому из пп. 1-21 и 23-42, в котором пациент является или был идентифицирован как имеющий статус 0, 1 или 2 согласно Eastern Cooperative Oncology Group Performance Status (ECOG).
44. Способ по любому из пп. 13, 17 и 19-43, в котором в момент или непосредственно перед введением дозы клеток пациент имел рецидив после ремиссии после лечения с или стал рефрактерным к одной или более предшествующим терапиям для лечения NHL кроме другой дозы клеток, экспрессирующих CAR.
45. Способ по любому из пп. 13, 17 и 19-44, в котором в момент или непосредственно перед введением дозы клеток пациент имел рецидив после ремиссии после лечения с или стал рефрактерным к двум или более предшествующим терапиям для лечения NHL кроме другой дозы клеток, экспрессирующих CAR.
46. Способ по любому из пп. 1-45, в котором в момент или до введения дозы клеток:
пациент является или был идентифицирован как имеющий лимфому double/triple hit;
пациент является или был идентифицирован как имеющий хеморефрактерную лимфому, необязательно хеморефрактерную DLBCL;
пациент не достиг полной ремиссии (CR) в ответ на предшествующую терапию; или
пациент имел рецидив в течение 1 года или спустя менее чем 1 год после получения трансплантата аутологичных стволовых клеток (ASCT).
47. Способ по любому из пп. 1-46, в котором CAR включает, в указанном порядке, scFv, специфичный для CD19, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, и цитоплазматический сигнальный домен, полученный из первичной сигнальной ITAM-содержащей молекулы.
48. Способ по любому из пп. 1-47, в котором CAR включает, в указанном порядке, scFv, специфичный для CD19, трансмембранный домен, цитоплазматический сигнальный домен, полученный из костимулирующей молекулы, которая представляет собой или содержит сигнальный домен 4-1BB, и цитоплазматический сигнальный домен, полученный из первичной сигнальной молекулы, содержащей ITAM, которая представляет собой сигнальный домен CD3-дзeta.
49. Способ по любому из пп. 1-48, в котором, до введения, пациента предварительно кондиционируют противолимфоцитарной терапией, включающей введение флударабина, циклофосфамида или флударабина и циклофосфамида.
50. Способ по любому из пп. 1-49, в котором введение дозы клеток осуществляют через амбулаторную доставку.
51. Способ по любому из пп. 1-50, в котором дозу клеток вводят парентерально, необязательно внутривенно.
| US 2016362472 A1, 15.12.2016 | |||
| WO 2016172606 A1, 27.10.2016 | |||
| WO 2016191756 A1, 01.12.2016 | |||
| US 2015283178 A1, 08.10.2015 | |||
| LANE K | |||
| LAW, What does it take to bind CAR?, Molecular therapy, Vol | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Коллекторный альтернатор многофазного тока с переменным числом периодов при постоянном числе оборотов | 1921 |
|
SU599A1 |
| КОМПОЗИЦИИ И СПОСОБЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2011 |
|
RU2623038C2 |
Авторы
Даты
2023-05-16—Публикация
2018-06-01—Подача