Перекрестная ссылка на родственные заявки
[1] Настоящая заявка испрашивает приоритет Временной заявки на патент США 62/538671, озаглавленной «РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ»” поданной 29 июля 2017 года; Временной заявки на патент США 62/596742, озаглавленной «РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ», поданной 8 декабря 2017 года; Временной заявки на патент США 62/628889, озаглавленной «РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ», поданной 9 февраля 2018 года; и Временной заявки на патент США 62/665468, озаглавленной «РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ», поданной 1 мая 2018 года; содержания которых тем самым включаются в качестве ссылок во всей своей полноте для всех целей.
Включение в качестве ссылки списка последовательностей
[2] Настоящая заявка подается вместе со Списком последовательностей в электронном формате. Список последовательностей предлагается как файл, озаглавленный 735042009640SeqList.TXT, созданный 27 июля 2018 года, который имеет размер 123336 байт. Информация в электронном формате Списка последовательностей включается в качестве ссылки во всей своей полноте.
Область техники, к которой относится изобретение
[3] Настоящее описание предлагает композиции и способы стимуляции, обогащения, размножения и/или активации генно-инженерных клеток, которые экспрессируют рекомбинантный рецептор, например, химерный рецептор антигена. В некоторых вариантах осуществления, предлагаемые способы включают ex vivo или in vitro стимуляцию, обогащение, размножение и/или активацию клеток посредством инкубирования вместе с частицами, например, сферическими частицами, с присоединенной связывающей молекулой, которая распознается или связывается рекомбинантным рецептором. В некоторых вариантах осуществления, присоединенная связывающая молекула представляет собой полипептид, например, полипептидный антиген или антиидиотипическое антитело, которое связывается с рекомбинантным рецептором. В некоторых вариантах осуществления, предлагаемые композиции можно использовать в способах приготовления клеток, например, генно-инженерных Т-лимфоцитов, для адоптивной иммунотерапии.
Уровень техники
[4] Доступны различные стратегии стимуляции или размножения популяций клеток in vitro или ex vivo, включая размножение антиген-специфичных Т-лимфоцитов in vitro для использования в адоптивной клеточной иммунотерапии или терапии рака. Необходимы улучшенные стратегии для стимуляции или размножения популяций клеток, включая исследовательские, диагностические и терапевтические цели. Предлагаются реагенты, способы и промышленные изделия, и наборы, которые удовлетворяют такие потребности.
Сущность изобретения
[5] В настоящем документе предлагается способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие рекомбинантный рецептор, антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген вместе с множеством частиц, каждая из множества частиц содержит связывающую молекулу, которая специфично связывается с антигенсвязывающим доменом, где связывание связывающей молекулы с антигенсвязывающим доменом индуцирует размножение клеток, содержащих рекомбинантный рецептор антигена, продуцируя тем самым выходную композицию, содержащую наращенные клетки. В некоторых вариантах осуществления, рекомбинантный рецептор антигена представляет собой химерный рецептор антигена (CAR). В некоторых вариантах осуществления, антигенсвязывающий домен содержит антитело или его антигенсвязывающий фрагмент. В некоторых случаях, антигенсвязывающий фрагмент представляет собой или содержит одноцепочечный фрагмент антитела. В некоторых вариантах осуществления, антигенсвязывающий фрагмент содержит вариабельные области антитела, соединенные гибким линкером. В некоторых из всех таких вариантов осуществления, антигенсвязывающий фрагмент представляет собой или содержит scFv.
[6] В некоторых из всех таких вариантов осуществления, антиген выбирается из интегрина αvβ6 (интегрина avb6), антигена созревания В-клеток (BCMA), B7-H3, B7-H6, угольной ангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, раково-тестикулярного антигена 1B (CTAG, известного также как NY-ESO-1 и LAGE-2), канцероэмбрионального антигена (CEA), циклина, циклина A2, лиганда 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, протеогликана хондроитин-4-сульфата (CSPG4), белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфрина B2, рецептора эфрина A2 (EPHa2), рецептора эстрогена, белка 5 подобного Fc-рецептору (FCRL5; также известного как гомолог 5 Fc-рецептора или FCRH5), рецептора фетального ацетилхолина (фетального AchR), фолатсвязывающего белка (FBP), рецептора фолата альфа, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), связанного с белком G рецептора 5D (GPRC5D), Her2/neu (тирозинкиназного рецептора erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеров erbB, высокомолекулярного антигена человека, ассоциированного с меланомой (HMW-MAA), поверхностного антигена гепатита B, антигена лейкоцита человека A1 (HLA-A1), антигена лейкоцита человека A2 (HLA-A2), рецептора IL-22 альфа(IL-22Ra), рецептора IL-13 альфа 2 (IL-13Ra2), домена рецептора вставки киназы (kdr), легкой цепи каппа, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, обогащенного лейцином повтора, содержащего член A семейства 8 (LRRC8A), антигена Ley, антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, мезотелина, c-Met, цитомегаловируса мышей (CMV), муцина 1 (MUC1), MUC16, лигандов элемента D группы природных киллеров 2 (NKG2D), мелана A (MART-1), молекулы адгезии нейральных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простата-специфичного антигена, антигена стволовых клеток простаты (PSCA), простата-специфичного мембранного антигена (PSMA), орфанного рецептора 1 подобного тирозинкиназному рецептору (ROR1), сурвивина, гликопротеина трофобластов (TPBG известного также как 5T4), ассоциированного с опухолью гликопротеина 72 (TAG72), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора 2 фактора роста эндотелия сосудов (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфичного или патоген-экспрессируемого антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекул, и/или молекул, экспрессируемых HIV, HCV, HBV, или другими патогенами.
[7] В некоторых из всех таких вариантов осуществления, антиген выбирается из ROR1, антигена созревания В-клеток (BCMA), угольной ангидразы 9 (CAIX), Her2/neu (тирозинкиназного рецептора erbB2), Ll-CAM, CD19, CD20, CD22, мезотелина, CEA и поверхностного антигена гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, фолатсвязывающего белка (FBP), FCRL5, FCRH5, рецептора фетального ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, домена рецептора вставки киназы (kdr), легкой цепи каппа, антигена Ley, молекулы клеточной адгезии L1, (L1-CAM), антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора IL-13 альфа 2 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора фолата a, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторов VEGF, 5T4, фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, антигена рака яичек, мезотелина, CMV мышей, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, канцероэмбрионального антигена (CEA), простата-специфичного антигена, PSMA, Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138, патоген-специфичного антигена и антигена, ассоциированного с универсальной меткой.
[8] В некоторых из всех таких вариантов осуществления, связывающая молекула не связывает или не распознает линкерную или спейсерную область рекомбинантного рецептора антигена, указанная линкерная или спейсерная область соединяет антигенсвязывающий домен с трансмембранным доменом рецептора антигена. В некоторых из всех таких вариантов осуществления, связывающая молекула представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом.
[9] В настоящем документе предлагается способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает антиген, вместе с множеством частиц, каждая из множества частиц, например, шариков, содержит связывающую молекулу, которая представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом, где связывание антиидиотипического антитела или его антигенсвязывающего фрагмента с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, продуцируя тем самым выходную композицию, содержащую наращенные клетки. В некоторых из всех таких вариантов осуществления, связывающая молекула содержит рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом.
[10] В настоящем документе предлагается способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает антиген, вместе с множеством частиц, например, шариков, каждая из множества частиц содержит связывающую молекулу, содержащую рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом, где связывание рекомбинантного антигена или его части с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки.
[11] В некоторых из всех таких вариантов осуществления, антиген выбирается из интегрина αvβ6 (интегрина avb6), антигена созревания В-клеток (BCMA), B7-H3, B7-H6, угольной ангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, раково-тестикулярного антигена 1B (CTAG, также известного как NY-ESO-1 и LAGE-2), канцероэмбрионального антигена (CEA), циклина, циклина A2, лиганда 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, протеогликана хондроитин-4-сульфата (CSPG4), белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфрина B2, рецептора эфрина A2 (EPHa2), рецептора эстрогена, белка 5 подобного Fc-рецептору (FCRL5; также известного как гомолог 5 Fc-рецептора или FCRH5), рецептора фетального ацетилхолина (фетального AchR), фолатсвязывающего белка (FBP), рецептора фолата альфа, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), глипикана-3 (GPC3), связанного с белком G рецептора 5D (GPRC5D), Her2/neu (тирозинкиназного рецептора erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеров erbB, высокомолекулярного антигена человека, ассоциированного с меланомой (HMW-MAA), поверхностного антигена гепатита B, антигена лейкоцита человека A1 (HLA-A1), антигена лейкоцита человека A2 (HLA-A2), рецептора IL-22 альфа(IL-22Rα), рецептора IL-13 альфа 2 (IL-13Rα2), домена рецептора вставки киназы (kdr), легкой цепи каппа, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, обогащенного лейцином повтора, содержащего член A семейства 8 (LRRC8A), антигена Ley, антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелина (MSLN), c-Met, цитомегаловируса мышей (CMV), муцина 1 (MUC1), MUC16, лигандов элемента D группы природных киллеров 2 (NKG2D), мелана A (MART-1), молекулы адгезии нейральных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простата-специфичного антигена, антигена стволовых клеток простаты (PSCA), простата-специфичного мембранного антигена (PSMA), орфанного рецептора 1 подобного тирозинкиназному рецептору (ROR1), сурвивина, гликопротеина трофобластов (TPBG также известного как 5T4), ассоциированного с опухолью гликопротеина 72 (TAG72), тирозиназа-зависимого белка 1 (TRP1, также известного как TYRP1 или gp75), тирозиназа-зависимого белка 2 (TRP2, также известного как допахромтаутомераза, допахром-дельта-изомераза или DCT), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора 2 фактора роста эндотелия сосудов (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфичного или патоген-экспрессируемого антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекул, и/или молекул, экспрессируемых HIV, HCV, HBV, или другими патогенами.
[12] В некоторых вариантах осуществления, рекомбинантный антиген выбирается из ROR1, антигена созревания В-клеток (BCMA), угольной ангидразы 9 (CAIX), Her2/neu (тирозинкиназного рецептора erbB2), Ll-CAM, CD19, CD20, CD22, мезотелина, CEA и поверхностного антигена гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, фолатсвязывающего белка (FBP), FCRL5, FCRH5, рецептора фетального ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, домена рецептора вставки киназы (kdr), легкой цепи каппа, антигена Ley, молекулы клеточной адгезии L1, (L1-CAM), антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора IL-13 альфа 2 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора фолата a, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторы VEGF, 5T4, Фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, антигена рака яичек, мезотелина, CMV мышей, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, канцероэмбрионального антигена (CEA), простата-специфичного антигена, PSMA, Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138 и патоген-специфичного антигена или части любого из указанных выше антигенов, распознаваемых антигенсвязывающим доменом. В некоторых случаях, рекомбинантный антиген представляет собой BCMA, CD22 или ROR1 или представляет собой его часть, распознаваемую антигенсвязывающим доменом.
[13] В некоторых из всех таких вариантов осуществления, часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, содержит внеклеточный домен или часть внеклеточного домена антигена. В некоторых из всех таких вариантов осуществления, часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, состоит в основном из внеклеточного домена или части внеклеточного домена антигена.
[14] В некоторых вариантах осуществления, в настоящем документе предлагается способ размножения клеток, включающий инкубирование исходной композиции, указанная исходная композиция содержит клетки, экспрессирующие химерный рецептор антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген, вместе с множеством частиц, которые представляют собой или содержат шарики, содержащие присоединенную связывающую молекулу, которая специфично связывает или распознает антигенсвязывающий домен, где (i) множество частиц происходит из композиции, имеющей концентрацию связывающей молекулы в пределах между или примерно между 0,5 мкг/мл и 500 мкг/мл, включительно, и, в ходе инкубирования, отношение клеток в целом, присутствующих в исходной композиции, ко множеству частиц составляет от или примерно от 5:1 до 1:5, включительно; и (ii) связывание связывающей молекулы с антигенсвязывающим доменом индуцирует размножение клеток, содержащий химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки.
[15] Также, в настоящем документе предлагается способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает антиген созревания В-клеток (BCMA), вместе с множеством частиц, например, шариков, каждая из множества частиц, например, шариков, содержит связывающую молекулу, содержащую внеклеточный домен BCMA или часть внеклеточного домена, распознаваемую антигенсвязывающим доменом, где связывание внеклеточного домена BCMA или его части с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки. В некоторых примерах, часть BCMA состоит в основном из внеклеточного домена или части внеклеточного домена.
[16] В некоторых из всех таких вариантов осуществления, связывающая молекула представляет собой слитый полипептид, содержащий рекомбинантный антиген или его часть, соединенную с некоторым остатком, где остаток необязательно, облегчает присоединение к частице. В некоторых случаях, остаток связывается с C-концом рекомбинантного антигена. В некоторых случаях, остаток является гидрофобным или обогащенным гидрофобными аминокислотами. В некоторых вариантах осуществления, остаток представляет собой или содержит Fc-домен. В некоторых примерах, Fc-область получают из IgG человека. В некоторых из всех таких вариантов осуществления, антиген представляет собой CD19.
[17] Также, в настоящем документе предлагается способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает CD19, вместе с множеством частиц, например, шариков, каждая из множества частиц содержит связывающую молекулу, которая представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом, где связывание антиидиотипического антитела или его антигенсвязывающего фрагмента с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки. В некоторых из всех таких вариантов осуществления, антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело SJ25C1 или его антигенсвязывающий фрагмент. В некоторых из всех таких вариантов осуществления, антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело FMC63 или его антигенсвязывающий фрагмент.
[18] В некоторых из всех таких вариантов осуществления, антигенсвязывающий фрагмент представляет собой или содержит scFv. В некоторых из всех таких вариантов осуществления, антиген или рекомбинантный антиген представляет собой антиген человека. В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит, по меньшей мере, часть константной области иммуноглобулина. В некоторых примерах, по меньшей мере, часть константной области иммуноглобулина содержит Fc-область или часть Fc, содержащую домены CH2 и CH3. В некоторых вариантах осуществления, константную область или Fc-область получают из IgG человека.
[19] В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент представляет собой интактное антитело или полноразмерное антитело. В некоторых из всех таких вариантов осуществления, связывающая молекула ковалентно или нековалентно связана с частицами, например, с шариками. В некоторых из всех таких вариантов осуществления, связывающая молекула присоединена к каждой из множества частиц, например, шариков, на С-концевом аминокислотном остатке связывающей молекулы или вблизи него, и/или присоединение связывающей молекулы к каждой из множества частиц, например, к шарику, осуществляется таким образом, что область или эпитоп связывающей молекулы, распознаваемый антигенсвязывающим доменом рецептора антигена, ориентируется таким образом, что он может распознаваться рецептором антигена.
[20] В некоторых из всех таких вариантов осуществления, частицы, например, шарики, представляют собой синтетические частицы, нерастворимые частицы, твердые частицы или представляют собой неклеточные частицы. В некоторых из всех таких вариантов осуществления, описанных в настоящем документе, частицы представляют собой шарики. В некоторых из всех таких вариантов осуществления, множество частиц содержит шарики. В некоторых из всех таких вариантов осуществления, частицы представляют собой или содержат один, или несколько полимеров или олигомеров и/или являются полимерными и/или олигомерными. В некоторых из всех таких вариантов осуществления, множество частиц содержит шарики, имеющие средний диаметр в пределах между или примерно между 1 мкм и 10 мкм или между или примерно между 2 мкм и 5 мкм. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, имеет средний диаметр примерно 2,8 мкм. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, имеет средний диаметр примерно 4,5 мкм. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, имеет среднюю плотность в пределах примерно между 0,5 г/см3 и 5,0 г/см3 или между или примерно между 1 г/см3 и примерно 2 г/см3. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, имеет среднюю плотность примерно 1,3 г/см3. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, имеет среднюю плотность примерно 1,5 г/см3.
[21] В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, является монодисперсным. В некоторых из всех таких вариантов осуществления, связывающая молекула ковалентно присоединена к частицам. В некоторых из всех таких вариантов осуществления, частица содержит поверхностно экспонируемую функциональную группу для присоединения связывающей молекулы, и/или при этом связывающая молекула ковалентно присоединена к частице посредством поверхностно экспонируемой функциональной группы.
[22] В некоторых из всех таких вариантов осуществления, поверхностно экспонируемая функциональная группа представляет собой амино группу, карбоксильную группу, тиольную группу, альдегидную группу, хлорметильную группу, эпокси группу, гидроксильную группу, тозильную группу или гидразиновую группу. В некоторых вариантах осуществления, поверхностно экспонируемая функциональная группа представляет собой тозильную группу.
[23] В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, является биологически совместимым или нетоксичным для клеток. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, содержит частицы, содержащие стекло, диоксид кремния, сложные полиэфиры гидроксикарбоновых кислот, полиангидриды дикарбоновых кислот, сополимеры гидроксикарбоновых кислот, сополимеры дикарбоновых кислот или металл. В некоторых из всех таких вариантов осуществления, частицы, например, шарики, имеют поверхность, содержащую полимер, полисахарид, диоксид кремния, жирную кислоту, углерод или их сочетание. В некоторых примерах, полимер представляет собой полиэтиленгликоль, сополимер молочная кислота - гликолевая кислота, полиглутаральдегид, полиуретан, полистирол и поливиниловый спирт или их сочетания. В некоторых из всех таких вариантов осуществления, множество частиц содержит частицы, имеющие гидрофобную поверхность. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, содержит частицы, имеющие полистирольную поверхность.
[24] В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, содержит частицы, которые являются магнитными и/или содержат магнитную сердцевину, парамагнитную сердцевину или суперпарамагнитную сердцевину.
[25] В некоторых из всех таких вариантов осуществления, частицы происходят из композиции, имеющей концентрацию связывающих молекул в пределах между или примерно между 0,5 мкг/мл и 500 мкг/мл, 1 мкг/мл и 200 мкг/мл или 5 мкг/мл и 100 мкг/мл, включительно. В некоторых из всех таких вариантов осуществления, частицы происходят из композиции, имеющей концентрацию связывающих молекул, по меньшей мере или, по меньшей мере, примерно 1 мкг/мл, 5 мкг/мл, 10 мкг/мл, 25 мкг/мл, 50 мкг/мл, 100 мкг/мл или 200 мкг/мл. В некоторых из всех таких вариантов осуществления, каждая из множества частиц, например, шариков, содержит, по меньшей мере или примерно, по меньшей мере, 10 копий, 102 копий, 103 копий, 104 копий, 105 копий или 106 копий связывающей молекулы.
[26] В некоторых из всех таких вариантов осуществления, по меньшей мере, часть инкубирования осуществляют в присутствии агента, который специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала. В некоторых из всех таких вариантов осуществления, агент предлагается вместе с частицами, например, шариками, необязательно, агент удерживается каждой из множества частиц или их подмножества. В некоторых из всех таких вариантов осуществления, агент предлагается отдельно от множества частиц, например, шариков.
[27] В некоторых из всех таких вариантов осуществления, частицы, например, шарики, дополнительно содержат агент, который специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала. В некоторых из всех таких вариантов осуществления, агент представляет собой лиганд или представляет собой антитело или его антигенсвязывающий фрагмент. В некоторых из всех таких вариантов осуществления, молекула представляет собой костимуляторную молекулу или представляет собой активирующий корецептор. В некоторых из всех таких вариантов осуществления, костимуляторная молекула или активирующий корецептор представляет собой OX-40, ICOS, DAP10, CD28 или 4-1BB. В некоторых вариантах осуществления, молекула представляет собой лиганд активирующего рецептора или корецептора, такого как OX-40L, ICOSL, B7-1, B7-2 или 4-1BBL. В некоторых из всех таких вариантов осуществления, молекула представляет собой ингибиторный рецептор. В некоторых примерах, ингибиторный рецептор представляет собой CTLA-4, PD-1, LAG-3, Tim-3, BTLA или TIGIT. В некоторых из всех таких вариантов осуществления, агент ковалентно присоединен к частицам, например, шарикам. В некоторых вариантах осуществления, молекула представляет собой лиганд ингибиторного рецептора, такого как PD-L1, PD-L2, CD155, CD112 или LIGHT.
[28] В некоторых из всех таких вариантов осуществления, отношение, необязательно, молярное или массовое отношение, связывающей молекулы и агента, удерживаемого частицами, например, шариками, составляет или составляет примерно 1:1. В некоторых из всех таких вариантов осуществления, отношение клеток в целом, присутствующих в исходной композиции, к частицам, например, шарикам, составляет от или примерно от 5:1 до 1:5, от 3:1 до 1:3 или от 2:1 до 1:2. В некоторых из всех таких вариантов осуществления, отношение клеток в целом, присутствующих в исходной композиции, к частицам, например, шарикам, составляет от или примерно от 1:0,1 до 1:5. В некоторых из всех таких вариантов осуществления, отношение клеток в целом, присутствующих в исходной композиции, к частицам, например, шарикам, составляет или составляет примерно 1:1.
[29] В некоторых из всех таких вариантов осуществления, инкубирование осуществляют в течение, по меньшей мере, или больше, или больше примерно 2 часов, 4 часов, 8 часов, 12 часов, 24 часов, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, 8 дней, 9 дней, 10 дней, 11 дней, 12 дней, 13 дней или 14 дней. В некоторых из всех таких вариантов осуществления, инкубирование осуществляют при температуре в пределах между или примерно между 30°C и 39°C, включительно. В некоторых из всех таких вариантов осуществления, инкубирование осуществляют при температуре 37° ± 2,0°C.
[30] В некоторых из всех таких вариантов осуществления, клетки включают иммунные клетки или индуцированные плюрипотентные стволовые клетки (iPSC). В некоторых из всех таких вариантов осуществления, иммунная клетка представляет собой Т-лимфоцит или NK-клетку. В некоторых из всех таких вариантов осуществления, клетки содержат Т-лимфоциты CD4+ и/или CD8+. В некоторых из всех таких вариантов осуществления, отношение клеток CD4+ к клеткам CD8+ составляет или составляет примерно 1:1, 1:2, 2:1, 1:3 или 3:1. В некоторых из всех таких вариантов осуществления, клетки представляют собой первичные клетки, полученные у субъекта, необязательно, у субъекта человека. В некоторых из всех таких вариантов осуществления, клетки представляют собой клетки человека.
[31] В некоторых из всех таких вариантов осуществления, исходная композиция получается с помощью способа, включающего приведение в контакт композиции клеток с молекулой нуклеиновой кислоты, кодирующей рекомбинантный рецептор антигена, при условиях для введения молекулы нуклеиновой кислоты в одну или несколько клеток в композиции.
[32] Также, в настоящем документе предлагается способ генной инженерии клеток, включающий приведение в контакт композиции клеток с молекулой нуклеиновой кислоты, кодирующей рекомбинантный рецептор антигена, при условиях введения молекулы нуклеиновой кислоты в одну или несколько клеток в композиции, тем самым продуцируя исходную композицию; и инкубирование клеток исходной композиции согласно способам, описанным в настоящем документе. В некоторых вариантах осуществления, по меньшей мере, часть приведения в контакт и инкубирования осуществляется одновременно.
[33] В некоторых из всех таких вариантов осуществления, молекула нуклеиновой кислоты включается в вирусный вектор, эписомальный вектор или транспозон. В некоторых из всех таких вариантов осуществления, приведение в контакт осуществляется с помощью переноса транспозонного/транспозазного гена. В некоторых из всех таких вариантов осуществления, приведение в контакт осуществляется посредством трансдуцирования вирусным вектором. В некоторых вариантах осуществления, вирусный вектор представляет собой ретровирус, который, необязательно, представляет собой гамма-ретровирусный вектор или лентивирусный вектор.
[34] В некоторых случаях, приведение в контакт включает стадию спинокуляции вирусного вектора вместе с композицией клеток. В некоторых случаях, спинокуляция включает вращение во внутренней полости камеры центрифуги частиц вирусного вектора и композиции клеток, где вращение происходит при относительной центробежной силе на внутренней поверхности боковой стенки полости, которая находится в пределах между или примерно между 500 g и 2500 g, 500 g и 2000 g, 500 g и 1600 g, 500 g, 1000 g, 600 g и 1600 g, 600 g и 1000 g, 1000 g и 2000 g или 1000 g и 1600 g, каждое включительно; или, по меньшей мере или, по меньшей мере, примерно 600 g, 800 g, 1000 g, 1200 g, 1600 g или 2000 g. В некоторых вариантах осуществления, спинокуляция осуществляется в течение времени, которое составляет примерно 5 минут или больше, примерно 10 минут или больше, примерно 15 минут или больше, примерно 20 минут или больше, примерно 30 минут или больше, примерно 45 минут или больше, примерно 60 минут или больше, примерно 90 минут или больше или примерно 120 минут или больше; или находится в пределах между или примерно между 5 минутами и 60 минутами, 10 минутами и 60 минутами, 15 минутами и 60 минутами, 15 минутами и 45 минутами, 30 минутами и 60 минутами или 45 минутами и 60 минутами, каждое, включительно.
[35] В некоторых из всех таких вариантов осуществления, приведение в контакт осуществляется в присутствии адъюванта трансдукции. В некоторых из всех таких вариантов осуществления, композиция клеток содержит множество Т-лимфоцитов и способ не включает, до приведения в контакт, стимуляции или активации Т-лимфоцитов.
[36] В некоторых из всех таких вариантов осуществления, композиция клеток содержит множество Т-лимфоцитов и способ не включает, до приведения в контакт, инкубирования композиции в присутствии агента или агентов, которые могут индуцировать сигнал через комплекс TCR и/или инкубирования в присутствии агента или агентов, которые могут индуцировать пролиферацию Т-лимфоцитов, Т-лимфоцитов CD4+ и/или Т-лимфоцитов CD8+; и/или CD3-связывающих молекул, CD28-связывающих молекул, рекомбинантного IL-2, рекомбинантного IL-15 и рекомбинантного IL-7 или их сочетания. В некоторых вариантах осуществления способ не включает, до приведения в контакт, стимуляции Т-лимфоцитов в присутствии антитела анти-CD3 и/или антитела анти-CD28.
[37] В некоторых из всех таких вариантов осуществления, композиция клеток содержит множество Т-лимфоцитов, указанное множество клеток получают из образца от субъекта, где приведение в контакт начинается не более, чем через 24 часа после получения образца от субъекта; и/или до приведения в контакт Т-лимфоциты не подвергаются воздействию температуры большей или большей примерно, чем 15°C, примерно 18°C, примерно 22°C или примерно 25°C в течение времени больше 1 часа, 2 часов, 4 часов, 6 часов, 8 часов, 12 часов или 24 часов после получения образца от субъекта; и/или до приведения в контакт Т-лимфоциты не подвергаются воздействию температуры равной, примерно равной, большей, чем или большей примерно, чем 37° ± 2,0°C в течение времени больше 15 минут, 30 минут, 1 часа или 2 часов после получения образца от субъекта. В некоторых из всех таких вариантов осуществления, до указанного приведения в контакт, не более 5%, 10%, 20%, 30% или 40% Т-лимфоцитов представляют собой активированные клетки, экспрессируют поверхностный маркер, селектированный из группы, состоящей из HLA-DR, CD25, CD69, CD71, CD40L и 4-1BB; имеют внутриклеточное экспрессирование цитокина, селектированного из группы, состоящей из IL-2, IFN-гамма, TNF-альфа, находятся в фазе G1 или в более поздней фазе клеточного цикла и/или способны к пролиферации.
[38] В некоторых из всех таких вариантов осуществления, способ дополнительно включает, перед инкубированием или приведением в контакт, получение биологического образца от субъекта, содержащего клетки, и, необязательно, селекцию или обогащение клеток, необязательно, Т-лимфоцитов, из образца. В некоторых из всех таких вариантов осуществления, процент клеток, экспрессирующих рекомбинантный рецептор, антигена, в исходной композиции меньше или меньше примерно 75%, 70%, 60%, 50%, 40%, 30%, 20%, 15%, 10% или меньше. В некоторых из всех таких вариантов осуществления, композиция клеток или исходная композиция содержит, по меньшей мере или, по меньшей мере, примерно 1 × 102 клеток, 1 × 103 клеток, 1 × 104 клеток, 1 × 105 клеток, 1 × 106 клеток или 1 × 107 клеток.
[39] В некоторых из всех таких вариантов осуществления, поверхностное экспрессирование маркера активации или маркера истощения клеток, присутствующих в выходной композиции, меньше, чем поверхностное экспрессирование маркера в композиции клеток, продуцируемой после сходного инкубирования, но в присутствии поликлональной стимуляторной молекулы, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В некоторых случаях, маркер истощения представляет собой ингибиторный рецептор. В некоторых случаях, маркер истощения представляет собой PD-1, CTLA-4, TIM-3, LAG-3, BTLA или TIGIT. В некоторых примерах, маркер активации представляет собой HLA-DR, CD25, CD69, CD71, CD40L или 4-1BB. В некоторых из всех таких вариантов осуществления, поверхностное экспрессирование является, по меньшей мере или, по меньшей мере, примерно 1,2-кратным, 1,5-кратным, 2,0-кратным, 3,0-кратным, 4,0-кратным, 5,0-кратным, 10,0-кратным или больше.
[40] В некоторых из всех таких вариантов осуществления, количество клеток в выходной композиции, по существу, такое же или больше, чем количество клеток в композиции клеток, полученной с помощью сходного инкубирования, но в присутствии поликлональной стимуляторной молекулы, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В некоторых из всех таких вариантов осуществления, поликлональная стимуляторная молекула содержит антитело анти-CD3 или его фрагмент и/или антитело анти-CD28 или его фрагмент.
[41] В некоторых из всех таких вариантов осуществления, количество клеток в выходной композиции превышает количество клеток в исходной композиции, больше, чем или больше примерно, чем 1,2-кратно, 1,5-кратно, 2,0-кратно, 3,0-кратно, 4,0-кратно, 5,0-кратно, 10,0-кратно, 25-кратно, 50-кратно, 100-кратно или больше. В некоторых из всех таких вариантов осуществления, процент клеток, содержащих рекомбинантный рецептор антигена, в выходной композиции больше или больше примерно 50%, 60%, 70%, 80%, 90%, 95%, или больше. В некоторых из всех таких вариантов осуществления, количество клеток в выходной композиции, содержащих рекомбинантный рецептор антигена, повышается или обогащается 1,2-кратно, 2,0-кратно, 3,0-кратно, 4,0-кратно, 5,0-кратно, 6,0-кратно, 7,0-кратно, 8,0-кратно, 9,0-кратно, 10-кратно, или больше по сравнению с количеством клеток, содержащих рецептор антигена, в исходной композиции.
[42] В некоторых из всех таких вариантов осуществления, по меньшей мере, часть инкубирования осуществляется в присутствии одного или нескольких дополнительных агентов, которые модулируют размножение или активность клеток. В некоторых случаях, один или несколько дополнительных агентов представляют собой леналидомид.
[43] В некоторых из всех таких вариантов осуществления, способ осуществляется in vitro или ex vivo. В некоторых из всех таких вариантов осуществления, рецептор антигена представляет собой CAR, и CAR дополнительно содержит внутриклеточный сигнальный домен, содержащий ITAM. В некоторых случаях, внутриклеточный сигнальный домен содержит внутриклеточный домен цепи CD3-зета (CD3ζ). В некоторых вариантах осуществления, CAR дополнительно содержит костимуляторную сигнальную область. В некоторых аспектах, костимуляторная сигнальная область содержит сигнальный домен CD28 или 4-1BB. В некоторых примерах, костимуляторный домен представляет собой CD28. В некоторых из всех таких вариантов осуществления, способ дополнительно включает удаление множества частиц, например, шариков, из выходной композиции.
[44] В настоящем документе предлагается композиция клеток, получаемых с помощью любого из способов, предлагаемых в настоящем документе. Также, в настоящем документе предлагается поверхностно модифицированная частица, содержащая частицу и связывающую молекулу, связанную с поверхностью частицы, где связывающая молекула специфично связывается с внеклеточным антигенсвязывающим доменом рецептора антигена. В некоторых вариантах осуществления, рецептор антигена представляет собой химерный рецептор антигена (CAR). В некоторых вариантах осуществления, связывающая молекула не связывает или не распознает линкерную или спейсерную область рекомбинантного рецептора антигена, указанная линкерная или спейсерная область, соединяет антигенсвязывающий домен с трансмембранным доменом рецептора антигена.
[45] В некоторых из всех таких вариантов осуществления, рекомбинантный антиген выбирается из интегрина αvβ6 (интегрина avb6), антигена созревания В-клеток (BCMA), B7-H3, B7-H6, угольной ангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, раково-тестикулярного антигена 1B (CTAG, также известного как NY-ESO-1 и LAGE-2), канцероэмбрионального антигена (CEA), циклина, циклина A2, лиганда 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, протеогликан 4хондроитин-4-сульфат (CSPG4), белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфрина B2, рецептора эфрина A2 (EPHa2), рецептора эстрогена, белка 5 подобного Fc-рецептору (FCRL5; также известного как гомолог 5 Fc-рецептора или FCRH5), рецептора фетального ацетилхолина (фетального AchR), фолатсвязывающего белка (FBP), рецептора фолата альфа, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), глипикана-3 (GPC3), связанного с белком G рецептора 5D (GPRC5D), Her2/neu (тирозинкиназного рецептора erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеров erbB, высокомолекулярного антигена человека, ассоциированного с меланомой (HMW-MAA), поверхностного антигена гепатита B, антигена лейкоцита человека A1 (HLA-A1), антигена лейкоцита человека A2 (HLA-A2), рецептора IL-22 альфа(IL-22Rα), рецептора IL-13 альфа 2 (IL-13Rα2), домена рецептора вставки киназы (kdr), легкой цепи каппа, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, обогащенного лейцином повтора, содержащего член A семейства 8 (LRRC8A), антигена Ley, антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелина (MSLN), c-Met, цитомегаловируса мышей (CMV), муцина 1 (MUC1), MUC16, лигандов элемента D группы природных киллеров 2 (NKG2D), мелана A (MART-1), молекулы адгезии нейральных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простата-специфичного антигена, антигена стволовых клеток простаты (PSCA), простата-специфичного мембранного антигена (PSMA), орфанного рецептора 1 подобного тирозинкиназному рецептору (ROR1), сурвивина, гликопротеина трофобластов (TPBG также известного как 5T4), ассоциированного с опухолью гликопротеина 72 (TAG72), тирозиназа-зависимого белка 1 (TRP1, также известного как TYRP1 или gp75), тирозиназа-зависимого белка 2 (TRP2, также известного как допахромтаутомераза, допахром-дельта-изомераза или DCT), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора 2 фактора роста эндотелия сосудов (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфичного или патоген-экспрессируемого антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекул, и/или молекул, экспрессируемых HIV, HCV, HBV, или другими патогенами.
[46] В некоторых из всех таких вариантов осуществления, связывающая молекула содержит рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом. В некоторых аспектах, рекомбинантный антиген выбирается из ROR1, антигена созревания В-клеток (BCMA), угольной ангидразы 9 (CAIX), Her2/neu (тирозинкиназного рецептора erbB2), Ll-CAM, CD19, CD20, CD22, мезотелина, CEA и поверхностного антигена гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, фолатсвязывающего белка (FBP), FCRL5, FCRH5, рецептора фетального ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, домена рецептора вставки киназы (kdr), легкой цепи каппа, антигена Ley, молекулы клеточной адгезии L1, (L1-CAM), антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора IL-13 альфа 2 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора фолата a, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторов VEGF, 5T4, фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, антигена рака яичек, мезотелина, CMV мышей, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, канцероэмбрионального антигена (CEA), простата-специфичного антигена, PSMA, Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138 и патоген-специфичного антигена или части любого из указанных выше антигенов, распознаваемых антигенсвязывающим доменом.
[47] В некоторых вариантах осуществления, рекомбинантный антиген представляет собой CD19, BCMA, CD22 или ROR1 или представляет собой их часть, распознаваемую антигенсвязывающим доменом. В некоторых из всех таких вариантов осуществления, часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, содержит внеклеточный домен или часть внеклеточного домена антигена. В некоторых из всех таких вариантов осуществления, часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, состоит в основном из внеклеточного домена или части внеклеточного домена антигена.
[48] В настоящем документе предлагается поверхностно модифицированная частица, содержащая частицу и связывающую молекулу, связанную с поверхностью частицы, где связывающая молекула содержит внеклеточный домен или его часть от антигена созревания В-клеток (BCMA). В некоторых из всех таких вариантов осуществления, связывающая молекула представляет собой слитый полипептид, содержащий рекомбинантный антиген или его часть, связанную с остатком, где остаток необязательно, облегчает присоединение к частице. В некоторых случаях, остаток связан C-концом рекомбинантного антигена. В некоторых вариантах осуществления, остаток является гидрофобным или обогащенным гидрофобными аминокислотами.
[49] В некоторых из всех таких вариантов осуществления, остаток представляет собой или содержит Fc-домен. В некоторых случаях, Fc-область получают из IgG человека. В некоторых из всех таких вариантов осуществления, рекомбинантный антиген представляет собой антиген человека.
[50] В некоторых из всех таких вариантов осуществления, связывающая молекула содержит антиидиотипическое антитело или его антигенсвязывающий фрагмент. В некоторых из всех таких вариантов осуществления, антиген, распознаваемый антигенсвязывающим доменом, представляет собой CD19. В некоторых из всех таких вариантов осуществления, антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело SJ25C1 или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления, антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело FMC63 или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления, антигенсвязывающий фрагмент представляет собой или содержит scFv.
[51] В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит, по меньшей мере, часть константной области иммуноглобулина. В некоторых случаях, по меньшей мере, часть константной области иммуноглобулина содержит Fc-область или часть Fc, содержащую домены CH2 и CH3. В некоторых вариантах осуществления, константная область или Fc-область получают из IgG человека. В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент представляет собой интактное антитело или полноразмерное антитело.
[52] В некоторых из всех таких вариантов осуществления, связывающая молекула ковалентно или нековалентно присоединена к частицам, например, шарикам. В некоторых из всех таких вариантов осуществления, связывающая молекула присоединена к каждой из множества частиц, например, шариков, на С-концевом аминокислотном остатке связывающей молекулы или вблизи него и/или присоединение связывающей молекулы к каждой из множества частиц, например, шариков, осуществляется таким образом, что область или эпитоп связывающей молекулы, распознаваемый антигенсвязывающим доменом рецептора антигена, ориентируется таким образом, что он может распознаваться рецептором антигена. В некоторых из всех таких вариантов осуществления, частицы, например, шарики, представляют собой синтетические частицы, нерастворимые частицы, твердые частицы или представляют собой неклеточные частицы.
[53] В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, содержит шарики. В некоторых из всех таких вариантов осуществления, частица имеет диаметр в пределах между или примерно между 1 мкм и 10 мкм или между или примерно между 2 мкм и 5 мкм, каждое, включительно. В некоторых из всех таких вариантов осуществления, частица имеет диаметр примерно 2,8 мкм. В некоторых из всех таких вариантов осуществления, частица имеет диаметр примерно 4,5 мкм. В некоторых из всех таких вариантов осуществления, связывающая молекула ковалентно присоединена к частицам, например, шарикам.
[54] В некоторых из всех таких вариантов осуществления, частица содержит поверхностно экспонируемую функциональную группу для присоединения связывающей молекулы, и/или при этом связывающая молекула ковалентно присоединена к частице посредством поверхностно экспонируемой функциональной группы. В некоторых вариантах осуществления, поверхностно экспонируемая функциональная группа представляет собой амино группу, карбоксильную группу, тиольную группу, альдегидную группу, хлорметильную группу, эпокси группу, гидроксильную группу, тозильную группу или гидразиновую группу. В некоторых случаях, поверхностно экспонируемая функциональная группа представляет собой тозильную группу.
[55] В некоторых из всех таких вариантов осуществления, частица является биологически совместимой или нетоксичной для клеток. В некоторых из всех таких вариантов осуществления, множество частиц, например, шариков, включает частицы, например, шарики, содержащие стекло, диоксид кремния, сложные полиэфиры гидроксикарбоновых кислот, полиангидриды дикарбоновых кислот, сополимеры гидроксикарбоновых кислот, сополимеры дикарбоновых кислот или металл. В некоторых из всех таких вариантов осуществления, частицы, например, шарики, имеют поверхность, содержащую полимер, полисахарид, диоксид кремния, жирную кислоту, углерод или их сочетание. В некоторых случаях, полимер представляет собой полиэтиленгликоль, сополимер молочная кислота - гликолевая кислота, полиглутаральдегид, полиуретан, полистирол и поливиниловый спирт или их сочетания.
[56] В некоторых из всех таких вариантов осуществления, частица содержит гидрофобную поверхность. В некоторых из всех таких вариантов осуществления, частицы, например, шарики, имеют полистирольную поверхность. В некоторых из всех таких вариантов осуществления, частица является магнитной и/или содержит магнитную сердцевину, парамагнитную сердцевину или суперпарамагнитную сердцевину. В некоторых из всех таких вариантов осуществления, частица содержит, по меньшей мере или примерно, по меньшей мере, 10 копий, 102 копий, 103 копий, 104 копий, 105 копий или 106 копий связывающей молекулы.
[57] В некоторых из всех таких вариантов осуществления, частица дополнительно содержит агент, который специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала, тем самым модулируя размножение клеток. В некоторых из всех таких вариантов осуществления, агент представляет собой лиганд или представляет собой антитело или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления, молекула представляет собой костимуляторную молекулу или представляет собой активирующий корецептор. В некоторых примерах, костимуляторная молекула или активирующий корецептор представляет собой OX-40, ICOS, DAP10, CD28 или 4-1BB. В некоторых вариантах осуществления, молекула представляет собой лиганд активирующего рецептора или корецептор, такой как OX-40L, ICOSL, B7-1, B7-2 или 4-1BBL. В некоторых случаях, молекула представляет собой ингибиторный рецептор. В некоторых примерах, ингибиторный рецептор представляет собой CTLA-4, PD-1, LAG-3, Tim-3, BTLA или TIGIT. В некоторых вариантах осуществления, молекула представляет собой лиганд ингибиторного рецептора, такой как PD-L1, PD-L2, CD155, CD112 или LIGHT.
[58] В некоторых из всех таких вариантов осуществления, агент ковалентно присоединен к частицам, например, шарикам. В некоторых из всех таких вариантов осуществления, отношение, необязательно, молярное или массовое отношение, связывающей молекулы и агента, удерживаемого частицей, составляет или составляет примерно 1:1.
[59] В настоящем документе предлагается композиция, содержащая множество поверхностно модифицированных частиц, например, шариков, описанных в настоящем документе. В некоторых вариантах осуществления, частицы происходят из композиции, имеющей концентрацию связывающей молекулы в пределах между или примерно между 0,5 мкг/мл и 500 мкг/мл, 1 мкг/мл и 200 мкг/мл или 5 мкг/мл и 100 мкг/мл, каждое, включительно. В некоторых вариантах осуществления, частицы происходят из композиции, имеющей концентрацию связывающей молекулы, которая составляет, по меньшей мере или, по меньшей мере, примерно 1 мкг/мл, 5 мкг/мл, 10 мкг/мл, 25 мкг/мл, 50 мкг/мл, 100 мкг/мл или 200 мкг/мл. В некоторых из всех таких вариантов осуществления, композиция является монодисперсной.
[60] Также, в настоящем документе предлагается набор, содержащий любые частицы, например, шарики, описанные в настоящем документе, или любую композицию, описанную в настоящем документе, и инструкции для применения. В некоторых случаях, инструкции предназначены для селекции или обогащения популяции клеток, клеток, экспрессирующих рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой. В некоторых случаях, инструкции предназначены для размножения, из популяции клеток, клеток, экспрессирующих рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой. В некоторых вариантах осуществления, процент клеток, экспрессирующих рекомбинантный рецептор, антигена, в популяции клеток меньше или примерно меньше 75%, 70%, 60%, 50%, 40%, 30%, 20%, 15%, 10%, или меньше.
[61] В настоящем документе предлагается способ размножения клеток, включающий инкубирование популяции клеток с помощью любых частиц, например, шариков, описанных в настоящем документе, или любых композиций, описанных в настоящем документе. Также предлагается способ селекции или обогащения клеток, включающий приведение в контакт популяции клеток с любыми частицами, например, шариками, описанными в настоящем документе, или с любыми композициями, описанными в настоящем документе.
[62] В настоящем документе предлагается способ долговременной стимуляции для оценки композиции клеток, включающий инкубирование в течение периода времени, по меньшей мере, 10 дней исходной композиции при условиях стимуляции CAR-зависимой активности клеток в исходной композиции, указанная исходная композиция, содержит Т-лимфоциты, экспрессирующие химерный рецептор антигена (CAR), содержащий внеклеточный антигенсвязывающ домен, который специфично связывает или распознает антиген, тем самым продуцируя выходную композицию; и оценку одного или нескольких факторов из фенотипа или активности одной или нескольких клеток выходной композиции.
[63] В некоторых из всех вариантов осуществления способа долговременной стимуляции условия стимуляции CAR-зависимой активности включают присутствие связывающей молекулы, которая специфично связывается с антигенсвязывающим доменом CAR. В некоторых вариантах осуществления, связывающая молекула присоединяется к подложке. В некоторых вариантах осуществления, подложка представляет собой твердую подложку. В некоторых вариантах осуществления, твердая подложка представляет собой поверхность лунки микропланшета или шарика. В некоторых вариантах осуществления, твердая подложка представляет собой микропланшет, содержащий связывающую молекулу, присоединенную к микропланшету, и инкубирование осуществляется на микропланшете. В некоторых вариантах осуществления, твердая подложка представляет собой шарик, содержащий присоединенную связывающую молекулу, и инкубирование осуществляется в присутствии множества шариков.
[64] В некоторых из всех вариантов осуществления способа долговременной стимуляции, связывающая молекула представляет собой или содержит рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом. В некоторых вариантах осуществления, рекомбинантный антиген или его часть представляет собой BCMA или представляет собой его часть, распознаваемую антигенсвязывающим доменом. В некоторых вариантах осуществления, связывающая молекула представляет собой или содержит антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом. В некоторых вариантах осуществления, антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело SJ25C1 или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления, антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело FMC63 или его антигенсвязывающий фрагмент.
[65] В некоторых из любых вариантов осуществления способа долговременной стимуляции, способ осуществляется in vitro или ex vivo.
[66] В некоторых из любых вариантов осуществления способа долговременной стимуляции, исходная композиция инкубируется в присутствии сред, которые не содержит рекомбинантных цитокинов. В некоторых вариантах осуществления, инкубирование осуществляется непрерывно или не прерывается в течение всего периода времени. В некоторых вариантах осуществления, в ходе инкубирования, клетки не пересевают, среды не заменяют и связывающей молекулы не добавляют.
[67] В некоторых из всех вариантов осуществления способа долговременной стимуляции, способ включает оценку одного или нескольких фенотипов из состояния активации, истощения или дифференциации одной, или нескольких клеток в выходной композиции. В некоторых вариантах осуществления, фенотип представляет собой истощение и оценка включает измерение экспрессирования, необязательно, поверхностного экспрессирования, одного или нескольких маркеров, выбранных из CTLA-4, FOXP3, PD-1, TIGIT, LAB-3, 2B4, BTLA, TIM3, VISTA или CD96. В некоторых вариантах осуществления, фенотип представляет собой активацию, и оценка включает измерение экспрессирования, необязательно, поверхностного экспрессирования, одного или нескольких маркеров, выбранных из CD25, CD26, CD27, CD28, CD30, CD71, CD154, CD40L, CD127, LAG3 или Ki67. В некоторых вариантах осуществления, фенотип представляет собой состояние дифференциации и оценка включает измерение одного или нескольких маркеров, выбранных из (i) одного или нескольких из CD25, CD45RO, CD56, KLRG1, CD95 и/или (ii) одного из CD45RA, CD27, CD28, CD62L и CCR7, необязательно, при этом один или несколько маркеров представляет собой маркеры, которые положительно или наоборот, отрицательно ассоциированы с наивно-подобными Т-лимфоцитами.
[68] В некоторых из всех вариантов осуществления способа долговременной стимуляции, способ включает оценку одной или нескольких активностей одной или нескольких клеток выходной композиции. В некоторых вариантах осуществления, одна или несколько активностей включают CAR-зависимую активность, необязательно, антиген-стимулированную активность. В некоторых из любых вариантов осуществления способа долговременной стимуляции, одна или несколько активностей включают цитолитическую активность или продуцирование цитокинов.
[69] В некоторых вариантах осуществления любого способа долговременной стимуляции, период времени составляет, по меньшей мере или, по меньшей мере, примерно 11 дней, 12 дней, 13 дней, 14 дней или 15 дней. В некоторых вариантах осуществления, период времени составляет или составляет примерно 11 дней, 12 дней, 13 дней, 14 дней или 15 дней.
[70] В некоторых из любых вариантов осуществления способа долговременной стимуляции, исходная композиция содержит клетки, которые экспонируются или вступают в контакт с исследуемым агентом или соединением до инкубирования, необязательно, при этом экспонирование или приведение в контакт осуществляется в ходе одной или нескольких стадий способа получения исходной композиции, содержащей Т-лимфоциты, экспрессирующие CAR. В некоторых вариантах осуществления, способ осуществляется на множестве исходных композиций, каждая указанная исходная композиция из множества получается с помощью иного способа.
[71] В некоторых из любых вариантов осуществления способа долговременной стимуляции, способ дополнительно включает сравнение фенотипа или активности выходной композиции с фенотипом или активностью контрольной композиции, при этом, необязательно, контрольная композиция представляет собой композицию Т-лимфоцитов, которые инкубируют в течение, по меньшей мере, 10 дней при таких же условиях для стимуляции CAR-зависимой активности, указанная композиция Т-лимфоцитов не получается в присутствии исследуемого агента или соединения или получается с помощью альтернативного способа по сравнению с исходной композицией. В некоторых вариантах осуществления, способ дополнительно включает идентификацию выходной композиции, которая демонстрирует уменьшенное истощение, уменьшенную активацию или уменьшенную дифференциацию, по сравнению с контрольной композицией. В некоторых вариантах осуществления, уменьшенная дифференциация включает увеличение экспрессирования одного или нескольких маркеров наивно-подобных Т-лимфоцитов.
Краткое описание чертежей
[72] Фиг. 1 показывает гистограмму окрашивания Cell Trace Violet (CTV) в Т-лимфоцитах CD3+ экспрессирующих CAR анти-BCMA (Т-лимфоциты CAR) и клеток CD3+, которые не экспрессируют CAR (имитация) после инкубирования вместе с BCMA- конъюгированными шариками.
[73] Фиг. 2A показывает точечные графики поверхностного экспрессирования CD25 (ось y) и интенсивности окрашивания CTV (ось x) в клетках после инкубирования вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28 (слева) или с BCMA-конъюгированными шариками (справа).
[74] Фиг. 2B показывает гистограмму окрашивания CTV клеток после обработки шариками, конъюгированными с антителом анти-CD3/анти-CD28 или с BCMA-конъюгированными шариками.
[75] Фиг. 2C показывает гистограммы экспрессирования PD-1 в клетках CD4+ (слева) или клетках CD8+ (справа) после инкубирования клеток вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28 или с BCMA-конъюгированными шариками.
[76] Фиг. 3A показывает процент Т-лимфоцитов CAR+ анти-BCMA после инкубирования каждой из трех различных композиций Т-лимфоцитов, содержащих CAR-экспрессирующие Т-лимфоциты (каждая генерируется иным донором), вместе с BCMA-конъюгированными шариками в течение до 14 дней. Результаты для каждой композиции клеток изображены на графике отдельно с помощью треугольников, квадратов и кружков.
[77] Фиг. 3B показывает поверхностное экспрессирование, как определяется с помощью средней интенсивности флуоресценции (MFI) для детектирования CD25 (слева), CCR7 (по центру) и CD27 (справа) в клетках CD8+ после четырех, семи или четырнадцати дней инкубирования вместе с BCMA-конъюгированными шариками в течение до 14 дней. Результаты показаны для каждой из трех различных композиций клеток, содержащих CAR-экспрессирующие клетки анти-BCMA, описанных на Фиг. 3A, и показаны на графике отдельно с помощью треугольников, квадратов и кружков.
[78] Фиг. 4A показывает графики поверхностного экспрессирования CD25 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитов CD8+ (правые панели) присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования вместе с различными количествами BCMA-конъюгированных шариков. Фиг. 4B показывает графики гистограмм поверхностного экспрессирования PD-1 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели), присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA, после инкубирования вместе с различными количествами BCMA-конъюгированных шариков. Обозначения BCMA 50, BCMA 25, BCMA 10 и BCMA 5 показывают BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 50, 25, 10 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[79] Фиг. 5A-B показывают графики, изображающие общее количество Т-лимфоцитов CD3+ (Фиг. 5A) или уровни красителя CTV, маркера пролиферации на Т-лимфоцитах CD4+ (Фиг. 5B), присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования вместе с различными количествами BCMA-конъюгированных шариков. BCMA 50, BCMA 25, BCMA 10 и BCMA 5 показывают BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 50, 25, 10 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[80] Фиг. 6 показывает график, изображающий поверхностное экспрессирование CD25 на Т-лимфоцитах CD4+, присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA, после инкубирования вместе с различными количествами BCMA-конъюгированных шариков. BCMA 50, BCMA 25, BCMA 10 и BCMA 5 показывают BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 50, 25, 10 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[81] Фигуры 7A-7H показывают окрашивание для различных маркеров или для различных уровней пролиферации в композициях Т-лимфоцитов CAR+ анти-BCMA, инкубируемых вместе с BCMA-конъюгированными шариками. Фиг. 7A показывает гистограммы проточной цитометрии относительно поверхностного экспрессирования CD25 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели), присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования вместе с различными количествами BCMA-конъюгированных шариков. Фиг. 7B показывает гистограммы проточной цитометрии относительно поверхностного экспрессирования CD25 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели), присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования при различных отношениях Т-лимфоцитов к шарикам (композиция 200 мкг/мл BCMA-конъюгированных шариков) или иммобилизованных анти-CD3. Фиг. 7C показывает гистограммы проточной цитометрии относительно поверхностного экспрессирования CD69 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели), присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA, после инкубирования при различных отношениях Т-лимфоцитов к шарикам (композиция 200 мкг/мл BCMA-конъюгированных шариков) или иммобилизованным анти-CD3. Фиг. 7D показывает гистограммы проточной цитометрии относительно поверхностного экспрессирования TIM3 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели), присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA, после инкубирования при различных отношениях Т-лимфоцитов к шарикам (композиция 200 мкг/мл BCMA-конъюгированных шариков) или к иммобилизованным анти-CD3. Фиг. 7E показывает гистограммы проточной цитометрии относительно поверхностного экспрессирования PD-1 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели), присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования при различных отношениях Т-лимфоцитов к шарикам (композиция 200 мкг/мл BCMA-конъюгированных шариков) или иммобилизованным анти-CD3. Фиг. 7F показывает график гистограммы окрашивания CTV (меры пролиферации) клеток в целом в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования вместе с шариками (композиция 200 мкг/мл BCMA-конъюгированных шариков) при отношении Т-лимфоцитов к шарикам 1:1 и в присутствии или в отсутствие 5 мкМ леналидомида. Фиг. 7G и Фиг. 7H показывают гистограммы проточной цитометрии относительно CD25 в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели). присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования вместе с шариками (композиция 200 мкг/мл BCMA-конъюгированных шариков) при отношении Т-лимфоцитов к шарикам или иммобилизованным анти-CD3 1:1, соответственно, в присутствии или в отсутствие леналидомида. На рассмотренных выше фигурах, обозначения “50”, “100” и “200” показывают BCMA-конъюгированные шарики, генерируемые посредством инкубирования BCMA вместе с шариками в количестве 50, 100 и 200 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[82] Фигуры 8A-8I показывают графики, изображающие уровни факторов транскрипции и маркеров активации в Т-лимфоцитах CD4+ (левые панели) или Т-лимфоцитах CD8+ (правые панели) или на них, присутствующих в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования без стимуляции или вместе с различными количествами BCMA-конъюгированных шариков или шариков, конъюгированных с анти-CD3 и анти-CD28, и в присутствии 0 мкМ, 0,5 мкМ или 50 мкМ леналидомида. Показаны уровни Blimp1 (Фиг. 8A), CD25 (Фиг. 8B), CD31 (Фиг. 8C), PD-1 (Фиг. 8D), Tbet (Фиг. 8E), EOMES (Фиг. 8F), GATA3 (Фиг. 8G), Helios (Фиг. 8H) и Ikaros (Фиг. 8I). Обозначения 200 BCMA, 50 BCMA и 5 BCMA указывают на BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 200, 50 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[83] Фиг. 9A-9C показывают графики, изображающие уровни внеклеточного IFN-гамма (Фиг. 9A), IL-2 (Фиг. 9B) и TNF альфа (Фиг. 9C) из культур после инкубирования композиции Т-лимфоцитов CAR+ анти-BCMA вместе с двумя различными количествами BCMA-конъюгированных шариков в присутствии или в отсутствие 5 мкМ леналидомида. Обозначения 50 мкг BCMA и 5 мкг BCMA указывают на BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 200, 50 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[84] Фиг. 9D показывает график, изображающие уровни внеклеточного IL-2 от культур после инкубирования композиции Т-лимфоцитов CAR+ анти-BCMA из клеток от двух различных доноров (донор A и донор B) вместе с различными количествами BCMA-конъюгированных шариков в присутствии 0 мкМ, 1 мкМ или 5 мкМ леналидомида. Обозначения 200 BCMA и 5 BCMA указывают на BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 200, 50 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[85] Фиг. 9E показывает проточно-цитометрический анализ фосфорилированного STAT5 (pSTAT5) после 2 часов стимуляции CAR (stim) вместе с 50 мкг шариков BCMA. Контроль без стимуляции показан точечной линией. Фиг. 9F показывает проточно-цитометрический анализ уровней внутриклеточных цитокинов для репрезентативного нормального донора CAR T после 24 часов стимуляции шариками BCMA (на гейтированных трансдуцированных живых CD3+).
[86] Фиг. 9G и Фиг. 9H показывают отсчеты клеток в целом после культивирования композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования в течение 4 дней (Фиг. 9G) или 7 дней (Фиг. 9H) вместе с различными количествами BCMA-конъюгированных шариков в присутствии 5 мкМ леналидомида. Обозначения 50 BCMA и 5 BCMA показывают BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 50 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[87] Фиг. 9I показывает графики гистограмм окрашивания CTV (меры пролиферации) Т-лимфоцитов CD4+ или Т-лимфоцитов CD8+ в композиции Т-лимфоцитов CAR+ анти-BCMA после инкубирования в течение 4 или 7 дней вместе с BCMA-конъюгированными шариками в присутствии 5 мкМ леналидомида (5 мкм Len) или в отсутствие леналидомида (лекарственная среда).
[88] Фиг. 9J и 9K показывают графики, изображающие процент клеток положительных относительно суррогатного маркера EGFRt, как определено с помощью антитела анти-EGFR после инкубирования композиции Т-лимфоцитов CAR+ анти-BCMA в течение 4 дней (Фиг. 9J) или 7 дней (Фиг. 9K) вместе с различными количествами BCMA-конъюгированных шариков в присутствии 5 мкМ леналидомида или в отсутствие леналидомида (лекарственная среда). Обозначения «50» и «5» показывают BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 50 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[89] Фиг. 9L показывает процент гибели клеток для целевых клеток RPMI-8226 под действием эффекторных Т-лимфоцитов CAR+ анти-BCMA, которые инкубируют вместе с различными количествами BCMA-конъюгированных шариков в присутствии 5 мкМ леналидомида или в отсутствие леналидомида (лекарственная среда). Показана цитолитическая активность композиций, имеющих отношение эффекторных клеток к целевым клеткам 3:1 или 1:1, и, кроме того, присутствие или отсутствие леналидомида. Обозначения «50» и «5» показывают BCMA-конъюгированные шарики, генерируемые посредством инкубирования ВСМС вместе с шариками в количестве 50 и 5 мкг BCMA приблизительно на 4×108 шариков, соответственно.
[90] Фиг. 9M показывает график, изображающий уровни внеклеточного IFN-гамма, продуцируемого в ходе анализа уничтожения в культуре, содержащей целевые клетки RPMI-8226 и свежие эффекторные Т-лимфоциты CAR+ анти-BCMA или эффекторные Т-лимфоциты CAR+ анти-BCMA, которые инкубируют в течение 24 часов или в течение семи дней вместе с BCMA-конъюгированными шариками (композиция 50 мкг/мл, генерируемая посредством инкубирования ВСМС вместе с шариками в количестве 50 мкг BCMA приблизительно на 4×108 шариков). Результаты показаны для культур, имеющих отношение эффекторных клеток к целевым клеткам 0,3:1 или 1:1.
[91] Фиг. 9N показывает гибель клеток, нормированную на отсчеты целевых клеток в культуре, содержащей целевые клетки RPMI-8226 и свежие эффекторные Т-лимфоциты CAR+ анти-BCMA или эффекторные Т-лимфоциты CAR+ анти-BCMA, которые инкубируют в течение 24 часов или в течение семи дней вместе с BCMA-конъюгированными шариками (композиция 50 мкг/мл, генерируемая посредством инкубирования ВСМС вместе с шариками в количестве 50 мкг BCMA приблизительно на 4×108 шариков). Результаты показаны для культур, имеющих отношение эффекторных клеток к целевым клеткам 0,3:1 или 1:1.
[92] Фиг. 10A-10B показывают результаты анализа серийной повторной стимуляции композиции Т-лимфоцитов анти-BCMA, которые инкубируют в течение семи дней вместе с BCMA-конъюгированными шариками (композиция 50 мкг/мл, генерируемая посредством инкубирования ВСМС вместе с шариками в количестве 50 мкг BCMA приблизительно на 4×108 шариков). Показаны результаты для композиций от трех различных доноров. Фиг. 10A и Фиг. 10B показывают цитолитическую активность Т-лимфоцитов CAR+ анти-BCMA в каждой из временных точек для двух различных доноров.
[93] Фиг. 11 показывает график, изображающий процент Т-лимфоцитов CAR+ как функцию времени в пяти различных композициях клеток CAR+ анти-BCMA, которые инкубируют в присутствии BCMA-конъюгированных шариков (сплошные линии) или вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28 (точечные линии), непосредственно после трансдуцирования лентивирусным вектором, кодирующим CAR анти-BCMA.
[94] Фиг. 12A и Фиг. 12B показывают кратный размножение и кумулятивные количества клеток Т-лимфоцитов EGFRt+/CD4+ или Т-лимфоцитов EGFRt+/CD4+, соответственно, стимулируемых при указанном отношении шариков, покрытых антиидиотипическим антителом (анти-ID B-1), или контрольных шариков, покрытых антителом анти-CD3/анти-CD28, в присутствии (сплошные линии) или в отсутствие (штриховые линии) цитокинов. Показаны результаты стимуляции при отношении шариков, покрытых антителом анти-CD3/анти-CD28, к клеткам 3:1 (кружки), при отношении шариков, покрытых анти-ID B-1, к клеткам 1:1 (квадраты) и при отношении шариков, покрытых анти-ID B-1, к клеткам 1:5 (треугольники).
[95] Фиг. 13 показывает уровни экспрессирования PD-1 Т-лимфоцитов CD4+ положительных относительно антитела анти-EGFR после стимуляции при указанном отношении шариков, покрытых антиидиотипическим антителом (анти-ID B-1), или контрольных шариков, покрытых антителом анти-CD3/анти-CD28, в присутствии (сплошные линии) или в отсутствие (штриховые линии) цитокинов, как оценивают с помощью проточной цитометрии в дни 3, 7, 10 и 14 культивирования. Показаны результаты стимуляции при отношении шариков, покрытых антителом анти-CD3/анти-CD28, к клеткам 3:1 (кружки), при отношении шариков, покрытых анти-ID B-1, к клеткам 1:1 (квадраты) и при отношении шариков, покрытых анти-ID B-1, к клеткам 1:5 (треугольники).
[96] Фиг. 14 показывает жизнеспособность Т-лимфоцитов CD4+ или CD8+ экспрессирующих CAR, полученных из FMC63, согласно оценкам с помощью проточной цитометрии после стимуляции при указанном отношении шариков, покрытых антиидиотипическим антителом (анти-ID B-1), или контрольных шариков, покрытых антителом анти-CD3/анти-CD28, в присутствии (сплошные линии) или в отсутствие (штриховые линии) цитокинов согласно оценкам с помощью проточной цитометрии в дни 3, 7, 10 и 14 культивирования. Показаны результаты стимуляции при отношении шариков, покрытых антителом анти-CD3/анти-CD28, к клеткам 1:3 (кружки), при отношении шариков, покрытых анти-ID B-1, к клеткам 1:1 (квадраты) и при отношении шариков, покрытых анти-ID B-1, к клеткам 1:5 (треугольники).
[97] Фиг. 15A показывает окрашивание внутриклеточных цитокинов относительно IL-2, TNFα и IFNγ в Т-лимфоцитах экспрессирующих CAR, полученных из FMC63, после стимуляции с помощью шариков, покрытых scFv-специфичным антиидиотипическим антителом (анти-ID B-1), полученным из FMC63. Показаны результаты для Т-лимфоцитов CD8+ положительных или отрицательных относительно суррогатного маркера EGFRt (EGFRt+ или EGFRt-).
[98] Фиг. 15B показывает окрашивание внутриклеточных цитокинов относительно IL-2, TNFα и IFNγ для Т-лимфоцитов, экспрессирующих CAR, полученных из FMC63, после стимуляции с помощью антиген-экспрессирующих клеток K562-CD19. Показаны результаты Т-лимфоцитов CD8+ положительных относительно суррогатного маркера EGFRt.
[99] Фиг. 16 показывает количество удвоений популяции при анализе серийных стимуляций в течение 14-дневного периода культивирования Т-лимфоцитов, экспрессирующих CAR, полученных из FMC63, после стимуляции при указанном отношении шариков, покрытых антиидиотипическим антителом (анти-ID B-1), или контрольных шариков, покрытых антителом анти-CD3/анти-CD28, в присутствии (сплошные линии) или в отсутствие (штриховые линии) цитокинов. Показаны результаты для Т-лимфоцитов CD4+ положительных относительно суррогатного маркера EFGRt (EGFRt+) или Т-лимфоцитов CD8+ положительных относительно суррогатного маркера EGFRt (EGFRt +). Показаны результаты стимуляции при отношении шариков, покрытых антителом анти-CD3/анти-CD28, к клеткам 1:3 (кружки), при отношении шариков, покрытых анти-ID B-1, к клеткам 1:1 (квадраты), и при отношении шариков, покрытых анти-ID B-1, к клеткам 1:5 (треугольники).
[100] Фиг. 17A-17C показывают результаты стимуляции Т-лимфоцитов CD4+ или CD8+, экспрессирующих CAR, полученные из FMC63-, культивируемых сами по себе (сплошные линии) или в виде сокультуры (штриховые линии), с помощью шариков, покрытых scFv-специфичным антиидиотипическим антителом (анти-ID B-1), полученным из FMC63. Результаты показаны для двух различных доноров (изображены как кружки и квадраты). Фиг. 17A показывает кратность размножения Т-лимфоцитов CD4+ или Т-лимфоцитов CD8+ в культурах, которые являются положительными относительно суррогатного маркера EGFRt (EGFRt+/CD4+ или EGFRt+/CD8+). Фиг. 17B показывает частоту Т-лимфоцитов CD4+ или Т-лимфоцитов CD8+ в культурах, которые являются положительными относительно суррогатного маркера EGFRt (EGFRt +/CD4+ или EGFRt +/CD8+). Фиг. 17C показывает жизнеспособность Т-лимфоцитов CD4+ или Т-лимфоцитов CD8+ в культурах.
[101] Фиг. 18A и 18B показывают результаты проточной цитометрии для поверхностных маркеров Т-лимфоцитов в дни 5, 7 и 9 культивирования после стимуляции Т-лимфоцитов CD4+ или CD8+ экспрессирующих CAR, полученный из FMC63, культивируемых сами по себе или в виде сокультуры, с помощью шариков, покрытых scFv-специфичным антиидиотипическим антителом (анти-ID B-1), полученным из FMC63. Фиг. 18A показывает поверхностное экспрессирование PD-1 на Т-лимфоцитах CD4+ или Т-лимфоцитах CD8+ в культурах, которые являются положительными относительно суррогатного маркера EGFRt (EGFRt+/CD4+ или EGFRt+/CD8+). Фиг. 18B показывает поверхностное экспрессирование CD25 на Т-лимфоцитах CD4+ или Т-лимфоцитах CD8+ в культурах, которые являются положительными относительно суррогатного маркера EGFRt (EGFRt+/CD4+ или EGFRt+/CD8+).
[102] Фиг. 19A показывает внутриклеточные уровни цитокинов TNFα, IFNγ и IL-2 согласно оценкам с помощью проточной цитометрии для Т-лимфоцитов CD4+ или CD8+, присутствующих в оттаявшей композиции, содержащей Т-лимфоциты, экспрессирующие CAR, полученные из FMC63, которые наращивают в культуре, либо вместе с клетками K562, экспрессирующими CD19, либо с PMA/иономицином. Показаны уровни цитокинов в Т-лимфоцитах CD4+ и CD8+, самих по себе или в виде сокультуры, при оттаивании (d=0) или после дополнительного культивирования в течение дополнительных 9 дней в присутствии шариков, конъюгированных с анти-ID B-1.
[103] Фиг. 19B показывает частоту клеток положительных относительно CD25 или Ki67 согласно оценкам с помощью проточной цитометрии Т-лимфоцитов CD4+ или CD8+, присутствующих в оттаявшей композиции, содержащей Т-лимфоциты, экспрессирующие CAR, полученные из FMC63, которые наращивают в культуре либо вместе с клетками K562, экспрессирующими CD19, либо с PMA/иономицином. Показаны уровни маркеров в Т-лимфоцитах CD4+ и CD8+, самих по себе или в виде сокультуры, при оттаивании (d=0) или после дополнительного культивирования в течение дополнительны 9 дней в присутствии шариков, конъюгированных с анти-ID B-1.
[104] Фиг. 20A показывает результаты для антиген-специфичной цитолитической активности CAR, и Фиг. 20B показывает результаты для продуцирования цитокинов T-лимфоцитами CAR анти-BCMA, которые предварительно стимулируются шариками BCMA (по сравнению со свежеоттаявшими (не стимулируемыми предварительно) T-лимфоцитами CAR анти-BCMA) в co-культурах, сравнивая клетки, культивируемые в присутствии леналидомида, и в его отсутствие. Фиг. 20C показывает общую жизнеспособность и отсчеты клеток, оцениваемые для трех доноров T-лимфоцитов CAR анти-BCMA. Фиг. 20D показывает результаты проточного цитометрического анализа с помощью поверхностного экспрессирования CD25 и PD-1 (средняя интенсивность флуоресценции (MFI), для T-лимфоцитов CAR CD4+ и CD8+ анти-BCMA после стимуляции (предварительной обработки) с помощью шариков BCMA в течение 7 дней, в присутствии или в отсутствие 1 мкМ леналидомида. Фиг. 20E показывает проточный цитометрический анализ среди доноров T-лимфоцитов CAR для медианной интенсивности флуоресценции (MFI; CD25 и Tim3) или процента положительных относительно PD-1 и Lag3 на поверхности маркеров Т-лимфоцитов в подмножествах CD4+ CAR+ и CD8+ CAR+ (гейтированных на живых клетках CD3+). Показанные значения представляют собой процентный фон (Veh) MFI, жизнеспособность или отсчеты.
[105] Фиг. 21A показывает анализ продуцирования эффекторных цитокинов после CAR-специфичной стимуляции на 50 мкг шариков BCMA в течение 24 часов в присутствии 1 мкМ леналидомида по сравнению с фоновой (от лекарственной среды) реакции для каждого из трех доноров.
[106] Фиг. 21B показывает воздействие T-лимфоцитов CAR анти-BCMA активированных на различных концентрациях шариков BCMA (то есть, 5 мкг, 50 мкг и 200 мкг) в отсутствие (левые столбики) или в присутствии 0,1 мкМ (средний столбик) или 1 мкМ (правые столбики) леналидомида на продуцирование эффекторных цитокинов T-лимфоцитами CAR.
[107] Фиг. 21C показывает продуцирование цитокинов T-лимфоцитами CAR анти-BCMA, полученными у репрезентативных здоровых доноров и у пациентов с множественной миеломой, стимулируемых шариками BCMA с добавлением PD-L1 или шарикакми без добавления, в присутствии или в отсутствие 1 мкМ леналидомида.
[108] Фигуры 22A и 22B представляют собой графики, показывающие продуцирование цитокинов CAR-экспрессирующими Т-лимфоцитами анти-BCMA. Фиг. 22A показывает концентрацию (пг/мл) IFN-гамма, IL-2, TNF-альфа, IL-6, GM-CSF и IL-4 в супернатанте, собранном с CAR-экспрессирующих Т-лимфоцитов анти-BCMA после 24 часового инкубирования вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28 (CD3/CD28), с BCMA-конъюгированными шариками при концентрации 200 мкг/мл, 50 мкг/мл или 5 мкг/мл конъюгированного BCMA приблизительно на 4×108 шариков (200 мкг, 50 мкг или 5 мкг BCMA, соответственно) или клетками, инкубируемыми без шариков (no stim). Штриховые горизонтальные линии показывают верхний предел количественного определения (ULOQ). Фиг. 22B показывает процент клеток CD4+CAR+ (верхний ряд) или CD8+CAR+ (нижний ряд) положительных относительно внутриклеточного окрашивания IFN-гамма, IL-2 или TNF-альфа после инкубирования вместе с шариками CD3/CD28, 200 мкг, 50 мкг или 5 мкг BCMA-конъюгированных шариков или no stim.
[109] Фигуры 23A и 23B представляют собой графики, показывающие активность композиций Т-лимфоцитов, содержащих Т-лимфоциты CAR+ анти-CD19, Клетки либо инкубируются вместе с шариками, конъюгированными с антителом анти-CD19 анти-ID, в течение 14 дней (день 14; вторичные), либо не инкубируются перед оценкой активности. Показаны результаты анализа цитотоксичности (Фиг. 23A) и анализа внутриклеточного окрашивания цитокинов (ICS) после экспонирования для клеток, экспрессирующих CD19 (Фиг. 23B).
[110] Фигуры 24A-24C представляют собой графики, показывающие характеристики композиций Т-лимфоцитов, содержащих Т-лимфоциты CAR+ анти-CD19, в ходе инкубирования вместе с шариками, конъюгированными с антителом анти-CD19 анти-ID в течение 14 дней, или после этого. Показаны результаты для композиций Т-лимфоцитов, которые генерируются в присутствии различных исследуемых соединений или лекарственной среды. Фигуры 24A и 24B показывают активность при реакции на экспонирование для клеток CD19 у композиций Т-лимфоцитов, которые не инкубируются (первичные) или инкубируются в течение 14 дней (вторичные). Показаны результаты для полифункционального окрашивания с помощью ICS (Фиг. 24A) и цитолитической активности (Фиг. 24B) после экспонирования для клеток, экспрессирующих CD19. Фиг. 24C показывает уровень секретируемых цитокинов из супернатанта композиций клеток, содержащих клетки, экспрессирующие CAR анти-CD19, которые инкубируют при отношении к клеткам, экспрессирующим CD19, 1:1 в течение 20 часов. Количества IL2, TNF и IFN-гамма измеряют, и показано среднее значение масштабированных оценок для всех трех цитокинов.
[111] Фигуры 25A-25D показывают графики, изображающие активности Т-лимфоцитов из генерируемых композиций T-лимфоцитов CAR анти-CD19, которые наращены в присутствии только среды, контрольной лекарственной среды DMSO, Соединения 1 или Соединения 2, после стимуляции шариками, поверхностно конъюгированными с антиидиотипическим антителом специфичным к CAR анти-CD19. Фиг. 25A показывает общие отсчеты живых Т-лимфоцитов на лунку для Т-лимфоцитов из генерируемых композиций T-лимфоцитов CAR анти-CD19, сокультивируемых вместе с шариками, поверхностно конъюгированными с антиидиотипическим антителом. Фиг. 25B показывает площадь под кривой (AUC), вычисленную для отсчетов живых Т-лимфоцитов, по отношению к одной только контрольной среде. Фиг. 25C показывает график, изображающий продуцирование TNF-альфа (TNF), IFN-гамма (IFNg) и IL-2 Т-лимфоцитами из генерируемых композиций T-лимфоцитов CAR анти-CD19 после стимуляции с помощью 16-часового сокультивирования вместе с облученными целевыми клетками K562-CD19, которое следует за 15-дневным инкубированием вместе с шариками, поверхностно конъюгированными с антиидиотипическим антителом. Показана кратность изменения внеклеточных TNF-альфа (TNF), IFN-гамма (IFNg) и IL-2 по сравнению с условиями сред самих по себе. Фиг. 25D показывает графики, изображающие профили полифункциональных цитокинов Т-лимфоцитов CD8+ из генерируемых композиций T-лимфоцитов CAR анти-CD19, которые следуют за 15-дневным инкубированием вместе с шариками, конъюгированными с антиидиотипическим антителом.
Подробное описание
[112] В настоящем документе предлагаются композиции и способы обогащения, размножения и/или активации генно-инженерных клеток, которые экспрессируют рекомбинантный рецептор, например, химерный рецептор антигена (CAR). В некоторых вариантах осуществления, предлагаемые способы включают ex vivo или in vitro обогащение, размножение и/или активацию клеток посредством инкубирования вместе с частицами, например, со сферическими частицами, с присоединенной связывающей молекулой, которая распознает или связывает рекомбинантный рецептор. В некоторых вариантах осуществления, присоединенная связывающая молекула представляет собой полипептид, например, полипептидный антиген или антиидиотипическое антитело, которое связывается с рекомбинантным рецептором.
[113] В некоторых вариантах осуществления, композиции и способы, предлагаемые в настоящем документе, имеют одно или несколько преимуществ по сравнению с существующими средствами размножения, обогащения или активации клеток, которые экспрессируют рекомбинантный рецептор, например, CAR. Многие существующие протоколы для ex vivo или in vitro размножения основаны на инкубировании клеток, например, Т-лимфоцитов, вместе с одной или несколькими поликлональными стимуляторными молекулами, способными активировать компоненты комплекса TCR. Например, распространенный протокол размножения клеток заключается в инкубировании клеток вместе с антителами анти-CD3 и анти-CD28, например, в инкубировании клеток с антителами анти-CD3 и анти-CD28, которые присоединены к парамагнитным шарикам. Одним из недостатков этого способа заключается в том, что все или почти все клетки данной композиции, например, культивируемые Т-лимфоциты, будут приводиться в контакт и стимулироваться антителами. Таким образом, в некоторых вариантах осуществления, для данной композиции клеток, приводимых в контакт с антителами анти-CD3 и анти-CD28, все или почти все клетки становятся активированными независимо от того, экспрессируют ли они рекомбинантный рецептор или нет. В противоположность этому, в конкретных вариантах осуществления, когда клетки инкубируются вместе с частицами, например, шариками, предлагаемых в настоящем документе, связывающие молекулы частиц, например, шариков, непосредственно связываются с рекомбинантным рецептором, таким образом давая в результате увеличение стимуляции, активации, пролиферации и/или размножения клеток, экспрессирующих рекомбинантный рецептор, по сравнению с клетками, у которых такого рецептора нет. В некоторых вариантах осуществления, инкубирование клеток, которые включают клетки, которые экспрессируют рекомбинантный рецептор, вместе с частицами, например, шариками, описанными в настоящем документе, увеличивает часть, долю или подмножество клеток, которые экспрессируют рекомбинантный рецептор.
[114] В конкретных вариантах осуществления, одно из преимуществ размножения, обогащения и/или активации клеток с помощью частиц, например, шариков, описанных в настоящем документе, по сравнению с другими способами, например, со стимуляцией антителами анти-CD3 и анти-CD28, заключается в том, что инкубирование вместе с частицами, предлагаемыми в настоящем документе, дает в результате уменьшение активации и/или истощения в противоположность клеткам, которые наращиваются, обогащаются и/или активируются с помощью других способов. Например, в некоторых вариантах осуществления, клетки, инкубированные вместе с частицами, предлагаемыми в настоящем документе, экспрессируют более низкие уровни маркеров, ассоциируемых с активацией или с истощением, например, имеют более низкое поверхностное экспрессирование CD25, например, более низкое экспрессирование PD1, по сравнению с клетками, которые инкубируют вместе с поликлональными стимуляторными молекулами, которые могут активировать компоненты комплекса TCR, например, с антителами анти-CD3 и анти-CD28.
[115] В определенных вариантах осуществления, предлагаются способы трансдуцирования или трансфицирования клеток с помощью вирусного или невирусного вектора для доставки нуклеиновой кислоты, которая кодирует рекомбинантный рецептор или CAR у клеток в то время, когда они вступают в контакт, обрабатываются или инкубируются вместе с частицами, например, шариками, описанными в настоящем документе, по меньшей мере, в течение части процесса трансдуцирования или трансфицирования. В некоторых вариантах осуществления, одно из преимуществ трансдуцирования или трансфицирования клеток в присутствии частиц, например, шариков, делает возможным трансфицирование или трансдуцирование клеток, которые предварительно не активируются поликлональными стимуляторными молекулами, например, антителами анти-CD3 и анти-CD28. Конкретные варианты осуществления предполагают, что клетки, которые трансдуцируются или трансфицируются без предварительной активации поликлональными молекулами, будет демонстрировать повышенную персистентность и/или уменьшение истощения по сравнению с клетками, которые активируются перед трансфицированием или трансдуцированием.
[116] Конкретные варианты осуществления предполагают, что конкретные рекомбинантные антигены или их фрагменты, присоединенные к частицам, например, шарикам, как описано, могут быть особенно пригодными для применений при специфичной стимуляции CAR, содержащего антигенсвязывающий домен, который распознает антиген. В некоторых случаях, определенные рекомбинантные антигены, например, BCMA, могут иметь всего несколько неспецифичных взаимодействий, таких как неспецифичные взаимодействия белок-белок или неспецифичные взаимодействия с клетками, или не иметь их, что предотвращает или сводит к минимуму неспецифичное прилипание антигена к клеткам или поглощение клетками. В некоторых случаях, это может улучшить качество стимуляции CAR-экспрессирующих клеток. В некоторых вариантах осуществления, присоединение к шарикам или частицам дает в результате повышенную, усиленную, консистентную и/или более надежную стимуляцию, активацию или размножение клеток по сравнению с условиями, когда рекомбинантный антиген является несвязанным или связанным с другой твердой подложкой, такой как поверхность планшета или чашки. В определенных вариантах осуществления, связывающая молекула представляет собой или содержит рекомбинантный BCMA или его фрагмент.
[117] В конкретных вариантах осуществления, частицы или шарики, содержащие присоединенный рекомбинантный BCMA (такой как рекомбинантный слитый белок BCMA-FC), используют в сочетании с предлагаемыми способами для активации, стимуляции или размножения клеток в композиции клеток. В некоторых вариантах осуществления, частицы или шарики, содержащие рекомбинантный BCMA, селективно активируют, стимулируют или вызывают размножение клеток, экспрессирующих рекомбинантный рецептор, содержащий антигенсвязывающий домен, который связывает или распознает BCMA, например, CAR анти-BCMA. В определенных вариантах осуществления, активация, стимуляция или размножение клеток, например, CAR-экспрессирующих клеток анти-BCMA, становится больше или увеличивается по сравнению с активацией, стимуляцией или размножением под действием других реагентов, таких, например, как реагенты шариков, конъюгированных с антителом анти-CD3/анти-CD28. В определенных вариантах осуществления, активация, стимуляция или размножение клеток, например, CAR-экспрессирующих клеток анти-BCMA, является более показательным для активации, стимуляции или размножения клеток in vivo и/или в ответ на эндогенный антиген по сравнению с активацией, стимуляцией или размножением под действием других реагентов, таких, например, как реагентов шариков, конъюгированных с антителом анти-CD3/анти-CD28. В некоторых аспектах, степень, до которой клетки активируются, стимулируются или наращиваются под действием частиц или шариков, содержащих присоединенный рекомбинантный BCMA, можно регулировать, модифицировать или контролировать посредством изменения количества рекомбинантного BCMA, присоединенного к частицам или шарикам, или посредством изменения отношения частиц или шариков к клеткам. В некоторых аспектах, активация, стимуляция или размножение клеток, например, CAR-экспрессирующих клеток анти-BCMA, под действием рекомбинантного BCMA более эффективны, когда рекомбинантный BCMA присоединяется к частицам или шарикам, чем когда рекомбинантный BCMA является свободно всплывающим или неприсоединенным или когда рекомбинантный BCMA присоединен к другой поверхности, например, к чашке или планшету для культивирования.
[118] В некоторых вариантах осуществления, связывающая молекула представляет собой антиидиотипическое антитело (анти-ID), которое связывает или распознает рекомбинантный рецептор, например, CAR. В конкретных вариантах осуществления, частицы или шарики, содержащие присоединенные рекомбинантные анти-ID, используют в сочетании с предлагаемыми способами для активации, стимуляции или размножения клеток в композиции клеток. В различных вариантах осуществления, частицы или шарики, содержащие анти-ID, селективно активируют, стимулируют или вызывают размножение клеток в композиции, таких как клетки, экспрессирующие рекомбинантный рецептор, например, CAR. В определенных вариантах осуществления, активация, стимуляция или размножение клеток, например, CAR-экспрессирующих клеток, становится больше или увеличивается по сравнению с активацией, стимуляцией или размножением под действием других реагентов, таких, например, как реагенты шариков, конъюгированных с антителом анти-CD3/анти-CD28. В определенных аспектах, степень, до которой клетки активируются, стимулируются или наращиваются под действием частиц или частиц шариков, или шариков, содержащих анти-ID, может регулироваться, модифицироваться или контролироваться посредством изменения количества анти-ID, присоединенных к частицам или шарикам, или посредством изменения отношения частиц или шариков к клеткам. В конкретных вариантах осуществления, анти-ID представляет собой антитело анти-CD19 анти-ID. В конкретных вариантах осуществления, активация, стимуляция или размножение CAR-экспрессирующих клеток анти-CD19 под действием частиц или шариков, содержащих антитело анти-CD19 анти-ID, становится больше или увеличивается по сравнению с активацией, стимуляцией или размножением под действием других реагентов, таких, например, как реагенты шариков, конъюгированных с антителом анти-CD3/анти-CD28.
[119] В некоторых вариантах осуществления, предлагаемые композиции и способы вызывают размножение и активируют генно-инженерные Т-лимфоциты, которые экспрессируют рекомбинантные рецепторы или CAR, которые, когда вводятся субъекту, демонстрируют повышенную персистентность и/или пониженное истощение по сравнению с генно-инженерными Т-лимфоцитами, которые наращивают с помощью других технологий. В некоторых вариантах осуществления, генно-инженерные Т-лимфоциты с повышенной персистентностью и/или пониженным истощением демонстрируют лучшее сильнодействие у субъекта, которому они вводятся.
[120] Все публикации, включая патентные документы, научные статьи и базы данных, упоминаемые в настоящей заявке, включаются в качестве ссылок во всей своей полноте, для всех целей до такой же степени, как если бы каждая индивидуальная публикация индивидуально включалась в качестве ссылки. Если определение, приведенное в настоящем документе, противоречит или иным образом не совпадает с определением, приведенным в патентах, заявках, опубликованных заявках и других публикациях, которые включаются в настоящий документ в качестве ссылок, определение, приведенное в настоящем документе, преобладает над определением, которое включается в настоящий документ в качестве ссылки.
[121] Заглавия разделов, используемые в настоящем документе, предназначены только для целей организации и не должны рассматриваться как ограничивающие описанный предмет изобретения.
I. КОНЪЮГАТЫ ЧАСТИЦ
[122] В настоящем документе предлагаются частицы, такие как шарики, которые конъюгируются или иным образом присоединены к связывающей молекуле, которая связывается или распознается с помощью антигенсвязывающего домена рекомбинантного рецептора, такого как химерный рецептор антигена (CAR), и способы их использования. В некоторых вариантах осуществления, частицы, например, шарики, представляют собой частицы иные, чем клетки.
A. Частицы
[123] В некоторых вариантах осуществления, связывающая молекула, которая связывается или распознается с помощью антигенсвязывающего домена рекомбинантного рецептора, такого как химерный рецептор антигена (CAR), связывается или иным образом присоединяется к частице (например, к сферическим частицам), например, к поверхности частицы. В определенных вариантах осуществления, частица представляет собой частицу иную, чем клетка. В конкретных вариантах осуществления, частица может включать коллоидную частицу, микросферу, наночастицу, шарик, такой как магнитный шарик, или что-либо подобное. В некоторых вариантах осуществления, частицы или шарики являются биологически совместимыми, то есть нетоксичными. В определенных вариантах осуществления, частицы или шарики являются нетоксичными для культивируемых клеток, например, культивируемых Т-лимфоцитов. В конкретных вариантах осуществления, частицы являются монодисперсными. В определенных вариантах осуществления, “монодисперсный" охватывает частицы (например, сферические частицы) с размером в дисперсиях, имеющим стандартное отклонение меньше 5%, например, имеющим меньше 5% стандартное отклонение в диаметре.
[124] В некоторых вариантах осуществления, частица, описанная в настоящем документе (например, сферическая частица), обеспечивает твердую подложку или матрицу, с которой может связываться или к которому может присоединяться связывающая молекула, такая как связывающая молекула, описанная в настоящем документе (например, антиген или антитело), способом, который делает возможным взаимодействие между связывающей молекулой и клеткой, в частности, связывание между связывающей молекулой и рекомбинантным рецептором, например, CAR, экспрессируемым на поверхности клетки. В конкретных вариантах осуществления, взаимодействие между конъюгированной или присоединенной связывающей молекулой и клеткой можно использовать в способах облегчения, обогащения, активации, стимуляции и/или размножения одного или нескольких типов клеток в популяции клеток на основе экспрессирования или уровня экспрессирования одного или нескольких рекомбинантных рецепторов на поверхности клетки. В определенных вариантах осуществления, частица (например, сферическая частица) содержит одну или несколько связывающих молекул (например, антитело или антиген), которые связываются с антигенсвязывающей областью рекомбинантного рецептора, например, CAR, который экспрессируется на поверхности клетки.
[125] В некоторых вариантах осуществления, частица или шарик является биологически совместимым, то есть, состоит из материала, который является пригодным для биологического использования. В некоторых вариантах осуществления, частицы, например, шарики, являются нетоксичными для культивируемых клеток, например, культивируемых Т-лимфоцитов. В некоторых вариантах осуществления, частицы, например, шарики, могут представлять собой любые частицы, которые могут присоединять связывающие молекулы способом, который делает возможным взаимодействие между связывающей молекулой и клеткой. В определенных вариантах осуществления, частицы, например, шарики, могут представлять собой любые частицы, которые могут модифицироваться, например, поверхностно функционализироваться, чтобы сделать возможным присоединение связывающей молекулы на поверхности частиц. В некоторых вариантах осуществления, частицы, например, шарики, состоят из стекла, диоксида кремния, сложных полиэфиров гидроксикарбоновых кислот, полиангидридов дикарбоновых кислот или сополимеров гидроксикарбоновых кислот и дикарбоновых кислот. В некоторых вариантах осуществления, частицы, например, шарики, могут состоять или, по меньшей мере, частично состоять из сложных полиэфиров прямоцепных или разветвленных, замещенных или незамещенных, насыщенных или ненасыщенных, линейных или поперечно сшитых, алканиловых, галогеналкиловых, тиоалкиловых, аминоалкиловых, арильных, аралкильных, алкенильных, аралкенильных, гетероарильных или алкоксигидрокси кислот или полиангидридов прямоцепных или разветвленных, замещенных или незамещенных, насыщенных или ненасыщенных, линейных или поперечно сшитых, алканильных, галогеналкильных, тиоалкильных, аминоалкильных, арильных, аралкильных, алкенильных, аралкенильных, гетероарильных или алкоксидикарбоновых кислот. В дополнение к этому, частицы, например, шарики, могут представлять собой квантовые точки или состоять из квантовых точек, таких как полистирольные частицы квантовых точек, например, шарики. Можно также использовать частицы, например, шарики, содержащие смеси сложноэфирных и ангидридных связей (например, сополимеры гликолевой и себациновой кислоты). Например, частицы, например, шарики, могут содержать материалы, включая полимеры полигликолевой кислоты (PGA), полимеры полимолочной кислоты (PLA), полимеры полисебациновой кислоты (PSA), сополимеры молочная кислота - гликолевая кислота (PLGA), сополимеры [rho] молочная кислота - себациновая кислота (PLSA), сополимеры гликолевая кислота - себациновая кислота (PGSA), и тому подобное. Полимеры иные, чем частицы, например, шарики, могут содержать полимеры или сополимеры капролактонов, карбонатов, амидов, аминокислот, сложных ортоэфиров, ацеталей, цианоакрилатов и разлагаемых уретанов, а также их сополимеры с прямоцепными или разветвленными, замещенными или незамещенными, алканильными, галогеналкильными, тиоалкильными, аминоалкильными, алкенильными или ароматическими гидрокси- или дикарбоновыми кислотами или состоять из них. В дополнение к этому, биологически важные аминокислоты с химически активными боковыми группами, такие как лизин, аргинин, аспарагиновая кислота, глутаминовая кислота, серин, треонин, тирозин и цистеин или их энантиомеры, могут включаться в сополимеры вместе с любыми рассмотренными выше материалами для получения химически активных групп для конъюгирования со связывающими молекулами, такими как полипептидный антиген или антитела.
[126] В некоторых вариантах осуществления, частицы или шарики имеют диаметр больше, чем 0,001 мкм, больше, чем 0,01 мкм, больше, чем 0,05 мкм, больше, чем 0,1 мкм, больше, чем 0,2 мкм, больше, чем 0,3 мкм, больше, чем 0,4 мкм, больше, чем 0,5 мкм, больше, чем 0,6 мкм, больше, чем 0,7 мкм, больше, чем 0,8 мкм, больше, чем 0,9 мкм, больше, чем 1 мкм, больше, чем 2 мкм, больше, чем 3 мкм, больше, чем 4 мкм, больше, чем 5 мкм, больше, чем 6 мкм, больше, чем 7 мкм, больше, чем 8 мкм, больше, чем 9 мкм, больше, чем 10 мкм, больше, чем 20 мкм, больше, чем 30 мкм, больше, чем 40 мкм, больше, чем 50 мкм, больше, чем 100 мкм, больше, чем 500 мкм и/или больше, чем 1000 мкм. В некоторых вариантах осуществления, частицы или шарики имеют диаметр в пределах между или примерно между 0,001 мкм и 1000 мкм, 0,01 мкм и 100 мкм, 0,1 мкм и 10, мкм, 0,1 мкм и 100 мкм, 0,1 мкм и 10 мкм, 0,001 мкм и 0,01 мкм, 0,01 мкм и 0,1 мкм, 0,1 мкм и 1 мкм, 1 мкм и 10 мкм, 1 мкм и 2 мкм, 2 мкм и 3 мкм, 3 мкм и 4 мкм, 4 мкм и 5 мкм, 1 мкм и 5 мкм, и/или 5 мкм и 10 мкм, каждое, включительно. В определенных вариантах осуществления, частицы или шарики имеют средний диаметр 1 мкм и 10 мкм, каждое, включительно. В определенных вариантах осуществления, частицы, например, шарики, имеют диаметр 1 мкм или примерно 1 мкм. В конкретных вариантах осуществления, частицы, например, шарики, имеют средний диаметр 2,8 мкм или примерно 2,8 мкм. В некоторых вариантах осуществления, частицы, например, шарики, имеют диаметр 4,8 или примерно 4,8 мкм.
[127] В определенных вариантах осуществления, множество частиц, например, шариков, имеют однородный размер частиц. В некоторых вариантах осуществления, однородный размер частиц включает стандартное отклонение диаметра меньше, чем 10%, меньше, чем 5% или меньше, чем 1% от среднего диаметра множества. В конкретных вариантах осуществления, множество частиц, например, шариков, имеют стандартное отклонение диаметра меньше 10%, меньше 5% или меньше 1% от среднего диаметра множества.
[128] В конкретных вариантах осуществления, частицы (например, сферические частицы) имеют однородную форму. В некоторых вариантах осуществления, частицы, например, шарики, являются сферическими. В определенных вариантах осуществления, частицы, например, шарики, являются несферическими.
[129] В некоторых вариантах осуществления, частицы, например, шарики, имеют плотность больше, чем 0,001 г/см3, больше, чем 0,01 г/см3, больше, чем 0,05 г/см3, больше, чем 0,1 г/см3, больше, чем 0,5 г/см3, больше, чем 0,6 г/см3, больше, чем 0,7 г/см3, больше, чем 0,8 г/см3, больше, чем 0,9 г/см3, больше, чем 1 г/см3, больше, чем 1,1 г/см3, больше, чем 1,2 г/см3, больше, чем 1,3 г/см3, больше, чем 1,4 г/см3, больше, чем 1,5 г/см3, больше, чем 2 г/см3, больше, чем 3 г/см3, больше, чем 4 г/см3 или больше, чем 5 г/см3. В некоторых вариантах осуществления, частицы или шарики имеют плотность в пределах между или примерно между 0,001 г/см3 и 100 г/см3, 0,01 г/см3 и 50 г/см3, 0,1 г/см3 и 10 г/см3, 0,1 г/см3 и 0,5 г/см3, 0,5 г/см3 и 1 г/см3, 0,5 г/см3 и 1,5 г/см3, 1 г/см3 и 1,5 г/см3, 1 г/см3 и 2 г/см3 или 1 г/см3 и 5 г/см3. В некоторых вариантах осуществления, частицы или шарики имеют плотность, по меньшей мере, или примерно 0,5 г/см3, 0,5 г/см3, 0,6 г/см3, 0,7 г/см3, 0,8 г/см3, 0,9 г/см3, 1,0 г/см3, 1,1 г/см3, 1,2 г/см3, 1,3 г/см3, 1,4 г/см3, 1,5 г/см3, 1,6 г/см3, 1,7 г/см3, 1,8 г/см3, 1,9 г/см3 или 2,0 г/см3, каждое, включительно. В определенных вариантах осуществления, шарики или частицы имеют плотность равную или примерно равную 1,6 г/см3. В конкретных вариантах осуществления, шарики или частицы имеют плотность равную или примерно равную 1,5 г/см3. В определенных вариантах осуществления, частицы, например, шарики, имеют плотность равную или примерно равную 1,3 г/см3.
[130] В определенных вариантах осуществления, множество частиц или шариков имеют однородную плотность. В определенных вариантах осуществления, однородная плотность включает стандартное отклонение плотности меньше 10%, меньше 5% или меньше 1% от средней плотности частиц.
[131] В некоторых вариантах осуществления, частицы или шарики имеют удельную площадь поверхности в пределах между или примерно между 0,001 м2 на каждый грамм частиц, например, шариков, (м2/г) и 1000 м2/г, 0,010 м2/г и 100 м2/г, 0,1 м2/г и 10 м2/г, 0,1 м2/г и 1 м2/г, 1 м2/г и 10 м2/г, 10 м2/г и 100 м2/г, 0,5 м2/г и 20 м2/г, 0,5 м2/г и 5 м2/г или 1 м2/г и 4 м2/г, каждое, включительно. В некоторых вариантах осуществления, частицы или шарики имеют удельную площадь поверхности от или примерно от 1 м2/г до 4 м2/г.
[132] В конкретных вариантах осуществления, частицы (например, сферические частицы) имеют относительную плотность, то есть отношение плотности частиц, например, шариков, к плотности воды, в пределах между или примерно между 0,01 и 100, 0,1 и 10, 0,5 и 5, 1 и 10, 1 и 2, 1,1 и 1,8 или 1,2 и 1,5, каждое, включительно. В определенных вариантах осуществления, частицы, например, шарики, имеют относительную плотность 1,2 и 1,5. В определенных вариантах осуществления, частицы, например, шарики, являются монодисперсными, и их относительная плотность является однородной. В конкретных вариантах осуществления, частицы, например, шарики, с однородной относительной плотностью имеют стандартное отклонение относительной плотности меньше 10%, меньше 5% или меньше 1%. В различных вариантах осуществления, частицы являются монодисперсными и имеют относительную плотность со стандартным отклонением меньше 10%, меньше 5% или меньше 1%.
[133] В определенных вариантах осуществления, поверхность частицы содержит присоединенные биомолекулы, которые могут связывать или присоединять связывающие молекулы. В конкретных вариантах осуществления, биомолекулы представляют собой полипептиды. В некоторых вариантах осуществления, частицы, например, шарики, содержат поверхностно экспонируемый белок A, белок G или биотин.
[134] В некоторых вариантах осуществления, частица содержит одно или несколько слоев покрытия или покрытия, таких как один или несколько слоев покрытий или покрытия на поверхности частицы (например, поверхностное покрытие). В некоторых вариантах осуществления, один или несколько слоев покрытий или покрытия создают материал для конъюгирования или связывания со связывающей молекулой, например, слой покрытия, который является или может быть поверхностно функционализированным. В определенных вариантах осуществления, слой покрытия содержит или может присоединять поверхностно экспонируемые функциональные группы. В конкретных вариантах осуществления, покрытие содержит или может присоединять поверхностно экспонируемые карбоксильные группы, амино группы, гидроксильные группы, тозильные группы, эпокси группы, хлорметильные группы или их сочетания. В некоторых вариантах осуществления, слой покрытия или покрытия является гидрофобным. В конкретных вариантах осуществления слой покрытия или покрытия является негидрофобным.
1. Магнитные частицы
[135] В некоторых вариантах осуществления, частица (например, сферическая частица) взаимодействует с магнитным полем. В некоторых вариантах осуществления, частица представляет собой магнитную частицу (например, магнитную сферическую частицу). В некоторых вариантах осуществления, магнитная частица является парамагнитной. В конкретных вариантах осуществления, магнитная частица является суперпарамагнитной. В определенных вариантах осуществления, частицы, например, шарики, не проявляются никаких магнитных свойств, если только они не экспонируются для магнитного поля.
[136] В конкретных вариантах осуществления, частица может представлять собой композитную частицу, содержащую внутреннюю сердцевину. В некоторых вариантах осуществления, внутренняя сердцевина представляет собой магнитную сердцевину, парамагнитную сердцевину или суперпарамагнитную сердцевину. В некоторых вариантах осуществления, внутренняя сердцевина (например, магнитная сердцевина) представляет собой или содержит металл. В некоторых вариантах осуществления, металл может представлять собой, но, не ограничиваясь этим, железо, никель, медь, кобальт, гадолиний, марганец, тантал, цинк, цирконий или любые их сочетания. Пригодные для использования вещества, которые могут включаться во внутреннюю сердцевину, описанную в настоящем документе (например, магнитную сердцевину), включают, но, не ограничиваясь этим, оксиды металлов (например, оксиды железа), ферриты (например, марганцевые ферриты, кобальтовые ферриты, никелевые ферриты, и тому подобное), гематит и сплавы металлов (например, CoTaZn). В некоторых вариантах осуществления, внутренняя сердцевина содержит один или несколько компонентов из феррита, металла, сплава металла, оксида железа или диоксида хрома. В некоторых вариантах осуществления, внутренняя сердцевина содержит элементарное железо или его соединение. В некоторых вариантах осуществления, внутренняя сердцевина содержит одно или несколько соединений из магнетита (Fe3O4), магхемита (γFe2O3) или грейгита (Fe3S4). В некоторых вариантах осуществления, внутренняя сердцевина содержит оксид железа (например, Fe3O4).
[137] В определенных вариантах осуществления, частица содержит магнитную, парамагнитную и/или суперпарамагнитную сердцевину, которая покрыта поверхностно функционализированным слоем покрытия или покрытием. В некоторых вариантах осуществления, частица содержит поверхностно экспонируемые тозильные группы.
[138] В некоторых вариантах осуществления, слой покрытия может содержать материал, который может включать, но, не ограничиваясь этим, полимер, полисахарид, диоксид кремния, жирную кислоту, белок, углерод или их сочетание. В некоторых вариантах осуществления, полимер может представлять собой полиэтиленгликоль, сополимер молочная кислота - гликолевая кислота, полиглутаральдегид, полиуретан, полистирол или поливиниловый спирт. В определенных вариантах осуществления, наружный слой покрытия или покрытия содержит полистирол. В некоторых вариантах осуществления, слой покрытия содержит или включает материал, который представляет собой или содержит белок, который представляет собой альбумин, например, сывороточный альбумин человека), белок A и белок G. В некоторых вариантах осуществления, углерод представляет собой акриламид или малеиновую кислоту. В некоторых вариантах осуществления, материал соединен, связан или конъюгирован со связывающей молекулой, описанной в настоящем документе.
[139] В некоторых вариантах осуществления, частица, описанная в настоящем документе (например, сферическая частица) может иметь внутреннюю сердцевину и слой покрытия (например, защитное покрытие), где слой покрытия содержит один или несколько материалов, описанных в настоящем документе. В некоторых вариантах осуществления, слой покрытия является гидрофобным. В определенных вариантах осуществления, слой покрытия является гидрофильным. В некоторых вариантах осуществления, частица, описанная в настоящем документе (например, сферическая частица), имеет сердцевину из оксида металла (например, внутреннюю сердцевину из оксида железа) и слой покрытия (например, защитный слой покрытия), где слой покрытия содержит полистирол.
[140] Частицы (например, сферические частицы), используемые в способах, описанных в настоящем документе, могут быть произведены или получены коммерчески. Частицы, например, шарики, включая способы получения частиц, например, шариков, хорошо известны в данной области. Смотри, например, патенты США №№6074884; 5834121; 5395688; 5356713; 5318797; 5283079; 5232782; 5091206; 4774265; 4654267; 4554088; 4490436; 4452773; публикацию заявки на патент США №20100207051; и Sharpe, Pau T., Methods of Cell Separation, Elsevier, 1988. Коммерчески доступные частицы, например, шарики, (например, сферические частицы) включают, но, не ограничиваясь этим, ProMagTM (PolySciences, Inc.); COMPELTM (PolySciences, Inc.); BioMag® (PolySciences, Inc.), включая BioMag® Plus (PolySciences, Inc.) и BioMag® Maxi (Bang Laboratories, Inc.); M-PVA (Cehmagen Biopolymer Technologie AG); SiMAG (Chemicell GmbH); beadMAG (Chemicell GmbH); MagaPhase® (Cortex Biochem); Dynabeads® (Invitrogen), включая Dynabeads® M-280 Sheep Anti-rabbit IgG (Invitrogen), Dynabeads® FlowCompTM (например, Dynabeads® FlowCompTMHuman CD3, Invitrogen), Dynabeads® M-450 (например, Dynabeads® M-450 Tosylactivated, Invitrogen), Dynabeads® UntouchedTM (например, Dynabeads® UntouchedTM Human CD8 T Cells, Invitrogen) и Dynabeads®, которые связывают, вызывают размножение и/или активируют Т-лимфоциты (например, Dynabeads® Human T-Activator CD3/CD28 for T Cell Expansion and Activation, Invitrogen); Estapor® M (Merk Chimie SAS); Estapor® EM (Merk Chimie SAS); MACSiBeadsTM Particles (например, anti-biotin MACSiBead Particles, Miltenyi Biotec, catalog #130-091-147); Streptamer® Magnetic Beads (IBA BioTAGnology); Strep-Tactin® Magnetic Beads (IBA BioTAGnology); Sicastar®-M (Micormod Partikeltechnologie GmbH) Micromer®-M (Micromod Partikeltechnologie); MagneSilTM (Promega GmbH); MGP (Roche Applied Science Inc.); Pierce™ Protein G Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™ Protein A Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™ Protein A/G Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™ NHS-Activated Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™ Protein L Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™ Anti-HA Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™Anti-c-Myc Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™ Glutathione Magnetic Beads (Thermo Fisher Scientific Inc.); Pierce™ Streptavidin Magnetic Beads (Thermo Fisher Scientific Inc.); MagnaBindTM Magnetic Beads (Thermo Fisher Scientific Inc.); Sera-MagTM Magnetic Beads (Thermo Fisher Scientific Inc.); Anti-FLAG® M2 Magnetic Beads (Sigma-Aldrich); SPHEROTM Magnetic Particles (Spherotech Inc.); и HisPurTM Ni-NTA Magnetic Beads (Thermo Fisher Scientific Inc.).
[141] В определенных вариантах осуществления, частица представляет собой монодисперсную суперпарамагнитную сферическую частицу, содержащую суперпарамагнитную железную сердцевину, например, сердцевину из магнетита (Fe3O4) или магхемита (γFe2O3), полистирольный слой покрытия или покрытие, и функционализированную поверхность, содержащую экспонируемые тозильные группы. В определенных вариантах осуществления, частицы, например, шарики, имеют плотность примерно 1,5 г/см3 и площадь поверхности примерно от 1 м2/г примерно до 4 м2/г. В конкретных вариантах осуществления, частицы, например, шарики, представляют собой монодисперсные суперпарамагнитные частицы, например, шарики, которые имеют диаметр примерно 4,5 мкм и плотность примерно 1,5 г/см3. В некоторых вариантах осуществления, частицы, например, шарики, частицы представляют собой монодисперсные суперпарамагнитные частицы, которые имеют средний диаметр примерно 2,8 мкм и плотность примерно 1,3 г/см3.
2. Олигомерные частицы
[142] В некоторых вариантах осуществления, частица представляет собой олигомер или полимер. В некоторых вариантах осуществления, частица представляет собой олигомер или полимер, состоящий из белков, например, стрептавидина. В некоторых вариантах осуществления, частица представляет собой олигомер или полимер, который может генерироваться посредством прямого или косвенного связывания индивидуальных молекул белка, например, стрептавидина или его варианта, как он встречается в природе, либо посредством прямого или косвенного связывания индивидуальных молекул мономера или комплекса субъединиц, которые составляют индивидуальную молекулу (например, прямого или косвенного связывания димеров, тримеров, тетрамеров, и тому подобное, белка как он встречается в природе). Например, тетрамерный гомодимер или гетеродимер стрептавидина или авидина может упоминаться как индивидуальная молекула или как наименьший строительный блок соответствующего олигомера или полимера. В некоторых вариантах осуществления, олигомер или полимер может содержать связь, по меньшей мере, 2 индивидуальных молекул белка (например, представлять собой 2-мер) или может представлять собой, по меньшей мере, 3-мер, 4-мер, 5-мер, 6-мер, 7-мер, 8-мер, 9-мер, 10-мер, 11-мер, 12-мер, 13-мер, 14-мер, 15-мер, 16-мер, 17-мер, 18-мер, 19-мер, 20-мер, 25-мер, 30-мер, 35-мер, 40-мер, 45-мер или 50-мер из индивидуальных молекул белка (например, мономеров, тетрамеров). В некоторых вариантах осуществления, реагент представляет собой мультимер или олигомерный реагент представляет собой мультимерный реагент. В конкретных вариантах осуществления, частица представляет собой олигомер или полимер, который содержит стрептавидин или мутеин стрептавидина (например, STREP-TACTIN® или STREP-TACTIN® XT мутеины стрептавидина)
[143] Олигомеры могут генерироваться с использованием любых способов, известных в данной области, таких как любые способы, описанные в опубликованной заявке на патент США № US 2004/0082012. В некоторых вариантах осуществления, олигомер или полимер содержит две или более индивидуальных молекул, которые могут поперечно сшиваться, например, с помощью полисахарида или бифункционального линкера.
[144] В некоторых вариантах осуществления, частица представляет собой олигомер или полимер, который получают посредством поперечной сшивки индивидуальных молекул или комплекса субъединиц, которые составляют индивидуальную молекулу, в присутствии полисахарида. В некоторых вариантах осуществления, частицы представляют собой олигомеры или полимеры, которые можно получить посредством введения карбоксильных остатков в полисахарид, например, декстран. В некоторых аспектах, индивидуальные молекулы частицы (например, мономеры, тетрамеры) могут связываться через первичные амино группы внутренних лизиновых остатков и/или свободного N-конца с карбоксильными группами в основной цепи декстрана с использованием обычного карбодиимидного химического механизма. В некоторых вариантах осуществления, реакция связывания осуществляется при молярном отношении примерно 60 моль индивидуальных молекул реагента (например, мономеров, тетрамеров) на моль декстрана.
[145] В некоторых вариантах осуществления частица представляет собой олигомер или полимер одного или нескольких соединений из стрептавидина или авидина или любого аналога или мутеина стрептавидина, например, Strep-Tactin® или Strep-Tactin® XT) или аналога или мутеина авидина (например, нейтравидина). В некоторых вариантах осуществления, авидин или стрептавидин содержит сайт связывания Z, который представляет собой природный сайт связывания биотина авидина или стрептавидина, для которого могут иметься до четырех сайтов связывания в индивидуальной молекуле (например, тетрамер содержит четыре сайты связывания Z), при этом гомо-тетрамер может содержать до 4 сайтов связывания, которые являются одинаковыми, например, Z1, в то время как гетеро-тетрамер может содержать до 4 сайты связывания, которые могут быть различными, например, содержать Z1 и Z2. В некоторых вариантах осуществления, олигомер генерируется или получается из множества индивидуальных молекул (например, множества гомо-тетрамеров) одного и тоже стрептавидина, мутеина стрептавидина, авидина или мутеина авидина, в этом случае все сайт связывания Z, например, Z1, олигомера являются одинаковыми. Например, в некоторых случаях, олигомер может содержать множество сайтов связывания Z1, например, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 40, 45, 50 или более сайтов связывания Z1. В некоторых вариантах осуществления, олигомер генерируется или получается из множества индивидуальных молекул, которые могут представлять собой гетеротетрамеры стрептавидина, мутеин стрептавидина, авидин или мутеин авидина, и/или из множества двух или более различных индивидуальных молекул (например, различных гомотетрамеров) стрептавидина, мутеина стрептавидина, авидина или мутеина авидина, которые отличаются своими сайтами связывания Z, например, Z1 и Z2, в этом случае в олигомере может присутствовать множество различных сайтов связывания Z, например, Z1 и Z2. Например, в некоторых случаях, олигомер может содержать множество сайтов связывания Z1 и множество сайтов связывания Z, которые, в сочетании, могут включать, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 40, 45, 50 или более объединенных сайтов связывания Z1 и Z2.
[146] В некоторых вариантах осуществления, частица представляет собой олигомер или полимер, который получают посредством поперечной сшивки индивидуальных молекул или комплекса субъединиц, которые составляют индивидуальную молекулу, с использованием бифункционального линкера или другого химического линкера, такого как авидин, или с помощью других способов, известных в данной области. В некоторых аспектах, поперечно сшитые олигомеры или полимеры стрептавидина или авидина или любого мутеина или аналога стрептавидина или авидина могут быть получены посредством поперечной сшивки индивидуальных молекул стрептавидина или авидина с помощью бифункциональных молекул, служащих как линкер, таких как глютаральдегид, или с помощью других способов, описанных в данной области. Например, можно генерировать олигомеры мутеинов стрептавидина посредством введения тиольных групп в мутеин стрептавидина (это можно сделать, например, посредством взаимодействия мутеина стрептавидина с 2-иминотиоланом (реагент Трота) и посредством активации, например, в отдельной реакции амино групп, доступных в мутеине стрептавидина. В некоторых вариантах осуществления, эта активация амино групп может достигаться посредством реакции мутеина стрептавидина с коммерчески доступным гетеробифункциональным кросслинкером, таким как сульфосукцинимидил 4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо SMCC) или сукцинимидил-6-[(β-малеимидопропионамид)гексаноат (SMPH). В некоторых таких вариантах осуществления, два продукта реакции, полученные таким образом, смешиваются вместе, как правило, это приводит к реакции тиольных групп, содержащихся в одной загрузке модифицированного мутеина стрептавидина, с активированными (например, с помощью малеинимидных функциональных групп) аминокислотами другой загрузки модифицированного мутеина стрептавидина. В некоторых случаях, при этой реакции образуются мультимеры/олигомеры мутеина стрептавидина. Эти олигомеры могут иметь любое пригодное для использования количество индивидуальных молекул, например, по меньшей мере, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 40, 45, 50 или больше, и степень олигомеризации может изменяться согласно условиям реакции.
[147] В некоторых вариантах осуществления, олигомерный или полимерный реагент может быть выделен с помощью эксклюзионной хроматографии и в качестве частиц можно использовать любую желаемую фракцию. В некоторых вариантах осуществления, после взаимодействия, модифицированного мутеина стрептавидина в присутствии 2-иминотиола и гетеробифункционального кросслинкера, такого как сульфо SMCC, олигомерный или полимерный реагент может быть выделен с помощью эксклюзионной хроматографии и любую желаемую фракцию можно использовать в качестве частиц. В некоторых вариантах осуществления, олигомеры не имеют (и не должны иметь) одну молекулярную массу, но для них можно наблюдать статистическое распределение масс, такое как распределение Гаусса. В некоторых случаях, любой олигомер с более, чем тремя тетрамерами стрептавидина или мутеина, например, гомотетрамерами или гетеротетрамерами, можно использовать в качестве растворимой частицы, например, как правило, 3-50 тетрамеров, например, гомотетрамеров или гетеротетрамеров, 10-40 тетрамеров, например, гомотетрамеров или гетеротетрамеров или 25-35 тетрамеров, например, гомотетрамеров или гетеротетрамеров. Олигомеры могут иметь, например, от 3 до 25 тетрамеров мутеина стрептавидина, например, гомотетрамеров или гетеротетрамеров. В некоторых аспектах, при молекулярной массе примерно 50 кДа для мутеинов стрептавидина, растворимые олигомеры могут иметь молекулярную массу от или примерно от 150 кДа до 2000 кДа, от 150 кДа до 1500 кДа, от 150 кДа до 1250 кДа, от 150 кДа до 1000 кДа, от 150 кДа до 500 кДа или от 150 кДа до 300 кДа, от 300 кДа до 2000 кДа, от 300 кДа до 1500 кДа, от 300 кДа до 1250 кДа, от 300 кДа до 1000 кДа, от 300 кДа до 500 кДа, от 500 кДа до 2000 кДа, от 500 кДа до 1500 кДа, от 500 кДа до 1250 кДа, от 500 кДа до 1000 кДа, от 1000 кДа до 2000 кДа, от 1000 кДа до 1500 кДа, от 1000 кДа до 1250 кДа, от 1250 кДа до 2000 кДа или от 1500 кДа до 2000 кДа. Как правило, поскольку каждая молекула/мутеин стрептавидина имеет четыре сайта связывания биотина, так что реагент может обеспечить 12-160 сайтов связывания Z, например, 12-100 сайтов связывания Z.
B. Связывающие молекулы
[148] В настоящем документе предлагаются связывающие молекулы, например, полипептидные антигены или антитела, которые связываются или распознаются антигенсвязывающим доменом рекомбинантного рецептора, такого как CAR, которые конъюгируются или присоединяются к частице, например, сферической частице. В некоторых вариантах осуществления, связывающая молекула представляет собой полипептид. В определенных вариантах осуществления, связывающая молекула включает любой полипептид, для связывания или распознавания которого может конструироваться рекомбинантный рецептор, такой как рецептор антигена, например, CAR. В конкретных вариантах осуществления, связывающая молекула представляет собой антиидиотипическое антитело, которое связывает или распознает антигенсвязывающий домен рекомбинантного рецептора, такого как рецептор антигена, например, CAR. В конкретных вариантах осуществления, связывающая молекула представляет собой полипептид, который связывается или распознается антигенсвязывающим доменом рекомбинантного рецептора, такого рецептор антигена, например, CAR. В определенных вариантах осуществления, связывающая молекула представляет собой полипептид, который связывается или распознается антигенсвязывающим доменом CAR.
[149] В некоторых вариантах осуществления, связывающая молекула связывается или распознается CAR, который не содержит трансмембранного домена или внутриклеточного сигнального домена иммуноглобулиноподобного рецептора клеток киллеров (KIR). В определенных вариантах осуществления, связывающая молекула связывается или распознается CAR, который не содержит трансмембранного домена или внутриклеточного домена, из любых из KIR2DS2, KIR2DL3, KIR2DL1, KIR2DL2, KIR2DL4, KIR2DL5A, KIR2DL5B, KIR2DS1, KIR2DS3, KIR2DS4, KIR2DS5, KIR3DL1, KIR3DS1, KIR3DL2, KIR3DL3, KIR2DP1 и KIR3DP1.
1. Антигены
[150] В некоторых вариантах осуществления, связывающая молекула представляет собой антиген, например, рекомбинантный антиген или его фрагмент. В определенных вариантах осуществления, антиген представляет собой полипептид или часть полипептида, которая ассоциируется с заболеванием, например, раком. В некоторых вариантах осуществления, антиген представляет собой полипептид или вариант или фрагмент полипептида, который экспрессируется на поверхности клетки, которая ассоциируется с заболеванием, например, на раковой клетке и/или опухолевой клетке.
[151] В некоторых вариантах осуществления, антиген представляет собой или включает интегрин αvβ6 (интегрин avb6), антиген созревания В-клеток (BCMA), B7-H3, B7-H6, угольную ангидразу 9 (CA9, также известную как CAIX или G250), антиген рака яичек, раково-тестикулярный антиген 1B (CTAG, также известный как NY-ESO-1 и LAGE-2), канцероэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, протеогликан хондроитин-4-сульфат (CSPG4), белок эпидермального фактора роста (EGFR), мутацию рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), эфрин B2, рецептор эфрина A2 (EPHa2), рецептор эстрогена, белок 5 подобный Fc-рецептору (FCRL5; также известный как гомолог 5 Fc-рецептора или FCRH5), рецептор фетального ацетилхолина (фетального AchR), фолатсвязывающий белок (FBP), рецептор фолата альфа, ганглиозид GD2, O-ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), глипикана-3 (GPC3), связанный с белком G рецептор 5D (GPRC5D), Her2/neu (тирозинкиназный рецептор erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеры erbB, высокомолекулярный антиген человека, ассоциированный с меланомой (HMW-MAA), поверхностный антиген гепатита B, антиген лейкоцита человека A1 (HLA-A1), антиген лейкоцита человека A2 (HLA-A2), рецептор IL-22 альфа(IL-22Rα), рецептор IL-13 альфа 2 (IL-13Rα2), домен рецептора вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1-CAM), эпитоп CE7 L1-CAM, обогащенную лейцином повторяющуюся единицу, содержащую член A семейства 8 (LRRC8A), антиген Ley, антиген, ассоциированный с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелин (MSLN), c-Met, цитомегаловирус мышей (CMV), муцин 1 (MUC1), MUC16, лиганды элемента D группы природных киллеров 2 (NKG2D), мелан A (MART-1), молекулу адгезии нейральных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простата-специфичный антиген, антиген стволовых клеток простаты (PSCA), простата-специфичный мембранный антиген (PSMA), орфанный рецептор 1 подобный тирозинкиназному рецептору (ROR1), сурвивин, гликопротеин трофобластов (TPBG также известный как 5T4), ассоциированный с опухолью гликопротеин 72 (TAG72), тирозиназа-зависимый белок 1 (TRP1, также известный как TYRP1 или gp75), тирозиназа-зависимый белок 2 (TRP2, также известный как допахромтаутомераза, допахром-дельта-изомераза или DCT), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор 2 фактора роста эндотелия сосудов (VEGFR2), опухоль Вильмса 1 (WT-1), патоген-специфичный или патоген-экспрессируемый антиген или антиген, ассоциированный с универсальной меткой, и/или биотинилированные молекулы, и/или молекулы, экспрессируемые HIV, HCV, HBV или другими патогенами. Антигены целевые для рецепторов в некоторых вариантах осуществления включают антигены, ассоциируемые с В-клеточным лейкозом, такие как любой из ряда известных маркеров В-клеток. В некоторых вариантах осуществления, антиген представляет собой или содержит CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig каппа, Ig лямбда, CD79a, CD79b или CD30.
[152] В некоторых вариантах осуществления, связывающая молекула содержит часть полипептидного антигена, который распознается или связывается рекомбинантным рецептором и/или CAR. В конкретных вариантах осуществления, связывающая молекула содержит эпитоп, который распознается или связывается рекомбинантным рецептором и/или CAR. В определенных вариантах осуществления, часть полипептидного антигена содержит, примерно или содержит, по меньшей мере, 10, 15, 20, 25, 30, 35, 40, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 250, 300, 400 или 500 аминокислот, в некоторых случаях, заменимых аминокислот, полипептида, который распознается или связывается рекомбинантным рецептором и/или CAR. В определенных вариантах осуществления, часть полипептида содержит последовательность аминокислот эпитопа, который распознается рекомбинантным рецептором и/или CAR.
[153] В определенных вариантах осуществления, связывающая молекула представляет собой полипептидный вариант, который имеет, примерно имеет или имеет, по меньшей мере, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 99,5% идентичность последовательности аминокислот с полипептидом, который связывается и/или распознается рекомбинантным рецептором и/или CAR.
[154] В определенных вариантах осуществления, частица связывается со связывающей молекулой, содержащей часть полипептида антиген, где часть представляет собой часть антигена, которая связывается и/или распознается или может потенциально связываться или распознаваться рекомбинантным рецептором, то есть CAR. В некоторых вариантах осуществления, связывающая молекула содержит часть антигена, содержащую эпитоп, который распознается рекомбинантным рецептором. В определенных вариантах осуществления, часть антигена представляет собой часть… В некоторых вариантах осуществления, антиген представляет собой или содержит интегрин αvβ6 (интегрин avb6), антиген созревания В-клеток (BCMA), B7-H3, B7-H6, угольную ангидразу 9 (CA9, также известную как CAIX или G250), антиген рака яичек, раково-тестикулярный антиген 1B (CTAG, также известный как NY-ESO-1 и LAGE-2), канцероэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, протеогликан хондроитин-4-сульфат (CSPG4), белок эпидермального фактора роста (EGFR), мутацию рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), эфринВ2, рецептор эфрина A2 (EPHa2), рецептор эстрогена, белок 5 подобный Fc-рецептору (FCRL5; также известный как гомолог 5 Fc-рецептора или FCRH5), рецептор фетального ацетилхолина (фетального AchR), фолатсвязывающий белок (FBP), рецептор фолата альфа, ганглиозид GD2, O-ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), глипикан-3 (GPC3), связанный с белком G рецептор 5D (GPRC5D), Her2/neu (тирозинкиназный рецептор erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеры erbB, высокомолекулярный антиген человека, ассоциированный с меланомой (HMW-MAA), поверхностный антиген гепатита B, антиген лейкоцита человека A1 (HLA-A1), антиген лейкоцита человека A2 (HLA-A2), рецептор IL-22 альфа(IL-22Rα), рецептор IL-13 альфа 2 (IL-13Rα2), домен рецептора вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1-CAM), эпитоп CE7 L1-CAM, обогащенный лейцином повторяющаяся единица, содержащее член A семейство 8 (LRRC8A), антиген Ley, антиген, ассоциированный с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелин (MSLN), c-Met, цитомегаловирус мышей (CMV), муцин 1 (MUC1), MUC16, лиганды элемента D группы природных киллеров 2 (NKG2D), мелану A (MART-1), молекула адгезии нейральных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простата-специфичный антиген, антиген стволовых клеток простаты (PSCA), простата-специфичный мембранный антиген (PSMA), орфанный рецептор 1 подобный тирозинкиназному рецептору (ROR1), сурвивин, гликопротеин трофобластов (TPBG также известный как 5T4), ассоциированный с опухолью гликопротеин 72 (TAG72), тирозиназа-зависимый белок 1 (TRP1, также известный как TYRP1 или gp75), тирозиназа-зависимый белок 2 (TRP2, также известный как допахромтаутомераза, допахром-дельта-изомераза или DCT), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор 2 фактора роста эндотелия сосудов (VEGFR2), опухоль Вильмса 1 (WT-1), патоген-специфичный или патоген-экспрессируемый антиген или антиген, ассоциированный с универсальной меткой, и/или биотинилированные молекулы, и/или молекулы, экспрессируемые HIV, HCV, HBV или другими патогенами. Антигены целевые для рецепторов в некоторых вариантах осуществления включают антигены, ассоциируемые с В-клеточным лейкозом, такой как любой из ряда известных маркеров В-клеток. В некоторых вариантах осуществления, антиген представляет собой или содержит CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig каппа, Ig лямбда, CD79a, CD79b или CD30.
[155] В определенных вариантах осуществления, частица связывается со связывающей молекулой, содержащей часть полипептида BCMA. В некоторых вариантах осуществления, частица связывается со связывающей молекулой, содержащей часть полипептида CD22. В определенных вариантах осуществления, частица связывается с связывающей молекулой, содержащей часть полипептида ROR1.
[156] В определенных вариантах осуществления, часть полипептидного антигена представляет собой часть полипептида BCMA. В определенных вариантах осуществления, полипептидный антиген имеет, имеет примерно или имеет, по меньшей мере, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 99,5% идентичность последовательности аминокислот, по меньшей мере, с 10, по меньшей мере, с 15, по меньшей мере, с 20, по меньшей мере, с 25, по меньшей мере, с 30, по меньшей мере, с 35, по меньшей мере, с 40, по меньшей мере, с 50, по меньшей мере, с 55, по меньшей мере, с 60, по меньшей мере, с 65, по меньшей мере, с 70, по меньшей мере, с 75, по меньшей мере, с 80, по меньшей мере, с 85, по меньшей мере, с 90, по меньшей мере, с 95, по меньшей мере, с 100, по меньшей мере, с 110, по меньшей мере, с 120, по меньшей мере, с 130, по меньшей мере, с 140, по меньшей мере, с 150, по меньшей мере, с 160, по меньшей мере, с 170 или, по меньшей мере, с 180 заменимыми аминокислотами полипептида BCMA. В конкретных вариантах осуществления, вариант полипептид BCMA содержит последовательность аминокислот, которая является примерно или является, по меньшей мере, на 70%, 75%, 80%, 85%, 90%, 95%, 97% или 98% идентичной последовательности аминокислот эпитопа BCMA, который связывается и/или распознается рекомбинантным рецептором и/или CAR.
[157] В конкретных вариантах осуществления, антиген представляет собой BCMA или его часть или вариант. В некоторых вариантах осуществления, полипептид BCMA представляет собой полипептид BCMA млекопитающих. В конкретных вариантах осуществления, полипептид BCMA представляет собой полипептид BCMA человека. В некоторых вариантах осуществления, антиген BCMA представляет собой или содержит внеклеточный домен BCMA или его часть, содержащую эпитоп, распознаваемый рецептором антигена, например, CAR. В определенных вариантах осуществления, антиген BCMA представляет собой или содержит полипептид с последовательностью аминокислот, по меньшей мере, с 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичностью последовательностей с SEQ ID NO: 1 или его фрагмент, содержащий, по меньшей мере, 50, по меньшей мере, 55, по меньшей мере, 60, по меньшей мере, 65, по меньшей мере, 70, по меньшей мере, 75, по меньшей мере, 80, по меньшей мере, 85, по меньшей мере, 90, по меньшей мере, 95, по меньшей мере, 100, по меньшей мере, 110, по меньшей мере, 120, по меньшей мере, 130, по меньшей мере, 140, по меньшей мере, 150, по меньшей мере, 160, по меньшей мере, 170 или, по меньшей мере, 180 заменимых аминокислот из SEQ ID NO: 1. В некоторых вариантах осуществления, антиген BCMA представляет собой или содержит последовательность, приведенную в SEQ ID NO: 1, или ее часть, которая представляет собой или содержит эпитоп, распознаваемый рецептором антигена, например, CAR.
[158] В некоторых вариантах осуществления, антиген представляет собой ROR1 или его часть или вариант. В определенных вариантах осуществления, полипептид ROR1 является полипептидом млекопитающих. В конкретных вариантах осуществления, полипептид ROR1 представляет собой полипептид человека. В некоторых вариантах осуществления, антиген ROR1 представляет собой или содержит внеклеточный домен ROR1 или его часть, содержащую эпитоп, распознаваемый рецептором антигена, например, CAR. В некоторых вариантах осуществления, антиген ROR1 представляет собой полипептид с последовательностью аминокислот, по меньшей мере, с 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичностью последовательностей с SEQ ID NO: 31 или его фрагмент, содержащий, по меньшей мере, 50, по меньшей мере, 55, по меньшей мере, 60, по меньшей мере, 65, по меньшей мере, 70, по меньшей мере, 75, по меньшей мере, 80, по меньшей мере, 85, по меньшей мере, 90, по меньшей мере, 95, по меньшей мере, 100, по меньшей мере, 110, по меньшей мере, 120, по меньшей мере, 130, по меньшей мере, 140, по меньшей мере, 150, по меньшей мере, 160, по меньшей мере, 170 или, по меньшей мере, 180 заменимых аминокислот из SEQ ID NO: 31. В некоторых вариантах осуществления, антиген ROR содержит последовательность, приведенную в SEQ ID NO: 31, или ее часть, содержащую эпитоп, распознаваемый рецептором антигена, например, CAR.
[159] В некоторых вариантах осуществления, антиген представляет собой CD22 или его часть или вариант. В определенных вариантах осуществления, полипептид CD22 представляет собой полипептид млекопитающего. В конкретных вариантах осуществления, полипептид CD22 представляет собой полипептид человека. В некоторых вариантах осуществления, антиген представляет собой внеклеточный домен CD22 или его часть, содержащую эпитоп, распознаваемый рецептором антигена, например, CAR. В некоторых вариантах осуществления, антиген представляет собой полипептид с последовательностью аминокислот, по меньшей мере, с 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичностью последовательностей с SEQ ID NO: 29 или его фрагмент, содержащий, по меньшей мере, 50, по меньшей мере, 55, по меньшей мере, 60, по меньшей мере, 65, по меньшей мере, 70, по меньшей мере, 75, по меньшей мере, 80, по меньшей мере, 85, по меньшей мере, 90, по меньшей мере, 95, по меньшей мере, 100, по меньшей мере, 110, по меньшей мере, 120, по меньшей мере, 130, по меньшей мере, 140, по меньшей мере, 150, по меньшей мере, 160, по меньшей мере, 170 или, по меньшей мере, 180 заменимых аминокислот из SEQ ID NO: 29. В некоторых вариантах осуществления, антиген CD22 содержит последовательность, приведенную в SEQ ID NO: 29, или ее часть, содержащую эпитоп, распознаваемый рецептором антигена, например, CAR.
[160] В некоторых вариантах осуществления, часть полипептидного антигена представляет собой часть полипептида BCMA. В определенных вариантах осуществления, часть полипептидного антиген представляет собой часть полипептида CD22. В конкретных вариантах осуществления, часть полипептидного антигена представляет собой часть полипептида ROR1. В определенных вариантах осуществления, часть полипептида содержит, по меньшей мере, 10, по меньшей мере, 15, по меньшей мере, 20, по меньшей мере, 25, по меньшей мере, 30, по меньшей мере, 35, по меньшей мере, 40, по меньшей мере, 50, по меньшей мере, 55, по меньшей мере, 60, по меньшей мере, 65, по меньшей мере, 70, по меньшей мере, 75, по меньшей мере, 80, по меньшей мере, 85, по меньшей мере, 90, по меньшей мере, 95, по меньшей мере, 100, по меньшей мере, 110, по меньшей мере, 120, по меньшей мере, 130, по меньшей мере, 140, по меньшей мере, 150, по меньшей мере, 160, по меньшей мере, 170 или, по меньшей мере, 180 заменимых аминокислот из последовательностей аминокислот, приведенных в SEQ ID NOS: 1, 29 или 31.
[161] В некоторых вариантах осуществления, клетка экспрессирует CAR, который связывает и распознает универсальную метку, которая может сливаться с антителом или его фрагментом или вариантом. В конкретных вариантах осуществления, клетки, экспрессирующие такие CAR, могут специфично распознавать и уничтожать целевые клетки, например, клетки опухоли, которые связаны с антителами, которые являются слитыми с универсальной меткой. Один из примеров включает, но, не ограничиваясь этим, CAR-экспрессирующие Т-лимфоциты анти-FITC, которые могут связывать и/или распознавать различные раковые клетки человека, когда эти клетки связаны с реагирующими на рак FITC-меченными антителами. Таким образом, в некоторых вариантах осуществления, такой же CAR, который связывается с универсальной меткой, является полезным при лечении различных раковых заболеваний, при условии, что имеются доступные антитела, которые распознают антигены, ассоциируемые с раковыми заболеваниями, которые содержат универсальную метку. В конкретных вариантах осуществления, частица (например, сферическая частица) содержит поверхностно экспонируемую связывающую молекулу, которая содержит антиген или его часть, которая связывается или распознается рецептором антигена, например, CAR, который связывается с универсальной меткой. В определенных вариантах осуществления, связывающая молекула представляет собой универсальную метку или ее часть, которая связывается или распознается рецептором антигена, например, CAR.
[162] Конкретные варианты осуществления предполагают, что любой домен полипептида, который может сливаться с антителом или его антигенсвязывающим фрагментом или их вариантом, который не мешает связыванию антитела с соответствующей его мишенью, является пригодным для использования в качестве универсальной метки. В некоторых вариантах осуществления, частица связана со связывающей молекулой, которая содержит универсальную метку, или с ее частью, выбранной из группы, состоящей из: FITC, стрептавидина, биотина, гистидина, динитрофенола, комплекса перидинин - белок хлорофилла, зеленого флуоресцентного белка, PE, HRP, пальмитоилирования, нитрозилирования, щелочной фосфатазы, глюкозаоксидазы и мальтозасвязывающего белка.
[163] В некоторых вариантах осуществления, связывающая молекула представляет собой мультимер, например, димер, содержащий два или более полипептидных антигена, или его часть или вариант, который распознается и/или связывается рекомбинантным рецептором, таким как рецептор антигена (например, CAR). В некоторых вариантах осуществления, полипептидный антиген или его часть являются идентичными. В определенных вариантах осуществления, полипептидный антиген связан, прямо или опосредованно, с областью или доменом, например, доменом мультимеризации, который облегчает или стабилизирует взаимодействие между двумя или более полипептидными антигенами посредством комплементарных взаимодействий между доменами или областями. В некоторых вариантах осуществления, создание полипептидного антигена как мультимера, например, димера, обеспечивает мультивалентное взаимодействие между связывающей молекулой и антигенсвязывающим доменом рецептора антигена, например, CAR, это, в некоторых аспектах, может повысить авидность взаимодействия. В некоторых вариантах осуществления, повышенная авидность может содействовать стимуляторной или агонистической активности рецептора антигена, например, CAR, посредством связывания молекулы, конъюгированной с шариком.
[164] В некоторых вариантах осуществления, полипептид соединяется прямо или опосредованно с доменом мультимеризации. Иллюстративные домены мультимеризации включают последовательности иммуноглобулина или их части, лейциновые молнии, гидрофобные области, гидрофильные области и совместимые домены взаимодействия белок-белок. Домен мультимеризации, например, может представлять собой константную область или домен иммуноглобулина, такой, например, как Fc-домен, или его части из IgG, включая субтипы IgG1, IgG2, IgG3 или IgG4, IgA, IgE, IgD и IgM и их модифицированные формы. В конкретных вариантах осуществления, полипептидный антиген связывается, прямо или опосредованно, с Fc-доменом. В некоторых вариантах осуществления, полипептид представляет собой слитый полипептид, содержащий полипептидный антиген или его часть и Fc-домен.
[165] В конкретных вариантах осуществления, связывающая молекула представляет собой слитый полипептид, который содержит Fc-домен. В некоторых вариантах осуществления, Fc-домен состоит из второго и третьего константных доменов (то есть, доменов CH2 и CH3) тяжелой цепи изотипа IgG, IgA или IgD, например, CH2 или CH3 изотипов IgG, IgA и IgD. В некоторых вариантах осуществления, Fc-домен состоит из трех константных доменов тяжелой цепи (то есть, доменов CH2, CH3, и CH4) изотипа IgM или IgE. В некоторых вариантах осуществления, Fc-домен может дополнительно содержать шарнирную последовательность или ее часть. В определенных аспектах, Fc-домен содержит часть шарнирного домена молекулы иммуноглобулина или весь шарнирный домен плюс домены CH2 и CH3. В некоторых случаях, Fc-домен может образовывать димер двух полипептидных цепей, соединенных одной или несколькими дисульфидными связями. В некоторых вариантах осуществления, Fc-домен получают из иммуноглобулина (например, IgG, IgA, IgM или IgE) соответствующего млекопитающего (например, человека, мыши, крысы, козы, овцы или обезьяны). В некоторых вариантах осуществления, Fc-домен содержит домены CH2 и CH3 IgG. В определенных вариантах осуществления, Fc-домен является слитым с C-концом полипептидного антигена. В конкретных вариантах осуществления, Fc-домен является слитым с N-концом полипептидного антигена.
[166] В некоторых вариантах осуществления, Fc-домен представляет собой Fc-домен IgG или его часть или вариант. В некоторых вариантах осуществления, Fc-домен представляет собой Fc-домен IgG человека или его часть или вариант, который содержит последовательность аминокислот, приведенную в SEQ ID NO: 2, или последовательность аминокислот, которая имеет, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с последовательностью, приведенной в SEQ ID NO: 2. В конкретных вариантах осуществления, Fc-домен представляет собой Fc-домен IgG человека дикого типа или его часть или вариант. В конкретных вариантах осуществления, Fc-домен представляет собой вариант Fc-домена IgG1 человека дикого типа.
[167] В некоторых вариантах осуществления, слитый полипептид содержит вариант Fc-домена. В определенных вариантах осуществления, вариант Fc-домена IgG человека содержит мутацию, например, замещение, делецию или вставку, которая сокращает, уменьшает и/или ослабляет связывание между Fc-доменом и легкой цепью. В некоторых вариантах осуществления, вариант Fc-домена IgG человека содержит мутацию, которая уменьшает аффиность связывания между Fc-доменом и Fc-рецептором. В конкретных вариантах осуществления, вариант Fc-домена IgG человека содержит мутацию, которая сокращает, уменьшает и/или ослабляет взаимодействия или вероятность, или возможность взаимодействия между Fc-доменом и Fc-рецептором. В некоторых вариантах осуществления, вариант Fc-домена IgG человека содержит мутацию, которая уменьшает аффиность связывания между Fc-доменом и белком системы комплемента. В конкретных вариантах осуществления, вариант Fc-домена IgG человека содержит мутацию, которая сокращает, уменьшает и/или ослабляет взаимодействие или вероятность, или возможность взаимодействия, между Fc-доменом и белком системы комплемента.
[168] В некоторых вариантах осуществления, связывающая молекула содержит вариант Fc-домена IgG1 человека. В некоторых вариантах осуществления, вариант Fc-домена IgG человека содержит замещение цистина серином в шарнирной области Fc-домена. В некоторых вариантах осуществления, вариант Fc-домена IgG человека содержит замещение лейцина аланином в шарнирной области Fc-домена. В конкретных вариантах осуществления, вариант Fc-домена IgG человека содержит замещение глицина аланином в шарнирной области. В определенных вариантах осуществления, вариант Fc-домен IgG человека содержит замещение аланина серином в области CH2 Fc-домена. В некоторых вариантах осуществления, вариант Fc-домен IgG человека содержит замещение пролина серином в области CH2 Fc-домена. В некоторых вариантах осуществления, вариант Fc-домена IgG человека содержит последовательность аминокислот, как приведено в SEQ ID NO: 28.
[169] В некоторых вариантах осуществления, связывающая молекула содержит слитый полипептид, содержащий Fc-домен, где Fc-домен присутствует на C-конце слитого полипептида.
[170] В некоторых вариантах осуществления, связывающая молекула представляет собой слитый полипептид, содержащий полипептид BCMA или его часть и Fc-домен. В некоторых вариантах осуществления, полипептид BCMA или его часть содержит последовательность аминокислот, приведенную в SEQ ID NO: 1, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 1 и содержит эпитоп, распознаваемый рецептором антигена, например, CAR. В некоторых вариантах осуществления, Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 2, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 2. В некоторых вариантах осуществления, Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 28, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 28. В некоторых вариантах осуществления, антиген BCMA содержит BCMA или его часть или вариант, и метку или слитый домен, например, Fc-домен. В конкретных вариантах осуществления, антиген BCMA содержит всю последовательность аминокислот, приведенную в SEQ ID NO: 35, или ее часть или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 35, и которая содержит эпитоп, распознаваемый рецептором антигена, например, CAR.
[171] В некоторых вариантах осуществления, связывающая молекула представляет собой слитый полипептид, содержащий полипептид ROR1 или его часть и Fc-домен. В некоторых вариантах осуществления, полипептид ROR1 или его часть содержит последовательность аминокислот, приведенную в SEQ ID NO: 31, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 31 и содержит эпитоп, распознаваемый рецептором антигена, например, CAR, и Fc-домен. В некоторых вариантах осуществления, Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 2, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 2. В некоторых вариантах осуществления, Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 28, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 28. В определенных вариантах осуществления, связывающая молекула представляет собой слитый полипептид, содержащий последовательность аминокислот, приведенную в SEQ ID NO: 33, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 33 и которая содержит эпитоп, распознаваемый рецептором антигена, например, CAR.
[172] В конкретных вариантах осуществления, связывающая молекула представляет собой слитый полипептид, содержащий полипептид CD22, приведенный в SEQ ID NO: 29, или его часть, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 29 и содержит эпитоп, распознаваемый рецептором антигена, например, CAR и Fc-домен. В некоторых вариантах осуществления, Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 2, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 2. В некоторых вариантах осуществления Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 28, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 28. В определенных вариантах осуществления, слитый полипептид содержит аминокислотную последовательность, приведенную в SEQ ID NO: 34, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 34 и которая содержит эпитоп, распознаваемый рецептором антигена, например, CAR.
[173] В некоторых вариантах осуществления, антиген и домен мультимеризации, такой как Fc-домен, соединены линкером, таким как аминокислотный линкер. В определенных вариантах осуществления, антиген является слитым с N-концом аминокислотного линкера, и домен мультимеризации, такой как Fc-домен, является слитым с C-концом линкера. Хотя аминокислотные линкеры могут иметь любую длину и содержать любое сочетание аминокислот, длина линкера может быть относительно малой (например, десять или меньше аминокислот) для уменьшения взаимодействия между связанными доменами. Композиция аминокислот линкера также может регулироваться для уменьшения количества аминокислот с объемными боковыми цепями или аминокислот, вероятно, вводящих вторичную структуру. Пригодные для использования аминокислотные линкеры включают, но, не ограничиваясь этим, группы до 3, 4, 5, 6, 7, 10, 15, 20 или 25 аминокислот в длину. Репрезентативные последовательности аминокислотных линкеров включают GGGGS (SEQ ID NO: 27) и линкеры, содержащие 2, 3, 4 или 5 копий GGGGS (SEQ ID NO: 27).
[174] В некоторых вариантах осуществления, связывающая молекула представляет собой димер, образованный двумя слитыми Fc-полипептидами, содержащими полипептидный антиген или его часть и Fc-домен, например, BCMA-Fc, ROR1-Fc или CD22-Fc. Также предлагаются молекулы нуклеиновых кислот, кодирующие любые слитые Fc-полипептиды. Также предлагаются векторы, включая векторы экспрессии, кодирующие молекулы нуклеиновых кислот. В некоторых вариантах осуществления, связывающая молекула может продуцироваться в клетках посредством экспрессии в соответствующей клетке-хозяине. В некоторых вариантах осуществления, клетка-хозяин представляет собой линию клеток млекопитающего. Иллюстративные клетки млекопитающих для рекомбинантного экспрессирования белков включают клетки HEK293 или клетки CHO, или их производные. В некоторых аспектах, связывающая молекула дополнительно содержит сигнальный пептид для секреции из клеток. В иллюстративном варианте осуществления, сигнальный пептид представляет собой CD33 (например, приведенный в SEQ ID NO: 30). В некоторых вариантах осуществления, получаемый в результате слитый белок полипептидный антиген-Fc, например, BCMA-Fc, ROR1-Fc или CD22-Fc, может экспрессироваться в клетках-хозяевах, например, трансформированных с помощью векторов экспрессии, при этом сборка Fc-доменов может осуществляться посредством межцепных дисульфидных связей, образующихся между Fc остатками, с получением димерного, например, двухвалентного, слитого белка полипептидного антигена.
[175] В конкретных вариантах осуществления, связывающая молекула представляет собой или содержит BCMA человека или его часть. В некоторых вариантах осуществления, связывающая молекула содержит внеклеточный домен BCMA человека. В конкретных вариантах осуществления, связывающая молекула содержит часть ВСМС человека с последовательностью полипептида, приведенной в SEQ ID NO: 1. В конкретных вариантах осуществления, связывающая молекула представляет собой слитый полипептид, который содержит внеклеточный домен BCMA человека и Fc-домен. В определенных вариантах осуществления, Fc-домен представляет собой вариант Fc-домена IgG1 человека. В определенных вариантах осуществления, Fc-домен располагается на C-конце слитого полипептида. В конкретных вариантах осуществления, слитый полипептид содержит часть BCMA человека, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариант Fc-домена IgG1 человека, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 29. В некоторых вариантах осуществления, слитый полипептид содержит линкер, который соединяет полипептид BCMA с Fc-доменом. В конкретных вариантах осуществления, линкер содержит аминокислотную последовательность, приведенную в SEQ ID NO: 27. В определенных вариантах осуществления, связывающая молекула представляет собой слитый полипептид, содержащий полипептид BCMA человека (или его часть или вариант) и C-концевой Fc-домен, и она поверхностно конъюгирована или иным образом присоединена к частице (например, к сферической частице). В конкретных вариантах осуществления, слитый полипептид присоединен к частице на сайте в пределах Fc-домена. В некоторых вариантах осуществления, частица дополнительно содержит поверхностно конъюгированное антитело или его фрагмент, или вариант, который связывает и распознает CD28.
2. Антиидиотипические антитела
[176] В некоторых вариантах осуществления, связывающая молекула, конъюгированная с частицей, например, шариком, как предлагается в настоящем документе, представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, (“анти-ID”), который связывается с целевым рецептором антигена, например, CAR или с его активным фрагментом. В определенных вариантах осуществления, связывающая молекула представляет собой анти-ID, которое связывается с антигенсвязывающим доменом CAR. В конкретных вариантах осуществления, антигенсвязывающий домен CAR содержит домен scFv. В некоторых вариантах осуществления, связывающая молекула представляет собой анти-ID, которое связывается с CAR на антигенсвязывающем домене и не связывается с линкерной или спейсерной областью CAR, которая соединяет антигенсвязывающий домен, например, scFv, с трансмембранным доменом CAR.
[177] В некоторых вариантах осуществления, анти-ID представляет собой антиидиотипическое антитело или антигенсвязывающий фрагмент, который специфично распознает антитело, которое связывается с целевым антигеном, таким как целевой антиген, ассоциируемый или экспрессируемый на клетке или ткани заболевания или состояния, например, рака. В некоторых вариантах осуществления, анти-ID представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично распознает целевое антитело, которое связывает антиген, который представляет собой или содержит… В некоторых вариантах осуществления, антиген представляет собой или содержит интегрин αvβ6 (интегрин avb6), антиген созревания В-клеток (BCMA), B7-H3, B7-H6, угольную ангидразу 9 (CA9, также известную как CAIX или G250), антиген рака яичек, раково-тестикулярный антиген 1B (CTAG, также известный как NY-ESO-1 и LAGE-2), канцероэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, протеогликан хондроитин-4-сульфат (CSPG4), белок эпидермального фактора роста (EGFR), мутацию рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), эфринВ2, рецептор эфрина A2 (EPHa2), рецептор эстрогена, белок 5 подобный Fc-рецептору (FCRL5; также известный как гомолог 5 Fc-рецептора или FCRH5), рецептор фетального ацетилхолина (фетальный AchR), фолатсвязывающего белка (FBP), рецептор фолата альфа, ганглиозид GD2, O-ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), глипикан-3 (GPC3), связанный с белком G рецептора 5D (GPRC5D), Her2/neu (тирозинкиназный рецептор erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеры erbB, высокомолекулярный антиген человека, ассоциированный с меланомой (HMW-MAA), поверхностный антиген гепатита B, антиген лейкоцита человека A1 (HLA-A1), антиген лейкоцита человека A2 (HLA-A2), рецептор IL-22 альфа(IL-22Rα), рецептор IL-13 альфа 2 (IL-13Rα2), домен рецептора вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1-CAM), эпитоп CE7 L1-CAM, обогащенный лейцином повтор, содержащий член A семейства 8 (LRRC8A), антиген Ley, антиген, ассоциированный с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелин (MSLN), c-Met, цитомегаловирус мышей (CMV), муцин 1 (MUC1), MUC16, лиганды элемента D группы природных киллеров 2 (NKG2D), мелан A (MART-1), молекулу адгезии нейральных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простата-специфичный антиген, антиген стволовых клеток простаты (PSCA), простата-специфичный мембранный антиген (PSMA), орфанный рецептор 1 подобный тирозинкиназному рецептору (ROR1), сурвивин, гликопротеин трофобластов (TPBG также известный как 5T4), ассоциированный с опухолью гликопротеин 72 (TAG72), тирозиназа-зависимый белок 1 (TRP1, также известный как TYRP1 или gp75), тирозиназа-зависимый белок 2 (TRP2, также известный как допахромтаутомераза, допахром-дельта-изомераза или DCT), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор 2 фактора роста эндотелия сосудов (VEGFR2), опухоль Вильмса 1 (WT-1), патоген-специфичный или патоген-экспрессируемый антиген или антиген, ассоциированный с универсальной меткой, и/или биотинилированные молекулы, и/или молекулы, экспрессируемые HIV, HCV, HBV или другими патогенами. Антигены целевые для рецепторов в некоторых вариантах осуществления включают антигены, ассоциируемые с В-клеточным лейкозом, такие как любой из ряда известных маркеров В-клеток. В некоторых вариантах осуществления, антиген представляет собой или содержит CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig каппа, Ig лямбда, CD79a, CD79b или CD30.
[178] В некоторых вариантах осуществления, анти-ID представляет собой антиидиотипическое антитело или антигенсвязывающие фрагменты, которые специфически распознают целевое антитело, которое связывает ROR1, антиген созревания В-клеток (BCMA), угольную ангидразу 9 (CAIX), Her2/neu (тирозинкиназный рецептор erbB2), Ll-CAM, CD19, CD20, CD22, мезотелин, CEA и поверхностный антиген гепатита B, антифолатный рецептор, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеры erbB, EGFR vIII, фолатсвязывающего белка (FBP), FCRL5, FCRH5, рецептор фетального ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, домен рецептора вставки киназы (kdr), легкую цепь каппа, антиген Ley, молекулу клеточной адгезии L1, (L1-CAM), антиген, ассоциированный с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемый антиген меланомы (PRAME), сурвивин, TAG72, B7-H6, рецептор IL-13 альфа 2 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептор фолата a, CD44v6, CD44v7/8, интегрин avb6, 8H9, NCAM, рецепторы VEGF, 5T4, фетальный AchR, лиганды NKG2D, CD44v6, двойной антиген, антиген рака яичек, мезотелин, CMV мышей, муцин 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетальный антиген, ROR1, TAG72, VEGF-R2, канцероэмбриональный антиген (CEA), простата-специфичный антиген, PSMA, Her2/neu, рецептор эстрогена, рецептор прогестерона, эфринВ2, CD123, c-Met, GD-2, O-ацетилированный GD2 (OGD2), CE7, опухоль Вильмса 1 (WT-1), циклин, циклин A2, CCL-1, CD138 или патоген-специфичный антиген.
[179] В некоторых вариантах осуществления, анти-ID представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент (“анти-ID”), который специфично распознает целевой остаток антитела анти-CD19. В некоторых вариантах осуществления, предлагаемые антитела распознают целевое антитело анти-CD19, которое представляет собой SJ25C1 или его антигенсвязывающий фрагмент, или представляет собой антитело или антигенсвязывающий фрагмент, полученный из SJ25C1. В некоторых вариантах осуществления, предлагаемые антитела распознают целевое антитело анти-CD19, которое представляет собой FMC63, или его антигенсвязывающий фрагмент представляет собой антитело или антигенсвязывающий фрагмент, полученный из FMC63.
[180] SJ25C1 представляет собой моноклональное антитело IgG1 мыши, наращенное против клеток Nalm-1 и -16, экспрессирующих CD19 человеческого происхождения (Ling, N. R., et al. (1987). Leucocyte typing III. 302). Антитело SJ25C1 содержит CDRH1, H2 и H3, приведенные в SEQ ID NOS: 40-42, соответственно, и последовательности CDRL1, L2 и L3, приведенные в SEQ ID NOS: 43-45, соответственно. Антитело SJ25C1 содержит вариабельную область тяжелой цепи (VH), содержащую последовательность аминокислот SEQ ID NO: 36, и вариабельную область легкой цепи (VL), содержащую последовательность аминокислот SEQ ID NO: 37.
[181] В некоторых вариантах осуществления, целевое антитело представляет собой SJ25C1 или антитело, полученное из SJ25C1. В некоторых вариантах осуществления, “антитело, полученное из SJ25C1”, представляет собой антитело или антигенсвязывающий фрагмент, который содержит VH и/или VL из SJ25C1, идиотип SJ25C1, паратоп SJ25C1 или одну или несколько областей, определяющих комплементарность (CDR) SJ25C1. В некоторых вариантах осуществления, целевое антитело, которое представляет собой SJ25C1 или антитело, полученное из SJ25C1, представляет собой антитело или антигенсвязывающий фрагмент, который содержит VH SJ25C1, приведенную в SEQ ID NO: 36, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью, приведенной в SEQ ID NO: 36, и/или VL SJ25C1, приведенную в SEQ ID NO: 37, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью SEQ ID NO: 37. В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит VH SJ25C1, приведенную в SEQ ID NO: 36, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью SEQ ID NO: 36, и VL SJ25C1, приведенную в SEQ ID NO: 37, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью SEQ ID NO: 37. В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит VH и VL SJ25C1, приведенные в SEQ ID NO: 36 и SEQ ID NO: 37, соответственно. В некоторых вариантах осуществления, вариант имеет, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность с последовательностями SEQ ID NO: 36 и/или SEQ ID NO: 37.
[182] В некоторых вариантах осуществления, целевое антитело, которое представляет собой SJ25C1 или антитело, полученное из SJ25C1, представляет собой антитело или антигенсвязывающий фрагмент, который содержит одну или несколько CDR тяжелой цепи (CDR-H) SJ25C1 VH, приведенных в SEQ ID NO: 36, например, приведенных в SEQ ID NOS: 40-42, и/или одну или несколько легких цепей CDR (CDR-L) SJ25C1 VL, приведенных в SEQ ID NO: 37, например, приведенных в SEQ ID NOS: 43-45. В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит CDR-H3 SJ25C1 (например, приведенную в SEQ ID NO: 42) и/или CDR-L3 SJ25C1 (например, приведенную в SEQ ID NO: 45). В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит CDR-H3 и CDR-L3 SJ25C1 (например, приведенные в SEQ ID NO: 42 и SEQ ID NO: 43, соответственно). В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит одну или несколько областей из CDR-H1, CDR-H2 и CDR-H3 SJ25C1 (например, приведенных в SEQ ID NOS: 40, 41, 42, соответственно) и/или одну или несколько из CDR-L1, CDR-L2, и CDR-L3 из SJ25C1 (например, приведенных в SEQ ID NOS: 43, 44, 45, соответственно). В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит CDR-H1, CDR-H2 и CDR-H3 SJ25C1 (например, приведенные в SEQ ID NOS: 40, 41, 42, соответственно) и/или CDR-L1, CDR-L2 и CDR-L3 SJ25C1 (например, приведенные в SEQ ID NOS: 43, 44, 45, соответственно). В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит CDR-H1, CDR-H2 и CDR-H3 SJ25C1 (например, приведенные в SEQ ID NOS: 40, 41, 42, соответственно) и CDR-L1, CDR-L2 и CDR-L3 SJ25C1 (например, приведенные в SEQ ID NOS: 43, 44, 45, соответственно). В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит антигенсвязывающий фрагмент, такой как антигенсвязывающий фрагмент (Fab), F(ab')2, Fab', фрагмент вариабельного (Fv) или одноцепочечного Fv (scFv). Смотри, например, Bejcek, B. E., et al. (1995). Cancer research. 55(11): 2346-2351,
[183] FMC63 представляет собой моноклональное антитело IgG1 мыши, наращенное против клеток JVM3, экспрессирующих CD19 человеческого происхождения (Nicholson., et al. (1997). Molecular Immunology. 34(16-17):1157-1165). Антитело FMC63 содержит CDRH1, H2 и H3, приведенные в SEQ ID NOS: 46-48, соответственно, и последовательности CDRL1, L2 и L3, приведенные в SEQ ID NOS: 49-51, соответственно. Антитело FMC63 содержит вариабельную область тяжелой цепи (VH), содержащую последовательность аминокислот SEQ ID NO: 38, и вариабельную область легкой цепи (VL), содержащую последовательность аминокислот SEQ ID NO: 39.
[184] В некоторых вариантах осуществления, целевое антитело представляет собой FMC63 или антитело, полученное из FMC63. В некоторых вариантах осуществления, антитело, полученное из FMC63, представляет собой антитело или антигенсвязывающий фрагмент, который содержит VH и/или VL FMC63, идиотип FMC63, паратоп FMC63 или одну или несколько областей, определяющих комплементарность (CDR) FMC63. В некоторых вариантах осуществления, целевое антитело, которое представляет собой FMC63 или антитело, полученное из FMC63, представляет собой антитело или антигенсвязывающий фрагмент, который содержит VH FMC63, приведенную в SEQ ID NO: 38, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью SEQ ID NO: 38, и/или VL FMC63, приведенной в SEQ ID NO: 39, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью SEQ ID NO: 39. В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит VH FMC63, приведенную в SEQ ID NO: 38, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью SEQ ID NO: 38, и VL FMC63, приведенную в SEQ ID NO: 39, или ее вариант, имеющий, по меньшей мере, 90% идентичность с последовательностью SEQ ID NO: 39. В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит VH и VL из FMC63, приведенные в SEQ ID NO: 38 и 39, соответственно. В некоторых вариантах осуществления, вариант имеет, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность с последовательностями SEQ ID NO: 38 и/или SEQ ID NO: 39
[185] В некоторых вариантах осуществления, целевое антитело, которое представляет собой FMC63, или антитело, полученное из FMC63, представляет собой антитело или антигенсвязывающий фрагмент, который содержит одну или несколько CDR тяжелой цепи (CDR-H) FMC63 VH, приведенной в SEQ ID NO: 38, например, приведенные в SEQ ID NOS: 46-48, и/или одну или несколько CDR легкой цепи (CDR-L) из FMC63VL, приведенных в SEQ ID NO: 39, например, приведенных в SEQ ID NOS: 49-51. В некоторых вариантах осуществления, целевое антитело, которое представляет собой FMC63 или антитело, полученное из FMC63, представляет собой антитело или антигенсвязывающий фрагмент, который содержит CDR-H3 FMC63 (например, приведенную в SEQ ID NO: 48) и/или CDR-L3 FMC63 (например, приведенную в SEQ ID NO: 51). В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит CDR-H3 (например, приведенную в SEQ ID NO: 48) и CDR-L3 FMC63 (например, приведенную в SEQ ID NO: 51). В некоторых вариантах осуществления, целевое антитело, которое представляет собой FMC63 или антитело, полученное из FMC63, представляет собой антитело или антигенсвязывающий фрагмент, который содержит одну или несколько из CDR-H1, CDR-H2 и CDR-H3 FMC63 (например, приведенных в SEQ ID NOS: 46, 47, 48, соответственно) и/или одну или несколько из CDR-L1, CDR-L2, и CDR-L3 из FMC63 (например, приведенных в SEQ ID NOS: 49, 50, 51, соответственно). В некоторых вариантах осуществления, целевое антитело, которое представляет собой FMC63 или антитело, полученное из FMC63, представляет собой антитело или антигенсвязывающий фрагмент, который содержит CDR-H1, CDR-H2, и CDR-H3 из FMC63 (например, приведенных в SEQ ID NOS: 46, 47, 48, соответственно) и/или CDR-L1, CDR-L2 и CDR-L3 FMC63 (например, приведенных в SEQ ID NOS: 49, 50, 51, соответственно). В некоторых вариантах осуществления, целевое антитело, которое представляет собой FMC63 или антитело, полученное из FMC63, представляет собой антитело или антигенсвязывающий фрагмент, который содержит CDR-H1, CDR-H2, и CDR-H3 FMC63 (например, приведенные в SEQ ID NOS: 46, 47, 48, соответственно) и CDR-L1, CDR-L2, и CDR-L3 из FMC63 (например, приведенные в SEQ ID NOS: 49, 50, 51, соответственно). В некоторых вариантах осуществления, антитело или антигенсвязывающий фрагмент содержит антигенсвязывающий фрагмент, такой как антигенсвязывающий фрагмент (Fab), F(ab')2, Fab', фрагмент вариабельного (Fv) или одноцепочечного Fv (scFv).
[186] В некоторых вариантах осуществления, предлагаемые антиидиотипические антитела включают антитела, которые специфично связываются с вариабельным доменом (Fv), таким как одноцепочечный Fv (scFv), полученный из SJ25C1 или FMC63. В некоторых вариантах осуществления, антиидиотипические антитела специфично связываются с конкретным эпитопом или областью Fv, как правило, с эпитопом или с областью, содержащей одну или несколько областей, определяющих комплементарность. В некоторых вариантах осуществления, антиидиотипические антитела специфично связываются с эпитопом или областью, перекрывающей паратоп Fv.
[187] В некоторых вариантах осуществления, предлагаемые антиидиотипические антитела включают антитела, которые могут специфично связываться с остатком анти-CD19, полученным из SJ25C1 или FMC63, который содержится как часть внеклеточного домена целевого химерного рецептора антигена (CAR). В некоторых вариантах осуществления, целевой CAR содержит антигенсвязывающую часть, которая содержит молекулу антитела SJ25C1 или FMC63, или антигенсвязывающий фрагмент или часть антитела SJ25C1 или FMC63. В некоторых вариантах осуществления, целевой CAR содержит антигенсвязывающий домен, который представляет собой scFv, полученный из цепей VH и VL антитела SJ25C1 или FMC63. В некоторых вариантах осуществления, предлагается антиидиотипическое антитело, которое специфично связывается с CAR анти-CD19, которое содержит scFv полученный из антитела SJ25C1 или FMC63. Иллюстративные признаки CAR дополнительно описываются ниже.
[188] Термин “антитело” в настоящем документе используется в самом широком смысле и включает поликлональные и моноклональные антитела, включая интактные антитела и функциональные (антигенсвязывающие) фрагменты антител, включая фрагменты антигенсвязывающих фрагментов (Fab), фрагменты F(ab')2, фрагменты Fab', фрагменты Fv, фрагменты рекомбинантных IgG (rIgG), одноцепочечные фрагменты антител, включая одноцепочечные вариабельные фрагменты (scFv) и однодоменные фрагменты (например, sdAb, sdFv нанотело) антител. Термин охватывает генно-инженерные и/или иным образом модифицированные формы иммуноглобулинов, такие как интратела, пептитела, химерные антитела, полностью человеческие антитела, гуманизированные антитела и гетероконъюгированные антитела, мультиспецифичные, например, биспецифичные, антитела, диатела, триатела и тетратела, тандемные ди-scFv, тандемные три-scFv. Если не утверждается иного, термин “антитело” должен пониматься как охватывающий функциональное антитело и его фрагменты. Термин также охватывает интактные или полноразмерные антитела, включая антитела любого класса или подкласса, включая IgG и его подклассы, IgM, IgE, IgA и IgD.
[189] Термин “антиидиотипическое антитело” относится к антителу, включая его антигенсвязывающие фрагменты, которое специфично распознает, является специфично нацеленным и/или специфично связывается с идиотопом антитела, таким как антигенсвязывающий фрагмент. Идиотопы антитела могут включать, но, не ограничиваясь этим обязательно, остатки в пределах одной или нескольких областей, определяющих комплементарность (CDR) антитела, вариабельные области антитела и/или дробные части или части таких вариабельных областей и/или таких CDR, и/или любое сочетание рассмотренного выше. CDR может представлять собой одну или несколько областей, выбранных из группы, состоящей из CDR-H1, CDR-H2, CDR-H3, CDR-L1, CDR-L2 и CDR-L3. Вариабельные области антитела могут представлять собой вариабельные области тяжелой цепи, вариабельные области легкой цепи или сочетание вариабельных областей тяжелой цепи и вариабельных областей легкой цепи. Дробные фрагменты или части вариабельных областей тяжелой цепи и/или вариабельных областей легкой цепи антитела могут представлять собой фрагменты, содержащие 2 или более, 5 или более или 10 или более заменимых аминокислот, например, от или примерно от 2 до 100, от 5 до 100, от 10 до 100, от 2 до 50, от 5 до 50 или от 10 до 50 заменимых аминокислот в пределах вариабельных областей тяжелой цепи или вариабельных областей легкой цепи антитела; идиотоп может содержать множество незаменимых фрагментов секвенирования аминокислот. Дробные фрагменты вариабельных областей тяжелой цепи и вариабельных областей легкой цепи антитела могут представлять собой фрагменты, содержащие 2 или более, 5 или более или 10 или более заменимых аминокислот, например, от или примерно от 2 до 100, от 5 до 100, от 10 до 100, от 2 до 50, от 5 до 50 или от 10 до 50 заменимых аминокислот в пределах вариабельных областей, а в некоторых вариантах осуществления, они содержат один или несколько фрагментов CDR или CDR. Фрагменты CDR могут быть последовательными или непоследовательными фрагментами из 2 или более или 5 или более аминокислот в пределах CDR. Следовательно, идиотопы антитела могут содержать от или примерно от 2 до 100, от 5 до 100, от 10 до 100, от 2 до 50, от 5 до 50 или от 10 до 50 заменимых аминокислот, содержащих одну или несколько CDR или один или несколько фрагментов CDR в вариабельных областях тяжелой цепи или вариабельных областях легкой цепи антитела. В другом варианте осуществления, идиотопы могут представлять собой отдельную аминокислоту, которая располагается на вариабельных областях антитела, например, на сайтах CDR.
[190] В некоторых вариантах осуществления, идиотоп представляет собой любой одинарный антигенный детерминант или эпитоп в пределах вариабельной части антитела. В некоторых случаях он может перекрывать реальный антигенсвязывающий сайт антитела, в некоторых случаях он может содержать последовательности вариабельных областей вне антигенсвязывающего сайта антитела. Набор индивидуальных идиотопов антитела в некоторых вариантах осуществления упоминается как “идиотип” такого антитела.
[191] Термины “область, определяющая комплементарность” и “CDR” синонимы “гипервариабельной области” или “HVR”, как известно в данной области, относятся к последовательностям незаменимых аминокислот в вариабельных областях антитела, которые придают специфичность и/или аффиность связывания относительно антигена. Как правило, имеется три CDR в каждой вариабельной области тяжелой цепи (CDR-H1, CDR-H2, CDR-H3) и три CDR в каждой вариабельной области легкой цепи (CDR-L1, CDR-L2, CDR-L3). “Каркасные области” и “FR”, как известно в данной области, относятся к отличным от CDR частям вариабельных областей тяжелой и легкой цепей. Как правило, имеется четыре FR в каждой полноразмерной вариабельной области тяжелой цепи (FR-H1, FR-H2, FR-H3 и FR-H4) и четыре FR в каждой полноразмерной вариабельной области легкой цепи (FR-L1, FR-L2, FR-L3 и FR-L4).
[192] Точные границы последовательности аминокислот данных CDR или FR можно легко определить с использованием ряда хорошо известных схем, включая схемы, которые описаны Kabat et al. (1991), “Sequences of Proteins of Immunological Interest,” 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (“схема нумерации Kabat), Al-Lazikani et al., (1997) JMB 273,927-948 (схема нумерации “Chothia”), MacCallum et al., J. Mol. Biol. 262: 732-745 (1996), “Antibody-antigen interactions: Contact analysis and binding site topography,” J. Mol. Biol. 262, 732-745.” (схема нумерации “Contact”), Lefranc MP et al., “IMGT unique numbering for immunoglobulin and T cell receptor variable domains and Ig superfamily V-like domains,” Dev Comp Immunol, 2003 Jan; 27(1): 55-77 (“IMGT” схема нумерации), и Honegger A and  A, “Yet another numbering scheme for immunoglobulin variable domains: an automatic modeling and analysis tool,” J Mol. Biol, 2001 Jun 8; 309(3): 657-70, (схема нумерации “Aho”).
A, “Yet another numbering scheme for immunoglobulin variable domains: an automatic modeling and analysis tool,” J Mol. Biol, 2001 Jun 8; 309(3): 657-70, (схема нумерации “Aho”).
[193] Границы данных CDR или FR могут изменяться в зависимости от схемы, используемой для идентификации. Например, схема Kabat основана на структурных выравниваниях, в то время как схема Chothia основана на структурной информации. Нумерация в обеих схемах как Kabat, так и Chothia основана на наиболее распространенных длинах последовательностей областей антитела, со вставками, аккомодированными с помощью буквенных обозначений вставки, например, “30a,” и делециями, появляющимися в некоторых антителах. Две схемы размещают определенные вставки и делеции (“indels”) в различных положениях, что приводит к отличающейся нумерации. Схема Contact основана на анализе кристаллических структур комплексов и сходна во многих отношениях со схемой нумерации Chothia.
[194] Таблица 1, ниже, перечисляет иллюстративные границы положений CDR-L1, CDR-L2, CDR-L3 и CDR-H1, CDR-H2, CDR-H3, как определяется с помощью схем Kabat, Chothia и Contact, соответственно. Для CDR-H1, нумерация остатков перечисляется с использованием схем нумерации как Kabat, так и Chothia. FR располагаются между CDR, например, FR-L1 располагается между CDR-L1 и CDR-L2, и так далее. Отметим, что поскольку, показанная схема нумерации Kabat помещает вставки на H35A и H35B, конец петли CDR-H1 Chothia, при нумерации с использованием показанного условия нумерации Kabat может лежать в пределах между H32 и H34, в зависимости от длины петли.
Таблица 1
1 - Kabat et al. (1991), “Sequences of Proteins of Immunological Interest,” 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD
2 - Al-Lazikani et al., (1997) JMB 273,927-948
[195] Таким образом, если не указано иного, “CDR” или “область, определяющая комплементарность” или индивидуальные указанные CDR, например, “CDR-H1, CDR-H2), данного антитела или его области, такой как его вариабельная область, как понимается, должны охватывать некоторую (или конкретную) область, определяющую комплементарность, как определено с помощью любой из рассмотренных выше схем. Например, когда утверждается, что конкретная CDR (например, CDR-H3) содержит последовательность аминокислот соответствующей CDR в данной последовательности аминокислот VH или VL, понимается, что такая CDR имеет последовательность соответствующей CDR (например, CDR-H3) в вариабельной области, как определено с помощью любой из рассмотренных выше схем. В некоторых вариантах осуществления, определены указанные последовательности CDR.
[196] Подобным же образом, если не указано иного, некоторая FR или индивидуальная указанная FR (несколько FR) (например, FR-H1, FR-H2), данного антитела или его области, например, его вариабельной области, как понимается, должна охватывать некоторую (или конкретную) каркасную область, как определено с помощью любых известных схем. В некоторых случаях, указывается схема для идентификации конкретных CDR, FR или нескольких FR, или CDR, например, CDR, как определено по способу Kabat, Chothia или Contact. В других случаях, приводится конкретная последовательность аминокислот CDR или FR.
[197] Термин “вариабельная область” или “вариабельный домен” относится к домену тяжелой или легкой цепи антитела, который участвует в связывании антитела с антигеном. Вариабельные домены тяжелой цепи и легкой цепи (VH и VL, соответственно) нативного антитела, как правило, имеют сходные структуры, при этом каждый домен содержит четыре консервативных каркасных области (FR) и три CDR. (Смотри, например, Kindt et al. Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007). Один домен VH или VL может быть достаточным для придания антигенсвязывающей специфичности. Кроме того, антитела, которые связывают конкретный антиген, могут изолироваться с использованием домена VH или VL от антитела, который связывает антиген, для скрининга библиотеки комплементарных доменов VL или VH, соответственно. Смотри, например, Portolano et al., J. Immunol. 150: 880-887 (1993); Clarkson et al., Nature 352: 624-628 (1991).
[198] Среди предлагаемых антител имеются фрагменты антител. “Фрагмент антитела” относится к молекуле иной, чем интактное антитело, которое содержит часть интактного антитела, которое связывается с антигеном, с которым связывается интактное антитело. Примеры фрагментов антитела включают, но, не ограничиваясь этим, Fv, Fab, Fab', Fab'-SH, F(ab')2; диатела; линейные антитела; одноцепочечные молекулы антител, (например, scFv); и мультиспецифичные антитела, сформированные из фрагментов антител. В конкретных вариантах осуществления, антитела представляют собой одноцепочечные фрагменты антител, содержащие вариабельную область тяжелой цепи и/или вариабельную область легкой цепи, такие как scFv.
[199] Однодоменные антитела представляют собой фрагменты антител, содержащие весь вариабельный домен тяжелой цепи или его часть, или весь вариабельный домен легкой цепи или его часть антитела. В определенных вариантах осуществления, однодоменное антитело представляет собой однодоменное антитело человека.
[200] Фрагменты антител можно получать с помощью различных технологий, включая, но, не ограничиваясь этим, протеолитическое переваривание интактного антитела, а также продуцирование рекомбинантными клетками-хозяевами. В некоторых вариантах осуществления, антитела представляют собой рекомбинантно продуцируемые фрагменты, такие как фрагменты, содержащие расположения, которые не встречаются в природе, такие как фрагменты с двумя или более областями или с цепями антитела, соединенными синтетическими линкерами, например, пептидными линкерами, и/или которые могут не получаться посредством ферментативного переваривания встречающегося в природе интактного антитела. В некоторых аспектах, фрагменты антител представляют собой scFv.
[201] “Гуманизированное” антитело представляет собой антитело, в котором, по существу, все остатки аминокислот CDR получены не из CDR человека, а все или, по существу, все остатки аминокислот FR получены из FR человека. Гуманизированное антитело необязательно, может содержать, по меньшей мере, часть константной области антитела, полученную от антитела человека. “Гуманизированная форма” не принадлежащего человеку антитела относится к варианту не принадлежащего человеку антитела, которое подвергается гуманизации, как правило, для понижения иммуногенности для людей, в то же время сохраняя специфичность и аффиность родительского антитела, не принадлежащего человеку. В некоторых вариантах осуществления, некоторые остатки FR в гуманизированном антителе замещаются соответствующими остатками из не принадлежащего человеку антитела (например, антитела, из которого получены остатки CDR), например, для восстановления или улучшения специфичности, или аффиности антитела.
[202] Среди предлагаемых антител имеются антитела человека. “Антитело человека” представляет собой антитело с последовательностью аминокислот, соответствующей антителу, продуцируемому человеком или клеткой человека, или не человеческим источником иным, чем человек, который использует репертуары антител человека или другие последовательности, кодирующие антитела человека, включая библиотеки антител человека. Термин исключает гуманизированные формы не принадлежащих человеку антител, содержащие не принадлежащие человеку антигенсвязывающие области, например, такие в которых все или, по существу, все CDR являются не принадлежащими человеку.
[203] Антитела человека можно получить посредством введения иммуногена трансгенному животному, которое модифицируют для получения интактных антител человека или интактных антител с вариабельными областями человека в ответ на антигенное провоцирование. Такие животные, как правило, содержат все локусы иммуноглобулина человека, которые заменяют эндогенные локусы иммуноглобулина или которые присутствуют экстрахромосомно или встраиваются случайным образом в хромосомы животного, или их часть. У таких трансгенных животных, эндогенные локусы иммуноглобулина, как правило, дезактивируются. Антитела человека можно также получать из библиотек антитела человека, включая библиотеки фаговых дисплеев и бесклеточные библиотеки, содержащие последовательности, кодирующие антитела, полученные из репертуара человека.
[204] Среди предлагаемых антител имеются моноклональные антитела, включая моноклональные фрагменты антител. Термин “моноклональное антитело”, как используется в настоящем документе, относится к антителу, полученному из популяции, по существу, гомогенных антител или в ее пределах, то есть, индивидуальные антитела, составляющие популяцию, являются идентичными, за исключением возможных вариантов, содержащих встречающиеся в природе мутации или возникающих в ходе получения препарата моноклонального антитела, такие варианты, как правило, присутствуют в малых количествах. В противоположность препаратам поликлональных антител, которые, как правило, содержат различные антитела, направленные против различных эпитопов, каждое моноклональное антитело препарата моноклонального антитела направлено против одного эпитопа на антигене. Этот термин не должен рассматриваться как требование получения антитела с помощью какого-либо конкретного способа. Моноклональное антитело может быть получено с помощью разнообразных технологий, включая, но, не ограничиваясь этим, генерирование из гибридомы, методы рекомбинантной ДНК, методы фагового дисплея и других дисплеев антител.
a. Антитела полученные из SJ25C1
[205] В некоторых вариантах осуществления, антиидиотипическое антитело является специфичным к целевому антителу анти-CD19, которое представляет собой или получено из антитела SJ25C1 или его антигенсвязывающего фрагмента.
[206] В некоторых вариантах осуществления, антиидиотипические антитела или их антигенсвязывающие фрагменты содержат вариабельную (VH) область тяжелой цепи, имеющую, по меньшей мере, 90% идентичность последовательности с последовательностью аминокислот области VH, приведенной в SEQ ID NO: 52, например, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с ней.
[207] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающие фрагменты содержат вариабельную (VH) область тяжелой цепи, содержащую область, определяющую комплементарность, тяжелой цепи 3 (CDR-H3), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 53 или 54, и/или CDR-H3 содержащуюся в вариабельной последовательности (VH) тяжелой цепи, приведенной в SEQ ID NO: 52.
[208] В некоторых из всех таких вариантов осуществления, область VH содержит область, определяющую комплементарность, тяжелой цепи 1 (CDR-H1), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 55, 56, 57 или 58, и/или CDR-H1 содержащуюся в последовательности VH, приведенной в SEQ ID NO: 52; и/или область, определяющую комплементарность, тяжелой цепи 2 (CDR-H2), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 59, 60, 61 или 62, и/или CDR-H2 содержащуюся в последовательности VH, приведенной в SEQ ID NO: 52.
[209] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит вариабельную (VH) область тяжелой цепи, содержащую области, определяющие комплементарность тяжелой цепи 1 (CDR-H1), CDR-H2 и CDR-H3, где CDR-H1 содержит последовательность аминокислот, приведенную в SEQ ID NO: 55, 56, 57 или 58; CDR-H2 содержит последовательность аминокислот, приведенную в SEQ ID NO: 59, 60, 61 или 62; и/или CDR-H3 содержит последовательность аминокислот, приведенную в SEQ ID NO: 53 или 54. В некоторых вариантах осуществления, предлагаются антитела или их антигенсвязывающие фрагменты, которые содержат CDR-H1, содержащую последовательность аминокислот, приведенную в SEQ ID NO: 55, 56, 57 или 58; CDR-H2, содержащую последовательность аминокислот, приведенную в SEQ ID NO: 59, 60, 61 или 62; и CDR-H3, содержащую последовательность аминокислот, приведенную в SEQ ID NO: 53 или 54.
[210] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент, который содержит область, определяющую комплементарность, тяжелой цепи 1 (CDR-H1), CDR-H2 и CDR-H3, соответственно, содержит последовательности аминокислот CDR-H1, CDR-H2 и CDR-H3, содержащиеся в последовательности аминокислот области VH, приведенной в SEQ ID NO: 52.
[211] В некоторых из всех таких вариантов осуществления, область VH содержит последовательности каркасных областей 1 (FR1), FR2, FR3 и/или FR4, имеющие, по меньшей мере, 90% идентичность последовательности, соответственно, с FR1, FR2, FR3 и/или FR4 последовательности аминокислот, приведенной в SEQ ID NO: 52. В некоторых вариантах осуществления, область VH содержит последовательности каркасных областей 1 (FR1), FR2, FR3 и/или FR4, имеющие, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательности, соответственно, с FR1, FR2, FR3 и/или FR4 последовательности аминокислот, приведенной в SEQ ID NO: 52. В некоторых вариантах осуществления, область VH содержит последовательности каркасных областей 1 (FR1), FR2, FR3 и/или FR4, имеющие, по меньшей мере, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательности, соответственно, с FR1, FR2, FR3 и FR4 последовательности аминокислот, приведенной в SEQ ID NO: 52.
[212] В некоторых из всех таких вариантов осуществления, область VH содержит последовательность аминокислот, приведенную в SEQ ID NO: 52.
[213] В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент представляет собой только тяжелую цепь, только VH и/или не содержит его части VL или антигенсвязывающей части, и/или антигенсвязывающий сайт антиидиотипического антитела или его фрагмент содержит остатки только из тяжелой цепи и/или не содержит остатков из легкой цепи.
[214] В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или его фрагмент не содержит вариабельной (VL) области легкой цепи, не содержит CDR-L1, CDR-L2 и/или CDR-L3, и/или представляет собой однодоменное антитело (sdAb), содержащее только область VH. В некоторых вариантах осуществления, антитело или его фрагмент представляет собой sdAb, который содержит только область VH из того, что описано выше.
[215] В некоторых вариантах осуществления любых антиидиотипических антител или фрагментов, содержащих любую из указанных выше последовательностей области VH, антиидиотипическое антитело или его фрагмент дополнительно содержит вариабельную (VL) область легкой цепи. В некоторых таких вариантах осуществления, область VL имеет, по меньшей мере, 90% идентичность последовательности с последовательностью аминокислот области VL, приведенной в SEQ ID NO: 63, например, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с последовательностью аминокислот области VL, приведенной в SEQ ID NO: 63.
[216] В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 3 (CDR-L3), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 64 или 65. В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 3 (CDR-L3), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 64 или 65.
[217] В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 1 (CDR-L1), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 66 или 67, и/или CDR-L1 содержащуюся в последовательности VL, приведенной в SEQ ID NO: 63; и/или область, определяющую комплементарность, легкой цепи 2 (CDR-L2), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 68 или 69, и/или CDR-L2 содержащуюся в последовательности VL, приведенной в SEQ ID NO: 63. В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 1 (CDR-L1), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 66 или 67, и/или CDR-L1, содержащуюся в последовательности VL, приведенной в SEQ ID NO: 63; и/или область, определяющую комплементарность, легкой цепи 2 (CDR-L2), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 68 или 69, и/или CDR-L2 содержащуюся в последовательности VL, приведенной в SEQ ID NO: 63.
[218] В некоторых из всех таких вариантов осуществления, область VL содержит CDR-L1, содержащую последовательности аминокислот, приведенные в SEQ ID NO: 66 или 67; CDR-L2, содержащую последовательности аминокислот, приведенные в SEQ ID NO: 68 или 69; и CDR-L3, содержащую последовательности аминокислот, приведенные в SEQ ID NO: 64 или 65.
[219] В некоторых из всех таких вариантов осуществления, область VL содержит CDR-L1, CDR-L2 и CDR-L3, соответственно, содержащие последовательности аминокислот CDR-L1, CDR-L2 и CDR-L3, содержащихся в последовательности аминокислот области VL, приведенной в SEQ ID NO: 63.
[220] В некоторых из всех таких вариантов осуществления, область VL содержит каркасную область 1 (FR1), FR2, FR3 и/или FR4, имеющую, по меньшей мере, 90% идентичность последовательности, соответственно, с FR1, FR2, FR3 и/или FR4 последовательности аминокислот, приведенной в SEQ ID NO: 63. В некоторых вариантах осуществления, область VL содержит последовательность каркасную область 1 (FR1), FR2, FR3 и/или FR4, имеющую, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательности, соответственно, с FR1, FR2, FR3 и/или FR4 последовательности аминокислот, приведенной в SEQ ID NO: 63. В некоторых вариантах осуществления, область VL содержит последовательности каркасных областей 1 (FR1), FR2, FR3 и/или FR4, имеющие, по меньшей мере, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательности, соответственно, с FR1, FR2, FR3 и FR4 последовательности аминокислот, приведенной в SEQ ID NO: 63.
[221] В некоторых из всех таких вариантов осуществления, область VL содержит последовательность аминокислот, приведенную в SEQ ID NO: 63.
[222] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит последовательности аминокислот CDR-H1, CDR-H2 и CDR-H3 последовательностей, содержащихся в последовательности аминокислот области VH, приведенной в SEQ ID NO: 52; и/или содержит последовательности аминокислот CDR-L1, CDR-L2 и CDR-L3 последовательностей, содержащихся в последовательности аминокислот вариабельной (VL) области легкой цепи, приведенной в SEQ ID NO: 63.
[223] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит области VH и VL, имеющие последовательности аминокислот, имеющих, по меньшей мере, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность с SEQ ID NOS: 52 и 63, соответственно.
[224] В некоторых вариантах осуществления, предлагаются антиидиотипические антитела или его антигенсвязывающие фрагменты, которые содержат области VH и VL, имеющие последовательности аминокислот, приведенные в SEQ ID NOS: 52 и 63, соответственно.
[225] В некоторых из всех таких вариантов осуществления, области VH и VL содержат последовательности аминокислот SEQ ID NOS: 52 и 63, соответственно.
[226] В некоторых вариантах осуществления, антиидиотипическое антитело специфичное к антителу SJ25C1 или его антигенсвязывающий фрагмент представляет собой одноцепочечный фрагмент антитела, такой как scFv или диатело. В некоторых вариантах осуществления, одноцепочечное антитело содержит один или несколько линкеров, соединяющих два домена или области антитела, такие как вариабельная область (VH) тяжелой цепи и вариабельная область (VL) легкой цепи. Линкер, как правило, представляет собой пептидный линкер, например, гибкий и/или растворимый пептидный линкер. Среди линкеров имеются линкеры, обогащенные глицином и серином и/или в некоторых случаях треонином. В некоторых вариантах осуществления, линкеры дополнительно содержат заряженные остатки, такие как лизин и/или глютамат, которые могут улучшить растворимость. В некоторых вариантах осуществления, линкеры дополнительно содержат один или несколько пролинов.
[227] В некоторых вариантах осуществления, антиидиотипическое антитело представляет собой интактное антитело или полноразмерное антитело. В некоторых вариантах осуществления, анти-ID может содержать, по меньшей мере, часть константной области иммуноглобулина, например, один или несколько доменов константной области. В некоторых вариантах осуществления, константные области содержат константную область легкой цепи (CL) и/или константную область тяжелой цепи 1 (CH1). В некоторых вариантах осуществления, анти-ID содержит домен CH2 и/или CH3, например, Fc-область. В некоторых вариантах осуществления, Fc-область представляет собой Fc-область IgG человека, например, IgG1 или IgG4. В некоторых вариантах осуществления, антиидиотипическое антитело содержит домен CH, приведенный в SEQ ID NO: 115, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 115. В некоторых вариантах осуществления, антиидиотипическое антитело содержит домен CL, приведенный в SEQ ID NO: 118, или его часть, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 118, или ее часть.
[228] В некоторых вариантах осуществления, антиидиотипическое антитело специфичное к SJ25C1 содержит последовательность тяжелой цепи, приведенную в SEQ ID NO: 116, или последовательность, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 116 и/или содержит последовательность легкой цепи, приведенную в SEQ ID NO: 119 или последовательность, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 119. В некоторых вариантах осуществления, антиидиотипическое антитело специфичное к SJ25C1, содержит последовательность тяжелой цепи, приведенную в SEQ ID NO: 116, и/или последовательность легкой цепи, приведенную в SEQ ID NO: 119. В некоторых вариантах осуществления, тяжелая цепь и/или легкая цепь антиидиотипического антитела дополнительно содержит сигнальный пептид. В некоторых случаях, сигнальные пептиды имеют последовательности, приведенные в SEQ ID NO: 117 или SEQ ID NO: 120.
[229] В некоторых вариантах осуществления, антиидиотипическое антитело представляет собой антигенсвязывающий фрагмент. В некоторых вариантах осуществления, антигенсвязывающий фрагмент выбирается из группы, состоящей из антигенсвязывающих фрагментов (Fab), фрагментов F(ab')2, фрагментов Fab', фрагментов Fv, одноцепочечного вариабельного фрагмента (scFv) или однодоменного антитела.
[230] Соответственно, предлагаются одноцепочечные фрагменты антитела, такие как scFv и диатела, в частности, одноцепочечные фрагменты человека, как правило, содержащие линкер (линкеры), соединяющие два домена или области антиидиотипического антитела, таких как домены VH и VL. Линкер, как правило, представляет собой пептидный линкер, например, гибкий и/или растворимый пептидный линкер, такой как линкер, обогащенный глицином и серином.
[231] В некоторых аспектах, линкеры, обогащенные глицином и серином (и/или треонином), содержат, по меньшей мере, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% такой аминокислоты (аминокислот). В некоторых вариантах осуществления, они содержат, по меньшей мере, или, по меньшей мере, примерно 50%, 55%, 60%, 70% или 75%, глицина, серина и/или треонина. В некоторых вариантах осуществления, линкер состоит, по существу, полностью из глицина, серина и/или треонина. Линкеры, как правило, имеют длину в пределах между или примерно между 5 и 50 аминокислотами, как правило, между или примерно между 10 и 30 или примерно 30, например, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30, а в некоторых примерах, длину в пределах между 10 и 25 аминокислотами. Иллюстративные линкеры включают линкеры, имеющие различные количество повторов последовательности GGGS (3GS; SEQ ID NO: 70) или GGGGS (4GS; SEQ ID NO: 27), например, между 2, 3, 4 и 5 повторами такой последовательности. Иллюстративные линкеры включают линкеры, содержащие последовательность, приведенную в SEQ ID NO: 71 (GGGGSGGGGSGGGGS), или состоящие из нее. Иллюстративные линкеры дополнительно включают линкеры, содержащие имеющие последовательности, приведенные в SEQ ID NO: 72 (GSTSGSGKPGSGEGSTKG), или состоящие из них.
[232] В некоторых вариантах осуществления, антиидиотипические антитела включают выделенные антитела. В некоторых вариантах осуществления, анти-ID является гуманизированным, рекомбинантным и/или моноклональным. В некоторых вариантах осуществления, анти-ID представляет собой антитело человека.
b. Антитела, полученные из FMC63
[233] В некоторых вариантах осуществления, антиидиотипическое антитело является специфичным к целевому антителу анти-CD19, которое представляет собой антитело FMC63 или его антигенсвязывающий фрагмент, или получено из него.
[234] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит вариабельную (VH) область тяжелой цепи имеющую, по меньшей мере, 90% идентичность последовательности с последовательностями аминокислот области VH, приведенными в SEQ ID NO: 73 или 74, такие как, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с ней.
[235] В некоторых вариантах осуществления, антитело или его антигенсвязывающий фрагмент содержит область VH, имеющую область, определяющую комплементарность, тяжелой цепи 1 (CDR-H1), содержащую последовательность аминокислот GYX3FX5X6YX8MX10 (SEQ ID NO: 95), где X3 представляет собой T или S, X5 представляет собой T или S, X6 представляет собой D или R, X8 представляет собой Y или W, и X10 представляет собой K или N; и/или область, определяющую комплементарность, тяжелой цепи 2 (CDR-H2), содержащую последовательность аминокислот WIGX4IX6PX8X9X10X11TX13X14NQX17FKX20 (SEQ ID NO: 96), где X4 представляет собой D или M, X6 представляет собой N или H, X8 представляет собой N или S, X9 представляет собой N или D, X10 представляет собой G или S, X11 представляет собой G или E, X13 представляет собой D или R, X14 представляет собой Y или L, X17 представляет собой N или K, и X20 представляет собой G или D; и/или область, определяющую комплементарность, тяжелой цепи 3 (CDR-H3), содержащую последовательность аминокислот AX2X3X4X5X6X7X8X9X10X11X12X13X14X15 (SEQ ID NO: 97), где X2 представляет собой R или S, X3 представляет собой E или I, X4 представляет собой G или Y, X5 представляет собой N или Y, X6 представляет собой N или E, X7 представляет собой Y или ноль, X8 представляет собой G или ноль, X9 представляет собой S или ноль, X10 представляет собой R или ноль, X11 представляет собой D или ноль, X12 представляет собой A или ноль, X13 представляет собой M или ноль, X14 представляет собой D или E, и X15 представляет собой Y или A.
[236] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит вариабельную (VH) область тяжелой цепи, содержащую область, определяющую комплементарность, тяжелой цепи 3 (CDR-H3), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 75, 76, 77 или 78, и/или CDR-H3, содержащуюся в последовательностях вариабельной (VH) тяжелой цепи, приведенных в SEQ ID NO: 73 или 74.
[237] В некоторых из всех таких вариантов осуществления, область VH содержит область, определяющую комплементарность, тяжелой цепи 1 (CDR-H1), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 79, 80, 81, 82, 83, 84, 85 или 86, и/или CDR-H1, содержащуюся в последовательностях VH, приведенных в SEQ ID NO: 73 или 74; и/или области, определяющие комплементарность, тяжелой цепи 2 (CDR-H2), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 87, 88, 89, 90, 91, 92, 93 или 94, и/или CDR-H2, содержащуюся в последовательности VH, приведенных в SEQ ID NO: 73 или 74.
[238] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит вариабельную (VH) область тяжелой цепи, содержащую области, определяющие комплементарность, тяжелой цепи 1 (CDR-H1), CDR-H2 и CDR-H3, где CDR-H1 содержит последовательности аминокислот, приведенные в SEQ ID NO: 79, 80, 81, 82, 83, 84, 85 или 86; CDR-H2 содержит последовательности аминокислот, приведенные в SEQ ID NO: 87, 88, 89, 90, 91, 92, 93 или 94; и/или CDR-H3 содержит последовательности аминокислот, приведенные в SEQ ID NO: 75, 76, 77 или 78. В некоторых вариантах осуществления, предлагаются антитела или их антигенсвязывающие фрагменты, которые содержат CDR-H1, содержащую последовательности аминокислот, приведенные в SEQ ID NO: 79, 80, 81, 82, 83, 84, 85 или 86; CDR-H2, содержащие последовательности аминокислот, приведенные в SEQ ID NO: 87, 88, 89, 90, 91, 92, 93 или 94; и CDR-H3, содержащие последовательности аминокислот, приведенные в SEQ ID NO: 75, 76, 77 или 78.
[239] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающие фрагменты содержат области, определяющие комплементарность, тяжелой цепи 1 (CDR-H1), CDR-H2 и CDR-H3, соответственно, содержащие последовательности аминокислот CDR-H1, CDR-H2 и CDR-H3, содержащиеся в последовательностях аминокислот области VH, приведенных в SEQ ID NO: 73 или 74.
[240] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит CDR-H1, приведенные в SEQ ID NOS: 79, 81, 82, 83; CDR-H2, приведенные в SEQ ID NOS: 87, 89, 90, 91; и/или CDR-H3, приведенные в SEQ ID NO: 71 или 77. В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит CDR-H1, приведенные в SEQ ID NO: 80, 84, 85, 86; CDR-H2, приведенные в SEQ ID NO: 88, 92, 93, 94; и/или CDR-H3, приведенные в SEQ ID NO: 76, 78, соответственно.
[241] В некоторых из всех таких вариантов осуществления, область VH содержит последовательности каркасных областей 1 (FR1), FR2, FR3 и/или FR4, имеющие, по меньшей мере, 90% идентичность последовательности, соответственно, с FR1, FR2, FR3 и/или FR4 последовательностей аминокислот, приведенных в SEQ ID NO: 73 или 74. В некоторых вариантах осуществления, область VH содержит последовательности каркасных областей 1 (FR1), FR2, FR3 и/или FR4, имеющие, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательности, соответственно, с FR1, FR2, FR3, и/или FR4 последовательностей аминокислот, приведенных в SEQ ID NO: 73 или 74. В некоторых вариантах осуществления, область VH содержит последовательности каркасных областей 1 (FR1), FR2, FR3 и/или FR4, имеющие, по меньшей мере, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательности, соответственно, с FR1, FR2, FR3, и FR4 последовательностями аминокислот, приведенными в SEQ ID NO: 73 или 74.
[242] В некоторых из всех таких вариантов осуществления, область VH содержит последовательности аминокислот, приведенные в SEQ ID NO: 73 или 74.
[243] В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или антигенсвязывающий фрагмент представляет собой только тяжелую цепь, только VH и/или не содержит его части VL или антигенсвязывающей части, и/или антигенсвязывающий сайт антиидиотипического антитела или фрагмент содержит остатки только из тяжелой цепи и/или не содержит остатки из легкой цепи.
[244] В некоторых из всех таких вариантов осуществления, антиидиотипическое антитело или его фрагмент не содержит вариабельную (VL) область легкой цепи, не содержит CDR-L1, CDR-L2 и/или CDR-L3 и/или представляет собой однодоменное антитело (sdAb), содержащее только область VH. В некоторых вариантах осуществления, антитело или его фрагмент представляет собой sdAb, который содержит только область VH из того, что описано выше.
[245] В некоторых вариантах осуществления любых из антиидиотипических антител или фрагментов, содержащих любую из указанных выше последовательностей области VH, антиидиотипическое антитело или его фрагмент дополнительно содержит вариабельную (VL) область легкой цепи. В некоторых таких вариантах осуществления, область VL имеет, по меньшей мере, 90% идентичность последовательности с последовательностями аминокислот области VL, приведенными в SEQ ID NO: 98 или 99, например, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с последовательностями аминокислот области VL, приведенными в SEQ ID NO: 98 или 99.
[246] В некоторых вариантах осуществления, предлагаются антитела или их антигенсвязывающие фрагменты, которые включают область VH, имеющую область, определяющую комплементарность, легкой цепи 1 (CDR-L1), содержащую последовательность аминокислот X1AX3X4X5X6X7X8YX10X11WY (SEQ ID NO: 112), где X1 представляет собой S или R, X3 представляет собой S или R, X4 представляет собой S или G, X5 представляет собой G или N, X6 представляет собой V или I, X7 представляет собой I или H, X8 представляет собой N или ноль, X10 представляет собой M или L, и X11 представляет собой Y или A; и/или область, определяющую комплементарность, легкой цепи 2 (CDR-L2), содержащую последовательность аминокислот X1X2X3YX5X6X7X8LAX11 (SEQ ID NO: 113), где X1 представляет собой P или L, X2 представляет собой W или L, X3 представляет собой I или V, X5 представляет собой L или N, X6 представляет собой T или A, X7 представляет собой S или K, X8 представляет собой N или T, и X11 представляет собой S или D; и/или область, определяющую комплементарность, легкой цепи 3 (CDR-L3), содержащую последовательность аминокислот QX2X3X4X5X6PX8T (SEQ ID NO: 114), где X2 представляет собой Q или H, X3 представляет собой W или F, X4 представляет собой S или W, X5 представляет собой S или W, X6 представляет собой N или T, и X8 представляет собой L или Y.
[247] В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 3 (CDR-L3), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 100, 101, 102 или 103. В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 3 (CDR-L3), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 100, 101, 102 или 103.
[248] В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 1 (CDR-L1), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 104, 105, 106 или 107, и/или CDR-L1, содержащиеся в последовательностях VL, приведенных в SEQ ID NO: 98 или 99; и/или области, определяющие комплементарность, легкой цепи 2 (CDR-L2), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 108, 109, 110 или 111, и/или CDR-L2, содержащиеся в последовательностях VL, приведенных в SEQ ID NO: 98 или 99. В некоторых из всех таких вариантов осуществления, область VL содержит области, определяющие комплементарность, легкой цепи 1 (CDR-L1), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 104, 105, 106 или 107, и/или CDR-L1, содержащиеся в последовательностях VL, приведенных в SEQ ID NO: 98 или 99; и/или области, определяющие комплементарность, легкой цепи 2 (CDR-L2), содержащие последовательности аминокислот, приведенные в SEQ ID NO: 108, 109, 110 или 111, и/или CDR-L2, содержащиеся в последовательностях VL, приведенных в SEQ ID NO: 98 или 99.
[249] В некоторых из всех таких вариантов осуществления, область VL содержит CDR-L1, содержащие последовательности аминокислот, приведенные в SEQ ID NO: 104, 105, 106 или 107; CDR-L2, содержащие последовательности аминокислот, приведенные в SEQ ID NO: 108, 109, 110 или 111; и CDR-L3, содержащие последовательности аминокислот, приведенные в SEQ ID NO: 100, 101, 102 или 103.
[250] В некоторых из всех таких вариантов осуществления, область VL содержит CDR-L1, CDR-L2 и CDR-L3, соответственно, содержащие последовательности аминокислот CDR-L1, CDR-L2 и CDR-L3, содержащиеся в последовательностях областей VL аминокислот, приведенных в SEQ ID NO: 98 или 99.
[251] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит CDR-L1, приведенные в SEQ ID NOS: 104 или 106; CDR-L2, приведенные в SEQ ID NOS: 108 или 110; и/или CDR-L3, приведенные в SEQ ID NO: 100 или 101. В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит CDR-L1, приведенные в SEQ ID NO: 105 или 07; CDR-L2, приведенные в SEQ ID NO: 109 или 111; и/или CDR-L3, приведенные в SEQ ID NO: 102 или 103, соответственно.
[252] В некоторых из всех таких вариантов осуществления, область VL содержит каркасные области 1 (FR1), FR2, FR3, и/или FR4, имеющие, по меньшей мере, 90% идентичность последовательности, соответственно, с FR1, FR2, FR3, и/или FR4 последовательностей аминокислот, приведенных в SEQ ID NO: 98 или 99. В некоторых вариантах осуществления, область VL содержит последовательности каркасной области 1 (FR1), FR2, FR3, и/или FR4, имеющих, по меньшей мере, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательности, соответственно, с FR1, FR2, FR3, и/или FR4 последовательностей аминокислот, приведенных в SEQ ID NO: 98 или 99. В некоторых вариантах осуществления, область VL содержит последовательности каркасных областей 1 (FR1), FR2, FR3, и FR4, имеющих, по меньшей мере, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 98%, 99% идентичность последовательностей, соответственно, с FR1, FR2, FR3 и FR4 последовательностей аминокислот, приведенных в SEQ ID NO: 98 или 99.
[253] В некоторых из всех таких вариантов осуществления, область VL содержит последовательности аминокислот, приведенные в SEQ ID NO: 98 или 99.
[254] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит последовательности аминокислот последовательностей CDR-H1, CDR-H2 и CDR-H3, содержащихся в последовательности аминокислот области VH, приведенные в SEQ ID NO: 73 или 74; и/или содержит последовательности аминокислот последовательностей CDR-L1, CDR-L2 и CDR-L3 содержащихся в последовательностях аминокислот вариабельной области (VL) легкой цепи, приведенных в SEQ ID NO: 98 или 99.
[255] В некоторых вариантах осуществления, антиидиотипическое антитело или его антигенсвязывающие фрагменты содержат области VH, содержащие последовательности аминокислот, имеющие, по меньшей мере, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность со SEQ ID NOS: 73 или 74, и области VL, имеющие последовательности аминокислот, имеющие, по меньшей мере, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность с SEQ ID NOS: 98 или 99.
[256] В некоторых вариантах осуществления, предлагаются антиидиотипические антитела или их антигенсвязывающие фрагменты, которые содержат области VH, имеющие последовательности аминокислот, приведенные в SEQ ID NOS: 73 или 74, и области VL, имеющие последовательности аминокислот, приведенные в SEQ ID NOS: 98 или 99. В некоторых вариантах осуществления, предлагаемое антитело содержит область VH, приведенную в SEQ ID NO: 73 и область VL, приведенную в SEQ ID NO: 98. В некоторых вариантах осуществления, предлагаемое антитело содержит область VH, приведенную в SEQ ID NO: 74, и область VL, приведенную в SEQ ID NO: 99.
[257] В некоторых вариантах осуществления, антиидиотипическое антитело представляет собой одноцепочечный фрагмент антитела, такой как scFv или диатело. В некоторых вариантах осуществления, одноцепочечное антитело содержит один или несколько линкеров, соединяющих два домена или две области антитела, таких как вариабельная область тяжелой цепи (VH) и вариабельная область легкой цепи (VL). Линкер, как правило, представляет собой пептидный линкер, например, гибкий и/или растворимый пептидный линкер. Среди линкеров имеются линкеры, обогащенные глицином и серином, и/или, в некоторых случаях, треонином. В некоторых вариантах осуществления, линкеры дополнительно содержат заряженные остатки, такие как лизин и/или глютамат, которые могут улучшить растворимость. В некоторых вариантах осуществления, линкеры дополнительно содержат один или несколько пролинов.
[258] В некоторых вариантах осуществления, антиидиотипическое антитело представляет собой интактное антитело или полноразмерное антитело. В некоторых вариантах осуществления, анти-ID может содержать, по меньшей мере, часть константной области иммуноглобулина, такую как одна или несколько доменов константной области. В некоторых вариантах осуществления, константные области содержат константную область легкой цепи (CL) и/или константную область тяжелой цепи 1 (CH1). В некоторых вариантах осуществления, анти-ID содержит домен CH2 и/или CH3, например, Fc-область. В некоторых вариантах осуществления, Fc-область представляет собой Fc-область IgG человека, такую как IgG1 или IgG4. В некоторых вариантах осуществления, антиидиотипическое антитело содержит домены CH, приведенные в SEQ ID NO: 121 или 127 или их часть, или последовательности аминокислот, которые демонстрируют, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 121 или 127, или их часть. В некоторых вариантах осуществления, антиидиотипическое антитело содержит домены CL, приведенные в SEQ ID NO: 124 или 130, или их часть, или последовательности аминокислот, которые демонстрируют, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 124 или 130 или их часть.
[259] В некоторых вариантах осуществления, антиидиотипическое антитело специфичное к SJ25C1 содержит последовательности тяжелой цепи, приведенные в SEQ ID NO: 122 или 128, или последовательности, которые демонстрируют, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 122 или 128, и/или содержат последовательности легкой цепи, приведенные в SEQ ID NO: 125 или 131, или последовательности, которые демонстрируют, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичность последовательности с SEQ ID NO: 125 или 131, В некоторых вариантах осуществления, антиидиотипическое антитело специфичное к SJ25C1 содержит последовательность тяжелой цепи, приведенную в SEQ ID NO: 122 и/или последовательность легкой цепи, приведенную в SEQ ID NO: 131. В некоторых вариантах осуществления, антиидиотипическое антитело специфичное к SJ25C1 содержит последовательность тяжелой цепи, приведенную в SEQ ID NO: 128 и/или последовательность легкой цепи, приведенную в SEQ ID NO: 131. В некоторых вариантах осуществления, тяжелая цепь и/или легкая цепь антиидиотипического антитела дополнительно содержит сигнальный пептид. В некоторых случаях, сигнальные пептиды имеют последовательности, приведенные в SEQ ID NO: 123, 126, 129 или 132.
[260] В некоторых вариантах осуществления, антиидиотипическое антитело представляет собой антигенсвязывающий фрагмент. В некоторых вариантах осуществления, антигенсвязывающий фрагмент выбирается из группы, состоящей из антигенсвязывающих фрагментов (Fab), фрагментов F(ab')2, фрагментов Fab', фрагментов Fv, одноцепочечного вариабельного фрагмента (scFv) или однодоменного антитела.
[261] Соответственно, предлагаются одноцепочечные фрагменты антитела, такие как scFv и диатела, в частности, одноцепочечные фрагменты человека, как правило, содержащие линкер (линкеры), соединяющий два домена или области антиидиотипического антитела, такие как домены VH и VL. Линкер, как правило, представляет собой пептидный линкер, например, гибкий и/или растворимый пептидный линкер, такой как линкер, обогащенный глицином и серином.
[262] В некоторых аспектах, линкеры, обогащенные глицином, и серином (и/или треонином), содержат, по меньшей мере, 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% таких аминокислот. В некоторых вариантах осуществления, они содержат, по меньшей мере, или, по меньшей мере, примерно 50%, 55%, 60%, 70% или 75% глицина, серина и/или треонина. В некоторых вариантах осуществления, линкер состоит, по существу, полностью из глицина, серина и/или треонина. Линкеры, как правило, содержат в пределах между или примерно между 5 и 50 аминокислотами, как правило, между или примерно между 10 и 30 или примерно 30, например, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30, и в некоторых примерах, имеют длину в пределах между 10 и 25 аминокислотами. Иллюстративные линкеры включают линкеры, имеющие различное количество повторов последовательности GGGS (3GS; SEQ ID NO: 70) или GGGGS (4GS; SEQ ID NO: 27), например, между 2, 3, 4, и 5 повторами такой последовательности. Иллюстративные линкеры включают линкеры, имеющие последовательность, приведенную в SEQ ID NO: 71 (GGGGSGGGGSGGGGS), или состоящие из нее. Иллюстративные линкеры дополнительно включают линкеры, содержащие последовательность, приведенную в SEQ ID NO: 72 (GSTSGSGKPGSGEGSTKG). или состоящие из нее.
[263] В некоторых вариантах осуществления, антиидиотипические антитела содержат выделенные антитела. В некоторых вариантах осуществления, анти-ID является гуманизированным, рекомбинантным и/или моноклональным. В некоторых вариантах осуществления, анти-ID представляет собой антитело человека.
3. Дополнительные компоненты
[264] В определенных вариантах осуществления, частицы, например, сферические частицы, содержат поверхностно конъюгированную или иным образом присоединенную связывающую молекулу, которая связывается или распознается антигенсвязывающим доменом рекомбинантного рецептора, например, CAR, и один или несколько дополнительных агентов, которые могут связывать и/или распознавать дополнительную молекулу на клетке. В некоторых вариантах осуществления, один или несколько дополнительных агентов представляет собой дополнительную связывающую молекулу. В некоторых вариантах осуществления, одна или несколько дополнительных связывающих молекул представляют собой антитела (или их фрагменты или варианты), которые связываются с полипептидами (например, гликопротеинами), которые присутствуют на поверхности клеток, которые экспрессируют рекомбинантный рецептор. В конкретных вариантах осуществления, одна или несколько дополнительных связывающих молекул представляют собой полипептиды или их части, которые связываются с молекулой на поверхности клеток, такой как рецептор, например, активирующий, костимуляторный или корецептор, экспрессируемый на поверхности клетки, такой как клетка, которая экспрессирует рекомбинантный рецептор. В конкретных вариантах осуществления, одна или несколько дополнительных связывающих молекул представляют собой лиганды или их части, которые связываются с полипептидами, которые присутствуют на поверхности клеток, таких как клетки, которые экспрессируют рекомбинантный рецептор. В определенных вариантах осуществления, один или несколько дополнительных агентов экспонируются на поверхности частицы.
[265] В конкретных вариантах осуществления, один или несколько дополнительных агентов могут модулировать функцию клетки, например, размножение, посредством связывания дополнительной молекулы на поверхности клетки. В некоторых вариантах осуществления, агент связывается с дополнительной молекулой на клетке и активирует дополнительный сигнал на клетке, то есть, связывание дополнительного агента с дополнительной молекулой на поверхности клетки оказывает такие же или сходные воздействия на одну или несколько функций клетки, например, размножение, как и связывание дополнительной молекулы с дополнительной молекулой на поверхности клетки. В некоторых вариантах осуществления, дополнительный агент представляет собой антитело или его фрагмент, который связывает и распознает дополнительную молекулу на поверхности клетки. В конкретных вариантах осуществления, агент представляет собой лиганд или его часть, которая связывает или распознает дополнительную молекулу на поверхности клетки.
[266] В некоторых вариантах осуществления, молекула распознаваемая или связываемая одним или несколькими дополнительными агентами, представляет собой CD2, CD3, CD4, CD5, CD8, CD25, CD27, CD28, CD29, CD31, CD44, CD45RA, CD45RO, CD54 (ICAM-1), CD127, MHCI, MHCII, CTLA-4, ICOS, ICOSL, PD-1 (CD279), PD-L1 (CD274, B7-H1), PDL2 (CD273, B7-DC), OX40 (CD134, TNFRSF4), OX-40L, DAP10, CD27L (CD70), 4-1BB (CD137), 4-1BBL, CD30L, LIGHT, IL-2R, IL-12R, IL-1R, IL-15R; IFN-гаммаR, TNF-альфаR, IL-4R, IL- 10R, CD18/CDl la (LFA-1), CD62L (L-селектин), CD29/CD49d (VLA-4), лиганд сложного локуса (например, дельта-образный 1/4, зубчатый 1/2, и тому подобное), CCR1, CCR2, CCR3, CCR4, CCR5, CCR7, CXCR3, CTLA-4, LAG-3 (CD223), TIM-3, 4-1BB (CD137), GITR (TNFRSF18, AITR), CD40, CXCR2, антигены, ассоциированные с опухолью (TAA), B7-H3, B7-H4, BTLA, HVEM, GAL9, B7H3, B7H4, VISTA, KIR, 2B4 (принадлежит к семейству молекул CD2 и экспрессируется на всех клетках NK, γδ и на Т-лимфоцитах памяти CD8+ (αβ)), CD160 (также упоминается как BY55), CGEN-15049, CEACAM, например, CEACAM-1, CEACAM-3 и/или CEACAM-5), TIGIT, CD155, CD155, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), HIGHT, KIR, A2aR, MHC класс I, MHC класс II, GAL9, аденозин или рецептор трансформирующего фактора роста (TGFR; например, TGFR бета).
[267] В некоторых вариантах осуществления, частицы, например, шарики, имеют поверхность, конъюгированную или иным образом присоединенную к связывающей молекуле, которая связывается или распознается антигенсвязывающим доменом рекомбинантного рецептора, например, CAR, и с одной или несколькими дополнительными связывающими молекулами, которые связываются с молекулой контрольной точки, такой как ингибиторный рецептор или активирующий рецептор, или его лиганд. В некоторых вариантах осуществления, связывающая молекула содержит внеклеточный домен или его связывающую часть от ингибиторного рецептора или его лиганда, или от активирующего рецептора или его лиганда. В некоторых вариантах осуществления, связывающая молекула сливается с доменом мультимеризации, таким как Fc-область или -домен. В конкретных вариантах осуществления, частицы, например, шарики, имеют поверхность, конъюгированную или иным образом присоединенную к связывающей молекуле, которая связывается или распознается антигенсвязывающим доменом рекомбинантного рецептора, например, CAR, и одну или несколько дополнительных связывающих молекул, которые связываются с OX-40, ICOS, DAP10, CD28 или 4-1BB, CTLA-4, PD-1, LAG-3, Tim-3, BTLA или TIGIT. В некоторых вариантах осуществления, частицы, например, шарики, имеют поверхность, конъюгированную или иным образом присоединенную к связывающей молекуле, которая связывается или распознается антигенсвязывающим доменом рекомбинантного рецептора, например, CAR, и одну или несколько дополнительных связывающих молекул, которые связываются с OX-40L, ICOSL, B7-1, B7-2 или 4-1BBL, PD-L1, PD-L2, CD155, CD112 или LIGHT.
[268] В конкретных вариантах осуществления, частицы, например, шарики, содержат поверхностно конъюгированную или иным образом присоединенную связывающую молекулу, которая связывается или распознается антигенсвязывающим доменом рекомбинантного рецептора, например, CAR, и одну или несколько дополнительных связывающих молекул, например, антител или их фрагментов или вариантов, которые связываются с CD3 и/или CD28. В некоторых вариантах осуществления, одна или несколько дополнительных молекул связываются с CD2 или CD28. В конкретных вариантах осуществления, частицы, например, шарики, содержат поверхностно конъюгированную или иным образом присоединенную связывающую молекулу, которая связывается или распознается антигенсвязывающим доменом рекомбинантного рецептора, например, CAR, и одну или несколько дополнительных связывающих молекул, которые связываются с CD28.
[269] В некоторых вариантах осуществления, частица содержит поверхностно конъюгированную связывающую молекулу и дополнительный поверхностно конъюгированный агент, который связывается с CD2. В определенных вариантах осуществления, частица содержит поверхностно конъюгированную связывающую молекулу и поверхностно конъюгированное антитело анти-CD2. В конкретных вариантах осуществления, частица содержит поверхностно конъюгированную связывающую молекулу и дополнительный поверхностно конъюгированный агент, который связывается с CD28. В различных вариантах осуществления, частица содержит поверхностно конъюгированную связывающую молекулу и поверхностно конъюгированное антитело анти-CD28. В некоторых вариантах осуществления, частица содержит поверхностно конъюгированную связывающую молекулу и дополнительные поверхностно конъюгированные агенты, которые связываются с CD2 и CD28. В различных вариантах осуществления, частица содержит поверхностно конъюгированную связывающую молекулу и поверхностно конъюгированные антитела анти-CD2 и анти-CD28. В определенных вариантах осуществления, связывающая молекула представляет собой или содержит антиген BCMA, ROR1 или CD22 или фрагмент, содержащий эпитоп. В определенных вариантах осуществления, связывающая молекула представляет собой анти-ID, которое связывает или распознает рекомбинантный рецептор, например, CAR.
[270] В конкретных вариантах осуществления, частица содержит поверхностно конъюгированное анти-ID, например, анти-ID, которое связывается и распознается CAR, таким как CAR анти-CD19, и поверхностно конъюгированное антитело анти-CD2. В определенных вариантах осуществления, частица содержит поверхностно конъюгированное анти-ID, например, анти-ID, которое связывается и распознается CAR, таким как CAR анти-CD19, и поверхностно конъюгированное антитело анти-CD28. В различных вариантах осуществления, частица содержит поверхностно конъюгированное анти-ID, например, анти-ID, которое связывается и распознается CAR, таким как CAR анти-CD19, и поверхностно конъюгированные антитела анти-CD2 и анти-CD28.
[271] В некоторых вариантах осуществления, отношение, такое как молярное или массовое отношение, связывающей молекулы и дополнительного агента или молекулы составляет от или примерно от 1:10 до 10:1, например, от 1:5 до 5:1 или от 1:2 до 2:1 или составляет примерно 1:1. В определенных вариантах осуществления, отношение, например, молярное или массовое отношение, связывающей молекулы к двум дополнительным агентам составляет или составляет примерно 1:1:1.
C. Способы конъюгирования
[272] В настоящем документе предлагаются частицы (например, сферические частицы), которые конъюгируются и/или соединяются со связывающими молекулами (например, с полипептидным антигеном или антителом), которые связываются или распознаются рекомбинантным рецептором (например, CAR). Для конъюгирования связывающих молекул можно использовать разнообразные средства, хорошо известные в данной области, например, полипептидные антигены и антиидиотипические антитела, вместе с частицами (например, сферическими частицами). Эти способы включают любые стандартные химические механизмы, которые не разрушают или не ограничивают жестко биологическую активность или структуру связывающей молекулы и которые делают возможным конъюгирование значительного количества связывающих молекул с частицей способом, который делает возможным взаимодействие связывающей молекулы, например, пептидного или белкового антигена, с рекомбинантным рецептором. В некоторых вариантах осуществления, выбирают способ конъюгирования, который конъюгирует C-концевую область связывающей молекулы, например, полипептидной связывающей молекулы, с частицей. Специалист в данной области поймет, что конкретные химические механизмы конъюгирования могут зависеть от природы материала частиц, от функциональных групп, экспонируемых на поверхности частицы, от присутствия или отсутствия C-концевых слияний со связывающей молекулой, и присутствия или отсутствия конъюгирующих остатков. Независимо от селектированного химического механизма важно, чтобы способ конъюгирования не изменял функцию и/или структурное подтверждение связывающей молекулы. Например, если связывающая молекула представляет собой антиген, способ, селектированный для конъюгирования антигена с частицей, не должен мешать распознаванию антигена конъюгированным рецептором. В определенных вариантах осуществления, если связывающая молекула представляет собой антитело, например, анти-ID, способ конъюгирования не должен мешать связыванию антитела с его целевым антигеном.
[273] В некоторых вариантах осуществления, связывающая молекула (например, полипептидный антиген или анти-ID) присоединяется к частице (например, сферической частице) посредством пассивного поглощения обычной поверхностью частицы. Присоединение с помощью этого способа, как правило, основывается на гидрофобных взаимодействиях, которые связывают связывающую молекулу с шариком. Хотя этот способ относительно прост, в некоторых вариантах осуществления, способ обеспечивает небольшой контроль конечной ориентации присоединенной молекулы по сравнению с другими технологиями присоединения связывающей молекулы, такими как любые технологии, обсуждаемые в настоящем документе, такие как в Раздел I-C.
1. Связывание с поверхностью частицы
[274] В определенных вариантах осуществления, связывающие молекулы связываются с носителем с помощью ковалентной химической связи. В конкретных вариантах осуществления, связывающая молекула представляет собой полипептид и химически активная группа или остаток аминокислоты конъюгируется непосредственно с химически активной группой или остатком на поверхности частицы посредством прямой химической реакции. В определенных вариантах осуществления, карбоксильная группа аминокислоты (например, C-концевая карбоксильная группа), гидроксильная, тиольная или аминовая группа (такая как группа боковой цепи аминокислоты) связывающей молекулы конъюгируется непосредственно с гидроксильной или карбоксильной группой полимера PLA или PGA, конечной аминовой или карбоксильной группой дендримера или с гидроксильной, карбоксильной или фосфатной группой фосфолипида на поверхности частицы посредством прямой химической реакции. В некоторых вариантах осуществления, конъюгирующий остаток конъюгируется, например, ковалентно связывается, как со связывающей молекулой, так и с частицей, тем самым связывая их вместе.
[275] В определенных вариантах осуществления, поверхность частицы содержит химические остатки и/или функциональные группы, которые делают возможным присоединение (например, ковалентное, нековалентное) связывающей молекулы (например, полипептидного антигена или антитела). В некоторых вариантах осуществления, количество, ориентация, расстояние друг от друга, и тому подобное, химических остатков и/или функциональных групп на частице изменяется в соответствии с химией частицы и свойствами связывающей молекулы. В конкретных вариантах осуществления, частицы, например, шарики, имеют введенные модифицированные поверхности. В конкретных вариантах осуществления, поверхности частиц содержат экспонируемые функциональные группы. Соответствующие поверхностно экспонируемые функциональные группы включают, но, не ограничиваясь этим, карбоксильные, амино, гидроксильные, сульфатные группы, тозильные, эпокси, и хлорметильные группы.
[276] В некоторых вариантах осуществления, связывающая молекула представляет собой полипептид и конъюгируется с поверхностно экспонируемыми функциональными группами. В некоторых вариантах осуществления, поверхностно экспонируемая функциональная группа должна активироваться, то есть, должна подвергаться химической реакции для получения промежуточного продукта, который может непосредственно связывать полипептид. Конкретные варианты осуществления предполагают, что активация поверхностно экспонируемых функциональных групп на частице сделает возможным конъюгирование связывающей молекулы способом обычным в данной области и что специалист легко идентифицировал бы соответствующие реагенты и протоколы для осуществления любых необходимых стадий активации для конъюгирования связывающей молекулы с частицей.
[277] В некоторых вариантах осуществления, для связывания полипептидной связывающей молекулы с карбоксилированной частицей, например, со сферической частицей, поверхностно экспонируемые карбоксильные группы частицы требуют активации посредством приведения в контакт функциональной группы с агентом, который будет давать промежуточный сложный эфир, который может непосредственно связывать аминовую группу. Химически активные (то есть активированные) карбоксильные группы на поверхности частицы могут конъюгироваться со свободными аминами (например, из остатков Lys) на полипептиде. Пригодные для использования агенты включают, например, но не ограничиваясь этим, карбодиимид (EDC), этиленкарбодиимид (ECDI), гексаметилендиизоцианат, простой диглициидиловый эфир пропиленгликоля, который содержит 2 эпокси остатка, эпихлоргидрин, N-гидроксисукцинимид (NHS) или сульфо-NHS, или этил(диметиламинопропил). В некоторых вариантах осуществления, полипептидная связывающая молекула ковалентно присоединяется к частице на поверхностно экспонируемой карбоксильной группе. В конкретных вариантах осуществления, полипептидная связывающая молекула ковалентно присоединяется к поверхностно экспонируемой карбоксильной группе посредством приведения сначала в контакт карбоксильной группы с агентом для генерирования промежуточного сложного эфира.
[278] В некоторых вариантах осуществления, функциональная группа полипептидной связывающей молекулы активируется перед конъюгированием полипептида с поверхностно экспонируемой функциональной группой. Например, карбоксильная группа полипептидной молекулы может активироваться агентами, описанными выше с генерированием промежуточных сложных эфиров способных непосредственно связываться с поверхностно экспонируемыми амино группами частицы. В некоторых вариантах осуществления, полипептидная связывающая молекула конъюгируется с частицей на поверхностно экспонируемой аминовой группе. В конкретных вариантах осуществления, карбоксильная группа полипептидной связывающей молекулы приводится в контакт с агентом для генерирования промежуточного сложного эфира перед ковалентным присоединением частицы к поверхностно экспонируемой карбоксильной группе частицы. Альтернативно, свободные аминовые группы на поверхности носителя могут ковалентно связываться с антигенными пептидами и белками или слитым белком антигенного пептида или белка, с использованием химического механизма сульфосукцинимидил(4-йодацетил)аминобензоата (сульфо-SIAB).
[279] В конкретных вариантах осуществления, полипептидная связывающая молекула ковалентно присоединяется к частице, например, сферической частице, на поверхностно экспонируемой функциональной группе, которая не требует активации агентом до образования ковалентного присоединения. Примеры таких функциональных групп включают, но, не ограничиваясь этим, тозильные, эпокси и хлорметильные группы. В конкретных вариантах осуществления, ковалентное присоединение может осуществляться в присутствии конкретных буферов, в конкретных диапазонах pH, в конкретных диапазонах температуры, и в течение конкретных периодов времени, что может легко определяться и осуществляться для любой такой функциональной группы специалистом в данной области. Например, в некоторых вариантах осуществления, тозильные группы на поверхности частицы связываются с амино или с сульфгидрильными группами связывающей молекулы (например, полипептидного антигена или антитела) в зависимости от pH. Для связывания сульфгидрильных групп полипептида с тозильной группой используют нейтральные pH, в то время как для связывания амино групп полипептида с тозильной группой используют более основные pH. В конкретных вариантах осуществления, полипептидная связывающая молекула (например, антиген или антитело) ковалентно присоединяется к частице (например, сферической частице) на поверхностно экспонируемой тозильной группе, эпокси группе или хлорметильной группе частицы. В конкретных вариантах осуществления, полипептидная связывающая молекула присоединяется к тозилированной частице (то есть частице, содержащей поверхностно экспонируемые тозильные группы).
[280] В некоторых вариантах осуществления, нековалентная связь между лигандом связанным с пептидом или белком антигена и анти-лигандом, присоединенным к носителю, может конъюгировать антиген с носителем. В некоторых вариантах осуществления, метка последовательности распознавания биотинлигазы может соединяться с C-концом пептида или белка антигена, и эта метка может биотинилироваться с помощью биотинлигазы. Затем биотин может служить как лиганд для нековалентного конъюгирования пептида или белка антигена с авидином или стрептавидином, который адсорбируется или иным образом связывается с поверхностью носителя как анти-лиганд. Альтернативно, если пептиды и белки антигена сливаются с доменом иммуноглобулина, несущим Fc-область, как описано выше, Fc-домен может действовать как лиганд, и белок A, либо ковалентно, либо нековалентно связанный с поверхностью носителя, может служить как анти-лиганд для нековалентного конъюгирования пептида или белка антигена с носителем. В данной области хорошо известны другие средства, которые можно использовать для нековалентного конъюгирования пептидов и белков антигенов с носителями, включая технологии хелатирования ионов металлов (например, используя метку поли-His на C-конце антигенного пептида или белка, или слитых белков антигенного пептида или белка, и носителя с покрытием из Ni), и эти способы можно использовать вместо того, что описано в настоящем документе.
[281] В некоторых вариантах осуществления, связывающая молекула конъюгируется с частицей с помощью линкера. В определенных вариантах осуществления, линкеры могут включать, но, не ограничиваясь этим, разнообразные бифункциональные агенты связывания белков, такие как N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP), сукцинимидил-4-(N-малеимидометил)циклогексан-l-карбоксилат, иминотиолан (IT), бифункциональные производные сложных имидоэфиров (такие как диметиладипимидат HCL), активные сложные эфиры (такие как дисукцинимидилсуберат), альдегиды (такие как глютаральдегид), бис-азидо соединения (такие как бис (п-азидобензоил)гександиамин), производные бис-диазония (такие как бис-(п-диазонийбензоил)-этилендиамин), диизоцианаты (такие как толуол 2,6-диизоцианат), и бис-активные соединения фтора (такие как l,5-дифтор-2,4-динитробензол). Конкретные связывающие агенты включают N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) и N-сукцинимидил-4-(2-пиридилтио)пентаноат (SPP) для получения дисульфидной связи.
2. Обратимое связывание
[282] В некоторых вариантах осуществления, связывающая молекула обратимо присоединена или иным образом ассоциирована с частицей, например, сферической частицей. В определенном варианте осуществления, связывающая молекула обратимо присоединена или иным образом ассоциирована с реагентом, который присоединен к частице. В конкретных вариантах осуществления, реагент экспонируется на поверхности частицы. В определенных вариантах осуществления, реагент содержит множество сайтов связывания, которые могут обратимо связываться со связывающей молекулой. В некоторых вариантах осуществления, реагент представляет собой реагент мультимеризации. В некоторых вариантах осуществления, взаимодействие связывания между связывающей молекулой и реагентом представляет собой нековалентное взаимодействие. В некоторых вариантах осуществления, взаимодействие связывания между связывающей молекулой и реагентом, например, нековалентное взаимодействие связывания, является обратимым. В некоторых вариантах осуществления, связывающая молекула обратимо присоединена к частице, которая представляет собой олигомер или полимер, состоящий из белков, например, стрептавидин.
[283] В некоторых вариантах осуществления, обратимая ассоциация между связывающей молекулой и реагентом может медиироваться присутствием вещества, такого как конкурентный реагент (также называемый элюирующий реагент), который представляет собой или содержит сайт связывания, который также может связываться с таким же сайтом (или сайтами) связывания реагента, который связан со связывающей молекулой. Как правило, вещество (например, конкурентный реагент) может действовать как конкурент из-за более высокой аффиности связывания для сайта связывания, присутствующего в реагенте и/или из-за присутствия при более высоких концентрациях, чем связывающая молекула, тем самым вызывая отсоединение и/или диссоциацию связывающей молекулы и реагента. В некоторых вариантах осуществления, аффиность вещества (например, конкурентного реагента), по меньшей мере, к одному сайту связывания на реагенте больше, чем аффиность связывающей молекулы, по меньшей мере, к одному сайту связывания на реагенте. Таким образом, в некоторых вариантах осуществления, связь между связыванием реагента и связывающей молекулой может разрушаться при добавлении вещества (например, конкурентного реагента), тем самым делая ассоциацию агента (например, рецепторсвязывающего агента или селекционного агента) и реагента, обратимой.
[284] Реагенты, которые можно использовать в таких обратимых системах, описаны и известны в данной области, смотри, например, патенты США №№5168049; 5506121; 6103493; 7776562; 7981632; 8298782; 8735540; 9023604 и Международные опубликованные заявки PCT №№ WO 2013/124474 и WO 2014/076277. Неограничивающие примеры реагентов и партнеров по связыванию способных формировать обратимое взаимодействие, а также веществ (например, конкурентных реагентов) способных обращать такое связывание, описаны ниже.
[285] В некоторых вариантах осуществления, реагент присоединен и экспонируется на поверхности частицы, например, сферической частицы, и содержит множество сайтов связывания, которые могут специфично связываться со связывающей молекулой, так что реагент может обратимо связываться со множеством связывающих молекул, например, представляет собой реагент мультимеризации. В некоторых вариантах осуществления, реагент представляет собой олигомер или полимер из индивидуальных молекул (например, мономеров) или комплексов, которые составляют индивидуальную молекулу (например, тетрамер), которые присоединены к поверхности частицы, каждый из них содержит, по меньшей мере, один сайт связывания способный связываться со связывающей молекулой. В некоторых вариантах осуществления, частица состоит из реагента, то есть частица представляет собой олигомер или полимер реагента.
[286] В некоторых вариантах осуществления, реагент представляет собой стрептавидин, мутеин или аналог стрептавидина, авидин, мутеин или аналог авидина (такой как нейтравидин) или их смесь, в которой такой реагент содержит один или несколько сайтов связывания способных к обратимой ассоциации со связывающей молекулой. В некоторых вариантах осуществления, связывающая молекула содержит биотин, производное или аналог биотина, или стрептавидинсвязывающий пептид или другую молекулу, которая может специфично связываться с реагентом. В некоторых вариантах осуществления, связывающая молекула содержит биотин, производное или аналог биотина, или стрептавидинсвязывающий пептид или другую молекулу, которая может специфично связываться со стрептавидином, мутеином или аналогом стрептавидина, авидином или мутеином или аналогом авидина. В определенных вариантах осуществления, связывающая молекула представляет собой полипептид, например, полипептидный антиген или антитело, которое содержит слитый домен, который представляет собой биотин, производное или аналог биотина, или стрептавидинсвязывающий пептид или другую молекулу, которая может специфично связываться со стрептавидином, мутеином или аналогом стрептавидина, авидином или мутеином или аналогом авидина. В некоторых вариантах осуществления, связывающая молекула представляет собой полипептид, который содержит слитый домен, который представляет собой биотин, производное или аналог биотина или стрептавидинсвязывающий пептид или другую молекулу, которая может специфично связываться с стрептавидином, мутеином или аналогом стрептавидина, авидином или мутеином или аналогом авидина, и реагент представляет собой или содержит стрептавидин, авидин, аналог или мутеин стрептавидина или аналог или мутеин авидина, который обратимо связывает биотин, аналог биотина или его биологически активный фрагмент. В определенных вариантах осуществления, слитый домен располагается на C-конце связывающей молекулы. В некоторых вариантах осуществления, реагент представляет собой или содержит аналог или мутеин стрептавидина или аналог или мутеин авидина, который обратимо связывает стрептавидинсвязывающий пептид. В некоторых вариантах осуществления, вещество (например, конкурентный реагент) может представлять собой биотин, производное или аналог биотина, или стрептавидинсвязывающий пептид способный конкурировать за связывание со связывающей молекулой на одном или нескольких сайтах связывания реагента. В некоторых вариантах осуществления, слитые домены связывающей молекулы и вещества (например, конкурентного реагента) различаются, и вещество (например, конкурентный реагент) демонстрирует более высокую аффиность связывания с реагентом по сравнению с аффиностью связывающей молекулы к реагенту. В определенных вариантах осуществления, слитый домен и вещество, например, конкурентный реагент, являются одинаковыми.
[287] В некоторых вариантах осуществления, стрептавидин может представлять собой стрептавидин дикого типа, мутеины или аналоги стрептавидина, такие как стрептавидиноподобные полипептиды. Подобным же образом, авидин, в некоторых аспектах, включает авидин дикого типа или мутеины или аналоги авидина, такие как нейтравидин, дегликозилированный авидин с модифицированными аргининами, который, как правило, демонстрирует более нейтральную изоэлектрическую точку и доступен как альтернатива нативному авидину. Как правило, дегликозилированные, нейтральные формы авидина включают коммерчески доступные формы такие, например, как "Extravidin", доступный от Sigma Aldrich или "NeutrAvidin" доступный от Thermo Scientific или Invitrogen.
[288] В некоторых вариантах осуществления, реагент представляет собой стрептавидин или мутеин или аналог стрептавидина. В некоторых вариантах осуществления, стрептавидин дикого типа (wt-стрептавидин) содержит последовательность аминокислот, описанную Argarana et al, Nucleic Acids Res. 14 (1986) 1871-1882 (SEQ ID NO: 21). Как правило, стрептавидин встречается в природе как тетрамер из четырех идентичных субъединиц, то есть он представляет собой гомо-тетрамер, где каждая субъединица содержит один сайт связывания для биотина, производного или аналога биотина, или миметика биотина. Иллюстративная последовательность субъединицы стрептавидина представляет собой последовательность аминокислот, приведенную в SEQ ID NO: 21, но такая последовательность также может включать последовательность, представленную в ее гомологах от других видов Streptomyces. В частности, каждая субъединица стрептавидина может демонстрировать сильную аффиность связывания с биотином с равновесной константной диссоциации (KD) порядка примерно 10-14 M. В некоторых случаях, стрептавидин может существовать как одновалентный тетрамер, в котором только один из четырех сайтов связывания является функциональным (Howarth et al. (2006) Nat. Methods, 3:267-73; Zhang et al. (2015) Biochem. Biophys. Res. Commun., 463:1059-63)), двухвалентный тетрамер, в котором два из четырех сайтов связывания являются функциональными (Fairhead et al. (2013) J. Mol. Biol., 426:199-214), или может присутствовать в мономерной или димерной форме (Wu et al. (2005) J. Biol. Chem., 280:23225-31; Lim et al. (2010) Biochemistry, 50:8682-91).
[289] В некоторых вариантах осуществления, связывающая молекула содержит слитый домен, который представляет собой Strep-tag, например, как описано в патенте США № 5506121, который представляет собой пептидную последовательность, которая действует как миметик биотина и демонстрирует аффиность связывания стрептавидина. В некоторых случаях, аффиность связывания может дополнительно быть улучшена посредством осуществления мутации в молекуле стрептавидина, смотри, например, патент США №6103493 или Международную опубликованную заявку PCT № WO 2014/076277. В некоторых вариантах осуществления, аффиность связывания может определяться с помощью способов известных в данной области.
[290] В некоторых вариантах осуществления, реагент, такой как стрептавидин или мутеин стрептавидина, демонстрирует аффиность связывания со слитым доменом связывающей молекулы. В некоторых вариантах осуществления, слитый домен содержит пептидную последовательность, которая содержит последовательность с общей формулой, приведенной в SEQ ID NO: 11, например, содержит последовательность, приведенную в SEQ ID NO: 12. В некоторых вариантах осуществления, пептидная последовательность имеет общую формулу, приведенную в SEQ ID NO: 13, например, как приведено в SEQ ID NO: 43. В одном из примеров, пептидная последовательность приведена в SEQ ID NO: 9. В одном из примеров, пептидная последовательность приведена в SEQ ID NO: 10, она известна также как стрептавидиновый полипептид STREP - STREP® II. В некоторых вариантах осуществления, пептидный лиганд содержит последовательное расположение, по меньшей мере, двух стрептавидинсвязывающих модулей, где расстояние между двумя модулями составляет, по меньшей мере, 0 и не больше 50 аминокислот, где один связывающий модуль имеет 3-8 аминокислот и содержит, по меньшей мере, последовательность His-Pro-Xaa (SEQ ID NO: 11), где Xaa представляет собой глютамин, аспарагин или метионин, и где другой связывающий модуль имеет такой же или иной стрептавидиновый пептидный лиганд, например, как приведено в SEQ ID NO: 13 (смотри, например, Международную опубликованную заявку PCT № WO 02/077018; патент США №7981632). В некоторых вариантах осуществления, пептидный лиганд содержит последовательности, имеющие формулы, приведенные в любой из SEQ ID NO: 15 или 16. В некоторых вариантах осуществления, пептидный лиганд содержит последовательности аминокислот, приведенные в любой из SEQ ID NOS: 15-22.
[291] В некоторых вариантах осуществления, реагент представляет собой стрептавидин или мутеин стрептавидина (или его часть), который связывается и распознается другими лигандами стрептавидина, такими как, но, не ограничиваясь этим, биотин, иминобиотин, липоевая кислота, детиобиотин, диаминобиотин, HABA (гидроксиазобензолбензойная кислота) и/или диметил-HABA. В некоторых вариантах осуществления, мутеин стрептавидина демонстрирует аффиность связывания с другим стрептавидиновым лигандом, таким как биотин или детиобиотин, которая больше, чем аффиность связывания мутеина стрептавидина с пептидным лигандом миметика биотина, например, как приведено в любой из SEQ ID NOS: 7-19. Таким образом, в некоторых вариантах осуществления, биотин или аналог или производное биотина (например, детиобиотин) можно использовать в качестве конкурентного реагента в предлагаемых способах. Например, в качестве примера, это взаимодействие мутеина стрептавидина, обозначенного Strep-tactin® (например, содержащего последовательность, приведенную в SEQ ID NO: 23).
[292] В некоторых вариантах осуществления, реагент содержит, по меньшей мере, две хелатирующие группы K, которые могут связываться с ионом переходного металла. В некоторых вариантах осуществления, реагент может связываться с меткой аффиности из олигогистидина, глютатион-S-трансферазы, кальмодулина или его аналога, связывающего пептида кальмодулина (CBP), FLAG-пептида, HA-tag, связывающего белка мальтозы (MBP), эпитопа HSV, эпитопа myc и/или биотинилированного белка-носителя.
3. Ориентация связывающей молекулы
[293] В некоторых вариантах осуществления, связывающая молекула связывается или присоединяется к частице, например, к сферической частице, в ориентации, которая оптимизируется, чтобы сделать возможным взаимодействие между связывающей молекулой и клеткой, которая экспрессирует рекомбинантный рецептор, например, CAR, который связывается или распознается связывающей молекулой. В некоторых вариантах осуществления, оптимизированная ориентация дает возможность для связывания связывающей молекулы и рекомбинантного рецептора при минимальном или нулевом влиянии частицы, с которой связана связывающая молекула. В некоторых вариантах осуществления, относительное положение частицы по отношению к области связывающей молекулы, которая связывает или распознает CAR, например, антигена или анти-ID, не мешает доступу к этой области для контактных клеток, которые экспрессируют рекомбинантный рецептор, например, CAR. В некоторых вариантах осуществления, связывающая молекула присоединена к частице в другой области, например, в слитом домене, отличной от области, которая связывает или распознает рекомбинантный рецептор целевой клетки, например, антигена или анти-ID. В определенных вариантах осуществления, связывающая молекула не присоединяется к частице в области, которая связывает или распознает рекомбинантный рецептор. В определенных вариантах осуществления, связывающая молекула с меньшей вероятностью присоединяется к частице в области, которая связывает или распознает рекомбинантный рецептор, по сравнению с другой областью связывающей молекулы.
[294] Конкретные варианты осуществления предполагают, что, когда связывающая молекула связывается с частицей, например, с сферической частицей, на одном конце связывающей молекулы, например, на C-конце, это обеспечивает оптимальную ориентацию связывающей молекулы для связывания с рекомбинантным рецептором. В некоторых вариантах осуществления, связывающая молекула связывается с частицей на конце противоположном области, которая связывает или распознает рекомбинантный рецептор. В определенных вариантах осуществления, связывающая молекула присоединена к частице таким образом, что область, которая связывается с рекомбинантным рецептором, например, антиген или анти-ID, располагается вдали от частицы. В конкретных вариантах осуществления, связывающая молекула присоединяется к частице на одном конце, например, на своем C-конце, а область, которая связывается с рекомбинантным рецептором, на противоположном конце, например, N-конце связывающей молекулы. В конкретных вариантах осуществления, связывающая молекула присоединяется к частице таким образом, что антиген или анти-ID связывающей молекулы располагается в ориентации наружу по отношению к частице. В некоторых вариантах осуществления предполагается, что ориентация наружу от частицы для области, которая связывает рекомбинантный рецептор, обеспечивает самую наибольшую вероятность взаимодействий между связывающими молекулами и клетками, которые экспрессируют рекомбинантный рецептор.
[295] В некоторых вариантах осуществления, связывающая молекула, например, полипептид, содержит область, которая связывает или распознает рекомбинантный рецептор целевых клеток, например, и антиген или анти-ID, и присоединяется или связывается с частицей в отдельной области, например, в слитом домене. В определенных вариантах осуществления, область, которая связывает или распознает рекомбинантный рецептор, и отдельная область, например, слитый домен, находятся на противоположных концах связывающей молекулы. В определенных вариантах осуществления, связывающая молекула содержит область, которая связывает или распознает рекомбинантный рецептор целевой клетки, который находится на N-конце связывающей молекулы или вблизи него, и отдельную область, например, слитый домен, который находится на C-концевом домене или вблизи него. В некоторых вариантах осуществления, связывающая молекула содержит область, которая связывает или распознает рекомбинантный рецептор целевой клетки, которая находится на C-конце связывающей молекулы или вблизи него, и отдельную область, например, слитый домен, который находится на его N-концевом домене или вблизи него. В некоторых вариантах осуществления, область связывающей молекулы, например, полипептидный антиген или антитело, находится вблизи N-конца или C-конца, если область располагается в пределах одной, двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, пятнадцати, двадцати, двадцати пяти, тридцати, тридцати пяти, сорока, сорока пяти, пятидесяти, шестидесяти, семидесяти, восьмидесяти, девяноста или ста аминокислот от N-конца или C-конца.
[296] В некоторых вариантах осуществления, связывающая молекула представляет собой полипептид, например, полипептидный антиген или антитело, которое содержит слитый домен, который связывается с частицей. В некоторых вариантах осуществления, связывающая молекула связывается с частицей на одном или нескольких сайтах в пределах слитого домена. В определенных вариантах осуществления, связывающая молекула с большей вероятностью связывается с частицей на одном или нескольких сайтах в пределах слитого домен, чем на одном или нескольких сайтах связывающей молекулы, которые не попадают в слитый домен. В некоторых вариантах осуществления, связывающая молекула связывается с вероятностью большей, по меньшей мере, на 1%, по меньшей мере, на 5%, по меньшей мере, на 10%, по меньшей мере, на 15%, по меньшей мере, на 20%, по меньшей мере, на 25%, по меньшей мере, на 30%, по меньшей мере, на 35%, по меньшей мере, на 40%, по меньшей мере, на 45%, по меньшей мере, на 50%, по меньшей мере, на 55%, по меньшей мере, на 60%, по меньшей мере, на 65%, по меньшей мере, на 70%, по меньшей мере, на 75%, по меньшей мере, на 80%, по меньшей мере, на 85%, по меньшей мере, на 90%, по меньшей мере, на 95%, по меньшей мере, на 99%, по меньшей мере, на 99,9% или, по меньшей мере, на 100% с частицей на одном или нескольких сайтах в пределах слитого домена, чем на одном или нескольких сайтах связывающей молекулы, которые не попадают в слитый домен. В определенных вариантах осуществления, связывающая молекула имеет, по меньшей мере, 1-кратно, по меньшей мере, 2-кратно, по меньшей мере, 3-кратно, по меньшей мере, 4-кратно, по меньшей мере, 5-кратно, по меньшей мере, 6-кратно, по меньшей мере, 7-кратно, по меньшей мере, 8-кратно, по меньшей мере, 9-кратно, по меньшей мере, 10-кратно, по меньшей мере, 20-кратно, по меньшей мере, 30-кратно, по меньшей мере, 40-кратно, по меньшей мере, 50-кратно, по меньшей мере, 100-кратно, по меньшей мере, 500-кратно или, по меньшей мере, 1000-кратно большую вероятность связывания с частицей на одном или нескольких сайтах в пределах слитого домена, чем на одном или нескольких сайтах связывающей молекулы, которые не попадают в слитый домен.
[297] В определенных вариантах осуществления, связывающая молекула связывается со слитым доменом или меткой. В некоторых вариантах осуществления, связывающая молекула представляет собой или содержит антиген или анти-ID, которое распознается и/или связывается рекомбинантным рецептором, таким как рецептор антигена или CAR, связывается, прямо или опосредованно, со слитым доменом или меткой. В некоторых вариантах осуществления, связывающая молекула представляет собой слитый полипептид, содержащий антиген или его часть и слитый домен или метку. В некоторых вариантах осуществления, связывающая молекула конъюгируется с частицей на сайте (например, на боковой цепи аминокислоты) на слитом домене или метке, или в ее пределах. В определенных вариантах осуществления, присоединение связывающей молекулы к частице на слитом домене или метке дает в результате оптимальную ориентацию для связывающей молекулы, которая конъюгирована с частицей, для связывания или распознавания рекомбинантным рецептором или CAR. В некоторых вариантах осуществления, связывающая молекула содержащая антиген или анти-ID, которое распознается рецептором антигена, например, CAR, связывается со слитым доменом или меткой на C-конце, в этом случае, конъюгирование частицы посредством слитого домена или метки предпочтительно ориентирует или экспонирует N-концевую область связанной связывающей молекулы для взаимодействий с рецептором антигена, например, CAR.
[298] Слитые домены или метки хорошо известны в данной области, и могут связываться с антигеном в предлагаемых связывающих молекулах для придания желаемого свойства, например, для выделения слитого полипептида с помощью аффинной хроматографии или для ковалентного присоединения к функциональной группе на поверхности частицы. Хорошо известные примеры таких слитых доменов включают, но, не ограничиваясь этим, полигистидин, Glu-Glu, авидин, глютатион S трансферазу (GST), тиоредоксин, белок A, белок G, константную область тяжелой цепи иммуноглобулина (Fc), мальтозасвяывающийз белок (MBP) или сывороточный альбумин человека. В некоторых вариантах осуществления, слитый домен представляет собой полипептидную метку. Хорошо известные примеры полипептидных меток включают, но, не ограничиваясь этим, AviTag (SEQ ID NO: 3), кальмодулиновую метку (SEQ ID NO: 4), полиглютаматную метку (SEQ ID NO: 5), FLAG-tag (SEQ ID NO: 6), HA-tag (SEQ ID NO: 7), His-tag, (5-10 гистидинов), Myc-tag (SEQ ID NO: 8) и метки - флуоресцентные белки (например, EGFP).
[299] В некоторых вариантах осуществления, слитый домен или метка содержит стрептавидинсвязывающую пептидную последовательность. В некоторых вариантах осуществления, последовательность представляет собой стрептавидинсвязывающую пептидную последовательность STREP-TAG® как иллюстрируется SEQ ID NOS: 9 и 10. В некоторых вариантах осуществления, слитый домен содержит стрептавидинсвязывающую пептидную последовательность как иллюстрируется последовательностью аминокислот, приведенными в SEQ ID NOS: 11-19.
[300] В некоторых вариантах осуществления, связывающая молекула содержит слитый домен GST, который связывается с поверхностно экспонируемым глютатионом частицы. В конкретных вариантах осуществления, слитый домен GST расположен на C-конце связывающей молекулы или вблизи него. В некоторых вариантах осуществления, связывающая молекула содержит слитый домен strep-tag, который связывается с поверхностно экспонируемым биотиновым или стрептавидиновым лигандом частицы. В некоторых вариантах осуществления, слитый домен strep-tag расположен на C-конце связывающей молекулы или вблизи него. В конкретных вариантах осуществления, связывающая молекула содержит слитый домен белка A, который связывается с полипептидом Fc, присоединенным к поверхности частицы. В некоторых вариантах осуществления, слитый домен белка A расположен на C-конце связывающей молекулы или вблизи него. В определенных вариантах осуществления, связывающая молекула содержит слитый домен белка G, который связывается с альбумином или полипептидом Fc, присоединенным к поверхности частицы. В некоторых вариантах осуществления, слитый домен белка A расположен на C-конце связывающей молекулы или вблизи него.
[301] В конкретных вариантах осуществления, связывающая молекула содержит гидрофобную область или область, которая является более гидрофобной, чем остальная часть связывающей молекулы. В некоторых вариантах осуществления, связывающая молекула содержит область, которая является более гидрофобной, чем сайты связывающей молекулы, которые не попадают в гидрофобную область. В некоторых вариантах осуществления, гидрофобная область представляет собой слитый домен. В конкретных вариантах осуществления, гидрофобная область представляет собой Fc-домен. В определенных вариантах осуществления, связывающая молекула имеет большую вероятность для связывания или присоединения к частице, на одном или нескольких сайтах в гидрофобной области, чем в другой области связывающей молекулы, если поверхность частицы является гидрофобной. В различных вариантах осуществления, гидрофобная область связывающей молекулы связывает поверхностно экспонируемую функциональную группу частицы. В некоторых вариантах осуществления, функциональная группа представляет собой или содержит тозильную группу.
[302] В некоторых вариантах осуществления, связывающая молекула содержит Fc-домен, где Fc-домен присутствует на C-конце слитого полипептида. В некоторых вариантах осуществления, связывающая молекула представляет собой антитело, например, антиидиотипическое антитело, содержащее Fc-домен. В конкретных вариантах осуществления, Fc-домен связывается или присоединяется к поверхностно экспонируемому белку G или белку A частицы. В некоторых вариантах осуществления, одна или несколько функциональных групп одной или нескольких аминокислот, присутствующих на Fc-домене, связываются с функциональной группой частицы. В конкретных вариантах осуществления, Fc-домен слитого полипептида или антитела является более гидрофобным, чем область антигена или антитела связывающей молекулы, и сайты в пределах Fc-домена с большей вероятностью связываются с частицей, например, при поверхностно экспонируемых функциональных группах, когда поверхность частицы является менее гидрофобной, чем сайты связывающей молекулы, которые располагаются вне Fc-домена.
[303] В конкретных вариантах осуществления, связывающая молекула, содержащая Fc-домен, связывается с частицей на одном или нескольких сайтах в пределах Fc-области. Связывание связывающей молекулы на сайте, расположенном на Fc-области, с частицей, например, сферической частицей, может легко осуществляться с помощью технологий стандартных для данной области. Например, Fc-домены имеют тенденцию к гидрофобности, и когда Fc-домен является более гидрофобным, чем другие домены связывающей молекулы (например, полипептидный антиген), тогда связывание между боковыми цепями аминокислот, расположенных в пределах Fc-домена, и поверхностно экспонируемыми функциональными группами, расположенными на частице (например, тозильными группами), может осуществляться, если поверхность частицы является гидрофобной. В некоторых вариантах осуществления, поверхность частицы является гидрофобной. В некоторых вариантах осуществления, поверхность частицы является негидрофильной. В конкретных вариантах осуществления, поверхность частицы является гидрофобной и содержит поверхностно экспонируемые тозильные группы.
[304] В некоторых вариантах осуществления, частица является негидрофобной. В определенных вариантах осуществления, частица является гидрофильной. В некоторых вариантах осуществления, поверхность частицы является негидрофобной. В некоторых вариантах осуществления, поверхность частицы является гидрофильной.
4. Конъюгированные частицы
[305] В некоторых вариантах осуществления, связывающая молекула (например, полипептидный антиген или антитело) присоединяется к частице, например, сферической частице. В определенных вариантах осуществления, полипептид ковалентно связывается с частицей. В некоторых вариантах осуществления, полипептид нековалентно связывается с частицей. В некоторых вариантах осуществления, по меньшей мере, 1 связывающая молекула, по меньшей мере, 10 связывающих молекул, по меньшей мере, 102 связывающих молекул, по меньшей мере, 103 связывающих молекул, по меньшей мере, 104 связывающих молекул, по меньшей мере, 105 связывающих молекул, по меньшей мере, 106 связывающих молекул, по меньшей мере, 107 связывающих молекул, по меньшей мере, 108 связывающих молекул или, по меньшей мере, 109 связывающих молекул присоединяются к каждой частице. В конкретных вариантах осуществления, в пределах между или примерно между 102 связывающих молекул и 109 связывающих молекул, 102 связывающих молекул и 107 связывающих молекул, 103 связывающих молекул и 109 связывающих молекул, 103 связывающих молекул и 108 связывающих молекул или 103 связывающих молекул и 106 связывающих молекул ковалентно присоединяются к каждой частице, каждое включительно. В конкретных вариантах осуществления, в пределах между или примерно между 103 связывающих молекул и 106 связывающих молекул, включительно, ковалентно присоединены к каждой частице. В конкретных вариантах осуществления, между или примерно между 104 связывающих молекул и 106 связывающих молекул, включительно, ковалентно присоединяются к каждой частице. В определенных вариантах осуществления, в пределах между или примерно между 104 связывающих молекул и 105 связывающих молекул ковалентно присоединяются к каждой частице. В некоторых вариантах осуществления, примерно в пределах между 105 связывающих молекул и 106 связывающих молекул, включительно, ковалентно присоединяются к каждой частице.
[306] В определенных вариантах осуществления, связывающая молекула ковалентно присоединяется к частице, например, сферической частице. В конкретных вариантах осуществления, количество, по меньшей мере, 0,001 мкг, по меньшей мере, 0,01 мкг, по меньшей мере, 0, 1 мкг, по меньшей мере, 0,5 мкг, по меньшей мере, 1 мкг, по меньшей мере, 1,5 мкг, по меньшей мере, 2 мкг, по меньшей мере, 2,5 мкг, по меньшей мере, 3 мкг, по меньшей мере, 3,5 мкг, по меньшей мере, 4 мкг, по меньшей мере, 4,5 мкг, по меньшей мере, 5 мкг, по меньшей мере, 6 мкг, по меньшей мере, 7 мкг, по меньшей мере, 8 мкг, по меньшей мере, 9 мкг, по меньшей мере, 10 мкг или, по меньшей мере, 50 мкг полипептидных связывающих молекул ковалентно присоединяется к частицам, например, шарикам, на каждые 107 частиц. В некоторых вариантах осуществления, в пределах между или примерно между 0,001 мкг и 100 мкг, 0,01 мкг и 50 мкг, 0,1 мкг и 10 мкг, 0,5 мкг и 10 мкг, 0,1 мкг и 1 мкг, 1 мкг и 10 мкг, 0,5 мкг и 5 мкг или 1 мкг и 5 мкг, каждое, включительно, полипептидных связывающих молекул ковалентно присоединяются к частицам, например, шарикам, на каждые 107 частиц. В конкретных вариантах осуществления, в пределах между или примерно между 1 мкг и примерно 10 мкг, включительно, полипептидных связывающих молекул ковалентно присоединяются к частицам, например, шарикам, на каждые 107 частиц.
[307] В определенных вариантах осуществления, связывающая молекула связывается или присоединяется к частице, например, сферической частице. В конкретных вариантах осуществления, в среднем, примерно или, по меньшей мере, 0,0001 пг, 0,001 пг, 0,005 пг, 0,01 пг, 0,02 пг, 0,03 пг, 0,04 пг, 0,05 пг, 0,06 пг, 0,07 пг, 0,08 пг, 0,09 пг, 0,1 пг, 0,2 пг, 0,3 пг, 0,4 пг, 0,5 пг, 0,6 пг, 0,7 пг, 0,8 пг, 0,9 пг, 1,0 пг или 5,0 пг полипептидных связывающих молекул связывается или присоединяется к каждой частице. В некоторых вариантах осуществления, в пределах между или примерно между 0,0001 пг и примерно 10 пг, 0,001 пг и 1 пг, 0,001 пг и 1 пг, 0,001 мкг и 0,1 пг, 0,01 пг и 0,1 пг, 1 пг и 10 пг, 0,5 пг и 5 пг или 1 пг и 5 пг, каждое, включительно, связывающих молекул связывается или присоединяется к частице. В конкретных вариантах осуществления, в среднем количество равное или меньшее, чем 0,0001 пг, 0,001 пг, 0,005 пг, 0,01 пг, 0,02 пг, 0,03 пг, 0,04 пг, 0,05 пг, 0,06 пг, 0,07 пг, 0,08 пг, 0,09 пг, 0,1 пг, 0,2 пг, 0,3 пг, 0,4 пг, 0,5 пг, 0,6 пг, 0,7 пг, 0,8 пг, 0,9 пг, 1,0 пг или 5,0 пг полипептидных связывающих молекул связывается или присоединяется к каждой частице. В конкретных вариантах осуществления, частица имеет диаметр примерно 2,8 мкм, и в пределах между или примерно между 0,001 и 0,1 пг, включительно, связывающих молекул связывается или присоединяется к частице. В конкретных вариантах осуществления, частица имеет диаметр примерно 4,5 мкм, и в пределах между или примерно между 0,01 и примерно 1 пг, включительно, связывающих молекул связывается или присоединяется к частице.
[308] В конкретных вариантах осуществления, связывающая молекула связывается или присоединяется к частице, например, сферической частице в количестве, по меньшей мере, 10-16 моль, по меньшей мере, 10-15 моль, по меньшей мере, 10-14 моль, по меньшей мере, 10-13 моль, по меньшей мере, 10-12 моль, по меньшей мере, 10-11 моль, по меньшей мере, 10-10 моль, по меньшей мере, 10-9 моль, по меньшей мере, 10-8 моль, по меньшей мере, 10-7 моль, по меньшей мере, 10-6 моль, по меньшей мере, 10-5 моль, по меньшей мере, 10-4 моль, по меньшей мере, 10-3 моль, по меньшей мере, 10-2 моль, по меньшей мере, 10-1 моль или, по меньшей мере, 1 моль на каждые 107 частиц. В некоторых вариантах осуществления, в пределах между или примерно между 1 × 10-13 моль и 1 × 10-9 моль, 1 × 10-12 моль и 1 × 10-9 моль, 1 × 10-13 моль и 1 × 10-10 моль, or 1 × 10-12 моль и 1 × 10-9 моль, каждое, включительно, связывается или присоединяется к частицам на каждые 107 частиц.
[309] В некоторых вариантах осуществления, связывающая молекула связывается или присоединяется к частице, например, сферической частице, в количестве, по меньшей мере, 10-20 моль, по меньшей мере, 10-19 моль, по меньшей мере, 10-18 моль, по меньшей мере, 10-17 моль, по меньшей мере, 10-16 моль, по меньшей мере, 10-15 моль, по меньшей мере, 10-14 моль, по меньшей мере, 10-13 моль, по меньшей мере, 10-12 моль, по меньшей мере, 10-11 моль или, по меньшей мере, 10-10 моль на каждую частицу. В некоторых вариантах осуществления, в пределах между или примерно между 10-21 моль и 10-10 моль, 10-20 моль и 10-18 моль, 10-19 моль и 10-17 моль или 10-21 моль и 10-19 моль, каждое, включительно, ковалентно присоединяются к частицам, например, шарикам, на каждую частицу. В некоторых вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 2,8 мкм и связывающая молекула связывается или присоединяется к частице в количестве в пределах между или примерно между 10-20 моль и 10-18 моль, включительно. В определенных вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 4,5 мкм и связывающая молекула связывается или присоединяется к частице в количестве в пределах между или примерно между 10-19 моль и 10-17 моль, включительно.
[310] В определенных вариантах осуществления, связывающая молекула инкубируется вместе с частицами, например, шариками, например, тозилактивированными шариками, для присоединения и/или конъюгирования связывающих молекул на частицах, например, шариках. В конкретных вариантах осуществления, связывающие молекулы и частицы, например, шарики, инкубируются при концентрации 1 мкг, 2 мкг, 2,5 мкг, 5 мкг, 10 мкг, 20 мкг, 25 мкг, 30 мкг, 40 мкг, 50 мкг, 60 мкг, 70 мкг, 75 мкг, 100 мкг, 125 мкг, 150 мкг, 175 мкг или 200 мкг или примерно при таких концентрациях связывающих молекул на 1×108-1×1010 частиц включительно, и связывающие молекулы присоединяются и/или конъюгируются на частицах, например, шариках, при эффективности равной, примерно равной или большей, чем 50%, 60%, 70%, 80%, 90%, 95%, 97%, 98%, 99%, 99,9% или 100% или примерно 100%. В некоторых вариантах осуществления, связывающие молекулы и частицы, например, шарики, инкубируются при концентрации равной или примерно равной 1 мкг, 2 мкг, 2,5 мкг, 5 мкг, 10 мкг, 20 мкг, 25 мкг, 30 мкг, 40 мкг, 50 мкг, 60 мкг, 70 мкг, 75 мкг, 100 мкг, 125 мкг, 150 мкг, 175 мкг или 200 мкг связывающих молекул на 4×108-5×108 частиц, включительно, и связывающие молекулы присоединяются и/или конъюгируются на частицах, например, шариках, при эффективности равной или примерно равной или большей, чем 50%, 60%, 70%, 80%, 90%, 95%, 97%, 98%, 99%, 99,9% или 100% или примерно 100%. В конкретных вариантах осуществления, связывающие молекулы и частицы, например, шарики, инкубируются при концентрации равной или примерно равной 1 мкг, 2 мкг, 2,5 мкг, 5 мкг, 10 мкг, 20 мкг, 25 мкг, 30 мкг, 40 мкг, 50 мкг, 60 мкг, 70 мкг, 75 мкг, 100 мкг, 125 мкг, 150 мкг, 175 мкг или 200 мкг связывающих молекул на 3,5×109-4,5×109 частиц, включительно, и связывающие молекулы присоединяются и/или конъюгируются на частицах при эффективности равной или примерно равной или большей, чем 50%, 60%, 70%, 80%, 90%, 95%, 97%, 98%, 99%, 99,9% или 100% или примерно 100%. В конкретных вариантах осуществления, в пределах между 1 мкг и 5 мкг, между 5 мкг и 25 мкг, между 1 мкг и 50 мкг, между 10 мкг и 50 мкг, 0,1 мкг и 10 мкг или 50 мкг и 200 мкг, каждое, включительно, связывающих молекул инкубируются вместе с 4×108-5×108 частиц или примерно 4×108-5×108 частиц или 3,5×109-4,5×109 частиц, каждое, включительно, и связывающие молекулы присоединяются и/или конъюгируются на частицах, например, шариках, при эффективности равной или примерно равной или большей, чем 50%, 60%, 70%, 80%, 90%, 95%, 97%, 98%, 99%, 99,9% или 100% или примерно 100%.
[311] В некоторых вариантах осуществления, среднее количество связывающих молекул, ,,конъюгированных или присоединенных на частице, составляет, примерно составляет или составляет, по меньшей мере, 2×10-16 г/частица, 1×10-15 г/частица, 2×10-15 г/частица, 5×10-15 г/частица, 1×10-14 г/частица, 2×10-14 г/частица, 5×10-14 г/частица, 1×10-13 г/частица, 2×10-13 г/частица, 5×10-13 г/частица, 1×10-13 г/частица, и 2×10-13 г/частица ±50%, ±40%, ±30%, ±25%, ±20%, ±10%, ±5% или ±1%. В определенных вариантах осуществления, среднее количество связывающих молекул, ,конъюгированных или присоединенных на частице, составляет или составляет примерно 2×10-16 г/частица ±50%, ±40%, ±30%, ±25%, ±20%, ±10%, ±5% или ±1%. В конкретных вариантах осуществления, среднее количество связывающих молекул, ,,,конъюгированных или присоединенных на частице, составляет или составляет примерно 1×10-15 г/частица ±50%, ±40%, ±30%, ±25%, ±20%, ±10%, ±5% или ±1%. В определенных вариантах осуществления, среднее количество связывающих молекул, ,конъюгированных или присоединенных на частице, составляет или составляет примерно 2×10-15 г/частица ±50%, ±40%, ±30%, ±25%, ±20%, ±10%, ±5% или ±1%. В конкретных вариантах осуществления, среднее количество связывающих молекул, ,конъюгированных или присоединенных на частице, составляет или составляет примерно 1×10-14 г/частица ±50%, ±40%, ±30%, ±25%, ±20%, ±10%, ±5% или ±1%. В определенных вариантах осуществления, среднее количество связывающих молекул, ,конъюгированных или присоединенных на частице, равно или меньше, чем 5×10-13 г/частица, 2×10-13 г/частица, 1×10-13 г/частица, 5×→10-14 г/частица, 2×10-14 г/частица, 1×10-14 г/частица, 5×10-15 г/частица, 2×10-15 г/частица, 1×10-15 г/частица или 2×10-16 г/частица.
[312] В некоторых вариантах осуществления, частицы, например, шарики, содержат связывающие молекулы, которые представляют собой антиидиотипические антитела или их активные фрагменты, которые связываются с антигенсвязывающим доменом CAR. В определенных вариантах осуществления, антиидиотипическое анти-CAR антитело или его активный фрагмент связывается с поверхностно экспонируемой тозильной группой частицы на сайте (например, на амино группе боковой цепи или сульфгидрильной группе аминокислоты), расположенном в пределах Fc-домена антитела. В конкретных вариантах осуществления, частицы, например, шарики, являются монодисперсными и суперпарамагнитными. В конкретных вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 2,8 мкм и содержат в пределах примерно между 104 и примерно 106 копий, включительно, связывающей молекулы, например, антиидиотипического антитела анти-CAR, на частицу. В некоторых вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 4,5 мкм, и содержат в пределах примерно между 5×105 и примерно 5×106 копий, включительно, антиидиотипического антитела анти-CAR на частицу.
[313] В определенных вариантах осуществления, частицы, например, шарики, содержат связывающую молекулу, которая представляет собой или содержит полипептидный антиген BCMA. В конкретных вариантах осуществления, связывающая молекула содержит внеклеточный домен BCMA человека и Fc-домен, который, в некоторых случаях, представляет собой C-концевой Fc-домен. В конкретных вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 280 мкм и содержат примерно 105 копий связывающей молекулы, например, слитого полипептида BCMA, на частицу. В определенных вариантах осуществления, слитый полипептид BCMA связан с поверхностно экспонируемой тозильной группой частицы на сайте, (например, на амино группе боковой цепи или на сульфгидрильной группе аминокислоты) расположенном в пределах Fc-домена слитого полипептида. В конкретных вариантах осуществления, частицы, например, шарики, являются монодисперсными и суперпарамагнитными. В конкретных вариантах осуществления, частицы, например, шарики, и имеют диаметр примерно 2,8 мкм, в пределах примерно между 104 и примерно 106 копий, включительно, связывающей молекулы, например, слитого полипептида BCMA, на частицу. В некоторых вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 4,5 мкм и содержат в пределах между или примерно между 5 × 105 и 5 × 106 копий, включительно, слитого полипептида BCMA на частицу.
II. СТИМУЛЯЦИЯ EX VIVO ИЛИ РАЗМНОЖЕНИЕ КЛЕТОК
[314] В настоящем документе предлагается способ стимуляции или размножения клеток, которые экспрессируют рекомбинантный рецептор, например, CAR, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие CAR, вместе с частицами, например, шариками, которые содержат связывающую молекулу, которая специфично связывает или распознает рекомбинантный рецептор, например, конъюгированные с шариками реагенты, как предлагается, например, анти-ID-конъюгированные шарики или BCMA-конъюгированные шарики. В некоторых вариантах осуществления, связывание между связывающей молекулой и рекомбинантным рецептором, например, CAR, индуцирует размножение клеток, экспрессирующих CAR, тем самым продуцируя выходную композицию, содержащую наращенные клетки. В конкретных вариантах осуществления, рекомбинантный рецептор представляет собой CAR. В определенных вариантах осуществления, связывающая молекула представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который связывается с антигенсвязывающим фрагментом рекомбинантного рецептора. В определенных вариантах осуществления, связывающая молекула представляет собой антиген, который связывается и распознается CAR.
[315] В некоторых вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, приводятся в контакт или инкубируются вместе с исходной композицией, содержащей одну или несколько клеток, для генерирования выходной композиции. В определенных вариантах осуществления, исходная композиция или исходные клетки относятся к композиции и/или множеству клеток, которые желательно обрабатывать, инкубировать или приводить в контакт при условиях, которые стимулируют, активируют, вызывают, генерируют и/или продуцируют одно или несколько изменений, по меньшей мере, в части клеток исходной композиции, тем самым преобразуя исходную композицию в выходную композицию. В некоторых вариантах осуществления, исходные клетки представляют собой композицию иммунных клеток, например, композицию Т-лимфоцитов, которая содержит клетки, экспрессирующие рекомбинантный рецептор, например, CAR. В конкретных вариантах осуществления, по меньшей мере, часть клеток исходной композиции активируется, наращивается и/или обогащается в генерируемой выходной композиции посредством осуществления предлагаемых способов.
[316] В определенных вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, приводятся в контакт или инкубируются вместе с клетками из исходной композиции для генерирования выходной композиции посредством размножения, обогащения и/или активации, по меньшей мере, части, например, подгруппы или фракции исходных клеток. В конкретных вариантах осуществления, клетки из исходной композиции содержат, по меньшей мере, часть клеток, которые экспрессируют рекомбинантный рецептор, например, CAR, и/или, по меньшей мере, часть клеток, которые содержат молекулу гетерологичной нуклеиновой кислоты, которая кодирует рекомбинантный рецептор. В некоторых вариантах осуществления, исходная композиция содержит клетки, которые должны обрабатываться, приводиться в контакт или инкубироваться вместе с частицей, содержащей связывающую молекулу, где обработка, приведение контакт или инкубирование вместе с агентом будет изменять, по меньшей мере, часть клеток исходной композиции, тем самым генерируя выходную композицию. Такие изменения могут включать, но, не ограничиваясь этим, размножение и/или обогащение части клеток, активацию, по меньшей мере, части клеток, и/или увеличение или уменьшение экспрессирования, по меньшей мере, одного гена, по меньшей мере, в части клеток. В определенных вариантах осуществления, выходная композиция содержит, по меньшей мере, часть клеток из исходной композиции, которая подвергается изменению после изменения посредством обработки, приведения в контакт или инкубирования вместе с агентом.
[317] В некоторых вариантах осуществления, размножение, обогащение, стимуляция и/или активация, достигаемые посредством инкубирования клеток вместе с частицами, например, шариками, содержащими связывающую молекулу, может титроваться, регулироваться и/или контролироваться посредством селекции частиц, например, шариков, с конкретным числом, уровнем или количеством связывающих молекул, которые конъюгированы или иным образом присоединены к каждой частице. В конкретных вариантах осуществления, увеличение количества связывающих молекул, конъюгированных или иным образом присоединенных к каждой частице, увеличивает размножение, обогащение, стимуляцию и/или активацию, достигаемые посредством инкубирования клеток вместе с частицами, например, шариками. В определенных вариантах осуществления, уменьшение количества связывающих молекул, конъюгированных или иным образом присоединенных к каждой частице, уменьшает размножение, обогащение, стимуляцию и/или активацию, достигаемые посредством инкубирования клеток вместе с частицами, например, шариками. В конкретных вариантах осуществления, размножение, обогащение, стимуляция и/или активация измеряется с помощью любых пригодных для использования известных средств. В конкретных вариантах осуществления, увеличение размножения, обогащения, стимуляции и/или активации представляет собой статистически значимое увеличение и/или, по меньшей мере или примерно, по меньшей мере, на 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100%, это 1-кратное, 2-кратное, 3-кратное, 5-кратное, 10-кратное, 100-кратное увеличение, например, по сравнению с контролем и/или инкубированием при других условиях, измерения связанного с размножением, обогащением, стимуляцией и/или активацией, осуществляемого для клеток в ходе инкубирования вместе с частицами, например, шариками, или после него. В определенных вариантах осуществления, уменьшение размножения, обогащения, стимуляции и/или активации представляет собой статистически значимое уменьшение и/или, по меньшей мере или примерно, по меньшей мере, на 1%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99% или 99,9% уменьшение измерения, связанного с размножением, обогащением, стимуляцией и/или активацией осуществляемого для клеток в ходе или после инкубирования вместе с частицами, например, шариками.
[318] В некоторых вариантах осуществления, исходная композиция содержит эукариотические клетки, такие как клетки млекопитающего. В определенных вариантах осуществления, исходная композиция содержит клетки человека. В некоторых вариантах осуществления, исходная композиция содержит клетки, которые получают из крови, костного мозга, лимфы или лимфоидных органов. В конкретных вариантах осуществления, исходная композиция содержит клетки иммунной системы, то есть, клетки врожденного или адаптивного иммунитета, например, миелоидные или лимфоидные клетки, включая лимфоциты, как правило, Т-лимфоциты и/или NK-клетки. В некоторых вариантах осуществления, исходная композиция содержит стволовые клетки, такие как мультипотентные и плюрипотентные стволовые клетки, включая индуцированные плюрипотентные стволовые клетки (iPSC). В конкретных вариантах осуществления, исходная композиция содержит клетки CD3+. В определенных вариантах осуществления, выходная композиция содержит клетки CD4+. В некоторых вариантах осуществления, исходная композиция содержит клетки CD8+. В некоторых вариантах осуществления, исходная композиция содержит клетки CD3+, которые также экспрессируют низкие уровни CD28 или не экспрессируют CD28.
[319] В некоторых вариантах осуществления, связывающая молекула стимулирует активацию и/или размножение клеток, экспрессирующих низкие уровни CD28, или клеток, которые являются CD28-отрицательными. В определенных вариантах осуществления, клетки не приводятся в контакт с реагентами, конъюгированными с анти-CD3/анти-CD28, до приведения в контакт клеток с связывающей молекулой.
[320] В некоторых вариантах осуществления способы и частицы, например, шарики, содержащие связывающую молекулу (например, реагенты, конъюгированные с шариками, как предлагается, такие как анти-ID-конъюгированные шарики или BCMA-конъюгированные шарики) могут стимулировать Т-лимфоциты дефицитные или даун-регулируемые по одной или нескольким природным сигнальным молекулам, таким как один или несколько костимуляторных рецепторов или рецепторов антигенов или рецепторов цитокинов, но которые экспрессируют химерный рецептор, например, CAR, распознаваемый связывающей молекулой предлагаемых реагентов, конъюгированных с шариками. В некоторых вариантах осуществления, клетки исходной композиции имеют низкое поверхностное экспрессирование другой костимуляторной молекулы или другой сигнальной молекулы CD28 или являются отрицательными по этому параметру. Таким образом в некоторых вариантах осуществления, предлагаемые реагенты и способы имеют определенные преимущества по сравнению с определенными другими активационными или стимуляторными агентами, или способами, которые могут потребовать, поверхностного экспрессирования CD28 или других эндогенных сигнальных молекул, для обеспечения желаемого сигнала и/или всей полноты такого сигнала, например, для обеспечения костимуляторного сигнала и/или для достижения полной активации или зависеть от него. В некоторых вариантах осуществления, предлагаемые агенты и способы являются преимущественными в этих отношениях по сравнению с реагентами анти-CD3/анти-CD28 (например, шариками); в некоторых аспектах, предлагаемые частицы, например, шарики, содержащие связывающую молекулу (например, реагенты, конъюгированные с шариками, как предлагается, такие как анти-ID конъюгированные шарики или BCMA-конъюгированные шарики) являются преимущественными будучи способными стимулировать или достигать желаемого воздействия, такого как активация или пролиферация клеток, имеющих низкие уровни или отрицательных относительно CD28 или другой природной сигнальной молекулы. В некоторых аспектах, передача сигналов через CAR посредством стимуляции антителом анти-ID дает в результате как в первичный, так и вторичный (костимуляторный) сигнал посредством CAR с использованием только одного реагента. В некоторых вариантах осуществления, исходная композиция содержит клетки CD3+, которые экспрессируют низкие уровни CD28 или другой эндогенной сигнальной молекулы. В некоторых вариантах осуществления, исходная композиция содержит клетки CD3+, которые являются CD28-отрицательными или являются отрицательными по другой эндогенной сигнальной молекуле. В некоторых вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу (например, реагенты, конъюгированные с шариками, как предлагается, такие как анти-ID конъюгированные шарики или BCMA-конъюгированные шарики) стимулируют активацию и/или размножение клеток, экспрессирующих низкие уровни CD28, или клеток, которые являются CD28-отрицательными.
[321] В конкретных вариантах осуществления, исходная композиция представляет собой или содержит первичные Т-лимфоциты человека. В некоторых вариантах осуществления, исходная композиция представляет собой или содержит обогащенные Т-лимфоциты CD4+. В некоторых вариантах осуществления, исходная композиция представляет собой или содержит обогащенные Т-лимфоциты CD8+. В определенных вариантах осуществления, исходная композиция содержит клетки CD4+ и клетки CD8+. В конкретных вариантах осуществления, отношение клеток CD4+ к клеткам CD8+ в исходной композиции больше примерно, чем 50:1 или находится в пределах между или примерно между 25:1 и 50:1, 10: и 25:1, 5:1 и 10:1, 3:1 и 5:1, 2:1 и 3:1, 1:1 и 2:1, 1:1 и 1:2, 2:1 и 1:2, 1:2 и 1:3, 1:3 и 1:5, 1:5 и 1:10, 1:10 и 1:25 или 1:25 и 1:50, каждое, включительно.
[322] В некоторых вариантах осуществления, исходная композиция содержит популяцию клеток, которые трансдуцируются или трансфицируются, или клеток, которые получают из клеток, которые трансдуцируются или трансфицируются одной или несколькими нуклеиновыми кислотами, кодирующими рекомбинантный рецептор, например, CAR, который связывается или распознается связывающей молекулой частиц, например, шариков. В некоторых вариантах осуществления, исходная композиция содержит популяции клеток, которые трансдуцируются или трансфицируются, или клеток, которые получают из клеток, которые трансдуцируются или трансфицируются одной или несколькими нуклеиновыми кислотами, кодирующими рекомбинантный рецептор, который связывается или распознается связывающей молекулой. В конкретных вариантах осуществления, клетки из исходной композиции трансфицируются или трансдуцируются с помощью любого способа, как описано в настоящем документе, например, в Разделе III. В определенных вариантах осуществления, одна или несколько нуклеиновых кислот трансфицируются в клетку с помощью вируса, как описано в настоящем документе, например, в Разделе III. В некоторых вариантах осуществления, одна или несколько нуклеиновых кислот трансфицируются в клетку с помощью невирусной плазмиды, например, эписомы или транспозона, как описано в настоящем документе, например, в Разделе III. В конкретных вариантах осуществления, исходная композиция содержит клетки, которые экспрессируют рекомбинантный рецептор, например, CAR, на поверхности клетки, который связывается или распознается связывающей молекулой частиц, например, шариков.
[323] В конкретных вариантах осуществления, исходная композиция содержит клетку, которая экспрессирует рекомбинантный рецептор, например, CAR, который получают, например, с помощью любого из способов, описанных в настоящем документе, например, в Разделе III.
[324] В конкретных вариантах осуществления, исходная композиция сначала не содержит клеток, которые экспрессируют рекомбинантный рецептор, например, CAR. В некоторых вариантах осуществления, клетки исходной композиции, которые сначала не содержат клеток, которые экспрессируют рекомбинантный рецептор, приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, по меньшей мере, в ходе части трансфицирования или трансдуцирования клеток одной или несколькими нуклеиновыми кислотами, которые содержат ген, экспрессирующий рекомбинантный рецептор, который связывается или распознается связывающей молекулой. В некоторых вариантах осуществления, трансфицирование или трансдуцирование осуществляется, как описано в настоящем документе, например, в Разделе III. В некоторых вариантах осуществления, в ходе, по меньшей мере, части инкубирования вместе со связывающей молекулой, при введении нуклеиновой кислоты в клетки, рекомбинантный рецептор начинает экспрессироваться на поверхности клеток, где он может взаимодействовать со связывающей молекулой. В конкретных вариантах осуществления, трансфицирование или трансдуцирование осуществляется без каких-либо предварительных стадий размножения, активации и/или выделения. В определенных вариантах осуществления, клетки не инкубируют, не обрабатывают или не приводят в контакт, с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR перед трансфицированием или трансдуцированием. В конкретных вариантах осуществления, клетки не приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами, которые представляют собой антитела анти-CD3 и анти-CD28, перед трансдуцированием или трансфицированием.
[325] В определенных вариантах осуществления, исходная композиция содержит как клетки, которые экспрессируют, так и клетки, которые не экспрессируют рекомбинантный рецептор, например, CAR, который связывается или распознается связывающей молекулой. В некоторых вариантах осуществления, обработка, приведение в контакт или инкубирование клеток исходной композиции вместе с частицами, например, шариками, содержащими связывающую молекулу, будет стимулировать активацию и/или размножение клеток, экспрессирующих рекомбинантный рецептор, например, CAR, но не будут стимулировать активацию и/или размножение клеток, которые не экспрессируют рекомбинантный рецептор. В определенных вариантах осуществления, обработка, приведение в контакт или инкубирование клеток исходной композиции вместе с частицами, например, шариками, содержащими связывающую молекулу, которая связывает или распознает рекомбинантный рецептор, будет стимулировать активацию и/или размножение клеток, которые не экспрессируют рекомбинантный рецептор, до меньшей степени, чем размножение клеток, которые экспрессируют рекомбинантный рецептор.
[326] В конкретных вариантах осуществления часть клеток исходной композиции экспрессирует или содержит гетерологичную ДНК, которая кодирует рекомбинантный рецептор, например, CAR. В определенных вариантах осуществления, меньше, чем 0,01%, меньше, чем 0,1%, меньше, чем 1%, меньше, чем 5%, меньше, чем 10%, меньше, чем 20%, меньше, чем 25%, меньше, чем 30%, меньше, чем 35%, меньше, чем 40%, меньше, чем 45%, меньше, чем 50%, меньше, чем 55%, меньше, чем 60%, меньше, чем 65%, меньше, чем 70%, меньше, чем 80% или меньше, чем 90% клеток экспрессируют или содержат одну или несколько нуклеиновых кислот, которые содержат ген, кодирующий рекомбинантный рецептор. Клетки, которые экспрессируют рекомбинантный рецептор, или содержат гетерологичную ДНК, которая кодирует рекомбинантный рецептор, может идентифицироваться с помощью любых средств известных в данной области, например, но, не ограничиваясь этим, детектирования мРНК, кодирующей рекомбинантный рецептор, в клетке, прямого детектирования гетерологичного рецептора, например, посредством детектирования связывания меченого зонда или антитела, которое связывается с рекомбинантным рецептором, или детектирования суррогатного маркера, который кодируется гетерологичной ДНК. В некоторых вариантах осуществления, клетки, которые экспрессируют рекомбинантный рецептор, идентифицируются посредством детектирования суррогатного маркера. В определенных вариантах осуществления, суррогатный маркер представляет собой усеченный полипептид EGFR.
[327] В конкретных вариантах осуществления, исходные клетки представляют собой или содержат клетки, которые трансфицированы и/или трансдуцированы малым количеством вирусных частиц, например, шариков, с малым отношением копий частиц вирусных векторов, например, шариков, к клеткам, и/или инфекционным единицам (IU), перед контактом с частицами, например, шариками. В конкретных вариантах осуществления, исходные клетки, например, клетки, которые приводятся в контакт, инкубируются и/или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, представляют собой клетки, которые трансдуцируются более низким количеством вирусных частиц, при меньшем отношении копий частиц вирусных векторов, например, шариков, к клеткам, и/или к IU, чем у исходных клеток, которые наращивают и/или обогащают с помощью поликлональной стимуляции, например, частицами, покрытыми антителом анти-CD3 и/или анти-CD28, например, в некоторых вариантах осуществления, исходная композиция, которая инкубируется вместе с частицами, например, шариками, содержащими связывающие молекулы, генерируется из клеток, которые трансдуцируют или трансдуцируют, по меньшей мере, количеством IU на клетку, которое на 0,5, 1, 2, 3, 4, 5, 10, 15, 20, 30, 40, 50 или 60 меньше, чем для исходной композиции, которая наращивается и/или обогащается с помощью поликлональной стимуляции. В некоторых вариантах осуществления, исходная композиция, которая инкубируется вместе с частицами, например, шариками, содержащими связывающую молекулу, генерируется из клеток, которые трансдуцируются некоторым титром частиц вирусных векторов, например, шариков, который на или, по меньшей мере, на 1 × 105 IU/мл, 5 × 105 IU/мл, 1 × 106 IU/мл, 5 × 10 6 IU/мл, 6 × 106 IU/мл, 7 × 106 IU/мл, 8 × 106 IU/мл, 9 × 106 IU/мл или 1 × 107 IU/мл меньше, чем для исходной композиции, которую наращивают и/или обогащают с помощью поликлональной стимуляции.
[328] В конкретных вариантах осуществления, трансдуцирование клеток с помощью высоких значений IU/клетка будет приводить к высокой эффективности трансдуцирования, но, в некоторых вариантах осуществления, это может также приводить к трансфицированным клеткам с высоким количеством копий вектора (VCN), которые могут представлять риски для безопасности и которые могут не удовлетворять регулирующим стандартам. В конкретных вариантах осуществления, понижение количества IU/клетка, при котором трансдуцируются клетки, будет понижать эффективность трансдуцирования, но будет понижать VCN. В конкретных вариантах осуществления, увеличение величины IU/клетка, при котором трансдуцируются клетки, при увеличении эффективности трансдуцирования, будет также увеличивать VCN.
[329] В конкретных вариантах осуществления, инкубирование, приведение в контакт или обработка клеток из исходной композиции вместе с частицами, например, шариками, содержащими связывающую молекулу, осуществляется при условиях стимуляции, размножения и/или активации клеток, эти условия могут включать одну или несколько конкретных сред, температуру, содержание кислорода, содержание диоксида углерода, время, агенты, например, питательные вещества, аминокислоты, антибиотики, ионы и/или стимуляторные факторы, такие как цитокины, хемокины, антигены, партнеры по связыванию, слитые белки, рекомбинантные растворимые рецепторы и любые другие агенты, разработанные для активации клеток.
[330] В некоторых вариантах осуществления, клетки в исходной композиции не экспрессируют рекомбинантного рецептора, например, CAR, и инкубируются, приводятся в контакт или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, в то время как они вступают в контакт с одной или несколькими нуклеиновыми кислотами, которые содержат ген, кодирующий рекомбинантный рецептор. В определенных вариантах осуществления, связывающая молекула частиц, например, шариков, связывает или распознает рекомбинантный рецептор, который кодируется геном. В некоторых вариантах осуществления, одна или несколько нуклеиновых кислот доставляются в вирусной частице. В конкретных вариантах осуществления, одна или несколько нуклеиновых кислот представляют собой эписомальный вектор. В некоторых вариантах осуществления, одна или несколько нуклеиновых кислот представляют собой транспозон. В определенных вариантах осуществления, клетки исходной композиции обрабатывают, инкубируют или приводят в контакт с частицами, например, шариками, содержащими связывающую молекулу, по меньшей мере, в течение части времени, когда одна или несколько нуклеиновых кислот вступает в контакт с клетками исходной композиции. В конкретных вариантах осуществления, клетки приводятся в контакт с одной или несколькими нуклеиновыми кислотами, как описано в настоящем документе, например, в Разделе III.
[331] В некоторых вариантах осуществления, клетки исходной композиции трансфицируются или трансдуцируются одной нуклеиновой кислотой, содержащей ген, кодирующий рекомбинантный рецептор, например, CAR; исходная композиция содержит клетки, которые экспрессируют рекомбинантный рецептор, например, CAR; и клетки приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающие молекулы, которые связывают или распознают рекомбинантный рецептор. В некоторых вариантах осуществления, клетки исходной композиции обрабатывают, инкубируют или приводят в контакт с частицами, например, шариками, содержащими связывающую молекулу, после того как клетки трансдуцируются или трансфицируются. В некоторых вариантах осуществления, клетки исходной композиции обрабатываются, инкубируются или приводятся в контакт с частицами, например, шариками, содержащими связывающую молекулу, после того как клетки трансдуцируются или трансфицируются одной или несколькими нуклеиновыми кислотами, как описано в настоящем документе, например, в Разделе III. В конкретных вариантах осуществления, клетки исходной композиции обрабатываются, инкубируются или приводятся в контакт с частицами, например, шариками, содержащими связывающую молекулу, сразу, в пределах примерно 1 минуты, в пределах примерно 5 минут, в пределах примерно 30 минут, в пределах примерно 1 часа, в пределах примерно 2 часов, в пределах примерно 4 часов, в пределах примерно 6 часов, в пределах примерно 8 часов, в пределах примерно 12 часов, в пределах примерно 24 часов, в пределах примерно 2 дней, в пределах примерно 3 дней, в пределах примерно 4 дней, в пределах примерно 5 дней, в пределах примерно 6 дней, в пределах примерно 1 недели, в пределах примерно 2 недель, в пределах примерно 3 недели, в пределах примерно 4 недель, в пределах примерно 5 недель или в пределах примерно 6 недель после того как клетки приводятся в контакт с одной или несколькими нуклеиновыми кислотами.
[332] В некоторых вариантах осуществления, клетки исходной композиции трансдуцируются или трансфицируются одной или несколькими нуклеиновыми кислотами, которые содержат ген, кодирующий рекомбинантный рецептор, например, как описано в Разделе III, и затем клетки криоконсервируются и хранятся в течение некоторого периода времени перед оттаиванием и размножением клеток. В некоторых вариантах осуществления, клетки исходной композиции криоконсервируются и приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, в пределах или в пределах примерно 1 минуты, 5 минут, 30 минут, 1 часа, 2 часов, 4 часов, 6 часов, 8 часов, 12 часов, 24 часов, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 1 недели, 2 недель, 3 недель, 4 недель, 5 недель или 6 недель, после чего клетки оттаивают.
[333] В некоторых вариантах осуществления, приведение в контакт, инкубирование или обработка клеток исходной композиции вместе с частицами (например, шариками), содержащими связывающую молекулу, осуществляется в контейнере, например, в чашке для культивирования клеток, в лунке для культивирования или в мешке.
[334] В некоторых вариантах осуществления, клетки исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, при отношении клеток исходной композиции в целом к частицам, например, шарикам, в пределах или примерно в пределах от 100:1 до 1:100, от 50:1 до 1:50, от 25:1 до 1:25, от 10:1 до 1:10, от 5:1 до 1:5, от 3:1 до 1:3 или от 2:1 до 1:2. В конкретных вариантах осуществления, отношение составляет от или примерно от 1:0,1 примерно до 1:5. В некоторых вариантах осуществления, отношение клеток исходной композиции в целом к частицам, например, шариков, составляет примерно 1:1.
[335] В некоторых вариантах осуществления, в пределах между или примерно между 102 и 1012, 103 и 1010, 104 и 109, 103 и 106, 104 и 108, 102 и 104, 103 и 105, 104 и 106, 105 и 107 или 106 и 108 клеток, каждое, включительно, из исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу. В определенных вариантах осуществления, меньше примерно, чем 102 или в пределах между или примерно между 102 и 103, 103 и 104, 104 и 105, 105 и 106, 106 и 107, 107 и 108, 108 и 109,109 и 1010, 1010 и 1011 или 1011 и 1012 клеток из исходной композиции, каждое, включительно, приводится в контакт, инкубируется или обрабатывается вместе с частицами, например, шариками, содержащими связывающую молекулу.
[336] В некоторых вариантах осуществления, инкубирование или приведение в контакт с клетками исходной композиции осуществляется при достаточном количестве частиц, например, шариков, содержащих связывающую молекулу, чтобы сделать возможным связывание связывающей молекулы с одной или несколькими клетками в исходной композиции и/или для индуцирования, стимуляции, активации и/или пролиферации одной или нескольких клеток в исходной композиции. Конкретное количество или отношение частиц, например, шариков, к клеткам исходной композиции может определяться эмпирически в зависимости от конкретного количества связывающей молекулы на один шарик, конкретного антигена, источника клеток исходной композиции и других факторов известных специалисту в данной области.
[337] В некоторых вариантах осуществления, количество частиц, например, шариков, добавляемых к клеткам исходной композиции, представляет собой количество обеспечивающее в пределах между или примерно между 1 связывающей молекулой и 1012 связывающими молекулами на одну клетку исходной композиции в ходе инкубирования или приведения в контакт, например, между или примерно между 102 связывающих молекул и 1010 связывающих молекул, 103 связывающих молекул и 108 связывающих молекул, 104 связывающих молекул и 106 связывающих молекул, 1 связывающей молекулы и 102 связывающих молекул, 102 связывающих молекул и 103 связывающих молекул, 103 связывающих молекул и 104 связывающих молекул, 104 связывающих молекул и 105 связывающих молекул, 105 связывающих молекул и 106 связывающих молекул, 105 связывающих молекул и 106 связывающих молекул, 106 связывающих молекул и 107 связывающих молекул, 107 связывающих молекул и 108 связывающих молекул, 109 связывающих молекул и 1010 связывающих молекул, 1010 связывающих молекул и 1011 связывающих молекул или 1011 связывающих молекул и 1012 связывающих молекул на клетку, каждое, включительно, в исходной композиции в ходе инкубирования или приведения в контакт. В некоторых вариантах осуществления, количество частиц, например, шариков, добавляемых к исходной композиции, представляет собой количество, обеспечивающее в пределах примерно между 104 связывающих молекул и примерно 106 связывающих молекул на каждую клетку в исходной композиции в ходе инкубирования или приведения в контакт. В некоторых вариантах осуществления, количество частиц, например, шариков, содержит примерно 105 связывающих молекул на каждую клетку в исходной композиции в ходе инкубирования или приведения в контакт.
[338] В некоторых вариантах осуществления, количество частиц, например, шариков, содержащих связывающую молекулу, добавляемых в исходную композицию в ходе инкубирования или приведения в контакт, представляет собой количество частиц, например, шариков, которые содержат в пределах между или примерно между 0,0001 пг и примерно 10 пг, 0,001 пг и 1 пг, 0,001 пг и 1 пг, 0,001 пг и 0,1 пг, 0,005 пг и 0,05 пг, 0,005 пг и 0,02 пг или 0,01 пг и 0,05 пг связывающих молекул, каждое, включительно, на каждую клетку в исходной композиции в ходе инкубирования или приведения в контакт. В некоторых вариантах осуществления, общее количество частиц, например, шариков, добавляемых к клеткам исходной композиции, представляет собой количество, обеспечивающее в пределах между или примерно между 0,0001 мкг и 10 мкг, 0,001 мкг и 1 мкг, 0,001 мкг и 1 мкг, 0,001 мкг и 0,1 мкг, 0,005 мкг и 0,05 мкг, 0,005 мкг и 0,02 мкг или 0,01 мкг и 0,05 мкг связывающих молекул, каждое, включительно.
[339] В некоторых вариантах осуществления, количество частиц, например, шариков, содержащих связывающую молекулу, добавляемых к исходной композиции в ходе инкубирования или приведения в контакт, представляет собой количество частиц, например, шариков, которые содержат, по меньшей мере, 10-20 моль, по меньшей мере, 10-19 моль, по меньшей мере, 10-18 моль, по меньшей мере, 10-17 моль, по меньшей мере, 10-16 моль, по меньшей мере, 10-15 моль, по меньшей мере, 10-14 моль, по меньшей мере, 10-13 моль, по меньшей мере, 10-12 моль, по меньшей мере, 10-11 моль или, по меньшей мере, 10-10 моль связывающих молекул на каждую клетку в исходной композиции в ходе инкубирования или приведения в контакт. В некоторых вариантах осуществления, это количество содержит в пределах между или примерно между 10-21 моль и 10-10 моль, 10-20 моль и 10-18 моль, 10-19 моль и 10-17 моль или 10-21 моль и 10-19 моль связывающих молекул, каждое, включительно, на каждую клетку в исходной композиции в ходе инкубирования или приведения в контакт. В некоторых вариантах осуществления, общее количество частиц, например, шариков, добавляемых к клеткам исходной композиции представляет собой количество, обеспечивающее, по меньшей мере, 10-16 моль, по меньшей мере, 10-15 моль, по меньшей мере, 10-14 моль, по меньшей мере, 10-13 моль, по меньшей мере, 10-12 моль, по меньшей мере, 10-11 моль, по меньшей мере, 10-10 моль, по меньшей мере, 10-9 моль, по меньшей мере, 10-8 моль, по меньшей мере, 10-7 моль, по меньшей мере, 10-6 моль, по меньшей мере, 10-5 моль, по меньшей мере, 10-4 моль, по меньшей мере, 10-3 моль, по меньшей мере, 10-2 моль, по меньшей мере, 10-1 моль или, по меньшей мере, 1 моль связывающих молекул.
[340] В некоторых вариантах осуществления, приведение в контакт или инкубирование частиц, например, шариков, содержащих связывающую молекулу, вместе с исходной композицией осуществляется в объеме, который находится в пределах между или примерно между 0,01 мл и 100 мл, например, между 0,01 мл и 50 мл, 0,01 мл и 25 мл, 0,01 мл и 10 мл, 0,01 мл и 5 мл, 0,01 мл и 1 мл, 0,01 мл и 0,5 мл, 0,01 мл и 0,1 мл, 0,01 мл и 0,05 мл, 0,05 мл и 100 мл, 0,05 мл и 50 мл, 0,05 мл и 25 мл, 0,05 мл и 10 мл, 0,05 мл и 5 мл, 0,05 мл и 1 мл, 0,05 мл и 0,5 мл, 0,05 мл и 0,1 мл, 0,1 мл и 100 мл, 0,1 мл и 50 мл, 0,1 мл и 25 мл, 0,1 мл и 10 мл, 0,1 мл и 5 мл, 0,1 мл и 1 мл, 0,1 мл и 0,5 мл, 0,5 мл и 100 мл, 0,5 мл и 50 мл, 0,5 мл и 25 мл, 0,5 мл и 10 мл, 0,5 мл и 5 мл, 0,5 мл и 1 мл, 1 мл и 100 мл, 1 мл и 50 мл, 1 мл и 25 мл, 1 мл и 10 мл, 1 мл и 5 мл, 5 мл и 100 мл, 5 мл и 50 мл, 5 мл и 25 мл, 5 мл и 10 мл, 10 мл и 100 мл, 10 мл и 50 мл, 10 мл и 25 мл, 25 мл и 100 мл, 25 мл и 50 мл или 50 мл и 100 мл, каждое, включительно. В некоторых вариантах осуществления, объем обеспечивается раствором, таким как среда или фармацевтически приемлемый буфер.
[341] В некоторых вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, происходят из композиции частиц, например, шариков, которые имеют концентрацию связывающих молекул, по меньшей мере, 0,001 мкг/мл, по меньшей мере, 0,01 мкг/мл, по меньшей мере, 0,1 мкг/мл, по меньшей мере, 0,5 мкг/мл, по меньшей мере, 1 мкг/мл, по меньшей мере, 1,5 мкг/мл, по меньшей мере, 2 мкг/мл, по меньшей мере, 3 мкг/мл, по меньшей мере, 4 мкг/мл, по меньшей мере, 5 мкг/мл, по меньшей мере, 6 мкг/мл, по меньшей мере, 7 мкг/мл, по меньшей мере, 8 мкг/мл, по меньшей мере, 9 мкг/мл, по меньшей мере, 10 мкг/мл, по меньшей мере, 50 мкг/мл, по меньшей мере, 100 мкг/мл, по меньшей мере, 500 мкг/мл, по меньшей мере, 1 мг/мл или, по меньшей мере, 10 мг/мл. В некоторых вариантах осуществления, композиция частиц содержит в пределах между или примерно между 5×107 и 1×1010 частиц или шариков на мл, включительно. В конкретных вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, происходят из композиции частиц, например, шариков, которые имеют концентрацию связывающих молекул в пределах между или примерно между 0,001 мкг/мл и 10 мг/мл, 0,001 мкг/мл и 1 мкг/мл, 0,001 мкг/мл и 1 мкг/мл, 0,001 мкг/мл и 0,1 мкг/мл, 0,01 мкг/мл и 1 мкг/мл, 1 мкг/мл и 10 мкг/мл, 0,5 мкг/мл и 5 мкг/мл или 1 мкг/мл и 5 мкг/мл. В некоторых вариантах осуществления, композиция частиц содержит в пределах между или примерно между 5×107 и 1×1010, 1×108 и 5×109 или 4×108 и 4×109 частиц или шариков на мл, каждое, включительно.
[342] В определенных вариантах осуществления, количество частиц, например, шариков, содержащих связывающую молекулу, добавляемых к исходной композиции в ходе инкубирования или приведения в контакт, составляет количество частиц, например, шариков, которое обеспечивает концентрацию 10-13 M, по меньшей мере, 10-12 M, по меньшей мере, 10-11 M, по меньшей мере, 10-10 M, по меньшей мере, 10-9 M, по меньшей мере, 10-8 M, по меньшей мере, 10-7 M, по меньшей мере, 10-6 M, по меньшей мере, 10-5 M, по меньшей мере, 10-4 M, по меньшей мере, 10-3 M, по меньшей мере, 10-2 M, по меньшей мере, 0,1 M, по меньшей мере, 1 M или, по меньшей мере, 10 M связывающей молекулы. В некоторых вариантах осуществления, количество частиц, например, шариков, содержащих связывающую молекулу, добавляемое к исходной композиции в ходе инкубирования или приведения в контакт, составляет количество частиц, например, шариков, которое обеспечивает концентрацию в пределах между или примерно между 10-10 M и 10-3 M, 10-9 M и 10-6 M, 10-10 M и 10-7 M или 10-9 M и примерно 10-6 M, включительно.
[343] В конкретных вариантах осуществления, клетки из исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, в течение, по меньшей мере или, по меньшей мере, примерно 2 часов, 4 часов, 6 часов, 12 часов, 24 часов, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, 8 дней, 9 дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 3 недель или 4 недель. В конкретных вариантах осуществления, клетки из исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, в течение меньше или меньше примерно 30 минут, 1 часа, 2 часов, 6 часов, 12 часов, 1 дня, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней или меньше, чем или примерно 12 дней. В некоторых вариантах осуществления, клетки из исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, в течение времени в пределах между или примерно между 1 днем и примерно 14 днями, 3 днями и 7 днями или 4 днями и 6 днями, включительно. В некоторых вариантах осуществления, клетки из исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, в течение примерно 5 дней. В определенных вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, приводятся в контакт или инкубируются вместе с клетками из исходной композиции, например, содержащей клетки, которые экспрессируют рекомбинантный рецептор, например, CAR, в течение периода времени для размножения одной или нескольких клеток исходной композиции, например, для размножения клеток исходной композиции, которая экспрессирует рекомбинантный рецептор. В конкретных вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, приводятся в контакт или инкубируются вместе с клетками из исходной композиции, например, содержащей клетки, которые экспрессируют рекомбинантный рецептор, например, CAR, в течение периода времени достаточного для хронической стимуляции исходной композиции.
[344] В конкретных вариантах осуществления, клетки из исходной композиции, например, содержащей клетки, которые экспрессируют рекомбинантный рецептор, например, CAR, инкубируются, приводятся в контакт или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, при температурах больше, чем комнатная температура для размножения клеток исходной композиции, которые экспрессирует рекомбинантный рецептор. В некоторых вариантах осуществления, обработка, инкубирование или приведение в контакт осуществляется при температуре больше примерно, чем 25°C, например, как правило, больше или больше примерно, чем 32°C, 35°C или 37°C. В некоторых вариантах осуществления, обработка, приведение в контакт или инкубирование осуществляется при температуре равной или примерно равной 37°C ± 2°C, например, при температуре равной или примерно равной 37°C.
[345] В некоторых вариантах осуществления, клетки исходной композиции, например, содержащие клетки, экспрессирующие рекомбинантный рецептор, например, CAR, инкубируются, обрабатываются или приводятся в контакт вместе с частицами, например, шариками, содержащими связывающую молекулу и один или несколько дополнительных агентов (например, стимуляторные и/или дополнительные агенты), например, лиганд, который может активировать внутриклеточный сигнальный домен комплекса TCR.
[346] В некоторых вариантах осуществления, дополнительный агент присоединяется на поверхности частицы.
[347] В определенных вариантах осуществления, один или несколько дополнительных агентов присутствуют отдельно от частиц, например, шариков. В некоторых вариантах осуществления, один или несколько дополнительных агентов представляют собой один или несколько цитокинов. В конкретных вариантах осуществления, один или несколько дополнительных агентов представляют собой или содержат один или несколько рекомбинантных цитокинов. В некоторых вариантах осуществления, один или несколько цитокинов представляют собой рекомбинантные цитокины человека. В определенных вариантах осуществления, один или несколько цитокинов связываются и/или могут связываться с рецепторами, которые экспрессируются Т-лимфоцитами и/или являются эндогенными для них. В конкретных вариантах осуществления, один или несколько цитокинов представляют собой или содержат один или несколько членов семейства цитокинов с пучками 4-альфа-спиралей. В некоторых вариантах осуществления, один или несколько цитокинов могут включать, но, не ограничиваясь этим, интерлейкин-2 (IL-2), интерлейкин-4 (IL-4), интерлейкин-7 (IL-7), интерлейкин-9 (IL-9), интерлейкин 12 (IL-12), интерлейкин 15 (IL-15), колониестимулирующий фактор гранулоцитов (G-CSF) и колониестимулирующий фактор гранулоцитов-макрофагов (GM-CSF). В некоторых вариантах осуществления, один или несколько цитокинов представляет собой или включает один, или несколько из IL-2, IL-7 и IL-15.
[348] В некоторых вариантах осуществления, по меньшей мере, часть клеток исходной композиции экспрессируют CAR, и клетки инкубируются, обрабатываются или приводятся в контакт с частицами, например, шариками, с присоединенными связывающими молекулами, где связывающие молекулы представляют собой антиидиотипические антитела или их активные фрагменты, которые связываются с антигенсвязывающим доменом CAR. В некоторых вариантах осуществления, клетки инкубируются в течение в пределах примерно 3-7 дней, включительно. В конкретных вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 280 мкм, частицы, например, шарики, содержат примерно 105 копий связывающих молекул, то есть, антиидиотипического антитела анти-CAR, на частицу, и клетки инкубируются, приводятся в контакт и/или обрабатываются вместе с частицами при отношении частиц, например, шариков, к клеткам примерно 1:1. В некоторых вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 450 мкм, частицы, например, шарики, содержат в пределах примерно между 1×106 и примерно 2×106 копий антиидиотипического антитела анти-CAR, на частицу, и клетки инкубируются, приводятся в контакт и/или обрабатываются вместе с частицами при отношении частиц, например, шариков, к клеткам примерно 1:1.
[349] Конкретные варианты осуществления приведены для способа размножения клеток, включающего инкубирование исходной композиции, содержащей клетки, экспрессирующие CAR с антигенсвязывающим доменом, который специфично связывает или, например, распознает частицы ВСМС, вместе с частицами, шариками, которые содержат связывающую молекулу, которая связывает с или распознает CAR. В некоторых вариантах осуществления, связывающая молекула представляет собой слитый полипептид, содержащий внеклеточный домен BCMA человека и C-концевой Fc-домен. В некоторых вариантах осуществления, клетки инкубируются в пределах примерно 3-7 дней. В конкретных вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 280 мкм, частицы, например, шарики, содержат примерно 105 копий связывающих молекул, то есть, слитых полипептидов BCMA, на одну частицу, и инкубируются, приводятся в контакт и/или обрабатываются вместе с частицами при отношении частиц, например, шариков, к клеткам примерно 1:1. В некоторых вариантах осуществления, частицы, например, шарики, имеют диаметр примерно 450 мкм, частицы, например, шарики, содержат примерно в пределах между 1×106 и примерно 2×106 копий связывающих молекул, то есть, слитых полипептидов BCMA, на частицу, и инкубируются, приводятся в контакт и/или обрабатываются вместе с частицами при отношении частиц, например, шариков, к клеткам примерно от 1:1.
[350] В конкретных вариантах осуществления, клетки из исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, в течение продолжительного периода времени для осуществления долговременной стимуляции, например, дольше 10 дней. В некоторых вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, инкубируются, например, инкубируются непрерывно или без перерыва, вместе с частицами или шариками, содержащими связывающую молекулу, в течение, по меньшей мере, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней или 16 дней. В некоторых аспектах, период времени, выбираемый для инкубирования, представляет, собой время, при котором одна или несколько функций, или активностей клеток композиции демонстрирует признаки хронически стимулируемых клеток или клеток, имеющих продолжительное экспонирование для антигена, при окончании или в конце инкубирования. В некоторых вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, инкубируются вместе с частицами или шариками для осуществления способа долговременной стимуляции, например, для моделирования признаков хронически стимулируемых клеток или клеток, имеющих долговременное экспонирование для антигена.
Иллюстративные признаки выходных композиций
[351] В конкретных вариантах осуществления, приведение в контакт клеток исходной композиции с частицами, например, шариками, содержащими связывающую молекулу (например, с реагентами, конъюгированными с шариками, как предлагается (например, с анти-ID-конъюгированными шариками или BCMA-конъюгированными шариками) дает в результате выходную композицию, содержащую, по меньшей мере, одно свойство, например, общее количество клеток, часть или подмножество клеток, которые экспрессируют рекомбинантный рецептор, скорость пролиферации клеток, и/или экспрессирование гена, например, маркер активации или маркер истощения, которое отличается от свойств соответствующей клетки исходной композиции. В некоторых вариантах осуществления, способы дают в результате пролиферацию, активацию, стимуляцию, высвобождение цитокинов или другой функциональный результат, такой как ап-регулирование маркера активации или высвобождение или продуцирование цитокинов для клеток, экспрессирующих химерный рецептор, такой как CAR, распознаваемый связывающей молекулой. В некоторых аспектах, такая пролиферация или другая функциональная реакция или результат индуцируется в таких клетках до степени, которая сходна или больше, чем индуцируется при инкубировании клеток вместе с агентом и/или при условиях, которые стимулируют пролиферацию Т-лимфоцитов, например, шарики анти-CD3/CD28 и/или поперечно сшитые анти-CD3.
[352] В некоторых вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, удаляют из выходной композиции. В некоторых вариантах осуществления, частицы, например, шарики, являются намагничиваемыми или магниточувствительными, то есть, парамагнитными или суперпарамагнитными частицами, например, шариками. В некоторых вариантах осуществления, частицы, например, шарики, представляют собой олигомеры стрептавидина. Способы удаления частиц, например, шариков, например, сферических частиц (например, шариков или намагничиваемых частиц) из клеток известны. В некоторых вариантах осуществления, можно использовать применение конкурентных немеченых антител, которые, например, связываются со связывающей молекулой и изменяют ее аффиность относительно рекомбинантного рецептора на клетке, тем самым делая возможным осторожное отсоединение связывающей молекулы и, следовательно, частицы. В некоторых случаях, после отсоединения, конкурентные антитела могут оставаться ассоциированными со связывающей молекулой частицы, в то время как непрореагировавшее немеченое антитело отмывается или может отмываться, и клетка освобождается от антитела и связывающей молекулы. Иллюстрацией такого реагента является DETACaBEAD (Friedl et al. 1995; Entschladen et al. 1997). В некоторых вариантах осуществления, частицы (например, сферические частицы) могут удаляться в присутствии расщепляемого линкера (например, линкера из ДНК), при этом связанные с частицей антитела конъюгируются с линкером (например, CELLection, Dynal). В некоторых случаях, линкерная область обеспечивает расщепляемый сайт для удаления частиц (например, сферических частиц) с клеток после выделения, например, посредством добавления ДНКазы или другого высвобождающего буфера. В некоторых вариантах осуществления, можно также использовать другие ферментативные способы для высвобождения частицы (например, сферической частицы) с клеток. В некоторых вариантах осуществления, частицы (например, сферические частицы или намагничиваемые частицы) являются биодеградируемыми.
[353] В некоторых вариантах осуществления, клетки из выходной композиции, которые инкубируются, приводятся в контакт или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, сравниваются с выходной композицией, которую получают из идентичной исходной композиции, например, из исходной композиции с таким же клеточным составом, которую инкубируют, обрабатывают или приводят в контакт, с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В определенных вариантах осуществления, идентичная исходная композиция не обрабатывается частицами, например, шариками, содержащими связывающие молекулы. В некоторых вариантах осуществления, клетки из идентичной исходной композиции приводятся в контакт, инкубируются или обрабатываются вместе с одной или несколькими поликлональными стимуляторными молекулами при таких же условиях (например, в такой же среде, при такой же температуре, при таком же времени и при таком же количестве и/или концентрации одной или нескольких поликлональных стимуляторных молекул как количество и/или концентрация связывающих молекул), как и клетки из исходной композиции, которые обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, клетки идентичной исходной композиции приводятся в контакт с одной или несколькими поликлональными стимуляторными молекулами, которые присоединяются к поверхности. В определенных вариантах осуществления, клетки идентичной исходной композиции приводятся в контакт с одной или несколькими поликлональными стимуляторными молекулами, которые присоединены к поверхности частицы (например, сферической частицы). В конкретных вариантах осуществления, клетки идентичной исходной композиции приводятся в контакт с одной или несколькими поликлональными стимуляторными молекулами, которые представляют собой антитело анти-CD3 и анти-CD28.
[354] В конкретных вариантах осуществления, количество клеток в выходной композиции больше, по меньшей мере, примерно на 1%, по меньшей мере, примерно на 5%, по меньшей мере, примерно на 10%, по меньшей мере, примерно на 15%, по меньшей мере, примерно на 20%, по меньшей мере, примерно на 25%, по меньшей мере, примерно на 30%, по меньшей мере, примерно на 35%, по меньшей мере, примерно на 40%, по меньшей мере, примерно на 45%, по меньшей мере, примерно на 50%, по меньшей мере, примерно на 55%, по меньшей мере, примерно на 60%, по меньшей мере, примерно на 65%, по меньшей мере, примерно на 70%, по меньшей мере, примерно на 75%, по меньшей мере, примерно на 80%, по меньшей мере, примерно на 85%, по меньшей мере, примерно на 95%, по меньшей мере, примерно на 100%, по меньшей мере, примерно 2-кратно, по меньшей мере, примерно 3-кратно, по меньшей мере, примерно 4-кратно, по меньшей мере, примерно 5-кратно, по меньшей мере, примерно 6-кратно, по меньшей мере, примерно 7-кратно, по меньшей мере, примерно 8-кратно, по меньшей мере, примерно 9-кратно, по меньшей мере, примерно 10-кратно, по меньшей мере, примерно 15-кратно, по меньшей мере, примерно 20-кратно, по меньшей мере, примерно 25-кратно, по меньшей мере, примерно 50-кратно или, по меньшей мере, примерно 100-кратно больше, чем количество клеток в исходной композиции.
[355] В определенных вариантах осуществления, выходная композиция содержит большее количество клеток после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем выходная композиция, которую получают из идентичной исходной композиции, то есть, исходной композиции с таким же клеточным составом, которую инкубируют, обрабатывают или приводятся в контакт, с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR, например, с антителами анти-CD3 и анти-CD28. В некоторых вариантах осуществления, количество клеток выходной композиции, которые обрабатывают вместе с частицами, например, шариками, содержащими связывающую молекулу, составляет, по меньшей мере или, по меньшей мере, примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 100% больше, оно 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно больше, чем количество клеток из выходной композиции из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами.
[356] В конкретных вариантах осуществления, клетки исходной композиции обрабатывают, приводят в контакт или инкубируют вместе с частицами, например, шариками, содержащими связывающую молекулу, которая связывается или распознается рекомбинантным рецептором, экспрессируемым подмножеством клеток исходной композиции, тем самым давая в результате выходную композицию, содержащую большее подмножество клеток, экспрессирующих рекомбинантный рецептор, чем в исходной композиции. В определенных вариантах осуществления, подмножество клеток, экспрессирующих рекомбинантный рецептор, составляет, по меньшей мере или, по меньшей мере, примерно 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 100%, оно 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно больше в выходной композиции, чем в исходной композиции.
[357] В некоторых вариантах осуществления, выходная композиция содержит большее подмножество клеток, экспрессирующих рекомбинантный рецептор, после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем исходная композиция перед инкубированием, приведением в контакт или обработкой вместе с частицами, например, шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, по меньшей мере или, по меньшей мере, примерно 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%,50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 98%, 99% или 99,9% клеток выходной композиции экспрессируют рекомбинантный рецептор.
[358] В определенных вариантах осуществления, выходная композиция содержит большее подмножество клеток, экспрессирующих рекомбинантный рецептор, который связывается или распознается связывающей молекулой, после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем подмножество клеток, экспрессирующих рекомбинантный рецептор, в выходной композиции, которую получают из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько компонентов комплекса TCR, например, с антителами анти-CD3 и анти-CD28. В некоторых вариантах осуществления, подмножество клеток, экспрессирующих рекомбинантный рецептор, в выходной композиции клеток, которые обрабатывают вместе с частицами, например, шариками, содержащими связывающую молекулу составляет, по меньшей мере или, по меньшей мере, примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 100% больше, оно 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно больше, чем подмножество клеток, экспрессирующих рекомбинантный рецептор, из выходной композиции, которую получают из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт вместе с одной или несколькими поликлональными стимуляторными молекулами.
[359] В некоторых вариантах осуществления, клетки, которые экспрессируют рекомбинантный рецептор, например, CAR, в выходной композиции, которую инкубируют, обрабатывают и/или приводят в контакт вместе с частицами, например, шариками, содержащими связывающую молекулу, содержат, по меньшей мере или, по меньшей мере, примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%,50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 98%, 99% или на 99,9% более низкое значение VCN, чем клетки выходной композиции, которые получают поликлональную стимуляцию, например, при инкубировании вместе с антителами анти-CD3 и/или анти-CD28. В некоторых вариантах осуществления, среднее значение VCN CAR-экспрессирующих клеток выходной композиции не более, чем или не более примерно, чем 10, 5, 4, 2,5, 1,5 или 1.
[360] В некоторых вариантах осуществления, выходная композиция содержит большее подмножество активированных клеток после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем исходная композиция перед инкубированием, приведением в контакт или обработкой вместе с частицами, например, шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, активированные клетки представляют собой клетки, которые экспрессируют, по меньшей мере, один маркер активации, то есть, полинуклеотид или полипептид, ассоциируемый с активацией. В некоторых вариантах осуществления, активированные клетки экспрессируют, по меньшей мере, один, по меньшей мере, два, по меньшей мере, три, по меньшей мере, четыре, по меньшей мере, пять, по меньшей мере, шесть, по меньшей мере, семь, по меньшей мере, восемь, по меньшей мере, девять, по меньшей мере, десять или больше десяти различных маркеров активации. В некоторых вариантах осуществления, маркер активации представляет собой лейкоцитарный антиген человека родственный антигену D (HLA-DR), CD25, CD69, CD71, CD40L или 4-1BB (CD137). В конкретных вариантах осуществления, маркер активации представляет собой IL-2, IFN гамма или TNF-альфа. В некоторых вариантах осуществления, маркер активации представляет собой внутриклеточное экспрессирование IL-2, IFN гамма или TNF-альфа. В определенных вариантах осуществления, маркер активации представляет собой секретируемые IL-2, IFN гамма или TNF-альфа. В определенных вариантах осуществления, подмножество клеток, экспрессирующих маркер активации, по меньшей мере или, по меньшей мере, примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 100% больше, оно 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно больше в выходной композиции, чем в исходной композиции.
[361] В некоторых вариантах осуществления, выходная композиция содержит большее количество активированных клеток после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем исходная композиция перед инкубированием, приведением в контакт или обработкой вместе с частицами, например, шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, по меньшей мере или, по меньшей мере, примерно 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%,50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 98%, 99% или 99,9% клеток выходной композиции являются активированными. В некоторых вариантах осуществления, меньше, чем или меньше примерно, чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65% или 70% клеток являются активированными.
[362] В некоторых вариантах осуществления, выходная композиция содержит меньшее подмножество активированных клеток после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем выходная композиция, которую получают из идентичной исходной композиции, то есть, из исходной композиция с таким же клеточным составом, которую инкубируют, обрабатывают или приводят в контакт, с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В некоторых вариантах осуществления, подмножество активированных клеток выходной композиции, которые обрабатывают вместе с частицами, например, шариками, содержащими связывающую молекулу, составляет меньше, чем или меньше примерно, чем 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 99% или 99,9% от подмножества активированных клеток выходной композиции, полученной из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами.
[363] В конкретных вариантах осуществления, клетки выходной композиции являются более активированными после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем в исходной композиции перед инкубированием, приведением в контакт или обработкой вместе с частицами, например, шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, клетки являются более активированными, когда они экспрессируют более высокий уровень, по меньшей мере, одного маркера активации, чем клетки, которые являются менее активированными или клетки, которые не активированы. В некоторых вариантах осуществления, более активированные клетки экспрессируют, по меньшей мере, один, по меньшей мере, два, по меньшей мере, три, по меньшей мере, четыре, по меньшей мере, пять, по меньшей мере, шесть, по меньшей мере, семь, по меньшей мере, восемь, по меньшей мере, девять, по меньшей мере, десять или больше десяти различных маркеров активации при уровнях более высоких, чем клетки, которые являются менее активированными или не активированными. В некоторых вариантах осуществления, активированные клетки экспрессируют большее количество, по меньшей мере, одного белка из лейкоцитарного антигена человека родственного антигену D (HLA-DR), CD25, CD69, CD71, CD40L или 4-1BB (CD137), чем клетки из исходной композиции. В конкретных вариантах осуществления, активированные клетки экспрессируют более высокий уровень IL-2, IFN гамма или TNF-альфа, например, мРНК или полипептидов. В некоторых вариантах осуществления, активированные клетки экспрессируют большее количество внутриклеточного IL-2, IFN гамма или TNF-альфа. В определенных вариантах осуществления, активированные клетки секретируют большее количество IL-2, IFN гамма или TNF-альфа. В определенных вариантах осуществления, активированные клетки экспрессируют количество маркера активации, который, по меньшей мере или, по меньшей мере, примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 100% больше, оно 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно больше, чем количество маркера активации экспрессируемое клетками из исходной композиции.
[364] В некоторых вариантах осуществления, выходная композиция содержит клетки, которые являются менее активированными после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем выходная композиция, которую получают из идентичной исходной композиции, то есть, из исходной композиции с таким же клеточным составом, которую инкубируют, обрабатывают или приводят в контакт, с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В некоторых вариантах осуществления, экспрессирование, по меньшей мере, одного маркера активации в клетках выходной композиции, которую обрабатывают вместе с частицами, например, шариками, содержащими связывающую молекулу, меньше, чем или меньше примерно, чем 1%, 5%, 10%, 15%, 20%, l 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 99% или 99,9% от экспрессирования, по меньшей мере, одного маркера активации в клетках из выходной композиции, полученной из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами.
[365] В некоторых вариантах осуществления, большее подмножество клеток, экспрессирующих рекомбинантный рецептор, (который распознается связывающей молекулой) из выходной композиции активируется после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем клеток, экспрессирующих рекомбинантный рецептор, исходной композиции перед инкубированием, приведением в контакт или обработкой вместе с частицами, например, шариками, содержащими связывающую молекулу. В определенных вариантах осуществления, подмножество клеток, экспрессирующих рекомбинантный рецептор, которые активируются, по меньшей мере или, по меньшей мере, примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 100% больше, оно 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно больше в выходной композиции, чем подмножество активированных клеток, экспрессирующих рекомбинантный рецептор, из исходной композиции.
[366] В некоторых вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, (который связывается или распознается связывающей молекулой), в выходной композиции содержат большее подмножество активированных клеток после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем исходная композиция перед инкубированием, приведением в контакт или обработкой вместе с частицами, например, шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, по меньшей мере или, по меньшей мере, примерно 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 98%, 99% или 99,9% клеток, экспрессирующих рекомбинантный рецептор, из выходной композиции являются активированными. В некоторых вариантах осуществления, меньше, чем или меньше примерно, чем 1%, 5%, 10%, 15%, 20%, l 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70% клеток, экспрессирующих рекомбинантный рецептор, являются активированными.
[367] В некоторых вариантах осуществления, меньшее подмножество клеток, экспрессирующих рекомбинантный рецептор, (который связывается или распознается связывающей молекулой) из выходной композиции активируется после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, по сравнению с клетками, экспрессирующими рекомбинантный рецептор, из выходной композиции, которую получают из идентичной исходной композиции, то есть, из исходной композиции с таким же клеточным составом, которую инкубируют, обрабатывают или приводят в контакт, с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В некоторых вариантах осуществления, подмножество клеток, экспрессирующих рекомбинантный рецептор, из выходной композиции, которая активируется меньше или меньше примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 99% или 99,9%, чем подмножество клеток, экспрессирующих рекомбинантный рецептор, из выходной композиции, полученной из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами.
[368] В конкретных вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, (который связывается или распознается связывающей молекулой), в выходной композиции являются более активированными после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем клетки, экспрессирующие рекомбинантный рецептор, из исходной композиции перед инкубированием, приведением в контакт или обработкой вместе с частицами, например, шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, клетки, которые экспрессируют рекомбинантный рецептор, из выходной композиции экспрессируют большее количество, по меньшей мере, одного маркера активации по сравнению с клетками, которые экспрессируют рекомбинантный рецептор, из исходной композиции. В конкретных вариантах осуществления, клетки, которые экспрессируют рекомбинантный рецептор, из выходной композиции, экспрессируют большее количество, по меньшей мере, одного белка из лейкоцитарного антигена человека родственного антигену D (HLA-DR), CD25, CD69, CD71, CD40L или 4-1BB (CD137), чем клетки, экспрессирующие рекомбинантный рецептор, из исходной композиции.
[369] В конкретных вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, экспрессируют более высокий уровень IL-2, IFN гамма или TNF-альфа. В некоторых вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, экспрессируют большее количество внутриклеточного IL-2, IFN гамма или TNF-альфа. В определенных вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, секретируют большее количество IL-2, IFN гамма или TNF-альфа. В определенных вариантах осуществления, клетки, которые экспрессируют рекомбинантный рецептор, из выходной композиции экспрессируют количество маркера активации, которое, по меньшей мере или, по меньшей мере, примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 100% больше, оно 2-кратно, 3-кратно, 4-кратно, 5-кратно, 6-кратно, 7-кратно, 8-кратно, 9-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно больше, чем количество маркера активации экспрессируемого клетками, экспрессирующими рекомбинантный рецептор из исходной композиции.
[370] В некоторых вариантах осуществления, выходная композиция содержит клетки, которые экспрессируют рекомбинантный рецептор, (который связывается или распознается связывающей молекулой), которые являются менее активированными после инкубирования, приведения в контакт или обработки вместе с частицами, например, шариками, содержащими связывающую молекулу, чем клетки, экспрессирующие рекомбинантный рецептор, из выходной композиции, которую получают из идентичной исходной композиции, то есть, из исходной композиция с таким же клеточным составом, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В некоторых вариантах осуществления, экспрессирование, по меньшей мере, одного маркера активации в клетках, которые экспрессируют рекомбинантный рецептор, из выходной композиции, который обрабатывают вместе с частицами, например, шариками, содержащими связывающую молекулу, меньше, чем или меньше примерно, чем 1%, 5%, 10%, 15%, 20%, l 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 99% или 99,9% от экспрессирования, по меньшей мере, одного маркера активации в клетках, экспрессирующих рекомбинантный рецептор, из выходной композиции, полученной из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами.
[371] В некоторых вариантах осуществления, клетки из выходной композиции, которые инкубируются, приводятся в контакт или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, демонстрируют уменьшенный или более низкий уровень истощения по сравнению с клетками, экспрессирующими рекомбинантный рецептор, из выходной композиции, которую получают из идентичной исходной композиции, то есть, из исходной композиции с таким же клеточным составом, которую инкубируют, обрабатывают или приводятся в контакт, при таких же условиях, вместе с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В конкретных вариантах осуществления, клетки выходной композиции, которые инкубируются, приводятся в контакт или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, демонстрируют уменьшенное или более низкое экспрессирование маркера истощения по сравнению с клетками из выходной композиции, которые получают из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами. В некоторых вариантах осуществления, маркер истощения представляет собой полипептид, который ассоциируется с истощением или представляет собой полинуклеотид, который кодирует полипептид, который ассоциируется с истощением. В некоторых вариантах осуществления, экспрессирование маркера истощения включает поверхностное экспрессирование полипептида маркера истощения. В некоторых вариантах осуществления, маркер истощения представляет собой ингибиторный рецептор, то есть, рецептор, который, когда связывается соответствующим своим лигандом, уменьшает, по меньшей мере, одну иммунную или клеточную активность клетки. В определенных вариантах осуществления, маркер истощения представляет собой PD-1, CTLA-4, TIM-3, LAG-3, BTLA или TIGIT. В конкретных вариантах осуществления, клетки из выходной композиции, которые приводятся в контакт, обрабатываются или инкубируются вместе с частицами, например, шариками, содержащими связывающую молекулу, имеют меньше или меньше примерно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 99% или 99,9% от экспрессирования, по меньшей мере, одного маркера истощения, чем клетки из выходной композиции, которые приводятся в контакт, обрабатываются или инкубируются вместе с одной или несколькими поликлональными стимуляторными молекулами.
[372] В конкретных вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, выходной композиции, которые инкубируются, приводятся в контакт или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, демонстрируют уменьшенный или более низкий уровень истощения по сравнению с клетками, экспрессирующими рекомбинантный рецептор, из выходной композиции, которые получают из идентичной исходной композиции, которую инкубируют, обрабатывают или приводят в контакт с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В конкретных вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, выходной композиции, которые инкубируются, приводятся в контакт или обрабатываются вместе с частицами, например, шариками, содержащими связывающую молекулу, демонстрируют уменьшенное или более низкое экспрессирование маркера истощения по сравнению с клетками, экспрессирующими рекомбинантный рецептор, из выходной композиции, которые получают из идентичной исходной композиции, которые инкубируют, обрабатывают или приводят в контакт, при таких же условиях, с одной или несколькими поликлональными стимуляторными молекулами, которые могут активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR. В конкретных вариантах осуществления, клетки, которые экспрессируют рекомбинантный рецептор, из выходной композиции, которые приводят в контакт, обрабатывают или инкубируются вместе с частицами, например, шариками, содержащими связывающую молекулу, имеют меньше или меньше примерно на 1%, 5%, 10%, 15%, 20%, l 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 95%, 99% или 99,9% от экспрессирования, по меньшей мере, одного маркера истощения, чем клетки, которые экспрессируют рекомбинантный рецептор, из выходной композиции, которую приводят в контакт, обрабатывают или инкубируют вместе с одной или несколькими поликлональными стимуляторными молекулами.
III. СПОСОБЫ ОЦЕНКИ ДОЛГОВРЕМЕННОЙ СТИМУЛЯЦИИ
[373] В настоящем документе предлагается способ долговременной стимуляции (также упоминаемый в настоящем документе как способ долговременной стимуляции), который является пригодным, среди прочего, для оценки фенотипов, характеристик или активностей композиции клеток, например, клеточной композиции. В некоторых вариантах осуществления, способ долговременной стимуляции представляет собой или включает инкубирование композиции клеток, например, исходной композиции, содержащей клетки, экспрессирующие рекомбинантный рецептор, такой как CAR, при условиях стимуляции активности, зависимой от рекомбинантного рецептора (например, CAR-зависимой активности) клеток. В некоторых аспектах, композиция клеток, например, исходная композиция, содержит Т-лимфоциты, экспрессирующие рекомбинантный рецептор (например, CAR), содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген. В некоторых аспектах, инкубирование дает в результате композицию Т-лимфоцитов, например, выходные композиции, содержащие клетки, которые демонстрируют признаки хронически стимулируемых клеток или клеток, имеющих пролонгированное экспонирование для антигена.
[374] В некоторых вариантах осуществления, способ долговременной стимуляции представляет собой или включает инкубирование композиции клеток, например, исходной композиции, содержащей клетки, экспрессирующие рекомбинантный рецептор, такой как CAR, при условиях стимуляции активности, зависимой от рекомбинантного рецептора (например, CAR-зависимой активности) клеток. В таких вариантах осуществления, активность, зависимая от рекомбинантного рецептора представляет собой активность, которая является специфичной относительно стимуляции рекомбинантного рецептора, например, CAR, например, посредством присутствия антигена или другого агента, распознаваемого антигенсвязывающим доменом рекомбинантного рецептора, например, CAR или того, который специфично стимулирует рекомбинантный рецептор. В некоторых аспектах, композиция клеток, например, исходная композиция содержит Т-лимфоциты, экспрессирующие рекомбинантный рецептор (например, CAR), содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген. В некоторых аспектах, инкубирование дает в результате композицию Т-лимфоцита, например, выходные композиции, содержащие клетки, которые демонстрируют признаки хронически стимулированных клеток или клеток, имеющих пролонгированное экспонирование для антигена. В определенных вариантах осуществления, инкубирование осуществляется непрерывно без перерывов.
[375] В определенных вариантах осуществления, способы долговременной стимуляции, предложенные в настоящем документе, являются пригодными для использования, среди прочего, для идентификации композиций клеток, которые могут иметь желаемые признаки, когда вводятся in vivo, например, поддерживаемую или более продолжительную персистентность, жизнеспособность или активность. В некоторых вариантах осуществления, способы осуществляются на двух или более различных композициях клеток для идентификации различий, которые могут усилить или пролонгировать персистентность, активность или жизнеспособность или уменьшить истощение или дифференциацию, например, когда клетки вводятся in vivo. В некоторых вариантах осуществления, такие различия могут включать, но, не ограничиваясь этим, аспекты способа приготовления, такие как временной график, условия или реагенты, используемые на различных стадиях процесса генной инженерии, различия рекомбинантного рецептора (например, различия в последовательности аминокислот, различия в конструкциях или векторах, используемых для доставки рекомбинантного рецептора, или в различных способах доставки гена), различия клеток (например, различия типов или субтипов клеток или источников клеток, такие как различия образцов или субъектов, у которых получают клетки), различные условия хранения (например, количество предыдущих циклов заморозки-оттаивания, температура хранения, приготовления сред для хранения, контейнер для хранения, криоконсервант или плотность клеток) или условия анализа (такие как присутствие или отсутствие контроля или исследуемого соединения в ходе инкубирования).
[376] В некоторых вариантах осуществления, связывающая молекула представляет собой антиген (такой как рекомбинантный антиген или его фрагмент), который связывается или распознается рекомбинантным рецептором. В определенных вариантах осуществления, связывающая молекула представляет собой анти-ID, которое связывает или распознает рекомбинантный рецептор. В некоторых вариантах осуществления, такие признаки могут включать доказательство уменьшения жизнеспособности, активности или персистентности или увеличения истощения или дифференциации. В различных вариантах осуществления, клетки инкубируются вместе со связывающими молекулами в присутствии сред без дополнительных агентов для облегчения деления, роста, размножения или активации клеток. В некоторых вариантах осуществления, клетки инкубируются вместе с частицами в течение продолжительного периода времени. Например, 14 дней, без каких-либо дополнительных манипуляций, например, замены сред, замены шариков или разделения, или пересева клеток.
[377] Конкретные варианты осуществления предполагают, что способы долговременной стимуляции, предложенные в настоящем документе, являются пригодными, среди прочего, для моделирования ex vivo условий, воздействию которых подвергаются клетки при клеточной терапии, когда вводятся субъекту, например, субъекту человеку, in vivo. Таким образом, в некоторых аспектах, предлагаемый анализ является полезным для идентификации композиций клеток, которые могут иметь желаемые признаки, когда вводятся in vivo, такие как, но, не ограничиваясь этим, поддерживаемая или более продолжительная персистентность, жизнеспособность или активность.
[378] В конкретных вариантах осуществления, способ долговременной стимуляции осуществляется в двух или более композициях клеток, например, в исходных композициях, для идентификации композиции клеток, которые увеличивают или поддерживают жизнеспособность, активность или персистентность или увеличивают или поддерживают экспрессирование маркеров, например, биомаркеров, показателей увеличения жизнеспособности, активности или персистентности. В определенных вариантах осуществления, способ долговременной стимуляции осуществляется в двух или более композиций клеток для идентификации различий в композициях клеток, которые уменьшают или предотвращают истощение или дифференциацию (например, такую как дифференциация в сенесцентное состояние) или уменьшают экспрессирование маркеров показателей увеличения истощения или дифференциации. В некоторых вариантах осуществления, связывающая молекула присоединяется или конъюгируется на твердой поверхности, такой как поверхность планшета или чашки для культивирования клеток. В конкретных вариантах осуществления, связывающие молекулы конъюгируются или присоединяются на частицах, например, шариках.
[379] В определенных вариантах осуществления, способы включают стадии инкубирования клеток в присутствии частиц, например, шариков, содержащих связывающую молекулу, например, связывающую молекулу, которая связывает или распознает рекомбинантный рецептор. В некоторых вариантах осуществления, частицы, например, шарики, содержащие связывающую молекулу, представляют собой или содержат реагенты, конъюгированные с шариками, как предлагается, например, анти-ID-конъюгированные шарики или BCMA-конъюгированные шарики. В конкретных вариантах осуществления, клетки или композиции клеток инкубируются вместе с частицами с присоединенной связывающей молекулой, которая описана в настоящем документе, например, в Разделе I. В определенных вариантах осуществления, частица представляет собой частицу, описанную в настоящем документе, например, в Разделе I-A. В определенных вариантах осуществления, связывающая молекула представляет собой связывающую молекулу, описанную в настоящем документе, например, в Разделе I-B. В конкретных вариантах осуществления, связывающая молекула связывает или распознает рекомбинантный рецептор.
[380] В конкретных вариантах осуществления, исходная композиция инкубируется вместе со связывающей молекулой, например, вместе с частицами или шариками, которые содержат связывающую молекулу, в течение, в течение примерно или в течение, по меньшей мере, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней, 16 дней, 17 дней, 18 дней, 19 дней, 20 дней или 21 дня. В различных вариантах осуществления, исходная композиция инкубируется вместе со связывающей молекулой, например, вместе с частицами или шариками, которые содержат связывающую молекулу, в пределах или примерно между 10 днями и 21 днем, 12 днями и 18 днями или 14 днями и 16 днями, включительно. В определенных вариантах осуществления, клетки инкубируются вместе со связывающей молекулой, например, вместе с частицами или шариками, которые содержат связывающую молекулу, в течение, в течение примерно или в течение, по меньшей мере, 14 дней. В конкретных вариантах осуществления, клетки композиции инкубируются вместе со связывающей молекулой при температурах больше комнатной температуры. В некоторых вариантах осуществления, инкубирование осуществляется при температуре больше примерно 25°C, например, как правило, больше или больше примерно 32°C, 35°C или 37°C. В некоторых вариантах осуществления, инкубирование осуществляется при температуре при 37°C ± 2°C или примерно при 37°C ± 2°C, например, при температуре 37°C или примерно при 37°C.
[381] В некоторых вариантах осуществления, клетки инкубируются вместе со связывающей молекулой, например, с частицами или шариками, содержащими связывающие молекулы, в присутствии сред без дополнительных агентов, которые облегчают деление, рост, размножение или активацию клеток, например, Т-лимфоцитов. В некоторых вариантах осуществления, клетки инкубируются вместе со связывающей молекулой в отсутствие каких-либо рекомбинантных цитокинов. В конкретных вариантах осуществления, инкубирование имеет место без перерыва, например, без пересева, замены сред или добавления свежей связывающей молекулы, и тому подобное. В определенных вариантах осуществления, инкубирование имеет место при статических условиях. В конкретных вариантах осуществления, инкубирование имеет место без какой-либо перфузии, смешивания, покачивания или встряхивания. В некоторых аспектах, частицы, например, шарики, содержащие связывающую молекулу, присутствуют в течение всего срока инкубирования. В определенных вариантах осуществления, связывающие молекулы не изменяются или не заменяются в ходе инкубирования. Конкретные варианты осуществления, предполагают, что поскольку, в некоторых аспектах, среды не содержит каких-либо рекомбинантных цитокинов, и цитокины, присутствующие в средах в ходе инкубирования, должны продуцироваться клетками, например, в ответ на взаимодействие между рекомбинантным рецептором клетки и связывающей молекулы частицы.
[382] В некоторых вариантах осуществления, предлагаемые способы долговременной стимуляции можно использовать для сравнения различных клеток или композиций клеток. Например, в некоторых вариантах осуществления, две или более композиций клеток, каждая из которых содержит клетки, экспрессирующие один и тот же рекомбинантный рецептор, например, один и тот же CAR, можно сравнивать посредством инкубирования клеток вместе с одной и той же связывающей молекулой, например, частицами или шариками, содержащими одну и ту же связывающую молекулу, которая связывает или распознает рекомбинантный рецептор. В определенных вариантах осуществления, две или более композиций клеток генерируются с помощью различных процессов генной инженерии, таких как процессы, включающие различные условия, различные временные графики и продолжительности или различное оборудование, или реагенты. В конкретных вариантах осуществления, композиции клеток инкубируются вместе с частицами, например, шариками, содержащими связывающую молекулу, в присутствии одного или нескольких исследуемых агентов или соединений, таких как агенты, подозреваемые в уменьшении истощения или в содействии персистентности. В конкретных вариантах осуществления, композиции клеток можно сравнивать с контрольной или эталонной композицией клеток. В некоторых аспектах, контрольные или эталонные композиции клеток могут включать, но, не ограничиваясь этим, композиции клеток, которые не подвергаются какому-либо инкубированию, композиции клеток, которые не инкубируются в присутствии частиц, например, шариков, содержащих связывающую молекулу, композиции клеток, которые не содержат клеток, экспрессирующих рекомбинантный рецептор, композиции клеток, которые генерируются из другого процесса генной инженерии, и/или композиции клеток, которые инкубируются в присутствии лекарственной среды или контрольного соединения.
[383] В некоторых вариантах осуществления, способ долговременной стимуляции осуществляется в присутствии одного или нескольких исследуемых агентов или соединений. В конкретных вариантах осуществления, исследуемый агент или соединение представляет собой агент, подозреваемый или являющийся кандидатом на изменение или воздействие на одну или несколько характеристик, фенотипов или активностей клеток композиций клеток, например, клеток, экспрессирующих рекомбинантный рецептор, в ходе инкубирования или после него. В некоторых аспектах, исследуемый агент или соединение увеличивает, или уменьшает или подозревается в увеличении или уменьшении одного или нескольких параметров из фенотипов, характеристик или активностей Т-лимфоцитов, таких как рост, деление, размножение, деление, персистентность, дифференциация, активация или истощение, или таких активностей, как антиген-стимулируемые активности, включая, но, не ограничиваясь этим, цитолитическую активность или продуцирование цитокинов. В определенных вариантах осуществления, исследуемый агент или соединение представляет собой природный или химически модифицированный полипептид, антитело, природный или химически модифицированный малый олигопептид, природную, неприродную или химически модифицированную аминокислоту, полинуклеотид, природный или химически модифицированный олигонуклеотид, RNAi, shRNA, siRNA, малый нуклеотид, природный или химически модифицированный мононуклеотид, липопептид, антимикробное соединение, малую молекулу или фармацевтическую молекулу.
[384] В конкретных вариантах осуществления, две или более композиций клеток, каждая из которых содержит клетки, экспрессирующие иной рекомбинантный рецептор, например, различные CAR, могут сравниваться посредством инкубирования клеток вместе со связывающими молекулами, например, с частицами или шариками, содержащими различные связывающие молекулы, которые связывают или распознают различные рекомбинантные рецепторы.
[385] В некоторых вариантах осуществления, выходная композиция состоит из клеток, которые подвергаются, полностью или частично, воздействию способа долговременной стимуляции, например, способа долговременной стимуляции, описанного в настоящем документе. В определенных вариантах осуществления, клетки, подвергающиеся воздействию способа долговременной стимуляции, оцениваются в различных временных точках в ходе инкубирования. Например, в некоторых аспектах, фенотип, характеристики или активность клеток из одной или нескольких композиций клеток оценивается в промежуточной временной точке, например, во временной точке, которая соответствует, примерно соответствует или, по меньшей мере, соответствует 5%, 10%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 90% завершению инкубирования. В определенных вариантах осуществления, клетки оценивают один раз, два раза, три раза, четыре раза, пять раз, шесть раз, семь раз, восемь раз, девять раз, десять раз или больше десяти раз в ходе инкубирования. В определенных вариантах осуществления, клетки оценивают после различных интервалов в ходе инкубирования, например, с интервалом, равным, примерно равным или равным, по меньшей мере, 6 часам, 12 часам, 18 часам, 24 часам, 36 часам, 48 часам, 1 дню, 2 дням, 3 дням, 4 дням, 5 дням, 6 дням, 7 дням или 8 дням. В некоторых вариантах осуществления, клетки оценивают каждый день. В некоторых вариантах осуществления, клетки оценивают каждые три дня. В определенных вариантах осуществления, клетки оценивают каждые 7 дней.
[386] В определенных вариантах осуществления, клетки выходной композиции, например, клетки, которые подвергаются воздействию способа долговременной стимуляции, оцениваются на активность, например, на активность, стимулируемую антигеном, на фенотип или характеристику. В некоторых вариантах осуществления, активность, стимулируемая антигеном, оценивается у клеток в ходе способа или после его завершения, например, в ходе инкубирования вместе со связывающими молекулами или после него. В конкретных вариантах осуществления, результаты оценки сравнивают с оценкой такой же или сходной активности, измеренной у клеток из другой композиции клеток, например, из контрольной или эталонной композиции клеток.
[387] В некоторых вариантах осуществления, активность представляет собой антиген-стимулируемую активность. Конкретные варианты осуществления предполагают, что антиген-стимулируемая активность клеток, таких как Т-лимфоциты, экспрессирующие рекомбинантный рецептор, может оцениваться с помощью любой из ряда известных соответствующих технологий. В некоторых вариантах осуществления, продуцирование одного или нескольких цитокинов измеряется, детектируется и/или количественно определяется с помощью внутриклеточного окрашивания цитокинов. В некоторых аспектах, внутриклеточное окрашивание цитокинов (ICS) с помощью проточной цитометрии представляет собой методику, хорошо приспособленную для изучения продуцирования цитокинов на уровне одной клетки. В определенных аспектах, ICS является полезным при детектировании продуцирования и аккумуляции цитокинов в эндоплазматическом ретикулуме после стимуляции клеток, например, с помощью клетки, экспрессирующей антиген, или частицы, например, сферической частицы, с конъюгированным антигеном, с получением возможности для идентификации популяций клеток, которые являются положительными или отрицательными относительно продуцирования конкретного цитокина или для разделения клеток с высоким продуцированием и низким продуцированием по отношению к некоторому порогу. ICS можно также использовать в сочетании с другими протоколами проточной цитометрии для иммунофенотипирования с использованием клеточных поверхностных маркеров, например, CD4 или CD8, для оценки продуцирования цитокинов в конкретной подгруппе клеток. Другие одноклеточные методики измерения или детектирования продуцирования цитокинов включают, но, не ограничиваясь этим, ELISPOT, предельное разведение и клонирование Т-лимфоцитов.
[388] В некоторых вариантах осуществления, антиген-стимулируемая активность представляет собой продуцирование одного или нескольких цитокинов. Цитокины, которые могут продуцироваться в ответ на стимуляцию антигеном, могут включать, но, не ограничиваясь этим, IL-1, IL-1β, IL-2, sIL-2Ra, IL-3, IL-5, IL-6, IL-7, IL-8, IL-10, IL-12, IL-13, IL 27, IL-33, IL-35, TNF, TNF альфа, CXCL2, CCL2, CCL3, CCL5, CCL17, CCL24, PGD2, LTB4, интерферон гамма (IFN-γ), колониестимулирующий фактор гранулоцитов макрофагов (GM-CSF), воспалительный белок макрофагов (MIP)-1a, MIP-1b, Flt-3L, фракталкин и/или IL-5. В некоторых вариантах осуществления, один или несколько цитокинов представляют собой или включают один или несколько белков из IL-2, IFN-гамма или TNF-альфа. В некоторых вариантах осуществления, секреция цитокинов оценивается посредством измерения, детектирования или количественного определения количества или концентрации внеклеточных цитокинов после сокультивирования вместе с антиген-экспрессирующими клетками или после инкубирования с частицами, например, шариками, содержащими присоединенный антиген или фрагменты антигена.
[389] В конкретных вариантах осуществления, антиген-стимулируемая активность представляет собой цитолитическую (цитотоксическую) активность. В некоторых вариантах осуществления, цитолитическая активность оценивается посредством экспонирования, инкубирования и/или приведения в контакт клеток композиции, например, клеток, экспрессирующих рекомбинантный рецептор, с целевой клеткой, которая экспрессирует антиген или эпитоп, который распознается рекомбинантным рецептором. Цитолитическая активность может измеряться посредством прямого или опосредованного измерения количества целевых клеток со временем. Например, целевые клетки могут инкубироваться вместе с детектируемым маркером перед инкубированием вместе с клетками, экспрессирующими рекомбинантный рецептор, с таким маркером, который детектируется, когда целевая клетка лизируется, или с детектируемым маркером, который детектируется только в жизнеспособных целевых клетках. Эти данные дают прямо или опосредованно количество целевых клеток и/или гибель целевых клеток, и могут измеряться в различных временных точках в ходе анализа. Уменьшение количества целевых клеток и/или увеличение гибели целевых клеток показывает цитолитическую активность клеток. Пригодные для использования способы осуществления цитолитических анализов известны в данной области и включают, но, не ограничиваясь этим, анализы высвобождения хрома-51, анализы с нерадиоактивным хромом, проточные цитометрические анализы, которые используют флуоресцентные красители, такие как сложный сукцинимидиловый эфир карбоксифлуоресцеина (CFSE), PKH-2 и PKH-26.
[390] В определенных вариантах осуществления, клетки, например, клетки, экспрессирующие рекомбинантный рецептор, из композиции оцениваются на одну или несколько характеристик или фенотипов в ходе анализа или после него, например, в ходе инкубирования вместе с частицами, например, шариками, содержащим связывающий рецептор, или после него. В некоторых вариантах осуществления, одна или несколько характеристик или фенотипов представляют собой или связаны с одним или нескольким процессами из активации, истощения или дифференциации. В определенных вариантах осуществления, один или несколько фенотипов, или характеристик оцениваются посредством измерения, детектирования или количественного определения присутствия, отсутствия, количества или уровня одного или нескольких маркеров.
[391] В некоторых вариантах осуществления, экспрессирование маркера, например, биомаркера, который положительно или отрицательно ассоциируется с активацией, истощением или дифференциацией, представляет собой или включает оценку, измерение, определение/или количественное определение уровня, количества или концентрации маркера в образце. В определенных вариантах осуществления, маркер представляет собой генный продукт, например, любую биологическую молекулу, которая собирается, генерируется и/или синтезируется с помощью информации, кодируемой геном, и может включать полинуклеотиды и/или полипептиды. В определенных вариантах осуществления, уровень, количество или концентрация маркера могут преобразовываться (например, нормироваться) или анализироваться непосредственно (например, как есть). В некоторых вариантах осуществления, маркер представляет собой белок. В определенных вариантах осуществления, маркер представляет собой полинуклеотид, например, мРНК или белок, который кодируется геном.
[392] В конкретных вариантах осуществления, количество или уровень маркера, который представляет собой полинуклеотид, может оцениваться, измеряться, определяться и/или количественно определяться с помощью любых соответствующих известных средств. Например, в некоторых вариантах осуществления, количество или уровень полинуклеотидного маркера может оцениваться, измеряться, определяться и/или количественно определяться с помощью цепной реакции полимеразы (PCR), включая методы PCR с обратной транскриптазой (rt), капельную цифровую PCR, PCR в реальном времени и количественный PCR (включая, например, TAQMAN®, молекулярный маяк, LIGHTUP™, SCORPION™, SIMPLEPROBES®; смотри, например, патенты США №№5538848; 5925517; 6174670; 6329144; 6326145 и 6635427); нозерн-блоттинг; саузерн-блоттинг, например, продукты и производные обратной транскрипции; методы на основе массивов, включая блот-массивы, микромассивы или in situ-синтетзированные массивы arrays; и секвенирование, например, секвенирование с помощью синтеза, пиросеквенирование, дидезокси-секвенирование или секвенирование посредством лигирования, или любые другие методы, известные в данной области, такие как обсуждается в Shendure et al., Nat. Rev. Genet. 5:335-44 (2004) или Nowrousian, Euk. Cell 9(9): 1300-1310 (2010), включая такие конкретные платформы как секвенирование HELICOS®, ROCHE® 454, ILLUMINA®/SOLEXA®, ABI SOLiD® и POLONATOR®. В конкретных вариантах осуществления, уровни генных продуктов нуклеиновых кислот измеряют с помощью qRT-PCR. В некоторых вариантах осуществления, qRT-PCR использует три набора нуклеиновых кислот для каждого гена, где три нуклеиновые кислоты содержат пару праймеров вместе с зондом, который связывает вместе области целевой нуклеиновой кислоты, где связаны праймеры, это известно коммерчески как анализ TAQMAN®.
[393] В конкретных вариантах осуществления, экспрессирование двух или более полинуклеотидных маркеров измеряется или оценивается одновременно. В определенных вариантах осуществления, мультиплексная PCR, например, мультиплексная rt-PCR, оценивает измеряет, определяет и/или количественно определяет уровень, количество или концентрацию двух, или более генных продуктов. В некоторых вариантах осуществления, микромассивы (например, массивы AFFYMETRIX®, AGILENT® и массивы в стиле ILLUMINA®) используют для оценки, измерения, определения и/или количественного определения уровня, количества или концентрации двух или более генных продуктов. В некоторых вариантах осуществления, микромассивы используют для оценки, измерения, определения и/или количественного определения уровня, количества или концентрации полинуклеотида кДНК, который получают из генного продукта РНК.
[394] В некоторых вариантах осуществления, экспрессирование одного или нескольких полинуклеотидных маркеров определяется посредством секвенирования маркера мРНК или полинуклеотида кДНК, который получают из маркера мРНК. В некоторых вариантах осуществления, секвенирование осуществляют с помощью способа секвенирования не-Сэнджера и/или методики секвенирования следующего поколения (NGS). Примеры методик секвенирования следующего поколения включают, но, не ограничиваясь этим, массовое параллельное сигнатурное секвенирование (MPSS), полоний-секвенирование, пиросеквенирование, терминаторное секвенирование с обратимым красителем, SOLiD секвенирование, ионное полупроводниковое секвенирование, секвенирование ДНК на нанносферах, секвенирование отдельных молекул в гелиоскопе, секвенирование отдельных молекул в реальном времени (SMRT), секвенирование отдельных молекул в реальном времени (RNAP) и нанопоровое секвенирование ДНК.
[395] В некоторых вариантах осуществления, технология NGS представляет собой секвенирование РНК (RNA-Seq). В конкретных вариантах осуществления, экспрессирование одного или нескольких полинуклеотидных генных продуктов измеряется, определяется и/или количественно определяется с помощью RNA-Seq. RNA-Seq, называемого также шотган-секвенированием полного транскриптома, которое определяет присутствие и количество РНК в образце. Методы секвенирования РНК адаптированы для наиболее распространенных платформ секвенирования ДНК [HiSeq systems (Illumina), 454 Genome Sequencer FLX System (Roche), Applied Biosystems SOLiD (Life Technologies), IonTorrent (Life Technologies)]. Эти платформы требуют начальной обратной транскрипции РНК в кДНК. Наоборот, одномолекулярный секвенсер HeliScope (Helicos BioSciences) может использовать РНК в качестве шаблона для секвенирования. Доказательство принципа прямого секвенирования РНК на платформе PacBio RS также продемонстрировано (Pacific Bioscience). В некоторых вариантах осуществления, один или несколько генных продуктов РНК оценивают, измеряют, определяют и/или количественно определяют с помощью RNA-seq. В некоторых вариантах осуществления, RNA-seq представляет собой основанную на тегах RNA-seq или шотган RNA-seq.
[396] В конкретных вариантах осуществления, маркер представляет собой белок или его фрагмент. В определенных вариантах осуществления, один или несколько белковых маркеров измеряют с помощью любых соответствующих средств известных в данной области. Соответствующие методы оценки, измерения, определения и/или количественного определения уровня, количества или концентрации одного или нескольких белковых маркеров включают, но, не ограничиваясь этим, детектирование с помощью иммунноанализов, аптамерные технологии на основе нуклеиновых кислот или на основе белков, HPLC (высокоточную жидкостную хроматографию), пептидное секвенирование (такое как секвенирование с помощью деградации Эдмана или масс-спектрометрия (такая как MS/MS), необязательно, объединенная с HPLC), и микромассивные адаптации всего, что рассмотрено выше (включая массивы нуклеиновых кислот, антител или белок-белок (то есть, не антител)). В некоторых вариантах осуществления, иммуноанализ представляет собой или включает методы или анализы, которые детектируют белки на основе иммунологической реакции, например, посредством детектирования связывания антитела или фрагмента антитела, связывающего антиген, с генным продуктом. Иммуноанализы включают, но, не ограничиваясь этим, количественную иммуноцитохимию или иммуногистохимию, ELISA (включая прямой, опосредованный, сэндвич-, конкурентный, множественный и портативный ELISA (смотри, например, патент США №7510687), вестерн-блоттинг (включая одно-, двухмерный блоттинг или блоттинг с большим количеством измерений или другие хроматографические средства, необязательно, включающие пептидное секвенирование), ферментативный иммуноанализ (EIA), RIA (радиоиммуноанализ), и SPR (поверхностный плазмонный резонанс).
[397] В некоторых вариантах осуществления, белковый маркер измеряют, детектируют или количественно определяют с помощью проточной цитометрии. В некоторых аспектах, проточная цитометрия представляет собой биофизическую технологию на основе лазера или импеданса, используемую при детектировании маркера, посредством суспендирования клеток в потоке текучей среды и ее прохождения через электронное детектирующее устройство. Маркеры, присутствующие на клетках, могут метиться, например, флуоресцентным меченым антителом, для детектирования с помощью проточной цитометрии. В некоторых аспектах, проточная цитометрия используется для измерения, детектирования или количественного определения присутствия, отсутствия, количества или уровня маркера, присутствующего в популяции клеток. В некоторых аспектах популяция клеток может представлять собой клетки в целом или жизнеспособные клетки в целом из композиции клеток или из подмножества клеток из композиции клеток, например, клетки положительные по рекомбинантному рецептору, Т-лимфоциты CD4+ или Т-лимфоциты CD8+.
[398] В конкретных вариантах осуществления, маркер положительно ассоциируется или коррелирует с состоянием активации или с состоянием подобным активации. В некоторых вариантах осуществления, маркер представляет собой или содержит CD25, CD26, CD27, CD28, CD30, CD71, CD154, CD40L, CD127, LAG3 или Ki67. В некоторых вариантах осуществления, он положительно ассоциируется или коррелирует с истощением или с состоянием, связанным с истощением. В конкретных вариантах осуществления, маркер представляет собой или включает один или несколько белков из CTLA-4, FOXP3, PD-1, TIGIT, LAB-3, 2B4, BTLA, TIM3, VISTA или CD96. В некоторых вариантах осуществления, маркер ассоциируется с дифференциацией Т-лимфоцита. В конкретных вариантах осуществления, маркер представляет собой или включает один или несколько из CD25, CD45RO, CD56, KLRG1, CD95 и/или один или несколько из CD45RA, CD27, CD28, CD62L и CCR7. В некоторых вариантах осуществления, клетки, например, клетки выходной композиции, оцениваются относительно клеток, которые являются поверхностно положительными относительно маркера активации Т-лимфоцитов, селектированного из группы, состоящей из CD45RA, CD27, CD28, CD62L и CCR7; и/или которые являются поверхностно отрицательными относительно маркера, селектированного из группы, состоящей из CD25, CD45RO, CD56, KLRG1; и/или имеют низкое экспрессирование CD95; и/или являются отрицательными относительно внутриклеточного экспрессирования цитокина, селектированного из группы, состоящей из IL-2, IFN-γ, IL-4, IL-10. В некоторых вариантах осуществления, выходная композиция оценивается относительно клеток, которые являются CD45RA+, CD27+, CCR7+ и/или CD45RO-.
[399] В некоторых вариантах осуществления, клетки из композиции клеток, например, выходной композиции клеток, демонстрируют признаки клеток, которые подвергаются пролонгированной или хронической стимуляции после способа долговременной стимуляции, например, после инкубирования вместе с частицами, например, с шариками, содержащими связывающую молекулу. В некоторых вариантах осуществления, клетки, экспрессирующие рекомбинантный рецептор, из композиции клеток, например, эталонной или контрольной композиции клекот, демонстрируют признаки клеток, которые подвергаются пролонгированной или хронической стимуляции после анализа, например, после инкубирования вместе с частицами, например, шариками, содержащими связывающую молекулу.
[400] В некоторых вариантах осуществления, клетки из выходных композиций, которые подвергаются воздействию способа долговременной стимуляции, например, инкубированию вместе с частицами, например, шариками, содержащими связывающую молекулу, демонстрируют уменьшенную антиген-стимулируемую активность по сравнению с клетками из композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, антиген-стимулируемая активность уменьшается на, примерно на или, по меньшей мере, на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 99,9% или на или примерно на 100% по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, антиген-стимулируемая активность уменьшается на детектируемую, статистически значимую величину по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В некоторых вариантах осуществления, антиген-стимулируемое продуцирование цитокинов уменьшается по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В конкретных вариантах осуществления, антиген-стимулируемое секретирование цитокинов уменьшается по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В конкретных вариантах осуществления, антиген-стимулируемая цитолитическая активность уменьшается по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции.
[401] В конкретных вариантах осуществления, клетки из выходных композиций, такие как клетки из контрольных или эталонных композиций, демонстрируют пониженный уровень экспрессирования или количество клеток положительных относительно маркера, ассоциированного с наивно-подобными Т-лимфоцитами, по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, количество клеток положительных относительно маркера, такого как маркер, например, имеющих детектируемые количества маркера или количество или экспрессирование выше порогового уровня или величины окрашивания, уменьшается на, примерно на или, по меньшей мере, на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 99,9% или на или примерно на 100% по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, количество клеток положительных относительно маркера уменьшается на детектируемую, статистически значимую величину по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции.
[402] В некоторых вариантах осуществления, среднее, усредненное или медианное экспрессирование, количество или уровень маркера, такого как маркер, ассоциированный с активацией, или маркер, положительно ассоциированный с наивно-подобным состоянием клеток или подмножества клеток выходной композиции, уменьшается на, примерно на или, по меньшей мере, на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 99,9% или на или примерно на 100% по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, количество клеток положительных относительно маркера, ассоциируемого с активацией, уменьшается на детектируемую, статистически значимую величину по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции.
[403] В определенных вариантах осуществления, клетки из выходных композиций, например, выходных композиций или контрольных или эталонных композиций, которые подвергаются воздействию способа долговременной стимуляции, например, инкубированию вместе с частицами, например, шариками, содержащими связывающую молекулу, демонстрируют повышенный уровень, экспрессирование или количества клеток положительных относительно маркера, такого как маркер, положительно ассоциированный с истощением, или маркер, положительно ассоциированный с дифференцированными Т-лимфоцитамиы, по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, количество клеток положительных относительно маркера, например, имеющих детектируемые количества маркера или величину экспрессирования выше порогового уровня или величину окрашивания, увеличивается на, примерно на или, по меньшей мере, на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90%, 95%, 100%, 150%, 200%, 1-кратно, 2-кратно, 3-кратно, 4-кратно, 5-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, количество клеток положительных относительно маркера увеличивается на детектируемую, статистически значимую величину по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции.
[404] В различных вариантах осуществления, среднее, усредненное или медианное экспрессирование, количество или уровень маркера, такого как маркер, положительно ассоциированный с истощением, или маркер, положительно ассоциированный с дифференцированными Т-лимфоцитами, клеток или подмножества клеток, которые подвергаются воздействию способа долговременной стимуляции увеличивается на, примерно на или, по меньшей мере, на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90%, 95%, 100%, 150%, 200%, 1-кратно, 2-кратно, 3-кратно, 4-кратно, 5-кратно, 10-кратно, 20-кратно, 50-кратно или 100-кратно по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции. В определенных вариантах осуществления, количество клеток положительных относительно маркера, положительно ассоциированного с истощением, увеличивается на детектируемую, статистически значимую величину по сравнению с клетками композиции, которые не подвергаются воздействию способа долговременной стимуляции.
[405] В определенных вариантах осуществления, композиция клеток, содержащая клетки, экспрессирующие рекомбинантный рецептор, инкубируется в присутствии частицы, содержащей связывающую молекулу, в течение времени между 7 днями и 21 днем. В конкретных вариантах осуществления, клетки из композиции клеток, содержащей CAR-экспрессирующие клетки, инкубируются вместе с частицами, например, шариками, содержащими связывающую молекулу, в течение, по меньшей мере, 14 дней в отсутствие рекомбинантных цитокинов. В определенных вариантах осуществления, после осуществления способа долговременной стимуляции, клетки или подмножества клеток, например, клетки CAR+, оцениваются на антиген-стимулируемую активность, такую как продуцирование цитокинов или цитолитическая активность. В конкретных вариантах осуществления, после анализа ex-vivo, клетки или подмножество клеток композиции оценивается на экспрессирование одного или нескольких маркеров. В конкретных вариантах осуществления, две или более композиций клеток, которые подвергаются воздействию способа долговременной стимуляции, сравниваются для идентификации разбросов или реагентов, которые улучшают персистентность, жизнеспособность или активность композиций клеток, когда их вводят субъекту in vivo.
IV. ГЕННО-ИНЖЕНЕРНЫЕ КЛЕТКИ И РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ
[406] В некоторых вариантах осуществления, предлагаемые способы, например, стимуляции или размножения клеток, экспрессирующих рекомбинантный рецептор, осуществляются на исходной композиции, содержащей клетки, экспрессирующие рекомбинантный рецептор, и/или в сочетании со способом генной инженерии клеток с рекомбинантным рецептором. В некоторых аспектах, генная инженерия клетки с рекомбинантным рецептором включает приведение в контакт композиции клеток с молекулой нуклеиновой кислоты, например, с вирусом или невирусной плазмидой, которая содержит ген, кодирующий рекомбинантный рецептор, например, CAR, при условиях для доставки молекулы нуклеиновой кислоты в одну или несколько клеток композиции.
[407] В некоторых вариантах осуществления, клетки содержат одну или несколько нуклеиновых кислот, введенных посредством генной инженерии согласно предлагаемым способам, и тем самым экспрессируют рекомбинантные или генно-инженерные продукты таких нуклеиновых кислот. В некоторых вариантах осуществления, нуклеиновые кислоты являются гетерологичными, то есть, обычно не присутствуют в клетке или образце, полученном из клетки, например, они получены из другого организма или клетки, которая, например, обычно не находится в клетке, полученной с помощью генной инженерии, и/или в организме, из которого такая клетка получается. В некоторых вариантах осуществления, нуклеиновые кислоты не встречаются в природе, например, это нуклеиновая кислота, не встречающаяся в природе, включая химерные сочетания нуклеиновых кислот, кодирующих различные домены из множества различных типов клеток. В конкретных вариантах осуществления, нуклеиновые кислоты содержат ген, который кодирует рекомбинантный рецептор, например, CAR.
[408] В некоторых вариантах осуществления, предлагаемые способы могут осуществляться одновременно, последовательно или согласованно с одной или несколькими стадиями процессинга получения или приготовления генно-инженерных клеток. Стадии процессинга способов могут включать одну или несколько из ряда стадий процессинга клеток, по отдельности или в сочетании. В конкретных вариантах осуществления, стадии процессинга включают трансдуцирование или трансфицирование клеток одной или несколькими нуклеиновыми кислотами, например, гетерологичным полинуклеотидом, содержащим ген, кодирующий рекомбинантный рецептор. В определенных вариантах осуществления, клетки трансдуцируются частицами вирусных векторов, содержащих ретровирусный вектор, такой как вектор, кодирующий рекомбинантный продукт для экспрессирования в клетках. В определенных вариантах осуществления, клетки трансфицируются одной или несколькими невирусными нуклеиновыми кислотами, например, эписомальной плазмидой или транспозоном. Способы могут дополнительно и/или альтернативно включать другие стадии процессинга, такие как стадии выделения, разделения, селекции, промывки, суспендирования, разведения, концентрирования и/или приготовления клеток. В некоторых случаях, способы также могут включать стадию ex vivo культивирования, стимуляции или размножения клеток (например, стимуляцию клеток, например, для индуцирования их пролиферации и/или активации), которая, в некоторых случаях, может согласно предлагаемым способам. В некоторых вариантах осуществления, способы включают выделение клеток у субъекта, их приготовление, процессинг, культивирование и/или генную инженерию и их повторное введение тому же субъекту, перед или после криоконсервирования.
[409] В некоторых вариантах осуществления, способ включает стадии процессинга, осуществляемые в таком порядке: клетки, например, первичные клетки, сначала выделяются, например, селектируются или отделяются из биологического образца; селектированные клетки инкубируются вместе с частицами вирусного вектора для трансдуцирования; и трансдуцированные клетки приготавливаются в композиции. В некоторых случаях, трансдуцированные клетки активируются, наращиваются или размножаются ex vivo, например, посредством стимуляции в присутствии стимулирующего реагента, например, согласно предлагаемым способам. В некоторых вариантах осуществления, способ может включать одну или несколько стадий процессинга из промывки, суспендирования, разведения и/или концентрирования клеток, которые могут осуществляться до, в ходе или одновременно, или после одной или нескольких стадий выделения, таких как стадии разделения или селекции, трансдуцирования, стимуляции и/или приготовления.
[410] В конкретных вариантах осуществления, клетки, которые должны трансфицироваться или трансдуцироваться, не выделяют, не селектируют или не обогащают перед приведением контакт с одной или несколькими нуклеиновыми кислотами. В некоторых вариантах осуществления, клетки не селектируют до приведения в контакт клеток с одной или несколькими нуклеиновыми кислотами. В некоторых вариантах осуществления, клетки, которые должны трансфицироваться или трансдуцироваться, не обогащают до приведения в контакт клеток с одной или несколькими нуклеиновыми кислотами.
[411] В некоторых вариантах осуществления, одна или несколько, или все стадии процессинга, например, выделение, селекция и/или обогащение, процессинг, инкубирование в сочетании со стадиями трансдуцирования и генной инженерии, стимуляции и/или активации и приготовления осуществляются с использованием системы, устройства или аппарата во встроенной или самодостаточной системе и/или автоматизируемым или программируемым образом. В некоторых аспектах, система или устройство содержит компьютер и/или компьютерную программу в сообщении с системой или устройством, которая дает возможность пользователю программировать, контролировать, оценивать результаты и/или регулировать различные аспекты стадий процессинга, выделения, генной инженерии и приготовления. В одном из примеров, система представляет собой систему, как описано в Международный публикации заявки патент, номер WO 2009/072003 или в заявке на патент США US 20110003380 A1. В одном из примеров, система представляет собой систему, как описано в Международной публикации номер WO 2016/073602.
[412] В некоторых вариантах осуществления, одна или несколько стадий процессинга клеток в сочетании с приготовлением, процессингом и/или инкубированием клеток в сочетании с предлагаемым способом, включая сочетание с приготовлением композиции, содержащей генно-инженерные клетки, может осуществляться во внутренней полости камеры центрифуги, такой как, по существу, жесткая камера, которая, в целом, имеет цилиндрическую форму и может вращаться вокруг оси вращения, что может обеспечить определенные преимущества по сравнению с другими доступными способами. В некоторых вариантах осуществления, все стадии процессинга осуществляют в одной камере центрифуги. В некоторых вариантах осуществления, одну или несколько стадий процессинга осуществляют в различных камерах центрифуги, например, во множестве камер центрифуги одного типа. Такие способы включают любые способы, как описано в Международной публикации номер WO 2016/073602.
[413] Иллюстративные камеры центрифуг включают камеры, производимые и продаваемые Biosafe SA, включая камеры для применения вместе с системой Sepax® и Sepax® 2, включая камеры центрифуг A-200/F и A-200 и различные наборы для использования вместе с такими системами. Иллюстративные камеры, системы и инструментарий, и боксы для процессинга описаны, например, в патенте США № 6123655, патенте США №6733433 и в опубликованной заявке на патент США №: US 2008/0171951, и опубликованной Международный заявке на патент, № публикации WO 00/38762, содержания каждого из которых включается в настоящий документ в качестве ссылки во всей своей полноте. В зависимости от конкретного процесса (например, разведения, промывки, трансдуцирования, приготовления), специалист в данной области может выбрать конкретный набор, который соответствует процессу. Иллюстративные наборы для применения вместе с такими системами включают, но, не ограничиваясь этим, одноразовые наборы, продаваемые BioSafe SA под торговыми наименованиями продуктов CS-430.1, CS-490.1, CS-600.1 или CS-900.2.
[414] В некоторых вариантах осуществления, система включается и/или размещается в ассоциации с другим инструментарием, включая инструментарий для аспектов работы, автоматизации, контроля и/или мониторинга различных стадий процессинга, осуществляемых в системе. Этот инструментарий в некоторых вариантах осуществления содержится внутри бокса. В некоторых вариантах осуществления, инструментарий включает бокс, который содержит корпус, содержащий контрольную схему, центрифугу, крышку, двигатели, насосы, сенсоры, дисплеи и интерфейс пользователя. Иллюстративное устройство описано в патенте США №6123655, патенте США №6733433 и в заявке на патент США 2008/0171951.
[415] В некоторых вариантах осуществления, система содержит ряд контейнеров, например, мешков, трубопроводов, кранов, защелок, коннекторов и камеру центрифуги. В некоторых вариантах осуществления, контейнеры, такие как мешки, включают один или несколько контейнеров, таких как мешки, содержащие клетки, которые должны трансдуцироваться или трансфицироваться, и частицы векторов, например, частиц вирусных векторов или невирусных плазмид, в одном контейнере или в отдельных контейнерах, например, в одном мешке или в отдельных мешках. В некоторых вариантах осуществления, система дополнительно содержит один или несколько контейнеров, таких как мешки, содержащие среду, такую как разбавитель и/или промывочный раствор, который вводится в камеру, и/или другие компоненты для разведения, повторного суспендирования и/или промывки компонентов и/или композиций в ходе осуществления способов. Контейнеры могут соединяться в одном или в нескольких положениях в системе, например, в положении, соответствующем входной линии, линии разбавителя, линии промывки, линии для отходов и/или выходной линии.
[416] В некоторых вариантах осуществления, система, такая как замкнутая система, является стерильной. В некоторых вариантах осуществления, все соединения компонентов системы, например, между линиями трубопроводов и контейнеров через коннекторы, осуществляют при стерильных условиях. В некоторых вариантах осуществления, соединения осуществляют в ламинарном потоке. В некоторых вариантах осуществления, соединения осуществляют с использованием стерильного соединительного устройства, которое производит стерильные соединения, такие как стерильные сварные швы между трубопроводом и контейнером. В некоторых вариантах осуществления, стерильное соединительное устройство осуществляет соединение при термических условиях достаточно высоких для поддержания стерильности, например, при температурах, по меньшей мере, 200°C, например, по меньшей мере, 260°C или 300°C.
[417] В некоторых вариантах осуществления, система может быть одноразовой, например, представлять собой одноразовый набор. В некоторых вариантах осуществления, одноразовый набор можно использовать во множестве циклов процесса или процессов, например, по меньшей мере, 2, 3, 4, 5 или более раз, например, в процессах, которые осуществляются непрерывным или полунепрерывным образом. В некоторых вариантах осуществления, система, такая как одноразовый набор, используется для процессинга клеток от одного пациента. В аспектах способов, процессы не должны осуществляться в одной и той же замкнутой системе, например, в одной камере центрифуги, но могут осуществляться в другой замкнутой системе, например, в другой камере центрифуги; в некоторых вариантах осуществления, такие различные камеры центрифуги находятся в соответствующих точках в способах, размещенных в ассоциации с этой же системой, например, размещаться в ассоциации с этой же центрифугой. В некоторых вариантах осуществления, все стадии процессинга осуществляются в замкнутой системе, в которой все стадии процессинга или подмножество из каждой одной или нескольких стадий процессинга осуществляется в одной и той же камере центрифуги или в разных камерах.
A. Приготовление образцов и клеток
[418] В настоящем документе предлагаются клетки, включая генно-инженерные клетки, которые содержат рекомбинантный рецептор. Также предлагаются популяции таких клеток и композиции, содержащие такие клетки. Среди композиций имеются исходные композиции, содержащие клетки, в которых одна или несколько клеток являются известными или сходными или будут экспрессировать рекомбинантный рецептор, который может распознаваться или связываться связывающей молекулой, присутствующей на одной или нескольких частицах, вместе с которыми клетки инкубируются или приводятся в контакт. Также среди композиций имеются композиции, получаемые с помощью предлагаемых способов, включая выходные композиции, в которых содержатся стимулированные или наращенные клетки, включая композиции обогащенные клетками, содержащими рекомбинантный рецептор, связывающийся или распознающийся связывающей молекулой частицы, например, в котором клетки, экспрессирующие рекомбинантный рецептор, например, химерный рецептор, составляют, по меньшей мере, 50, 60, 70, 80, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или более процентов от клеток в целом в композиции или от клеток определенного типа, таких как Т-лимфоциты или клетки CD8+ или CD4+. Таким образом, предлагаются генно-инженерные клетки, экспрессирующие рекомбинантные рецепторы, например, CAR.
[419] Среди композиций имеются фармацевтические композиции и препараты для введения, например, для адоптивной клеточной терапии. Также предлагаются способы генной инженерии, продуцирования или генерирования таких клеток, терапевтические способы введения клеток и композиций субтипам, например, пациентам, и способы детектирования селекции, выделения или разделения таких клеток.
[420] Клетки, как правило, представляют собой эукариотические клетки, такие как клетки млекопитающего, и, как правило, представляют собой клетки человека. В некоторых вариантах осуществления, клетки получают из крови, костного мозга, лимфы или лимфоидных органов, они представляют собой клетки иммунной системы, такие как клетки врожденного или адаптивного иммунитета, например, миелоидные или лимфоидные клетки, включая лимфоциты, как правило, Т-лимфоциты и/или NK-клетки. Другие иллюстративные клетки включают стволовые клетки, такие как мультипотентные и плюрипотентные стволовые клетки, включая индуцированные плюрипотентные стволовые клетки (iPSC).
[421] Клетки, как правило, представляют собой первичные клетки, такие как клетки, выделенные непосредственно у субъекта и/или выделенные у субъекта и замороженные. В некоторых вариантах осуществления, клетки содержат одно или несколько подмножеств Т-лимфоцитов или других типов клеток, таких как популяции цельных Т-лимфоцитов, клеток CD4+, клеток CD8+, и их субпопуляции, такие как те, которые определяются функцией, состоянием активации, зрелостью, потенциалом дифференциация, размножением, рециркуляцией, локализацией и/или способностями к персистентности, антиген-специфичностью, типом рецептора антигена, присутствием в конкретном органе или компартменте, профилем секреции маркера или цитокинов, и/или степенью дифференциации. Относительно субъекта, который должен лечиться, клетки могут быть аллогенными и/или аутогенными. Способы включают стандартные способы. В некоторых аспектах, например, для стандартных технологий, клетки являются плюрипотентными и/или мультипотентными, такими как стволовые клетки, например, индуцированные плюрипотентные стволовые клетки (iPSC).
[422] Среди субтипов и субпопуляций Т-лимфоцитов и/или Т-лимфоцитов CD4+ и/или CD8+ имеются наивные T-лимфоциты (TN), эффекторные Т-лимфоциты (TEFF), Т-лимфоциты памяти и их субтипы, такие как стволовые T-лимфоциты памяти (TSCM), Т-лимфоциты центральной памяти (TCM), эффекторные T-лимфоциты памяти (TEM) или терминально дифференцированные эффекторные Т-лимфоциты памяти, лимфоциты, инфильтрующие опухоль (TIL), незрелые Т-лимфоциты, зрелые Т-лимфоциты, хелперные Т-лимфоциты, цитотоксичные Т-лимфоциты, мукоза-ассоциированные инвариантные T-лимфоциты (MAIT), встречающиеся в природе и адаптивные регуляторные T-лимфоциты (Treg), хелперные Т-лимфоциты, такие как TH1-лимфоциты, TH2-лимфоциты, TH3-лимфоциты, TH17-лимфоциты, TH9-лимфоциты, TH22-лимфоциты, фолликулярные хелперные Т-лимфоциты, альфа/бета Т-лимфоциты и дельта/гамма Т-лимфоциты.
[423] В некоторых вариантах осуществления, клетки представляют собой природные клетки-киллеры (NK). В некоторых вариантах осуществления, клетки представляют собой моноциты или гранулоциты, например, миелоидные клетки, макрофаги, нейтрофилы, дендритные клетки, тучные клетки, эозинофилы и/или базофилы.
[424] В некоторых вариантах осуществления, клетки получают из линий клеток, например, линий Т-лимфоцитов. В некоторых вариантах осуществления клетки получают из ксеногенного источника, например, от мыши, крысы, примата отличного от человека и свиньи.
[425] В некоторых вариантах осуществления, клетки могут выделяться из образца, такого как биологический образец, например, образец, полученный или извлеченный у субъекта. В некоторых вариантах осуществления, субъект, у которого выделяют клетки, представляет собой субъекта, имеющего заболевание или состояние, или необходимость в клеточной терапии или субъекта, которому будет вводиться клеточная терапия. В некоторых вариантах осуществления субъект представляет собой человека, нуждающегося в конкретном терапевтическом вмешательстве, таком как адоптивная клеточная терапия, для которой клетки выделяются, процессируются и/или получаются с помощью генной инженерии.
[426] Соответственно, клетки в некоторых вариантах осуществления представляют собой первичные клетки, например, первичные клетки человека. Образцы включают ткани, текучую среду и другие образцы, взятые непосредственно у субъекта, а также образцы, полученные в результате одной или нескольких стадий процессинга, таких как разделение, центрифугирование, генная инженерия, (например, трансдуцирование вирусным вектором), промывка и/или инкубирование. Биологический образец может представлять собой образец, полученный непосредственно из биологического источника или образец, который процессируют. Биологические образцы включают, но, не ограничиваясь этим, телесные жидкости, такие как кровь, плазма, сыворотка, спинномозговая жидкость, синовиальная жидкость, моча и пот, образцы ткани и органов, включая процессированные образцы, полученные из них.
[427] В некоторых примерах, клетки из циркулирующей крови субъекта получают, например, посредством афереза или лейкафереза. В определенных вариантах осуществления, клетки крови содержат лимфоциты, включая Т-лимфоциты, моноциты, гранулоциты, B-клетки, другие ядросодержащие лейкоциты, эритроциты и/или тромбоциты, а в некоторых аспектах, содержат клетки иные, чем эритроциты и тромбоциты. В некоторых вариантах осуществления, перед селекцией и/или обогащением клеток, образец или клетки в образце могут покоиться или выдерживаться перед дальнейшими стадиями процессинга. В некоторых вариантах осуществления, образец поддерживается или выдерживается при температуре от или примерно от 2°C до 8°C в течение до 48 часов, например, до 12 часов, 24 часов или 36 часов. В определенных вариантах осуществления, клетки не селектируются и/или не обогащаются перед приведением в контакт клеток с одной или несколькими нуклеиновыми кислотами. В некоторых вариантах осуществления, образец или клетки могут покоиться или выдерживаться перед приведением в контакт или инкубированием клеток вместе с одной или несколькими нуклеиновыми кислотами. В определенных вариантах осуществления, образец поддерживается или выдерживается при температуре от или примерно от 2°C до 8°C в течение до 48 часов, например, до 12 часов, 24 часов или 36 часов до приведения в контакт или инкубирования клеток с одной или несколькими нуклеиновыми кислотами.
[428] В некоторых вариантах осуществления, способы приготовления включают стадии замораживания, например, криоконсервирование клеток, либо до, либо после выделения, селекции и/или обогащения, инкубирования для трансдуцирования и генной инженерии и/или стимуляции, активации и/или размножения клеток. В некоторых вариантах осуществления, клетки суспендируются в растворе для замораживания, например, после стадии промывки, для удаления плазмы и тромбоцитов. В некоторых аспектах можно использовать любой из известных растворов для замораживания и параметров. Один из примеров включает использование PBS, содержащего 20% DMSO и 8% сывороточного альбумина человека (HSA), или другие пригодные для использования среды для замораживания клеток. Затем их разбавляют 1:1 средами, так что конечные концентрации DMSO и HSA составляют 10% и 4%, соответственно. Клетки, как правило, затем замораживают до -80°C при скорости 1° в минуту и хранят в паровой фазе танка хранилища с жидким азотом.
[429] В некоторых вариантах осуществления, выделение клеток включает одну или несколько стадий приготовления и/или разделения клеток не на основе аффиности. В некоторых примерах, клетки промывают, центрифугируют и/или инкубируют в присутствии одного или нескольких реагентов, например, для удаления нежелательных компонентов, обогащения желательными компонентами, лизиса или удаления клеток, чувствительных к конкретным реагентам. В некоторых примерах, клетки разделяют на основе одного или нескольких свойств, таких как плотность, свойства приклеивания, размер, чувствительность и/или стойкость к конкретным компонентам.
[430] В некоторых вариантах осуществления, способы включают способы разделения клеток на основе плотности, например, приготовление лейкоцитов из периферической крови посредством лизиса эритроцитов и центрифугирования в градиенте Percoll или Ficoll.
[431] В некоторых вариантах осуществления, способы выделения включают разделение различных типов клеток на основе экспрессирования или присутствия в клетке одной или нескольких специфичных молекул, таких как поверхностные маркеры, например, поверхностные белки, внутриклеточные маркеры или нуклеиновая кислота. В некоторых вариантах осуществления, можно использовать любой известный способ разделения на основе таких маркеров. В некоторых вариантах осуществления, разделение представляет собой разделение на основе аффиности или иммунноаффиности. Например, выделение в некоторых аспектах включает разделение клеток и популяций клеток на основе экспрессирования клеток или на уровне экспрессирования одного или нескольких маркеров, как правило, поверхностных маркеров клеток, например, посредством инкубирования вместе с антитело или партнеров по связыванию, который специфично связывается с такими маркерами, как правило, с последующими стадиями промывки и разделения клеток, имеющих связанное антитело или партнер по связыванию, от клеток, не имеющих связанного антитела или партнер по связыванию.
[432] Такая стадии разделения могут основываться на положительной селекции, при которой клетки, имеющие связывающие реагенты, удерживаются для дальнейшего использования, и/или отрицательной селекции, при которой удерживаются клетки, не имеющие связанного антитела или партнера по связыванию. В некоторых примерах, обе фракции удерживаются для дальнейшего использования. В некоторых аспектах, отрицательная селекция может быть особенно полезной, когда нет доступного антитела, которое специфично идентифицирует тип клетки в гетерогенной популяции, так что разделение лучше всего осуществляется на основе маркеров, экспрессируемых клетками иными, чем желаемая популяция.
[433] Разделение не должно давать в результате 100% обогащение или удаление конкретной популяции клеток или клеток, экспрессирующих конкретный маркер. Например, положительная селекция или обогащение клетками конкретного типа, например, которые экспрессируют маркер, относится к увеличению количества или процента таких клеток, но не должно давать в результате полное отсутствие клеток, не экспрессирующих маркер. Подобным же образом, отрицательная селекция, удаление или обеднение клеток конкретного типа, например, экспрессирующих маркер, относится к уменьшению количества или процента таких клеток, но не должно давать в результате полного удаления всех таких клеток.
[434] В некоторых примерах, осуществляют множество заходов стадий разделения, где положительно или отрицательно селектированная фракция от одной стадии подвергается воздействию другой стадии разделения, такие как следующая далее положительная или отрицательная селекция. В некоторых примерах, одна стадия разделения может обеднять клетки, экспрессирующие множество маркеров одновременно, например, посредством инкубирования клеток вместе с множеством антител или партнеров по связыванию, каждый из которых является специфичным относительно целевого маркера для отрицательной селекции. Подобным же образом, множество типов клеток можно одновременно подвергать положительной селекции посредством инкубирования клеток вместе с множеством антител или партнеров по связыванию, экспрессируемых на различных типах клеток.
[435] Например, в некоторых аспектах, конкретные субпопуляции Т-лимфоцитов, таких как клетки положительные относительно одного или нескольких поверхностных маркеров, например, Т-лимфоциты CD28+, CD62L+, CCR7+, CD27+, CD127+, CD4+, CD8+, CD45RA+ и/или CD45RO+, или экспрессирующие высокие их уровни, выделяют посредством технологий положительной или отрицательной селекции.
[436] Например, Т-лимфоциты CD3+, CD28+ можно подвергать положительной селекции с использованием магнитных шариков, конъюгированных с анти-CD3/анти-CD28 (например, DYNABEADS® M-450 CD3/CD28 T Cell Expander). В конкретных вариантах осуществления, клетки приводятся в контакт с магнитными шариками, конъюгированными с анти-CD3/анти-CD28, например, DYNABEADS® M-450 CD3/CD28 T Cell Expander), для размножения Т-лимфоцитов CD3+, CD28+ до приведения в контакт клеток с одной или несколькими нуклеиновыми кислотами. В определенных вариантах осуществления, клетки не приводятся в контакт с магнитными шариками, конъюгированными с анти-CD3/анти-CD28, до приведения в контакт клеток с одной или несколькими нуклеиновыми кислотами.
[437] В некоторых вариантах осуществления, выделение осуществляется посредством обогащения конкретной популяции клеток посредством положительной селекции или обеднения конкретной популяции клеток, посредством отрицательной селекции. В некоторых вариантах осуществления, положительную или отрицательную селекцию осуществляют посредством инкубирования клеток вместе с одним или несколькими антителами или с другим связывающем агентом, который специфично связывается с одним или несколькими поверхностными маркерами, которые экспрессируются или экспрессируются (маркер+) при относительно высоком уровне (маркерhigh) на клетках от положительной или отрицательной селекции, соответственно.
[438] В некоторых вариантах осуществления, Т-лимфоциты отделяются из образца PBMC посредством отрицательной селекции маркеров экспрессируемых не на Т-лимфоцитах, например, на B-клетках, моноцитах или других лейкоцитах, таких как CD14. В некоторых аспектах, стадия селекции CD4+ или CD8+ используется для разделения хелперных Т-лимфоцитов CD4+ и цитотоксичных Т-лимфоцитов CD8+. Такие популяции CD4+ и CD8+ могут дополнительно сортироваться на субпопуляции посредством положительной или отрицательной селекции относительно маркеров, экспрессируемых или экспрессируемых на относительно более высоком уровне в одной или нескольких субпопуляциях наивных Т-лимфоцитов, Т-лимфоцитов памяти и/или эффекторных Т-лимфоцитов.
[439] В некоторых вариантах осуществления, клетки CD8+ дополнительно обогащаются или обедняются наивными клетками, клетками центральной памяти, эффекторными клетками памяти или стволовыми клетками центральной памяти, например, посредством положительной или отрицательной селекции на основе поверхностных антигенов, ассоциированных с соответствующей субпопуляцией. В некоторых вариантах осуществления, обогащение Т-лимфоцитами центральной памяти (TCM) осуществляется для увеличения эффективности, например, для улучшения долговременной выживаемости, размножения и/или приживления после введения, которое в некоторых аспектах является особенно стойким в таких субпопуляциях. Смотри Terakura et al. (2012) Blood,1:72-82; Wang et al. (2012) J Immunother. 35(9):689-701, В некоторых вариантах осуществления, объединение TCM-обогащенных Т-лимфоцитов CD8+ и Т-лимфоцитов CD4+ дополнительно усиливает эффективность.
[440] В вариантах осуществления, Т-лимфоциты памяти присутствуют в подмножествах как CD62L+, так и CD62L- лимфоцитов CD8+ периферической крови. PBMC могут быть обогащенными или обедненными относительно фракций CD62L-CD8+ и/или CD62L+CD8+, например, при использовании антител анти-CD8 и анти-CD62L.
[441] В некоторых вариантах осуществления, обогащение Т-лимфоцитами центральной памяти (TCM) основано на положительном или высоком поверхностном экспрессировании CD45RO, CD62L, CCR7, CD28, CD3 и/или CD 127; в некоторых аспектах, оно основано на отрицательной селекции относительно клеток, экспрессирующих или интенсивно экспрессирующих CD45RA и/или гранзим B. В некоторых аспектах, выделение популяции CD8+ обогащенной TCM-лимфоцитами, осуществляется посредством обеднения клеток, экспрессирующих CD4, CD14, CD45RA, и положительной селекции или обогащения клеток, экспрессирующих CD62L. В одном из аспектов, обогащение Т-лимфоцитов центральной памяти (TCM) осуществляется, начиная с отрицательной фракции клеток от селекции на основе экспрессирования CD4, которая подвергается отрицательной селекции на основе экспрессирования CD14 и CD45RA, и положительной селекции на основе CD62L. Такая селекция в некоторых аспектах осуществляется одновременно, а в других аспектах она осуществляется последовательно, в любом порядке. В некоторых аспектах, такая же стадия селекции на основе экспрессирования CD4, как используется при приготовлении популяции или субпопуляции клеток CD8+, также используется для генерирования популяции или субпопуляции клеток CD4+, так что как положительные, так и отрицательные фракции от разделения на основе CD4 удерживаются и используются на последующих стадиях способов, необязательно, после одной или нескольких дополнительных стадий положительной или отрицательной селекции.
[442] В конкретном примере, образец PBMC или образец других лейкоцитов подвергают селекции клеток CD4+, где удерживаются как отрицательные, так и положительные фракции. Затем отрицательная фракция подвергается отрицательной селекции на основе экспрессирования CD14 и CD45RA или CD19, и положительной селекции на основе характеристики маркера Т-лимфоцитов центральной памяти, такого как CD62L или CCR7, где положительная и отрицательная селекция осуществляется в любом порядке.
[443] Хелперные T-лимфоциты CD4+ сортируются на наивные клетки, клетки центральной памяти и эффекторные клетки посредством идентификации популяций клеток, которые имеют антигены на поверхности клеток. Лимфоциты CD4+ можно получить с помощью стандартных способов. В некоторых вариантах осуществления, наивные T-лимфоциты CD4+ представляют собой Т-лимфоциты CD45RO-, CD45RA+, CD62L+ и CD4+. В некоторых вариантах осуществления, клетки центральной памяти CD4+ являются CD62L+ и CD45RO+. В некоторых вариантах осуществления, эффекторные клетки CD4+ являются CD62L- и CD45RO-.
[444] В одном из примеров, для обогащения клеток CD4+ посредством отрицательной селекции, коктейль моноклональных антител, как правило, содержит антитела к CD14, CD20, CD11b, CD16, HLA-DR и CD8. В некоторых вариантах осуществления, антитело или партнер по связыванию связывается с твердой подложкой или матрицей, такой как магнитный шарик или парамагнитный шарик, чтобы сделать возможным разделение клеток для положительной и/или отрицательной селекции. Например, в некоторых вариантах осуществления, клетки и популяции клеток разделяются или выделяются с использованием технологий иммуномагнитного (или аффиномагнитного) разделения (обсуждается в Methods in Molecular Medicine, vol. 58: Metastasis Research Protocols, Vol. 2: Cell Behavior In vitro and In vivo, p 17-25 Edited by: S. A. Brooks and U. Schumacher © Humana Press Inc., Totowa, NJ).
[445] В некоторых аспектах, образец или композиция клеток, которая должна разделяться, инкубируется вместе с малым, намагниченным или магниточувствительным материалом, таким как магниточувствительные частицы или микрочастицы, такие как парамагнитные шарики (например, такие как шарики Dynalbeads или MACS). Магниточувствительный материал, например, частица, как правило, прямо или опосредованно присоединена к партнеру по связыванию, например, антителу, которое специфично связывается с молекулой, например, поверхностным маркером, присутствующим на клетке, в клетках или в популяции клеток, которую желательно разделить, например, которую желательно подвергнуть отрицательной или положительной селекции.
[446] В некоторых вариантах осуществления, магнитная частица или шарик содержит магниточувствительный материал, связанный со специфичным связывающим элементом, таким как антитело или другой партнер по связыванию. Имеется множество хорошо известных магниточувствительных материалов, используемых в способах магнитной сепарации. Пригодные для использования магнитные частицы включают частицы, описанные в Molday, патент США №4452773 и в описании Европейского патента EP 452342 B, которые тем самым включаются в качестве ссылок. Частицы коллоидных размеров, такие как частицы, описанные Owen, в патенте США №4795698 и Liberti et al., в патенте США №5200084 представляют собой другие примеры.
[447] Инкубирование, как правило, осуществляется при условиях, когда антитела или партнеров по связыванию или молекулы, такие как вторичные антитела или другие реагенты, которые специфично связываются с такими антителами или партнерами по связыванию, которые присоединены к магнитной частице или шарику, специфично связываются с молекулами на поверхности клетки, если они присутствуют на клетках в образце.
[448] В некоторых аспектах, образец помещается в магнитное поле, и клетки, имеющие магниточувствительные или намагниченные частицы, присоединенные к ним, будут присоединяться к магниту и отделяться от немеченых клеток. Для положительной селекции, клетки, которые присоединены к магниту, удерживаются; для отрицательной селекции, клетки, которые не присоединяются (немеченые клетки), удерживаются. В некоторых аспектах, сочетание положительной и отрицательной селекции осуществляется в ходе одной и той же стадии селекция, где положительные и отрицательные фракции удерживаются, а затем процессируются или подвергаются воздействию дополнительных стадий разделения.
[449] В определенных вариантах осуществления, магниточувствительные частицы покрываются первичными антителами или другими партнерами по связыванию, вторичными антителами, лектинами, ферментами или стрептавидинов. В определенных вариантах осуществления, магнитные частицы присоединяются к клеткам посредством покрытия из первичных антител специфичных к одному или нескольким маркерам. В определенных вариантах осуществления, клетки, вместо шариков, метятся первичным антителом или партнером по связыванию, а затем добавляют магнитные частицы с покрытием из вторичного антитела специфичного к типу клеток или к другим партнерам по связыванию (например, стрептавидину). В определенных вариантах осуществления, магнитные частицы, покрытые стрептавидином, используются в сочетании с биотинилированными первичными или вторичными антителами.
[450] В некоторых вариантах осуществления, магниточувствительные частицы оставляют присоединенными к клеткам, которые впоследствии должны инкубироваться, культивироваться и/или подвергаться воздействию генной инженерии; в некоторых аспектах, частицы оставляют присоединенными к клеткам для введения пациенту. В некоторых вариантах осуществления, намагничиваемые или магниточувствительные частицы удаляют с клеток. Способы удаления намагничиваемых частиц с клеток известны и включают, например, применение конкурентных немеченых антител и намагничиваемых частиц или антител, конъюгированных с расщепляемыми линкерами. В некоторых вариантах осуществления, намагничиваемые частицы являются биодеградируемыми.
[451] В некоторых вариантах осуществления, селекция на основе аффиности осуществляется посредством сортинга магнитных-активированных клеток (MACS) (Miltenyi Biotec, Auburn, CA). Системы сортинга магнитных активированных клеток (MACS) могут осуществлять селекцию клеток высокой чистоты, имеющих намагниченные частицы, присоединенные к ним. В определенных вариантах осуществления, MACS работает в режиме, где нецелевые и целевые частицы последовательно элюируются после приложения внешнего магнитного поля. То есть, клетки, присоединенные к намагничиваемым частицам, удерживают на месте, в то время как неприсоединенные частицы элюируются. Затем, после завершения этой первой стадии элюирования, частицы, которые захватываются в магнитном поле и не могут элюироваться, высвобождаются некоторым образом, так что их можно элюировать и извлечь. В определенных вариантах осуществления, нецелевые клетки метятся и обедняются из гетерогенной популяции клеток.
[452] В определенных вариантах осуществления, выделение или разделение осуществляется с использованием системы, устройства или аппарата, которое осуществляет одну или несколько стадий способов из выделения, подготовки клеток, разделения, процессинга, инкубирования, культивирования и/или приготовления. В некоторых аспектах, система используется для осуществления каждой из этих стадий в замкнутой или стерильной окружающей среде, например, для сведения к минимуму ошибки, манипуляций пользователя и/или загрязнения. В одном из примеров, система представляет собой систему, как описано в Международной публикации заявки на патент, номер WO 2009/072003 или в заявке на патент США US 20110003380 A1. В одном из примеров, система представляет собой систему, как описано в Международной публикации номер WO 2016/073602.
[453] В некоторых аспектах, разделение и/или другие стадии осуществляется с использованием системы CliniMACS (Miltenyi Biotec), например, для автоматизированного разделения клеток на уровне клинического масштаба в замкнутой и стерильной системе. Компоненты могут включать встроенный микрокомпьютер, узел магнитной сепарации, перистальтический насос и различные клапаны с зажимами. Встроенный компьютер в некоторых аспектах контролирует все компоненты инструмента и направляет систему на осуществление повторяющихся процедур в стандартизированной последовательности. Узел магнитной сепарации в некоторых аспектах содержит подвижный постоянный магнит и держатель для селекционной колонки. Перистальтический насос контролирует скорость потока через набор трубок и вместе с клапанами с зажимами обеспечивает контролируемый поток буфера через систему и непрерывное суспендирование клеток.
[454] В некоторых аспектах система CliniMACS использует связанные с антителом намагничиваемые частицы, которые подаются в стерильном, непирогенном растворе. В некоторых вариантах осуществления, после мечения клеток магнитными частицами, клетки промывают для удаления избытка частиц. Затем мешок для приготовления клеток соединяется с набором трубок, который, в свою очередь, соединяется с мешком, содержащим буфер, и с мешком для сбора клеток. Набор трубок состоит из предварительно собранного стерильного трубопровода, включая предварительную колонку и разделительную колонку, и они предназначены только для одноразового использования. После начала программы разделения, система автоматически вводит образец клеток в разделительную колонку. Меченые клетки удерживаются в колонке, в то время как немеченые клетки удаляются с помощью ряда стадий промывки. В некоторых вариантах осуществления, популяции клеток для использования вместе со способами, описанными в настоящем документе, являются немечеными и не удерживаются в колонке. В некоторых вариантах осуществления, популяции клеток для использования вместе со способами, описанными в настоящем документе, являются мечеными и удерживаются в колонке. В некоторых вариантах осуществления, популяции клеток для использования вместе со способами, описанными в настоящем документе, элюируются из колонки после удаления магнитного поля и собираются в мешке для сбора клеток.
[455] В определенных вариантах осуществления, разделение и/или другие стадии осуществляются с использованием системы CliniMACS Prodigy (Miltenyi Biotec). В некоторых аспектах система CliniMACS Prodigy снабжается узлом процессинга клеток, который делает возможным автоматическую промывку и фракционирование клеток посредством центрифугирования. Система CliniMACS Prodigy может также содержать встроенную камеру и программное обеспечение для распознавания изображений, которая определяет оптимальную конечную точку фракционирования клеток посредством распознавания макроскопических слоев продукта исходных клеток. Например, периферическая кровь автоматически разделяется на слои эритроцитов, лейкоцитов и плазмы. Система CliniMACS Prodigy может также содержать встроенную камеру для культивирования клеток, которая осуществляет протоколы культивирования клеток, такие, например, как дифференциация и размножение клеток, нагрузка антигена и долговременное культивирование клеток. Входные порты могут сделать возможным стерильное удаление и пополнение сред, и клетки могут отслеживаться с использованием встроенного микроскопа. Смотри, например, Klebanoff et al. (2012) J Immunother. 35(9): 651-660, Terakura et al. (2012) Blood, 1:72-82 и Wang et al. (2012) J Immunother. 35(9):689-701.
[456] В некоторых вариантах осуществления, популяция клеток, описанная в настоящем документе, собирается и обогащается (или обедняется) с помощью проточной цитометрии, при которой клетки, окрашенные на множество клеточных поверхностных маркеров, переносятся в потоке текучей среды. В некоторых вариантах осуществления, популяция клеток, описанная в настоящем документе, собирается и обогащается (или обедняется) посредством препаративного (FACS)-сортинга. В определенных вариантах осуществления, популяция клеток, описанная в настоящем документе, собирается и обогащается (или обедняется) с использованием чипов микроэлектромеханических систем (MEMS) в сочетании с системой детектирования на основе FACS (смотри, например, WO 2010/033140, Cho et al. (2010) Lab Chip 10, 1567-1573; и Godin et al. (2008) J Biophoton. 1(5):355-376. В обеих случаях, клетки могут метится с помощью множества маркеров, делая возможным выделение хорошо определенных подмножеств Т-лимфоцитов с высокой чистотой.
[457] В некоторых вариантах осуществления, антитела или партнеры по связыванию метятся одним или несколькими детектируемыми маркерами, для облегчения разделения для положительной и/или отрицательной селекции. Например, разделение может основываться на связывании с флуоресцентно мечеными антителами. В некоторых примерах, разделение клеток на основе связывания антител или других партнеров по связыванию специфичных к одному или нескольким клеточным поверхностным маркерам осуществляется в потоке текучей среды, например, посредством сортинга флуоресцентных-активированных клеток (FACS), включая препаративный (FACS) и/или чипы микроэлектромеханических систем (MEMS), например, в сочетании с системой проточного цитометрического детектирования. Такие способы делают возможной положительную и отрицательную селекцию на основе множества маркеров одновременно.
[458] В некоторых вариантах осуществления, клетки активируются или стимулируются перед одной или несколькими стадиями генной инженерии клеток, например, посредством трансдуцирования или трансфицирования клеток. В конкретных вариантах осуществления, клетки культивируют или инкубируют при условиях стимуляции перед одной или несколькими стадиями генной инженерии клеток. В некоторых вариантах осуществления, условия агенты стимуляции или включают один или несколько агентов, например, лигандов, которые могут активировать внутриклеточный сигнальный домен комплекса TCR. В некоторых аспектах, агент включает или инициирует внутриклеточный сигнальный каскад TCR/CD3 в Т-лимфоците. Такие агенты могут содержать антитела, например, специфичные к TCR, например, анти-CD3. В некоторых вариантах осуществления, условия стимуляции включают один или несколько агентов, например, лиганд, который может стимулировать костимуляторный рецептор, например, анти-CD28. В некоторых вариантах осуществления, такие агенты и/или лиганды могут связываться с твердой подложкой, такой как шарик и/или представлять собой один или несколько цитокинов. Необязательно, активация или стимуляция может дополнительно включать стадию добавления антитела анти-CD3 и/или анти-CD28 в культурную среду (например, при концентрации, по меньшей мере, примерно 0,5 нг/мл). В некоторых вариантах осуществления, стимулирующие агенты включают IL-2, IL-15 и/или IL-7. В некоторых аспектах, концентрация IL-2 составляет, по меньшей мере, примерно 10 единиц/мл.
B. Нуклеиновая кислота, кодирующая гетерологичный белок
[459] Также предлагается один или несколько полинуклеотидов (например, молекул нуклеиновой кислоты), кодирующих рекомбинантные рецепторы, векторы для генной инженерии клеток для экспрессирования таких рецепторов и способы продуцирования генно-инженерных клеток. В некоторых вариантах осуществления, вектор содержит нуклеиновую кислоту, кодирующую рекомбинантный рецептор. В конкретных вариантах осуществления, вектор представляет собой вирусный вектор или невирусный вектор. В некоторых случаях, вектор представляет собой вирусный вектор, такой как ретровирусный вектор, например, лентивирусный вектор или гамма ретровирусный вектор.
[460] В некоторых вариантах осуществления, клетки приводятся в контакт с вектором без предварительной активации клеток и/или в пределах периода времени, который начинается не более, чем через 24 часа после получения клеток от субъекта и/или при этом клетки не подвергаются воздействию температуры больше 15°C - 25°C, например, больше, чем или больше примерно, чем 37° ± 2,0°C, в течение не более 24 часов после того клетки получают от субъекта. В определенных вариантах осуществления, вектор приводится в контакт с клетками без первой, то есть предваряющей генную инженерию (например, трансдуцирование или трансфицирование) активации и/или стимуляции Т-лимфоцитов ex vivo стимуляционным реагентом (например, реагентом анти-CD3/анти-CD28) до приведения в контакт или инкубирования клеток вместе с вирусными частицами и/или в сочетании с ними. В некоторых вариантах осуществления, векторы включают вирусные векторы, например, ретровирусные или лентивирусные, невирусные векторы или транспозоны, например, систему транспозонов Sleeping Beauty, векторы, полученные от вируса обезьян 40 (SV40), аденовирусов, аденоассоциированного вируса (AAV), лентивирусных векторов или ретровирусных векторов, таких как гамма-ретровирусные векторы, ретровирусный вектор, полученный из вируса лейкемии Молони мышиных (MoMLV), вируса миелопролиферативной саркомы (MPSV), вируса эмбриональных стволовых клеток мышиных (MESV), вируса стволовых клеток мышиных (MSCV), вируса некроза селезенки (SFFV) или аденоассоциированного вируса (AAV).
[461] В некоторых вариантах осуществления, вирусный вектор или невирусная ДНК содержит нуклеиновую кислоту, которая кодирует гетерологичный рекомбинантный белок. В некоторых вариантах осуществления, гетерологичная рекомбинантная молекула представляет собой или содержит рекомбинантный рецептор, например, рецептор антигена, SB-транспозоны, например, для сайленсинга гена, заключенные в капсиды транспозоны, гомологичную двухнитевую нуклеиновую кислоту, например, для геномной рекомбинации или репортерные гены (например, флуоресцентные белки, такие как GFP или люциферазу).
[462] В некоторых вариантах осуществления, вирусный вектор или невирусная ДНК содержит нуклеиновую кислоту, которая кодирует рекомбинантный рецептор и/или химерный рецептор, такой как белок гетерологичного рецептора. Рекомбинантный рецептор, такой как гетерологичный рецептор, может включать рецепторы антигенов, такие как функциональные рецепторы антигенов, отличные от TCR, включая химерные рецепторы антигенов (CAR) и другие антигенсвязывающие рецепторы, такие как рецепторы трансгенных Т-лимфоцитов (TCR). Рецепторы могут также включать другие рецепторы, такие как другие химерные рецепторы, такие как рецепторы, которые связываются с конкретными лигандами и имеют трансмембранные и/или внутриклеточные сигнальные домены сходные с теми, которые присутствуют в CAR.
[463] В некоторых вариантах осуществления, нуклеиновая кислота вставляется или располагается в области вирусного вектора, например, как правило, в неосновной области вирусного генома. В некоторых вариантах осуществления, нуклеиновая кислота вставляется в вирусный геном вместо определенных вирусных последовательностей для получения вируса, который является репликационно-дефектным. В определенных вариантах осуществления, нуклеиновая кислота располагается в невирусной ДНК, например, в транспозоне.
[464] Рецепторы антигенов, включая CAR и рекомбинантные TCR, и их продуцирование и перенос, в некоторых вариантах осуществления, включают рецепторы, описанные, например, в Международных публикациях заявок на патент, номера WO 200014257, WO 2013126726, WO 2012/129514, WO 2014031687, WO 2013/166321, WO 2013/071154, WO 2013/123061, в публикациях заявок на патент США, номера US 2002131960, US 2013287748, US 20130149337, в патентах США №№:6451995, 7446190, 8252592, 8339645, 8398282, 7446179, 6410319, 7070995, 7265209, 7354762, 7446191, 8324353 и 8479118, и в заявке на Европейский патент номер EP 2537416, и/или те, которые описаны Sadelain et al., Cancer Discov. 2013 April; 3(4): 388-398; Davila et al. (2013) PLoS ONE 8(4): e61338; Turtle et al., Curr. Opin. Immunol., 2012 October; 24(5): 633-39; Wu et al., Cancer, 2012 March 18(2): 160-75.
1. Химерный рецептор антигена
[465] В некоторых вариантах осуществления, предлагаются генно-инженерные клетки, такие как Т-лимфоциты, которые экспрессируют CAR со специфичностью к конкретному антигену (или маркеру или лиганду), такому как антиген, экспрессируемый на поверхности конкретного типа клеток. В некоторых вариантах осуществления, антиген представляет собой полипептид. В некоторых вариантах осуществления, он представляет собой углевод или другую молекулу. В некоторых вариантах осуществления, антиген селективно экспрессируется или сверхэкспрессируется на клетках заболевания или состояния, например, опухоли, или на патогенных клетках, по сравнению с нормальными или нецелевыми клетками, или тканями. В других вариантах осуществления, антиген экспрессируется на нормальных клетках и/или экспрессируется на генно-инженерных клетках.
[466] В конкретных вариантах осуществления, рекомбинантный рецептор, такой как химерный рецептор, содержит внутриклеточную сигнальную область, которая включает цитоплазматический сигнальный домен (также взаимозаменяемо называемый внутриклеточным сигнальным доменом), такую как цитоплазматическая (внутриклеточная) область, которая может индуцировать первичный активационный сигнал в Т-лимфоците, например, цитоплазматический сигнальный домен компонента рецептора Т-лимфоцита (TCR) (например, цитоплазматический сигнальный домен зета цепи CD3-зета (CD3ζ) цепи или ее функционального варианта или сигнальной части) и/или который содержит иммунорецепторный тирозиновый актирующий мотив (ITAM).
[467] В некоторых вариантах осуществления, химерный рецептор дополнительно содержит внеклеточный лигандсвязывающий домен, который специфично связывается с лигандом антигена (например, антигеном). В некоторых вариантах осуществления, химерный рецептор представляет собой CAR, который содержит внеклеточный антигенраспознающий домен, который специфично связывается с антигеном. В некоторых вариантах осуществления, лиганд, такой как антиген, представляет собой белок, экспрессируемый на поверхности клеток. В некоторых вариантах осуществления, CAR представляет собой TCR-подобный CAR и антиген представляет собой процессированный пептидный антиген, такой как пептидный антиген внутриклеточного белка, который, подобно TCR, распознается на клеточной поверхности в контексте молекулы главного комплекса гистосовместимости (MHC).
[468] Иллюстративные рецепторы антигенов, включая CAR, и способы генной инженерии и переноса таких рецепторов в клетки включают рецепторы, описанные, например, в Международных публикациях заявок на патент, номера WO 200014257, WO 2013126726, WO 2012/129514, WO 2014031687, WO 2013/166321, WO 2013/071154, WO 2013/123061, в публикациях заявок на патент США, номера US 2002131960, US 2013287748, US 20130149337, в патентах США №№:6451995, 7446190, 8252592, 8339645, 8398282, 7446179, 6410319, 7070995, 7265209, 7354762, 7446191, 8324353 и 8479118, и в заявке на Европейский патент номер EP 2537416, и/или описанные в Sadelain et al., Cancer Discov. 2013 April; 3(4): 388-398; Davila et al. (2013) PLoS ONE 8(4): e61338; Turtle et al., Curr. Opin. Immunol., 2012 October; 24(5): 633-39; Wu et al., Cancer, 2012 March 18(2): 160-75. В некоторых аспектах, рецепторы антигенов включают CAR, как описано в патенте США №:7446190, и описанные в Международной публикации заявки на патент, номер: WO/2014055668 A1. Примеры CAR включают CAR, как описано в любой из рассмотренных выше публикаций, например, в WO 2014031687, US 8339645, US 7446179, US 2013/0149337, патент США №:7446190, патент США №:8389282, Kochenderfer et al., 2013, Nature Reviews Clinical Oncology, 10, 267-276 (2013); Wang et al. (2012) J. Immunother. 35(9): 689-701; и Brentjens et al., Sci Transl Med. 2013 5(177). Смотри также WO 2014031687, патент США №8339645, патент США №7446179, патент США №2013/0149337, патент США №:7446190 и патент США №:8389282.
[469] В некоторых вариантах осуществления, CAR конструируется со специфичностью к конкретному антигену (или маркеру или лиганду), такому как антиген, экспрессируемый в конкретном типе клеток, которые должны быть целевыми для адоптивной терапии, например, онкомаркер и/или антиген, предназначенный для демпфирования реакции, такой как антиген, экспрессируемый на нормальном или неболезненном типе клеток. Таким образом, CAR как правило, содержит в своей внеклеточной части одну или несколько антигенсвязывающих молекул, таких как один или несколько антигенсвязывающих фрагментов доменов или частей, или один или несколько вариабельных доменов антител и/или молекул антител. В некоторых вариантах осуществления, CAR содержит антигенсвязывающую часть или части молекулы антитела, например, одноцепочечный фрагмент антитела (scFv), полученный из вариабельной области тяжелой (VH) и вариабельной области легкой (VL) цепи моноклонального антитела (mAb).
[470] В некоторых вариантах осуществления, антитело или его антигенсвязывающая часть экспрессируется на клетках как часть рекомбинантного рецептора, такого как рецептор антигена. Среди рецепторов антигенов имеются функциональные рецепторы антигенов, отличные от TCR, такие как химерные рецепторы антигенов (CAR). Как правило, CAR, содержащий антитело или антигенсвязывающий фрагмент, который демонстрирует TCR-подобную специфичность, направленную против комплексов пептид-MHC, также может упоминаться как TCR-подобный CAR. В некоторых вариантах осуществления, внеклеточный антигенсвязывающий домен специфичный к комплексу MHC-пептид TCR-подобного CAR связан с одним или несколькими внутриклеточными сигнальными компонентами, в некоторых аспектах, через линкеры и/или трансмембранный домен (домены). В некоторых вариантах осуществления, такие молекулы, как правило, могут воспроизводить или примерно воспроизводить сигнал через природный рецептор антигена, такой как TCR, и, необязательно, сигнал через такой рецептор в сочетании с костимуляторным рецептором.
[471] В некоторых вариантах осуществления, рекомбинантный рецептор, такой как химерный рецептор (например, CAR), содержит лигандсвязывающий домен, который связывается, например, специфично связывается с антигеном (или лигандом). Среди антигенов целевых для химерных рецепторов имеются антигены, экспрессируемые в контексте заболевания, состояния или типа клеток, который должен целевым при адоптивной клеточной терапии. Среди заболеваний и состояний имеются пролиферативные, неопластические и злокачественные заболевания и расстройства, включая раковые заболевания и опухоли, включая гематологические раковые заболевания, раковые заболевания иммунной системы, такие как лимфомы, лейкозы и/или миеломы, такие как B-, T- и миелоидные лейкозы, лимфомы, и множественные миеломы.
[472] В некоторых вариантах осуществления, антиген (или лиганд) представляет собой полипептид. В некоторых вариантах осуществления, он представляет собой углевод или другую молекулу. В некоторых вариантах осуществления, антиген (или лиганд) селективно экспрессируется или сверхэкспрессируется на клетках заболевания или состояния, например, опухоли, или на патогенных клетках, по сравнению с нормальными или нецелевыми клетками или тканями. В других вариантах осуществления, антиген экспрессируется на нормальных клетках и/или экспрессируется на генно-инженерных клетках.
[473] В некоторых вариантах осуществления, CAR содержит антитело или антигенсвязывающий фрагмент (например, scFv), который специфично распознает антиген, такой как интактный антиген, экспрессируемый на поверхности клетки.
[474] В некоторых вариантах осуществления, антиген представляет собой или включает интегрин αvβ6 (интегрин avb6), антиген созревания В-клеток (BCMA), B7-H3, B7-H6, угольную ангидразу 9 (CA9, также известную как CAIX или G250), антиген рака яичек, раково-тестикулярный антиген 1B (CTAG, также известный как NY-ESO-1 и LAGE-2), канцероэмбриональный антиген (CEA), циклин, циклин A2, лиганд 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD133, CD138, CD171, протеогликан хондроитин-4-сульфат (CSPG4), белок эпидермального фактора роста (EGFR), мутация рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиальный гликопротеин 2 (EPG-2), эпителиальный гликопротеин 40 (EPG-40), эфринВ2, рецептор эфрина A2 (EPHa2), рецептор эстрогена, белок 5 подобный Fc-рецептору (FCRL5; также известный как гомолог 5 Fc-рецептора или FCRH5), рецептор фетального ацетилхолина (фетальный AchR), фолатсвязывающего белка (FBP), рецептор фолата альфа, ганглиозид GD2, O-ацетилированный GD2 (OGD2), ганглиозид GD3, гликопротеин 100 (gp100), глипикан-3 (GPC3), связанный с белком G рецептор 5D (GPRC5D), Her2/neu (тирозинкиназный рецептор erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеры erbB, высокомолекулярный антиген человека, ассоциированный с меланомой (HMW-MAA), поверхностный антиген гепатита B, антиген лейкоцита человека A1 (HLA-A1), антиген лейкоцита человека A2 (HLA-A2), рецептор IL-22 альфа(IL-22Rα), рецептор IL-13 альфа 2 (IL-13Rα2), домен рецептора вставки киназы (kdr), легкую цепь каппа, молекулу клеточной адгезии L1 (L1-CAM), эпитоп CE7 L1-CAM, обогащенный лейцином повтор, содержащее член A семейство 8 (LRRC8A), антиген Ley, антиген, ассоциированный с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, MAGE-A10, мезотелин (MSLN), c-Met, цитомегаловирус мышей (CMV), муцин 1 (MUC1), MUC16, лиганды элемента D группы природных киллеров 2 (NKG2D), мелан A (MART-1), молекула адгезии нейральных клеток (NCAM), онкофетальный антиген, предпочтительно экспрессируемый антиген меланомы (PRAME), рецептор прогестерона, простата-специфичный антиген, антиген стволовых клеток простаты (PSCA), простата-специфичный мембранный антиген (PSMA), орфанный рецептор 1 подобный тирозинкиназному рецептору (ROR1), сурвивин, гликопротеин трофобластов (TPBG также известный как 5T4), ассоциированный с опухолью гликопротеин 72 (TAG72), тирозиназа-зависимый белок 1 (TRP1, также известный как TYRP1 или gp75), тирозиназа-зависимый белок 2 (TRP2, также известный как допахромтаутомераза, допахром-дельта-изомераза или DCT), рецептор фактора роста эндотелия сосудов (VEGFR), рецептор 2 фактора роста эндотелия сосудов (VEGFR2), опухоль Вильмса 1 (WT-1), патоген-специфичный или патоген-экспрессируемый антиген или антиген, ассоциированный с универсальной меткой, и/или биотинилированные молекулы, и/или молекулы, экспрессируемые HIV, HCV, HBV или другими патогенами. Антигены целевые для рецепторов в некоторых вариантах осуществления включают антигены, ассоциируемые с В-клеточным лейкозом, такие как любой из ряда известных маркеров В-клеток. В некоторых вариантах осуществления, антиген представляет собой или содержит CD20, CD19, CD22, ROR1, CD45, CD21, CD5, CD33, Ig каппаа, Ig лямбда, CD79a, CD79b или CD30.
[475] В некоторых вариантах осуществления, антиген представляет собой патоген-специфичный антиген. В некоторых вариантах осуществления, антиген представляет собой вирусный антиген (такой как вирусный антиген от HIV, HCV, HBV, и тому подобное), бактериальные антигены, и/или паразитарные антигены.
[476] В некоторых вариантах осуществления, CAR содержит TCR-подобное антитело, такое как антитело или антигенсвязывающий фрагмент (например, scFv), который специфично распознает внутриклеточный антиген, такой как антиген, ассоциированный с опухолью, презентированный на поверхности клетки как комплекс MHC-пептид. В некоторых вариантах осуществления, антитело или его антигенсвязывающая часть, которая распознает комплекс MHC-пептид, может экспрессироваться на клетках как часть рекомбинантного рецептора, такого как рецептор антигена. Среди рецепторов антигенов имеются функциональные рецепторы антигенов отличные от TCR, такие как химерные рецепторы антигенов (CAR). Как правило, CAR, содержащий антитело или антигенсвязывающий фрагмент, который демонстрирует TCR-подобную специфичность, направленную против комплексов пептид-MHC, также может упоминаться как TCR-подобный CAR.
[477] Упоминание “главного комплекса гистосовместимости” (MHC) относится к белку, как правило, гликопротеину, который содержит полиморфный сайт связывания пептида или связывающую бороздку, которая может, в некоторых случаях, образовывать комплекс с пептидными антигенами полипептидов, включая пептидные антигены, процессируемые с помощью клеточного аппарата. В некоторых случаях, молекулы MHC могут проявляться или экспрессироваться на поверхности клетки, в том числе как комплекс с пептидом, то есть комплекс MHC-пептид, для презентирования антигена в конформации, распознаваемой рецептором антигена на Т-лимфоцитах, таким как TCR или TCR-подобное антитело. Как правило, молекулы MHC класса I представляют собой гетеродимеры, имеющие α цепь, простирающуюся по мембране, в некоторых случаях, с тремя α доменами, и нековалентно ассоциированный β2 микроглобулин. Как правило, молекулы MHC класса II состоят из двух трансмембранных гликопротеинов, α и β, которые оба, как правило, простираются по мембране. Молекула MHC может содержать эффективную часть MHC, которая содержит сайт связывания антигена или сайты для связывания пептида и последовательностей, необходимых для распознавания соответствующим рецептором антигена. В некоторых вариантах осуществления, молекулы MHC класса I доставляют пептиды, возникающие в цитозоле, к поверхности клетки, где комплекс MHC-пептид распознается Т-лимфоцитами, как правило, такими как Т-лимфоциты CD8+, но в некоторых случаях, Т-лимфоцитами CD4+. В некоторых вариантах осуществления, молекулы MHC класса II доставляют пептиды, возникающие в везикулярной системе, к поверхности клетки, где они, как правило, распознаются Т-лимфоцитами CD4+. Как правило, молекулы MHC кодируются группой связанных локусов, которые коллективно называются H-2 у мышей и лейкоцитарный антиген человека (HLA) у людей. Следовательно, как правило, MHC человека может также упоминаться как лейкоцитарный антиген человека (HLA).
[478] Термин “комплекс MHC-пептид” или “комплекс пептид-MHC”, или его варианты относятся к комплексу или ассоциации пептидного антигена и молекулы MHC, как правило, например, с помощью нековалентных взаимодействий пептида в связывающей бороздке или углублении молекулы MHC. В некоторых вариантах осуществления, комплекс MHC-пептид присутствует или проявляется на поверхности клеток. В некоторых вариантах осуществления, комплекс MHC-пептид может специфично распознаваться рецептором антигена, таким как TCR, TCR-подобный CAR или их антигенсвязывающие части.
[479] В некоторых вариантах осуществления, пептид, такой как пептидный антиген или эпитоп полипептида, может ассоциироваться с молекулой MHC, например, для распознавания рецептором антигена. Как правило, пептид получают из фрагмента более длинной биологической молекулы, такой как полипептид или белок, или на ее основе. В некоторых вариантах осуществления, пептид, как правило, имеет длину примерно от 8 примерно до 24 аминокислот. В некоторых вариантах осуществления, пептид имеет длину от или примерно от 9 до 22 аминокислот для распознавания комплекса MHC класса II. В некоторых вариантах осуществления, пептид имеет длину от или примерно от 8 до 13 аминокислот для распознавания комплекса MHC класса I. В некоторых вариантах осуществления, при распознавании пептида в контексте молекулы MHC, такой как комплекс MHC-пептид, рецептор антигена, такой как TCR или TCR-подобный CAR, производит или запускает сигнал активации для Т-лимфоцита, который индуцирует реакцию Т-лимфоцита, такую как пролиферация Т-лимфоцита, продуцирование цитокинов, цитотоксичная реакция Т-лимфоцита или другая реакция.
[480] В некоторых вариантах осуществления, TCR-подобное антитело или его антигенсвязывающая часть известны или могут быть получены с помощью способов известных в данной области (смотри, например, опубликованные заявки на патент США №№ US 2002/0150914; US 2003/0223994; US 2004/0191260; US 2006/0034850; US 2007/00992530; US 20090226474; US 20090304679; и Международную публикацию PCT № WO 03/068201).
[481] В некоторых вариантах осуществления, антитело или его антигенсвязывающая часть, которая специфично связывается с комплексом MHC-пептид, может быть получена посредством иммунизации хозяина эффективным количеством иммуногена, содержащего конкретный комплекс MHC-пептид. В некоторых случаях, пептид комплекса MHC-пептид представляет собой эпитоп антигена, который может связываться с MHC, такого как антиген опухоли, например, универсальный антиген опухоли, антиген миеломы или другой антиген, как описано ниже. В некоторых вариантах осуществления, эффективное количество иммуногена затем вводится хозяину, чтобы вызвать иммунную реакцию, при этом иммуноген поддерживает свою трехмерную форму в течение периода времени достаточного, чтобы вызвать иммунную реакцию против трехмерной презентации пептида в связывающей бороздке молекулы MHC. Сыворотку, собранную у хозяина, затем анализируют для определения того, продуцируются ли желаемые антитела, которые распознают трехмерную презентацию пептида в связывающей бороздке молекулы MHC. В некоторых вариантах осуществления, продуцируемые антитела могут оцениваться для подтверждения того, что антитело может дифференцировать комплекс MHC-пептид от самой молекулы MHC, самого рассматриваемого пептида и комплекса MHC и иррелевантного пептида. Затем желаемые антитела могут выделяться.
[482] В некоторых вариантах осуществления, антитело или его антигенсвязывающая часть, которая специфично связывается с комплексом MHC-пептид, может продуцироваться посредством использования способов дисплея библиотеки антител, таких как фаговые библиотеки антител. В некоторых вариантах осуществления, библиотеки фаговых дисплеев могут генерироваться, например, из мутантных Fab, scFv или других форм антитела, в них элементы библиотеки мутируют на одном или нескольких остатках CDR или нескольких CDR. Смотри, например, опубликованные заявки на патент США № US 20020150914, US 2014/0294841; и Cohen CJ. et al. (2003) J Methods, Recogn. 16:324-332.
[483] Термин “антитело” в настоящем документе используется в самом широком смысле и включает поликлональные и моноклональные антитела, включая интактные антитела и функциональные (антигенсвязывающие) фрагменты антител, включая антигенсвязывающие фрагменты (Fab), фрагменты F(ab')2, фрагменты Fab', рекомбинантные фрагменты IgG (rIgG), вариабельные области (VH) тяжелой цепи, которые могут специфично связывать антиген, одноцепочечные фрагменты антител, включая одноцепочечные вариабельные фрагменты (scFv), и однодоменные фрагменты антител (например, sdAb, sdFv, нанотело). Термин охватывает генно-инженерные и/или иным образом модифицированные формы иммуноглобулинов, такие как интратела, пептитела, химерные антитела, полностью человеческие антитела, гуманизированные антитела и гетероконъюгированные антитела, мультиспецифичные, например, биспецифичные, антитела, диатела, триатела и тетратела, тандемные ди-scFv, тандемные три-scFv. Если не утверждается иного, термин “антитело” должен, как понимается, охватывать антитело и его функциональные фрагменты. Термин также охватывает интактные или полноразмерные антитела, включая антитела любого класса или подкласса, включая IgG и его подклассы, IgM, IgE, IgA и IgD.
[484] В некоторых вариантах осуществления, антигенсвязывающие белки, антитела и их антигенсвязывающие фрагменты специфично распознают антиген полноразмерного антитела. В некоторых вариантах осуществления, тяжелые и легкие цепи антитела могут быть полноразмерными или могут представлять собой антигенсвязывающую часть (Fab, F(ab')2, Fv или одноцепочечный фрагмент Fv (scFv)). В других вариантах осуществления, константная область тяжелой цепи антитела выбирается, например, из IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE, в частности, выбирается, например, из IgG1, IgG2, IgG3, и IgG4, более конкретно, из IgG1 (например, IgG1 человека). В другом варианте осуществления, константная область легкой цепи антитела выбирается, например, из каппа, или лямбда, в частности, каппа.
[485] Среди предлагаемых антител имеются фрагменты антител. “Фрагмент антитела” относится к молекуле иной, чем интактное антитело, которая содержит часть интактного антитела, которая связывает антиген, с которым связывается интактное антитело. Примеры фрагментов антитела включают, но, не ограничиваясь этим, Fv, Fab, Fab', Fab'-SH, F(ab')2; диатела; линейные антитела; вариабельные области тяжелой цепи (VH), одноцепочечные молекулы антител, такие как scFv и однодоменные одинарные антитела VH; и мультиспецифичные антитела, сформированные из фрагментов антител. В конкретных вариантах осуществления, антитела представляют собой одноцепочечные фрагменты антител, содержащие вариабельную область тяжелой цепи и/или вариабельную область легкой цепи, такие как scFv.
[486] Термин “вариабельная область” или “вариабельный домен” относится к домену тяжелой или легкой цепи антитела, который участвует в связывании антитела с антигеном. Вариабельные домены тяжелой цепи и легкой цепи (VH и VL, соответственно) нативного антитела, как правило, имеют сходные структуры, при этом каждый домен содержит четыре консервативных каркасных области (FR) и три CDR. (смотри, например, Kindt et al. Kuby Immunology, 6th ed., W.H. Freem и Co., page 91 (2007). Домен из одной VH или VL может быть достаточным для придания антигенсвязывающей специфичности. Кроме того, антитела, которые связываются с конкретным антигеном, могут выделяться с использованием домена VH или VL антитела, который связывает антиген, для скрининга библиотеки комплементарных доменов VL или VH, соответственно. Смотри, например, Portolano et al., J. Immunol. 150:880-887 (1993); Clarkson et al., Nature 352:624-628 (1991).
[487] Однодоменные антитела представляют собой фрагменты антител, содержащие весь вариабельный домен тяжелой цепи или его часть, или весь вариабельный домен легкой цепи или его часть. В определенных вариантах осуществления, однодоменное антитело представляет собой однодоменное антитело человека. В некоторых вариантах осуществления, CAR содержит домен тяжелой цепи антитела, который специфично связывается с антигеном, таким как онкомаркер или клеточный поверхностный антиген клетки или заболевания, которое должно быть целевым, например, опухолевой клетки или раковой клетки, такой как любой из целевых антигенов, описанных в настоящем документе или известных в данной области.
[488] Фрагменты антител могут быть получены с помощью различных технологий, включая, но, не ограничиваясь этим, протеолитическое переваривание интактного антитела, а также продуцирование рекомбинантными клетками-хозяевами. В некоторых вариантах осуществления, антитела представляют собой рекомбинантно-продуцируемые фрагменты, такие как фрагменты, содержащие расположения, которые не встречаются в природе, например, с двумя или более областями, или цепями антитела, соединенными синтетическими линкерами, например, пептидными линкерами, и/или которые не могут быть получены посредством ферментативного переваривания, встречающегося в природе интактного антитела. В некоторых вариантах осуществления, фрагменты антител представляют собой scFv.
[489] “Гуманизированное” антитело представляет собой антитело, в котором все или, по существу, все остатки аминокислот CDR получают из CDR не человека, а все или, по существу, все остатки аминокислота FR получают из FR человека. Гуманизированное антитело необязательно, может содержать, по меньшей мере, часть константной области антитела, полученную из антитела человека. “Гуманизированная форма” антитела, не принадлежащего человеку, относится к варианту антитела, не принадлежащего человеку, которое подвергается гуманизации, как правило, для уменьшения иммуногенности для людей, в то же время сохраняя специфичность и аффиность родительского антитела, не принадлежащего человеку. В некоторых вариантах осуществления, некоторые остатки FR в гуманизированном антителе замещаются соответствующими остатками антитела, не принадлежащего человеку (например, антитела, из которого получают остатки CDR), например, для восстановления или улучшения специфичности, или аффиности антитела.
[490] Таким образом, в некоторых вариантах осуществления, химерный рецептор антигена, включая TCR-подобные CAR, содержит внеклеточную часть, содержащую антитело или фрагмент антитела. В некоторых вариантах осуществления, антитело или его фрагмент содержит scFv. В некоторых аспектах, химерный рецептор антигена содержит внеклеточную часть, содержащую антитело или его фрагмент, и внутриклеточную сигнальную область. В некоторых вариантах осуществления, внутриклеточная сигнальная область содержит внутриклеточный сигнальный домен. В некоторых вариантах осуществления, внутриклеточный сигнальный домен представляет собой или содержит первичный сигнальный домен, сигнальный домен, который может индуцировать первичный сигнал активации в Т-лимфоците, сигнальный домен компонента рецептора Т-лимфоцита (TCR) и/или сигнальный домен, содержащий иммунорецепторный тирозиновый активирующий мотив (ITAM).
[491] В некоторых вариантах осуществления, рекомбинантный рецептор, такой как CAR, например, часть его антитела, дополнительно включает спейсер, который может представлять собой или содержать по меньшей мере часть константной области иммуноглобулина или его варианта или его модифицированной версии, такую как шарнирная область, например, шарнирная область IgG4, и/или CH1/CL и/или Fc-область. В некоторых вариантах осуществления, рекомбинантный рецептор дополнительно содержит спейсерную и/или шарнирную область. В некоторых вариантах осуществления, константная область или часть относится к IgG человека, например, IgG4 или IgG1. В некоторых аспектах, часть константной области служит в качестве спейсерной области между антигенраспознающим компонентом, например, scFv и трансмембранным доменом. Спейсер может иметь длину, которая обеспечивает повышенную чувствительность клетки после связывания с антигеном, по сравнению с отсутствием спейсера. В некоторых примерах, спейсер имеет длину 12 или примерно 12 аминокислот или имеет длину не более 12 аминокислот. Иллюстративные спейсеры включают спейсеры, имеющие, по меньшей мере, примерно 10-229 аминокислот, примерно 10-200 аминокислот, примерно 10-175 аминокислот, примерно 10-150 аминокислот, примерно 10-125 аминокислот, примерно 10-100 аминокислот, примерно 10-75 аминокислот, примерно 10-50 аминокислот, примерно 10-40 аминокислот, примерно 10-30 аминокислот, примерно 10-20 аминокислот или примерно 10-15 аминокислот, и включая любое целое число между конечными точками любого из перечисленных диапазонов. В некоторых вариантах осуществления, спейсерная область имеет примерно 12 аминокислот или меньше, примерно 119 аминокислот или меньше, или примерно 229 аминокислот или меньше. Иллюстративные спейсеры включают шарнир IgG4 сам по себе, шарнир IgG4, связанный с доменами CH2 и CH3, или шарнир IgG4, связанный с доменом CH3. Иллюстративные спейсеры включают, но, не ограничиваясь этим, спейсеры, описанные в Hudecek et al. (2013) Clin. Cancer Res., 19:3153 или в Международной публикации заявки на патент номер WO 2014031687. В некоторых вариантах осуществления, спейсер имеет последовательность, приведенную в SEQ ID NO: 133, и кодируется последовательностью, приведенной в SEQ ID NO: 134. В некоторых вариантах осуществления, спейсер имеет последовательность, приведенную в SEQ ID NO: 135. В некоторых вариантах осуществления, спейсер имеет последовательность, приведенную в SEQ ID NO: 136.
[492] В некоторых вариантах осуществления, константная область или часть относится к IgD. В некоторых вариантах осуществления, спейсер имеет последовательность, приведенную в SEQ ID NO: 137. В некоторых вариантах осуществления, спейсер содержит последовательность аминокислот, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с любой из SEQ ID NOS: 133, 135, 136 и 137.
[493] Антигенраспознающий домен, как правило, связывается с одним или несколькими внутриклеточными сигнальными компонентами, такими как сигнальные компоненты, которые воспроизводят активацию через комплекс рецептора антигена, такой как комплекс TCR, в случае CAR, и/или сигнала через другой клеточный поверхностный рецептор. Таким образом, в некоторых вариантах осуществления, антигенсвязывающий компонент (например, антитело) связывается с одной или несколькими трансмембранными и внутриклеточными сигнальными областями. В некоторых вариантах осуществления, трансмембранный домен является слитым с внеклеточным доменом. В одном из вариантов осуществления используется трансмембранный домен, который в природе ассоциируется с одним из доменов в рецепторе, например, CAR. В некоторых случаях, трансмембранный домен селектируется или модифицируется посредством замещения аминокислот для предотвращения связывания таких доменов с трансмембранным доменами таких же или других поверхностных мембранных белков, для сведения к минимуму взаимодействий с другими элементами комплекса рецептора.
[494] В некоторых вариантах осуществления трансмембранный домен получают либо из природного, либо из синтетического источника. Когда источник природный, в некоторых аспектах, домен получают из любого мембранно-связанного или трансмембранного белка. Трансмембранные области включают области, полученные из (то есть они содержат, по меньшей мере, трансмембранную область (области) из) альфа, бета или зета цепи рецептора Т-лимфоцита, CD28, CD3 эпсилон, CD45, CD4, CD5, CD8, CD9, CD 16, CD22, CD33, CD37, CD64, CD80, CD86, CD 134, CD137, CD 154. Альтернативно, в некоторых вариантах осуществления трансмембранный домен является синтетическим. В некоторых аспектах, синтетический трансмембранный домен содержит в основном гидрофобные остатки, такие как лейцин и валин. В некоторых аспектах, триплет фенилаланина, триптофана и валина будет находиться на каждом конце синтетического трансмембранного домена. В некоторых вариантах осуществления, связь осуществляется с помощью линкеров, спейсеров и/или трансмембранного домена (доменов).
[495] Среди внутриклеточных сигнальных областей имеются такие, которые воспроизводят или примерно воспроизводят сигнал через природный рецептор антигена, сигнал через такой рецептор в сочетании с костимуляторным рецептором и/или сигнал через костимуляторный рецептор сам по себе. В некоторых вариантах осуществления, короткий олиго- или полипептидный линкер, например, линкер длиной в пределах между 2 и 10 аминокислотами, например, линкер, содержащий глицины и серины, например, дублет глицин-серин, присутствует и образует связь между трансмембранным доменом и цитоплазматическим сигнальным доменом CAR.
[496] Рецептор, например, CAR, как правило, содержит, по меньшей мере, один внутриклеточный сигнальный компонент или компоненты. В некоторых вариантах осуществления, рецептор содержит внутриклеточный компонент комплекса TCR, такой как CD3 цепь TCR, которая медиирует активацию и цитотоксичность Т-лимфоцита, например, цепь CD3 зета. Таким образом, в некоторых аспектах, антигенсвязывающий домен CAR связан с одним или несколькими клеточными сигнальными модулями. В некоторых вариантах осуществления, клеточные сигнальные модули включают трансмембранный домен CD3, внутриклеточные сигнальные домены CD3 и/или другие трансмембранные домены CD. В некоторых вариантах осуществления, рецептор, например, CAR, дополнительно содержит часть одной или нескольких дополнительных молекул, таких как Fc-рецептор γ, CD8, CD4, CD25 или CD16. Например, в некоторых аспектах, CAR содержит химерную молекулу между CD3-зета (CD3-ζ) или Fc-рецептором γ и CD8, CD4, CD25 или CD16.
[497] В некоторых вариантах осуществления, при лигировании CAR, цитоплазматический домен или внутриклеточная сигнальная область CAR активирует, по меньшей мере, одну из нормальных эффекторных функций или реакций иммунной клетки, например, генно-инженерного Т-лимфоцита, предназначенного для экспрессирования CAR. Например, в некоторых контекстах, CAR индуцирует функцию Т-лимфоцита, такую как цитолитическая активность или T-хелперная активность, такую как секретирование цитокинов или других факторов. В некоторых вариантах осуществления, усеченная часть внутриклеточной сигнальной области компонента рецептора антигена или костимуляторной молекулы используют вместо интактной иммуностимуляторной цепи, например, если она трансдуцирует сигнал эффекторной функции. В некоторых вариантах осуществления, внутриклеточные сигнальные области, например, содержащие внутриклеточный домен или домены, включают цитоплазматические последовательности рецептора Т-лимфоцита (TCR), а в некоторых аспектах, также те корецепторы, которые в природном контексте действуют согласованно с таким рецептором для инициирования трансдуцирования сигнала после зацепления с рецептором антигена, и/или любое производное или вариант таких молекул и/или любую синтетическую последовательность, которая имеет такую же функциональную возможность.
[498] В контексте природных TCR, полная активация, как правило, требует не только передачи сигналов через TCR, но также и костимуляторного сигнала. Таким образом, в некоторых вариантах осуществления, для облегчения полной активации, компонент для генерирования вторичного или костимуляторного сигнала также включается в CAR. В других вариантах осуществления, CAR не содержит компонента для генерирования костимуляторного сигнала. В некоторых аспектах, дополнительный CAR экспрессируется в этой же клетке и обеспечивает компонент для генерирования вторичного или костимуляторного сигнала.
[499] В некоторых аспектах описывается активация Т-лимфоцитов как медиируемая двумя классами цитоплазматических сигнальных последовательностей: одни инициируют антиген-зависимую первичную активацию через TCR (первичные цитоплазматические сигнальные последовательности), а другие действуют антиген-независимым образом обеспечивая вторичный или костимуляторный сигнал (вторичные цитоплазматические сигнальные последовательности). В некоторых аспектах, CAR содержит один или оба таких сигнальных компонента.
[500] В некоторых аспектах, CAR содержит первичную цитоплазматическую сигнальную последовательность, которая регулирует первичную активацию комплекса TCR. Первичные цитоплазматические сигнальные последовательности, которые действуют стимуляторным образом, могут содержать сигнальные мотивы, которые известны как иммунорецепторные тирозиновые актиирующие мотивы или ITAM. Примеры ITAM, содержащих первичные цитоплазматические сигнальные последовательности, включают мотивы, полученные из TCR или зета CD3, FcR гамма или FcR бета. В некоторых вариантах осуществления, цитоплазматическая сигнальная молекула (молекулы) в CAR содержит (содержат) цитоплазматический сигнальный домен, его часть или последовательность, полученную из CD3 зета.
[501] В некоторых вариантах осуществления, CAR содержит сигнальную область и/или трансмембранную часть костимуляторного рецептора, такую как CD28, 4-1BB, OX40, DAP10 и ICOS. В некоторых аспектах, этот же CAR содержит как сигнальную область, так и костимуляторные компоненты.
[502] В некоторых вариантах осуществления, сигнальная область заключена в одном CAR, в то время как костимуляторный компонент создается другим CAR, распознающим другой антиген. В некоторых вариантах осуществления, CAR включают активационные или стимуляторные CAR и костимуляторные CAR, и те, и другие экспрессируются на одной и той же клетке (смотри, WO 2014/055668).
[503] В определенных вариантах осуществления, внутриклеточная сигнальная область содержит трансмембранный и сигнальный домен CD28, соединенный с внутриклеточным доменом CD3 (например, CD3-зета). В некоторых вариантах осуществления, внутриклеточная сигнальная область содержит химерный домен CD28 и костимуляторный домен CD137 (4-1BB, TNFRSF9), соединенные с внутриклеточным доменом CD3 зета.
[504] В некоторых вариантах осуществления, CAR охватывает один или несколько, например, два или более, костимуляторных доменов, и активационный домен, например, первичный активационный домен, в цитоплазматической части. Иллюстративные CAR включают внутриклеточные компоненты CD3-зета, CD28 и 4-1BB.
[505] В некоторых случаях, CAR упоминается как первое, второе и/или третье поколение CAR. В некоторых аспектах, CAR первого поколение представляет собой рецептор, который обеспечивает только индуцируемый CD3-цепью сигнал при связывании антигена; в некоторых аспектах, CAR второго поколения представляет собой рецептор, который обеспечивает такой сигнал и костимуляторный сигнал, например, содержащий внутриклеточный сигнальный домен от костимуляторного рецептора, такого как CD28 или CD137; в некоторых аспектах, CAR третьего поколения представляет собой рецептор, который содержит множество костимуляторных доменов различных костимуляторных рецепторов.
[506] В некоторых вариантах осуществления, химерный рецептор антигена содержит внеклеточную часть, содержащую антитело или его фрагмент, описанный в настоящем документе. В некоторых аспектах, химерный рецептор антигена содержит внеклеточную часть, содержащую антитело или его фрагмент, описанный в настоящем документе, и внутриклеточный сигнальный домен. В некоторых вариантах осуществления, антитело или его фрагмент содержит scFv или однодоменное антитело VH и внутриклеточный домен содержит ITAM. В некоторых аспектах, внутриклеточный сигнальный домен содержит сигнальный домен зета цепи, цепи CD3-зета (CD3ζ). В некоторых вариантах осуществления, химерный рецептор антигена содержит трансмембранный домен, расположенный между внеклеточным доменом и внутриклеточной сигнальной областью.
[507] В некоторых аспектах, трансмембранный домен содержит трансмембранную часть CD28. Внеклеточный домен и трансмембранная область могут связываться прямо или опосредованно. В некоторых вариантах осуществления, внеклеточный домен и трансмембранная область связаны спейсером, таким как любой спейсер, описанный в настоящем документе. В некоторых вариантах осуществления, химерный рецептор антигена содержит внутриклеточный домен костимуляторной молекулы Т-лимфоцита, например, между трансмембранным доменом и внутриклеточным сигнальным доменом. В некоторых аспектах, костимуляторная молекула Т-лимфоцита представляет собой CD28 или 4-1BB.
[508] В некоторых вариантах осуществления, CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранную часть CD28 или его функционального варианта, и внутриклеточный сигнальный домен, содержащий сигнальную часть CD28 или его функционального варианта и сигнальную часть CD3 зета или его функционального варианта. В некоторых вариантах осуществления, CAR содержит антитело, например, фрагмент антитела, трансмембранный домен, который представляет собой или содержит трансмембранную часть CD28 или его функционального варианта, и внутриклеточный сигнальный домен, содержащий сигнальную часть 4-1BB или его функционального варианта, и сигнальную часть CD3 зета или его функционального варианта. В некоторых таких вариантах осуществления, рецептор дополнительно содержит спейсер, содержащий часть молекулы Ig, такой как молекула Ig человека, такую как шарнир Ig, например, шарнир IgG4, такой как спейсер только из шарнира.
[509] В некоторых вариантах осуществления, трансмембранный домен рецептора, например, CAR представляет собой трансмембранный домен CD28 человека или его вариант, например, трансмембранный домен из 27-аминокислот CD28 человека (Accession No.: P10747,1) или представляет собой трансмембранный домен, который содержит последовательность аминокислот, приведенную в SEQ ID NO: 138, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 138; в некоторых вариантах осуществления, трансмембранный домен, содержащий часть рекомбинантного рецептора содержит последовательность аминокислот, приведенную в SEQ ID NO: 139, или последовательность аминокислот, имеющую, по меньшей мере, или, по меньшей мере, примерно 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с ней.
[510] В некоторых вариантах осуществления, химерный рецептор антигена содержит внутриклеточный домен костимуляторной молекулы Т-лимфоцита. В некоторых аспектах, костимуляторная молекула Т-лимфоцита представляет собой CD28 или 4-1BB.
[511] В некоторых вариантах осуществления, внутриклеточная сигнальная область содержит внутриклеточный костимуляторный сигнальный домен CD28 человека или его функционального варианта или части, например, его домен из 41 аминокислоты и/или такой домен с замещением LL вместо GG в положениях 186-187 нативного белка CD28. В некоторых вариантах осуществления, внутриклеточный сигнальный домен может содержать последовательность аминокислот, приведенную в SEQ ID NO: 140 или 141, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 140 или 141. В некоторых вариантах осуществления, внутриклеточная область содержит внутриклеточный костимуляторный сигнальный домен 4-1BB или его функционального варианта или части, например, цитоплазматический домен из 42-аминокислот 4-1BB человека (Accession No. Q07011.1) или его функционального варианта или части, такой как последовательность аминокислот, приведенная в SEQ ID NO: 142, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 142.
[512] В некоторых вариантах осуществления, внутриклеточная сигнальная область содержит CD3 цепь человека, необязательно, CD3 зета стимуляторного сигнального домена или его функционального варианта, такую как цитоплазматический домен 112 AA изоформы 3 CD3ζ человека (Accession No.: P20963.2) или сигнальный домен CD3 зета, как описано в патенте США №:7446190 или в патенте США № 8911993. В некоторых вариантах осуществления, внутриклеточная сигнальная область содержит последовательность аминокислот, приведенную в SEQ ID NO: 143, 144 или 145, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичность последовательности с SEQ ID NO: 143, 144 или 145.
[513] В некоторых аспектах, спейсер содержит только шарнирную область IgG, например, только шарнир IgG4 или IgG1, такой как спейсер только из шарнира, приведенный в SEQ ID NO: 133. В других вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный с доменами CH2 и/или CH3. В некоторых вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный с доменами CH2 и CH3, например, как приведено в SEQ ID NO: 135. В некоторых вариантах осуществления, спейсер представляет собой шарнир Ig, например, шарнир IgG4, связанный только с доменом CH3, например, как приведено в SEQ ID NO: 136. В некоторых вариантах осуществления, спейсер представляет собой или содержит обогащенную глицином-серином последовательность или другой гибкий линкер, такой как известные гибкие линкеры.
[514] В некоторых вариантах осуществления, рекомбинантный рецептор, например, CAR или другой рецептор антигена, дополнительно содержит маркер, такой как клеточный поверхностный маркер, который можно использовать для подтверждения трансдуцирования или генной инженерии клетки для экспедирования рецептора, такого как усеченная версия клеточного поверхностного рецептора, такого как усеченный EGFR (tEGFR). В некоторых аспектах, маркер содержит весь CD34 или его часть (например, усеченную форму), NGFR или рецептор эпидермального фактора роста (например, tEGFR). В определенных вариантах осуществления, tEGFR содержит последовательность аминокислот, которая приводится в SEQ ID NO: 147 или 148. В конкретных вариантах осуществления, tEGFR содержит последовательность аминокислот, имеющую или имеющую примерно, или, по меньшей мере, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 99% идентичность с последовательностями, приведенными в SEQ ID NO: 147 или 148. В некоторых вариантах осуществления, нуклеиновая кислота, кодирующая маркер, функционально связана с полинуклеотидом, кодирующим последовательность линкера, такую как последовательность расщепляемого линкера, например, T2A. Например, последовательность маркера и, необязательно, линкера, может представлять собой любую последовательность, как описано в опубликованной заявке на патент WO 2014031687. Например, маркер может представлять собой усеченный EGFR (tEGFR), который необязательно, связан с последовательностью линкера, такой как последовательность расщепляемого линкера T2A.
[515] В определенных случаях, когда молекулы нуклеиновых кислот кодируют две или более различных полипептидных цепей, каждая из полипептидных цепей может кодироваться с помощью отдельной молекулы нуклеиновой кислоты. Например, могут предусматриваться две отдельных нуклеиновых кислоты, и каждая может индивидуально переноситься или вводиться в клетку для экспрессирования в клетке.
[516] В некоторых вариантах осуществления, например, когда полинуклеотид содержит первую и вторую последовательности нуклеиновых кислот, кодирующие последовательности, кодирующие каждую из различных полипептидных цепей, могут функционально связываться с промотором, они могут быть одинаковыми или различными. В некоторых вариантах осуществления, молекула нуклеиновой кислоты может содержать промотор, который запускает экспрессирование двух или более различных полипептидных цепей. В некоторых вариантах осуществления, такие молекулы нуклеиновых кислот могут быть мультицистронными (бицистронными или трицистронными, смотри, например, патент США №6060273). В некоторых вариантах осуществления, единицы транскрипции могут получаться с помощью генной инженерии как бицитронная единица, содержащая IRES (внутренний участок посадки рибосомы), что делает возможным соэкспрессирование генных продуктов (например, кодирование PSMA или его модифицированной формы и кодирование рекомбинантного рецептора) посредством сигнала от одного промотора. Альтернативно, в некоторых случаях, один промотор может направлять экспрессирование РНК, которая содержит, в одной открытой рамке считывания (ORF), два или три гена (например, кодирующих PSMA или его модифицированную форму и кодирующих рекомбинантный рецептор), отделенных друг от друга последовательностями, кодирующими саморасщепляющийся пептид, например, последовательности 2A), или сайт распознавания протеазы (например, фурин). ORF, таким образом, кодирует один полипептид, который, либо в ходе (в случае 2A), либо после трансляции, процессируется в индивидуальные белки. В некоторых случаях, пептид, такой как T2A, может заставлять рибосому перескакивать (рибосомное перескакивание) синтез пептидной связи на C-конце элемента 2A, приводя к разделению между концом последовательности 2A и следующим по ходу пептидом (смотри, например, de Felipe. Genetic Vaccines and Ther. 2:13 (2004) и deFelipe et al. Traffic 5:616-626 (2004)). Различные элементы 2A известны. Примеры последовательностей 2A, которые можно использовать в способах и системе, описанных в настоящем документе, включают, без ограничения, последовательности 2A из вируса ящура (F2A, например, SEQ ID NO: 32), вируса ринита лошадей A (E2A, например, SEQ ID NO: 153), вируса Thosea asigna (T2A, например, SEQ ID NO: 146 или 149), и тешовируса-1 свиней (P2A, например, SEQ ID NO: 151 или 152), как описано в публикации патента США №20070116690.
2. Рецепторы T-лимфоцитов (TCR)
[517] В некоторых вариантах осуществления, предлагаются генно-инженерные клетки, такие как Т-лимфоциты, которые экспрессируют рецептор Т-лимфоцитов (TCR) или его антигенсвязывающую часть, которая распознает пептидный эпитоп или эпитоп Т-лимфоцита целевого полипептида, такого как антиген опухоли, вирусный или аутоиммунный белок.
[518] В некоторых вариантах осуществления, “рецептор Т-лимфоцитов” или “TCR” представляет собой молекулу, которая содержит вариабельные цепи α и β (также известные как TCRα и TCRβ, соответственно) или вариабельные цепи γ и δ (также известные как TCR γ и TCRδ, соответственно) или их антигенсвязывающие части, и которая может специфично связываться с пептидной связью молекулы MHC. В некоторых вариантах осуществления, TCR имеет форму αβ. Как правило, TCR, которые существуют в формах αβ и γδ, являются, в целом, структурно подобными, но Т-лимфоциты, экспрессирующие их, могут иметь различные анатомические локализации или функции. TCR может находиться на поверхности клетки или в растворимой форме. Как правило, TCR находится на поверхности Т-клеток (или T-лимфоцитов), где он, как правило, является ответственным за распознавание антигенов, связанных с молекулами главного комплекса гистосовместимости (MHC).
[519] Если не указано иного, термин “TCR” должен пониматься как охватывающий полноразмерные TCR, а также их антигенсвязывающие части или антигенсвязывающие фрагменты. В некоторых вариантах осуществления, TCR представляет собой интактный или полноразмерный TCR, включая TCR в форме αβ или форме γδ. В некоторых вариантах осуществления, TCR представляет собой антигенсвязывающую часть, которая меньше полноразмерного TCR, но которая связывается с конкретной пептидной связью в молекуле MHC, например, связывается с комплексом MHC-пептид. В некоторых случаях, антигенсвязывающая часть или фрагмент TCR может содержать только часть структурных доменов полноразмерного или интактного TCR, но все еще может связываться с пептидным эпитопом, таким как комплекс MHC-пептид, с которым связывается полноразмерный TCR. В некоторых случаях, антигенсвязывающая часть содержит вариабельные домены TCR, такие как вариабельная цепь α и вариабельная цепь β TCR, достаточные для формирования сайта связывания для связывания с конкретным комплексом MHC-пептид. Как правило, вариабельные цепи TCR содержат области, определяющие комплементарность, участвующие в распознавании пептида MHC и/или комплекса MHC-пептид.
[520] В некоторых вариантах осуществления, вариабельные домены TCR содержат гипервариабельные петли или области, определяющие комплементарность (CDR), которые, как правило, вносят главный вклад в распознавание антигена и способности к связыванию и специфичность. В некоторых вариантах осуществления, CDR TCR или их сочетание формирует весь или, по существу, весь антигенсвязывающий сайт данной молекулы TCR. Различные CDR в вариабельной области цепи TCR, как правило, разделяются каркасными областями (FR), которые, как правило, демонстрируют меньшую вариабельность среди молекул TCR по сравнению с CDR (смотри, например, Jores et al., Proc. Nat'l Acad. Sci. U.S.A. 87:9138, 1990; Chothia et al., EMBO J. 7:3745, 1988; смотри также Lefranc et al., Dev. Comp. Immunol. 27:55, 2003). В некоторых вариантах осуществления, CDR3 представляет собой главную CDR ответственную за связывание антигена или за специфичность, или является самой важной среди трех CDR на данной вариабельной области TCR для распознавания антигена, и/или для взаимодействия с частью процессированного пептида комплекса пептид-MHC. В некоторых контекстах, CDR1 альфа-цепи может взаимодействовать с N-концевой частью определенных антигенных пептидов. В некоторых контекстах, CDR1 бета-цепи может взаимодействовать с C-концевой частью пептида. В некоторых контекстах, CDR2 вносит самый большой вклад в первичную CDR ответственную за взаимодействие с частью MHC комплекса MHC-пептид или за ее распознавание, или представляет собой ее. В некоторых вариантах осуществления, вариабельная область β-цепи может содержать дополнительную гипервариабельную область (CDR4 или HVR4), которая, как правило, участвует в связывании суперантигена, а не в распознавании антигена (Kotb (1995) Clinical Microbiology Reviews, 8:411-426).
[521] В некоторых вариантах осуществления, TCR также может содержать константный домен, трансмембранный домен и/или короткий цитоплазматический хвост (смотри, например, Janeway et al., Immunobiology: The Immune System in Health and Disease, 3rd Ed., Current Biology Publications, p. 4:33, 1997). В некоторых аспектах, каждая цепь TCR может содержать один N-концевой вариабельный домен иммуноглобулина, один константный домен иммуноглобулина, трансмембранную область и короткий цитоплазматический хвост на C-концевой области. В некоторых вариантах осуществления, TCR ассоциируется с инвариантными белками комплекса CD3, участвующими в медиировании трансдуцирования сигнала.
[522] В некоторых вариантах осуществления, цепь TCR содержит один или несколько константных доменов. Например, внеклеточная часть данной цепи TCR, (например, α-цепи или β-цепи) может содержать два иммуноглобулиноподобных домена, таких как вариабельный домен, например, Vα или Vβ; как правило, аминокислоты 1-116 на основе нумерации Kabat, Kabat et al., “Sequences of Proteins of Immunological Interest, US Dept. Health and Human Services, Public Health Service National Institutes of Health, 1991, 5th ed.) и константный домен (например, константный домен α-цепи или Cα, как правило, положения 117-259 цепи на основе нумерации Kabat или константный домен β цепи или Cβ, как правило, положения 117-295 цепи на основе Kabat) рядом с клеточной мембраной. Например, в некоторых случаях, внеклеточная часть TCR сформированная из двух цепей содержит два ближних к мембране константных домена, и два дальних от мембраны вариабельных домена, каждый из этих вариабельных доменов содержит CDR. Константный домен TCR может содержать короткие соединительные последовательности, в которых цистеиновый остаток образует дисульфидную связь, тем самым соединяя две цепи TCR. В некоторых вариантах осуществления, TCR может иметь дополнительный цистеиновый остаток в каждой из α и β цепей, так что TCR содержит две дисульфидные связи в константных доменах.
[523] В некоторых вариантах осуществления, цепи TCR содержат трансмембранный домен. В некоторых вариантах осуществления, трансмембранный домен является положительно заряженным. В некоторых случаях, цепь TCR содержит цитоплазматический хвост. В некоторых случаях, структура дает возможность для ассоциирования TCR с другими молекулами, подобными CD3 и с их субъединицами. Например, TCR, содержащий константные домены с трансмембранной областью, может фиксировать белок в клеточной мембране и ассоциироваться с инвариантными субъединицами сигнального аппарата CD3 или комплекса. Внутриклеточные хвосты сигнальных субъединиц CD3 (например, CD3γ, CD3δ, CD3ε и CD3ζ цепи) содержат один или несколько иммунорецепторных тирозиновых активирующих мотивов или ITAM, которые являются частью возможности передачи сигналов комплекса TCR.
[524] В некоторых вариантах осуществления, TCR может представлять собой гетеродимер из двух цепей α и β (или необязательно, γ и δ) или он может представлять собой одноцепочечная конструкция TCR. В некоторых вариантах осуществления, TCR представляет собой гетеродимер, содержащий две отдельных цепи (α и β цепи или γ и δ цепи), которые связаны, например, дисульфидной связью или дисульфидными связями.
[525] В некоторых вариантах осуществления, TCR может генерироваться из известной последовательности (последовательностей) TCR, такой как последовательности цепей Vα,β, для которых легко доступна, по существу, полноразмерная, кодирующая последовательность. Способы получения полноразмерной последовательности TCR, включая последовательности V цепи из клеточных источников, хорошо известны. В некоторых вариантах осуществления, нуклеиновые кислоты, кодирующие TCR, можно получить из различных источников, например, с помощью амплификации посредством цепной реакции полимеразы (PCR) TCR-кодирующих нуклеиновых кислот внутри данной клетки или клеток, или выделенных из них, или синтеза публично доступных последовательностей ДНК TCR.
[526] В некоторых вариантах осуществления, TCR получают из биологического источника, например, из клеток, например, из Т-лимфоцита, (например, цитотоксичного Т-лимфоцита), гибридом Т-лимфоцитов или другого публично доступного источника. В некоторых вариантах осуществления, T-лимфоциты можно получать из клеток, выделенных in vivo. В некоторых вариантах осуществления, TCR представляет собой TCR, полученный путем тимической селекции. В некоторых вариантах осуществления, TCR представляет собой неоэпитоп-рестриктированную TCR. В некоторых вариантах осуществления, T-лимфоциты могут представлять собой гибридому или клон культивированных Т-лимфоцитов. В некоторых вариантах осуществления, TCR или его антигенсвязывающая часть или его антигенсвязывающий фрагмент может генерироваться синтетически, зная последовательность TCR.
[527] В некоторых вариантах осуществления, TCR генерируют из TCR идентифицированного или полученного в результате селекции от скрининга библиотеки кандидатов в TCR против целевого полипептидного антигена или его эпитопа в целевом Т-лимфоците. Библиотеки TCR могут генерироваться посредством амплификации репертуара Vα и Vβ из Т-лимфоцитов, выделенных у субъекта, включая клетки, присутствующие в PBMC, селезенке или другом лимфоидном органе. В некоторых случаях, Т-лимфоциты могут амплифицироваться из лимфоцитов, инфильтрующих опухоль (TIL). В некоторых вариантах осуществления, библиотеки TCR могут генерироваться из клеток CD4+ или CD8+. В некоторых вариантах осуществления, TCR могут амплифицироваться из источника Т-лимфоцитов у нормального здорового субъекта, то есть из библиотек нормальных TCR. В некоторых вариантах осуществления, TCR могут амплифицироваться из источника Т-лимфоцитов болезненного субъекта, то есть из библиотек болезненных TCR. В некоторых вариантах осуществления, используют дегенеративные праймеры для амплификации репертуара генов Vα и Vβ, например, посредством RT-PCR в образцах, таких как Т-лимфоциты, полученных у людей. В некоторых вариантах осуществления, библиотеки scTv могут быть собраны из библиотек наивных Vα и Vβ, в которых амплифицируемые продукты клонируются или собираются, чтобы они разделялись линкером. В зависимости от источника субъекта и клеток, библиотеки могут быть специфичными к аллели HLA. Альтернативно, в некоторых вариантах осуществления, библиотеки TCR могут генерироваться посредством мутагенеза или диверсификации родительской или каркасной молекулы TCR. В некоторых аспектах, TCR подвергаются воздействию направленной эволюции, например, под действием мутагенеза, например, цепи α или β. В некоторых аспектах, конкретные остатки в CDR TCR изменяются. В некоторых вариантах осуществления, селектированные TCR могут модифицироваться посредством созревания аффиности. В некоторых вариантах осуществления, антиген-специфичные Т-лимфоциты могут выбираться, например, посредством скрининга для оценки активности CTL против пептида. В некоторых аспектах, TCR, например, присутствующие на антиген-специфичных Т-лимфоцитах, могут подвергаться селекции, например, по активности связывания, то есть, по конкретной аффиности или авидности к антигену.
[528] В некоторых вариантах осуществления, TCR или его антигенсвязывающая часть представляет собой рецептор, который модифицируется или получается с помощью генной инженерии. В некоторых вариантах осуществления, способы направленной эволюции используют для генерирования TCR с измененными свойствами, например, с более высокой аффиностью к конкретному комплексу MHC-пептид. В некоторых вариантах осуществления, направленная эволюция достигается с помощью способов дисплеев, включая, но, не ограничиваясь этим, дрожжевой дисплей (Holler et al. (2003) Nat Immunol, 4, 55-62; Holler et al. (2000) Proc Natl Acad Sci USA, 97, 5387-92), фаговый дисплей (Li et al. (2005) Nat Biotechnol, 23, 349-54) или Т-лимфоцитный дисплей (Chervin et al. (2008) J Immunol Methods, 339, 175-84). В некоторых вариантах осуществления, подходы с дисплеями включают генную инженерию или модификацию известного, родительского или эталонного TCR. Например, в некоторых случаях, TCR дикого типа можно использовать в качестве шаблона для продуцирования мутагенизированных TCR, в котором один или несколько остатков CDR мутируют, и мутанты с желаемым измененным свойством, таким как повышенная аффиность к желаемую целевому антигену, селектируются.
[529] В некоторых вариантах осуществления, пептиды целевого полипептида для использования при продуцировании или генерировании TCR, представляющего интерес, известны или могут легко идентифицироваться специалистом в данной области. В некоторых вариантах осуществления, пептиды пригодные для использования при генерировании TCR или их антигенсвязывающих частей могут определяться на основе присутствия HLA-рестриктированного мотива в целевом полипептиде, представляющем интерес, таком как целевой полипептид, описанный ниже. В некоторых вариантах осуществления, пептиды идентифицируются с использованием доступных компьютерных моделей прогнозирования. В некоторых вариантах осуществления, для предсказания сайтов связывания MHC класс I, такие модели включают, но, не ограничиваясь этим, ProPred1 (Singh and Raghava (2001) Bioinformatics 17(12):1236-1237 и SYFPEITHI (смотри Schuler et al. (2007) Immunoinformatics Methods in Molecular Biology, 409(1): 75-93 2007). В некоторых вариантах осуществления, MHC-рестриктированный эпитоп представляет собой HLA-A0201, который экспрессируется примерно у 39-46% всех европеоидов и, следовательно, представляет собой подходящий выбор антигена MHC для использования при приготовлении TCR или другой молекулы, связывающей MHC-пептид.
[530] HLA-A0201-связывающие мотивы и сайты расщепления для протеасом и иммунопротеасом с использованием компьютерных моделей прогнозирования известны специалистам в данной области. Например, для предсказания сайтов связывания MHC класс I, такие модели включают, но, не ограничиваясь этим, ProPred1 (описано более подробно в Singh and Raghava, ProPred: prediction of HLA-DR binding sites. BIOINFORMATICS 17(12):1236-1237 2001) и SYFPEITHI (смотри Schuler et al. SYFPEITHI, Database for Searching and T-Cell Epitope Prediction. in Immunoinformatics Methods in Molecular Biology, vol. 409(1): 75-93 2007)
[531] В некоторых вариантах осуществления, TCR или его антигенсвязывающая часть может представлять собой рекомбинантно продуцируемый природный белок или его мутировавшую форму, в котором одно или несколько свойств, таких как характеристики связывания, изменяются. В некоторых вариантах осуществления, TCR можно получить из одного из различных видов животных, таких как человек, мышь, крыса или другое млекопитающее. TCR может быть связан с клеткой или находиться в растворимой форме. В некоторых вариантах осуществления, для целей предлагаемых способов, TCR находится в связанной с клеткой форме, экспрессируемой на поверхности клеток.
[532] В некоторых вариантах осуществления, TCR представляет собой полноразмерный TCR. В некоторых вариантах осуществления, TCR представляет собой его антигенсвязывающую часть. В некоторых вариантах осуществления, TCR представляет собой димерный TCR (dTCR). В некоторых вариантах осуществления, TCR представляет собой одноцепочечный TCR (sc-TCR). В некоторых вариантах осуществления, dTCR или scTCR имеют структуры, как описано в WO 03/020763, WO 04/033685, WO 2011/044186.
[533] В некоторых вариантах осуществления, TCR содержит последовательность, соответствующую трансмембранной последовательности. В некоторых вариантах осуществления, TCR содержит последовательность, соответствующую цитоплазматическим последовательностям. В некоторых вариантах осуществления, TCR может формировать комплекс TCR с CD3. В некоторых вариантах осуществления, любой из TCR, включая dTCR или scTCR, может связываться с сигнальными доменами, что дает активный TCR на поверхности Т-лимфоцита. В некоторых вариантах осуществления, TCR экспрессируется на поверхности клеток.
[534] В некоторых вариантах осуществления dTCR содержит первый полипептид, где последовательность, соответствующая последовательности вариабельной области α цепи TCR, слита с N-окончанием последовательности, соответствующей внеклеточной последовательности константной области α цепи TCR, и второй полипептид, где последовательность, соответствующая последовательности вариабельной области β цепи TCR, слита с N-окончанием последовательности, соответствующей внеклеточной последовательности константной области β цепи TCR, первый и второй полипептиды связаны дисульфидной связью. В некоторых вариантах осуществления, связь может соответствовать нативной межцепной дисульфидной связи, присутствующей в нативных димерных αβ TCR. В некоторых вариантах осуществления, межцепные дисульфидные связи отсутствуют в нативных TCR. Например, в некоторых вариантах осуществления, один или несколько цистеинов могут вводиться во внеклеточные последовательности константной области полипептидной пары dTCR. В некоторых случаях может быть желательной как нативная, так и не нативная дисульфидная связь. В некоторых вариантах осуществления, TCR содержит трансмембранную последовательность для фиксирования мембране.
[535] В некоторых вариантах осуществления, dTCR содержит α цепь TCR, содержащую вариабельный α домен, константный α домен и первый мотив димеризации, присоединенный к C-концу константного α домена, и β цепь TCR, содержащую вариабельный β домен, константный β домен и первый мотив димеризации, присоединенный к C-концу константного β домена, где первый и второй мотивы димеризации легко взаимодействуют с образованием ковалентной связи между аминокислотой в первом мотиве димеризации и аминокислотой во втором мотиве димеризации, соединяя вместе α цепь TCR и β цепь TCR.
[536] В некоторых вариантах осуществления, TCR представляет собой scTCR. Как правило, scTCR может генерироваться с использованием способов, известных специалистам в данной области, смотри, например, Soo Hoo, W. F. et al. PNAS (USA) 89, 4759 (1992);  C. and
C. and  A., J. Mol. Biol. 242, 655 (1994); Kurucz, I. et al. PNAS (USA) 90 3830 (1993); Международные публикации PCT №№ WO 96/13593, WO 96/18105, WO 99/60120, WO 99/18129, WO 03/020763, WO 2011/044186; и Schlueter, C. J. et al. J. Mol. Biol. 256, 859 (1996). В некоторых вариантах осуществления, scTCR содержит введенную ненативную дисульфидную межцепную связь для облегчения ассоциации цепей TCR (смотри, например, Международную публикацию PCT № WO 03/020763). В некоторых вариантах осуществления, scTCR представляет собой усеченный TCR без дисульфидной связи, в котором гетерологичные лейциновые молнии, слитые с его C-концом, облегчают ассоциацию цепей (смотри, например, Международную публикацию PCT № WO 99/60120). В некоторых вариантах осуществления, scTCR содержат вариабельный домен TCRα ковалентно связанный с вариабельным доменом TCRβ через пептидный линкер (смотри, например, Международную публикацию PCT № WO 99/18129).
A., J. Mol. Biol. 242, 655 (1994); Kurucz, I. et al. PNAS (USA) 90 3830 (1993); Международные публикации PCT №№ WO 96/13593, WO 96/18105, WO 99/60120, WO 99/18129, WO 03/020763, WO 2011/044186; и Schlueter, C. J. et al. J. Mol. Biol. 256, 859 (1996). В некоторых вариантах осуществления, scTCR содержит введенную ненативную дисульфидную межцепную связь для облегчения ассоциации цепей TCR (смотри, например, Международную публикацию PCT № WO 03/020763). В некоторых вариантах осуществления, scTCR представляет собой усеченный TCR без дисульфидной связи, в котором гетерологичные лейциновые молнии, слитые с его C-концом, облегчают ассоциацию цепей (смотри, например, Международную публикацию PCT № WO 99/60120). В некоторых вариантах осуществления, scTCR содержат вариабельный домен TCRα ковалентно связанный с вариабельным доменом TCRβ через пептидный линкер (смотри, например, Международную публикацию PCT № WO 99/18129).
[537] В некоторых вариантах осуществления, scTCR содержит первый сегмент, состоящий из последовательности аминокислот, соответствующей вариабельной области α цепи TCR, второй сегмент, состоящий из последовательности аминокислот, соответствующей последовательности вариабельной области β цепи TCR слитой с N-окончанием последовательности аминокислот, соответствующей внеклеточной последовательности константного домена β цепи TCR, и линкерную последовательность связывающую C-окончание первого сегмента с N-окончанием второго сегмента.
[538] В некоторых вариантах осуществления, scTCR содержит первый сегмент, состоящий из последовательности вариабельной области α цепи, слитой с N-окончанием последовательности внеклеточного константного домена α цепи, и второй сегмент, состоящий из последовательности вариабельной области β цепи, слитой с N-окончанием последовательности внеклеточного константного домена β цепи и трансмембранную последовательность, и, необязательно, линкерную последовательность, связывающую C-окончание первого сегмента с N окончанием второго сегмента.
[539] В некоторых вариантах осуществления, scTCR содержит первый сегмент, состоящий из последовательности вариабельной области β цепи TCR, слитой с N-окончанием последовательности внеклеточного константного домена β цепи, и второй сегмент, состоящий из последовательности вариабельной области α цепи, слитой с N-окончанием последовательности внеклеточного константного домена α цепи, и трансмембранную последовательность, и, необязательно, линкерную последовательность, связывающую C-окончание первого сегмента с N-окончанием второго сегмента.
[540] В некоторых вариантах осуществления, линкер scTCR, который связывает первый и второй сегменты TCR, может представлять собой любой линкер, который может формировать одну полипептидную нить, сохраняя при этом специфичность связывания TCR. В некоторых вариантах осуществления, линкерная последовательность может, например, иметь формулу -P-AA-P-, где P представляет собой пролин, а AA представляет последовательность аминокислот, где аминокислоты представляют собой глицин и серин. В некоторых вариантах осуществления, первый и второй сегменты спариваются, так что их последовательности вариабельных областей ориентируются для такого связывания. Следовательно, в некоторых случаях, линкер имеет достаточную длину, чтобы он простирался на расстояние между C-окончанием первого сегмента и N-окончанием второго сегмента или наоборот, но он не является слишком длинным, чтобы блокировать или уменьшать связывание scTCR с целевым лигандом. В некоторых вариантах осуществления, линкер может содержать от или примерно от 10 до 45 аминокислот, например, 10-30 аминокислот или 26-41 остатков аминокислот, например, 29, 30, 31 или 32 аминокислоты. В некоторых вариантах осуществления, линкер имеет формулу -PGGG-(SGGGG)5-P-, где P представляет собой пролин, G представляет собой глицин и S представляет собой серин (SEQ ID NO: 28). В некоторых вариантах осуществления, линкер имеет последовательность GSADDAKKDAAKKDGKS (SEQ ID NO: 29)
[541] В некоторых вариантах осуществления, scTCR содержит ковалентную дисульфидную связь, связывающую остаток области константного домена α цепи иммуноглобулина с остатком области константного домена β цепи иммуноглобулина. В некоторых вариантах осуществления, межцепная дисульфидная связь в нативном TCR отсутствует. Например, в некоторых вариантах осуществления, один или несколько цистеинов могут вводиться во внеклеточные последовательности константной области первого и второго сегмента полипептида scTCR. В некоторых случаях может быть желательной как нативная, так и ненативная дисульфидная связь.
[542] В некоторых вариантах осуществления dTCR или scTCR, содержащих введенные межцепные дисульфидные связи, нативные дисульфидные связи отсутствуют. В некоторых вариантах осуществления, один или несколько нативных цистеинов, образующих нативные межцепные дисульфидные связи, замещаются другим остатком, таким как серин или аланин. В некоторых вариантах осуществления, введенная дисульфидная связь может формироваться посредством мутаций не-цистеиновых остатков на первом и втором сегментах с их заменой на цистеин. Иллюстративные ненативные дисульфидные связи TCR описаны в Международной публикации PCT № WO 2006/000830.
[543] В некоторых вариантах осуществления, TCR или его антигенсвязывающий фрагмент демонстрирует аффиность с некоторой равновесной константой связывания к целевому антигену в пределах между или примерно между 10-5 и 10-12 M и со всеми индивидуальными значениями в этих диапазонах. В некоторых вариантах осуществления, целевой антиген представляет собой комплекс MHC-пептид или лиганд.
[544] В некоторых вариантах осуществления, нуклеиновая кислота или нуклеиновые кислоты, кодирующие TCR, такие как α и β цепи, могут амплифицироваться посредством PCR, клонирования или других соответствующих средств и клонироваться в пригодный для использования вектор или векторы экспрессии. Вектор экспрессии может представлять собой любой пригодный для использования рекомбинантный вектор экспрессии и может использоваться для трансформации или трансфекции любого соответствующего хозяина. Пригодные для использования векторы включают векторы, сконструированные для размножения и размножения или для экспрессирования, или как для того, так и для другого, такие как плазмиды и вирусы.
[545] В некоторых вариантах осуществления, вектор может представлять собой вектор из серии pUC (Fermentas Life Sciences), серии pBluescript (Stratagene, LaJolla, Calif.), серии pET (Novagen, Madison, Wis.), серии pGEX (Pharmacia Biotech, Uppsala, Sweden) или серии pEX (Clontech, Palo Alto, Calif.). В некоторых случаях, также можно использовать векторы на основе бактериофагов, таких как λG10, λGT11, λZapII (Stratagene), λEMBL4 и λNM1149. В некоторых вариантах осуществления можно использовать векторы экспрессии растений, и они включают pBI01, pBI101.2, pBI101.3, pBI121 и pBIN19 (Clontech). В некоторых вариантах осуществления, векторы экспрессии животных включают pEUK-Cl, pMAM и pMAMneo (Clontech). В некоторых вариантах осуществления, используют вирусный вектор, такой как ретровирусный вектор.
[546] В некоторых вариантах осуществления, могут быть приготовлены рекомбинантные векторы экспрессии с использованием стандартных технологий рекомбинантной ДНК. В некоторых вариантах осуществления, векторы могут содержать регуляторные последовательности, например, для инициирования транскрипции и трансляции и стоп-кодоны, которые являются специфичными к типу хозяина (например, бактерии, грибка, растения или животного), которому должен вводиться вектор, соответствующим образом и принимая во внимание то, основан ли вектор на ДНК или РНК. В некоторых вариантах осуществления, вектор может содержать ненативный промотор, функционально связанный с нуклеотидной последовательностью, кодирующей TCR, или его антигенсвязывающую часть (или другую связывающую молекулу для комплекса MHC-пептид). В некоторых вариантах осуществления, промотор может представлять собой невирусный промотор или вирусный промотор, такой как промотор цитомегаловируса (CMV), промотор SV40, промотор RSV и промотор, находящийся в длинноконцевом повторе вируса стволовых клеток мышей. Другие известные промоторы также рассматриваются.
[547] В некоторых вариантах осуществления, для генерирования вектора, кодирующего TCR, α и β цепи амплифицируются с помощью PCR из цельной кДНК, выделенной из клона Т-лимфоцитов, экспрессирующего TCR, представляющий интерес, и клонированной в вектор экспрессии. В некоторых вариантах осуществления, α и β цепи клонируют в один и тот же вектор. В некоторых вариантах осуществления, α и β цепи клонируют в разные вектора. В некоторых вариантах осуществления, генерируемые α и β цепи вводят в ретровирусный, например, лентивирусный, вектор.
C. Введение нуклеиновых кислот и векторов в клетки
[548] Различные способы введения генно-инженерных компонентов, например, рекомбинантных рецепторов, например, CAR или TCR, также известны и могут использоваться вместе с предлагаемыми способами и композициями. Иллюстративные способы включают способы для переноса нуклеиновых кислот, кодирующих полипептиды или рецепторы, в том числе, с помощью вирусных векторов, например, ретровирусных или лентивирусных, невирусных векторов или транспозонов, например, системы транспозонов Sleeping Beauty. Способы переноса гена могут включать трансдуцирование, электропорообразование или другой способ, который дает в результате перенос гена в клетку.
[549] В некоторых вариантах осуществления, перенос гена осуществляется посредством сначала стимуляции клетки, например, ее объединения со стимулом, который индуцирует реакцию, такую как пролиферация, выживание и/или активация, например, как измерено по экспрессированию цитокина или маркера активации, с последующим трансдуцированием активированных клеток и их размножением в культуре до количеств, достаточных для клинических применений.
[550] В некоторых контекстах, может быть желательной защита против такой возможности, что сверхэкспрессирование стимуляторного фактора (например, лимфокина или цитокина) может потенциально давать в результате нежелательный результат или понижать эффективность у субъекта, например, это фактор, ассоциированный с токсичностью у субъекта. Таким образом, в некоторых контекстах, генно-инженерные клетки содержат сегменты генов, которые делают клетки чувствительными к отрицательной селекции in vivo, например, при введении при адоптивной иммунотерапии. Например, в некоторых аспектах, клетки получают с помощью генной инженерии таким образом, что они могут устраняться в результате изменения состояния in vivo пациента, которому их вводят. Отрицательно селективный фенотип может возникать в результате вставки гена, который придает чувствительность к вводимому агенту, например, соединению. Отрицательно селективные гены включают ген тимидинкиназы вируса простого герпеса типа I (HSV-I TK) (Wigler et al., Cell 2:223, I977), который придает чувствительность к ганцикловиру; ген клеточной гипоксантинфосфрибосилтрансферазы (HPRT), ген клеточной аденинфосфорибосилтрансферазы (APRT), ген бактериальной цитозиндезаминазы, (Mullen et al., Proc. Natl. Acad. Sci. USA. 89:33 (1992)).
[551] В некоторых вариантах осуществления, клетки, например, Т-лимфоциты, могут трансфицироваться либо в ходе, либо после размножения, например, нуклеиновыми кислотами, кодирующими рекомбинантный рецептор, например, либо рецептор Т-лимфоцитов (TCR), либо химерный рецептор антигена (CAR). Это трансфицирование для введения гена желаемого полипептида или рецептора может осуществляться с помощью любой пригодной для использования системы переноса на основе гена, включая ретровирусный вектор. В некоторых вариантах осуществления, популяция генно-инженерных клеток может согласованно, одновременно или последовательно стимулироваться антигенным стимулом, например, вводимым de novo рецептором, например, согласно предлагаемым способам. В некоторых вариантах осуществления, связывание молекулы, присутствующей на предлагаемых частицах, например, шариках, обеспечивает антигенный стимул, например, обеспечиваемый в форме когнатного (поперечно сшитого) антигена или лиганда генетически введенного рецептора (например, природного лиганда CAR) или антиидиотипического антитела, которое непосредственно связывает или распознает рекомбинантный рецептор.
[552] Среди дополнительных нуклеиновых кислот, например, генов для введения, имеются нуклеиновые кислоты для улучшения эффективности терапии, например, способствующие жизнеспособности и/или функции переносимых клеток; гены для обеспечения генетического маркера для селекции и/или оценки клеток, например, для оценки in vivo выживаемости или локализации; гены для улучшения безопасности, например, делая клетки, чувствительными к отрицательной селекции in vivo, как описано Lupton S. D. et al., Methods, and Cell Biol., 11:6 (1991); и Riddell et al., Human Gene Therapy 3:319-338 (1992); смотри также публикации PCT/US 91/08442 и PCT/US 94/05601, Lupton et al, описывающие использование бифункциональных селективных слитых генов, полученных от слияния доминантного положительного селективного маркера с отрицательным селективным маркером. Смотри, например, Riddell et al., патент США №6040177, столбцы 14-17.
[553] Как описано выше, в некоторых вариантах осуществления, клетки инкубируются и/или культивируются до генной инженерии или в связи с ней. Стадии инкубирования могут включать культуру, культивирование, стимуляцию, активацию, размножение и/или замораживание для консервирования, например, криоконсервирования.
1. Частицы вирусных векторов
[554] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносятся в клетки с использованием рекомбинантных, инфекционных вирусных частиц, таких, например, как векторы, полученные из вируса обезьян 40 (SV40), аденовирусов, аденоассоциированных вирусов (AAV). В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносятся в Т-лимфоциты с использованием рекомбинантных лентивирусных векторов или ретровирусных векторов, таких как гамма-ретровирусные векторы (смотри, например, Koste et al. (2014) Gene Therapy 2014 Apr 3. doi: 10.1038/gt.2014.25; Carlens et al. (2000) Exp Hematol 28(10): 1137-46; Alonso-Camino et al. (2013) Mol Ther Nucl Acids 2, e93; Park et al., Trends Biotechnol. 2011 November 29(11): 550-557.
[555] В некоторых вариантах осуществления, ретровирусный вектор имеет последовательность длинноконцевого повтора (LTR), например, ретровирусного вектора, полученного из вируса лейкемии Молони мышиных (MoMLV), вируса миелопролиферативной саркомы (MPSV), вируса эмбриональных стволовых клеток мышиных (MESV), вируса стволовых клеток мышиных (MSCV), вируса некроза селезенки (SFFV) или аденоассоциированного вируса (AAV). Большинство ретровирусных векторов получают из ретровирусов мышиных. В некоторых вариантах осуществления, ретровирусы включают вирусы, полученные из любого источника клеток птиц или млекопитающих. Ретровирусы как правило, являются амфотропными, это означает, что они могут инфицировать клетки-хозяина нескольких видов, включая людей. В одном из вариантов осуществления, ген, который должен экспрессироваться, заменяет ретровирусные последовательности gag, pol и/или env. Описан ряд иллюстративных ретровирусных систем (например, патенты США №№5219740; 6207453; 5219740; Miller and Rosman (1989) BioTechniques 7:980-990; Miller, A. D. (1990) Human Gene Therapy 1:5-14; Scarpa et al. (1991) Virology 180:849-852; Burns et al. (1993) Proc. Natl. Acad. Sci. USA 90:8033-8037; и Boris-Lawrie and Temin (1993) Cur. Opin. Genet. Develop. 3:102-109.
[556] Способы лентивирусного трансдуцирования известны. Иллюстративные способы описаны, например, в Wang et al. (2012) J. Immunother. 35(9): 689-701; Cooper et al. (2003) Blood. 101:1637-1644; Verhoeyen et al. (2009) Methods Mol Biol. 506: 97-114; и Cavalieri et al. (2003) Blood. 102(2): 497-505.
[557] В некоторых вариантах осуществления, частицы вирусного вектора содержат геном, полученный из вектора на основе ретровирусного генома, например, полученный из вектора на основе лентивирусного генома. В некоторых аспектах предлагаемых вирусных векторов, гетерологичная нуклеиновая кислота, кодирующая рекомбинантный рецептор, такой как рецептор антигена, например, CAR, содержится и/или локализуется между последовательностями 5' LTR и 3' LTR генома вектора.
[558] В некоторых вариантах осуществления, геном вирусного вектора представляет собой геном лентивируса, например, геном HIV-1 или геном SIV. Например, лентивирусные векторы генерируются посредством множественного ослабления вирулентных генов, например, могут быть устранены гены env, vif, vpu и nef, делая вектор безопаснее для терапевтических целей. Лентивирусные векторы известны. Смотри Naldini et al., (1996 и 1998); Zufferey et al., (1997); Dull et al., 1998, патенты США №№6013516; и 5994136). В некоторых вариантах осуществления, эти вирусные векторы основываются на плазмидах или основываются на вирусах и конфигурируются для переноса основных последовательностей для введения чужеродной нуклеиновой кислоты, для селекции и для переноса нуклеиновой кислоты в клетку-хозяин. Известные лентивирусы могут легко быть получены из депозитариев или коллекций, таких как American Type Culture Collection (“ATCC”; 10801 University Blvd., Manassas, Va. 20110-2209) или выделены из известных источников с использованием повсеместно доступных технологий.
[559] Неограничивающие примеры лентивирусных векторов включают векторы, полученные из лентивируса, такого как вирус иммуннодефицита человека 1 (HIV-1), HIV-2, вирус иммунодефицита обезьян (SIV), T-лимфотропный вирус человека 1 (HTLV-1), HTLV-2 или вирус инфекционной анемии лошадей (E1AV). Например, лентивирусные векторы генерируются посредством многократного ослабления вирулентных генов HIV, например, гены env, vif, vpr, vpu и nef устраняются, делая вектор безопаснее для терапевтических целей. Лентивирусные векторы известны в данной области, смотри Naldini et al., (1996 и 1998); Zufferey et al., (1997); Dull et al., 1998, патенты США №№6013516; и 5994136). В некоторых вариантах осуществления, эти вирусные векторы основываются на плазмидах или основываются на вирусах и конфигурируются для переноса основных последовательностей для введения чужеродной нуклеиновой кислоты, для селекции и для переноса нуклеиновой кислоты в клетку-хозяина. Известные лентивирусы могут легко быть получены из депозитариев или коллекций, например, из American Type Culture Collection (“ATCC”; 10801 University Blvd., Manassas, Va. 20110-2209) или выделены от известных источников с использованием повсеместно доступных технологий.
[560] В некоторых вариантах осуществления, вектор вирусного генома может содержать последовательности LTR 5' и 3' ретровируса, такого как лентивирус. В некоторых аспектах, констрция вирусного генома может содержать последовательности LTR 5' и 3' лентивируса, и в частности, может содержать последовательности R и U5 из 5' LTR лентивируса и инактивированных или самодезактивированных 3' LTR лентивируса. Последовательности LTR могут представлять собой последовательности LTR от любого лентивируса от любых видов. Например, они могут представлять собой последовательности LTR от HIV, SIV, FIV или BIV. Как правило, последовательности LTR представляют собой последовательности LTR HIV.
[561] В некоторых вариантах осуществления, нуклеиновая кислота вирусного вектора, такого как вирусный вектор HIV, не имеет дополнительных транскрипционных единиц. Геном вектора может содержать дезактивированный или самодезактивированный 3' LTR (Zufferey et al. J Virol 72: 9873, 1998; Miyoshi et al., J Virol 72:8150, 1998). Например, делеция области U3 3' LTR нуклеиновой кислоты, используемой для продуцирования вирусного вектора РНК, может использоваться для генерирования самодезактивирующихся векторов (SIN). Затем эта делеция может переноситься в 5' LTR провирусной ДНК в ходе обратной транскрипции. Самодезактивирующийся вектор, как правило, имеет делецию энхансерной и промоторной последовательностей от длинноконцевого повтора (LTR) 3', которая копируется в 5' LTR в ходе встраивания вектора. В некоторых вариантах осуществления достаточная часть последовательности может удаляться, включая удаление TATA-бокса, для разрушения транскрипционной активности LTR. Это может помешать продуцированию полноразмерного вектора РНК в трансдуцированных клетках. В некоторых аспектах, элемент U3 3' LTR содержит делецию своей энхансерной последовательности, TATA-бокса, Sp1 и сайтов NF-каппа B. В результате самодезактивирования 3' LTR, провирус, который генерируется после введения и обратной транскрипции содержит дезактивированный 5' LTR. Это может улучшить безопасность, уменьшая риск мобилизации генома вектора и влияние LTR на соседние клеточные промоторы. Самодезактивирование 3' LTR может конструироваться с помощью любого способа, известного в данной области. В некоторых вариантах осуществления, это не влияет на титры вектора или на свойства вектора in vitro или in vivo.
[562] Необязательно, последовательность U3 из лентивирусного 5' LTR может заменяться промоторной последовательностью в вирусной конструкции, такой как гетерологичная промоторная последовательность. Это может повысить титр вируса, извлекаемого из пакующей клеточной линии. Энхансерная последовательность также может включаться. Можно использовать любое сочетание энхансер/промотор, которое повышает экспрессирование генома вирусной РНК в пакующей клеточной линии. В одном из примеров, используется энхансерная/промоторная последовательность CMV (патент США №5385839 и патент США №5168062).
[563] В определенных вариантах осуществления, риск инсерционного мутагенеза может сводиться к минимуму посредством конструирования генома ретровирусного вектора, такого как геном лентивирусного вектора, чтобы он был дефектным при встраивании. Можно использовать разнообразные подходы для получения генома невстраиваемого вектора. В некоторых вариантах осуществления, мутация (мутации) может быть получена с помощью генной инженерии в компоненте фермента интегразы гена pol, так что он кодирует белок с неактивной интегразой. В некоторых вариантах осуществления, сам геном вектора может модифицироваться для предотвращения встраивания, например, посредством мутации или делеции одного или обоих сайтов присоединения или делая 3' LTR-проксимальный полипуриновый тракт (PPT) нефункциональным с помощью делеции или модификации. В некоторых вариантах осуществления, доступны негенетические подходы; они включают фармакологические агенты, которые ингибируют одну или несколько функций интегразы. Эти подходы не являются взаимоисключающими; то есть, их можно использовать по несколько одновременно. Например, как интеграза, так и сайты присоединения могут быть нефункциональными, или нефункциональными могут быть интеграза и сайт PPT, или могут быть нефункциональными сайты присоединения и сайт PPT, или все они могут быть нефункциональными. Такие способы и геномы вирусных векторов известны и доступны (смотри Philpott and Thrasher, Human Gene Therapy 18:483, 2007; Engelman et al. J Virol 69:2729, 1995; Brown et al J Virol 73:9011 (1999); WO 2009/076524; McWilliams et al., J Virol 77:11150, 2003; Powell and Levin J Virol 70:5288, 1996).
[564] В некоторых вариантах осуществления, вектор содержит последовательности для размножения в клетке-хозяине, такой как прокариотическая клетка-хозяин. В некоторых вариантах осуществления, нуклеиновая кислота вирусного вектора содержит один или несколько источников репликации для размножения в прокариотической клетке, такой как бактериальная клетка. В некоторых вариантах осуществления, векторы, которые содержат прокариотический источник репликации, также могут содержать ген, экспрессирование которого дает детектируемый или селективный маркер, такой как стойкость к лекарственному средству.
[565] Геном вирусного вектора, как правило, конструируется в форме плазмиды, которая может трансфицироваться в пакующую или продуцентную линию клеток. Можно использовать любой из множества известных способов для получения ретровирусных частиц, геном которых содержит копию РНК генома вирусного вектора. В некоторых вариантах осуществления, по меньшей мере, два компонента участвуют в приготовлении системы доставки гена на основе вируса: первый, пакующие плазмиды, охватывающие структурные белки, а также ферменты необходимые для генерирования частицы вирусного вектора, и второй, сам вирусный вектор, то есть, генетический материал, который должен переноситься. Средства защиты для биологической безопасности могут вводиться в дизайн одного или обоих этих компонентов.
[566] В некоторых вариантах осуществления, пакующая плазмида может содержать все ретровирусные белки, такие как белки HIV-1, кроме белков оболочки (Naldini et al., 1998). В других вариантах осуществления, в вирусных векторах могут отсутствовать дополнительные вирусные гены, такие как те, которые ассоциированы с вирулентностью, например, vpr, vif, vpu и nef, и/или Tat, первичный трансактиватор HIV. В некоторых вариантах осуществления, лентивирусные векторы, такие как лентивирусные векторы на основе HIV, могут содержать только три гена родительского вируса: gag, pol и rev, что уменьшает или устраняет возможность восстановления вируса дикого типа посредством рекомбинации.
[567] В некоторых вариантах осуществления, геном вирусного вектора вводится в пакующую клеточную линию, которая содержит все компоненты необходимые для упаковки вирусной геномной РНК, транскрибированной из генома вирусного вектора, в вирусные частицы. Альтернативно, геном вирусного вектора может содержать один или несколько генов, кодирующих вирусные компоненты, в дополнение к одной или нескольким последовательностям, например, рекомбинантным нуклеиновым кислотам, представляющим интерес. Однако, в некоторых аспектах, для предотвращения репликации генома в целевой клетке, эндогенные вирусные гены, необходимые для репликации, удаляются и обеспечиваются отдельно в пакующей клеточной линии.
[568] В некоторых вариантах осуществления, пакующая клеточная линия трансфицируется одним или несколькими векторами плазмид, содержащими компоненты необходимые для генерирования частиц. В некоторых вариантах осуществления, пакующая клеточная линия трансфицируется плазмидой, содержащей геном вирусного вектора, включая LTR, цис-действующую пакующую последовательность и последовательность представляющую интерес, то есть нуклеиновую кислоту, кодирующую рецептор антигена, такой как CAR; и одну или несколько хелперных плазмид, кодирующих ферментативные и/или структурные компоненты вируса, такие как Gag, pol и/или rev. В некоторых вариантах осуществления, используют множество векторов для разделения различных генетических компонентов, которые генерируют частицы ретровирусных векторов. В некоторых таких вариантах осуществления, поставка отдельных векторов в пакующую клетку уменьшает шанс событий рекомбинации, которые могли бы в ином случае генерировать репликационно компетентные вирусы. В некоторых вариантах осуществления, можно использовать один вектор плазмиды, содержащий все ретровирусные компоненты.
[569] В некоторых вариантах осуществления, частица ретровирусного вектора, например, частица лентивирусного вектора, псевдотипируется для увеличения эффективности трансдуцирования клеток-хозяев. Например, частица ретровирусного вектора, такая как частица лентивирусного вектора, в некоторых вариантах осуществления псевдотипируется с помощью гликопротеина VSV-G, что обеспечивает широкой диапазон клеток-хозяев, расширяя типы клеток, которые могут трансдуцироваться. В некоторых вариантах осуществления, пакующая клеточная линия трансфицируется плазмидой или полинуклеотидом, кодирующим ненативный гликопротеин оболочки, например, чтобы включить ксенотропные, политропные или амфотропые оболочки, такие как оболочка вируса Sindbis, GALV или VSV-G.
[570] В некоторых вариантах осуществления, пакующая клеточная линия обеспечивает компоненты, включая вирусные регуляторные и структурные белки, которые требуются при переносе для упаковки вирусной геномной РНК в виде частиц лентивирусных векторов. В некоторых вариантах осуществления, пакующая клеточная линия может представлять собой любую линию клеток, которая может экспрессировать лентивирусные белки и продуцировать функциональные частицы лентивирусных векторов. В некоторых аспектах, пригодные для использования пакующие клеточные линии включают клетки 293 (ATCC CCL X), 293T, HeLA (ATCC CCL 2), D17 (ATCC CCL 183), MDCK (ATCC CCL 34), BHK (ATCC CCL-10) и Cf2Th (ATCC CRL 1430).
[571] В некоторых вариантах осуществления, пакующая клеточная линия стабильно экспрессирует вирусный белок (белки). Например, в некоторых аспектах, может конструироваться пакующая клеточная линия, содержащая gag, pol, rev и/или другие структурные гены, но без LTR и пакующих компонентов. В некоторых вариантах осуществления, пакующая клеточная линия может транзиентно трансфицироваться молекулами нуклеиновых кислот, кодирующими один или несколько вирусных белков, вместе с геномом вирусного вектора, содержащим молекулу нуклеиновой кислоты, кодирующую гетерологичный белок, и/или нуклеиновой кислоты, кодирующей гликопротеин оболочки.
[572] В некоторых вариантах осуществления, вирусные векторы и пакующие и/или хелперные плазмиды вводятся посредством трансфицирования или инфицирования в пакующую клеточную линию. Пакующая клеточная линия продуцирует частицы вирусных векторов, которые содержат геном вирусного вектора. Способы трансфицирования или инфицирования хорошо известны. Неограничивающие примеры включают кальций-фосфатный, DEAE-декстрановый способ и способы липофицирования, электропорообразования и микроинъекцию.
[573] Когда рекомбинантная плазмида и ретровирусный LTR, и пакующие последовательности вводятся в специальную линию клеток (например, с помощью кальций-фосфатной преципитации), пакующие последовательности могут сделать возможным упаковку транскрипта РНК рекомбинантной плазмиды в вирусные частицы, которые затем могут секретироваться в культурных средах. Затем среды, содержащие рекомбинантные ретровирусы, в некоторых вариантах осуществления, собираются, необязательно, концентрируются и используются для переноса гена. Например, в некоторых аспектах, после сотрансфицирования пакующих плазмид и вектора переноса в пакующую клеточную линию, частиц вирусных векторов извлекаются из культурных сред и титруются с помощью стандартных способов, используемых специалистами в данной области.
[574] В некоторых вариантах осуществления, ретровирусный вектор, такой как лентивирусный вектор, может продуцироваться в пакующей клеточной линии, такой как иллюстративная линия клеток HEK 293Т, посредством введения плазмид, чтобы сделать возможным генерирование лентивирусных частиц. В некоторых вариантах осуществления, пакующая клетка трансфицируется и/или содержит полинуклеотид, кодирующий gag и pol, и полинуклеотид, кодирующий рекомбинантный рецептор, такой как рецептор антигена, например, CAR. В некоторых вариантах осуществления, пакующая клеточная линия необязательно, и/или дополнительно трансфицируется и/или содержит полинуклеотид, кодирующий белок rev. В некоторых вариантах осуществления, пакующая клеточная линия необязательно, и/или дополнительно трансфицируется и/или содержит полинуклеотид, кодирующий ненативный гликопротеин оболочки, такой как VSV-G. В некоторых таких вариантах осуществления, приблизительно через два дня после трансфицирования клеток, например, клеток HEK 293Т, клеточный супернатант содержит рекомбинантные лентивирусные векторы, которые можно извлекать и титровать.
[575] Извлекаемые и/или продуцируемые частицы ретровирусных векторов можно использовать для трансдуцирования целевых клеток, используя способы, как описано. Попадая в целевые клетки, вирусная РНК обратно транскрибируется, импортируется в ядро и стабильно встраивается в геном хозяина. Через один или два дня после встраивания вирусной РНК, можно детектировать экспрессирование рекомбинантного белка, например, рецептор антигена, такого как CAR.
[576] В некоторых вариантах осуществления, предлагаемые способы включают способы трансдуцирования клеток посредством приведения в контакт, например, инкубирования, композиции клеток, содержащей множество клеток, с вирусной частицей. В некоторых вариантах осуществления, клетки, которые должны трансфицироваться или трансдуцироваться, представляют собой или содержат первичные клетки, полученные у субъекта, такие как обогащенные и/или селектированные клетки субъекта.
[577] В некоторых вариантах осуществления, концентрация клеток, которые должны трансдуцироваться, в композиции составляет от или примерно от 1,0 × 105 клетки/мл до 1,0 × 108 клеток/мл, например, по меньшей мере, или примерно, по меньшей мере, или примерно 1,0 × 105 клеток/мл, 5 × 105 клеток/мл, 1 × 106 клеток/мл, 5 × 106 клеток/мл, 1 × 107 клеток/мл, 5 × 107 клеток/мл или 1 × 108 клеток/мл.
[578] В некоторых вариантах осуществления, вирусные частицы получаются при определенном отношении копий частиц вирусных векторов или их инфекционных единиц (IU) к общему количеству клеток, которые должны трансдуцироваться (IU/клетка). Например, в некоторых вариантах осуществления, вирусные частицы присутствуют в ходе приведения в контакт при, или примерно при, или, по меньшей мере при, или примерно при 0,5, 1, 2, 3, 4, 5, 10, 15, 20, 30, 40, 50 или 60 IU частиц вирусного вектора на одну клеток.
[579] В некоторых вариантах осуществления, титр частиц вирусных векторов находится в пределах между или примерно между 1 × 106 IU/мл и 1 × 108 IU/мл, например, в пределах между или примерно между 5 × 10 6 IU/мл и 5 × 107 IU/мл, например, составляет, по меньшей мере, 6 × 106 IU/мл, 7 × 106 IU/мл, 8 × 106 IU/мл, 9 × 106 IU/мл, 1 × 107 IU/мл, 2 × 107 IU/мл, 3 × 107 IU/мл, 4 × 107 IU/мл или 5 × 107 IU/мл.
[580] В некоторых вариантах осуществления, трансдуцирование может достигаться при множественности инфицирования (MOI) меньше 100, например, как правило, меньше 60, 50, 40, 30, 20, 10, 5 или меньше.
[581] В некоторых вариантах осуществления, способ включает приведение в контакт или инкубирование клеток вместе с вирусными частицами. В некоторых вариантах осуществления, приведение в контакт осуществляется в течение 30 минут - 72 часов, например, 30 минут - 48 часов, 30 минут - 24 часов или 1 часа - 24 часов, например, по меньшей мере или примерно, по меньшей мере, 30 минут, 1 часа, 2 часов, 6 часов, 12 часов, 24 часов, 36 часов или более.
[582] В некоторых вариантах осуществления, приведение в контакт осуществляется в растворе. В некоторых вариантах осуществления, клетки и вирусные частицы приводятся в контакт в объеме от или примерно от 0,5 мл до 500 мл, например, от или примерно от 0,5 мл до 200 мл, от 0,5 мл до 100 мл, от 0,5 мл до 50 мл, от 0,5 мл до 10 мл, от 0,5 мл до 5 мл, от 5 мл до 500 мл, от 5 мл до 200 мл, от 5 мл до 100 мл, от 5 мл до 50 мл, от 5 мл до 10 мл, от 10 мл до 500 мл, от 10 мл до 200 мл, от 10 мл до 100 мл, от 10 мл до 50 мл, от 50 мл до 500 мл, от 50 мл до 200 мл, от 50 мл до 100 мл, от 100 мл до 500 мл, от 100 мл до 200 мл или от 200 мл до 500 мл.
[583] В некоторых вариантах осуществления приведение в контакт может осуществляться с помощью центрифугирования, такого как спинокуляция (например, центробежная инокуляция). В некоторых вариантах осуществления, композиция, содержащая клетки, вирусные частицы и реагент, может перемешиваться вращательным движением, как правило, при относительно низком усилии или скорости, например, при скорости ниже, чем используется для осаждения клеток, например, от или примерно от 600 об/мин до 1700 об/мин (например, при или примерно при, или, по меньшей мере, при 600 об/мин, 1000 об/мин или 1500 об/мин или 1700 об/мин). В некоторых вариантах осуществления, перемешивание вращательным движением осуществляется при силе, например, относительной центробежной силе, от или примерно от 100 g до 3200 g (например, при или примерно при, или, по меньшей мере при, или примерно при 100 g, 200 g, 300 g, 400 g, 500 g, 1000 g, 1500 g, 2000 g, 2500 g, 3000 g или 3200 g), как измерено, например, на внутренней или наружной стенке камеры или полости. Термин “относительная центробежная сила” или RCF, как правило, понимается как эффективная сила, прикладываемая к объекту или веществу (такому как клетка, образец или осадок и/или точка в камере или в другом контейнере, который вращается), по отношению к силе земного тяготения, в конкретной точке в пространстве относительно оси вращения. Величина может определяться с использованием хорошо известных формул, учитывая силу тяжести, скорость вращения и радиус вращения (расстояние от оси вращения до объекта, вещества или частицы, где измеряется RCF).
[584] В определенных вариантах осуществления, исходные клетки обрабатывают, инкубируют или приводят в контакт с частицами, например, шариками, которые содержат связывающие молекулы, которые связывают или распознают рекомбинантный рецептор, который кодируется вирусной ДНК.
[585] В некоторых вариантах осуществления, инкубирование клеток вместе с частицами вирусных векторов дает в результате или продуцирует выходную композицию, содержащую клетки, трансдуцированные частицами вирусных векторов.
2. Невирусные векторы
[586] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносятся в Т-лимфоциты посредством электропорообразования (смотри, например, Chicaybam et al, (2013) PLoS ONE 8(3): e60298 и Van Tedeloo et al. (2000) Gene Therapy 7(16): 1431-1437). В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносятся в Т-лимфоциты посредством транспозиции (смотри, например, Manuri et al. (2010) Hum Gene Ther 21(4): 427-437; Sharma et al. (2013) Molec Ther Nucl Acids 2, e74; и Huang et al. (2009) Methods Mol Biol 506: 115-126). Другие способы введения и экспрессирования генетического материала в иммунных клетках включают кальций-фосфатное трансфицирование (например, как описано в Current Protocols в Molecular Biology, John Wiley & Sons, New York. N.Y.), слияние протопластов, катионное медиируемое липосомами трансфицирование; бомбардировку микрочастицами, облегченную вольфрамовыми частицами (Johnston, Nature, 346: 776-777 (1990)); и стронций-фосфатную сопреципитацию ДНК (Brash et al., Methods, Cell Biol., 7: 2031-2034 (1987)).
[587] Другие подходы и векторы для переноса нуклеиновых кислот, кодирующих рекомбинантные продукты, описаны, например, в Международной заявке на патент, публикация номер: WO 2014055668, и в патенте США №7446190.
[588] В некоторых вариантах осуществления, рекомбинантные нуклеиновые кислоты переносятся в Т-лимфоциты с помощью транспозонов. Транспозоны (транспозируемые элементы) представляют собой подвижные сегменты ДНК, которые могут перемещаться от одного локуса в другой в геномах. Эти элементы перемещаются через консервативный механизм “разрежь и склей”: транспозаза катализирует вырезание транспозона из его исходного места и способствует его повторному встраиванию где-то еще в геноме. Транспозаза-дефицитные элементы могут мобилизироваться, если транспозаза обеспечивается другим геном транспозазы. Таким образом, транспозоны можно использовать для введения чужеродной ДНК в геном хозяина без использования вирусной системы трансдуцирования. Примеры транспозонов, пригодных для использования вместе с клетками млекопитающих, например, с первичными лейкоцитами человека, включают, но, не ограничиваясь этим, Sleeping Beauty и Piggybac.
[589] Трансфицирование на основе транспозона представляет собой двухкомпонентную систему, состоящую из транспозазы и транспозона. В некоторых вариантах осуществления, система содержит генно-инженерный транспозон, содержащий чужеродную ДНК (также упоминаемую в настоящем документе как карго ДНК), например, ген, кодирующий рекомбинантный рецептор, который фланкирован последовательностями инвертированного повтора/прямого повтора (IR/DR), которые распознаются соответствующей транспозазой. В некоторых вариантах осуществления, невирусная плазмида кодирует транспозазу под контролем промотора. Трансфицирование плазмиды в клетку-хозяина дает в результате транзиторное экспрессирование транспозазы, таким образом в течение начального периода после трансфицирования, транспозаза экспрессируется при уровнях достаточных для встраивания транспозона в геномную ДНК. В некоторых вариантах осуществления, сама транспозаза не встраивается в геномную ДНК, и поэтому экспрессирование транспозазы уменьшается со временем. В некоторых вариантах осуществления, транспозаза экспрессируется клеткой-хозяином на уровнях, достаточных для встраивания соответствующего транспозона, в течение примерно меньше 4 часов, примерно меньше 8 часов, примерно меньше 12 часов, примерно меньше 24 часов, примерно меньше 2 дней, примерно меньше 3 дней, примерно меньше 4 дней, примерно меньше 5 дней, примерно меньше 6 дней, примерно меньше 7 дней, примерно меньше 2 недель, примерно меньше 3 недель, примерно меньше 4 недель, примерно меньше недели или примерно меньше 8 недель. В некоторых вариантах осуществления, карго ДНК, которая вводится в геном хозяина, впоследствии не удаляется из генома хозяина, по меньшей мере, потому что хозяин не экспрессирует эндогенную транспозазу, которая может вырезать карго ДНК.
[590] Sleeping Beauty (SB) представляет собой синтетический элемент суперсемейства транспозонов Tc/1-mariner, реконструированный из спящих элементов, фиксированных в геноме лососевых рыб. Трансфицирование на основе SB транспозона представляет собой двухкомпонентную систему, состоящую из транспозазы и транспозона, содержащего последовательности инвертированного повтора/прямого повтора (IR/DR), которые дают в результате прецизионное встраивание в динуклеотид TA. Транспозон конструируется с помощью кассеты экспрессии, представляющей интерес, фланкированной IR/DR. Транспозаза SB связывает конкретные сайты связывания, которые расположены на IR транспозона Sleeping Beauty. Транспозаза SB медиирует встраивание транспозона, подвижного элемента, кодирующего карго последовательность, фланкируемую на обеих сторонах инвертированными концевыми повторами, которые фиксируют сайты связывания для каталитического фермента (SB). Стабильное экспрессирование возникает в результате, когда SB вставляет последовательности генов в хромосомы позвоночных на целевом динуклеотиде TA с помощью механизма разрежь и склей. Это система используется для генной инженерии разнообразных типов клеток позвоночных, включая первичные лейкоциты периферической крови человека. В некоторых вариантах осуществления, клетки приводятся в контакт, инкубируются и/или обрабатываются транспозоном SB, содержащим карго ген, например, ген, кодирующий рекомбинантный рецептор или CAR, фланкированный IR последовательностями SB. В конкретных вариантах осуществления, клетки, которые должны трансфицироваться, приводятся в контакт, инкубируются и/или обрабатываются вместе с плазмидой, содержащей SB транспозона, содержащий карго ген, например, ген, кодирующий CAR, фланкированный IR последовательностями SB. В определенных вариантах осуществления, плазмида дополнительно содержит ген, кодирующий транспозазу SB, которая не фланкируется IR последовательностями SB.
[591] Иллюстративная IR последовательность SB приводится в SEQ ID NO: 26. Иллюстративная полинуклеотидная последовательность, кодирующая транспозазу SB, и последовательность аминокислот иллюстративной SB транспозазы приводятся в SEQ ID NOS: 24 и 25, соответственно.
[592] PiggyBac (PB) представляет собой другую систему транспозона, которую можно использовать для встраивания карго ДНК в геномную ДНК хозяина, например, человека. Транспозаза PB распознает специфичные к PB транспозона последовательности инвертированных концевых повторов (ITR), расположенные на обоих концах транспозона, и эффективно перемещает содержание с исходных сайтов, и эффективно встраивает их в хромосомальные сайты TTAA. Система транспозона PB дает возможность мобилизации генов, представляющих интерес, между двумя ITR в векторе PB в целевых геномах. Система PB используется для генной инженерии различных типов клеток позвоночных, включая первичные клетки человека. В некоторых вариантах осуществления, клетки, которые должны трансфицироваться, приводятся в контакт, инкубируются и/или обрабатываются вместе с транспозоном PB, содержащим карго ген, например, ген, кодирующий CAR, фланкированный IR последовательностями PB. В конкретных вариантах осуществления, клетки, которые должны трансфицироваться, приводятся в контакт, инкубируются и/или обрабатываются вместе с плазмидой, содержащей транспозон PB, содержащий карго ген, например, ген, кодирующий CAR, фланкированный IR последовательностями PB. В определенных вариантах осуществления, плазмида дополнительно содержит ген, кодирующий транспозазу SB, которая не фланкируется IR последовательностями PB.
[593] Иллюстративная IR последовательность PB иллюстрируется SEQ ID NO: 27. Иллюстративная полинуклеотидная последовательность, кодирующая транспозазу PB иллюстрируется SEQ ID NO: 28. Последовательность аминокислот иллюстративной транспозазы PB иллюстрируется SEQ ID NO: 29.
[594] В некоторых вариантах осуществления, различные элементы транспозона/транспозазы, используемые в рассматриваемых способах, например, вектор (векторы) SB или PB, могут быть получены с помощью стандартных способов рестрикционного ферментативного расщепления, лигирования и молекулярного клонирования. Один из протоколов для конструирования рассматриваемых векторов включает следующие стадии. Сначала, очищенные фрагменты нуклеиновых кислот, содержащие последовательности нуклеотидов желаемого компонента, а также дополнительные последовательности отщепляются с помощью рестрикционных эндонуклеаз от начальных источников, например, вектора, содержащего ген транспозазы. Затем фрагменты, содержащие последовательности желаемых нуклеотидов, отделяются от нежелательных фрагментов различных размеров с использованием обычных способов разделения, например, с помощью электрофореза на агарозном геле. Желаемые фрагменты вырезают из геля и лигируют вместе в соответствующей конфигурации, так что получается круговая нуклеиновая кислота или плазмида, содержащая желаемые последовательности, например, последовательности, соответствующие различным элементам рассматриваемых векторов, как описано выше. При желании, круговые молекулы, сконструированные таким образом, затем амплифицируются в прокариотическом хозяине, например, E. coli. Процедуры расщепления, конструирования плазмиды, трансформации клеток и получения плазмиды, участвующие в этих стадиях, хорошо известны специалистам в данной области, и ферменты необходимые для рестрикции и лигирования доступны коммерчески. (Смотри, например, R. Wu, Ed., Methods in Enzymology, Vol. 68, Academic Press, N.Y. (1979); T. Maniatis, E. F. Fritsch и J. Sambrook, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1982); Catalog 1982-83, New England Biolabs, Inc.; Catalog 1982-83, Bethesda Research Laboratories, Inc. Пример того, как конструируют векторы, используемые в рассматриваемых способах, приводится в Экспериментальном разделе, ниже. Приготовление репрезентативной системы транспозона Sleeping Beauty описывается также в WO 98/40510 и WO 99/25817).
[595] В некоторых вариантах осуществления, трансдуцирование с помощью транспозонов осуществляется с помощью плазмиды, которая содержит ген транспозазы, и плазмиды, которая содержит транспозон, который содержит последовательность карго ДНК, которая фланкирована последовательностями инвертированный повтор/прямой повтор (IR/DR), которые распознаются транспозазой. В определенных вариантах осуществления, последовательность карго ДНК кодирует гетерологичный белок, например, рекомбинантный рецептор Т-лимфоцита или CAR. В некоторых вариантах осуществления, плазмида содержит транспозазу и транспозон. В некоторых вариантах осуществления, транспозаза находится под контролем убиквитарного промотора или любого промотора пригодного для запуска экспрессирования транспозазы в целевой клетке. Убиквитарные промоторы включают, но, не ограничиваясь этим, EF1a, CMB, SV40, PGK1, Ubc, β-актин человека, CAG, TRE, UAS, Ac5, CaMKIIa и U6. В некоторых вариантах осуществления, карго ДНК содержит кассету селекции, делающую возможной селекцию клеток со стабильным встраиванием карго ДНК в геномную ДНК. Пригодные для использования кассеты селекции включают, но, не ограничиваясь этим, кассеты селекции, кодирующие ген устойчивости к канамицину, ген устойчивости к спектиномицину, ген устойчивости к стрептомицину, ген устойчивости к ампициллину, ген устойчивости к карбенициллину, ген устойчивости к гигромицину, ген устойчивости к блеомицину, ген устойчивости к эритромицину и ген устойчивости к полимиксину B.
[596] В некоторых вариантах осуществления, компоненты трансдуцирования с помощью транспозона, например, плазмид, содержащих SB транспозазы и SB транспозона, вводятся в целевую клетку. Можно использовать любой удобный протокол, когда протокол может обеспечить введение in vitro или in vivo системы компонентов в целевую клетку, в зависимости от положения целевой клетки. Например, когда целевая клетка представляет собой выделенную клетку, система может вводиться прямо в клетку при условиях культивирования клеток, дающих возможность для жизнеспособности целевой клетки, например, с использованием стандартной технологии трансформации. Такие технологии включают, но, необязательно, ограничиваясь этим: вирусное инфицирование, трансформацию, конъюгирование, слияние протопластов, электропорообразование, технологию генной пушки, кальций-фосфатную преципитацию, прямую микроинъекцию, доставку с помощью вирусного вектора, и тому подобное. Выбор способа, как правило, зависит от типа клетки, которая трансформируется, и от обстоятельств, при которых трансформация имеет место (то есть, in vitro, ex vivo или in vivo). Общее обсуждение этих способов можно найти в Ausubel, et al, Short Protocols in Molecular Biology, 3rd ed., Wiley & Sons,1995.
[597] В некоторых вариантах осуществления, SB транспозона и источник SB транспозазы вводятся в целевую клетку многоклеточного организма, например, млекопитающего или человека, при условиях достаточных для вырезания фланкированной нуклеиновой кислоты инвертированного повтора из вектора, несущего транспозон, и для последующего встраивания вырезанной нуклеиновой кислоты в геном целевой клетки. Кроме того, некоторые варианты осуществления включают стадии обеспечения того, что необходимая активность транспозазы имеет место в целевой клетке вместе с введенным транспозоном. В зависимости от структуры самого вектора транспозона, то есть от того содержит ли вектор область, кодирующую продукт, имеющий активность транспозазы, способ может дополнительно включать введение в целевую клетку второго вектора, который кодирует необходимую активность транспозазы.
[598] В некоторых вариантах осуществления, количество нуклеиновой кислоты вектора, содержащего транспозон, и количество нуклеиновой кислоты вектора, кодирующего транспозазу, которое вводится в клетку, является достаточным для желаемого вырезания и вставки нуклеиновой кислоты транспозона в геном целевой клетки. Как таковое, количество вводимой нуклеиновой кислоты вектора должно обеспечить достаточную величину активности транспозазы и достаточное количество копий нуклеиновой кислоты, которую желательно вставить в целевую клетку. Количество нуклеиновой кислоты вектора, которая вводится в целевую клетку, изменяется в зависимости от эффективности конкретного протокола введения, который используется, например, от конкретного протокола введения ex vivo, который используется.
[599] После того как ДНК вектора поступает в целевую клетку в сочетании с необходимой транспозазой, область нуклеиновой кислоты вектора, которая фланкируется инвертированными повторами, то есть нуклеиновая кислота вектора, расположенная между инвертированными повторами, распознаваемыми транспозазой Sleeping Beauty, вырезается из вектора с помощью имеющейся транспозазы и вставляется в геном целевой клетки. За введением ДНК вектора в целевую клетку как таковым следует последующее медиируемое транспозазой вырезание и вставка экзогенной нуклеиновой кислоты, переносимой вектором, в геном целевой клетки. В конкретных вариантах осуществления, вектор встраивается в геномы, по меньшей мере, 1%, по меньшей мере, 2%, по меньшей мере, 3%, по меньшей мере, 4%, по меньшей мере, 5%, по меньшей мере, 6%, по меньшей мере, 7%, по меньшей мере, 8%, по меньшей мере, 9%, по меньшей мере, 10%, по меньшей мере, 15% или, по меньшей мере, 20% клеток, которые трансфицируются с помощью SB транспозона и/или SB транспозазы. В некоторых вариантах осуществления, встраивание нуклеиновой кислоты в геном целевой клетки является стабильным, то есть, нуклеиновая кислота вектора остается присутствовать в геноме целевой клетки и после транзиентного периода времени и переносится на часть хромосомального генетического материала потомства целевой клетки.
[600] В определенных вариантах осуществления, транспозоны используют для встраивания нуклеиновых кислот, то есть полинуклеотидов различных размеров в геном целевой клетки. В некоторых вариантах осуществления, размер ДНК, которую вставляют в геном целевой клетки с использованием рассматриваемых способов, находится в пределах примерно от 0,1 kb до 200 kb, примерно от 0,5 kb до 100 kb, примерно от 1,0 kb примерно до 8,0 kb, примерно от 1,0 примерно до 200 kb, примерно от 1,0 примерно до 10 kb, примерно от 10 kb примерно до 50 kb, примерно от 50 kb примерно до 100 kb или примерно от 100 kb примерно до 200 kb. В некоторых вариантах осуществления, размер ДНК, которую вставляют в геном целевой клетки с использованием рассматриваемых способов, находится в пределах примерно от 1,0 kb примерно до 8,0 kb. В некоторых вариантах осуществления, размер ДНК, которую вставляют в геном целевой клетки с использованием рассматриваемых способов, находится в пределах примерно от 1,0 примерно до 200 kb. В конкретных вариантах осуществления, размер ДНК, которую вставляют в геном целевой клетки с использованием рассматриваемых способов, находится в пределах примерно от 1,0 kb примерно до 8,0 kb.
V. СПОСОБЫ ДЕТЕКТИРОВАНИЯ И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ
[601] В настоящем документе предлагаются способы детектирования химерного рецептора антигена (CAR), содержащего внеклеточный антигенсвязывающий домен, который представляет собой антитело анти-BCMA, посредством приведения в контакт композиции или биологического образца, содержащего клетки, экспрессирующие CAR (CAR-экспрессирующие клетки), со слитым белком BCMA-Fc. В некоторых вариантах осуществления, способ дополнительно включает детектирование того, образуется ли комплекс между слитым белком BCMA-Fc и CAR, экспрессируемого клетками или на них, в композиции или биологическом образце, например, детектирование присутствия или отсутствия, или уровня такого связывания. В некоторых вариантах осуществления, детектирование включает детектирование клеток, связанных со слитым белком BCMA-Fc. В некоторых вариантах осуществления, слитый белок BCMA-Fc прямо или опосредованно метится для детектирования.
[602] В некоторых вариантах осуществления, антиген BCMA слитого белка BCMA-Fc представляет собой или содержит внеклеточный домен BCMA или его часть, содержащую эпитоп, распознаваемый рецептором антигена, например, CAR. В определенных вариантах осуществления, рекомбинантный слитый белок BCMA-Fc содержит антиген BCMA, который содержит внеклеточный домен BCMA человека или его часть, который представляет собой или содержит эпитоп, распознаваемый CAR. В некоторых вариантах осуществления, антиген BCMA слитого белка BCMA-Fc не содержит трансмембранного домена и цитоплазматического домена нативного BCMA человека. Таким образом, в некоторых вариантах осуществления, антиген BCMA слитого белка BCMA-Fc представляет собой, состоит или в основном состоит из внеклеточного домена или его части от нативного BCMA человека. В некоторых вариантах осуществления, антиген BCMA слитого белка BCMA-Fc представляет собой или содержит, в некоторых случаях, состоит или в основном состоит из полипептида с последовательностью аминокислот, по меньшей мере, с 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичностью последовательностей с SEQ ID NO: 1 или представляет собой ее фрагмент, содержащий, по меньшей мере, 50, по меньшей мере, 55, по меньшей мере, 60, по меньшей мере, 65, по меньшей мере, 70, по меньшей мере, 75, по меньшей мере, 80, по меньшей мере, 85, по меньшей мере, 90, по меньшей мере, 95, по меньшей мере, 100, по меньшей мере, 110, по меньшей мере, 120, по меньшей мере, 130, по меньшей мере, 140, по меньшей мере, 150, по меньшей мере, 160, по меньшей мере, 170 или, по меньшей мере, 180 заменимых аминокислот SEQ ID NO: 1, который распознается или специфически связывается антигенсвязывающим доменом CAR. В некоторых вариантах осуществления, антиген BCMA представляет собой или содержит, в некоторых случаях, состоит или в основном состоит из последовательности, приведенной в SEQ ID NO: 1, или ее части, которая представляет собой или содержит эпитоп, распознаваемый рецептором антигена, например, CAR.
[603] В некоторых вариантах осуществления, рекомбинантный антиген BCMA или его часть сливается прямо или опосредованно с константной областью или доменом иммуноглобулина, таким, например, как Fc-домен или его часть IgG, включая субтипы IgG1, IgG2, IgG3 или IgG4, IgA, IgE, IgD и IgM и их модифицированные формы. В конкретных вариантах осуществления, антиген BCMA связывается, прямо или опосредованно с Fc-доменом. В некоторых вариантах осуществления, полипептид представляет собой слитый полипептид, содержащий антиген BCMA, или его часть и Fc-домен.
[604] В некоторых вариантах осуществления, Fc-домен состоит из второго и третьего константных доменов (то есть, доменов CH2 и CH3) тяжелой цепи изотипа IgG, IgA или IgD, например, CH2 или CH3 изотипов IgG, IgA и IgD. В некоторых вариантах осуществления, Fc-домен состоит из трех константных доменов тяжелой цепи (то есть, доменов CH2, CH3 и CH4) изотипа IgM или IgE. В некоторых вариантах осуществления, Fc-домен может дополнительно включать шарнирную последовательность или ее часть. В определенных аспектах, Fc-домен содержит часть шарнирного домена молекулы иммуноглобулина плюс домены CH2 и CH3 или все их. В некоторых случаях, Fc-домен может образовывать димер из двух полипептидных цепей, соединенных одной или несколькими дисульфинимидными связями. В некоторых вариантах осуществления, Fc-домен получают из иммуноглобулина (например, IgG, IgA, IgM или IgE) от соответствующего млекопитающего (например, человека, мыши, крысы, козы, овцы или обезьяны). В некоторых вариантах осуществления, Fc-домен содержит домены CH2 и CH3 IgG. В определенных вариантах осуществления, Fc-домен сливается с C-концом антигена BCMA. В конкретных вариантах осуществления, Fc-домен сливается с N-концом антигена BCMA.
[605] В некоторых вариантах осуществления, Fc-домен представляет собой Fc-домен IgG или его часть или вариант. В некоторых вариантах осуществления, Fc-домен представляет собой Fc-домен IgG человека или его часть или вариант, который содержит последовательность аминокислот, приведенную в SEQ ID NO: 2, или последовательность аминокислот, которая имеет, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с последовательностью, приведенной в SEQ ID NO: 2. В конкретных вариантах осуществления, Fc-домен представляет собой Fc-домен IgG человека дикого типа или его часть или вариант. В конкретных вариантах осуществления, Fc-домен представляет собой вариант Fc-домен IgG1 человека дикого типа.
[606] В некоторых вариантах осуществления, слитый полипептид содержит вариантный Fc-домен. В определенных вариантах осуществления, вариантный Fc-домен IgG человека содержит мутацию, например, замещение, делецию или вставку, которая сокращает, уменьшает и/или ослабляет спаривание между Fc-доменом и легкой цепью. В некоторых вариантах осуществления, вариантный Fc-домен IgG человека содержит мутацию, которая уменьшает аффиность связывания между Fc-доменом и Fc-рецептором. В конкретных вариантах осуществления, вариантный Fc-домен IgG человека содержит мутацию, которая сокращает, уменьшает и/или ослабляет взаимодействие или вероятность, или правдоподобие взаимодействия между Fc-доменом и Fc-рецептором. В некоторых вариантах осуществления, вариантный Fc-домен IgG человека содержит мутацию, которая уменьшает аффиность связывания между Fc-доменом и белком системы комплемента. В конкретных вариантах осуществления, вариантный Fc-домен IgG человека содержит мутацию, которая сокращает, уменьшает и/или ослабляет взаимодействие или вероятность, или правдоподобие взаимодействия между Fc-доменом и белок системы комплемента.
[607] В некоторых вариантах осуществления, BCMA-Fc содержит вариантный Fc-домен IgG1 человека. В некоторых вариантах осуществления, вариантный Fc-домен IgG человека содержит замещение цистина серином в шарнирной области Fc-домена. В некоторых вариантах осуществления, вариантный Fc-домен IgG человека содержит замещение лейцина аланином в шарнирной области Fc-домена. В конкретных вариантах осуществления, вариантный Fc-домен IgG человека содержит замещение глицина аланином в шарнирной области. В определенных вариантах осуществления, вариантный Fc-домен IgG человека содержит замещение аланина серином в области CH2 Fc-домена. В некоторых вариантах осуществления, вариантный Fc-домен IgG человека содержит замещение пролина серином в области CH2 Fc-домена. В некоторых вариантах осуществления, вариантный Fc-домен IgG человека содержит последовательность аминокислот, как приведено в SEQ ID NO: 28.
[608] В некоторых вариантах осуществления, BCMA-Fc содержит слитый полипептид, содержащий Fc-домен, где Fc-домен присутствует на C-конце слитого полипептида.
[609] В некоторых вариантах осуществления, BCMA-Fc представляет собой слитый полипептид, содержащий BCMA полипептид или его часть, и Fc-домен. В некоторых вариантах осуществления, BCMA полипептид или его часть содержит последовательность аминокислот, приведенную в SEQ ID NO: 1, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 1 и содержит эпитоп, распознаваемый рецептором антигена, например, CAR. В некоторых вариантах осуществления, Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 2, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 2. В некоторых вариантах осуществления, Fc-домен содержит последовательность аминокислот, приведенную в SEQ ID NO: 28, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 28. В некоторых вариантах осуществления, антиген BCMA содержит BCMA или его часть или вариант и метку или слитый домен, например, Fc-домен. В конкретных вариантах осуществления, антиген BCMA содержит всю последовательность аминокислот, приведенную в SEQ ID NO: 35, или ее часть, или последовательность аминокислот, которая демонстрирует, по меньшей мере, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичность последовательности с SEQ ID NO: 35 и которая содержит эпитоп, распознаваемый рецептором антигена, например, CAR.
[610] В некоторых вариантах осуществления, BCMA-F представляет собой димер, содержащий два или более антигенов BCMA, как описано, каждый из которых распознается и/или связывается CAR. В некоторых вариантах осуществления, антигены BCMA являются идентичными.
[611] В определенных вариантах осуществления, способы детектирования CAR-экспрессирующих клеток со слитым белком BCMA-Fc, описанным в настоящем документе, используют для оценки CAR-экспрессирующих клеток у субъекта. В некоторых вариантах осуществления, в настоящем документе предлагаются способы использования слитого белка BCMA-Fc для оценки, измерения и/или количественного определения in vivo фармакокинетики, размножения и/или персистентности CAR-экспрессирующих клеток терапевтической композиции клеток. В некоторых вариантах осуществления, in vivo фармакокинетика, размножение и/или персистентность клеток, и/или изменения фенотипов клеток или функциональной активности клеток, таких как CAR-экспрессирующие клетки, вводимые для иммунотерапии, например, Т-клеточной терапии CAR, в способах, предлагаемых в настоящем документе, могут измеряться с помощью слитого белка BCMA-Fc. В некоторых вариантах осуществления, фармакокинетика, размножение и/или персистентность CAR-экспрессирующих клеток измеряются или оцениваются с помощью детектирования, присутствия и/или количества клеток, экспрессирующих CAR, у субъекта и/или в биологическом образце, полученном от субъекта, после введения терапевтической композиции клеток в ходе и/или после введения терапии.
[612] В некоторых аспектах, слитый белок BCMA-Fc используют вместе с проточной цитометрией для оценки количества CAR-экспрессирующих клеток в образце крови или сыворотки или органа или ткани, например, с болезненного места (например, образца опухоли) у субъекта. В некоторых аспектах, персистентность количественно определяется как количество CAR-экспрессирующих клеток на микролитр образца, например, крови или сыворотки, или как общее количество мононуклеаров периферической крови (PBMC) или лейкоцитов или Т-лимфоцитов на микролитр образца. В определенных аспектах, размножение количественно определяется как увеличение количества CAR-экспрессирующих клеток на микролитр между образцами, например, крови или сыворотки, или на общее количество мононуклеаров периферической крови (PBMC) или лейкоцитов или Т-лимфоцитов на микролитр образцов со временем. В некоторых вариантах осуществления, фармакокинетика, размножение и/или персистентность измеряют или оцениваются с помощью детектирования количества CAR-экспрессирующих клеток у субъекта и/или в образцах, собранных у субъекта, во множестве временных точек. В определенных вариантах осуществления, один или несколько образцов собирают, получают и/или отбирают у субъекта в пределах 24 часов, 48 часов, 72 часов, 4 дней, 5 дней, 6 дней, 7 дней, 10 дней, 14 дней, 21 дней, 3 недель, 4 недель, 5 недель, 6 недель, 7 недель, 8 недель, 9 недель, 10 недель, 11 недель, 12 недель, 3 месяцев, 4 месяцев, 6 месяцев, одного года или более одного года после введения терапевтической композиции клеток.
[613] В некоторых вариантах осуществления, предлагается способ оценки Т-клеточной терапии CAR анти-BCMA у индивидуума, где CAR содержит антитело анти-BCMA или его антигенсвязывающий фрагмент, и способ включает инкубирование образца от субъекта вместе со слитым белком BCMA-Fc и определение количества Т-лимфоцитов, связанных со слитым белком BCMA-Fc. В некоторых вариантах осуществления, слитый белок BCMA-Fc метится, и Т-лимфоциты, связанные со слитым белком BCMA-Fc, анализируют с помощью проточной цитометрии. В некоторых вариантах осуществления, образец представляет собой образец, полученный из крови, или представляет собой продукт афереза или лейкафереза, или получается из него. В некоторых аспектах, введение осуществляют после инициирования первой дозы терапии.
[614] В одном из вариантов осуществления, BCMA-Fc используют для определения того, необходима ли регулировка Т-клеточной терапии CAR у индивидуума, например, когда низкие уровни Т-лимфоцитов CAR у индивидуума указывают на необходимость регулировки терапии. В некоторых аспектах, терапию регулируют (i) если количество клеток Т-клеточной терапии, детектируемых в крови или другом биологическом образце, после того как они детектировались, становится недетектируемым или уменьшается, необязательно, уменьшается по сравнению с предыдущей временной точкой после введения Т-клеточной терапии; (ii) количество клеток Т-клеточной терапии, детектируемых в крови или другом биологическом образце, уменьшается более, чем 1,5-кратно, 2,0-кратно, 3,0-кратно, 4,0-кратно, 5,0-кратно, 10-кратно или более от пикового или максимального количества клеток Т-клеточной терапии, детектируемых в крови или в биологическом образце от субъекта, после инициирования введения Т-клеточной терапии, необязательно, первой, второй или последующей дозы; (iii) в некоторый момент времени после детектирования пикового или максимального уровня клеток Т-клеточной терапии в крови субъекта, количество клеток, Т-лимфоцитов или клеток, полученных из них, детектируемых в крови субъекта, меньше 10%, меньше 5%, меньше 1% или меньше 0,1% от мононуклеаров периферической крови в целом (PBMC), в крови субъекта; и/или (iv) если количество клеток CD3+ или CD8+ клеточной терапии, детектируемое в крови, меньше 20 клеток на мкл, 15 клеток на мкл, 10 клеток на мкл, меньше 5 клеток на мкл или меньше 1 клетки на мкл. В некоторых вариантах осуществления, терапию регулируют посредством введения одной или нескольких дополнительных доз Т-клеточной терапии CAR, введения увеличенной дозы Т-клеточной терапии CAR, введения альтернативной Т-клеточной терапии CAR специфичной к этому же или другому антигену, введения одного или нескольких иммунномодуляторных агентов или другого агента для содействия или увеличения размножения или персистентности T-лимфоцитов CAR.
[615] Можно использовать различные способы известные в данной области, для детектирования связывания слитого белка BCMA-Fc с CAR-экспрессирующими клетками. В некоторых вариантах осуществления, способ включает проточную цитометрию или иммуноанализ. Индикаторный остаток или метящая группа может присоединяться к слитому белку BCMA-Fc, и они выбираются так, чтобы они удовлетворяли потребности различных применений способа, которые часто диктуются доступностью оборудования для анализа и совместимыми процедурами иммуноанализа. В некоторых вариантах осуществления, метка выбирается из флуоресцентных остатков или белков (например, флуоресцеина, родамина, фикоэритрина, GFP или BFP) или люминесцентных остатков (например, наночастиц Qdot™, поставляемых Quantum Dot Corporation, Palo Alto, Calif.). Известны различные общие технологии для использования при осуществлении различных иммуноанализов, указанных выше.
[616] В некоторых вариантах осуществления, слитые белки BCMA-Fc не должны метиться, и их присутствие может детектироваться с использованием меченого антитела, которое связывается со слитым белком BCMA-Fc. В некоторых вариантах осуществления, меченое антитело является специфичным к Fc части молекулы.
[617] В некоторых вариантах осуществления, слитый белок BCMA-Fc иммобилизуется или связывается на твердой подложке, когда композиция или биологический образец, содержащий одну или несколько целевых клеток, содержащая T-лимфоциты CAR, приводится в контакт с твердой подложкой. В некоторых вариантах осуществления, твердая подложка представляет собой шарик. В некоторых вариантах осуществления, твердая подложка представляет собой поверхность лунки или планшета, например, планшета для культивирования клеток. В некоторых вариантах осуществления, твердая подложка представляет собой смолу или матрицу, присутствующую или содержащуюся в хроматографической колонке, например, чтобы дать возможность для хроматографического выделения или селекции Т-лимфоцитов CAR+. В некоторых вариантах осуществления, слитый белок BCMA-Fc обратимо связывается с твердой подложкой или может это делать. В некоторых вариантах осуществления, твердая подложка представляет собой матрицу для аффинной хроматографии, содержащую один или несколько сайтов связывания, которые могут связываться, например, обратимо связываться, с партнером по связыванию, присутствующем в слитом белке BCMA-Fc. В одном из иллюстративных вариантов осуществления, слитый белок BCMA-Fc содержит стрептавидинсвязывающий пептид или другой остаток, связывающий стрептавидин, который может связываться с молекулой стрептавидина или мутеина стрептавидина, присутствующей на или иммобилизованной на твердой подложке, который, в некоторых случаях, может диссоциировать в присутствии конкурирующего вещества, такого как биотин. Иллюстрации таких систем включают системы, описанные в опубликованной заявке на патент US 20150024411,
VI. ПРОМЫШЛЕННЫЕ ИЗДЕЛИЯ И НАБОРЫ
[618] В некоторых вариантах осуществления, предлагаются также системы, устройства и наборы, пригодные для использования при осуществлении предлагаемых способов. В некоторых вариантах осуществления, предлагаются промышленные изделия, такие как наборы или устройства, содержащие частицы, например, шарики, описанные в настоящем документе, то есть, частицы, например, шарики, с присоединенными связывающими молекулами. В некоторых вариантах осуществления, связывающие молекулы содержат антиген или антитело, которое связывает или распознает рекомбинантный рецептор или CAR. В некоторых вариантах осуществления, наборы можно использовать в способах размножения, селекции и/или обогащения клеток, например, в соответствии с приготовлением генно-инженерных клеток для адоптивной клеточной терапии. В конкретных вариантах осуществления, генно-инженерные клетки экспрессируют рекомбинантный рецептор, например, CAR, который связывается или распознается присоединенными связывающими молекулами.
[619] В некоторых вариантах осуществления, промышленные изделия включают один или несколько контейнеров, как правило, множество контейнеров, упаковочный материал и этикетку или вставку в упаковку на контейнере или контейнерах и/или на упаковке, или ассоциированную с ними, как правило, содержащую инструкции для размножения клеток, таких как клетки от субъекта, которые трансдуцируются или трансфицируются одной или несколькими нуклеиновыми кислотами, например, одной или несколькими нуклеиновыми кислотами, содержащими ген, кодирующий рекомбинантный рецептор или CAR.
[620] В определенных вариантах осуществления, набор дополнительно содержит инструкции для использования частиц, например, шариков, описанных в настоящем документе, для селекции или обогащения клеток, экспрессирующих рекомбинантный рецептор, из популяции клеток. В некоторых вариантах осуществления, набор содержит инструкции для использования частиц, например, шариков, описанных в настоящем документе, для обогащения клеток, которые экспрессируют CAR. В конкретных вариантах осуществления, набор содержит инструкции для инкубирования, приведения в контакт или обработки композиции, содержащей клетки, вместе с частицами, например, шариками, описанными в настоящем документе, где не все клетки экспрессируют CAR. В некоторых вариантах осуществления, набор содержит инструкции для активации, размножения и/или обогащения клеток, которые экспрессируют CAR. В определенных вариантах осуществления, набор содержит инструкции для активации, размножения и/или обогащения клеток, которые экспрессируют CAR, из популяции клеток, где меньше 0,01%, меньше 0,1%, меньше 1%, меньше 5%, меньше 10%, меньше 15%, меньше 20%, меньше 25%, меньше 30%, меньше 35%, меньше 40%, меньше 45%, меньше 50%, меньше 55%, меньше 60%, меньше 65%, меньше 70%, меньше 80% или меньше 90% клеток экспрессируют CAR.
[621] В некоторых вариантах осуществления, набор дополнительно содержит инструкции для трансфицирования или трансдуцирования клеток одной или несколькими нуклеиновыми кислотами, которые кодируют рекомбинантный рецептор, например, CAR, которые не наращиваются, не активируются и/или не обогащаются до трансфицирования или трансдуцирования, посредством приведения в контакт, инкубирования или обработки клеток вместе с частицами, например, шариками, описанными в настоящем документе.
VII. ОПРЕДЕЛЕНИЯ
[622] Если не определено иного, все термины из данной области, обозначения и другие технические и научные термины или терминология, используемая в настоящем документе, как предполагается, имеют такое же значение как обычно понимается специалистами в области, к которой относится предмет изобретения. В некоторых случаях, термины со всем понятными значениями определяются в настоящем документе для ясности и/или для простоты упоминания, и включение таких определений в настоящий документ не должно обязательно рассматриваться как некоторое существенное отличие от того, что, понимается всеми в данной области.
[623] Как используется в настоящем документе, упоминание “соответствующей формы” антитела означает, что при сравнении свойства или активности двух антител, свойство сравнивают с использованием одной и той же формы антитела. Например, если утверждается, что антитело имеет более высокую активность по сравнению с активностью соответствующей формы первого антитела, это означает, что конкретная форма, такая как scFv этого антитела, имеет более активность по сравнению с формой scFv первого антитела.
[624] Как используется в настоящем документе, упоминание того, что положения нуклеотидов или аминокислот "соответствуют" положениям нуклеотидов или аминокислот в описанной последовательности, как приведено в Списке последовательностей, относится к положениям нуклеотидов или аминокислот, идентифицируемым при выравнивании с описанной последовательностью, до доведения до максимума идентичности с использованием стандартного алгоритма выравнивания, такого как алгоритм GAP. При выравнивании последовательностей, специалист в данной области может идентифицировать соответствующие остатки, например, используя консервативные и идентичные аминокислотные остатки в качестве критериев. Как правило, для идентификации соответствующих положений, последовательности аминокислот выравниваются таким образом, чтобы получить наивысший порядок соответствия (смотри, например: Computational Molecular Biology, Lesk, A.M., ed., Oxford University Press, New York, 1988; Biocomputing: Informatics and Genome Projects, Smith, D.W., ed., Academic Press, New York, 1993; Computer Analysis of Sequence Data, Part I, Griffin, A.M., and Griffin, H.G., eds., Humana Press, New.Jersey, 1994; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987; и Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M Stockton Press, New York, 1991; Carrillo et al. (1988) SIAM J Applied Math 48: 1073).
[625] “Эффекторные функции” относятся к тем биологическим активностям, приписываемым Fc-области антитела, которые изменяются с изотопом антитела. Примеры эффекторных функций антитела включают: связывание C1q и комплемент-зависимую цитотоксичность (CDC); связывание Fc-рецептора; антитело-зависимую моделируемую клетками цитотоксичность (ADCC); фагоцитоз; даун-регулирование клеточных поверхностных рецепторов (например, рецепторов В-клеток); и активацию В-клеток.
[626] Термин “Fc-область” в настоящем документе используется для определения C-концевой области тяжелой цепи иммуноглобулина, которая содержит, по меньшей мере, часть константной области. Термин включает Fc-области нативных последовательностей и вариантные Fc-области. В одном из вариантов осуществления, Fc-область тяжелой цепи IgG человека простирается от Cyst226 или от Pro230, до карбоксильного конца тяжелой цепи. Однако, C-концевой лизин (Lys447) Fc-области может присутствовать или отсутствовать. Если в настоящем документе не указано иного, нумерация остатков аминокислот в Fc-области или в константной области осуществляется согласно системе нумерации EU, называемой также EU index, как описано в Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991,
[627] Термины “полноразмерное антитело”, “интактное антитело” и “цельное антитело” используются в настоящем документе взаимозаменяемо для упоминания антитела, имеющего структуру, по существу, сходную со структурой нативного антитела или имеющего тяжелые цепи, которые содержат Fc-область, как определено в настоящем документе.
[628] “Выделенное” антитело представляет собой антитело, которое отделено от компонента его природной окружающей среды. В некоторых вариантах осуществления, антитело очищено до чистоты более 95% или 99%, как определено, например, электрофоретически (например, SDS-PAGE, изоэлектрическим фокусированием (IEF), капиллярным электрофорезом) или хроматографически (например, ионообменной хроматографией или HPLC с обращенной фазой). Относительно обзора способов оценки чистоты антитела, смотри, например, Flatman et al., J. Chromatogr. B 848:79-87 (2007).
[629] “Выделенная” нуклеиновая кислота относится к молекуле нуклеиновой кислоты, которая отделена от компонента ее природной окружающей среды. Выделенная нуклеиновая кислота содержит молекулу нуклеиновой кислоты, содержащуюся в клетках, которые обычно содержат молекулу нуклеиновой кислоты, но молекула нуклеиновой кислоты присутствует экстрахромосомально или в хромосомальном положении, которое отличается от ее природного хромосомального положения.
[630] “Выделенная нуклеиновая кислота, кодирующая антиидиотипическое антитело” относится к одной или нескольким молекулам нуклеиновых кислот, кодирующим тяжелые и легкие цепи антитела (или их фрагменты), включая такую молекулу (молекулы) нуклеиновой кислоты в одном векторе или отдельных векторах и такую молекулу (молекулы) нуклеиновой кислоты, присутствующую в одном или нескольких местах в клетке-хозяине.
[631] Термины “клетка-хозяин”, “линия клеток-хозяев” и “культура клеток-хозяев” используются взаимозаменяемо и упоминают клетки, в которые введена экзогенная нуклеиновая кислота, включая потомство таких клеток. Клетки-хозяева включают “трансформанты” и “трансформированные клетки”, которые включают первичную трансформированную клетку и потомство, полученное из нее, вне зависимости от количества пассажей. Потомство может не быть полностью идентичным по содержанию нуклеиновых кислот с родительской клеткой, но может содержать мутации. Мутантное потомство, которое имеет такую же функцию или биологическую активность, как после скрининга или селекции для исходной трансформированной клетки, включается в настоящий документ.
[632] Как используется в настоящем документе, “процент (%) идентичности последовательности аминокислот” и “процент идентичности”, когда используется относительно последовательности аминокислот (эталонной последовательности полипептидов), определяется как процент остатков аминокислот в последовательности- кандидате (например, в антителе субъекта или в его фрагменте), которые идентичны остаткам аминокислот в эталонной последовательности полипептидов, после выравнивания последовательностей и введения разрывов, при необходимости, для достижения максимального процента идентичности последовательностей, и не рассматривая любые консервативные замещения как часть идентичности последовательностей. Выравнивание для целей определения процента идентичности последовательностей аминокислот может быть достигнуто различными путями, например, используя публично доступное компьютерное программное обеспечение, такое как программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалист в данной области может определить соответствующие параметры для выравнивания последовательностей, включая любые алгоритмы необходимые для достижения максимального выравнивания по всей длине последовательностей, которые сравнивают.
[633] Замещение аминокислот может включать замену одной аминокислоты в полипептиде другой аминокислотой. Замещение может представлять собой консервативное замещение аминокислоты или неконсервативное замещение аминокислоты. Замещение аминокислот может вводиться в связывающую молекулу, например, антитело, представляющее интерес, и в продукты, просматриваемые относительно желаемой активности, например, сохраняемого/улучшенного связывания антигена, пониженной иммуногенности или улучшенного ADCC или CDC.
[634] Аминокислоты, в целом, могут группироваться согласно следующим общим свойствам боковых цепей:
(1) гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтрально гидрофильные: Cyst, Ser, Thr, Asn, Gln;
(3) кислотные: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, которые влияют на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
[635] В некоторых вариантах осуществления, консервативные замещения могут включать обмен элемента одного из этих классов на другой элемент этого же класса. В некоторых вариантах осуществления, неконсервативные замещения аминокислот могут включать замену элемента одного из этих классов на другой класс. Неконсервативные замещения аминокислоты будут включать замену элемента одного из этих классов на другой класс.
[636] Термин “вектор”, как используется в настоящем документе, относится к молекуле нуклеиновой кислоты, способной размножать другую нуклеиновую кислоту, с которой она связана. Термин включает вектор как самореплицирующуюся структуру нуклеиновых кислот, а также как вектор, введенный в геном клетки-хозяина, в которую его вводят. Определенные векторы способны направлять экспрессирование нуклеиновых кислот, с которыми они функционально связаны. Такие векторы упоминаются в настоящем документе как “векторы экспрессии”.
[637] Как используется в настоящем документе, формы единственного числа включают ссылки на множественное число, если контекст четко не диктует иного. Например, упоминание предмета в единственном числе означает “по меньшей мере, один” или “один или несколько”. Понятно, что аспекты и варианты, описанные в настоящем документе, включают аспекты и варианты “содержащий” и/или “состоящий, по существу, из”.
[638] В настоящем описании, различные аспекты заявляемого предмета изобретения представлены в формате диапазонов. Необходимо понять, что описание в формате диапазонов осуществляется только для удобства и краткости и не должно рассматриваться как негибкое ограничение рамок заявляемого предмета изобретения. Соответственно, описание диапазона должно рассматриваться как содержащее конкретно описанные все возможные субдиапазоны, а также индивидуальные численные значения в этих диапазонах. Например, когда приводится диапазон значений, понимается, что каждое промежуточное значение между верхним и нижним пределом этого диапазона и любое другое сформулированное или промежуточное значение в этом сформулированном диапазоне охватывается заявляемым предметом изобретения. Верхние и нижние пределы этих меньших диапазонов могут независимо включаться в меньшие диапазоны, и они также охватываются заявляемым предметом изобретения, являясь субъектами любого конкретно исключаемого предела в сформулированном диапазоне. Когда сформулированный диапазон включает один или оба предела, диапазоны, исключающие один или оба этих включенных предела, также включаются в заявляемый предмет изобретения. Это применимо независимо от ширины диапазона.
[639] Термин “примерно” как используется в настоящем документе, относится к обычному диапазону ошибок для соответствующего значения, хорошо известному в данной области техники. Упоминание “примерного” значения или параметра в настоящем документе включает (и описывает) варианты осуществления, которые направлены на это значение или параметр сам по себе. Например, описание, упоминающее “примерно X” включает описание “X”. В некоторых вариантах осуществления, “примерно” относится к значению параметра в пределах ±20%, ±15%, ±10%, ±5% или ±1% от величины параметра.
[640] Термины “полипептид” и “белок” используют взаимозаменяемо для упоминания полимера из остатков аминокислот, и они не ограничиваются минимальной длиной. Полипептиды, включая предлагаемые антитела и цепи антител, и другие пептиды, например, линкеры, могут содержать остатки аминокислот, включая остатки природных и/или искусственных аминокислот. Термины также включают пост-экспрессионные модификации полипептида, например, после гликозилирования, сиалилирования, ацетилирования, фосфолирирования, и тому подобное. В некоторых аспектах, полипептиды могут содержать модификации относительно нативной или природной последовательности постольку, поскольку белок поддерживает желаемую активность. Эти модификации могут быть намерены, например, посредством сайт-направленного мутагенеза, или они могут быть случайными, например, при мутациях хозяев, которые продуцируют белки, или при ошибках из-за PCR амплификации.
[641] Как используется в настоящем документе, «композиция» относится к любой смеси двух или более продуктов, веществ или соединений, включая клетки. Она может представлять собой раствор, суспензию, жидкость, порошок, пасту, быть водной, неводной или представлять собой любое их сочетание.
[642] Как используется в настоящем документе, утверждение, что клетка или популяция клеток является “положительной” относительно конкретного маркера относится к детектируемому присутствию на клетке или в ней конкретного маркера, как правило, поверхностного маркера. При упоминании поверхностного маркера, термин относится к присутствию поверхностного экспрессирования, как детектируется с помощью проточной цитометрии, например, посредством окрашивания антителом, которое специфично связывается с маркером, и детектирования указанного антитела, где окрашивание может детектироваться с помощью проточной цитометрии на уровне существенно выше уровня окрашивания, детектируемого при осуществлении такой же процедуры с изотипически сходным контролем при идентичных в остальном условиях и/или на уровне, по существу, сходном с уровнем для клетки известной как положительная относительно маркера, и/или на уровне существенно выше, чем для клетки известной как отрицательная относительно маркера.
[643] Как используется в настоящем документе, утверждение, что клетка или популяция клеток является “отрицательной” относительно конкретного маркера, относится к отсутствию существенного детектируемого присутствия на клетке или в ней конкретного маркера, как правило, поверхностного маркера. При упоминании поверхностного маркера, термин относится к отсутствию поверхностного экспрессирования, как детектируется с помощью проточной цитометрии, например, посредством окрашивания антителом, которое специфично связывается с маркером, и детектирования указанного антитела, где окрашивание не детектируется с помощью проточной цитометрии на уроне существенно выше окрашивания, детектируемого при осуществлении такой же процедуры с помощью изотипически сходного контроля при идентичных в остальном условиях, и/или детектируется на уровне существенно ниже, чем для клетки, известной как положительная относительно маркера, и/или на уровне, по существу, сходном по сравнению с клеткой, известной как отрицательная относительно маркера.
VIII. Иллюстративные варианты осуществления
[644] Среди предлагаемых вариантов осуществления имеются:
1. Способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие рекомбинантный рецептор, антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген, вместе с множеством частиц, например, шариков, каждая из множества частиц, например, шариков, содержит связывающую молекулу, которая специфично связывается с антигенсвязывающим доменом, где связывание связывающей молекулы с антигенсвязывающим доменом индуцирует размножение клеток, содержащих рекомбинантный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки.
2. Способ по варианту осуществления 1, где рекомбинантный рецептор антигена представляет собой химерный рецептор антигена (CAR).
3. Способ по варианту осуществления 1 или вариант осуществления 2, где антигенсвязывающий домен содержит антитело или его антигенсвязывающий фрагмент.
4. Способ по варианту осуществления 3, где антигенсвязывающий фрагмент представляет собой или содержит одноцепочечный фрагмент антитела.
5. Способ по варианту осуществления 3 или вариант осуществления 4, где его антигенсвязывающий фрагмент содержит вариабельные области антитела, соединенные гибким линкером.
6. Способ по любому из вариантов осуществления 3-5, где его антигенсвязывающий фрагмент представляет собой или содержит scFv.
7. Способ по любому из вариантов осуществления 1-6, где антиген выбирается из ROR1, антигена созревания В-клеток (BCMA), угольной ангидразы 9 (CAIX), Her2/neu (тирозинкиназного рецептора erbB2), Ll-CAM, CD19, CD20, CD22, мезотелина, CEA, и поверхностного антигена гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, фолатсвязывающего белка (FBP), FCRL5, FCRH5, рецептора фетального ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, домена рецептора вставки киназы (kdr), легкой цепи каппа, антигена Ley, молекулы клеточной адгезии L1, (L1-CAM), антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора IL-13 альфа 2 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора фолата a, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторов VEGF, 5T4, фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, антигена рака яичек, мезотелина, CMV мышей, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, канцероэмбрионального антигена (CEA), простата-специфичного антигена, PSMA, Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138, патоген-специфичного антигена и антигена, ассоциированного с универсальной меткой, и/или антиген выбирается из интегрина αvβ6 (интегрина avb6), антигена созревания В-клеток (BCMA), B7-H3, B7-H6, угольной ангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, раково-тестикулярного антигена 1B (CTAG, также известного как NY-ESO-1 и LAGE-2), канцероэмбрионального антигена (CEA), циклина, циклина A2, лиганда 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, протеогликана хондроитин-4-сульфата (CSPG4), белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфрина B2, рецептора эфрина A2 (EPHa2), рецептора эстрогена, белка 5 подобного Fc-рецептору (FCRL5; также известного как гомолог 5 Fc-рецептора или FCRH5), рецептора фетального ацетилхолина (фетального AchR), фолатсвязывающего белка (FBP), рецептора фолата альфа, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), связанного с белком G рецептора 5D (GPRC5D), Her2/neu (тирозинкиназного рецептора erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеров erbB, высокомолекулярного антигена человека, ассоциированного с меланомой (HMW-MAA), поверхностного антигена гепатита B, антигена лейкоцита человека A1 (HLA-A1), антигена лейкоцита человека A2 (HLA-A2), рецептора IL-22 альфа(IL-22Ra), рецептора IL-13 альфа 2 (IL-13Ra2), домена рецептора вставки киназы (kdr), легкой цепи каппа, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, обогащенного лейцином повтора, содержащего член A семейства 8 (LRRC8A), антигена Ley, антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, мезотелина, c-Met, цитомегаловируса мышей (CMV), муцина 1 (MUC1), MUC16, лигандов элемента D группы природных киллеров 2 (NKG2D), мелана A (MART-1), молекулы адгезии нейральных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простата-специфичного антигена, антигена стволовых клеток простаты (PSCA), простата-специфичного мембранного антигена (PSMA), орфанного рецептора 1 подобного тирозинкиназному рецептору (ROR1), сурвивина, гликопротеина трофобластов (TPBG также известного как 5T4), ассоциированного с опухолью гликопротеина 72 (TAG72), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора 2 фактора роста эндотелия сосудов (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфичного или патоген-экспрессируемого антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекул, и/или молекул, экспрессируемых HIV, HCV, HBV, или других патогенов.
8. Способ по любому из вариантов осуществления 1-7, где связывающая молекула не связывает или не распознает линкерную или спейсерную область рекомбинантного рецептора антигена, указанная линкерная или спейсерная область, соединяет антигенсвязывающий домен с трансмембранным доменом рецептора антигена.
9. Способ по любому из вариантов осуществления 1-8, где связывающая молекула представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом.
10. Способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает антиген, вместе с множеством частиц, например, шариков, каждая из множества частиц, например, шариков, содержит связывающую молекулу, которая представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом, где связывание антиидиотипического антитела или его антигенсвязывающего фрагмента с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки.
11. Способ по любому из вариантов осуществления 1-8, где связывающая молекула содержит рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом.
12. Способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает антиген, вместе с множеством частиц, например, шариков, каждая из множества частиц, например, шариков, содержит связывающую молекулу, содержащую рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом, где связывание рекомбинантного антигена или его части с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки.
13. Способ по варианту осуществления 11 или варианту осуществления 12, где рекомбинантный антиген выбирается из ROR1, антигена созревания В-клеток (BCMA), угольной ангидразы 9 (CAIX), Her2/neu (тирозинкиназного рецептора erbB2), Ll-CAM, CD19, CD20, CD22, мезотелина, CEA, и поверхностного антигена гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, фолатсвязывающего белка (FBP), FCRL5, FCRH5, рецептора фетального ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, домена рецептора вставки киназы (kdr), легкой цепи каппа, антигена Ley, молекулы клеточной адгезии L1, (L1-CAM), антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора IL-13 альфа 2 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора фолата a, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторов VEGF, 5T4, фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, антигена рака яичек, мезотелина, CMV мышей, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, канцероэмбрионального антигена (CEA), простата-специфичного антигена, PSMA, Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138 и патоген-специфичного антигена или части любого из указанных выше антигенов, распознаваемых антигенсвязывающим доменом, и/или антиген выбирается из интегрина αvβ6 (интегрина avb6), антигена созревания В-клеток (BCMA), B7-H3, B7-H6, угольной ангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, раково-тестикулярного антигена 1B (CTAG, также известного как NY-ESO-1 и LAGE-2), канцероэмбрионального антигена (CEA), циклина, циклина A2, лиганда 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфрина B2, рецептора эфрина A2 (EPHa2), рецептора эстрогена, белка 5 подобного Fc-рецептору (FCRL5; также известного как гомолог 5 Fc-рецептора или FCRH5), рецептора фетального ацетилхолина (фетального AchR), фолатсвязывающего белка (FBP), рецептора фолата альфа, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), связанного с белком G рецептора 5D (GPRC5D), Her2/neu (тирозинкиназного рецептора erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеров erbB, высокомолекулярного антигена человека, ассоциированного с меланомой (HMW-MAA), поверхностного антигена гепатита B, антигена лейкоцита человека A1 (HLA-A1), антигена лейкоцита человека A2 (HLA-A2), рецептора IL-22 альфа(IL-22Ra), рецептора IL-13 альфа 2 (IL-13Ra2), домена рецептора вставки киназы (kdr), легкой цепи каппа, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, обогащенного лейцином повтора, содержащего член A семейства 8 (LRRC8A), антигена Ley, антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, мезотелина, c-Met, цитомегаловируса мышей (CMV), муцина 1 (MUC1), MUC16, лигандов элемента D группы природных киллеров 2 (NKG2D), мелана A (MART-1), молекулы адгезии нейральных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простата-специфичного антигена, антигена стволовых клеток простаты (PSCA), простата-специфичного мембранного антигена (PSMA), орфанного рецептора 1 подобного тирозинкиназному рецептору (ROR1), сурвивина, гликопротеина трофобластов (TPBG также известного как 5T4), ассоциированного с опухолью гликопротеина 72 (TAG72), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора 2 фактора роста эндотелия сосудов (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфичного или патоген-экспрессируемого антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекул, и/или молекул, экспрессируемых HIV, HCV, HBV, или другими патогенами.
14. Способ по любому из вариантов осуществления 11-13, где рекомбинантный антиген представляет собой BCMA, CD22 или ROR1, или представляет собой его часть, распознаваемую антигенсвязывающим доменом.
15. Способ по любому из вариантов осуществления 11-14, где часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, содержит внеклеточный домен или часть внеклеточного домена антигена.
16. Способ по любому из вариантов осуществления 11-14, где часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, состоит, по существу, из внеклеточного домена или части внеклеточного домена антигена.
17. Способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает антиген созревания В-клеток (BCMA), вместе с множеством частиц, например, шариков, каждая из множества частиц, например, шариков, содержит связывающую молекулу, содержащую внеклеточный домен BCMA или часть внеклеточного домена, распознаваемую антигенсвязывающим доменом, где связывание внеклеточного домена BCMA или его части с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки.
18. Способ по варианту осуществления 17, где часть BCMA состоит, по существу, из внеклеточного домена или части внеклеточного домена.
19. Способ по любому из вариантов осуществления 11-18, где связывающая молекула представляет собой слитый полипептид, содержащий рекомбинантный антиген или его часть, связанную с остатком, где остаток необязательно, облегчает присоединение к частице.
20. Способ по варианту осуществления 19, где остаток связывается с C-концом рекомбинантного антигена.
21. Способ по варианту осуществления 19 или варианту осуществления 20, где остаток является гидрофобным или обогащенным гидрофобными аминокислотами.
22. Способ по любому из вариантов осуществления 19-21, где остаток представляет собой или содержит Fc-домен.
23. Способ по варианту осуществления 22, где Fc-область получают из IgG человека.
24. Способ по любому из вариантов осуществления 1-12, где антиген представляет собой CD19.
25. Способ размножения клеток, включающий инкубирование исходной композиции, содержащей клетки, экспрессирующие химерный рецептор антигена (CAR), содержащий антигенсвязывающий домен, который специфично связывает или распознает CD19, вместе с множеством частиц, например, шариков, каждая из множества частиц, например, шариков, содержит связывающую молекулу, которая представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом, где связывание антиидиотипического антитела или его антигенсвязывающего фрагмента с антигенсвязывающим доменом индуцирует размножение клеток, содержащих химерный рецептор антигена, тем самым продуцируя выходную композицию, содержащую наращенные клетки.
26. Способ по варианту осуществления 9, варианту осуществления 24 или варианту осуществления 25, где антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело SJ25C1 или его антигенсвязывающий фрагмент.
27. Способ по варианту осуществления 9, варианту осуществления 24 или варианту осуществления 25, где антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело FMC63 или его антигенсвязывающий фрагмент.
28. Способ по варианту осуществления 26 или вариант осуществления 27, где антигенсвязывающ фрагмент представляет собой или содержит scFv.
29. Способ по любому из вариантов осуществления 1-28, где антиген или рекомбинантный антиген представляет собой человека.
30. Способ по любому из вариантов осуществления 9, 10 и 25-29, где антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит, по меньшей мере, часть константной области иммуноглобулина.
31. Способ по варианту осуществления 30, где, по меньшей мере, часть константной области иммуноглобулина содержит Fc-область или часть Fc, содержащую домены CH2 и CH3.
32. Способ по варианту осуществления 30 или варианту осуществления 31, где константную область или Fc-область получают из IgG человека.
33. Способ по любому из вариантов осуществления 9, 10 и 25-32, где антиидиотипическое антитело или его антигенсвязывающий фрагмент представляет собой интактное антитело или полноразмерное антитело.
34. Способ по любому из вариантов осуществления 1-33, где связывающая молекула ковалентно или нековалентно связана с частицами, например, с шариками.
35. Способ по любому из вариантов осуществления 1-34, где связывающая молекула присоединена к каждой из множества частиц, например, шариков, на С-концевом аминокислотном остатке связывающей молекулы или вблизи него и/или присоединение связывающей молекулы к каждой из множества частиц, например, шариков, осуществляется так, что область или эпитоп связывающей молекулы, распознаваемый антигенсвязывающим доменом рецептора антигена, ориентируется так, что он может распознаваться рецептором антигена.
36. Способ по любому из вариантов осуществления 1-35, где частицы, например, шарики, представляют собой синтетические частицы, нерастворимые частицы, твердые частицы или представляют собой частицы отличные от клеток.
37. Способ по любому из вариантов осуществления 1-35, где множество частиц содержит шарики.
38. Способ по любому из вариантов осуществления 1-37, где множество частиц, например, шариков, имеет средний диаметр в пределах между или примерно между 1 мкм и 10 мкм, или между или примерно между 2 мкм и 5 мкм.
39. Способ по любому из вариантов осуществления 1-38, где множество частиц, например, шариков, имеет средний диаметр примерно 2,8 мкм.
40. Способ по любому из вариантов осуществления 1-38, где множество частиц, например, шариков, имеет средний диаметр примерно 4,5 мкм.
41. Способ по любому из вариантов осуществления 1-40, где множество частиц, например, шариков, имеет среднюю плотность примерно между 0,5 г/см3 и 5,0 г/см3 или между или примерно между 1 г/см3 и примерно 2 г/см3.
42. Способ по любому из вариантов осуществления 1-41, где множество частиц, например, шариков, имеет среднюю плотность примерно от 1,3 г/см3.
43. Способ по вариантам осуществления 1-42, где множество частиц, например, шариков, имеет среднюю плотность примерно от 1,5 г/см3.
44. Способ по любому из вариантов осуществления 1-43, где множество частиц, например, шариков, является монодисперсным.
45. Способ по любому из вариантов осуществления 1-44, где связывающая молекула ковалентно присоединена к частицам, например, шарикам.
46. Способ по любому из вариантов осуществления 1-45, где частица содержит поверхностно экспонируемую функциональную группу для присоединения связывающей молекулы, и/или, где связывающая молекула ковалентно присоединена к частице посредством поверхностно экспонируемой функциональной группы.
47. Способ по варианту осуществления 46, где поверхностно экспонируемая функциональная группа представляет собой амино группу, карбоксильную группу, тиольную группу, альдегидную группу, хлорметильную группу, эпокси группу, гидроксильную группу, тозильную группу или гидразиновую группу.
48. Способ по варианту осуществления 46 или варианту осуществления 47, где поверхностно экспонируемая функциональная группа представляет собой тозильную группу.
49. Способ по любому из вариантов осуществления 1-48, где множество частиц, например, шариков, являются биологически совместимыми или нетоксичными для клетки.
50. Способ по любому из вариантов осуществления 1-49, где множество частиц, например, шариков, содержат частицы, содержащие стекло, диоксид кремния, сложные полиэфиры гидроксикарбоновых кислот, полиангидриды дикарбоновых кислот, сополимеры гидроксикарбоновых кислот, сополимеры дикарбоновых кислот или металл.
51. Способ по любому из вариантов осуществления 1-50, где частицы, например, шарики, имеют поверхность, содержащую полимер, полисахарид, диоксид кремния, жирную кислоту, углерод или их сочетание.
52. Способ по варианту осуществления 51, где полимер представляет собой полиэтиленгликоль, сополимер молочная кислота - гликолевая кислота, полиглутаральдегид, полиуретан, полистирол и поливиниловый спирт или их сочетания.
53. Способ по любому из вариантов осуществления 1-52, где множество частиц, например, шариков, содержит частицы, содержащие гидрофобную поверхность.
54. Способ по любому из вариантов осуществления 1-53, где множество частиц, например, шариков, содержит частицы, содержащие полистирольную поверхность.
55. Способ по любому из вариантов осуществления 1-54, множество частиц, например, шариков, содержит частицы, которые являются магнитными и/или содержат магнитную сердцевину, парамагнитную сердцевину или суперпарамагнитную сердцевину.
56. Способ по любому из вариантов осуществления 1-55, где концентрация связывающей молекулы находится в пределах между или примерно между 0,5 мкг/мл и 500 мкг/мл, 1 мкг/мл и 200 мкг/мл или 5 мкг/мл и 100 мкг/мл.
57. Способ по любому из вариантов осуществления 1-56, где концентрация связывающей молекулы составляет, по меньшей мере или, по меньшей мере, примерно 1 мкг/мл, 5 мкг/мл, 10 мкг/мл, 25 мкг/мл, 50 мкг/мл, 100 мкг/мл или 200 мкг/мл.
58. Способ по любому из вариантов осуществления 1-57, где каждая из множества частиц, например, шариков, содержит, по меньшей мере или примерно, по меньшей мере, 10 копий, 102 копий, 103 копий, 104 копий, 105 копий или 106 копий связывающей молекулы.
59. Способ по любому из вариантов осуществления 1-58, где, по меньшей мере, часть инкубирования осуществляют в присутствии агента, который специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала.
60. Способ по любому из вариантов осуществления 1-59, где агент предлагается вместе с частицами, например, шариками, необязательно, агент содержится в каждой из множества частиц, например, шариков, или в их подмножестве.
61. Способ по любому из вариантов осуществления 1-59, где агент предлагается по отдельности из множества частиц, например, шариков.
62. Способ по любому из вариантов осуществления 1-60, где частицы, например, шарики, дополнительно содержат агент, который специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала.
63. Способ по любому из вариантов осуществления 59-62, где агент представляет собой лиганд или представляет собой антитело или его антигенсвязывающий фрагмент.
64. Способ по любому из вариантов осуществления 58-63, где молекула представляет собой костимуляторную молекулу или представляет собой активирующий корецептор или его лиганд.
65. Способ по варианту осуществления 64, где костимуляторная молекула или активирующий корецептор представляет собой OX-40, ICOS, DAP10, CD28 или 4-1BB или представляет собой их лиганд, необязательно, OX-40L, ICOSL, B7-1, B7-2 или 4-1BBL.
66. Способ по любому из вариантов осуществления 58-63, где молекула представляет собой ингибиторный рецептор или его лиганд.
67. Способ по варианту осуществления 66, где ингибиторный рецептор представляет собой CTLA-4, PD-1, LAG-3, Tim-3, BTLA или TIGIT или представляет собой его лиганд, необязательно, PD-L1, PD-L2, CD155, CD112 или LIGHT.
68. Способ по любому из вариантов осуществления 62-67, где агент ковалентно присоединен к частицам, например, шарикам.
69. Способ по любому из вариантов осуществления 62-68, где отношение, необязательно, молярное или массовое отношение, связывающей молекулы и агента, удерживаемого частицами, например, шариками, составляет или составляет примерно 1:1,
70. Способ по любому из вариантов осуществления 1-69, где отношение клеток в целом, присутствующих в исходной композиции, к частицам, например, шарикам, составляет от или примерно от 5:1 до 1:5, от 3:1 до 1:3 или от 2:1 до 1:2.
71. Способ по любому из вариантов осуществления 1-70, где отношение клеток в целом, присутствующих в исходной композиции, к частицам, например, шарикам, составляет от или примерно от 1:0,1 до 1:5.
72. Способ по любому из вариантов осуществления 1-71, где отношение клеток в целом, присутствующих в исходной композиции, к частицам, например, шарикам, составляет или составляет примерно 1:1.
73. Способ по любому из вариантов осуществления 1-72, где инкубирование осуществляют в течение больше, чем или больше примерно, чем 2 часов, 4 часов, 8 часов, 12 часов, 24 часов, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, 8 дней, 9 дней, 10 дней, 11 дней или 12 дней.
74. Способ по любому из вариантов осуществления 1-73, где инкубирование осуществляют при температуре в пределах между или примерно между 30°C и 39°C.
75. Способ по любому из вариантов осуществления 1-74, где инкубирование осуществляют при температуре 37° ± 2,0°C.
76. Способ по любому из вариантов осуществления 1-75, где клетки содержат иммунные клетки или индуцированные плюрипотентные стволовые клетки (iPSC).
77. Способ по любому из вариантов осуществления 1-76, где иммунная клетка представляет собой Т-лимфоцит или NK-клетку.
78. Способ по любому из вариантов осуществления 1-77, где клетки содержат Т-лимфоциты CD4+ и/или CD8+.
79. Способ по любому из пп.1-78, где отношение клеток CD4+ к клеткам CD8+ составляет или составляет примерно 1:1, 1:2, 2:1, 1:3 или 3:1.
80. Способ по любому из вариантов осуществления 1-79, где клетки представляют собой первичные клетки, полученные от субъекта, необязательно, субъекта человека.
81. Способ по любому из вариантов осуществления 1-80, где клетки представляют собой клетки человека.
82. Способ по любому из вариантов осуществления 1-81, где исходная композиция получается с помощью способа, включающего приведение в контакт композиции клеток с молекулой нуклеиновой кислоты, кодирующей рекомбинантный рецептор антигена, при условиях для введения молекулы нуклеиновой кислоты в одну или несколько клеток в композиции.
83. Способ генной инженерии клеток, включающий:
(a) приведение в контакт композиции клеток с молекулой нуклеиновой кислоты, кодирующей рекомбинантный рецептор антигена, при условиях для введения молекулы нуклеиновой кислоты в одну или несколько клеток в композиции, тем самым продуцируя исходную композицию; и
(b) инкубирование клеток исходной композиции согласно способу по любому из вариантов осуществления 1-74.
84. Способ по варианту осуществления 82 или варианту осуществления 83, где, по меньшей мере, часть приведения в контакт и инкубирования осуществляют одновременно.
85. Способ по любому из вариантов осуществления 82-84, где молекула нуклеиновой кислоты содержится в вирусном векторе, эписомальном векторе или транспозоне.
86. Способ по любому из вариантов осуществления 82-85, где приведение в контакт осуществляется посредством переноса транспозона/гена транспозазы.
87. Способ по любому из вариантов осуществления 82-85, где приведение в контакт осуществляется посредством трансдуцирования вирусным вектором.
88. Способ по варианту осуществления 85 или варианту осуществления 87, где вирусный вектор представляет собой ретровирус, который, необязательно, представляет собой гамма-ретровирусный вектор или лентивирусный вектор.
89. Способ по варианту осуществления 87 или варианту осуществления 88, где приведение в контакт включает стадию спинокуляции вирусного вектора вместе с композицией клеток.
90. Способ по варианту осуществления 89, где спинокуляция включает вращение, во внутренней полости камеры центрифуги, частиц вирусного вектора и композиции клеток, где вращение происходит при относительной центробежной силе на внутренней поверхности боковой стенки полости, которая находится:
в пределах между или примерно между 500 g и 2500 g, 500 g и 2000 g, 500 g и 1600 g, 500 g, 1000 g, 600 g и 1600 g, 600 g и 1000 g, 1000 g и 2000 g или 1000 g и 1600 g, каждое, включительно; или составляет
по меньшей мере или, по меньшей мере, примерно 600 g, 800 g, 1000 g, 1200 g, 1600 g или 2000 g.
91. Способ по варианту осуществления 89 или варианту осуществления 90, где спинокуляция осуществляется в течение времени, которое:
больше, чем или больше примерно, чем 5 минут, больше, чем или больше примерно, чем 10 минут, больше, чем или больше примерно, чем 15 минут, больше, чем или больше примерно, чем 20 минут, больше, чем или больше примерно, чем 30 минут, больше, чем или больше примерно, чем 45 минут, больше, чем или больше примерно, чем 60 минут, больше, чем или больше примерно, чем 90 минут или больше, чем или больше примерно, чем 120 минут; или
находится в пределах между или примерно между 5 минутами и 60 минутами, 10 минутами и 60 минутами, 15 минутами и 60 минутами, 15 минутами и 45 минутами, 30 минутами и 60 минутами или 45 минутами и 60 минутами, каждое, включительно.
92. Способ по любому из вариантов осуществления 87-91, где приведение в контакт осуществляется в присутствии адъюванта трансдукции.
93. Способ по любому из вариантов осуществления 82-92, где композиция клеток содержит множество Т-лимфоцитов, и до приведения в контакт, способ не включает стимуляции или активации Т-лимфоцитов.
94. Способ по любому из вариантов осуществления 82-93, где композиция клеток содержит множество Т-лимфоцитов, и до приведения в контакт, способ не включает инкубирования композиции в присутствии агента или агентов, которые могут индуцировать сигнал через комплекс TCR, и/или инкубирования в присутствии агента или агентов способных индуцировать пролиферацию Т-лимфоцитов, Т-лимфоцитов CD4+ и/или Т-лимфоцитов CD8+; и/или CD3-связывающих молекул, CD28-связывающих молекул, рекомбинантного IL-2, рекомбинантного IL-15 и рекомбинантного IL-7 или их сочетания.
95. Способ по п.93 или варианту осуществления 94, где, до приведения в контакт, способ не включает стимуляции Т-лимфоцитов в присутствии антитела анти-CD3 и/или антитела анти-CD28
96. Способ по любому из вариантов осуществления 82-95, где композиция клеток содержит множество Т-лимфоцитов, указанное множество клеток получают из образца от субъекта, где:
приведение в контакт инициируется не более, чем через 24 часа после получения образца от субъекта; и/или
до приведения в контакт, Т-лимфоциты не подвергаются воздействию температуры большей, чем или большей примерно, чем 15°C, примерно 18°C, примерно 22°C или примерно 25°C в течение времени больше 1 часа, 2 часов, 4 часов, 6 часов, 8 часов, 12 часов или 24 часов после получения образца от субъекта; и/или
до приведения в контакт, Т-лимфоциты не подвергаются воздействию температуры равной, примерно равной, большей, чем или большей примерно, чем 37° ± 2,0°C в течение времени больше 15 минут, 30 минут, 1 часа или 2 часов после получения образца от субъекта.
97. Способ по любому из вариантов осуществления 82-96, до указанного приведения в контакт, не более 5%, 10%, 20%, 30% или 40% Т-лимфоцитов представляют собой активированные клетки, которые экспрессируют поверхностный маркер, селектированный из группы, состоящей из HLA-DR, CD25, CD69, CD71, CD40L и 4-1BB; включая внутриклеточное экспрессирование цитокина, селектированного из группы, состоящей из IL-2, IFN-гамма, TNF-альфа, находятся в фазе G1 или в более поздней фазе клеточного цикла и/или способны к пролиферации.
98. Способ по любому из вариантов осуществления 1-97, дополнительно включающий, перед инкубированием или приведением в контакт, получение биологического образца от субъекта, содержащего клетки, и, необязательно, селекцию или обогащение клеток, необязательно, Т-лимфоцитов, из образца.
99. Способ по любому из вариантов осуществления 1-98, где процент клеток, экспрессирующих рекомбинантный рецептор антигена, в исходной композиции меньше или меньше примерно 75%, 70%, 60%, 50%, 40%, 30%, 20%, 15%, 10% или меньше.
100. Способ по любому из вариантов осуществления 1-99, где композиция клеток или исходная композиция содержит, по меньшей мере или, по меньшей мере, примерно 1 × 102 клеток, 1 × 103 клеток, 1 × 104 клеток, 1 × 105 клеток, 1 × 106 клеток или 1 × 107 клеток.
101. Способ по любому из вариантов осуществления 1-100, где поверхностное экспрессирование маркера активации или маркера истощения клеток, присутствующих в выходной композиции, меньше, чем поверхностное экспрессирование маркера в композиции клеток, продуцируемой после сходного инкубирования, но в присутствии поликлональной стимуляторной молекулы, которая может активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR.
102. Способ по варианту осуществления 101, где маркер истощения представляет собой ингибиторный рецептор.
103. Способ по варианту осуществления 101 или варианту осуществления 102, где маркер истощения представляет собой PD-1, CTLA-4, TIM-3, LAG-3, BTLA или TIGIT.
104. Способ по варианту осуществления 103, где маркер активации представляет собой HLA-DR, CD25, CD69, CD71, CD40L или 4-1BB.
105. Способ по любому из вариантов осуществления 93-96, где поверхностное экспрессирование увеличивается, по меньшей мере или, по меньшей мере, примерно 1,2-кратно, 1,5-кратно, 2,0-кратно, 3,0-кратным, 4,0-кратно, 5,0-кратно, 10,0-кратно или больше.
106. Способ по любому из вариантов осуществления 1-105, где количество клеток в выходной композиции, по существу, такое же или больше, чем количество клеток в композиции клеток, полученной с помощью сходного инкубирования, но в присутствии поликлональной стимуляторной молекулы, которая может активировать один или несколько внутриклеточных сигнальных доменов одного или нескольких компонентов комплекса TCR.
107. Способ по любому из вариантов осуществления 101-106, где поликлональная стимуляторная молекула содержит антитело анти-CD3 или его фрагмент и/или антитело анти-CD28 или его фрагмент.
108. Способ по любому из вариантов осуществления 1-107, количество клеток в выходной композиции количество клеток в исходной композиции больше, чем или больше примерно, чем 1,2-кратно, 1,5-кратно, 2,0-кратно, 3,0-кратно, 4,0-кратно, 5,0-кратно, 10,0-кратно, 25-кратно, 50-кратно, 100-кратно, или больше.
109. Способ по любому из вариантов осуществления 1-108, где процент клеток, содержащих рекомбинантный рецептор антигена, в выходной композиции больше или больше примерно 50%, 60%, 70%, 80%, 90%, 95%, или больше.
110. Способ по любому из вариантов осуществления 1-109, где количество клеток в выходной композиции, содержащих рекомбинантный рецептор антигена, повышается или обогащается 1,2-кратно, 2,0-кратно, 3,0-кратно, 4,0-кратно, 5,0-кратно, 6,0-кратно, 7,0-кратно, 8,0-кратно, 9,0-кратно, 10-кратно или больше по сравнению с количеством клеток, содержащих рецептор антигена, в исходной композиции.
111. Способ по любому из вариантов осуществления 1-110, где, по меньшей мере, часть инкубирования осуществляется в присутствии одного или нескольких дополнительных агентов, которые модулируют размножение или активность клеток
112. Способ по варианту осуществления 111, где один или несколько дополнительных агентов представляет собой один или несколько цитокинов.
113. Способ по любому из вариантов осуществления 1-112, который осуществляют in vitro или ex vivo.
114. Способ по любому из вариантов осуществления 1-113, где рецептор антигена представляет собой CAR и CAR дополнительно содержит внутриклеточный сигнальный домен, содержащий ITAM
115. Способ по варианту осуществления 114, где внутриклеточный сигнальный домен содержит внутриклеточный домен цепи CD3-зета (CD3ζ).
116. Способ по варианту осуществления 114 или вариант осуществления 115, где CAR дополнительно содержит костимуляторную сигнальную область.
117. Способ по варианту осуществления 116, где костимуляторная сигнальная область содержит сигнальный домен CD28 или 4-1BB.
118. Способ по варианту осуществления 117, где костимуляторный домен представляет собой CD28.
119. Способ по любому из вариантов осуществления 1-118, способ дополнительно включает удаление множества частиц, например, шариков, из выходной композиции.
120. Композиция клеток, полученная с помощью способа по любому из вариантов осуществления 1-119.
121. Поверхностно модифицированная частица, содержащая частицу и связывающую молекулу, связанную с поверхностью частицы, где связывающая молекула специфично связывается с внеклеточным антигенсвязывающим доменом рецептора антигена.
122. Поверхностно модифицированная частица по варианту осуществления 121, где рецептор антигена представляет собой химерный рецептор антигена (CAR).
123. Поверхностно модифицированная частица по варианту осуществления 121 или варианту осуществления 122, где связывающая молекула не связывает или не распознает линкерную или спейсерную область рекомбинантного рецептора антигена, указанная линкерная или спейсерная область соединяет антигенсвязывающий домен с трансмембранным доменом рецептора антигена.
124. Поверхностно модифицированная частица по любому из вариантов осуществления 121-123, где связывающая молекула содержит рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом.
125. Поверхностно модифицированная частица по варианту осуществления 124, где рекомбинантный антиген выбирается из ROR1, антигена созревания В-клеток (BCMA), угольной ангидразы 9 (CAIX), Her2/neu (тирозинкиназного рецептора erbB2), Ll-CAM, CD19, CD20, CD22, мезотелина, CEA, и поверхностного антигена гепатита B, антифолатного рецептора, CD23, CD24, CD30, CD33, CD38, CD44, EGFR, эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), EPHa2, erb-B2, erb-B3, erb-B4, димеров erbB, EGFR vIII, фолатсвязывающего белка (FBP), FCRL5, FCRH5, рецептора фетального ацетилхолина, GD2, GD3, HMW-MAA, IL-22R-альфа, IL-13R-альфа2, домена рецептора вставки киназы (kdr), легкой цепи каппа, антигена Ley, молекулы клеточной адгезии L1, (L1-CAM), антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, предпочтительно экспрессируемого антигена меланомы (PRAME), сурвивина, TAG72, B7-H6, рецептора IL-13 альфа 2 (IL-13Ra2), CA9, GD3, HMW-MAA, CD171, G250/CAIX, HLA-AI MAGE Al, HLA-A2 NY-ESO-1, PSCA, рецептора фолата a, CD44v6, CD44v7/8, интегрина avb6, 8H9, NCAM, рецепторов VEGF, 5T4, фетального AchR, лигандов NKG2D, CD44v6, двойного антигена, антигена рака яичек, мезотелина, CMV мышей, муцина 1 (MUC1), MUC16, PSCA, NKG2D, NY-ESO-1, MART-1, gp100, онкофетального антигена, ROR1, TAG72, VEGF-R2, канцероэмбрионального антигена (CEA), простата-специфичного антигена, PSMA, Her2/neu, рецептора эстрогена, рецептора прогестерона, эфрина B2, CD123, c-Met, GD-2, O-ацетилированного GD2 (OGD2), CE7, опухоли Вильмса 1 (WT-1), циклина, циклина A2, CCL-1, CD138 и патоген-специфичного антигена или части любого из указанных выше антигенов, распознаваемых антигенсвязывающим доменом и/или антиген выбирается из интегрина αvβ6 (интегрина avb6), антигена созревания В-клеток (BCMA), B7-H3, B7-H6, угольной ангидразы 9 (CA9, также известной как CAIX или G250), антигена рака яичек, раково-тестикулярного антигена 1B (CTAG, также известного как NY-ESO-1 и LAGE-2), канцероэмбрионального антигена (CEA), циклина, циклина A2, лиганда 1 хемокина мотива C-C (CCL-1), CD19, CD20, CD22, CD23, CD24, CD30, CD33, CD38, CD44, CD44v6, CD44v7/8, CD123, CD138, CD171, белка эпидермального фактора роста (EGFR), мутации рецептора эпидермального фактора роста типа III (EGFR vIII), эпителиального гликопротеина 2 (EPG-2), эпителиального гликопротеина 40 (EPG-40), эфрина B2, рецептора эфрина A2 (EPHa2), рецептора эстрогена, белка 5 подобного Fc-рецептору (FCRL5; также известного как гомолог 5 Fc-рецептора или FCRH5), рецептора фетального ацетилхолина (фетального AchR), фолатсвязывающего белка (FBP), рецептора фолата альфа, ганглиозида GD2, O-ацетилированного GD2 (OGD2), ганглиозида GD3, гликопротеина 100 (gp100), связанного с белком G рецептора 5D (GPRC5D), Her2/neu (тирозинкиназного рецептора erb-B2), Her3 (erb-B3), Her4 (erb-B4), димеров erbB, высокомолекулярного антигена человека, ассоциированного с меланомой (HMW-MAA), поверхностного антигена гепатита B, антигена лейкоцита человека A1 (HLA-A1), антигена лейкоцита человека A2 (HLA-A2), рецептора IL-22 альфа(IL-22Ra), рецептора IL-13 альфа 2 (IL-13Ra2), домена рецептора вставки киназы (kdr), легкой цепи каппа, молекулы клеточной адгезии L1 (L1-CAM), эпитопа CE7 L1-CAM, обогащенного лейцином повтора, содержащего член A семейства 8 (LRRC8A), антигена Ley, антигена, ассоциированного с меланомой (MAGE)-A1, MAGE-A3, MAGE-A6, мезотелина, c-Met, цитомегаловируса мышей (CMV), муцина 1 (MUC1), MUC16, лигандов элемента D группы природных киллеров 2 (NKG2D), мелана A (MART-1), молекулы адгезии нейральных клеток (NCAM), онкофетального антигена, предпочтительно экспрессируемого антигена меланомы (PRAME), рецептора прогестерона, простата-специфичного антигена, антигена стволовых клеток простаты (PSCA), простата-специфичного мембранного антигена (PSMA), орфанного рецептора 1 подобного тирозинкиназному рецептору (ROR1), сурвивина, гликопротеина трофобластов (TPBG также известной как 5T4), ассоциированного с опухолью гликопротеина 72 (TAG72), рецептора фактора роста эндотелия сосудов (VEGFR), рецептора 2 фактора роста эндотелия сосудов (VEGFR2), опухоли Вильмса 1 (WT-1), патоген-специфичного или патоген-экспрессируемого антигена или антигена, ассоциированного с универсальной меткой, и/или биотинилированных молекулы, и/или молекул, экспрессируемых HIV, HCV, HBV, или другими патогенами.
126. Поверхностно модифицированная частица по варианту осуществления 124 или варианту осуществления 125, где рекомбинантный антиген представляет собой BCMA, CD22 или ROR1 или представляет собой его часть, распознаваемую антигенсвязывающим доменом.
127. Способ по любому из вариантов осуществления 124-126, где часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, содержит внеклеточный домен или часть внеклеточного домена антигена.
128. Способ по любому из вариантов осуществления 124-126, где часть рекомбинантного антигена, распознаваемая антигенсвязывающим доменом, состоит, по существу, из внеклеточного домена или части внеклеточного домена антигена.
129. Поверхностно модифицированная частица, содержащая частицу и связывающую молекулу, связанную с поверхностью частицы, где связывающая молекула содержит внеклеточный домен или его часть от антигена созревания В-клеток (BCMA).
130. Поверхностно модифицированная частица по любому из вариантов осуществления 124-129, где связывающая молекула представляет собой слитый полипептид, содержащий рекомбинантный антиген или его часть, связанную с остатком, где остаток, необязательно, облегчает присоединение к частице.
131. Поверхностно модифицированная частица по варианту осуществления 130, где остаток связывается с C-концом рекомбинантного антигена.
132. Поверхностно модифицированная частица по варианту осуществления 130 или вариант осуществления 131, где остаток является гидрофобным или обогащенным гидрофобными аминокислотами.
133. Поверхностно модифицированная частица по любому из вариантов осуществления 130-132, где остаток представляет собой или содержит Fc-домен.
134. Поверхностно модифицированная частица по варианту осуществления 133, где Fc-область получают из IgG человека.
135. Поверхностно модифицированная частица по любому из вариантов осуществления 130-134, где рекомбинантный антиген представляет собой антиген человека.
136. Поверхностно модифицированная частица по любому из вариантов осуществления 121-123, где связывающая молекула содержит антиидиотипическое антитело или его антигенсвязывающий фрагмент.
137. Поверхностно модифицированная частица по любому из вариантов осуществления 121-123 и 136, где антиген, распознаваемый антигенсвязывающим доменом, представляет собой CD19.
138. Поверхностно модифицированная частица по варианту осуществления 136 или варианту осуществления 137, где антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело SJ25C1 или его антигенсвязывающий фрагмент.
139. Поверхностно модифицированная частица по варианту осуществления 136 или варианту осуществления 137, где антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело FMC63 или его антигенсвязывающий фрагмент.
140. Поверхностно модифицированная частица по варианту осуществления 138 или вариант осуществления 139, где антигенсвязывающ фрагмент представляет собой или содержит scFv.
141. Поверхностно модифицированная частица по любому из вариантов осуществления 136-140, где антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит, по меньшей мере, часть константной области иммуноглобулина.
142. Поверхностно модифицированная частица по варианту осуществления 141, где, по меньшей мере, часть константной области иммуноглобулина содержит Fc-область или часть Fc, содержащую домены CH2 и CH3.
143. Поверхностно модифицированная частица по варианту осуществления 141 или вариант осуществления 142, где константную область или Fc-область получают из IgG человека.
144. Поверхностно модифицированная частица по любому из вариантов осуществления 136-143, где антиидиотипическое антитело или его антигенсвязывающий фрагмент представляет собой интактное антитело или полноразмерное антитело.
145. Поверхностно модифицированная частица по любому из вариантов осуществления 121-144, где связывающая молекула ковалентно или нековалентно связана с частицами, например, с шариками.
146. Поверхностно модифицированная частица по любому из вариантов осуществления 121-145, где связывающая молекула присоединена к каждой из множества частиц, например, шариков, на С-концевом аминокислотном остатке связывающей молекулы или вблизи него и/или присоединение связывающей молекулы к каждой из множества частицам, например, с шариков, осуществляется таким образом, что область или эпитоп связывающей молекулы, распознаваемый антигенсвязывающим доменом рецептора антигена, ориентируется таким образом, что он может распознаваться рецептором антигена.
147. Поверхностно модифицированная частица по любому из вариантов осуществления 121-146, где частицы, например, шарики, представляют собой синтетические частицы, нерастворимые частицы, твердые частицы или представляют собой неклеточные частицы.
148. Поверхностно модифицированная частица по любому из вариантов осуществления 121-147, где множество частиц содержит шарики.
149. Поверхностно модифицированная частица по любому из вариантов осуществления 121-148, где частица имеет диаметр в пределах между или примерно между 1 мкм и 10 мкм или между или примерно между 2 мкм и 5 мкм.
150. Поверхностно модифицированная частица по любому из вариантов осуществления 121-149, где частица имеет диаметр примерно 2,8 мкм.
151. Поверхностно модифицированная частица по любому из вариантов осуществления 121-149, где частица имеет диаметр примерно 4,5 мкм.
152. Поверхностно модифицированная частица по любому из вариантов осуществления 121-151, где связывающая молекула ковалентно присоединена к частицам, например, шарикам.
153. Поверхностно модифицированная частица по любому из вариантов осуществления 121-152, где частица содержит поверхностно экспонируемую функциональную группу для присоединения связывающей молекулы и/или, где связывающая молекула ковалентно присоединена к частице посредством поверхностно экспонируемой функциональной группы.
154. Поверхностно модифицированная частица по варианту осуществления 153, где поверхностно экспонируемая функциональная группа представляет собой амино группу, карбоксильную группу, тиольную группу, альдегидную группу, хлорметильную группу, эпокси группу, гидроксильную группу, тозильную группу или гидразиновую группу.
155. Поверхностно модифицированная частица по варианту осуществления 154, где поверхностно экспонируемая функциональная группа представляет собой тозильную группу.
156. Поверхностно модифицированная частица по любому из вариантов осуществления 121-155, где частица является биологически совместимой или нетоксичной для клеток.
157. Поверхностно модифицированная частица по любому из вариантов осуществления 121-156, где множество частиц, например, шариков, содержит частицы, содержащие стекло, диоксид кремния, сложные полиэфиры гидроксикарбоновых кислот, полиангидриды дикарбоновых кислот, сополимеры гидроксикарбоновых кислот, сополимеры дикарбоновых кислот или металл.
158. Поверхностно модифицированная частица по любому из вариантов осуществления 121-157, где частицы, например, шарики, имеют поверхность, содержащую полимер, полисахарид, диоксид кремния, жирную кислоту, углерод или их сочетание.
159. Поверхностно модифицированная частица по варианту осуществления 158, где полимер представляет собой полиэтиленгликоль, сополимер молочная кислота - гликолевая кислота, полиглутаральдегид, полиуретан, полистирол и поливиниловый спирт или их сочетания.
160. Поверхностно модифицированная частица по любому из вариантов осуществления 121-149, где частица содержит гидрофобную поверхность.
161. Поверхностно модифицированная частица по любому из вариантов осуществления 121-160, где частицы, например, шарики, содержат полистирольную поверхность.
162. Поверхностно модифицированная частица по любому из вариантов осуществления 121-161, частица содержит частицы, которые являются магнитными и/или содержат магнитную сердцевину, парамагнитную сердцевину или суперпарамагнитную сердцевину.
163. Поверхностно модифицированная частица по любому из вариантов осуществления 121-162, где частица содержит, по меньшей мере или примерно, по меньшей мере, 10 копий, 102 копий, 103 копий, 104 копий, 105 копий или 106 копий связывающей молекулы.
164. Поверхностно модифицированная частица по любому из вариантов осуществления 121-163, где частица дополнительно содержит агент, который специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала, тем самым модулируя размножение клеток.
165. Поверхностно модифицированная частица по варианту осуществления 165, где агент представляет собой лиганд или представляет собой антитело или его антигенсвязывающий фрагмент.
166. Поверхностно модифицированная частица по варианту осуществления 164 или вариант осуществления 165, где молекула представляет собой костимуляторную молекулу или представляет собой активирующий корецептор или его лиганд.
167. Поверхностно модифицированная частица по варианту осуществления 166, где костимуляторная молекула или активирующий корецептор представляет собой OX-40, ICOS, DAP10, CD28 или 4-1BB или представляет собой его лиганд, необязательно, OX-40L, ICOSL, B7-1, B7-2 или 4-1BBL.
168. Поверхностно модифицированная частица по варианту осуществления 164 или варианту осуществления 165, где молекула представляет собой ингибиторный рецептор или его лиганд.
169. Поверхностно модифицированная частица по варианту осуществления 168, где ингибиторный рецептор представляет собой CTLA-4, PD-1, LAG-3, Tim-3, BTLA или TIGIT или представляет собой его лиганд, необязательно, PD-L1, PD-L2, CD155, CD112 или HIGHT.
170. Поверхностно модифицированная частица по любому из вариантов осуществления 164-169, где агент ковалентно присоединен к частицам, например, шарикам.
171. Поверхностно модифицированная частица по любому из вариантов осуществления 164-170, где отношение, необязательно, молярное или массовое отношение, связывающей молекулы и агента, удерживаемого частицами, составляет или составляет примерно 1:1.
172. Композиция, содержащая множество поверхностно модифицированных частиц, например, шариков, по любому из вариантов осуществления 113-153.
173. Композиция по варианту осуществления 172, где концентрация связывающей молекулы находится в пределах между или примерно между 0,5 мкг/мл и 500 мкг/мл, 1 мкг/мл и 200 мкг/мл или 5 мкг/мл и 100 мкг/мл.
174. Композиция по варианту осуществления 172 или варианту осуществления 173, где концентрация связывающей молекулы составляет, по меньшей мере, или, по меньшей мере, примерно 1 мкг/мл, 5 мкг/мл, 10 мкг/мл, 25 мкг/мл, 50 мкг/мл, 100 мкг/мл или 200 мкг/мл.
175. Композиция по любому из вариантов осуществления 172-174, которая является монодисперсной.
176. Набор, содержащий частицы по любому из вариантов осуществления 121-171 или композицию по любому из вариантов осуществления 154-158 и инструкции для применения.
177. Набор по варианту осуществления 176, где инструкции предназначены для селекции или обогащения популяции клеток, клеток, экспрессирующих рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой.
178. Набор по варианту осуществления 176, где инструкции предназначены для размножения в популяции клеток, клеток, экспрессирующих рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой
179. Набор по варианту осуществления 177 или варианту осуществления 178, где процент клеток, экспрессирующих рекомбинантный рецептор антигена, в популяции клеток меньше или примерно меньше 75%, 70%, 60%, 50%, 40%, 30%, 20%, 15%, 10% или меньше.
180. Способ размножения клеток, включающий инкубирование популяции клеток вместе с частицами по любому из вариантов осуществления 121-171 или с композицией по любому из вариантов осуществления 172-175.
181. Способ селекции или обогащения клеток, включающий приведение в контакт популяции клеток с частицей по любому из вариантов осуществления 121-171 или композицией по любому из вариантов осуществления 172-175.
182. Способ долговременной стимуляции для оценки композиции клеток, способ включает:
инкубирование в течение периода времени, по меньшей мере, 10 дней исходной композиции при условиях стимуляции CAR-зависимой активности клеток в исходной композиции, указанная исходная композиция содержит Т-лимфоциты, экспрессирующие химерный рецептор антигена (CAR), содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген, тем самым продуцируя выходную композицию; и
оценку одного или нескольких факторов из фенотипа или активности одной или нескольких клеток выходной композиции.
183. Способ по варианту осуществления 182, где условия стимуляции CAR-зависимой активности включают присутствие связывающей молекулы, которая специфично связывается с антигенсвязывающим доменом CAR.
184. Способ по варианту осуществления 183, где связывающая молекула присоединяется к подложке.
185. Способ по варианту осуществления 184, где подложка представляет собой твердую подложку.
186. Способ по варианту осуществления 185, где твердая подложка представляет собой поверхность лунки микропланшета или шарика.
187. Способ по любому из вариантов осуществления 183-186, где твердая подложка представляет собой микропланшет, имеющий связывающую молекулу, присоединенную к микропланшету, и инкубирование осуществляют в микропланшете.
188. Способ по любому из вариантов осуществления 183-187, где твердая подложка представляет собой шарик, содержащий присоединенную связывающую молекулу, и инкубирование осуществляют в присутствии множества шариков.
189. Способ по любому из вариантов осуществления 183-187, где связывающая молекула представляет собой или содержит рекомбинантный антиген или его часть, распознаваемую антигенсвязывающим доменом.
190. Способ по варианту осуществления 189, где рекомбинантный антиген или его часть представляет собой BCMA или представляет собой его часть, распознаваемую антигенсвязывающим доменом.
191. Способ по любому из вариантов осуществления 183-190, где связывающая молекула представляет собой или содержит антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфично связывается с антигенсвязывающим доменом.
192. Способ по варианту осуществления 191, где антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело SJ25C1 или его антигенсвязывающий фрагмент.
193. Способ по варианту осуществления 192, где антигенсвязывающий домен рецептора антигена представляет собой или содержит антитело FMC63 или его антигенсвязывающий фрагмент.
194. Способ по любому из вариантов осуществления 183-193, где способ осуществляется in vitro или ex vivo.
195. Способ по любому из вариантов осуществления 182-194, где исходную композицию инкубируют в присутствии сред, которые не содержат рекомбинантных цитокинов.
196. Способ по любому из вариантов осуществления 182-195, где инкубирование осуществляется непрерывно или не прерывается в течение периода времени.
197. Способ по любому из вариантов осуществления 182-196, где в ходе инкубирования, клетки не пересевают, среду не заменяют и связывающую молекулу не добавляют.
198. Способ по любому из вариантов осуществления 182-197, включающий оценку одного или нескольких фенотипов состояния активации, истощения или дифференциации одной, или нескольких клеток выходной композиции.
199. Способ по варианту осуществления 198, где фенотип представляет собой истощение и оценка включает измерение экспрессирования, необязательно, поверхностного экспрессирования, одного или нескольких маркеров, выбранных из CTLA-4, FOXP3, PD-1, TIGIT, LAB-3, 2B4, BTLA, TIM3, VISTA или CD96.
200. Способ по варианту осуществления 198, где фенотип представляет собой активацию, и оценка включает измерение экспрессирования, необязательно, поверхностного экспрессирования, одного или нескольких маркеров, выбранных из CD25, CD26, CD27, CD28, CD30, CD71, CD154, CD40L, CD127, LAG3 или Ki67.
201. Способ по варианту осуществления 198, где фенотип представляет собой состояние дифференциации и оценка включает измерение одного или нескольких маркеров, выбранных из (i) одного или нескольких из CD25, CD45RO, CD56, KLRG1, CD95 и/или (ii) одного из CD45RA, CD27, CD28, CD62L и CCR7, необязательно, при этом один или несколько маркеров представляет собой маркеры, которые положительно или наоборот, отрицательно ассоциируются с наивно-подобными Т-лимфоцитами.
202. Способ по любому из вариантов осуществления 182-201, включающий оценку одной или нескольких активностей одной или нескольких клеток выходной композиции.
203. Способ по любому из вариантов осуществления 182-202, где одна или несколько активностей включают CAR-зависимую активность, необязательно, антиген-стимулированную активность
204. Способ по варианту осуществления 202 или 203, где одна или несколько активностей включают цитолитическую активность или продуцирование цитокинов.
205. Способ по любому из вариантов осуществления 182-204, где период времени составляет, по меньшей мере или, по меньшей мере, примерно 11 дней, 12 дней, 13 дней, 14 дней или 15 дней.
206. Способ по любому из вариантов осуществления 182-205, где период времени составляет или составляет примерно 11 дней, 12 дней, 13 дней, 14 дней или 15 дней.
207. Способ по любому из вариантов осуществления 182-206, где исходная композиция содержит клетки, которые экспонируются или приводятся в контакт с исследуемым агентом или соединением до инкубирования, необязательно, при этом экспонирование или приведение в контакт осуществляется в ходе одной или нескольких стадий способа получения исходной композиции, содержащей Т-лимфоциты, экспрессирующие CAR.
208. Способ по любому из вариантов осуществления 182-207, где способ осуществляется на множестве исходных композиций, каждая указанная исходная композиция из множества получается с помощью иного способа.
209. Способ по любому из вариантов осуществления 182-208, дополнительно включающий сравнение фенотипа или активности выходной композиции с фенотипом или активностью контрольной композиции, при этом, необязательно, контрольная композиция представляет собой композицию Т-лимфоцитов, которые инкубируют в течение, по меньшей мере, 10 дней при таких же условиях для стимуляции CAR-зависимой активности, указанная композиция Т-лимфоцитов не получается в присутствии исследуемого агента или соединения или получается с помощью способа альтернативного по сравнению с исходной композицией.
210. Способ по любому из вариантов осуществления 182-209, дополнительно включающий идентификацию выходной композиции, которая демонстрирует уменьшение истощения, уменьшение активации или уменьшение дифференциации, необязательно, при этом уменьшение дифференциации включает увеличение экспрессирования одного или нескольких маркеров наивно-подобных Т-лимфоцитов.
IX. ПРИМЕРЫ
[645] Следующие далее примеры включаются только для иллюстративных целей и не предназначены для ограничения рамок настоящего изобретения.
Пример 1 Генерирование BCMA-конъюгированных шариков
[646] Антиген созревания В-клеток (BCMA) конъюгируется с шариками посредством ковалентного связывания слитого полипептида BCMA-Fc, содержащего растворимый BCMA человека, слитой на его C-конце с Fc-областью IgG, на поверхности коммерчески доступных тозилактивированных магнитных шариков (ThermoFisher, Waltham MA). Шарики представляют собой суперпарамагнитные, непористые, монодисперсные, тозилактивированные шарики, которые ковалентно связывают первичные амино и сульфгидрильные группы. Конъюгирование осуществляют с использованием шариков, имеющих диаметр приблизительно 2,8 мкм (обозначаемых M-280) или 4,5 мкм (обозначаемых M-450).
[647] BCMA-Fc (SEQ ID NO: 35) содержит внеклеточный домен BCMA человека (GenBank No. NP_001183.2) и Fc IgG1 человека, соединенный с линкером следующим образом:
MLQMAGQCSQNEYFDSLLHACIPCQLRCSSNTPPLTCQRYCNASVTNSVKGTNA (внеклеточный домен BCMA; SEQ ID NO: 1)
GGGGS (линкер; SEQ ID NO: 27)
PKSSDKTHTCPPCPAPEAEGAPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPSSIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (Fc IgG1 человека; SEQ ID NO: 28).
[648] Клон, кодирующий рекомбинантную слитую конструкцию BCMA-Fc человека с N-концевой CD33 лидерной последовательностью (SEQ ID NO: 30), вставляется в вектор экспрессии и экспрессируется в клетках HEK 293. Супернатант от транзиентно трансфицированных клеток HEK харвестируют через 5 дней и слитый белок BCMA-FC очищают с помощью аффинной хроматографии на белке A и эксклюзионной хроматографии (SEC). Полученный в результате слитый белок BCMA-Fc, как определяют, имеет чистоту больше, чем 95% по оценкам гель-проникающей хроматографии. Для исследования связывания, слитый белок BCMA-Fc инкубируют вместе с Т-лимфоцитами, экспрессирующими CAR анти-BCMA, и Т-лимфоцитами, экспрессирующими CAR, которые не связываются с BCMA. Результаты проточной цитометрии показывают, что слитый белок BCMA-Fc специфично связывается с Т-лимфоцитами, экспрессирующими CAR анти-BCMA.
[649] Различные концентрации слитого белка BCMA-Fc в пределах от 5 мкг до 200 мкг добавляют приблизительно к 1 мл тозилактивированных шариков (например, содержащему примерно 4×109 тозилактивированных шариков, имеющих диаметр 2,8 мкм, или примерно 4×108 тозилактивированных шариков, имеющих диаметр 4,5 мкм). Ковалентное связывание осуществляют посредством инкубирования в течение ночи при 37°C в фосфатном буферном растворе (PBS), содержащем 0,1% сывороточного альбумина человека (HSA). Шарики промывают и повторно суспендируют в 1 мл PBS с 0,1% HSA. До и после конъюгирования, концентрацию шариков определяют с использованием Cellometer. Процент антигена BCMA-Fc, который связывается с шариками, определяют с помощью анализа SDS PAGE. В примерах ниже, BCMA-конъюгированные шарики, используемые при различных исследованиях, упоминаются либо со ссылками на количество антигена BCMA-Fc, добавляемого на мл, либо на концентрацию антигена (мкг/мл) в ходе конъюгирования, например, 5 мкг или 5 мкг/мл; 50 мкг или 50 мкг/мл; 200 мкг или 200 мкг/мл, и так далее.
[650] Для некоторых исследований, описанных ниже, шарики являются двояко - конъюгированными с BCMA-Fc и антителом анти-CD28 при отношении 1:1 с использованием процедур, по существу, как описано выше.
Пример 2: Стимуляция шариками, конъюгированными с антителом анти-BCMA Т-лимфоцитов CAR
[651] BCMA-конъюгированные шарики (диаметр 4,5 мкм), генерируемые, как описано в Примере 1, инкубируют вместе с Т-лимфоцитами, экспрессирующими CAR BCMA. Т-лимфоциты выделяют посредством иммунноаффиного обогащения образцов от лейкафереза от здоровых доноров. Выделенные Т-лимфоциты трансдуцируют вирусным вектором, кодирующим один из двух CAR анти-BCMA, каждый содержит иной антигенсвязывающий домен scFv специфичный к BCMA, спейсер, трансмембранную область CD28, костимуляторную сигнальную область 4-1BB и внутриклеточный сигнальный домен, полученный из CD3-зета (обозначаются как CAR анти-BCMA #1 и CAR анти-BCMA #2, отличающиеся только в части scFv). Кроме того, конструкция вирусного вектора кодирует усеченный EGFR (EGFRt), который служит как суррогатный маркер для экспрессирования CAR; EGFRt-кодирующая область отделяется от последовательности CAR перескакивающей последовательностью T2A. После трансдуцирования, клетки наращивают, приготавливают при отношении Т-лимфоцитов CAR+ CD4+ к Т-лимфоцитам CAR+ CD8+ приблизительно 1:1 и полученные в результате композиции замораживают посредством криоконсервирования. Для описанных исследований, эффективность трансдуцирования композиций Т-лимфоцитов, экспрессирующих CAR анти-BCMA #1и CAR анти-BCMA #2, составляет либо 45%, либо 56%, соответственно, как определено с использованием антитела анти-EGFR для детектирования суррогатного маркера EGFRt.
[652] Композицию Т-лимфоцитов, содержащих Т-лимфоциты CAR+ анти-BCMA, оттаивают, и добавляют к клеткам шарики из 100 мкг/мл композиции BCMA-конъюгированных шариков при отношении шарики:клетки 1:1 и инкубируют в течение пяти дней. При положительном контроле, клетки культивируют вместе с шариками анти-CD3/анти-CD28 при отношении шарики:клетки 1:1 в течение пяти дней. Т-лимфоциты, которые не экспрессируют CAR (группа имитационных исследований), также оценивают после инкубирования вместе с BCMA-конъюгированными шариками.
[653] Для оценки пролиферации, композиция клеток, содержащая Т-лимфоциты, экспрессирующие CAR анти-BCMA, метится с помощью красителя-маркера пролиферации CELLTRACE VIOLET (CTV; ThermoFisher Scientific, Waltham MA) в соответствии с протоколом производителя до инкубирования вместе с BCMA-конъюгированными шариками. Иллюстративные результаты, показанные на Фиг. 1, демонстрируют, что инкубирование вместе с BCMA-конъюгированными шариками дает в результате уменьшение интенсивности флуоресценции CTV окрашивания в Т-лимфоцитах CD3+, указывая на разбавление пролиферационного красителя, представляющего степень пролиферации, согласно количеству делений клеток. Для имитационных клеток, очень мало Т-лимфоцитов CD3+ выживает после инкубирования, и для имитационных клеток, которые не экспрессируют CAR анти-BCMA, не наблюдается уменьшения интенсивности CTV. Эти данные показывают, что инкубирование вместе с BCMA-конъюгированными шариками специфично увеличивает пролиферацию клеток для Т-лимфоцитов, экспрессирующих CAR анти-BCMA.
[654] Для оценки того обогащается ли специфично размножение Т-лимфоцитов CAR+ после инкубирования вместе с BCMA-конъюгированными шариками, клетки композиции Т-лимфоцитов окрашивают на поверхностное экспрессирование CD4 или CD8 и на экспрессирование маркера трансдуцирования EGFRt с использованием антитела анти-EGFR, и анализируют с помощью проточной цитометрии. Степень обогащения Т-лимфоцитов CAR+ (как детектируется по экспрессированию суррогатного маркера EGFRt) после инкубирования вместе с BCMA-конъюгированными шариками сравнивают с обогащением после поликлональной стимуляции с использованием шариков анти-CD3/анти-CD28. Степень пролиферации клеток (как определено по разбавлению интенсивности окрашивания пролиферационным красителем CTV) и степень активации (как определено по поверхностному экспрессированию CD25 или PD-1) также сравнивают с композициями Т-лимфоцитов, инкубируемых либо вместе с BCMA-конъюгированными шариками, либо вместе с контрольными шариками анти-CD3/анти-CD28.
[655] Как показано в Таблице E1, инкубирование композиций Т-лимфоцитов, содержащих Т-лимфоциты CAR+ анти-BCMA вместе с BCMA-конъюгированными шариками в течение пяти дней дает в результате в больший процент клеток CD4+ и клеток CD8+, которые экспрессируют EGFRt, по сравнению с инкубированием таких же композиций Т-лимфоцитов вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28, это указывает, что BCMA-конъюгированные шарики обогащают Т-лимфоциты CAR+ анти-BCMA.
Таблица E1: Процент клеток EGFRt+ после инкубирования вместе с BCMA-конъюгированными шариками
[656] Как показано на Фиг. 2A, по сравнению с инкубированием вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28, инкубирование композиции Т-лимфоцитов, содержащей CAR-экспрессирующие Т-лимфоциты анти-BCMA, вместе с BCMA-конъюгированными шариками в течение пяти дней, дает в результате уменьшение экспрессирования CD25, но некоторое увеличение способности к пролиферации как доказывает большее уменьшение интенсивности пролиферационного красителя CTV. Фиг. 2B приводит гистограмму, на которой ось х показывает интенсивность CTV окрашивания, а ось y показывает нормальное количество клеток для изображения данных в терминах “% max” согласно программному обеспечению FlowJo (обозначается “нормированное к модальному значению интегральной флуоресценции”). % max обозначает количество клеток в каждом столбике гистограммы (численные диапазоны для параметра на оси х) деленное на количество клеток в столбике, который содержит наибольшее количество клеток. FlowJo использует 256 столбиков и каждый график нормируется на процент от его максимального столбика. Как показано, небольшое уменьшение интенсивности CTV окрашивания (увеличение разбавления показывает пролиферацию клеток) наблюдается, по меньшей мере, для подмножества клеток по сравнению с Т-лимфоцитами, инкубируемыми вместе с шариками, конъюгированными с анти-CD3/анти-CD28. В дополнение к этому, как показано на Фиг. 2C, экспрессирование PD-1 увеличивается в Т-лимфоцитах CD4+ и CD8+ инкубируемых вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28, при этом инкубирование Т-лимфоцитов CD4+ и CD8+ вместе с BCMA-конъюгированными шариками не дает в результате увеличения экспрессирования PD-1, в частности, в Т-лимфоцитах CD8+.
[657] Для дополнительной оценки степени обогащения Т-лимфоцитов CAR+, три отдельных композиции Т-лимфоцитов, содержащие Т-лимфоциты, полученные от трех различных доноров, на которых воздействуют генной инженерией для экспрессирования CAR анти-BCMA, инкубируют вместе с BCMA-конъюгированными шариками. Клетки анализируют с помощью проточной цитометрии через четыре, семь или четырнадцать дней инкубирования (клетки пересевают в день 7). Как показано на Фиг. 3A, процент Т-лимфоцитов экспрессирующих CAR анти-BCMA увеличивается со временем во всех трех композициях Т-лимфоцитов. Клетки CD8+ CAR+ из каждой композиции анализируют с помощью проточной цитометрии на поверхностное экспрессирование CD25, CD27 или CCR7 через четыре, семь или четырнадцать дней инкубирования. Как показано на Фиг. 3B, уровни поверхностного экспрессирования CD25 и CCR7 уменьшаются в ходе инкубирования по сравнению с измерениями в день 4. В противоположность этому, поверхностное экспрессирование CD27 в клетках CAR+CD8+ остается относительно постоянным.
Пример 3: Воздействия титрования BCMA-конъюгированных шариков на Т-лимфоцитах CAR
[658] Композиция Т-лимфоцитов, содержащая Т-лимфоциты CAR+ CD4/CD8 анти-BCMA генерируется, по существу, как описано в Примере 2, за исключением того, что приготовленная в результате композиция содержит приблизительно 74% клеток CD8+ и 21% клеток CD4+, из которых 82% клеток в целом были положительными относительно CAR анти-BCMA (как детектируется с использованием растворимого BCMA-FC) и 68% были положительными относительно EGFRt как определено с использованием антитела анти-EGFR. Композицию, содержащую Т-лимфоциты CAR+ анти-BCMA, замораживают посредством криоконсервирования и оттаивают перед использованием в следующих далее исследованиях.
[659] Различные препараты BCMA-конъюгированных шариков (диаметр 4,5 мкм; включая шарики из 50 мкг/мл, 25 мкг/мл, 10 мкг/мл или 5 мкг/мл композиции BCMA-конъюгированных шариков), приготовленные как описано в Примере 1, добавляют к композиции клеток при отношении шарики:клетки 1:1, содержащей Т-лимфоциты, экспрессирующие CAR анти-BCMA, а затем инкубируют в течение 4 дней. Т-лимфоциты, которые метятся красителем маркером пролиферации CTV, отслеживают с помощью проточной цитометрии на интенсивность сигнала CTV как индикатор пролиферации клеток. Клетки также оценивают на поверхностное экспрессирование CD3, CD4, CD8, CD25, PD1 и суррогатного маркера EGFRt с помощью проточной цитометрии.
[660] Фиг. 4A показывает столбчатые диаграммы уровней поверхностного окрашивания CD25 в клетках CD4+ и CD8+, а Фиг. 4B показывает гистограммы, нормированные к модальному значению интегральной флуоресценции, как описано выше, для поверхностного экспрессирования PD-1 в Т-лимфоцитах CD4+ или CD8+ после инкубирования вместе с указанным концентрациями BCMA-конъюгированных шариков. Как показано на Фигурах 4A и 4B, инкубирование вместе с BCMA-конъюгированными шариками дает в результате доза-зависимое увеличение поверхностного экспрессирования CD25 (верхние панели) и PD-1 (нижние панели) как в клетках CD4+, так и в клетках CD8+.
[661] Как показано на Фиг. 5A и Фиг. 5B, нет доза-зависимого различия в общих отсчетах Т-лимфоцитов, как оценивается по количеству клеток CD3+ (Фиг. 5A), однако, имеется небольшое доза-зависимое уменьшение средней интенсивности флуоресценции CTV (MFI) в клетках CD4+ (Фиг. 5B) после инкубирования вместе с BCMA-конъюгированными шариками. Как показано на Фиг. 6, инкубирование вместе с BCMA-конъюгированными шариками дает в результате доза-зависимое увеличение поверхностного экспрессирования CD25 в клетках CD4+.
[662] Вместе, эти данные показывают, что BCMA-конъюгированные шарики с более низкой концентрацией BCMA демонстрируют более низкое экспрессирование маркера активации и более высокую пролиферацию. Эти данные показывают, что определенные атрибуты композиции Т-лимфоцитов, содержащей Т-лимфоциты CAR+ анти-BCMA, могут подвергаться манипуляциям посредством титрования количества антигена BCMA, конъюгированного с шариками.
Пример 4: Оценка маркеров Т-лимфоцитов на Т-лимфоците CAR+ анти-BCMA, стимулируемом с помощью BCMA-конъюгированных шариков
[663] BCMA-конъюгированные шарики (диаметр 4,5 мкм), конъюгированные с различными количествами антигена BCMA, как описано в Примере 1, инкубируют вместе с Т-лимфоцитами CAR+ анти-BCMA, и оценивается экспрессирование маркеров Т-лимфоцитов.
[664] В одном из экспериментов, криоконсервированные T-лимфоциты CAR анти-BCMA, полученные, по существу, как описано в Примере 2, и приготовленные при отношении Т-лимфоцитов CD4+ и CD8+ 1:1, оттаивают и высевают при 1,5 × 106 клеток на лунку в 12-луночный планшет. Клетки инкубируют в течение трех дней в присутствии шариков из 50 мкг/мл, 100 мкг/мл или 200 мкг/мл композиции BCMA-конъюгированных шариков. Инкубирование осуществляют при отношении Т-лимфоцитов к шарикам 1:1. Анализ поверхностного экспрессирования CD25 на клетках CD4+ и CD8+ с помощью проточной цитометрии показывает сходное индуцирование CD25 для всех концентраций BCMA-конъюгированных шариков (Фиг. 7A).
[665] В другом эксперименте, приблизительно 1,5 × 106 Т-лимфоцитов CAR+, приготовленных, как описано выше, добавляют в лунки 12-луночного планшета и инкубируют вместе с шариками из 200 мкг композиции BCMA-конъюгированных шариков при отношении Т-лимфоцитов CAR+ к BCMA-конъюгированным шарикам 1:0,3, 1:1 или 1:3 (приблизительно 0,5×106, 1,5×106 и 4,5×106 шариков на лунку, соответственно). В качестве контроля, 5 мкг/мл антитела анти-CD3 наносят в виде покрытия на лунки (субоптимальная концентрация для стимуляции) или клетки высевают в отсутствие какого-либо агента (без контроля стимуляции). Каждое состояние инкубируют в присутствии или в отсутствие 5 мкМ леналидомида. Клетки инкубируют в течение четырех дней, а затем анализируют с помощью проточной цитометрии на поверхностное экспрессирование CD4, CD8, Tim3, PD-1, CD25 и CD69. Инкубирование Т-лимфоцитов CAR+ анти-BCMA вместе с BCMA-конъюгированными шариками увеличивает поверхностное экспрессирование CD25 (Фиг. 7B), CD69 (Фиг. 7C) и Tim3 (Фиг. 7D) на Т-лимфоцитах CD4+ и CD8+. Клетки, которые стимулируют в присутствии наибольшего количества шариков, обеспечиваемого при отношении Т-лимфоцитов CAR+ к шарикам 1:3, демонстрирует наибольшее увеличение экспрессирования этих маркеров. Как показано на Фиг. 7E, поверхностное экспрессирование PD-1 на Т-лимфоцитах CAR+ анти-BCMA также является наибольшим, когда клетки CD4+ инкубируются при отношении Т-лимфоцитов CAR+ к шарикам 1:3. Имеется также небольшое увеличение поверхностного экспрессирования PD-1 на клетках CD8+, при стимулировании BCMA-конъюгированными шариками при более высокой концентрации шариков BCMA, обеспечиваемой при отношении Т-лимфоцитов CAR+ к шарикам 1:3. Результаты согласуются с теми данными, что концентрация BCMA, присутствующего в ходе инкубирования, может по-разному модулировать экспрессирование поверхностного маркера на Т-лимфоцитах CAR+.
[666] Как показано на Фиг. 7F, присутствие 5 мкМ леналидомида повышает пролиферативную способность Т-лимфоцитов (наблюдаемую по уменьшению интенсивности красителя CTV) после инкубирования в течение трех дней вместе с шариками, конъюгированными с 200 мкг антигена BCMA при отношении Т-лимфоцитов к шарикам 1:1 по сравнению с инкубированием вместе с шариками в отсутствие леналидомида (контрольная лекарственная среда). Как показано на Фигурах 7G и 7H, присутствие леналидомида в ходе инкубирования дополнительно повышает степень поверхностного экспрессирования CD25 в Т-лимфоцитах CD4+ и CD8+, индуцируемого после инкубирования Т-лимфоцитов CAR+ анти-BCMA вместе с BCMA-конъюгированными шариками (Фиг. 7G) или стимуляции анти-CD3 (Фиг. 7H).
[667] В другом эксперименте, композиции T-лимфоцитов CAR анти-BCMA полученные, по существу, как описано в Примере 1, высевают в 96-луночные планшеты при плотности 5×105 клеток на лунку. Исследуемые композиции T-лимфоцитов CAR содержат в среднем приблизительно 45% клеток CAR+ анти-BCMA при высевании. Клетки из каждой композиции инкубируют в течение 18 часов в присутствии шариков из 5 мкг/мл, 50 мкг/мл или 200 мкг/мл композиции BCMA-конъюгированных шариков при отношении Т-лимфоцитов к шарикам 1:1. В качестве контроля, клетки инкубируют вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28 (положительный контроль), или без добавляемого агента (отрицательный контроль). Инкубирование осуществляют в отсутствие леналидомида или в присутствии 0,5 мкМ или 5 мкМ леналидомида. После инкубирования, клетки обрабатывают реагентами, которые дают возможность для внеклеточного и внутриклеточного окрашивания антитела, с помощью проточной цитометрии, на факторы транскрипции Blimp1, EOMES, GATA-3, ikaros, helios, и Tbet и маркеры CD25, CD31 и PD-1.
[668] Уровни маркеров после инкубирования композиции Т-лимфоцитов CAR+ от одного иллюстративного донора показаны для BLIMP-1 (Фиг. 8A), CD25 (Фиг. 8B), CD31 (Фиг. 8C), PD-1 (Фиг. 8D), Tbet (Фиг. 8E), и EOMES (Фиг. 8F), GATA-3 (Фиг. 8G) Helios (Фиг. 8H) и Ikaros (Фиг. 8I). Как показано, экспрессирование ряда оцениваемых факторов транскрипции, ассоциированных с эффекторными T-лимфоцитами, и маркеров активации увеличивается после стимуляции BCMA-конъюгированными шариками. Для множества оцениваемых маркеров, степень повышения экспрессирования является сходной с экспрессированием, индуцируемым стимуляцией с помощью шариков анти-CD3/анти-CD28. В некоторых случаях, степень стимуляции с помощью BCMA-конъюгированных шариков наибольшая в присутствии 5 мкг шариков. Как показано на Фиг. 8I, уровень экспрессирования Ikaros уменьшается в присутствии леналидомида при всех условиях. Сходные результаты наблюдают в композиции Т-лимфоцитов CAR+, генерируемой от второго донора, за исключением того, что не наблюдается изменения экспрессирования Helios из клеток от этого донора, когда они стимулируются при условиях исследования.
Пример 5: Оценка активности T-лимфоцитов CAR анти-BCMA, стимулируемых с помощью BCMA-конъюгированных шариков
[669] Оценивается активность T-лимфоцитов CAR анти-BCMA, которые генерируются из процесса, который включает размножение в присутствии BCMA-конъюгированных шариков.
A. Эффекторные реакции
Криоконсервированные T-лимфоциты CAR анти-BCMA полученные, по существу, как описано в Примере 2, и приготовленные при отношении Т-лимфоцитов CD4+ и CD8+ 1:1, оттаивают. Если не указано иного, шарики (диаметр примерно 4,5 мкм) из 5 мкг/мл или 50 мкг/мл композиции BCMA-конъюгированных шариков, генерируемых, как описано в Примере 1, добавляют в лунки при отношении Т-лимфоцитов к шарикам 1:2 в присутствии или в отсутствие 5 мкМ леналидомида. Клетки инкубируют до 14 дней и анализируют в различных временных точках на секретирование цитокинов, размножение клеток с помощью проточной цитометрии, на суррогатный маркер EGFRt и на цитолитическую активность.
a. Экспрессирование цитокинов
(i) Присутствие цитокинов в супернатанте
[670] Через двадцать четыре часа после добавления BCMA-конъюгированных шариков, оценивают присутствие TNF-α, IFNγ и IL-2 в супернатантах культур. Как показано на Фигурах 9A-9C, инкубирование вместе с BCMA-конъюгированными шариками индуцирует секретирование IFNγ (Фиг. 9A), IL-2 (Фиг. 9B) и TNF-α (Фиг. 9C) в супернатантах культур. Степень продуцирования цитокинов выше, когда клетки инкубируются с шариками из 50 мкг/мл композиции BCMA-конъюгированных шариков, по сравнению с 5 мкг/мл композицией BCMA-конъюгированных шариков, это демонстрирует, что CAR стимуляция посредством BCMA шариков является доза-зависимой. Как показано, леналидомид повышает BCMA-индуцированное продуцирование цитокинов Т-лимфоцитами CAR+ после стимуляции с помощью BCMA-конъюгированных шариков.
[671] В другом иллюстративном исследовании, две различных композиции Т-лимфоцитов CAR анти-BCMA генерируются от различных доноров, каждая из них содержит Т-лимфоциты, экспрессирующие одинаковые CAR анти-BCMA. Клетки оттаивают и инкубируют вместе с шариками (диаметр примерно 4,5 мкм) из 5 мкг/мл или 200 мкг/мл композиции BCMA-конъюгированных шариков, генерируемой, как описано в Примере 1. Инкубирование осуществляют при отношении Т-лимфоцитов к шарикам 1:1 в присутствии или в отсутствие 1 мкМ или 5 мкМ леналидомида. Через двадцать четыре часа после добавления BCMA-конъюгированных шариков, оценивают продуцирование IL-2 Т-лимфоцитами CAR+ анти-BCMA в супернатантах культур. Как показано на Фиг. 9D, более высокое продуцирование IL-2 наблюдают в присутствии высокой стимуляции антигеном (200 мкг/мл BCMA-конъюгированных шариков) по сравнению с более низкой стимуляцией антигеном (5 мкг/мл BCMA-конъюгированных шариков). Леналидомид, либо при 1 мкМ, либо при 5 мкМ, повышает продуцирование цитокинов в присутствии как высокой, так и низкой стимуляции антигеном.
(ii) Внутриклеточные уровни цитокинов
[672] Т-лимфоциты CAR+ анти-BCMA инкубируют в присутствии 1 мкМ леналидомида или лекарственной среды и 50 мкг/мл шариков, конъюгированных с BCMA-Fc, в течение 2 часов, и клетки оцениваются с помощью проточной цитометрии на фосфорилированный STAT 5. Для оценки уровней цитокинов IFNγ и TNFα, Т-лимфоциты CAR+ анти-BCMA инкубируют в присутствии 0,1 мкМ или 1 мкМ леналидомида или лекарственной среды и 5 мкг/мл, 50 мкг/мл или 200 мкг/мл шариков, конъюгированных с BCMA-Fc, в течение 24 часов. Клетки гейтируются на трансдуцированных, живых клетках CD3+, и оцениваются с помощью проточной цитометрии на внутриклеточную аккумуляцию цитокинов IFNγ и TNFα в клетках CD4+ и CD8+.
[673] Как показано на Фиг. 9E, 2-часовая стимуляция антигеном увеличивает процент клеток положительных относительно фосфор-STAT5 по сравнению с контролем без стимуляции (показанным точечной линией). Результаты для внутриклеточных уровней цитокинов IFNγ и TNFα из T-лимфоцитов CAR анти-BCMA, генерируемых репрезентативным нормальным донором T-лимфоцитов CAR, показаны на Фиг. 9F. В этом исследовании, продуцирование цитокинов T-лимфоцитами CAR анти-BCMA повышается под действием леналидомида в широком диапазоне уровней антигена и концентраций.
b. Пролиферация клеток
[674] Отсчеты клеток, в целом, отслеживаемые в день 4 (Фиг. 9G) и день 7 (Фиг. 9H), повышаются после стимуляции Т-лимфоцитов CAR+ анти-BCMA с помощью шариков из 50 мкг/мл композиции BCMA-конъюгированных шариков, но не из 5 мкг/мл композиции BCMA-конъюгированных шариков, по сравнению с клетками, присутствующими в момент начала инкубирования (штриховая линия). Небольшое увеличение пролиферации наблюдается в клетках, инкубируемых вместе с 50 мкг шариков, в присутствии леналидомида в день 7.
[675] Для дополнительной оценки пролиферации, клетки, содержащие Т-лимфоциты, экспрессирующие CAR BCMA, метятся красителем - маркером пролиферации CELLTRACE VIOLET (CTV; ThermoFisher Scientific, Waltham MA) в соответствии с протоколом производителя перед инкубированием вместе с BCMA-конъюгированными шариками. Пролиферацию оценивают с помощью разбавления красителя с использованием проточной цитометрии на клетках, которые стимулируются шариками из 50 мкг/мл композиции BCMA-конъюгированных шариков. По сравнению с пролиферацией в отсутствие леналидомида, имеется небольшая задержка в пролиферации, как оценивается по разбавлению CTV в присутствии леналидомида в день 4, но не в день 7 (Фиг. 9I).
c. Размножение
[676] Через четыре дня и семь дней после добавления BCMA-конъюгированных шариков, инкубированные клетки окрашивают с помощью CD4 или CD8 и с помощью антитела анти-EGFR для определения процента клеток положительных относительно EGFRt в качестве суррогата для Т-лимфоцитов CAR+. Во время высевания, 26% клеток CD4+ экспрессируют CAR анти-BCMA и 39% клеток CD8+ экспрессируют CAR анти-BCMA, как определяется посредством окрашивания с помощью BCMA-Fc. Процент Т-лимфоцитов CD4+ EGFRt+ увеличивается примерно от 26% при начале инкубирования до больше 40% в день 4 (Фиг. 9J) и больше 60% в день 7 (Фиг. 9K), когда клетки инкубируют в присутствии шариков из 50 мкг/мл композиции BCMA-конъюгированных шариков. Как показано на Фиг. 9K, процент Т-лимфоцитов CD8+ EGFRt+ увеличивается в день 7 примерно от 38% при начале инкубирования до больше 60%, когда клетки инкубируются в присутствии шариков из 50 мкг/мл композиции BCMA-конъюгированных шариков. Степень размножения клеток наибольшая, когда клетки инкубируются в присутствии шариков из 50 мкг/мл композиции BCMA-конъюгированных шариков по сравнению с шариками из 5 мкг/мл композиции BCMA-конъюгированных шариков. Присутствие леналидомида, по существу, не влияет на степень размножения Т-лимфоцитов CAR+ в этом исследовании.
d. Цитолитическая активность
[677] Цитолитическая активность Т-лимфоцитов CAR+ после инкубирования вместе с BCMA-конъюгированными шариками оценивают посредством инкубирования вместе с BCMA-экспрессирующей целевой линией клеток RPMI-8226, которая представляет собой линию клеток множественной миеломы BCMA+. Через семь дней инкубирования Т-лимфоцитов CAR+ анти-BCMA вместе с BCMA-конъюгированными шариками (5 мкг/мл или 50 мкг/мл) в присутствии или в отсутствие леналидомида, шарики удаляют из культур и клетки высевают вместе с целевыми клетками RPMI-8226 при отношении эффекторных клеток к целевым клеткам 3:1 или 1:1, кроме того, в присутствии или в отсутствие 5 мкМ леналидомида. Для осуществления цитолитического анализа, целевые клетки RPMI-8226 метятся NucLight Red (NLR), чтобы сделать возможным отслеживание целевых клеток с помощью микроскопии. Цитолитическую активность оценивают посредством измерения потерь жизнеспособных целевых клеток за период четырех дней, как определяют с помощью сигнала красной флуоресценции (с использованием INCUCYTE® Live Cell Analysis System, Essen Bioscience). Количество жизнеспособных клеток нормируют на клетки в день 0 перед инкубированием вместе с целевыми клетками RPMI-8226.
[678] Иллюстративные результаты при отношении эффекторных клеток к целевым 1:1 показаны на Фиг. 9L. Как показано, Т-лимфоциты CAR+ анти-BCMA демонстрируют эффективное уничтожение в этом анализе. Т-лимфоциты CAR+ анти-BCMA, которые стимулируются с помощью шариков из 5 мкг/мл композиции BCMA-конъюгированных шариков, является чуть менее эффективными при уничтожении клеток, чем Т-лимфоциты CAR+ анти-BCMA, которые стимулируют с помощью шариков из 5 мкг/мл композиции BCMA-конъюгированных шариков. Для всех условий, предварительное инкубирование вместе с леналидомидом в ходе семидневного инкубирования перед анализом уничтожения повышает цитолитическую активность Т-лимфоцитов CAR+. Присутствие леналидомида в ходе анализа уничтожения клеток не влияет существенно на активность уничтожения. Уничтожения клеток не наблюдается, когда клетки RPMI 8226 культивируются сами по себе или в присутствии леналидомида, это демонстрирует, что леналидомид не влияет прямо на жизнеспособность целевых клеток в этом анализе.
[679] В другом иллюстративном исследовании, Т-лимфоциты CAR+ анти-BCMA не обрабатываются или инкубируются в течение 24 часов или в течение семи дней вместе с шариками (диаметр примерно 4,5 мкм) из 50 мкг/мл композиции BCMA-конъюгированных шариков, генерируемых, как описано в Примере 1, при отношении шариков к клеткам 1:1. T-лимфоциты CAR+ анти-BCMA удаляются из культуры и инкубируются вместе с целевыми клетками RPMI-8226 при отношении эффекторных клеток к целевым клеткам 0,3:1 или 1:1. Для оценки реакции цитокинов на целевые клетки после инкубирования вместе с BCMA-конъюгированными шариками, измеряют уровни IFN гамма в супернатанте. Как показано на Фиг. 9M, Т-лимфоциты CAR+ анти-BCMA, которые инкубируются в течение 24 часов вместе с BCMA-конъюгированными шариками, продуцируют больше IFN-гамма по сравнению с другими исследуемыми клетками, когда культивируются вместе с целевыми клетками RPMI-8226 при любом отношении. Как показано на Фиг. 9N для отношения эффекторных клеток к целевым 1:1, T-лимфоциты CAR анти-BCMA демонстрируют эффективное уничтожение после инкубирования вместе с BCMA-конъюгированными шариками в течение 24 часов или 7 дней, это демонстрирует, что клетки сохраняют функцию после стимуляции с помощью шариков.
B. Последовательная повторная стимуляция
[680] Композиции Т-лимфоцитов CAR анти-BCMA генерируются от трех различных доноров, каждая содержит Т-лимфоциты, экспрессирующие один и тот же CAR анти-BCMA, оттаиваются и инкубируются в течение семи дней вместе с шариками (диаметр примерно 4,5 мкм) из 50 мкг/мл композиции BCMA-конъюгированных шариков, генерируемой, как описано в Примере 1, при отношении шариков к клеткам 1:1. Инкубирование осуществляют в присутствии 5 мкМ леналидомида или в отсутствие леналидомида (контрольная лекарственная среда). Клетки харвестируют через 7 дней и повторно высевают для трех дополнительных заходов в пределах до 28 дней, каждый заход включает восстановление начальной плотности высевания и инкубирование в течение дополнительных 7 дней в присутствии одной и той же концентрации леналидомида.
[681] При каждом возврате в исходное состояние после предварительной обработки, цитолитическую активность оценивают посредством инкубирования вместе с BCMA-экспрессирующей целевой линией клеток RPMI-8226 (меченой NucLight Red (NLR)) при отношении эффекторных клеток к целевым (E:T) 1:1, дополнительно, присутствии или в отсутствие леналидомида. Цитолитическую активность оценивают посредством измерения потерь жизнеспособных целевых клеток за период до 80-150 часов, как определяется по сигналу красной флуоресценции (с использованием IncuCyte® Live Cell Analysis System, Essen Bioscience). Клетки от каждого условия высеваются в трех параллельных опытах. Определяют % уничтожения клеток по сравнению с одной только контрольной лекарственной средой (как 100%).
[682] Фиг. 10A показывает результаты по цитолитической активности Т-лимфоцитов CAR+ анти-BCMA от иллюстративного донора после предварительной обработки в течение 7 дней, 14 дней или 21 дня. Как показано, Т-лимфоциты CAR+ анти-BCMA, которые предварительно инкубируются вместе с леналидомидом в течение 7 дней или 14 дней, демонстрируют более высокую цитолитическую активность по сравнению с клетками, которые не инкубируются предварительно в присутствии леналидомида. У этого донора, общее уменьшение эффективности уничтожения наблюдают для Т-лимфоцитов CAR+ анти-BCMA, которые предварительно инкубируют вместе с леналидомидом в течение 14 или 21 дня, по сравнению с днем 7. Сходные воздействия на цитолитическую активность Т-лимфоцитов CAR+ анти-BCMA после предварительной обработки леналидомидом в течение 7 или 14 дней наблюдают у донора; цитолитическую активность через 21 день предварительной обработки леналидомидом у этого донора не оценивают. Как показано на Фиг. 10B, увеличение эффективности уничтожения Т-лимфоцитов CAR+ анти-BCMA наблюдают у этого донора на клетках, которые предварительно инкубируются вместе с леналидомидом, во всех временных точках.
Пример 6: Трансдуцирование и размножение Т-лимфоцитов CAR+ анти-BCMA в присутствии BCMA-конъюгированных шариков
[683] Образцы от лейкафереза человека, обогащенные мононуклеарными клетками, получают из образца цельной крови у субъекта с использованием системы сбора лейкафереза. В тот же день, когда осуществляют лейкаферез, клетки из образца от лейкафереза промывают и повторно суспендируют в буфере для использования при селекции на основе аффиности, буфер содержит солевой фосфатный буфер (PBS), EDTA и сывороточный альбумин человека. Для селекции на основе иммунноаффиности Т-лимфоцитов, промытые клетки в буфере для селекции инкубируют в течение 30 минут при комнатной температуре вместе с магнитными шариками, связанными с моноклональными антителами специфичными к CD4 и CD8, и обогащают посредством положительной селекции с использованием колонки для магнитной сепарации. Обогащенные клетки CD4+ и CD8+, при отношении 1:1, повторно суспендируют в средах для криоконсервирования, и клетки криоконсервируют в морозилке с контролируемой скоростью и хранят в жидком азоте до использования в будущем. Используют криоконсервированные клетки от 4 различных доноров.
[684] Криоконсервированные Т-лимфоциты CD4+ и CD8+ оттаивают, промывают, а затем приводят в контакт с частицами лентивирусного вектора без предварительной активации клеток с помощью агента для активации Т-лимфоцитов, то есть, без инкубирования клеток вместе с анти-CD3/анти-CD28. Для трансдуцирования, приблизительно 1 × 106 оттаявших Т-лимфоцитов добавляют в индивидуальные лунки 96-луночного планшета. Частицы лентивирусного вектора, которые предварительно смешивают с поликатионным трансдукционным адъювантом (в это случае, 100 мкг/мл протамина сульфата), добавляют в лунки. Частицы лентивирусного вектора, содержащиеся в нуклеиновой кислоте, кодирующей трансгенное кодирование CAR анти-BCMA, и усеченную последовательность EGFR (EGFRt) для использования в качестве маркера трансдуцирования, отделяют от последовательности CAR с помощью саморасщепляющейся последовательности T2A. Конечный объем на одну лунку устанавливают при 100 мкл. Приготавливают пять различных композиций, содержащих генно-инженерные клетки, для экспрессирования CAR анти-BCMA, с использованием процедур, описанных выше.
[685] Шарики, конъюгированные с BMCA-Fc и анти-CD28 (обозначаются как шарики, конъюгированные с BCMA/анти-CD28), приготавливают, по существу, как описано в Примере 1. Непосредственно после трансдуцирования, приблизительно 50 мкл клеток, генерируемых от каждого донора, добавляют к 500 мкл среды, содержащей шарики, конъюгированные с BCMA/анти-CD28, или шарики, конъюгированные с анти-CD3/анти-CD28, при отношении шариков к клеткам 1:1 и инкубируют 12 дней.
[686] Клетки считают через день, и окрашивают на экспрессирование EGFRt (суррогатный маркер для экспрессирования CAR) с использованием антитела анти-EGFR в дни 3, 7, 10 и 12 после трансфицирования. Данные показывают, что композиции Т-лимфоцитов, инкубируемые в течение до 12 дней в присутствии шариков, конъюгированных с анти-CD3/анти-CD28, наращиваются в культуре при размножении в пределах между приблизительно 95-кратным и 140-кратным размножением, происходящим в день 12 культивирования. Размножение контрольных имитационных Т-лимфоцитов, которые не трансдуцируются, но инкубируются вместе с шариками, конъюгированными с анти-CD3/анти-CD28, также демонстрируют примерно 65-кратное размножение в день 12 по сравнению с началом инкубирования, кратность размножения композиций Т-лимфоцитов, которые инкубируют вместе с шариками BCMA/анти-CD28, непосредственно после трансдуцирования составляет примерно от 1,0-кратной до 7,0-кратной в день 12.
[687] Как показано на Фиг. 11, композиции Т-лимфоцитов, которые инкубируются в присутствии анти-CD3/анти-CD28, демонстрируют высокое экспрессирование маркера трансдуцирования EGFRt, даже без активации клеток перед трансдуцированием с помощью вирусных частиц. Этот результат согласуется с непосредственной стимуляцией, которая ассоциируется с поверхностным экспрессированием CAR. Т-лимфоциты, стимулируемые шариками BCMA/анти-CD28, демонстрируют более медленную кинетику достижения такого же процента клеток положительных относительно EGFRt, хотя в день 12 в пределах примерно 60% и 90% клеток являются положительными относительно EGFRt. Результаты показывают, что несмотря на более медленное размножение клеток после инкубирования вместе с шариками BCMA/анти-CD28 по сравнению с шариками анти-CD3/анти-CD28, Т-лимфоциты CAR+ могут обогащаться в течение 12 дней культивирования, указывая на то, что шарики BCMA/анти-CD28 способствуют росту Т-лимфоцитов CAR+.
[688] Т-лимфоциты, инкубируемые при условиях, описанных выше, без активации клеток перед трансдуцированием с помощью частиц лентивирусных векторов, также окрашиваются в день 12 на поверхностное экспрессирование CD4 и CD8 и анализируются с помощью проточной цитометрии. В качестве контроля, композиция Т-лимфоцитов, генерируемая из клеток донора, также при отношении клеток CD4+ и CD8+ 1:1, активируется перед трансдуцированием посредством стимуляции шариками анти-CD3/анти-CD28 в течение 24 часов до приведения в контакт активированных клеток с частицами лентивирусного вектора, экспрессирующими CAR анти-BCMA, как описано выше; при таких условиях клетки дополнительно инкубируются в течение 12 дней, но в отсутствие каких-либо конъюгированных шариков.
[689] Таблица E2 приводит результаты для клеток от того же донора, инкубируемых при указанных выше условиях. Как показано, инкубирование клеток вместе с шариками, конъюгированными с анти-CD3/анти-CD28, или с шариками, конъюгированными с BCMA/анти-CD28, без активации клеток перед трансдуцированием, изменяет отношение Т-лимфоцитов CD4/CD8 по сравнению с клетками, которые сначала активируются 24 часа в присутствии шариков, конъюгированных с анти-CD3/анти-CD28, перед трансдуцированием. Кроме того, эти результаты показывают, что инкубирование вместе с шариками, конъюгированными с BCMA/антителом анти-CD28, или с шариками, конъюгированными с антителом анти-CD3/анти-CD28, без предварительной активации Т-лимфоцитов, дает в результате сходные уровни экспрессирования CAR и фенотипы клеток CD4/CD8. Как показано в Таблице E3, сходное обращение отношения Т-лимфоцитов CD4/CD8 наблюдают у Т-лимфоцитов, полученных от 4 различных доноров, когда они инкубируются с шариками анти-CD3/анти-CD28, без активации клеток перед трансдуцированием, по сравнению с клетками, которые сначала активируются в течение 24 часов в присутствии шариков, конъюгированных с анти-CD3/анти-CD28, перед трансдуцированием.
Таблица E2: Процент клеток CD4+ и CD8+ в культурах Т-лимфоцитов, которые обрабатывают шариками, конъюгированными с антигеном и/или антителом.
Таблица E3: Процент клеток CD4+ и CD8+ в культурах Т-лимфоцитов, которые обрабатывают шариками, конъюгированными с антителом.
Пример 7: Генерирование шариков, конъюгированных с ROR1
[690] Подобный рецептору тирозинкиназы орфанный рецептор 1 (ROR1) конъюгируется с шариками посредством ковалентного связывания слитого полипептида ROR1-Fc, содержащего внеклеточный домен ROR1 человека, слитой на своем C-конце с Fc-областью IgG, на поверхности коммерчески доступных тозилактивированных магнитных шариков (ThermoFisher, Waltham MA). Шарики представляют собой суперпарамагнитные, непористые, монодисперсные, тозилактивированные шарики, которые ковалентно связывают первичные амино и сульфгидрильные группы. Конъюгирование осуществляют с использованием шариков, имеющих диаметр приблизительно 2,8 мкм (обозначают M-280) или 4,5 мкм (обозначают M-450).
[691] ROR1-Fc содержит фрагмент ROR1 человека и Fc IgG1 человека, соединенные линкером, следующим образом:
[692]
QETELSVSAELVPTSSWNISSELNKDSYLTLDEPMNNITTSLGQTAELHCKVSGNPPPTIRWFKNDAPVVQEPRRLSFRSTIYGSRLRIRNLDTTDTGYFQCVATNGKEVVSSTGVLFVKFGPPPTASPGYSDEYEEDGFCQPYRGIACARFIGNRTVYMESLHMQGEIENQITAAFTMIGTSSHLSDKCSQFAIPSLCHYAFPYCDETSSVPKPRDLCRDECEILENVLCQTEYIFARSNPMILMRLKLPNCEDLPQPESPEAANCIRIGIPMADPINKNHKCYNSTGVDYRGTVSVTKSGRQCQPWNSQYPHTHTFTALRFPELNGGHSYCRNPGNQKEAPWCFTLDENFKSDLCDIPACDSKDSKEKNKMEILYGGGGSPKSSDKTHTCPPCPAPEAEGAPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPSSIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 33).
[693] Различные концентрации слитого белка ROR1-Fc добавляют приблизительно к 1 мл тозилактивированных шариков (например, к 4×109 тозилактивированных шариков, имеющих диаметр 2,8 мкм). Ковалентное связывание осуществляют посредством инкубирования в течение ночи при 37°C в растворе фосфатного буфера (PBS), содержащего 0,1% сывороточный альбумин человека (HSA). Шарики промывают и повторно суспендируют в 1 мл PBS с 0,1% HSA. После конъюгирования, концентрацию шариков определяют с использованием Cellometer.
[694] Т-лимфоциты экспрессирующие CAR анти-ROR1, стимулируют посредством инкубирования вместе с шариками, конъюгированными с ROR1 Fc.
Пример 8 Генерирование шариков, конъюгированных с CD22
[695] CD22 конъюгируются с шариками посредством ковалентного связывания слитого полипептида CD22-Fc, содержащего внеклеточный домен CD22 человека, слитой на своем C-конце с Fc-областью IgG, на поверхности коммерчески доступных тозилактивированных магнитных шариков (ThermoFisher, Waltham MA). Шарики представляют собой суперпарамагнитные, непористые, монодисперсные, тозилактивированные шарики, которые ковалентно связывают первичные амино и сульфгидрильные группы. Конъюгирование осуществляют с использованием шариков, имеющих диаметр приблизительно 2,8 мкм (обозначаются M-280) или 4,5 мкм (обозначаются M-450).
[696] CD22-Fc содержит внеклеточный домен CD22 человека и Fc IgG1 человека, соединенные линкером, следующим образом:
DSSKWVFEHPETLYAWEGACVWIPCTYRALDGDLESFILFHNPEYNKNTSKFDGTRLYESTKDGKVPSEQKRVQFLGDKNKNCTLSIHPVHLNDSGQLGLRMESKTEKWMERIHLNVSERPFPPHIQLPPEIQESQEVTLTCLLNFSCYGYPIQLQWLLEGVPMRQAAVTSTSLTIKSVFTRSELKFSPQWSHHGKIVTCQLQDADGKFLSNDTVQLNVKHTPKLEIKVTPSDAIVREGDSVTMTCEVSSSNPEYTTVSWLKDGTSLKKQNTFTLNLREVTKDQSGKYCCQVSNDVGPGRSEEVFLQVQYAPEPSTVQILHSPAVEGSQVEFLCMSLANPLPTNYTWYHNGKEMQGRTEEKVHIPKILPWHAGTYSCVAENILGTGQRGPGAELDVQYPPKKVTTVIQNPMPIREGDTVTLSCNYNSSNPSVTRYEWKPHGAWEEPSLGVLKIQNVGWDNTTIACAACNSWCSWASPVALNVQYAPRDVRVRKIKPLSEIHSGNSVSLQCDFSSSHPKEVQFFWEKNGRLLGKESQLNFDSISPEDAGSYSCWVNNSIGQTASKAWTLEVLYAPRRLRVSMSPGDQVMEGKSATLTCESDANPPVSHYTWFDWNNQSLPYHSQKLRLEPVKVQHSGAYWCQGTNSVGKGRSPLSTLTVYYSPETIGRRGGGGSPKSSDKTHTCPPCPAPEAEGAPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPSSIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK (SEQ ID NO: 34).
[697] Различные концентрации слитого белка CD22-Fc добавляют приблизительно к 1 мл тозилактивированных шариков (например, к 4×109 тозилактивированных шариков, имеющих диаметр 2,8 мкм). Ковалентное связывание осуществляют посредством инкубирования в течение ночи при 37°C в растворе фосфатного буфера (PBS). Шарики промывают и повторно суспендируют в 1 мл PBS с 0,1% HSA. После конъюгирования, концентрацию шариков определяют с использованием Cellometer.
[698] Т-лимфоциты, экспрессирующие CAR анти-CD22, стимулируют посредством инкубирования вместе с шариками, конъюгированными с CD22-Fc.
Пример 9: Конъюгирование антиидиотипического антитела с шариками
[699] Одно из двух различных антител: антиидиотипическое антитело (ID) анти-CD19, scFv-специфичное антитело анти-ID, полученное из FMC63 (последовательности, приведены в Таблице E4), ковалентно связывается на поверхности коммерчески доступных тозилактивированных магнитных шариков (ThermoFisher, Waltham MA), которые представляют собой суперпарамагнитные, непористые, монодисперсные, тозилактивированные шарики. Шарики ковалентно связывают первичные амино и сульфгидрильные группы. Конъюгирование осуществляют с использованием шариков, имеющих диаметр приблизительно 2,8 мкм (обозначаются M-280) или 4,5 мкм (обозначаются M-450).
Таблица E4. Последовательности анти-ID B-1 и B-2
[700] 200 мкг антитела анти-ID добавляют приблизительно к 1 мл тозилактивированных шариков (например, приблизительно к 4×109 тозилактивированных шарики, имеющих диаметр 2,8 мкм, или примерно к 4×108 тозилактивированных шариков, имеющих диаметр 4,5 мкм) и осуществляют ковалентное связывание посредством инкубирования в течение ночи при 37°C в растворе фосфатного буфера (PBS), содержащем 0,1% сывороточного альбумина человека (HSA). Шарики промывают и повторно суспендируют в 1 мл PBS с 0,1% HSA. После конъюгирования, концентрацию шариков определяют с использованием Cellometer.
[701] Для оценки стабильности шариков, конъюгированных с анти-ID, шарики осаждают, супернатант удаляют и загружают его на 4-12% Bis-Tris гель для SDS-PAGE, и гель окрашивают Кумасси синим. В качестве контроля для белка в целом, конъюгированного на шариках, осажденные шарики кипятят в 4X LDS (литий- додецилсульфатном) буфере для образца примерно при 70°C в течение 20 минут, и приблизительно 12,5 мкл или 25 мкл кипяченого супернатанта также наносят на гель для SDS-PAGE и оценивают с помощью Кумасси синего. Приблизительно 2,5 мкг или 5,0 мкг антитела анти-ID, которое не конъюгировано с шариками (положительный контроль), или 5 мкл 0,1% HSA (отрицательный контроль) также оценивают с помощью SDS-PAGE и окрашивания Кумасси синим. Антитело анти-ID не детектируется в супернатанте от конъюгированных образцов, которые не кипятили, это указывает на то, что конъюгирование является стабильным, в то время как антитело анти-ID детектируют в супернатанте от конъюгированных образцов, которые кипятят.
Пример 10: Оценка стимуляции Т-лимфоцитов, культивируемых вместе с шариками, конъюгированными с антиидиотипическим антителом
[702] Шарики, конъюгированные с полученным из FMC63 scFv-специфичным анти-ID B-1, инкубируют вместе с Т-лимфоцитами. Очищенные от CD3 Т-лимфоциты выделяют с помощью иммунноаффинного обогащения из образцов от лейкафереза от здоровых доноров. Выделенные клетки трансдуцируют вирусным вектором, кодирующим CAR анти-CD19, содержащим scFv, полученный из FMC63. Конструкция вирусного вектора в дальнейшем кодирует усеченный EGFR (EGFRt), который служит в качестве суррогатного маркера для экспрессирования CAR; EGFRt-кодирующая область отделяется от последовательности CAR перескакивающей последовательностью T2A. После трансдуцирования, клетки наращивают в культуре и замораживают посредством криоконсервирования.
[703] Для исследований стимуляции Т-лимфоцитов, оттаявшие CAR-экспрессирующие клетки CD4+ или CD8+ по отдельности высевают приблизительно при 50000 клеток в целом на лунку. В некоторых случаях, культурная среда дополнительно дополняется цитокинами следующим образом: для клеток CD4+, приблизительно 1200 IU/мл рекомбинантного IL-7, 20 IU/мл рекомбинантного IL-15 и 100 IU/мл рекомбинантного IL-2; для клеток CD8+, приблизительно 200 IU/мл рекомбинантного IL-2 и 20 IU/мл рекомбинантного IL-15. Шарики, конъюгированные с анти-ID B-1, добавляют к клеткам при отношении клетки:шарики 1:1 или 1:5 и инкубируют до 14 дней с 50% заменой сред каждые 2-3 дня. В качестве положительного контроля, клетки культивируют вместе с магнитными шариками анти-CD3/анти-CD28 при отношении клетки:шарики 3:1 в присутствии или в отсутствие указанных цитокинов.
[704] В различные моменты времени культивирования, трансдуцированные клетки CD4+ или CD8+ (как детектируется с помощью анти-EGFR для экспрессирования суррогатного маркера) оценивают на размножение, экспрессирование PD-1 и жизнеспособность.
[705] Как показано на Фиг. 12A и 12B, размножение Т-лимфоцитов CD4+ и CD8+, соответственно, наблюдают, когда клетки культивируются вместе с шариками, конъюгированными с анти-ID, при отношении клетки:шарики либо 1:1, либо 1:5, в частности, в присутствии цитокинов. Степень размножения больше, чем тогда, когда клетки культивируют с контрольными вместе с магнитными шариками анти-CD3/анти-CD28.
[706] Поверхностное экспрессирование PD-1 в подмножестве клеток CD4+ оценивают с помощью проточной цитометрии в дни 3, 7, 10 и 14 культивирования. Как показано на Фиг. 13, экспрессирование PD-1 является высоким на клетках, культивируемых вместе с магнитными шариками анти-CD3/анти-CD28, однако, уровни PD-1 существенно ниже или не детектируются на клетках, которые культивируются вместе с шариками, конъюгированными с анти-ID.
[707] Как показано на Фиг. 14, процент жизнеспособности Т-лимфоцитов CD4+ и CD8+, культивируемых вместе с шариками, конъюгированными с анти-ID, или с контрольными шариками, конъюгированными с анти-CD3/анти-CD28, при отношении либо 1:1, либо 1:5, остается консистентно высоким в ходе периода культивирования, когда клетки дополнительно культивируются в присутствии цитокинов. При всех условиях, однако, жизнеспособность клеток уменьшается в отсутствие добавляемых цитокинов, при этом самые большие потери клеток жизнеспособности происходят в последние дни культивирования клеток.
Пример 11: Оценка продуцирования цитокинов Т-лимфоцитами, культивируемых вместе с шариками, конъюгированными с антиидиотипическим антителом
[708] Генно-инженерные Т-лимфоциты с CAR анти-CD19, имеющим scFv, полученный от FMC63, генерируют, по существу, как описано в Примере 10. Оттаявшие Т-лимфоциты CD8+ культивируют вместе с шариками, конъюгированными с анти-ID B-1, в течение 4 часов в присутствии ингибитора Гольджи. Внутриклеточные уровни цитокинов TNFα, IFNγ и IL-2 определяют с помощью проточной цитометрии либо в подмножестве Т-лимфоцитов CAR+ (как определено с помощью положительного поверхностного окрашивания анти-EGFR для суррогатного маркера), либо в подмножестве Т-лимфоцитов CAR- (как определено с помощью отрицательного поверхностного окрашивания анти-EGFR). Для сравнения, Т-лимфоциты CAR+ (EGFRt+) также культивируют вместе с CD19-экспрессирующими целевыми клетками (клетками K562, трансдуцированными для экспрессирования CD19, K562-CD19) при отношении эффекторы:Т-лимфоциты 1:2.
[709] Как показано на Фиг. 15A, внутриклеточные уровни цитокинов TNFα, IFNγ и IL2 индуцируются в Т-лимфоцитах CAR+ (EGFRt+), но не в Т-лимфоцитах CAR- (EGFRt-), когда клетки культивируют в присутствии шариков, конъюгированных с анти-ID B-1. В этом исследовании, степень стимуляции, наблюдаемая в присутствии шариков, конъюгированных с анти-ID, сходна со стимуляцией Т-лимфоцитов CAR+ с использованием антиген-экспрессирующих клеток K562-CD19, которые представляют собой альтернативный CAR-специфичный реагент стимуляции (Фиг. 15B). Эти результаты демонстрируют, что анти-ID, конъюгированные с шариками, являются агонистическими и специфично стимулируют Т-лимфоциты, экспрессирующие CAR, имеющий антигенсвязывающий домен, распознаваемый антителом анти-ID. Кроме того, реагент шариков обеспечивает лучший CAR-специфичный реагент стимуляции по сравнению с линиями клеток, которые требуют культивирования клеток и склонны к разбросу от партии к партии.
Пример 12 Оценка размножения после последовательной повторной стимуляции
[710] Способность клеток расти ex vivo после многократных стимуляций может представлять собой потенциальный суррогат для оценки способности Т-лимфоцитов CAR+ к персистентности (например, после начальной активации) и/или является показателем функционирования in vivo (Zhao et al. (2015) Cancer Cell, 28:415-28). Т-лимфоциты CAR+ генерируются, как описано выше, и оттаявшие CAR-экспрессирующие Т-лимфоциты CD4+ или CD8+ высеваются по отдельности при 50000 CAR+ клеток/лунка. Шарики, конъюгированные с анти-ID B-1, добавляют к клеткам при отношении клетки:шарики 1:1 или 1:5 в присутствии или в отсутствие цитокинов, как описано в Примере 10. В качестве контроля, магнитные шарики анти-CD3/анти-CD28 добавляют к клеткам при отношении клетки:шарики 3:1 в присутствии или в отсутствие цитокинов. Клетки харвестируют каждые 3-4 дня и считают, и повторно стимулируют новыми целевыми клетками, используя такие же условия культивирования после восстановления количества клеток до начальной плотности посева для каждого захода. Осуществляют в целом 4 захода стимуляции в ходе 14-дневного периода культивирования. Для каждого захода стимуляции, определяют количество удвоений.
[711] Как показано на Фиг. 16, непрерывное размножение CAR-экспрессирующих клеток CD4+ (EGFRt+) наблюдают после повторной стимуляции шариками, конъюгированными с анти-ID, хотя степень размножения больше, когда клетки культивируют в присутствии цитокинов. Также, степень размножения больше, чем, при культивировании клеток вместе с шариками анти-CD3/анти-CD28. Для Т-лимфоцитов CD8+, наблюдают сходную кинетику размножения, когда клетки культивируют в присутствии либо шариков, конъюгированных с анти-ID, либо шариков, конъюгированных с анти-CD3/анти-CD28, хотя размножение несколько больше, когда клетки культивируют вместе с шариками, конъюгированными анти-ID, в особенности, в отсутствие добавляемых рекомбинантных цитокинов.
Пример 13: Дальнейший анализ размножения CAR-специфичных клеток с использованием шариков, конъюгированных с антиидиотипическим антителом
[712] Осуществляют исследования, сходные с теми, что описаны в Примерах 11 и 12, за исключением использования CAR-экспрессирующих Т-лимфоцитов, генерируемых двумя различными пациентами донорами, Очищенные от CD3 Т-лимфоциты выделяют из мононуклеаров периферической крови (PBMC) от двух пациентов доноров, трансдуцируют вирусный вектор, кодирующий CAR анти-CD19, имеющий scFv, полученный от FMC63, наращивают их в культуре, замораживают и оттаивают.
[713] Оттаявшие CD4+, CD8+ или co-культуры CD4/CD8 (отношение 1:1) высевают в лунках 6-луночного планшета приблизительно при 5 × 106 клеток/лунка в целом в культурной среде, которую дополнительно дополняют цитокинами, следующим образом: для клеток CD4+ или сокультур CD4+/CD8+ среды дополняют приблизительно 1200 IU/мл рекомбинантного IL-7, 20 IU/мл рекомбинантного IL-15 и 100 IU/мл рекомбинантного IL-2; для клеток CD8+ среды дополняют 200 IU/мл рекомбинантного IL-2 и 20 IU/мл рекомбинантного IL-15. Шарики, конъюгированные с анти-ID B-1, добавляют в клеткам при отношении клетки:шарики 1:1 и инкубируют до 9 дней при 50% замене сред каждые 2-3 дня.
[714] В различные моменты времени культивирования, количество трансдуцированных клеток CD4+ или CD8+ (как детектируется с помощью анти-EGFR для экспрессирования суррогатного маркера EGFRt), присутствующих культуре, для каждых условий, оценивается, и определяется кратность размножения или частота CAR-экспрессирующих клеток как процент от клеток в целом. Также определяют экспрессирование PD-1 и CD25 и жизнеспособность клеток.
[715] Как показано на Фиг. 17A, более, чем 60-кратное размножение CAR-экспрессирующих Т-лимфоцитов CD4+ (EGFRt+) наблюдается, когда клетки CD4+ культивируются сами по себе вместе шариками, конъюгированными с анти-ID. Для Т-лимфоцитов CD8+, происходит значительно более высокое размножение CAR-экспрессирующих Т-лимфоцитов CD8+ (EGFRt+) в присутствии шариков, конъюгированных с анти-ID, когда Т-лимфоциты CD8+ со-культивируются с клетками CD4+. Как показано на Фиг. 17B, частота CAR-экспрессирующих CD4+ или CD8+ (EGFRt+) увеличивается в ходе 9 дней культивирования в присутствии шариков, конъюгированных с анти-ID, при >90% трансдуцированных клеток (EGFRt+), присутствующих в культуре в день 9. Жизнеспособность клеток CD4+ и CD8+ также остается близкой к 100% в ходе культивирования, при несколько большей жизнеспособности Т-лимфоцитов CD8+, наблюдаемой при сокультивировании вместе с Т-лимфоцитами CD4+ (Фиг. 17C). Наблюдают сходные результаты для обеих доноров. Эти результаты согласуются с обогащением Т-лимфоцитов CAR+ без предварительной селекции CAR посредством использования CAR-специфичных конъюгированных с антиидиотипическим антителом шариков.
[716] Поверхностное экспрессирование PD-1 и CD25 на трансдуцированных клетках CD4+ или CD8+ (EGFR+) оценивают с помощью проточной цитометрии в дни 5, 7 и 9 культивирования вместе с шариками, конъюгированными с анти-ID. Как показано на Фиг. 18A, экспрессирование PD-1 в Т-лимфоцитах, как CD4+, так и CD8+, существенно уменьшается со временем культивирования вместе с шариками, конъюгированными с анти-ID. Как показано на Фиг. 18B, экспрессирование CD25 также уменьшается после 9 дней культивирования в присутствии шариков, конъюгированных с анти-ID. Сходные результаты наблюдаются для обеих доноров.
Пример 14: Сравнение уровней цитокинов и фенотипа после культивирования вместе с шариками, конъюгированными с антиидиотипическим антителом
[717] Очищенные от CD3 Т-лимфоциты выделяют из мононуклеаров периферической крови (PBMC) двух пациентов доноров, трансдуцируют вирусным вектором, кодирующим CAR анти-CD19, имеющий scFv, полученный из FMC63, и наращивают в культуре вместе с шариками, покрытыми антителом анти-CD3 и анти-CD28. После размножения, наращенные Т-лимфоциты замораживают посредством криоконсервирования. Для исследований, замороженные Т-лимфоциты оттаивают и Т-лимфоциты CD4+ и CD8+, оцениваемые на внутриклеточные уровни цитокинов или поверхностный фенотип (d=0), или оттаявшие Т-лимфоциты CD4+, CD8+, или co-культивируемые CD4+/CD8+ культивируют в течение дополнительных 9 дней в присутствии шариков, конъюгированных с анти-ID B-1, перед оценкой внутриклеточных уровней цитокинов и фенотипа поверхностного маркера после стимуляции PMA/иономицином или клетками K562, трансдуцированными CD19 (d=9).
[718] Для оценки внутриклеточных уровней цитокинов, добавляют ингибитор Гольджи в течение 4 часов, а затем оценивают TNFα, IFNγ и IL-2 с помощью проточной цитометрии. Для всех условий, степень экспрессирования внутриклеточных цитокинов существенно выше, когда клетки стимулируются PMA/иономицином по сравнению с CAR-специфичной стимуляцией клетками K562, трансдуцированными CD19. Как показано на Фиг. 19A, уровни цитокинов TNFα и IL-2 сходны в клетках CD4+ или CD8+ непосредственно после оттаивания по сравнению с соответствующими клетками CD4+ или CD8+ или с сокультурами Т-лимфоцитов CD4/CD8, дополнительно культивируемыми в присутствии шариков, конъюгированных с анти-ID в течение 9 дней. Повышенные уровни IFNγ наблюдаются в оттаявших Т-лимфоцитах CD4+, CD8+ или со-культивируемых CD4/CD8, которые дополнительно культивируют в присутствии шариков, конъюгированных с анти-ID, в течение 9 дней по сравнению с уровнем IFNγ в Т-лимфоцитах CD4+ или CD8+ непосредственно после оттаивания. Эти результаты демонстрируют, что функция Т-лимфоцитов поддерживается по сравнению со свежеоттаявшими Т-лимфоцитами CAR+, после 9-дневного размножения вместе с шариками, конъюгированными с анти-ID. Получают сходные результаты в клетках от двух доноров.
[719] Поверхностное экспрессирование маркера активации CD25, поверхностное экспрессирование ингибиторных рецепторов PD-1 и LAG-3, и ядерное экспрессирование маркера пролиферации Ki-67 также оценивается в клетках CD4+ или CD8+ непосредственно после оттаивания (d=0) или в Т-лимфоцитах CD4+ или CD8+, наращенных сами по себе или как co-культура CD4/CD8, в течение дополнительных 9 дней в присутствии шариков, конъюгированных с анти-ID (d=9). Как показано на Фиг. 19B, уменьшение экспрессирования CD25, но не Ki-67, наблюдается в клетках, которые дополнительно культивируются в присутствии шариков, конъюгированных с анти-ID, в течение 9 дней по сравнению с Т-лимфоцитами непосредственно после оттаивания. Уменьшение экспрессирования CD25 существенно больше в клетках CD8+, чем в клетках CD4+. В дополнение к этому, уменьшение экспрессирования PD-1 и LAG-3 также наблюдается в клетках как CD4+, так и CD8+, культивируемых сами по себе или как co-культура CD4/CD8, после инкубирования в течение 9 дней вместе с шариками, конъюгированными с анти-ID, по сравнению с экспрессированием в клетках непосредственно после оттаивания. Этот результат демонстрирует, что после инкубирования вместе с шариками, конъюгированными с анти-ID, ранее замороженные трансдуцированные клетки сохраняют функциональные способности, как видно по высокому проценту клеток, которые являются положительными относительно маркера Ki-67, показателя клеточной пролиферации, но он также демонстрирует другое состояние активации, отличающееся низким поверхностным экспрессированием маркера активации CD25 и маркеров ингибиторных рецепторов PD-1 и LAG-3.
Пример 15: Воздействие стимуляции шариками, конъюгированными с анти-BCMA, или шариками, конъюгированными с анти-BCMA/PD-L1, на экспрессирование и/или передачу сигналов PD-1
[720] T-лимфоциты CAR анти-BCMA генерируют из образцов от репрезентативных здоровых доноров или из материала, полученного от пациента с множественной миеломой, и культивируют вместе с 50 мкг/мл шариков, конъюгированных с BCMA-Fc (генерируемых как описано в Примере 1) при отношении шарики:Т-лимфоциты CAR+ 1:1, в течение 7 дней, в присутствии 1 мкМ леналидомида или контрольной лекарственной среды. Экспрессирование CD25, PD-1, Tim3 и Lag3 на Т-лимфоцитах CAR (с использованием антитела для суррогатного маркера CAR) культивируемых при различных условиях, затем оценивают с помощью проточной цитометрии.
[721] Такие Т-лимфоциты CAR анти-BCMA, предварительно стимулированные шариками в присутствии или в отсутствие леналидомида, или свежеоттаявшие T-лимфоциты CAR анти-BCMA, генерируемые из сравнимых образцов от доноров, затем освобождают от шариков, промывают и культивируют вместе с целевыми клетками RPMI-8226 (мечеными с NucLight Red (NLR), чтобы сделать возможным их отслеживание с помощью микроскопии), в присутствии 1 мкМ леналидомида или контрольной лекарственной среды. Конкретно, предварительно обработанные клетки, в которых предварительная обработка осуществляется в присутствии леналидомида, эти клетки культивируются вместе с целевыми клетками в присутствии леналидомида; подобным же образом, для предварительно обработанных клеток, в которых предварительная обработка осуществляется в присутствии лекарственной среды, эти клетки культивируются вместе с целевыми клетками в присутствии лекарственной среды. После совместного культивирования, цитолитическую активность оценивают посредством измерения потерь жизнеспособных целевых клеток за период семь дней, как определяется по сигналу красной флуоресценции. Процент уничтожения нормируется на T-лимфоциты CAR анти-BCMA, предварительно стимулируемые на шариках в присутствии лекарственной среды. Продуцирование цитокинов оценивают с помощью ELISA супернатанта после культивирования вместе с целевыми клетками в течение 24 часов. Эксперименты осуществляют дважды на 3 донорах. Линейные модели фиксированного воздействия или смешанного воздействия используют для оценки значимости обработки леналидомидом для цитолитической активности и продуцирования цитокинов, при этом обработка, донор и время рассматриваются как фиксированные воздействия, а леченое животное рассматривается как случайное воздействие, вложенные с помощью времени, когда повторяющиеся измерения получают от одного и того же животного. Значения P получают с помощью тестов отношения вероятностей, сравнивая полную модель с представляющим интерес воздействием с моделью без воздействия, представляющего интерес.
[722] Фиг. 20A показывает результаты цитолитической активности специфичной к антигену CAR, и Фиг. 20B показывает результаты для продуцирования цитокинов T-лимфоцитами CAR анти-BCMA, которые предварительно стимулируются шариками BCMA (по сравнению со свежеоттаявшими (не стимулируемыми предварительно) T-лимфоцитами CAR анти-BCMA) в co-культурах, сравнивая клетки, культивируемые в присутствии и в отсутствие леналидомида. Предварительно стимулируемые Т-лимфоциты CAR показывают уменьшение цитолитической активности (P=2,1 × 10-4) и продуцирование цитокинов (P=0,03 для IFN-γ) по сравнению со свежеоттаявшими T-лимфоцитами CAR анти-BCMA.
[723] В отсутствие леналидомида при предварительной обработке и последующем co-культивировании, результаты для предварительно стимулируемых T-лимфоцитов CAR демонстрируют уменьшение уничтожения клеток и продуцирования цитокинов по сравнению со свежими T-лимфоцитами CAR, это показывает, что хроническая предварительная стимуляция приводит к функциональному ослаблению. Эти результаты согласуются с фенотипом подобным истощению, индуцируемому при предварительной стимуляции на BCMA-конъюгированных шариках. Присутствие леналидомида в ходе периода предварительной стимуляции сохраняет цитолитическую функцию (P=0,04), и имеется тренд к увеличению продуцирования цитокинов по сравнению с клетками, экспонируемыми для лекарственной среды в период предварительной стимуляции (Фиг. 24B). Присутствие леналидомида в этом анализе согласуется с тем наблюдением, что леналидомид может уменьшить долю фенотипов подобных функциональному истощению в предварительно стимулируемых T-лимфоцитах CAR.
[724] Как показано на Фиг. 20C, оценивается фенотип T-лимфоцитов CAR анти-BCMA, стимулируемых в течение 7 дней на шариках BCMA, и добавление леналидомида значительно увеличивает жизнеспособность материала CAR+ T-лимфоцитов CAR анти-BCMA для 3 здоровых доноров (P=0,04). Добавление леналидомида не изменяет общего отсчета клеток в целом для всех доноров в этот 7-дневный период, и не наблюдается значительных различий в проценте CAR+ между Т-лимфоцитами CAR, обрабатываемыми лекарственной средой и леналидомидом. Фиг. 20D показывает репрезентативные результаты проточного цитометрического анализа поверхностного экспрессирования CD25 и PD-1 (средняя интенсивность флуоресценции (MFI), для T-лимфоцитов CAR CD4+ или CD8+ анти-BCMA после стимуляции (предварительной обработки) шариками BCMA в течение 7 дней, в присутствии или в отсутствие 1 мкМ леналидомида). Как показано, результаты показывают, что леналидомид уменьшает экспрессирование PD-1 для T-лимфоцитов CAR BCMA, повышая при этом экспрессирование CD25 после пролонгированной стимуляции. Как показано на Фиг. 20E, проточный цитометрический анализ для трех доноров Т-лимфоцитов CAR показывает, что добавление леналидомида увеличивает поверхностное экспрессирование Tim3 в популяции CD8+ (P=4,0 × 10-4), со смешанными воздействиями на популяцию CAR+ CD4+. Среди всех доноров и в популяциях CAR+ как в CD4+, так и в CD8+, леналидомид повышает уровень CD25 (CD4+ и CD8+; P=2,2 × 10-16) и процент клеток положительных относительно экспрессирования Lag3 (CD8+, P < 0,03; CD4+, P=0,002). Заметим, что уменьшение процента клеток PD-1+ наблюдается также в популяции CD4+ (P=0,04), при этом 2 из 3 доноров показывают также уменьшение популяции CD8+.
[725] В другом исследовании шарики, конъюгированные с рекомбинантным BCMA человека, используются для стимуляции Т-лимфоцитов CAR при различных концентрациях для титрования амплитуды стимуляции, либо низкой (5 мкг/ мл), либо средней (50 мкг/ мл), либо высокой (200 мкг/ мл) стимуляции. При условиях средней стимуляции, измеряют продуцирование секретированных цитокинов через 24 часа после стимуляции, и наблюдают 200% увеличение концентраций IL-2 и TNF-α по сравнению с контрольной лекарственной средой, с донор-зависимыми увеличениями для IFN-γ (Фиг. 21A). Клетки стимулируют с помощью BCMA-конъюгированных шариков в течение 24 часов в присутствии 0,1 мкМ или 1,0 мкМ леналидомида или контрольной лекарственной среды. Ингибитор переноса белков добавляют в конечные часы инкубирования, и клетки окрашивают на внутриклеточный IL-2, IFN-γ и TNF-α.
[726] T-лимфоциты CAR анти-BCMA, активированные на шариках BCMA, показывают зависимые от уровня воздействия стимуляции на продуцирование цитокинов, при этом 5-мкг шарики BCMA вызывают ограниченное продуцирование цитокинов эффекторными Т-лимфоцитами CAR по сравнению с 50-мкг и 200-мкг шариками BCMA (Фиг. 21B). Леналидомид увеличивает процент внутриклеточного окрашивания IFN-γ+ и TNF-α+ при всех уровнях стимуляции для Т-лимфоцитов CAR, как для CD4+, так и для CD8+. Амплитуда стимуляции либо увеличивает, либо уменьшает уровень IL-2 в ответ на леналидомид, при этом леналидомид уменьшает процент Т-лимфоцитов CAR+ IL-2+ при 50-мкг и 200-мкг стимуляции, но увеличивает процент Т-лимфоцитов CAR+ IL-2+ при условиях 5-мкг стимуляции. В отсутствие стимуляции, леналидомид не оказывает воздействия на продуцирование цитокинов Т-лимфоцитами CAR, показывая, что усиление продуцирования цитокинов, обеспечиваемое леналидомидом, требует стимуляции.
[727] В другом исследовании, клетки культивируют в присутствии шариков BCMA, генерируемых, как описано в Примере 1, с дополнительным конъюгированием рекомбинантного PD-L1-Fc человека или без него. Полученные от здоровых доноров или пациентов Т-лимфоциты CAR стимулируются в присутствии BCMA-конъюгированных шариков или шариков, конъюгированных с BCMA/PD-L1, в течение 24 часов в присутствии 1 мкМ леналидомида. Продуцирование цитокинов измеряют в супернатанте. Результаты показаны на Фиг. 21C. Как показано на Фиг. 25C, оценка Т-лимфоцитов CAR, как от здоровых доноров, так и от доноров-пациентов, демонстрирует, что добавление рекомбинантного PD-L1 к рекомбинантным шарикам BCMA уменьшает уровни IFN-γ, IL-2 и TNF-α. Показано, что обработка леналидомидом потенциирует уровни секретируемых цитокинов, кроме тех, что от Т-лимфоцитов CAR, обрабатываемых лекарственной средой, в присутствии PD-L1. Результаты согласуются с тем выводом, что продуцирование цитокинов Т-лимфоцитами CAR анти-BCMA после инкубирования вместе с BCMA-конъюгированными шариками повышается под действием леналидомида в присутствии ингибирования медиируемого PD-L1.
Пример 16: Оценка продуцирования цитокинов T-лимфоцитами CAR анти-BCMA, стимулируемых с помощью BCMA-конъюгированных шариков
[728] T-лимфоциты CAR анти-BCMA генерируют в целом, как описано в Примере 2. T-лимфоциты CAR анти-BCMA приготавливаются при отношении Т-лимфоцитов CD4+ и CD8+ 1:1 и оттаиваются, и культивируются при 5,0 × 105 клеток на лунку в 96-луночном планшете. Шарики, конъюгированные с антителом анти-CD3/анти CD28, или BCMA-конъюгированные шарики диаметром 4,5 или 2,8 мкм (из композиции 5 мкг/мл, 50 мкг/мл или 200 мкг/мл BCMA-конъюгированных шариков, генерируемых как описано в Примере 1) добавляют к культурам при отношении T-лимфоцитов CAR анти-BCMA к шарикам 1:1. T-лимфоциты CAR анти-BCMA, культивируемые в отсутствие антитела анти-CD3/анти-CD28, или BCMA-конъюгированных шариков, служат в качестве контроля.
[729] После двадцати четырехчасового инкубирования, присутствие IFN-гамма, IL-2, TNF-альфа, IL-6, GM-CSF и IL-4 в супернатантах культур оценивают с использованием мультиплексного иммуноанализа цитокинов (Luminex®). Как показано на Фиг. 22A, инкубирование вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28, дает в результате повышение концентраций цитокинов, присутствующих в супернатанте, по сравнению с инкубированием вместе с BCMA-конъюгированными шариками. В этом анализе, амплитуда продуцирования цитокинов клетками, инкубируемыми вместе с BCMA-конъюгированными шариками, является доза-зависимой, коррелирует с увеличением концентраций BCMA (то есть, 5 мкг/мл, 50 мкг/мл или 200 мкг/мл) используемых для конъюгирования шариков. Этот результат согласуется с теми данными, что BCMA-направленная активация CAR могла бы контролироваться и титроваться посредством варьирования количества BCMA конъюгированного с шариками. Сравнение высвобождения цитокинов после инкубирования вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28 или с BCMA-конъюгированными шариками, доказывает различия в амплитуде и качестве продуцирования цитокинов, при этом более Th1-подобный профиль высвобождения цитокинов наблюдают после стимуляции с помощью BCMA-конъюгированных шариков.
[730] T-лимфоциты CAR анти-BCMA культивируются, как описано выше, и оцениваются на внутриклеточные уровни цитокинов с помощью проточной цитометрии. T-лимфоциты CAR анти-BCMA инкубируют вместе с шариками, конъюгированными с антителом анти-CD3/анти-CD28, или BCMA-конъюгированными шариками при отношении T-лимфоцитов CAR анти-BCMA к шарикам 1:1 в течение двадцати часов с последующим четыре-часовым инкубированием вместе с ингибитором переноса белков. Клетки окрашивают на жизнеспособность, экспрессирование CAR, CD4 и CD8, затем фиксируют, пермеализируют и окрашивают на внутриклеточные уровни IFN-гамма, IL-2 и TNF-альфа. Как показано на Фиг. 22B, стимуляция с помощью BCMA-конъюгированных шариков дает в результате продуцирование цитокинов в CAR-экспрессирующих клетках анти-BCMA, как CD4+, так и CD8+. Подобно тому, что изложено выше, амплитуда внутриклеточных уровней цитокинов, видимо, коррелирует с количеством BCMA, конъюгированного с шариками.
Пример 17: Генерирование шариков, конъюгированных с антителом анти-CD19, анти-ID и антителом анти-CD2
[731] Генерируются шарики, покрытые антителом анти-CD2 и антителом анти-CD19, анти-ID. Антитело анти-CD2 мыши (clone RPA-2,10, ED biosciences) и антиидиотипическое антитело анти-ID B-2, описанное в Примере 9, ковалентно связываются с поверхностью коммерчески доступных тозилактивированных суперпарамагнитных шариков, имеющих диаметр приблизительно 4,5 мкм (обозначается M-450; ThermoFisher, Waltham MA).
[732] Приблизительно 6,67×10-10 моль каждого антитела добавляют на 1 мл тозилактивированных шарики (например, приблизительно 4×108 шариков/мл) и осуществляют ковалентное связывание посредством инкубирования в течение ночи при 37°C в растворе фосфатного буфера (PBS), содержащем 0,1% сывороточного альбумина человека (HSA). Шарики промывают и повторно суспендируют в 1 мл PBS с 0,1% HSA. После конъюгирования, концентрацию шариков определяют с использованием Cellometer. На основе концентрации связывания и отсчета шариков, приблизительное количество молекул на шариках составляет 1,58×106 молекул антитела на шарик. Шарики, покрытые антителом, суспендируют в растворе при концентрации 4,1×108 шариков/мл.
[733] Стабильность шариков, конъюгированных с антителом, оценивают посредством осаждения антитело-конъюгированных шариков, нанесения полученного в результате супернатанта на 4-12% гель Bis-Tris и окрашивания геля Кумасси синим на белок. В качестве контроля для белка в целом, конъюгированного на шариках, 10-мкл образец супернатанта с осажденных шариков, который кипятят в буфере LDS для образца, также оценивают. Контроль также включает оценку 1 мкг антитела анти-CD2, 1 мкг антитела анти-ID B-2, которое не конъюгировано с шариками (положительный контроль), и 5 мкл 0,1% HSA (отрицательный контроль). Полосы, соответствующие антителам, детектируются в образце с супернатантом из кипяченого образца. Антитело анти-ID не детектируется в супернатанте с конъюгированных образцов, которые не кипятили, это согласуется со стабильным конъюгированием.
Пример 18: Генерирование шариков, конъюгированных с антителом анти-ID анти-CD19 и антителом анти-CD28
[734] Генерируются шарики, покрытые антителом анти-CD28 и антителом анти-ID анти-CD19. Антитело анти-CD28 мыши (очищенный клон CD28.2 (Biolegend) низкий уровень эндотоксина, не содержит азида (LEAF)) и антиидиотипическое антитело анти-ID B-2, описанное в Примере 9, ковалентно связывается на поверхности коммерчески доступного тозилактивированного суперпарамагнитного шарика, имеющего диаметр приблизительно 4,5 мкм (обозначается M-450; ThermoFisher, Waltham MA). Приблизительно 6,67×10-10 моль каждого антитела добавляют на 1 мл тозилактивированных шариков, например, приблизительно 4×108 шариков/мл) и ковалентно связывают, по существу, как описано в Примере 17. На основе связывающейся концентрации и отсчета шариков, приблизительное количество молекул на шариках составляет 1,79×106 молекул антитела на шарик. Шарики, покрытые антителом, суспендируют в растворе при концентрации 3,2×108 шариков/мл как определено с помощью Cellometer.
Пример 19: Генерирование шариков, содержащих поверхностно конъюгированные антитело анти-ID анти-CD19, анти-CD2 и антитело анти-CD28
[735] Генерируют парамагнитные шарики, покрытые антителом анти-CD2 анти-CD28, и шарики, покрытые антителом анти-ID анти-CD19. Антитело мыши анти-CD2 (клон RPA-2.10, ED biosciences), анти-CD28 мыши (очищенный клон LEAF CD28.2, Biolegend) и антиидиотипическое антитело анти-ID B-2, описанное в Примере 9, ковалентно связываются с поверхностью коммерчески доступных тозилактивированных суперпарамагнитных шариков, имеющих диаметр приблизительно 4,5 мкм (обозначаются M-450; ThermoFisher, Waltham MA).
[736] Приблизительно 4,44×10-10 моль каждого антитела добавляют на 1 мл тозилактивированных шариков (например, приблизительно 4×108 шариков/мл) и ковалентно связывают, по существу, как описано в Примере 17. На основе концентрации связывания и отсчета шариков, приблизительное количество молекул на шариках составляет 1,56×106 молекул антитела на шарик. Шарики, покрытые антителом, суспендируют в растворе при концентрации 3,91×108 шариков/мл.
[737] Стабильность шариков, конъюгированных с антителом, оценивают посредством осаждения антитело-конъюгированных шариков, нанесения полученного в результате супернатанта на 4-12% гель Bis-Tris и окрашивания геля Кумасси синим на белок. В качестве контроля для белка в целом, конъюгированного на шариках, оценивают 10-мкл супернатанта с осажденных шариков, который кипятят в буфере LDS для образца. Дополнительные контроли, которые также оценивают, представляют собой 1 мкг антитела анти-CD2, 1 мкг антитела анти-ID B-2, которые не конъюгируются с шариками (положительный контроль), и 5 мкл 0,1% HSA (отрицательный контроль). Антитело анти-ID не детектируется в супернатанте от конъюгированных образцов, которые не кипятят, это указывает на то, что конъюгирование является стабильным, при этом полосы, соответствующие антителам, детектируют в загруженном супернатанте из кипяченого образца.
Пример 20: Анализ in vitro хронической стимуляции Т-лимфоцитов CAR+ с использованием шариков, конъюгированных с анти-ID
[738] Отдельные композиции клеток CD4+ и CD8+ выделяют у доноров людей, активируют и трансдуцируют вирусным вектором, кодирующим CAR анти-CD19, имеющим scFv, полученный из FMC63. Затем Т-лимфоциты CD4+ и CD8+ от каждого донора харвестируют отдельно, приготавливают и криоконсервируют. Криоконсервированные генно-инженерные Т-лимфоциты CD4+ и CD8+ оттаивают и приготавливают при отношении Т-лимфоцитов CD4+ и CD8+ 1:1 от одного и того же донора, генерируя композицию Т-лимфоцитов, содержащую Т-лимфоциты CAR+. Шарики, конъюгированные с анти-ID против CAR анти-CD19, инкубируют вместе с клетками при отношении шарики:клетки 1:1 в течение 14 дней.
[739] Вторичную реакцию T-лимфоцитов CAR, харвестированных в день 14 после CAR-специфичной стимуляции с помощью шариков, конъюгированных с анти-ID (день 14; вторичные), оценивают после стимуляции с помощью целевых клеток, экспрессирующих антиген K562-CD19, при отношении эффекторных клеток к целевым 1:1 (для оценки уровней цитокинов) или (3:1 для оценки цитолитической активности). Первичная реакция Т-лимфоцитов из композиции Т-лимфоцитов, которые не инкубируются вместе с шариками, конъюгированными с анти-ID, также определяется посредством сходной стимуляции с помощью антиген-экспрессирующих клеток (день 0; “первичные”). Для оценки цитолитической активности, целевые клетки метят NucLight Red (NLR), чтобы сделать возможным отслеживание с помощью флуоресцентной микроскопии. Активность уничтожения оценивается посредством измерения потерь жизнеспособных целевых клеток в течение 72 часов, как определяется по потерям флуоресцентного сигнала со временем с помощью кинетической флуоресцентной микроскопии (используя INCUCYTE® Live Cell Analysis System, Essen Bioscience). Показатель уничтожения определяют, как обратную величину площади под кривой (AUC) для целевой флуоресценции со временем. Внутриклеточные уровни цитокинов IL-2 и TNF-альфа также оценивают с помощью проточной цитометрии в со-культивируемых Т-лимфоцитов после инкубирования в присутствии ингибитора Гольджи.
[740] Как показано на Фиг. 23A, уничтожение целевых клеток посредством композиции Т-лимфоцитов, содержащей Т-лимфоциты CAR+, собранные после CAR-специфичной стимуляции в течение 14 дней вместе с шариками, конъюгированными с анти-ID, уменьшается по сравнению с цитолитической активностью Т-лимфоцитов CAR+, которые не подвергаются предварительной CAR-специфичной стимуляции. Внутриклеточные уровни цитокинов IL-2 и TNF-альфа также уменьшаются в Т-лимфоцитах CAR+, которые принимают долговременную CAR-специфичную стимуляцию с помощью шариков, конъюгированных с анти-ID (Фиг. 23B). Эти результаты согласуются с тем наблюдением, что долговременная CAR-специфичная стимуляция, например, посредством инкубирования с помощью шариков, конъюгированных с анти-ID, в течение 14 дней, приводит к хронической стимуляции CAR и к потерям поддерживаемой функции.
[741] Анализ хронической стимуляции, описанной выше, используется для оценки воздействия различных соединений на улучшение функции Т-лимфоцитов CAR+ после долговременной стимуляции. Композиции Т-лимфоцитов CAR+ анти-CD19, генерируются, как описано выше, за исключением присутствия другого соединения или контрольной лекарственной среды. Клетки из каждой генерируемой композиции T-лимфоцитов CAR инкубируются вместе с парамагнитными шариками, конъюгированными с анти-ID, при отношении шариков к клеткам 1:1 в течение 14 дней.
[742] Первичная реакция композиций T-лимфоцитов CAR при оттаивании (без стимуляции с помощью шариков, конъюгированных с анти-ID), или вторичная реакция композиций, CAR-стимулированных Т-лимфоцитов CAR (после 14 дней CAR-специфичной стимуляции с помощью шариков, конъюгированных с анти-ID) оценивается после стимуляции с помощью антиген-экспрессирующих клеток. Композиции T-лимфоцитов CAR культивируют при отношении 1:1 вместе с антиген-экспрессирующими клетками K562-CD19 в присутствии ингибитора Гольджи, и продуцирование полифункциональных цитокинов оценивают с помощью проточной цитометрии после окрашивания внутриклеточных цитокинов на IL-2, IFN-гамма и TNF-альфа. Полифункциональную оценку определяют по кумулятивным уровням цитокинов, как определено в клетках CD8+ после нормировки данных посредством масштабирования в когортах доноров (Фиг. 24A). Определяют секретируемые цитокины IL-2, TNF и IFN-гамма в целом от супернатанта клеточной культуры от co-культур после 20 часов инкубирования вместе с целевыми клетками, и средние значения масштабированных оценок для всех трех цитокинов вычисляют, как показано на Фиг. 24B. Как показано на Фигурах 24A и 24B, определенные соединения дают в результате улучшенные первичные или вторичные реакции по отношению к способности композиций T-лимфоцитов CAR к продуцированию цитокинов. Улучшения первичной или вторичной цитолитической реакции, после co-культивирования вместе с целевыми клетками при отношении эффекторные клетки:целевые клетки 3:1, как описано выше, также наблюдается среди композиций Т-лимфоцитов, продуцируемых в присутствии определенных соединений (Фиг. 24C).
[743] Эти результаты демонстрируют полезность анализа хронической стимуляции для оценок композиций T-лимфоцитов CAR, включая различные композиции T-лимфоцитов CAR, продуцируемые при различных условиях или в присутствии соединений или других агентов, на их способность к демонстрации долговременного выживания и/или поддержания функции после хронической стимуляции T-лимфоцитов CAR, например, как может происходить после пролонгированного экспонирования для антигена in vivo.
Пример 21: Функциональная оценка Т-лимфоцитов, трансдуцированных химерным рецептором антигена (CAR) (Т-лимфоциты CAR), наращенных в присутствии низкомолекулярных соединений
[744] Композиции генно-инженерных Т-лимфоцитов, содержащие Т-лимфоциты, которые экспрессируют CAR анти-CD19, генерируются от трех отдельных доноров в присутствии различных соединений или контрольной лекарственной среды.
[745] Способность клеток из различных композиций Т-лимфоцитов расти после стимуляции CAR оценивают посредством инкубирования клеток генерируемых композиций T-лимфоцитов CAR анти-CD19 вместе с шариками, поверхностно конъюгированными с антиидиотипическим антителом специфичным к CAR анти-CD19. Шарики, конъюгированные с анти-ID, инкубируются вместе с клетками при отношении шарики:клетки 1:1 в лунках 24-луночных емкостей для размножения G-rex (Argos Technologies) в течение 15 дней. Количество живых Т-лимфоцитов на одну лунку в целом определяют посредством отсчета клеток в культурах каждые 5 дней (Фиг. 25A). Среднюю площадь под кривой (AUC) как функцию количества Т-лимфоцитов от времени вычисляют по отношению к AUC клеток, наращенных вместе только со средами (Фиг. 25B).
[746] Как показано на Фиг. 25A, стимуляция клеток с помощью шариков, конъюгированных с антиидиотипическим антителом, дает в результате начальное размножение, за которым следует уменьшение количества клеток. Т-лимфоциты из генерируемых композиций Т-лимфоцитов анти-CD19, которые ранее выращивались посредством инкубирования вместе с соединениями, имеют более высокую среднюю AUC по сравнению с Т-лимфоцитами, ранее наращенными вместе с контрольной лекарственной средой (Фиг. 25B). Результаты показывают, что присутствие анализа долговременной стимуляции можно использовать для идентификации соединений, которые, в некоторых случаях, улучшают способность генерируемых композиций Т-лимфоцитов к росту и выживанию после одной CAR-специфичной стимуляции.
[747] Оценивается вторичная реакция цитокинов после стимуляции с помощью антиген-экспрессирующих клеток на T-лимфоциты CAR из композиций Т-лимфоцитов, харвестированных в день 11 после размножения вместе с шариками, конъюгированными с анти-ID. Клетки, стимулируемые анти-ID, инкубируются вместе с облучаемыми целевыми клетками K562-CD19 при отношении эффекторные клетки:целевые клетки 1:1 в течение приблизительно 16 часов. Супернатант собирают, и измеряют продуцирование TNF-альфа, IFN-гамма и IL-2 цитокинов с использованием Luminex Multiplex Assay. Кратность изменения продуцирования цитокинов наблюдаемую в супернатантах co-культур, определяют для генерируемых композиций T-лимфоцитов CAR анти-CD19, выращиваемых в присутствии соединений или контрольной лекарственной среды, по сравнению с клетками, выращиваемыми в одних только в средах. Как показано на Фиг. 25C, этот анализ идентифицирует композиции Т-лимфоцитов, генерируемые из композиций Т-лимфоцитов CAR анти-CD19, которые предварительно наращивают в присутствии определенных соединений, которые демонстрируют улучшенное вторичное продуцирование цитокинов после последующей стимуляции с помощью антигена. В дополнение к этому, анализ идентифицирует композицию Т-лимфоцитов из некоторых клеток, полученных от доноров, которые, когда являются генно-инженерными и наращенными в присутствии соединения, демонстрируют увеличение частоты Т-лимфоцитов CD8+, которые представляют собой клетки CD107a+IFNγ+, в день 11, как определяется посредством внутриклеточного окрашивания цитокинов после инкубирования вместе с ингибитором Гольджи в течение 4 часов, по существу, как описано выше (Фиг. 25D). Эти результаты согласуются с использованием анализа долговременной стимуляции для идентификации воздействий соединений, используемых в процессе генной инженерии Т-лимфоцитов, для улучшения функции композиции генно-инженерных Т-лимфоцитов.
[748] Настоящее изобретение, как предполагается, не ограничивается рамками конкретных описанных вариантов осуществления, которые приведены, например, для иллюстрации различных аспектов настоящего изобретения. Различные модификации описанных композиций и способов станут очевидными из описания и его концепций. Такие варианты могут осуществляться без отклонения от истинных рамок и духа изобретения и, как предполагается, попадают в рамки настоящего изобретения.
Последовательности
(Xaa представляет собой любую аминокислоту; n равно либо 8, либо 12)
X3=T или S;
X5=T или S;
X6=D или R;
X8=Y или W;
X10=K или N
X4=D или M;
X6=N или H;
X8=N или S;
X9=N или D;
X10=G или S;
X11=G или E;
X13=D или R;
X14=Y или L;
X17=N или K;
X20=G или D
X2=R или S;
X3=E или I;
X4=G или Y;
X5=N или Y;
X6=N или E;
X7=Y или ноль;
X8=G или ноль;
X9=S или ноль;
X10=R или ноль;
X11=D или ноль;
X12=A или ноль;
X13=M или ноль;
X14=D или E;
X15=Y или A;
X1=S или R;
X3=S или R;
X4=S или G;
X5=G или N;
X6=V или I;
X7=I или H;
X8=N или ноль;
X10=M или L;
X11=Y или A
X1=P или L;
X2=W или L;
X3=I или V;
X5=L или N;
X6=T или A;
X7=S или K;
X8=N или T;
X11=S или D
X2=Q или H;
X3 =W или F;
X4=S или W;
X5=S или W;
X6=N или T;
X8=L или Y
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Juno Therapeutics, Inc.
HAUSKINS, Collin
HUSSELL, Scott
SIERRA, Catherine
W или KS, Melissa
<120> РЕАГЕНТЫ ДЛЯ РАЗМНОЖЕНИЯ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ РЕКОМБИНАНТНЫЕ РЕЦЕПТОРЫ
<130> 735042007340
<140> Еще не присвоено
<141> Одновременно с настоящим
<150> 62/538,671
<151> 2017-07-29
<150> 62/596,742
<151> 2017-12-08
<150> 62/628,889
<151> 2018-02-09
<150> 62/665,468
<151> 2018-05-01
<160> 154
<170> PatentIn version 3.5
<210> 1
<211> 54
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Met Leu Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser
1 5 10 15
Leu Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr
20 25 30
Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser
35 40 45
Val Lys Gly Thr Asn Ala
50
<210> 2
<211> 232
<212> БЕЛОК
<213> Homo sapiens
<400> 2
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
20 25 30
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
35 40 45
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
50 55 60
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
65 70 75 80
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
85 90 95
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
100 105 110
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
115 120 125
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
130 135 140
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
145 150 155 160
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
165 170 175
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
180 185 190
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
195 200 205
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
210 215 220
Ser Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 3
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> AviTag
<400> 3
Gly Leu Asn Asp Ile Phe Glu Ala Gln Lys Ile Glu Trp His Glu
1 5 10 15
<210> 4
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Кальмодулиновая метка
<400> 4
Lys Arg Arg Trp Lys Lys Asn Phe Ile Ala Val Ser Ala Ala Asn Arg
1 5 10 15
Phe Lys Lys Ile Ser Ser Ser Gly Ala Leu
20 25
<210> 5
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Полиглутаминовая метка
<400> 5
Glu Glu Glu Glu Glu Glu
1 5
<210> 6
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Flag-tag
<400> 6
Asp Tyr Lys Asp Asp Asp Asp Lys
1 5
<210> 7
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HA-tag
<400> 7
Tyr Pro Tyr Asp Val Pro Asp Tyr Ala
1 5
<210> 8
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Myc-tag
<400> 8
Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
1 5 10
<210> 9
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> STREP-TAG(r) I Стрептавидинсвязывающая пептидная последовательность
<400> 9
Trp Arg His Pro Gln Phe Gly Gly
1 5
<210> 10
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> STREP-TAG(r) II Стрептавидинсвязывающая пептидная последовательность
<400> 10
Trp Ser His Pro Gln Phe Glu Lys
1 5
<210> 11
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<220>
<221> вспомогательный признак
<222> (3)..(3)
<223> X выбирается из глутамина, аспарагина и метионина
<220>
<221> вспомогательный признак
<222> (4)..(4)
<223> X представляет собой аминокислоту
<400> 11
His Pro Xaa Xaa
1
<210> 12
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<400> 12
His Pro Gln Phe
1
<210> 13
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<220>
<221> вспомогательный признак
<222> (1)..(1)
<223> Xaa = is Trp, Lys или Arg
<220>
<221> вспомогательный признак
<222> (2)..(2)
<223> Xaa = любая аминокислота
<220>
<221> вспомогательный признак
<222> (7)..(7)
<223> Xaa = Gly или Glu
<220>
<221> вспомогательный признак
<222> (8)..(8)
<223> Xaa = Gly, Lys или Arg
<400> 13
Xaa Xaa His Pro Gln Phe Xaa Xaa
1 5
<210> 14
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<220>
<221> вспомогательный признак
<222> (2)..(2)
<223> Xaa представляет собой любую аминокислоту
<220>
<221> вспомогательный признак
<222> (7)..(7)
<223> Xaa is Gly или Glu
<220>
<221> вспомогательный признак
<222> (8)..(8)
<223> Xaa is Gly, Lys или Arg
<400> 14
Trp Xaa His Pro Gln Phe Xaa Xaa
1 5
<210> 15
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<220>
<221> вспомогательный признак
<222> (9)..(9)
<223> Xaa представляет собой любую амино
<220>
<221> ПОВТОР
<222> (9)..(9)
<223> n = 8 или 12
<400> 15
Trp Ser His Pro Gln Phe Glu Lys Xaa Trp Ser His Pro Gln Phe Glu
1 5 10 15
Lys
<210> 16
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<220>
<221> вспомогательный признак
<223> Стрептавидинсвязывающий пептид
<220>
<221> ПОВТОР
<222> (9)..(12)
<223> N = 2 или 3
<400> 16
Trp Ser His Pro Gln Phe Glu Lys Gly Gly Gly Ser Asn Trp Ser His
1 5 10 15
Pro Gln Phe Glu Lys
20
<210> 17
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<400> 17
Ser Ala Trp Ser His Pro Gln Phe Glu Lys Gly Gly Gly Ser Gly Gly
1 5 10 15
Gly Ser Gly Gly Gly Ser Trp Ser His Pro Gln Phe Glu Lys
20 25 30
<210> 18
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<400> 18
Ser Ala Trp Ser His Pro Gln Phe Glu Lys Gly Gly Gly Ser Gly Gly
1 5 10 15
Gly Ser Gly Gly Ser Ala Trp Ser His Pro Gln Phe Glu Lys
20 25 30
<210> 19
<211> 28
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<400> 19
Trp Ser His Pro Gln Phe Glu Lys Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Ser Trp Ser His Pro Gln Phe Glu Lys
20 25
<210> 20
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<400> 20
Trp Ser His Pro Gln Phe Glu Lys Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Trp Ser His Pro Gln Phe Glu Lys
20
<210> 21
<211> 28
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Стрептавидинсвязывающий пептид
<400> 21
Trp Ser His Pro Gln Phe Glu Lys Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Gly Gly Ser Ala Trp Ser His Pro Gln Phe Glu Lys
20 25
<210> 22
<211> 159
<212> БЕЛОК
<213> Streptomyces avidinii
<220>
<221> вспомогательный признак
<223> Последовательность стрептавидина дикого типа
(Стрептавидин: виды: Streptomyces avidinii - UniProt No.
P22629
<400> 22
Asp Pro Ser Lys Asp Ser Lys Ala Gln Val Ser Ala Ala Glu Ala Gly
1 5 10 15
Ile Thr Gly Thr Trp Tyr Asn Gln Leu Gly Ser Thr Phe Ile Val Thr
20 25 30
Ala Gly Ala Asp Gly Ala Leu Thr Gly Thr Tyr Glu Ser Ala Val Gly
35 40 45
Asn Ala Glu Ser Arg Tyr Val Leu Thr Gly Arg Tyr Asp Ser Ala Pro
50 55 60
Ala Thr Asp Gly Ser Gly Thr Ala Leu Gly Trp Thr Val Ala Trp Lys
65 70 75 80
Asn Asn Tyr Arg Asn Ala His Ser Ala Thr Thr Trp Ser Gly Gln Tyr
85 90 95
Val Gly Gly Ala Glu Ala Arg Ile Asn Thr Gln Trp Leu Leu Thr Ser
100 105 110
Gly Thr Thr Glu Ala Asn Ala Trp Lys Ser Thr Leu Val Gly His Asp
115 120 125
Thr Phe Thr Lys Val Lys Pro Ser Ala Ala Ser Ile Asp Ala Ala Lys
130 135 140
Lys Ala Gly Val Asn Asn Gly Asn Pro Leu Asp Ala Val Gln Gln
145 150 155
<210> 23
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> мутеин стрептавидина, обозначаемый Strep-tactin(r)
<400> 23
Glu Ala Gly Ile Thr Gly Thr Trp Tyr Asn Gln Leu Gly Ser Thr Phe
1 5 10 15
Ile Val Thr Ala Gly Ala Asp Gly Ala Leu Thr Gly Thr Tyr Val Thr
20 25 30
Ala Arg Gly Asn Ala Glu Ser Arg Tyr Val Leu Thr Gly Arg Tyr Asp
35 40 45
Ser Ala Pro Ala Thr Asp Gly Ser Gly Thr Ala Leu Gly Trp Thr Val
50 55 60
Ala Trp Lys Asn Asn Tyr Arg Asn Ala His Ser Ala Thr Thr Trp Ser
65 70 75 80
Gly Gln Tyr Val Gly Gly Ala Glu Ala Arg Ile Asn Thr Gln Trp Leu
85 90 95
Leu Thr Ser Gly Thr Thr Glu Ala Asn Ala Trp Lys Ser Thr Leu Val
100 105 110
Gly His Asp Thr Phe Thr Lys Val Lys Pro Ser Ala Ala Ser
115 120 125
<210> 24
<211> 340
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Транспозаза Sleeping Beauty
<400> 24
Met Gly Lys Ser Lys Glu Ile Ser Gln Asp Leu Arg Lys Lys Ile Val
1 5 10 15
Asp Leu His Lys Ser Gly Ser Ser Leu Gly Ala Ile Ser Lys Arg Leu
20 25 30
Lys Val Pro Arg Ser Ser Val Gln Thr Ile Val Arg Lys Tyr Lys His
35 40 45
His Gly Thr Thr Gln Pro Ser Tyr Arg Ser Gly Arg Arg Arg Val Leu
50 55 60
Ser Pro Arg Asp Glu Arg Thr Leu Val Arg Lys Val Gln Ile Asn Pro
65 70 75 80
Arg Thr Thr Ala Lys Asp Leu Val Lys Met Leu Glu Glu Thr Gly Thr
85 90 95
Lys Val Ser Ile Ser Thr Val Lys Arg Val Leu Tyr Arg His Asn Leu
100 105 110
Lys Gly Arg Ser Ala Arg Lys Lys Pro Leu Leu Gln Asn Arg His Lys
115 120 125
Lys Ala Arg Leu Arg Phe Ala Thr Ala His Gly Asp Lys Asp Arg Thr
130 135 140
Phe Trp Arg Asn Val Leu Trp Ser Asp Glu Thr Lys Ile Glu Leu Phe
145 150 155 160
Gly His Asn Asp His Arg Tyr Val Trp Arg Lys Lys Gly Glu Ala Cys
165 170 175
Lys Pro Lys Asn Thr Ile Pro Thr Val Lys His Gly Gly Gly Ser Ile
180 185 190
Met Leu Trp Cys Gly Phe Ala Ala Gly Gly Thr Gly Ala Leu His Lys
195 200 205
Ile Asp Gly Ile Met Arg Lys Glu Asn Tyr Val Asp Ile Leu Lys Gln
210 215 220
His Leu Lys Thr Ser Val Arg Lys Leu Lys Leu Gly Arg Lys Trp Val
225 230 235 240
Phe Gln Met Asp Asn Asp Pro Lys His Thr Ser Lys Val Val Ala Lys
245 250 255
Trp Leu Lys Asp Asn Lys Val Lys Val Leu Glu Trp Pro Ser Gln Ser
260 265 270
Pro Asp Leu Asn Pro Ile Glu Asn Leu Trp Ala Glu Leu Lys Lys Arg
275 280 285
Val Arg Ala Arg Arg Pro Thr Asn Leu Thr Gln Leu His Gln Leu Cys
290 295 300
Gln Glu Glu Trp Ala Lys Ile His Pro Thr Tyr Cys Gly Lys Leu Val
305 310 315 320
Glu Gly Tyr Pro Lys Arg Leu Thr Gln Val Lys Gln Phe Lys Gly Asn
325 330 335
Ala Thr Lys Tyr
340
<210> 25
<211> 1083
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Транспозаза Sleeping Beauty
<400> 25
atgggaaaat caaaagaaat cagccaagac ctcagaaaaa aaattgtaga cctccacaag 60
tctggttcat ccttgggagc aatttccaaa cgcctgaaag taccacgttc atctgtacaa 120
tctggttcat ccttgggagc aatttccaaa cgcctgaaag taccacgttc atctgtacaa 180
acaatagtac gcaagtataa acaccatggg accacgcagc cgtcataccg ctcaggaagg 240
agacgcgttc tgtctcctag agatgaacgt actttggtgc gaaaagtgca aatcaatccc 300
agaacaacag caaaggacct tgtgaagatg ctggaggaaa caggtacaaa agtatctata 360
tccacagtaa aacgagtcct atatcgacat aacctgaaag gccgctcagc aaggaagaag 420
ccactgctcc aaaaccgaca taagaaagcc agactacggt ttgcaactgc acatggggac 480
aaagatcgta ctttttggag aaatgtcctc tggtctgatg aaacaaaaat agaactgttt 540
ggccataatg accatcgtta tgtttggagg aagaaggggg aggcttgcaa gccgaagaac 600
accatcccaa ccgtgaagca cgggggtggc agcatcatgt tgtgggggtg ctttgctgca 660
ggagggactg gtgcacttca caaaatagat ggcatcatga ggaaggaaaa ttatgtggat 720
atattgaagc aacatctcaa gacatgagtc aggaagttaa agcttggtcg caaatgggtc 780
ttccaaatgg acaatgaccc caagcatact tccaaagttg tggcaaaatg gcttaaggac 840
aacaaagtca aggtattgga gtggccatca caaagccctg acctcaatcc tatagaaaat 900
ttgtgggcag aactgaaaaa gcgtgtgcga gcaaggaggc ctacaaacct gactcagtta 960
caccagctct gtcaggagga atgggccaaa attcacccaa cttattgtgg gaagcttgtg 1020
gaaggctacc cgaaacgttt gacccaagtt aaacaattta aaggcaatgc taccaaatac 1080
tag 1083
<210> 26
<211> 352
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность инвертированного повтора Sleeping Beauty
<400> 26
cagttgaagt cggaagttta catacactta agttggagtc attaaaactc gtttttcaac 60
tactccacaa atttcttgtt aacaaacaat agttttggca agtcagttag gacatctact 120
ttgtgcatga cacaagtcat ttttccaaca attgtttaca gacagattat ttcacttata 180
attcactgta tcacaattcc agtgggtcag aagtttacat acactaagtt gactgtgcct 240
ttaaacagct tggaaaattc cagaaaatga tgtcatggct ttagaagctt ctgatagact 300
aattgacatc atttgagtca attggaggtg tacctgtgga tgtatttcaa gg 352
<210> 27
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Линкерная последовательность
<400> 27
Gly Gly Gly Gly Ser
1 5
<210> 28
<211> 231
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Модифицированный Fc IgG1 человека
<400> 28
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
1 5 10 15
Glu Ala Glu Gly Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 29
<211> 668
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> вспомогательный признак
<223> Внеклеточный домен CD22 человека
<400> 29
Asp Ser Ser Lys Trp Val Phe Glu His Pro Glu Thr Leu Tyr Ala Trp
1 5 10 15
Glu Gly Ala Cys Val Trp Ile Pro Cys Thr Tyr Arg Ala Leu Asp Gly
20 25 30
Asp Leu Glu Ser Phe Ile Leu Phe His Asn Pro Glu Tyr Asn Lys Asn
35 40 45
Thr Ser Lys Phe Asp Gly Thr Arg Leu Tyr Glu Ser Thr Lys Asp Gly
50 55 60
Lys Val Pro Ser Glu Gln Lys Arg Val Gln Phe Leu Gly Asp Lys Asn
65 70 75 80
Lys Asn Cys Thr Leu Ser Ile His Pro Val His Leu Asn Asp Ser Gly
85 90 95
Gln Leu Gly Leu Arg Met Glu Ser Lys Thr Glu Lys Trp Met Glu Arg
100 105 110
Ile His Leu Asn Val Ser Glu Arg Pro Phe Pro Pro His Ile Gln Leu
115 120 125
Pro Pro Glu Ile Gln Glu Ser Gln Glu Val Thr Leu Thr Cys Leu Leu
130 135 140
Asn Phe Ser Cys Tyr Gly Tyr Pro Ile Gln Leu Gln Trp Leu Leu Glu
145 150 155 160
Gly Val Pro Met Arg Gln Ala Ala Val Thr Ser Thr Ser Leu Thr Ile
165 170 175
Lys Ser Val Phe Thr Arg Ser Glu Leu Lys Phe Ser Pro Gln Trp Ser
180 185 190
His His Gly Lys Ile Val Thr Cys Gln Leu Gln Asp Ala Asp Gly Lys
195 200 205
Phe Leu Ser Asn Asp Thr Val Gln Leu Asn Val Lys His Thr Pro Lys
210 215 220
Leu Glu Ile Lys Val Thr Pro Ser Asp Ala Ile Val Arg Glu Gly Asp
225 230 235 240
Ser Val Thr Met Thr Cys Glu Val Ser Ser Ser Asn Pro Glu Tyr Thr
245 250 255
Thr Val Ser Trp Leu Lys Asp Gly Thr Ser Leu Lys Lys Gln Asn Thr
260 265 270
Phe Thr Leu Asn Leu Arg Glu Val Thr Lys Asp Gln Ser Gly Lys Tyr
275 280 285
Cys Cys Gln Val Ser Asn Asp Val Gly Pro Gly Arg Ser Glu Glu Val
290 295 300
Phe Leu Gln Val Gln Tyr Ala Pro Glu Pro Ser Thr Val Gln Ile Leu
305 310 315 320
His Ser Pro Ala Val Glu Gly Ser Gln Val Glu Phe Leu Cys Met Ser
325 330 335
Leu Ala Asn Pro Leu Pro Thr Asn Tyr Thr Trp Tyr His Asn Gly Lys
340 345 350
Glu Met Gln Gly Arg Thr Glu Glu Lys Val His Ile Pro Lys Ile Leu
355 360 365
Pro Trp His Ala Gly Thr Tyr Ser Cys Val Ala Glu Asn Ile Leu Gly
370 375 380
Thr Gly Gln Arg Gly Pro Gly Ala Glu Leu Asp Val Gln Tyr Pro Pro
385 390 395 400
Lys Lys Val Thr Thr Val Ile Gln Asn Pro Met Pro Ile Arg Glu Gly
405 410 415
Asp Thr Val Thr Leu Ser Cys Asn Tyr Asn Ser Ser Asn Pro Ser Val
420 425 430
Thr Arg Tyr Glu Trp Lys Pro His Gly Ala Trp Glu Glu Pro Ser Leu
435 440 445
Gly Val Leu Lys Ile Gln Asn Val Gly Trp Asp Asn Thr Thr Ile Ala
450 455 460
Cys Ala Ala Cys Asn Ser Trp Cys Ser Trp Ala Ser Pro Val Ala Leu
465 470 475 480
Asn Val Gln Tyr Ala Pro Arg Asp Val Arg Val Arg Lys Ile Lys Pro
485 490 495
Leu Ser Glu Ile His Ser Gly Asn Ser Val Ser Leu Gln Cys Asp Phe
500 505 510
Ser Ser Ser His Pro Lys Glu Val Gln Phe Phe Trp Glu Lys Asn Gly
515 520 525
Arg Leu Leu Gly Lys Glu Ser Gln Leu Asn Phe Asp Ser Ile Ser Pro
530 535 540
Glu Asp Ala Gly Ser Tyr Ser Cys Trp Val Asn Asn Ser Ile Gly Gln
545 550 555 560
Thr Ala Ser Lys Ala Trp Thr Leu Glu Val Leu Tyr Ala Pro Arg Arg
565 570 575
Leu Arg Val Ser Met Ser Pro Gly Asp Gln Val Met Glu Gly Lys Ser
580 585 590
Ala Thr Leu Thr Cys Glu Ser Asp Ala Asn Pro Pro Val Ser His Tyr
595 600 605
Thr Trp Phe Asp Trp Asn Asn Gln Ser Leu Pro Tyr His Ser Gln Lys
610 615 620
Leu Arg Leu Glu Pro Val Lys Val Gln His Ser Gly Ala Tyr Trp Cys
625 630 635 640
Gln Gly Thr Asn Ser Val Gly Lys Gly Arg Ser Pro Leu Ser Thr Leu
645 650 655
Thr Val Tyr Tyr Ser Pro Glu Thr Ile Gly Arg Arg
660 665
<210> 30
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальный пептид CD33
<400> 30
Met Pro Leu Leu Leu Leu Leu Pro Leu Leu Trp Ala Gly Ala Leu Ala
1 5 10 15
<210> 31
<211> 377
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> вспомогательный признак
<223> Фрагмент R или 1 человека
<400> 31
Gln Glu Thr Glu Leu Ser Val Ser Ala Glu Leu Val Pro Thr Ser Ser
1 5 10 15
Trp Asn Ile Ser Ser Glu Leu Asn Lys Asp Ser Tyr Leu Thr Leu Asp
20 25 30
Glu Pro Met Asn Asn Ile Thr Thr Ser Leu Gly Gln Thr Ala Glu Leu
35 40 45
His Cys Lys Val Ser Gly Asn Pro Pro Pro Thr Ile Arg Trp Phe Lys
50 55 60
Asn Asp Ala Pro Val Val Gln Glu Pro Arg Arg Leu Ser Phe Arg Ser
65 70 75 80
Thr Ile Tyr Gly Ser Arg Leu Arg Ile Arg Asn Leu Asp Thr Thr Asp
85 90 95
Thr Gly Tyr Phe Gln Cys Val Ala Thr Asn Gly Lys Glu Val Val Ser
100 105 110
Ser Thr Gly Val Leu Phe Val Lys Phe Gly Pro Pro Pro Thr Ala Ser
115 120 125
Pro Gly Tyr Ser Asp Glu Tyr Glu Glu Asp Gly Phe Cys Gln Pro Tyr
130 135 140
Arg Gly Ile Ala Cys Ala Arg Phe Ile Gly Asn Arg Thr Val Tyr Met
145 150 155 160
Glu Ser Leu His Met Gln Gly Glu Ile Glu Asn Gln Ile Thr Ala Ala
165 170 175
Phe Thr Met Ile Gly Thr Ser Ser His Leu Ser Asp Lys Cys Ser Gln
180 185 190
Phe Ala Ile Pro Ser Leu Cys His Tyr Ala Phe Pro Tyr Cys Asp Glu
195 200 205
Thr Ser Ser Val Pro Lys Pro Arg Asp Leu Cys Arg Asp Glu Cys Glu
210 215 220
Ile Leu Glu Asn Val Leu Cys Gln Thr Glu Tyr Ile Phe Ala Arg Ser
225 230 235 240
Asn Pro Met Ile Leu Met Arg Leu Lys Leu Pro Asn Cys Glu Asp Leu
245 250 255
Pro Gln Pro Glu Ser Pro Glu Ala Ala Asn Cys Ile Arg Ile Gly Ile
260 265 270
Pro Met Ala Asp Pro Ile Asn Lys Asn His Lys Cys Tyr Asn Ser Thr
275 280 285
Gly Val Asp Tyr Arg Gly Thr Val Ser Val Thr Lys Ser Gly Arg Gln
290 295 300
Cys Gln Pro Trp Asn Ser Gln Tyr Pro His Thr His Thr Phe Thr Ala
305 310 315 320
Leu Arg Phe Pro Glu Leu Asn Gly Gly His Ser Tyr Cys Arg Asn Pro
325 330 335
Gly Asn Gln Lys Glu Ala Pro Trp Cys Phe Thr Leu Asp Glu Asn Phe
340 345 350
Lys Ser Asp Leu Cys Asp Ile Pro Ala Cys Asp Ser Lys Asp Ser Lys
355 360 365
Glu Lys Asn Lys Met Glu Ile Leu Tyr
370 375
<210> 32
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> F2A
<400> 32
Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala Gly Asp Val
1 5 10 15
Glu Ser Asn Pro Gly Pro
20
<210> 33
<211> 613
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Белок слияния R или 1-Fc
<400> 33
Gln Glu Thr Glu Leu Ser Val Ser Ala Glu Leu Val Pro Thr Ser Ser
1 5 10 15
Trp Asn Ile Ser Ser Glu Leu Asn Lys Asp Ser Tyr Leu Thr Leu Asp
20 25 30
Glu Pro Met Asn Asn Ile Thr Thr Ser Leu Gly Gln Thr Ala Glu Leu
35 40 45
His Cys Lys Val Ser Gly Asn Pro Pro Pro Thr Ile Arg Trp Phe Lys
50 55 60
Asn Asp Ala Pro Val Val Gln Glu Pro Arg Arg Leu Ser Phe Arg Ser
65 70 75 80
Thr Ile Tyr Gly Ser Arg Leu Arg Ile Arg Asn Leu Asp Thr Thr Asp
85 90 95
Thr Gly Tyr Phe Gln Cys Val Ala Thr Asn Gly Lys Glu Val Val Ser
100 105 110
Ser Thr Gly Val Leu Phe Val Lys Phe Gly Pro Pro Pro Thr Ala Ser
115 120 125
Pro Gly Tyr Ser Asp Glu Tyr Glu Glu Asp Gly Phe Cys Gln Pro Tyr
130 135 140
Arg Gly Ile Ala Cys Ala Arg Phe Ile Gly Asn Arg Thr Val Tyr Met
145 150 155 160
Glu Ser Leu His Met Gln Gly Glu Ile Glu Asn Gln Ile Thr Ala Ala
165 170 175
Phe Thr Met Ile Gly Thr Ser Ser His Leu Ser Asp Lys Cys Ser Gln
180 185 190
Phe Ala Ile Pro Ser Leu Cys His Tyr Ala Phe Pro Tyr Cys Asp Glu
195 200 205
Thr Ser Ser Val Pro Lys Pro Arg Asp Leu Cys Arg Asp Glu Cys Glu
210 215 220
Ile Leu Glu Asn Val Leu Cys Gln Thr Glu Tyr Ile Phe Ala Arg Ser
225 230 235 240
Asn Pro Met Ile Leu Met Arg Leu Lys Leu Pro Asn Cys Glu Asp Leu
245 250 255
Pro Gln Pro Glu Ser Pro Glu Ala Ala Asn Cys Ile Arg Ile Gly Ile
260 265 270
Pro Met Ala Asp Pro Ile Asn Lys Asn His Lys Cys Tyr Asn Ser Thr
275 280 285
Gly Val Asp Tyr Arg Gly Thr Val Ser Val Thr Lys Ser Gly Arg Gln
290 295 300
Cys Gln Pro Trp Asn Ser Gln Tyr Pro His Thr His Thr Phe Thr Ala
305 310 315 320
Leu Arg Phe Pro Glu Leu Asn Gly Gly His Ser Tyr Cys Arg Asn Pro
325 330 335
Gly Asn Gln Lys Glu Ala Pro Trp Cys Phe Thr Leu Asp Glu Asn Phe
340 345 350
Lys Ser Asp Leu Cys Asp Ile Pro Ala Cys Asp Ser Lys Asp Ser Lys
355 360 365
Glu Lys Asn Lys Met Glu Ile Leu Tyr Gly Gly Gly Gly Ser Pro Lys
370 375 380
Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
385 390 395 400
Glu Gly Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
405 410 415
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
420 425 430
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
435 440 445
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
450 455 460
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
465 470 475 480
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ser
485 490 495
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
500 505 510
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
515 520 525
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
530 535 540
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
545 550 555 560
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
565 570 575
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
580 585 590
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
595 600 605
Leu Ser Pro Gly Lys
610
<210> 34
<211> 904
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Полипептид слияния CD22-Fc
<400> 34
Asp Ser Ser Lys Trp Val Phe Glu His Pro Glu Thr Leu Tyr Ala Trp
1 5 10 15
Glu Gly Ala Cys Val Trp Ile Pro Cys Thr Tyr Arg Ala Leu Asp Gly
20 25 30
Asp Leu Glu Ser Phe Ile Leu Phe His Asn Pro Glu Tyr Asn Lys Asn
35 40 45
Thr Ser Lys Phe Asp Gly Thr Arg Leu Tyr Glu Ser Thr Lys Asp Gly
50 55 60
Lys Val Pro Ser Glu Gln Lys Arg Val Gln Phe Leu Gly Asp Lys Asn
65 70 75 80
Lys Asn Cys Thr Leu Ser Ile His Pro Val His Leu Asn Asp Ser Gly
85 90 95
Gln Leu Gly Leu Arg Met Glu Ser Lys Thr Glu Lys Trp Met Glu Arg
100 105 110
Ile His Leu Asn Val Ser Glu Arg Pro Phe Pro Pro His Ile Gln Leu
115 120 125
Pro Pro Glu Ile Gln Glu Ser Gln Glu Val Thr Leu Thr Cys Leu Leu
130 135 140
Asn Phe Ser Cys Tyr Gly Tyr Pro Ile Gln Leu Gln Trp Leu Leu Glu
145 150 155 160
Gly Val Pro Met Arg Gln Ala Ala Val Thr Ser Thr Ser Leu Thr Ile
165 170 175
Lys Ser Val Phe Thr Arg Ser Glu Leu Lys Phe Ser Pro Gln Trp Ser
180 185 190
His His Gly Lys Ile Val Thr Cys Gln Leu Gln Asp Ala Asp Gly Lys
195 200 205
Phe Leu Ser Asn Asp Thr Val Gln Leu Asn Val Lys His Thr Pro Lys
210 215 220
Leu Glu Ile Lys Val Thr Pro Ser Asp Ala Ile Val Arg Glu Gly Asp
225 230 235 240
Ser Val Thr Met Thr Cys Glu Val Ser Ser Ser Asn Pro Glu Tyr Thr
245 250 255
Thr Val Ser Trp Leu Lys Asp Gly Thr Ser Leu Lys Lys Gln Asn Thr
260 265 270
Phe Thr Leu Asn Leu Arg Glu Val Thr Lys Asp Gln Ser Gly Lys Tyr
275 280 285
Cys Cys Gln Val Ser Asn Asp Val Gly Pro Gly Arg Ser Glu Glu Val
290 295 300
Phe Leu Gln Val Gln Tyr Ala Pro Glu Pro Ser Thr Val Gln Ile Leu
305 310 315 320
His Ser Pro Ala Val Glu Gly Ser Gln Val Glu Phe Leu Cys Met Ser
325 330 335
Leu Ala Asn Pro Leu Pro Thr Asn Tyr Thr Trp Tyr His Asn Gly Lys
340 345 350
Glu Met Gln Gly Arg Thr Glu Glu Lys Val His Ile Pro Lys Ile Leu
355 360 365
Pro Trp His Ala Gly Thr Tyr Ser Cys Val Ala Glu Asn Ile Leu Gly
370 375 380
Thr Gly Gln Arg Gly Pro Gly Ala Glu Leu Asp Val Gln Tyr Pro Pro
385 390 395 400
Lys Lys Val Thr Thr Val Ile Gln Asn Pro Met Pro Ile Arg Glu Gly
405 410 415
Asp Thr Val Thr Leu Ser Cys Asn Tyr Asn Ser Ser Asn Pro Ser Val
420 425 430
Thr Arg Tyr Glu Trp Lys Pro His Gly Ala Trp Glu Glu Pro Ser Leu
435 440 445
Gly Val Leu Lys Ile Gln Asn Val Gly Trp Asp Asn Thr Thr Ile Ala
450 455 460
Cys Ala Ala Cys Asn Ser Trp Cys Ser Trp Ala Ser Pro Val Ala Leu
465 470 475 480
Asn Val Gln Tyr Ala Pro Arg Asp Val Arg Val Arg Lys Ile Lys Pro
485 490 495
Leu Ser Glu Ile His Ser Gly Asn Ser Val Ser Leu Gln Cys Asp Phe
500 505 510
Ser Ser Ser His Pro Lys Glu Val Gln Phe Phe Trp Glu Lys Asn Gly
515 520 525
Arg Leu Leu Gly Lys Glu Ser Gln Leu Asn Phe Asp Ser Ile Ser Pro
530 535 540
Glu Asp Ala Gly Ser Tyr Ser Cys Trp Val Asn Asn Ser Ile Gly Gln
545 550 555 560
Thr Ala Ser Lys Ala Trp Thr Leu Glu Val Leu Tyr Ala Pro Arg Arg
565 570 575
Leu Arg Val Ser Met Ser Pro Gly Asp Gln Val Met Glu Gly Lys Ser
580 585 590
Ala Thr Leu Thr Cys Glu Ser Asp Ala Asn Pro Pro Val Ser His Tyr
595 600 605
Thr Trp Phe Asp Trp Asn Asn Gln Ser Leu Pro Tyr His Ser Gln Lys
610 615 620
Leu Arg Leu Glu Pro Val Lys Val Gln His Ser Gly Ala Tyr Trp Cys
625 630 635 640
Gln Gly Thr Asn Ser Val Gly Lys Gly Arg Ser Pro Leu Ser Thr Leu
645 650 655
Thr Val Tyr Tyr Ser Pro Glu Thr Ile Gly Arg Arg Gly Gly Gly Gly
660 665 670
Ser Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
675 680 685
Pro Glu Ala Glu Gly Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
690 695 700
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
705 710 715 720
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
725 730 735
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
740 745 750
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
755 760 765
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
770 775 780
Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
785 790 795 800
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
805 810 815
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
820 825 830
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
835 840 845
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
850 855 860
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
865 870 875 880
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
885 890 895
Ser Leu Ser Leu Ser Pro Gly Lys
900
<210> 35
<211> 290
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Полипептид слияния BCMA-Fc
<400> 35
Met Leu Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser
1 5 10 15
Leu Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr
20 25 30
Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser
35 40 45
Val Lys Gly Thr Asn Ala Gly Gly Gly Gly Ser Pro Lys Ser Ser Asp
50 55 60
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Glu Gly Ala
65 70 75 80
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
85 90 95
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
100 105 110
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
115 120 125
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
130 135 140
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
145 150 155 160
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ser Ser Ile Glu
165 170 175
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
180 185 190
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
195 200 205
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
210 215 220
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
225 230 235 240
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
245 250 255
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
260 265 270
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
275 280 285
Gly Lys
290
<210> 36
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельная Тяжелая цепь SJ25C1
<400> 36
Glu Val Lys Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 37
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельная легкая цепь SJ25C1
<400> 37
Asp Ile Glu Leu Thr Gln Ser Pro Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Pro Leu Ile
35 40 45
Tyr Ser Ala Thr Tyr Arg Asn Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Lys Asp Leu Ala Asp Tyr Phe Cys Gln Gln Tyr Asn Arg Tyr Pro Tyr
85 90 95
Thr Ser Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 38
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельная Тяжелая цепь FMC63
<400> 38
Glu Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 39
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Вариабельная легкая цепь FMC63
<400> 39
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
100 105
<210> 40
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 SJ25C1
<400> 40
Ser Tyr Trp Met Asn
1 5
<210> 41
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 SJ25C1
<400> 41
Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe Lys
1 5 10 15
Gly
<210> 42
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 SJ25C1
<400> 42
Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr
1 5 10
<210> 43
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 SJ25C1
<400> 43
Lys Ala Ser Gln Asn Val Gly Thr Asn Val Ala
1 5 10
<210> 44
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 SJ25C1
<400> 44
Ser Ala Thr Tyr Arg Asn Ser
1 5
<210> 45
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR3 SJ25C1
<400> 45
Gln Gln Tyr Asn Arg Tyr Pro Tyr Thr
1 5
<210> 46
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 FMC63
<400> 46
Asp Tyr Gly Val Ser
1 5
<210> 47
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 FMC63
<400> 47
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 48
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 FMC63
<400> 48
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
1 5 10
<210> 49
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 FMC63
<400> 49
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
1 5 10
<210> 50
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 FMC63
<400> 50
His Thr Ser Arg Leu His Ser
1 5
<210> 51
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR3 FMC63
<400> 51
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 52
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH анти-ID
<400> 52
Gln Val Gln Leu Gln Gln Pro Gly Ser Glu Leu Val Arg Pro Gly Gly
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Asp Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asn Ile Tyr Pro Gly Ser Gly Gly Thr Asn Tyr Asp Glu Lys Phe
50 55 60
Lys Arg Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Glu Val Thr Thr Val Ala Tyr Tyr Tyr Ser Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 53
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 анти-ID
<400> 53
Glu Val Thr Thr Val Ala Tyr Tyr Tyr Ser Met Asp Tyr
1 5 10
<210> 54
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 анти-ID
<400> 54
Thr Arg Glu Val Thr Thr Val Ala Tyr Tyr Tyr Ser Met Asp
1 5 10
<210> 55
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID
<400> 55
Ser Tyr Trp Met His
1 5
<210> 56
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID
<400> 56
Asp Tyr Thr Phe Thr Ser Tyr
1 5
<210> 57
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID
<400> 57
Asp Tyr Thr Phe Thr Ser Tyr Trp Met His
1 5 10
<210> 58
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID
<400> 58
Thr Ser Tyr Trp Met His
1 5
<210> 59
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID
<400> 59
Asn Ile Tyr Pro Gly Ser Gly Gly Thr Asn Tyr Asp Glu Lys Phe Lys
1 5 10 15
Arg
<210> 60
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID
<400> 60
Tyr Pro Gly Ser Gly Gly
1 5
<210> 61
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID
<400> 61
Asn Ile Tyr Pro Gly Ser Gly Gly Thr Asn
1 5 10
<210> 62
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID
<400> 62
Trp Ile Gly Asn Ile Tyr Pro Gly Ser Gly Gly Thr Asn
1 5 10
<210> 63
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL анти-ID
<400> 63
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Lys Thr Val Pro Phe
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 64
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR3 анти-ID
<400> 64
Gln Gln Gly Lys Thr Val Pro Phe Thr
1 5
<210> 65
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR3 анти-ID
<400> 65
Gln Gln Gly Lys Thr Val Pro Phe
1 5
<210> 66
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 анти-ID
<400> 66
Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn
1 5 10
<210> 67
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 анти-ID
<400> 67
Ser Asn Tyr Leu Asn Trp Tyr
1 5
<210> 68
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 анти-ID
<400> 68
Tyr Thr Ser Arg Leu His Ser
1 5
<210> 69
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 анти-ID
<400> 69
Leu Leu Ile Tyr Tyr Thr Ser Arg Leu His
1 5 10
<210> 70
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Линкерная последовательность
<400> 70
Gly Gly Gly Ser
1
<210> 71
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Линкерная последовательность
<400> 71
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 72
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Линкер
<400> 72
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 73
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH анти-ID B-1
<400> 73
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Cys His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Asn Gly Gly Thr Asp Tyr Asn Gln Asn Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Asn Asn Tyr Gly Ser Arg Asp Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 74
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH анти-ID B-2
<400> 74
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Thr Ser Gly Tyr Ser Phe Thr Arg Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Asn Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ile Tyr Tyr Glu Glu Ala Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 75
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 анти-ID B-1
<400> 75
Glu Gly Asn Asn Tyr Gly Ser Arg Asp Ala Met Asp Tyr
1 5 10
<210> 76
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 анти-ID B-2
<400> 76
Ile Tyr Tyr Glu Glu Ala
1 5
<210> 77
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 анти-ID B-1
<400> 77
Ala Arg Glu Gly Asn Asn Tyr Gly Ser Arg Asp Ala Met Asp
1 5 10
<210> 78
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3 анти-ID B-2
<400> 78
Ala Ser Ile Tyr Tyr Glu Glu
1 5
<210> 79
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-1
<400> 79
Asp Tyr Tyr Met Lys
1 5
<210> 80
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-2
<400> 80
Arg Tyr Trp Met Asn
1 5
<210> 81
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-1
<400> 81
Gly Tyr Thr Phe Thr Asp Tyr
1 5
<210> 82
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-1
<400> 82
Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Lys
1 5 10
<210> 83
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-1
<400> 83
Thr Asp Tyr Tyr Met Lys
1 5
<210> 84
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-2
<400> 84
Gly Tyr Ser Phe Thr Arg Tyr
1 5
<210> 85
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-2
<400> 85
Gly Tyr Ser Phe Thr Arg Tyr Trp Met Asn
1 5 10
<210> 86
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR1 анти-ID B-2
<400> 86
Thr Arg Tyr Trp Met Asn
1 5
<210> 87
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-1
<400> 87
Asp Ile Asn Pro Asn Asn Gly Gly Thr Asp Tyr Asn Gln Asn Phe Lys
1 5 10 15
Gly
<210> 88
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-2
<400> 88
Met Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 89
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-1
<400> 89
Asn Pro Asn Asn Gly Gly
1 5
<210> 90
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-1
<400> 90
Asp Ile Asn Pro Asn Asn Gly Gly Thr Asp
1 5 10
<210> 91
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-1
<400> 91
Trp Ile Gly Asp Ile Asn Pro Asn Asn Gly Gly Thr Asp
1 5 10
<210> 92
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-2
<400> 92
His Pro Ser Asp Ser Glu
1 5
<210> 93
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-2
<400> 93
Met Ile His Pro Ser Asp Ser Glu Thr Arg
1 5 10
<210> 94
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR2 анти-ID B-2
<400> 94
Trp Ile Gly Met Ile His Pro Ser Asp Ser Glu Thr Arg
1 5 10
<210> 95
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Консенсусная HC-CDR1
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> X = T или S
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> X = T или S
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> X = D или R
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> X = Y или W
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> X = K или N
<400> 95
Gly Tyr Xaa Phe Xaa Xaa Tyr Xaa Met Xaa
1 5 10
<210> 96
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Консенсусная HC-CDR2
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> X = D или M
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> X = N или H
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> X = N или S
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> X = N или D
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> X = G или S
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> X = G или E
<220>
<221> ВАРИАНТ
<222> (13)..(13)
<223> X = D или R
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> X = Y или L
<220>
<221> ВАРИАНТ
<222> (17)..(17)
<223> X = N или K
<220>
<221> ВАРИАНТ
<222> (20)..(20)
<223> X = G или D
<400> 96
Trp Ile Gly Xaa Ile Xaa Pro Xaa Xaa Xaa Xaa Thr Xaa Xaa Asn Gln
1 5 10 15
Xaa Phe Lys Xaa
20
<210> 97
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Консенсусная HC-CDR3
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> X=R или S
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> X=E или I
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> X=G или Y
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> X=N или Y
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> X=N или E
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> X=Y или null
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> X=G или null
<220>
<221> ВАРИАНТ
<222> (9)..(9)
<223> X=S или null
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> X=R или null
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> X=D или null
<220>
<221> ВАРИАНТ
<222> (12)..(12)
<223> X=A или null
<220>
<221> ВАРИАНТ
<222> (13)..(13)
<223> X=M или null
<220>
<221> ВАРИАНТ
<222> (14)..(14)
<223> X=D или E
<220>
<221> ВАРИАНТ
<222> (15)..(15)
<223> X=Y или A
<400> 97
Ala Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
<210> 98
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL анти-ID B-1
<400> 98
Gln Ile Val Leu Thr Gln Ser Pro Ala Leu Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Gly Val Ile Tyr Met
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Arg Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Leu Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 99
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL анти-ID B-2
<400> 99
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Asp Ser Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Gly Ser Tyr Tyr Cys Gln His Phe Trp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 100
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> HC-CDR3
<400> 100
Gln Gln Trp Ser Ser Asn Pro Leu Thr
1 5
<210> 101
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR3 анти-ID B-1
<400> 101
Gln Gln Trp Ser Ser Asn Pro Leu
1 5
<210> 102
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> анти-ID B-2 LC-CDR3
<400> 102
Gln His Phe Trp Ser Thr Pro Tyr Thr
1 5
<210> 103
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR3 анти-ID B-2
<400> 103
Gln His Phe Trp Ser Thr Pro Tyr
1 5
<210> 104
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 анти-ID B-1
<400> 104
Ser Ala Ser Ser Gly Val Ile Tyr Met Tyr
1 5 10
<210> 105
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 анти-ID B-2
<400> 105
Arg Ala Ser Gly Asn Ile His Asn Tyr Leu Ala
1 5 10
<210> 106
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 анти-ID B-1
<400> 106
Ile Tyr Met Tyr Trp Tyr
1 5
<210> 107
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR1 анти-ID B-2
<400> 107
His Asn Tyr Leu Ala Trp Tyr
1 5
<210> 108
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 анти-ID B-1
<400> 108
Leu Thr Ser Asn Leu Ala Ser
1 5
<210> 109
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 анти-ID B-2
<400> 109
Asn Ala Lys Thr Leu Ala Asp
1 5
<210> 110
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 анти-ID B-1
<400> 110
Pro Trp Ile Tyr Leu Thr Ser Asn Leu Ala
1 5 10
<210> 111
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> LC-CDR2 анти-ID B-2
<400> 111
Leu Leu Val Tyr Asn Ala Lys Thr Leu Ala
1 5 10
<210> 112
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Консенсусная LC-CDR1
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> X= S или R
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> X= S или R
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> X= S или G
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> X= G или N
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> X= V или I
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> X= I или H
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> X= N или null
<220>
<221> ВАРИАНТ
<222> (10)..(10)
<223> X= M или L
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> X= Y или A
<400> 112
Xaa Ala Xaa Xaa Xaa Xaa Xaa Xaa Tyr Xaa Xaa Trp Tyr
1 5 10
<210> 113
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Консенсусная LC-CDR2
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> X= P или L
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> X= W или L
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> X= I или V
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> X= L или N
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> X= T или A
<220>
<221> ВАРИАНТ
<222> (7)..(7)
<223> X= S или K
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> X= N или T
<220>
<221> ВАРИАНТ
<222> (11)..(11)
<223> X= S или D
<400> 113
Xaa Xaa Xaa Tyr Xaa Xaa Xaa Xaa Leu Ala Xaa
1 5 10
<210> 114
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Консенсусная LC-CDR3
<220>
<221> ВАРИАНТ
<222> (2)..(2)
<223> X= Q или H
<220>
<221> ВАРИАНТ
<222> (3)..(3)
<223> X= W или F
<220>
<221> ВАРИАНТ
<222> (4)..(4)
<223> X= S или W
<220>
<221> ВАРИАНТ
<222> (5)..(5)
<223> X= S или W
<220>
<221> ВАРИАНТ
<222> (6)..(6)
<223> X= N или T
<220>
<221> ВАРИАНТ
<222> (8)..(8)
<223> X= L или Y
<400> 114
Gln Xaa Xaa Xaa Xaa Xaa Pro Xaa Thr
1 5
<210> 115
<211> 324
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CH анти-ID
<400> 115
Ala Lys Thr Thr Pro Pro Ser Val Tyr Pro Leu Ala Pro Gly Ser Ala
1 5 10 15
Ala Gln Thr Asn Ser Met Val Thr Leu Gly Cys Leu Val Lys Gly Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Thr Trp Asn Ser Gly Ser Leu Ser Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu
50 55 60
Ser Ser Ser Val Thr Val Pro Ser Ser Thr Trp Pro Ser Glu Thr Val
65 70 75 80
Thr Cys Asn Val Ala His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys
85 90 95
Ile Val Pro Arg Asp Cys Gly Cys Lys Pro Cys Ile Cys Thr Val Pro
100 105 110
Glu Val Ser Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Val Leu
115 120 125
Thr Ile Thr Leu Thr Pro Lys Val Thr Cys Val Val Val Asp Ile Ser
130 135 140
Lys Asp Asp Pro Glu Val Gln Phe Ser Trp Phe Val Asp Asp Val Glu
145 150 155 160
Val His Thr Ala Gln Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr
165 170 175
Phe Arg Ser Val Ser Glu Leu Pro Ile Met His Gln Asp Trp Leu Asn
180 185 190
Gly Lys Glu Phe Lys Cys Arg Val Asn Ser Ala Ala Phe Pro Ala Pro
195 200 205
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln
210 215 220
Val Tyr Thr Ile Pro Pro Pro Lys Glu Gln Met Ala Lys Asp Lys Val
225 230 235 240
Ser Leu Thr Cys Met Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr Val
245 250 255
Glu Trp Gln Trp Asn Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln
260 265 270
Pro Ile Met Asp Thr Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn
275 280 285
Val Gln Lys Ser Asn Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser Val
290 295 300
Leu His Glu Gly Leu His Asn His His Thr Glu Lys Ser Leu Ser His
305 310 315 320
Ser Pro Gly Lys
<210> 116
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь анти-ID
<400> 116
Gln Val Gln Leu Gln Gln Pro Gly Ser Glu Leu Val Arg Pro Gly Gly
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Asp Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asn Ile Tyr Pro Gly Ser Gly Gly Thr Asn Tyr Asp Glu Lys Phe
50 55 60
Lys Arg Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Glu Val Thr Thr Val Ala Tyr Tyr Tyr Ser Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Lys Thr Thr Pro Pro
115 120 125
Ser Val Tyr Pro Leu Ala Pro Gly Ser Ala Ala Gln Thr Asn Ser Met
130 135 140
Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr Val
180 185 190
Pro Ser Ser Thr Trp Pro Ser Glu Thr Val Thr Cys Asn Val Ala His
195 200 205
Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Val Pro Arg Asp Cys
210 215 220
Gly Cys Lys Pro Cys Ile Cys Thr Val Pro Glu Val Ser Ser Val Phe
225 230 235 240
Ile Phe Pro Pro Lys Pro Lys Asp Val Leu Thr Ile Thr Leu Thr Pro
245 250 255
Lys Val Thr Cys Val Val Val Asp Ile Ser Lys Asp Asp Pro Glu Val
260 265 270
Gln Phe Ser Trp Phe Val Asp Asp Val Glu Val His Thr Ala Gln Thr
275 280 285
Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Ser Val Ser Glu
290 295 300
Leu Pro Ile Met His Gln Asp Trp Leu Asn Gly Lys Glu Phe Lys Cys
305 310 315 320
Arg Val Asn Ser Ala Ala Phe Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln Val Tyr Thr Ile Pro Pro
340 345 350
Pro Lys Glu Gln Met Ala Lys Asp Lys Val Ser Leu Thr Cys Met Ile
355 360 365
Thr Asp Phe Phe Pro Glu Asp Ile Thr Val Glu Trp Gln Trp Asn Gly
370 375 380
Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln Pro Ile Met Asp Thr Asp
385 390 395 400
Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn Val Gln Lys Ser Asn Trp
405 410 415
Glu Ala Gly Asn Thr Phe Thr Cys Ser Val Leu His Glu Gly Leu His
420 425 430
Asn His His Thr Glu Lys Ser Leu Ser His Ser Pro Gly Lys
435 440 445
<210> 117
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальная последовательность HC анти-ID
<400> 117
Met Gly Trp Ser Ser Ile Ile Leu Phe Leu Val Ala Thr Ala Ser Gly
1 5 10 15
Val His Ser
<210> 118
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CL анти-ID
<400> 118
Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu
1 5 10 15
Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe
20 25 30
Tyr Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg
35 40 45
Gln Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu
65 70 75 80
Arg His Asn Asn Tyr Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser
85 90 95
Pro Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
100 105
<210> 119
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь анти-ID
<400> 119
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Lys Thr Val Pro Phe
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
100 105 110
Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln Leu Thr Ser Gly
115 120 125
Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr Pro Lys Asp Ile
130 135 140
Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg Gln Asn Gly Val Leu
145 150 155 160
Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser Thr Tyr Ser Met Ser
165 170 175
Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu Arg His Asn Asn Tyr
180 185 190
Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser Pro Ile Val Lys Ser
195 200 205
Phe Asn Arg Asn Glu Cys
210
<210> 120
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальная последовательность LC анти-ID
<400> 120
Met Met Ser Ser Ala Gln Phe Leu Gly Leu Leu Leu Leu Cys Phe Gln
1 5 10 15
Gly Thr Arg Cys
20
<210> 121
<211> 330
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CH анти-ID B-1
<400> 121
Ala Lys Thr Thr Ala Pro Ser Val Tyr Pro Leu Ala Pro Val Cys Gly
1 5 10 15
Asp Thr Thr Gly Ser Ser Val Thr Leu Gly Cys Leu Val Lys Gly Tyr
20 25 30
Phe Pro Glu Pro Val Thr Leu Thr Trp Asn Ser Gly Ser Leu Ser Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu
50 55 60
Ser Ser Ser Val Thr Val Thr Ser Ser Thr Trp Pro Ser Gln Ser Ile
65 70 75 80
Thr Cys Asn Val Ala His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys
85 90 95
Ile Glu Pro Arg Gly Pro Thr Ile Lys Pro Cys Pro Pro Cys Lys Cys
100 105 110
Pro Ala Pro Asn Leu Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
115 120 125
Lys Ile Lys Asp Val Leu Met Ile Ser Leu Ser Pro Ile Val Thr Cys
130 135 140
Val Val Val Asp Val Ser Glu Asp Asp Pro Asp Val Gln Ile Ser Trp
145 150 155 160
Phe Val Asn Asn Val Glu Val His Thr Ala Gln Thr Gln Thr His Arg
165 170 175
Glu Asp Tyr Asn Ser Thr Leu Arg Val Val Ser Ala Leu Pro Ile Gln
180 185 190
His Gln Asp Trp Met Ser Gly Lys Glu Phe Lys Cys Lys Val Asn Asn
195 200 205
Lys Asp Leu Pro Ala Pro Ile Glu Arg Thr Ile Ser Lys Pro Lys Gly
210 215 220
Ser Val Arg Ala Pro Gln Val Tyr Val Leu Pro Pro Pro Glu Glu Glu
225 230 235 240
Met Thr Lys Lys Gln Val Thr Leu Thr Cys Met Val Thr Asp Phe Met
245 250 255
Pro Glu Asp Ile Tyr Val Glu Trp Thr Asn Asn Gly Lys Thr Glu Leu
260 265 270
Asn Tyr Lys Asn Thr Glu Pro Val Leu Asp Ser Asp Gly Ser Tyr Phe
275 280 285
Met Tyr Ser Lys Leu Arg Val Glu Lys Lys Asn Trp Val Glu Arg Asn
290 295 300
Ser Tyr Ser Cys Ser Val Val His Glu Gly Leu His Asn His His Thr
305 310 315 320
Thr Lys Ser Phe Ser Arg Thr Pro Gly Lys
325 330
<210> 122
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь анти-ID B-1
<400> 122
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Lys Trp Val Lys Gln Cys His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Asn Gly Gly Thr Asp Tyr Asn Gln Asn Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Asn Asn Tyr Gly Ser Arg Asp Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Lys Thr Thr Ala Pro
115 120 125
Ser Val Tyr Pro Leu Ala Pro Val Cys Gly Asp Thr Thr Gly Ser Ser
130 135 140
Val Thr Leu Gly Cys Leu Val Lys Gly Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Leu Thr Trp Asn Ser Gly Ser Leu Ser Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu Ser Ser Ser Val Thr Val
180 185 190
Thr Ser Ser Thr Trp Pro Ser Gln Ser Ile Thr Cys Asn Val Ala His
195 200 205
Pro Ala Ser Ser Thr Lys Val Asp Lys Lys Ile Glu Pro Arg Gly Pro
210 215 220
Thr Ile Lys Pro Cys Pro Pro Cys Lys Cys Pro Ala Pro Asn Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Ile Lys Asp Val Leu
245 250 255
Met Ile Ser Leu Ser Pro Ile Val Thr Cys Val Val Val Asp Val Ser
260 265 270
Glu Asp Asp Pro Asp Val Gln Ile Ser Trp Phe Val Asn Asn Val Glu
275 280 285
Val His Thr Ala Gln Thr Gln Thr His Arg Glu Asp Tyr Asn Ser Thr
290 295 300
Leu Arg Val Val Ser Ala Leu Pro Ile Gln His Gln Asp Trp Met Ser
305 310 315 320
Gly Lys Glu Phe Lys Cys Lys Val Asn Asn Lys Asp Leu Pro Ala Pro
325 330 335
Ile Glu Arg Thr Ile Ser Lys Pro Lys Gly Ser Val Arg Ala Pro Gln
340 345 350
Val Tyr Val Leu Pro Pro Pro Glu Glu Glu Met Thr Lys Lys Gln Val
355 360 365
Thr Leu Thr Cys Met Val Thr Asp Phe Met Pro Glu Asp Ile Tyr Val
370 375 380
Glu Trp Thr Asn Asn Gly Lys Thr Glu Leu Asn Tyr Lys Asn Thr Glu
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Tyr Phe Met Tyr Ser Lys Leu Arg
405 410 415
Val Glu Lys Lys Asn Trp Val Glu Arg Asn Ser Tyr Ser Cys Ser Val
420 425 430
Val His Glu Gly Leu His Asn His His Thr Thr Lys Ser Phe Ser Arg
435 440 445
Thr Pro Gly Lys
450
<210> 123
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальная последовательность HC анти-ID B-1
<400> 123
Met Gly Trp Ser Trp Ile Phe Leu Phe Leu Leu Ser Gly Thr Ala Gly
1 5 10 15
Val Leu Ser
<210> 124
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CL анти-ID B-1
<400> 124
Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu
1 5 10 15
Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe
20 25 30
Tyr Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg
35 40 45
Gln Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu
65 70 75 80
Arg His Asn Ser Tyr Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser
85 90 95
Pro Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
100 105
<210> 125
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь анти-ID B-1
<400> 125
Gln Ile Val Leu Thr Gln Ser Pro Ala Leu Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Gly Val Ile Tyr Met
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Arg Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Leu Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Ala Asp Ala Ala Pro
100 105 110
Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln Leu Thr Ser Gly Gly
115 120 125
Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr Pro Lys Asp Ile Asn
130 135 140
Val Lys Trp Lys Ile Asp Gly Ser Glu Arg Gln Asn Gly Val Leu Asn
145 150 155 160
Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser Thr Tyr Ser Met Ser Ser
165 170 175
Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu Arg His Asn Ser Tyr Thr
180 185 190
Cys Glu Ala Thr His Lys Thr Ser Thr Ser Pro Ile Val Lys Ser Phe
195 200 205
Asn Arg Asn Glu Cys
210
<210> 126
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальная последовательность LC анти-ID B-1
<400> 126
Met Asp Phe Gln Val Gln Ile Phe Ser Phe Leu Leu Met Ser Ala Ser
1 5 10 15
Val Ile Met Ser Arg Gly
20
<210> 127
<211> 324
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CH анти-ID B-2
<400> 127
Ala Lys Thr Thr Pro Pro Ser Val Tyr Pro Leu Ala Pro Gly Ser Ala
1 5 10 15
Ala Gln Thr Asn Ser Met Val Thr Leu Gly Cys Leu Val Lys Gly Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Thr Trp Asn Ser Gly Ser Leu Ser Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Asp Leu Tyr Thr Leu
50 55 60
Ser Ser Ser Val Thr Val Pro Ser Ser Thr Trp Pro Ser Glu Thr Val
65 70 75 80
Thr Cys Asn Val Ala His Pro Ala Ser Ser Thr Lys Val Asp Lys Lys
85 90 95
Ile Val Pro Arg Asp Cys Gly Cys Lys Pro Cys Ile Cys Thr Val Pro
100 105 110
Glu Val Ser Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Val Leu
115 120 125
Thr Ile Thr Leu Thr Pro Lys Val Thr Cys Val Val Val Asp Ile Ser
130 135 140
Lys Asp Asp Pro Glu Val Gln Phe Ser Trp Phe Val Asp Asp Val Glu
145 150 155 160
Val His Thr Ala Gln Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr
165 170 175
Phe Arg Ser Val Ser Glu Leu Pro Ile Met His Gln Asp Trp Leu Asn
180 185 190
Gly Lys Glu Phe Lys Cys Arg Val Asn Ser Ala Ala Phe Pro Ala Pro
195 200 205
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln
210 215 220
Val Tyr Thr Ile Pro Pro Pro Lys Glu Gln Met Ala Lys Asp Lys Val
225 230 235 240
Ser Leu Thr Cys Met Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr Val
245 250 255
Glu Trp Gln Trp Asn Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln
260 265 270
Pro Ile Met Asp Thr Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn
275 280 285
Val Gln Lys Ser Asn Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser Val
290 295 300
Leu His Glu Gly Leu His Asn His His Thr Glu Lys Ser Leu Ser His
305 310 315 320
Ser Pro Gly Lys
<210> 128
<211> 439
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Тяжелая цепь анти-ID B-2
<400> 128
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Thr Ser Gly Tyr Ser Phe Thr Arg Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Met Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Asn Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Ile Tyr Tyr Glu Glu Ala Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala Ala Lys Thr Thr Pro Pro Ser Val Tyr Pro Leu Ala Pro
115 120 125
Gly Ser Ala Ala Gln Thr Asn Ser Met Val Thr Leu Gly Cys Leu Val
130 135 140
Lys Gly Tyr Phe Pro Glu Pro Val Thr Val Thr Trp Asn Ser Gly Ser
145 150 155 160
Leu Ser Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Asp Leu
165 170 175
Tyr Thr Leu Ser Ser Ser Val Thr Val Pro Ser Ser Thr Trp Pro Ser
180 185 190
Glu Thr Val Thr Cys Asn Val Ala His Pro Ala Ser Ser Thr Lys Val
195 200 205
Asp Lys Lys Ile Val Pro Arg Asp Cys Gly Cys Lys Pro Cys Ile Cys
210 215 220
Thr Val Pro Glu Val Ser Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
225 230 235 240
Asp Val Leu Thr Ile Thr Leu Thr Pro Lys Val Thr Cys Val Val Val
245 250 255
Asp Ile Ser Lys Asp Asp Pro Glu Val Gln Phe Ser Trp Phe Val Asp
260 265 270
Asp Val Glu Val His Thr Ala Gln Thr Gln Pro Arg Glu Glu Gln Phe
275 280 285
Asn Ser Thr Phe Arg Ser Val Ser Glu Leu Pro Ile Met His Gln Asp
290 295 300
Trp Leu Asn Gly Lys Glu Phe Lys Cys Arg Val Asn Ser Ala Ala Phe
305 310 315 320
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Arg Pro Lys
325 330 335
Ala Pro Gln Val Tyr Thr Ile Pro Pro Pro Lys Glu Gln Met Ala Lys
340 345 350
Asp Lys Val Ser Leu Thr Cys Met Ile Thr Asp Phe Phe Pro Glu Asp
355 360 365
Ile Thr Val Glu Trp Gln Trp Asn Gly Gln Pro Ala Glu Asn Tyr Lys
370 375 380
Asn Thr Gln Pro Ile Met Asp Thr Asp Gly Ser Tyr Phe Val Tyr Ser
385 390 395 400
Lys Leu Asn Val Gln Lys Ser Asn Trp Glu Ala Gly Asn Thr Phe Thr
405 410 415
Cys Ser Val Leu His Glu Gly Leu His Asn His His Thr Glu Lys Ser
420 425 430
Leu Ser His Ser Pro Gly Lys
435
<210> 129
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальная последовательность HC анти-ID B-2
<400> 129
Met Gly Trp Ser Ser Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser
<210> 130
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL анти-ID B-2
<400> 130
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Asp Ser Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Gly Ser Tyr Tyr Cys Gln His Phe Trp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 131
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Легкая цепь анти-ID B-2
<400> 131
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Gly Asn Ile His Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Asp Ser Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Tyr Ser Leu Lys Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Gly Ser Tyr Tyr Cys Gln His Phe Trp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala
100 105 110
Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln Leu Thr Ser Gly
115 120 125
Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr Pro Lys Asp Ile
130 135 140
Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg Gln Asn Gly Val Leu
145 150 155 160
Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser Thr Tyr Ser Met Ser
165 170 175
Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu Arg His Asn Ser Tyr
180 185 190
Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser Pro Ile Val Lys Ser
195 200 205
Phe Asn Arg Asn Glu Cys
210
<210> 132
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Сигнальная последовательность LC анти-ID B-2
<400> 132
Met Ser Val Leu Thr Gln Val Leu Ala Leu Leu Leu Leu Trp Leu Thr
1 5 10 15
Gly Ala Arg Cys
20
<210> 133
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Спейсер (шарнир IgG4)
<400> 133
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 134
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Спейсер (шарнир IgG4)
<400> 134
gaatctaagt acggaccgcc ctgcccccct tgccct 36
<210> 135
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Спейсер шарнир-CH3
<400> 135
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Gly Gln Pro Arg
1 5 10 15
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
20 25 30
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
35 40 45
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
50 55 60
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
65 70 75 80
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
85 90 95
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
100 105 110
Leu Ser Leu Ser Leu Gly Lys
115
<210> 136
<211> 229
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Спейсер шарнир-CH2-CH3
<400> 136
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys
225
<210> 137
<211> 282
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> IgD-шарнир-Fc
<400> 137
Arg Trp Pro Glu Ser Pro Lys Ala Gln Ala Ser Ser Val Pro Thr Ala
1 5 10 15
Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala
20 25 30
Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys
35 40 45
Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
50 55 60
Ser His Thr Gln Pro Leu Gly Val Tyr Leu Leu Thr Pro Ala Val Gln
65 70 75 80
Asp Leu Trp Leu Arg Asp Lys Ala Thr Phe Thr Cys Phe Val Val Gly
85 90 95
Ser Asp Leu Lys Asp Ala His Leu Thr Trp Glu Val Ala Gly Lys Val
100 105 110
Pro Thr Gly Gly Val Glu Glu Gly Leu Leu Glu Arg His Ser Asn Gly
115 120 125
Ser Gln Ser Gln His Ser Arg Leu Thr Leu Pro Arg Ser Leu Trp Asn
130 135 140
Ala Gly Thr Ser Val Thr Cys Thr Leu Asn His Pro Ser Leu Pro Pro
145 150 155 160
Gln Arg Leu Met Ala Leu Arg Glu Pro Ala Ala Gln Ala Pro Val Lys
165 170 175
Leu Ser Leu Asn Leu Leu Ala Ser Ser Asp Pro Pro Glu Ala Ala Ser
180 185 190
Trp Leu Leu Cys Glu Val Ser Gly Phe Ser Pro Pro Asn Ile Leu Leu
195 200 205
Met Trp Leu Glu Asp Gln Arg Glu Val Asn Thr Ser Gly Phe Ala Pro
210 215 220
Ala Arg Pro Pro Pro Gln Pro Gly Ser Thr Thr Phe Trp Ala Trp Ser
225 230 235 240
Val Leu Arg Val Pro Ala Pro Pro Ser Pro Gln Pro Ala Thr Tyr Thr
245 250 255
Cys Val Val Ser His Glu Asp Ser Arg Thr Leu Leu Asn Ala Ser Arg
260 265 270
Ser Leu Glu Val Ser Tyr Val Thr Asp His
275 280
<210> 138
<211> 27
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CD28 (аминокислоты 153-179 из Accession No. P10747)
<400> 138
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 139
<211> 66
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CD28 (аминокислоты 114-179 из Accession No. P10747)
<400> 139
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
1 5 10 15
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
20 25 30
Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly Gly
35 40 45
Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe
50 55 60
Trp Val
65
<210> 140
<211> 41
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CD28 (аминокислоты 180-220 из P10747)
<400> 140
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 141
<211> 41
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CD28 (LL - GG)
<400> 141
Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 142
<211> 42
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> 4-1BB (аминокислоты 214-255 из Q07011.1)
<400> 142
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 143
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CD3 зета
<400> 143
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 144
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CD3 зета
<400> 144
Arg Val Lys Phe Ser Arg Ser Ala Glu Pro Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 145
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CD3 зета
<400> 145
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 146
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусств.T2A
<400> 146
Leu Glu Gly Gly Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp
1 5 10 15
Val Glu Glu Asn Pro Gly Pro Arg
20
<210> 147
<211> 357
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусств. tEGFR
<400> 147
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro Arg Lys Val Cys Asn Gly Ile Gly Ile Gly
20 25 30
Glu Phe Lys Asp Ser Leu Ser Ile Asn Ala Thr Asn Ile Lys His Phe
35 40 45
Lys Asn Cys Thr Ser Ile Ser Gly Asp Leu His Ile Leu Pro Val Ala
50 55 60
Phe Arg Gly Asp Ser Phe Thr His Thr Pro Pro Leu Asp Pro Gln Glu
65 70 75 80
Leu Asp Ile Leu Lys Thr Val Lys Glu Ile Thr Gly Phe Leu Leu Ile
85 90 95
Gln Ala Trp Pro Glu Asn Arg Thr Asp Leu His Ala Phe Glu Asn Leu
100 105 110
Glu Ile Ile Arg Gly Arg Thr Lys Gln His Gly Gln Phe Ser Leu Ala
115 120 125
Val Val Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu
130 135 140
Ile Ser Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr
145 150 155 160
Ala Asn Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys
165 170 175
Thr Lys Ile Ile Ser Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly
180 185 190
Gln Val Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu
195 200 205
Pro Arg Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys
210 215 220
Val Asp Lys Cys Asn Leu Leu Glu Gly Glu Pro Arg Glu Phe Val Glu
225 230 235 240
Asn Ser Glu Cys Ile Gln Cys His Pro Glu Cys Leu Pro Gln Ala Met
245 250 255
Asn Ile Thr Cys Thr Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala
260 265 270
His Tyr Ile Asp Gly Pro His Cys Val Lys Thr Cys Pro Ala Gly Val
275 280 285
Met Gly Glu Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His
290 295 300
Val Cys His Leu Cys His Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro
305 310 315 320
Gly Leu Glu Gly Cys Pro Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala
325 330 335
Thr Gly Met Val Gly Ala Leu Leu Leu Leu Leu Val Val Ala Leu Gly
340 345 350
Ile Gly Leu Phe Met
355
<210> 148
<211> 335
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусств. tEGFR
<400> 148
Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp Ser Leu
1 5 10 15
Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn Cys Thr Ser Ile
20 25 30
Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg Gly Asp Ser Phe
35 40 45
Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp Ile Leu Lys Thr
50 55 60
Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala Trp Pro Glu Asn
65 70 75 80
Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile Ile Arg Gly Arg
85 90 95
Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val Ser Leu Asn Ile
100 105 110
Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser Asp Gly Asp Val
115 120 125
Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn Thr Ile Asn Trp
130 135 140
Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys Ile Ile Ser Asn
145 150 155 160
Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val Cys His Ala Leu
165 170 175
Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg Asp Cys Val Ser
180 185 190
Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp Lys Cys Asn Leu
195 200 205
Leu Glu Gly Glu Pro Arg Glu Phe Val Glu Asn Ser Glu Cys Ile Gln
210 215 220
Cys His Pro Glu Cys Leu Pro Gln Ala Met Asn Ile Thr Cys Thr Gly
225 230 235 240
Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile Asp Gly Pro
245 250 255
His Cys Val Lys Thr Cys Pro Ala Gly Val Met Gly Glu Asn Asn Thr
260 265 270
Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His Leu Cys His
275 280 285
Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro Gly Leu Glu Gly Cys Pro
290 295 300
Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala Thr Gly Met Val Gly Ala
305 310 315 320
Leu Leu Leu Leu Leu Val Val Ala Leu Gly Ile Gly Leu Phe Met
325 330 335
<210> 149
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Искусств. T2A
<400> 149
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
1 5 10 15
Gly Pro
<210> 150
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Расщепляемый линкер MMP
<400> 150
Pro Leu Gly Leu Trp Ala
1 5
<210> 151
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> P2A
<400> 151
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 152
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> P2A
<400> 152
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 153
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> E2A
<400> 153
Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp Val Glu Ser
1 5 10 15
Asn Pro Gly Pro
20
<210> 154
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> F2A
<400> 154
Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala Gly Asp Val
1 5 10 15
Glu Ser Asn Pro Gly Pro
20
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЧЕТАНИЕ КЛЕТОЧНОЙ ТЕРАПИИ И ИММУНОМОДУЛЯТОРНОГО СОЕДИНЕНИЯ | 2018 |
|
RU2777911C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО К BCMA И BCMA-CAR-T-КЛЕТКИ | 2020 |
|
RU2762942C1 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО К BCMA И BCMA-CAR-NK-КЛЕТКИ | 2020 |
|
RU2795443C2 |
| АНТИ-BCMA АНТИТЕЛА, СОДЕРЖАЩИЕ ТОЛЬКО ТЯЖЁЛУЮ ЦЕПЬ | 2017 |
|
RU2781301C2 |
| АНТИИДИОТИПИЧЕСКИЕ АНТИТЕЛА И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2017 |
|
RU2773355C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2841244C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2019 |
|
RU2810092C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ К BCMA | 2015 |
|
RU2747457C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ЭКСПРЕССИРУЮЩИХ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР КЛЕТОК | 2015 |
|
RU2751362C2 |
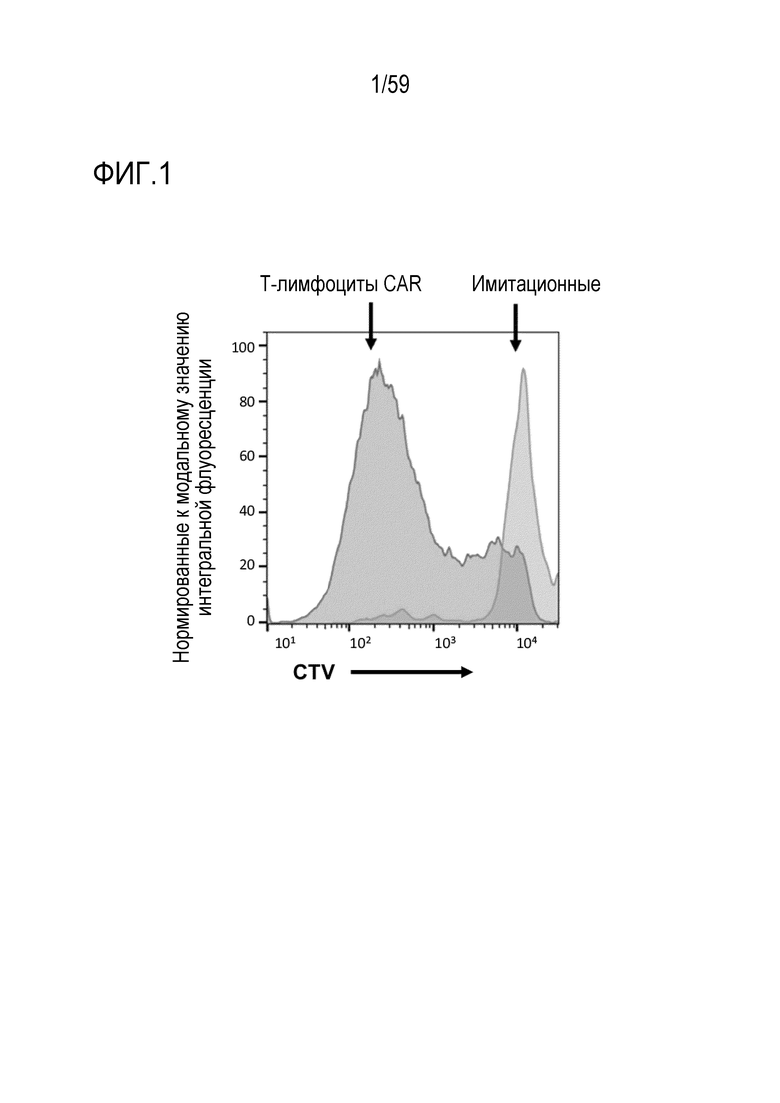
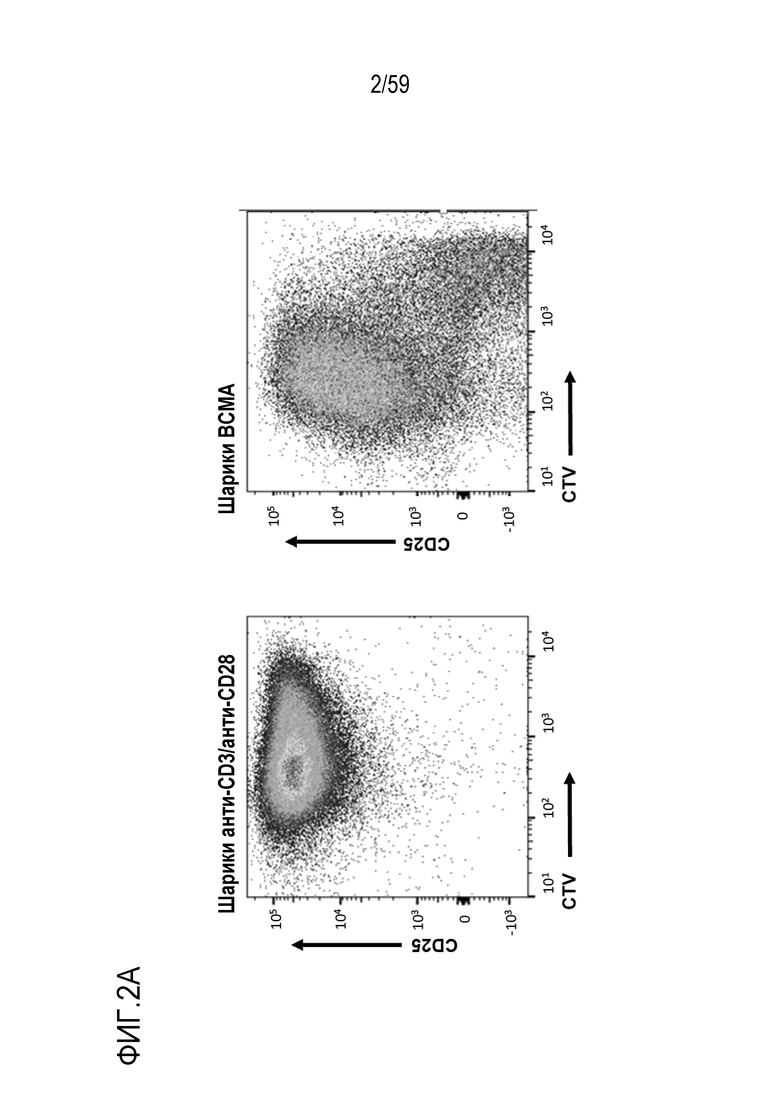
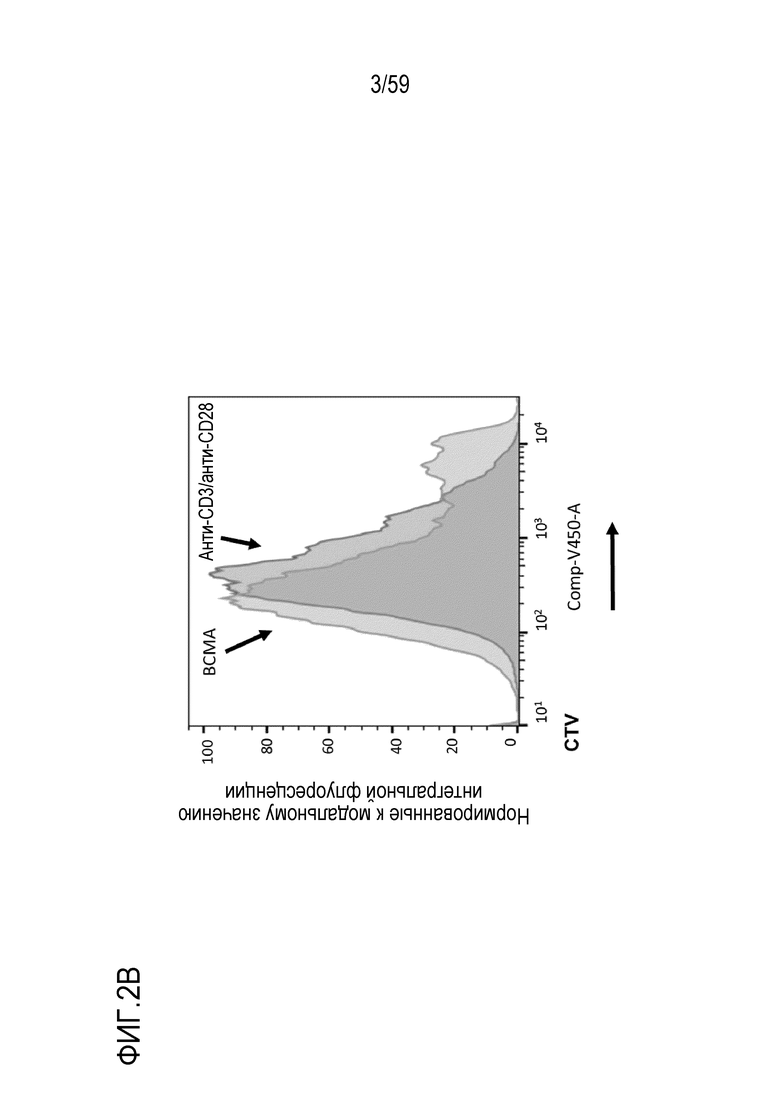
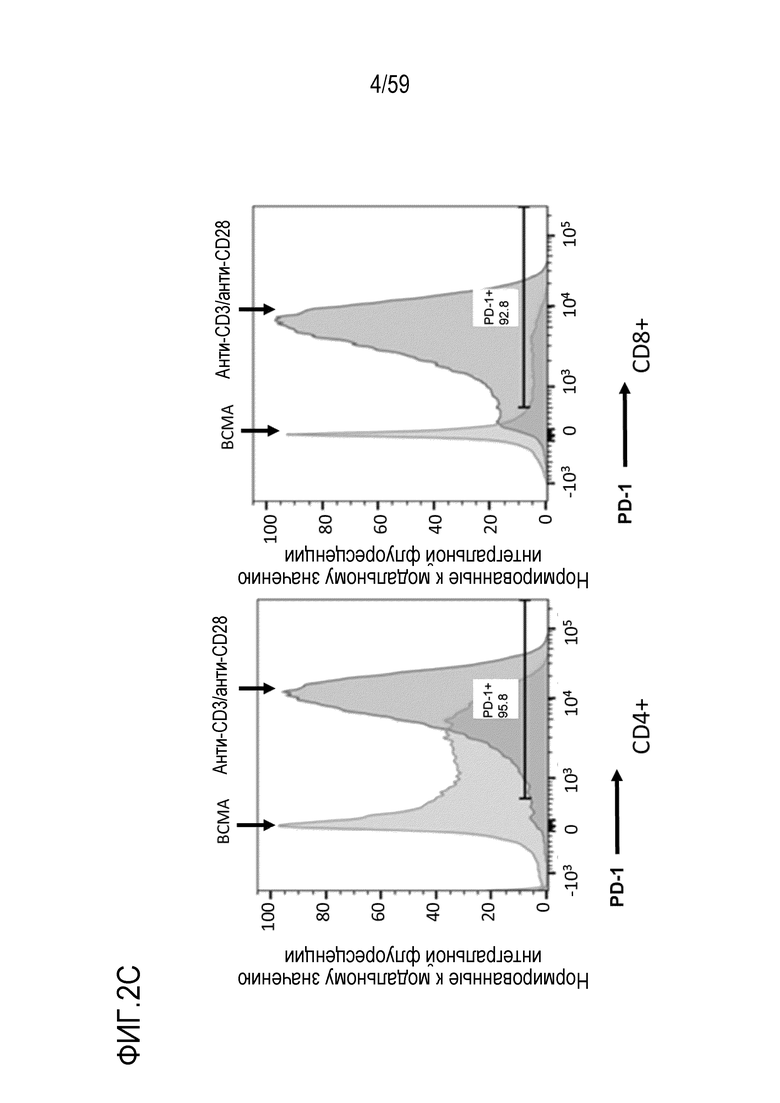
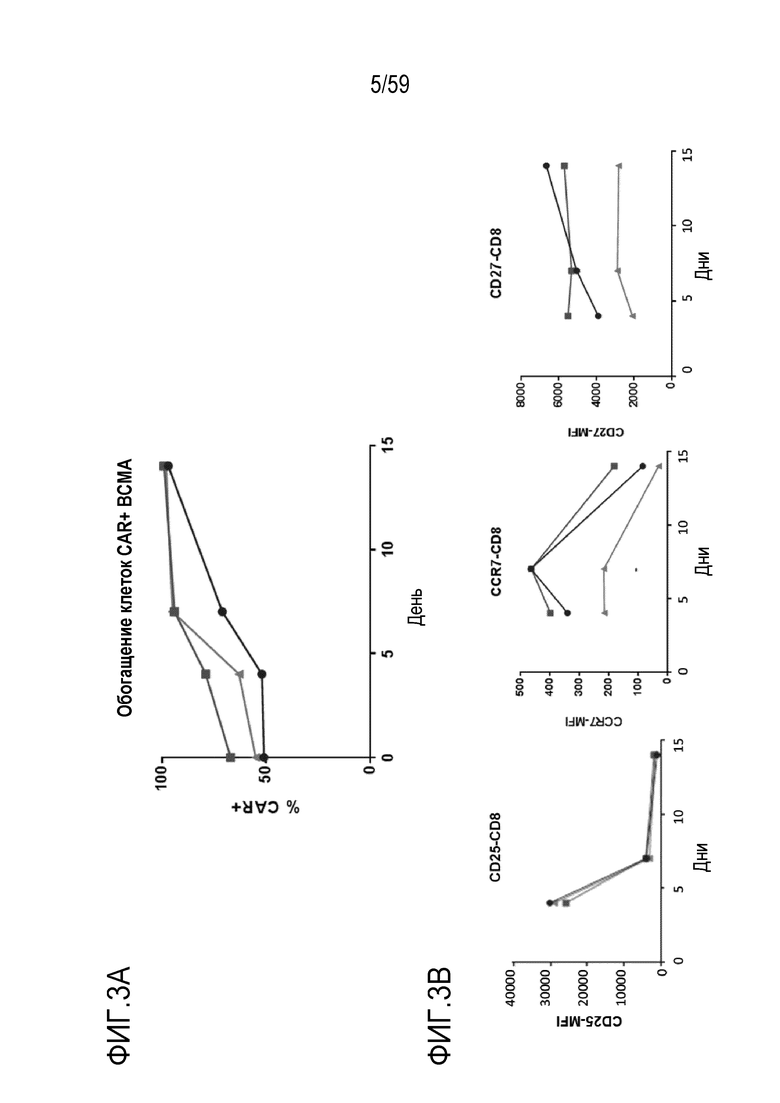
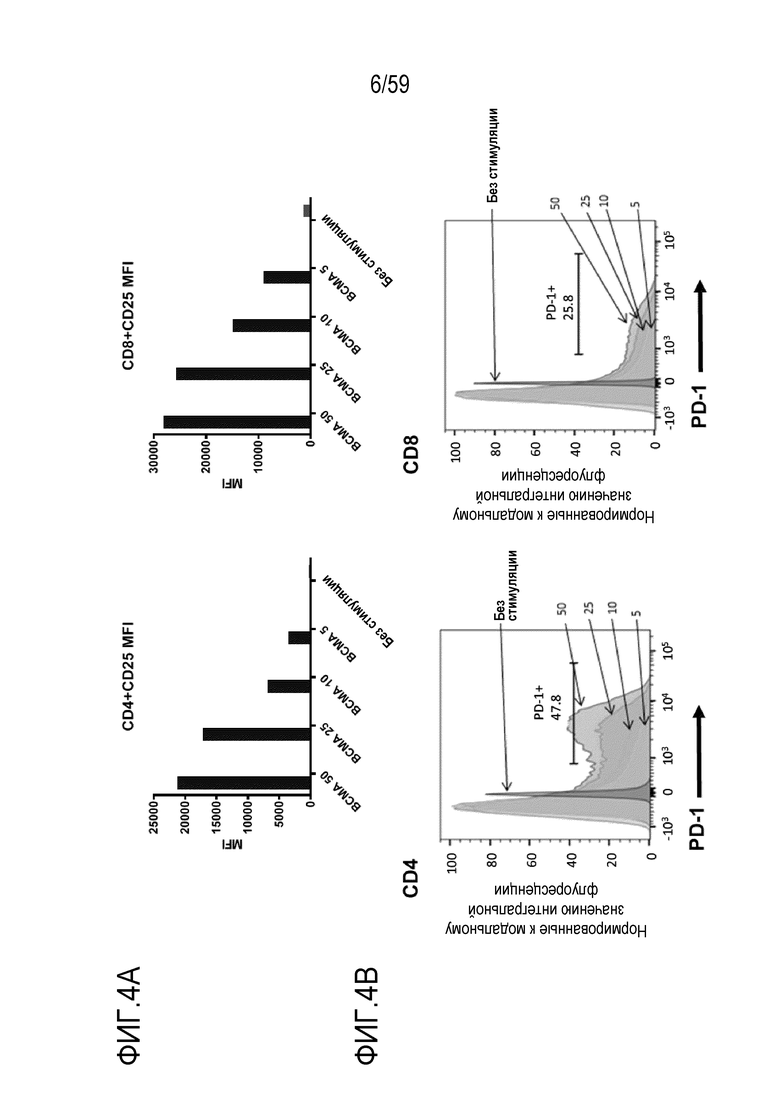
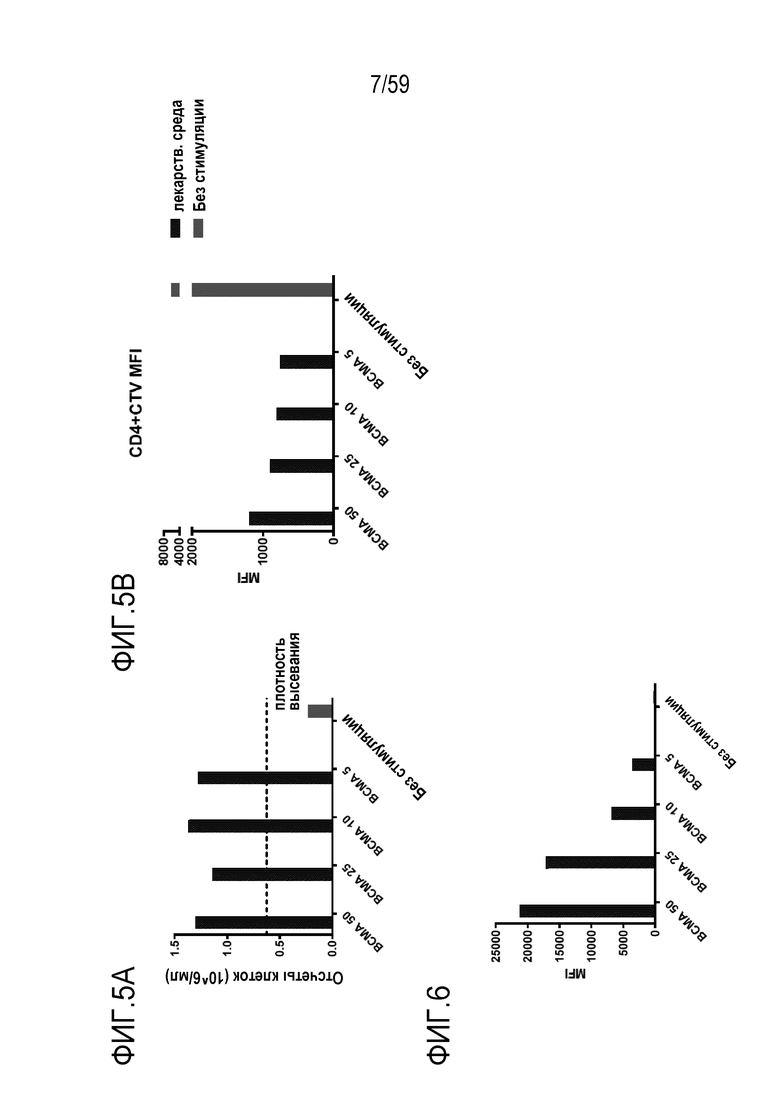
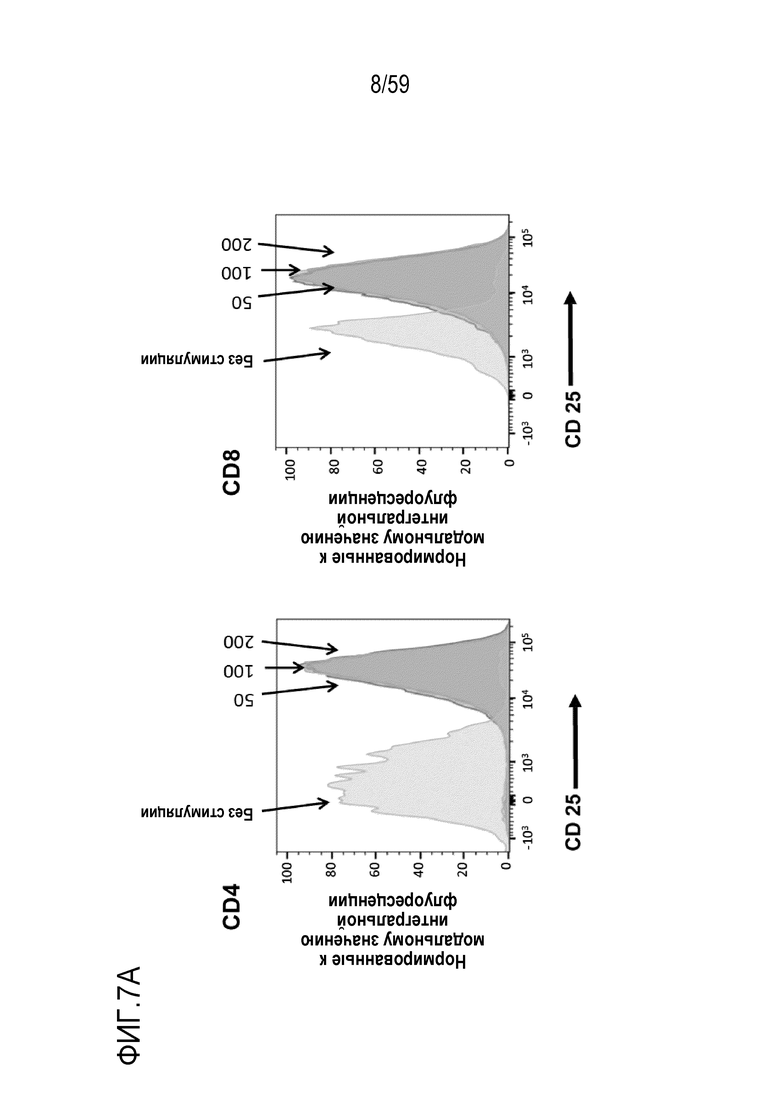
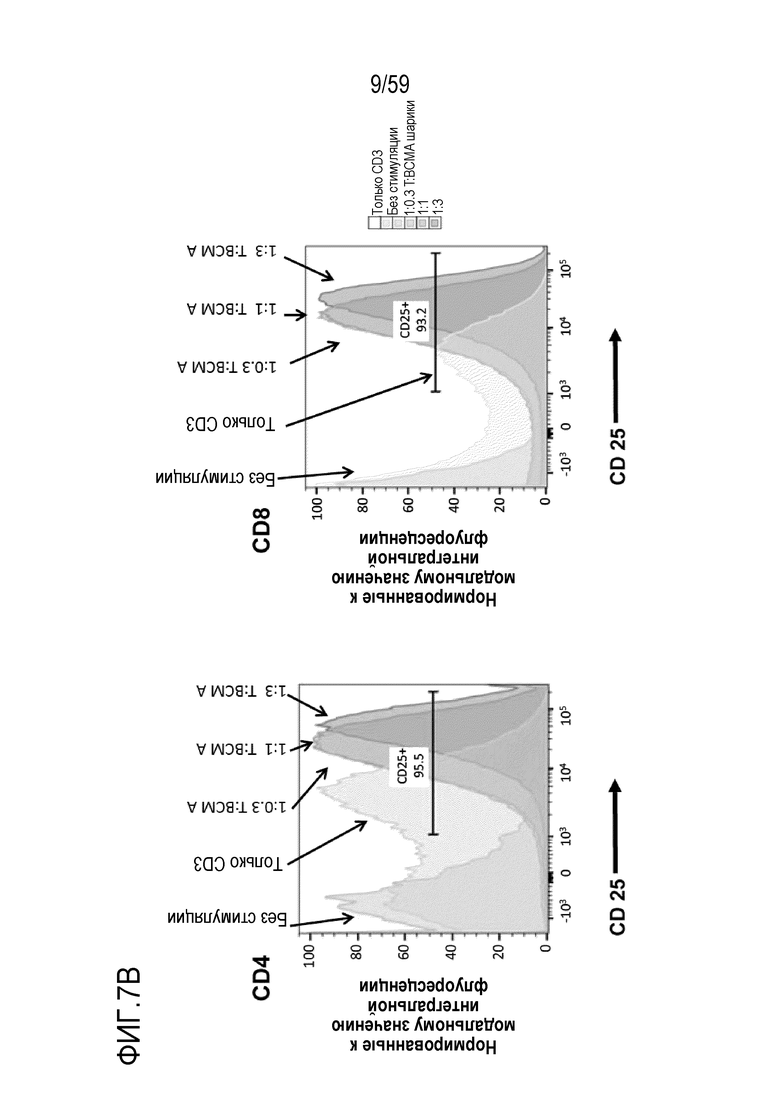
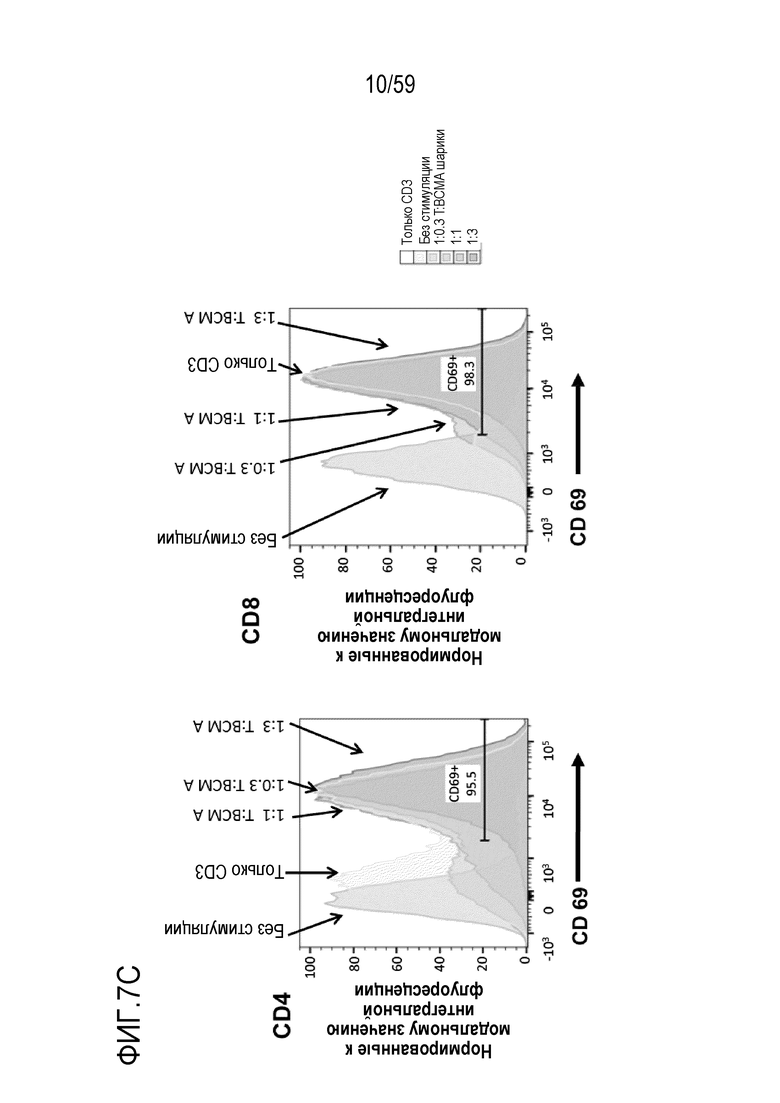
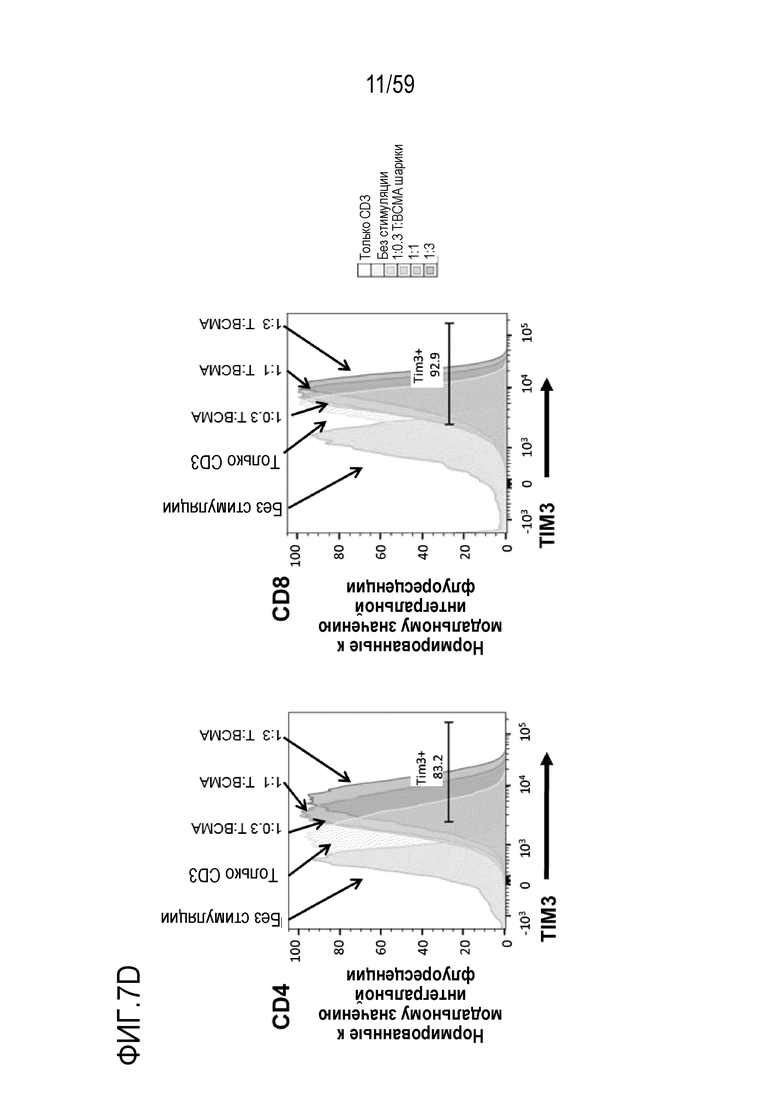
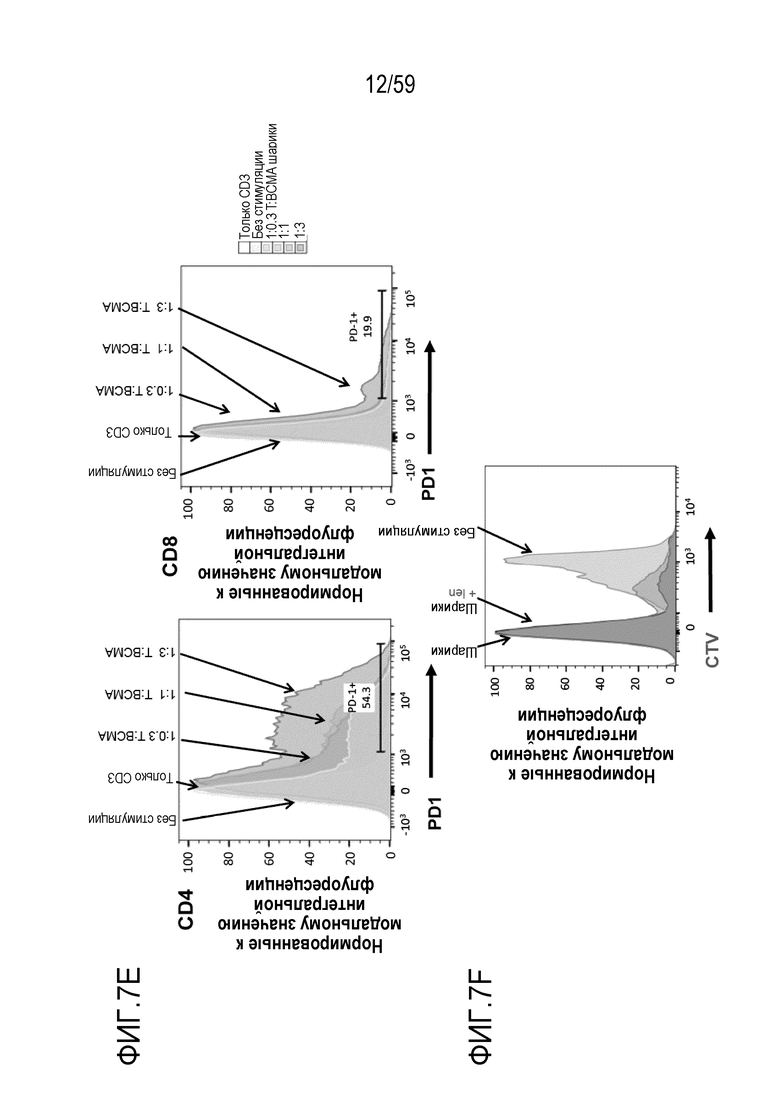
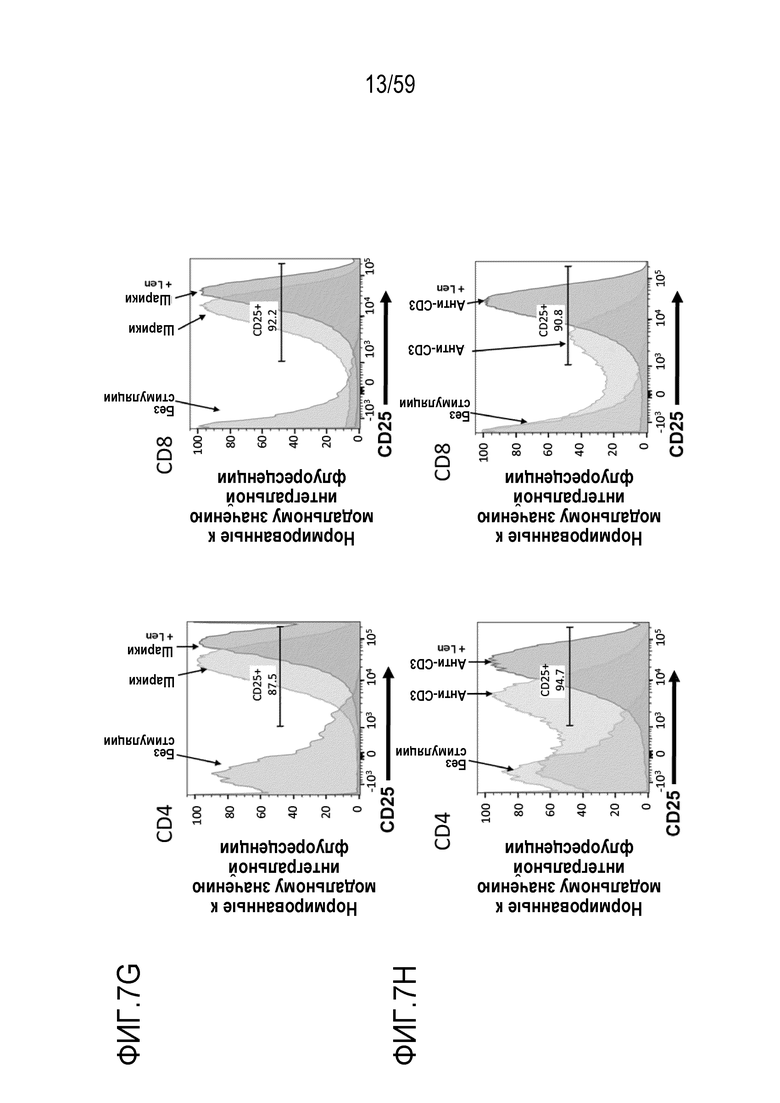
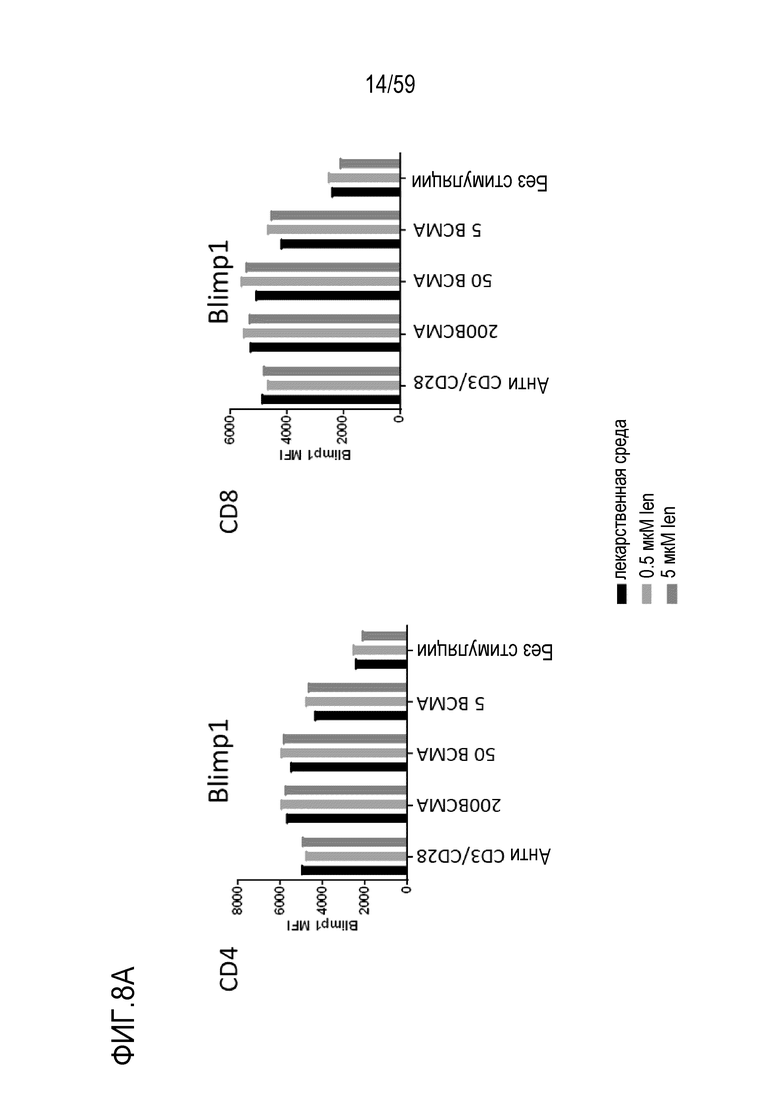
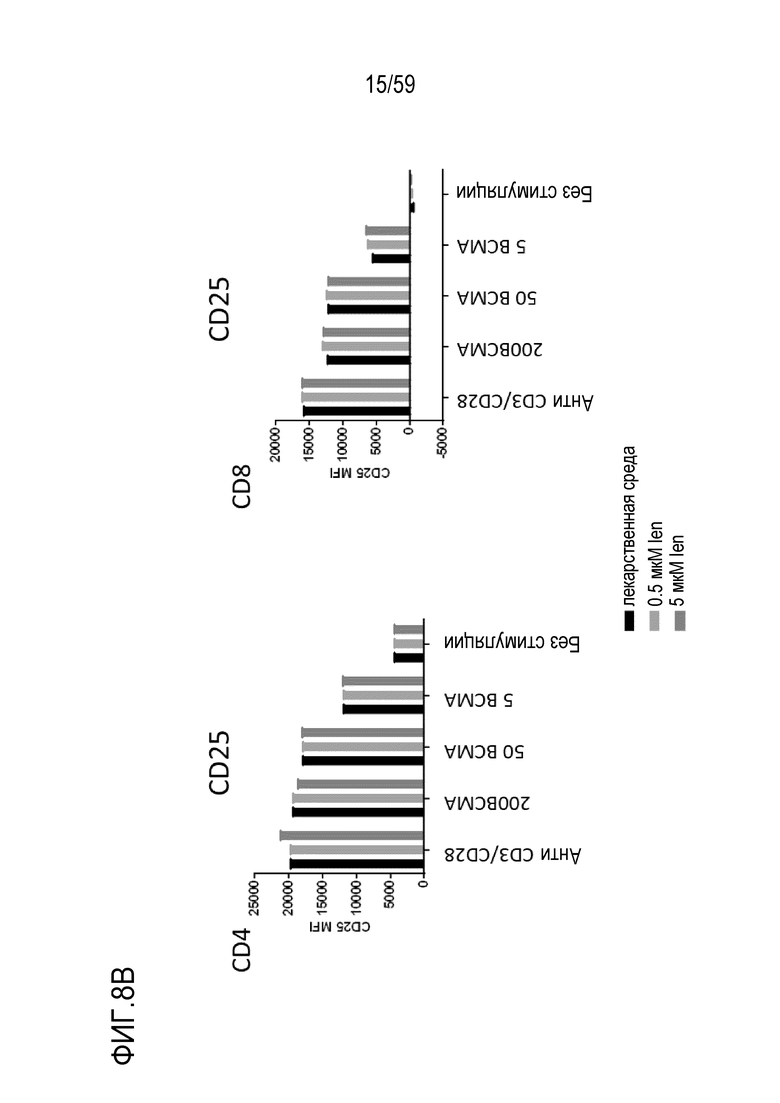
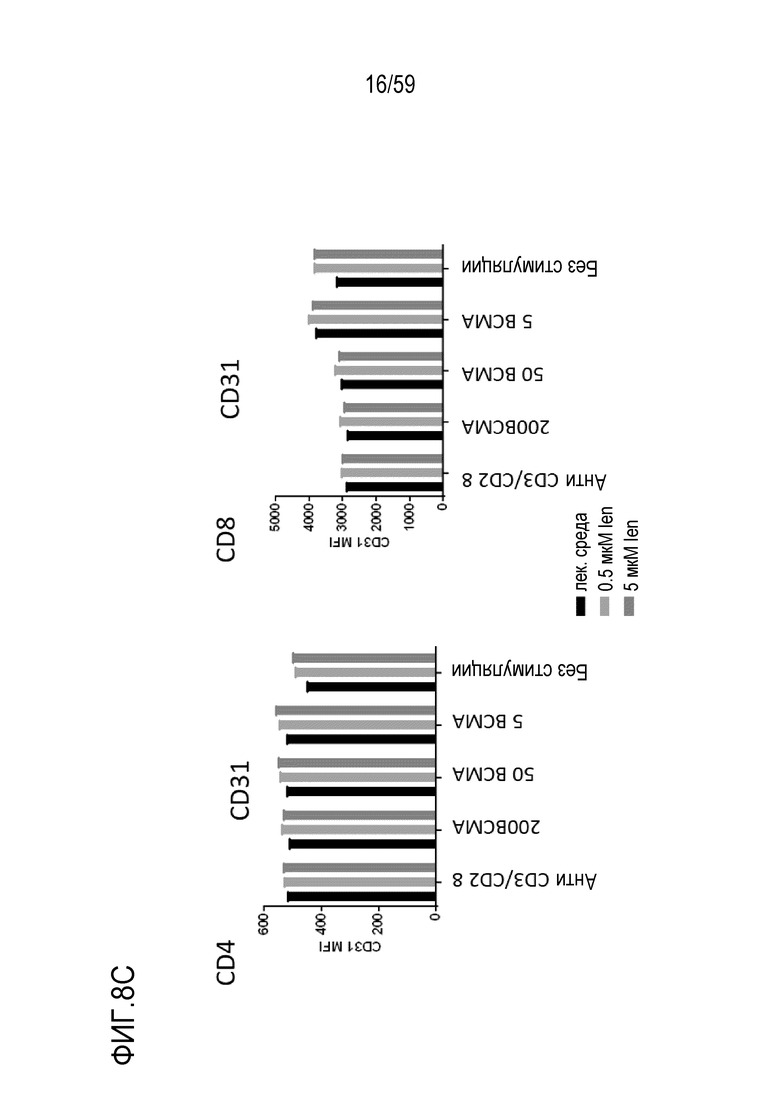
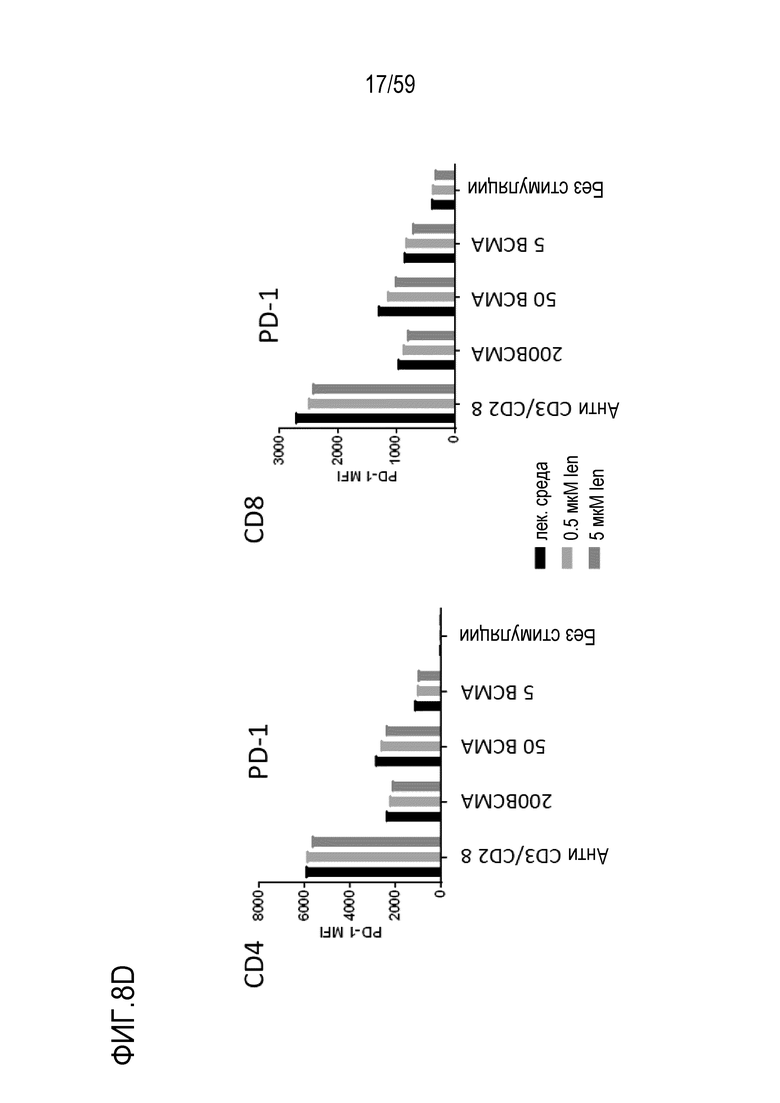
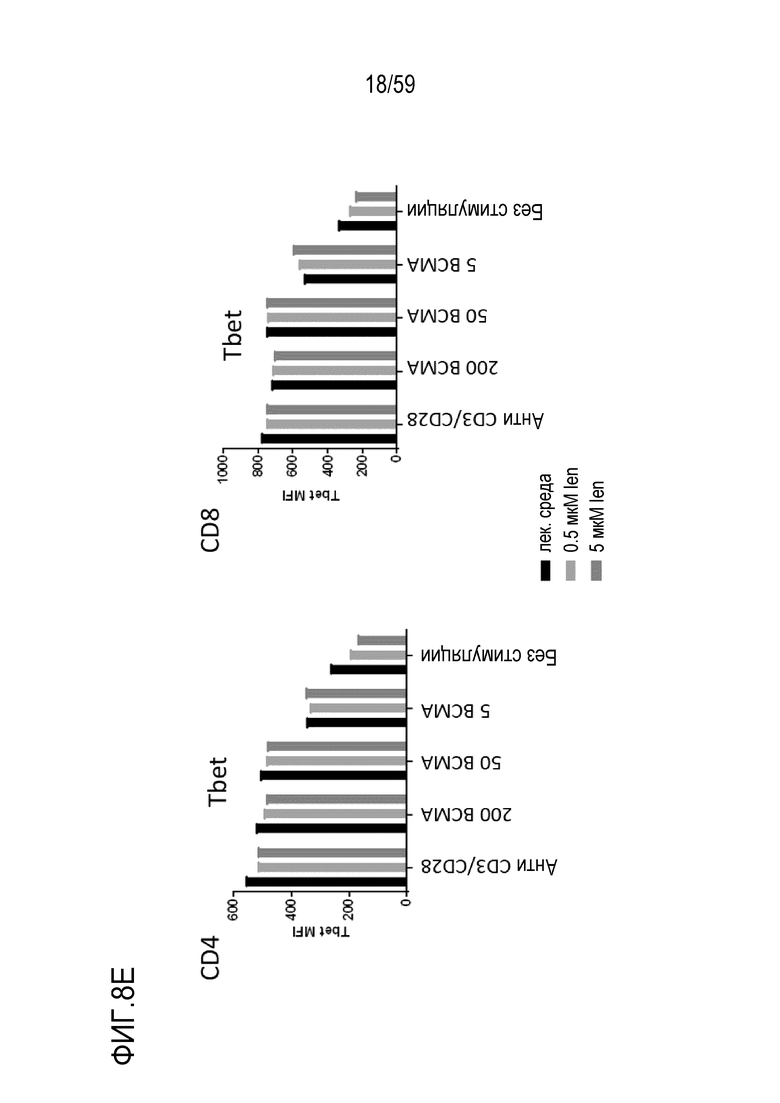
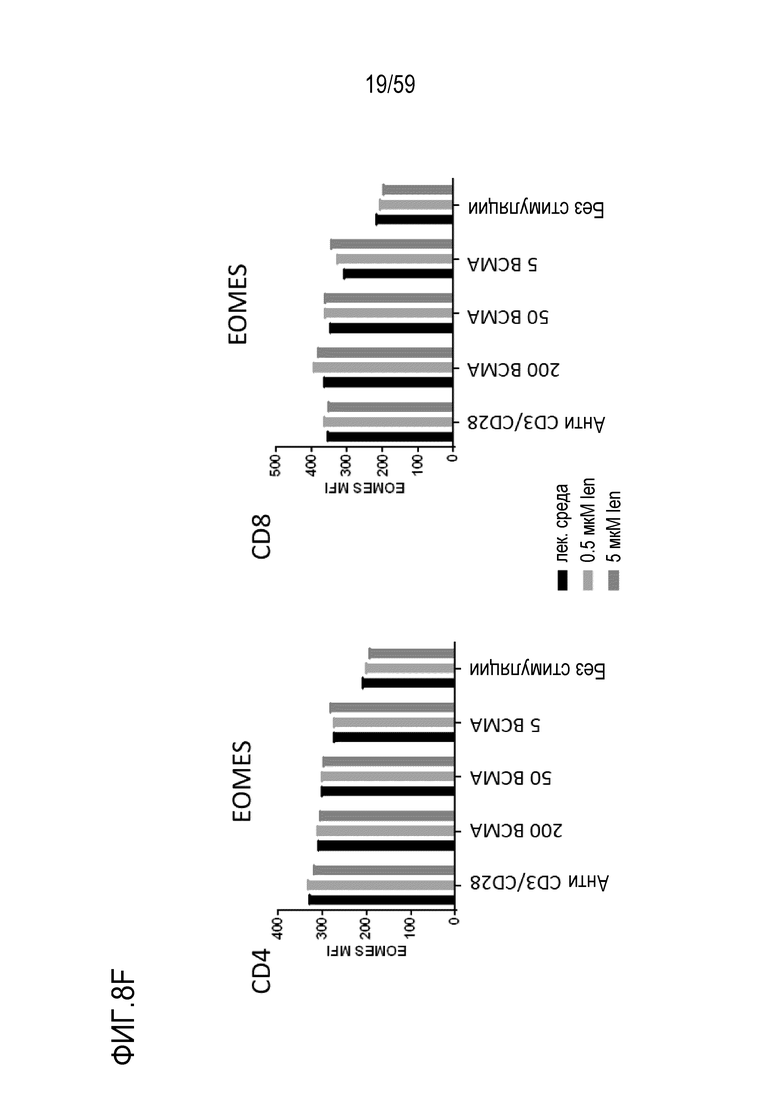
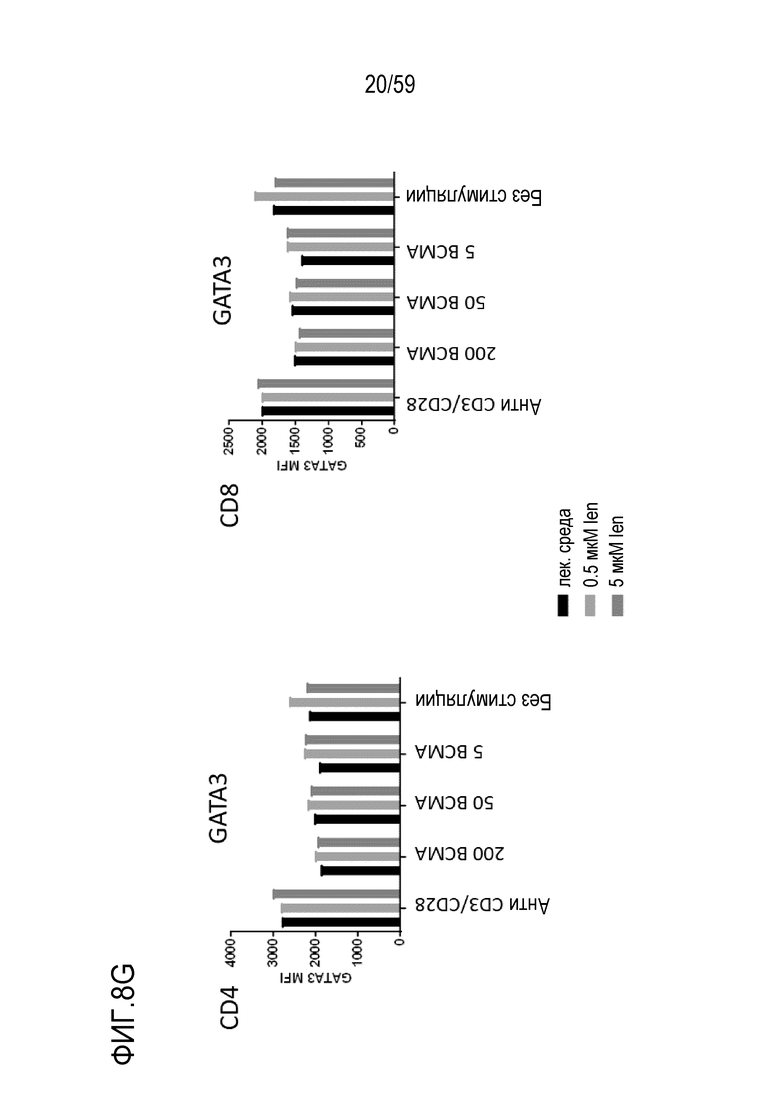
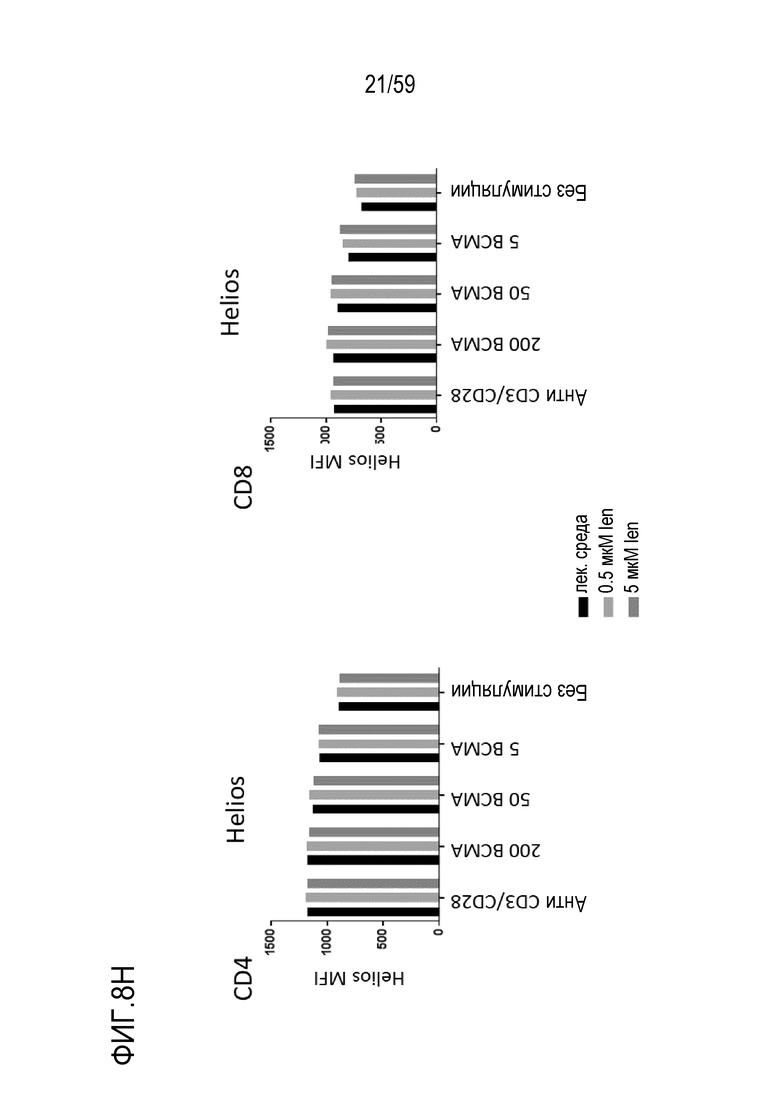
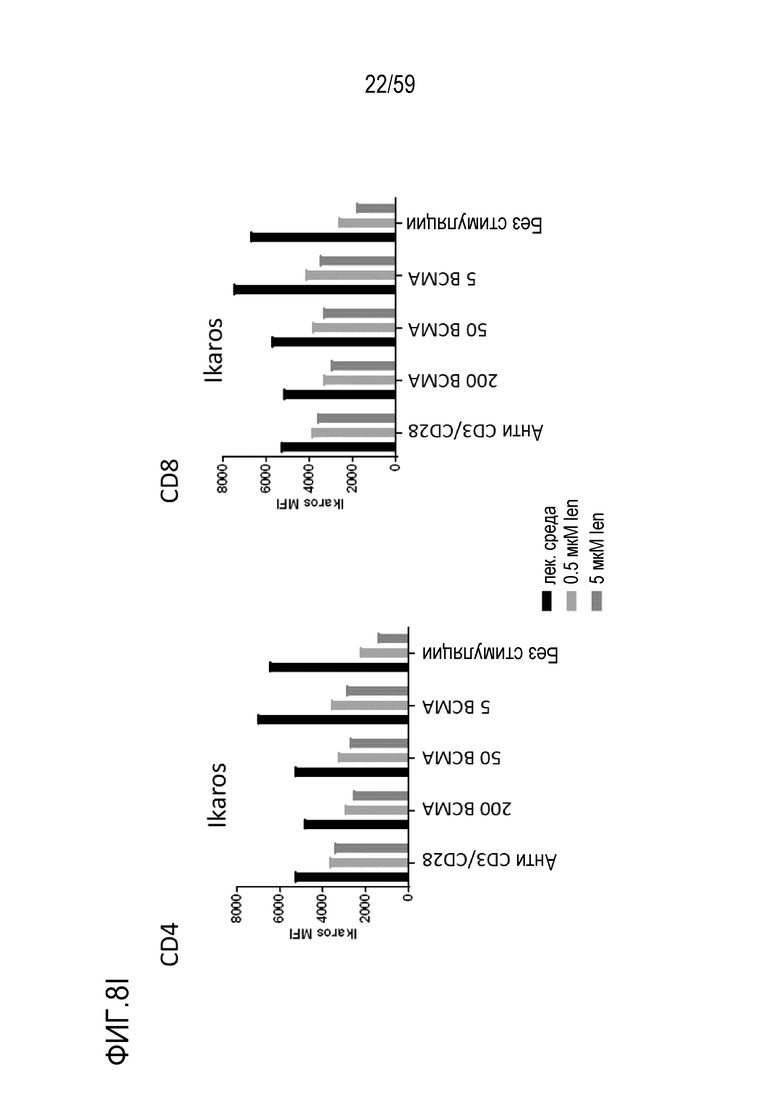
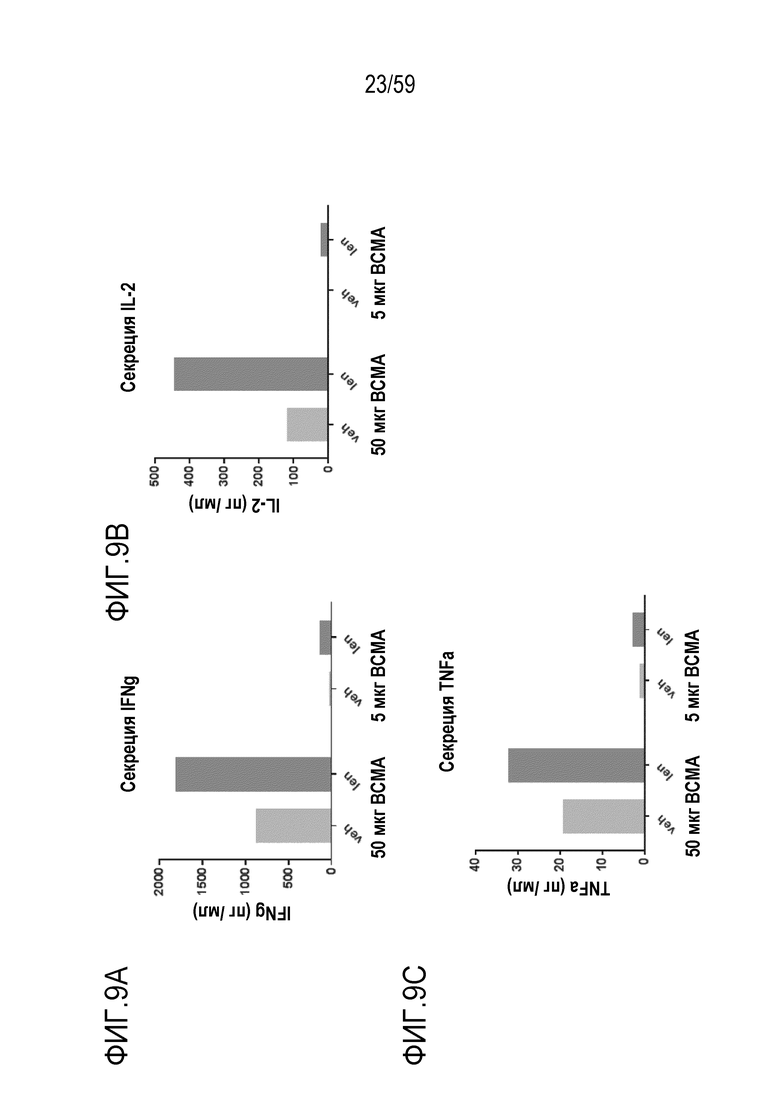
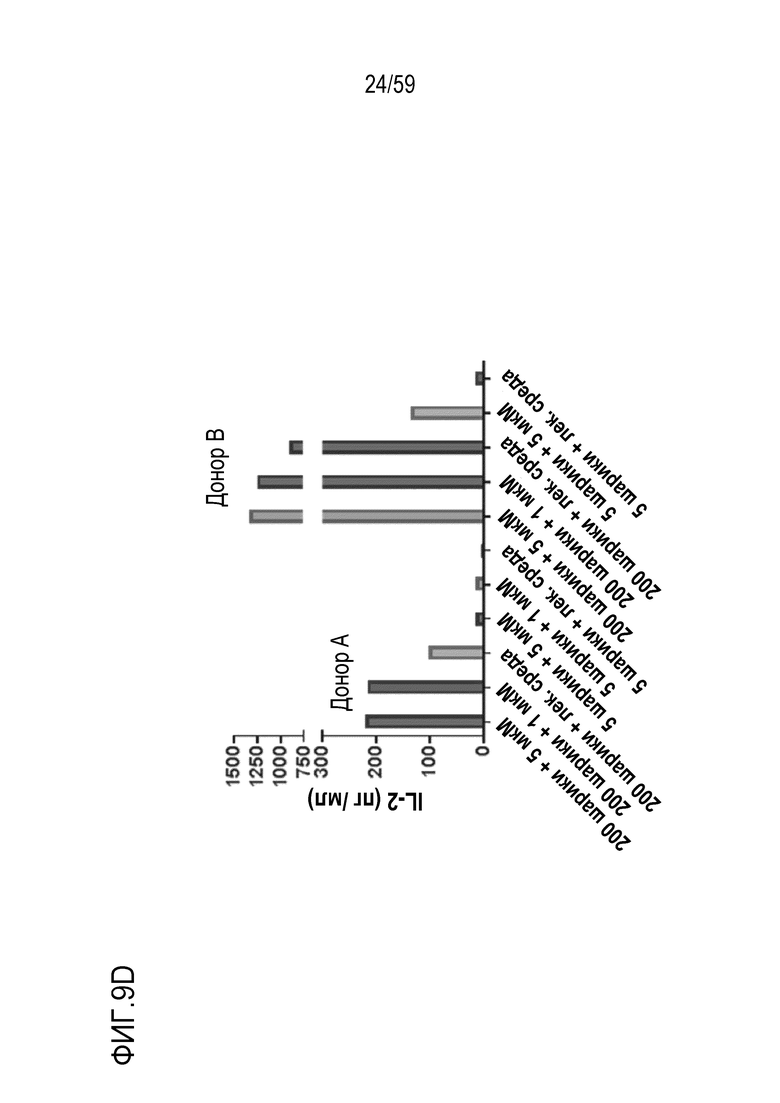
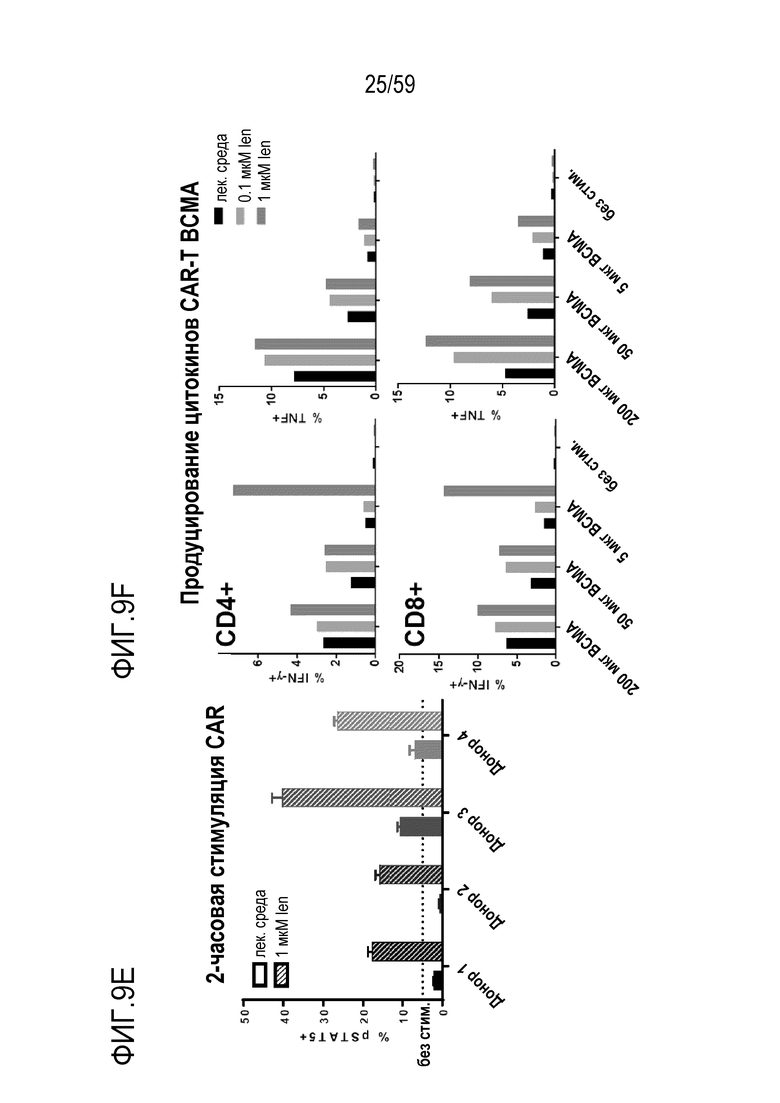
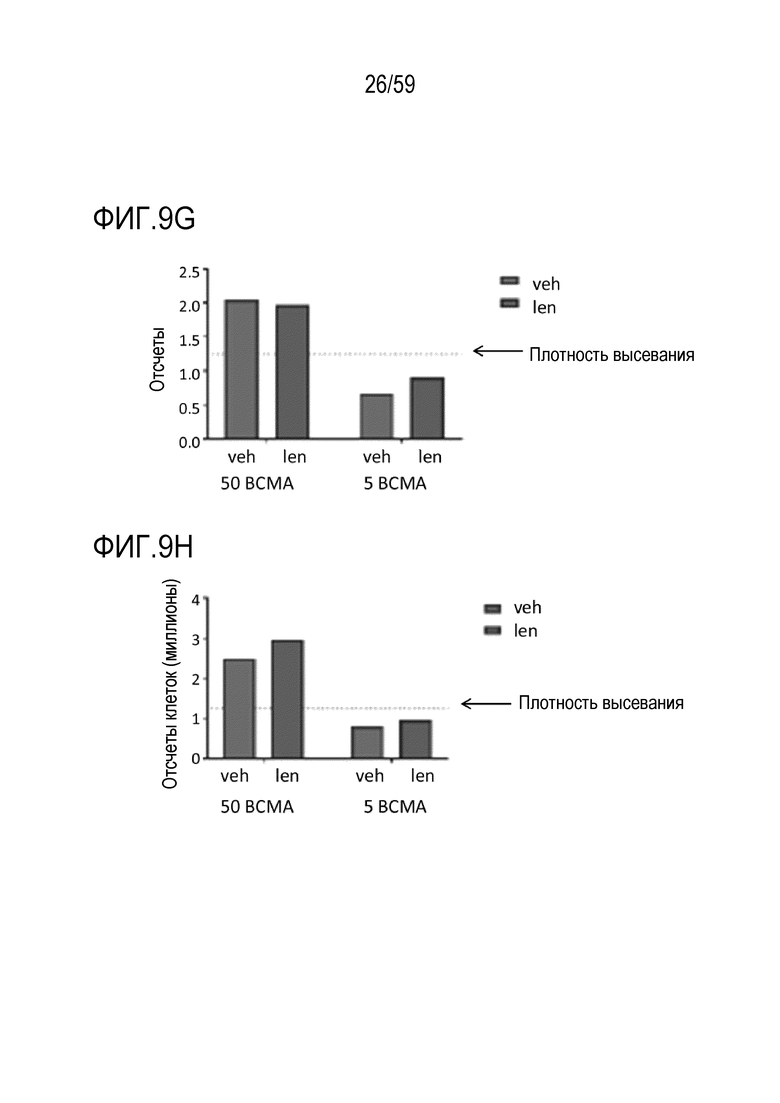
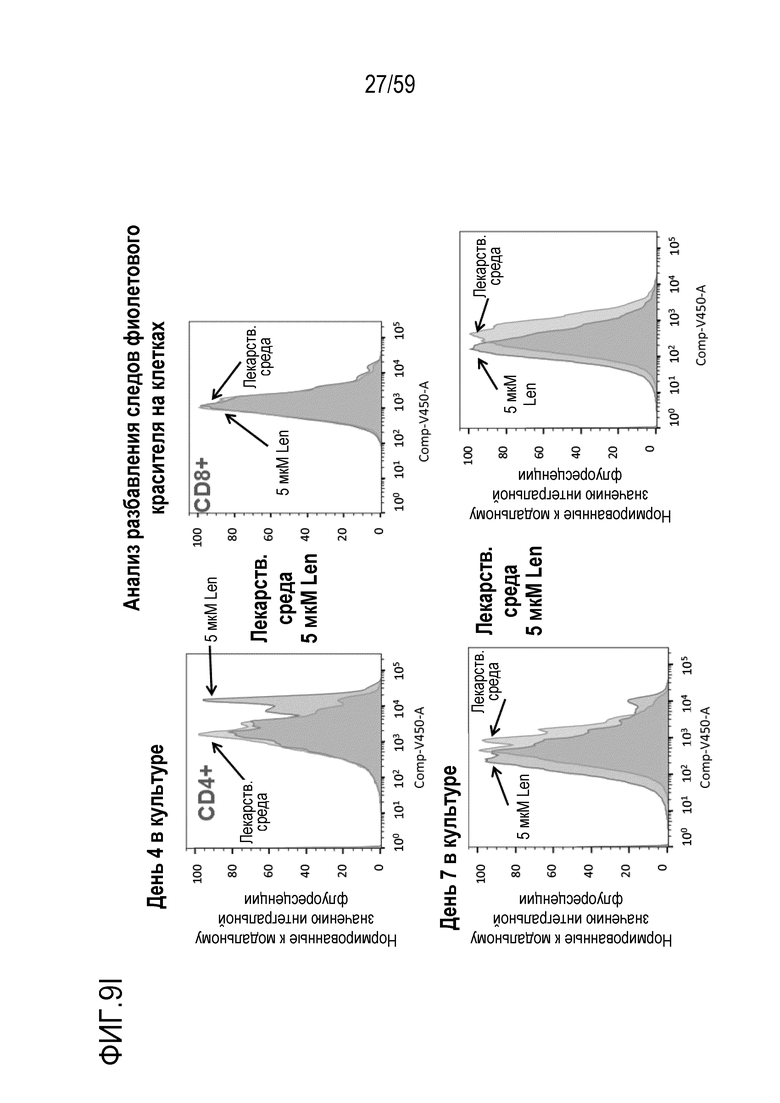
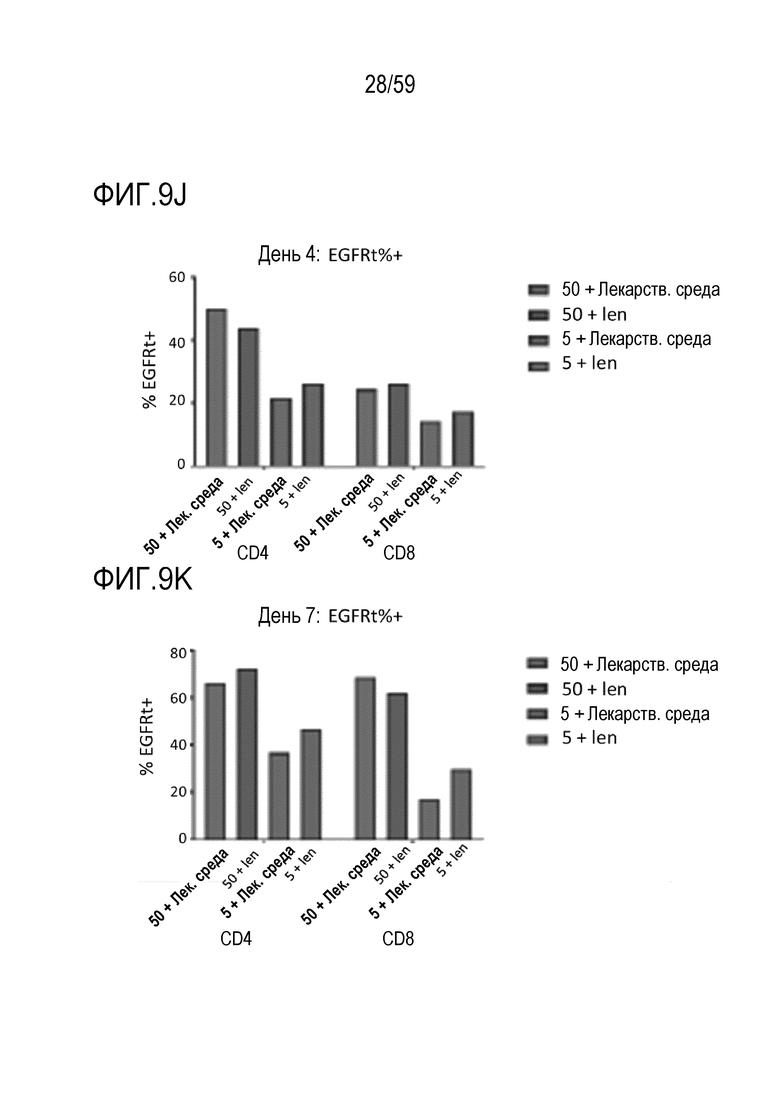
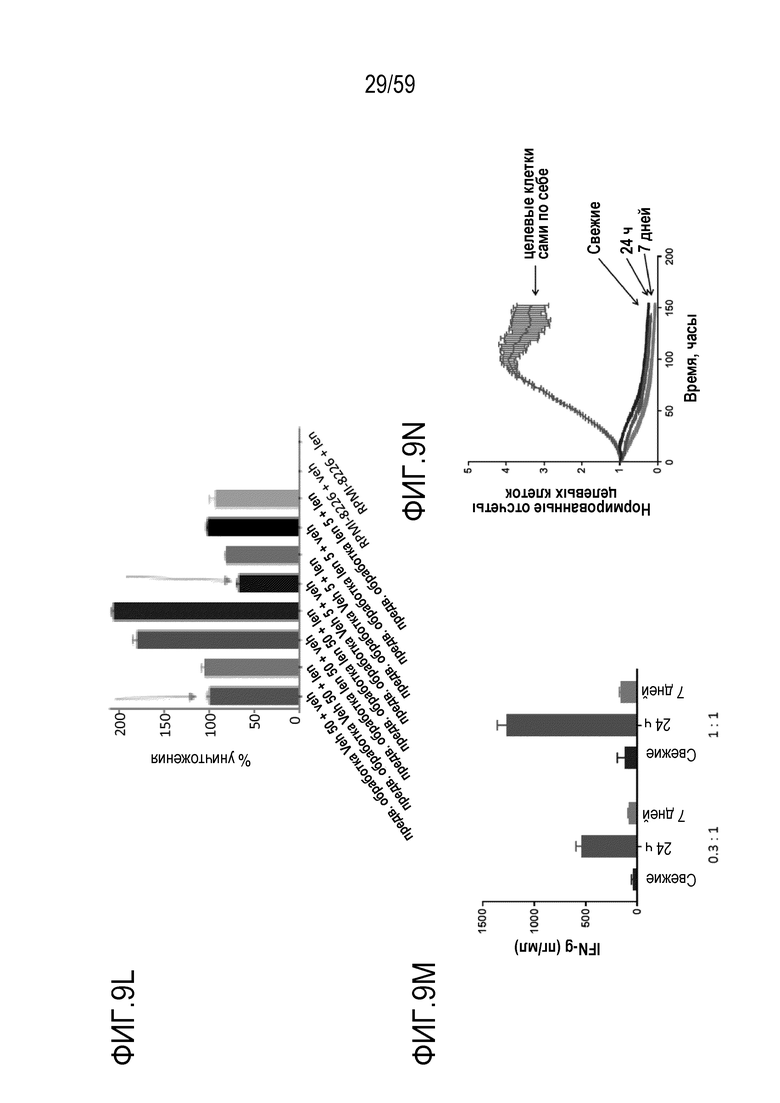

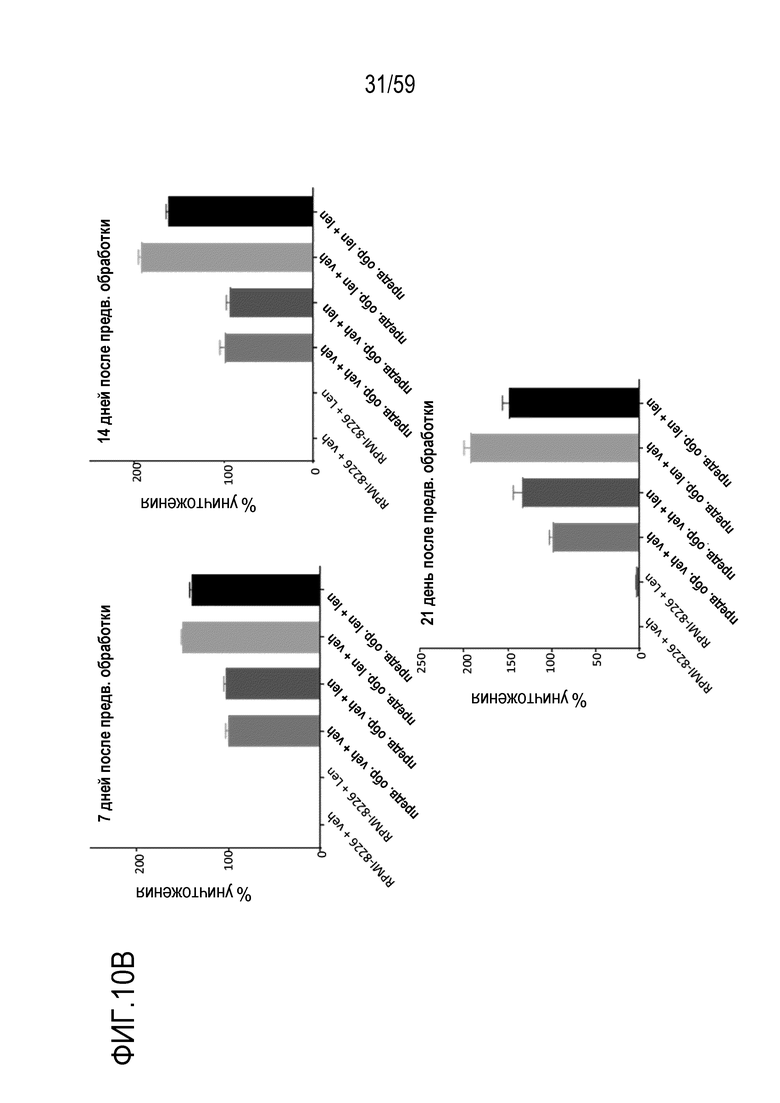
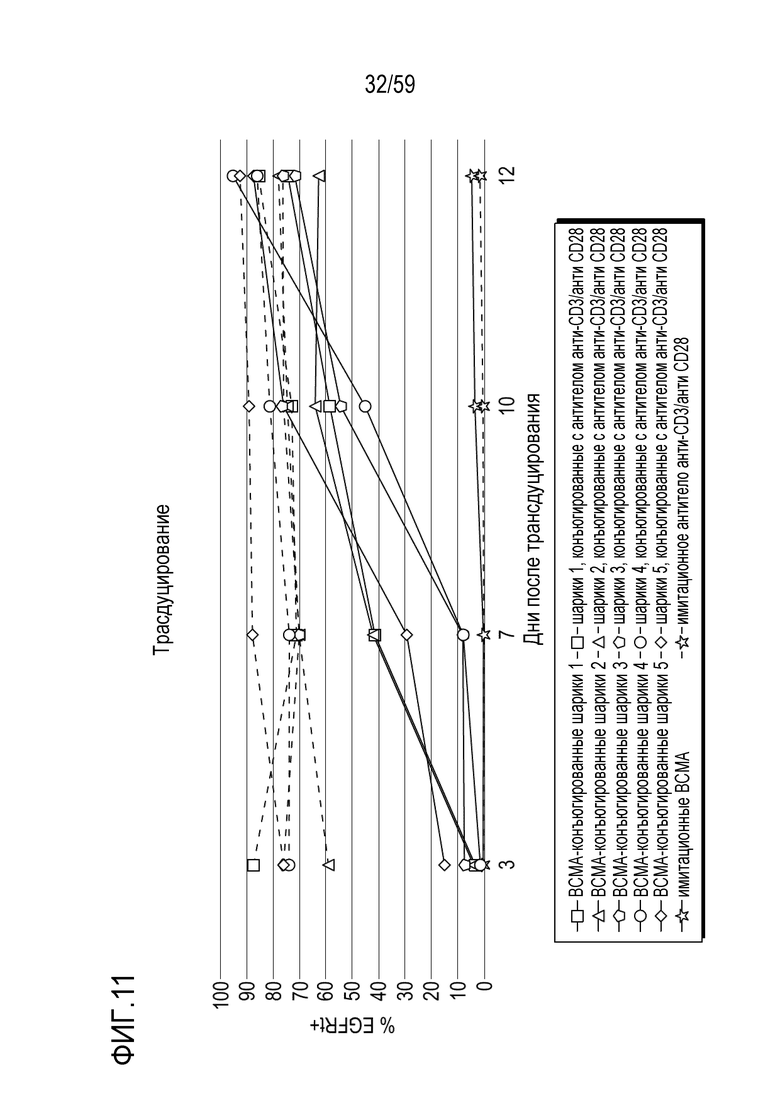
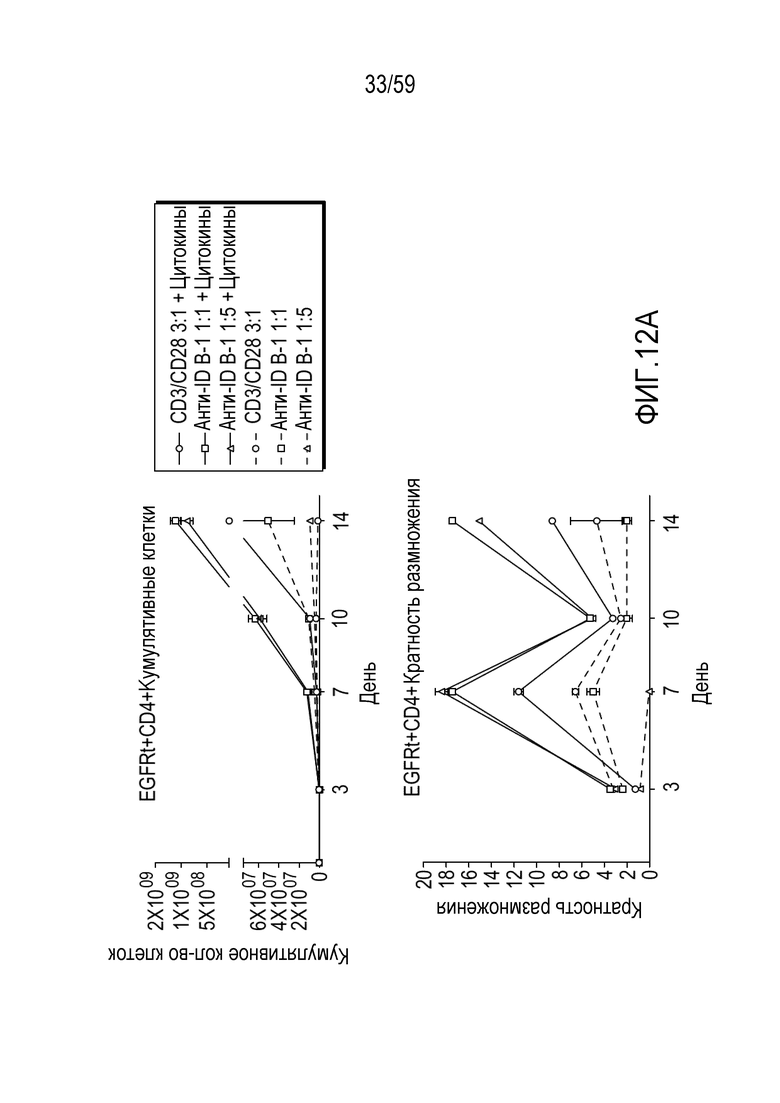
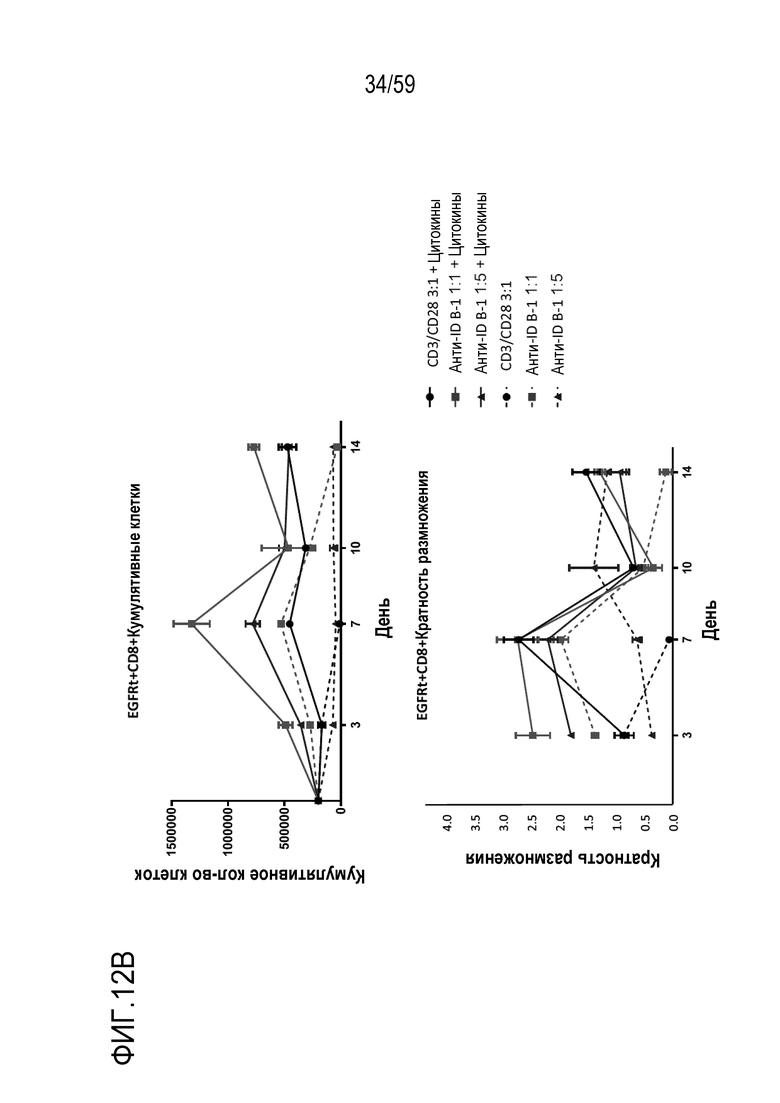
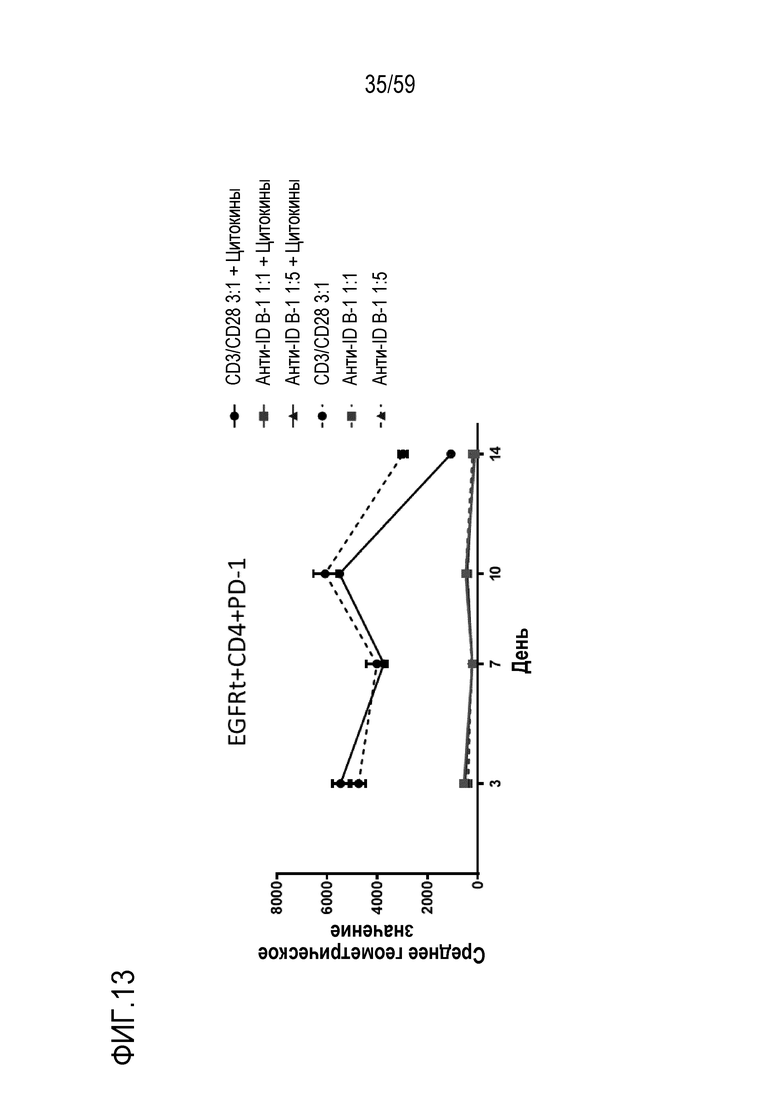
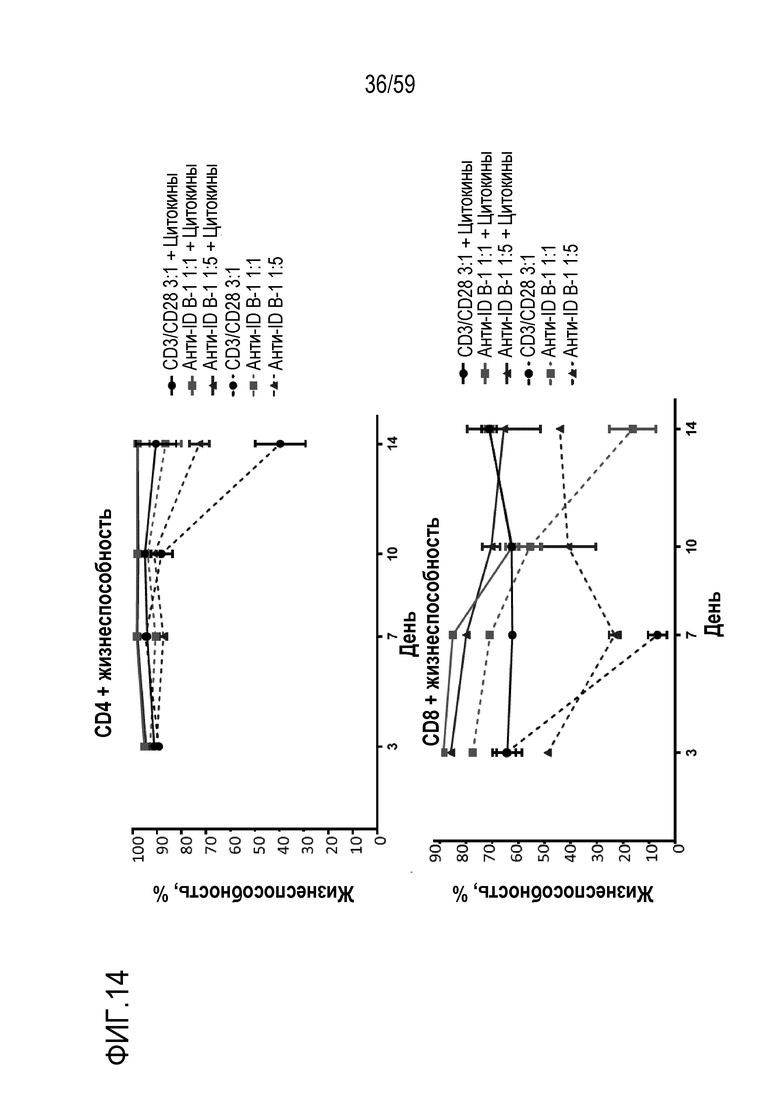
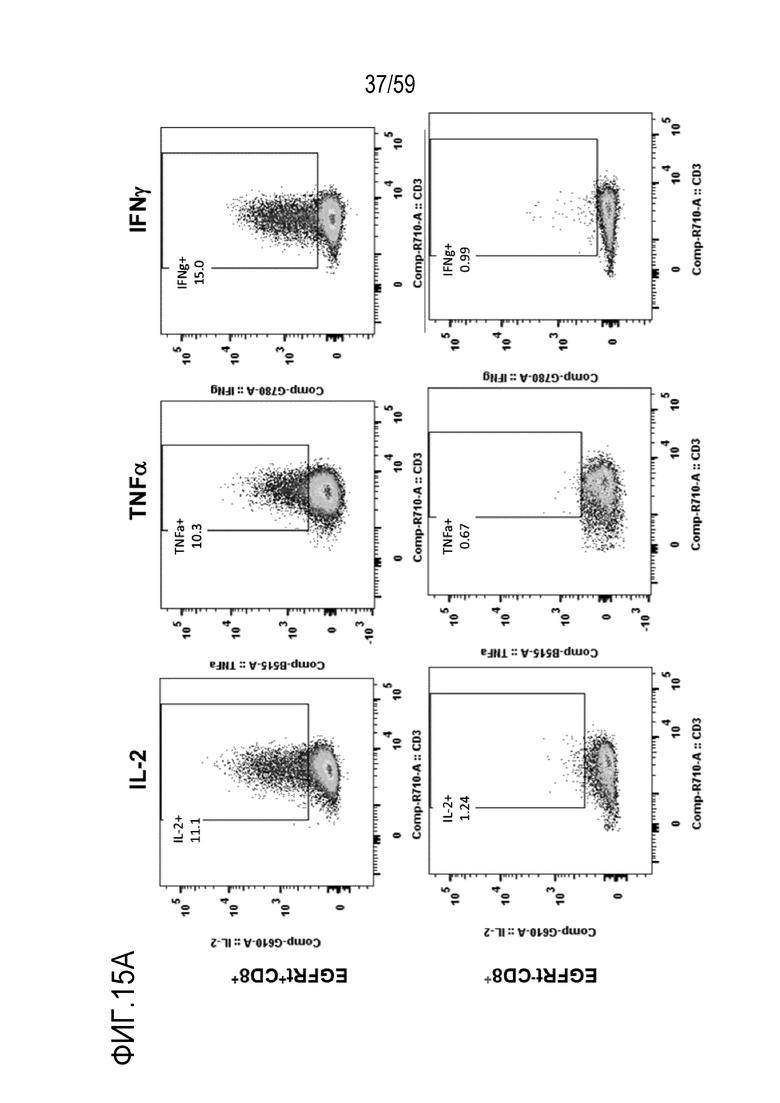
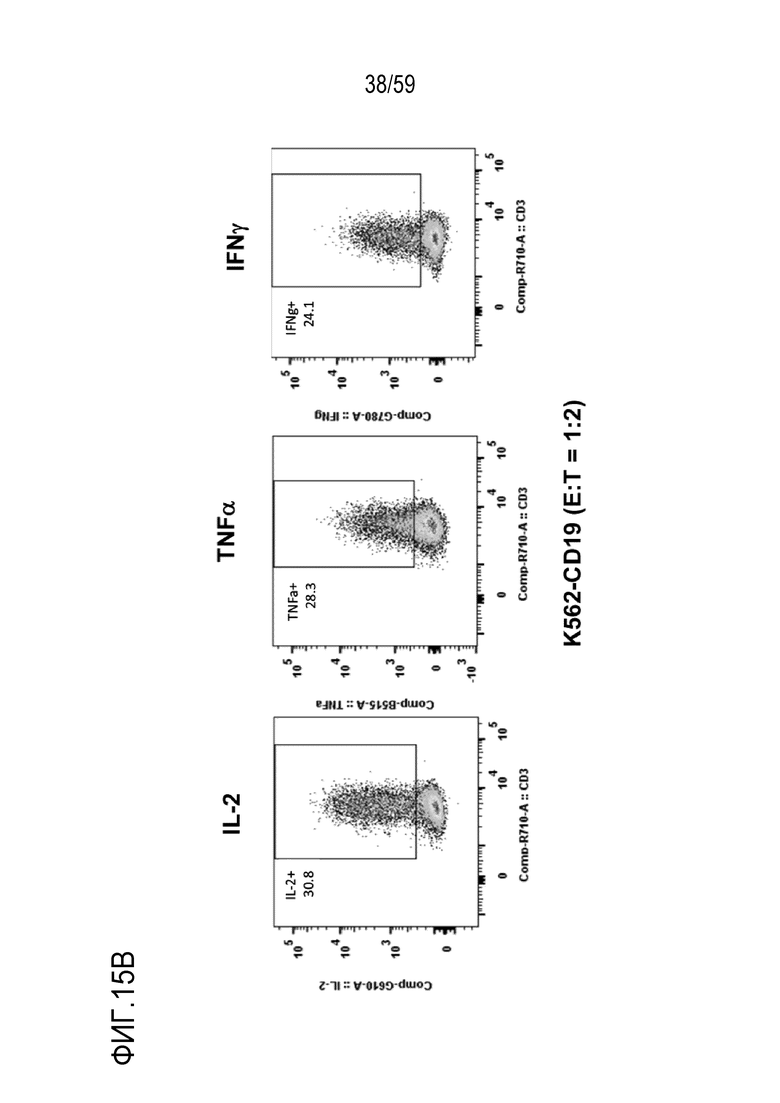
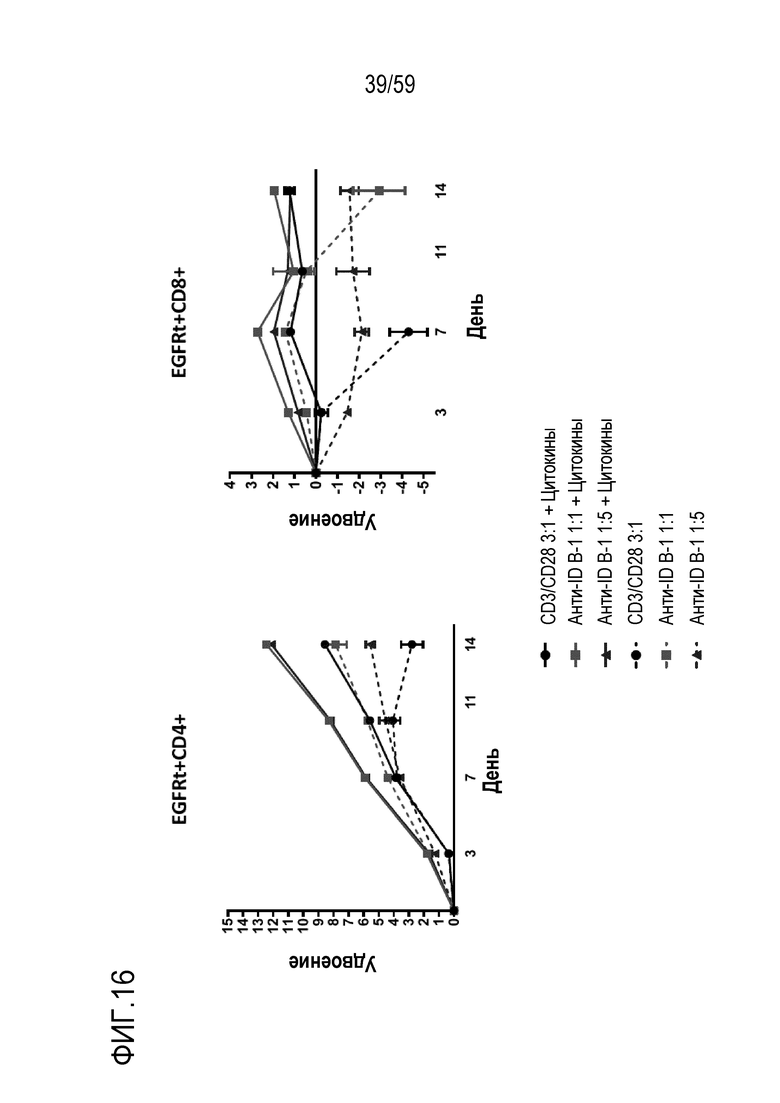
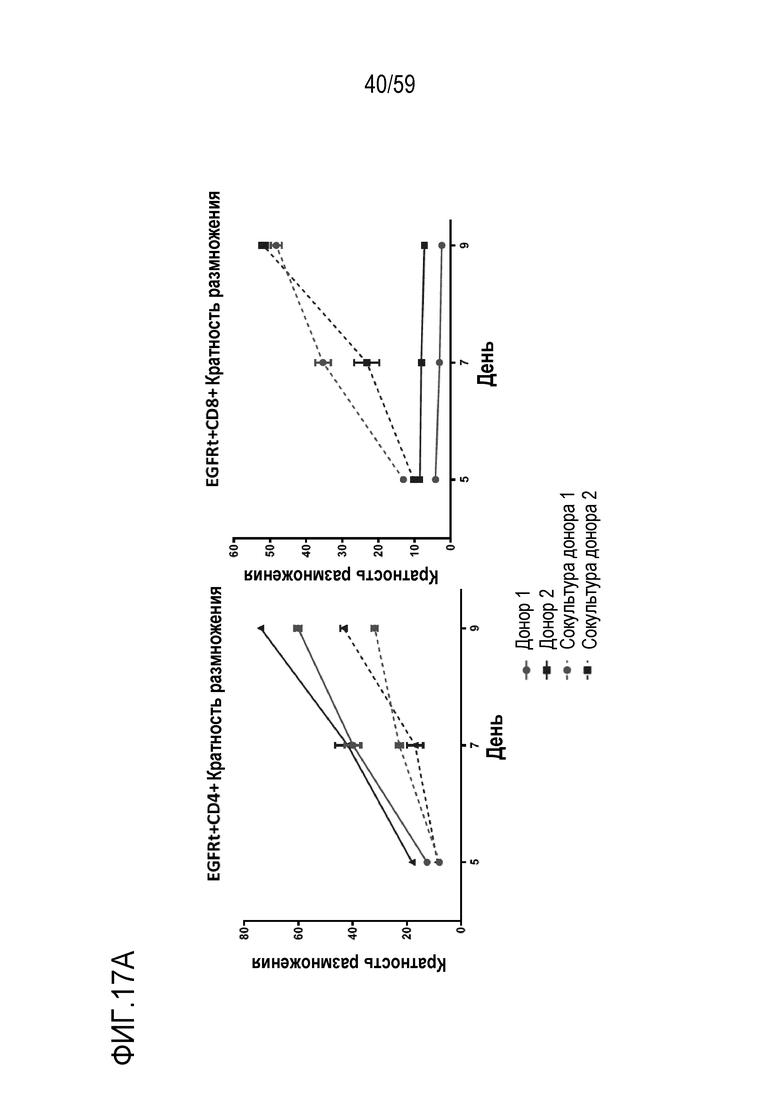
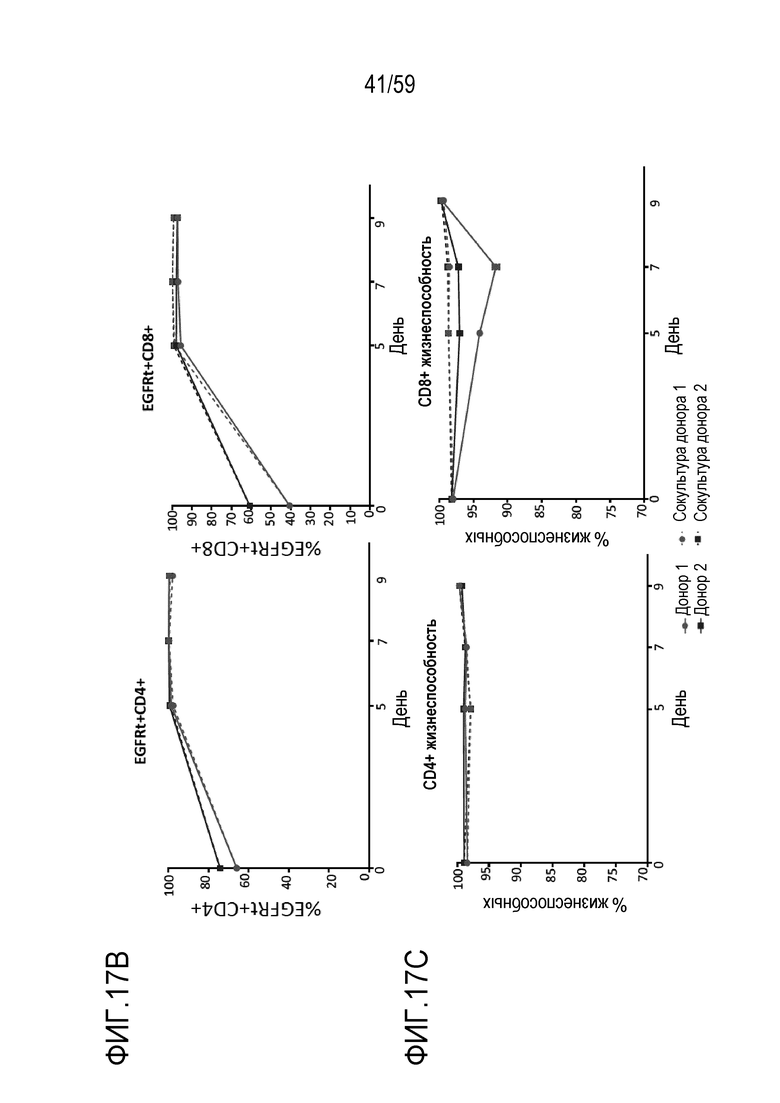
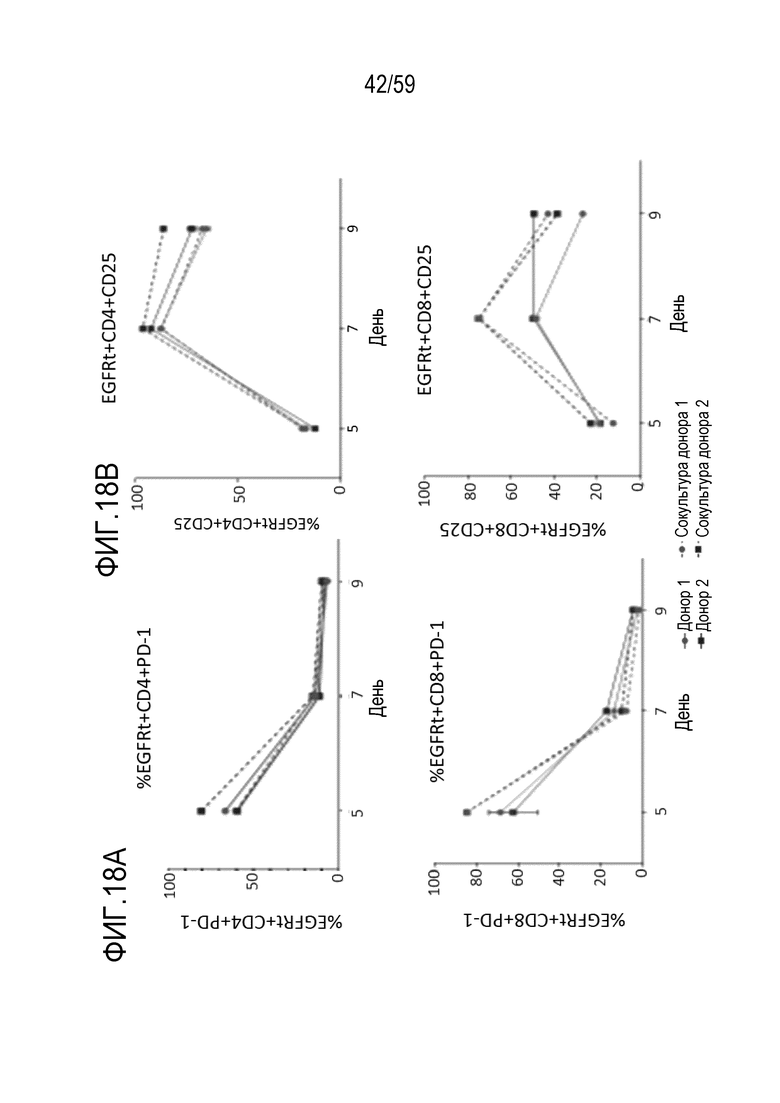
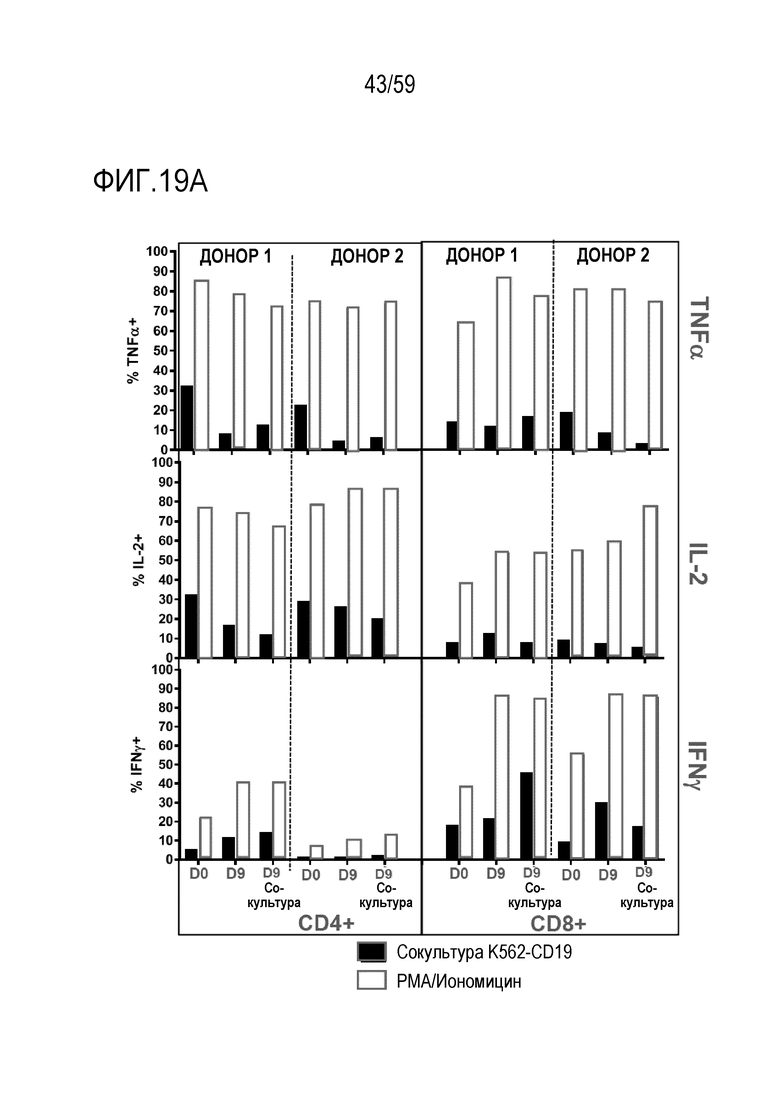
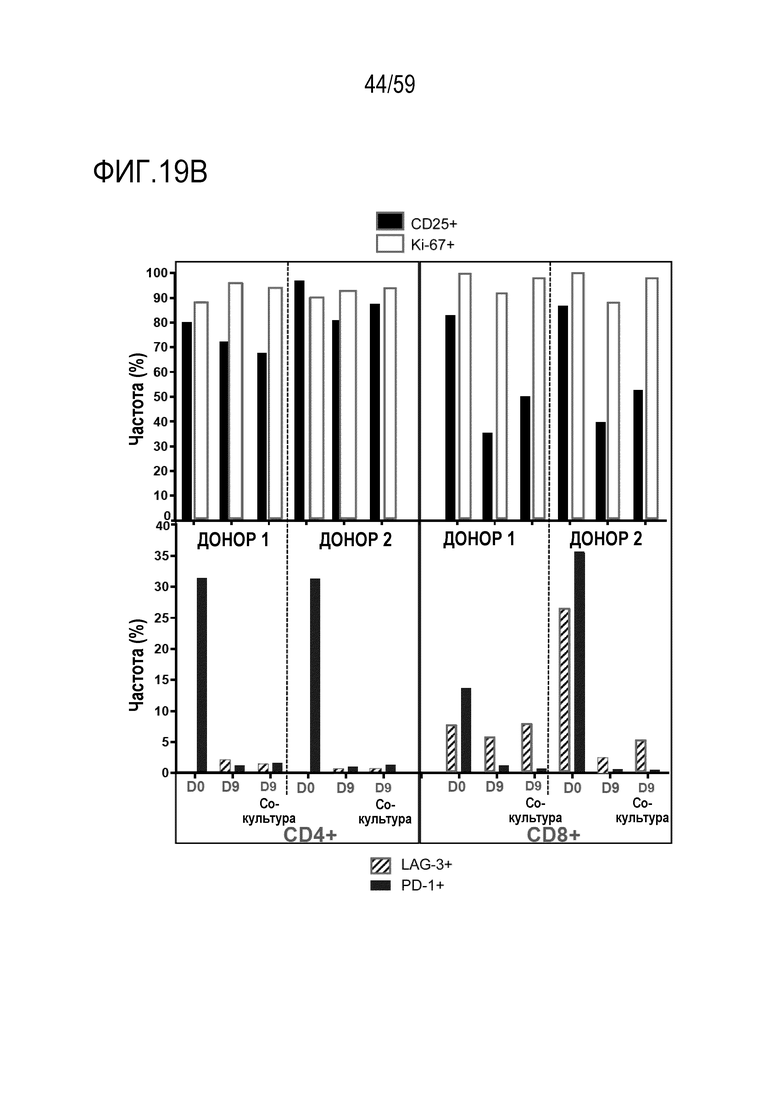
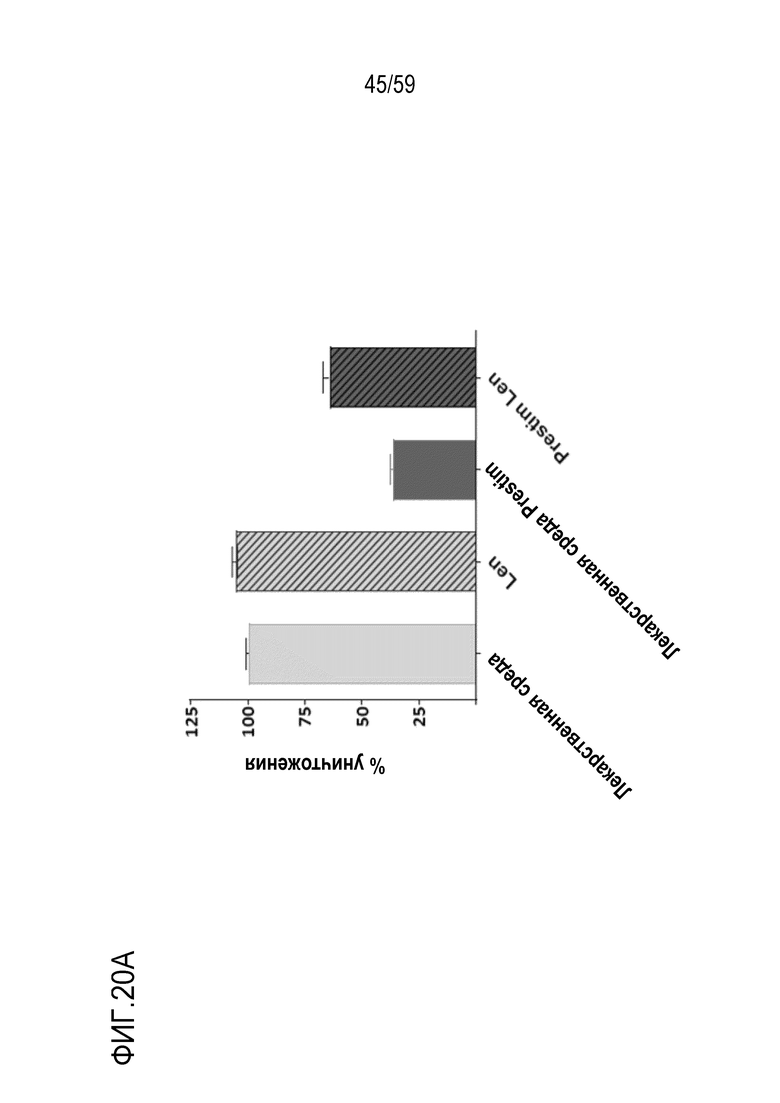
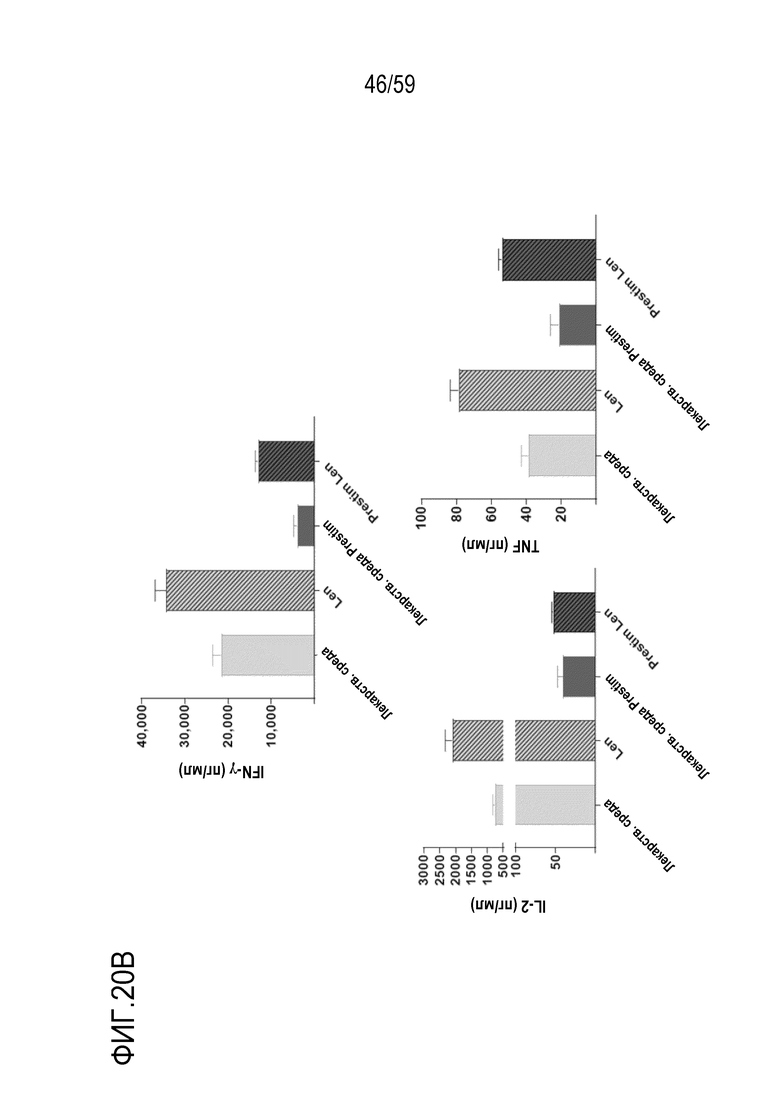
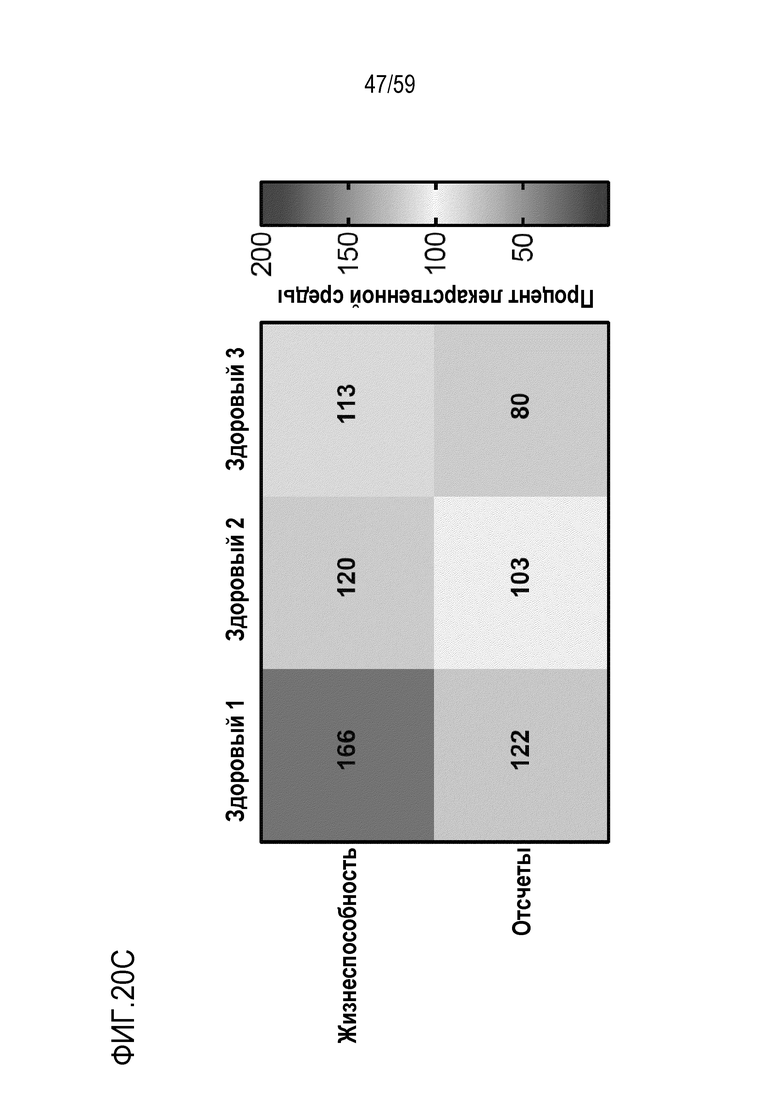
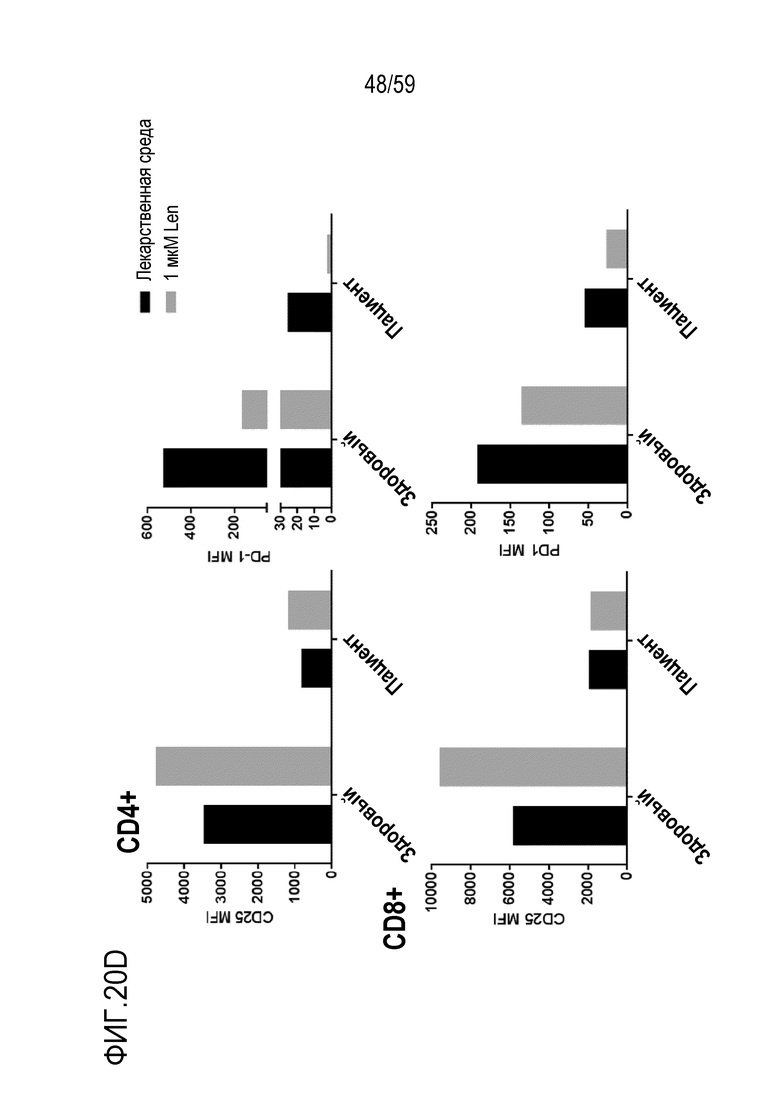
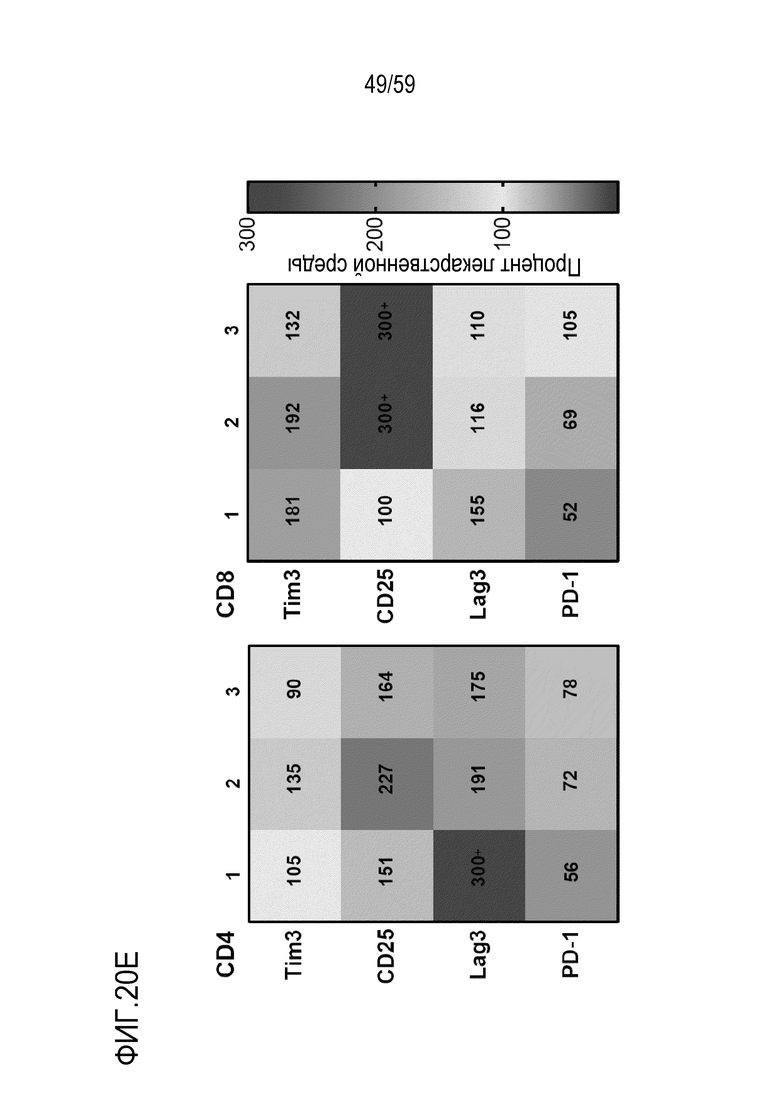
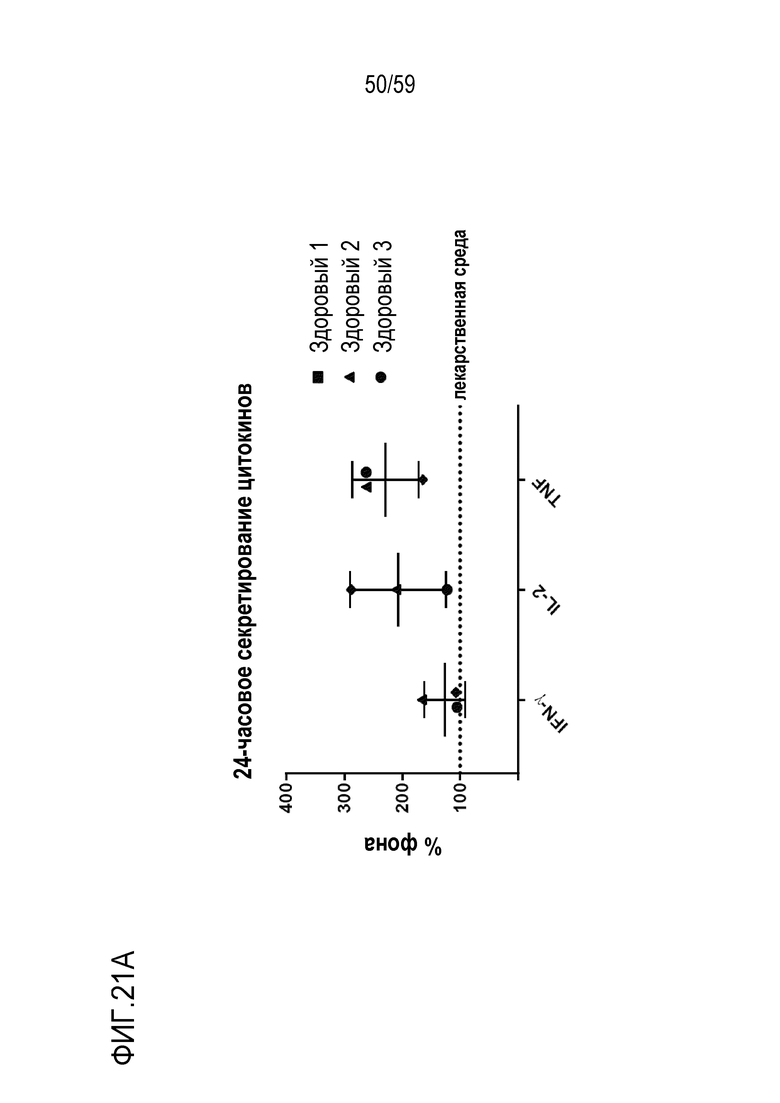
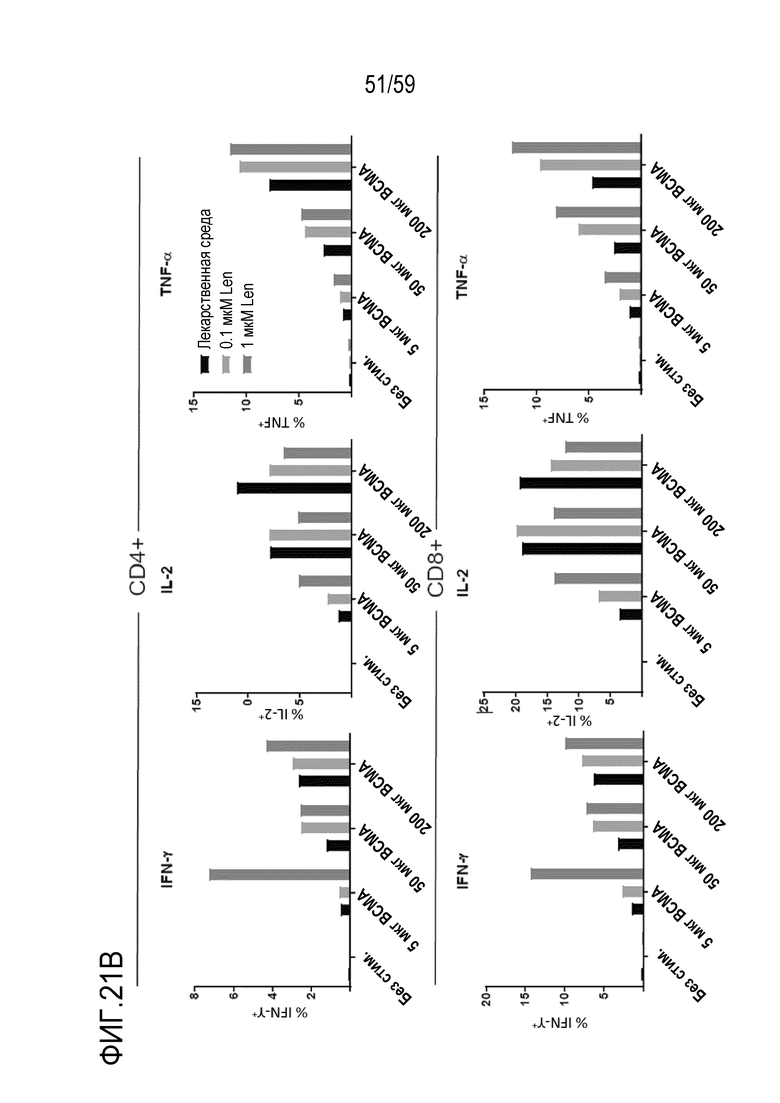
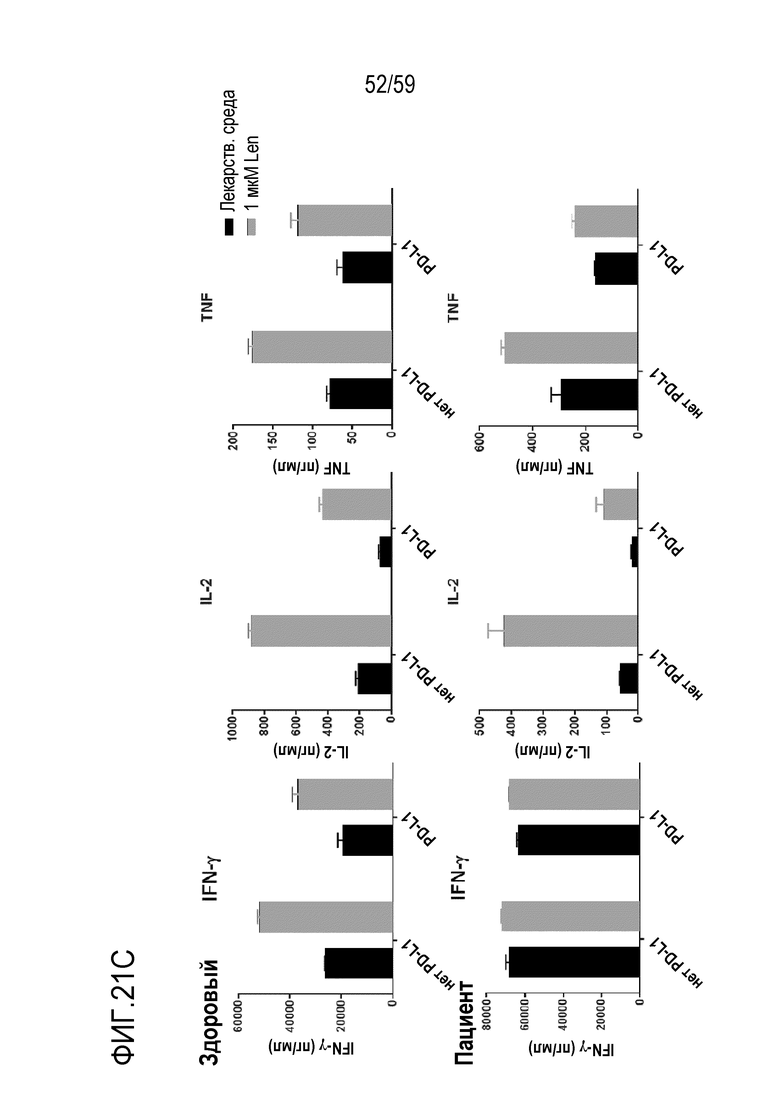
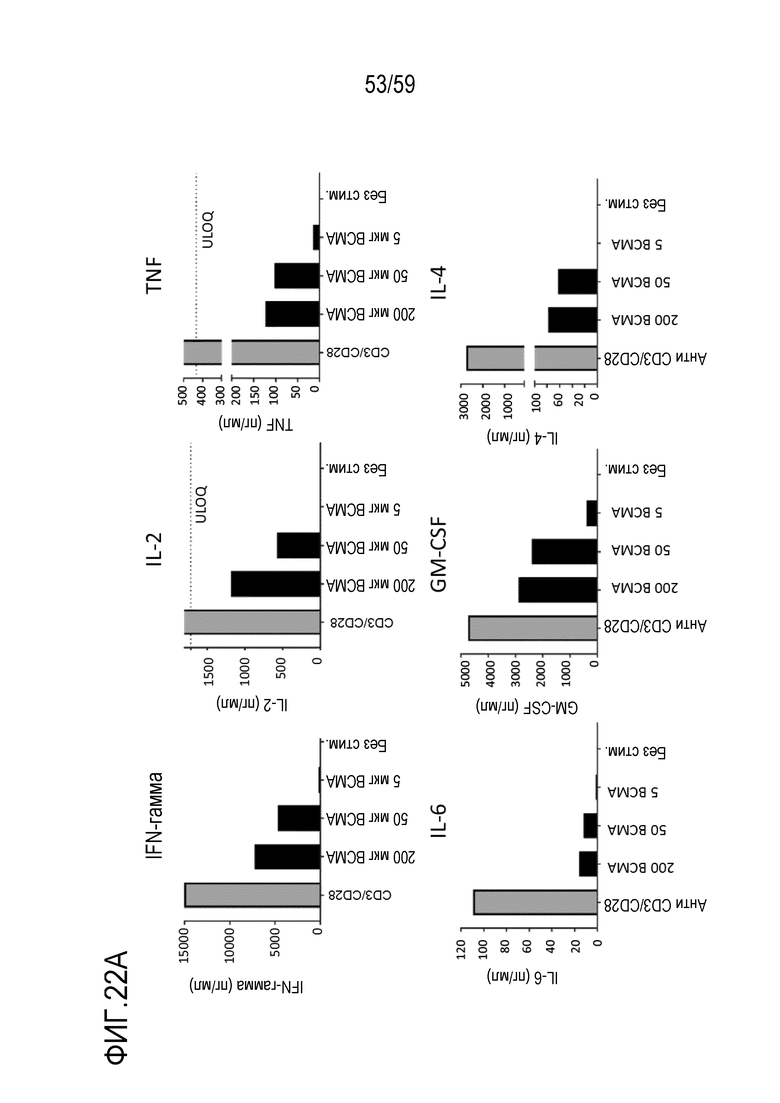
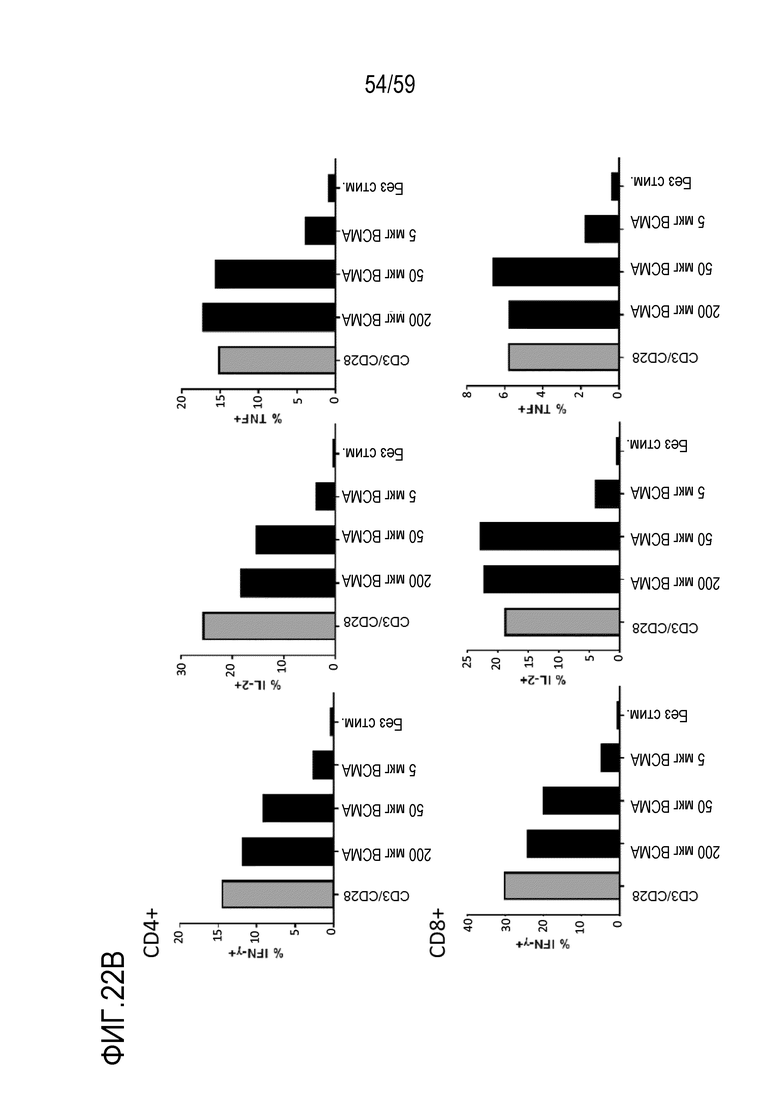
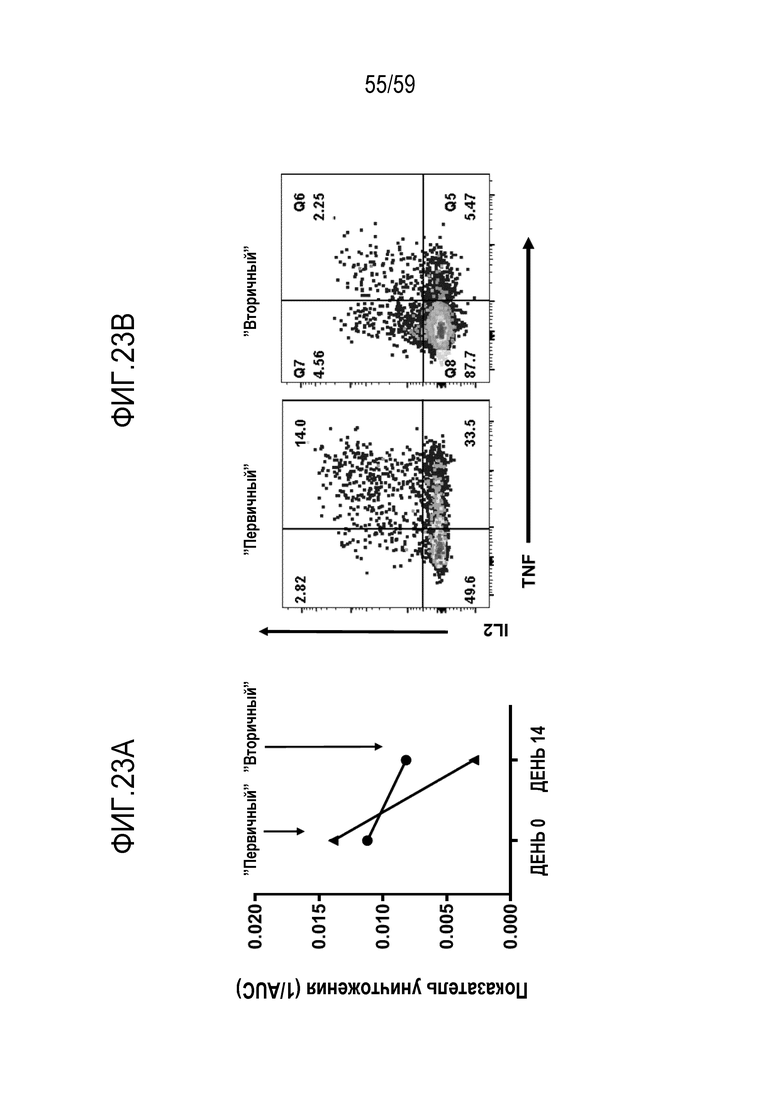
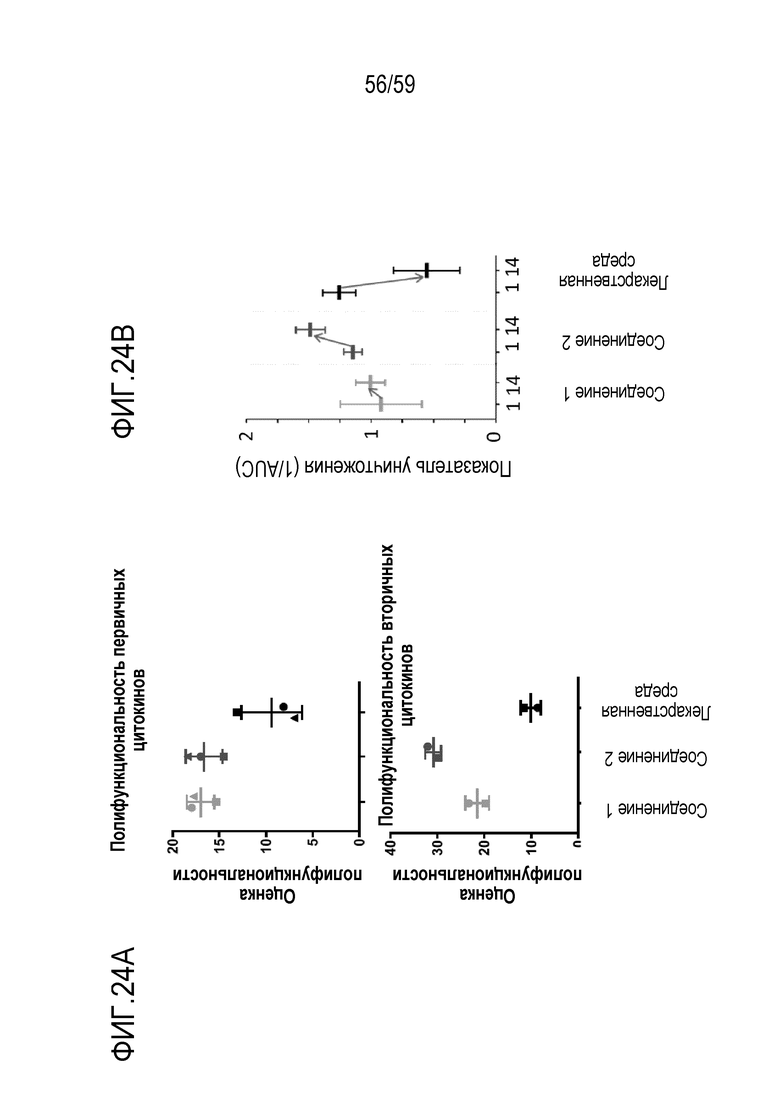
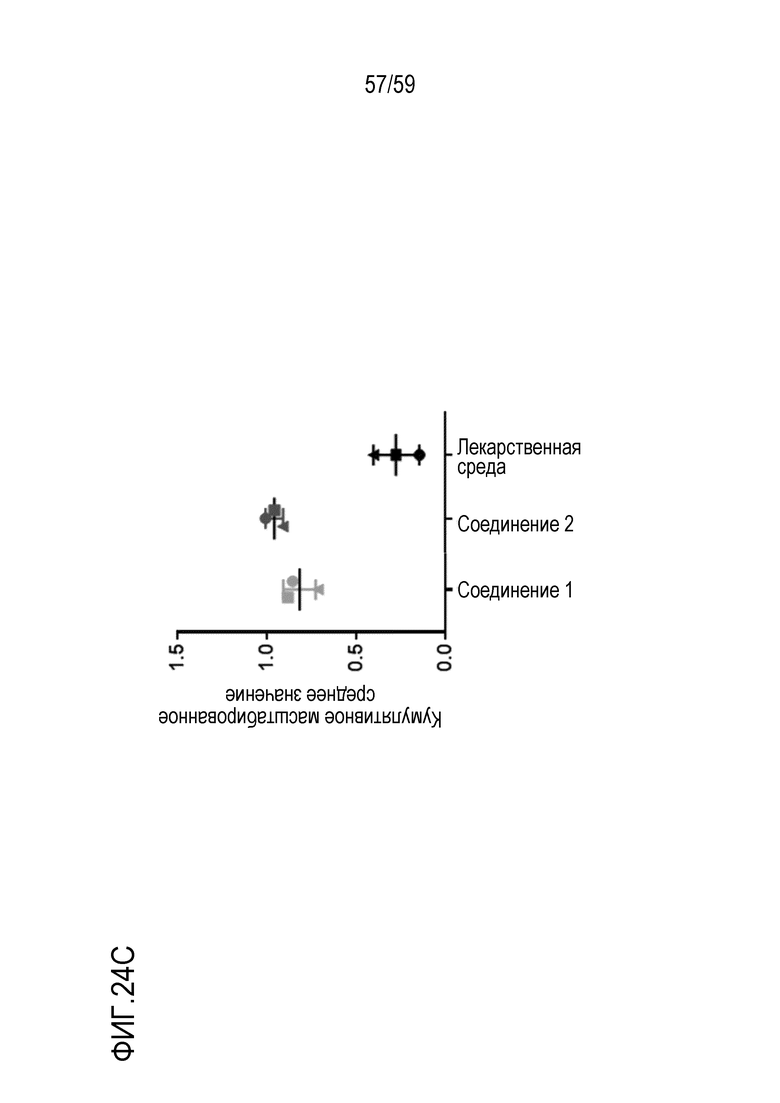
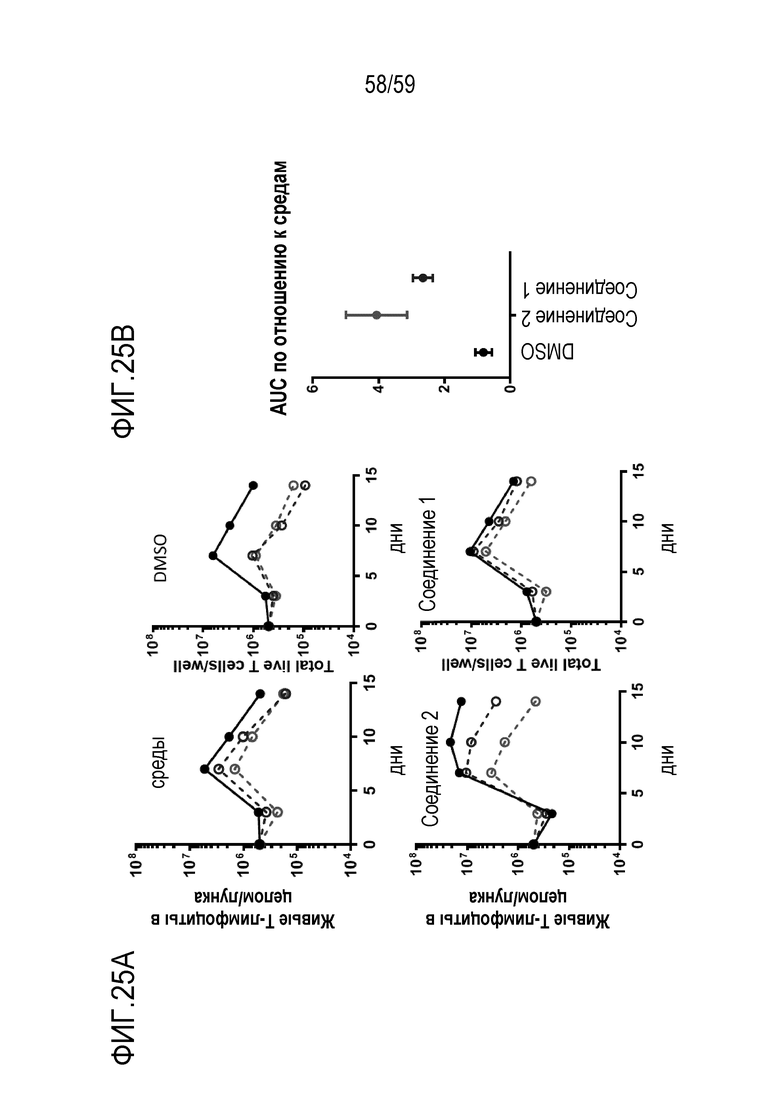
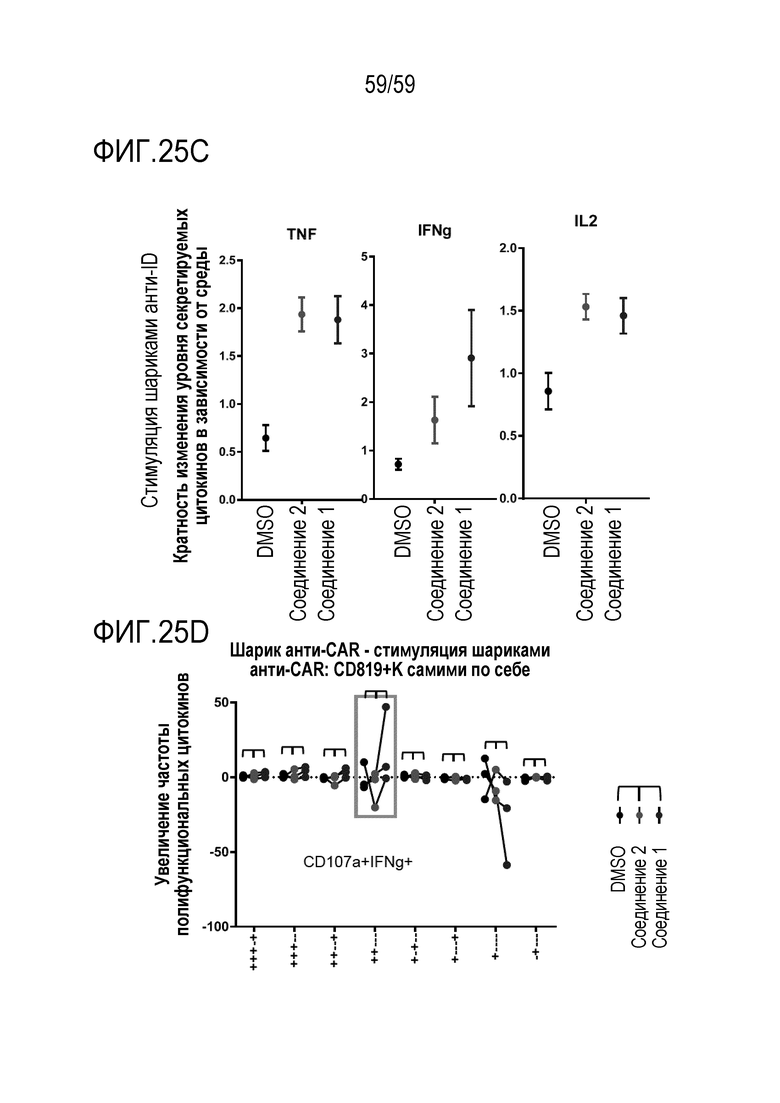
Изобретение относится к области биотехнологии, в частности к поверхностно-модифицированной частице, содержащей частицу, которая представляет собой шарик, имеющий диаметр в пределах между или примерно между 2 мкм и 5 мкм, и связывающую молекулу, присоединенную к поверхности шарика, а также к содержащей ее композиции и набору. Также раскрыты способ размножения клеток, способ генной инженерии клеток, способ селекции клетки и способ обогащения клетки, предусматривающие использование вышеуказанной частицы. Изобретение эффективно для стимуляции клеток. 13 н. и 40 з.п. ф-лы, 25 ил., 5 табл., 21 пр.
1. Поверхностно-модифицированная частица для стимуляции клеток, содержащая (i) частицу, которая представляет собой шарик, имеющий диаметр в пределах между или примерно между 2 мкм и 5 мкм, и (ii) связывающую молекулу, присоединенную к поверхности шарика, где:
связывающая молекула специфично связывается с внеклеточным антигенсвязывающим доменом химерного рецептора антигена (CAR), где антиген, распознаваемый антигенсвязывающим доменом, представляет собой домен BCMA; и
связывающая молекула представляет собой рекомбинантный антиген BCMA-Fc или представляет собой его часть, распознаваемую антигенсвязывающим доменом.
2. Поверхностно-модифицированная частица для стимуляции клеток, содержащая (i) частицу, которая представляет собой шарик, имеющий диаметр в пределах между или примерно между 2 мкм и 5 мкм, и (ii) связывающую молекулу, присоединенную к поверхности шарика, где:
связывающая молекула представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, которое специфически связывается с внеклеточным антигенсвязывающим доменом химерного рецептора антигена (CAR), где антиген, распознаваемый антигенсвязывающим доменом, представляет собой CD19 и где антигенсвязывающий домен CAR содержит:
вариабельную область тяжелой цепи (VH), содержащую последовательность аминокислот SEQ ID NO: 36, и вариабельную область легкой цепи (VL), содержащую последовательность аминокислот SEQ ID NO: 37; или
вариабельную область тяжелой цепи (VH), содержащую последовательность аминокислот SEQ ID NO: 38, и вариабельную область легкой цепи (VL), содержащую последовательность аминокислот SEQ ID NO: 39; и
частица дополнительно содержит по меньшей мере один агент, присоединенный к поверхности частицы, где по меньшей мере один агент специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала.
3. Поверхностно-модифицированная частица по п. 1 или 2, где связывающая молекула не связывает или не распознает линкерную или спейсерную область химерного рецептора антигена, где указанная линкерная или спейсерная область соединяет антигенсвязывающий домен с трансмембранным доменом рецептора антигена.
4. Поверхностно-модифицированная частица по п. 1, где связывающая молекула представляет собой слитый полипептид, содержащий рекомбинантный антиген или его часть, связанную с остатком, где остаток облегчает присоединение к частице.
5. Поверхностно-модифицированная частица по п. 4, где:
остаток связывается с C-концом рекомбинантного антигена; и/или
остаток представляет собой или содержит Fc-домен.
6. Поверхностно-модифицированная частица по п. 2 или 3, где антигенсвязывающий фрагмент представляет собой или содержит scFv.
7. Поверхностно-модифицированная частица по любому из пп. 2, 3 и 6, где:
антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит по меньшей мере часть константной области иммуноглобулина; и/или
антиидиотипическое антитело или его антигенсвязывающий фрагмент содержит по меньшей мере часть Fc-области или часть Fc, содержащую домены CH2 и CH3; и/или
антиидиотипическое антитело или его антигенсвязывающий фрагмент представляет собой интактное антитело или полноразмерное антитело.
8. Поверхностно-модифицированная частица по любому из пп. 1-7, где:
связывающая молекула присоединена к частице на С-концевом аминокислотном остатке связывающей молекулы или вблизи него; и/или
связывающая молекула ковалентно присоединена к частицам; и/или
связывающая молекула ковалентно присоединена к частице посредством поверхностно экспонируемой функциональной группы, выбранной из аминогруппы, карбоксильной группы, тиольной группы, альдегидной группы, хлорметильной группы, эпоксигруппы, гидроксильной группы, тозильной группы или гидразиновой группы.
9. Поверхностно-модифицированная частица по п. 8, где связывающая молекула ковалентно присоединена к частице через поверхностно экспонируемую функционильную группу, представляющую собой тозильную группу.
10. Поверхностно-модифицированная частица по любому из пп. 1-9, где частица представляет собой синтетическую частицу, нерастворимую частицу, твердую частицу или неклеточную частицу.
11. Поверхностно-модифицированная частица по любому из пп. 1-10, где частица имеет диаметр, равный или примерно равный 2,8 мкм или 4,5 мкм.
12. Поверхностно-модифицированная частица по любому из пп. 1-11, где:
частица представляет собой или содержит стекло, диоксид кремния, сложные полиэфиры гидроксикарбоновых кислот, полиангидриды дикарбоновых кислот, сополимеры гидроксикарбоновых кислот, сополимеры дикарбоновых кислот или металл.
13. Поверхностно-модифицированная частица по любому из пп. 1-12, где частица содержит поверхность, содержащую полимер, полисахарид, диоксид кремния, жирную кислоту, углерод или их сочетание.
14. Поверхностно-модифицированная частица по п. 13, где частица содержит поверхность, содержащую полимер, который представляет собой полиэтиленгликоль, сополимер молочная кислота - гликолевая кислота, полиглутаральдегид, полиуретан, полистирол и поливиниловый спирт или их сочетания.
15. Поверхностно-модифицированная частица по любому из пп. 1-14, где частица имеет гидрофобную поверхность.
16. Поверхностно-модифицированная частица по любому из пп. 1-15, где частица имеет полистирольную поверхность.
17. Поверхностно-модифицированная частица по любому из пп. 1-16, где частица является магнитной и/или содержит магнитную сердцевину, парамагнитную сердцевину или суперпарамагнитную сердцевину.
18. Поверхностно-модифицированная частица по любому из пп. 1-17, где частица содержит по меньшей мере или примерно по меньшей мере 10 копий, 102 копий, 103 копий, 104 копий, 105 копий или 106 копий связывающей молекулы.
19. Поверхностно-модифицированная частица по п. 1, где частица дополнительно содержит по меньшей мере один агент, присоединенный к поверхности частицы, где по меньшей мере один агент специфично связывается с дополнительной молекулой на клетке для обеспечения дополнительного сигнала и/или для блокировки ингибиторного сигнала.
20. Поверхностно-модифицированная частица по любому из пп. 2, 3 и 6-19, где:
по меньшей мере один агент представляет собой лиганд или представляет собой антитело или его антигенсвязывающий фрагмент; и/или
по меньшей мере один агент ковалентно присоединен к частице; и/или
соотношение связывающей молекулы и по меньшей мере одного агента, удерживаемого частицей, составляет или составляет примерно 1:1.
21. Поверхностно-модифицированная частица по п. 2 или 19, где:
дополнительная молекула представляет собой костимуляторную молекулу или активирующий корецептор; или
дополнительная молекула представляет собой OX-40, ICOS, DAP10, B7-1, B7-2, CD28 или 4-1BB; или
дополнительная молекула представляет собой ингибиторный рецептор; или
дополнительная молекула представляет собой CTLA-4, PD-1, LAG-3, Tim-3, BTLA или TIGIT; или
дополнительная молекула представляет собой поверхностный белок Т-лимфоцита; или
дополнительная молекула представляет собой CD2, CD3 или CD28.
22. Поверхностно-модифицированная частица по п. 21, где частица содержит одно или оба антитела из антитела анти-CD2 и антитела анти-CD28.
23. Композиция для стимуляции клеток, содержащая множество поверхностно-модифицированных частиц по любому из пп. 1, 4, 5 и 8-22.
24. Композиция по п. 23, где:
концентрация связывающей молекулы в композиции находится в пределах между или примерно между 0,5 мкг/мл и 500 мкг/мл, 1 мкг/мл и 200 мкг/мл или 5 мкг/мл и 100 мкг/мл; или
концентрация связывающей молекулы в композиции составляет по меньшей мере или по меньшей мере примерно 1 мкг/мл, 5 мкг/мл, 10 мкг/мл, 25 мкг/мл, 50 мкг/мл, 100 мкг/мл или 200 мкг/мл.
25. Композиция по п. 23 или 24, где:
множество поверхностно-модифицированных частиц имеет средний диаметр в пределах между или примерно между 2 мкм и 5 мкм; или
множество поверхностно-модифицированных частиц имеет среднюю плотность в пределах между или примерно между 1 г/см3 и примерно 2 г/см3.
26. Композиция для стимуляции клеток, содержащая множество поверхностно-модифицированных частиц по любому из пп. 2, 3 и 6-22.
27. Композиция по п. 26, где:
концентрация связывающей молекулы в композиции находится в пределах между или примерно между 0,5 мкг/мл и 500 мкг/мл, 1 мкг/мл и 200 мкг/мл или 5 мкг/мл и 100 мкг/мл; или
концентрация связывающей молекулы в композиции составляет по меньшей мере или по меньшей мере примерно 1 мкг/мл, 5 мкг/мл, 10 мкг/мл, 25 мкг/мл, 50 мкг/мл, 100 мкг/мл или 200 мкг/мл.
28. Композиция по п. 26 или 27, где:
множество поверхностно-модифицированных частиц имеет средний диаметр в пределах между или примерно между 2 мкм и 5 мкм; или
множество поверхностно-модифицированных частиц имеет среднюю плотность в пределах между или примерно между 1 г/см3 и примерно 2 г/см3.
29. Набор для стимуляции клеток, содержащий поверхностно-модифицированную частицу по любому из пп. 1, 4, 5 и 8-22 или композицию по любому из пп. 23-25 и инструкции для применения.
30. Набор по п. 29, где:
инструкции предназначены для селекции или обогащения популяции клеток, клеток, экспрессирующих химерный рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой; или
инструкции предназначены для стимуляции или размножения в популяции клеток, клеток, экспрессирующих химерный рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой.
31. Набор для стимуляции клеток, содержащий поверхностно-модифицированную частицу по любому из пп. 2, 3 и 6-22 или композицию по любому из пп. 26-28 и инструкции для применения.
32. Набор по п. 31, где:
инструкции предназначены для селекции или обогащения популяции клеток, клеток, экспрессирующих химерный рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой; или
инструкции предназначены для стимуляции или размножения в популяции клеток, клеток, экспрессирующих химерный рецептор антигена, содержащий антигенсвязывающий домен, специфично распознаваемый связывающей молекулой.
33. Способ размножения клеток, включающий инкубирование популяции клеток вместе с поверхностно-модифицированной частицей по любому из пп. 1, 4, 5 и 8-22 или с композицией по любому из пп. 23-25, где:
популяция клеток включает клетки, экспрессирующие химерный рецептор антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген; и
связывающая молекула поверхностно-модифицированной частицы или каждая из поверхностно-модифицированных частиц композиции специфически связывается или распознает внеклеточный антигенсвязывающий домен химерного рецептора антигена.
34. Способ размножения клеток, включающий инкубирование популяции клеток вместе с поверхностно-модифицированной частицей по любому из пп. 2, 3 и 6-22 или с композицией по любому из пп. 26-28, где:
популяция клеток включает клетки, экспрессирующие химерный рецептор антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген; и
связывающая молекула поверхностно-модифицированной частицы или каждая из поверхностно-модифицированных частиц композиции специфически связывается или распознает внеклеточный антигенсвязывающий домен химерного рецептора антигена.
35. Способ по п. 33, отличающийся тем, что:
внеклеточный антигенсвязывающий домен специфически связывает или распознает BCMA; и
связывающая молекула содержит внеклеточный домен BCMA или часть внеклеточного домена, распознаваемую внеклеточным антигенсвязывающим доменом.
36. Способ по п. 34, отличающийся тем, что:
внеклеточный антигенсвязывающий домен специфически связывает или распознает CD19; и
связывающая молекула представляет собой антиидиотипическое антитело или его антигенсвязывающий фрагмент, который специфически связывается с антигенсвязывающим доменом.
37. Способ по любому из пп. 33-36, отличающийся тем, что в ходе инкубирования отношение общего количества клеток в популяции к множеству частиц композиции с модифицированной поверхностью составляет от или примерно от 5:1 до 1:5, от 3:1 до 1:3 или от 2:1 до 1:2 включительно.
38. Способ по п. 37, отличающийся тем, что соотношение составляет или составляет примерно 1:1.
39. Способ по любому из пп. 33-38, отличающийся тем, что инкубирование проводят в течение более или более примерно 2 часов, 4 часов, 8 часов, 12 часов, 24 часов, 2 дней, 3 дней, 4 дней, 5 дней, 6 дней, 7 дней, 8 дней, 9 дней, 10 дней, 11 дней, 12 дней, 13 дней, 14 дней, 15 дней или 16 дней.
40. Способ по любому из пп. 33-39, отличающийся тем, что:
популяция включает иммунные клетки; и/или
популяция включает индуцированные плюрипотентные стволовые клетки (iPSC).
41. Способ по любому из пп. 33-40, где популяция включает T-клетки или NK-клетки.
42. Способ по любому из пп. 33-41, где популяция включает один или оба из CD4+ T-клеток и CD8+ T-клеток.
43. Способ по п. 42, отличающийся тем, что отношение клеток CD4+ к клеткам CD8+ составляет примерно от 1:2 до 2:1 или от 1:3 до 3:1 или равно или равно примерно 1:1.
44. Способ по любому из пп. 33-43, где популяция включает первичные клетки, полученные от человека.
45. Способ генной инженерии клетки, включающий:
(a) приведение в контакт композиции клеток с молекулой нуклеиновой кислоты, кодирующей химерный рецептор антигена, при условиях для введения молекулы нуклеиновой кислоты в одну или несколько клеток в композиции, тем самым продуцируя исходную композицию; и
(b) инкубирование клеток исходной композиции согласно способу по любому из пп. 33-44.
46. Способ по п. 45, в котором по меньшей мере часть приведения в контакт и инкубирования проводят одновременно.
47. Способ по п. 45 или 46, отличающийся тем, что приведение в контакт осуществляют путем трансдуцирования вирусным вектором.
48. Способ по п. 47, где вирусный вектор представляет собой ретровирусный вектор, гамма-ретровирусный вектор или лентивирусный вектор.
49. Способ по любому из пп. 45-48, отличающийся тем, что количество клеток в выходной композиции, содержащих химерный рецептор антигена, повышается или обогащается 1,2-кратно, 2,0-кратно, 3,0-кратно, 4,0-кратно, 5,0-кратно, 6,0-кратно, 7,0-кратно, 8,0-кратно, 9,0-кратно, 10-кратно или больше по сравнению с количеством клеток, содержащих рецептор антигена, в исходной композиции.
50. Способ селекции клеток, включающий приведение в контакт популяции клеток вместе с поверхностно-модифицированной частицей по любому из пп. 1, 4, 5 и 8-22 или с композицией по любому из пп. 23-25, где:
популяция клеток включает клетки, экспрессирующие химерный рецептор антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген; и
связывающая молекула поверхностно-модифицированной частицы или каждая из поверхностно-модифицированных частиц композиции специфически связывается или распознает внеклеточный антигенсвязывающий домен химерного рецептора антигена.
51. Способ обогащения клеток, включающий приведение в контакт популяции клеток вместе с поверхностно-модифицированной частицей по любому из пп. 1, 4, 5 и 8-22 или с композицией по любому из пп. 23-25, где:
популяция клеток включает клетки, экспрессирующие химерный рецептор антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген; и
связывающая молекула поверхностно-модифицированной частицы или каждая из поверхностно-модифицированных частиц композиции специфически связывается или распознает внеклеточный антигенсвязывающий домен химерного рецептора антигена.
52. Способ селекции клеток, включающий приведение в контакт популяции клеток вместе с поверхностно-модифицированной частицей по любому из пп. 2, 3 и 6-22 или с композицией по любому из пп. 26-28, где:
популяция клеток включает клетки, экспрессирующие химерный рецептор антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген; и
связывающая молекула поверхностно-модифицированной частицы или каждая из поверхностно-модифицированных частиц композиции специфически связывается или распознает внеклеточный антигенсвязывающий домен химерного рецептора антигена.
53. Способ обогащения клеток, включающий приведение в контакт популяции клеток вместе с поверхностно-модифицированной частицей по любому из пп. 2, 3 и 6-22 или с композицией по любому из пп. 26-28, где:
популяция клеток включает клетки, экспрессирующие химерный рецептор антигена, содержащий внеклеточный антигенсвязывающий домен, который специфично связывает или распознает антиген; и
связывающая молекула поверхностно-модифицированной частицы или каждая из поверхностно-модифицированных частиц композиции специфически связывается или распознает внеклеточный антигенсвязывающий домен химерного рецептора антигена.
| WO2017059796 A1, 13.04.2017 | |||
| WO2016166544 A1, 20.10.2016 | |||
| MARC PELLETIER et al., Comparison of Soluble Decoy IgG Fusion Proteins of BAFF-R and BCMA as Antagonists for BAFF, THE JOURNAL OF BIOLOGICAL CHEMISTRY, 2003, Vol | |||
| ПАРОВАЯ ИЛИ ГАЗОВАЯ ТУРБИНА | 1914 |
|
SU278A1 |
| Скоропечатный станок для печатания со стеклянных пластинок | 1922 |
|
SU35A1 |
| 33127-33133 | |||
| LINA CUI et al., Supramolecular Complexing of Membane Siglec CD22 Mediated by | |||
Авторы
Даты
2022-11-22—Публикация
2018-07-28—Подача