Область техники
Изобретение относится к медицине, а именно, к молекулярно-генетической диагностике, которая может быть использована для выявления индивидуумов, подверженных наибольшему риску необходимости применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19. Для оказания медицинской помощи пациентам из группы риска при COVID-19 на ранних этапах могут быть использованы скорректированные алгоритмы административных и медицинских действий.
Уровень техники
Известно, что риск применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при инфицировании новой коронавирусной инфекцией повышается в зависимости от ряда факторов, в числе которых возраст, мужской пол (вероятность смерти при заражении коронавирусом выше для мужчин, чем для женщин), индекс массы тела, уровень глюкозы. Тяжелое течение с необходимостью применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) наиболее часто регистрируют у людей старшей возрастной группы с заболеваниями сердечно-сосудистой системы, цереброваскулярной патологией и злокачественными новообразованиями. Из всех хронических заболеваний наиболее опасным при COVID-19 является сахарный диабет. На втором месте после диабета по опасности при COVID-19 находятся болезни почек и сердечно-сосудистые заболевания [Wang T., Du Z., Zhu F., Cao Z., An Y., Gao Y., et al. Comorbidities and multi-organ injuries in the treatment of COVID-19 // Lancet. 2020. Vol. 395, № 10228. P. e52. DOI: 10.1016/S0140-6736(20)30558-4].
Известно, что на характер течения заболевания COVID-19 также влияет фактор генетической предрасположенности. При этом из уровня техники известно, что молекулы HLA класса I являются одним из ключевых медиаторов первых звеньев в развитии специфического иммунного ответа на COVID-19. Сразу после попадания в клетку SARS-CoV-2 индуцирует трансляцию белков вируса. Некоторые из этих белков попадают в протеасомы инфицированной клетки, расщепляются до пептидов длиной 8-12 аминокислотных остатков и связываются с рецепторами HLA класса I. После связывания комплекс, состоящий из молекулы HLA класса I и пептида, переносится на поверхность инфицированной клетки, где он может взаимодействовать с Т-клеточным рецептором CD8+ Т-лимфоцитов. В ответ на взаимодействие с комплексом молекулы HLA класса I и вирусного пептида CD8+ Т-лимфоцит начинает процесс разрушения инфицированной клетки с помощью перфоринов и сериновых протеаз [Wherry EJ, Ahmed R. Memory CD8 T-Cell Differentiation during Viral Infection. J Virol. 2004;78(11):5535-5545. doi:10.1128/jvi.78.11.5535-5545.2004].
Существует три основных типа рецепторов HLA класса I: HLA-A, HLA-B и HLA-C. Рецепторы каждого типа присутствуют в двух вариантах, унаследованных от родителей. Существуют десятки вариантов каждой аллели рецепторов HLA-I; каждая аллель обладает индивидуальной способностью распознавать различные чужеродные белки. Распределение аллелей является специфичным для отдельных популяций [Wang JH, Zheng X, Ke X, Dorak MT, Shen J, Boodram B, et al. Ethnic and geographical differences in HLA associations with the outcome of hepatitis C virus infection. Virol J. 2009;6. doi:10.1186/1743-422X-6-46]. Комбинации рецепторов HLA класса I существенно влияют на тяжесть течения различных инфекционных заболеваний, включая малярию [Lima-Junior JdC, Pratt-Riccio LR. Major histocompatibility complex and malaria: Focus on Plasmodium vivax Infection. Front Immunol. 2016;7(JAN). doi:10.3389/fimmu.2016.00013], туберкулез [Mazzaccaro R0, Gedde M, Jensen ER, Van Santen HM, Ploegh HL, Rock KL, et al. Major histocompatibility class I presentation of soluble antigen facilitated by Mycobacterium tuberculosis infection. Proc Natl Acad Sci U S A. 1996;93(21):11786-11791. doi:10.1073/pnas.93.21.11786.], ВИЧ [Goulder PJR, Watkins DI. Impact of MHC class I diversity on immune control of immunodeficiency virus replication. Nat Rev Immunol. 2008;8(8):619-630. doi:10.1038/nri2357] и вирусный гепатит [Wang JH, Zheng X, Ke X, Dorak MT, Shen J, Boodram B, et al. Ethnic and geographical differences in HLA associations with the outcome of hepatitis C virus infection. Virol J. 2009;6. doi:10.1186/1743-422X-6-46].
Существуют ряд публикаций, в которых описаны взаимосвязи между генотипом HLA и чувствительностью к SARS-CoV. В частности известно, что аллели HLA-B*07:03 [Ng MHL, Lau KM, Li L, Cheng SH, Chan WY, Hui PK, et al. Association of human-leukocyte-antigen class I (B*0703) and class II (DRB1*0301) genotypes with susceptibility and resistance to the development of severe acute respiratory syndrome. J Infect Dis. 2004;190(3):515-518. doi:10.1086/421523], HLA-B*46:01 [Lin M, Tseng HK, Trejaut JA, Lee HL, Loo JH, Chu CC, et al. Association of HLA class I with severe acute respiratory syndrome coronavirus infection. BMC Med Genet. 2003;4. doi:10.1186/1471-2350-4-9] и HLA-C*08:01 [Chen YMA, Liang SY, Shih YP, Chen CY, Lee YM, Chang L, et al. Epidemiological and genetic correlates of severe acute respiratory syndrome coronavirus infection in the hospital with the highest nosocomial infection rate in Taiwan in 2003. J Clin Microbiol. 2006;44(2):359-365. doi:10.1128/JCM.44.2.359-365.2006] являются факторами предрасположенности к тяжелой форме заболевания; аллель 21 HLA-C*15:02 ассоциирован с легкой формой [Wang SF, Chen KH, Chen M, Li WY, Chen YJ, Tsao CH, et al. Human-leukocyte antigen class i Cw 1502 and Class II DR 0301 genotypes are associated with resistance to severe acute respiratory syndrome (SARS) infection. Viral Immunol. 2011;24(5):421-426. doi:10.1089/vim.2011.0024].
В исследовании, проведенном китайскими учеными, было выявлено наличие редких аллелей HLA-C*07:29 и HLA-B*15:27 у китайских пациентов с COVID-19 [Wang W, Zhang W, Zhang J, He J, Zhu F. Distribution of HLA allele frequencies in 82 Chinese individuals with coronavirus disease-2019 (COVID-19). Hla. 2020;96(2):194-196. doi:10.1111/tan.13941].
Из уровня техники известна взаимосвязь количества пептидов с высокой константой взаимодействия с индивидуальным генотипом HLA: чем больше вирусных пептидов с высокой аффинностью связывается с HLA I класса, тем легче протекает заболевание. Также было показано, что частота встречаемости аллелей HLA-A*01:01 и HLA-A*02:01 связана с числом случаев COVID-19 и смертей от нее в различных регионах Италии [Pisanti S, Deelen J, Gallina AM, Caputo M, Citro M, Abate M, et al. Correlation of the two most frequent HLA haplotypes in the Italian population to the differential regional incidence of Covid-19. J Transl Med. 2020;18(1). doi:10.1186/s12967-020-02515-].
Таким образом, из уровня техники известно влияние различных сочетаний аллелей HLA I класса на течение заболевания, вызванного SARS-CoV-2. При этом очевидно, что сочетание отдельных аллелей, прогностически значимых для оценки риска развития тяжелого течения COVID-19, для разных популяций может отличаться. Из уровня техники не выявлено результатов исследований комбинации аллелей HLA I класса для российской популяции, которые бы обеспечивали получение достоверных прогнозных оценок по течению данного заболевания и необходимости применения кислородной терапии.
Наиболее близким к заявляемому решению является способ оценки риска развития тяжелой формы COVID-19 [Iturrieta-Zuazo, I., Rita, C. G., García-Soidán, A., de Malet Pintos-Fonseca, A., Alonso-Alarcón, N., Pariente-Rodríguez, R., Tejeda-Velarde, A., Serrano-Villar, S., Castañer-Alabau, J. L., & Nieto-Gañán, I. (2020). Possible role of HLA class-I genotype in SARS-CoV-2 infection and progression: A pilot study in a cohort of Covid-19 Spanish patients. Clinical Immunology, 219, 108572. https://doi.org/10.1016/j.clim.2020.108572], включающий забор биологического материала, выделение геномной ДНК с последующим генотипированием аллелей генов HLA-A, HLA-B, HLA-C, обработку результатов генотипирования и прогнозирование риска развития тяжелой форма COVID-19 с необходимостью применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких). Известный способ основан на исследовании биологического материала 5 пациентов с легкой формой, 20 пациентов средней тяжести и 20 пациентов с тяжелой формой COVID-19. Выделение геномной ДНК с последующим генотипированием аллелей генов HLA-A, HLA-B, HLA-C было проведено с помощью наборов реагентов RSSOW1A, RSSOW1B и RSSOW1C (One lambda inc) и мультиплексного анализатора FlexMap 3D. Критерии для оценки риска развития тяжелой формы COVID-19 были получены на основе анализа аффинности взаимодействия пептидов вируса SARS-CoV-2 c молекулами HLA-I пациента, относящегося к одной из трех групп по тяжести течения заболевания; в случае, если аффинность взаимодействия пептида с одной из молекул HLA-I была менее 50 нМоль, то Индекс высокоаффинных пептидов увеличивали на 1; пороговые значения для прогноза риска развития тяжелой формы COVID-19 для всех пациентов определяли после определения Индекса высокоаффинных пептидов.
Однако в известном способе пороговые значения для прогноза риска развития тяжелой формы COVID-19 определялись на основе выборки без учета данных об умерших пациентах. При этом малый объем выборки, использование только качественных, а не количественных характеристик взаимодействия вирусный пептид - молекула HLA-I, отсутствие этапа проверки чувствительности и специфичности критериев прогноза риска развития тяжелой форма COVID-19 на контрольной выборке, ставят под сомнение точность и достоверность получаемых прогнозных оценок развития тяжелой формы COVID-19.
Технической проблемой, решаемой заявляемым изобретением, является разработка способа оценки риска необходимости применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19, который может быть применен для российской популяции, с получением достоверных и высокоточных прогнозных оценок.
Раскрытие изобретения
Техническим результатом заявляемого изобретения является повышение точности прогнозных оценок риска необходимости применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19 для лиц российской популяции возрастом от 35 до 60 лет.
Технический результат достигается тем, что способ оценки риска развития тяжелой формы COVID-19 и необходимости применения кислородной терапии включает забор биологического материала, выделение геномной ДНК с последующим генотипированием аллелей гена HLA-С и прогнозирование по результатам генотипирования риска применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19. При этом по результатам генотипирования определяют наличие аллели HLA-С*12:03, и прогнозируют высокий риск применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19.
В качестве биологического материала для оценки риска развития тяжелой формы COVID-19 может быть использована венозная или капиллярная кровь, букальный соскоб.
Геномная ДНК может быть выделена с помощью различных наборов реагентов, например, QIAamp DNA Blood, или HigherPurity™ Blood DNA Extraction Kit (Convax), или GeneJET Whole Blood Genomic DNA Purification Mini Kit (Thermo Scientific), или любого аналогичного набора для выделения геномной ДНК. Генотипирование осуществляют с применением набора реагентов для подготовки библиотек фрагментов ДНК генов HLA-A для генотипирования секвенированием нового поколения, например, HLA-Эксперт (ООО «ДНК-Технология») или любого аналогичного набора, известного из уровня техники для указанного применения.
Заявляемый способ был разработан по итогам проведенных исследований генетического материала около 750 пациентов, составляющих российскую популяцию, включая генетически материал 78 пациентов в возрасте до 60 лет проходивших лечение от COVID-19 в условиях стационара. В результате выявлены возможные связи между генотипами пациентов и необходимостью применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при лечении COVID-19, на основании которых выявлен генетический фактор, ассоциированный с необходимостью применения кислородной терапии при COVID-19.
Использование в заявляемом способе данных HLA-генотипа пациентов проходивших лечение от COVID-19 в условиях стационара в возрасте до 60 лет значимо повлияло на повышение точности получаемых оценок. Необходимость применения кислородотерапии при лечении COVID-19 у пациентов в возрасте до 60 лет - проявление тяжелого течения заболевания - сочетание сопутствующих заболеваний, неадекватного ответа иммунной системы, одной из причин которого является генетическая предрасположенность.
В процессе разработки заявляемого способа было выявлено, что для российской популяции значительный вклад в оценку риска применения кислородной терапии вносит аллель HLA-С*12:03. В частности, носители аллели HLA-С*12:03 в 4,3 раз чаще нуждались в применении кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19.
Применение способа, описанного в работе Iturrieta-Zuazo и соавторов, к данным генотипов выборки пациентов, предложенной в заявляемом способе, показало значение площади под ROC-кривой равное 0.57, p = 0.15 при пороге на аффинность равным 500 нМ и 0.59, p = 0.07 при пороге на аффинность равным 50 нМоль. При этом площадь под ROC-кривой при использовании заявляемого способа составила 0,71, p = 0,0008, что свидетельствует о ее большей чувствительности и специфичности.
Кроме того, при получении заявляемого комплекса генетических маркеров были использованы иные критерии оценки аффинности пептидов и аллелей HLA-I. В способе, описанном в работе Iturrieta-Zuazo и соавторов, упоминается два способа интерпретации математического моделирования аффинности пептида и аллели HLA-I: при аффинности менее 50 нМоль взаимодействие считалось возможным, при более и равно 50 нМоль - нет; при аффинности менее 500 нМоль взаимодействие считалось возможным, при более и равно 500 нМоль - нет. Заявляемые оценочные критерии были получены при использовании непрерывной шкалы значений аффинности от 1 до 5000 в отличие от способа Iturrieta-Zuazo и соавторов, который бинаризует (0 или 1) значение аффинности. Учитывая, что значение площади под ROC-кривой заявляемого способа превосходит значение для прототипа, использование непрерывной шкалы аффинностей позволяет повысить точность прогноза.
Таким образом, заявляемый способ демонстрирует более высокую точность получения прогнозных оценок по течению COVID-19 по сравнению со способом - прототипом, что является важным для применения/изменения тактики лечения пациента.
Краткое описание чертежей
Изобретение поясняется иллюстративными материалами.
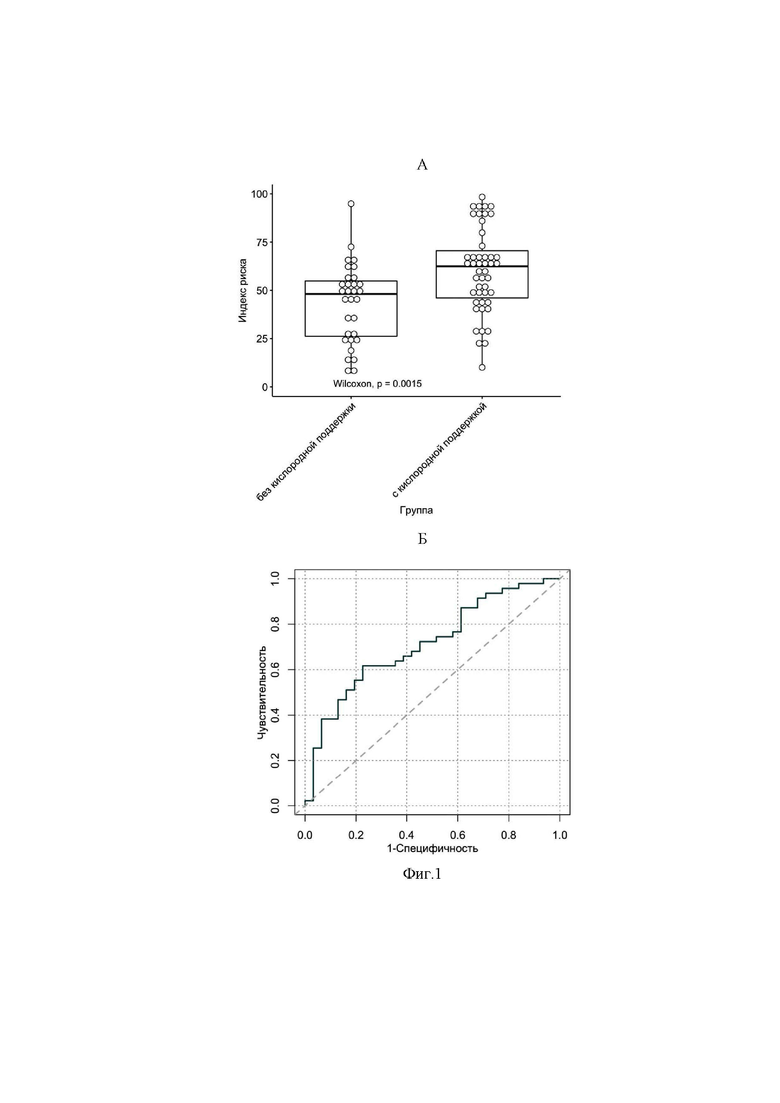
На фиг. 1 представлена оценка риска, разделяющая группы пациентов российской популяции в возрасте до 60 лет, получавших и не получавших кислородотерапию. А: распределение индекса риска в рассматриваемых группах. Б: рабочая характеристическая кривая приемника для индекса риска (площадь под кривой (AUC) равна 0,71).
Осуществление изобретения
Оценку риска развития тяжелой формы COVID-19 у пациента из российской популяции проводят в два этапа.
Забор биологического материала и генотипирование.
Для проведения генотипирования аллелей HLA-C получают биологический материал индивидуума, выделяют из него геномную ДНК и проводят анализ секвенирования нового поколения. Биологическим материалом может служить венозная или капиллярная кровь, букальный соскоб. Выделение геномной ДНК можно проводить с помощью различных наборов реагентов, например, QIAamp DNA Blood, или HigherPurity™ Blood DNA Extraction Kit (Convax), или GeneJET Whole Blood Genomic DNA Purification Mini Kit (Thermo Scientific), или использовать любой аналогичный набор для выделения геномной ДНК.
Генотипирование осуществляют с применением набора реагентов для подготовки библиотек фрагментов ДНК генов HLA-C для генотипирования секвенированием нового поколения HLA-Эксперт (ООО «ДНК-Технология»), или TruSight HLA v2 Sequencing Panel Library Preparation Kits (Illumina), или любого аналогичного набора для подготовки фрагментов ДНК генов HLA-A. Секвенирование производят в обоих направлениях 2-4 экзонов, аннотация генотипов может быть произведена, например, с использованием базы данных IMGT/HLA [Robinson J, Barker DJ, Georgiou X, Cooper MA, Flicek P, Marsh SGE. IPD-IMGT/HLA Database. Nucleic Acids Res. 2020;48(D1):D948-D955. doi:10.1093/nar/gkz950].
Оценка результатов генотипирования.
По результатам генотипирования определяют наличие аллели HLA-C*12:03, и прогнозируют высокий риск необходимости применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19.
Данный оценочный критерий был получен в результате исследования, которое включало формирование для российской популяции БД аллелей генов HLA-A, HLA-В, HLA-C со значениями главных компонент по итогам соответствующего генотипирования популяции. Популяционный срез включал не менее 500 человек, в т.ч. пациентов, умерших от COVID-19 - предпочтительно не менее 35 пациентов в возрасте до 60 лет, не менее 80 пациентов в возрасте от 60 лет. Из выборки были исключены пациенты с иммуносупрессией (например, больные ВИЧ, принимающие химиотерапию, лица с автоиммунными заболеваниями, принимающие иммуносупрессанты, пациенты с трансплантациями).
В процессе проведения исследования была сформирована матрица связывания вирусных пептидов и аллелей.
Для формирования матрицы связывания были использованы последовательности белков SARS-CoV-2 требуемого штамма, а также последовательности белков SARS-CoV-2, опубликованные на портале GISAID [Elbe S, Buckland-Merrett G. Data, disease and diplomacy: GISAID's innovative contribution to global health. Glob Challenges. 2017;1(1):33{46. doi:10.1002/gch2.1018.]. Выравнивание белковых последовательностей с целью получения консенсусной последовательности может быть произведено с помощью таких программных продуктов, как Clustal Omega [Sievers F, Higgins DG. Clustal Omega for making accurate alignments of many protein sequences. Protein Sci. 2018;27(1):135{145. doi:10.1002/pro.3290.], или Kalign [https://doi.org/10.1186/1471-2105-6-298], или любого аналогичного продукта для осуществления множественного выравнивания аминокислотных последовательностей. Для каждой аминокислоты каждого вирусного белка производили расчет вероятности разрезания протеасомой в данной позиции, которое может быть реализовано, например, с использованием программного продукта NetChop [https://doi.org/10.1007/s00251-005-0781-7]. Список вирусных пептидов определяли в виде множества всевозможных фрагментов белков, состоящих из 8-12 аминокислот, имеющих вероятность протеасомного разреза не менее 0.1 с каждого из концов фрагмента.
Далее определяли аффинности связывания вирусных пептидов с рецепторами HLA-I, которые могут быть реализованы с использованием программы netMHCpan [https://doi.org/10.1093/nar/gkaa379], или MHCflurry [https://doi.org/10.1016/j.cels.2018.05.014], или любой аналогичной программой для предсказания аффинностей связывания аллелей HLA класса I и множества пептидов. Пептиды, имеющие низкую аффинность связывания ко всем аллелям из данной популяции, исключали. В качестве порогового значения, характеризующего низкую аффинность, использовали 500 нмоль. Для оставшихся пептидов аффинности инвертировали, умножали на 500 и логарифмировали по основанию 10 (константы 500 и 10 не влияли на дальнейший статистический анализ и были введены для удобства визуального исследования). Результат вычислений записывали в матрицу, строкам которой соответствовали аллели популяции, а столбцам - вирусные пептиды.
Далее проводили обработку матрицы связывания методом главных компонент. Для чего в рамках данного метода исходный набор пептидов заменяли на их наиболее информативные линейные комбинации. Количество главных компонент определяли таким образом, чтобы доля дисперсии, обусловленная каждой компонентой, составляла не менее 5%.
Для каждого индивидуума с определенным генотипом рецепторов HLA-I, производили суммирование главных компонент, соответствующих каждой паре двух аллелей (HLA-A, HLA-C). При этом в суммировании участвуют вторая и третья главные компоненты по аллелям HLA-A, и четвертая компонента по HLA-C. Итоговая формула выглядит следующим образом:
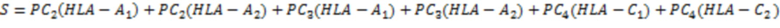
где HLA-A1, HLA-A2, HLA-C1, HLA-C2 - аллели, соответствующие генотипу рассматриваемого индивидуума; РС2, РС3, РС 4 - вторая, третья и четвертая главная компонента генов HLA-A, HLA-A и HLA-C, соответственно.
Далее, полученную сумму 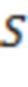 приводили к диапазону
приводили к диапазону 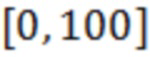 путем линейной нормировки:
путем линейной нормировки: 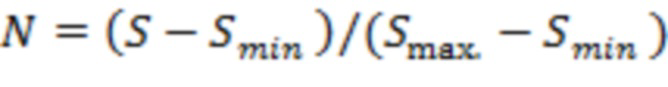 , где
, где 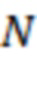 - нормированный индекс риска,
- нормированный индекс риска, 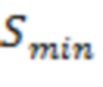 - минимально возможная сумма среди рассматриваемой популяции,
- минимально возможная сумма среди рассматриваемой популяции, 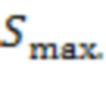 - максимально возможная сумма среди рассматриваемой популяции.
- максимально возможная сумма среди рассматриваемой популяции.
Заявляемый способ был разработан по итогам проведенных исследований на основе данных контрольной группы из 428 добровольцев, которая была сформирована с использованием электронных записей генотипов HLA Федерального регистра доноров костного мозга (Российский национальный исследовательский медицинский университет им. Н. И. Пирогова) и 126 пациентов, инфицированных COVID-19, которые умерли в период с мая по июль 2020 года по данным Городской клинической больницы № 15 им. О. М. Филатова (Москва, Россия). Для изучения влияния генотипа HLA класса I на течение COVID-19 было проведено генотипирование HLA для умерших пациентов с COVID-19, а также контрольной группы (n = 428) и исследована взаимосвязь между генотипами и возрастом на момент смерти. Все пациенты имели, по крайней мере, один положительный результат теста на SARS-CoV-2 с помощью RT-qPCR из мазков носоглотки или бронхоальвеолярного лаважа. Из исследований были исключены пациенты с патологиями ВИЧ, рак и принимавшие иммуносупрессивные препараты.
Кровь (2 мл) пациентов была взята врачом в флакон с ЭДТА. Пациенты были разделены на две группы: пациенты нуждавшиеся в кислородной терапии (возраст ≤ 60 лет, n = 47) и пациенты не нуждавшиеся в кислородной терапии (возраст ≤ 60 лет, n = 31). Полученные значения нормированного индекса риска достоверно разделяли группы пациентов получавших и не получавших кислородную терапию (P = 0,0015, W-критерий Вилкоксона) и площадью под кривой рабочей характеристики приемника (AUC ROC), равной 0,71 (перестановочный тест P = 0.00076), см. фиг. 1.
В проведенных исследованиях были использованы следующие функции из модуля scipy.stats Python [Virtanen P, Gommers R, Oliphant TE, Haberland M, Reddy T, Cournapeau D, et al. SciPy 1.0: fundamental algorithms for scientific computing in Python. Nat Methods. 2020;17(3):261-272. doi:10.1038/s41592-019-0686-2]: fisher exact для точного теста Фишера, mannwhitneyu для U-теста Манна-Уитни. Процедура Бенджамини-Хохберга использовалась для выполнения множественной коррекции тестирования. Анализ главных компонент проводился с помощью модуля scikit-learn Python [Pedregosa F, Varoquaux G, Gramfort A, Michel V, Thirion B, Grisel O, et al. Scikit-learn: Machine Learning in Python. Journal of Machine Learning Research. 2011;12(85):2825-2830]. Участки ROC-кривой были построены с помощью Seaborn и Matplotlib [Hunter JD. Matplotlib: A 2D graphics environment. Comput Sci Eng. 2007;9(3):90-95. doi:10.1109/MCSE.2007.55].
При анализе группы, получавшей кислородную поддержку было выявлено, что более 30% (15 из 47) пациентов были носителями аллели HLA-С*12:03, в то время как в группе пациентов не получавших кислородную поддержку носителями аллели HLA-С*12:03 были только 9,6% (точный критерий Фишера Р = 0,019).
Таким образом, в результате проведенных исследований был разработан способ прогнозирования риска необходимости применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких) при COVID-19, основанный на анализе представленности аллели HLA-С*12:03. Наличие аллели HLA-С*12:03 связано с высоким риском необходимости применения кислородной терапии (и/или неинвазивной искусственной вентиляции легких и/или искусственной вентиляции легких).
Ниже представлены примеры реализации заявляемого изобретения.
Пример 1
Юрий Н., 57 лет. Был произведен забор венозной крови. Геномная ДНК была выделена с помощью набора QIAamp DNA Blood. В процессе генотипирования с помощью секвенирования нового поколения был использован набор реагентов HLA-Эксперт. В результате было определено, что индивидуум является носителем аллели HLA-С*12:03, и индивидуум был отнесен к группе высокого риска.
Через год после анализа индивидуум переболел тяжелой формой COVID-19 (реанимация, искусственная вентиляция легких, ЧДД 35/мин, SpO2 89%, PaO2/FiO2 293 мм рт.ст).
Пример 2
Юлия З., 44 года. Был произведен забор капиллярной крови. Геномная ДНК была выделена с помощью набора GeneJET Whole Blood Genomic DNA Purification Mini Kit. В процессе генотипирования с помощью секвенирования нового поколения был использован набор реагентов HLA-Эксперт. В результате было определено, что индивидуум не является носителем аллели HLA-С*12:03, и индивидуум был отнесен к группе низкого риска.
Через три недели после анализа индивидуум бессимптомно переболел COVID-19 (диагностика проведена с помощью ПЦР теста).
Таким образом, заявляемый способ продемонстрировал высокую точность получения прогнозных оценок.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ ТЯЖЕЛОЙ ФОРМЫ COVID-19 | 2021 |
|
RU2751410C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ ТЯЖЕЛОЙ ФОРМЫ COVID-19 | 2021 |
|
RU2747097C1 |
| Способ прогнозирования риска развития COVID-19 у больных гемобластозами | 2022 |
|
RU2783422C1 |
| Способ оценки риска развития тяжелого течения COVID-19 | 2022 |
|
RU2782796C1 |
| Способ прогнозирования риска летального исхода у пациентов с тяжелым и среднетяжёлым течением COVID-19 при проведении упреждающей противовоспалительной терапии | 2021 |
|
RU2770357C1 |
| Способ прогнозирования риска тяжелого течения COVID-19 у пациента | 2022 |
|
RU2791487C1 |
| Способ оценки риска развития тяжелого течения коронавирусной инфекции у женщин | 2021 |
|
RU2761138C1 |
| Способ прогноза риска летального исхода COVID-19 у пациентов молодого возраста | 2023 |
|
RU2803002C1 |
| Искусственный ген, кодирующий белок-иммуноген BSI-COV-Ub, рекомбинантная плазмидная ДНК pBSI-COV-Ub, обеспечивающая экспрессию целевого гена, и искусственный полиэпитопный белок-иммуноген BSI-COV-Ub, содержащий убиквитин и эпитопы антигенов вируса SARS-CoV-2 и индуцирующий SARS-CoV-2-специфический Т-клеточный иммунитет | 2023 |
|
RU2806590C1 |
| Способ прогнозирования исхода острого заболевания, вызванного новой коронавирусной инфекцией COVID-19 | 2021 |
|
RU2766347C1 |
Изобретение относится к области медицины, в частности к молекулярно-генетической диагностике. Осуществляют забор биологического материала, выделение геномной ДНК с последующим генотипированием аллелей гена HLA-С. В случае определения наличия аллеля HLA-С*12:03 прогнозируют высокий риск необходимости применения кислородной терапии при COVID-19. Изобретение обеспечивает повышение точности прогнозных оценок риска необходимости применения кислородной терапии при COVID-19 для лиц российской популяции возрастом от 35 до 60 лет. 2 з.п. ф-лы, 1 ил., 2 пр.
1. Способ оценки риска необходимости применения кислородной терапии при COVID-19 для лиц возрастом от 35 до 60 лет, включающий забор биологического материала, выделение геномной ДНК с последующим генотипированием аллелей гена HLA-С и в случае определения наличия аллели HLA-С*12:03 прогнозируют высокий риск необходимости применения кислородной терапии при COVID-19.
2. Способ по п.1, отличающийся тем, что геномную ДНК выделяют с помощью набора реагентов QIAamp DNA Blood, или HigherPurity™ Blood DNA Extraction Kit, или GeneJET Whole Blood Genomic DNA Purification Mini Kit.
3. Способ по п.1, отличающийся тем, что генотипирование осуществляют с применением набора реагентов для подготовки библиотек фрагментов ДНК гена HLA-С для генотипирования секвенированием нового поколения HLA-Эксперт.
| WO 2021204902 A1, 14.10.2021 | |||
| WO 2020169819 A1, 27.08.2020 | |||
| БУБНОВА Л.Н | |||
| и др | |||
| Особенности распределения групп аллелей HLA-А*, B*, DRB1* среди лиц, перенесших COVID-19 | |||
| Медицинская иммунология | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| КОРКУШКО О.В | |||
| и др | |||
| Возрастные изменения дыхательной системы при старении и их роль в развитии бронхо-легочной патологии | |||
Авторы
Даты
2022-08-04—Публикация
2021-12-11—Подача