Настоящее изобретение относится к области фармацевтики, а именно к средствам для лечения бактериальных инфекций, повышения эффективности терапевтического действия антибиотиков, в том числе в отношении резистентных бактерий и снижения терапевтической дозы антибиотиков, а также к способу лечения бактериальных инфекций, способу снижения терапевтической дозы антибиотика и способу повышения терапевтической эффективности антибиотиков в отношении резистентных к ним бактерий.
Бактериальные инфекции - это заболевания, спровоцированные бактериями. Особенностью бактериальных инфекций является то, что в процессе жизнедеятельности и после гибели бактерий происходит выделение токсинов, вызывающих воспаление, интоксикацию и повреждение тканей. При диагностировании бактериальной инфекции назначается лечение антибактериальными препаратами. Бактерии, вызывающие те или иные заболевания, рано или поздно вырабатывают резистентность (устойчивость) к антибиотикам, применяемым в ходе лечения. Это естественный процесс адаптации, который называется антимикробной резистентностью. Возникновение большого количества резистентных бактерий ведет к появлению все большего числа неизлечимых инфекций, в результате чего все больше увеличиваются риски бактериальных инфекций, возрастают медицинские расходы на лечение бактериальных инфекций, становится более продолжительные госпитализации и увеличивается смертность [ВОЗ. Возрастающая угроза развития антимикробной резистентности: возможные меры. 2013 г.].
В мае 2015 г. Всемирная ассамблея здравоохранения утвердила Глобальный план действий по устойчивости к противомикробным препаратам, включающий и устойчивость к антибиотикам. Глобальный план действий направлен на обеспечение профилактики и лечения инфекционных болезней с помощью безопасных и эффективных лекарств [http://www.who.int/mediacentre/factsheets/antibiotic-resistance/ru/].
Таким образом, лечение бактериальных инфекций, а также снижение резистентности бактерий к антибиотикам и повышение чувствительности бактерий к антибиотикам является серьезной проблемой и актуальной задачей в области медицины.
Из уровня техники известно лекарственное средство, содержащее активированную форму сверхмалых доз моноклональных, поликлональных иммунных или естественных антител к антигену главного комплекса гистосовместимости (система HLA) или к комплексу антигена системы HLA и ассоциированного с ним пептида [патент RU 2205025C1, 26.12.2001]. Полученное в соответствии с изобретением иммунотропное лекарственное средство представляет собой новый фармакологический препарат, который характеризуется наличием иммунотропной активности, отсутствием побочных эффектов, экологической чистотой и низкой себестоимостью.
Из уровня техники известны препараты для лечения инфекционных заболеваний в частности лекарственные препараты для лечения бактериальных инфекций, например, «Амоксициллин», «Гентамицин», «Тетрациклин», «Левомецитин» и другие. Препараты класса антибиотиков обладают двумя основными проблемами: увеличивающееся число микроорганизмов, резистентных к антибиотикам, и широкий спектр противопоказаний и побочных эффектов при применении антибиотиков [Белозерцева В.Н. и др. Антибиотики - резистентность и токсичность. Новые Санкт-Петербургские врачебные ведомости, г. 2017. - N 2. - С. 59-61]. Так, например, препарат «Амоксициллин» может вызывать аллергические реакции (ренит, дерматит, зуд и др.), тошноту, диарею, судорожные реакции, тахикардию, боль в суставах и другое [https://www.rlsnet.ru/tn_iridex_id_222.htm]. При выборе препарата «Тетрациклин» обязательно нужно сдавать анализ на чувствительность к антибиотику, так как за годы применения препарата многие бактерии приобрели к нему резистентность, кроме того, при пероральном применении антибиотик может вызывать сильные побочные реакции, считается токсичным, поэтому противопоказан для детей до 8 лет и беременных женщин [https://www.rlsnet.ru/mnn_index_id_82.html. Препарат «Гентамицин» также обладает высокой токсичностью, может вызывать эпилептические припадки, головную боль, снижение слуха, анемию, лихорадку, развитие суперинфекции и другие симптомы, таким образом, назначают его с осторожностью, только после окончательного подтверждения диагноза [https://www.rlsnet.ru/tn_index_id_876.htm]. Современные исследования показали опасность препарата «Левомецитин», в частности, вещество может угнетать кроветворение, вызывая апластическую анемию - уменьшение или прекращение производства костным мозгом компонентов крови [https://medaboutme.ru/zdorove/spravochnik/slovar-medicinskih-terminov/antibiotiki/; https://www.rlsnet.ru/tn_index_id_4699.htm].
Таким образом, неправильный и неконтролируемый прием антибиотиков может серьезно навредить здоровью. Как говорилось ранее, лечение антибиотиками может сопровождаться не только неблагоприятными побочными действиями, такими как, аллергия, токсические осложнения со стороны печени и почек, нарушение сердечно-сосудистой системы и крови, нервной системы, но и привести к образованию антибиотикоустойчивых микробов. В настоящий момент Правительством РФ утверждена Стратегия предупреждения распространения антимикробной резистентности в РФ на период до 2030 года. Целью стратегии является предупреждение и ограничение распространения антимикробной резистентности [ПРАВИТЕЛЬСТВО РОССИЙСКОЙ ФЕДЕРАЦИИ, Распоряжение от 25.09.2017 г. «2045-р Москва, Стратегия предупреждения распространения антимикробной резистентности в Российской Федерации на период до 2030 года]. Таким образом, идет повсеместная, комплексная работа по снижению уровня резистентности микроорганизмов к антибиотикам и рационального потребления антибиотиков.
Известен способ преодоления лекарственной устойчивости бактерий, включающий применение антибиотиков в комбинации с ингибиторами бактериальных ферментов. Например, клавулановая кислота (или клавуланат) - ингибитор бета-лактамаз, чья химическая структура напоминает бета-лактамные антибиотики. Подобно другим бета-лактамам, клавулановая кислота способна связываться с пенициллинсвязывающими белками (ПСБ) грамположительных и грамотрицательных бактерий и способствовать лизису бактериальной стенки. Кроме того, клавулановая кислота обладает собственной антибактериальной активностью. На этой основе созданы комбинированные препараты, содержащие аминопенициллиновый антибиотик и один из ингибиторов бета-лактамаз (амоксициллин/клавуланат). Недостатком данного способа является ограниченный спектр антагонистического действия применяемых комбинаций препаратов (активны только в отношении микробов, резистентность которых обусловлена выработкой бета-лактамаз). Также внутривенно препараты клавулановой кислоты используют с осторожностью у больных с тяжелыми нарушениями функционального состояния печени; при появлении крапивницы или эритематозной сыпи прием лекарств необходимо прекратить. Клавулановая кислота противопоказана при индивидуальной непереносимости. В период беременности допускается использование этого препарата с «Амоксициллином» или «Тикарциллином» только по жизненным показаниям. В период лактации применять лекарство не рекомендуется. К побочным действиям клавулановой кислоты относятся: диспепсия, холестатическая желтуха, нарушение функционального состояния печени, гепатит, псевдомембранозный колит, кандидоз, аллергические реакции (многоформная эритема, отек Квинке, эксфолиативный дерматит, крапивница, анафилактический шок) [https://www.kakprosto.ru/kak-899440-klavulanovaya-kislota-deystvie-i-svoystva-#ixzz5eejsFIpF].
Из уровня техники известен способ преодоления лекарственной устойчивости бактерий и грибов, позволяющий повысить эффективность
преодоления лекарственной устойчивости микроорганизмов к антимикробным препаратам с различным механизмом действия, за счет комбинированного действия низких концентраций анилиновых красителей и антимикробных препаратов [патент RU 2363470 C1, 10.08.2009]. При этом следует учитывать, что анилиновые красители широко используются в гистологической технике, обладают бактерицидным, а некоторые - канцерогенным действием.
Из уровня техники известна фармацевтическая комбинированная композиция для наружного и местного применения, содержащая активный комплекс бактериолитических и протеолитических ферментов, например, лизоамидазу, основу, и, по меньшей мере, одну целевую добавку, выбранную из ряда: антибиотик, синтетическое антибактериальное средство, в том числе вещество, снижающее резистентность микроорганизмов, антимикотик, анестетик, стимулятор репаративных процессов. Изобретение обеспечивает повышение по сравнению с известными средствами терапевтической активности фармацевтической композиции, в том числе к штаммам, резистентным к отдельным компонентам композиции, улучшение течения раневого процесса, быстрое очищение раны, сокращение времени реконвалесценции [патент RU 2655808 C2, 29.05.2018]. При этом следует учитывать, что ферменты являются чувствительными к различным внешним факторам (рН среды, температура, давление и прочее) и любое внешнее воздействие может привести к денатурации и необратимым изменениям структуры фермента с утратой его свойств. Например, фермент лизоамидазу рекомендуется хранить в сухом, защищенном от света месте при температуре не выше +10°С, что вызывает дополнительные сложности при его производстве, транспортировке и хранении, а также на любом из этих этапов может привести к снижению эффективности препарата.
Настоящее изобретение направлено на создание нового эффективного комплексного лекарственного средства, обладающего антибактериальной, иммуномодулирующей активностью и являющегося эффективным также
против бактерий, обладающих резистентностью в отношении одного или более известных антибактериальных средств (антибиотиков), при этом не оказывающего токсического или мутагенного действия на организм пациента, также изобретение направлено на создание средства, повышающего эффективность фармакологического действия антибиотика, в том числе в отношении резистентных к нему бактерий, и снижающего терапевтическую дозу антибиотика.
Решение поставленной задачи обеспечивается тем, что заявленное лекарственное средство для лечения бактериальных инфекций, способствующее повышению эффективности терапевтического действия антибиотиков, снижению резистентности бактерий к терапии антибиотиками, и способствующее снижению терапевтической дозы антибиотиков, представляет собой продукт технологической обработки методом последовательных множественных разведений исходных субстанций антител к β1 - домену молекулы главного комплекса гистосовместимости класса 2 (HLA-DRB1) и β2-микроглобулину (β2-МГ).
Лекарственное средство по настоящему изобретению, представляющее собой продукт технологической обработки методом последовательных множественных разведений исходных субстанций антител к β1 - домену молекулы главного комплекса гистосовместимости класса 2 (HLA-DRB1) и β2-микроглобулину (β2-МГ) эффективно для профилактики и лечения бактериальных инфекций, вызванных разными группами бактерий. При этом указанные группы бактерий, представляют собой, например: спирохеты (например, Treponema, Borrelia, Leptospira); аэробные и микроаэрофильные, подвижные, спиральные и изогнутые грамотрицательные бактерии (например, Campylobacter, Helicobacter, Spirillum); грамотрицательные аэробные и микроаэрофильные палочки и кокки (например, Achromobacter, Bordetella, Kingella, Neisseria); факультативно-анаэробные грамотрицательные палочки (например,
Cedecea, Escherihia, Klebsiella, Plesiomona, Haemophilus, Streptobacillus (коли-инфекции)); грамотрицательные анаэробные прямые, изогнутые и спиральные бактерии (например, Anaerobiospirrilum, Bacteroides, Porphyromonas); анаэробные грамотрицательные кокки (например, Veillonella); риккетсии и хламидии (например, Ehrlichia, Chlamydophila); грамположительные кокки (например, Aerococcus, Staphylococcus, Streptococcus); грамположительные палочки и кокки, образующие эндоспоры (например, Bacillus, Clostridium); не образующие спор грамположительные палочки правильной формы (например, Erysipelothrix, Listeria); не образующие спор грамположительные палочки неправильное формы (например, Bifidobacterium, Corinebacterium, Rothia); микобактерии (например, Mycobacterium); актиномицеты (например, Actinomadura, Nocardia, Streptomyces); микоплазмы (например, Mycoplasma, Ureaplasma) и прочее [И.В. Смирнов. Возбудители бактериальных инфекций человека. Клиническая микробиология и антимикробная химиотерапия, №2, Том 2, 2000, с. 4-11].
Заявленное лекарственное средство проявляет эффективность также в отношении бактерий, проявляющих резистентность к одному или нескольким антибиотикам.
Бактериальные инфекции, в отношении которых эффективно заявленное средство, могут быть систематизированы не только по виду бактерии, вызывающей заболевание, но также по механизму передачи:
Бактериальные инфекции пищеварительной системы/кишечные бактериальные инфекции, могут быть вызваны шигеллами, стафилококками, холерными вибрионами, брюшнотифозной палочкой, сальмонеллезами - преимущественно фекально-оральный путь передачи (сальмонеллез, брюшной тиф, дизентерии, пищевые токсикоинфекции, кампилобактериоз, дизентерия, энтерит, эширихиоз, кампилобактериоз, колит, пищевое отравление, гастрит, язвенные заболевания, ботулизм, дизентерия).
Бактериальные инфекции дыхательных путей - аспирационный путь передачи, могут бывать вызваны стафилококками, пневмококками, стрептококками, коклюшной палочкой, менингококками, хламидиями микобактериями, микоплазмами и прочими (синуситы, ринит, ангина, ларингит, трахеит, тонзиллиты, эпиглоттиты, гайморит, пневмонии, бронхиты, туберкулез и пр.).
Бактериальные инфекции мочеполовой системы - бактериальный вагиноз (гарднереллез), хламидиоз, цистит, дисбактериоз, пиелонефрит, гломерулонефрит, уретрит, бактериальным баланит, простатит, бактериальный цистит, пиелонефрит, уретрит, бактериальный простатит, везикулит и прочее.
Бактериальные инфекции кожи и мягких тканей, вызываемые, например, стафилоккоками, стрептококками - контактный путь передачи (рожа, импетиго, целлюлит, флегмона, фурункулез, гидраденит и т.д.).
Кровяные бактериальные инфекции, вызываемые, например, риккетсиями, иерсиниями, коккобактериями - трансмиссивный механизм передачи (туляремия, чума, сыпной тиф, окопная лихорадка и др.).
Инфекции лимфатической системы, например, лимфаденит, лимфангит могут быть вызваны стрептококком, стафилококком.
Инфекция нервной системы, например, менингиты, энцефалиты, миелиты и прочее вызываемые менингококками, пневмококками, гемофильными палочками тип b, боррелеими, микоплазмами, грибками рода Кандида и др. могут передаваться воздушно капельным путем, а также может быть лимфогенный путь передачи.
Инфекция костей и суставов может быть вызвана бактериями-возбудителями болезни Лайма, стафилококками, стрептококками, микобактериями, гонококковыми бактериями - механизм передачи через кровоток, через прямое проникновение, например, раны, хирургические вмешательства и т.д., через инфекции в ближайших структурах (инфекционный артрит, остеомиелит, болезни Рейтера и др.).
Инфекция уха, инфекция сосцевидного отростка и пазух, может быть вызвана стрептококками и стафилококками, грибками рода Кандида, гемофильными палочками и др. - передача инфекции происходит через евстахиеву трубу, со стороны наружного слухового прохода, или через кровь (лабиринтиты, нейросенсорная тугоухость, мастоидит и прочее).
Фармацевтическая комбинация по настоящему изобретению, представляет собой набор активных ингредиентов для лечения бактериальных инфекций, то есть, лекарственное средство, представляющее собой продукт технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 и антител к β2-МГ и соответствующий антибиотик, при этом оба вводят пациенту путем совместного введения. Совместное применение лекарственного средства и соответствующего антибиотика может осуществляться посредствам одновременного приема препаратов независимо друг от друга (в отдельных лекарственных формах) в одно и то же время или последовательно в рамках временных интервалов, особенно когда такие временные интервалы позволяют препаратам в комбинации проявлять улучшенный эффект. Заявленный препарат применяется в эффективной дозе, при этом антибиотик следует принимать согласно инструкции или по назначению врача. При этом указанный антибиотик может быть выбран из группы, например: бета-лактамные (пенициллины (амоксициллин, метициллин, оксациллин, бензилпенициллин и др.); цефалоспорины (цефалексин, цефазолин, цефтриаксон, цефепим и др.); карбапенемы (меропенем, дорипенем, биапенем и др.)); макролиды (кетолиды, эритромицин, рокситромицин, кларитромицин и др.); тетрациклины (тетрациклин, окситетрациклин, доксициклин, метациклин и др.); аминогликозиды (стрептомицин, канамицин, амикацин, гентамицин и др.); левомицетины; оксазолидиноны; гликопептиды (таргоцид, даптомицин, ванкомицин и др.); линкозамиды (делацин С); фторхинолоны (левофлоксацин, гемифлоксацин, спарфлоксацин и др.); противогрибковые
антибиотики (нистатин, амфотерицин В и др.); противотуберкулезные антибиотики (фтивазид, метазид, салюзид и др.); противолепрозные препараты (солюсульфон, диуцифон и др.); противоопухолевые препараты (доксорубицин, рубомицин, карминомицин и др.); разные антибиотики (фосфомицин, фузидин, рифампицин и др.) [https://ru.wikipedia.org/wiki/Антибиотики].
Также настоящее изобретение направлено на повышение эффективности фармакологического действия антибиотика, в том числе в отношении резистентных к нему бактерий, путем одновременного или последовательного введения соответствующего антибиотика и заявленного лекарственного средства, представляющего собой продукт технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 и β2-МГ. Таким образом, при дополнительном введении заявленного лекарственного средства при приеме антибиотиков происходит снижение терапевтической дозы антибиотика.
Технический результат настоящего изобретения заключается в расширении арсенала лекарственных антибактериальных средств, создании антибактериального средства широкого спектра действия, эффективного в отношении, в том числе, резистентных к одному или нескольким антибиотикам бактерий, обладающего низкой токсичностью и мутагенностью, что позволяет снижать нагрузку на организм пациента при антибактериальной терапии; также заявленное средство повышает эффективность фармакологического действия антибиотика, в том числе в отношении резистентных бактерий, и снижает терапевтическую дозу антибиотика, что приводит к снижению побочных эффектов во время их приема и после курса приема антибиотиков.
Продукты технологической обработки методом последовательных множественных разведений исходных субстанций антител к β1 - домену молекулы главного комплекса гистосовместимости класса 2 (HLA-DRB1) и β2-микроглобулину (β2-МГ) представляют собой водное или водно-
спиртовое разведения антител (или сочетание таких разведений), полученные путем последовательного многократного разведения (потенцирования) матричного исходного раствора антител в сочетании с внешним воздействием - встряхиванием каждого разведения.
В предшествующих работах, например, в патенте RU 2205025 C1, 26.12.2001 заявитель для описания продуктов технологической обработки методом последовательных множественных разведений исходных субстанций антител использовал термин «активированная-потенцированная форма антител», «сверхмалые дозы антител». При этом заявитель обращает внимание на то, что термин «продукт технологической обработки методом последовательных множественных разведений исходных субстанций антител» и термин «активированная - потенцированная форма антител», «сверхмалые дозы антител», «сверхвысокие разведения антител», «потенцированные антитела», «релиз-активные антитела» полностью взаимозаменяемые [Эпштейн О.И. Релиз-активность (современный взгляд на гомеопатию и негомеопатию). М.: Издательство РАМН, 2017. 48 с. // Эпштейн О.И. Сверхмалые дозы (история одного исследования). М.: Издательство РАМН, 2008. 336 с.].
При этом под разведением антител к HLA-DRB1 и антител к β2-МГ следует понимать любые, в том числе десятичные, сотенные, тысячные разведения матричного раствора антител, начиная с С2 (т.е. с разведения матричного раствора в 1002 раз), а также любые их сочетания (например, C2+D34+M45, D20+C4 и др.) и соотношения (например, 1:1:2, 2:3 и др.).
Для приготовления заявленного лекарственного средства в качестве исходной субстанции антител используют естественные, моноклональные или поликлональные антитела, которые могут быть получены по известным технологиям - методикам описанным, например, в: Мягкова М.А., Морозова B.C. Иммунохимические свойства естественных антител к физиологически активным соединениям, Фундаментальные исследования №11, 2014, с. 1066-1070 и Иммунологические методы, под
ред. Г. Фримеля, М., «Медицина», 1987, с. 9-33; или, например, в статье Laffly Е., Sodoyer R. Hum. Antibodies. Monoclonal and recombinant antibodies, 30 years after. - 2005 - Vol.14. - N 1-2. P.33-55 и обладающие специфичностью в отношении антигенов - HLA-DRB1 и β2-МГ.
Естественные антитела - иммуноглобулины, которые вырабатываются организмом в строго определенных количествах в полном отсутствии какой-либо внешней антигенной стимуляции, поэтому эти антитела, как правило, циркулируют в кровотоке даже здоровых людей. Естественные аутоантитела как правило полиреактивны и имеют достаточно низкую аффинность к определенному набору аутоантигенов.
Моноклональные антитела - это гетерогенные антитела к конкретному эпитопу антигена, полученные из одного клона антител-продуцирующих В-клеток [Lipman NS1, Jackson LR, Trudel LJ, Weis-Garcia F. Monoclonal versus polyclonal antibodies: distinguishing characteristics, applications, and information resources. ILAR J. 2005; 46(3):258-68. // IHC Staining Methods. Fifth edition. Preface Chapter 1. Thomas Boenisch. Antibodies. р:1-9]. Моноклональные антитела получают, например, с помощью гибридомной технологии. Причем начальная стадия процесса включает иммунизацию, основанную на принципах, уже разработанных при приготовлении поликлональных антисывороток. Дальнейшие этапы работы предусматривают получение гибридных клеток, продуцирующих клоны одинаковых по специфичности антител. Их выделение в индивидуальном виде проводится теми же методами, что и в случае поликлональных антисывороток.
Поликлональные антитела - это совокупность иммуноглобулинов, реагирующих с различными эпитопами специфического антигена и секретируемые В-клетками различных линий организма [Lipman NS1, Jackson LR, Trudel LJ, Weis-Garcia F. Monoclonal versus polyclonal antibodies: distinguishing characteristics, applications, and information resources. ILAR J. 2005; 46(3):258-68. // IHC Staining Methods. Fifth edition.
Preface Chapter 1. Thomas Boenisch. Antibodies. р:1-9]. Поликлональные антитела могут быть получены активной иммунизацией животных. Для этого по специально разработанной схеме животным делают серию инъекций требуемым в соответствии с изобретением веществом -антигеном. В результате проведения такой процедуры получают моноспецифические антисыворотки с высоким содержанием антител, которые используют в технологической обработке исходных субстанций методом последовательных множественных разведений для получения конечного продукта. При необходимости проводят очистку антител, присутствующих в антисыворотке, например, методом аффинной хроматографии, путем применения фракционирования солевым осаждением или ионообменной хроматографии.
Согласно вышесказанному, под термином «антитела» понимают иммуноглобулины любого происхождения (естественные, поликлональные или моноклональные антитела), которые специфически связываются с молекулой-мишенью (антигеном). При этом, способность антител распознавать определенный тип эпитопов молекулы антигена и взаимодействовать с ним - специфичность - ключевое свойство антител, определяющее весь спектр эффектов того или иного антитела [Boyd WC. Fundamentals of immunology. Fundam. Immunol. 1946; Langman RE. The specificity of immunological reactions. Mol. Immunol. 2000; 37: 555-561]. Специфичность не зависит от природы происхождения и способа получения последних: естественные, поликлональные или моноклональные антитела при одной и той же специфичности будут воздействовать на одну и ту же мишень [А. Ройт и др., Иммунология. Пер. с англ. - М.: Мир, 2000, с. 149-161, 527-544], а следовательно, могут применяться для получения заявленного средства.
Вариантом для приготовления заявленного лекарственного средства является использование поликлональных антител, которые в качестве матричного (первичного) раствора с концентрацией 0,5÷5,0 мг/мл,
используют для технологической обработки методом последовательных множественных разведений для получения конечного продукта.
Технологическая обработка методом последовательных множественных разведений исходных субстанций антител представляет собой равномерное уменьшение концентрации в результате последовательного разведения 1 части упомянутого матричного раствора в 9 частях (для десятичного разведения D) или в 99 частях (для сотенного разведения С) или в 999 частях (для тысячного разведения М) нейтрального растворителя в сочетании с внешним воздействием (например, в виде встряхивания) на каждое полученное разведение и использованием отдельных емкостей для каждого последующего разведения [В. Швабе "Гомеопатические лекарственные средства", М., 1967 г., с. 14-29].
Было установлено, что внешне простая процедура последовательного многократного уменьшения концентрации веществ является сложной технологией, продукты которой приобретают уникальные свойства. Исторически продукты технологии потенцирования называют «малыми дозами», «потенцированными препаратами», «высокими разведениями».
Конечный продукт может быть представлен в различных лекарственных формах [ОФС.1.6.2.001.18 Государственная фармакопея РФ, издание XIV] и содержать фармацевтически приемлемые добавки.
Так, например, заявленное лекарственное средство может быть выполнено в твердой лекарственной форме и содержать технологически необходимое (эффективное) количество фармацевтически приемлемой добавки, представляющей собой нейтральный носитель (например, лактоза), насыщенный смесью продуктов технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 и β2-МГ, и фармацевтически приемлемые вспомогательные вещества (эксципиенты), которые включают, например,
гипромеллоза, мальтитол, глицерол, сорбат калия, лиманная кислота безводная, изомальт, кремния диоксид, цикламат натрия, сахарин натрия, целлюлозу микрокристаллическую, магния стеарат и другие.
Для получения твердой оральной формы заявленного лекарственного средства в установке кипящего слоя (например, типа « Pilotlab» производства компании
Pilotlab» производства компании  GmbH) производят орошение до насыщения вводимых в псевдоожиженный - кипящий слой гранул нейтрального носителя - лактозы (молочного сахара), предварительно полученным водным или водно-спиртовым раствором (концентрация подбирается экспериментальным путем,
GmbH) производят орошение до насыщения вводимых в псевдоожиженный - кипящий слой гранул нейтрального носителя - лактозы (молочного сахара), предварительно полученным водным или водно-спиртовым раствором (концентрация подбирается экспериментальным путем,
ОФС.1.6.2.0010.18 Государственная Фармакопея) продуктов технологической обработки методом последовательных множественных разведений исходных субстанций антител с одновременной сушкой в потоке подаваемого под решетку нагретого воздуха при температуре не выше 40°С. Полученную таблеточную массу равномерно перемешивают и таблетируют прямым сухим прессованием (например, в таблет-прессе Korsch - XL 400) [WO 2007105981(А1), 20.09.2007]. После таблетирования получают таблетки массой 300 мг, пропитанные водным или водно-спиртовым раствором продуктов технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 и к β2-МГ.
Также заявленное лекарственное средство вместе с известным антибиотиком может составлять фиксированную или нефиксированную фармацевтическую комбинацию, применяемую для лечения бактериальных инфекций. Термин "фиксированная комбинация" обозначает, что активные ингредиенты, заявленное лекарственное средство и партнер по комбинации - антибиотик, оба вводят пациенту одновременно в единой лекарственной форме или дозировке. Термины "нефиксированная комбинация" или "набор" обозначает, что активные ингредиенты, заявленное лекарственное средство и партнер по
комбинации - антибиотик, оба вводят пациенту в виде отдельных элементов или одновременно или последовательно без специфических временных рамок, где такое введение обеспечивает терапевтически эффективные уровни двух активных ингредиентов в организме пациента. Заявленная комбинация лекарственного средства и антибиотика может использоваться для одновременного или последовательно применения для лечения бактериальных инфекций. При этом антибиотик вводится в известной терапевтической дозе.
Настоящее изобретение проиллюстрировано ниже представленными примерами вместе с прилагаемыми чертежами:
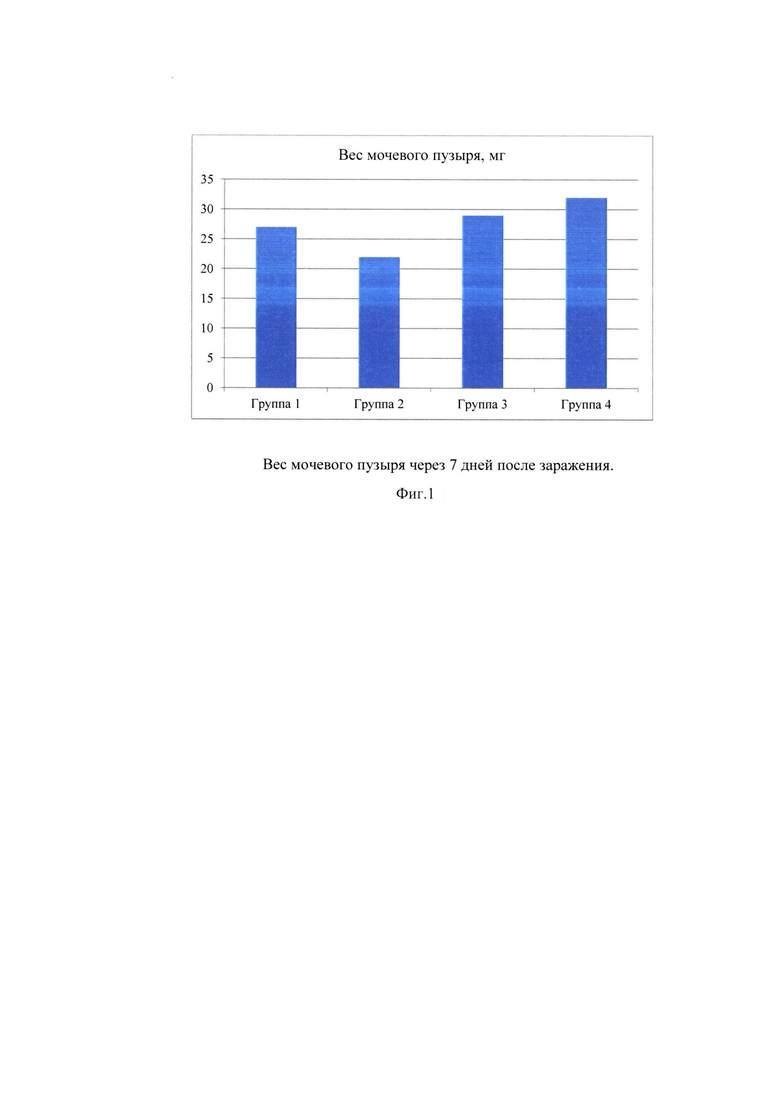
Фиг. 1. Вес мочевого пузыря через 7 дней после заражения.
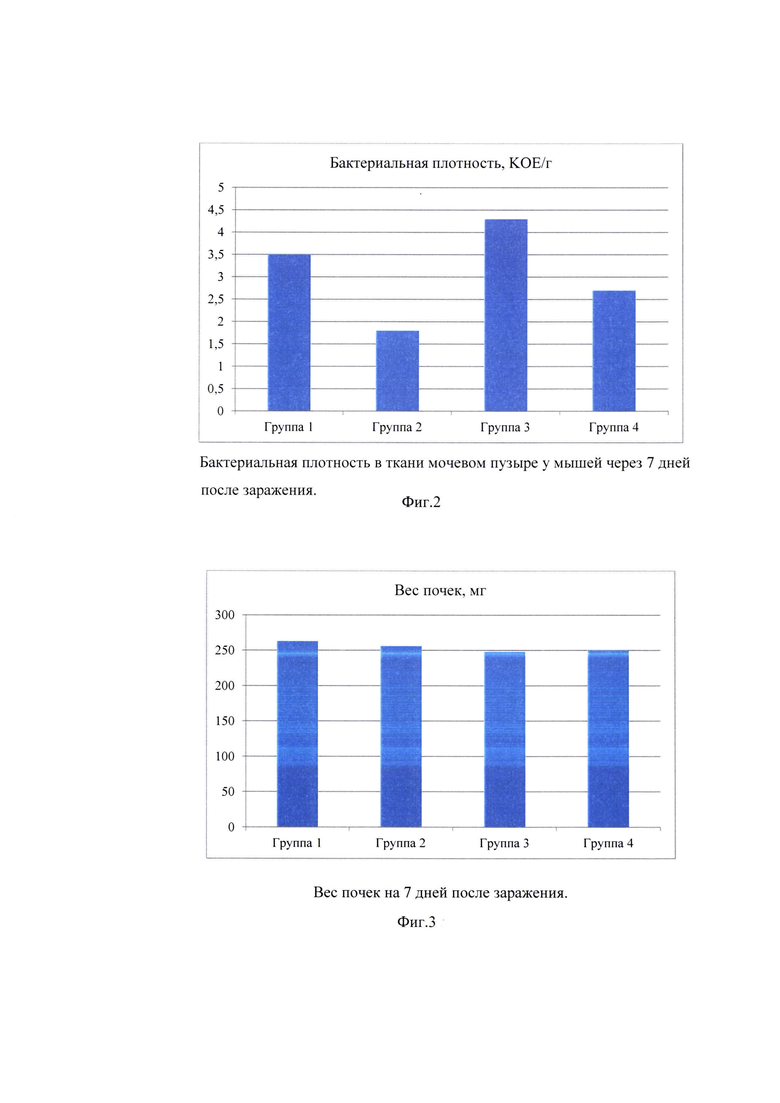
Фиг. 2. Бактериальная плотность в ткани мочевом пузыре у мышей через 7 дней после заражения.
Фиг. 3. Вес почек на 7 дней после заражения.
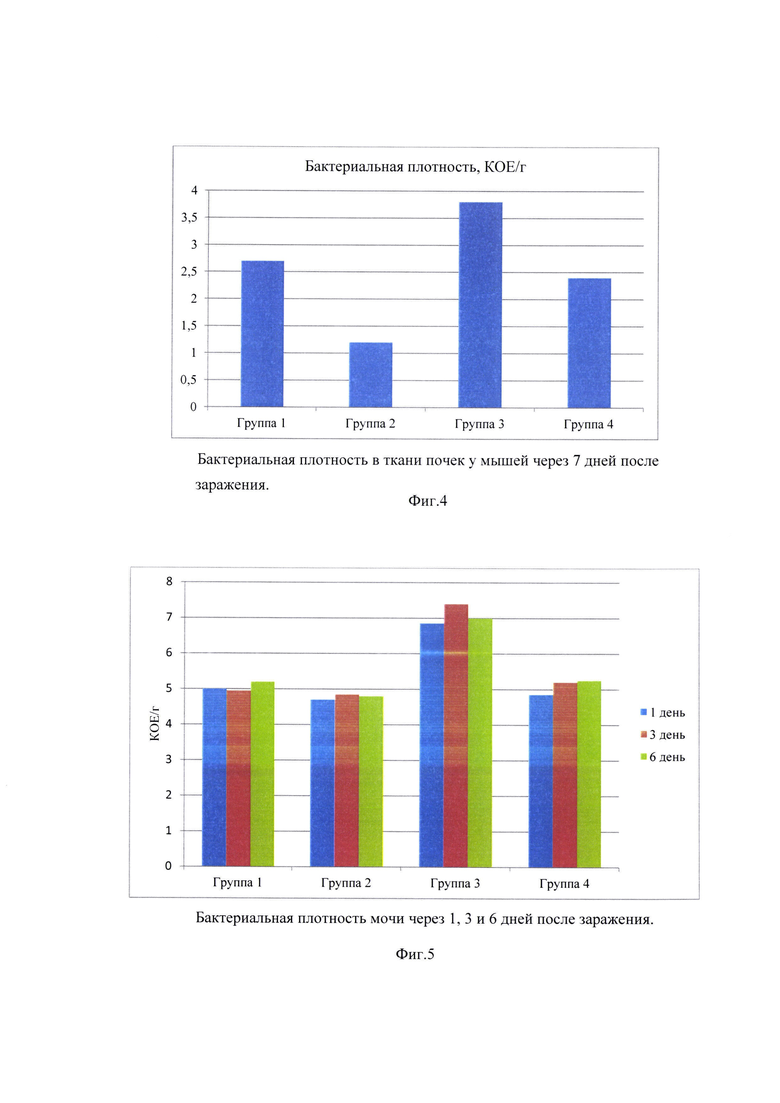
Фиг. 4. Бактериальная плотность в ткани почек у мышей через 7 дней после заражения.
Фиг. 5. Бактериальная плотность мочи через 1, 3 и 6 дней после заражения.
Пример 1
Противотуберкулезная активность заявленного лекарственного средства в отношении Mycobacterium tuberculosis вызванного у морских свинок.
Цель исследования изучить противотуберкулезную активность заявленного препарата в отношении Mycobacterium tuberculosis на модели экспериментального туберкулеза у морских свинок в сравнении с противотуберкулезным препаратом Изониазидом. Препарат по настоящему изобретению содержит в соотношении 1:2 по объему, продукт технологической обработки методом последовательных множественных разведений исходных субстанции антител к HLA-DRB1 (в водно-спиртовом
разведении С12С150 в соотношении 2:3, моноклональные антитела к HLA-DRB1) и продукт технологической обработки методом последовательных множественных разведений исходных субстанции антител к β2-МГ (в водном разведении С12С150 в соотношении 2:3, моноклональные антитела к β2-МГ). Экспериментальные группы:
Группа 1 - интактный контроль, незараженные животные (n=7);
Группа 2 - отрицательный контроль (зараженные, нелеченные животные) (n=7);
Группа 3 - животные, получавшие плацебо (вода очищенная) перорально 2 раза в день в течение 5 суток до заражения и 6 дней в неделю в течение двух месяцев через две недели после заражения в объеме 4 мл/кг (n=14);
Группа 4 - животные, получавшие плацебо (вода очищенная) перорально 2 раза в день в течение 5 суток до заражения и 6 дней в неделю в течение двух месяцев через две недели после заражения в объеме 4 мл/кг и Изониазид в дозе 10 мг/кг в объеме 0,4 мл 6 дней в неделю в течение двух месяцев через две недели после заражения (n=14);
Группа 5 - животные, получавшие препарат перорально 2 раза в день в течение 5 суток до заражения и 6 дней в неделю в течение двух месяцев через две недели после заражения в объеме 4 мл/кг (n=14);
Дизайн исследования:
Длительность настоящего исследования составила (196 дней, 6,5 месяцев): сентябрь-декабрь - наблюдение за экспериментальными животными и их лечение; январь-март - изучение отобранного при некропсии диагностического материала микробиологическими и гистологическими методами. Клинический осмотр, оценку внешнего вида, общего состояния здоровья, выявление смертности проводили ежедневно перед кормлением животных.
Исследуемые препараты вводили морским свинкам перорально с помощью шприца без иглы в общем объеме 8 мл/кг два раза в день в течение
5 суток до заражения и шесть дней в неделю (ежедневно, кроме воскресенья) в течение 2 месяцев после заражения. Доза препаратов корректировалась один раз в каждую неделю по результатам взвешивания животных. Водно-крахмальная суспензия изониазида вводилась животным в то же время и тем же способом, что и тестируемые образцы. Доза изониазида - 10 мг/кг веса в 0,4 мл водно-крахмальной кашицы.
В процессе исследования во всех группах морских свинок оценивали выживаемость, вес, интенсивность роста M.tuberculosis в посевах, гистологические изменения в органах животных.
Результаты исследования:
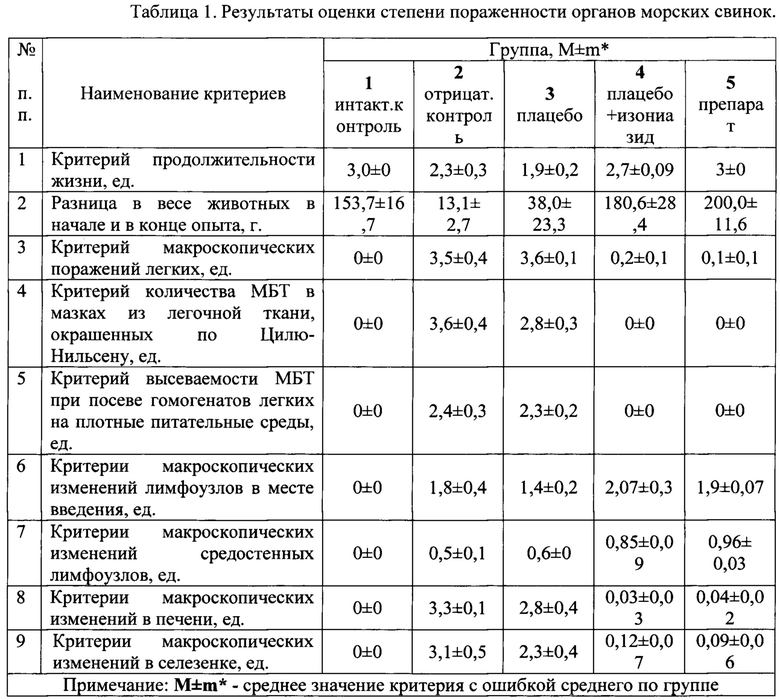
Вывод:
Анализ полученных в ходе исследования данных позволяет заключить, что положительный терапевтический эффект был одинаково отмечен в группе при лечении лабораторных животных Изониозидом и в группе при лечении заявленным Препаратом. Гистологическое исследование органов животных данных двух групп показало наличие признаков терапевтического патоморфоза. Также была продемонстрирована эффективность заявленного лекарственного средства в отношении легочных инфекций.
Пример 2
Антибактериальная активность заявленного лекарственного средства в отношении Streptococcus pyogenes у мышей в сочетании с антибиотиком и без него.
Данное исследование является слепым плацебоконтролируемым. Цель исследования оценить эффективность заявленного препарата с линезолидом (синтетический антибиотик) или телитромицином (антибиотик класса кетолидов) или без антибиотиков против Streptococcus pyogenes в модели нейтропенической инфекции мягких тканей мыши. Препарат по настоящему изобретению содержит в соотношении 2:3 по объему, продукт технологической обработки методом последовательных множественных разведений исходных субстанции антител к HLA-DRB1 (в водно-спиртовом разведении C4D20 в соотношении 3:2; моноклональные антитела) и продукт технологической обработки методом последовательных множественных разведений исходных субстанции антител к β2-МГ (в водно-спиртовом разведении С10С150 в соотношении 1:2; естественные антитела).
Экспериментальные группы:
Группа 1 - отрицательный контроль, мыши-самки были заражены S. pyogenes и не получали введение препарата или антибиотика в течение периода исследования; n=3.
Группа 2 - мыши-самки, получали плацебо (глициновый буфер) перорально ежедневно в объеме 20 мл/кг 5 дней до и в день заражения S. pyogenes; n=6.
Группа 3 - мыши-самки, получали плацебо (глициновый буфер) перорально ежедневно в объеме 20 мл/кг 5 дней до и в день заражения S. pyogenes; в сочетании с линезолидом (50 мг/кг) в день заражения через 2 и 14 часов после заражения; n=6.
Группа 4 - мыши-самки, получали плацебо (глициновый буфер) перорально ежедневно в объеме 20 мл/кг 5 дней до и в день заражения S. pyogenes; в сочетании с телитромицином (10 мг/кг) в день заражения через 2 и 14 часов после заражения; n=6.
Группа 5 - мыши-самки, получали препарат перорально ежедневно в объеме 20 мл/кг 5 дней до и в день заражения S. pyogenes; n=6.
Группа 6 - мыши-самки, получали препарат перорально ежедневно в объеме 20 мл/кг 5 дней до и в день заражения S. pyogenes; в сочетании с линезолидом (50 мг/кг) в день заражения через 2 и 14 часов после заражения; n=6.
Группа 7 - мыши-самки, получали препарат перорально ежедневно в объеме 20 мл/кг 5 дней до и в день заражения S. pyogenes; в сочетании с телитромицином (10 мг/кг) в день заражения через 2 и 14 часов после заражения; n=6.
Дизайн исследования:
Продолжительность исследования составила 7 дней. Нейтропения у мышей была вызвана двумя интраперитонеальными дозами циклофосфамида (за 4 дня до заражения - 150 мг/кг и за 1 день - 100 мг/кг). Мыши не получали дальнейшую иммуносупрессию на протяжении всего исследования.
Экспериментальные образцы вводили в течение 5 дней до заражения, а также в день заражения (через 2 и 14 часов) перорально в дозе 20 мл/кг. В день заражения мышам вводили в мышцу бедра штамм S. pyogenes (АТСС ВАА-2469) в дозе 5,4 lg КОЕ. Также через 2 и 14 часов после заражения
животным вводили антибиотики - линезолид (50 мг/кг), к которому данный штамм S. pyogenes чувствителен, и телитромицин (10 мг/кг), к которому штамм резистентен.
В процессе исследования во всех группах мышей оценивали выживаемость, клинические проявления инфекции, массу тела.
Результаты исследования:
Через 2 часа после заражения у мышей, не получавших лечения (Группа 1), забиралась мышца бедра для оценки бактериальной плотности (КОЕ/г, log10). В остальных группах мышца бедра для оценки бактериальной плотности забиралась через 24 часа после заражения. Полученные данные представлены в таблице 2.
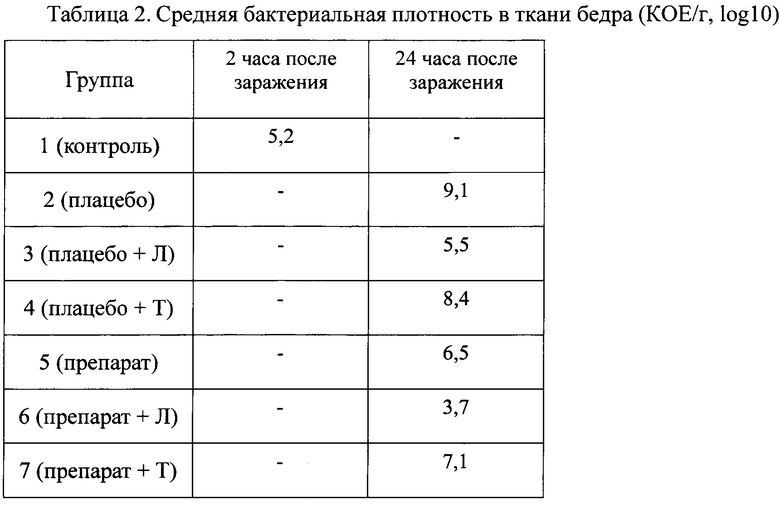
Вывод:
Через 24 часа после заражения испытуемые группы (Группа 3 и 6) при введении в комбинации с линезолидом продемонстрировали статистически значимое снижение средней бактериальной нагрузки. Таким образом, заявленное лекарственное средство эффективно в отношении инфекций костно-мышечной системы, а также в комбинации с антибиотиками, повышает их эффективность.
Пример 3
Эффективность заявленного лекарственного средства отдельно и в комбинации с антибиотиком в отношении E.coli на модели инфекции мочевыводящих путей у мышей.
Цель исследования оценить влияние тестируемого препарата в условиях экспериментальной инфекции у мышей, вызванной E.coli в сочетании с антибиотиком Норфлоксацином и без него. Препарат по настоящему изобретению содержит, в соотношении 1:1 по объему, продукты технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 (в водном разведении С12С30С50 в соотношении 1:1:1; поликлональные антитела) и антител к β2-МГ (в водном разведении С12С30С50 в соотношении 1:1:1; моноклональные антитела).
Экспериментальные группы:
Группа 1 - мыши обоего пола (n=10) получали заявленный препарат (20 мл/кг) ежедневно через пероральный зонд в течение 5 дней до заражения и 7 дней после заражения и через 1 час после заражения внутрибрюшинно (объем 10 мл / кг).
Группа 2 - мыши обоего пола (n=10) получали заявленный препарат (20 мл/кг) ежедневно через пероральный зонд в течение 5 дней до заражения и 7 дней после заражения. Через 1 час после заражения внутрибрюшинно вводили Норфлоксацин 5 мг/кг (объем 10 мл / кг).
Группа 3 - контроль, мыши обоего пола (n=10) получали глициновый буфер (20 мл/кг) ежедневно через пероральный зонд в течение 5 дней до заражения и 7 дней после заражения и через 1 час после заражения внутрибрюшинно (объем 10 мл / кг).
Группа 4 - мыши обоего пола (n=10) получали глициновый буфер (20 мл/кг) ежедневно через пероральный зонд в течение 5 дней до заражения и 7 дней после заражения. Через 1 час после заражения внутрибрюшинно вводили Норфлоксацин 5 мг/кг (объем 10 мл / кг).
Дизайн исследования:
Мышей инфицировали E.coli UTI89 (2,107 КОЕ/мышь) путем интрауретральной инокуляции в мочевой пузырь (день 0).
Через 1, 3 и 6 дней после заражения мочу собирали для определения КОЕ. Через семь дней после заражения умерщвляли по 10 животных в каждой группе и собирали почки и мочевой пузырь для анализа бактериальной нагрузки. Массу тела регистрировали каждые 2 дня в течение всего эксперимента.
Результаты исследования:
Динамика массы тела во всех группах была положительной, это свидетельствует о хорошей переносимости экспериментальных образцов животными.
Вес мочевого пузыря был статистически значимо ниже в Группе 2 (препарат + норфлоксацин) по сравнению с Группой 4 (гл.буфер + норфлоксацин). Это может указывать на то, что заявленный препарат в сочетании с антибиотиками может уменьшить отек мочевого пузыря.
Заявленный препарат в сочетании с норфлоксацином (Группа 2) статистически значимо уменьшал бактериальную нагрузку в мочевом пузыре. Таким образом, эта комбинация может быть перспективной в качестве терапевтической схемы (Фиг. 1, 2).
Статистически значимых различий между группами по весу почек не было зарегистрировано.
Заявленный препарат в сочетании с норфлоксацином (Группа 2) статистически значимо уменьшал бактериальную нагрузку в почках по сравнению с глициновым буфером (Группа 3). Таким образом, эта комбинация может быть перспективной в качестве терапевтической схемы (Фиг. 3, 4).
Начиная с 3-го дня, образец Группы 2 (препарат + норфлоксацин) имел пониженную бактериальную плотность в моче по сравнению с Группой 4 (гл.буфер + норфлоксацин). Образец Группы 3 (гл.буфер) имел более высокий
КОЕ в моче во всех временных точках по сравнению с образцом Группы 1 (препарат) (Фиг. 5). Вывод:
Таким образом, заявленное лекарственное средство в сочетании с антибиотиком Норфлоксацином проявляет антибактериальную активность в отношении E.coli на модели инфекции мочевыводящих путей у мышей.
Пример 4. Токсичность
Токсикологические исследования были проведены в соответствии с принципами надлежащей лабораторной практики (ГОСТ 33044-2014) и «Руководством по проведению доклинических исследований лекарственных средств» [Миронов А.Н., Бунатян Н.Д. Руководство по проведению доклинических исследований лекарственных средств. М. Гриф и К. 2012; 944 с.].
В связи с тем, что привычные параллели фармакокинетики и фармакодинамики (связь доза - концентрация - эффект), принятые для большинства лекарственных средств, к заявленному лекарственному средству (продукт технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 и β2-МГ) не применимы (существующие физико-химические и иммунологические методы не позволяют регистрировать концентрации препарата в биологических средах организма) при подборе доз для токсикологических исследований ориентировались на физиологически приемлемые объемы носителя (в экспериментальных исследованиях - очищенной воды), в которых вносится лекарственный препарат.
Токсичность при остром введении:
Исследование выполнено на нелинейных половозрелых белых мышах обоего пола (масса 22-26 г, возраст 2,5 мес) и половозрелых крысах линии Вистар обоего пола (масса 225-250 г, возраст 4 мес) при внутрижелудочном
введении. Исследуемый препарат (n=18) или очищенную воду (контроль, n=18) вводили дважды с интервалом в 2 часа в максимально допустимых объемах: внутрижелудочно - 25 мл/кг мышам и 20 мл/кг крысам. Интактная группа не получала никаких веществ (n=18). После введения веществ наблюдение за животными вели в течение 2 недель.
Полученные данные анализировали с помощью многофакторного дисперсионного анализа (two-way ANOVA) с последующим сравнением всех групп друг с другом пост-хок критерием Тьюки. Различия считали статистически значимыми при р<0,05.
Введение заявленного препарата, содержащего продукт технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 (в водном разведении С12С30С50 в соотношении 2:1:3; поликлональные антитела) и антител к β2-МГ (в водном разведении С12С30С50 в соотношении 2:1:3; поликлональные антитела) внутрижелудочно в максимально допустимых объемах половозрелым мышам и крысам не меняло общего состояния животных (отсутствовали признаки беспокойства, изменения аппетита, выделений, состояния слизистых, шерсти, кожи и др.) и не влияло на прирост общей массы крыс и мышей (как самок, так и самцов).
Отсутствие летальности у животных, получавших препарат, не позволило определить показатель ЛД50. Условно за ЛД50 приняли дозу, превышающую максимальный введенный животным объем препарата.
Учитывая, что двукратное внутрижелудочное введение заявленного препарата в максимально допустимых объемах не оказало токсического действия на организм животных, можно сделать вывод о его безвредности и основание отнести к классу малотоксичных или к 5 категории по классификации GHS.
Токсичность при введении повторных доз:
Исследование проведено на 200 половозрелых белых конвенциональных крысах обоего пола (масса 180-242 г, возраст 3,5-4 мес.) и
24 половозрелых кроликах породы «Шиншилла» обоего пола (масса 1,9 кг, возраст 2,5-3 мес). Поскольку не удалось определить величину ЛД50 для препарата, в исследовании хронической токсичности на крысах препарат или очищенную воду вводили внутрижелудочно в максимально допустимом объеме для внутрижелудочного введения и в 1/4 максимально допустимого объема. Кролики получали препарат в объеме, приближенном к ежесуточной норме потребления воды.
Продолжительность введения составляла 6 месяцев, состояние крыс и кроликов оценивали через 3 и 6 месяцев после начала введения препарата, а также спустя месяц отмены.
Хроническое внутрижелудочное введение препарата по настоящему изобретению взрослым крысам обоего пола в дозах, превышающих более чем в 100 раз рекомендованные суточные дозы для человека, не вызывало гибели животных в течение 6 месяцев введения, значимых изменений по сравнению с контрольной группой в поведенческой активности, морфологических и функциональных показателей периферической крови - через 3 и 6 месяцев введения, а также через 1 месяц после отмены препарата
Хроническое введение препарата в указанных дозах также не сопровождалось значимыми изменениями в макро- и микроморфологическом состоянии и гистологической архитектоники внутренних органов крыс.
В исследовании на кроликах весь период исследования также не было отмечено гибели животных. Хроническое введение препарата не оказывало значимого влияния на общее состояние, поведение, массу тела животных, а также на показатели периферической крови и костномозгового кроветворения. По результатам биохимических исследований плазмы крови у кроликов существенных изменений не обнаружено. Не выявлено также изменений при обследовании мочи у кроликов, получавших препарат в течение 6-ти месяцев. При макроскопическом обзоре внутренних органов кроликов, получавших препарат в течение 6-ти месяцев, патологических
изменений не выявлено. При гистологическом исследовании тканей органов также не зафиксировано патологических изменений.
Таким образом, на основании проведенных исследований можно заключить, что заявленный препарат при шестимесячном внутрижелудочном введении половозрелым крысам в дозе 10 мл/кг и кроликам в дозе 50 мл/кг (более чем в 100 раз превышающих средние суточные дозы для человека) не оказывает существенного влияния на общее состояние и поведение животных; не вызывает патологических и морфофункциональных изменений со стороны сердечно-сосудистой, пищеварительной и выделительной систем.
Изобретение относится к фармацевтической промышленности, а именно к лекарственному средству для лечения бактериальных инфекций. Лекарственное средство для лечения бактериальных инфекций, вызванных бактериями, выбранными из Mycobacterium tuberculosis, Streptococcus pyogenes, Salmonella enteritidis, Escherichia coli, Klebsiella pneumoniae, Chlamydophila pneumonia, а также бактериями Klebsiella pneumoniae, резистентными к амоксициллину и клавулановой кислоте, бактериями Salmonella enterica, резистентными к стрептомицину или налидиксовой кислоте, представляющее собой смесь, включающую в эффективном количестве в виде десятичных и сотенных разведений в соотношении 1:1, 1:2 или 2:3 продукта технологической обработки методом последовательных множественных разведений исходных субстанций антител к β1 - домену молекулы главного комплекса гистосовместимости класса 2 (HLA-DRB1) и продукта технологической обработки методом последовательных множественных разведений исходной субстанции антител к β2-микроглобулину (β2-МГ), где продукт технологической обработки методом последовательных множественных разведений исходной субстанции антител представляет собой водный или водно-спиртовой раствор, полученный путем многократного последовательного разведения матричного исходного раствора антител в сочетании с внешним механическим воздействием - многократным встряхиванием каждого разведения, при этом в качестве матричного раствора используется концентрация антител 0,5÷5,0 мг/мл. Изобретение обеспечивает эффективное лечение бактериальных инфекций, снижение резистентности антибиотиков, повышение эффективности терапевтического действия антибиотиков, в том числе в отношении резистентных бактерий. 8 з.п. ф-лы, 2 табл., 4 пр., 5 ил.
1. Лекарственное средство для лечения бактериальных инфекций, вызванных бактериями, выбранными из Mycobacterium tuberculosis, Streptococcus pyogenes, Salmonella enteritidis, Escherichia coli, Klebsiella pneumoniae, Chlamydophila pneumonia, а также бактериями Klebsiella pneumoniae, резистентными к амоксициллину и клавулановой кислоте, бактериями Salmonella enterica, резистентными к стрептомицину или налидиксовой кислоте, представляющее собой смесь, включающую в эффективном количестве в виде десятичных и сотенных разведений в соотношении 1:1, 1:2 или 2:3 продукта технологической обработки методом последовательных множественных разведений исходных субстанций антител к β1 - домену молекулы главного комплекса гистосовместимости класса 2 (HLA-DRB1) и продукта технологической обработки методом последовательных множественных разведений исходной субстанции антител к β2-микроглобулину (β2-МГ), где продукт технологической обработки методом последовательных множественных разведений исходной субстанции антител представляет собой водный или водно-спиртовой раствор, полученный путем многократного последовательного разведения матричного исходного раствора антител в сочетании с внешним механическим воздействием - многократным встряхиванием каждого разведения, при этом в качестве матричного раствора используется концентрация антител 0,5÷5,0 мг/мл.
2. Лекарственное средство по п. 1, где бактериальная инфекция представляет собой туберкулез.
3. Лекарственное средство по п. 1, где бактериальная инфекция представляет собой сальмонеллез.
4. Лекарственное средство по п. 1, где бактериальная инфекция представляет собой коли-инфекцию.
5. Лекарственное средство по п. 1, где бактериальная инфекция представляет собой стрептококковую инфекцию.
6. Лекарственное средство по п. 1, где антитело представляет собой моноклональное, поликлональное или естественное антитело к HLA-DRB1.
7. Лекарственное средство по п. 1, где антитело представляет собой моноклональное, поликлональное или естественное антитело к β2-микроглобулину.
8. Лекарственное средство по п. 1, дополнительно включающее фармацевтически приемлемые добавки.
9. Лекарственное средство по п. 1, выполненное в твердой лекарственной форме и содержащее эффективное количество гранул нейтрального носителя, насыщенного смесью продуктов технологической обработки методом последовательных множественных разведений исходных субстанций антител к HLA-DRB1 и антител к β2-микроглобулину, и фармацевтически приемлемые вспомогательные вещества.
| СПОСОБ КОРРЕКЦИИ ИММУННОГО ОТВЕТА И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2001 |
|
RU2205025C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| ЛЕЧЕНИЕ ИНФЕКЦИИ, ВЫЗЫВАЕМОЙ МИКРООРГАНИЗМАМИ | 2002 |
|
RU2303460C2 |
Авторы
Даты
2022-08-22—Публикация
2019-08-29—Подача