Изобретение относится к химической технологии и может быть использовано для очистки жидких щелочных металлов от кислорода.
Известным техническим решением является способ очистки натрия от кислорода с использованием геттеров (фольга йодидного циркония), в котором за счет химического взаимодействия происходит поглощение кислорода из натрия при температуре 550-650°C. [Козлов Ф.А., Кузнецов Э.К. Очистка натрия от кислорода с помощью горячих ловушек / Жидкие металлы. Сборник статей. - 1967. - С. 340-355].
Очистка происходит следующим образом. Фольгу йодидного циркония помещают в камеру и размещают камеру в циркуляционном контуре установки. Натрий прокачивают через камеру при температуре 550-670°C. Концентрацию кислорода контролируют пробоотборником-дистиллятором.
К недостаткам известного технического решения относятся:
- охрупчивание (разрушение) геттера при длительной работе ловушки, что приводит к выносу геттера в жидкометаллический контур;
- необходимость обеспечения относительно высокой рабочей температуры очистки натрия геттером, поскольку при более низкой температуре скорость поглощения кислорода фольгой йодидного циркония относительно низкая. Высокая рабочая температура очистки натрия усложняет процесс очистки.
Наиболее близкий по технической сущности к заявляемому техническому решению является способ очистки натрия от кислорода [АС СССР №246055. Способ очистки натрия от кислорода. Описание изобретения к авторскому свидетельству]. Способ очистки состоит из следующих этапов. В циркуляционную систему с натрием при температуре не ниже 400-450°C с помощью дозирующего устройства добавляют не более 1% металлического лития с работающей одновременно холодной ловушкой. Выдерживают систему некоторое время при 400-450°C. Натрий подвергают фильтрации при температуре 110-130°C с помощью холодной ловушки. Натрий нагревают на входе в циркуляционную систему до температуры 400-450°C.
К недостаткам данного способа относятся:
- неполное взаимодействие геттера с кислородом и попадание геттера в очищенный натрий из-за отсутствия учета баланса между реагирующими компонентами;
- выполнение относительно большого количества операций, таких как введение в натрий с помощью дозирующего устройства металлического лития, охлаждение натрия, фильтрация и нагрев натрия;
- необходимость использования холодной ловушки для фильтрации.
Задачей заявленного технического решения является снижение концентрации кислорода и растворенного геттера в очищенном жидком щелочном металле и уменьшение количества операций при очистке.
Для исключения недостатков в способе очистки жидкого щелочного металла от кислорода, включающем нагрев, прокачку жидкого щелочного металла и его фильтрацию предлагается:
- подавать жидкий щелочной металл в ограниченное обечайкой пространство;
- определять температуру жидкого щелочного металла и концентрацию кислорода в нем;
- прокачивать жидкий щелочной металл через последовательно установленные в ограниченном обечайкой пространстве слой растворимого геттера и реакционную объем;
- фильтровать путем прокачки через сепаратор частиц, установленный в ограниченном обечайкой пространстве вслед за слоем растворимого геттера и реакционным объемом;
- отводить жидкий щелочной металл из ограниченного обечайкой пространства;
- массовый расход жидкого щелочного металла через ограниченное обечайкой пространство определять из соотношения, описывающего связь между массовым расходом жидкого щелочного металла через слой растворимого геттера, концентрациями кислорода в исходном и очищенном жидком щелочном металле, концентрацией насыщения растворимого геттера в жидком щелочном металле при температуре очистки, относительной атомной массой кислорода и растворимого геттера в образующемся оксиде геттера, количеством атомов кислорода и растворимого геттера в образующемся оксиде геттера, константой скорости растворения геттера в жидком щелочном металле, объемом слоя растворимого геттера, удельной поверхностью геттера (отношением поверхности геттерной насадки к объему растворимого геттера), пористостью слоя растворимого геттера и плотность жидкого щелочного металла.
В частных случаях осуществления способа предлагается:
- подачу жидкого щелочного металла в ограниченное обечайкой пространство осуществлять с помощью электромагнитного насоса;
- определять температуру жидкого щелочного металла и концентрацию кислорода в нем соответственно с помощью датчика температуры и электрохимического датчика кислорода;
- фильтрацию жидкого щелочного металла осуществлять с помощью сепаратора частиц;
- для обеспечения взаимодействия растворимого геттера с кислородом в жидком щелочном металле в качестве растворимого геттера использовать магний;
- для обеспечения взаимодействия растворимого геттера с кислородом в жидком щелочном металле в качестве растворимого геттера использовать барий;
- для обеспечения взаимодействия растворимого геттера с кислородом в жидком щелочном металле в качестве растворимого геттера использовать кальций;
- температуру жидкого щелочного металла в ограниченном обечайкой пространстве во время взаимодействия растворимого геттера с кислородом в жидком щелочном металле и в процессе фильтрации поддерживать одинаковой.
Технический результат - увеличение эффективности очистки жидкого щелочного металла и упрощение процесса очистки.
Сущность способа очистки жидкого щелочного металла от кислорода заключается в следующем.
Жидкий щелочной металл подают в ограниченное обечайкой пространство. Температуру жидкого щелочного металла и концентрацию кислорода в нем определяют.
Жидкий щелочной металл прокачивают через последовательно установленные в ограниченном обечайкой пространстве слой растворимого геттера и реакционный объем.
Жидкий щелочной металл фильтруют путем прокачки через сепаратор частиц, установленный в ограниченном обечайкой пространстве вслед за слоем растворимого геттера и реакционной емкостью.
Очищенный жидкий щелочной металл отводят из ограниченного обечайкой пространства.
Прокачку через ограниченное обечайкой пространство производят с расходом, определенным из соотношения:
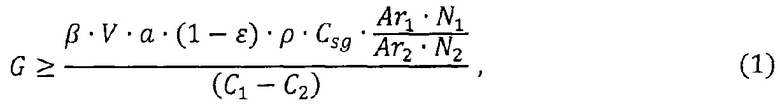
где: G - массовый расход жидкого щелочного металла через слой растворимого геттера, кг/с; C1 и С2 - концентрации кислорода в исходном и очищенном жидком щелочном металле соответственно, млн-1; Csg - концентрация насыщения растворимого геттера в жидком щелочном металле при температуре очистки, млн-1 (справочные данные); Ar1 и Ar2 - относительная атомная масса кислорода и растворимого геттера в образующемся оксиде геттера соответственно (справочные данные); N1 и N2 - количество атомов кислорода и растворимого геттера в образующемся оксиде геттера соответственно (справочные данные); β - константа скорости растворения геттера в жидком щелочном металле, м/с; V - объем слоя растворимого геттера, м3; а - удельная поверхность геттера (отношение поверхности геттерной насадки к объему растворимого геттера), м2/м3; ε - пористость слоя растворимого геттера; ρ - плотность жидкого щелочного металла, кг/м3 (справочные данные).
Очистка жидкого щелочного металла от кислорода происходит непрерывно, основным условием которой является установленная величина расхода через ограниченное обечайкой пространство.
Семь частных случаев реализации способа.
- Подачу жидкого щелочного металла в ограниченное обечайкой пространство осуществляют с помощью электромагнитного насоса.
- Температуру жидкого щелочного металла и концентрации кислорода определяют в нем соответственно с помощью датчика температуры и электрохимического датчика кислорода.
- Фильтрацию осуществляют с помощью сепаратора частиц.
- Температуру жидкого щелочного металла в ограниченном обечайкой пространстве во время взаимодействия растворимого геттера с кислородом в жидком щелочном металле и в процессе фильтрации поддерживают одинаковой.
- В качестве растворимого геттера используют магний.
- В качестве растворимого геттера используют барий.
- В качестве растворимого геттера используют кальций.
Перечисленные металлы обладают относительно высокой способностью взаимодействия с кислородом в жидких щелочных металлах.
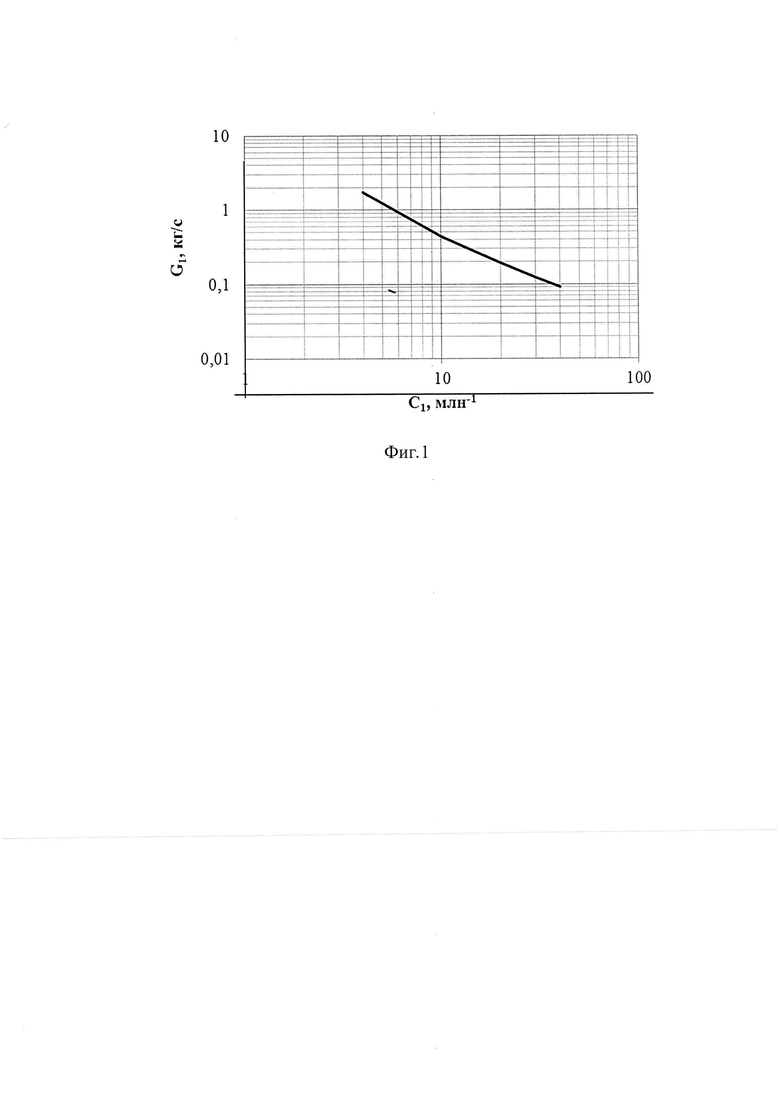
Зависимость расхода натрия через магний от исходной концентрации кислорода в натрии (для условий очистки, указанных в таблице 1) представлена на фиг. 1.
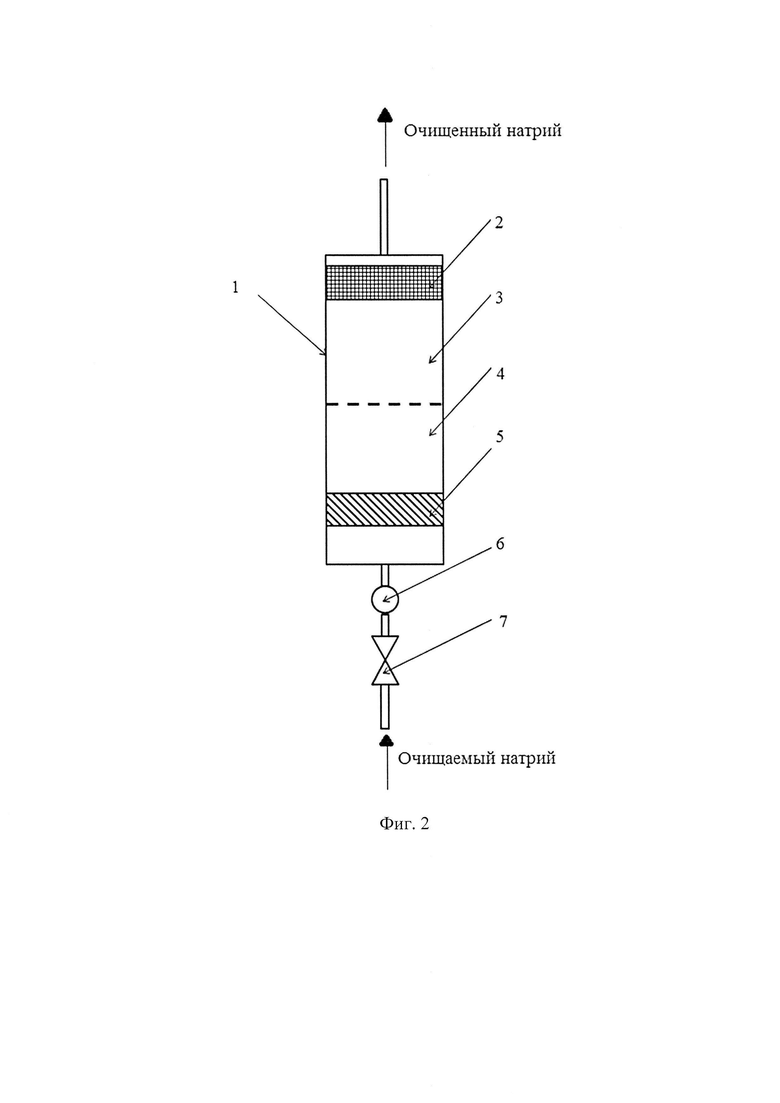
Схема реализации способа очистки натрия от кислорода представлена на фиг. 2. На фиг. 2 приняты следующие позиционные обозначения: 1 - ограниченное обечайкой пространство; 2 - сепаратор частиц; 3 - область выдержки (коагуляции); 4 - область гомогенного химического взаимодействия в потоке натрия; 5 - слой растворимого геттера; 6 - расходомер; 7 - регулирующий клапан.
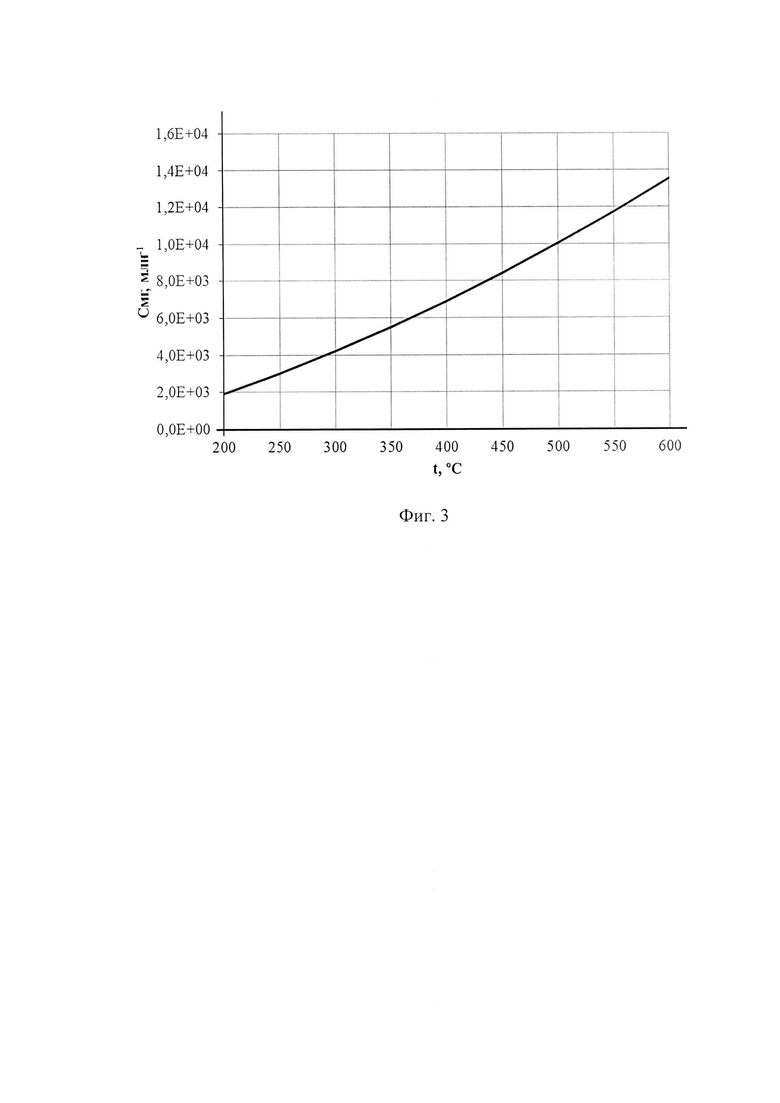
Кривая растворимости магния в натрии представлена на фиг. 3.
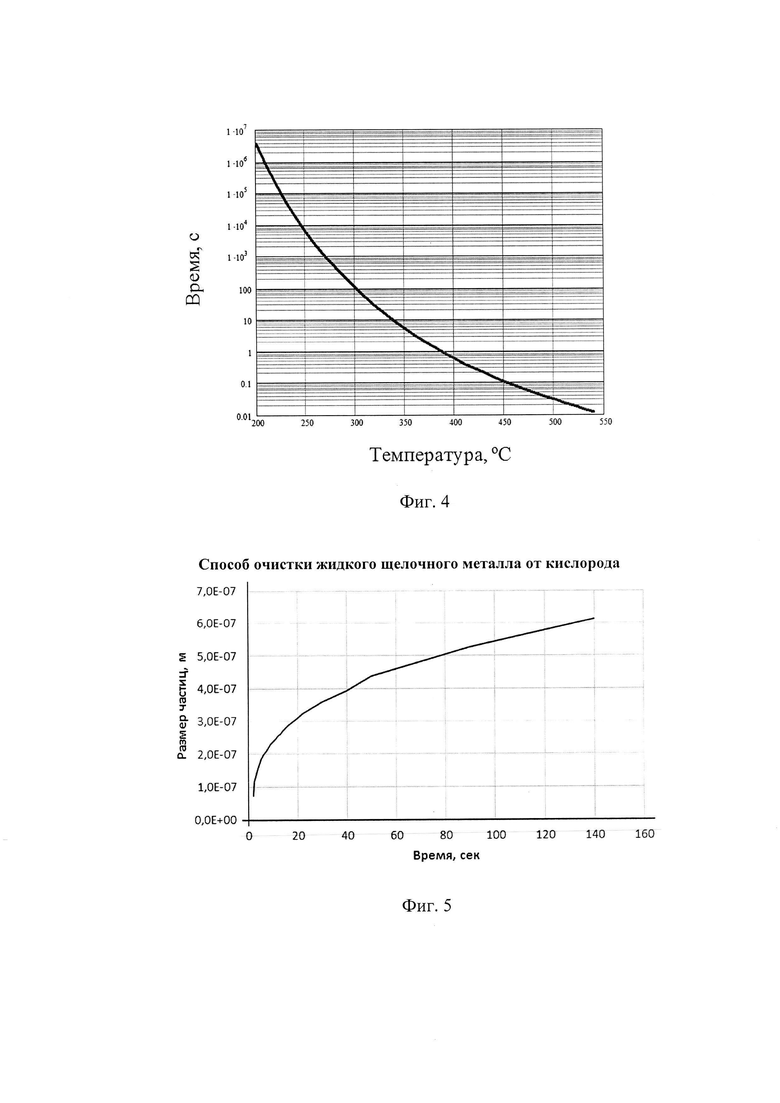
Зависимость времени взаимодействия магния с оксидом натрия в натрии от температуры представлена на фиг. 4.
Зависимость среднего размера ансамбля частиц взвеси от времени, температура теплоносителя 300°C представлена на фиг. 5.
Определение массового расхода, необходимого для обеспечения требуемой концентрации кислорода в очищенном натрии, осуществляется по соотношение (1).
Концентрация кислорода в исходном и очищенном натрии задаются в соответствии с требуемыми условиями.
Концентрация насыщения магния в натрии рассчитывается по уравнению растворимости (фиг. 3) [2], млн-1:
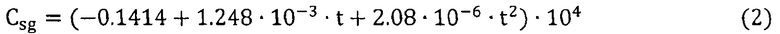
где Csg - концентрация насыщения магния в натрии при температуре очистки, млн-1; t - температура, °C.
Относительные атомные массы и количество атомов для кислорода и магния в образующемся оксиде магния являются справочными данными.
Константа скорости растворения магния в натрии также является справочной величиной.
Объем слоя магния в зависимости от необходимого количества очищаемого натрия рассчитывается по формуле:

где V - объем слоя магния, м3; MNa - масса очищаемого натрия, кг; ρMg - плотность магния, кг/м3; C1 и С2 - концентрации кислорода в исходном и очищенном натрии соответственно, млн-1; ε - пористость слоя магния.
Соотношение (3) получено исходя из условия взаимодействия всего магния с оксидом натрия, с учетом стехиометрии реакции магния с оксидом натрия и учета соотношения:

где V - объем слоя магния, м3; VMg - объем магния, м3; ε - пористость слоя магния.
Удельная поверхность магния и пористость слоя магния - справочные данные.
Массовый расход, определенный из соотношения (1) необходим для написания уравнения баланса кислорода в системе:

где G - массовый расход, кг/с; C1 - концентрация кислорода в натрии на входе в ограниченное обечайкой пространство, млн-1; С2 - концентрация кислорода в натрии на выходе из ограниченного обечайкой пространства, млн-1; Csg - концентрация магния в потоке натрия с расходом G, поступающего за счет растворения в слое магния, млн-1; Ar1 и Ar2 - относительная атомная масса кислорода и магния в образующемся оксиде магния соответственно; N1 и N2 - количество атомов кислорода и магния в образующемся оксиде магния соответственно.
Определение времени, достаточного для окисления геттера
В рассматриваемом процессе связывание кислорода в натрии происходит за счет образования соединения кислород-магний и протекания следующей реакции в теплоносителе:

Кинетика этой реакции ранее нигде не изучалась, поэтому используем аналогичные данные, полученные в экспериментах с вводом в натриевый контур расплавленного гидроксида натрия [1].
Температурная зависимость константы скорости прямой реакции (6) представлена в виде [1]:

где К - константа скорости прямой реакции, 1/с; Т - температура, К.
Время взаимодействия магния с оксидом натрия (время, достаточное для окисления геттера) оценивается по формуле:

где τ - время взаимодействия магния с оксидом натрия, с; Смг - изменение концентрации магния в натрии за счет реакции (6), млн-1; V - скорость реакции магния с оксидом натрия в натрии, млн-1/с, определяется из соотношения (9).

где К - константа скорости прямой реакции, 1/с; V - скорость реакции магния с оксидом натрия в натрии, млн-1/с.
Максимальная концентрация магния, растворенного в натрии, рассчитывается по формуле (3).
Расчеты в соответствии с зависимостью (8) позволили оценить время взаимодействия растворенного магния, при максимальном исходном его количестве, с оксидом натрия в натрии при различных температурах (полное срабатывание растворенного магния от состояния насыщения). На фиг. 4 показан график зависимости времени взаимодействия магния с оксидом натрия от температуры. Следует отметить, что при температуре 300°C значение времени взаимодействия составляет 100 секунд, это приемлемо для практической реализации способа.
Определение времени, достаточного для коагуляции
Время, достаточное для коагуляции, в течение которого размер взвешенных частиц оксида геттера достигает максимального значения, вычисляется решением кинетического уравнения коагуляции [3]:
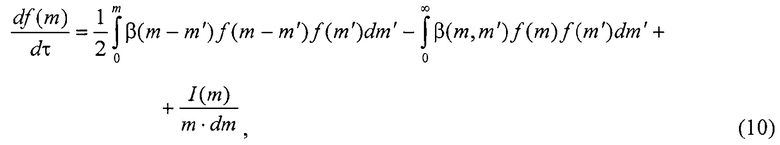
где f(m) - плотность распределения частиц оксида геттера по массам; m, m' - массы соударяющихся частиц, кг; β - ядро кинетического уравнения; I(m) - интенсивность объемного источника взвеси для частиц массой m, кг/(м3⋅с), определяемая по формуле (11).

где fи(m) - плотность распределения массы зародышей частиц по массам, определяемая из формулы (12); m - масса частиц, кг.

где си - концентрация образующихся зародышей частиц, которая определяется из решения кинетического уравнения реакции образования оксида геттера (13); ϕи(l) - плотность распределения массы зародышей частиц по размерам, определяемая по формуле (14); m - масса частиц, кг; l - размер частиц, м.
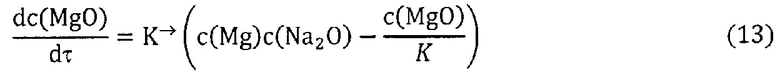
где c(MgO) - концентрация оксида магния, м.д.; c(Mg) - концентрация магния, м.д.; c(Na2O) - концентрация оксида натрия, м.д.; К - константа равновесия реакции.
Задана следующая функция плотности распределения массы зародышей частиц по размерам:
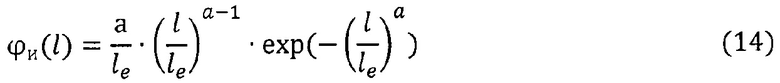
где ϕи(l) - плотность распределения массы зародышей частиц по размерам; le и а - постоянные для данной дисперсной системы (а=9; le=4⋅10-9).
Зависимость среднего размера ансамбля частиц взвеси от времени при температуре теплоносителя 300°C отображена на фиг. 5. Расчет проводился для реакции (6). Из графика видно, что на первой стадии образования частиц имеет место их быстрый рост - примерно до 50 секунд, затем скорость роста частиц уменьшается, использовать эту стадию коагуляции в процессе очистки нецелесообразно ввиду увеличения размеров устройства и времени очистки.
Конкретный пример реализации способа
В конкретном примере реализации способа в качестве жидкого щелочного металла используют натрий, а в качестве растворимого геттера - магний. Температура натрия равна 300°C. Исходные данные, используемые для реализации конкретного примера, представлены в таблице 1.
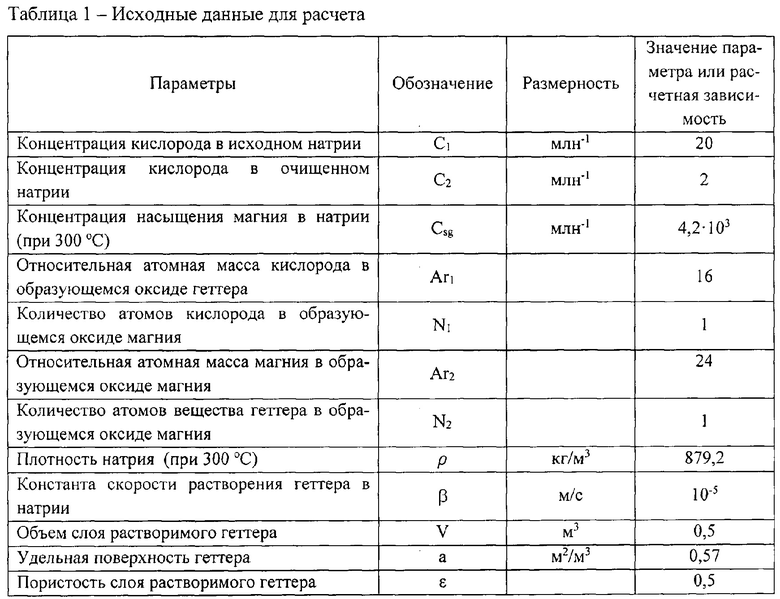
Концентрация кислорода в исходном и очищенном натрии соответственно составляет 20 и 2 млн-1.
Концентрация насыщения магния в натрии при температуре 300°C рассчитанная по формуле (2) составляет 4,2⋅103 млн-1.
Относительные атомные массы и количество атомов для кислорода и магния в образующемся оксиде магния, константа скорости растворения магния в натрии, удельная поверхность магния и пористость слоя магния представлены в таблице 1.
Объем слоя магния в зависимости от необходимого количества очищаемого натрия, рассчитанный по формуле (3) составляет 0,5 м3.
Используя исходные данные, описывающие свойства магния и натрия и соотношения (1)-(5), можно получить, что массовый расход необходимый для понижения концентрации кислорода в натрии с 20 до 2 млн-1 должен быть не менее 0,2 кг/с.
Установленный массовый расход позволяет избежать выноса растворимого геттера за ограниченное обечайкой пространство, в котором осуществляется очистка натрия от кислорода, в результате чего увеличивается эффективность очистки натрия. Также можно получить натрий с любой концентрацией кислорода, варьируя расходом и характеристиками растворимого геттера.
Представленный способ очистки характеризуется относительно малым количеством операций. Основная операция - установление расхода, определенного по соотношению (1). В данном способе нет необходимости использования холодной ловушки для фильтрации натрия от кислорода. Также температуру натрия поддерживают одинаковой на всех этапах очистки. Соответственно данный способ позволяет сильно упростить процесс очистки.
Список литературы
1. Сергеев Г.П. Состояние экспериментальных исследований в условиях натриевого контура равновесия и кинетики реакций с натрием продуктов его взаимодействия с водой. Препринт ФЭИ-2742, Обнинск, 1998.
2. Загорулько Ю.И. Дополнительные данные по растворимости индивидуальных веществ в натрии / Ю.И. Загорулько, Ф.А. Козлов, Т.А. Воробьева. Препринт ФЭИ-2412, - Обнинск: Физико-энергетический институт, 1997.
3. Волощук В.М. Кинетическая теория коагуляции. - Л. Гидрометеоиздат, 1984. - 284 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА МАГНИЯ ИЗ ВЫСОКОМИНЕРАЛИЗОВАННЫХ РАССОЛОВ | 2005 |
|
RU2281248C1 |
| СПОСОБ КОМПЛЕКСНОЙ ОЧИСТКИ ВОДНЫХ РАСТВОРОВ ХЛОРИДОВ МЕТАЛЛОВ ОТ ПРИМЕСЕЙ ЖЕЛЕЗА И СУЛЬФАТ-ИОНОВ | 2008 |
|
RU2373140C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДА КАЛЬЦИЯ | 2003 |
|
RU2255899C1 |
| Способ получения бромидных солей при комплексной переработке бромоносных поликомпонентных промысловых рассолов нефтегазодобывающих предприятий (варианты) | 2021 |
|
RU2780216C2 |
| УСТРОЙСТВО ДЛЯ ОЧИСТКИ ЩЕЛОЧНЫХ МЕТАЛЛОВ ОТ ПРИМЕСЕЙ | 1989 |
|
SU1678067A1 |
| ФИЛЬТРУЮЩИЙ ПАТРОН | 2024 |
|
RU2833703C1 |
| СПОСОБ ПЕРЕРАБОТКИ ВАНАДИЕВОГО КОНЦЕНТРАТА ГЛИНОЗЕМНОГО ПРОИЗВОДСТВА | 1992 |
|
RU2045477C1 |
| Способ получения литиевого концентрата из литиеносных природных рассолов и его переработки в хлорид лития или карбонат лития | 2017 |
|
RU2659968C1 |
| Способ очистки отходящих газов от хлора и оксида серы с получением вяжущих | 2019 |
|
RU2740015C1 |
| СПОСОБ ВОДОПОДГОТОВКИ | 2006 |
|
RU2316479C1 |
Изобретение относится к химической технологии и может быть использовано для очистки жидких щелочных металлов от кислорода. Способ включает нагрев, прокачку и фильтрацию жидкого щелочного металла. Жидкий щелочной металл последовательно подают в ограниченное обечайкой пространство. Определяют температуру жидкого щелочного металла и концентрацию кислорода в нем, прокачивают через последовательно установленные в ограниченном обечайкой пространстве слой растворимого геттера и реакционный объем. Жидкий щелочной металл фильтруют путем прокачки через сепаратор частиц и отводят очищенный жидкий щелочной металл из ограниченного обечайкой пространства. Прокачку производят с расходом, определенным из соотношения с учетом массового расхода жидкого щелочного металла через слой растворимого геттера, концентраций кислорода в исходном и очищенном жидком щелочном металле, концентрации насыщения растворимого геттера в жидком щелочном металле при температуре очистки, относительной атомной массы кислорода и растворимого геттера в образующемся оксиде геттера, количества атомов кислорода и растворимого геттера в образующемся оксиде геттера, константы скорости растворения геттера в жидком щелочном металле, объема слоя растворимого геттера, удельной поверхности геттера, пористости слоя растворимого геттера и плотности жидкого щелочного металла. Способ позволяет увеличить эффективность очистки жидкого щелочного металла и упростить процесс очистки. 7 з.п. ф-лы, 5 ил., 1 табл.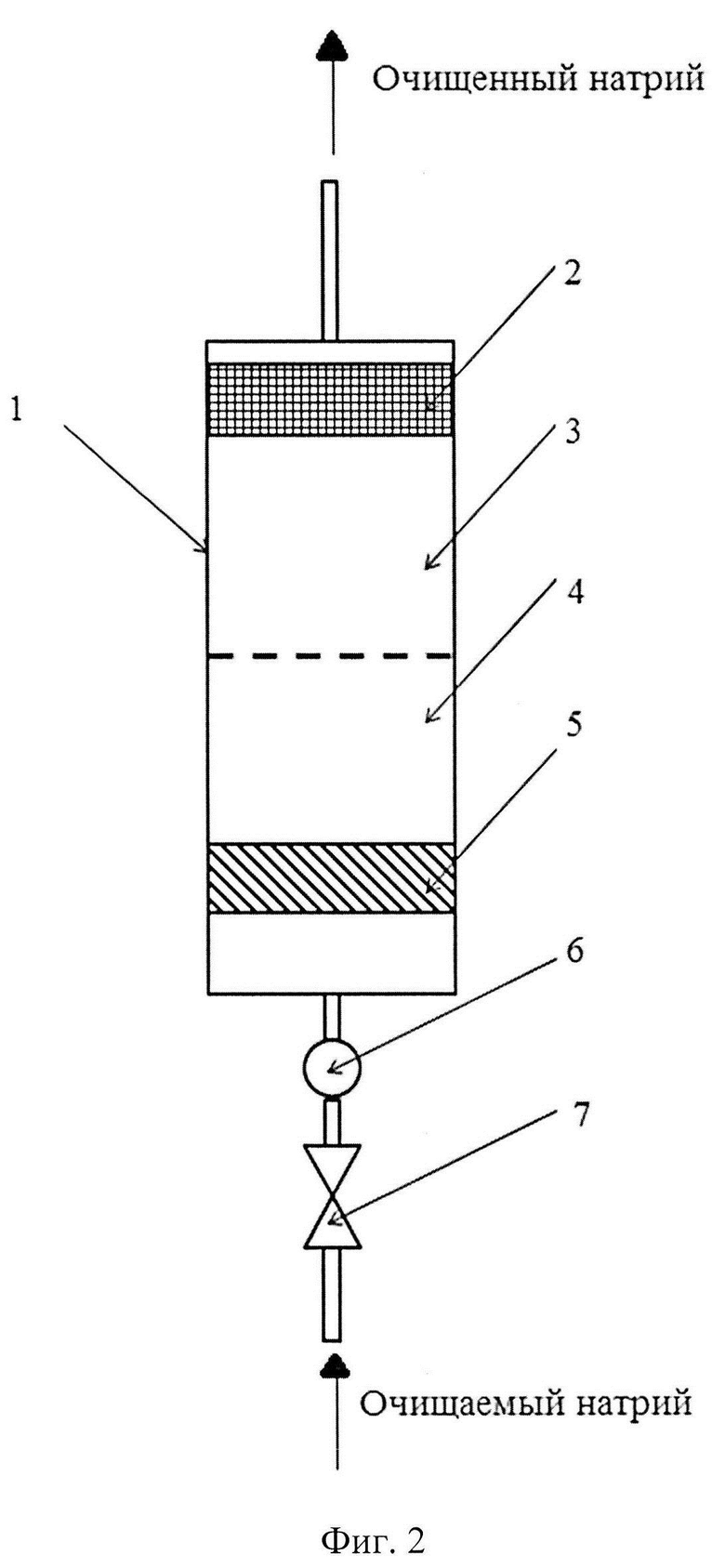
1. Способ очистки жидкого щелочного металла от кислорода, включающий нагрев, прокачку и фильтрацию жидкого щелочного металла, отличающийся тем, что последовательно подают жидкий щелочной металл в ограниченное обечайкой пространство, определяют температуру жидкого щелочного металла и концентрацию кислорода в нем, прокачивают жидкий щелочной металл через последовательно установленные в ограниченном обечайкой пространстве слой растворимого геттера и реакционный объем, фильтруют жидкий щелочной металл путем прокачки через сепаратор частиц и отводят очищенный жидкий щелочной металл из ограниченного обечайкой пространства, а прокачку производят с массовым расходом, определенным из соотношения:
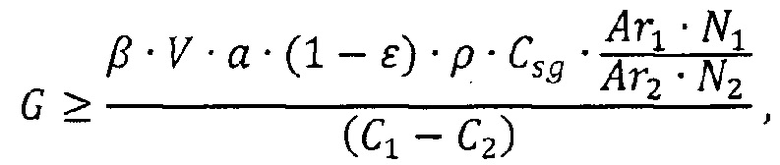
где: G - массовый расход жидкого щелочного металла через слой растворимого геттера, кг/с,
C1 и C2 - концентрации кислорода в исходном и очищенном жидком щелочном металле соответственно, млн-1,
Csg - концентрация насыщения растворимого геттера в жидком щелочном металле при температуре очистки, млн-1,
Ar1 и Ar2 - относительная атомная масса кислорода и растворимого геттера в образующемся оксиде геттера соответственно,
N1 и N2 - количество атомов кислорода и растворимого геттера в образующемся оксиде геттера соответственно,
β - константа скорости растворения геттера в жидком щелочном металле, м/с,
V - объем слоя растворимого геттера, м3,
а - удельная поверхность геттера в виде отношения поверхности геттерной насадки к объему материала геттера, м2/м3,
ε - пористость слоя растворимого геттера,
ρ - плотность жидкого щелочного металла, кг/м3.
2. Способ очистки по п. 1, отличающийся тем, что подачу жидкого щелочного металла в ограниченное обечайкой пространство осуществляют с помощью электромагнитного насоса.
3. Способ очистки по п. 1, отличающийся тем, что перед началом очистки жидкого щелочного металла проводят определение его температуры металла и концентрации кислорода в нем с помощью датчика температуры и электрохимического датчика кислорода соответственно.
4. Способ очистки по п. 1, отличающийся тем, что фильтрацию жидкого щелочного металла осуществляют с помощью сепаратора частиц.
5. Способ очистки по п. 1, отличающийся тем, что для обеспечения взаимодействия растворимого геттера с кислородом в жидком щелочном металле в качестве растворимого геттера используют магний.
6. Способ очистки по п. 1, отличающийся тем, что для обеспечения взаимодействия растворимого геттера с кислородом в жидком щелочном металле в качестве растворимого геттера используют барий.
7. Способ очистки по п. 1, отличающийся тем, что для обеспечения взаимодействия растворимого геттера с кислородом в жидком щелочном металле в качестве растворимого геттера используют кальций.
8. Способ очистки по п. 1, отличающийся тем, что температуру жидкого щелочного металла в ограниченном обечайкой пространстве во время взаимодействия растворимого геттера с кислородом в жидком щелочном металле и в процессе фильтрации обеспечивают одинаковой.
| СПОСОБ ОЧИСТКИ НАТРИЯ ОТ КИСЛОРОДА | 0 |
|
SU246055A1 |
| АЛЕКСЕЕВ В.В | |||
| и др | |||
| Оценки и обоснование геттерной очистки натрия от кислорода | |||
| Вопросы атомной науки и техники | |||
| Серия: Ядерно-реакторные константы | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Способ непрерывной очистки жидкого натрия, применяемого в качестве теплоносителя в первичной системе охлаждения плавильного агрегата | 2017 |
|
RU2660486C1 |
| СПОСОБ ОЧИСТКИ ЩЕЛОЧНЫХ МЕТАЛЛОВ И СПЛАВОВ НА ОСНОВЕ НАТРИЯ, КАЛИЯ И ЦЕЗИЯ ОТ ПРИМЕСЕЙ | 1997 |
|
RU2123061C1 |
| СПОСОБ ОБРАБОТКИ РАСТЕНИЙ И ИСПОЛЬЗУЕМАЯ В НЁМ КОМПОЗИЦИЯ ДЛЯ ЗАЩИТЫ РАСТЕНИЙ | 2001 |
|
RU2210898C2 |
Авторы
Даты
2022-10-07—Публикация
2021-12-29—Подача