Изобретение относится к медицине, а именно к оториноларингологии, и может найти применение при консервативном лечении острой акустической травмы.
Воздействие на орган слуха шумов высокой интенсивности (более 90 дБ) в зависимости от его индивидуальной чувствительности может приводить как к временному, так и к постоянному смещению порогов слуха и в дальнейшем к развитию сенсоневральной тугоухости.
Чаще всего причиной этого являются выстрелы из различных образцов огнестрельного оружия и взрывы. При этом эффективность лечения при акутравматическом поражении органа слуха, зависит от времени оказания медицинской помощи и составляет от 7 до 10 суток.
Установлено, что однократное высокоинтенсивное шумовое воздействие в отличие от среднеинтенсивного, приводит к худшему прогнозу в отношении слуха с течением времени из-за развития кохлеарной синаптопатии.
Существующие в настоящее время подходы к лечению острой акустической травмы недостаточно эффективны и требуют усовершенствования.
Известен способ лечения острой сенсоневральной тугоухости путем введения сосудистых, гормональных, нейропептидных и ноотропных препаратов, при этом в качестве нейропептидного и ноотропного препарата больному вводят кортексин по 10,0 мг, разведенный в 2,0 мл физраствора внутримышечно, ежедневно, в течение 8-10 дней (см. патент RU №2357744, МПК A61K 35/30, A61K 31/373, A61K 35/44, А61Р 27/16, 2009).
Недостатком данного способа является то, что многие клинические исследования препарата кортексин проведены с низким уровнем доказательности. По европейским и американским медицинским стандартам и законодательству он не может быть использован в медицинской практике.
Известен также способ лечения акустических травм с применением рилузола, при этом больному вводят лекарственное средство, которое содержит от 25,0 до 200,0 мг рилузола (см. заявка на изобретение RU №2001119471, МПК A61K 31/425, А61Р 27/16, 2003).
Известно, что рилузол используется в качестве противосудорожного, анксиолитического и снотворного средства, при лечении шизофрении, при лечении расстройств сна и депрессии, при лечении сосудисто-мозговых нарушений и в качестве анестезирующего средства.
Недостатком данного способа является низкая доказательность в отношении улучшения слуховой функции, вследствие случайно обнаруженных эффектов препарата.
Известен также способ лечения острой и внезапной сенсоневральной тугоухости и глухоты, включающий одномоментное введение комплекса лекарственных средств (см. патент RU №2563829, МПК A61K 31/375, A61K 31/4415, A61K 31/417, A61K 31/455, A61K 31/472/, A61K 31/52, A61K 31/522, A61K 31/53, А61Р 27/16, 2015).
При осуществлении данного способа внутривенно вводят эуфиллин, трентал, никотиновую кислоту, аскорбиновую кислоту и витамины группы B1 и В6, внутримышечно вводят папаверин и дибазол в стандартных дозах и дополнительно назначают внутривенные инъекции томпаслина в объеме 40 мг ежедневно в течение 10 дней.
Недостатком данного способа является то, что в предложенную схему входит одномоментно большое количество лекарственных средств (8 препаратов). Причем все они имеют низкий уровень убедительности рекомендаций (С) согласно клиническим рекомендациям «Сенсоневральная тугоухость у взрослых» от 2016 года и направлены в основном на коррекцию нарушений микроциркуляции.
Известен также способ лечения острой сенсоневральной тугоухости путем интратимпанального введения раствора дексаметазона 4 мг - 1 мл (см. Вишняков В.В., Сорокина М.В. «Транстимпанальное введение стероидов при лечении острой нейросенсорной тугоухости», журнал «Вестник оториноларингологии», №4, Москва, Медиасфера, 2014, стр. 75-78).
При осуществлении данного способа под местной анестезией специальной тонкой инъекционной иглой проводят тимпанопункцию в задне-нижнем квадранте барабанной перепонки, вводят 4 мг/мл - 1 мл раствора дексаметазона. Голову больного поворачивают больным ухом кверху, чтобы раствор покрывал нишу круглого окна в течение 20 мин, больной не должен делать глотательных движений.
Недостатком данного способа является необходимость выполнение инвазивных процедур (тимпанопункции), а также то, что введение препарата должно осуществляться подготовленным специалистом (врачом).
Наиболее близким по технической сущности к заявляемому решению является способ лечения острой и внезапной сенсоневральной тугоухости и глухоты, включающий проведение инфузионной внутривенной терапии: глюкокортикоиды по убывающей схеме, при этом вводят дексаметазон 4 мг/мл на 100 мл физиологического раствора в первый и второй дни - 24 мг, третий и четвертый дни - 16 мг, пятый день - 8 мг, шестой день - 4 мг, седьмой день - препарат не вводится, восьмой день - 4 мг (Клинические рекомендаций «Сенсоневральная тугоухость у взрослых», пункт 3.1 Консервативное лечение, утверждены Минздравом Росси, разработаны Национальной медицинской ассоциацией оториноларингологов, 2016).
Технический результат заявляемого решения заключается в повышении эффективности лечения и сокращении его сроков при устойчивом характере восстановления слуховой функции и отсутствии побочных явлений путем улучшения биоэнергетики волосковых клеток Кортиева органа.
Для достижения указанного технического результата в способе лечения острой акустической травмы, включающем проведение инфузионной внутривенной терапии: глюкокортикоиды по убывающей схеме, при этом вводят дексаметазон 4 мг/мл на 100 мл физиологического раствора, причем в первый и второй дни - 24 мг, третий и четвертый дни - 16 мг, пятый день - 8 мг, шестой день - 4 мг, седьмой день - препарат не вводится, восьмой день - 4 мг, согласно изобретению пациенту осуществляют комплексное лечение, для этого терапию глюкокортикоидами сочетают с дополнительным лечением, при котором вводят производное триазино-индола 10 мг/мл - 4 мл на 100 мл физиологического раствора ежедневно в течение 7 суток, при этом полученный раствор вводят внутривенно капельно по 60-70 капель в минуту один раз в день.
Основной группой препаратов, используемых для купирования острого нарушения слуха акутравматического генеза, являются глюкокортикоиды. Однако при акустической травме эффективность лечения глюкокортикоидами ниже, чем при других типах острой сенсоневральной тугоухости.
Научно доказан факт, что действие шума высокой интенсивности приводит к нарушению микроциркуляции во внутреннем ухе и развитию гипоксии, возникающей в результате либо ограничения поступления кислорода в клетки Кортиева органа, либо связанной с потерей способности последних утилизировать его в реакциях биологического окисления, что играет чрезвычайно важную роль в патогенезе острой сенсоневральной тугоухости.
В результате вышеуказанных процессов происходит изменение биоэнергетики клетки и как следствии нарушения окислительного фосфорилирования с накоплением активных форм кислорода и азота, приводящих к окислительному стрессу, а затем к программируемой и/или некротической гибели клеток. Помимо повреждения волосковых клеток происходит и необратимое повреждение нейронов слухового пути и ганглия.
По данным современных исследований устойчивость волосковых клеток Кортиева органа к гипоксии связана с молекулой гипоксией индуцированного фактора (далее - HIF).
Известно, что производное триазино-индола обладает способностью улучшать биоэнергетический обмен клетки при гипоксии и хорошо проникает в лабиринтную жидкость, за счет чего достигается нормализация биохимических и электрофизиологических процессов в клетках внутреннего уха. Помимо этого, оно способствует увеличению экспрессии HIF в волосковых клетках и нейронах спирального ганглия.
В связи с этим в заявляемом способе данное соединение было использовано как дополнительное лечение для коррекции слуха при акустической травме.
Экспериментально было доказано, что именно сочетание стандартного (традиционного) лечения глюкокортикоидами с дополнительным применением производного триазино-индола способствует значимому (р<0,05) улучшению порогов слуха, позволяет улучшить биоэнергетику волосковых клеток.
Приводим полученные данные исследований.
В исследовании приняли участие 14 пациентов с острой акустической травмой мужского пола, возрастом от 19 до 28 лет, без сопутствующей соматической патологии. Время поступления в стационар после акустического воздействия не превышало 7 суток.
Больные с острой акустической травмой были разделены на две группы по 7 человек в каждой.
Первая группа больных получала только стандартное (традиционное) лечение, которое проводилось согласно клиническим рекомендациям «Лечение сенсоневральной тугоухости у взрослых».
Лечение заключалось во внутривенном капельном введении дексаметазона 4 мг/мл на 100 мл физиологического раствора: в первый и второй дни - 24 мг, третий и четвертый дни - 16 мг, пятый день - 8 мг, шестой день - 4 мг, седьмой день - препарат не вводится, восьмой день - 4 мг.
Лечение второй группы помимо представленной выше схемы включало внутривенное капельное введение производного триазино-индола 10 мг/мл - 4 мл на 100 мл физиологического раствора ежедневно в течение 7 суток.
После сбора жалоб и анамнеза, всем пациентам выполнялось:
- эндоскопическое исследование ЛОР органов, оценка восприятия шепотной речи;
- тональная пороговая аудиометрия в диапазоне 125-8000 Гц с использованием клинического аудиометра АД - 226 (Interacoustics, Дания);
- исследование задержанной вызванной отоакустической эмиссии (далее - ЗВОАЭ) и отоакустической эмиссии на частоте продукта искажения (далее - ОАЭЧПИ) с использованием системы для отоакустической эмиссии (далее - ОАЭ), коротколатентных слуховых вызванных потенциалов мозга (далее - КСВП), импедансометрии и аудиологического скрининга «Аудио-СМАРТ» (Россия) при поступлении, на первые, третьи и седьмые сутки лечения.
Концентрацию HIF1α определяли с помощью высокочувствительного набора HEA798Hu для количественного определения HIF 1α с помощью сэндвич-метода, иммуноферментного анализа (далее - ИФА) в сыворотке крови.
Критериями эффективности предложенного способа лечения служили: отсутствие или уменьшение жалоб пациентов (на шум в ушах, снижение слуха), степень восстановления слуха по данным тональной пороговой аудиометрии (повышение порогов слуха на 10 дБ и более по сравнению с исходными значениями при поступлении), прохождение теста ЗВОАЭ и ОАЭЧПИ.
Все пациенты предъявляли жалобы на высокочастотный шум, чувство «заложенности» в ушах. В 3-х случаях имело место снижение восприятия шепотной речи до четырех метров, в 6-ти до 5 метров, у остальных пациентов показатели слуха были в пределах нормы.
При анализе тональных пороговых аудиограмм пациентов имел место косо-нисходящий тип кривых, без костно-воздушного интервала, наибольшее повышение порогов слуха отмечалось в диапазоне частот от 3 до 8 кГц.
В группе традиционного лечения на фоне проведенной терапии у 4 пациентов шум в ушах исчез, в 2-х случаях уменьшился, в одном усилился. Показатели шепотной речи улучшились до нормальных значений у 6 пациентов, в одном случае составили 5,0 метров.
В группе комплексного лечения у 6 пациентов шум в ушах исчез, в 1-м уменьшился. Показатели шепотной речи улучшились до нормальных значений у всех пациентов.
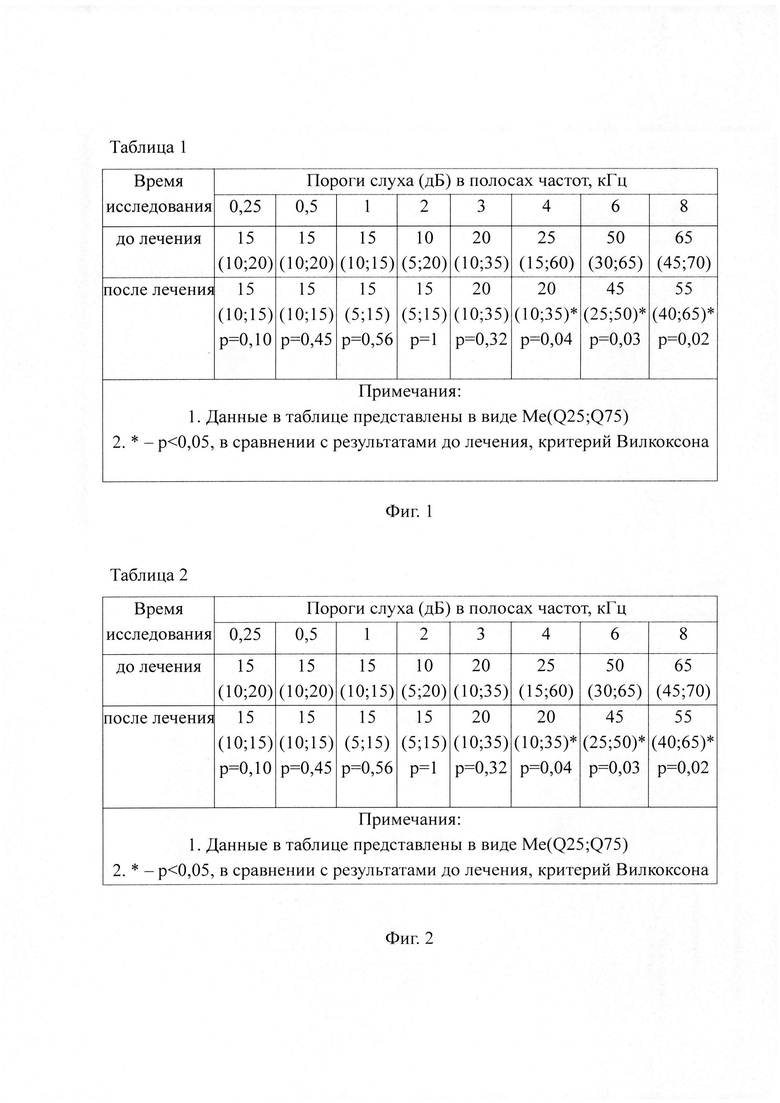
В группе применения традиционного лечения отмечалось статистически значимое (р<0,05) улучшение порогов слуха на частотах 4, 6, 8 кГц (данные представлены в таблице 1).
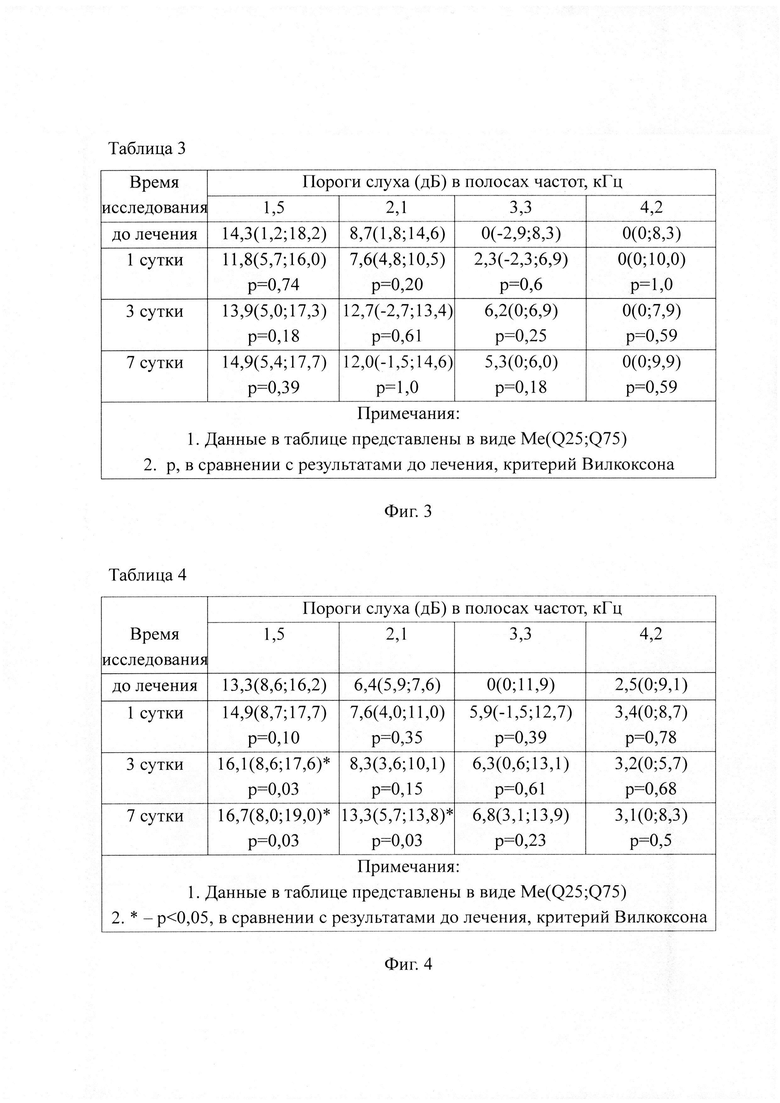
В группе применения производного триазино-индола улучшение порогов слуха было значимо (р<0,05) практически на всех исследуемых частотах, за исключением 1 и 2 кГц (данные представлены в таблице 2).
При этом среднее улучшение порогов слуха в первой группе составляло 5-10 дБ, во второй группе 15-20 дБ.
При исследовании теста прохождения ЗВОАЭ в первой группе положительный результат теста наблюдался у одного пациента на 3-й сутки и у трех пациентов на 7-е сутки после начала лечения. Во второй группе пациентов трое прошли тест на 3 сутки и один пациент на седьмые сутки лечения.
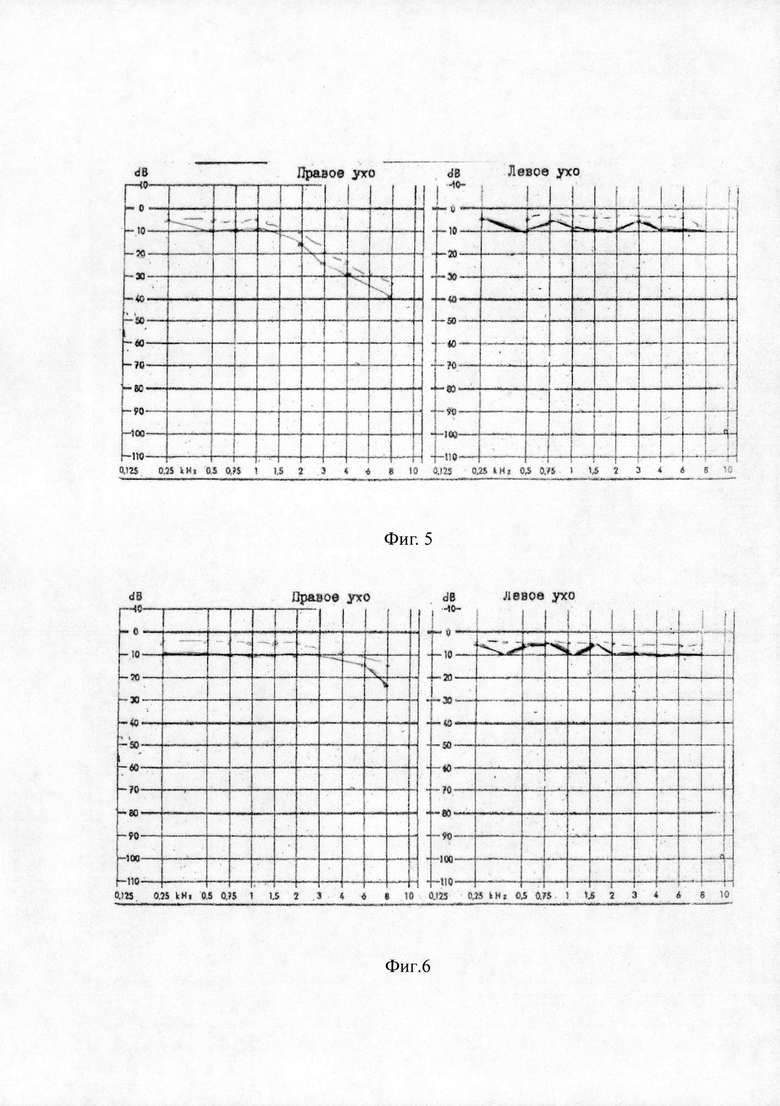
При анализе показателей ОАЭЧПИ в первой группе в различные сроки после начала лечения изменение их было не значимо (р>0,05) на всех исследуемых частотах. Тенденция к восстановлению показателей ОАЭ была выражена слабо, особенно в области частоты 4,2 кГц. Это позволяет предположить выраженное угнетение функции наружных волосковых клеток (данные представлены в таблице 3).
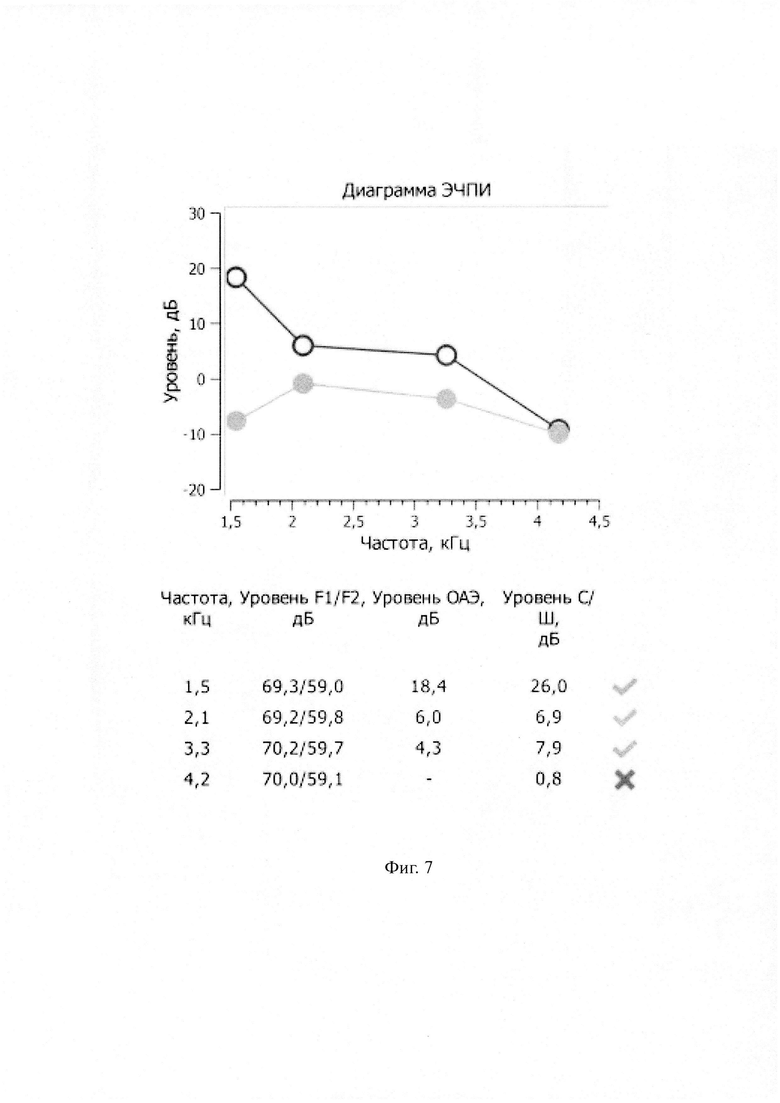
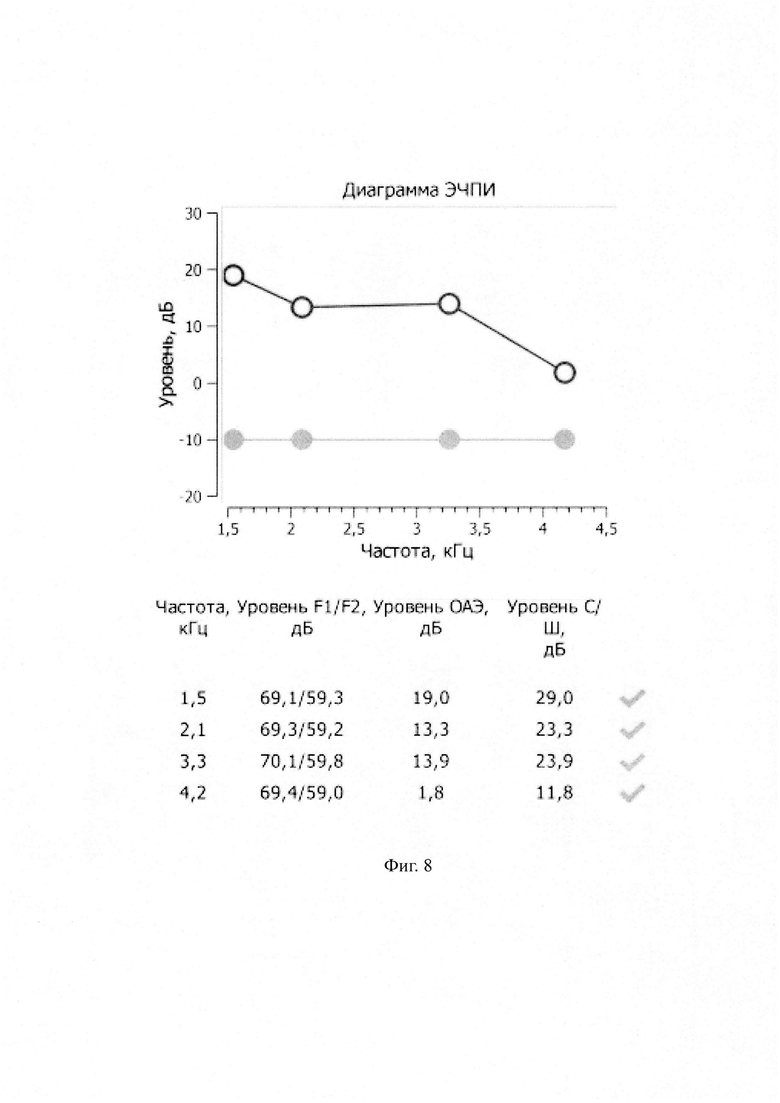
Напротив, во второй группе отмечалась значимое восстановление ОАЭ на частоте 1,5 кГц уже на 3-й сутки после начала лечения (р=0,03), а на частоте 2,1 кГц на 7-е сутки (р=0,03). На частоте 3,3 кГц наблюдалась положительная динамика к восстановлению ОАЭ с течением времени, на частоте 4,2 кГц стабилизация показателя ОАЭ без тенденции к ухудшению. Это связано с улучшением биоэнергетики волосковых клеток, связанное с применением производного триазино-инола (данные представлены в таблице 4).
Таким образом, эксперименты показали, что применение производного триазино-индола в схеме комплексного лечения пациентов с острой акустической травмой в отличие от традиционной терапии уменьшает, как выраженность патологических изменений в волосковых клетках Кортиева органа, так и срок восстановления временного смещения порогов слуха после чрезмерного акустического воздействия, при этом снижется риск постоянного смещения порогов слуха и развития тугоухости.
Из вышесказанного следует, что введенные отличительные признаки влияют на указанный технический результат, находятся с ним в причинно-следственной связи.
Способ иллюстрируется чертежами, где: на фиг. 1 представлена таблица 1 «Динамика показателей тональной пороговой аудиометрии до и после лечения в 1-ой группе (n=7)»; на фиг. 2 представлена таблица 2 «Динамика показателей тональной пороговой аудиометрии до и после лечения во 2-ой группе (n=7)»; на фиг. 3 представлена таблица 3 «Динамика показателей ОАЭЧПИ до и после лечения в 1-ой группе (n=7)»; на фиг. 4 представлена таблица 4 «Динамика показателей ОАЭЧПИ до и после лечения во 2-ой группе (n=7)»; на фиг. 5 представлены данные клинического примера: тональные пороговые аудиограммы по правому и левому уху при поступлении в стационар; на фиг. 6 - то же самое на седьмые сутки лечения; на фиг. 7 представлены клинического примера: графики ОАЭЧПИ по правому уху при поступлении в стационар; на фиг. 8 - то же самое на седьмые сутки лечения.
Способ осуществляют следующим образом.
После сбора жалоб и анамнеза пациента проводят сбор следующих данных: эндоскопическое исследование ЛОР органов, оценка восприятия шепотной речи. Выполняют тональную пороговую аудиометрию в диапазоне 125-8000 Гц, используя клинический аудиометр АД - 226 (Interacoustics, Дания).
Затем осуществляют исследование задержанной вызванной отоакустической эмиссии (ЗВОАЭ) и отоакустической эмиссии на частоте продукта искажения (ОАЭЧПИ) с использованием системы для ОАЭ, КСВП, импедансометрии и аудиологического скрининга «Аудио-СМАРТ» (Россия).
Сбор данных выполняют при поступлении, на первые, третьи и седьмые сутки лечения.
Концентрацию HIF1α определяют с помощью высокочувствительного набора HEA798Hu для количественного определения HIF 1α сэндвич-методом ИФА в сыворотке крови.
Пациенту первоначально осуществляют традиционное лечение.
Традиционное лечение включает внутривенное капельное введение раствора дексаметазона, при этом первоначально 4 мг/мл растворяют в 100 мл физиологического раствора.
Лечение осуществляют по следующей схеме.
В первый и второй дни вводят 24 мг полученного раствора.
В третий и четвертый дни - 16 мг, в пятый день - 8 мг, шестой день - 4 мг, седьмой день - препарат не вводят, восьмой день больной получает 4 мг.
Затем осуществляют дополнительное лечение, а именно ежедневно в течение 7 дней больному вводят производное триазино-индола.
Сначала содержимое одной ампулы 10 мг/мл - 4 мл раствора триазино-индола растворяют в 100 мл физиологического раствора.
После этого полученный раствор вводят внутривенно капельно по 60-70 капель в минуту, один раз в день.
После окончания курса лечения оценивают восприятие шепотной речи, выполняют тональную пороговую аудиометрию в диапазоне частот 125-8000 Гц, исследование ЗВОАЭ и ОАЭЧПИ, определяют концентрацию HIF1α в сыворотке крови.
Способ поясняется следующими примерами.
Пример 1.
Пациент Б., 20 лет, находился на стационарном лечении с диагнозом: Акустическая травма. Острая правосторонняя сенсоневральная тугоухость I степени.
Акустическая травма получена в результате проведения стрельбы из охотничьего ружья на открытой местности (выполнил 5 одиночных выстрелов, без применения средств индивидуальной защиты).
При поступлении предъявлял жалобы на шум в правом ухе высокочастотного характера, снижение слуха на правое ухо. ШР AD/AS=5 м/6 м. Давность заболевания - 5 дней.
Пациент получил курс комбинированной терапии: традиционной (дексаметазон) и дополнительной (производное триазино-индола).
При традиционном лечении пациенту дней вводили раствор дексаметазона 4 мг/мл, предварительно растворенный в 100 мл физиологического раствора.
Лечение осуществляли по следующей схеме.
В первый и второй дни вводили 24 мг полученного раствора.
В третий и четвертый дни - 16 мг, в пятый день - 8 мг, шестой день - 4 мг, седьмой день - препарат не вводят, восьмой день пациент получил 4 мг.
Затем пациенту осуществили дополнительное лечение, а именно ежедневно в течение 7 дней вводили производное триазино-индола.
Для этого подготовили раствор: производное триазино-индола 10 мг/мл - 4 мл раствора растворили в 100 мл физиологического раствора Затем осуществляли его внутривенное капельное 60 капель в минуту введение ежедневно в течение 7 дней.
После курса терапии пациент субъективно отметил исчезновение шума в правом ухе, улучшение слуха справа. ШР AD/AS=6 м/6 м.
Тональная пороговая аудиометрия от 05.10.2021 г. AD: повышение порогов слуха по воздушной проводимости на частотах с 2 кГц до 8 кГц от 15 до 40 дБ, косо-нисходящий тип кривых, без костно-воздушного интервала.
Тональная пороговая аудиометрия от 12.10.2021 г. норма.
Прохождение теста ЗВОАЭ: 1-е сутки - не прошел, 3-е сутки - прошел, 7-е сутки - прошел.
Прохождение теста ОАЧПИ: 1-е сутки - прошел, 3-е сутки - прошел, 7-е сутки - прошел.
Определение концентрации HIF в сыворотке крови: 1 сутки - 15 пг/мл, 3 сутки - 20 пг/мл, 7 сутки - 25 пг/мл.
Таким образом, данный способ позволил улучшить субъективное состояние пациента (исчезновение ушного шума), показатели восприятия шепотной речи, пороги слуха по данным тональной пороговой аудиометрии, показатели отоакустической эмиссии за счет улучшения биоэнергетики клетки (рост концентрации HIF в сыворотке крови в процессе лечения).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ | 2016 |
|
RU2627155C1 |
| СРЕДСТВО И СПОСОБ ДЛЯ ЛЕЧЕНИЯ НЕЙРОСЕНСОРНОЙ ТУГОУХОСТИ | 2018 |
|
RU2698451C1 |
| Способ скрининга для выявления нарушений слуха у детей дошкольного возраста | 2020 |
|
RU2759485C1 |
| Способ профилактики нарушений слуховой функции у человека при воздействии шума | 2021 |
|
RU2779973C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОЙ И ВНЕЗАПНОЙ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ И ГЛУХОТЫ | 2014 |
|
RU2563829C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОСТРОЙ И ВНЕЗАПНОЙ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ И ГЛУХОТЫ | 1997 |
|
RU2119335C1 |
| СПОСОБ РАННЕЙ РАСШИРЕННОЙ АУДИОЛОГИЧЕСКОЙ ДИАГНОСТИКИ СЛУХОВЫХ НАРУШЕНИЙ, ОБУСЛОВЛЕННЫХ РАССЕЯННЫМ СКЛЕРОЗОМ | 2007 |
|
RU2374983C2 |
| Способ коррекции ушного шума у пациентов с нарушением слуховой функции | 2024 |
|
RU2838812C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ВТОРИЧНОЙ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ | 2016 |
|
RU2651110C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕЙРОСЕНСОРНОЙ ТУГОУХОСТИ | 2001 |
|
RU2188642C1 |
Изобретение относится к оториноларингологии. Способ включает проведение инфузионной внутривенной терапии: дексаметазоном по убывающей схеме, при этом вводят дексаметазон 4 мг/мл на 100 мл физиологического раствора, причем в первый и второй дни - 24 мг, третий и четвертый дни - 16 мг, пятый день - 8 мг, шестой день - 4 мг, седьмой день - препарат не вводится, восьмой день - 4 мг. При этом дексаметазон сочетают с производным триазино-индолом 10 мг/мл - 4 мл на 100 мл физиологического раствора ежедневно в течение 7 суток, при этом полученный раствор вводят внутривенно капельно по 60-70 капель в минуту один раз в день. Способ позволяет улучшить субъективное состояние пациента: устранить ушной шум и повысить восприятия шепотной речи, а также пороги слуха по данным тональной пороговой аудиометрии, показатели отоакустической эмиссии. 8 ил.
Способ лечения острой акустической травмы, включающий проведение инфузионной внутривенной терапии: дексаметазон по убывающей схеме, при этом вводят дексаметазон 4 мг/мл на 100 мл физиологического раствора, причем в первый и второй дни - 24 мг, третий и четвертый дни - 16 мг, пятый день - 8 мг, шестой день - 4 мг, седьмой день - препарат не вводится, восьмой день 4 мг, отличающийся тем, что пациенту осуществляют комплексное лечение, для этого терапию дексаметазоном сочетают с дополнительным лечением, при котором вводят производное триазино-индола 10 мг/мл - 4 мл на 100 мл физиологического раствора ежедневно в течение 7 суток, при этом полученный раствор вводят внутривенно капельно по 60-70 капель в минуту один раз в день.
| СПОСОБ ЛЕЧЕНИЯ ОСТРОЙ И ВНЕЗАПНОЙ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ И ГЛУХОТЫ | 2014 |
|
RU2563829C1 |
| 3-(БЕНЗИЛАМИНОКАРБОНИЛМЕТИЛТИО)-1,2,4-ТРИАЗИНО [5,6-B]-ИНДОЛ, ПОВЫШАЮЩИЙ ФИЗИЧЕСКУЮ ВЫНОСЛИВОСТЬ | 1989 |
|
SU1626644A1 |
| СПОСОБ ИССЛЕДОВАНИЯ И ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СЛУХОВОЙ ТРУБЫ | 2016 |
|
RU2630352C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОСТРОЙ И ВНЕЗАПНОЙ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ И ГЛУХОТЫ | 1997 |
|
RU2119335C1 |
| Способ предотвращения отложений неорганических солей в пласте и нефтепромысловом оборудовании | 1989 |
|
SU1738815A1 |
| БАБАЕВ С.Ю | |||
| и др | |||
| Лечение акустической травмы, полученной после стрельб, в условиях многопрофильного госпиталя | |||
| Известия вузов | |||
| Поволжский регион | |||
| Медицинские науки | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| ZLOCZOWER E | |||
| et al | |||
Авторы
Даты
2022-11-10—Публикация
2022-03-11—Подача