Изобретение относится к медицине, а именно к отоларингологии, и может быть использовано при лечении острой и внезапной сенсоневральной тугоухости и глухоты.
Сенсоневральная тугоухость является полиэтиологическим заболеванием, на развитие которого оказывают влияние сосудистые, инфекционные, токсические, физические, психические и другие факторы. Внезапная сенсоневральная тугоухость поражает преимущественно лиц активного трудоспособного возраста и является серьезным инвалидизирующим фактором.
Известно средство для лечения острой и внезапной сенсоневральной тугоухости и глухоты, содержащее в качестве активного вещества никотиновую кислоту, обладающую сосудорасширяющим действием (Асламазова В.Л., Богомильский М. Р. Компламин в терапии острой кохлеарной тугоухости. Тезисы докладов пленума правления Всесоюзного научного общества отоларингологов. - М., 1978, с. 160-167).
Известно средство для лечения острой и внезапной сенсоневральной тугоухости и глухоты фенибут, обладающее седативным действием (Логинов В.Н., Ускова В.В. Использование фенибута в лечении нейросенсорной тугоухости. Материалы конференции оториноларингологов. - Иркутск, 1983, с. 273-274).
Известно средство для лечения острой и внезапной сенсоневральной тугоухости и глухоты, содержащее в качестве активного вещества аденозинтрифосфат (АТФ) (Максимова М.С. Лечение больных острым кохлеарным невритом аденозинтрифосфорной кислотой. Вестник оториноларингологии. - 1986, - с. 104-105).
Все перечисленные средства обладают общим недостатком - низкой эффективностью лечения острой и внезапной сенсоневральной тугоухости и глухоты.
Задачей изобретения является создание средства для лечения острой и внезапной сенсоневральной тугоухости и глухоты, обладающего высокой эффективностью.
Поставленная задача решается тем, что в средстве для лечения острой и внезапной сенсоневральной тугоухости и глухоты, содержащем активное вещество, согласно изобретению в качестве активного вещества используют дигидрохлорид моногидрат 3-(2-морфолиноэтилтио)-1,2,4-триазино[5,6-b]индиола (трисан) в эффективных количествах.
Поставленная задача решается также тем, что для внутривенного введения средство дополнительно содержит натрия хлорид, NaOH и воду при следующем соотношении массовой концентрации ингредиентов, г/л:
Дигидрохлорид моногидрат 3-(2-морфолиноэтилтио)-1,2,4-триазино [5,6-b] индола - 2,5 - 12,5
Натрия хлорид - 6 - 9
NaOH - 0,2 - 1,0
Вода - Остальное
Дигидрохлорид моногидрат 3-(2-морфолиноэтилтио)-1,2,4-триазино[5,6-b]индола (трисан) получают известным способом. При взаимодействии 3-меркапто-1,2,4-триазино[5,6-b] индола с гидробромидом 2-морфолиноэтилбромида в присутствии избытка щелочи получают основание 3-(2-морфолиноэтилтио)-1,2,4-триазино[5,6-b] индола с выходом около 75% от теоретического. Последний обрабатывают газообразным хлористым водородом или соляной кислотой в изопропиловом спирте и получают трисан - дигидрохлорид моногидрат 3-(2-морфолиноэтилтио)-1,2,4-триазино[5,6-b] индола с выходом около 87% от теоретического. Последний очищают перекристаллизацией из смеси изопропилового спирта с разбавленной соляной кислотой, сушат на воздухе и получают в виде лимонно-желтых кристаллов, температура плавления 238 - 240oC (с разложением). Вещество однородно по данным тонкослойной хроматографии. Этот вывод подтвержден хроматографированием на окиси алюминия II степени активности, растворитель для нанесения - метиловый спирт, подвижный растворитель - бензол-спирт, 7,5: 1 Rf 0,44.
Строение вещества подтверждается данными элементного анализа, потенциометрического титрования щелочью, а также ПМР- и УФ-спектров.
Спектр ПМР в D2O, г, м.д.: Ar-H 2,50 - 3,02 ( μ, 4H), CH2O 5,74 - 6,10 ( μ, 4H), CH2S, CH2N 6,22 - 6,63 (μ, 8H).
Спектр снят на пробе Tesla B S 487 C, рабочая частота 100 МГц.
УФ-спектр, λ макс.нм (IgE) : 220 пл (4,26), 264 (4,51), 340 (4,00). Спектр снят для раствора в воде на приборе СФ-20. Положение полос поглощения характерно для 3-S-алкильных производных 1,2,4-триазино[5,6-b]индола.
Полученное вещество удовлетворяет фармакопейным требованиям. Важнейшим из них является прозрачность раствора (0,1 г препарата в 10 мл воды).
Найдено,%: C 44,01, H 5,27, N 17,60, S 7,53. C15H17N5OS • 2 HCl • H2O (M 406,33). Вычислено %: C 44,34, H 5,21, N 17,24, S 7,89.
Определение острой токсичности трисана проводилось на крысах массой 180-190 г. Вводили внутривенно 2%-ный раствор трисана. В данных условиях опыта ЛД50 для крыс составляет 58,5 мг/кг массы тела. Кролики без летательного исхода переносят внутривенное введение вещества в дозе 100 мг/кг.
Внутрибрюшинное введение вещества в дозе 40 мг/кг в течение 6 дней мышам не сопровождалось какими-либо видами токсических реакций со стороны желудочно-кишечного тракта, а также общего состояния животных. Изъявлений слизистой желудка и кишечника отмечено не было.
Ежедневное внутривенное введение крысам, кроликам и собакам трисана в дозе 10-15 мг/кг в течение 30 дней не сопровождалось изменениями в общих анализах крови и мочи, не наблюдалось также изменений в показателях трансаминаз, щелочной фосфатазы, холестерина, билирубина, остаточного азота, креатинина, глюкозы, натрия, калия и хлора, определяемых в сыворотке крови животных. Установлено, что испытываемое средство не обладает мутагенным действием на хромосомный аппарат мышей.
Исследование субхронической токсичности средства проводилось на 32 белых беспородных крысах (самцах и самках) массой тела 170-250 г. В качестве контроля использовали изотонический раствор натрия хлорида. Препараты вводили внутривенно. Субхроническую токсичность препарата изучали по тесту Lim в нашей модификации (определение биохимических показателей и данных периферической крови), позволяющей оценивать кумулятивные свойства и токсичность изучаемого образца. Опыт проводили в течение 28 дней. Животным ежедневно препарат вводили внутривенно в начальной дозе равной 1/10 ЛД50 (5,85 мг/кг), нарастающей в каждые последующие 4 дня в полтора раза по сравнению с предыдущей. Оценивали общее состояние животных, определяли гематологические показатели в начале и в конце эксперимента. Биохимические показатели определяли в конце опыта.
У крыс, получавших трисан, отмечено увеличение количества лейкоцитов в крови по сравнению с контрольными животными. Количество эритроцитов изменялось и в контрольной, и в опытной группах однонаправленно, при этом колебания показателя не выходили за пределы физиологической нормы для крыс. Масса тела опытной группы животных не отличалась от контроля. Ни одно животное не погибло в период опыта. При патологоанатомическом исследовании животных после опыта во внутренних органах их не отмечено каких-либо изменений.
Сопоставляя результаты, полученные в контроле и в опыте, был сделан вывод о том, что длительное введение больших доз трисана не оказывает токсического действия на развитие самцов и самок крыс и не кумулируется в организме.
Исследование средства для лечения острой и внезапной сенсоневральной тугоухости и глухоты проводили на моделях внезапной тугоухости, вызываемой гипоксией, токсическим поражением и острой акустической травмой.
Объективную оценку функции периферического отдела звукового анализатора осуществляли путем регистрации суммарного электрического ответа улитки кошки и измерения его амплитудных и временных параметров. С помощью специальной электрофизиологической установки в ответ на короткий звуковой сигнал "щелчок" длительностью 100 мс с мембраны круглого окна улитки кошки, находящейся в электроэкранированной звукоизолированной камере, регистрировали суммарный электрический ответ (СОЭ), представленный микрофонным потенциалом МП и двумя компонентами N1, N2 акционного потенциала АП. Измерение показателей проводили в динамическом диапазоне "щелчка" от 10 до 80 дБ над порогом обнаружения ответа.
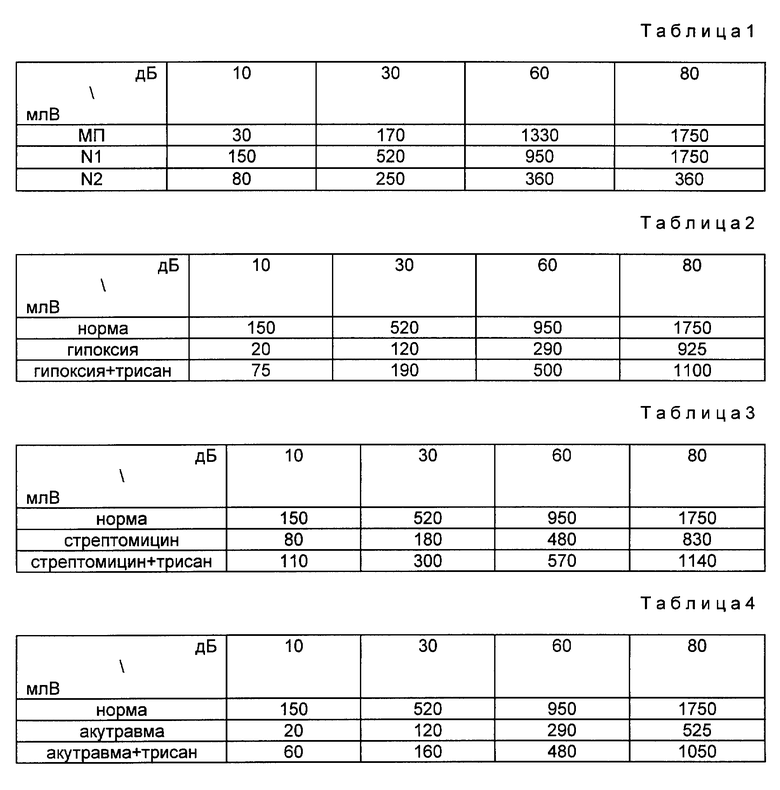
В таблице 1 представлены средние значения амплитуд МП, N1, N2 в физиологических условиях.
При экспериментальном введении средства в физиологических условиях оно не оказывает влияния на функцию улитки кошки.
При острой гипоксической гипоксии, вызываемой в эксперименте вдыханием газовой смеси, содержащей 7% кислорода и 93% азота, СОЭ улитки значительно отличается от нормы. Установлено, что непосредственно после действия 5 - 30-минутной гипоксии амплитуда МП снижается на 30-50%. В условиях гипоксии более существенно снижается амплитуда N1 акционного потенциала. В таблице 2 приведены значения амплитуды N1 АП после гипоксии при введении 10 мг/кг трисана.
Снижение амплитуды N1 после 30-минутной гипоксии на фоне введения трисана в 1,8 раз меньше, чем без его введения.
С целью оценки функции улитки при токсическом поражении внутреннее ухо кошки заполняли ототоксическим антибиотиком - стрептомицином и измеряли СОЭ улитки в течение 2-х часов. После действия стрептомицина биоэлектрическая активность улитки снижается, при этом происходит изменение функции как волосковых клеток, так и нервных структур без видимой тенденции восстановления. В таблице 3 приведены значения амплитуды N1 АП после стрептомициновой интоксикации при введении средства.
Таким образом средство обладает протективным действием при развитии интоксикации улитки.
Моделирование острой акустической травмы осуществляли путем озвучивания "белым шумом" интенсивностью 105 дБ над нормальным порогом слышимости в течение 5 минут. В таблице 4 приведены значения амплитуды N1 АП после акутравмы и при введении средства.
Была проведена серия опытов по определению концентрации трисана в ликворе и лабиринтной жидкости. Через 30 минут после внутривенного введения 10 мг/кг массы тела животного концентрация препарата составляет 100 нг/мл, что подтверждает способность трисана проникать через гематоэнцефалический и гематолабиринтный барьеры.
Таким образом исследование средства на моделях внезапной тугоухости показало его способность повышать функциональную устойчивость звукового анализатора к различным патогенным факторам.
При лечении острой и внезапной сенсоневральной тугоухости и глухоты больным назначают средство, содержащее трисан, в дозах 0,5-5,0 мг/кг массы тела в сутки в зависимости от тяжести заболевания и формы введения.
Для инъекционного введения целесообразно использовать средство, дополнительно содержащее натрия хлорид, NaOH и воду при следующем соотношении массовой концентрации ингредиентов, г/л:
Дигидрохлорид моногидрат 3-(2-морфолиноэтилтио)-1,2,4-триазино [5,6-b] индола - 2,5 - 12,5
Натрия хлорид - 6 - 9
NaOH - 0,2 - 1,0
Вода - Остальное
Ингредиенты определены в результате экспериментальных исследований, являются стабилизаторами для трисана, в указанных концентрациях обеспечивают получение изотонического раствора и длительность хранения лекарственной формы в течение 2 лет.
Состав получают следующим образом. Растворяют в 600-700 мл воды для инъекций необходимые количества трисана и натрия хлорида, а затем прибавляют 0,1М раствор NaOH, доводят до объема 1000 мл. Раствор фильтруют через фильтры "миллипор", подвергая стерилизующей фильтрации, укупоривают под обкатку или же запаивают в ампулы.
При внутривенном введении перед использованием 5 мл раствора трисана смешивают с 150 мл 0,9% раствора натрия хлорида и вводят со скоростью 60-80 капель в минуту.
Изобретение иллюстрируется следующими клиническими примерами.
1. Больная Т., 34 лет. Страдает гипертонической болезнью 8 лет. Накануне заболевания в течение 2-х недель наблюдалось повышение АД до 170/100 мм рт. ст. Начало заболевания сопровождалось появлением шума в правом ухе, снижением слуха в течение часа, заложенностью уха, чувством онемения в области ушной раковины, легким головокружением, нарушением равновесия. На 10 день госпитализирована. Диагноз: острая сенсоневральная тугоухость правосторонняя. Слух на правое ухо - крик у ушной раковины при выключении левого уха трещеткой. Основными жалобами при поступлении были сильный шум в правом ухе, высокочастотный, отсутствие слуха, тяжесть в голове. Больной были назначены внутривенные инъекции средством, содержащим трисана - 10,0 г; натрия хлорида - 8,0 г; 0,1М раствора NaOH - 200 мл; воды для инъекций до 1000 мл; pH раствора составляет 4,5.
Перед введением 5 мл раствора смешивали со 150 мл 0,9%-ного раствора натрия хлорида и вводили внутривенно со скоростью 60 капель в минуту один раз в сутки в течение 7 дней. На фоне лечения шум в ухе сначала уменьшился, а затем полностью исчез, слуховая функция на 4-5-й день начала восстанавливаться и на 10-й день достигла уровня слуха на здоровое ухо.
2. Больная Ф., 39 лет. Обратилась в клинику на 10 день от начала заболевания. На фоне полного здоровья после сна обнаружила отсутствие слуха на левое ухо. Шума, субъективных вестибулярных расстройств не было. Отмечала чувство онемения в области ушной раковины. При поступлении слух - слышала крик у ушной раковины при заглушении трещеткой правого уха. При обследовании рентгенологически со стороны внутренних слуховых проходов и в области шейного отдела позвоночника патологических изменений не выявлено. Диагноз: внезапная сенсоневральная тугоухость левосторонняя. Больной были назначены внутривенные инъекции средством, содержащим: трисана - 5,0 г; натрия хлорида - 6,0 г; 0,1М раствора NaOH - 100 мл; воды для инъекций до 1000 мл; pH раствора составляет 4,5.
Перед введением 5 мл раствора смешивали со 150 мл 0,9%-ного раствора натрия хлорида и вводили внутривенно со скоростью 60 капель в минуту один раз в сутки в течение 10 дней. На фоне проводимого лечения слуховая функция на левое ухо на 6-й день лечения стала восстанавливаться, а на 19-й день почти полностью восстановилась.
3. Больной Соколов А., 48 лет. После перенесенной респираторной вирусной инфекции обратился с жалобами на снижение слуха на правое ухо, которое развилось 7 дней тому назад и сопровождалось шумом в ухе и легким головокружением. При исследовании слуховой функции выявлено повышение порогов восприятия по кости до 40-50 дБ, а по воздуху до 70-90 дБ в зоне речевых частот. Диагноз: острая сенсоневральная тугоухость правосторонняя. Проводилось лечение: трисан per os по 0,1 г 3 раза в день после еды в течение 10 дней. На 5-й день от начала лечения интенсивность шума в ухе снизилась, отмечено улучшение слуховой функции. После проведенного лечения пороги слуха по кости понизились до 20-30 дБ, по воздуху - до 50-70 дБ в зоне речевых частот.
4. Больная Кузьмина Л., 36 лет. Обратилась с жалобам на резкое снижение слуха на левое ухо, которое возникло после сна. Из анамнеза не было выявлено причин, обусловивших снижение слуха. Госпитализирована на 5-й день от начала заболевания. Диагноз: внезапная сенсоневральная тугоухость. При исследовании слуховой функции было выявлено повышение порогов в зоне речевых частот по кости до 40-50 дБ, а по воздуху - до 70-80 дБ. Проведено лечение: трисан per os по 0,05 г 3 раза в день после еды в течение 10 дней. На 7-й день от начала лечения отметила улучшение слуховой функции. На 12-й день от начала лечения пороги слуха в зоне речевых частот понизились по кости и воздуху до уровня 10-20 дБ.
Для сравнения приводим пример лечения сенсоневральной тугоухости известными средствами.
Больной Белов Е., 41 год. Обратился 15.02.95 г. с жалобами на снижение слуха на левое ухо, которое возникло 09.02.95 г. на фоне повышения артериального давления, страдает гипертонической болезнью в течение последних 5 лет. При обращении пороги слуха в зоне речевых частот по кости составляли 40-50 дБ, по воздуху - 60-80 дБ. На фоне проводимой гипотензивной терапии получал АТФ 2 мл внутривенно, кокарбоксиллазу и трентал в общепринятых дозах, никотиновую кислоту по схеме в течение 10 дней. После лечения больной отмечал уменьшение интенсивности шума в ухе и незначительное улучшение слуховой функции. При исследовании отмечено изменение порогов слуха в зоне речевых частот по кости 30-40 дБ, по воздуху - 40-60 дБ.
Предложенное средство для лечения острой и внезапной сенсоневральной тугоухости и глухоты позволяет эффективно лечить заболевание.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ОСТРОЙ И ВНЕЗАПНОЙ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ И ГЛУХОТЫ | 2014 |
|
RU2563829C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ УКАЧИВАНИЯ И СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ УКАЧИВАНИЯ (ВАРИАНТЫ) | 2019 |
|
RU2753952C2 |
| Способ получения дигидрохлорида 3-(2-морфолино-этилтио)-1,2,4-триазино[5,6-b]индола | 2016 |
|
RU2643315C2 |
| СРЕДСТВО И СПОСОБ ДЛЯ ЛЕЧЕНИЯ НЕЙРОСЕНСОРНОЙ ТУГОУХОСТИ | 2018 |
|
RU2698451C1 |
| Способ лечения острой акустической травмы | 2022 |
|
RU2783255C1 |
| Тромбоцитарный дезагрегант | 1988 |
|
SU1672373A1 |
| СПОСОБ ЛЕЧЕНИЯ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ | 2003 |
|
RU2232014C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ ВТОРИЧНОЙ СЕНСОНЕВРАЛЬНОЙ ТУГОУХОСТИ | 2016 |
|
RU2651110C1 |
| ГИДРОХЛОРИД 3-ЭТИЛТИО-5-(2-МОРФОЛИНО)-ЭТИЛ-1,2,4-ТРИАЗИНО[5,6-В]ИНДОЛА, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБНОСТЬЮ ПОВЫШАТЬ УСТОЙЧИВОСТЬ К ПОВТОРНОЙ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЕ | 1982 |
|
SU1059866A1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ НЕЙРОСЕНСОРНОЙ ТУГОУХОСТИ | 2002 |
|
RU2223741C1 |
Изобретение относится к области медицины, а именно к отоларингологии. Средство для лечения острой и внезапной сенсоневральной тугоухости и глухоты содержит активное вещество - дигидрохлорид моногидрат 3-(2-морфолиноэтилтио)-1,2,4-триазино [5,6-b] индола в эффективных количествах, для внутривенного введения средства дополнительно содержит натрия хлорид, NaOH, воду, взятых в определенных количественных соотношениях. Средство позволяет эффективно лечить острую и внезапную сенсоневральную тугоухость и глухоту. 1 з. п.ф-лы, 4 табл.
Дигидрохлорид моногидрат 3-(2-морфолиноэтилтио)-1,2,4-триазино[5,6-b] индола - 2,5 - 12,5
Натрий хлорид - 6,0 - 9,0
NaOH - 0,2 - 1,0
Вода - Остальное
| Способ лечения тугоухости и глухоты | 1988 |
|
SU1577792A1 |
| Способ лечения тугоухости при отосклерозе | 1988 |
|
SU1657181A1 |
| DE 3030646, 26.03.81 | |||
| Максимов А.М | |||
| Лечение больных острым кохлеарным невритом АТФ-кислотой | |||
| - Вестник оториноларингологии, 1986, с.104 - 105. | |||
Авторы
Даты
1998-09-27—Публикация
1997-12-25—Подача