Изобретение относится к области медицины, а именно - к биохимии и может быть использовано для выделения и очистки альфа-2-макроглобулина (α-2-МГ).
В биохимической практике известен способ получения препарата α-2-МГ (Song М.К., Adham N.F., Rindercknecht Н. // Biochem. Med. - 1975. - V.14. - №2. - P. 162-169), включающий поэтапное осаждение глобулинов исходного материала полиэтиленгликолем-300 с последующей хроматографией на колонке с сефадексом G-200.
Несмотря на простоту данного способа, он имеет существенный недостаток - невысокая степень очистки получаемого белка.
Известен также способ выделения α-2-МГ (Luis F. // Protein Expression and Purification. - 1997. - V. 10. - P.301-308.), заключающийся в получении препарата α-2-МГ, сочетанием обработки исходного материала (сыворотка крови беременных женщин) лизин-сефарозой, фракционирования полиэти-ленгликолем 6000, ионообменной хроматографии на ДЕАЕ-сефацеле в градиенте ионной силы и ионообменной хроматографии на цинк-иминодиацетилсефарозе в градиенте рН (от 6,8 до 5,5).
Однако недостатками известного способа являются:
• его техническая сложность, трудоемкость;
• получение препарата α-2-МГ очень низкой концентрации, что существенно затрудняет его дальнейшее использование и требует дополнительных манипуляций по концентрированию;
• большие временные затраты, необходимые для осуществления полного процесса очистки (7-9 дней);
• дороговизна и малодоступность сорбентов, реактивов и вспомогательной аппаратуры, необходимых для практической реализации данного способа.
Наиболее близким к предлагаемому является способ получения препарата трофобластического бета-глобулина (Никулина Д.М., Кривенцев Ю.А. Способ получения препарата трофобластического бета-глобулина / Патент на изобретение RU 2258221 С2, 10.08.2005. Заявка №2003110311/15 от 10.04.2003), включающий одновременное получение очищенных препаратов α-2-МГ, трофобластического бета-глобулина (ТБГ) и связанного с беременностью α2-гликопротеина (α-2-PAG) сочетанием обработки исходного материала (сыворотка крови беременных женщин) методами ионообменной хроматографии на сефадексе А-50 в ступенчатом градиенте ионной силы, осаждения сульфатом аммония 40% насыщения, гидрофобная хроматография на фенил-сефарозе и гель-проникающей хроматографии на Тоуореаг1-65 с 0,5М мочевиной.
Недостатками прототипа являются:
• дороговизна и малодоступность сорбентов, реактивов и вспомогательной аппаратуры, необходимых для практической реализации данного способа;
• получение препарата α-2-МГ низкой концентрации, что существенно затрудняет его дальнейшее использование и требует дополнительных манипуляций по концентрированию;
• техническая сложность, трудоемкость.
Предлагаемое изобретение направлено на повышение эффективности способа выделения и очистки α-2-МГ.
Указанный технический результат в изобретении достигается тем, что в качестве исходного материала используют сыворотку крови здоровых мужчин, гель-фильтрацию проводят на Sephadex G-200 на 0,1 М натрий-фосфатном буфере, рН-7,3 при отношении высоты гидравлического столба к высоте рабочей части колонки - 1/5 и скорости элюции - 15-25 мл/см2⋅ч, заключительный этап очистки проводят методом ионообменной хроматографии на QAE-sephadex А-50 в 0,05М трис-HCl буфере с рН-6,2, а элюцию альфа-2-макроглобулина проводят в одноступенчатом градиенте ионной силы до 0,45 Моль/л.
Предлагаемый способ основан на том, что в качестве ключевого заключительного этапа очистки α-2-МГ используют ионообменную хроматографию на QAE-sephadex А-50 с резким однократным подъемом ионной силы буфера, что позволяет не только очищать, но и значительно концентрировать α-2-МГ, полученный на предыдущем этапе (очень низкая концентрация очищенного α-2-МГ является основной проблемой при его многоэтапной тонкой очистке большинством методов) и параллельно консервировать его в гипертоническом солевом растворе элюата. В качестве рабочего буфера выбран трис-HCl буфер 0,05М, рН 6,2 (исходя из того, что изоэлектрическая точка α-2-МГ - 5,4). QAE-sephadex выбран как сорбент по двум причинам:
• Он обладает очень высокой емкостью, что является очевидным преимуществом при обработке больших объемов растворов с малой концентрацией белка.
• Серия экспериментов показала, что QAE-sephadex настолько эффективен на финальной стадии очистки α-2-МГ, что это позволило полностью исключить из алгоритма получения данного белка этап гидрофобной хроматографии на фенил-сефарозе.
Следует указать, что мы отказались от широко используемой для получения α-2-МГ сыворотки крови беременных женщин в качестве исходного материала ввиду высокой концентрации в ней ТБГ и α-2-PAG, которые, как было показано (Кривенцев Ю.А. Изучение физико-химических свойств и межмолекулярных взаимодействий сывороточных белков беременности / Автореферат диссертации на соискание ученой степени кандидата медицинских наук. - Астрахань. - 1999. - 20 с), имеют выраженные межмолекулярные взаимодействия с α-2-МГ, что является существенной проблемой при их отделении от искомого протеина. В результате эмпирического поиска и анализа, в качестве исходного биоматериала нами выбрана сыворотка крови здоровых мужчин, в которой концентрация вышеуказанных балластных белков имеет следовые значения, что является безусловным преимуществом. Забор материала производился при участии квалифицированных специалистов.
В ходе разработки предлагаемого способа выявлены оптимальные параметры проведения методики: рН, состав и ионная сила рабочего буфера.
Для получения статистически значимых результатов каждый из нижеописанных экспериментов повторялся пятикратно, с соблюдением всех параметров и условий. Определение концентрации α-2-МГ проводили после каждого этапа очистки путем количественного иммунохимического анализа методом радиальной иммунодиффузии по Манчини с использованием моноспецифических тест-систем на α-2-МГ. Оценку эффективности способа проводили по основным характеристикам очистки: абсолютным количествам α-2-МГ в растворах, его относительной массовой доле и степени очистки. Для оценки концентрации искомого белка в препаратах использовались моновалентные антисыворотки к α-2-МГ, полученные самостоятельно и прошедшие строгий контроль чистоты и специфичности.
Предлагаемый способ был успешно апробирован в научной лаборатории кафедры биологической химии и клинической лабораторной диагностики Астраханского государственного медицинского университета в течение 2018-2021 гг.
Ниже приводятся результаты апробации:
Пример №1
В ходе работы апробирован оригинальный алгоритм выделения и очистки α-2-МГ, включающий последовательные этапы:
1. Фракционирование сульфатом аммония
Использовали сухой, хорошо измельченный порошок сернокислого аммония (ч.д.а.). В сливную сыворотку крови здоровых мужчин добавляли сухой порошок сульфата аммония в количестве, соответствующем 40% от насыщающей концентрации. Осаждение проводили в течение 6 часов при комнатной температуре. Затем раствор центрифугировали при 6000 об/мин в течение 18 минут. Осадок, содержащий α-2-МГ, растворяли в 0,01 М Трис-HCl буфере, рН - 7,4; при этом объем буферного раствора превышал объем осадка в 5 раз.
2. Гель-фильтрация на Sephadex G-200.
Рабочим буферным раствором служил 0,1 М натрий-фосфатный буфер, рН-7,3.
Полученный на предыдущих этапах очистки белковый препарат (объем которого составлял 1,5-2% от рабочего объема колонки), предварительно смешанный с рабочим буфером в объемном соотношении 1:1 и голубым декстраном 2000 (до 0,2% концентрации), вносили в колонку и наслаивали элюэнт на верхний слой геля на высоту 0.5-1 см.
Процесс хроматографического разделения проводили при отношении высоты гидравлического столба к высоте рабочей части колонки - 1/5 и скорости элюции - 20 мл/см2⋅ч.
3. Ионообменная хроматография на DEAE-sephadex А-50.
Белковый раствор вносили в колонку из расчета: 12 мл раствора на 1 мл геля. Элюцию фиксированного на геле белка проводили восходящем градиенте ионной силы буфера до 0,5 Моль/л (добавлением NaCl).
Вывод: Концентрация α-2-МГ в очищенном препарате и степень его очистки оказались исчезающее малыми, ниже пороговой чувствительности иммунохимической тест-системы к α-2-МГ (см. табл.1).
Пример №2
Выделение и очистку α-2-МГ проводили по методике примера №1, но со следующими отличиями: скорость элюции на 2-м этапе составляла 15 мл/см2⋅ч, а на 3-м этапе очистки, вместо DEAE-sephadex А-50 использовали QAE-sephadex А-50, отличающийся большей емкостью, белковый раствор на 3-м этапе вносили в колонку из расчета: 55 мл раствора на 1 мл геля, элюцию проводили путем резкого однократного подъема ионной силы до 0,45 М; в таких условиях весь фиксированный на геле белок быстро элюируется в малом объеме (эффект концентрирования).
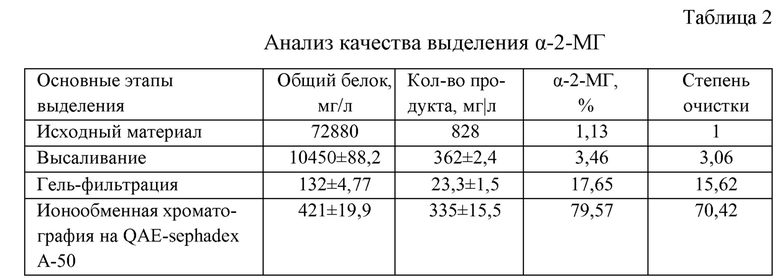
Вывод: Концентрация α-2-МГ в очищенном препарате и степень его очистки оказались высокими (см. табл.2. Анализ качества выделения α-2-МГ).
Пример №3
Выделение и очистку α-2-МГ проводили по методике примера №2, но со следующим отличием: скорость элюции на 2-м этапе составляла 25 мл/см2⋅ч.
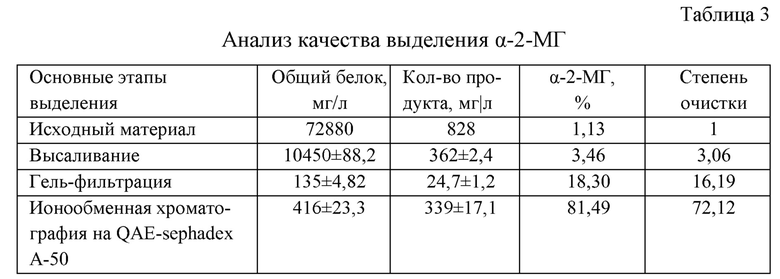
Вывод: Параметры и условия эксперимента в данном примере оказались оптимальными. Концентрация α-2-МГ в очищенном препарате и степень его очистки оказались максимальными (см. табл.3. Анализ качества выделения α-2-МГ). Контроль качества очистки, проводимый электрофорезом в полиакриламидном геле, показал одну полосу в полученных белковых препаратах (см. фиг.1.: 1. - Осадок после высаливания; 2. - Препарат после гель-фильтрации на Sephadex G-200; 3. - Ощищенный препарат α-2-МГ после ионообменной хроматографии на QAE-sephadex А-50).
Предлагаемый способ имеет следующие преимущества:
1. Концентрирование материала - заключительный этап реализует сразу две задачи: тонкая очистка белка и параллельное эффективное его концентрирование в 72,12 раза.
2. Простота и доступность - для получения очищенного препарата α-2-МГ достаточно всего трех доступных этапов;
3. Экономичность трудозатрат - благодаря простоте способа, для его полного воплощения достаточно одного квалифицированного лаборанта;
4. Параллельная консервация - поскольку полученный на заключительном этапе очищенный препарат α-2-МГ находится в гипертоническом солевом растворе (0,45 М NaCl), нет нужды в дополнительных манипуляциях по консервации;
5. Способность обработки больших объемов материала, обеспечиваемая высокой емкостью ионообменного сорбента;
6. Многократность использования сорбентов на 2-м и 3- этапах;

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЭСТРОГЕНСВЯЗЫВАЮЩЕГО БЕЛКА, АССОЦИИРОВАННОГО СО ЗЛОКАЧЕСТВЕННЫМИ НОВООБРАЗОВАНИЯМИ | 2012 |
|
RU2489440C1 |
| СПОСОБ ОЧИСТКИ АЛЬФА-ФЕТОПРОТЕИНА ЧЕЛОВЕКА | 1994 |
|
RU2074193C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-МАКРОГЛОБУЛИНА | 1990 |
|
RU2049470C1 |
| СПОСОБ ВЫДЕЛЕНИЯ РЕКОМБИНАНТНОГО ЧЕЛОВЕЧЕСКОГО АЛЬФА-ФАКТОРА НЕКРОЗА ОПУХОЛИ | 1992 |
|
RU2101292C1 |
| СПОСОБ ПОЛУЧЕНИЯ С1-ЭСТЕРАЗНОГО ИНГИБИТОРА ЧЕЛОВЕКА И ПРОДУКТ ДЛЯ ИСПОЛЬЗОВАНИЯ В МЕДИЦИНЕ | 2004 |
|
RU2256464C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУБСТАНЦИИ L-ЛИЗИН-АЛЬФА-ОКСИДАЗЫ | 2011 |
|
RU2471866C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО АНТАГОНИСТА РЕЦЕПТОРА ИНТЕРЛЕЙКИНА-1 ЧЕЛОВЕКА "АРИЛ" | 2004 |
|
RU2326947C2 |
| Способ получения протеолитического препарата для медицинского применения | 2015 |
|
RU2610669C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРОМБИНОПОДОБНЫХ ФЕРМЕНТОВ ИЗ ЯДА ЗМЕИ | 2004 |
|
RU2271219C1 |
| Способ получения макроглобулина | 1980 |
|
SU961695A1 |

Изобретение относится к области биотехнологии, конкретно к получению белков из сыворотки крови, и может быть использовано для выделения и очистки альфа-2-макроглобулина (альфа-2-МГ). Предложен способ выделения и очистки альфа-2-МГ, включающий фракционирование белков сульфатом аммония 40% насыщения, гель-фильтрацию и ионообменную хроматографию. В качестве исходного материала используют сыворотку крови здоровых мужчин, гель-фильтрацию проводят на Sephadex G-200 на 0,1 М натрий-фосфатном буфере, рН-7,3 при отношении высоты гидравлического столба к высоте рабочей части колонки - 1/5 и скорости элюции - 15-25 мл/см2⋅ч, заключительный этап очистки проводят методом ионообменной хроматографии на QAE-sephadex А-50 в 0,05М трис-HCl буфере с рН-6,2, а элюцию альфа-2-МГ проводят в одноступенчатом градиенте ионной силы до 0,45 моль/л. Изобретение обеспечивает повышение эффективности выделения и очистки альфа-2-МГ. 1 ил., 3 табл., 3 пр.
Способ выделения и очистки альфа-2-макроглобулина, включающий фракционирование белков сульфатом аммония 40% насыщения, гель-фильтрацию и ионообменную хроматографию, отличающийся тем, что в качестве исходного материала используют сыворотку крови здоровых мужчин, гель-фильтрацию проводят на Sephadex G-200 на 0,1 М натрий-фосфатном буфере, рН-7,3 при отношении высоты гидравлического столба к высоте рабочей части колонки - 1/5 и скорости элюции - 15-25 мл/см2⋅ч, заключительный этап очистки проводят методом ионообменной хроматографии на QAE-sephadex А-50 в 0,05М трис-HCl буфере с рН-6,2, а элюцию альфа-2-макроглобулина проводят в одноступенчатом градиенте ионной силы до 0,45 моль/л.
| WO 2013126587 A1, 29.08.2013, RU 2258221 C2, 10.08.2005. КРИВЕНЦЕВ Ю.А | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2023-01-11—Публикация
2022-06-30—Подача