Область техники, к которой относится изобретение
Настоящее изобретение относится к германийорганическому соединению, обладающему новой структурой. Уровень техники
Германий (Ge) является элементом, который в течение многих лет исследовали, как полупроводник, а также активно исследовали органические соединения германия и были синтезированы германийорганические соединения разных типов.
Так, например, Ge-132 (также называющийся, как поли-транс-[(2-карбоксиэтил)гермасесквиоксан], репагерманий или германий Asai) является германийорганическим соединением, оказывающим физиологические воздействия разного рода, такие как иммуностимулирующие воздействия, противоопухолевые воздействия, противовоспалительные воздействия, анальгетические воздействия и совместные с морфином воздействия. Ge-132 является кристаллическим соединением, находящимся при комнатной температуре в твердой форме и обладающим циклической структурой, состоящей всего из 12 атомов германия и кислорода, и оно гидролизуется в воде с образованием мономера, а именно, 3-(тригидроксигермил)пропановой кислоты (ТГГП). Поскольку в живом организме содержится большое количество воды, полагают, что Ge-132 гидролизуется в живом организме с образованием ТГГП или ее соли.
Полагают, что ТГГП образует комплекс ТГГП-цис-диол типа лактона вследствие дегидратации и конденсации с содержащим цис-диольную группу соединением и, таким образом, регулирует физиологические функции содержащего цис-диольную группу соединения (например, непатентная публикация 1). В качестве примера регулирования физиологических функций, происходящих при взаимодействии этих соединений, сообщали, что ТГГП образует комплекс с аденозином или АТФ (аденозинтрифосфат) и ингибирует связывание аденозина или АТФ с рецептором Р1 или Р2, и, таким образом, ее можно использовать для ослабления боли (непатентная публикация 2). Эти данные свидетельствуют о том, что Ge-132 оказывает физиологические воздействия разного рода вследствие взаимодействия ТГГП, которая образуется вследствие гидролиза в живом организме, с компонентами, содержащимися в организме.
Сушка раствора ТГГП приводит к получению твердых германийорганических соединений, обладающих полимерной структурой, в которой множество молекул ТГГП дегидратированы и сконденсированы. Ge-132 является одним из твердых германийорганических соединений, полученных таким путем, и существуют другие известные твердые германийорганические соединения, такие как поли-[(2-карбоксиэтилгидроксигерманий)оксид], твердое германийорганическое соединение, обладающее линейной полимерной структурой, и полимер пропагерманий(3-оксигермилпропионовой кислоты), твердое германийорганическое соединение, обладающее лестничной структурой (циклическая структура, образованная всего из 8 атомов германия и кислорода) (патентная публикация 1, непатентные публикации 3 и 4). Полагают, что эти твердые германийорганические соединения гидролизуются в растворителе, содержащем воду, с образованием ТГГП, которая, в свою очередь, оказывает физиологические воздействия разного рода, описанные выше. Поэтому предпочтительно, если твердые германийорганическими соединениями, для которых ожидается, что они оказывают физиологические воздействия, являются такие, из которых легче образуется ТГГП, т.е. такие, которые превосходно растворимы, в особенности такие, которые обладают хорошей растворимостью и высокой скоростью растворения.
Однако обычные твердые германийорганические соединения недостаточно растворимы в воде и для растворения и гидролиза в воде обычных твердых германийорганических соединений необходимо время, другими словами, обычные твердые германийорганические соединения обладают низкой скоростью растворения. Кроме того, растворы обычных твердых германийорганических соединений обладают значением рН, соответствующим кислой среде, и, соответственно, если раствор вводят в живой организм, может потребоваться нейтрализация раствора.
Список цитированной литературы Патентная литература
Патентная публикация 1: Japanese Patent Application Laid-open Publication No. 57-102895.
Непатентная литература
Непатентная публикация 1: Nakamura et al., Future. Med. Chem., 2015, 7 (10), 1233-1246.
Непатентная публикация 2: Shimada et al., Biol. Trace Elem. Res., 2018, 181 (1), 164-172.
Непатентная публикация 3: Tsutsui et al., J. Am. Chem. Soc, 1976, 98 (25), 8287-8289.
Непатентная публикация 4: Mizuno et al., J. Pharm. Sci., 2015, 104 (8), 2482-2488.
Краткое изложение сущности изобретения Техническая задача
Задачей настоящего изобретения является получение нового германийорганического соединения, обладающего превосходной растворимостью.
Решение задачи
Авторы настоящего изобретения провели тщательное исследование кристаллизации ТГГП. В результате этого авторы настоящего изобретения обнаружили, что однородные отдельные кристаллы образуются при нейтрализации щелочью водного раствора, содержащего ТГГП при высокой концентрации, и добавлении органического растворителя, смешивающегося с водой, и что эти кристаллы представляют собой октамеры ячеистого типа, в которых соединены 8 молекул ТГГП, и завершили следующее изобретение.
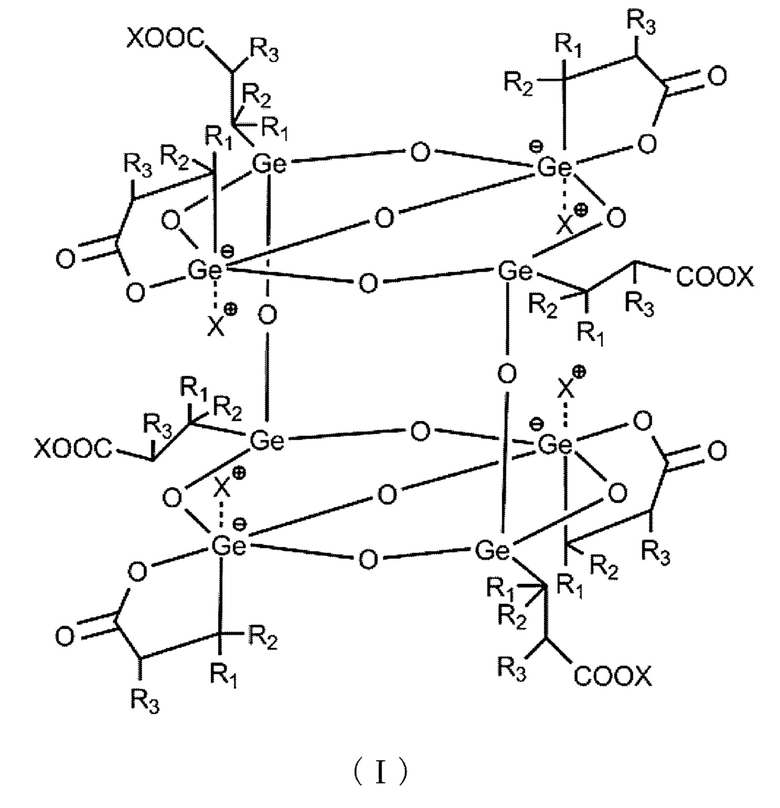
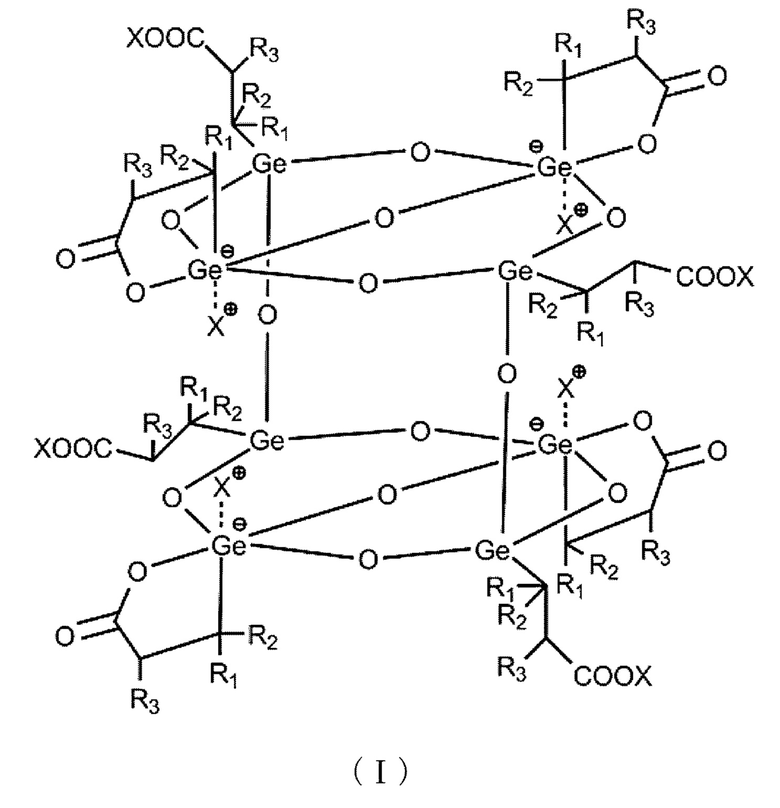
(1) Соединение формулы (I),
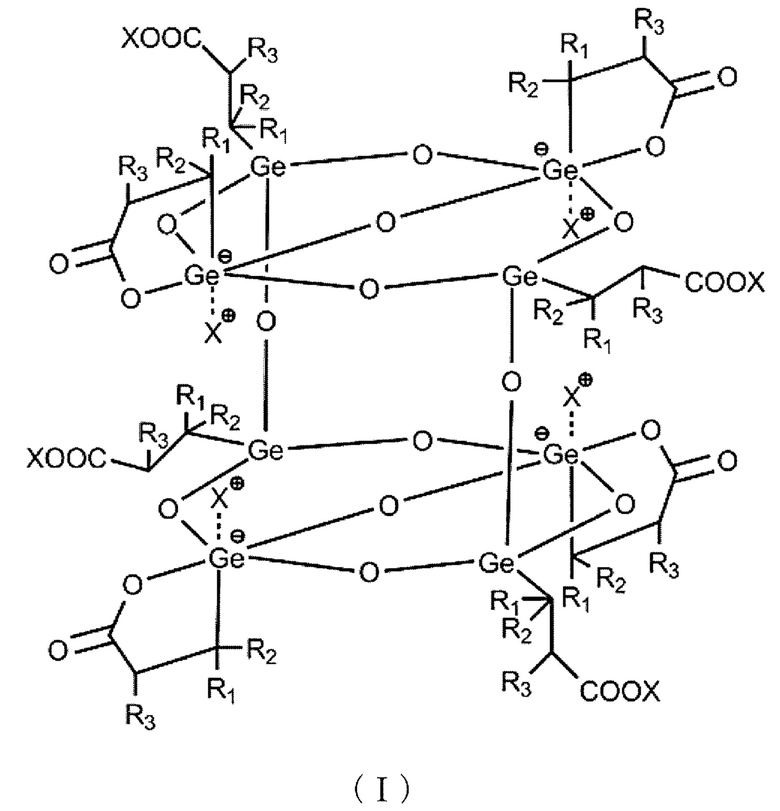
Химическая формула 1 в которой R1, R2 и R3 все независимо обозначают водород или низший алкил и X обозначает катион щелочного металла, аммониевый катион или четвертичный аммониевый катион.
(2) Соединение, соответствующее параграфу (1), в котором все R1, R2 и R3 обозначают водород.
(3) Соединение, соответствующее параграфу (1), в котором X обозначает катион натрия.
(4) Соединение, соответствующее параграфу (1), в котором все R1, R2 и R3 обозначают водород и X обозначает катион натрия.
Преимущества настоящего изобретения
В соответствии с настоящим изобретением можно получить германийорганическое соединение, которое является превосходно растворимым в воде, и отсутствует необходимость проведения его нейтрализации при введении в живой организм.
Краткое описание чертежей
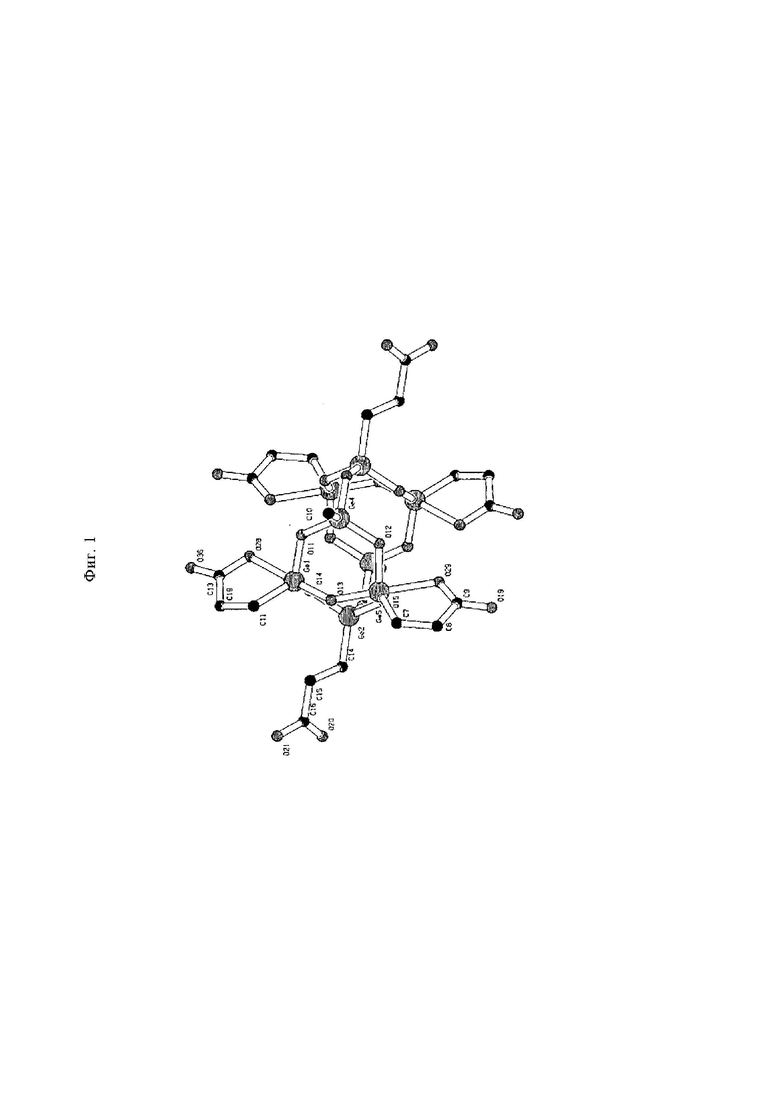
На фиг. 1 представлена схематическая модель структуры октамера ТГГП, являющегося примером соединения, предлагаемого в настоящем изобретении.
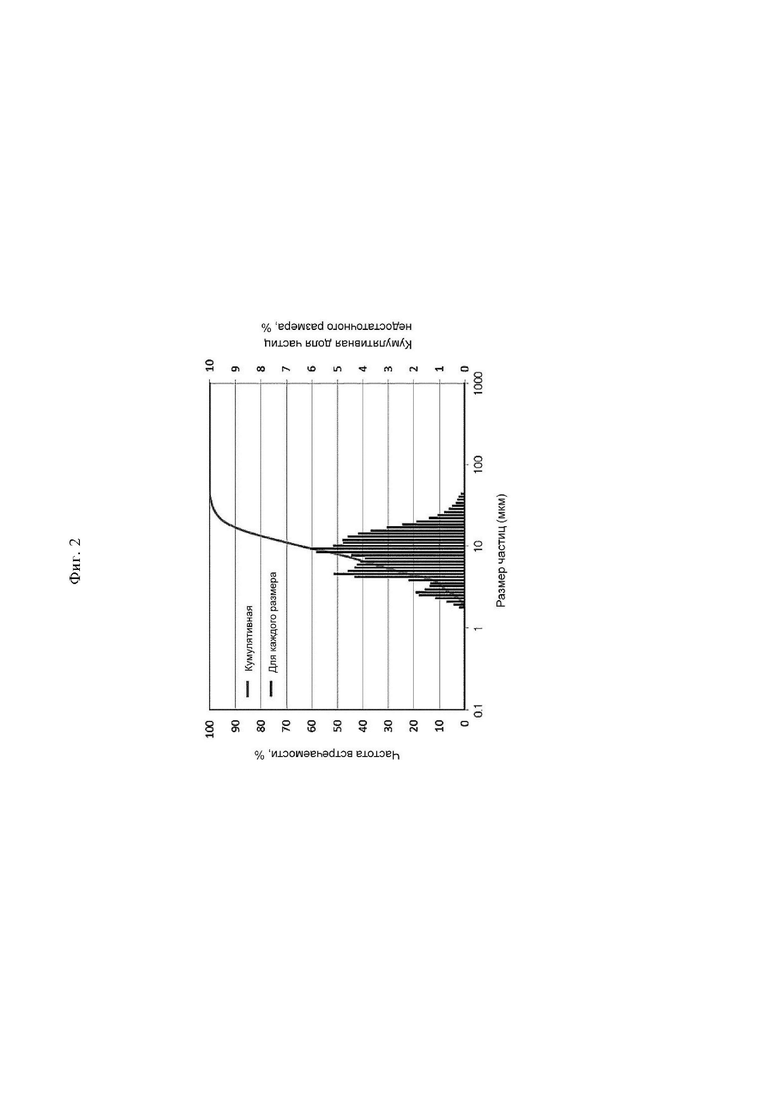
На фиг. 2 представлена диаграмма, иллюстрирующая распределение частиц октамера ТГГП по размерам.
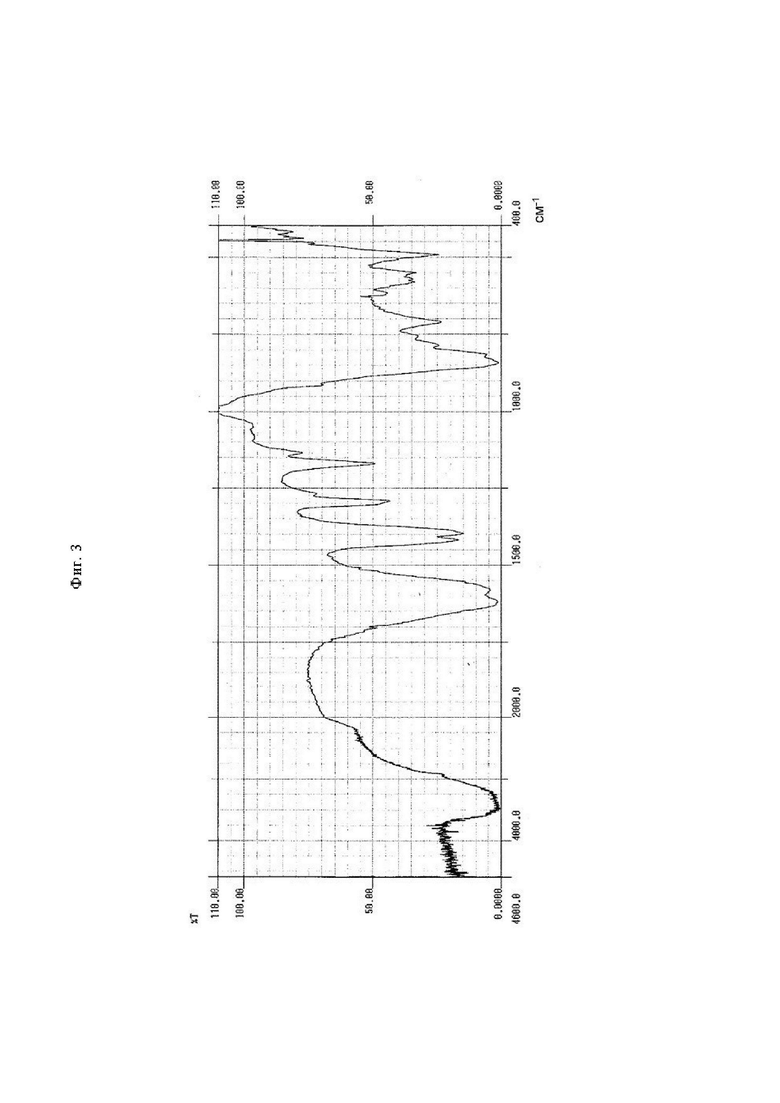
На фиг. 3 представлена диаграмма, иллюстрирующая инфракрасный спектр поглощения октамера ТГГП.
На фиг. 4 представлена диаграмма, иллюстрирующая полученный с помощью времяпролетной масс-спектрометрии (ВПР-МС) масс-спектр октамера ТГГП и теоретический спектр октамера ТГГП.
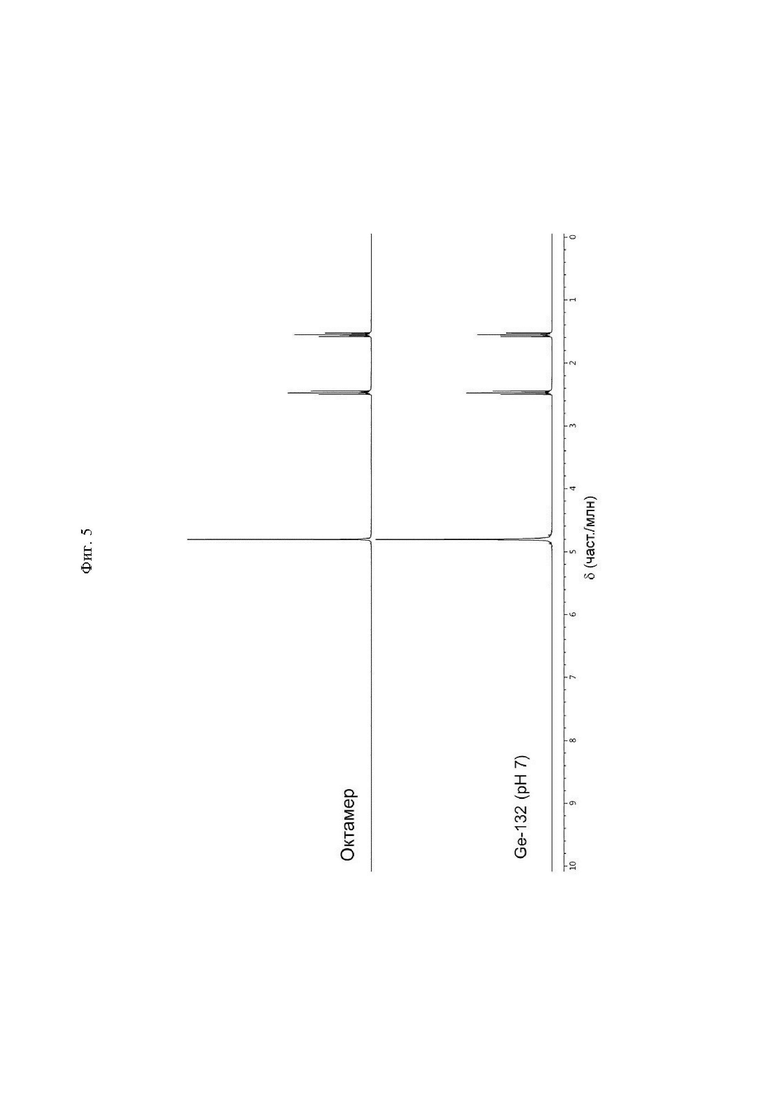
На фиг. 5 представлена диаграмма, иллюстрирующая полученный с помощью 1Н ЯМР (ядерный магнитный резонанс) спектр октамера ТГГП и полученный с помощью 1Н ЯМР спектр Ge-132.
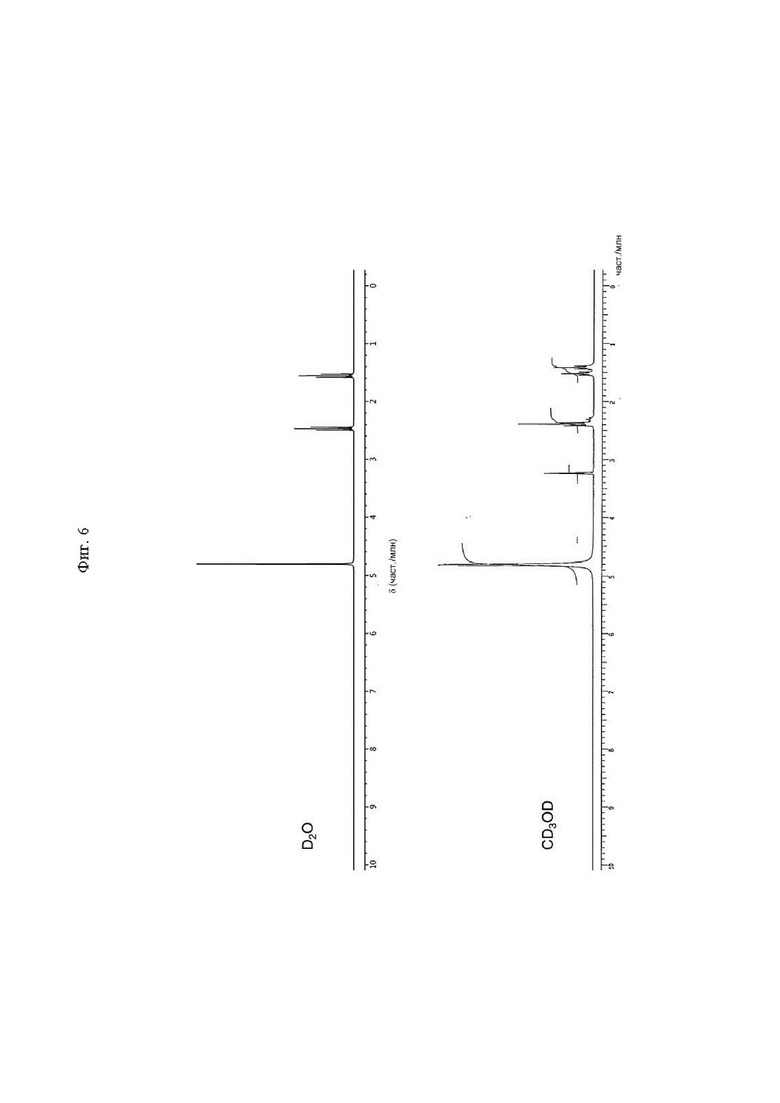
На фиг. 6 представлена диаграмма, иллюстрирующая полученные с помощью 1Н ЯМР спектры октамера ТГГП, полученные с использованием в качестве растворителей тяжелой воды и тяжелого метанола.
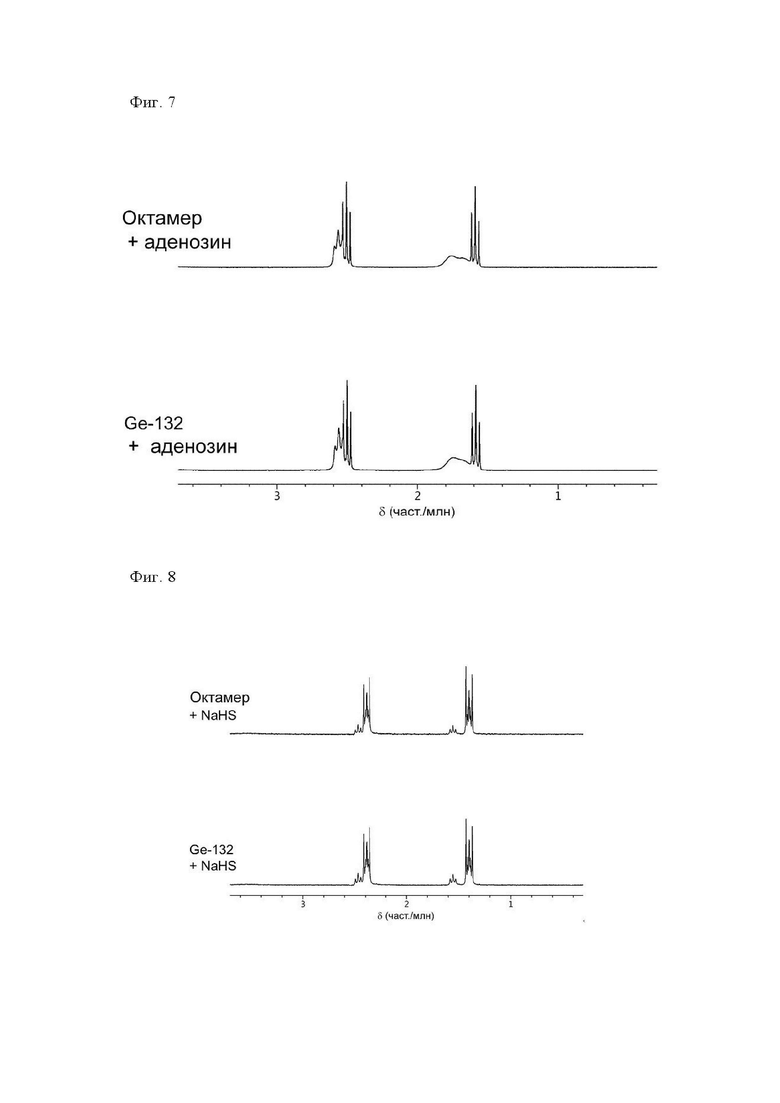
На фиг. 7 представлена диаграмма, иллюстрирующая полученные с помощью 1Н ЯМР спектры смешанных растворов, содержащих аденозин и октамер ТГГП или Ge-132.
На фиг. 8 представлена диаграмма, иллюстрирующая полученные с помощью 1Н ЯМР спектры смешанных растворов, содержащих NaHS (натриевая соль H2S) и октамер ТГГП или Ge-132.
Описание вариантов осуществления
Хотя приведенное ниже описание настоящего изобретение может быть основано на типичных вариантах осуществления или конкретных примерах, настоящее изобретение не ограничивается такими вариантами осуществления или примерами. Следует отметить, что приведенные в настоящем описании верхние предельные значения и нижние предельные значения числовых диапазонов можно объединить произвольным образом. Кроме того, приведенный в настоящем описании числовой диапазон, указанный с использованием слова "до" или знака означает диапазон, включающий числовые значения, находящиеся на обеих границах диапазона, являющиеся верхним предельным значением и нижним предельным значением, если не указано иное.
Первым объектом настоящего изобретения является соединение формулы (I),
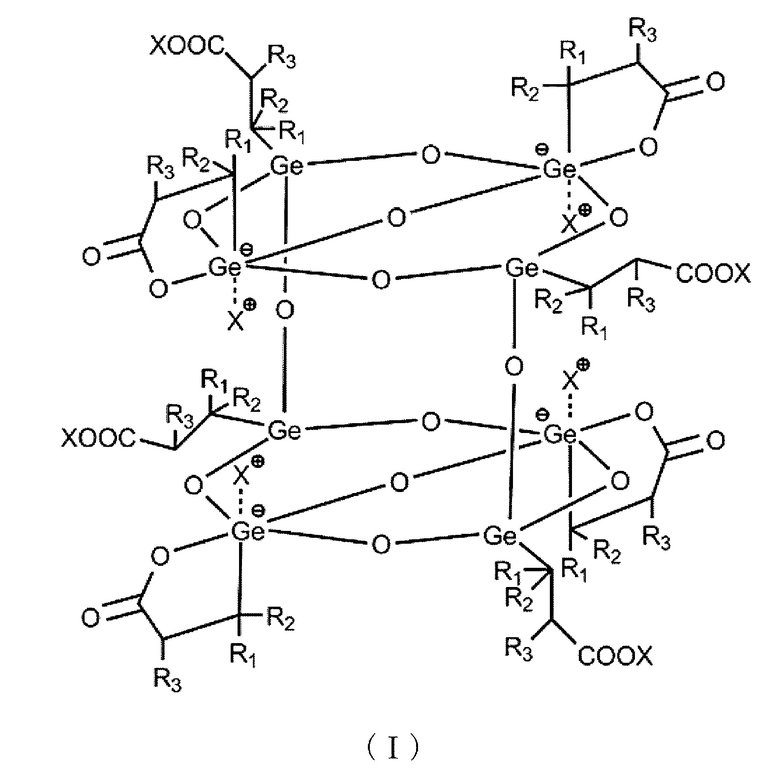
Химическая формула 2 в которой R1, R2 и R3 все независимо обозначают водород или низший алкил и X обозначает катион щелочного металла, аммониевый катион или четвертичный аммониевый катион.
В формуле (I): R1, R2 и R3 все независимо обозначают водород или низший алкил. Низший алкил означает линейный или разветвленный алкил, содержащий от 1 до 6, предпочтительно от 1 до 4 и более предпочтительно от 1 до 3 атомов углерода. В предпочтительном варианте осуществления R1, R2 и R3 все обозначают водород.
В формуле (I): X обозначает катион щелочного металла, такой как Na или K+, аммониевый катион или четвертичный аммониевый катион. Четвертичный аммониевый катион представляет собой катион, в котором 4 алкильные группы и/или арильные группы соединены с атомом азота. Предпочтительно, если четвертичным аммониевым катионом, использующемся в настоящем изобретении, является катион, в котором 4 линейные или разветвленные алкильные группы, содержащие от 1 до 6, предпочтительно от 1 до 4 и более предпочтительно от 1 до 3 атомов углерода, соединены с атомом азота. Примеры четвертичного аммониевого катиона включают тетраметиламмониевый катион, тетраэтиламмониевый катион, тетрапропиламмониевый катион, этилтриметиламмониевый катион и триэтилметиламмониевый катион. В предпочтительном варианте осуществления X обозначает Na+.
Соединение формулы (I) также может быть описано формулой (II). В формуле (II): R1, R2, R3 и X являются такими же, как определенные в формуле (I).
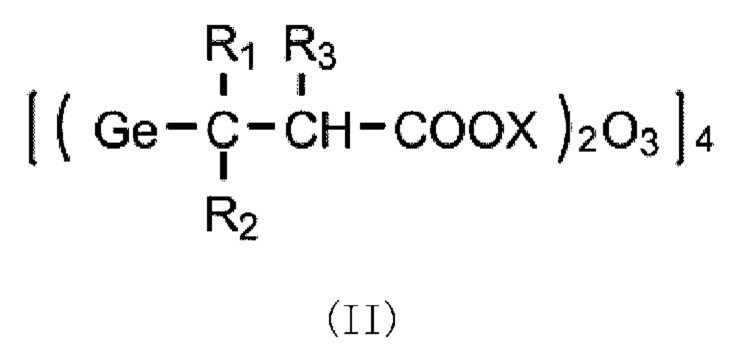
Химическая формула 3 Предпочтительные примеры соединения формулы (I) могут включать соединение формулы (I), в которой R1-R3 все обозначают водород и X обозначает Na+, т.е. 1,7,9,15-тетра(2'-натрий-карбоксиэтилгерманий)-3,5,11,13-тетра-[натрий-пропанато(2-)-С3',О']-германий-2,4,6,8,10,12,14,16,17,18,19,20-додекаоксапентацикло[8.11,5.17,11.19,13.13,15.]эйкозан (ниже в настоящем изобретении обозначенный, как октамер ТГГП).
Соединение формулы (I) можно получить путем кристаллизации соединения формулы (III) (в которой R1-R3 являются такими же, как указанные в описании формулы (I)) из смеси растворителей, содержащей воду и органический растворитель, смешивающийся с водой.
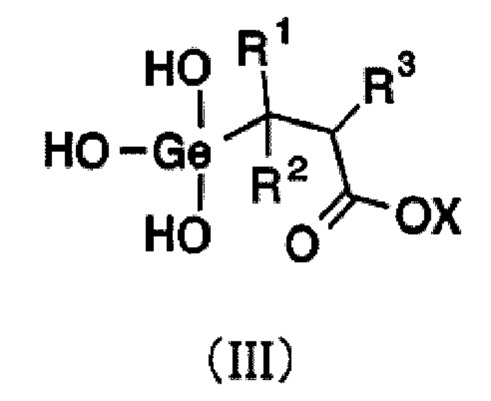
Химическая формула 4 Соединение формулы (III) можно синтезировать с использованием производного акриловой кислоты формулы (IV) и трихлоргермана, как это показано на приведенной ниже схеме.
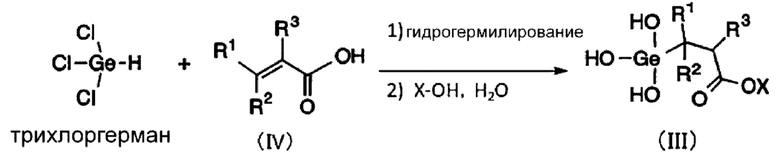
Химическая формула 5
Гидрогермилирование производного акриловой кислоты формулы (IV) и трихлоргермана можно провести, например, с использованием концентрированной хлористоводородной кислоты, диэтилового эфира или хлороформа в качестве растворителя, при температуре, равной примерно от 25 до 40°С. Затем соединение, полученное по реакции гидрогермилирования, вводят в реакцию с гидроксидом щелочного металла или амином в присутствии воды, обычно в водном растворе, для проведения реакции гидролиза и нейтрализации, таким образом можно получить соединение формулы (III).
Альтернативно, известный полимер ТГГП, такой как Ge-132, вводят в реакцию с гидроксидом щелочного металла или амином в присутствии воды, таким образом можно получить соединение формулы (III), в которой R1-R3 все обозначают водород.
Полученное соединение формулы (III) кристаллизуют из смеси растворителей, содержащей воду и органический растворитель, смешивающийся с водой. В смеси растворителей соотношение смешивания вода:органический растворитель может составлять от 1:3 до 1:20 (об./об.), предпочтительно от 1:3 до 1:10 (об./об.) и более предпочтительно от 1:3 до 1:5 (об./об.). Примеры использующегося органического растворителя включают ацетон или низший спирт, такой как метанол, этанол, 1-пропанол или 2-пропанол, и более предпочтительно использовать этанол.
К водному раствору соединения формулы (III) добавляют указанный выше органический растворитель в количестве, которое обеспечивает соотношений смешивания, находящееся в указанном выше диапазоне, таким образом получают смешанный раствор, предназначенный для кристаллизации. Концентрация соединения формулы (III) в смешанном растворе может составлять от 2 до 12% (мас./об.), например, от 4 до 12% (мас./об.), от 6 до 12% (мас./об.) или от 8 до 12% (мас./об.), и предпочтительно, если она равна от 8 до 12% (мас./об.).
Указанный выше смешанный раствор в достаточной степени перемешивают и затем выдерживают при комнатной температуре в течение 12 ч или более, предпочтительно в течение 24 ч или более, при этом могут осаждаться кристаллы соединения формулы (I). Для содействия кристаллизации в качестве затравочных кристаллов можно добавить кристаллы соединения формулы (I). Полученные кристаллы можно выделить из смешанного раствора и очистить с использованием обычной методики, такой как фильтрование, промывка органическим растворителем, таким как низший спирт, и сушка при пониженном давлении.
Таким образом, настоящее изобретение также относится к способу получения соединения формулы (I), способ включает смешивание раствора, в котором растворено соединение формулы (III), и смеси растворителя, в которой вода и органический растворитель, смешивающийся с водой, смешаны в соотношении, составляющем от 1:3 до 1:20 (об./об.), с целью обеспечения концентрации соединения формулы (III), равной от 2 до 12% (мас./об.); и выдерживание полученного смешанного раствора для осаждения кристаллов соединения формулы (I).
С помощью способа получения, указанного выше, можно получить соединение формулы (I) в виде кристаллов и кристаллы являются другим объектом настоящего изобретения. Кристаллы октамера ТГГП обладают размером, равным 8 мкмх2 мкм, и они обладают пластинчатой формой. Кроме того, кристаллы можно перекристаллизовать путем выпаривания органического растворителя из насыщенного раствора этих кристаллов в органическом растворителе. При проводимом с помощью рентгенографии исследовании с помощью отдельных кристаллов октамера ТГГП, перекристаллизованных с использованием метанола в качестве органического растворителя, показано, что они обладают приведенными кристаллографическими характеристиками.
Кристаллографическая система: триклинная
Пространственная группа: Р-1
Постоянная решетки: а=11,8879(7), b=20,6589(12), с=22,5198(13), α=63,5610(10), β=76,4800(10), γ=81,3480(10)
Объем элементарной ячейки: V=4808,14
При проведении исследований с помощью рентгенографии в зависимости от условий проведения исследования могут возникать погрешности измерения. Поэтому кристаллы соединения формулы (I) не ограничиваются кристаллами, которые обладают кристаллографическими характеристиками, идентичными кристаллографическим характеристикам, описанным выше, и в объем настоящего изобретения также входят кристаллы, которые обладают кристаллографическими характеристиками, в основном идентичными кристаллографическим характеристикам, описанным выше. Путем внесения подходящих изменений в условия проведения исследования специалисты в данной области техники могут подтвердить, что кристаллографические характеристики являются в основном идентичными.
Не все кристаллы соединения формулы (I) обладают указанными выше кристаллографическими характеристиками. Для специалистов в данной области техники должно быть очевидно, что кристаллы, обладающие указанными выше кристаллографическими характеристиками, являются лишь одной формой кристаллов соединения формулы (I) и могут существовать другие формы кристаллов соединения формулы (I).
Соединения формулы (I) чрезвычайно хорошо растворимы в воде и быстро растворяются. Так, например, растворимость (масса (г) растворенного вещества в 100 г насыщенного раствора) Ge-132 в воде, обладающей температурой, равной 20°С, составляет примерно 1% (другими словами, масса Ge-132, содержащегося в 100 г насыщенного раствора, обладающего температурой, равной 20°С, равна примерно 1 г), и количество времени, необходимое для полного растворения 1% Ge-132 в воде при такой же температуре, составляет 30 мин или более. При таких же условиях растворимость октамера ТГГП составляет 58,8% и продолжительность растворения октамера ТГГП составляет примерно 10 с. Значение рН водного раствора, в котором растворен октамер ТГГП, соответствует нейтральной среде и сходно со значением рН живого организма. Кроме того, соединение формулы (I) растворимо в некоторых органических растворителях, таких как метанол, в которых нерастворимы существующие полимеры ТГГП.
Соединение формулы (I) гидролизуется в воде с образованием растворимого в воде германийорганического соединения, которое является составным звеном соединения формулы (I). Такое растворимое в воде германийорганическое соединение в водном растворе способно взаимодействовать с соединением, обладающим структурой цис-диола (таким как аденозин или фруктоза), или с соединением, обладающим структурой тиола (таким как H2S или глутатион). Растворимое в воде германийорганическое соединение также способно ослаблять боль и механическую аллодинию, вызванную веществом, которое может взаимодействовать с растворимым в воде германийорганическим соединением. Кроме того, растворимое в воде германийорганическое соединение способно обеспечить защиту функциональной группы вещества, которое может взаимодействовать с растворимым в воде германийорганическим соединением, или оно способно уменьшить летучесть вещества при его растворении в воде вместе с веществом. Поэтому соединение формулы (I) можно применять в таких же случаях, как и Ge-132, таких как ослабление боли и механической аллодинии, обеспечение защиты соединения, содержащего цис-диольную группу, обеспечение защиты соединения, содержащего тиольную группу, ослабление боли или зуда, вызванного сульфидом водорода, устранение запаха или предотвращение появления запаха, и подавление продуцирования интерферона типа I.
Для живого организма соединение формулы (I) можно применять в форме фармацевтической композиции, пищевой композиции или косметической композиции, каждая из них дополнительно содержит фармацевтически приемлемые ингредиенты, включая буфер, стабилизатор, консервант и инертный наполнитель и т.п., и/или другие активные ингредиенты. Эти композиции являются другим объектом настоящего изобретения. Фармацевтически приемлемые ингредиенты хорошо известны специалистам в данной области техники и специалисты в данной области техники на основании общих знаний по воплощению могут соответствующим образом их выбрать и использовать, например, выбрать из числа ингредиентов, описанных в Фармакопее Японии, 17-е издание, или, в зависимости от формы препарата, в других стандартных руководствах.
Фармацевтическую композицию, содержащую соединение формулы (I), можно применять для лечения заболевания или ослабления симптома, по отношению к которым германийорганические соединения, предпочтительно ТГГП, являются эффективными, например, для лечения рака или инфекционных заболеваний, или для ослабления воспаления или боли. Таким образом, настоящее изобретение относится к способу лечения заболевания или ослабления симптомов, по отношению к которым являются эффективными германийорганические соединения, предпочтительно ТГГП, способ включает введение субъекту эффективной дозы фармацевтической композиции, содержащей соединение формулы (I). Примеры заболевания включают опухоли и инфекционные заболевания. Примеры симптома включают воспаление и боль.
В контексте настоящего изобретения фармацевтическая композиция, описанная выше, может находиться в любой форме и предпочтительные примеры формы включают препараты для перорального введения (такие как таблетки, капсулы, порошки, гранулы, мелкие гранулы, пилюли, суспензии, эмульсии, растворы и сиропы) и препараты для местного введения (такие как мази и пластыри).
На путь введения фармацевтической композиции не налагаются особые ограничения и его можно подходящим образом выбрать в зависимости от дозированной формы. В одном предпочтительном варианте осуществления композицию вводят в живой организм перорально или чрескожно.
Дозу композиции выбирают подходящим образом в зависимости от случая применения, возраста субъекта, типа и места расположения заболевания и других условий, и она обычно составляет от 10 до 2000 мкг, предпочтительно от 50 до 1000 мкг и более предпочтительно от 100 до 500 мкг в пересчете на 1 кг массы тела взрослого субъекта. Дозу фармацевтической композиции можно вводить один раз в сутки или ее можно разделить на несколько доз и вводить несколько раз в сутки, или ее можно вводить периодически.
Настоящее изобретение более подробно описано с помощью приведенных ниже примеров, однако оно не ограничивается примерами.
Примеры
Пример 1. Синтез и структурный анализ октамера ТГГП
1) Синтез
Ge-132 (500 г, 2,95 моля в пересчете на мономер) отвешивали в стакан объемом 2 л и добавляли 1 л дистиллированной воды, затем суспендировали. В изготовленный из тефлона (зарегистрированная торговая марка) контейнер отвешивали 95% гидроксид натрия (124 г, 2,95 моля) и добавляли 500 мл дистиллированной воды, затем растворяли. К суспензии Ge-132 в воде при перемешивании несколькими порциями добавляли водный раствор гидроксида натрия суспензия для нейтрализации и растворения Ge-132. Нейтрализованный раствор переносили в обладающую формой баклажана колбу объемом 2 л и нагревали при пониженном давлении и концентрировали до объема, равного примерно 1 л. Концентрированный раствор переносили в контейнер объемом 5 добавляли 3 л этанола и смесь тщательно перемешивали и выдерживали при комнатной температуре в течение 24 ч. Осадившиеся кристаллы собирали фильтрованием с отсасыванием, сушили на воздухе и затем нагревали досуха в представляющем собой стеклянную трубку сушильном устройстве при 105°С и при пониженном давлении в течение 8 ч или более, и получали искомое соединение в виде белого кристаллического вещества с выходом, равным 95%. Полученные кристаллы обладали размером, равным 8 мкм х2 мкм, и обладали пластинчатой формой.
2) Рентгеноструктурный анализ отдельных кристаллов
Кристаллы, полученные в разделе 1), растворяли в метаноле и получали насыщенный метанольный раствор. Насыщенный метанольный раствор выдерживали неплотно закрытым при комнатной температуре и метанол постепенно выпаривали и получали пластинчатые кристаллы, которые увеличивались до размера, равного 1 мм или более. Кристаллы собирали и определяли интенсивности дифракции рентгеновских лучей с использованием рентгеноструктурного анализатора монокристалла (SMART APEX II ULTRA,
Bruker) при следующих условиях.
Детектор: двумерный детектор Bruker АРЕХII CCD
Тип источника света: вращающийся анод с тонкой фокусировкой Bruker TXS
Использующаяся длина волны: Мо, 0,71073 
Ток трубки: 24 мА
Напряжение трубки: 50 кВ
Ширина сканирования: 0,5°
Длительность облучения: 3 с
Программное обеспечение для анализа и методика:
Сбор данных: 'АРЕХ2'
Уточнение параметров ячейки: 'АРЕХ2 (Bruker AXS, 2006)'
Обработка данных: 'SAINT (Bruker AXS, 2004)'
Расчет структуры: 'SHELXS-97 (Sheldrick, 1997)'
Уточнение структуры: 'SHELXL-97 (Sheldrick, 1997)'
Молекулярная графика: 'XSHEL (Bruker AXS, 2002)'
Опубликованный материал: 'XCIF (Bruker AXS, 2001)'
Параметры определенной кристаллической структуры приведены ниже, атомные координаты приведены в таблице 1 и построенная на их основании молекулярная структура представлена на фиг. 1.
Кристаллографическая система: триклинная
Пространственная группа: Р-1
Постоянная решетки: а=11,8879(7), b=20,6589(12), с=22,5198(13), α=63,5610(10), β=76,4800(10), γ=81,3480(10)
Объем элементарной ячейки: V=4808,14
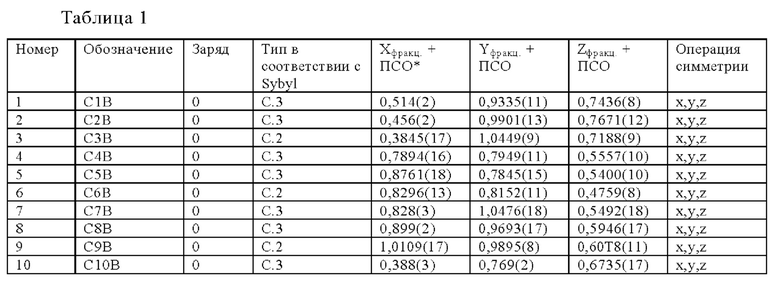
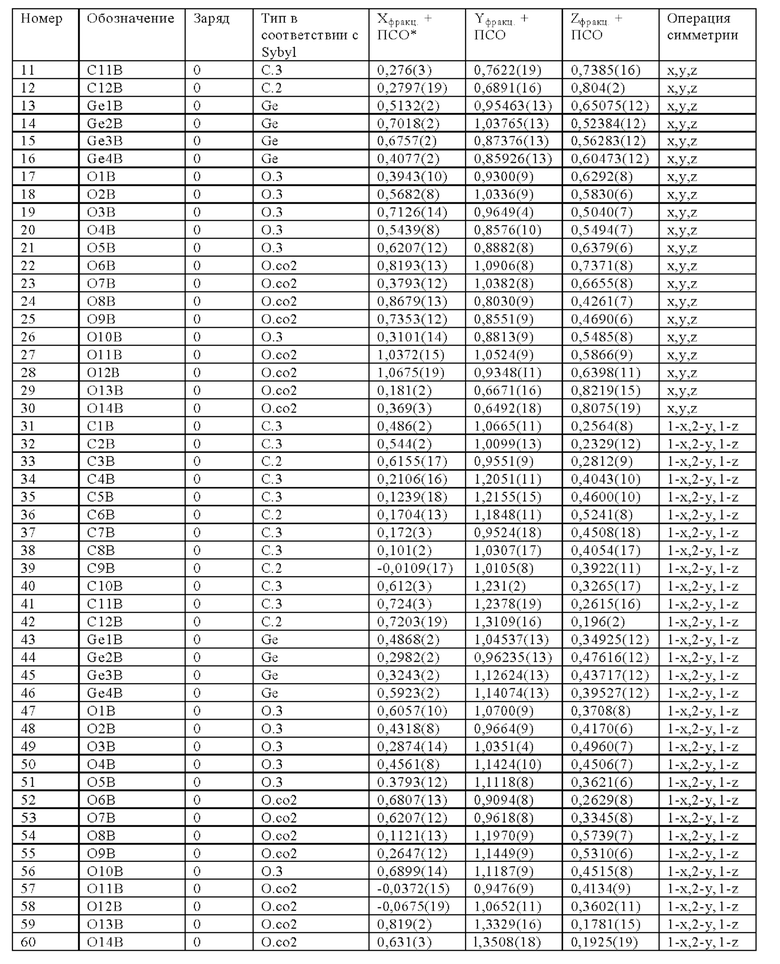
*ПСО - предполагаемое значение стандартного отклонения
Подтверждено, что кристаллы, полученные в разделе 1), представляли собой германийорганические соединения, обладающие структурой, в которой 8 молекул ТГГП дегидратированы и сконденсированы ((1,7,9,15-тетра(2'-натрий-карбоксиэтилгерманий)-3,5,11,13-тетра-[натрий-пропанато(2-)-С3',O']-германий-2,4,6,8,10,12,14,16,17,18,19,20-додекаоксапентацикло[8.11,5.17,11.19,13.13,15.]эйкозан), октамер ТГГП) (см. фиг. 1 и таблицу 1). Характерными особенностями октамера являются следующие: 4 из пропионовых цепей, содержащихся в 8 молекулах ТГГП, образующих октамер, обладают линейной структурой, тогда как оставшиеся 4 пропионовые цепи, обладают структурой лактона, и атомы германия, содержащиеся в структуре лактона, являются пятикоординированными.
3) Растворимость
К 100 мг октамера ТГГП, полученного в разделе 1), небольшими порциями многократно добавляли очищенную воду или метанол и перемешивали при комнатной температуре в течение 30 мин и определяли объем раствора, когда визуально наблюдали полное растворение октамера ТГГП. Из определенного объема рассчитывали растворимость октамера ТГГП (количество растворившегося вещества (г)/полная масса (г) ×100%). Кроме того, когда октамер ТГГП полностью растворялся, определяли значение рН раствора.
Обычные полимеры ТГГП, включая Ge-132, обладают растворимостью в воде, составляющей примерно 1%, и нерастворимы в органических растворителях, таких как метанол. В отличие от них, растворимость октамера ТГГП в воде составляла 58,8% и в метаноле она составляла 1,4% соответственно. Кроме того, значение рН водного раствора составляло примерно 7,5, которое соответствует практически нейтральной среде.
4) Скорость растворения
100 мг Ge-132 и 100 мг октамера ТГГП соответственно добавляли к 10 мл очищенной воды и смеси перемешивали при комнатной температуре при скорости, равной 300 об/мин, и затем определяли количество времени, необходимое для полного растворения, которое определяли путем визуального наблюдения.
Когда обычные полимеры ТГГП, включая Ge-132, растворяют в воде при комнатной температуре, для полного растворения кристаллов необходимо некоторое время. Определяли количество времени, необходимое для полного растворения во время получения 1% водного раствора Ge-132, и подтверждено, что необходимо 30 мин или более. В отличие от этого октамер ТГГП полностью растворялся в течение примерно 10 с.
5) Определение распределения частиц по размерам с помощью дифракции лазерного излучения
Распределение частиц октамера ТГГП по размерам определяли с помощью лазерного дифракционного анализатора размера частиц (HRA, Microtrac) с использованием этанола в качестве диспергирующего средства через 1 мин после ультразвукового диспергирования. Условия проведения исследования являлись следующими.
Диапазон измерений: от 0,06 до 1400 мкм
Использовавшийся источник света: углекислотный лазер ×3
Детектор: детектор светорассеяния
Подтверждено, что октамер ТГГП обладает чрезвычайно мелкими частицами, при этом Dp10=3,4 мкм, Dp50 (медианный диаметр) =8,0 мкм и Dp90=16,9 мкм (см. фиг. 2).
6) Анализ с помощью инфракрасной спектрофотометрии
Смесь бромида калия (KBr) и октамера ТГГП, и смесь KBr и Ge-132, каждую в форме пеллеты, исследовали с помощью инфракрасной спектрофотометрии с использованием инфракрасного спектрофотометра (FTIR-8100М, Shimadzu Corporation). Условия проведения исследования являлись следующими.
Методика исследования: методика с использованием содержащих KBr пеллет
Диапазон измерений: от 400 до 4600 см-1
Разрешение: 4 см-1
Скорость вращения зеркала: 2,8 мм/с
Количество сканирований: 40
Подтверждено, что полоса поглощения, возникающая вследствие наличия группы С=O, наблюдающаяся при 1700 см-1 в случае Ge-132, в случае октамера ТГГП смещается в сторону более низкого волнового числа, равного от 1650 до 1550 см-1 что полоса поглощения, возникающая вследствие наличия карбоксигруппы, наблюдающаяся при 3000 см-1 в случае Ge-132, в случае октамера ТГГП исчезает, и что спектр Ge-132 и спектр октамера ТГГП отличаются друг от друга в характеристической области при 1500 см-1 или менее (см. фиг. 3).
7) Масс-спектроскопия
Для проведения массового анализа метанольный раствор октамера ТГГП исследовали с помощью масс-спектрометрия (ВПР-МС, QToF Ultima, Waters). Условия проведения исследования являлись следующими. Режим ионизации: ИЭР+(ионизация электрораспылением в режиме положительных ионов) Подвижная фаза: метанол
На фиг. 4 представлен полученный с помощью ВПР-МС масс-спектр октамера ТГГП и теоретический спектр, рассчитанный на основании количества природного изотопа. Подтверждено, что определенные значения в основном совпадали с теоретическими значениями.
8) Исследование с помощью 1Н ЯМР
Спектры 1Н ЯМР растворов октамера ТГГП в тяжелой воде и тяжелом метаноле соответственно снимали с использованием спектрометра ядерного магнитного резонанса (Gemini 2000, Agilent Technologies, Inc.). Для сопоставления получали раствор Ge-132 в тяжелой воде и затем его нейтрализовывали раствором тяжелого гидроксида натрия и проводили исследование таким же образом. Условия проведения исследования являлись следующими: 25°С, 16 сканирований, 300 МГц, и сигнал остаточных протонов HOD находился при 4,80 част./млн.
На фиг. 5 и фиг. 6 представлены полученные с помощью 1Н ЯМР спектры образцов. На спектре 1Н ЯМР, полученном для раствора октамера ТГГП в тяжелой воде, наблюдались триплетные пики при 1,56 част./млн и 2,47 част./млн соответственно. Этот результат находится в соответствии с результатами, полученными в случае спектра 1Н ЯМР, полученного для водного раствора Ge-132, это указывает на то, что в обоих случаях происходило образование ТГГП (см. фиг. 5). В отличие от этого, на спектре 1Н ЯМР, полученном для раствора октамера ТГГП в тяжелом метаноле, триплетные пики наблюдались при 1,40 част./млн, 1,51 част./млн, 2,30 част./млн и 2,38 част./млн соответственно (фиг.6). Полагали, что в случае использования тяжелой воды октамер ТГГП гидролизовался с образованием ТГГП, и пики, соответствующие двум группам СН2, содержащимся в пропионовой цепи, наблюдались в двух положениях, тогда как в случае в случае использования тяжелого метанола октамер ТГГП не гидролизовался и включенные в октамер две группы СН2, содержащиеся в линейной пропионовой цепи, и две группы СН2, содержащиеся в циклической пропионовой цепи, отличались и наблюдались пики всего в 4 положениях.
Пример 2. Подтверждение взаимодействия с аденозином
Снимали спектр 1Н ЯМР смешанного раствора, полученного путем растворения октамера ТГГП и аденозина (соотношение смешивания =1:1, рН=от 7,0 до 7,5, 100 мМ) в тяжелой воде, при следующих условиях проведения исследования: 30°С, количество сканирований=16, 300 МГц. Сигнал остаточных протонов HOD находился при 4,80 част./млн. Для сопоставления таким же образом проводили исследование смешанного раствора, содержащего Ge-132 и аденозина.
На фиг. 7 представлены полученные с помощью 1Н ЯМР спектры образцов. На спектре 1Н ЯМР смешанного раствора, содержащего октамер ТГГП и аденозин, в дополнение к триплетным пикам, соответствующим ТГГП, наблюдающимся при 1,56 част./млн (вследствие наличия Gе-СН2) и 2,47 част./млн (вследствие наличия СН2-СОО-), наблюдались новые пики при 1,76 част./млн и 2,57 част./млн. Поскольку спектр самого аденозина не находится вблизи области указанных выше химических сдвигов, новые наблюдающиеся пики, вероятно, соответствуют комплексу аденозина и ТГГП. Этот результат находится в соответствии с результатами, полученными в случае спектра 1Н ЯМР, полученного при использовании Ge-132 вместо октамера ТГГП, это указывает на то, что из октамера ТГГП образуется ТГГП и он обладает такой же реакционной способностью при взаимодействии с аденозином, как и Ge-132.
Пример 3. Подтверждение взаимодействия с H2S
Снимали спектр 1Н ЯМР смешанного раствора, полученного путем растворения октамера ТГГП и NaHS (натриевая соль H2S) (соотношение смешивания =1:1, рН= от 7,0 до 7,5, 20 мМ) в 10 мМ фосфатном буфере (рН 7,4), полученном с использованием тяжелой воды, при следующих условиях проведения исследования: 25°С, количество сканирований =16, 300 МГц. Сигнал остаточных протонов HOD находился при 4,80 част./млн. Для сопоставления таким же образом проводили исследование смешанного раствора, содержащего Ge-132 и NaHS.
На фиг. 8 представлены полученные с помощью 1Н ЯМР спектры образцов. На спектре 1Н ЯМР смешанного раствора, содержащего октамер ТГГП и NaHS, в дополнение к триплетным пикам, соответствующим ТГГП, наблюдающимся при 1,56 част./млн (вследствие наличия Ge-CH2) и 2,47 част./млн (вследствие наличия СН2-СОО), наблюдались новые пики при 1,40 част./млн и 2,39 част./млн. Поскольку спектр самого NaHS не находится вблизи области указанных выше химических сдвигов, новые наблюдающиеся пики, вероятно, соответствуют комплексу ТГГП и NaHS. Этот результат находится в соответствии с результатами, полученными в случае спектра 1Н ЯМР, полученного при использовании Ge-132 вместо октамера ТГГП, это указывает на то, что из октамера ТГГП образуется ТГГП и он обладает такой же реакционной способностью при взаимодействии с NaHS, как и Ge-132.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ГЕРМАНИЯ С АМИНОКИСЛОТАМИ И ЛИПОЕВОЙ КИСЛОТОЙ | 2015 |
|
RU2626954C2 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ГЕРМАНИЯ С ПЕПТИДАМИ И ПЕПТИДАМИ И ГИДРОКСИКАРБОНОВЫМИ КИСЛОТАМИ | 2016 |
|
RU2636788C2 |
| МЕТАЛЛООРГАНИЧЕСКИЕ КОМПЛЕКСЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, КАТАЛИЗАТОР ГИДРОФОРМИЛИРОВАНИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЙ ПРОДУКТ | 1999 |
|
RU2188202C1 |
| ПРОИЗВОДНЫЕ ТИАЗОЛИДИН-2,4-ДИОНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2103265C1 |
| ЧЕТЫРЕХКООРДИНАЦИОННЫЕ КОМПЛЕКСЫ ДВУХВАЛЕНТНОЙ ПЛАТИНЫ | 1992 |
|
RU2039064C1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛО [1,5-А] ПИРИДИНА, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2069662C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИС(ТРИФТОРМЕТИЛ)ИМИДО-СОЛЕЙ | 2002 |
|
RU2278109C2 |
| ФЛЮОРЕСЦЕНТНЫЙ КОНТРАСТИРУЮЩИЙ АГЕНТ БЛИЖНЕЙ ИНФРАКРАСНОЙ ОБЛАСТИ СПЕКТРА И СПОСОБ ФЛУОРЕСЦЕНТНОЙ ТОМОГРАФИИ | 2003 |
|
RU2350355C9 |
| НОВЫЕ ПРОИЗВОДНЫЕ КАТЕХОЛА И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 1997 |
|
RU2180898C2 |
| СПОСОБ ВЫДЕЛЕНИЯ И РЕГЕНЕРАЦИИ ГЕРМАНИЙОРГАНИЧЕСКОГО СОЕДИНЕНИЯ | 1995 |
|
RU2136689C1 |

Изобретение относится к новому германийорганическому соединению общей формулы (I), в которой все R1, R2 и R3 обозначают водород, X обозначает катион щелочного металла. Предложенное соединение является хорошо растворимым в воде и отсутствует необходимость его нейтрализации при введении в живой организм. Соединение способно взаимодействовать с соединением, обладающим структурой цис-диола, или с соединением, обладающим структурой тиола, и способно ослаблять боль и механическую аллодинию, вызванную веществом, которое может взаимодействовать с растворимым в воде германийорганическим соединением, а также способно уменьшить летучесть вещества при растворении в воде вместе с веществом. 1 з.п. ф-лы, 8 ил., 1 табл., 3 пр.
1. Соединение формулы (I),
Химическая формула I
в которой все R1, R2 и R3 обозначают водород и X обозначает катион щелочного металла.
2. Соединение по п. 1, в котором X обозначает катион натрия.
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| АМБРОСОВ И.В | |||
| и др., Использование органических соединений германия в медицине, Разработка и регистрация лекарственных средств, 2015, N 11, с | |||
| Аппарат для электрической передачи изображений без проводов | 1920 |
|
SU144A1 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ГЕРМАНИЯ С АМИНОКИСЛОТАМИ И КАРБОНОВЫМИ КИСЛОТАМИ | 2012 |
|
RU2476436C1 |
Авторы
Даты
2023-01-17—Публикация
2020-10-26—Подача