Изобретение относится к области медицины, конкретно к фармакологии, и может быть использовано в качестве ранозаживляющего средства.
Поиск и разработка новых средств, стимулирующих процессы регенерации, является важной задачей фармакологии. Раны, в том числе хронические, являющиеся последствием сахарного диабета, ожогов, заболеваний вен, синдрома длительного сдавления представляют большую практическую и научную проблему. Длительно персистируя, раневые дефекты формируют стойкий болевой синдром, депрессивные состояния, являются источником инфекции [1]. Модели кожных ран наиболее адекватны для использования в экспериментальных исследованиях, поскольку только в этих тканях наиболее наглядно прослеживается динамика и механизм регенераторных процессов, что позволяет эффективно оценить влияние исследуемых средств на них [2]. Естественный процесс заживления включает три этапа: I этап - воспаление; II этап - пролиферация, которая характеризуется повышением митотического индекса и активацией репарации; III этап - эпителизация [3]. Интенсивность репаративной регенерации зависит от большого количества факторов: состояния иммунной системы, микроциркуляторного русла, функциональных возможностей клеток стромы кожи [4].
Известно большое количество ранозаживляющих лекарственных средств для наружного применения, выполненных в виде различных лекарственных форм - мазей, эмульсий, аппликаций, гелей. Комплексным воздействием на раневую поверхность обладают многокомпонентные мази на осмотически активной основе - "Левомеколь", "Левосин" [5]. Хорошо известны и продолжают применяться в клинической практике растительные средства - облепиховое масло, сок каланхоэ, сок алоэ. Наиболее близким по природе происхождения является сок алоэ (Succus aloes), ускоряющий процессы регенерации. Сок алоэ назначают при лечении гнойных ран, ожогов, воспалительных заболеваний кожи, язвенной болезни желудка и двенадцатиперстной кишки [5].
Задачей предлагаемого изобретения является расширение арсенала отечественных средств на основе природного растительного сырья, обладающих ранозаживляющей активностью.
Для получения предлагаемого средства, индивидуального соединения С-дигликозид апигенина - шафтозида, выделенного из надземной части Lychnis chalcedonica, ключевым этапом было использование многократной экстракции концентрированного этанольного экстракта н-бутанолом с последующим разделением с помощью колоночной адсорбционной хроматографии и препаративной высокоэффективной жидкостной хроматографии.
Поставленная задача решается применением в качестве ранозаживляющего средства, индивидуального соединения ряда С-дигликозид апигенина - апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид (шафтозид), выделенный из надземной части Lychnis chalcedonica.
Впервые показано, что средство, индивидуальное соединение - апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид (шафтозид), выделенный из Lychnis chalcedonica, оказывает ранозаживляющее действие.
В проанализированной патентной и научно-медицинской литературе сведений о ранозаживляющем действии апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид - шафтозид, не обнаружено. Ранозаживляющее действие апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид (шафтозида) явным образом не вытекает из уровня техники в данной области и не является очевидным для специалиста. Экспериментально установлено новое свойство шафтозида, а также возможность использования шафтозида в качестве средства, обладающего ранозаживляющей активностью в практическом здравоохранении.
Таким образом, предлагаемое изобретение соответствует критериям патентоспособности "новизна", "изобретательский уровень", "промышленная применимость".
В качестве препарата сравнения выбран сок алоэ (ЗАО «ВИФИТЕХ», Россия), который использовали при наружном (местном) применении. Известно, что алоэ древовидное - многолетнее вечнозеленое растение, произрастающее в Южной Африке, в России разводится только в культуре при выращивании в оранжереях и теплицах, что является недостатком данного препарата.
У лихниса халцедонского (Lychnis chalcedonica L, сем. Caryophyllaceae) широкий ареал распространения: произрастает в Европейской части России, в районах Восточной Сибири и Средней Азии. [6]. Кроме того, индивидуальное соединение шафтозид содержится и в других растениях: фиалке маньчжурской Viola mandshurica и фиалке эдоской Viola yedoensis [7], в смолевках (Silene aprica L., S. italica, S. nutans S. repens, S. samojedorum, S. scafta) [8], S. sibirica L. [9], крапиве коноплевой Urtica cannabina [10] и других растениях. Таким образом, ресурсная база для выделения индивидуального вещества шафтозида очень большая, в сравнении с препаратом сравнения - соком алоэ древовидного.
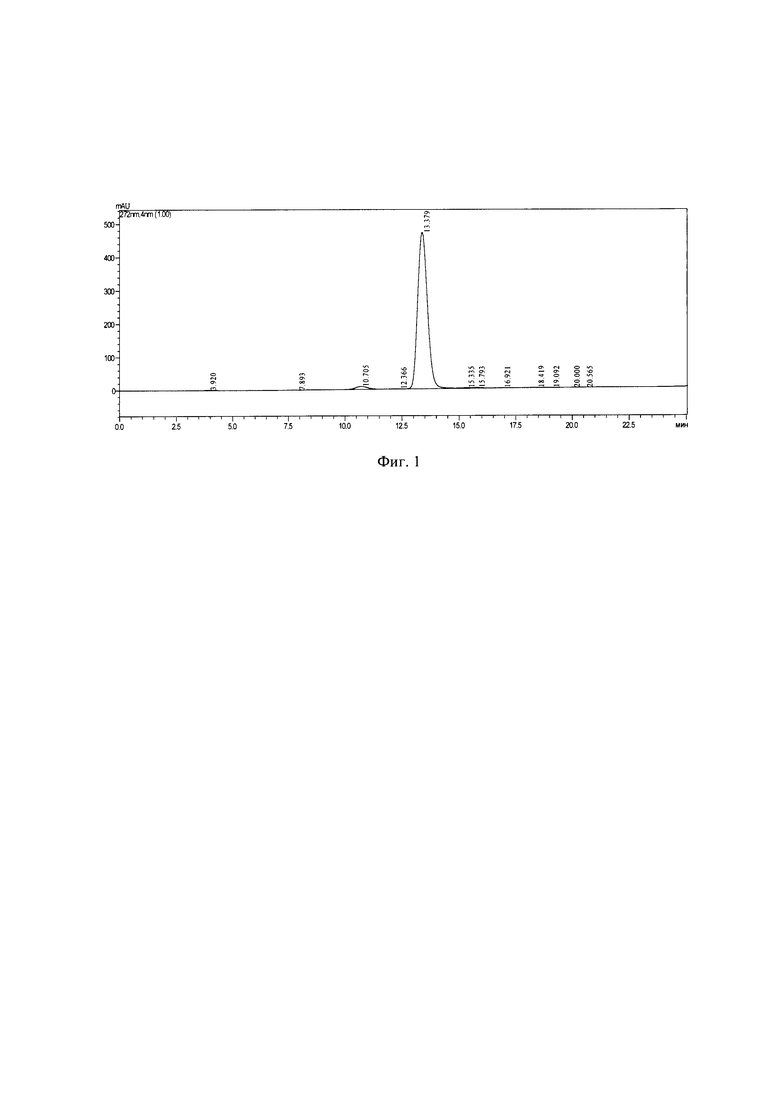
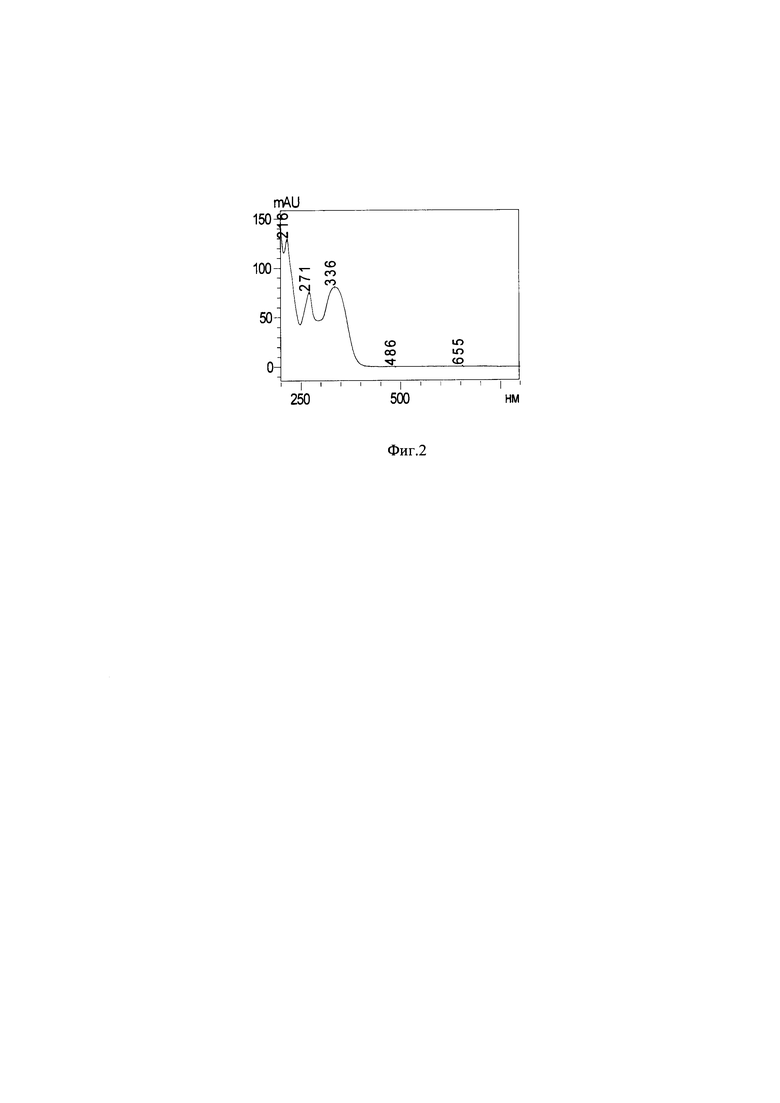
Изобретение будет понятно из следующего описания и приложенных к нему фигур: на фиг. 1 - ВЭЖХ чистого шафтозида, выделенного из Lychnis chalcedonica. на фиг. 2 - УФ-спектр выделенного флавоноида - шафтозида.
Средство, обладающее ранозаживляющим действием, представляет собой индивидуальное соединение - апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид - флавоноид шафтозид (С26Н28О14), выделенный из надземной части Lychnis chalcedonica.
Предлагаемое нами средство получают следующим образом.
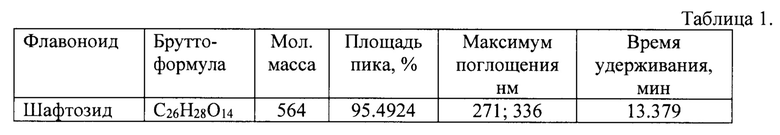
Экстракцию воздушно-сухого сырья (200 г) растения лихниса халцедонского Lychnis chalcedonica проводили 70% этиловым спиртом. Затем для удаления экстрагента объединенный экстракт концентрировали при температуре 50°С с помощью вакуумного ротационного испарителя IKA НВ 10 digital (Германия). Концентрированный экстракт разбавляли водой до соотношения 1:3 (v:v) и фильтровали. Затем фильтрат очищали от липофильных веществ при помощи н-гексана. Извлечение суммы биологически активных веществ, содержащей экдистероиды, флавоноиды и др. из очищенного фильтрата осуществляют многократной экстракцией н-бутанолом. При этом из водной фракции выпадал осадок желто-коричневого цвета, который отделяли. Контроль содержания БАВ во фракциях осуществляют методом ТСХ. Выход бутанольной фракции составлял 5,8%. В последующем комплекс выделенных соединений подвергали очистке селективной экстракцией системами растворителей этилацетат: этанол в соотношении 5:1 и 3:1. Полученный порошок имел желтоватую окраску. Далее фильтрат подвергали хроматографическому разделению на колонке, заполненной силикагелем марки КСКГ 0,1-0,16 мм (Хроманалит), с использованием подвижных фаз хлороформ: этиловый спирт в соотношении 1:9-1:1. Перекристаллизацию флавоноида проводили 96% этанолом. ВЭЖХ анализ (фиг. 1) свидетельствует о том, что выделенное соединение представляет собой индивидуальный флавоноид с временем удерживания 13.379 мин. Выделенный флавоноид имеет два максимума поглощения, соответствующие двум ароматическим кольцам А и В (фиг. 2, табл. 1). Индивидуальное соединение было идентифицировано методами ВЭЖХ, масс-спектрометрии, ЯМР 1Н и 13С-спектроскопии [11].
Характеристика выделенного индивидуального соединения - апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид - флавоноид шафтозид (С26Н28О14), представлена в таблице 1. Чистота выделенного индивидуального соединения шафтозида составила 95,49%.
Ранозаживляюще действие индивидуального соединения - апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид (шафтозида) Lychnis chalcedonica было найдено в результате экспериментальных исследований. Эксперименты выполнены на аутбредных мышах линии CDI (самцы) (I категории согласно сертификату) массой 20-27 г. Животные получены из отдела экспериментальных биологических моделей НИИФиРМ им. Е.Д. Гольдберга. Работу с экспериментальными животными осуществляли в соответствии с правилами, принятыми Европейской Конвенцией по защите позвоночных животных, используемых для экспериментальных и научных целей (г.Страсбург, 1986).
Для исследования использовали модель плоскостной кожной раны [Фролова Н.Ю. и др., 2009]. На депилированном участке спины у мышей под эфирным наркозом вырезали лоскут кожи размером 10x10 мм. Для моделирования более длительного заживления струп с раны регулярно удаляли (через каждые сутки). Критериями развития патологического процесса служили следующие показатели: средний диаметр раны, число животных (%) с зажившими ранами, ускорение сроков заживления (УСЗ = время полного заживления ран в контроле - время полного заживления ран в опыте / время полного заживления ран в контроле × 100%). На основе этих данных рассчитывалась скорость уменьшения диаметра раны в мм/сут и в %. В конце полного заживления ран все животные подвергались эвтаназии, иссеченный раневой дефект морфометрически исследовался: оценивалась полноценность эпителизации, толщина кожного дефекта, наличия волосяных фолликул [12].
Животные в экспериментах были распределены на следующие группы: контрольная, сравнения, опытная. Группе контроля на рану наносился растворитель (дистиллированная вода) по 100 мкл на рану. В группе сравнения в качестве препаратов сравнения использовали сок алоэ по 100 мкл на рану - наружно (местно).
В опытной группе животные получали предлагаемое средство - индивидуальное соединение шафтозид, разведенный дистиллированной водой до концентрации 0,1 мкг/мл; 1,5 мкг/мл; 3,0 мкг/мл. Исследуемое средство наносили наружно (местно) в виде водного раствора с помощью пипетки по 100 мкл на рану в концентрации либо 0,1 мкг/мл, либо 1,5 мкг/мл, либо 3,0 мкг/мл начиная с первого дня после индуцирования раны, 1 раз в сутки в течение всего периода заживления раневого повреждения. Аналогично получали растворитель группа контроля и сок алоэ - группа сравнения. Оценку эффекта исследуемого средства осуществляли, сравнивая соответствующие показатели животных опытной группы с контрольной и группой, получавшей препарат сравнения - сока алоэ.
Статистическую обработку полученных результатов проводили методами вариационной статистики с использованием программного обеспечения IBM. Вычисляли среднее арифметическое 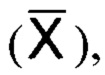 ошибку среднего арифметического (т), значение вероятности (Р). Различие двух сравниваемых величин считали достоверным, в случае если вероятность их тождества была меньше 5% (р<0,05). Используя выборочные коэффициенты асимметрии и эксцесса, оценивали степень приближения закона распределения исследуемого признака к нормальному. В случаях нормального распределения признаков для статистической оценки применяли параметрический t-критерий Стьюдента. При больших отклонениях распределений признака от нормального вида для независимых выборок использовали непараметрический критерий U-критерий Уилкоксона-Манна-Уитни. Для сравнения результатов экспериментов, где показатели выражались в долях, достоверность определяли с помощью метода углового преобразования Фишера. Значимость различий считали достоверной при Р<0,05 [13]. Использовалась программа «Statistica 6.0».
ошибку среднего арифметического (т), значение вероятности (Р). Различие двух сравниваемых величин считали достоверным, в случае если вероятность их тождества была меньше 5% (р<0,05). Используя выборочные коэффициенты асимметрии и эксцесса, оценивали степень приближения закона распределения исследуемого признака к нормальному. В случаях нормального распределения признаков для статистической оценки применяли параметрический t-критерий Стьюдента. При больших отклонениях распределений признака от нормального вида для независимых выборок использовали непараметрический критерий U-критерий Уилкоксона-Манна-Уитни. Для сравнения результатов экспериментов, где показатели выражались в долях, достоверность определяли с помощью метода углового преобразования Фишера. Значимость различий считали достоверной при Р<0,05 [13]. Использовалась программа «Statistica 6.0».
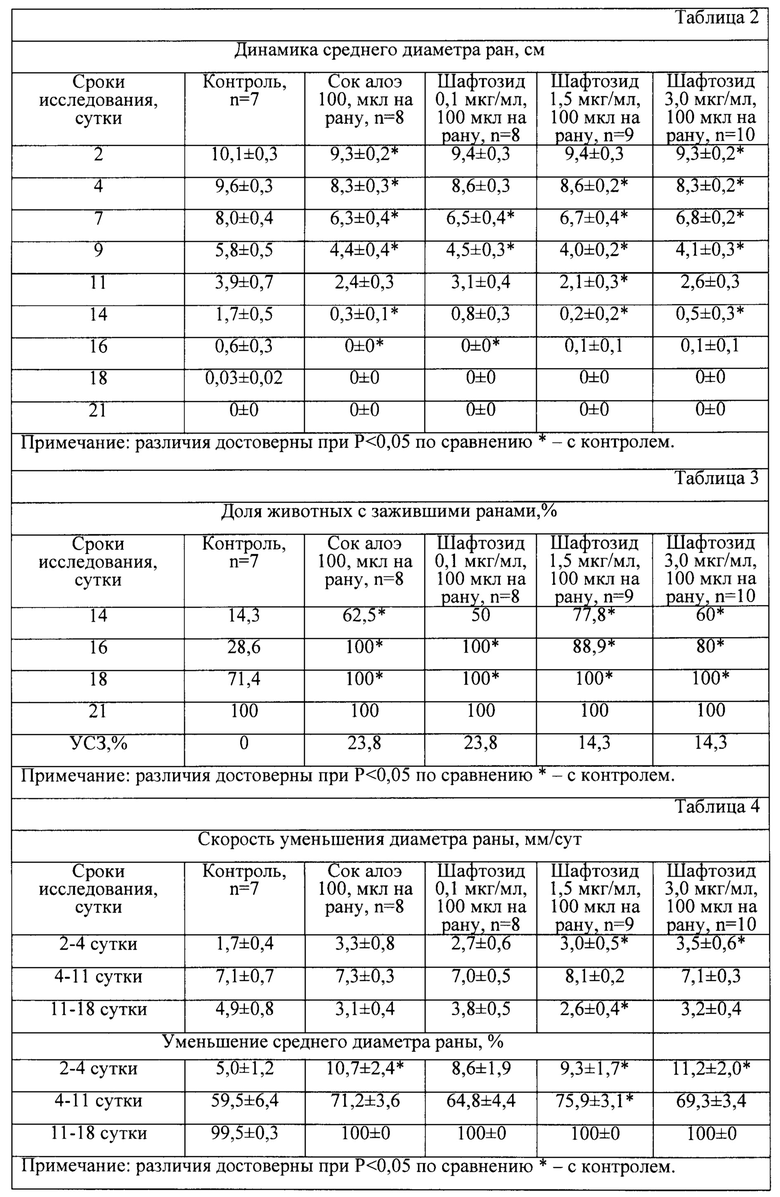
Пример 1. В ходе выполнения эксперимента предлагаемое средство, содержащее индивидуальное соединение шафтозид из Lychnis chalcedonica, наносили наружно (местно) в виде водного раствора. Лечение аутбредных мышей-самцов CDI начинали в первые часы после нанесения ран и продолжали до полной эпителизации. В ходе эксперимента наблюдалась закономерная динамика раневого процесса. Согласно полученным данным у мышей в группе контроля полное заживление ран наблюдали к 21 дню (таблица 2, 3).
В условиях курсового использования предлагаемого средства, содержащего индивидуальное соединие - шафтозид из лихниса халцедонского Lychnis chalcedonica (ФЛХ) раны полностью затянулись на 16 сутки в группах мышей, которым наносили 100 мкл раствора шафтозида наружно в концентрации 0,1 мкг/мл, а также в группе, где мыши получали препарат прототип сок алоэ в том же объеме. Под действием этих средств наблюдалась благоприятная динамика, раны зажили на 5 дней раньше, чем в контроле. Ускорение сроков заживления (УСЗ) ран составила 23,8% (таблица 3). Предлагаемое средство в концентрациях 1,5 мкл/мл и 3,0 мкл/мл способствовало полному заживлению ран на 18 сутки.
С 4 суток исследования в группе животных, которым наносили раствор шафтозида, зафиксировали достоверные различия размеров раны в сравнении с контрольной группой. Стойкое снижение диаметра ран во всех опытных группах и группе прототипа появилось на 7-е сутки после нанесения повреждения: в 1,2-1,3 раза средний диаметр ран был меньше контрольных значений; на 9-е сутки - в 1,3-1,5 раза. Это свидетельствует о наличии ранозаживляющего действия у шафтозида, сопоставимое по эффективности с препаратом прототипом соком алоэ (таблица 2). Более того, шафтозид в концентрации 1,5 и 3,0 мкг/мл существенно увеличивал скорость заживления ран на начальном периоде (2-4 сутки, таблица 4). После завершения видимой эпителизации раны процесс дифференцировки эпидермиса продолжается еще длительное время.
Анализ морфологических процессов, протекающих в области раневого дефекта кожи мышей на 21 сутки показал, что в контрольной группе имело место формирование неполноценного регенерата, у большинства животных наблюдали непрерывный, но тонкий слой эпителия (таблица 5).

Под влиянием предлагаемого средства шафтозида в концентрации 3,0 мкг/мл у 50% мышей была полноценная эпителизация, только у 10% животных дефект был покрыт тонким эпителием, что достоверно было меньше, чем в группе контроля и группе, получавших сок алоэ (прототип). Шафтозид в концентрациях 0,1 мкг/мл и 1,5 мкг/мл в сравнении с контрольными показателями также достоверно улучшал качество регенерата, но в сравнении с препаратом сравнения, соком алоэ - наблюдалась только тенденция к улучшению структуры кожного регенерата.
Таким образом, результаты проведенного исследования на модели плоскостной кожной раны позволили установить, что предлагаемое средство, индивидуальное соединение шафтозид из Lychnis chalcedonica, в концентрациях 0,1 мкг/мл, 1,5 мкг/мл, 3,0 мкг/мл при наружном (местном) применении способствует существенному сокращению размеров плоскостных кожных ран, сопоставимое по активности с действием сока алоэ (препарат сравнения). Ранозаживляющий эффект более выражен на 1, 2 и 3 неделе процесса заживления (I и II этапы), т.е. на этапе воспаления, пролиферации и активации репарации, если применить наиболее объективную классификацию, отражающую самые существенные признаки раневого процесса.
Предлагаемое в качестве изобретения средство, содержащее индивидуальное соединение - апигенин -6-C-β-D глюкопиранозил 8-C-α-L арабинопиранозид (шафтозид) из Lychnis chalcedonica, оказывает ранозаживляющее действие при наружном (местном) применении.
Источники информации:
1. Блинова, Е.В. Регенерация инфицированной кожной раны на фоне топического воздействия солями п-ацетил-6-аминогексановой кислоты / Е.В. Блинова, М.А. Миронов, Д.С. Блинов // Журнал научных статей здоровье и образование в XXI веке. - 2018. - Т. 20, №7. - С. 80-83.
2. Фролова, Н.Ю. Методические подходы к экспериментальному изучению дерматотропных средств / Н.Ю. Фролова, Т.И. Мельникова, А.В. Бурякина и др. // Экспериментальная и клиническая фармакология. - 2009. - Т. 72, №5. - С. 56-60.
3. Фенчин, К.М. Заживление ран. / К.М. Фенчин. - Киев,  1979. - С. 7-11.
1979. - С. 7-11.
4. Носенко, М.А. Противовоспалительные цитокины и заживление кожных ран у мышей / М.А. Носенко, С.Г. Амбарян, М.С. Друцкая // Молекулярная биология. - 2019. - Т. 53, №5. -С. 741-754.
5. Машковский, М.Д. Лекарственные средства / М.Д. Машковский. - 16 изд. перераб., испр. и доп. - М.: Новая волна, 2012. - С. 812; С. 711.
6. Растительные ресурсы СССР: Цветковые растения, их химический состав, использование. Семейства Magnoliaceae - Limoniaceae. - Л.: Наука, 1985. - С. 200-201.
7. Петрова, Н.В. компонентный состав и биологическая активность видов рода Viola (Violaceae) флоры России / Н.В. Петрова, Н.А. Медведева // Химия растительного сырья. - 2020. - №2. - С. 19-45.
8. Зибарева, Л.Н. Экдистероиды и фенольные соединения некоторых видов Caryophyllaceae / Л.Н. Зибарева, Е.С. Филоненко, Е.А. Кастерова и др. // Растительные ресурсы. - 2020. - Т. 56, №2. - С. 165-172.
9. Оленников, Д.Н. Экдистероиды и гликозилфлавоны Silene Sibirica (Caryophyllaceae) / Д.Н. Оленников, Н.И. Кащенко // Химия растительного сырья. - 2020. - №4. - С. 109-119.
10. Федосеева, Л.М. Определение показателей качества капсулированной лекарственной формы с экстрактом травы крапивы коноплевой сухим / Л.М. Федосеева, В.О. Кирьякова // Химия растительного сырья. - 2017. - №2. - С. 149-153.
11. Зибарева, Л.Н. Растения родов Silene L. (Caryophyllaceaeae): состав химических компонентов и биологическая активность / Л.Н. Зибарева, Е.Н. Амосова, С.Г. Крылова, и др. - Томск: Издательство Томского государственного университета, 2021. С. 58-60.
12. Ефимов, Е.А. Посттравматическая регенерация кожи (Экспериментальное исследование). - Москва, «Медицина», 1075. - С. 127-129.
13. Лакин, Г.Ф. Биометрия / Г.Ф. Лакин - М.: Высшая школа, 1980. - 293 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, обладающее антигипоксическим действием | 2023 |
|
RU2813662C1 |
| Средство, обладающее ноотропным действием | 2024 |
|
RU2834002C1 |
| Средство, обладающее гастропротекторной активностью | 2016 |
|
RU2629090C1 |
| Средство, обладающее противовоспалительным и анальгетическим действием | 2016 |
|
RU2629607C1 |
| СРЕДСТВО, УСКОРЯЮЩЕЕ ПРОЦЕССЫ РЕГЕНЕРАЦИИ | 2008 |
|
RU2372932C1 |
| СПОСОБ УВЕЛИЧЕНИЯ СТЕПЕНИ ИЗВЛЕЧЕНИЯ ЭКДИСТЕРОИДОВ И ФЛАВОНОИДОВ ИЗ РАСТИТЕЛЬНЫХ ОБЪЕКТОВ | 2014 |
|
RU2563616C1 |
| КАЛИЕВАЯ СОЛЬ КАУЛОЗИДА C, СТИМУЛИРУЮЩАЯ РЕПАРАТИВНУЮ РЕГЕНЕРАЦИЮ КОЖИ | 1994 |
|
RU2078086C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОГРИБКОВОГО СРЕДСТВА ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2010 |
|
RU2435602C1 |
| ПРИМЕНЕНИЕ ГЕДЕРАГЕНИН 3-О-АЛЬФА-L-РАМНОПИРАНОЗИЛ (1→2)-[БЕТА-D-ГЛЮКОПИРАНОЗИЛ (1→4)]-АЛЬФА-L-АРАБИНОПИРАНОЗИДА ИЛИ СОДЕРЖАЩЕГО ЕГО ЭКСТРАКТА ИЗ PULSATILLAE RADIX В КАЧЕСТВЕ ТЕРАПЕВТИЧЕСКОГО СРЕДСТВА ДЛЯ СОЛИДНЫХ ОПУХОЛЕЙ | 2003 |
|
RU2325178C2 |
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ РАН У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ | 2010 |
|
RU2456016C2 |
Изобретение относится к области медицины, а именно к фармакологии и терапии, и может быть использовано в качестве ранозаживляющего средства. Применяют апигенин 6-C-β-D-глюкопиранозил-8-C-α-L-арабинопиранозид, выделенный из надземной части Lychnis chalcedonica, в качестве ранозаживляющего средства. Использование изобретения обеспечивает средство на основе природного растительного сырья, обладающее ранозаживляющей активностью. 2 ил., 5 табл., 1 пр.
Применение индивидуального соединения - апигенин 6-C-β-D-глюкопиранозил-8-C-α-L-арабинопиранозид, выделенного из надземной части Lychnis chalcedonica, в качестве ранозаживляющего средства.
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ СМЕСЬ ЭКСТРАКТОВ РАСТЕНИЙ ИЛИ СМЕСЬ МОЛЕКУЛ, СОДЕРЖАЩИХСЯ В УКАЗАННЫХ РАСТЕНИЯХ, И ПРИМЕНЕНИЕ ДЛЯ КОНТРОЛИРОВАНИЯ МЕТАБОЛИЗМА УГЛЕВОДОВ И/ИЛИ ЛИПИДОВ | 2015 |
|
RU2712625C2 |
| CN 113185501 A, 30.07.2021 | |||
| KR 102001043 B1, 17.07.2019 | |||
| US 6471973 B2, 29.10.2002. | |||
Авторы
Даты
2023-01-19—Публикация
2022-07-18—Подача