[Область техники]
[0001]
Настоящее изобретение относится к способу получения соединения следующей формулы (3), которое представляет собой нитрозосоединение.
[0002]
[формула 1]
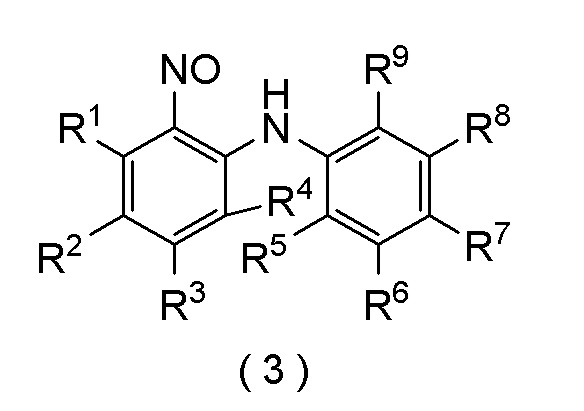
В которой R1, R2, R3, R4, R5, R6, R7, R8, и R9 представляют собой, как определено ниже.
[0003]
Настоящее изобретение также относится к способу получения соединения следующей формулы (5), которое представляет собой хиноксалиновое соединение.
[0004]
[формула 2]
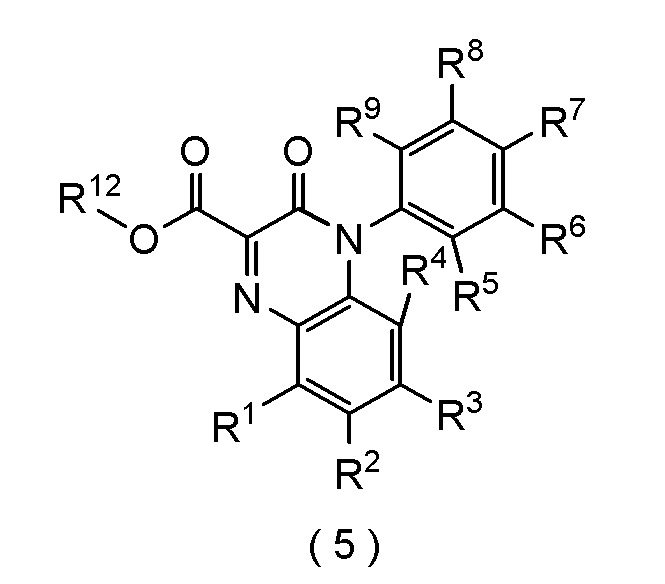
В которой R1, R2, R3, R4, R5, R6, R7, R8, R9 и R12 представляют собой, как определено ниже.
[Уровень техники]
[0005]
Нитрозосоединение формулы (3) (в настоящем изобретении далее называют просто соединение формулы (3)) и хиноксалиновое соединение формулы (5) (в настоящем изобретении далее называют просто соединение формулы (5)) являются пригодными в качестве промежуточных продуктов для производства физиологически активных органических соединений, таких как агрохимикаты, лекарственные средства и подобные. В WO2009/016841 (патентная литература 1) описаны полезные гербициды. Среди них соединение № II-62 и соединение № II-194 являются отличными гербицидами. В частности, соединение № II-194, то есть фенхинотрион, известно как гербицид, обладающий чрезвычайно превосходным эффектом прополки и высокой безопасностью для риса-сырца.
[0006]
Кроме того, WO2009/016841 (Патентная литература 1) также описывает, что соединение формулы (5) является пригодным в качестве промежуточного соединения для производства гербицидов (смотри в частности, например, пример 6).
[0007]
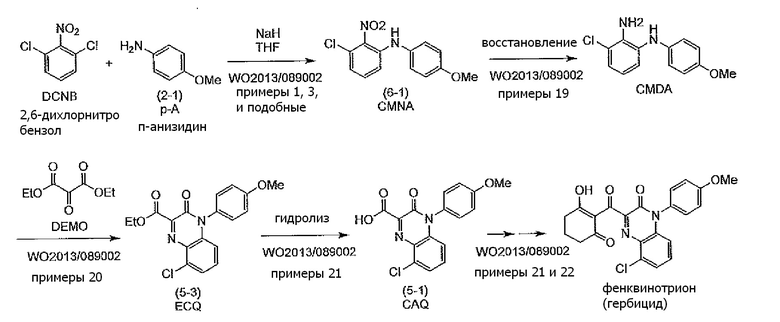
WO2013/089002 (патентная литература 2) описывает способ получения, как показано на схеме ниже (смотри примеры 1, 3, 19, 20-23 и подобные).
[0008]
[формула 3]
[0009]
Как видно из приведенной выше схемы, способ, описанный в WO2013/089002 (патентная литература 2), требует трех стадий для получения соединения формулы (5), в частности соединения формулы (5-3), из 2,6-дихлорнитробензола. Следовательно, желателен способ получения с меньшим числом стадий. Кроме того, 2,6-дихлорнитробензол и сложный диэфир кетомалоновой кислоты (например, DEMO на приведенной выше схеме) являются менее доступными, и желательно более легкодоступное сырье.
[0010]
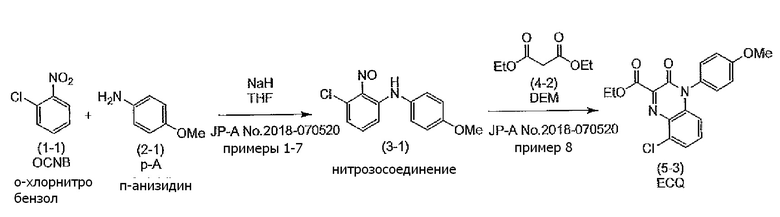
С другой стороны, опубликованный патент Японии № 2018-70520 (патентная литература 3) описывает, что 3-хлор-N-(4-метоксифенил) -2-нитрозоанилин (3-1) можно получить взаимодействием 2-хлорнитробензола (1-1) с п-анизидином (2-1). Кроме того, в данной литературе сообщается, что соединение формулы (5-3) можно получить из 3-хлор-N-(4-метоксифенил)-2-нитрозоанилина (3-1). Данный способ показан на схеме ниже.
[0011]
[формула 4]
[0012]
По сравнению со способом WO2013/089002 (патентная литература 2), соединение формулы (5-3) можно получить, применяя более легкодоступные исходные соединения в способе опубликованного патента Японии № 2018-70520 (патентная литература 3). Но в способе, описанном в опубликованном патенте Японии № 2018-70520 (патентная литература 3), требуется 2 эквивалента на 3 эквивалента пара-анизидина (2-1) на основе 2-хлорнитробензола (1-1), и, следовательно, желательно уменьшить количество применяемого п-анизидина. Кроме того, условия примеров данного способа включают низкую температуру от -70°C до 0°C.
[0013]
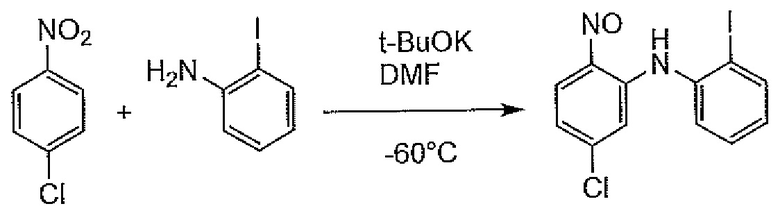
Synlett (2015), 1352-1356 (непатентная литература 1) описывает, что соединение формулы (3) можно получить с высоким выходом. Но для данного способа требуется низкая температура от -70°C до -30°C. Конкретный пример показан на схеме ниже.
[0014]
[формула 5]
[0015]
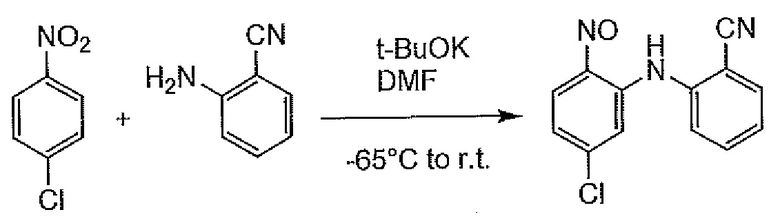
Кроме того, Tetrahedron (2016), 8252-8260 (непатентная литература 2) описывает, что соединение формулы (3) можно получить с умеренным выходом. В данной литературе описан способ, включающий начало реакции при -65°C и последующее повышение температуры до комнатной температуры. Но данный способ также требует экстремально низких температур. Конкретный пример показан на схеме ниже.
[0016]
[формула 6]
[0017]
Как описано выше, условия реакции предшествующего уровня техники включают чрезвычайно низкую температуру. Следовательно, требуются специальные производственные мощности, и поэтому данные способы не являются предпочтительными в промышленном отношении. Соответственно, желателен способ получения, который не требует очень низкой температуры.
[Список цитирований]
[Патентная литература]
[0018]
[Патентная литература 1] WO2009/016841
[Патентная литература 2] WO2013/089002
[Патентная литература 3] Japanese Patent Laid-Open No. 2018-70520
[непатентная литература]
[0019]
[Непатентная литература 1] Synlett (2015), 1352-1356
[Непатентная литература 2] Tetrahedron (2016), 8252-8260
[Непатентная литература 3] Chemistry of Heterocyclic Compounds 2018, 54(9), 875-886
[Сущность настоящего изобретения]
[Техническая проблема]
[0020]
Цель настоящего изобретения заключается в обеспечении способов получения нитрозосоединения формулы (3) и хиноксалинового соединения формулы (5), причем способ является промышленно предпочтительным, экономичным, а также экологически чистым
[0021]
Конкретная цель настоящего изобретения заключается в обеспечении промышленно предпочтительных способов получения соединения формулы (3) и соединения формулы (5), которые могут решить один или несколько недостатков или проблем в традиционной области технике, описанной выше
[Решение проблемы]
[0022]
Ввиду обстоятельств, описанных выше, авторы настоящего изобретения тщательно изучили способы получения соединения формулы (3) и формулы соединения (5). В результате неожиданно было обнаружено, что проблема может быть решена путем предоставления следующих способов получения соединения (формулы 3) и соединения (формулы 5). На основании данных находок авторы настоящего изобретения завершили настоящее изобретение.
[0023]
Конкретно, настоящее изобретение является следующим.
[0024]
[I-1] Способ получения соединения формулы (3), включающий реакцию соединения формулы (1) с соединением формулы (2), применяя третичный спирт и основание:
[формула 7]
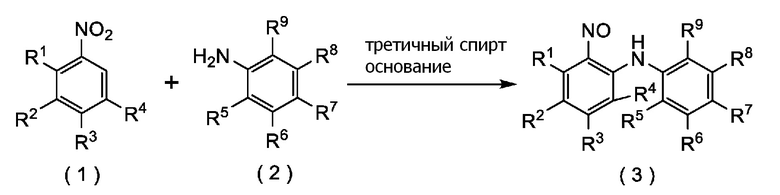
где R1, R2, R3, R4, R5, R6, R7, R8, и R9 каждый независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил или (C1-C4) алкокси.
[0025]
[I-2] Способ по [I-1], где реакцию соединения формулы (1) с соединением формулы (2) проводят после добавления третичного спирта и основания.
[0026]
[I-3] Способ по [I-1] или [I-2], где количество применяемого основания является большим, чем количество применяемого третичного спирта, в пересчете на эквиваленты.
[0027]
[I-4] Способ по любому из [I-1]-[I-3], где основание представляет собой соединение, выбранное из гидридов щелочных металлов и амидов щелочных металлов, или множества соединений, включающих основание, содержащее литий, в качестве первого соединения, и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований.
[0028]
[I-5] Способ по любому из [I-1]-[I-3], где основание представляет собой соединение, выбранное из гидридов щелочных металлов и амидов щелочных металлов, или множества соединений, включающих основание, содержащее литий, в качестве первого соединения, и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов и алкоксидов.
[0029]
[I-6] Способ по любому из [I-1]-[I-3], где основание представляет собой гидрид натрия, амид лития, два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
[0030]
[I-7] Способ по любому из [I-4]-[I-6], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0031]
[I-8] Способ по любому из [I-4]-[I-6], где количество применяемого основания составляет 2,5 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0032]
[I-9] Способ по любому из [I-4]-[I-6], где количество применяемого основания составляет 2,8 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0033]
[I-10] Способ по любому из [I-4]-[I-9], где количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0034]
[I-11] Способ по любому из [I-4]-[I-9], где количество применяемого третичного спирта составляет 0,5 эквивалента-2,0 эквивалента на 1 эквивалент соединения формулы (2).
[0035]
[I-12] Способ по любому из [I-4]-[I-9], где количество применяемого третичного спирта составляет 0,5 эквивалента-1,5 эквивалента на 1 эквивалент соединения формулы (2).
[0036]
[I-13] Способ по любому из [I-4]-[I-12], где реакцию проводят при -5°C-80°C (предпочтительно -5°C-50°C).
[0037]
[I-14] Способ по любому из [I-4]-[I-12], где реакцию проводят при -5°C-50°C.
[0038]
[I-15] Способ по любому из [I-4]-[I-12], где реакцию проводят при 0°C-50°C.
[0039]
[I-16] Способ по любому из [I-4]-[I-12], где реакцию проводят при 0°C-40°C.
[0040]
[I-17] Способ по любому из [I-1]-[I-3], где основание представляет собой гидрид щелочного металла.
[0041]
[I-18] Способ по любому из [I-1]-[I-3], где основание представляет собой гидрид натрия.
[0042]
[I-19] Способ по [I-17] или [I-18], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0043]
[I-20] Способ по [I-17] или [I-18], где количество применяемого основания составляет 2,5 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0044]
[I-21] Способ по [I-17] или [I-18], где количество применяемого основания составляет 2,8 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0045]
[I-22] Способ по любому из [I-17]-[I-21], где количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0046]
[I-23] Способ по любому из [I-17]-[I-21], где количество применяемого третичного спирта составляет 0,5 эквивалента-2,0 эквивалента на 1 эквивалент соединения формулы (2).
[0047]
[I-24] Способ по любому из [I-17]-[I-21], где количество применяемого третичного спирта составляет 0,5 эквивалента-1,5 эквивалента на 1 эквивалент соединения формулы (2).
[0048]
[I-25] Способ по любому из [I-17]-[I-21], где количество применяемого третичного спирта составляет 0,9 эквивалента-2,1 эквивалента на 1 эквивалент соединения формулы (2).
[0049]
[I-26] Способ по любому из [I-17]-[I-25], где реакцию проводят при -5°C-80°C (предпочтительно -5°C-50°C).
[0050]
[I-27] Способ по любому из [I-17]-[I-25], где реакцию проводят при 0°C-50°C.
[0051]
[I-28] Способ по любому из [I-17]-[I-25], где реакцию проводят при 20°C-70°C.
[0052]
[I-29] Способ по любому из [I-17]-[I-25], где реакцию проводят при 20°C-40°C.
[0053]
[I-30] Способ по любому из [I-1]-[I-3], где основание представляет собой амид щелочного металла.
[0054]
[I-31] Способ по любому из [I-1]-[I-3], где основание представляет собой амид лития.
[0055]
[I-32] Способ по [I-30] или [I-31], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0056]
[I-33] Способ по [I-30] или [I-31], где количество применяемого основания составляет 2,5 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0057]
[I-34] Способ по [I-30] или [I-31], где количество применяемого основания составляет 2,8 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0058]
[I-35] Способ по любому из [I-30]-[I-34], где количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0059]
[I-36] Способ по любому из [I-30]-[I-34], где количество применяемого третичного спирта составляет 0,3 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2).
[0060]
[I-37] Способ по любому из [I-30]-[I-34], где количество применяемого третичного спирта составляет 0,5 эквивалента-2,0 эквивалента на 1 эквивалент соединения формулы (2).
[0061]
[I-38] Способ по любому из [I-30]-[I-34], где количество применяемого третичного спирта составляет 0,5 эквивалента-1,5 эквивалента на 1 эквивалент соединения формулы (2).
[0062]
[I-39] Способ по любому из [I-30]-[I-34], где количество применяемого третичного спирта составляет 0,4 эквивалента-1,1 эквивалента на 1 эквивалент соединения формулы (2).
[0063]
[I-40] Способ по любому из [I-30]-[I-39], где реакцию проводят при -5°C-80°C (предпочтительно -5°C-50°C, более предпочтительно -5°C-15°C).
[0064]
[I-41] Способ по любому из [I-30]-[I-39], где реакцию проводят при 0°C-50°C.
[0065]
[I-42] Способ по любому из [I-30]-[I-39], где реакцию проводят при 0°C-30°C.
[0066]
[I-43] Способ по любому из [I-30]-[I-39], где реакцию проводят при 0°C-15°C.
[0067]
[I-44] Способ по любому из [I-1]-[I-3], где основание включает множество соединений.
[0068]
[I-45] Способ по любому из [I-1]-[I-3], где основание включает два или три соединения.
[0069]
[I-46] Способ по любому из [I-1]-[I-3], где основание состоит из двух соединений.
[0070]
[I-47] Способ по [I-44], где множество соединений включает основание, содержащее литий, (предпочтительно амид лития) в качестве первого соединения и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований.
[0071]
[I-48] Способ по [I-45], где два или три соединения включают основание, содержащее литий, (предпочтительно амид лития) в качестве первого соединения, и одно или два других соединения, выбранные из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований.
[0072]
[I-49] Способ по [I-46], где два соединения представляют собой основание, содержащее литий, (предпочтительно амид лития) в качестве первого соединения, и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований.
[0073]
[I-50] Способ по [I-44], где множество соединений включает основание, содержащее литий, в качестве первого соединения, и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов и алкоксидов.
[0074]
[I-51] Способ по [I-45], где два или три соединения включают основание, содержащее литий, в качестве первого соединения, и одно или два других соединения, выбранные из гидридов щелочных металлов, амидов щелочных металлов и алкоксидов.
[0075]
[I-52] Способ по [I-46], где два соединения представляют собой основание, содержащее литий, в качестве первого соединения, и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов и алкоксидов.
[0076]
[I-53] Способ по [I-44], где множество соединений включает амид лития в качестве первого соединения, и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов и алкоксидов.
[0077]
[I-54] Способ по [I-45], где два или три соединения включают амид лития в качестве первого соединения, и одно или два других соединения, выбранные из гидридов щелочных металлов, амидов щелочных металлов и алкоксидов.
[0078]
[I-55] Способ по [I-46], где два соединения представляют собой амид лития в качестве первого соединения, и другое соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов и алкоксидов.
[0079]
[I-56] Способ по [I-44], где множество соединений включает два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
[0080]
[I-57] Способ по [I-45], где два или три соединения включают два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
[0081]
[I-58] Способ по [I-46], где два соединения представляют собой два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
[0082]
[I-59] Способ по [I-44], где множество соединений включает два из амида лития и гидрида натрия.
[0083]
[I-60] Способ по [I-45], где два или три соединения включают два из амида лития и гидрида натрия.
[0084]
[I-61] Способ по [I-46], где два соединения представляют собой амид лития и гидрид натрия.
[0085]
[I-62] Способ по любому из [I-44]-[I-61], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0086]
[I-63] Способ по любому из [I-44]-[I-61], где количество применяемого основания составляет 2,5 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0087]
[I-64] Способ по любому из [I-44]-[I-61], где количество применяемого основания составляет 2,8 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2).
[0088]
[I-65] Способ по любому из [I-44]-[I-64], где количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0089]
[I-66] Способ по любому из [I-44]-[I-64], где количество применяемого третичного спирта составляет 0,3 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2).
[0090]
[I-67] Способ по любому из [I-44]-[I-64], где количество применяемого третичного спирта составляет 0,5 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2).
[0091]
[I-68] Способ по любому из [I-44]-[I-64], где количество применяемого третичного спирта составляет 0,5 эквивалента-2,0 эквивалента на 1 эквивалент соединения формулы (2).
[0092]
[I-69] Способ по любому из [I-44]-[I-64], где количество применяемого третичного спирта составляет 0,5 эквивалента-1,5 эквивалента на 1 эквивалент соединения формулы (2).
[0093]
[I-70] Способ по любому из [I-47]-[I-69], где отношение другого соединения составляет более чем 0 эквивалента и 2,0 эквивалента или меньше на 1 эквивалент первого соединения.
[0094]
[I-71] Способ по любому из [I-47]-[I-69], где отношение другого соединения составляет более чем 0 (ноль) эквивалента и 0,5 эквивалента или меньше на 1 эквивалент первого соединения.
[0095]
[I-72] Способ по любому из [I-47]-[I-69], где отношение другого соединения составляет 0,2 эквивалента-0,5 эквивалента на 1 эквивалент первого соединения.
[0096]
[I-73] Способ по любому из [I-44]-[I-72], где реакцию проводят при -5°C-80°C (предпочтительно -5°C -50°C).
[0097]
[I-74] Способ по любому из [I-44]-[I-72], где реакцию проводят при 0°C-60°C.
[0098]
[I-75] Способ по любому из [I-44]-[I-72], где реакцию проводят при 0°C-50°C.
[0099]
[I-76] Способ по любому из [I-44]-[I-72], где реакцию проводят при 0°C-30°C.
[0100]
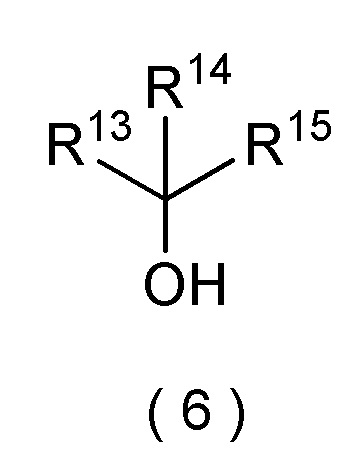
[I-77] Способ по любому из [I-1]-[I-76], где третичный спирт представляет собой соединение формулы (6):
[формула 8]
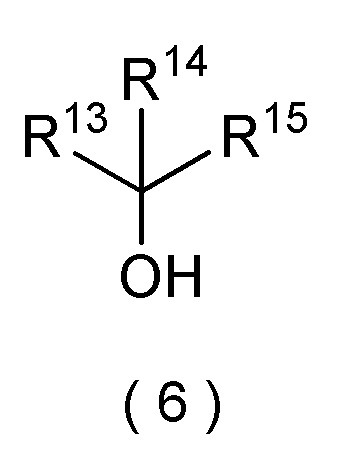
где R13, R14, и R15 могут быть одинаковыми или отличными и каждый представляет собой (C1-C6) алкил, (C3-C6) циклоалкил, (C2-C6) алкенил, (C2-C6) алкинил, (C6-C10) арил, или (C6-C10) арил (C1-C4) алкил, и два, выбранные из R13, R14, и R15 могут быть соединены друг с другом, образуя кольцо.
[0101]
[I-78] Способ по [I-77], где R13, R14 и R15 могут быть одинаковыми или отличными и выбраны из метила, этила, этенила, этинила, пропила, бензила и фенила.
[0102]
[I-79] Способ по любому из [I-1]-[I-76], где третичный спирт выбран из трет-бутанола, 2-метил-2-бутанола, 2-метил-3-бутен-2-ола и 2-метил-1-фенил-2-пропанола.
[0103]
[I-80] Способ по любому из [I-1]-[I-76], где третичный спирт представляет собой трет-бутанол.
[0104]
[I-81] Способ по любому из [I-1]-[I-80], где реакцию проводят в присутствии растворителя.
[0105]
[I-82] Способ по [I-81], где реакцию соединения формулы (1) с соединением формулы (2) проводят после добавления третичного спирта и основания к растворителю.
[0106]
[I-83] Способ по [I-81] или [I-82], где растворитель представляет собой толуол, ксилол, хлорбензол, дихлорбензол, или их смесь.
[0107]
[I-84] Способ по [I-81] или [I-82], где растворитель представляет собой толуол, ксилол, или их смесь.
[0108]
[I-85] Способ по [I-81] или [I-82], где растворитель представляет собой толуол.
[0109]
[I-86] Способ по любому из [I-1]-[I-85], где
каждый R1, R2, R3, и R4 независимо представляет собой атом водорода, атом фтора или атом хлора; и
каждый R5, R6, R7, R8, и R9 независимо представляет собой атом водорода, (C1-C4) алкил или (C1-C4) алкокси.
[0110]
[I-87] Способ по любому из [I-1]-[I-85], где
каждый R1, R2, R3, и R4 независимо представляет собой атом водорода или атом хлора; и
каждый R5, R6, R7, R8, и R9 независимо представляет собой атом водорода или (C1-C4) алкокси.
[0111]
[I-88] Способ по любому из [I-1]-[I-85], где
R1 представляет собой атом водорода или атом хлора;
каждый R2, R3, и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой атом водорода или метокси.
[0112]
[I-89] Способ по любому из [I-1]-[I-85], где
R1 представляет собой атом водорода или атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой метокси.
[0113]
[I-90] Способ по любому из [I-1]-[I-85], где
R1 представляет собой атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой метокси.
[0114]
[II-1] Способ получения соединение формулы (5):
[формула 9]
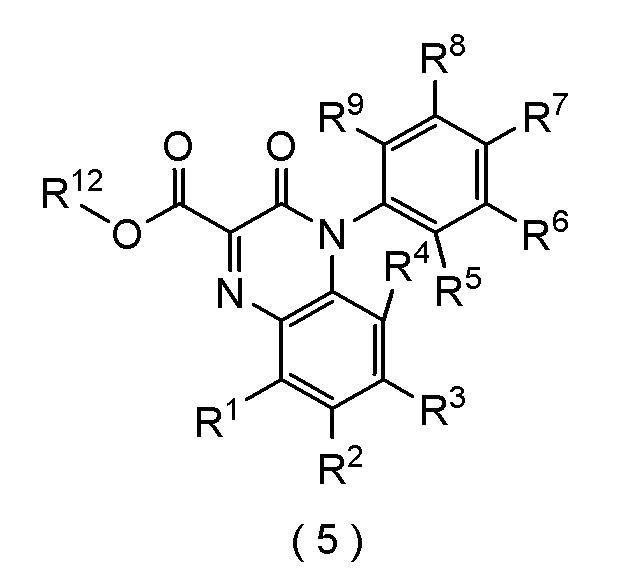
где каждый R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил или (C1-C4) алкокси; и
R12 представляет собой атом водорода, атом щелочного металла или (C1-C4) алкил,
причем способ включает следующие стадии;
стадию (i) реакции соединения формулы (1) с соединением формулы (2), применяя третичный спирт и основание, получая соединение формулы (3):
[формула 10]
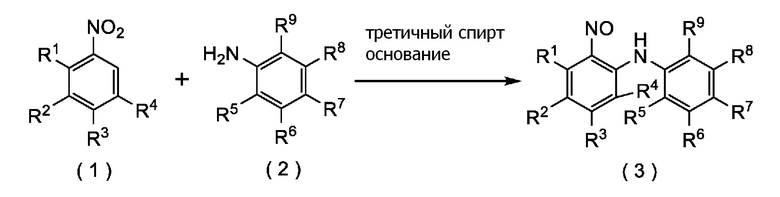
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше,
и где стадию (i) проводят способом по любому из [I-1]-[I-90],
стадию (ii) реакции соединения формулы (3) с соединением формулы (4), получая соединение формулы (5):
[формула 11]
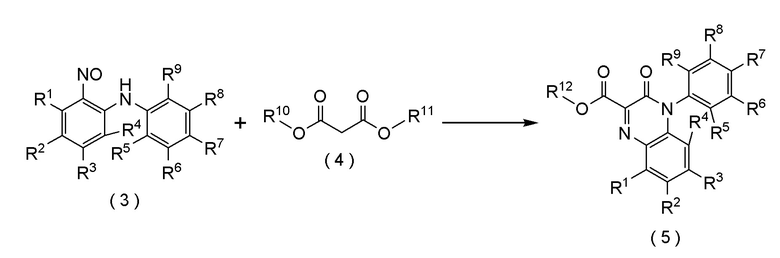
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше;
каждый R10 и R11 независимо представляет собой (C1-C4) алкил; и
R12 представляет собой, как определено выше.
[0115]
[II-2] Способ получения соединение формулы (5):
[формула 12]
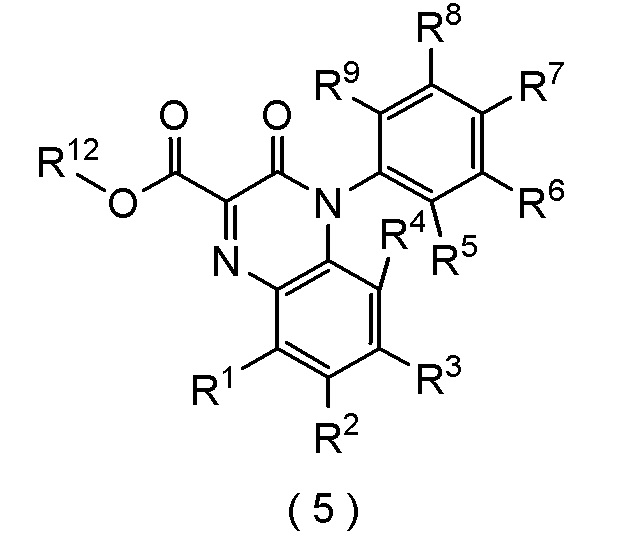
где каждый R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил или (C1-C4) алкокси; и
R12 представляет собой атом водорода, атом щелочного металла или (C1-C4) алкил,
причем способ включает применение соединения формулы (3):
[формула 13]
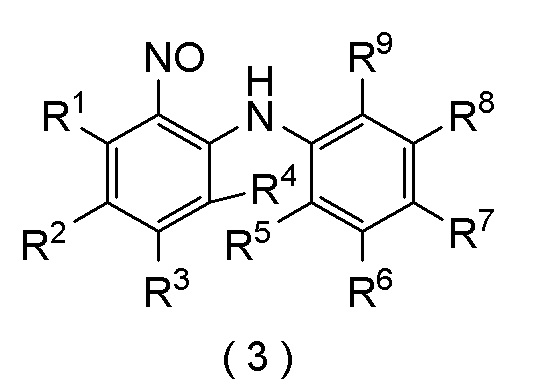
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше,
где соединение формулы (3) получают способом по любому из [I-1]-[I-90].
[0116]
[II-3] Способ получения соединение формулы (5):
[формула 14]
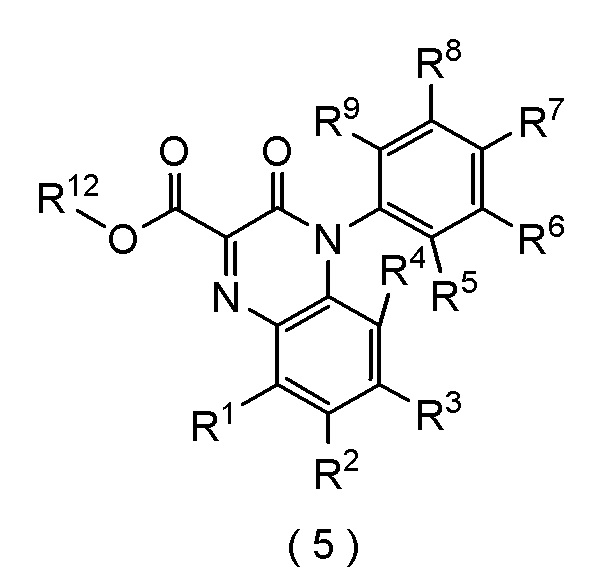
где каждый R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил, или (C1-C4) алкокси; и
R12 представляет собой атом водорода, атом щелочного металла или (C1-C4) алкил,
причем способ включает применение соединения формулы (3):
[формула 15]
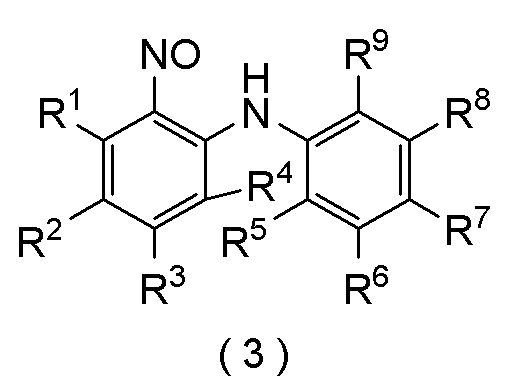
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше,
где в качестве соединения формулы (3), применяют соединение формулы (3), полученное способом по любому из [I-1]-[I-90].
[0117]
[II-4] Способ получения соединение формулы (5):
[формула 16]
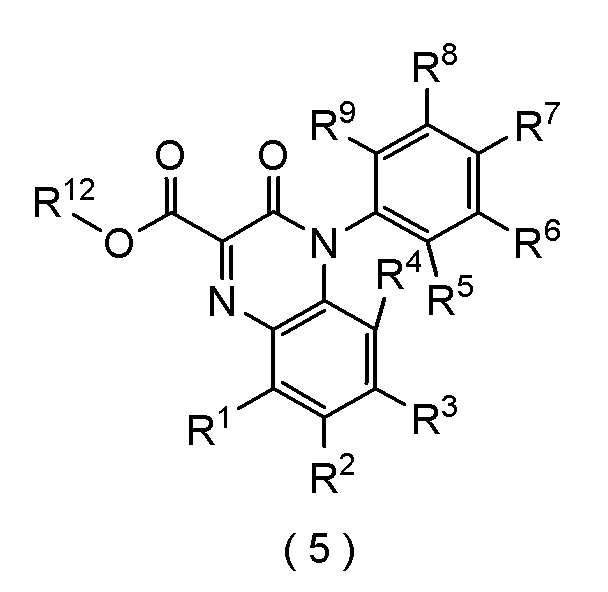
где каждый R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил, или (C1-C4) алкокси; и
R12 представляет собой атом водорода, атом щелочного металла или (C1-C4) алкил,
причем способ включает следующие стадии;
стадию (i) получения соединения формулы (3) способом по любому из [I-1]-[I-90]:
[формула 17]
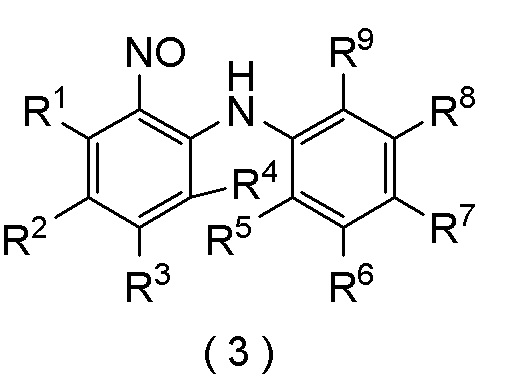
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше,
стадию (ii) реакции соединения формулы (3) с соединением формулы (4), получая соединение формулы (5):
[формула 18]
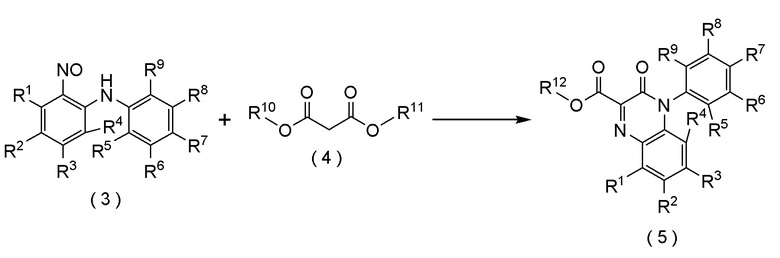
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 и R12 представляют собой, как определено выше.
[0118]
[II-5] Способ по [II-1] или [II-4], где соединение формулы (4) представляет собой диметилмалонат или диэтилмалонат.
[0119]
[II-6] Способ по [II-1] или [II-4], где реакцию на стадии (ii) проводят при pH 8 или более.
[0120]
[II-7] Способ по [II-1] или [II-4], где реакцию на стадии (ii) проводят при pH 8-14.
[0121]
[II-8] Способ по любому из [II-1], [II-4]-[II-7], где реакцию на стадии (ii) проводят в отсутствии катализатора фазового переноса.
[0122]
[II-9] Способ по любому из [II-1], [II-4]-[II-7], где реакцию на стадии (ii) проводят в присутствии катализатора фазового переноса.
[0123]
[II-10] Способ по любому из [II-1], [II-4]-[II-9], где реакцию на стадии (ii) проводят в присутствии воды.
[0124]
[II-11] Способ по любому из [II-1]-[II-10], где
каждый R1, R2, R3 и R4 независимо представляет собой атом водорода, атом фтора или атом хлора; и
каждый R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, (C1-C4) алкил или (C1-C4) алкокси.
[0125]
[II-12] Способ по любому из [II-1]-[II-10], где
каждый R1, R2, R3 и R4 независимо представляет собой атом водорода или атом хлора; и
каждый R5, R6, R7, R8, и R9 независимо представляет собой атом водорода или (C1-C4) алкокси.
[0126]
[II-13] Способ по любому из [II-1]-[II-10], где
R1 представляет собой атом водорода или атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой атом водорода или метокси.
[0127]
[II-14] Способ по любому из [II-1]-[II-10], где
R1 представляет собой атом водорода или атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой метокси.
[0128]
[II-15] Способ по любому из [II-1]-[II-10], где
R1 представляет собой атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой метокси.
[0129]
[II-16] Способ по любому из [II-1]-[II-15], где
Каждый R10 и R11 представляет собой метил или этил; и
R12 представляет собой атом водорода, атом лития, атом натрия, атом калия, метил или этил.
[0130]
[II-17] Способ по любому из [II-1]-[II-15], где
каждый R10 и R11 представляет собой метил или этил; и
R12 представляет собой атом водорода, атом лития, атом натрия, метил, или этил.
[0131]
[II-18] Способ по любому из [II-1]-[II-15], где
каждый R10 и R11 представляет собой метил или этил; и
R12 представляет собой атом водорода, атом лития или атом натрия.
[0132]
[II-19] Способ по любому из [II-1]-[II-15], где
каждый R10 и R11 представляет собой метил или этил; и
R12 представляет собой атом водорода.
[0133]
[III-1] Способ получения соединение формулы (3), включающий реакцию соединения формулы (1) с соединением формулы (2), применяя третичный спирт и основание:
[формула 19]
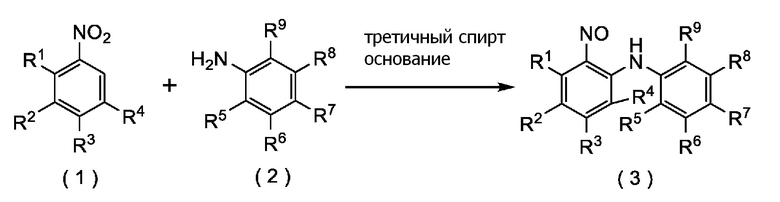
каждый где R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил или (C1-C4) алкокси.
[0134]
[III-2] Способ по [III-1], где реакцию соединения формулы (1) с соединением формулы (2) проводят после добавления третичного спирта и основания.
[0135]
[III-3] Способ по [III-1] или [III-2], где количество применяемого основания является большим, чем количество применяемого третичного спирта, в пересчете на эквиваленты.
[0136]
[III-4] Способ по любому из [III-1]-[III-3], где основание представляет собой соединение, выбранное из гидридов щелочных металлов и амидов щелочных металлов, или множества соединений, включающего основание, содержащее литий, в качестве первого соединения, и второе соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований.
[0137]
[III-5] Способ по любому из [III-1]-[III-3], где основание представляет собой гидрид натрия, амид лития, два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
[0138]
[III-6] Способ по [III-4] или [III-5], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2), и количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0139]
[III-7] Способ по любому из [III-1]-[III-3], где основание представляет собой гидрид щелочного металла.
[0140]
[III-8] Способ по любому из [III-1]-[III-3], где основание представляет собой гидрид натрия.
[0141]
[III-9] Способ по [III-7] или [III-8], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2), и количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
[0142]
[III-10] Способ по любому из [III-1]-[III-3], где основание представляет собой амид щелочного металла.
[0143]
[III-11] Способ по любому из [III-1]-[III-3], где основание представляет собой амид лития.
[0144]
[III-12] Способ по [III-10] или [III-11], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2), и количество применяемого третичного спирта составляет 0,3 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2).
[0145]
[III-13] Способ по любому из [III-1]-[III-3], где основание включает множество соединений.
[0146]
[III-14] Способ по [III-13], где множество соединений включает основание, содержащее литий, в качестве первого соединения, и второе соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований.
[0147]
[III-15] Способ по [III-13], где множество соединений включает два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
[0148]
[III-16] Способ по [III-13], где множество соединений включает два из амида лития и гидрида натрия.
[0149]
[III-17] Способ по любому из [III-13]-[III-16], где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2), и количество применяемого третичного спирта составляет 0,3 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2).
[0150]
[III-18] Способ по любому из [III-1]-[III-17], где третичный спирт представляет собой соединение формулы (6):
[формула 20]
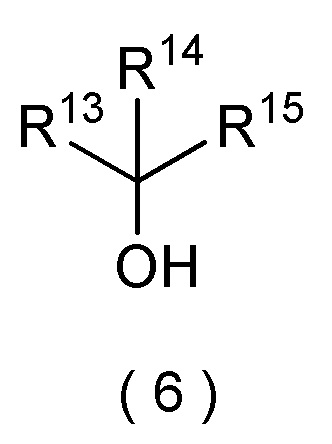
где R13, R14 и R15 могут быть одинаковыми или отличными, и каждый представляет собой (C1-C6) алкил, (C3-C6) циклоалкил, (C2-C6) алкенил, (C2-C6) алкинил, (C6-C10) арил, или (C6-C10) арил (C1-C4) алкил, и два, выбранные из R13, R14, и R15 могут быть соединены друг с другом, образуя кольцо.
[0151]
[III-19] Способ по любому из [III-1]-[III-17], где третичный спирт выбран из трет-бутанола, 2-метил-2-бутанола, 2-метил-3-бутен-2-ола и 2-метил-1-фенил-2-пропанола.
[0152]
[III-20] Способ по любому из [III-1]-[III-19], где реакцию проводят при -5°C-80°C.
[0153]
[III-21] Способ по любому из [III-1]-[III-19], где реакцию проводят при 0°C-50°C.
[0154]
[III-22] Способ по любому из [III-1]-[III-21], где
R1 представляет собой атом водорода или атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой атом водорода или метокси.
[0155]
[III-23] Способ по любому из [III-1]-[III-21], где
R1 представляет собой атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода; и
R7 представляет собой метокси.
[0156]
[III-24] Способ получения соединение формулы (5):
[формула 21]
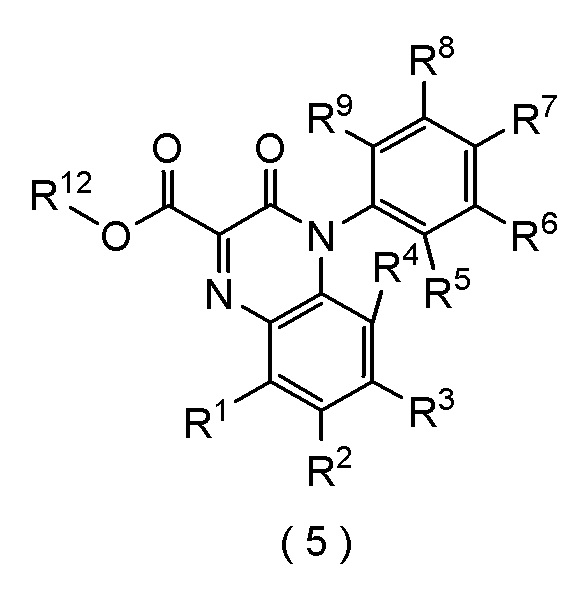
где каждый R1, R2, R3, R4, R5, R6, R7, R8, и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил, или (C1-C4) алкокси; и
R12 представляет собой атом водорода, атом щелочного металла или (C1-C4) алкил,
причем способ включает следующие стадии;
стадию (i) получения соединения формулы (3) способом по любому из [III-1]-[III-23]:
[формула 22]
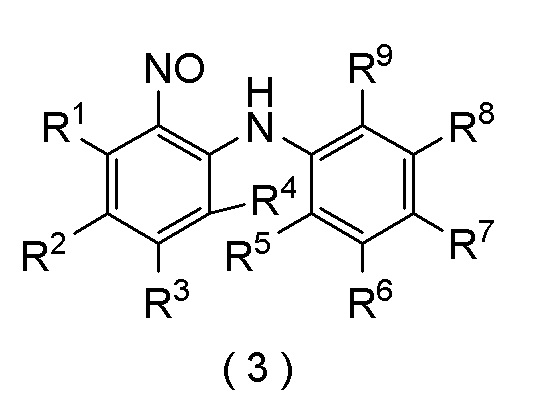
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше,
стадию (ii) реакции соединения формулы (3) с соединением формулы (4), получая соединение формулы (5):
[формула 23]
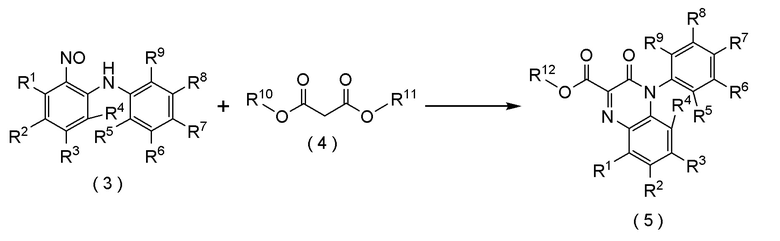
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 и R12 представляют собой, как определено выше.
[0157]
[III-25] Способ по [III-24], где реакцию на стадии (ii) проводят при pH 8 или более.
[0158]
[III-26] Способ по [III-24], где реакцию на стадии (ii) проводят при pH 8-14.
[0159]
[III-27] Способ по любому из [III-24]-[III-26], где реакцию на стадии (ii) проводят в отсутствии катализатора фазового переноса.
[0160]
[III-28] Способ по любому из [III-24]-[III-26], где реакцию на стадии (ii) проводят в присутствии катализатора фазового переноса.
[0161]
[III-29] Способ по любому из [III-24]-[III-28], где реакцию на стадии (ii) проводят в присутствии воды.
[0162]
[III-30] Способ по любому из [III-24]-[III-29], где
каждый R10 и R11 представляет собой метил или этил; и
R12 представляет собой атом водорода, атом лития, атом натрия, атом калия, метил или этил.
[0163]
[III-31] Способ по любому из [III-24]-[III-29], где
каждый R10 и R11 представляет собой метил или этил; и
R12 представляет собой атом водорода.
[Полезные свойства настоящего изобретения]
[0164]
Согласно настоящему изобретению, обеспечивают новые способы получения соединения формулы (3) и соединения формулы (5), причем способы являются промышленно предпочтительными, экономичными и также экологически чистыми. Согласно настоящему изобретению, обеспечивают способы получения соединения формулы (3) и соединения формулы (5), которые могут решить один или более недостатков или проблем в общепринятой области техники, описанной выше.
Описание вариантов осуществления
[0165]
Настоящее изобретение будет описано подробно ниже.
[0166]
В настоящем изобретении можно применять следующие сокращения и префиксы, и их значения являются следующими:
Me: метил
Et: этил
Pr, n-Pr, и Pr-n: пропил (то есть нормальный пропил)
i-Pr и Pr-i: изопропил
Bu, n-Bu, и Bu-n: бутил (то есть нормальный бутил)
s-Bu и Bu-s: втор-бутил (то есть, вторичный бутил)
i-Bu и Bu-i: изобутил
t-Bu и Bu-t: трет-бутил (то есть, третичный бутил)
Ph: фенил
n-: нормальный
s- и втор-: вторичный
i- и iso-: изо
t- и трет-: третичный
neo-: нео
c- и cyc-: цикло
o-: орто
m-: мета
p-: пара
трет-BuOH: трет-бутанол
[0167]
Примеры атома галогена включают атом фтора, атом хлора, атом брома и атом йода.
[0168]
Как применяют в настоящем изобретении, считают, что общие термины, такие как «алкил», включают как нормальные, так и разветвленные цепи, такие как бутил и трет-бутил. С другой стороны, например, конкретный термин «бутил» обозначает «нормальный бутил» с нормальной цепью и не обозначает «трет-бутил» с разветвленной цепью. Изомеры с разветвленной цепью, такие как «трет-бутил», специально упоминаются при назначении.
[0169]
(Ca-Cb) обозначает то, что количество атомов углерода представляет собой a-b. Например, "(C1-C4)" "(C1-C4) алкила" обозначает то, что количество атомов углерода алкила составляет 1-4.
[0170]
(C1-C6) алкил обозначает алкил с нормальной или разветвленной цепью, содержащий 1-6 атомов углерода. Примеры (C1-C6) алкила включают, но не ограничиваются, метил, этил, пропил, изопропил, бутил, втор-бутил, изобутил, трет-бутил, пентил и гексил.
(C1-C4) алкил обозначает алкил с нормальной или разветвленной цепью, содержащий 1-4 атома углерода. Примеры (C1-C4) алкила представляют собой метил, этил, пропил, изопропил, бутил, втор-бутил, изобутил и трет-бутил.
[0171]
(C3-C6) циклоалкил обозначает циклоалкил, содержащий 3-6 атомов углерода. Примеры (C3-C6) циклоалкила представляют собой циклопропил, циклобутил, циклопентил и циклогексил.
[0172]
(C2-C6) алкенил обозначает алкенил с нормальной или разветвленной цепью, содержащей 2-6 атомов углерода. Примеры (C2-C6) алкенила включают, но не ограничиваются, винил (то есть, этенил), 1-пропенил, изопропенил, 2-пропенил, 1-бутенил, 1-метил-1-пропенил, 2-метил-1-пропенил, 2-бутенил, 3-бутенил, 1,3-бутадиенил, 1-пентенил и 1-гексенил.
[0173]
(C2-C6) алкинил обозначает алкинил с нормальной или разветвленной цепью, содержащей 2-6 атомов углерода. Примеры (C2-C6) алкинила включают, но не ограничиваются, этинил, 1-пропинил, 2-пропинил, 1-бутинил, 1-метил-2-пропинил, 2-бутинил, 3-бутинил, 1-пентинил и 1-гексинил.
[0174]
Примеры (C6-C10) арила представляют собой фенил, 1-нафтил и 2-нафтил.
[0175]
(C6-C10) арил (C1-C4) алкил обозначает (C1-C4 алкил), замещенный (C6-C10) арилом (в настоящем изобретении, C6-C10 арильный фрагмент и C1-C4 алкильный фрагмент имеют те же значения, как определения выше). Примеры (C6-C10) арил (C1-C4) алкила включают, но не ограничиваются, бензильную, 1-фенилэтильную, 2-фенилэтильную, 3-фенилпропильную, 4-фенилбутильную, нафталин-1-илметильную и нафталин-2-илметильную группу.
[0176]
A (C1-C4) алкокси обозначает (C1-C4) алкил-O- (в настоящем изобретении, (C1-C4) алкильный фрагмент имеет то же значение, как определение выше). Примеры (C1-C4) алкокси включают метокси, этокси, пропокси, изопропокси, бутокси, втор-бутокси, изобутокси, и трет-бутокси.
[0177]
Примеры "кольца" в выражении "два могут быть соединены друг с другом, образуя кольцо" включают, но не ограничиваются, циклопропан, циклобутан, циклопентан, циклогексан, циклопентен и циклогексен. "Кольцо" может быть конденсировано с другим "кольцом".
[0178]
Как применяют в настоящем изобретении, каждый из неограничивающих терминов "включает (включают)/включающий" можно необязательно заменять ограничивающими выражениями "состоит из (состоят из)/состоящий из."
Как применяют в настоящем изобретении, выражение "после ... каждый добавляют" можно заменять выражением "после ... добавляют отдельно".
Как видно из примеров, описанных ниже, ясно, что выражение "каждый из третичного спирта и основания добавляют" обозначает, например, что "каждый из третичного спирта и основания добавляют в реакционную систему," но это не интерпретируют как ограничение. Следовательно, как применяют в настоящем изобретении, выражение "после добавления третичного спирта и основания" можно заменить на выражение, например, "после добавления третичного спирта и основания в реакционную систему."
Как применяют в настоящем изобретении, выражение "второе соединение" можно заменять выражением "другое соединение".
[0179]
Далее будет описан способ настоящего изобретения.
[0180]
(Стадия (i))
[0181]
Далее будет описана стадия (i).
[0182]
Стадия (i) представляет собой стадию реакции соединения формулы (1) с соединением формулы (2), применяя третичный спирт и основание, получая соединение формулы (3).
[0183]
[формула 24]
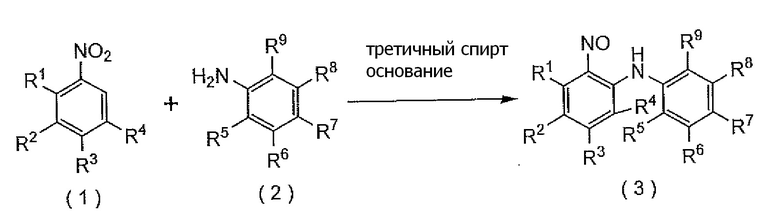
[0184]
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше.
[0185]
(Исходное соединение: соединение формулы (1), которое представляет собой нитросоединение)
В качестве исходного соединения на стадии (i), применяют соединение формулы (1), которое представляет собой нитросоединение. Соединение формулы (1) представляет собой известное соединение, или его можно получить из известного соединения согласно известному способу.
[0186]
Конкретные примеры соединения формулы (1) включают, но не ограничиваются, следующие;
нитробензол, 2-хлорнитробензол, 3-хлорнитробензол, 4-хлорнитробензол, 2-фторнитробензол, 3-фторнитробензол и 4-фторнитробензол.
[0187]
С учетом выхода, доступности, цены, полезности продукта и подобных, предпочтительные конкретные примеры соединения формулы (1) включают нитробензол и 2-хлорнитробензол, более предпочтительно 2-хлорнитробензол.
[0188]
Применяемое количество соединения формулы (1) может быть произвольным количеством, при условии, что реакция протекает. Однако, в одном аспекте, применяемое количество соединения формулы (1) (нитросоединения) составляет, например, 0,7 эквивалента-2,0 эквивалента, предпочтительно 0,9 эквивалента-1,8 эквивалента, более предпочтительно 0,9 эквивалента-1,6 эквивалента, более предпочтительно 0,9 эквивалента-1,5 эквивалента, и особенно предпочтительно 1,0-1,5 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение), с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобные. С точки зрения, как показано выше, в другом аспекте, применяемое количество соединения формулы (1) (нитросоединение) составляет, например, 1,0 эквивалент-2,0 эквивалента, предпочтительно 1,0 эквивалент-1,8 эквивалента, более предпочтительно 1,0 эквивалент-1,6 эквивалента, и особенно предпочтительно 1,0 эквивалент-1,5 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение).
[0189]
Как применяют в настоящем изобретении, определение " эквивалент соединения формулы (1) (нитросоединение)" является следующим, или термин "эквивалент" толкуется согласно следующим примерам. Например, "1 эквивалент соединения формулы (1) (нитросоединение) на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "1 моль соединения формулы (1) (нитросоединение) на 1 моль соединения формулы (2) (анилиновое соединение)." Например, "0,5 эквивалента соединения формулы (1) (нитросоединение) на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "0,5 моль соединения формулы (1) (нитросоединение) на 1 моль соединения формулы (2) (анилиновое соединение)."
[0190]
(Исходное соединение: соединение общей формулы (2), которое представляет собой анилиновое соединение)
В качестве исходного соединения на стадии (i), применяют соединение формулы (2), которое представляет собой анилиновое соединение. Соединение формулы (2) представляет собой известное соединение, или его можно получить из известного соединения согласно известному способу.
[0191]
Конкретные примеры соединения формулы (2) включают, но не ограничиваются, следующие;
анилин, 4-метоксианилин (то есть п-анизидин), 4-этоксианилин, 4-н-пропоксианилин, 4-н-бутоксианилин, 4-метиланилин, 4-этиланилин, 4-н-пропиланилин, 4-н-бутиланилин и 4-трет-бутиланилин.
[0192]
С точки зрения выхода, полезности продукта и/или подобных, предпочтительные конкретные примеры соединения формулы (2) включают анилин или 4-метоксианилин. С точки зрения полезности продукта и подобных, более предпочтительный конкретный пример соединения формулы (2) представляет собой 4-метоксианилин.
[0193]
С точки зрения улучшения экономии, снижения экологической нагрузки и подобных, применение избыточного количества 2-хлорнитробензола или нитробензола является приемлемым. С другой стороны, применение избыточного количества п-анизидина предпочтительно избегать, но это не следует понимать как ограничение. Например, ясно, что п-анизидин является более дорогим по сравнению с 2-хлорнитробензолом и нитробензолом. В способе опубликованного японского патента No. 2018-70520 (патентная литература 3), 2 эквивалента или более п-анизидина требуется в качестве единственного применяемого исходного соединения. Действительно, в примерах опубликованного японского патента No. 2018-70520 (патентная литература 3), применяют вплоть до 2 эквивалентов-3 эквивалентов п-анизидина. С другой стороны, в способе настоящего изобретения, 2 эквивалента или меньше 2-хлорнитробензола или хлорнитробензола является достаточным в качестве единственного применяемого исходного соединения. Как показано в примерах, описанных ниже, даже 1 эквивалент-1,5 эквивалента 2-хлорнитробензола или хлорнитробензола обепечивают удовлетворительный выход.
[0194]
(Основание на стадии (i))
Примеры основания на стадии (i) включают, но не ограничиваются, следующие;
гидриды щелочных металлов (например, гидрид лития, гидрид натрия, и гидрид калия, предпочтительно гидрид натрия и гидрид калия, и более предпочтительно гидрид натрия),
гидриды щелочноземельных металлов (например, гидрид кальция),
алкоксиды (например, трет-бутоксид лития, трет-бутоксид натрия, трет-бутоксид калия, метоксид лития, метоксид натрия, метоксид калия, этоксид лития, этоксид натрия, этоксид калия, изопропоксид лития, изопропоксид натрия и изопропоксид калия, предпочтительно трет-бутоксид лития, трет-бутоксид натрия и трет-бутоксид калия, и более предпочтительно трет-бутоксид натрия),
алкилметаллы (например, бутиллитий, втор-бутиллитий и трет-бутиллитий),
амиды щелочных металлов (например, амид лития, амид натрия, амид калия, лития диизопропиламид и гексаметилдисилазид калия, предпочтительно амид лития, амид натрия и амид калия, более предпочтительно амид лития и амид натрия, и более предпочтительно амид лития), щелочные металлы (например, металлический литий, металлический натрий и металлический калий),
органические основания (например, триметиламин, триэтиламин, трипропиламин, трибутиламин, диизопропилэтиламин, 1,8-диазабицикло[5,4,0]-7-ундец-7-ен (DBU), 1,5-диазабицикло[4,3,0]нон-5-ен (DBN), 1,4-диазабицикло[2,2,2]октан (DABCO), пиридин, N, N-диметил-4-аминопиридин, N, N-диметиланилин и N, N-диэтиланилин), и
любую их комбинацию в произвольном соотношении.
[0195]
С точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, предпочтительные примеры основания на стадии (i) включают гидриды щелочных металлов, амиды щелочных металлов и любую их комбинацию в произвольном соотношении. Предпочтительные конкретные примеры основания на стадии (i) включают гидрид лития, гидрид натрия, гидрид калия, амид лития, амид натрия и любую их комбинацию в произвольном соотношении, более предпочтительно гидрид лития, гидрид натрия, гидрид калия и амид лития, и более предпочтительно гидрид натрия и амид лития.
[0196]
Основание на стадии (i) может включать множества соединений. Первое соединение предпочтительно представляет собой основание, содержащее литий. Второе соединение (также называемое другим соединением) можно выбрать из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов, и органических оснований.
[0197]
Примеры основания, содержащего литий, включают, но не ограничиваются, гидрид лития, амид лития, диизопропиламид лития, трет-бутоксид лития, бутиллитий, втор-бутиллитий, трет-бутиллитий, металлический литий, гидроксид лития, карбонат лития и гидрокарбонат лития. Предпочтительные примеры основания, содержащего литий, представляют собой гидрид лития, амид лития, диизопропиламид лития, трет-бутоксид лития, бутиллитий, втор-бутиллитий, трет-бутиллитий и металлический литий, более предпочтительно гидрид лития и амид лития, и особенно предпочтительно амид лития.
[0198]
Первое соединение и второе соединение можно применять в произвольном соотношении. Подходящее отношение выбирают в зависимости от типа применяемых соединений. В одном аспекте, например, отношение второго соединения к первому соединению составляет более чем 0 (ноль) эквивалента и 3,0 эквивалента или меньше, или более чем 0 (ноль) эквивалента и 2,0 эквивалента или меньше, предпочтительно более чем 0 (ноль) эквивалента и 1,5 эквивалента или меньше, более предпочтительно более чем 0 (ноль) эквивалента и 1,0 эквивалент или меньше, и более предпочтительно более чем 0 (ноль) эквивалента и 0,5 эквивалента или меньше. В другом аспекте, например, отношение второго соединения к первому соединению предпочтительно составляет 0,05 эквивалента-1,5 эквивалента, более предпочтительно 0,1 эквивалента-1,0 эквивалент, и более предпочтительно 0,2 эквивалента-0,5 эквивалента на 1 эквивалент первого соединения.
[0199]
Предпочтительный конкретный пример комбинации множества соединений составляет два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия, в одном аспекте. В настоящем изобретении, "множество" обозначает, например, "два или более" и предпочтительно представляет собой "два или три" или "два," более предпочтительно "два." В другом аспекте, предпочтительный конкретный пример комбинации множества соединения представляет собой два из амида лития в качестве первого соединения и гидрида натрия в качестве второго соединения, два из амида лития в качестве первого соединения и амида натрия в качестве второго соединения, или два из амида лития в качестве первого соединения и трет-бутоксида натрия в качестве второго соединения.
[0200]
Форма основания на стадии (i) может быть любой формой при условии, что реакция протекает. Форма основания на стадии (i) может быть подходящим образом выбрана специалистом в данной области техники.
[0201]
Количество применяемого основания на стадии (i) может представлять собой произвольное соотношение при условии, что реакция протекает. Однако, с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, когда основание представляет собой гидрид щелочного металла (предпочтительно гидрид натрия), количество применяемого основания на стадии (i) составляет, например, обычно 2,0 эквивалента или более, предпочтительно 2,0 эквивалента-4,0 эквивалента, более предпочтительно 2,5 эквивалента-3,5 эквивалента, и более предпочтительно 2,5 эквивалента-3,1 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение), в одном аспекте, и, например, предпочтительно 2,8 эквивалента-3,5 эквивалента, в другом аспекте.
[0202]
С точки зрения представленного выше, когда основание представляет собой амид щелочного металла (предпочтительно амид лития), количество применяемого основания на стадии (i) составляет, например, обычно 2,0 эквивалента или более, предпочтительно 2,0 эквивалента-4,0 эквивалента, и более предпочтительно 2,5 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение), в одном аспекте, и, например, предпочтительно 2,8 эквивалента-3,5 эквивалента, в другом аспекте.
[0203]
Когда основание включает множество соединений, количество применяемого основания (общее количество применяемых соединений) на стадии (i) составляет, например, обычно 2,0 эквивалента или более, предпочтительно 2,0 эквивалента-4,0 эквивалента, и более предпочтительно 2,5 эквивалента-3,5 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение), в одном аспекте, и, например, более предпочтительно 2,8 эквивалента-3,5 эквивалента, в другом аспекте.
[0204]
Как описано выше, определение" эквивалент основания", как применяют в настоящем изобретении, является следующим, или термин "эквивалент" толкуется в соответствии со следующими примерами. Например, когда основание представляет собой моновалентное основание, такое как гидрид натрия (NaH) и амид лития (LiNH2), "1 эквивалент основания на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "1 моль основания на 1 моль соединения формулы (2) (анилиновое соединение)," и "0,5 эквивалента основания на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "0,5 моль основания на 1 моль соединения формулы (2) (анилиновое соединение)." В качестве другого примера, когда основание представляет собой двухвалентное основание, такое как гидрид кальция (CaH2), "1 эквивалент основания на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "0,5 моль основания на 1 моль соединения формулы (2) (анилиновое соединение)," и "0,5 эквивалента основания на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "0,25 моль основания на 1 моль соединения формулы (2) (анилиновое соединение)."
[0205]
Заранее определенное количество применяемого основания можно добавлять в реакцию сразу. Альтернативно, основание можно добавлять множеством порций или по каплям.
[0206]
(Третичный спирт на стадии (i))
Третичный спирт на стадии (i) включает соединение формулы (6).
[формула 25]
[0207]
где R13, R14 и R15 могут быть одинаковыми или отличными, и каждый представляет собой (C1-C6) алкил, (C3-C6) циклоалкил, (C2-C6) алкенил, (C2-C6) алкинил, (C6-C10) арил или (C6-C10) арил (C1-C4) алкил, и два, выбранные из R13, R14 и R15, могут быть соединены друг с другом, образуя кольцо.
[0208]
Примеры третичного спирта на стадии (i) включают, но не ограничиваются, трет-бутанол, 2-метил-2-бутанол, 2-метил-2-пентанол, 3-метил-3-пентанол, 3-этил-3-пентанол, 2-метил-3-бутен-2-ол, 2-метил-3-бутин-2-ол, 1-метилциклопентанол, 1-этилциклопентанол, 1-пропилциклопентанол, 1-метилциклогексанол, 1-этилциклогексанол, 1-пропилциклопентанол, 2-метиладамантанол, 3-фенил-3-пентанол, 2-фенил-2-бутанол, 2-метил-1-фенил-2-пропанол, 2-метил-1-фенил-2-бутанол, 3-бензил-3-гексанол, 2-α-нафтил-2-пропанол, и 2-метил-1- β-нафтил-2-пропанол, предпочтительно трет-бутанол, 2-метил-2-бутанол, 2-метил-2-пентанол, 3-метил-3-пентанол, 3-этил-3-пентанол, 2-метил-3-бутен-2-ол и 2-метил-1-фенил-2-пропанол, и более предпочтительно трет-бутанол, 2-метил-2-бутанол, 2-метил-3-бутен-2-ол и 2-метил-1-фенил-2-пропанол. Данные третичные спирты можно применять отдельно или в комбинации двух или более в произвольном соотношении. "Трет-бутанол" также называют "трет-бутиловым спиртом."
[0209]
Количество применяемого третичного спирта на стадии (i) может представлять собой произвольное количество при условии, что реакция протекает. Однако, с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, когда основание представляет собой гидрид щелочного металла (предпочтительно гидрид натрия), количество применяемого третичного спирта на стадии (i) составляет, например, 0,3 эквивалента или более, предпочтительно 0,3 эквивалента-4,0 эквивалента, более предпочтительно 0,4 эквивалента-2,1 эквивалента, более предпочтительно 0,5 эквивалента-2,0 эквивалента, и более предпочтительно 0,5 эквивалента-1,5 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение), в одном аспекте, и предпочтительно 0,4 эквивалента-3,2 эквивалента, более предпочтительно 0,9 эквивалента-2,1 эквивалента, и более предпочтительно 1,0 эквивалент-2,0 эквивалента в другом аспекте.
[0210]
С точки зрения того, что представлено выше, когда основание представляет собой амид щелочного металла (предпочтительно амид лития), количество применяемого третичного спирта на стадии (i) составляет, например, 0,3 эквивалента или более, предпочтительно 0,3 эквивалента-4,0 эквивалента, более предпочтительно 0,3 эквивалента-2,5 эквивалента, более предпочтительно 0,5 эквивалента-2,0 эквивалента, и более предпочтительно 0,5 эквивалента-1,5 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение), в одном аспекте, и предпочтительно 0,4 эквивалента-1,1 эквивалента в другом аспекте.
[0211]
Когда основание включает множество соединений, количество применяемого третичного спирта на стадии (i) составляет, например, 0,3 эквивалента или более, предпочтительно 0,3 эквивалента-4,0 эквивалента, и более предпочтительно 0,3 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2) (анилиновое соединение), в одном аспекте, and, например, 0,5 эквивалента-2,5 эквивалента, предпочтительно 0,5 эквивалента-2,0 эквивалента, и более предпочтительно 0,5 эквивалента-1,5 эквивалента, в другом аспекте.
[0212]
Как описано выше, определение "эквивалент третичного спирта", как применяют в настоящем изобретении, является следующим, или термин "эквивалент" толкуется в соответствии со следующими примерами. Например, "1 эквивалент трет-бутанола на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "1 моль трет-бутанола на 1 моль соединения формулы (2) (анилиновое соединение)." Например, "0,5 эквивалента трет-бутанола на 1 эквивалент соединения формулы (2) (анилиновое соединение)" обозначает "0,5 моль трет-бутанола на 1 моль соединения формулы (2) (анилиновое соединение)."
[0213]
Заранее определенное количество применяемого третичного спирта можно добавлять в реакцию сразу. Альтернативно, третичный спирт можно добавлять множеством порций или по каплям.
[0214]
(Растворитель на стадии (i))
С точки зрения плавного протекания реакции и подобных, реакцию на стадии (i) предпочтительно проводят в присутствии растворителя. Примеры растворителя на стадии (i) включают, но не ограничиваются, следующие; ароматические углеводородные производные (например, бензол, толуол, ксилол, хлорбензол и дихлорбензол), галогенированные алифатические углеводороды (например, дихлорметан и 1,2-дихлорэтан), простые эфиры (например, диэтиловый эфир, диизопропиловый эфир, циклопентилметиловый эфир (CPME), тетрагидрофуран (THF), 1,4-диоксан, моноглим и диглим), амиды (например, N, N-диметилформамид (DMF), N, N-диметилацетамид (DMAC) и N-метилпирролидон (NMP)), сульфоксиды (например, диметилсульфоксид (DMSO)), и любую их комбинацию в произвольном соотношении.
[0215]
Растворитель на стадии (i) может представлять собой любой растворитель при условии, что реакция на стадии (i) протекает. Однако, с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, предпочтительные примеры растворителя на стадии (i) включают толуол, ксилол, хлорбензол, дихлорбензол, дихлорметан, тетрагидрофуран (THF), N, N-диметилформамид (DMF), и любую их комбинацию в произвольном соотношении, более предпочтительно толуол, ксилол, хлорбензол и дихлорбензол, более предпочтительно толуол и ксилол, и более предпочтительно толуол.
[0216]
Количество растворителя, применяемого на стадии (i), может представлять собой произвольное количество при условии, что реакционная система может перемешиваться в достаточной степени. С точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, примерный диапазон представляет собой 10 л (литров) или меньше, предпочтительно 0,1-10 л, более предпочтительно 0,1-5 л, и более предпочтительно 0,5-5 л на 1 моль соединения формулы (2) (анилиновое соединение).
[0217]
(Реакционная температура на стадии (i))
С точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, когда основание представляет собой гидрид щелочного металла (предпочтительно гидрид натрия), реакционная температура на стадии (i) составляет, например, -5°C (минус 5°C)-80°C, предпочтительно -5°C-50°C, более предпочтительно 0°C-50°C и более предпочтительно 0°C-40°C, в одном аспекте, и, например, 0°C-80°C, предпочтительно 10°C-80°C, более предпочтительно 20°C-70°C, более предпочтительно 20°C-40°C, и самое предпочтительное 25°C-35°C, в другом аспекте.
[0218]
С точки зрения того, что представлено выше, когда основание представляет собой амид щелочного металла (предпочтительно амид лития), реакционная температура на стадии (i) составляет, например, -5°C (минус 5°C)-80°C, предпочтительно -5°C-50°C, более предпочтительно 0°C-50°C, и более предпочтительно 0°C-40°C, в одном аспекте, и, например, -20°C (минус 20°C)-60°C, предпочтительно -10°C-40°C, более предпочтительно 0°C-30°C, и более предпочтительно 0°C-15°C, в другом аспекте.
[0219]
Когда основание включает множество соединений, реакционная температура на стадии (i) составляет, например, -5°C (минус 5°C)-80°C, предпочтительно -5°C-50°C, более предпочтительно 0°C-50°C, и более предпочтительно 0°C-40°C в одном аспекте, и составляет, например, 0°C-80°C, более предпочтительно 0°C-60°C, более предпочтительно 10°C-80°C, более предпочтительно 20°C-70°C, более предпочтительно 20°C-40°C, и самое предпочтительное 25°C-35°C в другом аспекте. Она составляет, например, -20°C (минус 20°C)-60°C, предпочтительно -10°C-40°C, более предпочтительно 0°C-30°C, и более предпочтительно 0°C-15°C в еще другом аспекте.
[0220]
(Продолжительность реакции на стадии (i))
Продолжительность реакции на стадии (i) конкретно не ограничена. Однако, с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, продолжительность реакции составляет, например, 0,1 ч-48 ч, предпочтительно 1 ч-48 ч, более предпочтительно 1 ч-36 ч и более предпочтительно 1 ч-24 ч.
[0221]
Соединение формулы (3) можно применять в качестве исходного соединения на стадии (ii). Соединение формулы (3) можно выделять и применять в следующей стадии, дополнительно очищать и применять в следующей стадии, или применять в следующей стадии без выделения при условии, что реакции на стадии (ii) протекает. Кроме того, после завершения реакции на стадии (i), хлористоводородную кислоту или уксусную кислоту можно применять, например, для постобработки на стадии (i). Кроме того, после завершения реакции на стадии (i) через раствор можно продувать инертный газ, такой как азот, для удаления побочных продуктов (как постобработка на стадии (i)). Удаление побочных продуктов можно производить при пониженном давлении. Примеры побочных продуктов включают аммиак.
[0222]
(Продукт на стадии (i); соединение формулы (3), которое представляет собой нитрозосоединение)
[0223]
Конкретные примеры соединения формулы (3) полученного на стадии (i) включают, но не ограничиваются, следующие;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин,
N-(4-метоксифенил)-2-нитрозоанилин, и
3-хлор-2-нитрозо-N-фениланилин.
[0224]
С точки зрения полезности продукта и подобных, предпочтительные конкретные примеры соединения формулы (3) включают следующие;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин и
N-(4-метоксифенил)-2-нитрозоанилин.
С точки зрения того, что представлено выше, предпочтительный конкретный пример соединения формулы (3) представляет собой следующий;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин.
[0225]
(Стадия (ii))
[0226]
Далее буде описана стадия (ii).
[0227]
Стадия (ii) представляет собой стадию реакции соединения формулы (3) с соединением формулы (4), получая соединение формулы (5).
[0228]
[формула 26]
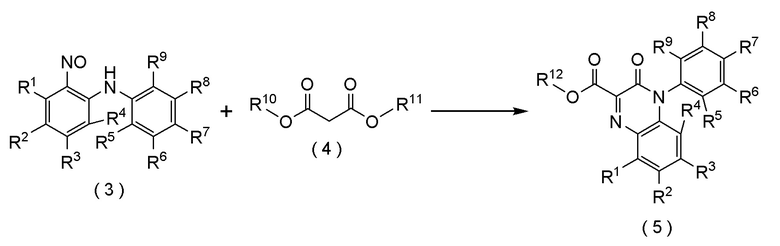
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 и R12 представляют собой, как определено выше.
[0229]
(Исходное соединение; соединение, являющееся диэфиром малоновой кислоты)
В качестве исходного соединения на стадии (ii), применяют соединение формулы (4), которое представляет собой соединение, являющееся диэфиром малоновой кислоты. Соединение формулы (4) представляет собой известное соединение, или его можно получить из известного соединения согласно известному способу.
[0230]
Примеры соединения формулы (4) включают, но не ограничиваются, диметилмалонат, диэтилмалонат, дипропилмалонат, диизопропилмалонат, дибутилмалонат, диизобутилмалонат, и ди-трет-бутилмалонат, предпочтительно диметилмалонат и диэтилмалонат.
[0231]
Применяемое количество соединения формулы (4) может представлять собой произвольное количество при условии, что реакция протекает. Применяемое количество соединения формулы (4) может быть соответствующим образом отрегулировано специалистом в данной области техники. Однако, с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, применяемое количество соединения формулы (4) составляет 1,0 моль-3,0 моль, предпочтительно 1,0 моль-2,0 моль, и более предпочтительно 1,0 моль-1,5 моль на 1 моль соединения формулы (3) (нитрозосоединение).
[0232]
(Условия стадии (ii))
Реакцию на стадии (ii) предпочтительно проводят в основных условиях. В одном аспекте, реакцию на стадии (ii) обычно проводят при pH 9 или более, предпочтительно pH 9-pH 20, и более предпочтительно pH 9-pH 14. В другом аспекте, реакцию на стадии (ii) проводят при pH 8 или более, предпочтительно pH 8-pH 20, и более предпочтительно pH 8-pH 14. В еще другом аспекте, реакцию на стадии (ii) проводят при pH 8-pH 12, предпочтительно pH 9-pH 12 и более предпочтительно pH 10-pH 12. Следовательно, pH можно регулировать до реакции на стадии (ii). Для регулирования pH, применяют кислое вещество, и, например, можно применять уксусную кислоту и хлористоводородную кислоту. Количество применяемой кислоты представляет собой количество, с которым получают требуемый pH. Следовательно, количество применяемой кислоты может подходящим образом регулировать специалист в данной области техники. Кроме того, реакцию на стадии (ii) можно проводить в присутствии основания. Основание, применяемое на стадии (ii), может представлять собой любое основание при условии, что реакция протекает.
[0233]
Примеры основания на стадии (ii) включают, но не ограничиваются, следующие;
Гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия и гидроксид калия),
гидроксиды щелочноземельных металлов (например, гидроксид магния, гидроксид кальция и гидроксид бария),
карбонаты щелочных металлов (например, карбонат лития, карбонат калия, карбонат натрия и карбонат цезия),
карбонаты щелочноземельных металлов (например, карбонат магния, карбонат кальция и карбонат бария),
гидрокарбонаты щелочных металлов (например, гидрокарбонат лития и гидрокарбонат натрия),
гидрокарбонаты щелочноземельных металлов (например, гидрокарбонат кальция), и
органические основания (например, триэтиламин, диизопропилэтиламин, 1,8-диазабицикло[5,4,0]-7-ундец-7-ен (DBU), 1,5-диазабицикло[4,3,0]нон-5-ен (DBN), 1,4-диазабицикло[2,2,2]октан (DABCO), пиридин и N, N-диметил-4-аминопиридин).
С точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, предпочтительные конкретные примеры основания на стадии (ii) включают гидроксид лития, гидроксид натрия, гидроксид калия, карбонат калия и триэтиламин.
[0234]
Данные основания на стадии (ii) можно применять отдельно или в комбинации двух или более в произвольном соотношении. Форма основания на стадии (ii) может представлять собой любую форму при условии, что реакция протекает. Форма основания на стадии (ii) может быть подходящим образом выбрана специалистом в данной области техники.
[0235]
Количество применяемого основания на стадии (ii) может представлять собой произвольное количество при условии, что реакция протекает. Однако, с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, количество применяемого основания на стадии (ii) составляет, например, обычно 1 эквивалент или более, предпочтительно 1 эквивалент-20 эквивалента, более предпочтительно 1 эквивалент-15 эквивалентов, и более предпочтительно 1 эквивалент-10 эквивалентов на 1 эквивалент соединения формулы (3) (нитрозосоединение). Однако, количество применяемого основания на стадии (ii) может быть подходящим образом подобрано специалистом в данной области техники.
[0236]
Реакция на стадии (ii) можно проводить в присутствии или отсутствии катализатора фазового переноса. Применяют ли катализатор фазового переноса или нет, может подходящим образом определить специалист в данной области техники. Примеры катализатора фазового переноса включают, но не ограничиваются, четвертичные аммониевые соли (например, бромид тетрабутиламмония (TBAB), гидросульфат тетрабутиламмония и хлорид триметилбензиламмония), четвертичные фосфониевые соли (например, бромид тетрабутилфосфония, бромид тетраоктилфосфония и бромид тетрафенилфосфония), и краун эфиры (например, 12-краун-4, 15-краун-5, и 18-краун-6).
[0237]
Когда катализатор фазового переноса применяют на стадии (ii), применяемое количество катализатора фазового переноса на стадии (ii) составляет, например, обычно 0,001 моль-0,5 моль, предпочтительно 0,005 моль-0,3 моль, на 1 моль соединения формулы (3) (нитрозосоединение).
[0238]
(Вода на стадии (ii))
Реакцию на стадии (ii) можно проводить в присутствии или отсутствии воды. Однако, реакцию на стадии (ii) предпочтительно проводят в присутствии воды. Применяемое количество воды на стадии (ii) составляет, например, обычно 0,5 моль-10,0 моль, предпочтительно 1,0 моль-5,0 моль, на 1 моль соединения формулы (3) (нитрозосоединение). Воду можно добавлять отдельно или получать из хлористоводородной кислоты, применяемое в регулировании pH выше.
[0239]
(Растворитель на стадии (ii))
С точки зрения гладкости протекания реакции и подобных, реакцию на стадии (i) предпочтительно проводят в присутствии растворителя. Растворитель, применяемое количество растворителя и подобные на стадии (ii) могут быть такими же, как на стадии (ii). Кроме того, может присутствовать вода.
[0240]
(Реакционная температура на стадии (ii))
Реакционная температура на стадии (ii) конкретно не ограничена. Однако, с точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, реакционная температура составляет, например, -10°C-80°C, предпочтительно 0°C-60°C, более предпочтительно 0°C-30°C, и более предпочтительно 0°C-20°C.
[0241]
(Продолжительность реакции на стадии (ii))
Продолжительность реакции на стадии (ii) конкретно не ограничена. С точки зрения выхода, подавления побочных продуктов, экономической эффективности и подобных, продолжительность реакции составляет, например, 0,1 ч-48 ч, предпочтительно 0,1 ч-24 ч, и более предпочтительно 0,5 ч-15 ч.
[0242]
(Постобработка и очистка)
Можно проводить Получение карбоксилата с основанием или соли, и/или получение свободной карбоновой кислоты с кислотой. Например, можно проводить операции, такие как экстракция продукта водой, экстракция продукта органическим растворителем, осаждение кристаллов кислотой и осаждение кристаллов основанием. Например, водный раствор, содержащий целевой карбоксилат натрия или карбоксилат лития или подобные, можно обработать кислотой для осаждения кристаллов целевой свободной карбоновой кислоты.
Целевой карбоксилат натрия или карбоксилат лития можно экстрагировать водой. Раствор органического растворителя, содержащий целевую свободную карбоновую кислоту или подобные, можно обработать основанием для осаждения кристаллов целевого карбоксилата натрия или карбоксилата лития. Водный раствор, содержащий целевой карбоксилат натрия или карбоксилат лития или подобные, можно обработать солью калия или солью кальция для осаждения кристаллов карбоксилата калия или карбоксилата кальция. Целевую свободную карбоновую кислоту можно экстрагировать органическим растворителем.
Кроме того, в некоторых случаях, целевой карбоксилат натрия или карбоксилат лития или целевую свободную карбоновую кислоту или их водный раствор или раствор органического растворителя можно промывать водой или органическим растворителем или любым их смешанным растворителем в произвольном соотношении, выбранном подходящим образом. Кроме того, в некоторых случаях может производиться извлечение растворителя. Например, растворитель, применяемый в реакции, можно извлекать, и можно извлекать растворитель, применяемый в постобработке и очистке.
[0243]
(Продукт на стадии (ii); соединение формулы (5), которое представляет собой хиноксалиновое соединение)
[0244]
Конкретные примеры соединения формулы (5), полученного на стадии (ii), включают, но не ограничиваются, следующие;
5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-этоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-пропоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-изопропоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-бутоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-трет-бутоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-метилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-этилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-пропилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-изопропилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-бутилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-(4-трет-бутилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
5-хлор-1-фенил-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-этоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-пропоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-изопропоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-бутоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-t-бутоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-метилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-этилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-пропилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-изопропилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-бутилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-(4-трет-бутилфенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
1-фенил-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
и
их калиевые соли, натриевые соли, литиевые соли, метиловые эфиры и этиловые эфиры.
[0245]
С точки зрения полезности продукта и подобные, предпочтительные конкретные примеры соединения формулы (5) включают следующие;
5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота и
1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота,
более предпочтительно 5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновая кислота.
[Примеры]
[0246]
Настоящее изобретение будет описано более подробно следующими примерами, но настоящее изобретение никоим образом не ограничивается данными примерами.
[0247]
Как применяют в настоящем изобретении, комнатная температура представляет собой 10°C-35°C.
[0248]
В настоящем изобретении для измерения физических свойств и выхода в примерах и сравнительных примерах можно применять следующее оборудование. Кроме того, продукты, полученные в настоящем изобретении, представляют собой известные соединения, и которые были идентифицированы и количественно определены обычными способами, известными специалистам в данной области техники.
Измерение pH; тип: HM-20P или HM-30P (изготовленный DKK-TOA CORPORATION) как индикатор концентрации ионов водорода со стеклянным электродом, и модель: 3200I (изготовленный Agilent Technologies Japan, Ltd.) в качестве электрохимического измерителя.
Анализ высокоэффективной жидкостной хроматографией (ВЭЖХ); тип: LC-2010A HT (изготовленный SHIMADZU CORPORATION).
[0249]
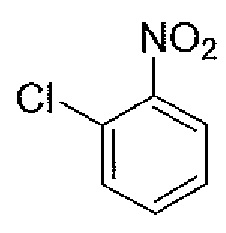
"OCNB" обозначает "2-хлорнитробензол", как показано ниже.
[формула 27]
[0250]
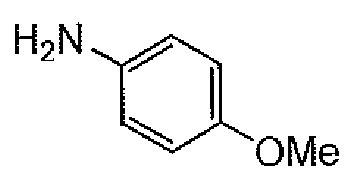
"p-A" обозначает "п-анизидин", как показано ниже.
[формула 28]
[0251]
"MNA" обозначает "N-(4-метоксифенил)-2-нитроанилин", как показано ниже.
[формула 29]
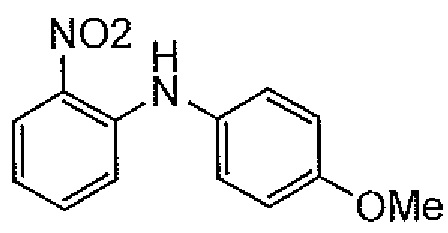
[0252]
"CMNA" обозначает "3-хлор-N-(4-метоксифенил)-2-нитроанилин", как показано ниже.
[формула 30]
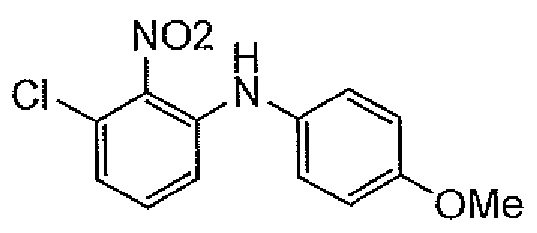
[0253]
"DMM" обозначает "диметилмалонат", как показано ниже.
[формула 31]
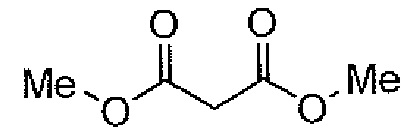
[0254]
"DEM" обозначает "диэтилмалонат", как показано ниже.
[формула 32]
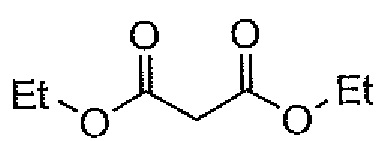
[0255]
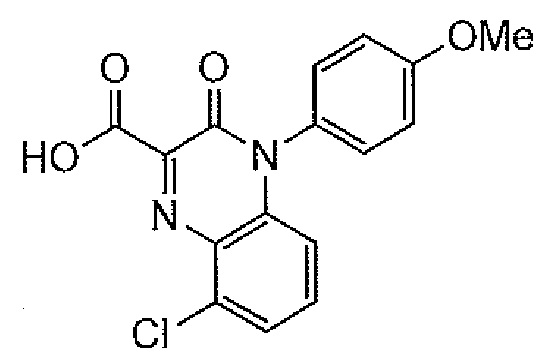
"CAQ" обозначает "5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновую кислоту", как показано ниже.
[формула 33]
[0256]
Пример 1
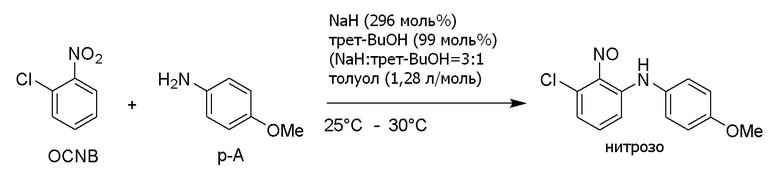
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0257]
[формула 34]
[0258]
Гидрид натрия (чистота: 65,1%, диспергированный в жидком парафине, 5,5 г, 149,2 ммоль, 296 моль%) суспендировали в толуоле (28,0 г, 0,64 л/моль) в потоке газообразного азота. Толуольный (14,0 г, 0,32 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 55-60°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы охлаждали до 25-30°C, и раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%) и 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенных в толуоле (14,0 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0259]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 50,7%,
OCNB (исходное соединение): 0,6%,
п-анизидин (исходное соединение): 0,1%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 31,1%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 2,4%.
[0260]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 53,5% (выход),
OCNB (исходное соединение): 0,8% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 25,0%.
[0261]
Примеры 2-4
Реакцию и анализ проводили так же, как в примере 1, за исключением того, что количество трет-бутанола заменяли, как показано в таблице 1. Результаты показаны в таблице 1. Кроме того, результаты примера 1 также представлены в таблице 1.
[0262]
[Таблица 1]
No
эквиваленты)
[0263]
Пример 5
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0264]
[формула 35]
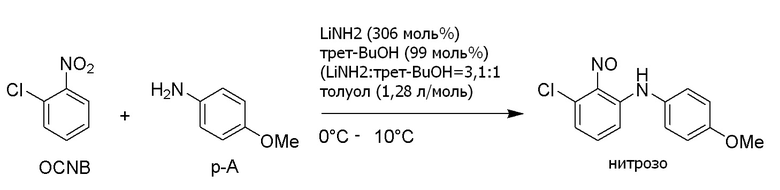
[0265]
Амид лития (чистота: 95,0%, 3,72 г, 153,9 ммоль, 306 моль%) суспендировали в толуоле (28,0 г, 0,64 л/моль) в потоке газообразного азота. Толуольный (14,0 г, 0,32 л/моль) раствор трет-бутанола (3,7 г, 49,9 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, и раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%) и 2-хлорнитробензол (7,9 г, 50,1 ммоль, 100 моль%), растворенные в толуоле (14,0 г, 0,32 л/моль) прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0266]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 67,6%,
OCNB (исходное соединение): 11,2%,
п-анизидин (исходное соединение): 1,7%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 6,6%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 3,0%.
[0267]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 74,9% (выход),
OCNB (исходное соединение): 4,3% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 2,8%.
[0268]
Примеры 6-10
Реакцию и анализ проводили так же, как в примере 5, за исключением того, что количество амида лития и количество трет-бутанола заменяли, как показано в таблице 2. Результаты показаны в таблице 2. Кроме того, результаты примера 5 также представлены в таблице 2. Видно, что выход увеличивается при соответствующей корректировке количества применяемых основания и трет-бутанола.
[0269]
[Таблица 2]
(эквиваленты)
N.D=не обнаруживали
[0270]
Пример 11
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0271]
[формула 36]
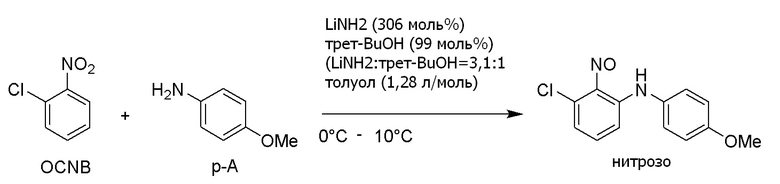
[0272]
Амид лития (чистота: 95,0%, 3,72 г, 153,9 ммоль, 306 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,7 г, 49,9 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,96 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0273]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 80,9%,
OCNB (исходное соединение): 1,1%,
п-анизидин (исходное соединение): 0,2%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 5,2%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 3,4%.
[0274]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 75,0% (выход),
OCNB (исходное соединение): следы (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 1,9%.
[0275]
Пример 12
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0276]
[формула 37]

[0277]
Амид лития (чистота: 95,0%, 3,72 г, 153,9 ммоль, 306 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,7 г, 49,9 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (11,8 г, 74,9 ммоль, 149 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,96 л/моль) прикапывали в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0278]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 73,5%,
OCNB (исходное соединение): 14,4%,
п-анизидин (исходное соединение): 0,3%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 3,3%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 2,1%.
[0279]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 84,1% (выход),
OCNB (исходное соединение): 48,0% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 1,1%.
[0280]
Пример 13
Получение N-(4-метоксифенил)-2-нитрозоанилина
[0281]
[формула 38]
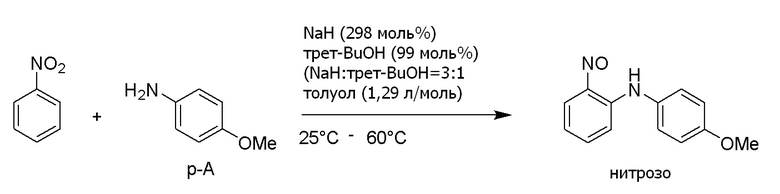
[0282]
Гидрид натрия (чистота: 65,1%, диспергированный в жидком парафине, 5,5 г, 149,2 ммоль, 298 моль%) суспендировали в толуоле (28,0 г, 0,65 л/моль) в потоке газообразного азота. Толуольный (14,0 г, 0,32 л/моль) раствор трет-бутанола (3,7 г, 49,9 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 55°C-60°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы охлаждали до 25-30°C, и раствор п-анизидина (6,2 г, 50,0 ммоль, 100 моль%) и нитробензола (6,2 г, 50,0 ммоль, 100 моль%), растворенных в толуоле (14,0 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0283]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 56,1%,
нитробензол (исходное соединение): 20,8%,
п-анизидин (исходное соединение): 0,7%.
[0284]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 51,3% (выход),
нитробензол (исходное соединение): 18,4% (степень извлечения).
[0285]
Пример 14
Получение N-(4-Метоксифенил)-2-нитрозоанилина
[0286]
[формула 39]
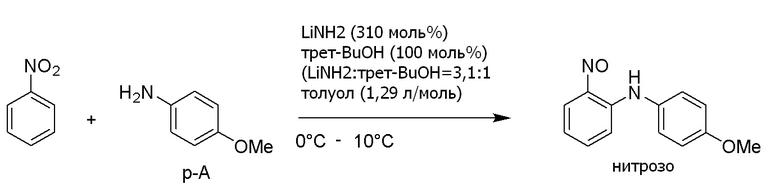
[0287]
Амид лития (чистота: 95,0%, 3,75 г, 155,2 ммоль, 310 моль%) суспендировали в толуоле (28,1 г, 0,65 л/моль) в потоке газообразного азота. Толуольный (14,0 г, 0,32 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, и раствор п-анизидина (6,2 г, 50,0 ммоль, 100 моль%) и нитробензола (6,2 г, 50,0 ммоль, 100 моль%), растворенных в толуоле (14,0 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 55,1%,
нитробензол (исходное соединение): 12,7%,
п-анизидин (исходное соединение): 0,5%.
[0288]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 44,6% (выход),
нитробензол (исходное соединение): 30,3% (степень извлечения).
[0289]
Согласно примерам 1-14, целевое нитрозосоединение можно получить, не требуя экстремально низких температур. Кроме того, согласно примерам 1-14, применяемое количество анилинового соединения, исходного соединения, можно уменьшить.
[0290]
Пример 15
Получение 5-Хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновой кислоты
[0291]
[формула 40]
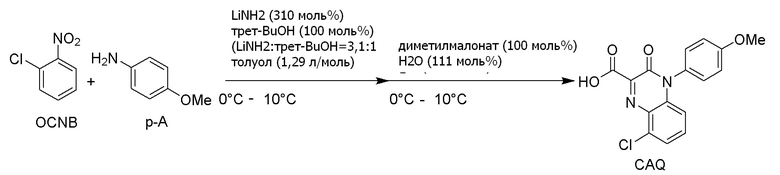
[0292]
Стадия (i)
Амид лития (чистота: 95,0%, 7,50 г, 310,3 ммоль, 311 моль%) суспендировали в толуоле (56,1 г, 0,65 л/моль) в потоке газообразного азота. Толуольный (28,0 г, 0,32 л/моль) раствор трет-бутанола (7,4 г, 99,8 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Раствор п-анизидина (12,3 г, 99,9 ммоль, 100 моль%) и 2-хлорнитробензола (15,8 г, 100,3 ммоль, 100 моль%), растворенных в толуоле (28,0 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч. Получали реакционную смесь, содержащую целевое промежуточное соединение 3-хлор-N-(4-метоксифенил)-2-нитрозоанилин.
[0293]
Стадия (ii)
Воду (1,8 г, 99,9 ммоль, 100 моль% (относительно п-анизидина)) прикапывали в реакционную смесь, полученную на стадии (i) выше, при температуре внутри колбы 0-10°C. Затем диэтилмалонат (16,0 г, 99,9 ммоль, 100 моль% (относительно п-анизидина)) прикапывали при той же температуре в течение 1 ч, и смесь перемешивали при той же температуре в течение 2 ч. Воду (0,2 г) добавляли в нее, и смесь дополнительно перемешивали в течение 2 ч.
[0294]
4% хлористоводородную кислоту (231,8 г) прикапывали к ней, регулируя pH раствора до 9,5. Температуру внутри колбы повышали до 35-40°C, и смесь разделялась на толуол и воду. Толуольную фазу удаляли. Полученную водную фазу промывали толуолом (43,5 г × дважды), и затем 35% хлористоводородную кислоту (31,9 г) прикапывали в водную фазу при температуре внутри колбы 25-30°. Смесь перемешивали в течение 30 мин, и затем кристаллы фильтровали. Кристаллы промывали толуолом (19,8 г) и водой (25,0 г). Полученные кристаллы сушили, получая 5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновую кислоту (21,1 г, чистота 96,4%, выход 61,4%) в качестве целевого продукта.
[0295]
Пример 16
Получение 5-Хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновой кислоты
[0296]
[формула 41]
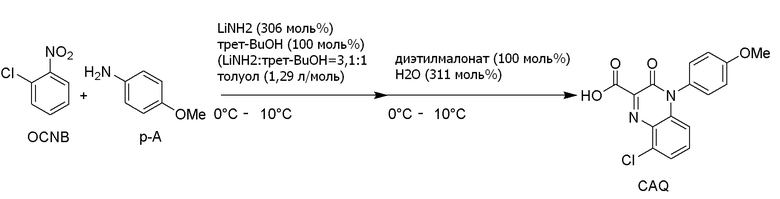
[0297]
Стадия (i)
Амид лития (чистота: 95,0%, 3,7 г, 153,1 ммоль, 306 моль%) суспендировали в толуоле (28,0 г, 0,65 л/моль) в потоке газообразного азота. Толуольный (11,0 г, 0,25 л/моль) раствор трет-бутанола (3,7 г, 49,9 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенного в толуоле (3,0 г, 0,1 л/моль), добавляли в нее, и затем раствор п-анизидина (6,2 г, 50,0 ммоль, 100 моль%), растворенного в толуоле (14,0 г, 0,3 л/моль), прикапывали в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч. Получали реакционную смесь, содержащую целевое промежуточное соединение 3-хлор-N-(4-метоксифенил)-2-нитрозоанилин.
[0298]
Стадия (ii)
Температуру внутри колбы поддерживали равной 0-10°C, и воду (2,8 г, 155,4 ммоль, 311 моль% (относительно п-анизидина)) прикапывали в реакционную смесь, полученную на стадии выше (i), в течение 15 мин. Затем диэтилмалонат (8,0 г, 50,0 ммоль, 100 моль% (относительно п-анизидина)) прикапывали при той же температуре в течение 1 ч, и смесь перемешивали при той же температуре в течение 1 ч.
[0299]
4% хлористоводородную кислоту (94,0 г) прикапывали к нему в течение 1 ч, доводя pH до 8,3. Температуру внутри колбы повышали до 35-40°C, добавляли воду (5,0 г), и затем смесь разделялась на толуол и воду. Толуольную фазу удаляли. Полученную водную фазу промывали толуолом (21,8 г×дважды), и затем 35% хлористоводородную кислоту (10,4 г) прикапывали в водную фазу при температуре внутри колбы 20-30° в течение 1 ч. Смесь перемешивали в течение 30 мин, и затем кристаллы фильтровали. Кристаллы впоследствии промывали толуолом (9,9 г) и водой (12,5 г). Полученные кристаллы сушили, получая 5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновую кислоту (11,0 г, чистота 95,7%, выход 66,5%) в качестве целевого продукта.
[0300]
Пример 17
Получение 5-Хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновой кислоты
[0301]
[формула 42]
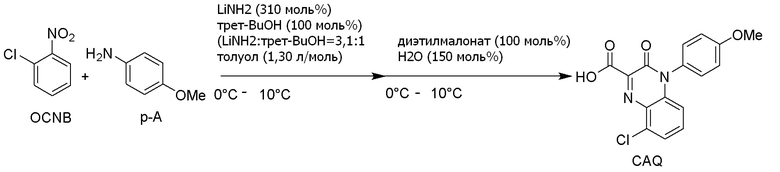
[0302]
Стадия (i)
Амид лития (чистота: 95,0%, 7,5 г, 310,3 ммоль, 311 моль%) суспендировали в толуоле (20,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (4,0 г, 0,05 л/моль) раствор трет-бутанола (7,4 г, 99,8 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (23,6 г, 149,8 ммоль, 150 моль%), растворенного в толуоле (4,0 г, 0,05 л/моль), добавляли в нее, и затем раствор п-анизидина (12,3 г, 99,9 ммоль, 100 моль%), растворенного в толуоле (84,4 г, 0,97 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 20 ч. Затем азот барботировали через реакционный раствор в течение 8 ч, удаляя аммиак. Получали реакционную смесь, содержащую целевое промежуточное соединение 3-хлор-N-(4-метоксифенил)-2-нитрозоанилин.
[0303]
Стадия (ii)
Температуру внутри колбы поддерживали равной 0-10°C, и воду (2,3 г, 149,9 ммоль, 150 моль% (относительно п-анизидина)) добавляли в реакционную смесь, полученную на стадии выше (i). Затем диэтилмалонат (16,0 г, 99,9 ммоль, 100 моль% (относительно п-анизидина)) прикапывали при той же температуре в течение 1 ч, и смесь перемешивали при той же температуре в течение 7 ч. 4% хлористоводородную кислоту прикапывали к ней в течение 1 ч, доводя pH до 8,1. Температуру внутри колбы повышали до 35-40°C, добавляли воду (5,0 г), и затем смесь разделялась на толуол и воду. Толуольную фазу удаляли. Полученную водную фазу промывали толуолом (43,5 г×дважды), и затем 35% хлористоводородную кислоту (20,8 г) прикапывали в водную фазу при температуре внутри колбы 20-30° в течение 1 ч. Смесь перемешивали в течение 30 мин, и затем кристаллы фильтровали. Кристаллы впоследствии промывали толуолом (19,8 г) и водой (25,0 г). Полученные кристаллы сушили, получая 5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновую кислоту (25,40 г, чистота 98,0%, выход 75,3%) в качестве целевого продукта.
[0304]
Пример 18
Получение 5-Хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновой кислоты
[0305]
[формула 43]
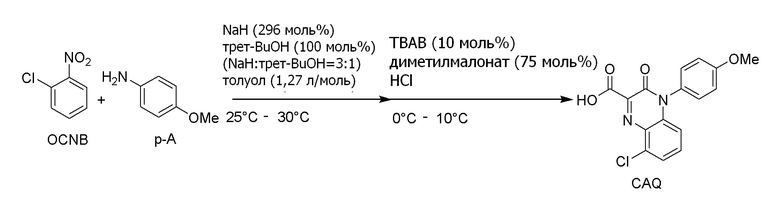
[0306]
Гидрид натрия (чистота: 65,1%, диспергированный в жидком парафине, 10,9 г, 295,7 ммоль, 296 моль%) суспендировали в толуоле (56,1 г, 0,65 л/моль) в потоке газообразного азота. Толуольный (27,0 г, 0,31 л/моль) раствор трет-бутанола (7,4 г, 99,8 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 55-60°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы охлаждали до 25-30°C, и раствор 2-хлорнитробензола (16,5 г, 104,7 ммоль, 105 моль%) и п-анизидина (12,3 г, 99,9 ммоль, 100 моль%), растворенных в толуоле (27,0 г, 0,31 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 2 ч. Реакционную смесь, содержащую целевое промежуточное соединение 3-хлор-N-(4-метоксифенил)-2-нитрозоанилин получали.
[0307]
Стадия (ii)
Температуру внутри колбы охлаждали до 0°C-10°C, и затем 35% хлористоводородную кислоту (26,0 г) прикапывали до достижения pH 9,7. Добавляли TBAB (3,2 г, 9,9 ммоль, 10 моль% (относительно п-анизидина)) и диметилмалонат (9,9 г, 74,9 ммоль, 75 моль% (относительно п-анизидина)). Смесь перемешивали при той же температуре в течение 30 мин, и затем a 48% KOH водный раствор (4,3 г) прикапывали в течение 2 ч до достижения pH 13,3. Смесь перемешивали в течение 2 ч, и затем 48% KOH водный раствор (19,1 г) прикапывали в течение 3 ч. Смесь перемешивали в течение 17 ч.
[0308]
4% хлористоводородную кислоту (87,0 г) прикапывали при той же температуре в течение 1 ч, доводя pH до 7,7. Температуру внутри колбы повышали до 35-40°C, и смесь разделялась на толуол и воду. Толуольную фазу удаляли. Полученную водную фазу промывали толуолом (43,5 г×дважды), и затем 35% хлористоводородную кислоту (10,4 г) прикапывали в водную фазу при температуре внутри колбы 25-30° в течение 2 ч. Смесь перемешивали в течение 30 мин, и затем кристаллы фильтровали. Кристаллы впоследствии промывали толуолом (19,8 г) и водой (25,0 г). Полученные кристаллы сушили, получая 5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновую кислоту (13,9 г, чистота 95,2%, выход 39,9%) в качестве целевого продукта.
[0309]
Пример 19
Получение 5-Хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновой кислоты
[0310]
[формула 44]
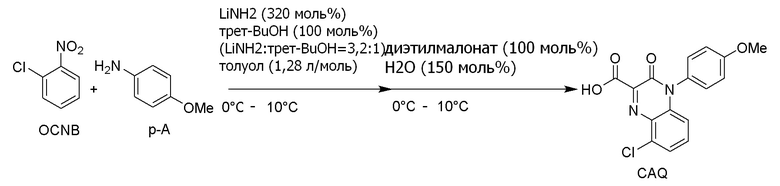
[0311]
Стадия (i)
Амид лития (чистота: 98,0%, 7,50 г, 320,1 ммоль, 320 моль%) суспендировали в толуоле (20,0 г, 0,23 л/моль) в реакционном контейнере в потоке газообразного азота. Толуольный (4,0 г, 0,05 л/моль) раствор трет-бутанола (7,4 г, 99,8 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (23,6 г, 149,8 ммоль, 150 моль%), растворенного в толуоле (4,0 г, 0,05 л/моль), добавляли в нее, и затем раствор п-анизидина (12,3 г, 99,9 ммоль, 100 моль%), растворенного в толуоле (126,2 г, 1,46 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 1 ч. Получали реакционную смесь, содержащую целевое промежуточное соединение 3-хлор-N-(4-метоксифенил)-2-нитрозоанилин.
[0312]
Стадия (ii)
Температуру внутри колбы поддерживали равной 0-10°C, и воду (2,7 г, 149,8 ммоль, 150 моль% (относительно п-анизидина)) прикапывали в реакционную смесь, полученную на стадии выше (i), в течение 30 мин. После прикапывания, аммиак удаляли при пониженном давлении. Затем диэтилмалонат (16,0 г, 99,9 ммоль, 100 моль% (относительно п-анизидина)) прикапывали при той же температуре в течение 2 ч, и смесь перемешивали при той же температуре в течение 1 ч (конечную точку определяли анализом).
[0313]
Смешанный раствор трет-бутанола (7,4 г, 99,8 ммоль, 100 моль%) и воды (75 мл, 0,8 л/моль) добавляли в другой реакционный контейнер, и температуру внутри колбы охлаждали до 0-10°C. Ранее прореагировавшую реакционную смесь и 35% хлористоводородную кислоту (23,7 г) одновременно прикапывали к нему в течение 30 мин, доводя pH до 7,8. Температуру внутри колбы повышали до 25-30°C, и 35% хлористоводородную кислоту (20,8 г) прикапывали в течение приблизительно 1 ч. Смесь перемешивали при той же температуре в течение 30 мин, и затем кристаллы фильтровали. Кристаллы впоследствии промывали толуолом (39,6 г) и водой (25,0 г). Полученные кристаллы сушили, получая 5-хлор-1-(4-метоксифенил)-2-оксо-1,2-дигидрохиноксалин-3-карбоновую кислоту (24,37 г, чистота 99,33%, выход 73,2%) в качестве целевого продукта.
[0314]
Согласно примерам 15-19, целевое хиноксалиновое соединение формулы (5) можно получить, не требуя экстремально низких температур. Кроме того, согласно примерам 15-19, применяемое количество анилинового соединения, исходного соединения, можно уменьшить.
[0315]
Пример 20
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0316]
[формула 45]
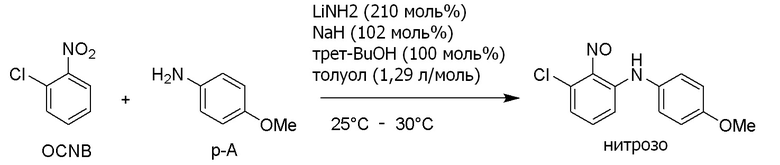
[0317]
Амид лития (чистота: 95,0%, 2,54 г, 105,1 ммоль, 210 моль%) и гидрид натрия (чистота: 66,3%, диспергированный в жидком парафине, 1,85 г, 51,1 ммоль, 102 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (11,8 г, 74,9 ммоль, 150 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем температуру внутри колбы повышали до 25°C-30°C. Температуру внутри колбы поддерживали при той же температуре, и раствор п-анизидина (6,16 г, 50,0 ммоль, 100 моль%), растворенного в толуоле (42,1 г, 0,97 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 1 ч.
[0318]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 68,2%,
OCNB (исходное соединение): 14,8%,
п-анизидин (исходное соединение): 0,1%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 8,7%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 2,1%.
[0319]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 81,0% (выход),
OCNB (исходное соединение): 45,9% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 6,9%.
[0320]
Пример 21
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0321]
[формула 46]
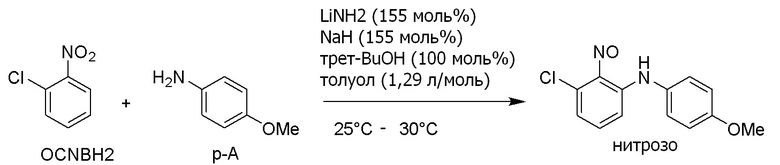
[0322]
Амид лития (чистота: 95,0%, 1,87 г, 77,4 ммоль, 155 моль%) и гидрид натрия (чистота: 66,3%, диспергированный в жидком парафине, 2,81 г, 77,6 ммоль, 155 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (11,8 г, 74,9 ммоль, 150 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем температуру внутри колбы повышали до 25°C-30°C. Температуру внутри колбы поддерживали при той же температуре, и раствор п-анизидина (6,16 г, 50,0 ммоль, 100 моль%), растворенного в толуоле (42,1 г, 0,97 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 1 ч.
[0323]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 51,0%,
OCNB (исходное соединение): 13,2%,
п-анизидин (исходное соединение): 0,2%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 23,0%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 3,5%.
[0324]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 57,9% (выход),
OCNB (исходное соединение): 45,4% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 20,0%.
[0325]
Пример 22
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0326]
[формула 47]
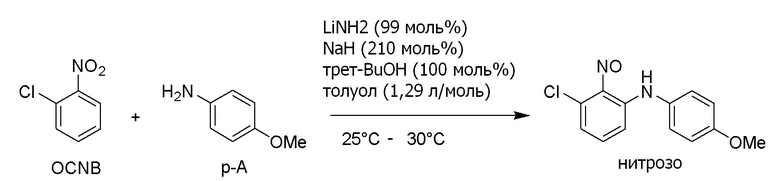
[0327]
Амид лития (чистота: 95,0%, 1,2 г, 49,7 ммоль, 99 моль%) и гидрид натрия (чистота: 66,3%, диспергированный в жидком парафине, 3,8 г, 105,0 ммоль, 210 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (11,8 г, 74,9 ммоль, 150 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем температуру внутри колбы повышали до 25°C-30°C. Температуру внутри колбы поддерживали при той же температуре, и раствор п-анизидина (6,16 г, 50,0 ммоль, 100 моль%), растворенного в толуоле (42,1 г, 0,97 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 1 ч.
[0328]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 42,8%,
OCNB (исходное соединение): 12,2%,
п-анизидин (исходное соединение): 0,3%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 28,1%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 5,4%.
[0329]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 51,7% (выход),
OCNB (исходное соединение): 44,8% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 26,0%.
[0330]
Пример 23
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0331]
[формула 48]
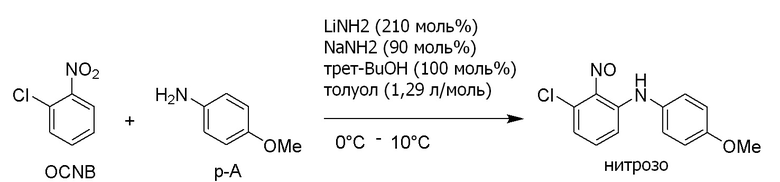
[0332]
Амид лития (чистота: 98,0%, 2,46 г, 105,0 ммоль, 210 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, и раствор 2-хлорнитробензола (11,8 г, 74,9 ммоль, 150 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль) добавляли в нее. Затем добавляли амид натрия (чистота: 90,0%, 1,95 г, 45,0 ммоль, 90 моль%), и раствор п-анизидина (6,16 г, 50,0 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,97 л/моль), прикапывали в течение 4 ч. Смесь перемешивали при той же температуре в течение 17 ч.
[0333]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 53,9%,
OCNB (исходное соединение): 14,2%,
п-анизидин (исходное соединение): 0,2%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 18,8%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 3,5%.
[0334]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 61,6% (выход),
OCNB (исходное соединение): 48,1% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 16,2%.
[0335]
Пример 24
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0336]
[формула 49]
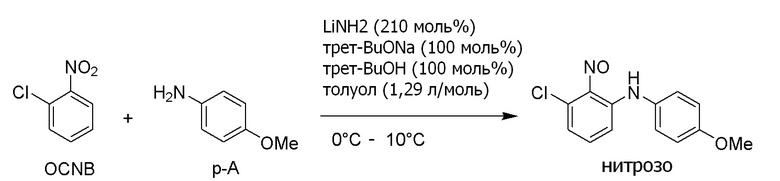
[0337]
Амид лития (чистота: 98,0%, 2,46 г, 105,0 ммоль, 210 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, и раствор 2-хлорнитробензола (11,8 г, 75,0 ммоль, 150 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее. Затем добавляли трет-бутоксид натрия (чистота: 98,0%, 4,91 г, 50,1 ммоль, 100 моль%), и раствор п-анизидина (6,16 г, 50,0 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,97 л/моль) прикапывали в течение 4 ч. Смесь перемешивали при той же температуре в течение 17 ч.
[0338]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 47,5%,
OCNB (исходное соединение): 21,8%,
п-анизидин (исходное соединение): 0,1%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 18,7%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 1,9%.
[0339]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 54,9% (выход),
OCNB (исходное соединение): 70,4% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 15,2%.
[0340]
Пример 25
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0341]
[формула 50]
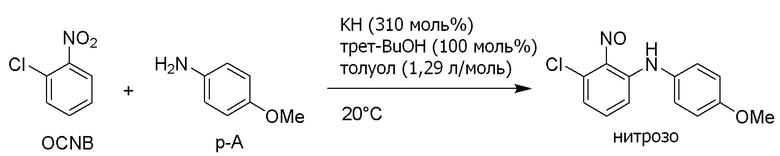
[0342]
Гидрид калия (чистота: 30,0%, 20,72 г, 155,0 ммоль, 310 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, и раствор 2-хлорнитробензола (11,82 г, 75,0 ммоль, 150 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль) добавляли в нее. Температуру внутри колбы повышали до 20°C, и раствор п-анизидина (6,16 г, 50,0 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,97 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0343]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 42,6%,
OCNB (исходное соединение): 11,3%,
п-анизидин (исходное соединение): N.D,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 28,3%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 6,7%.
[0344]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 52,0% (выход),
OCNB (исходное соединение): 41,7% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 26,4%.
[0345]
Пример 26
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0346]
[формула 51]
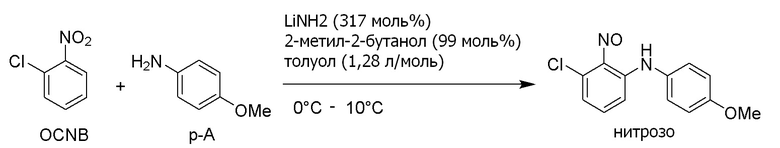
[0347]
Амид лития (чистота: 99,0%, 3,7 г, 160,0 ммоль, 317 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор 2-метил-2-бутанола (4,4 г, 49,9 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,96 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0348]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные, были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 78,2%,
OCNB (исходное соединение): 0,2%,
п-анизидин (исходное соединение): 0,1%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 4,1%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 1,7%.
[0349]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 74,0% (выход),
OCNB (исходное соединение): следы,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 3,0%.
[0350]
Пример 27
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0351]
[формула 52]
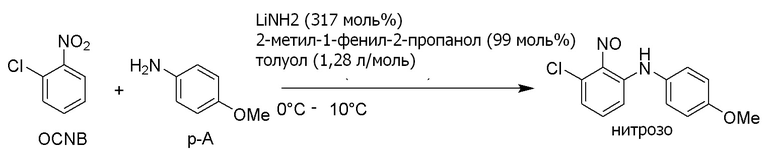
[0352]
Амид лития (чистота: 99,0%, 3,7 г, 160,0 ммоль, 317 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор 2-метил-1-фенил-2-пропанола (7,5 г, 49,9 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,96 л/моль), прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0353]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 66,8%,
OCNB (исходное соединение): 0,4%,
п-анизидин (исходное соединение): 0,1%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 7,9%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 0,3%.
[0354]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 65,7% (выход),
OCNB (исходное соединение): 1,3% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 5,9%.
[0355]
Пример 28
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0356]
[формула 53]
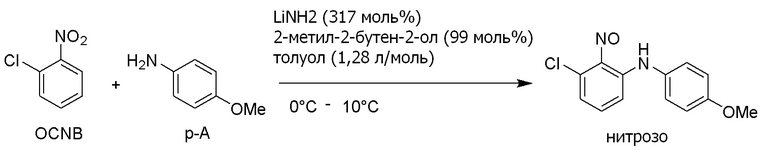
[0357]
Амид лития (чистота: 99,0%, 3,7 г, 160,0 ммоль, 317 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор 2-метил-3-бутен-2-ола (4,3 г, 49,9 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль) добавляли в нее, и затем раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%), растворенного в толуоле (42,0 г, 0,96 л/моль) прикапывали в течение 3 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0358]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 71,9%,
OCNB (исходное соединение): 2,5%,
п-анизидин (исходное соединение): 0,1%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 5,8%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 1,8%.
[0359]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 78,8% (выход),
OCNB (исходное соединение): 3,0% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 4,8%.
[0360]
Пример 29
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина (2-метил-3-фенил-1-пропанола)
[0361]
[формула 54]

[0362]
Гидрид натрия (чистота: 66,3%, диспергированный в жидком парафине, 5,4 г, 149,2 ммоль, 296 моль%) суспендировали в толуоле (28,0 г, 0,64 л/моль) в потоке газообразного азота. Толуольный (14,0 г, 0,32 л/моль) раствор 2-метил-3-бутен-2-ола (4,3 г, 49,9 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 55-60°C в течение 30 мин, и смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы охлаждали до 25-30°C, и раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%) и 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенных в толуоле (14,0 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0363]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 55,0%,
OCNB (исходное соединение): 2,5%,
п-анизидин (исходное соединение): 0,4%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 28,8%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 3,5%.
[0364]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 45,0% (выход),
OCNB (исходное соединение): 6,2% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 18,0%.
[0365]
Пример 30
Получение 3-Хлор-2-нитрозо-N-фениланилина
[0366]
[формула 55]
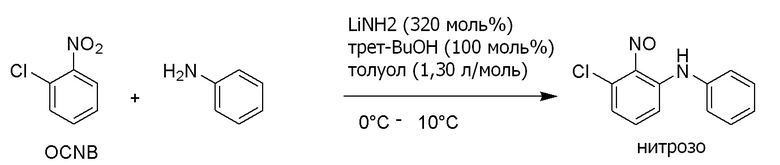
[0367]
Амид лития (чистота: 99,0%, 3,7 г, 160,0 ммоль, 320 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль) добавляли в нее, и затем раствор анилина (4,65 г, 49,9 ммоль, 100 моль%), растворенного в толуоле (42,1 г, 0,97 л/моль) прикапывали в течение 30 мин. Смесь перемешивали при той же температуре в течение 20 ч.
[0368]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-2-нитрозо-N-фениланилин (целевой продукт): 89,5%,
анилин (исходное соединение): N.D,
OCNB (исходное соединение): 1,6%.
[0369]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-2-нитрозо-N-фениланилин (целевой продукт): 91,5% (выход),
OCNB (исходное соединение): 5,0% (степень извлечения).
[0370]
Пример 31
Получение 3-Хлор-2-нитрозо-N-фениланилина
[0371]
[формула 56]
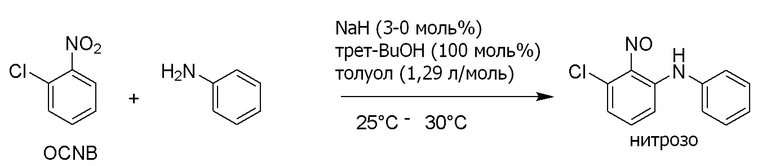
[0372]
Гидрид натрия (чистота: 66,3%, диспергированный в жидком парафине, 5,44 г, 150,3 ммоль, 300 моль%) суспендировали в толуоле (28,0 г, 0,65 л/моль) в потоке газообразного азота. Толуольный (14,0 г, 0,32 л/моль) раствор трет-бутанола (3,71 г, 50,1 ммоль, 100 моль%) прикапывали к нему при температуре внутри колбы 55-60°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы охлаждали до 25-30°C, и раствор анилина (4,66 г, 50,0 ммоль, 100 моль%) и 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенных в толуоле (14,0 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0373]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-2-нитрозо-N-фениланилин (целевой продукт): 54,9%,
OCNB (исходное соединение): 2,2%,
анилин (исходное соединение): N.D.
[0374]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-2-нитрозо-N-фениланилин (целевой продукт): 55,0% (выход),
OCNB (исходное соединение): 6,8% (степень извлечения).
[0375]
Согласно примерам 20-31, целевое нитрозосоединение можно получить, не требуя экстремально низких температур. Кроме того, согласно примерам 20-31, применяемое количество анилинового соединения, исходного соединения, можно снизить.
[0376]
Сравнительный пример 1
Реакцию и анализ проводили так же, как в примере 1, за исключением того, что трет-бутанол (трет-BuOH) не применяли.
[0377]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 0,5%,
OCNB (исходное соединение): 82,6%,
п-анизидин (исходное соединение): 11,6%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 2,7%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 0,3%.
[0378]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): следы (выход),
OCNB (исходное соединение): 94,6% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): следы.
[0379]
Сравнительный пример 2
Реакцию и анализ проводили так же, как в примере 5, за исключением того, что трет-BuOH не применяли.
[0380]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): N.D,
OCNB (исходное соединение): 87,4%,
п-анизидин (исходное соединение): 12,6%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): N.D,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): N.D.
[0381]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): N.D (выход),
OCNB (исходное соединение): 100% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): N.D.
[0382]
Сравнительный пример 3
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0383]
[формула 57]
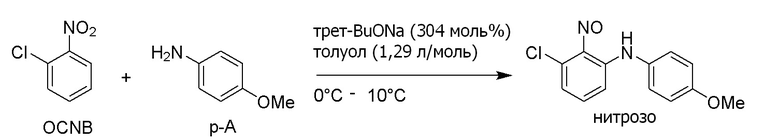
[0384]
трет-Бутоксид натрия (чистота: 98,0%, 5,96 г, 60,8 ммоль, 304 моль%) суспендировали в толуоле (16,8 г, 0,97 л/моль) в потоке газообразного азота. Суспензию перемешивали при температуре внутри колбы 0-10°C в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, и раствор п-анизидина (2,46 г, 20,0 ммоль, 100 моль%) и 2-хлорнитробензола (3,15 г, 20,0 ммоль, 100 моль%), растворенных в толуоле (5,6 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч.
[0385]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 36,7%,
OCNB (исходное соединение): 17,6%,
п-анизидин (исходное соединение): 2,4%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 29,7%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 5,7%.
[0386]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 30,6%(выход),
OCNB (исходное соединение): 43,3% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 17,0%.
[0387]
Сравнительный пример 4
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0388]
[формула 58]

В потоке газообразного азота, трет-бутоксид лития (чистота: 97,0%, 12,8 г, 155,1 ммоль, 308 моль%) суспендировали в толуоле (42,0 г, 0,96 л/моль), и суспензию перемешивали при температуре внутри колбы 0°C-10°C в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, и раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%) и 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенных в толуоле (14,0 г, 0,32 л/моль), прикапывали к нему в течение 1 ч. Смесь перемешивали при той же температуре в течение 20 ч. Когда анализ проводили тем же способом, как в примере 1, целевое нитрозосоединение получали в небольшом количестве, и оставалась большая часть непрореагировавших исходных соединений.
[0389]
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 0,6%,
OCNB (исходное соединение): 76,9%,
п-анизидин (исходное соединение): 22,0%.
[0390]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): следы (выход),
OCNB (исходное соединение): 100,0% (степень извлечения).
[0391]
Сравнительный пример 5
Способ, описанный в Tetrahedron (2016) 8252-8260 (Непатентная литература 2)
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0392]
[формула 59]
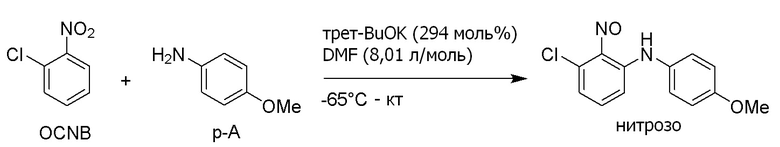
В потоке газообразного азота, температуру внутри колбы охлаждали до -65°C, и трет-бутоксид калия (чистота: 97,0%, 3,4 г, 29,4 ммоль, 294 моль%) суспендировали в N, N-диметилформамиде (DMF) (60,0 мл, 6,0 л/моль). Как результат, смесь замерзала. Температуру внутри колбы поддерживали при той же температуре, раствор п-анизидина (1,23 г, 10,0 ммоль, 100 моль%), растворенного в N, N-диметилформамиде (10,0 мл, 1,0 л/моль), добавляли в нее, и затем прикапывали раствор 2-хлорнитробензола (1,58 г, 10,0 ммоль, 100 моль%), растворенного в N, N-диметилформамиде (10,0 мл, 1,0 л/моль). Смесь перемешивали при той же температуре в течение 30 мин. Затем охлаждающую баню удаляли, и температуру повышали до комнатной температуры в течение 30 мин. Смесь перемешивали при комнатной температуре в течение 50 мин, и затем реакционную смесь выливали в насыщенный водный раствор хлорида аммония (250,0 мл), с последующей экстракцией этилацетатом (100,0 мл). Полученный органический слой впоследствии промывали водой (50,0 мл) и насыщенным соляным раствором (50,0 мл), получая этилацетатный раствор, содержащий целевой продукт.
[0393]
Как результат ВЭЖХ анализа (процент площади; 254 нм) полученного этилацетатного раствора, основные компоненты были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 29,3%,
OCNB (исходное соединение): 0,7%,
п-анизидин (исходное соединение): 0,9%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 15,0%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 0,1%.
[0394]
Полученный этилацетатный раствор анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 30,5%,
OCNB (исходное соединение): 0,7%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 11,3%.
[0395]
Сравнительный пример 6
Реакцию и последующую обработку проводили тем же способом, как описано в Tetrahedron (2016) 8252-8260 (непатентная литература 2), за исключением того, что реакционную температуру заменяли на комнатную.
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0396]
[формула 60]
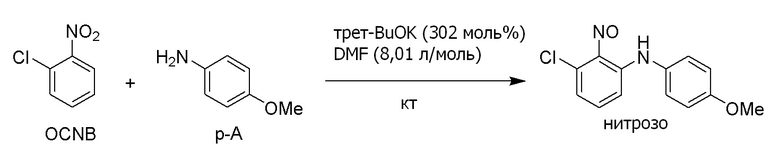
[0397]
трет-Бутоксид калия (чистота: 97,0%, 3,4 г, 29,4 ммоль, 302 моль%) суспендировали в N, N-диметилформамиде (60,0 мл, 6,01 л/моль) в потоке газообразного азота. Раствор п-анизидина (1,2 г, 9,7 ммоль, 100 моль%), растворенного в N, N-диметилформамиде (10,0 мл, 1,00 л/моль), добавляли в нее при комнатной температуре, и затем раствор 2-хлорнитробензола (1,5 г, 9,5 ммоль, 98 моль%), растворенного в N, N-диметилформамиде (10,0 мл, 1,00 л/моль), прикапывали при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь выливали в насыщенный водный раствор хлорида аммония (250,0 мл), с последующей экстракцией этилацетатом (100,0 мл). Полученный органический слой впоследствии промывали водой (50,0 мл) и насыщенным соляным раствором (50,0 мл), получая этилацетатный раствор, содержащий целевой продукт.
[0398]
Как результат ВЭЖХ анализа (процент площади; 254 нм) полученного этилацетатного раствора, основные компоненты были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 7,3%,
OCNB (исходное соединение): 3,6%,
п-анизидин (исходное соединение): 1,4%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 1,6%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 0,1%.
[0399]
Полученный этилацетатный раствор анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 0,5%,
OCNB (исходное соединение): 10,8%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 1,2%.
[0400]
Сравнительный пример 7
Способ, описанный в Synlett (2015) 1352-1356 (непатентная литература 1)
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0401]
[формула 61]
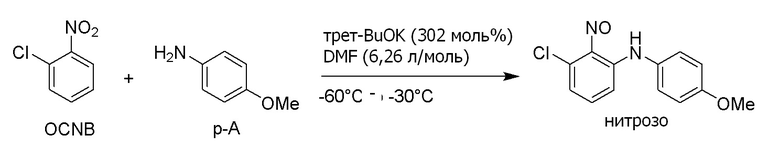
В потоке газообразного азота, температуру внутри колбы охлаждали до -60°C, и трет-бутоксид калия (чистота: 97,0%, 3,4 г, 29,4 ммоль, 302 моль%) суспендировали в N, N-диметилформамиде (50,0 мл, 5,13 л/моль). Раствор п-анизидина (1,2 г, 9,7 ммоль, 100 моль%), растворенного в N, N-диметилформамиде (3,0 мл, 0,31 л/моль), добавляли в нее, и затем прикапывали раствор 2-хлорнитробензола (1,5 г, 9,5 ммоль, 98 моль%), растворенного в N, N-диметилформамиде (8,0 мл, 0,82 л/моль). Температуру внутри колбы поддерживали при той же температуре, и смесь перемешивали в течение 30 мин. Температуру внутри колбы повышали до -30°C, и смесь перемешивали в течение 1 ч. Смесь выливали в насыщенный водный раствор хлорида аммония (250,0 мл), с последующей экстракцией этилацетатом (100,0 мл). Полученный органический слой впоследствии промывали водой (50,0 мл) и насыщенным соляным раствором (50,0 мл), получая этилацетатный раствор, содержащий целевой продукт.
[0402]
Как результат ВЭЖХ анализа (процент площади; 254 нм) полученного этилацетатного раствора, основные компоненты были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 22,2%,
OCNB (исходное соединение): 7,0%,
п-анизидин (исходное соединение): 0,9%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 31,1%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 0,2%.
[0403]
Полученный этилацетатный раствор анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 18,2%,
OCNB (исходное соединение): 16,1%,
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 4,2%.
[0404]
Сравнительный пример 8
Способ, описанный в Chemistry of Heterocyclic Compounds 2018, 54(9), 875-886 (непатентная литература 3)
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
[0405]
[формула 62]
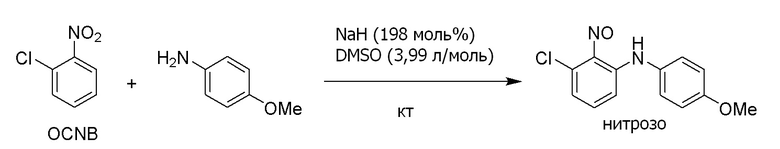
[0406]
п-Анизидин (1,23 г, 10,0 ммоль, 199 моль%) растворяли в диметилсульфоксиде (DMSO) (20,0 мл, 4,00 л/моль) в потоке газообразного азота. Гидрид натрия (66,3%, диспергированный в жидком парафине, 0,36 г, 9,95 ммоль, 198 моль%) добавляли в нее при комнатной температуре, и затем добавляли 2-хлорнитробензол (0,79 г, 5,0 ммоль, 100 моль%). Температуру внутри колбы поддерживали при комнатной температуре, и смесь перемешивали в течение 1 ч. Смесь выливали в насыщенный соляной раствор, охлажденный ледяной водой, и выпавшие кристаллы фильтровали. Полученные кристаллы растворяли в толуоле, получая толуольный раствор, содержащий целевой продукт.
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 0,5%,
OCNB (исходное соединение): 27,5%,
п-анизидин (исходное соединение): 1,5%
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 15,5%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 0,3%.
[0407]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 0,8% (выход),
OCNB (исходное соединение): 56,5% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 8,0%.
[0408]
Сравнительный пример 9
Получение 3-Хлор-N-(4-метоксифенил)-2-нитрозоанилина
Как описано выше, в способе опубликованного японского патента No. 2018-70520 (патентная литература 3), реакция 2-хлорнитробензола требует низкой температуры. В сравнительном примере 9, способ опубликованного японского патента No. 2018-70520 (Патентная литература 3) проводили с температурой реакция, измененной на 25-30°C, избегая данную низкую температуру. Как результат, низкой выход получали, как описано ниже. В способе опубликованного японского патента No. 2018-70520 (патентная литература 3), данную низкую температуру нельзя было избежать.
[0409]
[формула 63]
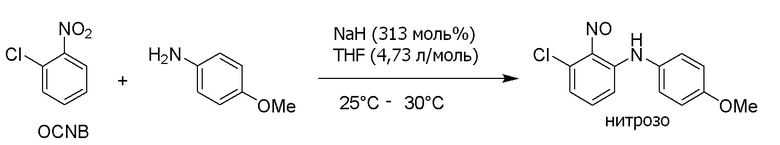
[0410]
Гидрид натрия (66,3%, диспергированный в жидком парафине, 0,36 г, 9,95 ммоль, 313 моль%) суспендировали в THF (5 мл, 1,58 л/моль). В потоке газообразного азота, раствор п-анизидина (1,17 г, 9,50 ммоль, 299 моль%), растворенного в THF (5 мл, 1,58 л/моль), добавляли при поддержании температуры внутри колбы равной 55-60°C, и смесь перемешивали при той же температуре в течение 2 ч. Смесь охлаждали до комнатной температуры. Отдельно, 2-хлорнитробензол (0,50 г, 3,17 ммоль, 100 моль%) растворяли в THF (5 мл, 1,58 л/моль) в потоке газообразного азота. Смесь, полученную заранее, применяя п-анизидин и гидрид натрия, добавляли в нее при температуре внутри колбы 25-30°C, и полученную смесь перемешивали при той же температуре в течение 2 ч. Смесь выливали в насыщенный водный раствор хлорида аммония. Затем смесь подвергали экстракции этилацетатом. Полученный органический слой промывали насыщенным соляным раствором, получая этилацетатный раствор, содержащий целевой продукт.
Как результат ВЭЖХ анализа (процент площади; 254 нм) реакционной смеси, основные компоненты в реакционной смеси, исключая растворитель и подобные были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 23,4%,
OCNB (исходное соединение): 0,9%,
п-анизидин (исходное соединение): N.D
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 34,5%,
CMNA (побочный продукт; нитро производное, соответствующее целевому продукту): 2,1%.
[0411]
Реакционную смесь анализировали способом абсолютной калибровочной кривой ВЭЖХ, получая выход и подобные. Результаты анализа были следующими;
3-хлор-N-(4-метоксифенил)-2-нитрозоанилин (целевой продукт): 31,0% (выход),
OCNB (исходное соединение): 3,8% (степень извлечения),
MNA (побочный продукт; соединение с замещением Cl (соединение с удалением Cl)): 34,8%.
[0412]
Сравнительный пример 10
Получение 3-хлор-N-(4-метоксифенил)-2-нитрозоанилина
Реакцию и анализ проводили так же, как в примере 5, за исключением того, что вторичный спирт (2-пропанол, то есть, 2-пропанол) применяли вместо третичного спирта (трет-бутанол).
[0413]
[формула 64]
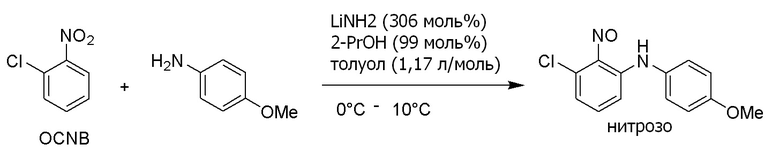
[0414]
Амид лития (чистота: 95,0%, 3,72 г, 153,9 ммоль, 306 моль%) суспендировали в толуоле (10,0 г, 0,23 л/моль) в потоке газообразного азота. Толуольный (2,0 г, 0,05 л/моль) раствор 2-пропанола (2,99 г, 49,8 ммоль, 99 моль%) прикапывали к нему при температуре внутри колбы 0-10°C в течение 30 мин, и затем смесь перемешивали при той же температуре в течение 30 мин. Температуру внутри колбы поддерживали при той же температуре, раствор 2-хлорнитробензола (7,9 г, 50,1 ммоль, 100 моль%), растворенного в толуоле (2,0 г, 0,05 л/моль), добавляли в нее, и затем прикапывали раствор п-анизидина (6,2 г, 50,3 ммоль, 100 моль%), растворенного в толуоле (37,0 г, 0,85 л/моль). После прикапывания, температуру повышали до 50°C или более, и генерировали черный дым. Следовательно, реакция прекращалась.
[0415]
Как показано в сравнительных примерах 1-4 и 9-10, видно, что когда один из третичного спирта и основания не применяют, целевое нитрозное соединение формулы (3) не может быть получено или получается с низким выходом.
Как показано в сравнительных примерах 5-8, даже если к исходным соединениям, имеющим комбинацию заместителей гербицида фенхинотриона, применяли способы предшествующего уровня техники, реакции не протекали в достаточной степени. В итоге было подтверждено, что соответствующий уровень техники не может быть применен к получению гербицида фенхинотрион.
Например, как показано в сравнительном примере 8, соответствующий уровень техники, способный производить нитрозосоединение, не требуя экстремально низких температур, не обеспечивает удовлетворительный выход при применении к получению гербицида фенхинотриона.
[Промышленная применимость]
[0416]
Согласно настоящему изобретению, обеспечивают промышленно предпочтительные способы получения соединения формулы (3) и соединения формулы (5). Соединение формулы (3) и соединение формулы (5), которые можно получить способами настоящего изобретения, являются пригодными в качестве промежуточных соединений для агрохимии и медицины, особенно в качестве промежуточных соединений для гербицидов. Кроме того, способы настоящего изобретения подходят для получения в крупных масштабах, таких как экспериментальная установка или промышленное получение. Другими словами, способы настоящего изобретения являются экономичными, а также экологически безопасными и имеют высокую ценность для промышленного применения. Таким образом, настоящее изобретение имеет высокую промышленную применимость.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ДИПИРИДО-ДИАЗЕПИНА И ИХ ФАРМАКОЛОГИЧЕСКИ ПЕРЕНОСИМЫЕ СОЛИ, ОБЛАДАЮЩИЕ БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2024522C1 |
| МОСТИКОВЫЕ ХИРАЛЬНЫЕ МЕТАЛЛОЦЕНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1992 |
|
RU2081876C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО АРОМАТИЧЕСКОГО АМИДА КАРБОНОВОЙ КИСЛОТЫ | 2012 |
|
RU2556004C2 |
| ФТОРАЛКИЛИРУЮЩИЙ АГЕНТ | 2015 |
|
RU2716008C2 |
| ПРОИЗВОДНЫЕ ДИПИРИДО-ДИАЗЕПИНА И ИХ ГИДРАТЫ, ОБЛАДАЮЩИЕ БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2040527C1 |
| ПРОИЗВОДНЫЕ ЦИКЛОАЛКАНО-ПИРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1997 |
|
RU2194698C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАРИЛЦИКЛОАЛКИЛПРОИЗВОДНЫХ | 2005 |
|
RU2414459C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИПРИЕМЛЕМЫХ СОЛЕЙ | 1990 |
|
RU2026296C1 |
| БИЦИКЛИЧЕСКИЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ И КОСМЕТИЧЕСКАЯ КОМПОЗИЦИИ | 1996 |
|
RU2138474C1 |
| 1-ОКСА-3-АЗАДИБЕНЗОАЗУЛЕНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОДУЦИРОВАНИЯ ФАКТОРА НЕКРОЗА ОПУХОЛИ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ | 2003 |
|
RU2323222C2 |
Изобретение относится к способу получения соединения формулы (3), которое является пригодным в качестве промежуточного продукта для производства физиологически активных органических соединений, таких как агрохимикаты, лекарственные средства и т.д. Способ включает реакцию соединения формулы (1) с соединением формулы (2) с применением третичного спирта и основания. Основание представляет собой соединение, выбранное из гидридов щелочных металлов и амидов щелочных металлов, или множества соединений, включающих основание, содержащее литий, в качестве первого соединения, и второе соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований. Реакцию проводят в присутствии растворителя, где растворитель содержит толуол, ксилол, хлорбензол, дихлорбензол или их смесь, при -5°C-80°C. Каждый R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил или (C1-C4) алкокси. Предлагаемый способ не требует очень низкой температуры и является экономичным и экологически чистым. Изобретение относится также к способу получения соединения формулы (5). 2 н. и 27 з.п. ф-лы, 2 табл., 31 пр.
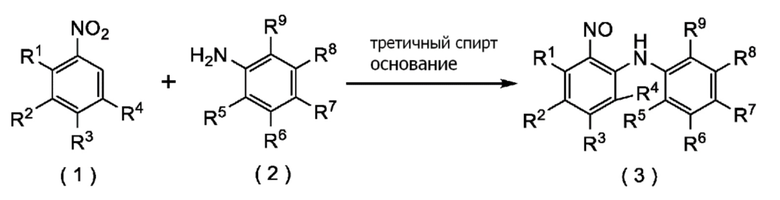
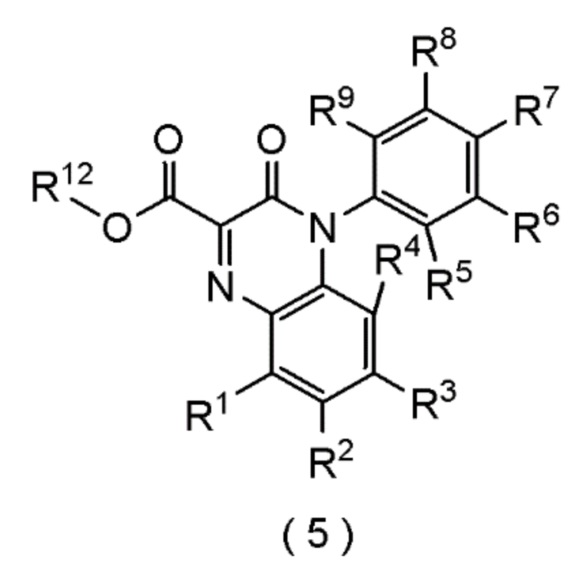
1. Способ получения соединения формулы (3), включающий реакцию соединения формулы (1) с соединением формулы (2), применяя третичный спирт и основание:
[формула 1]
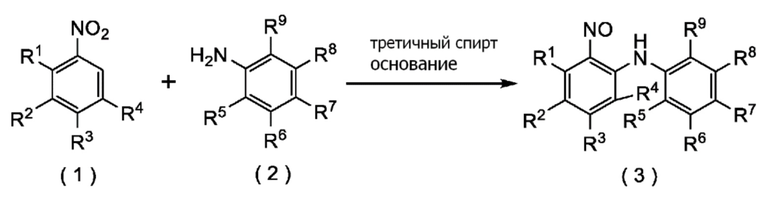 ,
,
где каждый R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил или (C1-C4) алкокси,
где основание представляет собой соединение, выбранное из гидридов щелочных металлов и амидов щелочных металлов, или множества соединений, включающих основание, содержащее литий, в качестве первого соединения, и второе соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований,
где реакцию проводят в присутствии растворителя,
где растворитель содержит толуол, ксилол, хлорбензол, дихлорбензол или их смесь, и
где реакцию проводят при -5°C-80°C.
2. Способ по п. 1, где реакцию соединения формулы (1) с соединением формулы (2) проводят после добавления третичного спирта и основания.
3. Способ по п. 1 или 2, где количество применяемого основания является большим, чем количество применяемого третичного спирта, в пересчете на эквиваленты.
4. Способ по любому из пп. 1-3, где основание представляет собой гидрид натрия, амид лития, два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
5. Способ по п. 4, где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2) и количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
6. Способ по любому из пп. 1-3, где основание представляет собой гидрид щелочного металла.
7. Способ по любому из пп. 1-3, где основание представляет собой гидрид натрия.
8. Способ по п. 6 или 7, где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2) и количество применяемого третичного спирта составляет 0,3 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2).
9. Способ по любому из пп. 1-3, где основание представляет собой амид щелочного металла.
10. Способ по любому из пп. 1-3, где основание представляет собой амид лития.
11. Способ по п. 9 или 10, где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2) и количество применяемого третичного спирта составляет 0,3 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2).
12. Способ по любому из пп. 1-3, где основание включает множество соединений.
13. Способ по п. 12, где множество соединений включает основание, содержащее литий, в качестве первого соединения, и второе соединение, выбранное из гидридов щелочных металлов, амидов щелочных металлов, алкоксидов, алкилметаллов, щелочных металлов и органических оснований.
14. Способ по п. 12, где множество соединений включает два из амида лития и гидрида натрия, два из амида лития и амида натрия, или два из амида лития и трет-бутоксида натрия.
15. Способ по п. 12, где множество соединений включает два из амида лития и гидрида натрия.
16. Способ по любому из пп. 12-15, где количество применяемого основания составляет 2,0 эквивалента-4,0 эквивалента на 1 эквивалент соединения формулы (2) и количество применяемого третичного спирта составляет 0,3 эквивалента-2,5 эквивалента на 1 эквивалент соединения формулы (2).
17. Способ по любому из пп. 1-16, где третичный спирт представляет собой соединение формулы (6):
[формула 2]
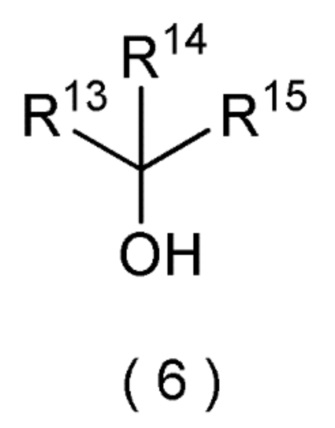 ,
,
где R13, R14 и R15 могут быть одинаковыми или отличными и каждый представляет собой (C1-C6) алкил, (C3-C6) циклоалкил, (C2-C6) алкенил, (C2-C6) алкинил, (C6-C10) арил или (C6-C10) арил (C1-C4) алкил, и два, выбранные из R13, R14 и R15, могут быть соединены друг с другом, образуя кольцо.
18. Способ по любому из пп. 1-16, где третичный спирт выбран из трет-бутанола, 2-метил-2-бутанола, 2-метил-3-бутен-2-ола и 2-метил-1-фенил-2-пропанола.
19. Способ по любому из пп. 1-18, где реакцию проводят при 0-50°C.
20. Способ по любому из пп. 1-19, где R1 представляет собой атом водорода или атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода и
R7 представляет собой атом водорода или метокси.
21. Способ по любому из пп. 1-19, где R1 представляет собой атом хлора;
каждый R2, R3 и R4 представляет собой атом водорода;
каждый R5, R6, R8 и R9 представляет собой атом водорода и
R7 представляет собой метокси.
22. Способ получения соединения формулы (5):
[формула 3]
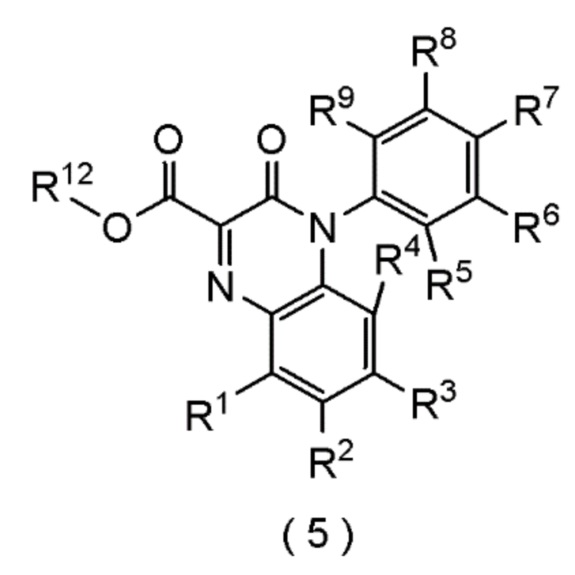 ,
,
где каждый R1, R2, R3, R4, R5, R6, R7, R8 и R9 независимо представляет собой атом водорода, атом галогена, (C1-C4) алкил или (C1-C4) алкокси и
R12 представляет собой атом водорода, атом щелочного металла или (C1-C4) алкил,
включающий следующие стадии:
стадию (i) получения соединения формулы (3) способом по любому из пп. 1-21
[формула 4]
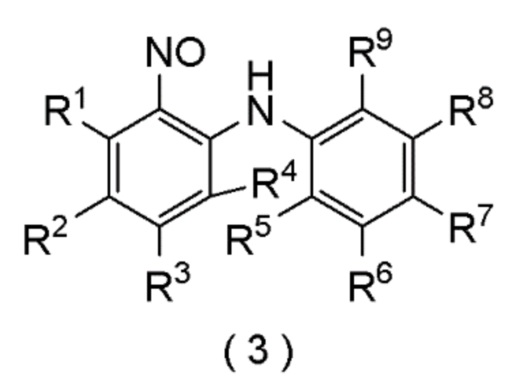 ,
,
где R1, R2, R3, R4, R5, R6, R7, R8 и R9 представляют собой, как определено выше,
стадию (ii) взаимодействия соединения формулы (3) с соединением формулы (4) с получением соединения формулы (5):
[формула 5]
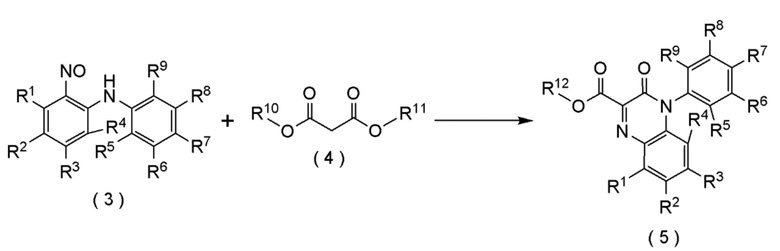 ,
,
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 и R12 представляют собой, как определено выше, и
R10 и R11 каждый независимо представляет собой (C1-C4) алкил.
23. Способ по п. 22, где реакцию на стадии (ii) проводят при pH 8 или более.
24. Способ по п. 22, где реакцию на стадии (ii) проводят при pH 8-14.
25. Способ по любому из пп. 22-24, где реакцию на стадии (ii) проводят в отсутствие катализатора фазового переноса.
26. Способ по любому из пп. 22-24, где реакцию на стадии (ii) проводят в присутствии катализатора фазового переноса.
27. Способ по любому из пп. 22-24, где реакцию на стадии (ii) проводят в присутствии воды.
28. Способ по любому из пп. 22-27, где каждый R10 и R11 представляет собой метил или этил и R12 представляет собой атом водорода, атом лития, атом натрия, атом калия, метил или этил.
29. Способ по любому из пп. 22-27, где каждый R10 и R11 представляет собой метил или этил и R12 представляет собой атом водорода.
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Z | |||
| WROBEL уе et al., Simple Synthesis of N-Aryl-2-nitrosoanilines in the Reaction of Nitroarenes with Aniline Anion Derivatives, SYNTHESIS, 2010, no | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| ПРИБОР ДЛЯ ОТБИРАНИЯ СРЕДНЕЙ ПРОБЫ ЖИДКОСТИ | 1925 |
|
SU3865A1 |
| О | |||
| П | |||
| ДЕМИДОВ и др., SNH-Ариламинирование нитрохинолинов: синтез нитро- и нитрозопроизводных ариламинохинолинов, ХИМИЯ | |||
Авторы
Даты
2023-03-09—Публикация
2020-01-31—Подача