Изобретение относится к области промышленного производства продуктов нефтехимического синтеза, в частности к процессу производства гидропероксида изопропилбензола (кумола) для последующего разложения его на фенол и ацетон.
Известен способ получения гидропероксида кумола путем жидкофазного окисления кислородом воздуха при повышенной температуре, см. Б.Д. Кружалов, Б.И. Голованенко Совместное получение фенола и ацетата. Госхимиздат, 1963. Процесс окисления ведется до содержания в реакционной массе 20-35 мас. % гидропероксида кумола.
Основным недостатком данного способа является образование существенного количества побочных продуктов.
Известны способы окисления кумола в присутствии солей металлов подгруппы цинка, а именно этилгексаноатов цинка, кадмия и ртути. В присутствии этилгексаноатов ртути и кадмия возможно получение гидропероксида изопропилбензола 19,5% и 26,7% в реакционной смеси, соответственно, см. Влияние на образование гидропероксида при окислении кумола, см. X.Э. Харлампиди, Н.М. Нуруллина, Н.Н. Батыршин Нефтехимия, 2009, том 49, №5, с. 405-408.
Недостатком является активность соединений в каталитическом распаде образовавшегося гидропероксида, а также токсичность соединений кадмия и ртути.
Наиболее близким к заявляемому объекту по технической сущности является способ получения гидропероксида изопропилбензола, заключающийся в жидкофазном окислении изопропилбензола кислородом воздуха в присутствии солей металлов непереходной валентности подгруппы цинка. [Каталитические системы на основе соединений магния и цинка в реакциях окисления алкиларенов и распада соответствующих гидропероксидов, см. X.Э. Харлампиди, Н.М. Нуруллина, Н.Н. Батыршин, Ю.X. Усманова Кинетика и катализ, 2018, том 59, №3, с. 335-339. Исследования показали, что в присутствии этилгексаноата магния концентрация гидропероксида в реакционной смеси при температуре 110°С достигает 24,3%.
Недостатком данного метода является каталитический распад образовавшегося в процессе окисления гидропероксида изопропилбензола в присутствии как индивидуальных этилгексаноатов магния и цинка, так и их смесей.
Технической проблемой изобретения является повышение содержания гидропероксида в реакционной смеси и технологических показателей процесса окисления изопропилбензола, селективности и конверсии.
Техническая проблема решается способом окисления изопропилбензола в присутствии катализатора в количестве 0,005 моль/л при температуре 120°С, отличающийся тем, что в качестве катализатора используется этилгексаноат кальция.
Решение технической проблемы позволяет увеличить конверсию изопропилбензола до 35% при селективности по гидропероксиду изопропилбензола 82%.
Каталитическое окисление изопропилбензола проводят в стеклянном барботажном реакторе при атмосферном давлении и температуре 120°С в кинетическом режиме в течение 6 часов в присутствии катализатора этилгексаноата кальция с концентрацией 0,005 моль/л.
Диапазон оптимальных температур протекания реакции от 110°С до 130°С. При более низких температурах имеет место низкое накопление гидропероксида изопропилбензола, при более высоких температурах увеличивается скорость накопления побочных продуктов.
В способе окисления изопропилбензола с получением гибропероксида в качестве катализатора берут 2-этилгексаноат кальция, который получают путем взаимодействия гидроксида кальция и 2-этилгексановой кислоты в бензоле при температуре 80°С. Катализатор представляет собой мелкокристаллическое вещество белого цвета. Молекулярная формула: (С8Н15О2)2Са, молекулярная масса соли составляет 326 г/моль.
После 6 часов окисления йодометрическим способом определяют концентрацию гидропероксида изопропилбензола в реакционной смеси, см. Антоновский В.Л., Бузланова М.М. Аналитическая химия органических пероксидных соединений. М.: Химия, 1978. 308 с. Для анализа продуктов окисления используют метод газожидкостной хроматографии.
Конверсия изопропилбензола в условиях окисления составила 34,77%, селективность по гидропероксиду изопропилбензола - 81,81%.
Для лучшего понимания изобретения приводим примеры конкретного выполнения.
Пример 1.
Окисление изопропилбензола с получением гидропероксида изопропилбензола ведут в присутствии катализатора 2-этилгексаноата кальция (Са(ЭГ)2), концентрация Са(ЭГ)2 - 0,005 моль/л в изопропилбензоле.
Процесс окисления ведут в стеклянном реакторе при перемешивании в течение 6 часов.
Полученную реакционную смесь йодометрически анализируют на содержание гидропероксида изопропилбензола, состав продуктов разложения определяют хромато графически.
Процесс окисления проводят следующим образом:
В стеклянный реактор компрессором подают очищенный и осушенный воздух, включают электрообогрев. При достижении температуры 60-65°С в реактор загружают 60 мл исходного изопропилбензола с растворенным в нем катализатором с концентрацией 0,005 моль/л. Момент достижения заданной температуры (120°С) и подачи требуемого количества воздуха (0,3 л/мин) фиксируют, как время начала эксперимента.
По истечении 6-и часов реакционную смесь йодометрически анализируют на содержание гидропероксида изопропилбензола, состав продуктов окисления определяют хроматографически.
Конверсия изопропилбензола составляет 34,77%, селективность по гидропероксиду изопропилбензола - 81,81%.
Пример 2.
Окисление проводят аналогично примеру 1, но в присутствии катализатора этилгексаноата магния, концентрация в исходной смеси составляет 0,005 моль/л. Конверсия гидропероксида составила 34,77%), селективность - 61,1%.
Пример 3.
Окисление проводят аналогично примеру 1, но в присутствии катализатора этилгексаноата цинка, концентрация в исходной смеси составляет 0,005 моль/л. Конверсия гидропероксида составила 10,86%), селективность - 66,61%.
В таблице 1 приведен состав продуктов процесса окисления изопропилбензола по прототипу и заявляемому объекту.
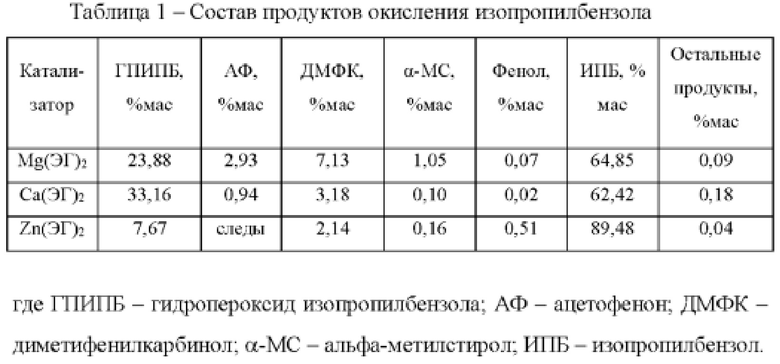
Как видно из примеров конкретного выполнения 2 и 3, совокупность признаков заявляемого способа окисления изопропилбензола с получением гидропероксида по сравнению с прототипом позволяет увеличить конверсию гидропероксида изопропилбензола до 35%, при селективности по гидропероксиду до 82%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гидропероксида изопропилбензола | 2023 |
|
RU2826579C1 |
| Способ разложения гидропероксида изопропилбензола с получением диметилфенилкарбинола | 2020 |
|
RU2750718C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛИФАТИЧЕСКИХ ИЛИ АЛКИЛАРОМАТИЧЕСКИХ ГИДРОПЕРОКСИДОВ | 1992 |
|
RU2035451C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОПЕРОКСИДОВ АЛКИЛАРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2016 |
|
RU2659403C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНОКСИДА | 2004 |
|
RU2333206C2 |
| СПОСОБ ДИСПРОПОРЦИОНИРОВАНИЯ ИЗОПРОПИЛБЕНЗОЛА С ИСПОЛЬЗОВАНИЕМ КАТАЛИЗАТОРА С МИКРОМЕЗОПОРИСТОЙ СТРУКТУРОЙ | 2006 |
|
RU2320631C1 |
| Способ получения изопропилбензола | 1980 |
|
SU910562A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОПЕРОКСИДА ЭТИЛБЕНЗОЛА | 1998 |
|
RU2128647C1 |
| Способ получения фенола | 1989 |
|
SU1839668A3 |
| СПОСОБ АЛКИЛИРОВАНИЯ БЕНЗОЛА ИЗОПРОПИЛОВЫМ СПИРТОМ ИЛИ СМЕСЬЮ ИЗОПРОПИЛОВОГО СПИРТА И ПРОПИЛЕНА | 2009 |
|
RU2525122C2 |
Изобретение относится к способу получения гидропероксида изопропилбензола. Данный способ содержит этап, на котором в реакторе окисляют изопропилбензол с растворенным в нем катализатором. При этом в качестве катализатора используют этилгексаноат кальция и окисление проводят при температуре 110-130°С. Технический результат - повышение содержания гидропероксида в реакционной смеси и технологических показателей процесса окисления изопропилбензола, селективности и конверсии. 1 табл., 3 пр.
Способ получения гидропероксида изопропилбензола, содержащий этап, на котором в реакторе окисляют изопропилбензол с растворенным в нем катализатором, характеризующийся тем, что в качестве катализатора используют этилгексаноат кальция, причем окисление проводят при температуре 110-130°С.
| Харлампиди и др., Каталитические системы на основе соединений магния и цинка в реакциях окисления алкиларенов и распада соответствующих гидропероксидов | |||
| Кинетика и катализ, 2018, 59(3), 335-339 | |||
| Усманова Ю | |||
| Х., Катализ распада гидропероксида изопропилбензола соединениями на основе непереходных металлов подгруппы кальция: дисс.канд | |||
| хим | |||
| наук/ |
Авторы
Даты
2023-03-09—Публикация
2022-05-05—Подача