ОТСЫЛКИ К РОДСТВЕННЫМ ЗАЯВКАМ
[0001] Данная заявка является частичным продолжением совместно рассматриваемой заявки № 16/224 463, поданной 18 декабря 2018 г., в которой утверждается преимущество предварительной заявки США № 62/610 575, поданной 27 декабря 2017 г., которые таким образом включены в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
1. Область техники, к которой относится настоящее изобретение:
[0002] Настоящее изобретение в целом относится к способам извлечения ионов из соляных растворов и, в частности, к способам извлечения ионов лития из соляного раствора.
УРОВЕНЬ ТЕХНИКИ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
2. Известный уровень техники:
[0003] В результате недавнего интереса к использованию литий-ионных батарей для электромобилей и стационарных аккумуляторов в области электроэнергии, связанных с системами возобновляемой энергии, извлекаемой в том числе из ветровых, солнечных и приливных источников, спрос на литий существенно увеличился и может скоро опередить предложение. Потенциально большой запас лития доступен из различных источников, таких как морская вода, соляные растворы, геотермальные жидкости и континентальные соленые озера. Используемые в настоящей заявке термины «соляной раствор» и «соляные растворы» относятся к вышеупомянутым различным литийсодержащим растворам. Однако на сегодняшний день существует несколько эффективных способов извлечения лития из указанных источников без использования значительного концентрирования путем испарения, поскольку концентрация лития в данных источниках обычно весьма низкая. Кроме того, гораздо более высокая концентрация ионов других металлов таких как, натрий, калий, кальций и магний, препятствует извлечению лития.
[0004] Ионный обмен - хорошо известная технология извлечения ионов металлов в низких концентрациях из водных растворов. Однако обычные ионообменные смолы, такие как сильнокислотные катионообменные смолы с функциональными группами сульфоновой кислоты и хелатирующие смолы с иминодиацетатными группами, имеют более высокое сродство к таким многозарядным ионам, как кальций и магний, которые могут присутствовать в представленном соляном растворе. Несмотря на то, что селективность по отношению к литию сопоставима с селективностью к другими одновалентными ионами, такими как натрий и калий, присутствие данных конкурирующих одновалентных ионов, которые чаще всего присутствуют в большом избытке в соляных растворах, делает извлечение лития невозможным.
[0005] Ранее было установлено, что неорганические ионообменные среды, такие как ионные сита на основе оксидов марганца, титана или других оксидов других металлов являются потенциально полезными для извлечения лития из соляных растворов, в которых содержатся высокие концентрации конкурирующих ионов, таких как кальций, магний, натрий и калий. Данные среды возможно назвать ионно-литиевыми ситами (LIS). LIS имеет высокое сродство к литию, потому что сайты обмена LIS настолько малы, что Na+ (0,102 нм), K+ (0,138 нм) и Ca2+ (0,100 нм), ионные радиусы которых больше, чем у Li+ (0,074 нм), не могут проникать в данные обменные сайты. Хотя ионный радиус иона Mg2+ (0,072 нм) аналогичен ионному радиусу Li+, для дегидратации ионов магния требуется большое количество энергии, чтобы позволить им проникнуть в центры обмена, для сохранения селективности относительно Mg2+.
[0006] Однако LIS имеет ряд недостатков. Во-первых, данные ионные сита имеют слабокислую природу и, как следствие, имеют пониженную емкость при более низких уровнях pH. Во-вторых, они нестабильны в кислых растворах, поскольку некоторые компоненты растворяются в кислоте. По мере разложения они теряют способность поглощать литий, следовательно их необходимо часто заменять. Замена LIS требует значительных затрат. Кроме того, удаление и замена вышедшей из строя LIS, когда она установлена в обычной колонне, трудны и требуют значительного количества времени. В заключение, LIS синтезируется в виде тонкодисперсного порошка и, следовательно, из-за высокого перепада давления не может быть использован в неподвижных слоях, что характерно для типичных ионообменных смол. Был предпринят ряд попыток улучшить форму с помощью, например, гранулирования, вспенивания, мембран, волокон и намагничивания. Однако, когда данные порошки агломерируются в более крупные геометрические формы, кинетика сильно ухудшается в результате закупорки пор и активных центров обмена связующими агентами и, как правило, из-за более низкого отношения площади поверхности к объему/массе при больших размерах частиц.
[0007] Например, статья, Chitrakar и др., Lithium Recovery from Salt Lake Brine by H2TiO3,” Dalton Transactions, 43(23), стр. 8933-8939, 21 июня 2014 г. (далее именуем «Chitrakar»), относится к синтезу, характеристике и лабораторной оценке литиевых селективных адсорбентов на основе метатитановой кислоты. Однако Chitrakar не упоминает промышленный процесс и не обсуждает вопросы, касающиеся разделения твердой и жидкой фаз или отмывки соляного раствора и элюента от адсорбента в промышленных масштабах. Например, тесты адсорбции в Chitrakar проводились в лабораторных стаканах при концентрации твердых веществ адсорбента 20 г/л, а тесты на элюирование с HCl проводились при концентрации твердых частиц адсорбента 10 г/л. Chitrakar в своей работе не раскрывает, как использовать адсорбент в непрерывном промышленном масштабе. В частности, лабораторная фильтрация, использованная в данных испытаниях, не может применяться в промышленных масштабах.
[0008] Таким образом, все еще существует потребность в улучшении способа извлечения лития из соляного с использованием литий-ионных сит, которые преодолевают указанные выше недостатки.
СУЩНОСТЬ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
[0009] В одном из вариантов осуществления настоящего изобретение обеспечивает способ извлечения ионов лития из литийсодержащего соляного раствора путем контактирования в первом реакторе с перемешиванием литийсодержащего соляного раствора с литий-ионными ситами с образованием комплекса ионов лития с литий-ионными ситами и дальнейшего извлечения ионов лития из комплекса с литиево-ионными ситами во втором реакторе с перемешиванием с образованием литий-ионных сит и кислого элюата на основе литиевой соли.
[0010] В одном из вариантов осуществления настоящего изобретения способ извлечения ионов лития из литийсодержащего соляного раствора происходит путем контактирования литийсодержащего соляного раствора с литий-ионным ситами в первом реакторе при перемешивании с образованием комплекса ионов лития с литий-ионным ситами. Далее данный процесс включает в себя стадию извлечения ионов лития из комплекса с литиево-ионными во втором реакторе при перемешивании с образованием элюата, кислого раствора соли лития, отделенного от литий-ионных сит. Литий-ионные сита могут содержать оксид титана или ниобия (например, метатитановую кислоту или ниобат лития).
[0010] Декомплексирование можно проводить путем элюирования кислотой. Концентрация кислоты может поддерживаться на постоянной с помощью добавления указанной кислоты. Концентрация кислоты должна быть менее 0,1 М и предпочтительно при pH от более 1 до менее 3 и наиболее предпочтительно при pH около 2. Среднее время контакта литий-ионного комплекса с литий-ионным ситами и кислотой может быть меньше 1 часа. Кислота может быть соляной или серной кислотой.
[0012] pH первого реактора можно поддерживать на постоянном уровне путем добавления основания. pH может поддерживаться на постоянном уровне больше 4 и меньше 9 или больше 6 и меньше 8. Основание может быть гидроксидом натрия (NaOH), гидратом аммиака, гидроксидом калия, карбонатом натрия, гидроксидом магния, гидроксидом кальция или безводным аммиаком. Например, используемое основание может быть гидроксидом натрия при его массовой концентрации менее 8%.
[0013] Более 90% литий-ионных сит могут иметь средний диаметр частиц менее 40 мкм, а более 90% литий-ионных сит могут иметь средний диаметр частиц более 0,4 мкм. Более 90% по объему частиц литий-ионных сит могут иметь диаметр менее 100 мкм и диаметр более 0,5 мкм. Более 90% по объему частиц литий-ионных сит могут иметь диаметр более 0,5 мкм. Настоящий способ может дополнительно включать стадию удаления литий-ионных сит, имеющих средний диаметр частиц менее 1 мкм, перед контактированием содержащего литий соляного раствора с литий-ионными ситами.
[0014] Настоящий способ может дополнительно включать стадии отделения комплекса лития с литий-ионными ситами из соляного раствора с помощью устройства для разделения твердой и жидкой фаз; и дальнейшее контактирование комплекса лития с литий-ионными ситами с водой перед разрушением комплекса во втором реакторе. Способ также может дополнительно включать стадии отделения литий-ионных сит от элюата, кислого раствора соли лития, с помощью устройства для разделения твердой и жидкой фаз; контактирование литий-ионных сит с водой после извлечения лития из комплекса во втором реакторе для получения регенерированных литий-ионных сит и промывки разбавленной кислотой; и добавление регенерированных литий-ионных сит в первый реактор. Данный процесс может дополнительно включать стадию удаления воды из комплекса лития с ионами литий-ионными ситами до содержания влаги менее 90% по массе перед извлечением ионов лития из комплекса с литий-ионными ситами во втором реакторе. Данный процесс может также дополнительно включать стадию осушения регенерированных литий-ионных сит перед добавлением в первый реактор. Стадия контактирования литий-ионных сит с водой может включать контактирование литий-ионных сит с достаточным количеством воды, так что более 50% ионов лития, извлеченных из комплекса с литий-ионными ситами, вымывается из литий-ионных сит перед добавлением регенерированных литий-ионных сит в первый реактор. Стадия контактирования литий-ионных сит с водой может включать контактирование литий-ионных сит с водой на нескольких стадиях противотока, так что более 50% ионов лития, извлеченных из комплекса с литий-ионными ситами, вымывается из литий-ионных сит перед добавлением регенерированных литий-ионных сит в первый реактор. Данный способ также может дополнительно включать стадию добавления разбавленной кислоты и дополнительной концентрированной кислоты во второй реактор.
[0015] Первый реактор может содержать мембраны для ультрафильтрации или микрофильтрации. Для перемешивания содержимого первого реактора можно использовать воздух или другой газ. Скорость потока через ультрафильтрационную мембрану или микрофильтрационную мембрану может быть больше 30 л/час при трансмембранном давлении менее 30 кПа.
[0016] Концентрация литий-ионных сит может быть больше 50 г/л или больше 100 г/л.
[0017] Дальнейшая область применимости настоящего изобретения станет более очевидной из подробного описания, приведенного ниже. Однако следует понимать, что подробное описание и конкретные примеры, хотя и указывают предпочтительные варианты осуществления настоящего изобретения, даны только для иллюстрации, поскольку другие различные изменения и модификации в пределах сущности и объема изобретения будут весьма очевидными для любого специалиста данной области.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0018] Настоящее изобретение станет более понятным из подробного описания, приведенного ниже, и сопроводительных чертежей, которые приведены только для иллюстрации и, таким образом, не ограничивают настоящее изобретение. На чертежах одинаковые ссылки используются для обозначения одинаковых элементов на различных видах.
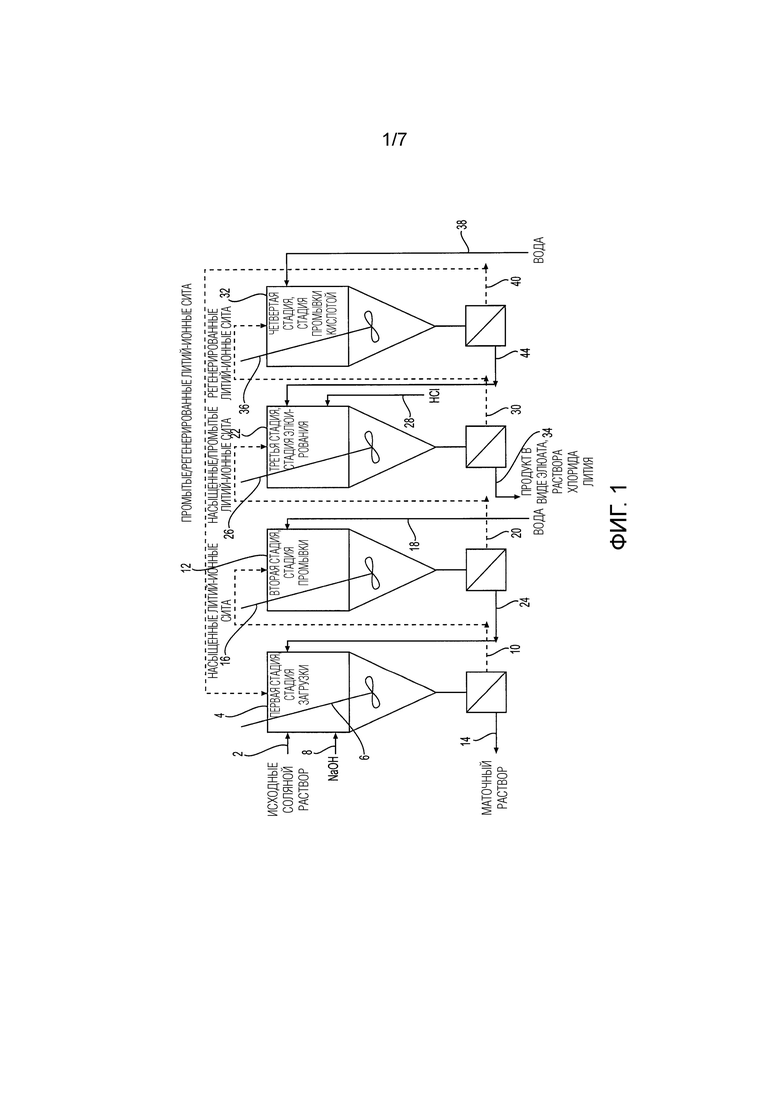
[0019] Фиг. 1 представляет собой схематический вид типичной системы выделения лития для настоящего процесса.
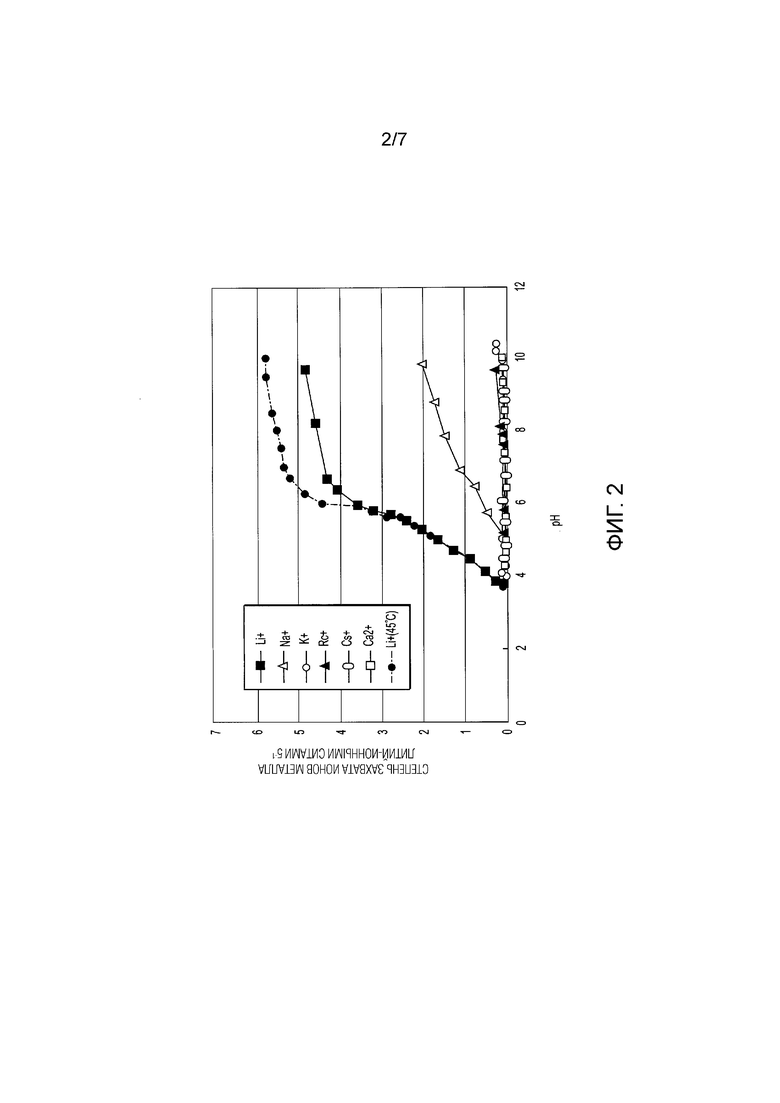
[0020] Фиг. 2 представляет собой график, показывающий степень поглощения ионов металла как функцию от pH.
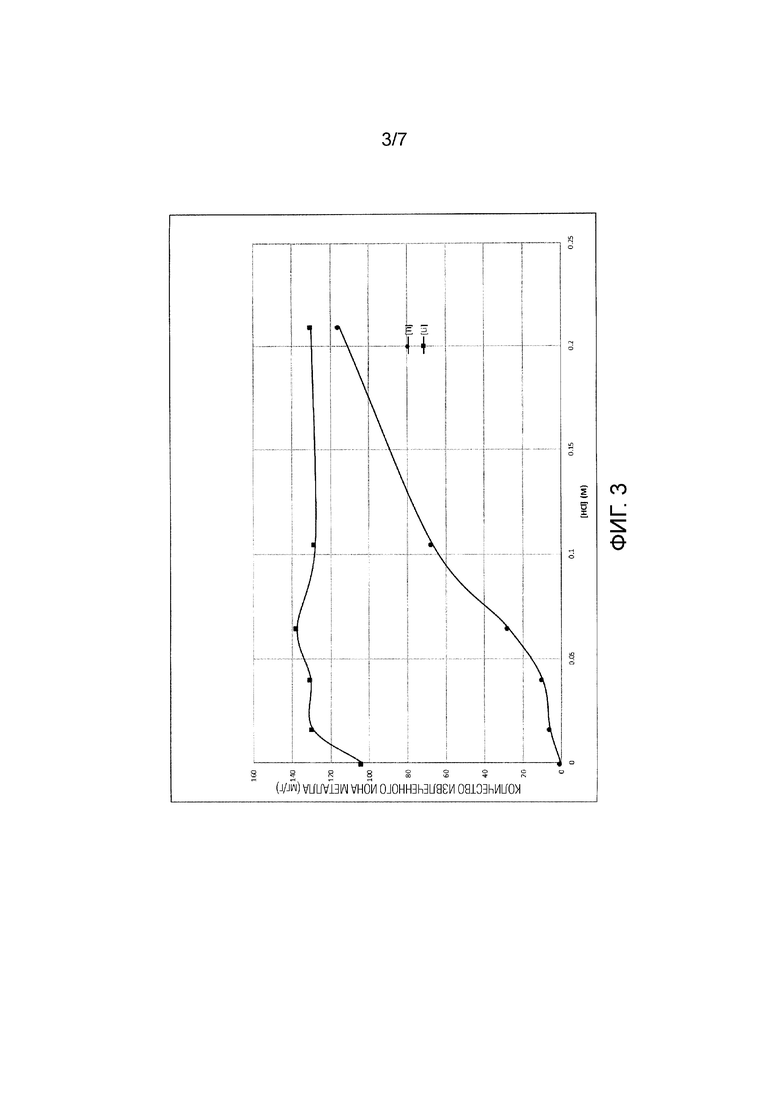
[0021] Фиг. 3 представляет собой график, показывающий количество выделенного лития и титана в зависимости от концентрации соляной кислоты.
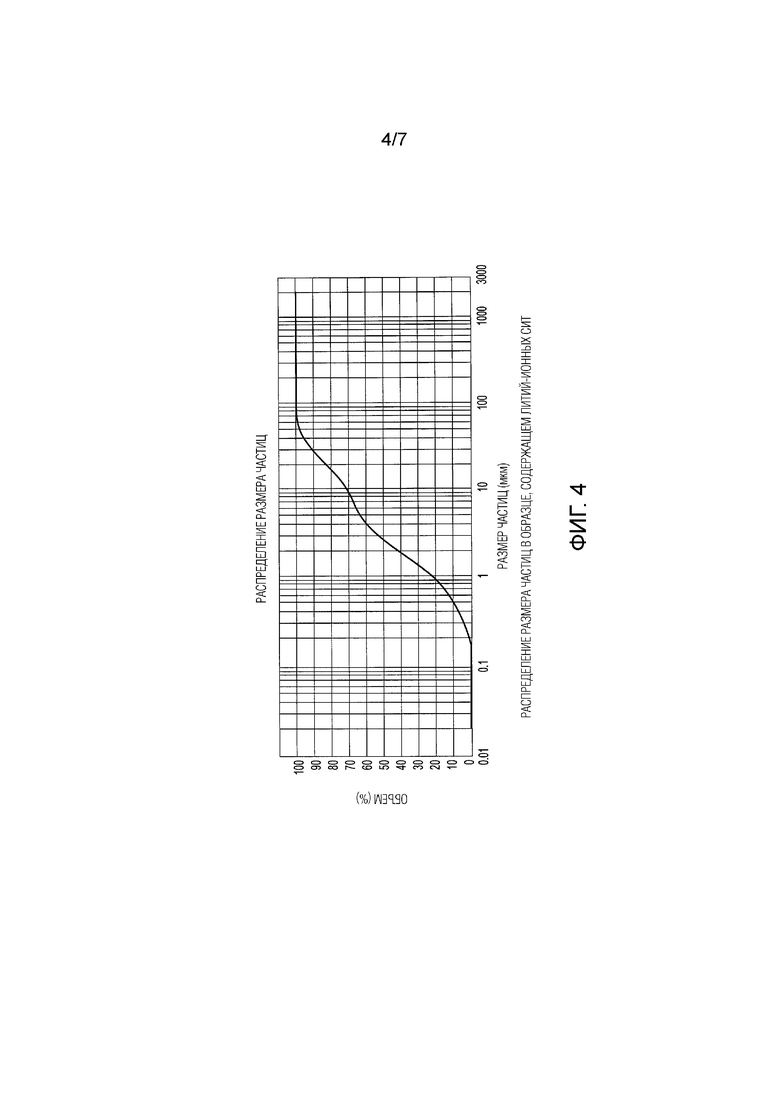
[0022] Фиг. 4 представляет собой график, показывающий типичное распределение LIS- частиц образца литий-ионных сит с применением метатитановой кислоты, взятого после нескольких часов перемешивания на воздухе в суспензии.
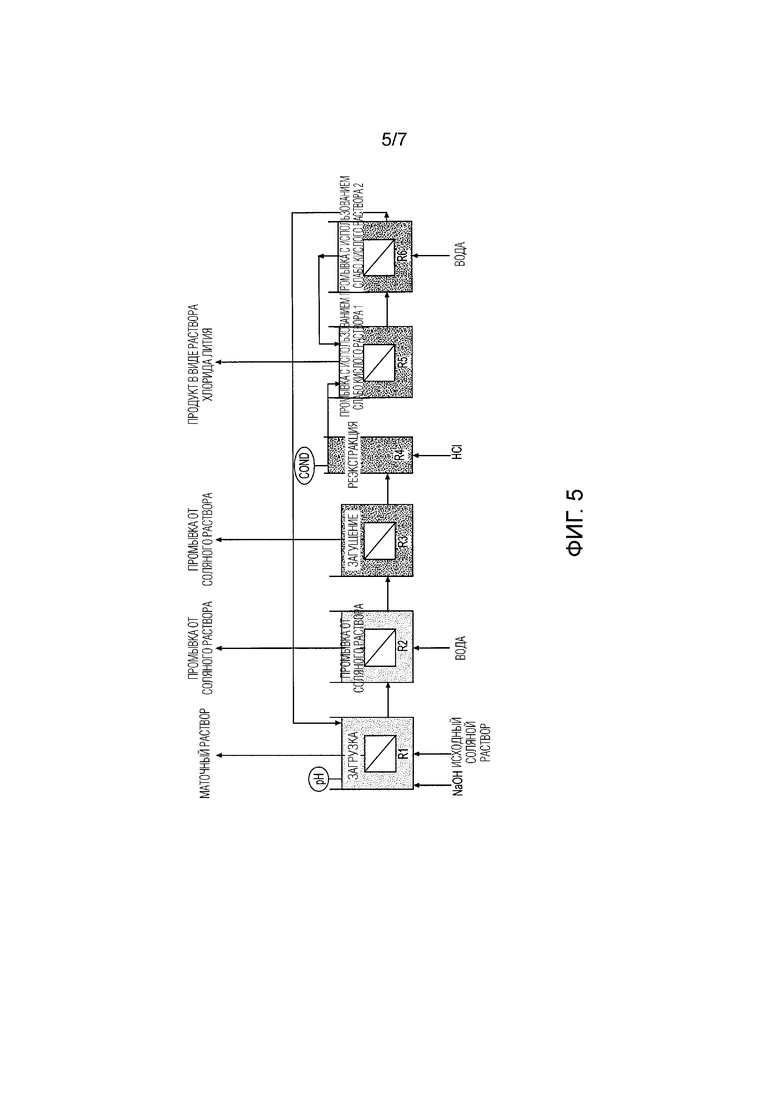
[0023] Фиг. 5 - схематический вид альтернативной системы выделения лития для настоящего процесса.
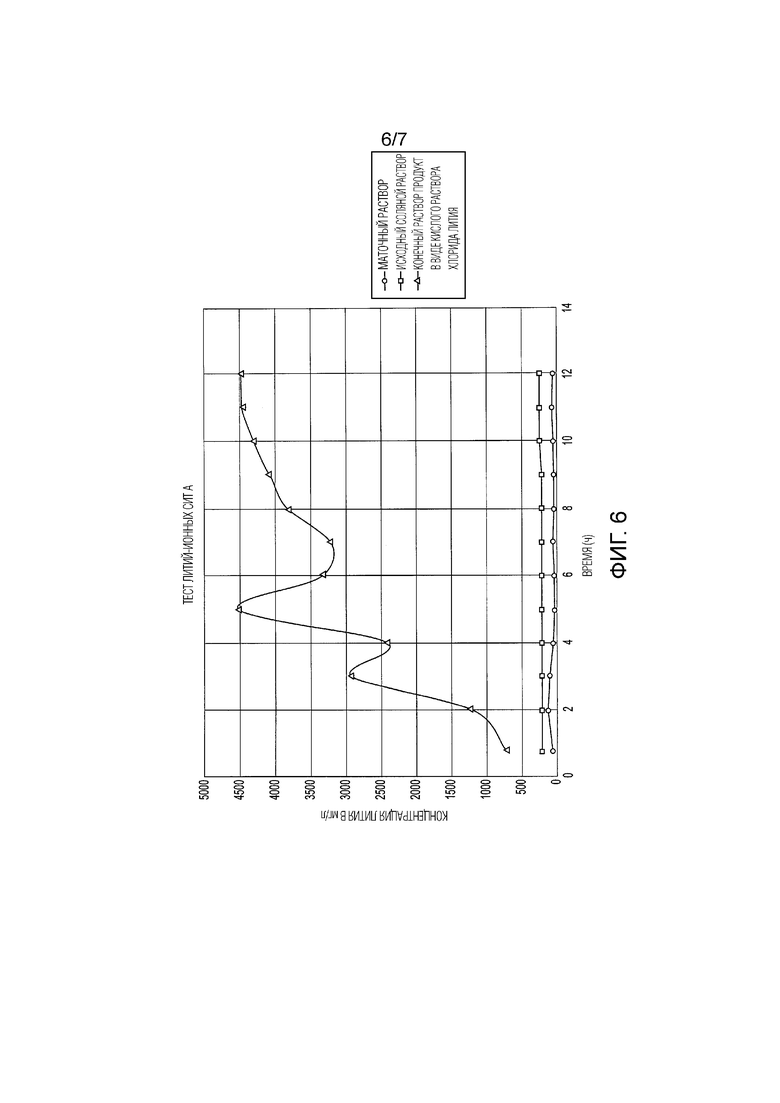
[0024] Фиг. 6 представляет собой график зависимости концентрации лития от времени для типичного опыта извлечения лития.
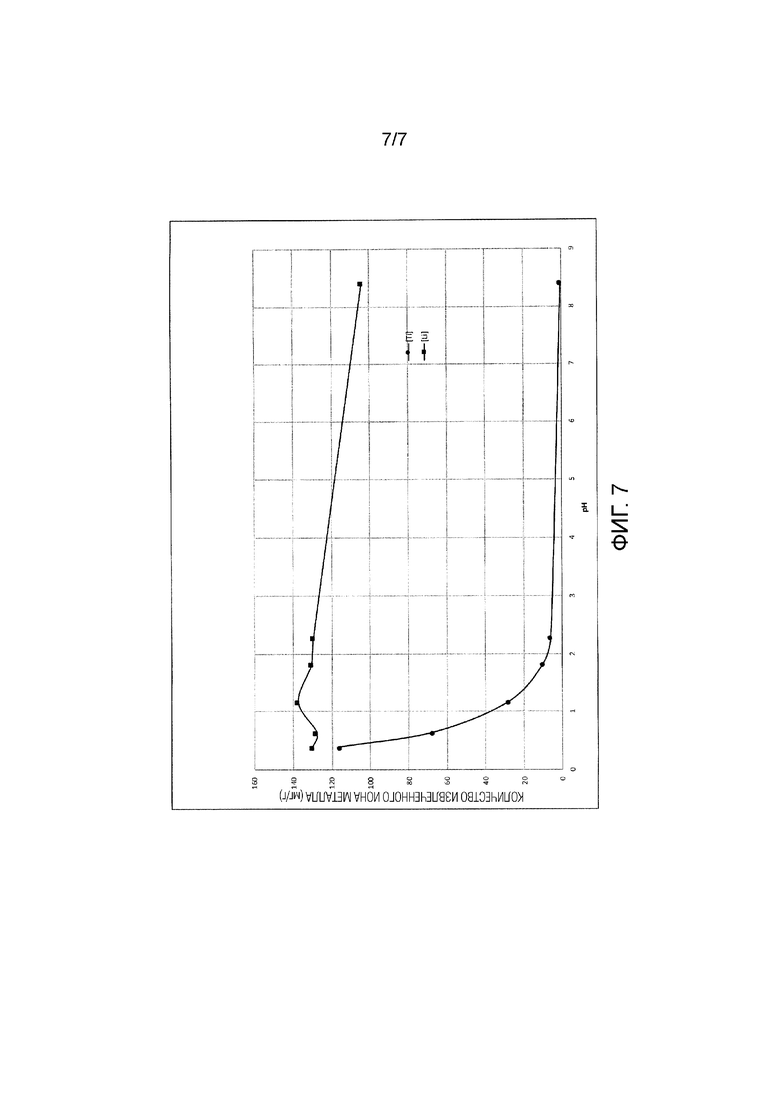
Фиг. 7 представляет собой график, показывающий количество выделенного лития и титана в зависимости от pH.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0025] В результате описанных выше недостатков литий-ионные сита до сих пор не нашли широкого применения для извлечения лития из соляного раствора в промышленных масштабах. Настоящее изобретение преодолевает данные недостатки, делая использование литий-ионных сит для селективного извлечения лития из соляного раствора более коммерчески целесообразным.
[0026] Средний диаметр частиц типичных ионообменных смол обычно составляет около 400-1250 микрометров. В процессе ионного обмена с тонким слоем, RECOFLO®, используются частицы, которые обычно считаются самыми мелкими частицами, используемыми в крупномасштабных промышленных целях. Данные частицы обычно имеют средний диаметр 100-200 микрометров.
[0027] В качестве сравнения: литий-ионные сита, используемые в настоящем изобретении, предпочтительно находятся в порошковой форме. Не обязательно ограничивать средний размер частиц порошка. Однако средний размер частиц предпочтительно составляет менее примерно 100 мкм, более предпочтительно от 10 до 100 мкм, даже более предпочтительно от 20 до 100 мкм и еще более предпочтительно от 20 до 95 мкм. Кроме того, средний размер частиц может составлять от 0,4 до 40 мкм. Например, более 90% (по объему) частиц литий-ионных сит могут иметь диаметр менее 100 мкм и диаметр более 0,5 мкм. В одном и том же или различных вариантах осуществления настоящего изобретения более 90% (по объему) частиц литий-ионных сит могут иметь диаметр более 0,5 мкм. Поскольку данные материалы производятся в виде порошков, можно избежать затрат на агломерацию. Кроме того, большая площадь поверхности, обеспечиваемая таким порошком, значительно улучшает кинетику процесса ионного обмена. Иными словами, литий-ионные сита не представляют собой композит, связанный с полимером или другим связующим агентом.
[0028] Различные литий-ионные сита потенциально полезны для извлечения лития. Примеры LIS включают, но не ограничиваются ими, оксиды марганца и титана. В частности, типичный LIS может включать оксид титана, предпочтительно метатитановую кислоту (MTA). Однако настоящее изобретение в равной степени применимо к другим типам литий-ионных сит с применением оксида марганца и ниобата лития (т.е. ниобиевая кислота кислота). Литий-ионные сита могут также содержать легирующие добавки в дополнение к оксиду титана, ниобия или марганца. Однако литий-ионные сита будут преимущественно представлять собой оксид титана, ниобия или марганца.
[0029] В одном из вариантов осуществления настоящего изобретения порошкообразные литий-ионные сита могут контактировать с литийсодержащим соляным раствором в реакторе с мешалкой (STR или реактор). Например, реактор может представлять собой емкость, содержащую жидкость, подлежащую обработке, вместе с литий-ионными ситами. Литий-ионные сита могут поддерживаться в виде суспензии с помощью смесителя или с применением псевдоожижения восходящим потоком жидкости или газа, что обеспечивает тесный контакт между литий-ионными ситами и соляным раствором. pH соляного раствора в реакторе можно поддерживать на постоянном уровне путем добавления основания, такого как гидроксид натрия (NaOH), гидроксид аммония, гидроксид калия, карбонат натрия, гидроксид магния и гидроксид кальция. Например, pH соляного раствора в реакторе можно поддерживать на уровне от более 5 до менее 9.
[0030] Множество соляных растворов, которые можно обрабатывать с помощью настоящего изобретения, содержат заметные концентрации магния. Нейтрализация соляного раствора основанием может создать некоторые проблемы для соляных растворов, содержащих высокие концентрации магния. Хотя гидроксид магния обычно не осаждается при pH ниже примерно 8, при добавлении основания локальные высокие значения pH в точке, где основание контактирует с соляным раствором, приводят к осаждению гидроксида магния. Несмотря на то, что pH основной массы соляного раствора ниже теоретического pH осаждения, осадок не растворяется быстро. Присутствие гидроксида магния вызывает ряд проблем. Например, он может прилипать к поверхности LIS, ингибируя поглощение лития. Если для разделения твердой и жидкой фаз используется мембрана, она может уменьшить поток фильтрата и, возможно, засорить мембрану.
[0031] В тех случаях, когда используется гидроксид натрия, проблема осаждения гидроксида магния становится особенно острой и более выраженной при более высоких концентрациях NaOH. При использовании 50% мас. NaOH образуются большие количества Mg(OH)2, которые не растворяются повторно. Если используется более разбавленный раствор NaOH, количество полученного Mg(OH)2 меньше, и Mg(OH)2 повторно растворяется быстрее. Если используется 4% мас. NaOH, образуются только очень небольшие количества Mg(OH)2, которые повторно растворяются всего за несколько секунд. Таким образом, в случае использования гидроксида натрия, гидроксид натрия предпочтительно должен находиться в массовой концентрации менее 8%.
[0032] Использование разбавленного раствора NaOH невыгодно, поскольку таким образом происходит разбавление маточного раствора. В случае, когда маточный раствор необходимо повторно закачать под землю, возникающий в результате чрезмерный объем соляного раствора приводит к возникновению проблем, поскольку физически не может больше соляного раствора быть закачано обратно в землю, чем было извлечено ранее.
[0033] Данной проблемы можно избежать, используя аммиак для нейтрализации. Аммиак может быть в форме безводного газообразного аммиака или жидкого гидроксида аммония, так что избыточный объем рассола незначителен. Только небольшие количества Mg(OH)2 выпадают в осадок в точке добавления, даже если используется безводный газообразный аммиак или 30% мас. гидроксид аммония, и указанный осадок повторно растворяется, не оказывая отрицательного воздействия на сам процесс.
[0034] После завершения реакции ионного обмена обедненный литием (т.е. маточный) раствор может быть отделен от литий-ионных сит и удален из реактора различными способами. Например, суспензия раствора/литий-ионных сит (т.е. насыщенный слой литий-ионных сит) может контактировать с водой в дополнительном реакторе при премешивании для удаления остаточного маточного раствора перед переходом к следующему этапу. Если размер частиц литий-ионных сит больше примерно 10 микрон, можно использовать осаждение под действием силы тяжести. Если размер частиц менее 10 микрон, можно использовать устройства фильтрации, такие как вакуумный роторный барабан или ленточные фильтры. Если размер частиц меньше 1 микрона, можно использовать мембранную фильтрацию. Возможно с успехом использовать комбинации данных устройств для разделения твердой и жидкой фаз. Одним из примеров возможного устройства для разделения твердой и жидкой фаз может быть центрифуга.
[0035] После удаления маточного раствора содержащееся в реакторе литий-ионные сита могут контактировать с элюентом. Указанный элюент может быть, среди прочего, кислотой, такой как соляная кислота (HCl) или серная кислота (H2SO4). Например, кислота может быть добавлена в концентрации менее 0,1 М, предпочтительно при pH от более 1 до менее 3 и наиболее предпочтительно при pH около 2. На основе практических данных, в отсутствие связи с какой-либо конкретной теорией, считается, что кислота элюирует (декомплексует) литий из комплекса с LIS, таким образом образуя концентрированный раствор литиевой соли, продукта, и регенерируя LIS. Используемый в настоящей заявке термин «комплекс» представляет собой комбинацию отдельных групп атомов, ионов или молекул, которые объединяются, чтобы создать один суммарный ион или молекулу. Используемый в настоящей заявке термин «декомплексирование» представляет собой акт отделения отдельных групп атомов, ионов или молекул от такого суммарного иона или молекулы. Из-за селективности литий-ионных сит по отношению к литию по сравнению с другими металлами, отношение лития к другим металлам в конечном растворе продукта может быть значительно выше, чем в исходном соляном растворе.
[0036] После регенерации литий-ионных сит, литий-ионные сита можно повторно использовать для обработки большего количества соляного раствора и извлечения большего количества лития.
[0037] В одном из вариантов осуществления настоящего изобретения процесс может осуществляться непрерывно. В таком непрерывном процессе могут потребоваться две реактора. Соляной раствор можно непрерывно подавать на стадию загрузки, на которой литий-ионные сита контактируют с соляным раствором в виде непрерывно перемешиваемой суспензии. Затем ионы лития могут быть удалены из соляного раствора путем поглощения на литий-ионных ситах, в результате чего образуется маточный раствор и комплекс ионов лития с LIS. Затем маточный раствор может быть отделен от литий-ионных сит, содержащих литий, и удален из реактора. Насыщенные литием литий-ионные сита, теперь отделенные от соляного раствора, могут быть перенесены на стадию элюирования.
[0038] Элюент можно непрерывно подавать на стадию элюирования, и литий-ионные сита, перенесенные со стадии загрузки, могут контактировать с элюентом в виде непрерывно перемешиваемой суспензии. Литий-ионные сита и жидкость разделяются, и данная отделенная жидкость (т.е. элюат) представляет собой раствор продукта, соли лития.
[0039] Содержание лития в комплексе с литий-ионными ситами, перенесенного со стадии элюирования, заметно снижается, и литий-ионные сита можно возвращать обратно на стадию загрузки для повторного использования. Таким образом, литий-ионные можно использовать многократно, и процесс можно проводить непрерывно.
[0040] В одном из вариантов осуществления настоящего изобретения могут использоваться дополнительные стадии, как показано на Фиг. 1. В частности, исходный соляной раствор течет по линии (2) в первый реактор (4) с мешалкой, который содержит литий-ионные сита, как часть стадии загрузки. Литий-ионные сита поддерживаются в виде суспензии с помощью смесителя (6). Суспензия литий-ионных сит с соляным раствором/ионами лития поддерживается при постоянном pH за счет добавления NaOH по линии (8). Литий ионные сита, насыщенные соляным раствором, проходят по линии (10) в дополнительный реактор с мешалкой. Реактор (12) как часть стадии промывки. Маточный раствор отделяется от насыщенных литий-ионных сит и проходит по линии (14). Литий-ионные сита, насыщенные соляным раствором, поддерживаются в виде суспензии с помощью смесителя (16). На стадии промывки литий-ионные сита контактируют с водой по линии (18) для промывки литий-ионных сит от соляного раствора, что, как считается, снижает перекрестное загрязнение продукта соли лития ионами загрязняющих веществ, присутствующими в исходном соляном растворе. Промытые и насыщенные литий-ионные сита текут по линии (20) во второй реактор с мешалкой (22) как часть стадии элюирования. Промывные воды отделяются от промытых и насыщенных литий-ионных сит и текут по линии (24), чтобы вернуться в первый реактор с мешалкой (4). Промытые и насыщенные литий-ионные сита поддерживаются в виде суспензии с помощью смесителя (26). На стадии элюирования промытые и насыщенные литий-ионные сита контактируют с HCl по линии (28) для элюирования ионов лития из литий-ионных сит. Концентрация кислоты во втором реакторе с мешалкой (22) поддерживается на постоянном уровне за счет добавления HCl по линии (28). Регенерированные литий-ионные сита протекают по линии (30) в другой реактор (32) с мешалкой как часть стадии промывки кислотой. Ионы лития в виде продукта LiCl отделяются от регенерированных литий-ионных сит и проходят по линии (34). Регенерированные литий-ионные сита поддерживаются в виде суспензии с помощью смесителя (36). На стадии промывки кислотой литий-ионные сита промывают от остаточной кислоты путем добавления воды по линии (38), так что исходный соляной раствор не подкисляется на стадии загрузки, когда литий-ионные сита рециркулируют, а извлеченный литий не рециркулирует обратно на стадию загрузки. Промытые и регенерированные литий-ионные сита текут по линии (40) обратно в первый реактор (4) с мешалкой для вторичного использования на стадии загрузки. Промывные воды, разбавленные кислотой, отделяются от промытых и регенерированных литий-ионных сит и проходят по линии (44) для использования вместе с дополнительной концентрированной кислотой на стадии элюирования.
[0041] В одном из вариантов осуществления настоящего изобретения несколько ступеней загрузки могут использоваться последовательно и работать противотоком. Соляной раствор можно сначала обработать на первой стадии загрузки. Обработанный соляной раствор из первой стадии загрузки, все еще содержащий некоторое количество остаточного лития, может быть передан на вторую стадию загрузки, где контакт с литий-ионными ситами дополнительно снижает содержание лития в соляном растворе. Литий-ионные сита со второй стадии загрузки, содержащие некоторое количество лития, но все еще имеющие доступную литиевую емкость, могут быть переданы на первую стадию загрузки. Насыщенные литий-ионные сита из первой стадии загрузки могут быть затем перенесены на стадию элюирования. Таким образом можно еще больше снизить содержание лития в маточном растворе. Для дальнейшего снижения содержания лития в маточном растворе таким образом можно использовать дополнительные стадии загрузки.
[0042] Насыщенные литий-ионные сита можно аналогичным образом обрабатывать на нескольких стадиях элюирования, в данном случае литий-ионные сита проходят противотоком по отношению к потоку элюата. Таким образом, можно дополнительно снизить содержание лития в литий-ионных ситах и повысить концентрацию лития в элюате (то есть в литиевом продукте).
[0043] Реакция обмена поглощения ионов лития литий-ионными ситами из соляного раствора показана в уравнении (1).
LIS.H+Li+ → LIS.Li+H+ (1)
где LIS.H обозначает литий-ионные сита непосредственно в регенерированной форме, а LIS.Li обозначает литий-ионные сита в комплексе с ионами лития непосредственно в своей насыщенной форме.
[0044] По мере протекания реакции ионы гидроксония выделяются в соляной раствор, снижая pH данного соляного раствора. Активным компонентом литий-ионных сит может быть, например, оксид титана, такой как метатитановая кислота (МТА). МТА - слабая кислота и, следовательно, имеет высокое сродство к ионам гидроксония. В результате при низком pH, где доступны ионы гидроксония, MTA может с трудом обменивать ионы водорода на литий. Литий-ионные сита могут также дополнительно содержать небольшие количества легирующих добавок.
[0045] На Фиг. 2 изображен график зависимости степени поглощения ионов металла от pH. На данном графике можно наблюдать, что поглощение лития значительно снижается при значениях рН ниже примерно 6,5, а также небольшое количество лития будет поглощаться при рН ниже примерно 4. По мере того, как насыщение литием продолжается, рН соляного падает. Когда pH падает до значений примерно 4, дальнейшее поглощение лития не происходит.
[0046] Данное явление аналогично тому, которое наблюдается в случае обычных полимерных слабокислотных катионообменных смол. Традиционный подход к решению настоящей проблемы заключается в предварительной нейтрализации ионообменной смолы гидроксидом натрия, который переводит ионообменную смолу в форму натриевой соли, так что во время загрузки pH раствора остается постоянным. Однако указанный подход не будет работать в случае литий-ионных сит, поскольку ион натрия слишком велик, чтобы проникнуть через литий-ионные сита.
[0047] В одном из вариантов осуществления настоящего изобретения pH раствора может быть отрегулирован перед контактом соляного раствора с LIS путем добавления NaOH к соляному раствору или иного основания, такого как карбонат натрия или гидроксид аммония, перед обработкой. Такая предварительная обработка повысит начальный pH, так что конечный pH не будет настолько низким, чтобы предотвратить поглощение лития. Однако недостатком указанного подхода является то, что, как показано на Фиг. 2, при повышенных уровнях pH увеличивается количество ионов натрия, поглощаемых ситом наравне с ионами лития. Кроме того, если pH повышается до значений выше 8, гидроксид магния может выпадать в осадок из раствора.
[0048] В одном из вариантов осуществления настоящего изобретения суспензия соляной раствор/литий-ионные сита в загрузочном реакторе может быть нейтрализована основанием, таким как NaOH, для поддержания pH, чтобы максимизировать поглощение лития при минимальном поглощении натрия. Чаще всего, значение pH может быть примерно больше 5 и примерно меньше 9, в предпочтительном варианте осуществления в диапазоне больше 6 и меньше 8. В том случае, когда литий-ионные сита представляет собой MTA, предпочтительный диапозон pH составляет от 6 до 7.
[0049] Литий обычно элюируется из LIS кислотой, такой как соляная кислота, для одновременной регенерации литий-ионных сит и получения литиевого продукта, как показано в уравнении (2). Литий-ионные сита эффективно нейтрализуют кислоту в результате данной реакции.
LIS.Li+H+ → LIS.H+Li+ (2)
[0050] Как показано на Фиг. 3, количество лития, извлекаемого из литий-ионных сит, повышается с увеличением концентрации HCl. Для оптимальной эффективности элюирования концентрацию кислоты можно поддерживать на уровне менее 0,1 М (определяемом как количество моль, деленное дм-3 на Фиг. 3). Как показано на Фиг. 7, для оптимальной эффективности элюирования концентрация кислоты может соответствовать pH менее 3 и более 1 и в предпочтительном варианте осуществления pH составляет приблизительно 2.
[0051] Тем не менее, на Фиг. 3 также показано, что при концентрациях кислоты более 0,1 М повышается количество титана, извлекаемое из литий-ионных сит, тем самым происходит разрушение литий-ионных сит и сокращение срока их службы. При концентрации кислоты выше примерно 0,1 М извлекается избыточное количество титана, что приводит к недопустимо короткому сроку службы.
[0052] Один из способов минимизировать такое разрушение литий-ионных сит заключается в том, чтобы уменьшить время контакта между LIS и кислотой. Поскольку в одном из вариантов осуществления настоящего изобретения литий-ионные сита находится в порошкообразной форме, ионообменный процесс носит высоко кинетический характер, и реакция обмена, соответствующая уравнению (2), приведенному выше, в основном завершается менее чем за один час. В одном из вариантов осуществления настоящего изобретения время контакта между LIS и элюирующей кислотой составляет менее одного часа. Таким образом, литий практически полностью удаляется из литий-ионных сит, сводя к минимуму деградацию литий-ионных сит.
[0053] Кроме всего прочего, размер частиц литий-ионных сит играет важную роль в создании системы, описанной в настоящей заявке. На Фиг. 4 показано типичное распределение частиц по размерам в образце литий ионных сит с применением метатитановой кислоты, взятого после нескольких часов перемешивания суспензии на воздухе. Эффективный размер частиц (d10) составляет около 0,5 мкм, а 90% (по объему) материала находится в диапазоне 0,4-40 мкм. Эффективный размер - диаметр частицы, для которой 10 процентов от общего числа зерен меньше, а 90 процентов от общего числа зерен больше по весу или объему. Эффективный размер данного материала составляет около 0,5 мкм. В то время как более крупный материал может осесть из водной суспензии под действием силы тяжести менее чем за час, более мелкие частицы не оседают легко даже через день. Без обоснованной связи с конкретной теорией, считается, что более крупные частицы литий-ионных сит представляют собой агломераты мелких частиц, полученных спеканием в процессе получения данных сит. В результате крупные частицы подвержены механическому истиранию во время смешивания с технологическими жидкостями, так что со временем увеличивается доля мелких частиц. Следовательно, отделение литий-ионных сит от технологических жидкостей путем осаждения под действием силы тяжести не является идеальным.
[0054] Мембраны все чаще используются в биореакторах для очистки сточных вод. В типичном мембранном биореакторе (MBR) для микрофильтрации или ультрафильтрации мембраны с размером пор менее 0,1 мкм в форме полых волокон, трубок или плоских листов, погружены в суспензию сточных вод и твердых биологических отходов. Чистые отфильтрованные/очищенные сточные воды выкачиваются через мембраны с помощью вакуума. Суспензию сточных вод/твердых биологических отходов обычно перемешивают путем барботирования воздуха. Барботирование способствует переносу кислорода к твердым биологическим отходам и предотвращает загрязнение мембраны из-за накопления твердых биологических отходов на поверхности мембраны.
[0055] В мембранных биореакторах концентрация взвешенных твердых частиц обычно составляет менее 30 г/л и более характерно 10-15 г/л. Более высокие концентрации взвешенных веществ не используются, поскольку перенос кислорода затрудняется из-за более высокой и неньютоновской вязкости жидкости. Кроме того, более высокие концентрации взвешенных твердых частиц снижают скорость потока через мембрану и/или увеличивают трансмембранное давление. Типичная скорость потока для погружных мембран в мембранных биореакторах составляет 10-30 литров в час на квадратный метр (данные единицы обычно сокращенно обозначают как «LMH»).
[0056] В одном из вариантов осуществления настоящего изобретения процесс глубокой ультрафильтрации или микрофильтрации через мембрану используется в качестве средства отделения литий-ионных сит от технологических жидкостей. Размер мембранных пор, обычно менее примерно 1 мкм, меньше, чем у самых маленьких ситовых частиц литий-ионных сит, следовательно может быть достигнуто почти 100% разделение твердых частиц. В настоящем изобретении перенос кислорода не является проблемой. Однако погружная аэрация (воздушное перемешивание) может обеспечить необходимое перемешивание суспензии, в то время как поднимающиеся пузырьки очищают поверхности мембраны, чтобы уменьшить загрязнение мембраны и уменьшить истирание и сдвиг частиц LIS по сравнению с механическим перемешиванием.
[0057] Описанные в настоящей заявке варианты осуществления изобретения значительно отличаются от типичных вариантов, с применением погружных мембран, таких как MBR. Частицы литий-ионных сит позволяют обрабатывать гораздо более высокие концентрации взвешенных твердых частиц при достижении значительно более высоких значений скорости потока. Скорость потока, получаемые при обычном применении MBR, чаще всего составляет менее чем 30 л/час при трансмембранном давлении 10-30 кПа и показателе общего содержания взвешенных твердых частиц (TSS) менее 30 г/л. В противоположность вышеуказанному примеру, в варианте осуществления настоящего изобретения возможно достижение скорости потока до 300 л/час при трансмембранном давлении 20 кПа, которая была получена с использование литий-ионных сит при показателе TSS более 100 г/л.
[0058] Согласно настоящему изобретению, концентрация взвешенных твердых веществ может составлять примерно более 50 г/л и предпочтительно более 100 г/л. Без обоснованной связи с какой-либо конкретной теорией, считается, что, более высокая концентрация твердых веществ в реакторе является предпочтительной, поскольку она уменьшает объем реактора, требуемый для достижения заданного времени контакта литий-ионных сит с жидкостью.
[0059] В ионнообменной системе с неподвижным слоем в кислом элюенте понижается внутренняя концентрация кислоты, когда он проходит через слой, и нейтрализуется реакцией, соответствующей уравнению (2), указанному выше. Чтобы поддерживать pH кислоты, контактирующей с литий-ионными ситами, на уровне менее 3,а также чтобы поддерживать эффективность элюирования, pH кислоты, поступающей в слой, может быть значительно меньше, чем 1. Следовательно, если литий-ионные сита регенерируются в неподвижном слое, литий-ионные сита, расположенные ближе по направлению к входному концу слоя, будут значительно разрушены более концентрированной кислотой.
[0060] Согласно настоящему изобретению, литий-ионные сита могут быть регенерированы в виде суспензии в емкости реактора, где литий-ионные сита контактируют с кислотой в однородной концентрации. Концентрация кислоты может поддерживаться на уровне менее 0,1 М, предпочтительна концентрация кислоты, соответствующая pH менее 3 и более 1, и предпочтительно pH приблизительно равное 2. Данную концентрацию можно поддерживать путем непрерывного измерения. концентрации кислоты в жидкости в реакторе подходящими способами и добавлением концентрированной кислоты, если требуется, для поддержания концентрации в желаемом диапазоне (например, при pH=2).
[0061] Для минимизации примесей, таких как кальций, магний, калий и натрий, в конечном продукте - соли лития, полученные элюированием литий-ионных сит с применением кислоты, остаточный исходный соляной раствор может быть удален из литий-ионных сит после загрузки и до элюирования с использованием кислоты путем смешивания насыщенных литий-ионных сит с водой и последующего отделения воды. В альтернативном варианте осуществления настоящего изобретения остаточный исходный соляной раствор может быть удален путем прямой фильтрации насыщенных литий-ионных сит через подходящий фильтр. Согласно настоящему изобретению, предпочтительный размер частиц литий-ионных сит находится в диапазоне 0,4-40 мкм. Твердые частицы в данном диапазоне могут быть отфильтрованы и обезвожены с помощью обычных устройств для разделения твердой и жидкой фаз с использованием фильтрующих материалов, таких как фильтровальные ткани с отверстиями более 10 мкм вместо мембран с размером пор менее 1 мкм. Таким образом, основная масса исходного соляного раствора будет отделена от насыщенных литий-ионных сит. Обезвоженные литий-ионные сита затем можно промыть непосредственно на фильтре для удаления остаточного соляного раствора с литий-ионных сит без необходимости повторного суспендирования литий-ионных сит. Примеры типов фильтров включают, но не ограничиваются ими, горизонтальные ленточные вакуумные и нагнетательные фильтры, вакуумные и нагнетательные фильтры с вращающимся барабаном и вакуумные и нагнетательные фильтры с вращающимся диском, нагнетательные фильтр-прессы и центрифуги.
[0062] Как обсуждалось выше, элюирование лития с литий-ионных сит кислотой дает кислый раствор соли лития. Литий-ионные сита предпочтительно отделяют от кислого раствора элюата литиевой соли, чтобы минимизировать возврат регенерированного лития с регенерированными литий-ионными ситами обратно в загрузочный реактор. Можно использовать аналогичный подход, который используется для отделения исходного соляного раствора от насыщенных литий-ионных сит. Таким образом, регенерированные литий-ионные сита смешивают с водой и затем отделяют их от воды. В качестве альтернативы литий-ионные сита можно фильтровать через подходящий фильтр, предпочтительно с возможностью промывки водой.
[0063] Следует проявлять осторожность, чтобы свести к минимуму содержание влаги в литий-ионных ситах, переносимых в реактор регенерации. Если вместе с литий-ионными ситами в реактор регенерации переносится чрезмерное количество воды, регенерированный раствор элюата соли лития будет слишком разбавленным. Аналогично следует извлекать литий с жидкостью, захваченной литий-ионными ситами, которые переносятся из реактора регенерации.
[0064] Как показано в Примере 1 ниже, рабочая емкость литий-ионных сит с применением метатитановой кислоты может составлять около 0,01 г лития на грамм литий-ионных сит. Поток литий-ионных сит при пересчете на сухое вещество тогда будет составлять 100 г литий-ионных сит/г извлеченного Li. Когда суспензия в загрузочном реакторе содержит концентрацию взвешенных твердых частиц 100 г/л (т.е. около 90% влаги по массе и около 10% массы твердых веществ; 1 литр воды на 100 грамм литий-ионных сит), и данная суспензия переносится напрямую в реактор регенерации, количество добавочной воды составит (1 г литий-ионных сит/0,01 г Li/100 г/л литий-ионных сит) = 1,0 литр воды на грамм извлеченного лития. Если не брать в расчет воду в концентрированной кислоте, то концентрация лития в элюате будет 1 г/л.
[0065] Если концентрация взвешенных твердых частиц в реакторе регенерации также поддерживается на уровне 100 г/л и переносится при данной концентрации, количество лития, захваченного регенерированными литий-ионными ситами, будет (1 л/г Li x 1 г/л Li ) = 1 г Li/г извлеченного Li. Другими словами, весь литий, элюированный с литий-ионных сит, будет обратно захватываться литий-ионными ситами. Если данные литий-ионные ситам затем рециркулировать непосредственно обратно в загрузочный реактор, чистый литий не будет извлечен.
[0066] Суспензия регенерированных литий-ионных сит может быть смешана с водой в промывочном реакторе для извлечения захваченного лития перед рециркуляцией литий-ионных сит в загрузочный реактор. Чтобы отделить 90% лития от литий-ионных сит, потребуется 9 литров воды на грамм извлеченного лития. Разбавленная жидкость в промывном реакторе затем может быть отделена, например, под действием силы тяжести или с помощью мембраны. В таком случае концентрация лития будет всего 0,1 г/л. Тем не менее данная концентрация слишком мала для практического использования. Таким образом, литий-ионные сита необходимо обезвоживать до содержания влаги значительно меньше 90%.
[0067] Например, если суспензию насыщенных литий-ионных сит обезвоживают до содержания влаги 50% по весу (например, 1 литр воды/1000 литий-ионных сит), литий-ионные сита будут содержать только (1 литр воды/1000 г литий-ионного сита) /(0,01 г Li/г литий-ионного сита ) = 0,1 литра воды на грамм извлеченного лития. Если не брать в расчет воду в концентрированной кислоте, концентрация лития в элюате будет составлять 10 г/литр.
[0068] Помимо всего прочего, регенерированные литий-ионные сита следует обезвоживать в тот момент, когда они извлекаются из реактора регенерации. В противном случае большая часть извлеченного лития будет рециркулирована вместе с литий-ионными ситами обратно в загрузочный реактор. Даже если регенерированные литий-ионные сита обезвожены в высокой степени, потери лития из-за влаги, захваченной литий-ионными ситами, могут являться проблемой. Например, если регенерированные литий-ионные сита обезвожены до содержания влаги 50% по весу (т. е. 1 литр воды на 1000 г литий-ионных сит), количество лития, унесенного литий-ионными ситами, составляет (1 литр/1000 г литий-ионных сит) / (0,01 г Li/г литий-ионных сит) x 10 г Li/1 л) = 1 г Li/г извлеченного Li. Другими словами, весь литий, элюированный с литий-ионных сит, будет выводиться с литий-ионными ситами. В том случае, если данные литий-ионные сита затем были возвращены обратно в загрузочный реактор, чистый литий не извлекается из раствора.
[0069] Таким образом, литий из жидкости, унесенной обезвоженным литий-ионными ситами, должен быть извлечен. Например, регенерированные литий-ионные сита можно промывать водой. Затем литий извлекается в виде промывных вод. Количество промывочной воды должно быть достаточным для извлечения большей части лития, но не настолько, чтобы чрезмерно разбавить получаемый конечный раствор соли лития. Одним из способов достижения данного условия является повторное суспендирование литий-ионных сит в воде, а затем повторная фильтрация литий-ионных сит из суспензии. Чтобы отмыть 90% лития из литий-ионных сит, потребуется около 9 мл воды на 1 мл жидкости, захваченной литий-ионными ситами, что позволяет извлекать раствор соли лития, содержащий 1 г/л лития в указанных условиях.
[0069] Количество промывных вод может быть уменьшено, а концентрация лития может быть одновременно увеличена за счет использования двух или более промывок противотоком. Соответственно, обезвоженные литий-ионные сита, извлеченные из первой стадии промывки, повторно суспендируют в воде на второй стадии промывки, а затем снова обезвоживают. Промывная вода, извлеченная из устройства для обезвоживания на второй стадии, используется на первой стадии промывки вместо пресной воды. С помощью двух стадий противоточной промывки количество воды, необходимое для 90% извлечения лития, может быть уменьшено с примерно 9 мл воды на мл захваченной жидкости до примерно 3 мл воды на мл захваченной жидкости, а концентрация извлеченного лития может быть увеличена с 1 г/л до примерно 3 г/л.
[0071] В другом варианте осуществления настоящего изобретения суспензия может быть обезвожена с помощью такого устройства, как горизонтальный вакуумный ленточный фильтр. Обезвоженные литий-ионные сита можно затем промыть непосредственно на фильтре. На фильтре можно использовать одну или несколько стадий обратной промывки. В качестве другого варианта можно использовать центрифугу. Если используется центрифуга, твердые частицы можно повторно суспендировать в воде, а затем обезвоживать с помощью центрифуги. В случае использования нескольких стадий промывки, обезвоженные твердые частицы из первой центрифуги можно снова суспендировать с водой, а затем обезвоживать во второй центрифуге. Центрифугат из второй центрифуги можно использовать в качестве жидкости для суспендирования твердых частиц, подаваемых в первую центрифугу. Таким образом можно использовать дополнительные центрифуги для эффективной многоступенчатой противоточной промывки твердых частиц.
[0072] В тому случае, если размер частиц литий-ионных сит слишком мал, такое обезвоживание становится более трудоемким. Фактически, даже если большинство частиц имеют диаметр более 10 микрометров, присутствие частиц, диаметр которых намного меньше 10 микрометров, затрудняет обезвоживание. В частности, если средний размер частиц литий-ионных сит составляет 0,1 мкм или меньше, обезвоживание становится практически невозможным.
[0073] В другом варианте осуществления настоящего изобретения обезвоженные литий-ионные сита могут быть классифицированы с помощью подходящего устройства, такого как воздушный классификатор, или влажные литий-ионные сита могут быть классифицированы путем декантирования для удаления мелких частиц диаметром менее 1-10 мкм. Таким образом облегчается отделение литий-ионных сит от обрабатываемой жидкости. Удаление мелких частиц значительно улучшит скорость фильтрации, предотвратит засорение фильтрующей среды и даст осадок на фильтре с более низким содержанием влаги. Удаляя мелкие частицы указанным образом, можно более эффективно использовать обычные устройства для разделения твердой и жидкой фаз, такие как горизонтальные ленточные вакуумные и нагнетательные фильтры, вакуумные и нагнетательные фильтры с вращающимся барабаном, вакуумные и нагнетательные фильтры с вращающимся диском, прессы с нагнетательные фильтром, центрифуги и т.п.
[0074] Чтобы увеличить чистоту продукта, регенерированной соли лития, исходный соляной раствор должен быть эффективно отделен от насыщенных литий-ионных сит. Например, требования к чистоте карбоната лития для аккумуляторных батарей очень строгие. Любой остаточный исходный соляной раствор, оставшийся в насыщенных литий-ионных ситах, будет загрязнять продукт примесями в исходном соляном растворе, такими как кальций, магний, натрий, калий и т. д. Поскольку концентрация указанных примесей в соляном растворе намного выше, чем концентрация лития, даже минимальное количество переносимого соляного раствора является проблемой. Фактически, в большинстве случаев вклад примесей из захваченного соляного раствора насыщенными литий-ионными ситами потенциально больше, чем количество примесей, фактичекски занимаемое центры обмена литий-ионных сит. Хотя для очистки регенерированного раствора лития можно использовать дополнительные процессы, такие как размягчение извести/соды и ионный обмен, данные дополнительные этапы процесса требуют дополнительных капитальных и эксплуатационных затрат. Однако эффективное обезвоживание и промывка насыщенного литий-ионных сит перед подачей их в реактор регенерации может минимизировать потребность в указанных дорогостоящих процессах. Как обсуждалось выше, эффективное обезвоживание может быть достигнуто с помощью обычных устройств для разделения твердых частиц и жидкости при условии, что литий-ионные сита не содержат значительных количеств частиц диаметром менее 1-10 микрометров. Помимо всего прочего, потребность в воде для промывки сит может быть снижена за счет использования многоступенчатой промывки противотоком.
[0075] Настоящее изобретение в дальнейшем будет описано со ссылкой на иллюстративные варианты осуществления, которые приведены для понимания, как примеры и не предназначены для ограничения объема настоящей заявки.
ИЛЛЮСТРАТИВНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[0076] Испытательная установка была сконструирована для демонстрации процесса согласно одному из вариантов осуществления настоящего изобретения. Схематический чертеж испытательной установки показан на Фиг. 5.
[0077] Испытательная установка состояла из шести реакторов (R1-R6), каждый из которых был оборудован аэрораспылителями для перемешивания, а пять из которых были оснащены модулями с погружными мембранами. Реактор R4, используемый для регенерации литий-ионных сит с использованием кислоты, не был оборудован мембраной. Рабочий объем каждого из реакторов составлял приблизительно 5 литров, за исключением реактора R4, который имел рабочий объем приблизительно 1,1 литра.
[0078] Титанат лития (LTO) использовали в качестве литий-ионных сит. LTO был синтезирован путем взаимодействия гидроксида лития с диоксидом титана при молярном соотношении приблизительно 2,2: 1 при температуре 700°C в течение 4 часов. На Фиг. 4, обсуждаемом ранее, показан гранулометрический состав LTO, использованный в данном примере. Первоначальный LTO, полученный в результате синтеза, был преобразован в метатитановую кислоту (HTO) путем травления LTO в 0,2 N HCl в течение 16 часов и затем промывки полученного HTO водой. В реактор R1 и реактор R2 первоначально были загружены водные суспензии LIS 100 г/л, в то время как в остальные реакторы первоначально были загружены суспензии LIS 500 г/л. Литий-ионные сита перемещались из реактора в реактор в виде суспензии перистальтическими насосами. Скорость потока суспензий литий-ионных сит регулировали так, чтобы скорость переноса твердых частиц составляла приблизительно 100 г/ч в пересчете на сухую массу.
[0079] Мембранные модули представляли собой лабораторные установки погружного типа POREFLON ™, производимые Sumitomo Electric Corporation, каждая из которых имела эффективную площадь мембраны 0,1 м2. Жидкость пропускали через мембраны с помощью вакуума с использованием перистальтических насосов. Вакуум поддерживали на уровне менее 40 кПа.
[0080] Литийсодержащий соляной раствор был приготовлен из соляного раствора, полученного из отложения Смаковер в южном Арканзасе, и имел состав, указанный в таблице 1 ниже. После извлечения лития из соляного раствора в соответствии с указанным процессом, соляной раствор повторно обогащали хлоридом лития и возвращали в процесс. В результате концентрация лития в исходном соляном растворе была несколько выше, чем в исходном растворе в том виде, в котором он был получен. Концентрации натрия и калия были определены на основании опубликованных анализов солевого раствора.
(мг/л)
(мг/л)
(мг/л)
(мг/л)
(мг/л)
* - Определено из опубликованных данных анализа соляных растворов
[0081] Реактор R1, загрузочный реактор, был оборудован регулятором pH, который автоматически контролировал добавление 1 н. NaOH таким образом, чтобы поддерживать pH 7,8. Таким образом, кислота, образовавшаяся в результате реакции ионного обмена, постоянно нейтрализовалась. Исходный соляной раствор вводили в реактор R1 и приводили в контакт с HTO. HTO подавали в реактор R1 из реактора R6 в виде суспензии 500 г/л. В результате смешивания концентрированной суспензии из реактора R6 с исходным соляным раствором концентрация твердых частиц литий-ионных сит в реакторе R1 составила около 100 г/л. Поскольку HTO извлекает ионы лития из соляного, HTO частично превращается обратно в LTO. Обедненный литием (т.е. маточный) раствор пропускался через мембраны с помощью насоса.
[0082] Насыщенные литий-ионные сита (т.е. LTO) переносились из реактора R1 в виде суспензии с соляным раствором и направлялись в реактор R2, в котором происходила промывка сит от остаточно соляного раствора. В реактор R2 подавали воду, чтобы вымыть остаточный соляной раствор из LTO. Промывные воды отводились из реактора R2 через другой модуль с погружными мембранами.
[0082] Насыщенный/промытый LIS отводили из реактора R2 в виде водной суспензии и направляли в реактор R3, который был реактором-загустителем. Воду отводили из реактора R3 через другой модуль с погружной мембраной, таким образом увеличивая концентрацию твердых веществ в реакторе R3 примерно до 500 г/л.
[0084] Загущенную суспензию насыщенного/промытого LIS с концентрацией твердых веществ около 500 г/л отводили из реактора R3 и направляли в реактор R4, который был реактором регенерации. Литий-ионные сита в реакторе R4 приводили в контакт с соляной кислотой при концентрации примерно 0,2 М. Концентрация твердых частиц литий-ионных сит в реакторе R4 составляла примерно 500 г/л. Концентрацию кислоты контролировали и поддерживали на постоянном уровне с помощью регулятора проводимости путем добавления 5 М HCl до заданного значения проводимости 150 мСм/см. В ходе контакта литий-ионных сит с кислотой происходило преобразование LTO обратно в форму HTO, и в результате чего образовалась суспензия литий-ионных сит, содержащая около 0,2 М соляной кислоты вместе с хлоридом лития. Реактор R4 не был снабжен мембраной, и суспензия литий-ионных сит, содержащая HCl/хлорид лития, свободно перетекала в реактор R5. Известно, что концентрация кислоты 0,2 М не является предпочтительной из-за чрезмерного растворения титана, содержащегося в LIS, но данный пример все же иллюстрирует вариант осуществления настоящего изобретения.
[0085] Реактор R5 был первым из двух реакторов промывки с использованием кислоты противотоком. Большая часть HCl/хлорида лития была вымыта с литий-ионных сит в реакторе R5, тогда как большая часть остаточных HCl/хлорида лития была вымыта с литий-ионных сит в реакторе R6. Литий-ионные сита в реакторе R5 при концентрации твердых веществ около 500 г/л контактировали с промывной водой из реактора R6. Промывные воды, содержащие кислоту, отводили из реактора R5 через другой модуль с погружными мембранами. Промывные воды, имеющие кислую среду и отводимые из реактора R5, представляли собой продукт хлорида лития, извлеченный в ходе данного процесса. Суспензию литий-ионных сит с концентрацией твердых частиц около 500 г/л отбирали из реактора R5 и направляли в реактор R6.
[0086] Свежая вода, добавленная в реактор R6, смывала большую часть оставшейся HCl/хлорида лития с литий-ионных сит. Промывные воды отводились из реактора R6 через другой модуль с погружными мембранами и направлялись в реактор R5. Таким образом, концентрация хлорида лития в промывных водах в реакторе R6 была снижена до менее чем 10% от концентрации лития в реакторе R4. Суспензию литий-ионных сит/промывных вод отводили из реактора R6 и направляли обратно в реактор R1, где повторно использовали для извлечения лития из исходного соляного.
[0087] Был проведен непрерывный 12-часовой тестовый запуск. Аликвоты маточного раствора и конечного раствора отбирали и анализировали каждый час. График, показывающий концентрации веществ в маточном растворе и конечном растворе в ходе эксперимента, изображен на Фиг. 6. Результаты, приведенные в Таблице 1, получены для объединенных проб, взятых после 10 часов работы с интервалом в 1 час. Концентрация лития была снижена с 244 мг/л до 61 мг/л, степень извлечения 75%. Время пребывания жидкости в загрузочном реакторе составляло около 1 часа.
[0088] Конечный продукт содержал литий в концентрации 4300 мг/л. Из конечного раствора извлекли больше лития (2322 мг/ч), чем было фактически извлечено из исходного соляного раствора (957 мг/ч). Без обоснованной связи с конкретной теорией, считается, что разница (1365 мг/ч), вероятно, связана с остаточным литием на литий-ионных ситах, который не был полностью удален из LTO во время первоначального травления в HCl. При перерасчете на литий, который фактически был извлечен из соляного раствора, емкость литий-ионных сит составила 9,6 мг/г. Время пребывания жидкости в реэкстракционном реакторе составляло 2,2 часа. На основании количества загруженного и извлеченного лития коэффициент концентрации лития был примерно в 10 раз выше.
[0089] Исходный соляной раствор содержал концентрацию кальция 22000 мг/л, в то время как конечный раствор содержал концентрацию кальция только 1400 мг/л. Отношение кальция к литию в сырье составляло 90. Отношение в продукте составляло 0,33. Однако фактически из исходного соляного была извлечена только около половины содержащегося в продукте лития. Если рассматривать только литий в продукте, который был извлечен из соляного раствора, отношение Ca к Li в продукте составляло 0,62, что представляет собой коэффициент обогащения 90/0,62=145.
[0090] Исходный соляной раствор содержал расчетную концентрацию натрия 43000 мг/л, в то время как продукт содержал концентрацию натрия только 9770 мг/л. Отношение натрия к литию в сырье составляло 176. Отношение в продукте составляло 2,3. Если рассматривать только литий в продукте, который был извлечен из соляного раствора, отношение Na к Li в продукте составляло 4,3, что представляет коэффициент обогащения 176/4,3=41.
[0091] Исходный соляной содержал концентрацию магния 2170 мг/л, в то время как продукт содержал концентрацию магния только 76 мг/л. Отношение магния к литию в сырье составляло 8,9. Соотношение в продукте составляло 0,018. Если рассматривать только литий в продукте, который был извлечен из соляного раствора, отношение Mg к Li в продукте составляло 0,034, что представляет собой коэффициент обогащения 8,9/0,034=262.
[0092] Таким образом, описанные в настоящей заявке система и способ обладают способностью селективно извлекать литий из соляных растворов, содержащих высокие концентрации кальция, натрия и магния.
[0093] В данном примере использовался только один реактор промывки от соляного раствора, следовательно некоторое количество соляного раствора могло попасть в реактор регенерации путем насыщенных литий-ионных ситах, таким образом, неся некоторое количество кальция, натрия и/или магния в реактор регенерации на насыщенных литий-ионных ситах. Без обоснованной связи с конкретной теорией считается, что результаты могут быть улучшены путем включения второго реактора промывки от соляного раствора. Кроме того, как обсуждалось выше, за счет снижения pH при загрузке до 6-7 количество натрия, поглощенного литий-ионными ситами, может быть уменьшено без значительного уменьшения емкости по литию.
СРАВНИТЕЛЬНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[0094] Ключевой тест был проведен в работе Chitrakar для оценки влияния концентрации HCl на начальное извлечение лития и титана из адсорбента, что показано на рисунке 4a в статье Chitrakar. На Фиг. 4а в статье Chitrakar показано количество экстрагированного лития и титана в зависимости от концентрации HCl. Данные в в статье Chitrakar показывают, что концентрация HCl должна быть 0,2 М или более. Фактически, на риг. 4a в статье Chitrakar не показаны данные для экстракции лития из адсорбента при концентрации кислоты ниже 0,1 М, которая является предпочтительной концентрацией кислоты, при которой действует настоящее изобретение. В настоящем изобретении литиевые и титановые компоненты адсорбента LTO экстрагируются при гораздо более низких концентрациях кислоты, чем предсказал в своей статье Chitrakar.
[0095] Ссылки в настоящей заявке на такие термины, как «вертикальный», «горизонтальный» и т.д. сделаны в качестве примера, а не в качестве ограничения, чтобы установить систему отсчета. Очевидно, что для описания изобретения могут использоваться различные другие системы отсчета, не выходящие за рамки сущности и объема изобретения. Также очевидно, что признаки изобретения не обязательно показаны в масштабе на чертежах. Кроме того, термины «состоящий из», «включает», «имеющий», «имеет», «с» или их варианты, использованные либо в подробном описании изобретения, либо в формуле изобретения, предназначены для обозначения состава объекта и носят постоянный характер, аналогично термину «содержащий».
[0096] Ссылки в данном документе, использующие термины, обозначающие приблизительность, такие как «примерно», «приблизительно» и «по существу», не должны ограничиваться указанным рядом синонимов. Используемые термины находятся в соответствии с точностью инструмента, используемого для измерения заданного значения, и, если иное не зависит от точности инструмента, то данные термины обозначают +/- 10% от заявленного значения (значений).
[0097] Элемент, «связанный» или «сопряженный» с другим элементом, может быть напрямую связан или сопряжен с другим элементом, или вместо такового могут присутствовать один или несколько промежуточных элементов. Элемент может быть «напрямую связан» или «напрямую сопряжен» с другим элементом, если промежуточные элементы отсутствуют. Элемент может быть «косвенно связан» или «косвенно сопряжен» с другим элементом, если присутствует по крайней мере один промежуточный элемент. Элемент «на» или «контактирующий» с другим элементом может находиться непосредственно на другом элементе или в прямом контакте с ним, или, вместо такового, могут присутствовать один или несколько промежуточных элементов. Элемент может находиться «непосредственно» или в «прямом контакте» с другим элементом, если промежуточные элементы отсутствуют. Элемент может быть «косвенно на» или находиться в «косвенном контакте» с другим элементом, если присутствует по крайней мере один промежуточный элемент.
[0098] Используемая в настоящей заявке терминология предназначена только для описания конкретных вариантов осуществления изобретения и не предназначена для ограничения изобретения. Используемые в настоящей заявке формы единственного числа могут быть заменены на формы множественного числа, если контекст явно не указывает иное. Кроме того, очевидно, что термины «содержит» и/или «содержащий», когда они используются в настоящем описании, определяют наличие заявленных функций, целых чисел, шагов, операций, элементов и/или компонентов, но не исключают наличие или добавление одной или нескольких других функций, целых чисел, шагов, операций, элементов, компонентов и/или их групп.
[0099] Несмотря на то, что настоящее изобретение проиллюстрировано описанием различных вариантов осуществления, и несмотря на то, что указанные варианты осуществления были описаны достаточно подробно, заявитель не намерен заключать в определенные пределы или каким-либо образом ограничивать объем прилагаемой формулы изобретения такими деталями. Дополнительные преимущества и модификации будут очевидны специалистам в данной области техники. Таким образом, настоящее изобретение в его более широких аспектах не ограничивается конкретными деталями, типичным устройством и способом, а также показанными и описанными иллюстративными примерами. В интересах полного предоставления возможности специалистам в данной области техники создавать и использовать заявленное изобретение, заявитель предоставил информацию как о преимуществах, так и о недостатках различных подробных вариантов осуществления настоящего изобретения. Специалисты в данной области техники могут наблюдать, что в некоторых приложениях недостатки конкретного варианта осуществления, как подробно описано выше, могут быть устранены полностью или перевешены общими преимуществами, обеспечиваемыми заявленным изобретением. Следовательно, могут быть сделаны отклонения от подробных изложений, приведенных выше, без отступления от существа или объема общей концепции изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОЦЕСС ДЛЯ ИЗВЛЕЧЕНИЯ ЛИТИЯ ИЗ РАССОЛА | 2018 |
|
RU2750318C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЛИТИЯ ИЗ РАССОЛА | 2020 |
|
RU2810199C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНАТА ЛИТИЯ ИЗ ЛИТИЙСОДЕРЖАЩЕГО РАСТВОРА И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2024 |
|
RU2837934C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЛИТИЯ | 2020 |
|
RU2787034C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГАЛЛИЯ ИЗ ЛЕТУЧЕЙ ЗОЛЫ | 2011 |
|
RU2506332C1 |
| СПОСОБ ОБРАБОТКИ ЛИТИЙСОДЕРЖАЩЕГО РАСТВОРА ДЛЯ ПОЛУЧЕНИЯ КАРБОНАТА ЛИТИЯ | 2024 |
|
RU2839385C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГРАНУЛИРОВАННОГО СОРБЕНТА ДЛЯ ИЗВЛЕЧЕНИЯ ЛИТИЯ ИЗ ЛИТИЙСОДЕРЖАЩИХ РАССОЛОВ | 2010 |
|
RU2455063C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГАЛЛИЯ ИЗ ЛЕТУЧЕЙ ЗОЛЫ | 2011 |
|
RU2507282C1 |
| СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАЧИСТОГО КАРБОНАТА ЛИТИЯ ИЗ ТЕХНИЧЕСКОГО КАРБОНАТА ЛИТИЯ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2013 |
|
RU2564806C2 |
| ИЗВЛЕЧЕНИЕ ЛИТИЯ ИЗ КИСЛОГО РАСТВОРА | 2018 |
|
RU2739764C1 |
Изобретение относится к цветной металлургии, в частности к извлечению ионов лития из литийсодержащего соляного раствора. Включает контактирование литийсодержащего рассола с литий-ионными ситами, которые содержат оксид титана или ниобия, в первом реакторе при перемешивании для образования ионов лития с литий-ионными ситами. Разрушение комплекса ионов лития с литий-ионными ситами во втором реакторе при перемешивании с образованием непосредственно литий-ионных сит и кислого раствора элюата соли лития, отделение литий-ионных сит от кислого раствора элюата литиевой соли, контактирование литий-ионных сит с водой после декомплексирования во втором реакторе для получения регенерированных литий-ионных сит и промывки разбавленной кислотой. Время pH первого реактора поддерживается на постоянном уровне путем добавления основания, такого как безводный аммиак или гидроксид аммония, или путем добавления основания, представляющего собой гидроксид натрия, в концентрации менее 8 мас.%. Изобретение позволяет осуществлять процесс извлечения ионов лития непрерывно, используя дополнительные этапы промывки. 2 н. и 22 з.п. ф-лы, 7 ил., 1 табл.
1. Способ извлечения ионов лития из литийсодержащего соляного раствора, включающий:
контактирование литийсодержащего соляного раствора с литий-ионными ситами в первом реакторе с образованием комплекса ионов лития с литий-ионными ситами;
отделение комплекса ионов лития с литий-ионными ситами от соляного раствора с помощью устройства для разделения твердой и жидкой фаз;
контактирование комплекса ионов лития с литий-ионными ситами с водой перед декомплексированием во втором реакторе,
декомплексирование ионов лития из комплекса с литий-ионными ситами во втором реакторе с образованием кислого раствора элюата соли лития, отделенного от литий-ионных сит;
отделение литий-ионных сит от кислого раствора элюата литиевой соли с помощью устройства для разделения твердой и жидкой фаз;
контактирование литий-ионных сит с водой после декомплексирования во втором реакторе для получения регенерированных литий-ионных сит и промывки разбавленной кислотой;
где литий-ионные сита содержат оксид титана или ниобия;
в то же время pH первого реактора поддерживается на постоянном уровне путем добавления основания, такого как безводный аммиак или гидроксид аммония,
в котором декомплексирование ионов лития из комплекса с литий-ионными ситами проводят при помощи элюирования кислотой,
в котором среднее время контакта литий-ионных сит и кислоты составляет менее 1 часа,
в котором концентрацию кислоты поддерживают на постоянном уровне путем добавления указанной кислоты, и
в котором концентрация кислоты составляет менее 0,1 М.
2. Способ по п.1, в котором pH кислоты больше 1 и меньше 3.
3. Способ по п.1 или 2, в котором pH кислоты составляет приблизительно 2.
4. Способ по п.1, в котором pH поддерживают на постоянном уровне от более 4 до менее 9.
5. Способ согласно любому из пп.1-4, в котором pH в первом реакторе составляет более 6 и менее 8.
6. Способ согласно любому из пп.1-5, в котором более 90% литий-ионных сит имеет средний диаметр частиц менее 40 мкм и более 90% литий-ионных сит имеет средний диаметр частиц более чем 0,4 мкм.
7. Способ согласно любому из пп.1-5, в котором более 90% по объему частиц литий-ионных сит имеет диаметр менее 100 мкм и диаметр более 0,5 мкм.
8. Способ согласно любому из пп.1-7, в котором более 90% по объему частиц литий-ионных сит имеет диаметр более 0,5 мкм.
9. Способ согласно любому из пп.1-8, в котором литий-ионные сита содержат метатитановую кислоту.
10. Способ по п.1, дополнительно включающий:
добавление регенерированных литий-ионных сит в первый реактор.
11. Способ согласно любому из пп.1-10, дополнительно включающий добавление промывных вод, содержащих разбавленную кислоту, и дополнительной концентрированной кислоты во второй реактор.
12. Способ согласно любому из пп.1-11, в котором первый реактор содержит мембраны для ультрафильтрации или микрофильтрации.
13. Способ согласно любому из пп.1-12, в котором для перемешивания содержимого первого реактора используют барботирование воздухом.
14. Способ согласно любому из пп.1-13, в котором концентрация литий-ионных сит превышает 50 г/л.
15. Способ согласно любому из пп.12-14, в котором скорость потока через ультрафильтрационную мембрану или микрофильтрационную мембрану составляет более 30 л/час при трансмембранном давлении менее 30 кПа.
16. Способ согласно любому из пп.1-15, дополнительно включающий удаление литий-ионных сит, имеющих средний диаметр частиц менее 1 мкм, перед контактированием литийсодержащего соляного раствора с литий-ионными ситами.
17. Способ согласно любому из пп.1-16, дополнительно включающий обезвоживание комплекса ионов лития с литий-ионными ситами до содержания влаги менее 90% по весу перед декомплексированием.
18. Способ согласно любому из пп. 10-17, дополнительно включающий обезвоживание регенерированных литий-ионных сит перед добавлением в первый реактор.
19. Способ согласно любому из пп. 10-18, отличающийся тем, что приведение в контакт литий-ионных сит с водой включает контактирование литий-ионных сит с достаточным количеством воды, так что более 50% ионов лития извлекается из литий-ионных сит и удаляется из литий-ионных сит с помощью промывки перед добавлением регенерированных литий-ионных сит в первый реактор.
20. Способ согласно п.19, в котором приведение в контакт литий-ионных сит с водой включает контактирование литий-ионных сит водой более чем на одной стадии противотока, так что более 50% ионов лития извлекается из литий-ионных сит и удаляется из литий-ионных сит путем промывки перед добавлением регенерированных литий-ионных сит в первый реактор.
21. Способ согласно любому из пп.1-20, в котором используются такие основания, как гидроксид натрия, гидроксид калия, карбонат натрия, гидроксид магния или гидроксид кальция.
22. Способ согласно любому из пп.1-21, в котором используемая кислота представляет собой соляную кислоту или серную кислоту.
23. Способ согласно любому из пп.1-22, в котором концентрация литий-ионных сит превышает 100 г/л.
24. Способ извлечения ионов лития из литийсодержащего соляного раствора, включающий:
контактирование литийсодержащего соляного раствора с литий-ионными ситами в первом реакторе с образованием комплекса ионов лития с литий-ионными ситами;
отделение комплекса ионов лития с литий-ионными ситами от соляного раствора с помощью устройства для разделения твердой и жидкой фаз;
контактирование комплекса ионов лития с литий-ионными ситами с водой перед декомплексированием во втором реакторе,
декомплексирование ионов лития из комплекса с литий-ионными ситами во втором реакторе с образованием кислого раствора элюата соли лития, отделенного от литий-ионных сит;
отделение литий-ионных сит от кислого раствора элюата литиевой соли с помощью устройства для разделения твердой и жидкой фаз;
контактирование литий-ионных сит с водой после декомплексирования во втором реакторе для получения регенерированных литий-ионных сит и промывки разбавленной кислотой;
где литий-ионные сита содержат оксид титана или ниобия;
в то же время pH первого реактора поддерживается на постоянном уровне путем добавления основания, представляющего собой гидроксид натрия, в концентрации менее 8% мас.,
в котором декомплексирование ионов лития из комплекса с литий-ионными ситами проводят при помощи элюирования кислотой,
в котором среднее время контакта литий-ионных сит и кислоты составляет менее 1 часа,
в котором концентрацию кислоты поддерживают на постоянном уровне путем добавления указанной кислоты и
в котором концентрация кислоты составляет менее 0,1 М.
| WO 2017020090 А1, 09.02.2017 | |||
| Способ ионообменного извлечения лития из природной воды | 1989 |
|
SU1726379A1 |
| US 2017298475 A1, 19.10.2017 | |||
| СПОСОБ ИЗВЛЕЧЕНИЯ ИОНОВ ЗАГРЯЗНЯЮЩИХ МЕТАЛЛОВ ИЗ ПОТОКОВ ЖИДКОСТЕЙ | 1998 |
|
RU2176155C2 |
Авторы
Даты
2023-03-22—Публикация
2019-05-14—Подача