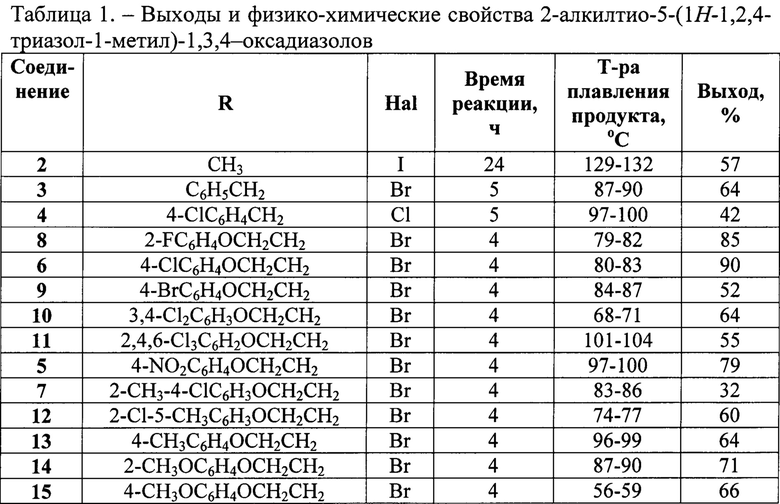
Изобретение относится к химии гетероциклических соединений, а именно к 2-алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазолам общей формулой I:
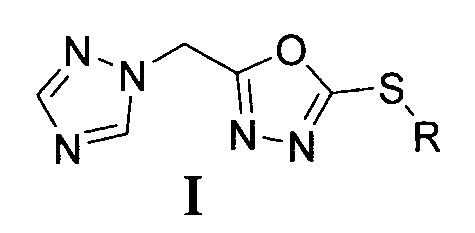
где R означает арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, нитро-группу, n означает целое число от 0 до 5, m означает целое число от 1 до 2, за исключением 2-(2-(3-метилфенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола и 2-(2-(2-фторфенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола, к их агрохимически, а также фармацевтически приемлемым солям.
Соединения общей формулой I могут найти применение в качестве сельскохозяйственных, промышленных, медицинских или ветеринарных фунгицидов.
Изобретение относится также к способам получения соединений общей формулы I, и использованию этих соединений в композициях с другими активными и вспомогательными соединениями для борьбы с грибковыми болезнями сельскохозяйственных культур, животных и человека.
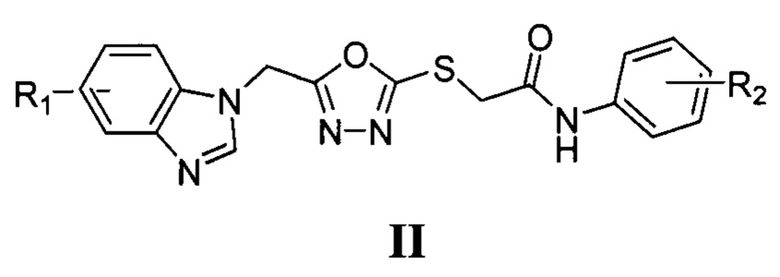
Одним из близких по биологической активности к заявленным 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолам общей формулой I, является ряд 2-алкилтио-5-(бензимидазол-1-метил)-1,3,4-оксадиазолов II, где R1 представлен галогеном, алкильной группой, алкилокси группой, нитро группой, нитрильной группой или аминоацетильной группой, a R2 представлен галогеном, алкильной группой, алкилокси группой, нитро группой или нитрильной группой. Соединения II обладают умеренной фунгицидной активностью в отношении возбудителей грибковых заболеваний растений и человека и подавляют развитие грибков при МИК до 100 мкг/диск. [Patel R.V. et. al. Synthesis of benzimidazolyl-l,3,4-oxadiazol-2-ylthio-N-phenyl-(benzothiazolyl)acetamides as antibacterial, antifungal and antituberculosis agents // Eur. J. Med. Chem. - 2012. - Vol. 53. - P. 41-51].
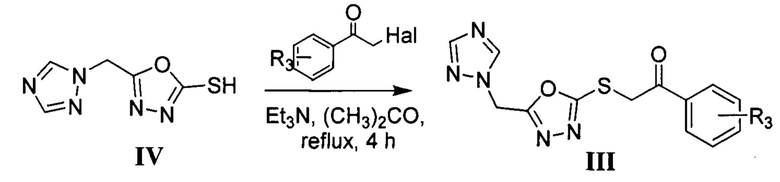
Наиболее близким по способу получения и биологической активности соединений общей формулы I, является способ получения веществ общей формулы III, где R3 представлен галогеном, алкильной группой, алкилокси группой, нитро группой или нитрильной группой, которые получают алкилированием 5-(1Н-1,2,4-триазол-1-ил)метил-1,3,4-оксадиазол-2-тиола IV α-галогенацетофенонами в ацетоне в присутствии триэтиламина при кипячении в течение 4 ч [Xu L. et. al. Structure and biological activities of novel triazole compounds containing 1, 3, 4-oxadiazole ring // Chem. Res. Chin. Univ. - 2008. - Vol. 24, №.3. - P. 299-302]. Также авторы приводят результаты фунгицидной активности в отношении Gibberella zeae, Alternaria solani, Phoma asparagi, Physalospora pircola и Cercospora arachidicola при конц. 50 мг/л, однако соединения проявляют низкую фунгицидную активность и уступают эталону дифеноконазолу.
Задача, решаемая данным изобретением, состоит в увеличении эффективности борьбы с вредоносными грибами и расширении ассортимента фунгицидных препаратов.
Поставленная задача решается получением соединений общей формулы I, где R означает арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, нитро-группу, n означает целое число от 0 до 5, m означает целое число от 1 до 2, обладающих фунгицидной активностью, а также увеличением эффективности фунгицидных препаратов за счет применения 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов общей формулы I и расширением ассортимента фунгицидов.
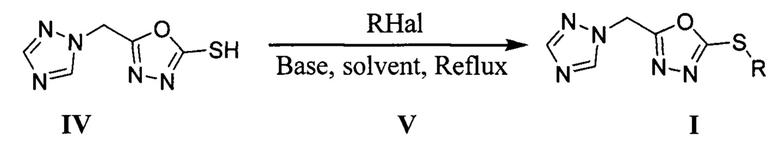
Поставленная задача решается разработкой способа получения 2-алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов общей формулой I, где R означает арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, нитро-группу, n означает целое число от 0 до 5, m означает целое число от 1 до 2, которые получают взаимодействием 5-(1,2,4-триазол-1 -илметил)-1,3,4-оксадиазол-2-тиола IV с различными алкилгалогенидами V, где R означает арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 8, алкилокси группу с числом атомов углерода от 1 до 8, нитро-группу, n означает целое число от 0 до 5, m означает целое число от 1 до 2, в присутствии третичных аминов в полярных апротонных растворителях.
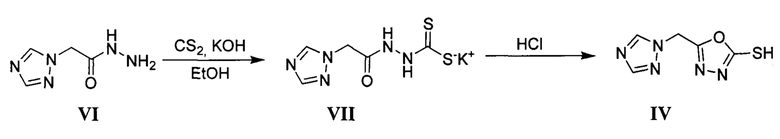
1,2,4-Триазол-1-илацетгидразид VI получают по описанной в литературе методике [Попков С.В., Алексеенко А.Л., Тихомиров Д.С. Синтез, строение и фунгицидная активность замещенных N2-фенилалкилиден-2-(азол-1-ил)ацетгидразидов // Изв. вузов. Химия и хим. технология. - 2007. - Т. 50, В. 6. - С. 98-101]. Далее полученный гидразид VI вводят в реакцию с сероуглеродом в присутствии основания гидроксида калия при кипячении на протяжении 24 ч. Полученную калиевую соль 2-(1,2,4-триазол-1-илацетил)гидразинкарбодитионовой кислоты VII подвергают реакции циклоконденсации под действием соляной кислоты с получением 5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол-2-тиола IV [Xu L. et. al. Structure and biological activities of novel triazole compounds containing 1, 3, 4-oxadiazole ring // Chem. Res. Chin. Univ. - 2008. - Vol.24, №.3. - P. 299-302].
Эффективность пестицидов напрямую зависит от препаративной формы препарата и условий, при которых действующее вещество контактирует с вредителями и возбудителями заболеваний растений. Наиболее эффективная и экономичная препаративная форма определяется исходя из физико-химических свойств препарата, его назначения и способа применения. Это могут быть, например, дусты, гранулы, микрокапсулированные препараты, смачивающиеся порошки, концентраты эмульсий, мази, вододиспергируемые гранулы, суспензионные концентраты. Также в состав препаративной формы помимо действующего вещества, могут входить вспомогательные вещества: наполнители, растворители, поверхностно-активные вещества, умягчители воды, синергические добавки и др. Известен препарат триадимефон, который применяют в виде 5, 25%-ного смачивающегося порошка, 10%-ного эмульгирующего концентрата для борьбы с болезнями пшеницы, ржи, ячменя, сахарной свеклы, яблони, огурцов в период вегетации, а также как протравитель семян. [Пестициды и регуляторы роста растений: Справ, изд. / Н.Н. Мельников, К.В. Новожилов, С.Р. Белан. - М.: Химия, 1995, с. 24, с. 287.]
Поставленная задача решается разработкой фунгицидных композиций, состоящих из 2-алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов с общей формулой I, где R означает арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, нитро-группу, n означает целое число от 0 до 5, m означает целое число от 1 до 2, агрохимически, а также их фармацевтически приемлемые соли, в концентрации 0.3-25% масс. и вспомогательных веществ, которые успешно могут быть применены для борьбы с вредоносными грибковыми болезнями сельскохозяйственных культур, животных или человека.
Изобретение может быть проиллюстрировано следующими примерами:
Пример 1. Получение (5-(1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола (1).
К раствору 1,41 г (0,01 моль) 2-(1H-1,2,4-триазол-1-ил) ацетогидразида и 0,659 г (0,01 моль) 85%-го гидроксида калия в 80 мл абс. этанола добавляют по каплям 0,87 г (0,01 моль) сероуглерода, реакционную массу кипятят в течение 20 ч, добавляют 100 мл воды и подкисляют конц. соляной кислотой до рН=7. Осадок отфильтровывают, промывают 50 мл холодной воды и перекристаллизовывают из 1 мл безводного этанола. Получают 2,1 г (40%) 5-(1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола с т.пл. 190-190°С.
1Н ЯМР-Спектр (δ, м.д., J, Гц): 5.69 с (2Н, СН2), 8.08 с (1H, C5HTrz), 8.72 с (1Н, C3HTrz), 14.69 уш.с.(1H, NH).
Масс-спектр, m/z: 183 [М+Н]+.
Пример 2. Получение 2-метилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола (2).
К раствору 0,1 г (0,000546 моль) 5-(1Н-1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола и 0,055 г (0,000546 моль) триэтиламина в 3 мл ацетона добавляют 0,078 г (0,000546 моль) йодметана и перемешивают в течение 24 ч при 20°С. Затем растворитель отгоняют на РПИ в вакууме водоструйного насоса, к остатку добавляют 4 мл воды и 4 мл хлороформа. Органическую фазу отделяют, водный слой промывают хлороформом (2×5 мл). Органические фазы объединяют и сушат над сульфатом магния, растворитель удаляют на РПИ в вакууме водоструйного насоса. К остатку добавляют 3 мл диэтилового эфира, захолаживают, осадок отфильтровывают. Получают 0,060 г (57%) 2-метилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола с т.пл. 129-132°С.
1H ЯМР-Спектр (δ, м.д., J3, Гц): 2.51 с (3Н, (CH3S), 5.82 с (2Н, CH2N), 8.06 с (1H, C5HTrz), 8.73 с (1H, C3HTrz).
Пример 3. Получение 2-бензилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола (3).
К раствору 0,1 г (0,000546 моль) 5-(1H-1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола и 0,0705 г (0,000546 моль) диизопропилэтиламина в 3 мл ацетона добавляют 0,093 г (0,000546 моль) бензилбромида, кипятят в течение 5 ч при 56°С. Избыток растворителя удаляют на РПИ в вакууме водоструйного насоса, к остатку добавляют 5 мл воды и 5 мл хлороформа. Органическую фазу отделяют, водный слой промывают хлороформом (2×5 мл). Органические фазы объединяют и сушат над сульфатом магния, хлороформ удаляют на РПИ в вакууме водоструйного насоса. К остатку добавляют 3 мл диэтилового эфира, осадок отфильтровывают. Получают 0,095 г (64%) 2-бензилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола с т.пл. 87-90°С.
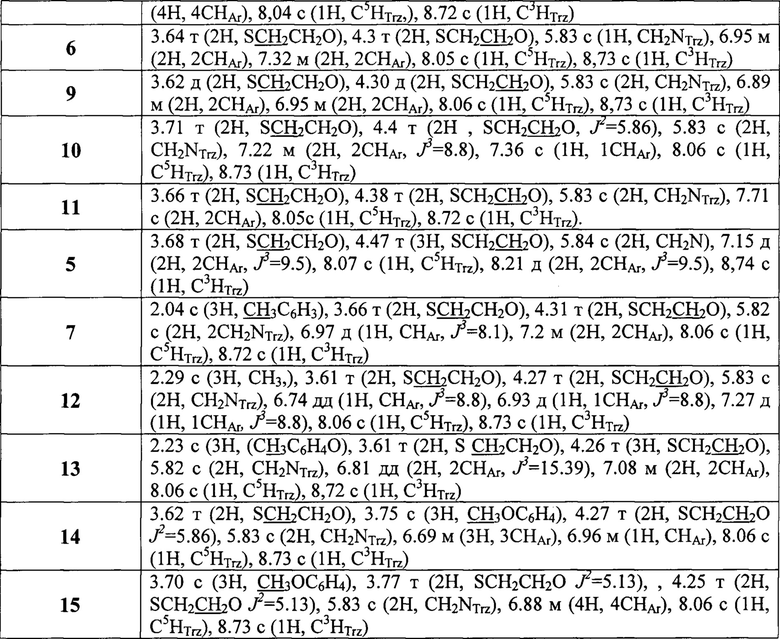
1Н ЯМР-Спектр (δ, м.д., J, Гц): 4.48 с (2Н, SCH2C6H5), 5.83 с (2Н, CH2NTrz), 7.31 м (3Н, CHAr), 7.38 м (2Н, CHAr), 8.08 с (1H, CH5Trz), 8.73 с (1Н, CH3Trz).
Пример 4. Получение 2-((4-хлорфенил)метил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола (4).
К раствору 0,1 г (0,000546 моль) 5-(1H-1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола и 0,055 г (0,000546 моль) триэтиламина в 3 мл ДМФА и добавляют 0,088 г (0,000546 моль) п-хлорбензилхлорида, кипятят в течение 5 ч при 153°С. Затем избыток ДМФА удаляется на РПИ в вакууме мембранного насоса, к остатку добавляют 4 мл воды и 4 мл хлороформа. Органическую фазу отделяют, водный слой промывают хлороформом (2×4 мл). Органические фазы объединяют и сушат над сульфатом магния, растворитель удаляют на РПИ в вакууме водоструйного насоса. К остатку добавляют 8 мл диэтилового эфира, осадок отфильтровывают. Получают 0,070 г (42%) 2-((4-хлорфенил)метил)тио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола с т.пл. 97-100°С.
1H ЯМР-Спектр (δ, м.д., J3, Гц): 4.47 с (2Н, SCH2C6H4), 5.82 с (2Н, CH2N), 7.39 м (2Н, 4CHAr), 8.07 с (1H, C5HTrz), 8.72 с (1Н, C3HTrz).
Масс-спектр, m/z: 308.18 [М+Н]+
Пример 5. Получение 2-(2-(4-нитрофенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола (5).
К раствору 0,1 г (0,000546 моль) 5-(1Н-1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола и 0,044 мл (0,000546 моль) пиридина в 3 мл ацетона добавляют 0,134 г (0,000546 моль) 1-(2-бромэтокси)-4-нитробензола), кипятят в течение 4 ч при 56°С. Избыток ацетона удаляют на РПИ в вакууме водоструйного насоса. Затем к остатку добавляют 5 мл воды и 5 мл хлороформа. Органическую фазу отделяют, водный слой промывают хлороформом (2×5 мл). Органические фазы объединяют и сушат над сульфатом магния, растворитель удаляют на РПИ в вакууме водоструйного насоса. К остатку добавляют 5 мл диэтилового эфира, осадок отфильтровывают. Получают 0,150 г (79%) 2-(2-(4-нитрофенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола с т.пл. 97-100°С.
1Н ЯМР-Спектр (δ, м.д., J3, Гц): 3.68 т (2Н, SCH2CH2O), 4.47 т (3Н, SCH2CH2O), 5.84 с (2Н, CH2N), 7.15 д (2Н, 2CHAr, J3=9.5), 8.07 с (1Н, C5HTrz), 8.21 д (2Н, 2CHAr, J3=9.5), 8,74 с (1Н, C3HTrz).
Пример 6. Получение 2-(2-(4-хлорфенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола (6).
К раствору 0,1 г (0,000546 моль) 5-(1H-1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола и 0,055 г (0,000546 моль) триэтиламина в 3 мл метилэтилктона добавляют 0,134 г (0,000546 моль) 1-(2-бромэтокси)-4-хлорбензола, кипятят в течение 5 ч при 80°С. Избыток растворителя удаляют на РПИ в вакууме водоструйного насоса, к остатку добавляют 4 мл воды и 4 мл хлороформа. Органическую фазу отделяют, водный слой промывают хлороформом (2×5 мл). Органические фазы объединяют и сушат над сульфатом магния, растворитель удаляют на РПИ в вакууме водоструйного насоса. К остатку добавляют 3 мл диэтилового эфира, осадок отфильтровывают. Техн. продукт перекристаллизовывают из изопропанола. Получают 0,167 г (90%) 2-(2-(4-хлорфенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола с т.пл. 80-83°С.
1H ЯМР-Спектр (δ, м.д., J3 Гц): 3.64 т (2Н, SCH2CH2O), 4.3 т (2Н, SCH2CH2O), 5.83 с (1Н, CH2NTrz), 6.95 м (2Н, 2CHAr), 7.32 м (2Н, 2CHAr), 8.05 с(1Н, C5HTrz), 8,73 с (1H, C3HTrz).
Пример 7. Получение 2-(2-(4-хлор-2-метилфенилокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола (7).
К раствору 0,1 г (0,000546 моль) 5-(1H-1,2,4-триазол-1-метил)-1,3,4-оксадиазол-2-тиола и 0,055 г (0,000546 моль) триэтиламина в 3 мл ацетонитрила добавляют 0,128 г (0,000546 моль) 1-(2-бромэтокси)-4-хлор-2-метилбензола, кипятят в течение 5 ч при 82°С. Избыток ацетонитрила удаляют на РПИ в вакууме водоструйного насоса, к остатку добавляют 5 мл воды и 5 мл хлороформа. Органическую фазу отделяют, водный слой промывают хлороформом (2×4 мл). Органические фазы объединяют и сушат над сульфатом магния, хлороформ удаляют на РПИ в вакууме водоструйного насоса. К остатку добавляют 5 мл диэтилового эфира, осадок отфильтровывают. Получают 0,061 г (32%) 2-(2-(4-хлор-2-метилфенилокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола с т.пл. 83-86°С.
1H ЯМР-Спектр (δ, м.д., J3, Гц): 2.04 с (3Н, СН3С6Н3), 3.66 т (2Н, SCH2CH2O), 4.31 т (2Н, SCH2CH2O), 5.82 с (2Н, 2CH2NTrz), 6.97 д (1Н, CHAr J3=8.1), 7.2 м (2Н, 2CHAr), 8.06 с (1Н, C5HTrz), 8.72 с (1Н, C3HTrz).

Пример 9.
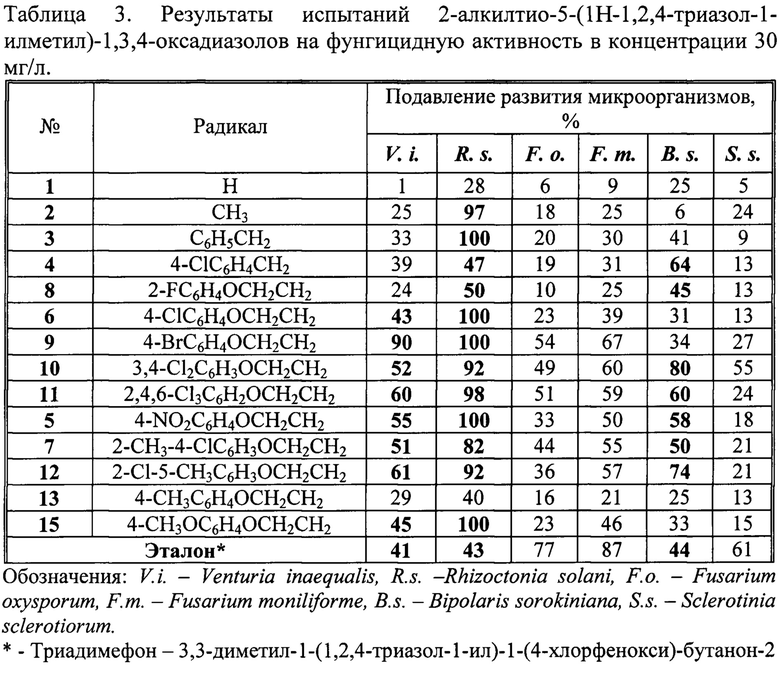
Испытания на фунгицидную активность соединений общей формулы I, проводили в экспериментах in vitro [Методические рекомендации по определению фунгицидной активности новых соединений. Черкассы: НИИТЭХИМ. 1984. 34 с.]. Действие препаратов на радиальный рост мицелия определяли растворением композиции соединения в ацетоне (0.3%) и внесением аликвоты в картофеле-сахарозный агар при 50°С до концентрации 30 мг/л по действующему веществу. Конечная концентрация ацетона в контрольных растворах с действующими веществами составили 1%. В чашки Петри, содержащие 15 мл агаровой среды, наносили иглой культуры грибов на агаровую поверхность. Образцы выдерживали в инкубаторе при 25°С и измеряли радиальный рост через 3 суток. Процент ингибирования рассчитывали по Эбботу по отношению к необработанному контролю. В качестве эталона использовали коммерческий фунгицид триадимефон в той же концентрации. Результаты испытаний представлены в таблице 3.
Пример 10. Композиция концентрата эмульсии соединения 11 (6% масс).
Действующее вещество 5-(1Н-1,2,4-триазол-1-илметил)-2-[2-(2,4,6-трихлорфенокси)этилтио]-1,3,4-оксадиазол (11) - 6 г
Алкилбензолсульфокислоты кальциевая соль (АБСК) - 2 г
Оксиэтилированный октилфенол (ОП-7) - 8 г
Циклогексанон - 29 г
о-Ксилол - 16 г
Нефтяной сольвент - 39 г.
По результатам фунгицидных испытаний in vitro 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов I, выбранные из группы, соединения 5, 7, 10, 11, 12 превосходят по фунгитоксичности эталон, известный фунгицид триадимефон (3,3-диметил-1-(1,2,4-триазол-1-ил)-1-(4-хлорфенокси)-2-бутанон) по отношению к 3 видам грибов фитопатогенов: Venturia inaequalis, Rhizoctonia solani, Bipolaris sorokiniana. Указанные соединения значительно превосходят по результатам фунгицидной активности соединения общей формулы III, представленных в прототипе. Замещенные 2-фенацилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолы ингибируют рост мицелия фитопатогенов при большей концентрации 50 мг/л не более чем на 56%, что значительно уступает фунгитоксичности наших 2-алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов I.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-Алкилтио-5-(1Н-1,2,4,-триазол-1-илметил)-1,3,4-тиадиазолы, способ их получения и фунгицидные композиции на их основе | 2020 |
|
RU2757808C1 |
| 5-Алкилтио-4-арилиденамино-3-(1,2,4-триазол-1-илметил)-1,2,4-триазолы, способ их получения и фунгицидные композиции на их основе | 2023 |
|
RU2810785C1 |
| N-Замещенные 3-алкилсульфанил-5-(1,2,4-триазол-1-илметил)-1,2,4-триазолы, способ их получения, фунгицидные и рострегуляторные композиции на их основе | 2017 |
|
RU2668212C1 |
| Способ получения 4,5-дизамещенных-1,2,4-триазол-3-тионов | 2023 |
|
RU2819169C1 |
| N-(5-(1,2,4-Триазол-1-илметил)-1,2,4-триазол-3-ил)-метанимины и способ их получения | 2023 |
|
RU2827565C1 |
| Замещенные 4-(азол-1-илметил)-1-фенил-5,5-диалкилспиро-[2.5]октан-4-олы, способ их получения (варианты), фунгицидная и рострегуляторная композиции на их основе | 2016 |
|
RU2648240C1 |
| Способ получения 3-азолилпропанолов | 2022 |
|
RU2786670C1 |
| Фунгицидная композиция N-(5-(1,2,4-триазол-1-илметил)-1,2,4-триазол-3-ил)-метаниминов | 2023 |
|
RU2819160C1 |
| Замещенные 4-(азол-1-илметил)-1,6-бисфенилдиспиро[2.1.2.3]декан-4-олы, способ их получения и фунгицидная композиция на их основе | 2019 |
|
RU2730490C1 |
| ЗАМЕЩЕННЫЕ 2-(1,2,4-ТРИАЗОЛ-1-ИЛМЕТИЛ)-6-БЕНЗИЛИДЕН-1,4-ДИОКСАСПИРО[4.5]ДЕКАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2326878C1 |
Изобретение относится к 2-алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазолам общей формулы I
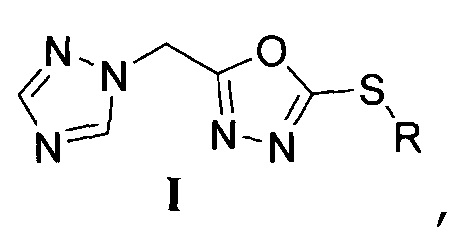
где R арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, нитрогруппу, n означает целое число от 0 до 5, m означает целое число от 1 до 2. Также изобретение относится к способу получения соединений формулы I и к фунгицидной композиции, их содержащей. Технический результат - соединения общей формулы I, обладающие фунгицидной активностью. 3 н.п. ф-лы, 3 табл., 10 пр.
1. 2-Алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазол общей формулы I
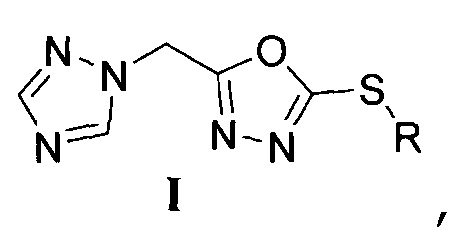
где R означает арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилоксигруппу с числом атомов углерода от 1 до 4, нитрогруппу, n означает целое число от 0 до 5, m означает целое число от 1 до 2, за исключением 2-(2-(3-метилфенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола и 2-(2-(2-фторфенокси)этилтио)-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазола, или его агрохимически или фармацевтически приемлемые соли.
2. Способ получения 2-алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазолов общей формулы I по п. 1

где R означает арилоксиалкильную группу общей формулы XnC6H5-nO(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилоксигруппу с числом атомов углерода от 1 до 4, нитрогруппу, n означает целое число от 0 до 5, m означает целое число от 1 до 2,
заключающийся в том, что 5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазол-2-тиол IV вводят во взаимодействие с алкилгалогенидами V в присутствии третичных аминов в полярных апротонных растворителях при температурах от 20 до 155°С:
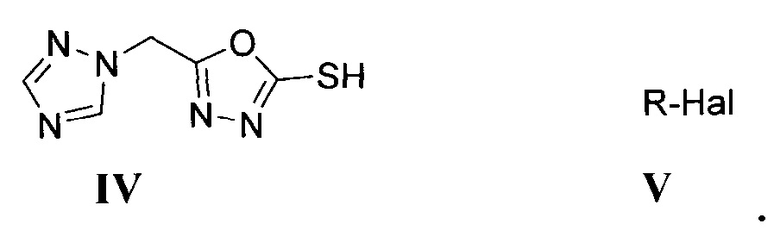
3. Фунгицидная композиция, содержащая фунгицид в концентрации 0.3-25 мас.% и вспомогательные вещества, отличающаяся тем, что в качестве фунгицида используют 2-алкилтио-5-(1Н-1,2,4-триазол-1-илметил)-1,3,4-оксадиазол формулы I по п. 1.
| Xu Liang-zhong et al., Structure and biological activities of novel triazole compounds containing 1,3,4-oxadiazole ring | |||
| Chemical Research in Chinese Universities, 2008, 24 (3), pp.299-302 | |||
| PubChem, PubChem CID: 60593342 (18.10.12), 71976933 (01.12.13), 71976936 (01.12.13), 71993052 (01.12.13), 78804603 (19.10.14), 60593317 (18.10.12), 100680942 |
Авторы
Даты
2023-04-17—Публикация
2022-03-21—Подача