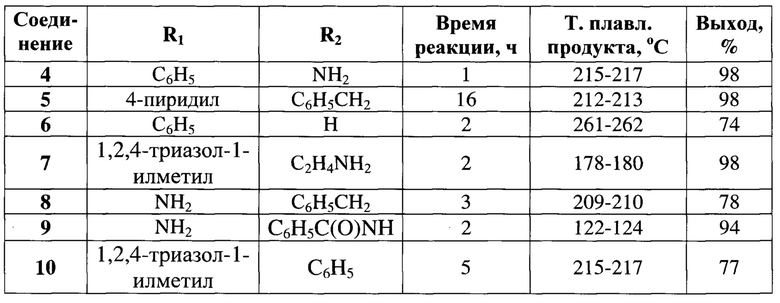
Изобретение относится к новому способу получения 4,5-дизамещенных-1,2,4-триазол-3-тионов, соединений общей формулы I:
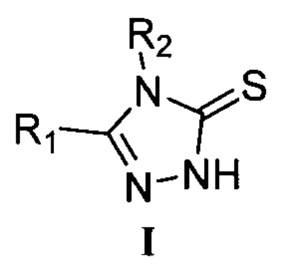
где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, гетерильную группу, выбираемую из группы: пиридил, хинолин, пиразолил, или гетерилалкильную группу, выбираемую из группы: 1,2,4-триазол-1-илметил, бензимидазол-1-илметил, a R2 означает атом водорода, амино-группу, алкильную группу с числом атомов углерода от 1 до 10, арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, арилалкильную группу общей формулы XnC6H5-n(CH2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, аминоалкил-группу общей формулы NH2(CH2)m, бензоиламино группу общей формулы (XnC6H5-n)C(O)NH, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, n означает целое число от 0 до 5, m означает целое число от 1 до 4.
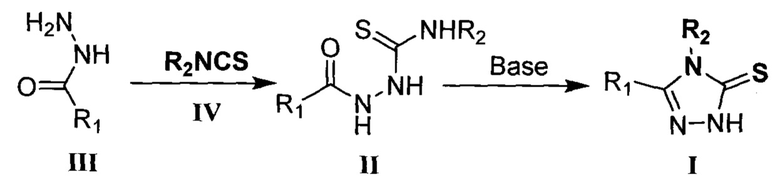
Соединения I получают методом циклоконденсации N,N'-дизамещенных тиосемикаразидов II в щелочной среде, которые получают из соответствующих гидразидов карбоновых кислот III и тиоизоцианатов IV, R1 означает гетерильную группу, выбираемую из группы: пиридил, a R2 означает алкильную группу с числом атомов углерода от 1 до 4, арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, арилалкильную группу общей формулы XnC6H5-n(CH2)m, где X, одинаковые или разные, означают атом водорода или галогена, n означает целое число от 0 до 5, m означает целое число от 1 до 4 [Gulerman N.N. et al. Synthesis and structure elucidation of some new thioether derivatives of l,2,4-triazoline-3-thiones and their antimicrobial activities /Д1 Farmaco. - 2001. -Vol. 56, №. 12. - P. 953-958.]. Недостатком такого метода получения является использование малодоступных тиоизоцианатов IV, получаемых взаимодействием аминов с высокотоксичным тиофосгеном. Данный метод позволяет получить целевые соединения с суммарным выходом от 60 до 80%.
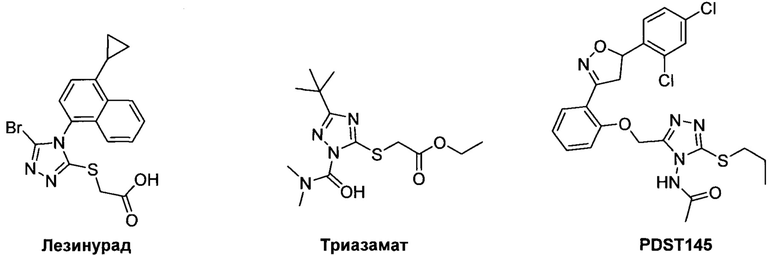
Производные 1,2,4-триазол-3-тионов представляют собой классгетероциклических соединений с широким спектром биологической активности. На рынок современных лекарственных препаратов недавно вышел препарат лезинурад, являющийся ингибитором переносчика мочевой кислоты (URAT1) [Dalbeth N. Lesinurad, a selective uric acid reabsorption inhibitor, in combination with febuxostat in patients with tophaceous gout: findings of a phase III clinical trial //Arthritis & Rheumatology. - 2017. - V. 69. - №. 9. - P. 1903-1913.], применяющийся при лечении гиперурикемии, в его структуру входит 3-алкилтио-1,2,4-триазольный фрагмент, предшественником которого является соответствующий 5-бром-4-(4-циклопропилнафталин-1-ил)-1,2,4-триазол-3-тион. Также производные 1,2,4-триазол-3-тиона могут выступать в качестве промежуточных соединений для получения инсектицидов, например, триазамата, который применяется в современной агрохимии для борьбы с тлей [Moores G.D., Devine G.J., DEvoNsHIRE A. L. Insecticide-insensitive acetylcholinesterase can enhance esterase-based resistance in Myzus persicae and Myzus nicotianae //Pesticide Biochemistry and Physiology. - 1994. - V. 49. - №. 2. - P. 114-120.]. Кроме того, серия S- и N-замещенных-4-амино-1,2,4-триазол-3-тионов, обладающая противотуберкулезной активностью, известная в научной литературе как PDST-drugs, находится на стадии клинических испытаний [Dixit P.P., Dixit P.P., Thore S.N. Hybrid triazoles: Design and synthesis as potential dual inhibitor of growth and efflux inhibition in tuberculosis //European journal of medicinal chemistry. - 2016. - V. 107. - P. 38-47.].
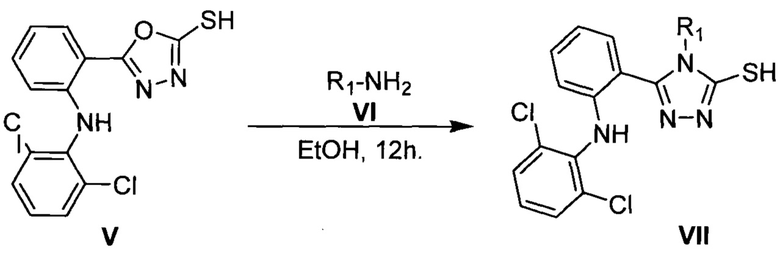
Наиболее близким к заявленному методу получения соединений общей формулы I является реакция конденсации 5-(2-(2,6-дихлорфениламино)бензил)-1,3,4-оксадиазол-2-тиолов V с различными аминами VI, где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают амино- или гидрокси-группу; гетерильную группу, выбираемую из группы: пиридил, тиазол; в этаноле с получением 5-(2-(2,6-дихлорфениламино)бензил-4-замещенных-1,2,4-триазол-3-тиолов VII [Chidambaranathan N. et al. Synthesis and evaluation of anti-ulcerogenic studies of some novel 1,3,4-oxadiazole and 3-mercapto-1,2,4-triazole. // International Journal of Toxicological and Pharmacological Research. -2010. -Vol. 2, №. 2. - P. 59-67.]. Целевые 4-арил- и 4-гетерил-5-дизамещенные-1,2,4-триазол-3-тиолы были получены с выходами от 57 до90%. Авторы не приводят примеров данной реакции с алкил-, арилалкил- или гетерилалкиламинами.
Поставленная задача решается разработкой нового способа получения 4,5-дизамещенных-1,2,4-триазол-3-тионов, соединений общей формулы I, где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, гетерильную группу, выбираемую из группы: пиридил, хинолинил, пиразолил, или гетерилалкильную группу, выбираемую из группы: 1,2,4-триазол-1-илметил, бензимидазол-1-илметил, a R2 означает атом водорода, амино-группу, алкильную группу с числом атомов углерода от 1 до 10, арильную группу общей формулы XnC6H5-n где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, арилалкильную группу общей формулы XnC6H5-n(СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, аминоалкил-группу общей формулы NH2(CH2)m, бензоиламино группу общей формулы (XnC6H5-n)C(O)NH, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, n означает целое число от 0 до 5, m означает целое число от 1 до 4, которые получают взаимодействием 5-замещенных-1,3,4-тиадиазол-2-тионов с общей формулой VIII, где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означаютатом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, гетерильную группу, выбираемую из группы: пиридил, хинолинил, пиразолил, или гетерилалкильную группу, выбираемую из группы: 1,2,4-триазол-1-илметил, бензимидазол-1-илметил, по реакции типа ANRORC с аминами IX, где R2 означает атом водорода, амино-группу, алкильную группу с числом атомов углерода от 1 до 10, арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, арилалкильную группу общей формулы XnC6H5-n (CH2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, аминоалкил-группу общей формулы NH2(CH2)m, бензоиламино группу общей формулы (XnC6H5-n)C(O)NH, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, n означает целое число от 0 до 5, m означает целое число от 1 до 4, и нагревают при температуре от 65 до 175°С в полярных протонных растворителях.
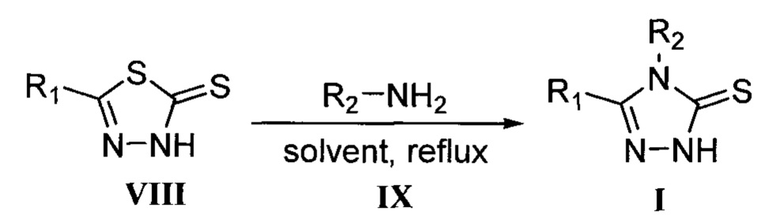
Исходные 5-замещенные-1,3,4-тиадиазол-2-тионы получают в две стадии из ацилгидразидов. Гидразиды кислот X получают по общеизвестным описанным в литературе методикам. Далее их вводят в реакцию с сероуглеродом в присутствии основания гидроксида калия при комнатной температуре в этаноле на протяжении 2 ч, затем полученную калиевую соль XI растворяют в концентрированной серной кислоте (98%) и перемешивают в течение 2-3 ч. Реакционную массу подщелачивают водным раствором аммиака до рН=6-7 и получают 5-замещенных-1,3,4-тиадиазол-2-тионы VIIIс хорошим выходом. Во всех случаях R1 означает алкильную группу с числом атомов углерода от 1 до 10, арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4; арилалкильную группу общей формулы XnC6H5-n (СН2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4; гетерильную группу, выбираемую из группы: пиридил. [Karabanovich G. Development of 3,5-dinitrobenzylsulfanyl-l,3,4-oxadiazoles and thiadiazoles as selective antitubercular agents active against replicating and nonreplicating Mycobacterium tuberculosis //Journal of Medicinal Chemistry. - 2016. - V. 59, №. 6. - P. 2362-2380.].
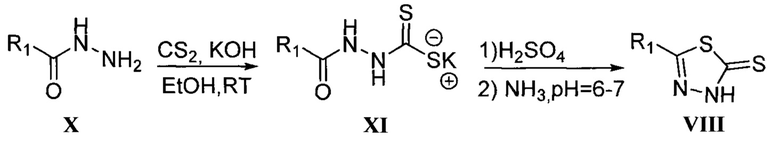
Ключевые исходные 5-замещенные-1,3,4-тиадиазол-2-тионы с общей формулой VIII, где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, гетерильную группу, выбираемую из группы: пиридил, хинолинил, пиразолил, или гетерилалкильную группу, выбираемую из группы: 1,2,4-триазол-1-илметил, бензимидазол-1-илметил, были получены по аналогичным методикам из гидразидов соответствующих кислот X с выходами от 32 до 85%.
Изобретение может быть проиллюстрировано следующими примерами:
Пример 1. Получение 5-(1,2,4-триазол-1-илметил)-1,3,4-тиадиазол-2-тиона (1).
К 14 мл (0,26 моль) 96%-ной концентрированной серной кислоты, охлажденной в ледяной бане до 5°С, добавляют 1,28 г калиевой соли 2-(1,2,4-триазол-1-илацетил) гидразинкарбодитионовой кислоты и перемешивают реакционную смесь в течение 2 ч. Затем реакционную массу подщелачивают 25% раствором аммиака до рН=6-7, при температуре реакционной массы не выше 15-20°С.Осадок отфильтровывают, добавляют 15 мл изопропанола, кипятят 15 мин и декантируют. Процедуру повторяют 4 раза. Органические фазы объединяют и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Остаток перекристаллизовывают из 2 мл изопропанола. Получают 0,846 г (85%) 5-(1,2,4-триазол-1-илметил)-1,3,4-тиадиазол-2-тиона с т.пл. 179-181°С.
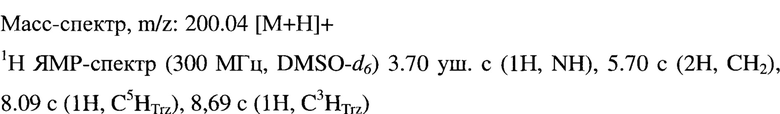
Пример 2. Получение 5-(4-пиридил)-1,3,4-тиадиазол-2-тиона (2).
К 14 мл (0,26 моль) 96%-ной концентрированной серной кислоты, охлажденной в ледяной бане до 5°С, добавляют 1,25 г (5 ммоль) калиевой соли 2-(4-пиридил) гидразинкарбодитионовой кислоты и перемешивают реакционную смесь в течение 2 ч. Затем реакционную массу подщелачивают 25% раствором аммиака до рН=6-7, при температуре реакционной массы не выше 15-20°С. Осадок отфильтровывают, добавляют 15 мл изопропанола, кипятят 15 мин и декантируют. Процедуру повторяют 4 раза. Органические фазы объединяют и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Остаток перекристаллизовывают из 2 мл изопропанола. Получают 0,310 г (32%) 5-(4-пиридил)-1,3,4-тиадиазол-2-тиона с т.пл. 276-277°С. 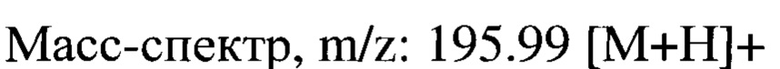

Пример 3. Получение 5-фенил-1,3,4-тиадиазол-2-тиона (3).
К 14 мл (0,26 моль) 96%-ной концентрированной серной кислоты, охлажденной в ледяной бане до 5°С, добавляют 1,25 г калиевой соли 2-фенил гидразинкарбодитионовой кислоты и перемешивают реакционную смесь в течение 2 ч. Затем реакционную массу подщелачивают 25% раствором аммиака до рН=6-7, при температуре реакционной массы не выше 15-20°С. Осадок отфильтровывают, добавляют 15 мл изопропанола, кипятят 15 мин и декантируют. Процедуру повторяют 4 раза. Органические фазы объединяют и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Остаток перекристаллизовывают из 2 мл изопропанола. Получают 0,43 г (44,1%) 5-фенил-1,3,4-тиадиазол-2-тиона с т.пл. 214-216°С.
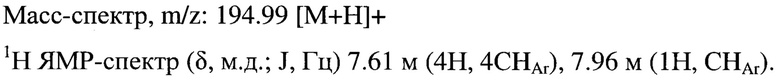
Пример 4. Получение 5-фенил-4-амино-1,2,4-триазол-3-тиона (4).
К раствору 30 мг 5-фенил-1,3,4-тиадиазол-2-тиона (0.15 ммоль) в 8 мл этанола добавляют 7,8 мг (0.15 ммоль) 98%-ного гидразин гидрата и кипятят с обратным холодильником в течение 1 ч. Реакционную массу охлаждают, отфильтровывают осадок и промывают ацетонитрилом (3×2 мл). Получают 29 мг (98%) 5-фенил-4-амино-1,2,4-триазол-3-тиона с т.пл. 215-217°С.
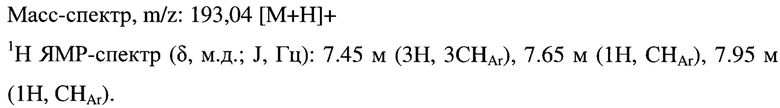
Пример 5. Получение 5-(4-пиридил)-4-бензил-1,2,4-триазол-3-тиона (5).
К раствору 60 мг 5-(4-пиридил)-1,3,4-тиадиазол-2-тиона (0.3 ммоль) в 8 мл н-пропанола добавляют 32 мг (0.3 ммоль) бензиламина и кипятят с обратным холодильником в течение 16 ч. Реакционную массу охлаждают и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Получают78,3 мг (98%) 5-(4-пиридил)-4-бензил-1,2,4-триазол-3-тиона с т.пл. 212-213°С.

Пример 6. Получение 5-фенил-2,4-дигидро-1,2,4-триазол-3-тиона (6).
К раствору 60 мг 5-фенил-1,3,4-тиадиазол-2-тиона (0.3 ммоль) в 8 мл н-пропанола добавляют 20 мг (0.3 ммоль) формиата аммония и кипятят с обратным холодильником в течение 2 ч. Реакционную массу охлаждают и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Получают 40,5 мг (74%) 5-фенил-2,4-дигидро-1,2,4-триазол-3-тиона с т.пл. 261-262°С.

Пример 7. Получение 5-(1,2,4-триазол-1-илметил)-4-(2-аминоэтил)-1,2,4-триазол-3-тиона (7).
К раствору 40 мг 5-(1,2,4-триазол-1-илметил)-1,3,4-тиадиазол-2-тиона (0.2 ммоль) в 8 мл этанола добавляют 12 мг (0.2 ммоль) этилендиамина и кипятят с обратным холодильником в течение 2 ч. Реакционную массу охлаждают и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Получают 45 мг (98%) 5-(1,2,4-триазол-1-илметил)-4-(2-аминоэтил)-1,2,4-триазол-3-тиона с т.пл. 178-180°С.
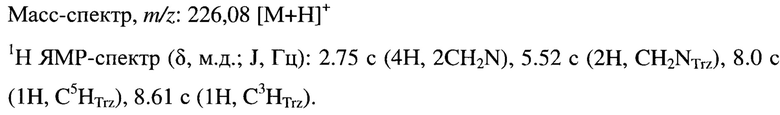
Пример 8. Получение 5-амино-4-бензил-1,2,4-триазол-3-тиона (8).
К раствору 55 мг 5-амино-1,3,4-тиадиазол-2-тиона (0.41 ммоль) в 10 мл н-бутанола добавляют 45 мг (0.41 ммоль) бензиламина и кипятят с обратным холодильником в течение 3 ч. Реакционную массу охлаждают и отгоняютрастворитель на РПИ в вакууме водоструйного насоса. Получают 65,9 мг (78%) 5-амино-4-бензил-1,2,4-триазол-3-тиона с т.пл. 209-210°С.
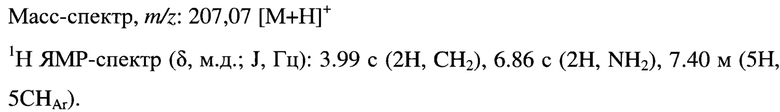
Пример 9. Получение N-(3-амино-5-тиоксо-1,2,4-триазол-4-ил) бензамида (9).
К раствору 80 мг 5-(4-пиридил)-1,3,4-тиадиазол-2-тиона (0.6 ммоль) в 10 мл изопропанола добавляют 82 мг (0.6 ммоль) бензоил гидразида и кипятят с обратным холодильником в течение 2 ч. Реакционную массу охлаждают и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Получают 141,1 мг (94%) 1Ч-(3-амино-5-тиоксо-1,2,4-триазол-4-ил) бензамида с т.пл. 122-124°С.

Пример 10. Получение 5-(1,2,4-триазол-1-илметил)-4-фенил-1,2,4-триазол-3-тиона (10).
К раствору 60 мг 5-(1,2,4-триазол-1-илметил)-1,3,4-тиадиазол-2-тиона (0.3 ммоль) в 10 мл бутанола добавляют 28 мг (0.3 ммоль) анилина и кипятят с обратным холодильником в течение 5 ч. Реакционную массу охлаждают и отгоняют растворитель на РПИ в вакууме водоструйного насоса. Получают 60 мг (77,7%) 5-(1,2,4-триазол-1-илметил)-4-фенил-1,2,4-триазол-3-тиона, с т.пл. 217-219°С.

Представленный нами способ получения 4,5-дизамещенных-1,2,4-триазол-3-тионов, соединений общей формулы I, является более удобным, по сравнению с ранее представленным, по реакции конденсации 5-(2-(2,6-дихлорфениламино)бензил)-1,3,4-оксадиазол-2-тиолов V с различными аминами VI. Реакция протекает значительно быстрее на аналогичных субстратах и с более высокими выходами до 98%. Было показано, что с помощью данного способа в реакцию можно вводить алкил-, арилалкил- или гетерилалкил амины, что позволяет значительно расширить ряд получаемых целевых 4,5-дизамещенных-1,2,4-триазол-3-тионов общей формулы I.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-Алкилтио-5-(1Н-1,2,4,-триазол-1-илметил)-1,3,4-тиадиазолы, способ их получения и фунгицидные композиции на их основе | 2020 |
|
RU2757808C1 |
| 5-Алкилтио-4-арилиденамино-3-(1,2,4-триазол-1-илметил)-1,2,4-триазолы, способ их получения и фунгицидные композиции на их основе | 2023 |
|
RU2810785C1 |
| N-(5-(1,2,4-Триазол-1-илметил)-1,2,4-триазол-3-ил)-метанимины и способ их получения | 2023 |
|
RU2827565C1 |
| Фунгицидная композиция N-(5-(1,2,4-триазол-1-илметил)-1,2,4-триазол-3-ил)-метаниминов | 2023 |
|
RU2819160C1 |
| 2-Алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолы, способ их получения и фунгицидные композиции на их основе | 2022 |
|
RU2794339C1 |
| N-Замещенные 3-алкилсульфанил-5-(1,2,4-триазол-1-илметил)-1,2,4-триазолы, способ их получения, фунгицидные и рострегуляторные композиции на их основе | 2017 |
|
RU2668212C1 |
| ЗАМЕЩЕННЫЕ 2-(1,2,4-ТРИАЗОЛ-1-ИЛМЕТИЛ)-6-БЕНЗИЛИДЕН-1,4-ДИОКСАСПИРО[4.5]ДЕКАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2326878C1 |
| Замещенные 4-(азол-1-илметил)-1,6-бисфенилдиспиро[2.1.2.3]декан-4-олы, способ их получения и фунгицидная композиция на их основе | 2019 |
|
RU2730490C1 |
| [2-(АЗОЛ-1-ИЛ)АЛКИЛБЕНЗИМИДАЗОЛ-1-ИЛ]АЛКАНОВЫЕ КИСЛОТЫ И ИХ ЭФИРЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И РОСТРЕГУЛЯТОРНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2008 |
|
RU2379294C1 |
| Замещенные 4-(азол-1-илметил)-1-фенил-5,5-диалкилспиро-[2.5]октан-4-олы, способ их получения (варианты), фунгицидная и рострегуляторная композиции на их основе | 2016 |
|
RU2648240C1 |
Изобретение относится к способу получения 4,5-дизамещенных-1,2,4-триазол-3-тионов, соединений общей формулы I, где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4; гетерильную группу, выбираемую из группы: пиридил, хинолинил, пиразолил, или гетерилалкильную группу, выбираемую из группы: 1,2,4-триазол-1-илметил, бензимидазол-1-илметил, a R2 означает атом водорода, аминогруппу, алкильную группу с числом атомов углерода от 1 до 10, арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, арилалкильную группу общей формулы XnC6H5-n(CH2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, аминоалкил-группу общей формулы NH2(CH2)m, бензоиламиногруппу общей формулы (XnC6H5-n)C(O)NH, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, n означает целое число от 0 до 5, m означает целое число от 1 до 4, 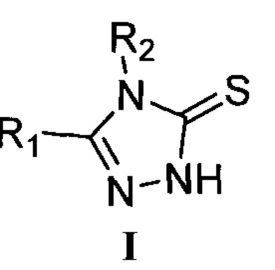 , заключающемуся в том, что 5-замещенные-1,3,4-тиадиазол-2-тионы с общей формулой VIII вводят в реакцию с аминами IX и нагревают при температуре от 65 до 175°С в полярных протонных растворителях,
, заключающемуся в том, что 5-замещенные-1,3,4-тиадиазол-2-тионы с общей формулой VIII вводят в реакцию с аминами IX и нагревают при температуре от 65 до 175°С в полярных протонных растворителях, 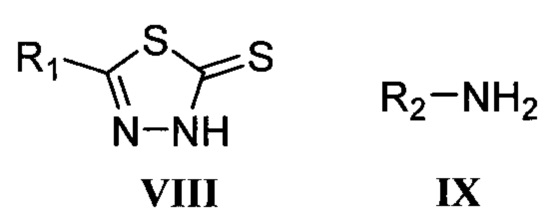 . Технический результат: разработан новый способ получения 4,5-дизамещенных-1,2,4-триазол-3-тионов, который является более удобным, более быстрым и протекает с более высокими выходами до 98%. 2 табл., 10 пр.
. Технический результат: разработан новый способ получения 4,5-дизамещенных-1,2,4-триазол-3-тионов, который является более удобным, более быстрым и протекает с более высокими выходами до 98%. 2 табл., 10 пр.
Способ получения 4,5-дизамещенных-1,2,4-триазол-3-тионов, соединений общей формулы I, где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4; гетерильную группу, выбираемую из группы: пиридил, хинолинил, пиразолил, или гетерилалкильную группу, выбираемую из группы: 1,2,4-триазол-1-илметил, бензимидазол-1-илметил, a R2 означает атом водорода, аминогруппу, алкильную группу с числом атомов углерода от 1 до 10, арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, арилалкильную группу общей формулы XnC6H5-n(CH2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, аминоалкил-группу общей формулы NH2(CH2)m, бензоиламиногруппу общей формулы (XnC6H5-n)C(O)NH, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, n означает целое число от 0 до 5, m означает целое число от 1 до 4,
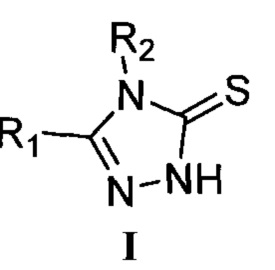
заключающийся в том, что 5-замещенные-1,3,4-тиадиазол-2-тионы с общей формулой VIII, где R1 означает арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, гетерильную группу, выбираемую из группы: пиридил, хинолинил, пиразолил, или гетерилалкильную группу, выбираемую из группы: 1,2,4-триазол-1-илметил, бензимидазол-1-илметил, вводят в реакцию с аминами IX, где R2 означает атом водорода, аминогруппу, алкильную группу с числом атомов углерода от 1 до 10, арильную группу общей формулы XnC6H5-n, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, арилалкильную группу общей формулы XnC6H5-n (CH2)m, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, аминоалкил-группу общей формулы NH2(CH2)m, бензоиламиногруппу общей формулы (XnC6H5-n)C(O)NH, где X, одинаковые или разные, означают атом водорода или галогена, алкильную группу с числом атомов углерода от 1 до 4, алкилокси группу с числом атомов углерода от 1 до 4, n означает целое число от 0 до 5, m означает целое число от 1 до 4, и нагревают при температуре от 65 до 175°С в полярных протонных растворителях. 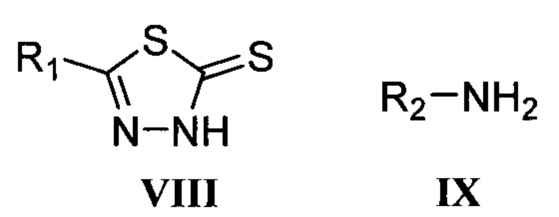
| Шуракова А.О., Цаплин Г.В., Попков С.В | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Успехи в химии и химической технологии | |||
| ТОМ XXXVI, 8, стр | |||
| Способ образования азокрасителей на волокнах | 1918 |
|
SU152A1 |
| Климонов А.И., Цаплин Г.В., Попков С.В | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Успехи в | |||
Авторы
Даты
2024-05-14—Публикация
2023-11-01—Подача