РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет предварительной заявки на патент США № 62/597226, поданной 11 декабря 2017 г., и заявки на патент Кореи №10-2017-0084805, поданной 4 июля 2017 г. Содержание каждой из этих заявок полностью включено в настоящее описание посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Конъюгаты антитело-лекарственный препарат (ADC - antibody-drug conjugate) являются новым высокоэффективным классом противораковых агентов с эффективностью при ряде раковых заболеваний. ADC обычно состоят из трех различных компонентов: связывающего клетки агента или нацеливающего фрагмента; линкера и цитотоксического агента. Линкерный компонент ADC является важным признаком при разработке противораковых агентов направленного действия, которые обладают желательной специфичностью к мишени, то есть высокой активностью в опухолевых клетках, но низкой активностью в здоровых клетках.
Поэтому существует необходимость в улучшенных линкерах, пригодных для получения ADC.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящем документе предложены конъюгаты формулы (I'):
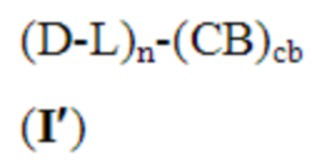
или их фармацевтически приемлемая соль,
где:
CB представляет собой нацеливающий фрагмент;
каждый из cb и n независимо представляет собой целые числа, имеющие значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый из D-L независимо представляет собой группу, имеющую структуру формулы (I''):
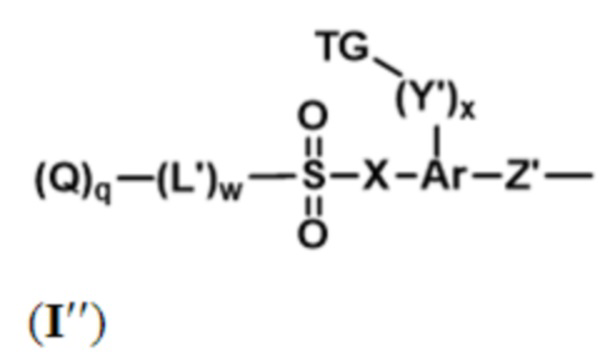
Q представляет собой активный агент, связанный с L' посредством гетероатома, предпочтительно О или N;
Z' представляет собой связующую группу;
L' представляет собой спейсерный фрагмент, присоединенный к SO2 посредством гетероатома, выбранного из O, S и N, предпочтительно O или N, и выбранного таким образом, что расщепление связи между L' и SO2 способствует расщеплению связи между L' и Q для высвобождения активного агента;
X представляет собой -O-, -C(Rb)2- или -N(Rc)-, предпочтительно -O-;
Ar представляет собой кольцо, например, такое как арил, гетероарил, циклоалкил или гетероциклоалкил, предпочтительно, арил или гетероарил;
Y' представляет собой -(CRb2)yN(Ra)-, -(CRb2)yO- или -(CRb2)yS-, расположенный таким образом, что атом N, O или S присоединен к TG, если y равно 1;
X и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, которая при активации генерирует атом N, O или S, способный вступать в реакцию с SO2 для вытеснения (Q)q-(L')w и образования 5- или 6-членного кольца, включая X-SO2 и промежуточные атомы Ar;
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый w, x и y независимо представляет собой целое число, имеющее значение 0 или 1;
каждый из Ra и Rc независимо представляет собой водород или низший алкил; и
каждый Rb независимо представляет собой водород или низший алкил; или
два Rb вместе с атомом, к которому они присоединены, образуют 3-5-членное кольцо, предпочтительно 3-4-членное кольцо;
при условии, что когда w равно 0, то q равно 1.
Настоящее изобретение также относится к композициям (например, фармацевтическим композициям), содержащим соединение формулы (I') и носитель (например, фармацевтически приемлемый носитель).
В одном аспекте изобретение относится к конъюгатам формулы (I') и композициям, содержащим такие конъюгаты, например, для применения при проведении терапии, визуализации, в качестве сенсоров, в качестве молекулярных переключателей, в качестве молекулярных машин и/или в качестве наномашин.
В другом аспекте изобретение дополнительно относится к конъюгатам формулы (I') и их фармацевтическим композициям для применения в способе доставки активного агента к клетке, причем нацеливающий фрагмент выбран для связывания с молекулой, ассоциированной с клеткой-мишенью. В частности, настоящие соединения, конъюгаты и композиции могут быть пригодны для ингибирования аномального клеточного роста или лечения пролиферативного расстройства у млекопитающего (например, человека), такого как, где клетка-мишень представляет собой раковую клетку, а нацеливающий фрагмент выбран для связывания с молекулой, ассоциированной с раковой клеткой (и не ассоциированной со здоровыми клетками или по меньшей мере преимущественно ассоциированной с опухолевыми клетками, а не здоровыми клетками).
Настоящие конъюгаты формулы (I') и их фармацевтические композиции могут быть пригодны для лечения состояний, таких как рак, ревматоидный артрит, рассеянный склероз, болезнь «трансплантат против хозяина» (БТПХ), отторжение трансплантата, волчанка, миозит, инфекция, иммунодефицит, например, СПИД и воспалительные заболевания у млекопитающего (например, человека).
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
ФИГ. 1 проиллюстрированы результаты анализа ферментативного расщепления соединения A-1.
ФИГ. 2 проиллюстрированы результаты анализа ферментативного расщепления соединения A-2.
ФИГ. 3 проиллюстрированы результаты анализа ферментативного расщепления соединения A-3.
ФИГ. 4 проиллюстрированы результаты анализа ферментативного расщепления соединения A-4.
ФИГ. 5 проиллюстрированы результаты анализа ферментативного расщепления соединения B-1.
ФИГ. 6 проиллюстрированы результаты анализа ферментативного расщепления соединения B-3.
ФИГ. 7 проиллюстрированы результаты анализа ферментативного расщепления (pH 7,4) соединения B-2.
ФИГ. 8 проиллюстрированы результаты анализа ферментативного расщепления (pH 5,0) соединения B-2.
ФИГ. 9 проиллюстрированы результаты анализа ферментативного расщепления соединения B-4.
ФИГ. 10 проиллюстрированы результаты анализа ферментативного расщепления соединения C-3.
ФИГ. 11 проиллюстрированы результаты анализа стабильности соединения A-1.
ФИГ. 12 проиллюстрированы результаты анализа in vitro соединения D-1-AB.
ФИГ. 13 проиллюстрированы результаты испытания in vivo соединения D-1-AB, D-2-AB, D-8-AB и D-16-AB.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединениям и конъюгатам, содержащим расщепляемый линкер, и способам их применения. Репрезентативные соединения и конъюгаты, описанные в данном документе, включают активный агент (например, химический фактор, биологический фактор, гормон, олигонуклеотид, лекарственный препарат, токсин, лиганд, зонд для обнаружения и т. д.), имеющий желаемую функцию или активность, функциональную группу, которая подвергается химической реакции (например, физико-химической реакции и/или биологической реакции) в заданных условиях для высвобождения нуклеофильного гетероатома, и функциональную группу SO2, расположенную проксимально относительно нуклеофильного гетероатома таким образом, что она может вступать в реакцию с нуклеофильным гетероатомом в ходе реакции внутримолекулярной циклизации с высвобождением активного агента. В некоторых вариантах осуществления соединения и конъюгаты, описанные в данном документе, дополнительно содержат нацеливающий фрагмент (например, олигопептид, полипептид, антитело и т. д.), обладающий специфичностью связывания для желаемого рецептора-мишени или другой молекулы, ассоциированной с клеткой-мишенью.
Определения
Значение термина «алкил» понятно в данной области техники. Например, термин «алкил», используемый отдельно или в качестве большего фрагмента, такого как «алкокси», «галогеналкил», «циклоалкил», «гетероциклоалкил» и тому подобное, может относиться к углеводороду с линейной или разветвленной цепью, который является полностью насыщенным. Как правило, алкильная группа с линейной или разветвленной цепью представляет собой ациклическую группу, имеющую от 1 до около 20 атомов углерода, предпочтительно от 1 до около 10 атомов углерода, если не указано иное. Примеры линейных и разветвленных алкильных групп включают, но не ограничиваются ими, метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, н-пентил, н-гексил, н-гептил и н-октил. C1-C6 алкильная группа с линейной или разветвленной цепью также называется «низшей алкильной» группой. Алкильные группы, имеющие две открытые валентности, иногда обозначаются суффиксом «ен», как в термине «алкилен». Типичные алкиленовые группы включают метилен, этилен, пропилен и тому подобное.
Кроме того, термин «алкил» (или «низший алкил») может включать как «незамещенные алкилы», так и «замещенные алкилы», последний из которых относится к алкильным фрагментам, имеющим заместители, замещающие водород на одном или более атомах углерода углеводородного каркаса. Такие заместители, если не указано иное, могут включать, например, галоген, гидроксил, карбонил (такой как карбоксил, алкоксикарбонил, формил или ацил), тиокарбонил (такой как тиоэфир, тиоацетат или тиоформиат), алкоксил, фосфорил, фосфат, фосфонат, фосфинат, амино, амидо, амидин, имин, циано, нитро, азидо, сульфгидрил, алкилтио, сульфат, сульфонат, сульфамоил, сульфонамидо, сульфонил, гетероциклил, аралкил или ароматический или гетероароматический фрагмент. Специалисту в данной области техники будет понятно, что фрагменты, замещенные в углеводородной цепи, сами могут быть замещены, если это необходимо. Например, заместители замещенного алкила могут включать замещенные и незамещенные формы алкила, амино, азидо, имино, амидо, фосфорила (включая фосфонат и фосфинат), сульфонила (включая сульфат, сульфонамидо, сульфамоил и сульфонат) и силильные группы, а также простые эфиры, алкилтио, карбонилы (включая кетоны, альдегиды, карбоксилаты и сложные эфиры), -CF3, -CN и тому подобное. Типичные замещенные алкилы описаны ниже. Циклоалкилы могут быть дополнительно замещены алкилами, алкенилами, алкокси, алкилтио, аминоалкилами, карбонилзамещенными алкилами, -CF3, -CN и тому подобными.
Термин «Cx-Cy» при использовании в сочетании с химическим фрагментом, таким как, например, ацил, ацилокси, алкил, алкенил, алкинил или алкокси, может включать группы, которые содержат от x до y атомов углерода в цепи, где «x» и «y» представляют собой целые числа, выбранные из 1 до около 20, и где x представляет собой целое число с меньшим значением, чем y, а x и y имеют неодинаковые значения. Например, термин «Cx-Cy-алкил» относится к замещенным или незамещенным насыщенным углеводородным группам, включая алкильные группы с линейной или разветвленной цепью, которые содержат от x до y атомов углерода в цепи, включая галогеналкильные группы, такие как трифторметил и 2,2,2-трифторэтил и т. д. Термины «C2-Cy-алкенил» и «C2-Cy-алкинил» относятся к замещенным или незамещенным ненасыщенным алифатическим группам, которые являются аналогичными по длине и возможному замещению алкилами, описанным выше, но которые содержат по меньшей мере одну двойную или тройную связь, соответственно. Применительно к гетероалкилам «Cx-Cy» указывает на то, что группа содержит от x до y атомов углерода и гетероатомов в цепи. Применительно к карбоциклическим структурам, таким как арильные и циклоалкильные группы, «Cx-Cy» указывает на то, что кольцо содержит от x до y атомов углерода в кольце.
Значение термина «алкокси» понятно в данной области техники и, например, может относиться к алкильной группе, предпочтительно низшей алкильной группе, имеющей присоединенный к ней кислород. Типичные алкоксильные группы включают метокси, этокси, пропокси, трет-бутокси и тому подобное.
Термин «галоген» используется по всему тексту документа и относится к фтору (F), хлору (Cl), брому (Br), или иоду (I).
Значение термина «циклоалкил» понятно в данной области техники и, например, может относиться к замещенному или незамещенному циклическому углеводороду, который является полностью насыщенным. Циклоалкил включает моноциклические и бициклические кольца. Как правило, моноциклическая циклоалкильная группа имеет от 3 до около 10 атомов углерода, более типично от 3 до 8 атомов углерода, если не указано иное. Второе кольцо бициклического циклоалкила может быть выбрано из насыщенных, ненасыщенных и ароматических колец. Циклоалкил включает бициклические молекулы, в которых один, два или три или более атомов распределены между двумя кольцами. Термин «конденсированный циклоалкил» относится к бициклическому циклоалкилу, в котором каждое из колец имеет два общих смежных атома с другим кольцом. Второе кольцо конденсированного бициклического циклоалкила может быть выбрано из насыщенных, ненасыщенных и ароматических колец. «Циклоалкенильная» группа представляет собой циклический углеводород, содержащий одну или более двойных связей.
Значение термина «арил» понятно в данной области техники и, например, может относиться к замещенным или незамещенным ароматическим группам с одним кольцом, в которых каждый атом кольца представляет собой углерод. Предпочтительно, кольцо представляет собой 5-7-членное кольцо, более предпочтительно 6-членное кольцо. Термин «арил» также включает полициклические кольцевые системы, имеющие два или более циклических колец, в которых два или более атомов углерода являются общими для двух смежных колец, при этом по меньшей мере одно из колец является ароматическим, например, другие циклические кольца могут представлять собой циклоалкилы, циклоалкенилы, циклоалкилы, арилы, гетероарилы и/или гетероциклилы. Арильные группы включают бензол, нафталин, фенантрен, фенол, анилин и т. п.
Значение терминов «гетероциклил» и «гетероцикл» понятно в данной области и, например, может относиться к замещенным или незамещенным неароматическим кольцевым структурам, предпочтительно, от 3 до 10-членных колец, более предпочтительно, 3-7-членным кольцам, чьи кольцевые структуры включают по меньшей мере один гетероатом, предпочтительно, от одного до четырех гетероатомов, более предпочтительно, один или два гетероатома. Такие гетероциклы также включают полициклические кольцевые системы, имеющие два или более циклических колец, в которых два или более атомов углерода являются общими для двух смежных колец, при этом по меньшей мере одно из колец является гетероциклическим, например, другие циклические кольца могут представлять собой циклоалкилы, циклоалкенилы, циклоалкилы, арилы, гетероарилы и/или гетероциклилы. Гетероциклильные группы включают, например, пиперидин, пиперазин, пирролидин, морфолин, лактоны, лактамы и тому подобное.
Значение термина «гетероарил» понятно в данной области техники и, например, может относиться к замещенным или незамещенным ароматическим однокольцевым структурам, предпочтительно, 5-7-членным кольцам, более предпочтительно, 5-6-членным кольцам, чьи кольцевые структуры включают по меньшей мере один гетероатом, предпочтительно, от одного до четырех гетероатомов, более предпочтительно, один или два гетероатома. Термины «гетероарил» и «гетарил» также включают полициклические кольцевые системы, имеющие два или более циклических колец, в которых два или более атомов углерода являются общими для двух смежных колец, причем по меньшей мере одно из колец является гетероароматическим, например, другие циклические кольца могут представлять собой циклоалкилы, циклоалкенилы, циклоалкилы, арилы, гетероарилы и/или гетероциклилы. Гетероарильные группы включают, например, пиррол, фуран, тиофен, имидазол, оксазол, тиазол, пиразол, пиридин, пиразин, пиридазин и пиримидин и тому подобное.
Термин «замещенный» относится к фрагментам, имеющим заместители, заменяющие водород при одном или более атомах углерода или гетероатомах фрагмента. Специалистам в данной области техники будет понятно, что «замещение» или «замещенный» включает в себя неявное условие, что такое замещение соответствует допустимой валентности замещенного атома и заместителя, и что замещение приводит к стабильному соединению, например, которое самопроизвольно не подвергается трансформации, такой как перегруппировка, циклизация, элиминирование и т. д. Используемый в настоящем документе термин «замещенный» предполагает включение всех допустимых заместителей органических соединений.
В некоторых вариантах осуществления допустимые заместители включают ациклические и циклические, разветвленные и неразветвленные, карбоциклические и гетероциклические, ароматические и неароматические заместители органических соединений. Допустимые заместители могут быть одним или более и одинаковыми или разными для соответствующих органических соединений. Для целей данного изобретения гетероатомы, такие как азот, могут иметь водородные заместители и/или любые допустимые заместители органических соединений, описанных в данном документе, которые удовлетворяют валентности гетероатомов. Заместители могут включать любые заместители, описанные в данном документе, например, галоген, гидроксил, карбонил (такой как карбоксил, алкоксикарбонил, формил или ацил), тиокарбонил (такой как тиоэфир, тиоацетат или тиоформиат), алкоксил, фосфорил, фосфат, фосфонат, фосфинат, амино, амидо, амидин, имин, циано, нитро, азидо, сульфгидрил, алкилтио, сульфат, сульфонат, сульфамоил, сульфонамидо, сульфонил, гетероциклил, алкил, аралкил или ароматический или гетероароматический фрагмент. Специалисту в данной области техники будет понятно, что заместители сами могут быть замещены, если это необходимо. Если специально не указано, что они являются «незамещенными», подразумевается, что ссылки на химические фрагменты в данном описании включают замещенные варианты. Например, ссылка на «арильную» группу или фрагмент неявно включает как замещенные, так и незамещенные варианты.
Термин «субъект», для которого предполагается введение, включает, например, людей (то есть мужчин или женщин любой возрастной группы, например, педиатрических субъектов (например, младенцев, детей, подростков) или взрослых (например, молодых взрослых, взрослых среднего возраста или взрослых старшего возраста)) и/или других приматов (например, яванских макак, макак-резус); млекопитающих, включая коммерчески значимых млекопитающих, таких как крупный рогатый скот, свиньи, лошади, овцы, козы, кошки и/или собаки; и/или птиц, включая коммерчески значимых птиц, таких как куры, утки, гуси, перепела и/или индейки. Предпочтительными субъектами являются люди.
В контексте данного документа терапевтическое средство, которое «предотвращает» расстройство или состояние, может, например, относиться к соединению, которое в статистической выборке снижает вероятность возникновения расстройства или состояния в получавшей лечение выборке по сравнению с не получавшей лечение контрольной выборкой, или задерживает начало или уменьшает степень тяжести одного или более симптомов расстройства или состояния относительно не получавшей лечение контрольной выборки.
Термин «лечение» включает профилактическое и/или терапевтическое лечение. Термин «профилактическое или терапевтическое» лечение признан в данной области техники и включает введение хозяину одной или более рассматриваемых композиций. Если ее вводят до клинического проявления нежелательного состояния (например, заболевания или другого нежелательного состояния животного-хозяина), тогда лечение является профилактическим (т.е. оно защищает хозяина от развития нежелательного состояния), тогда как если оно вводится после проявления нежелательного состояния лечение является терапевтическим (т.е. оно предназначено для уменьшения, улучшения или стабилизации существующего нежелательного состояния или его побочных эффектов).
В определенных вариантах осуществления соединения и конъюгаты, описанные в данном документе, могут использоваться отдельно или совместно с другим типом терапевтического соединения или агента. Используемое здесь выражение «совместное введение» относится к любой форме введения двух или более различных терапевтических соединений таким образом, что второе соединение вводят в то время как ранее введенное терапевтическое соединение все еще действует в организме (например, два соединения являются одновременно эффективными у субъекта, что может включать синергетическое действие двух соединений). Например, различные терапевтические соединения и конъюгаты могут вводиться либо в одной и той же композиции, либо в отдельных композициях, одновременно или последовательно. В определенных вариантах осуществления различные терапевтические соединения и конъюгаты могут вводиться в течение одного часа, 12 часов, 24 часов, 36 часов, 48 часов, 72 часов или недели после введения другого. Таким образом, субъект, который получает такое лечение, может получить благоприятный эффект от комбинированного действия различных терапевтических соединений и конъюгатов.
Термины «аномальный рост клеток» и «пролиферативное расстройство» используются в данной заявке взаимозаменяемо. Термин «аномальный рост клеток» в контексте данного документа, если не указано иное, относится к росту клеток, который не зависит от нормальных регуляторных механизмов (например, от потери контактного ингибирования). Это включает, например, аномальный рост: (1) опухолевых клеток (опухолей), которые распространяются путем экспрессии мутированной тирозинкиназы или сверхэкспрессии рецепторной тирозинкиназы; (2) доброкачественных и злокачественных клеток других пролиферативных заболеваний, при которых происходит аберрантная активация тирозинкиназы; (3) любых опухолей, которые распространяются с помощью рецепторных тирозинкиназ; (4) любых опухолей, которые распространяются за счет аберрантной активации серина/треонин-киназы; и (5) доброкачественных и злокачественных клеток других пролиферативных заболеваний, при которых происходит аберрантная активация серина/треонин-киназы.
Термины «рак» и «раковый» относятся или описывают физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым ростом клеток. Термин «опухоль» включает одну или более раковых клеток. Примеры рака включают, но не ограничиваются ими, карциному, лимфому, бластому, саркому и лейкоз или лимфоидные злокачественные новообразования. Более конкретные примеры таких видов рака включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого («НМКРЛ»), аденокарциному легкого и плоскоклеточный рак легкого, рак брюшины, гепатоцеллюлярный рак, рак желудка, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, рак эндометрия или рак матки, рак слюнной железы, рак почки, рак простаты, рак влагалища, рак щитовидной железы, карциному печени, рак анального канала, рак полового члена, острый лейкоз, а также рак головы/мозга и шеи.
Соединения и конъюгаты по настоящему изобретению
В настоящем изобретении представлены конъюгаты формулы (I'):

или их фармацевтически приемлемая соль,
где:
CB представляет собой нацеливающий фрагмент;
каждый из cb и n независимо представляет собой целые числа, имеющие значение от 1 до около 20, предпочтительно, от 1 до около 10;
каждый из D-L независимо представляет собой группу, имеющую структуру формулы (I''):
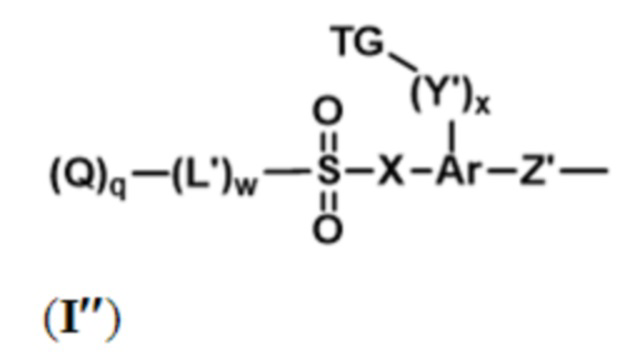
каждый Q независимо представляет собой активный агент, связанный с L' через гетероатом, предпочтительно О или N;
Z' представляет собой связующую группу;
L' представляет собой спейсерный фрагмент, присоединенный к SO2 посредством гетероатома, выбранного из O, S и N, предпочтительно O или N, и выбранного таким образом, что расщепление связи между L' и SO2 способствует расщеплению связи между L' и Q для высвобождения активного агента;
X представляет собой -O-, -C(Rb)2- или -N(Rc)-, предпочтительно -O-;
Ar представляет собой кольцо, например, такое как арил, гетероарил, циклоалкил или гетероциклоалкил, предпочтительно, арил или гетероарил;
Y' представляет собой -(CRb2)yN(Ra)-, -(CRb2)yO- или -(CRb2)yS-, расположенный таким образом, что атом N, O или S присоединен к TG, если y равно 1;
X и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, которая при активации генерирует атом N, O или S, способный вступать в реакцию с SO2 для вытеснения (Q)q-(L')w и образования 5-6-членного кольца, включая X-SO2 и промежуточные атомы Ar;
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый w, x и y независимо представляет собой целое число, имеющее значение 0 или 1;
каждый из Ra и Rc независимо представляет собой водород или низший алкил; и
каждый Rb независимо представляет собой водород или низший алкил; или
два Rb вместе с атомом, к которому они присоединены, образуют 3-5-членное кольцо, предпочтительно 3-4-членное кольцо,
при условии, что когда w равно 0, то q равно 1.
Каждый активный агент может быть любым подходящим активным агентом, как более подробно описано ниже. Хотя многие традиционные способы конъюгации требуют наличия определенных функциональных групп, таких как амины или гидроксильные группы, для образования стабильной связи, в данном документе раскрываются стратегии формирования соединений с использованием функциональных групп, таких как фенолы и третичные амины, для образования стабильных связей в конъюгатах, описанных в данном документе, в то же время обеспечивая высвобождение при заданных условиях, которые активируют триггерную группу.
Многие подходящие триггерные группы известны в данной области техники, а типичные триггерные группы и условия, которые их активируют, описаны ниже, такие как фрагменты, описанные ниже для Y. Некоторые триггерные группы содержат атомы N, O или S, но в ненуклеофильной форме. Например, группа NO2 представляет собой триггерную группу, которая в восстановительных условиях восстанавливается до группы NH2 или NHOH, которая может вступать в реакцию с SO2, а ацетатная группа представляет собой триггерную группу, которая в гидролитических условиях гидролизуется до гидроксильной группы, которая может вступать в реакцию с SO2. Другие триггерные группы не включают атом N, O или S, но при активации превращаются в нуклеофильный атом N, O или S. Например, боронатная группа является триггерной группой, которая в окислительных условиях (таких как пероксид) превращается в гидроксильную группу, которая может вступать в реакцию с SO2. Предпочтительно, триггерную группу выбирают таким образом, чтобы условия, которые ее активируют, делали это выборочно, без расщепления или деградации других частей конъюгата, таких как нацеливающий фрагмент. После генерирования нуклеофильного атома N, O или S, этот атом внутримолекулярно атакует фрагмент SO2 с образованием кольца, вытесняя фрагмент (Q)q-(L')w-H, где H связан с гетероатомом Q или L', который ранее был присоединен к фрагменту SO2.
В вариантах осуществления, где w равно 0, q равно 1 и Q непосредственно присоединен к SO2 посредством гетероатома. Соответственно, активация триггерной группы генерирует нуклеофильный гетероатом, который внутримолекулярно атакует фрагмент SO2 с образованием кольца, вытесняя активный агент Q-H, где H связан с гетероатомом, ранее присоединенным к SO2.
В вариантах осуществления, где w равно 1, L' может быть выбран для обеспечения присоединения множества вариантов Q, которые могут быть одинаковыми или разными. Соответственно, каждый случай Q непрямо присоединен к SO2 посредством спейсерного фрагмента. В таких вариантах осуществления активация триггерной группы генерирует нуклеофильный гетероатом, который внутримолекулярно атакует фрагмент SO2 с образованием кольца, вытесняя фрагмент (Q)q-L'-H, где H связан с гетероатомом в L', который ранее был прикреплен к SO2. В таких вариантах осуществления высвобождаемый гетероатом инициирует внутримолекулярную реакцию, которая вытесняет активный(-ые) агент(-ы) Q (например, если Q имеет третичный амин, который был присоединен к L' в виде четвертичного аммония) или Q-H. Например, гетероатом может подвергаться внутримолекулярной реакции циклизации с фрагментом сложного эфира, образованным с гидроксилом Q-H, образующим кольцо и выталкивающим активный агент Q-H. Альтернативно, гетероатом может подвергаться внутримолекулярной таутомеризации, которая вытесняет активный агент Q или Q-H.
Ar может представлять собой любое подходящее кольцо, включая кольцо бицикла или другой полицикл, так что фрагменты, которые подвергаются внутримолекулярной циклизации, удерживаются в непосредственной близости для облегчения данной реакции после активации триггерной группы. Планарный характер ароматических и гетероароматических колец является предпочтительным, поскольку жесткая геометрия заместителей на таких кольцах обеспечивает благоприятное расположение реакционноспособных фрагментов, хотя другие типы колец, такие как циклоалкенил или гетероциклоалкенил, могут обеспечивать аналогичную геометрию. Пяти- или шестичленное кольцо и/или число или идентичность гетероатомов в кольце и/или заместителей (например, электронодонорных или электроноакцепторных заместителей) в другом кольце могут быть выбраны для модуляции скорости циклизации на основе полученных углов связи кольца. Аналогично, более гибкие конформации циклоалкильных и гетероциклильных колец могут быть применимы, когда желательно замедлить скорость внутримолекулярной циклизации.
Z' может представлять собой любую подходящую связующую группу, которая соединяет Ar с одной или более CB группами. Как правило, связующая группа должна быть достаточно гидрофильной для обеспечения растворимости в воде и предупреждения агрегации конъюгата, например, путем включения фрагментов, таких как фрагменты полиэтиленгликоля, пептидные последовательности, фрагменты, несущие заряд (такие как карбоксилаты, амины, азотсодержащие кольца и т. д.) и т. д., чтобы сбалансировать гидрофобный характер любых алкильных цепей, которые могут быть включены. Поскольку часто выгодно получать конъюгаты модульным способом, Z' может содержать связующее звено, функциональную группу, которая возникает в результате конъюгирования одного реакционноспособного фрагмента с другим. Типичные связующие звенья более подробно описаны ниже (например, в связи с переменной Z), а типичные связующие группы включают амиды, триазолы, оксимы, карбаматы и т. д. Репрезентативные группы Z' включают группы L1'-Z, как более подробно описано ниже. В некоторых вариантах осуществления все группы D-L, присоединенные к каждому CB, являются идентичными, тогда как в других вариантах осуществления каждый CB может быть присоединен к двум или более отдельным группам D-L . Например, некоторые группы D-L могут иметь триггерную группу, которая активируется при первом условии, в то время как другие группы D-L могут иметь триггерную группу, которая активируется при втором условии, таким образом, например, один активный агент может избирательно высвобождаться при первом условии, а второй активный агент может избирательно высвобождаться при втором условии.
В описании изобретения также предложены соединения, которые могут служить в качестве промежуточных соединений или реагентов при образовании группы D-L в формуле (I'), как описано в формуле (I''). Таким образом, в некоторых вариантах осуществления, в настоящем документе предложены соединения формулы (Ia):
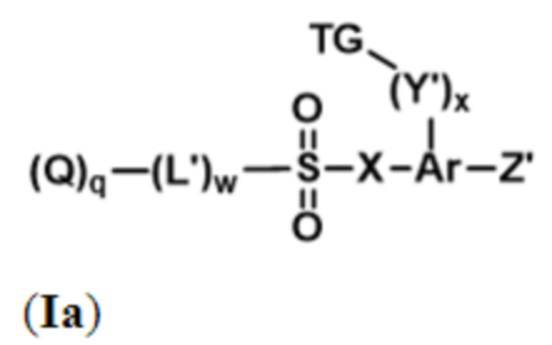
или их фармацевтически приемлемая соль, где:
каждый Q независимо представляет собой активный агент, связанный с L' через гетероатом, предпочтительно О или N;
Z' отсутствует или представляет собой связующую группу;
L' представляет собой спейсерный фрагмент, присоединенный к SO2 посредством гетероатома, выбранного из O, S и N, предпочтительно O или N, и выбранного таким образом, что расщепление связи между L' и SO2 способствует расщеплению связи между L' и Q для высвобождения активного агента;
X представляет собой -O-, -CRa2- или -NR'-, предпочтительно -O-;
Ar представляет собой кольцо, например, такое как арил, гетероарил, циклоалкил или гетероциклоалкил, предпочтительно, арил или гетероарил;
Y' представляет собой -(CRb2)yN(Ra)-, -(CRb2)yO- или -(CRb2)yS-, расположенный таким образом, что атом N, O или S присоединен к TG, если y равно 1;
X и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, которая при активации генерирует атом N, O или S, способный вступать в реакцию с SO2 для вытеснения (Q)q-(L')w и образования 5-6-членного кольца, включая X-SO2 и промежуточные атомы Ar;
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый w, x и y независимо представляет собой целое число, имеющее значение 0 или 1;
каждый из Ra и Rc независимо представляет собой водород или низший алкил; и
каждый Rb независимо представляет собой водород или низший алкил; или
два Rb вместе с атомом углерода, к которому они присоединены, образуют 3-5-членное кольцо, предпочтительно 3-4-членное кольцо,
В некоторых вариантах осуществления формул (I') и (Ia), -Y' представляет собой -(CH2)yNR''-, -(CH2)yO- или -(CH2)yS-, расположенные таким образом, что атом N, O или S присоединен к TG, если y равно 1; R'' представляет собой водород или C1-C6-алкил; и у представляет собой целое число, имеющее значение 0 или 1. В некоторых таких вариантах осуществления TG представляет собой β-галактозид, β-глюкуронид или комбинацию β-галактозида и β-глюкуронида.
В некоторых вариантах осуществления формул (I') и (Ia), (L')w связывает каждый Q с -SO2-; а каждый Q представляет собой активный агент, связанный с одной из групп L' посредством гетероатома, предпочтительно О или N, и образующий -O-, -OC(O)-, -OC(O)O- или -OC(O)NH- связь, включая гетероатом Q.
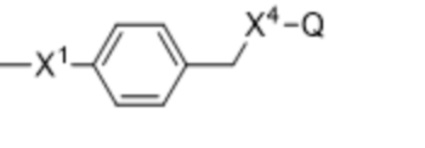
В других вариантах осуществления (Q)q-(L')w- выбран из:
 ;
;  ; и
; и 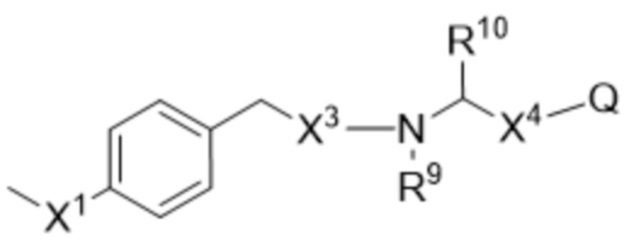 ;
;
где:
Q представляет собой активный агент, связанный с L' через гетероатом, предпочтительно О или N,
X4 отсутствует или образует -O-, -OC(O)-, -OC(O)O- или -OC(O)NH- связь, включая гетероатом Q;
X1 представляет собой -O- или -NRa-;
X2 представляет собой -O-, -OC(O)-, -OC(O)O- или -OC(O)NH-;
X3 представляет собой -OC(=O)-;
w' представляет собой целое число, имеющее значение 1, 2, 3, 4 или 5;
каждый из R9 и R10 независимо представляет собой водород, алкил, арил или гетероарил, где алкил, арил и гетероарил являются незамещенными или замещены одним или более заместителями, например, выбранными из алкила, -(CH2)uNH2, -(CH2)uNRu1Ru2 и -(CH2)uSO2Ru3;
каждый из Ru1, Ru2 и Ru3 независимо представляет собой водород, алкил, арил или гетероарил; и
u представляет собой целое число, имеющее значение от 1 до 10.
В некоторых таких вариантах осуществления (Q)q-(L')w- выбран из:
 ;
;  .
.
Кроме того, изобретение относится к промежуточным продуктам для получения конъюгатов формулы (I') или соединений в соответствии с формулой (Ia), где (Q)q-(L')w в этих формулах заменен уходящей группой, такой как галоген (предпочтительно фтор) для обеспечения присоединения (Q)q-(L')w.
В определенных таких вариантах осуществления Z' включает реакционноспособную группу (например, группу предшественника, как более подробно описано ниже в отношении Z), которую можно использовать для присоединения соединения к триггерному агенту, такому как CB (например, для получения соединения формулы (I'), как более подробно описано выше), к твердой поверхности (например, для образования матрицы на твердой подложке или сенсорных частиц) или к любой другой молекуле или подложке, представляющей интерес. В определенных предпочтительных вариантах осуществления соединение формулы (I') выбрано из: 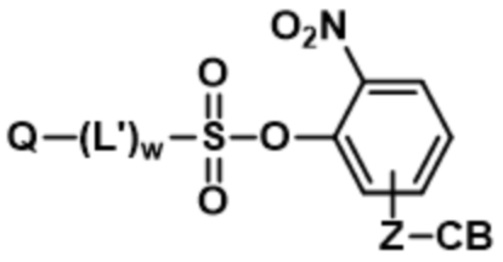 ;
;  ;
;  ;
; 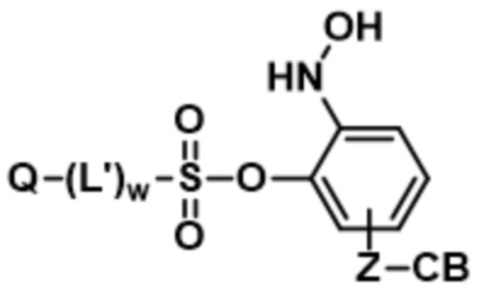 ;
; 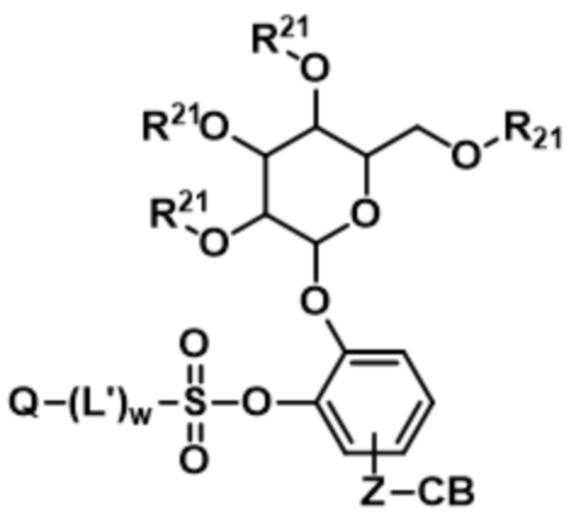 ;
;  ; и
; и 
где:
R1 представляет собой C1-C6-алкил; и
каждый из R21 и R22 независимо представляет собой водород или C1-C6алкил;
В других вариантах осуществления соединение формулы (I') выбрано из:  ;
;  ;
;  ; и
; и  .
.
В дополнительных других вариантах осуществления соединение формулы (I') выбрано из:
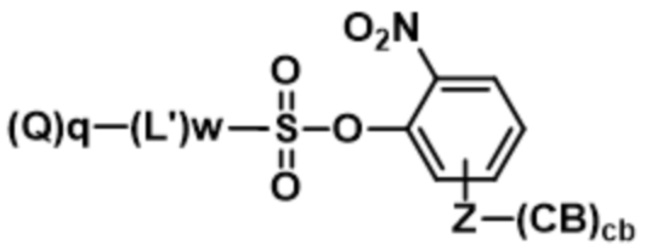 ;
; 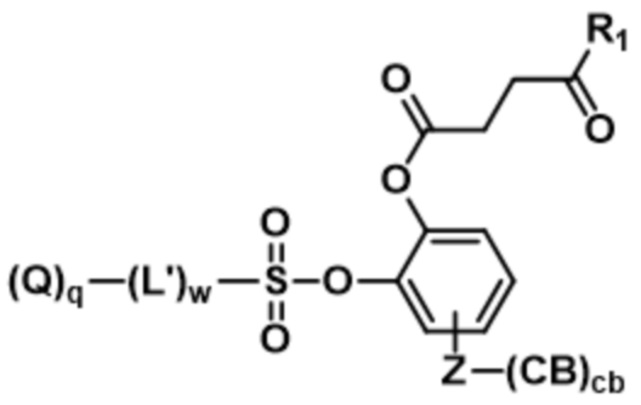 ;
;  ;
; 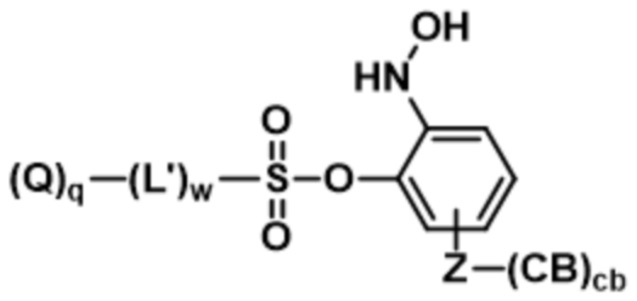 ;
; 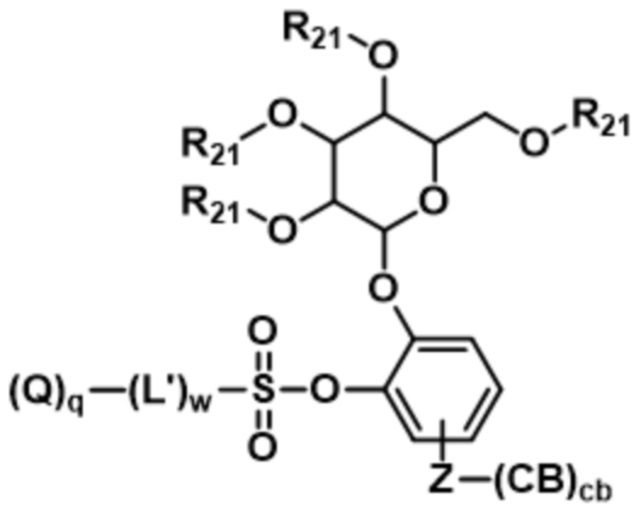 ;
;  ; и
; и  .
.
В других вариантах осуществления соединение формулы (I') выбрано из:  ;
;  ;
;  ; и
; и  .
.
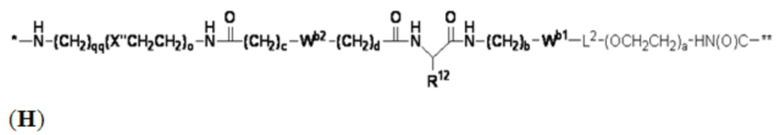
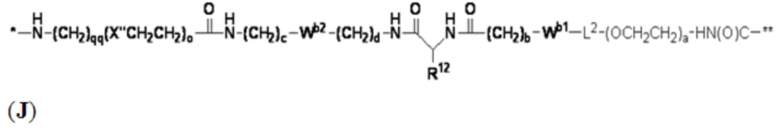
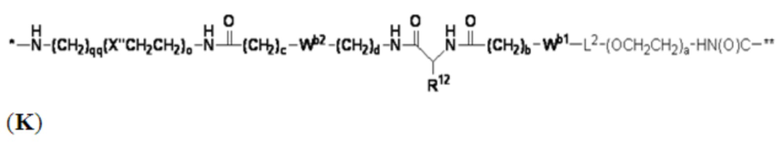
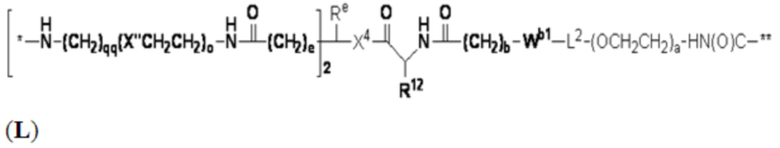
В определенных предпочтительных вариантах осуществления Z представляет собой связующую группу, имеющую структуру формул (F), (G), (H), (J), (K), (L), (M) или (N):
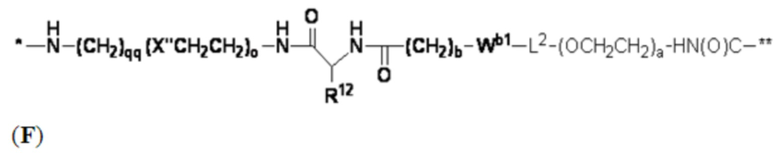
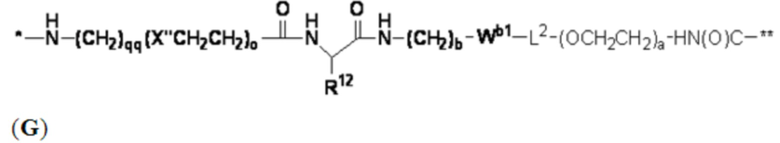
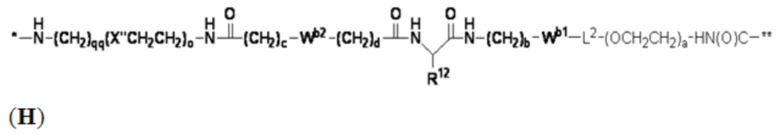
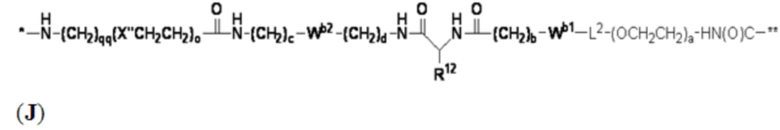

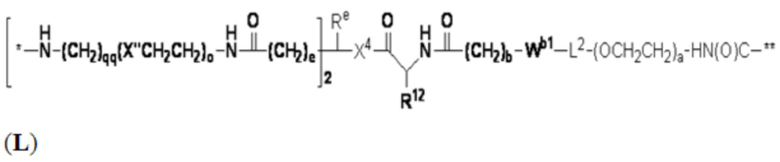
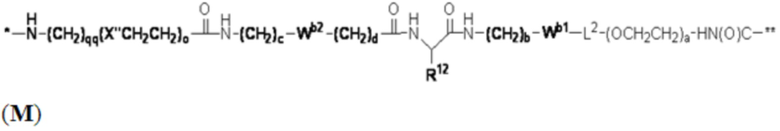

где:
* представляет собой точку присоединения к CB;
** представляет собой точку присоединения к Ar;
Re представляет собой алкил;
X'' представляет собой -O-, -S-, -NH- или -CH2-;
X4 представляет собой -NHC(O)-(CH2)g-NH- или -C(O)NH-(CH2)h-NH-;
каждый из Wb1 и Wb2 независимо представляет собой -C(O)NH-, -NHC(O)-, 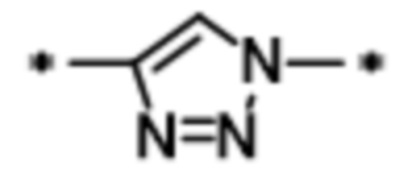 или
или 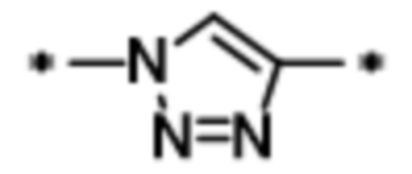 ;
;
L2 представляет собой необязательно присутствующий спейсерный фрагмент и может быть дополнительно замещен одним или более заместителями, такими как C1-C6-алкил, C5-C14-арил и C3-C8 гетероарил, причем алкил, арил и гетероарил могут быть дополнительно замещены, например, одним или более заместителями, выбранными из группы, состоящей из C1-C10-алкила, -(CH2)uNH2, -(CH2)uNRu1Ru2, -(CH2)uCO2H, -(CH2)uCO2Ru1 и -(CH2)uSO2Ru3, где каждый из Ru1, Ru2 и Ru3 независимо представляет собой водород, C1-C15 алкил, C6-C20 арил или C3-C10 гетероарил; а u представляет собой целое число, имеющее значение от 1 до около 10;
R12 представляет собой водород, C1-C8 алкил или аминокислотный фрагмент, такой как фрагмент природной аминокислоты;
каждый из b, c, d, e, g, h, o и qq независимо представляет собой целое число, имеющее значение от 1 до около 10; и
s' представляет собой целое число, имеющее значение от 1 до около 10.
В других вариантах осуществления Z представляет собой связующую группу, имеющую структуру формул (F'), (G'), (H'), (J'), (K'), (L'), (M') или (N'):

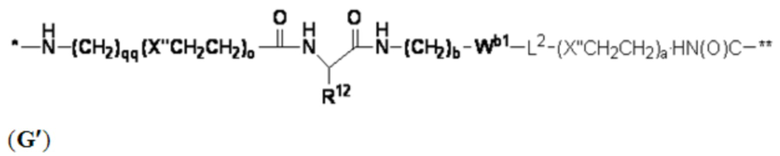



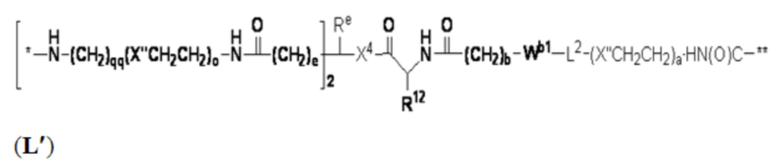

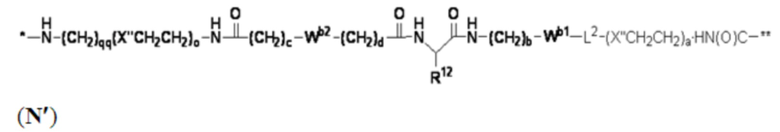
В определенных предпочтительных вариантах осуществления CB выбран из:
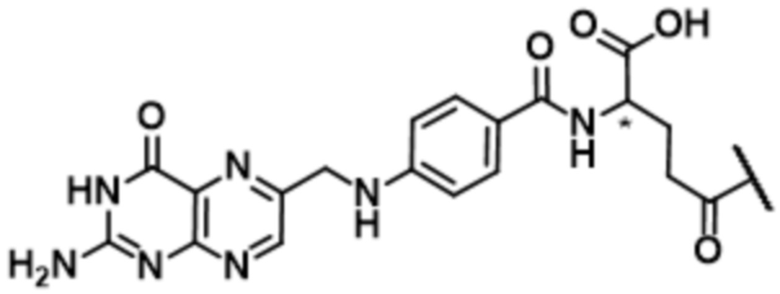 ,
, 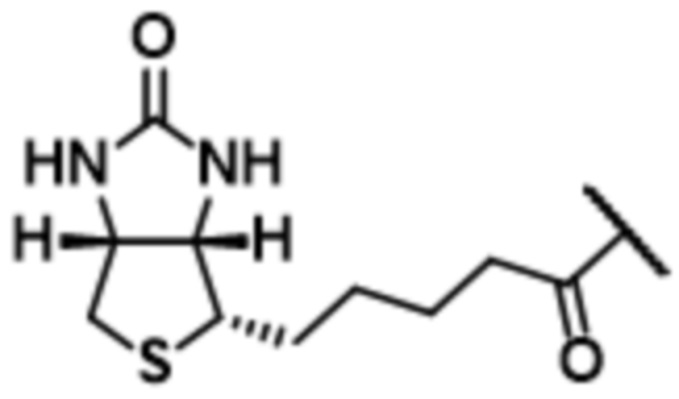 , и
, и
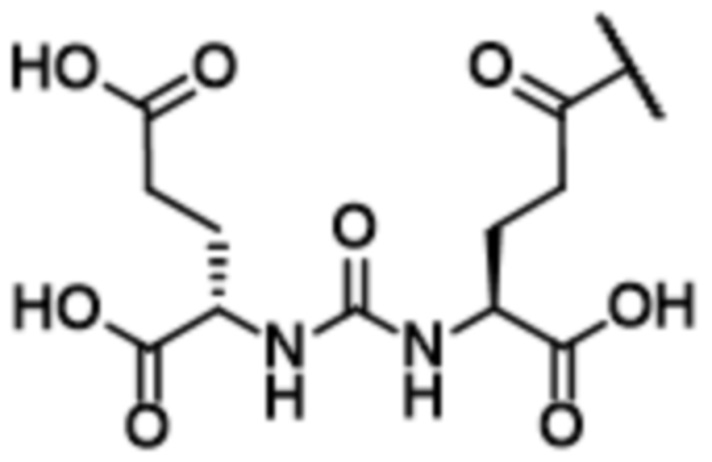 .
.
В определенных предпочтительных вариантах осуществления (Q)q-(L')w выбран из:
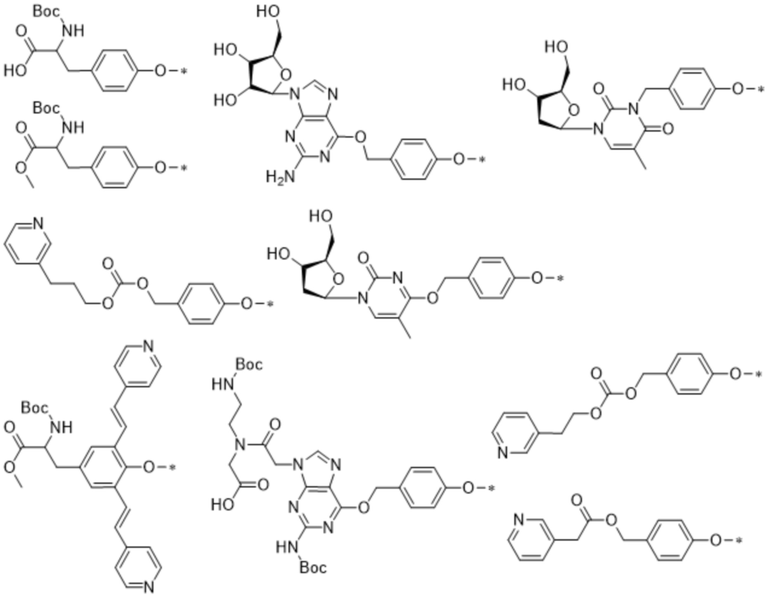
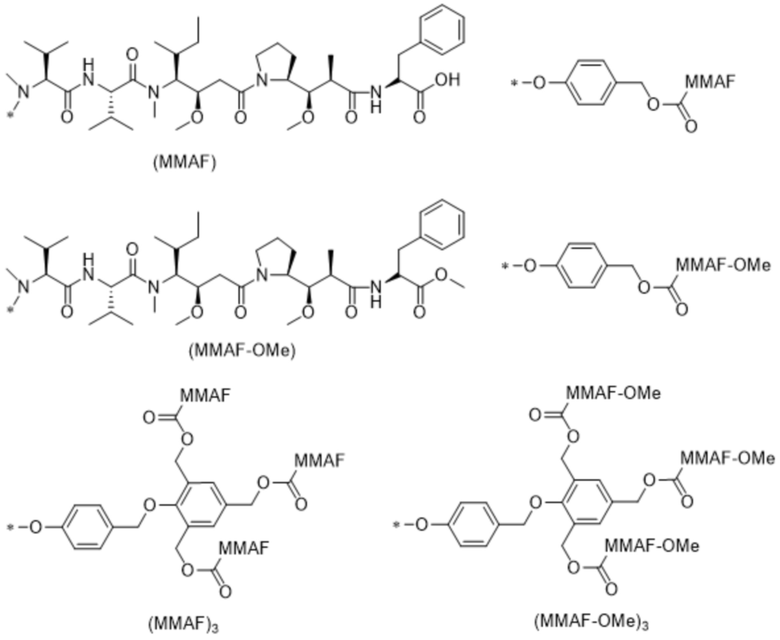
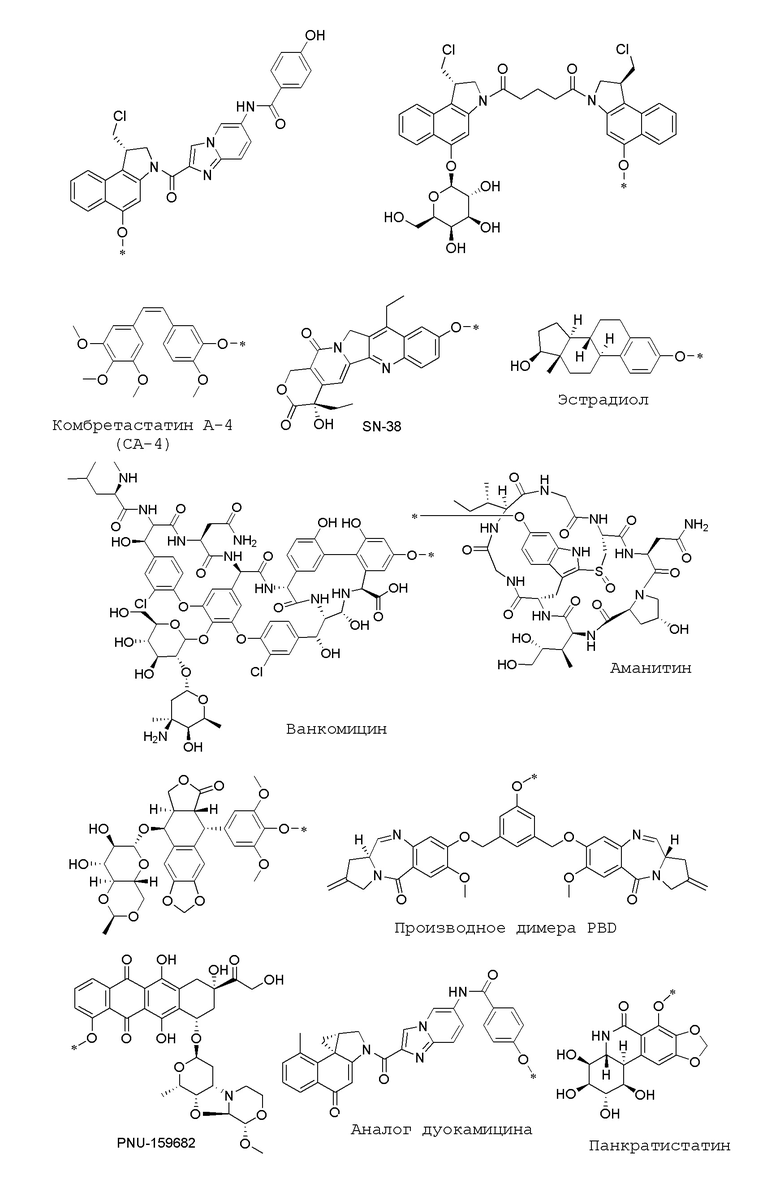

 .
.
В данном документе также предложены соединения формулы (I):

(I)
или их фармацевтически приемлемая соль, где:
X представляет собой -O-, -CH2- или -NR'-;
R' представляет собой водород, C1-C6-алкил, C6-C14-арил или C2-C20-гетероарил;
Ar представляет собой C5-C20-ароматическое кольцо, C2-C20-гетероароматическое кольцо, C2-C30-конденсированное кольцо или C5-C20-ароматическое кольцо, C2-C20-гетероароматическое кольцо;
R представляет собой заместитель на Ar или -L1'-Z-(CB)cb, предпочтительно -L1'-Z-(CB)cb;
L1' представляет собой C1-C200-алкилен или C1-C200алкилен, дополнительно содержащий по меньшей мере одну из пептидной связи, аминосвязи эфирной связи, триазольной связи, тетразольной связи, гликозидной связи, сульфонамидной связи, фосфонатной связи, сульфо-связи или дендримерную структуру;
Z представляет собой связующее звено, соединяющее CB и L1'или реакционноспособную группу (например, которая обеспечивает соединение с CB);
CB представляет собой нацеливающий фрагмент, такой как лиганд, обладающий свойством, согласно которому он связывается с рецептором;
cb представляет собой целое число, имеющее значение 0, 1 или 2;
n представляет собой представляет собой целое число, имеющее значение 1, 2, 3 или 4;
Y представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHOH, -NHNH2, -BR2R3,  или -Y'-TG, предпочтительно Y представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHNH2, -BR2R3,
или -Y'-TG, предпочтительно Y представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHNH2, -BR2R3,  или -Y'-TG;
или -Y'-TG;
R1 представляет собой C1-C6-алкил;
r представляет собой целое число, имеющее значение 1, 2, 3, 4 или 5;
Ar1 представляет собой C6-C20-арилен;
каждый из R2 и R3 независимо представляет собой водород, C1-C6алкил, C1-C6-алкокси или гидрокси;
каждый из Ra, Rb, Rc и Rd независимо представляет собой водород или C1-C6алкил;
Y' представляет собой -(CH2)xNR''-, -(CH2)xO- или -(CH2)xS-;
R'' представляет собой водород или C1-C6-алкил;
x представляет собой целое число, имеющее значение 0 или 1;
TG представляет собой триггерную группу;
Q представляет собой -Q1 или -L'-(Q1)w;
L' представляет собой C7-C30-углеводородный спейсер, имеющий -O- или -NR'''- на одном конце и -O-,-OC(O)-, -O(CO)O-, -OC(O)NR'''- или -OC(O)NR4CH2O- на другом конце, где -O-, -OC(O)-, -O(CO)O- или -OC(O)NR''''- могут быть дополнительно включены в C7-C30-углеводородный спейсер, при этом C7-C30-углеводородный спейсер дополнительно замещен одним или более заместителями, такими как C1-C6 алкил, C5-C14-арил и C3-C8-гетероарил, причем алкил, арил и гетероарил могут быть дополнительно замещены, например, одним или более заместителями, выбранными из группы, состоящей из C1-C10-алкила, -(CH2)uNH2, -(CH2)uNRu1Ru2, -(CH2)uCO2H, -(CH2)uCO2Ru1 и -(CH2)uSO2Ru3, где каждый из Ru1, Ru2 и Ru3 независимо представляет собой водород, C1-C15-алкил, C6-C20-арил или C3-C10-гетероарил; а u представляет собой целое число, имеющее значение от 1 до около 10;
Q1 представляет собой активный агент, включающий по меньшей мере одну функциональную группу из -OH, -NH-, -NR5R6, -SH, -SO2NH2 или -COOH;
R4 представляет собой водород, C1-C6-алкил, C5-C14-арил или C3-C8-гетероарил, причем алкил, арил и гетероарил являются замещенными или незамещенными;
каждый из R5 и R6 независимо представляет собой водород, C1-C6-алкил, C3-C9-циклоалкил или C5-C10-гетероарил, причем гетероарил является замещенным или незамещенным;
каждый из R''' и R'''' независимо представляет собой водород или C1-C6алкил; и
w представляет собой целое число, имеющее значение 1, 2, 3, 4 или 5.
В некоторых вариантах осуществления соединение формулы (I) содержит функциональную группу (например, Y), способную индуцировать внутримолекулярную циклизацию посредством внешней стимуляции. В определенных вариантах осуществления указанная функциональная группа вводится в орто-положении относительно X.
В некоторых вариантах осуществления R' представляет собой C1-C6-алкил, C6-C14-арил или C2-C20-гетероарил.
В некоторых вариантах осуществления Ar представляет собой C5-C20-ароматическое кольцо, C2-C20-гетероароматическое кольцо, C2-C30-конденсированное кольцо или C5-C20-ароматическое кольцо- C2-C20-гетероароматическое кольцо. Например, Ar может представлять собой бензольное кольцо, нафталиновое кольцо, пиридиновое кольцо или хинолоновое кольцо. Предпочтительно, Ar представляет собой бензольное кольцо или нафталиновое кольцо. В некоторых вариантах осуществления соединение формулы (I) представляет собой соединение, имеющее структуру в соответствии с формулой (II):

или его фармацевтически приемлемую соль.
В других вариантах осуществления соединение формулы (I) представляет собой соединение, имеющее структуру в соответствии с формулой (III):
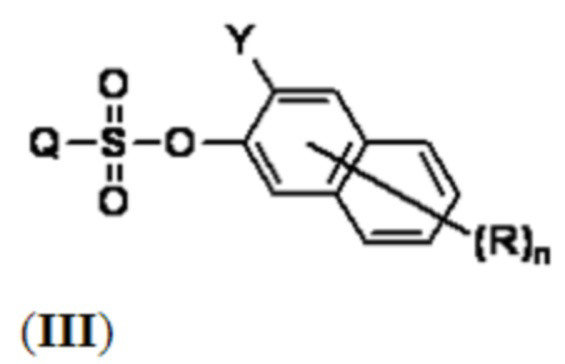
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления соединение представляет собой соединение формулы (I), (II) или (III), где R выбран из водорода, галогена (галоген), альдегида, ацеталя, кеталя, -R*, -OR*, -SR*, -NR*R**, -C(галоген)3, -CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2, -N3, -NC, -C(O)R*, -OC(O)R*, -OS(O)R*, -S(O)2R*, -S(O)2OR*, -OS(O)OR*, -OS(O)2OR*, -S(O)NR*R**, -S(O)2NR*R**, -S(O)R*, -OP(O)(OR*)2, -P(O)(OR*)2, -OP(OR*)2, -OP(OR*)N(R**)2, -OP(O)(OR*)N(R**)2, -PR*, -P(O)2, -P(O)R*, -C(O)галоген, -C(S)R*, -CO2R*, -C(S)OR*, -C(O)SR*, -C(S)SR*, -C(O)NR*R**, -C(S)NR*R**, -C(=NR*)NR*R**, -NR*C(O)R**, -NR*S(O)2OR**, -NR*S(O)R**, -NR*C(O)NR**, -SS-R* или -R*SSR**, где: каждый из R* и R** независимо представляет собой водород, C1-C18 алкил, C6-C20 арил, C3-C15 гетероцикл или C3-C20 гетероарил.
В некоторых вариантах осуществления соединение представляет собой соединение формулы (I), (II) или (III), где R представляет собой водород или *-(La-A1-Lb-Lc-Z)m-CB; где:
La представляет собой одинарную связь или C1-C20-алкилен;
A1 представляет собой -C(O)NR*-, -NR*C(O)-, -NR*-, -O-, -PO3-, -OPO3-, -SO-, -SO2- или -SO3-;
Lb представляет собой -(CH2CH2O)a- или -(CH2)a-;
R* представляет собой водород, C1-C18 алкил, C6-C20 арил, C3-C15 гетероцикл или C3-C20 гетероарил;
a представляет собой целое число, имеющее значение от 1 до около 20;
Lc представляет собой одинарную связь или C1-C20-алкилен;
n представляет собой целое число, имеющее значение 1 или 2; и
Z представляет собой связующее звено, соединяющее CB и Lc; или
Z представляет собой предшественник, выбранный из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2);
, фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2);
CB представляет собой нацеливающий фрагмент, такой как лиганд, способный связываться с рецептором; и
m представляет собой целое число, имеющее значение 0, 1 или 2;
В некоторых вариантах осуществления соединение представляет собой соединение формулы (I), (II) или (III), где R представляет собой водород или *-La-A1-Lb-Lc-Z; где:
La представляет собой одинарную связь или C1-C20-алкилен;
A1 представляет собой -C(O)NR*-, -NR*C(O)-, -NR*-, -O-, -PO3-, -PO4-, -SO-, -SO2- или -SO3-;
Lb представляет собой -(CH2CH2O)a- или -(CH2)a-;
R* представляет собой водород, C1-C18 алкил, C6-C20 арил, C3-C15 гетероцикл или C3-C20 гетероарил;
a представляет собой целое число, имеющее значение от 1 до около 20;
Lc представляет собой одинарную связь или C1-C20-алкилен;
n представляет собой целое число, имеющее значение 1 или 2; и
Z представляет собой предшественник, выбранный из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
В некоторых вариантах осуществления соединение представляет собой соединение формулы (I), (II) или (III), где R представляет собой *(-La-A1-Lb-Lc-Z)m-CB; где:
La представляет собой одинарную связь или C1-C20-алкилен;
A1 представляет собой -C(O)NR*-, -NR*C(O)-, -NR*-, -O-, -PO3-, -PO4-, -SO-, -SO2- или -SO3-;
Lb представляет собой -(CH2CH2O)a- или -(CH2)a-;
R* представляет собой водород, C1-C18 алкил, C6-C20 арил, C3-C15 гетероцикл или C3-C20 гетероарил;
a представляет собой целое число, имеющее значение от 1 до около 20;
Lc представляет собой одинарную связь или C1-C20-алкилен;
n представляет собой целое число, имеющее значение 1 или 2;
Z представляет собой связующее звено, соединяющее CB и Lc;
CB представляет собой нацеливающий фрагмент, такой как лиганд, обладающий свойством, согласно которому он связывается с рецептором; и
m представляет собой целое число, имеющее значение 1 или 2.
В некоторых вариантах осуществления соединение представляет собой соединение формулы (I), (II) или (III), где L' представляет собой C7-C30 углеводородный спейсер, дополнительно содержащий -O-, -OC(O)-, -O(CO)O- или -OC(O)NR''''-.
В некоторых вариантах осуществления соединение представляет собой соединение формулы (I), (II) или (III), где Q представляет собой -L'-(Q1)w, выбранный из:
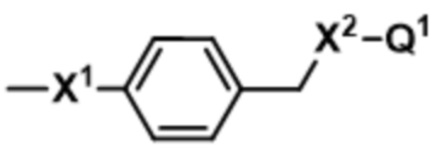 ;
; 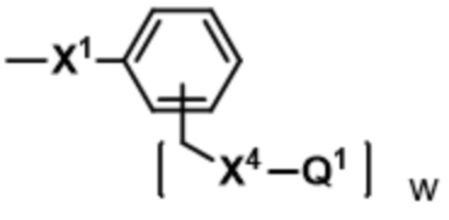 ;
; 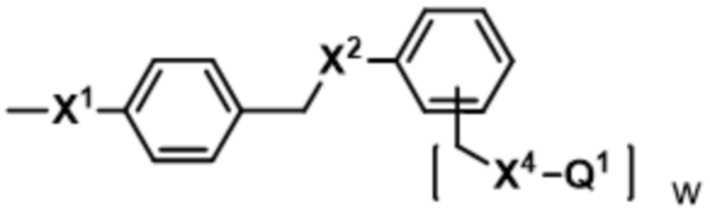 ;
; 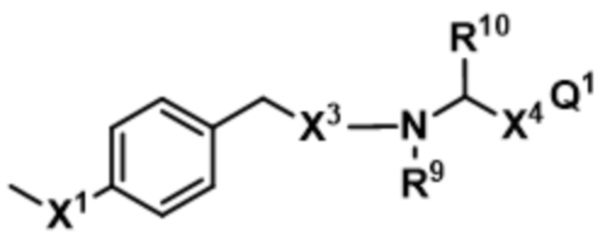 ; и
; и 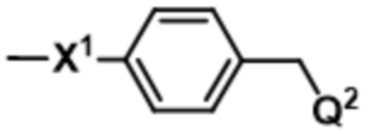
где:
Q1 представляет собой активный агент, содержащий по меньшей мере одну функциональную группу, выбранную из -OH, -NR5R6, -SH и -COOH;
Q2 представляет собой активный агент, содержащий -NR5R6;
X1 представляет собой -O- или -NR'''-;
каждый из X2 и X4 независимо отсутствуют или выбраны из -O-, -OC(O)-, -OC(O)O- и -OC(O)NH-;
X3 представляет собой -OC(=O)-;
R5 и R6 соответствуют определениям выше;
каждый из R9 и R10 независимо представляет собой водород, C1-C6-алкил, C6-C14-арил или C3-C9 гетероарил, причем указанные алкил, арил и гетероарил R9 и R10 могут быть дополнительно замещены одним или более заместителями, выбранными из группы, состоящей из C1-C10 алкила, -(CH2)uNH2, -(CH2)uNRu1Ru2 и -(CH2)uSO2Ru3, и каждый из Ru1, Ru2 и Ru3 независимо представляет собой водород, C1-C15-алкил, C6-C20-арил или C3-C10-гетероарил; а u представляет собой целое число, имеющее значение от 1 до около 10;
R''' представляет собой водород или C1-C6алкил; и
w представляет собой целое число, имеющее значение 1, 2, 3, 4 или 5.
В определенных вариантах осуществления -L'-(Q1)w выбран из:
 .
.
По меньшей мере, одна функциональная группа из Q, Q1 или Q2 выбрана из -OH, -NR5R6, -SH, а -COOH служит в качестве точки соединения активного агента с L'. Функциональная группа может существовать в виде части сложного эфира, тиоэфира, карбоната, карбамата, амида, сульфонамида, сульфоната, сульфата или другой подходящей связи; то есть фрагмент -OH, -NR5R6, -SH, и -COOH как таковой не существует, в то время как активный агент является частью конъюгата.
В некоторых вариантах осуществления Q2 представляет собой активный агент, содержащий -NR5R6, причем активный агент способен связываться в структуре четвертичного амина, например, фрагмент -NR5R6 в активном агенте способен образовывать связь четвертичного амина с L'.
В некоторых вариантах осуществления формул (I''), (Ia), (I), (II) и (III) R4 представляет собой замещенный алкил, арил или гетероарил. В некоторых таких вариантах осуществления R4 замещен одним или более заместителями, выбранными из C1-C10-алкила, -(CH2)uNH2, -(CH2)uNRu1Ru2, -(CH2)uCO2H, -(CH2)uCO2Ru1 и -(CH2)uSO2Ru3, где каждый из Ru1, Ru2 и Ru3 независимо представляет собой водород, C1-C15-алкил, C6-C20-арил или C3-C10-гетероарил; а u представляет собой целое число, имеющее значение от 1 до около 10.
В некоторых вариантах осуществления формул (I''), (Ia), (I), (II) и (III) R5 и/или R6 представляет собой гетероарил, замещенный -NR7R8, где каждый из R7 и R8 независимо, представляют собой водород, C1-C6-алкил, C3-C9-циклоалкил или C5-C14-арил.
В некоторых вариантах осуществления формул (I''), (Ia), (I), (II) и (III), Q или -(L')w-(Q)q выбран из:
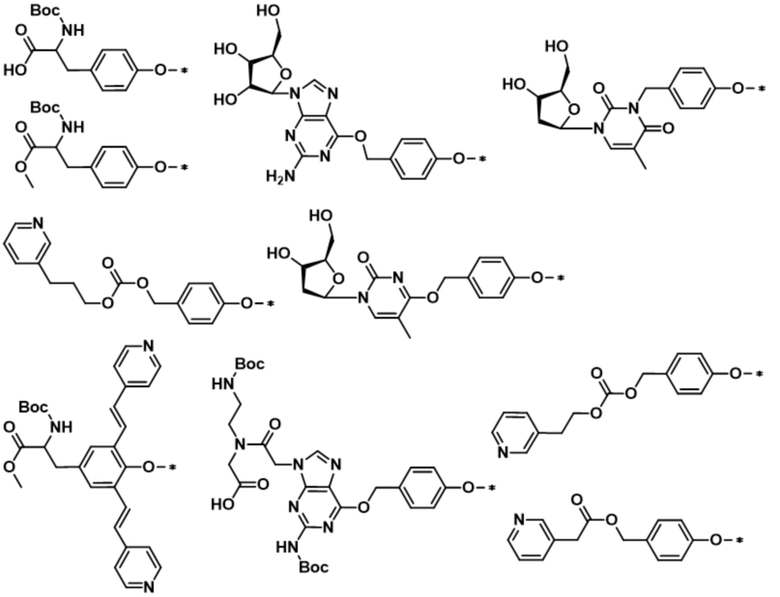

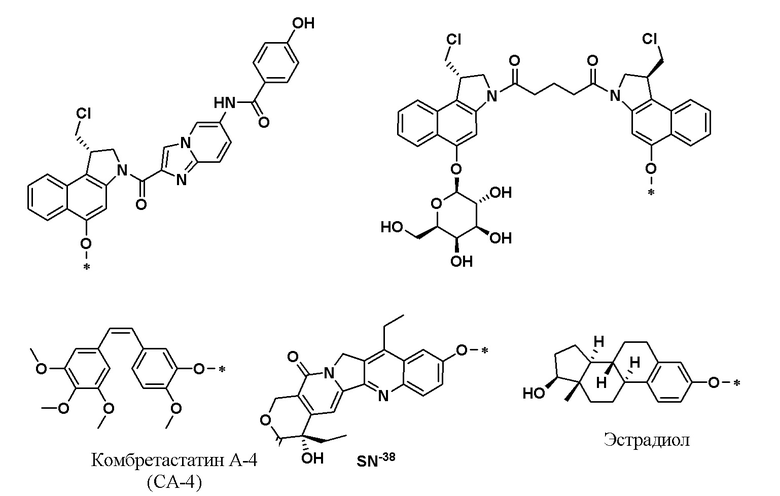
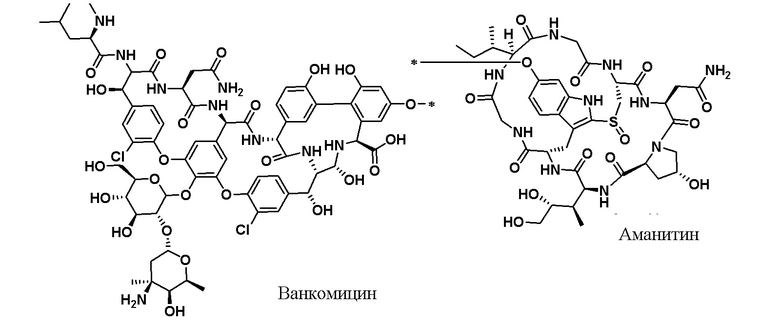
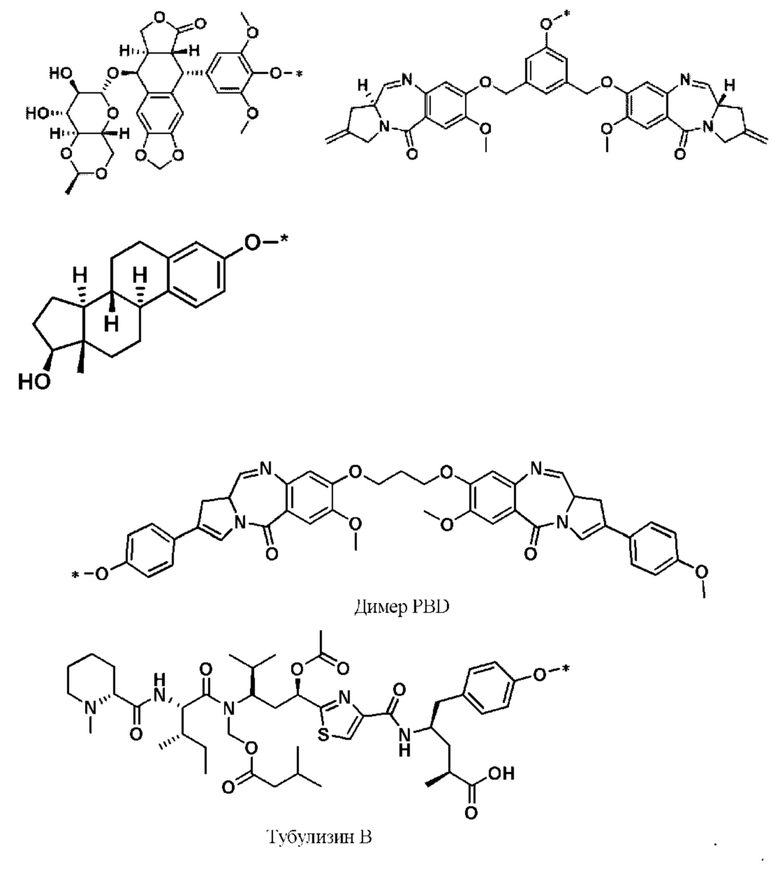
В определенных вариантах осуществления предложено соединение формулы (I), (II) или (III), где:
Y представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHOH, -BR2R3 или -Y'-TG, предпочтительно Y представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -BR2R3 или -Y'-TG;
R1 представляет собой C1-C6-алкил;
r представляет собой целое число, имеющее значение 1, 2, 3, 4 или 5;
Ar1 представляет собой фенилен, бифенилен или нафтилен;
каждый из R2 и R3 независимо представляет собой водород, C1-C6алкил, C1-C6-алкокси или гидрокси;
Y' представляет собой -(CH2)xNR''-, -(CH2)xO- или -(CH2)xS-;
R'' представляет собой водород или C1-C6-алкил;
x представляет собой целое число, имеющее значение 0 или 1;
R'' представляет собой водород или C1-C6-алкил; и
TG собой триггерную группу, такую как β-галактозид, β-глюкуронид или комбинацию β-галактозида и β-глюкуронида.
В определенных вариантах осуществления соединение формулы (I), (II) или (III) выбрано из:
 ;
; 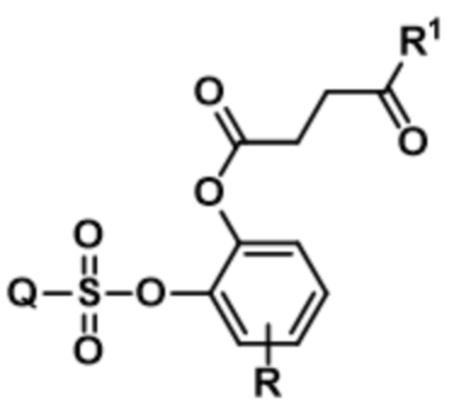 ;
; 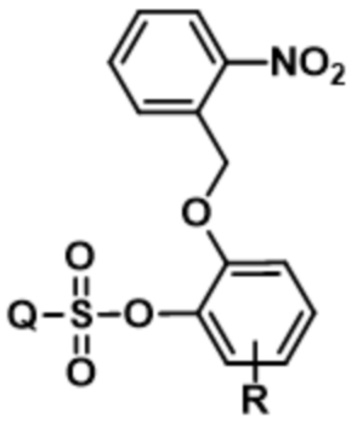 ;
; 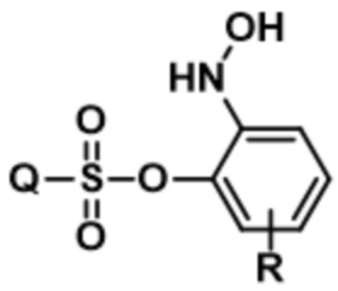 ;
;  ;
;  ; и
; и 
где:
R1 представляет собой C1-C6-алкил;
каждый из R21 и R22 независимо представляет собой водород или ацетил;
R представляет собой водород, связующую группу, *-La-A1-Lb-Lc-Z или группу, имеющую структуру формул (F), (G), (H), (J), (K), (L), (M) или (N):
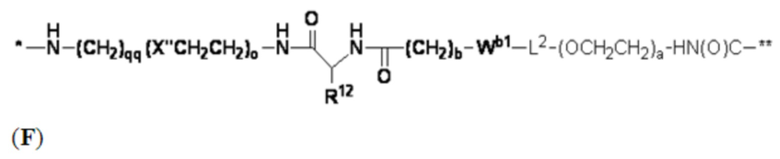

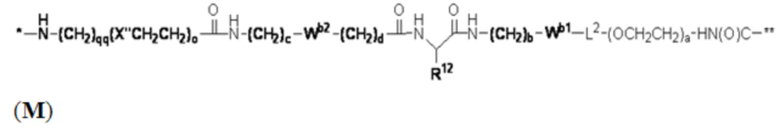

La представляет собой одинарную связь или C1-C20-алкилен;
A1 представляет собой -C(O)NH-, -NHC(O)-, -NH-, -O-, -PO3-, -PO4-, -SO-, -SO2- или -SO3-;
Lb представляет собой -(CH2CH2O)a- или -(CH2)a-;
a представляет собой целое число, имеющее значение от 1 до около 20;
Lc представляет собой C1-C20-алкилен;
X'' представляет собой -O-, -S-, -NH- или -CH2-;
каждый из Wb1 и Wb2 независимо представляет собой -C(O)NH-, -NHC(O)-,  или
или  ;
;
R12 представляет собой водород, C1-C8-алкил, аминокислотный фрагмент, -(CH2)sCOR13 или -(CH2)pNR14R15;
R13 представляет собой ОН или -NH(CH2)s'(X''CH2CH2)s''Z;
каждый из R14 и R15 независимо представляет собой водород или -(C(O)(CH2)s'(X''CH2CH2)s''Z)m-CB;
X'' представляет собой -O-, -S-, -NH- или -CH2-;
Re представляет собой C1-C8-алкил или -(L1'-Z)m-CB;
X4 представляет собой -NHC(O)-(CH2)g-NH- или -C(O)NH-(CH2)h-NH-;
каждый из b, c, d, e, g, h, o и q независимо представляет собой целое число, имеющее значение от 1 до около 10;
p представляет собой целое число, имеющее значение от 1 до около 10;
каждый из s и s'' независимо представляет собой целое число, имеющее значение от 0 до около 10;
s' представляет собой целое число, имеющее значение от 1 до около 10;
m представляет собой целое число, имеющее значение 0 или 1;
Z представляет собой изоцианид, изотиоцианид, 2-пиридилдисульфид, галоацетамид (-NHC(O)CH2-галоген), малеимид, диен, алкен, галогенид, тозилат (TsO-), альдегид, сульфонат (R-SO3-), 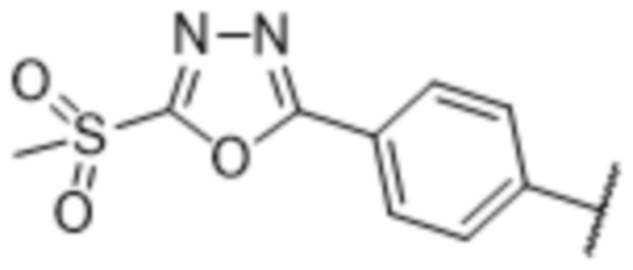 ,
,  , фосфоновую кислоту (-P(=O)(OH)2), кетон, C8-C10-циклоалкинил, -OH, -NHOH, -NHNH2, -SH, карбоновую кислоту (-COOH), ацетилен (-C≡CH), азид (-N3), амино (-NH2), сульфоновую кислоту (-SO3H), производное алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновую кислоту (-P(=O)(OH)2), кетон, C8-C10-циклоалкинил, -OH, -NHOH, -NHNH2, -SH, карбоновую кислоту (-COOH), ацетилен (-C≡CH), азид (-N3), амино (-NH2), сульфоновую кислоту (-SO3H), производное алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
CB представляет собой лиганд, выбранный из:

Q выбран из:




Высвобождение активного агента
Как описано выше, в определенных вариантах осуществления соединения и конъюгаты, описанные в данном документе, способны диссоциировать на один или более активных агентов (представленных Q, Q1, Q2) посредством реакции внутримолекулярной циклизации после химической реакции, которая активирует триггерную группу. В определенных вариантах осуществления химическая реакция представляет собой физико-химическую реакцию и/или биохимическую реакцию.
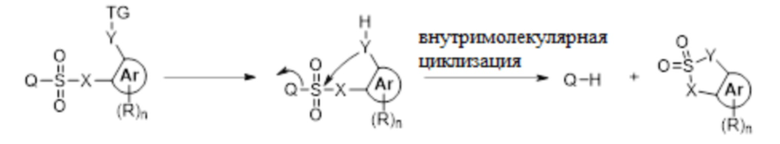
В некоторых вариантах осуществления соединения и конъюгаты, описанные в данном документе, содержат нуклеофильную функциональную группу (Y или Y'), введенную при смежном атоме на Ar относительно X (например, O). Как правило, нуклеофильную функциональную группу маскирует триггерная группа (TG), как более подробно описано ниже. После активации триггерная группа высвобождает нуклеофильную функциональную группу для вступления в реакцию с близлежащим фрагментом SO2 в ходе внутримолекулярной циклизации, в конечном итоге высвобождая один или более активных агентов (Q, Q1 или Q2). В некоторых таких вариантах осуществления один или более активных агентов высвобождаются посредством реакции внутримолекулярной циклизации после химической реакции, физико-химической реакции и/или биохимической реакции (см., например, Схему реакции 1), или активный агент высвобождается посредством 1,6-элиминирования или 1,4-элиминирования после реакции внутримолекулярной циклизации (см., например, Схему реакции 2).
В качестве примера, механизм, когда Y представляет собой -Y'-TG, проиллюстрирован на Схеме реакции 1:
Схема реакции 1:
Механизм, когда Q представляет собой 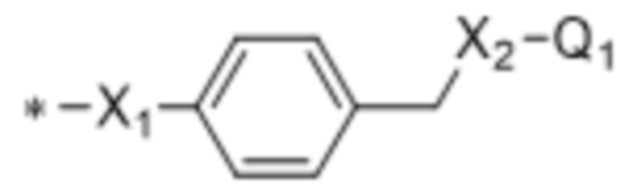 , проиллюстрирован на Схеме реакции 2:
, проиллюстрирован на Схеме реакции 2:
Схема реакции 2:
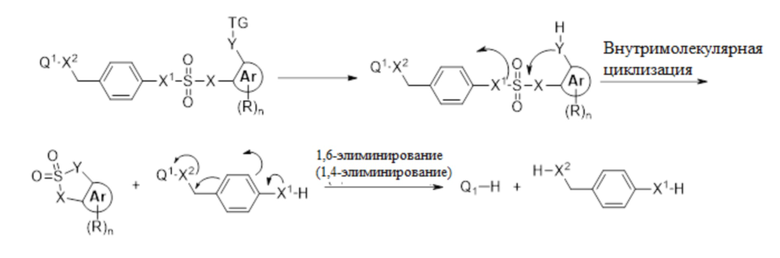 .
.
В некоторых вариантах осуществления при высвобождении Q1 представляет собой активный агент, содержащий по меньшей мере одну функциональную группу, выбранную из -OH, -NH-, -SH и -COOH. В соответствии с этими вариантами осуществления, как дополнительно описано в данном документе, Q1 конъюгирован с соединением, как описано в настоящем документе, -OH, -NH-, -SH и -COOH, например, посредством функциональной группы, выбранной из сложного эфира, амида, тиоэфира, карбамата, мочевины, оксима, гидразона и т. д. В некоторых таких вариантах осуществления Q2 используется вместо Q1, а Q2 представляет собой лекарственный препарат, содержащий аминогруппу. В других вариантах осуществления Q2 представляет собой активный агент, способный связываться с аммониевым звеном. В других вариантах осуществления Q2 способен диссоциировать в своей исходной форме, имеющей аминогруппу, после высвобождения Q2, причем активный агент может представлять собой лекарственный препарат, токсин, аффинный лиганд, зонд для обнаружения или их комбинацию.
В некоторых вариантах осуществления соединения и конъюгаты, описанные в данном документе, являются химически и физиологически стабильными. В некоторых таких вариантах осуществления соединения и конъюгаты, описанные в данном документе, достигают желаемой клетки-мишени в состоянии, при котором происходит незначительная диссоциация активного агента в крови, тем самым селективно высвобождая лекарственный препарат.
Триггерные группы (TG)
В некоторых вариантах осуществления конъюгаты по настоящему изобретению включают триггерную группу (TG). TG представляют собой группы, которые могут быть расщеплены, предпочтительно селективно расщеплены в ходе химической реакции, такой как биологическая реакция. Как правило, триггерные группы служат для маскировки нуклеофильной природы группы Y или Y', тем самым обеспечивая стабильность (например, предотвращая саморасщепление или внутримолекулярную циклизацию до того, как конъюгат достигнет целевого местоположения или испытывает предварительно заданное условие триггера) для соединений и конъюгатов, описанных в настоящем документе. После активации триггерная группа высвобождает нуклеофильную группу Y или Y' и допускает процесс саморасщепления или внутримолекулярной циклизации, как описано выше.
В некоторых вариантах осуществления TG содержит последовательность (такую как пептидная последовательность) или фрагмент, распознаваемый TEV, трипсином, тромбином, катепсином B, каспином D, катепсином K, каспазой 1, матриксной металлопротеиназой (MMP) и т. п., который может быть гидролизован ферментом (например, оксидоредуктазой, трансферазой, гидролазой, лиазой, изомеразой, лигазой и т.д.) и/или может включать фрагмент, выбранный из фосфодиэфира, фосфолипида, сложного эфира, β-галактозы, β-глюкозы, фукозы, олигосахара и т. п.
В некоторых вариантах осуществления TG содержит реакционноспособный химический фрагмент или функциональную группу, которые могут быть расщеплены в условиях использования нуклеофильного реагента (например, силиловый эфир, 2-N-ацилнитробензолсульфонамид, ненасыщенный винилсульфид, сульфонамид после активации, производное малонового диальдегида-индола, левулиноиловый эфир, гидразон или ацилгидразон).
В некоторых вариантах осуществления TG может содержать реакционноспособный химический фрагмент или функциональную группу, которые могут быть расщеплены в условиях использования основного реагента (например, 2-цианоэтиловый эфир, этиленгликолилдисукцинат, 2-сульфонилэтиловый эфир, алкилтиоэфир или тиофениловый эфир).
В некоторых вариантах осуществления TG может содержать реакционноспособный химический фрагмент или функциональную группу, которые могут быть расщеплены фотооблучением (например, производное 2-нитробензила, фенациловый эфир, 8-хинолинилбензолсульфонат, кумарин, фосфотриэфир, бис-арилгидразон или производное биман би-тиопропионовой кислоты).
В некоторых вариантах осуществления TG может содержать реакционноспособный химический фрагмент или функциональную группу, которые могут быть расщеплены в условиях использования восстанавливающего агента (например, гидроксиламин, дисульфид, левулинат, нитро или производное 4-нитробензила).
В некоторых вариантах осуществления TG может содержать реакционноспособный химический фрагмент или функциональную группу, которые могут быть расщеплены в кислой среде (например, сахариды, аналог трет-бутилкарбамата, диалкил- или диарилдиалкоксисилан, ортоэфир, ацеталь, аконитил, гидразон, β-тиопропионат, производное фосфорамидата, имин, тритил, виниловый эфир, поликеталь и производное алкил-2-(дифенилфосфино)бензоата; алкиловый сложный эфир, сложный эфир 8-гидроксихинолина и сложный эфир пиколината).
В некоторых вариантах осуществления TG может содержать реакционноспособный химический фрагмент или функциональную группу, которые могут быть расщеплены в окислительных условиях (например, боронат, вицинальный диол, производное параметоксибензила или соединение селена).
В определенных предпочтительных вариантах осуществления TG содержит сахарид, который может быть расщеплен в кислых или ферментативных условиях. В определенных предпочтительных вариантах осуществления триггерная группа представляет собой -NO2, которая может быть расщеплена в восстанавливающих условиях. В определенных предпочтительных вариантах осуществления триггерная группа представляет собой боронат, который может быть расщеплен в окислительных условиях. В определенных предпочтительных вариантах осуществления триггерная группа представляет собой сложный эфир, который может быть расщеплен в кислых, основных или ферментативных условиях. В определенных предпочтительных вариантах триггерная группа представляет собой гидразон, который может быть расщеплен в нуклеофильных условиях или в кислой среде. В определенных предпочтительных вариантах осуществления триггерная группа представляет собой гидроксиламин, который может быть расщеплен в восстанавливающих условиях.
Сахаридные триггерные группы
В некоторых вариантах осуществления соединения и конъюгаты, описанные в данном документе, включают сахаридную триггерную группу, например, триггерную группу, выбранную из:
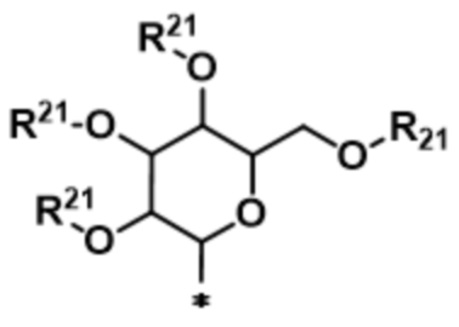 ;
;  ; и
; и 
где каждый R21 независимо представляет собой водород или выбран таким образом, что O-R21 представляет собой гидроксизащитную группу (например, ацетил); а R22 представляет собой водород или низший алкил (например, C1-C6-алкил). В определенных вариантах осуществления гидроксизащитная группа может использоваться в органическом синтезе, включая, но не ограничиваясь ими: метиловый эфир, метоксиметиловый эфир, метилтиометиловый эфир, 2-метоксиэтоксиметиловый эфир, бис(2-хлорэтокси)метиловый эфир, тетрагидропираниловый эфир, тетрагидротиопираниловый эфир, 4-метокситетрагидропираниловый эфир, 4-метокситетрагидротиопираниловый эфир, тетрагидрофураниловый эфир, 1-этоксиэтиловый эфир, 1-метил-1-метоксиэтиловый эфир, 2-(фенилселенил)этиловый эфир, трет-бутиловый эфир, аллиловый эфир, бензиловый эфир, о-нитробензиловый эфир, трифенилметиловый эфир, α-нафтилдифенилметиловый эфир, п-метоксифенилдифенилметиловый эфир, 9-(9-фенил-10-оксо)антриловый эфир, триметилсилиловый эфир, изопропилдиметилсилиловый эфир, трет-бутилдиметилсилиловый эфир, трет-бутилдифенилсилиловый эфир, трибензилсилиловый эфир, триизопропилсилиловый эфир, формиатный сложный эфир, ацетатный сложный эфир, трихлорацетатный сложный эфир, феноксиацетатный сложный эфир, изобутиратный сложный эфир, пивалоатный сложный эфир, адамантоатный сложный эфир, бензоатный сложный эфир, 2,4,6-триметилбензоатный сложный эфир, метилкарбонат, 2,2,2-трихлорэтилкарбонат, аллилкарбонат, п-нитрофенилкарбонат, бензилкарбонат, п-нитробензилкарбонат, S-бензилтиокарбонат, N-фенилкарбамат, нитратный сложный эфир, 2,4-динитрофенилсульфенатный сложный эфир и т. д., но не ограничиваясь ими.
Защитные группы в качестве триггерных групп
В некоторых вариантах осуществления TG представляет собой группу, которая способна расщепляться посредством химической реакции, физико-химической реакции и/или биологической реакции. В определенных вариантах осуществления TG представляет собой защитную группу. В некоторых таких вариантах осуществления защитная группа представляет собой аминную защитную группу, спиртовую защитную группу или тиоловую защитную группу.
Аминные защитные группы
В определенных вариантах осуществления аминная защитная группа представляет собой общую защитную группу, которую можно использовать в органическом синтезе, включая, но не ограничиваясь ими, м-нитрофенилкарбамат, 3,5-диметоксибензилкарбамат, о-нитробензилкарбамат, фенил(о-нитрофенил)метилкарбамат, алкилкарбамат, 9-флуоренилметилкарбамат, 2,2,2-трихлорэтилкарбамат, 2-триметилсилилэтилкарбамат (Teoc), трет-бутилкарбамат (Boc), винилкарбамат (Voc), аллилкарбамат (Alloc), 1-изопропилаллилкарбамат (Ipaoc), 8-хинолилкарбамат, N-гидроксипиперидинилкарбамат, бензилкарбамат, п-метоксибензилкарбамат, п-нитробензилкарбамат, дифенилметилкарбамат, ацетамид, хлорацетамид, трихлорацетамид, фенилацетамид, бензамид, N-фталимид, N-2,3-дифенилмалеимид, N-2,5-диметилпиррол, N-1,1-диметилтиометиленамин, N-бензилиденамин, бензолсульфенамид, о-нитробензолсульфенамид, трифенилметилсульфанамид, п-толуолсульфонамид, метансульфонамид, и т.д., но не ограничиваясь ими.
Спиртовые защитные группы
В определенных вариантах осуществления спиртовая защитная группа представляет собой общую защитную группу, которую можно использовать в органическом синтезе, включая, но не ограничиваясь ими: метиловый эфир, метоксиметиловый эфир (эфир MOM), бензилоксиметиловый эфир (эфир BOM), 2-(триметилсилил)этоксиметиловый эфир (эфир SEM), фенилтиометиловый эфир (эфир PTM), 2,2-дихлор-1,1-дифторэтиловый эфир, п-бромфенациловый эфир, хлорпропилметиловый эфир, изопропиловый эфир, циклогексиловый эфир, 4-метоксибензиловый, 2,6-дихлорбензиловый эфир, 4-(диметиламинокарбонил)бензиловый эфир, 9-антрилметиловый эфир, 4-пиколиловый эфир, метилтиометиловый эфир (эфир МТМ), 2-метоксиэтоксиметиловый эфир (эфир МЭМ), бис(2-хлорэтокси)метиловый эфир, тетрагидропираниловый эфир (эфир THP), тетрагидротиопираниловый эфир, 4-метокситетрагидропираниловый эфир, 4-метокситетрагидротиопираниловый эфир, тетрагидрофураниловый эфир, 1-этоксиэтиловый эфир, 1-метил-1-метоксиэтиловый эфир, 2-(фенилселенил)этиловый эфир), трет-бутиловый эфир, аллиловый эфир, бензиловый эфир, о-нитробензиловый эфир, трифенилметиловый эфир, α-нафтилдифенилметиловый эфир, п-метоксифенилдифенилметиловый эфир, 9-(9-фенил-10-оксо)антриловый эфир, триметилсилиловый эфир (эфир TMS), изопропилдиметилсилиловый эфир, трет-бутилдиметилсилиловый эфир (эфир TBDMS), трет-бутилдифенилсилиловый эфир, трибензилсилиловый эфир, триизопропилсилиловый эфир, формиатный сложный эфир, ацетатный сложный эфир, трихлорацетатный сложный эфир, феноксиацетатный сложный эфир, изобутиратный сложный эфир, пивалоатный сложный эфир, адамантоатный сложный эфир, бензоатный сложный эфир, сложный эфир 2,4,6-триметилбензоат(мезитоат), метилкарбонат, 2,2,2-трихлорэтилкарбонат, аллилкарбонат, п-нитрофенилкарбонат, бензилкарбонат, п-нитробензилкарбонат, S-бензилтиокарбонат, N-фенилкарбамат, нитратный сложный эфир, 2,4-динитрофенилсульфенатный сложный эфир, диметилфосфиниловый сложный эфир (сложный эфир DMP), диметилтиофосфиниловый сложный эфир (сложный эфир MPT), арилметансульфонат, арилтолуолсульфонат и т. д., но не ограничиваясь ими.
Тиоловые защитные группы
В определенных вариантах осуществления тиоловую защитную группу можно использовать в органическом синтезе, включая, но не ограничиваясь ими: S-бензилтиоэфир, S-п-метоксибензилтиоэфир, S-o-или п-гидроксил- или ацетоксибензилтиоэфир, S-п-нитробензилтиоэфир, S-4-пиколилтиоэфир, S-2-пиколил-N-оксид-тиоэфир, S-9-антрилметилтиоэфир, S-9-флуоренилметилтиоэфир, S-метоксиметилмонотиоацеталь, производное A-ацетила, производное S-бензоила, S-(N-этилкарбамат), S-(N-метоксиметилкарбамат) и т. д., но не ограничиваясь ими.
Связующая группа
В некоторых вариантах осуществления соединения и конъюгаты, описанные в данном документе, содержат связующую группу, соединяющую каждый CB и Ar посредством ковалентной связи. Типичными связующими группами являются стабильные негидролизуемые фрагменты, такие как, например, линейный или разветвленный, насыщенный или ненасыщенный C10-C100-алкилен. В определенных вариантах осуществления связующее звено удовлетворяет по меньшей мере двум, а более предпочтительно по меньшей мере трем из четырех следующих критериев:
(i) по меньшей мере один -CH2- в алкиленовом фрагменте замещен (то есть заменен) одним или более гетероатомами, выбранными из -NH-, -C(=O), -O-, -S- и -P-;
(ii) по меньшей мере один гетероарилен включен в алкиленовый фрагмент;
(iii) по меньшей мере один аминокислотный фрагмент, гликозидная связь, пептидная связь или амидная связь включены в алкиленовый фрагмент; и
(iv) алкилен может быть дополнительно замещен одним или более заместителями, выбранными из группы, состоящей из C1-C20-алкила, C6-C20-арила, C1-C8-алкила, -(CH2)sCOOH и (CH2)pNH2, где s представляет собой целое число, имеющее значение от 0 до 10, а p представляет собой целое число, имеющее значение от 1 до около 10.
В определенных вариантах осуществления связующее звено содержит по меньшей мере два, а более предпочтительно по меньшей мере три из следующих:
(i) по меньшей мере, один гетероатом, выбранный из -NH-, -C(=O), -O-, -S- и -P-;
(ii) по меньшей мере один гетероарилен;
(iii) по меньшей мере один аминокислотный фрагмент, гликозидную связь, пептидную связь или амидную связь; и
(iv) алкилен может быть дополнительно замещен одним или более заместителями, выбранными из группы, состоящей из C1-C20-алкила, C6-C20-арила, C1-C8-алкила, -(CH2)sCOOH и (CH2)pNH2, где s представляет собой целое число, имеющее значение от 0 до 10, а p представляет собой целое число, имеющее значение от 1 до около 10.
В других вариантах осуществления связующая группа, соединяющая каждый из CB и Ar, содержит функциональную группу, полученную в результате химической клик-реакции.
В альтернативных вариантах осуществления связующее звено содержит реакционноспособную функциональную группу, способную участвовать в химической клик-реакции.
Химическая клик-реакция представляет собой реакцию, которая может быть выполнена в мягких условиях и является чрезвычайно селективной для функциональных групп, которые обычно не обнаруживаются в биологических молекулах (например, азидная группа, ацетиленовая группа и т. д.). Соответственно, эту реакцию можно проводить в присутствии сложных триггерных групп, целевых фрагментов и т. д. Кроме того, клик-химия обладает высокой реакционной специфичностью. Например, химическая клик-реакция между азидной группой и ацетиленовой группой протекает селективно, без вмешательства других функциональных групп, присутствующих в молекуле. Например, в результате азид-ацетиленовой клик-химии можно получить триазольный фрагмент с высоким выходом.

 Таким образом, в некоторых вариантах осуществления связывающая группа, соединяющая каждый из CB и Ar, содержит
Таким образом, в некоторых вариантах осуществления связывающая группа, соединяющая каждый из CB и Ar, содержит  ,
,  или
или 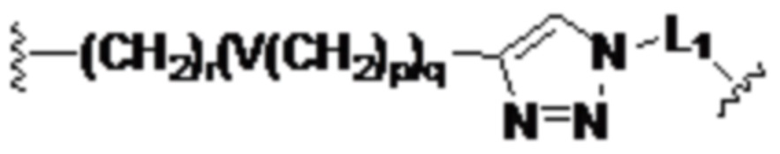 , V может представлять собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22 -, -NR23C(O)-, -NR24SO2- или -SO2NR25-, каждый из R21-R25 могут независимо представлять собой водород, (C1-C6)-алкил, (C1-C6)-алкил-(C6-C20)-арил или (C1-C6)алкил(C3-C20)гетероарил, r может представлять собой целое число, имеющее значение от 1 до 10, p может представлять собой целое число, имеющее значение от 0 до 10, q может представлять собой целое число, имеющее значение от 1 до 10, и L'' может представлять собой одинарную связь.
, V может представлять собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22 -, -NR23C(O)-, -NR24SO2- или -SO2NR25-, каждый из R21-R25 могут независимо представлять собой водород, (C1-C6)-алкил, (C1-C6)-алкил-(C6-C20)-арил или (C1-C6)алкил(C3-C20)гетероарил, r может представлять собой целое число, имеющее значение от 1 до 10, p может представлять собой целое число, имеющее значение от 0 до 10, q может представлять собой целое число, имеющее значение от 1 до 10, и L'' может представлять собой одинарную связь.
В других вариантах осуществления связующее звено, соединяющее каждый из CB и Ar, представляет собой связующую группу, представленную формулой (A):
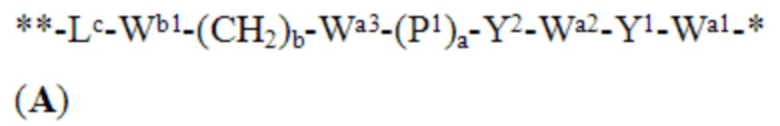
где:
* представляет собой точку присоединения к CB;
** представляет собой точку присоединения к Ar;
каждый из Wa1, Wa2 и Wa3 независимо представляет собой -NH-, -C(=O)- или (-CH2-)b;
Wb1 представляет собой амидную связь или триазолилен;
P1 представляет собой линкер, соединяющий Wa3 и Y2, и представляет собой аминокислотный фрагмент, пептидную связь или амидную связь;
Lc представляет собой алкилен;
Y2 представляет собой одинарную связь, -Wa4-(CH2)c-Wb2-(CH2)d-Wa5- или -Wa6-(CH2)e-CReRf-X-;
Re представляет собой C1-C8-алкил или CB-Wa7-Y3-Wc1-(CH2)f-;
Rf представляет собой B-Wa7-Y3-Wc1-(CH2)f-;
X представляет собой -NHC(=O)-(CH2)g-Wa8- или -C(=O)NH-(CH2)h-Wa9-;
каждый из Wa4, Wa5, Wa6, Wa7, Wa8 и Wa9 независимо представляет собой -NH-, -C(=O)- или -CH2-;
Wb2 представляет собой амидную связь или триазолилен;
Wc1 представляет собой -NHC(=O)- или -C(=O)NH-;
Y3 представляет собой -(CH2)i-(X'CH2CH2)j-(CH2)k-;
X' представляет собой -O-, -S-, -NH- или -CH2-;
CB соответствует определению выше;
каждый из b, c, d, e, f, g, h, i и j независимо представляет собой целое число, имеющее значение от 1 до около 10;
каждый из k и y независимо представляет собой целое число, имеющее значение от 0 до около 10;
Y1 представляет собой -(CH2)q-(CH2CH2X'')o- или -(CH2)q-(X''CH2CH2)o-;
X'' представляет собой -O-, -S-, -NH- или -CH2-; и
o и q представляют собой целое число, имеющее значение от 1 до около 10;
В некоторых вариантах осуществления P1 содержит по меньшей мере одно звено, представленное формулой (B) или (C):
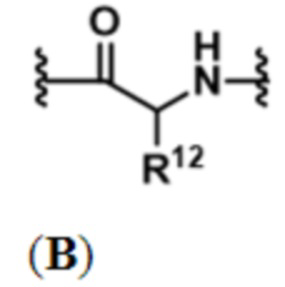
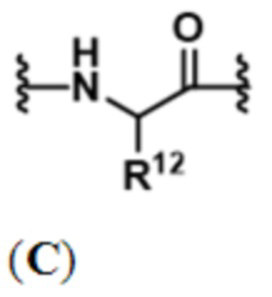
где:
R12 представляет собой водород, C1-C8-алкил, боковую цепь аминокислоты, такую как боковая цепь природной аминокислоты (например, H, метил, изопропил, изобутил, втор-бутил, S-метилтиоэфир, бензил, индол, пирролидин, пирролин, гидроксиметил, тирозил, лизил, имидазол, глицил, глутамил, карбамоилбутановая кислота, карбоксамид, аспарагиновая кислота, 1-гидроксиэтил и 2-гидроксиэтил), -(CH2)sCOR13 или -(CH2)pNR14R15;
R13 представляет собой OH или -NH(CH2)s'(X''CH2CH2)s''Z;
каждый из R14 и R15 независимо представляет собой водород или -(C(O)(CH2)s'(X''CH2CH2)s''Z)m-CB;
X'' представляет собой -O-, -S-, -NH- или -CH2-;
Z и CB соответствуют определению выше;
p представляет собой целое число, имеющее значение от 1 до около 10;
s и s'' представляют собой целое число, имеющее значение от 0 до около 10;
s' представляет собой целое число, имеющее значение от 1 до около 10; и
m представляет собой целое число, имеющее значение 0 или 1.
В некоторых вариантах осуществления формулы (B) или (C):
R12 представляет собой водород, алкил, боковую цепь аминокислоты, -(CH2)sC(O)R13 или -(CH2)pNR14R15;
p представляет собой целое число, имеющее значение от 1 до около 10;
s представляет собой целое число, имеющее значение от 0 до около 10;
R13 представляет собой ОН или -NH(CH2)s'(X'''CH2CH2)s''Z''-(CB)m;
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s''Z''-(CB)m;
s'' представляет собой целое число, имеющее значение от 0 до около 10;
s' представляет собой целое число, имеющее значение от 1 до около 10;
m представляет собой целое число, имеющее значение 0 или 1;
X''' представляет собой -O-, -S-, -NH- или -CH2-; и
Z'' представляет собой связующую группу, соединяющую CB с остатком R14 или R15; или Z'' представляет собой связующую группу, содержащую реакционноспособную группу.
В некоторых таких вариантах осуществления формулы (B) или (C):
R13 представляет собой OH или -NH(CH2)s'(X'''CH2CH2)s''Z'';
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s''Z''; и
Z'' представляет собой реакционноспособный предшественник связующего звена, выбранный из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
В других таких вариантах осуществления формулы (B) или (C):
R13 представляет собой OH -NH(CH2)s'(X'''CH2CH2)s''Z''CB;
каждый из R14 и R15 независимо представляет собой водород или C(O)(CH2)s'(X'''CH2CH2)s''Z''CB; и
Z'' представляет собой связующее звено, соединяющее CB с остатком R14 или R15, образованным из предшественника, выбранного из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
В некоторых вариантах осуществления Y2 представляет собой одинарную связь, выбранную из
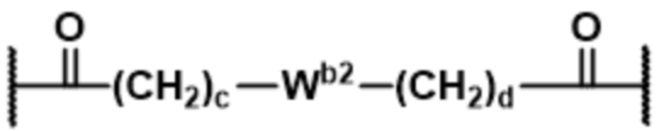 ;
; 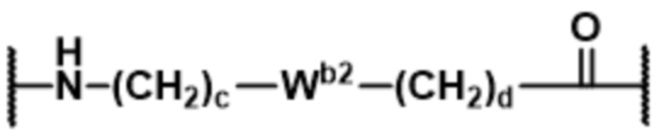 ;
; 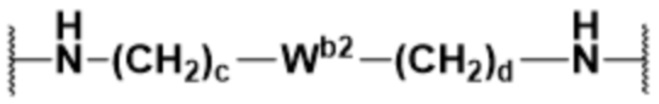 ;
; 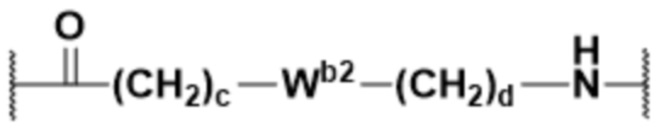 ; и
; и 
где:
Wb2 представляет собой -C(O)NH-, -NHC(O)-, 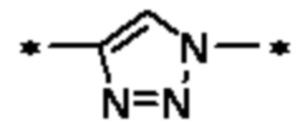 или
или 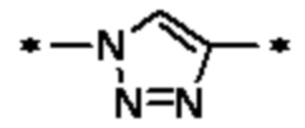 ;
;
Re представляет собой C1-C8-алкил или -(L1'-Z-)mCB;
Rf представляет собой B-Wb2'-(CH2)i-(X''CH2CH2)j-NH-C(=O)-(CH2)f-;
Xa представляет собой -NHC(=O)-(CH2)g-NH- или -C(O)NH-(CH2)h-NH-;
Wb2 представляет собой -C(O)NH- или -NHC(=O)-;
каждый из c, d, e, f, g, h, i и j независимо представляет собой целое число, имеющее значение от 1 до около 10;
X'' представляет собой -O-, -S-, -NH- или -CH2-; и
L1', Z, m и B соответствуют определению выше;
В определенных вариантах осуществления связующее звено, соединяющее каждый из CB и Ar, представляет собой связующую группу, содержащую группы (CH2)b, Lc, (P1)a, Wa1, Wa2, Wa3, Y1 и Y2, связанные друг с другом ковалентными связями, где:
каждый из Wa1, Wa2 и Wa3 независимо представляет собой -NH-, -C(O)- или -CH2-;
Wb1 представляет собой амидную связь или триазолилен;
P1 представляет собой амидную связь, аминокислотный остаток или пептид;
Lc представляет собой алкилен;
Y1 представляет собой -(CH2)q-(CH2CH2X'')o- или -(CH2)q-(X''CH2CH2X'')o-;
X'' представляет собой -O-, -S-, -NH- или -CH2-;
Y2 представляет собой одинарную связь или группу, выбранную из:
 ;
;  ;
;
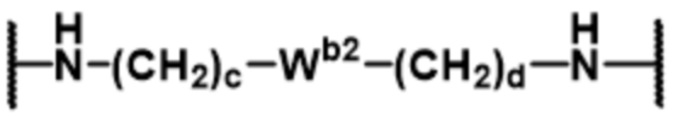 ; и
; и 
Wb2 представляет собой амидную связь или триазолилен;
a равно от 0 до 10;
каждый из b, c и d независимо представляет собой целое число, имеющее значение от 1 до около 10; и
каждый из o и q независимо представляет собой целое число, имеющее значение от 1 до около 10.
В некоторых вариантах осуществления R12 представляет собой боковую цепь природной аминокислоты. В других вариантах осуществления R12 представляет собой боковую цепь неприродной аминокислоты.
В некоторых вариантах осуществления связующее звено, соединяющее каждый из CB и Ar, представляет собой связующую группу, представленную формулой (A):

где:
* представляет собой точку присоединения к CB; и
** представляет собой точку присоединения к Ar.
В некоторых таких вариантах осуществления P1 представляет собой
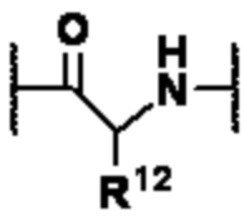 или
или 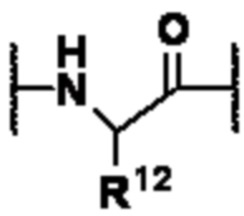
где:
R12 представляет собой водород, алкил, боковую цепь аминокислоты, -(CH2)sCOOH или -(CH2)pNH2;
p представляет собой целое число, имеющее значение от 1 до около 10; и
каждый из s и s'' независимо представляет собой целое число, имеющее значение от 0 до около 10.
В некоторых вариантах осуществления P1 представляет собой
 или
или 
где:
R12 представляет собой водород, алкил, боковую цепь аминокислоты, -(CH2)sC(O)R13 или -(CH2)pNR14R15;
p представляет собой целое число, имеющее значение от 1 до около 10;
s представляет собой целое число, имеющее значение от 0 до около 10;
R13 представляет собой ОН или -NH(CH2)s'(X'''CH2CH2)s''Z''-(CB)m;
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s''Z''-(CB)m;
s'' представляет собой целое число, имеющее значение от 0 до около 10;
s' представляет собой целое число, имеющее значение от 1 до около 10;
m представляет собой целое число, имеющее значение 0 или 1;
X''' представляет собой -O-, -S-, -NH- или -CH2-; и
Z'' представляет собой связующую группу, соединяющую CB с остатком R14 или R15; или Z'' представляет собой связующую группу, содержащую реакционноспособную группу.
В некоторых таких вариантах осуществления P1:
R13 представляет собой OH или -NH(CH2)s'(X'''CH2CH2)s''Z'';
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s''Z''; и
Z'' представляет собой реакционноспособный предшественник связующего звена, выбранный из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
В других таких вариантах осуществления P1:
R13 представляет собой OH -NH(CH2)s'(X'''CH2CH2)s''Z''CB;
каждый из R14 и R15 независимо представляет собой водород или C(O)(CH2)s'(X'''CH2CH2)s''Z''CB; и
Z'' представляет собой связующее звено, соединяющее CB с остатком R14 или R15, образованным из предшественника, выбранного из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
В альтернативных вариантах осуществления связующее звено, соединяющее CB и Ar, представляет собой связующую группу, представленную формулами (F), (G), (H), (J), (K), (L), (M) или (N):
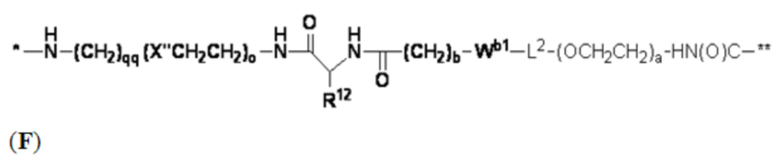



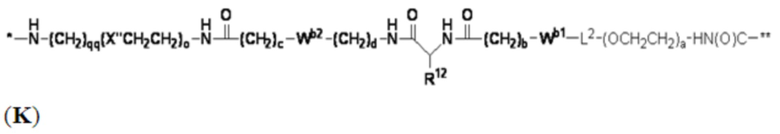
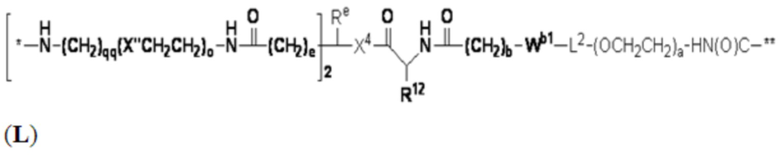

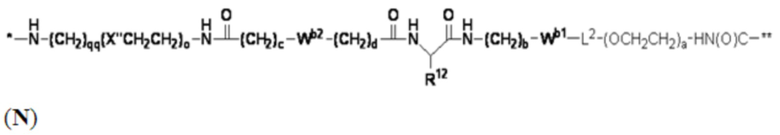
где:
Re представляет собой алкил;
X4 представляет собой -NHC(O)-(CH2)g-NH- или -C(O)NH-(CH2)h-NH-;
каждый из e, g и h независимо представляет собой целое число, имеющее значение от 1 до около 10; и
s' представляет собой целое число, имеющее значение от 1 до около 10.
В некоторых вариантах осуществления формулы (F), (G), (H), (I), (J), (K), (L) или (M):
R12 представляет собой водород, алкил, боковую цепь аминокислоты, -(CH2)sC(O)R13 или -(CH2)pNR14R15;
p представляет собой целое число, имеющее значение от 1 до около 10;
s представляет собой целое число, имеющее значение от 0 до около 10;
R13 представляет собой ОН или -NH(CH2)s'(X'''CH2CH2)s''Z''-(CB)m;
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s''Z''-(CB)m;
s'' представляет собой целое число, имеющее значение от 0 до около 10;
s' представляет собой целое число, имеющее значение от 1 до около 10;
m представляет собой целое число, имеющее значение 0 или 1;
X''' представляет собой -O-, -S-, -NH- или -CH2-; и
Z'' представляет собой связующую группу, соединяющую CB с остатком R14 или R15; или Z'' представляет собой связующую группу, содержащую реакционноспособную группу.
В некоторых вариантах осуществления формулы (F), (G), (H), (I), (J), (K), (L) или (M):
R13 представляет собой OH или -NH(CH2)s'(X'''CH2CH2)s''Z'';
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s''Z''; и
Z'' представляет собой реакционноспособный предшественник связующего звена, выбранный из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
В некоторых вариантах осуществления формулы (F), (G), (H), (I), (J), (K), (L) или (M):
R13 представляет собой OH -NH(CH2)s'(X'''CH2CH2)s''Z''CB;
каждый из R14 и R15 независимо представляет собой водород или C(O)(CH2)s'(X'''CH2CH2)s''Z''CB; и
Z'' представляет собой связующее звено, соединяющее CB с остатком R14 или R15, образованным из предшественника, выбранного из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
Нацеливающие фрагменты
Соединения и конъюгаты по настоящему изобретению могут дополнительно содержать лиганд или нацеливающий фрагмент, CB. В некоторых вариантах осуществления изобретения лиганд или нацеливающий фрагмент представляет собой любой элемент молекулярного распознавания, который может подвергаться специфическому взаимодействию по меньшей мере с одним другим молекулярным фрагментом посредством, например, нековалентных связей, таких как водородные связи, координация металлов, гидрофобные силы, силы Ван-дер-Ваальса, π-π-взаимодействия, галогенные связи, электростатические и/или электромагнитные эффекты. В определенных вариантах осуществления CB выбран из наночастиц, иммуноглобулина, нуклеиновой кислоты, белка, олигопептида, полипептида, антитела, фрагмента антигенного полипептида, репетела (repebody) и т. п.
Соединения и конъюгаты по настоящему изобретению могут содержать один или более нацеливающих фрагментов. То есть переменная cb может иметь значение целого числа, выбранного из 1, 2, 3, 4, 5, 1-10 или 1-20.
В некоторых вариантах осуществления CB содержит две или более независимо выбранных природных аминокислот или неприродных аминокислот, конъюгированных ковалентными связями (например, пептидными связями), а пептид может включать 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более природных аминокислот или неприродных аминокислот, которые конъюгированы пептидными связями. В некоторых вариантах осуществления лиганд содержит более короткие аминокислотные последовательности (например, фрагменты природных белков или фрагменты синтетического полипептида), а также полноразмерные белки (например, предварительно сконструированные белки).
В некоторых вариантах осуществления CB выбран из антитела, гормона, лекарственного препарата, аналога антитела (например, не являющегося IgG), белка, олигопептида, полипептида и т. д., которые связываются с рецептором. В определенных вариантах осуществления CB селективно нацеливает лекарственный препарат в конкретный орган, ткань или клетку. В других вариантах осуществления CB специфически связывается с рецептором, сверхэкспрессированным в раковых клетках, по сравнению с нормальными клетками и может быть классифицирован на моноклональное антитело (mAb) или фрагмент антитела и низкомолекулярное вещество, не являющееся антителом. Предпочтительно, CB выбирают из пептидов, специфических для опухолевых клеток пептидов, специфических для опухолевых клеток аптамеров, специфических для опухолевых клеток углеводов, специфических для опухолевых клеток моноклональных антител, поликлональных антител и фрагментов антител, которые были идентифицированы при скрининге библиотеки.
Типичные лиганды или нацеливающие фрагменты включают, но не ограничиваются ими, карнитин, инозит, липоевую кислоту, пиридоксаль, аскорбиновую кислоту, ниацин, пантотеновую кислоту, фолиевую кислоту, рибофлавин, тиамин, биотин, витамин B12, другие водорастворимые витамины (витамин B), жирорастворимые витамины (витамин A, D, E, K), RGD (Arg-Gly-Asp), NGR (Asn-Gly-Arg), трансферрин, рецептор VIP (вазоактивный интестинальный пептид), пептид APRPG (Ala-Pro-Arg-Pro-Gly), TRX-20 (тиоредоксин-20), интегрин, нуклеолин, аминопептидазу N (CD13), эндоглин, рецептор фактора роста сосудистого эпителия, рецептор липопротеина низкой плотности, рецептор трансферрина, рецептор соматостатина, бомбезин, нейропептид Y, гормональный рецептор, высвобождающий лютеинизирующий гормон, рецептор фолиевой кислоты, рецептор эпидермального фактора роста, трансформирующий фактор роста, рецептор фактора роста фибробластов, рецептор асиалогликопротеина, рецептор галектина-3, рецептор Е-селектина, рецептор гиалуроновой кислоты, простат-специфический мембранный антиген (PSMA), рецептор холецистокинина А, рецептор холецистокинина B, рецептор домена дискоидина, рецептор муцина, опиоидный рецептор, рецептор плазминогена, рецептор брадикинина, рецептор инсулина, рецептор инсулиноподобного фактора роста, рецептор ангиотензина AT1, рецептор ангиотензина AT2, рецептор гранулоцитарно-макрофагального колониестимулирующего фактора (рецептор GM-CSF), рецептор галактозамина, рецептор сигма-2, дельта-подобный лиганд-3 (DLL-3), аминопептидаза P, меланотрансферрин, лептин, столбнячный токсин Tet1, столбнячный токсин G23, пептид RVG (гликопротеин вируса бешенства), HER2 (рецептор 2 эпидермального фактора роста человека), GPNMB (неметастатический гликопротеин b), Ley, CA6, CanAng, SLC44A4 (семейство транспортеров растворенных веществ 44, член 4), CEACAM5 (молекула клеточной адгезии 5, связанная с карциноэмбриональным антигеном), нектин-4, карбоновая ангидраза 9, TNNB2, 5T4, CD30, CD37, CD74, CD70, PMEL17, EphA2(рецептор эфрина A2), Trop-2, SC-16, тканевой фактор, ENPP-3(AGS-16), SLITRK6 (SLIT- и NTRK-подобный член семейства 6), CD27, антиген Льюиса Y, LIV1, GPR161 (G-белок-связанный рецептор 161), PBR (периферический бензодиазеоиновый рецептор), рецептор MERTK (тирозинкиназа рецептора Mer), CD71, LLT1 (лектиноподобный транскрипт 1 или CLED2D), рецептор интерлейкина-22, рецептор сигма-1, рецептор, активируемый пролифераторами пероксисом, DLL3, C4.4a, cKIT, EphrinA, CTLA4 (белок, ассоциированный с цитотоксическим T-лимфоцитом 4), FGFR2b (рецептор 2b фактора роста фибробластов), рецептор N-ацетилхолина, рецептор рилизинг-гормона гонадотропина, рецептор гастрин-рилизинг-пептида, рецептор морфогенетического белка костей, тип рецептора 1B (BMPR1B), E16 (LAT1, SLC7A5), STEAP1 (шестой трансмембранный эпителиальный антиген простаты), 0772P (CA125, MUC16), MPF (MSLN, мезотелин), Napi3b (SLC34A2), Sema5b (семафорин 5b), ETBR (рецептор эндотелина типа B), MSG783(RNF124), STEAP2 (шестой трансмембранный эпителиальный антиген простаты 2), TrpM4 (катионный канал транзиторного рецепторного потенциала 5, подсемейство М, член 4), CRIPTO (фактор роста, происходящий от тератокарциномы),CD21, CD79b, FcRH2 (IFGP4), HER2 (ErbB2), NCA (CEACM6), MDP (DPEP1), IL20R-альфа (IN20Ra), Brevican (BCAN), EphB2R, ASLG659 (B7h), CD276, PSCA (предшественник антигена простатических стволовых клеток), GEDA, BAFF-R (BR3), CD22 (BL-CAM), CD79a, CXCR5, HLA-DOB, P2X5, CD72, LY64, FcRH1, IRTA2, TENB2, SSTR2, SSTR5, SSTR1, SSTR3, SSTR4, ITGAV (интегрин, альфа 5), ITGB6 (интегрин, бета 6), MET, MUC1, EGFRvIII, CD33, CD19, IL2RA (рецептор интерлейкина 2, альфа), AXL, BCMA, CTA (раково-тестикулярные антигены), CD174, CLEC14A, GPR78, CD25, CD32, LGR5 (GPR49), CD133 (проминин), ASG5, ENPP3 (эктонуклеотид-пирофосфатаза/фосфодиэстераза 3), PRR4 (пролин-богатый белок 4), GCC (гуанилат циклаза 2C), Liv-1 (SLC39A6), CD56, CanAg, TIM-1, RG-1, B7-H4, PTK7, CD138, Claudins, Her3 (ErbB3), RON (MST1R), CD20, TNC (тенасцин C), FAP, DKK-1, CD52, CS1 (SLAMF7), аннексин A1, V-CAM, gp100, MART-1, MAGE-1 (ген-1, кодирующий антиген меланомы), MAGE-3 (меланома-ассоциированные антиген 3), BAGE, GAGE-1, MUM-1(онкоген множественной миеломы 1), CDK4, TRP-1(gp75), TAG-72 (ассоциированный с опухолью гликопротеин-72), ганглиозид GD2, GD3, GM2, GM3, VEP8, VEP9, My1, VIM-D5, D156-22, OX40, RNAK, PD-L1, TNFR1, TNFR2, и т. д.
Мишени
В некоторых вариантах осуществления мишень или мишени элемента молекулярного распознавания специфично связаны с одним или более конкретными типами клеток или тканей. В некоторых вариантах осуществления мишени специфично связаны с одним или более конкретными болезненными состояниями. В некоторых вариантах осуществления мишени специфично связаны с одним или более конкретными стадиями развития. Например, специфический в отношении клеточного типа маркер обычно экспрессируется на уровнях по меньшей мере в 2 раза больше в этом типе клеток, чем в эталонной популяции клеток. В некоторых вариантах осуществления специфический в отношении клеточного типа маркер присутствует на уровнях по меньшей мере в 3 раза, по меньшей мере в 4 раза, по меньшей мере в 5 раз, по меньшей мере в 6 раз, по меньшей мере в 7 раз, по меньшей мере в 8 раз, по меньшей мере в 9 раз, по меньшей мере в 10 раз, по меньшей мере в 50 раз, по меньшей мере в 100 раз или по меньшей мере в 1000 раз больше, чем его усредненное выражение в контрольной популяции. Обнаружение или измерение специфического в отношении клеточного типа маркера может позволить отличить тип или типы клеток, представляющих интерес, от клеток многих, большинства или всех других типов. В некоторых вариантах осуществления мишень может содержать белок, углевод, липид и/или нуклеиновую кислоту, как описано в настоящем документе.
В некоторых вариантах осуществления вещество считается «нацеленным», если оно специфически связывается с нацеливающим фрагментом, таким как нацеливающий фрагмент нуклеиновой кислоты. В некоторых вариантах осуществления нацеливающий фрагмент, такой как нацеливающий фрагмент нуклеиновой кислоты, специфически связывается с мишенью в жестких условиях.
В определенных вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который специфически связывается с одной или более мишенями (например, антигенами), связанными с органом, тканью, клеткой, компонентом внеклеточного матрикса и/или внутриклеточным компартментом. В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который специфически связывается с мишенями, связанными с конкретным органом или системой органов. В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который специфически связывается с одной или более внутриклеточными мишенями (например, органеллой, внутриклеточным белком). В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который специфически связывается с мишенями, связанными с больными органами, тканями, клетками, компонентами внеклеточного матрикса и/или внутриклеточными компартментами. В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который специфически связывается с мишенями, ассоциированными с конкретными типами клеток (например, эндотелиальные клетки, раковые клетки, злокачественные клетки, клетки рака предстательной железы и т. д.).
В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который связывается с мишенью, которая является специфичной для одного или более конкретных типов тканей (например, ткани печени или ткани предстательной железы). В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который связывается с мишенью, которая является специфичной для одного или более конкретных типов клеток (например, T-клетки по сравнению с B-клетками). В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который связывается с мишенью, которая является специфичной для одного или более конкретных болезненных состояний (например, опухолевые клетки по сравнению со здоровыми клетками). В некоторых вариантах осуществления конъюгаты и соединения, описанные в настоящем документе, содержат нацеливающий фрагмент, который связывается с мишенью, которая является специфичной для одного или более конкретных стадий развития (например, стволовые клетки по сравнению с дифференцированными клетками).
В некоторых вариантах осуществления мишенью может быть маркер, который исключительно или в первую очередь связан с одним или более типами клеток, с одним или более заболеваниями и/или с одной или более стадиями развития. Специфический в отношении клеточного типа маркер обычно экспрессируется на уровнях по меньшей мере в 2 раза больше в этом типе клеток, чем в эталонной популяции клеток, которая может состоять, например, из смеси, содержащей клетки из множества (например, 5-10 или более) различных тканей или органов в примерно равных количествах. В некоторых вариантах осуществления специфический в отношении клеточного типа маркер присутствует на уровнях по меньшей мере в 3 раза, по меньшей мере в 4 раза, по меньшей мере в 5 раз, по меньшей мере в 6 раз, по меньшей мере в 7 раз, по меньшей мере в 8 раз, по меньшей мере в 9 раз, по меньшей мере в 10 раз, по меньшей мере в 50 раз, по меньшей мере в 100 раз или по меньшей мере в 1000 раз больше, чем его усредненное выражение в контрольной популяции. Обнаружение или измерение специфического в отношении клеточного типа маркера может позволить отличить тип или типы клеток, представляющих интерес, от клеток многих, большинства или всех других типов.
В некоторых вариантах осуществления мишень содержит белок, углевод, липид и/или нуклеиновую кислоту. В некоторых вариантах осуществления мишень содержит белок и/или его характерную часть, такую как опухолевый маркер, интегрин, рецептор клеточной поверхности, трансмембранный белок, межклеточный белок, ионный канал, мембранный транспортный белок, фермент, антитело, химерный белок, гликопротеин, и т. д. В некоторых вариантах осуществления мишень содержит углевод и/или его характерную часть, такую как гликопротеин, сахар (например, моносахарид, дисахарид, полисахарид), гликокаликс (то есть периферийная зона, богатая углеводами, на внешней поверхности большинства эукариотических клеток) и т. д. В некоторых вариантах осуществления мишень содержит липид и/или его характерную часть, такую как масло, жирная кислота, глицерид, гормон, стероид (например, холестерин, желчная кислота), витамин (например, витамин Е), фосфолипид, сфинголипид, липопротеин и др. В некоторых вариантах осуществления мишень содержит нуклеиновую кислоту и/или ее характерную часть, такую как нуклеиновая кислота ДНК; нуклеиновая кислота РНК; модифицированная нуклеиновая кислота ДНК; модифицированная нуклеиновая кислота РНК; нуклеиновая кислота, которая включает любую комбинацию ДНК, РНК, модифицированной ДНК и модифицированной РНК.
В данной области техники известны многочисленные маркеры. Типичные маркеры включают белки клеточной поверхности, например рецепторы. Типичные рецепторы включают, но не ограничиваются ими, рецептор трансферрина; Рецептор ЛПНП; рецепторы фактора роста, такие как члены семейства рецепторов эпидермального фактора роста (например, EGFR, Her2, Her3, Her4) или рецепторы фактора роста эндотелия сосудов, рецепторы цитокинов, молекулы клеточной адгезии, интегрины, селектины и молекулы CD. Маркер может представлять собой молекулу, которая присутствует исключительно или в больших количествах в злокачественной клетке, например, в опухолевом антигене.
Наночастицы
В некоторых вариантах осуществления нацеливающий фрагмент содержит частицу (например, целевую частицу), предпочтительно наночастицу, необязательно целевую наночастицу, прикрепленную к нацеливающей молекуле, которая может специфически или предпочтительно связываться с мишенью. В некоторых вариантах осуществления нацеливающая частица сама направляет соединение по настоящему изобретению (например, путем обогащения в опухолевых клетках или ткани), и к ней не прикрепляются дополнительные нацеливающие молекулы.
Под термином «наночастица» в настоящем документе подразумевается любая частица, имеющая диаметр менее 1000 нм. В некоторых вариантах осуществления терапевтический агент и/или нацеливающая молекула могут быть связаны с телом частицы, например, в полимерной матрице. В некоторых вариантах осуществления нацеливающая молекула может быть ковалентно связана с поверхностью полимерной матрицы. В некоторых вариантах осуществления ковалентная ассоциация опосредуется линкером. В некоторых вариантах осуществления терапевтический агент может быть связан с поверхностью, инкапсулирован внутри, окружен и/или диспергирован по всей полимерной матрице. См., например, патент США №8246968, который в полном объеме включен в настоящий документ.
В целом наночастицы по настоящему изобретению содержат частицы любого типа. Любая частица может быть использована в соответствии с настоящим изобретением. В некоторых вариантах осуществления частицы являются биоразлагаемыми и биосовместимыми. Как правило, биосовместимое вещество не является токсичным для клеток. В некоторых вариантах осуществления вещество считается биосовместимым, если его добавление к клеткам приводит к менее чем определенному порогу гибели клеток. В некоторых вариантах осуществления вещество считается биосовместимым, если его добавление к клеткам не вызывает побочных эффектов. Как правило, биоразлагаемое вещество представляет собой вещество, которое подвергается распаду в физиологических условиях в течение терапевтически значимого периода времени (например, недель, месяцев или годов). В некоторых вариантах осуществления биоразлагаемое вещество представляет собой вещество, которое может разрушаться клеточным механизмом. В некоторых вариантах осуществления биоразлагаемое вещество представляет собой вещество, которое может разрушаться в результате химических процессов. В некоторых вариантах осуществления частица представляет собой вещество, которое является как биосовместимым, так и биоразлагаемым. В некоторых вариантах осуществления частица представляет собой вещество, которое является биосовместимым, но не является биоразлагаемым. В некоторых вариантах осуществления частица представляет собой вещество, которое является биоразлагаемым, но не является биосовместимым.
Часто желательно использовать популяцию частиц, которая является относительно однородной с точки зрения размера, формы и/или состава, чтобы каждая частица имела сходные свойства. Например, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% частиц могут иметь диаметр или наибольший размер, который находится в пределах 5%, 10% или 20% от среднего диаметра или наибольшего размера. В некоторых вариантах осуществления популяция частиц может быть неоднородной по размеру, форме и/или составу. В соответствии с настоящим изобретением может быть использовано множество различных частиц. В некоторых вариантах осуществления частицы представляют собой сферы или сфероиды. В некоторых вариантах осуществления частицы представляют собой сферы или сфероиды. В некоторых вариантах частицы имеют плоскую или пластинчатую форму. В некоторых вариантах осуществления частицы представляют собой кубы или кубоиды. В некоторых вариантах осуществления частицы представляют собой овалы или эллипсы. В некоторых вариантах осуществления частицы представляют собой цилиндры, конусы или пирамиды.
В некоторых вариантах осуществления частицы представляют собой микрочастицы (например, микросферы). В общем, «микрочастица» относится к любой частице, имеющей диаметр менее 1000 мкм. В некоторых вариантах осуществления частицы представляют собой пикочастицы (например, пикосферы). В общем случае «пикочастица» относится к любой частице, имеющей диаметр менее 1 нм. В некоторых вариантах осуществления частицы представляют собой липосомы. В некоторых вариантах осуществления частицы представляют собой мицеллы.
Частицы могут быть твердыми или полыми и могут содержать один или более слоев (например, нанооболочки, нанокольца). В некоторых вариантах осуществления каждый слой имеет уникальный состав и уникальные свойства по отношению к другому слою (слоям). Например, частицы могут иметь структуру ядра/оболочки, где ядро представляет собой один слой, а оболочка представляет собой второй слой. Частицы могут содержать множество различных слоев. В некоторых вариантах осуществления один слой может быть по существу сшитым, второй слой по существу не сшитым и так далее. В некоторых вариантах осуществления один, более или все разные слои могут содержать один или более терапевтических или диагностических агентов, которые необходимо доставить. В некоторых вариантах осуществления один слой содержит агент, который необходимо доставить, второй слой не содержит агент, который необходимо доставить, и так далее. В некоторых вариантах осуществления каждый отдельный слой содержит различный агент или набор агентов, которые необходимо доставить.
В некоторых вариантах осуществления частица является пористой, что означает, что частица содержит отверстия или каналы, которые обычно являются небольшими по сравнению с размером частицы. Например, частица может быть частицей пористого диоксида кремния, например наночастицей мезопористого диоксида кремния, или может иметь покрытие из мезопористого диоксида кремния (Lin et al., 2005, J. Am. Chem. Soc, 17:4570). Частицы могут иметь поры в диапазоне от приблизительно 1 нм до приблизительно 50 нм, например, от приблизительно 1 до 20 нм в диаметре. От приблизительно 10% до 95% объема частицы может состоять из пустот внутри пор или каналов.
Частицы могут иметь слой покрытия. Использование биосовместимого покрывающего слоя может быть полезным, например, если частицы содержат материалы, которые являются токсичными для клеток. Подходящие материалы для покрытия включают, но не ограничиваются ими, природные белки, такие как бычий сывороточный альбумин (BSA), биосовместимые гидрофильные полимеры, такие как полиэтиленгликоль (PEG) или производное PEG, фосфолипид-(PEG), диоксид кремния, липиды, полимеры, углеводы. такие как декстран, другие наночастицы, которые могут быть связаны с наночастицами по настоящему изобретению и т. д. Покрытия могут наноситься или собираться различными способами, такими как погружение, послойная технология, самосборка, сопряжение и т. д. Самосборка относится к процессу самопроизвольной сборки структуры более высокого порядка, которая зависит от естественного притяжения компонентов структуры более высокого порядка (например, молекул) друг к другу. Обычно это происходит в результате случайных движений молекул и образования связей в зависимости от размера, формы, состава или химических свойств.
Примеры полимеров включают полиалкилены (например, полиэтилены), поликарбонаты (например, поли(1,3-диоксан-2-он)), полиангидриды (например, поли(себациновый ангидрид)), полигидроксикислоты (например, поли(3-гидроксиалканоат)), полифумараты, поликапролактоны, полиамиды (например, поликапролактам), полиацетали, полиэфиры, сложные полиэфиры (например, полилактид, полигликолид), поли(ортоэфиры), поливиниловые спирты, полиуретаны, полифосфазены, полиакрилаты, полиметакрилаты, полицианоакрилаты, полимочевины, полистиролы, и полиамины. В некоторых вариантах осуществления полимеры в соответствии с настоящим изобретением включают полимеры, которые были одобрены для использования у людей Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) согласно 21 C.F.R. (Кодекс федеральных правил) § 177.2600, включая, но не ограничиваясь ими, сложные полиэфиры (например, полимолочная кислота, полигликолевая кислота, поли(молочная-гликолевая кислота), поликапролактон, поливалеролактон, поли(1,3-диоксан-2-он)); полиангидриды (например, поли(себациновый ангидрид)); простые полиэфиры (например, полиэтиленгликоль); полиуретаны; полиметакрилаты; полиакрилаты; и полицианоакрилаты.
В некоторых вариантах осуществления изобретения частицы могут представлять собой неполимерные частицы (например, частицы металла, квантовые точки, керамические частицы, полимеры, содержащие неорганические материалы, материалы, полученные из кости, заменители кости, вирусные частицы и т. д.). В некоторых вариантах осуществления терапевтический или диагностический агент, который необходимо доставить, может быть связан с поверхностью такой неполимерной частицы. В некоторых вариантах осуществления неполимерная частица представляет собой совокупность неполимерных компонентов, таких как совокупность атомов металла (например, атомов золота). В некоторых вариантах осуществления терапевтический или диагностический агент, который необходимо доставить, может быть связан с поверхностью и/или инкапсулирован внутри, окружен и/или диспергирован в совокупности неполимерных компонентов.
Частицы (например, наночастицы, микрочастицы) могут быть получены любым способом, известным в данной области техники. Например, составы в виде частиц могут быть получены такими способами, как нанопреципитация, флюидные каналы с фокусировкой потока, распылительная сушка, испарение растворителя с одинарной и двойной эмульсией, экстракция растворителем, фазовое разделение, измельчение, процедуры микроэмульсии, микрообработка, нанообработка, жертвенные слои, простая и сложная коацервация и другими подходящими способами. В качестве альтернативы или дополнительно был описан синтез водных и органических растворителей для монодисперсных полупроводниковых, проводящих, магнитных, органических и других наночастиц (Pellegrino et al., 2005, Small, 1:48; Murray et al., 2000, Ann. Rev. Mat. Sci., 30:545; и Trindade et al., 2001, Chem. Mat., 13:3843).
Способы изготовления микрочастиц для доставки инкапсулированных агентов описаны в литературе (см., например, Doubrow, Ed., "Microcapsules and Nanoparticles in Medicine and Pharmacy," CRC Press, Boca Raton, 1992; Mathiowitz et al., 1987, J. Control. Release, 5:13; Mathiowitz et al., 1987, Reactive Polymers, δ: 275; и Mathiowitz et al., 1988, J. Appl. Polymer Sci., 35:755).
Нацеливающие фрагменты нуклеиновых кислот
В некоторых вариантах осуществления нацеливающий фрагмент содержит нацеливающий фрагмент нуклеиновой кислоты.
Как правило, нацеливающий фрагмент нуклеиновой кислоты, представляет собой любой полинуклеотид, который связывается с компонентом, связанным с органом, тканью, клеткой, компонентом внеклеточного матрикса и/или внутриклеточным компартментом (мишенью).
В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты представляют собой аптамеры. Аптамер обычно представляет собой полинуклеотид, который связывается с определенной структурой-мишенью, которая связана с конкретным органом, тканью, клеткой, компонентом внеклеточного матрикса и/или внутриклеточным компартментом. Как правило, нацеливающая функция аптамера основана на трехмерной структуре аптамера. В некоторых вариантах осуществления связывание аптамера с мишенью обычно опосредуется взаимодействием двух- и/или трехмерных структур как аптамера, так и мишени. В некоторых вариантах осуществления связывание аптамера с мишенью основано не только на первичной последовательности аптамера, но зависит от трехмерной структуры (структур) аптамера и/или мишени. В некоторых вариантах осуществления аптамеры связываются со своими мишенями посредством комплементарного спаривания оснований по Уотсону-Крику, которое прерывается структурами (например, петлями типа «шпилька»), которые нарушают спаривание оснований.
В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновых кислот представляют собой шпигельмеры (публикации PCT WO 98/08856, WO 02/100442 и WO 06/117217). В целом, шпигельмеры представляют собой синтетические нуклеиновые кислоты с зеркальным отображением, которые могут специфически связываться с мишенью (то есть с аптамерами с зеркальным отображением). Шпигельмеры характеризуются структурными особенностями, которые делают их невосприимчивыми к экзо- и эндонуклеазам.
Специалисту в данной области техники будет понятно, что в соответствии с настоящим изобретением может использоваться любой нацеливающий фрагмент нуклеиновой кислоты (например, аптамер или шпигельмер), который способен специфически связываться с мишенью. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты, которые должны использоваться в соответствии с настоящим изобретением, могут нацеливаться на маркер, связанный с заболеванием, расстройством и/или состоянием. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты, которые должны использоваться в соответствии с настоящим изобретением, могут нацеливаться на связанные с раком мишени. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты, которые должны использоваться в соответствии с настоящим изобретением, могут нацеливаться на опухолевые маркеры. Любой тип рака и/или любой опухолевый маркер может быть нацелен с использованием нацеливающих фрагментов нуклеиновой кислоты в соответствии с настоящим изобретением. Чтобы привести лишь несколько примеров, нацеливающие фрагменты нуклеиновой кислоты могут нацеливаться на маркеры, связанные с раком простаты, раком легких, раком молочной железы, колоректальным раком, раком мочевого пузыря, раком поджелудочной железы, раком эндометрия, раком яичников, раком кости, раком пищевода, раком печени, раком желудка, опухолью головного мозга, меланомой кожи и/или лейкозом.
Нуклеиновые кислоты по настоящему изобретению (включая нацеливающие фрагменты нуклеиновых кислот и/или функциональные РНК, подлежащие доставке, например, РНК-индуцирующие объекты, рибозимы, тРНК и т. д., более подробно описанные ниже), могут быть получены в соответствии с любой доступной методикой, включающая, но не ограничиваясь ими, химическим синтезом, ферментативным синтезом, ферментативным или химическим расщеплением более длинного предшественника и т. д.
Способы синтеза РНК известны в данной области техники (см., например, Gait, M. J. (ed.) Oligonucleotide synthesis: a practical approach, Oxford [Oxfordshire], Washington, D.C.: IRL Press, 1984; и Herdewijn, P. (ed.) Oligonucleotide synthesis: methods and applications, Methods in molecular biology, v. 288 (Clifton, NJ.) Totowa, N.J.: Humana Press, 2005).
Нуклеиновая кислота, которая образует нацеливающий фрагмент нуклеиновой кислоты, может включать встречающиеся в природе нуклеозиды, модифицированные нуклеозиды, встречающиеся в природе нуклеозиды с углеводородными линкерами (например, алкиленом) или полиэфирным линкером (например, линкером PEG), вставленным между одним или более нуклеозидами модифицированные нуклеозиды с углеводородными или линкерами PEG, вставленными между одним или более нуклеозидами, или их комбинацией. В некоторых вариантах осуществления нуклеотиды или модифицированные нуклеотиды нацеливающего фрагмента нуклеиновой кислоты могут быть заменены углеводородным линкером или полиэфирным линкером при условии, что аффинность связывания и селективность нацеливающего фрагмента нуклеиновой кислоты существенно не снижается за счет замены (например, константа нацеливающего фрагмента нуклеиновой кислоты на мишень не должна превышать около 1 × 10-3 М).
Специалистам в данной области техники будет понятно, что нуклеиновые кислоты в соответствии с настоящим изобретением могут содержать нуклеотиды, полностью принадлежащие к типам, встречающимся в природных нуклеиновых кислотах, или вместо этого могут включать один или более нуклеотидных аналогов или иметь структуру, которая в противном случае отличается от природной нуклеиновой кислоты. Патенты США №№ 6403779; 6399754; 6225460; 6127533; 6031086; 6005087; 5977089; и ссылки в, приведенные в них, раскрывают широкий спектр конкретных нуклеотидных аналогов и модификаций, которые могут быть использованы. См. Crooke, S. (ed.) Antisense Drug Technology: Principles, Strategies, and Applications (1 st ed), Marcel Dekker; ISBN: 0824705661; 1st edition (2001) и ссылки приведенные в нем. Например, 2'-модификации включают галоген, алкокси и аллилоксигруппы. В некоторых вариантах осуществления группа 2'-ОН заменена группой, выбранной из H, OR, R, галогена, SH, SR, NH2, NHR, NR2 или CN, где R представляет собой C1-C6-алкил, алкенил или алкинил, а галоген представляет собой F, Cl, Br или I. Примеры модифицированных связей включают фосфоротиоатные и 5'-N-фосфорамидитные связи.
Нуклеиновые кислоты, содержащие множество различных аналогов нуклеотидов, модифицированные основные цепи или не встречающиеся в природе межнуклеозидные связи, могут быть использованы в соответствии с настоящим изобретением. Нуклеиновые кислоты по настоящему изобретению могут включать природные нуклеозиды (то есть аденозин, тимидин, гуанозин, цитидин, уридин, дезоксиаденозин, дезокситимидин, дезоксигуанозин и дезоксицитидин) или модифицированные нуклеозиды. Примеры модифицированных нуклеотидов включают нуклеозид, модифицированный основанием (например, арацитидин, инозин, изогуанозин, небуларин, псевдоуридин, 2,6-диаминопурин, 2-аминопурин, 2-тиотимидин, 3-деаза-5-азацитидин, 2'-дезоксиуридин, 3-ниторпиррол, 4-метилиндол, 4-тиоуридин, 4-тиотимидин, 2-аминоаденозин, 2-тиотимидин, 2-тиоуридин, 5-бромцитидин, 5-иодуридин, инозин, 6-азауридин, 6-хлорпурин, 7-деазааденозин, 7-деазагуанозин, 8-азааденозин, 8-азидоаденозин, бензимидазол, Ml-метиладенозин, пирролопиримидин, 2-амино-6-хлорпурин, 3-метиладенозин, 5-пропинилцитидин, 5-пропинилуридин, 5-бромуридин, 5-фторуридин, 5-метилцитидин, 7-деазааденозин, 7-деазагуанозин, 8-оксоаденозин, 8-оксогуанозин, 0(6)-метилгуанин и 2-тиоцитидин), химически или биологически модифицированные основания (например, метилированные основания), модифицированные сахара (например, 2'-фторибоза, 2'-аминорибоза, 2'-азидорибоза, 2'-O-метилрибоза, L-энантиомерные нуклеозиды, арабиноза и гексоза), модифицированные фосфатные группы (например, фосфоротиоаты и 5'-N-фосфорамидитные связи) и их комбинации. Природные и модифицированные нуклеотидные мономеры для химического синтеза нуклеиновых кислот являются легко доступными. В некоторых случаях нуклеиновые кислоты, содержащие такие модификации, проявляют улучшенные свойства по сравнению с нуклеиновыми кислотами, состоящими только из встречающихся в природе нуклеотидов. В некоторых вариантах осуществления модификации нуклеиновой кислоты, описанные в настоящем документе, используются для уменьшения и/или предотвращения расщепления нуклеазами (например, экзонуклеазами, эндонуклеазами и т. д.). Например, структура нуклеиновой кислоты может быть стабилизирована путем включения аналогов нуклеотидов на 3'-конце одной или обеих цепей, чтобы уменьшить расщепление.
Модифицированные нуклеиновые кислоты не должны быть однородно модифицированы по всей длине молекулы. Различные модификации нуклеотидов и/или структуры остова могут существовать в различных положениях в нуклеиновой кислоте. Специалисту в данной области техники будет понятно, что аналоги нуклеотидов или другие модификации могут быть расположены в любом(-ых) положении(-ях) нуклеиновой кислоты, таким образом функция нуклеиновой кислоты существенно не изменяется. Чтобы привести только один пример, модификации могут быть расположены в любом положении нацеливающего фрагмента нуклеиновой кислоты, так что это существенно не влияет на способность нацеливающего фрагмента нуклеиновой кислоты специфически связываться с мишенью. Модифицированная область может находиться на 5'-конце и/или 3'-конце одной или обеих цепей. Например, использовались модифицированные нацеливающие фрагменты нуклеиновой кислоты, в которых приблизительно 1-5 остатков на 5' и/или 3'-конце любой из обеих цепей являются нуклеотидными аналогами и/или имеют модификацию остова. Модификация может быть 5' или 3' терминальной модификацией. Одна или обе цепи нуклеиновой кислоты могут содержать по меньшей мере 50% немодифицированных нуклеотидов, по меньшей мере 80% немодифицированных нуклеотидов, по меньшей мере 90% немодифицированных нуклеотидов или 100% немодифицированных нуклеотидов.
Нуклеиновые кислоты в соответствии с настоящим изобретением могут, например, содержать модификацию гликозидной, нуклеозидной или межнуклеозидной связи, такую как описана в публикациях заявок на патенты США 2003/0175950, 2004/0192626, 2004/0092470, 2005/0020525, и 2005/0032733. Настоящее изобретение охватывает применение любой нуклеиновой кислоты, имеющей любую одну или более модификаций, описанных в настоящем документе. Например, сообщается, что ряд концевых конъюгатов, например липидов, таких как холестерин, литохолевая кислота, алюровая кислота или длинные алкильные разветвленные цепи, улучшают клеточное поглощение. Аналоги и модификации могут быть протестированы с использованием, например, любого подходящего анализа, известного в данной области техники, например, для выбора тех, которые приводят к улучшенной доставке терапевтического или диагностического агента, улучшенному специфическому связыванию нацеливающего фрагмента нуклеиновой кислоты с мишенью, и т. д. В некоторых вариантах осуществления нуклеиновые кислоты в соответствии с настоящим изобретением могут содержать одну или более неприродных нуклеозидных связей. В некоторых вариантах осуществления один или более внутренних нуклеотидов на 3'-конце, 5'-конце или на обоих 3'- и 5'-концах нацеливающего фрагмента нуклеиновой кислоты инвертированы с образованием связи, такой как 3'-3' связь или 5'-5' связь.
В некоторых вариантах осуществления нуклеиновые кислоты в соответствии с настоящим изобретением не являются синтетическими, но представляют собой природные объекты, которые были выделены из их природных сред.
Любой метод может быть использован для создания новых нацеливающих фрагментов нуклеиновой кислоты (см., например, патенты США №№6716583; 6465189; 6482594; 6458543; 6458539; 6376190; 6344318; 6242246; 6184364; 6001577; 5958691; 5874218; 5853984; 5843732; 5843653; 5817785; 5789163; 5763177; 5696249; 5660985; 5595877; 5567588; и 5270163; и публикации заявок на патенты США 2005/0069910, 2004/0072234, 2004/0043923, 2003/0087301, 2003/0054360 и 2002/0064780).
Нацеливающие фрагменты нуклеиновой кислоты, которые связываются с белком, углеводом, липидом и/или нуклеиновой кислотой, могут быть сконструированы и/или идентифицированы. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты могут быть сконструированы и/или идентифицированы для использования в комплексах по изобретению, которые связываются с белками и/или их характерными частями, такими как опухолевые маркеры, интегрины, рецепторы клеточной поверхности, трансмембранные белки, межклеточные белки, ионные каналы, мембранные транспортерные белки, ферменты, антитела, химерные белки и т. д. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты могут быть сконструированы и/или идентифицированы для использования в комплексах по изобретению, которые связываются с углеводами и/или их характерными частями такими как гликопротеины, сахара (например, моносахариды, дисахариды и полисахариды), гликокаликс (то есть обогащенная углеводами периферическая зона на внешней поверхности большинства эукариотических клеток) и т. д. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты могут быть сконструированы и или идентифицированы для использования в комплексах по изобретению, которые связываются с липидами и/или их характерными частями, такими как масла, насыщенные жирные кислоты, ненасыщенные жирные кислоты, глицериды, гормоны, стероиды (например, холестерин, желчные кислоты), витамины (например, витамин Е), фосфолипиды, сфинголипиды, липопротеины и т. д. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты могут быть сконструированы и/или идентифицированы для использования в комплексах по изобретению, которые связываются с нуклеиновыми кислотами и/или их характерными частями, такими как нуклеиновые кислоты ДНК; нуклеиновые кислоты РНК; модифицированные нуклеиновые кислоты ДНК; модифицированные нуклеиновые кислоты РНК; и нуклеиновые кислоты, которые включают любую комбинацию ДНК, РНК, модифицированной ДНК и модифицированной РНК; и т. п.
Нацеливающие фрагменты нуклеиновой кислоты (например, аптамеры или шпигельмеры) могут быть сконструированы и/или идентифицированы с использованием любого доступного способа. В некоторых вариантах осуществления нацеливающие фрагменты нуклеиновой кислоты сконструированы и/или идентифицированы путем идентификации нацеливающих фрагментов нуклеиновой кислоты из смеси кандидатов нуклеиновых кислот.
Способы получения соединений по изобретению
Соединения и конъюгаты, описанные в данном описании, могут быть получены простыми способами получения (см., например, примеры 1-78). Легкое очищение позволяет использовать такие способы получения.
Таким образом, в настоящем документе также предложены способы получения соединений по изобретению. Например, соединения по изобретению могут быть получены, как показано на любой из Схем реакций 3, 4, 5, 6 или 7:
Схема реакции 3:
 ;
;
Схема реакции 4:
 ;
;
Схема реакции 5:
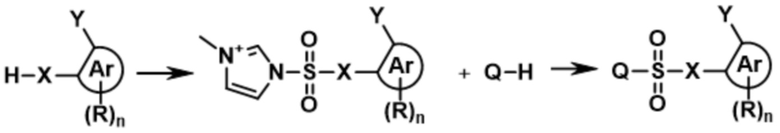 ;
;
Схема реакции 6:
 ;
;
Схема реакции 7:
 ;
;
где X, Y, Ar, R и n соответствуют определению выше.
В настоящем документе также предложены способы получения соединения, включающие введения в реакцию соединения формулы (IIc):
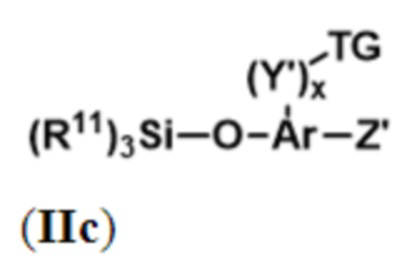
или его фармацевтически приемлемой соли с сульфонилгалогенидом:
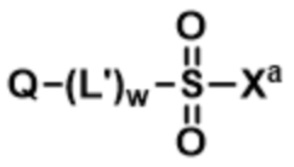
для получения соединения формулы (Iaa):
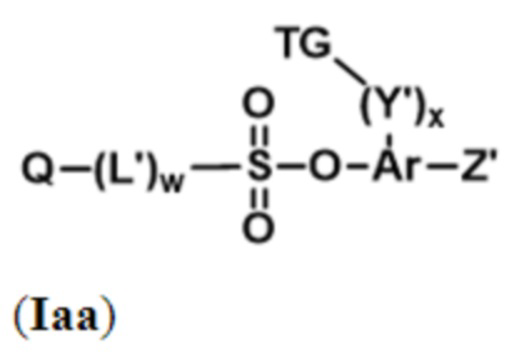
или его фармацевтически приемлемой соли, где:
Xa представляет собой галоген (предпочтительно, фтор), каждый R11 независимо представляет собой алкильный, арильный, аралкильный или алкоксизаместитель, а остальные группы могут быть выбраны в соответствии с любым определением, представленным в данном документе.
Например, в некоторых таких вариантах осуществления
Q представляет собой активный агент, связанный с L' посредством гетероатома, предпочтительно О или N;
Z' отсутствует или представляет собой связующую группу, содержащую по меньшей мере одну реакционноспособную группу, такую как предшественник, описанный выше в связи с Z;
L' представляет собой спейсерный фрагмент, присоединенный к SO2 посредством гетероатома, выбранного из O, S и N, предпочтительно O или N, и выбранного таким образом, что расщепление связи между L' и SO2 способствует расщеплению связи между L' и Q для высвобождения активного агента;
Ar представляет собой арил, гетероарил, циклоалкил или гетероциклоалкил, предпочтительно арил или гетероарил;
Y' представляет собой -(CRb2)yN(Ra)-, -(CRb2)yO- или -(CRb2)yS- таким образом, что атом N, O или S присоединен к TG, если y равно 1;
O и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, которая при активации образует атом N, O или S, способный вступать в реакцию с SO2 для вытеснения (Q)q-(L')w и образования 5-6-членного кольца, включая X-SO2 и промежуточные атомы Ar;
каждый w, x и y независимо представляет собой целое число, имеющее значение 0 или 1;
каждый из Ra и Rc независимо представляет собой водород или низший алкил; и
каждый Rb независимо представляет собой водород или низший алкил; или
два Rb вместе с атомом углерода, к которому они присоединены, образуют 3-5-членное кольцо, предпочтительно 3-4-членное кольцо,
Реакционноспособной группой связывающей группы может быть фрагмент, способный участвовать в реакциях 1,3-дипольного циклоприсоединения, реакциях гетеро-Дильса - Альдера, реакциях нуклеофильного замещения, карбонильных реакциях неальдольного типа, присоединениях к многократным связям углерод-углерод, реакциях окисления, клик-реакциях или любой другой реакции межмолекулярного взаимодействия. Предпочтительно, реакционноспособная группа выбирается для участия в селективной реакции с реагирующим партнером, который не является обычным в биологических молекулах, таких как реакция 1,3-диполярного циклоприсоединения, реакция гетеро-Дильса - Альдера, реакция конденсации оксима/гидразона или клик-реакция.
В некоторых предпочтительных вариантах осуществления связывающая группа может включать алкин или азид (который вступает в реакцию с образованием триазола), алкин и оксид нитрила (которые вступают в реакцию с образованием изоксазола) или карбонил (например, альдегид или кетон) или гидразин или гидроксиламин (которые вступают в реакцию с образованием оксима или гидразона).
В других вариантах осуществления, описанных в настоящем документе, предложены способы получения соединения, включающие:
(a) введение в реакцию соединения формулы (IIa):
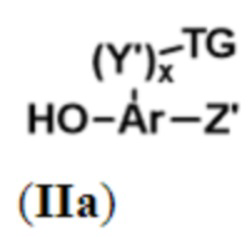
или его фармацевтически приемлемой соли с 1,1'-сульфонилбис(1Н-имидазолом):
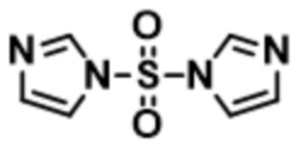
для получения соединения формулы (IIbb):

или его фармацевтически приемлемой соли, где переменные могут быть выбраны в соответствии с любым определением, приведенным в данном документе.
Например, в некоторых таких вариантах осуществления
Z' отсутствует или представляет собой связующую группу, содержащую реакционноспособную группу, как более подробно описано выше;
Ar представляет собой арил, гетероарил, циклоалкил или гетероциклоалкил, предпочтительно арил или гетероарил;
Y' представляет собой -(CRb2)yN(Ra)-, -(CRb2)yO- или -(CRb2)yS-, расположенный таким образом, что атом N, O или S присоединен к TG, если y равно 1;
-SO2- и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, которая при активации образует атом N, O или S, способный вступать в реакцию с SO2 для вытеснения (Q)q-(L')w и образования 5-6-членного кольца, включая X-SO2 и промежуточные атомы Ar;
каждый w, x и y независимо представляет собой целое число, имеющее значение 0 или 1;
каждый из Ra и Rc независимо представляет собой водород или низший алкил; и
каждый Rb независимо представляет собой водород или низший алкил; или
два Rb вместе с атомом углерода, к которому они присоединены, образуют 3-5-членное кольцо, предпочтительно 3-4-членное кольцо,
Затем соединение формулы (IIbb) можно дополнительно подвергнуть реакции с соединением формулы (Ia'), Q-(L')w-H, или его фармацевтически приемлемой солью для получения соединения (Ia):

или его фармацевтически приемлемой соли, где переменные могут быть выбраны в соответствии с любым определением, приведенным в данном документе.
Например, в некоторых вариантах осуществления
X представляет собой O;
Q представляет собой активный агент, связанный с L' посредством гетероатома, предпочтительно О или N;
L' представляет собой связующую группу, присоединенную к SO2 посредством гетероатома, выбранного из O, S и N, предпочтительно O или N, и выбранного таким образом, что расщепление связи между L' и SO2 способствует расщеплению связи между L' и Q для высвобождения активного агента; и
w равен 0 или 1.
В некоторых вариантах осуществления в способах используют промежуточное соединение формулы (IIa), (IIb) или (IIc) для получения соединения формулы (Iaa), где Ar, TG, Y' Z' и Raсоответствуют определению выше для конъюгатов формулы (I') или соединения формулы (Ia).
В изобретение дополнительно предлагаются соединения, описанные выше, которые применимы в этих способах.
Промежуточные соединения
В некоторых вариантах осуществления, описанные в настоящем документе соединения и конъюгаты могут быть получены способом, в котором используется промежуточное соединение, имеющее структуру в соответствии с формулой (IV):
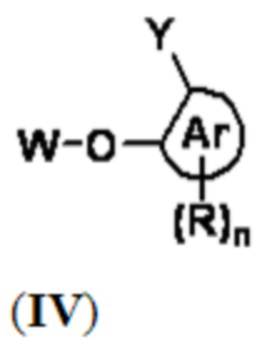
или его фармацевтически приемлемая соль, где:
W представляет собой водород, -SiR16R17R18 или -SO2-G;
каждый из R16, R17 и R18 независимо представляет собой C1-C6-алкил;
G представляет собой галоген (предпочтительно фтор), имидазол или N-метилимидазолий;
R представляет собой заместитель или -L1'-Z;
L1' представляет собой C1-C200-алкилен, необязательно содержащий по меньшей мере одну из пептидной связи, аминогруппы, эфирной связи, триазольной связи, тетразольной связи, гликозидной связи, сульфонамидной связи, фосфонатной связи, сульфо-связи или дендримерную структуру;
Z представляет собой предшественник, выбранный из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra, где Ra представляет собой C1-C10-алкил) и дигидрофосфат (-OP(=O)(OH)2).
n представляет собой целое число, имеющее значение от 1 до 4;
Y представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHOH, -NHNH2, -BR2R3,  или -Y'-TG, такой как -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHNH2, -BR2R3,
или -Y'-TG, такой как -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHNH2, -BR2R3,  или -Y'-TG;
или -Y'-TG;
R1 представляет собой C1-C6-алкил;
r представляет собой целое число от 1 до 5;
Ar1 представляет собой C6-C20-арилен;
каждый из R2 и R3 независимо представляет собой водород, C1-C6алкил, C1-C6-алкокси или гидрокси;
каждый из Ra, Rb, Rc и Rd независимо представляет собой водород или C1-C6--алкил;
Y' представляет собой -(CH2)xNR''-, -(CH2)xO- или -(CH2)xS-;
R'' представляет собой водород или C1-C6-алкил;
x представляет собой целое число, имеющее значение 0 или 1; и
TG представляет собой триггерную группу.
В некоторых вариантах осуществления, описанные в настоящем документе соединения и конъюгаты могут быть получены способом, в котором используется промежуточное соединение, имеющее структуру в соответствии с формулой (V):
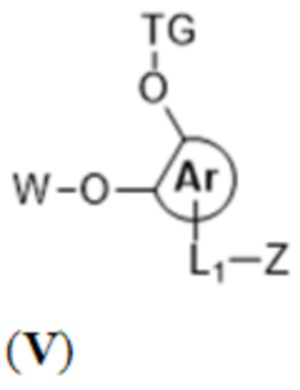
или его фармацевтически приемлемая соль, где:
W, L1' и Z соответствуют определению для формулы (IV); и
TG собой триггерную группу, такую как β-галактозид, β-глюкуронид или комбинацию β-галактозида и β-глюкуронида.
В других вариантах осуществления, описанные в настоящем документе соединения и конъюгаты могут быть получены способом, в котором используется промежуточное соединение, имеющее структуру в соответствии с формулой (VI):
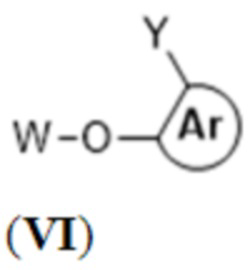
или его фармацевтически приемлемая соль, где:
W соответствует определению для формулы (IV);
Y представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHOH, -NHNH2, -BR2R3 или -O-TG;
R1 представляет собой C1-C6-алкил, такой как -NO2, -OC(O)(CH2)rC(O)R1, -O(CH2)r-Ar1-NO2, -NHOH, -NHNH2, -BR2R3 или -O-TG;
R1 представляет собой C1-C6-алкил;
r представляет собой целое число от 1 до 5;
Ar1 представляет собой фенилен, бифенилен или нафтален;
каждый из R2 и R3 независимо представляет собой водород, C1-C6алкил, C1-C6-алкокси или гидрокси;
каждый из Ra, Rb, Rc и Rd независимо представляет собой водород или C1-C6-алкил; и
TG представляет собой триггерную группу, такую как β-галактозид, β-глюкуронид или комбинацию β-галактозида и β-глюкуронида.
В настоящем документе также предложены промежуточные соединения формулы (IIa), (IIb) или (IIc):
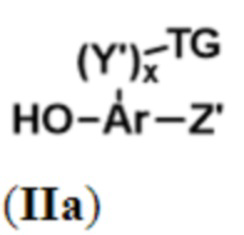
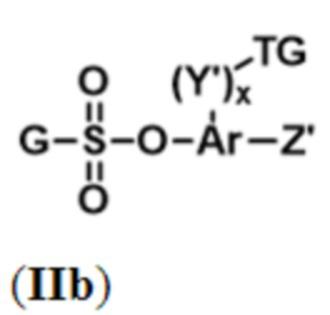

или их фармацевтически приемлемые соли, где:
G представляет собой галоген, имидазол или N-метилимидазолий;
каждый R11 независимо представляет собой C1-C6-алкил;
Ar представляет собой арил, гетероарил, циклоалкил или гетероциклоалкил;
TG представляет собой триггерную группу, которая при активации образует атом N, O или S, способный образовывать 5-6-членное кольцо, включая X-SO2 и промежуточные атомы Ar;
Y' представляет собой -(CRb2)yN(Ra)-, -(CRb2)yO- или -(CRb2)yS-, расположенный таким образом, что атом N, O или S присоединен к TG, если y равно 1;
O и Y' расположены на смежных атомах Ar;
каждый из x и y независимо представляет собой целое число, имеющее значение 0 или 1;
Z' отсутствует или представляет собой связующее звено, содержащее, например, реакционноспособное или связывающее звено; и
каждый Ra независимо представляет собой водород или алкил; или
два Ra вместе с атомом углерода, к которому они присоединены, образуют трехчленное кольцо.
В некоторых вариантах осуществления промежуточное соединение представляет собой соединение формулы (IIa), (IIb) или (IIc), где Ar, TG, Y' Z' и Ra соответствуют определению выше для конъюгатов формулы (I') или соединения формулы (Ia).
В предпочтительных вариантах осуществления промежуточное соединение представляет собой соединение формулы (IIa), (IIb) или (IIc), где Ar представляет собой арил (например, фенил или нафтил).
В некоторых вариантах осуществления, в настоящем документе предложено промежуточное соединение, которое представляет собой соединение формулы (IIa), (IIb) или (IIc), где Z' представляет собой связующую группу, содержащую одну или более групп, выбранных из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3-),  ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra и дигидрофосфата (-OP(=O)(OH)2.
, фосфоновой кислоты (-P(=O)(OH)2), кетона,C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra и дигидрофосфата (-OP(=O)(OH)2.
В других вариантах осуществления промежуточные соединения представляет собой соединение формулы (IIa), (IIb) или (IIc), где x равно 0. В некоторых таких вариантах осуществления TG представляет собой -NO2, -OC(O)(CH2)rC(O)R1, -NHOH, -NHNH2, -BR2R3, 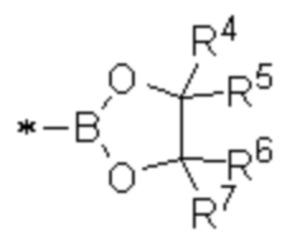 , такой как NO2, -OC(O)(CH2)rC(O)R1, -NHNH2, -BR2R3,
, такой как NO2, -OC(O)(CH2)rC(O)R1, -NHNH2, -BR2R3,  , где:
, где:
R1 представляет собой C1-C6-алкил;
каждый из R2 и R3 независимо представляет собой водород, C1-C6-алкил, C1-C6-алкокси или гидрокси;
каждый из R4, R5, R6 и R7 независимо представляет собой водород или C1-C6-алкил; и
r представляет собой целое число, имеющее значение 1, 2, 3, 4 или 5;
В альтернативных вариантах осуществления промежуточное соединение представляет собой соединение формулы (IIa), (IIb) или (IIc), где TG представляет собой триггерную группу, включающую β-галактозид, β-глюкуронид или комбинацию β-галактозида и β-глюкуронида.
В конкретных вариантах осуществления промежуточное соединение представляет собой:
 или
или 
или их фармацевтически приемлемую соль.
В некоторых других вариантах осуществления промежуточное соединение представляет собой:
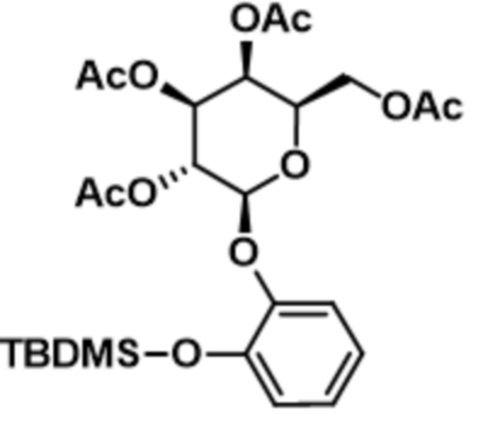 ;
;  ;
; 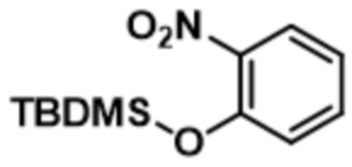 ;
; 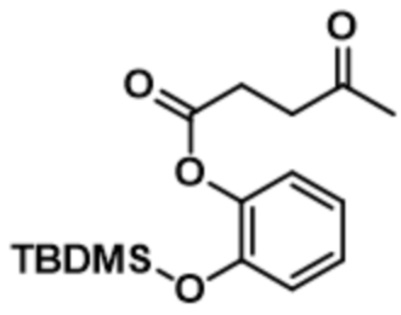 ;
; 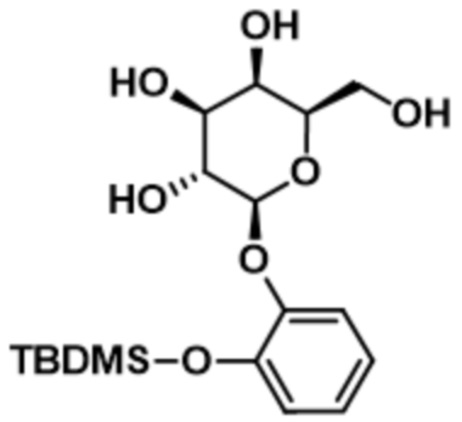 ;
; 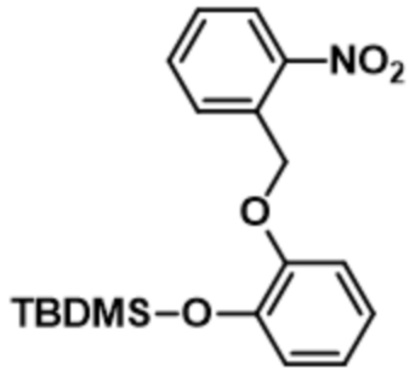 ; или
; или 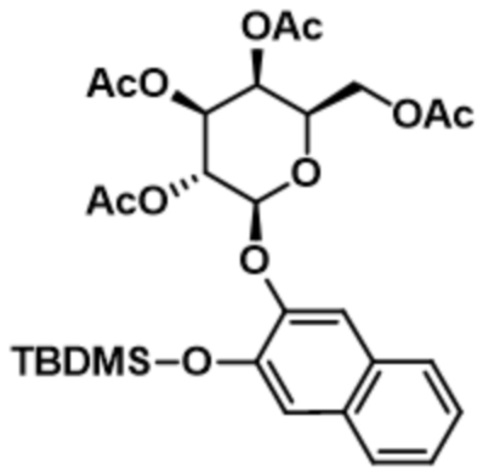
или их фармацевтически приемлемую соль.
Конъюгаты антитело-лекарственный препарат (ADC)
В некоторых вариантах осуществления CB представляет собой антитело, а Q представляет собой лекарственный препарат. Соответственно, соединения и конъюгаты, описанные в данном документе, могут быть использованы для конъюгирования антитела с лекарственным фрагментом с образованием конъюгата антитело-лекарственный препарат (ADC). Конъюгаты антитело-лекарственный препарата (ADC) могут повышать терапевтическую эффективность при лечении заболевания, например рака, вследствие способности ADC избирательно доставлять один или более лекарственных компонентов к тканям-мишеням, например, ассоциированный с опухолью антиген. Таким образом, в определенных вариантах осуществления в изобретении предлагается ADC для терапевтического применения, например, лечения рака.
ADC настоящему по изобретению содержат антитело, связанное с одним или более лекарственными фрагментами. Специфичность ADC определяется специфичностью антитела. В одном варианте осуществления антитело связано с одним или более цитотоксическими лекарственными препаратами, которые доставляются к раковой клетке.
Примеры препаратов, которые можно использовать в ADC по изобретению, приведены ниже. Термины «лекарственный препарат», «агент» и «лекарственный фрагмент» используются в настоящем документе взаимозаменяемо. Термины «связанный» и «конъюгированный» также используются в настоящем документе взаимозаменяемо и указывают на то, что антитело и фрагмент ковалентно связаны.
В некоторых вариантах осуществления ADC имеет следующую формулу (формула VII):
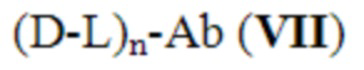
где Ab представляет собой антитело, а (D-L) представляет собой линкер-лекарственный фрагмент. Линкер-лекарственный фрагмент состоит из линкера L и фрагмента лекарственного препарата D. Фрагмент лекарственного препарата может обладать, например, цитостатической, цитотоксической или иной терапевтической активностью в отношении клетки-мишени. n представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10. Предпочтительно D-L имеет структуру формулы (I''):

Q представляет собой активный агент, связанный с L' посредством гетероатома, предпочтительно О или N;
Z' представляет собой связующую группу;
L' представляет собой спейсерный фрагмент, присоединенный к SO2 посредством гетероатома, выбранного из O, S и N, предпочтительно O или N, и выбранного таким образом, что расщепление связи между L' и SO2 способствует расщеплению связи между L' и Q для высвобождения активного агента;
X представляет собой -O-, -C(Rb)2- или -N(Rc)-, предпочтительно -O-;
Ar представляет собой арил, гетероарил, циклоалкил или гетероциклоалкил, предпочтительно арил или гетероарил;
Y' представляет собой -(CRb2)yN(Ra)-, -(CRb2)yO- или -(CRb2)yS-, расположенный таким образом, что атом N, O или S присоединен к TG, если y равно 1;
X и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, которая при активации образует атом N, O или S, способный вступать в реакцию с SO2 для вытеснения (Q)q-(L')w и образования 5-6-членного кольца, включая X-SO2 и промежуточные атомы Ar;
каждый w, x и y независимо представляет собой целое число, имеющее значение 0 или 1;
каждый из Ra и Rc независимо представляет собой водород или низший алкил; и
каждый Rb независимо представляет собой водород или низший алкил; или
два Rb вместе с атомом, к которому они присоединены, образуют 3-5-членное кольцо, предпочтительно 3-4-членное кольцо.
В некоторых вариантах осуществления n имеет значение в диапазоне от 1 до 8, от 1 до 7, от 1 до 6, от 1 до 5, от 1 до 4, от 1 до 3, от 1 до 2, или представляет собой целое число, имеющее значение 1. Когда cb равно 1, а n равно 1, отношение лекарственный препарат-антитело (DAR) ADC эквивалентно количеству лекарственных препаратов, присутствующих в (D-L). Когда cb не равно 1, отношение лекарственный препарат-антитело (DAR) ADC эквивалентно отношению количества лекарственных препаратов, присутствующих в (D-L) к количеству антител, присутствующих в конъюгате.
Примеры лекарственных препаратов для конъюгирования
ADC по изобретению обеспечивают целевую терапию, которая может, например, снижать степень побочных эффектов, часто наблюдаемые при противораковой терапии, поскольку один или более активных агентов или лекарственных препаратов доставляются в конкретную клетку.
Например, лекарственный препарат может быть выбран из группы, состоящей из эрлотиниба (TARCEVA; Genentech/OSI Pharm.); бортезомиба (VELCADE; MilleniumPharm.); фулвестранта (FASLODEX; AstraZeneca); сутента (SU11248; Pfizer); летрозола (FEMARA; Novartis); мезилата иматиниба (GLEEVEC; Novartis); PTK787 ZK 222584 (Novartis); оксалиплатина (Eloxatin; Sanofi); 5-фторурацила (5-FU); лейковорина; рапамицина (сиролимус, RAPAMUNE; Wyeth); лапатиниба (TYKERB, GSK572016; GlaxoSmithKline); лонафарниба (SCH 66336); сорафениба (BAY43-9006; Bayer Labs.); гефитиниба (IRESSA; Astrazeneca); AG1478, AG1571 (SU 5271; Sugen); алкилирующего агента (например, тиотепа или циклофосфамид CYTOXAN®); алкилсульфоната (например, бусульфан, импросульфан или пипосульфан); азиридина (например, бензодопа, карбоквон, метуредопа или уредопа); этиленимина, метилмеламина, альтретамина, триэтиленмеламина, триэтиленфосфорамида, триэтилентиофосфорамида, триметилолмеламина; ацетогенинов (например, булатацин или булатацинон); камптотецина, включая синтетический аналог топотекан; бриостатин; каллистатин; CC-1065 (включая синтетические аналоги адозелезина, карзелезина или бизелезина); криптофицинов (например, криптофицин 1 или криптофицин 8); доластатина; дуокармицина (включая синтетический аналог, KW-2189 и CB1-TM1); элейтеробина; панкратистатина; саркодиктиина; спонгистатина; азотистых ипритов (например, хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлоретамин, гидрохлорид окиси мехлорэтамина, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид или урациловый иприт); нитрозомочевины (например, кармустин, хлорозотоцин, фотемустин, ломустин, нимустин или ранимнустин); антибиотиков (например, калихеамицин, выбранный из калихеамициновой гамма II и калихеамициновой омега II или динемицина, включая динемицин А в качестве энедииновых антибиотиков); бисфосфоната (например, клодронат); эсперамицина, хромофора неокарзиностатин или родственных хромофор антибиотика хромопротеин энедиина, аклациномицина, актиномицина, антрамицина, азазерина, блеомицина, кактиномицина, карабицина, карниномицина, карзинофилина, хромомицина, дактиномицина, даунорубицина, деторубицина, 6-диазо-5-оксо-L-норлейцина, доксорубицина ADRLIMYCIN® (например, морфолино-доксорубицин, цианоморфолино-доксорубицин, 2-пирролино-доксорубицин, липосомальный доксорубицин или дезоксидоксорубицин), эпирубицина, эзорубицина, марцеломицина, митомицина (например, митомицин С, микофеноловая кислота, ногаламицин, оливомицин, пепломицин, потфиромицин, пуромицин, келамицин, родорубицин, стрептомигрин, стрептозоцин, туберцидин, убенимекс, зиностатин или зорубицин); антиметаболитов (например, 5-фторурацил (5-FU)); аналогов фолиевой кислоты (например, деноптерин, метотрексат, птероптерин или триметрексат); аналогов пурина (например, флударабин, 6-меркаптопурин, тиамиприн или тигуанин); аналогов пиримидина (например, анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин или флоксуридин); андрогена (например, калустерон, дромостанолона пропионат, эпитиостанол, мепитиостан или тестолактон); антиадреналового препарата (например, аминоглутетимид, митотан или трилостан); пополнителя фолиевой кислоты (например, фолиевая кислота); ацеглатона; альдофосфамидного гликозида; аминолевулиновой кислоты; энилурацила; амсакрина; бестрабуцила; бизантрена; эдатраксата; дефофамина; демеколцина; диазиквона; элфорнитина; ацетата эллиптиния; эпотилона; этоглюцида; нитрата галлия; гидроксимочевины; лентинана; лонидамина; мейтансиноида (например, майтанзин или ансамитоцин); трихотецена (например, токсин Т-2, верракурин А, роридин А или ангидин); митогуазона; митоксантрона; мопиданмола; нитраэрина; пентостатина; фенамета; пирарубицина; лозоксантрона; 2-этилгидразида; прокарбазина; полисахарида PSK®; разоксана; ризоксина; сизофирана; спирогермания; тенуазоновой кислоты; триазиквона; 2,2',2''-трихлортриэтиламина; трихотецена (в частности, токсин Т-2, верракурин А, роридин А или ангидин); уретана; виндезина; дакарбазина; манномустина; митобронитола; митолактола; пипобромана; гацитозина; арабинозида («Ara-C»); циклофосфамида; тиотепа; таксоидов (например, паклитаксел TAXOL® (Bristol-Myers Squibb Oncology, Princeton, NJ), ABRAXANE™ без кремофора, альбуминовые нанокомпозиции паклитаксела, American Pharmaceutical Partners, Schaumber, I11. или доксетаксел TAXOTERE® ((Rhone-Poulenc Rorer, Antony, France))); хлоранбуцила; гемцитабина; 6-тиогуанина; меркаптопурина; аналога платины (например, цисплатин или карбоплатин); винбластин; платины; этопозид, ифосфамид; митоксантрон; винкристин; винорелбин NAVELBINE®; новантрона; тенипозида; эдатрексата; дауномицина; аминоптерина; кселоды; ибандроната; СРТ-11; ингибитора топоизомеразы RFS 2000; дифторметилорнитина (DMFO); ретиноида (например, ретиноевая кислота); капецитабина; и его фармацевтически приемлемой соли, сольвата, кислоты или ее производного.
Митотические ингибиторы
В некоторых вариантах осуществления линкеры по настоящему изобретению можно использовать для конъюгирования антитела с одним или более митотическими ингибиторами для формирования ADC для лечения рака. Используемый в настоящем документе термин «митотический ингибитор» относится к цитотоксическому и/или терапевтическому агенту, который блокирует митоз или деление клеток, биологический процесс, в частности важный для раковых клеток. Митотический ингибитор разрушает микротрубочки, так что предотвращается деление клеток, часто оказывая влияние на полимеризацию микротрубочек или деполимеризацию микротрубочек. Таким образом, в определенных вариантах осуществления антитело конъюгировано с одним или более митотическими ингибиторами, которые нарушают образование микротрубочек путем ингибирования полимеризации тубулина. В одном варианте осуществления митотический ингибитор, используемый в ADC по настоящему изобретению, представляет собой Taxol® (паклитаксел), Taxotere® (доцетаксел) или Ixempra® (иксабепилон). Примеры митотических ингибиторов, которые могут быть использованы в ADC, описанных в настоящем документе, представлены ниже. К роду митотических ингибиторов относятся ауристатины, описанные выше.
Ауристатины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним ауристатином. Ауристатины представляют собой группу аналогов доластатина, которые, как было показано, обладают противоопухолевой активностью, влияя на динамику микротрубочек и гидролиз GTP, тем самым ингибируя деление клеток. Например, ауристатин E (патент США № 5635483) является синтетическим аналогом морского натурального продукта доластатина 10, соединения, которое ингибирует полимеризацию тубулина, связываясь с тем же участком на тубулине, что и противораковый лекарственный препарат винкристин (G. R. Pettit, Prog. Chem. Org. Nat. Prod, 70: 1-79 (1997)). Доластатин 10, ауристатин РЕ и ауристатин Е представляют собой линейные пептиды, имеющие четыре аминокислоты, три из которых являются уникальными для класса соединений доластатина. Типичные варианты осуществления подкласса ауристатина митотических ингибиторов включают, но не ограничиваются ими, монометилауристатин D (MMAD или производное ауристатина D), монометилауристатин E (MMAE или производное ауристатина E), монометилауристатин F (MMAF или производное ауристатина F), фенилендиамин ауристатина F (AFP), ауристатин EB (AEB), ауристатин EFP (AEFP) и 5-бензоилвалериановая кислота-сложный эфир AE (AEVB). Синтез и структура производных ауристатина описаны в публикациях патентных заявок США №№ 2003-0083263, 2005-0238649 и 2005-0009751; международной патентной публикации № WO 04/010957, международной патентной публикации № WO 02/088172 и патентах США №№ 6323315; 6239104; 6034065; 5780588; 5665860; 5663149; 5635483; 5599902; 5554725; 5530097; 5521284; 5504191; 5410024; 5,138036; 5076973; 4986988; 4978744; 4879278; 4816444; и 4486414, каждый из которых включен в настоящее описание посредством ссылки.
Доластатины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним доластатином с образованием ADC. Доластатины представляют собой короткие пептидные соединения, выделенные из морского зайца из Индийского океана Dolabella auricularia (см. Pettit et al., J. Am. Chem. Soc., 1976, 98, 4677). Примеры доластатинов включают доластатин 10 и долатстин 15. Доластатин 15, депсипептид из семи субъединиц, полученный из Dolabella auricularia, является мощным антимитотическим агентом, структурно связанным с противотубулиновым агентом доластатином 10, пептидом из пяти субъединиц, полученным из того же организма. Таким образом, в одном варианте осуществления ADC по настоящему изобретению содержит антитело, линкер, как описано в настоящем документе, и по меньшей мере один доластатин. Ауристатины, описанные выше, представляют собой синтетические производные доластатина 10.
Майтанзиноиды
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним майтанзиноидом с образованием ADC. Майтанзиноиды являются мощными противоопухолевыми агентами, которые первоначально были выделены из представителей семейства высших растений Celastraceae, Rhamnaceae и Euphorbiaceae, а также некоторых видов мхов (Kupchan et al, J. Am. Chem. Soc. 94:1354-1356 [1972]; Wani et al, J. Chem. Soc. Chem. Commun 390: [1973]; Powell et al, J. Nat. Prod. 46:660-666 [1983]; Sakai et al, J. Nat. Prod. 51:845-850 [1988]; и Suwanborirux et al, Experientia 46:117-120 [1990]). Имеющиеся данные свидетельствуют о том, что майтанзиноиды ингибируют митоз, ингибируя полимеризацию микротрубочкового белка тубулина, тем самым предотвращая образование микротрубочек (см., например, патент США № 6441163 и Remillard et al., Science, 189, 1002-1005 (1975)). Было показано, что майтанзиноиды ингибируют рост опухолевых клеток in vitro с использованием моделей клеточных культур и in vivo с использованием систем лабораторных животных. Кроме того, цитотоксичность майтанзиноидов в 1000 раз выше, чем у обычных химиотерапевтических средств, таких как, например, метотрексат, даунорубицин и винкристин (см., например, патент США № 5208020).
Майтанзиноиды включают майтанзин, майтанзинол, С-3-сложные эфиры майтанзинола и другие аналоги и производные майтанзинола (см., например, патенты США №№ 5208020 и 6441163, каждый из которых включен в настоящее описание посредством ссылки). С-3-сложные эфиры майтанзинола могут быть природными или полученными синтетическим способом. Кроме того, как природные, так и синтетические сложные эфиры C-3 майтанзинола могут быть классифицированы как C-3-сложный эфир с простыми карбоновыми кислотами или C-3-сложный эфир с производными N-метил-L-аланина, причем последние являются более цитотоксичными, чем предыдущий. Синтетические аналоги майтанзиноидов описаны, например, в Kupchan et al., J. Med. Chem., 21, 31-37 (1978).
Подходящие майтанзиноиды для использования в ADC по настоящему изобретению могут быть выделены из природных источников, получены синтетическим путем или получены полусинтетическим путем. Кроме того, майтанзиноид может быть модифицирован любым подходящим способом, при условии, что в конечной молекуле конъюгата сохраняется достаточная цитотоксичность. Структура типичного майтанзиноида, мертанзина (DM1), представлена ниже.
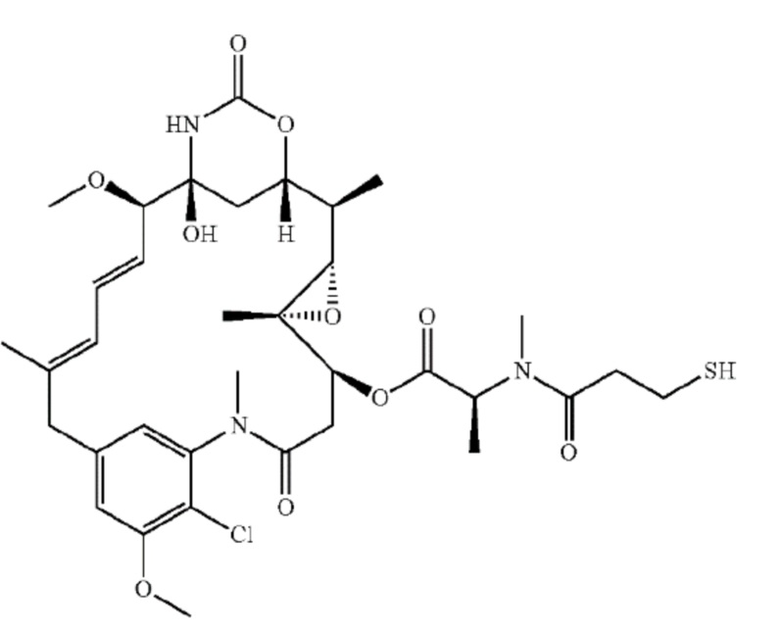
Мертанзин (DM1)
Типичные примеры майтанзиноидов включают, но не ограничиваются ими, DM1 (N2'-деацетил-N2'-(3-меркапто-1-оксопропил)-майтанзин, также называемый мертанзином, лекарственный препарат майтанзиноид 1; ImmunoGen, Inc.; см. также Chari et al. (1992) Cancer Res 52:127), DM2, DM3 (N2'-деацетил-N2'-(4-меркапто-1-оксопентил)-майтанзин), DM4 (4-метил-4-меркапто-1-оксопентил)-майтанзин) и майтанзинол (синтетический аналог майтанзиноидов). Другие примеры майтанзиноидов описаны в патенте США № 8142784, который включен в настоящий документ посредством ссылки.
Ансамитоцины представляют собой группу майтанзиноидных антибиотиков, которые были выделены из различных бактериальных источников. Эти соединения обладают сильной противоопухолевой активностью. Типичные примеры включают, но не ограничиваются ими, ансамитоцин P1, ансамитоцин P2, ансамитоцин P3 и ансамитоцин P4.
Растительные алкалоиды
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним растительным алкалоидом, например, таксаном или алкалоидом барвинка. Растительные алкалоиды представляют собой химиотерапевтические средства, полученные из определенных видов растений. Алкалоиды барвинка производятся из барвинка (Catharanthus rosea), а таксаны - из коры тихоокеанского тиса (Taxus). И алкалоиды барвинка, и таксаны также известны как антимикротрубочковые агенты и более подробно описаны ниже.
Таксаны
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним таксаном. Используемый в данном документе термин «таксан» относится к классу противоопухолевых агентов, имеющих механизм действия на микротрубочки и имеющих структуру, которая включает структуру кольца таксана и стереоспецифическую боковую цепь, которая требуется для цитостатической активности. Термин «таксан» также включает различные известные производные, включая как гидрофильные производные, так и гидрофобные производные. Производные таксана включают, но не ограничиваются ими, производные галактозы и маннозы, описанные в международной заявке на патент № WO 99/18113; пиперазино и другие производные, описанные в WO 99/14209; производные таксана, описанные в WO 99/09021, WO 98/22451 и патенте США № 5869680; производные 6-тио, описанные в WO 98/28288; производные сульфенамида, описанные в патенте США № 5821263; и производное таксола, описанное в патенте США № 5415869, каждый из которых включен в настоящий документ посредством ссылки. Соединения таксана также были ранее описаны в патентах США №№ 5641803, 5665671, 5380751, 5728687, 5415869, 5407683, 5399363, 5424073, 5157049, 5773464, 5821263, 5840929, 4814470, 5438072, 5403858, 4960790, 5433364, 4942184, 5362831, 5705503, и 5278324, все из которых напрямую включены в настоящий документ посредством ссылки. Дополнительные примеры таксанов включают, но не ограничиваются ими, доцетаксел (Taxotere®; Sanofi Aventis), паклитаксел (Abraxane® или Taxol®; Abraxis Oncology) и наночастицы паклитаксела (ABI-007/Abraxene®; Abraxis Bioscience).
В одном варианте осуществления линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним доцетакселом. В одном варианте осуществления линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним паклитакселом.
Алкалоиды барвинка
В одном варианте осуществления линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним алкалоидом барвинка. Алкалоиды барвинка представляют собой класс препаратов, специфичных для клеточного цикла, которые действуют путем ингибирования способности раковых клеток делиться, воздействуя на тубулин и предотвращая образование микротрубочек. Примеры алкалоидов барвинка, которые можно использовать в ADC по настоящему изобретению включают, но не ограничиваются ими, виндезин сульфат, винкристин, винбластин и винорелбин.
Противоопухолевые антибиотики
Линкеры по настоящему изобретению можно использовать для конъюгирования антитела с одним или более противоопухолевыми антибиотиками для лечения рака. Используемый в настоящем документе термин «противоопухолевый антибиотик» означает противоопухолевый препарат, который блокирует рост клеток, воздействуя на ДНК, его изготавливают из микроорганизма. Зачастую противоопухолевые антибиотики либо разрушают нити ДНК, либо замедляют или останавливают синтез ДНК. Примеры противоопухолевых антибиотиков, которые могут быть включены в ADC, описанные в данном документе, включают, но не ограничиваются ими, актиномицины (например, пирроло[2,1-c][1,4]бензодиазепины), антрациклины, калихеамицины и дуокармицины, описанные более подробно ниже.
Актиномицины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним актиномицином. Актиномицины представляют собой подкласс противоопухолевых антибиотиков, выделенных из бактерий рода Streptomyces. Типичные примеры актиномицинов включают, но не ограничиваются ими, актиномицин D (Cosmegen [также известный как актиномицин, дактиномицин, актиномицин IV, актиномицин C1], Lundbeck, Inc.), антрамицин, чикамицин A, DC-81, мазетрамицин, неотрамицин A, неотрамицин В, поротрамицин, протракарцин В, SG2285, сибаномицин, сибиромицин и томаймицин. В одном варианте осуществления D представляет собой пирролобензодиазепин (PBD). Примеры PBD включают, но не ограничиваются ими, антрамицин, чикамицин A, DC-81, мазетрамицин, неотрамицин A, неотрамицин B, поротрамицин, протракарцин B, SG2000 (SJG-136), SG2202 (ZC-207), SG2285 (ZC-423), сибаномицин, сибиромицин и томаймицин. Таким образом, в одном варианте осуществления D представляет собой актиномицин, например, актиномицин D, или PBD, например, димер пирролобензодиазепина (PBD).
Структуры PBD можно найти, например, в публикациях заявки на патенты США №№ 2013/0028917 и 2013/0028919, а также в WO 2011/130598 А1, каждый из которых полностью включен в настоящий документ посредством ссылки. Общая структура PBD представлена ниже.
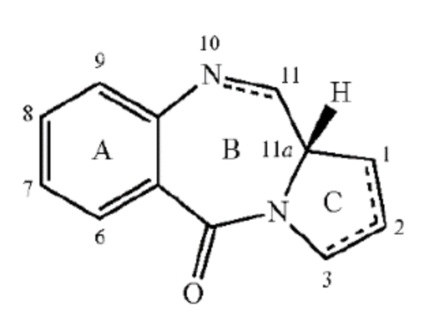
PBD различаются по количеству, типу и положению заместителей, как в их ароматических кольцах А, так и в пирроло С-кольцах, а также по степени насыщения С-кольца. В B-кольце обычно присутствует имин (N=C), карбиноламин (NH-CH(OH)) или метиловый эфир карбиноламина (NH-CH(OMe)) в положении N10-C11, которое является электрофильным центром, ответственным за алкилирование ДНК. Все известные натуральные продукты имеют (S)-конфигурацию в хиральном положении C11α, что дает им поворот вправо, если смотреть с кольца C на кольцо A. Дополнительные примеры PBD, которые могут быть конъюгированы с антителами посредством линкеров, описанные в данном документе, можно найти, например, в публикациях патентных заявок США №№ 2013/0028917 А1 и 2013/0028919 А1, в патенте США № 7741319 B2, а также в WO 2011/130598 A1 и WO 2006/111759 A1, каждый из которых полностью включен в настоящий документ посредством ссылки.
Антрациклины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антрациклином. Антрациклины представляют собой подкласс противоопухолевых антибиотиков, выделенных из бактерий рода Streptomyces. Типичные примеры включают, но не ограничиваются ими, даунорубицин (Cerubidine, Bedford Laboratories), доксорубицин (Adriamycin, Bedford Laboratories, также именуемый как доксорубицина гидрохлорид, гидроксидаунорубицин и Rubex), эпирубицин (Ellence, Pfizer), и идарубицин (Idamycin; Pfizer Inc.). Таким образом, в одном варианте осуществления D представляет собой антрациклин, например, доксорубицин.
Калихеамицины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним калихеамицином. Калихеамицины представляют собой семейство энедииновых антибиотиков, полученных из почвенного организма Micromonospora echinospora. Калихеамицины связывают малую бороздку ДНК и вызывают разрывы двухцепочечной ДНК, что приводит к гибели клеток со 100-кратным увеличением по сравнению с другими химиотерапевтическими средствами (Damle et al. (2003) Curr Opin Pharmacol 3:386). Получение калихеамицинов, которые могут быть использованы в качестве лекарственных конъюгатов в изобретении уже было описано, см. патенты США №№ 5712374; 5714586; 5739116; 5767285; 5770701; 5770710; 5773001; и 5877296. Структурные аналоги калихеамицина, которые можно использовать, включают, но не ограничиваются ими, γ1I, α2I, α3I, N-ацетил-γ1I, PSAG и θI1 (Hinman et al., Cancer Research 53:3336-3342 (1993), Lode et al., Cancer Research 58:2925-2928 (1998) и вышеупомянутые патенты США №№ 5712374; 5714586; 5739116; 5767285; 5770701; 5770710; 5773001; и 5877296). Таким образом, в одном варианте осуществления D представляет собой калихеамицин.
Дуокармицины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним дуокармицином. Дуокармицины представляют собой подкласс противоопухолевых антибиотиков, выделенных из бактерий рода Streptomyces. (см. Nagamura and Saito (1998) Chemistry of Heterocyclic Compounds, Vol. 34, No. 12). Дуокармицины связываются с малой бороздкой ДНК и алкилируют нуклеотидное основание аденин в положении N3 (Boger (1993) Pure and Appl Chem 65(6):1123; и Boger и Johnson (1995) PNAS USA 92:3642). Синтетические аналоги дуокармицинов включают, но не ограничиваются ими, адозелезин, бизелезин и карзелезин. Таким образом, в одном варианте осуществления D представляет собой дуокармицин.
Другие противоопухолевые антибиотики
В дополнение к вышеизложенному, дополнительные противоопухолевые антибиотики, которые могут быть использованы в ADC по настоящему изобретению, включают блеомицин (Blenoxane, Bristol-Myers Squibb), митомицин и пликамицин (также известный как митрамицин).
Иммуномодуляторы
В некоторых вариантах осуществления линкеры по изобретению можно использовать для конъюгирования антитела по меньшей мере с одним иммуномодулятором. Используемый в настоящем документе термин «иммуномодуляторы» относится к агенту, который может стимулировать или модифицировать иммунный ответ. В одном варианте осуществления иммуномодуляторы представляет собой иммуностимулятор, который усиливает иммунный ответ субъекта. В некоторых вариантах осуществления иммуномодуляторы представляет собой иммунодепрессант, который предотвращает или уменьшает иммунный ответ субъекта. Иммуномодулятор может модулировать миелоидные клетки (моноциты, макрофаги, дендритные клетки, мегакариоциты и гранулоциты) или лимфоидные клетки (Т-клетки, В-клетки и естественные клетки-киллеры (NK)) и любые дополнительно дифференцированные клетки. Типичные примеры включают, но не ограничиваются ими, бацилла Кальмета - Герена (BCG) и левамизол (Ergamisol). Другие примеры иммуномодуляторов, которые можно использовать в ADC по настоящему изобретению, включают, но не ограничиваются ими, противораковые вакцины, цитокины и иммуномодулирующую генную терапию.
Противораковые вакцины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела с противораковой вакциной. Используемый в настоящем документе термин «противораковая вакцина» относится к композиции (например, опухолевому антигену и цитокину), которая вызывает специфический для опухоли иммунный ответ. Ответ вызывается из собственной иммунной системы субъекта путем введения противораковой вакцины или, в случае настоящего изобретения, путем введения ADC, включающего антитело и противораковую вакцину. В предпочтительных вариантах осуществления иммунный ответ приводит к эрадикации опухолевых клеток в организме (например, первичных или метастатических опухолевых клеток). Применение противораковых вакцин обычно включает введение определенного антигена или группы антигенов, которые, например, присутствуют на поверхности конкретной раковой клетки или присутствуют на поверхности конкретного инфекционного агента, который, как показано, стимулирует образование рака. В некоторых вариантах осуществления противораковые вакцины используются в профилактических целях, тогда как в других вариантах осуществления используются для терапевтических целей. Неограничивающие примеры противораковых вакцин, которые можно использовать в описываемых в настоящем документе ADC, включают в себя рекомбинантную двухвалентную вакцину против вируса папилломы человека (HPV) типов 16 и 18 (Cervarix, GlaxoSmithKline), рекомбинантную четырехвалентную вакцину против вируса папилломы человека (HPV) типов 6, 11, 16 и 18 (Gardasil, Merck & Company) и сипулеуцел-Т (Provenge, Dendreon). Таким образом, в одном варианте осуществления D представляет собой противораковую вакцину, которая является либо иммуностимулятором, либо иммунодепрессантом.
Цитокины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним цитокином. Термин «цитокин» обычно относится к белкам, высвобождаемым одной клеточной популяцией, которые действуют на другую клетку в качестве межклеточных медиаторов. Цитокины непосредственно стимулируют иммунные эффекторные клетки и стромальные клетки в месте опухоли и улучшают распознавание опухолевых клеток цитотоксическими эффекторными клетками (Lee and Margolin (2011) Cancers 3:3856). Многочисленные исследования на животных моделях опухолей показали, что цитокины обладают широкой противоопухолевой активностью, и это было воплощено в ряде основанных на цитокинах подходов к противораковой терапии (Lee and Margoli, supra). В последние годы ряд цитокинов, в том числе GM-CSF, IL-7, IL-12, IL-15, IL-18 и IL-21, был включен в клинические испытания для пациентов с распространенным раком (Lee and Margoli, supra).
Примеры цитокинов, которые можно использовать в ADC по настоящему изобретению, включают, но не ограничиваются ими, паратиреоидный гормон; тироксин; инсулин; проинсулин; релаксин; прорелаксин; гликопротеиновые гормоны, такие как фолликулостимулирующий гормон (FSH), тиреотропный гормон (TSH) и лютеинизирующий гормон (LH); фактор роста печени; фактор роста фибробластов; пролактин; плацентарный лактоген; фактор некроза опухоли; мюллеровская ингибирующая субстанция; пептид, связанный с гонадотропином мыши; ингибин; активин; фактор роста эндотелия сосудов; интегрин; тромбопоэтин (TPO); факторы роста нервов, такие как NGF; фактор роста тромбоцитов; трансформирующие факторы роста (TGF); инсулиноподобный фактор роста-I и -II; эритропоэтин (EPO); остеоиндуктивные факторы; интерфероны, такие как интерферон α, β и γ, колониестимулирующие факторы (CSF); гранулоцитарно-макрофагальный-C-SF (GM-CSF); и гранулоцитарный-CSF (G-CSF); интерлейкины (IL), такие как IL-1, IL-1a, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-11, IL-12; фактор некроза опухоли; и другие полипептидные факторы, включая LIF и комплектный лиганд (KL). Применяемый в данном документе термин цитокин включает белки из натуральных источников или из рекомбинантной клеточной культуры и биологически активные эквиваленты цитокинов исходной последовательности. Таким образом, в одном варианте осуществления D представляет собой цитокин.
Колониестимулирующие факторы (CSF)
Линкеры по изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним колониестимулирующим фактором (CSF). Колониестимулирующие факторы (CSF) представляют собой факторы роста, которые помогают костному мозгу в выработке эритроцитов. Поскольку некоторые виды лечения рака (например, химиотерапия) могут воздействовать на лейкоциты (которые помогают бороться с инфекцией), колониестимулирующие факторы могут вводится в качестве вспомогательного средства для поддержания уровней лейкоцитов и укрепления иммунной системы. Колонестимулирующие факторы также могут использоваться после пересадки костного мозга в качестве вспомогательного средства для начала выработки лейкоцитов. Типичные примеры CSF, которые могут использоваться в ADC, описанные в настоящем документе, включают, но не ограничиваются ими, эритропоэтин (Epoetin), филграстим (Neopogen (также известный как гранулоцитарный колониестимулирующий фактор (G-CSF); Amgen, Inc.), сарграмостим (лейкин (гранулоцитарно-макрофагальный колониестимулирующий фактор и GM-CSF); Genzyme Corporation), промегапоэтин и опрелвекин (рекомбинантный IL-11; Pfizer, Inc.). Таким образом, в одном варианте осуществления D представляет собой CSF.
Генная терапия
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одной нуклеиновой кислотой (непосредственно или опосредованно посредством носителя) для генной терапии. Генная терапия обычно относится к введению генетического материала в клетку, причем генетический материал предназначен для лечения заболевания. Поскольку это относится к иммуномодуляторам, генная терапия используется для стимуляции природной способности субъекта ингибировать пролиферацию раковых клеток или убивать раковые клетки. В одном варианте осуществления ADC по изобретению содержит нуклеиновую кислоту, кодирующую функциональный терапевтический ген, который используется для замены мутированного или иным образом дисфункционального (например, усеченного) гена, связанного с раком. В других вариантах осуществления ADC по изобретению содержит нуклеиновую кислоту, которая кодирует или иным образом обеспечивает выработку терапевтического белка для лечения рака. Нуклеиновая кислота, которая кодирует терапевтический ген, может быть непосредственно конъюгирована с антителом или, альтернативно, может быть конъюгирована с антителом посредством носителя. Примеры носителей, которые можно использовать для доставки нуклеиновой кислоты для генной терапии, включают, но не ограничиваются ими, вирусные векторы или липосомы.
Алкилирующие агенты
Линкеры по настоящему изобретению можно использовать для конъюгирования антитела с одним или более алкилирующими агентами. Алкилирующие агенты представляют собой класс противоопухолевых соединений, которые присоединяют алкильную группу к ДНК. Примеры алкилирующих агентов, которые можно использовать в ADC по изобретению, включают, но не ограничиваются ими, алкилсульфонаты, этиленимины, производные метиламина, эпоксиды, азотистые иприты, нитрозомочевины, триазины и гидразины.
Алкилсульфонаты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним алкилсульфонатом. Алкилсульфонаты являются подклассом алкилирующих агентов с общей формулой: R-SO2-O-R1, где R и R1 обычно представляют собой алкильные или арильные группы. Типичным примером алкилсульфоната является бусульфан (Myleran®, GlaxoSmithKline; Busulfex IV®, PDL BioPharma, Inc.).
Азотистые иприты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним азотистым ипритом. Типичные примеры этого подкласса противораковых соединений включают, но не ограничиваются ими, хлорамбуцил (Leukeran®, GlaxoSmithKline), циклофосфамид (Cytoxan®, Bristol-Myers Squibb; Neosar, Pfizer, Inc.), эстрамустин (эстрамустина фосфат натрия или Estracyt®), Pfizer, Inc.), ифосфамид (Ifex®, Bristol-Myers Squibb), мехлоретамин (Mustargen®, Lundbeck Inc.) и мелфалан (Alkeran® или L-Pam® или иприт фенилаланина; GlaxoSmithKline).
Нитрозомочевины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одной нитрозомочевиной. Нитрозомочевины представляют собой подкласс алкилирующих агентов, которые являются растворимыми в липидах. Типичные примеры включают, но не ограничиваются ими, кармустин (BCNU [также известный как BiCNU, N, N-бис(2-хлорэтил)-N-нитрозомочевина или 1,3-бис(2-хлорэтил)-1-нитрозомочевина], Bristol-Myers Squibb), фотемустин (также известный как Muphoran®), ломустин (CCNU или 1-(2-хлорэтил)-3-циклогексил-1-нитрозомочевина, Bristol-Myers Squibb), нимустин (также известный как ACNU) и стрептозоцин (Zanosar®, Teva Pharmaceuticals).
Триазины и гидразины
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним триазином или гидразином. Триазины и гидразины представляют собой подкласс азотсодержащих алкилирующих агентов. В некоторых вариантах осуществления эти соединения спонтанно разлагаются или могут метаболизироваться с образованием промежуточных соединений алкилдиазония, которые облегчают перенос алкильной группы в нуклеиновые кислоты, пептиды и/или полипептиды, тем самым вызывая мутагенные, канцерогенные или цитотоксические эффекты. Типичные примеры включают, но не ограничиваются ими, дакарбазин (DTIC-Dome, Bayer Healthcare Pharmaceuticals Inc.), прокарбазин (Mutalane®, Sigma-Tau Pharmaceuticals, Inc.), и темозоломид (Temodar®, Schering Plough).
Другие алкилирующие агенты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним с одним этиленимином, производным метиламина или эпоксидом. Этиленимины представляют собой подкласс алкилирующих агентов, которые обычно содержат по меньшей мере одно азиридиновое кольцо. Эпоксиды представляют собой подкласс алкилирующих агентов, которые характеризуются как циклические простые эфиры только с тремя кольцевыми атомами.
Типичные примеры этилениминов включают, но не ограничиваются ими, тиопету (Thioplex, Amgen), диазихон (также известный как азиридинилбензохинон (AZQ)) и митомицин C. Митомицин C является природным продуктом, который содержит азиридиновое кольцо и, по-видимому, вызывает цитотоксичность посредством сшивания ДНК (Dorr R T, et al. Cancer Res. 1985; 45:3510; Kennedy K A, et al Cancer Res. 1985; 45:3541). Типичные примеры производных метиламина и их аналогов включают, но не ограничиваются ими, альтретамин (Hexalen, MGI Pharma, Inc.), который также известен как гексаметиламин и гексастат. Типичные примеры эпоксидов этого класса противораковых соединений включают, но не ограничиваются ими, диангидрогалактитол. Диангидрогалактитол (1,2:5,6-диангидродульцитол) химически связан с азиридинами и обычно облегчает перенос алкильной группы посредством механизма, аналогичного описанному выше. Дибромодульцитол гидролизуется до диангидрогалактитола и, таким образом, является пролекарством эпоксида (Sellei C, et al. Cancer Chemother Rep. 1969; 53:377).
Антиангиогенные агенты
В некоторых вариантах осуществления линкеры по изобретению можно использовать для конъюгирования антитела по меньшей мере с одним антиангиогенным агентом. Антиангиогенные агенты ингибируют рост новых кровеносных сосудов. Антиангиогенные агенты оказывают свой эффект различными способами. В некоторых вариантах осуществления данные агенты влияют на способность фактора роста достигать своей цели. Например, фактор роста эндотелия сосудов (VEGF) является одним из первичных белков, участвующих в инициации ангиогенеза путем связывания с конкретными рецепторами на поверхности клетки. Таким образом, определенные антиангиогенные агенты, которые предотвращают взаимодействие VEGF с его родственным рецептором, предотвращают инициацию ангиогенеза VEGF. В других вариантах осуществления эти агенты оказывают влияние на внутриклеточные сигнальные каскады. Например, после запуска определенного рецептора на клеточной поверхности инициируется каскад других химических сигналов, способствующих росту кровеносных сосудов. Таким образом, определенные ферменты, например некоторые тирозинкиназы, которые, как известно, облегчают внутриклеточные сигнальные каскады, способствующие, например, пролиферации клеток, являются мишенями для лечения рака. В других вариантах осуществления эти агенты оказывают влияние на межклеточные сигнальные каскады. Тем не менее, в других вариантах осуществления эти агенты блокируют специфические мишени, которые активируют и стимулируют рост клеток или непосредственно препятствуют росту клеток кровеносных сосудов. Ингибирующие свойства ангиогенеза были обнаружены в более чем 300 веществах с многочисленными прямыми и непрямыми ингибирующими эффектами.
Типичные примеры антиангиогенных агентов, которые можно использовать в ADC по настоящему изобретению, включают, но не ограничиваются ими, ангиостатин, ABX EGF, C1-1033, PKI-166, вакцину EGF, EKB-569, GW2016, ICR-62, EMD 55900, CP358, PD153035, AG1478, IMC-C225 (Erbitux, ZD1839 (Iressa), OSI-774, Эрлотиниб (тарцева), ангиостатин, аррестин, эндостатин, BAY 12-9566 и с фторурацилом или доксорубицином, канстатином, карбоксиамидотриозолом и паклитакселом, EMD121974, S-24, витаксин, диметилксантенон уксусная кислота, IM862, Интерлейкин-12, Интерлейкин-2, NM-3, HuMV833, PTK787, RhuMab, ангиозим (рибозим), IMC-1C11, неовастат, маримстат, приномастат, BMS-275291, COL-3, MM1270, SU101, SU6668, SU11248, SU5416, с паклитакселом, с гемцитабином и цисплатином и с иринотеканом и цисплатином, а также с лучевой терапией, техогалан, темозоломид и ПЭГ-интерферон α2b, тетратиомолибдат, TNP-470, талидомид, CC-5013 и с таксотером, тумстатин, 2-метоксиэстрадиол, ловушка VEGF, ингибиторы mTOR (дефоролимус, эверолимус (Afinitor, Novartis Pharmaceutical Corporation) и темсиролимус (Torisel, Pfizer, Inc.)), ингибиторы тирозинкиназы (например, эрлотиниб (Tarceva, Genentech, Inc.), иматиниб (Gleevec, Novartis Pharmaceutical Corporation), гефитиниб (Iressa, AstraZeneca Pharmaceuticals), дазатиниб (Sprycel, Brystol-Myers Squibb), сунитиниб (Sutent, Pfizer, Inc.), нилотиниб (Tasigna, Novartis Pharmaceutical Corporation), лапатиниб (Tykerb, GlaxoSmithKline Pharmaceuticals), сорафениб (Nexavar, Bayer и Onyx), фосфоинозитид-3-киназы (PI3K).
Антиметаболиты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антиметаболитом. Антиметаболиты представляют собой варианты химиотерапии, которые очень похожи на обычные вещества, содержащиеся в клетке. Когда клетки включают антиметаболит в клеточный метаболизм, результат для клетки является отрицательным, например, клетка не способна делиться. Антиметаболиты классифицируются по веществам, с которыми они интерферируют. Примеры антиметаболитов, которые могут быть использованы в ADC по настоящему изобретению, включают, но не ограничиваются ими, антагонист фолиевой кислоты (например, метотрексат), антагонист пиримидина (например, 5-фторурацил, фоксуридин, цитарабин, капецитабин и гемцитабин), антагонист пурина (например, 6-меркаптопурин и 6-тиогуанин) и ингибитор аденозиндеаминазы (например, кладрибин, флударабин, неларабин и пентостатин), как более подробно описано ниже.
Антифолаты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антифолатом. Антифолаты представляют собой подкласс антиметаболитов, которые структурно похожи на фолат. Типичные примеры включают, но не ограничиваются ими, метотрексат, 4-амино-фолиевую кислоту (также известную как аминоптерин и 4-аминоптероевая кислота), лометрексол (LMTX), пеметрексед (Alimpta, Eli Lilly and Company) и триметрексат (Neutrexin, Ben Venue Laboratories, Inc.)
Антагонисты пуринов
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антагонистом пурина. Аналоги пурина представляют собой подкласс антиметаболитов, которые структурно аналогичны группе соединений, известных как пурины. Типичные примеры антагонистов пуринов включают, но не ограничиваются ими, азатиоприн (Azasan, Salix; Imuran, GlaxoSmithKline), кладрибин (Leustatin [также известный как 2-CdA], Janssen Biotech, Inc.), меркаптопурин (Purinethol [также известный как 6-меркаптоэтанол], GlaxoSmithKline), флударабин (Fludara, Genzyme Corporation), пентостатин (Nipent, также известный как 2′-дезоксикоформин (DCF)), 6-тиогуанин (Lanvis [также известный как тиогуанин]), GlaxoSmithKline).
Антагонисты пиримидина
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антагонистом пиримидина. Антагонисты пиримидина представляют собой подкласс антиметаболитов, которые структурно аналогичны группе соединений, известных как пурины. Типичные примеры антагонистов пиримидина включают, но не ограничиваются ими, азацитидин (Vidaza, Celgene Corporation), капецитабин (Xeloda, Roche Laboratories), цитарабин (также известный как цитозина арабинозид и арабинозилцитозин, Bedford Laboratories), децитабин (Dacogen, Eisai Pharmaceuticals), 5-фторурацил (Adrucil, Teva Pharmaceuticals; Efudex, Valeant Pharmaceuticals, Inc), 5-фтор-2′-дезоксиуридин-5′-фосфат (FdUMP), 5-фторуридинтрифосфат и гемцитабин (Gemzar, Eli Lilly and Company).
Борсодержащие агенты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним борсодержащим агентом. Борсодержащие агенты включают класс противораковых терапевтических соединений, которые препятствуют пролиферации клеток. Типичные примеры борсодержащих агентов включают, но не ограничиваются ими, борофицин и бортезомиб (Velcade, Millenium Pharmaceuticals).
Химиопротекторные агенты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним химиопротекторным агентом. Химиопротекторные препараты представляют собой класс соединений, которые помогают защитить организм от специфических токсических эффектов химиотерапии. Химиопротекторные агенты можно вводить при проведении различных вариантов химиотерапии, чтобы защитить здоровые клетки от токсического воздействия химиотерапевтических препаратов, одновременно позволяя лечить раковые клетки вводимым химиотерапевтическим препаратом. Типичные химиопротекторные агенты включают, но не ограничиваются ими, амифостин (Ethyol, Medimmune, Inc.), который используется для снижения почечной токсичности, связанной с кумулятивными дозами цисплатина, дексразоксан (Totect, Apricus Pharma; Zinecard), для лечения экстравазации, вызванной введением антрациклина (Totect) и для лечения сердечно-сосудистых осложнений, вызванных введением противоопухолевого антибиотика доксорубицина (Zinecard) и месну (Mesnex, Bristol-Myers Squibb), которая используется для предотвращения геморрагического цистита во время проведения химиотерапии с применением ифосфамида.
Гормональные агенты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним гормональным агентом. Гормональный агент (включая синтетические гормоны) представляет собой соединение, которое препятствует выработке или активности эндогенно продуцируемых гормонов эндокринной системы. В некоторых вариантах осуществления эти соединения препятствуют росту клеток или оказывают цитотоксическое действие. Неограничивающие примеры включают андрогены, эстрогены, медроксипрогестерона ацетат (Provera, Pfizer, Inc.) и прогестины.
Антигормональные агенты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антигормональным агентом. «Антигормональный» агент представляет собой агент, который подавляет выработку и/или предотвращает функционирование определенных эндогенных гормонов. В одном варианте осуществления антигормональный агент препятствует активности гормона, выбранного из группы, включающей андрогены, эстрогены, прогестерон и гоанадотропин-рилизинг-гормон, тем самым препятствуя росту различных раковых клеток. Типичные примеры антигормональных агентов включают, но не ограничиваются ими, аминоглутетимид, анастрозол (Arimidex, AstraZeneca Pharmaceuticals), бикалутамид (Casodex, AstraZeneca Pharmaceuticals), ципротерона ацетат (Cyprostat, Bayer PLC), дегареликс (Firmagon, Ferring Pharmaceuticals), экземестан (Aromasin, Pfizer Inc.), флутамид (Drogenil, Schering-Plough Ltd), фулвестрант (Faslodex, AstraZeneca Pharmaceuticals), гозерелин (Zolodex, AstraZeneca Pharmaceuticals), летрозол (Femara, Novartis Pharmaceuticals Corporation), лейпролид (Prostap), лупрон, медроксипрогестерона ацетат (Provera, Pfizer Inc.), мегестрола ацетат (Megace, Bristol-Myers Squibb Company), тамоксифен (Nolvadex, AstraZeneca Pharmaceuticals) и трипторелин (Decapetyl, Ferring).
Кортикостероиды
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним кортикостероидом. Кортикостероиды могут быть использованы в ADC по настоящему изобретению для уменьшения воспаления. Примеры кортикостероидов включают, но не ограничивается ими, глюкокортикоид, например, преднизон (Deltasone, Pharmacia & Upjohn Company, подразделение компании Pfizer, Inc.).
Фотоактивные терапевтические агенты
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним фотоактивным терапевтическим агентом. Фотоактивные терапевтические агенты включают соединения, которые могут быть использованы для уничтожения обработанных клеток при воздействии электромагнитного излучения определенной длины волны. Терапевтически значимые соединения поглощают электромагнитное излучение на длинах волн, которые проникают в ткани. В предпочтительных вариантах осуществления соединение вводят в нетоксичной форме, которая способна вызывать фотохимический эффект, являющийся токсичным для клеток или тканей при достаточной активации. В других предпочтительных вариантах осуществления данные соединения удерживаются раковой тканью и легко удаляются из нормальных тканей. Неограничивающие примеры включают различные хромагены и красители.
Олигонуклеотиды
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним олигонуклеотидом. Олигонуклеотиды состоят из коротких цепей нуклеиновых кислот, которые действуют путем препятствования обработке генетической информации. В некоторых вариантах осуществления олигонуклеотиды для использования в ADC представляют собой немодифицированные одноцепочечные и/или двухцепочечные молекулы ДНК или РНК, тогда как в других вариантах осуществления эти терапевтические олигонуклеотиды представляют собой химически модифицированные одноцепочечные и/или двухцепочечные молекулы ДНК или РНК. В одном варианте осуществления олигонуклеотиды, используемые в ADC, являются относительно короткими (19-25 нуклеотидов) и гибридизуются с уникальной последовательностью нуклеиновой кислоты в общем пуле мишеней нуклеиновых кислот, присутствующих в клетках. Некоторые из важных олигонуклеотидных технологий включают антисмысловые олигонуклеотиды (включая РНК-интерференцию (RNAi)), аптамеры, CpG-олигонуклеотиды и рибозимы.
Антисмысловые олигонуклеотиды
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антисмысловым олигонуклеотидом. Антисмысловые олигонуклеотиды предназначены для связывания с РНК посредством гибридизации Уотсона - Крика. В некоторых вариантах осуществления антисмысловой олигонуклеотид является комплементарным нуклеотиду, кодирующему область, домен, часть или сегмент конъюгированного антитела. В некоторых вариантах осуществления антисмысловой олигонуклеотид содержит от приблизительно 5 до приблизительно 100 нуклеотидов, от приблизительно 10 до приблизительно 50 нуклеотидов, от приблизительно 12 до приблизительно 35 и от приблизительно 18 до приблизительно 25 нуклеотидов
Существует множество механизмов, которые можно использовать для ингибирования функции РНК после связывания олигонуклеотида РНК-мишенью (Crooke ST. (1999). Biochim. Biophys. Acta, 1489, 30-42). Лучше всего охарактеризованный антисмысловой механизм приводит к расщеплению целевой РНК эндогенными клеточными нуклеазами, такими как РНаза Н или нуклеаза, связанная с механизмом РНК-интерференции. Однако олигонуклеотиды, которые ингибируют экспрессию гена-мишени некаталитическими механизмами, такими как модуляция сплайсинга или остановка трансляции, также могут быть мощными и селективными модуляторами функции гена.
Другой РНаза-зависимый антисмысловой механизм, которому в последнее время уделяется много внимания, - это РНКи (Fire et al. (1998). Nature, 391, 806-811; Zamore PD. (2002). Science, 296, 1265-1269.). РНК-интерференция (РНКи) представляет собой посттранскрипционный процесс, при котором двухцепочечная РНК ингибирует экспрессию генов в определенной последовательности. В некоторых вариантах осуществления эффект РНКи достигается посредством введения относительно более длинной двухцепочечной РНК (дцРНК), в то время как в предпочтительных вариантах осуществления этот эффект РНКи достигается путем введения более коротких двухцепочечных РНК, например, малой интерферирующей РНК (миРНК) и/или микроРНК (микроРНК). В еще одном варианте осуществления РНКи также может быть достигнута путем введения плазмиды, которая генерирует дцРНК, комплементарную гену-мишени. В каждом из вышеизложенных вариантов осуществления двухцепочечная РНК предназначена для вмешательства в экспрессию гена конкретной последовательности-мишени в клетках. Обычно этот механизм включает превращение дцРНК в короткие РНК, которые направляют рибонуклеазы к гомологичным мишеням мРНК (обобщено, RRuvkun, Science 2294:797 (2001)), что затем приводит к деградации соответствующей эндогенной мРНК, тем самым приводя к модуляции экспрессии генов. Примечательно, что дцРНК обладает антипролиферативными свойствами, что позволяет также предусмотреть терапевтические применения (Aubel et al., Proc. Natl. Acad. Sci., USA 88:906 (1991)). Например, было показано, что синтетическая дцРНК ингибирует рост опухоли у мышей (Levy et al. Proc. Nat. Acad. Sci. USA, 62:357-361 (1969)), активно участвует в лечении лейкоза у мышей (Zeleznick et al., Proc. Soc. Exp. Biol. Med. 130:126-128 (1969)), и ингибирует химически индуцированный онкогенез в коже мыши (Gelboin et al., Science 167:205-207 (1970)). Таким образом, в предпочтительных вариантах осуществления изобретение предусматривает использование антисмысловых олигонуклеотидов в ADC для лечения рака молочной железы. В других вариантах осуществления изобретение относится к композициям и способам инициирования лечения антисмысловыми олигонуклеотидами, где дцРНК препятствует экспрессии EGFR клетками-мишенями на уровне мРНК. Используемый выше термин «дцРНК» относится к природной РНК, частично очищенной РНК, рекомбинантно полученной РНК, синтетической РНК, а также измененной РНК, которая отличается от природной РНК включением нестандартных нуклеотидов, ненуклеотидного материала, аналогов нуклеотидов (например, закрытой нуклеиновой кислоты (ЗНК)), дезоксирибонуклеотидов и любых их комбинаций. РНК по изобретению должна быть в достаточной степени схожей с природной РНК, чтобы иметь возможность опосредовать антисмысловую модуляцию на основе олигонуклеотидов, описанную в настоящем документе.
Аптамеры
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним аптамером. Аптамер представляет собой молекулу нуклеиновой кислоты, которая была выбрана из случайных пулов на основе ее способности связывать другие молекулы. Как и антитела, аптамеры могут связывать молекулы-мишени с необычайной аффинностью и специфичностью. Во многих вариантах осуществления аптамеры принимают сложные, зависимые от последовательности, трехмерные формы, которые позволяют им взаимодействовать с целевым белком, в результате чего образуется прочно связанный комплекс, аналогичный взаимодействию антитело-антиген, таким образом нарушая функцию указанного белка. Особая способность аптамеров прочно и специфически связываться с целевым белком подчеркивает их потенциал в качестве прицельной молекулярной терапии.
Олигонуклеотиды CpG
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним антисмысловым олигонуклеотидом CpG. Известно, что бактериальная и вирусная ДНК являются мощными активаторами как врожденного, так и специфического иммунитета у людей. Эти иммунологические характеристики были связаны с неметилированными CpG-динуклеотидными мотивами, обнаруженными в бактериальной ДНК. В связи с тем, что эти мотивы редко встречаются у людей, иммунная система человека выработала способность распознавать эти мотивы в качестве раннего признака инфекции и впоследствии инициировать иммунные ответы. Следовательно, олигонуклеотиды, содержащие этот мотив CpG, могут быть использованы для инициирования противоопухолевого иммунного ответа.
Рибозимы
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним рибозимом. Рибозимы представляют собой каталитические молекулы РНК длиной приблизительно от 40 до 155 нуклеотидов. Способность рибозимов распознавать и разрезать определенные молекулы РНК делает их потенциальными кандидатами для терапевтических средств. Типичный пример включает ангиозим.
Радионуклидные агенты (радиоактивные изотопы)
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним адионуклидным агентом. Радионуклидные агенты включают агенты, которые характеризуются нестабильным ядром, способным подвергаться радиоактивному распаду. Основа успешного лечения радионуклидами зависит от достаточной концентрации и длительного удержания радионуклида раковой клеткой. Другие факторы, которые следует учитывать, включают период полураспада радионуклидов, энергию испускаемых частиц и максимальное расстояние, которое может пройти испускаемая частица. В предпочтительных вариантах осуществления терапевтический агент представляет собой радионуклид, выбранный из группы, состоящей из 111In, 177Lu, 212Bi, 213Bi, 211At, 62Cu, 64Cu, 67Cu, 90Y, 125I, 131I, 32P, 33P, 47Sc, 111Ag, 67Ga, 142Pr, 153Sm, 161Tb, 166Dy, 166Ho, 186Re, 188Re, 189Re, 212Pb, 223Ra, 225Ac, 59Fe, 75Se, 77As, 89Sr, 99Mo, 105Rh, 109Pd, 143Pr, 149Pm, 169Er, 194Ir, 198Au, 199Au и 211Pb. Также предпочтительными являются радионуклиды, которые по существу распадаются с испускающими частицами Оже. Например, Co-58, Ga-67, Br-80m, Tc-99m, Rh-103m, Pt-109, In-111 1, Sb-119, 1-125, Ho-161, Os-189m и Ir-192. Энергиями распада используемых нуклидов, излучающих бета-частицы, предпочтительно являются Dy-152, At-211, Bi-212, Ra-223, Rn-219, Po-215, Bi-21 1, Ac-225, Fr-221, At-217, Bi-213 и Fm-255. Энергии распада используемых радионуклидов, испускающих альфа-частицы, предпочтительно составляют 2000-10000 кэВ, более предпочтительно 3000-8000 кэВ и наиболее предпочтительно 4000-7000 кэВ. Дополнительные потенциальные используемые радиоизотопы включают 11C, 13N, 150, 75Br, 198Au, 95Ru, 97Ru, 103Ru, 105Ru, 107Hg, 203Hg, 121mTe, 122mTe, 125mTe, 165Tm, 167Tm, 168Tm, 197Pt, 109Pd, 105Rh, 142Pr, 143Pr, 161Tb, 166Ho, 199Au, 57Co, 58Co, 51Cr, 59Fe, 75Se, 201Tl, 225Ac, 76Br, 169Yb и т. п.
Радиосенсибилизаторы
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним радиосенсибилизатором. Используемый в настоящем документе термин «радиосенсибилизатор» определяется как молекула, предпочтительно низкомолекулярная молекула, вводимая животным в терапевтически эффективных количествах для повышения чувствительности клеток, подвергаемых радиосенсибилизации, к электромагнитному излучению и/или для стимуляции лечения заболеваний, которые поддаются лечению электромагнитным излучением. Радиосенсибилизаторы представляют собой агенты, которые делают раковые клетки более чувствительными к лучевой терапии, но обычно оказывают гораздо меньшее влияние на нормальные клетки. Таким образом, радиосенсибилизатор можно использовать в сочетании с радиоактивно меченным антителом или ADC. Добавление радиосенсибилизатора может привести к повышенной эффективности по сравнению с лечением только радиоактивно меченным антителом или фрагментом антитела. Радиосенсибилизаторы описаны в D. M. Goldberg (ed.), Cancer Therapy with Radiolabeled Antibodies, CRC Press (1995). Примеры радиосенсибилизаторов включают гемцитабин, 5-фторурацил, таксан и цисплатин.
Радиосенсибилизаторы могут быть активированы электромагнитным излучением рентгеновских лучей. Типичные примеры активированных рентгеновским излучением сенсибилизаторов включают следующие, но не ограничиваются ими: метронидазол, мизонидазол, десметилмизонидазол, пимонидазол, этанидазол, ниморазол, митомицин C, RSU 1069, SR 4233, E09, RB 6145, никотинамид, 5-бромдезоксиуридин (BUdR), 5-иододезоксиуридин (IUdR), бромодезоксицитидин, фтордезоксиуридин (FUdR), гидроксимочевину, цисплатин, а также их терапевтически эффективные аналоги и производные. Альтернативно, радиосенсибилизаторы могут быть активированы с использованием фотодинамической терапии (ФДТ). Типичные примеры фотодинамических радиосенсибилизаторов включают, но не ограничиваются ими, производные гематопорфирина, фотофрин(r), производные бензопорфирина, NPe6, этиопорфирин олова (SnET2), феоборбид а, бактериохлорофилл а, нафталоцианины, фталоцианины, фталоцианины цинка, а также их терапевтически эффективные аналоги и производные.
Ингибиторы топоизомеразы
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним ингибитором топоизомеразы. Ингибиторы топоизомеразы представляют собой химиотерапевтические агенты, предназначенные для вмешательства в действие ферментов топоизомеразы (топоизомеразы I и II), которые являются ферментами, контролирующими изменения в структуре ДНК, катализируя, а затем разрушая и повторно соединяя фосфодиэфирный остов цепей ДНК во время нормального клеточного цикла. Типичные примеры ингибиторов ДНК-топоизомеразы I включают, но не ограничиваются ими, камптотецины и их производные иринотекан (CPT-11, Camptosar, Pfizer, Inc.) и топотекан (Hycamtin, GlaxoSmithKline Pharmaceuticals). Типичные примеры ингибиторов ДНК-топоизомеразы II включают, но не ограничиваются ими, амсакрин, даунорубицин, доксотрубицин, эпиподофиллотоксины, эллиптицины, эпирубицин, этопозид, разоксан и тенипозид.
Ингибиторы тирозинкиназы
Линкеры по настоящему изобретению могут быть использованы для конъюгирования антитела по меньшей мере с одним ингибитором тирозинкиназы. Тирозинкиназы представляют собой ферменты в клетке, которые функционируют для присоединения фосфатных групп к аминокислоте тирозину. Рост опухоли может быть ингибирован путем блокирования способности протеинтирозинкиназ функционировать. Примеры тирозинкиназ, которые могут быть использованы в ADC по настоящему изобретению, включают, но не ограничиваются ими, Акситиниб, Босутиниб, Седираниб, Дазатиниб, Эрлотиниб, Гефитиниб, Иматиниб, Лапатиниб, Лестауртиниб, Нилотиниб, Семаксаниб, Сунитиниб и Вандетаниб.
Другие агенты
Примеры других агентов, которые могут быть использованы в ADC по настоящему изобретению, включают, но не ограничиваются ими, абрин (например, цепь абрина А), альфа-токсин, белки Aleurites fordii, белки аматоксина, кротина, курцина, диантина, дифтерийный токсин (например, цепи A дифтерийного токсина, не связывающихся активных фрагментов дифтерийного токсина), дезоксирибонуклеазу (ДНКазу), гелонин, митогеллин, цепи A модекцина, ингибитор Memordica charantia, неомицин, онконазу, феномицин, белки Phytolaca americana (PAPI, PAPII и PAPe S), противовирусный белок лаконоса, эндотоксин Pseudomonas, экзотоксин Pseudomonas (например, цепь A экзотоксина (Pseudomonas aeruginosa)), рестриктоцин, рицин, цепь A рицина, рибонуклеазу (РНК-азу), ингибитор Saponaria officinalis, сапорин, альфа-сарцин, стафиллококковый энтеротоксин A, столбнячный токсин, цисплатин, карбоплатин и оксалиплатин (Eloxatin, Sanofi Aventis), ингибиторы протеосом, (например, PS-341 [бортезомиб или велкейд]), ингибиторы HDAC (вориностат (Zolinza, Merck & Company, Inc.)), белиностат, энтиностат, моцетиностат и панобиностат), ингибиторы ЦОГ-2, замещенные мочевины, ингибиторы белков теплового шока (например, гелданамицин и его многочисленные аналоги), адренокортикальные супрессанты и трихотецены. (См., например, WO 93/21232). Другие агенты также включают аспарагиназу (Espar, Lundbeck Inc.), гидроксимочевину, левамизол, митотан (Lysodren, Bristol-Myers Squibb) и третиноин (Renova, Valeant Pharmaceuticals Inc.).
Следует отметить, что вышеупомянутые группы лекарственных фрагментов, которые могут быть использованы в ADC по настоящему изобретению, не являются исключительными, поскольку некоторые примеры лекарственных препаратов можно найти в более чем одной категории, например, ансамитоцины являются как митотическими ингибиторами, так и противоопухолевыми антибиотиками.
Все стереоизомеры вышеуказанных лекарственных фрагментов рассматриваются для соединений по настоящему изобретению, то есть для любой комбинации конфигураций R и S на хиральных углеродах D.
Термины «обнаруживаемый фрагмент» или «маркер» относится к композиции, которую можно обнаружить спектроскопическим, фотохимическим, биохимическим, иммунохимическим, радиоактивным или химическим способом. Например, используемая метка включает 32P, 35S, флуоресцентные красители, электронно-плотные реагенты, ферменты (например, ферменты, которые обычно используются в ИФА), биотин-стрептавидин, диоксигенин, гаптен и белки, для которых доступны антисыворотка или моноклональные антитела, или молекулы нуклеиновой кислоты с последовательностью, комплементарной мишени. Обнаруживаемый фрагмент часто генерирует измеримый сигнал, например, радиоактивный сигнал, цветовой сигнал или флуоресцентный сигнал, который можно использовать для количественного определения количества обнаруживаемого фрагмента, который связывается в образце. Количественная оценка сигнала может быть выполнена, например, с помощью сцинтилляционного подсчета, прибором для измерения плотности, проточного клеточного анализа, ИФА или прямого анализа с помощью масс-спектроскопии кольцевых или впоследствии расщепленных пептидов (можно анализировать один или более пептидов). Специалисты в данной области техники знакомы с методами и средствами обнаружения интересующего соединения-метки. Эти методы и способы являются общепринятыми и хорошо известны в данной области техники
Зонд для обнаружения относится к (i) материалу, способному обеспечить обнаруживаемый сигнал, (ii) материалу, способному взаимодействовать с первым зондом или вторым зондом с изменением обнаруживаемого сигнала, обеспечиваемого первым зондом или вторым зондом, таким как резонансный перенос энергии флуоресценции (FRET), (iii) материалу, способному стабилизировать взаимодействие с антигеном или лигандом или повышать аффинность связывания, (iv) материалу, способному влиять на электрическую подвижность или инвазивное действие на клетки с помощью физических параметров, таких как заряд, гидрофобность и т. д. или (v) материалу, способному регулировать аффинность лиганда, связывание антигена с антителом или образование ионного комплекса.
Антитела
Антитело ADC может представлять собой любое антитело, которое обычно, но необязательно специфически, связывается с антигеном, экспрессируемым на поверхности интересующей клетки-мишени. Антиген не обязательно, но в некоторых вариантах осуществления способен к интернализации связанного с ним ADC в клетку. Интересующие клетки-мишени могут включать клетки, в которых желательна индукция апоптоза. Целевые антигены могут представлять собой любой белок, гликопротеин, полисахарид, липопротеин и т. д., экспрессируемые в интересующей клетке-мишени, но обычно они представляют собой белки, которые либо уникально экспрессируются в клетке-мишени, а не в нормальных или здоровых клетках, или которые избыточно экспрессируются на клетке-мишени по сравнению с нормальными или здоровыми клетками, так что ADC селективно нацеливаются на конкретные интересующие клетки, такие как, например, опухолевые клетки. Как будет понятно специалистам в данной области техники, специфический антиген и, следовательно, выбранное антитело будут зависеть от идентичности желаемой клетки-мишени, представляющей интерес. В конкретных вариантах осуществления антитело ADC представляет собой антитело, подходящее для введения человеку.
Антитела (Ab) и иммуноглобулины (Igs) представляют собой гликопротеины, имеющие аналогичные структурные характеристики. Хотя антитела проявляют специфичность связывания с конкретной мишенью, иммуноглобулины включают как антитела, так и другие подобные антителам молекулы, которые не обладают специфичностью мишени. Нативные антитела и иммуноглобулины обычно представляют собой гетеротетрамерные гликопротеины около 150 000 дальтон, состоящие из двух идентичных легких (L) цепей и двух идентичных тяжелых (H) цепей. Каждая тяжелая цепь имеет на одном конце вариабельный домен (VH), за которым следует ряд константных доменов. Каждая легкая цепь имеет вариабельный домен (VL) на одном конце и константный домен на другом конце.
Ссылки на «VH» относятся к вариабельной области тяжелой цепи иммуноглобулина антитела, включая тяжелую цепь Fv, scFv или Fab. Ссылки на «VL» относятся к вариабельной области легкой цепи иммуноглобулина, включая легкую цепь Fv, scFv, dsFv или Fab.
Термин «антитело» используется в настоящем документе в самом широком смысле и относится к молекуле иммуноглобулина, которая специфически связывается или является иммунологически реактивной с конкретным антигеном и включает поликлональные, моноклональные, полученная с помощью генной инженерии и иным образом модифицированные формы антител, включая, но не ограничиваясь ими, мышиные, химерные антитела, гуманизированные антитела, гетероконъюгатные антитела (например, биспецифичные антитела, диатела, триателами и тетратела) и антигенсвязывающие фрагменты антител, включая, например, фрагменты Fab', F(ab')2, Fab, Fv, rIgG и scFv Термин «scFv» относится к одноцепочечному антителу Fv, в котором вариабельные домены тяжелой цепи и легкой цепи из традиционного антитела были соединены с образованием одной цепи.
Антитела могут быть мышиными, человеческими, гуманизированными, химерными или полученными из других видов. Антитело представляет собой белок, генерируемый иммунной системой, который способен распознавать и связываться с конкретным антигеном. (Janeway, C., Travers, P., Walport, M., Shlomchik (2001) Immuno Biology, 5th Ed., Garland Publishing, New York). Целевой антиген обычно имеет множество сайтов связывания, также называемых эпитопами, распознаваемых CDR на множественных антителах. Каждое антитело, которое специфически связывается с другим эпитопом, имеет различную структуру. Таким образом, один антиген может иметь более одного соответствующего антитела. Антитело включает полноразмерную молекулу иммуноглобулина или иммунологически активную часть полноразмерной молекулы иммуноглобулина, то есть молекулу, которая содержит антигенсвязывающий сайт, который иммуноспецифически связывает антиген интересующей мишени или его часть, причем такие мишени включают, но не ограничиваясь ими, раковую клетку или клетки, которые продуцируют аутоиммунные антитела, связанные с аутоиммунным заболеванием. Описываемый в настоящем документе иммуноглобулин может быть любого типа (например, IgG, IgE, IgM, IgD и IgA), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса молекулы иммуноглобулина. Иммуноглобулины могут быть получены из любых видов. Однако в одном аспекте иммуноглобулин имеет происхождение от человека, мыши или кролика.
Термин «фрагмент антитела» относится к части полноразмерного антитела, обычно к мишени связывания или вариабельной области. Примеры фрагментов антител включают фрагменты Fab, Fab′, F(ab′)2 и Fv. Фрагмент «Fv» представляет собой минимальный фрагмент антитела, который содержит полный сайт распознавания и связывания мишени. Эта область состоит из димера одного вариабельного Тяжелая тяжелой цепи и одного Легкая цепь легкой цепи в a плотной нековалентной ассоциации (димер VH-VL). Именно в указанной конфигурации три CDR каждого вариабельного домена взаимодействуют для того, чтобы определить целевой сайт связывания на поверхности димера VH-VL. Часто шесть CDR придают антителу специфичность связывания с мишенью. Однако в некоторых случаях даже один вариабельный домен (или половина Fv, содержащего только три CDR, специфичных для мишени) может иметь способность распознавать и связывать цель. «Одноцепочечные Fv» или «scFv» фрагменты антитела содержат домены VH и VL антитела в одной полипептидной цепи. В целом, полипептид Fv дополнительно содержит полипептидный линкер между доменами VH и VL, дающий возможность sFv образовываться требуемой структуре для связывания с мишенью. «Однодоменные антитела» состоят из отдельных доменов VH или VL, которые проявляют достаточную аффинность к мишени. В конкретном варианте осуществления однодоменное антитело представляет собой верблюжье антитело (см., например, Riechmann, 1999, Journal of Immunological Methods 231:25-38).
Фрагмент Fab содержит константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Фрагменты Fab′ отличаются от фрагментов Fab добавлением нескольких остатков на карбоксильном конце домена CH1 тяжелой цепи, в том числе одного или более цистеинов из шарнирной области антитела. Фрагменты F(ab′) получают путем расщепления дисульфидной связи в шарнирных цистеинах продукта расщепления пепсина F(ab′)2. Дополнительные способы химического связывания фрагментов антител хорошо известны специалистам в данной области техники.
Вариабельные домены как легкой цепи, так и тяжелой цепи имеют определяющие комплементарность области (CDR), также известные как гипервариабельные области. Более консервативные фрагменты вариабельных доменов называются каркасными (FR). Как известно в данной области техники, позиция/граница аминокислоты, определяющая гипервариабельную область антитела, может варьироваться в зависимости от контекста и различных определений, известных в данной области техники. Некоторые позиции в вариабельной области могут рассматриваться как гибридные гипервариабельные позиции в том смысле, что эти позиции можно считать находящимися внутри гипервариабельной области по одному набору критериев, в то время как считается, что они находятся вне гипервариабельной области по другому набору критериев. Одну или более из этих позиций также можно найти в расширенных гипервариабельных областях. CDR в каждой цепи удерживаются вместе в непосредственной близости с помощью областей FR и, вместе с CDR из другой цепи, участвуют в образовании сайта связывания антител с мишенью (см. Kabat et al., Sequences of Proteins of Immunological Interest (National Institute of Health, Bethesda, Md. 1987). В контексте данного документа нумерация аминокислотных остатков иммуноглобулина осуществляется в соответствии с системой нумерации аминокислотных остатков иммуноглобулина Kabat et al., если не указано иное.
В определенных вариантах осуществления антитела ADC по настоящему изобретению представляют собой моноклональные антитела. Термин «моноклональное антитело» (mAb) относится к антителу, которое получено из одной копии или клона, включая, например, любой эукариотический, прокариотический или фаговый клон, а не к способу, с помощью которого его получают. Предпочтительно моноклональное антитело по настоящему изобретению существует в гомогенной или по существу гомогенной популяции. Моноклональное антитело включает как интактные молекулы, так и фрагменты антител (такие как, например, фрагменты Fab и F(ab')2), которые способны специфически связываться с белком. Фрагменты Fab и F(ab ')2 лишены фрагмента Fc интактного антитела, быстрее выводятся из системы кровообращения животного и могут иметь меньшее неспецифическое связывание с тканью, чем интактное антитело (Wahl et al., 1983, J. Nucl. Med 24:316). Моноклональные антитела, пригодные для использования в настоящем изобретении, могут быть получены с использованием широкого спектра методов, известных в данной области техники, включая использование технологий гибридомной, рекомбинантной и фаговой индикации или их комбинации. Антитела по настоящему изобретению включают химерные, приматизированные, гуманизированные или человеческие антитела.
Хотя в большинстве случаев антитела состоят только из генетически кодируемых аминокислот, в некоторых вариантах осуществления некодируемые аминокислоты могут быть специфически включены. Примеры некодированных аминокислот, которые могут быть включены в антитела для использования в контролирующей стехиометрии и местоположении прикрепления, а также способы получения таких модифицированных антител, обсуждаются в Tian et al., 2014, Proc Nat'l Acad Sci USA 111(5):1766-1771 и Axup et al., 2012, Proc Nat'l Acad Sci USA 109(40):16101-16106, полное содержание которых в настоящий документ посредством ссылки.
В определенных вариантах осуществления антитело ADC, описанное в настоящем документе, представляет собой химерное антитело. Используемый в настоящем документе термин «химерное» антитело относится к антителу, имеющему вариабельные последовательности, полученные из нечеловеческого иммуноглобулина, такого как антитело крысы или мыши, и константные области человеческого иммуноглобулина, обычно выбираемые из матрицы иммуноглобулина человека. Способы получения химерных антител известны в данной области техники. См., например, Morrison, 1985, Science 229(4719):1202-7; Oi et al., 1986, BioTechniques 4:214-221; Gillies et al., 1985, J. Immunol. Methods 125:191-202; патенты США №№ 5807715; 4816567; и 4816397, содержание которых в полном объеме включено в данный документ посредством ссылки.
В определенных вариантах осуществления антитело ADC, описанное в настоящем документе, представляет собой гуманизированное антитело. «Гуманизированные» формы антител нечеловеческого происхождения (например, мышиные) представляют собой химерные иммуноглобулины, цепи иммуноглобулинов или их фрагменты (такие как Fv, Fab, Fab', F(ab')2 или другие субдомены связывания антител с мишенью), которые содержат минимальные последовательности, полученные из иммуноглобулина нечеловеческого происхождения. В целом, гуманизированное антитело будет содержать по существу все из по меньшей мере одного и, как правило, двух вариабельных доменов, в которых все или по существу все области CDR соответствуют доменам иммуноглобулина, не относящегося к человеку, и все или по существу все области FR являются последовательностями последовательности иммуноглобулина человека. Гуманизированное антитело также может содержать по меньшей мере часть константной области (Fc) иммуноглобулина, как правило, иммуноглобулина консенсусную последовательность человека. Способы получения гуманизации антител известны в данной области техники. См., например, Riechmann et al., 1988, Nature 332:323-7; патенты США №№ 5530101; 5585089; 5693761; 5693762; и патент США № 6180370, выданный Queen et al.; EP239400; публикацию PCT WO 91/09967; патент США № 5225539; EP592106; EP519596; Padlan, 1991, Mol. Immunol., 28:489-498; Studnicka et al., 1994, Prot. Eng. 7:805-814; Roguska et al., 1994, Proc. Natl. Acad Sci. USA 91:969-973; и патент США № 5565332, которые все в полном объеме включены в данный документ посредством ссылки.
В определенных вариантах осуществления антитело ADC, описанное в настоящем документе, представляет собой человеческое антитело. Полностью «человеческие» антитела могут быть желательны для терапевтического лечения пациентов-людей. Используемый в настоящем документе термин « человеческие антитела» включает антитела, имеющие аминокислотную последовательность иммуноглобулина человека, и включает антитела, выделенные из библиотек иммуноглобулина человека или животных, трансгенных по одному или более иммуноглобулинам человека, и которые не экспрессируют эндогенные иммуноглобулины. Человеческие антитела могут быть получены различными способами, известными в данной области техники, включая способы фагового дисплея с использованием библиотек антител, полученных из последовательностей иммуноглобулина человека. См. патенты США №№ 4444887, 4716111, 6114598, 6207418, 6235883, 7227002, 8809151, а также опубликованную заявку на патент США № 2013/189218, содержание которых полностью включено в настоящий документ посредством ссылки. Человеческие антитела также могут быть получены с использованием трансгенных мышей, которые не способны экспрессировать функциональные эндогенные иммуноглобулины, но которые могут экспрессировать гены иммуноглобулина человека. См., например, патенты США №№ 5413923; 5625126; 5633425; 5569825; 5661016; 5545806; 5814318; 5885793; 5916771; 5939598; 7723270; 8809051, а также опубликованную заявку на патент США № 2013/117871, содержание которых полностью включено в настоящий документ посредством ссылки. Кроме того, можно привлекать такие компании, как Medarex (Принстон, штат Нью-Джерси), Astellas Pharma (Дирфилд, штат Иллинойс) и Regeneron (Тарритаун, штат Нью-Йорк), которые могут предоставлять человеческие антитела, направленные против выбранного антигена, используя технологию, аналогичную описанной выше. Полностью человеческие антитела, которые распознают выбранный эпитоп, могут быть получены с использованием методики, называемой «направляемый отбор». В этом подходе выбранное нечеловеческое моноклональное антитело, например, мышиное антитело, используется для направления отбора полностью человеческого антитела, распознающего один и тот же эпитоп (Jespers et al., 1988, Biotechnology 12:899-903).
В определенных вариантах осуществления антитело ADC, описанное в настоящем документе, представляет собой приматизированное антитело. Термин «приматизированное антитело» относится к антителу, содержащему вариабельные области обезьяны и константные области человека. Способы получения приматизированных антител известны в данной области техники. См., например, патенты США №№ 5658570; 5681722; и 5693780, содержание которых в полном объеме включено в данный документ посредством ссылки.
В определенных вариантах осуществления антитело ADC, описанное в настоящем документе, представляет собой биспецифическое антитело или антитело с двумя вариабельными доменами (DVD). Биспецифические антитела и DVD-антитела представляют собой моноклональные, часто человеческие или гуманизированные антитела, которые обладают специфичностью связывания по меньшей мере для двух разных антигенов. DVD описаны, например, в патенте США №7612181, описание которого включено в настоящий документ посредством ссылки.
В определенных вариантах осуществления антитело ADC, описанное в настоящем документе, представляет собой дериватизированное антитело. Например, но не в качестве ограничения, дериватизированные антитела обычно модифицируют гликозилированием, ацетилированием, пегилированием, фосфорилированием, амидированием, дериватизацией известными защитными/блокирующими группами, протеолитическим расщеплением, связыванием с клеточным лигандом или другим белком и т. д. Любой из многочисленных способов химической модификации может быть выполнен согласно известным методикам, включая, но не ограничиваясь ими, специфическое химическое расщепление, ацетилирование, формилирование, метаболический синтез туникамицина и т. д. Кроме того, производное может содержать одну или более неприродных аминокислот, например, используя технологию ambrx (см., например, Wolfson, 2006, Chem. Biol. 13(10):1011-2).
В определенных вариантах осуществления антитело ADC, описанное в данном документе, имеет последовательность, которая была модифицирована для изменения по меньшей мере одной биологической эффекторной функции, опосредованной константной областью, относительно соответствующей последовательности дикого типа. Например, в некоторых вариантах осуществления антитело может быть модифицировано для снижения по меньшей мере одной биологической эффекторной функции, опосредованной константной областью по сравнению с немодифицированным антителом, например, сниженного связывания с Fc-рецептором (FcR). Связывание FcR может быть снижено посредством мутации сегмента константной области иммуноглобулина антитела в определенных областях, необходимых для взаимодействий FcR (см., например, Canfield and Morrison, 1991, Med 173:1483-1491; и Lund et al., 1991, J. Immunol. 147:2657-2662).
В определенных вариантах осуществления антитело ADC, описанное в настоящем документе, модифицировано для приобретения или улучшения по меньшей мере одной опосредованной константной областью биологической эффекторной функции относительно немодифицированного антитела, например, для усиления взаимодействий FcγR (см., например, US 2006/0134709). Например, антитело с константной областью, которая связывает FcγRIIA, FcγRIIB и/или FcγRIIIA с большей аффинностью, чем соответствующая константная область дикого типа, может быть получено в соответствии со способами, описанными в настоящем документе.
В некоторых конкретных вариантах осуществления антитело ADC, описанное в настоящем документе, представляет собой антитело, которое связывает опухолевые клетки, такое как антитело против рецептора клеточной поверхности или ассоциированный с опухолью антиген (TAA). В попытках открыть эффективные клеточные мишени для диагностики и лечения рака, исследователи пытались идентифицировать трансмембранные или иным образом связанные с опухолью полипептиды, которые специфически экспрессируются на поверхности одного или более конкретных типов раковых клеток по сравнению с одной или более нормальными нераковыми клетками. Часто такие ассоциированные с опухолью полипептиды экспрессируются на поверхности раковых клеток в большей степени, чем на поверхности нераковых клеток. Такие рецепторы клеточной поверхности и опухолевые антигены известны в данной области техники и могут быть получены для использования при генерировании антител с использованием методов и информации, которые хорошо известны в данной области техники.
Типичные рецепторы клеточной поверхности и TAA
Примеры рецепторов клеточной поверхности и TAA, на которые может быть нацелено антитело ADC, описанные в настоящем документе, включают, но не ограничиваются ими, различные рецепторы и TAA, перечисленные ниже в Таблице 1. Для удобства информация, относящаяся к этим антигенам, все из которых известны в данной области техники, приведена ниже и включает названия, альтернативные названия, номера доступа Genbank и первичные справочные материалы, с соблюдением соглашениям по идентификации последовательностей нуклеиновых кислот и белков Национального центра биотехнологической информации (NCBI). Последовательности нуклеиновой кислоты и белков, соответствующие перечисленным рецепторам клеточной поверхности и TAA, доступны в общедоступных базах данных, таких как GenBank.
Таблица 1.
Типовые антитела
Типовые антитела, которые следует использовать с ADC по настоящему изобретению, включают, но не ограничиваются ими, 3F8 (GD2), абаговомаб (CA-125 (имитация)), адекатумумаб (EpCAM), афутузумаб (CD20), алазизумаба пегол (VEGFR2), ALD518 (IL-6), алемтузумнаб (CD52), алтумомаба пентетат (CEA), аматуксимаб (мезотелин), анатумомнаба мафенатокс (TAG-72), аполизумаб (HLA-DR), арцитумомаб (CEA), бавитуксимаб (фосфатидилсерин), бектумомаб (CD22), белимумаб (BAFF), бесилесомаб (CEA-ассоциированный антиген), бевацизумаб (VEGF-A), биватузумаба мертанзин (CD44 v6), блинатумомаб (CD19), брентуксимаба ведотин ((CD30 (TNFRSF8)), кантузумаба мертанзин (муциноподобный рако-ассоциированный антиген), кантузумаба равтансин (MUC1), капромаба пендетид (клетки рака предстательной железы), карлумаб (MCP-1), катумаксомаб (EpCAM, CD3), CC49 (Tag-72), cBR96-DOX ADC (антиген Льюиса Y), цетуксимаб (EGFR), цитатузумаба богатокс (EpCAM), циксутумумаб (рецептор IGF-1), кливатузумаба тетраксетан (MUC1), конатумумаб (TRAIL-E2), дацетузумаб (CD40), далотузумаб (инсулиноподобный рецептор фактора роста 1), дератумумаб ((CD38 (гидролаза циклической АДФ-рибозы)), демцизумаб (DLL4), денозумаб (RANKL), детумомаб (клетка В-лимфомы), дрозитумаб (DR5), дусигитумаб (ILGF2), экромексимаб (ганглиозид D3), экулизумаб (C5), эдреколомаб (EpCAM), элотузумаб (SLAMF7), элсилимомаб (IL-6), энаватузумаб (рецептор TWEAK), энотикумаб (DLL4), энситуксимаб (5AC), эпитумомаба цитуксетан (эпизиалин), эпратузумаб (CD22), эртумаксомаб ((HER2/neu, CD3)), этанзицумаб (интегрин αvβ3), фарлетузумаб (рецептор фолата 1), FBTA05 (CD20), фиклатузумаб (HGF), фигитумумаб (рецептор IGF-1), фланвотумаб ((TYRP1 (гликопротеин 75)), фрезолимумаб (TGF-1), галиксимаб (CD80), ганитумаб (IGF-I), гемтузумаба озогамицин (CD33), гирентуксимаб ((карбоновая ангидраза 9 (CA-IX)), глембатумумаба ведотин (GPNMB), ибритумомаба тиуксетан (CD20), икрукумаб (VEGFR-1), иговомаб (CA-125), IMAB362 (CLDN18.2), имгатузумаб (EGFR), индатуксимаба равтанзин (SDC1), интетумумаб (CD51), инотузумаба озогамицин (CD22), ипилимумаб (CD152), иратумумаб ((CD30 (TNFRSF8)), лабетузумаб (CEA), ламбролизумаб (PDCD1), лексатумумаб (TRAIL-R2), линтузумаб (CD33), лорвотузумаба мертанзин (CD56), лукатумумаб (CD40), лумиликсимаб ((CD23 (рецептор IgE)), мапатумумаб (TRAIL-R1), маргетуксимаб (ch4DS), матузумаб (EGFR), милатузумаб (CD74), митумомаб (ганглиозид GD3), могамулизумаб (CCR4), моксетумомаба пазудотокс (CD22), наколомаба тафенатокс (C2-42 антиген), наптумомаба эстафенатокс (5T4), нарнатумаб (RON), натализумаб (интегрин α4), нецитумумаб (EGFR), несвакумаб (ангиопоэтин 2), нимотузумаб (EGFR), ниволумаб (IgG4), окаратузумаб (CD20), офатумумаб (CD20), оларатумаб (PDGF-R α), онартузумаб (киназа рецептора фактора рассеяния человека), онтуксизумаб (TEM1), опортузумаба монато (EpCAM), ореговомаб (CA-125), отлертузумаб (CD37), панитумумаб (EGFR) панкомаб (специфичное для опухоли гликозилирование MUC1), парзатузумаб (EGFL7), патритумаб (HER3), пемтумомаб (MUC1), пертузумаб (HER2/neu), пидилизумаб (PD-1), пинатузумаба ведотин (CD22), притумумаб (виментин), ракотумомаб (N-гликолилнейраминовая кислота), радретумаб (экстра домен-B фибронектина), рамуцирумаб (VEGFR2), рилотумумаб (HGF), ритуксимаб (CD20), робатумумаб (рецептор IGF-1), самализумаб (CD200), сатумомаба пендетид (TAG-72), серибантумаб (ERBB3), сибротузумаб (FAP), SGN-CD19A (CD19), SGN-CD33A (CD33), силтуксимаб (IL-6), солитомаб (EpCAM), сонепцизумаб (сфингозин-1-фосфат), табалумб (BAFF), такатузумаба тетраксетан (альфа-фетопротеин), таплитумомаба паптокс (CD19), тенатумомаб (тенасцин C), тепротумумаб (CD221), TGN1412 (CD28), тицилимумаб (CTLA-4), тигатузумаб (TRAIL-R2), TNX-650 (IL-13), товетумаб (CD40a), трастузумаб (HER2/neu), TRBS07 (GD2), тремелимумаб (CTLA-4), тукотузумаба целмолейкин (EpCAM), ублитуксимаб (MS4A), урелумаб (4-1BB), вандетаниб (VEGF), вантиктумаб (рецептор Frizzled), волоциксимаб (интегрин α5β1), ворзетузумаба мафодотин (CD70), вотумумаб (Tопухолевый CTAA16.88), залутумумаб (EGFR), занолимумаб (CD4) и затуксимаб (HER1).
Способы получения антител
Антитело ADC может быть получено путем рекомбинантной экспрессии генов легкой и тяжелой цепей иммуноглобулина в клетке-хозяине. Например, для экспрессии антитела рекомбинантным способом клетку-хозяина трансфицируют одним или более рекомбинантными векторами экспрессии, несущими фрагменты ДНК, кодирующие легкие и тяжелые цепи иммуноглобулина антитела таким образом, что легкие и тяжелые цепи экспрессируются в клетке-хозяине и, необязательно, секретируются в среду, в которой культивируются клетки-хозяева, из которой можно извлечь антитела. Стандартные методики рекомбинантной ДНК используются для получения генов тяжелых и легких цепей антител, включения этих генов в рекомбинантные векторы экспрессии и введения векторов в клетки-хозяева, такие как описаны в Molecular Cloning; A Laboratory Manual, Second Edition (Sambrook, Fritsch and Maniatis (eds), Cold Spring Harbor, N. Y., 1989), Current Protocols in Molecular Biology (Ausubel, F. M. et al., eds., Greene Publishing Associates, 1989) и в патенте США № 4816397.
В одном варианте осуществления антитела к варианту Fc аналогичны их эквивалентам дикого типа, но по изменениям в их доменах Fc. Для получения нуклеиновых кислот, кодирующих такие антитела к варианту Fc, можно синтезировать фрагмент ДНК, кодирующий домен Fc или часть домена Fc антитела дикого типа (называемого «домен Fc дикого типа»), и использовать его в качестве матрицы для мутагенеза с целью генерации антитела, как описано в настоящем документе, с использованием рутинных методов мутагенеза; альтернативно, фрагмент ДНК, кодирующий антитело, может быть синтезирован напрямую.
Сразу после получения фрагментов ДНК, кодирующих домены Fc дикого типа, можно проводить последующие манипуляции с этими фрагментами ДНК с помощью стандартных методов рекомбинантной ДНК, например, для преобразования генов константной области в гены цепи полноразмерного антитела. В ходе данных манипуляций фрагмент ДНК, кодирующий СН, функционально связан с другим фрагментом ДНК, кодирующим другой белок, такой как вариабельная область антитела или гибкий линкер. В контексте данного документа термин «функционально связанный» означает, что два фрагмента ДНК объединены таким образом, что аминокислотные последовательности, кодируемые этими двумя фрагментами ДНК, остаются в рамке.
Для экспрессии антител варианта Fc ДНК, кодирующие частичную или полноразмерную легкую и тяжелую цепи, полученные, как описано выше, вставляют в векторы экспрессии таким образом, что гены оперативно связаны с транскрипционными и трансляционными регуляторными последовательностями. В этом контексте термин «функционально связанный» означает, что ген антитела лигируется в вектор таким образом, что транскрипционные и трансляционные регуляторные последовательности в векторе выполняют свою предусмотренную функцию регуляции транскрипции и трансляции гена антитела. Вектор экспрессии и последовательности регуляции экспрессии выбираются так, чтобы быть совместимыми с используемой клеткой-хозяином экспрессии. Вариант gne легкой цепи антитела и ген тяжелой цепи антитела могут быть вставлены в отдельные векторы или, что более типично, оба гена вставлены в один и тот же вектор экспрессии.
Гены антител вставляют в вектор экспрессии стандартными способами (например, лигированием комплементарных сайтов рестрикции на фрагменте и векторе гена антитела или лигированием тупого конца, в случае отсутствия сайтов рестрикции). До вставки последовательностей вариантного Fc-домена вектор экспрессии уже может нести последовательности вариабельной области антитела. Дополнительно или альтернативно рекомбинантный вектор экспрессии может кодировать сигнальный пептид, который облегчает секрецию цепи антитела из клетки-хозяина. Ген цепи антитела может быть клонирован в вектор так, чтобы сигнальный пептид в рамке был связан с аминоконцом гена цепи антитела. Сигнальный пептид может представлять собой сигнальный пептид иммуноглобулина или гетерологичный сигнальный пептид (то есть сигнальный пептидом из белка, не являющегося иммуноглобулином).
В дополнение к генам цепи антител рекомбинантные векторы экспрессии несут регуляторные последовательности, которые контролируют экспрессию генов цепи антител в клетке-хозяине. Предполагается, что термин «регуляторная последовательность» включает промоторы, энхансеры и другие элементы регуляции экспрессии (например, сигналы полиаденилирования), которые регулируют транскрипцию или трансляцию генов цепи антитела. Такие регуляторные последовательности описаны, например, в Goeddel, Gene Expression Technology: Methods in Enzymology 185 (Academic Press, San Diego, Calif., 1990). Специалистам в данной области техники будет понятно, что конструкция вектора экспрессии, включая выбор регуляторных последовательностей, может зависеть от таких факторов, как выбор клетки-хозяина, подлежащей трансформации, желаемый уровень экспрессии белка и т. д. Подходящие регуляторные последовательности для экспрессии клеток-хозяев млекопитающих включают вирусные элементы, которые направляют высокие уровни экспрессии белка в клетках млекопитающих, такие как промоторы и/или энхансеры, полученные из цитомегаловируса (ЦМВ) (такого как промотор/энхансер ЦМВ), вируса обезьяны 40 (SV40) (такого как промотор/энхансер SV40), аденовируса (например, аденовирусный главный поздний промотор (AdMLP)) и полиомы. Для дальнейшего описания вирусных регуляторных элементов и их последовательностей см., например, патент США № 5168062, за авторством Stinski, патент США № 4510245 за авторством Bell et al., и патенты США № 4968615 за авторством Schaffner et al.
В дополнение к генам цепи антител и регуляторным последовательностям, рекомбинантные векторы экспрессии могут нести дополнительные последовательности, такие как последовательности, которые регулируют репликацию вектора в клетках-хозяевах (например, точки начала репликации), и селектируемые маркерные гены. Селектируемый маркерный ген облегчает отбор клеток-хозяев, в которые был введен вектор (см., например, патенты США №№ 4399216, 4634665 и 5179017, все за авторством et al.). Например, селектируемый маркерный ген обычно придает устойчивость по отношению к лекарственным препаратам, таким как G418, пуромицин, бластидин, гигромицин или метотрексат, клетке-хозяину, в которую был введен вектор. Подходящие гены селективных маркеров включают ген дигидрофолатредуктазы (DHFR) (для применения в клетках-хозяевах DHFR с селекцией/амплификацией с помощью метотрексата) и ген neo (для селекции G418). Для экспрессии легкой и тяжелой цепей вектор(ы) экспрессии, кодирующие тяжелую и легкую цепи, трансфицируют в клетку-хозяина стандартными методами. Предполагается, что различные формы термина «трансфекция» охватывают широкий спектр методов, широко используемых для введения экзогенной ДНК в прокариотическую или эукариотическую клетку-хозяина, например электропорацию, липофекцию, осаждение фосфатом кальция, трансфекцию DEAE-декстраном, и тому подобное.
Можно экспрессировать антитела либо в прокариотических, либо в эукариотических клетках-хозяевах. В некоторых вариантах осуществления экспрессия антител осуществляется в эукариотических клетках, например, в клетках-хозяевах млекопитающих, для оптимальной секреции правильно свернутого и иммунологически активного антитела. Типовые клетки-хозяева млекопитающих для экспрессии рекомбинантных антител включают клетки яичника китайского хомячка (клетки CHO) (в том числе клетки DHFR- CHO, описанные в Urlaub и Chasin (1980) Proc. Natl. Acad. Sci. USA 77:4216-4220, используемые с селектируемым маркером DHFR, например, как описано в Kaufman и Sharp (1982) Mol. Biol. 159:601-621), клетки миеломы NS0, клетки COS, клетки 293 и клетки SP2/0. При введении рекомбинантных векторов экспрессии, кодирующих гены антител в клетки-хозяева млекопитающих, антитела получают путем культивирования клеток-хозяев в течение периода времени, достаточного для обеспечения возможности экспрессии антитела в клетках-хозяевах или секреции антитела в культуральную среду, в которой выращивают клетки-хозяева. Антитела могут быть выделены из культуральной среды с использованием стандартных методов очистки белка. Клетки-хозяева также можно использовать для получения частей интактных антител, таких как фрагменты Fab или молекулы scFv.
В некоторых вариантах осуществления антитело ADC может представлять собой бифункциональное антитело. Такие антитела, в которых одна тяжелая и одна легкая цепь являются специфичными для одного антигена, а другая тяжелая и легкая цепь являются специфичными для второго антигена, могут быть получены путем сшивания антитела со вторым антителом стандартными методами химического сшивания. Бифункциональные антитела также могут быть получены путем экспрессии нуклеиновой кислоты, сконструированной для кодирования бифункционального антитела.
В некоторых вариантах осуществления двойные специфические антитела, то есть антитела, которые связывают один антиген и второй, неродственный антиген с использованием одного и того же сайта связывания, могут быть получены путем мутации аминокислотных остатков в CDR легкой цепи и/или тяжелой цепи. Типовые вторые антигены включают провоспалительный цитокин (такой как, например, лимфотоксин, интерферон-γ или интерлейкин-1). Двойные специфические антитела могут быть получены, например, путем мутации аминокислотных остатков на периферии антигенсвязывающего сайта (см., например, Bostrom et al., 2009, Science 323:1610-1614). Двойные функциональные антитела могут быть получены путем экспрессии нуклеиновой кислоты, сконструированной для кодирования двойного специфического антитела.
Антитела также могут быть получены с помощью химического синтеза (например, способами, описанными в Solid Phase Peptide Synthesis, 2nd ed., 1984 The Pierce Chemical Co., Rockford, Ill.). Антитела также могут быть получены с использованием бесклеточной платформы (см., например, Chu et al., Biochemia No. 2, 2001 (Roche Molecular Biologicals)).
Способы рекомбинантной экспрессии гибридных белков Fc описаны в Flanagan et al., Methods in Molecular Biology, vol. 378: Monoclonal Antibodies: Methods and Protocols.
Сразу после получения антитела методом рекомбинантной экспрессии, его можно очистить любым способом, известным в данной области техники, для очистки молекулы иммуноглобулина, например, хроматографией (например, ионный обмен, аффинность, в частности, по аффинности к антигену после выбора белка А или белка G и колоночная хроматография с распределением по размерам), центрифугированием, дифференциальной растворимостью или любой другой стандартной методикой очистки белков.
После выделения антитело, в случае необходимости, может быть дополнительно очищено, например, с помощью высокоэффективной жидкостной хроматографии (см., например, Fisher, Laboratory Techniques In Biochemistry And Molecular Biology (Work and Burdon, eds., Elsevier, 1980)), or by gel filtration chromatography on a Superdex™ 75 column (Pharmacia Biotech AB, Uppsala, Sweden).
Соединения и датчики визуализации
В определенных вариантах осуществления в настоящем документе предложены способы применения для описываемых соединений в композициях для визуализации и в качестве датчиков.
Датчик может быть биодатчиком, химическим датчиком или молекулярным переключателем. Биодатчики способны идентифицировать наличие или количество конкретного материала путем введения в реакцию определенных материалов (например, раковых клеток, вирусов, различных химических веществ и т. д.) с биорецепторами (части, разработанные с возможностью адсорбировать и вступать в реакцию с биоматериалами, такими как ДНК, РНК, антитела, ферментные белки, клетки, биологические мембраны, гормональные рецепторы и т. д.), имеющими специфичность отбора и выполняющими измерение с использованием преобразователя сигнала (устройства, которое преобразует реакцию между конкретным материалом и биологическим рецептором в электрический сигнал с помощью различных методов), и могут быть использованы в медицинских, экологических целях, для перерабатывающей промышленности, в военных (химическое оружие), исследовательских целях, для пищевой промышленности и т. д. (см., например, Biosensors and Bioelectronics, 2016, 32-45; Pol. J. Environ. Stud. 2015, 19-25; Analytica Chimica Acta 568 (2006) 200-210; Biosensors and Bioelectronics 2017, 217-231; ACS Appl. Mater. Interfaces 2015, 7, 20190-20199; Journal of Coastal Life Medicine 2016; 4(3): 200-202; Artificial Cells, Blood Substitutes, and Biotechnology, 39: 281-288; Journal of Controlled Release 159 (2012) 154-163).
Химические датчики обеспечивают быстрый и точный мониторинг конкретных материалов во многих областях, таких как клиническая диагностика, медицинские исследования, измерение химических материалов, измерение окружающей среды и т. д., с помощью метода использования электрических свойств, таких как наэлектризованность, сопротивление, разность потенциалов и т. д., и оптических свойства, такие как цвет, флуоресценция и т. д., и включают газовый датчик (водород, кислород, монооксид углерода), ионный датчик (катион, анион, чувствительный к газу ион), компонентный датчик (паровая фаза, жидкая фаза, люминесцентный компонент), датчик влажности (относительная влажность, абсолютная влажность, конденсация), датчик пыли/сажи (взвешенная пыль, грязная пыль, сажа, мутность) и т. д. (см., например, Chem. Soc. Rev., 2015, 44, 3358; Journal of the Korean Chemical Society, 2010, 451-459; Chem. Sci., 2015, 6, 1150-1158; KR 10-1549347; J. Phys. Chem. B 2016, 120, 7053-7061; ACS Appl. Mater. Interfaces 2015, 7, 704-712; J. Am. Chem. Soc. 2011, 133, 10960-10965; J. Am. Chem. Soc. 2012, 134, 20412-20420; Org. Lett. 2014, 16, 1680-1683; J. Org. Chem. 2013, 78, 702-705; J. Org. Chem. 2015, 80, 12129-12136; ACS Macro Lett. 2014, 3, 1191-1195; New J. Chem., 2012, 36, 386-393; Chem. Commun., 2010, 46, 6575-6577; 2013).
Молекулярный переключатель представляет собой молекулу, способную обратимо переключаться между двумя или более стабильными состояниями. Молекулы могут переключаться между состояниями в ответ на раздражители окружающей среды, такие как изменения в химической среде (например, pH), облучение светом (например, свет определенной длины волны), температура, электрический ток, микросреда или присутствие лиганда. В некоторых случаях переключение между состояниями может зависеть от комбинации стимулов. Самые старые формы синтетических молекулярных переключателей - это индикаторы pH, которые отображают различные цвета в зависимости от pH. Синтетические молекулярные переключатели могут применяться в молекулярных компьютерах или адаптивных системах доставки лекарственных препаратов. Молекулярные переключатели также важны в биологии, потому что на них основаны многие биологические функции, например, аллостерическая регуляция и зрение.
Такие биодатчики, химические датчики и молекулярные переключатели могут дополнительно содержать дополнительные фотореактивные фрагменты, такие как родамин, феноловый красный, оранжевый азокраситель, папа красный, несульфированный цианин, сульфированный цианин, хемилюминесцентный фторидный датчик (производное 1,2-диоксетана), и красители D2A (NIR-флуоресцентные красители). Альтернативно, фотореактивный фрагмент может быть выбран из соединения, имеющего функциональные группы и структуры, аналогичные следующим:

где:
R100 представляет собой H или C1-C6-алкил;
R101 представляет собой H или SO3H; R102 представляет собой C1-C6-алкил или -(CH2)zCOOH;
z представляет собой целое число от 3 до 8;
R103 и R104 в каждом случае независимо представляют собой Н или C1-C6-алкил; и
R105 и R106 независимо представляют собой водород COOH или SO3H.
В данной области техники известны дополнительные фотореактивные фрагменты. См., например, Org. Lett. 2014, 16, 1680-1683; J. Am. Chem. Soc. 2011, 133, 10960-10965; Dye Lasers, 3rd Ed. (Springer-Verlag, Berlin, 1990); J. Am. Chem. Soc. 2012, 134, 20412-20420).
Способы лечения
Варианты прицельного лечения
Нацеливающий фрагмент конъюгата может распознаваться клеткой, обеспечивая тем самым так называемое прицельное лечение.
В некоторых вариантах осуществления конъюгат содержит активный агент для применения в прицельном лечении для лечения аутоиммунного заболевания. В некоторых таких вариантах осуществления активные агенты выбирают из циклоспорина, циклоспорина А, мофетила микофенилата, сиролимуса, такролимуса, энанерцепта, преднизона, азатиоприна, метотрексата, циклофосфамида, аминокапроновой кислоты, хлорохина, гидроксихлорохина, гидрокортизона, дексаметазона, хлорамбуцила, ДГЭА, даназола, бромокриптина, мелоксикама, инфликсимаба и т. д.
В некоторых вариантах осуществления соединение содержит активный агент Q для применения в прицельном лечении для лечения инфекционного заболевания. В некоторых таких вариантах осуществления Q выбран из: ряда бета-лактама (пенициллин G, пенициллин V, клоксациллин, диклоксациллин, метициллин, нафциллин, оксациллин, ампициллин, амоксициллин, бекампициллин, азлоциллин, карбенициллин, мезлоциллин, пиперациллин, тикарциллин), ряда аминогликозид (амикацин, гентамицин, канамицин, неомицин, нетилмицин, стрептомицин, тобрамицин), ряда макролидов (азитромицин, кларитромицин, эритромицин, линкомицин, клиндамицин), ряда тетрациклинов (демеклоциклин, доксицилин, миноциклин, тетрациклин), ряда хинолон (циноксацин, налидиксовая кислота), ряда фторхинолонов (ципрофлоксацин, эноксацин, грепафлоксацин, левофлоксацин, ломефлоксацин, норфлоксацин, офлоксацин, спарфлоксацин, тровафлоксицин), ряда полипептидов (бацитрацин, колистин, полимиксин B), ряда сульфонамидов (сульфизоксазол, сульфаметоксазол, сульфадиазин, сульфаметизол, сульфацетамид), других антибиотиков (триметоприм, сульфаметоксазол, хлорамфеникол, ванкомицин, метронидазол, хинупристин, дальфопристин, рифампицин, спектиномицин, нитрофурантоин), общих антивирусных агентов (идоксурадин, видарабин, ацикловир, фамцикловир, пенцикловир, валацикловир, ганцикловир, фоскарнет, рибавирин, амантадин, римантадин, цидофовир, антисмысловые олигонуклеотиды, иммуноглобулины, интерфероны), терапевтические агенты для лечения ВИЧ-инфекции (тенофовир, эмтрицитабин, зидовудин, диданозин, залцитабин, ставудин, ламивудин, невирапин, делавиридин, саквинавир, ритонавир, индинавир, нелфинавир) и др.
В некоторых вариантах осуществления соединения и конъюгаты, описанные в данном документе, содержат активный агент Q для применения в способе доставки активного агента в клетку для лечения опухоли, где нацеливающий фрагмент выбран для связывания с клеткой-мишенью (то есть раковой клеткой). В частности, настоящие соединения, конъюгаты и композиции могут быть применимы для ингибирования аномального клеточного роста или лечения пролиферативного расстройства у млекопитающего (например, человека), такого как, где клетка-мишень представляет собой раковую клетку, а нацеливающий фрагмент выбран для связывания с молекулой, ассоциированной с раковой клеткой (и не ассоциированной со здоровыми клетками или по меньшей мере преимущественно ассоциированной с опухолевыми клетками, а не здоровыми клетками).
В некоторых таких вариантах осуществления активный агент выбран из: цитотоксического или иммуномодулирующего агента, противоракового агента, противотубулинового агента, цитотоксического агента и т. д. Предпочтительно, цитотоксический или иммуномодулирующий агент включает противотубулиновый агент, ауристатин, вещество связующее малые бороздки ДНК, ингибитор транскрипции ДНК, алкилирующий агент, антрациклин, антибиотик, антифолат, антиметаболит, ингибитор кальмодулина, сенсибилизатор химиотерапии, дуокармицин, этопозид, фторированный пиримидин, ионофор, лекситропсин, майтанзиноид, нитрозомочевину, платинол, порообразующее соединение, пуриновый антиметаболит, пуромицин, сенсибилизатор лучевой терапии, рапамицин, стероид, таксан, ингибитор топоизомеразы, алкалоид барвинка и т. д.; противораковый агент включает в себя метотрексат, таксол, L-аспарагиназу, меркаптопурин, тиогуанин, гидроксимочевину, цитарабин, циклофосфамид, ифосфамид, нитрозомочевины, цисплатин, карбоплатин, митомицин, дакарбазин, прокарбазин, топотекан, азотистые иприты, цитоксан, этопозид, 5-фторурацил BCNU, иринотекан, камптотецины, блеомицин, доксорубицин, идарибицин, даунорубицин, дактиномицин, пликамицин, митоксантрон, аспарагиназу, винбластин, винкристин, винорелбин, паклитаксел, доцетаксел и т. д.; противотубулиновый агент включает таксан (например, паклитаксел, доцетаксел), Т67, алкилоид барвинка (например, винкристин, винбластин, виндезин, винорелбин), производное баккатина, производное таксана, эпотиолон (например, эпотилон А, эпотилон В), нокодазол, колхицин, колцимид, эстрамустин, критофицины, цемадотин, майтанзиноиды, комбрестатины, дискодермолид, элеутеробин, производное ауристатина (AFP, MMAF, MMAE) и т. д.; цитотоксический агент включает в себя андроген, антрамицин (AMC), аспарагиназу, 5-азацитидин, азатиоприн, блеомицин, бусульфан, бутионина сульфоксимин, калихеамицин, производное калихеамицина, камптотецин, карбоплатин, кармустин(BSNU), СС-1065, хлорамбуцин, цисплатин, колхицин, циклофосфамид, цитарабин, цитидина арабинозид, цитохалазин B, дакарбазин, дактиномицин(актиномицин), даунорубицин, декарбазин, DM1, DM4, доцетаксел, доксорубицин, этопозид, эстроген, 5-фтордезоксиуридин, 5-фторурацил, гемцитабин, грамицидин D, гидроксимочевину, идарибицин, ифосфамид, иринотекан, ломустин(CCNU), майтанзин, мехлорэтамин, мелфалан, 6-меркаптопурин, метотрексат, митрамицин, митомицин С, митоксантрон, нитроимидазол, паклитаксел, палитоксин, пликамицин, прокарбизин, ризоксин, стрептозотоцин, тенопозид, 6-тиогуанин, тиоТЕПА, топотекан, винбластин, винкристин, винорелбин, VP-16, VM-26; вещество связующее малые бороздки ДНК (например, энедиин, лекситропсин, соединение CBI), дуокармицин, таксан (например, паклитаксел, доцетаксел), пуромицины, алкалоиды барвинка, CC-1065, SN-38, топотекан, морфолино-доксорубицин, ризоксин, цианоморфолино-доксорубицин, эхиномицин, комбретастатин, нетропсин, эпотилон А, эпотилон В, эстрамустин, криптофицины, цемадотин, майтанзиноиды, дискодермолид, элеутеробин, митоксантрон и т. д.
Клеточная пролиферация и апоптоз
Описанные в настоящем документе соединения и конъюгаты могут быть использованы в способах индукции апоптоза в клетках.
Нарушение регуляции апоптоза связано с различными заболеваниями, включая, например, аутоиммунные расстройства (например, системная красную волчанку, ревматоидный артрит, болезнь «трансплантат против хозяина», миастения или синдром Шегрена), хронические воспалительные состояния (например, псориаз, астма или болезнь Крона), гиперпролиферативные расстройства (например, рак молочной железы, рак легкого), вирусные инфекции (например, герпес, папиллома или ВИЧ) и другие состояния, такие как остеоартрит и атеросклероз. Соединения, конъюгаты и композиции, описанные в настоящем документе, могут использоваться для лечения или ослабления любого из этих заболеваний. Такие способы лечения обычно включают введение субъекту, страдающего заболеванием, количества соединения, конъюгата или композиции, описанных в данном документе, достаточного для обеспечения терапевтического эффекта. Идентичность антитела вводимого соединения, конъюгата или композиции будет зависеть от заболевания, подлежащего лечению, поэтому антитело должно связывать антиген клеточной поверхности, экспрессируемый в клеточном типе, где было бы полезным ингибирование. Достигнутый терапевтический эффект также будет зависеть от конкретного заболевания, подлежащего лечению. В определенных случаях соединения и композиции, описанные в данном документе, могут лечить или ослаблять само заболевание или симптомы заболевания при применении в виде монотерапии. В других случаях соединения и композиции, описанные в данном документе, могут быть частью общей схемы лечения, включая другие агенты, которые вместе с ингибитором или соединениями и композициями, описанными в данном документе, лечат или ослабляют заболевание, подлежащее лечению, или симптомы заболевания. Агенты, используемые для лечения или ослабления специфических заболеваний, которые можно вводить в дополнение к соединениям и композициям, описанным в данном документе, или вместе с ними, будут очевидны для специалистов в данной области техники.
Хотя полное излечение всегда желательно в любом терапевтическом режиме, для достижения терапевтическоого эффекта не требуется достижения излечения. Терапевтический эффект может включать остановку или замедление прогрессирования заболевания, регрессию заболевания без излечения и/или ослабление или замедление прогрессирования симптомов заболевания. Продленная выживаемость по сравнению со статистическими средними показателями и или улучшенное качество жизни также могут рассматриваться как терапевтический эффект.
Одним конкретным классом заболеваний, которые включают в себя нарушение регуляции апоптоза и, которые представляют собой поистине значимое бремя для здоровья во всем мире, являются различные виды рака. В конкретном варианте осуществления соединения и композиции, описанные в данном документе, могут быть использованы для лечения различных видов рака. Рак может представлять собой, например, солидные опухоли или гематологические опухоли. Виды рака, которые можно лечить с помощью описанных в настоящем документе соединений и композиций, включают, но не ограничиваются ими, рак мочевого пузыря, рак головного мозга, рак молочной железы, рак костного мозга, рак шейки матки, хронический лимфоцитарный лейкоз, колоректальный рак, рак пищевода, гепатоцеллюлярный рак, лимфобластный лейкоз, фолликулярную лимфому, лимфоидные злокачественные опухоли Т-клеточного или В-клеточного происхождения, меланому, миелогенный лейкоз, миелому, рак полости рта, рак яичников, немелкоклеточный рак легкого, хронический лимфоцитарный лейкоз, миелому, рак предстательной железы, мелкоклеточный рак легких и рак селезенки. Соединения и композиции, описанные в данном документе, могут быть особенно полезны при лечении рака, поскольку антитело может быть использовано для специфического воздействия на опухолевую клетку, тем самым потенциально предотвращая или ослабляя нежелательные побочные эффекты и/или токсичность, которые могут быть связаны с системным введением неконъюгированных ингибиторов. Один из вариантов осуществления относится к способу лечения заболевания, включающего нарушение регуляции внутреннего апоптоза, включающему введение субъекту, страдающему заболеванием, связанным с нарушением регуляции апоптоза, количества описанных в данном документе соединения и композиции, эффективных для обеспечения терапевтического эффекта, в котором лиганд соединений и композиций, описанных в данном документе, связывает рецептор клеточной поверхности на клетке с нарушенным внутренним апоптозом. Один вариант осуществления относится к способу лечения рака, включающему введение субъекту, страдающему раком, соединения и композиции, описанных в данном документе, в котором лиганд способен связывать рецептор клеточной поверхности или ассоциированный с опухолью антиген, экспрессируемый на поверхности раковых клеток, в количестве, эффективном для обеспечения терапевтического эффекта.
В контексте онкогенного рака терапевтический эффект, помимо включения эффектов, обсуждаемых выше, может также конкретно включать остановку или замедление прогрессирования роста опухоли, регрессирование роста опухоли, эрадикацию одной или более опухолей и/или повышение выживаемости пациентов по сравнению со статистическими средними показателями для типа и стадии рака, подлежащего лечению. В одном варианте осуществления рак, подлежащий лечению, представляет собой онкогенный рак.
Соединения и конъюгаты, описанные в данном документе, могут применяться в виде монотерапии для обеспечения терапевтического эффекта или могут применяться в дополнение к другим химиотерапевтическим агентам и/или лучевой терапии или вместе с ними. Химиотерапевтические агенты, в дополнение к которым соединения и композиции, описанные в данном документе, могут быть использованы в качестве вспомогательной терапии, могут быть нацеленными (например, ADC, ингибиторы протеинкиназы и т. д.) или ненацеленнными (например, неспецифические цитотоксические агенты, такие как радионуклеотиды, алкилирующие агенты и интеркалирующие агенты). Ненацеленные химиотерапевтические агенты, в дополнение к которым могут быть введены соединения и композиции, описанные в данном документе, включают, но не ограничиваются ими, метотрексат, таксол, L-аспарагиназу, меркаптопурин, тиогуанин, гидроксимочевину, цитарабин, циклофосфамид, ифосфамид, нитрозомочевину, цисплатин, карбоплатин, митомицин, дакарбазин, прокарбизин, топотекан, азотистые иприты, цитоксан, этопозид, 5-фторурацил, BCNU, иринотекан, камптотецины, блеомицин, доксорубицин, идарубицин, даунорубицин, дактиномицин, пликамицин, митоксантрон, аспарагиназу, винбластин, винкристин, винорелбин, паклитаксел, калихеамицин и доцетаксел.
Описанные в данном документе соединения и конъюгаты, которые могут быть неэффективными в качестве монотерапии для лечения рака, могут вводиться в дополнение к другим химиотерапевтическим агентам или лучевой терапии или вместе с ними для обеспечения терапевтического эффекта. Один вариант осуществления относится к способу, в котором соединение или композицию, описанную в данном документе, вводят в количестве, эффективном для повышения чувствительности опухолевых клеток к стандартной химиотерапии и/или лучевой терапии. Соответственно, в контексте лечения различных видов рака термин «терапевтический эффект» включает введение соединений и композиций, описанных в настоящем документе, в добавление к химиотерапевтическим агентам и/или лучевой терапии или вместе с ними, либо пациентам, которые еще не начали прохождение такой терапии, либо у которых имеются, но еще не проявлялись признаки резистентности или пациентам, у которых начали проявляться признаки резистентности, в качестве средства сенсибилизации опухолей к химиотерапии и/или лучевой терапии.
Фармацевтические композиции и способы их введения
Соединения и конъюгаты, описанные в настоящем документе могут быть использованы для лечения индивидуума, нуждающегося в этом. В определенных вариантах осуществления изобретения индивидуум представляет собой млекопитающее, такое как человек, или млекопитающее, не являющееся человеком. При введении животному, такому как человек, композицию или соединение предпочтительно вводят в виде фармацевтической композиции, содержащей, например, описанное соединение и фармацевтически приемлемый носитель.
Фармацевтически приемлемые носители хорошо известны в данной области и включают, например, водные растворы, такие как вода или физиологически забуференный солевой раствор, или другие растворители или носители, такие как гликоли, глицерин, масла, такие как оливковое масло, или инъекционные органические сложные эфиры. В предпочтительных вариантах осуществления изобретения, когда такие фармацевтические композиции предназначены для введения человеку, особенно для инвазивных путей введения (то есть путей, таких как инъекция или имплантация, которые обеспечивают преодолевающий перенос или диффузию через эпителиальный барьер), водный раствор не содержит пирогенов или практически не содержит пирогенов. Эксципиенты могут быть выбраны, например, для осуществления отсроченного высвобождения агента или для избирательного нацеливания на одну или более клеток, тканей или органов. Фармацевтическая композиция может быть в форме единичной дозы, такой как таблетка, капсула (включая вскрываемую капсулу и желатиновую капсулу), гранула, лиофильный препарат для разведения, порошок, раствор, сироп, суппозиторий, инъекция или тому подобное. Композиция также может присутствовать в системе трансдермальной доставки, например кожном пластыре. Композиция также может присутствовать в растворе, подходящем для местного применения, таком как мазь или крем.
Фармацевтически приемлемый носитель может содержать физиологически приемлемые агенты, которые действуют, например, для стабилизации, увеличения растворимости или увеличения абсорбции соединения, такого как соединение изобретения. Такие физиологически приемлемые агенты включают, например, углеводы, такие как глюкоза, сахароза или декстраны, антиоксиданты, такие как аскорбиновая кислота или глутатион, хелатирующие агенты, низкомолекулярные белки или другие стабилизаторы или эксципиенты. Выбор фармацевтически приемлемого носителя, включая физиологически приемлемый агент, зависит, например, от пути введения композиции. Препарат фармацевтической композиции может быть самоэмульгирующей системой доставки лекарств или системой лекарственной доставки с самопроизвольным формированием микроэмульсии. Фармацевтическая композиция (препарат) также может представлять собой липосому или другую полимерную матрицу, которая может включать в себя, например, соединение изобретения. Например, липосомы, которые содержат фосфолипиды или другие липиды, являются нетоксичными, физиологически приемлемыми и метаболизируемыми носителями, которые относительно просты в изготовлении и применении.
Фраза «фармацевтически приемлемый» используется в данном документе для обозначения таких соединений, материалов, композиций и/или лекарственных форм, которые в рамках рационального медицинского решения, являются подходящими для применения в контакте с тканями людей и животных без чрезмерной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, соразмерно разумному соотношению пользы/риска.
Фраза «фармацевтически приемлемый носитель» при использовании в настоящем документе означает фармацевтически приемлемый материал, композицию или носитель, такой как жидкий или твердый наполнитель, разбавитель, эксципиент, растворитель или инкапсулирующий материал. Каждый носитель должен быть «приемлемым» в смысле совместимости с другими ингредиентами препарата и не причинять вреда пациенту. Некоторые примеры материалов, которые могут служить в качестве фармацевтически приемлемых носителей, включают: (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмалы, такие как кукурузный крахмал и картофельный крахмал; (3) целлюлоза и ее производные, такие как натриевая соль карбоксиметилцеллюлозы, этилцеллюлоза и ацетат целлюлозы; (4) порошкообразный трагакант; (5) солод; (6) желатин; (7) тальк; (8) эксципиенты, такие как масло какао и воски для суппозиториев; (9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль; (11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) буферные агенты, такие как гидроксид магния и гидроксид алюминия; (15) альгиновая кислота; (16) апирогенная вода; (17) изотонический солевой раствор; (18) раствор Рингера; (19) этиловый спирт; (20) фосфатные буферные растворы и (21) другие нетоксичные совместимые вещества, используемые в фармацевтических составах.
Фармацевтическую композицию (препарат) можно вводить субъекту любым из ряда способов введения, включая, например, пероральное введение (например, капли, как в водных или неводных растворах или суспензиях, таблетки, капсулы (включая вскрываемые капсулы и желатиновые капсулы), болюсы, порошки, гранулы, пасты для нанесения на язык); всасывание через слизистую оболочку полости рта (например, сублингвально); анально, ректально или вагинально (например, в виде пессария, крема или пены); парентерально (включая внутримышечно, внутривенно, подкожно или интратекально, как, например, стерильный раствор или суспензию); интраназально; внутрибрюшинно; подкожно; трансдермально (например, в виде пластыря, нанесенного на кожу); и местно (например, в виде крема, мази или спрея, нанесенных на кожу или в виде глазных капель). Соединение также может быть составлено для ингаляции. В определенных вариантах осуществления изобретения соединение может быть просто растворено или суспендировано в стерильной воде. Подробности подходящих путей введения и подходящих для них композиций можно найти, например, в патентах США №№ 6110973, 5763493, 5731000, 5541231, 5427798, 5358970 и 4172896, а также в цитированных в них патентах.
Составы можно удобно предоставлять в стандартной дозированной форме и можно получать любыми способами, хорошо известными в области фармации. Количество активного ингредиента, которое можно комбинировать с материалом-носителем для получения единичной дозированной формы, будет варьироваться в зависимости от организма, который лечат, конкретного способа введения. Количество активного ингредиента, которое можно комбинировать с материалом носителя для получения единичной дозированной формы, обычно будет таким количеством соединения, которое оказывает терапевтический эффект. В целом, из ста процентов это количество будет варьировать от около 1 процента до около девяноста девяти процентов активного ингредиента, предпочтительно от около 5 процентов до около 70 процентов, наиболее предпочтительно от около 10 процентов до около 30 процентов.
Способы приготовления этих составов или композиций включают стадию объединения активного соединения, такого как соединение изобретения, с носителем и, необязательно, одним или более дополнительными ингредиентами. Обычно составы получают путем равномерного и тщательного объединения соединения настоящего изобретения с жидкими носителями или тонкоизмельченными твердыми носителями, или ими обоими, а затем, при необходимости, формованием продукта.
Композиции изобретения, подходящие для перорального введения, могут быть в форме капсул (включая вскрываемые капсулы и желатиновые капсулы), крахмальных капсул, пилюль, таблеток, леденцов (с использованием ароматизированной основы, обычно сахарозы и гуммиарабика или трагаканта), лиофильных препаратов, порошков, гранул или в виде раствора или суспензии в водной или неводной жидкости, или в виде жидкой эмульсии масло-в-воде или вода-в-масле, или в виде эликсира или сиропа, или в виде пастилок (с использованием инертной основы, такой как желатин и глицерин, или сахароза и гуммиарабик) и/или в виде средств для полоскания рта и тому подобного, каждая из которых содержит заранее определенное количество соединения настоящего изобретения в качестве активного ингредиента. Соединения, конъюгаты или композиции также можно вводить в виде болюса, электуария или пасты.
Для приготовления твердых дозированных форм для перорального введения (капсулы (включая вскрываемые капсулы и желатиновые капсулы), таблетки, пилюли, драже, порошки, гранулы и тому подобное) активный ингредиент смешивают с одним или более фармацевтически приемлемыми носителями, такими как цитрат натрия или фосфат дикальция и/или любым из следующего: (1) наполнители или добавки, такие как крахмалы, лактоза, сахароза, глюкоза, маннит и/или кремниевая кислота; (2) связующие, такие как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и/или гуммиарабик; (3) увлажнители, такие как глицерин; (4) разрыхлители, такие как агар-агар, карбонат кальция, картофельный крахмал или крахмал из тапиоки, альгиновая кислота, некоторые силикаты и карбонат натрия; (5) замедляющие растворение агенты, такие как парафин; (6) ускорители абсорбции, такие как четвертичные аммониевые соединения; (7) смачивающие агенты, такие как, например, цетиловый спирт и моностеарат глицерина; (8) абсорбенты, такие как каолин и бентонитовая глина; (9) смазывающие вещества, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси; (10) комплексообразующие агенты, такие как модифицированные и немодифицированные циклодекстрины; и (11) красители. В случае капсул (включая вскрываемые капсулы и желатиновые капсулы), таблеток и пилюль фармацевтические композиции также могут содержать буферные агенты. Твердые композиции подобного типа также могут применяться в качестве наполнителей в мягких и твердых желатиновых капсулах с применением таких эксципиентов как лактоза или молочные сахара, а также высокомолекулярные полиэтиленгликоли и тому подобное
Таблетки можно получать путем прессования или формовки, необязательно, с одним или более вспомогательными ингредиентами. Прессованные таблетки могут быть приготовлены с использованием связующего (например, желатина или гидроксипропилметилцеллюлозы), смазывающего вещества, инертного разбавителя, консерванта, дезинтегранта (например, натрий гликолята крахмала или сшитой натрий карбоксиметилцеллюлозы), поверхностно-активного или диспергирующего агента. Формованные таблетки могут быть изготовлены путем формования в подходящем аппарате смеси порошкообразного соединения, увлажненного инертным жидким разбавителем.
Таблетки и другие твердые лекарственные формы фармацевтических композиций, такие как драже, капсулы (включая вскрываемые капсулы и желатиновые капсулы), пилюли и гранулы, могут быть необязательно с насечкой или приготовлены с покрытиями и оболочками, такими как кишечнорастворимые покрытия и другие покрытия, хорошо известные в области фармацевтики. Они также могут быть составлены таким образом, чтобы обеспечить медленное или контролируемое высвобождение в нем активного ингредиента с использованием, например, гидроксипропилметилцеллюлозы в различных пропорциях, чтобы обеспечить желаемый профиль высвобождения, другие полимерные матрицы, липосомы и/или микросферы. Они могут быть стерилизованы, например, фильтрованием через задерживающий бактерии фильтр или включением стерилизующих агентов в форме стерильных твердых композиций, которые можно растворить в стерильной воде или в некоторой другой стерильной инъекционной среде непосредственно перед использованием. Эти композиции также могут, необязательно, содержать замутнители и могут представлять собой композицию, из которой они высвобождают только активный(ые) ингредиент(ы) или предпочтительно, в определенной части желудочно-кишечного тракта, необязательно, с задержкой. Примерами заливочных композиций, которые можно использовать, являются полимерные вещества и воски. Активный ингредиент также может находиться в микроинкапсулированной форме, если это уместно, с одним или более вышеописанными эксципиентами.
Жидкие лекарственные формы, пригодные для перорального введения, включают фармацевтически приемлемые эмульсии, лиофильные препараты для разведения, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активному ингредиенту жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в данной области, такие как, например, вода или другие растворители, циклодекстрины и их производные, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (в частности, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот с сорбитаном и их смеси.
Помимо инертных разбавителей, композиции для ухода за полостью рта могут также включать вспомогательные вещества, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подсластители, ароматизаторы, красители, отдушки и консерванты.
Суспензии, в дополнение к активным соединениям, могут содержать суспендирующие агенты, такие как, например, этоксилированные изостеариловые спирты, сложные эфиры полиоксиэтиленсорбита и сорбитана, микрокристаллическую целлюлозу, метагидроксид алюминия, бентонит, агар-агар и трагакант и их смеси.
Составы фармацевтических композиций для ректального, вагинального или уретрального введения могут быть представлены в виде суппозитория, который может быть приготовлен путем смешивания одного или более активных соединений с одним или более подходящими нераздражающими вспомогательными веществами или носителями, включающими, например, масло какао, полиэтиленгликоль, воск для суппозиториев или салицилат, которые являются твердыми при комнатной температуре, но жидкими при температуре тела и, следовательно, растают в ректальной или вагинальной полости с высвобождением активного соединения.
Составы фармацевтических композиций для введения в полость рта могут быть представлены в виде жидкости для полоскания рта или перорального спрея, или пероральной мази.
Альтернативно или дополнительно, композиции могут быть составлены для доставки через катетер, стент, проводник или другое внутрипросветное устройство. Доставка через такие устройства может быть в частности применима для доставки в мочевой пузырь, мочеиспускательный канал, мочеточник, прямую кишку или кишечник.
Составы, которые подходят для вагинального введения, также включают формы в виде пессариев, тампонов, кремов, гелей, паст, пен или спрея, содержащие носители, являющиеся известными в данной области техники.
Лекарственные формы для местного или трансдермального введения включают порошки, аэрозоли, мази, пасты, кремы, лосьоны, гели, растворы, пластыри и ингаляторы. Активное соединение может быть смешано в стерильных условиях с фармацевтически приемлемым носителем и с любыми консервантами, буферами или пропеллентами, которые могут потребоваться.
Мази, пасты, кремы и гели могут содержать в дополнение к активному соединению эксципиенты, такие как животные и растительные жиры, масла, воски, парафины, крахмал, трагакант, производные целлюлозы, полиэтиленгликоли, силиконы, бентониты, кремниевую кислоту, тальк и оксид цинка или их смеси.
Порошки и аэрозоли могут содержать, в дополнение к активному соединению, эксципиенты, такие как лактоза, тальк, кремниевая кислота, гидроксид алюминия, силикаты кальция и порошок полиамидов, или смеси этих веществ. Аэрозоли могут дополнительно содержать обычные пропелленты, такие как хлорфторуглеводороды и летучие незамещенные углеводороды, такие как бутан и пропан.
Трансдермальные пластыри имеют дополнительное преимущество, заключающееся в обеспечении контролируемой доставки соединения настоящего изобретения в организм. Такие лекарственные формы могут быть изготовлены путем растворения или диспергирования активного соединения в подходящей среде. Усилители абсорбции также могут быть использованы для увеличения потока соединения через кожу. Скорость такого потока может контролироваться либо предоставлением регулирующей скорость мембраны, либо диспергированием соединения в полимерной матрице или геле.
Офтальмологические составы, глазные мази, порошки, растворы и тому подобное также рассматриваются как входящие в объем данного изобретения. Типичные офтальмологические составы описаны в публикациях США 2005/0080056, 2005/0059744, 2005/0031697 и 2005/004074; и патенте США № 6583124, содержание которого включено в настоящий документ посредством ссылки. Если желательно, жидкие офтальмологические составы имеют свойства, подобные свойствам слезных жидкостей, внутриглазной жидкости или жидкой части стекловидного тела, или совместимы с такими жидкостями.
Фразы «парентеральное введение» и «введенный парентерально», используемые в данном документе, означают способы введения, отличные от энтерального и местного введения, обычно путем инъекции, и включают, без ограничения, внутривенную, внутримышечную, внутриартериальную, интратекальную, внутрикапсулярную, интраорбитальную, внутрисердечную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, субкапсулярную, субарахноидальную, интраспинальную и интрастернальную инъекцию и инфузию.
Фармацевтические композиции, подходящие для парентерального введения, содержат одно или более активных соединений в сочетании с одним или более фармацевтически приемлемыми стерильными изотоническими водными или неводными растворами, дисперсиями, суспензиями или эмульсиями или стерильными порошками, которые могут быть разведены в стерильные инъекционные растворы или дисперсии непосредственно перед применением, которые могут содержать антиоксиданты, буферы, бактериостатические агенты, растворимые вещества, которые делают состав изотоническим с кровью предполагаемого реципиента, или суспендирующими или загущающими агентами.
Примеры подходящих водных и неводных носителей, которые могут использоваться в фармацевтических композициях изобретения, включают воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и тому подобное) и их подходящие смеси, растительные масла, такие как оливковое масло и инъекционные органические сложные эфиры, такие как этилолеат. Надлежащая текучесть может поддерживаться, например, путем использования материалов для покрытия, таких как лецитин, путем поддержания требуемого размера частиц в случае дисперсий и путем использования поверхностно-активных веществ.
Эти композиции также могут содержать вспомогательные вещества, такие как консерванты, смачивающие агенты, эмульгирующие агенты и диспергирующие агенты. Предотвращение действия микроорганизмов может быть обеспечено включением различных антибактериальных и противогрибковых агентов, например, парабена, хлорбутанола, фенолсорбиновой кислоты и тому подобного. Также может быть желательно включать в композиции изотонические агенты, такие как сахара, хлорид натрия и тому подобное. Кроме того, пролонгированное всасывание инъекционной фармацевтической формы может быть вызвано включением агентов, которые замедляют всасывание, таких как моностеарат алюминия и желатин.
В некоторых случаях для пролонгирования действия лекарственного средства, желательно замедлять абсорбцию лекарственного средства при подкожной или внутримышечной инъекции. Это можно осуществлять посредством применения жидкой суспензии кристаллического или аморфного материала, имеющего плохую растворимость в воде. Скорость абсорбции лекарственного средства зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристалла и кристаллической формы. Альтернативно, замедленное всасывание парентерально вводимой лекарственной формы осуществляют путем растворения или суспендирования лекарственного средства в масляном носителе.
Инъекционные депо-формы получают путем формирования микрокапсулированных матриц рассматриваемых соединений в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от соотношения лекарственного средства и полимера и природы конкретного используемого полимера скорость высвобождения лекарства можно контролировать. Примеры других биологически разлагаемых полимеров включают сложные поли(ортоэфиры) и поли(ангидриды). Депо-инъекционные составы также готовят путем заключения лекарственного средства в липосомы или микроэмульсии, которые совместимы с тканями организма.
Для использования в способах этого изобретения активные соединения могут быть даны сами по себе или в виде фармацевтической композиции, содержащей, например, от 0,1 до приблизительно 99,5% (более предпочтительно от приблизительно 0,5 до приблизительно 90,0%) активного ингредиента в сочетании с фармацевтически приемлемым носителем.
В некоторых вариантах осуществления изобретения соединение по настоящему изобретению вводят совместно с одним или более дополнительными соединениями/агентами.
В определенных таких вариантах осуществления совместное введение является одновременным. В определенных таких вариантах осуществления соединение по настоящему изобретению вводят совместно с одним или более дополнительными соединениями. В определенных других таких вариантах осуществления соединение по изобретению вводят отдельно, но одновременно с одним или более дополнительными соединениями. В определенных таких вариантах осуществления совместное введение является последовательным, причем введение соединения по изобретению предшествует или следует за введением одного или более дополнительных соединений в течение минут или часов.
Способы введения соединения по настоящему изобретению также могут обеспечиваться перезаряжаемыми или биоразлагаемыми устройствами. В последние годы были разработаны и испытаны in vivo различные полимерные устройства с медленным высвобождением для контролируемой доставки лекарств, включая белковые биофармацевтические препараты. Различные биосовместимые полимеры (включая гидрогели), включая как биоразлагаемые, так и неразлагаемые полимеры, могут быть использованы для формирования имплантата для замедленного высвобождения соединения в конкретном целевом месте.
Фактические уровни дозировки активных ингредиентов в фармацевтических композициях можно варьировать, чтобы получить количество активного ингредиента, которое эффективно для достижения желаемого терапевтического ответа для конкретного пациента, композиции и способа введения, без токсического эффекта для пациента.
Выбранный уровень дозировки будет зависеть от множества факторов, включая активность конкретного используемого соединения, конъюгата или комбинации соединений и/или используемых конъюгатов, сложного эфира, соли или амида, путь введения, время введения, скорость выведения конкретного используемого(ых) соединения(й), продолжительность лечения, другие лекарственные средства, соединения и/или материалы, используемые в комбинации с применяемыми конкретным(ыми) соединением(ями), возраст, пол, вес, состояние, общее состояние здоровья и предшествующую историю болезни пациента, которого лечат, и подобные факторы, хорошо известные в данной области медицины.
Врач или ветеринар, имеющий обычные навыки в данной области, может легко определять и назначать терапевтически эффективное количество требуемой фармацевтической композиции. Например, врач или ветеринар может начинать прием доз фармацевтической композиции или соединения с уровней ниже, чем требуется для достижения желаемого терапевтического эффекта, и постепенно увеличивать дозировку до тех пор, пока не будет достигнут желаемый эффект. «Терапевтически эффективное количеством» означает концентрацию соединения, которая является достаточной для достижения желаемого терапевтического эффекта. Обычно считается, что эффективное количество соединения будет варьироваться в зависимости от веса, пола, возраста и истории болезни субъекта. Другие факторы, которые влияют на эффективное количество, могут включать, но не ограничиваются ими, тяжесть состояния пациента, расстройство, которое лечат, стабильность соединения и, если желательно, другой тип терапевтического средства, вводимого с соединением изобретения. Большая общая доза может быть доставлена путем многократного введения агента. Методы определения эффективности и дозировки известны специалистам в данной области (Isselbacher et al. (1996) Harrison's Principles of Internal Medicine 13 ed., 1814-1882, включенный сюда посредством ссылки).
В общем, подходящая суточная доза активного соединения, используемого в композициях и способах изобретения, будет представлять собой такое количество соединения, которое является самой низкой дозой, эффективной для получения терапевтического эффекта. Такая эффективная доза обычно будет зависеть от описанных выше факторов.
При желании эффективную суточную дозу активного соединения или конъюгата можно вводить в виде одной, двух, трех, четырех, пяти, шести или более субдоз, вводимых раздельно с соответствующими интервалами в течение дня, необязательно, в единичных дозированных формах. В определенных вариантах осуществления настоящего изобретения активное соединение может вводиться два или три раза в день. В предпочтительных вариантах осуществления активное соединение будет вводиться один раз в день.
Пациентом, получающим такое лечение, является любое нуждающееся животное, включая приматов, в частности людей; и другие млекопитающие, такие как лошади, крупный рогатый скот, свиньи и овцы; и домашние животные в целом.
В определенных вариантах осуществления соединения или конъюгаты, описанные в данном документе, могут использоваться отдельно или совместно с другим типом терапевтического агента. Используемое здесь выражение «совместное введение» относится к любой форме введения двух или более различных терапевтических соединений или конъюгатов таким образом, что второе соединение вводят в то время как ранее введенное терапевтическое соединение или конъюгат все еще действует в организме (например, два соединения или конъюгата являются одновременно эффективными у пациента, что может включать синергетическое действие двух соединений или конъюгатов). Например, различные терапевтические соединения или конъюгаты могут вводиться либо в одной и той же композиции, либо в отдельных композициях, одновременно или последовательно. В определенных вариантах осуществления различные терапевтические соединения или конъюгаты могут вводиться в течение одного часа, 12 часов, 24 часов, 36 часов, 48 часов, 72 часа или недели после введения другого. Таким образом, индивидуум, который получает такое лечение, может получить пользу от комбинированного действия различных терапевтических соединений или конъюгатов.
Данное изобретение включает использование фармацевтически приемлемых солей соединений или конъюгатов, раскрытых в настоящем документе. В определенных вариантах осуществления предполагаемые соли изобретения включают, но не ограничиваются ими, соли алкила, диалкила, триалкила или тетраалкиламмония. В определенных вариантах осуществления предполагаемые соли изобретения включают, но не ограничиваются ими, L-аргинин, бенентамин, бензатин, бетаин, гидроксид кальция, холин, динол, диэтаноламин, диэтиламин, 2-(диэтиламино)этанол, этаноламин, этилендиамин, N-метилглюкамин, гидрабамин, 1Н-имидазол, литий, L-лизин, магний, 4-(2-гидроксиэтил)морфолин, пиперазин, калий, 1-(2-гидроксиэтил)пирролидин, натрий, триэтаноламин, трометамин и соли цинка. В определенных вариантах осуществления предполагаемые соли изобретения включают, но не ограничиваются ими, соли Na, Ca, K, Mg, Zn или других металлов.
Фармацевтически приемлемые соли присоединения кислот также могут существовать в виде различных сольватов, таких как вода, метанол, этанол, диметилформамид и тому подобное. Могут быть также приготовлены смеси таких сольватов. Источником такого сольвата может быть растворитель кристаллизации, принадлежащий к растворителю для приготовления или кристаллизации или случайный для такого растворителя.
В композициях также могут присутствовать увлажняющие агенты, эмульгаторы и смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, антиадгезивные агенты, покрытия, подсластители, вкусовые добавки и ароматизаторы, консерванты и антиоксиданты.
Примеры фармацевтически приемлемых антиоксидантов включают: (1) водорастворимые антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфит натрия, сульфит натрия и тому подобное; (2) маслорастворимые антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, альфа-токоферол и тому подобное; и (3) металлохелатирующие агенты, такие как лимонная кислота, этилендиаминтетрауксусная кислота (ЭДТА), сорбит, винная кислота, фосфорная кислота и тому подобное.
Теперь изобретение, в целом описываемое, будет более легко понято со ссылкой на следующие примеры, которые включены только в целях иллюстрации определенных аспектов и вариантов осуществления настоящего изобретения и не предназначены для ограничения изобретения.
ИЛЛЮСТРАТИВНЫЕ ПРИМЕРЫ
Протоколы синтеза
Аббревиатуры
AcO : ацетил
AcOH : уксусная кислота
EA : этилацетат
ДХМ : дихлорметан
m-CPBA : метахлорпероксибензойная кислота
TBTf : трет-бутилдиметилсилилтрифлат
TBDMS : трет-бутилдиметилсилил
ДМФА : диметилформамид
EDCI : 1-этил-3-(3-диметиламинопропил)карбодиимид
HOBt : 1-гидроксибензотриазола гидрат
ACN : ацетонитрил
TBDMS-Cl : трет-бутилдиметилсилилхлорид
DBU : 1,8-диазабицикло[5.4.0]ундец-7-ен
ТГФ : тетрагидрофуран
DCC : N, N'-дициклогексилкарбодиимид
DMAP : 4-диметиламинопиридин
NHS : N-гидроксисукцинимид
DIPEA : диизопропилэтиламин
TEA : триэтиламин
DEAD : диэтилазодикарбоксилат
Boc: трет-бутилоксикарбонил
ЛАГ : литийалюминийгидрид
CDI : 1,1'-карбонилдиимидазол
BEMP : 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро-1,3,2-диазофосфорин
TPSCl : трифенилхлоросилан
tfa : трифторацетил
PyBop : бензотриазол-1-ил-окситрипирролидинофосфонийгексафторфосфат
HBTU : N, N,N′,N′-тетраметил-O- (1H-бензотриазол-1-ил)урония гексафторфосфат
ТФУ : Трифторуксусная кислота
DIC : N, N'-диизопропилкарбодиимид
DMPA : 2,2-диметокси-2-фенилацетофенон
TBAF : Тетра-н-бутиламмонийфторид
AgOTf : Трифторметансульфонат серебра
(BimC4A)3 : Трикалия 5,5′,5′′-[2,2′,2′′-нитрилотрис (метилен)трис(1H-бензимидазол-2,1-диил)]трипентаноат
[Пример 1] Получение BGal-Br (далее именуемый «Int-TG»)
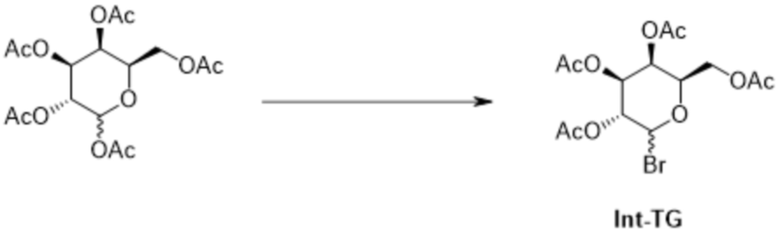
Пентаацетат β-D-галактозы (Alfa, CAS 4163-60-4, 5,0 г, 12,81 ммоль) растворяли в 33% HBr в AcOH (20 мл) при 0° в атмосфере N2 . Смесь нагревали до комнатной температуры. После перемешивания при комнатной температуре в течение 4 часов смесь концентрировали при пониженном давлении, а затем добавляли EA (1000 мл) и насыщенный бикарбонат натрия (1000 мл) . Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG (5,2 г, 99%).
1H ЯМР (400 МГц, CDCl3) δ 6,70 (д, J=4,0 Гц, 1H), 5,52 (д, J=2,4 Гц, 1H), 5,41 (дд, J=7,6, 2,8 Гц, 1H), 5,05 (дд, J=6,4, 4,0 Гц, 1H), 4,49 (т, J=6,4 Гц, 1H), 4,22-4,09 (м, 2H), 2,16-2,01 (м, 12H).
[Пример 2] Получение соединения Int-TG1

Получение соединения Int-TG1-1
К раствору салицилового альдегида (Aldrich, CAS 90-02-8, 148 мг, 1,22 ммоль) и соединению Int-TG(0,5 г, 1,22 ммоль) в ацетонитриле (10 мл) добавляли высушенное молекулярное сито (2,5 г) и Ag2O (845 мг, 3,65 ммоль) в атмосфере N2. После перемешивания при комнатной температуре в течение 1 часа добавляли дистиллированную воду (50 мл) и EA (50 мл × 2). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG1-1 (441 мг, 81%).
1H ЯМР (400 МГц, CDCl3) δ 10,37 (с, 1H), 7,88 (т, J=7,6 Гц, 1H), 7,21 (т, J=7,4 Гц, 1H), 7,14 (т, J=8,4 Гц, 1H), 5,62 (м, 1H), 5,48 (м, 1H), 5,16 (д, J=7,2 Гц, 2H), 4,27-4,23 (м, 1H), 4,18-4,09 (м, 2H), м 2,21 (с, 3H), 2,07 (с, 6H), 2,03 (с, 3H).
Получение соединения Int-TG1-2
К раствору соединения Int-TG1-1 (260 мг, 0,575 ммоль) в ДХМ (3 мл) добавляли m-CPBA (283 мг, 1,149 ммоль)при 0° в атмосфере N2. Через 5 часов смесь концентрировали при пониженном давлении. Затем добавляли EA (50 мл × 2) и водный раствор бикарбоната натрия (30 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении с получением соединения Int-TG1-2 (270 мг, колич.). Соединение Int-TG1-2 напрямую, без очистки, использовали в следующей реакции.
1H ЯМР (400 МГц, CDCl3) δ 8,18 (с, 1H), 7,90 (д, J=8,0 Гц, 1H), 7,64 (д, J=8,0 Гц, 1H), 7,46 (т, J=7,6 Гц, 1H ), 7,15 (д, J=8,4 Гц, 1H), 5,51 (м, 2H), 5,11 (д, J=8,8 Гц, 1H), 5,04 (д, J=8,0 Гц, 1H), 4,24 (м, 1H), 4,16 (м, 1Н), 4,08 (м, 1Н), 2,18 (с, 3Н), 2,09 (с, 3Н), 2,07 (с, 3Н), 2,02 (с, 3Н). ЭИ-МС m/z: 491(M++Na).
Получение соединения Int-TG1-3
К раствору соединения Int-TG1-2 в CHCl3 (3 мл) добавляли гидразин-гидрат (21 мкл, 0,427 ммоль) при 0° в атмосфере N2. После перемешивания при 0° в течение 0,5 часа добавляли EA (30 мл X 2) и 1M водного раствора HCl (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении с получением соединения Int-TG1-3 (161 мг, 86%).
1Н ЯМР (400 МГц, CDCl3) δ 7,03 (т, J=8,0 Гц, 1H), 6,98-6,95 (м, 2H), 6,83 (т, J=7,6 Гц, 1H), 6,02 (с, 1H), 5,47 (д, J=3,2 Гц, 2H), 5,13 (дд, J=10,8, 2,8 Гц, 1H), 4,93 (д, J=7,6 Гц, 1H), 4,26 (м, 1H), 4,19-4,09 (м, 2H), 4,06 (м, 1H), 2,21 (с, 3H), 2,13 (с, 3H), 2,08 (с, 3H), 2,03 (с, 3H). ЭИ-МС m/z: 463(M++Na).
Получение соединения Int-TG1
К раствору соединения Int-TG1-3 (161 мг, 0,366 ммоль) в ДХМ (3 мл) добавляли Et3N (102 мкл, 0,732 ммоль) и TBDMS-OTf (126 мкл, 0,549 ммоль) при 0° в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 2 часов. Затем добавляли ДХМ (30 мл X 2) и 1M водный раствор HCl (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG1 (147 мг, 91%).
1H ЯМР (400 МГц, CDCl3) δ 7,02 (д, J=7,6 Гц, 1H), 6,95-6,84 (м, 3H), 5,48-5,43 (м, 2H), 5,15 (д, J=8,0 Гц, 1H) 5,10 (д, J=10,4 Гц, 1H), 4,21-4,11 (м, 2H), 4,03-3,99 (м, 1H), 2,19 (с, 3H), 2,04 (с, 3H), 2,02 (с, 3H), 2,00 (с, 3Н), 0,99 (с, 9Н), 0,20 (с, 3Н), 0,16 (с, 3Н). ЭИ-МС m/z: 555(M+).
[Пример 3] Получение соединения Int-TG2
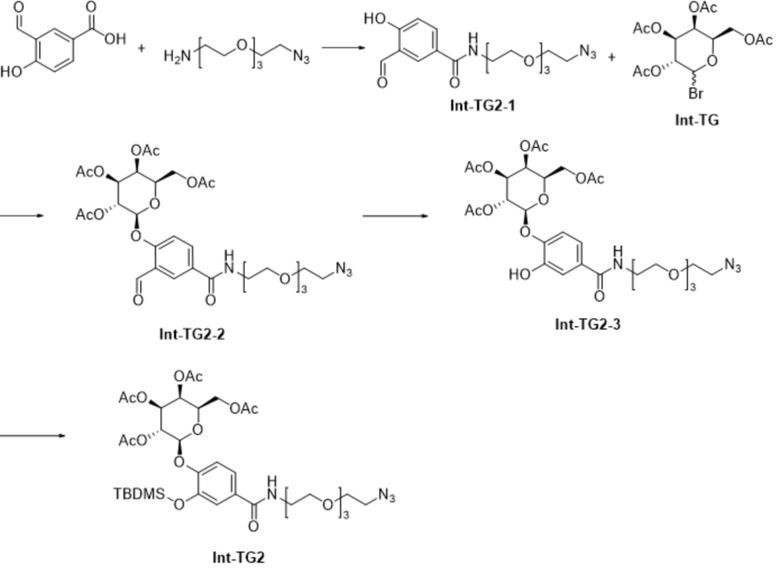
Получение соединения Int-TG2-1
К раствору 3-формил-4-гидроксибензойной кислоты (3 г, 18,06 ммоль) и 11-азидо-3,6,9-триоксаундекан-1-амина (Aldrich, CAS 134179-38-7, 5,98 г, 23,48 ммоль) в ДМФА (20 мл) добавляли EDCI (5,19 г, 27,09 ммоль), HOBt (4,15 г, 27,09 ммоль) и Et3N (10,1 мл, 72,24 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при комнатной температуре в атмосфере N2 в течение ночи. Реакцию гасили EA (60 мл × 2) и лимонной кислотой (60 мл). Органический слой экстрагировали водным раствором бикарбоната натрия (80 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG2-1 (2,56 g, 39%).
1H ЯМР (400 МГц, CDCl3) δ 11,26 (с, 1Н), 9,96 (с, 1Н), 8,16 (с, 1Н), 7,98-7,96 (д, J=8,4 Гц, 1Н), 7,04-7,02 (д, J=9,2 Гц, 1H), 6,91 (с, 1H), 3,68-3,61 (м, 14H), 3,37-3,34 (м, 2H), ЭИ-МС m/z: 367(M+).
Получение соединения Int-TG2-2
К раствору соединения Int-TG2-1 (1,41 г, 3,85 ммоль) и соединению Int-TG (1,74 г, 4,24 ммоль) в безводном ADC (20 мл) добавляли молекулярное сито (8 г) и Ag2O (2,68 г, 11,55 ммоль) при комнатной температуре в атмосфере N2 Смесь перемешивали при комнатной температуре в течение 3 часов, затем фильтровали через целит. Органический слой сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG2-2 (1,88 г, 70%).
1H ЯМР (400 МГц, CDCl3) δ 10,35 (с, 1H), 8,20-8,17 (м, 2H), 7,26 (с, 1H), 7,20-7,18 (д, J=9,2 Гц, 1H), 6,96 (с, 1H), 5,63-5,58 (м, 1H), 5,50-5,49 (м, 1H), 5,23-5,21 (м, 1H), 5,18-5,14 (м, 1H), 4,24-4,14 (м, 3H), 3,69- 3,64 (м, 14H), 3,37-3,35 (м, 2H), 2,21 (с, 3H), 2,08-2,07 (м, 6H), 2,03 (с, 3H). ЭИ-МС m/z: 697(M+).
Получение соединения Int-TG2-3
К раствору соединения Int-TG2-2 (1,69 г, 2,42 ммоль) в ДХМ (15 мл) добавляли m-CPBA (2,4 г, 9,70 ммоль)при 0° в атмосфере N2. После перемешивания в течение 7 часов при 0°С смесь гасили добавлением насыщенного бикарбоната натрия (40 мл × 2). Смесь разделяли и органические слои промывали солевым раствором, сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG2-3 (1,25 g, 76%).
1H ЯМР (400 МГц, CDCl3) δ 7,36-7,33 (м, 2Н), 7,01-6,99 (д, J=8,4 Гц, 1Н), 6,71 (м, 1Н), 6,06 (с, 1Н), 5,49-5,44 ( м, 2Н), 5,15-5,12 (м, 1Н), 4,99-4,97 (д, J=8,0 Гц, 1Н), 4,24-4,09 (м, 3Н), 3,69-3,63 (м, 14Н), 3,37-3,34 ( м, 2H), 2,20 (с, 3H), 2,13 (с, 3H), 2,12 (с, 3H), 2,03 (с, 3H), ЭИ-MCm/z: 685(M+).
Получение соединения Int-TG2
К раствору соединения Int-TG2-3 (750 мг, 1,09 ммоль) в ДХМ (10 мл) добавляли TBDMS-OTf (504 мкл, 2,19 ммоль) и Et3N (458 мкл, 3,29 ммоль) при 0°С в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре, а затем гасили добавлением лимонной кислоты (20 мл). Органический слой промывали солевым раствором (20 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG2 (799 мг, 91%).
1H ЯМР (400 МГц, CDCl3) δ 7,35 (д, J=2,4 Гц, 1H), 7,30 (дд, J=8,4, 2,0 Гц, 1H), 7,02 (д, J=8,0 Гц, 1H), 6,65 (т, J=5,2 Гц, 1H), 5,49-5,44 (м, 2H), 5,20 (д, J=7,6 Гц, 1H), 5,12 (дд, J=10,0, 3,6 Гц, 1H), 4,20-4,11 (м, 2H), 4,06-4,03 (м, 1H), 3,69-3,62 (м, 15H), 3,37 (т, J=5,2 Гц, 2H), 2,19 (с, 3H), 2,05 (с, 3H), 2,02 (с)., 3H), 2,01 (с, 3H), 1,01 (с, 9H), 0,22 (с, 3H), 0,18 (с, 3H). ЭИ-МС m/z: 799(M+).
[Пример 4] Получение соединения Int-TG3

Получение соединения Int-TG3-1
К раствору салицилового альдегида (Aldrich, 200 мг, 1,64 ммоль) и соединения Bg-Br (813 мг, 1,64 ммоль) в ацетонитриле (12 мл) добавляли высушенное молекулярное сито (1,0 г) и Ag2O (1,42 г, 4,92 ммоль). при комнатной температуре. Смесь перемешивали в течение ночи и добавляли дистиллированную воду (50 мл) и EA (50 мл × 2). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG-3-1 (218 мг, 30%).
1H ЯМР (400 МГц, CDCl3) δ 10,35 (с, 1H), 7,86 (дд, J=6,0, 1,6 Гц, 1H), 7,56 (тд, J=7,6, 1,6 Гц, 1H), 7,20 (т, J=7,6 Гц, 1H), 7,13 (д, J=8,8 Гц, 1H), 5,39-5,31 (м, 3H), 5,27-5,25 (м, 1H), 5,24-4,19 (м, 1H), 3,75 (с, 3H), 2,07-2,04 (м, 9H). ЭИ-МС m/z: 461(M++Na).
Получение соединения Int-TG3-2
К раствору соединения Int-TG3-1 (217,6 мг, 0,50 ммоль) в ДХМ (10 мл) добавляли m-CPBA (367,1 мг, 1,50 ммоль) при 0°С в атмосфере. Смесь перемешивали в течение ночи при комнатной температуре и добавляли 40 мл ДХМ. Органический слой промывали насыщенным бикарбонатом натрия (10 мл) и сушили над безводным Na2SO4, фильтровали, концентрировали при пониженном давлении.
Остаток снова растворяли в CHCl3 (5 мл). Затем добавляли гидразин (36,2 мкл, 0,74 ммоль). Через 30 минут добавляли ДХМ (20 мл × 2) и воду (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении, а остаток очищали колоночной хроматографией с получением соединения Int-TG1-3-2 (195 мг, 92%).
1H ЯМР (400 МГц, CDCl3) δ 7,09 (т, J=8,0 Гц, 1H), 7,00-6,95 (м, 2H), 6,83 (тд, J=6,8, 1,6 Гц, 1H), 5,38-5,24 (м, 4H), 4,19-4,13 (м, 1H), 3,75 (с, 3H), 2,06-2,02 (м, 9H). ЭИ-МС m/z: 449(M++Na).
Получение соединения Int-TG3
К раствору соединения Int-TG3-2 (194 мг, 0,46 ммоль) в ДХМ (5 мл) добавляли Et3N (190,8 мкл, 1,37 ммоль) и TBDMS-OTf (209,8 мкл, 0,91 ммоль) при 0°С в атмосфере N2. После перемешивания при 0°С в течение 1 часа добавляли ДХМ (30 мл × 2) и воду (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG3 (188,6 мг, 76%).
1H ЯМР (400 МГц, CDCl3) δ 7,00 (дд, J=6,0, 1,6 Гц, 1H), 6,94-6,88 (м, 2H), 6,84 (дд, J=6,0, 2,0 Гц, 1H), 5,38-5,21 ( м, 5H), 3,72 (с, 3H), 2,03 (д, J=6,8 Гц, 9H), 0,98 (с, 9H), 0,18 (с, 3H), 0,15 (с, 3H). ЭИ-МС m/z: 563(M++Na).
[Пример 5] Получение соединения Int-TG4
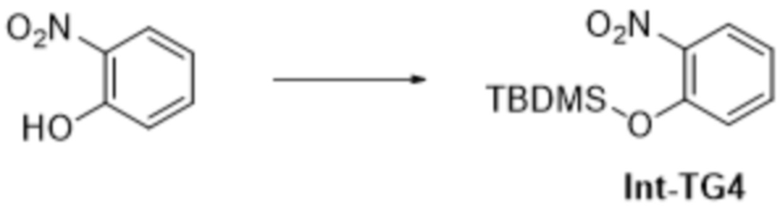
К раствору 2-нитрофенола (500 мг, 3,59 ммоль) в безводном пиридине (20 мл) добавляли TBDMS-Cl (650 мг, 4,31 ммоль) при комнатной температуре в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре и добавляли ДХМ (30 мл × 2) и воду (20 мл). Полученный органический слой промывали 2N водным раствором HCl, сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG4 (410 мг, 94%).
1H ЯМР (400 МГц, CDCl3) δ 7,80 (дд, J=6,8, 0,8 Гц, 1H), 7,43 (т, J=7,2 Гц, 1H), 7,04-6,97 (м, 2H), 1,01 (с, 9H) 0,26 (с, 6H).
[Пример 6] Получение соединения Int-TG5

Получение соединения Int-TG5-1a
К раствору 4-гидроксибензальдегида (1 г, 8,19 ммоль) в ДХМ (3 мл) добавляли Et3N (2,28 мл, 16,38 ммоль) при комнатной температуре в атмосфере N2. Газ SO2F2 вводили через баллон, и смесь перемешивали при комнатной температуре в течение 2 часов. Затем смесь промывали ДХМ (30 мл × 3) и солевым раствором (30 мл), органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG5-1a (790 мг, 63%).
1H ЯМР (400 МГц, CDCl3) δ 10,06 (с, 1H), 8,05 (д, J=8,0 Гц, 2H), 7,55 (д, J=8,8 Гц, 2H).
Получение соединения Int-TG5-1
К раствору соединения Int-TG2 (100 мг, 0,13 ммоль) и соединения Int-TG5-1a (26 мг, 0,13 ммоль) в безводном ACN (3 мл) добавляли DBU (4 мкл, 25 мкмоль). Смесь перемешивали при комнатной температуре в течение 1 часа и промывали дистиллированной водой (10 мл) и EA (10 мл × 2). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG5-1 (103 мг, 94%).
ЭИ-МС m/z: 869(M+).
Получение соединения Int-TG5-2
К раствору соединения Int-TG5-1 (103 мг, 0,12 ммоль) в ТГФ (8 мл) добавляли NaBH4 (9 мг, 0,24 ммоль) при 0°С в атмосфере N2. После перемешивания при комнатной температуре в течение 2 часов добавляли дистиллированную воду (10 мл) и EA (10 мл × 2). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении с получением соединения Int-TG5-2 (101 мг, 98%).
ЭИ-МС m/z: 871(M+).
Получение соединения Int-TG5
К раствору соединения Int-TG5-2 (47 мг, 54 мкмоль) в ДМФА (2 мл) добавляли бис(4-нитрофенил)карбонат (25 мг, 81 мкмоль) и DIPEA (14 мкл, 81 мкмоль) при комнатной температуре в атмосфере азота. Смесь перемешивали в течение ночи при комнатной температуре. Затем добавляли дистиллированную воду (10 мл) и EA (10 мл × 2), органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG5 (53 мг, 94%).
ЭИ-МС m/z: 1036(M+).
[Пример 7] Получение соединения Int-TG6
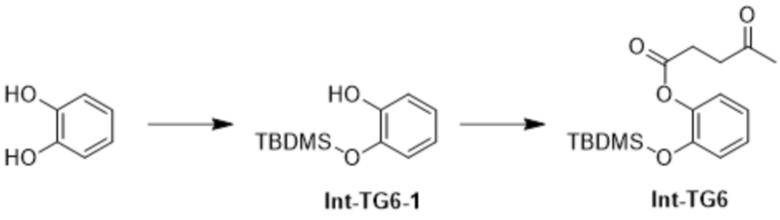
Получение соединения Int-TG6-1
К раствору 1,2-дигидроксибензола (1,0 г, 9,08 ммоль) в ДМФА (15 мл) добавляли TBDMS-Cl (1,64 г, 10,88 ммоль) и имидазол (1,24 г, 18,21 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 2 часов. Добавляли EA (30 мл × 2) и дистиллированную воду (20 мл). Полученный органический слой снова промывали солевым водным раствором, сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG6-1 (1,27 g, 64%).
1H ЯМР (400 МГц, CDCl3) δ 6,94 (д, J=8,0 Гц, 1H), 6,89-6,82 (м, 2H), 6,76 (т, J=7,6 Гц, 1H), 5,48 (с, 1H), 1,02 (с, 9Н), 0,28 (с, 6Н).
Получение соединения Int-TG6
К раствору Int-TG6-1 (300 мг, 1,34 ммоль) и левулиновой кислоты (310,5 мг, 2,67 ммоль) в 1,4-диоксане (12 мл) добавляли DCC (551,7 мг, 2,67 ммоль) и DMAP (13,07 мг, 0,11 ммоль). Смесь перемешивали при комнатной температуре в течение 3 часов. Затем добавляли дистиллированную воду (50 мл) и EA (50 мл × 2) и органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG6 (380,1 мг, 88%).
1H ЯМР (400 МГц, CDCl3) δ 7,09 (тд, J=6,0, 1,6 Гц, 1H), 7,03 (дд, J=6,4, 1,6 Гц, 1H), 6,95-6,88 (м, 2H), 2,84 (с, 4H). ), 2,22 (с, 3Н), 0,98 (с, 9Н), 0,20 (с, 6Н).
[Пример 8] Получение соединения Int-TG7
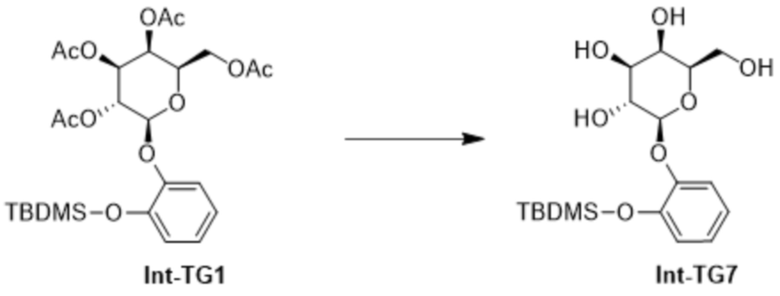
Соединение Int-TG1 (80 мг, 0,14 ммоль) растворяли в безводном метаноле (2 мл), добавляли к нему K2CO3 (99,7 мг, 0,72 ммоль) при 0°С. Смесь перемешивали при 0°С в течение 1 часа. Остаток разбавляли ЕА (10 мл × 2), органический слой промывали 1N водной HCl (2 мл) и водой (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток подвергали препаративной ТСХ для получения соединения Int-TG7 (17,4 мг, 31%).
1H ЯМР (400 МГц, CDCl3) δ 7,12 (д, J=8,0 Гц, 1H), 6,95-6,85 (м, 3H), 4,74 (д, J=7,2 Гц, 1H), 4,05 (д, J=3,2 Гц), 1H), 3,97 (дд, J=6,0, 5,6 Гц, 1H), 3,90-3,85 (м, 2H), 3,68 (дд, J=6,8, 2,8 Гц, 1H), 3,63 (т, J=5,6 Гц, 1H), 3,48 (с, 1H), 1,03 (с, 9H), 0,20 (д, J=12,0 Гц, 6H). ЭИ-МС m/z: 409(M++Na).
[Пример 9] Получение соединения Int-TG8

Получение соединения Int-TG8-1
К раствору катехола (500 мг, 0,4,54 ммоль) и 2-нитробензилбромида (333,5 мг, 1,54 ммоль) в ацетоне (30 мл) добавляли K2CO3 (401,6 мг, 2,91 ммоль). Смесь кипятили с обратным холодильником в течение 15 часов. После охлаждения до комнатной температуры смесь концентрировали при пониженном давлении и разбавляли ЕА (50 мл × 2) и водным раствором 1N NaOH (20 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG8-1 (300,3 мг, 79%).
1H ЯМР (400 МГц, CDCl3) δ 8,19 (дд, J=6,8, 1,2 Гц, 1H), 7,75 (д, J=7,6 Гц, 1H), 7,69 (тд, J=7,2, 1,2 Гц, 1H), 7,53 (тд, J=6,8, 1,6 Гц, 1H), 6,99 (дд, J=7,2, 1,2 Гц, 1H), 6,93 (тд, J=5,2, 2,4 Гц, 1H), 6,85-6,79 (м, 2H), 5,64 (с, 1Н), 5,58 (с, 2Н).
Получение соединения Int-TG8
К раствору соединения Int-TG8-1 (300 мг, 1,22 ммоль) в ДХМ (5 мл) добавляли Et3N (342 мкл, 2,50 ммоль) и TBDMS-OTf (421,8 мкл, 1,83 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 3 часов и разбавляли ДХМ (30 мл × 2) и водным раствором 2N HCl (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG8 (410 мг, 94%).
1H ЯМР (400 МГц, CDCl3) δ 8,19 (дд, J=6,8, 1,2 Гц, 1H), 8,01 (дд, J=8,0, 0,8 Гц, 1H), 7,67 (тд, J=6,4, 1,2 Гц, 1H) 7,48 (т, J=7,6 Гц, 1H), 6,92-6,87 (м, 4H), 5,49 (с, 2H), 1,01 (с, 9H), 0,18 (с, 6H).
[Пример 10] Получение соединения Int-TG9
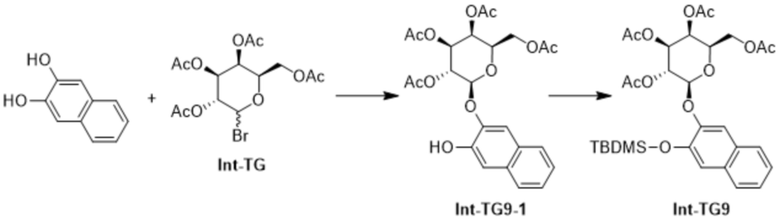
Получение соединения Int-TG9-1
К раствору 2,3-дигидроксинафталина (930 мг, 5,83 ммоль) и соединения Int-TG (1,0 г, 2,43 ммоль) в ацетоне (10 мл) добавляли NaOH (230 мг, 5,75 ммоль) при комнатной температуре в атмосфере азота. Смесь перемешивали в течение ночи при комнатной температуре и концентрировали при пониженном давлении. Смесь разбавляли дистиллированной водой (20 мл) и EA (30 мл × 2). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG9-1 (560 мг, 47%).
1H ЯМР (400 МГц, CDCl3) δ 7,67 (т, J=9,2 Гц, 2H), 7,39-7,29 (м, 4H), 6,07 (с, 1H), 5,53-5,50 (м, 2H), 5,18 (дд, J=7,2, 3,6 Гц, 1H), 5,10 (д, J=7,6 Гц, 1H), 4,31-4,11 (м, 3H), 2,21 (с, 3H), 2,12 (д, J=8,8 Гц, 6H), 2,05 (с, 3Н).
Получение соединения Int-TG9
К раствору соединения Int-TG9-1 (200 мг, 0,41 ммоль) в ДХМ (7 мл) добавляли TBDMS-OTf (0,12 мл, 0,53 ммоль) и Et3N (0,11 мл, 0,82 ммоль) при 0°С в атмосфере N2. После перемешивания в течение ночи при комнатной температуре смесь разбавляли ДХМ (30 мл × 2) и экстрагировали дистиллированной водой (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG9 (230 мг, 96%).
1H ЯМР (400 МГц, CDCl3) δ 7,67-7,63 (м, 2Н), 7,36-7,33 (м, 3Н), 7,20 (с, 1Н), 5,52 (дд, J=8,4, 2,0 Гц, 1Н), 5,47 ( д, J=3,2 Гц, 1H), 5,31 (д, J=8,0 Гц, 1H), 5,15 (дд, J=6,8, 3,6 Гц, 1H), 4,23-4,13 (м, 3H), 2,20 (с, 3H), 2,05 (с, 3H), 2,02 (д, J=3,6 Гц, 6H), 1,03 (с, 9H), 0,26 (с, 3H), 0,22 (с, 3H).
[Пример 11] Получение соединения Int-TG10
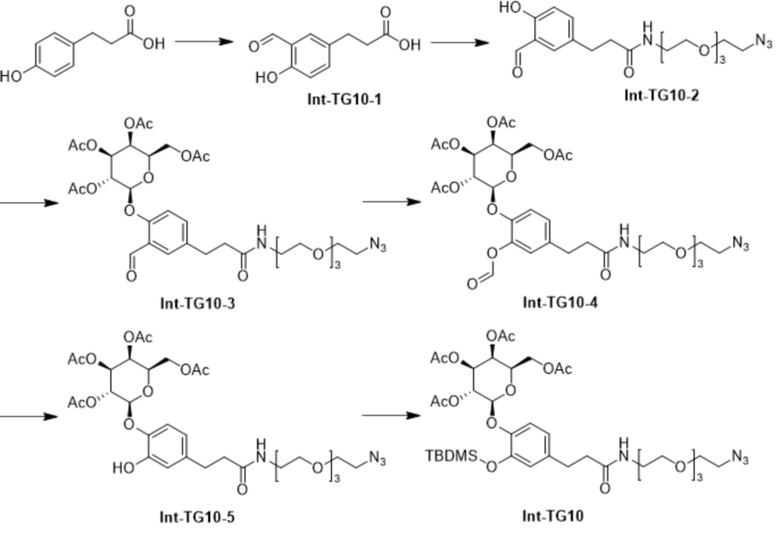
Получение соединения Int-TG10-1
К раствору 3-(4-гидроксифенил)пропионовой кислоты (500 мг, 3,01 ммоль) в CHCl3 (10 мл) добавляли 4 М NaOH (7,5 мл, 30 ммоль), а затем кипятили с обратным холодильником в течение 6 часов. После завершения реакции смесь подкисляли 4 М HCl и концентрировали для удаления CHCl3. EA (30 мл × 3), H2O (20 мл) и солевой раствор (20 мл) добавляли для проведения экстракции, а полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG10-1 (408 мг, продукт: SM=4:6 методом ВЭЖХ).
1H ЯМР (400 МГц, CDCl3) δ 10,90 (с, 1H), 9,87 (с, 1H), 7,41-7,38 (м, 2H), 6,94 (д, J=9,6 Гц, 1H), 2,96 (т, J=7,4 Гц, 2H), 2,69 (т, J=7,4 Гц, 2H).
Получение соединения Int-TG10-2
К раствору соединения Int-TG10-1 (408 мг, 2,1 ммоль) в ДМФА (10 мл) добавляли NHS (363 мг, 3,15 ммоль) и EDCI (604 мг, 3,15 ммоль) и перемешивали в течение ночи при комнатной температуре. Затем добавляли 11-азидо-3,6,9-триоксаундекан-1-амин (636 мг, 2,5 ммоль), растворенный в ДМФА (3 мл), и DIPEA (3,66 мл, 21 ммоль) и перемешивали при комнатной температуре в течение 1 часа. После завершения реакции смесь подкисляли 4 М HCl, разбавляли EA (30 мл × 5) и промывали H2O (30 мл) и солевым раствором (30 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG10-2 (288 мг, чистота 50% методом ВЭЖХ).
ЭИ-МС m/z: 395(M+).
Получение соединения Int-TG10-3
К раствору соединения Int-TG10-2 (288 мг, 0,73 ммоль) и соединения Int-TG (303 мг, 0,74 ммоль) в ACN (10 мл) добавляли молекулярное сито (1,5 г) в атмосфере N2. После перемешивания в течение 10 минут при комнатной температуре к нему добавляли Ag2O (508 мг, 2,19 ммоль). Смесь перемешивали при комнатной температуре в течение 3 часов и разбавляли водой (5 мл) с последующей фильтрацией с использованием целита. Фильтрат промывали ЕА (20 мл × 2), Н2О (20 мл) и солевым раствором (20 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG10-3 (195 мг).
ЭИ-МС m/z: 725(M+).
Получение соединения Int-TG10-4
К раствору соединения Int-TG10-3 (195 мг, 0,27 ммоль) в ДХМ (5 мл) добавляли 70% m-CPBA (133 мг, 0,54 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при 0°С в течение 3 часов. Затем к нему добавляли 70% m-CPBA (66 мг, 0,27 ммоль) и смесь перемешивали в течение ночи при 0°С. Реакцию гасили насыщенным NaHCO3 (20 мл × 3) и разбавляли ДХМ (20 мл). Органический слой промывали солевым раствором (20 мл) и сушили над безводным Na2SO4, фильтровали, концентрировали при пониженном давлении. Соединение Int-TG10-4 использовали непосредственно в следующей реакции без очистки (199 мг, неочищенный).
ЭИ-МС m/z: 741(M+).
Получение соединения Int-TG10-5
К раствору соединения Int-TG10-4 (199 мг, 0,27 ммоль) в CHCl3 (4 мл) добавляли CHCl3 (133 мг, 0,54 ммоль) при 0°C в атмосфере N2. После перемешивания при комнатной температуре в течение 30 минут смесь гасили EA (20 мл) и насыщенной лимонной кислотой (20 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG10-5 (146 мг).
ЭИ-МС m/z: 713(M+).
Получение соединения Int-TG10
К раствору соединения Int-TG10-5 (146 мг, 0,21 ммоль) в ДМФА (2 мл) добавляли TEA (133 мкл, 0,62 ммоль) и TBDMS-OTf (94 мкл, 0,41 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при 0°С в течение 20 минут и продолжали перемешивать при комнатной температуре в течение 3 часов. Смесь экстрагировали ЕА (20 мл), насыщенной лимонной кислотой (20 мл) и солевым раствором (30 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с последующим очисткой препаративной ТСХ с получением соединения Int-TG10 (32 мг, 19%).
ЭИ-МС m/z: 827(M+).
[Пример 12] Получение соединения IntA-Q1

К раствору Boc-Tyr-OMe (300 мг, 1,02 ммоль) в ДХМ (3 мл) добавляли Et3N (212 мкл, 1,52 ммоль) при комнатной температуре в атмосфере N2. Газ SO2F2 вводили через баллон, и смесь перемешивали при комнатной температуре в течение 2 часов в атмосфере SO2F2. Смесь экстрагировали ДХМ (30 мл × 3) и солевым раствором (30 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q1 (363 мг, 95%).
1H ЯМР (400 МГц, CDCl3) δ 7,26 (с, 4H), 5,03 (д, J=8,0 Гц, 1H), 4,62 (м, 1H), 3,73 (с, 3H), 3,21 (дд, J=13,2, 4,8 Гц, 1H), 3,07 (дд, J=13,2, 6,0 Гц, 1H), 1,41 (с, 9H). ЭИ-МС m/z: 400(M++Na).
[Пример 13] Получение соединения IntA-Q2

Получение соединения IntA-Q2-1
К раствору гуанозина (1 г, 3,53 ммоль) в ДМФА (30 мл) добавляли имидазол (1,92 г, 28,45 ммоль) и TBDMS-Cl (3,193 г, 21,18 ммоль) при комнатной температуре. Смесь перемешивали в течение ночи при комнатной температуре и экстрагировали ЕА (100 мл × 3), Н2О (100 мл), NH4Cl (100 мл) и солевым раствором (100 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q2-1 (1,56 g, 70%).
1H ЯМР (400 МГц, CDCl3) δ 12,05 (с, 1Н), 7,89 (с, 1Н), 6,40 (уш. c, 1Н), 5,82-5,79 (м, 1Н), 4,44-4,38 (м, 1Н), 4,29- 4,26 (м, 1H), 4,10-4,09 (м, 1H), 4,02-3,99 (м, 1H), 3,80-3,77 (м, 1H), 0,96 (с, 9H), 0,92 (с, 9H), 0,87 ( с, 9Н), 0,14 (с, 3Н), 0,13 (с, 3Н), 0,09 (с, 3Н), 0,08 (с, 3Н), 0,02 (с, 3Н), -0,02 (с, 3Н). ЭИ-МС m/z: 627(M+).
Получение соединения IntA-Q2-2
К раствору 4-гидроксибензилового спирта (1,00 г, 8,06 ммоль) в ДХМ (40 мл) и H2O (40 мл) добавляли Et3N (1,70 мл, 12,085 ммоль) при комнатной температуре в атмосфере N2. Газ SO2F2 вводили через баллон, и смесь перемешивали при комнатной температуре в течение 5 часов. После завершения реакции смесь концентрировали при пониженном давлении и остаток очищали колоночной хроматографией с получением соединения IntA-Q2-2 (711 мг, 43%).
1H ЯМР (400 МГц, CDCl3) δ 7,49 (д, J=8,4 Гц, 2H), 7,34 (д, J=8,0 Гц, 2H), 4,76 (д, J=6,0 Гц, 2H), 1,80 (т, J=4,2 Гц, 1H).
Получение соединения IntA-Q2
К раствору соединения IntA-Q2-1 (350 мг, 0,56 ммоль) в ТГФ (10 мл) добавляли соединение IntA-Q2-2 (253 мг, 1,23 ммоль) и PPh3 (235 мг, 0,90 ммоль) при комнатной температуре. в атмосфере N2. После охлаждения смеси до 0°С по каплям добавляли DEAD (0,41 мл, 0,9 ммоль) и перемешивали при 0°С в течение 3 часов. Смесь экстрагировали EA (30 мл × 3), Н2О (30 мл) и солевым раствором (30 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток отделяли и очищали один раз препаративной ВЭЖХ, а затем очищали колоночной хроматографией с получением соединения IntA-Q2 (62 мг, 14%).
1H ЯМР (400 МГц, CDCl3) δ 8,00 (с, 1H), 7,62 (д, J=8,4 Гц, 2H), 7,33 (д, J=8,4 Гц, 2H), 5,91 (д, J=5,2 Гц, 1H ), 5,57 (с, 2H), 4,82-4,78 (м, 2H), 4,52-4,50 (м, 1H), 4,30-4,28 (м, 1H), 4,12-4,08 (м, 1H), 3,98 (дд, J=11,2, 3,6 Гц, 1H), 3,93 (дд, J=11,2, 2,4 Гц, 1H), 0,94 (с, 9H), 0,93 (с, 9H), 0,82 (с, 9H), 0,13 (с, 3H) 0,12 (с, 3Н), 0,10 (с, 3Н), 0,09 (с, 3Н), -0,02 (с, 3Н), -0,15 (с, 3Н). ЭИ-МС m/z: 815(M+).
[Пример 14] Получение соединения IntA-Q3

Получение соединения IntA-Q3
К раствору гидрохлорида 3-пиридилуксусной кислоты (1,0 г, 5,76 ммоль) в ТГФ (20 мл) добавляли ЛАГ (1,1 г, 28,8 ммоль) при 0°С в атмосфере N2. Смесь нагревали до комнатной температуры и кипятили с обратным холодильником в течение 24 часов. Смесь гасили добавлением метанола (10 мл) и воды (20 мл). Водный слой подвергали экстракции эфиром (50 мл × 2), а полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-Q3a (396,3 мг, 56%).
1H ЯМР (400 МГц, CDCl3) δ 8,48-8,45 (м, 2Н), 7,58-7,56 (м, 1Н), 7,25-7,22 (м, 2Н), 3,89 (т, J=6,8 Гц, 2Н), 2,87 (т J=6,8 Гц, 2H). ЭИ-МС m/z: 124(M++1).
Получение соединения Int-Q3b
Раствор соединения Int-Q3a (260 мг, 2,11 ммоль) и CDI (684,6 мг, 4,22 ммоль) в ДХМ (5 мл) перемешивали в течение ночи при 50°С в атмосфере N2. После завершения реакции смесь охлаждали до комнатной температуры с последующей экстракцией ДХМ (20 мл × 2) и водой (10 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-Q3b (296,5 мг, 65%).
1H ЯМР (400 МГц, CDCl3) δ 8,53 (дд, J=3,6, 1,6 Гц, 2H), 8,08 (с, 1H), 7,59-7,57 (м, 1H), 7,37 (с, 1H), 7,29-7,26 ( м, 1H), 7,06 (с, 1H), 4,63 (т, J=6,8 Гц, 2H), 3,12 (т, J=6,8 Гц, 1H). ЭИ-МС m/z: 218(M++1).
Способ получения соединения IntA-Q3
К раствору соединения Int-Q3b (47,6 мг, 0,22 ммоль) и соединения IntA-Q2-2 (45,2 мг, 0,22 ммоль) в ТГФ (400 мкл) добавляли NaH (2,6 мг, 0,07 ммоль) при 0°С в атмосфере N2. После перемешивания при 0°С в течение 30 минут смесь экстрагировали диэтиловым эфиром (10 мл × 2) и водой (5 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-Q3 (296,5 мг, 65%).
1H ЯМР (400 МГц, CDCl3) δ 8,50-8,49 (м, 2H), 7,56-7,54 (м, 1H), 7,48 (д, J=8,8 Гц, 2H), 7,35 (д, J=8,8 Гц, 2H) 7,24-7,22 (м, 1H), 5,30 (с, 2H), 4,38 (т, J=6,4 Гц, 2H), 3,00 (т, J=6,8 Гц, 1H). ЭИ-МС m/z: 356(M++1).
[Пример 15] Получение соединения IntA-Q4

Соединение IntA-Q4 (178,2 мг, 0,86 ммоль) получали из соединения IntA-Q2-2 (178,2 мг, 0,86 ммоль) и гидрохлорида 3-пиридилуксусной кислоты (100 мг, 0,58 ммоль) аналогичным способом получения Int-TG5-1а, приведенном в примере 6. (161 мг, 86%).
1H ЯМР (400 МГц, CDCl3) δ 8,55-8,54 (м, 2H), 7,65-7,62 (м, 1H), 7,58 (д, J=8,4 Гц, 2H), 7,33 (д, J=8,4 Гц, 2H) 7,29-7,27 (м, 1Н), 5,20 (с, 2Н), 3,70 (с, 2Н). ЭИ-МС m/z: 326(M++1).
[Пример 16] Получение соединения IntA-Q5

Получение соединения IntB-Q5-1
Соединение IntA-Q2-2 (230 мг, 1,12 ммоль) растворяли в эфире (10 мл) и добавляли 1M PBr3 (446 мкл, 0,45 ммоль), растворенный в ДХМ, и перемешивали при 0°C в течение 2 часов. После завершения реакции добавляли эфир (50 мл) и водный раствор бикарбоната натрия (50 мл) для экстракции. Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении с получением соединения IntB-Q5-1 (201 мг, 67%).
1H ЯМР (400 Гц, CDCl3) δ 7,51 (д, J=8,4 Гц, 2H), 7,33 (д, J=8,4 Гц, 2H), 4,49 (с, 2H).
Получение соединения IntA-Q5-1
Тимидин (100 мг, 0,41 ммоль) и 60% NaH (25 мг, 0,62 ммоль) растворяли в ДМФА (3 мл) в атмосфере азота, и смесь охлаждали до 0°С. Соединение IntB-Q5-1 (167 мг, 0,62 ммоль) добавляли при 0°С и смесь перемешивали при той же температуре в течение 1 часа. После завершения реакции добавляли ЕА (30 мл × 3) и водный раствор лимонной кислоты (30 мл) для проведения экстракции, и полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q5-1 (79 мг, 45%).
1H ЯМР (400 МГц, ДМСО-d6) δ 7,84 (с, 1H), 7,54 (д, J=8,8 Гц, 2H), 7,47 (д, J=8,8 Гц, 2H), 6,20 (т, J=6,8 Гц), 1H), 5,25 (д, J=4 Гц, 1H), 5,07-5,02 (м, 3H), 4,28-4,22 (м, 1H), 3,78-3,76 (м, 1H), 3,64-3,54 (м, 2H ), 2,16-2,11 (м, 2H), 1,84 (с, 3H). ЭИ-МС m/z: 431(M+).
Получение соединения IntA-Q5-2
Соединение IntA-Q5-1 (40 мг, 0,09 ммоль) и соединение Int-TG1 (62 мг, 0,11 ммоль) растворяли в ACN (3 мл) в атмосфере азота, а затем добавляли BEMP (14 мкл, 0,05 ммоль). Смесь перемешивали в течение ночи при комнатной температуре, далее добавляли DBU (7 мкл, 0,05 ммоль) и смесь перемешивали при той же температуре в течение 1 часа. После завершения реакции добавляли EA (20 мл × 3), водный раствор лимонной кислоты (20 мл) и солевой раствор (20 мл) для проведения экстракции, и полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q5-2 (26 мг, 33%).
ЭИ-МС m/z: 851(M+).
Получение соединения IntA-Q5
Соединение IntA-Q5-2 (16 мг, 0,02 ммоль) растворяли в МеОН (2 мл) в атмосфере азота и затем охлаждали до 0°С. K2CO3 (13 мг, 0,09 ммоль) добавляли при 0°С и смесь перемешивали при той же температуре в течение 1 часа. После завершения реакции реакционный раствор подвергали препаративной ВЭЖХ с получением соединения IntA-Q5 (10,3 мг, 80%).
ЭИ-МС m/z: 705(M++Na).
[Пример 17] Получение соединения IntA-Q6
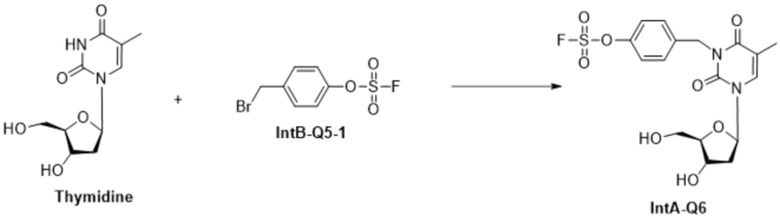
60% NaH (25 мг, 0,62 ммоль) добавляли к перемешиваемому раствору тимидина (100 мг, 0,41 ммоль) в ДМФА (3мл) в атмосфере N2. Смесь охлаждали до 0°С и добавляли соединение IntB-Q5-1 (167 мг, 0,62 ммоль). Смесь перемешивали в течение 1 часа. После завершения реакции реакцию гасили добавлением EA (30 мл × 3) и насыщенной лимонной кислоты (30 мл). Полученный органический слой предназначался для получения соединения IntA-Q5-1 (79 мг, 45%).
[Пример 18] Получение соединения IntB-Q1
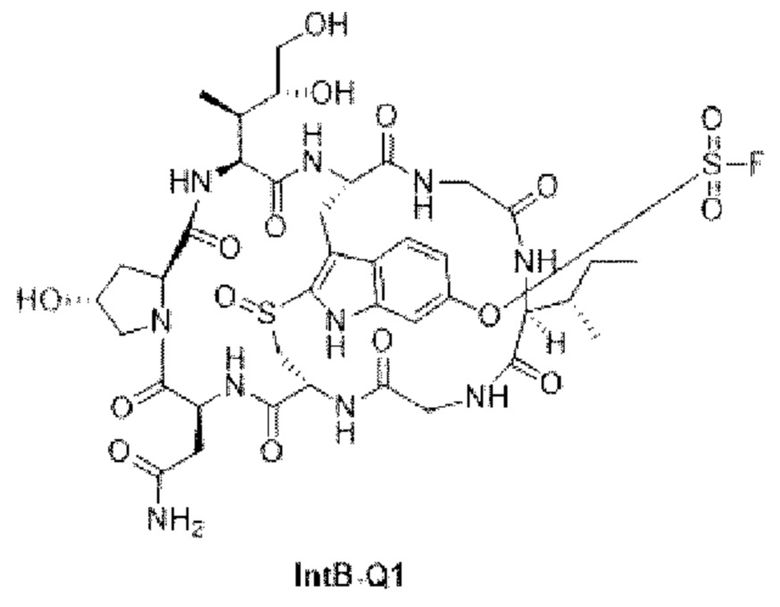
IntB-Q1 (19,5 мг, 89%) получали из аманитина (20 мг, 0,022 ммоль) аналогичным способом получения соединения Int-TG5-1a, приведенном в примере 6.
ЭИ-МС m/z: 1002(M+).
[Пример 19] Получение соединения IntB-Q3

IntB-Q3 (19,5 мг, 89%) получали из SN-38 (300 мг, 1,02 ммоль) аналогичным способом получения соединения Int-TG5-1a, приведенном в примере 6. Остаток очищали колоночной хроматографией с получением соединения IntB-Q3 (340 мг, 94%).
1H ЯМР (400 МГц, CDCl3) δ 8,60 (д, J=2,4 Гц, 1H), 8,39 (д, J=9,2 Гц, 1H), 8,09 (дд, J=9,2, 2,4 Гц, 1H), 7,37 (с, 1H), 6,56 (с, 1H), 5,45 (с, 2H), 5,38 (с, 2H), 3,25 (м, 2H), 1,91-1,84 (м, 2H), 1,32 (т, J=7,6 Гц, 3H), 0,89 (т, J=6,8 Гц, 3H). ЭИ-МС m/z: 475(M+).
[Пример 20] Получение соединения IntB-Q4
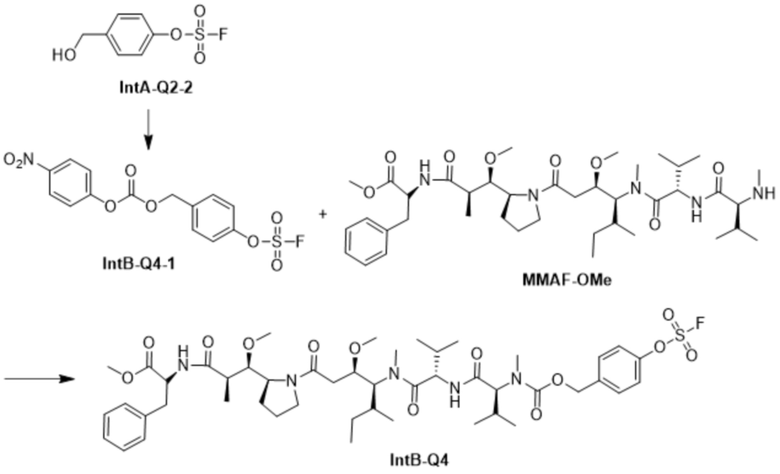
Получение соединения IntB-Q4-1
К раствору соединения IntA-Q2-2 (110 мг, 0,53 ммоль) в ДМФА (3 мл) добавляли бис(4-нитрофенил)карбонат (179 мг, 0,59 ммоль) и DIPEA (139 мкл, 0,80 ммоль) при комнатной температуре. После перемешивания в течение 15 часов смесь экстрагировали дистиллированной водой (10 мл) и EA (10 мл × 2). Органический слой промывали солевым раствором (10 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q4-1 (184 мг, 93%).
1H ЯМР (400 МГц, CDCl3) δ 8,29-8,27 (д, J=8,4 Гц, 2H), 7,58-7,56 (д, J=8,8 Гц, 2H), 7,41-7,38 (м, 4H), 5,32 (с, 2H).
Получение соединения IntB-Q4
Соединение IntB-Q4-1 (36 мг, 0,097 ммоль) и MMAF-OMe (80 мг, 0,107 ммоль), которое получали способом, аналогичным способу, описанному в ChemPharmBull, 1995, 43 (10), 1706-1718, растворяли в ДМФА (1 мл) при комнатной температуре в атмосфере азота. Затем туда добавляли HOBt (3 мг, 0,019 ммоль), DIPEA (19 мкл, 0,107 ммоль) и пиридин (330 мкл) и перемешивали в течение ночи. pH смеси доводили до 2-3 с помощью 1N HCl, а затем разбавляли дистиллированной водой (8 мл) и EA (8 мл X 2). Органический слой промывали солевым раствором (12 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q4 (62 мг, 65%).
ЭИ-МС m/z: 979(M+).
[Пример 21] Получение соединения IntB-Q5

Получение соединения IntB-Q5-2a
К раствору соединения метил 4-гидроксибензоата (3,00 г, 19,72 ммоль) в 12% водном растворе NaOH (20 мл) добавляли 40% водный раствор формальдегида (20 мл) при комнатной температуре в атмосфере N2. Смесь перемешивали при 50°С в течение 3 дней. После завершения реакции смесь экстрагировали EA (200 мл) и насыщенным NH4Cl (200 мл). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q5-2a (2,30 г, 55%).
1H ЯМР (400 Гц, ДМСО-d6) δ 7,84 (с, 2Н), 4,56 (с, 4Н), 3,80 (с, 3Н).
Получение соединения IntB-Q5-2
К раствору соединения IntB-Q5-1 (300 мг, 1,12 ммоль) и соединения IntB-Q5-2a (237 мг, 1,12 ммоль) в ДМФА (10 мл) добавляли K2CO3 (308 мг, 2,23 ммоль) при комнатной температуре в атмосфере N2. После перемешивания в течение 6 часов смесь разбавляли ЕА (100 мл) и промывали 2N водным раствором HCl (30 мл). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q5-2 (140 мг, 32%).
1H ЯМР (400 МГц, CDCl3) δ 8,07 (с, 2H), 7,58 (д, J=8,4 Гц, 2H), 7,39 (д, J=8,4 Гц, 2H), 5,07 (с, 2H), 4,73 (с, 4Н), 3,91 (с, 3Н).
Получение соединения IntB-Q5-3
К раствору соединения IntB-Q5-2 (68,8 мг, 1,12 ммоль) в ТГФ (2 мл) добавляли 4 М LiBH4 (3,8 мл, 15,20 ммоль), растворенный в ТГФ при комнатной температуре. Смесь перемешивали в течение 19 часов и добавляли ЕА (50 мл). Органический слой промывали насыщенным NH4Cl (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q5-3 (23 мг, 36%).
1H ЯМР (400 МГц, CDCl3+CD3OD) δ 7,59 (д, J=8,8 Гц, 2H), 7,38 (д, J=8,0 Гц, 2H), 7,32 (с, 2H), 4,94 (с, 2H), 4,65 (с, 4Н), 4,56 (с, 2Н).
Получение соединения IntB-Q5-4
К раствору соединения IntB-Q5-3 (33 мг, 0,09 ммоль) в ТГФ (4 мл) добавляли 4-нитрофенилхлорформиат (536 мг, 2,66 ммоль) и пиридин (0,20 мл, 2,66 ммоль) при 0°С в атмосфере N2. Смесь перемешивали в течение 3 часов и разбавляли EA (50 мл). Органический слой промывали 2N водного HCl (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q5-4 (57 мг, 72%).
1H ЯМР (400 МГц, CDCl3) δ 8,27 (д, J=8,8 Гц, 6H), 7,68 (с, 2H), 7,64 (д, J=8,0 Гц, 2H), 7,43-7,34 (м, 8H), 5,41 (с, 4Н), 5,33 (с, 2Н), 5,13 (с, 2Н).
Получение соединения IntB-Q5
К раствору соединения IntB-Q5-4 (55 мг, 0,06 ммоль) и MMAF-OMe (142 мг, 0,19 ммоль) в ДМФА (3 мл) добавляли HOBt (24 мг, 0,16 ммоль), пиридин (1,5 мл) и DIPEA (55 мкл, 0,32 ммоль) при комнатной температуре в атмосфере N2. Смесь перемешивали в течение 15 часов и разбавляли ЕА (100 мл). Органический слой промывали 2N водной HCl (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении с последующим разделением и очисткой с использованием препаративной ВЭЖХ с получением соединения IntB-Q5 (92 мг, 54%).
ЭИ-МС m/z: 2689(M+).
[Пример 22] Получение соединения IntB-Q6

К раствору β-эстрадиола (300 мг, 1,10 ммоль) в ДХМ (3 мл), H2O (2 мл) и ДМФА (2 мл) добавляли TEA (230 мкл, 1,65 ммоль) в атмосфере азота. Смесь перемешивали в течение ночи при комнатной температуре, при введении газа SO2F2. После завершения реакции было подтверждено, что продукт и исходный материал присутствовали в соотношении 1: 1 методом ВЭЖХ, а затем препаративной ВЭЖХ с получением соединения IntB-Q6 (было получено 120 мг, 31%, 134 мг исходного материала).
1H ЯМР (400 Гц, ДМСО-d6) δ 7,45 (д, J=8,8 Гц, 1H), 7,29-7,24 (м, 2H), 5,01 (уш. c, 1H), 4,93-4,89 (м, 1H), 3,52 (т, J=8,4 Гц, 1H), 2,32-2,16 (м, 2H), 1,93-1,77 (м, 3H), 1,63-1,54 (м, 1H), 1,47-1,07 (м, 8H), 0,66 (с, 3H). ЭИ-МС m/z: 378 (M++Na).
[Пример 23] Получение соединения IntB-Q7

Комбретастатин А4 (18 мг, 0,057 ммоль) растворяли в ДХМ (3 мл) в атмосфере азота, добавляли TEA (88 мкл, 0,57 ммоль) и смесь перемешивали при комнатной температуре в течение 3 часов, при введении газа SO2F2. После завершения реакции добавляли насыщенный водный раствор лимонной кислоты (6 мл) и ДХМ (6 мл), чтобы экстрагировать органический слой, и органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q7 (22 мг, 97%).
ЭИ-МС m/z: 399(M+).
[Пример 24] Получение соединения FA-Int
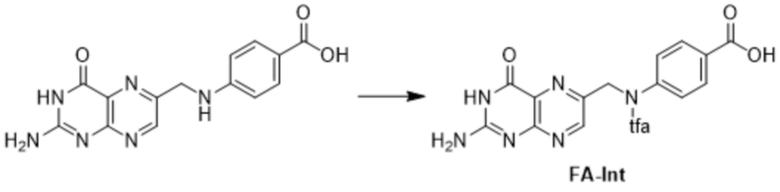
Соединение FA-Int было получено путем проведения реакции аналогичным способом, описанным в публикации заявки на патент США № 20070276018.
[Пример 25] Получение соединения IntC-L-1

Получение соединения IntCl-L-1a
К раствору 2,2- (этилендиокси)бис(этиламина) (50 г, 337,4 ммоль) в ДХМ (300 мл) добавляли Boc2O (14,7 г, 67,47 ммоль), растворенный в ДХМ (200 мл) в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре и гасили водой (500 мл) и солевым раствором (150 мл × 3). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. После концентрирования соединение IntCl-L-1a использовали непосредственно в следующей реакции без очистки (13,01 г, 78%).
1H ЯМР (400 МГц, CDCl3) δ 5,20 (с, 1H), 3,62-3,62 (м, 4H), 3,55-3,51 (м, 4H), 3,35-3,25 (м, 2H), 2,90-2,87 (м, 2H). ), 1,45 (с, 9H).
Получение соединения IntCl-L-1b
К раствору соединения IntCl-L-1a (6 г, 24,16 ммоль) и z-L-Glu-OMe (5,94 г, 20,13 ммоль) в ДМФА (30 мл) добавляли PyBOP (15,72 г, 30,20 ммоль) и DIPEA (10,52). мл, 60,39 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 2 часов. EA (20 мл × 6), H2O (20 мл) и солевой раствор (200 мл) добавляли к смеси. Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntCl-L-1b (10,6 г, колич.).
1H ЯМР (400 МГц, CDCl3) δ 7,40-7,28 (м, 5H), 6,32 (с, 1H), 5,80 (с, 1H), 5,11 (с, 2H), 5,02 (с, 1H), 4,36 (с, 1H), 3,74 (с, 3H), 3,60 (с, 4H), 3,54 (с, 4H), 3,44-3,43 (м, 2H), 3,38-3,21 (м, 2H), 2,30-2,20 (м, 3H). 2,04-2,00 (м, 1Н), 1,76 (с, 1Н), 1,44 (с, 9Н). ЭИ-МС m/z: 526 (M+).
Получение соединения IntCl-L-1c
К раствору соединения IntCl-L-1b (3 г, 5,71 ммоль) в МеОН (25 мл) добавляли Pd/C (900 мг) при комнатной температуре в атмосфере H2. Смесь перемешивали в течение 3 часов и фильтровали через целит, а затем концентрировали при пониженном давлении. Соединение IntCl-L-1c использовали непосредственно на следующей стадии без дополнительной очистки (2,23 г, неочищенный).
1H ЯМР (400 МГц, CDCl3) δ 6,56 (с, 1Н), 5,20 (с, 1Н), 3,73 (с, 3Н), 3,61 (с, 4Н), 3,57-3,55 (м, 4Н), 3,53-3,50 ( м, 1Н), 3,48-3,44 (м, 4Н), 2,40-2,32 (м, 2Н), 2,18-2,10 (м, 1Н), 1,88-1,81 (м, 1Н), 1,44 (с, 9Н). ЭИ-МС m/z: 392 (M+).
Получение соединения IntCl-L-1d
К раствору соединения IntCl-L-1c (2,23 г, 5,71 ммоль) и соединения FA-Int (2,12 г, 5,19 ммоль) в ДМФА (15 мл) добавляли HBTU (2,36 г, 6,23 ммоль) и DIPEA (1,36 мл, 7,78 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 2,5 часов и добавляли EA (100 мл × 7) и H2O (100 мл). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntCl-L-1d (4,06 г, колич.).
1H ЯМР (400 Гц, ДМСО-d6) δ 8,89 (д, J=7,6 Гц, 1H), 8,63 (с, 1H), 7,90 (д, J=8 Гц, 2H), 7,64 (д, J=8,4 Гц, 2H), 6,76-6,75 (м, 1H), 5,12 (с, 1H), 4,41-4,36 (м, 1H), 3,64 (с, 3H), 3,47 (с, 4H), 3,39-3,35 (м, 4H) 3,20-3,12 (м, 2H), 3,07-3,02 (м, 2H), 2,23 (т, J=7,4 Гц, 2H), 2,09-2,06 (м, 1H), 1,96-1,91 (м, 1H), 1,36 (с, 9H). ЭИ-МС m/z: 782 (M+).
Получение соединения IntCl-L-1
К раствору соединения IntCl-L-1d (4,68 г, 5,99 ммоль) в ДХМ (50 мл) по каплям добавляли ТФУ (10 мл) при 0°С. Реакцию оставляли нагреваться до комнатной температуры и перемешивали в течение 3 часов. Смесь концентрировали при пониженном давлении и использовали непосредственно на следующей стадии без дополнительной очистки (4,08 г, неочищенный).
ЭИ-МС m/z: 682 (M+).
[Пример 26] Получение соединения IntC-L

Получение соединения K-1
К раствору L-Lys(Boc)-OMe (3 г, 10,11 ммоль) и 4-пентиновой кислоты (992 мг, 10,11 ммоль) в ДМФА (30 мл) добавляют одну порцию PyBop (7,89 г, 15,16 ммоль), затем DIPEA (5,26 мл, 30,32 ммоль) при 0°С в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре. К смеси добавляли EA (80 мл × 4) и насыщенный раствор лимонной кислоты (60 мл), и органический слой промывали NaHCO3 (120 мл), солевым раствором (100 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения К-1 (3,29 г, 95%).
ЭИ-МС m/z: 341 (M+).
Получение соединения K-2
К раствору соединения K-1 (3,29 г, 9,66 ммоль) в МеОН (15 мл) добавляли LiOH⋅H2O (2,03 г, 48,32 ммоль), растворенный в H2O (15 мл) при 0°С в атмосфере N2.
Смесь перемешивали при 0°С в течение 30 минут и нагревали до комнатной температуры в течение 2 часов. Смесь подкисляли насыщенным водным раствором лимонной кислоты и к смеси добавляли EA (40 мл × 2). Органический слой промывали H2O (30 мл) и солевым раствором (30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Соединение К-2 использовали непосредственно на следующей стадии без дополнительной очистки (3,15 г, неочищенный).
ЭИ-МС m/z: 327 (M+).
Получение соединения K
К раствору соединения K-2 (3,69 г, 11,31 ммоль) в ДМФА (20 мл) добавляли NHS (1,69 мг, 14,7 ммоль) и EDCI (2,93 г, 15,26 ммоль) в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре и концентрировали. Остаток, соединение K, использовали непосредственно на следующей стадии без дальнейшей очистки (4,79 г, неочищенный).
ЭИ-МС m/z: 446 (M++Na).
Получение соединения IntC-L-2
К раствору соединения IntC-L-1 (4,08 г, 5,99 ммоль) и соединения K (4,79 г, 11,31 ммоль) в ДМФА (25 мл) добавляли DIPEA (5,21 мл, 29,93 ммоль) в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре. К смеси добавляли Н2О (70 мл) и солевой раствор (60 мл) и экстрагировали EA (70 мл × 7). А органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntC-L-2 (1,12 г, 19%).
ЭИ-МС m/z: 991 (M+).
Получение соединения IntC-L-3
К раствору соединения IntA-L-2 (1,12 г, 1,13 ммоль) в МеОН (27 мл) добавляли LiOH⋅H2O (356 мг, 8,48 ммоль), растворенный в H2O (10 мл) при 0°С в атмосфере N2. Смесь перемешивали при 0°С в течение 30 минут и нагревали до комнатной температуры в течение 3 часов. Смесь подкисляли 2 М HCl и концентрировали при пониженном давлении. Остаток, соединение IntC-L-3, использовали непосредственно на следующей стадии без дополнительной очистки (996 мг, неочищенный).
ЭИ-МС m/z: 880 (M+).
Получение соединения IntC-L
К раствору соединения IntC-L-3 (996 мг, 1,13 ммоль) в ДХМ (30 мл) добавляли ТФУ (8 мл) при 0°С в атмосфере N2. После перемешивания при 0°С в течение 1 часа смесь концентрировали при пониженном давлении. Остаток растворяли в ДМСО (5 мл) и очищали препаративной ВЭЖХ, в результате чего получали соединение IntC-L (409 мг, 32%).
ЭИ-МС m/z: 780 (M+).
[Пример 27] Получение соединения MPS-D1
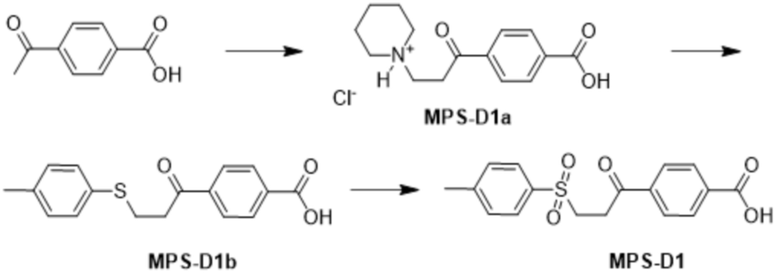
Получение соединения MPS-D1a
К раствору 4-ацетилбензойной кислоты (9 г, 54,82 ммоль) в EtOH (50 мл) добавляли гидрохлорид пиперидина (6,66 г, 54,82 ммоль), параформальдегид (4,95 г, 164,5 ммоль) и конц. HCl (0,6 мл) при комнатной температуре в атмосфере N2. Смесь перемешивали при 100°С в течение 16 часов и охлаждали до комнатной температуры, к ней по каплям добавляли ацетон (90 мл). Смесь перемешивали при 0°С в течение 1 часа. Твердое вещество отфильтровывали и промывали диэтиловым эфиром (30 мл × 2), с получением соединения MPS-D1a (6,11 г, 38%).
1H ЯМР (400 МГц, ДМСО-d6) δ 8,08 (с, 4H), 5,73 (с, 1H), 3,65 (т, J=7,2 Гц, 2H), 3,35 (т, J=7,2 Гц, 2H), 3,31 (м, 6H), 1,74 (с, 4H).
Получение соединения MPS-D1b
К раствору MPS-D1a (6,11 г, 20,52 ммоль) в EtOH (40 мл) и MeOH (26 мл) добавляли 4-метоксибензолтиол (2,55 г, 20,52 ммоль) и пиперидин (0,3 мл, 3,08 ммоль) при комнатной температуре. Смесь перемешивали при 100°С в течение 16 часов, охлаждали до 0°С и дополнительно перемешивали в течение 1 часа. Твердое вещество отфильтровывали и промывали эфиром (30 мл × 2), с получением соединения MPS-D1b (5,56 г, 90%).
1H ЯМР (400 МГц, CDCl3) δ 8,04-7,99 (м, 4H), 7,27 (д, J=8,4 Гц, 2H), 7,15 (д, J=7,6 Гц, 2H), 3,39-3,36 (м, 2H) 3,25-3,21 (м, 2H), 2,27 (с, 3H).
Получение соединения MPS-D1
К раствору MPS-D1b (5,56 г, 18,51 ммоль) в МеОН (90 мл) и дистиллированной воде (90 мл) добавляли оксон (25,03 г, 40,72 ммоль) при 0°С в атмосфере N2. После перемешивания при комнатной температуре в течение 14 часов смесь гасили дистиллированной водой (100 мл) и хлороформом (150 мл × 3). Органический слой промывали солевым раствором (200 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении, с получением соединения MPS-D1 (5,29 г, 86%).
1H ЯМР (400 МГц, CDCl3) δ 8,04-7,99 (м, 4H), 7,81 (д, J=8,4 Гц, 2H), 7,46 (д, J=8,4 Гц, 2H), 3,63 (т, J=7,2 Гц), 2H), 3,41 (т, J=7,2 Гц, 2H), 2,44 (с, 3H). ЭИ-МС m/z: 333 (M+).
[Пример 28] Получение соединения MPS-D2
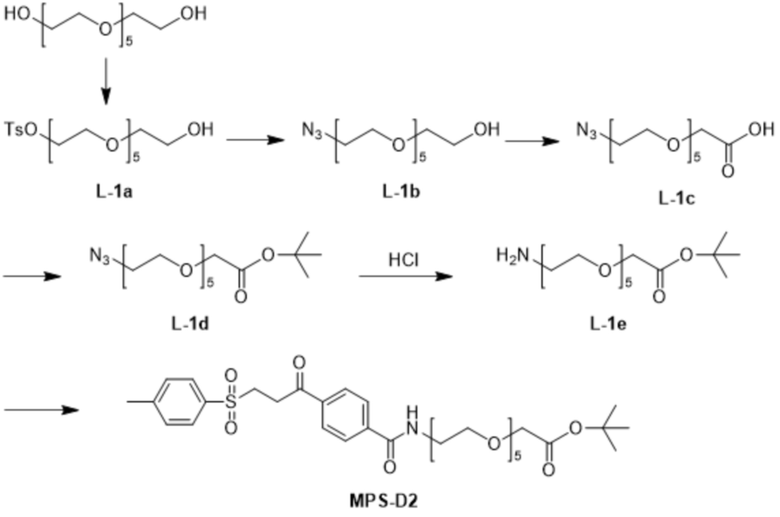
Получение соединения L-1a
К раствору гексаэтиленгликоля (5,0 г, 17,71 ммоль) в безводном ДХМ (178 мл) добавляли KI (294 мг, 1,77 ммоль) и Ag2O (4,92 г, 19,48 ммоль) в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции смесь фильтровали через целит и промывали ДХМ (100 мл). Фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения L-1a (5,98 г, 73%).
1H ЯМР (400 МГц, CDCl3) δ 7,80 (д, J=8,4 Гц, 2H), 7,35 (д, J=8,4 Гц, 2H), 4,16 (т, J=4,8 Гц, 2H), 3,71-3,58 (м, 22Н), 2,88 (уш. с, 1Н), 2,45 (с, 3Н).
Получение соединения L-1b
К раствору соединения L-1a (5,98 г, 13,7 ммоль) ДМФА (30 мл) добавляли NaN3 (1,34 г, 20,55 ммоль) в атмосфере N2. Смесь перемешивали при 110°С в течение 1 часа и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения L-1b (4,1 g, 97%).
1H ЯМР (400 МГц, CDCl3) δ 3,72-3,60 (м, 22H), 3,39 (т, J=4,8 Гц, 2H), 2,78 (уш. с, 1H).
Получение соединения L-1c
К раствору соединения L-1b (2 г, 6,51 ммоль) в ацетоне (56 мл) медленно по каплям добавляли раствор реагента Джонса (5 мл) при -5°С в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 2 часов и фильтровали через целит, и фильтрат концентрировали при пониженном давлении. Фильтрат разбавляли ДХМ (20 мл × 2) и водой (5 мл). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения L-1c (1,85 г, 89%).
1H ЯМР (400 МГц, CDCl3) δ 4,15 (с, 2H), 3,76-3,67 (м, 18H), 3,40 (т, J=4,8 Гц, 2H).
Получение соединения L-1d
К раствору соединения L-1c (500 мг, 1,56 ммоль) в ДХМ (10 мл) добавляли t-BuOH (305 мкл, 3,11 ммоль), DIC (292,5 мкл, 1,87 ммоль) и DMAP (19 мг, 0,16 ммоль) в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 4 часов и разбавляли ДХМ (30 мл × 2). Органический слой промывали водой (5 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения L-1d (278,5 мг, 47%).
1H ЯМР (400 МГц, CDCl3) δ 4,01 (с, 2H), 3,70-3,66 (м, 18H), 3,38 (т, J=4,8 Гц, 2H), 1,47 (с, 9H).
Получение соединения L-1e
К раствору соединения L-1d (278 мг, 0,74 ммоль) в EtOH (5 мл) добавляли Pd/C (236 мг, 0,11 ммоль) и 4М-HCl (в 1,4-диоксане) в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 1 часа. Смесь фильтровали через целит для удаления Pd/C и концентрировали с получением соединения L-1e (255,3 мг, 89,2%).
1H ЯМР (400 МГц, ДМСО-d6) δ 8,32 (с, 1Н), 3,98 (с, 2Н), 3,55-3,40 (м, 18Н), 3,86 (т, J=5,6 Гц, 2Н), 2,70-2,64 ( м, 2Н), 1,42 (с, 9Н)
Получение соединения MPS-D2
К раствору соединения L-1e (255,3 мг, 0,66 ммоль) и соединения MPS-D1 (240,6 мг, 0,72 ммоль) в ДМФА (6 мл) добавляли HBTU (300 мг, 0,79 ммоль) и DIPEA (229,3 мкл, 1,32 ммоль) в атмосфере азота. Смесь перемешивали при комнатной температуре в течение 2 часов и разбавляли EA (20 мл × 2) и водой (5 мл). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения MPS-D2 (306 мг, 71%).
1H ЯМР (400 МГц, CDCl3) δ 7,95 (с, 4H), 7,82 (д, J=8,0 Гц, 2H), 7,38 (д, J=8,0 Гц, 2H), 7,33-7,30 (м, 1H), 3,98 (с, 2Н), 3,68-3,63 (м, 18Н), 3,55-3,53 (м, 2Н), 3,49-3,47 (м, 2Н), 2,95 (с, 1Н), 2,88 (с, 1Н), 2,46 (с, 3H) 1,46 (с, 9H). ЭИ-МС m/z: 666(M++1).
[Пример 29] Получение соединения MPS-D4
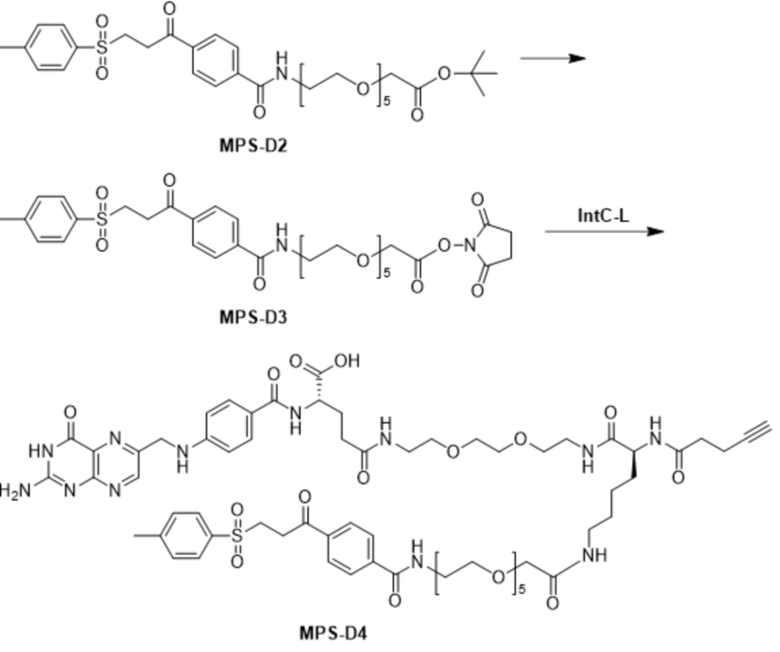
Получение соединения MPS-D3
К раствору соединения MPS-D2 (120 мг, 0,18 ммоль) в ДХМ (8 мл) добавляли ТФУ (4 мл) при 0°С. Реакцию оставляли нагреваться до комнатной температуры в течение 2 часов в атмосфере N2. После завершения реакции смесь концентрировали три раза при пониженном давлении, используя толуол в качестве сорастворителя, удаляя тем самым ТФУ. Затем смесь снова растворяли в ДМФА и добавляли NHS (31 мг, 0,27 ммоль) и EDCI (52 мг, 0,27 ммоль). Смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции соединение MPS-D3 использовали непосредственно на следующей стадии без дополнительной очистки (127 мг, неочищенный).
ЭИ-МС m/z: 707 (M+).
Получение соединения MPS-D4
К раствору соединения IntC-L (60 мг, 0,08 ммоль) и соединения MPS-D3 (82 мг, 0,12 ммоль) в ДМФА (6 мл) добавляли DIPEA (112 мкл, 0,64 ммоль) в атмосфере N2. Смесь перемешивали в течение 30 минут и растворяли в ДМСО (3 мл) и очищали ВЭЖХ, в результате чего получали соединение MPS-D4 (77 мг, 73%).
ЭИ-МС m/z: 1373 (M+).
[Пример 30] Получение соединения MPS-D5
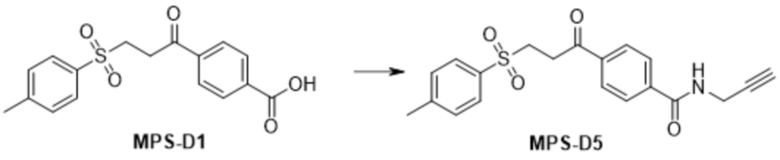
К раствору соединения MPS-D1 (500 мг, 1,50 ммоль) в ДМФА (8 мл) добавляли пропаргиламин (106 мкл, 1,65 ммоль) при комнатной температуре в атмосфере N2. Реакционную смесь охлаждали до 0°С и к ней добавляли PyBop (1,17 г, 2,26 ммоль) и DIPEA (524 мкл, 3,01 ммоль). Смесь перемешивали при комнатной температуре в течение 2 часов и разбавляли EA (30 мл × 2) и дистиллированной водой (20 мл). Органический слой экстрагировали и промывали солевым раствором (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения MPS-D5 (510 мг, 92%).
1H ЯМР (400 МГц, CDCl3) δ 9,11 (т, J=5,2 Гц, 1H), 7,98-7,89 (м, 4H), 7,79 (д, J=8,0 Гц, 2H), 7,43 (д, J=8,4 Гц, 2H), 4,05-4,03 (м, 2H), 3,60 (т, J=7,6 Гц, 2H), 3,39 (т, J=7,2 Гц, 2H), 3,12 (с, 1H), 2,38 (с, 3H).
[Пример 31] Получение соединения IntA-Q7

Получение соединения IntA-Q7-1
К раствору дигидрата 3,5-дииодо-L-тирозина (3 г, 6,39 ммоль) в МеОН (20 мл) по каплям добавляли тионилхлорид (836 мкл, 11,5 ммоль) при 0°С в атмосфере N2. Смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции смесь концентрировали с получением соединения IntA-Q7-1 (2,86 г, колич.).
ЭИ-МС m/z: 448(M+).
Получение соединения IntA-Q7-2
К раствору соединения IntA-Q7-1 (1 г, 2,24 ммоль) в ACN (10 мл) добавляли Boc2O (730 мг, 3,36 ммоль) и Et3N (940 мкл, 6,72 ммоль) при 0°С в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 15 часов и гасили EA (30 мл × 2) и лимонной кислотой (30 мл). Органический слой экстрагировали и промывали солевым раствором (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении, с получением соединения IntA-Q7-2 (1,22 г, колич.).
1H ЯМР (400 МГц, ДМСО-d6) δ 9,38 (с, 1Н), 7,60 (с, 2Н), 7,30 (д, J=8,4 Гц, 1Н), 4,15 (м, 1Н), 3,63 (с, 3Н) 2,76-2,62 (м, 2H), 1,33 (с, 9H).
Получение соединения IntA-Q7-3
К раствору соединения IntA-Q7-2 (1,1 г, 2,01 ммоль) и 4-винилпиридина (650 мкл, 6,30 ммоль) в ДМФА (12 мл) добавляли Pd(OAc)2 (23 мг, 0,101 ммоль), P(o-tol)3 (43 мг, 0,141 ммоль) и DIPEA (1,75 мл) при комнатной температуре в атмосфере N2. Смесь перемешивали при 100°С в течение 3 часов. Смесь охлаждали до комнатной температуры с последующей фильтрацией через целит и затем промывали ЕА (20 мл). Фильтрат концентрировали при пониженном давлении, и остаток очищали колоночной хроматографией с получением соединения IntA-Q7-3 (790 мг, 78%).
ЭИ-МС m/z: 502(M+).
Получение соединения IntA-Q7
К раствору соединения IntA-Q7-3 (100 мг, 0,2 ммоль) в ACN (6 мл) и ДМФА (3 мл) добавляли Et3N (280 мкл, 2,0 ммоль) при комнатной температуре в атмосфере N2. Газ SO2F2 вводили через баллон, и смесь перемешивали при комнатной температуре в течение 3 часов. Смесь гасили насыщенным NaHCO3 (10 мл × 2) и разбавляли EA (20 мл). Органический слой экстрагировали солевым раствором (10 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q7 (75 мг, 65%).
ЭИ-МС m/z: 584(M+).
[Пример 32] Получение соединения A-15-1
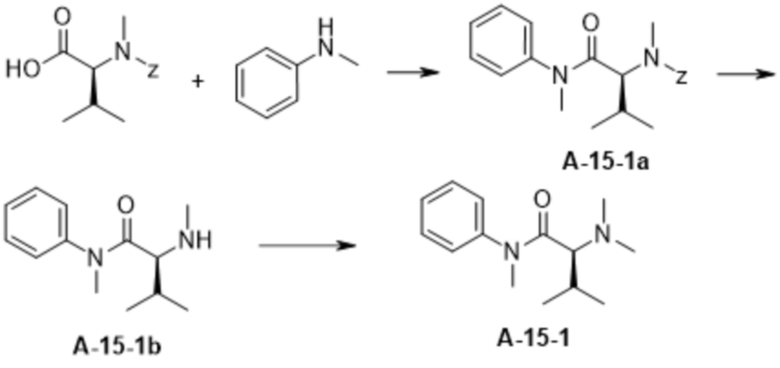
Получение соединения A-15-1a
К раствору z-валина (1,01 г, 3,81 ммоль) и N-метиланилина (412 мкл, 3,81 ммоль) в ДХМ (15 мл) добавляли DCC (1,18 г, 5,71 ммоль) и DMAP (92 мг, 0,76 ммоль) при комнатной температуре в атмосфере N2 с последующим перемешиванием при комнатной температуре в течение 3 часов. Смесь фильтровали через целит и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения A-15-1a (1,05 г, 78%).
ЭИ-МС m/z: 584(M+).
Получение соединения A-15-1b
Соединение A-15-1a (1,05 г, 2,96 ммоль) растворяли в MeOH (15 мл) в атмосфере азота, добавляли Pd/C (378 мг, 0,18 ммоль). После перемешивания при комнатной температуре в течение 2 часов в атмосфере H2 смесь фильтровали через целит и промывали МеОН (30 мл). Фильтрат концентрировали с получением соединения A-15-1b (560 мг, 86,0%).
1H ЯМР (400 МГц, CDCl3) δ 7,45-7,41 (м, 2Н), 7,38-7,36 (м, 1Н), 7,19 (д, J=7,6 Гц, 1Н), 3,32 (с, 3Н), 2,88 (д, J=6,0 Гц, 1H), 2,33 (с, 3H), 1,73 (кв, J=6,8 Гц, 1H), 0,86 (д, J=6,8 Гц, 3H), 0,80 (д, J=6,8 Гц, 3H).
Получение соединения A-15-1
К раствору соединения A-15-1b (220 мг, 0,99 ммоль) в ДМФА (8 мл) добавляли 37% формальдегид (223 мкл, 2,99 ммоль) и AcOH (1,14 мл, 19,8 ммоль) в атмосфере N2. После перемешивания при комнатной температуре в течение 5 минут добавляли NaCNBH3 (125 мг, 1,98 ммоль). Смесь перемешивали при комнатной температуре в течение 2 часов и гасили насыщенным NaHCO3 (15 мл × 2). К смеси добавляли EA (20 мл × 2) и солевой раствор (20 мл). Органический слой сушили над безводным Na2SO4, фильтровали, концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения A-15-1 (189 мг, 81%).
ЭИ-МС m/z: 235(M+).
[Пример 33] Получение соединения IntA-Q8

Получение соединения IntA-Q8-1
К раствору соединения Int-TG1 (пример 2, 120 мг, 0,22 ммоль) и IntA-Q2-2 (пример 13, 50 мг, 0,24 ммоль) в ACN (2 мл) в атмосфере N2 по каплям добавляли BEMP (13 мкл, 44 мкмоль). Смесь перемешивали при комнатной температуре в течение 2 часов и добавляли ЕА (10 мл × 2) и лимонную кислоту (15 мл). Органический слой промывали солевым раствором (50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q8-1 (72 мг, 54%).
ЭИ-МС m/z: 649(M++Na).
Получение соединения IntA-Q8
К раствору соединения IntA-Q8-1 (72 мг, 0,12 ммоль) в ТГФ (4 мл) добавляли NBS (31 мг, 0,18 ммоль) и PPh3 (45 мг, 0,18 ммоль) в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 3 часов и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q8 (53 мг, 67%).
ЭИ-МС m/z: 713(M++Na).
[Пример 34] Получение соединения IntA-Q9
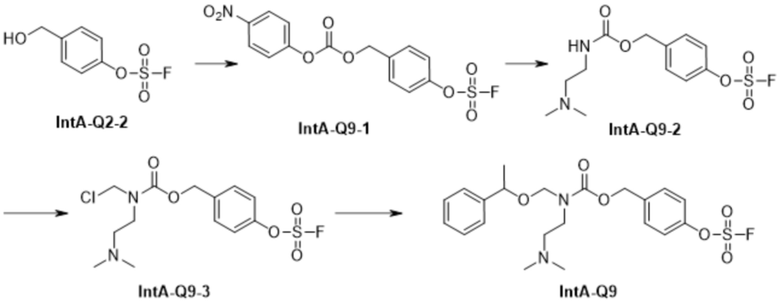
Получение соединения IntA-Q9-1
К раствору соединения IntA-Q2-2 (пример 13, 300 мг, 1,45 ммоль) в ДМФА (5 мл) добавляли 4-нитрофенилхлорформиат (664 мг, 2,18 ммоль) и DIPEA (0,51 мл, 2,91 ммоль) при комнатной температуре в атмосфере N2. После перемешивания в течение ночи добавляли ЕА (50 мл) и воду (50 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q9-1 (461,3 мг, 85%).
1H ЯМР (400 МГц, CDCl3) δ 8,29 (д, J=9,2 Гц, 2H), 7,58 (д, J=8,8 Гц, 2H), 7,42-7,38 (м, 4H), 5,33 (с, 2H).
Получение соединения IntA-Q9-2
К раствору соединения IntA-Q9-1 (461,3 мг, 1,24 ммоль) в ДМФА (10 мл) и пиридине (2 мл) добавляли 4-N, N-диметилэтилендиамин (0,14 мл, 1,24 ммоль), HOBT (38 мг, 0,25 ммоль) и DIPEA (0,22 мл, 1,24 ммоль) при комнатной температуре в атмосфере N2. После перемешивания в течение 3 часов добавляли ЕА (60 мл) и воду (60 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q9-2 (337 мг, 89%).
1H ЯМР (400 МГц, CDCl3) δ 7,48 (д, J=8,8 Гц, 2H), 7,33 (д, J=8,4 Гц, 2H), 5,35 (уш. с, 1H), 5,12 (с, 2H), 3,30 (кв, J=5,6, 5,2 Гц, 2H), 2,43 (т, J=5,6 Гц, 2H), 2,24 (с, 6H). ЭИ-МС m/z: 321(M+).
Получение соединения IntA-Q9-3
К раствору соединения IntA-Q9-2 (100 мг, 0,31 ммоль) в безводном ДХМ (3 мл) добавляли параформальдегид (13,1 мг, 0,437 ммоль) и TMS-Cl (0,06 мл, 0,47 ммоль) при комнатной температуре в атмосфере N2. После перемешивания в течение 3 часов к нему дополнительно добавляли параформальдегид и TMS-Cl, каждый из которых имел количество 10 эквивалентов, и смесь перемешивали при 50°С в течение 30 минут.
Неочищенное соединение IntA-Q9-3 использовали непосредственно на следующей стадии без дальнейшей очистки.
ЭИ-МС m/z: 365(M+).
Получение соединения IntA-Q9
К раствору соединения IntA-Q9-3 (20 мг, 0,054 ммоль) в безводном ДХМ (1,5 мл) добавляли избыточное количество фенилэтилового спирта и DIPEA при комнатной температуре в атмосфере N2. После перемешивания в течение 2 часов смесь концентрировали при пониженном давлении. Остаток растворяли в ДМСО (4 мл) и очищали препаративной ВЭЖХ, в результате чего получали соединение IntA-Q9 (11,8 мг, 48%).
ЭИ-МС m/z: 455(M+).
[Пример 35] Получение соединения IntB-Q2
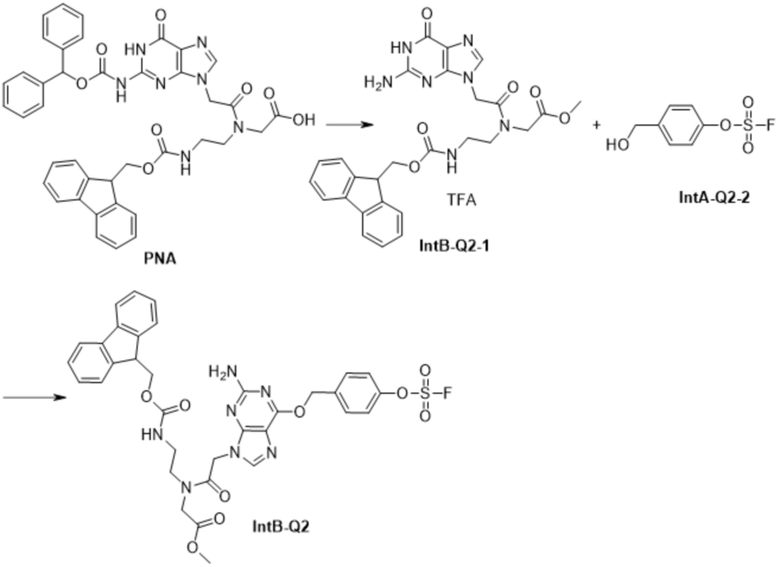
Получение соединения IntB-Q2-1
К раствору PNA (380 мг, 0,51 ммоль) в МеОН (4 мл) по каплям добавляли SOCl2 (112 мкл, 1,54 ммоль) в атмосфере N2. После перемешивания в течение ночи при 40°С к нему дополнительно добавляли SOCl2 (112 мкл, 1,54 ммоль) с последующим перемешиванием при 40°С в течение 3 часов. Смесь концентрировали при пониженном давлении. Остаток растворяли в ДМСО и очищали препаративной ВЭЖХ, в результате чего получали соединение IntB-Q2-1 (233 мг, 69%).
ЭИ-МС m/z: 546(M+).
Получение соединения IntB-Q2
К раствору соединения IntB-Q2-1 (233 мг, 0,35 ммоль) в ТГФ (2 мл) добавляли соединение IntA-Q2-2 (пример 13, 160 мг, 0,78 ммоль) и PPh3 (148 мг, 0,57 ммоль) в атмосфере N2. Смесь охлаждали до 0°С. DEAD добавляли по каплям и смесь перемешивали в течение 3 часов и разбавляли EA (50 мл × 1). Органический слой промывали H2O (50 мл X 2) и солевым раствором (30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q2 (118 мг, 38%).
ЭИ-МС m/z: 734(M+).
[Пример 36] Получение соединения POS-D1
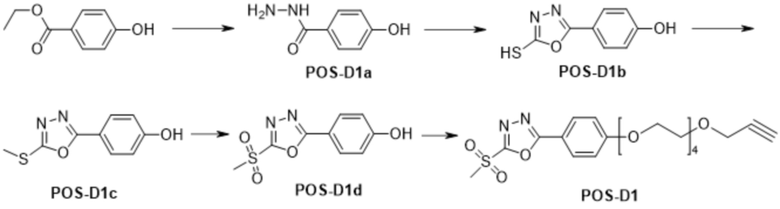
Получение соединения POS-D1a
К раствору этил 4-гидробензоата (20 г, 120,35 ммоль) в EtOH (60 мл) добавляли NH2NH2⋅H2O (88 мл, 1805,4 ммоль) в атмосфере N2. Смесь перемешивали в течение ночи с обратным холодильником. После завершения реакции смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении с последующим растиранием с EtOH, получая при этом соединение POS-D1a (17,539 г, 96%).
1H ЯМР (400 МГц, ДМСО-d6) δ 9,50 (с, 1H), 7,68 (д, J=8,4 Гц, 2H), 6,78 (д, J=8,8 Гц, 2H), 4,37 (с, 2H). ЭИ-МС m/z: 431(M+).
Получение соединения POS-D1b
К раствору соединения POS-D1a (17,54 г, 115,28 ммоль) в EtOH (200 мл) и ДМФА (100 мл) добавляли CS2 (45 мл, 749,32 ммоль) и KOH (6,5 г, 115,28 ммоль) в атмосфере N2. После перемешивания при 85°С в течение 18 часов добавляли ЕА (500 мл) и Н2О (500 мл) и подкисляли 1 М HCl. Органический слой промывали H2O (500 мл) и солевым раствором (500 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток подвергали растиранию в эфире/НХ с получением соединения POS-D1b (20,7 г, 93%).
1H ЯМР (400 МГц, ДМСО-d6) δ 10,44 (с, 1H), 7,72 (д, J=8,4 Гц, 2H), 6,94 (д, J=8,0 Гц, 2H). ЭИ-МС m/z: 195(M+).
Получение соединения POS-D1c
К раствору соединения POS-D1b (5 г, 25,75 ммоль) в ТГФ (100 мл) по каплям добавляли Et3N (4,3 мл, 30,9 ммоль) и MeI (1,76 мл, 28,33 ммоль) при 0°С. После перемешивания при 0°С в течение 10 минут смесь нагревали до комнатной температуры. И затем смесь перемешивали в течение 2 часов и разбавляли ЕА (100 мл × 2). Органический слой промывали H2O (100 мл) и солевым раствором (100 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток подвергали растиранию в эфире с получением соединения POS-D1c (5,15 г, 96%).
1H ЯМР (400 МГц, ДМСО-d6) δ 7,80 (д, J=8,4 Гц, 2H), 6,94 (д, J=8,4 Гц, 2H), 2,74 (с, 3H). ЭИ-МС m/z: 209(M+).
Получение соединения POS-D1d
К раствору соединения POS-D1c (3,2 г, 15,37 ммоль) в EtOH (150 мл) добавляли 70% m-CPBA (11,4 г, 46,11 ммоль) при 0°С в атмосфере N2. После перемешивания при комнатной температуре в течение 5 часов, дополнительно добавляли 70% m-CPBA (11,4 г, 46,11 ммоль). Затем смесь перемешивали в течение ночи при комнатной температуре и гасили H2O (500 мл), насыщенным NaHCO3 (300 мл), разбавленным EA (500 мл × 2). Органический слой промывали солевым раствором (300 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток подвергали растиранию в HX/EA=1: 1 (100 мл), с получением соединения POS-D1d (3,2 мг, 89%).
1H ЯМР (400 МГц, ДМСО-d6) δ 7,95 (д, J=8,8 Гц, 2H), 7,01 (д, J=8,8 Гц, 2H), 3,69 (4 с, 3H). ЭИ-МС m/z: 241(M+).
Получение соединения POS-D1
К раствору тетраэтиленгликоля (17,3 мл, 0,10 моль) в ТГФ (50 мл) по каплям добавляли NaH (2,6 г, 0,065 ммоль) при 0°С. После перемешивания при 0°С в течение 1 часа добавляли пропаргилбромид (5,95 г, 0,05 моль). Смесь перемешивали в течение ночи при комнатной температуре и гасили льдом/водой, разбавленной EA (100 мл × 2). Органический слой промывали H2O (100 мл) и солевым раствором (100 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. 660 мг (2,84 ммоль) соединения, полученного растиранием в эфире из остатка, то есть 3,6,9,12-тетраоксапентадец-14-ин-1-ол (5,87 г, 51%, 1H ЯМР (400 МГц, CDCl3) 4,21 (с, 2H), 3,73-3,66 (м, 14H), 3,59-3,61 (м, 2H), 2,60 (с, 1H), 2,42 (т, J=2,4 Гц, 1H)) и соединение D-4-5 (310 мг, 1,29 ммоль) растворяли в ТГФ (8 мл) и ДМФА (0,8 мл) и добавляли PPh3 (667 мг, 2,58 ммоль). Смесь охлаждали до 0°С. К нему добавляли 2,2 М DEAD (1,17 мл, 2,58 ммоль) и смесь перемешивали при 0°С в течение 3 часов. После завершения реакции добавляли ЕА (15 мл × 2) и дистиллированную воду (15 мл), а органический слой экстрагировали и промывали солевым раствором (20 мл). Полученный органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении с получением соединения POS-D1 205 мг, 30%).
ЭИ-МС m/z: 455(M+).
[Пример 37] Получение соединения Int-TG11
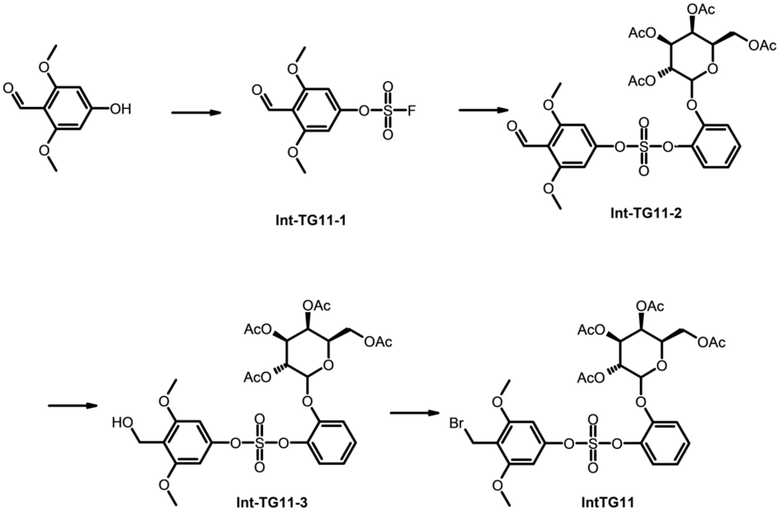
Int-TG11-3 синтезировали аналогичным путем синтеза, как описано в Примере 6 и Примере 33.
Получение соединения Int-TG11-1
Выход 99%
ЭИ-МС m/z: 265(M+). 1H-ЯМР (400 МГц, CDCl3) δ 10,41 (с, 1H), 6,54 (с, 2H), 3,91 (с, 6H).
Получение соединения Int-TG11-2
Выход 99%
ЭИ-МС m/z: 685(M+). 1H-ЯМР (400 МГц, CDCl3) δ 10,42 (с, 1H), 7,37 (д, J=8 Гц, 1H), 7,31-7,26 (м, 2H), 7,15-7,11 (м, 1H), 6,58 (с, 2H), 5,54-5,45 (м, 2H), 5,09 (т, J=8,4 Гц, 2H), 4,27-4,22 (м, 1H), 4,16-4,05 (м, 2H), 3,89 (с, 6H), 2,19 (с, 3Н), 2,08 (с, 3Н), 2,06 (с, 3Н), 2,01 (с, 3Н)
Получение соединения Int-TG11-3
Выход 97% ЭИ-МС m/z: 669 (M+).
1H-ЯМР (400 МГц, CDCl3) δ 7,41 (д, J=8 Гц, 1H), 7,27 (т, J=5,2 Гц, 2H), 7,15-7,11 (м, 1H), 6,53 (с, 2H), 5,53-5,44 (м, 2H), 5,29 (с, 1H), 5,11-5,06 (м, 1H), 4,99 (д, J=8 Гц, 1H), 4,77 (с, 2H), 4,26-4,22 (м, 1H), 4,15-4,11 (м, 1H), 4,06-4,02 (м, 1H), 3,87 (с, 6H), 2,19 (с, 3H), 2,06-2,03 (м, 6H), 1,99 (с, 3H)
Получение соединения Int-TG11
К раствору соединения Int-TG11-3 (137 мг, 0,199 ммоль) в сухом ТГФ (5 мл) добавляли NBS (53 мг, 0,299 ммоль) и трифенилфосфин (78 мг, 0,299 ммоль) при комнатной температуре. После перемешивания в течение 2 часов смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения Int-TG11 (129 мг, 86%).
ЭИ-МС m/z: 750 (M+1). 1H-ЯМР (400 МГц, CDCl3) δ 7,36 (м, 1H), 7,29-7,28 (м, 2H), 6,56 (с, 1H), 6,53 (с, 1H), 5,58-5,51 (м, 1H), 5,46 (д, J=2,8 Гц, 1H), 5,12-5,06 (м, 2H), 4,60 (с, 2H), 4,27-4,23 (м, 1H), 4,17-4,11 (м, 1H), 4,08-4,05 (м, 1Н), 3,88 (с, 3Н), 3,86 (с, 3Н), 2,20 (с, 3Н), 2,09 (с, 3Н), 2,08 (с, 3Н), 2,01 (с, 3Н)
[Пример 38] Получение соединения Int-TG12

К раствору соединения Int-TG1-3 (530 мг, 1,2 ммоль) в сухом ТГФ (25 мл) добавляли 1,1'-сульфонилдиимидазол (477 мг, 2,4 ммоль) и Cs2CO3 (196 мг, 0,6 ммоль). После 18 ч кипячения с обратным холодильником смесь гасили 2 N водной HCl (100 мл). Органический слой экстрагировали EtOAc (2 × 20 мл), сушили над безводным MgSO4, фильтровали и концентрировали. Остаток очищали колоночной хроматографией с получением соединения Int-TG12 (396 мг, 58%).
1H-ЯМР (400 МГц, CDCl3) δ 7,84 (с, 1H), 7,35 (с, 1H), 7,34-7,31 (м, 1H), 7,20-7,16 (м, 2H), 7,05 (т, 1H), 6,86 (м, 1H), 5,51-5,45 (м, 2H), 5,10 (дд, J=3,6 Гц, 1H), 4,98 (д, J=8 Гц, 1H), 2,24 (с, 3H), 2,13 (с, 3H), 2,07 (с, 3H), 2,04 (с, 3H).
[Пример 39] Получение соединения Int-TG13
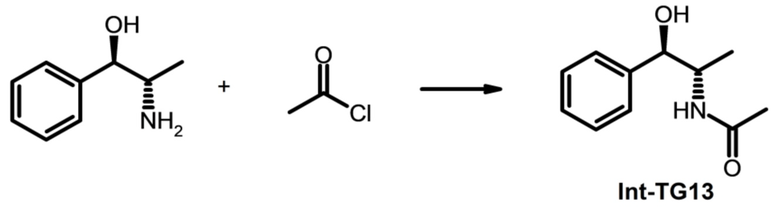
К раствору соединения(1R,2S)-(-)-норэфедрина (1 г, 6,61 ммоль) в ДХМ (5 мл) добавляли TEA (0,92 мл, 6,61 ммоль) и ацетилхлорид (0,47 мл, 6,61 ммоль) при 0°C в атмосфере N2. После перемешивания при комнатной температуре в течение 2 часов смесь гасили H2O (7 мл). Органический слой экстрагировали ДХМ (2 × 8 мл, сушили над безводным MgSO4, фильтровали и концентрировали. Остаток очищали колоночной хроматографией с получением соединения Int-TG13 (987 мг, 78%).
1H-ЯМР (400 МГц, CDCl3) δ 7,28 (м, 5H), 5,70 (м, 1H), 4,86 (с, 1H), 4,34-4,30 (м, 1H), 3,65 (м, 1H), 2,00 (с, 3H), 1,01 (д, J=7,2 Гц, 3H)
[Пример 40] Получение соединения Int-TG14

Соединение Int-TG14 синтезировали аналогичным путем синтеза, как описано в Примере 6 и Примере 37.
Получение соединения Int-TG14-1
Выход 99%; ЭИ-МС m/z: 929(M+1).
Получение соединения Int-TG14-2
Выход 96%; ЭИ-МС m/z: 931 (M+1).
Получение соединения Int-TG14
Выход 75%; ЭИ-МС m/z: 750 (M+1).
[Пример 41] Получение соединения IntB-Q3
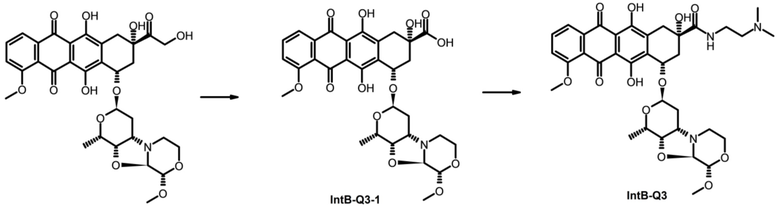
Получение соединения IntB-Q3-1
К раствору PNU-1529682 (52 мг, 0,081 ммоль) в MeOH (5 мл) / дистиллированной воде (3 мл) добавляли NaIO4 (18 мг, 0,081 ммоль) при комнатной температуре. После перемешивания в течение 2 часов смесь концентрировали при пониженном давлении, в результате чего получали неочищенное соединение IntB-Q3-1 (51 мг, 99%). ЭИ-МС m/z: 628 (M+1).
Получение соединения IntB-Q3
К раствору соединения IntB-Q3-1 (51 мг, 0,081 ммоль) в сухом ДХМ (5 мл) добавляли 2-(диметиламино)этиламин (6,1 мкл, 0,089 ммоль) и TEA (34 мкл, 0,243 ммоль), TBTU (52 мг, 0,162 ммоль) при комнатной температуре. После перемешивания в течение 1 часа смесь разбавляли ДХМ (2 × 8 мл). Органический слой промывали H2O (8 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q3 (38 мг, 67%).
ЭИ-МС m/z: 698 (M+1).
[Пример 42] Получение соединения IntB-Q4

Получение соединения IntA-Q-12-1
К раствору (3,4-метилендиокси)-коричной кислоты (1,5 г, 7,8 ммоль) в МеОН (200 мл), уксусной кислоте (10 мл) добавляли 10% Pd/C (500 мг) в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 22 часов в атмосфере H2. Затем смесь фильтровали через целит и промывали МеОН (200 мл). Фильтрат концентрировали, с получением соединения IntA-Q-12-1 в виде практически белого кристаллического твердого вещества (1,51 г, 99%).
1H ЯМР (400 МГц, CDCl3) δ 6,74-6,64 (м, 3H), 5,92 (с, 2H), 2,87 (т, J=7,8 Гц, 2H), 2,63 (т, J=7,2 Гц, 2H).
Получение соединения IntA-Q-12-2
К раствору соединения IntA-Q-12-2 (750 мг, 3,86 ммоль) и TEA (540 мкл, 3,86 ммоль) в безводном толуоле (15 мл) по каплям добавляли дифенилфосфорилазид (832 мкл, 3,86 ммоль) при комнатной температуре в атмосфере N2. Смесь нагревали до 90°С в течение 90 мин. После завершения реакции большую часть растворителя удаляли при пониженном давлении. Остаток охлаждали до 0°С в атмосфере N2. BF3⋅OEt2 (2,4 мл, 5,79 ммоль) добавляли по каплям к перемешиваемой смеси и затем перемешивали при комнатной температуре в течение 1 часа. Смесь разбавляли ЕА (50 мл) и промывали насыщенным водным раствором NaHCO3 (100 мл). Органический слой сушили над MgSO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q-12-2 (650 мг, 88%).
1H ЯМР (400 МГц, CDCl3) δ 7,51 (с, 1H), 6,65 (с, 1H), 6,06 (уш. c, 1H), 6,00 (с, 2H), 3,51 (м, 2H), 2,90 (т, J=6,8 Гц, 2H). ЭИ-МС m/z: 192 (M+1).
Получение соединения IntA-Q-12-3
К раствору соединения IntA-Q-12-2 (200 мг, 1,04 ммоль) в ТГФ (10 мл) по каплям добавляли н-BuLi (2,5 М в гексане, 1 мл) при -78°С в атмосфере N2. Светло-фиолетовый раствор перемешивали при -78°С в течение 30 минут и добавляли B(OMe)3 (200 мкл, 1,77 ммоль). Реакционную смесь нагревали до 0°C, затем добавляли AcOH (154 мкл) с последующим медленным добавлением 35% H2O2 (230 мкл). После перемешивания при комнатной температуре в течение 5 часов разбавляли ЕА (50 мл). Органический слой промывали насыщенным водным NaCl (100 мл), сушили над MgSO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q-12-3 (60 мг, 27%).
1H ЯМР (400 МГц, CDCl3) δ 12,33 (с, 1Н), 6,29 (с, 1Н), 6,03 (с, 2Н), 5,89 (уш. c, 1Н), 3,55 (м, 2Н), 2,92 (т, J =). 6,8 Гц, 2H). ЭИ-МС m/z: 208 (M+1).
Получение соединения IntA-Q-12-4
К раствору соединения IntA-Q-12-3 (38 мг, 0,184 ммоль) в ТГФ (3 мл) добавляли 1 М-tBuOK (1 М в ТГФ, 220 мкл, 0,220 ммоль) при комнатной температуре. Смесь перемешивали при комнатной температуре в течение 1 часа в атмосфере SO2F2, гасили 10% водным раствором HCl до рН 7 и разбавляли EA (50 мл). Органический слой насыщали водным NaCl (100 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q-12-4 (17 мг, 32%).
1H ЯМР (400 МГц, CDCl3) δ 6,71 (с, 1H), 6,15 (с, 2H), 5,77 (м, 1H), 3,50 (м, 2H), 2,93 (т, J=6,8 Гц, 2H). ЭИ-МС m/z: 290(M+1)
[Пример 43] Получение соединения Int-TG15

Соединение Int-TG15 синтезировали аналогичным путем синтеза, как описано в Примере 6 и Примере 37.
Выход 75%; ЭИ-МС m/z: 934 (M+1).
[Пример 44] Получение соединения L-2
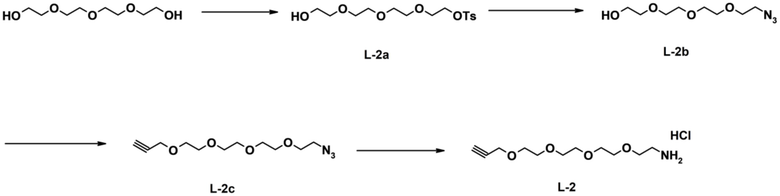
Соединение L-2 синтезировали аналогичным путем синтеза, как описано в документе Journal of Polymer Science, Part A: Polymer Chemistry, 2012, 50(19), 3986-3995, включенном в настоящий документ посредством ссылки.
Получение соединения L-2a
Выход 30%
1H ЯМР (400 МГц, CDCl3) δ 7,80 (д, J=8,4 Гц, 2H), 7,34 (д, J=8,4 Гц, 2H), 4,16 (т, J=4,8 Гц, 2H), 3,74-3,58 (м 14H) 2,45 (с, 3H).
Получение соединения L-2b
Выход 68%
1H ЯМР (400 МГц, CDCl3) δ 3,74-3,61 (м, 14H), 3,40 (т, J=4,8 Гц, 2H), 2,45 (т, J=6,0 Гц, 1H).
Получение соединения L-2c
Выход 63%
1H ЯМР (400 МГц, CDCl3) δ 4,21 (д, J=2,4 Гц, 2H), 3,72-3,67 (м, 14H), 3,39 (т, J=5,2 Гц, 2H), 2,43 (т, J=2,4 Гц, 1Н).
Получение соединения L-2
Выход 76%
1H ЯМР (400 МГц, CDCl3) δ 4,20 (д, J=2,4 Гц, 2H), 3,71-3,61 (м, 12H), 3,51 (т, J=4,8 Гц, 2H), 2,87 (т, J=5,6 Гц), 2H), 2,43 (т, J=2,4 Гц, 1H).
[Пример 45] Получение соединения L-3
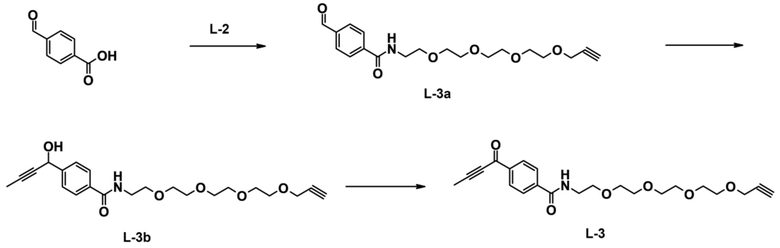
Соединение L-3 синтезировали аналогичным путем синтеза, как описано в Journal of Organic Chemistry, 2002, 67, 5032-5035, включенном в настоящий документ путем ссылки.
Получение соединения L-3a
Выход 92%
1H ЯМР (400 МГц, CDCl3) δ 10,08 (с, 1H), 7,97 (кв, J=8,8 Гц, 8,8 Гц, 4H), 7,16 (уш. c, 1H), 4,14 (д, J=2,4 Гц, 2H), 3,70-3,62 (м, 16H), 2,41 (т, J=2,4 Гц, 1H). ЭИ-МС m/z: 384(M+1)
Получение соединения L-3b
Выход 69%
1H ЯМР (400 МГц, CDCl3) δ 7,82 (д, J=8,0 Гц, 2H), 7,60 (д, J=7,6 Гц, 2H), 6,88 (уш. c, 1H), 5,47 (уш. c, 1H), 4,14 (д. J=2,4 Гц, 2H), 3,70-3,63 (м, 16H), 2,42 (уш. c, 1H), 2,19 (с, 3H). ЭИ-МС m/z: 404 (M+1)
Получение соединения L-3
Выход 81%
1H ЯМР (400 МГц, CDCl3) δ 8,19 (д, J=7,2 Гц, 2H), 7,92 (д, J=7,6 Гц, 2H), 7,07 (уш. c., 1H), 4,16 (с, 2H), 3,70-3,49 (м, 16Н), 2,42 (уш. c, 1Н), 2,19 (с, 3Н). ЭИ-МС m/z: 402(M+1)
[Пример 46] Получение соединения L-4
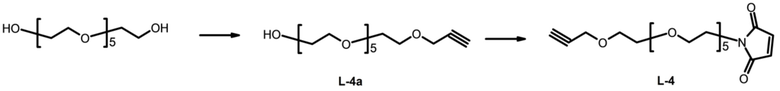
Соединение L-4 синтезировали аналогичным путем синтеза, как описано в Journal of Medicinal Chemistry, 52 (19), 5816-5825; 2009, включенном в настоящий документ путем ссылки.
Получение соединения L-4a
Выход 55%
1H ЯМР (400 МГц, CDCl3) δ 4,21 (д, J=2,0 Гц, 2H), 3,72-3,60 (м, 24H), 2,79 (уш. c, 1H), 2,43 (т, J=2,4 Гц, 1H).
Получение соединения L-4
ЭИ-МС m/z: 400(M+1)
[Пример 47] Получение соединения MPS-D6

Соединение L-5 синтезировали аналогичным путем синтеза, как описано в Примере 44 и Примере 45.
Получение соединения MPS-D6aВыход 91%
1H ЯМР (400 МГц, CDCl3) δ 7,80 (д, J=8,4 Гц, 2H), 7,35 (д, J=8,4 Гц, 2H), 4,16 (т, J=4,8 Гц, 2H), 3,70-3,61 (м., 20H), 3,39 (т, J=4,8 Гц, 2H), 2,45 (с, 3H). ЭИ-МС m/z: 462(M+1)
Получение соединения MPS-D6b
Выход 93%; ЭИ-МС m/z: 610(M+1)
Получение соединения MPS-D6c
Выход 54% ЭИ-МС m/z: 584 (M+1)
Получение соединения MPS-D6
Выход 72%; ЭИ-МС m/z: 899(M+1)
[Пример 48] Получение соединения MPS-D7
 Соединение MPS-D7 синтезировали аналогичным путем синтеза, как описано в Примере 28.
Соединение MPS-D7 синтезировали аналогичным путем синтеза, как описано в Примере 28.
Выход 80%; ЭИ-МС m/z: 546(M+1)
1H ЯМР (400 МГц, CDCl3) δ 8,11-7,94 (м, 4H), 7,83 (д, J=7,6 Гц, 2H), 7,44 (уш. c, 1H), 7,38 (д, J=8,0 Гц, 2H), 4,15 (с, 2Н), 3,69-3,65 (м, 14Н), 3,58-3,48 (м, 4Н), 2,80 (с, 1Н), 2,46 (с, 3Н).
[Пример 49] Получение соединения Int-TG16
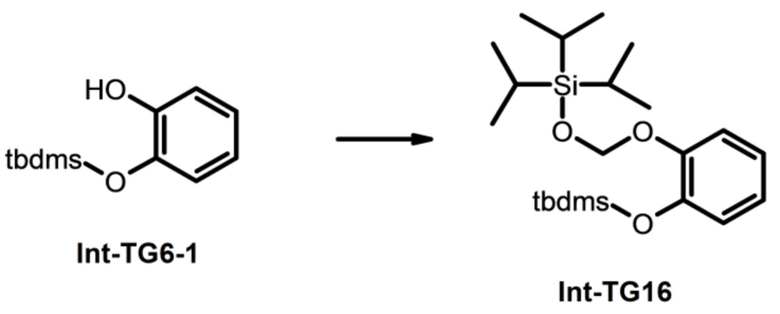
К раствору соединения Int-TG6-1 (300 мг, 1,34 ммоль) и TOM-Cl (310 мкл, 1,34 ммоль) в ДХМ (2 мл) добавляли DIPEA (291 мкл, 1,67 ммоль) в атмосфере N2. После перемешивания при комнатной температуре в течение 2 часов к нему дополнительно добавляли TOM-Cl (310 мкл, 1,34 ммоль) и DIPEA (466 мкл, 2,67 ммоль). Смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции смесь очищали препаративной ВЭЖХ с получением соединения Int-TG16 (165 мг, 30%).
1H ЯМР (400 МГц, CDCl3) δ 7,22-7,20 (м, 1H), 6,92-6,87 (м, 3H), 5,43 (с, 2H), 1,21-1,08 (м, 21H), 1,03 (с, 9H), 0,19 (с, 6H).
[Пример 50] Получение соединения Int-TG17
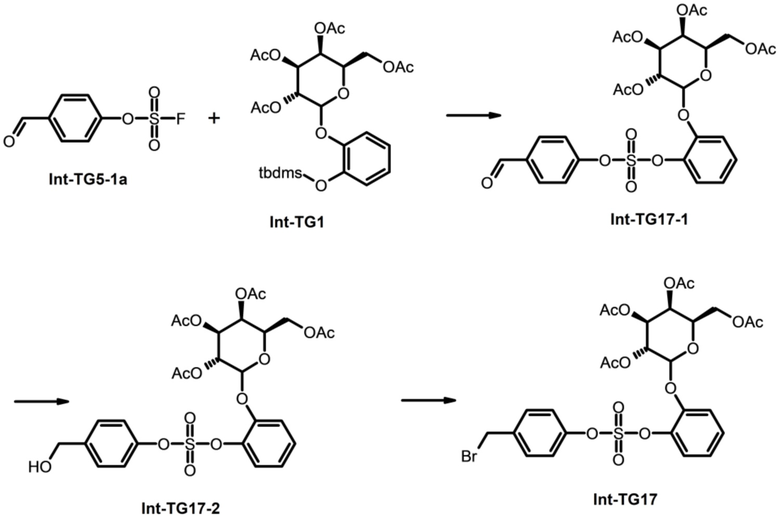
Соединение Int-TG17 синтезировали аналогичным путем синтеза, как описано в Примере 37.
Получение соединения Int-TG17-1
Выход 84%; ЭИ-МС m/z: 888 (M+1).
1H ЯМР (400 МГц, CDCl3) δ 10,04 (с, 1Н), 7,99-7,97 (м, 1Н), 7,56-7,51 (м, 2Н), 7,38-7,34 (м, 2Н), 7,31-7,27 (м, 2Н ), 7,15-7,08 (м, 1H), 5,58-5,51 (м, 1H), 5,48-5,45 (м, 1H), 5,12-5,07 (м, 2H), 4,27-4,22 (м, 1H), 4,18-4,13 (м, 1Н), 4,08-4,04 (м, 1Н), 2,19 (с, 3Н), 2,07 (с, 3Н), 2,06 (с, 3Н), 2,01 (с, 3Н).
Получение соединения Int-TG17-2
Выход 33% ЭИ-MCm/z: 649(M+1 Na).
1H ЯМР (400 МГц, CDCl3) δ 7,45-7,41 (м, 3Н), 7,35-7,33 (м, 2Н), 7,30-7,25 (м, 2Н), 7,15-7,10 (м, 1Н), 5,51-5,44 (м, 2H), 5,08-5,02 (м, 2H), 4,72 (д, J=5,2 Гц, 2H), 4,26-4,21 (м, 1H), 4,16-4,12 (м, 1H), 4,05-4,01 (м, 1H ), 2,22 (с, 3Н), 2,05 (с, 3Н), 2,04 (с, 3Н), 2,00 (с, 3Н).
Получение соединения Int-TG17
Выход 71% ЭИ-MCm/z: 713(M+ Na).
1H ЯМР (400 МГц, CDCl3) δ 7,46 (д, J=8,4 Гц, 2H), 7,35-7,32 (м, 3H), 7,28-7,26 (м, 2H), 7,14-7,09 (м, 1H), 5,58- 5,54 (м, 1H), 5,46-5,45 (м, 1H), 5,12-5,07 (м, 2H), 4,48 (с, 2H), 4,27-4,23 (м, 1H), 4,17-4,11 (м, 1H), 4,07-4,04 (м, 1H), 2,18 (с, 3H), 2,07 (с, 3H), 2,06 (с, 3H), 2,01 (с, 3H).
[Пример 51] Получение соединения IntA-Q10

К раствору N-метилбензолсульфонамида (208 мг, 1,21 ммоль) в ТГФ (5 мл) добавляли соединение IntA-Q2-2 (100 мг, 0,48 ммоль) и PPh3 (382 мг, 1,45 ммоль) в атмосфере N2. И затем по каплям добавляли DEAD (221 мкл, 1,21 ммоль), и смесь перемешивали в течение ночи при комнатной температуре и разбавляли EA (50 мл). Органический слой промывали H2O (40 мл) и солевым раствором (40 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntA-Q10 (143 мг, 82%).
1H ЯМР (400 МГц, CDCl3) δ 7,84 (д, J=7,6 Гц, 2H), 7,66-7,63 (м, 1H), 7,60-7,53 (м, 2H), 7,44 (д, J=8,8 Гц, 2H) 7,32 (д, J=8,4 Гц, 2H), 4,19 (с, 2H), 2,65 (с, 3H).
ЭИ-МС m/z: 360(M+1).
[Пример 52] Получение соединения IntB-Q8

Соединение IntB-Q8 синтезировали аналогичным путем синтеза, как описано в Примере 12.
Выход 16%; ЭИ-МС m/z: 656(M+1).
[Пример 53] Получение соединения IntB-Q9
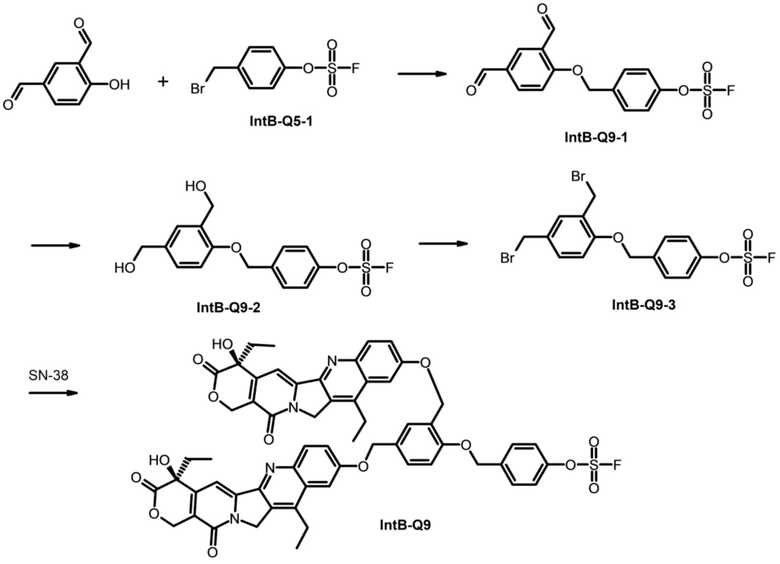
Соединение IntB-Q9 синтезировали аналогичным путем синтеза, как описано в Примере 37 и Примере 2.
Получение соединения IntB-Q9-1
Выход 77%
1H ЯМР (400 МГц, CDCl3) δ 10,54 (с, 1H), 9,97 (с, 1H), 8,38 (с, 1H), 8,14 (д, J=8,4 Гц, 1H), 7,59 (д, J=8 Гц, 2H), 7,43 (д, J=8,8 Гц, 2H), 7,19 (д, J=8,4 Гц, 1H), 5,33 (с, 2H).
Получение соединения IntB-Q9-2
Выход 94%; ЭИ-МС m/z: 365(M++Na).
1H ЯМР (400 МГц, ДМСО-d6) δ 7,67-7,61 (м, 4H), 7,37 (с, 1H), 7,12 (д, J=8,8 Гц, 1H), 6,94 (д, J=8,4 Гц, 1H) 5,19 (с, 2H), 5,06-5,02 (м, 2H), 4,56 (д, J=4,8 Гц, 2H), 4,42 (д, J=5,6 Гц, 2H).
Получение соединения IntB-Q9-3
Выход 82%
1H ЯМР (400 МГц, CDCl3) δ 7,62 (д, J=8,4 Гц, 2H), 7,41-7,38 (м, 3H), 7,32 (д, J=8,4 Гц, 1H), 6,86 (д, J=8,8 Гц, 1H), 5,19 (с, 2H), 4,57 (с, 2H), 4,47 (с, 2H).
Получение соединения IntB-Q9
ЭИ-МС m/z: 1092(M+1).
[Пример 54] Получение соединения IntB-Q10
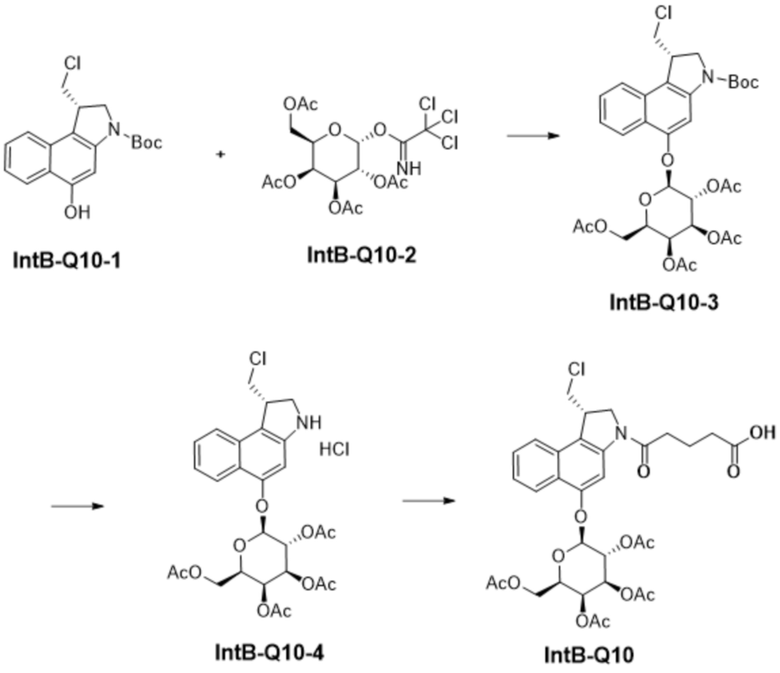
Получение соединения IntB-Q10-1
Соединение IntB-Q10-1 синтезировали аналогичным путем синтеза, как описано в документе [см. Mol. Pharmaceutics 2015, 12, 1813-1835]
Получение соединения IntB-Q10-2
Соединение IntB-Q10-2 синтезировали аналогичным путем синтеза, как описано в документе [см. Angew. Chem. Int. Ed. 2010, 49, 7336-7339 и WO2015110935A1]
Получение соединения IntB-Q10-3
К раствору соединения IntB-Q10-1 (80 мг, 0,239 ммоль) и соединения IntB-Q10-2 (118 мг, 0,239 ммоль) в ДХМ (10 мл) добавляли молекулярное сито и BF3⋅OEt2 (14,8 мкл, 0,12 ммоль) при 0°С в атмосфере N2. После перемешивания в течение 2 часов смесь фильтровали через целит, промывали ДХМ (50 мл) и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q10-3 (105 мг, 66%) в виде белой пены.
1H ЯМР (400 МГц, CDCl3) δ 8,12 (д, J=8,0 Гц, 1H), 7,89 (уш. с, 1H), 7,63 (д, J=8,0 Гц, 1H), 7,50 (м, 1H), 7,35 (м., 1H), 5,70 (м, 1H), 5,51 (с, 1H), 5,33 (м, 1H), 5,20 (м, 1H), 4,23 (м, 3H), 4,11 (м, 2H), 3,93 (м, 2H), 3,42 (т, J=10,8 Гц, 1H), 2,18 (с, 3H), 2,08 (с, 3H), 2,04 (с, 3H), 2,00 (с, 3H), 1,55 (с, 9H). ЭИ-МС m/z: 564,4(M+1).
Получение соединения IntB-Q10-4
Соединение IntB-Q10-3 (100 мг, 0,15 ммоль) растворяли в ДХМ (2 мл) и затем добавляли 4N HCl в 1,4-диоксане (1 мл) при 0°C в атмосфере N2. После перемешивания в течение 4 часов реакционную смесь концентрировали при пониженном давлении.
Реакционную смесь перемешивали при комнатной температуре в течение 4 часов в атмосфере N2. Соединение IntB-Q10-3 использовали непосредственно на следующей стадии без дополнительной очистки (90 мг, 99%).
ЭИ-МС m/z: 564,2(M+1).
Получение соединения IntB-Q10
К раствору соединения IntB-Q10-3 (90 мг, 0,149 ммоль) в ТГФ (5 мл) добавляли глутаровый ангидрид (18,8 мкл, 0,164 ммоль), Et3N (52 мкл, 0,373 ммоль) и 4-DMAP (2 мг, 0,015 ммоль) при комнатной температуре в атмосфере N2. Реакционную смесь перемешивали при комнатной температуре в течение 2 часов и очищали препаративной ВЭЖХ, в результате чего получали соединение IntB-Q10 (30 мг, 30%) в виде белого твердого вещества.
ЭИ-МС m/z: 678,3(M+1).
[Пример 55] Получение соединения IntB-Q11 и IntB-Q12

Соединения IntB-Q11-2 и IntB-Q12-2 синтезировали аналогичным путем синтеза, как описано в Примере 6 и Примере 6.
Получение соединения IntB-Q11-1
Выход 98%
1H ЯМР (400 МГц, CDCl3) δ 8,37 (уш.с, 1H) 8,02 (д, J=8,8 Гц, 1H), 7,75 (д, J=8,4 Гц, 1H), 7,61 (т, J=7,2, 1H), 7,51 (т, J=8,0 Гц, 1H), 4,32 (уш. с, 1H), 4,18 (т, J=8,8, 1H), 4,05 (м, 1H), 3,93 (дд, J=11,2, 2,8 Гц, 1H) 3,52 (т, J=10,8 Гц, 1H), 1,61 (с, 9H). ЭИ-МС m/z: 438,2(M+1+Na).
Получение соединения IntB-Q11-2
Выход 79%
1H ЯМР (400 МГц, CDCl3) δ 8,09 (уш. с, 1H) 7,77 (м, 3H), 7,57 (т, J=7,2 Гц, 1H), 7,46 (т, J=7,6 Гц, 1H), 7,32 (м, 1H), 6,78 (м, 1H), 5,56 (м, 1H), 5,46 (д, J=2,8 Гц, 1H), 5,22 (д, J=7,6 Гц, 1H), 5,12 (дд, J=10,4, 3,2 Гц, 1H), 4,30 (уш. с, 1H), 4,25-4,02 (м, 5H), 3,93 (м, 1H), 3,60 (м, 15H), 3,31 (м, 2H), 2,17 (с, 3H), 2,04 (с, 3Н), 1,95 (с, 6Н), 1,56 (с, 9Н). ЭИ-МС m/z: 1080,6(M+1).
Получение соединения IntB-Q11
Соединение IntB-11-2 (50 мг, 0,046 ммоль) растворяли в 4N HCl в 1,4-диоксане (1 мл) при 0°C в атмосфере N2. После перемешивания при комнатной температуре в течение 4 часов смесь разбавляли ДХМ (5 мл) и концентрировали. Соединение IntB-Q11 использовали непосредственно на следующей стадии без дополнительной очистки (47 мг, 99%).
ЭИ-МС m/z: 980,5(M+1).
Получение соединения IntB-Q12-1
Выход 46%; ЭИ-МС m/z: 452,2(M+1+Na).
1H ЯМР (400 МГц, CDCl3) δ 8,4 (уш. с, 1H) 7,91 (дд, J=6,8, 2,4 Гц, 1H), 7,38 (м, 2H), 4,34 (м, 1H), 4,23 (м, 1H), 4,05 (м, 1H), 3,62 (д, J=10,4, 1H), 3,30 (т, J=11,2, 1H), 2,83 (с, 1H), 1,61 (с, 9H).
Получение соединения IntB-Q12-2
Выход 71%; ЭИ-МС m/z: 1094,4(M+1).
1H ЯМР (400 МГц, CDCl3) δ 8,33 (уш. с, 1H) 7,99 (д, J=7,2 Гц, 1H), 7,78 (м, 2H), 7,35 (м, 3H), 6,87 (м, 1H), 5,54 ( м, 1H), 5,46 (д, J=2,8 Гц, 1H), 5,22 (д, J=8,0 Гц, 1H), 5,12 (дд, J=10,4, 3,2 Гц, 1H), 4,33 (м, 1H), 4,26-4,01 (м, 5H), 3,61 (м, 14H), 3,32 (м, 3H), 2,83 (с, 1H), 2,21 (с, 3H), 2,07 (с, 3H), 1,99 (с, 6H) 1,57 (с, 9H).
Получение соединения IntB-Q12
Выход 99%; ЭИ-МС m/z: 994,5(M+1).
[Пример 55a] Получение соединения IntB-Q13

Соединение IntB-Q13 синтезировали аналогичным путем синтеза, как описано в документе Mol. Pharmaceutics 2015, 12, 1813-1835, включенном в настоящий документ посредством ссылки.
[Пример 56] Получение соединения IntB-Q14

Соединение IntB-Q14 синтезировали аналогичным путем синтеза, как описано в документе WO 2015038426A1, включенном в настоящий документ путем ссылки.
[Пример 56] Получение соединения IntB-Q15

Получение соединения IntB-Q15-1
К раствору соединения IntB-Q10-1 (55 мг, 0,016 ммоль) в ДХМ (2 мл) добавляли ацетилхлорид (26,8 мкл, 0,032 ммоль) и пиридин (30 мкл, 0,032 ммоль) при 0°С в атмосфере N2. После перемешивания в течение 30 минут реакционную смесь нагревали до комнатной температуры и дополнительно перемешивали в течение 1 часа. Смесь разбавляли ЕА (20 мл) и промывали Н2О (10 мл). Соединение IntB-Q15-1 (50 мг, 80%) в виде бледно-желтой пены.
ЭИ-МС m/z: 398,2(M+1+Na).
1H ЯМР (400 МГц, CDCl3) δ 8,02 (уш. с, 1H) 7,79 (д, J=8,0 Гц, 1H), 7,72 (т, J=8,8 Гц, 1H), 7,51 (м, 1H), 7,38 (м, 1H), 4,16 (м, 1H), 4,04 (м, 1H), 3,92 (м, 1H), 3,71 (м, 1H), 3,36 (м, 1H), 2,27, (с, 3H), 1,54 (с, 9H).
Получение соединения IntB-Q15
Соединение IntB-Q15 синтезировали аналогичным путем синтеза, как описано в Примере 55.
Выход 99%; ЭИ-МС m/z: 276,2(M+1).
[Пример 57] Получение соединения IntB-Q16

Получение соединения IntB-Q16-1
К раствору диметил-5-гидроксиизофталата (5,0 г, 23,79 ммоль) в ТГФ (300 мл) добавляли ЛАГ (3,6 г, 95,15 ммоль) при 0°С в атмосфере азота. После перемешивания при комнатной температуре в течение 17 часов добавляли 15% водный раствор NaOH (10 мл) и дистиллированную воду (30 мл). После того как смесь экстрагировали ЕА (500 мл), органический слой промывали солевым раствором (100 мл), сушили над Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q16-1 (3,02 г, 82%).
1H ЯМР (400 МГц, ДМСО-d6) δ 9,21 (с, 1H), 6,66 (с, 1H), 6,58 (с, 2H), 5,07 (т, J=5,6 Гц, 2H), 4,38 (д, J=5,6 Гц, 4H).
Получение соединения IntB-Q16-2
К раствору соединения IntB-Q16-1 (881,1 мг, 5,72 ммоль) в АсОН (15 мл) добавляли 33% HBr в АсОН (2,6 мл, 14,29 ммоль) при 0°С в атмосфере N2. После этого смесь нагревали до 65°С и перемешивали в течение 8 часов, и снова перемешивали при комнатной температуре в течение 2 дней. Добавляли ДХМ (50 мл) и воду (30 мл). Органический слой промывали водным раствором NaHCO3, сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматограммой с получением соединения IntB-Q16-2 (1,1 г, 71%).
1H ЯМР (400 МГц, CDCl3) δ 6,99 (с, 1Н), 6,81 (с, 2Н), 4,85 (с, 1Н), 4,41 (с, 4Н).
Получение соединения IntB-Q16-3
К раствору соединения IntB-Q16-2 (1,0 г, 3,57 ммоль) в ДХМ (35 мл) добавляли TEA (0,45 мл, 3,21 ммоль) при комнатной температуре в атмосфере N2. Смесь перемешивали в течение 1 часа и добавляли ДХМ (50 мл) и воду (30 мл). Органический слой промывали водным раствором NaHCO3, сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q16-3 (941,7 мг, 73%).
1H ЯМР (400 МГц, CDCl3) δ 7,47 (с, 1H), 7,32 (с, 2H), 4,46 (с, 4H).
Получение соединения IntB-Q16
К раствору соединения IntB-Q16-3 (200 мг, 0,55 ммоль) и мономеру PBD (342,3 мг, 1,32 ммоль), полученному способом, аналогичным описанному в ЕР 20071813614 А1 в ДМФА (5 мл) добавляли K2CO3 (183,2 мг, 1,32 ммоль) при комнатной температуре в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 2 часов и добавляли ЕА (20 мл) и воду (5 мл). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения IntB-Q8 (254 мг, 64%).
1H ЯМР (400 МГц, CDCl3) δ 7,66 (д, J=4,4 Гц, 2H), 7,55 (с, 3H), 7,42 (с, 2H), 6,81 (с, 2H), 5,27-5,17 (м, 8H) 4,29 (с, 4), 3,97 (с, 6H), 3,89-3,85 (м, 2H), 3,15-3,09 (м, 2H), 2,93 (д, J=16 Гц, 2H). ЭИ-МС m/z: 717(M+1).
[Пример 58] Получение соединения A-1

Получение соединения A-1a
К раствору соединения IntA-Q1 (46 мг, 0,135 ммоль) и соединения Int-TG1 (75 мг, 0,135 ммоль) в ацетонитриле (3 мл) добавляли DBU (4 мкл, 0,027 ммоль). Смесь перемешивали при комнатной температуре в течение 12 часов в атмосфере N2. Смесь экстрагировали EA (30 мл × 2). Органический слой промывали водой (30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения A-1a (105 мг, 98%).
1H ЯМР (400 МГц, CDCl3) δ 7,33-7,26 (м, 5H), 7,21-7,17 (м, 2H), 7,14-7,08 (м, 1H), 5,56 (дд, J=2,4 Гц, 8,0 Гц, 1H) 5,46 (д, J=3,2 Гц, 1H), 5,12-5,08 (м, 2H), 5,06-5,00 (м, 1H), 4,63-4,56 (м, 1H), 4,28-4,23 (м, 1H), 4,18 -4,13 (м, 1Н), 4,08-4,04 (м, 1Н), 3,72 (с, 3Н), 3,18-3,03 (м, 2Н), 2,19 (с, 3Н), 2,07 (с, 3Н), 2,06 (с, 3Н), 2,01 (с, 3Н), 1,42 (с, 9Н). ЭИ-МС m/z: 798(M+1).
Получение соединения A-1
К раствору соединения A-1a (100 мг, 0,13 ммоль) в ТГФ (4 мл) и метаноле (1 мл) по каплям добавляли LiOH⋅H2O (33 мг, 0,79 ммоль), растворенный в воде (1 мл) при 0°С. После перемешивания при 0°С в течение 2 часов реакцию гасили 1N водной соляной кислотой (3 мл). Смесь очищали ВЭЖХ с получением соединения А-1 (65 мг, 85%).
ЭИ-МС m/z: 616(M+1).
[Пример59] Получение соединения A-2

Соединение A-2a синтезировали аналогичным путем синтеза, как описано в Примере 58.
Выход 95%; ЭИ-МС m/z: 1043(M+1).
1H ЯМР (400 МГц, CDCl3) δ 7,80 (с, 1H), 7,75 (дд, J=8,0 Гц, 1H), 7,33-7,20 (м, 5H), 7,0 (м, 1H), 5,76 (дд, J=8,0, 10,4 Гц, 1H), 7,47 (д, J=3,2 Гц, 1H), 5,17-5,10 (м, 3H), 4,58 (м, 1H), 4,25-4,08 (м, 3H), 3,72 (с, 3H) ), 3,66-3,60 (м, 13H), 3,34 (т, J=4,4 Гц, 2H), 2,17 (с, 3H), 2,07 (с, 3H), 2,06 (с, 3H), 2,01 (с, 3H) 1,41 (с, 9H).
Получение соединения A-2
Выход 53%; ЭИ-MCm/z: 860(M+1).
[Пример 60] Получение соединения A-3
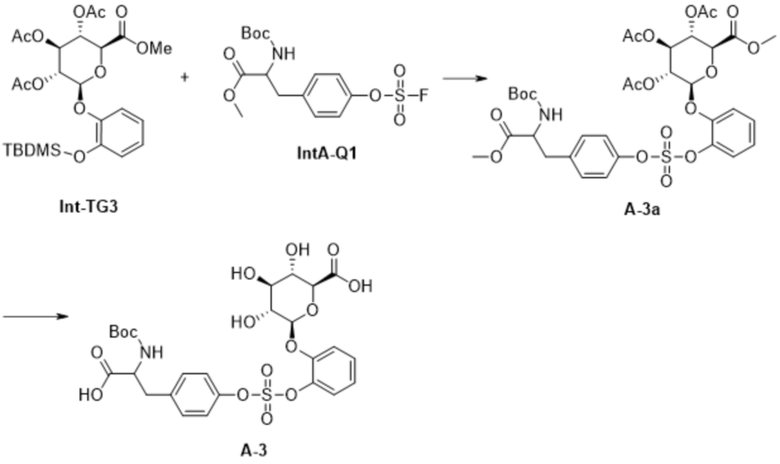
Соединение A-3 синтезировали аналогичным путем синтеза, как описано в Примере 58.
Получение соединения A-3a
ЭИ-МС m/z: 806(M+1+Na).
Получение соединения A-3
Выход 33%; ЭИ-МС m/z: 652(M+1+Na).
1H ЯМР (400 Гц, CD3OD) δ 7,42-7,31 (м, 7H), 7,14-7,10 (м, 1H), 5,13 (д, J=7,2 Гц, 1H), 4,42-4,38 (м, 1H), 4,03 (д, J=10 Гц, 1H), 3,67 (т, J=9,6 Гц, 1H), 3,55-3,43 (м, 2H), 3,27 дд, J=9,2, 5,2 Гц, 1H), 3,16-2,97 ( м, 1Н), 1,39 (с, 9Н).
[Пример 61] Получение соединения A-4

Получение соединения A-4a
Соединение A-4a синтезировали аналогичным путем синтеза, как описано в Примере 58.
ЭИ-МС m/z: 1235(M+1).
Получение соединения A-4b
К раствору соединения A-4a (41 мг, 0,03 ммоль) в MeOH (2,66 мл) добавляли K2CO3 (14 мг, 0,10 ммоль) при 0°С и смесь перемешивали при 0°C в течение 2 часов. К ней добавляли K2CO3 (9 мг, 0,07 ммоль), и смесь перемешивали при 0°С и разбавляли EA (20 мл × 2). Органический слой промывали H2O (20 мл) и солевым раствором (20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении с получением соединения A-4a (35 мг), которое использовали для дальнейшей очистки.
ЭИ-МС m/z: 1067(M+1).
Получение соединения A-4
К раствору соединения A-4b (17 мг, 0,02 ммоль) в ТГФ (640 мкл) добавляли AcOH (3 мкл, 0,05 ммоль) и TBAF (48 мкл, 0,05 ммоль) при 0°С в атмосфере N2. После перемешивания в течение 1,5 часов дополнительно добавляли TBAF (48 мкл, 0,05 ммоль) и перемешивали при 0°С в течение 2 часов. Смесь очищали препаративной ВЭЖХ, в результате чего получали соединение А-4 (3 мг, 22%).
ЭИ-МС m/z: 724(M+1).
[Пример 62] Получение соединения A-5
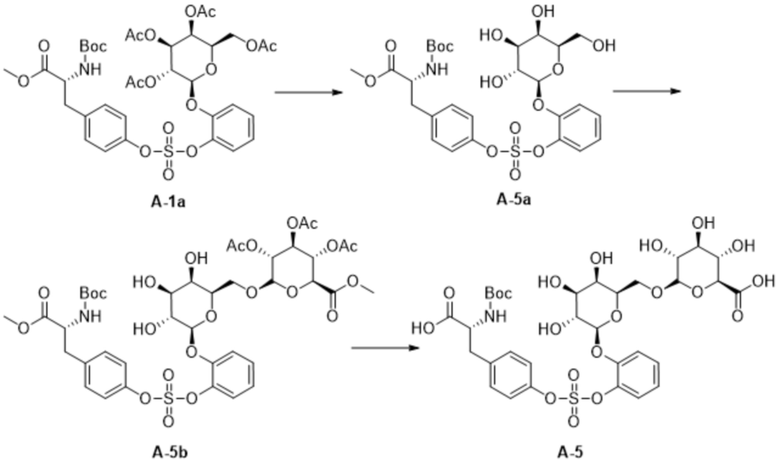
Получение соединения A-5a
Соединение A-5a синтезировали аналогичным путем синтеза, как описано в Примере 58.
Выход 88%; ЭИ-MCm/z: 630(M+1).
Получение соединения A-5b
К раствору соединения A-5a (100 мг, 0,16 ммоль) и метилового эфира ацетобром-α-D-глюкуроновой кислоты (64 мг, 0,16 ммоль, CAS # 21085-72-3) в Et2O (10 мл) добавляли AgOTf (204 мг, 0,79 ммоль) и триметилпиридин (106 мг, 0,87 ммоль) при 0°С. Смесь перемешивали при комнатной температуре в течение 6 часов и разбавляли EA (50 мл). Промывали водным раствором 2N HCl (10 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток отделяли и очищали препаративной ВЭЖХ с получением соединения A-5b (14 мг, 9%).
ЭИ-МС m/z: 946(M+1).
Получение соединения A-5
Соединение A-5 синтезировали аналогичным путем синтеза, как описано в Примере 58.
ЭИ-МС m/z: 792(M+1).
[Пример 63] Получение соединения A-6
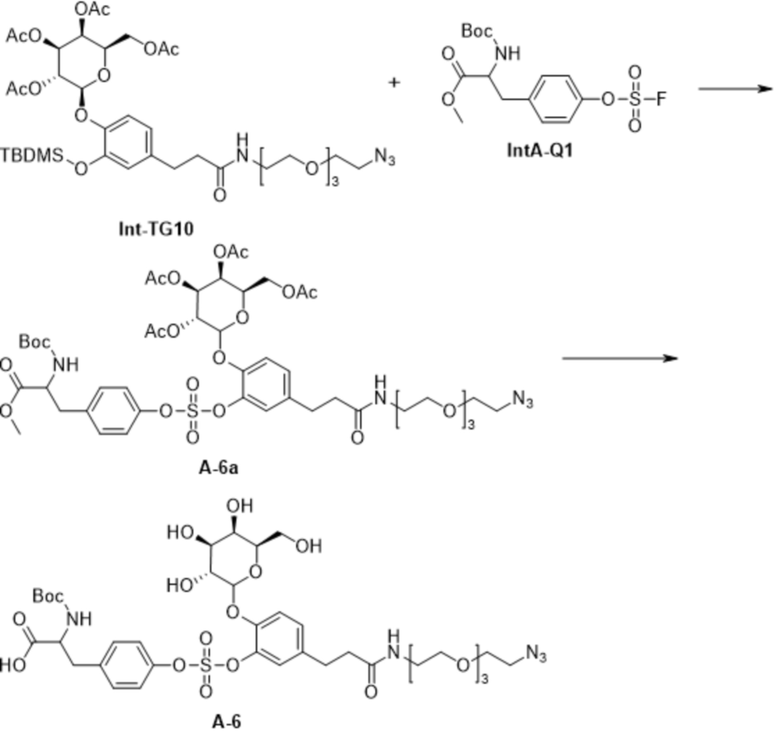
Соединение A-6 синтезировали аналогичным путем синтеза, как описано в Примере 60.
Получение соединения A-6a
Выход 53%
ЭИ-МС m/z: 1071(M+1).
Получение соединения A-6
Выход 16%
ЭИ-МС m/z: 888(M+1).
[Пример 64] Получение соединения A-7

Получение соединения A-7a
К раствору соединения Int-TG4 (73,9 мг, 0,29 ммоль) и соединения IntA-Q1 (100 мг, 0,27 ммоль) в безводном ацетонитриле (2 мл) добавляли BEMP (31 мкл, 0,11 ммоль) при комнатной температуре в атмосфере N2. Смесь перемешивали при 100°С в течение 5 часов в условиях микроволнового излучения. Смесь разделяли и очищали препаративной ВЭЖХ с получением соединения A-7a (61,2 мг, 46%).
ЭИ-МС m/z: 519(M+1+Na).
Получение соединения A-7b
Соединение A-7b синтезировали аналогичным путем синтеза, как описано в Примере 58.
Выход 64%; ЭИ-MCm/z: 505(M+1+Na).
Получение соединения A-7
К раствору соединения A-7b (39 мг, 0,08 ммоль) в метаноле (2 мл) по каплям добавляли пыль Zn (6,4 мг, 0,10 ммоль) и формиат аммония (8,22 мг, 0,13 ммоль) при комнатной температуре в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 2 часов и фильтровали через целит, промывали МеОН и концентрировали. Остаток отделяли и очищали препаративной ВЭЖХ с получением соединения А-7.
ЭИ-МС m/z: 469(M+1).
[Пример 65] Получение соединения A-8

Соединение A-8 синтезировали аналогичным путем синтеза, как описано в Примере 60.
ЭИ-МС m/z: 588(M+1+Na).
[Пример 66] Получение соединения A-9

Соединение A-9 синтезировали аналогичным путем синтеза, как описано в Примере 60.
ЭИ-МС m/z: 608(M+1).
[Пример 67] Получение соединения A-10
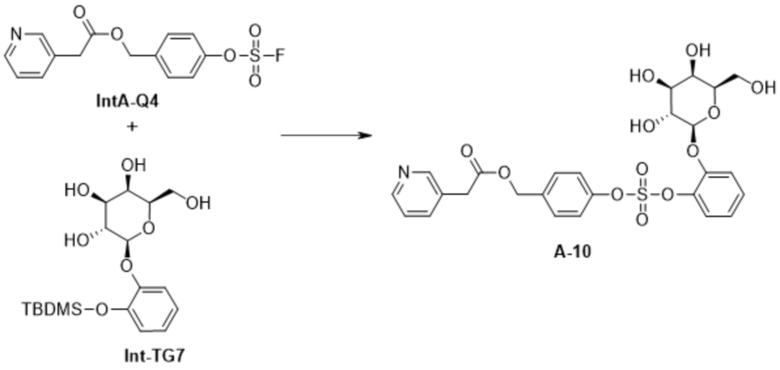
К раствору соединения IntA-Q4 (23 мг, 0,07 ммоль) и соединения Int-TG7 (30 мг, 0,08 ммоль) в безводном ацетонитриле (1 мл) добавляли BEMP (11,2 мкл, 0,04 ммоль) при комнатной температуре в атмосфере N2.
Смесь перемешивали в течение ночи при комнатной температуре, разделяли и очищали препаративной ВЭЖХ с получением соединения А-10 (0,3 мг).
ЭИ-МС m/z: 578(M+1).
[Пример 68] Получение соединения A-11

Соединение A-11 синтезировали аналогичным путем синтеза, как описано в Примере 67.
Выход 65%; ЭИ-МС m/z: 603(M+1).
1H ЯМР (400 МГц, CDCl3) δ 8,19 (дд, J=6,8, 1,2 Гц, 1H), 8,02 (д, J=8,0 Гц, 1H), 7,68 (т, J=6,4 Гц, 1H), 7,49 (т, J=7,2 Гц, 1H), 7,33-7,23 (м, 3H), 7,22 (д, J=8,0 Гц, 1H), 7,17 (д, J=8,8 Гц, 2H), 7,08 (дд, J=7,2, 1,2 Гц, 1H), 7,01 (тд, J=6,8, 1,2 Гц, 1H), 5,56 (с, 2H), 4,99 (д, J=8,4 Гц, 1H), 4,59 (кв, J=7,2, 6,4 Гц, 1H), 3,14 (дд, J=8,4, 5,6 Гц, 1H), 3,03 (дд, J=7,6, 6,0 Гц, 1H), 1,42 (с, 9H).
[Пример 69] Получение соединения A-12
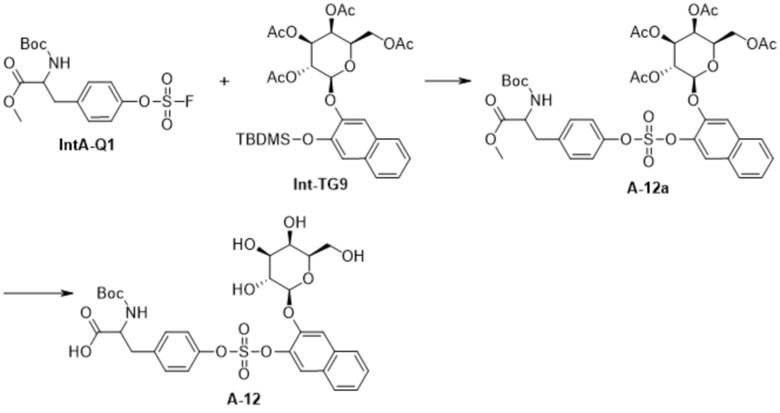
Получение соединения A-12a
Соединение A-12a синтезировали аналогичным путем синтеза, как описано в Примере 67.
Выход 82%; ЭИ-МС m/z: 870(M+1+Na).
1H ЯМР (400 МГц, CDCl3) δ 7,80-7,75 (м, 3Н), 7,61 (с, 1Н), 7,52-7,47 (м, 2Н), 7,33 (д, J=8,0 Гц, 2Н), 7,21 (д, J=8,1 Гц, 2H), 5,63 (т, J=2,2 Гц, 1H), 5,50 (с, 1H), 5,23 (д, J=7,6 Гц, 1H), 5,15 (д, J=10,4 Гц, 1H) 5,08-4,98 (м, 1H), 4,62-4,54 (м, 1H), 4,36-4,26 (м, 1H), 4,24-4,14 (м, 2H), 3,72 (с, 3H), 3,22-3,02 (м, 2H), 2,20 (с, 3H), 2,08 (с, 6H), 2,02 (с, 3H), 1,42 (с, 9H)
Получение соединения A-12
Соединение A-12 синтезировали аналогичным путем синтеза, как описано в Примере 58.
Выход 93%; ЭИ-MCm/z: 688(M+1+Na).
[Пример 70] Получение соединения A-13
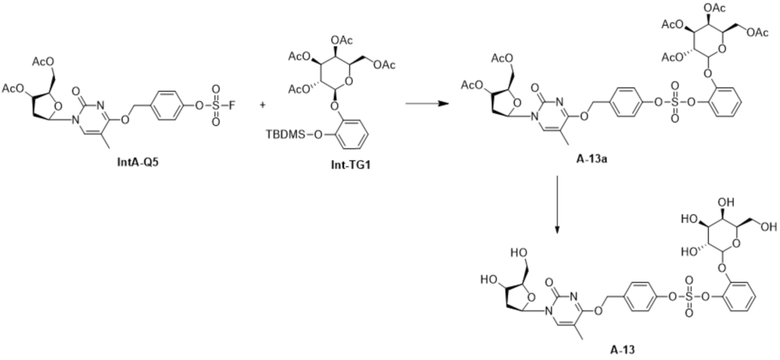
Получение соединения A-13a
Соединение A-13a синтезировали аналогичным путем синтеза, как описано в Примере 67.
Выход 43%; ЭИ-МС m/z: 935(M+1).
Получение соединения A-13
Соединение A-13 синтезировали аналогичным путем синтеза, как описано в Примере 61.
Выход 61%; ЭИ-MCm/z: 683(M+1).
[Пример71] Получение соединения A-14
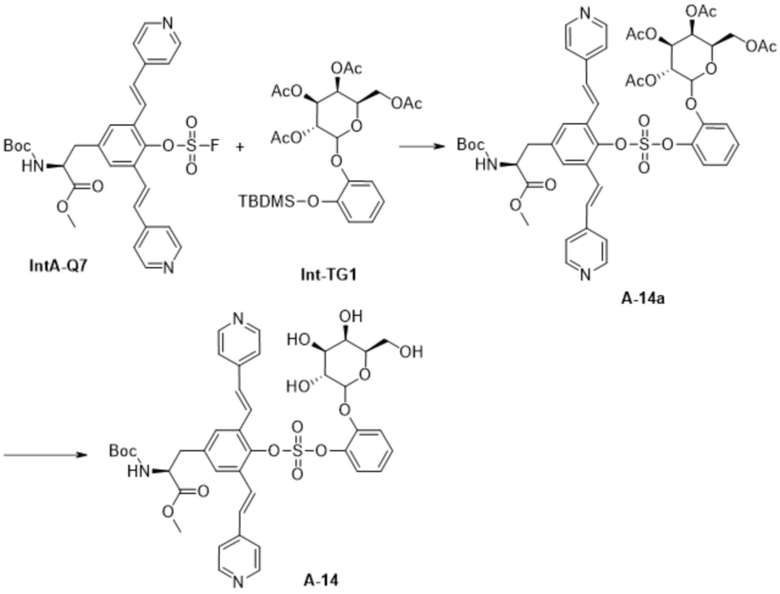
Получение соединения A-14a
Соединение A-14a синтезировали аналогичным путем синтеза, как описано в Примере 66.
Выход колич.; ЭИ-MCm/z: 1004(M+1).
Получение соединения A-14
Соединение A-14a синтезировали аналогичным путем синтеза, как описано в Примере 61.
Выход 88%; ЭИ-MCm/z: 836(M+1).
[Пример72] Получение соединения A-15
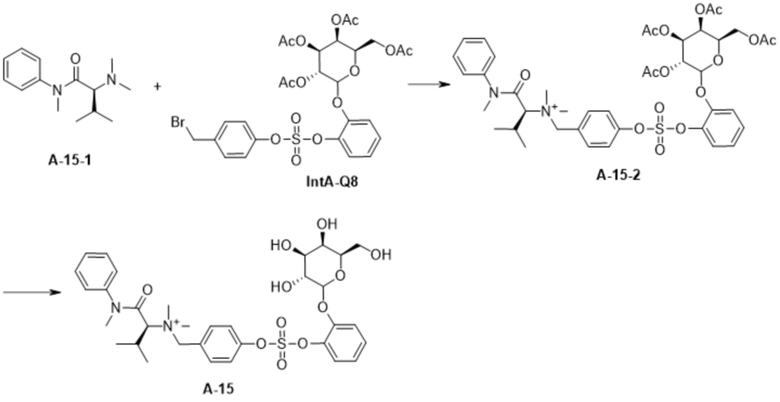
Получение соединения A-15-2
К раствору соединения A-15-1 (53 мг, 76,9 мкмоль) и IntA-Q8 (22 мг, 92,3 мкмоль) в ДМФА (2 мл) по каплям добавляли DIPEA (27 мкл, 0,15 ммоль) в атмосфере N2. После перемешивания в течение ночи при комнатной температуре смесь разделяли и очищали препаративной ВЭЖХ с получением соединения А-15-2 (25,9 мг, 40%).
ЭИ-МС m/z: 843(M+1).
Получение соединения A-15
Соединение A-15 синтезировали аналогичным путем синтеза, как описано в Примере 61.
Выход 51%; ЭИ-МС m/z: 675(M+1).
[Пример 73] Получение соединения A-17
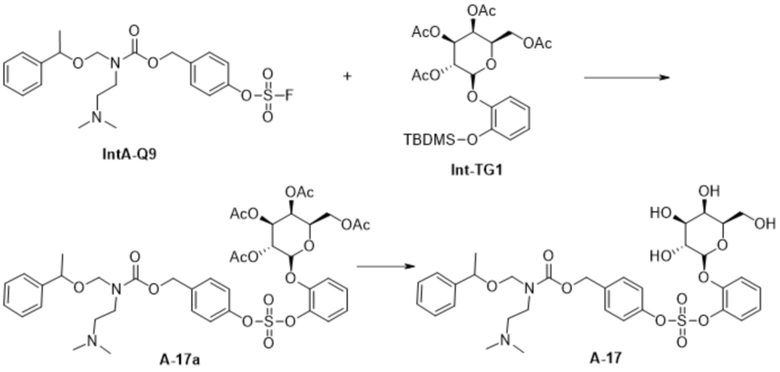
Получение соединения A-17a
Соединение A-17a синтезировали аналогичным путем синтеза, как описано в Примере 60.
Выход 51%; ЭИ-МС m/z: 875(M+1).
Получение соединения A-17
Соединение A-17 синтезировали аналогичным путем синтеза, как описано в Примере 71.
Выход 52,2%; ЭИ-MCm/z: 707(M+1).
[Пример74] Получение соединения A-18
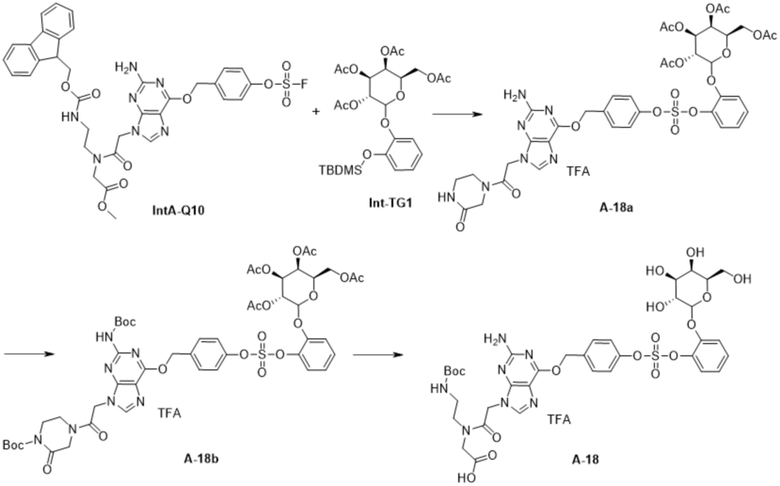
Получение соединения A-18a
К раствору соединения IntA-Q10 (118 мг, 0,16 ммоль) и соединения Int-TG1 (107 мг, 0,19 ммоль) в ACN (2 мл) и ДМФА (0,2 мл) добавляли BEMP (23,3 мкл, 0,08 ммоль) в атмосфере N2. После перемешивания при комнатной температуре в течение 2,5 минут к нему дополнительно добавляли DBU (12 мкл, 0,08 ммоль), и смесь перемешивали при комнатной температуре в течение 2 часов и разбавляли EA (30 мл × 2). Органический слой промывали H2O (30 мл) и солевым раствором (20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток отделяли и очищали препаративной ВЭЖХ с получением соединения А-18а (22,5 мг, 14%).
ЭИ-МС m/z: 900(M+1).
Получение соединения A-18b
К раствору соединения A-18a (22,5 мг, 0,022 ммоль) в ACN (1 мл) добавляли Boc2O (14,5 мг, 0,066 ммоль) и DMAP (2,7 мг, 0,022 ммоль) в атмосфере N2. После перемешивания в течение ночи при комнатной температуре к нему дополнительно добавляли Boc2O (4,8 мг, 0,022 ммоль) и DMAP (1,4 мг, 0,011 ммоль), и смесь перемешивали при комнатной температуре в течение 5 часов. Смесь разделяли и очищали препаративной ВЭЖХ с получением соединения А-18 (10 мг, 37%).
ЭИ-МС m/z: 1101(M+1).
Получение соединения A-18
Соединение A-18 синтезировали аналогичным путем синтеза, как описано в Примере 58.
ЭИ-МС m/z: 850(M+1).
[Пример 75] Получение соединения A-19
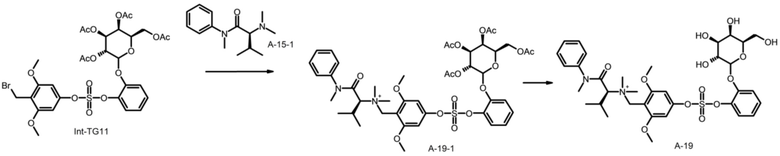
Соединение A-19 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения A-19-1
Выход 44%; ЭИ-МС m/z: 904 (M+1).
Получение соединения A-19
Выход 70%; ЭИ-МС m/z: 736 (M+1).
[Пример 76] Получение соединения A-20
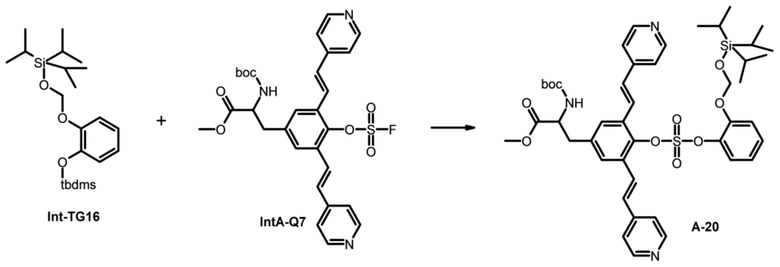
Соединение A-20 синтезировали аналогичным путем синтеза, как описано в Примере 71.
Выход 68%; ЭИ-MCm/z: 861(M+1).
[Пример 77] Получение соединения A-21

Получение соединения A-21a
N-Boc-3-(4-пиридил)-D-аланин (300 мг, 0,06 ммоль) и DMAP (275 мг, 2,25 ммоль) растворяли в МеОН (5 при 0°С). DCC (465 мг, 2,25 ммоль) добавляли при 0°С, смесь перемешивали при 0°С в течение 2 часов. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение ночи. Смесь разбавляли ЕА (30 мл), фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения A-21a.
1H ЯМР (400 МГц, ДМСО-d6) δ 8,46 (д, J=5,6 Гц, 2H), 7,37 (д, J=8 Гц, 1H), 7,26 (д, J=5,6 Гц, 2H), 4,29-4,23 (м, 1Н), 3,63 (с, 3Н), 3,06-3,01 (м, 1Н), 2,89-2,83 (м, 1Н), 1,31 (с, 9Н).
ЭИ-МС m/z: 281(M+1).
Соединение A-21 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения A-21b
Выход 29%; ЭИ-МС m/z: 950(M+1)
Получение соединения A-21
Выход 47%; ЭИ-MCm/z: 768(M+1).
[Пример 78] Получение соединения A-22
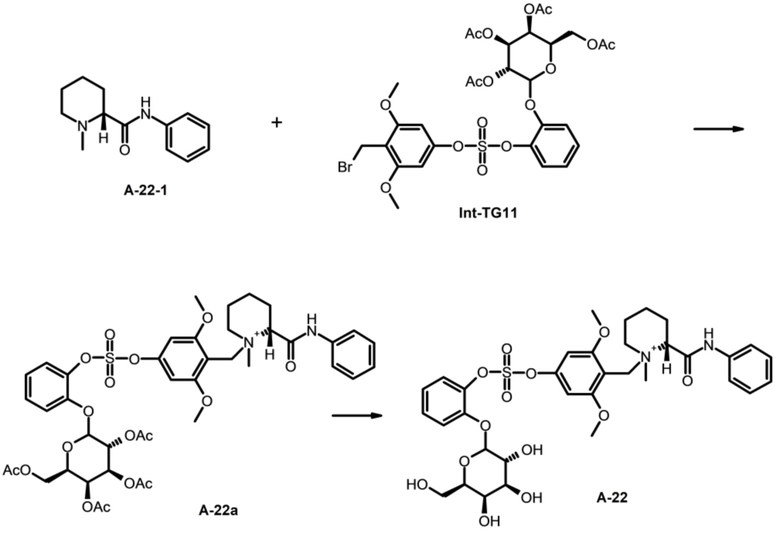
Соединение A-22 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения A-22a
Выход 68% ЭИ-MCm/z: 888(M+1).
Получение соединения A-22
Выход 56% ЭИ-MCm/z: 720(M+1).
[Пример 79] Получение соединения A-23
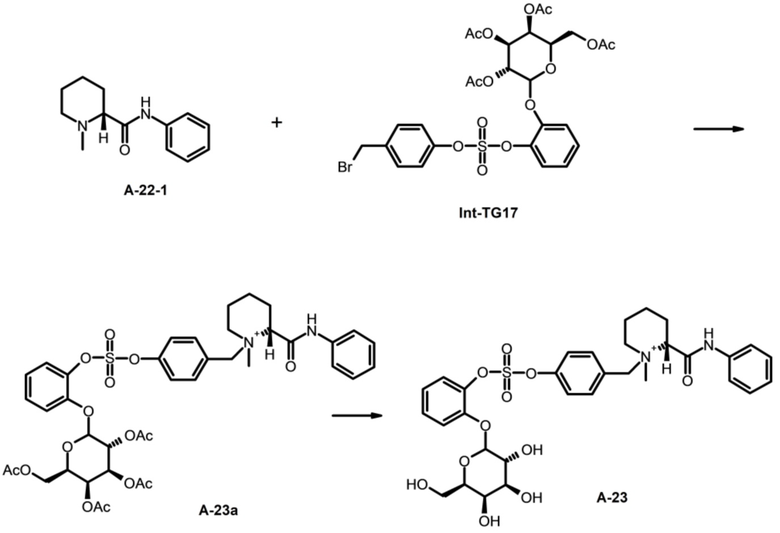
Соединение A-22 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения A-22a
Выход 57% ЭИ-MCm/z: 828(M+1).
Получение соединения A-22
Выход 72% ЭИ-MCm/z: 660(M+1).
[Пример 80] Получение соединения A-24
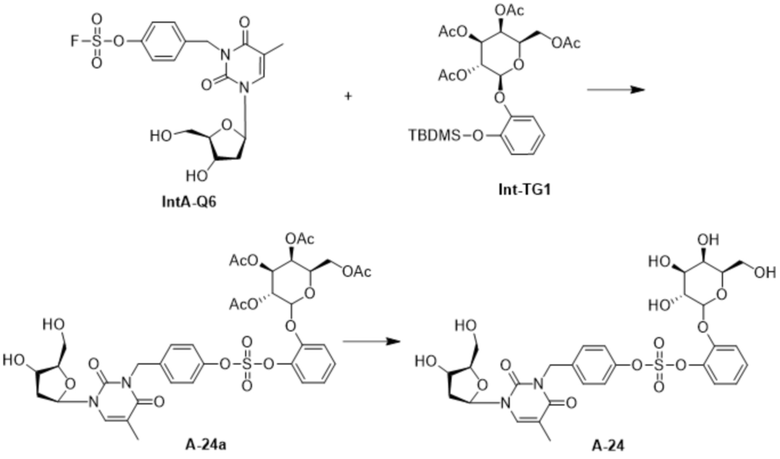
Соединение A-24 синтезировали аналогичным путем синтеза, как описано в Примере 69.
Получение соединения A-24a
Выход 33%; ЭИ-МС m/z: 851(M+1).
Получение соединения IntA-Q5
Выход 80%; ЭИ-MCm/z: 705(M+1+Na).
[Пример 81] Получение соединения A-25
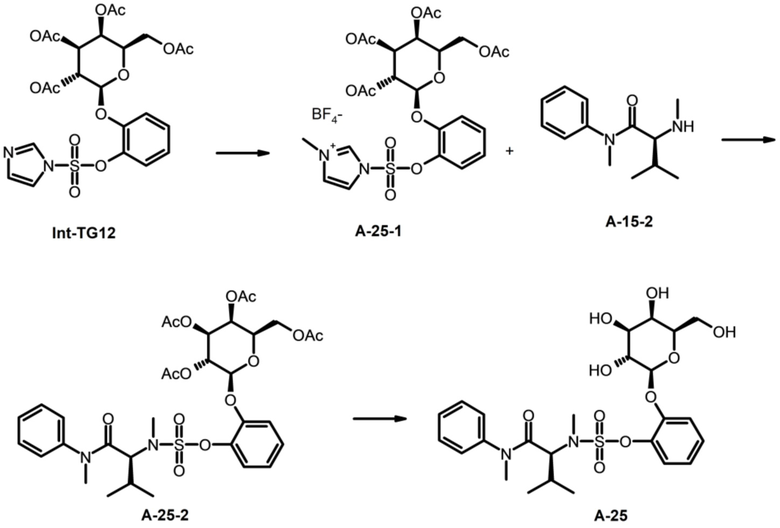
Получение соединения A-25-2
К раствору соединения Int-TG12 (100 мг, 0,175 ммоль) в ДХМ (6 мл) добавляли метилтрифлат (30мкл, 0,263 ммоль) при 0°C в атмосфере N2. Смесь перемешивали при комнатной температуре в течение 4 часов и концентрировали при пониженном давлении. Остаток растворяли в сухом ACN (5 мл) и добавляли соединение A-15-2 (46 мг, 0,21 ммоль) при комнатной температуре. Смесь нагревали при 40°С в течение 8 часов, гасили 2 N водного HCl (8 мл) и экстрагировали EtOAc (2 × 10 мл). Органический слой сушили над безводным MgSO4, фильтровали и концентрировали. Остаток растворяли в ДМСО (1 мл) и очищали препаративной ВЭЖХ, в результате чего получали соединение А-25-2 (43,5 мг, 35%).
ЭИ-МС m/z: 723 (M+1).
Получение соединения A-25
Соединение A-25 синтезировали аналогичным путем синтеза, как описано в Примере 61.
Выход 60%; ЭИ-МС m/z: 555 (M+1).
[Пример 82] Получение соединения A-26

Соединение A-26 синтезировали аналогичным путем синтеза, как описано в Примере 81.
Получение соединения A-26-1
Выход 8%; ЭИ-МС m/z: 696 (M+1).
Получение соединения A-26
Выход 32%; ЭИ-МС m/z: 528 (M+1).
[Пример 83] Получение соединения A-27
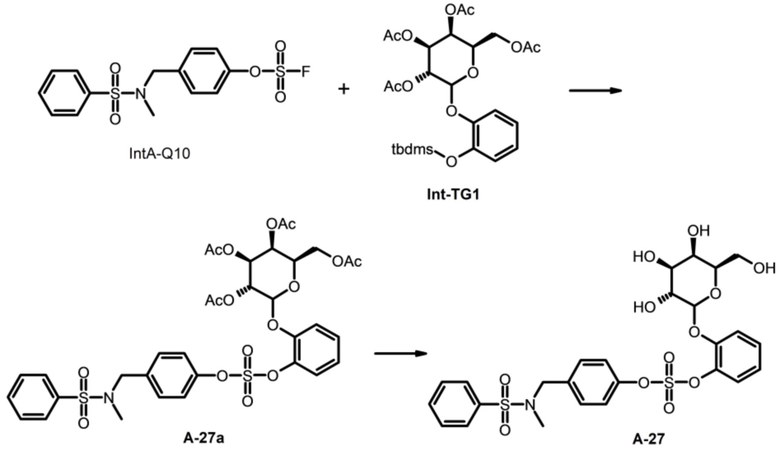
Соединение A-27 синтезировали аналогичным путем синтеза, как описано в Примере 81.
Получение соединения A-26-1
Выход 72%; ЭИ-МС m/z: 802 (M+1+Na).
Получение соединения A-26
Выход 79%; ЭИ-МС m/z: 634 (M+1+Na).
[Пример 84] Получение соединения B-1
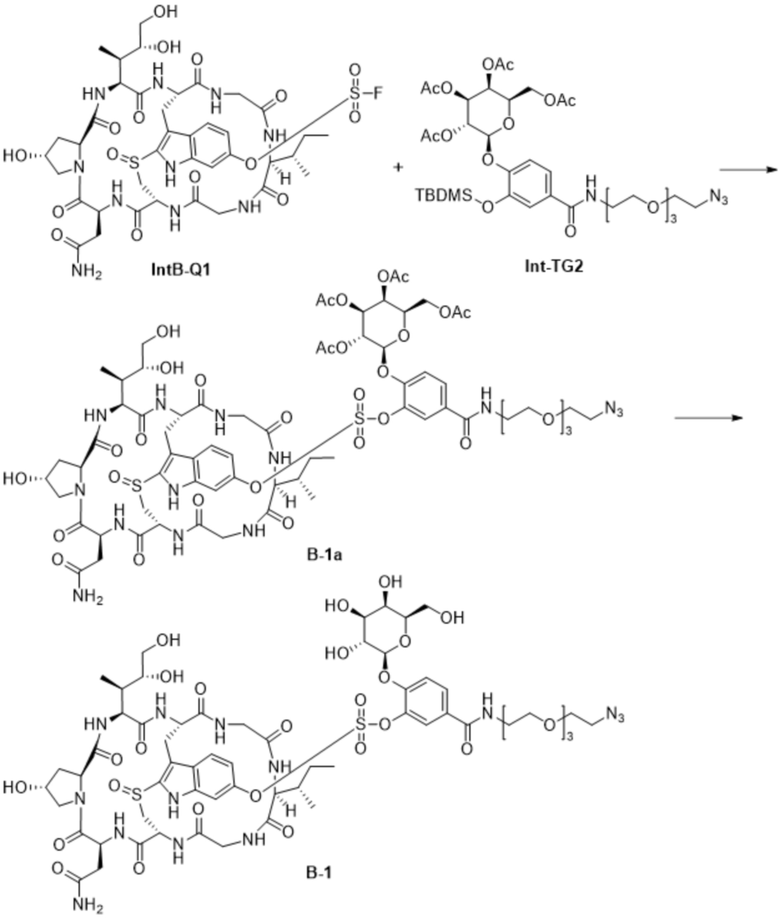
Соединение B-1 синтезировали аналогичным путем синтеза, как описано в Примере 67 и Примере 61.
Получение соединения B-1a
ЭИ-МС m/z: 1666(M+1).
Получение соединения B-1
Выход 19% за 2 стадии; ЭИ-MCm/z: 1498(M+1).
[Пример 85] Получение соединения B-2
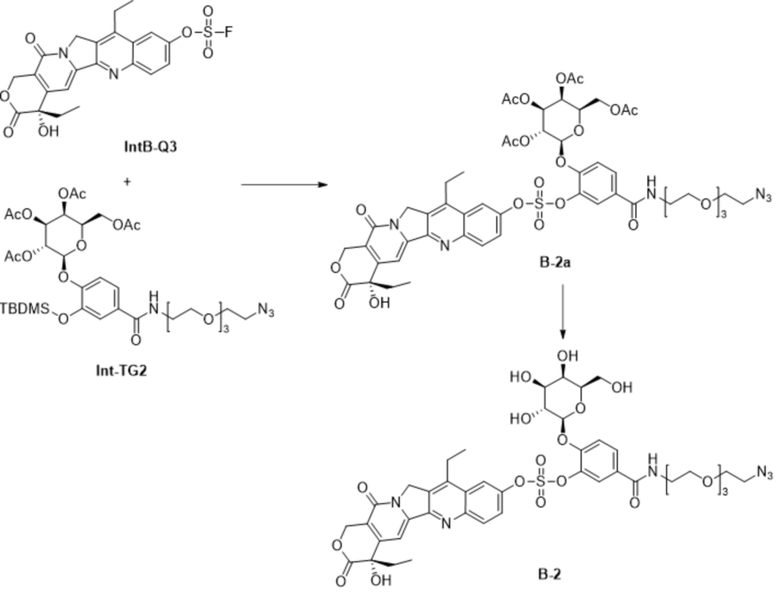
Соединение B-2 синтезировали аналогичным путем синтеза, как описано в Примере 67 и Примере 61.
Получение соединения B-2a
Выход 58%; ЭИ-МС m/z: 1140(M+1).
Получение соединения B-2
Выход 76%; ЭИ-МС m/z: 971(M+1).
[Пример 86] Получение соединения B-3
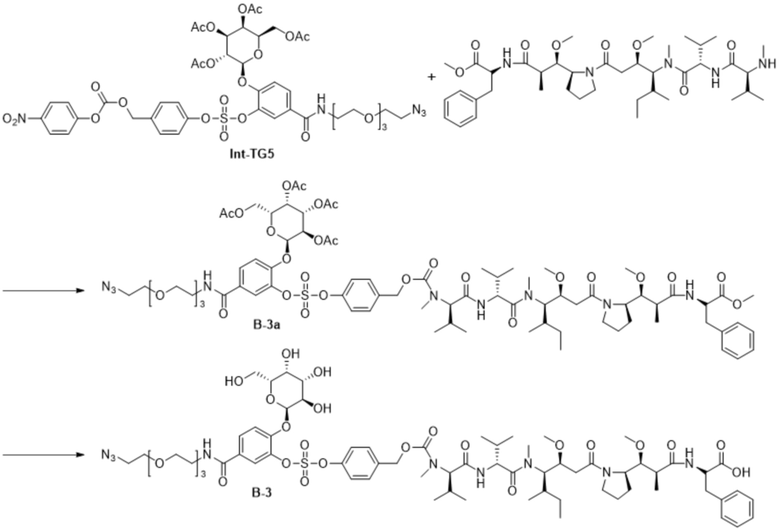
Получение соединения B-3a
К раствору соединения Int-TG5 (65 мг, 0,063 ммоль) и MMAF-OMe (52 мг, 0,069 ммоль) в ДМФА (1 мл) добавляли HOBt (2 мг, 0,013 ммоль), DIPEA (12 мкл, 0,069 ммоль) и пиридин (330 мкл) при комнатной температуре в атмосфере N2. После перемешивания в течение ночи смесь доводили до рН 2-3 с помощью 1N HCl, экстрагировали ЕА (8 мл × 2). Органический слой промывали дистиллированной водой (8 мл) и солевым раствором (12 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением соединения B-3a (73 мг, 71%).
ЭИ-МС m/z: 1644(M+1).
Получение соединения B-3
Соединение B-3 синтезировали аналогичным путем синтеза, как описано в Примере 61.
Выход 69%; ЭИ-МС m/z: 1462(M+1).
[Пример 87] Получение соединения B-4
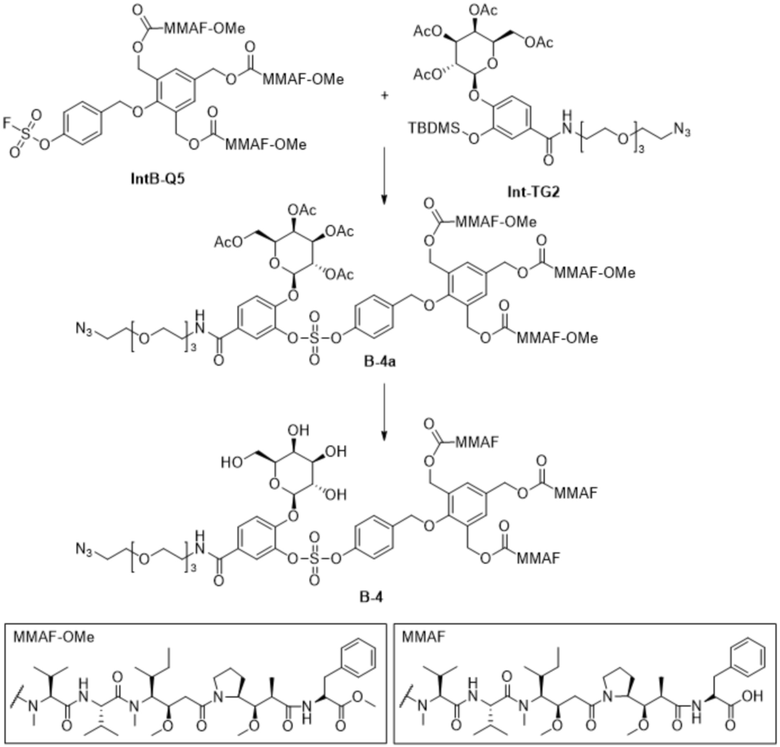
Соединение B-4 синтезировали аналогичным путем синтеза, как описано в Примере 67 и Примере 61.
Получение соединения B-4a
Выход 68%; ЭИ-МС m/z: 1678(M+1/2).
Получение соединения B-4
Выход 91%; ЭИ-МС m/z: 1572(M+1/2).
[Пример 87] Получение соединения B-6

Соединение B-6 синтезировали аналогичным путем синтеза, как описано в Примере 67 и Примере 61.
Получение соединения B-6a
Выход 100%; неочищенное; ЭИ-MCm/z: 1020 (M+1).
Получение соединения B-6
Выход 17%;
[Пример 87] Получение соединения B-7
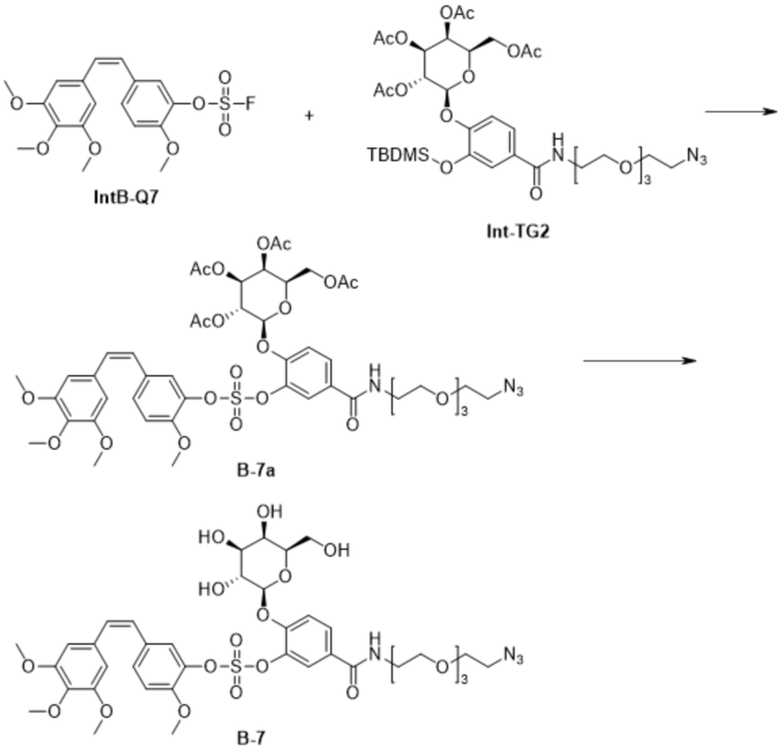
Соединение B-7 синтезировали аналогичным путем синтеза, как описано в Примере 67 и Примере 61.
Получение соединения B-7a
Выход 99%; ЭИ-МС m/z: 1063 (M+1).
Получение соединения B-7
ЭИ-МС m/z: 895 (M+1).
[Пример 89] Получение соединения B-8

Получение соединения B-8a
Соединение B-8a синтезировали аналогичным путем синтеза, как описано в Примере 67.
Выход 16%; ЭИ-МС m/z: 954(M+1), 976 (M+1+Na)
Получение соединения B-8
К раствору соединения B-8a (3,1 мг, 0,0032 ммоль) в метаноле (1 мл) добавляли 25%-NaOMe в MeOH (3 мкл, 0,012 ммоль) при 0°C. После перемешивания при комнатной температуре в течение 1,5 часов смесь нейтрализовали водным раствором 2 М-HCl и затем очищали препаративной ВЭЖХ с получением соединения B-8 в виде твердого вещества розового цвета (1,2 мг, 47%).
[Пример 90] Получение соединения B-9
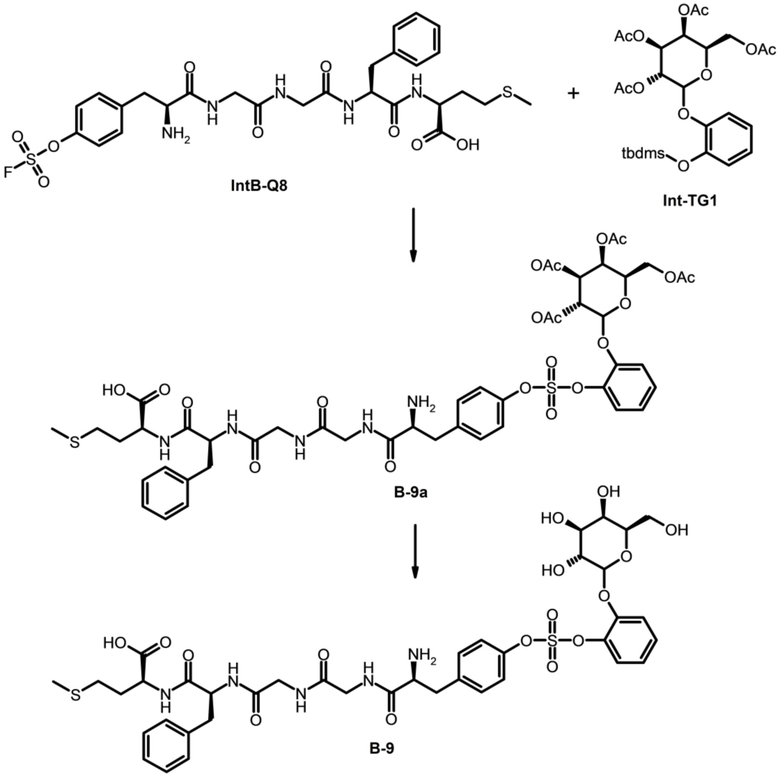
Соединение B-9 синтезировали аналогичным путем синтеза, как описано в Примере 67 и Примере 61.
Получение соединения B-9a
Выход 50%; ЭИ-MCm/z: 1077 (M+1).
Получение соединения B-9
Выход 32%; ЭИ-МС m/z: 908 (M+1).
[Пример 91] Получение соединения B-10

Получение соединения AF-OMe
К раствору соединения MMAF-OMe (120 мг, 0,161 ммоль) в ДМФА (4 мл) добавляли 37% формальдегид (36 мкл, 0,483 ммоль) и AcOH (184 мкл, 3,22 ммоль)) при комнатной температуре. После перемешивания в течение 5 минут к смеси добавляли NaCNBH3 (21 мг, 0,322 ммоль), перемешивали в течение 2 часов и гасили насыщенным NaHCO3 (10 мл). Добавляли EtOAc (20 мл). Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией с получением соединения соединения AF-OMe (98 мг, 80%). ЭИ-МС m/z: 761(M+1).
Соединение B-10 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения B-10-1
Выход 27%; ЭИ-MCm/z: 1673 (M+1).
Получение соединения B-10
Выход 81%; ЭИ-МС m/z: 1491 (M+1).
[Пример 92] Получение соединения B-11
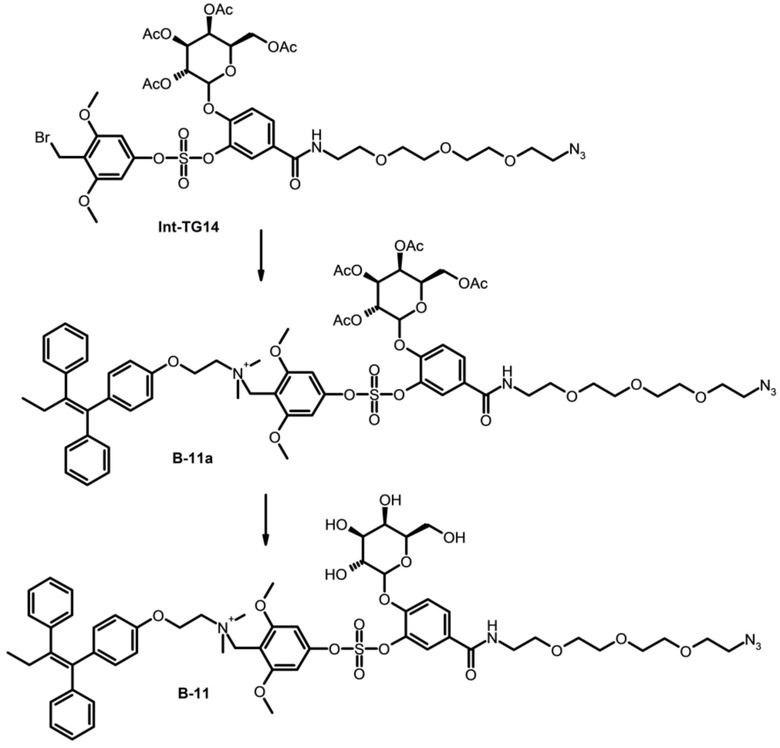
Соединение B-11 синтезировали аналогичным путем синтеза, как описано в Примере 91.
Получение соединения B-11a
Выход 87%; ЭИ-МС m/z: 1285 (M+1).
Получение соединения B-11
Выход 53%; ЭИ-MCm/z: 1117 (M+1).
[Пример 93] Получение соединения B-12

Соединение B-12 синтезировали аналогичным путем синтеза, как описано в Примере 30 и Примере 73.
Получение соединения B-12a
Выход 53%; ЭИ-МС m/z: 1254,7 (M+1).
Получение соединения B-12
Выход 58%; ЭИ-МС m/z: 1086,6(M+1).
[Пример 94] Получение соединения B-13
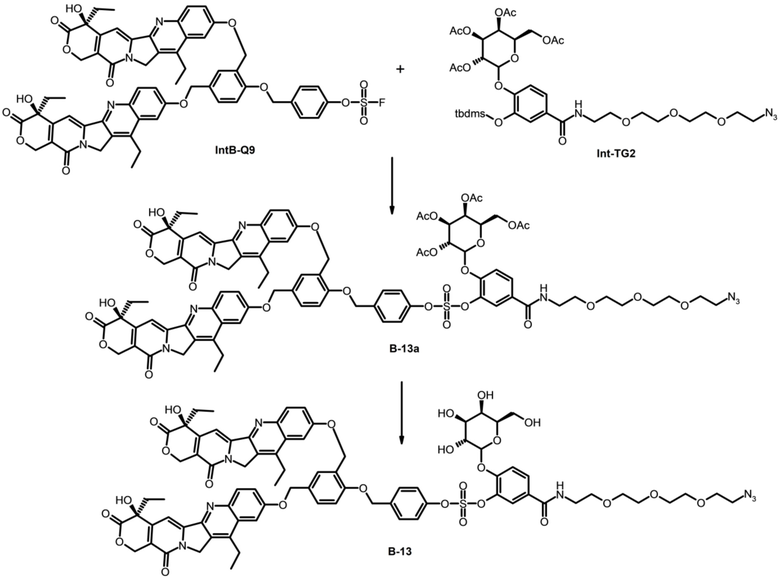
Соединение B-13 синтезировали аналогичным путем синтеза, как описано в Примере 74.
Получение соединения B-13a
Выход 9%; ЭИ-МС m/z: 878(M+1/2).
Получение соединения B-13
Выход 33%; ЭИ-МС m/z: 1610(M+1).
[Пример 95] Получение соединения B-14

Соединение B-14 синтезировали аналогичным путем синтеза, как описано в Примере 61.
Выход 30%; ЭИ-MCm/z: 1474 (M+).
[Пример 96] Получение соединения B-15

Соединение B-15 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения B-15a
Выход 45%; ЭИ-MCm/z: 1116 (M+).
1H ЯМР (400 МГц, ДМСО-d6) δ 8,73 (с, 1H), 8,01 (м, 1H), 7,97 (с, 1H), 7,68 (м, 1H), 7,51 (т, J=9,2 Гц, 1H) 7,45 (д, J=8 Гц, 1H), 7,36 (м, 2H), 7,26 (с, 1H), 7,10-7,07 (м, 1H), 6,89 (с, 2H), 4,97 (д, J=7,2 Гц, 1H), 4,62 (с, 2H), 4,27 (м, 2H), 4,04-3,95 (м, 7H), 3,96 (с, 6H)
Получение соединения B-15
Выход 70%; ЭИ-МС m/z: 948 (M+1).
[Пример 97] Получение соединения B-16
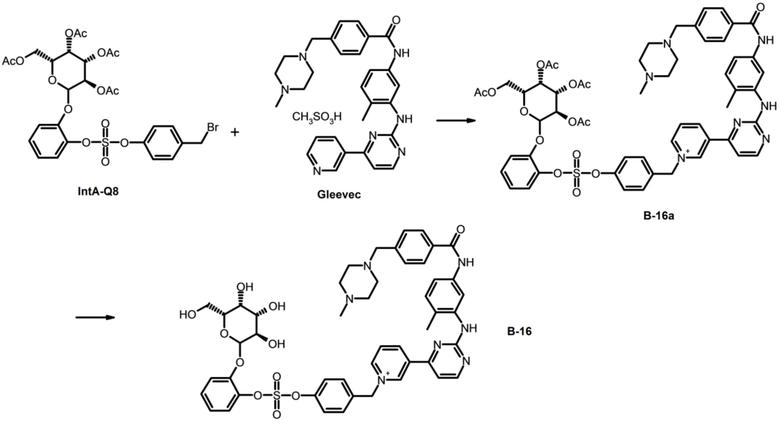
Соединение B-16 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения B-16a
Выход 99%; ЭИ-МС m/z: 1103 (M+1).
Получение соединения B-16
Выход 85%; ЭИ-MCm/z: 935 (M+1).
[Пример 98] Получение соединения B-17

Соединение B-17 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения B-17a
Выход 55%; ЭИ-МС m/z: 991 (M+1).
Получение соединения B-17
Выход 60%; ЭИ-МС m/z: 823 (M+1).
[Пример 99] Получение соединения B-18
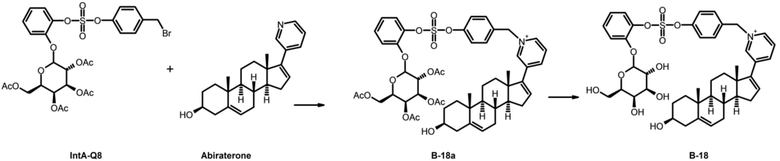
Соединение B-18 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения B-18a
Выход 72%; ЭИ-МС m/z: 960 (M+1).
Получение соединения B-18
Выход 54%; ЭИ-MCm/z: 791 (M+1).
[Пример 100] Получение соединения B-19

Соединение B-19 синтезировали аналогичным путем синтеза, как описано в Примере 92 и Примере 70.
Получение соединения B-19a
Выход 38%; ЭИ-MCm/z: 914(M+1/2).
Получение соединения B-19b
Выход 60%; ЭИ-МС m/z: 831(M+1/3).
Получение соединения B-19
Выход 17%; ЭИ-МС m/z: 1148(M+1/2).
[Пример 101] Получение соединения B-20

Соединение B-20 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения B-20a
Выход 14%; ЭИ-МС m/z: 1614 (M+1).
Получение соединения B-20
Выход 37%; ЭИ-МС m/z: 1432 (M+1).
[Пример 102] Получение соединения B-21

Соединение B-21 синтезировали аналогичным путем синтеза, как описано в Примере 72.
Получение соединения B-21a
Выход 38 ЭИ-MCm/z: 1551(M+1).
Получение соединения B-21
Выход 54%; ЭИ-MCm/z: 1383 (M+1).
[Пример 103] Получение соединения B-22
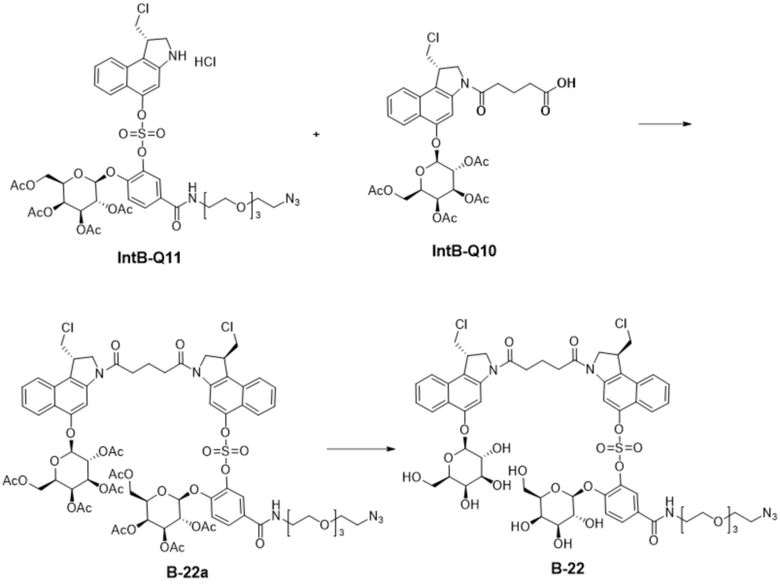
Получение соединения B-22a
К раствору соединения IntB-10 (30 мг, 0,043 ммоль) и соединения IntB-Q11 (51 мг, 0,05 ммоль) в ДМФА (3 мл) добавляли EDC⋅HCl (27,2 мг, 0,142 ммоль) при 0°C в атмосфере N2. После перемешивания в течение 11 часов смесь очищали препаративной ВЭЖХ с получением соединения B-22a (20 мг, 28%) в виде светло-коричневого твердого вещества.
ЭИ-МС m/z: 821,7(M+1/2).
Получение соединения B-22
К раствору соединения B-22a (10 мг, 0,006 ммоль) в MeOH (1,5 мл) добавляли 25% NaOMe в MeOH (11 мкл, 0,048 ммоль) при 0°C в атмосфере N2. Реакционную смесь перемешивали при комнатной температуре в течение 1 часа в атмосфере N2 и доводили до pH 7 добавлением 5% ТФУ в растворе ACN. Смесь очищали препаративной ВЭЖХ с получением соединения B-22 (5 мг, 63%) в виде бледно-желтого твердого вещества.
ЭИ-МС m/z: 1305,3(M+1).
[Пример104] Получение соединения B-23

Соединение B-23 синтезировали аналогичным путем синтеза, как описано в Примере 103.
Получение соединения B-23a
Выход 53%; ЭИ-МС m/z: 1303,5(M+1).
Получение соединения B-23b
К раствору соединения B-23a (30 мг, 0,023 ммоль) добавляли 4N HCl в 1,4-диоксане (1 мл) при комнатной температуре в атмосфере N2. После перемешивания в течение 1 часа смесь разбавляли ДХМ (5 мл) и концентрировали. Соединение B-23b использовали непосредственно на следующей стадии без дополнительной очистки (28 мг, 97%).
ЭИ-МС m/z: 1259,5(M+1).
Получение соединения B-23
Выход 68%; ЭИ-МС m/z: 1259,5(M+1).
[Пример 105] Получение соединения B-24

Соединение B-24 синтезировали аналогичным путем синтеза, как описано в Примере 104.
Получение соединения B-24a
Выход 53%; ЭИ-МС m/z: 1254,7(M+1).
Получение соединения B-24
Выход 58%; ЭИ-MCm/z: 1086,6(M+1).
[Пример 106] Получение соединения B-25
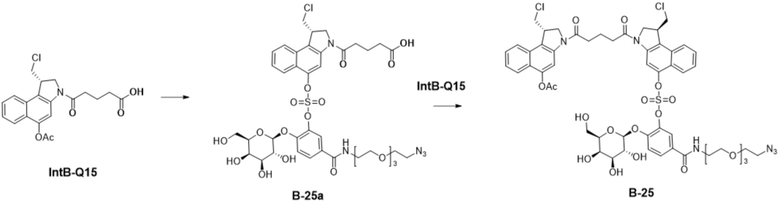
Соединение B-25 синтезировали аналогичным путем синтеза, как описано в Примере 104.
Получение соединения B-25a
Выход 33%; ЭИ-МС m/z: 1094,5(M+1).
Получение соединения B-25
Выход 36%; ЭИ-MCm/z: 926,4(M+1).
[Пример 107] Получение соединения B-26
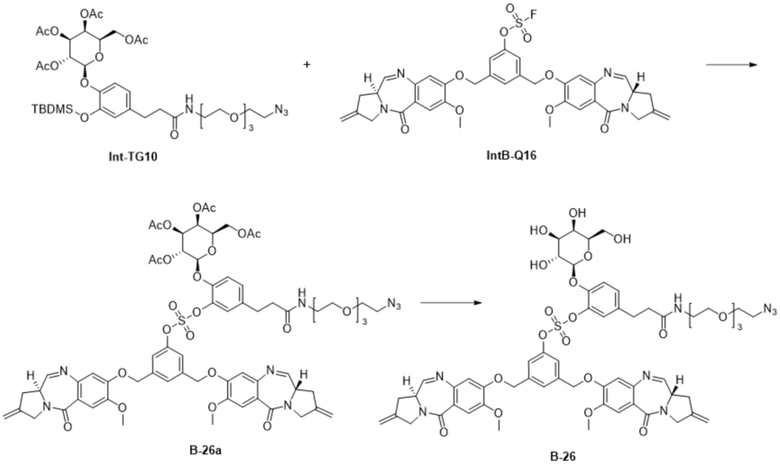
Соединение B-26 синтезировали аналогичным путем синтеза, как описано в Примере 74.
Получение соединения B-26a
Выход 51%; ЭИ-МС m/z: 1382(M+1).
Получение соединения B-8
Выход 56%; ЭИ-МС m/z: 1214(M+1).
[Пример 108] Получение соединения конъюгата лиганд-лекарственный препарат C-1
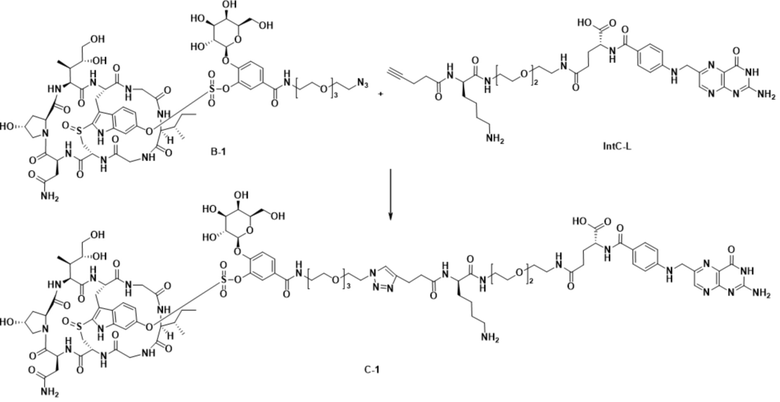
К раствору соединения IntC-L (1,8 мг, 0,0016 ммоль) и соединения B-1 (1,6 мг, 0,0011 ммоль) в EtOH (2 мл) и дистиллированной воде (0,5 мл) добавляли 1 М аскорбата натрия (11 мкл, 0,011 ммоль) и 0,1 М CuSO4 (21 мкл, 0,0021 ммоль) при комнатной температуре в атмосфере азота N2. После перемешивания в течение 12 часов смесь разделяли и очищали препаративной ВЭЖХ с получением соединения C-1 (1,7 мг, 61%).
ЭИ-МС m/z: 2278(M+1).
[Пример 109] Получение соединения конъюгата лиганд-лекарственный препарат C-2

Соединение C-2 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 54%; ЭИ-МС m/z: 1751 (M+1).
[Пример 110] Получение соединения конъюгата лиганд-лекарственный препарат C-3

Соединение C-3 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 24%; ЭИ-МС m/z: 2242 (M+1).
[Пример 111] Получение соединения C-4

Соединение C-4 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 1043,3 (M+1/2).
[Пример 112] Получение соединения C-5
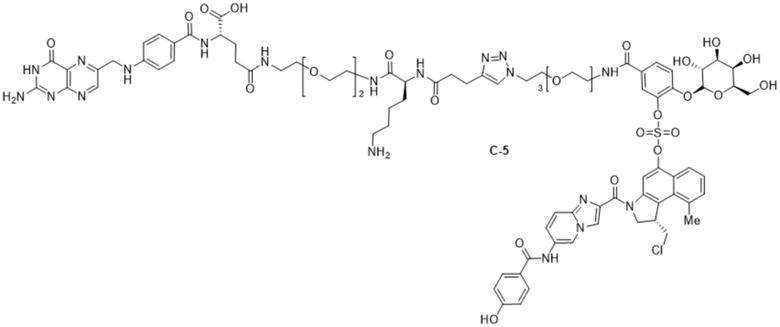
Соединение C-6 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 1886,3 (M+1).
[Пример 113] Получение соединения C-6
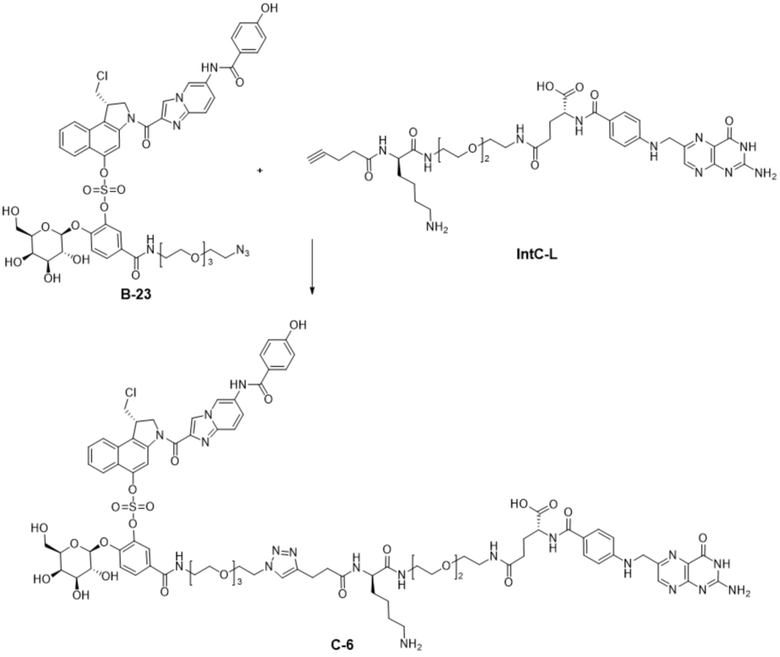
Соединение C-6 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 936,7 (M+1/2).
[Пример 114] Получение соединения C-7

Соединение C-7 синтезировали аналогичным путем синтеза, как описано в Примере 61 и Примере 108.
Получение соединения B-3b
Выход 30%; ЭИ-МС m/z: 1497(M+1+Na).
Получение соединения C-7
Выход 8,7%; ЭИ-MCm/z: 1128(M+1/2).
[Пример115] Получение соединения C-8
Соединение C-8 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 934,0 (M+1/2).
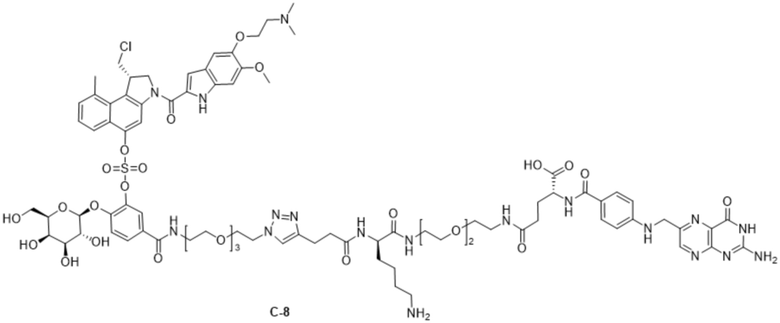
[Пример 116] Получение соединения C-9
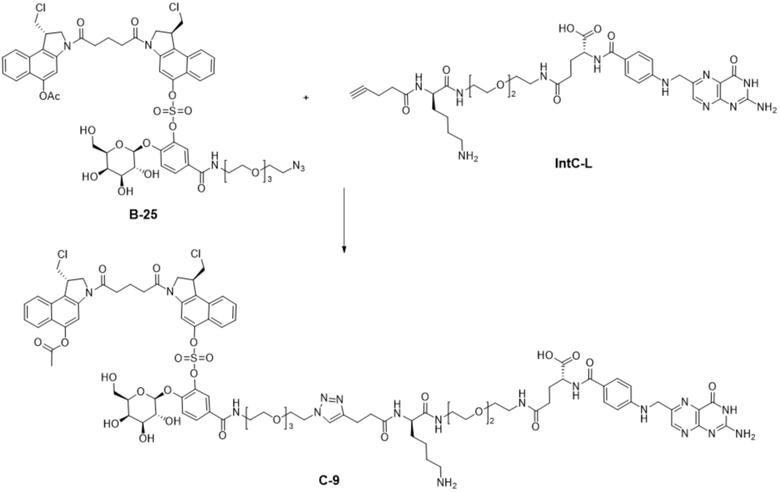
Соединение C-9 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 983,0 (M+1).
[Пример 117] Получение соединения конъюгата лиганд-лекарственный препарат D 1
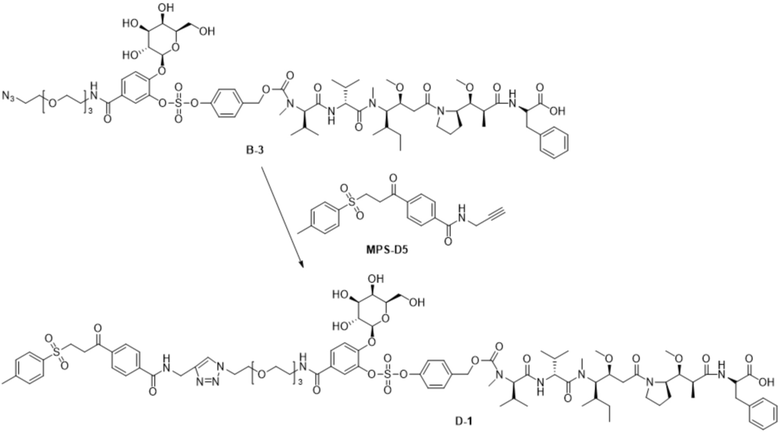
К раствору соединения B-3 (пример 72, 10 мг, 6,85 мкмоль) в ДМСО (685 мкл+7671 мкл) добавляли (BimC4A)3 (1142 мкл), приготовленный с концентрацией 50 ммоль. Затем к нему добавляли CuBr, приготовленный с концентрацией 10 ммоль, в количестве 685 мкл. Смесь перемешивали в течение 2 минут. Соединение MPS-D5 (4,6 мг, 12,3 мкмоль) растворяли в ДМСО (685 мкл) и добавляли к нему с последующим перемешиванием в течение 10 минут. После завершения реакции смешанный раствор отделяли и очищали препаративной ВЭЖХ с получением соединения D-1 (5,4 мг, 43%).
ЭИ-МС m/z: 916 (M+1/2).
[Пример118] Получение соединения конъюгата лиганд-лекарственный препарат D-2
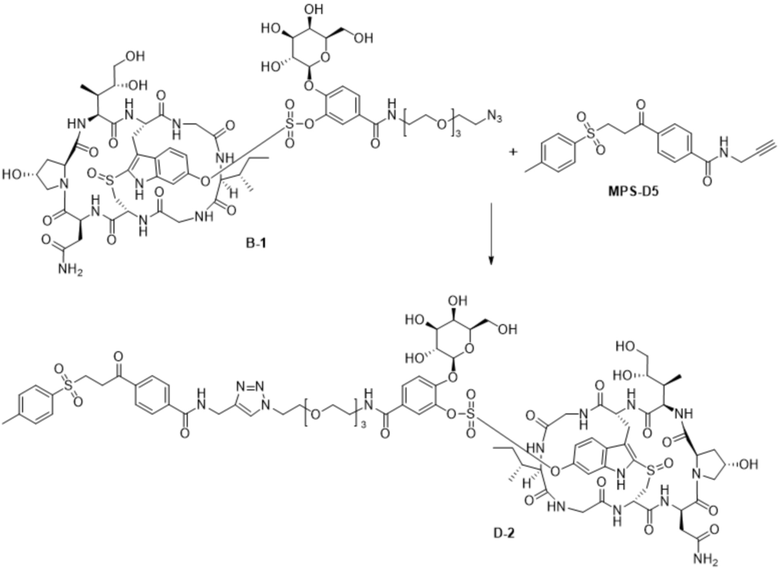
Соединение D-2 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 35%; ЭИ-МС m/z: 934 (M+1/2).
[Пример 119] Получение соединения D-4
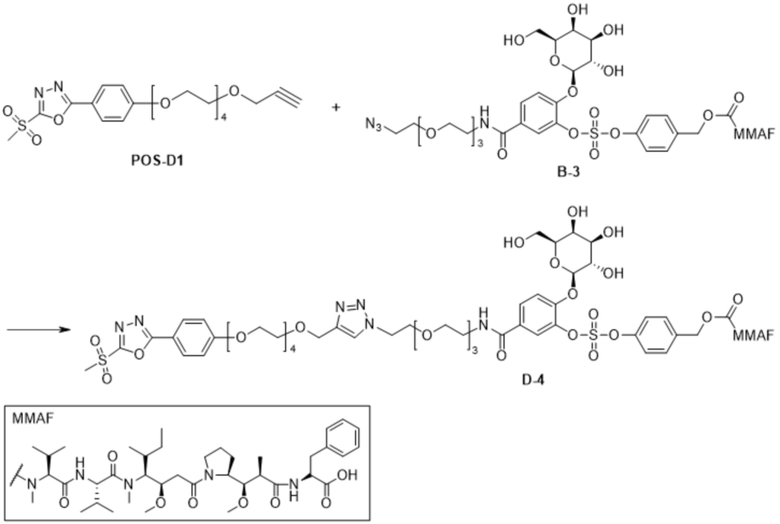
К раствору соединения B-3 (10 мг, 6,85 мкмоль) в ДМСО (685 мкл) добавляли (BimC4A)3 (1142 мкл 50 ммоль исходного раствора) при комнатной температуре в атмосфере N2. После добавления ДМСО (6179 мкл) добавляли CuBr (685 мкл), приготовленный с концентрацией 100 ммоль. Затем смесь перемешивали в течение 2 минут. Соединение POS-D1 (12,4 мг, 27,4 мкмоль) растворяли в ДМСО (685 мкл) и добавляли к нему с последующим перемешиванием в течение 10 минут. После завершения реакции смешанный раствор разделяли и очищали препаративной ВЭЖХ с получением соединения D-4 (0,5 мг, 3,8%).
ЭИ-МС m/z: 958 (M+1/2).
[Пример 120] Получение соединения D-5

Соединение D-5 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 53%; ЭИ-МС m/z: 1417 (M+1/2).
[Пример 121] Получение соединения D-6
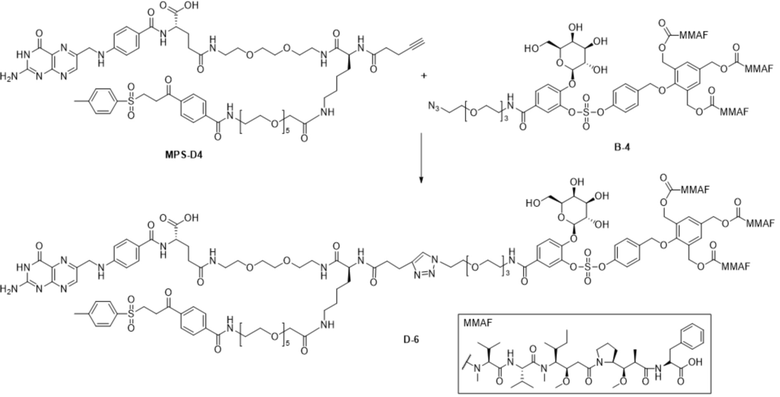
Соединение D-6 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 42%; ЭИ-MCm/z: 4515(M+), 2258(M/2+), 1505(M/3+).
[Пример 122] Получение соединения D-7
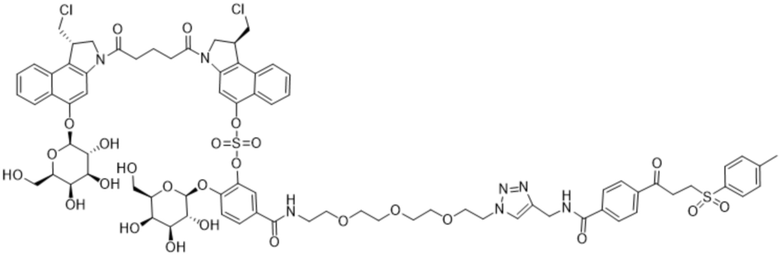
Соединение D-7 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 1673,0(M+).
[Пример 123] Получение соединения D-8
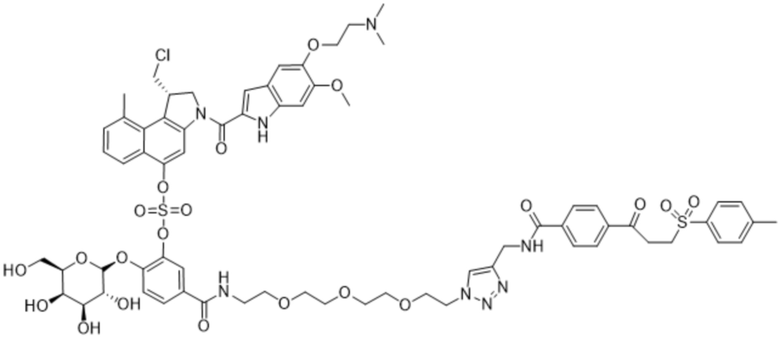
Соединение D-8 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 728,8(M+/2).
[Пример 124] Получение соединения D-9

Соединение D-9 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 50%; ЭИ-МС m/z: 1264 (M+).
[Пример 125] Получение соединения D-10
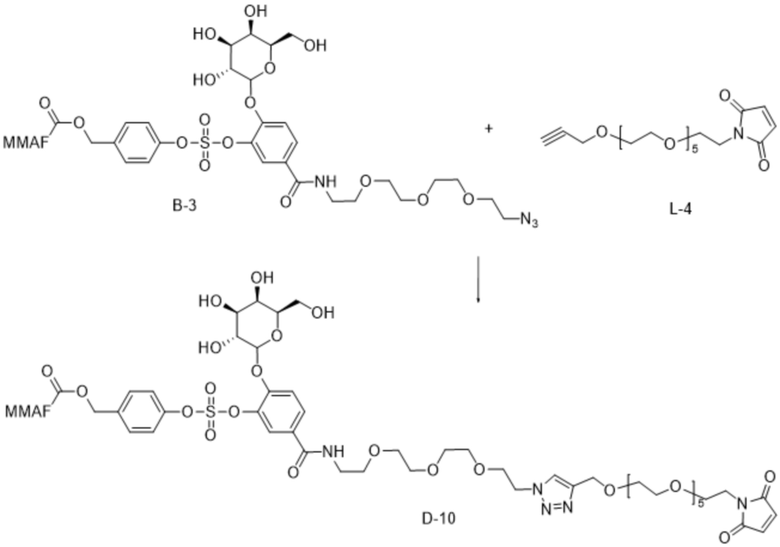
Соединение D-10 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 17%; ЭИ-МС m/z: 1861(M+).
[Пример 126] Получение соединения D-11

Соединение D-11 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 25%; ЭИ-МС m/z: 1863(M+).
[Пример 127] Получение соединения D-12
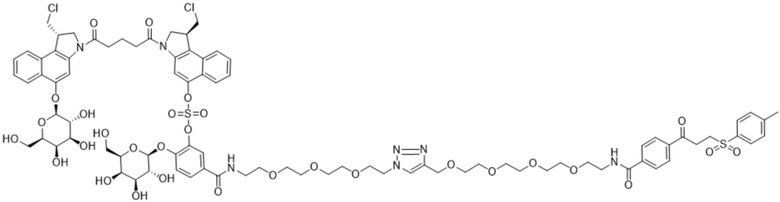
Соединение D-12 синтезировали аналогичным путем синтеза, как описано в Примере 108.
ЭИ-МС m/z: 1850,8(M+).
[Пример 128] Получение соединения D-13

Соединение D-13 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 18%; ЭИ-МС m/z: 930 (M/2+).
[Пример 129] Получение соединения D-14

Получение соединения (A)
Полный синтез Соединения (А) был получен в соответствии с работами (J. Org. Chem. 2004, 69, 112-121, J. Am. Chem. SOC1. 995,117, 10143-10144).
Получение соединения D-14a
К раствору соединения (A) (10 мг, 0,018 ммоль) и соединения Int-TG15 (16,8 мг, 0,018 ммоль) в ACN (1 мл) добавляли молекулярное сито (100 мг) в атмосфере N2. После перемешивания при комнатной температуре в течение 10 минут добавляли Ag2O (12,5 мг, 0,054 ммоль). Смесь перемешивали при комнатной температуре в течение 5 часов, фильтровали через целит и концентрировали при пониженном давлении. Остаток очищали препаративной ВЭЖХ с получением соединения D-14a (18 мг, 71%).
1H ЯМР (400 МГц, CDCl3) δ 7,99 (м, 2H), 7,85 (с, 1H), 7,77 (д, J=8,8 Гц, 2H), 7,65 (д, J=8,4 Гц, 2H), 7,58 (м, 1H), 7,44-7,40 (м, 2H), 7,36 (J=8,4 Гц, 2H), 7,29 (д, J=8,8 Гц, 1H), 6,94 (м, 1H), 6,46 (с, 1H), 6,11 (с, 1Н), 5,94 (м, 2Н), 5,80 (с, 1Н), 5,56 (м, 1Н), 5,50-5,46 (м, 2Н), 5,35-5,31 (м, 2Н), 5,25 ~ 5,22 (м., 2H), 5,15-5,13 (м, 2H), 4,38 (м, 1H), 4,25-4,08 (м, 4H), 3,65 ~ 3,59 (м, 15H), 3,54-3,49 (м, 1H), 3,33 (м, 2H), 2,17 (с, 3H), 2,13 (с, 3H), 2,09 (с, 3H), 2,06 (с, 3H), 2,04 (с, 3H), 2,00 (с, 3H), 1,81 (с, 3H). ЭИ-МС m/z: 705 (1/2M+), 1408 (M+), 1430(M+Na).
Получение соединения D-14b
К раствору соединения D-14a (16 мг, 0,011 ммоль) в ДХМ (4 мл) добавляли 1M-NaOMe в метаноле (20 мкл) при 0°C. После перемешивания при 0°С в течение 20 минут смесь гасили водным раствором 1M-HCl (30 мкл) и затем очищали препаративной ВЭЖХ с получением соединения D-14b (4 мг, 32%).
ЭИ-МС m/z: 557 (1/2M+), 1114 (M+), 1136 (M++Na).
Получение соединения D-14
Соединение D-14 синтезировали аналогичным путем синтеза, как описано в Примере 56.
Выход 12%; ЭИ-МС m/z: 830 (M+1/2).
[Пример 130] Получение соединения D-15
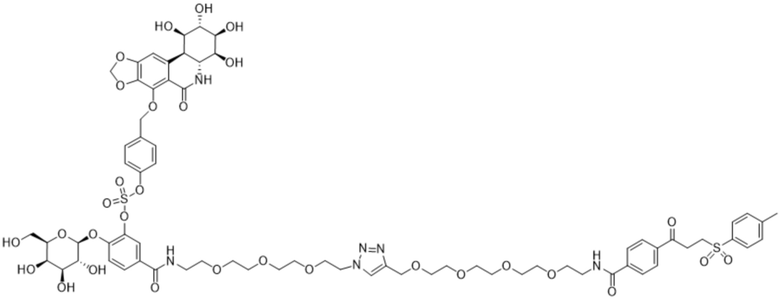
Соединение D-15 синтезировали аналогичным путем синтеза, как описано в Примере 119.
Выход 19%; ЭИ-МС m/z: 1556 (M+), 778 (1/2M+).
[Пример 131] Получение соединения D-16
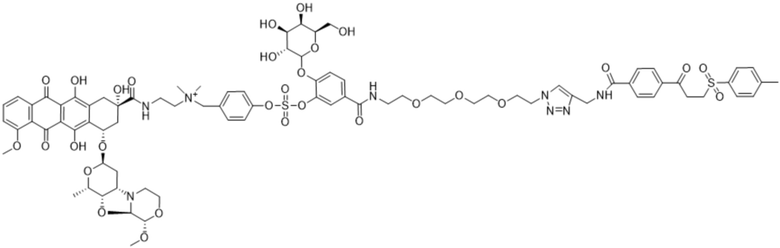
Соединение D-16 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 13%; ЭИ-МС m/z: 1753 (M+).
[Пример 132] Получение соединения D-17
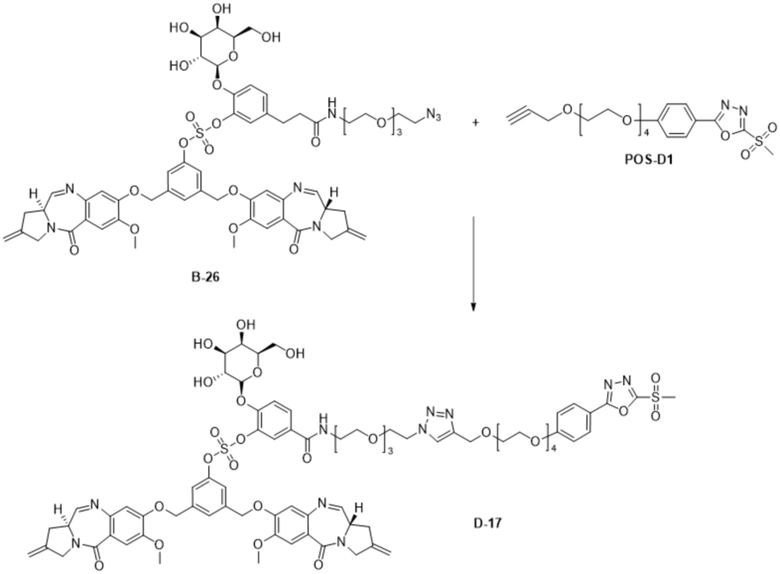
Соединение D-17 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 12%; ЭИ-МС m/z: 1668 (M+).
[Пример 133] Получение соединения D-18

Соединение D-18 синтезировали аналогичным путем синтеза, как описано в Примере 108.
Выход 7,4%; ЭИ-МС m/z: 1759 (M+).
[Пример 134] Получение соединения димера CBI
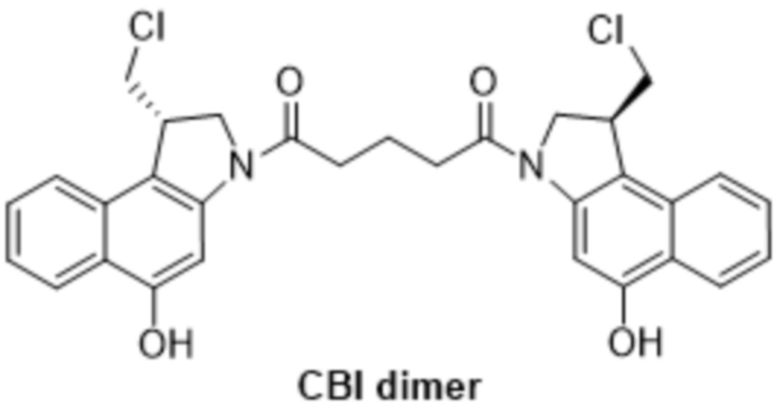
Димер CBI синтезировали аналогичным способом синтеза, как описано в WO2015110935A.
[Пример135] Получение соединения seco-DUBA
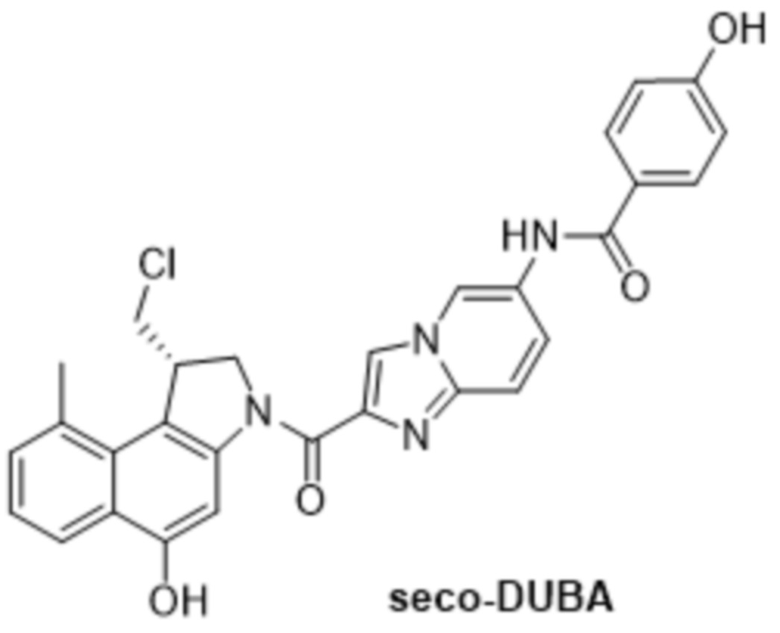
seco-DUBA синтезировали аналогичным способом синтезирования, как описано в документе [см. Mol. Pharmaceutics 2015, 12, 1813-1835].
[Пример136] Получение соединения seco-CBI-индола
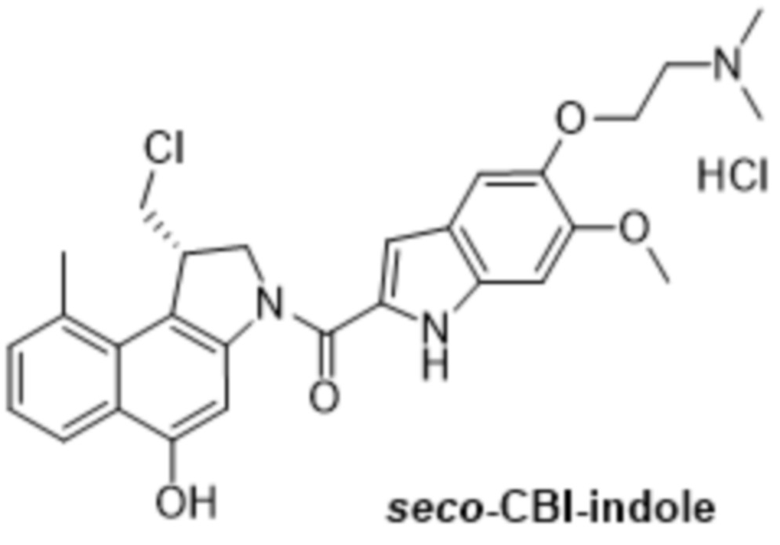
seco-CBI-индол синтезировали аналогичным синтетическим методом, как описано в документе [см. ChemMedChem 2008, 3, 1946-1955].
[Пример 137] Получение соединения D-3

Соединение B-8 (15 мг, 0,01 ммоль) растворяли в ДМСО (7 мл) при комнатной температуре в атмосфере азота, а затем (BimC4A)3 (33 мг, 0,04 ммоль) растворяли в ДМСО (2 мл), CuBr (17 мг). 0,12 ммоль), растворенного в ДМСО (3 мл), и POS-D1 (получение примера 36, 7 мг, 0,01 ммоль), растворенного в ДМСО (1 мл), с последующим перемешиванием в течение 2 часов. Смесь разделяли и очищали препаративной ВЭЖХ с получением соединения D-3 (2,5 мг, 12%).
ЭИ-МС m/z: 1668(M+).
Биологические и биохимические исследования
[Пример 138] Кинетическое исследование анализа ферментативного расщепления
Метод 1) β-галактозидаза, выделенная из Escherichia coli
Соединения по настоящему изобретению (соединения A-2, A-4, A-5, A-6, A-9, A-10, A-12, A-13, A-14, A-15, A-17, A-18, A-19, A-21, A-22, A-23, B-1, B-2, B-3, B-4, B-6, B-7, B-8, B-9, B-10, B-11, B-14, B-15, B-16, B-19 и C-3) растворяли в ДМСО и смешивали с буферным раствором ФСБ для получения 500 мкМ исходного раствора (5% ДМСО). MPS, используемый в качестве стандартного материала, растворяли в буферном растворе ФСБ для получения 500 мкМ раствора. Смешивали 406 мкл буферного раствора ФСБ (pH 7,4) и 140 мкл соединения (500 мкМ) по настоящему изобретению и 140 мкл MPS . После этого добавляли раствор фермента (14 мкл 1 мг/мл). При сравнении с β-галактозидазой человека добавляли 21 мкл раствора фермента(1 мг/мл) для достижения той же молярной концентрации, и смешивали соединение по настоящему изобретению и MPS, каждое из которых имело количество буфера 140 мкл и 399 мкл буферного раствора (рН 7,4). Полученную реакционную смесь инкубировали при 37°С. Фермент β-галактозидазы Escherichia coli (Sigma G4155) использовали в реакционной смеси. Реакционный раствор фермента разделяли на аликвоты за 0 мин до реакции и в заранее определенное время после реакции, соответственно, где каждая аликвота составляла 70 мкл. Затем оставшееся соединение по настоящему изобретению или MPS и материал, выделенный в результате ферментативной реакции, количественно анализировали с помощью ВЭЖХ.
Метод 2) β-галактозидаза человека
Каждое из соединений A-3, B-2и B-10 по настоящему изобретению растворяли в ДМСО, и смешивали с буферным раствором ФСБ для получения 500 мкМ исходного раствора (5% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 500 мкМ в буферном растворе ФСБ. 280 мкл буферного раствора ФСБ (pH 7,4) и соединения B-2 (500 мкМ) по настоящему изобретению и MPS, каждый из которых имеет количество 140 мкл, смешивали друг с другом. Затем к ним добавляли 140 мкл 0,1 мг/мл раствора фермента, получая таким образом реакционный раствор фермента в общем количестве 700 мкл. Реакционную смесь инкубировали при 37°С. Фермент β-галактозидазы человека (R&D 6464-GH-020) использовали в реакционной смеси. Реакционную смесь фермента разделяли на аликвоты за 0 мин до реакции и в заранее определенное время после реакции, соответственно, где каждая аликвота составляла 70 мкл. Затем оставшееся соединение по настоящему изобретению или MPS и SN38, выделенный в результате ферментативной реакции, количественно анализировали с помощью ВЭЖХ.
Метод 3) β-глюкуронидаза, выделенная из Escherichia coli
Соединения A-1 и A-5 по настоящему изобретению растворяли в ДМСО, и смешивали с буферным раствором ФСБ для получения раствора, имеющего концентрацию 500 мкМ (5% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 500 мкМ в буферном растворе ФСБ. Смешивали 406 мкл буферного раствора ФСБ (pH 7,4) и 140 мкл соединения (500 мкМ) по настоящему изобретению и 140 мкл MPS. Затем к нему добавляли 14 мкл раствора фермента (1 мг/мл), получая таким образом реакционный раствор фермента в общем количестве 700 мкл. Реакционную смесь инкубировали при 37°С. Фермент β-глюкуронидазы Escherichia coli (Sigma G7396) использовали в реакционной смеси. Реакционную смесь фермента разделяли на аликвоты за 0 мин до реакции и в заранее определенное время после реакции, соответственно, где каждая аликвота составляла 70 мкл. Затем оставшееся соединение по настоящему изобретению или MPS и материал, выделенный в результате ферментативной реакции, количественно анализировали с помощью ВЭЖХ.
Метод 4) β-галактозидаза+β-глюкуронидаза Escherichia coli
Соединение A-5 по настоящему изобретению растворяли в ДМСО и смешивали с буферным раствором ФСБ для получения раствора, имеющего концентрацию 500 мкМ (5% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 500 мкМ в буферном растворе ФСБ. Смешивали 392 мкл буферного раствора ФСБ (pH 7,4) и 140 мкл соединения A-5 (500 мкМ) по настоящему изобретению и MPS. Затем добавляли 14 мкл 1 мг/мл β-галактозидазы (Sigma G4155) и 14 мкл 1 мг/мл β-глюкуронидазы (Sigma G7396), получая таким образом реакционный раствор фермента в общем количестве 700 мкл. Реакционную смесь инкубировали при 37°С. Реакционную смесь фермента разделяли на аликвоты за 0 мин до реакции и в заранее определенное время после реакции, соответственно, где каждая аликвота составляла 70 мкл. Затем оставшееся соединение по настоящему изобретению или MPS и материал, выделенный в результате ферментативной реакции, количественно анализировали с помощью ВЭЖХ.
[Таблица 1]
(Н/О=не обнаружено при проведении ВЭЖХ)
[Пример 139] Испытание на высвобождение лекарственного препарата
Способ с использованием восстановителя
Соединение А-8, полученное в Примере 65, растворяли в ДМСО до концентрации 10 мМ и смешивали с раствором МеОН для получения раствора с концентрацией 300 мкМ (40% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 300 мкМ с буферным раствором ФСБ. NaBH4, восстановитель, растворяли в МеОН до концентрации 10 мМ и добавляли 3,0 эквивалента соединения А-8. Затем реакционную смесь инкубировали при 37°С. Смесь для реакции восстановления разделяли на аликвоты за 0 мин до реакции, через 5, 10 и 30 мин после реакции, соответственно, где каждая аликвота составляла 80 мкл. Затем оставшееся соединение A-8 по настоящему изобретению или MPS, и BOC-Tyr-OMe, высвобождаемые посредством ферментативной реакции, количественно анализировали с помощью ВЭЖХ.
Метод с использованием фотореакции
Соединение A-11, полученное в Примере68, растворяли в ДМСО, и смешивали с буферным раствором ФСБ, имеющим рН 7,4, и раствором ДМСО для получения раствора с концентрацией 300 мкМ (50% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 300 мкМ в буферном растворе ФСБ.
Затем реакцию инициировали путем перемешивания в фотореакторе мощностью 300 Вт. Реакционную смесь разделяли на аликвоты за 0 минут до реакции, через 5 минут, 10 минут, 30 минут, 180 минут, 300 минут, 420 минут, 24 часа и 48 часов после реакции, соответственно, где каждая аликвота составляла 80 мкл. Затем оставшееся соединение A-11 по настоящему изобретению или MPS, и BOC-Tyr-OH, высвобождаемые посредством фотореакции, количественно анализировали с помощью ВЭЖХ.
Условия гидролиза в буфере с pH 9,2 (пример испытания в соответствии с pH)
Соединения A-7 и A-8, полученные в примерах 63 и 64 растворяли в ДМСО и смешивали с буферным раствором ФСБ, имеющим рН 9,2, с получением раствора, имеющего концентрацию 300 мкМ (40% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 300 мкМ в буферном растворе ФСБ. Затем реакционную смесь инкубировали при 37°С. Реакционную смесь соединения A-7 с pH 9,2 разделяли на аликвоты за 0 минут до реакции, через 5 минут, 10 минут, 30 минут, 60 минут, 120 минут и 180 минут после реакции, соответственно, где каждая аликвота составляла 80 мкл. Затем оставшееся соединение A-7 по настоящему изобретению или MPS и BOC-Tyr-OH, высвобожденные в буферном растворе с pH 9,2, количественно анализировали с помощью ВЭЖХ. Реакционную смесь соединения A-8 с pH 9,2 разделяли на аликвоты за 0 минут до реакции, через 5 минут, 10 минут, 30 минут, 60 минут, 120 минут, 180 минут, 240 минут и 300 минут после реакции, соответственно, где каждая аликвота составляла 80 мкл. Затем оставшееся соединение A-8 по настоящему изобретению или MPS и BOC-Tyr-OMe высвобожденные в буферном растворе с pH 9,2, количественно анализировали с помощью ВЭЖХ.
Условия гидролиза в буфере с pH 5,0 (пример испытания в соответствии с pH)
Соединение A-8, полученное в Примере65, растворяли в ДМСО, и смешивали с буферным раствором ФСБ, имеющим рН 5,0, и раствором ДМСО для получения раствора с концентрацией 300 мкМ (40% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 300 мкМ с буферным раствором ФСБ. Затем реакционную смесь инкубировали при 37°С. Реакционную смесь соединения A-8 с pH 5,0 разделяли на аликвоты за 0 минут до реакции, соответственно через 20 минут, 180 минут, 630 минут и 1 день после реакции, соответственно, где каждая аликвота составляла 80 мкл. Затем оставшееся соединение A-8 по настоящему изобретению или MPS и BOC-Tyr-OMe высвобожденные в буферном растворе с pH 5,0, количественно анализировали с помощью ВЭЖХ.
Снятие защиты при концентрации иона фтора
Соединение А-20 растворяли в ДМСО для приготовления раствора, имеющего концентрацию 100 мкМ (90% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 100 мкМ в буферном растворе ФСБ. К раствору TBAF в ТГФ (100 мМ) добавляли 1,0, 10,0 и 100 эквивалентов соединения A-20. Реакционную смесь инкубировали при 37°С и разделяли на аликвоты при 0°С до реакции, через 5, 20, 44, 68 и 116 часов после реакции, соответственно, где каждая аликвота составляла 80 мкл. Затем оставшееся соединение А-20 или MPS, высвобожденные в ходе реакции, количественно анализировали с помощью ВЭЖХ.
[Таблица 2]
[Пример 140] Анализ in vitro конъюгата лиганд-лекарственный препарат
Раковые клетки KB собирали и высевали в 24-луночные планшеты с плотностью 30 000 клеток на лунку в 2 мл среды и культивировали в течение 24 часов. Затем серийные разведения соединения C-1, полученного в примере 108 использовали для обработки при от 30 нМ до 0,0096 нМ, серийные разведения соединения C-2, полученные в примере 109 использовали для обработки при от 1000 нМ до 0,32 нМ, серийные разведения соединения C-3, полученные в примере 110 и соединение C-7, полученное в примере 114 использовали для обработки при от 25 нМ до 0,0016 нМ, и серийные разведения лекарственного препарата MMAF-OMe использовали для обработки при от 10 нМ до 0,0097 нМ. Серийные разведения соединений C-5 и C-6, полученные в Примере 112 и Примере 113 использовали для обработки при от 100 нМ до 0,0001 нМ, а серийные разведения лекарственного препарата seco-DUBA использовали для обработки при 100 нМ до 0,001 нМ. Серийные разведения соединений C-4 и C-9, полученные в Примере 111 и Примере 116 использовали для обработки при от 1000 нМ до 0,001 нМ, а серийные разведения димера CBI лекарственного препарата использовали для обработки при 10 нМ до 0,00001 нМ. Серийные разведения соединения C-8, полученные в Примере 115 и CBI-индола лекарственного препарата использовали для обработки при от 100 нМ до 0,0001 нМ. Через 72 часа, 96 часов или 144 часа инкубации, 0,2 мл красителя 3-(4,5-диметилтиазол-2-ил) -2,5-дифенилтетразолия бромида (MTT), растворенного в буферном растворе ФСБ (5 мг/мл), добавляли в каждую лунку планшетов. Формазаны, образованные восстановлением красителя МТТ митохондриальными оксидоредуктазами в живых клетках растворяли в ДМСО иизмеряли с использованием поглощения при 550 нм. Результаты приведены в Таблице 3 ниже.
[Таблица 3] Клеточная цитотоксичность конъюгата лиганд-лекарственный препарат
[Пример141] Испытания стабильности плазмы мыши, крысы, собаки и человека
Соединение A-1, полученное в Примере 58 и MPS, используемый в качестве стандартного материала, растворяли в ДМСО до до концентрации 60 мМ. Затем каждую из человеческой плазмы (Biochemed 752R-SC-PMG), мышиной плазмы (Biochemed 029-APSC-MP), крысиной плазмы (Biochemed 031-APSC-MP) и плазмы собаки породы бигль (Biochemed 013-APSC-MP) смешивали с соединением и MPS до конечной концентрации o300 мкМ (конечная конц. 0,5% ДМСО). Полученные плазменные смеси инкубировали при 37°С на водяной бане. Аликвоты отбирали до реакции и через 1, 2, 4 и 7 дней после реакции, причем каждая аликвота составляла 300 мкл. Для завершения реакции добавляли двукратные объемы ацетонитрила с последующим кратковременным вортексным перемешиваниеми центрифугированием для осаждения белков плазмы. Каждый супернатант, полученный после центрифугирования, собирали и анализировали с помощью ВЭЖХ. Соединение A-1 обнаруживали и количественно определяли в плазме мыши, крысы, собаки породы бигль и человека в течение 7 дней (> 95%). Это исследование продемонстрировало превосходную стабильность β-галактозидного линкера в плазме.
[Пример 142] Химическая стабильность
Соединение A-1, полученное в Примере 58, растворяли в ДМСО и смешивали с буферным раствором ФСБ (pH 7,4) для приготовления раствора, имеющего концентрацию 500 мкМ (5% ДМСО). MPS, используемый в качестве стандартного материала, готовили в виде раствора с концентрацией 500 мкМ в буферном растворе ФСБ. 420 мкл буферного раствора и 140 мкл раствора соединения A-1 и 140 мкл раствора MPS смешивали, получая таким образом реакционную смесь в общем количестве 700 мкл. Реакционную смесь инкубировали при комнатной температуре, блокируя свет. Реакционную смесь разделяли на аликвоты за 0 дней до реакции и через 1 день, 2 дня, 4 дня и 7 дней после реакции, где количество каждой аликвоты составляло 70 мкл. Затем оставшееся соединение A-1, MPS и высвобожденный тирозин количественно определяли при помощи анализа методом ВЭЖХ. Анализ ВЭЖХ подтвердил, что соединение А-1 присутствовало (> 95%) в течение 7-дневного инкубационного периода, что было признано очень стабильным.
[Пример испытания 6] Получение конъюгата (альбумин и антитело)
Соединение D-1, полученное в Примере 117, соединение D-2, полученное в Примере 118, соединение D-5, полученное в Примере 110, и соединение D-6, полученное в Примере 111, использовали для проведения реакции конъюгирования с тиольной группой сконструированного цистеина трастузумаба (или человеческого сывороточного альбумина и т. д.), тем самым получая D-1-AB, D-2-AB, Albu-D-5 и Albu-D-6 в качестве конъюгатов с лекарственным препаратом тиомаб (TDC), соответственно, со ссылкой на методы, представленные в документе [см. Nature Biotechnology, 2008, 26, 925-932, Bioconjugate Chem., 2013, 24, 1256-1263, Bioconjugate Chem., 2016, 27, 1324-1331, Bioconjugate Chem. 2014, 25, 460-469]. Анализ ЖХ/МС подтвердил, что молекулярная масса тиомаба составляла 145 450 Да, и также присутствовало небольшое количество (~146,895 Да) формы гликирования. Анализ ЖХ/МС полученного конъюгата антитело лекарственный препарат D-1-AB показал наличие масс около 148 563 Да и около 150 038 Да. Эти сдвиги массы соответствовали конъюгации двух молекул D-1.
[Пример 143] Анализ in vitro конъюгата белок-лекарственный препарат
Раковые клетки KB, SKBR-3, BT-474, NCI-N87 высевали в 96-луночные планшеты с плотностью 2000-8000 клеток на лунку в 100 мкл среды и культивировали в течение 24 часов. Четыре соединения, полученные в примере испытания 6, обрабатывали серийными разведениями 1:4 от 600 нМ до 0,009 нМ, лекарственный препарат MMAF-OMe обрабатывали серийными разведениями 1:4 от 100 нМ до 0,0015 нМ, а конъюгат антитело с лекарственным препаратом T-DM1 обрабатывали серийными разведениями 1:4 от 200 нМ до 0,003 нМ. Эксперименты проводили аналогично примеру испытания 3 для количественной оценки живых клеток спустя 96 часов, и результаты показаны в таблицах 4 и 5 ниже. Кроме того, результаты анализа in vitro соединения D-1-AB представлены на ФИГ. 12.
[Таблица 4] Клеточная цитотоксичность конъюгата белок-лекарственный препарат
[Таблица 5] Клеточная цитотоксичность конъюгата антитело-лекарственный препарат
(*T-DM1 : Номер CAS компании Roche: 1018448-65-1)
[Пример 144] Эффективность in vivo
Эффективность in vivo конъюгатов антитело-лекарственный препарат по изобретению измеряли с помощью исследований ксенотрансплантата опухоли на мышах. Самцу мыши линии BALB/c nu/nu вводили подкожно в правый бок суспензии 1 X106 клеток NCI-N87 соответственно в ФСБ. Мыши были рандомизированы в исследуемые группы, когда опухоли достигли размера приблизительно 100 мм3. Конъюгаты T-DM1 (2 мг/кг), D-1-AB, D-2-AB, D-8-AB и D-18-AB (0,5 мг/кг или 2 мг/кг) вводили внутривенно. (однократная инъекция в день лечения 0). Все группы лечения состояли из 6-10 животных в группе, а размер опухоли контролировали два раза в неделю путем измерения штангенциркулем. Массу опухоли рассчитывали как объем = (ширина X ширина X длина)/2. Конъюгаты D-1-AB, D-2-AB и D-8-AB приводили к регрессии опухоли в течение периода наблюдения, то есть 80 дней от начала эксперимента. Контрольный конъюгат T-DM1 был менее активен, чем конъюгаты по изобретению.
Включение путем ссылки
Все публикации, патенты, упомянутые в данном документе, включены в данный документ посредством ссылки в той же степени, в которой каждая индивидуальная публикация, патент, специфично и индивидуально указана для включения посредством ссылки. В случае конфликта настоящая заявка, включая любые определения в этом документе, будет иметь преимущественную силу.
Эквиваленты
Хотя были обсуждены конкретные варианты осуществления предмета изобретения, приведенное выше описание является иллюстративным, а не ограничивающим. Многие варианты изобретения станут очевидными для специалистов в данной области техники после рассмотрения этого описания и формулы изобретения ниже. Полный объем изобретения должен быть определен посредством ссылки на формулу изобретения вместе с их полным объемом эквивалентов и описания вместе с такими вариантами.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2711502C2 |
| СОЕДИНЕНИЯ, ВКЛЮЧАЮЩИЕ САМОРАСЩЕПЛЯЮЩУЮСЯ ГРУППУ | 2015 |
|
RU2712744C2 |
| КОНЪЮГАТЫ БЕЛОК-АКТИВНОЕ ВЕЩЕСТВО И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2613906C2 |
| НОВОЕ СОЕДИНЕНИЕ, ПРОЯВЛЯЮЩЕЕ ИНГИБИРУЮЩУЮ АКТИВНОСТЬ В ОТНОШЕНИИ ЭНТЕРОПЕПТИДАЗЫ | 2019 |
|
RU2768755C1 |
| КОНДЕНСИРОВАННЫЕ КОЛЬЦЕВЫЕ ГЕТЕРОАРИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ TRK | 2015 |
|
RU2708674C2 |
| СЛИТЫЕ ТРИЦИКЛИЧЕСКИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ИНТЕГРАЗЫ ВИЧ | 2016 |
|
RU2740187C2 |
| СОЕДИНЕНИЕ ДЛЯ РАЗРУШЕНИЯ АНДРОГЕНОВОГО РЕЦЕПТОРА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2817356C1 |
| ХИМИЧЕСКИЕ ЛИНКЕРЫ И ИХ КОНЪЮГАТЫ | 2005 |
|
RU2402548C2 |
| 5-5 КОНДЕНСИРОВАННЫЕ КОЛЬЦА КАК ИНГИБИТОРЫ С5а | 2018 |
|
RU2780322C2 |
| СОЕДИНЕНИЯ ИНДОЛА И ИНДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРА НЕКРОЗА КЛЕТКИ | 2008 |
|
RU2437883C1 |
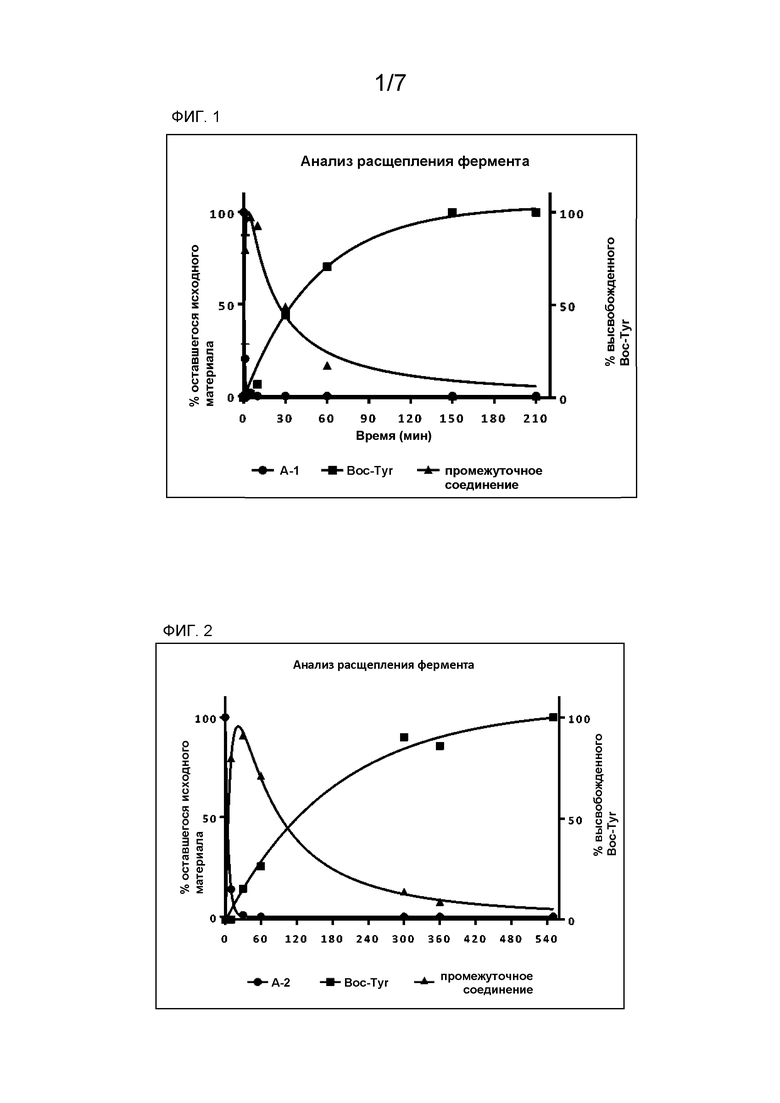





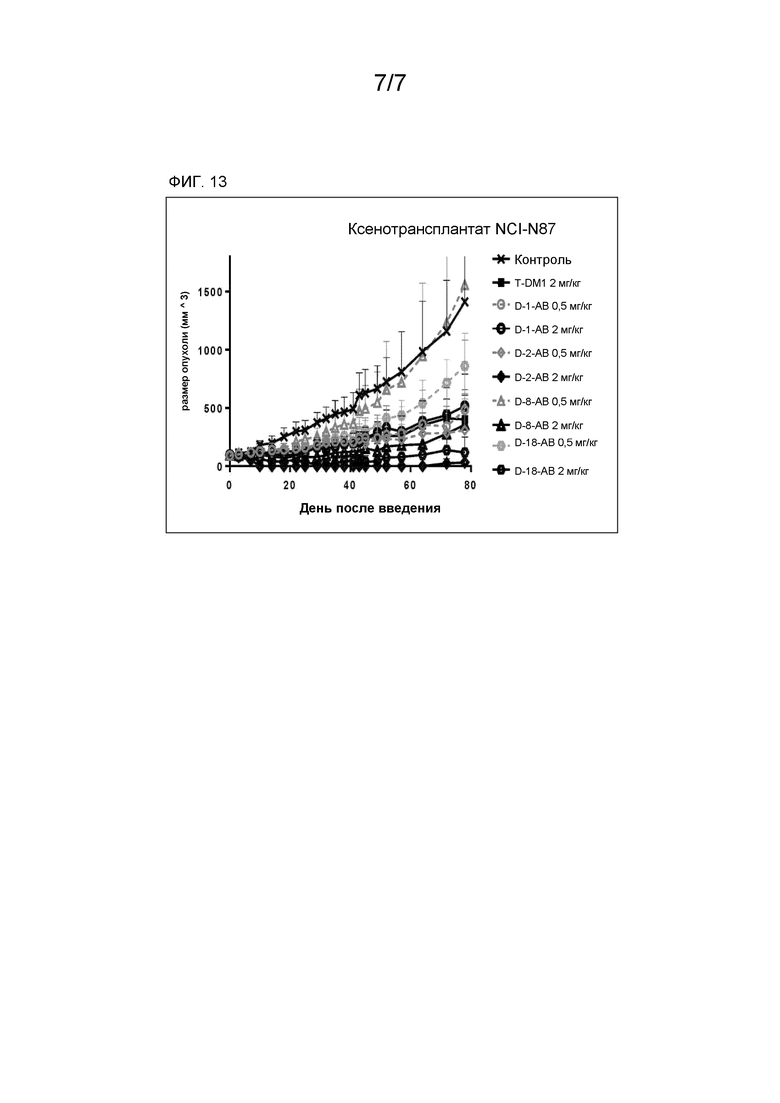
Изобретение относится к конъюгату антитело-активный агент, содержащему расщепляемый линкер, функциональную группу SO2, которая способна селективно высвобождать активный агент, и функциональную группу, которая запускает химическую реакцию, физико-химическую реакцию и/или биологическую реакцию путем внешней стимуляции. Также предложены промежуточные соединения и способы получения конъюгата. Конъюгат предназначен для лечения пролиферативных заболеваний. 9 н. и 13 з.п. ф-лы, 7 ил., 5 табл., 144 пр.
1. Конъюгат формулы (I')

или его фармацевтически приемлемая соль,
где CB представляет собой нацеливающий фрагмент, содержащий антитело, выбранное из интактного поликлонального антитела, интактного моноклонального антитела, фрагмента антитела, одноцепочечного мутанта Fv (scFv), мультиспецифического антитела, биспецифического антитела, химерного антитела, гуманизированного антитела, человеческого антитела и гибридного белка, содержащего антигенную детерминантную часть антитела;
каждый из cb и n независимо представляет собой целые числа, имеющие значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый из D-L независимо представляет собой группу, имеющую структуру формулы (I”)
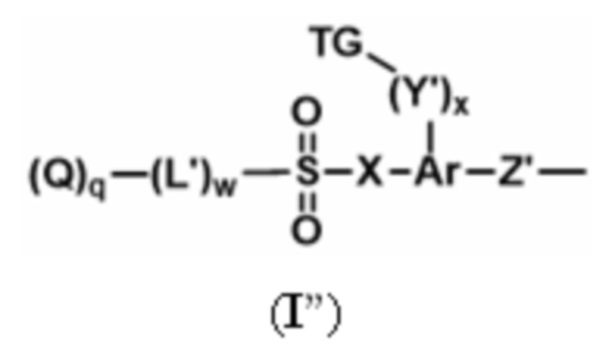 ,
,
где (Q)q-(L')w- выбран из:
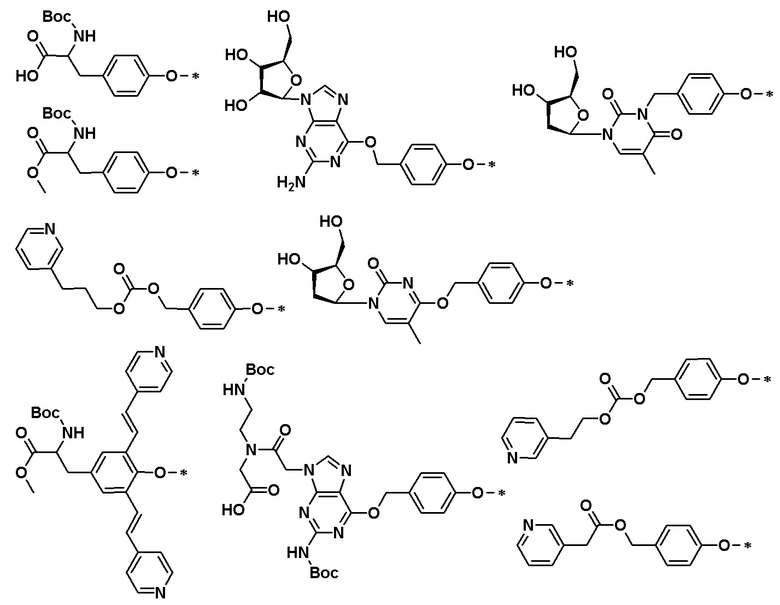
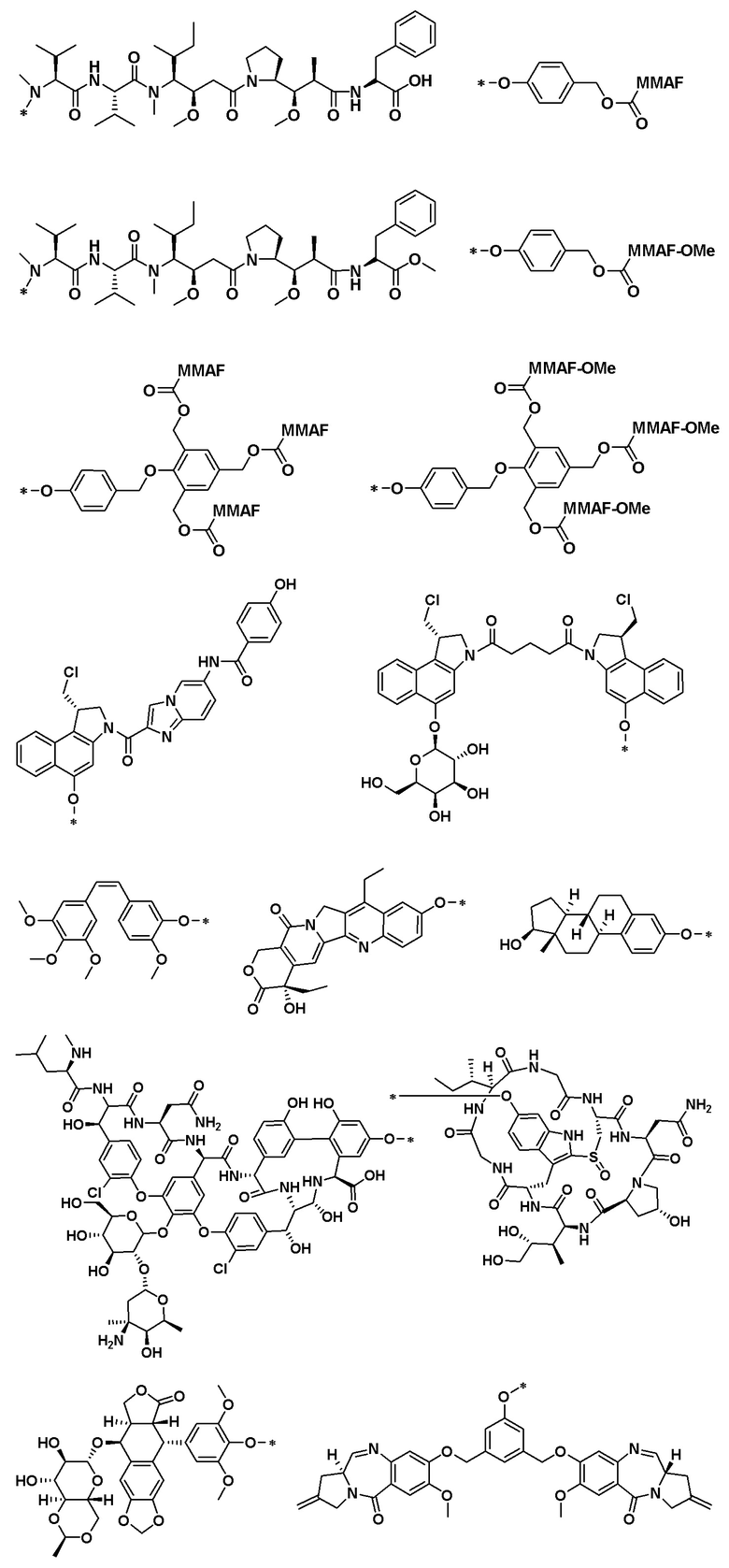

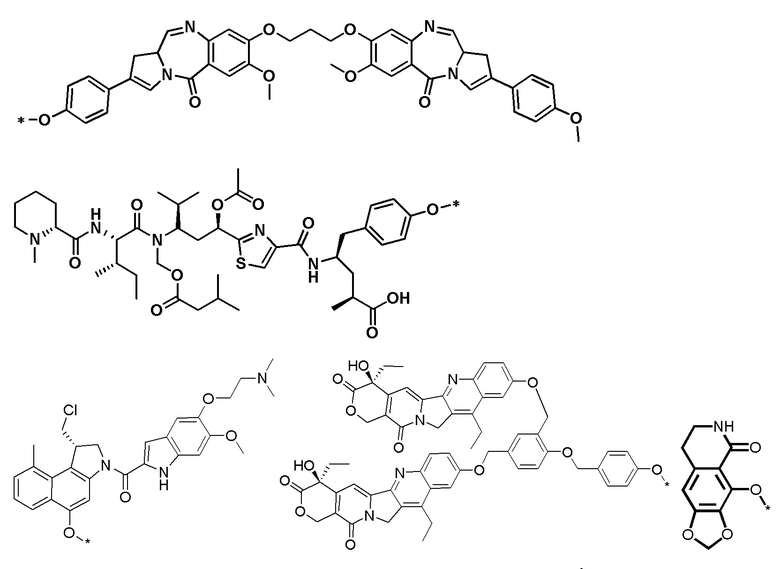
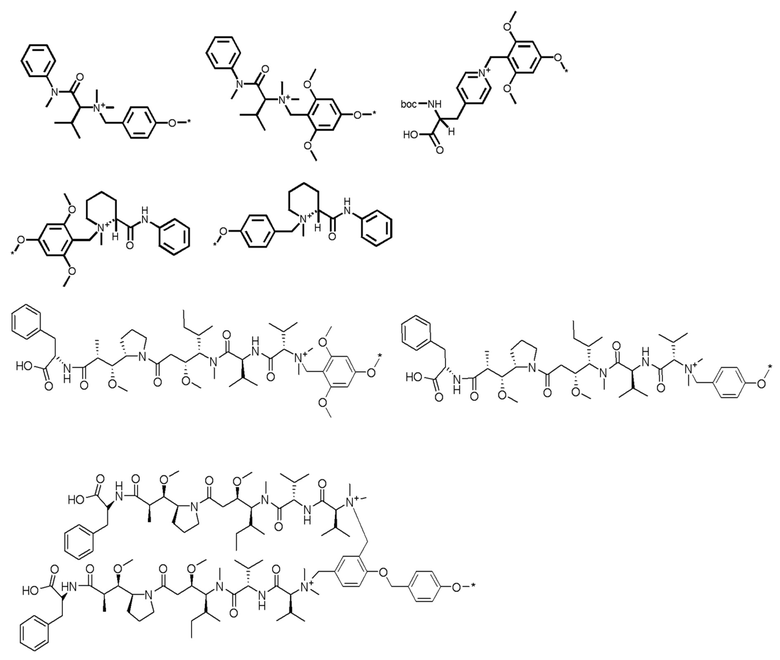

где * означает точку присоединения (Q)q-(L')w к -SO2-;
Z' представляет собой связующую группу, содержащую
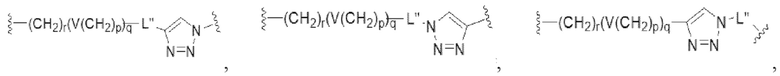
формулы (F'), (G'), (H'), (J'), (K'), (L'), (M') или (N'):


где Re представляет собой (C1-C6)алкил;
X'' представляет собой -O-, -S-, -NH- или -CH2-;
L2 представляет собой спейсерный фрагмент, незамещенный или замещенный одним или более C1-C6 алкилами, C5-C14 арилами и C3-C8 гетероарилами, где алкил, арил и гетероарил являются незамещенными или замещены одним или более заместителями, выбранными из C1-C10 алкила, -(CH2)uNH2, -(CH2)uNRu1Ru2, -(CH2)uCO2H, -(CH2)uCO2Ru1 и -(CH2)uSO2Ru3, где каждый из Ru1, Ru2 и Ru3 независимо представляет собой водород, C1-C15 алкил, C6-C20 арил или C3-C10 гетероарил; и u представляет собой целое число, имеющее значение от 0 до 10;
X4 представляет собой -NHC(O)-(CH2)g-NH- или -C(O)NH-(CH2)h-NH-;
каждый из Wb1 и Wb2 независимо представляет собой -C(O)NH-, -NHC(O)-, 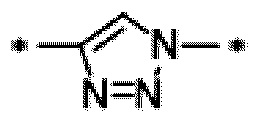 или
или  ;
;
R12 представляет собой водород, алкил, боковую цепь аминокислоты, -(CH2)sC(O)R13 или -(CH2)pNR14R15;
R13 представляет собой ОН или -NH(CH2)s'(X'''CH2CH2)s”Z''-(CB)m;
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s”Z''-(CB)m;
каждый из s и s'' независимо представляет собой целое число, имеющее значение от 0 до около 10;
m представляет собой целое число, имеющее значение 0 или 1;
X''' представляет собой -O-, -S-, -NH- или -CH2-;
Z'' представляет собой связующую группу, соединяющую CB с остатком R14 или R15; или Z'' представляет собой связующую группу, содержащую реакционноспособную группу;
каждый из a, b, c, d, e, g, h, o, p и qq независимо представляет собой целое число, имеющее значение от 1 до около 10; и
s' представляет собой целое число, имеющее значение от 1 до около 10,
где каждый из V независимо представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
каждый из R21, R22, R23, R24 и R25 независимо представляет собой водород, C1-C6алкил, C1-C6алкилC6-C20арил или C1-C6алкилC3-C20гетероарил;
r представляет собой целое число, имеющее значение от 1 до около 10;
p представляет собой целое число, имеющее значение от 0 до около 10;
q представляет собой целое число, имеющее значение от 1 до около 10; и
L” представляет собой одинарную связь;
X представляет собой -O-;
Ar представляет фенил;
Y' представляет собой -O-;
X и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, выбранную из: -NO2, -C(O)-(CH2)2C(O)-(C1-C6)алкила, нитробензила,  ,
,  и
и 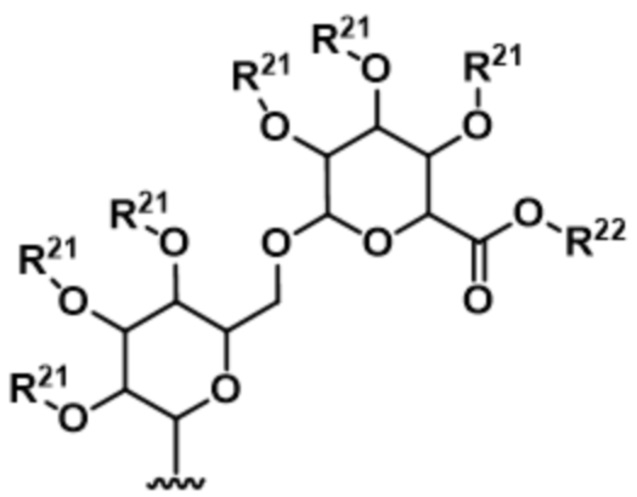 ,
,
где R21 представляет собой водород; и
R22 представляет собой водород или (C1-C6)алкил; и
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый w и x независимо представляет собой целое число, имеющее значение 0 или 1;
при условии, что когда w равно 0, то q равно 1.
2. Конъюгат по п.1, где Z' представляет собой связующую группу формулы (F'), (G'), (H'), (J'), (K'), (L'), (M') или (N'):
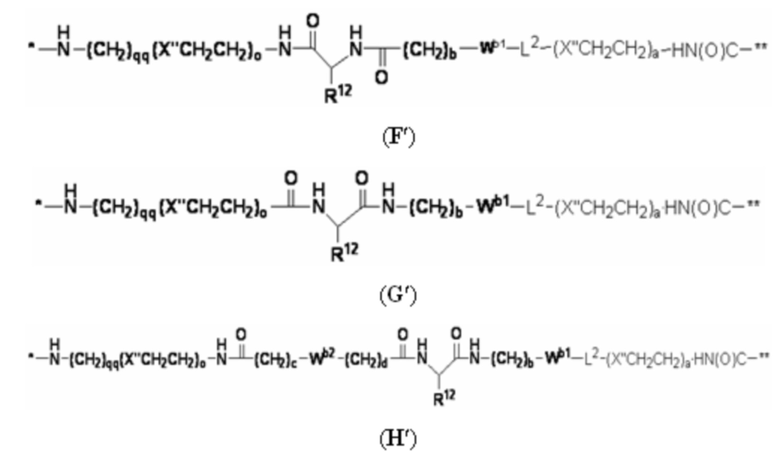

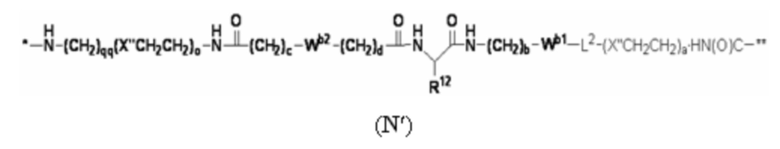
где Re представляет собой (C1-C6)алкил;
X'' представляет собой -O-, -S-, -NH- или -CH2-;
L2 представляет собой спейсерный фрагмент, незамещенный или замещенный одним или более C1-C6 алкилами, C5-C14 арилами и C3-C8 гетероарилами, где алкил, арил и гетероарил являются незамещенными или замещены одним или более заместителями, выбранными из C1-C10 алкила, -(CH2)uNH2, -(CH2)uNRu1Ru2, -(CH2)uCO2H, -(CH2)uCO2Ru1 и -(CH2)uSO2Ru3, где каждый из Ru1, Ru2 и Ru3 независимо представляет собой водород, C1-C15 алкил, C6-C20 арил или C3-C10 гетероарил; и u представляет собой целое число, имеющее значение от 0 до 10;
X4 представляет собой -NHC(O)-(CH2)g-NH- или -C(O)NH-(CH2)h-NH-;
каждый из Wb1 и Wb2 независимо представляет собой -C(O)NH-, -NHC(O)-,  или
или  ;
;
R12 представляет собой водород, алкил, боковую цепь аминокислоты, -(CH2)sC(O)R13 или -(CH2)pNR14R15;
R13 представляет собой ОН или -NH(CH2)s'(X'''CH2CH2)s”Z''-(CB)m;
каждый из R14 и R15 независимо представляет собой водород или -C(O)(CH2)s'(X'''CH2CH2)s”Z''-(CB)m;
каждый из s и s'' независимо представляет собой целое число, имеющее значение от 0 до около 10;
m представляет собой целое число, имеющее значение 0 или 1;
X''' представляет собой -O-, -S-, -NH- или -CH2-;
Z'' представляет собой связующую группу, соединяющую CB с остатком R14 или R15; или Z'' представляет собой связующую группу, содержащую реакционноспособную группу;
каждый из a, b, c, d, e, g, h, o, p и qq независимо представляет собой целое число, имеющее значение от 1 до около 10; и
s' представляет собой целое число, имеющее значение от 1 до около 10.
3. Конъюгат по п.1 или 2, где TG может быть расщеплена в условиях использования нуклеофильного реагента, в условиях использования основного реагента, фотооблучением, в условиях использования восстанавливающего агента, в кислой среде, ферментативных условиях или окислительных условиях.
4. Конъюгат по п.1 или 2, где x равно 0.
5. Конъюгат по п.1, отличающийся тем, что антитело выбрано из муромонаба-CD3, абциксимаба, ритуксимаба, даклизумаба, паливизумаба, инфликсимаба, трастузумаба (герцептина), этанерцепта, базиликсимаба, гемтузумаба озогамицина, алемтузумаба, ибритумомаба тиуксетана, адалимумаба, алефацепта, омализумаба, эфализумаба, тозитумомаба-I131, цетуксимаба, бевацизумаба, натализумаба, ранибизумаба, панитумумаба, экулизумаба, рилонацепта, цертолизумаба пегола, ромиплостима, AMG-531, CNTO-148, CNTO-1275, ABT-874, LEA-29Y, белимумаба, TACI-Ig, анти-CD20 второго поколения, ACZ-885, тоцилизумаба, атлизумаба, меполизумаба, пертузумаба, Humax CD20, тремелимумаба (CP-675 206), тицилимумаба, MDX-010, IDEC-114, инотузумаба озогамицина, HuMax EGFR, афлиберцепта, HuMax-CD4, Ala-Ala, ChAglyCD3, TRX4, катумаксомаба, IGN101, MT-201, преговомаба, CH-14.18, WX-G250, AMG-162, AAB-001, мотавизумаба, MEDI-524, эфумгумаба, аурограба (Aurograb), раксибакумаба, анти-CD20 третьего поколения, LY2469298 и велтузумаба.
6. Соединение формулы (Ia)

или его фармацевтически приемлемая соль,
где (Q)q-(L')w- выбран из:

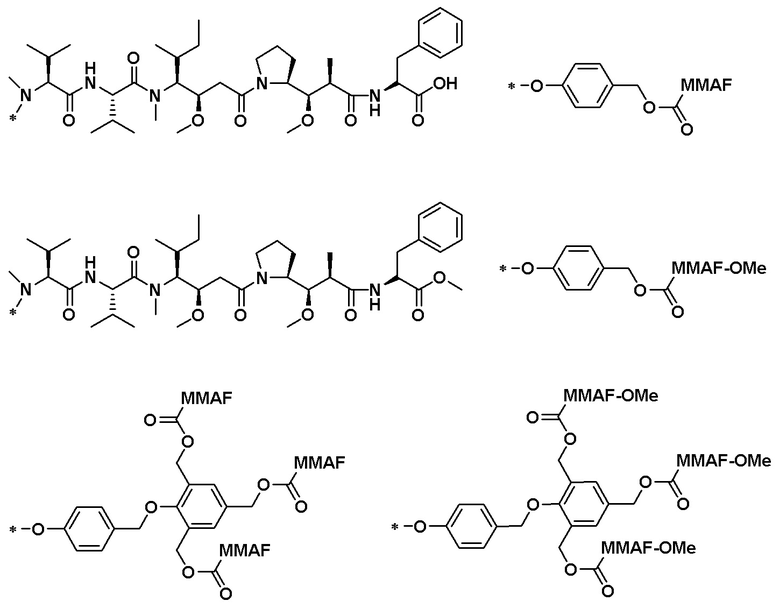
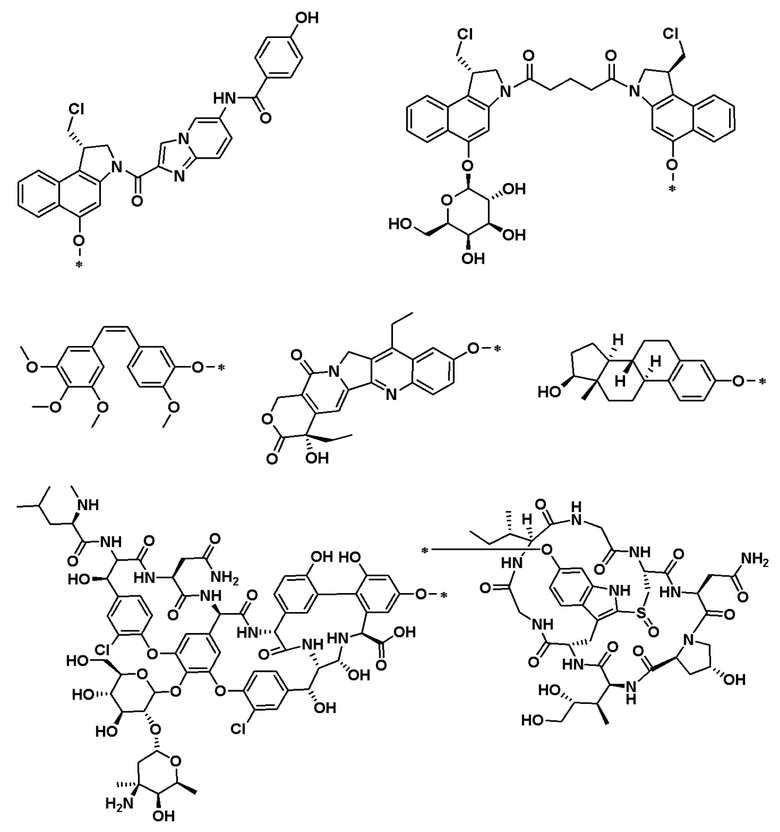
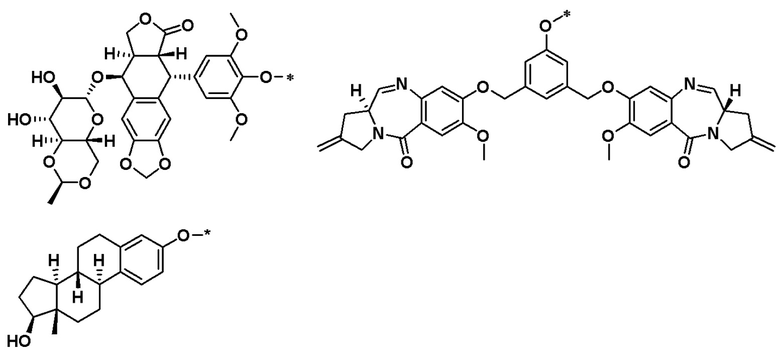
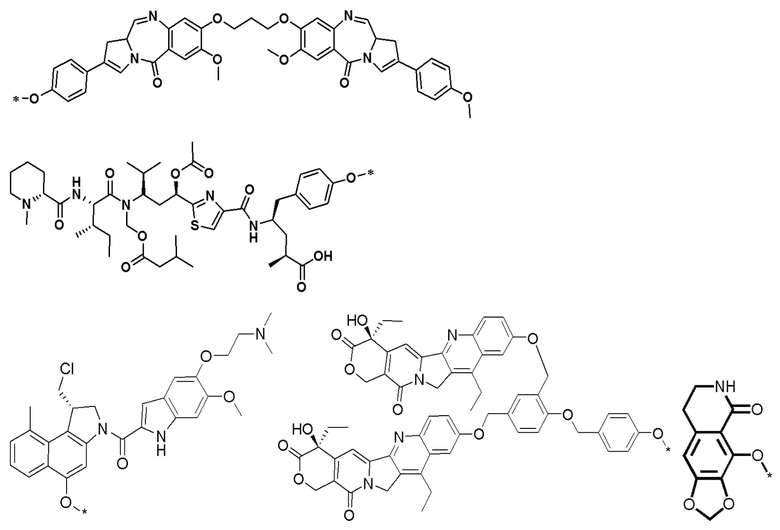



где * означает точку присоединения (Q)q-( L')w- к -SO2-;
Z' отсутствует или представляет собой связующую группу, содержащую:

где каждый из V независимо представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
каждый из R21, R22, R23, R24 и R25 независимо представляет собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
r представляет собой целое число, имеющее значение от 1 до около 10;
p представляет собой целое число, имеющее значение от 0 до около 10;
q представляет собой целое число, имеющее значение от 1 до около 10; и
L” представляет собой одинарную связь;
X представляет собой -O-;
Ar представляет собой фенил;
Y' представляет собой -O-;
X и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, выбранную из: -NO2, -C(O)-(CH2)2C(O)-(C1-C6)алкила, нитробензила,  ,
,  и
и  ,
,
где R21 представляет собой водород; и
R22 представляет собой водород или (C1-C6)алкил;
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый w и x независимо представляет собой целое число, имеющее значение 0 или 1; и
при условии, что когда w равно 0, то q равно 1.
7. Соединение по п.6, где Z' представляет собой связующую группу и дополнительно содержит одну или более групп, выбранных из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3−), 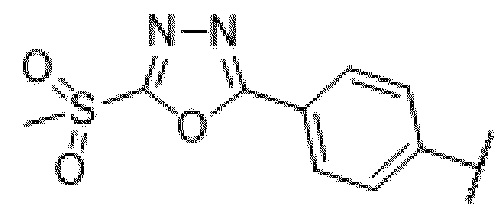 ,
, 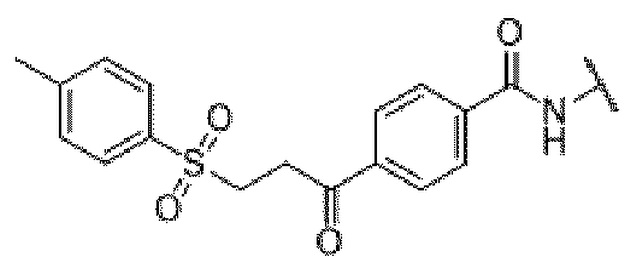 , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra и дигидрофосфата (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra и дигидрофосфата (-OP(=O)(OH)2).
8. Соединение по п.6 или 7, где x равно 0.
9. Способ получения конъюгата по п.1, включающий введение в реакцию соединения по любому из пп.6-8 с нацеливающим фрагментом, где нацеливающий фрагмент представляет собой антитело, выбранное из интактного поликлонального антитела, интактного моноклонального антитела, фрагмента антитела, одноцепочечного мутанта Fv (scFv), мультиспецифического антитела, биспецифического антитела, химерного антитела, гуманизированного антитела, человеческого антитела, гибридного белка, содержащего антигенную детерминантную часть антитела и другие модифицированные молекулы иммуноглобулина, содержащие сайты распознавания антигена.
10. Способ по п.9, отличающийся тем, что антитело выбрано из муромонаба-CD3, абциксимаба, ритуксимаба, даклизумаба, паливизумаба, инфликсимаба, трастузумаба (герцептина), этанерцепта, базиликсимаба, гемтузумаба озогамицина, алемтузумаба, ибритумомаба тиуксетана, адалимумаба, алефацепта, омализумаба, эфализумаба, тозитумомаба-I131, цетуксимаба, бевацизумаба, натализумаба, ранибизумаба, панитумумаба, экулизумаба, рилонацепта, цертолизумаба пегола, ромиплостима, AMG-531, CNTO-148, CNTO-1275, ABT-874, LEA-29Y, белимумаба, TACI-Ig, анти-CD20 второго поколения, ACZ-885, тоцилизумаба, атлизумаба, меполизумаба, пертузумаба, Humax CD20, тремелимумаба (CP-675 206), тицилимумаба, MDX-010, IDEC-114, инотузумаба озогамицина, HuMax EGFR, афлиберцепта, HuMax-CD4, Ala-Ala, ChAglyCD3, TRX4, катумаксомаба, IGN101, MT-201, преговомаба, CH-14.18, WX-G250, AMG-162, AAB-001, мотавизумаба, MEDI-524, эфумгумаба, аурограба (Aurograb), раксибакумаба, анти-CD20 третьего поколения, LY2469298 и велтузумаба.
11. Фармацевтическая композиция для лечения пролиферативного заболевания, содержащая эффективное количество конъюгата по любому из пп.1-5 и фармацевтически приемлемый носитель или вспомогательное вещество для лечения пролиферативного заболевания или состояния.
12. Способ лечения пролиферативного заболевания, включающий введение конъюгата по любому из пп.1-5 субъекту, нуждающемуся в этом.
13. Способ по п.12, отличающийся тем, что пролиферативное заболевание выбрано из аутоиммунных расстройств (например, системной красной волчанки, ревматоидного артрита, болезни «трансплантат против хозяина», миастении или синдрома Шегрена), хронических воспалительных состояний (например, псориаза, астмы или болезни Крона), гиперпролиферативных расстройств (например, рака молочной железы, рака легкого), вирусных инфекций (например, герпеса, папилломы или ВИЧ), остеоартрита и атеросклероза.
14. Способ по п.13, отличающийся тем, что пролиферативное заболевание представляет собой рак, выбранный из карциномы, лимфомы, бластомы, саркомы, лейкоза или лимфоидного злокачественного новообразования.
15. Способ по п.14, отличающийся тем, что рак представляет собой плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого (например, мелкоклеточный рак легкого, немелкоклеточный рак легкого («НМКРЛ»), аденокарцинома легкого и плоскоклеточный рак легкого), рак брюшины, гепатоцеллюлярный рак, рак желудка (например, рак желудочно-кишечного тракта), рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, рак эндометрия или рак матки, рак слюнной железы, рак почки, рак простаты, рак влагалища, рак щитовидной железы, карциному печени, рак анального канала, рак полового члена, острый лейкоз и рак головы/головного мозга и шеи.
16. Способ по п.15, отличающийся тем, что рак представляет собой карциному шейки матки.
17. Соединение, выбранное из:
 и
и 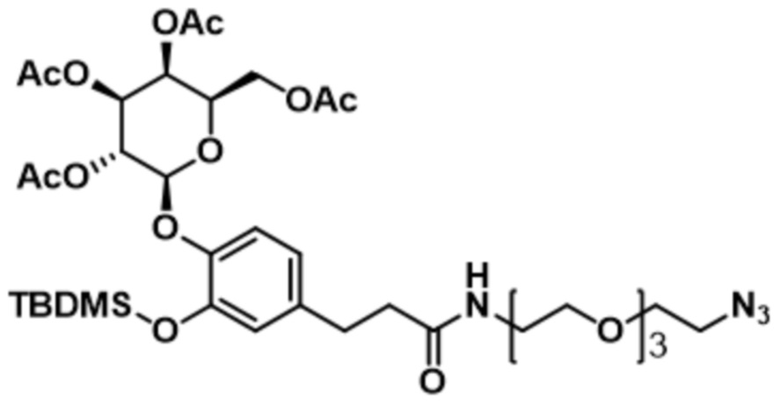
или их фармацевтически приемлемой соли.
18. Способ получения соединения по п.1, включающий введение в реакцию соединения формулы (IIc)

или его фармацевтически приемлемой соли с сульфонилгалогенидом

для получения соединения по п.1
или его фармацевтически приемлемой соли,
где Xa представляет собой галоген;
Q, L', Z', Ar, Y', TG, q, w и x, такие как определено в п.1;
каждый R11 независимо представляет собой C1-C6алкил.
19. Способ получения соединения формулы (Iaa) или его фармацевтически приемлемой соли, где способ включает:
(a) введение в реакцию соединения формулы (IIa)
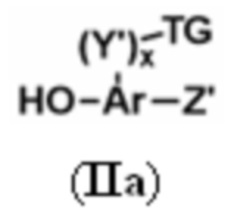
или его фармацевтически приемлемой соли с 1,1'-сульфонилбис(1Н-имидазолом)

для получения соединения формулы (IIbb)

или его фармацевтически приемлемой соли;
соединение формулы (IIbb) дополнительно взаимодействует с соединением формулы (Ia'), (Q)q-(L')w-H или его фармацевтически приемлемой солью для получения соединения формулы (Iaa)
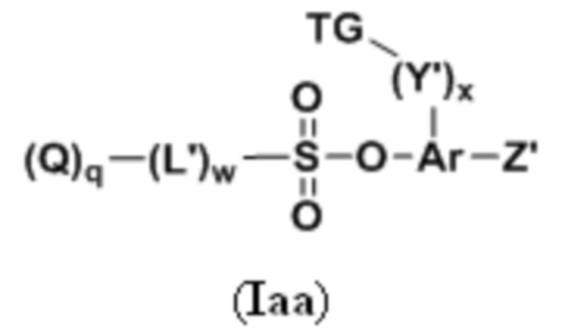
или его фармацевтически приемлемой соли,
где (Q)q-(L')w- выбран из:
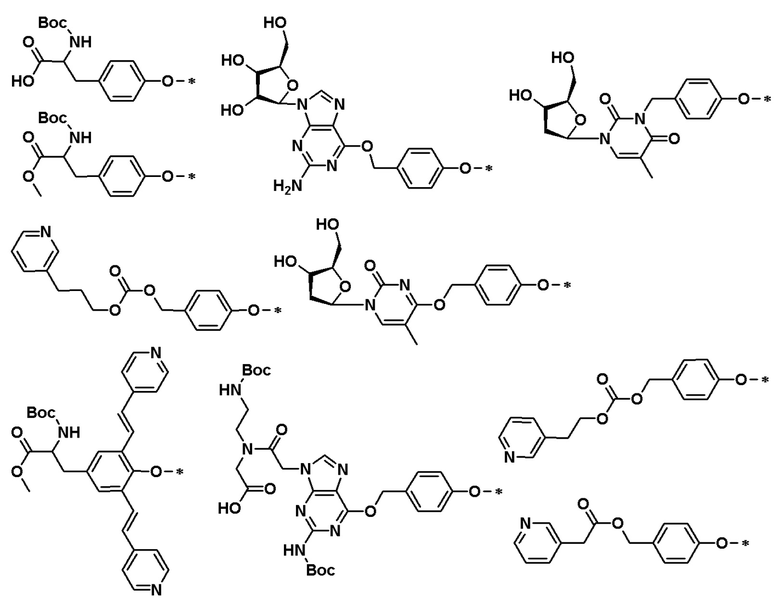

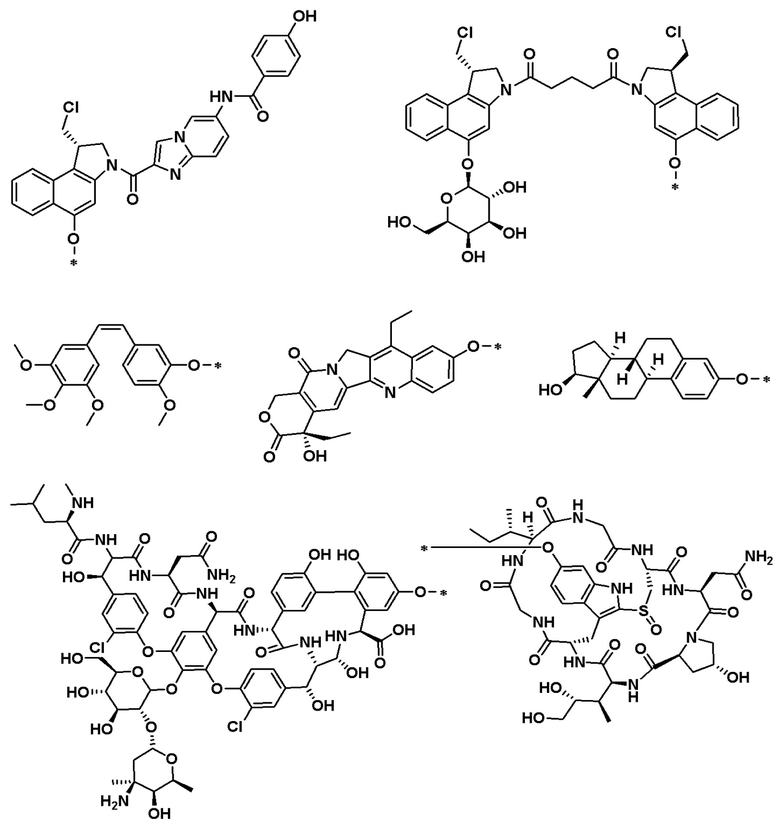
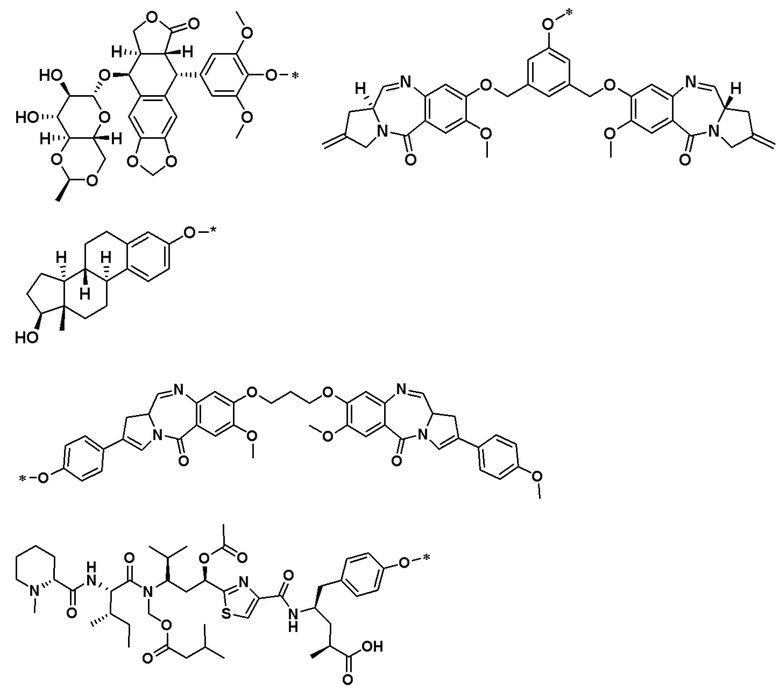

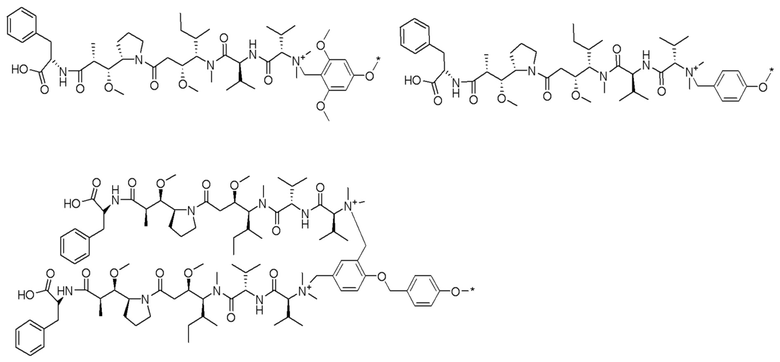

где * означает точку присоединения Q-(L')w- к -SO2-;
Z' отсутствует или представляет собой связующую группу, содержащую:
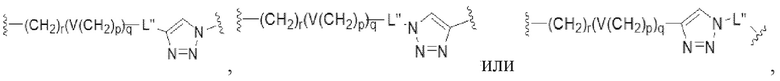
где каждый из V независимо представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
каждый из R21, R22, R23, R24 и R25 независимо представляет собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
r представляет собой целое число, имеющее значение от 1 до около 10;
p представляет собой целое число, имеющее значение от 0 до около 10;
q представляет собой целое число, имеющее значение от 1 до около 10;
L'' представляет собой одинарную связь;
Ar представляет собой фенил;
Y' представляет собой -O-;
O и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, выбранную из: -NO2, -C(O)-(CH2)2C(O)-(C1-C6)алкила, нитробензила,  ,
,  и
и  ,
,
где R21 представляет собой водород; и
R22 представляет собой водород или (C1-C6)алкил; и
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10; и
каждый w и x независимо представляет собой целое число, имеющее значение 0 или 1.
20. Способ по любому из пп.17-19, где Z' представляет собой связующую группу и дополнительно содержит одну или более групп, выбранных из изоцианида, изотиоцианида, 2-пиридилдисульфида, галоацетамида (-NHC(O)CH2-галоген), малеимида, диена, алкена, галогенида, тозилата (TsO-), альдегида, сульфоната (R-SO3−), 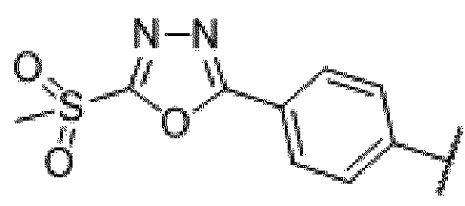 ,
,  , фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra и дигидрофосфата (-OP(=O)(OH)2).
, фосфоновой кислоты (-P(=O)(OH)2), кетона, C8-C10 циклоалкинила, -OH, -NHOH, -NHNH2, -SH, карбоновой кислоты (-COOH), ацетилена (-C≡CH), азида (-N3), амино (-NH2), сульфоновой кислоты (-SO3H), производного алкинона (-C(O)C≡C-Ra и дигидрофосфата (-OP(=O)(OH)2).
21. Способ по любому из пп.18-20, где x равно 0.
22. Способ получения соединения формулы (Iaa)
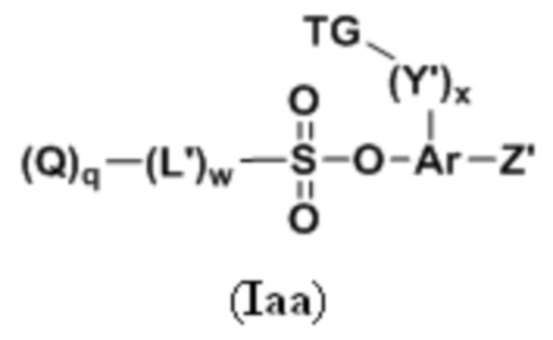
или его фармацевтически приемлемой соли,
где (Q)q-(L')w- выбран из:


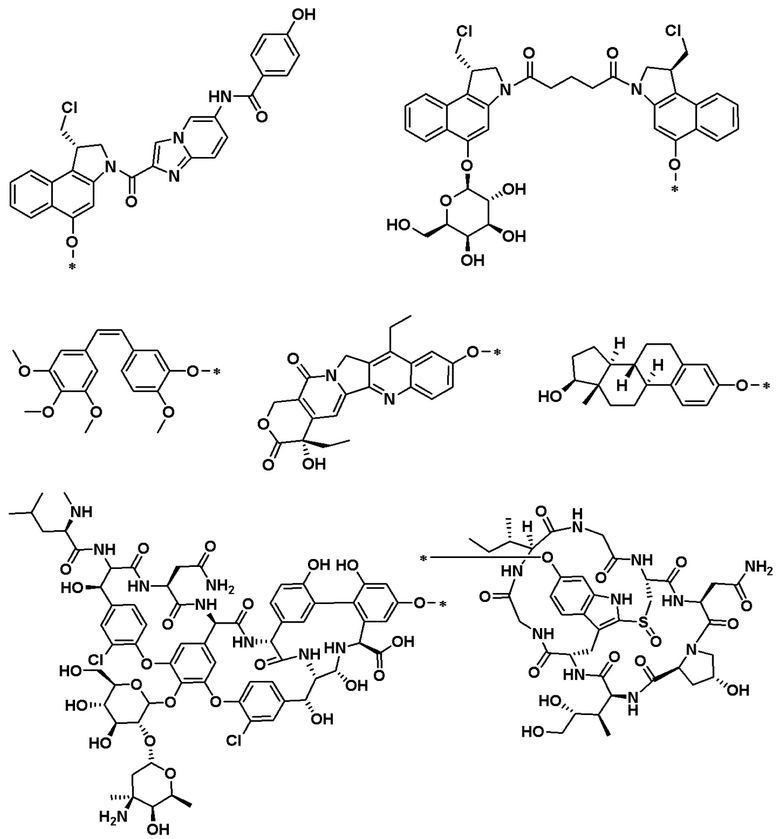
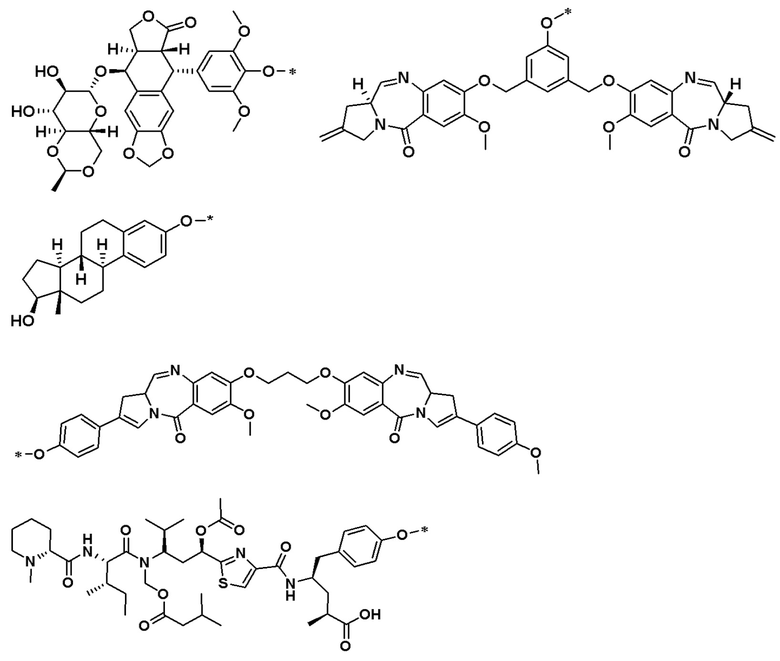

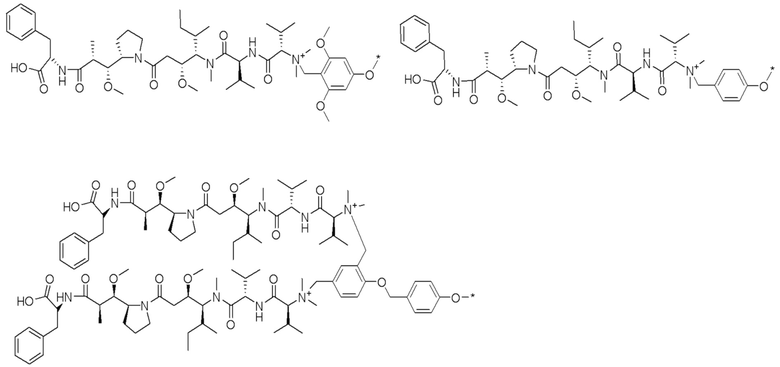

где * означает точку присоединения (Q)q-( L')w- к -SO2-;
Z' отсутствует или представляет собой связующую группу, содержащую:

где каждый из V независимо представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
каждый из R21, R22, R23, R24 и R25 независимо представляет собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
r представляет собой целое число, имеющее значение от 1 до около 10;
p представляет собой целое число, имеющее значение от 0 до около 10;
q представляет собой целое число, имеющее значение от 1 до около 10; и
L” представляет собой одинарную связь;
Ar представляет собой фенил;
Y' представляет собой -O-;
O и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, выбранную из: -NO2, -C(O)-(CH2)2C(O)-(C1-C6)алкила, нитробензила,  ,
,  и
и  ,
,
где R21 представляет собой водород; и
R22 представляет собой водород или (C1-C6)алкил;
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый w и x независимо представляет собой целое число, имеющее значение 0 или 1,
или его фармацевтически приемлемой соли, где способ включает:
дополнительно взаимодействие соединения формулы (Iaa) с нацеливающим фрагментом для обеспечения конъюгата формулы (I')
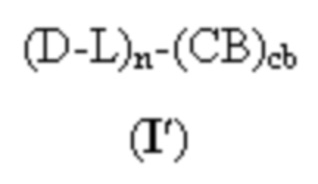
или его фармацевтически приемлемой соли,
где CB представляет собой нацеливающий фрагмент, содержащий антитело, выбранное из интактного поликлонального антитела, интактного моноклонального антитела, фрагмента антитела, одноцепочечного мутанта Fv (scFv), мультиспецифического антитела, биспецифического антитела, химерного антитела, гуманизированного антитела, человеческого антитела и гибридного белка, содержащего антигенную детерминантную часть антитела;
каждый из cb и n независимо представляет собой целые числа, имеющие значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый из D-L независимо представляет собой группу, имеющую структуру формулы (I”)
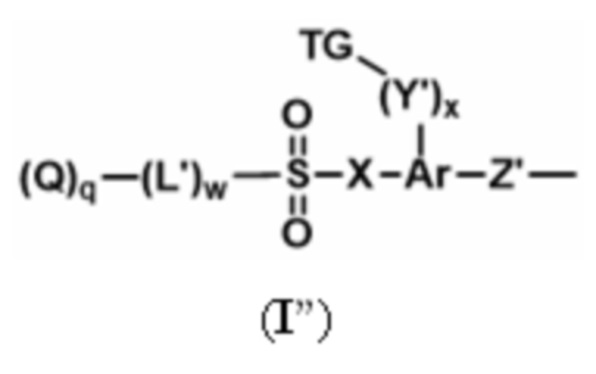 ,
,
где (Q)q-(L')w- выбран из:



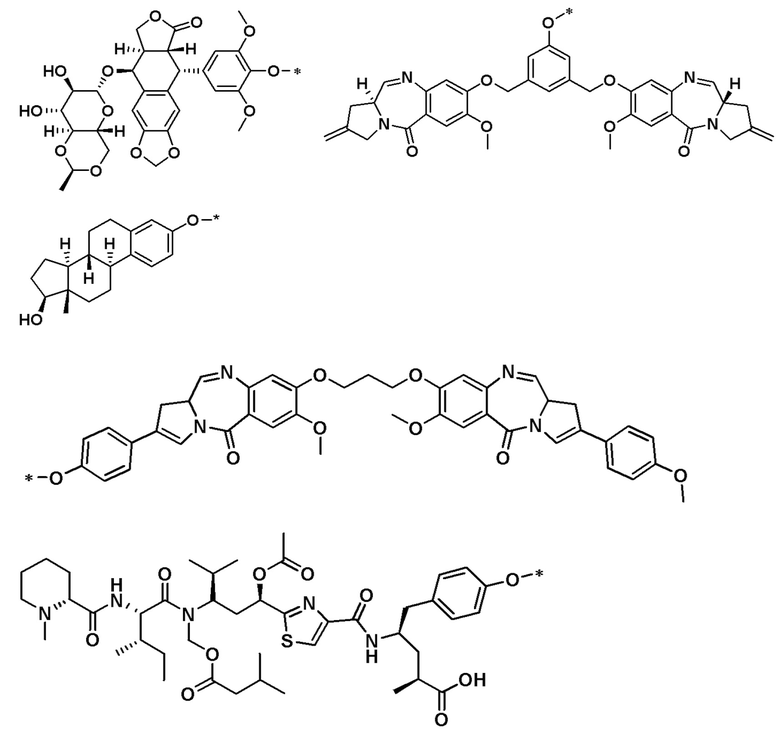
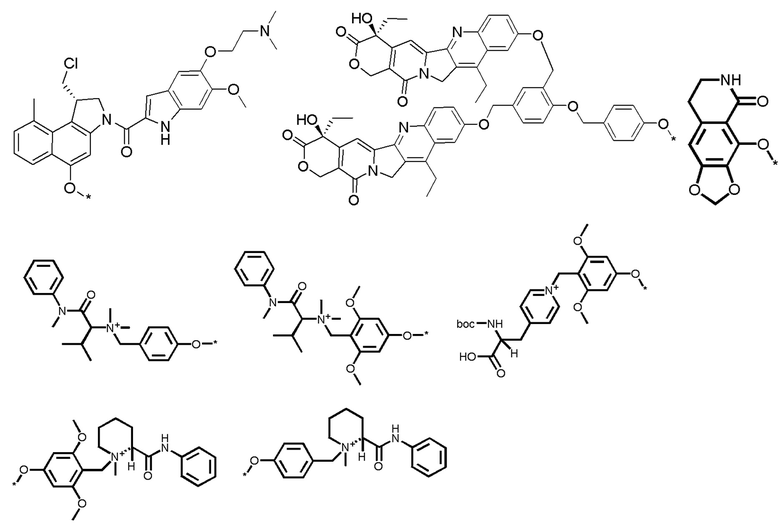
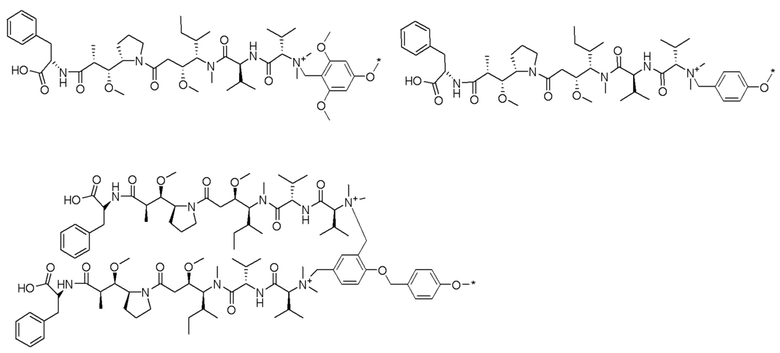
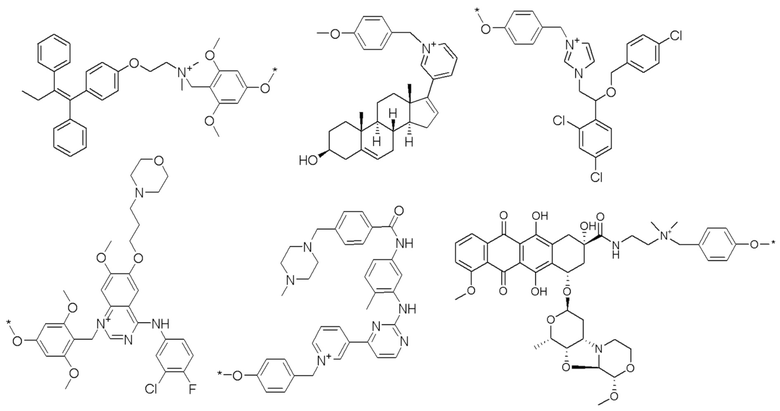
где * означает точку присоединения (Q)q-(L')w к -SO2-;
Z' представляет собой связующую группу, содержащую

где каждый из V независимо представляет собой одинарную связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
каждый из R21, R22, R23, R24 и R25 независимо представляет собой водород, C1-C6алкил, C1-C6алкилC6-C20арил или C1-C6алкилC3-C20гетероарил;
r представляет собой целое число, имеющее значение от 1 до около 10;
p представляет собой целое число, имеющее значение от 0 до около 10;
q представляет собой целое число, имеющее значение от 1 до около 10; и
L” представляет собой одинарную связь;
X представляет собой -O-;
Ar представляет фенил;
Y' представляет собой -O-;
X и Y' расположены на смежных атомах Ar;
TG представляет собой триггерную группу, выбранную из: -NO2, -C(O)-(CH2)2C(O)-(C1-C6)алкила, нитробензила,  ,
,  и
и  ,
,
где R21 представляет собой водород; и
R22 представляет собой водород или (C1-C6)алкил; и
q представляет собой целое число, имеющее значение от 1 до около 20, предпочтительно от 1 до около 10;
каждый w и x независимо представляет собой целое число, имеющее значение 0 или 1;
при условии, что когда w равно 0, то q равно 1,
где нацеливающий фрагмент содержит антитело, выбранное из интактного поликлонального антитела, интактного моноклонального антитела, фрагмента антитела, одноцепочечного мутанта Fv (scFv), мультиспецифического антитела, биспецифического антитела, химерного антитела, гуманизированного антитела, человеческого антитела, гибридного белка, содержащего антигенную детерминантную часть антитела, другие модифицированные молекулы иммуноглобулина, содержащие сайты распознавания антигена и антитело, выбранное из муромонаба-CD3, абциксимаба, ритуксимаба, даклизумаба, паливизумаба, инфликсимаба, трастузумаба (герцептина), этанерцепта, базиликсимаба, гемтузумаба озогамицина, алемтузумаба, ибритумомаба тиуксетана, адалимумаба, алефацепта, омализумаба, эфализумаба, тозитумомаба-I131, цетуксимаба, бевацизумаба, натализумаба, ранибизумаба, панитумумаба, экулизумаба, рилонацепта, цертолизумаба пегола, ромиплостима, AMG-531, CNTO-148, CNTO-1275, ABT-874, LEA-29Y, белимумаба, TACI-Ig, анти-CD20 второго поколения, ACZ-885, тоцилизумаба, атлизумаба, меполизумаба, пертузумаба, Humax CD20, тремелимумаба (CP-675 206), тицилимумаба, MDX-010, IDEC-114, инотузумаба озогамицина, HuMax EGFR, афлиберцепта, HuMax-CD4, Ala-Ala, ChAglyCD3, TRX4, катумаксомаба, IGN101, MT-201, преговомаба, CH-14.18, WX-G250, AMG-162, AAB-001, мотавизумаба, MEDI-524, эфумгумаба, аурограба (Aurograb), раксибакумаба, анти-CD20 третьего поколения, LY2469298 и велтузумаба.
| WO 2017044043 A1, 16.03.2017 | |||
| US 2014309390 A1, 16.10.2014 | |||
| KR 20170031307 A, 21.03.2017 | |||
| US 20140249099 A1, 04.09.2014 | |||
| WO2016029324 A1, 03.03.2016 | |||
| PAQUET, V, "Synthesis and in vitro biological properties of novel cationic derivatives of amphotericin B", Chemistry - A European Journal, 2008, vol | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| FINNEGAN, T | |||
| et | |||
Авторы
Даты
2023-04-28—Публикация
2018-07-03—Подача