Область техники, к которой относится изобретение
[0001] Настоящее изобретение относится к соединениям, включающим саморасщепляющуюся группу, и соединения, включающие саморасщепляющуюся группу, в соответствии с настоящим изобретением могут включать белок (например, олигопептид, полипептид, антитело или подобные), обладающий субстрат-специфичностью в отношении мишени, и активное вещество (например, лекарственное средство, токсин, лиганд, детекторный зонд или подобные), обладающее специфической функцией или активностью.
Предпосылки создания изобретения
[0002] Технология конъюгатов антитела с лекарственным препаратом (ADC) представляет собой новую мишень-ориентированную технологию для индукции апоптоза раковых клеток путем высвобождения токсичного вещества в клетках после связывания токсина с антителом, связывающимся с антигеном. Поскольку ADC технология может обеспечить точную доставку лекарственного средства в целевые раковые клетки и его высвобождение только в специфических условиях, минимизируя при этом воздействие на здоровые клетки, ADC технология может быть существенно более эффективной по сравнению с терапевтическим антителом как таковым, и значительно снижает риск возникновения побочных реакций по сравнению с существующими противораковыми лекарственными средствами.
[0003] Базовая структура конъюгатов антитела с лекарственным препаратом, указанных выше, состоит из ʺантитело-линкер-низкомолекулярное лекарственное средство (токсин)ʺ. В настоящем изобретении, линкер должен дать возможность лекарственному средству проявить лекарственный эффект на целевые раковые клетки, являясь при этом легко отделяемым посредством феномена диссоциации антитела и лекарственного средства (например, в результате гидролиза под действием фермента), после того, как лекарственное средство стабильно достигает клеток-мишеней во время циркуляции и вводится в клетки, помимо этого просто выполняя функциональную роль связывания антитела и лекарственного средства. То есть, поскольку эффективность, системная токсичность и тому подобное конъюгатов антитела с лекарственным препаратом зависит от стабильности линкера, линкер играет важную роль с точки зрения безопасности (Discovery Medicine 2010, 10(53): 329-39).
[0004] Линкеры конъюгатов антитела с лекарственным препаратом, разрабатываемые до настоящего времени, примерно подразделяются на нерасщепляемый тип и расщепляемый тип.
[0005] В качестве нерасщепляемого линкера в основном используют тиоэфир, и лекарственное средство не диссоциирует в результате отделения линкера в клетках, но лекарственное средство диссоциирует в форме, в которой лекарственное средство включает линкер и одну аминокислоту, происходящую из антитела. В случае, когда в основном используют способ связывания тиол-малеимид, реакцию легко осуществляют при значении pH около 6-7, но также легко может химически осуществляться обратная реакция, таким образом, существует проблема стабильности.
[0006] В качестве расщепляемого линкера, в основном используют линкер, отделяемый химическим способом, или линкер, гидролизуемый путем ферментативной реакции. В качестве линкера, имеющего механизм химического разделения, репрезентативным является линкер, содержащий дисульфидную связь. Кроме того, также используют гидразоновые или оксимные линкеры.
[0007] Дисульфидный линкер, использующий то обстоятельство, что диссоциация лекарственного средства происходит с использованием реакции тиольного обмена, использует тот факт, что концентрация тиола (в частности, глутатиона) в клетках выше, чем в крови. Однако, поскольку в крови присутствуют разные виды тиолов (например, альбумин и глутатион), выделение лекарственного средства может происходить во время циркуляции. Что касается гидразонового линкера, известно, что гидразоновый линкер является относительно стабильным в крови, но нестабильным в клетках, эндосомах или лизосомах, в которых кислотность является высокой, и, таким образом, гидразоновый линкер быстро гиролизуется (Bioconjugate Chem. 2008, 19, 759-765; Bioconjugate Chem., 2010, 21, 5-13).
[0008] Для решения описанной выше проблемы был разработан линкер, гидролизуемый путем ферментативной реакции в клетках, и к нему относятся пептидный линкер (например, валин-цитруллин) и β-глюкуронидный линкер. Валин-цитруллин и β-глюкуронид не связаны непосредственно с лекарственным средством, но связываются с саморасщепляющимися группами, таким образом, лекарственное средство диссоциирует посредством механизма, такого как 1,6-элиминирование или механизм циклизации после гидролиза в результате ферментативной реакции, проявляя, таким образом, эффективность (Clinical Cancer Res., 2005, 11, 843-852).
[0009] Сообщалось, что пептидный линкер валин-цитруллин, подвергается селективному разложению под воздействием лизосомальной протеазы, такой как катепсин B, и повышает стабильность в крови по сравнению с гидразоновым линкером, который химически разлагается, и, таким образом, повышается противораковый эффект (Bioconjugate Chem. 2008, 19, 1960-1963; J. Org. Chem., 2002, 67, 1866-1872). Однако пептидный линкер обладает гидрофобностью, и поэтому существуют недостатки, такие как аггрегация полученных конъюгатов антитела с лекарственным препаратом.
[0010] β-Глюкуронидный линкер, который, как было определено, гидролизуется под действием β-глюкуронидазы, имеет высокую гидрофильность в отличие от пептидного линкера, благодаря чему при связывании β-глюкуронидного линкера с лекарственным средством, обладающим высокой гидрофобностью, растворимость конъюгатов антитела с лекарственным препаратом может увеличиваться. Были описаны примеры связывания антител с различными лекарственными средствами (например, монометилауристатином F, монометилауристатином E, доксорубицинпропилоксазолином (DPO)) с использованием β-глюкуронидного линкера для получения конъюгатов антитела с лекарственным препаратом (Conjugation Chem., 2006, 17, 831-840; US2012/0107332). В соответствии с этим сообщением, конъюгаты антитела с лекарственным препаратом, полученные с использованием глюкуронидного линкера, обладают существенной стабильностью в плазме крыс, но не сообщалось об их стабильности в плазме мышей.
[0011] Поэтому настоящее изобретение состоит в разработке эффективного линкера, включающего саморасщепляющуюся группу, способного быть более стабильным в плазме, будучи стабильным в кровотоке, и дающего возможность лекарственному средству легко высвобождаться в раковых клетках для проявления действия лекарства.
Раскрытие
Техническая задача
[0012] Целью настоящего изобретения является обеспечение соединений, включающих саморасщепляющуюся группу.
Техническое решение
[0013] В одном общем аспекте, соединения, включающие саморасщепляющуюся группу, представлены следующей химической формулой 1:
[0014] [Химическая формула 1]
[0015] 
[0016] G представляет собой группу глюкуроновой кислоты или ее производное;
[0017] A представляет собой (C1-C20)гидрокарбил, биоматериал или модифицированный биоматериал;
[0018] B представляет собой (C1-C100)гидрокарбил;
[0019] W представляет собой электроноакцепторную группу;
[0020] Z представляет собой водород, (C1-C8)алкил, галоген, циано или нитро;
[0021] n представляет собой целое число от 1 до 3, и, когда n представляет собой целое число 2 или более, каждый из заместителей Z являются одинаковыми или отличными друг от друга;
[0022] L представляет собой линкер, связывающий A и W саморасщепляющейся группы при помощи ковалентных связей; и
[0023] R1 и R2 каждый, независимо, представляют собой водород, (C1-C8)алкил или (C3-C8)циклоалкил.
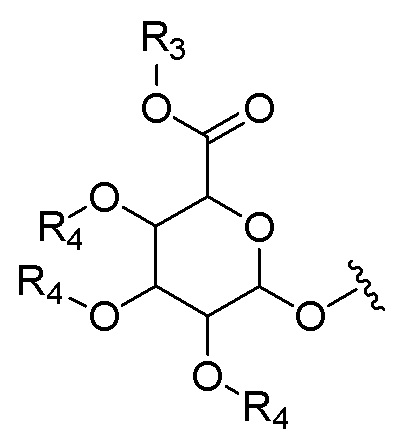
[0024] G может представлять собой, R3 может представлять собой водород или защитную группу карбоксила, и заместители R4, каждый независимо, представляют собой водород или защитную группу гидроксила.
[0025] W может представлять собой -C(O)-, -C(O)NRʹ-, -C(O)O-, -SO2NRʹ-, -P(O)RʹʹNRʹ-, -SONRʹ- или -PO2NRʹ-, и Rʹ и Rʺ каждый независимо, могут представлять собой водород, (C1-C8)алкил, (C3-C8)циклоалкил, (C1-C8)алкокси, (C1-C8)алкилтио, моно- или ди-(C1-C8)алкиламино, (C3-C20)гетероарил или (C6-C20)арил.
[0026] Линкер L может представлять собой алкилен, содержащий от 1 до 50 атомов углерода, и соответствует по меньшей мере одному из следующих условий (i) - (iv):
[0027] (i) алкилен включает по меньшей мере одну ненасыщенную связь,
[0028] (ii) алкилен включает по меньшей мере один гетероарилен,
[0029] (iii) атом углерода алкилена замещен одним или несколькими гетероатомами, выбранными из азота (N), кислорода (О) и серы (S), и
[0030] (iv) алкилен дополнительно замещен одним или несколькими алкилами, содержащими от 1 до 20 атомов углерода.
[0031] Линкер L может включать по меньшей мере одно звено, представляющее собой изопрениловое производное, представленное следующей химической формулой A, которое может распознаваться изопреноидтрансферазой.
[0032] [Химическая формула A]
[0033] 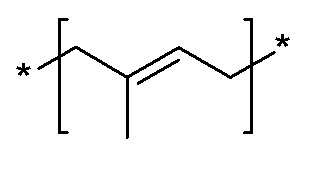
[0034] Линкер L может дополнительно включать связывающее звено, образованное в результате путем реакций 1,3-диполярного циклоприсоединения, гетеро-реакций Дильса-Альдера, реакций нуклеофильного замещения, реакций карбонильных соединений не-альдольного типа, присоединений по месту кратных связей углерод-углерод, реакций окисления или клик-реакций.
[0035] Связывающее звено может образоваться путем реакции между ацетиленом и азидом или реакции между альдегидной или кетоновой группой и гидразином или гидроксиламином.
[0036] Связывающее звено можно представить следующей химической формулой B, C, D или E:
[0037] [Химическая формула B]
[0038] 
[0039] [Химическая формула C]
[0040] 
[0041] [Химическая формула D]
[0042] 
[0043] [Химическая формула E]
[0044] 
[0045] L1 представляет собой простую связь или алкилен, содержащий от 1 до 30 атомов углерода;
[0046] R11 представляет собой водород или алкил, содержащий от 1 до 10 атомов углерода; и
[0047] L2 представляет собой алкилен, содержащий от 1 до 30 атомов углерода.
[0048]
[0049] Линкер L может дополнительно включать соединительное звено, представленное следующей химической формулой F или G:
[0050] [Химическая формула F]
[0051] -(CH2)r(V(CH2)p)q-
[0052] [Химическая формула G]
[0053] -(CH2CH2X)w-
[0054] V представляет собой простую связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
[0055] X представляет собой -O-, (C1-C8)алкилен или -NR21-;
[0056] R21 - R25 каждый, независимо, представляют собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
[0057] r представляет собой целое число от 1 до 10;
[0058] p представляет собой целое число от 0 до 10;
[0059] q представляет собой целое число от 1 до 10; и
[0060] w представляет собой целое число от 1 до 10.
[0061] Когда A представляет собой гидрокарбил, содержащий от 1 до 20 атомов углерода, L может представлять собой 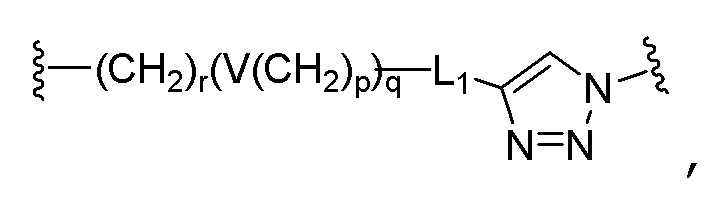 ,
, 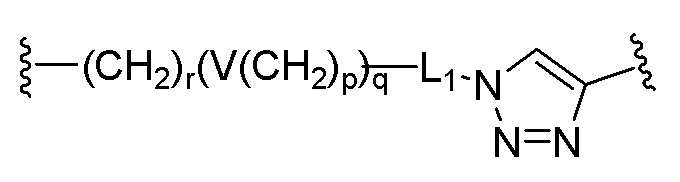 или
или  , V может представлять собой простую связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-, R21 - R25 каждый, независимо, могут представлять собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил, r может представлять собой целое число от 1 до 10, p может представлять собой целое число от 0 до 10, q может представлять собой целое число от 1 до 10, и L1 может представлять собой простую связь.
, V может представлять собой простую связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-, R21 - R25 каждый, независимо, могут представлять собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил, r может представлять собой целое число от 1 до 10, p может представлять собой целое число от 0 до 10, q может представлять собой целое число от 1 до 10, и L1 может представлять собой простую связь.
[0062] Биоматериалом может быть белок.
[0063] Белок может представлять собой олигопептид, полипептид, антитело или «repebody».
[0064] Белок может содержать аминокислотный мотив, который может распознаваться изопреноид-трансферазой.
[0065] Белок может дополнительно включать спейсерное звено, состоящее из аминокислоты, олигопептида или полипептида между белком и аминокислотным мотивом.
[0066] Белок может быть ковалентно связан с линкером L через аминокислотный мотив.
[0067] Аминокислотный мотив может быть ковалентно связан с С-концом белка или ковалентно связан с по меньшей мере одним спейсерным звеном, ковалентно связанным с С-концом белка.
[0068] С-конец белка может представлять собой C-конец легкой цепи или тяжелой цепи антитела.
[0069] Изопреноид-трансфераза может представлять собой фарнезилпротеинтрансферазу (FTаза) или геранилгеранилтрансферазу (GGTаза).
[0070] Антитело может быть выбрано из группы, включающей интактные поликлональные антитела, интактные моноклональные антитела, фрагменты антител, одноцепочечные Fv-мутанты (scFv), мультиспецифичные антитела, биспецифичные антитела, химерные антитела, гуманизированные антитела, человеческие антитела, гибридные белки, включая антиген-определяющую часть антитела, и другие модифицированные молекулы иммуноглобулинов, включающие сайт распознавания антигена.
[0071] Антитело может быть выбрано из группы, включающей муромонаб-CD3 абциксимаб, ритуксимаб, даклизумаб, паливизумаб, инфликсимаб, трастузумаб (известный как ʹГерцептинʹ), этанерцепт, базиликсимаб, гемтузумаб озогамицин, алемтузумаб, ибритутомаб тиуксетан, адалимумаб, алефацепт, омализумаб, эфализумаб, тозитумомаб-I131, цетуксимаб, бевацизумаб, натализумаб, ранибизумаб, панитумумаб, экулизумаб, рилонацепт, цертолизумаб пегол, ромиплостим, AMG-531, CNTO-148, CNTO-1275, ABT-874, LEA-29Y, белимумаб, TACI-Ig, анти-CD20 второго поколения, ACZ-885, тоцилизумаб, атлизумаб, меполизумаб, пертузумаб, HuMax CD20, тремелимумаб (CP-675 206), тицилимумаб, MDX-010, IDEC-114, инотузумаб озогамицин, HuMax EGFR, афлиберцепт, VEGF Trap-Eye, HuMax-CD4, Ala-Ala, ChAglyCD3, TRX4, катумаксомаб, IGN101, MT-201, преговомаб, CH-14,18, WX-G250, AMG-162, AAB-001, мотавизумаб, MEDI-524, эфунгумаб, Aurograb®, раксибацумаб, анти-CD20 третьего поколения, LY2469298 и велтузумаб.
[0072] Белок может представлять собой моноклональное антитело.
[0073] Аминокислотный мотив может представлять собой CYYX, XXCC, XCXC или CXX, где C представляет собой цистеин, Y представляет собой алифатическую аминокислоту, и X представляет собой аминокислоту, которая определяет субстрат-специфичность изопреноид-трансферазы.
[0074] B может представлять собой активное вещество.
[0075] Активное вещество может представлять собой лекарственное средство, токсин, аффинный лиганд, детекторный зонд или их комбинацию.
[0076] Активное вещество может представлять собой иммуномодулирующее соединение, противораковое средство, противовирусное средство, антибактериальное средство, противогрибковое средство, противопаразитарное средство или их комбинацию.
[0077] Белок, содержащий аминокислотный мотив, может быть выбран из группы, включающей A-HC-(G)zCVIM, A-HC-(G)zCVLL, A-LC-(G)zCVIM и A-LC-(G)zCVLL, где A представляет собой антитело, HC представляет собой тяжелую цепь, LC представляет собой легкую цепь, G представляет собой глициновое звено, и z представляет собой целое число от 0 до 20.
[0078] Соединения могут быть выбраны из соединений, имеющих следующую структуру:
[0079]
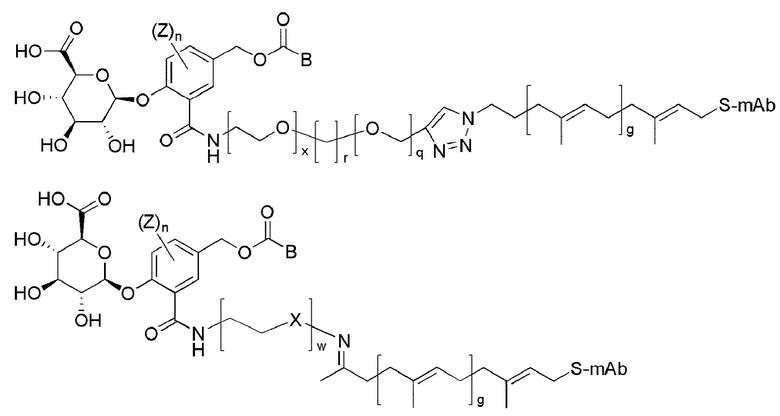
[0080] где,
[0081] Z представляет собой водород, (C1-C8)алкил, галоген, циано или нитро;
[0082] X представляет собой -O-, (C1-C8)алкилен или -NR21-;
[0083] R21 представляет собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
[0084] n представляет собой целое число от 1 до 3, и, когда n представляет собой целое число 2 или более, каждый из заместителей Z являются одинаковыми или отличными друг от друга;
[0085] r представляет собой целое число от 1 до 10;
[0086] q представляет собой целое число от 1 до 10;
[0087] w представляет собой целое число от 1 до 10.
[0088] x представляет собой целое число от 0 до 10;
[0089] g представляет собой целое число от 1 до 10;
[0090] -S-mAb представляет собой A-HC-(G)zCVIM-, A-HC-(G)zCVLL-, A-LC-(G)zCVIM- или A-LC-(G)zCVLL-, где A представляет собой антитело, HC представляет собой тяжелую цепь, LC представляет собой легкую цепь, G представляет собой глициновое звено, и z представляет собой целое число от 0 до 20;
[0091] B представляет собой лекарственное средство, имеющее структуру, выбранную из следующих структур; и
[0092] 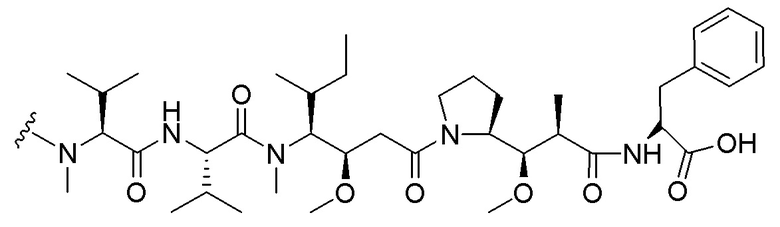
[0093] 
[0094] 
[0095] 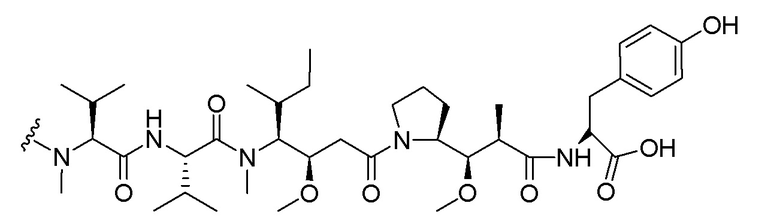
[0096] 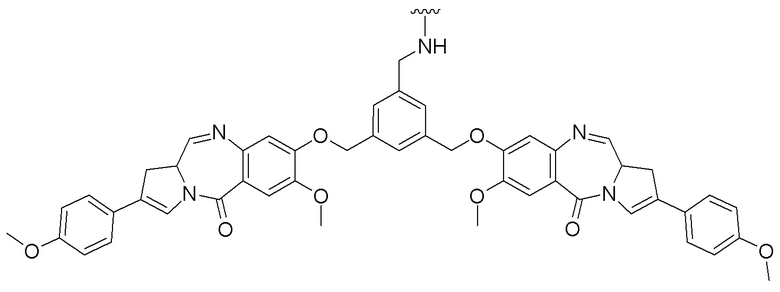
[0097] 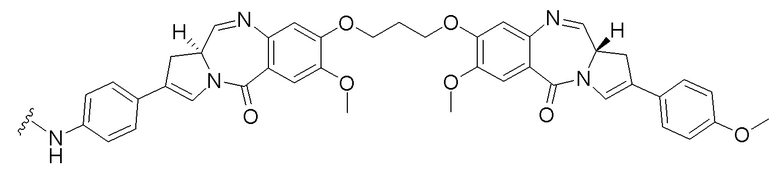
[0098] 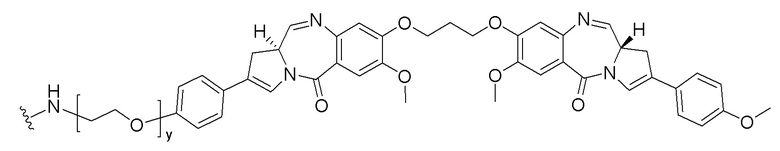
[0099] 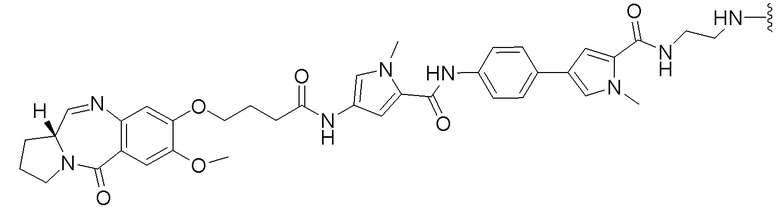
[00100] 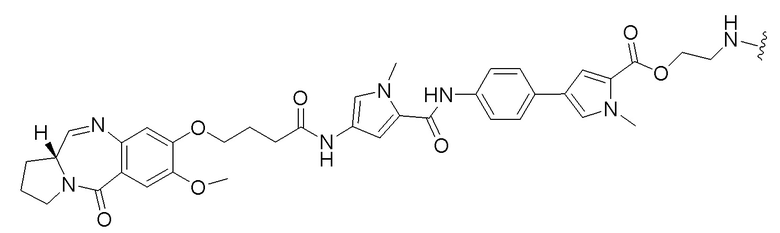
[00101] 
[00102] y представляет собой целое число от 1 до 10.
Преимущества изобретения
[00103] Соединения, включающие саморасщепляющуюся группу, в соответствии с настоящим изобретением могут включать белок (например, олигопептид, полипептид, антитело или подобные), обладающий субстрат-специфичностью в отношении мишени, и активное вещество (например, лекарственное средство, токсин, лиганд, детекторный зонд или подобные), обладающее специфической функцией или активностью. Саморасщепляющаяся группа может быть более стабильной в крови, плазме и тому подобном, по сравнению с существующим линкером, и при этом специфически связываясь с белком, который сверхэкспрессируется в клетках, вызывая заболевание, но может отделяться в раковых клетках-мишенях, благодаря чему активное вещество может специфически воздействовать на клетки, вызывающие заболевание, таким образом, делая возможным использование соединений для лечения заболеваний.
Описание чертежей
[00104] Фиг. 1 иллюстрирует механизм высвобождения активного лекарственного средства из линкера на основе β-глюкуронида.
[00105] Фиг. 2 иллюстрирует результат, полученный путем измерения скорости гидролиза под действием β-глюкуронидазы в Экспериментальном Примере 1.
[00106] Фиг. 3 иллюстрирует результат, полученный путем измерения стабильности в плазме в Экспериментальном Примере 2.
[00107] Фиг. 4 иллюстрирует результат, полученный путем измерения стабильности в плазме соединения LCB14-0648, полученного в Примере 5.
[00108] Фиг. 5 иллюстрирует результат, полученный путем измерения стабильности в плазме соединения LCB14-0663, полученного в Примере 6.
[00109] Фиг. 6 иллюстрирует результат, полученный путем измерения стабильности в плазме соединения LCB14-0664, полученного в Примере 7.
[00110] Фиг. 7 представляет собой схему, иллюстрирующую реакции в Примере 9.
[00111] Фиг. 8 иллюстрирует результат, полученный путем измерения стабильности в плазме мышей соединения ADC (LCB14-0109), полученного в Примере 8.
[00112] Фиг. 9 иллюстрирует результат, полученный путем различных измерений стабильности в плазме соединения ADC (LCB14-0110), полученного в Примере 9.
[00113] Фиг. 10 представляет график, иллюстрирующий результат, полученный путем наблюдения объема опухоли в зависимости от дозы QW(раз в неделю) в Экспериментальном Примере 6 (Растворитель, Герцептин (5 мг/кг) и ADC109 (0,1, 1, 5мг/кг)).
[00114] Фиг. 11 представляет график, иллюстрирующий результат, полученный путем наблюдения эффекта лекарственного средства в зависимости от повторного введения в Экспериментальном Примере 6 (Растворитель, Герцептин (5 мг/кг), ADC109 (5 мг/кг) и ADC110 (5 мг/кг)).
[00115] Фиг. 12 представляет график, иллюстрирующий результат, полученный путем наблюдения эффекта лекарственного средства в зависимости от введения разовой дозы в Экспериментальном Примере 6 (Растворитель, Герцептин (5 мг/кг), ADC109 (5 мг/кг) и ADC110 (5 мг/кг)).
[00116] Фиг. 13 иллюстрирует результат, полученный путем оценки стабильности в плазме in vitro соединения ADC 110 (Пример 10) в Экспериментальном Примере 7.
[00117] Фиг. 14 иллюстрирует результат, полученный путем оценки стабильности в плазме in vitro соединения ADC 113 (Пример 11) в Экспериментальном Примере 7.
[00118] Фиг. 15 иллюстрирует результат, полученный путем оценки стабильности в плазме in vitro препарата Кадсила в Экспериментальном Примере 7.
[00119] Фиг. 16 представляет график, иллюстрирующий результат, полученный путем in vivo наблюдения фармакокинетического профиля у мыши, в Экспериментальном Примере 8.
[00120] Фиг. 17 представляет график, иллюстрирующий результат, полученный путем in vivo наблюдения фармакокинетического профиля соединения ADC 110 (Пример 10) у крыс в Экспериментальном Примере 8.
[00121] Фиг. 18 представляет график, иллюстрирующий результат, полученный путем in vivo наблюдения соотношения лекарственное средство-антитело (DAR) ADC 110 (Пример 10) у крыс в Экспериментальном Примере 8.
[00122] Фиг. 19 представляет график, иллюстрирующий результат, полученный путем in vivo наблюдения концентрации свободной нагрузки ADC 110 (Пример 10) у крыс в Экспериментальном Примере 8.
[00123] Фиг. 20 представляет график, иллюстрирующий результат, полученный путем in vivo наблюдения фармакокинетического профиля ADC 110 (Пример 10) у обезьян в Экспериментальном Примере 8.
[00124] Фиг. 21 представляет график, иллюстрирующий результат, полученный путем in vivo наблюдения соотношения лекарственное средство-антитело (DAR) ADC 110 (Пример 10) у обезьян в Экспериментальном Примере 8.
[00125] Фиг. 22 представляет график, иллюстрирующий результат, полученный путем in vivo наблюдения концентрации свободной нагрузки ADC 110 (Пример 10) у обезьян в Экспериментальном Примере 8.
Лучший вариант осуществления изобретения
[00126] Настоящее изобретение относится к соединениям, включающим саморасщепляющуюся группу. Более подробно, соединения, включающие саморасщепляющуюся группу, в соответствии с настоящим изобретением можно представить следующей химической формулой 1, и они включают белок (например, олигопептид, полипептид, антитело или подобные), обладающий субстрат-специфичностью в отношении мишени, и активное вещество (например, a лекарственное средство, токсин, лиганд, детекторный зонд или подобные), обладающее специфической функцией или активностью.
[00127] [Химическая формула 1]
[00128] 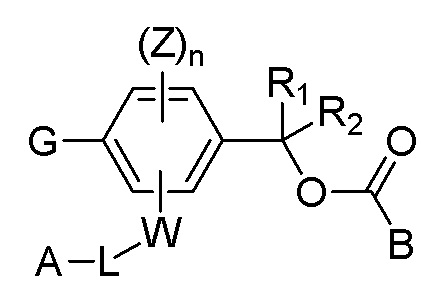
[00129] G представляет собой группу глюкуроновой кислоты или ее производное;
[00130] A представляет собой (C1-C20)гидрокарбил, биоматериал или модифицированный биоматериал;
[00131] B представляет собой (C1-C100)гидрокарбил;
[00132] W представляет собой электроноакцепторную группу;
[00133] Z представляет собой водород, (C1-C8)алкил, галоген, циано или нитро;
[00134] n представляет собой целое число от 1 до 3, и, когда n представляет собой целое число 2 или более, каждый из заместителей Z являются одинаковыми или отличными друг от друга;
[00135] L представляет собой линкер, связывающий A и W саморасщепляющейся группы при помощи ковалентных связей; и
[00136] R1 и R2 каждый, независимо, представляют собой водород, (C1-C8)алкил или (C3-C8)циклоалкил.
[00137] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, где саморасщепляющаяся группа может быть связана с глюкуронидом, способным к разделению под действием β-глюкуронидазы G, который представляет собой глюкуронидную группу или ее производное, способное к разделению под действием β-глюкуронидазы, может быть представлена следующей структурой.
[00138] 
[00139] (R3 представляет собой водород или защитную группу карбоксила, и R4, каждый независимо, представляют собой водород или защитную группу гидроксила.)
[00140] Защитная группа карбоксила, которая представляет собой традиционную защитную группу, которую можно использовать в органическом синтезе, предпочтительно может представлять собой метил, метоксиметил, метилтиометил, тетрагидропиранил, бензилоксиметил, фенацил, N-фталимидометил, 2,2,2-трихлорэтил, 2-галогенэтил, 2-(пара-толуолсульфонил)этил, трет-бутил, циннамил, бензил, трифенилметил, бис(орто-нитрофенил)метил, 9-антраметил, 2-(9,10-диоксо)антрилметил, пиперонил, триметилсилил, трет-бутилдиметилсилил или S-трет-бутил, 2-алкил-1,3-оксазолинил, но не ограничивается этим. Кроме того, защитная группа гидроксила, которая представляет собой традиционную защитную группу, которую можно использовать в органическом синтезе, предпочтительно может представлять собой ацетил, метил, этоксиэтил, бензоил, бензил, 4-метоксибензил, 3,4-диметоксибензил, тетрагидропиранил (THP), тетрагидрофуран (THF), трет-бутилдиметилсилил (TBDMS), триметилсилил (TMS), триэтилсилил (TES), триизопропилсилил (TIP), трет-бутилдифенилсилил (TBDPS), три-изо-пропилсилилоксиметил (TOM), β-метоксиэтоксиметил (MEM), метоксиметил (MOM), аллил или тритил, но не ограничивается этим.
[00141] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, W, который представляет собой электроноакцепторную группу, предпочтительно может представлять собой -C(O)-, -C(O)NRʹ-, -C(O)O-, -SO2NRʹ-, -P(O)RʹʹNRʹ-, -SONRʹ- или -PO2NRʹ-, но не ограничивается этим, и Rʹ и Rʺ, каждый независимо, могут представлять собой водород, (C1-C8)алкил, (C3-C8)циклоалкил, (C1-C8)алкокси, (C1-C8)алкилтио, моно- или ди-(C1-C8)алкиламино, (C3-C20)гетероарил или (C6-C20)арил.
[00142] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, линкер L может представлять собой алкилен, содержащий от 1 до 50 атомов углерода, и может удовлетворять по меньшей мере одному, предпочтительно, по меньшей мере двум из следующих условий (i) - (iv):
[00143] (i) алкилен включает по меньшей мере одну ненасыщенную связь,
[00144] (ii) алкилен включает по меньшей мере один гетероарилен,
[00145] (iii) атом углерода алкилена замещен одним или несколькими гетероатомами, выбранными из азота (N), кислорода (О) и серы (S) и
[00146] (iv) алкилен дополнительно замещен одним или несколькими алкилами, содержащими от 1 до 20 атомов углерода.
[00147] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, линкер L может включать по меньшей мере одно звено, представляющее собой изопрениловое производное, представленное следующей химической формулой A, которое может распознаваться изопреноидтрансферазой.
[00148] [Химическая формула A]
[00149] 
[00150] Кроме того, линкер L может дополнительно включать связывающее звено, образованное путем реакций 1,3-диполярного циклоприсоединения, гетеро-реакции Дильса-Альдера, реакций нуклеофильного замещения, реакций карбонильных соединений не-альдольного типа, присоединений по месту кратных связей углерод-углерод, реакций окисления или клик-реакций. Связывающее звено, которое образовано путем реакции между ацетиленом и азидом или реакциии между альдегидной или кетоновой группой и гидразином или гидроксиламином, предпочтительно может быть представлена следующей химической формулой B, C, D или E.
[00151] [Химическая формула B]
[00152] 
[00153] [Химическая формула C]
[00154] 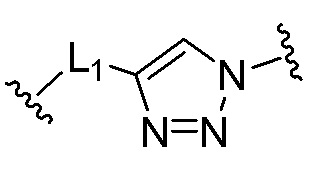
[00155] [Химическая формула D]
[00156] 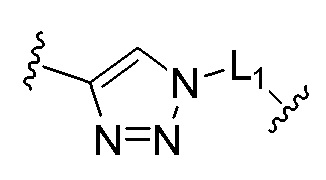
[00157] [Химическая формула E]
[00158] 
[00159] L1 представляет собой простую связь или алкилен, содержащий от 1 до 30 атомов углерода;
[00160] R11 представляет собой водород или алкил, содержащий от 1 до 10 атомов углерода; и
[00161] L2 представляет собой алкилен, содержащий от 1 до 30 атомов углерода.
[00162] Клик-химические реакции осуществляют в мягких условиях, тем самым делая возможным легко манипулировать с белками. Клик-химическая реакция показывает значительно высокую специфичность реакции. Поэтому, даже при том, что белок содержит другие функциональные группы (например, остаток боковой цепи или на C- или N-конце), эти функциональные группы не затрагиваются клик-химической реакцией. Например, может иметь место клик-химическая реакция между азидной группой и ацетиленовой группой белка, в то время как другие функциональные группы белка не затрагиваются клик-химической реакцией. Кроме того, клик-химическая реакция может протекать специфическим образом независимо от вида участвующего лиганда. В некоторых случаях, лиганд может быть выбран таким образом, чтобы улучшить общую эффективность реакции. Например, азид-ацетиленовая клик-химическая реакция может продуцировать триазол с высоким выходом (см. Rhiannon K. Hia et al, Chem. Rev. 2009, 109, 5620; Morten Meldal and Christian Wenzel Tornoe, Chem Rev., 2008, 108, 2952; Hartmuth C. Kolb et al, Angew. Chemie Int. Ed. Engl., 2001, 40, 2004, все из которых включены в настоящую заявку посредством ссылки).
[00163] Азидная и ацетиленовая группы представляют собой функциональные группы, которые не существуют в аминокислотной последовательности природных белков. В случае, когда имеет место реакция конъюгации с использованием этих функциональных групп, никакой из остатков боковых цепей и никакие из N-концевых или C-концевых функциональных групп не затрагиваются клик-химической реакцией.
[00164] Кроме того, линкер L может дополнительно включать соединительное звено, представленное Химической формулой F или G:
[00165] [Химическая формула F]
[00166] -(CH2)r(V(CH2)p)q-
[00167] [Химическая формула G]
[00168] -(CH2CH2X)w-
[00169] V представляет собой простую связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
[00170] X представляет собой -O-, (C1-C8)алкилен или -NR21-;
[00171] R21 - R25, каждый независимо, представляют собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
[00172] r представляет собой целое число от 1 до 10;
[00173] p представляет собой целое число от 0 до 10;
[00174] q представляет собой целое число от 1 до 10; и
[00175] w представляет собой целое число от 1 до 10.
[00176] Более предпочтительно, линкер L может включать по меньшей мере одно звено, представляющее собой изопрениловое производное, представленное химической формулой A, связывающее звено, представленное химической формулой B, C, D или E, и соединительное звено, представленное химической формулой F или G.
[00177] Более предпочтительно, линкер L может быть представлен следующими структурами.
[00178]
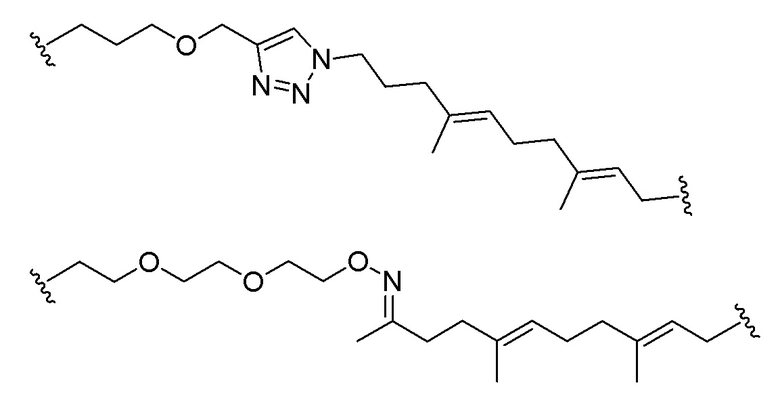
[00179] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, когда A представляет собой гидрокарбил, содержащий от 1 до 20 атомов углерода, L может представлять собой
 ,
, 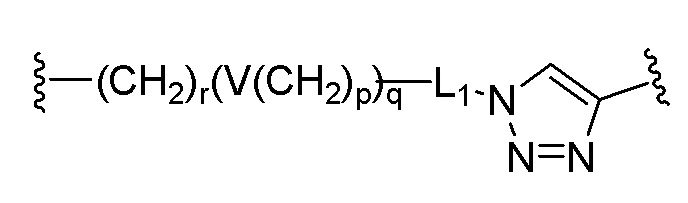 или
или 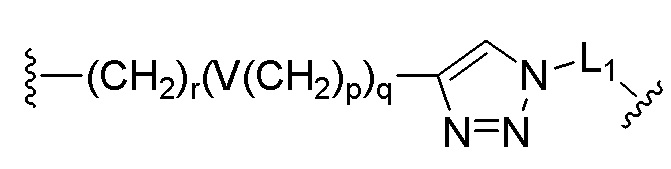 ,
,
V может представлять собой простую связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-, R21 - R25, каждый независимо, могут представлять собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил, r может представлять собой целое число от 1 до 10, p может представлять собой целое число от 0 до 10, q может представлять собой целое число от 1 до 10, и L1 может представлять собой простую связь.
[00180] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, биоматериал может представлять собой белок, где белок включает олигопептид, полипептид, антитело, фрагмент антигенного полипептида и repebody.
[00181] Белок содержит аминокислотный мотив, который может распознаваться изопреноид-трансферазой. То есть, C-конец (фрагмент, аналог или его производное) белка может быть связан с аминокислотным мотивом, который может распознаваться изопреноид-трансферазой. Кроме того, белок может дополнительно включать спейсерное звено, состоящее из аминокислоты, олигопептида или полипептида, между белком и аминокислотным мотивом. Белок имеет делецию на карбоксильном (C) конце белка или присоединение при помощи ковалентной связи спейсерного звена на карбоксильном конце белка. Белок может быть непосредственно ковалентно связан с аминокислотным мотивом или быть ковалентно связан со спейсерным звеном, посредством чего он связывается с аминокислотным мотивом. Аминокислотное спейсерное звено состоит из 1-20 аминокислот, среди них глициновое звено является предпочтительным.
[00182] Белок имеет аминокислотный мотив, который может распознаваться изопреноид-трансферазой. То есть, С-конец (фрагмент, аналог или его производное) белка может связываться с аминокислотным мотивом, который может распознаваться изопреноид-трансферазой. Кроме того, белок может дополнительно включать спейсерное звено, состоящее из аминокислоты, олигопептида или полипептида между белком и аминокислотным мотивом. Белок имеет делецию на карбоксильном (C) конце белка или добавленное при помощи ковалентной связи спейсерное звено на карбоксильном конце белка. Белок может быть напрямую ковалентно связан с аминокислотным мотивом или быть ковалентно связан со спейсерным звеном, чтобы посредством этого связаться с аминокислотным мотивом. Аминокислотное спейсерное звено содержит от 1 до 20 аминокислот, среди них, предпочтительной является глицин-единица.
[00183] Примеры изопреноид-трансферазы могут включать фарнезилпротеинтрансферазу (FTаза) или геранилгеранилтрансферазу (GGTаза), которые участвуют в переносе фарнезилового или геранил-геранилового остатка к С-концевому цистеину(цистеинам) целевого белка, соответственно. GGTаза может подразделяться на GGTазу I и GGTазу II. FTаза и GGTаза I могут распознавать CAAX мотив, и GGTаза II может распознавать XXCC, XCXC или CXX мотив (здесь, C представляет собой цистеин, A представляет собой алифатическую аминокислоту, и X представляет собой аминокислоту, определяющую субстрат-специфичность изопреноид-трансфераз) (см. Nature Rev. Cancer 2005, 5(5), pp. 405-12; Nature Chemical Biology, 2010, 17, pp. 498-506; Lane KT, Bees LS, Structural Biology of Protein of Farnesyltransferase and Geranylgeranyl transferase Type I, Journal of Lipid Research, 47, pp. 681-699 (2006); Patrick J. Kasey, Miguel C. Seabra; Protein Prenyl transferases, The Journal of Biological Chemistry, Vol. 271, No. 10, Issue of March 8, pp. 5289-5292 (1996), содержание этих ссылочных документов включено посредством ссылки во всей их полноте).
[00184] В настоящем изобретении могут быть использованы изопреноид-трансферазы из различных источников, например, людей, животных, растений, бактерий, вирусов и подобных. В некоторых вариантах осуществления настоящего изобретения можно использовать встречающиеся в природе изопреноид-трансферазы. В некоторых других вариантах осуществления настоящего изобретения можно использовать естественно или искусственно модифицированные изопреноид-трансферазы. Например, существует изопреноид-трансфераза, имеющая по меньшей мере одну естественно измененную аминокислотную последовательность (включая посттрансляционную модификацию), естественно или искусственно процессированная форма встречающейся в природе изопреноид-трансферазы и изопреноид-трансфераза, модифицированная по меньшей мере одним из (His)-tag, GST, GFP, MBP, CBP, Iospeptag, BCCP, Myc-tag, кальмодулин-tag, FLAG-tag, HA-tag, мальтозосвязывающий белок-tag, Nus-tag, Глутатион-S-трансфераза-tag, зеленый флуоресцентный белок-tag, Тиоредоксин-tag, S-tag, Softag 1, Softag 3, Strep-tag, SBP-tag, Ty-tag и т.п.
[00185] Изопреноид-трансферазы может распознавать изосубстрат, также как и субстрат. Изосубстрат относится к аналогу субстрата, который содержит модификацию в субстрате. Изопреноид-трансферазы алкилируют специфический аминокислотный мотив (например, CAAX мотив) на С-конце белка (см. Benjamin P. Duckworth et al, ChemBioChem 2007, 8, 98; Uyen T. T. Nguyen et al, ChemBioChem 2007, 8, 408; Guillermo R. Labadie et al, J. Org. Chem. 2007, 72(24), 9291; James W. Wollack et al, ChemBioChem 2009, 10, 2934, содержание этих ссылочных документов включено посредством ссылки). Функционализированный белок можно получить с использованием изопреноид-трансферазы и изосубстрата через алкилирование по С-концевому цистеину(цистеинам).
[00186] Например, цистеиновый остаток С-концевого CAAX мотива можно подвергнуть взатмодействию с изосубстратом с использованием изопреноид-трансферазы. В некоторых случаях, AAX затем может быть удален посредством протеазы. Полученный цистеин затем может быть метилирован на карбоксильном конце при помощи фермента (см. Iran M. Bell, J. Med. Chem. 2004, 47(8), 1869, который включен в настоящую заявку посредством ссылки).
[00187] Белки по настоящему изобретению можно получить с использованием любого молекулярного биологического способа или клеточного биологического способа, хорошо известного в данной области техники. Например, можно использовать способы транзиторной трансфекции. Генетические последовательности, кодирующие специфический аминокислотный мотив, который может распознаваться изопреноид-трансферазой, можно встроить в известный плазмидный вектор с использованием стандартной ПЦР технологии, для экспрессии белка (его фрагмента или аналога), содержащего специфический аминокислотный мотив на C-конце. Как описано выше, может экспрессироваться белок, содержащий по меньшей мере один аминокислотный мотив, который может распознаваться изопреноид-трансферазой.
[00188] Термин ʺбелокʺ, как он используется в настоящей заявке, означает две или более независимо выбранных природных или не встречающихся в природе аминокислот, связанных ковалентной связью (например, пептидной связью). Пептид может включать 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более природных или не встречающихся в природе аминокислот, связанных пептидными связями. Полипептиды, описанные в настоящей заявке, включают полноразмерные белки (например, полностью процессированные белки), а также более короткие аминокислотные последовательности (например, фрагменты природных белков или фрагменты синтетических полипептидов).
[00189] Термин ʺбелокʺ, как он используется в настоящей заявке, также включает антитело, фрагмент антигенного полипептида или его аналог или производное. Термин ʺантителоʺ относится к молекуле иммуноглобулина, которая распознает и специфически связывается с мишенью, например, белком, полипептидом, пептидом, углеводом, полинуклеотидом, липидом или их комбинацией через по меньшей мере один сайт распознавания антигена в вариабельной области молекулы иммуноглобулина. Как используется в настоящей заявке, термин ʺантителоʺ включает интактные поликлональные антитела, интактные моноклональные антитела, фрагменты антител (например, Fab, Fab′, F(ab′)2, Fd и Fv фрагменты), одноцепочечные Fv-мутанты (scFv), мультиспецифичные антитела, такие как биспецифичные антитела, образованные из двух или более интактных антител, химерные антитела, гуманизированные антитела, человеческие антитела, гибридные белки, включая антиген-определяющую часть антитела, и любую другую модифицированную молекулу иммуноглобулина, включающую сайт распознавания антигена, при условии, что антитела демонстрируют желаемую биологическую активность. Антитело может представлять собой любой из пяти основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM, или их подклассов (изотипы) (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2), на основании идентичности константных доменов их тяжелых цепей, известных как альфа, дельта, эпсилон, гамма и мю, соответственно. Разные классы иммуноглобулинов имеют разные и хорошо известные структуры субъединиц и трехмерные конфигурации.
[00190] Термин ʺфрагмент антителаʺ относится к части интактного антитела и относится к антиген-определяющим вариабельным областям интактного антитела. Примеры фрагментов антитела включают Fab, Fab′, F(ab′)2, Fd и Fv фрагменты, линейные антитела, одноцепочечные антитела и мультиспецифичные антитела, образованные из фрагментов антител.
[00191] Термин ʺмоноклональное антителоʺ относится к гомогенной популяции антител, вовлеченных в высокоспецифическое распознавание и связывание с одной антигенной детерминантой или эпитопом. Это является их отличием от поликлональных антител, которые обычно включают различные антитела, направленные против ряда различных антигенных детерминант. Термин ʺмоноклональное антителоʺ включает фрагменты антител (такие как Fab, Fab′, F(ab′)2, Fd, Fv), одноцепочечные (scFv) мутанты, гибридные белки, включающие часть антитела, и любую другую модифицированную молекулу иммуноглобулина, включающую сайт распознавания антигена, а также как интактные, так и полноразмерные моноклональные антитела, но не ограничивается этим. Кроме того, ʺмоноклональное антителоʺ относится к таким антителам, полученным любым из различных способов, включая, но не ограничиваясь этим, гибридому, селекцию фагов, рекомбинантную экспрессию и трансгенных животных.
[00192] Термин ʺгуманизированные антителоʺ относится к формам не-человеческих (например, мышиных) антител, которые представляют собой специфические цепи иммуноглобулинов, химерные иммуноглобулины или их фрагменты, которые содержат минимальные не-человеческие (например, мышиные) последовательности. Как правило, гуманизированные антитела представляют собой иммуноглобулины человека, в которых остатки из определяющей комплементарность области (CDR) заменены остатками из CDR отличного от человека вида (например, мыши, крысы кролика и хомяка), обладающими желаемой специфичностью, аффинностью и способностью (см. Jones et al., 1986, Nature, 321:522-525; Riechmann et al., 1988, Nature, 332:323-327; Verhoeyen et al., 1988, Science, 239:1534-1536). В некоторых случаях, остатки Fv каркасной области (FR) человеческого иммуноглобулина заменены соответствующими остатками в антителе из отличного от человека вида, обладающими желаемой специфичностью, аффинностью и/или способностью к связыванию. Гуманизированные антитело может быть дополнительно модифицировано путем замены дополнительных остатков в Fv каркасной области и/или в замененных остатках, происходящих из отличного от человека вида, для улучшения и оптимизации специфичности, аффинности и/или способности к связыванию антитела. Как правило, гуманизированное антитело включает по существу все из по меньшей мере одного, и обычно двух или трех вариабельных доменов, содержащих все или по существу все из CDRs, которые соответствуют нечеловеческому иммуноглобулину, тогда как все или по существу все из каркасных областей (FRs) содержат такие, которые происходят консенсусной последовательности человеческого иммуноглобулина. Гуманизированное антитело также может включать по меньшей мере часть константной области или домена (Fc) иммуноглобулина, типично человеческого иммуноглобулина. Примеры способов, используемых для получения гуманизированных антител, описаны в Патенте США № 5225539.
[00193] Термин ʺчеловеческое антителоʺ, как он используется в настоящей заявке, относится к антителу, продуцируемому человеком, или антителу, содержащему аминокислотную последовательность, соответствующую антителу, продуцируемому человеком, с использованием любого метода, известного в данной области техники. Это определение человеческого антитела включает интактные или полноразмерные антитела, их фрагменты и/или антитела, включающие по меньшей мере один полипептид тяжелой и/или легкой цепи человека, такие как, например, антитело, включающее полипептиды легкой цепи мыши и тяжелой цепи человека.
[00194] Термин ʺхимерное антителоʺ относится к антителу, где аминокислотная последовательность молекулы иммуноглобулина происходит из двух или более видов. Как правило, вариабельные области как легкой, так и тяжелой цепи соответствуют вариабельным областям антител, происходящих из одного вида млекопитающих (например, мыши, крысы, кролика и т.д.) с желаемой специфичностью, аффинностью и способностью, тогда как константные области гомологичны последовательностям в антителах, происходящих из другого вида (обычно человека), чтобы избежать иммунного ответа у этого вида.
[00195] Термины ʺэпитопʺ и ʺантигенная детерминантаʺ используются взаимозаменяемо в настоящей заявке и относятся к части антигена, которая может распознаваться и специфически связываться с определенным антителом. Когда антиген представляет собой полипептид, эпитопы могут быть образованы как из несмежных аминокислот, так и из смежных аминокислот, объединенных вместе третичной укладкой белка. Эпитопы, образованные из смежных аминокислот, обычно сохраняются при денатурации белка, тогда как эпитопы, образованные третичной укладкой, обычно теряются при денатурации белка. Эпитоп обычно включает три или более, пять или более или 8-10 или более аминокислот в уникальной пространственной конформации.
[00196] Антитело, которое ʺспецифически связываетсяʺ с эпитопом или молекулой антигена, означает антитело, которое взаимодействует или вступает в ассоциацию более часто, более быстро, с большей продолжительностью, с большей аффинностью или с некоторой комбинацией вышеперечисленных с эпитопом или молекулой антигена, чем альтернативные вещества, включая неродственные белки. В конкретных вариантах осуществления ʺспецифически связываетсяʺ означает, например, что антитело связывается с белком с KD около 0,1 мМ или меньше, но более типично меньше чем около 1 мкМ. В конкретных вариантах осуществления ʺспецифически связываетсяʺ означает, что антитело связывается с белком в некоторых случаях с KD около 0,1 мкМ или меньше, и в других случаях с KD около 0,01 мкМ или меньше. Как результат идентичности последовательностей между гомологичными белками из разных видов, специфическое связывание может включать антитело, распознающее определенный белок в более чем одном виде. Должно быть понятно, что антитело или связывающийся остаток, который специфически связывается с первой мишенью, может специфически связываться или может не связываться со второй мишенью. Как описано выше, ʺспецифическое связываниеʺ необязательно требует (хотя может включать) эксклюзивного связывания, то есть связывания с одной мишенью. Как правило, но необязательно, ссылка на связывание означает специфическое связывание.
[00197] Антитела, включая их фрагменты/производные и моноклональные антитела, можно получить с использованием способов, известных в данной области техники (см. McCafferty et al., Nature 348:552-554 (1990); Clackson et al., Nature 352:624-628; Marks et al., J. Mol. Biol. 222:581-597 (1991); Marks et al., Bio/Technology 10:779-783 (1992); Waterhouse et al., Nucleic. Acids Res. 21:2265-2266 (1993); Morimoto et al., Journal of Biochemical and Biophysical Methods 24:107-117 (1992); Brennan et al., Science 229:81(1985); Carter et al., Bio/technology 10:163-167 (1992); Kohler et al., Nature 256:495 (1975); U.S. Pat. No. 4,816,567); Kilpatrick et al., Hybridoma 16(4):381-389 (1997); Wring et al., J. Pharm. Biomed. Anal. 19(5):695-707 (1999); Bynum et al., Hybridoma 18(5):407-411 (1999), Jakobovits et al., Proc. Natl. Acad. Sci. USA,90:2551 (1993); Jakobovits et al., Nature, 362:255-258 (1993); Bruggemann et al., Year in Immuno. 7:33 (1993); Barbas et al., Proc. Nat. Acad. Sci. USA 91:3809-3813 (1994); Schier et al., Gene 169:147-155 (1995); Yelton et al., J. Immunol. 155:1994-2004 (1995); Jackson et. al., J. Immunol. 154(7):3310-9 (1995); Hawkins et al., J. Mol. Biol. 226:889-896 (1992), Патенты США №№ 5514548, 5545806, 5569825, 5591669, 5545807; WO 97/17852, которые все включены в настоящую заявку посредством ссылки во всей их полноте).
[00198] Не ограничиваясь этим, антитело предпочтительно может быть выбрано из группы, включающей муромонаб-CD3, абциксимаб, ритуксимаб, даклизумаб, паливизумаб, инфликсимаб, трастузумаб (известный как ʹГерцептинʹ), этанерцепт, базиликсимаб, гемтузумаб озогамицин, алемтузумаб, ибритутомаб тиуксетан, адалимумаб, алефацепт, омализумаб, эфализумаб, тозитумомаб-I131, цетуксимаб, бевацизумаб, натализумаб, ранибизумаб, панитумумаб, экулизумаб, рилонацепт, цертолизумаб пегол, ромиплостим, AMG-531, CNTO-148, CNTO-1275, ABT-874, LEA-29Y, белимумаб, TACI-Ig, анти-CD20 второго поколения, ACZ-885, тоцилизумаб, атлизумаб, меполизумаб, пертузумаб, HuMax CD20, тремелимумаб (CP-675 206), тицилимумаб, MDX-010, IDEC-114, инотузумаб озогамицин, HuMax EGFR, афлиберцепт, VEGF Trap-Eye, HuMax-CD4, Ala-Ala, ChAglyCD3, TRX4, катумаксомаб, IGN101, MT-201, преговомаб, CH-14,18, WX-G250, AMG-162, AAB-001, мотавизумаб, MEDI-524, эфунгумаб, Aurograb®, раксибацумаб, анти-CD20 третьего поколения, LY2469298 и велтузумаб.
[00199] Термин ʺбелокʺ, как он используется в настоящей заявке, также включает repebody, которое представляет собой полипептид, оптимизированный консенсусной конструкцией через слияние N-конца интерналина, содержащего белковую структуру с лейцин-обогащеннымм повторами (LRR), и вариабельного участка рецептора лимфоцитов (VLR) на основании их структурной схожести. Repebody может включать все гибридные белки LRR семейства, полученные с использованием всех белков, включенных в LRR семейство, содержащих повторяющийся модуль, для улучшения водорастворимости, экспрессии и биофизических свойств белкой вышеуказанным способом.
[00200] Когда белок представляет собой моноклональное антитело, по меньшей мере одна легкая цепь моноклонального антитела или по меньшей мере одна тяжелая цепь моноклонального антитела или и та и другая могут включать аминокислотную область, содержащую аминокислотный мотив, который может распознаваться изопреноид-трансферазой.
[00201] Специалисты в данной области техники легко смогут выбрать белок (например, клетка-мишень субъекта), селективно связывающийся с мишенью, представляющей интерес. Не ограничиваясь указанными выше белками, белок включает фрагмент антитела или антигена, специфически связывающийся с мишенью, представляющей интерес.
[00202] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, аминокислотный мотив может представлять собой CYYX, XXCC, XCXC или CXX, (где C представляет собой цистеин, Y представляет собой алифатическую аминокислоту, и X представляет собой аминокислоту, которая определяет субстрат-специфичность изопреноид-трансферазы), и более предпочтительно аминокислотный мотив представляет собой CYYX.
[00203] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, более предпочтительно, когда белок представляет собой антитело или repebody.
[00204] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, B, который представляет собой активное вещество, может быть ковалентно связан с аминокислотным мотивом, существующим на карбоксильном конце белка, через один или несколько линкеров.
[00205] Активное вещество включает лекарственное средство, токсин, аффинный лиганд, детекторный зонд или их комбинацию.
[00206] Лекарственное средство может быть выбрано из группы, включающей эрлотиниб (TARCEVA; Genentech/OSI Pharm.); бортезомиб (VELCADE; Millenium Pharm.); фулвестрант (FASLODEX; AstraZeneca); сутент (SU11248; Pfizer); летрозол (FEMARA; Novartis); иматиниб мезилат (GLEEVEC; Novartis); PTK787/ZK 222584 (Novartis); оксалиплатин (Eloxatin; Sanofi); 5-фторурацил (5-FU); лейковорин; рапамицин (Сиролимус, RAPAMUNE; Wyeth); лапатиниб (TYKERB, GSK572016; GlaxoSmithKline); лонафарниб (SCH 66336); сорафениб (BAY43-9006; Bayer Labs.); гефитиниб (IRESSA; Astrazeneca); AG1478, AG1571 (SU 5271; Sugen); алкилирующие средства (например, тиотепа или CYTOXAN® циклофосфамид); алкилсульфонат (например, бусульфан, импросульфан или пипосульфан); азиридин (например, бензодопа, карбоквон, метуредопа или уредопа); этиленимин, метилмеламин, алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид, триметилолмеламин; ацетогенины (например, буллатацин или буллатацинон); камптотецин, включая синтетический аналог топотекан; бриостатин; каллистатин; CC-1065 (включая его синтетические аналоги адоцелезин, карцелезин или бицелезин; криптофицины (например, криптофицин 1 или криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги KW-2189 и CB1-TM1); элеутеробин; панкратистатин; саркодиктиин; спонгистатин; азотистый иприт (например, хлорамбуцил, хлорнафазин, хлорфосфамид, эстрамустин, ифосфамид, мехлоретамин, мехлоретамин оксид гидрохлорид, мелфалан, новембикин, фенестерин, преднимустин, трофосфамид или урацил иприт); нитрозомочевина (например, кармустин, хлорозоцин, фотемустин, ломустин, нимустин или ранимустин); антибиотики (например, энедииновые антибиотики, такие как калихеамицин, выбранный из калихеамицина гамма 1I и калихеамицина омега I1, или динемицин, включая динемицин A); бисфосфонат (например, клодронат; эсперамицин, неокарциностатин хромофор или родственные хромопротеиновые энедииновые антибиотические хромофоры, аклациномизины, актиномицин, антрамицин, азасерин, блеомицины, кактиномицин, карабицин, карниномицин, карцинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, ADRLIMYCIN® (доксорубицин) (например, морфолино-доксорубицин, цианоморфолино-доксорубицин, 2-пирролино-доксорубицин, липосомальный доксорубицин или дезоксидоксорубицин), эпирубицин, эзорубицин, марцелломицин, митомицины (например, митомицин C, микофеноловая кислота, ногаламицин, оливомицин, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептомигрин, стрептозоцин, туберцидин, убенимекс, зиностатин или зорубицин); антиметаболиты (например, 5-фторурацил (5-FU); аналоги фолиевой кислот (например, деноптерин, метотрексат, птероптерин или триметрексат); пуриновые аналоги (например, флударабин, 6-меркаптопурин, тиамиприн или тигуанин); пиримидиновые аналоги (например, анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин или флоксуридин); андрогены (например, калустерон, дромостанолон пропионат, эпитиостанол, мепитиостан) или тестолактон); анти-адренергические средства (например, аминоглутетимид, митотан или трилостан); компенсатор фолиевой кислоты (например, фолиновая кислота); ацеглатон; альдофосфамид гликозид; аминолевулиновую кислоту; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазиквон; элфорнитин; эллиптиниум ацетат; эпотилон; этоглуцид; нитрат галлия; гидроксимочевину; лентинан; лонидаинин; майтансиноиды (например, майтансин или ансамитоцины); трихотецены (в частности, T-2 токсин, верракурин A, роридин A или ангвидин); митоквазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лосоксантрон; 2-этилгидразид; прокарбазин; PSK® полисахаридный комплекс; разоксан; рихоксин; сизофиран; спирогерманий; тенуазоновую кислоту; триазиквон; 2,2ʹ,2ʺ-трихлортриэтиламин; трихотецены (в частности, T-2 токсин, верракурин A, роридин A или ангвидин); уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид (ʹAra-Cʹ); циклофосфамид; тиотепа; таксоиды (например, TAXOL® паклитаксел (Bristol-Myers Squibb Oncology, Princeton, N.J.), препарат паклитаксела на основе альбумина в форме наночастиц ABRAXANETM без кремофора (American Pharmaceutical Partners, Schaumber, I11.) или TAXOTERE® доцетаксел (Rhone-Poulenc Rorer, Antony, France); хлорамбуцил; гемцитабин; 6-тиогуанин; меркаптопурин; аналог платины (например, цисплатин или карбоплатин); винбластин; платину; этопозид, ифосфамид; митоксантрон; винкристин; NAVELBINE® винорелбин; новантрон; тенипозид; эдатрексат; дауномицин; аминоптерин; кселода; ибандронат; CPT-11; ингибитор топоизомеразы (RFS 2000); дифторметилорнитин (DFMO); ретиноид (например, ретиноевая кислота); капецитабин и их фармацевтически приемлемые соли, сольваты, кислоты или производные, но необязательно ограничиваясь этим.
[00207] Не ограничиваясь перечисленным далее, дополнительные лекарственные средства включают (i) анти-гормональные средства, которые действуют как регуляторы или ингибиторы действия гормонов на опухоли, такие как анти-эстрогены и селективные модуляторы рецепторов эстрогена (SERMs), включая, например, тамоксифен (включая NOLVADEX® тамоксифен), ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и FAREATON® торемифен; (ii) ингибиторы ароматазы, которые ингибируют фермент ароматазу, которая регулирует продукцию эстрогена в надпочечниках, например, 4(5)-имидазолы, аминоглутетимид, MEGASE® мегестрол ацетат, AROMASIN® экземестан, FEMARA® летрозол и ARIMIDEX® анастрозол; (iii) анти-андрогены, такие как флутамид, нилутамид, бикалутамид, леупролид и госерелин; а также троксацитабин (1,3-диоксолановый нуклеозидный цитозиновый аналог); (iv) ингибиторы ароматазы; (v) ингибиторы протеинкиназы; (vi) ингибиторы липид-киназы; (vii) антисмысловые олигонуклеотиды, в частности, такие, которые ингибируют экспрессию генов в сигнальных путях в прилипающих клетках, например, PKC-альфа, Raf, H-Ras; (viii) рибозим, например, ингибитор VEGF, такой как ANGIOZYME рибозим, и ингибиторы экспрессии HER2; (ix) вакцины, такие как генно-терапевтическая вакцина; ALLOVECTIN® вакцина, LEUVECTIN вакцина и VAXID вакцина; PROLEUKIN®rlL-2; LURTOTECAN® ингибитор топоизомеразы 1; ABARELIX® rmRH; (x) анти-ангиогенное средство, такое как Бевацизумаб (AVASTIN, Genentech); и (xi) их фармацевтически приемлемые соли, сольваты, кислоты или производные.
[00208] Кроме того, цитокины можно использовать в качестве лекарственного средства. Цитокины представляют собой малые молекулы белков клеточной сигнализации, которые секретируются различными клетками и представляют собой класс сигнальных молекул, широко используемых в межклеточной коммуникации. Цитокины включают монокины, лимфокины, традиционные полипептидные гормоны и т.п. Примеры цитокинов включают гормон роста (например, человеческий гормон роста, N-метионил человеческий гормон роста или бычий гормон роста); паратиреоидный гормон; тироксин; инсулин; проинсулин; релаксин; прорелаксин; гликопротеиновый гормон (например, фолликулостимулирующий гормон (FSH), тиреоидный стимулирующий гормон (TSH) или лютеинизирующий гормон (LH)); фактор роста гепатоцитов; фактор роста фибробластов; пролактин; планцетарный лактоген; фактор некроза опухоли-α; фактор некроза опухоли-β; мюллерову ингибирующую субстанцию; мышиный гонадотропин-ассоциированный пептид; ингибин; активин; сосудистый эндотелиальный фактор роста; интегрин, тромбопоэтин (TPO); фактор роста нервов (например, NGF-β); тромбоцитарный фактор роста; трансформирующий фактор роста (TGF) (например, TGF-α или TGF-β); инсулиноподобный фактор роста-I, инсулиноподобный фактор роста-II; эритропоэтин (EPO); остеоиндуктивный фактор; интерферон (например, интерферон-α, интерферон-β или интерферон-γ); колониестимулирующий фактор (CSF) (например, макрофагальный CSF (M-CSF), гранулоцитарно-макрофагальный CSF (GM-CSF) или гранулоцитарный CSF (G-CSF)); интерлейкин (IL) (например, IL-1, IL-1α, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11 или IL-12); фактор некроза опухоли (TNF) (например, TNF-α или TNF-β); и полипептидный фактор (например, LIF или kit лиганд (KL)), но не ограничиваются этим. Кроме того, термин ʺцитокинʺ также включает цитокины из природных источников или рекомбинантных клеточных культур и биологически активные эквиваленты природных последовательностей цитокинов.
[00209] Термин ʺтоксинʺ относится к ядовитому веществу, продуцируемому в живых клетках или организмах. Токсины могут представлять собой малые молекулы, пептиды или белки, способные вызывать заболевания во время контактирования с, или абсорбции, тканью организма путем взаимодействия с биологическими макромолекулами, такими как фермент или клеточные рецепторы. Кроме того, токсины включают растительные токсины и токсины животного происхождения. Примеры токсинов животного происхождения включают дифтерийный токсин, ботулинический токсин, коклюшный токсин, дизентерийный токсин, холерный токсин, тетродотоксин, бреветоксин и сигуатоксин, но не ограничиваются этим. Примеры растительных токсинов включают рицин и AM-токсин, но не ограничиваются этим.
[00210] Примеры малых молекул токсинов включают ауристатин, тубулизин, гелданaмицин (Kerr et al., 1997, Bioconjugate Chem. 8(6):781-784), майтансиноид (EP 1391213, ACR 2008, 41, 98-107), калихеамицин (US 2009105461, Cancer Res. 1993, 53, 3336-3342), дауномицин, доксорубицин, метотрексат, виндезин, SG2285 (Cancer Res. 2010, 70(17), 6849-6858), доластатин, аналоги доластатина, ауристатин (US563548603), криптофицин, камптотецин, производное ризоксина, аналог или производное CC 1065, дуокармицин, энедииновый антибиотик, эсперамицин, эпотилон, пирролобензодиазепиновые (PBD) производные, α-аманитин и токсоид, но не ограничиваются этим. Токсины могут проявлять цитотоксичность и активность, направленную на ингибирование клеточного роста, путем связывания тубулина, связывания ДНК, супрессии топоизомеразы и т.п.
[00211] Термин ʺлигандʺ относится к молекуле, способной образовывать комплекс с биомолекулой-мишенью. Примером лиганда является молекула, связанная с предварительно определенным положением целевого белка для передачи сигнала. Лиганд может представлять собой субстрат, ингибитор, стимулятор, нейротрансмиттер или радиоизотоп.
[00212] ʺДетектируемая молекулаʺ или ʺметкаʺ относится к композиции, определяемой спектроскопическими, фотохимическими, биохимическими, иммунохимическими, радиоактивными или химическими средствами. Например, полезные метки включают 32P, 35S, флуоресцентные красители, электроноплотные реагенты, ферменты (например, ферменты, традиционно используемые в ELISA), биотин-стрептавидин, диоксигенин, гаптены и белки, для которых имеются антисыворотки или моноклональные антитела, или молекулы нуклеиновых кислот с последовательностью, комплементарной мишени. Детектируемая молекула часто генерирует измеряемый сигнал, такой как радиоактивный, хромогенный или флуоресцентный сигнал, который можно использовать для определения количества связанной детектируемой молекулы в образце. Количественное определение сигнала осуществляют, например, методом сцинтилляционного счета, денситометрии, проточной цитометрии, ELISA или путем прямого масс-спектрометрического анализа интактных или впоследствии расщепленных пептидов (можно анализировать один или несколько пептидов). Специалистам в данной области известны методы мечения соединений, представляющих интерес, средства детекции. Такие процедуры и методы являются традиционными и хорошо известны в данной области техники.
[00213] Термин ʺзондʺ, как он используется в настоящей заявке, относится к веществу, которое может (i) обеспечивать детектируемый сигнал, (ii) обеспечивать взаимодействие первого зонда или второго зонда для модификации детектируемого сигнала, обеспечиваемого первым или вторым зондом, такого как резонансный перенос энергии флуоресценции (FRET), (iii) стабилизировать взаимодействие с антигеном или лигандом или повышать аффинность связывания; (iv) влиять на подвижность электрофореза или активность внедрения в клетку посредством физического параметра, такого как заряд, гидрофобность и т.п., или (v) контролировать аффинность лиганда, связывание антиген-антитело или образование ионного комплекса.
[00214] Активное вещество включает иммуномодулирующее соединение, противораковое средство, противовирусное средство, антибактериальное средство, противогрибковое средство, противопаразитарное средство или их комбинацию.
[00215] Иммуномодулирующее соединение может быть выбрано из группы, включающей аминокапроновую кислоту, азатиоприн, бромокриптин, хлорохин, хлорамбуцил, циклоспорин, циклоспорин A, даназол, дегидроэпиандростерон (DHEA), дексаметазон, этанерцепт, гидроксихлорохин, гидрокортизон, инфликсимаб, мелоксикам, метотрексат, циклофосфамид, микофенилат мофетил, преднизон, сиролимус и такролимус. Противораковое средство может быть выбрано из группы, включающей метотрексат, таксол, L-аспарагиназу, меркаптопурин, тиогуанин, гидроксимочевину, цитарабин, циклофосфамид, ифосфамид, нитрозомочевину, цисплатин, карбоплатин, митомицин, дакарбазин, прокарбазин, топотекан, азотистый иприт, цитоксан, этопозид, 5-фторурацил, бис-хлорэтилнитрозомочевину (BCNU), иринотекан, камптотецин, блеомицин, доксорубицин, идарубицин, даунорубицин, дактиномицин, пликамицин, митоксантрон, аспарагиназу, винбластин, винкристин, винорелбин, паклитаксел, доцетаксел, хлорамбуцил, мелфалан, кармустин, ломустин, бусульфан, треосульфан, декарбазин, этопозид, тенипозид, топотекан, 9-аминокамптотецин, криснатол, митомицин C, триметрексат, микофеноловую кислоту, тиазофурин, рибавирин, 5-этинил-1-бета-D-рибофуранозилимидазол-4-карбоксамид (EICAR), гидроксимочевину, дефероксамин, флоксиридин, доксифлуридин, ралтитрексед, цитарабин (ara C), цитозин арабинозид, флударабин, тамоксифен, ралоксифен, мегестрол, госерелин, леупролид ацетат, флутамид, бикалутамид, EB1089, CB1093, KH1060, вертепорфин, фталoцианин, фотосенсибилизатор Pe4, деметокси-гипокреллин A, интерферон-α, интерферон-γ, фактор некроза опухоли, гемцитабин, велкаде, ревлимит, таломид, ловастатин, 1-метил-4-фенилпиридиниевый ион, стауроспорин, актиномицин D, дактиномицин, блеомицин A2, блеомицин B2, пепломицин, эпирубицин, пирарубицин, зорубицин, митоксантрон, верапамил и тапсигаргин. Противовирусное средство может быть выбрано из группы, включающей пенцицикловир, валацикловир, ганцицикловир, фоскарнет, рибавирин, идоксуридин, видарабин, трифлуридин, aцикловир, фамцицикловир, амантадин, римантадин, цидофовир, антисмысловой олигонуклеотид, иммуноглобулин и интерферон. Антибактериальное средство может быть выбрано из группы, включающей хлорамфеникол, ванкомицин, метронидазол, триметоприн, сульфаметазол, квинупристин, далфопристин, рифампин, спектиномицин и нитрофурантоин. Противогрибковое средство может быть выбрано из группы, включающей амфотерицин B, кандицидин, филипин, гамицин, натамицин, нистатин, римоцидин, бифоназол, бутоконазол, клотримазол, эконазол, фентиконазол, изоконазол, кетоконазол, луликоназол, миконазол, омоконазол, оксиконазол, сертаконазол, сулконазол, тиоконазол, альбаконазол, флуконазол, изавуконазол, итраконазол, посаконазол, равуконазол, терконазол, вориконазол, абафунгин, аморолфин, бутенафин, нафтифин, тербинафин, анидулафунгин, каспофунгин, микафунгин, бензойную кислоту, циклопирокс, флуцитозин, гризеофулвин, галопрогин, толнафтат, ундециленовую кислоту, кристаллический фиолетовый, перуанский бальзам, циклопирокс оламин, пироктон оламин, цинк пиритион и сульфид селена. Противопаразитарное средство может быть выбрано из группы, включающей мебендазол, пирантел памоат, тиабендазол, диэтилкарбамазин, ивермектин, никлосамид, празиквантел, албендазол, рифампин, амфотерицин B, меларсопрол, эфлорнитин, метронидазол, тинидазол и милтефосин.
[00216] В соединениях, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, белок, содержащий аминокислотный мотив, может быть выбран из группы, включающей A-HC-(G)zCVIM, A-HC-(G)zCVLL, A-LC-(G)zCVIM и A-LC-(G)zCVLL, где A представляет собой антитело, HC представляет собой тяжелую цепь, LC представляет собой легкую цепь, G представляет собой глициновое звено, и z представляет собой целое число от 0 до 20.
[00217] Соединения, включающие саморасщепляющуюся группу в соответствии с настоящим изобретением, может быть выбрано из соединений, имеющих следующую структуру.
[00218]


[00219] где
[00220] Z представляет собой водород, (C1-C8)алкил, галоген, циано или нитро;
[00221] X представляет собой -O-, (C1-C8)алкилен или -NR21-;
[00222] R21 представляет собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
[00223] n представляет собой целое число от 1 до 3, и, когда n представляет собой целое число 2 или более, каждый из заместителей Z являются одинаковыми или отличными друг от друга;
[00224] r представляет собой целое число от 1 до 10;
[00225] q представляет собой целое число от 1 до 10;
[00226] w представляет собой целое число от 1 до 10.
[00227] x представляет собой целое число от 0 до 10;
[00228] g представляет собой целое число от 1 до 10;
[00229] -S-mAb представляет собой A-HC-(G)zCVIM-, A-HC-(G)zCVLL-, A-LC-(G)zCVIM- или A-LC-(G)zCVLL-, где A представляет собой антитело, HC представляет собой тяжелую цепь, LC представляет собой легкую цепь, G представляет собой глициновое звено, и z представляет собой целое число от 0 до 20;
[00230] B представляет собой лекарственное средство, имеющее структуру, выбранную из следующих структур; и
[00231] 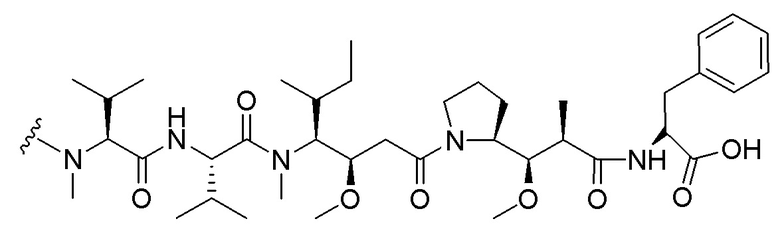
[00232] 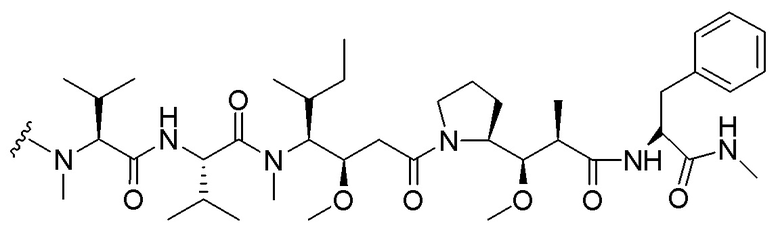
[00233] 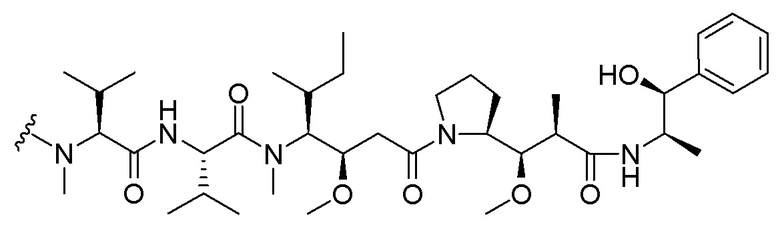
[00234] 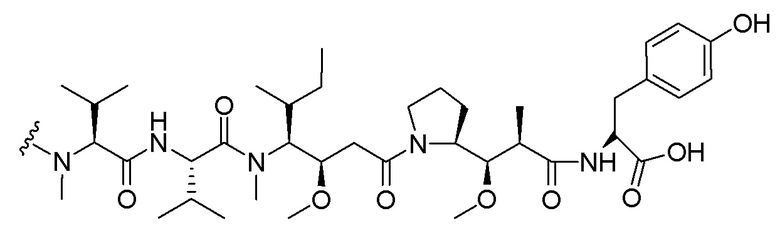
[00235] 
[00236] 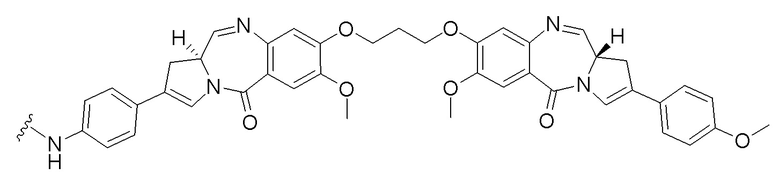
[00237] 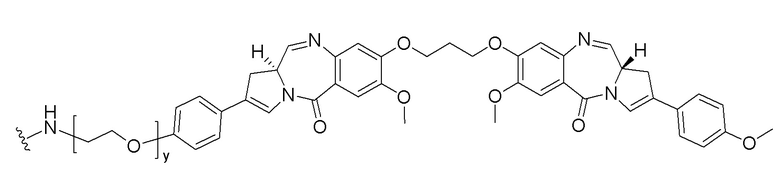
[00238] 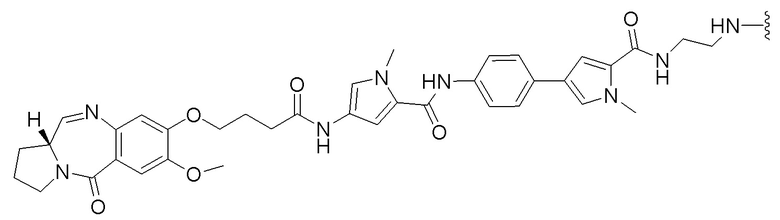
[00239] 
[00240] 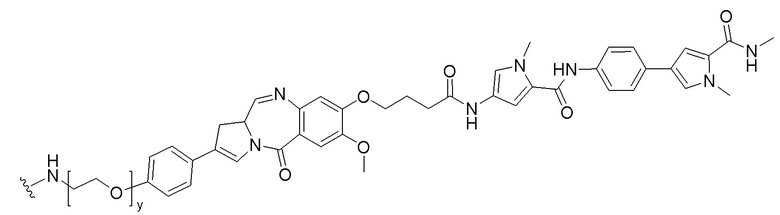
[00241] y представляет собой целое число от 1 до 10.
[00242] В соединениях, включающих саморасщепляющуюся группу Химической формулы 1 в соответствии с настоящим изобретением, когда A представляет собой белок и B представляет собой активное вещество, соединение можно использовать для переноса активного вещества в клетку-мишень субъекта для лечения субъекта с использованием способа получения композиции, известного специалисту в данной области.
[00243] Композиции получают в форме для инъекций, либо в виде жидкого раствора, либо в виде суспензии. Твердые формы, подходящие для инъекции, также можно получить в виде эмульсий или с полипептидами, инкапсулированными в липосомах. Соединения, включающие саморасщепляющуюся группу, можно объединить с фармацевтически приемлемым носителем, который включает любой носитель, который не индуцирует продукцию антител, вредных для субъекта, получающего носитель. Подходящие носители обычно включают большие макромолекулы, которые медленно метаболизируются, например, белки, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, сополимеры аминокислот, липидные агрегаты и подобные. Эти носители хорошо известны специалистам в данной области.
[00244] Композиции также могут содержать разбавители, например, воду, насыщенный солевой раствор, глицерин и этанол. Вспомогательные вещества, например, увлажнители или эмульгаторы, pH-регулирующие буферные вещества и подобные, также могут быть представлены в этих композициях. Белки можно формулировать с получением вакцин в виде нейтральных или солевых форм. Композиции можно вводить парентерально путем инъекции, где такая инъекция может представлять собой либо подкожную, либо внутримышечную инъекцию. Дополнительные композиции подходят для других форм введения, таких как суппозитории или композиции для перорального введения. Композиции для перорального введения можно вводить в виде раствора, суспензии, таблетки, пилюли, капсулы или композиции замедленного высвобождения.
[00245] Композиции вводят способом, совместимым с дозой и лекарственной формой. Композиция включает терапевтически эффективное количество соединения, включающего саморасщепляющуюся группу. Под ʺтерапевтически эффективным количествомʺ подразумевают разовую дозу или композицию, вводимую по схеме многократного введения, которая является эффективной для лечения или профилактики заболевания или расстройства. Вводимая доза может варьировать в зависимости от нуждающегося в лечении субъекта, здоровья субъекта и физического состояния, степени защиты, которая может быть желательной, и других важных факторов. Точное требуемое количество активного ингредиента зависит от заключения врача.
[00246] Например, терапевтически эффективное количество соединения, включающего саморасщепляющуюся группу, или композиции, содержащей такое соединение, можно вводить пациенту с раковым заболеванием или злокачественной опухолью для лечения рака или опухоли.
[00247] Терапевтически эффективное количество соединения, включающего саморасщепляющуюся группу, или композиции, содержащей такое соединение, можно вводить пациенту для лечения или профилактики инфекции, вызываемой патогенными микроорганизмами (например, вирусами, бактериями, грибами, паразитами или подобными). Эти способы включают введение терапевтического или профилактического количества соединения, включающего саморасщепляющуюся группу, достаточного для лечения заболевания или расстройства или их симптомов, млекопитающим животным, в условиях, при которых заболевание или расстройство можно предотвратить или вылечить.
[00248] Соединение, включающее саморасщепляющуюся группу в соответствии с настоящим изобретением, или композицию, содержащую такое соединение, можно вводить в форме их фармацевтически приемлемой соли или сольвата. В некоторых вариантах осуществления соединение, включающее саморасщепляющуюся группу в соответствии с настоящим изобретением, или композицию, содержащую такое соединение, можно вводить с фармацевтически приемлемым носителем, фармацевтически приемлемым эксципиентом и/или фармацевтически приемлемой добавкой. Фармацевтически эффективное количество и тип фармацевтически приемлемой соли или сольвата, эксципиента и добавки можно определить с использованием стандартных способов (см. Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, PA, 18th Edition, 1990).
[00249] Термин ʺтерапевтически эффективное количествоʺ по отношению к раку или опуходи означает количество, которое может снижать количество раковых клеток; уменьшать размер раковых клеток; препятствовать вторжению раковых клеток в периферические системы или снизить вторжение; препятствовать распространению раковых клеток на другие системы или уменьшить распространение; препятствовать росту раковых клеток; и/или улучшить хотя бы один из симптомов, связанных с раком. В лечении рака, эффективность лекарственного средства можно оценить на основании времени до прогрессирования опухоли (TTP) и/или процента пациентов с объективным ответом (RR).
[00250] Термин ʺтерапевтически эффективное количествоʺ по отношению к инфекции, вызываемой патогенными микроорганизмами, означает количество, которое предотвращает, лечит или снижает симптомы, связанные с инфекцией.
[00251] Термин ʺфармацевтически приемлемые солиʺ при использовании в настоящей заявке включает органические соли и неорганические соли. Примеры этих солей включают гидрохлорид, гидробромид, гидройодид, сульфат, цитрат, ацетат, оксалат, хлорид, бромид, йодид, нитрат, бисульфат, фосфат, кислотный фосфат, изоникотинат, лактат, салицилат, кислотный цитрат, тартрат, олеат, таннат, пантонат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкуронат, сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, пара-толуолсульфонат и памоат (то есть, 1,1′-метиленбис-(2-гидрокси-3-нафтоат)), но не ограничиваются этим. Фармацевтически приемлемая соль может включать другую молекулу (например, ацетатные йоны, сукцинатные йоны и другие противоионы и т.д.). Фармацевтически приемлемая соль также может включать по меньшей мере один заряженный атом. Фармацевтически приемлемая соль также может включать по меньшей мере один противоион.
[00252] Примеры сольватов, которые можно использовать для фармацевтически приемлемых сольватов соединений, включающих саморасщепляющуюся группу в соответствии с настоящим изобретением, включают воду, изопропанол, этанол, метанол, диметилсульфоксид (DMSO), этилацетат, уксусную кислоту и этаноламин, но не ограничиваются этим.
[00253]
[00254] Далее будут более подробно описаны конфигурации настоящего изобретения при помощи Примеров, но представленные ниже Примеры служат только для понимания настоящего изобретения. Поэтому объем настоящего изобретения не ограничивается ими.
[00255]
[00256] [Пример 1] Получение соединения 1k
[00257]
[00258]
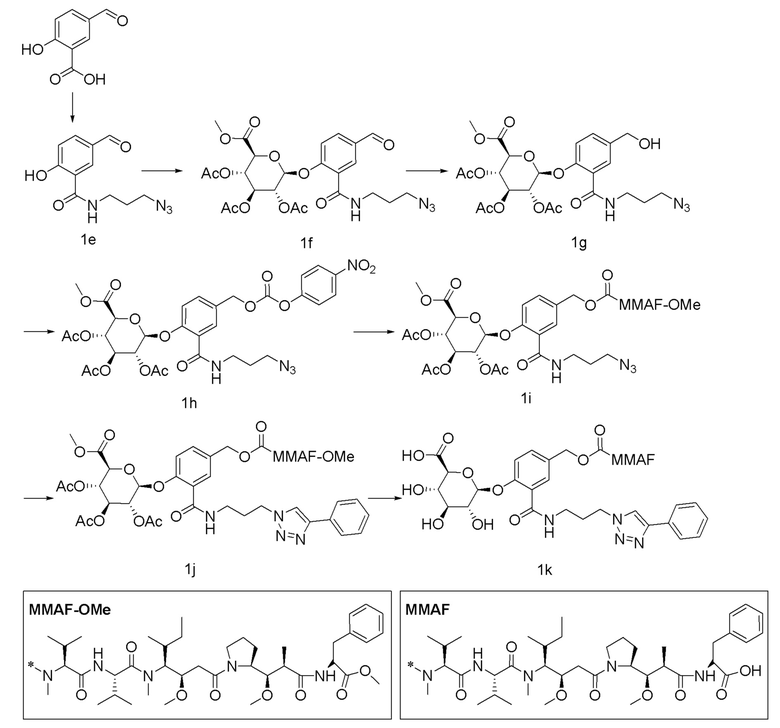
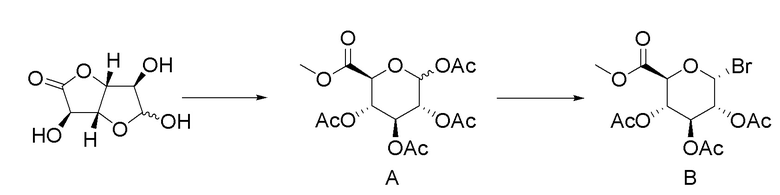
[00259] Получение соединения A
[00260] D-глюкуроно-6,3-лактон (19 г, 107,88 ммоль) растворяли в метаноле (250 мл) при комнатной температуре в атмосфере азота, к этой смеси медленно добавляли раствор NaOH (100 мг) в метаноле (100 мл) и перемешивали в течение 2 часов и затем добавляли к смеси раствор NaOH (200 мл) в метаноле (15 мл) и перемешивали в течение 3 часов. После завершения реакции метанольный растворитель смеси удаляли при пониженном давлении и к этой смеси при температуре 10°С или ниже добавляли пиридин (50 мл) и уксусный ангидрид (54 мл) и перемешивали при комнатной температуре в течение 4 часов. После завершения реакции полученную смесь концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения A (20 г, 50%).
[00261] 1H ЯМР (600МГц, CDCl3) δ 5,77 (д, J=7,8Гц, 1H), 5,31 (т, J=9,6Гц, 1H), 5,24 (т, J=9,6Гц, 1H), 5,14 (м, 1H), 4,17 (д, J=9Гц, 1H), 3,74 (с, 3H), 2,12 (с, 3H), 2,04 (м, 9H)
[00262] Получение соединения B
[00263] Соединение A (5 г, 13,28 ммоль) растворяли в 33% растворе HBr в AcOH (20 мл) при 0°С в атмосфере азота и затем перемешивали при комнатной температуре в течение 2 часов. После завершения реакции к этой смеси добавляли толуол (50 л) и смесь концентрировали при пониженном давлении. После этого к смеси добавляли этилацетат (100 мл) и раствор NaHCO3 (100 мл) для экстрагирования органического слоя и полученный органический слой сушили над безводным сульфатом натрия, затем концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения B (5,27 г, 100%).
[00264] 1H ЯМР (600МГц, CDCl3) δ 6,64 (д, J=3,6Гц, 1H), 5,61 (т, J=3,6Гц, 1H), 5,24 (т, J=3,6Гц, 1H), 4,85 (м, 1H), 4,58 (д, д, J=10,2Гц, 1H), 3,76 (с, 3H), 2,10 (с, 3H), 2,06 (с, 3H), 2,05 (с, 3H)
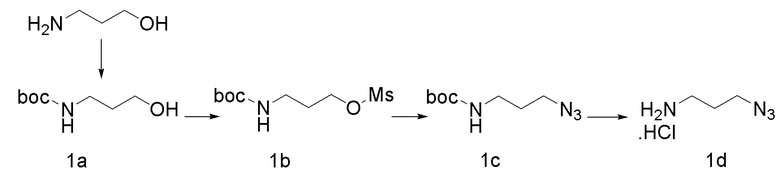
[00265] Получение соединения 1a (US6414148, 2002)
[00266] 3-Амино-1-пропанол (3,0 г, 66,569 ммоль) растворяли в дихлорметане (150 мл) при 0°С в атмосфере азота и к этой смеси добавляли ди-трет-бутилдикарбонат (16 г, 73,226 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 12 часов. После завершения реакции растворитель концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1a (6,4 г, 92%).
[00267] 1H ЯМР (400Гц, CDCl3) δ 4,78 (с, 1H), 3,65 (м, 2H), 3,30 (м, 2H), 2,90 (с, 1H), 1,68 (м, 2H), 1,48 (с, 9H); EI-MS m/z: 176(M+)
[00268] Получение соединения 1b (WO2008/157726)
[00269] Соединение 1a (6,04 г, 34,469 ммоль) и триэтиламин (TEA, 14,4 мл, 103,407 ммоль) растворяли в тетрагидрофуране при 0°С в атмосфере азота и затем медленно обрабатывали метансульфоновым ангидридом (7,21 г, 41,363 ммоль). Полученную смесь перемешивали при комнатной температуре в атмосфере азота в течение 12 часов. После завершения реакции растворитель концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1b (9,01 г, 98%).
[00270] 1H ЯМР (400Гц, CDCl3) δ 4,73 (с, 1H), 4,30 (т, J =5,9МГц, 2H), 3,31-3,24 (м, 2H), 3,04 (с, 3H), 1,94 (т, J=6,1МГц, 2H), 1,44 (с, 9H). EI-MS m/z: 254(M+)
[00271] Получение соединения 1c (WO2013/166319)
[00272] Соединение 1b (3,0 г, 11,842 mol) растворяли в диметилформамиде (40 мл) при комнатной температуре в атмосфере азота и затем обрабатывали азидом натрия (924 мг, 14,211 ммоль) и полученную смесь перемешивали при 60°С в течение 12 часов. После завершения реакции к этой смеси добавляли этилацетат (50 мл), дистиллированную воду (50 мл) и 1N раствор HCl (5 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1c (2,3 г, 99%).
[00273] 1H ЯМР (600Гц, CDCl3) δ 4,63 (с, 1H), 3,36 (т, J =6,6МГц, 2H), 3,24-3,18 (м, 2H), 1,80-1,75 (м, 2H), 1,45 (с, 9H). EI-MS m/z: 201(M+)
[00274] Получение соединения 1d
[00275] После того, как соединение 1c (3,8 г, 18,977 ммоль) растворяли в дихлорметане (10 мл) при 0°С в атмосфере азота, к смеси медленно добавляли 4M-HCl в диоксане (10 мл). Полученную смесь перемешивали в течение 12 часов. После завершения реакции полученную смесь концентрировали при пониженном давлении с получением Соединения 1d (2,5 г, 99%).
[00276] 1H ЯМР (600Гц, DMSO-d6) δ 8,06 (с, 3H), 3,47 (т, J =6,6МГц, 2H), 2,82 (т, J =7,2МГц, 2H), 1,84-1,79 (м, 2H). EI-MS m/z: 101(M+)
[00277] Получение соединения 1e
[00278] После того, как соединение 1d (58 мг, 0,420 ммоль) и 5-формилсалициловую кислоту (100 мг, 0,601 ммоль) растворяли в диметилформамиде (DMF, 2 мл) при 0°С в атмосфере азота, к смешанному раствору добавляли диизопропилэтиламин (DIPEA, 0,2 мл, 1,202 ммоль) и PyBop (375 мг, 0,721 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 3 часов. После завершения реакции к этой смеси добавляли этилацетат (30 мл) и дистиллированную воду (10 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1e (82 мг, 79%).
[00279] 1H ЯМР (400Гц, CDCl3) δ 13,39 (с, 1H), 9,87 (с, 1H), 8,29 (с, 1H), 7,89 (дд, J =1,6, 7,2МГц. 1H), 7,60 (с, 1H), 7,10 (д, J =8,8МГц), 3,63-3,57 (м, 2H), 3,48 (т, J =6,4МГц, 2H), 1,99-1,92 (м, 2H). EI-MS m/z: 249(M+)
[00280] Получение соединения 1f
[00281] После того, как соединение 1e (78 мг, 0,314 ммоль) и Соединение B (125 мг, 0,314 ммоль) растворяли в ацетонитриле (3 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли оксид серебра (291 мг, 1,256 ммоль) и молекулярные сита (125 мг). Полученную смесь перемешивали при комнатной температуре в течение 3 часов. После завершения реакции смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1f (160 мг, 90%).
[00282] 1H ЯМР (400Гц, CDCl3) δ 10,00 (с, 1H), 8,66 (д, J=2,4МГц, 1H), 8,02 (дд, J=2,0, 6,4МГц, 1H), 7,46 (т, J =6,4МГц, 1H), 7,14 (д, J =8,4МГц, 1H), 5,48-5,33 (м, 4H), 4,28 (д, J =8,8МГц, 1H), 3,74 (с, 3H), 3,73-3,64 (м, 1H), 3,50-3,42 (м, 3H), 2,09-2,07 (м, 9H), 2,00-1,92(м, 2H). EI-MS m/z: 565(M+)
[00283] Получение соединения 1g
[00284] После того, как соединение 1f (160 мг, 1,510 ммоль) растворяли в 2-пропаноле (0,4 мл) и хлороформе (2 мл) при 0°С в атмосфере азота, к полученной смеси добавляли силикагель (2 г) и борогидрид натрия (27 мг, 0,708 ммоль). После перемешивания полученной смеси при 0°С в течение 2 часов реакционную смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1g (115 мг, 71%).
[00285] 1H ЯМР (600Гц, CDCl3) δ 8,06 (д, J=2,4МГц, 1H), 7,50-7,44 (м, 2H), 7,01 (д, J =90МГц, 1H), 5,45-5,31 (м, 4H), 4,38 (с, 2H), 4,22 (д, J =9,0МГц, 1H), 3,74 (с, 3H), 3,67-3,61 (м, 1H), 3,46-3,41 (м, 3H), 2,07-2,04 (м, 9H), 1,97-1,91 (м, 2H). EI-MS m/z: 567(M+)
[00286] Получение соединения 1h
[00287] После того, как соединение 1g (100 мг, 0,177 ммоль) растворяли в DMF (1 мл) при 0°С в атмосфере азота, к полученной смеси добавляли бис(4-нитрофенил)карбонат (110 мг, 0,353 ммоль) и DIPEA (50 мкл, 0,265 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 2 часов. После завершения реакции к смеси добавляли этилацетат (30 мл) и дистиллированную воду (10 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1h (75 мг, 58%).
[00288] 1H ЯМР (600Гц, CDCl3) δ 8,29-8,27 (м, 2H), 8,23 (д, J=2,4МГц, 1H), 7,54 (дд, J =2,4, 6,6МГц, 1H), 7,49 (т, J =6,4МГц, 1H), 7,39-7,37 (м, 2H), 7,04 (д, J=8,4МГц, 1H), 5,45-5,29 (м, 4H), 5,28 (с, 2H), 4,23 (д, J =9,0МГц, 1H), 3,75 (с, 3H), 3,68-3,64 (м, 1H), 3,46-3,42 (м, 3H), 2,08-2,05 (м, 9H), 1,98-1,93 (м, 2H). EI-MS m/z: 732(M+)
[00289] Получение соединения 1i
[00290] После того, как соединение 1h (50 мг, 0,068 ммоль) растворяли в DMF (0,8 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли MMAF-OMe (51 мг, 0,068 ммоль) и затем полученную смесь обрабатывали при помощи безводного 1-гидроксибензотриазола (HOBT, 2 мг, 0,013 ммоль), пиридина (0,24 мл) и DIPEA (12 мкл, 0,068 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 18 часов. После завершения реакции к смеси добавляли этилацетат (20 мл) и дистиллированную воду (10 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1i (71 мг, 78%).
[00291] EI-MS m/z: 1339(M+)
[00292] Получение соединения 1j
[00293] После того, как соединение 1i (30 мг, 0,022 ммоль) и фенилацетилен (3,7 мкл, 0,033 ммоль) растворяли в этаноле (0,2 мл) и воде (30 мкл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли водный раствор 0,1M CuSO4 (30 мкл) и водный раствор 1,0M аскорбата натрия (30 мкл) и затем полученную смесь обрабатывали при помощи HOBT (2 мг, 0,013 ммоль), пиридина (0,24 мл) и DIPEA (12 мкл, 0,068 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 5 часов. После завершения реакции к смеси добавляли этилацетат (20 мл) и дистиллированную воду (5 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1j (26 мг, 81%).
[00294] EI-MS m/z: 1441(M+)
[00295] Получение соединения 1k
[00296] После того, как соединение 1j (20 мг, 0,013 ммоль) растворяли в метаноле (0,2 мл) при 0°С в атмосфере азота, к полученной смеси добавляли LiOH⋅H2O (6 мг, 0,138 ммоль) в воде (0,2 мл). Полученную смесь перемешивали при комнатной температуре в течение 1 часа. После завершения реакции к смеси добавляли хлороформ (10 мл), метанол (1 мл), дистиллированную воду (10 мл) и 0,5N раствор HCl (1 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 1k (17 мг, 87%).
[00297] EI-MS m/z: 1286(M+)
[00298]
[00299] [Примеры 2 и 3] Получение Соединений 2i и 3i
[00300]
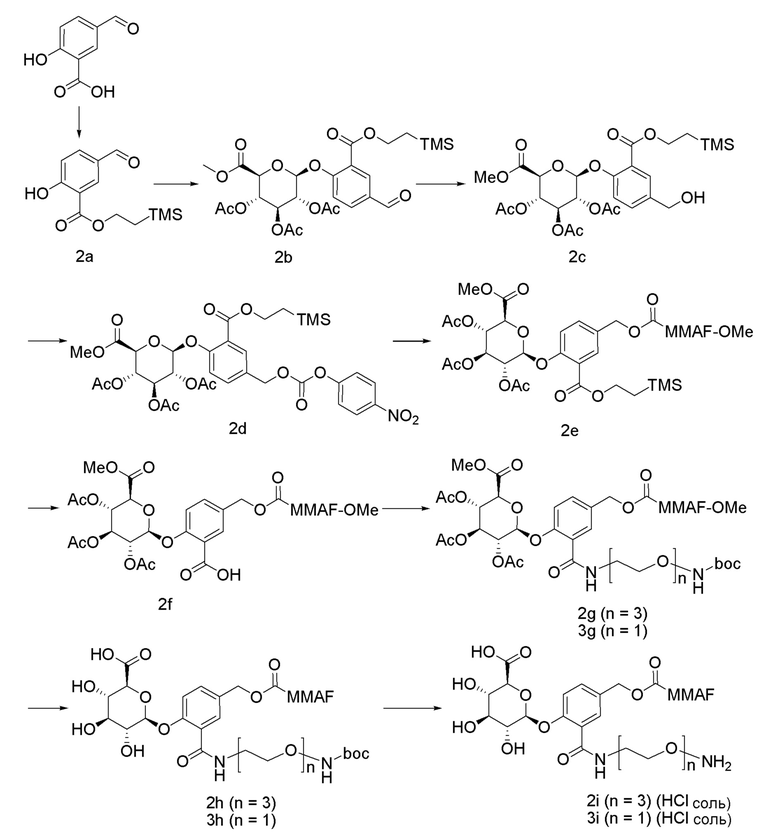
[00301]

[00302]
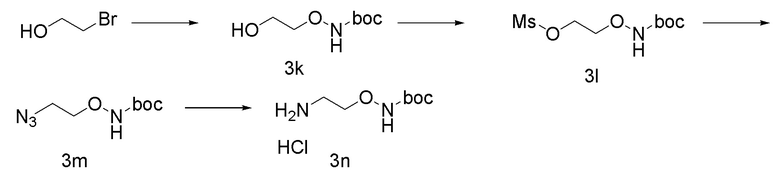
[00303] Получение соединения 2a
[00304] После того, как 5-формилсалициловую кислоту (2 г, 12,038 ммоль) растворяли в DMF при 0°С в атмосфере азота, к полученной смеси добавляли 2-(триметилсилил)этанол (1,72 мл, 12,038 ммоль) и диметиламинопиридин (DMAP, 147 мг, 1,204 ммоль) и дициклогексилкарбодиимид (DCC, 2,5 г, 12,038 ммоль). Смесь перемешивали при комнатной температуре в течение 12 часов. После завершения реакции к смеси добавляли этилацетат (100 мл) и дистиллированную воду (100 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2a (1,6 г, 50%).
[00305] 1H ЯМР (400МГц, CDCl3) δ 11,38 (с, 1H), 9,77 (с, 1H), 7,48 (д,, J=8,4МГц, 1H), 6,61 (дд, J=8,4, 2,0МГц, 1H), 6,53 (д, J=2,0МГц, 1H), 5,36~5,25 (м, 4H), 4,23 (м, 1H), 3,73 (с, 1H), 2,06 (с, 9H)
[00306] Получение соединения 2b
[00307] После того, как соединение 2a (60 мг, 0,225 ммоль) растворяли в ацетонитриле (2 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли Соединение C (90 мг, 0,225 ммоль), оксид серебра (209 мг, 0,900 ммоль) и молекулярные сита (90 мг). Смесь перемешивали при комнатной температуре в течение 2 часов. После завершения реакции к смеси добавляли этилацетат (50 мл) и дистиллированную воду (30 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2b (103 мг, 79%).
[00308] 1H ЯМР (400МГц, CDCl3) δ 9,93 (с, 1H), 8,22 (д, J=2,0МГц, 1H), 7,97 (дд, J=6,4, 2,0МГц, 1H), 7,26 (д, J=9,2МГц, 1H), 5,42-5,27 (м, 4H), 4,42-4,30 (м, 2H), 4,24 (д, J =9,2МГц, 1H), 3,70 (с, 3H), 2,06-2,04 (м, 9H), 1,14-1,08 (м, 2H), 0,07 (с, 9H)
[00309] Получение соединения 2c
[00310] После того, как соединение 2b (100 мг, 0,171 ммоль) растворяли в 2-пропаноле (0,3 мл) и хлороформе (1,5 мл) при 0°С в атмосфере азота, к полученной смеси добавляли силикагель (720 мг) и борогидрид натрия (16 мг, 0,427 ммоль). Смесь перемешивали в течение 3 часов. После завершения реакции к смеси добавляли этилацетат (50 мл) и дистиллированную воду (20 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2c (94 мг, 94%).
[00311] 1H ЯМР (400МГц, CDCl3) δ 7,71 (д, J=2,0МГц, 1H), 7,45 (дд, J=6,4, 2,0МГц, 1H), 7,17 (д, J=8,4МГц, 1H), 5,40-5,30 (м, 3H), 5,16-5,14 (м, 1H), 4,67 (с, 2H), 4,40-4,29 (м, 2H), 4,18 (д, J =8,8МГц, 1H), 3,74 (с, 3H), 2,08-2,04 (м, 9H), 1,14-1,09 (м, 2H), 0,08 (с, 9H)
[00312] Получение соединения 2d
[00313] После того, как соединение 2c (90 мг, 0,154 ммоль) растворяли в DMF (1,0 мл) при 0°С в атмосфере азота, к полученной смеси добавляли бис(4-нитрофенил)карбонат (94 мг, 0,308 ммоль) и DIPEA (40 мкл, 0,231 ммоль). Смесь перемешивали при комнатной температуре в течение 3 часов. После завершения реакции к смеси добавляли этилацетат (50 мл) и дистиллированную воду (20 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2d (104 мг, 90%).
[00314] 1H ЯМР (400 МГц, CDCl3) δ 8,28 (м, 2H), 7,80 (д, J =2,4 МГц, 1H), 7,53 (дд, J=6,4, 2,0 МГц, 1H), 7,37 (м, 2H), 7,20 (д, J=8,8 МГц, 1H), 5,41-5,33 (м, 3H), 5,25 (с, 2H), 5,20-5,18(м, 1H), 4,41-4,30 (м, 2H), 4,20 (д, J =8,8 МГц, 1H), 3,74 (с, 3H), 2,08-2,05 (м, 9H), 1,18-1,06 (м, 2H), 0,08 (с, 9H)
[00315] Получение соединения 2e
[00316] После того, как соединение 2d (1,5 г, 2,00 ммоль) растворяли в DMF (8 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли MMAF-OMe (1,34 г, 1,80 ммоль) и затем полученную смесь обрабатывали при помощи HOBT (54 мг, 0,4 ммоль), пиридина (5,4 мл) и DIPEA (0,383 мл, 2,2 ммоль). Смесь перемешивали при комнатной температуре в течение 12 часов. После завершения реакции к смеси добавляли этилацетат (200 мл) и дистиллированную воду (300 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2e (1,7 г, 70%).
[00317] EI-MS m/z: 1357(M+)
[00318] Получение соединения 2f
[00319] После того, как соединение 2e (1,7 г, 1,253 ммоль) растворяли в THF (15 мл) при 0°С в атмосфере азота, к полученной смеси добавляли фторид тетрабутиламмония (1M в THF) (2,5 мл, 2,506 ммоль) и перемешивали при комнатной температуре в течение 4 часов. После завершения реакции к смеси добавляли этилацетат (200 мл) и дистиллированную воду (300 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2f (1,34 г, 85%).
[00320] EI-MS m/z: 1257(M+)
[00321] Получение соединения 2k
[00322] После того, как соединение 2j (10 г, 59,3 ммоль) растворяли в DMF (90 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли азид натрия (5,78 г, 88,9 ммоль) и смесь перемешивали при 100°С в течение 13 часов. После завершения реакции к смеси добавляли хлороформ (200 мл) и дистиллированную воду (300 мл) для экстрагирования органического слоя и экстрагированный органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2k (10,3 г, 99%).
[00323] 1H ЯМР (600 МГц, CDCl3) δ 3,75-3,73 (м, 2H), 3,70-3,68 (м, 6H), 3,63-3,61 (м, 2H), 3,40 (т, J =5,4 МГц, 2H), 2,20 (т, J =6,0 МГц, 1H)
[00324] Получение соединения 2l
[00325] После того, как CBr4 (21,4 г, 64,6 ммоль) растворяли в метиленхлориде (MC, 100 мл) при 0°С в атмосфере азота, к полученной смеси добавляли трифенилфосфин (16,9 г, 64,6 ммоль) в MC (100 мл) и Соединение 2k (10,3 г, 58,7 ммоль) и смесь перемешивали при комнатной температуре в течение 13 часов. После завершения реакции к смеси добавляли MC (300 мл) и дистиллированную воду (300 мл) для экстрагирования органического слоя и экстрагированный органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2l (12 г, 85%).
[00326] 1H ЯМР (400 МГц, CDCl3) δ 3,83 (т, J =6,4 МГц, 2H), 3,72-3,67 (м, 6H), 3,48 (т, J =6,0 МГц, 2H), 3,40 (т, J =4,8 МГц, 2H)
[00327] Получение соединения 2m
[00328] После того, как соединение 2l (1 г, 4,20 ммоль) растворяли в ацетонитриле при комнатной температуре в атмосфере азота, к полученной смеси добавляли N-Boc-гидроксиламин (643 мг, 4,82 ммоль) и DBU (0,659 мл, 4,41 ммоль) и смесь перемешивали при 60°С в течение 13 часов. После завершения реакции к смеси добавляли MC (300 мл) и дистиллированную воду (300 мл) для экстрагирования органического слоя и экстрагированный органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2m (748 мг, 70%).
[00329] 1H ЯМР (400 МГц, CDCl3) δ 7,55 (с, 1H), 4,05-4,03 (м, 2H), 3,76-3,74 (м, 2H), 3,74-3,69 (м, 6H), 3,42 (т, J =4,8 МГц, 2H), 1,49 (с, 9H). EI-MS m/z: 291(M+)
[00330] Получение соединения 2n
[00331] После того, как соединение 2m (200 мг, 0,688 ммоль) растворяли в метаноле (5 мл), к полученной смеси добавляли Pd/C(10%) (70 мг) и перемешивали в атмосфере водорода в течение 3 часов. После завершения реакции смесь фильтровали через целит и концентрировали при пониженном давлении, с получением Соединения 2n (180 мг, 98%).
[00332] 1H ЯМР (400 МГц, CDCl3) δ 4,04-4,01 (м, 2H), 3,74-3,62 (м, 7H), 3,55 (т, J =5,2 МГц, 1H), 2,88 (т, J =5,2 МГц, 1H), 2,81 (т, J =5,2 МГц, 1H), 1,64 (с, 2H), 1,48 (с, 9H). EI-MS m/z: 265(M+)
[00333] Получение соединения 2g
[00334] После того, как соединение 2f (1,34 г, 1,066 ммоль) и Соединение 2n (384 мг, 1,28 ммоль) растворяли в DMF (10 мл) при 0°С в атмосфере азота, к полученной смеси добавляли DIPEA (464 мкл, 2,665 ммоль) и PyBOP (832 мг, 1,599 ммоль) и перемешивали при комнатной температуре в течение 4 часов. После завершения реакции к смеси добавляли этилацетат (200 мл) и дистиллированную воду (300 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2g (1,2 г, 75%).
[00335] EI-MS m/z: 1503(M+)
[00336] Получение соединения 2h
[00337] После того, как соединение 2g (530 мг, 0,352 ммоль) растворяли в метаноле (10 мл) при -10°С в атмосфере азота, к полученной смеси медленно добавляли LiOH (147 мг, 7,98 ммоль) в воде (8 мл) и перемешивали в течение 1 часа. После завершения реакции к смеси добавляли хлороформ (200 мл) и дистиллированную воду (30 мл, pH 2). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 2h (260 мг, 45%).
[00338] EI-MS m/z: 1349(M+)
[00339] Получение соединения 2i
[00340] После того, как соединение 2h (260 мг, 0,192 ммоль) растворяли в метиленхлориде (4 мл) и воде (2 мл) при 0°С в атмосфере азота, к полученной смеси добавляли 4M-HCl (в диоксане, 4 мл) и перемешивали при 0°С в течение 1 часа. После завершения реакции полученную смесь концентрировали при пониженном давлении с получением Соединения 2i (210 мг, 85%).
[00341] EI-MS m/z: 1249(M+)
[00342] Получение соединения 3k
[00343] После того, как 2-бромэтанол (1,92 мл, 27,037 ммоль) растворяли в ацетонитриле (15 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли Boc-гидроксиламин (3,0 г, 22,531 ммоль) и DBU (3,7 мл, 24,8 ммоль) и смесь перемешивали при 40°С в течение 24 часов. После завершения реакции к смеси добавляли этилацетат (100 мл) и дистиллированную воду (100 мл) для экстрагирования органического слоя и экстрагированный органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 3k (2,75 г, 69%).
[00344] 1H ЯМР (400 МГц, CDCl3) δ 7,28 (с, 1H), 3,93-3,91 (м, 2H), 3,76-3,74 (м, 2H), 1,50 (с, 9H).
[00345] Получение соединения 3l
[00346] После того, как соединение 3k (2,75 г, 15,697 ммоль) растворяли в THF (30 мл) при 0°С в атмосфере азота, к полученной смеси добавляли TEA (3,3 мл, 23,518 ммоль) и Ms2O (3,28 г, 18,814 ммоль) и смесь перемешивали при комнатной температуре в течение 4 часов. После завершения реакции к смеси добавляли этилацетат (200 мл) и дистиллированную воду (100 мл) для экстрагирования органического слоя и экстрагированный органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении, с получением Соединения 3l (3,83 г, 96%).
[00347] 1H ЯМР (400 МГц, CDCl3) δ 7,37 (с, 1H), 4,48-4,46 (м, 2H), 4,13-4,09 (м, 2H), 3,11 (с, 3H), 1,50(с, 9H).
[00348] Получение соединения 3m
[00349] После того, как соединение 3l (3,83 г, 15,00 ммоль) растворяли в DMF (20 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли NaN3 (1,95 г, 30,00 ммоль) и смесь перемешивали при 60°С в течение 13 часов. После завершения реакции к смеси добавляли этилацетат (300 мл) и дистиллированную воду (300 мл) для экстрагирования органического слоя и экстрагированный органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 3m (2,02 г, 67%).
[00350] 1H ЯМР (400 МГц, CDCl3) δ 7,22-7,20 (м, 1H), 4,05-4,02 (м, 2H), 3,51-3,48 (м, 2H), 1,50(с, 9H).
[00351] Получение соединения 3n
[00352] После того, как соединение 3m (2,02 г, 9,98 ммоль) растворяли в метаноле (30 мл), к полученной смеси добавляли Pd/C (10%) (1,0 г) и 4M HCl в диоксане (2,5 мл) и перемешивали в атмосфере водорода в течение 3 часов. После завершения реакции смесь фильтровали через целит и концентрировали при пониженном давлении, с получением Соединения 3n (1,98 г, 93%).
[00353] 1H ЯМР (400 МГц, CDCl3) δ 10,26 (с, 1H), 8,05 (с, 3H), 3,91-3,88 (м, 2H), 3,1-2,98 (м, 2H), 1,44(с, 9H).
[00354] Получение соединения 3g
[00355] После того, как соединение 2f (280 мг, 0,222 ммоль) и Соединение 3n (56 мг, 0,266 ммоль) растворяли в DMF (5 мл) при 0°С в атмосфере азота, к полученной смеси добавляли DIPEA (58 мкл, 0,334 ммоль) и PyBOP (174 мг, 0,334 ммоль) и перемешивали при комнатной температуре в течение 4 часов. После завершения реакции к смеси добавляли этилацетат (100 мл) и дистиллированную воду (150 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 3g (221 мг, 69%).
[00356] EI-MS m/z: 1415(M+)
[00357] Получение соединения 3h
[00358] После того, как соединение 3g (150 мг, 0,106 ммоль) растворяли в метаноле (2 мл) при -10°С в атмосфере азота, к полученной смеси медленно добавляли LiOH (40 мг, 0,954 ммоль) в воде (2 мл) и перемешивали в течение 1 часа. После завершения реакции к смеси добавляли хлороформ (150 мл) и дистиллированную воду (30 мл, pH 2). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 3h (94 мг, 71%).
[00359] EI-MS m/z: 1261(M+)
[00360] Получение соединения 3i
[00361] После того, как соединение 3h (90 мг, 0,071 ммоль) растворяли в метиленхлориде (1 мл) при 0°С в атмосфере азота, к полученной смеси добавляли трифторуксусную кислоту (TFA, 0,2 мл) и перемешивали при 0°С в течение 3 часов. После завершения реакции полученную смесь очищали с использованием препаративной ВЭЖХ, с получением Соединения 3i (47 мг, 52%).
[00362] EI-MS m/z: 1161(M+)
[00363]
[00364] [Пример 4] Получение соединения 4i
[00365]
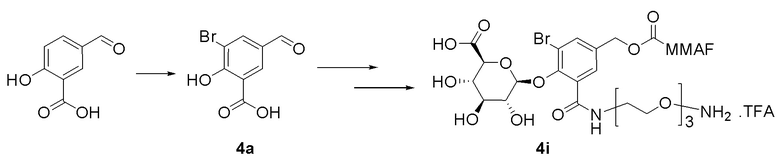
[00366] Получение 3-бром-5-формилсалициловой кислоты (Соединение 4a)
[00367] После того, как 5-формилсалициловую кислоту (1 г, 6,019 ммоль) растворяли в DMF при 0°С в атмосфере азота, к полученной смеси добавляли N-бромсукцинимид (1,07 г, 6,109 ммоль) и смесь перемешивали при 70°С в течение 3 часов. После завершения реакции к смеси добавляли этилацетат (100 мл), 2N-HCl водный раствор (2 мл) и дистиллированную воду (100 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 4a (1,2 г, 84%).
[00368] 1H ЯМР (400 Гц, DMSO-d6) δ 9,64 (с, 1H), 8,19 (д, J=2,4 МГц, 1H), 8,00 (д, J=2,0 МГц, 1H), 3,16 (с, 1H)
[00369]
[00370] Соединение 4i получали с использованием полученной 3-бром-5-формилсалициловой кислоты (Соединение 4a) способом, подобным способам получения Соединений 2i и 3i Примеров 2 и 3.
[00371] EI-MS m/z: 1328(M+)
[00372]
[00373] [Примеры 5-7] Получение LCB14-0648, LCB14-0664 и LCB14-0663
[00374]

[00375]
[00376] Соединение C получали способом, раскрытым в выложенной публикации корейского патента № 10-2014-0035393.
[00377]
[00378] Получение LCB14-0648 (Пример 5)
[00379]После того, как соединение 2i (20 мг, 0,014 ммоль) растворяли в этаноле (0,7 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли Соединение C (3,7 мг, 0,017 ммоль) и смесь перемешивали при 45°С в течение 2 часов. После завершения реакции получали LCB14-0648 (10,2 мг, 49%) с использованием препаративной ВЭЖХ.
[00380] EI-MS m/z: 1441(M+)
[00381] LCB14-0663 (Пример 6) и LCB14-0664 (Пример 7) получали способом, подобным способу получения LCB14-0648 (Пример 5).
[00382] EI-MS of LCB14-0663: m/z: 1520(M+)
[00383] EI-MS of LCB14-0664: m/z: 1353(M+)
[00384]
[00385] [Сравнительный пример 1] Получение соединения 5k
[00386]

[00387] Получение соединения 5a
[00388] После того, как этил 4-бромбутаноат (5,0 мл, 34,604 ммоль) растворяли в MeOH (75 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли азид натрия (4,5 г, 69,209 ммоль) в воде (25 мл) и перемешивали при 85°С в течение 8 часов. После завершения реакции растворитель концентрировали при пониженном давлении и к смеси добавляли хлороформ (300 мл) и дистиллированную воду (200 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5a (5,1 г, 94%).
[00389] 1H ЯМР (600 Гц, CDCl3) δ 4,15 (кв., J =7,2 МГц, 2H), 3,36 (т, J =7,2 МГц, 2H), 2,41 (т, J =7,2 МГц, 2H), 1,94-1,89 (м, 2H), 1,28 (т, J =8,4 МГц, 3H).
[00390] Получение соединения 5b
[00391] После того, как соединение 5a (2,0 г, 12,725 ммоль) растворяли в MeOH (32 мл) при 0°С в атмосфере азота, к полученной смеси медленно добавляли KOH (3,56 г, 63,625 ммоль) в воде (26 мл) и перемешивали при комнатной температуре в течение 6 часов. После завершения реакции растворитель концентрировали при пониженном давлении и к смеси добавляли хлороформ (300 мл), 1N раствор HCl (100 мл) и дистиллированную воду (100 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5b (1,28 г, 78%).
[00392] 1H ЯМР (600 Гц, CDCl3) δ 3,38 (т, J =7,2 МГц, 2H), 2,48 (т, J =7,2 МГц, 2H), 1,95-1,90 (м, 2H).
[00393] Получение соединения 5c
[00394] После того, как соединение 5b (850 мг, 6,580 ммоль) растворяли в MeOH (10 мл) при 0°С в атмосфере азота, к полученной смеси добавляли оксалилхлорид (1,1 мл, 13,160 ммоль) и DMF (1 каплю) и перемешивали при комнатной температуре в течение 6 часов. После завершения реакции растворитель концентрировали при пониженном давлении с получением, таким образом, Соединения 5c (965 мг, Qu), соответствующего неочищенному продукту, и его использовали в следующей реакции без очистки.
[00395] Получение соединения 5d
[00396] После того, как 4-гидрокси-3-нитробензойную кислоту (5 г, 27,304 ммоль) растворяли в THF (120 мл) при 0°С в атмосфере азота, к полученной смеси добавляли 1M BH3-THF комплекс (54,6 мл, 54,6 ммоль) и перемешивали при комнатной температуре в течение 20 часов. После завершения реакции к смеси добавляли этилацетат (200 мл), 0,5N раствор HCl (20 мл) и дистиллированную воду (100 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5d (4,20 г, 91%).
[00397] 1H ЯМР (600 Гц, CD3OD) δ 8,06 (д, J =1,2 МГц, 1H), 7,59 (дд, J=1,2, 7,8 МГц, 1H), 7,12 (д, J=8,4 МГц, 1H), 4,83 (с, 2H)
[00398] Получение соединения 5e
[00399] После того, как соединение 5d (937 мг, 5,539 ммоль) растворяли в ацетонитриле (15 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли Соединение 5c (2,0 г, 5,035 ммоль), оксид серебра (4,66 г, 20,108 ммоль) и молекулярные сита (2,0 г) и перемешивали при комнатной температуре в течение 14 часов. После завершения реакции смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5e (1,0 г, 40%).
[00400] 1H ЯМР (600 Гц, CDCl3) δ 7,81 (д, J =1,8 МГц, 1H), 7,54 (дд, J=1,8, 6,6 МГц, 1H), 7,37 (д, J=8,4 МГц, 1H), 5,37-5,27 (м, 3H), 5,20 (д, J=6,6 МГц, 1H), 4,72 (д, J =6,0 МГц, 2H), 4,21 (д, J =9,0 МГц, 1H), 3,75 (с, 3H), 2,12 (с, 3H), 2,06 (с, 3H), 2,05 (с, 3H), 2,04-2,02 (м, 1H).
[00401] Получение соединения 5f
[00402] После того, как соединение 5e (900 мг, 6,35 ммоль) растворяли в этилацетате (100 мл), к полученной смеси добавляли оксид платины (IV) (84,2 мг, 0,370 ммоль) и перемешивали при комнатной температуре в атмосфере водорода в течение 3 часов. После завершения реакции смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении, с получением, таким образом, Соединения 5f (700 мг, 83%), соответствующего неочищенному продукту, и его использовали в следующей реакции без очистки.
[00403] Получение соединения 5g
[00404] После того, как соединение 5f (350 мг, 0,768 ммоль) растворяли в MC (10 мл) при 0°С в атмосфере азота, к полученной смеси добавляли Соединение 5c (136 мг, 0,921 ммоль) и DIPEA (268 мкл, 1,536 ммоль) и перемешивали при комнатной температуре в течение 20 минут. После завершения реакции к смеси добавляли этилацетат (50 мл) и дистиллированную воду (50 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5g (280 мг, 65%).
[00405] 1H ЯМР (600 Гц, CDCl3) δ 8,37 (д, J =1,2 МГц, 1H), 8,00 (с, 1H), 7,07 (дд, J=1,8, 6,6 МГц, 1H), 6,93 (д, J=8,4 МГц, 1H), 5,43-5,28 (м, 3H), 5,06 (д, J=7,8 МГц, 1H), 4,63 (с, 2H), 4,19 (д, J =9,6 МГц, 1H), 3,76 (с, 3H), 3,44-3,41 (м, 2H), 2,56 (т, J =7,8 МГц, 2H), 2,17-2,00 (м, 12H). EI-MS m/z: 567(M+)
[00406] Получение соединения 5h
[00407] После того, как соединение 5g (250 мг, 0,441 ммоль) растворяли в DMF (4 мл) при 0°С в атмосфере азота, к полученной смеси добавляли бис(4-нитрофенил)карбонат (270 мг, 0,882 ммоль) и DIPEA (115 мкл, 0,661 ммоль) и перемешивали при комнатной температуре в течение 1 часа. После завершения реакции к смеси добавляли этилацетат (50 мл) и дистиллированную воду (50 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5h (290 мг, 90%).
[00408] 1H ЯМР (600 Гц, CDCl3) δ 8,54 (д, J =1,8 МГц, 1H), 8,28-8,25 (м, 2H), 8,02 (с, 1H), 7,40-7,36 (м, 2H), 7,11 (дд, J=1,8, 6,6 МГц, 1H), 6,96 (д, J=8,4 МГц, 1H), 5,44-5,29 (м, 3H), 5,23 (с, 2H), 5,10 (д, J=7,8 МГц, 1H), 4,21 (д, J =9,6 МГц, 1H), 3,76 (с, 3H), 3,45-3,42 (м, 2H), 2,58 (т, J =7,2 МГц, 2H), 2,11-2,00 (м, 12H). EI-MS m/z: 732(M+)
[00409] Получение соединения 5i
[00410] После того, как соединение 5h (250 мг, 0,341 ммоль) растворяли в DMF (4 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли MMAF-OMe (255 мг, 0,341 ммоль) и затем полученную смесь обрабатывали при помощи HOBT (9 мг, 0,068 ммоль), пиридина (1,2 мл) и DIPEA (60 мкл, 0,341 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 2 дней. После завершения реакции к смеси добавляли этилацетат (50 мл), 2N раствор HCl (5 мл) и дистиллированную воду (50 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5i (340 мг, 74%).
[00411] EI-MS m/z: 1339(M+)
[00412] Получение соединения 5j
[00413] После того, как соединение 5i (210 мг, 0,156 ммоль) растворяли в метаноле (2 мл) при 0°С в атмосфере азота, к полученной смеси добавляли LiOH⋅H2O (66 мг, 1,560 ммоль) в воде (2 мл). Полученную смесь перемешивали при комнатной температуре в течение 1,5 часа. После завершения реакции к смеси добавляли хлороформ (50 мл), метанол (5 мл), дистиллированную воду (50 мл) и 0,5N раствор HCl (5 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5j (107 мг, 57%).
[00414] EI-MS m/z: 1184(M+)
[00415] Получение соединения 5k
[00416] После того, как соединение 5j (10 мг, 0,008 ммоль) и фенилацетилен (0,92 мкл, 0,008 ммоль) растворяли в этаноле (150 мкл) и воде (10 мкл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли водный раствор 0,1M CuSO4 (10 мкл) и водный раствор 1,0M аскорбата натрия (10 мкл). Полученную смесь перемешивали при комнатной температуре в течение 5 часов. После завершения реакции к смеси добавляли этилацетат (10 мл) и дистиллированную воду (5 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 5k (5 мг, 46%).
[00417] EI-MS m/z: 1286(M+)
[00418]
[00419] [Пример 8] Получение соединения 6e
[00420]
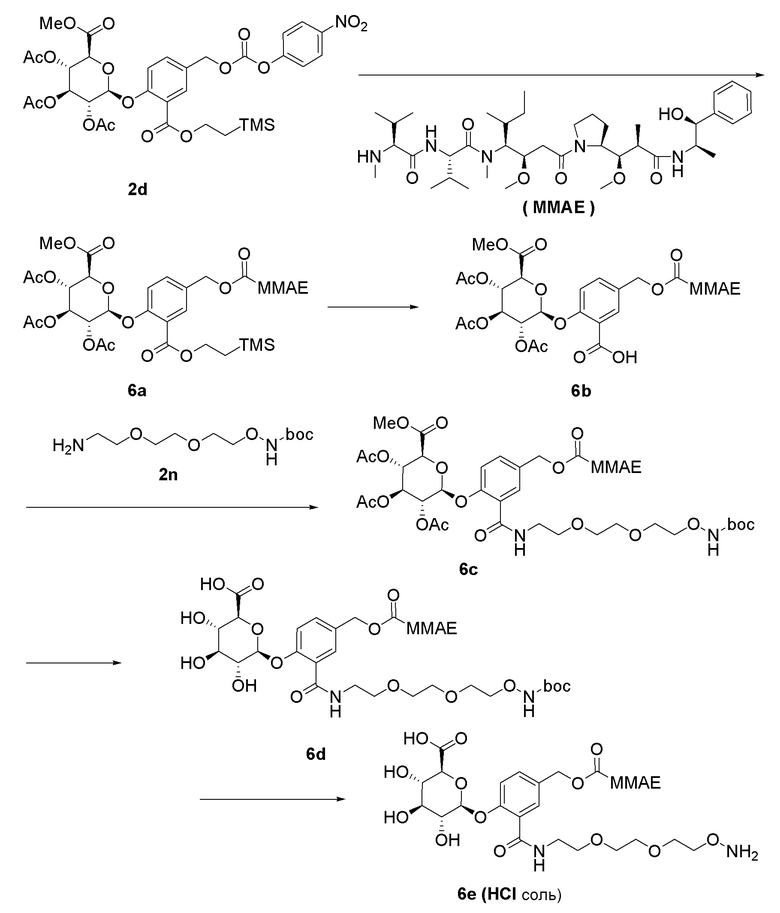
[00421] Получение соединения 6a
[00422] После того, как соединение 2d (229 мг, 0,30 ммоль) растворяли в DMF (2 мл) при комнатной температуре в атмосфере азота, к полученной смеси добавляли MMAE (1,34 г, 1,80 ммоль) и затем полученную смесь обрабатывали при помощи HOBT (8,2 мг, 0,06 ммоль), пиридина (0,8 мл) и DIPEA (56 мкл, 0,29 ммоль). Смесь перемешивали при комнатной температуре в течение 12 часов. После завершения реакции к смеси добавляли этилацетат (100 мл) и дистиллированную воду (100 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 6a (239 мг, 65%).
[00423] EI-MS m/z: 1328(M+)
[00424] Получение соединения 6b
[00425] После того, как соединение 6a (239 мг, 0,18 ммоль) растворяли в THF (5 мл) при 0°С в атмосфере азота, к полученной смеси добавляли тетрабутиламмонийфторид (1M в THF) (540 мкл, 2,50,58 моль) и перемешивали при комнатной температуре в течение 3 часов. После завершения реакции к смеси добавляли метиленхлорид (100 мл) и дистиллированную воду (100 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 6b (212 мг, 95%).
[00426] EI-MS m/z: 1228(M+)
[00427] Получение соединения 6c
[00428] После того, как соединение 6b (200 мг, 0,16 ммоль) и Соединение 2n (51 мг, 0,19 ммоль) растворяли в DMF (4 мл) при 0°С в атмосфере азота, к полученной смеси добавляли DIPEA (42 мкл, 0,32 ммоль) и PyBOP (126 мг, 0,24 ммоль) и перемешивали при комнатной температуре в течение 4 часов. После завершения реакции к смеси добавляли этилацетат (100 мл) и дистиллированную воду (100 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток подвергали колоночной хроматографии с получением Соединения 6c (142 мг, 60%).
[00429] EI-MS m/z: 1474(M+)
[00430] Получение соединения 6d
[00431] После того, как соединение 6c (142 мг, 0,09 ммоль) растворяли в метаноле (2 мл) при -20°С в атмосфере азота, к полученной смеси медленно добавляли LiOH (36 мг, 0,86 ммоль) в воде (2 мл) и перемешивали при 0°С в течение 1 часа. После завершения реакции к смеси добавляли хлороформ (100 мл), дистиллированную воду (50 мл) и водный раствор 2N-HCl (2 мл). Органический слой, полученный как описано выше, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток (6d, 128 мг, 99%) использовали в следующей реакции без очистки.
[00432] EI-MS m/z: 1334(M+)
[00433] Получение соединения 6e
[00434] После того, как соединение 6d (105 мг, 0,08 ммоль) растворяли в метиленхлориде (3 мл) при -20°С в атмосфере азота, к полученной смеси добавляли 4M-HCl (в диоксане, 1 мл) и перемешивали при 0°С в течение 1 часа. После завершения реакции полученную смесь концентрировали при пониженном давлении. Остаток очищали с использованием препаративной ВЭЖХ, с получением Соединения 6e (47 мг, 46%).
[00435] EI-MS m/z: 1234(M+)
[00436]
[00437] [Экспериментальный Пример 1] Сравнительное испытание респонсивности в отношении β-Глюкуронидазы
[00438] Для сравнения респонсивности соединения 1k Примера 1 и Соединения 5k Сравнительного примера 1 к действию β-глюкуронидазы осуществляли сравнительное испытание, как описано ниже.
[00439] Соединение 1k Примера 1 и Соединение 5k Сравнительного примера 1 каждое получали в виде исходных растворов в DMSO 500 мкМ и 50 мкМ. Получали реакционные растворы, в которых 880 мкл фосфатно-солевого буферного раствора (PBS) и 100 мкл исходных растворов Соединения 1k и Соединения 5k смешивали друг с другом, соответственно (их конечные концентрации были 50 мкМ и 5 мкМ, соответственно). После того, как 20 мкл фермента β-глюкуронидазы E. coli (1 мг/мл, Sigma: E.C.3.2.1.31 Type IX-A; 1 мг/ мл в PBS; 3,6 мкг, 13 мкмоль) добавляли к реакционным растворам, реакции инициировали на водяной бане с постоянной температурой 37°С. 100 мкл смешанных растворов отбирали в точках времени 0 мин, 25 мин, 60мин и 90 мин, соответственно, и к ним добавляли 200 мкл ацетонитрила. Осуществляли количественный анализ MMAF, высвобождаемого из каждого из супернатантов, полученного путем осуществления центрифугирования (4°С, 15 мин, 14000 об/мин) образцов смеси, с использованием ЖХ-МС/МС (эксперимент осуществляли способом, подобным способу, раскрытому в US2012-0107332).
[00440] Результаты испытания проиллюстрированы на Фиг. 2, и было подтверждено на основании Фиг. 2, что MMAF существенно быстро высвобождался из каждого Соединения 1k Примера 1 и Соединения 5k Сравнительного примера 1 через реакцию 1,6-элиминирования после ферментативных реакций под действием β-глюкуронидазы (Ref. US2112-0107332).
[00441]
[00442] [Экспериментальный Пример 2] Сравнительное испытание стабильности в плазме
[00443] Для сравнения стабильности в плазме соединения 1k Примера 1 и Соединение 5k Сравнительного примера 1 у мыши осуществляли сравнительное испытание, как описано ниже.
[00444] 10 мкл растворов каждого из соединений 1k и 5k, растворенных в DMSO при 5 мМ, смешивали с 990 мкл не содержащей соединений плазмы, с получением, таким образом, 50 мкМ образцов для подтверждения стабильности в плазме. Осуществляли взаимодействие растворов плазмы, смешанных с соединениями, при 37°С в течение 6 дней. В процессе реакции в течение 6 дней 100 мкл растворов подразделяли в каждой точке времени (0, 1, 2, 3 и 6 дней) и смешивали с 200 мкл ацетонитрила, содержащего внутренний стандарт, для осаждения плазменного белка после завершения реакции. Осуществляли количественный анализ супернатантов, полученных путем осуществления центрифугирования (4°С, 15 мин, 14000 об/мин) образцов смеси, с использованием ЖХ-МС/МС (эксперимент осуществляли способом, подобным способу, раскрытому в Journal of Chromatography B, 780 (2002) 451-457).
[00445] Результат, полученный путем подтверждения содержания каждого Соединения 1k Примера 1 и Соединения 5k Сравнительного примера 1 с использованием ЖХ-МС/МС, проиллюстрирован на Фиг. 3 и в Таблице 1, и, как результат, стабильность соединения 5k Сравнительного примера 1 и стабильность Соединения 1k Примера 1 была 14% и 80% через 1 день, соответственно, таким образом, стабильность соединения 1k Примера 1 в плазме мыши была существенно лучше по сравнению с Соединением 5k Сравнительного примера 1.
[00446]
(у мыши)
(@7дней)
(@1день)
[00447]
[00448] [Экспериментальный Пример 3] Испытание стабильности в плазме
[00449] Для подтверждения стабильности в различных плазмах с использованием LCB14-0648 (Пример 5), LCB14-0664 (Пример 6) и LCB14-0663 (Пример 7), которые представляют собой соединения, полученные в Примерах 5-7, испытание стабильности в плазме осуществляли таким же способом, как в Экспериментальном Примере 2, и результаты проиллюстрированы на Фиг. 4-6.
[00450] Было подтверждено, что LCB14-0648 (Пример 5), LCB14-0664 (Пример 6) и LCB14-0663 (Пример 7), которые представляют собой соединения, полученные в Примерах 5-7, все были стабильными в плазме мыши, крысы, собаки и человека вплоть до 7 дней.
[00451]
[00452] Примеры 9-11: Получение конъюгата антитела с лекарственным средством (ADC)
[00453] [Пример 9] Получение Герцептин (LC)-Глюкуронид Линкер-MMAF (далее указан как ʹLCB14-0109ʹ или ʹADC109ʹ)
[00454]
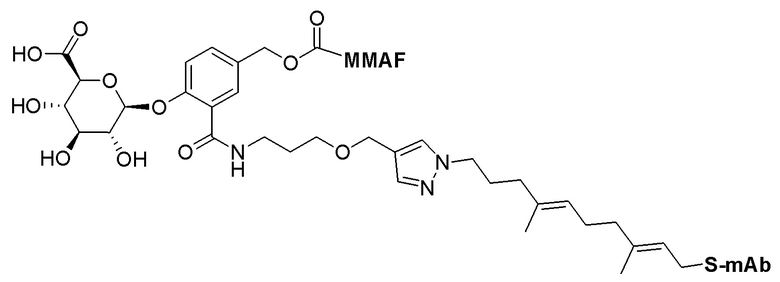
[00455] LCB14-0109 получали аналогично получению LCB14-0105 с использованием способа, раскрытого в US2012/0308584.
[00456]
[00457] [Пример 10] Получение Герцептин (LC)-Глюкуронид Линкер-MMAF (далее указан как ʹLCB14-0110ʹ или ʹADC110ʹ) (Фиг. 7)
[00458]

[00459] LCB14-0606 получали способом, раскрытым в выложенной публикации корейского патента №10-2014-0035393.
[00460]
[00461] Стадия 1 (Пренилированное Антитело, D) Получение субстрата (D), раскрытого в US2012/0308584
[00462] Получали реакционную смесь антитела для пренилирования и осуществляли взаимодействие при 30°С в течение 12 часов. Реакционная смесь состояла из буферного раствора (50 мМ Tris-HCl (pH7,4), 5 мМ MgCl2, 10 мкМ ZnCl2, 5 мМ DTT), содержащего 24 мкМ антитела, 200 нМ FTазы (Calbiochem #344145) и 1 мМ LCB14-0606 (внутрифирменный, US2012/0308584). После завершения реакции пренилированное антитело очищали на колонке с Сефарозой G25 на AKTA очистителе (GE healthcare), которую уравновешивали буферным раствором PBS. Пренилированное антитело (конечная концентрация: 12 мкМ) обрабатывали при помощи 1 мМ CuSO4 и осуществляли взаимодействие при 30°С в течение 3 часов для повторного окисления. После завершения реакции к этой смеси добавляли 2 мМ (конечная концентрация) EDTA и выдерживали при 30°С в течение 30 минут при слабом перемешивании. Для удаления избыточного количества малых молекул, используемых в реакции, полученную смесь очищали при помощи FPLC.
[00463]
[00464] Стадия 2 (Способ получения LCB14-0110)
[00465] Смесь для реакции образования оксимной связи между пренилированным антителом (A) и токсином (3l) получали путем смешивания 100 мМ Na-ацетатного буфера (pH 4,5, 10% DMSO), 12 мкМ антитела и 360 мкМ LCB14-0645 (внутрифирменный) и слабого перемешивания при 30°С. После осуществления реакции в течение 24 часов осуществляли FPLC (AKTA очиститель, GE healthcare) для удаления избыточного количества малых молекул, используемых в реакции, так, чтобы удалить избыточное количество малых молекул, и фракцию, содержащую белок, собирали для концентрирования.
[00466]
[00467] [Пример 11] Получение Герцептин (LC)-Глюкуронид Линкер-MMAE (далее указан как ʹLCB14-0113ʹ или ʹADC113ʹ)
[00468]
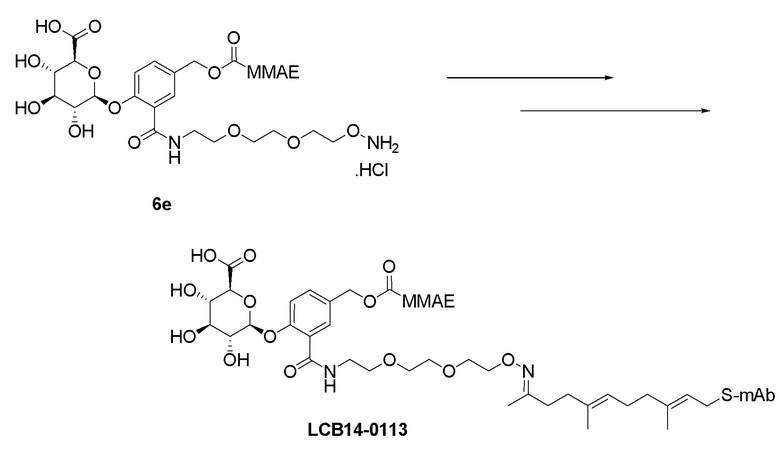
[00469] LCB14-0113 (ADC113) получали с использованием полученного Соединения 6e способом, аналогичным способу получения Примера 10.
[00470]
[00471] [Экспериментальный Пример 4] Испытание стабильности ADC в плазме
[00472] На основании того, что LCB-SI (Соединение 1k Примера 1) был более стабильным в плазме по сравнению с SG-SI (Соединение 5k Сравнительного примера 1), как результат модельного исследования с использованием Соединения 1k Примера 1 и Соединения 5k Сравнительного примера 1 в Экспериментальном Примере 2, результаты стабильности ADC(s) (LCB14-0109 (ADC109), полученный в Примере 9, и LCB14-0110 (ADC110), полученный в Примере 10), полученные путем связывания антитела и лекарственного средства, сравнивали друг с другом.
[00473] Стабильность в плазме ADC(s) (LCB14-0109 (ADC109) полученный в Примере 9, и LCB14-0110 (ADC110) полученный в Примере 10), полученных как описано выше, оценивали следующим способом, и результаты проиллюстрированы на Фиг. 8 и 9.
[00474]
[00475] (Метод испытания стабильности ADC в плазме)
[00476] ADC получали при концентрации 0,5 мг/мл (MMAF концентрация: 6,8 мкМ) в не содержащей соединений плазме и инкубировали при 37°С. Отбирали 50 мкл аликвоту образца в дни 0, 1, 2 и 7 и хранили при -70°С до анализа. Измеряли количество токсина (свободный ММAF), высвобождаемого из образца, определяя таким образом стабильность ADC в плазме.
[00477]
[00478] (Анализ стабильности с использованием ЖХ-МС/МС)
[00479] 20 мМ исходный раствор ММAF получали с использованием DMSO и стандартные растворы 0,02, 0,04, 0,2, 0,4, 2, 4, 20, 40 и 80 мкМ ММAF получали путем разбавления исходного раствора ММAF ацетонитрилом. Каждый из стандартных растворов ММAF разбавляли 20-кратно не содержащей соединений плазмой, чтобы, таким образом, использовать в качестве образца для калибровочной кривой.
[00480] 100 мкл ацетонитрила, содержащего внутренний стандарт (0,2 мкМ ММAE), добавляли и смешивали с 50 мкл образца для калибровочной кривой и определения стабильности, с последующим центрифугированием. 80 мкл супернатанта экстрагировали и смешивали с подвижной фазой A (80 мкл) и смесь анализировали с использованием ЖХ-МС/МС. Использовали 1200 ВЭЖХ (Agilent Technologies), API4000 (AB SCIEX) и Analyst программу (Version 1.6.1) для ЖХ-МС/МС анализа. 5мкл образца вводили в ODP2 HP-2D (2×150мм, 5мкм, Shodex) колонку и разделяли с использованием композиции 1 мМ формиата аммония (подвижная фаза A, 40%) и 90% ацетонитрила в 0,1% мурвьиной кислоте (подвижная фаза B, 60%). ММAF измеряли в ESI+ режиме при m/z 732,6/170,1 (родительский/дочерний ион).
[00481]
[00482] В ADC, полученном в Примере 9 настоящего изобретения, LCB14-0109 (ADC109), количество свободного ММAF было меньше чем 0,5%, даже через 7 дней, таким образом, был получен существенно стабильный экспериментальный результат. Кроме того, должно быть понятно, что время полужизни ADC, полученного в Примере 10 настоящего изобретения, LCB14-0110 (ADC110), было 7 дней или больше (в плазме мыши, крысы, собаки и человека), таким образом, LCB14-0110 (ADC110) был существенно стабильным.
[00483]
[00484] [Экспериментальный Пример 5] Анализ анти-пролиферационной активности ADC
[00485] Измеряли антипролиферационные активности антител, лекарственного средства и ADC(s), проиллюстрированные ниже в Таблице 2, в отношении раковых клеточных линий.
[00436] В качестве раковых клеточных линий использовали коммерционализированные клеточные линии рака молочной железы человека MCF-7 (HER2-отрицательная или -нормальная) и SK-Br3 (HER2-положительная) и коммерционализированные клеточных линий рака яичников SK-OV3 (HER2-положительные). В качестве лекарственного средства использовали ММAF. В качестве антитела использовали коммерционализированный Герцептин-G7-CVIM (LC) и Герцептин-G7-CVIM(HC). В качестве ADC использовали LCB14-0109 (ADC109) Примера 8 и LCB14-0110 (ADC110) Примера 9.
[00487] После того, как каждую из раковых клеточных линий высевали в 96-луночный планшет при 10000 клеток/лунка и культивировали в течение 24 часов, антитело и ADC обрабатывали при концентрации 0,01563~2мкг/мл (2-кратное серийное разведение) и лекарственное средство обрабатывали при концентрации 4~500нМ (2-кратное серийное разведение). Через 72 часа количество живых клеток определяли с использованием Сульфородаминового B (SRB) красителя.
[00488]
SK-OV3
[00489] Можно утверждать, что эффективность LCB14-0109 (ADC109) и LCB14-0110(ADC110), соответствующих конъюгатам антитела с лекарственным препаратом, эффективность в SK-Br3 была равной или больше чем в 10 раз активности антитела, таким образом, эффективность ADC(s) была намного лучше, чем активность антитела как такового.
[00490]
[00491] [Экспериментальный Пример 6] Оценка эффективности in vivo
[00492] Оценка in vivo противоопухолевой эффективности LCB14-0109 (ADC109) и LCB14-0110 (ADC110)
[00493] Эффективность лекарственного средства в зависимости от введения одной дозы или нескольких доз оценивали с использованием ортотопической модели.
[00494] Клеточную линию карциномы молочной железы человека BT-474 закупали у Korea Cell Line Bank и культивировали с использованием RPMI 1640 (10% FBS, 1% пенициллина/стрептомицина) в инкубаторе (37°С, 5% CO2), в котором поддерживали постоянную температуру и влажность. В качестве экспериментальных животных использовали самок Balb/c-nu мышей (6-недельного возраста), которых закупали у Japan SLC, и после периода акклиматизации в течение 1 недели вводили подкожно пеллету 17b-эстрадиола (1,72 мг/пеллета, Innovative Research of America, Sarasota, FL). Через 6 дней BT474 клетки (5×106 клеток в 100 мкл) подходящим образом смешивали с 50% PBS/50% Matrigel без фенолового красного (Becton Dickinson Bioscience) и вводили путем инъекции во второе жировое тело молочной железы, создавая, таким образом, ортотопические модели. Размер опухоли измеряли два раза в неделю и объем рассчитывали по формуле 1/2 [длина (мм)] × [ширина (мм)]2. Мышей разделяли на группы так, чтобы средний объем опухоли в каждой группе был 100 мм3, через 3 недели после инъекции клеток и затем использовали в эксперименте. Закупали и использовали Герцептин от компании-изготовителя Roche, и различные ADCs были получены авторами настоящего изобретения, и их вводили один раз в неделю или один раз экспериментальным животным через латеральную хвостовую вену.
[00495]
[00496] 1) Наблюдаемый объем опухоли в зависимости от BT474 ортотопической модели опухоли молочной железы-QW дозы (QW=один раз в неделю)
[00497] Использовали в общей сложности 5 групп животных, то есть группу введения растворителя, группу введения Герцептина (5 мг/кг) и группы введения ADC109 (0,1, 1, 5 мг/кг), и использовали по 11 мышей на группу. Лекарственное средство вводили один раз в неделю в общей сложности три раза через хвостовую вену, и, как результат, в группе введения герцептина (5 мг/кг) рост опухоли частично ингибировался вплоть до конечной временной точки эксперимента. Этот результат был аналогичным результату в группе введения ADC109 (1 мг/кг). Наоборот, в группе введения ADC109 (5 мг/кг) ингибирование опухолевого роста начиналось через 4 дня после первого введения, и регрессию опухоли наблюдали в течение экспериментального периода, составляющего 2 недели (Фиг. 10).
[00498]
[00499] 2) Наблюдаемое изменение массы тела в зависимости от LCB14-0109 (ADC109) дозы в ортотопической модели BT474 рака молочной железы
[00500] Лекарственное средство вводили таким же способом, как в 1), и наблюдали изменение массы тела в зависимости от дозы ADC109. Как результат, в течение всего экспериментального периода изменение массы тела не наблюдали, и результат проиллюстрирован ниже в Таблице 3.
[00501]
Изменение массы тела
[00502]
[00503] 3) Оценка эффективности в зависимости от мультидозового введения
[00504] Осуществляли эксперимент для оценки эффективности лекарственного средства Герцептина, ADC109 и ADC110 в ортотопической модели рецептор эпидермального фактора роста человека 2 (Her2)-положительного рака молочной железы человека в зависимости от мульти-дозового введение. Использовали в общей сложности 4 группы животных, то есть группу введения растворителя, группу введения Герцептина (5 мг/кг), группу введения ADC109 (5 мг/кг) и группу введения ADC110 (5 мг/кг), использовали в общей сложности 11 BT474 ортотопических мышей на группу, и лекарственные средства вводили один раз в неделю в общей сложности 4 раза через хвостовую вену. В группе введения герцептина (5 мг/кг) рост опухоли частично ингибировался вплоть до конечной временной точки эксперимента, но в группах введения ADC109 и ADC110, были получены аналогичные результаты, т.е. реакция на лекарственное средство достигалась через 4 дня после первого введения, полная регрессия опухоли достигалась через 10 дней, и регрессию опухоли поддерживали без повторения роста вплоть до конечной временной точки эксперимента (Фиг. 11). Наблюдали, что изменение массы тела и умершие животные в течение всего экспериментального периода не имели отношение к вводимым лекарственным средствам.
[00505]
[00506] 4) Оценка эффективности в зависимости от введения разовой дозы
[00507] Осуществляли эксперимент для оценки эффективности лекарственного средства Герцептина, ADC109 и ADC110 в ортотопической модели Her2-положительного рака молочной железы человека в зависимости от введения разовой дозы. Группы животных были такими же, как в модели мульти-дозового введения, использовали в общей сложности 4 BT474 ортотопических мышей на группу, лекарственные средства вводили один раз в начальной временной точке эксперимента через хвостовую вену, и только наблюдение осуществляли в течение экспериментального периода, составляющего 5 недель, без дополнительного введения лекарственных средств. В группах введения ADC109 и ADC 110 ответы на рост опухоли были аналогичными полученным в эксперименте с мульти-дозовым введением, и, что касается группы введения герцептина, наблюдали повторный рост опухоли, начиная с 10 дня после введения разовой дозы. Однако в группах введения ADC109 и ADC 110 регрессия опухоли поддерживалась вплоть до конечной временной точки эксперимента (Фиг. 12). Наблюдали, что изменение массы тела и умершие животные в течение всего экспериментального периода не имели отношение к вводимым лекарственным средствам.
[00508]
[00509] [Экспериментальный Пример 7] Испытание стабильности ADC в плазме
[00510] Стабильность в плазме оценивали на ADC110 Примера 10, ADC113 Примера 11 и Кадсила следующим способом, и результаты проиллюстрированы на Фиг. 13-15.
[00511]
[00512] (In vitro стабильность в плазме метод испытания ADC)
[00513] ADC разбавляли при концентрации 1 мг/мл с использованием PBS и смешивали с плазмой для получения конечной концентрации 0,16 мг/ мл. Смесь культивировали при 37°С, отбирали образец плазмы в предварительно определенных точках времени (1 день, 3 дня, 5 дней и 7 дней) и из образца плазмы выделяли только антитело с использованием магнитных шариков с белком A. Испытываемое вещество, полученное из супернатанта, полученного путем промывки магнитных шариков раствором, содержащим 30% ацетонитрила и 1% мурввьиной кислоты, анализировали с использованием ЖХ-МС и наблюдали изменение соотношения лекарственное средство-антитело (DAR). Что касается Кадсила (T-DM1), который использовали качестве контрольного вещества, наблюдали только его стабильность в PBS. Как результат, должно быть понятно, что ADC110 Примера 10 и ADC113 Примера 11 были в значительной степени стабильными, в отличие от результата Кадсила (T-DM-1), который был нестабильным даже в PBS.
[00514]
[00515] [Экспериментальный Пример 8] Оценка фармакокинетики (PK) in vivo
[00516] 1) Фармакокинетический профиль мыши in vivo
[00517] Для подтверждения фармакокинетики тотального антитела при внутривенном введении разовой дозы Герцептина, ADC109 и ADC110 мыши ICR, осуществляли следующий эксперимент. Испытываемые вещества, то есть Герцептин (G1), ADC109 (G2) и ADC110 (G3), внутривенно вводили самцам мышей ICR, соответственно (доза: 2,5 мг/кг). На момент сбора крови, 50 мкл крови собирали из ретроорбитальной вены с использованием капиллярной трубки, покрытой натрий-гепарином в предварительно определенных точках времени (15 минут, 1 час, 2 часа, 4 часа, 6 часов, 1 день, 2 дня, 3 дня, 7 дней, 10 дней и 14 дней после введения). Собранную кровь переносили в 1,5-мл полиэтиленовую пробирку (Denvil, USA) и хранили на ледяной бане и плазму получали путем центрифугирования крови при 14000 об/мин в течение 5 минут не более чем через 1 час после хранения при глубокой заморозке в морозильнике при -70°С до использования в анализе. Испытываемое вещество в плазме мыши измеряли с использованием твердофазного иммуноферментного анализа (ELISA). Фармакокинетику анализировали при помощи не-компартментного анализа с использованием Phoenix™ WinNonlin® (ver. 6.3, Pharsight) и рассчитывали площадь под кривыми концентрация в плазме-время (AUC), максимальные концентрации в крови (Cmax), время полужизни (t1/2), клиренс (CL) и объемы дистрибуции (Vss), Фиг. 16.
[00518] После введения испытываемого вещества было обнаружено, что анализируемое вещество присутствовало в плазме мыши вплоть до 14 дней во всех группах испытания. Во всех группах испытания не было никакой существенной разницы (в 2 раза или более) в фармакокинетических параметрах между группами. Однако, даже если вводили одну и ту же дозу, в случае DC109 и ADC110 экспозиция была низкой по сравнению с Герцептином. Поскольку ADC109 и ADC110 представляют собой конъюгаты антитела с лекарственным препаратом (ADCs), в отличие от Герцептина, описанный выше результат связан с разницей в аффинности связывания с анти-человеческим IgG (Fab специфическим или Fc специфическим) антителом, используемом в анализе ELISA.
[00519] В группе испытания G1 (Герцептин), значение AUCINF Герцептина было 356,00 день*мкг/мл, C0 значение было 39,20 мкг/мл, CL значение было 7,04 мл/день/кг, Vss значение было 186,00 мл/кг, T1/2 значение было 18,40 дней, которые были аналогичны значениям фармакокинетического профиля в документе. Кроме того, в группе испытания G2 (ADC109), значения AUCINF, C0, CL, Vss и T1/2 были 235,55 день*мкг/мл, 31,56 мкг/мл, 11,25 мл/день/кг, 239,28 мл/кг и 15,04 дней, соответственно, и в группе испытания G3 (ADC110), значения AUCINF, C0, CL, Vss и T1/2 были 373,60 день*мкг/ мл, 35,11 мкг/ мл, 7,49 мл/день/кг, 326,68 мл/кг и 35,72 дней, соответственно. Эти результаты были аналогичны результатам в группе испытания G1 (Герцептин), но экспозиция была немного ниже.
[00520]
[00521] 2) Испытание фармакокинетики у крыс in vivo
[00522] Для подтверждения фармакокинетики испытываемых веществ при внутривенном введении разовой дозы Герцептина и ADC110 крысе, осуществляли следующий эксперимент. Испытываемые вещества, Герцептин и ADC110, внутривенно вводили самкам крыс, соответственно (Доза: 3,0 мг/кг). 0,4 мл крови собирали из яремной вены с использованием 1 мл шприц (размер иглы 25), обработанный гепарином (85 МЕд/мл, 35 мкл), в предварительно определенных точках времени (3 минуты, 1 час, 3 часа, 6 часов, 1 день, 2 дня, 3 дня, 4 дня, 7 дней, 9 дней, 14 дней, 17 дней, 21 день и 28 дней после введения), помещали в микропробирку, обрабатывали с использованием вращающегося смесителя в течение нескольких минут и затем центрифугировали при 14000 об/мин в течение 5 минут для отделения плазмы. Отделенную плазму помещали в микропробирку и хранили при глубокой заморозке до анализа. Испытываемые вещества в плазме измеряли с использованием ЖХ-МС. Фармакокинетический анализ осуществляли с использованием компартметной модели 2, используя Phoenix™ WinNonlin® (ver. 6.3, Pharsight), и соотношение лекарственное средство-антитело определяли при помощи ЖХ-МС/МС после выделения ADC110 с использованием шариков с белком A. Результаты проиллюстрированы на Фиг. 17-19, соответственно. Кроме того, рассчитывали площадь под кривыми концентрация в плазме-время (AUC), максимальные концентрации в крови (Cmax), время полужизни (t1/2), клиренс (CL), дистрибуцию время полужизни (Альфа HL), секрецию время полужизни (бета HL), объемы дистрибуции (V1) и объемы дистрибуции (Vss), как показано в Таблице 4.
[00523] В случае АDC110, значение AUC было 684,83 мкг*день/мл, CL значение было 4,38 мл/день/кг, Cmax значение было 92,18 мкг/ мл, Vss значение было 43,83 мл/кг и T1/2 значение было 8,55 дней, и в случае Герцептина значение AUC было 622,87 мкг*день/мл, CL значение было 4,87 мл/день/кг, Cmax значение было 81,70 мкг/ мл, Vss значение было 56,53 мл/кг, T1/2 значение было 10,10 дней. Можно утверждать, что фармакокинетические профили Герцептина и ADC110 были схожими друг с другом, таким образом, связывание лекарственного средства с антителом вряд ли влияло на фармакокинетику у крысы.
[00524]
Фармакокинетика ADC110 и Герцептина у крыс
[00525]
[00526] 3) Испытание фармакокинетики у обезьян in vivo
[00527] Для подтверждения фармакокинетики испытываемых веществ при внутривенном введении разовой дозы Герцептина и ADC110 обезьяне, осуществляли следующий эксперимент. Испытываемые вещества, Герцептин и ADC110, внутривенно вводили самкам обезьян, соответственно (Доза: 3,0 мг/кг). Около 1,5 мл крови собирали из цефалической или бедренной вены в предварительно определенных точках времени (30 минут, 3 часа, 7 часов, 12 часов, 24 часа (2 дня), 3 дня, 4 дня, 5 дней, 6 дней, 11 дней, 15 дней, 22 дня, 29 дней и 36 дней после введения), помещали в пробирку, заполненную антикоагулянтом (EDTA-K2), хранили в мокром льду/Kryorack и затем центрифугировали при 3000 об/мин в течение 10 минут в охлажденном состоянии для отделения плазмы. Отделенную плазму переносили в микропробирку и хранили при глубокой заморозке до анализа. Испытываемые вещества в плазме измеряли с использованием ЖХ-МС. Фармакокинетический анализ осуществляли с использованием компартметной модели 2, используя Phoenix™ WinNonlin® (ver. 6.3, Pharsight), и для определения соотношения лекарственное средство-антитело определяли количество свободного ММAF при помощи ЖХ-МС/МС, после разделения ADC110 с использованием шариков с белком A и обработки бета-глюкуронидазой. Результаты проиллюстрированы на Фиг. 20-22, соответственно. Рассчитывали площадь под кривыми концентрация в плазме-время (AUC), максимальные концентрации в крови (Cmax), время полужизни (t1/2), клиренс (CL), дистрибуцию время полужизни (Альфа HL), секрецию время полужизни (бета HL), объемы дистрибуции (V1) и объемы дистрибуции (Vss), как показано в Таблице 5.
[00528] В случае АDC110, значение AUC было 965,54 мкг*день/мл, CL значение было 3,11 мл/день/кг, Cmax значение было 117,56 мкг/ мл, Vss значение было 55,65 мл/кг и T1/2 значение было 12,79 дней, и в случае Герцептина значение AUC было 689,30 мкг*день/мл, CL значение было 4,35 мл/день/кг, Cmax значение было 83,14 мкг/ мл, Vss значение было 80,92 мл/кг, T1/2 значение было 13,44 дней. Было подтверждено, что, хотя значение AUC для ADC 110 было несколько выше, фармакокинетические профили Герцептина и ADC110 были абсолютно схожими друг с другом, таким образом, связывание лекарственного средства с антителом вряд ли влияло на фармакокинетику у обезьян.
[00529]
Фармакокинетика ADC110 и Герцептина у обезьян
[00530]
[00531] При сравнении значений времени полужизни, показанных ниже в Таблице 6, в случае Кадсила, лекарственное средство было связано с антителом, таким образом, время полужизни было существенно ниже по сравнению с Герцептином, котор представлял собой исходное антитело, но в случае АDC 110, полученного в Примере 10 настоящего изобретения, время полужизни было аналогичным времени полужизни исходного антитела. Это значит, что влияние ADC в соответствии с настоящим изобретением на время полужизни исходного антитела было незначительным.
[00532]
Сравнение времени полужизни ADC110, Герцептина и Кадсила
(0,3~20 мг/кг массы тела)
10,1 (3 мг/кг массы тела)
5,3 (30 мг/кг массы тела)
[00533] Как проиллюстрировано на Фиг. 18 и 21, было подтверждено, что ADC110 был стабильно связан с антителом и ММAF лекарственным средством в крови живых организмов, что является основной причиной высокой активности ADC110 в испытании эффективности in vivo по сравнению с Кадсила. На основании полученных результатов стабильности, как описано выше, можно заключить, что ADC110 может вносить вклад в повышение вероятности, что ADC110 будет демонстрировать более высокую эффективность у пациентов по сравнению с Кадсила, который представляет собой контрольное лекарственное средство. Было подтверждено, что лекарственное средство, отделяемое от антитела, не было обнаружено при содержании больше, чем в калибровочной кривой (Фиг. 19 и 22), и этот результат может означать, что ADC 110 может быть более превосходным, чем Кадсила, что касается стабильности.
Промышленная применимость
[00514] Соединения, включающие саморасщепляющуюся группу в соответствии с настоящим изобретением, могут включать белок (например, олигопептид, полипептид, антитело или подобные), обладающий субстрат-специфичностью в отношении мишени, и активное вещество (например, лекарственное средство, токсин, лиганд, детекторный зонд или подобные), обладающее специфической функцией или активностью. Саморасщепляющаяся группа может быть более стабильной в крови, плазме и т.п. по сравнению с существующим линкером, и при этом специфически связываясь с белком, который сверхэкспрессируется в клетках, вызывая заболевание, но может отделяться в раковых клетках-мишенях, благодаря чему активное вещество может специфически воздействовать на клетки, вызывающие заболевание, таким образом, делая возможным использование соединений для лечения заболеваний.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ, СОДЕРЖАЩИЕ РАСЩЕПЛЯЕМЫЙ ЛИНКЕР, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2795168C2 |
| КОМПОЗИЦИИ И СПОСОБЫ, ОТНОСЯЩИЕСЯ К КОНЪЮГАТАМ ЛЕКАРСТВЕННЫХ СРЕДСТВ С АНТИТЕЛАМИ ПРОТИВ CD19 | 2019 |
|
RU2806333C2 |
| КОНЪЮГАТЫ БЕЛОК-АКТИВНОЕ ВЕЩЕСТВО И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2613906C2 |
| СОЕДИНЕНИЕ ДЛЯ РАЗРУШЕНИЯ АНДРОГЕНОВОГО РЕЦЕПТОРА И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2817356C1 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2016 |
|
RU2710743C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗО[1,2-A]ПИРИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2017 |
|
RU2725147C1 |
| НОВОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ | 2019 |
|
RU2792163C2 |
| СПОСОБ СИНТЕЗА БИЛИРУБИНА | 2022 |
|
RU2838556C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ДИФЕНИЛМЕТАНА | 2017 |
|
RU2797392C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ДИФЕНИЛМЕТАНА | 2023 |
|
RU2814846C1 |
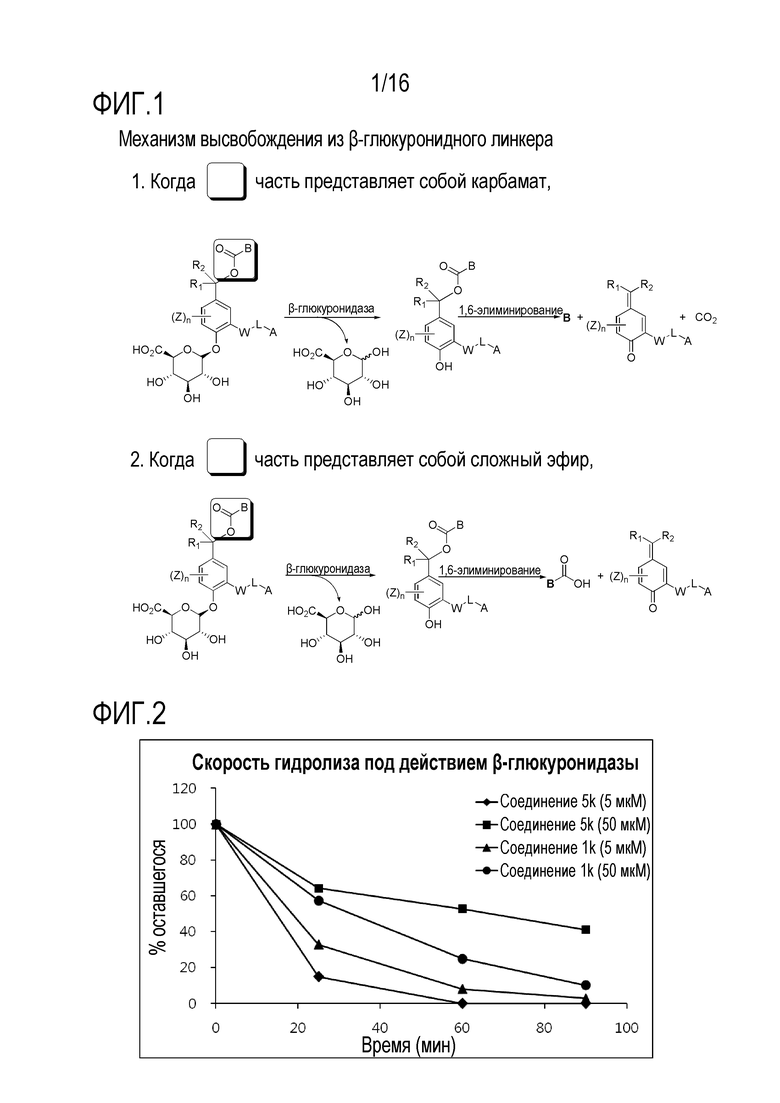

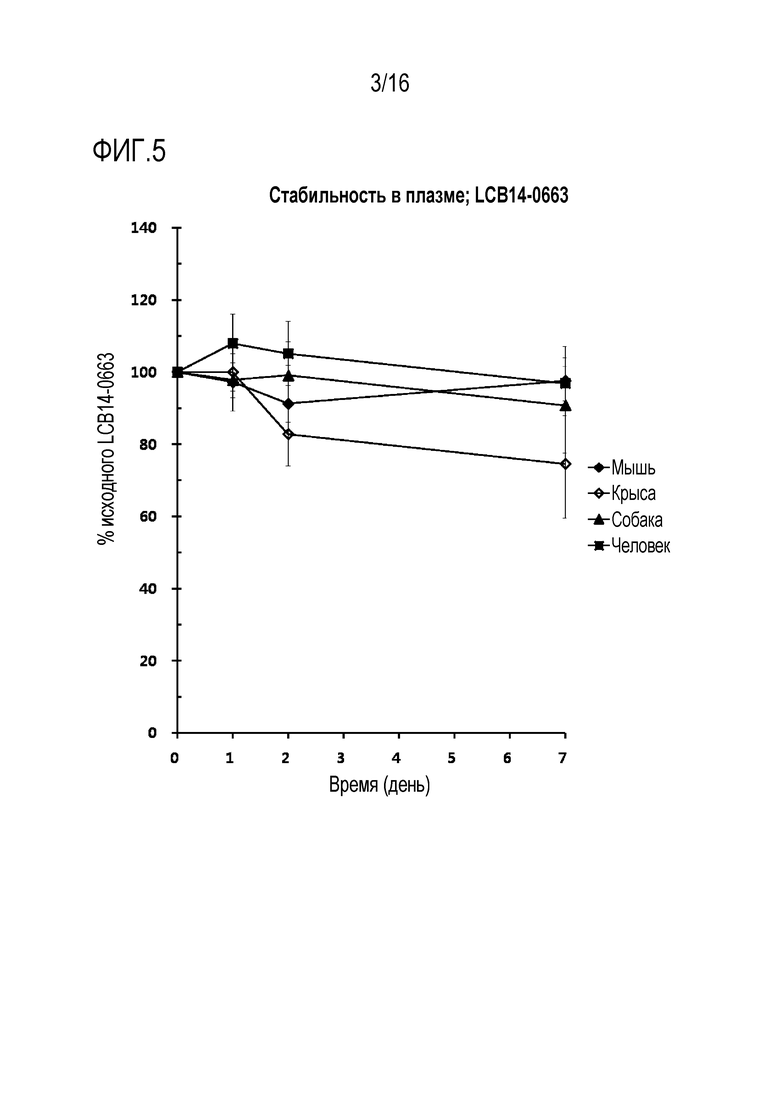
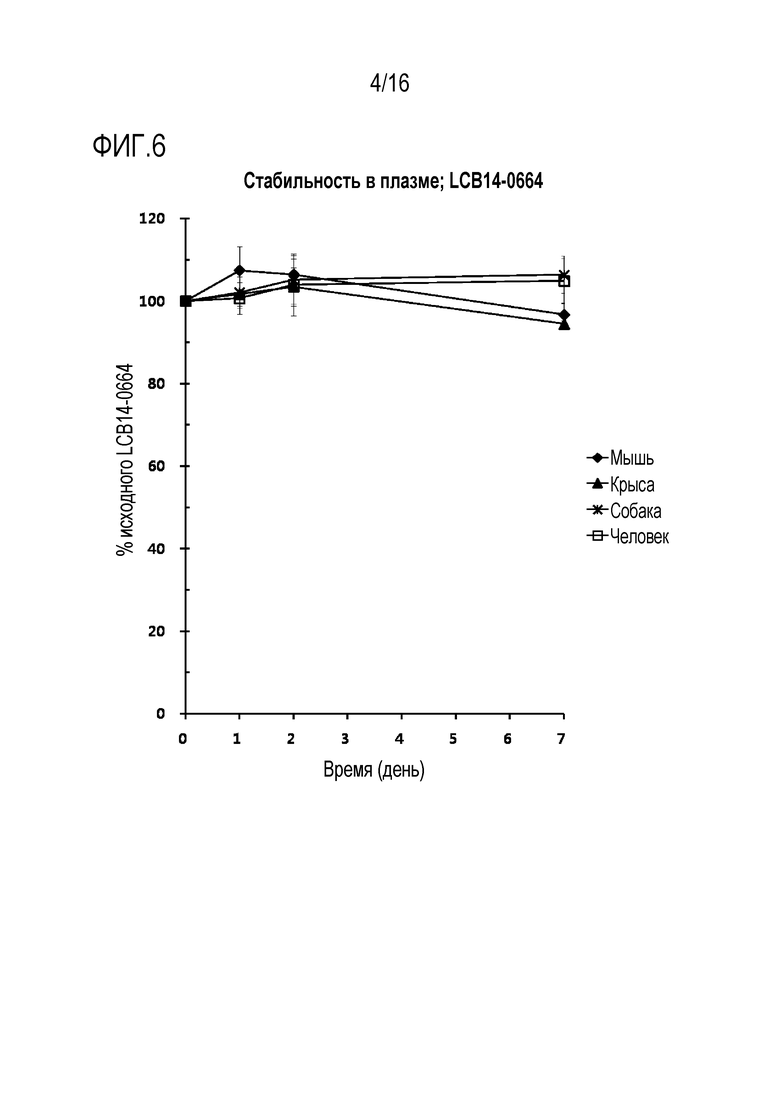


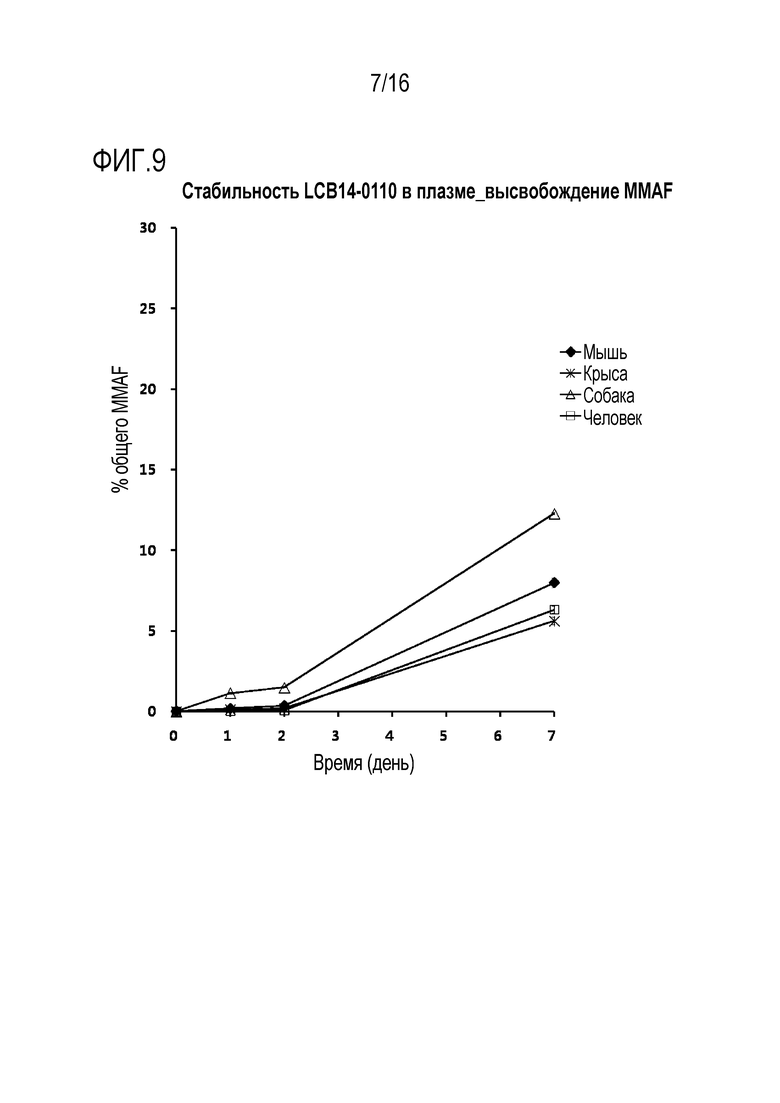
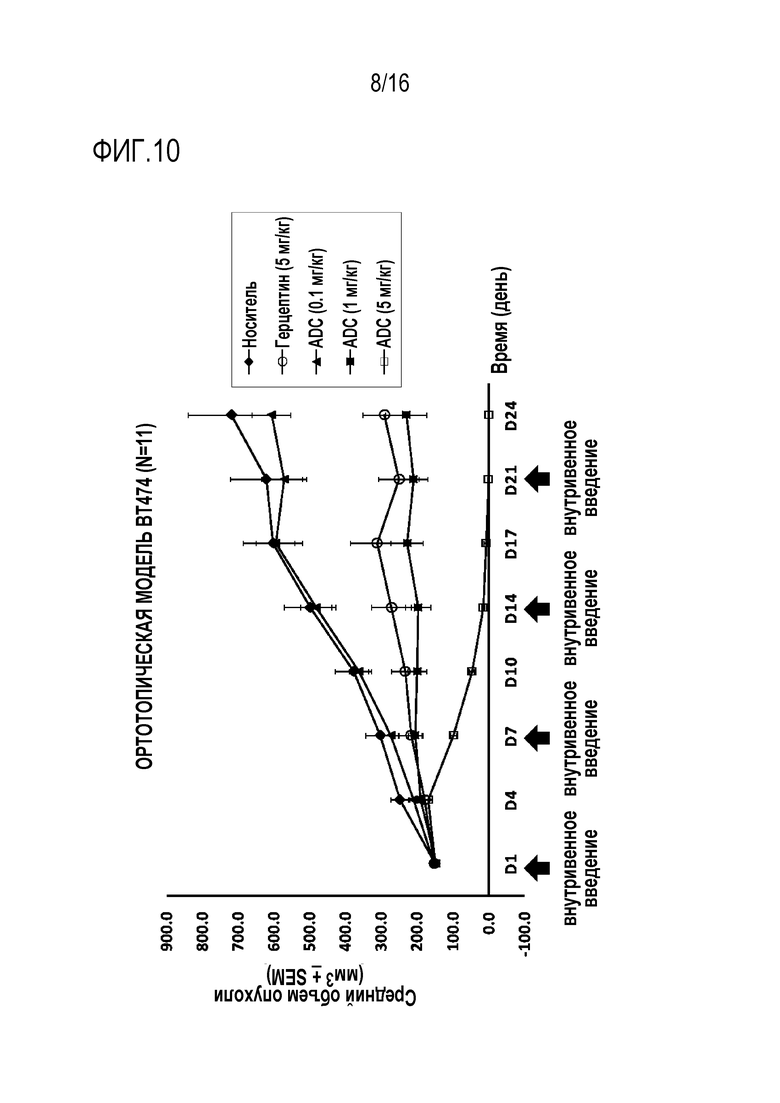


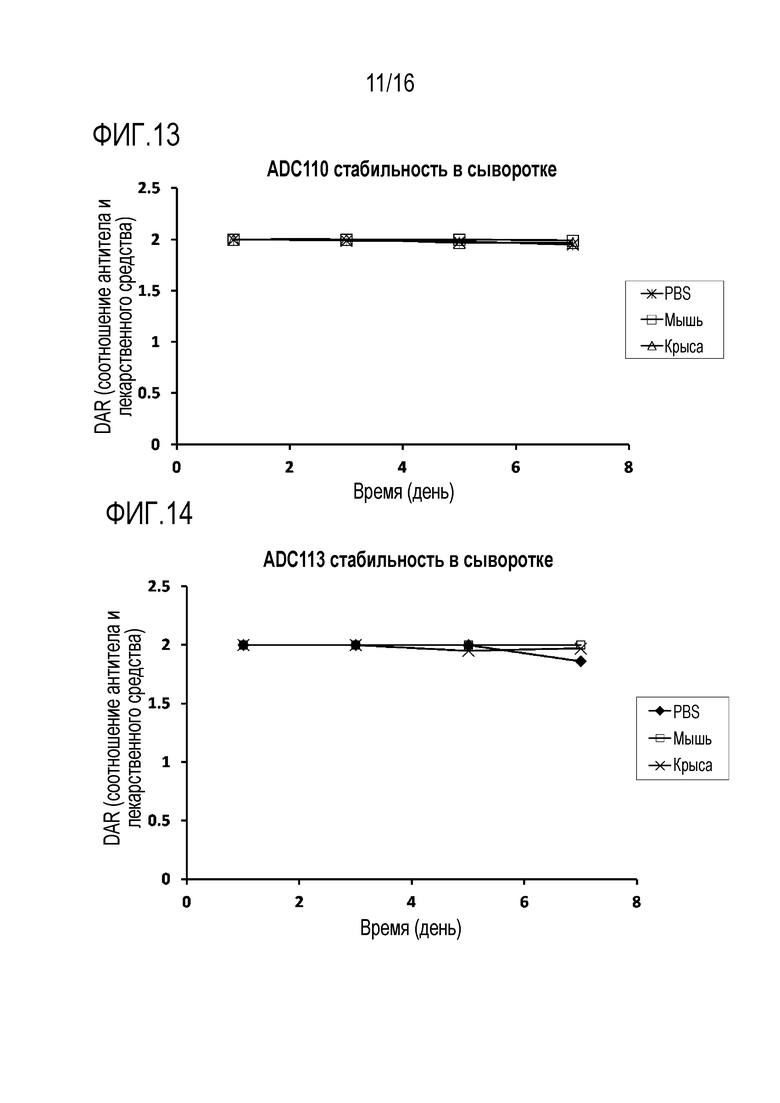





Изобретение относится к биотехнологии и медицине, в частности к технологии конъюгатов антитела с лекарственным средством. Предложено соединение химической формулы 1:  , включающее саморасщепляющуюся группу, антитело, обладающее субстрат-специфичностью в отношении мишени, и лекарственное средство. Линкер L представляет собой линкер, связывающий A и W саморасщепляющейся группы при помощи ковалентных связей, и включает по меньшей мере одно звено, представляющее собой изопрениловое производное:
, включающее саморасщепляющуюся группу, антитело, обладающее субстрат-специфичностью в отношении мишени, и лекарственное средство. Линкер L представляет собой линкер, связывающий A и W саморасщепляющейся группы при помощи ковалентных связей, и включает по меньшей мере одно звено, представляющее собой изопрениловое производное:  , которое распознается изопреноид-трансферазой. Предложенные соединения обладают повышенной стабильностью в плазме и дают возможность лекарственному средству легко высвобождаться в целевых клетках для проявления действия лекарства. 21 з.п. ф-лы, 22 ил., 6 табл., 20 пр.
, которое распознается изопреноид-трансферазой. Предложенные соединения обладают повышенной стабильностью в плазме и дают возможность лекарственному средству легко высвобождаться в целевых клетках для проявления действия лекарства. 21 з.п. ф-лы, 22 ил., 6 табл., 20 пр.
1. Соединение, представленное следующей химической формулой 1:
[Химическая формула 1]
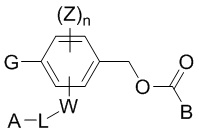 ,
,
где G представляет собой 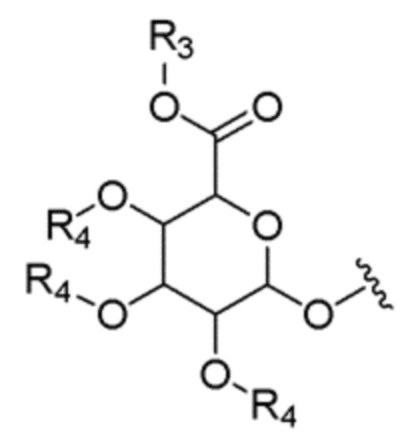 , R3 представляет собой водород или защитную группу карбоксила, и каждый R4 представляет собой независимо водород или защитную группу гидроксила;
, R3 представляет собой водород или защитную группу карбоксила, и каждый R4 представляет собой независимо водород или защитную группу гидроксила;
A представляет собой антитело;
B представляет собой лекарственное средство;
W представляет собой -C(O)-, -C(O)NR'- или -C(O)O-, где С(О) напрямую связан с фенильным кольцом, и R' и Rʺ каждый независимо представляют собой водород, (C1-C8)алкил, (C3-C8)циклоалкил, (C1-C8)алкокси, (C1-C8)алкилтио, моно- или ди-(C1-C8)алкиламино, (C3-C20)гетероарил или (C6-C20)арил;
Z представляет собой водород, (C1-C8)алкил, галоген, циано или нитро;
n представляет собой целое число от 1 до 3; и
L представляет собой линкер, связывающий A и W, который включает по меньшей мере одно звено, представляющее собой изопрениловое производное, представленное химической формулой A:
[Химическая формула A]
 ,
,
где звено, представляющее собой изопрениловое производное, распознается изопреноид-трансферазой.
2. Соединение по п. 1, где каждый R4 представляет собой водород.
3. Соединение по п. 1, где L представляет собой алкилен, содержащий от 1 до 50 атомов углерода, и удовлетворяет по меньшей мере одному из следующих условий (i)-(iv):
(i) алкилен включает по меньшей мере одну ненасыщенную связь;
(ii) алкилен включает по меньшей мере один гетероарилен;
(iii) атом углерода алкилена замещен одним или несколькими гетероатомами, выбранными из азота (N), кислорода (О) и серы (S); или
(iv) алкилен дополнительно замещен одним или несколькими алкилами, содержащими от 1 до 20 атомов углерода.
4. Соединение по п. 1, где n представляет собой 1.
5. Соединение по п. 1, где линкер L дополнительно содержит связывающее звено, образованное в результате реакций 1,3-диполярного циклоприсоединения, гетеро-реакций Дильса-Альдера, реакций нуклеофильного замещения, реакций карбонильных соединений неальдольного типа, присоединений по месту кратных связей углерод-углерод, реакций окисления или клик-реакций.
6. Соединение по п. 5, где связывающее звено образовано путем реакции между ацетиленом и азидом или реакции между группой альдегида или кетона и гидразином или гидроксиламином.
7. Соединение по п. 6, где связывающее звено представлено следующей химической формулой B, C, D или E:
[Химическая формула B]

[Химическая формула C]

[Химическая формула D]

[Химическая формула E]
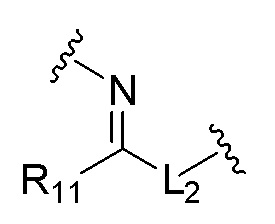
L1 представляет собой простую связь или алкилен, содержащий от 1 до 30 атомов углерода;
R11 представляет собой водород или алкил, содержащий от 1 до 10 атомов углерода; и
L2 представляет собой алкилен, содержащий от 1 до 30 атомов углерода.
8. Соединение по п. 5, где L дополнительно содержит соединительное звено, представленное следующей химической формулой F или G:
[Химическая формула F]
-(CH2)r(V(CH2)p)q-
[Химическая формула G]
-(CH2CH2X)w-
V представляет собой простую связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-;
X представляет собой -O-, (C1-C8)алкилен или -NR21-;
R21-R25, каждый независимо, представляют собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
r представляет собой целое число от 1 до 10;
p представляет собой целое число от 0 до 10;
q представляет собой целое число от 1 до 10; и
w представляет собой целое число от 1 до 10.
9. Соединение по п. 1, где L содержит 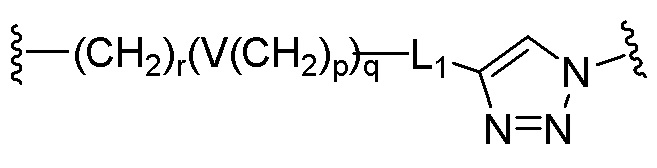 ,
, 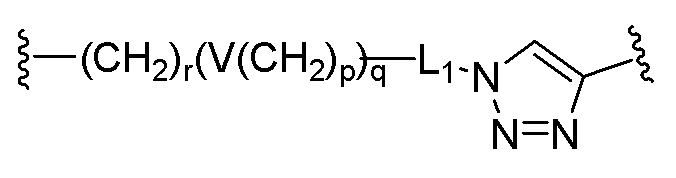 или
или  ,
,
где V представляет собой простую связь, -O-, -S-, -NR21-, -C(O)NR22-, -NR23C(O)-, -NR24SO2- или -SO2NR25-, R21-R25 каждый независимо представляют собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил,
r представляет собой целое число от 1 до 10,
p представляет собой целое число от 0 до 10,
q представляет собой целое число от 1 до 10, и
L1 представляет собой простую связь.
10. Соединение по п. 1, где антитело содержит аминокислотный мотив, который должен распознаваться изопреноид-трансферазой.
11. Соединение по п. 10, где изопреноид-трансфераза представляет собой фарнезилпротеинтрансферазу (FTаза) или геранилгеранилтрансферазу (GGTаза).
12. Соединение по п. 10, где антитело дополнительно включает спейсерное звено, состоящее из аминокислоты, олигопептида или полипептида, между белком и аминокислотным мотивом.
13. Соединение по п. 12, где антитело ковалентно связано с линкером L через аминокислотный мотив.
14. Соединение по п. 12, где аминокислотный мотив ковалентно связан с C-концом антитела или ковалентно связан с по меньшей мере одним спейсерным звеном, ковалентно связанным с C-концом антитела.
15. Соединение по п. 10 или 12, где аминокислотный мотив представляет собой CYYX, XXCC, XCXC или CXX, где C представляет собой цистеин, Y представляет собой алифатическую аминокислоту, и X представляет собой аминокислоту, которая определяет специфичность субстрата изопреноид-трансферазы.
16. Соединение по п. 15, где аминокислотный мотив выбирают из группы, состоящей из (G)zCVIM и (G)zCVLL, где дополнительно G представляет собой глициновое звено, и z представляет собой целое число от 0 до 20.
17. Соединение по п. 14, где C-конец антитела представляет собой C-конец легкой цепи или тяжелой цепи антитела.
18. Соединение по п. 1, где лекарственное средство представляет собой иммуномодулирующее соединение, противораковое средство, противовирусное средство, антибактериальное средство, противогрибковое средство, противопаразитарное средство или их комбинацию.
19. Соединение по п. 16, где соединение представляет собой
 или
или
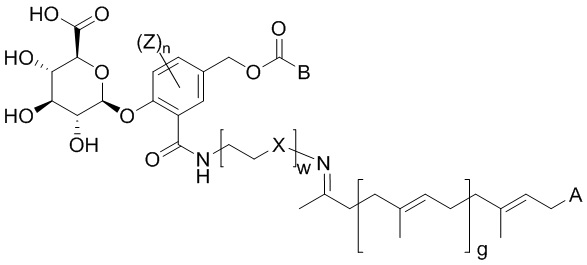
и где
Z представляет собой водород, (C1-C8)алкил, галоген, циано или нитро;
X представляет собой -O-, (C1-C8)алкилен или -NR21-;
R21 представляет собой водород, (C1-C6)алкил, (C1-C6)алкил(C6-C20)арил или (C1-C6)алкил(C3-C20)гетероарил;
n представляет собой целое число от 1 до 3;
r представляет собой целое число от 1 до 10;
q представляет собой целое число от 1 до 10;
w представляет собой целое число от 1 до 10;
x представляет собой целое число от 0 до 10;
g представляет собой целое число от 1 до 10;
A представляет собой антитело;
B представляет собой
 ,
,
 ,
,
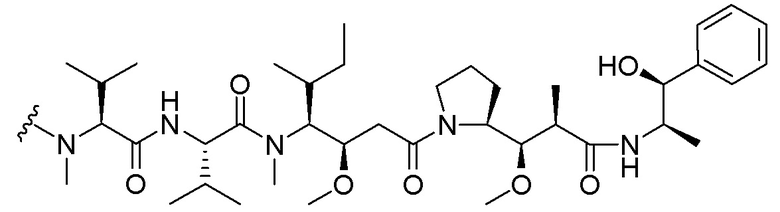 ,
,
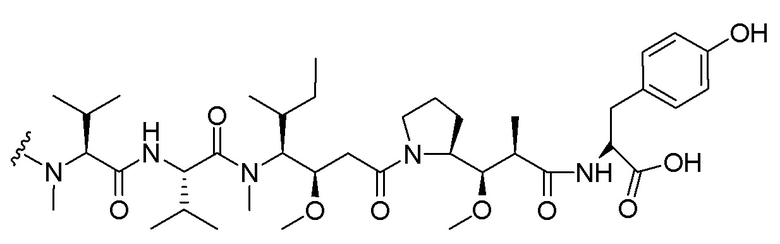 ,
,
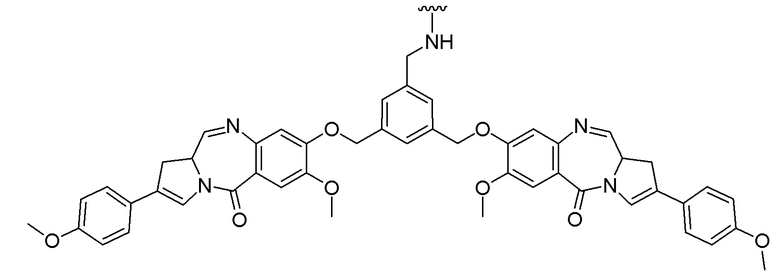 ,
,
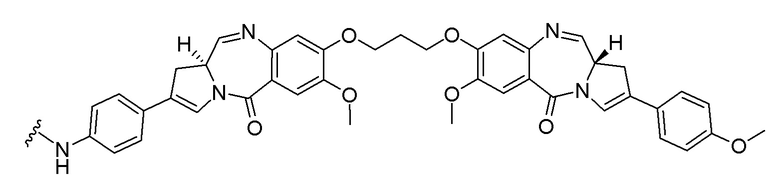 ,
,
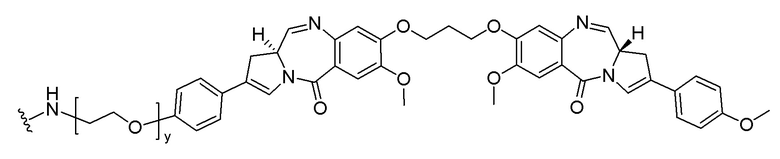 ,
,
 ,
,
 ,
,
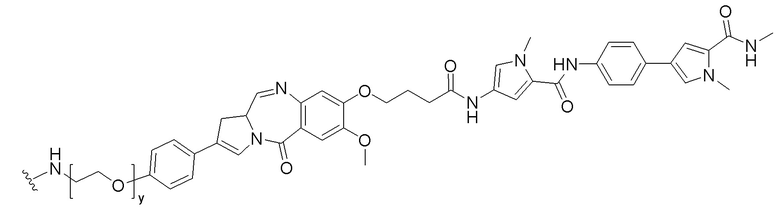 ;
;
и y представляет собой целое число от 1 до 10.
20. Соединение по любому из пп. 1-19, где антитело выбрано из группы, состоящей из интактных поликлональных антител, интактных моноклональных антител, фрагментов антител, одноцепочечных Fv-мутантов (scFv), мультиспецифичных антител, биспецифичных антител, химерных антител, гуманизированных антител, человеческих антител, гибридных белков, включающих антиген-определяющую часть антитела, и других модифицированных молекул иммуноглобулинов, включающих сайт распознавания антигена.
21. Соединение по п. 20, где антитело представляет собой моноклональное антитело.
22. Соединение по любому из пп. 1-19, где антитело выбрано из группы, состоящей из муромонаба-CD3, абциксимаба, ритуксимаба, даклизумаба, паливизумаба, инфликсимаба, трастузумаба, этанерцепта, базиликсимаба, гемтузумаба, алемтузумаба, ибритутомаба тиуксетана, адалимумаба, алефацепта, омализумаба, эфализумаба, тозитумомаба-I131, цетуксимаба, бевацизумаба, натализумаба, ранибизумаба, панитумумаба, экулизумаба, рилонацепта, цертолизумаба пегола, ромиплостима, AMG-531, CNTO-148, CNTO-1275, ABT-874, LEA-29Y, белимумаба, TACI-Ig, анти-CD20 второго поколения, ACZ-885, тоцилизумаба, атлизумаба, меполизумаба, пертузумаба, HuMax CD20, тремелимумаба (CP-675 206), тицилимумаба, MDX-010, IDEC-114, инотузумаба HuMax EGFR, афлиберцепта, VEGF Trap-Eye, HuMax-CD4, Ala-Ala, ChAglyCD3, TRX4, катумаксомаба, IGN101, MT-201, преговомаба, CH-14,18, WX-G250, AMG-162, AAB-001, мотавизумаба, MEDI-524, эфунгумаба, аурограб (Aurograb), раксибацумаба, анти-CD20 третьего поколения, LY2469298 и велтузумаба.
| US 2012107332 A1, 03.05.2012 | |||
| US 2012308584 A1, 06.12.2012 | |||
| TRANOY-OPALINSKI I | |||
| ET AL | |||
| "[beta]-Glucuronidase-responsive prodrugs for selective cancer chemotherapy: An update", European Journal of Medicinal Chemistry, 11.01.2014, v.74, p.302-313, DOI: 10.1016/J.EJMECH.2013.12.045 | |||
| JEFFREY S | |||
| C | |||
| et al | |||
| "Development and Properties of β-Glucuronide |
Авторы
Даты
2020-01-30—Публикация
2015-05-27—Подача