РОДСТВЕННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет на основании патентной заявки США с серийным №: 62/322931, поданной 15 апреля 2016 г., и патентной заявки США с серийным №: 62/481094, поданной 3 апреля 2017 г., полное содержание каждой из этих заявок включено в настоящий документ посредством ссылки.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей, который был подан в электронном виде в формате ASCII и включен в настоящий документ посредством ссылки в полном объеме. Указанная копия в формате ASCII, созданная 14 апреля 2017 г., носит название N2067-7128WO_SL.txt и имеет размер 2326027 байтов.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Разработаны различные конструкты, позволяющие избирательно экспрессировать интересующий белок. В последнее время были протестированы конструкты, содержащие домен, спроектированный для деградации в отсутствие стабилизирующего лиганда (известные в данной области как «дегроны»). Другие конструкты содержат домен, спроектированный для агрегации в отсутствие дезагрегирующего лиганда (например, домен агрегации). Такие домены могут быть слиты с интересующими белками для осуществления избирательной экспрессии таких белков лишь в присутствии стабилизирующего или дезагрегирующего лиганда.
Дегроны и домены агрегации, известные в данной области, могут в некоторых случаях иметь определенные недостатки, связанные с нарушением нужной функции интересующего белка из-за размера и/или конформации слитого белка. Такие недостатки могут быть особенно очевидны в случае, когда интересующий белок представляет собой трансмембранный белок. Таким образом, существует потребность в усовершенствовании технологии дегронов/доменов агрегации. Кроме того, существует потребность в способах модификации T-клеток для лечения различных заболеваний и состояний, таких как, но без ограничения, рак, аутоиммунные и аллоиммунные нарушения, без постоянной модификации или подавления иммунной системы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте изобретение относится к слитым белкам, содержащим два белковых домена, разделенные гетерологичным сайтом расщепления протеазы (например, сайтом расщепления протеазы, который расщепляется внутриклеточной или внеклеточной протеазой), при этом первый из белковых доменов представляет собой домен условной экспрессии, например, домен деградации или домен агрегации, и второй белок представляет собой интересующий белок, например, трансмембранный белок (например, CAR).
В некоторых вариантах осуществления домен условной экспрессии представляет собой домен деградации, например, домен деградации, описанный в настоящем документе. Без связи с конкретной теорией, в некоторых вариантах осуществления домен деградации является нестабильным и/или неспособным сворачиваться в стабильную конформацию в отсутствие экспрессионного соединения, например, стабилизирующего соединения. Неправильно свернутый/несвернутый домен деградации может подвергаться деградации во внутриклеточных путях деградации наряду с другим доменом(ами) слитого белка (смотри, например, Фигуру 25). В присутствии экспрессионного соединения домен деградации способен сворачиваться в стабильную конформацию и менее подвержен деградации во внутриклеточных путях, например, в сравнении с доменом деградации в отсутствие экспрессионного соединения. Вследствие этого, уровень и/или степень клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка увеличивается, например, по меньшей мере в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз, в присутствии экспрессионного соединения в сравнении с показателями в отсутствие экспрессионного соединения. В некоторых вариантах осуществления после того, как домен деградации слитого белка принимает правильную конформацию, гетерологичный сайт расщепления экспонируется, что приводит к удалению домена деградации и, таким образом, высвобождению второго белкового домена.
В других вариантах осуществления домен условной экспрессии представляет собой домен агрегации. Без связи с конкретной теорией, в некоторых вариантах осуществления в отсутствие экспрессионного соединения, например, дезагрегирующего соединения, домен агрегации слитого белка связывается с одним или более другими доменами агрегации в олигомеры и агрегирует (смотри, например, Фигуру 26). Агрегированный слитый белок может быть секвестрирован в клеточном компартменте, в котором он агрегировал. В присутствии экспрессионного соединения, например, дезагрегирующего соединения, домены агрегации отделяются друг от друга, и слитые белки солюбилизируются (например, принимают мономерную конфигурацию). Вследствие этого, уровень и/или степень клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка увеличивается, например, по меньшей мере в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз, в присутствии экспрессионного соединения в сравнении с показателями в отсутствие экспрессионного соединения. В некоторых вариантах осуществления после того, как домен агрегации слитого белка солюбилизирован, гетерологичный сайт расщепления экспонируется, что приводит к удалению домена агрегации и, таким образом, высвобождению второго белкового домена.
В любом из вышеуказанных аспектов и вариантов осуществления слитый белок содержит первый белковый домен, который представляет собой, или содержит, домен условной экспрессии, например, домен деградации или домен агрегации, и второй белковый домен, который представляет собой, или содержит, интересующий белок, например, трансмембранный белок (например, CAR), при этом первый и второй домены слитого белка разделены гетерологичным сайтом расщепления протеазы (например, сайтом расщепления протеазы, который расщепляется внутриклеточной или внеклеточной протеазой). В некоторых вариантах осуществления домен условной экспрессии, например, домен деградации или агрегации, расположен в N-концевом направлении относительно второго белкового домена. В конкретных вариантах осуществления слитый белок также содержит сигнальный пептид в N-концевом направлении относительно домена деградации.
В одном аспекте изобретение относится к слитому белку, содержащему два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов представляет собой домен условной экспрессии и второй из указанных белковых доменов представляет собой трансмембранный белок, причем домен условной экспрессии имеет первое состояние, связанное с первым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, и второе состояние, связанное со вторым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, при этом второй уровень повышен, например, по меньшей мере в 2, 3, 4, 5, 10, 20 или 30 раз повышен, относительно первого уровня, в присутствии экспрессионного соединения.
В другом аспекте изобретение относится к слитому белку, содержащему два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов представляет собой домен условной экспрессии, и второй из указанных белковых доменов представляет собой трансмембранный белок, при этом гетерологичный сайт расщепления протеазы представляет собой сайт расщепления фурина, при условии, что сайт расщепления фурина не содержит аминокислотную последовательность SARNRQKR (SEQ ID NO: 981).
В другом аспекте изобретение относится к слитому белку, содержащему два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов представляет собой домен условной экспрессии, и второй из указанных белковых доменов представляет собой химерный антигенный рецептор (CAR).
В некоторых вариантах осуществления домен условной экспрессии представляет собой домен деградации.
В некоторых вариантах осуществления домен условной экспрессии представляет собой домен агрегации.
В некоторых вариантах осуществления слитый белок содержит два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов (в настоящем документе также называемый первым белковым доменом) представляет собой, или содержит, домен деградации, например, домен деградации, описанный в настоящем документе, и второй из указанных белковых доменов (в настоящем документе также называемый вторым белковым доменом) представляет собой интересующий белок. В одном варианте осуществления интересующий белок представляет собой трансмембранный белок, например, CAR.
В некоторых вариантах осуществления домен деградации выбирают из домена рецептора эстрогена (ER), домена белка FKB (FKBP) или дигидрофолатредуктазы (DHFR).
В некоторых вариантах осуществления домен деградации имеет первое состояние, связанное с первым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, и второе состояние, связанное со вторым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, при этом второй уровень повышен, например, по меньшей мере в 2, 3, 4, 5, 10, 20 или 30 раз повышен, относительно первого уровня, в присутствии стабилизирующего соединения.
В конкретных вариантах осуществления домен деградации получен из рецептора эстрогена. Например, домен деградации может содержать аминокислотную последовательность, выбранную из SEQ ID NO: 58 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичности с ней, или SEQ ID NO: 121, или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 58 или SEQ ID NO: 121. Если домен деградации получен из рецептора эстрогена, стабилизирующее соединение может быть выбрано из базедоксифена или 4-гидрокситамоксифена (4-OHT). В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен. Тамоксифен и базедоксифен являются одобренными FDA лекарственными средствами и, таким образом, безопасны для использования людьми.
В конкретных вариантах осуществления домен деградации получен из белка FKB (FKBP). Например, домен деградации может содержать аминокислотную последовательность SEQ ID NO: 56 или последовательность, имеющую по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит SEQ ID NO: 56. Если домен деградации получен из FKBP, стабилизирующее соединение может представлять собой Shield-1.
В некоторых вариантах осуществления домен деградации получен из дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 57 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98%, или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит SEQ ID NO: 57. Если домен деградации получен из DHFR, стабилизирующее соединение может представлять собой триметоприм.
В других вариантах осуществления домен деградации получен не из белка FKB или рецептора эстрогена.
В некоторых вариантах осуществления слитый белок содержит два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов (в настоящем документе также называемый первым белковым доменом) представляет собой, или содержит, домен агрегации, например, домен агрегации, описанный в настоящем документе, и второй из указанных белковых доменов (в настоящем документе также называемый вторым белковым доменом) представляет собой интересующий белок. В одном варианте осуществления интересующий белок представляет собой трансмембранный белок, например, CAR.
В некоторых вариантах осуществления слитый белок содержит два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов представляет собой домен агрегации, и второй из указанных белковых доменов представляет собой трансмембранный белок, причем домен агрегации имеет первое состояние, связанное с первым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, и второе состояние, связанное со вторым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, и при этом второй уровень повышен, например, по меньшей мере в 2, 3, 4, 5, 10, 20 или 30 раз повышен, относительно первого уровня, в присутствии дезагрегирующего соединения.
В некоторых вариантах осуществления слитый белок содержит два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов представляет собой домен агрегации и второй из указанных белковых доменов представляет собой трансмембранный белок, при этом гетерологичный сайт расщепления протеазы представляет собой сайт расщепления фурина, при условии, что сайт расщепления фурина не содержит аминокислотную последовательность SARNRQKR (SEQ ID NO: 981).
В некоторых вариантах осуществления слитый белок содержит два белковых домена, разделенные гетерологичным сайтом расщепления протеазы, при этом первый из указанных белковых доменов представляет собой домен агрегации и второй из указанных белковых доменов представляет собой химерный антигенный рецептор (CAR).
В некоторых вариантах осуществления домен агрегации содержит 1, 2, 3, 4 5, 6, 7, 8 или более повторов домена димеризации, например, домена гомодимеризации или гетеродимеризации.
В некоторых вариантах осуществления домен агрегации получен из белка FKB (FKBP).
В некоторых вариантах осуществления домен агрегации представляет собой домен FKBP F36M.
В некоторых вариантах осуществления домен агрегации получен из белка FKB (FKBP) и содержит аминокислотную последовательность, которая по меньшей мере на 90, 95, 97, 98, 99, или 100% идентична любой из SEQ ID NOs: 975 или 976.
В некоторых вариантах осуществления слитый белок также содержит 2-й, 3-й, 4-й, 5-й, 6-й, 7-й, 8-й, 9-й или 10-й домен агрегации.
В некоторых вариантах осуществления 2-й, 3-й, 4-й, 5-й, 6-й, 7-й, 8-й, 9-й или 10-й домен агрегации представляет собой домен агрегации того же типа, что и первый домен агрегации.
В некоторых вариантах осуществления домен агрегации образует гомодимеры с таким же доменом агрегации.
В некоторых вариантах осуществления слитый белок содержит множество доменов агрегации, при этом множество включает домены агрегации более, чем одного, например, двух типов, и домен агрегации первого типа образует гетеродимеры с доменом агрегации второго типа.
В некоторых вариантах осуществления слитый белок содержит 2, 4, 6, 8 или 10 доменов агрегации, при этом слитый белок содержит равные количества доменов агрегации первого типа и доменов агрегации второго типа.
В некоторых вариантах осуществления домены агрегации первого типа и второго типа расположены в слитом белке в чередующемся порядке, например, первый, второй, первый, второй, или второй, первый, второй, первый.
В некоторых вариантах осуществления указанное дезагрегирующее соединение выбирают из FK506, рапамицина, AP22542, AP21998 и Shield-1, если слитый белок содержит домен агрегации, полученный из белка FKB (FKBP), например, FKBP F36M.
В некоторых вариантах осуществления указанный гетерологичный сайт расщепления расщепляется внутриклеточной протеазой млекопитающих.
В некоторых вариантах осуществления указанный сайт расщепления расщепляется протеазой, выбранной из группы, состоящей из фурина, PCSK1, PCSK5, PCSK6, PCSK7, катепсина B, гранзима B, фактора XA, энтерокиназы, гененазы, сортазы, PreScission протеазы, тромбина, TEV-протеазы и эластазы 1.
В некоторых вариантах осуществления указанный сайт расщепления содержит полипептид, имеющий мотив расщепления, выбранный из группы, состоящей из консенсусного мотива RX(K/R)R, консенсусного мотива RXXX[KR]R, консенсусного мотива RRX, консенсусного мотива I-E-P-D-X (SEQ ID NO: 35), Glu/Asp-Gly-Arg, Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 36), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 37), консенсусного мотива LPXTG/A, Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 38), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 40), E-N-L-Y-F-Q-G (SEQ ID NO: 41) и [AGSV]-x (SEQ ID NO: 42).
В некоторых вариантах осуществления указанный сайт расщепления расщепляется фурином.
В некоторых вариантах осуществления слитый белок содержит сайт расщепления фурина, выбранный из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135) или CKINGYPKRGRKRR (SEQ ID NO: 137).
В некоторых вариантах осуществления слитый белок содержит сайт расщепления фурина, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или GTGAEDPRPSRKRR (SEQ ID NO: 127).
В некоторых вариантах осуществления слитый белок содержит сайт расщепления фурина GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125).
В некоторых вариантах осуществления указанный гетерологичный сайт расщепления протеазы расщепляется внеклеточной протеазой млекопитающих.
В некоторых вариантах осуществления указанную внеклеточную протеазу млекопитающих выбирают из группы, состоящей из фактора XA, энтерокиназы, гененазы, сортазы, PreScission протеазы, тромбина, TEV-протеазы и эластазы 1.
В некоторых вариантах осуществления указанный сайт расщепления содержит полипептид, имеющий аминокислотную последовательность, выбранную из группы, состоящей из Glu/Asp-Gly-Arg, Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 36), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 37), консенсусного мотива LPXTG/A, Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 38), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 40), E-N-L-Y-F-Q-G (SEQ ID NO: 41) и [AGSV]-x (SEQ ID NO: 42).
В любом из вышеуказанных аспектов и вариантов осуществления гетерологичный сайт расщепления расщепляется фурином, PCSK1, PCSK5, PCSK6, PCSK7, катепсином B, гранзимом B, фактором XA, энтерокиназой, гененазой, сортазой, PreScission протеазой, тромбином, TEV-протеазой или эластазой 1. Например, сайт расщепления протеазы может содержать полипептид, имеющий мотив расщепления, выбранный из консенсусного мотива RX(K/R)R, консенсусного мотива RXXX[KR]R, консенсусного мотива RRX, консенсусного мотива I-E-P-D-X (SEQ ID NO: 35), Glu/Asp-Gly-Arg, Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 36), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 37), консенсусного мотива LPXTG/A, Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 38), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 40), E-N-L-Y-F-Q-G (SEQ ID NO: 41) или [AGSV]-x (SEQ ID NO: 42). В конкретных вариантах осуществления внеклеточную протеазу млекопитающих выбирают из фактора XA, энтерокиназы, гененазы, сортазы, PreScission протеазы, тромбина, TEV-протеазы или эластазы 1 (например, сайт расщепления может содержать полипептид, имеющий аминокислотную последовательность, выбранную из Glu/Asp-Gly-Arg, Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 36), Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 37), консенсусного мотива LPXTG/A, Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 38), Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 40), E-N-L-Y-F-Q-G (SEQ ID NO: 41) или [AGSV]-x (SEQ ID NO: 42)).
В некоторых вариантах осуществления слитый белок, описанный в настоящем документе, содержит сайт расщепления фурина. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат любой из сайтов расщепления фурина, приведенных в Таблице 20. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из RTKR (SEQ ID NO: 123) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; LQWLEQQVAKRRTKR (SEQ ID NO: 129) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLG (SEQ ID NO: 133) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; SLNLTESHNSRKKR (SEQ ID NO: 135) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; или CKINGYPKRGRKRR (SEQ ID NO: 137) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней, или GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательность, имеющую по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней.
В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135) или CKINGYPKRGRKRR (SEQ ID NO: 137). В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или GTGAEDPRPSRKRR (SEQ ID NO: 127). В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125).
В некоторых вариантах осуществления домен условной экспрессии, например, домен агрегации или домен деградации, расположен в N-концевом направлении относительно указанного второго белкового домена или C-концевом направлении относительно указанного второго белкового домена.
В некоторых вариантах осуществления указанный слитый белок также содержит сигнальный пептид в N-концевом направлении относительно указанного домена условной экспрессии, например, домена агрегации или домена деградации. В некоторых вариантах осуществления слитый белок также содержит линкер, расположенный между сигнальным пептидом и указанным доменом условной экспрессии, например, доменом агрегации или доменом деградации. В некоторых вариантах осуществления линкер представляет собой линкер в любом из слитых белков, приведенных в Таблицах 23 и 24.
В некоторых вариантах осуществления слитый белок содержит аминокислотную последовательность любого из слитых белков, приведенных в Таблицах 22, 23 или 24.
В любом из вышеуказанных аспектов и вариантов осуществления второй из белковых доменов представляет собой трансмембранный белок (например, трансмембранный рецептор). В любом из вышеуказанных аспектов трансмембранный рецептор может представлять собой, например, синтетический белок (например, химерный антигенный рецептор). Химерные антигенные рецепторы могут содержать, например, в направлении от N-конца к C-концу, антигенсвязывающий домен, трансмембранный домен и один или более внутриклеточных сигнальных доменов. Сигнальный домен может содержать один или более основных сигнальных доменов (например, cтимулирующий домен CD3-дзета) и, необязательно, один или более костимулирующих сигнальных доменов (например, внутриклеточный домен из костимулирующего белка, выбранного из CD27, CD28, 4-1BB (CD137), OX40, GITR, CD30, CD40, ICOS, BAFFR, HVEM, ICAM-1, антигена 1, ассоциированного с функцией лимфоцитов (LFA-1), CD2, CDS, CD7, CD287, LIGHT, NKG2C, NKG2D, SLAMF7, NKp80, NKp30, NKp44, NKp46, CD160, B7-H3, или лиганда, который специфически связывает CD83).
В некоторых из вышеуказанных вариантов осуществления антигенсвязывающий домен представляет собой scFv. Кроме того, антигенсвязывающий домен может связывать антиген, выбранный из CD19; CD123; CD22; CD30; CD171; CS-1; подобной лектину C-типа молекулы 1, CD33; рецептора варианта III эпидермального фактора роста (EGFRvIII); ганглиозида G2 (GD2); ганглиозида GD3; представителя семейства TNF-рецепторов, антигена созревания B-клеток (BCMA); Tn-антигена ((Tn Ag) или (GalNAcα-Ser/Thr)); простатического специфического мембранного антигена (PSMA); подобного рецепторной тирозинкиназе рецептора-сироты 1 (ROR1); Fms-подобной тирозинкиназы 3 (FLT3); опухоль-ассоциированного гликопротеина 72 (TAG72); CD38; CD44v6; канцероэмбрионального антигена (CEA); молекулы адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицы альфа-2 рецептора интерлейкина-13; мезотелина; субъединицы альфа рецептора интерлейкина-11 (IL-11Ra); антигена простатических стволовых клеток (PSCA); сериновой протеазы 21; рецептора 2 фактора роста эндотелия сосудов (VEGFR2); Lewis(Y) антигена; CD24; рецептора бета фактора роста тромбоцитов (PDGFR-бета); стадиеспецифического эмбрионального антигена-4 (SSEA-4); CD20; фолатного рецептора альфа; рецепторной тирозин-специфической протеинкиназы ERBB2 (Her2/neu); муцина 1, связанного с клеточной поверхностью (MUC1); рецептора эпидермального фактора роста (EGFR); молекулы адгезии нейронов (NCAM); простазы; простатической кислой фосфатазы (PAP); мутантного фактора элонгации 2 (ELF2M); эфрина B2; белка альфа активации фибробластов (FAP); рецептора инсулиноподобного фактора роста 1 (рецептора IGF-I), карбоангидразы IX (CAIX); субъединицы протеасомы (просома, макропаин), типа бета, 9 (LMP2); гликопротеина 100 (gp100); онкогенного слитого белка, включающего область локализации сайта инициации реаранжировки (BCR) и гомолог 1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназы; рецептора эфрина A2 (EphA2); фукозила GM1; молекулы адгезии сиалил-Льюис (sLe); ганглиозида GM3; трансглутаминазы 5 (TGS5); высокомолекулярного меланома-ассоциированного антигена (HMWMAA); o-ацетил-GD2 ганглиозида (OAcGD2); фолатного рецептора бета; опухолевого эндотелиального маркера 1 (TEM1/CD248); антигена, родственного опухолевому эндотелиальному маркеру 7 (TEM7R); клаудина 6 (CLDN6); рецептора тиреостимулирующего гормона (TSHR); связанных с G-белками рецепторов класса C, группы 5, представителя D (GPRC5D); открытой рамки считывания 61 хромосомы X (CXORF61); CD97; CD179a; киназы анапластической лимфомы (ALK); полисиаловой кислоты; плацента-специфического белка 1 (PLAC1); гексасахаридной части гликоцерамида globoH (GloboH); дифференцировочного антигена молочной железы (NY-BR-1); уроплакина 2 (UPK2); клеточного рецептора 1 вируса гепатита A (HAVCR1); адренорецептора бета-3 (ADRB3); паннексина 3 (PANX3); связанного с G-белками рецептора 20 (GPR20); комплекса лимфоцитарного антигена 6, локуса K9 (LY6K); ольфакторного рецептора 51E2 (OR51E2); белка TCR-гамма с альтернативной рамкой считывания (TARP); белка опухоли Вильмса (WT1); антигена 1 рака яичка (NY-ESO-1); антигена 2 рака яичка (LAGE-1a); меланома-ассоциированного антигена 1 (MAGE-A1); транслокационного варианта 6 гена ETS, расположенного на хромосоме 12p (ETV6-AML); белка спермы 17 (SPA17); семейства X антигенов, представителя 1A (XAGE1); ангиопоэтин-связывающего клеточного поверхностного рецептора 2 (Tie 2); антигена 1 меланомы яичка (MAD-CT-1); антигена 2 меланомы яичка (MAD-CT-2); Fos-родственного антигена 1; опухолевого белка p53 (p53); мутанта p53; простеина; сурвивина; теломеразы; опухолевого антигена 1 карциномы предстательной железы, узнаваемого T-клетками антигена меланомы 1; мутанта белка вируса крысиной саркомы (Ras); обратной транскриптазы теломеразы человека (hTERT); точек разрыва при транслокации в случае саркомы; ингибитора апоптоза из клеток меланомы (ML-IAP); ERG (слитого гена трансмембранной сериновой протеазы 2 (TMPRSS2) и ETS); N-ацетилглюкозамин трансферазы V (NA17); белка парного бокса Pax-3 (PAX3); рецептора андрогена; циклина B1; полученного из нейробластомы гомолога онкогена v-myc вируса птичьего миелоцитоматоза (MYCN); представителя C семейства гомологов Ras (RhoC); родственного тирозиназе белка 2 (TRP-2); цитохрома P450 1B1 (CYP1B1); белка, подобного CCCTC-связывающему фактору (белку «цинковый палец»), узнаваемого T-клетками антигена плоскоклеточной карциномы 3 (SART3); белка парного бокса Pax-5 (PAX5); проакрозин-связывающего белка sp32 (OY-TES1); лимфоцит-специфической протеинтирозинкиназы (LCK); якорного белка 4 A-киназы (AKAP-4); точки разрыва 2 в X при синовиальной саркоме (SSX2); рецептора для конечных продуктов усиленного гликозилирования (RAGE-1); почечного убиквитарного белка 1 (RU1); почечного убиквитарного белка 2 (RU2); легумаина; белка E6 вируса папилломы человека (HPV E6); белка E7 вируса папилломы человека (HPV E7); кишечной карбоксилэстеразы; мутантного белка теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; связанного с лейкоцитами иммуноглобулиноподобного рецептора 1 (LAIR1); Fc-фрагмента рецептора IgA (FCAR или CD89); иммуноглобулиноподобных рецепторов лейкоцитов, подсемейства A, представителя 2 (LILRA2); семейства белков, подобных молекуле CD300, представителя f (CD300LF); семейства 12 доменных лектинов C-типа, представителя A (CLEC12A); антигена 2 стромальных клеток костного мозга (BST2); белка 2, подобного EGF-подобный домен-содержащему муциноподобному гормональному рецептору (EMR2); лимфоцитарного антигена 75 (LY75); глипикана-3 (GPC3); Fc-рецептор-подобного белка 5 (FCRL5) или подобного цепи лямбда иммуноглобулина полипептида 1 (IGLL1).
В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, который связывает CD19. В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 356-368 или 381. В некоторых вариантах осуществления слитый белок содержит химерный антигенный рецептор, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 897, 902, 907, 912, 917, 922, 927, 932, 937, 942, 947, 952, 956.
В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, который связывает CD123. В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 751, 756, 761 или 766. В некоторых вариантах осуществления слитый белок содержит химерный антигенный рецептор, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 750, 755, 760 или 765.
В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, который связывает BCMA. В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 382, 386, 390, 394, 398, 402, 406, 410, 414, 418, 422, 426, 430, 434, 438, 442, 446, 450, 454, 458, 462, 466, 470, 474, 478, 482, 486, 490, 494, 498, 502, 506, 510, 514, 518, 522, 528, 531, 534 или 537. В некоторых вариантах осуществления слитый белок содержит химерный антигенный рецептор, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 789, 791, 793, 795, 797, 799, 801, 803, 805, 807, 809, 811, 813, 815, 817, 819, 821, 823, 825, 827, 829, 831, 833, 835, 837, 839, 841, 843, 845, 847, 849, 851, 853, 855, 857 или 859.
В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, который связывает CD20. В некоторых вариантах осуществления слитый белок содержит антигенсвязывающий домен, содержащий аминокислотную последовательность, занимающую положения 470-712 или 470-939 в SEQ ID NO: 3033. В некоторых вариантах осуществления слитый белок содержит химерный антигенный рецептор, содержащий аминокислотную последовательность SEQ ID NO: 3033.
Клетки, нуклеиновые кислоты и способ получения слитых белков
В другом аспекте изобретение относится к клетке, например, клетке-хозяину, содержащей любой из вышеуказанных слитых белков. В некоторых вариантах осуществления клетка, например, клетка-хозяин, представляет собой иммунную клетку, например, иммунную эффекторную клетку. В некоторых вариантах осуществления клетка представляет собой T-клетку или NK-клетку.
В другом аспекте изобретение относится к нуклеиновой кислоте (например, молекуле мРНК или ДНК), кодирующей любой из вышеуказанных слитых белков. В другом аспекте изобретение относится к вектору (например, вирусному вектору (такому как лентивирусный вектор)), содержащему такую нуклеиновую кислоту. Изобретение также относится к вирусной частице, содержащей такой вирусный вектор.
В другом аспекте изобретение относится к клетке, например, клетке-хозяину (например, человеческой T-клетке), содержащей любые из вышеуказанных векторов, нуклеиновых кислот или слитых белков.
В конкретных вариантах осуществления клетка также содержит протеазу, способную расщеплять гетерологичный сайт расщепления протеазы. В конкретных вариантах осуществления клетка-хозяин может также содержать стабилизирующее соединение (например, базедоксифен, Shield-1 или 1 мкМ 4-OHT (4-гидрокситамоксифен)), при этом указанный домен деградации принимает конформацию, способствующую деградации в клетке в отсутствие указанного стабилизирующего соединения.
В некоторых вариантах осуществления в отсутствие экспрессионного соединения, например, стабилизирующего соединения, слитый белок деградирует в клеточных путях деградации, например, по меньшей мере 50%, 60%, 70%, 80%, 90% или более слитого белка деградирует.
В некоторых вариантах осуществления в отсутствие экспрессионного соединения, например, дезагрегирующего соединения, слитый белок находится в агрегированном состоянии в клетке, например, в эндоплазматическом ретикулуме или цитозоле, например, по меньшей мере 50%, 60%, 70%, 80%, 90% или более белка находится в агрегированном состоянии.
В некоторых вариантах осуществления указанная клетка также содержит экспрессионное соединение, например, стабилизирующее соединение.
В некоторых вариантах осуществления домен условной экспрессии, например, домен деградации, принимает конформацию, более устойчивую к деградации в клетке, в присутствии экспрессионного соединения, например, стабилизирующего соединения, в сравнении с конформацией в отсутствие экспрессионного соединения.
В некоторых вариантах осуществления конформация слитого белка является более подверженной расщеплению в гетерологичном сайте расщепления протеазы в присутствии экспрессионного соединения, например, стабилизирующего соединения, в сравнении с конформацией в отсутствие экспрессионного соединения.
В некоторых вариантах осуществления уровень клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка повышен, например, в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз повышен, относительно уровня клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка в клетке, не содержащей экспрессионное соединение, например, стабилизирующее соединение.
В некоторых вариантах осуществления указанная клетка также содержит экспрессионное соединение, например, дезагрегирующее соединение.
В некоторых вариантах осуществления домен условной экспрессии, например, домен агрегации, принимает конформацию, более устойчивую к олигомеризации или агрегации, в присутствии экспрессионного соединения, например, дезагрегирующего соединения, в сравнении с конформацией в отсутствие экспрессионного соединения.
В некоторых вариантах осуществления конформация слитого белка является более подверженной расщеплению в гетерологичном сайте расщепления протеазы в присутствии экспрессионного соединения, например, дезагрегирующего соединения, в сравнении с конформацией в отсутствие экспрессионного соединения.
В некоторых вариантах осуществления уровень клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка повышен, например, в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз повышен, относительно уровня клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка в клетке, не содержащей экспрессионное соединение, например, дезагрегирующее соединение.
В другом аспекте раскрыт способ получения слитого белка, описанного в настоящем документе. Способ включает получение клетки, например, клетки-хозяина, описанной в настоящем документе, например, клетки-хозяина, содержащей любые из вышеуказанных векторов, нуклеиновых кислот или слитых белков, в условиях, подходящих для экспрессии.
В другом аспекте изобретение также относится к способу условной экспрессии интересующего белка. В одном варианте осуществления интересующий белок представляет собой трансмембранный белок, например, CAR.
В некоторых вариантах осуществления изобретение также относится к способу условной экспрессии интересующего белка, трансмембранного белка или CAR на поверхности клетки (например, иммунной клетки, например, клетки-хозяина). Способ включает:
получение клетки, например, иммунной клетки (например, клетки-хозяина), содержащей слитый белок или нуклеиновую кислоту, кодирующую слитый белок (например, любой из слитых белков, описанных в настоящем документе);
создание контакта слитого белка или клетки, содержащей указанный слитый белок, с экспрессионным соединением, при этом:
(a) в присутствии указанного экспрессионного соединения поверхностная экспрессия указанного интересующего белка, трансмембранного белка или CAR повышена, например, в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз повышена, относительно эталонного значения, например, относительно уровня поверхностной экспрессии указанного интересующего белка, трансмембранного белка или CAR в отсутствие указанного экспрессионного соединения; и
(b) в отсутствие указанного экспрессионного соединения поверхностная экспрессия указанного интересующего белка, трансмембранного белка или CAR существенно снижена, например, в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз снижена, относительно эталонного значения, например, относительно уровня поверхностной экспрессии указанного интересующего белка, трансмембранного белка или CAR в присутствии экспрессионного соединения.
В некоторых вариантах осуществления присутствие указанного экспрессионного соединения связано с, например, вызывает, изменением конформации домена условной экспрессии из первого свернутого состояния во второе свернутое состояние, при этом первое свернутое состояние более подвержено деградации, например, деградации в клетке, или агрегации, в сравнении со вторым свернутым состоянием.
В некоторых вариантах осуществления присутствие указанного экспрессионного соединения приводит к экспонированию гетерологичного сайта расщепления протеазы, например, в большей степени, например, в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз большей, чем экспонирование сайта расщепления протеазы в отсутствие указанного экспрессионного соединения.
В некоторых вариантах осуществления изобретение также относится к способу условной экспрессии интересующего белка, трансмембранного белка или CAR, включающему создание контакта клетки, например, клетки-хозяина и/или клетки, описанной в настоящем документе, со стабилизирующим соединением, при этом:
(a) в присутствии указанного стабилизирующего соединения,
(i) указанный домен деградации принимает конформацию, более устойчивую к деградации в клетке в сравнении с конформацией в отсутствие стабилизирующего соединения,
что приводит к отщеплению указанного домена деградации от указанного интересующего белка, трансмембранного белка или CAR и экспрессии указанного интересующего белка, трансмембранного белка или CAR; и
(b) в отсутствие указанного стабилизирующего соединения указанный домен деградации принимает конформацию, более подверженную деградации в клетке в сравнении с конформацией в присутствии стабилизирующего соединения, что приводит к деградации указанного интересующего белка, трансмембранного белка или CAR.
В некоторых вариантах осуществления указанная клетка контактирует с указанным стабилизирующим соединением ex vivo.
В некоторых вариантах осуществления указанная клетка контактирует с указанным стабилизирующим соединением in vivo.
В некоторых вариантах осуществления изобретение также относится к способу условной экспрессии интересующего белка, трансмембранного белка или CAR, включающему создание контакта клетки, например, клетки-хозяина и/или клетки, описанной в настоящем документе, с дезагрегирующим соединением, при этом:
(a) в присутствии указанного дезагрегирующего соединения
(i) указанный домен агрегации принимает конформацию, более устойчивую к агрегации или олигомеризации в сравнении с конформацией в отсутствие дезагрегирующего соединения,
что приводит к отщеплению указанного домена агрегации от указанного интересующего белка, трансмембранного белка или CAR и экспрессии указанного интересующего белка, трансмембранного белка или CAR; и
(b) в отсутствие указанного дезагрегирующего соединения указанный домен агрегации принимает конформацию, более подверженную агрегации или олигомеризации в сравнении с конформацией в присутствии дезагрегирующего соединения, что приводит к агрегации указанного интересующего белка, трансмембранного белка или CAR.
В некоторых вариантах осуществления указанная клетка контактирует с указанным дезагрегирующим соединением ex vivo.
В некоторых вариантах осуществления указанная клетка контактирует с указанным дезагрегирующим соединением in vivo.
В другом аспекте изобретение относится к способу лечения субъекта, имеющего заболевание, связанное с экспрессией опухолевого антигена, включающему введение субъекту эффективного количества любой из вышеуказанных клеток-хозяев, при этом второй белок представляет собой химерный антигенный рецептор и содержит, в направлении от N-конца к C-концу, антигенсвязывающий домен, трансмембранный домен и один или более внутриклеточных сигнальных доменов, и антигенсвязывающий домен специфически связывает опухолевый антиген. В другом аспекте изобретение относится к способу лечения вызываемого аутоантителами или аллоантителами заболевания или состояния, включающему введение субъекту эффективного количества вышеуказанной клетки-хозяина, при этом указанный второй белок представляет собой химерный антигенный рецептор и содержит, в направлении от N-конца к C-концу, антигенсвязывающий домен, трансмембранный домен, и один или более внутриклеточных сигнальных доменов, и указанный антигенсвязывающий домен специфически связывает антиген, специфичный для указанного вызываемого аутоантителами или аллоантителами заболевания. В таких способах клетка-хозяин может быть либо аутологичной, либо не аутологичной, например, аллогенной, для субъекта. Такие способы также могут включать этап создания контакта клетки-хозяина, in vivo или ex vivo, с вышеуказанными стабилизирующими соединениями.
В некоторых вариантах осуществления клетка контактирует с экспрессионным соединением и:
(a) в присутствии указанного экспрессионного соединения
(i) указанный домен условной экспрессии принимает конформацию, более устойчивую к деградации или агрегации в клетке в сравнении с конформацией в отсутствие указанного экспрессионного соединения, что приводит к отщеплению указанного домена условной экспрессии от указанного химерного антигенного рецептора (CAR) и экспрессии указанного CAR; и
(b) в отсутствие указанного экспрессионного соединения указанный домен условной экспрессии принимает конформацию, более подверженную деградации или агрегации в клетке в сравнении с конформацией в присутствии указанного экспрессионного соединения, что приводит к деградации или агрегации указанного слитого белка.
В некоторых вариантах осуществления клетка, например, клетка-хозяин, контактирует со стабилизирующим соединением и:
(a) в присутствии указанного стабилизирующего соединения
(i) указанный домен деградации принимает конформацию, более устойчивую к деградации в клетке в сравнении с конформацией в отсутствие указанного стабилизирующего соединения,
что приводит к отщеплению указанного домена деградации от указанного химерного антигенного рецептора (CAR) и экспрессии указанного CAR; и
(b) в отсутствие указанного стабилизирующего соединения указанный домен деградации принимает конформацию, более подверженную деградации в клетке в сравнении с конформацией в присутствии указанного стабилизирующего соединения, что приводит к деградация указанного слитого белка.
В некоторых вариантах осуществления указанное стабилизирующее соединение выбирают из базедоксифена или 4-гидрокситамоксифена (4-OHT), если слитый белок содержит домен деградации, полученный из рецептора эстрогена.
В некоторых вариантах осуществления указанное стабилизирующее соединение представляет собой Shield-1, если слитый белок содержит домен деградации, полученный из белка FKB.
В некоторых вариантах осуществления клетка контактирует с дезагрегирующим соединением и:
(a) в присутствии указанного дезагрегирующего соединения
(i) указанный домен агрегации принимает конформацию, более устойчивую к агрегации или олигомеризации в сравнении с конформацией в отсутствие указанного дезагрегирующего соединения,
что приводит к отщеплению указанного домена агрегации от указанного химерного антигенного рецептора (CAR) и экспрессии указанного CAR; и
(b) в отсутствие указанного дезагрегирующего соединения указанный домен агрегации принимает конформацию, более подверженную агрегации или олигомеризации в сравнении с конформацией в присутствии указанного дезагрегирующего соединения, что приводит к агрегации указанного слитого белка.
В некоторых вариантах осуществления указанное дезагрегирующее соединение выбирают из FK506, рапамицина, AP22542 и AP21998, если слитый белок содержит домен агрегации, полученный из белка FKB (FKBP), например, FKBP F36M.
В некоторых вариантах осуществления вызываемое аутоантителами заболевание или состояние выбирают из группы, состоящей из буллезного пемфигоида, приобретенного буллезного эпидермолиза, p200 пемфигоида, линеарного IgA-зависимого буллезного дерматоза, других заболеваний группы пемфигоидных заболеваний, герпетиформного дерматита, глютенчувствительной целиакии, миастении, синдрома Гудпасчера, гранулематоза с полиангиитом и других ANCA+ форм васкулита, аутоиммунного энцефалита с поражением лимбической системы, анти-NMDA-рецепторного энцефалита, нейромиелита зрительного нерва, аутоиммунной гемолитической анемии, вызываемого аутоантителами повреждения органов-мишеней при волчанке и других заболеваниях соединительной ткани (вызываемого анти-дцДНК, анти-Ro и другими аутоантителами), болезни Грейвса и тиреоидита Хашимото, продуцирования антител против инсулина при диабете, антител против инсулиновых рецепторов при аутоиммунной гипогликемии, криоглобулинемии, ревматоидного артрита, рассеянного склероза, синдрома Шегрена, дерматомиозита, продуцирования антител против рецепторов Fc-эпсилон при хронической идиопатической крапивнице, антител против фолатных рецепторов, антител против эндотелиальных рецепторов или против адренергических рецепторов при легочной артериальной гипертензии, рефрактерной гипертензии, расширенной кардиомиопатии, аутовоспалительного синдрома, нейромиелита зрительного нерва, синдрома Гудпасчера, анти-NMDAR энцефалита, AIHA, ITP, TTP, болезни Грейвса/Хашимото, первичного билиарного цирроза, неонатальной волчанки, продуцирования материнских аутоантител, вызывающих разрушение T-клеток, легочного альвеолярного протеиноза, продуцирования антител против фолатных рецепторов, хронической воспалительной демиелинизирующей полинейропатии и идиопатической мембранозной нефропатии. В некоторых вариантах осуществления вызываемое аллоантителами заболевание или состояние представляет собой иммунную реакцию в ответ на трансплантацию органа, переливание крови, беременность или белковую заместительную терапию.
В некоторых вариантах осуществления рак представляет собой мезотелиому (например, злокачественную мезотелиому плевры), например, у субъекта, у которого он прогрессировал при по меньшей мере одной предшествующей стандартной терапии; рак легкого (например, немелкоклеточный рак легкого, мелкоклеточный рак легкого, плоскоклеточный рак легкого или крупноклеточный рак легкого); рак поджелудочной железы (например, протоковую аденокарциному поджелудочной железы или метастатическую протоковую аденокарциному поджелудочной железы (PDA), например, у субъекта, у которого она прогрессировала при по меньшей мере одной предшествующей стандартной терапии); аденокарциному пищевода, рак яичника (например, серозный эпителиальный рак яичника, например, у субъекта, у которого он прогрессировал после по меньшей мере одной предшествующей схемы стандартной терапии), рак молочной железы, колоректальный рак, рак мочевого пузыря или любое их сочетание.
В некоторых вариантах осуществления заболевание, связанное с экспрессией опухолевого антигена, представляет собой рак.
В некоторых вариантах осуществления заболевание, связанное с экспрессией опухолевого антигена, представляет собой гематологический рак, например, гематологический рак, выбранный из лейкоза или лимфомы.
В некоторых вариантах осуществления рак выбирают из: хронического лимфоцитарного лейкоза (CLL), лимфомы из клеток мантийной зоны (MCL), множественной миеломы, острого лимфоидного лейкоза (ALL), лимфомы Ходжкина, B-клеточного острого лимфоидного лейкоза (BALL), T-клеточного острого лимфоидного лейкоза (TALL), мелкоклеточной лимфоцитарной лимфомы (SLL), B-клеточного пролимфоцитарного лейкоза, новообразования из бластных плазмацитоидных дендритных клеток, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), DLBCL, связанной с хроническим воспалением, хронического миелоидного лейкоза, миелопролиферативных новообразований, фолликулярной лимфомы, фолликулярной лимфомы у детей, волосатоклеточного лейкоза, мелкоклеточной или крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы MALT-типа (экстранодальная лимфома маргинальной зоны, возникающая из лимфоидной ткани, ассоциированной со слизистыми оболочками), лимфомы маргинальной зоны, миелодисплазии и миелодиспластического синдрома, неходжскинской лимфомы, плазмабластной лимфомы, новообразования из плазмацитоидных дендритных клеток, макроглобулинемии Вальденстрема, лимфомы маргинальной зоны селезенки, лимфомы/лейкоза клеток селезенки, диффузной мелкоклеточной В-клеточной лимфомы красной пульпы селезенки, волосатоклеточного лейкоза - варианта, лимфоплазматической лимфомы, болезни тяжелых цепей, миеломы из плазматических клеток, одиночной плазмоцитомы кости, внекостной плазмоцитомы, нодальной лимфомы маргинальной зоны, нодальной лимфомы маргинальной зоны у детей, первичной кожной фолликулярной лимфомы, лимфогранулематоза, первичной медиастинальной крупноклеточной В-клеточной лимфомы (тимуса), внутрисосудистой крупноклеточной В-клеточной лимфомы, ALK+ крупноклеточной В-клеточной лимфомы, крупноклеточной В-клеточной лимфомы, возникающей при HHV8-ассоциированной многоочаговой болезни Кастлемана, первичной эффузионной лимфомы, В-клеточной лимфомы, острого миелоидного лейкоза (AML) или неподдающейся классификации лимфомы.
В некоторых вариантах осуществления рак выбирают из MCL, CLL, ALL, лимфомы Ходжкина, AML или множественной миеломы.
В другом аспекте изобретение относится к слитому белку, клетке, нуклеиновой кислоте, вирусной частице или вектору, описанным в настоящем документе, для использования в качестве лекарственного средства.
В другом аспекте изобретение относится к слитому белку, клетке, нуклеиновой кислоте, вектору или способу, описанным в настоящем документе, для использования в лечении заболевания, при котором экспрессируется опухолевый антиген.
Способы и композиции для использования в лечении вызываемого аутоантителами или аллоантителами заболевания
В одном аспекте изобретение относится к способам лечения вызываемого аутоантителами или аллоантителами заболевания или состояния у субъекта, который нуждается в этом, включающим введение эффективного количества фармацевтической композиции, содержащей модифицированную T-клетку, субъекту, при этом модифицированная T-клетка содержит нуклеиновую кислоту, содержащую суицидный ген, и нуклеиновую кислоту, кодирующую химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен. В другом аспекте изобретение относится к способам лечения вызываемого аутоантителами или аллоантителами заболевания или состояния у субъекта, который нуждается в этом, включающим введение эффективного количества фармацевтической композиции, содержащей модифицированную T-клетку, субъекту, при этом модифицированная T-клетка содержит нуклеиновую кислоту, кодирующую домен димеризации и химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В некоторых вариантах осуществления суицидный ген кодирует аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 3005-3007.
В некоторых вариантах осуществления продукт суицидного гена также содержит домен димеризации, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3013 и 3014.
В некоторых вариантах осуществления домен димеризации содержит аминокислотную последовательность SEQ ID NO: 980.
В некоторых вариантах осуществления домен димеризации также содержит сайт расщепления фурина, содержащий аминокислотную последовательность SEQ ID NO: 980.
В некоторых вариантах осуществления CAR также содержит сигнальный пептид.
В некоторых вариантах осуществления сигнальный пептид содержит аминокислотную последовательность SEQ ID NO: 3035.
В некоторых вариантах осуществления введение эффективного количества включает активацию модифицированной T-клетки для оказания цитотоксического действия на B-клетки.
В некоторых вариантах осуществления способ дополнительно включает активацию продукта суицидного гена для индукции клеточной гибели модифицированной T-клетки.
В некоторых вариантах осуществления активация продукта суицидного гена также включает введение димеризующего средства для стимуляции димеризации продукта суицидного гена.
В некоторых вариантах осуществления активация продукта суицидного гена происходит после того, как модифицированная T-клетка оказывает цитотоксическое действие на B-клетки.
В некоторых вариантах осуществления активация продукта суицидного гена происходит после начала развития у субъекта неблагоприятной реакции на модифицированную T-клетку.
В некоторых вариантах осуществления способ дополнительно включает подавление активации продукта суицидного гена для подавления клеточной гибели модифицированной T-клетки.
В некоторых вариантах осуществления подавление активации продукта суицидного гена также включает введение солюбилизирующего средства для предотвращения димеризации продукта суицидного гена.
В некоторых вариантах осуществления введение солюбилизирующего средства происходит одновременно с введением модифицированной T-клетки и продолжается пока модифицированная T-клетка оказывает цитотоксическое действие на B-клетки.
В некоторых вариантах осуществления введение солюбилизирующего средства прекращается после начала развития у субъекта неблагоприятной реакции на модифицированную T-клетку.
В некоторых вариантах осуществления анти-B-клеточный связывающий домен CAR содержит антитело, выбранное из группы, состоящей из моноклонального антитела, поликлонального антитела, синтетического антитела, человеческого антитела, гуманизированного антитела, однодоменного антитела, одноцепочечного вариабельного фрагмента и их антигенсвязывающих фрагментов.
В некоторых вариантах осуществления анти-B-клеточный связывающий домен CAR специфически связывает B-клеточный маркер, выбранный из группы, состоящей из CD19, BCMA, CD20, CD21, CD27, CD38, CD138, а также любого их сочетания.
В некоторых вариантах осуществления анти-B-клеточный связывающий домен CAR специфически связывает B-клеточный маркер, выбранный из группы, состоящей из CD20, CD21, CD27, CD38, CD138, любого их сочетания, и по меньшей мере одного поверхностного маркера, находящегося исключительно на про-B-клетке, пре-B-клетке, незрелой B-клетке, зрелой B-клетке, B-клетке памяти и плазматической клетке.
В некоторых вариантах осуществления внутриклеточный домен CAR содержит двойные сигнальные домены.
В некоторых вариантах осуществления костимулирующий домен выбирают из группы, состоящей из CD3, CD27, CD28, CD83, CD86, CD127, 4-1BB, 4-1BBL, PD-1, PD-1L, T-клеточного рецептора (TCR), любого их производного или варианта, любой их синтетической последовательности, которая обладает такими же функциональными свойствами, а также любого их сочетания.
В некоторых вариантах осуществления способ дополнительно включает введение солюбилизирующего средства для предотвращения димеризации CAR.
В некоторых вариантах осуществления введение солюбилизирующего средства происходит одновременно с введением модифицированной T-клетки и продолжается пока модифицированная T-клетка оказывает цитотоксическое действие на B-клетки.
В некоторых вариантах осуществления введение солюбилизирующего средства прекращается после начала развития у субъекта неблагоприятной реакции на модифицированную T-клетку.
В некоторых вариантах осуществления вызываемое аутоантителами заболевание или состояние выбирают из группы, состоящей из буллезного пемфигоида, приобретенного буллезного эпидермолиза, p200 пемфигоида, линеарного IgA-зависимого буллезного дерматоза, других заболеваний группы пемфигоидных заболеваний, герпетиформного дерматита, глютенчувствительной целиакии, миастении, синдрома Гудпасчера, гранулематоза с полиангиитом и других ANCA+ форм васкулита, аутоиммунного энцефалита с поражением лимбической системы, анти-NMDA-рецепторного энцефалита, нейромиелита зрительного нерва, аутоиммунной гемолитической анемии, вызываемого аутоантителами повреждения органов-мишеней при волчанке и других заболеваниях соединительной ткани (вызываемого анти-дцДНК, анти-Ro и другими аутоантителами), болезни Грейвса и тиреоидита Хашимото, продуцирования антител против инсулина при диабете, антител против инсулиновых рецепторов при аутоиммунной гипогликемии, криоглобулинемии, ревматоидного артрита, рассеянного склероза, синдрома Шегрена, дерматомиозита, продуцирования антител против рецепторов Fc-эпсилон при хронической идиопатической крапивнице, антител против фолатных рецепторов, антител против эндотелиальных рецепторов или против адренергических рецепторов при легочной артериальной гипертензии, рефрактерной гипертензии, расширенной кардиомиопатии и аутовоспалительного синдрома.
В некоторых вариантах осуществления вызываемое аллоантителами заболевание или состояние представляет собой иммунную реакцию в ответ на трансплантацию органа, переливание крови, беременность или белковую заместительную терапию.
В некоторых вариантах осуществления модифицированную T-клетку дополнительно модифицируют путем делеции гена, выбранного из группы, состоящей из генов цепи T-клеточного рецептора (TCR), белка главного комплекса гистосовместимости, а также любых их сочетаний.
В некоторых вариантах осуществления модифицированную T-клетку дополнительно модифицируют перед введением субъекту, который нуждается в этом.
В некоторых вариантах осуществления модифицированную T-клетку дополнительно модифицируют путем индукции системы CRISPR/Cas.
В одном аспекте изобретение относится к фармацевтической композиции, сформулированной для использования в способе, описанном в настоящем документе, содержащей модифицированную T-клетку, содержащую нуклеиновую кислоту, кодирующую суицидный ген, и нуклеиновую кислоту, кодирующую химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В одном аспекте изобретение относится к фармацевтической композиции, сформулированной для использования в способе, описанном в настоящем документе, содержащей модифицированную T-клетку, содержащую нуклеиновую кислоту, кодирующую домен димеризации и химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В некоторых вариантах осуществления суицидный ген кодирует аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 3005-3007.
В некоторых вариантах осуществления продукт суицидного гена также содержит домен димеризации, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 3013 и 3014.
В некоторых вариантах осуществления домен димеризации содержит аминокислотную последовательность SEQ ID NO: 980.
В некоторых вариантах осуществления домен димеризации также содержит сайт расщепления фурина, содержащий аминокислотную последовательность SEQ ID NO: 980.
В некоторых вариантах осуществления CAR также содержит сигнальный пептид.
В некоторых вариантах осуществления сигнальный пептид содержит аминокислотную последовательность SEQ ID NO: 3035.
В некоторых вариантах осуществления композиция также содержит индуцирующее средство для индукции активации суицидного гена.
В некоторых вариантах осуществления модифицированная T-клетка лишена по меньшей мере одного гена, кодирующего цепь T-клеточного рецептора (TCR) и белок главного комплекса гистосовместимости.
В одном аспекте изобретение относится к выделенной нуклеотидной последовательности, представляющей собой нуклеотидную последовательность, содержащую (i) суицидный ген, содержащий нуклеотидную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 3001-3004, и (ii) нуклеотидную последовательность, кодирующую химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В некоторых вариантах осуществления выделенная нуклеотидная последовательность содержит SEQ ID NO: 3018, 3020, 3024, 3026, 3028 или 3030.
В одном аспекте изобретение относится к выделенному полипептиду, содержащему (i) аминокислотную последовательность, закодированную суицидным геном, при этом аминокислотную последовательность выбирают из группы, состоящей из SEQ ID NOs: 3005-3007, и (ii) химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В некоторых вариантах осуществления выделенный полипептид содержит аминокислотную последовательность SEQ ID NO: 3019, 3021, 3026, 3028, 3030 или 3034.
В одном аспекте изобретение относится к выделенной нуклеотидной последовательности, содержащей (i) нуклеиновую кислоту, кодирующую домен димеризации и (ii) химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В некоторых вариантах осуществления домен димеризации содержит аминокислотную последовательность SEQ ID NO: 980.
В некоторых вариантах осуществления выделенная нуклеотидная последовательность содержит SEQ ID NO: 977 или 3032.
В одном аспекте изобретение относится к выделенному полипептиду, содержащему (i) домен димеризации и (ii) химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В некоторых вариантах осуществления выделенный полипептид содержит аминокислотную последовательность SEQ ID NO: 978 или 3033.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ. 1 представляет собой график, показывающий экспрессию представителей семейства PCSK (пропротеин конвертаз) в первичных человеческих T-клетках. Экспрессию представителей семейства PCSK измеряли методом кОТ-ПЦР. РНК выделяли из нормальных донорских T-клеток в дни 0, 4 и 11 после стимуляции активирующими гранулами с анти-CD3/анти-CD28. В дополнительной группе в среду добавляли 100 Ед/мл IL-2 в процессе культивирования и РНК выделяли в день 11.
ФИГ. 2 представляет собой серию графиков, показывающих зависимую от соединения экспрессию CAR в T-клетках Jurkat, трансдуцированных конструктом анти-CD19 scFv CAR, слитым с указанным фуриновым доменом деградации (FKBPFD, ERαFD или DHFRFD), с последующей обработкой соответствующим стабилизирующим соединением. FKBPFD-трансдуцированные клетки обрабатывали 1 мкМ раствором Shield-1; ERαFD-трансдуцированные клетки обрабатывали 1 мкМ раствором базедоксифена; DHFRFD-трансдуцированные клетки обрабатывали 1 мМ раствором триметоприма (TMP). Экспрессию анти-CD19 scFv индуцировали стабилизирующим соединением. Черный цвет=НТ (не трансдуцированные клетки); серый цвет=конструкт, без соединения; белый цвет=конструкт, с соединением.
ФИГ. 3 представляет собой график, показывающий кинетику экспрессии CAR в T-клетках Jurkat, трансдуцированных конструктом анти-CD19 scFv CAR, слитым с указанным фуриновым доменом деградации (FKBPFD или ERαFD), с последующим добавлением стабилизирующего соединения. FKBPFD-трансдуцированные клетки обрабатывали 1 мкМ раствором Shield-1 и ERαFD-трансдуцированные клетки обрабатывали 1 мкМ раствором 4-OHT (4-гидрокситамоксифена) в течение указанного времени; и экспрессию CAR определяли методом FACS.
ФИГ. 4 представляет собой серию гистограмм, показывающих, что фуриновый дегрон-домен ERαFD может регулировать экспрессию CAR19 зависимым от базедоксифена образом в первичных человеческих T-клетках, и что стабилизация усиливается в присутствии IL-2 in vitro. Первичные человеческие T-клетки трансдуцировали доменом ERαFD, слитым с конструктом анти-CD19 scFv CAR. 100 Ед/мл IL-2 добавляли в день 9 после активации стимулирующими гранулами c анти-CD3/CD28. Базедоксифен добавляли в день 10, и экспрессию CAR определяли методом FACS в день 11.
ФИГ. 5 представляет собой пару графиков, показывающих кинетику экспрессии CAR после вымывания соединения в первичных T-клетках, трансдуцированных конструктом CAR, слитым с фуриновым доменом деградации. Первичные человеческие T-клетки трансдуцировали указанным фуриновым доменом деградации (FKBPFD или ERαFD), слитым с конструктом анти-CD19 scFv CAR. 100 Ед/мл IL-2 добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28. Базедоксифен добавляли в день 10, и T-клетки замораживали в день 11. T-клетки размораживали, обильно промывали и культивировали в течение указанных периодов времени, с последующим определением экспрессии CAR методом FACS.
ФИГ. 6 представляет собой серию графиков, показывающих, что несколько нацеленных на ERα лекарственных средств стабилизируют FurOn CART. T-клетки Jurkat трансдуцировали доменом деградации ERαFD, слитым с конструктом анти-CD19 scFv CAR, с последующей обработкой указанными соединениями в течение 24 часов. Используемыми нацеленными на ERα лекарственными средствами были: 10 мкМ 4-OHT, 1 мкМ базедоксифен или 1 мкМ лазофоксифен.
ФИГ. 7 представляет собой график, показывающий зависимую от дозы базедоксифена экспрессию ERαFD, слитого с CAR. Первичные человеческие T-клетки трансдуцировали доменом деградации ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и культивировали с базедоксифеном в указанных концентрациях в течение 48 часов. Экспрессию CAR определяли методом FACS.
ФИГ. 8 представляет собой пару графиков, показывающих зависимое от соединения специфичное для мишени уничтожение клеток FurON CART на основе ER-альфа. Первичные человеческие T-клетки трансдуцировали доменом деградации ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и базедоксифен добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали в течение 20 часов с содержащими люциферазу клетками-мишенями указанных линий, K562 (CD19-) или NALM6 (CD19+). Процент уничтожения клеток определяли путем анализа остаточной активности люциферазы.
ФИГ. 9 представляет собой пару графиков, показывающих зависимое от соединения специфичное для мишени уничтожение клеток FurON CART на основе FKBP. Первичные человеческие T-клетки трансдуцировали фуриновым доменом деградации FKBPFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и Shield-1 добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали в течение 20 часов с содержащими люциферазу клетками-мишенями указанных линий, K562 (CD19-) или NALM6 (CD19+). Процент уничтожения клеток определяли путем анализа остаточной активности люциферазы.
ФИГ. 10 представляет собой пару графиков, показывающих зависимое от соединения продуцирование цитокинов в ER-альфа FurOn CART. Первичные человеческие T-клетки трансдуцировали фуриновым доменом деградации ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и базедоксифен добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали с клетками-мишенями указанных линий в течение 20 часов. Супернатанты собирали и анализировали с помощью набора гранул с антицитокиновыми антителами.
ФИГ. 11 представляет собой график, показывающий зависимую от соединения пролиферацию ER-альфа FurOn CART. Первичные человеческие T-клетки трансдуцировали доменом деградации ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и базедоксифен добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали с клетками-мишенями указанных линий в течение 4 дней. Количество FurON-CAR T-клеток анализировали методом FACS.
ФИГ. 12A-12B представляют собой репрезентативные иммуноблоты, показывающие степень расщепления фурином различных протестированных сайтов расщепления фурина в конструктах ERα-FurON для CAR19. Протестированные сайты расщепления фурина представляют собой:
№ 105 - LQWLEQQVAKRRTKR (SEQ ID NO: 129); № 106 - GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); № 107 - GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); № 108 - GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); № 102 - SLNLTESHNSRKKR (SEQ ID NO: 135); № 103 - GTGAEDPRPSRKRR (SEQ ID NO: 127); № 104 - CKINGYPKRGRKRR (SEQ ID NO: 137); № 73 - RTKR (SEQ ID NO: 123).
ФИГ. 13 представляет собой таблицу, показывающую, что домен FurON (фуриновый дегрон) регулирует экспрессию CAR19 зависимым от стабилизирующего соединения образом в человеческих первичных T-клетках, но не влияет на жизнеспособность клеток и пролиферацию клеток.
ФИГ. 14 представляет собой серию линейных графиков, показывающих, что CAR19 с фуриновым дегрон-доменом приводит к уничтожению CD19+ клеток опухолей зависимым от дозы стабилизирующего соединения образом и является не менее эффективным, чем родительский конструкт CAR.
ФИГ. 15 представляет собой гистограмму, показывающую, что первичные человеческие T-клетки, экспрессирующие ERαFurON CAR19, секретируют IFNγ в присутствии CD19+ клеток опухолей зависимым от дозы стабилизирующего соединения образом и являются не менее эффективными, чем клетки с родительским конструктом CAR.
ФИГ. 16 представляет собой серию гистограмм, показывающих, что первичные человеческие T-клетки, экспрессирующие ERαFurON CAR19, пролиферируют в присутствии CD19+ клеток опухолей зависимым от дозы стабилизирующего соединения образом и не уступают в этом клеткам с родительским конструктом CAR19.
ФИГ. 17 представляет собой серию графиков, показывающих, что протестированные домены FurON регулируют экспрессию CAR19 в T-клетках Jurkat зависимым от соединения образом, независимо от числа мутаций; и никакой поверхностной экспрессии CAR не было обнаружено в отсутствие стабилизирующего соединения.
ФИГ. 18 представляет собой таблицу, показывающую, что домен FurON регулирует экспрессию CAR19 зависимым от стабилизирующего соединения и зависимым от IL-2 образом в человеческих первичных T-клетках. Поверхностную экспрессию CAR невозможно обнаружить в отсутствие стабилизирующего соединения базедоксифена, когда фрагмент FurON слит с CAR19.
ФИГ. 19A-19B представляют собой линейные графики, показывающие, что CAR T-клетки, экспрессирующие FurON CAR19, имеющий ограниченное число мутаций в дегрон-домене, уничтожают CD19+ клетки опухолей зависимым от стабилизирующего соединения и зависимым от мишени образом, и являются не менее эффективными, чем клетки с родительским конструктом CAR.
ФИГ. 20 представляет собой гистограмму, показывающую, что CAR T-клетки, экспрессирующие FurON CAR19, имеющий ограниченное число мутаций в дегрон-домене, секретируют цитокины в присутствии CD19+ клеток опухолей зависимым от стабилизирующего соединения образом и не уступают в этом клеткам с родительским конструктом CAR.
ФИГ. 21 представляет собой гистограмму, показывающую, что CD3+ T-клетки, содержащие FurON CAR19, пролиферируют в присутствии CD19+ клеток опухолей зависимым от стабилизирующего соединения образом и не уступают в этом клеткам с родительским конструктом CAR.
ФИГ. 22 представляет собой серию графиков, показывающих, что домен FurON регулирует экспрессию CAR123 в первичных человеческих T-клетках зависимым от стабилизирующего соединения образом.
ФИГ. 23 представляет собой серию гистограмм, показывающих, что CAR T-клетки, экспрессирующие FurON CAR123, уничтожают CD123+ клетки опухолей зависимым от стабилизирующего соединения и зависимым от мишени образом, и являются не менее эффективными, чем клетки с родительским конструктом CAR.
ФИГ. 24 представляет собой серию гистограмм, показывающих, что CAR T-клетки, экспрессирующие FurON CAR123, секретируют цитокины в присутствии CD123+ клеток опухолей зависимым от стабилизирующего соединения образом и не уступают в этом клеткам с родительским конструктом CAR.
ФИГ. 25 представляет собой схематическое изображение иллюстративного слитого белка, содержащего домен деградации (дегрон), сайт расщепления протеазы и второй белковый домен (CAR), а также изменение деградации слитого белка в присутствии лекарственного средства, например, стабилизирующего соединения.
ФИГ. 26 представляет собой схематическое изображение иллюстративного слитого белка, содержащего четыре копии домена агрегации (FKBP12F36M), сайт расщепления протеазы (сайт расщепления фурина) и второй белковый домен (scFv с цитоплазматическим «хвостом»), а также изменение агрегации слитого белка в присутствии соединения, например, дезагрегирующего соединения. Данная фигура является иллюстрацией регуляторной системы onCAR, которая представляет собой другой вариант осуществления для контроля клеточной поверхностной экспрессии и, таким образом, функции CAR. CAR экспрессируется далее по ходу транскрипции от модифицированных доменов FKBP12, с разделением сайтом расщепления фурина. В отсутствие солюбилизирующего соединения молекулы CAR спонтанно агрегируют в эндоплазматическом ретикулуме и меньшее число молекул CAR могут выходить на поверхность T-клетки, например, никакие молекулы CAR. Это приводит к ослаблению опосредованной CAR функции T-клеток, например, отсутствию опосредованной CAR функции T-клеток. В присутствии солюбилизирующего соединения домены агрегации CAR разделены, и агрегация предотвращается. Сайт расщепления фурина, который находится в N-концевом положении по отношению к scFv, становится доступным для расщепления. После удаления доменов агрегации фурином в поздних цистернах аппарата Гольджи, молекулы CAR выходят на поверхность T-клеток и может осуществляться CAR-опосредованная функция T-клеток.
ФИГ. 27 представляет собой иллюстрацию конструкта анти-CD19 или анти-CD20 химерного антигенного рецептора с суицидным переключателем (индуцируемой каспазой-9 или iCasp9, или iC9), называемого CD19 sCAR или CD20 sCAR, сконструированного для индукции полного, но временного истощения B-клеток. CD19/CD20 sCAR T-клетки проявляют свой терапевтический эффект за счет истощения B-клеток после инфузии. Последующее введение низкомолекулярных соединений приводит к димеризации каспазы-9 и активации каспазной активности, что приводит к самоуничтожению CD19/CD20 sCAR T-клеток, вследствие чего может происходить восстановление популяции B-клеток.
ФИГ. 28 представляет собой схематическое изображение обратимой суицидной кассеты каспазы-9, которая представляет собой другой вариант осуществления суицидной кассеты каспазы-9. В системе CD19/CD20 revCAR каспаза-9 конститутивно экспрессируется и спонтанно димеризуется, тем самым по умолчанию индуцируя апоптоз в CD19 revCAR T-клетках. В присутствии низкомолекулярного соединения, которое солюбилизирует молекулы каспазы-9 (то есть, ингибирует димеризацию), активность каспазы ингибируется. Таким образом, обработка низкомолекулярным солюбилизатором приводит к ингибированию активности каспазы-9 в процессе размножения и инфузии revCAR T-клеток, и удаление низкомолекулярного солюбилизатора приводит к активации каспазы-9 и самоуничтожению revCAR T-клеток, вследствие чего может происходить восстановление популяции B-клеток.
ФИГ. 29A-29F представляют собой серию графиков, показывающих эффективную экспрессию конструктов CD19 sCAR, CD19revCAR и CD20 CAR в первичных человеческих T-клетках.
ФИГ. 30 представляет собой график, показывающий специфическое уничтожение мишеней in vitro CD19 sCAR клетками. NALM6 представляет собой линию B-клеток, экспрессирующих CD19 (дт, дикого типа). CD19 sCAR T-клетки уничтожали CD19+ NALM6 клетки, при этом не трансдуцированные (НТ) T-клетки или T-клетки, экспрессирующие контрольный sCAR (отрицательный контроль), не узнавали клетки NALM6 дт.
ФИГ. 31 представляет собой график, показывающий специфическую и надежную элиминацию CD19 sCAR T-клеток после активации суицидного переключателя каспазы-9 с помощью AP20187. CAR T-клетки инкубировали в присутствии AP20187 в указанных концентрациях в течение 16 часов при 37°C. Мертвые клетки обнаруживали при помощи фиолетового красителя для окрашивания живых/мертвых клеток и количественно определяли методом проточной цитометрии. Только T-клетки, экспрессирующие индуцируемую каспазу, были элиминированы (содержащие FMC63 iC9 или CD19 sCAR, а также iC9 контрольный CAR). T-клетки, не экспрессирующие контрольный CAR, не были затронуты (не трансдуцированные, НТ, или с контрольным CAR, не экспрессирующие iC9).
ФИГ. 32 представляет собой график, показывающий, что CD19 sCAR T-клетки, экспрессирующие индуцируемую каспазу-9, являются эффективными in vivo. Мышам NSG вводили инъекцией 1×106 CD19+ клеток NALM6. Через пять дней мышам вводили либо CD19 CAR T-клетки, экспрессирующие индуцируемую каспазу-9, или не трансдуцированные контрольные T-клетки.
ФИГ. 33 представляет собой график, показывающий обнаружение CD19 sCAR T-клеток, экспрессирующих индуцируемую каспазу-9, в крови и селезенке методом проточной цитометрии после завершения in vivo эксперимента, что указывало на приживление клеток.
ФИГ. 34 представляет собой серию графиков, показывающих результаты анализа на уничтожение: CD20sCAR, 20revCAR и CD20 onCAR. 4-часовой анализ с высвобождением хрома для оценки уничтожения клеток NALM6, сконструированных для экспрессии CD20. Kдт=клетки K562 дикого типа, которые являются CD20-отрицательными, служили в качестве посторонней мишени для демонстрации специфического уничтожения. CD20sCAR, 20revCAR и CD20 onCAR демонстрируют эквивалентное и специфическое уничтожение CD20+ клеток-мишеней. On-CAR тестировали в присутствии 500 нМ раствора Shield-1.
ФИГ. 35 представляет собой серию гистограмм, показывающих, что в отсутствие солюбилизирующего лиганда FKBP (например, shield-1) ингибируется функция CAR. Показано уменьшение, в процентах, уничтожения в отсутствие shield-1, относительно уничтожения в присутствии 500 нМ shield-1. Клетки Jeko экспрессируют CD20. При более низком значении соотношения Э:М функция On-CAR сильно ингибируется в отсутствие лиганда FKBP.
ФИГ. 36 представляет собой серию графиков, показывающих модуляцию поверхностной экспрессии CAR лигандом FKBP Shield-1. CD20 on-CAR T-клетки окрашивали на экспрессию CAR и строили график зависимости средней интенсивности флуоресценции (СИФ, измеренная методом проточной цитометрии) сигнала CAR от концентрации Shield-1. Shield-1 вызывает зависимое от дозы увеличение экспрессии CAR. Отсутствие Shield-1 приводит к ~60% уменьшению экспрессии CD20 on-CAR (нижний график).
ФИГ. 37 представляет собой серию графически представленных результатов проточной цитометрии, показывающих титрование Shield-1 для CD19rev CAR. CD19rev CAR T-клетки (~38% трансдуцированных) инкубировали с Shield-1 в разных дозах в течение 24 ч для оценки зависимой от дозы активации каспазы-9. Оставшиеся CAR+ клетки количественно определяли методом проточной цитометрии. В системе CD19rev CAR более низкие дозы Shield-1 приводили к более высокой активации каспазы-9 и увеличению апоптоза (меньшая доля CAR+ клеток).
ФИГ. 38 представляет собой график, показывающий in vivo оценку эффективности апоптоза в анти-CD19 revCAR T-клетках. Клетки NALM6 (экспрессирующие люциферазу щелкунов), которые являются CD19-положительными, вводили инъекцией (в/в) мышам NSG в день 0. В день 4 мышам вводили инъекцией T-клетки с нацеленным на CD19 revCAR, 19sCAR, или посторонние (не трансдуцированные) T-клетки. Сигналы биолюминесценции клеток NALM6 количественно определяли в указанных временных точках. Получавшим revCAR мышам дважды вводили инъекцией 10 мг/кг aquashield-1 в указанных временных точках, ожидалось, что эти инъекции будут недостаточными для сохранения revCAR T-клеток живыми. Таким образом, кривые биолюминесценции для получавших revCAR и НТ клетки мышей сильно перекрываются, свидетельствуя о достаточном in vivo апоптозе revCAR T-клеток.
ФИГ. 39 представляет собой схематическое изображение временной шкалы и график, показывающий in vivo эффективность CD19 revCAR T-клеток. Клетки NALM6 (экспрессирующие люциферазу щелкунов), которые являются CD19-положительными, вводили инъекцией (в/в) мышам NSG в день 0. В день 4 мышам имплантировали осмотические инфузионные насосы для секреции aquashield-1 в дозе 20 мг/кг/сутки. CD19rev CAR T-клетки вводили инъекцией через 4 часа после успешной имплантации насоса (нижний график, черная стрелка). Сигналы биолюминесценции клеток NALM6 количественно определяли в указанных временных точках. Инфузионные насосы секретировали aquashield-1 в течение 7 дней, после чего биолюминесценция клеток NALM6 начала увеличиваться (кривые CD19 revCAR).
ФИГ. 40 представляет собой серию графиков проточной цитометрии, показывающих, что активация самоуничтожения приводит к периферическому истощению суицидных CAR T-клеток. Мышам вводили инъекцией клетки NALM6 и через 5 дней вводили CD19 sCAR T-клетки. Перед инъекцией CD19 sCAR T-клетки были подвергнуты сортировке, основанной на экспрессии scFV. Диаграммы проточной цитометрии показывают периферические T-клетки (CD3+, CD45+) в день 8 и день 26. CD19 sCAR T-клетки были истощены в день 10 в результате инъекции AP1903 (10 мг/кг). В случае мышей, получавших AP1903, 2 графика слева показывают, что T-клетки с трудом поддаются обнаружению после активации самоуничтожения, и в случае мышей, получавших растворитель, 2 графика справа показывают стабильное процентное содержание T-клеток.
ФИГ. 41 представляет собой серию графиков, показывающих, что активация самоуничтожения приводит к периферическому истощению sCAR T-клеток. Количественное определение T-клеток выполняли для нескольких мышей. Мышам вводили AP1903 в день 10 для истощения sCAR T-клеток. После введения процентное содержание T-клеток уменьшалось в группе получения AP1903, в отличие от группы получения растворителя.
ФИГ. 42 представляет собой серию изображений и графиков, показывающих, что активация самоуничтожения приводит к истощению sCAR T-клеток в лимфоидных органах. Верхняя секция изображений: селезенки мышей собирали спустя >2 недель после введения AP1903 и окрашивали на CD3 человека; у получавших AP1903 мышей T-клетки не поддаются обнаружению, в отличие от мышей, получавших растворитель. Нижний график: проводили количественную ПЦР для обнаружения sCAR T-клеток в селезенках мышей, получавших AP1903 и растворитель, результаты показывают почти полное отсутствие sCAR у большинства мышей.
ФИГ. 43 представляет собой схематическое изображение хронологической последовательности действий и графики, показывающие, что для использования BT (костный мозг, печень, тимус) мышей в качестве реципиентов необходимы «универсальные» T-клетки, у которых отсутствует экспрессия TCR и MHCI. T-клетки трансдуцировали в день 1 после активации с помощью CD19 sCAR-кодирующего лентивируса, в клетки методом электропорации вводили направляющую РНК Cas9 в день 3 (10 мкг/106 клеток) и вновь в день 4 методом электропорации вводили направляющие РНК, нацеленные на бета-цепь TCR и бета-2-микроглобулин. Диаграммы проточной цитометрии показывают экспрессию sCAR19 в 45,2% клеток через 10 дней после активации и двойной нокаут бета-цепи TCR и бета-2-микроглобулина в ~20% клеток. Схема показывает временную шкалу для получения T-клеток.
ФИГ. 44 представляет собой схематическое изображение хронологической последовательности действий для дизайна in vivo эксперимента по настоящему изобретению. Использовали BT (костный мозг, печень и тимус) мышей для оценки функции универсального sCAR в нераковой мышиной модели. Человеческие эмбриональные костный мозг и тимус имплантировали мышам NSG в день -91. Оценку приживаемости проводили методом проточной цитометрии в день -27. Универсальные T-клетки, экспрессирующие CD19 sCAR T-клетки, вводили инъекцией в день 0, истощение B-клеток оценивали в день 10, и мышам вводили AP1903 (3 ежедневные инъекции по 10 мг/кг). Выживание sCAR оценивали методом кПЦР.
ФИГ. 45 представляет собой серию графиков проточной цитометрии, показывающих, что «универсальные» sCAR T-клетки вызывают истощение периферических B-клеток у не аутологичных BT (костный мозг, печень и тимус) мышей. Универсальные CAR T-клетки были способны вызывать истощение человеческих B-клеток в нераковой гуманизированной мышиной модели. Диаграммы проточной цитометрии в день 0 и день 10 показывают полное отсутствие CD19-положительных клеток в периферическом кровообращении.
ФИГ. 46 представляет собой график, показывающий, что универсальные sCAR T-клетки могут быть истощены при введении AP1903. Проводили количественную ПЦР для обнаружения sCAR T-клеток в периферической крови у мышей, получавших AP1903 и растворитель, результаты показывают почти полное отсутствие sCAR в 2/3 мышей. Для определения в периферической крови числа копий WPRE проводили кПЦР с гДНК через 4 недели после введения AP1903.
ФИГ. 47 представляет собой график, показывающий, что рост опухоли CD19+ NALM6 был ингибирован у мышей, которым инфузией вводили CART19 или инфузией вводили FurON CART19, и которые получали BZA, с добавлением или без добавления IL2.
ПОДРОБНОЕ ОПИСАНИЕ
В целом, изобретение относится к регулируемой экспрессии рекомбинантных слитых белков. Эта регуляция имеет место при экспрессии слитых белков, содержащих интересующий белок, слитый с доменом условной экспрессии, например, доменом деградации (в данной области часто называемым «дегрон») или доменом агрегации. Как правило, такие домены деградации сворачиваются в стабильную конформацию только в присутствии определенного лиганда (например, растворимого лиганда или лиганда, связанного со слитым белком). В отсутствие такого лиганда домен деградации принимает дезорганизованную структуру, что приводит к деградации всего слитого белка за счет естественных внутриклеточных механизмов. Как правило, такие домены агрегации соединяются в олигомеры и/или агрегируют в отсутствие определенного лиганда (например, растворимого лиганда или лиганда, связанного со слитым белком), что приводит к агрегации и/или секвестрации всего слитого белка. Изобретение основано на понимании того, что домен деградации или домен агрегации может быть отделен от интересующего белка сайтом расщепления (например, сайтом расщепления протеазы) при экспрессии в стабилизирующих условиях (например, в присутствии стабилизирующего соединения) или дезагрегирующих условиях (например, в присутствии дезагрегирующего соединения). Таким образом, в отсутствие когнатной протеазы слитый белок, содержащий домен деградации, не будет подвержен деградации лишь в присутствии стабилизирующего соединения, и слитый белок, содержащий домен агрегации, не будет подвержен агрегации лишь в присутствии дезагрегирующего соединения. Однако после того, как сайт расщепления расщепляется когнатной протеазой, присутствие стабилизирующего соединения или дезагрегирующего соединения больше не является необходимым для того, чтобы интересующий белок не подвергался деградации или агрегации, поскольку он более не связан с доменом деградации или доменом агрегации. Таким образом, в начале экспрессии слитый белок, содержащий домен деградации, подвержен деградации и слитый белок, содержащий домен агрегации, подвержен агрегации, однако после расщепления полученный интересующий белок становится неотличимым от его не слитого аналога.
Таким образом, слитые белки по изобретению содержат три основных элемента: домен условной экспрессии (например, домен деградации или домен агрегации), домен, содержащий интересующий белок, и расщепляемый домен, разделяющий эти два домена. В каждом из этих элементов конкретные домены являются взаимозаменяемыми и описаны ниже. Примечательно, что слитый белок может быть организован так, что домен условной экспрессии расположен либо в N-концевом, либо в C-концевом направлении относительно интересующего белка. Однако в конкретных вариантах осуществления домен условной экспрессии расположен в N-концевом направлении относительно интересующего белка. В таких вариантах осуществления, если домен условной экспрессии представляет собой домен деградации, домен деградации, будучи дезорганизованным, делает весь слитый белок мишенью для деградации до расщепления расщепляемого домена. В случае C-концевого слияния, сайт расщепления протеазы должен быть ориентирован в сторону компартмента, в котором находится протеаза. В конкретном случае с фурином, C-концевой дегрон должен быть направлен в сторону просвета эндоплазматического ретикулума и аппарата Гольджи.
Определения
Используемый в настоящем документе термин «домен условной экспрессии» означает домен слитого белка, который имеет первое состояние и второе состояние, например, состояния агрегации или конформационные состояния, например, состояния стабилизации/дестабилизации или состояния правильного/неправильного сворачивания. Первое состояние связано с, является причиной, или опосредует клеточную поверхностную экспрессию или внеклеточную экспрессию одного или более (например, всех) фрагментов слитого белка в первой степени, или на первом уровне, и второе состояние связано с, является причиной, или опосредует клеточную поверхностную экспрессию или внеклеточную экспрессию одного или более (например, всех) фрагментов слитого белка во второй степени, или на втором уровне. В отсутствие экспрессионного соединения, при экспрессии в интересующей клетке большая часть слитого белка, содержащего домен условной экспрессии, не поддается обнаружению, как на клеточной поверхности, так и за пределами клетки. И наоборот, в присутствии экспрессионного соединения поверхностная экспрессия и/или внеклеточная экспрессия одного или более (например, всех) доменов слитого белка существенно возрастает. Таким образом, домен условной экспрессии обладает следующими характеристиками: (1) он не присутствует естественным образом в контексте слитого белка; (2) поверхностная экспрессия и/или внеклеточная экспрессия регулируется котрансляционно или посттрансляционно; (3) степень поверхностной экспрессии и/или внеклеточной экспрессии существенно возрастает в присутствии экспрессионного соединения. В вариантах осуществления домен условной экспрессии представляет собой домен деградации, например, описанный в настоящем документе. В других вариантах осуществления домен условной экспрессии представляет собой домен агрегации, например, описанный в настоящем документе. В вариантах осуществления слитый белок, содержащий домен условной экспрессии, содержит химерный антигенный рецептор (CAR), например, описанный в настоящем документе. В вариантах осуществления слитый белок содержит гетерологичный сайт расщепления протеазы, расположенный между доменом условной экспрессии и вторым доменом. В таких вариантах осуществления в отсутствие экспрессионного соединения сайт расщепления протеазы большой части слитых белков является недоступным для когнатной протеазы, и судьба слитого белка в клетке определяется доменом условной экспрессии. В присутствии экспрессионного соединения сайт расщепления протеазы большой части слитых белков становится доступным для когнатной протеазы, домен условной экспрессии отщепляется от слитого белка, и на судьбу оставшейся части слитого белка в клетке больше не влияет домен условной экспрессии.
Используемый в настоящем документе термин «домен агрегации» означает домен слитого белка, вызывающий внутриклеточную агрегацию слитого белка. В отсутствие дезагрегирующего соединения, при экспрессии в интересующей клетке большая часть слитого белка, содержащего домен агрегации, находится в агрегатах, которые, например, секвестрированы в клетке до достижения завершающих стадий экспрессии, например, до экспрессии на поверхности клетки или до внеклеточной секреции. И наоборот, в присутствии дезагрегирующего соединения поверхностная экспрессия и/или внеклеточная экспрессия одного или более (например, всех) доменов слитого белка существенно возрастает. Таким образом, домен агрегации обладает следующими характеристиками: (1) он не присутствует естественным образом в контексте слитого белка; (2) поверхностная экспрессия и/или внеклеточная экспрессия регулируется котрансляционно или посттрансляционно; (3) степень поверхностной экспрессии и/или внеклеточной экспрессии существенно возрастает в присутствии дезагрегирующего соединения. В вариантах осуществления домен агрегации содержит один или более, например, 1, 2, 3, 4, 5, 6, 7 или более, повторов домена димеризации. В вариантах осуществления домен димеризации представляет собой домен гомодимеризации. В других вариантах осуществления домен димеризации представляет собой домен гетеродимеризации.
Используемый в настоящем документе термин «экспрессионное соединение» означает соединение, которое при добавлении в клетку, экспрессирующую слитый белок, содержащий домен условной экспрессии, связывается с доменом условной экспрессии и приводит к увеличению поверхностной экспрессии и/или внеклеточной экспрессии одного или более (например, всех) доменов слитого белка. Экспрессионные соединения могут быть природными или синтетическими.
Используемый в настоящем документе термин «дезагрегирующее соединение» означает соединение, которое при добавлении в клетку, экспрессирующую слитый белок, содержащий домен агрегации, связывается с доменом агрегации и приводит к увеличению поверхностной экспрессии и/или внеклеточной экспрессии одного или более (например, всех) доменов слитого белка. Дезагрегирующие соединения могут быть природными или синтетическими.
Термин «домен деградации» означает домен слитого белка, который принимает стабильную конформацию при экспрессии в присутствии стабилизирующего соединения. В отсутствие стабильной конформации, при экспрессии в интересующей клетке большая часть доменов деградации (и, как правило, любой белок, с которым они слиты) будет подвергаться деградации за счет эндогенного клеточного аппарата. Примечательно, что домен деградации не является естественным доменом белка, а сконструирован, чтобы быть нестабильным в отсутствие контакта со стабилизирующим соединением. Таким образом, домен деградации обладает следующими характеристиками: (1) он не является естественным; (2) его экспрессия регулируется котрансляционно или посттрансляционно за счет увеличения или уменьшения степени деградации; (3) степень деградации существенно снижена в присутствии стабилизирующего соединения. В некоторых вариантах осуществления домен деградации не приводит к агрегации слитых белков. В некоторых вариантах осуществления в отсутствие стабилизирующего соединения домен деградации или другой домен слитого белка практически не поддается обнаружению в, или на, клетке.
В настоящем документе термины «деагрегация» и «дезагрегация» используют взаимозаменяемо.
Используемые в настоящем документе термины «слитый белок» или «химерный белок» означают белок, созданный путем соединения двух или более гетерологичных белковых доменов в один непрерывный белок.
Термин «гетерологичный» относится к домену (например, белковому домену), который имеет иное происхождение (то есть, не является естественным образом связанным с по меньшей мере одним из других эталонных доменов), чем один или более белковых доменов, с которыми он слит. Кроме того, «гетерологичный сайт расщепления протеазы» означает сайт расщепления протеазы, который не расщепляется каким-либо доменом слитого белка, в котором он находится.
Термин «протеаза» означает белок, который расщепляет другой белок в случае присутствия сайта расщепления в белке, который будет расщеплен.
Термин «внутриклеточная протеаза» означает протеазу, которая естественным образом экспрессируется внутри интересующей клетки.
Термин «внеклеточная протеаза» означает протеазу, которая естественным образом экспрессируется в организме (например, млекопитающего) и секретируется или экспонируется снаружи клеток (например, в крови или на поверхности кожи).
Термины «соединение стабилизации» или «стабилизирующее соединение» означают соединение, которое при добавлении в клетку, экспрессирующую домен деградации, стабилизирует домен деградации и приводит к уменьшению степени, в которой он впоследствии деградирует. Соединения стабилизации или стабилизирующие соединения могут быть природными или синтетическими.
Грамматическая форма единственного числа существительных означает «один или более, чем один» (то есть, по меньшей мере один). В качестве примера, «элемент» означает один элемент или более, чем один элемент.
Термин «примерно», применительно к измеримой величине, такой как количество, продолжительность по времени и тому подобное, должен включать вариации в размере ±20% или в некоторых случаях ±10%, или в некоторых случаях ±5%, или в некоторых случаях ±1%, или в некоторых случаях ±0,1%, от конкретного значения, поскольку такие вариации подходят для осуществления раскрытых способов.
Термин «химерный антигенный рецептор» или, альтернативно, «CAR» означает рекомбинантный полипептидный конструкт, содержащий по меньшей мере внеклеточный антигенсвязывающий домен, трансмембранный домен и цитоплазматический сигнальный домен (также называемый в настоящем документе «внутриклеточный сигнальный домен»), содержащий функциональный сигнальный домен, полученный из стимулирующей молекулы, описанной ниже. В некоторых вариантах осуществления домены в полипептидном конструкте CAR находятся в одной и той же полипептидной цепи, например, составляют химерный слитый белок. В некоторых вариантах осуществления домены в полипептидном конструкте CAR не являются смежными, например, находятся в разных полипептидных цепях, например, в регулируемом химерном антигенном рецепторе (RCAR).
В одном аспекте стимулирующая молекула представляет собой дзета-цепь, ассоциированную с T-клеточным рецепторным комплексом. В одном аспекте цитоплазматический сигнальный домен содержит основной сигнальный домен (например, основной сигнальный домен CD3-дзета). В одном аспекте цитоплазматический сигнальный домен также содержит один или более функциональных сигнальных доменов, полученных из по меньшей мере одной костимулирующей молекулы, описанной ниже. В одном аспекте костимулирующую молекулу выбирают из 4 1BB (то есть, CD137), CD27, ICOS и/или CD28. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий функциональный сигнальный домен, полученный из костимулирующей молекулы, и функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий два функциональных сигнальных домена, полученных из одной или более костимулирующих молекул, и функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит химерный слитый белок, содержащий внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный сигнальный домен, содержащий по меньшей мере два функциональных сигнальных домена, полученных из одной или более костимулирующих молекул, и функциональный сигнальный домен, полученный из стимулирующей молекулы. В одном аспекте CAR содержит, необязательно, лидерную последовательность на амино-конце (N-конце) слитого белка CAR. В одном аспекте CAR также содержит лидерную последовательность на N-конце внеклеточного антигенсвязывающего домена, при этом лидерная последовательность, необязательно, отщепляется от узнающего антиген домена (например, scFv) во время клеточного процессинга и локализации CAR на клеточной мембране.
CAR, содержащий антигенсвязывающий домен (например, scFv или TCR), который нацелен на, например, связывает, специфический антиген X, такой как те, которые описаны в настоящем документе, также называют XCAR, X-CAR или X-нацеленный CAR. Например, CAR, содержащий антигенсвязывающий домен, который нацелен на CD19, называют CD19 CAR.
Термин «сигнальный домен» означает функциональную часть белка, которая действует, передавая информацию внутри клетки для регуляции клеточной активности через определенные сигнальные пути за счет создания вторичных мессенджеров, или функционируя в качестве эффектора за счет ответа на такие мессенджеры. В некоторых аспектах сигнальный домен CAR, описанных в настоящем документе, получен из стимулирующей молекулы или костимулирующей молекулы, описанных в настоящем документе, либо представляет собой синтезированный или рекомбинантный сигнальный домен.
Используемый в настоящем документе термин «антитело» означает белковую или полипептидную последовательность, полученную из молекулы иммуноглобулина, которая специфически связывается с антигеном. Антитела могут представлять собой поликлональные или моноклональные, многоцепочечные или одноцепочечные, либо интактные иммуноглобулины, и могут быть получены из природных источников или из рекомбинантных источников. Антитела могут представлять собой тетрамерные молекулы иммуноглобулинов.
Термин «фрагмент антитела» означает по меньшей мере одну часть интактного антитела, или его рекомбинантных вариантов, и относится к антигенсвязывающему домену, например, узнающей антиген вариабельной области интактного антитела, которая достаточна для обеспечения узнавания и специфического связывания фрагмента антитела с мишенью, такой как антиген. Примеры фрагментов антител включают, но без ограничения, фрагменты Fab, Fab', F(ab')2 и Fv, фрагменты scFv антител, линейные антитела, однодоменные антитела, такие как sdAb (либо VL, либо VH), домены VHH верблюдовых и мультиспецифические антитела, образованные из фрагментов антител, такие как двухвалентный фрагмент, содержащий два Fab-фрагмента, связанные дисульфидным мостом в шарнирной области, а также выделенные CDR или другие связывающие эпитоп фрагменты антитела. Антигенсвязывающий фрагмент также может быть включен в однодоменные антитела, макситела, минитела, нанотела, интратела, диатела, триатела, тетратела, v-NAR и бис-scFv (смотри, например, Hollinger and Hudson, Nature Biotechnology 23:1126-1136, 2005). Антигенсвязывающие фрагменты также могут быть привиты на каркасы на основе таких полипептидов, как фибронектин III типа (Fn3) (смотри патент США №: 6703199, в котором описаны минитела на основе полипептида фибронектина).
Термин «scFv» означает слитый белок, содержащий по меньшей мере один фрагмент антитела, содержащий вариабельную область легкой цепи, и по меньшей мере один фрагмент антитела, содержащий вариабельную область тяжелой цепи, причем вариабельные области легкой и тяжелой цепей располагаются рядом, связанные коротким гибким полипептидным линкером, и могут экспрессироваться в виде одноцепочечного полипептида, и при этом scFv сохраняет специфичность интактного антитела, из которого он получен. Если нет иных указаний, описанные в настоящем документе scFv могут иметь вариабельные области VL и VH в любом порядке, например, относительно N-конца и C-конца полипептида scFv может содержать VL-линкер-VH или может содержать VH-линкер-VL.
Используемый в настоящем документе термин «определяющая комплементарность область» или «CDR» означает аминокислотные последовательности в вариабельных областях антитела, которые отвечают за антигенную специфичность и аффинность связывания. Например, как правило, имеются три области CDR в каждой вариабельной области тяжелой цепи (например, HCDR1, HCDR2 и HCDR3) и три области CDR в каждой вариабельной области легкой цепи (LCDR1, LCDR2 и LCDR3). Точные границы аминокислотной последовательности конкретной CDR могут быть определены с использованием любого количества хорошо известных систем, включая те, которые описаны в публикациях Kabat et al. (1991), «Sequences of Proteins of Immunological Interest» 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (система нумерации «Kabat»), Al-Lazikani et al., (1997) JMB 273, 927-948 (система нумерации «Chothia»), или их сочетания. В соответствии с системой нумерации Kabat, в некоторых вариантах осуществления аминокислотные остатки CDR в вариабельном домене тяжелой цепи (VH) имеют номера 31-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3); и аминокислотные остатки CDR в вариабельном домене легкой цепи (VL) имеют номера 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3). В соответствии с системой нумерации Chothia, в некоторых вариантах осуществления аминокислоты CDR в VH имеют номера 26-32 (HCDR1), 52-56 (HCDR2) и 95-102 (HCDR3); и аминокислотные остатки CDR в VL имеют номера 26-32 (LCDR1), 50-52 (LCDR2) и 91-96 (LCDR3). В соответствии с комбинированной системой нумерации Kabat и Chothia, в некоторых вариантах осуществления области CDR соответствуют аминокислотным остаткам, которые являются частью Kabat CDR, Chothia CDR, или и тех и других. Например, в некоторых вариантах осуществления области CDR соответствуют аминокислотным остаткам 26-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3) в VH, например, VH млекопитающего, например, VH человека; и аминокислотным остаткам 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3) в VL, например, VL млекопитающего, например, VL человека.
Часть CAR по изобретению, содержащая антитело или фрагмент антитела, может существовать в различных формах, в которых антигенсвязывающий домен экспрессируется в виде части непрерывной полипептидной цепи, содержащей, например, фрагменты scFv антитела, линейные антитела, однодоменные антитела, такие как sdAb (либо VL, либо VH), домены VHH верблюдовых, гуманизированное антитело, биспецифическое антитело, конъюгат антитела (Harlow et al., 1999, в: Using Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory Press, NY; Harlow et al., 1989, в: Antibodies: A Laboratory Manual, Cold Spring Harbor, New York; Houston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-5883; Bird et al., 1988, Science 242:423-426). В одном аспекте антигенсвязывающий домен CAR по изобретению содержит фрагмент антитела. В следующем аспекте CAR содержит фрагмент антитела, который представляет собой scFv.
Используемый в настоящем документе термин «связывающий домен» или «молекула антитела» (другое название «направленный против мишени (например, CD19) связывающий домен») означает белок, например, цепь иммуноглобулина или ее фрагмент, содержащий по меньшей мере одну последовательность вариабельного домена иммуноглобулина. Термин «связывающий домен» или «молекула антитела» охватывает антитела и фрагменты антител. В одном из вариантов осуществления молекула антитела представляет собой мультиспецифическую молекулу антитела, например, она содержит множество последовательностей вариабельных доменов иммуноглобулинов, при этом первая последовательность вариабельного домена иммуноглобулина из множества имеет специфичность связывания для первого эпитопа и вторая последовательность вариабельного домена иммуноглобулина из множества имеет специфичность связывания для второго эпитопа. В одном из вариантов осуществления мультиспецифическая молекула антитела представляет собой биспецифическую молекулу антитела. Биспецифическое антитело имеет специфичность для не более, чем двух антигенов. Биспецифическую молекулу антитела характеризуют по первой последовательности вариабельного домена иммуноглобулина, которая имеет специфичность связывания для первого эпитопа, и второй последовательности вариабельного домена иммуноглобулина, которая имеет специфичность связывания для второго эпитопа.
Термин «тяжелая цепь антитела» означает большую по размеру из двух видов полипептидных цепей, присутствующих в молекулах антител в их естественных конформациях, которая, как правило, определяет класс, к которому относится антитело.
Термин «легкая цепь антитела» означает меньшую по размеру из двух видов полипептидных цепей, присутствующих в молекулах антител в их естественных конформациях. Каппа (κ) и лямбда (λ) легкие цепи являются двумя основными изотипами легких цепей антитела.
Термин «рекомбинантное антитело» означает антитело, которое получено с использованием технологии рекомбинантных ДНК, такое как, например, антитело, экспрессированное в экспрессионной системе бактериофагов или дрожжей. Термин также должен означать антитело, которое получено путем синтеза молекулы ДНК, кодирующей антитело, и эта молекула ДНК экспрессирует белок антитела или аминокислотную последовательность, определяющую антитело, при этом ДНК или аминокислотную последовательность получали с использованием технологии рекомбинантных ДНК или аминокислотных последовательностей, которая доступна и хорошо известна в данной области.
Используемый в настоящем документе термин «иммуноглобулин» или «Ig» относится к классу белков, которые действуют как антитела. Антитела, экспрессируемые B-клетками, иногда называют BCR (B-клеточный рецептор) или антигенный рецептор. Пять представителей, входящих в данный класс белков, представляют собой IgA, IgG, IgM, IgD и IgE. IgA является основным антителом, присутствующим в секретах тела, таких как слюна, слезы, грудное молоко, желудочно-кишечные секреты и слизистые секреты дыхательных и мочеполовых путей. IgG является наиболее распространенным циркулирующим антителом. IgM является основным иммуноглобулином, продуцируемым при первичном иммунном ответе у большинства субъектов. Он является наиболее эффективным иммуноглобулином в агглютинации, фиксации комплемента и других гуморальных ответах, и важен для защиты от бактерий и вирусов. IgD является иммуноглобулином, у которого отсутствует какая-либо из известных функций антител, но который может служить в качестве антигенного рецептора. IgE является иммуноглобулином, который опосредует реакцию гиперчувствительности немедленного типа, вызывая высвобождение медиаторов из тучных клеток и базофилов под воздействием аллергена.
Термин «антиген» или «Аг» означает молекулу, которая вызывает иммунный ответ. Данный иммунный ответ может включать или продуцирование антител, или активацию специфических иммунологически компетентных клеток, либо и то, и другое. Квалифицированный специалист понимает, что любая макромолекула, включая практически все белки или пептиды, может служить антигеном. Более того, антигены могут быть получены из рекомбинантной или геномной ДНК. Квалифицированный специалист понимает, что любая ДНК, которая содержит нуклеотидную последовательность или частичную нуклеотидную последовательность, кодирующую белок, вызывающий иммунный ответ, таким образом, кодирует «антиген» в том значении, которое используют в настоящем документе. Кроме того, специалист в данной области понимает, что данный антиген не обязательно должен быть закодирован только полноразмерной нуклеотидной последовательностью гена. Очевидно, что настоящее изобретение включает, но без ограничения, применение частичных нуклеотидных последовательностей более чем одного гена, и что эти нуклеотидные последовательности собирают в разных сочетаниях для кодирования полипептидов, вызывающих желаемый иммунный ответ. Кроме того, квалифицированный специалист понимает, что антиген совсем не обязательно должен быть закодирован «геном». Очевидно, что антиген может быть создан или может быть получен из биологического образца, или может представлять собой макромолекулу помимо полипептида. Такой биологический образец может включать, но не ограничивается ими, образец ткани, образец опухоли, клетку или жидкость с другими биологическими компонентами.
Используемый в настоящем документе термин «аутоантиген» означает любой собственный антиген, который распознается иммунной системой как чужеродный. Аутоантигены включают, но не ограничиваются ими, клеточные белки, фосфобелки, клеточные поверхностные белки, клеточные липиды, нуклеиновые кислоты, гликопротеины, включая клеточные поверхностные рецепторы.
Термин «аутоантитело» означает антитело, которое продуцируется B-клеткой, специфичной для аутоантигена.
Используемый в настоящем документе термин «вызываемое аутоантителами заболевание» означает нарушение, возникающее вследствие иммунного ответа в виде продуцирования аутоантител. Вызываемое аутоантителами заболевание является результатом неадекватного и избыточного продуцирования аутоантител. Примеры вызываемых аутоантителами заболеваний включают, но не ограничиваются ими, буллезный пемфигоид, приобретенный буллезный эпидермолиз, p200 пемфигоид, линеарный IgA-зависимый буллезный дерматоз, другие заболевания группы пемфигоидных заболеваний, герпетиформный дерматит, глютенчувствительную целиакию, миастению, синдром Гудпасчера, гранулематоз с полиангиитом и другие ANCA+ формы васкулита, аутоиммунный энцефалит с поражением лимбической системы, анти-NMDA-рецепторный энцефалит, нейромиелит зрительного нерва, аутоиммунную гемолитическую анемию, вызываемое аутоантителами повреждение органов-мишеней при волчанке и других заболеваниях соединительной ткани (вызываемое анти-дцДНК, анти-Ro и другими аутоантителами), болезнь Грейвса и тиреоидит Хашимото, продуцирование антител против инсулина при диабете, антител против инсулиновых рецепторов при аутоиммунной гипогликемии, криоглобулинемию, ревматоидный артрит, рассеянный склероз, синдром Шегрена, дерматомиозит, продуцирование антител против рецепторов Fc-эпсилон при хронической идиопатической крапивнице, антител против фолатных рецепторов, антител против эндотелиальных рецепторов или против адренергических рецепторов при легочной артериальной гипертензии, рефрактерной гипертензии, расширенной кардиомиопатии, а также аутовоспалительные синдромы, такие как IgG4-связанная болезнь, в числе прочих.
Используемый в настоящем документе термин «аутоиммунное заболевание» означает заболевание или состояние, возникающее вследствие опосредованного антителами аутоиммунного ответа на аутоантигены. При аутоиммунном заболевании происходит продуцирование аутоантител, которые неадекватно продуцируются и/или избыточно продуцируются против собственного антигена или аутоантигена.
Термин «аутологичный» относится к любому материалу, полученному от того же индивидуума, которому он позже будет повторно введен.
Термины «противоопухолевый эффект» или «противоопухолевая активность» означают биологический эффект, который может проявляться по-разному, включая, но без ограничения, например, уменьшение объема опухоли, уменьшение количества клеток опухоли, уменьшение количества метастазов, увеличение продолжительности жизни, уменьшение пролиферации клеток опухоли, уменьшение выживаемости клеток опухоли или ослабление различных физиологических симптомов, ассоциированных с онкологическим состоянием. «Противоопухолевый эффект» также может проявляться в виде способности пептидов, полинуклеотидов, клеток и антител по изобретению изначально предотвращать возникновение опухоли.
Термин «аллогенный» относится к любому материалу, полученному от другого животного того же биологического вида, что и индивидуум, которому вводят материал. Говорят, что два или более индивидуумов являются аллогенными друг для друга, когда их гены в одном или более локусах не идентичны. В некоторых аспектах аллогенный материал от индивидуумов того же биологического вида может достаточно отличаться генетически, чтобы действовать в качестве антигена.
Термин «ксеногенный» относится к имплантату, полученному от животного другого биологического вида.
Используемый в настоящем документе термин «аферез» означает экстракорпоральный процесс, при котором кровь от донора или пациента забирают у донора или пациента и пропускают через аппарат, который отделяет выбранный конкретный компонент(ы) и возвращает оставшуюся часть в систему кровообращения донора или пациента, например, путем ретрансфузии. Таким образом, в данном контексте «аферезный образец» означает образец, полученный с использованием афереза.
Термин «расщепление» означает разрушение ковалентных связей, например, в каркасе молекулы нуклеиновой кислоты, или гидролиз пептидных связей. Расщепление может быть инициировано различными способами, включая, но без ограничения, ферментативный или химический гидролиз фосфодиэфирной связи. Может происходить как одноцепочечное расщепление, так и двухцепочечное расщепление. Двухцепочечное расщепление может происходить в результате двух отдельных событий одноцепочечного расщепления. Расщепление ДНК может приводить к возникновению либо тупых концов, либо ступенчатых концов. В конкретных вариантах осуществления слитые полипептиды можно использовать для нацеливания на расщепленную двухцепочечную ДНК.
Термины «рак» или «опухоль» означают заболевание, характеризующееся неконтролируемым ростом аберрантных клеток. Рак включает все виды злокачественного роста или онкогенных процессов, метастатические ткани или злокачественно трансформированные клетки, ткани или органы, независимо от гистопатологического типа или стадии инвазии. Раковые клетки могут распространяться локально или через кровеносную и лимфатическую систему в другие части тела. Примеры различных видов рака описаны в настоящем документе и включают, но не ограничиваются ими, рак молочной железы, рак предстательной железы, рак яичника, рак шейки матки, рак кожи, рак поджелудочной железы, колоректальный рак, рак почки, рак печени, рак головного мозга, лимфому, лейкоз, рак легкого и тому подобное.
Термины «CRISPR/CAS», «система набора коротких палиндромных повторов, регулярно расположенных группами» или «CRISPR» относятся к локусам ДНК, содержащим короткие повторы последовательностей оснований. За каждым повтором следуют короткие сегменты ДНК спейсеров от предыдущих воздействий вирусов. Бактерии и археи выработали адаптивную иммунную защиту, называемую CRISPR-CRISPR-ассоциированной (Cas) системой, в которой используются короткие РНК для управления деградацией чужеродных нуклеиновых кислот. У бактерий система CRISPR обеспечивает приобретенный иммунитет против вторгающейся чужеродной ДНК за счет управляемого РНК расщепления ДНК.
В системе CRISPR/Cas II типа короткие сегменты чужеродной ДНК, называемые «спейсерами», интегрируются в геномные локусы CRISPR, и транскрибируются и процессируются в короткие CRISPR РНК (crРНК). Эти crРНК отжигаются с транс-активирующими crРНК (tracrРНК) и управляют специфичным для последовательности расщеплением и сайленсингом патогенной ДНК белками Cas. Недавние исследования показали, что для узнавания мишени белком Cas9 необходима «затравочная» последовательность в crRNA и консервативная последовательность динуклеотид-содержащего мотива, прилегающего к протоспейсеру (PAM), выше crРНК-связывающей области.
Для направления Cas9 для расщепления интересующих последовательностей могут быть сконструированы слитые транскрипты crРНК-tracrРНК, далее в настоящем документе называемые «направляющими РНК» или «нРНК», из промотора U6 человеческой полимеразы III. Опосредованное CRISPR/CAS редактирование и регуляция генома продемонстрировало трансформационный потенциал в области фундаментальной науки, клеточной инженерии и терапии.
Термин «CRISPRi» означает систему CRISPR для специфичного для последовательности подавления генов или ингибирования экспрессии генов, например, на уровне транскрипции.
При использовании в настоящем документе термин «полученная из» указывает на связь между первой и второй молекулами. Он, как правило, относится к структурному сходству между первой молекулой и второй молекулой, и не подразумевает или не включает ограничение способа или источника для первой молекулы, которая получена из второй молекулы. Например, в случае внутриклеточного сигнального домена, который получен из молекулы CD3-дзета, внутриклеточный сигнальный домен в достаточной степени сохраняет структуру CD3-дзета для того, чтобы выполнять необходимую функцию, а именно, обладать способностью генерировать сигнал в соответствующих условиях. Термин не подразумевает или не включает ограничение в отношении конкретного способа получения внутриклеточного сигнального домена, например, он не означает, что для получения внутриклеточного сигнального домена необходимо начинать с последовательности CD3-дзета и удалять нежелательную последовательность или вносить мутации, получая в результате внутриклеточный сигнальный домен.
Выражение «заболевание, связанное с экспрессией опухолевого антигена» включает, но без ограничения, заболевание, связанное с экспрессией опухолевого антигена, описанного в настоящем документе, или состояние, связанное с клетками, экспрессирующими опухолевый антиген, описанный в настоящем документе, включая, например, пролиферативные заболевания, такие как рак или ранняя стадия рака, или предраковое состояние, такое как миелодисплазия, миелодиспластический синдром или предлейкоз; либо не раковое состояние, связанное с клетками, которые экспрессируют опухолевый антиген, описанный в настоящем документе. В одном аспекте рак, связанный с экспрессией опухолевого антигена, описанного в настоящем документе, представляет собой гематологический рак. В одном аспекте рак, связанный с экспрессией опухолевого антигена, описанного в настоящем документе, представляет собой солидный рак. Другие заболевания, связанные с экспрессией опухолевого антигена, описанного в настоящем документе, включают, но без ограничения, например, атипичные и/или неклассические формы рака, ранние стадии рака, предраковые состояния или пролиферативные заболевания, связанные с экспрессией опухолевого антигена, описанного в настоящем документе. Нераковые состояния, связанные с экспрессией опухолевого антигена, описанного в настоящем документе, включают, но без ограничения, например, аутоиммунное заболевание (например, волчанку), воспалительные заболевания (аллергию и астму) и трансплантацию.
Термин «консервативные модификации последовательности» означает аминокислотные модификации, которые существенно не влияют или не изменяют характеристики связывания антитела или фрагмента антитела, содержащего аминокислотную последовательность. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации можно вносить в антитело или фрагмент антитела по изобретению стандартными методами, известными в данной области, такими как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Консервативные аминокислотные замены представляют собой замены, при которых аминокислотный остаток заменяют аминокислотным остатком, имеющим аналогичную боковую цепь. Семейства аминокислотных остатков, имеющих аналогичные боковые цепи, известны в данной области. Эти семейства включают аминокислоты с основными боковыми цепями (например, лизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин, триптофан), неполярными боковыми цепями (например, аланин, валин, лейцин изолейцин, пролин, фенилаланин, метионин), бета-разветвленными боковыми цепями (например, треонин, валин изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин). Таким образом, один или более аминокислотных остатков в CAR по изобретению можно заменять другими аминокислотными остатками из того же семейства боковых цепей, и измененный CAR можно тестировать с использованием функциональных анализов, описанных в настоящем документе.
Термин «стимуляция» означает основной ответ, индуцируемый при связывании стимулирующей молекулы (например, комплекса TCR/CD3 или CAR) с узнаваемым ею лигандом (или опухолевым антигеном в случае CAR), который опосредует событие передачи сигнала, такое как, но без ограничения, передача сигнала через комплекс TCR/CD3, или передача сигнала через соответствующий рецептор NK или сигнальные домены CAR. Стимуляция может опосредовать изменение экспрессии некоторых молекул, например понижающую регуляцию TGF-β, и/или реорганизацию цитоскелетных структур и тому подобное.
Термин «стимулирующая молекула» означает молекулу, экспрессируемую иммунной эффекторной клеткой (например, T-клеткой, NK-клеткой, B-клеткой), которая представляет собой цитоплазматическую сигнальную последовательность(и), регулирующую активацию иммунной эффекторной клетки стимулирующим образом для по меньшей мере некоторых аспектов сигнального пути иммунной эффекторной клетки, например, сигнального пути T-клетки. В одном аспекте сигнал представляет собой основной сигнал, который инициируется, например, при связывании комплекса TCR/CD3 с молекулой MHC, нагруженной пептидом, и который приводит к опосредованному T-клеточному ответу, включая, но без ограничения, пролиферацию, активацию, дифференциацию и тому подобное. Основная цитоплазматическая сигнальная последовательность (также называемая «основной сигнальный домен»), которая действует стимулирующим образом, может содержать сигнальный мотив, известный как иммунорецепторный тирозиновый активирующий мотив, или ITAM. Примеры ITAM-содержащих основных цитоплазматических сигнальных последовательностей, которые особенно подходят для использования по изобретению, включают, но без ограничения, те, которые получены из CD3-дзета, общего FcR-гамма (FCER1G), Fc-гамма RIIa, FcR-бета (Fc-эпсилон R1b), CD3-гамма, CD3-дельта, CD3-эпсилон, CD5, CD22, CD79a, CD79b, CD278 (также известного как «ICOS»), FcεRI, DAP10, DAP12 и CD66d. В конкретном CAR по изобретению внутриклеточный сигнальный домен в любом одном или более CAR по изобретению содержит внутриклеточную сигнальную последовательность, например, основную сигнальную последовательность CD3-дзета. В конкретном CAR по изобретению основная сигнальная последовательность CD3-дзета представляет собой последовательность, приведенную в SEQ ID NO: 18, или эквивалентные остатки у биологических видов, отличных от человека, например, мыши, кролика, обезьяны, человекообразной обезьяны и тому подобных. В конкретном CAR по изобретению основная сигнальная последовательность CD3-дзета представляет собой последовательность, приведенную в SEQ ID NO: 20, или эквивалентные остатки у биологических видов, отличных от человека, например, мыши, кролика, обезьяны, человекообразной обезьяны и тому подобных.
Термин «антигенпредставляющая клетка», или «APC», означает клетку иммунной системы, такую как вспомогательная клетка (например, B-клетка, дендритная клетка и тому подобное), которая представляет чужеродный антиген в комплексе с молекулами главного комплекса гистосовместимости (MHC) на своей поверхности. T-клетки могут узнавать эти комплексы за счет T-клеточных рецепторов (TCR). APC процессируют антигены и представляют их T-клеткам.
Используемый в настоящем документе термин «внутриклеточный сигнальный домен» означает внутриклеточную часть молекулы. Внутриклеточный сигнальный домен генерирует сигнал, который стимулирует иммунную эффекторную функцию CAR-экспрессирующей клетки, например, CAR T-клетки или CAR-экспрессирующей NK-клетки. Примеры иммунной эффекторной функции, например, у CAR T-клетки или CAR-экспрессирующей NK-клетки, включают цитолитическую активность и хелперную активность, в том числе, секрецию цитокинов. Хотя можно использовать целый внутриклеточный сигнальный домен, в некоторых случаях нет необходимости использовать полную цепь. Касательно использования укороченного фрагмента внутриклеточного сигнального домена, такой укороченный фрагмент может быть использован вместо интактной цепи при условии, что он передает сигнал эффекторной функции. Таким образом, термин «внутриклеточный сигнальный домен» должен включать любой укороченный фрагмент внутриклеточного сигнального домена, достаточный для передачи сигнала эффекторной функции.
В одном из вариантов осуществления внутриклеточный сигнальный домен может содержать основной внутриклеточный сигнальный домен. Иллюстративные основные внутриклеточные сигнальные домены включают те, которые получены из молекул, отвечающих за основную стимуляцию, или антиген-зависимую стимуляцию. В одном из вариантов осуществления внутриклеточный сигнальный домен может содержать костимулирующий внутриклеточный домен. Иллюстративные костимулирующие внутриклеточные сигнальные домены включают те, которые получены из молекул, отвечающих за костимулирующие сигналы, или независимую от антигена стимуляцию. В одном из вариантов осуществления внутриклеточный сигнальный домен является синтезированным или рекомбинантным. Например, в случае CAR-экспрессирующей иммунной эффекторной клетки, например, CAR T-клетки или CAR-экспрессирующей NK-клетки, основной внутриклеточный сигнальный домен может содержать цитоплазматическую последовательность T-клеточного рецептора, основной внутриклеточный сигнальный домен может содержать цитоплазматическую последовательность T-клеточного рецептора, и костимулирующий внутриклеточный сигнальный домен может содержать цитоплазматическую последовательность из корецептора или костимулирующей молекулы.
Основной внутриклеточный сигнальный домен может содержать сигнальный мотив, известный как иммунорецепторный тирозиновый активирующий мотив, или ITAM. Примеры ITAM-содержащих основных цитоплазматических сигнальных последовательностей включают, но без ограничения, те, которые получены из CD3-дзета, общего FcR-гамма (FCER1G), Fc-гамма RIIa, FcR-бета, CD3-гамма, CD3-дельта, CD3-эпсилон, CD5, CD22, CD79a, CD79b, CD278 («ICOS»), FcεRI CD66d, DAP10 и DAP12.
Термины «дзета» или, альтернативно, «дзета-цепь», «CD3-дзета» или «TCR-дзета», означают белок, имеющий GenBank регистрационный № BAG36664.1, или эквивалентные остатки у биологических видов, отличных от человека, например, мыши, кролика, обезьяны, человекообразной обезьяны и тому подобных, и термины «стимулирующий домен дзета» или, альтернативно, «стимулирующий домен CD3-дзета» или «стимулирующий домен TCR-дзета» означают аминокислотные остатки из цитоплазматического домена дзета-цепи, достаточные для функциональной передачи первичного сигнала, необходимого для активации T-клетки. В одном аспекте цитоплазматический домен дзета содержит остатки 52-164 белка с GenBank регистрационным № BAG36664.1, или эквивалентные остатки у биологических видов, отличных от человека, например, мыши, кролика, обезьяны, человекообразной обезьяны и тому подобных, которые являются их функциональными ортологами. В одном аспекте «стимулирующий домен дзета» или «стимулирующий домен CD3-дзета» представляет собой последовательность, приведенную в SEQ ID NO: 18. В одном аспекте «стимулирующий домен дзета» или «стимулирующий домен CD3-дзета» представляет собой последовательность, приведенную в SEQ ID NO: 20. В настоящем документе также предусмотрены домены CD3-дзета, имеющие одну или более мутаций в аминокислотных последовательностях, описанных в настоящем документе, например, SEQ ID NO: 20.
Термин «костимулирующая молекула» относится к когнатному партнеру по связыванию на T-клетке, который специфически связывается с костимулирующим лигандом, тем самым опосредуя костимулирующий ответ T-клетки, такой как, но без ограничения, пролиферация. Костимулирующие молекулы представляют собой молекулы клеточной поверхности, отличные от антигенных рецепторов или их лигандов, которые необходимы для эффективного иммунного ответа. Костимулирующие молекулы включают, но без ограничения, молекулу MHC класса I, белок рецептора TNF, иммуноглобулиноподобный белок, рецептор цитокина, интегрин, сигнальную молекулу активации лимфоцитов (белок SLAM), активирующий рецептор NK-клеток, BTLA, Toll-подобный рецептор, OX40, CD2, CD7, CD27, CD28, CD30, CD40, CDS, ICAM-1, LFA-1 (CD11a/CD18), 4-1BB (CD137), B7-H3, CDS, ICAM-1, ICOS (CD278), GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CD8-альфа, CD8-бета, IL2R-бета, IL2R-гамма, IL7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, NKG2C, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (тактильный), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD19a, а также лиганд, который специфически связывается с CD83.
Костимулирующий внутриклеточный сигнальный домен, или костимулирующий сигнальный домен, может представлять собой внутриклеточную часть костимулирующей молекулы. Внутриклеточный сигнальный домен может содержать целую внутриклеточную часть или целый природный внутриклеточный сигнальный домен молекулы, из которой он получен, либо его функциональный фрагмент.
Термин «4-1BB» означает белок суперсемейства TNFR, имеющий аминокислотную последовательность с GenBank регистрационным № AAA62478.2, или эквивалентные остатки у биологических видов, отличных от человека, например, мыши, кролика, обезьяны, человекообразной обезьяны и тому подобных; и «костимулирующий домен 4-1BB» означает аминокислотные остатки 214-255 в белке с GenBank регистрационным № AAA62478.2 или эквивалентные остатки у биологических видов, отличных от человека, например, мыши, кролика, обезьяны, человекообразной обезьяны и тому подобных. В одном аспекте «костимулирующий домен 4-1BB» представляет собой последовательность, приведенную в SEQ ID NO: 14, или эквивалентные остатки у биологических видов, отличных от человека, например, мыши, кролика, обезьяны, человекообразной обезьяны и тому подобных.
Используемый в настоящем документе термин «иммунный ответ» означает клеточный ответ на антиген, который имеет место, когда лимфоциты идентифицируют антигенные молекулы как чужеродные и индуцируют образование антител и/или активируют лимфоциты для удаления антигена.
Если указано «иммунологически эффективное количество», «эффективное для ингибирования аутоиммунного заболевания количество» или «терапевтическое количество», точное вводимое количество композиций по настоящему изобретению может определять врач или исследователь с учетом индивидуальных различий в возрасте, массе тела, размере опухоли, степени инфицирования или метастазирования, а также состояния здоровья пациента (субъекта).
Используемый в настоящем документе термин «иммунная эффекторная клетка» означает клетку, вовлеченную в иммунный ответ, например, в стимуляцию иммунного эффекторного ответа. Примеры иммунных эффекторных клеток включают T-клетки, например, альфа/бета T-клетки и гамма/дельта T-клетки, B-клетки, клетки - естественные киллеры (NK), T-клетки - естественные киллеры (NKT), тучные клетки и фагоциты миелоидного происхождения.
Используемые в настоящем документе термины «иммунная эффекторная функция» или «иммунный эффекторный ответ» означают функцию или ответ, например, иммунной эффекторной клетки, который усиливает или стимулирует иммунную атаку клетки-мишени. Например, иммунная эффекторная функция, или ответ, означает свойство T- или NK-клетки, которое обеспечивает уничтожение, или ингибирование роста или пролиферации, клетки-мишени. В случае T-клетки основная стимуляция и костимуляция являются примерами иммунной эффекторной функции или ответа.
Термин «эффекторная функция» означает специализированную функцию клетки. Эффекторной функцией T-клетки, например, может быть цитолитическая активность или хелперная активность, в том числе секреция цитокинов.
Термин «кодирование» означает характерное свойство определенных последовательностей нуклеотидов в полинуклеотиде, таком как ген, кДНК или мРНК, служить в качестве матриц для синтеза в биологических процессах других полимеров и макромолекул, имеющих либо определенную последовательность нуклеотидов (например, рРНК, тРНК и мРНК), либо определенную последовательность аминокислот, и вытекающие из них биологические свойства. Таким образом, ген, кДНК или РНК кодирует белок, если транскрипция и трансляция мРНК, соответствующей данному гену, приводит к образованию белка в клетке или другой биологической системе. Можно сказать, что, как кодирующая цепь, нуклеотидная последовательность которой идентична последовательности мРНК и обычно приводится в списке последовательностей, так и некодирующая цепь, используемая в качестве матрицы для транскрипции гена или кДНК, кодируют белок или другой продукт данного гена или кДНК.
Если не указано иначе, выражение «нуклеотидная последовательность, кодирующая аминокислотную последовательность», охватывает все нуклеотидные последовательности, которые являются вырожденными вариантами друг друга и которые кодируют одну и ту же аминокислотную последовательность. Выражение «нуклеотидная последовательность, кодирующая белок или РНК» также может охватывать интроны в той степени, в которой нуклеотидная последовательность, кодирующая белок, в некоторых вариантах может содержать интрон(ы).
Термины «эффективное количество» или «терапевтически эффективное количество» в настоящем документе используются взаимозаменяемо и означают количество соединения, препарата, материала или композиции, описанных в настоящем документе, эффективное для достижения конкретного биологического результата.
Термин «эндогенный» означает любой материал из, или продуцируемый внутри, организма, клетки, ткани или системы.
Термин «экзогенный» означает любой материал, введенный извне, или продуцируемый за пределами организма, клетки, ткани или системы.
Термин «экспрессия» означает транскрипцию и/или трансляцию конкретной нуклеотидной последовательности, управляемую промотором.
Термин «переносящий вектор» означает химическое соединение, содержащее выделенную нуклеиновую кислоту, которое может быть использовано для доставки выделенной нуклеиновой кислоты внутрь клетки. Множество векторов известно в данной области, включая, но без ограничения, линейные полинуклеотиды, полинуклеотиды, связанные с ионными или амфифильными соединениями, плазмиды и вирусы. Таким образом, термин «переносящий вектор» включает автономно реплицируемые плазмиды или вирусы. Термин следует толковать, как включающий также неплазмидные и невирусные соединения, которые способствуют переносу нуклеиновой кислоты в клетки, такие как, например, соединение полилизина, липосома и тому подобное. Примеры вирусных переносящих векторов включают, но без ограничения, аденовирусные векторы, аденоассоциированные вирусные векторы, ретровирусные векторы, лентивирусные векторы и тому подобное.
Термин «экспрессионный вектор» означает вектор, содержащий рекомбинантный полинуклеотид, включающий последовательности контроля экспрессии, функционально связанные с нуклеотидной последовательностью, которая должна быть экспрессирована. Экспрессионный вектор содержит достаточное количество действующих в цис-положении элементов для экспрессии; другие элементы для экспрессии могут быть предоставлены клеткой-хозяином или присутствовать в in vitro экспрессионной системе. Экспрессионные векторы включают все векторы, известные в данной области, в том числе космиды, плазмиды (например, «голые» или заключенные в липосомы) и вирусы (например, лентивирусы, ретровирусы, аденовирусы и аденоассоциированные вирусы), которые заключают в себе рекомбинантный полинуклеотид.
Термин «лентивирус» относится к роду семейства Retroviridae. Лентивирусы являются уникальными среди ретровирусов в том, что они способны инфицировать не делящиеся клетки; они могут доставлять значительное количество генетической информации в ДНК клетки-хозяина, таким образом, они являются одним из наиболее эффективных векторов для доставки генов. HIV, SIV и FIV являются примерами лентивирусов.
Термин «лентивирусный вектор» означает вектор, полученный из по меньшей мере части лентивирусного генома, включая, в частности, самоинактивирующийся лентивирусный вектор, описанный в публикации Milone et al., Mol. Ther. 17(8): 1453-1464 (2009). Другие примеры лентивирусных векторов, которые могут быть использованы в клинике, включают, но не ограничиваются ими, например, технологию доставки генов LENTIVECTOR® от компании Oxford BioMedica, векторную систему LENTIMAX™ от компании Lentigen и тому подобные. Виды лентивирусных векторов не для клинического применения также доступны и известны специалисту в данной области.
Термины «гомология» или «идентичность» означают субъединичную идентичность последовательностей между двумя полимерными молекулами, например, между двумя молекулами нуклеиновой кислоты, например, двумя молекулами ДНК или двумя молекулами РНК, или между двумя полипептидными молекулами. Когда субъединичное положение в обеих из двух молекул занято одной и той же мономерной субъединицей; например, если положение в каждой из двух молекул ДНК занято аденином, эти молекулы являются гомологичными или идентичными в этом положении. Гомология между двумя последовательностями напрямую зависит от числа совпадающих или гомологичных положений; например, если половина (например, пять положений в полимере длиной десять субъединиц) положений в двух последовательностях являются гомологичными, то две последовательности являются гомологичными на 50%; если 90% положений (например, 9 из 10) являются совпадающими или гомологичными, то две последовательности являются гомологичными на 90%.
«Гуманизированные» формы антител, не принадлежащих человеку (например, мышиных), представляют собой химерные иммуноглобулины, цепи иммуноглобулинов или фрагменты антител (такие как Fv, Fab, Fab', F(ab')2 или другие антигенсвязывающие подпоследовательности антител), которые содержат минимальную последовательность, происходящую из иммуноглобулина, не принадлежащего человеку. В основном, гуманизированные антитела и фрагменты антител представляют собой человеческие иммуноглобулины (реципиентное антитело или фрагмент антитела), в котором остатки из определяющей комплементарность области (CDR) реципиента заменены остатками из CDR биологического вида, отличного от человека (донорское антитело), такого как мышь, крыса или кролик, имеющими нужную специфичность, аффинность и функциональные возможности. В некоторых случаях остатки каркасной области (FR) Fv человеческого иммуноглобулина заменяют соответствующими остатками, не принадлежащими человеку. Более того, гуманизированное антитело/фрагмент антитела может содержать остатки, которые не встречаются ни в реципиентном антителе, ни в импортированных последовательностях CDR или каркаса. Эти модификации могут приводить к дополнительному усовершенствованию и оптимизации выполняемой функции антитела или фрагмента антитела. Как правило, гуманизированное антитело или фрагмент антитела содержит практически все из по меньшей мере одного и, как правило, двух вариабельных доменов, в которых все или практически все из областей CDR соответствуют таковым из иммуноглобулина, не принадлежащего человеку, и все или значительная часть областей FR являются областями из последовательности иммуноглобулина человека. Гуманизированное антитело или фрагмент антитела также может содержать по меньшей мере часть константной области иммуноглобулина (Fc), как правило, из иммуноглобулина человека. Для более подробной информации, смотри Jones et al., Nature, 321: 522-525, 1986; Reichmann et al., Nature, 332: 323-329, 1988; Presta, Curr. Op. Struct. Biol., 2: 593-596, 1992.
Термин «полностью человеческие» относится к иммуноглобулинам, таким как антитело или фрагмент антитела, в которых вся молекула является человеческой или состоит из аминокислотной последовательности, идентичной человеческой форме антитела или иммуноглобулина.
Термин «выделенные» означает измененные или извлеченные из естественного окружения. Например, нуклеиновая кислота или пептид, естественным образом присутствующие в организме живого животного, не являются «выделенными», однако та же нуклеиновая кислота или пептид, частично или полностью отделенные от материалов, сосуществующих с ними в их естественном окружении, являются «выделенными». Выделенная нуклеиновая кислота или белок могут существовать в практически очищенной форме или могут существовать в неестественном для них окружении, таком как, например, клетка-хозяин.
В контексте настоящего изобретения использованы следующие сокращения для обычных оснований нуклеиновой кислоты. «A» означает аденозин, «C» означает цитозин, «G» означает гуанозин, «T» означает тимидин и «U» означает уридин.
Термины «функционально связанные» или «контроль транскрипции» относятся к функциональной связи между регуляторной последовательностью и гетерологичной нуклеотидной последовательностью, обеспечивающей экспрессию последней. Например, первая нуклеотидная последовательность функционально связана со второй нуклеотидной последовательностью, когда первая нуклеотидная последовательность приведена в функциональное взаимодействие со второй нуклеотидной последовательностью. Например, промотор функционально связан с кодирующей последовательностью, если промотор влияет на транскрипцию или экспрессию кодирующей последовательности. Функционально связанные последовательности ДНК могут быть смежными и, например, при необходимости объединения двух кодирующих областей белков, находиться в одной и той же рамке считывания.
Термин «парентеральное» введение иммуногенной композиции включает, например, подкожную (п/к), внутривенную (в/в), внутримышечную (в/м) или интрастернальную инъекцию, внутриопухолевые или инфузионные методы введения.
Термины «нуклеиновая кислота» или «полинуклеотид» означают дезоксирибонуклеиновые кислоты (ДНК) или рибонуклеиновые кислоты (РНК), а также их полимеры, в одно- или двухцепочечной форме. Если нет конкретных ограничений, термин охватывает нуклеиновые кислоты, содержащие известные аналоги природных нуклеотидов, которые имеют свойства связывания, аналогичные таковым у эталонной нуклеиновой кислоты, и которые метаболизируются аналогично природным нуклеотидам. Если нет иных указаний, подразумевается, что конкретная нуклеотидная последовательность также включает ее консервативно модифицированные варианты (например, с заменами вырожденных кодонов), аллели, ортологи, ОНП и комплементарные последовательности, а также указанную в прямой форме последовательность. В частности, замены вырожденных кодонов можно осуществлять, создавая последовательности, в которых третье положение одного или более выбранных (или всех) кодонов заменено смешанными основаниями и/или остатками дезоксиинозина (Batzer et al., Nucleic Acid Res. 19:5081 (1991); Ohtsuka et al., J. Biol. Chem. 260:2605-2608 (1985); и Rossolini et al., Mol. Cell. Probes 8:91-98 (1994)).
Термины «пептид», «полипептид» и «белок» используются взаимозаменяемо и означают соединение, состоящее из аминокислотных остатков, ковалентно связанных пептидными связями. Белок или пептид должен содержать по меньшей мере две аминокислоты, и максимальное число аминокислот, которые могут составлять последовательность белка или пептида, не ограничено. Полипептиды включают любой пептид или белок, содержащий две или более аминокислот, связанных между собой пептидными связями. Используемый в настоящем документе термин относится как к коротким цепям, в данной области обычно называемым пептидами, олигопептидами и олигомерами, например, так и к более длинным цепям, в данной области обычно называемым белками, которых существует множество видов. «Полипептиды» включают, например, биологически активные фрагменты, в значительной степени гомологичные полипептиды, олигопептиды, гомодимеры, гетеродимеры, вариантные полипептиды, модифицированные полипептиды, производные, аналоги, слитые белки, в числе прочих. Термин «полипептид» включает природный пептид, рекомбинантный пептид или их сочетание.
Термин «промотор» означает последовательность ДНК, узнаваемую синтетическим аппаратом клетки или привнесенным синтетическим аппаратом, которая необходима для инициации специфической транскрипции полинуклеотидной последовательности.
Термин «промотор/регуляторная последовательность» означает нуклеотидную последовательность, необходимую для экспрессии генного продукта, функционально связанного с промотором/регуляторной последовательностью. В некоторых случаях данная последовательность может представлять собой коровую последовательность промотора, а в других случаях данная последовательность также может включать последовательность энхансера и другие регуляторные элементы, необходимые для экспрессии генного продукта. Промотор/регуляторная последовательность может, например, представлять собой последовательность, которая обеспечивает экспрессию генного продукта тканеспецифическим образом.
Термин «конститутивный» промотор означает нуклеотидную последовательность, которая, будучи функционально связанной с полинуклеотидом, кодирующим или определяющим генный продукт, вызывает продуцирование продукта в клетке при большинстве или при всех физиологических условиях в клетке.
Термин «индуцируемый» промотор означает нуклеотидную последовательность, которая, будучи функционально связанной с полинуклеотидом, кодирующим или определяющим генный продукт, вызывает продуцирование продукта в клетке практически только в том случае, если в клетке присутствует индуктор, соответствующий промотору.
Термин «тканеспецифичный» промотор означает нуклеотидную последовательность, которая, будучи функционально связанной с полинуклеотидом, кодирующим или определяющим генный продукт, вызывает продуцирование продукта в клетке практически только в том случае, если клетка представляет собой клетку ткани, соответствующей данному промотору.
Термины «ассоциированный с раком антиген» или «опухолевый антиген» взаимозаменяемо означают молекулу (как правило, белок, углевод или липид), которая экспрессируется на поверхности раковой клетки, либо полностью, либо в виде фрагмента (например, MHC/пептид), и которая полезна для избирательного нацеливания фармакологического средства на раковую клетку. В некоторых вариантах осуществления опухолевый антиген представляет собой маркер, экспрессируемый как нормальными клетками, так и раковыми клетками, например, маркер линии дифференцировки, например, CD19 на B-клетках. В некоторых вариантах осуществления опухолевый антиген представляет собой молекулу клеточной поверхности, которая избыточно экспрессируется в раковой клетке, в сравнении с нормальной клеткой, например, имеет место 1-кратная избыточная экспрессия, 2-кратная избыточная экспрессия, 3-кратная избыточная экспрессия, или более, в сравнении с нормальной клеткой. В некоторых вариантах осуществления опухолевый антиген представляет собой молекулу клеточной поверхности, которая не надлежащим образом синтезируется на раковой клетке, например, молекулу, которая имеет делеции, добавления или мутации в сравнении с молекулой, экспрессируемой нормальной клеткой. В некоторых вариантах осуществления опухолевый антиген будет экспрессироваться исключительно на клеточной поверхности раковой клетки, полностью или в виде фрагмента (например, MHC/пептид), и не синтезироваться, или не экспрессироваться, на поверхности нормальной клетки. В некоторых вариантах осуществления иллюстративные опухолевые антигены включают: CD19; CD123; CD22; CD30; CD171; CS-1; подобную лектину C-типа молекулу 1, CD33; рецептор варианта III эпидермального фактора роста (EGFRvIII); ганглиозид G2 (GD2); ганглиозид GD3; представитель семейства TNF-рецепторов, антиген созревания B-клеток (BCMA); Tn-антиген ((Tn Ag) или (GalNAcα-Ser/Thr)); простатический специфический мембранный антиген (PSMA); подобный рецепторной тирозинкиназе рецептор-сироту 1 (ROR1); Fms-подобную тирозинкиназу 3 (FLT3); опухоль-ассоциированный гликопротеин 72 (TAG72); CD38; CD44v6; канцероэмбриональный антиген (CEA); молекулу адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицу альфа-2 рецептора интерлейкина-13; мезотелин; субъединицу альфа рецептора интерлейкина-11 (IL-11Ra); антиген простатических стволовых клеток (PSCA); сериновую протеазу 21; рецептор 2 фактора роста эндотелия сосудов (VEGFR2); Lewis(Y) антиген; CD24; рецептор бета фактора роста тромбоцитов (PDGFR-бета); стадиеспецифический эмбриональный антиген-4 (SSEA-4); CD20; фолатный рецептор альфа; рецепторную тирозин-специфическую протеинкиназу ERBB2 (Her2/neu); муцин 1, связанный с клеточной поверхностью (MUC1); рецептор эпидермального фактора роста (EGFR); молекулу адгезии нейронов (NCAM); простазу; простатическую кислую фосфатазу (PAP); мутантный фактор элонгации 2 (ELF2M); эфрин B2; белок альфа активации фибробластов (FAP); рецептор инсулиноподобного фактора роста 1 (рецептор IGF-I), карбоангидразу IX (CAIX); субъединицу протеасомы (просома, макропаин), типа бета, 9 (LMP2); гликопротеин 100 (gp100); онкогенный слитый белок, включающий область локализации сайта инициации реаранжировки (BCR) и гомолог 1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназу; рецептор эфрина A2 (EphA2); фукозил GM1; молекулу адгезии сиалил-Льюис (sLe); ганглиозид GM3; трансглутаминазу 5 (TGS5); высокомолекулярный меланома-ассоциированный антиген (HMWMAA); o-ацетил-GD2 ганглиозид (OAcGD2); фолатный рецептор бета; опухолевый эндотелиальный маркер 1 (TEM1/CD248); антиген, родственный опухолевому эндотелиальному маркеру 7 (TEM7R); клаудин 6 (CLDN6); рецептор тиреостимулирующего гормона (TSHR); связанных с G-белками рецепторов класса C, группы 5, представитель D (GPRC5D); открытую рамку считывания 61 хромосомы X (CXORF61); CD97; CD179a; киназу анапластической лимфомы (ALK); полисиаловую кислоту; плацента-специфический белок 1 (PLAC1); гексасахаридную часть гликоцерамида globoH (GloboH); дифференцировочный антиген молочной железы (NY-BR-1); уроплакин 2 (UPK2); клеточный рецептор 1 вируса гепатита A (HAVCR1); адренорецептор бета-3 (ADRB3); паннексин 3 (PANX3); связанный с G-белками рецептор 20 (GPR20); комплекс лимфоцитарного антигена 6, локуса K9 (LY6K); ольфакторный рецептор 51E2 (OR51E2); белок TCR-гамма с альтернативной рамкой считывания (TARP); белок опухоли Вильмса (WT1); антиген 1 рака яичка (NY-ESO-1); антиген 2 рака яичка (LAGE-1a); меланома-ассоциированный антиген 1 (MAGE-A1); транслокационный вариант 6 гена ETS, расположенный на хромосоме 12p (ETV6-AML); белок спермы 17 (SPA17); семейства X антигенов, представитель 1A (XAGE1); ангиопоэтин-связывающий клеточный поверхностный рецептор 2 (Tie 2); антиген 1 меланомы яичка (MAD-CT-1); антиген 2 меланомы яичка (MAD-CT-2); Fos-родственный антиген 1; опухолевый белок p53 (p53); мутант p53; простеин; сурвивин; теломеразу; опухолевый антиген 1 карциномы предстательной железы, узнаваемый T-клетками антиген меланомы 1; мутант белка вируса крысиной саркомы (Ras); обратную транскриптазу теломеразу человека (hTERT); точки разрыва при транслокации в случае саркомы; ингибитор апоптоза из клеток меланомы (ML-IAP); ERG (слитый ген трансмембранной сериновой протеазы 2 (TMPRSS2) и ETS); N-ацетилглюкозамин трансферазу V (NA17); белок парного бокса Pax-3 (PAX3); рецептор андрогена; циклин B1; полученный из нейробластомы гомолог онкогена v-myc вируса птичьего миелоцитоматоза (MYCN); представитель C семейства гомологов Ras (RhoC); родственный тирозиназе белок 2 (TRP-2); цитохром P450 1B1 (CYP1B1); белок, подобный CCCTC-связывающему фактору (белку «цинковый палец»), узнаваемый T-клетками антиген плоскоклеточной карциномы 3 (SART3); белок парного бокса Pax-5 (PAX5); проакрозин-связывающий белок sp32 (OY-TES1); лимфоцит-специфическую протеинтирозинкиназу (LCK); якорный белок 4 A-киназы (AKAP-4); точку разрыва 2 в X при синовиальной саркоме (SSX2); рецептор для конечных продуктов усиленного гликозилирования (RAGE-1); почечный убиквитарный белок 1 (RU1); почечный убиквитарный белок 2 (RU2); легумаин; белок E6 вируса папилломы человека (HPV E6); белок E7 вируса папилломы человека (HPV E7); кишечную карбоксилэстеразу; мутантный белок теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; связанный с лейкоцитами иммуноглобулиноподобный рецептор 1 (LAIR1); Fc-фрагмент рецептора IgA (FCAR или CD89); иммуноглобулиноподобных рецепторов лейкоцитов, подсемейства A, представитель 2 (LILRA2); семейства белков, подобных молекуле CD300, представитель f (CD300LF); семейства 12 доменных лектинов C-типа, представитель A (CLEC12A); антиген 2 стромальных клеток костного мозга (BST2); белок 2, подобный EGF-подобный домен-содержащему муциноподобному гормональному рецептору (EMR2); лимфоцитарный антиген 75 (LY75); глипикан-3 (GPC3); Fc-рецептор-подобный белок 5 (FCRL5); подобный цепи лямбда иммуноглобулина полипептид 1 (IGLL1); представитель семейства TNF-рецепторов; Fms-подобную тирозинкиназу 3 (FL T3); CD10; CD19; CD20; CD21; CD22; CD23; CD24; CD25; CD37; CD38; CD53; CD72; CD73; CD74; CD75; CD77; CD79a; CD79b; CD80; CD81; CD82; CD83; CD84; CD85; ROR1; BCMA; CD86; CD179b; CD1a; CD1b; CD1c; CD1d; CD2; CD5; CD6; CD9; CD11a; CD11b; CD11c; CD17; CD18; CD26; CD27; CD29; CD30; CD31; CD32a; CD32b; CD35; CD38; CD39; CD40; CD44; CD45; CD45RA; CD45RB; CD45RC; CD45RO; CD46; CD47; CD48; CD49b; CD49c; CD49d; CD50; CD52; CD54; CD55; CD58; CD60a; CD62L; CD63; CD63; CD68 CD69; CD70; CD85E; CD85I; CD85J; CD92; CD95; CD97; CD98; CD99; CD100; CD102; CD108; CD119; CD120a; CD120b; CD121b; CD122; CD124; CD125; CD126; CD130; CD132; CD137; CD138; CD139; CD147; CD148; CD150; CD152; CD162; CD164; CD166; CD167a; CD170; CD175; CD175s; CD180; CD184; CD185; CD192; CD196; CD197; CD200; CD205; CD210a; CDw210b; CD212; CD213a1; CD213a2; CD215; CD217; CD218a; CD218b; CD220; CD221; CD224; CD225; CD226; CD227; CD229; CD230; CD232; CD252; CD253; CD257; CD258; CD261; CD262; CD263; CD264; CD267; CD268; CD269; CD270; CD272; CD274; CD275; CD277; CD279; CD283; CD289; CD290; CD295; CD298; CD300a; CD300c; CD305; CD306; CD307a; CD307b; CD307c; CD307d; CD307e; CD314; CD315; CD316; CD317; CD319; CD321; CD327; CD328; CD329; CD338; CD351; CD352; CD353; CD354; CD355; CD357; CD358; CD360; CD361; CD362; CD363; а также пептид любого из этих антигенов, представленный в контексте MHC. Особенно предпочтительные антигены включают: CD19, CD20, CD22, FcRn5, FcRn2, BCMA, CS-1, CD138, CLDN6, мезотелин, EGFRvIII, CD123, CD33 и CLL-1. В некоторых вариантах осуществления CAR по настоящему изобретению включают CAR, содержащие антигенсвязывающий домен (например, антитело или фрагмент антитела), который связывается с MHC-представленным пептидом. Как правило, пептиды, полученные из эндогенных белков, помещаются в «карманах» молекул главного комплекса гистосовместимости (MHC) класса I и узнаются T-клеточными рецепторами (TCR) на CD8+ T-лимфоцитах. Комплексы MHC класса I конститутивно экспрессируются всеми ядросодержащими клетками. В раковых клетках вирус-специфические и/или опухоль-специфические комплексы пептид/MHC представляют собой уникальный класс мишеней на клеточной поверхности для иммунотерапии. TCR-подобные антитела, нацеленные на пептиды из вирусных или опухолевых антигенов в контексте человеческого лейкоцитарного антигена (HLA)-A1 или HLA-A2, описаны (смотри, например, Sastry et al., J Virol. 2011 85(5):1935-1942; Sergeeva et al., Blood, 2011 117(16):4262-4272; Verma et al., J Immunol 2010 184(4):2156-2165; Willemsen et al., Gene Ther 2001 8(21):1601-1608; Dao et al., Sci Transl Med 2013 5(176):176ra33; Tassev et al., Cancer Gene Ther 2012 19(2):84-100). Например, TCR-подобное антитело может быть идентифицировано при скрининге библиотеки, такой как фаг-дисплейная библиотека scFv человека. Соответственно, по настоящему изобретению предложены CAR, содержащие антигенсвязывающий домен, который связывается с MHC-представленным пептидом молекулы, выбранной из группы, состоящей из WT1, NY-ESO-1, LAGE-1a, MAGE-A1 и RAGE-1.
Термин «гибкий полипептидный линкер», или «линкер», используемый в настоящем документе в контексте scFv, означает пептидный линкер, состоящий из таких аминокислот, как остатки глицина и/или серина, используемые отдельно или в сочетании, который связывает вместе вариабельную область тяжелой цепи и вариабельную область легкой цепи. В одном варианте осуществления гибкий полипептидный линкер представляет собой Gly/Ser линкер и содержит аминокислотную последовательность (Gly-Gly-Gly-Ser)n, где n представляет собой положительное целое число, равное или превышающее 1, например, n=1, n=2, n=3, n=4, n=5 и n=6, n=7, n=8, n=9 и n=10 (SEQ ID NO: 28). В одном варианте осуществления гибкие полипептидные линкеры включают, но без ограничения, (Gly4Ser)4 (SEQ ID NO: 29) или (Gly4Ser)3 (SEQ ID NO: 30). В другом варианте осуществления линкеры включают несколько повторов из (Gly2Ser), (GlySer) или (Gly3Ser) (SEQ ID NO: 31). В объем изобретения также входят линкеры, описанные в WO2012/138475, содержание которого включено в настоящий документ посредством ссылки.
Используемый в настоящем документе термин «5'-кэп» (также называемый РНК-кэп, РНК 7-метилгуанозиновый кэп или РНК m7G кэп) означает модифицированный гуаниновый нуклеотид, который был добавлен «впереди» или на 5'-конце эукариотической матричной РНК вскоре после начала транскрипции. 5'-кэп состоит из концевой группы, которая связана с первым транскрибируемым нуклеотидом. Его присутствие является чрезвычайно важным для узнавания рибосомой и защиты от РНКаз. Добавление кэпа сопряжено с транскрипцией и происходит котранскрипционно, так что имеет место взаимное влияние. Вскоре после начала транскрипции 5'-конец синтезируемой мРНК связывается кэп-синтезирующим комплексом, связанным с РНК-полимеразой. Этот ферментативный комплекс катализирует химические реакции, необходимые для кэпирования мРНК. Синтез происходит в виде многостадийной биохимической реакции. Кэпирующий фрагмент может быть модифицирован для модулирования функциональных свойств мРНК, например, ее стабильности или эффективности трансляции.
Используемый в настоящем документе термин «in vitro транскрибированная РНК» означает РНК, предпочтительно мРНК, которая была синтезирована in vitro. Как правило, in vitro транскрибированную РНК получают из вектора для in vitro транскрипции. Вектор для in vitro транскрипции содержит матрицу, которую используют для создания in vitro транскрибированной РНК.
Используемый в настоящем документе термин «поли(A)» означает серию остатков аденозина, присоединенных в процессе полиаденилирования к мРНК. В предпочтительном варианте осуществления конструкта для временной экспрессии полиA состоит из 50-5000 (SEQ ID NO: 32), предпочтительно, более 64, более предпочтительно, более 100, наиболее предпочтительно, более 300 или 400 остатков. Последовательности поли(A) могут быть модифицированы химически или ферментативно для модулирования функциональных свойств мРНК, таких как локализация, стабильность или эффективность трансляции.
Используемый в настоящем документе термин «полиаденилирование» означает ковалентное присоединение полиаденилового фрагмента или его модифицированного варианта к молекуле матричной РНК. У эукариотических организмов большинство молекул матричной РНК (мРНК) являются полиаденилированными на 3'-конце. 3'-поли(A) «хвост» представляет собой длинную последовательность из адениновых нуклеотидов (часто нескольких сотен), добавленную к пре-мРНК под действием фермента полиаденилат-полимеразы. У высших эукариот поли(A) «хвост» добавляется на транскрипты, содержащие специфическую последовательность, сигнал полиаденилирования. Поли(A) «хвост» и связанный с ним белок способствуют защите мРНК от разрушения экзонуклеазами. Полиаденилирование также важно для терминации транскрипции, экспорта мРНК из ядра и трансляции. Полиаденилирование происходит в ядре непосредственно после транскрипции ДНК в РНК, но, кроме того, также может происходить позднее в цитоплазме. После завершения транскрипции цепь мРНК расщепляется под действием эндонуклеазного комплекса, связанного с РНК-полимеразой. Сайт расщепления, как правило, характеризуется наличием последовательности оснований AAUAAA рядом с сайтом расщепления. После расщепления мРНК остатки аденозина добавляются к свободному 3'-концу в сайте расщепления.
Используемый в настоящем документе термин «временная» относится к экспрессии не интегрированного трансгена в течение нескольких часов, дней или недель, при этом период времени экспрессии меньше, чем период времени экспрессии гена в случае его интеграции в геном или нахождения в стабильном плазмидном репликоне в клетке-хозяине.
Используемые в настоящем документе термины «лечить», «лечение» и «терапия» означают уменьшение или ослабление прогрессирования, степени тяжести и/или продолжительности пролиферативного заболевания, или ослабление одного или более симптомов (предпочтительно, одного или более явных симптомов) пролиферативного заболевания, возникающее в результате введения одного или более терапевтических средств (например, одного или более терапевтических средств, таких как CAR по изобретению). В конкретных вариантах осуществления термины «лечить», «лечение» и «терапия» означают уменьшение по меньшей мере одного измеримого физического параметра пролиферативного заболевания, такого как рост опухоли, не обязательно ощущаемое пациентом. В других вариантах осуществления термины «лечить», «лечение» и «терапия» означают ингибирование прогрессирования пролиферативного заболевания, либо физически, например, стабилизацию явного симптома, физиологически, например, стабилизацию физического параметра, либо и то, и другое. В других вариантах осуществления термины «лечить», «лечение» и «терапия» означают уменьшение или стабилизацию размера опухоли или количества раковых клеток.
Термин «путь передачи сигнала» означает биохимическое взаимодействие между разными передающими сигнал молекулами, которые играют определенную роль в передаче сигнала из одной части клетки в другую часть клетки. Выражение «рецептор клеточной поверхности» охватывает молекулы и комплексы молекул, способные получать сигнал и передавать сигнал через мембрану клетки.
Термин «субъект» должен включать живые организмы, у которых может быть вызван иммунный ответ (например, млекопитающих, человека). При использовании в настоящем документе термины «субъект» или «пациент» могут включать человека или млекопитающее, не являющееся человеком. Млекопитающие, не являющиеся людьми, включают, например, домашний скот и домашних питомцев, например, овец, крупный рогатый скот, свиней, собак, кошек и морских млекопитающих. Предпочтительно, субъект является человеком.
Термин «в значительной степени очищенная» клетка означает клетку, которая практически свободна от клеток других типов. «В значительной степени очищенная» клетка также означает клетку, которая была отделена от клеток других типов, с которыми она естественным образом связана в ее естественном окружении. В некоторых случаях популяция «в значительной степени очищенных» клеток означает гомогенную популяцию клеток. В других случаях данный термин просто означает клетку, которая была отделена от клеток, с которыми она естественным образом связана в ее естественном окружении. В некоторых аспектах клетки культивируют in vitro. В других аспектах клетки не культивируют in vitro.
Используемый в настоящем документе термин «суицидный ген» означает индуцирующий самоуничтожение или апоптоз ген, функционально связанный с промотором, который может быть конститутивным или индуцируемым. Примеры суицидного гена включают, но без ограничения, ген тимидинкиназы вируса простого герпеса (HSV-TK), цитоплазматического домена Fas, каспазы, такой как каспаза-8 или каспаза-9, цитозин-дезаминазы, E1A, FHIT, а также другие известные индуцирующие самоуничтожение или апоптоз гены.
Используемый в настоящем документе термин «продукт суицидного гена» или «суицидный домен» означает продукт экспрессии суицидного гена.
Используемый в настоящем документе термин «терапевтический» эффект означает лечение. Терапевтический эффект получают за счет уменьшения, подавления, ремиссии или устранения болезненного состояния.
Используемый в настоящем документе термин «толерантность» или «иммунная толерантность» означает состояние, при котором у субъекта уменьшен или отсутствует иммунный ответ на специфический антиген или группу антигенов, на которые субъект обычно реагирует. Толерантность достигается в условиях, которые вызывают подавление иммунной реакции, и представляет собой не только отсутствие иммунного ответа. В одном из вариантов осуществления толерантность у субъекта может быть охарактеризована, как одно или более из следующего: снижение уровня специфического иммунологического ответа (например, опосредованного антиген-специфическими эффекторными T-лимфоцитами, B-лимфоцитами или антителами); задержка начала или прогрессирования специфического иммунологического ответа; или снижение вероятности начала или прогрессирования специфического иммунологического ответа, в сравнении с не подвергнутыми воздействию субъектами.
Используемый в настоящем документе термин «профилактика» означает предотвращение, или упреждающее лечение, заболевания или болезненного состояния.
Термин «трансфекция» или «трансформация», или «трансдукция» означает процесс, за счет которого экзогенная нуклеиновая кислота переносится или вводится в клетку-хозяина. «Трансфицированная» или «трансформированная», или «трансдуцированная» клетка представляет собой клетку, которая была трансфицирована, трансформирована или трансдуцирована экзогенной нуклеиновой кислотой. Клетка включает первичную клетку субъекта и ее потомство.
Термин «специфически связывает» относится к антителу или лиганду, которые узнают и связываются с соответствующим белком - партнером по связыванию (например, стимулирующей и/или костимулирующей молекулой, присутствующей на T-клетке), присутствующим в образце, но при этом антитело или лиганд практически не узнают или не связывают другие молекулы в образце.
Используемый в настоящем документе термин «рефрактерный» относится к заболеванию, например, раку, которое на отвечает на лечение. В вариантах осуществления рефрактерный рак может быть резистентным к лечению до, или в начале, лечения. В других вариантах осуществления рефрактерный рак может становиться резистентным в процессе лечения. Рефрактерный рак также называют резистентным раком.
Используемые в настоящем документе термины «рецидивирующий» или «рецидив» означают возращение или повторное возникновение заболевания (например, рака), либо признаков и симптомов заболевания, такого как рак, после периода улучшения или ответа на лечение, например, после проведенного ранее лечения, например, лечения рака. Начальный период ответа на лечение может включать уменьшение количества раковых клеток до уровня ниже определенного предела, например, ниже 20%, 1%, 10%, 5%, 4%, 3%, 2% или 1%. Возвращение болезни может включать увеличение количества раковых клеток до уровня выше определенного предела, например, выше 20%, 1%, 10%, 5%, 4%, 3%, 2% или 1%. Например, в контексте B-ALL, возвращение болезни может включать, например, повторное появление бластов в крови, костном мозге (>5%) или любом экстрамедуллярном участке тела, после полного ответа на лечение. Полный ответ, в данном контексте, может включать наличие <5% КМ бластов. В более общем смысле, в одном из вариантов осуществления ответ (например, полный ответ или частичный ответ) может включать отсутствие поддающегося обнаружению МОЗ (минимального остаточного заболевания). В одном из вариантов осуществления начальный период ответа на лечение продолжается по меньшей мере 1, 2, 3, 4, 5 или 6 дней; по меньшей мере 1, 2, 3 или 4 недели; по меньшей мере 1, 2, 3, 4, 6, 8, 10 или 12 месяцев; или по меньшей мере 1, 2, 3, 4 или 5 лет.
Диапазоны: в тексте данной заявки различные аспекты изобретения могут быть представлены в формате диапазонов. Следует понимать, что описание в формате диапазона служит исключительно для удобства и краткости, и не должно быть воспринято как негибкое ограничение объема изобретения. Соответственно, описание диапазона следует понимать, как специально включающее все возможные поддиапазоны, а также отдельные числовые значения в пределах диапазона. Например, описание такого диапазона, как от 1 до 6, следует понимать, как включающее конкретно раскрытые поддиапазоны, такие как от 1 до 3, от 1 до 4, от 1 до 5, от 2 до 4, от 2 до 6, от 3 до 6 и так далее, а также отдельные числа в данном диапазоне, например, 1, 2, 2,7, 3, 4, 5, 5,3 и 6. В качестве другого примера, такой диапазон, как 95-99% идентичности, включает нечто, имеющее идентичность 95%, 96%, 97%, 98% или 99%, в том числе поддиапазоны, такие как 96-99%, 96-98%, 96-97%, 97-99%, 97-98% и 98-99% идентичности. Данное правило применимо независимо от широты диапазона.
Слитые белки
Настоящее изобретение относится к слитым белкам, содержащим два белковых домена, разделенные гетерологичным сайтом расщепления протеазы (например, сайтом расщепления протеазы, который расщепляется внутриклеточной или внеклеточной протеазой), при этом первый из белковых доменов представляет собой домен условной экспрессии, например, домен деградации или домен агрегации. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат три основных элемента: домен условной экспрессии, например, домен деградации или домен агрегации, домен, содержащий интересующий белок, и расщепляемый протеазой домен, разделяющий эти два домена. Эти элементы могут быть организованы таким образом, что домен условной экспрессии, например, домен деградации или домен агрегации, расположен либо в N-концевом, либо в C-концевом направлении относительно интересующего белка.
В некоторых вариантах осуществления слитый белок, описанный в настоящем документе, содержит сайт расщепления фурина. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат любой из сайтов расщепления фурина, приведенных в Таблице 20. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; LQWLEQQVAKRRTKR (SEQ ID NO: 129) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLG (SEQ ID NO: 133) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; SLNLTESHNSRKKR (SEQ ID NO: 135) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; или CKINGYPKRGRKRR (SEQ ID NO: 137) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней, или GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательность, имеющую по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней.
В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135) или CKINGYPKRGRKRR (SEQ ID NO: 137). В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или GTGAEDPRPSRKRR (SEQ ID NO: 127). В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125).
В некоторых вариантах осуществления слитый белок, описанный в настоящем документе, содержит фуриновый дегрон-домен (FurON), который включает два компонента: дегрон, или домен деградации, который представляет собой мутантный белковый домен, неспособный принимать правильную конформацию в отсутствие низкомолекулярного лиганда, и сайт расщепления фурина. Фуриновый дегрон-домен может быть слит с интересующим белком, который экспрессируется в эндоплазматическом ретикулуме. N- и/или C-конец интересующего белка могут быть использованы в качестве сайта слияния, при условии, что фуриновый дегрон-домен направлен в сторону просвета эндоплазматического ретикулума. Интересующий белок может представлять собой либо мембранный белок (независимо от числа трансмембранных доменов), либо растворимый белок. Ориентация сайта расщепления фурина относительно дегрон-домена должна быть такой, чтобы расщепление приводило к разделению фуринового дегрон-домена и интересующего белка. В отсутствие низкомолекулярного лиганда или стабилизирующего соединения фуриновый дегрон-домен приводит к дестабилизации или деградации всего слитого белка. В присутствии низкомолекулярного лиганда или стабилизирующего соединения слитый белок не подвергается деградации. Фуриновый дегрон-домен мутирован таким образом, что аффинность для его естественного эндогенного лиганда устранена; аффинность для низкомолекулярного лиганда или стабилизирующего соединения сохранена; и белок становится нестабильным в отсутствие низкомолекулярного лиганда.
В некоторых вариантах осуществления дегрон, или домен деградации, получен из белка, приведенного в Таблице 21. В некоторых вариантах осуществления дегрон, или домен деградации, получен из рецептора эстрогена. В некоторых вариантах осуществления дегрон, или домен деградации, содержит аминокислотную последовательность, выбранную из SEQ ID NO: 58 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней, или SEQ ID NO: 121 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления дегрон, или домен деградации, содержит аминокислотную последовательность, выбранную из SEQ ID NO: 58 или SEQ ID NO: 121.
В некоторых вариантах осуществления дегрон, или домен деградации, получен из белка FKB (FKBP). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность SEQ ID NO: 56 или последовательность, имеющую по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность SEQ ID NO: 56.
В некоторых вариантах осуществления дегрон, или домен деградации, получен из дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 57 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 57. В некоторых вариантах осуществления дегрон, или домен деградации, получен не из белка FKB, рецептора эстрогена или DHFR.
Интересующие белки
Слитые белки по изобретению могут содержать практически любой интересующий белок. В некоторых предпочтительных вариантах осуществления интересующий белок может представлять собой трансмембранный белок (например, трансмембранный рецептор). Формат слитых белков по изобретению является особенно полезным в случае таких трансмембранных белков, поскольку включение интактного домена условной экспрессии, например, домена деградации или, например, домена агрегации, на N-конце трансмембранного рецептора может приводить к нарушению активности интересующего белка, при этом включение на C-конце может приводить к плохой регуляции интересующего белка (поскольку, например, интегрирование в мембрану может приводить к достаточной стабилизации белка или домена деградации для отсутствия деградации и/или агрегации). Одним примером класса интересующих белков являются химерные антигенные T-клеточные рецепторы, описанные в следующем разделе.
Химерный антигенный рецептор
В некоторых вариантах осуществления интересующий белок представляет собой химерный антигенный рецептор (CAR), при этом CAR содержит антигенсвязывающий домен (например, антитело или фрагмент антитела, TCR или фрагмент TCR), который связывается с опухолевым антигеном, описанным в настоящем документе, трансмембранный домен (например, трансмембранный домен, описанный в настоящем документе) и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, описанный в настоящем документе) (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен (например, костимулирующий домен, описанный в настоящем документе) и/или основной сигнальный домен (например, основной сигнальный домен, описанный в настоящем документе). Конструкты нуклеиновой кислоты CAR, закодированные белки, содержащие их векторы, клетки-хозяева, фармацевтические композиции, а также способы введения и лечения, относящиеся к настоящему изобретению, описаны подробно в публикации международной патентной заявки № WO2015142675, полное содержание которой включено в настоящий документ посредством ссылки.
В некоторых вариантах осуществления интересующий белок представляет собой химерный антигенный рецептор (CAR), при этом CAR содержит антигенсвязывающий домен (например, антитело или фрагмент антитела, TCR или фрагмент TCR), который связывается с опухоль-специфическим антигеном (например, опухоль-специфическим антигеном, описанным в настоящем документе), трансмембранный домен (например, трансмембранный домен, описанный в настоящем документе) и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, описанный в настоящем документе) (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен (например, костимулирующий домен, описанный в настоящем документе) и/или основной сигнальный домен (например, основной сигнальный домен, описанный в настоящем документе). В некоторых вариантах осуществления опухоль-специфический антиген представляет собой антиген, присутствующий на стромальной клетке или миелоидной супрессорной клетке (MDSC). В других аспектах изобретение относится к полипептидам, кодируемым такими нуклеиновыми кислотами, и клеткам-хозяевам, содержащим такие нуклеиновые кислоты и/или полипептиды.
В некоторых вариантах осуществления молекула CAR содержит по меньшей мере один внутриклеточный сигнальный домен, выбранный из сигнального домена CD137 (4-1BB), сигнального домена CD28, сигнального домена CD27, сигнального домена ICOS, сигнального домена CD3-дзета, или любых их сочетаний. В некоторых вариантах осуществления молекула CAR содержит по меньшей мере один внутриклеточный сигнальный домен, выбранный из одной или более костимулирующих молекул, выбранных из CD137 (4-1BB), CD28, CD27 или ICOS.
В некоторых аспектах настоящее изобретение также относится к способу модификации T-клетки химерным антигенным рецептором (CAR) и суицидным геном. Таким образом, настоящее изобретение относится к нуклеиновой кислоте, кодирующей CAR, или модифицированной T-клетке, содержащей CAR, при этом CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен.
Иллюстративные CAR описаны в патентах США №№ 8911993, 8906682, 8975071, 8916381, 9102760, 9101584 и 9102761, содержание всех из которых включено в настоящий документ посредством ссылки в полном объеме.
Последовательности неограничивающих примеров различных компонентов, которые могут являться частью молекул CAR, приведены в Таблице 2, где «ак» означает аминокислотную последовательность и «нк» означает нуклеиновую кислоту, кодирующую соответствующий пептид.
Таблица 2. Последовательности различных компонентов CAR (ак - аминокислотная последовательность, нк - нуклеиновая кислота, кодирующая соответствующий белок)
В конкретных аспектах конструкт CAR содержит домен scFv, при этом домену scFv может предшествовать, необязательно, лидерная последовательность, такая как последовательность, приведенная в SEQ ID NO: 2, и за ним может следовать, необязательно, шарнирная последовательность, такая как последовательность, приведенная в SEQ ID NO: 4 или SEQ ID NO: 6, или SEQ ID NO: 8, или SEQ ID NO: 10, трансмембранную область, например, приведенную в SEQ ID NO: 12, внутриклеточный сигнальный домен, содержащий любую из последовательностей SEQ ID NO: 14, SEQ ID NO: 16, SEQ ID NO: 120 или SEQ ID NO: 124, и последовательность CD3-дзета, которая содержит SEQ ID NO: 18 или SEQ ID NO: 20, например, причем домены являются смежными и находятся в одной рамке считывания, образуя один слитый белок.
В одном аспекте иллюстративные конструкты CAR содержат, необязательно, лидерную последовательность (например, лидерную последовательность, описанную в настоящем документе), внеклеточный антигенсвязывающий домен (например, антигенсвязывающий домен, описанный в настоящем документе), шарнир (например, шарнирную область, описанную в настоящем документе), трансмембранный домен (например, трансмембранный домен, описанный в настоящем документе) и внутриклеточный стимулирующий домен (например, внутриклеточный стимулирующий домен, описанный в настоящем документе). В одном аспекте иллюстративный конструкт CAR содержит, необязательно, лидерную последовательность (например, лидерную последовательность, описанную в настоящем документе), внеклеточный антигенсвязывающий домен (например, антигенсвязывающий домен, описанный в настоящем документе), шарнир (например, шарнирную область, описанную в настоящем документе), трансмембранный домен (например, трансмембранный домен, описанный в настоящем документе), внутриклеточный костимулирующий сигнальный домен (например, костимулирующий сигнальный домен, описанный в настоящем документе) и/или внутриклеточный основной сигнальный домен (например, основной сигнальный домен, описанный в настоящем документе).
Иллюстративная лидерная последовательность приведена в SEQ ID NO: 2. Иллюстративная последовательность шарнира/спейсера приведена в SEQ ID NO: 4 или SEQ ID NO: 6, или SEQ ID NO: 8, или SEQ ID NO: 10. Иллюстративная последовательность трансмембранного домена приведена в SEQ ID NO: 12. Иллюстративная последовательность внутриклеточного сигнального домена белка 4-1BB приведена в SEQ ID NO: 14. Иллюстративная последовательность внутриклеточного сигнального домена CD27 приведена в SEQ ID NO: 16. Иллюстративная последовательность внутриклеточного сигнального домена ICOS приведена в ID NO: 120. Иллюстративная последовательность внутриклеточного сигнального домена CD28 приведена в ID NO: 124. Иллюстративная последовательность домена CD3-дзета приведена в ID NO: 18 или SEQ ID NO: 20.
Нуклеотидные последовательности, кодирующие нужные молекулы, можно получать рекомбинантными методами, известными в данной области, такими как, например, скрининг библиотек из клеток, экспрессирующих молекулу нуклеиновой кислоты, получение молекулы нуклеиновой кислоты из вектора, который, как известно, содержит ее, или путем непосредственного выделения из клеток и тканей, содержащих ее, с использованием стандартных методов. Альтернативно, интересующую нуклеиновую кислоту можно получать методами синтеза, а не клонирования.
Антигенсвязывающий домен
В одном аспекте химерный антигенный рецептор (CAR) содержит специфичный для мишени связывающий элемент, иначе называемый антигенсвязывающим доменом. Выбор фрагмента зависит от вида и числа лигандов, находящихся на поверхности клетки-мишени. Например, антигенсвязывающий домен может быть выбран или сконструирован для узнавания лиганда, который действует как клеточный поверхностный маркер на клетках-мишенях, связанных с конкретным болезненным состоянием, например, опухолевого антигена, связанного с конкретным видом рака (например, антигенсвязывающий домен, который связывается с опухолевым антигеном). В других вариантах осуществления антигенсвязывающий домен выбирают или конструируют для узнавания нормальных B-клеток или субпопуляции B-клеток для истощения нормальных B-клеток или целевой популяции B-клеток (например, антигенсвязывающий домен, который связывается с B-клеточным антигеном).
Антигенсвязывающий домен может представлять собой любой домен, который связывается с антигеном, включая, но без ограничения, моноклональное антитело, поликлональное антитело, рекомбинантное антитело, биспецифическое антитело, конъюгированное антитело, человеческое антитело, гуманизированное антитело и его функциональный фрагмент, включая, но без ограничения, однодоменное антитело, такое как вариабельный домен тяжелой цепи (VH), вариабельный домен легкой цепи (VL) и нанотело, полученное из вариабельного домена (VHH) верблюдовых, а также альтернативный каркас, известный в данной области, действующий в качестве антигенсвязывающего домена, например, рекомбинантный домен фибронектина, T-клеточный рецептор (TCR), рекомбинантный TCR с повышенной аффинностью или его фрагмент, например, одиночная цепь TCR, и тому подобное. В некоторых случаях предпочтительно, если антигенсвязывающий домен получен из того же биологического вида, для которого впоследствии будет использован CAR. Например, в случае использования в организме человека может быть предпочтительным антигенсвязывающий домен CAR, содержащий человеческие или гуманизированные остатки в антигенсвязывающем домене антитела или фрагмента антитела.
В некоторых вариантах осуществления антигенсвязывающий домен закодированной молекулы CAR содержит антитело, фрагмент антитела, scFv, Fv, Fab, (Fab')2, однодоменное антитело (SDAB), домен VH или VL, домен VHH верблюдовых или бифункциональное (например, биспецифическое) гибридное антитело (например, Lanzavecchia et al., Eur. J. Immunol. 17, 105 (1987)).
В некоторых вариантах осуществления антигенсвязывающий домен закодированной молекулы CAR содержит scFv. В некоторых случаях фрагменты scFv могут быть получены способом, известным в данной области (смотри, например, Bird et al., (1988) Science 242:423-426 и Huston et al., (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Молекулы scFv могут быть получены путем связывания между собой областей VH и VL при помощи гибких полипептидных линкеров.
В одном аспекте антигенсвязывающий домен CAR представляет собой фрагмент scFv антитела, который является гуманизированным, в сравнении с последовательностью мышиного scFv, из которого он получен.
В одном аспекте антигенсвязывающий домен CAR по изобретению (например, scFv) закодирован молекулой нуклеиновой кислоты, последовательность которой была кодон-оптимизирована для экспрессии в клетке млекопитающего. В одном аспекте весь конструкт CAR по изобретению закодирован молекулой нуклеиновой кислоты, вся последовательность которой была кодон-оптимизирована для экспрессии в клетке млекопитающего. Кодон-оптимизация является следствием того открытия, что частота встречаемости синонимичных кодонов (то есть, кодонов, кодирующих одну и ту же аминокислоту) в кодирующей ДНК отличается у разных биологических видов. Вследствие вырожденности кодонов один и тот же полипептид может быть закодирован разными нуклеотидными последовательностями. Различные способы кодон-оптимизации известны в данной области и включают, например, способы, раскрытые по меньшей мере в патентах США с номерами 5786464 и 6114148. В одном варианте осуществления CAR содержит антигенсвязывающий домен, который связывается с B-клеткой. Клеточные поверхностные маркеры, исключительно присутствующие на B-клетках, могут действовать в качестве антигена, который связывается с антигенсвязывающим доменом CAR. Анти-B-клеточный антигенсвязывающий домен может включать любой домен, который связывается с B-клеткой, и может включать, но без ограничения, моноклональное антитело, поликлональное антитело, синтетическое антитело, человеческое антитело, гуманизированное антитело, не принадлежащее человеку антитело, а также любой его фрагмент. Таким образом, в одном варианте осуществления антигенсвязывающий домен содержит антитело или фрагмент антитела млекопитающего, например, одноцепочечный вариабельный фрагмент (scFv). Антигенсвязывающий домен может связывать один или более антигенов, например, но без ограничения, любой поверхностный маркер, исключительно присутствующий на B-клетке, такой как про-B-клетка, пре-B-клетка, незрелая B-клетка, зрелая B-клетка, B-клетка памяти и плазматическая клетка. В одном варианте осуществления антигенсвязывающий домен связывает по меньшей мере один антиген, такой как CD19, BCMA, а также любое их сочетание. В другом варианте осуществления антигенсвязывающий домен связывает по меньшей мере один антиген, такой как CD20, CD21, CD27, CD38, CD138, а также любое их сочетание. В некоторых случаях предпочтительно, если антигенсвязывающий домен получен из того же биологического вида, для которого впоследствии будет использован CAR. Например, в случае использования в организме человека может быть предпочтительным антигенсвязывающий домен CAR, содержащий человеческое антитело, гуманизированное антитело, описанное в другом разделе настоящего документа, или его фрагмент.
Опухолевые антигены
В некоторых вариантах осуществления антигенсвязывающий домен CAR специфически нацелен на опухолевый антиген. Существуют два класса опухолевых антигенов (антигенов опухолей, TA), которые могут служить мишенью для CAR по настоящему изобретению: (1) опухолевый антиген, экспрессированный на поверхности раковых клеток; и (2) опухолевый антиген, который сам является внутриклеточным, однако фрагмент такого антигена (пептид) представлен на поверхности раковых клеток в контексте MHC (главного комплекса гистосовместимости).
В одном варианте осуществления опухолевый антиген экспрессирован как на нормальных клетках, так и на раковых клетках, однако на нормальных клетках он экспрессирован на более низком уровне. В одном варианте осуществления способ дополнительно включает выбор CAR, который связывает опухолевый антиген с аффинностью, позволяющей клетке, сконструированной для экспрессии CAR, связываться и уничтожать раковые клетки, экспрессирующие опухолевый антиген, но при этом уничтожать менее 30%, 25%, 20%, 15%, 10%, 5%, или менее, нормальных клеток, экспрессирующих опухолевый антиген, например, при определении в анализе, описанном в настоящем документе. Например, можно использовать анализ на уничтожение, такой как проточная цитометрия с использованием Cr-51 CTL. В одном варианте осуществления выбранный CAR имеет антигенсвязывающий домен, имеющий аффинность связывания KD от 10-4 M до 10-8 M, например, от 10-5 M до 10-7 M, например, 10-6 M или 10-7 M, для антигена-мишени. В одном варианте осуществления выбранный антигенсвязывающий домен имеет аффинность связывания, которая меньше по меньшей мере в пять раз, 10 раз, 20 раз, 30 раз, 50 раз, 100 раз или 1000 раз, чем у эталонного антитела, например, антитела, описанного в настоящем документе.
Соответственно, клетка может быть сконструирована для экспрессии CAR, содержащего антигенсвязывающий домен, который может быть нацелен, например, связываться с любым из следующих иллюстративных опухолевых антигенов (антигенов опухолей): CD123, CD30, CD171, CS-1, CLL-1 (CLECL1), CD33, EGFRvIII, GD2, GD3, Tn Ag, sTn Ag, Tn-O-гликопептиды, Stn-O-гликопептиды, PSMA, FLT3, FAP, TAG72, CD44v6, CEA, EPCAM, B7H3, KIT, IL-13Ra2, мезотелин, IL-11Ra, PSCA, VEGFR2, LewisY, PDGFR-бета, PRSS21, SSEA-4, фолатный рецептор альфа, ERBB2 (Her2/neu), MUC1, EGFR, NCAM, простаза, PAP, ELF2M, эфрин B2, рецептор IGF-I, CAIX, LMP2, gp100, bcr-abl, тирозиназа, EphA2, фукозил GM1, sLe, GM3, TGS5, HMWMAA, o-ацетил-GD2, фолатный рецептор бета, TEM1/CD248, TEM7R, CLDN6, TSHR, GPRC5D, CXORF61, CD97, CD179a, ALK, полисиаловая кислота, PLAC1, GloboH, NY-BR-1, UPK2, HAVCR1, ADRB3, PANX3, GPR20, LY6K, OR51E2, TARP, WT1, NY-ESO-1, LAGE-1a, легумаин, HPV E6,E7, MAGE-A1, MAGE A1, ETV6-AML, белок спермы 17, XAGE1, Tie 2, MAD-CT-1, MAD-CT-2, Fos-родственный антиген 1, p53, мутант p53, простеин, сурвивин и теломераза, PCTA-1/галектин 8, MelanA/MART1, мутант Ras, hTERT, точки разрыва при транслокации в случае саркомы, ML-IAP, ERG (TMPRSS2 ETS слитый ген), NA17, PAX3, рецептор андрогена, циклин B1, MYCN, RhoC, TRP-2, CYP1B1, BORIS, SART3, PAX5, OY-TES1, LCK, AKAP-4, SSX2, RAGE-1, обратная транскриптаза теломераза человека, RU1, RU2, кишечная карбоксилэстераза, mut hsp70-2, LAIR1, FCAR, LILRA2, CD300LF, CLEC12A, BST2, EMR2, LY75, GPC3, FCRL5, IGLL1, CD10, CD19, CD20, CD21, CD22, CD23, CD24, CD25, CD37, CD38, CD53, CD72, CD73, CD74, CD75, CD77, CD79a, CD79b, CD80, CD81, CD82, CD83, CD84, CD85, ROR1, BCMA, CD86, и CD179b. Другие B-клеточные антигены, на которые могут быть нацелены CAR, описанные в настоящем документе, включают: CD1a, CD1b, CD1c, CD1d, CD2, CD5, CD6, CD9, CD11a, CD11b, CD11c, CD17, CD18, CD26, CD27, CD29, CD30, CD31, CD32a, CD32b, CD35, CD38, CD39, CD40, CD44, CD45, CD45RA, CD45RB, CD45RC, CD45RO, CD46, CD47, CD48, CD49b, CD49c, CD49d, CD50, CD52, CD54, CD55, CD58, CD60a, CD62L, CD63, CD63, CD68 CD69, CD70, CD85E, CD85I, CD85J, CD92, CD95, CD97, CD98, CD99, CD100, CD102, CD108, CD119, CD120a, CD120b, CD121b, CD122, CD124, CD125, CD126, CD130, CD132, CD137, CD138, CD139, CD147, CD148, CD150, CD152, CD162, CD164, CD166, CD167a, CD170, CD175, CD175s, CD180, CD184, CD185, CD192, CD196, CD197, CD200, CD205, CD210a, CDw210b, CD212, CD213a1, CD213a2, CD215, CD217, CD218a, CD218b, CD220, CD221, CD224, CD225, CD226, CD227, CD229, CD230, CD232, CD252, CD253, CD257, CD258, CD261, CD262, CD263, CD264, CD267, CD268, CD269, CD270, CD272, CD274, CD275, CD277, CD279, CD283, CD289, CD290, CD295, CD298, CD300a, CD300c, CD305, CD306, CD307a, CD307b, CD307c, CD307d, CD307e, CD314, CD315, CD316, CD317, CD319, CD321, CD327, CD328, CD329, CD338, CD351, CD352, CD353, CD354, CD355, CD357, CD358, CD360, CD361, CD362, CD363, а также пептиды этих антигенов, представленные на MHC.
В некоторых вариантах осуществления антигенсвязывающий домен CAR нацелен на опухолевый антиген, связанный с солидной опухолью, например, экспрессируемый клеткой солидной опухоли, в настоящем документе называемый антигеном, связанным с солидной опухолью, например, антиген, связанный с мезотелиомой (например, злокачественной мезотелиомой плевры), раком легкого (например, немелкоклеточным раком легкого, мелкоклеточным раком легкого, плоскоклеточным раком легкого или крупноклеточным раком легкого), раком поджелудочной железы (например, протоковой аденокарциномой поджелудочной железы), аденокарциномой пищевода, раком яичника, раком молочной железы, колоректальным раком и раком мочевого пузыря, или любым их сочетанием. В одном варианте осуществления заболевание представляет собой рак поджелудочной железы, например, метастатическую протоковую аденокарциному поджелудочной железы (PDA), например, у субъекта, у которого он прогрессировал при по меньшей мере одной предшествующей стандартной терапии. В одном варианте осуществления заболевание представляет собой мезотелиому (например, злокачественную мезотелиому плевры), например, у субъекта, у которого он прогрессировал при по меньшей мере одной предшествующей стандартной терапии. В одном варианте осуществления заболевание представляет собой рак яичника, например, серозный эпителиальный рак яичника, например, у субъекта, у которого он прогрессировал после по меньшей мере одной предшествующей схемы стандартной терапии.
Примеры связанных с опухолью антигенов (то есть, антигенов солидной опухоли) включают, без ограничения: EGFRvIII, мезотелин, GD2, Tn-антиген, sTn-антиген, Tn-O-гликопептиды, sTn-O-гликопептиды, PSMA, CD97, TAG72, CD44v6, CEA, EPCAM, KIT, IL-13Ra2, легумаин, GD3, CD171, IL-11Ra, PSCA, MAD-CT-1, MAD-CT-2, VEGFR2, LewisY, CD24, PDGFR-бета, SSEA-4, фолатный рецептор альфа, ERBB (например, ERBB2), Her2/neu, MUC1, EGFR, NCAM, эфрин B2, CAIX, LMP2, sLe, HMWMAA, o-ацетил-GD2, фолатный рецептор бета, TEM1/CD248, TEM7R, FAP, легумаин, HPV E6 или E7, ML-IAP, CLDN6, TSHR, GPRC5D, ALK, полисиаловую кислоту, Fos-родственный антиген, нейтрофильную эластазу, TRP-2, CYP1B1, белок спермы 17, бета-субъединицу хорионического гонадотропина человека, AFP, тиреоглобулин, PLAC1, globoH, RAGE1, MN-CA IX, обратную транскриптазу теломеразу человека, кишечную карбоксилэстеразу, mut hsp 70-2, NA-17, NY-BR-1, UPK2, HAVCR1, ADRB3, PANX3, NY-ESO-1, GPR20, Ly6k, OR51E2, TARP, GFRα4, а также пептид любого из этих антигенов, представленный на MHC.
В одном из вариантов осуществления антигенсвязывающий домен CAR связывается с мезотелином человека. В одном из вариантов осуществления антигенсвязывающий домен представляет собой мышиный домен scFv, который связывается с мезотелином человека, например, SS1, приведенный в Таблице 3. В одном из вариантов осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела, например, домен scFv, полученный из мышиного SS1 scFv. В одном из вариантов осуществления антигенсвязывающий домен представляет собой человеческое антитело, или фрагмент антитела, которое связывается с мезотелином человека. Иллюстративные человеческие домены scFv (и их последовательности) и мышиные SS1 scFv, которые связываются с мезотелином, приведены в Таблице 3. Последовательности CDR подчеркнуты. Последовательности домена scFv, приведенные в Таблице 3, включают вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH связаны линкером, содержащим последовательность GGGGSGGGGSGGGGS (SEQ ID NO: 30) (например, как показано в доменах SS1 scFv) или GGGGSGGGGSGGGGSGGGGS (SEQ ID NO: 29) (например, как показано в M1, M2, M3, M4, M5, M6, M7, M8, M9, M10, M11, M12, M13, M14, M15, M16, M17, M18, M19, M20, M21, M22, M23 или M24 доменах scFv). Домены scFv, приведенные в Таблице 3, находятся в следующей ориентации: VL-линкер-VH.
Таблица 3. Антигенсвязывающие домены, которые связываются с мезотелином
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
(человека)
Последовательности CDR доменов scFv антигенсвязывающих доменов для мезотелина, приведенных в Таблице 3, приведены в Таблице 4 для вариабельных доменов тяжелой цепи и в Таблице 5 для вариабельных доменов легкой цепи.
Таблица 4. Аминокислотные последовательности областей CDR1, CDR2 и CDR3 тяжелой цепи (HC) scFv для мезотелина человека
Таблица 5. Аминокислотные последовательности областей CDR1, CDR2 и CDR3 легкой цепи (LC) scFv для мезотелина человека
Любой известный связывающий домен для мезотелина из, например, известного антитела, биспецифической молекулы или CAR, может быть подходящим для использования в CAR по настоящему изобретению. Например, антигенсвязывающий домен для мезотелина получен, или может быть получен, из антигенсвязывающих областей, например, CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в PCT публикации WO2015/090230. В вариантах осуществления антигенсвязывающий домен для мезотелина представляет собой, или получен из антигенсвязывающего фрагмента, например, CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в PCT публикациях WO1997/025068, WO1999/028471, WO2005/014652, WO2006/099141, WO2009/045957, WO2009/068204, WO2013/142034, WO2013/040557 или WO2013/063419.
В одном варианте осуществления мезотелин-связывающий домен содержит одну или более (например, все три) из определяющей комплементарность области 1 легкой цепи (LC CDR1), определяющей комплементарность области 2 легкой цепи (LC CDR2) и определяющей комплементарность области 3 легкой цепи (LC CDR3) мезотелин-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 3 или 5, и/или одну или более (например, все три) из определяющей комплементарность области 1 тяжелой цепи (HC CDR1), определяющей комплементарность области 2 тяжелой цепи (HC CDR2) и определяющей комплементарность области 3 тяжелой цепи (HC CDR3) мезотелин-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 3 или 4. В одном варианте осуществления мезотелин-связывающий домен содержит одну, две или все из LC CDR1, LC CDR2 и LC CDR3 с любыми аминокислотными последовательностями, приведенными в Таблице 5; и одну, две или все из HC CDR1, HC CDR2 и HC CDR3 с любыми аминокислотными последовательностями, приведенными в Таблице 4.
В одном варианте осуществления мезотелин-связывающий домен содержит вариабельную область легкой цепи, описанную в настоящем документе (например, в Таблице 3) и/или вариабельную область тяжелой цепи, описанную в настоящем документе (например, в Таблице 3). В одном варианте осуществления мезотелин-связывающий домен представляет собой scFv, содержащий легкую цепь и тяжелую цепь с аминокислотными последовательностями, приведенными Таблице 3. В одном из вариантов осуществления мезотелин-связывающий домен (например, scFv) содержит: вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области легкой цепи, приведенной в Таблице 3, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 3; и/или вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области тяжелой цепи, приведенной в Таблице 3, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 3.
В одном варианте осуществления мезотелин-связывающий домен содержит аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 201-225; или аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) в любой из вышеуказанных последовательностей; или последовательность, имеющую 95-99% идентичности с любой из вышеуказанных последовательностей. В одном варианте осуществления мезотелин-связывающий домен представляет собой scFv, и вариабельная область легкой цепи, содержащая аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 3, связана с вариабельной областью тяжелой цепи, содержащей аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 3, через линкер, например, линкер, описанный в настоящем документе. В одном варианте осуществления мезотелин-связывающий домен включает (Gly4-Ser)n линкер, где n равно 1, 2, 3, 4, 5 или 6, предпочтительно 4 (SEQ ID NO: 967). Вариабельная область легкой цепи и вариабельная область тяжелой цепи в scFv могут находиться, например, в любой из следующих ориентаций: вариабельная область легкой цепи-линкер-вариабельная область тяжелой цепи или вариабельная область тяжелой цепи-линкер-вариабельная область легкой цепи.
В одном из вариантов осуществления антигенсвязывающий домен CAR, например, CAR, экспрессируемого клеткой по изобретению, связывается с EGFRvIII человека. В одном из вариантов осуществления антигенсвязывающий домен представляет собой мышиный домен scFv, который связывается с EGFRvIII человека, такой как, например, mu310C. В одном из вариантов осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела, например, домен scFv, полученный из мышиного mu31°C scFv. Иллюстративные гуманизированные домены scFv (и их последовательности), а также мышиные SS1 scFv, которые связываются с EGFRvIII, приведены в Таблице 6.
В одном из вариантов осуществления антигенсвязывающий домен CAR связывается с клаудином-6 (CLDN6) человека. В одном из вариантов осуществления антигенсвязывающий домен представляет собой мышиный домен scFv, который связывается с CLDN6 человека. В одном из вариантов осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела. Иллюстративные домены scFv (и их последовательности), которые связываются с CLDN6, приведены в Таблице 6. Последовательности доменов scFv, приведенные в Таблице 6, включают вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH связаны линкером, содержащим последовательность GGGGSGGGGSGGGGSGGGGS (SEQ ID NO: 29), например, в следующей ориентации: VL-линкер-VH.
Таблица 6. Антигенсвязывающие домены, которые связываются с опухолевым антигеном EGFRvIII или CLDN6
В одном варианте осуществления EGFRvIII-связывающий домен содержит одну или более (например, все три) из определяющей комплементарность области 1 легкой цепи (LC CDR1), определяющей комплементарность области 2 легкой цепи (LC CDR2) и определяющей комплементарность области 3 легкой цепи (LC CDR3) EGFRvIII-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 6, и/или одну или более (например, все три) из определяющей комплементарность области 1 тяжелой цепи (HC CDR1), определяющей комплементарность области 2 тяжелой цепи (HC CDR2) и определяющей комплементарность области 3 тяжелой цепи (HC CDR3) EGFRvIII-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 6.
В одном варианте осуществления EGFRvIII-связывающий домен содержит вариабельную область легкой цепи, описанную в настоящем документе (например, в Таблице 6) и/или вариабельную область тяжелой цепи, описанную в настоящем документе (например, в Таблице 6). В одном варианте осуществления EGFRvIII-связывающий домен представляет собой scFv, содержащий легкую цепь и тяжелую цепь с аминокислотными последовательностями, приведенными Таблице 6. В одном из вариантов осуществления EGFRvIII-связывающий домен (например, scFv) содержит: вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области легкой цепи, приведенной в Таблице 6, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 6; и/или вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области тяжелой цепи, приведенной в Таблице 6, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 6.
В одном варианте осуществления EGFRvIII-связывающий домен содержит аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 344-352; или аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) в любой из вышеуказанных последовательностей; или последовательность, имеющую 95-99% идентичности с любой из вышеуказанных последовательностей. В одном варианте осуществления EGFRvIII-связывающий домен представляет собой scFv, и вариабельная область легкой цепи, содержащая аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 6, связана с вариабельной областью тяжелой цепи, содержащей аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 6, через линкер, например, линкер, описанный в настоящем документе. В одном варианте осуществления EGFRvIII-связывающий домен включает (Gly4-Ser)n линкер, где n равно 1, 2, 3, 4, 5 или 6, предпочтительно 4 (SEQ ID NO: 967). Вариабельная область легкой цепи и вариабельная область тяжелой цепи в scFv могут находиться, например, в любой из следующих ориентаций: вариабельная область легкой цепи-линкер-вариабельная область тяжелой цепи или вариабельная область тяжелой цепи-линкер-вариабельная область легкой цепи.
В одном варианте осуществления клаудин-6-связывающий домен содержит одну или более (например, все три) из определяющей комплементарность области 1 легкой цепи (LC CDR1), определяющей комплементарность области 2 легкой цепи (LC CDR2) и определяющей комплементарность области 3 легкой цепи (LC CDR3) клаудин-6-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 6, и/или одну или более (например, все три) из определяющей комплементарность области 1 тяжелой цепи (HC CDR1), определяющей комплементарность области 2 тяжелой цепи (HC CDR2) и определяющей комплементарность области 3 тяжелой цепи (HC CDR3) клаудин-6-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 6.
В одном варианте осуществления клаудин-6-связывающий домен содержит вариабельную область легкой цепи, описанную в настоящем документе (например, в Таблице 6) и/или вариабельную область тяжелой цепи, описанную в настоящем документе (например, в Таблице 6). В одном варианте осуществления клаудин-6 связывающий домен представляет собой scFv, содержащий легкую цепь и тяжелую цепь с аминокислотными последовательностями, приведенными Таблице 6. В одном из вариантов осуществления клаудин-6-связывающий домен (например, scFv) содержит: вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области легкой цепи, приведенной в Таблице 6, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 6; и/или вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области тяжелой цепи, приведенной в Таблице 6, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 6.
В одном варианте осуществления клаудин-6-связывающий домен содержит аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 353-355; или аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) в любой из вышеуказанных последовательностей; или последовательность, имеющую 95-99% идентичности с любой из вышеуказанных последовательностей. В одном варианте осуществления клаудин-6-связывающий домен представляет собой scFv, и вариабельная область легкой цепи, содержащая аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 6, связана с вариабельной областью тяжелой цепи, содержащей аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 6, через линкер, например, линкер, описанный в настоящем документе. В одном варианте осуществления клаудин-6-связывающий домен включает (Gly4-Ser)n линкер, где n равно 1, 2, 3, 4, 5 или 6, предпочтительно 4 (SEQ ID NO: 967). Вариабельная область легкой цепи и вариабельная область тяжелой цепи в scFv могут находиться, например, в любой из следующих ориентаций: вариабельная область легкой цепи-линкер-вариабельная область тяжелой цепи или вариабельная область тяжелой цепи-линкер-вариабельная область легкой цепи.
В одном варианте осуществления антигенсвязывающий домен для GD2 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Mujoo et al., Cancer Res. 47(4):1098-1104 (1987); Cheung et al., Cancer Res 45(6):2642-2649 (1985), Cheung et al., J Clin Oncol 5(9):1430-1440 (1987), Cheung et al., J Clin Oncol 16(9):3053-3060 (1998), Handgretinger et al., Cancer Immunol Immunother 35(3):199-204 (1992). В некоторых вариантах осуществления антигенсвязывающий домен для GD2 представляет собой антигенсвязывающий фрагмент антитела, выбранного из мАт 14.18, 14G2a, ch14.18, hu14.18, 3F8, hu3F8, 3G6, 8B6, 60C3, 10B8, ME36.1 и 8H9, смотри, например, WO2012033885, WO2013040371, WO2013192294, WO2013061273, WO2013123061, WO2013074916 и WO201385552. В некоторых вариантах осуществления антигенсвязывающий домен для GD2 представляет собой антигенсвязывающий фрагмент антитела, описанного в публикации патентной заявки США № 20100150910 или PCT публикации № WO2011160119.
В одном варианте осуществления антигенсвязывающий домен для Tn-антигена, sTn-антигена, Tn-O-гликопептидного антигена или sTn-O-гликопептидного антигена представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в US2014/0178365, US8440798, EP 2083868 A2, Brooks et al., PNAS 107(22):10056-10061 (2010) и Stone et al., OncoImmunology 1(6):863-873(2012).
В одном варианте осуществления антигенсвязывающий домен для PSMA представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Parker et al., Protein Expr Purif 89(2):136-145 (2013), US20110268656 (J591 ScFv); Frigerio et al, European J Cancer 49(9):2223-2232 (2013) (scFvD2B); WO2006125481 (мАт 3/A12, 3/E7 and 3/F11), и одноцепочечные фрагменты антитела (scFv A5 и D7).
В одном варианте осуществления антигенсвязывающий домен для CD97 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в US6846911; de Groot et al., J Immunol 183(6):4127-4134 (2009); или антитела из R&D:MAB3734.
В одном варианте осуществления антигенсвязывающий домен для TAG72 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Hombach et al., Gastroenterology 113(4):1163-1170 (1997); и Abcam ab691.
В одном варианте осуществления антигенсвязывающий домен для CD44v6 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Casucci et al., Blood 122(20):3461-3472 (2013).
В одном варианте осуществления антигенсвязывающий домен для CEA представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Chmielewski et al., Gastoenterology 143(4):1095-1107 (2012).
В одном варианте осуществления антигенсвязывающий домен для EPCAM представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, выбранного из MT110, EpCAM-CD3 биспецифического Ат (смотри, например, clinicaltrials.gov/ct2/show/NCT00635596); эдреколомаба; 3622W94; ING-1 и адекатумумаба (MT201).
В одном варианте осуществления антигенсвязывающий домен для KIT представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в US7915391, US20120288506, и некоторых каталогах коммерчески доступных антител.
В одном варианте осуществления антигенсвязывающий домен для IL-13Ra2 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в WO2008/146911, WO2004087758, некоторых каталогах коммерчески доступных антител и WO2004087758.
В одном варианте осуществления антигенсвязывающий домен для CD171 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Hong et al., J Immunother 37(2):93-104 (2014).
В одном варианте осуществления антигенсвязывающий домен для PSCA представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Morgenroth et al., Prostate 67(10):1121-1131 (2007) (scFv 7F5); Nejatollahi et al., J of Oncology 2013(2013), статье с ID 839831 (scFv C5-II) и патентной публикации США № 20090311181.
В одном варианте осуществления антигенсвязывающий домен для MAD-CT-2 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в PMID: 2450952; US7635753.
В одном варианте осуществления антигенсвязывающий домен для фолатного рецептора альфа представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела IMGN853, или антитела, описанного в US20120009181; US4851332, LK26: US5952484.
В одном варианте осуществления антигенсвязывающий домен для ERBB2 (Her2/neu) представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела трастузумаба или пертузумаба.
В одном варианте осуществления антигенсвязывающий домен для MUC1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела SAR566658.
В одном варианте осуществления антигенсвязывающий домен для EGFR представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела цетуксимаба, панитумумаба, залутумумаба, нимотузумаба или матузумаба.
В одном варианте осуществления антигенсвязывающий домен для NCAM представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела клона 2-2B: MAB5324 (EMD Millipore)
В одном варианте осуществления антигенсвязывающий домен для CAIX представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела клона 303123 (R&D Systems).
В одном варианте осуществления антигенсвязывающий домен для Fos-родственного антигена 1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела 12F9 (Novus Biologicals).
В одном варианте осуществления антигенсвязывающий домен для SSEA-4 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела MC813 (Cell Signaling), или других коммерчески доступных антител.
В одном варианте осуществления антигенсвязывающий домен для PDGFR-бета представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела Abcam ab32570.
В одном варианте осуществления антигенсвязывающий домен для ALK представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Mino-Kenudson et al., Clin Cancer Res 16(5):1561-1571 (2010).
В одном варианте осуществления антигенсвязывающий домен для полисиаловой кислоты представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Nagae et al., J Biol Chem 288(47):33784-33796 (2013).
В одном варианте осуществления антигенсвязывающий домен для PLAC1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Ghods et al., Biotechnol Appl Biochem 2013 doi:10,1002/bab.1177.
В одном варианте осуществления антигенсвязывающий домен для GloboH представляет собой антигенсвязывающий фрагмент антитела VK9; или антитела, описанного в, например, Kudryashov V et al, Glycoconj J.15(3):243-9 (1998), Lou et al., Proc Natl Acad Sci USA 111(7):2482-2487 (2014); MBr1: Bremer E-G et al. J Biol Chem 259:14773-14777 (1984).
В одном варианте осуществления антигенсвязывающий домен для NY-BR-1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Jager et al., Appl Immunohistochem Mol Morphol 15(1):77-83 (2007).
В одном варианте осуществления антигенсвязывающий домен для белка спермы 17 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Song et al., Target Oncol 2013 Aug 14 (PMID: 23943313); Song et al., Med Oncol 29(4):2923-2931 (2012).
В одном варианте осуществления антигенсвязывающий домен для TRP-2 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Wang et al., J Exp Med. 184(6):2207-16 (1996).
В одном варианте осуществления антигенсвязывающий домен для CYP1B1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Maecker et al, Blood 102 (9): 3287-3294 (2003).
В одном варианте осуществления антигенсвязывающий домен для RAGE-1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела MAB5328 (EMD Millipore).
В одном варианте осуществления антигенсвязывающий домен для обратной транскриптазы теломеразы человека представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела с каталожным №: LS-B95-100 (Lifespan Biosciences).
В одном варианте осуществления антигенсвязывающий домен для кишечной карбоксилэстеразы представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела 4F12 с каталожным №: LS-B6190-50 (Lifespan Biosciences).
В одном варианте осуществления антигенсвязывающий домен для mut hsp70-2 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела от компании Lifespan Biosciences: моноклонального, с каталожным №: LS-C133261-100 (Lifespan Biosciences).
В одном варианте осуществления антигенсвязывающий домен для MAD-CT-2 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в PMID: 2450952; US7635753.
В одном варианте осуществления антигенсвязывающий домен содержит одну, две, три (например, все три) из областей CDR тяжелой цепи, HC CDR1, HC CDR2 и HC CDR3, из антитела, перечисленного выше, и/или одну, две, три (например, все три) из областей CDR легкой цепи, LC CDR1, LC CDR2 и LC CDR3, из антитела, перечисленного выше. В одном варианте осуществления антигенсвязывающий домен содержит вариабельную область тяжелой цепи и/или вариабельную область легкой цепи антитела, перечисленного выше.
В некоторых вариантах осуществления антигенсвязывающий домен CAR нацелен на опухолевый антиген, который представляет собой антиген, экспрессируемый на миелоидной опухоли (либо поверхностный антиген, либо представленный MHC), и клетка, содержащая такой CAR, узнает антиген миелоидной опухоли.
В одном из вариантов осуществления антиген миелоидной опухоли представляет собой антиген, который предпочтительно или специфически экспрессируется на поверхности клетки миелоидной опухоли.
В одном варианте осуществления антигенсвязывающий домен CAR может быть выбран так, чтобы он был нацелен на популяцию клеток миелоидной опухоли. Альтернативно, если желательно нацеливание на миелоидную опухоль более чем одного вида, может быть выбран антигенсвязывающий домен, нацеленный на антиген миелоидной опухоли, экспрессируемый миелоидной опухолью более чем одного, например, всех видов.
CAR может быть нацелен на следующие дополнительные опухолевые антигены: CD123, CD34, Flt3, CD33 и CLL-1. В вариантах осуществления опухолевый антиген выбирают из CD123, CD33 и CLL-1. В некоторых вариантах осуществления опухолевый антиген представляет собой CD123. В некоторых вариантах осуществления опухолевый антиген представляет собой CD33. В некоторых вариантах осуществления опухолевый антиген представляет собой CD34. В некоторых вариантах осуществления опухолевый антиген представляет собой Flt3. В вариантах осуществления опухолевый антиген представляет собой CLL-1. В вариантах осуществления антигенсвязывающий домен нацелен на человеческий антиген.
В одном аспекте антигенсвязывающий домен CAR связывается с CD123, например, CD123 человека. Любой известный CD123-связывающий домен может быть использован по изобретению. В одном варианте осуществления антигенсвязывающий домен для CD123 представляет собой антигенсвязывающий фрагмент, например, области CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в PCT публикации WO2014/130635. В одном варианте осуществления антигенсвязывающий домен для CD123 представляет собой антигенсвязывающий фрагмент, например, области CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в PCT публикации WO2016/028896. В одном варианте осуществления антигенсвязывающий домен для CD123 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в PCT публикации WO1997/024373, WO2008/127735 (например, CD123-связывающий домен из 26292, 32701, 37716 или 32703), WO2014/138805 (например, CD123-связывающий домен из CSL362), WO2014/138819, WO2013/173820, WO2014/144622, WO2001/66139, WO2010/126066 (например, CD123-связывающий домен из любого из Old4, Old5, Old17, Old19, New102 или Old6), WO2014/144622, WO2016/028896 или US2009/0252742. В вариантах осуществления антигенсвязывающий домен представляет собой, или получен из мышиного связывающего домена для CD123 человека. В вариантах осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела, например, домен scFv. В одном из вариантов осуществления антигенсвязывающий домен представляет собой человеческое антитело, или фрагмент антитела, которое связывается с CD123 человека. В вариантах осуществления антигенсвязывающий домен представляет собой домен scFv, который содержит вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH могут быть связаны линкером, описанным в настоящем документе, например, содержащим последовательность GGGGSGGGGSGGGGS (SEQ ID NO: 30), и могут находиться в любой ориентации, например, VL-линкер-VH или VH-линкер-VL.
В некоторых вариантах осуществления антигенсвязывающий домен, который связывается с CD123, представляет собой домен scFv. В некоторых вариантах осуществления антигенсвязывающий домен, который связывается с CD123, представляет собой мышиный домен scFv. В одном из вариантов осуществления антигенсвязывающий домен, который связывается с CD123, представляет собой человеческий или гуманизированный домен scFv. Иллюстративные домены scFv (и их последовательности), которые связываются с CLDN6, приведены в Таблице 19. Последовательности доменов scFv, приведенные в Таблице 19, включают вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH связаны линкером, содержащим последовательность GGGGSGGGGSGGGGSGGGGS (SEQ ID NO: 29), например, в следующей ориентации: VL-линкер-VH. В одном варианте осуществления CD123-связывающий домен содержит аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 751, 756, 761 или 766; или аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) в любой из вышеуказанных последовательностей; или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, выбранной из любой из SEQ ID NOs: 751, 756, 761 или 766.
В одном аспекте антигенсвязывающий домен CAR связывается с CD33, например, CD33 человека. Любой известный CD33-связывающий домен может быть использован по изобретению. В одном варианте осуществления антигенсвязывающий домен для CD33 представляет собой антигенсвязывающий фрагмент, например, области CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в PCT публикации WO2016/014576 или патентной публикации США 2016-0096892-A1, полное содержание которых включено в настоящий документ посредством ссылки. В одном варианте осуществления антигенсвязывающий домен для CD33 представляет собой антигенсвязывающий фрагмент из, или полученный из, гемтузумаб-озагомицина (например, содержащий антигенсвязывающий домен, содержащий одну или более, например, одну, две или три, области CDR из вариабельного домена тяжелой цепи и/или одну или более, например, одну, две или три, области CDR из вариабельного домена легкой цепи, либо последовательность VH или VL, или scFv из последовательности scFv гемтузумаб-озагомицина) (ранее продаваемого под названием милотарг), например, Bross et al., Clin Cancer Res 7(6):1490-1496 (2001) (гемтузумаб-озагомицин, hP67.6). В одном варианте осуществления антигенсвязывающий домен для CD33 представляет собой антигенсвязывающий фрагмент из, или полученный из (например, содержащий антигенсвязывающий домен, содержащий одну или более, например, одну, две или три, области CDR из вариабельного домена тяжелой цепи и/или одну или более, например, одну, две или три, области CDR из вариабельного домена легкой цепи, либо последовательность VH или VL, или scFv) последовательности scFv, имеющей GenBank регистрационный № AM402974.1 (смотри, Wang et al., Mol. Ther., vol. 23:1, pp. 184-191 (2015), содержание документа включено посредством ссылки). В одном варианте осуществления антигенсвязывающий домен для CD33 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Caron et al., Cancer Res 52(24):6761-6767 (1992) (линтузумаб, HuM195), Lapusan et al., Invest New Drugs 30(3):1121-1131 (2012) (AVE9633), Aigner et al., Leukemia 27(5):1107-1115 (2013) (AMG330, CD33 BiTE), Dutour et al., Adv hematol 2012:683065 (2012) и Pizzitola et al., Leukemia doi:10,1038/Lue.2014,62 (2014). В вариантах осуществления антигенсвязывающий домен представляет собой, или получен из мышиного связывающего домена для CD33 человека. В вариантах осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела, например, домен scFv. В одном из вариантов осуществления антигенсвязывающий домен представляет собой человеческое антитело, или фрагмент антитела, которое связывается с CD33 человека. В вариантах осуществления антигенсвязывающий домен представляет собой домен scFv, который содержит вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH могут быть связаны линкером, описанным в настоящем документе, например, содержащим последовательность GGGGSGGGGSGGGGS (SEQ ID NO: 30), и могут находиться в любой ориентации, например, VL-линкер-VH или VH-линкер-VL.
В одном аспекте антигенсвязывающий домен CAR связывается с CLL-1, например, CLL-1 человека. Любой известный CLL-1-связывающий домен может быть использован по изобретению. В одном варианте осуществления антигенсвязывающий домен для CLL-1 представляет собой антигенсвязывающий фрагмент, например, области CDR или VH и VL, антитела, антигенсвязывающего фрагмента или CAR, описанных, например, в PCT публикации WO2016/014535 или патентной публикации США 2016-0051651-A1, полное содержание которых включено в настоящий документ посредством ссылки. В одном варианте осуществления антигенсвязывающий домен для CLL-1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, доступного от R&D, ebiosciences, Abcam, например, PE-CLL1-hu с каталожным № 353604 (BioLegend); и PE-CLL1 (CLEC12A) с каталожным № 562566 (BD). В вариантах осуществления антигенсвязывающий домен представляет собой, или получен из мышиного связывающего домена для CLL-1 человека. В вариантах осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела, например, домен scFv. В одном из вариантов осуществления антигенсвязывающий домен представляет собой человеческое антитело, или фрагмент антитела, которое связывается с CLL-1 человека. В вариантах осуществления антигенсвязывающий домен представляет собой домен scFv, который содержит вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH могут быть связаны линкером, описанным в настоящем документе, например, содержащим последовательность GGGGSGGGGSGGGGS (SEQ ID NO: 30), и могут находиться в любой ориентации, например, VL-линкер-VH или VH-линкер-VL.
В некоторых вариантах осуществления антигенсвязывающий домен CAR нацелен на B-клеточный антиген. В одном из вариантов осуществления B-клеточный антиген представляет собой антиген, который предпочтительно или специфически экспрессируется на поверхности B-клетки. Антиген может экспрессироваться на поверхности B-клеток любого из следующих типов: предшественники B-клеток (например, пре-B-клетки или про-B-клетки), ранние про-B-клетки, поздние про-B-клетки, крупные пре-B-клетки, мелкие пре-B-клетки, незрелые B-клетки, например, «необученные» B-клетки, зрелые B-клетки, плазматические B-клетки, плазмобласты, B-клетки памяти, B-1 клетки, B-2 клетки, B-клетки маргинальной зоны, фолликулярные B-клетки, B-клетки зародышевого центра или регуляторные B-клетки (Breg).
Настоящее изобретение относится к CAR, которые могут быть нацелены на следующие B-клеточные антигены: CD19; CD123; CD22; CD30; CD171; CS-1; подобную лектину C-типа молекулу 1, CD33; рецептор варианта III эпидермального фактора роста (EGFRvIII); ганглиозид G2 (GD2); ганглиозид GD3; представитель семейства TNF-рецепторов, антиген созревания B-клеток (BCMA); Tn-антиген ((Tn Ag) или (GalNAcα-Ser/Thr)); простатический специфический мембранный антиген (PSMA); подобный рецепторной тирозинкиназе рецептор-сироту 1 (ROR1); Fms-подобную тирозинкиназу 3 (FLT3); опухоль-ассоциированный гликопротеин 72 (TAG72); CD38; CD44v6; канцероэмбриональный антиген (CEA); молекулу адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицу альфа-2 рецептора интерлейкина-13; мезотелин; субъединицу альфа рецептора интерлейкина-11 (IL-11Ra); антиген простатических стволовых клеток (PSCA); сериновую протеазу 21; рецептор 2 фактора роста эндотелия сосудов (VEGFR2); Lewis(Y) антиген; CD24; рецептор бета фактора роста тромбоцитов (PDGFR-бета); стадиеспецифический эмбриональный антиген-4 (SSEA-4); CD20; фолатный рецептор альфа; рецепторную тирозин-специфическую протеинкиназу ERBB2 (Her2/neu); муцин 1, связанный с клеточной поверхностью (MUC1); рецептор эпидермального фактора роста (EGFR); молекулу адгезии нейронов (NCAM); простазу; простатическую кислую фосфатазу (PAP); мутантный фактор элонгации 2 (ELF2M); эфрин B2; белок альфа активации фибробластов (FAP); рецептор инсулиноподобного фактора роста 1 (рецептор IGF-I), карбоангидразу IX (CAIX); субъединицу протеасомы (просома, макропаин), типа бета, 9 (LMP2); гликопротеин 100 (gp100); онкогенный слитый белок, включающий область локализации сайта инициации реаранжировки (BCR) и гомолог 1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназу; рецептор эфрина A2 (EphA2); фукозил GM1; молекулу адгезии сиалил-Льюис (sLe); ганглиозид GM3; трансглутаминазу 5 (TGS5); высокомолекулярный меланома-ассоциированный антиген (HMWMAA); o-ацетил-GD2 ганглиозид (OAcGD2); фолатный рецептор бета; опухолевый эндотелиальный маркер 1 (TEM1/CD248); антиген, родственный опухолевому эндотелиальному маркеру 7 (TEM7R); клаудин-6 (CLDN6); рецептор тиреостимулирующего гормона (TSHR); связанных с G-белками рецепторов класса C, группы 5, представитель D (GPRC5D); открытую рамку считывания 61 хромосомы X (CXORF61); CD97; CD179a; киназу анапластической лимфомы (ALK); полисиаловую кислоту; плацента-специфический белок 1 (PLAC1); гексасахаридную часть гликоцерамида globoH (GloboH); дифференцировочный антиген молочной железы (NY-BR-1); уроплакин 2 (UPK2); клеточный рецептор 1 вируса гепатита A (HAVCR1); адренорецептор бета-3 (ADRB3); паннексин 3 (PANX3); связанный с G-белками рецептор 20 (GPR20); комплекс лимфоцитарного антигена 6, локуса K9 (LY6K); ольфакторный рецептор 51E2 (OR51E2); белок TCR-гамма с альтернативной рамкой считывания (TARP); белок опухоли Вильмса (WT1); антиген 1 рака яичка (NY-ESO-1); антиген 2 рака яичка (LAGE-1a); меланома-ассоциированный антиген 1 (MAGE-A1); транслокационный вариант 6 гена ETS, расположенный на хромосоме 12p (ETV6-AML); белок спермы 17 (SPA17); семейства X антигенов, представитель 1A (XAGE1); ангиопоэтин-связывающий клеточный поверхностный рецептор 2 (Tie 2); антиген 1 меланомы яичка (MAD-CT-1); антиген 2 меланомы яичка (MAD-CT-2); Fos-родственный антиген 1; опухолевый белок p53 (p53); мутант p53; простеин; сурвивин; теломеразу; опухолевый антиген 1 карциномы предстательной железы, узнаваемый T-клетками антиген меланомы 1; мутант белка вируса крысиной саркомы (Ras); обратную транскриптазу теломеразу человека (hTERT); точки разрыва при транслокации в случае саркомы; ингибитор апоптоза из клеток меланомы (ML-IAP); ERG (слитый ген трансмембранной сериновой протеазы 2 (TMPRSS2) и ETS); N-ацетилглюкозамин трансферазу V (NA17); белок парного бокса Pax-3 (PAX3); рецептор андрогена; циклин B1; полученный из нейробластомы гомолог онкогена v-myc вируса птичьего миелоцитоматоза (MYCN); представитель C семейства гомологов Ras (RhoC); родственный тирозиназе белок 2 (TRP-2); цитохром P450 1B1 (CYP1B1); белок, подобный CCCTC-связывающему фактору (белку «цинковый палец»), узнаваемый T-клетками антиген плоскоклеточной карциномы 3 (SART3); белок парного бокса Pax-5 (PAX5); проакрозин-связывающий белок sp32 (OY-TES1); лимфоцит-специфическую протеинтирозинкиназу (LCK); якорный белок 4 A-киназы (AKAP-4); точку разрыва 2 в X при синовиальной саркоме (SSX2); рецептор для конечных продуктов усиленного гликозилирования (RAGE-1); почечный убиквитарный белок 1 (RU1); почечный убиквитарный белок 2 (RU2); легумаин; белок E6 вируса папилломы человека (HPV E6); белок E7 вируса папилломы человека (HPV E7); кишечную карбоксилэстеразу; мутантный белок теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; связанный с лейкоцитами иммуноглобулиноподобный рецептор 1 (LAIR1); Fc-фрагмент рецептора IgA (FCAR или CD89); иммуноглобулиноподобных рецепторов лейкоцитов, подсемейства A, представитель 2 (LILRA2); семейства белков, подобных молекуле CD300, представитель f (CD300LF); семейства 12 доменных лектинов C-типа, представитель A (CLEC12A); антиген 2 стромальных клеток костного мозга (BST2); белок 2, подобный EGF-подобный домен-содержащему муциноподобному гормональному рецептору (EMR2); лимфоцитарный антиген 75 (LY75); глипикан-3 (GPC3); Fc-рецептор-подобный белок 5 (FCRL5); подобный цепи лямбда иммуноглобулина полипептид 1 (IGLL1); представитель семейства TNF-рецепторов; Fms-подобную тирозинкиназу 3 (FL T3); CD10, CD19, CD20, CD21, CD22, CD23, CD24, CD25, CD37, CD38, CD53, CD72, CD73, CD74, CD75, CD77, CD79a, CD79b, CD80, CD81, CD82, CD83, CD84, CD85, ROR1, BCMA, CD86, и CD179b. Другие B-клеточные антигены, на которые могут быть нацелены CAR, описанные в настоящем документе, включают: CD1a, CD1b, CD1c, CD1d, CD2, CD5, CD6, CD9, CD11a, CD11b, CD11c, CD17, CD18, CD26, CD27, CD29, CD30, CD31, CD32a, CD32b, CD35, CD38, CD39, CD40, CD44, CD45, CD45RA, CD45RB, CD45RC, CD45RO, CD46, CD47, CD48, CD49b, CD49c, CD49d, CD50, CD52, CD54, CD55, CD58, CD60a, CD62L, CD63, CD63, CD68 CD69, CD70, CD85E, CD85I, CD85J, CD92, CD95, CD97, CD98, CD99, CD100, CD102, CD108, CD119, CD120a, CD120b, CD121b, CD122, CD124, CD125, CD126, CD130, CD132, CD137, CD138, CD139, CD147, CD148, CD150, CD152, CD162, CD164, CD166, CD167a, CD170, CD175, CD175s, CD180, CD184, CD185, CD192, CD196, CD197, CD200, CD205, CD210a, CDw210b, CD212, CD213a1, CD213a2, CD215, CD217, CD218a, CD218b, CD220, CD221, CD224, CD225, CD226, CD227, CD229, CD230, CD232, CD252, CD253, CD257, CD258, CD261, CD262, CD263, CD264, CD267, CD268, CD269, CD270, CD272, CD274, CD275, CD277, CD279, CD283, CD289, CD290, CD295, CD298, CD300a, CD300c, CD305, CD306, CD307a, CD307b, CD307c, CD307d, CD307e, CD314, CD315, CD316, CD317, CD319, CD321, CD327, CD328, CD329, CD338, CD351, CD352, CD353, CD354, CD355, CD357, CD358, CD360, CD361, CD362 и CD363.
В другом варианте осуществления антиген, на который нацелен CAR, выбирают из CD19, BCMA, CD20, CD22, FcRn5, FcRn2, CS-1 и CD138. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой CD19. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой CD20. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой CD22. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой BCMA. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой FcRn5. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой FcRn2. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой CS-1. В одном из вариантов осуществления антиген, на который нацелен CAR, представляет собой CD138.
В одном варианте осуществления антигенсвязывающий домен CAR, например, CAR, экспрессируемого клеткой по изобретению (например, клеткой, которая также экспрессирует CAR), может быть выбран так, чтобы он был нацелен на предпочтительную популяцию B-клеток. Например, в одном из вариантов осуществления, в котором желательно нацеливание на регуляторные B-клетки, выбирают антигенсвязывающий домен, который нацелен на B-клеточный антиген, экспрессируемый на регуляторных B-клетках, но не B-клетках других популяций, например, плазматических B-клетках и B-клетках памяти. Клеточные поверхностные маркеры, экспрессируемые на регуляторных B-клетках, включают: CD19, CD24, CD25, CD38 или CD86, или маркеры, описанные в He et al., 2014, J Immunology Research, статья с ID 215471. Если желательно нацеливание на B-клетки более, чем одного вида, можно выбирать антигенсвязывающий домен, нацеленный на B-клеточный антиген, который экспрессируется всеми из желательных B-клеток-мишеней.
В одном из вариантов осуществления антигенсвязывающий домен CAR, например, CAR, экспрессируемого клеткой по изобретению, связывается с CD19. CD19 присутствует на B-клетках на всем протяжении дифференциации клеток данной линии дифференцировки от стадии про/пре-B-клетки до стадии окончательно дифференцированной плазматической клетки. В одном из вариантов осуществления антигенсвязывающий домен представляет собой мышиный домен scFv, который связывается с CD19 человека, например, CTL019 (например, SEQ ID NO: 356). В одном из вариантов осуществления антигенсвязывающий домен представляет собой гуманизированное антитело или фрагмент антитела, например, домен scFv, полученный из мышиного CTL019 scFv. В одном из вариантов осуществления антигенсвязывающий домен представляет собой человеческое антитело, или фрагмент антитела, которое связывается с CD19 человека. Иллюстративные домены scFv (и их последовательности, например, последовательности областей CDR, VL и VH), которые связываются с CD19, приведены в Таблице 7 и Таблице 15A. Последовательности доменов scFv, приведенные в Таблице 7, включают вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH связаны линкером, содержащим последовательность GGGGSGGGGSGGGGS (SEQ ID NO: 30), например, в следующей ориентации: VL-линкер-VH.
Таблица 7. Антигенсвязывающие домены, которые связывают CD19
Последовательности областей CDR доменов scFv антигенсвязывающих доменов для CD19, приведенных в Таблице 7, приведены в Таблицах 8 и 15B для вариабельных доменов тяжелой цепи и в Таблицах 9 и 15C для вариабельных доменов легкой цепи. «ID» означает соответствующую SEQ ID NO для каждой CDR.
Таблица 8. Области CDR вариабельных доменов тяжелой цепи
Таблица 9. Области CDR вариабельных доменов легкой цепи
В одном из вариантов осуществления антигенсвязывающий домен содержит анти-CD19 антитело или его фрагмент, например, scFv. Например, антигенсвязывающий домен содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, приведенные в Таблице 10. Последовательность линкера, соединяющая вариабельный домен тяжелой и вариабельный домен легкой цепей, может представлять собой любую из последовательностей линкера, описанных в настоящем документе, или, альтернативно, может представлять собой GSTSGSGKPGSGEGSTKG (SEQ ID NO: 378). Вариабельная область легкой цепи и вариабельная область тяжелой цепи в scFv могут находиться, например, в любой из следующих ориентаций: вариабельная область легкой цепи-линкер-вариабельная область тяжелой цепи или вариабельная область тяжелой цепи-линкер-вариабельная область легкой цепи.
Таблица 10. Дополнительные связывающие домены анти-CD19 антитела
scFv
В одном варианте осуществления CD19-связывающий домен содержит одну или более (например, все три) из определяющей комплементарность области 1 легкой цепи (LC CDR1), определяющей комплементарность области 2 легкой цепи (LC CDR2) и определяющей комплементарность области 3 легкой цепи (LC CDR3) CD19-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 7 или 9, и/или одну или более (например, все три) из определяющей комплементарность области 1 тяжелой цепи (HC CDR1), определяющей комплементарность области 2 тяжелой цепи (HC CDR2) и определяющей комплементарность области 3 тяжелой цепи (HC CDR3) CD19-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 7 или 8. В одном варианте осуществления CD19-связывающий домен содержит одну, две или все из LC CDR1, LC CDR2 и LC CDR3 с любыми аминокислотными последовательностями, приведенными в Таблице 9, содержание которой включено в настоящий документ посредством ссылки; и одну, две или все из HC CDR1, HC CDR2 и HC CDR3 с любыми аминокислотными последовательностями, приведенными в Таблице 8.
В одном варианте осуществления CD19-связывающий домен содержит вариабельную область легкой цепи, описанную в настоящем документе (например, в Таблице 7 или 10) и/или вариабельную область тяжелой цепи, описанную в настоящем документе (например, в Таблице 7 или 10). В одном варианте осуществления CD19-связывающий домен представляет собой scFv, содержащий легкую цепь и тяжелую цепь с аминокислотными последовательностями, приведенными Таблице 7 или 10. В одном из вариантов осуществления CD19-связывающий домен (например, scFv) содержит: вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области легкой цепи, приведенной в Таблице 7 или 10, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 7 или 10; и/или вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области тяжелой цепи, приведенной в Таблице 7 или 10, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 7 или 10.
В одном варианте осуществления CD19-связывающий домен содержит аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 356-368 и 381; или аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) в любой из вышеуказанных последовательностей; или последовательность, имеющую 95-99% идентичности с любой из вышеуказанных последовательностей. В одном варианте осуществления CD19-связывающий домен представляет собой scFv, и вариабельная область легкой цепи, содержащая аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 7 или 10, связана с вариабельной областью тяжелой цепи, содержащей аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 7 или 10, через линкер, например, линкер, описанный в настоящем документе. В одном варианте осуществления CD19-связывающий домен включает (Gly4-Ser)n линкер, где n равно 1, 2, 3, 4, 5 или 6, предпочтительно 4 (SEQ ID NO: 967). Вариабельная область легкой цепи и вариабельная область тяжелой цепи в scFv могут находиться, например, в любой из следующих ориентаций: вариабельная область легкой цепи-линкер-вариабельная область тяжелой цепи или вариабельная область тяжелой цепи-линкер-вариабельная область легкой цепи.
Любой известный CAR, например, антигенсвязывающий домен для CD19 любого известного в данной области CD19 CAR, может быть использован по настоящему изобретению для конструирования CAR. Например, LG-740; CAR, описанный в патенте США № 8399645; патенте США № 7446190; Xu et al., Leuk Lymphoma. 2013 54(2):255-260(2012); Cruz et al., Blood 122(17):2965-2973 (2013); Brentjens et al., Blood, 118(18):4817-4828 (2011); Kochenderfer et al., Blood 116(20):4099-102 (2010); Kochenderfer et al., Blood 122 (25):4129-39(2013); и 16th Annu Meet Am Soc Gen Cell Ther (ASGCT) (May 15-18, Salt Lake City) 2013, Abst 10. В одном варианте осуществления антигенсвязывающий домен для CD19 представляет собой антигенсвязывающий фрагмент, например, области CDR, CAR, антитела или его антигенсвязывающего фрагмента, описанных, например, в PCT публикации WO2012/079000; PCT публикации WO2014/153270; Kochenderfer, J.N. et al., J. Immunother. 32 (7), 689-702 (2009); Kochenderfer, J.N., et al., Blood, 116 (20), 4099-4102 (2010); PCT публикации WO2014/031687; Bejcek, Cancer Research, 55, 2346-2351, 1995; или патенте США № 7446190.
В одном из вариантов осуществления антигенсвязывающий домен CAR, например, CAR, экспрессируемого клеткой по изобретению, связывается с BCMA. BCMA преимущественно экспрессируется на зрелых B-лимфоцитах. В одном из вариантов осуществления антигенсвязывающий домен представляет собой мышиный домен scFv, который связывается с BCMA человека. В одном из вариантов осуществления антигенсвязывающий домен представляет собой гуманизированное антитело, или фрагмент антитела, например, домен scFv, которое связывается с BCMA человека. В одном из вариантов осуществления антигенсвязывающий домен представляет собой человеческое антитело, или фрагмент антитела, которое связывается с BCMA человека. Иллюстративные домены scFv (и их последовательности, например, последовательности областей CDR, VL и VH), которые связываются с BCMA, приведены в Таблице 11, Таблице 12, Таблице 13 и Таблице 14. Последовательности доменов scFv, приведенные в Таблице 11 и Таблице 12, включают вариабельную область легкой цепи (VL) и вариабельную область тяжелой цепи (VH). VL и VH связаны линкером, например, в следующей ориентации: VH-линкер-VL.
Таблица 11. Антигенсвязывающие домены, которые связывают BCMA
Также приведены аминокислотные последовательности вариабельного домена тяжелой цепи и вариабельного домена легкой цепи для каждого scFv.
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
Домен scFv
Домен scFv
VH
VL
В некоторых вариантах осуществления дополнительные иллюстративные конструкты CAR получают с использованием последовательностей VH и VL из PCT публикации WO2012/0163805 (содержание которой включено в настоящий документ посредством ссылки в полном объеме). В некоторых вариантах осуществления дополнительные иллюстративные конструкты CAR получают с использованием последовательностей VH и VL из PCT публикации WO2016/014565 (содержание которой включено в настоящий документ посредством ссылки в полном объеме). В некоторых вариантах осуществления дополнительные иллюстративные конструкты CAR получают с использованием последовательностей VH и VL из PCT публикации WO2014/122144 (содержание которой включено в настоящий документ посредством ссылки в полном объеме). В некоторых вариантах осуществления дополнительные иллюстративные конструкты CAR получают с использованием последовательностей молекул CAR и/или VH и VL из PCT публикации WO2016/014789 (содержание которой включено в настоящий документ посредством ссылки в полном объеме). В некоторых вариантах осуществления дополнительные иллюстративные конструкты CAR получают с использованием последовательностей молекул CAR и/или VH и VL из PCT публикации WO2014/089335 (содержание которой включено в настоящий документ посредством ссылки в полном объеме). В некоторых вариантах осуществления дополнительные иллюстративные конструкты CAR получают с использованием последовательностей молекул CAR и/или VH и VL из PCT публикации WO2014/140248 (содержание которой включено в настоящий документ посредством ссылки в полном объеме).
В некоторых вариантах осуществления дополнительные иллюстративные конструкты CAR также могут быть получены с использованием последовательностей VH и VL, приведенных в Таблице 12. Аминокислотные последовательности иллюстративных доменов scFv, содержащих домены VH и VL, а также последовательности линкера и полноразмерных CAR также приведены в Таблице 12.
Таблица 12. Дополнительные иллюстративные последовательности связывающего домена для BCMA
VH
VL
домен scFv
VH
VL
домен scFv
VH
VL
домен scFv
VH
VL
домен scFv
Последовательности человеческих областей CDR доменов scFv приведены в Таблице 13 для вариабельных доменов тяжелой цепи и в Таблице 14 для вариабельных доменов легкой цепи. «ID» означает соответствующую SEQ ID NO для каждой CDR. Области CDR приведены в соответствии с системой Kabat, однако CDR, соответствующие другой системе нумерации, например, Chothia или комбинированной системе Kabat/Chothia, могут быть с легкостью выведены из последовательностей VH и VL, приведенных выше.
Таблица 13. Области CDR вариабельного домена тяжелой цепи в соответствии с системой нумерации Kabat (Kabat et al. (1991), «Sequences of Proteins of Immunological Interest», 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD)
Таблица 14. Области CDR вариабельного домена легкой цепи в соответствии с системой нумерации Kabat (Kabat et al. (1991), «Sequences of Proteins of Immunological Interest», 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD)
В одном варианте осуществления BCMA-связывающий домен содержит одну или более (например, все три) из определяющей комплементарность области 1 легкой цепи (LC CDR1), определяющей комплементарность области 2 легкой цепи (LC CDR2) и определяющей комплементарность области 3 легкой цепи (LC CDR3) BCMA-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 11, 12 или 14, и/или одну или более (например, все три) из определяющей комплементарность области 1 тяжелой цепи (HC CDR1), определяющей комплементарность области 2 тяжелой цепи (HC CDR2) и определяющей комплементарность области 3 тяжелой цепи (HC CDR3) BCMA-связывающего домена, описанного в настоящем документе, например, приведенные в Таблице 11, 12 или 13. В одном варианте осуществления BCMA-связывающий домен содержит одну, две или все из LC CDR1, LC CDR2 и LC CDR3 с любыми аминокислотными последовательностями, приведенными в Таблице 11, содержание которой включено в настоящий документ посредством ссылки; и одну, две или все из HC CDR1, HC CDR2 и HC CDR3 с любыми аминокислотными последовательностями, приведенными в Таблице 11.
В одном варианте осуществления BCMA-связывающий домен содержит вариабельную область легкой цепи, описанную в настоящем документе (например, в Таблице 11 или 12) и/или вариабельную область тяжелой цепи, описанную в настоящем документе (например, в Таблице 11 или 12). В одном варианте осуществления BCMA-связывающий домен представляет собой scFv, содержащий легкую цепь и тяжелую цепь с аминокислотными последовательностями, приведенными Таблице 11 или 12. В одном из вариантов осуществления BCMA-связывающий домен (например, scFv) содержит: вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области легкой цепи, приведенной в Таблице 11 или 12, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 11 или 12; и/или вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области тяжелой цепи, приведенной в Таблице 11 или 12, или последовательность, имеющую 95-99% идентичности с аминокислотной последовательностью, приведенной в Таблице 11 или 12.
В одном варианте осуществления BCMA-связывающий домен содержит аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 382, 386, 390, 394, 398, 402, 406, 410, 414, 418, 422, 426, 430, 434, 438, 442, 446, 450, 454, 458, 462, 466, 470, 474, 478, 482, 486, 490, 494, 498, 502, 506, 510, 514, 518, 522, 528, 531, 534 или 537; или аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) в любой из вышеуказанных последовательностей; или последовательность, имеющую 95-99% идентичности с любой из вышеуказанных последовательностей. В одном варианте осуществления BCMA-связывающий домен представляет собой scFv, и вариабельная область легкой цепи, содержащая аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 11 или 12, связана с вариабельной областью тяжелой цепи, содержащей аминокислотную последовательность, описанную в настоящем документе, например, в Таблице 11 или 12, через линкер, например, линкер, описанный в настоящем документе. В одном варианте осуществления BCMA-связывающий домен включает (Gly4-Ser)n линкер, где n равно 1, 2, 3, 4, 5 или 6, предпочтительно 4 (SEQ ID NO: 967). Вариабельная область легкой цепи и вариабельная область тяжелой цепи в scFv могут находиться, например, в любой из следующих ориентаций: вариабельная область легкой цепи-линкер-вариабельная область тяжелой цепи или вариабельная область тяжелой цепи-линкер-вариабельная область легкой цепи.
Любой известный CAR, например, антигенсвязывающий домен для BMCА любого известного в данной области CAR, может быть использован по настоящему изобретению для конструирования CAR. Например, те, которые описаны в настоящем документе.
В одном варианте осуществления антигенсвязывающий домен для ROR1 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Hudecek et al., Clin Cancer Res 19(12):3153-3164 (2013); WO2011159847 и US20130101607.
В одном варианте осуществления антигенсвязывающий домен для CD22 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела, описанного, например, в Haso et al., Blood, 121(7): 1165-1174 (2013); Wayne et al., Clin Cancer Res 16(6): 1894-1903 (2010); Kato et al., Leuk Res 37(1):83-88 (2013); Creative BioMart (creativebiomart.net): MOM-18047-S(P).
В одном варианте осуществления антигенсвязывающий домен для CD20 представляет собой антигенсвязывающий фрагмент, например, области CDR, антитела ритуксимаба, офатумумаба, окрелизумаба, велтузумаба или GA101, или их производных. В одном варианте осуществления антигенсвязывающий домен для CD20 представляет собой антигенсвязывающий фрагмент, описанный в WO2016/164731, содержание документа включено в настоящий документ посредством ссылки в полном объеме.
В одном варианте осуществления антигенсвязывающий домен содержит одну, две, три (например, все три) из областей CDR тяжелой цепи, HC CDR1, HC CDR2 и HC CDR3, из антитела, перечисленного выше, и/или одну, две, три (например, все три) из областей CDR легкой цепи, LC CDR1, LC CDR2 и LC CDR3, из антитела, связывающего опухолевый антиген, перечисленного выше. В одном варианте осуществления антигенсвязывающий домен содержит вариабельную область тяжелой цепи и/или вариабельную область легкой цепи антитела, связывающего опухолевый антиген, перечисленного выше.
В одном варианте осуществления антигенсвязывающий домен CAR, описанного в настоящем документе, представляет собой фрагмент scFv антитела. В одном аспекте такой фрагмент антитела является функциональным в том, что он сохраняет эквивалентную аффинность связывания, например, он связывает тот же антиген с сопоставимой эффективностью, что и IgG антитело, из которого он получен. В других вариантах осуществления фрагмент антитела имеет более низкую аффинность связывания, например, он связывает тот же антиген с более низкой аффинностью связывания, чем антитело, из которого он получен, но является функциональным в том, что обеспечивает биологический ответ, описанный в настоящем документе. В одном варианте осуществления молекула CAR содержит фрагмент антитела, который имеет аффинность связывания KD от 10-4 M до 10-8 M, например, от 10-5 M до 10-7 M, например, 10-6 M или 10-7 M, для антигена-мишени. В одном варианте осуществления фрагмент антитела имеет аффинность связывания, которая по меньшей мере в пять раз, 10 раз, 20 раз, 30 раз, 50 раз, 100 раз или 1000 раз меньше, чем у эталонного антитела, например, антитела, описанного в настоящем документе.
В одном варианте осуществления антигенсвязывающий домен содержит не принадлежащее человеку антитело или фрагмент антитела, например, мышиное антитело или фрагмент антитела.
В другом варианте осуществления антигенсвязывающий домен содержит гуманизированное антитело или фрагмент антитела. В некоторых аспектах не принадлежащее человеку антитело является гуманизированным, при этом специфические последовательности или области антитела модифицированы для большего сходства с антителом, естественно продуцируемым в организме человека, или его фрагментом. В одном аспекте антигенсвязывающий домен является гуманизированным, в сравнении с последовательностью мышиного антитела или фрагмента антитела, например, scFv, из которого он получен.
Гуманизированное антитело может быть получено различными методами, известными в данной области, включая, но без ограничения, пересадку CDR (смотри, например, Европейский патент № EP 239400; международную патентную публикацию № WO91/09967 и патенты США №№ 5225539, 5530101 и 5585089, содержание каждого из документов включено в настоящий документ посредством ссылки в полном объеме), венирование или изменение поверхности (смотри, например, Европейские патенты №№ EP 592106 и EP 519596; Padlan, 1991, Molecular Immunology, 28(4/5):489-498; Studnicka et al., 1994, Protein Engineering, 7(6):805-814; и Roguska et al., 1994, PNAS, 91:969-973, содержание каждого из документов включено в настоящий документ посредством ссылки в полном объеме), перетасовку цепей (смотри, например, патент США № 5565332, содержание которого включено в настоящий документ посредством ссылки в полном объеме), а также методы, раскрытые, например, в публикации патентной заявки США № US2005/0042664, публикации патентной заявки США № US2005/0048617, патенте США № 6407213, патенте США № 5766886, международной патентной публикации № WO9317105, Tan et al., J. Immunol., 169:1119-25 (2002), Caldas et al., Protein Eng., 13(5):353-60 (2000), Morea et al., Methods, 20(3):267-79 (2000), Baca et al., J. Biol. Chem., 272(16):10678-84 (1997), Roguska et al., Protein Eng., 9(10):895-904 (1996), Couto et al., Cancer Res., 55 (23 Supp):5973s-5977s (1995), Couto et al., Cancer Res., 55(8):1717-22 (1995), Sandhu JS, Gene, 150(2):409-10 (1994) и Pedersen et al., J. Mol. Biol., 235(3):959-73 (1994), содержание каждого из документов включено в настоящий документ посредством ссылки в полном объеме. Часто каркасные остатки в каркасных областях заменяют соответствующими остатками из антитела - донора CDR для изменения, например, улучшения, связывания антигена. Такие подлежащие замене остатки в каркасе определяют способами, хорошо известными в данной области, например, путем моделирования взаимодействий CDR и каркасных остатков для идентификации каркасных остатков, важных для связывания антигена, и сравнения последовательностей для идентификации необычных каркасных остатков в конкретных положениях. (Смотри, например, Queen et al., патент США № 5585089; и Riechmann et al., 1988, Nature, 332:323, содержание указанных документов включено в настоящий документ посредством ссылки в полном объеме).
Гуманизированное антитело или фрагмент антитела имеет сохраненные в нем один или более аминокислотных остатков из источника, который не является человеком. Такие не принадлежащие человеку аминокислотные остатки часто называют «импортированными» остатками, которые, как правило, получают из «импортированного» вариабельного домена. Как описано в настоящем документе, гуманизированные антитела или фрагменты антител содержат одну или более областей CDR из не принадлежащих человеку молекул иммуноглобулинов и каркасные области, в которых аминокислотные остатки, составляющие каркас, получены полностью, или в основном, из последовательностей зародышевой линии человека. Различные методы гуманизации антител или фрагментов антител хорошо известны в данной области и, в основном, ее можно осуществлять методом, описанным Winter с соавторами (Jones et al., Nature, 321:522-525 (1986); Riechmann et al., Nature, 332:323-327 (1988); Verhoeyen et al., Science, 239:1534-1536 (1988)), путем замены областями CDR или последовательностями CDR грызунов соответствующих последовательностей человеческого антитела, то есть, путем пересадки CDR (EP 239400; PCT публикация № WO91/09967 и патенты США №№ 4816567; 6331415; 5225539; 5530101; 5585089; 6548640, содержание указанных документов включено в настоящий документ посредством ссылки в полном объеме). В таких гуманизированных антителах и фрагментах антител существенно меньше, чем целый, вариабельный домен антитела человека заменен соответствующей последовательностью из биологического вида, отличного от человека. Гуманизированные антитела часто представляют собой человеческие антитела, в которых некоторые остатки CDR и, возможно, некоторые каркасные (FR) остатки заменены остатками из аналогичных участков в антителах грызунов. Гуманизацию антител и фрагментов антител также можно осуществлять путем венирования или изменения поверхности (EP 592106; EP 519596; Padlan, 1991, Molecular Immunology, 28(4/5):489-498; Studnicka et al., Protein Engineering, 7(6):805-814 (1994); и Roguska et al., PNAS, 91:969-973 (1994)), или перетасовки цепей (патент США № 5565332), содержание указанных документов включено в настоящий документ посредством ссылки в полном объеме.
Выбор человеческих вариабельных доменов, как легкой, так и тяжелой, цепи, используемых для получения гуманизированных антител, направлен на уменьшение антигенности. В так называемом способе «наилучшего соответствия» проводят скрининг последовательности вариабельного домена антитела грызуна против полной библиотеки известных последовательностей человеческих вариабельных доменов. Человеческую последовательность, которая наиболее близка к последовательности грызуна, затем выбирают в качестве человеческой каркасной (FR) последовательности для гуманизированного антитела (Sims et al., J. Immunol., 151:2296 (1993); Chothia et al., J. Mol. Biol., 196:901 (1987), содержание указанных документов включено в настоящий документ посредством ссылки в полном объеме). В другом способе используют конкретную каркасную последовательность, полученную из консенсусной последовательности всех человеческих антител с конкретной подгруппой легких или тяжелых цепей. Один и тот же каркас может быть использован для нескольких разных гуманизированных антител (смотри, например, Nicholson et al. Mol. Immun. 34 (16-17): 1157-1165 (1997); Carter et al., Proc. Natl. Acad. Sci. USA, 89:4285 (1992); Presta et al., J. Immunol., 151:2623 (1993), содержание указанных документов включено в настоящий документ посредством ссылки в полном объеме). В некоторых вариантах осуществления каркасная область, например, все четыре каркасные области, вариабельной области тяжелой цепи получены из последовательности зародышевой линии VH4_4-59. В одном варианте осуществления каркасная область может иметь одну, две, три, четыре или пять модификаций, например, замен, например, на аминокислоту из соответствующей мышиной последовательности. В одном варианте осуществления каркасная область, например, все четыре каркасные области вариабельной области легкой цепи получены из последовательности зародышевой линии VK3_1.25. В одном варианте осуществления каркасная область может иметь одну, две, три, четыре или пять модификаций, например, замен, например, на аминокислоту из соответствующей мышиной последовательности.
В некоторых аспектах фрагмент антитела CAR является гуманизированным, с сохранением высокой аффинности для антигена-мишени и других благоприятных биологических свойств. В одном аспекте изобретения гуманизированные антитела и фрагменты антител получают методом анализа родительских последовательностей и различных концептуальных гуманизированных продуктов с использованием трехмерных моделей родительских и гуманизированных последовательностей. Трехмерные модели иммуноглобулинов легкодоступны и знакомы специалистам в данной области. Доступны компьютерные программы, иллюстрирующие и демонстрирующие возможные трехмерные конформационные структуры выбранных иммуноглобулиновых последовательностей-кандидатов. Изучение таких изображений позволяет анализировать вероятную роль остатков в функционировании иммуноглобулиновой последовательности-кандидата, например, анализировать остатки, которые влияют на способность иммуноглобулина-кандидата связывать антиген-мишень. В результате, остатки FR могут быть выбраны и скомбинированы с реципиентными и импортированными последовательностями таким образом, что достигается желательная характеристика антитела или фрагмента антитела, такая как повышенная аффинность для антигена-мишени. Как правило, остатки CDR напрямую и наиболее существенным образом влияют на связывание антигена.
Гуманизированное антитело или фрагмент антитела может сохранять антигенную специфичность, аналогичную специфичности исходного антитела, например, в настоящем изобретении способность связывать опухолевый антиген человека, описанный в настоящем документе. В некоторых вариантах осуществления гуманизированное антитело или фрагмент антитела может иметь повышенную аффинность и/или специфичность связывания с опухолевым антигеном, описанным в настоящем документе. В некоторых вариантах осуществления гуманизированное антитело или фрагмент антитела может иметь более низкую аффинность и/или специфичность связывания с опухолевым антигеном, описанным в настоящем документе, или B-клеточным антигеном, описанным в настоящем документе.
В одном аспекте антигенсвязывающий домен по изобретению характеризуется конкретными функциональными особенностями, или свойствами, антитела или фрагмента антитела. Например, в одном аспекте фрагмент CAR по изобретению, содержащий антигенсвязывающий домен, специфически связывает опухолевый антиген, описанный в настоящем документе.
В одном аспекте антигенсвязывающий домен представляет собой фрагмент, например, одноцепочечный вариабельный фрагмент (scFv). В одном аспекте домен, связывающий опухолевый антиген, описанный в настоящем документе, представляет собой Fv, Fab, (Fab')2 или бифункциональное (например, биспецифическое) гибридное антитело (например, Lanzavecchia et al., Eur. J. Immunol. 17, 105 (1987)). В одном аспекте антитела и их фрагменты по изобретению связывают белок опухолевого антигена, описанного в настоящем документе, с аффинностью антитела дикого типа или повышенной аффинностью.
В некоторых случаях фрагменты scFv могут быть получены способом, известным в данной области (смотри, например, Bird et al., (1988) Science 242:423-426 и Huston et al., (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Молекулы scFv могут быть получены путем связывания между собой областей VH и VL при помощи гибких полипептидных линкеров. Молекулы scFv содержат линкер (например, Ser-Gly линкер) с оптимизированной длиной и/или аминокислотным составом. Длина линкера может сильно влиять на сворачивание и взаимодействие вариабельных областей scFv. Фактически, в случае использования короткого полипептидного линкера (например, длиной 5-10 аминокислот) предотвращается внутрицепочечное сворачивание. Межцепочечное сворачивание также необходимо для сведения вместе двух вариабельных областей, с образованием функционального эпитоп-связывающего сайта. Примеры ориентации и размеров линкеров смотри, например, в Hollinger et al. 1993 Proc Natl Acad. Sci. U.S.A. 90:6444-6448, публикациях патентных заявок США №№ 2005/0100543, 2005/0175606, 2007/0014794 и PCT публикациях №№ WO2006/020258 и WO2007/024715, содержание которых включено в настоящий документ посредством ссылки.
Фрагмент scFv может содержать линкер длиной по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50 или более аминокислотных остатков между его областями VL и VH. Последовательность линкера может содержать любую природную аминокислоту. В некоторых вариантах осуществления последовательность линкера содержит аминокислоты глицин и серин. В другом варианте осуществления последовательность линкера содержит набор повторов из остатков глицина и серина, такой как (Gly4Ser)n, где n представляет собой положительное целое число, равное или превышающее 1 (SEQ ID NO: 22). В одном варианте осуществления линкер может представлять собой (Gly4Ser)4 (SEQ ID NO: 29) или (Gly4Ser)3(SEQ ID NO: 30). Варьирование длины линкера может способствовать сохранению или повышению активности, приводя к максимальной эффективности в исследованиях активности.
В другом аспекте антигенсвязывающий домен представляет собой T-клеточный рецептор («TCR»), рекомбинантный TCR или его фрагмент, например, одноцепочечный TCR (scTCR). Способы получения таких TCR известны в данной области. Смотри, например, Willemsen RA et al., Gene Therapy 7: 1369-1377 (2000); Zhang T et al., Cancer Gene Ther 11: 487-496 (2004); Aggen et al., Gene Ther. 19(4):365-74 (2012) (литературные источники включены в настоящий документ посредством ссылки). Например, может быть сконструирован scTCR, который содержит продукты генов Vα и Vβ из T-клеточного клона, связанные линкером (например, гибким пептидом). Такой подход очень полезен в случае связанного с раком антигена-мишени, который сам по себе является внутриклеточным, однако фрагмент такого антигена (пептид) представлен на поверхности раковых клеток в контексте MHC.
В одном аспекте антигенсвязывающий домен CAR содержит аминокислотную последовательность, которая является гомологичной аминокислотной последовательности антигенсвязывающего домена, описанного в настоящем документе, и антигенсвязывающий домен сохраняет желательные функциональные свойства антигенсвязывающего домена, описанного в настоящем документе.
В одном конкретном аспекте CAR по изобретению содержит фрагмент антитела. В следующем аспекте фрагмент антитела содержит scFv. В следующем аспекте фрагмент антитела содержит только вариабельный домен тяжелой цепи (VH).
В разных аспектах антигенсвязывающий домен CAR конструируют путем модификации одной или более аминокислот в одной или обеих вариабельных областях (например, VH и/или VL), например, в одной или более областях CDR и/или в одной или более каркасных областях. В одном конкретном аспекте CAR по изобретению содержит фрагмент антитела. В следующем аспекте фрагмент антитела содержит scFv.
Специалисты в данной области понимают, что антитело или фрагмент антитела по изобретению могут быть дополнительно модифицированы так, что они могут отличаться по аминокислотной последовательности (например, от дикого типа), но не по желаемой активности. Например, в случае такого белка могут быть выполнены дополнительные нуклеотидные замены, приводящие к аминокислотным заменам «несущественных» аминокислотных остатков. Например, несущественный аминокислотный остаток в молекуле может быть заменен другим аминокислотным остатком из того же семейства остатков с аналогичными боковыми цепями. В другом варианте осуществления последовательность аминокислот может быть заменена структурно сходной последовательностью, которая отличается по порядку расположения и/или составу представителей семейства остатков с аналогичными боковыми цепями, например, может быть выполнена консервативная замена, при которой аминокислотный остаток заменяют аминокислотным остатком с аналогичной боковой цепью.
Семейства аминокислотных остатков с аналогичными боковыми цепями известны в данной области, включая семейства остатков с основными боковыми цепями (например, лизин, аргинин, гистидин), кислыми боковыми цепями (например, аспарагиновая кислота, глутаминовая кислота), незаряженными полярными боковыми цепями (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин), неполярными боковыми цепями (например, аланин, валин, лейцин изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленными боковыми цепями (например, треонин, валин изолейцин) и ароматическими боковыми цепями (например, тирозин, фенилаланин, триптофан, гистидин).
Термин «процент идентичности» в контексте двух или более нуклеотидных, или полипептидных, последовательностей относится к двум или более последовательностями, которые являются одинаковыми. Две последовательности являются «в значительной степени идентичными», если две последовательности имеют определенную процентную долю аминокислотных остатков, или нуклеотидов, которые являются одинаковыми (например, 60% идентичности, необязательно 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичности на протяжении конкретной области или, если не указано, на протяжении всей последовательности) при сравнении и выравнивании для максимального соответствия в окне сравнения, или определенной области, что измеряют с использованием одного из следующих алгоритмов сравнения последовательностей или путем выравнивания вручную и визуальной инспекции. Необязательно, идентичность существует на протяжении области, которая имеет длину по меньшей мере примерно 50 нуклеотидов (или 10 аминокислот) или более, предпочтительно на протяжении области, которая имеет длину 100-500 или 1000, или более нуклеотидов (или 20, 50, 200 или более аминокислот).
При сравнении последовательностей, как правило, одна последовательность выступает в роли эталонной последовательности, с которой сравнивают тестируемые последовательности. При использовании алгоритма сравнения последовательностей информацию о тестируемых и эталонных последовательностях вводят в компьютер, определяют координаты подпоследовательностей, при необходимости, и определяют параметры программы алгоритма сравнения последовательностей. Можно использовать параметры по умолчанию программы, или можно устанавливать альтернативные параметры. Затем алгоритм сравнения последовательностей рассчитывает процент идентичности последовательностей для тестируемых последовательностей относительно эталонной последовательности, на основе параметров программы. Способы выравнивания последовательностей для целей сравнения хорошо известны в данной области. Оптимальное выравнивание последовательностей для целей сравнения можно осуществлять, например, с помощью алгоритма локальной гомологии Смита-Уотермана (1970) Adv. Appl. Math. 2:482c, с помощью алгоритма выравнивания областей гомологии Нидлмана-Вунша, (1970) J. Mol. Biol. 48:443, методом поиска подобия Пирсона-Липмана, (1988) Proc. Nat'l. Acad. Sci. USA 85:2444, с помощью компьютеризированной реализации этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в пакете программ Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Dr., Madison, WI), или путем выравнивания вручную и визуальной инспекции (смотри, например, Brent et al., (2003) Current Protocols in Molecular Biology).
Двумя примерами алгоритмов, которые подходят для определения процента идентичности последовательностей и сходства последовательностей, являются алгоритмы BLAST и BLAST 2.0, которые описаны в Altschul et al., (1977) Nuc. Acids Res. 25: 3389-3402; и Altschul et al., (1990) J. Mol. Biol. 215: 403-410, соответственно. Программа для выполнения анализов BLAST является общедоступной через Национальный центр биотехнологической информации.
Процент идентичности двух аминокислотных последовательностей также можно определять с использованием алгоритма Маерса-Миллера, (1988) Comput. Appl. Biosci. 4:11-17), который включен в программу ALIGN (версия 2.0), с использованием таблицы весов замен остатков PAM120, штрафа за удлинение делеции 12 и штрафа за внесение делеции 4. Кроме того, процент идентичности двух аминокислотных последовательностей можно определять с использованием алгоритма Нидлмана-Вунша (1970) J. Mol. Biol. 48:444-453), который включен в программу GAP в пакете программ GCG (доступном в сети интернет по сетевому адресу gcg.com), с использованием либо матрицы Blossom 62, либо матрицы PAM250, штрафа за внесение делеции 16, 14, 12, 10, 8, 6, или 4 и штрафа за удлинение делеции 1, 2, 3, 4, 5 или 6.
В одном аспекте настоящего изобретения предусмотрены модификации аминокислотной последовательности исходного антитела или фрагмента (например, scFv), которые приводят к получению функционально эквивалентных молекул. Например, VH или VL антигенсвязывающего домена для опухолевого антигена, описанного в настоящем документе, например, scFv, содержащегося в CAR, могут быть модифицированы для сохранения по меньшей мере примерно 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%,81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичности с исходной каркасной областью VH или VL антигенсвязывающего домена для опухолевого антигена, описанного в настоящем документе, например, scFv. По настоящему изобретению предусмотрены модификации всего конструкта CAR, например, модификации в одной или более аминокислотных последовательностях различных доменов конструкта CAR, для создания функционально эквивалентных молекул. Конструкт CAR может быть модифицирован для сохранения по меньшей мере примерно 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% идентичности с исходным конструктом CAR.
Биспецифические CAR
В одном из вариантов осуществления молекула мультиспецифического антитела представляет собой молекулу биспецифического антитела. Биспецифическое антитело обладает специфичностью для не более, чем двух антигенов. Молекула биспецифического антитела имеет первую последовательность вариабельного домена иммуноглобулина со специфичностью связывания для первого эпитопа и вторую последовательность вариабельного домена иммуноглобулина со специфичностью связывания для второго эпитопа. В одном из вариантов осуществления первый и второй эпитопы находятся на одном и том же антигене, например, одном и том же белке (или субъединице мультимерного белка). В одном из вариантов осуществления первый и второй эпитопы перекрываются. В одном из вариантов осуществления первый и второй эпитопы не перекрываются. В одном из вариантов осуществления первый и второй эпитопы находятся на разных антигенах, например, разных белках (или разных субъединицах мультимерного белка). В одном из вариантов осуществления молекула биспецифического антитела содержит последовательность вариабельного домена тяжелой цепи и последовательность вариабельного домена легкой цепи, которые имеют специфичность связывания для первого эпитопа, а также последовательность вариабельного домена тяжелой цепи и последовательность вариабельного домена легкой цепи, которые имеют специфичность связывания для второго эпитопа. В одном из вариантов осуществления молекула биспецифического антитела содержит половину антитела, имеющую специфичность связывания для первого эпитопа, и половину антитела, имеющую специфичность связывания для второго эпитопа. В одном из вариантов осуществления молекула биспецифического антитела содержит половину антитела или его фрагмент со специфичностью связывания для первого эпитопа и половину антитела или его фрагмент со специфичностью связывания для второго эпитопа. В одном из вариантов осуществления молекула биспецифического антитела содержит scFv или его фрагмент со специфичностью связывания для первого эпитопа и scFv или его фрагмент со специфичностью связывания для второго эпитопа.
В конкретных вариантах осуществления молекула антитела является мультиспецифической (например, биспецифической или триспецифической) молекулой антитела. Методы получения молекул биспецифических или гетеродимерных антител известны в данной области; включая, но без ограничения, например, подход «выступ во впадине», как описано, например, в US5731168; направляемое электростатическими силами спаривание Fc, как описано, например, в WO09/089004, WO06/106905 и WO2010/129304; образование гетеродимеров при помощи доменов, полученных путем замены цепей (SEED), как описано, например, в WO07/110205; замену Fab-фрагментов, как описано, например, в WO08/119353, WO2011/131746 и WO2013/060867; создание конъюгата двух антител, например, путем перекрестной сшивки антител, с получением биспецифической структуры, при помощи гетеробифункционального реагента, имеющего реакционноспособную аминогруппу и реакционноспособную сульфгидрильную группу, как описано, например, в US4433059; получение биспецифического антитела путем рекомбинации половин антител (пар тяжелая-легкая цепи или Fab) из разных антител в цикле восстановления и окисления дисульфидных связей между двумя тяжелыми цепями, как описано, например, в US4444878; создание трифункциональных антител, например, за счет трех Fab'-фрагментов, перекрестно сшитых через сульфгидрильные реакционноспособные группы, как описано, например, в US5273743; создание биосинтетических связывающих белков, например, пары scFv, перекрестно сшитых через C-концевые фрагменты, предпочтительно путем образования дисульфидных связей или химической сшивки через реакционноспособные аминогруппы, как описано, например, в US5534254; получение бифункциональных антител, например, Fab-фрагментов с разными специфичностями связывания, димеризованных за счет лейциновых застежек (например, c-fos и c-jun), которые заменили константный домен, как описано, например, в US5582996; получение биспецифических и олигоспецифических моно- и олиговалентных рецепторов, например, VH-CH1 областей из двух антител (два Fab-фрагмента), связанных через полипептидный спейсер между областью CH1 одного антитела и областью VH другого антитела, как правило, со связанными легкими цепями, как описано, например, в US5591828; создание биспецифических конъюгатов ДНК-антитело, например, путем перекрестной сшивки антител или Fab-фрагментов через двухцепочечный фрагмент ДНК, как описано, например, в US5635602; получение биспецифических слитых белков, например, экспрессионного конструкта, содержащего два фрагмента scFv с гидрофильным спиральным пептидным линкером между ними и полной константной областью, как описано, например, в US5637481; получение мультивалентных и мультиспецифических связывающих белков, например, димера из полипептидов, имеющих первый домен со связывающей областью из вариабельной области тяжелой цепи Ig и второй домен со связывающей областью из вариабельной области легкой цепи Ig, как правило, называемого диателом (также предусмотрено создание структур более высокого порядка для получения биспецифических, триспецифических или тетраспецифических молекул, как описано, например, в US5837242); создание конструктов минител со связанными цепями VL и VH, дополнительно соединенными при помощи пептидных спейсеров с шарнирной областью и областью CH3 антитела, которые могут быть димеризованы, с получением биспецифических/мультивалентных молекул, как описано, например, в US5837821; получение доменов VH и VL, связанных коротким пептидным линкером (например, из 5 или 10 аминокислот), или совсем без линкера, в любой ориентации, которые могут образовывать димеры, с получением биспецифических диател; получение тримеров и тетрамеров, как описано, например, в US5844094; создание последовательности из доменов VH (или доменов VL у представителей семейства), связанных пептидными связями через сшиваемые группы на C-конце, дополнительно связанных с доменами VL, с образованием серии FV (или фрагментов scFv), как описано, например, в US5864019; и получение одноцепочечных связывающих полипептидов, имеющих как VH, так и VL, домены, связанные через пептидный линкер, объединенных в мультивалентные структуры за счет нековалентных связей или химической сшивки, с образованием, например, гомобивалентных, гетеробивалентных, тривалентных и тетравалентных структур с использованием как scFV формата, так и формата диатела, как описано, например, в US5869620. Дополнительные иллюстративные мультиспецифические и биспецифические молекулы и способы их получения описаны, например, в US5910573, US5932448, US5959083, US5989830, US6005079, US6239259, US6294353, US6333396, US6476198, US6511663, US6670453, US6743896, US6809185, US6833441, US7129330, US7183076, US7521056, US7527787, US7534866, US7612181, US2002004587A1, US2002076406A1, US2002103345A1, US2003207346A1, US2003211078A1, US2004219643A1, US2004220388A1, US2004242847A1, US2005003403A1, US2005004352A1, US2005069552A1, US2005079170A1, US2005100543A1, US2005136049A1, US2005136051A1, US2005163782A1, US2005266425A1, US2006083747A1, US2006120960A1, US2006204493A1, US2006263367A1, US2007004909A1, US2007087381A1, US2007128150A1, US2007141049A1, US2007154901A1, US2007274985A1, US2008050370A1, US2008069820A1, US2008152645A1, US2008171855A1, US2008241884A1, US2008254512A1, US2008260738A1, US2009130106A1, US2009148905A1, US2009155275A1, US2009162359A1, US2009162360A1, US2009175851A1, US2009175867A1, US2009232811A1, US2009234105A1, US2009263392A1, US2009274649A1, EP346087A2, WO0006605A2, WO02072635A2, WO04081051A1, WO06020258A2, WO2007044887A2, WO2007095338A2, WO2007137760A2, WO2008119353A1, WO2009021754A2, WO2009068630A1, WO9103493A1, WO9323537A1, WO9409131A1, WO9412625A2, WO9509917A1, WO9637621A2, WO9964460A1. Содержание всех вышеперечисленных заявок включено в настоящий документ посредством ссылки в полном объеме.
В каждом антителе или фрагменте антитела (например, scFv) молекулы биспецифического антитела VH может находиться перед или после VL. В некоторых вариантах осуществления расположенное впереди антитело, или фрагмент антитела (например, scFv), организовано так, что его VH (VH1) находится перед его VL (VL1), и расположенное далее антитело, или фрагмент антитела (например, scFv), организовано так, что его VL (VL2) находится перед его VH (VH2), в результате чего вся молекула биспецифического антитела имеет структуру VH1-VL1-VL2-VH2. В других вариантах осуществления расположенное впереди антитело, или фрагмент антитела (например, scFv), организовано так, что его VL (VL1) находится перед его VH (VH1), и расположенное далее антитело, или фрагмент антитела (например, scFv), организовано так, что его VH (VH2) находится перед его (VL2), в результате чего вся молекула биспецифического антитела имеет структуру VL1-VH1-VH2-VL2. Необязательно, линкер находится между двумя антителами или фрагментами антител (например, scFv), например, между VL1 и VL2, если конструкт имеет структуру VH1-VL1-VL2-VH2, или между VH1 и VH2, если конструкт имеет структуру VL1-VH1-VH2-VL2. Линкер может представлять собой линкер, описанный в настоящем документе, например, (Gly4-Ser)n линкер, где n равно 1, 2, 3, 4, 5 или 6, предпочтительно 4 (SEQ ID NO: 967). Как правило, линкер между двумя scFv должен быть достаточно длинным, чтобы избежать ошибочного спаривания между доменами двух scFv. Необязательно, линкер находится между областями VL и VH первого scFv. Необязательно, линкер находится между областями VL и VH второго scFv. В конструктах, имеющих несколько линкеров, любые два или более линкеров могут быть одинаковыми или разными. Соответственно, в некоторых вариантах осуществления биспецифический CAR содержит области VL, VH и, необязательно, один или более линкеров в структуре, описанной в настоящем документе.
В одном аспекте химерный антигенный рецептор содержит биспецифический антигенсвязывающий домен, трансмембранный домен (например, описанный в настоящем документе) и внутриклеточный сигнальный домен (например, описанный в настоящем документе). В вариантах осуществления биспецифический антигенсвязывающий домен содержит первую последовательность вариабельного домена иммуноглобулина, например, scFv (или содержит области CDR легкой цепи и/или области CDR тяжелой цепи из scFv, описанного в настоящем документе), который связывает антиген, например, описанный в настоящем документе (например, CD19-связывающий домен или BCMA-связывающий домен, описанный в настоящем документе, например, в Таблице 6 или Таблице 12), и вторую последовательность вариабельного домена иммуноглобулина, например, scFv (или содержит области CDR легкой цепи и/или области CDR тяжелой цепи из scFv, описанного в настоящем документе), который имеет специфичность связывания для одного или более антигенов, описанных в настоящем документе, например, содержит scFv, описанный в настоящем документе, например, содержащий мезотелин-связывающий домен или EGFRvIII-связывающий домен (например, приведенный в Таблице 2 или Таблице 5). В вариантах осуществления биспецифический антигенсвязывающий домен содержит CD19-связывающий домен, описанный в настоящем документе, и мезотелин-связывающий домен, описанный в настоящем документе. В вариантах осуществления биспецифический антигенсвязывающий домен содержит BCMA-связывающий домен, описанный в настоящем документе, и мезотелин-связывающий домен, описанный в настоящем документе. В вариантах осуществления биспецифический антигенсвязывающий домен содержит CD19-связывающий домен, описанный в настоящем документе, и EGFRvIII-связывающий домен, описанный в настоящем документе. В вариантах осуществления биспецифический антигенсвязывающий домен содержит BCMA-связывающий домен, описанный в настоящем документе, и EGFRvIII-связывающий домен, описанный в настоящем документе. В другом аспекте изобретение относится к клетке (например, популяции клеток), например, иммунной эффекторной клетке, например, T-клетке или NK-клетке, например, описанной в настоящем документе, которая сконструирована для экспрессии (например, содержит) биспецифического CAR, описанного в настоящем документе, например, биспецифического CAR, содержащего два антигенсвязывающих домена, описанных в настоящем документе. Без связи с конкретной теорией, считается, что клетки, экспрессирующие такие биспецифические CAR (например, содержащие два антигенсвязывающих домена, например, описанные в настоящем документе), могут быть использованы в способах и композициях, описанных в настоящем документе.
Химерный TCR
В одном аспекте антигенсвязывающие домены, описанные в настоящем документе, например, антитела и фрагменты антител, например, приведенные в Таблицах настоящего документа, могут быть привиты на один или более константных доменов цепи T-клеточного рецептора («TCR»), например, альфа-цепи TCR или бета-цепи TCR, с получением химерного TCR, который имеет специфичность связывания для опухолевого антигена, описанного в настоящем документе. Без связи с конкретной теорией, считается, что химерные TCR будут сигнализировать через комплекс TCR при связывании антигена. Например, scFv для мезотелина или CD19, или его фрагмент, например, домен VL или домен VH, раскрытый в настоящем документе, может быть привит на константный домен, например, по меньшей мере часть внеклеточного константного домена, трансмембранный домен и цитоплазматический домен цепи TCR, например, альфа-цепи TCR и/или бета-цепи TCR. В качестве другого примера, области CDR антитела или фрагмента антитела, например, области CDR любого из антител или фрагментов антител, приведенных в Таблицах настоящего документа, могут быть привиты на альфа- и/или бета-цепь TCR, с получением химерного TCR, который связывается специфически с опухолевым антигеном, описанным в настоящем документе. Например, области LCDR, раскрытые в настоящем документе, могут быть привиты на вариабельный домен альфа-цепи TCR, и области HCDR, раскрытые в настоящем документе, могут быть привиты на вариабельный домен бета-цепи TCR, или наоборот. Такие химерные TCR могут быть получены методами, известными в данной области (например, Willemsen RA et al., Gene Therapy 2000; 7: 1369-1377; Zhang T et al., Cancer Gene Ther 2004; 11: 487-496; Aggen et al., Gene Ther. 2012 Apr;19(4):365-74).
Трансмембранный домен
Что касается трансмембранного домена, в различных вариантах осуществления CAR может быть сконструирован для содержания трансмембранного домена, который связан с внеклеточным доменом CAR, например, антигенсвязывающим доменом. Трансмембранный домен может содержать одну или более дополнительных аминокислот рядом с трансмембранной областью, например, одну или более аминокислот, связанных с внеклеточной областью белка, из которого получен трансмембранный домен (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, или до 15 аминокислот из внеклеточной области), и/или одну или более дополнительных аминокислот, связанных с внутриклеточной областью белка, из которого получен трансмембранный домен (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, или до 15 аминокислот из внутриклеточной области). В одном аспекте трансмембранный домен представляет собой домен, который связан с одним из других доменов CAR, например, трансмембранный домен из того же белка, что и внутриклеточный сигнальный домен, например, костимулирующий домен. В некоторых случаях трансмембранный домен может быть выбран или модифицирован путем аминокислотных замен для предотвращения связывания таких доменов с трансмембранными доменами того же самого или других поверхностных мембранных белков, например, для сведения к минимуму взаимодействий с другими членами рецепторного комплекса. В одном аспекте трансмембранный домен способен к гомодимеризации с другим CAR на клеточной поверхности CAR-экспрессирующей клетки. В другом аспекте аминокислотная последовательность трансмембранного домена может быть модифицирована или изменена для сведения к минимуму взаимодействий со связывающими доменами естественного партнера по связыванию, присутствующего на той же самой CAR-экспрессирующей клетке.
Трансмембранный домен может быть получен либо из природного, либо из рекомбинантного источника. Если источник является природным, домен может быть получен из любого связанного с мембраной или трансмембранного белка. В одном аспекте трансмембранный домен способен передавать сигнал внутриклеточному домену(ам) при связывании CAR с мишенью. Трансмембранный домен, особенно полезный по данному изобретению, может содержать по меньшей мере трансмембранную область(и), например, альфа, бета или дзета-цепи T-клеточного рецептора, CD28, CD27, CD3-эпсилон, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, CD154. В некоторых вариантах осуществления трансмембранный домен может содержать по меньшей мере трансмембранную область(и), например, KIRDS2, OX40, CD2, CD27, LFA-1 (CD11a, CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD40, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, IL2R-бета, IL2R-гамма, IL7Rα, ITGA1, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, TNFR2, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (тактильный), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, PAG/Cbp, NKG2D, NKG2C.
В некоторых случаях трансмембранный домен может быть связан с внеклеточной областью CAR, например, антигенсвязывающим доменом CAR, при помощи шарнира, например, шарнира из человеческого белка. Например, в одном варианте осуществления шарнир может представлять собой шарнир человеческого Ig (иммуноглобулина), например, шарнир IgG4, или шарнир CD8a. В одном варианте осуществления шарнир или спейсер содержит (например, состоит из) аминокислотную последовательность SEQ ID NO: 4. В одном аспекте трансмембранный домен содержит (например, состоит из) трансмембранный домен с SEQ ID NO: 12.
В одном аспекте шарнир или спейсер содержит шарнир IgG4. Например, в одном варианте осуществления шарнир или спейсер содержит шарнир с аминокислотной последовательностью SEQ ID NO: 6. В некоторых вариантах осуществления шарнир или спейсер содержит шарнир, кодируемый нуклеотидной последовательностью SEQ ID NO: 7. В одном аспекте шарнир или спейсер содержит шарнир IgD. Например, в одном варианте осуществления шарнир или спейсер содержит шарнир с аминокислотной последовательностью SEQ ID NO: 8. В некоторых вариантах осуществления шарнир или спейсер содержит шарнир, кодируемый нуклеотидной последовательностью SEQ ID NO: 9.
В одном аспекте трансмембранный домен может быть рекомбинантным, в этом случае он будет содержать преимущественно гидрофобные остатки, такие как лейцин и валин. В одном аспекте триплет из остатков фенилаланина, триптофана и валина может находиться на каждом конце рекомбинантного трансмембранного домена.
Необязательно, короткий олиго- или полипептидный линкер, длиной 2-10 аминокислот может связывать трансмембранный домен и цитоплазматическую область CAR. Особенно подходящим линкером может служить дублет глицин-серин. Например, в одном аспекте линкер содержит аминокислотную последовательность GGGGSGGGGS (SEQ ID NO: 10). В некоторых вариантах осуществления линкер закодирован нуклеотидной последовательностью GGTGGCGGAGGTTCTGGAGGTGGAGGTTCC (SEQ ID NO: 11).
В одном аспекте шарнир или спейсер содержит шарнир KIR2DS2.
Цитоплазматический домен
Цитоплазматический домен, или область, CAR содержит внутриклеточный сигнальный домен. Внутриклеточный сигнальный домен, как правило, отвечает за активацию по меньшей мере одной из нормальных эффекторных функций иммунной клетки, в которую был введен CAR. Термин «эффекторная функция» означает специализированную функцию клетки. Эффекторной функцией T-клетки, например, может быть цитолитическая активность или хелперная активность, включая секрецию цитокинов. Таким образом, термин «внутриклеточный сигнальный домен» означает фрагмент белка, который передает сигнал эффекторной функции и направляет клетку на выполнение специализированной функции. Хотя, как правило, можно использовать целый внутриклеточный сигнальный домен, во многих случаях нет необходимости использовать полную цепь. Если может быть использован укороченный фрагмент внутриклеточного сигнального домена, такой укороченный фрагмент может быть использован вместо интактной цепи при условии, что он передает сигнал эффекторной функции. Таким образом, термин «внутриклеточный сигнальный домен» должен включать любой укороченный фрагмент внутриклеточного сигнального домена, достаточный для передачи сигнала эффекторной функции.
Примеры внутриклеточных сигнальных доменов для использования в CAR по изобретению включают цитоплазматические последовательности T-клеточного рецептора (TCR) и корецепторов, которые действуют совместно, инициируя передачу сигнала после связывания антигена с рецептором, а также любое производное или вариант таких последовательностей и любую рекомбинантную последовательность, обладающую такими же функциональными свойствами.
Известно, что сигналы, создаваемые только за счет TCR, являются недостаточными для полной активации T-клетки, и что также необходим вторичный и/или костимулирующий сигнал. Таким образом, можно сказать, что активация T-клетки опосредуется двумя разными видами цитоплазматических сигнальных последовательностей: теми, которые инициируют антиген-зависимую первичную активацию через TCR (основные внутриклеточные сигнальные домены), и теми, которые действуют независимым от антигена образом, обеспечивая вторичный или костимулирующий сигнал (вторичный цитоплазматический домен, например, костимулирующий домен).
Основной сигнальный домен регулирует первичную активацию комплекса TCR либо стимулирующим, либо ингибирующим образом. Основные внутриклеточные сигнальные домены, которые действуют стимулирующим образом, могут содержать сигнальные мотивы, известные как иммунорецепторные тирозиновые активирующие мотивы, или ITAM.
Примеры ITAM-содержащих основных внутриклеточных сигнальных доменов, которые особенно подходят для использования по изобретению, включают домены TCR-дзета, FcR-гамма, FcR-бета, CD3-гамма, CD3-дельта, CD3-эпсилон, CD5, CD22, CD79a, CD79b, CD278 (также известный как «ICOS»), FcεRI, DAP10, DAP12 и CD66d. В одном варианте осуществления CAR по изобретению содержит внутриклеточный сигнальный домен, например, основной сигнальный домен CD3-дзета, например, последовательность CD3-дзета, описанную в настоящем документе.
В одном варианте осуществления основной сигнальный домен содержит модифицированный домен ITAM, например, мутантный домен ITAM, который имеет измененную (например, повышенную или сниженную) активность по сравнению с природным доменом ITAM. В одном варианте осуществления основной сигнальный домен представляет собой основной внутриклеточный сигнальный домен, содержащий модифицированный ITAM, например, основной внутриклеточный сигнальный домен, содержащий оптимизированный и/или укороченный ITAM. В одном из вариантов осуществления основной сигнальный домен содержит один, два, три, четыре или более мотивов ITAM.
Внутриклеточный сигнальный домен CAR может содержать только сигнальный домен CD3-дзета, или его в сочетании с любым другим нужным внутриклеточным сигнальным доменом(ами), полезным в контексте CAR по изобретению. Например, внутриклеточный сигнальный домен CAR может содержать часть цепи CD3-дзета и костимулирующий сигнальный домен. Костимулирующий сигнальный домен представляет собой фрагмент CAR, содержащий внутриклеточный домен костимулирующей молекулы. Костимулирующая молекула представляет собой молекулу клеточной поверхности, отличную от антигенного рецептора или его лигандов, которая необходима для эффективного ответа лимфоцитов на антиген. Примеры таких молекул включают CD27, CD28, 4-1BB (CD137), OX40, CD30, CD40, PD-1, ICOS, антиген 1, ассоциированный с функцией лимфоцитов (LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3, а также лиганд, который специфически связывается с CD83, и тому подобное. Например, показано, что костимуляция CD27 способствует повышению размножения, эффекторной функции и выживаемости человеческих CAR T-клеток in vitro, а также увеличению персистенции человеческих T-клеток и противоопухолевой активности in vivo (Song et al. Blood. 2012; 119(3):696-706). Дополнительные примеры таких костимулирующих молекул включают молекулу MHC класса I, белок рецептора TNF, иммуноглобулиноподобный белок, рецептор цитокина, интегрин, сигнальную молекулу активации лимфоцитов (белок SLAM), активирующий NK-клетку рецептор, BTLA, Toll-подобный рецептор, OX40, CD2, CD7, CD27, CD28, CD30, CD40, CDS, ICAM-1, LFA-1 (CD11a/CD18), 4-1BB (CD137), B7-H3, CDS, ICAM-1, ICOS (CD278), GITR, BAFFR, LIGHT, HVEM (LIGHTR), KIRDS2, SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD19, CD4, CD8-альфа, CD8-бета, IL2R-бета, IL2R-гамма, IL7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, NKG2C, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (тактильный), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, CD19a, а также лиганд, который специфически связывается с CD83.
Внутриклеточные сигнальные последовательности в цитоплазматическом фрагменте CAR по изобретению могут быть связаны друг с другом случайным или определенным образом. Необязательно, короткий олиго- или полипептидный линкер, например, длиной 2-10 аминокислот (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислот), может связывать внутриклеточные сигнальные последовательности. В одном варианте осуществления дублет глицин-серин может быть использован в качестве подходящего линкера. В одном варианте осуществления одна аминокислота, например, аланин, глицин, может быть использована в качестве подходящего линкера.
В одном аспекте внутриклеточный сигнальный домен сконструирован для содержания двух или более, например, 2, 3, 4, 5 или более, костимулирующих сигнальных доменов. В одном из вариантов осуществления два или более, например, 2, 3, 4, 5 или более, костимулирующих сигнальных доменов разделены молекулой линкера, например, молекулой линкера, описанной в настоящем документе. В одном варианте осуществления внутриклеточный сигнальный домен содержит два костимулирующих сигнальных домена. В некоторых вариантах осуществления молекула линкера представляет собой остаток глицина. В некоторых вариантах осуществления линкер представляет собой остаток аланина.
В одном аспекте внутриклеточный сигнальный домен сконструирован для содержания сигнального домена CD3-дзета и сигнального домена CD28. В одном аспекте внутриклеточный сигнальный домен сконструирован для содержания сигнального домена CD3-дзета и сигнального домена 4-1BB. В одном аспекте сигнальный домен 4-1BB представляет собой сигнальный домен с SEQ ID NO: 14. В одном аспекте сигнальный домен CD3-дзета представляет собой сигнальный домен с SEQ ID NO: 18.
В одном аспекте внутриклеточный сигнальный домен сконструирован для содержания сигнального домена CD3-дзета и сигнального домена CD27. В одном аспекте сигнальный домен CD27 содержит аминокислотную последовательность SEQ ID NO: 16. В одном аспекте сигнальный домен CD27 закодирован нуклеотидной последовательностью SEQ ID NO: 17.
В одном аспекте внутриклеточный сигнальный домен сконструирован для содержания сигнального домена CD3-дзета и сигнального домена CD28. В одном аспекте сигнальный домен CD28 содержит аминокислотную последовательность SEQ ID NO: 124. В одном аспекте сигнальный домен CD28 закодирован нуклеотидной последовательностью SEQ ID NO: 1113.
В одном аспекте внутриклеточный сигнальный домен сконструирован для содержания сигнального домена CD3-дзета и сигнального домена ICOS. В одном аспекте сигнальный домен ICOS содержит аминокислотную последовательность SEQ ID NO: 120. В одном аспекте сигнальный домен ICOS закодирован нуклеотидной последовательностью SEQ ID NO: 1111.
В одном аспекте клетка по изобретению, например, описанная в настоящем документе, например, клетка, экспрессирующая два разных CAR, имеет CAR, каждый из которых содержит антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен, основной сигнальный домен и костимулирующий сигнальный домен. В вариантах осуществления вышеуказанного аспекта костимулирующие домены двух разных CAR могут быть одинаковыми или разными. В вариантах осуществления один или более из двух разных CAR содержат более одного костимулирующего сигнального домена. В других аспектах клетка по изобретению, например, описанная в настоящем документе, например, клетка, экспрессирующая два разных CAR, имеет первый CAR, содержащий антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен, основной сигнальный домен, но не содержащий костимулирующий сигнальный домен, и второй CAR, содержащий антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен, и костимулирующий сигнальный домен, но не содержащий основной сигнальный домен.
В одном аспекте CAR-экспрессирующая клетка, описанная в настоящем документе, например, клетка, экспрессирующая два разных CAR, может также иметь другой, например, третий, CAR, например, другой CAR, содержащий другой антигенсвязывающий домен, например, для той же мишени или другой мишени (например, мишени, отличной от опухолевого антигена, описанного в настоящем документе, или другого опухолевого антигена, описанного в настоящем документе). Например, в одном из вариантов осуществления, в котором клетка по изобретению экспрессирует третий CAR, содержащий антигенсвязывающий домен, который связывает второй опухолевый антиген-мишень, третий CAR содержит антигенсвязывающий домен для мишени, экспрессируемой на того же типа раковой клетке, что и опухолевый антиген, являющийся мишенью для первого или второго CAR. В одном варианте осуществления CAR-экспрессирующая клетка имеет первый CAR, который нацелен на первый опухолевый антиген и содержит внутриклеточный сигнальный домен, содержащий костимулирующий сигнальный домен, но не основной сигнальный домен, и третий CAR, который нацелен на второй, отличающийся, опухолевый антиген и содержит внутриклеточный сигнальный домен, содержащий основной сигнальный домен, но не костимулирующий сигнальный домен. Без связи с конкретной теорией, размещение костимулирующего сигнального домена, например, 4-1BB, CD28, CD27 или OX-40, на первом CAR и основного сигнального домена, например, CD3-дзета, на третьем CAR может ограничивать активность CAR только клетками, на которых экспрессированы обе мишени. В одном варианте осуществления клетка по изобретению имеет первый CAR, содержащий антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен и костимулирующий домен, и второй CAR, нацеленный на другой антиген-мишень (например, антиген, экспрессируемый на того же типа раковой клетке, что и первый антиген-мишень) и содержит антигенсвязывающий домен, трансмембранный домен и основной сигнальный домен. В другом варианте осуществления клетка по изобретению имеет (то есть, генетически запрограммирована экспрессировать) первый CAR, содержащий антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен и основной сигнальный домен, и второй CAR, нацеленный на опухолевый антиген, отличный от первого антигена-мишени (например, антиген, экспрессируемый на того же типа раковой клетке, что и первый антиген-мишень) и содержит антигенсвязывающий домен для антигена, трансмембранный домен и костимулирующий сигнальный домен. В другом варианте осуществления клетка по изобретению имеет (то есть, генетически запрограммирована экспрессировать) первый CAR, содержащий антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен, костимулирующий сигнальный домен и основной сигнальный домен, и второй CAR, нацеленный на опухолевый антиген, отличный от первого антигена-мишени (например, антиген, экспрессируемый на того же типа раковой клетке, что и первый антиген-мишень) и содержит антигенсвязывающий домен для антигена, трансмембранный домен, костимулирующий сигнальный домен и основной сигнальный домен. В вариантах осуществления, в которых как первый, так и второй, CAR содержат костимулирующий сигнальный домен, костимулирующие сигнальные домены первого CAR и второго CAR могут быть получены из одного и того же белка, например, из костимулирующего белка, описанного в настоящем документе, например, 4-1BB, CD28, или ICOS. В других вариантах осуществления костимулирующие сигнальные домены первого CAR и второго CAR могут быть получены из разных белков, например, первый CAR содержит костимулирующий сигнальный домен, описанный в настоящем документе, например, из 4-1BB, и второй CAR содержит другой костимулирующий сигнальный домен, описанный в настоящем документе, например, из CD28.
В одном варианте осуществления CAR-экспрессирующая клетка имеет CAR, содержащий антигенсвязывающий домен, который связывает антигены-мишени, описанные в настоящем документе, и ингибирующий CAR. В одном варианте осуществления ингибирующий CAR содержит антигенсвязывающий домен, который связывает антиген, присутствующий на нормальных клетках, но не раковых клетках, например, нормальных клетках, которые также экспрессируют опухолевые антигены, являющиеся мишенью для CAR, содержащего антигенсвязывающий домен, который связывает антиген-мишень. В одном варианте осуществления ингибирующий CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен ингибирующей молекулы. Например, внутриклеточный домен ингибирующего CAR может представлять собой внутриклеточный домен PD-1, PD-L1, CTLA4, TIM3, LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), KIR, A2aR, MHC класса I, MHC класса II, GAL9, аденозина или TGF-бета.
В одном варианте осуществления антигенсвязывающие домены разных CAR могут быть такими, что антигенсвязывающие домены не взаимодействуют друг с другом. Например, клетка, экспрессирующая первый и второй CAR, может содержать антигенсвязывающий домен первого CAR, например, в виде фрагмента, например, scFv, который не связывается с антигенсвязывающим доменом второго CAR, например, антигенсвязывающим доменом второго CAR, представляющим собой VHH.
В некоторых вариантах осуществления антигенсвязывающий домен содержит однодоменные антигенсвязывающие (SDAB) молекулы, включая молекулы, определяющие комплементарность области которых являются частью однодоменного полипептида. Примеры включают, но без ограничения, вариабельные домены тяжелой цепи, связывающие молекулы, естественным образом лишенные легких цепей, одиночные домены, полученные из обычных 4-цепочечных антител, рекомбинантные домены и однодоменные каркасы, отличные от тех, которые получены из антител. Молекулы SDAB могут представлять собой любые известные в данной области или любые полученные в будущем однодоменные молекулы. Молекулы SDAB могут быть получены из любого биологического вида, включая, но без ограничения, мышь, человека, верблюда, ламу, миногу, рыбу, акулу, козу, кролика и крупный рогатый скот. Этот термин также включает природные молекулы однодоменных антител у биологических видов, отличных от верблюдовых и акул.
В одном аспекте молекула SDAB может быть получена из вариабельной области иммуноглобулина, встречающегося у рыб, например, такая, которая получена из изотипа иммуноглобулина, известного как новый антигенный рецептор (NAR), обнаруженного в сыворотке акулы. Способы получения однодоменных молекул, полученных из вариабельной области NAR («IgNAR»), описаны в WO03/014161 и Streltsov (2005) Protein Sci. 14:2901-2909.
В другом аспекте молекула SDAB представляет собой природную однодоменную антигенсвязывающую молекулу, известную как тяжелая цепь, лишенная легких цепей. Такие однодоменные молекулы раскрыты в WO9404678 и Hamers-Casterman, C. et al. (1993) Nature 363:446-448, например. Для ясности, данный вариабельный домен, полученный из молекулы тяжелой цепи, естественным образом лишенной легкой цепи, в настоящем документе называют VHH или нанотелом, чтобы отличать его от обычного VH из четырехцепочечных иммуноглобулинов. Такая молекула VHH может быть получена от животных семейства верблюдовых, таких как верблюд, лама, одногорбый верблюд, альпака и гуанако. И другие биологические виды, помимо верблюдовых, могут продуцировать молекулы тяжелых цепей, естественным образом лишенные легких цепей; такие VHH входят в объем изобретения.
Молекулы SDAB могут быть рекомбинантными, с пересаженными CDR, гуманизированными, верблюжьими, лишенными иммуногенности и/или полученными in vitro (например, отобранными методом фагового дисплея).
Также было установлено, что в случае клеток, имеющих множество химерных погруженных в мембрану рецепторов, содержащих антигенсвязывающие домены, взаимодействие между антигенсвязывающими доменами рецепторов может быть нежелательным, например, поскольку это ингибирует способность одного или более из антигенсвязывающих доменов связывать узнаваемый им антиген. Соответственно, в настоящем документе раскрыты клетки, имеющие первый и второй неприродные химерные погруженные в мембрану рецепторы, содержащие антигенсвязывающие домены, взаимодействие которых сведено к минимуму. В настоящем документе также раскрыты нуклеиновые кислоты, кодирующие первый и второй неприродные химерные погруженные в мембрану рецепторы, содержащие антигенсвязывающие домены, взаимодействие которых сведено к минимуму, а также способы получения и использования таких клеток и нуклеиновых кислот. В одном из вариантов осуществления антигенсвязывающий домен в одном из указанного первого и указанного второго неприродных химерных погруженных в мембрану рецепторов, содержит scFv, а в другом содержит один домен VH, например, один домен VH верблюдовых, акулы или миноги, или один домен VH, полученный из последовательности антитела человека или мыши.
В другом аспекте CAR-экспрессирующая клетка, описанная в настоящем документе, может дополнительно экспрессировать другое средство, например, средство, повышающее активность CAR-экспрессирующей клетки. Например, в одном варианте осуществления средство может представлять собой средство, которое ингибирует ингибирующую молекулу. Ингибирующие молекулы, например, PD-1, в некоторых вариантах осуществления могут снижать способность CAR-экспрессирующей клетки осуществлять иммунный эффекторный ответ. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA4, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), KIR, A2aR, MHC класса I, MHC класса II, GAL9, аденозин и TGF-бета.
В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, например, представляет собой молекулу, описанную в настоящем документе, например, средство, содержащее первый полипептид, например, ингибирующую молекулу, связанный со вторым полипептидом, который передает положительный сигнал клетке, например, внутриклеточному сигнальному домену, описанному в настоящем документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, PD-L1, CTLA4, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), KIR, A2aR, MHC класса I, MHC класса II, GAL9, аденозин и TGF-бета, либо фрагмент любой из них (например, по меньшей мере часть внеклеточного домена любой из них), и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в настоящем документе (например, содержащий костимулирующий домен (например, 41BB, CD27 или CD28, например, описанный в настоящем документе) и/или основной сигнальный домен (например, сигнальный домен CD3-дзета, описанный в настоящем документе)). В одном варианте осуществления средство содержит первый полипептид PD-1 или его фрагмент (например, по меньшей мере часть внеклеточного домена PD-1) и второй полипептид внутриклеточного сигнального домена, описанного в настоящем документе (например, сигнального домена CD28, описанного в настоящем документе, и/или сигнального домена CD3-дзета описанного в настоящем документе). PD-1 является ингибирующим представителем семейства рецепторов CD28, которое также включает CD28, CTLA-4, ICOS и BTLA. PD-1 экспрессируется на активированных B-клетках, T-клетках и миелоидных клетках (Agata et al. 1996 Int. Immunol 8:765-75). Показано, что два лиганда PD-1, PD-L1 и PD-L2, понижающе регулируют активацию T-клеток при связывании с PD-1 (Freeman et al. 2000 J Exp Med 192:1027-34; Latchman et al. 2001 Nat Immunol 2:261-8; Carter et al. 2002 Eur J Immunol 32:634-43). PD-L1 в изобилии присутствует в раковых опухолях человека (Dong et al. 2003 J Mol Med 81:281-7; Blank et al. 2005 Cancer Immunol. Immunother 54:307-314; Konishi et al. 2004 Clin Cancer Res 10:5094). Иммунная супрессия может быть обращена вспять путем ингибирования локального взаимодействия PD-1 с PD-L1.
В одном варианте осуществления средство содержит внеклеточный домен (ECD) ингибирующей молекулы, например, белка программируемой гибели клеток 1 (PD-1), слитый с трансмембранным доменом и внутриклеточным сигнальным доменом, таким как 41BB и CD3-дзета (в настоящем документе также называемый PD-1 CAR). В одном варианте осуществления PD-1 CAR, при использовании в сочетании с XCAR, описанным в настоящем документе, улучшает персистенцию T-клетки. В одном варианте осуществления CAR представляет собой PD-1 CAR, содержащий внеклеточный домен PD-1, подчеркнутый в SEQ ID NO: 26. В одном варианте осуществления PD-1 CAR содержит аминокислотную последовательность SEQ ID NO: 26. В одном варианте осуществления PD-1 CAR содержит аминокислотную последовательность SEQ ID NO: 39.
В одном варианте осуществления средство имеет нуклеотидную последовательность, кодирующую PD-1 CAR, например, PD-1 CAR, описанный в настоящем документе. В одном варианте осуществления нуклеотидная последовательность для PD-1 CAR приведена в SEQ ID NO: 27 в Таблице 1, с подчеркнутой последовательностью для PD-1 ECD.
В другом аспекте настоящее изобретение относится к популяции CAR-экспрессирующих клеток. В некоторых вариантах осуществления популяция CAR-экспрессирующих клеток содержит смесь клеток, экспрессирующих разные CAR. Например, в одном варианте осуществления популяция CAR T-клеток может включать первую клетку, экспрессирующую CAR, содержащий антигенсвязывающий домен для CAR антигена, описанного в настоящем документе, и вторую клетку, экспрессирующую CAR, содержащий другой антигенсвязывающий домен, например, антигенсвязывающий домен для другого антигена, описанного в настоящем документе, например, антигенсвязывающий домен для опухолевого антигена, описанного в настоящем документе, который отличается от опухолевого антигена, связываемого антигенсвязывающим доменом CAR, экспрессируемого первой клеткой. В качестве другого примера, популяция CAR-экспрессирующих клеток может включать первую клетку, экспрессирующую CAR, содержащий антигенсвязывающий домен для опухолевого антигена, описанного в настоящем документе, и вторую клетку, экспрессирующую CAR, содержащий антигенсвязывающий домен для мишени, отличной от опухолевого антигена, описанного в настоящем документе. В одном варианте осуществления популяция CAR-экспрессирующих клеток включает, например, первую клетку, экспрессирующую CAR, содержащий основной внутриклеточный сигнальный домен, и вторую клетку, экспрессирующую CAR, содержащий вторичный сигнальный домен.
В другом аспекте настоящее изобретение относится к популяции клеток, в которой по меньшей мере одна клетка экспрессирует CAR, содержащий антигенсвязывающий домен для опухолевого антигена, описанного в настоящем документе, и вторая клетка экспрессирует другое средство, например, средство, способствующее повышению активности CAR-экспрессирующей клетки. Например, в одном варианте осуществления средство может представлять собой средство, которое ингибирует ингибирующую молекулу. В некоторых вариантах осуществления ингибирующие молекулы, например, PD-1, могут уменьшать способность CAR-экспрессирующей клетки осуществлять иммунный эффекторный ответ. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA4, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), KIR, A2aR, MHC класса I, MHC класса II, GAL9, аденозин и TGF-бета. В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, например, представляет собой молекулу, описанную в настоящем документе, например, средство, содержащее первый полипептид, например, ингибирующую молекулу, связанный со вторым полипептидом, который передает положительный сигнал клетке, например, внутриклеточным сигнальным доменом, описанным в настоящем документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, PD-L1, CTLA4, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, CD80, CD86, B7-H3 (CD276), B7-H4 (VTCN1), HVEM (TNFRSF14 или CD270), KIR, A2aR, MHC класса I, MHC класса II, GAL9, аденозин и TGF-бета, либо фрагмент любой из них, и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в настоящем документе (например, содержащий костимулирующий домен (например, 41BB, CD27, OX40 или CD28, например, описанный в настоящем документе) и/или основной сигнальный домен (например, сигнальный домен CD3-дзета, описанный в настоящем документе)). В одном варианте осуществления средство содержит первый полипептид PD-1 или его фрагмент и второй полипептид внутриклеточного сигнального домена, описанного в настоящем документе (например, сигнального домена CD28, описанного в настоящем документе, и/или сигнального домена CD3-дзета описанного в настоящем документе).
В одном аспекте настоящее изобретение относится к способам, включающим введение популяции CAR-экспрессирующих клеток, например, смеси клеток, экспрессирующих разные CAR, в сочетании с другим средством, например, ингибитором киназы, таким как ингибитор киназы, описанный в настоящем документе. В другом аспекте настоящее изобретение относится к способам, включающим введение популяции клеток, в которой по меньшей мере одна клетка экспрессирует CAR, содержащий антигенсвязывающий домен для опухолевого антигена, описанного в настоящем документе, и вторая клетка экспрессирует другое средство, например, средство, способствующее повышению активности CAR-экспрессирующей клетки, в сочетании с другим средством, например, ингибитором киназы, таким как ингибитор киназы, описанный в настоящем документе.
Иллюстративные молекулы CAR
Молекулы CAR, раскрытые в настоящем документе, могут содержать связывающий домен, который связывается с мишенью, например, мишенью, описанной в настоящем документе; трансмембранный домен, например, трансмембранный домен, описанный в настоящем документе; и внутриклеточный сигнальный домен, например, внутриклеточный домен, описанный в настоящем документе. В вариантах осуществления связывающий домен содержит определяющую комплементарность область 1 тяжелой цепи (HC CDR1), определяющую комплементарность область 2 тяжелой цепи (HC CDR2) и определяющую комплементарность область 3 тяжелой цепи (HC CDR3) связывающего домена тяжелой цепи, описанного в настоящем документе, и/или определяющую комплементарность область 1 легкой цепи (LC CDR1), определяющую комплементарность область 2 легкой цепи (LC CDR2) и определяющую комплементарность область 3 легкой цепи (LC CDR3) связывающего домена легкой цепи, описанного в настоящем документе.
В других вариантах осуществления молекула CAR представляет собой молекулу CD19 CAR, описанного в настоящем документе, например, молекулу CD19 CAR, описанного в US-2015-0283178-A1, например, CTL019. В вариантах осуществления CD19 CAR содержит аминокислотную, или имеет нуклеотидную, последовательность, приведенную в US-2015-0283178-A1, содержание документа включено в настоящий документ посредством ссылки, или последовательность, в значительной степени идентичную ей (например, по меньшей мере на 85%, 90%, 95% или более идентичную ей).
В одном варианте осуществления CAR T-клетка, которая специфически связывается с CD19, имеет USAN обозначение TISAGENLECLEUCEL-T. CTL019 получают путем генетической модификации T-клеток, опосредованной стабильным введением методом трансдукции самоинактивирующегося, репликативно-дефектного лентивирусного (LV) вектора, содержащего трансген CTL019 под контролем промотора EF1-альфа. CTL019 может представлять собой смесь положительных и отрицательных в отношении трансгена T-клеток, которые доставляют в организм субъекта с учетом процентного содержания положительных в отношении трансгена T-клеток.
В одном варианте осуществления молекула CAR19 содержит (например, состоит из) аминокислотную последовательность, приведенную в Таблице 15A или в Таблице 3 в международной патентной публикации № WO2014/153270, поданной 15 марта 2014 г.; содержание которой включено в настоящий документ посредством ссылки. Аминокислотные и нуклеотидные последовательности, кодирующие молекулы CD19 CAR и антигенсвязывающие домены (например, содержащие одну, две, три VH CDR; и одну, две, три VL CDR по системе Kabat или Chothia), приведены в WO2014/153270. В вариантах осуществления CD19 CAR содержит аминокислотную, или имеет нуклеотидную, последовательность, приведенную в WO2014/153270, содержание документа включено в настоящий документ посредством ссылки, или последовательность, в значительной степени идентичную любой из вышеуказанных последовательностей (например, по меньшей мере на 85%, 90%, 95% или более идентичную любой из вышеуказанных последовательностей CD19 CAR). В одном варианте осуществления молекула CAR содержит (например, состоит из) аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 897, 902, 907, 912, 917, 922, 927, 932, 937, 942, 947, 952, 956; или аминокислотную последовательность, имеющую по меньшей мере одну, две, три, четыре, пять, 10, 15, 20 или 30 модификаций (например, замен, например, консервативных замен), но не более 60, 50 или 40 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности, выбранной из любой из SEQ ID NOs: 897, 902, 907, 912, 917, 922, 927, 932, 937, 942, 947, 952, 956; или аминокислотную последовательность, имеющую 85%, 90%, 95%, 96%, 97%, 98%, 99% идентичности с аминокислотной последовательностью, выбранной из любой из SEQ ID NOs: 897, 902, 907, 912, 917, 922, 927, 932, 937, 942, 947, 952, 956.
В одном варианте осуществления родительская последовательность мышиного scFv представляет собой конструкт CAR19, приведенный в PCT публикации WO2012/079000 (содержание которой включено в настоящий документ посредством ссылки) и приведенный в настоящем документе в Таблице 15A. В одном варианте осуществления анти-CD19 связывающий домен представляет собой scFv, описанный в WO2012/079000 и приведенный в настоящем документе в Таблице 15A.
В одном варианте осуществления CD19 CAR содержит аминокислотную последовательность, приведенную в SEQ ID NO: 12 в PCT публикации WO2012/079000. В варианте осуществления аминокислотная последовательность представляет собой:
MALPVTALLLPLALLLHAARPdiqmtqttsslsaslgdrvtiscrasqdiskylnwyqqkpdgtvklliyhtsrlhsgvpsrfsgsgsgtdysltisnleqediatyfcqqgntlpytfgggtkleitggggsggggsggggsevklqesgpglvapsqslsvtctvsgvslpdygvswirqpprkglewlgviwgsettyynsalksrltiikdnsksqvflkmnslqtddtaiyycakhyyyggsyamdywgqgtsvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO: 891), или последовательность, в значительной степени идентичную ей (например, по меньшей мере на 85%, 90% или 95% или более идентичную ей), с содержанием или без содержания последовательности сигнального пептида, обозначенной заглавными буквами.
В варианте осуществления аминокислотная последовательность представляет собой:
diqmtqttsslsaslgdrvtiscrasqdiskylnwyqqkpdgtvklliyhtsrlhsgvpsrfsgsgsgtdysltisnleqediatyfcqqgntlpytfgggtkleitggggsggggsggggsevklqesgpglvapsqslsvtctvsgvslpdygvswirqpprkglewlgviwgsettyynsalksrltiikdnsksqvflkmnslqtddtaiyycakhyyyggsyamdywgqgtsvtvsstttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapaykqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr (SEQ ID NO: 892), или последовательность, в значительной степени гомологичную ей (например, по меньшей мере на 85%, 90% или 95% или более идентичную ей).
В вариантах осуществления молекула CAR представляет собой молекулу CD19 CAR, описанного в настоящем документе, например, молекулу гуманизированного CAR, описанного в настоящем документе, например, молекулу гуманизированного CD19 CAR в Таблице 15A или содержащего области CDR, приведенные в Таблицах 15B и 15C.
В вариантах осуществления молекула CAR представляет собой молекулу CD19 CAR, описанного в настоящем документе, например, молекулу мышиного CAR, описанного в настоящем документе, например, молекулу мышиного CD19 CAR в Таблице 15A или содержащего области CDR, приведенные в Таблицах 15B и 15C.
В некоторых вариантах осуществления молекула CAR содержит одну, две и/или три области CDR из вариабельной области тяжелой цепи, и/или одну, две и/или три области CDR из вариабельной области легкой цепи мышиного или гуманизированного CD19 CAR в Таблицах 15B и 15C.
В одном варианте осуществления антигенсвязывающий домен содержит одну, две, три (например, все три) из областей CDR тяжелой цепи, HC CDR1, HC CDR2 и HC CDR3, из антитела, перечисленного выше, и/или одну, две, три (например, все три) из областей CDR легкой цепи, LC CDR1, LC CDR2 и LC CDR3, из антитела, перечисленного выше. В одном варианте осуществления антигенсвязывающий домен содержит вариабельную область тяжелой цепи и/или вариабельную область легкой цепи антитела, перечисленного или описанного в настоящем документе.
Иллюстративные CD19 CAR включают любой из CD19 CAR или анти-CD19 связывающих доменов, описанных в настоящем документе, например, в одной или более таблицах (например, Таблице 15A), приведенных в настоящем документе (например, или анти-CD19 CAR, описанных в Xu et al. Blood 123,24(2014):3750-9; Kochenderfer et al. Blood 122,25(2013):4129-39, Cruz et al. Blood 122,17(2013):2965-73, NCT00586391, NCT01087294, NCT02456350, NCT00840853, NCT02659943, NCT02650999, NCT02640209, NCT01747486, NCT02546739, NCT02656147, NCT02772198, NCT00709033, NCT02081937, NCT00924326, NCT02735083, NCT02794246, NCT02746952, NCT01593696, NCT02134262, NCT01853631, NCT02443831, NCT02277522, NCT02348216, NCT02614066, NCT02030834, NCT02624258, NCT02625480, NCT02030847, NCT02644655, NCT02349698, NCT02813837, NCT02050347, NCT01683279, NCT02529813, NCT02537977, NCT02799550, NCT02672501, NCT02819583, NCT02028455, NCT01840566, NCT01318317, NCT01864889, NCT02706405, NCT01475058, NCT01430390, NCT02146924, NCT02051257, NCT02431988, NCT01815749, NCT02153580, NCT01865617, NCT02208362, NCT02685670, NCT02535364, NCT02631044, NCT02728882, NCT02735291, NCT01860937, NCT02822326, NCT02737085, NCT02465983, NCT02132624, NCT02782351, NCT01493453, NCT02652910, NCT02247609, NCT01029366, NCT01626495, NCT02721407, NCT01044069, NCT00422383, NCT01680991, NCT02794961, или NCT02456207, содержание каждого из которых включено в настоящий документ посредством ссылки в полном объеме.
Иллюстративные конструкты CD19 CAR и антигенсвязывающего домена, которые могут быть использованы в способах, описанных в настоящем документе, приведены в Таблице 15A. Последовательности областей CDR легкой и тяжелой цепей в соответствии с системой Kabat выделены жирным шрифтом и подчеркнуты, и также приведены в Таблицах 15A-C. Участки сигнальной последовательности и гистидиновой метки также подчеркнуты. В вариантах осуществления последовательности CD19 CAR и их антигенсвязывающих фрагментов не включают сигнальную последовательность и/или последовательность гистидиновой метки.
В вариантах осуществления CD19 CAR содержит анти-CD19 связывающий домен (например, мышиный или гуманизированный анти-CD19 связывающий домен), трансмембранный домен и внутриклеточный сигнальный домен, при этом указанный анти-CD19 связывающий домен содержит определяющую комплементарность область 1 тяжелой цепи (HC CDR1), определяющую комплементарность область 2 тяжелой цепи (HC CDR2) и определяющую комплементарность область 3 тяжелой цепи (HC CDR3) любой из аминокислотных последовательностей анти-CD19 связывающего домена тяжелой цепи, приведенных в Таблице 15A-C, или последовательности, по меньшей мере на 85%, 90%, 95% или более идентичные им (например, имеющие менее 5, 4, 3, 2 или 1 аминокислотных замен, например, консервативных замен).
В одном варианте осуществления анти-CD19 связывающий домен содержит вариабельную область легкой цепи, описанную в настоящем документе (например, в Таблице 15A) и/или вариабельную область тяжелой цепи, описанную в настоящем документе (например, в Таблице 15A), или последовательности, по меньшей мере на 85%, 90%, 95% или более идентичные им.
В одном варианте осуществления закодированный анти-CD19 связывающий домен представляет собой scFv, содержащий легкую цепь и тяжелую цепь с аминокислотными последовательностями, приведенными в Таблице 5, или последовательностями, по меньшей мере на 85%, 90%, 95% или более идентичными им.
В одном из вариантов осуществления человеческий или гуманизированный анти-CD19 связывающий домен (например, scFv) содержит: вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области легкой цепи, приведенной в Таблице 15A, или последовательность, по меньшей мере на 85%, 90%, 95% или более идентичную ей; и/или вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере одну, две или три модификации (например, замены, например, консервативные замены), но не более 30, 20 или 10 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности вариабельной области тяжелой цепи, приведенной в Таблице 15A, или последовательность, по меньшей мере на 85%, 90%, 95% или более идентичную ей.
В одном варианте осуществления молекула CAR содержит антигенсвязывающий домен для CD19 (например, мышиное, человеческое или гуманизированное антитело, или фрагмент антитела, которое специфически связывается с CD19), трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен и/или основной сигнальный домен).
Иллюстративные молекулы CAR19 приведены в Таблице 15A (а также Таблице 7). Молекулы CAR в Таблице 15A содержат антигенсвязывающий домен для CD19, например, аминокислотную последовательность любого антигенсвязывающего домена для CD19, приведенного в Таблице 7 или 10.
Таблица 15A. Иллюстративные молекулы CD19 CAR
домен scFv
CAR1,
Растворимый scFv - нк
CAR1,
Растворимый scFv - ак
CAR1,
Целый - нк
CAR1,
Целый - ак
домен scFv
CAR2,
Растворимый scFv - нк
CAR2,
Растворимый scFv - ак
CAR2,
Целый - нк
CAR2,
Целый - ак
домен scFv
CAR3,
Растворимый scFv - нк
CAR3,
Растворимый scFv - ак
CAR3 - Целый - нк
CAR3,
Целый - ак
домен scFv
CAR4,
Растворимый scFv - нк
CAR4,
Растворимый scFv - ак
CAR4,
Целый - нк
CAR4,
Целый - ак
домен scFv
CAR5,
Растворимый scFv - нк
CAR5,
Растворимый scFv - ак
CAR5,
Целый - нк
CAR5,
Целый - ак
домен scFv
CAR6,
Растворимый scFv - нк
CAR6,
Растворимый scFv - ак
CAR6,
Целый - нк
CAR6,
Целый - ак
домен scFv
CAR7,
Растворимый scFv - нк
CAR7,
Растворимый scFv - ак
CAR7,
Целый - нк
CAR7,
Целый - ак
домен scFv
CAR8,
Растворимый scFv - нк
CAR8,
Растворимый scFv - ак
CAR8,
Целый - нк
CAR8,
Целый - ак
домен scFv
CAR9,
Растворимый scFv - нк
CAR9,
Растворимый scFv - ак
CAR9,
Целый - нк
CAR9,
Целый - ак
домен scFv
CAR10,
Растворимый scFv - нк
CAR10,
Растворимый scFv - ак
CAR10,
Целый - нк
CAR10,
Целый - ак
домен scFv
CAR11,
Растворимый scFv - нк
CAR11,
Растворимый scFv - ак
CAR11,
Целый - нк
CAR11,
Целый - ак
домен scFv
CAR12,
Растворимый scFv - нк
CAR12,
Растворимый scFv - ак
CAR12,
Целый - нк
CAR12,
Целый - ак
Растворимый scFv-His-метка - нк
Растворимый scFv-His-метка - ак
Целый - нк
Целый - ак
домен scFv
scFv
Целый - ак
CAR - ак
Целый - ак
scFv
Целый - ак
последовательность VH
последовательность VL
В некоторых вариантах осуществления CD19 CAR, или связывающий домен, содержит аминокислотную последовательность CTL019, или закодирован нуклеотидной последовательностью CTL019, приведенной в Таблице 5, с содержанием или без содержания лидерной последовательности или гистидиновой метки, или последовательность, в значительной степени идентичную ей (например, по меньшей мере, имеющую 85%, 90%, 95% или более идентичности).
В некоторых вариантах осуществления области CDR указаны в соответствии с системой нумерации Kabat, системой нумерации Chothia, или их сочетанием.
Последовательности гуманизированных областей CDR доменов scFv приведены в Таблице 15B для вариабельных доменов тяжелой цепи и в Таблице 15C для вариабельных доменов легкой цепи. «ID» означает соответствующую SEQ ID NO для каждой CDR.
Таблица 15B. Области CDR вариабельного домена тяжелой цепи (в соответствии с системой нумерации Kabat)
ID
ID
ID
Таблица 15C Области CDR вариабельного домена легкой цепи (в соответствии с системой нумерации Kabat)
ID
ID
ID
В одном варианте осуществления CAR представляет собой молекулу CAR, содержащую антигенсвязывающий домен для BCMA (например, мышиное, человеческое или гуманизированное антитело, или фрагмент антитела, которое специфически связывается с BCMA, например, BCMA человека), трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен и/или основной сигнальный домен).
Иллюстративные молекулы CAR приведены в Таблице 16 или Таблице 1 в WO2016/014565 или также приведены в настоящем документе. Молекулы CAR в Таблице 16 содержат антигенсвязывающий домен для BCMА, например, аминокислотную последовательность любого антигенсвязывающего домена для BCMА, приведенного в Таблице 11 или 12.
Таблица 16. Иллюстративные молекулы CAR. Последовательности приведены с лидерной последовательностью.
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CAR
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
Целый CART
В одном варианте осуществления CAR содержит (например, состоит из) аминокислотную последовательность, приведенную в Таблице 16 или Таблице 1 в WO2016/014565, или приведенную в настоящем документе. В одном варианте осуществления CAR содержит (например, состоит из) аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 789, 791, 793, 795, 797, 799, 801, 803, 805, 807, 809, 811, 813, 815, 817, 819, 821, 823, 825, 827, 829, 831, 833, 835, 837, 839, 841, 843, 845, 847, 849, 851, 853, 855, 857, 859; или аминокислотную последовательность, имеющую по меньшей мере одну, две, три, четыре, пять, 10, 15, 20 или 30 модификаций (например, замен, например, консервативных замен), но не более 60, 50 или 40 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности, выбранной из любой из SEQ ID NOs: 789, 791, 793, 795, 797, 799, 801, 803, 805, 807, 809, 811, 813, 815, 817, 819, 821, 823, 825, 827, 829, 831, 833, 835, 837, 839, 841, 843, 845, 847, 849, 851, 853, 855, 857, 859; или аминокислотную последовательность, имеющую 85%, 90%, 95%, 96%, 97%, 98%, 99% идентичности с аминокислотной последовательностью, выбранной из любой из SEQ ID NOs: 789, 791, 793, 795, 797, 799, 801, 803, 805, 807, 809, 811, 813, 815, 817, 819, 821, 823, 825, 827, 829, 831, 833, 835, 837, 839, 841, 843, 845, 847, 849, 851, 853, 855, 857, 859.
В одном варианте осуществления молекула CAR содержит антигенсвязывающий домен для мезотелина (например, мышиное, человеческое или гуманизированное антитело, или фрагмент антитела, которое специфически связывается с мезотелином), трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен и/или основной сигнальный домен).
Иллюстративные молекулы CAR, нацеленные на мезотелин, описаны в настоящем документе и приведены в Таблице 17. Молекулы CAR в Таблице 17 содержат антигенсвязывающий домен для мезотелина, например, аминокислотную последовательность любого антигенсвязывающего домена для мезотелина, приведенного в Таблице 3. Лидерная последовательность выделена жирным шрифтом и подчеркнута, области CDR подчеркнуты и последовательность линкера между тяжелой и легкой цепями антигенсвязывающей области затенена серым цветом.
Таблица 17. Иллюстративные молекулы CAR
В одном варианте осуществления молекула CAR, которая связывает мезотелин, содержит (например, состоит из) аминокислотную последовательность, приведенную в Таблице 17 или Таблице 2 в международной патентной публикации № WO2015/090230, поданной 19 декабря 2014 г.; содержание которой включено в настоящий документ посредством ссылки. В одном варианте осуществления молекула CAR содержит (например, состоит из) аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 724-748; или аминокислотную последовательность, имеющую по меньшей мере одну, две, три, четыре, пять, 10, 15, 20 или 30 модификаций (например, замен, например, консервативных замен), но не более 60, 50 или 40 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности, выбранной из любой из SEQ ID NOs: 724-748; или аминокислотную последовательность, имеющую 85%, 90%, 95%, 96%, 97%, 98%, 99% идентичности с аминокислотной последовательностью, выбранной из любой из SEQ ID NOs: 724-748.
В одном варианте осуществления молекула CAR содержит антигенсвязывающий домен для EGFRvIII (например, мышиное, человеческое или гуманизированное антитело, или фрагмент антитела, которое специфически связывается с EGFRvIII), трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен и/или основной сигнальный домен).
Иллюстративные молекулы CAR, нацеленные на EGFRvIII, описаны в настоящем документе и приведены в Таблице 18 или в Таблице 2 в WO/2014/130657, или описаны в WO2016/014789.
Таблица 18. Иллюстративные конструкты гуманизированного CAR. Последовательности приведены с лидерной последовательностью и области CDR подчеркнуты. Сокращение «нк» означает нуклеиновую кислоту и «ак» означает аминокислотную последовательность.
Целый - нк
Целый - ак
Целый - нк
Целый - ак
В одном варианте осуществления молекула CAR, который связывает EGFRvIII, содержит (например, состоит из) аминокислотную последовательность, приведенную в Таблице 18. В одном варианте осуществления CAR, который связывает EGFRvIII, содержит (например, состоит из) аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 770, 772, 774, 776, 778, 780, 782, 784, 786, 788; или аминокислотную последовательность, имеющую по меньшей мере одну, две, три, четыре, пять, 10, 15, 20 или 30 модификаций (например, замен, например, консервативных замен), но не более 60, 50 или 40 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности, выбранной из любой из SEQ ID NOs: 770, 772, 774, 776, 778, 780, 782, 784, 786, 788; или аминокислотную последовательность, имеющую 85%, 90%, 95%, 96%, 97%, 98%, 99% идентичности с аминокислотной последовательностью, выбранной из любой из SEQ ID NOs: 770, 772, 774, 776, 778, 780, 782, 784, 786, 788.
В одном варианте осуществления молекула CAR содержит антигенсвязывающий домен для CD123 (например, мышиное, человеческое или гуманизированное антитело, или фрагмент антитела, которое специфически связывается с CD123), трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен и/или основной сигнальный домен). Иллюстративные молекулы CAR, нацеленные на CD123, включают те, которые приведены в Таблице 19, и те, которые приведены в Таблицах 2, 6 и 9 в WO2016/028896. Другие иллюстративные молекулы CAR, которые направлены на CD123, описаны в WO/2014/130635 (например, Таблице 1 в WO/2014/130635). Другие иллюстративные молекулы CAR, которые направлены на CD123, описаны в WO/2014/144622.
В одном варианте осуществления молекула CAR, который связывает CD123, содержит (например, состоит из) аминокислотную последовательность, приведенную в Таблице 19. В одном варианте осуществления CAR, который связывает CD123, содержит (например, состоит из) аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 750, 755, 760, 765; или аминокислотную последовательность, имеющую по меньшей мере одну, две, три, четыре, пять, 10, 15, 20 или 30 модификаций (например, замен, например, консервативных замен), но не более 60, 50 или 40 модификаций (например, замен, например, консервативных замен) аминокислотной последовательности, выбранной из любой из SEQ ID NOs: 750, 755, 760, 765; или аминокислотную последовательность, имеющую 85%, 90%, 95%, 96%, 97%, 98%, 99% идентичности с аминокислотной последовательностью, выбранной из любой из SEQ ID NOs: 750, 755, 760, 765.
Таблица 19. Иллюстративные последовательности CAR
scFv
VH
VL
scFv
VH
VL
scFv
VH
VL
scFv
VH
VL
В одном варианте осуществления молекула CAR содержит антигенсвязывающий домен для CD33 (например, мышиное, человеческое или гуманизированное антитело, или фрагмент антитела, которое специфически связывается с CD33), трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен и/или основной сигнальный домен). Иллюстративные молекулы CAR, нацеленные на CD33, описаны в настоящем документе и приведены в WO2016/014576, например, в Таблице 2 в WO2016/014576.
В одном варианте осуществления молекула CAR содержит антигенсвязывающий домен для CLL-1 (например, мышиное, человеческое или гуманизированное антитело, или фрагмент антитела, которое специфически связывается с CLL-1), трансмембранный домен и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, содержащий костимулирующий домен и/или основной сигнальный домен). Иллюстративные молекулы CAR, нацеленные на CLL-1, описаны в настоящем документе и приведены в WO/2016/014535, например, в Таблице 2 в WO2016/014535.
CAR с компонентами рецептора клеток - естественных киллеров (NKR)
В одном из вариантов осуществления молекула CAR, описанная в настоящем документе, содержит один или более компонентов рецептора клетки - естественного киллера (NKR). Компонент NKR может представлять собой трансмембранный домен, шарнирный домен или цитоплазматический домен из любого из следующих рецепторов клетки - естественного киллера: иммуноглобулиноподобного рецептора клетки - естественного киллера (KIR), например, KIR2DL1, KIR2DL2/L3, KIR2DL4, KIR2DL5A, KIR2DL5B, KIR2DS1, KIR2DS2, KIR2DS3, KIR2DS4, DIR2DS5, KIR3DL1/S1, KIR3DL2, KIR3DL3, KIR2DP1 и KIR3DP1; опосредующего цитотоксичность рецептора клетки - естественного киллера (NCR), например, NKp30, NKp44, NKp46; семейства сигнальных молекул активации лимфоцитов (SLAM) рецепторов иммунных клеток, например, CD48, CD229, 2B4, CD84, NTB-A, CRACC, BLAME и CD2F-10; Fc-рецептора (FcR), например, CD16 и CD64; а также рецепторов Ly49, например, LY49A, LY49C. Молекулы CAR, содержащие компоненты NKR, описанные в настоящем документе, могут взаимодействовать с молекулой адаптера или внутриклеточным сигнальным доменом, например, DAP12. Иллюстративные конфигурации и последовательности молекул CAR, содержащих элементы NKR, описаны в международной патентной публикации № WO2014/145252, содержание которой включено в настоящий документ посредством ссылки.
Расщепленный CAR
В некоторых вариантах осуществления в CAR-экспрессирующей клетке, описанной в настоящем документе, используют расщепленный CAR. Подход с использованием расщепленного CAR более подробно описан в патентных публикациях WO2014/055442 и WO2014/055657, содержание которых включено в настоящий документ посредством ссылки. Вкратце, система расщепленного CAR включает клетку, экспрессирующую первый CAR, содержащий первый антигенсвязывающий домен и костимулирующий домен (например, 41BB), при этом клетка также экспрессирует второй CAR, содержащий второй антигенсвязывающий домен и внутриклеточный сигнальный домен (например, CD3-дзета). Когда клетка встречается с первым антигеном, костимулирующий домен активируется, и клетка пролиферирует. Когда клетка встречается со вторым антигеном, внутриклеточный сигнальный домен активируется, и запускается цитолитическая активность. Таким образом, CAR-экспрессирующая клетка полностью активируется лишь в присутствии обоих антигенов. В вариантах осуществления первый антигенсвязывающий домен узнает антиген, описанный в настоящем документе, например, представляет собой антигенсвязывающий домен, описанный в настоящем документе, и второй антигенсвязывающий домен узнает второй антиген, описанный в настоящем документе.
Иллюстративные характеристики временно экспрессируемых CAR по изобретению
В некоторых вариантах осуществления полезно, если антигенсвязывающий домен функционально связан с другим доменом CAR, таким как трансмембранный домен или внутриклеточный домен, оба из которых описаны в других разделах настоящего документа, для экспрессии в клетке. В одном варианте осуществления нуклеиновая кислота, кодирующая антигенсвязывающий домен, функционально связана с нуклеиновой кислотой, кодирующей трансмембранный домен, и нуклеиновой кислотой, кодирующей внутриклеточный домен.
Между антигенсвязывающим доменом и трансмембранным доменом CAR, или между внутриклеточным доменом и трансмембранным доменом CAR может быть вставлен спейсерный домен. Используемый в настоящем документе термин «спейсерный домен», как правило, означает любой олиго- или полипептид, который связывает трансмембранный домен либо с антигенсвязывающим доменом, либо внутриклеточным доменом в полипептидной цепи. В одном варианте осуществления спейсерный домен может содержать до 300 аминокислот, предпочтительно 10-100 аминокислот и наиболее предпочтительно 25-50 аминокислот. В другом варианте осуществления короткий олиго- или полипептидный линкер, предпочтительно длиной от 2 до 10 аминокислот может связывать трансмембранный домен и внутриклеточный домен CAR. Пример линкера включает дублет глицин-серин.
В некоторых вариантах осуществления CAR также содержит сигнальный пептид. В одном варианте осуществления сигнальный пептид содержит нуклеотидную последовательность, содержащую ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCG или SEQ ID NO: 3034. В другом варианте осуществления сигнальный пептид содержит аминокислотную последовательность, содержащую MALPVTALLLPLALLLHAARP или SEQ ID NO: 3035.
В некоторых вариантах осуществления CAR также содержит домен димеризации, такой как домен димеризации из FKBP или аналогичной молекулы. В таком варианте осуществления присутствие молекул CAR на поверхности модифицированной T-клетки предотвращается вследствие спонтанной агрегации молекул CAR в цитоплазме или других внутренних зонах в клетке.
В другом варианте осуществления домен димеризации содержит нуклеотидную последовательность, содержащую CGGGGCGTGCAGGTTGAGACAATTTCCCCAGGAGATGGGCGAACGTTCCCCAAGCGCGGACAGACATGCGTTGTGCACTACACAGGAATGTTGGAGGACGGAAAGAAAATGGACAGTTCAAGAGATCGGAACAAACCATTCAAATTCATGTTGGGAAAACAGGAAGTGATACGGGGCTGGGAAGAGGGTGTAGCGCAAATGTCCGTTGGTCAACGAGCAAAACTCACGATAAGTCCCGATTATGCTTACGGCGCAACCGGTCACCCGGGCATCATACCGCCTCATGCGACTTTGGTCTTTGATGTGGAGCTGTTGAAACTTGAAACTCGCGGAGTACAGGTTGAAACAATATCACCCGGGGACGGGCGGACTTTTCCGAAGAGAGGTCAGACCTGCGTCGTCCATTATACCGGTATGCTGGAGGACGGAAAGAAAATGGACAGCTCACGGGACCGAAATAAACCATTCAAATTTATGTTGGGGAAACAAGAGGTTATCAGGGGCTGGGAGGAGGGTGTGGCCCAGATGTCTGTCGGTCAGCGCGCGAAACTCACAATCTCTCCGGATTATGCGTATGGGGCGACAGGGCATCCGGGAATTATCCCTCCCCACGCTACCTTGGTTTTCGATGTTGAGCTTCTGAAGTTGGAGACCAGAGGAGTTCAAGTGGAGACAATATCTCCTGGGGATGGACGGACGTTCCCCAAGCGCGGCCAGACCTGTGTAGTCCACTACACAGGGATGCTTGAAGACGGAAAAAAGATGGATAGCAGTAGAGATCGCAACAAACCATTTAAGTTCATGCTGGGGAAGCAGGAAGTAATACGCGGCTGGGAGGAAGGCGTGGCACAGATGAGTGTTGGTCAACGGGCCAAACTTACTATTTCTCCCGATTATGCGTATGGAGCCACCGGGCACCCTGGCATTATCCCACCCCATGCCACATTGGTTTTTGACGTTGAATTGCTTAAATTGGAGACCAGGGGAGTCCAAGTGGAAACAATATCACCGGGGGATGGTCGGACTTTTCCTAAAAGGGGCCAAACCTGTGTAGTCCATTATACCGGAATGCTCGAAGACGGAAAGAAAATGGACTCTTCTAGAGACCGCAATAAGCCCTTCAAGTTCATGTTGGGTAAGCAAGAGGTGATCCGGGGCTGGGAAGAGGGGGTCGCTCAAATGTCCGTCGGTCAGCGAGCTAAACTGACTATTTCCCCAGACTACGCATATGGAGCGACTGGCCACCCCGGTATTATTCCTCCCCATGCGACTCTCGTGTTCGACGTAGAACTCTTGAAATTGGAAACG или SEQ ID NO: 3015.
В другом таком варианте осуществления домен димеризации содержит аминокислотную последовательность, содержащую RGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLET или SEQ ID NO: 980 (приведенную в другом разделе настоящего документа).
Солюбилизация доменов димеризации при помощи солюбилизирующего средства, введенного в клетку или животному, содержащему клетку, предотвращает димеризацию и позволяет конструкту выходить через секреторную систему, где он процессируется путем расщепления фурином, с экспрессией функционального CAR на клеточной поверхности.
В присутствии солюбилизирующего средства молекулы CAR разделены, и агрегация предотвращается. Введение солюбилизирующего средства предотвращает димеризацию или агрегацию молекул CAR и позволяет молекулам CAR быть представленными на поверхности T-клетки. В одном варианте осуществления сайт расщепления фурина содержит нуклеотидную последовательность, содержащую TCAGCCCGGAACAGGCGGAAGAGA или SEQ ID NO: 3016. В другом варианте осуществления сайт расщепления фурина содержит аминокислотную последовательность SARNRRKR или SEQ ID NO: 3017.
Композиция
В одном варианте осуществления изобретение относится к выделенной нуклеотидной последовательности, содержащей нуклеотидную последовательность, включающую суицидный ген, содержащий нуклеотидную последовательность, выбранную из группы, состоящей из SEQ ID NOs: 3001-3004; и нуклеотидную последовательность, кодирующую CAR, содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен. В некоторых вариантах осуществления выделенная нуклеотидная последовательность содержит SEQ ID NO: 3018, 3020, 3024, 3026, 3028 или 3030.
В одном варианте осуществления изобретение относится к выделенному полипептиду, содержащему аминокислотную последовательность, закодированную суицидным геном, при этом аминокислотную последовательность выбирают из группы, состоящей из SEQ ID NOs: 3005-3007; и CAR, содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен. В некоторых вариантах осуществления выделенный полипептид содержит аминокислотную последовательность SEQ ID NO: 3019, 3021, 3026, 3028, 3030 или 3034.
В другом варианте осуществления изобретение относится к выделенной нуклеотидной последовательности, содержащей нуклеиновую кислоту, кодирующую домен димеризации, и CAR, содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен. В некоторых вариантах осуществления домен димеризации содержит аминокислотную последовательность SEQ ID NO: 980. В других вариантах осуществления выделенная нуклеотидная последовательность содержит SEQ ID NO: 977 или 3032.
В другом варианте осуществления изобретение относится к выделенному полипептиду, содержащему домен димеризации и CAR, содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен. В некоторых вариантах осуществления выделенный полипептид содержит аминокислотную последовательность SEQ ID NO: 978 или 3033.
Сигнальный пептид
В некоторых предпочтительных вариантах осуществления слитые белки по изобретению также содержат сигнальный пептид. Сигнальные пептиды полезны, если нужно, чтобы белок проходил по секреторному пути. В предпочтительных вариантах осуществления данный сигнальный пептид будет сконструирован для присутствия на крайнем N-конце слитого белка. Иллюстративные сигнальные пептиды приведены ниже:
CD8: MALPVTALLLPLALLLHAARP (SEQ ID NO: 2)
GMCSFR: MLLLVTSLLLCELPHPAFLLIP (SEQ ID NO: 43)
IL2: MYRMQLLSCIALSLALVTNS (SEQ ID NO: 44)
Ig Κ-цепь: MAQVKLQESGTELAKPGAAVK (SEQ ID NO: 45)
NPC2: MRFLAATFLLLALSTAAQA (SEQ ID NO: 46)
LAMB1: MGLLQLLAFSFLALCRARVRA (SEQ ID NO: 1114)
P3IP1: MLLAWVQAFLVSNMLLAEAYG (SEQ ID NO: 1115)
DMKN: MKFQGPLACLLLALCLGSGEA (SEQ ID NO: 1116)
TPA: MDAMKRGLCCVLLLCGAVFVSP (SEQ ID NO: 1117)
PCSK9: MGTVSSRRSWWPLPLLLLLLLLLGPAGARAQEDED (SEQ ID NO: 1118)
KDEL (SEQ ID NO: 47) или KKXX и производные на крайнем C-конце интересующего белка могут быть спроектированы, если интересующий белок представляет собой ЭР-резидентный белок. Эти последовательности должны быть включены вместе с сигнальным пептидом.
Интересующие белки могут быть сконструированы так, чтобы иметь схемы гликозилирования для интернализации через манноза-6-фосфатный рецептор и направления в эндосомную/лизосомную систему. Они должны быть включены в сам интересующий белок, если он представляет собой белок, постоянно присутствующий в данном компартменте. Консенсусная последовательность для N-гликозилирования представляет собой Asn-X-Ser/Thr, где X является любой аминокислотой, за исключением пролина (Pro), серина (Ser) и треонина (Thr).
В вариантах осуществления, в которых нужно, чтобы интересующие белки были направлены в пероксисому, слитый белок может быть сконструирован для содержания C-концевого направляющего в пероксисому сигнала (например, PTS1: -SKL).
Сайты расщепления
Каждый слитый белок по изобретению содержит сайт расщепления. Сайт расщепления может представлять собой сайт саморасщепления и/или сайт расщепления протеазы. Сайт расщепления может быть предназначен для расщепления любой сайт-специфической протеазой, которая экспрессируется в интересующей клетке (в результате либо рекомбинантной экспрессии, либо эндогенной экспрессии) на уровне, достаточном для отщепления домена условной экспрессии, например, домена деградации или домена агрегации. В важных аспектах изобретения сайт расщепления протеазы выбирают так, чтобы он соответствовал протеазе, естественным образом (или вследствие генетической модификации клетки) присутствующей в клеточной компартменте, связанном с экспрессией интересующего белка. То есть, внутриклеточная направленная миграция протеазы должна перекрываться, или частично перекрываться, с внутриклеточной направленной миграцией интересующего белка, содержащего используемый домен условной экспрессии, например, домен деградации или домен агрегации. Например, если интересующий белок находится на клеточной поверхности, фермент для его расщепления может быть добавлен в клетку экзогенно.
Если интересующий белок находится в эндосомной/лизосомной системе, можно использовать сайт расщепления протеазы для фермента, постоянно присутствующего в данных компартментах. Такие мотивы для протеазы/консенсусные мотивы включают, например,
Фурин: консенсусный мотив RX(K/R)R
PCSK1: консенсусный мотив RX(K/R)R
PCSK5: консенсусный мотив RX(K/R)R
PCSK6: консенсусный мотив RX(K/R)R
PCSK7: консенсусный мотив RXXX[KR]R
Катепсин B: RRX
Гранзим B: I-E-P-D-X (SEQ ID NO: 35)
Фактор XA: Ile-Glu/Asp-Gly-Arg
Энтерокиназа: Asp-Asp-Asp-Asp-Lys (SEQ ID NO: 36)
Гененаза: Pro-Gly-Ala-Ala-His-Tyr (SEQ ID NO: 37)
Сортаза: LPXTG/A
PreScission протеаза: Leu-Glu-Val-Phe-Gln-Gly-Pro (SEQ ID NO: 38)
Тромбин: Leu-Val-Pro-Arg-Gly-Ser (SEQ ID NO: 40)
TEV-протеаза: E-N-L-Y-F-Q-G (SEQ ID NO: 41)
Эластаза 1: [AGSV]-x (SEQ ID NO: 42).
В некоторых вариантах осуществления слитый белок, описанный в настоящем документе, содержит сайт расщепления фурина. В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат любой из сайтов расщепления фурина, приведенных в Таблице 20.
В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из RTKR (SEQ ID NO: 123) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; LQWLEQQVAKRRTKR (SEQ ID NO: 129) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; GTGAEDPRPSRKRRSLG (SEQ ID NO: 133) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; SLNLTESHNSRKKR (SEQ ID NO: 135) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней; или CKINGYPKRGRKRR (SEQ ID NO: 137) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней.
В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135) или CKINGYPKRGRKRR (SEQ ID NO: 137).
В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней, или GTGAEDPRPSRKRR (SEQ ID NO: 127) или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней.
В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина, выбранный из GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125) или GTGAEDPRPSRKRR (SEQ ID NO: 127).
В некоторых вариантах осуществления слитые белки, описанные в настоящем документе, содержат сайт расщепления фурина GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125).
Таблица 20. Иллюстративные сайты расщепления фурина
ДОМЕНЫ УСЛОВНОЙ ЭКСПРЕССИИ
Слитый белок по изобретению может содержать домен условной экспрессии. В некоторых вариантах осуществления домен условной экспрессии имеет первое состояние и второе состояние, например, состояния агрегации или конформационные состояния, например, состояния стабилизации/дестабилизации или состояния правильного/неправильного сворачивания. Первое состояние связано с, является причиной, или опосредует клеточную поверхностную экспрессию или внеклеточную экспрессию одного или более (например, всех) фрагментов слитого белка в первой степени, или на первом уровне, и второе состояние связано с, является причиной, или опосредует клеточную поверхностную экспрессию или внеклеточную экспрессию одного или более (например, всех) фрагментов слитого белка во второй степени, или на втором уровне. В одном из вариантов осуществления второе состояние характеризуется уровнем или степенью, которые больше, например, в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз больше, чем степень или уровень в первом состоянии. В одном из вариантов осуществления одно из состояний, например, второе состояние, связано с, поддерживается, или вызвано присутствием экспрессионного соединения. В одном из вариантов осуществления присутствие экспрессионного соединения может быть связано с, вызывать или опосредовать изменение физического свойства, например, второе состояние связано с изменением уровня физического свойства, например, присутствие экспрессионного соединения связано с, вызывает или опосредует переход из первого состояния с первой величиной физического свойства во второе состояние со второй величиной физического свойства, например, при этом свойство может включать молекулярную массу, стабильность, поглощение на выбранной длине волны, способность к взаимодействию с другой молекулой или растворимость. В одном из вариантов осуществления присутствие экспрессионного соединения может быть связано с, вызывать или опосредовать переход из первого состояния сворачивания во второе состояние сворачивания, например, из состояния неправильного сворачивания в состояние более правильного сворачивания, например, из первого состояния, подверженного деградации, во второе состояние, менее подверженное деградации, чем первое состояние; или из первого состояния сворачивания, которое характеризуется первым уровнем деградации, во второе состояние сворачивания, которое характеризуется вторым, меньшим, уровнем деградации, например, в интересующей клетке. В одном из вариантов осуществления присутствие экспрессионного соединения может быть связано с, вызывать или опосредовать диссоциацию или дезагрегацию первого и второго доменов условной экспрессии, например, из ассоциации более высокого порядка в ассоциацию более низкого порядка, например, из димеров в мономеры, или из тетрамеров в структуры более низкого порядка, например, димеры или мономеры. В одном из вариантов осуществления присутствие экспрессионного соединения может быть связано с, вызывать или опосредовать изменение растворимости, например, второе состояние связано с более высоким уровнем растворимости, например, присутствие экспрессионного соединения связано с, вызывает или опосредует переход из первого состояния с более низкой растворимостью во второе состояние с более высокой растворимостью. В одном из вариантов осуществления присутствие экспрессионного соединения может быть связано с, вызывать или опосредовать переход из первого состояния локализации или компартментализации одного или более, или всех фрагментов слитого белка во второе состояние локализации или компартментализации одного или более, или всех фрагментов слитого белка, например, из аппарата Гольджи или ЭР в другой компартмент или зону локализации, например, цитозоль, мембрану, клеточную поверхность или внеклеточное пространство.
В одном из вариантов осуществления присутствие экспрессионного соединения может быть связано с, вызывать или опосредовать переход из первого состояния сворачивания во второе состояние сворачивания, например, из состояния неправильного сворачивания в состояние более правильного сворачивания, например, из первого состояния, подверженного деградации, во второе состояние, менее подверженное деградации, чем первое состояние; или из первого состояния сворачивания, которое характеризуется первым уровнем деградации, во второе состояние сворачивания, которое характеризуется вторым, меньшим, уровнем деградации, например, в интересующей клетке.
В одном из вариантов осуществления одно из состояний, например, второе состояние, связано с, вызывает или опосредует расщепление в сайте расщепления. Без связи с конкретной теорией, считается, что в некоторых вариантах осуществления расщепление приводит к, или связано с клеточной поверхностной экспрессией или внеклеточной экспрессией одного или более (например, всех) фрагментов слитого белка. В одном из вариантов осуществления в отсутствие экспрессионного соединения при экспрессии в интересующей клетке слитый белок, например, на первом уровне, например, большая часть слитого белка, содержащего домен условной экспрессии, не поддается обнаружению ни на клеточной поверхности, ни вне клетки, например, вследствие стерического препятствия расщеплению, создаваемого другим фрагментом, например, доменом условной экспрессии. И наоборот, в присутствии экспрессионного соединения поверхностная экспрессия и/или внеклеточная экспрессия одного или более (например, всех) доменов слитого белка переходит на второй уровень, который выше, чем первый уровень, например, значительно выше, например, в 2, 3, 4, 5 или 10 раз выше, чем первый уровень, или больше, например, по меньшей мере на 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 300, 400, 500, 600, 700, 800, 900 или 1000% больше, чем первый уровень. Таким образом, в одном из вариантов осуществления домен условной экспрессии обладает следующими характеристиками: (1) он не присутствует естественным образом в контексте слитого белка, например, он является рекомбинантным или сконструированным; (2) поверхностная экспрессия и/или внеклеточная экспрессия регулируется котрансляционно или посттрансляционно; (3) степень поверхностной экспрессии и/или внеклеточной экспрессии существенно возрастает в присутствии экспрессионного соединения.
В одном из вариантов осуществления добавление экспрессионного соединения, например, дезагрегирующего соединения или стабилизирующего соединения, к популяции клеток, например, клеток-хозяев или клеток, содержащих слитые белки, описанные в настоящем документе, вызывает переход субпопуляции клеток из первого состояния во второе состояние, например, состояния агрегации или конформационные состояния, например, состояния стабилизации/дестабилизации или состояния правильного/неправильного сворачивания, описанные в настоящем документе. В одном из вариантов осуществления в отсутствие экспрессионного соединения, например, дезагрегирующего соединения или стабилизирующего соединения, менее 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1% клеток в популяции имеют второе состояние, и более, или ровно, 90, 91, 92, 93, 94, 95, 96, 97, 98 или 99% клеток в популяции имеют первое состояние. В одном из вариантов осуществления в присутствии экспрессионного соединения, например, дезагрегирующего соединения или стабилизирующего соединения, более, или ровно, 20, 30, 40, 50, 60, 70, 80, 90, или 95% клеток в популяции имеют второе состояние, и менее 20, 15, 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1% клеток в популяции имеют первое состояние. Процентную долю клеток в популяции, имеющих определенное состояние, можно определять с использованием методов, описанных в спецификации, например, на Фигуре 4.
В вариантах осуществления домен условной экспрессии представляет собой домен деградации, например, описанный в настоящем документе. В других вариантах осуществления домен условной экспрессии представляет собой домен агрегации, например, описанный в настоящем документе. В одном из вариантов осуществления домен условной экспрессии не содержит домен деградации. В одном из вариантов осуществления домен условной экспрессии не содержит домен агрегации. В вариантах осуществления слитый белок, содержащий домен условной экспрессии, содержит трансмембранный белок, например, химерный антигенный рецептор (CAR), например, описанный в настоящем документе. В некоторых вариантах осуществления домен условной экспрессии представляет собой домен деградации. В некоторых вариантах осуществления домен условной экспрессии представляет собой домен агрегации.
Домены агрегации
В некоторых вариантах осуществления домен условной экспрессии представляет собой домен агрегации. Способы получения доменов агрегации, вызывающих внутриклеточную агрегацию в отсутствие экспрессионного соединения, например, дезагрегирующего соединения, известны в данной области и описаны более подробно ниже.
Настоящее изобретение охватывает домены агрегации, полученные из любого природного белка. Предпочтительно, слитые белки по изобретению будут содержать домен агрегации, для которого никакое дезагрегирующее соединение не экспрессируется естественным образом или не присутствует в клеточных компартментах интересующей клетки. Например, если слитый белок предназначен для экспрессии в T-клетках, предпочтительно выбирать домен агрегации, который составляет пару с дезагрегирующим соединением, не присутствующим естественным образом в T-клетках. Таким образом, домен агрегации при экспрессии в интересующей клетке будет дезагрегирован лишь в присутствии дезагрегирующего соединения. Примечательно, что это свойство может быть достигнуто либо за счет модифицирования домена агрегации для утраты связывания естественным образом экспрессируемого/присутствующего дезагрегирующего соединения (в этом случае домен агрегации будет дезагрегирован лишь в присутствии синтетического соединения), либо за счет экспрессии домена агрегации в компартменте, где отсутствует естественным образом экспрессируемый/присутствующий лиганд (например, домен агрегации может быть получен от биологического вида, отличного от вида, в организме которого слитый белок будет экспрессироваться).
Пары домен агрегации-дезагрегирующее соединение могут быть получены из любого природного или синтетического белка. Дезагрегирующие соединения могут представлять собой любые природные или синтетические соединения. В конкретных вариантах осуществления дезагрегирующие соединения будут представлять собой существующие отпускаемые по рецепту или без рецепта лекарственные средства. Примеры белков, которые могут быть модифицированы, чтобы обладать свойствами домена агрегации, приведены ниже наряду с соответствующими дезагрегирующими соединениями.
В одном варианте осуществления домен агрегации представляет собой домен димеризации, например, получен из белка FKB (FKBP). В некоторых вариантах осуществления домен агрегации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 975 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней, или SEQ ID NO: 976 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления домен агрегации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 979 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней, или SEQ ID NO: 980 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. Если домен агрегации получен из FKBP, дезагрегирующее соединение может быть выбрано из AP21998 или AP22542, известных в данной области и описанных в Rollins et al. 2000, PNAS vol. 97 no. 13, 7096-7101, WO/2000/023600, и Rivera, V. M., et al. (2000) Regulation of protein secretion through controlled aggregation in the endoplasmic reticulum. Science 287:826-30. Каждый из этих литературных источников включен посредством ссылки в полном объеме. Без связи с конкретной теорией, домены FKBP, имеющие замены F36M, объединяются в димеры. Димеры FKBP F36M могут быть диссоциированы, например, дезагрегированы, путем добавления лиганда, например, FK506, рапамицина, AP22542, AP21998 или Shield-1.
GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKFDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO: 975)
GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLE (SEQ ID NO: 976)
RGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKFDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLET (SEQ ID NO: 979)
RGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLET (SEQ ID NO: 980).
В другом варианте осуществления домен агрегации получен из белка UVR8. UVR8 представляет собой растительный фоторецепторный белок (Chen et al. 2013. J. Cell. Biol. v201 no. 4:631-640; Rizzini, L., et al. 2011. Science. 332:103-106; Christie, J.M., et al. 2012. Science. 335:1492-1496; Wu, D., et al. 2012. Nature. 484:214-219). Каждый из этих литературных источников включен посредством ссылки в полном объеме. UVR8 конститутивно образует фотолабильные гомодимеры, которые диссоциируют при поглощении ультрафиолетового излучения B (UVB) (280-320 нм). В одном из вариантов осуществления домен агрегации получен из домена UVR8, и дезагрегирующее соединение представляет собой соответствующую дозу UVB излучения. В одном из вариантов осуществления соответствующая доза UVB излучения является достаточной для диссоциации по меньшей мере 25, 50, 75 или 100% гомодимеров UVR8. В одном из вариантов осуществления соответствующая доза UVB является минимально токсичной для клетки, содержащей слитый белок.
В некоторых вариантах осуществления слитый белок по настоящему изобретению содержит множество, например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более, копий домена условной экспрессии, например, домена агрегации или домена деградации. В некоторых вариантах осуществления слитый белок по настоящему изобретению содержит множество, например, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более, доменов агрегации.
В некоторых вариантах осуществления каждый из множества доменов агрегации представляет собой копию одного и того же домена агрегации. Такие домены агрегации будут связываться друг с другом, образуя гомоолигомеры, например, гомодимеры.
В некоторых вариантах осуществления слитый белок по настоящему изобретению содержит множество, например, более одного, доменов агрегации, при этом множество включает домены агрегации более, чем одного типа, например, первого типа и второго типа. В некоторых вариантах осуществления домен агрегации первого типа соединяется, например, связывается, и стимулирует олигомеризацию или агрегацию, с доменом агрегации второго типа; такая ассоциация представляет собой гетеромерную ассоциацию или гетероолигомеризацию доменов агрегации, например, в гетеродимеры. В некоторых вариантах осуществления слитый белок по настоящему изобретению содержит два, четыре, шесть или восемь доменов агрегации, при этом слитый белок содержит по меньшей мере один домен агрегации каждого типа, например, первого типа и второго типа. В одном варианте осуществления слитый белок, содержащий множество доменов агрегации, при этом множество включает домены агрегации более, чем одного типа, например, первого типа и второго типа, содержит одинаковые количества доменов агрегации каждого типа. В некоторых вариантах осуществления, в которых слитый белок содержит четыре или более (например, шесть, восемь, десять или более) доменов агрегации, домены агрегации расположены в чередующемся порядке в слитом белке, например, домены 1 типа, 2 типа, 1 типа, 2 типа. В некоторых вариантах осуществления, в которых слитый белок содержит четыре или более (например, шесть, восемь, десять или более) доменов агрегации, домены агрегации расположены блоками в слитом белке, например, домены 1 типа, 1 типа, 2 типа, 2 типа. В некоторых вариантах осуществления домен агрегации первого типа ощутимо не объединяется с другими копиями домена агрегации первого типа, и домен агрегации второго типа ощутимо не объединяется с другими копиями домена агрегации второго типа. В некоторых вариантах осуществления домен агрегации первого типа лишь заметно объединяется с другими копиями домена агрегации первого типа, и домен агрегации второго типа лишь заметно объединяется с другими копиями домена агрегации второго типа.
В некоторых вариантах осуществления экспрессионное соединение, например, дезагрегирующее соединение, представляет собой AP21998 или AP22542 (химические структуры приведены в настоящем документе; AP21998 и AP22542 являются одинаковыми в части, расположенной слева от пунктирной линии, и отличаются в части, расположенной справа от пунктирной линии). Получение и применение AP21998 и AP22542 известно в данной области и описано в Rollins et al. 2000, Amara, J. F., et al. (1997) Proc. Natl. Acad. Sci. USA 94, 10618-10623, Clackson, T., et al. (1998) Proc. Natl. Acad. Sci. USA 95, 10437-10442 и Yang, W., et al. (2000) J. Med. Chem. 43, 1135-1142. Каждый из этих литературных источников включен посредством ссылки в полном объеме.
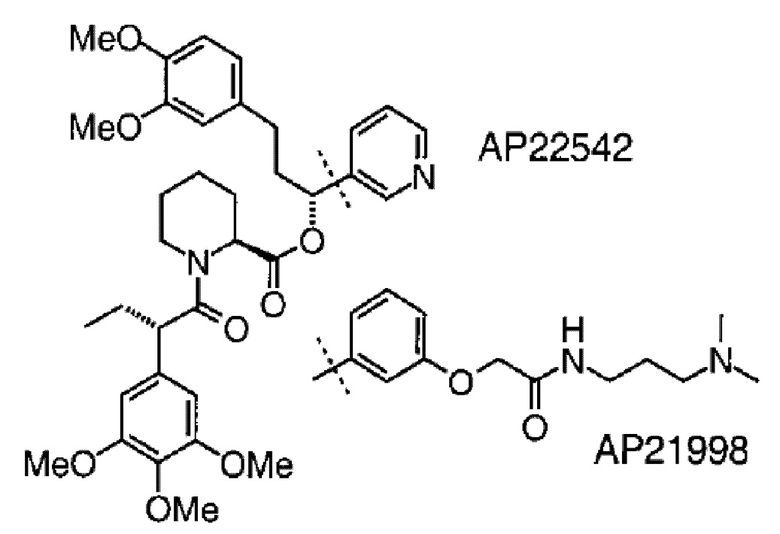
В некоторых вариантах осуществления экспрессионное соединение, например, дезагрегирующее соединение, представляет собой FK506 (такролимус) или рапамицин (сиролимус). В некоторых вариантах осуществления домен условной экспрессии, например, домен агрегации, получен из FKBP, и экспрессионное соединение, например, дезагрегирующее соединение, представляет собой FK506 (такролимус) или рапамицин (сиролимус). Получение и применение FK506 и рапамицина известно в данной области.
В некоторых вариантах осуществления экспрессионное соединение, например, дезагрегирующее соединение, ингибирует взаимодействие между доменами агрегации. В некоторых вариантах осуществления, в которых дезагрегирующее соединение представляет собой FK506, рапамицин, AP22542 или AP21998, дезагрегирующее соединение ингибирует взаимодействие между слитыми белками, содержащими домен агрегации, полученный из FKBP F36M.
Иллюстративная пара домен агрегации-дезагрегирующее соединение была получена и представлена в настоящем документе (SEQ ID NOs: 977 (нуклеиновая кислота) и 978 (аминокислотная последовательность)). Данный домен агрегации представляет собой домен FKBP F36M, описанный в «A ligand-reversible dimerization system for controlling protein-protein interactions», Rollins et al. PNAS vol. 97 no. 13, 7096-7101 и WO/2000/023600. Каждый из этих литературных источников включен посредством ссылки в полном объеме.
Нуклеотидная последовательность CD19bbz on-CAR, CD19 on-CAR (SEQ ID NO: 977)
Сигнальный пептид-домены условной агрегации (4 повтора)-сайт фурина-FMC63bbz
ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGGATCCCGGGGCGTGCAGGTTGAGACAATTTCCCCAGGAGATGGGCGAACGTTCCCCAAGCGCGGACAGACATGCGTTGTGCACTACACAGGAATGTTGGAGGACGGAAAGAAAATGGACAGTTCAAGAGATCGGAACAAACCATTCAAATTCATGTTGGGAAAACAGGAAGTGATACGGGGCTGGGAAGAGGGTGTAGCGCAAATGTCCGTTGGTCAACGAGCAAAACTCACGATAAGTCCCGATTATGCTTACGGCGCAACCGGTCACCCGGGCATCATACCGCCTCATGCGACTTTGGTCTTTGATGTGGAGCTGTTGAAACTTGAAACTCGCGGAGTACAGGTTGAAACAATATCACCCGGGGACGGGCGGACTTTTCCGAAGAGAGGTCAGACCTGCGTCGTCCATTATACCGGTATGCTGGAGGACGGAAAGAAAATGGACAGCTCACGGGACCGAAATAAACCATTCAAATTTATGTTGGGGAAACAAGAGGTTATCAGGGGCTGGGAGGAGGGTGTGGCCCAGATGTCTGTCGGTCAGCGCGCGAAACTCACAATCTCTCCGGATTATGCGTATGGGGCGACAGGGCATCCGGGAATTATCCCTCCCCACGCTACCTTGGTTTTCGATGTTGAGCTTCTGAAGTTGGAGACCAGAGGAGTTCAAGTGGAGACAATATCTCCTGGGGATGGACGGACGTTCCCCAAGCGCGGCCAGACCTGTGTAGTCCACTACACAGGGATGCTTGAAGACGGAAAAAAGATGGATAGCAGTAGAGATCGCAACAAACCATTTAAGTTCATGCTGGGGAAGCAGGAAGTAATACGCGGCTGGGAGGAAGGCGTGGCACAGATGAGTGTTGGTCAACGGGCCAAACTTACTATTTCTCCCGATTATGCGTATGGAGCCACCGGGCACCCTGGCATTATCCCACCCCATGCCACATTGGTTTTTGACGTTGAATTGCTTAAATTGGAGACCAGGGGAGTCCAAGTGGAAACAATATCACCGGGGGATGGTCGGACTTTTCCTAAAAGGGGCCAAACCTGTGTAGTCCATTATACCGGAATGCTCGAAGACGGAAAGAAAATGGACTCTTCTAGAGACCGCAATAAGCCCTTCAAGTTCATGTTGGGTAAGCAAGAGGTGATCCGGGGCTGGGAAGAGGGGGTCGCTCAAATGTCCGTCGGTCAGCGAGCTAAACTGACTATTTCCCCAGACTACGCATATGGAGCGACTGGCCACCCCGGTATTATTCCTCCCCATGCGACTCTCGTGTTCGACGTAGAACTCTTGAAATTGGAAACGTCAGCCCGGAACAGGCGGAAGAGAGGATCCGACATCCAGATGACACAGACTACATCCTCCCTGTCTGCCTCTCTGGGAGACAGAGTCACCATCAGTTGCAGGGCAAGTCAGGACATTAGTAAATATTTAAATTGGTATCAGCAGAAACCAGATGGAACTGTTAAACTCCTGATCTACCATACATCAAGATTACACTCAGGAGTCCCATCAAGGTTCAGTGGCAGTGGGTCTGGAACAGATTATTCTCTCACCATTAGCAACCTGGAGCAAGAAGATATTGCCACTTACTTTTGCCAACAGGGTAATACGCTTCCGTACACGTTCGGAGGGGGGACTAAGTTGGAAATAACAGGTGGCGGTGGCTCGGGCGGTGGTGGGTCGGGTGGCGGCGGATCTGAGGTGAAACTGCAGGAGTCAGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCGTCACATGCACTGTCTCAGGGGTCTCATTACCCGACTATGGTGTAAGCTGGATTCGCCAGCCTCCACGAAAGGGTCTGGAGTGGCTGGGAGTAATATGGGGTAGTGAAACCACATACTATAATTCAGCTCTCAAATCCAGACTGACCATCATCAAGGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTGCAAACTGATGACACAGCCATTTACTACTGTGCCAAACATTATTACTACGGTGGTAGCTATGCTATGGACTACTGGGGTCAAGGAACCTCAGTCACCGTCTCCTCAGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGCTAA
Аминокислотная последовательность CD19bbz on-CAR (SEQ ID NO: 978)
Сигнальный пептид-домены условной агрегации (4 повтора)-сайт фурина-FMC63bbz
MALPVTALLLPLALLLHAARPGSRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETSARNRRKRGSDIQMTQTTSSLSASLGDRVTISCRASQDISKYLNWYQQKPDGTVKLLIYHTSRLHSGVPSRFSGSGSGTDYSLTISNLEQEDIATYFCQQGNTLPYTFGGGTKLEITGGGGSGGGGSGGGGSEVKLQESGPGLVAPSQSLSVTCTVSGVSLPDYGVSWIRQPPRKGLEWLGVIWGSETTYYNSALKSRLTIIKDNSKSQVFLKMNSLQTDDTAIYYCAKHYYYGGSYAMDYWGQGTSVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRZ
Домены деградации
В некоторых вариантах осуществления домен условной экспрессии представляет собой домен деградации. Способы получения доменов деградации, которые избирательно стабильны в присутствии стабилизирующего соединения, хорошо известны в данной области и описаны более подробно ниже. Несколько таких пар домен-стабилизирующее соединение были получены до настоящего времени и описаны в настоящем документе. К ним относятся домены деградации на основе FKBP (например, с использованием стабилизирующего соединения «Shield»), описанные в «A Rapid, Reversible, and Tunable Method to Regulate Protein Function in Living Cells Using Synthetic Small Molecules'', Banaszynski, L. A.; Chen, L.-C.; Maynard-Smith, L. A.; Ooi, A. G. L.; Wandless, T. J. Cell, 2006, 126, 995-1004; домены на основе DHFR (например, с использованием триметоприма в качестве стабилизирующего соединения), описанные в «A general chemical method to regulate protein stability in the mammalian central nervous system. Iwamoto, M.; Björklund, T.; Lundberg, C.; Kirik, D.; Wandless, T. J. Chemistry & Biology, 2010, 17, 981-988; и домены на основе рецептора альфа эстрогена (например, с использованием в качестве стабилизирующего соединения 4-OHT), описанные в «Destabilizing domains derived from the human estrogen receptor» Y Miyazaki, H Imoto, L-c Chen, TJ Wandless J. Am. Chem. Soc. 2012, 134, 3942-3945. Каждый из этих литературных источников включен посредством ссылки в полном объеме.
Настоящее изобретение охватывает домены деградации, полученные из любого природного белка. Предпочтительно, слитые белки по изобретению будут содержать домен деградации, для которого отсутствует лиганд, естественным образом экспрессируемый в интересующих компартментах клетки. Например, если слитый белок предназначен для экспрессии в T-клетках, предпочтительно выбирать домен деградации, для которого отсутствует естественным образом экспрессируемый лиганд в T-клетках. Таким образом, домен деградации при экспрессии в интересующей клетке будет стабилизирован лишь в присутствии экзогенно добавленного соединения. Примечательно, что это свойство может быть достигнуто либо за счет модифицирования домена деградации для утраты связывания естественным образом экспрессируемого лиганда (в этом случае домен деградации будет стабильным лишь в присутствии синтетического соединения), либо за счет экспрессии домена деградации в компартменте, где отсутствует естественным образом экспрессируемый лиганд (например, домен деградации может быть получен от биологического вида, отличного от вида, в организме которого слитый белок будет экспрессироваться).
Пары домен деградации-стабилизирующее соединение могут быть получены из любого природного или синтетического белка. Стабилизирующие соединения могут представлять собой любые природные или синтетические соединения. В конкретных вариантах осуществления стабилизирующие соединения будут представлять собой существующие отпускаемые по рецепту или без рецепта лекарственные средства. Примеры белков, которые могут быть модифицированы, чтобы обладать свойствами домена деградации, приведены в Таблице 21, ниже, наряду с соответствующими стабилизирующими соединениями.
В некоторых вариантах осуществления домен деградации получен из белка, приведенного в Таблице 21.
В некоторых вариантах осуществления домен деградации получен из рецептора эстрогена (ER). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 58 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней, или SEQ ID NO: 121 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 58 или SEQ ID NO: 121. Если домен деградации получен из рецептора эстрогена, стабилизирующее соединение может быть выбрано из базедоксифена или 4-гидрокситамоксифена (4-OHT). В некоторых вариантах осуществления стабилизирующее соединение представляет собой базедоксифен. Тамоксифен и базедоксифен представляет собой одобренные FDA лекарственные средства и, таким образом, являются безопасными для использования людьми.
В некоторых вариантах осуществления домен деградации получен из белка FKB (FKBP). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность SEQ ID NO: 56 или последовательность, имеющую по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность SEQ ID NO: 56. Если домен деградации получен из FKBP, стабилизирующее соединение может представлять собой Shield-1.
В некоторых вариантах осуществления домен деградации получен из дигидрофолатредуктазы (DHFR). В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 57 или последовательности, имеющей по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления домен деградации содержит аминокислотную последовательность, выбранную из SEQ ID NO: 57. Если домен деградации получен из DHFR, стабилизирующее соединение может представлять собой триметоприм.
В некоторых вариантах осуществления домен деградации получен не из белка FKB, рецептора эстрогена или DHFR.
Таблица 21. Иллюстративные белки для получения доменов деградации
Домены деградации могут быть получены из известных белков (например, белков, указанных в вышеприведенной таблице) любым из множества стандартных методов, известных в данной области. Как правило, такие методы включают, во-первых, создание интересующей библиотеки, включающей белки, полученные, например, из природного белка. Во-вторых, клетки или популяции клеток, экспрессирующие белки из отдельных библиотечных конструктов, отбирают на основании того, зависит ли экспрессия производного белка от присутствия желаемого стабилизирующего соединения. Процесс получения производных и отбора может быть повторен на протяжении многих циклов, необходимых для идентификации подходящего кандидата.
Например, библиотеку можно создавать путем рационального дизайна белков на основании тестирования различных структур и предполагаемой аффинности белкового домена для выбранного соединения. Альтернативно, библиотеку можно создавать путем случайного мутагенеза целевого белка. В любом случае, например, клетки Jurkat можно трансдуцировать лентивирусной библиотекой, полученной из конструктов. Затем клетки Jurkat можно подвергать раунду сортировки методом FACS для элиминации клеток, конститутивно экспрессирующих интересующий белок. На следующей стадии сортированные клетки инкубируют с выбранным соединением в течение 24 часов, и положительные клетки сортируют методом FACS. Их размножают путем клонирования единичных клеток. После этого, отдельные трансдуцированные клоны будут оценены на способность индуцировать экспрессию интересующего белка зависимым от соединения образом.
Суицидные гены и домены
В настоящем изобретении частично используют технологию CAR в способах избирательного удаления или активации модифицированных T-клеток от субъекта после адоптивного переноса. В одном варианте осуществления модифицированную CAR T-клетку у субъекта избирательно удаляют, вызывая активацию суицидного домена в модифицированной T-клетке. В другом варианте осуществления модифицированную T-клетку у субъекта избирательно активируют путем активного предотвращения апоптоза модифицированной CAR T-клетки во время терапии. В другом варианте осуществления модифицированную T-клетку у субъекта избирательно активируют, создавая условия для клеточной поверхностной экспрессии конструкта CAR.
Некоторые из потенциальных побочных эффектов узнавания не являющихся мишенью клеток CAR T-клетками могут быть преодолены за счет совместной экспрессии суицидного гена в CAR T-клетке. Кроме того, CAR T-клетки могут быть избирательно удалены после нацеливания на B-клетки для их устранения с целью лечения вызываемых аутоантителами или аллоантителами заболеваний или состояний.
Изобретение относится к выделенной нуклеиновой кислоте, содержащей суицидный ген. Примеры суицидных генов включают, но без ограничения, ген тимидинкиназы вируса простого герпеса (HSV-TK), цитоплазматического домена Fas, каспазы, такой как каспаза-8 или каспаза-9, цитозин-дезаминазы, E1A, FHIT, а также другие известные индуцирующие самоуничтожение или апоптоз гены (Straathof et al., 2005, Blood 105:4247-4254; Cohen et al., 1999, Leuk. Lymphoma 34:473-480; Thomis et al., 2001, Blood 97:1249-1257; Tey et al., 2007, Biol. Blood Marrow Transplant 13:913-924 и Di Stasi et al., 2011, N. Engl. J. Med. 365:1673-1683).
Суицидный ген может быть функционально связан с промотором, например, с последовательностью индуцируемого промотора. Примеры индуцируемых промоторов включают, но без ограничения, промотор белка теплового шока, регулируемый тетрациклином промотор, регулируемый стероидом промотор, регулируемый металлом промотор, регулируемый рецептором эстрогена промотор, а также другие известные в данной области промоторы. В одном аспекте изобретение относится к выделенной нуклеотидной последовательности, представляющей собой нуклеотидную последовательность, включающую суицидный ген и нуклеиновую кислоту, кодирующую химерный антигенный рецептор. В другом аспекте изобретение относится к выделенной нуклеотидной последовательности, представляющей собой нуклеотидную последовательность, включающую суицидный ген и нуклеиновую кислоту, кодирующую химерный антигенный рецептор. В одном варианте осуществления суицидный ген содержит нуклеиновую кислоту, выбранную из группы, состоящей из ATGCTCGAGGGGGTTCAGGTGGAGACTATCAGCCCGGGCGACGGACGGACATTCCCAAAGCGCGGGCAGACGTGTGTGGTGCATTACACCGGGATGCTTGAGGACGGAAAGAAAGTGGACTCTTCCCGAGACCGAAATAAACCATTCAAGTTCATGTTGGGCAAGCAGGAGGTTATCAGAGGGTGGGAGGAGGGCGTCGCTCAGATGAGTGTCGGACAGAGGGCCAAGCTCACGATCTCCCCTGATTACGCCTACGGGGCAACTGGTCACCCCGGAATCATCCCCCCTCACGCAACCCTCGTGTTCGACGTCGAGCTGCTCAAACTGGAATCAGGCGGAGGCAGTGGCGCTAGCGGGTTTGGCGATGTCGGTGCCCTTGAAAGCTTGAGAGGAAATGCCGATCTCGCTTACATCTTGAGCATGGAGCCCTGTGGGCACTGTCTGATCATCAACAATGTTAACTTTTGCCGGGAGTCCGGCCTGCGCACACGCACAGGCTCCAACATTGACTGCGAAAAACTTCGAAGGAGGTTTAGCTCTCTGCATTTCATGGTAGAGGTGAAGGGGGATCTGACCGCCAAGAAAATGGTTCTCGCCCTTCTCGAGCTTGCGCAGCAGGACCATGGAGCGCTTGACTGTTGTGTCGTTGTGATACTGAGCCATGGCTGTCAGGCTTCCCATCTCCAGTTTCCAGGGGCCGTGTACGGAACCGATGGATGCCCTGTGTCAGTTGAAAAGATCGTAAACATCTTTAACGGAACATCTTGCCCGAGCCTCGGCGGTAAACCGAAGCTTTTTTTTATCCAGGCCTGCGGCGGTGAACAGAAAGATCATGGCTTCGAGGTTGCCAGTACCAGCCCTGAAGACGAATCCCCCGGGTCAAATCCTGAACCAGATGCGACCCCTTTCCAGGAAGGACTCCGCACTTTTGACCAGCTTGACGCCATTTCCTCCCTGCCAACACCTTCCGACATATTTGTAAGCTACTCCACCTTTCCAGGATTCGTGAGCTGGCGCGACCCAAAATCCGGCAGTTGGTATGTTGAAACCCTGGACGATATTTTCGAACAATGGGCCCACAGTGAGGACCTGCAGTCCCTTCTTCTGCGCGTAGCCAATGCCGTGTCAGTCAAAGGGATTTACAAGCAGATGCCAGGCTGCTTTAATTTCCTGCGCAAGAAACTGTTTTTTAAGACCAGT или SEQ ID NO: 3001;
CGGACGGACATTCCCAAAGCGCGGGCAGACGTGTGTGGTGCATTACACCGGGATGCTTGAGGACGGAAAGAAAGTGGACTCTTCCCGAGACCGAAATAAACCATTCAAGTTCATGTTGGGCAAGCAGGAGGTTATCAGAGGGTGGGAGGAGGGCGTCGCTCAGATGAGTGTCGGACAGAGGGCCAAGCTCACGATCTCCCCTGATTACGCCTACGGGGCAACTGGTCACCCCGGAATCATCCCCCCTCACGCAACCCTCGTGTTCGACGTCGAGCTGCTCAAACTGGAATCAGGCGGAGGCAGTGGCGGGTTTGGCGATGTCGGTGCCCTTGAAAGCTTGAGAGGAAATGCCGATCTCGCTTACATCTTGAGCATGGAGCCCTGTGGGCACTGTCTGATCATCAACAATGTTAACTTTTGCCGGGAGTCCGGCCTGCGCACACGCACAGGCTCCAACATTGACTGCGAAAAACTTCGAAGGAGGTTTAGCTCTCTGCATTTCATGGTAGAGGTGAAGGGGGATCTGACCGCCAAGAAAATGGTTCTCGCCCTTCTCGAGCTTGCGCAGCAGGACCATGGAGCGCTTGACTGTTGTGTCGTTGTGATACTGAGCCATGGCTGTCAGGCTTCCCATCTCCAGTTTCCAGGGGCCGTGTACGGAACCGATGGATGCCCTGTGTCAGTTGAAAAGATCGTAAACATCTTTAACGGAACATCTTGCCCGAGCCTCGGCGGTAAACCGAAGCTTTTTTTTATCCAGGCCTGCGGCGGTGAACAGAAAGATCATGGCTTCGAGGTTGCCAGTACCAGCCCTGAAGACGAATCCCCCGGGTCAAATCCTGAACCAGATGCGACCCCTTTCCAGGAAGGACTCCGCACTTTTGACCAGCTTGACGCCATTTCCTCCCTGCCAACACCTTCCGACATATTTGTAAGCTACTCCACCTTTCCAGGATTCGTGAGCTGGCGCGACCCAAAATCCGGCAGTTGGTATGTTGAAACCCTGGACGATATCTTCGAACAATGGGCCCACAGTGAGGACCTGCAGTCCCTTCTTCTGCGCGTAGCCAATGCCGTGTCAGTCAAAGGGATTTACAAGCAGATGCCAGGCTGCTTTAATTTCCTGCGCAAGAAACTGTTTTTTAAGACCAGTTGAGTCGACGGAGGAGGAG или SEQ ID NO: 3002;
GGGGTTCAGGTGGAGACTATCAGCCCGGGCGACGGACGGACATTCCCAAAGCGCGGGCAGACGTGTGTGGTGCATTACACCGGGATGCTTGAGGACGGAAAGAAAGTGGACTCTTCCCGAGACCGAAATAAACCATTCAAGTTCATGTTGGGCAAGCAGGAGGTTATCAGAGGGTGGGAGGAGGGCGTCGCTCAGATGAGTGTCGGACAGAGGGCCAAGCTCACGATCTCCCCTGATTACGCCTACGGGGCAACTGGTCACCCCGGAATCATCCCCCCTCACGCAACCCTCGTGTTCGACGTCGAGCTGCTCAAACTGGAATCAGGCGGAGGCAGTGGCGGGTTTGGCGATGTCGGTGCCCTTGAAAGCTTGAGAGGAAATGCCGATCTCGCTTACATCTTGAGCATGGAGCCCTGTGGGCACTGTCTGATCATCAACAATGTTAACTTTTGCCGGGAGTCCGGCCTGCGCACACGCACAGGCTCCAACATTGACTGCGAAAAACTTCGAAGGAGGTTTAGCTCTCTGCATTTCATGGTAGAGGTGAAGGGGGATCTGACCGCCAAGAAAATGGTTCTCGCCCTTCTCGAGCTTGCGCAGCAGGACCATGGAGCGCTTGACTGTTGTGTCGTTGTGATACTGAGCCATGGCTGTCAGGCTTCCCATCTCCAGTTTCCAGGGGCCGTGTACGGAACCGATGGATGCCCTGTGTCAGTTGAAAAGATCGTAAACATCTTTAACGGAACATCTTGCCCGAGCCTCGGCGGTAAACCGAAGCTTTTTTTTATCCAGGCCTGCGGCGGTGAACAGAAAGATCATGGCTTCGAGGTTGCCAGTACCAGCCCTGAAGACGAATCCCCCGGGTCAAATCCTGAACCAGATGCGACCCCTTTCCAGGAAGGACTCCGCACTTTTGACCAGCTTGACGCCATTTCCTCCCTGCCAACACCTTCCGACATATTTGTAAGCTACTCCACCTTTCCAGGATTCGTGAGCTGGCGCGACCCAAAATCCGGCAGTTGGTATGTTGAAACCCTGGACGATATCTTCGAACAATGGGCCCACAGTGAGGACCTGCAGTCCCTTCTTCTGCGCGTAGCCAATGCCGTGTCAGTCAAAGGGATTTACAAGCAGATGCCAGGCTGCTTTAATTTCCTGCGCAAGAAACTGTTTTTTAAGACCAGTTGA или SEQ ID NO: 3003; и
AGAGGCGTGCAGGTGGAAACCATCTCTCCCGGCGACGGCAGAACCTTCCCTAAGAGGGGCCAGACCTGCGTGGTGCACTACACCGGCATGCTGGAAGATGGCAAGAAGATGGACAGCTCCCGGGACCGGAACAAGCCCTTCAAGTTCATGCTGGGCAAGCAGGAAGTGATCCGGGGCTGGGAAGAGGGCGTGGCACAGATGTCTGTGGGCCAGAGAGCCAAGCTGACCATCAGCCCCGATTACGCCTACGGCGCCACAGGCCACCCTGGCATCATTCCTCCACACGCCACACTGGTGTTCGATGTGGAACTGCTGAAGCTGGAAACCCGGGGAGTGCAGGTGGAAACAATCAGCCCTGGCGACGGCCGGACCTTTCCAAAACGGGGACAGACATGTGTGGTGCATTATACAGGGATGCTGGAAGATGGGAAAAAAATGGATAGCAGCCGCGACCGCAACAAACCTTTTAAGTTTATGCTGGGGAAACAGGAAGTGATTAGAGGCTGGGAAGAGGGGGTGGCACAGATGAGCGTGGGACAGCGGGCCAAACTGACAATCTCCCCCGACTATGCCTATGGGGCCACCGGACACCCCGGAATCATCCCACCTCATGCTACCCTGGTGTTTGACGTGGAACTGCTGAAACTGGAAACAAGCGGCGGAGGCAGCGGCGGCTTTGGAGATGTGGGAGCCCTGGAAAGCCTGCGGGGCAATGCCGATCTGGCCTACATCCTGAGCATGGAACCCTGCGGCCACTGCCTGATTATCAACAACGTGAACTTCTGCAGAGAGAGCGGCCTGCGGACCAGAACCGGCAGCAACATCGACTGCGAGAAGCTGCGGCGGAGATTCAGCAGCCTGCACTTCATGGTGGAAGTGAAGGGGGACCTGACCGCCAAGAAAATGGTGCTGGCTCTGCTGGAACTGGCCCAGCAGGATCATGGCGCCCTGGACTGTTGCGTGGTCGTGATCCTGAGCCACGGCTGCCAGGCCAGCCATCTGCAGTTTCCCGGCGCTGTGTATGGCACCGATGGCTGCCCTGTGTCCGTGGAAAAGATCGTGAATATCTTCAACGGCACCAGCTGCCCCAGCCTGGGCGGAAAGCCTAAGCTGTTCTTTATTCAAGCCTGTGGGGGCGAGCAGAAGGACCACGGATTTGAGGTGGCCAGCACCTCCCCCGAGGATGAGAGCCCTGGCAGCAACCCTGAGCCTGACGCCACCCCATTCCAGGAAGGACTGCGGACCTTCGACCAGCTGGACGCCATCTCTAGCCTGCCCACCCCCAGCGACATCTTCGTGTCCTACAGCACCTTCCCTGGCTTTGTGTCCTGGCGGGACCCCAAGTCCGGCTCTTGGTACGTGGAAACCCTGGACGACATCTTTGAGCAGTGGGCCCATAGCGAGGACCTGCAGAGCCTGCTGCTGAGGGTGGCCAATGCCGTGTCCGTGAAGGGCATCTACAAGCAGATGCCCGGCTGCTTCAACTTCCTGCGGAAGAAGCTGTTTTTCAAGACCAGC или SEQ ID NO: 3004.
В другом варианте осуществления суицидный ген кодирует аминокислотную последовательность, выбранную из группы, состоящей из
MLEGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLESGGGSGASGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS или SEQ ID NO: 3005;
GVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLESGGGSGGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS или SEQ ID NO: 3006; и
RGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETSGGGSGGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS или SEQ ID NO: 3007. В другом варианте осуществления суицидный ген имеет индуцируемый промотор.
В некоторых вариантах осуществления суицидный ген находится в экспрессионном векторе. В иллюстративном варианте осуществления настоящее изобретение относится к вектору, содержащему нуклеотидную последовательность, содержащую суицидный ген, содержащий SEQ ID NOs: 3001, 3002, 3003 или 3004. Экспрессионный вектор также может включать и другие гены, например химерного антигенного рецептора и/или системы CRISPR, описанные в других разделах настоящего документа.
Изобретение также относится к клетке, содержащей суицидный ген. В иллюстративном аспекте настоящее изобретение относится к модифицированной клетке, содержащей нуклеиновую кислоту, содержащую суицидный ген, кодирующий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3005, 3006 и 3007, и нуклеиновую кислоту, кодирующую химерный антигенный рецептор. В другом аспекте настоящее изобретение относится к модифицированной клетке, содержащей нуклеиновую кислоту, содержащую суицидный ген, выбранный из группы, состоящей из SEQ ID NO: 3001, 3002, 3003 и 3004, и нуклеиновую кислоту, кодирующую химерный антигенный рецептор. В одном варианте осуществления суицидный ген кодирует аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3005, 3006 и 3007. В другом варианте осуществления суицидный ген имеет индуцируемый промотор.
В одном варианте осуществления модифицированная CAR T-клетка содержит нуклеиновую кислоту, кодирующую суицидный ген, в виде последовательности, отдельной от конструкта CAR, описанного в другом разделе настоящего документа. Например, HSV-TK, i-Casp9, цитоплазматический домен Fas или каспаза могут быть включены в генетически модифицированные T-клетки отдельно от конструкта CAR. В другом варианте осуществления модифицированная CAR T-клетка содержит суицидный ген в том же конструкте, что и нуклеиновые кислоты, кодирующие CAR. В этом варианте осуществления нуклеиновая кислота, содержащая суицидный ген, может быть расположена выше или ниже от нуклеиновых кислот, кодирующих CAR.
В одном варианте осуществления экспрессия суицидного гена активируется в клетке при контакте клетки с индуцирующим средством, введенным в клетку или млекопитающему, имеющему клетку. Затем индуцирующее средство активирует индуцируемый промотор для экспрессии суицидного гена. В таком варианте осуществления индуцирующее средство вводят субъекту для индукции экспрессии суицидного гена.
В другом варианте осуществления продукт суицидного гена, экспрессируемый с суицидного гена, активируется при помощи активирующего средства, такого как димеризующее средство. Например, димеризующее средство, такое как AP20187, стимулирует димеризацию и активацию молекул каспазы-9.
В некоторых вариантах осуществления с конститутивной экспрессией суицидного гена экспрессия суицидного гена может быть выключена в клетке при контакте клетки с ингибирующим средством, введенным в клетку или млекопитающему, имеющему клетку. Ингибирующее средство избирательно выключает экспрессию. Например, каспаза-9 конститутивно экспрессируется в клетке и добавление ингибирующего средства подавляет экспрессию или активацию каспазы-9. В одном варианте осуществления ингибирующее средство вводят субъекту для подавления экспрессии суицидного гена.
В некоторых вариантах осуществления с конститутивной экспрессией суицидного гена активация продукта суицидного гена может быть подавлена в клетке при контакте клетки с ингибирующим средством, таким как солюбилизирующее средство, введенным в клетку или млекопитающему, имеющему клетку. Ингибирующее средство подавляет активацию продукта суицидного гена, например, путем предотвращения димеризации молекул каспазы-9. В одном варианте осуществления солюбилизирующее средство вводят субъекту для подавления активации продукта суицидного гена.
В некоторых аспектах суицидный ген не является иммуногенным для клетки, содержащей суицидный ген, или хозяина, имеющего суицидный ген. Хотя можно использовать тимидинкиназу (TK), она может быть иммуногенной. Альтернативно, примеры суицидных генов, не являющихся иммуногенными для хозяина, включают гены каспазы-9, каспазы-8 и цитозин-дезаминазы.
В другом варианте осуществления экспрессия суицидного гена находится в тандеме с экспрессией одного или более доменов димеризации, которые вызывают агрегацию слитого белка, содержащего суицидный домен и домен димеризации, предотвращая клеточную поверхностную экспрессию и, следовательно, функционирование суицидного гена.
В другом варианте осуществления нуклеотидная последовательность, кодирующая домен димеризации, связанная с суицидным геном, содержит нуклеотидную последовательность, выбранную из группы, состоящей из
GGAAGCGGCGCCACCAATTTCAGCCTGCTGAAACAGGCCGGCGACGTGGAAGAGAACCCTGGCCCT или SEQ ID NO: 3008;
AGTGGCTCCGGCGCAACAAATTTCTCCTTGCTGAAACAGGCAGGCGACGTTGAGGAAAATCCCGGCCCA или SEQ ID NO: 3009;
GGCTCCGGCGCAACAAATTTCTCCTTGCTGAAACAGGCAGGCGACGTTGAGGAAAATCCCGGCCCA или SEQ ID NO: 3010;
GGGGTTCAGGTGGAGACTATCAGCCCGGGCGA или SEQ ID NO: 3011; и
GGCTCCGGCGCAACAAATTTCTCCTTGCTGAAACAGGCAGGCGACGTTGAGGAAAATCCCGGCCCA или SEQ ID NO: 3012.
В другом таком варианте осуществления домен димеризации, связанный с суицидным доменом, содержит аминокислотную последовательность, выбранную из группы, состоящей из GSGATNFSLLKQAGDVEENPGP или SEQ ID NO: 3013; и RKRRGSGATNFSLLKQAGDVEENPGP или SEQ ID NO: 3014.
Солюбилизация доменов димеризации при помощи солюбилизирующего средства, введенного в клетку или млекопитающему, имеющему клетку, предотвращает агрегацию и позволяет конструкту выходить через секреторную систему.
Как описано в настоящем документе, настоящее изобретение относится к способу модификации T-клетки химерным антигенным рецептором (CAR) и суицидным геном. Таким образом, настоящее изобретение относится к нуклеиновой кислоте, кодирующей CAR, или модифицированной T-клетке, содержащей CAR, при этом CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен.
Один или более доменов, или фрагментов доменов, CAR могут быть человеческими. В одном варианте осуществления настоящее изобретение относится к полностью человеческому CAR. The Нуклеотидные последовательности, кодирующие нужные домены, можно получать рекомбинантными методами, известными в данной области, такими как, например, скрининг библиотек из клеток, экспрессирующих ген, получение гена из вектора, который, как известно, содержит его, или путем непосредственного выделения из клеток и тканей, содержащих его, с использованием стандартных методов. Альтернативно, интересующий ген можно получать методами синтеза, а не клонирования.
Примеры CAR приведены в патентах США №№ 8911993, 8906682, 8975071, 8916381, 9102760, 9101584 и 9102761, содержание всех из которых включено в настоящий документ посредством ссылки в полном объеме.
Нуклеиновая кислота и векторы
В другом аспекте изобретение относится к нуклеиновой кислоте, кодирующей любой из слитых белков, описанных в настоящем документе, или вектору, содержащему такую нуклеиновую кислоту. В одном варианте осуществления вектор выбирают из ДНК вектора, РНК вектора, плазмиды, лентивирусного вектора, аденовирусного вектора или ретровирусного вектора. В одном варианте осуществления вектор представляет собой лентивирусный вектор.
В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат последовательность, кодирующую сайт расщепления фурина. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат любую из SEQ ID NOs: 1112, 126, 128, 130, 132, 134, 136 или 138, или последовательность, имеющую по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат любую из SEQ ID NOs: 1112, 126, 128, 130, 132, 134, 136 или 138. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат SEQ ID NO: 126 или SEQ ID NO: 128. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат SEQ ID NO: 126.
В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат последовательность, кодирующую домен условной экспрессии, например, домен агрегации или домен деградации. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат последовательность, кодирующую домен агрегации, полученный из FKBP, например, FKBP F36M. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат последовательность, кодирующую домен деградации, полученный из рецептора эстрогена (ER). В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат SEQ ID NO: 1110 или SEQ ID NO: 122, или последовательность, имеющую по меньшей мере 90%, 95%, 97%, 98% или 99% идентичности с ней. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат SEQ ID NO: 1110 или SEQ ID NO: 122. В некоторых вариантах осуществления нуклеиновые кислоты, описанные в настоящем документе, содержат SEQ ID NO: 122.
По настоящему изобретению также предложены векторы, в которые вставлена ДНК по настоящему изобретению. Векторы, полученные из ретровирусов, таких как лентивирус, являются подходящими инструментами для достижения долгосрочного переноса гена, поскольку они делают возможным долгосрочное стабильное интегрирование трансгена и его размножение в дочерних клетках. Лентивирусные векторы имеют дополнительное преимущество перед другими векторами, полученными из онко-ретровирусов, таких как вирусы мышиного лейкоза, в том, что они могут трансдуцировать неделящиеся клетки, такие как гепатоциты. Они также имеют дополнительное преимущество низкой иммуногенности. Ретровирусный вектор также может представлять собой, например, гамма-ретровирусный вектор. Гамма-ретровирусный вектор может включать, например, промотор, сигнал упаковки (ψ), сайт связывания праймера (PBS), один или более (например, два) длинных концевых повтора (LTR) и интересующий трансген, например, ген, кодирующий CAR. Гамма-ретровирусный вектор может быть лишен вирусных структурных генов, таких как gag, pol и env. Иллюстративные гамма-ретровирусные векторы включают вирус мышиного лейкоза (MLV), вирус некроза селезенки (SFFV) и вирус миелопролиферативной саркомы (MPSV), а также векторы, полученные из них. Другие гамма-ретровирусные векторы описаны, например, в Tobias Maetzig et al., «Gammaretroviral Vectors: Biology, Technology and Application», Viruses. 2011 Jun; 3(6): 677-713.
В другом варианте осуществления вектор, содержащий нуклеиновую кислоту, кодирующую нужный слитый белок по изобретению, представляет собой аденовирусный вектор (A5/35). В другом варианте осуществления экспрессию нуклеиновых кислот, кодирующих химерные молекулы, можно осуществлять с использованием транспозонов, таких как «спящая красавица», «криспер», CAS9 и нуклеазы «цинковые пальцы». Смотри ниже June et al. 2009 Nature Reviews Immunology 9,10: 704-716, содержание публикации включено в настоящий документ посредством ссылки.
Нуклеиновую кислоту можно клонировать в самые разные векторы. Например, нуклеиновую кислоту можно клонировать в вектор, включающий, но без ограничения, плазмиду, фагмид, производное фага, животный вирус и космиду. Векторы, представляющие особый интерес, включают экспрессионные векторы, реплицируемые векторы, векторы для получения зондов и векторы для секвенирования.
В настоящем документе раскрыты способы получения in vitro транскрибированной РНК химерной молекулы. Настоящее изобретение также охватывает кодирующий химерную молекулу РНК-конструкт, который может быть непосредственно трансфицирован в клетку. Способ получения мРНК для использования в трансфекции может включать in vitro транскрипцию (IVT) матрицы со специально разработанными праймерами, с последующим добавлением полиA, с получением конструкта, содержащего 3'- и 5'-нетранслируемую последовательность («UTR»), 5'-кэп и/или внутренний сайт связывания рибосомы (IRES), нуклеиновую кислоту, которую предстоит экспрессировать, и полиA «хвост», как правило, длиной 50-5000 оснований (SEQ ID NO: 32). Полученной таким образом РНК можно эффективно трансфицировать клетки разных видов. В одном аспекте матрица содержит последовательности для CAR.
Конструкты нуклеиновой кислоты, кодирующей слитый белок, содержащий CAR
Настоящее изобретение также относится к молекулам нуклеиновой кислоты, кодирующим слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит один или более конструктов CAR, нацеленных на антиген, описанный в настоящем документе. В одном аспекте предложена молекула нуклеиновой кислоты в виде матричной РНК-транскрипта. В одном аспекте предложена молекула нуклеиновой кислоты в виде ДНК конструкта.
Соответственно, в одном аспекте изобретение относится к молекуле нуклеиновой кислоты, кодирующей слитый белок, например, описанный в настоящем документе, содержащий химерный антигенный рецептор (CAR), при этом CAR содержит антигенсвязывающий домен, который связывается с антигеном, описанным в настоящем документе, трансмембранный домен (например, трансмембранный домен, описанный в настоящем документе) и внутриклеточный сигнальный домен (например, внутриклеточный сигнальный домен, описанный в настоящем документе), содержащий стимулирующий домен, например, костимулирующий сигнальный домен (например, костимулирующий сигнальный домен, описанный в настоящем документе) и/или основной сигнальный домен (например, основной сигнальный домен, описанный в настоящем документе, например, дзета-цепь, описанную в настоящем документе). В одном варианте осуществления трансмембранный домен представляет собой трансмембранный домен белка, выбранного из группы, состоящей из альфа, бета или дзета-цепи T-клеточного рецептора, CD28, CD3-эпсилон, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137 и CD154. В некоторых вариантах осуществления трансмембранный домен может содержать по меньшей мере трансмембранную область(и) из, например, KIRDS2, OX40, CD2, CD27, LFA-1 (CD11a, CD18), ICOS (CD278), 4-1BB (CD137), GITR, CD40, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, IL2R-бета, IL2R-гамма, IL7Rα, ITGA1, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, NKG2C, TNFR2, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (тактильный), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, PAG/Cbp, NKG2D и NKG2C.
В одном варианте осуществления трансмембранный домен содержит последовательность SEQ ID NO: 12 или последовательность, имеющую 95-99% идентичности с ней. В одном варианте осуществления антигенсвязывающий домен связан с трансмембранным доменом шарнирной областью, например, шарниром, описанным в настоящем документе. В одном варианте осуществления шарнирная область содержит SEQ ID NO: 4 или SEQ ID NO: 6, или SEQ ID NO: 8, или SEQ ID NO: 10, или последовательность, имеющую 95-99% идентичности с ними. В одном варианте осуществления выделенная молекула нуклеиновой кислоты дополнительно содержит последовательность, кодирующую костимулирующий домен. В одном варианте осуществления костимулирующий домен представляет собой функциональный сигнальный домен белка, выбранного из группы, состоящей из OX40, CD27, CD28, CDS, ICAM-1, LFA-1 (CD11a/CD18), ICOS (CD278) и 4-1BB (CD137). Дополнительные примеры таких костимулирующих молекул включают CDS, ICAM-1, GITR, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRF1), NKp44, NKp30, NKp46, CD160, CD19, CD4, CD8-альфа, CD8-бета, IL2R-бета, IL2R-гамма, IL7R-альфа, ITGA4, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CD11d, ITGAE, CD103, ITGAL, CD11a, LFA-1, ITGAM, CD11b, ITGAX, CD11c, ITGB1, CD29, ITGB2, CD18, LFA-1, ITGB7, NKG2D, NKG2C, TNFR2, TRANCE/RANKL, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (тактильный), CEACAM1, CRTAM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), CD69, SLAMF6 (NTB-A, Ly108), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, LAT, GADS, SLP-76, PAG/Cbp, NKG2D и NKG2C. В одном варианте осуществления внутриклеточный сигнальный домен содержит функциональный сигнальный домен 4-1BB и функциональный сигнальный домен CD3-дзета. В одном варианте осуществления внутриклеточный сигнальный домен содержит последовательность SEQ ID NO: 14, 16, 120 или 124, или последовательность, имеющую 95-99% идентичности с ними, и последовательность SEQ ID NO: 18 или SEQ ID NO: 20, или последовательность, имеющую 95-99% идентичности с ними, при этом последовательности, составляющие внутриклеточный сигнальный домен, экспрессируются в одной и той же рамке считывания и в виде одной полипептидной цепи.
В другом аспекте изобретение относится к выделенной молекуле нуклеиновой кислоты, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит конструкт CAR, содержащий лидерную последовательность SEQ ID NO: 2, домен scFv, описанный в настоящем документе, шарнирную область с SEQ ID NO: 4 или SEQ ID NO: 6, или SEQ ID NO: 8, или SEQ ID NO: 10 (или последовательностью, имеющей 95-99% идентичности с ними), трансмембранный домен, содержащий последовательность SEQ ID NO: 12 (или последовательность, имеющую 95-99% идентичности с ней), костимулирующий домен 4-1BB, содержащий последовательность SEQ ID NO: 14, костимулирующий домен CD27, содержащий последовательность SEQ ID NO: 16 (или последовательность, имеющую 95-99% идентичности с ней), костимулирующий домен ICOS, содержащий последовательность SEQ ID NO: 120 (или последовательность, имеющую 95-99% идентичности с ней) или костимулирующий домен CD28, содержащий последовательность SEQ ID NO: 124, а также стимулирующий домен CD3-дзета, содержащий последовательность SEQ ID NO: 18 или SEQ ID NO: 20 (или последовательность, имеющую 95-99% идентичности с ними).
Нуклеотидные последовательности, кодирующие нужные молекулы, могут быть получены рекомбинантными методами, известными в данной области, такими как, например, скрининг библиотек из клеток, экспрессирующих ген, получение гена из вектора, который, как известно, содержит его, или выделение непосредственно из клеток и тканей, содержащих его, с использованием стандартных методов. Альтернативно, интересующий ген можно получать методами синтеза, а не клонирования.
Настоящее изобретение также относится к векторам, в которые вставлена нуклеиновая кислота по настоящему изобретению. Векторы, полученные из ретровирусов, таких как лентивирус, являются подходящими инструментами для достижения долгосрочного переноса гена, поскольку они делают возможным долгосрочное стабильное интегрирование трансгена и его размножение в дочерних клетках. Лентивирусные векторы имеют дополнительное преимущество перед другими векторами, полученными из онко-ретровирусов, таких как вирусы мышиного лейкоза, в том, что они могут трансдуцировать неделящиеся клетки, такие как гепатоциты. Они также имеют дополнительное преимущество низкой иммуногенности.
В другом варианте осуществления вектор, содержащий нуклеиновую кислоту, кодирующую слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR по изобретению, представляет собой аденовирусный вектор (A5/35). В другом варианте осуществления экспрессию нуклеиновых кислот, кодирующих CAR, можно осуществлять с использованием транспозонов, таких как «спящая красавица», «криспер», CAS9 и нуклеазы «цинковые пальцы». Смотри ниже June et al. 2009 Nature Reviews Immunology 9,10:704-716, содержание публикации включено в настоящий документ посредством ссылки.
Вкратце, экспрессию природных или синтетических нуклеиновых кислот, кодирующих слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, как правило, осуществляют путем функционального связывания нуклеиновой кислоты, кодирующей полипептид CAR или его фрагменты, с промотором и включения конструкта в экспрессионный вектор. Векторы могут быть подходящими для репликации и интеграции в клетках эукариот. Типичные клонирующие векторы содержат терминаторы транскрипции и трансляции, последовательности инициации и промоторы, полезные для регуляции экспрессии нужной последовательности нуклеиновой кислоты.
Экспрессионные конструкты по настоящему изобретению также могут быть использованы для иммунизации нуклеиновой кислотой и генной терапии, с использованием стандартных протоколов доставки генов. Способы доставки генов известны в данной области. Смотри, например, патенты США №№ 5399346, 5580859, 5589466, включенные в настоящий документ посредством ссылки в полном объеме. В другом варианте осуществления изобретение относится к вектору для генной терапии.
Нуклеиновую кислоту можно клонировать в самые разные векторы. Например, нуклеиновую кислоту можно клонировать в вектор, включающий, но без ограничения, плазмиду, фагмид, производное фага, животный вирус и космиду. Векторы, представляющие особый интерес, включают экспрессионные векторы, реплицируемые векторы, векторы для получения зондов и векторы для секвенирования.
Кроме того, экспрессионный вектор может быть введен в клетку в форме вирусного вектора. Технология вирусных векторов хорошо известна в данной области и описана, например, в Sambrook et al., 2012, MOLECULAR CLONING: A LABORATORY MANUAL, volumes 1-4, Cold Spring Harbor Press, NY, и других руководствах по вирусологии и молекулярной биологии. Вирусы, полезные в качестве векторов, включают, но не ограничиваются ими, ретровирусы, аденовирусы, аденоассоциированные вирусы, вирусы герпеса и лентивирусы. Как правило, подходящий вектор содержит точку начала репликации, функциональную по меньшей мере в одном организме, последовательность промотора, удобные сайты для эндонуклеаз рестрикции и один или более селективных маркеров (например, WO 01/96584; WO 01/29058 и патент США № 6326193).
Различные системы на основе вирусов были разработаны для переноса генов в клетки млекопитающих. Например, ретровирусы представляют собой удобную платформу для систем доставки генов. Выбранный ген может быть вставлен в вектор и упакован в ретровирусные частицы с использованием методов, известных в данной области. Затем рекомбинантный вирус может быть выделен и доставлен в клетки субъекта либо in vivo, либо ex vivo. Множество ретровирусных систем известно в данной области. В некоторых вариантах осуществления используют аденовирусные векторы. Множество аденовирусных векторов известно в данной области. В одном варианте осуществления используют лентивирусные векторы.
Дополнительные элементы промотора, например, энхансеры, регулируют частоту инициации транскрипции. Как правило, они расположены в области, находящейся на 30-110 п.н. выше сайта начала транскрипции, хотя показано, что многие промоторы также содержат функциональные элементы, расположенные ниже сайта начала транскрипции. Пространство между элементами промотора часто бывает гибким, так что функция промотора сохраняется, когда элементы переворачиваются или движутся относительно друг друга. В промоторе тимидинкиназы (tk) пространство между элементами промотора может быть увеличено до 50 п.н., прежде чем активность начинает снижаться. В зависимости от промотора, отдельные элементы, судя по всему, могут действовать либо совместно, либо независимо, активируя транскрипцию. Иллюстративные промоторы включают промоторы гена CMV IE, EF-1α, убиквитина C или фосфоглицерокиназы (PGK).
Примером промотора, способного обеспечивать экспрессию молекулы нуклеиновой кислоты, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, в T-клетке млекопитающего, является промотор EF1a. Природный промотор EF1a управляет экспрессией альфа-субъединицы комплекса фактора элонгации 1, который отвечает за ферментативную доставку аминоацил-тРНК к рибосоме. Промотор EF1a был широко использован в экспрессионных плазмидах млекопитающих и, как показано, является эффективным в управлении экспрессией слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR, с молекул нуклеиновой кислоты, клонированных в лентивирусный вектор. Смотри, например, Milone et al., Mol. Ther. 17(8): 1453-1464 (2009). В одном аспекте промотор EF1a содержит последовательность, приведенную в SEQ ID NO: 1.
Другим примером промотора является последовательность предраннего промотора цитомегаловируса (CMV). Эта последовательность промотора представляет собой последовательность сильного конститутивного промотора, способную обеспечивать высокие уровни экспрессии любой полинуклеотидной последовательности, функционально связанной с ней. Однако также можно использовать и другие последовательности конститутивных промоторов, включая, но без ограничения, ранний промотор обезьяньего вируса 40 (SV40), промотор вируса опухоли молочной железы мышей (MMTV), промотор длинного концевого повтора (LTR) вируса иммунодефицита человека (ВИЧ), промотор MoMuLV, промотор вируса птичьего лейкоза, предранний промотор вируса Эпштейна-Барр, промотор вируса саркомы Рауса, а также промоторы человеческих генов, такие как, но без ограничения, промотор актина, промотор миозина, промотор фактора элонгации 1α, промотор гемоглобина и промотор креатинкиназы. Кроме того, изобретение не должно быть ограничено использованием конститутивных промоторов. Индуцируемые промоторы также предусмотрены по настоящему изобретению. Использование индуцируемых промоторов позволяет иметь молекулярный переключатель, способный включать экспрессию функционально связанной полинуклеотидной последовательности, когда такая экспрессия желательна, или выключать экспрессию, когда экспрессия нежелательна. Примеры индуцируемых промоторов включают, но без ограничения, металлотиониновый промотор, глюкокортикоидный промотор, прогестероновый промотор и тетрациклиновый промотор.
Другим примером промотора является промотор фосфоглицераткиназы (PGK). В вариантах осуществления может быть желательным использование укороченного промотора PGK (например, промотора PGK с одной или более, например, 1, 2, 5, 10, 100, 200, 300 или 400, нуклеотидными делециями в сравнении с последовательностью промотора PGK дикого типа). Нуклеотидные последовательности иллюстративных промоторов PGK приведены ниже.
Промотор PGK ДТ
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACGAGGGACCGCGACAGGCAGACGCTCCCATGATCACTCTGCACGCCGAAGGCAAATAGTGCAGGCCGTGCGGCGCTTGGCGTTCCTTGGAAGGGCTGAATCCCCGCCTCGTCCTTCGCAGCGGCCCCCCGGGTGTTCCCATCGCCGCTTCTAGGCCCACTGCGACGCTTGCCTGCACTTCTTACACGCTCTGGGTCCCAGCCGCGGCGACGCAAAGGGCCTTGGTGCGGGTCTCGTCGGCGCAGGGACGCGTTTGGGTCCCGACGGAACCTTTTCCGCGTTGGGGTTGGGGCACCATAAGCT (SEQ ID NO: 185)
Иллюстративные укороченные промоторы PGK:
PGK100:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTG (SEQ ID NO: 186)
PGK200:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACG (SEQ ID NO: 187)
PGK300:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACGAGGGACCGCGACAGGCAGACGCTCCCATGATCACTCTGCACGCCGAAGGCAAATAGTGCAGGCCGTGCGGCGCTTGGCGTTCCTTGGAAGGGCTGAATCCCCG (SEQ ID NO: 188)
PGK400:
ACCCCTCTCTCCAGCCACTAAGCCAGTTGCTCCCTCGGCTGACGGCTGCACGCGAGGCCTCCGAACGTCTTACGCCTTGTGGCGCGCCCGTCCTTGTCCCGGGTGTGATGGCGGGGTGTGGGGCGGAGGGCGTGGCGGGGAAGGGCCGGCGACGAGAGCCGCGCGGGACGACTCGTCGGCGATAACCGGTGTCGGGTAGCGCCAGCCGCGCGACGGTAACGAGGGACCGCGACAGGCAGACGCTCCCATGATCACTCTGCACGCCGAAGGCAAATAGTGCAGGCCGTGCGGCGCTTGGCGTTCCTTGGAAGGGCTGAATCCCCGCCTCGTCCTTCGCAGCGGCCCCCCGGGTGTTCCCATCGCCGCTTCTAGGCCCACTGCGACGCTTGCCTGCACTTCTTACACGCTCTGGGTCCCAGCCG (SEQ ID NO: 189)
Вектор также может содержать, например, сигнальную последовательность для облегчения секреции, сигнал полиаденилирования и терминатор транскрипции (например, из гена бычьего гормона роста (BGH)), элемент, делающий возможной эписомную репликацию и репликацию в клетках прокариот (например, точка начала репликации SV40 и ColE1 или другие, известные в данной области), и/или элементы, позволяющие производить отбор (например, ген устойчивости к ампициллину и/или маркер устойчивости к зеоцину).
Для оценки экспрессии слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит полипептид CAR или его фрагменты, экспрессионный вектор, вводимый в клетку, также может содержать или ген селективного маркера, или ген репортера, либо оба, для облегчения идентификации и отбора экспрессирующих клеток из популяции клеток, которые трансфицируют или инфицируют вирусными векторами. В других аспектах селективный маркер может находиться на отдельном фрагменте ДНК и быть использован в процедуре совместной трансфекции. Как селективные маркеры, так и гены репортеров, могут быть фланкированы соответствующими регуляторными последовательностями, делающими возможной экспрессию в клетках-хозяевах. Полезные селективные маркеры включают, например, гены устойчивости к антибиотикам, такие как neo и тому подобное.
Гены репортеров используют для идентификации потенциально трансфицированных клеток и для оценки функциональности регуляторных последовательностей. Как правило, ген репортера представляет собой ген, который не присутствует или не экспрессируется в организме или ткани реципиента и который кодирует полипептид, экспрессия которого проявляется в виде легко определяемого признака, например, ферментативной активности. Экспрессию гена репортера анализируют в соответствующее время после введения ДНК в клетки-реципиенты. Подходящие гены репортеров могут включать гены, кодирующие люциферазу, бета-галактозидазу, хлорамфениколацетил-трансферазу, секретируемую щелочную фосфатазу, или ген зеленого флуоресцентного белка (например, Ui-Tei et al., 2000 FEBS Letters 479: 79-82). Соответствующие экспрессионные системы хорошо известны и могут быть получены с использованием известных методов или приобретены коммерческим путем. Как правило, конструкт с минимальной 5'-фланкирующей областью, демонстрирующий максимальный уровень экспрессии гена репортера, определяют в качестве промотора. Такие области промоторов могут быть связаны с геном репортера и использованы для оценки средств на способность модулировать управляемую промотором транскрипцию.
В некоторых вариантах осуществления вектор, содержащий нуклеотидную последовательность, кодирующую слитый белок, описанный в настоящем документе, например, слитый белок, содержащий молекулу CAR, описанную в настоящем документе, может дополнительно содержать вторую нуклеотидную последовательность, кодирующую полипептид, например, средство, повышающее активность слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит молекулу CAR. В некоторых вариантах осуществления одна молекула нуклеиновой кислоты или вектор, содержащий указанную молекулу нуклеиновой кислоты, кодирует несколько слитых белков, например, описанных в настоящем документе, каждый из которых содержит домен, содержащий CAR, описанный в настоящем документе. В некоторых вариантах осуществления нуклеиновая кислота, кодирующая первый слитый белок, находится под регуляторным контролем (например, промотора, описанного в настоящем документе) отдельно от контроля нуклеиновой кислоты, кодирующей второй слитый белок (например, промотора, описанного в настоящем документе). В других вариантах осуществления две или более нуклеотидные последовательности закодированы одной молекулой нуклеиновой кислоты в одной рамке считывания и в виде одной полипептидной цепи. В данном аспекте два или более слитых белков, например, описанных в настоящем документе, каждый из которых содержит домен, содержащий CAR, могут, например, быть разделены одним или более пептидными сайтами расщепления (например, сайтом ауторасщепления или субстратом для внутриклеточной протеазы). Примеры пептидных сайтов расщепления включают следующие сайты, в которых остатки GSG являются необязательными:
T2A: (GSG) E G R G S L L T C G D V E E N P G P (SEQ ID NO: 190)
P2A: (GSG) A T N F S L L K Q A G D V E E N P G P (SEQ ID NO: 191)
E2A: (GSG) Q C T N Y A L L K L A G D V E S N P G P (SEQ ID NO: 192)
F2A: (GSG) V K Q T L N F D L L K L A G D V E S N P G P (SEQ ID NO: 193).
Способы введения генов в клетку и экспрессии известны в данной области. В контексте экспрессионного вектора, вектор может быть с легкостью введен в клетку-хозяина, например, клетку млекопитающего, бактерии, дрожжей или насекомых, любым способом, известным в данной области. Например, экспрессионный вектор может быть перенесен в клетку-хозяина физическими, химическими или биологическими методами.
Физические методы введения полинуклеотида в клетку-хозяина включают осаждение фосфатом кальция, липофекцию, бомбардировку частицами, микроинъекцию, электропорацию и тому подобные. Методы получения клеток, содержащих векторы и/или экзогенные нуклеиновые кислоты, хорошо известны в данной области. Смотри, например, Sambrook et al., 2012, MOLECULAR CLONING: A LABORATORY MANUAL, volumes 1-4, Cold Spring Harbor Press, NY. Предпочтительным методом введения полинуклеотида в клетку-хозяина является трансфекция с фосфатом кальция или электропорация.
Биологические методы введения интересующего полинуклеотида в клетку-хозяина включают использование ДНК и РНК векторов. Использование вирусных векторов и, в частности, ретровирусных векторов, стало наиболее широко используемым методом введения генов в клетки млекопитающего, например, клетки человека. Другие вирусные векторы могут быть получены из лентивирусов, поксвирусов, вируса простого герпеса I, аденовирусов, аденоассоциированных вирусов и тому подобного. Смотри, например, патенты США №№ 5350674 и 5585362.
Химические методы введения полинуклеотида в клетку-хозяина включают использование коллоидных дисперсионных систем, таких как макромолекулярные комплексы, нанокапсулы, микросферы, гранулы и системы на основе липидов, в том числе, эмульсии типа масло-в-воде, мицеллы, смешанные мицеллы и липосомы. Иллюстративной коллоидной системой для использования в качестве средства доставки in vitro и in vivo является липосома (например, искусственный мембранный везикул). Доступны и другие современные методы направленной доставки нуклеиновых кислот, такие как доставка полинуклеотидов с нацеленными наночастицами или другие подходящие системы доставки субмикронного размера.
В случае, когда используют не вирусную систему доставки, иллюстративным средством доставки является липосома. Использование липидных препаратов предусмотрено для введения нуклеиновых кислот в клетку-хозяина (in vitro, ex vivo или in vivo). В другом аспекте нуклеиновая кислота может быть связана с липидом. Нуклеиновая кислота, связанная с липидом, может быть инкапсулирована в водной внутренней среде липосомы, вкраплена в липидный бислой липосомы, присоединена к липосоме через связывающую молекулу, которая связана как с липосомой, так и с олигонуклеотидом, заключена в липосоме, находиться в комплексе с липосомой, быть диспергированной в растворе, содержащем липид, смешана с липидом, объединена с липидом, содержаться в виде суспензии в липиде, содержаться в мицеллах или находиться в комплексе с мицеллами, либо иным образом быть связанной с липидом. Композиции липида, липида/ДНК или липида/экспрессионного вектора не имеют ограничений в отношении конкретной структуры в растворе. Например, они могут находиться в бислойной структуре, в виде мицелл или иметь «разрушенную» структуру. Они также могут быть просто рассеяны в растворе, возможно, образуя агрегаты, неоднородные по размеру или форме. Липиды представляют собой жирные вещества, которые могут быть природными или синтетическими. Например, липиды включают жирные капли, естественным образом присутствующие в цитоплазме, а также класс соединений, включающих длинноцепочечные алифатические углеводороды и их производные, такие как жирные кислоты, спирты, амины, аминоспирты и альдегиды.
Липиды, подходящие для использования, могут быть получены из коммерческих источников. Например, димиристил фосфатидилхолин («DMPC») может быть приобретен у компании Sigma, St. Louis, MO; дицетил фосфат («DCP») может быть приобретен у компании K & K Laboratories (Plainview, NY); холестерин («Choi») может быть приобретен у компании Calbiochem-Behring; димиристил фосфатидилглицерин («DMPG») и другие липиды могут быть приобретены у компании Avanti Polar Lipids, Inc. (Birmingham, AL.). Матричные растворы липидов в хлороформе или смеси хлороформ/метанол можно хранить при температуре примерно -20°C. Хлороформ используют в качестве единственного растворителя, поскольку он испаряется быстрее, чем метанол. «Липосома» является общим термином, охватывающим множество одно- и многослойных липидных везикул, образующихся при создании замкнутых липидных бислоев или агрегатов. Липосомы могут быть охарактеризованы, как везикулярные структуры с фосфолипидной бислойной мембраной и внутренней водной средой. Многослойные липосомы имеют несколько липидных слоев, разделенных водной средой. Они образуются спонтанно, когда фосфолипиды суспендируют в избытке водного раствора. Липидные компоненты проходят стадию самостоятельного перераспределения, с последующим образованием замкнутых структур и захватом воды и растворенных веществ между липидными бислоями (Ghosh et al., 1991 Glycobiology 5: 505-10). Однако также охвачены композиции, имеющие структуры в растворе, отличные от обычных везикулярных структур. Например, липиды могут принимать структуру мицелл или просто существовать в виде неоднородных агрегатов липидных молекул. Также предусмотрены комплексы липофектамин-нуклеиновая кислота.
Независимо от способа, используемого для введения экзогенных нуклеиновых кислот в клетку-хозяина или иного воздействия на клетку ингибитора по настоящему изобретению, для подтверждения присутствия последовательности рекомбинантной ДНК в клетке-хозяине могут быть использованы различные анализы. Такие анализы включают, например, «молекулярно-биологические» анализы, хорошо известные специалистам в данной области, такие как саузерн- и нозерн-блоттинг, ОТ-ПЦР и ПЦР; «биохимические» анализы, такие как обнаружение присутствия или отсутствия конкретного пептида, например, иммунологическими методами (ELISA и вестерн-блоттинг), или анализы, описанные в настоящем документе для идентификации средств, входящих в объем изобретения.
Настоящее изобретение также относится к вектору, содержащему молекулу нуклеиновой кислоты, кодирующую слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR. В одном варианте осуществления вектор содержит CAR-кодирующую молекулу нуклеиновой кислоты, например, описанную в настоящем документе. В одном варианте осуществления вектор содержит две CAR-кодирующие молекулы нуклеиновой кислоты. В одном аспекте один или более векторов для CAR (например, вектор, содержащий первую CAR-кодирующую молекулу нуклеиновой кислоты, и вектор, содержащий вторую CAR-кодирующую молекулу нуклеиновой кислоты, или вектор, содержащий как первую, так и вторую CAR-кодирующие нуклеиновые кислоты) могут быть непосредственно трансдуцированы в клетку, например, T-клетку или NK-клетку. В одном аспекте вектор представляет собой клонирующий или экспрессионный вектор, например, вектор, включающий, но без ограничения, одну или более плазмид (например, экспрессионные плазмиды, клонирующие векторы, миникольца, минивекторы, двойные микрохромосомы), ретровирусные и лентивирусные векторные конструкты. В одном аспекте вектор способен экспрессировать конструкт CAR в иммунных эффекторных клетках млекопитающих (например, T-клетках, NK-клетках).
В одном варианте осуществления, когда необходима стабильная экспрессия одного или более (например, одного или двух) слитых белков, например, описанных в настоящем документе, каждый из которых содержит домен, содержащий CAR, вектор, содержащий одну или более (например, одну или две) CAR-кодирующих молекул нуклеиновой кислоты, трансдуцируют в иммунную эффекторную клетку. Например, иммунные эффекторные клетки со стабильной экспрессией двух слитых белков, например, описанных в настоящем документе, каждый из которых содержит домен, содержащий CAR, могут быть получены с использованием лентивирусных векторов. Клетки, стабильно экспрессирующие два слитых белка, например, описанных в настоящем документе, каждый из которых содержит домен, содержащий CAR, экспрессируют CAR в течение по меньшей мере 1 недели, 2 недель, 3 недель, 4 недель, 5 недель, 6 недель, 7 недель, 8 недель, 3 месяцев, 6 месяцев, 9 месяцев или 12 месяцев после трансдукции.
В одном варианте осуществления, когда необходима временная экспрессия одного или более (например, одного или двух) слитых белков, например, описанных в настоящем документе, каждый из которых содержит домен, содержащий CAR, одну или более (например, одну или две) кодирующие слитый белок молекулы нуклеиновой кислоты трансфицируют в иммунную эффекторную клетку. Одна или более (например, одна или две) молекул нуклеиновой кислоты, кодирующих слитые белки, например, описанные в настоящем документе, содержащие домен, который содержит CAR, могут представлять собой вектор, содержащий одну или более (например, одну или две) CAR-кодирующие молекулы нуклеиновой кислоты, или in vitro транскрибированную РНК одного или более (например, одного или двух) CAR. In vitro транскрибированные РНК CAR и методы трансфекции в иммунные эффекторные клетки дополнительно описаны ниже. Клетки, временно экспрессирующие один или более (например, один или два) CAR, экспрессируют один или более (например, один или два) CAR в течение 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 дней после трансфекции.
Трансфекция РНК
В настоящем документе раскрыты способы получения in vitro транскрибированной РНК, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR. Настоящее изобретение также охватывает РНК-конструкт, кодирующий слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, который может быть непосредственно трансфицирован в клетку. Способ получения мРНК для использования в трансфекции может включать in vitro транскрипцию (IVT) матрицы со специально разработанными праймерами, с последующим добавлением полиA, с получением конструкта, содержащего 3'- и 5'-нетранслируемую последовательность («UTR»), 5'-кэп и/или внутренний сайт связывания рибосомы (IRES), нуклеиновую кислоту, которую предстоит экспрессировать, и полиA «хвост», как правило, длиной 50-5000 оснований (SEQ ID NO: 32). Полученной таким образом РНК можно эффективно трансфицировать клетки разных видов. В одном аспекте матрица содержит последовательности для CAR.
В одном аспекте слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, по настоящему изобретению закодирован матричной РНК (мРНК). В одном аспекте мРНК, кодирующая CAR, описанный в настоящем документе, вводят в T-клетку или NK-клетку.
В одном варианте осуществления in vitro транскрибированная РНК, кодирующая слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, может быть введена в клетку в форме для временной трансфекции. РНК получают методом in vitro транскрипции с использованием матрицы, полученной с помощью полимеразной цепной реакции (ПЦР). Интересующую ДНК из любого источника можно непосредственно переводить методом ПЦР в матрицу для in vitro синтеза мРНК с использованием соответствующих праймеров и РНК-полимеразы. Источником ДНК может быть, например, геномная ДНК, плазмидная ДНК, фаговая ДНК, кДНК, синтетическая последовательность ДНК или любой другой подходящий источник ДНК. Нужная матрица для in vitro транскрипции представляет собой матрицу слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR, описанный в настоящем документе. Например, матрица для РНК CAR содержит последовательность для внеклеточной области, содержащей одноцепочечный вариабельный домен антитела для антигена, описанного в настоящем документе; шарнирной области (например, шарнирной области, описанной в настоящем документе), трансмембранного домена (например, трансмембранного домена, описанного в настоящем документе, такого как трансмембранный домен CD8a); и цитоплазматической области, которая содержит внутриклеточный сигнальный домен, например, внутриклеточный сигнальный домен, описанный в настоящем документе, например, содержащий сигнальный домен CD3-дзета и сигнальный домен 4-1BB.
В одном варианте осуществления ДНК, используемая для ПЦР, содержит открытую рамку считывания. ДНК может быть из природной последовательности ДНК из генома какого-либо организма. В одном варианте осуществления нуклеиновая кислота может содержать некоторые, или все, из 5'- и/или 3'-нетранслируемых областей (UTR). Нуклеиновая кислота может содержать экзоны и интроны. В одном варианте осуществления ДНК, используемая для ПЦР, представляет собой последовательность нуклеиновой кислоты человека. В другом варианте осуществления ДНК, используемая для ПЦР, представляет собой последовательность нуклеиновой кислоты человека, содержащую 5'- и 3'-UTR. Альтернативно, ДНК может представлять собой искусственную последовательность ДНК, которая обычно не экспрессируется в существующих в природе организмах. Иллюстративная искусственная последовательность ДНК представляет собой последовательность, содержащую фрагменты генов, лигированные вместе, с образованием открытой рамки считывания, кодирующей слитый белок. Фрагменты ДНК, лигированные вместе, могут быть из одного организма или из более, чем одного организма.
ПЦР используют для создания матрицы для in vitro транскрипции мРНК, которую используют для трансфекции. Методы проведения ПЦР хорошо известны в данной области. Праймеры для использования в ПЦР разрабатывают для содержания областей, которые в значительной степени комплементарны областям ДНК, используемым в качестве матрицы для ПЦР. Используемый в настоящем документе термин «в значительной степени комплементарны» относится к последовательностям нуклеотидов, когда большинство, или все, из оснований в последовательности праймера являются комплементарными, либо одно или более оснований являются некомплементарными или несовпадающими. В значительной степени комплементарные последовательности могут отжигаться или гибридизоваться с выбранной ДНК-мишенью в условиях отжига, используемых для ПЦР. Праймеры могут быть разработаны так, чтобы быть в значительной степени комплементарными какому-либо фрагменту ДНК-матрицы. Например, праймеры могут быть разработаны для амплификации фрагмента нуклеиновой кислоты, который обычно транскрибируется в клетках (открытая рамка считывания), включая 5'- и 3'-UTR. Праймеры также могут быть разработаны для амплификации фрагмента нуклеиновой кислоты, который кодирует конкретный интересующий домен. В одном варианте осуществления праймеры разработаны для амплификации кодирующей области кДНК человека, включая все или часть 5'- и 3'-UTR. Праймеры, полезные для ПЦР, могут быть получены методами синтеза, хорошо известными в данной области. «Прямые праймеры» представляют собой праймеры, содержащие область из нуклеотидов, в значительной степени комплементарных нуклеотидам на ДНК-матрице, которые находятся выше последовательности ДНК, которую предстоит амплифицировать. Используемый в настоящем документе термин «выше» означает расположение в направлении 5' от последовательности ДНК, которую предстоит амплифицировать, применительно к кодирующей цепи. «Обратные праймеры» представляют собой праймеры, содержащие область из нуклеотидов, в значительной степени комплементарных нуклеотидам на двухцепочечной ДНК-матрице, которые находятся ниже последовательности ДНК, которую предстоит амплифицировать. Используемый в настоящем документе термин «ниже» означает расположение в направлении 3' от последовательности ДНК, которую предстоит амплифицировать, применительно к кодирующей цепи.
Любую ДНК-полимеразу, используемую для ПЦР, можно использовать в способах, раскрытых в настоящем документе. Реагенты и полимераза коммерчески доступны из целого ряда источников.
Также можно использовать химические структуры, обладающие способностью повышать стабильность и/или эффективность трансляции. РНК предпочтительно содержит 5'- и 3'-UTR. В одном варианте осуществления 5'-UTR имеет длину от одного до 3000 нуклеотидов. Длину последовательностей 5'- и 3'-UTR, добавляемых к кодирующей области, можно изменять разными способами, включая, но без ограничения, разработку праймеров для ПЦР, которые отжигаются с разными областями UTR. С использованием данного подхода, специалист в данной области может изменять длину 5'- и 3'-UTR по мере необходимости для достижения оптимальной эффективности трансляции после трансфекции транскрибированной РНК.
5'- и 3'-UTR могут быть природными, эндогенными 5'- и 3'-UTR из интересующей нуклеиновой кислоты. Альтернативно, можно добавлять последовательности UTR, которые не являются эндогенными для интересующей нуклеиновой кислоты, путем включения последовательностей UTR в прямые и обратные праймеры, или путем другого изменения матрицы. Использование последовательностей UTR, которые не являются эндогенными для интересующей нуклеиновой кислоты, может быть полезным для изменения стабильности и/или эффективности трансляции РНК. Например, известно, что AU-богатые элементы в последовательностях 3'-UTR могут уменьшать стабильность мРНК. Таким образом, 3'-UTR можно выбирать или проектировать для повышения стабильности транскрибированной РНК, исходя из свойств UTR, хорошо известных в данной области.
В одном варианте осуществления 5'-UTR может содержать последовательность Kozak из эндогенной нуклеиновой кислоты. Альтернативно, если 5'-UTR, которая не является эндогенной для интересующей нуклеиновой кислоты, добавляют методом ПЦР, как описано выше, консенсусная последовательность Kozak может быть изменена путем добавления последовательности 5'-UTR. Последовательности Kozak могут повышать эффективность трансляции некоторых РНК-транскриптов, но, судя по всему, не являются необходимыми для эффективной трансляции всех РНК. Необходимость в последовательностях Kozak для многих мРНК известна в данной области. В других вариантах осуществления 5'-UTR может представлять собой 5'-UTR из РНК вируса, РНК-геном которого стабилен в клетках. В других вариантах осуществления в 3'- или 5'-UTR можно использовать различные нуклеотидные аналоги для блокирования деградации мРНК экзонуклеазами.
Чтобы сделать возможным синтез РНК с ДНК-матрицы без необходимости в клонировании гена, промотор транскрипции должен быть присоединен к ДНК-матрице выше последовательности, которая должна быть транскрибирована. Когда последовательность, действующую в качестве промотора для РНК-полимеразы, добавляют к 5'-концу прямого праймера, промотор РНК-полимеразы становится включенным в ПЦР-продукт выше открытой рамки считывания, которая должна быть транскрибирована. В одном предпочтительном варианте осуществления промотор представляет собой промотор полимеразы T7, как описано в другом разделе настоящего документа. Другие полезные промоторы включают, но без ограничения, промоторы РНК-полимеразы T3 и SP6. Консенсусные нуклеотидные последовательности для промоторов T7, T3 и SP6 известны в данной области.
В предпочтительном варианте осуществления мРНК имеет как кэп на 5'-конце, так и 3'-поли(A) «хвост», которые определяют связывание рибосомы, инициацию трансляции и стабильность мРНК в клетке. На кольцевой ДНК-матрице, например, плазмидной ДНК, РНК-полимераза создает длинный конкатемерный продукт, который не подходит для экспрессии в эукариотических клетках. Транскрипция плазмидной ДНК, линеаризованной на конце 3'-UTR, приводит к образованию мРНК нормального размера, которая не эффективна при трансфекции эукариотических клеток, даже если она полиаденилирована после транскрипции.
На линейной ДНК-матрице РНК-полимераза фага T7 может удлинять 3'-конец транскрипта за пределы последнего основания матрицы (Schenborn and Mierendorf, Nuc Acids Res., 13:6223-36 (1985); Nacheva and Berzal-Herranz, Eur. J. Biochem., 270:1485-65 (2003).
Общепринятым методом включения полиA/T участков в ДНК-матрицу является молекулярное клонирование. Однако полиA/T последовательность, включенная в плазмидную ДНК, может вызывать нестабильность плазмиды, вследствие чего плазмидные ДНК-матрицы, полученные из бактериальных клеток, часто являются сильно засоренными делециями и другими аберрациями. Это делает процедуры клонирования не только трудоемкими и занимающими много времени, но часто и ненадежными. Вследствие этого, существует насущная потребность в способе, позволяющем конструировать ДНК-матрицы с полиA/T 3'-участком без клонирования.
ПолиA/T сегмент транскрибируемой ДНК-матрицы может быть получен в процессе ПЦР за счет использования обратного праймера, содержащего полиT «хвост», например 100T «хвост» (SEQ ID NO: 968) (размер может составлять 50-5000 T (SEQ ID NO: 974)), или после ПЦР любым другим методом, включая, но без ограничения, лигирование ДНК или in vitro рекомбинацию. Поли(A) «хвосты» также обеспечивают стабильность молекул РНК и способствуют уменьшению их деградации. Как правило, длина поли(A) «хвоста» положительно коррелирует со стабильностью транскрибированной РНК. В одном варианте осуществления поли(A) «хвост» содержит от 100 до 5000 остатков аденозина (SEQ ID NO: 82).
Поли(A) «хвосты» молекул РНК можно дополнительно удлинять после in vitro транскрипции при помощи поли(A)-полимеразы, такой как полиA-полимераза E. coli (E-PAP). В одном варианте осуществления увеличение длины поли(A) «хвоста» от 100 нуклеотидов до 300-400 нуклеотидов (SEQ ID NO: 969) приводит примерно к двукратному увеличению эффективности трансляции РНК. Кроме того, присоединение разных химических групп к 3'-концу может приводить к повышению стабильности мРНК. Такой присоединенный фрагмент может содержать модифицированные/искусственные нуклеотиды, аптамеры и другие соединения. Например, в поли(A) «хвост» могут быть включены аналоги АТФ с использованием поли(A)-полимеразы. Аналоги АТФ могут дополнительно повышать стабильность РНК.
5'-кэпы также придают стабильность молекулам РНК. В предпочтительном варианте осуществления молекулы РНК, полученные способами, раскрытыми в настоящем документе, содержат 5'-кэп. 5'-кэп вводят методами, известными в данной области и описанными в настоящем документе (Cougot, et al., Trends in Biochem. Sci., 29:436-444 (2001); Stepinski, et al., РНК, 7:1468-95 (2001); Elango, et al., Biochim. Biophys. Res. Commun., 330:958-966 (2005)).
Молекулы РНК, полученные способами, раскрытыми в настоящем документе, также могут содержать последовательность внутреннего сайта связывания рибосомы (IRES). Последовательность IRES может представлять собой любую вирусную, хромосомную или искусственно созданную последовательность, которая инициирует кэп-независимое связывание рибосомы с мРНК и способствует инициации трансляции. Могут быть включены любые растворенные вещества, подходящие для электропорации клетки, которые включают факторы, повышающие проницаемость и жизнеспособность клеток, такие как сахара, пептиды, липиды, белки, антиоксиданты и сурфактанты.
РНК может быть введена в клетки-мишени с использованием любого из множества разных методов, например, коммерчески доступных методов, которые включают, но без ограничения, электропорацию (Amaxa Nucleofector-II (Amaxa Biosystems, Cologne, Germany)), (ECM 830 (BTX) (Harvard Instruments, Boston, Mass.) или Gene Pulser II (BioRad, Denver, Colo.), Multiporator (Eppendort, Hamburg Germany), опосредованную катионными липосомами трансфекцию с использованием липофекции, инкапсуляцию в полимер, опосредованную пептидами трансфекцию или биолистические системы доставки частиц, такие как «генные пушки» (смотри, например, Nishikawa, et al. Hum Gene Ther., 12(8):861-70 (2001).
Невирусные способы доставки
В некоторых аспектах для доставки нуклеиновой кислоты, кодирующей химерную молекулу или слитый белок, описанный в настоящем документе, в клетку или ткань, или организм субъекта могут быть использованы невирусные способы.
В некоторых вариантах осуществления невирусный способ включает использование транспозона (также называемого транспозиционным элементом). В некоторых вариантах осуществления транспозон представляет собой фрагмент ДНК, который может встраиваться в участок генома, например, фрагмент ДНК, который способен к саморепликации и встраиванию своей копии в геном, или фрагмент ДНК, который может быть вырезан из более длинной нуклеиновой кислоты и вставлен в другой участок генома. Например, транспозон содержит последовательность ДНК, состоящую из инвертированных повторов, фланкирующих гены, предназначенные для транспозиции.
В некоторых вариантах осуществления получают клетки, например, T- или NK-клетки, которые экспрессируют химерную молекулу или слитый белок, например, описанный в настоящем документе, например, используя сочетание вставки генов при помощи SBTS и генетическое редактирование при помощи нуклеазы (например, нуклеаз «цинковые пальцы» (ZFN), подобных активатору транскрипции эффекторных нуклеаз (TALEN), системы CRISPR/Cas или сконструированной мегануклеазы реконструированной хоуминг-эндонуклеазы).
В некоторых вариантах осуществления использование невирусного способа доставки позволяет перепрограммировать клетки, например, T- или NK-клетки, и вводить клетки субъекту прямой инфузией. Преимущества невирусных векторов включают, но не ограничиваются ими, легкость и относительно низкую стоимость получения достаточных количеств, удовлетворяющих потребностям пациентов, стабильность при хранении и отсутствие иммуногенности.
Клетки-хозяева
По настоящему изобретению также предложены клетки, например, иммунные эффекторные клетки (например, популяция клеток, например, популяция иммунных эффекторных клеток), содержащие молекулу нуклеиновой кислоты, молекулу слитого белка, или вектор, например, описанные в настоящем документе. В некоторых вариантах осуществления предложенные клетки содержат слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, молекулу нуклеиновой кислоты, кодирующую слитый белок, содержащий домен, который содержит CAR, или вектор, содержащий ее.
В некоторых аспектах иммунные эффекторные клетки, например, T-клетки или NK клетки, могут быть получены из образца крови, полученного от субъекта, с использованием разных методов, известных квалифицированному специалисту, например, разделения в градиенте фиколла™. В одном предпочтительном аспекте клетки из циркулирующей крови индивидуума получают путем афереза. Продукт афереза, как правило, содержит лимфоциты, в том числе T-клетки, моноциты, гранулоциты, B-клетки, другие ядросодержащие белые клетки крови, эритроциты и тромбоциты. В одном аспекте клетки, собранные при аферезе, можно промывать для удаления фракции плазмы и помещать клетки в соответствующий буфер или среду для последующих этапов обработки. В одном варианте осуществления клетки промывают фосфатно-солевым буфером (PBS). В альтернативном варианте осуществления в промывающем растворе отсутствует кальций и может отсутствовать магний, или могут отсутствовать многие, если не все, двухвалентные катионы.
Начальные этапы активации в отсутствие кальция могут приводить к повышению активации. Как понятно специалистам в данной области, этап промывания можно выполнять методами, известными в данной области, например, с использованием полуавтоматической «проточной» центрифуги (например, Cobe 2991 cell processor, Baxter CytoMate или Haemonetics Cell Saver 5) в соответствии с инструкциями производителя. После промывания клетки можно ресуспендировать в различных биосовместимых буферах, таких как, например, не содержащий Ca, не содержащий Мg PBS, PlasmaLyte A, или другом солевом растворе с буфером или без буфера. Альтернативно, нежелательные компоненты из образца, полученного при аферезе, можно удалять, и клетки непосредственно ресуспендировать в культуральной среде.
Признано, что в способах по данной заявке можно использовать культуральную среду, содержащую 5% или менее, например, 2%, человеческой AB сыворотки, и использовать известные среды и композиции для культивирования, например, те, которые описаны в Smith et al., «Ex vivo expansion of human T cells for adoptive immunotherapy using the novel Xeno-free CTS Immune Cell Serum Replacement» Clinical & Translational Immunology (2015) 4, e31; doi:10.1038/cti.2014.31.
В одном аспекте T-клетки выделяют из лимфоцитов периферической крови, проводя лизис эритроцитов и истощение моноцитов, например, методом центрифугирования в градиенте перколла™ или проточного элютриационного центрифугирования.
Способы, описанные в настоящем документе, могут включать, например, отбор конкретной субпопуляции иммунных эффекторных клеток, например, T-клеток, которая представляет собой популяцию, истощенную по регуляторным T-клеткам, истощенную по CD25+ клеткам, с использованием, например, метода отрицательного отбора, например, описанного в настоящем документе. Предпочтительно, популяция, истощенная по регуляторным T-клеткам, содержит менее 30%, 25%, 20%, 15%, 10%, 5%, 4%, 3%, 2%, 1% CD25+ клеток.
В одном варианте осуществления регуляторные T-клетки, например, CD25+ T-клетки, удаляют из популяции с использованием анти-CD25 антитела или его фрагмента, или CD25-связывающего лиганда, IL-2. В одном варианте осуществления анти-CD25 антитело или его фрагмент, или CD25-связывающий лиганд, конъюгированы с субстратом, например, гранулой, или иным образом нанесены на субстрат, например, гранулу. В одном варианте осуществления анти-CD25 антитело или его фрагмент конъюгированы с субстратом, как описано в настоящем документе.
В одном варианте осуществления регуляторные T-клетки, например, CD25+ T-клетки, удаляют из популяции с использованием CD25-истощающего реагента от компании Miltenyi™. В одном варианте осуществления соотношение клеток и CD25-истощающего реагента составляет 1e7 клеток на 20 мкл или 1e7 клеток на 15 мкл, или 1e7 клеток на 10 мкл, или 1e7 клеток на 5 мкл, или 1e7 клеток на 2,5 мкл, или 1e7 клеток на 1,25 мкл. В одном варианте осуществления, например, для истощения регуляторных T-клеток, например, истощения CD25+ клеток, используют более 500 миллионов клеток/мл. В следующем аспекте используют концентрацию клеток 600, 700, 800 или 900 миллионов клеток/мл.
В одном варианте осуществления популяция иммунных эффекторных клеток, подлежащих истощению, включает примерно 6×109 CD25+ T-клеток. В других аспектах популяция иммунных эффекторных клеток, подлежащих истощению, включает примерно от 1×109 до 1x 1010 CD25+ T-клеток, а также любое промежуточное целое значение. В одном варианте осуществления полученная популяция, истощенная по регуляторным T-клеткам, содержит 2×109 регуляторных T-клеток, например, CD25+ клеток, или менее (например, 1×109, 5×108, 1×108, 5×107, 1×107 или менее CD25+ клеток).
В одном варианте осуществления регуляторные T-клетки, например, CD25+ клетки, удаляют из популяции с использованием системы CliniMAC с комплектом трубок для истощения, таким как, например, трубки 162-01. В одном варианте осуществления систему CliniMAC используют с такими параметрами, как, например, DEPLETION2.1.
Без связи с конкретной теорией, снижение уровня отрицательных регуляторов иммунных клеток (например, уменьшение числа нежелательных иммунных клеток, например, TREG клеток) у субъекта перед проведением афереза или при производстве клеток, экспрессирующих слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, может уменьшать риск рецидива у субъекта. Например, способы истощения TREG клеток хорошо известны в данной области. Способы сокращения количества TREG клеток включают, но без ограничения, использование циклофосфамида, анти-GITR антитела (анти-GITR антитела, описанного в настоящем документе), CD25-истощения, а также их сочетания.
В некоторых вариантах осуществления способы производства включают уменьшение количества (например, истощение) TREG клеток перед получением клетки, экспрессирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR. Например, способы получения включают создание контакта образца, например, образца, полученного при аферезе, с анти-GITR антителом и/или анти-CD25 антителом (или его фрагментом, или CD25-связывающим лигандом), например, для истощения TREG клеток перед получением препарата CAR-экспрессирующей клетки (например, T-клетки, NK-клетки).
В одном из вариантов осуществления субъект предварительно получает одно или более терапевтических средств, которые уменьшают количество TREG клеток, перед сбором клеток для получения препарата клетки, экспрессирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, что приводит к уменьшению риска рецидива у субъекта при лечении клетками, экспрессирующими слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR. В одном из вариантов осуществления способы уменьшения количества TREG клеток включают, но без ограничения, введение субъекту одного или более из циклофосфамида, анти-GITR антитела, CD25-истощающего средства, или их сочетания. Введение одного или более из циклофосфамида, анти-GITR антитела, CD25-истощающего средства, или их сочетания может происходить до, в процессе или после инфузии препарата CAR-экспрессирующих клеток.
В одном из вариантов осуществления субъект предварительно получает циклофосфамид до сбора клеток для получения препарата CAR-экспрессирующих клеток, что приводит к уменьшению риска рецидива у субъекта при лечении клетками, экспрессирующими слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR. В одном из вариантов осуществления субъект предварительно получает анти-GITR антитело до сбора клеток для получения препарата CAR-экспрессирующих клеток, что приводит к уменьшению риска рецидива у субъекта при лечении CAR-экспрессирующими клетками.
В одном варианте осуществления популяция клеток, подлежащих удалению, представляет собой не регуляторные T-клетки или опухолевые клетки, но клетки, которые иным образом отрицательно влияют на размножение и/или функцию CAR T-клеток, например, клетки, экспрессирующие CD14, CD11b, CD33, CD15 или другие маркеры, экспрессируемые потенциально иммуносупрессорными клетками. В одном варианте осуществления предусмотрено, что такие клетки будут удалены одновременно с регуляторными T-клетками и/или опухолевыми клетками, или после указанного истощения, или в ином порядке.
Способы, описанные в настоящем документе, могут включать более одного этапа отбора, например, более одного этапа истощения. Обогащение популяции T-клеток за счет отрицательного отбора можно осуществлять с помощью комбинации антител, направленных на поверхностные маркеры, уникальные для отрицательно отбираемых клеток. Одним из способов является сортировка и/или отбор клеток за счет отрицательной магнитной иммунной адгезии или проточной цитометрии, где используют коктейль моноклональных антител, направленных на клеточные поверхностные маркеры, присутствующие на отрицательно отбираемых клетках. Например, для обогащения по CD4+ клеткам методом отрицательного отбора коктейль моноклональных антител, как правило, включает антитела к CD14, CD20, CD11b, CD16, HLA-DR и CD8.
Способы, описанные в настоящем документе, могут дополнительно включать удаление из популяции клеток, экспрессирующих опухолевый антиген, например, опухолевый антиген, не включающий CD25, например, CD19, CD30, CD38, CD123, CD20, CD14 или CD11b, для получения популяции клеток, истощенных по регуляторным T-клеткам, например, истощенных по CD25+ клеткам, и истощенных по клеткам с опухолевым антигеном, которые подходят для экспрессии слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR, например, CAR, описанный в настоящем документе. В одном варианте осуществления экспрессирующие опухолевый антиген клетки удаляют одновременно с регуляторными T-клетками, например, CD25+ клетками. Например, анти-CD25 антитело, или его фрагмент, и антитело против опухолевого антигена, или его фрагмент, можно присоединять к одному и тому же субстрату, например, грануле, которую можно использовать для удаления клеток, или анти-CD25 антитело, или его фрагмент, и антитело против опухолевого антигена, или его фрагмент, можно присоединять к разным гранулам, смесь которых можно использовать для удаления клеток. В других вариантах осуществления удаление регуляторных T-клеток, например, CD25+ клеток, и удаление экспрессирующих опухолевый антиген клеток проводят последовательно, например, в любом порядке.
Также предложены способы, включающие удаление из популяции клеток, экспрессирующих ингибитор иммунных контрольных точек, например, ингибитор иммунных контрольных точек, описанный в настоящем документе, например, один или более видов клеток из PD-1+ клеток, LAG3+ клеток и TIM3+ клеток, для получения популяции клеток, истощенной по регуляторным T-клеткам, например, истощенной по CD25+ клеткам, и истощенной по клеткам, экспрессирующим ингибитор иммунных контрольных точек, например, истощенной по PD-1+, LAG3+ и/или TIM3+ клеткам. Иллюстративные ингибиторы иммунных контрольных точек включают B7-H1, B7-1, CD160, P1H, 2B4, PD-1, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, TIGIT, CTLA-4, BTLA и LAIR1. В одном варианте осуществления экспрессирующие ингибитор иммунных контрольных точек клетки удаляют одновременно с регуляторными T-клетками, например, CD25+ клетками. Например, анти-CD25 антитело, или его фрагмент, и антитело против ингибитора иммунных контрольных точек, или его фрагмент, можно присоединять к одной и той же грануле, которую можно использовать для удаления клеток, или анти-CD25 антитело, или его фрагмент, и антитело против ингибитора иммунных контрольных точек, или его фрагмент, можно присоединять к разным гранулам, смесь которых можно использовать для удаления клеток. В других вариантах осуществления удаление регуляторных T-клеток, например, CD25+ клеток, и удаление экспрессирующих ингибитор иммунных контрольных точек клеток проводят последовательно, например, в любом порядке.
Способы, описанные в настоящем документе, могут включать этап положительного отбора. Например, T-клетки можно выделять путем инкубации с гранулами, конъюгированными с анти-CD3/анти-CD28 (например, 3×28) антителами, такими как DYNABEADS® M-450 CD3/CD28 T, в течение периода времени, достаточного для положительного отбора нужных T-клеток. В одном варианте осуществления период времени составляет примерно 30 минут. В следующем варианте осуществления период времени составляет от 30 минут до 36 часов или дольше, а также все промежуточные целые значения. В следующем варианте осуществления период времени составляет по меньшей мере 1, 2, 3, 4, 5 или 6 часов. В другом варианте осуществления период времени составляет от 10 до 24 часов, например, 24 часа. Можно использовать более длительное время инкубации для выделения T-клеток в том случае, когда T-клетки представлены в небольшом количестве, в сравнении с клетками других типов, например, при выделении опухоль-инфильтрирующих лимфоцитов (TIL) из опухолевой ткани, или из крови индивидуумов с иммунной недостаточностью. Кроме того, использование более продолжительного времени инкубации может повышать эффективность захвата CD8+ T-клеток. Таким образом, за счет простого сокращения или продления времени T-клеткам дают возможность связываться с CD3/CD28 гранулами, и/или за счет увеличения или уменьшения соотношения количества гранул и T-клеток (как описано далее в настоящем документе) можно проводить отбор предпочтительно в пользу или не в пользу субпопуляций T-клеток в начале или в другие моменты времени в процессе культивирования. Кроме того, за счет увеличения или уменьшения соотношения количества анти-CD3 и/или анти-CD28 антител на гранулах или другой поверхности можно проводить отбор предпочтительно в пользу или не в пользу субпопуляций T-клеток в начале культивирования или в другие нужные моменты времени.
В одном варианте осуществления можно выбирать популяцию T-клеток, которые экспрессируют одно или более из IFNγ, TNFα, IL-17A, IL-2, IL-3, IL-4, GM-CSF, IL-10, IL-13, гранзима B и перфорина, или другие соответствующие молекулы, например, другие цитокины. Можно использовать методы скрининга клеток на экспрессию, например, методы, описанные в PCT публикации № WO 2013/126712.
При выделении нужной популяции клеток методом положительного или отрицательного отбора концентрацию клеток и поверхностей (например, частиц, таких как гранулы) можно варьировать. В некоторых аспектах может быть желательно значительно уменьшать объем, в котором гранулы и клетки смешивают вместе (например, увеличивать концентрацию клеток), для обеспечения максимального контакта клеток и гранул. Например, в одном аспекте используют концентрацию 10 миллиардов клеток/мл, 9 миллиардов клеток/мл, 8 миллиардов клеток/мл, 7 миллиардов клеток/мл, 6 миллиардов клеток/мл или 5 миллиардов клеток/мл. В одном аспекте используют концентрацию 1 миллиард клеток/мл. В еще одном аспекте используют концентрацию клеток 75, 80, 85, 90, 95 или 100 миллионов клеток/мл. В следующих аспектах могут быть использованы концентрации 125 или 150 миллионов клеток/мл.
Использование высоких концентраций может приводить к увеличению выхода клеток, активации клеток и размножения клеток. Кроме того, использование высоких концентраций клеток позволяет более эффективно захватывать клетки, которые могут слабо экспрессировать интересующие антигены-мишени, например, CD28-отрицательные T-клетки, или клетки из образцов, где присутствует множество опухолевых клеток (таких как лейкозная кровь, опухолевая ткань и так далее). Такие популяции клеток могут иметь терапевтическую ценность, и их может быть желательно получать. Например, использование высокой концентрации клеток позволяет более эффективно производить отбор CD8+ T-клеток, которые обычно имеют более слабую экспрессию CD28.
В связанном аспекте может быть желательно использовать более низкие концентрации клеток. При значительном разбавлении смеси T-клеток и поверхностей (например, частиц, таких как гранулы) взаимодействие между частицами и клетками сводится к минимуму. Это позволяет отбирать клетки, экспрессирующие в большом количестве нужные антигены, связывающиеся с частицами. Например, CD4+ T-клетки экспрессируют CD28 на более высоком уровне и более эффективно захватываются, чем CD8+ T-клетки, при низких концентрациях. В одном аспекте используемая концентрация клеток составляет 5×106/мл. В других аспектах используемая концентрация может составлять от примерно 1×105/мл до 1×106/мл, а также любое промежуточное целое значение.
В других аспектах клетки можно инкубировать на ротаторе в течение разных периодов времени с разными скоростями, либо при 2-10°C, либо при комнатной температуре.
T-клетки, предназначенные для стимуляции, также можно замораживать после этапа промывания. Без связи с конкретной теорией, этап замораживания и последующего размораживания приводит к получению более однородного препарата за счет удаления гранулоцитов и, в некоторой степени, моноцитов из клеточной популяции. После этапа промывания, при котором удаляют плазму и тромбоциты, клетки можно суспендировать в растворе для замораживания. Хотя в данной области известно множество растворов для замораживания и параметров, которые будут полезны в данном контексте, один из способов включает использование PBS, содержащего 20% ДМСО и 8% человеческого сывороточного альбумина, или культуральной среды, содержащей 10% декстрана 40 и 5% декстрозы, 20% человеческого сывороточного альбумина и 7,5% ДМСО, или 31,25% плазмалита A, 31,25% декстрозы 5%, 0,45% NaCl, 10% декстрана 40 и 5% декстрозы, 20% человеческого сывороточного альбумина и 7,5% ДМСО, или другой подходящей среды для замораживания клеток, содержащей, например, геспан и плазмалит A; клетки затем замораживают до -80°C со скоростью 1° в минуту и хранят в паровой фазе в резервуаре с жидким азотом. Можно использовать и другие способы контролируемого замораживания, а также неконтролируемого немедленного замораживания при -20°C или в жидком азоте.
В некоторых аспектах криоконсервированные клетки размораживают и промывают, как описано в настоящем документе, и оставляют отстаиваться на один час при комнатной температуре перед активацией с использованием способов по настоящему изобретению.
В контексте изобретения также предусмотрен сбор образцов крови или продукта афереза от субъекта в период времени до того, когда могут понадобиться размноженные клетки, описанные в настоящем документе. В силу этого, источник клеток, которые будут размножены, можно собирать в любой желательный момент времени, и нужные клетки, такие как T-клетки, выделять и замораживать для более позднего использования в терапии иммунными эффекторными клетками ряда заболеваний или состояний, при которых может приносить пользу терапия иммунными эффекторными клетками, такими как те, которые описаны в настоящем документе. В одном аспекте образец крови или продукт афереза получают от, в целом, здорового субъекта. В некоторых аспектах образец крови или продукт афереза получают от, в целом, здорового субъекта, который имеет риск развития заболевания, но у которого заболевание пока не развилось, и интересующие клетки выделяют и замораживают для более позднего использования. В некоторых аспектах T-клетки могут быть размножены, заморожены и использованы в более позднее время. В некоторых аспектах образцы собирают от пациента вскоре после диагностирования конкретного заболевания, описанного в настоящем документе, но до проведения какого-либо лечения. В следующем аспекте клетки выделяют из образца крови или продукта афереза, полученного от субъекта до применения любого количества соответствующих методов лечения, включая, но без ограничения, лечение такими средствами, как натализумаб, эфализумаб, противовирусные средства, химиотерапия, лучевая терапия, иммуносупрессивные средства, такие как циклоспорин, азатиоприн, метотрексат, микофенолят и FK506, антитела или другие иммуноабляционные средства, например, кампат, анти-CD3 антитела, цитоксан, флударабин, циклоспорин, FK506, рапамицин, микофеноловая кислота, стероиды, FR901228 и облучение.
В следующем аспекте настоящего изобретения T-клетки получают от пациента непосредственно после лечения, которое оставляет у субъекта функциональные T-клетки. В этом отношении, было установлено, что после применения определенных методов лечения рака, в частности, лечения лекарственными средствами, повреждающими иммунную систему, вскоре после лечения в течение периода, когда пациенты, как правило, восстанавливаются после лечения, качество полученных T-клеток может быть оптимальным или улучшенным с точки зрения их способности размножаться ex vivo. Аналогично, после ex vivo манипуляции с использованием способов, описанных в настоящем документе, эти клетки могут находиться в предпочтительном состоянии для лучшей приживаемости и размножения in vivo. Таким образом, в контексте настоящего изобретения предусмотрен сбор клеток крови, включая T-клетки, дендритные клетки или другие клетки гемопоэтической линии дифференцировки, во время этой стадии восстановления. Кроме того, в некоторых аспектах можно использовать схемы мобилизации (например, мобилизации за счет GM-CSF) и кондиционирования для создания условий в организме субъекта, которые благоприятствуют репопуляции, рециркуляции, регенерации и/или размножению отдельных типов клеток, в частности, на протяжении определенного периода времени после терапии. Иллюстративные типы клеток включают T-клетки, B-клетки, дендритные клетки и другие клетки иммунной системы.
В одном варианте осуществления иммунные эффекторные клетки, экспрессирующие слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит молекулу CAR, например, молекулу CAR, описанную в настоящем документе, получают от субъекта, который получал низкую, иммуностимулирующую дозу ингибитора mTOR. В одном из вариантов осуществления популяцию иммунных эффекторных клеток, например, T-клеток, которые будут генетически модифицированы для экспрессии CAR, собирают после достаточного периода времени, или после достаточного введения низкой, иммуностимулирующей дозы ингибитора mTOR, так что уровень PD-1-отрицательных иммунных эффекторных клеток, например, T-клеток, или соотношение PD-1-отрицательных иммунных эффекторных клеток, например, T-клеток/PD-1-положительных иммунных эффекторных клеток, например, T-клеток, у субъекта, или полученных от субъекта, по меньшей мере временно, является повышенным.
В других вариантах осуществления популяцию иммунных эффекторных клеток, например, T-клеток, которые были, или будут генетически модифицированы для экспрессии слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR, можно обрабатывать ex vivo путем создания контакта с количеством ингибитора mTOR, повышающим число PD-1-отрицательных иммунных эффекторных клеток, например, T-клеток, или повышающим соотношение PD-1-отрицательных иммунных эффекторных клеток, например, T-клеток/PD-1-положительных иммунных эффекторных клеток, например, T-клеток.
В одном варианте осуществления T-клетки в популяции являются дефицитными по диацилглицеринкиназе (DGK). DGK-дефицитные клетки включают клетки, которые не экспрессируют РНК или белок DGK, или имеют сниженную или ингибированную активность DGK. DGK-дефицитные клетки могут быть получены генетическими методами, например, путем введения РНК-интерферирующих средств, например, киРНК, кшРНК, микроРНК, для уменьшения или предотвращения экспрессии DGK. Альтернативно, DGK-дефицитные клетки могут быть получены путем обработки ингибиторами DGK, описанными в настоящем документе.
В одном варианте осуществления T-клетки в популяции являются дефицитными по Ikaros. Ikaros-дефицитные клетки включают клетки, которые не экспрессируют РНК или белок Ikaros, или имеют сниженную или ингибированную активность Ikaros. Ikaros-дефицитные клетки могут быть получены генетическими методами, например, путем введения РНК-интерферирующих средств, например, киРНК, кшРНК, микроРНК, для уменьшения или предотвращения экспрессии Ikaros. Альтернативно, Ikaros-дефицитные клетки могут быть получены путем обработки ингибиторами Ikaros, например, леналидомидом.
В вариантах осуществления T-клетки в популяции являются дефицитными по DGK и дефицитными по Ikaros, например, не экспрессируют DGK и Ikaros, или имеют сниженную или ингибированную активность DGK и Ikaros. Такие дефицитные по DGK и Ikaros клетки могут быть получены любым из способов, описанных в настоящем документе.
В одном из вариантов осуществления NK-клетки получены от субъекта. В другом варианте осуществления NK-клетки представляют собой линию NK-клеток, например, линию клеток NK-92 (Conkwest).
Дополнительные экспрессируемые средства
В другом варианте осуществления иммунная эффекторная клетка, экспрессирующая слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, описанная в настоящем документе, также может экспрессировать другое средство, например, средство, повышающее активность CAR-экспрессирующей клетки. Например, в одном варианте осуществления средство может представлять собой средство, которое ингибирует ингибирующую молекулу. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета, например, описанные в настоящем документе. В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, содержит первый полипептид, например, ингибирующую молекулу, связанный со вторым полипептидом, который передает положительный сигнал клетке, например, внутриклеточным сигнальным доменом, описанным в настоящем документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 или TGFR-бета, либо фрагмент любой из них, и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в настоящем документе (например, содержащий костимулирующий домен (например, 41BB, CD27 или CD28, например, описанный в настоящем документе) и/или основной сигнальный домен (например, сигнальный домен CD3-дзета, описанный в настоящем документе). В одном варианте осуществления средство содержит первый полипептид PD-1 или его фрагмент и второй полипептид внутриклеточного сигнального домена, описанного в настоящем документе (например, сигнального домена CD28, CD27, OX40 или 4-IBB, описанного в настоящем документе, и/или сигнального домена CD3-дзета, описанного в настоящем документе).
В одном варианте осуществления иммунная эффекторная клетка, экспрессирующая слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, описанная в настоящем документе, также может содержать второй слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, например, второй CAR, содержащий другой антигенсвязывающий домен, например, для той же мишени (например, мишени, описанной выше) или другой мишени. В одном варианте осуществления второй CAR содержит антигенсвязывающий домен для мишени, экспрессируемой на того же типа раковой клетке, что и мишень для первого CAR. В одном варианте осуществления CAR-экспрессирующая иммунная эффекторная клетка имеет первый CAR, нацеленный на первый антиген и содержащий внутриклеточный сигнальный домен, содержащий костимулирующий сигнальный домен, но не основной сигнальный домен, и второй CAR, нацеленный на второй, отличающийся, антиген и содержащий внутриклеточный сигнальный домен, содержащий основной сигнальный домен, но не костимулирующий сигнальный домен.
Без связи с конкретной теорией, размещение костимулирующего сигнального домена, например, 4-1BB, CD28, CD27 или OX-40, на первом CAR и основного сигнального домена, например, CD3-дзета, на втором CAR может ограничивать активность CAR только клетками, на которых экспрессированы обе мишени. В одном варианте осуществления CAR-экспрессирующая иммунная эффекторная клетка имеет первый CAR, содержащий антигенсвязывающий домен, который нацелен, например, на мишень, описанную выше, трансмембранный домен и костимулирующий домен, и второй CAR, который нацелен на антиген, отличный от антигена, на который нацелен первый CAR (например, антиген, экспрессируемый на того же типа раковой клетке, что и первая мишень) и содержит антигенсвязывающий домен, трансмембранный домен и основной сигнальный домен. В другом варианте осуществления CAR-экспрессирующая иммунная эффекторная клетка имеет первый CAR, содержащий антигенсвязывающий домен, который нацелен, например, на мишень, описанную выше, трансмембранный домен и основной сигнальный домен, и второй CAR, нацеленный на антиген, отличный от антигена, на который нацелен первый CAR (например, антиген, экспрессируемый на того же типа раковой клетке, что и первая мишень) и содержит антигенсвязывающий домен для антигена, трансмембранный домен и костимулирующий сигнальный домен.
В одном варианте осуществления CAR-экспрессирующая иммунная эффекторная клетка имеет CAR, описанный в настоящем документе, например, CAR для мишени, описанной выше, и ингибирующий CAR. В одном варианте осуществления ингибирующий CAR содержит антигенсвязывающий домен, который связывает антиген, присутствующий на нормальных клетках, но не раковых клетках, например, нормальных клетках, которые также экспрессируют мишень. В одном варианте осуществления ингибирующий CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен ингибирующей молекулы. Например, внутриклеточный домен ингибирующего CAR может представлять собой внутриклеточный домен PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 или TGFR-бета.
В одном варианте осуществления иммунная эффекторная клетка (например, T-клетка, NK-клетка) имеет первый CAR, содержащий антигенсвязывающий домен, который связывается с опухолевым антигеном, описанным в настоящем документе, и второй CAR, содержащий внеклеточный домен PD-1 или его фрагмента.
В одном варианте осуществления клетка также содержит ингибирующую молекулу, описанную выше.
В одном варианте осуществления второй CAR в клетке представляет собой ингибирующий CAR, при этом ингибирующий CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен ингибирующей молекулы. Ингибирующую молекулу можно выбирать из одного или более из: PD-1, PD-L1, CTLA-4, TIM-3, LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, TGFR-бета, CEACAM-1, CEACAM-3, и CEACAM-5. В одном варианте осуществления вторая молекула CAR содержит внеклеточный домен PD-1 или его фрагмента.
В вариантах осуществления вторая молекула CAR в клетке также содержит внутриклеточный сигнальный домен, содержащий основной сигнальный домен и/или внутриклеточный сигнальный домен.
В других вариантах осуществления внутриклеточный сигнальный домен в клетке содержит основной сигнальный домен, содержащий функциональный домен CD3-дзета, и костимулирующий сигнальный домен, содержащий функциональный домен 4-1BB.
В одном варианте осуществления вторая молекула CAR в клетке содержит аминокислотную последовательность SEQ ID NO: 26.
В конкретных вариантах осуществления антигенсвязывающий домен первой молекулы CAR содержит scFv, а антигенсвязывающий домен второй молекулы CAR не содержит scFv. Например, антигенсвязывающий домен первой молекулы CAR содержит scFv, а антигенсвязывающий домен второй молекулы CAR содержит домен VHH верблюдовых.
Расщепленный CAR
В некоторых вариантах осуществления в CAR-экспрессирующей клетке используют расщепленный CAR. Подход с использованием расщепленного CAR более подробно описан в патентных публикациях WO2014/055442 и WO2014/055657. Вкратце, система расщепленного CAR включает клетку, экспрессирующую первый CAR, содержащий первый антигенсвязывающий домен и костимулирующий домен (например, 41BB), при этом клетка также экспрессирует второй CAR, содержащий второй антигенсвязывающий домен и внутриклеточный сигнальный домен (например, CD3-дзета). Когда клетка встречается с первым антигеном, костимулирующий домен активируется, и клетка пролиферирует. Когда клетка встречается со вторым антигеном, внутриклеточный сигнальный домен активируется, и запускается цитолитическая активность. Таким образом, CAR-экспрессирующая клетка полностью активируется лишь в присутствии обоих антигенов.
Экспрессия нескольких CAR
В одном аспекте клетка, экспрессирующая слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, описанный в настоящем документе, также может содержать второй слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, например, второй CAR, который содержит другой антигенсвязывающий домен, например, для той же мишени или иной мишени (например, для мишени, отличной от ассоциированного с раком антигена, описанного в настоящем документе, или для другого ассоциированного с раком антигена, описанного в настоящем документе). В одном варианте осуществления второй CAR содержит антигенсвязывающий домен для мишени, экспрессируемой на того же типа раковой клетке, что и ассоциированный с раком антиген. В одном варианте осуществления CAR-экспрессирующая клетка имеет первый CAR, который нацелен на первый антиген и содержит внутриклеточный сигнальный домен, содержащий костимулирующий сигнальный домен, но не основной сигнальный домен, и второй CAR, который нацелен на второй, отличающийся, антиген и содержит внутриклеточный сигнальный домен, содержащий основной сигнальный домен, но не костимулирующий сигнальный домен. Без связи с конкретной теорией, размещение костимулирующего сигнального домена, например, 4-1BB, CD28, CD27 или OX-40, на первом CAR и основного сигнального домена, например, CD3-дзета, на втором CAR может ограничивать активность CAR только клетками, на которых экспрессированы обе мишени. В одном варианте осуществления CAR-экспрессирующая клетка имеет первый CAR для ассоциированного с раком антигена, содержащий антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен и костимулирующий домен, и второй CAR, который нацелен на другой антиген-мишень (например, антиген, экспрессируемый на того же типа раковой клетке, что и первый антиген-мишень) и содержит антигенсвязывающий домен, трансмембранный домен и основной сигнальный домен. В другом варианте осуществления CAR-экспрессирующая клетка имеет первый CAR, содержащий антигенсвязывающий домен, который связывает антиген-мишень, описанный в настоящем документе, трансмембранный домен и основной сигнальный домен, и второй CAR, который нацелен на антиген, отличный от первого антигена-мишени (например, антиген, экспрессируемый на того же типа раковой клетке, что и первый антиген-мишень) и содержит антигенсвязывающий домен для антигена, трансмембранный домен и костимулирующий сигнальный домен.
В некоторых вариантах осуществления заявленное изобретение относится к первому и второму CAR, при этом антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR не содержит вариабельный домен легкой цепи и вариабельный домен тяжелой цепи. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR представляет собой scFv, и другой представляет собой не scFv. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR содержит один домен VH, например, один домен VH верблюдовых, акулы или миноги, или один домен VH, полученный из последовательности антитела человека или мыши. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR содержит нанотело. В некоторых вариантах осуществления антигенсвязывающий домен одного из указанного первого CAR и указанного второго CAR содержит домен VHH верблюдовых.
Аллогенные клетки
В вариантах осуществления, описанных в настоящем документе, иммунная эффекторная клетка может представлять собой аллогенную иммунную эффекторную клетку, например, T-клетку или NK-клетку. Например, клетка может представлять собой аллогенную T-клетку, например, аллогенную T-клетку, лишенную экспрессии функционального T-клеточного рецептора (TCR) и/или человеческого лейкоцитарного антигена (HLA), например, HLA класса I и/или HLA класса II, или бета-2-микроглобулина (B2M).
T-клетка, лишенная функционального TCR, может, например, быть сконструирована таким образом, что она не будет экспрессировать никакой функциональный TCR на своей поверхности, сконструирована таким образом, что она не будет экспрессировать одну или более субъединиц, составляющих функциональный TCR, например, TRAC, TRBC1, TRBC2, CD3E, CD3G или CD3D, или сконструирована таким образом, что она будет продуцировать очень небольшие количества функционального TCR на своей поверхности. Альтернативно, T-клетка может экспрессировать в значительной степени поврежденный TCR, например, в результате экспрессии мутантных или укороченных форм одной или более из субъединиц TCR. Термин «в значительной степени поврежденный TCR» означает, что данный TCR не будет вызывать неблагоприятную иммунную реакцию у хозяина.
T-клетка, описанная в настоящем документе, может, например, быть сконструирована таким образом, что она не будет экспрессировать функциональный HLA на своей поверхности. Например, T-клетка, описанная в настоящем документе, может быть сконструирована таким образом, что экспрессия на клеточной поверхности HLA, например, HLA класса I и/или HLA класса II, либо субъединицы или регулятора экспрессии HLA, например, B2M, будет снижена.
T-клетка, описанная в настоящем документе, может, например, быть сконструирована таким образом, что она не будет экспрессировать функциональный B2M на своей поверхности. Например, T-клетка, описанная в настоящем документе, может быть сконструирована таким образом, что поверхностная экспрессия B2M у такой клетки будет снижена.
В некоторых вариантах осуществления T-клетка может быть лишена функционального TCR и функционального HLA, например, HLA класса I и/или HLA класса II.
Модифицированные T-клетки, лишенные экспрессии функционального TCR и/или HLA, могут быть получены любым подходящим методом, включая нокаут или нокдаун одной или более субъединиц TCR или HLA. Например, в T-клетке может быть произведен нокдаун TCR и/или HLA с использованием киРНК, кшРНК, коротких палиндромных повторов, регулярно расположенных группами (CRISPR), эффекторной нуклеазы, подобной активаторам транскрипции (TALEN), или эндонуклеазы «цинковые пальцы» (ZFN).
В некоторых вариантах осуществления аллогенная клетка может представлять собой клетку, которая не экспрессирует или экспрессирует на низком уровне ингибирующую молекулу, полученную, например, любым способом, описанным в настоящем документе. Например, клетка может представлять собой клетку, которая не экспрессирует или экспрессирует на низком уровне ингибирующую молекулу, например, которая может уменьшать способность CAR-экспрессирующей клетки обеспечивать иммунный эффекторный ответ. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA4, TIM3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета. Ингибирование ингибирующей молекулы, например, путем ингибирования на уровне ДНК, РНК или белка, может приводить к оптимизации функционирования CAR-экспрессирующей клетки. В вариантах осуществления может быть использована ингибирующая нуклеиновая кислота, например, ингибирующая нуклеиновая кислота, например, дцРНК, например, киРНК или кшРНК, короткие палиндромные повторы, регулярно расположенные группами (CRISPR), эффекторная нуклеаза, подобная активаторам транскрипции (TALEN), или эндонуклеаза «цинковые пальцы» (ZFN), например, описанные в настоящем документе.
киРНК и кшРНК
В некоторых вариантах осуществления экспрессия TCR и/или экспрессия HLA или B2M может быть ингибирована при помощи киРНК или кшРНК, которая нацелена на нуклеиновую кислоту, кодирующую TCR и/или HLA в T-клетке.
CRISPR
Используемые в настоящем документе термины «CRISPR» или «CRISPR для TCR и/или HLA», или «CRISPR для ингибирования TCR и/или HLA» означают набор коротких палиндромных повторов, регулярно расположенных группами, или систему, содержащую такой набор повторов. Используемый в настоящем документе термин «Cas» означает CRISPR-ассоциированный белок. Система «CRISPR/Cas» означает систему, полученную из CRISPR и Cas, которая может быть использована для подавления или мутирования гена TCR и/или HLA или B2M.
Искусственные системы CRISPR/Cas, ингибирующие TCR и/или HLA, могут быть получены с использованием технологии, известной в данной области, например, которая описана в патентной публикации США № 20140068797, и Cong (2013) Science 339: 819-823. Другие искусственные системы CRISPR/Cas, ингибирующие TCR и/или HLA, которые известны в данной области, также могут быть получены, например, как описано в Tsai (2014) Nature Biotechnol., 32:6 569-576, патентах США №№ 8871445, 8865406, 8795965, 8771945 и 8697359.
TALEN
Термины «TALEN» или «TALEN для HLA и/или TCR», или «TALEN для ингибирования HLA и/или TCR» означают эффекторную нуклеазу, подобную активаторам транскрипции, искусственную нуклеазу, которая может быть использована для редактирования гена HLA или B2M и/или TCR.
TALEN получают искусственно путем слияния ДНК-связывающего домена TAL эффектора с доменом, расщепляющим ДНК. Эффекторы, подобные активаторам транскрипции (TALE), могут быть сконструированы для связывания любой нужной последовательности ДНК, включая фрагмент гена HLA или TCR. За счет объединения TALE с доменом, расщепляющим ДНК, может быть получен фермент рестрикции, который специфичен для любой нужной последовательности ДНК, включая последовательность HLA или TCR. Затем их можно вводить в клетку, где они могут быть использованы для редактирования генома. Boch (2011) Nature Biotech. 29: 135-6; и Boch et al. (2009) Science 326: 1509-12; Moscou et al. (2009) Science 326: 3501.
TALEN, специфичные для последовательностей в HLA или TCR, могут быть сконструированы с использованием любого способа, известного в данной области, включая различные схемы с использованием модульных компонентов. Zhang et al. (2011) Nature Biotech. 29: 149-53; Geibler et al. (2011) PLoS ONE 6: e19509.
Нуклеаза «цинковые пальцы» для ингибирования HLA и/или TCR
Термины «ZFN» или «нуклеаза «цинковые пальцы», или «ZFN для HLA и/или TCR», или «ZFN для ингибирования HLA и/или TCR» означают нуклеазу «цинковые пальцы», искусственную нуклеазу, которая может быть использована для редактирования гена HLA и/или TCR или B2M.
ZFN, специфичные для последовательностей в HLA и/или TCR, могут быть сконструированы с использованием любого способа, известного в данной области. Смотри, например, Provasi (2011) Nature Med. 18: 807-815; Torikai (2013) Blood 122: 1341-1349; Cathomen et al. (2008) Mol. Ther. 16: 1200-7; Guo et al. (2010) J. Mol. Biol. 400: 96; публикацию патента США 2011/0158957 и публикацию патента США 2012/0060230.
Экспрессия теломеразы
Без связи с конкретной теорией, в некоторых вариантах осуществления терапевтическая T-клетка отличается краткосрочной персистенцией в организме пациента из-за укороченных теломеров в T-клетке; соответственно, трансфекция гена теломеразы может приводить к удлинению теломеров T-клетки и улучшению персистенции T-клетки в организме пациента. Смотри Carl June, «Adoptive T cell therapy for cancer in the clinic», Journal of Clinical Investigation, 117:1466-1476 (2007). Таким образом, в одном из вариантов осуществления иммунная эффекторная клетка, например, T-клетка, эктопически экспрессирует субъединицу теломеразы, например, каталитическую субъединицу теломеразы, например, TERT, например, hTERT. В некоторых аспектах данное изобретение относится к способу получения CAR-экспрессирующей клетки, включающему создание контакта клетки с нуклеиновой кислотой, кодирующей субъединицу теломеразы, например, каталитическую субъединицу теломеразы, например, TERT, например, hTERT. Клетка может быть приведена в контакт с нуклеиновой кислотой до, одновременно с, или после контактирования с конструктом, кодирующим CAR.
Размножение и активация
Иммунные эффекторные клетки, такие как T-клетки, могут быть активированы и размножены, в целом, с использованием способов, описанных, например, в патентах США 6352694, 6534055, 6905680, 6692964, 5858358, 6887466, 6905681, 7144575, 7067318, 7172869, 7232566, 7175843, 5883223, 6905874, 6797514, 6867041 и публикации патентной заявки США № 20060121005, полное содержание всех из которых включено в настоящий документ посредством ссылок.
Как правило, популяция иммунных эффекторных клеток, например, клеток, истощенных по регуляторным T-клеткам, может быть размножена путем создания контакта клеток с поверхностью, на которой закреплено средство, которое стимулирует связанный с комплексом CD3/TCR сигнал, и лиганд, который стимулирует костимулирующую молекулу на поверхности T-клеток. В частности, популяции T-клеток могут быть стимулированы, как описано в настоящем документе, например, путем контакта с анти-CD3 антителом или его антигенсвязывающим фрагментом, или анти-CD2 антителом, иммобилизованным на поверхности, или путем контакта с активатором протеинкиназы C (например, бриостатином) в сочетании с кальциевым ионофором. Для костимуляции вспомогательной молекулы на поверхности T-клеток используют лиганд, который связывает вспомогательную молекулу. Например, можно создавать контакт популяции T-клеток с анти-CD3 антителом и анти-CD28 антителом в условиях, подходящих для стимуляции пролиферации T-клеток. Для стимуляции пролиферации либо CD4+ T-клеток, либо CD8+ T-клеток, можно использовать анти-CD3 антитело и анти-CD28 антитело. Примеры анти-CD28 антител, которые могут быть использованы, включают 9.3, B-T3, XR-CD28 (Diaclone,  France), а также можно использовать другие методы, общеизвестные в данной области (Berg et al., Transplant Proc. 30(8):3975-3977, 1998; Haanen et al., J. Exp. Med. 190(9):13191328, 1999; Garland et al., J. Immunol Meth. 227(1-2):53-63, 1999).
France), а также можно использовать другие методы, общеизвестные в данной области (Berg et al., Transplant Proc. 30(8):3975-3977, 1998; Haanen et al., J. Exp. Med. 190(9):13191328, 1999; Garland et al., J. Immunol Meth. 227(1-2):53-63, 1999).
В некоторых аспектах основной стимулирующий сигнал и костимулирующий сигнал для T-клетки могут быть предоставлены в соответствии с разными протоколами. Например, средства, обеспечивающие каждый сигнал, могут находиться в растворе или быть связаны с поверхностью. В случае, если они связаны с поверхностью, средства могут быть связаны с одной и той же поверхностью (то есть, в «цис» расположении) или с разными поверхностями (то есть, в «транс» расположении). Альтернативно, одно средство может быть связано с поверхностью, и другое средство может находиться в растворе. В одном аспекте средство, обеспечивающее костимулирующий сигнал, связано с клеточной поверхностью, и средство, обеспечивающее основной сигнал активации, находится в растворе или связано с поверхностью. В некоторых аспектах оба средства могут находиться в растворе. В одном аспекте средства могут находиться в растворенной форме, а затем быть перекрестно сшиты с поверхностью, такой как клетка, экспрессирующая Fc-рецепторы, или антитело, или другое связывающее вещество, которое будет связываться со средствами. В этом отношении, смотри, например, публикации патентных заявок США №№ 20040101519 и 20060034810 для описания искусственных антигенпредставляющих клеток (aAPC), которые предусмотрены по настоящему изобретению для использования в активации и размножении T-клеток.
В одном аспекте два средства иммобилизованы на гранулах, либо на одной грануле, то есть, «цис», либо на разных гранулах, то есть, «транс». В качестве примера, средство, обеспечивающее основной сигнал активации, представляет собой анти-CD3 антитело или его антигенсвязывающий фрагмент, и средство, обеспечивающее костимулирующий сигнал, представляет собой анти-CD28 антитело или его антигенсвязывающий фрагмент; и оба средства совместно иммобилизованы на одной и той же грануле в эквивалентных молекулярных количествах. В одном аспекте используют соотношение 1:1 всех антител, связанных с гранулами, для размножения CD4+ T-клеток и роста T-клеток. В некоторых аспектах настоящего изобретения используют такое соотношение анти-CD3:CD28 антител, связанных с гранулами, что имеет место увеличение размножения T-клеток в сравнении с размножением, наблюдаемым при использовании соотношения 1:1. В одном конкретном аспекте имеет место увеличение примерно в 1-3 раза в сравнении с размножением, наблюдаемым при использовании соотношения 1:1. В одном аспекте соотношение анти-CD3:CD28 антител, связанных с гранулами, находится в диапазоне от 100:1 до 1:100, включая все промежуточные целые значения. В одном аспекте настоящего изобретения с частицами связывают большее количество анти-CD28 антитела, чем анти-CD3 антитела, то есть, соотношение анти-CD3:CD28 составляет менее единицы. В конкретных аспектах изобретения соотношение анти-CD28 антитела и анти-CD3 антитела, связанных с гранулами, превышает 2:1. В одном конкретном аспекте используют соотношение 1:100 анти-CD3:CD28 антител, связанных с гранулами. В одном аспекте используют соотношение 1:75 анти-CD3:CD28 антител, связанных с гранулами. В следующем аспекте используют соотношение 1:50 анти-CD3:CD28 антител, связанных с гранулами. В одном аспекте используют соотношение 1:30 анти-CD3:CD28 антител, связанных с гранулами. В одном предпочтительном аспекте используют соотношение 1:10 анти-CD3:CD28 антител, связанных с гранулами. В одном аспекте используют соотношение 1:3 анти-CD3:CD28 антител, связанных с гранулами. В еще одном аспекте используют соотношение 3:1 анти-CD3:CD28 антител, связанных с гранулами.
Соотношение частиц и клеток, составляющее от 1:500 до 500:1, включая все промежуточные целые значения, можно использовать для стимуляции T-клеток или других клеток-мишеней. Как понятно специалистам в данной области, соотношение частиц и клеток может зависеть от размера частиц в сравнении с клеткой-мишенью. Например, мелкие гранулы могут связывать лишь несколько клеток, в то время как более крупные гранулы могут связывать большое количество клеток. В конкретных аспектах соотношение клеток и частиц находится в диапазоне от 1:100 до 100:1, включая все промежуточные целые значения, и в следующих аспектах соотношение от 1:9 до 9:1, включая все промежуточные целые значения, также можно использовать для стимуляции T-клеток. Соотношение анти-CD3- и анти-CD28-связанных частиц и T-клеток, которое приводит к стимуляции T-клеток, может варьироваться, как отмечено выше, однако конкретные предпочтительные значения включают 1:100, 1:50, 1:40, 1:30, 1:20, 1:10, 1:9, 1:8, 1:7, 1:6, 1:5, 1:4, 1:3, 1:2, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1 и 15:1, с одним предпочтительным соотношением, составляющим по меньшей мере 1:1 частиц и T-клеток. В одном аспекте используют соотношение частиц и клеток, составляющее 1:1 или менее. В одном конкретном аспекте предпочтительное соотношение частицы:клетки составляет 1:5. В следующих аспектах соотношение частиц и клеток может варьироваться в зависимости от дня стимуляции. Например, в одном аспекте соотношение частиц и клеток составляет от 1:1 до 10:1 в первый день, и затем дополнительные частицы добавляют к клеткам каждый день или через день в течение вплоть до 10 дней, с конечным соотношением, составляющим от 1:1 до 1:10 (в расчете на количество клеток в день добавления). В одном конкретном аспекте соотношение частиц и клеток составляет 1:1 в первый день стимуляции, и его доводят до 1:5 в третий и пятый дни стимуляции. В одном аспекте частицы добавляют ежедневно или через день, с конечным соотношением, составляющим 1:1 в первый день и 1:5 в третий и пятый дни стимуляции. В одном аспекте соотношение частиц и клеток составляет 2:1 в первый день стимуляции, и его доводят до 1:10 в третий и пятый дни стимуляции. В одном аспекте частицы добавляют ежедневно или через день, с конечным соотношением, составляющим 1:1 в первый день и 1:10 в третий и пятый дни стимуляции. Специалист в данной области понимает, что различные другие соотношения могут быть подходящими для использования по настоящему изобретению. В частности, соотношение будет варьироваться в зависимости от размера частиц, а также от размера и типа клеток. В одном аспекте наиболее типичные используемые соотношения находятся в пределах 1:1, 2:1 и 3:1 в первый день.
В следующих аспектах настоящего изобретения клетки, такие как T-клетки, объединяют с покрытыми средством гранулами, впоследствии гранулы и клетки разделяют, а затем клетки культивируют. В альтернативном аспекте перед культивированием покрытые средством гранулы и клетки не разделяют, а культивируют совместно. В следующем аспекте гранулы и клетки сначала концентрируют за счет применения силы, такой как магнитная сила, что приводит к усиленному лигированию клеточных поверхностных маркеров, за счет чего индуцируется стимуляция клеток.
В качестве примера, белки клеточной поверхности могут быть лигированы при создании контакта парамагнитных гранул, с которыми связаны анти-CD3 и анти-CD28 антитела (3×28 гранулы), с T-клетками. В одном аспекте клетки (например, 104-109 T-клеток) и гранулы (например, DYNABEADS® M-450 CD3/CD28 T парамагнитные гранулы в соотношении 1:1) объединяют в буфере, например, PBS (не содержащем двухвалентные катионы, такие как кальций и магний). Опять-таки, специалисты в данной области понимают, что можно использовать любую концентрацию клеток. Например, клетки-мишени могут быть очень редкими в образце и составлять лишь 0,01% от образца, или весь образец (то есть, 100%) может представлять собой интересующие клетки-мишени. Соответственно, любое количество клеток предусмотрено в контексте настоящего изобретения. В некоторых аспектах может быть желательно значительно уменьшать объем, в котором частицы и клетки смешивают вместе (то есть, увеличивать концентрацию клеток), для обеспечения максимального контакта клеток и частиц. Например, в одном аспекте используют концентрацию примерно 10 миллиардов клеток/мл, 9 миллиардов клеток/мл, 8 миллиардов клеток/мл, 7 миллиардов клеток/мл, 6 миллиардов клеток/мл, 5 миллиардов клеток/мл или 2 миллиарда клеток/мл. В одном аспекте используют концентрацию более 100 миллионов клеток/мл. В следующем аспекте используют концентрацию клеток, составляющую 10, 15, 20, 25, 30, 35, 40, 45 или 50 миллионов клеток/мл. В еще одном аспекте используют концентрацию клеток, составляющую 75, 80, 85, 90, 95 или 100 миллионов клеток/мл. В следующих аспектах можно использовать концентрации, составляющие 125 или 150 миллионов клеток/мл. Использование высоких концентраций может приводить к увеличению выхода клеток, активации клеток и размножения клеток. Кроме того, использование высоких концентраций клеток позволяет более эффективно захватывать клетки, которые могут слабо экспрессировать интересующие антигены-мишени, например, CD28-отрицательные T-клетки. Такие популяции клеток могут иметь терапевтическую ценность, и их может быть желательно получать в конкретных аспектах. Например, использование высокой концентрации клеток позволяет более эффективно производить отбор CD8+ T-клеток, которые обычно имеют более слабую экспрессию CD28.
В одном варианте осуществления клетки, трансдуцированные нуклеиновой кислотой, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, например, CAR, описанный в настоящем документе, размножают, например, способом, описанным в настоящем документе. В одном варианте осуществления клетки размножают в культуре в течение периода времени от нескольких часов (например, примерно 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 18, 21 часов) до примерно 14 дней (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 дней). В одном варианте осуществления клетки размножают в течение периода времени 4-9 дней. В одном варианте осуществления клетки размножают в течение периода времени 8 дней или менее, например, 7, 6 или 5 дней. В одном варианте осуществления клетки размножают в культуре в течение 5 дней, и полученные клетки являются более активными, чем такие же клетки, размножаемые в культуре в течение 9 дней в тех же условиях культивирования. Активность можно определять, например, на основании различных функций T-клеток, например, пролиферации, уничтожения клеток-мишеней, продуцирования цитокинов, активации, миграции или их сочетания. В одном варианте осуществления у клеток, размножаемых в течение 5 дней, наблюдается по меньшей мере одно-, двух-, трех- или четырехкратное увеличение удвоения клеток при стимуляции антигеном, в сравнении с такими же клетками, размножаемыми в культуре в течение 9 дней в тех же условиях культивирования. В одном варианте осуществления клетки размножают в культуре в течение 5 дней, и у полученных клеток наблюдается продуцирование более высоких уровней провоспалительных цитокинов, например, уровней IFN-γ и/или GM-CSF, в сравнении с такими же клетками, размножаемыми в культуре в течение 9 дней в тех же условиях культивирования. В одном варианте осуществления у клеток, размножаемых в течение 5 дней, наблюдается по меньшей мере одно-, двух-, трех-, пяти, десятикратное, или более, увеличение выражаемого в пг/мл продуцирования провоспалительных цитокинов, например, уровней IFN-γ и/или GM-CSF, в сравнении с такими же клетками, размножаемыми в культуре в течение 9 дней в тех же условиях культивирования.
Также может быть желательно проводить несколько циклов стимуляции, так что время культивирования T-клеток может составлять 60 дней или более. Условия, подходящие для культивирования T-клеток, включают соответствующую среду (например, минимальную эссенциальную среду или среду RPMI 1640, или X-vivo 15, (Lonza)), которая может содержать факторы, необходимые для пролиферации и жизнеспособности, включая сыворотку (например, эмбриональную бычью или человеческую сыворотку), интерлейкин-2 (IL-2), инсулин, IFN-γ, IL-4, IL-7, GM-CSF, IL-10, IL-12, IL-15, TGFβ и TNFα, или любые другие добавки для роста клеток, известные квалифицированному специалисту. Другие добавки для роста клеток включают, но без ограничения, сурфактант, плазманат и восстанавливающие агенты, такие как N-ацетилцистеин и 2-меркаптоэтанол. Среды могут включать RPMI 1640, AIM-V, DMEM, MEM, α-MEM, F-12, X-Vivo 15 и X-Vivo 20, Optimizer, с добавлением аминокислот, пирувата натрия и витаминов, либо без содержания сыворотки, либо с добавлением соответствующего количества сыворотки (или плазмы), или определенного набора гормонов и/или количества цитокина(ов), которые достаточны для роста и размножения T-клеток. Антибиотики, например, пенициллин и стрептомицин, включают только в экспериментальные культуры, но не в культуры клеток, которые будут введены инфузией субъекту. Клетки-мишени содержат в условиях, необходимых для поддержания роста, например, при соответствующей температуре (например, 37°C) и атмосферном составе (например, воздух плюс 5% CO2).
В одном варианте осуществления клетки размножают в соответствующей среде (например, среде, описанной в настоящем документе), содержащей один или более интерлейкинов, что приводит к по меньшей мере 200-кратному (например, 200-кратному, 250-кратному, 300-кратному, 350-кратному) увеличению количества клеток в течение 14-дневного периода размножения, например, при измерении методом, описанным в настоящем документе, таким как проточная цитометрия. В одном варианте осуществления клетки размножают в присутствии IL-15 и/или IL-7 (например, IL-15 и IL-7).
В вариантах осуществления способы, описанные в настоящем документе, например, способы получения клетки, экспрессирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, включают удаление регуляторных T-клеток, например, CD25+ T-клеток, из популяции клеток, например, с использованием анти-CD25 антитела или его фрагмента, или CD25-связывающего лиганда, IL-2. Способы удаления регуляторных T-клеток, например, CD25+ T-клеток, из популяции клеток описаны в настоящем документе. В вариантах осуществления способы, например, способы получения, дополнительно включают создание контакта популяции клеток (например, популяции клеток, в которой регуляторные T-клетки, такие как CD25+ T-клетки, были истощены; или популяции клеток, которые ранее контактировали с анти-CD25 антителом, его фрагментом или CD25-связывающим лигандом) с IL-15 и/или IL-7. Например, популяцию клеток (например, которые ранее контактировали с анти-CD25 антителом, его фрагментом или CD25-связывающим лигандом) размножают в присутствии IL-15 и/или IL-7.
В некоторых вариантах осуществления клетка, экспрессирующая слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, описанная в настоящем документе, контактирует с композицией, содержащей полипептид интерлейкина-15 (IL-15), полипептид альфа-субъединицы рецептора интерлейкина-15 (IL-15Ra), или сочетание полипептида IL-15 и полипептида IL-15Ra, например, hetIL-15, в процессе получения CAR-экспрессирующей клетки, например, ex vivo. В вариантах осуществления CAR-экспрессирующая клетка, описанная в настоящем документе, контактирует с композицией, содержащей полипептид IL-15, в процессе получения CAR-экспрессирующей клетки, например, ex vivo. В вариантах осуществления CAR-экспрессирующая клетка, описанная в настоящем документе, контактирует с композицией, содержащей сочетание полипептида IL-15 и полипептида IL-15Ra, в процессе получения CAR-экспрессирующей клетки, например, ex vivo. В вариантах осуществления CAR-экспрессирующая клетка, описанная в настоящем документе, контактирует с композицией, содержащей hetIL-15, в процессе получения CAR-экспрессирующей клетки, например, ex vivo.
В одном варианте осуществления клетка, экспрессирующая слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, описанная в настоящем документе, контактирует с композицией, содержащей hetIL-15, в процессе ex vivo размножения. В одном из вариантов осуществления CAR-экспрессирующая клетка, описанная в настоящем документе, контактирует с композицией, содержащей полипептид IL-15, в процессе ex vivo размножения. В одном из вариантов осуществления CAR-экспрессирующая клетка, описанная в настоящем документе, контактирует с композицией, содержащей как полипептид IL-15, так и полипептид IL-15Ra, в процессе ex vivo размножения. В одном варианте осуществления такой контакт приводит к выживанию и пролиферации субпопуляции лимфоцитов, например, CD8+ T-клеток.
T-клетки, которые были стимулированы в течение разного времени, могут проявлять разные характеристики. Например, типичные мононуклеарные клетки периферической крови, полученные из крови или продуктов афереза, имеют популяцию хелперных T-клеток (TH, CD4+), которая больше, чем популяция цитотоксических или супрессорных T-клеток (TC, CD8+). Ex vivo размножение T-клеток при стимуляции рецепторов CD3 и CD28 приводит к получению популяции T-клеток, которая до примерно 8-9 дня состоит преимущественно из TH клеток, в то время как после примерно 8-9 дней популяция T-клеток содержит намного большую популяцию TC клеток. Соответственно, в зависимости от цели лечения введение субъекту инфузией популяции T-клеток, состоящей преимущественно из TH клеток, может иметь преимущества. Аналогично, если была выделена подгруппа антиген-специфических TC клеток, может быть полезно размножить эту подгруппу в большей степени.
Кроме того, помимо маркеров CD4 и CD8, другие фенотипические маркеры также варьируются существенно, но в значительной степени воспроизводимо, в процессе клеточного деления. Таким образом, такая воспроизводимость позволяет адаптировать препарат активированных T-клеток для конкретных целей.
После того, как слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, описанный в настоящем документе, сконструирован, можно использовать различные анализы для оценки активности молекулы, такие как, но без ограничения, способность вызывать размножение T-клеток после стимуляции антигеном, поддерживать размножение T-клеток в отсутствие повторной стимуляции, а также противораковая активность в соответствующих in vitro и животных моделях. Анализы для оценки эффектов CAR по настоящему изобретению описаны более подробно ниже.
Можно использовать вестерн-блот анализ экспрессии слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR, в первичных T-клетках для обнаружения присутствия мономеров и димеров. Смотри, например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, T-клетки (1:1 смесь CD4+ и CD8+ T-клеток), экспрессирующие CAR, размножают in vitro в течение более 10 дней, с последующим лизисом и электрофорезом в SDS-ПААГ в восстанавливающих условиях. CAR, содержащие полноразмерный цитоплазматический домен TCR-ζ и эндогенную TCR-ζ цепь, обнаруживают методом вестерн-блоттинга с использованием антитела к TCR-ζ цепи. Те же наборы T-клеток используют для анализа методом электрофореза в SDS-ПААГ в не восстанавливающих условиях для оценки образования ковалентно связанных димеров.
In vitro размножение T-клеток, содержащих слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, например, CAR+ T-клеток, после стимуляции антигеном можно измерять методом проточной цитометрии. Например, смесь CD4+ и CD8+ T-клеток стимулируют αCD3/αCD28 aAPC, с последующей трансдукцией лентивирусными векторами, экспрессирующими GFP под контролем промоторов, которые предстоит анализировать. Иллюстративные промоторы включают промоторы генов CMV IE, EF-1α, убиквитина C или фосфоглицерокиназы (PGK). Флуоресценцию GFP оценивают в день 6 культивирования в подгруппах CD4+ и/или CD8+ T-клеток методом проточной цитометрии. Смотри, например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Альтернативно, смесь CD4+ и CD8+ T-клеток стимулируют покрытыми αCD3/αCD28 магнитными гранулами в день 0 и трансдуцируют CAR в день 1 с использованием бицистронного лентивирусного вектора, экспрессирующего CAR наряду с eGFP, используя 2A последовательность ухода с рибосомы. Культуры повторно стимулируют либо содержащими ассоциированный с раком антиген, описанный в настоящем документе, клетками K562 (K562, экспрессирующими ассоциированный с раком антиген, описанный в настоящем документе), клетками K562 дикого типа (K562 дикого типа) или клетками K562, экспрессирующими hCD32 и 4-1BBL, в присутствии анти-CD3 и анти-CD28 антител (K562-BBL-3/28) после промывания. Экзогенный IL-2 добавляют к культурам через день в концентрации 100 МЕ/мл. Количество GFP+ T-клеток определяют методом проточной цитометрии, подсчитывая количество гранул. Смотри, например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009).
Устойчивое размножение содержащих слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, T-клеток, например, CAR+ T-клеткок, в отсутствие повторной стимуляции также может быть измерено. Смотри, например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, измеряют средний объем T-клеток (фл) в день 8 культивирования с использованием счетчика частиц Coulter Multisizer III, Nexcelom Cellometer Vision или Millipore Scepter, с последующей стимуляцией покрытыми αCD3/αCD28 магнитными гранулами в день 0 и трансдукцией указанными CAR в день 1.
Для измерения активности CART также можно использовать животные модели. Например, можно использовать модель ксенотрансплантации, в которой используют человеческие, специфичные для ассоциированного с раком антигена, описанного в настоящем документе, CAR+ T-клетки для лечения первичного человеческого пре-B-ALL у иммунодефицитных мышей. Смотри, например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, после развития ALL мышей случайным образом распределяют в группы лечения. Разное количество специфичных для ассоциированного с раком антигена T-клеток, содержащих CAR, вводят совместной инъекцией в соотношении 1:1 мышам NOD-SCID-γ-/-, имеющим B-ALL. Число копий вектора для CAR, специфичного для ассоциированного с раком антигена, в ДНК из селезенки мышей оценивают в разные моменты времени после инъекции T-клеток. Животных оценивают на признаки лейкоза с недельными интервалами. Количество бластных клеток B-ALL, содержащих ассоциированный с раком антиген, описанный в настоящем документе, в периферической крови измеряют у мышей, которым инъекцией вводили T-клетки с CAR для ассоциированного с раком антигена, описанного в настоящем документе, или ложно трансдуцированные T-клетки. Кривые выживаемости для групп животных сравнивают с использованием логарифмического рангового критерия. Кроме того, также можно анализировать абсолютное количество в периферической крови CD4+ и CD8+ T-клеток через 4 недели после инъекции T-клеток мышам NOD-SCID-γ-/-. Мышам вводят инъекцией лейкозные клетки и через 3 недели вводят инъекцией T-клетки, сконструированные для экспрессии CAR, при помощи бицистронного лентивирусного вектора, кодирующего CAR, связанный с eGFP. T-клетки нормируют для введения 45-50% GFP+ T-клеток путем смешивания с ложно трансдуцированными клетками перед инъекцией, что подтверждают методом проточной цитометрии. Животных оценивают на признаки лейкоза с интервалами в 1 неделю. Кривые выживаемости для групп животных, которым вводили CAR+ T-клетки, сравнивают с использованием логарифмического рангового критерия.
Можно оценивать зависимость ответа на лечение от дозы слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR. Смотри, например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Например, периферическую кровь собирают через 35-70 дней после развития лейкоза у мышей, которым вводили в день 21 CAR T-клетки, эквивалентное количество ложно трансдуцированных T-клеток, или не вводили T-клетки. У произвольно выбранных мышей из каждой группы собирают кровь для определения в периферической крови количества бластных клеток ALL, содержащих ассоциированный с раком антиген, описанный в настоящем документе, а затем умерщвляют в день 35 и 49. Оставшихся животных оценивают в дни 57 и 70.
Методы оценки клеточной пролиферации и продуцирования цитокинов ранее описаны, например, в Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, оценку CAR-опосредованной пролиферации выполняют в микропланшетах для титрования, смешивая промытые T-клетки с клетками K562, экспрессирующими ассоциированный с раком антиген, описанный в настоящем документе (K19), или CD32 и CD137 (KT32-BBL), в конечном соотношении T-клетка:K562, составляющем 2:1. Клетки K562 перед использованием облучают гамма-излучением. Анти-CD3 (клон OKT3) и анти-CD28 (клон 9.3) моноклональные антитела добавляют в культуры с KT32-BBL клетками в качестве положительного контроля для стимуляции пролиферации T-клеток, поскольку эти сигналы поддерживают долгосрочное размножение CD8+ T-клеток ex vivo. Количество T-клеток подсчитывают в культурах с использованием флуоресцентных гранул CountBright™ (Invitrogen, Carlsbad, CA) и метода проточной цитометрии в соответствии с инструкциями производителя. CAR+ T-клетки определяют по экспрессии GFP в случае T-клеток, генетически модифицированных лентивирусными векторами, экспрессирующими связанный с eGFP-2A CAR. CAR+ T-клетки, не экспрессирующие GFP, обнаруживают при помощи биотинилированного рекомбинантного белка ассоциированного с раком антигена, описанного в настоящем документе, и вторичного конъюгата авидин-PE. Одновременно определяют экспрессию CD4+ и CD8+ на T-клетках при помощи специфических моноклональных антител (BD Biosciences). Количественное определение цитокинов выполняют в супернатантах, собранных через 24 часа после повторной стимуляции, с использованием набора с гранулами для определения человеческих TH1/TH2 цитокинов методом цитометрии (BD Biosciences, San Diego, CA) в соответствии с инструкциями производителя. Флуоресценцию определяют на проточном цитометре FACScalibur, и данные анализируют в соответствии с инструкциями производителя.
Цитотоксичность можно оценивать стандартным анализом с высвобождением 51Cr. Смотри, например, Milone et al., Molecular Therapy 17(8): 1453-1464 (2009). Вкратце, клетки-мишени (клетки линии K562 и первичные про-B-ALL клетки) нагружают 51Cr (в виде NaCrO4, New England Nuclear, Boston, MA) при 37°C в течение 2 часов с интенсивным перемешиванием, дважды промывают полной средой RPMI и вносят в лунки микропланшетов для титрования. Эффекторные T-клетки смешивают в лунках с клетками-мишенями в полной среде RPMI при разных соотношениях эффекторная клетка:клетка-мишень (E:T). Также готовят дополнительные лунки, содержащие только среду (спонтанное высвобождение, SR) или 1% раствор детергента тритон X-100 (полное высвобождение, TR). Через 4 часа инкубации при 37°C собирают супернатант из каждой лунки. Затем измеряют высвобождение 51Cr с использованием счетчика гамма-частиц (Packard Instrument Co., Waltham, MA). Каждую пробу выполняют по меньшей мере в тройном повторе, и процент лизиса рассчитывают по формуле: % лизиса=(ER - SR)/(TR - SR), где ER представляет собой среднее количество высвобожденного 51Cr для каждого экспериментального условия.
Можно использовать методы визуализации для оценки специфической направленной миграции и пролиферации CAR в животных моделях опухолей. Такие анализы описаны, например, в публикации Barrett et al., Human Gene Therapy 22: 1575-1586 (2011). Вкратце, мышам NOD/SCID/γc-/- (NSG) вводят в/в инъекцией клетки NALM6, а затем через 7 дней T-клетки через 4 часа после введения методом электропорации конструктов CAR. T-клетки стабильно трансфицируют лентивирусным конструктом для экспрессии люциферазы светляков, и биолюминесценцию в организме мышей визуализируют. Альтернативно, терапевтическую эффективность и специфичность при однократной инъекции CAR+ T-клеток мышам с ксенотрансплантатом опухоли NALM6 можно измерять следующим образом: мышам NSG вводят инъекцией клетки NALM6, трансдуцированные для стабильной экспрессии люциферазы светляков, а затем через 7 дней выполняют однократную инъекцию в хвостовую вену T-клеток, в которые методом электропорации введены конструкты CAR по настоящему изобретению. Проводят визуализацию животных в разных временных точках после инъекции. Например, можно получать тепловые карты плотности фотонов положительных по люциферазе светляков лейкозных клеток у репрезентативных мышей в день 5 (за 2 дня до лечения) и день 8 (24 часа после введения CAR+ PBL).
Другие анализы, включая те, которые описаны в разделе «Примеры» настоящего документа, а также те, которые известны в данной области, также можно использовать для оценки CAR, описанных в настоящем документе.
Способы получения CAR-экспрессирующих клеток
В другом аспекте изобретение относится к способу получения клетки (например, иммунной эффекторной клетки или их популяции), включающему введение (например, трансдуцирование) в клетку, например, T-клетку или NK-клетку, описанную в настоящем документе, вектора, содержащего нуклеиновую кислоту, кодирующую слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, например, CAR, описанный в настоящем документе; или нуклеиновую кислоту, кодирующую молекулу CAR, например, CAR, описанного в настоящем документе.
Клетка в способах представляет собой иммунную эффекторную клетку (например, T-клетку или NK-клетку, или их сочетание). В некоторых вариантах осуществления клетка в способах является дефицитной по диацилглицеринкиназе (DGK) и/или Ikaros.
В некоторых вариантах осуществления введение молекулы нуклеиновой кислоты, кодирующей CAR, включает трансдукцию вектора, содержащего молекулу нуклеиновой кислоты, кодирующую слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, или трансфекцию молекулы нуклеиновой кислоты, кодирующей CAR, при этом молекула нуклеиновой кислоты представляет собой in vitro транскрибированную РНК.
В некоторых вариантах осуществления способ дополнительно включает:
получение популяции иммунных эффекторных клеток (например, T-клеток или NK-клеток); и
удаление регуляторных T-клеток из популяции, с получением популяции, истощенной по регуляторным T-клеткам;
при этом этапы a) и b) выполняют до введения нуклеиновой кислоты, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, в популяцию клеток.
В вариантах осуществления способов регуляторные T-клетки представляют собой CD25+ T-клетки, и их удаляют из популяции клеток с использованием анти-CD25 антитела или его фрагмента. Анти-CD25 антитело или его фрагмент можно конъюгировать с субстратом, например, гранулой.
В других вариантах осуществления популяция, истощенная по регуляторным T-клеткам, полученная на этапе (b), содержит менее 30%, 25%, 20%, 15%, 10%, 5%, 4%, 3%, 2%, 1% CD25+ клеток.
В других вариантах осуществления способ дополнительно включает удаление из популяции клеток, экспрессирующих опухолевый антиген, не включающий CD25, с получением популяции клеток, истощенной по регуляторным T-клеткам и экспрессирующим опухолевый антиген клеткам, до введения нуклеиновой кислоты, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, в популяцию клеток. Опухолевый антиген может быть выбран из CD19, CD30, CD38, CD123, CD20, CD14 или CD11b, или их сочетания.
В других вариантах осуществления способ дополнительно включает удаление из популяции клеток, экспрессирующих ингибитор иммунных контрольных точек, с получением популяции клеток, истощенной по регуляторным T-клеткам и экспрессирующим ингибирующую молекулу клеткам, до введения нуклеиновой кислоты, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, в популяцию клеток. Ингибитор иммунных контрольных точек может быть выбран из PD-1, LAG-3, TIM3, B7-H1, CD160, P1H, 2B4, CEACAM (например, CEACAM-1, CEACAM-3, и/или CEACAM-5), TIGIT, CTLA-4, BTLA и LAIR1.
Следующие варианты осуществления, описанные в настоящем документе, включают получение популяции иммунных эффекторных клеток. Популяцию получаемых иммунных эффекторных клеток можно выбирать на основании экспрессии одного или более из CD3, CD28, CD4, CD8, CD45RA и/или CD45RO. В конкретных вариантах осуществления популяция получаемых иммунных эффекторных клеток представляет собой CD3+ и/или CD28+ клетки.
В конкретных вариантах осуществления способа способ дополнительно включает размножение популяции клетки после введения молекулы нуклеиновой кислоты, кодирующей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR.
В вариантах осуществления популяцию клеток размножают в течение 8 дней или менее.
В конкретных вариантах осуществления популяцию клеток размножают в культуре в течение 5 дней, и полученные клетки являются более активными, чем такие же клетки, размножаемые в культуре в течение 9 дней в тех же условиях культивирования.
В других вариантах осуществления у популяции клеток, размножаемых в культуре в течение 5 дней, наблюдается по меньшей мере одно-, двух-, трех- или четырехкратное увеличение удвоения клеток при стимуляции антигеном, в сравнении с такими же клетками, размножаемыми в культуре в течение 9 дней в тех же условиях культивирования.
В других вариантах осуществления популяцию клеток размножают в культуре в течение 5 дней, и у полученных клеток наблюдается продуцирование более высоких уровней провоспалительных цитокинов IFN-γ и/или GM-CSF, в сравнении с такими же клетками, размножаемыми в культуре в течение 9 дней в тех же условиях культивирования.
В других вариантах осуществления популяцию клеток размножают путем культивирования клеток в присутствии средства, стимулирующего связанный с комплексом CD3/TCR сигнал, и/или лиганда, стимулирующего костимулирующую молекулу на поверхности клеток. Средство может представлять собой гранулу, конъюгированную с анти-CD3 антителом или его фрагментом, и/или анти-CD28 антителом или его фрагментом.
В других вариантах осуществления популяцию клеток размножают в соответствующей среде, содержащей один или более интерлейкинов, что приводит по меньшей мере к 200-кратному, 250-кратному, 300-кратному или 350-кратному увеличению количества клеток в течение 14-дневного периода размножения, например, при измерении методом проточной цитометрии.
В других вариантах осуществления популяцию клеток размножают в присутствии IL-15 и/или IL-7.
В конкретных вариантах осуществления способ также включает криоконсервацию популяции клеток после соответствующего периода размножения.
В других вариантах осуществления способ получения, раскрытый в настоящем документе, также включает создание контакта популяции иммунных эффекторных клеток с нуклеиновой кислотой, кодирующей субъединицу теломеразы, например, hTERT. Нуклеиновая кислота, кодирующая субъединицу теломеразы, может представлять собой ДНК.
Настоящее изобретение также относится к способу получения популяции РНК-модифицированных клеток, например, клеток, описанных в настоящем документе, например, иммунных эффекторных клеток (например, T-клеток, NK-клеток), временно экспрессирующих экзогенную РНК. Способ включает введение in vitro транскрибированной РНК или синтетической РНК в клетку, при этом РНК содержит нуклеиновую кислоту, кодирующую слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит молекулу CAR, описанную в настоящем документе.
В другом аспекте изобретение относится к способу создания противоопухолевого иммунитета у субъекта, включающему введение субъекту эффективного количества клетки, содержащей слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит молекулу CAR, например, клетки, экспрессирующей молекулу CAR, описанную в настоящем документе. В одном варианте осуществления клетка представляет собой аутологичную T-клетку или NK-клетку. В одном варианте осуществления клетка представляет собой аллогенную T-клетку или NK-клетку. В одном варианте осуществления субъект является человеком.
В одном аспекте изобретение относится к популяции аутологичных клеток, которые трансфицированы или трансдуцированы вектором, содержащим молекулу нуклеиновой кислоты, кодирующую слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит молекулу CAR, например, описанную в настоящем документе. В одном варианте осуществления вектор представляет собой ретровирусный вектор. В одном варианте осуществления вектор представляет собой самоинактивирующийся лентивирусный вектор, описанный в другом разделе настоящего документа. В одном варианте осуществления вектор доставляют (например, трансфекцией или электропорацией) в клетку, например, T-клетку или NK-клетку, при этом вектор содержит молекулу нуклеиновой кислоты, кодирующую CAR по настоящему изобретению, описанный в настоящем документе, которая транскрибируется в виде молекулы мРНК, и CAR по настоящему изобретению транслируется с молекулы РНК и экспрессируется на поверхности клетки.
В другом аспекте настоящее изобретение относится к популяции клеток, экспрессирующих слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, например, CAR-экспрессирующих иммунных эффекторных клеток (например, T-клеток или NK-клеток). В некоторых вариантах осуществления популяция CAR-экспрессирующих клеток представляет собой смесь клеток, экспрессирующих разные CAR. Например, в одном варианте осуществления популяция CAR-экспрессирующих иммунных эффекторных клеток (например, T-клеток или NK-клеток) может включать первую клетку, экспрессирующую CAR, содержащий антигенсвязывающий домен, который связывается с первым опухолевым антигеном, описанным в настоящем документе, и вторую клетку, экспрессирующую CAR, содержащий другой антигенсвязывающий домен, который связывается со вторым опухолевым антигеном, описанным в настоящем документе. В качестве другого примера, популяция CAR-экспрессирующих клеток может включать первую клетку, экспрессирующую CAR, содержащий антигенсвязывающий домен, который связывается с опухолевым антигеном, описанным в настоящем документе, и вторую клетку, экспрессирующую CAR, содержащий антигенсвязывающий домен для мишени, отличной от опухолевого антигена, описанного в настоящем документе. В одном варианте осуществления популяция CAR-экспрессирующих клеток включает, например, первую клетку, экспрессирующую CAR, содержащий основной внутриклеточный сигнальный домен, и вторую клетку, экспрессирующую CAR, содержащий вторичный сигнальный домен, например, костимулирующий сигнальный домен.
В другом аспекте настоящее изобретение относится к популяции клеток, при этом по меньшей мере одна клетка в популяции экспрессирует слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, содержащий антигенсвязывающий домен, который связывается с опухолевым антигеном, описанным в настоящем документе, и вторая клетка экспрессирует другое средство, например, средство, повышающее активность CAR-экспрессирующей клетки. Например, в одном варианте осуществления средство может представлять собой средство, которое ингибирует ингибирующую молекулу. Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета. В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, например, представляет собой молекулу, описанную в настоящем документе, например, средство, которое содержит первый полипептид, например, ингибирующую молекулу, связанный со вторым полипептидом, который передает положительный сигнал клетке, например, внутриклеточным сигнальным доменом, описанным в настоящем документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 или TGFR-бета, либо фрагмент любой из них, и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в настоящем документе (например, содержащий костимулирующий домен (например, 41BB, CD27 или CD28, например, описанный в настоящем документе) и/или основной сигнальный домен (например, сигнальный домен CD3-дзета, описанный в настоящем документе). В одном варианте осуществления средство содержит первый полипептид PD-1 или его фрагмент и второй полипептид внутриклеточного сигнального домена, описанного в настоящем документе (например, сигнального домена CD28, CD27, OX40 или 4-IBB, описанного в настоящем документе, и/или сигнального домена CD3-дзета, описанного в настоящем документе).
В одном варианте осуществления молекула нуклеиновой кислоты, кодирующая слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит молекулу CAR по настоящему изобретению, например, описанную в настоящем документе, экспрессируется в виде молекулы мРНК. В одном варианте осуществления генетически модифицированные экспрессирующие CAR по настоящему изобретению клетки, например, иммунные эффекторные клетки (например, T-клетки, NK-клетки), могут быть получены путем введения методом трансфекции или электропорации молекулы РНК, кодирующей нужные CAR (например, без последовательности вектора), в клетку. В одном варианте осуществления молекула CAR по настоящему изобретению транслируется с молекулы РНК после ее введения в клетку и экспрессируется на поверхности рекомбинантной клетки.
Способ получения мРНК для использования в трансфекции включает in vitro транскрипцию (IVT) матрицы со специально разработанными праймерами, с последующим добавлением полиA, с получением конструкта, содержащего 3'- и 5'-нетранслируемую последовательность («UTR») (например, 3' и/или 5' UTR, описанные в настоящем документе), 5'-кэп (например, 5'-кэп, описанный в настоящем документе) и/или внутренний участок связывания рибосомы (IRES) (например, IRES, описанный в настоящем документе), нуклеиновую кислоту, которую предстоит экспрессировать, и полиA «хвост», как правило, длиной 50-5000 оснований (SEQ ID NO: 32). Полученной таким образом РНК можно эффективно трансфицировать клетки разных видов. В одном аспекте матрица содержит последовательности для слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR. В одном из вариантов осуществления вектор с РНК слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит CAR, трансдуцируют в клетку, например, T-клетку или NK-клетку, методом электропорации.
В одном варианте осуществления слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, вводят в иммунные эффекторные клетки (например, T-клетки, NK-клетки), например, с использованием in vitro транскрипции, и субъект (например, человек) получает начальное введение иммунных эффекторных клеток (например, T-клеток, NK-клеток) по изобретению, экспрессирующих слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, и одно или более последующих введений иммунных эффекторных клеток (например, T-клеток, NK-клеток) по изобретению, экспрессирующих слитый белок, например, описанный в настоящем документе, содержащий домен, который содержит CAR, при этом одно или более последующих введений выполняют через менее, чем 15 дней, например, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3 или 2 дня после предыдущего введения. В одном варианте осуществления более одного введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) по изобретению выполняют субъекту (например, человеку) в неделю, например, в неделю выполняют 2, 3 или 4 введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) по изобретению. В одном варианте осуществления субъекту (например, субъекту-человеку) выполняют более одного введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) в неделю (например, 2, 3 или 4 введения в неделю) (в настоящем документе также используют термин «цикл»), с последующей неделей без введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток), а затем субъекту выполняют одно или более дополнительных введений иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) (например, более одного введения иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток) в неделю). В другом варианте осуществления субъект (например, субъект-человек) получает более одного цикла введений иммунных эффекторных клеток с CAR (например, T-клеток, NK-клеток), и временной интервал между всеми циклами составляет менее 10, 9, 8, 7, 6, 5, 4 или 3 дней. В одном варианте осуществления иммунные эффекторные клетки с CAR (например, T-клетки, NK-клетки) вводят через день, по 3 введения в неделю. В одном варианте осуществления иммунные эффекторные клетки с CAR (например, T-клетки, NK-клетки) по изобретению вводят в течение по меньшей мере двух, трех, четырех, пяти, шести, семи, восьми или более недель.
В одном аспекте CAR-экспрессирующие клетки получают с использованием лентивирусных вирусных векторов, таких как лентивирус. Клетки, например, CART, полученные таким способом, будут иметь стабильную экспрессию CAR.
В одном аспекте CAR-экспрессирующие клетки, например, CART, получают с использованием вирусного вектора, такого как гамма-ретровирусный вектор, например, гамма-ретровирусный вектор, описанный в настоящем документе. CART, полученные с использованием таких векторов, могут иметь стабильную экспрессию CAR.
В одном аспекте CART временно экспрессируют векторы для CAR в течение 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 дней после трансдукции. Временную экспрессию CAR можно осуществлять путем доставки вектора с РНК CAR. В одном аспекте РНК CAR трансдуцируют в T-клетку методом электропорации.
Потенциальной проблемой, которая может возникать у пациентов, получающих лечение с использованием иммунных эффекторных клеток (например, T-клеток, NK-клеток), временно экспрессирующих CAR (в частности, CART, имеющих мышиный scFv), является анафилаксия после многократных введений препарата.
Без связи с конкретной теорией, считается, что такая анафилактическая реакция может возникать у пациента в результате развития гуморального ответа в виде анти-CAR антител, то есть, анти-CAR антител, имеющих изотип IgE. Считается, что в антитело-продуцирующих клетках пациента происходит переключение с изотипа IgG (который не вызывает анафилаксии) на изотип IgE, когда имеет место десяти-четырнадцатидневный перерыв в воздействии антигена. Если пациент имеет высокий риск развития иммунного ответа в виде продуцирования анти-CAR антител во время кратковременного курса терапии CAR (например, в случае трансдукции РНК), перерывы в инфузии CART не должны продолжаться более десяти-четырнадцати дней.
Способы условной экспрессии белка и терапевтическое применение
В настоящем документе также предложены способы условной экспрессии слитого белка (например, содержащего полипептид CAR). Такие способы могут включать создание контакта клетки-хозяина, содержащей любой из слитых белков, описанных в настоящем документе, или нуклеиновую кислоту, кодирующую такой слитый белок, с экспрессионным соединением, например, дезагрегирующим соединением или стабилизирующим соединением.
В присутствии стабилизирующего соединения домен деградации слитого белка принимает конформацию, устойчивую к деградации в клетке, и протеаза расщепляет сайт расщепления протеазы в слитом белке, что приводит к отщеплению домена деградации от нужного белка и экспрессии нужного белка. В отсутствие стабилизирующего соединения домен деградации слитого белка принимает конформацию, допускающую деградацию в клетке, что приводит к деградации слитого белка. В некоторых вариантах осуществления клетка-хозяин контактирует со стабилизирующим соединением in vivo. В некоторых вариантах осуществления клетка-хозяин контактирует со стабилизирующим соединением ex vivo.
В присутствии дезагрегирующего соединения домен агрегации слитого белка принимает конформацию, устойчивую к олигомеризации (например, димеризации), в результате чего слитый белок переходит в мономерное состояние, доступное для протеазы, и протеаза расщепляет сайт расщепления протеазы в слитом белке, что приводит к отщеплению домена агрегации от нужного белка и экспрессии нужного белка. В отсутствие дезагрегирующего соединения домен агрегации слитого белка принимает конформацию допускающую димеризацию, в результате чего слитый белок переходит в олигомерное, например, димерное, например, агрегированное состояние. Олигомерное, например, димерное, например, агрегированное состояние предотвращает перемещение слитого белка между клеточными компартментами или его секрецию. Олигомерное, например, димерное, например, агрегированное состояние является недоступным для протеазы. В некоторых вариантах осуществления клетка-хозяин контактирует с дезагрегирующим соединением in vivo. В некоторых вариантах осуществления клетка-хозяин контактирует с дезагрегирующим соединением ex vivo.
Стабилизирующее соединение может быть выбрано на основании домена деградации. Например, если домен деградации получен из рецептора эстрогена, стабилизирующее соединение может быть выбрано из базедоксифена или 4-гидрокситамоксифена (4-OHT). Тамоксифен и базедоксифен представляют собой одобренные FDA лекарственные средства и, таким образом, являются безопасными для использования людьми. Если домен деградации получен из белка FKB, стабилизирующее соединение может представлять собой Shield-1.
Дезагрегирующее соединение может быть выбрано на основании домена агрегации. Например, если домен агрегации получен из FKBP, дезагрегирующее соединение может быть выбрано из FK506, рапамицина, AP22542 или AP21998.
В другом аспекте настоящее изобретение относится к способам, включающим введение слитого белка по изобретению в качестве терапевтического средства. Как правило, такое введение будет производиться в форме введения субъекту клеток-хозяев (например, аутологичных или аллогенных клеток-хозяев), экспрессирующих слитый белок по изобретению. Соответственно, путем введения соответствующего стабилизирующего соединения (либо in vivo, либо ex vivo) можно регулировать экспрессию терапевтического средства (то есть, белка, оставшегося после отщепления домена деградации). Соответственно, путем введения соответствующего дезагрегирующего соединения (либо in vivo, либо ex vivo) можно регулировать экспрессию терапевтического средства (то есть, белка, оставшегося после отщепления домена агрегации). Таким образом, можно регулировать экспрессию известных синтетических терапевтических белков или трансмембранных рецепторов (например, слитого белка, например, описанного в настоящем документе, содержащего домен, который содержит молекулу CAR, описанную в настоящем документе). В одном варианте осуществления субъект имеет заболевание, описанное в настоящем документе, например, субъект имеет рак, например, субъект имеет рак, экспрессирующий антиген-мишень, описанный в настоящем документе. В одном варианте осуществления субъект является человеком.
В настоящем документе предложены способы лечения субъекта, имеющего заболевание, связанное с экспрессией опухолевого антигена, путем введения субъекту эффективного количества клетки-хозяина, содержащей любой из слитых белков, описанных в настоящем документе, или нуклеиновую кислоту, кодирующую такой слитый белок. В некоторых вариантах осуществления слитый белок содержит химерный антигенный рецептор (CAR), который содержит, в направлении от N-конца к C-концу, антигенсвязывающий домен, который специфически связывает опухолевый антиген, трансмембранный домен и один или более внутриклеточных сигнальных доменов. В некоторых вариантах осуществления клетка-хозяин является аутологичной для субъекта. В некоторых вариантах осуществления клетка-хозяин является аллогенной для указанного субъекта. В некоторых вариантах осуществления клетка-хозяин контактирует с экспрессионным соединением, например, стабилизирующим соединением или дезагрегирующим соединением. В присутствии стабилизирующего соединения домен деградации слитого белка принимает конформацию, устойчивую к деградации в клетке, и протеаза расщепляет сайт расщепления протеазы в слитом белке, что приводит к отщеплению домена деградации от нужного белка и экспрессии нужного белка. В отсутствие стабилизирующего соединения домен деградации слитого белка принимает конформацию, допускающую деградацию в клетке, что приводит к деградации слитого белка. В присутствии дезагрегирующего соединения домен агрегации слитого белка принимает конформацию, устойчивую к олигомеризации или агрегации, и протеаза расщепляет сайт расщепления протеазы в слитом белке, что приводит к отщеплению домена агрегации от нужного белка и экспрессии нужного белка. В отсутствие дезагрегирующего соединения домен агрегации слитого белка принимает конформацию, допускающую олигомеризацию или агрегацию, что приводит к агрегации слитого белка.
В другом аспекте изобретение относится к способу лечения субъекта, имеющего заболевание, связанное с экспрессией ассоциированного с раком антигена, описанного в настоящем документе, включающему введение субъекту эффективного количества клетки, содержащей слитый белок, содержащий молекулу CAR, например, слитый белок, содержащий молекулу CAR, описанную в настоящем документе.
В другом аспекте изобретение относится к способу лечения субъекта, имеющего заболевание, связанное с экспрессией опухолевого антигена (например, антигена, описанного в настоящем документе), включающему введение субъекту эффективного количества клетки, например, иммунной эффекторной клетки (например, популяции иммунных эффекторных клеток), содержащей слитый белок, содержащий молекулу CAR, при этом молекула CAR содержит антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен, причем указанный внутриклеточный домен содержит костимулирующий домен и/или основной сигнальный домен, при этом указанный антигенсвязывающий домен связывается с опухолевым антигеном, связанным с заболеванием, например, опухолевым антигеном, описанным в настоящем документе.
В связанном аспекте изобретение относится к способу лечения субъекта, имеющего заболевание, связанное с экспрессией опухолевого антигена. Способ включает введение субъекту эффективного количества клетки, например, иммунной эффекторной клетки (например, популяции иммунных эффекторных клеток), содержащей слитый белок, содержащий молекулу CAR, в сочетании со средством, повышающим эффективность иммунной клетки, при этом средство, повышающее эффективность иммунной клетки выбирают из одного или более из:
(i) ингибитора протеинфосфатазы;
(ii) ингибитора киназы;
(iii) цитокина;
(iv) ингибитора иммунной ингибирующей молекулы; или
(v) средства, снижающего уровень или активность TREG клетки.
В другом аспекте изобретение относится к композиции, содержащей иммунную эффекторную клетку (например, популяцию иммунных эффекторных клеток), содержащую слитый белок, содержащий молекулу CAR (например, слитый белок, содержащий молекулу CAR, описанную в настоящем документе), для использования в лечении субъекта, имеющего заболевание, связанное с экспрессией опухолевого антигена, например, заболевание, описанное в настоящем документе.
В конкретных вариантах осуществления любого из вышеуказанных способов или вариантов применения заболевание, связанное с опухолевым антигеном, например, опухолевым антигеном, описанным в настоящем документе, выбирают из пролиферативного заболевания, такого как рак или ранняя стадия рака, или предраковое состояние, миелодисплазия, миелодиспластический синдром или предлейкоз, или неракового состояния, связанного с экспрессией опухолевого антигена, описанного в настоящем документе. В одном варианте осуществления заболевание представляет собой рак, описанный в настоящем документе, например, рак, описанный в настоящем документе, как ассоциированный с мишенью, описанной в настоящем документе. В одном варианте осуществления заболевание представляет собой гематологический рак. В одном варианте осуществления гематологический рак представляет собой лейкоз. В одном варианте осуществления рак выбирают из группы, состоящей из одного или более видов острого лейкоза, включая, но без ограничения, B-клеточный острый лимфоидный лейкоз (BALL), T-клеточный острый лимфоидный лейкоз (TALL), острый лимфоидный лейкоз (ALL); одного или более видов хронического лейкоза, включая, но без ограничения, хронический миелогенный лейкоз (CML), хронический лимфоцитарный лейкоз (CLL); дополнительных видов гематологического рака или гематологических состояний, включая, но без ограничения, B-клеточный пролимфоцитарный лейкоз, новообразование из бластных плазмацитоидных дендритных клеток, лимфому Беркитта, диффузную крупноклеточную В-клеточную лимфому, фолликулярную лимфому, волосатоклеточный лейкоз, мелкоклеточную или крупноклеточную фолликулярную лимфому, злокачественные лимфопролиферативные состояния, лимфому MALT-типа, лимфому из клеток мантийной зоны, лимфому из клеток маргинальной зоны, множественную миелому, миелодисплазию и миелодиспластический синдром, неходжскинскую лимфому, лимфому Ходжкина, плазмабластную лимфому, новообразование из плазмацитоидных дендритных клеток, макроглобулинемию Вальденстрема и «предлейкоз», которые представляют собой разноплановый набор гематологических состояний, объединенных неэффективным продуцированием (или дисплазией) миелоидных клеток крови; кроме того, заболевания, связанные с экспрессией опухолевого антигена, описанного в настоящем документе, включают, но без ограничения, нетипичные и/или неклассические формы рака, ранние стадии рака, предраковые состояния или пролиферативные заболевания, при которых экспрессируется опухолевый антиген, описанный в настоящем документе; а также любые их сочетания. В другом варианте осуществления заболевание, связанное с опухолевым антигеном, описанным в настоящем документе, представляет собой солидную опухоль.
В конкретных вариантах осуществления способы или варианты применения осуществляют в сочетании с использованием средства, повышающего эффективность иммунной эффекторной клетки, например, средства, описанного в настоящем документе.
В любом из вышеуказанных способов и вариантов применения заболевание, связанное с экспрессией опухолевого антигена, выбирают из группы, состоящей из пролиферативного заболевания, предракового состояния, рака, а также нераковых состояний, связанных с экспрессией опухолевого антигена.
Рак может представлять собой гематологический рак, например, рак, выбранный из одного или более из хронического лимфоцитарного лейкоза (CLL), острых форм лейкоза, острого лимфоидного лейкоза (ALL), B-клеточного острого лимфоидного лейкоза (BALL), T-клеточного острого лимфоидного лейкоза (TALL), хронического миелогенного лейкоза (CML), B-клеточного пролимфоцитарного лейкоза, новообразования из бластных плазмацитоидных дендритных клеток, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы, фолликулярной лимфомы, волосатоклеточного лейкоза, мелкоклеточной или крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы MALT-типа, лимфомы из клеток мантийной зоны, лимфомы маргинальной зоны, множественной миеломы, миелодисплазии и миелодиспластического синдрома, неходжскинской лимфомы, лимфомы Ходжкина, плазмабластной лимфомы, новообразования из плазмацитоидных дендритных клеток, макроглобулинемии Вальденстрема или предлейкоза.
Рак также можно выбирать из рака толстого кишечника, рака прямой кишки, почечно-клеточной карциномы, рака печени, немелкоклеточной карциномы легкого, рака тонкого кишечника, рака пищевода, меланомы, рака кости, рака поджелудочной железы, рака кожи, рака головы и шеи, кожной или внутриглазной злокачественной меланомы, рака тела матки, рака яичника, рака прямой кишки, рака ануса, рака желудка, рака яичка, рака тела матки, карциномы фаллопиевых труб, карциномы эндометрия, карциномы шейки матки, карциномы влагалища, карциномы вульвы, болезни Ходжкина, неходжскинской лимфомы, рака эндокринной системы, рака щитовидной железы, рака паращитовидной железы, рака надпочечников, саркомы мягких тканей, рака уретры, рака пениса, солидных опухолей у детей, рака мочевого пузыря, рака почки или мочеточника, карциномы почечной лоханки, новообразования в центральной нервной системе (ЦНС), первичной лимфомы ЦНС, опухолевого ангиогенеза, опухоли оси позвоночника, глиомы ствола головного мозга, аденомы гипофиза, саркомы Капоши, эпидермоидного рака, плоскоклеточного рака, T-клеточной лимфомы, рака, вызываемого факторами окружающей среды, сочетания указанных видов рака, и метастатических очагов указанных видов рака.
В конкретных вариантах осуществления способов или вариантов применения, описанных в настоящем документе, клетку вводят в сочетании со средством, повышающим эффективность клетки, например, одним или более из ингибитора протеинфосфатазы, ингибитора киназы, цитокина, ингибитора иммунной ингибирующей молекулы или средства, снижающего уровень или активность TREG клетки.
В конкретных вариантах осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор протеинфосфатазы представляет собой ингибитор SHP-1 и/или ингибитор SHP-2.
В других вариантах осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы выбирают из одного или более из ингибитора CDK4, ингибитора CDK4/6 (например, палбоциклиба), ингибитора BTK (например, ибрутиниба или RN-486), ингибитора mTOR (например, рапамицина или эверолимуса (RAD001)), ингибитора MNK или двойного ингибитора P13K/mTOR. В одном варианте осуществления ингибитор BTK не уменьшает или не ингибирует киназную активность интерлейкин-2-индуцируемой киназы (ITK).
В других вариантах осуществления способов или вариантов применения, описанных в настоящем документе, средство, которое ингибирует иммунную ингибирующую молекулу, включает антитело или фрагмент антитела, ингибирующую нуклеиновую кислоту, короткие палиндромные повторы, регулярно расположенные группами (CRISPR), эффекторную нуклеазу, подобную активаторам транскрипции (TALEN), или эндонуклеазу «цинковые пальцы» (ZFN), ингибирующие экспрессию ингибирующей молекулы.
В других вариантах осуществления способов или вариантов применения, описанных в настоящем документе, средство, снижающее уровень или активность TREG клетки, выбирают из циклофосфамида, анти-GITR антитела, CD25-истощения или их сочетания.
В конкретных вариантах осуществления способов или вариантов применения, описанных в настоящем документе, иммунную ингибирующую молекулу выбирают из группы, состоящей из PD-1, PD-L1, CTLA-4, TIM-3, LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, TGFR-бета, CEACAM-1, CEACAM-3 и CEACAM-5.
В других вариантах осуществления средство, которое ингибирует ингибирующую молекулу, содержит первый полипептид, содержащий ингибирующую молекулу или ее фрагмент, и второй полипептид, который передает положительный сигнал клетке, и при этом первый и второй полипептиды экспрессируются на CAR-содержащих иммунных клетках, причем (i) первый полипептид включает PD-1, PD-L1, CTLA-4, TIM-3, LAG3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4, TGFR-бета, CEACAM-1, CEACAM-3 и CEACAM-5, или их фрагмент; и/или (ii) второй полипептид включает внутриклеточный сигнальный домен, содержащий основной сигнальный домен и/или костимулирующий сигнальный домен. В одном варианте осуществления основной сигнальный домен содержит функциональный домен CD3-дзета; и/или костимулирующий сигнальный домен содержит функциональный домен белка, выбранного из 41BB, CD27 и CD28.
В других вариантах осуществления цитокин выбирают из IL-7, IL-15, IL-18, или IL-21, или их сочетания.
В других вариантах осуществления иммунную эффекторную клетку, содержащую слитый белок, и второе средство, например, любое из средств комбинированной терапии, раскрытых в настоящем документе (например, средство, повышающее эффективность иммунной эффекторной клетки), вводят практически одновременно или последовательно.
В других вариантах осуществления иммунную клетку, содержащую слитый белок, вводят в сочетании с молекулой, которая нацелена на GITR и/или модулирует функцию GITR. В конкретных вариантах осуществления молекулу, которая нацелена на GITR и/или модулирует функцию GITR, вводят до введения CAR-экспрессирующей клетки или популяции клеток, или до проведения афереза.
В одном варианте осуществления инфузию лимфоцитов, например, инфузию аллогенных лимфоцитов, используют для лечения рака, при этом вводимые инфузией лимфоциты включают по меньшей мере одну CAR-экспрессирующую клетку по настоящему изобретению. В одном варианте осуществления инфузию аутологичных лимфоцитов используют в лечении рака, при этом вводимые инфузией аутологичные лимфоциты включают по меньшей мере одну CAR-экспрессирующую клетку, описанную в настоящем документе.
В одном варианте осуществления клетка представляет собой T-клетку, и T-клетка является дефицитной по диацилглицеринкиназе (DGK). В одном варианте осуществления клетка представляет собой T-клетку, и T-клетка является дефицитной по Ikaros. В одном варианте осуществления клетка представляет собой T-клетку, и T-клетка является дефицитной как по DGK, так и по Ikaros.
В одном варианте осуществления способ включает введение клетки, экспрессирующей слитый белок, содержащий молекулу CAR, описанную в настоящем документе, в сочетании со средством, повышающим активность CAR-экспрессирующей клетки, при этом средство представляет собой цитокин, например, IL-7, IL-15, IL-18, IL-21 или их сочетание. Цитокин можно доставлять в сочетании с введением CAR-экспрессирующей клетки, например, одновременно или вскоре после введения клетки. Альтернативно, цитокин можно доставлять через продолжительный период времени после введения CAR-экспрессирующей клетки, например, после оценки ответа субъекта на CAR-экспрессирующую клетку. В одном варианте осуществления цитокин вводят субъекту одновременно (например, вводят в тот же день) или вскоре после введения (например, вводят через 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней или 7 дней после введения) клетки или популяции клеток по любому из пп. 61-80. В других вариантах осуществления цитокин вводят субъекту через продолжительный период времени (например, по меньшей мере 2 недели, 3 недели, 4 недели, 6 недель, 8 недель, 10 недель или более) после введения клетки или популяции клеток по любому из пп. 61-80, или после оценки ответа субъекта на клетку.
В других вариантах осуществления клетки, экспрессирующие слитый белок, содержащий молекулу CAR, вводят в сочетании со средством, которое ослабляет один или более побочных эффектов, связанных с введением клетки, экспрессирующей молекулу CAR. Побочные эффекты, связанные с введением CAR-экспрессирующей клетки, могут быть выбраны из синдрома высвобождения цитокинов (CRS) или гемофагоцитарного лимфогистиоцитоза (HLH).
В вариантах осуществления любого из вышеуказанных способов или вариантов применения клетки, экспрессирующие молекулу CAR, вводят в сочетании со средством, лечащим заболевание, связанное с экспрессией опухолевого антигена, например, любым из второго или третьего видов терапии, раскрытых в настоящем документе. Дополнительные иллюстративные сочетания включают одно или более из следующего.
В другом варианте осуществления клетку, экспрессирующую молекулу CAR, например, описанную в настоящем документе, можно вводить в сочетании с другим средством, например, ингибитором киназы и/или ингибитором иммунных контрольных точек, описанным в настоящем документе. В одном из вариантов осуществления клетка, экспрессирующая молекулу CAR, также может экспрессировать другое средство, например, средство, повышающее активность CAR-экспрессирующей клетки.
Например, в одном варианте осуществления средство, повышающее активность CAR-экспрессирующей клетки, может представлять собой средство, которое ингибирует ингибирующую молекулу (например, иммунную ингибирующую молекулу). Примеры ингибирующих молекул включают PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета.
В одном варианте осуществления средство, которое ингибирует ингибирующую молекулу, представляет собой ингибирующую нуклеиновую кислоту, такую как дцРНК, киРНК или кшРНК. В вариантах осуществления ингибирующая нуклеиновая кислота связана с нуклеиновой кислотой, кодирующей компонент молекулы CAR. Например, ингибирующая молекула может экспрессироваться на CAR-экспрессирующей клетке.
В другом варианте осуществления средство, которое ингибирует ингибирующую молекулу, например, представляет собой молекулу, описанную в настоящем документе, например, средство, которое содержит первый полипептид, например, ингибирующую молекулу, связанный со вторым полипептидом, который передает положительный сигнал клетке, например, внутриклеточным сигнальным доменом, описанным в настоящем документе. В одном варианте осуществления средство содержит первый полипептид, например, ингибирующую молекулу, такую как PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 или TGFR-бета, либо фрагмент любой из них (например, по меньшей мере часть внеклеточного домена любой из них), и второй полипептид, который представляет собой внутриклеточный сигнальный домен, описанный в настоящем документе (например, содержащий костимулирующий домен (например, 41BB, CD27 или CD28, например, описанный в настоящем документе) и/или основной сигнальный домен (например, сигнальный домен CD3-дзета, описанный в настоящем документе). В одном варианте осуществления средство содержит первый полипептид PD-1 или его фрагмент (например, по меньшей мере часть внеклеточного домена PD-1), и второй полипептид внутриклеточного сигнального домена, описанного в настоящем документе (например, сигнального домена CD28, описанного в настоящем документе, и/или сигнального домена CD3-дзета, описанного в настоящем документе).
В одном варианте осуществления клетку по настоящему изобретению, например, T-клетку или NK-клетку, вводят субъекту, которому ранее была проведена трансплантация стволовых клеток, например, трансплантация аутологичных стволовых клеток.
В одном варианте осуществления клетку по настоящему изобретению, например, T-клетку или NK-клетку, вводят субъекту, который ранее получал дозу мелфалана.
В одном варианте осуществления клетку, экспрессирующую слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе, вводят в сочетании со средством, повышающим эффективность клетки, экспрессирующей молекулу CAR, например, средством, описанным в настоящем документе.
В одном варианте осуществления клетки, экспрессирующие слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе, вводят в сочетании с низкой, иммуностимулирующей дозой ингибитора mTOR. Без связи с конкретной теорией, считается, что введение низкой, иммуностимулирующей дозы (например, дозы, которая недостаточна для полного подавления иммунной системы, но достаточна для улучшения иммунной функции) сопровождается уменьшением количества PD-1-положительных T-клеток или увеличением количества PD-1-отрицательных клеток. PD-1-положительные T-клетки, но не PD-1-отрицательные T-клетки, могут быть истощены за счет взаимодействия с клетками, экспрессирующими лиганд PD-1, например, PD-L1 или PD-L2.
В одном из вариантов осуществления данный подход можно использовать для оптимизации эффективности CAR-клеток, описанных в настоящем документе, в организме субъекта. Без связи с конкретной теорией, считается, что в одном из вариантов осуществления эффективность эндогенных, не модифицированных иммунных эффекторных клеток, например, T-клеток или NK-клеток, улучшается. Без связи с конкретной теорией, считается, что в одном из вариантов осуществления эффективность клетки, экспрессирующей CAR для антигена-мишени, улучшается. В других вариантах осуществления клетки, например, T-клетки или NK-клетки, которые были, или будут, генетически модифицированы для экспрессии CAR, можно обрабатывать ex vivo путем контакта с таким количеством ингибитора mTOR, которое приводит к увеличению количества PD-1-отрицательных иммунных эффекторных клеток, например, T-клеток, либо увеличению соотношения PD-1-отрицательные иммунные эффекторные клетки, например, T-клетки/PD-1-положительные иммунные эффекторные клетки, например, T-клетки.
В одном из вариантов осуществления введение низкой, иммуностимулирующей дозы ингибитора mTOR, например, аллостерического ингибитора, например, RAD001, или каталитического ингибитора, начинают до введения CAR-экспрессирующей клетки, описанной в настоящем документе, например, T-клетки или NK-клетки. В одном из вариантов осуществления CAR-клетки вводят после достаточного периода времени после введения, или достаточного количества введений, доз ингибитора mTOR, для того, чтобы количество PD-1-отрицательных иммунных эффекторных клеток, например, T-клеток или NK-клеток, либо соотношение PD-1-отрицательные иммунные эффекторные клетки, например, T-клетки/PD-1-положительные иммунные эффекторные клетки, например, T-клетки, по меньшей мере временно, увеличилось.
В одном из вариантов осуществления клетку, например, T-клетку или NK-клетку, которая будет генетически модифицирована для экспрессии CAR, собирают после достаточного периода времени после введения, или достаточного количества введений, низкой, иммуностимулирующей дозы ингибитора mTOR, для того, чтобы количество PD-1-отрицательных иммунных эффекторных клеток, например, T-клеток или NK-клеток, либо соотношение PD-1-отрицательные иммунные эффекторные клетки, например, T-клетки/PD-1-положительные иммунные эффекторные клетки, например, T-клетки, у субъекта или в образце, полученном от субъекта, по меньшей мере временно, увеличилось.
В одном варианте осуществления клетку, экспрессирующую слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе, вводят в сочетании со средством, ослабляющим один или более побочных эффектов, связанных с введением клетки, экспрессирующей молекулу CAR, например, средством, описанным в настоящем документе.
В одном варианте осуществления клетку, экспрессирующую слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе, вводят в сочетании со средством, которое лечит заболевание, связанное с ассоциированным с раком антигеном, описанным в настоящем документе, например, средством, описанным в настоящем документе.
В одном варианте осуществления клетку, экспрессирующую два или более слитых белков, содержащих молекулы CAR, например, описанные в настоящем документе, вводят субъекту, который нуждается в этом, для лечения рака. В одном варианте осуществления популяцию клеток, включающую клетку, экспрессирующую слитый белок, содержащий CAR, например, описанный в настоящем документе, вводят субъекту, который нуждается в этом, для лечения рака.
В одном варианте осуществления клетку, экспрессирующую слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе, вводят в дозах и/или с использованием режимов введения, описанных в настоящем документе.
В одном варианте осуществления слитый белок, содержащий молекулу CAR, вводят в иммунные эффекторные клетки (например, T-клетки, NK-клетки), например, с использованием in vitro транскрипции, и субъект (например, человек) получает начальное введение клеток, содержащих слитый белок, содержащий молекулу CAR, и одно или более последующих введений клеток, содержащих слитый белок, содержащий молекулу CAR, при этом одно или более последующих введений выполняют через менее, чем 15 дней, например, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3 или 2 дня после предыдущего введения. В одном варианте осуществления более одного введения клеток, содержащих слитый белок, содержащий молекулу CAR, выполняют субъекту (например, человеку) в неделю, например, в неделю выполняют 2, 3 или 4 введения клеток, содержащих слитый белок, содержащий молекулу CAR. В одном варианте осуществления субъекту (например, субъекту-человеку) выполняют более одного введения клеток, содержащих слитый белок, содержащий молекулу CAR, в неделю (например, 2, 3 или 4 введения в неделю) (в настоящем документе также используют термин «цикл»), с последующей неделей без введения клеток, содержащих слитый белок, содержащий молекулу CAR, а затем субъекту выполняют одно или более дополнительных введений клеток, содержащих молекулу CAR (например, более одного введения клеток, содержащих молекулу CAR, в неделю). В другом варианте осуществления субъект (например, субъект-человек) получает более одного цикла введений клеток, содержащих слитый белок, содержащий молекулу CAR, и временной интервал между всеми циклами составляет менее 10, 9, 8, 7, 6, 5, 4 или 3 дней. В одном варианте осуществления клетки, содержащие слитый белок, содержащий молекулу CAR, вводят через день, по 3 введения в неделю. В одном варианте осуществления клетки, содержащие слитый белок, содержащий молекулу CAR, вводят в течение по меньшей мере двух, трех, четырех, пяти, шести, семи, восьми или более недель.
В одном варианте осуществления клетки, экспрессирующие слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе, вводят в качестве терапии первой линии для заболевания, например, рака, например, рака, описанного в настоящем документе. В другом варианте осуществления клетки, экспрессирующие слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе, вводят в качестве терапии второй, третьей, четвертой линии для заболевания, например, рака, например, рака, описанного в настоящем документе.
В одном варианте осуществления вводят популяцию клеток, описанных в настоящем документе.
В другом аспекте изобретение относится к клетке, экспрессирующей слитый белок, содержащий молекулу CAR, описанную в настоящем документе, для использования в качестве лекарственного средства в сочетании с ингибитором киназы и/или ингибитором иммунных контрольных точек, описанным в настоящем документе. В другом аспекте изобретение относится к ингибитору киназы и/или ингибитору иммунных контрольных точек, описанному в настоящем документе, для использования в качестве лекарственного средства в сочетании с клеткой, экспрессирующей молекулу CAR, описанную в настоящем документе.
В другом аспекте изобретение относится к клетке, экспрессирующей слитый белок, содержащий молекулу CAR, описанную в настоящем документе, для использования в сочетании с цитокином, например, IL-7, IL-15 и/или IL-21, описанным в настоящем документе, в лечении заболевания, связанного с экспрессией опухолевого антигена, являющегося мишенью для CAR. В другом аспекте изобретение относится к цитокину, описанному в настоящем документе, для использования в сочетании с клеткой, экспрессирующей слитый белок, содержащий молекулу CAR, описанную в настоящем документе, в лечении заболевания, связанного с экспрессией опухолевого антигена, являющегося мишенью для CAR.
В другом аспекте изобретение относится к клетке, экспрессирующей слитый белок, содержащий молекулу CAR, описанную в настоящем документе, для использования в сочетании с ингибитором киназы и/или ингибитором иммунных контрольных точек, описанным в настоящем документе, в лечении заболевания, связанного с экспрессией опухолевого антигена, являющегося мишенью для CAR. В другом аспекте изобретение относится к ингибитору киназы и/или ингибитору иммунных контрольных точек, описанному в настоящем документе, для использования в сочетании с клеткой, экспрессирующей слитый белок, содержащий молекулу CAR, описанную в настоящем документе, в лечении заболевания, связанного с экспрессией опухолевого антигена, являющегося мишенью для CAR.
В другом аспекте настоящее изобретение относится к способу, включающему введение слитого белка, содержащего молекулу CAR, например, молекулу CAR, описанную в настоящем документе, или клетки, содержащей нуклеиновую кислоту, кодирующую слитый белок, содержащий молекулу CAR, например, молекулу CAR, описанную в настоящем документе. В одном варианте осуществления субъект имеет заболевание, описанное в настоящем документе, например, субъект имеет рак, например, субъект имеет рак и имеет поддерживающие опухоль клетки, которые экспрессируют поддерживающий опухоль антиген, описанный в настоящем документе. В одном варианте осуществления субъект является человеком.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, слитый белок, содержащий молекулу CAR, вводят в сочетании с другим средством. В одном варианте осуществления средство может представлять собой ингибитор киназы, например, ингибитор CDK4/6, ингибитор BTK, ингибитор mTOR, ингибитор MNK или двойной ингибитор PI3K/mTOR, а также их сочетания. В одном варианте осуществления ингибитор киназы представляет собой ингибитор CDK4, например, ингибитор CDK4, описанный в настоящем документе, например, ингибитор CD4/6, такой как, например, 6-ацетил-8-циклопентил-5-метил-2-(5-пиперазин-1-ил-пиридин-2-иламино)-8H-пиридо[2,3-d]пиримидин-7-он, гидрохлорид (также называемый палбоциклиб или PD0332991). В одном варианте осуществления ингибитор киназы представляет собой ингибитор BTK, например, ингибитор BTK, описанный в настоящем документе, такой как, например, ибрутиниб. В одном варианте осуществления ингибитор киназы представляет собой ингибитор mTOR, например, ингибитор mTOR, описанный в настоящем документе, такой как, например, рапамицин, аналог рапамицина, OSI-027. Ингибитор mTOR может представлять собой, например, ингибитор mTORC1 и/или ингибитор mTORC2, например, ингибитор mTORC1 и/или ингибитор mTORC2, описанный в настоящем документе. В одном варианте осуществления ингибитор киназы представляет собой ингибитор MNK, например, ингибитор MNK, описанный в настоящем документе, такой как, например, 4-амино-5-(4-фторанилино)-пиразолo[3,4-d]пиримидин. Ингибитор MNK может представлять собой, например, ингибитор MNK1a, MNK1b, MNK2a и/или MNK2b. Двойной ингибитор PI3K/mTOR может представлять собой, например, PF-04695102.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор CDK4, выбранный из алоизина A; флавопиридола или HMR-1275, 2-(2-хлорфенил)-5,7-дигидрокси-8-[(3S,4R)-3-гидрокси-1-метил-4-пиперидинил]-4-хроменона; кризотиниба (PF-02341066; 2-(2-хлорфенил)-5,7-дигидрокси-8-[(2R,3S)-2-(гидроксиметил)-1-метил-3-пирролидинил]-4H-1-бензопиран-4-он гидрохлорида (P276-00); 1-метил-5-[[2-[5-(трифторметил)-1H-имидазол-2-ил]-4-пиридинил]окси]-N-[4-(трифторметил)фенил]-1H-бензимидазол-2-амина (RAF265); индисулама (E7070); росковитина (CYC202); палбоциклиба (PD0332991); динациклиба (SCH727965); N-[5-[[(5-трет-бутилоксазол-2-ил)метил]тио]тиазол-2-ил]пиперидин-4-карбоксамида (BMS 387032); 4-[[9-хлор-7-(2,6-дифторфенил)-5H-пиримидо[5,4-d][2]бензазепин-2-ил]амино]-бензойной кислоты (MLN8054); 5-[3-(4,6-дифтор-1H-бензимидазол-2-ил)-1H-индазол-5-ил]-N-этил-4-метил-3-пиридинметанамина (AG-024322); 4-(2,6-дихлорбензоиламино)-1H-пиразол-3-карбоновой кислоты N-(пиперидин-4-ил)амида (AT7519); 4-[2-метил-1-(1-метилэтил)-1H-имидазол-5-ил]-N-[4-(метилсульфонил)фенил]-2-пиримидинамина (AZD5438) и XL281 (BMS908662).
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор CDK4, например, палбоциклиб (PD0332991), и палбоциклиб вводят в дозе примерно 50 мг, 60 мг, 70 мг, 75 мг, 80 мг, 90 мг, 100 мг, 105 мг, 110 мг, 115 мг, 120 мг, 125 мг, 130 мг, 135 мг (например, 75 мг, 100 мг или 125 мг) ежедневно в течение некоторого периода времени, например, ежедневно в течение 14-21 дней 28-дневного цикла или ежедневно в течение 7-12 дней 21-дневного цикла. В одном варианте осуществления используют 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов введения палбоциклиба.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор BTK, выбранный из ибрутиниба (PCI-32765); GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13. В одном варианте осуществления ингибитор BTK не приводит к уменьшению или ингибированию киназной активности интерлейкин-2-индуцируемой киназы (ITK), и его выбирают из GDC-0834; RN-486; CGI-560; CGI-1764; HM-71224; CC-292; ONO-4059; CNX-774 и LFM-A13.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор BTK, например, ибрутиниб (PCI-32765), и ибрутиниб вводят в дозе примерно 250 мг, 300 мг, 350 мг, 400 мг, 420 мг, 440 мг, 460 мг, 480 мг, 500 мг, 520 мг, 540 мг, 560 мг, 580 мг, 600 мг (например, 250 мг, 420 мг или 560 мг) ежедневно в течение некоторого периода времени, например, ежедневно в течение 21-дневного цикла или ежедневно в течение 28-дневного цикла. В одном варианте осуществления используют 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов введения ибрутиниба.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор BTK, который не ингибирует киназную активность ITK, например, RN-486, и RN-486 вводят в дозе примерно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг, 220 мг, 230 мг, 240 мг, 250 мг (например, 150 мг, 200 мг или 250 мг) ежедневно в течение некоторого периода времени, например, ежедневно в течение 28-дневного цикла. В одном варианте осуществления используют 1, 2, 3, 4, 5, 6, 7 или более циклов введения RN-486.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор mTOR, выбранный из темсиролимуса; ридафоролимуса (1R,2R,4S)-4-[(2R)-2-[(1R,9S,12S,15R,16E,18R,19R,21R,23S,24E,26E,28Z,30S,32S,35R)-1,18-дигидрокси-19,30-диметокси-15,17,21,23,29,35-гексаметил-2,3,10,14,20-пентаоксо-11,36-диокса-4-азатрицикло[30,3,1,04,9]гексатриаконта-16,24,26,28-тетраен-12-ил]пропил]-2-метоксициклогексил диметилфосфината, также известного как AP23573 и MK8669; эверолимуса (RAD001); рапамицина (AY22989); симапимода; (5-{2,4-бис[(3S)-3-метилморфолин-4-ил]пиридо[2,3-d]пиримидин-7-ил}-2-метоксифенил)метанола (AZD8055); 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метилпиридо[2,3-d]пиримидин-7(8H)-она (PF04691502) и N2-[1,4-диоксо-4-[[4-(4-оксо-8-фенил-4H-1-бензопиран-2-ил)морфолиний-4-ил]метокси]бутил]-L-аргинилглицил-L-α-аспартил-L-серина (SEQ ID NO: 264), внутренней соли (SF1126), и XL765.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор mTOR, например, рапамицин, и рапамицин вводят в дозе примерно 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг (например, 6 мг) ежедневно в течение некоторого периода времени, например, ежедневно в течение 21-дневного цикла или ежедневно в течение 28-дневного цикла. В одном варианте осуществления используют 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов введения рапамицина. В одном варианте осуществления ингибитор киназы представляет собой ингибитор mTOR, например, эверолимус, и эверолимус вводят в дозе примерно 2 мг, 2,5 мг, 3 мг, 4 мг, 5 мг, 6 мг, 7 мг, 8 мг, 9 мг, 10 мг, 11 мг, 12 мг, 13 мг, 14 мг, 15 мг (например, 10 мг) ежедневно в течение некоторого периода времени, например, ежедневно в течение 28-дневного цикла. В одном варианте осуществления используют 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 или более циклов введения эверолимуса.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой ингибитор MNK, выбранный из CGP052088; 4-амино-3-(п-фторфениламино)пиразолo[3,4-d]пиримидина (CGP57380); церкоспорамида; ETC-1780445-2 и 4-амино-5-(4-фторанилино)пиразолo[3,4-d]пиримидина.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, ингибитор киназы представляет собой двойной ингибитор фосфатидилинозитол-3-киназы (PI3K) и mTOR, выбранный из 2-амино-8-[транс-4-(2-гидроксиэтокси)циклогексил]-6-(6-метокси-3-пиридинил)-4-метилпиридо[2,3-d]пиримидин-7(8H)-она (PF-04691502); N-[4-[[4-(диметиламино)-1-пиперидинил]карбонил]фенил]-N'-[4-(4,6-ди-4-морфолинил-1,3,5-триазин-2-ил)фенил]мочевины (PF-05212384, PKI-587); 2-метил-2-{4-[3-метил-2-оксо-8-(хинолин-3-ил)-2,3-дигидро-1H-имидазо[4,5-c]хинолин-1-ил]фенил}пропаннитрила (BEZ-235); апитолисиба (GDC-0980, RG7422); 2,4-дифтор-N-{2-(метилокси)-5-[4-(4-пиридазинил)-6-хинолинил]-3-пиридинил}бензолсульфонамида (GSK2126458); 8-(6-метоксипиридин-3-ил)-3-метил-1-(4-(пиперазин-1-ил)-3-(трифторметил)фенил)-1H-имидазо[4,5-c]хинолин-2(3H)-она малеиновой кислоты (NVP-BGT226); 3-[4-(4-морфолинилпиридо[3',2':4,5]фуро[3,2-d]пиримидин-2-ил]фенола (PI-103); 5-(9-изопропил-8-метил-2-морфолино-9H-пурин-6-ил)пиримидин-2-амина (VS-5584, SB2343) и N-[2-[(3,5-диметоксифенил)амино]хиноксалин-3-ил]-4-[(4-метил-3-метоксифенил)карбонил]аминофенилсульфонамида (XL765).
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, клетку, содержащую слитый белок, описанный в настоящем документе, вводят субъекту в сочетании с ингибитором протеинтирозинфосфатазы, например, ингибитором протеинтирозинфосфатазы, описанным в настоящем документе. В одном варианте осуществления ингибитор протеинтирозинфосфатазы представляет собой ингибитор SHP-1, например, ингибитор SHP-1, описанный в настоящем документе, такой как, например, стибоглюконат натрия. В одном варианте осуществления ингибитор протеинтирозинфосфатазы представляет собой ингибитор SHP-2.
В одном варианте осуществления способов или вариантов применения, описанных в настоящем документе, клетку, содержащую слитый белок, описанный в настоящем документе, вводят в сочетании с другим средством, и средство представляет собой цитокин. Цитокин может представлять собой, например, IL-7, IL-15, IL-21 или их сочетание. В другом варианте осуществления клетку, содержащую слитый белок, описанный в настоящем документе, вводят в сочетании с ингибитором иммунных контрольных точек, например, ингибитором иммунных контрольных точек, описанным в настоящем документе. Например, в одном варианте осуществления ингибитор иммунных контрольных точек ингибирует ингибирующую молекулу, выбранную из PD-1, PD-L1, CTLA-4, TIM-3, CEACAM (например, CEACAM-1, CEACAM-3 и/или CEACAM-5), LAG-3, VISTA, BTLA, TIGIT, LAIR1, CD160, 2B4 и TGFR-бета.
В одном аспекте слитый белок, описанный в настоящем документе, можно использовать для уничтожения нормальных клеток, экспрессирующих опухолевый антиген, описанный в настоящем документе, то есть, он подходит для использования в качестве клеточной кондиционирующей терапии перед трансплантацией клеток. В одном аспекте нормальная клетка, экспрессирующая опухолевый антиген, описанный в настоящем документе, представляет собой нормальную стволовую клетку, и трансплантация клеток представляет собой трансплантацию стволовых клеток.
Способы лечения вызываемых аутоантителами или аллоантителами состояний
Настоящее изобретение относится к способам лечения вызываемых аутоантителами или аллоантителами заболеваний или состояний у субъекта путем нацеливания на B-клетки, включая продуцирующие аутоантитела или аллоантитела B-клетки, модифицированных T-клеток, направленных против B-клеток. В одном варианте осуществления после истощения B-клеток модифицированными T-клетками или после возникновения неблагоприятной реакции на модифицированные T-клетки проводят избирательную абляцию модифицированных T-клеток у субъекта путем активации суицидного гена, который был введен в модифицированные T-клетки.
В одном аспекте изобретение относится к способу лечения вызываемого аутоантителами или аллоантителами заболевания или состояния у субъекта, который нуждается в этом, включающему введение субъекту эффективного количества фармацевтической композиции, содержащей модифицированную T-клетку. Модифицированная T-клетка содержит нуклеиновую кислоту, содержащую суицидный ген, и нуклеиновую кислоту, кодирующую химерный антигенный рецептор, содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В одном варианте осуществления способ дополнительно включает индукцию экспрессии суицидного гена для продуцирования продукта суицидного гена, вызывающего гибель модифицированной T-клетки. В одном таком варианте осуществления введение индуцирующего средства вызывает экспрессию суицидного гена. В другом варианте осуществления индукция экспрессии суицидного гена происходит после того, как модифицированная T-клетка окажет цитотоксическое действие на B-клетки, или после начала возникновения у субъекта неблагоприятной реакции на модифицированную T-клетку.
В другом варианте осуществления способ дополнительно включает активацию продукта суицидного гена для индукции гибели модифицированной T-клетки. В одном таком варианте осуществления используют введение активирующего средства для стимуляции димеризации продукта суицидного гена с целью активации продукта суицидного гена. В другом варианте осуществления активация продукта суицидного гена происходит после того, как модифицированная T-клетка окажет цитотоксическое действие на B-клетки, или после начала возникновения у субъекта неблагоприятной реакции на модифицированную T-клетку, или после достижения терапевтического эффекта.
В другом варианте осуществления способ дополнительно включает ингибирование экспрессии суицидного гена для ингибирования гибели модифицированной T-клетки. В одном таком варианте осуществления введение ингибирующего средства приводит к ингибированию экспрессии суицидного гена. В другом варианте осуществления введение ингибирующего средства выполняют одновременно с введением модифицированной T-клетки, продолжают, пока модифицированная T-клетка оказывает цитотоксическое действие на B-клетки, и могут прекращать после начала развития у субъекта неблагоприятной реакции на модифицированную T-клетку.
В другом варианте осуществления способ включает подавление активации продукта суицидного гена для подавления гибели модифицированной T-клетки. В одном таком варианте осуществления введение солюбилизирующего средства предотвращает димеризацию продукта суицидного гена для предотвращения активации продукта суицидного гена. В другом варианте осуществления введение солюбилизирующего средства выполняют одновременно с введением модифицированной T-клетки, продолжают, пока модифицированная T-клетка оказывает цитотоксическое действие на B-клетки, и могут прекращать после начала развития у субъекта неблагоприятной реакции на модифицированную T-клетку или после достижения терапевтического эффекта.
В другом варианте осуществления способ дополнительно включает введение солюбилизирующего средства для предотвращения димеризации CAR, при этом CAR связан с доменом димеризации, таким как домен димеризации FKBP или аналогичной молекулы. В таком варианте осуществления молекулы CAR спонтанно агрегируют в цитоплазме или другой внутренней зоне, тем самым предотвращая представление молекул CAR на поверхности модифицированной T-клетки. В другом варианте осуществления введение солюбилизирующего средства выполняют одновременно с введением модифицированной T-клетки, продолжают, пока модифицированная T-клетка оказывает цитотоксическое действие на B-клетки, и могут прекращать после начала развития у субъекта неблагоприятной реакции на модифицированную T-клетку или после достижения терапевтического эффекта.
Модифицированные T-клетки можно вводить животному, предпочтительно млекопитающему, даже более предпочтительно человеку, для подавления иммунной реакции, такой как реакции, являющиеся обычными при аутоиммунном заболевании или состоянии, либо при вызываемом аллоантителами заболевании или состоянии.
Кроме того, модифицированные T-клетки по настоящему изобретению можно использовать для лечения любого состояния, при котором желательно уменьшение или иное ингибирование иммунного ответа, особенно опосредованного клетками иммунного ответа, для лечения или ослабления заболевания. В одном аспекте изобретение относится к лечению состояния, такого как вызываемое аутоантителами или аллоантителами заболевание, у субъекта, включающему введение субъекту терапевтически эффективного количества фармацевтической композиции, содержащей модифицированную T-клетку, описанную в настоящем документе.
Примеры вызываемых аутоантителами заболеваний или состояний включают, но без ограничения, буллезный пемфигоид, приобретенный буллезный эпидермолиз, p200 пемфигоид, линеарный IgA-зависимый буллезный дерматоз, другие заболевания группы пемфигоидных заболеваний, герпетиформный дерматит, глютенчувствительную целиакию, миастению, синдром Гудпасчера, гранулематоз с полиангиитом и другие ANCA+ формы васкулита, аутоиммунный энцефалит с поражением лимбической системы, анти-NMDA-рецепторный энцефалит, нейромиелит зрительного нерва, аутоиммунную гемолитическую анемию, вызываемое аутоантителами повреждение органов-мишеней при волчанке и других заболеваниях соединительной ткани (вызываемое анти-дцДНК, анти-Ro и другими аутоантителами), болезнь Грейвса и тиреоидит Хашимото, продуцирование антител против инсулина при диабете, антител против инсулиновых рецепторов при аутоиммунной гипогликемии, криоглобулинемию, ревматоидный артрит, рассеянный склероз, синдром Шегрена, дерматомиозит, продуцирование антител против рецепторов Fc-эпсилон при хронической идиопатической крапивнице, антител против фолатных рецепторов, антител против эндотелиальных рецепторов или против адренергических рецепторов при легочной артериальной гипертензии, рефрактерной гипертензии, расширенной кардиомиопатии, а также аутовоспалительный синдром.
Примеры вызываемого аллоантителами заболевания или состояния включают, но не ограничиваются ими, иммунную реакцию в ответ на трансплантацию органа, переливание крови и продуцирование антител, специфичных для HLA и/или b2-микроглобулина донора, сенсибилизацию при беременности антигенами группы крови или Rh, или при белковой заместительной терапии, например, фактором VIII, α-L-идуронидазой, коллагеном VII типа и так далее, включая, но без ограничения, заместительные белки, перечисленные в Gorzelany, et al. (Sci. Transl. Med., 5(178):178s10, 2013).
В одном варианте осуществления заболевание или состояние представляет собой пемфигус. Продольный анализ репертуаров B-клеток у пациентов с пемфигусом в процессе лечения показал, что пациенты с пемфигусом испытывают рецидив с теми же анти-Dsg B-клеточными клонами, которые наблюдаются при активном заболевании. В совокупности эти данные указывают на то, что однократное, но действительно полное истощение B-клеток, приводящее к элиминации анти-Dsg B-клеточных клонов за счет нацеливания на пан-B-клеточный маркер, такой как CD20 или, альтернативно, CD19, может приводить к полному исцелению пациентов с пемфигусом. Патологические клоны будут элиминированы, а репертуар здоровых B-клеток будет реформирован, и другое редкое нарушение толерантности вряд ли возникнет вновь.
По аналогии, тот же подход также должен быть эффективным в случае любого вызываемого B-клетками или опосредованного антителами заболевания; например, заболеваний, вызываемых аллоантителами, появляющимися вследствие переливания крови или сенсибилизации при беременности, специфичными для HLA донора аллоантителами, осложняющими трансплантацию органов, и аллоантителами, возникающими в результате белковой заместительной терапии при генетических заболеваниях. Даже если аллоантитела вновь появляются вследствие повторного воздействия аллоантигена, периодически повторяемое лечение для полной, но временной, элиминации B-клеток (и, как следствие, аллоантител) будет полезным при таких заболеваниях.
Фармацевтические композиции
Фармацевтические композиции по настоящему изобретению могут содержать любой слитый белок, нуклеиновую кислоту, кодирующую такой слитый белок, описанный в настоящем документе, и один или более фармацевтически или физиологически приемлемых носителей, разбавителей или эксципиентов. Такие композиции могут содержать буферы, такие как нейтральный буферный солевой раствор, фосфатно-солевой буфер и тому подобное; углеводы, такие как глюкоза, манноза, сахароза или декстраны, маннит; белки; полипептиды или аминокислоты, такие как глицин; антиоксиданты; хелатирующие агенты, такие как ЭДТА или глутатион; адъюванты (например, гидроксид алюминия) и консерванты. В одном аспекте композиции по настоящему изобретению сформулированы для внутривенного введения.
Фармацевтические композиции по настоящему изобретению можно вводить способом, соответствующим заболеванию, которое предстоит лечить (или предотвращать). Количество и частота введений будут определяться такими факторами, как состояние здоровья пациента, а также тип и степень тяжести заболевания пациента, хотя соответствующие дозы могут быть определены в клинических испытаниях.
В одном аспекте изобретение относится к фармацевтической композиции, сформулированной для использования в способе, описанном в настоящем документе, которая содержит модифицированную T-клетку, содержащую нуклеиновую кислоту, кодирующую суицидный ген, и нуклеиновую кислоту, кодирующую химерный антигенный рецептор, содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В другом аспекте изобретение относится к фармацевтической композиции, сформулированной для использования в способе, описанном в настоящем документе, которая содержит модифицированную T-клетку, содержащую нуклеиновую кислоту, кодирующую домен димеризации и химерный антигенный рецептор (CAR), содержащий анти-B-клеточный связывающий домен, трансмембранный домен, костимулирующий домен и внутриклеточный сигнальный домен.
В одном варианте осуществления фармацевтическая композиция в значительной степени свободна от, например, не содержит поддающиеся определению уровни, загрязнителя, например, выбранного из группы, состоящей из эндотоксина, микоплазмы, репликативно-компетентного лентивируса (RCL), p24, нуклеиновой кислоты VSV-G, HIV gag, остаточных гранул, покрытых анти-CD3/анти-CD28 антителами, мышиных антител, объединенной человеческой сыворотки, бычьего сывороточного альбумина, бычьей сыворотки, компонентов культуральной среды, клеток-упаковщиков вектора или компонентов плазмиды, бактерий и грибков. В одном варианте осуществления бактерия представляет собой по меньшей мере одну бактерию, выбранную из группы, состоящей из Alcaligenes faecalis, Candida albicans, Escherichia coli, Haemophilus influenza, Neisseria meningitides, Pseudomonas aeruginosa, Staphylococcus aureus, Streptococcus pneumonia и Streptococcus pyogenes группы A.
Если указано «иммунологически эффективное количество», «эффективное против опухоли количество», «эффективное для ингибирования опухоли количество» или «терапевтическое количество», точное вводимое количество композиций по настоящему изобретению может определять врач с учетом индивидуальных различий в возрасте, массе тела, размере опухоли, степени инфицирования или метастазирования, а также состояния здоровья пациента (субъекта). В целом, можно отметить, что фармацевтическую композицию, содержащую иммунные эффекторные клетки (например, T-клетки, NK-клетки), описанные в настоящем документе, можно вводить в дозе 104-109 клеток/кг массы тела, в некоторых случаях 105-106 клеток/кг массы тела, включая все промежуточные целые значения в данных диапазонах. T-клеточные композиции также можно вводить в этих дозах несколько раз. Клетки можно вводить с использованием метода инфузии, широко применяемого в иммунотерапии (смотри, например, Rosenberg et al., New Eng. J. of Med. 319:1676, 1988).
В некоторых аспектах может быть желательно вводить субъекту активированные иммунные эффекторные клетки (например, T-клетки, NK-клетки), с последующим повторным сбором крови (или проведением афереза), активацией иммунных эффекторных клеток (например, T-клеток, NK-клеток) из крови в соответствии с настоящим изобретением и повторным вливанием пациенту этих активированных и размноженных иммунных эффекторных клеток (например, T-клеток, NK-клеток). Этот процесс можно осуществлять множество раз каждые несколько недель. В конкретных аспектах можно активировать иммунные эффекторные клетки (например, T-клетки, NK-клетки) из объема собранной крови, составляющего от 10 см3 до 400 см3. В конкретных аспектах иммунные эффекторные клетки (например, T-клетки, NK-клетки) активируют из объема собранной крови, составляющего 20 см3, 30 см3, 40 см3, 50 см3, 60 см3, 70 см3, 80 см3, 90 см3 или 100 см3.
Введение субъекту композиций можно выполнять любым удобным способом, включая ингаляцию аэрозоля, инъекцию, проглатывание, трансфузию, имплантацию или трансплантацию. Композиции, описанные в настоящем документе, можно вводить пациенту трансартериальной, подкожной, внутрикожной, внутриопухолевой, внутриузловой, интрамедуллярной, внутримышечной, внутривенной (в/в) инъекцией или внутрибрюшинно. В одном аспекте композиции клеток по настоящему изобретению вводят пациенту внутрикожной или подкожной инъекцией. В одном аспекте композиции клеток по настоящему изобретению вводят в/в инъекцией. Композиции иммунных эффекторных клеток (например, T-клеток, NK-клеток) можно вводить инъекцией непосредственно в опухоль, лимфатический узел или зону инфекции.
В конкретном иллюстративном аспекте субъекты могут быть подвергнуты лейкаферезу, при этом лейкоциты собирают, обогащают или истощают ex vivo для отбора и/или выделения интересующих клеток, например, T-клеток. Эти выделенные T-клетки можно размножать способами, известными в данной области, и обрабатывать для введения одного или более конструктов CAR по изобретению, тем самым создавая CAR T-клетку по изобретению. Субъекты, которые нуждаются в этом, затем могут получать стандартное лечение химиотерапевтическими средствами в высоких дозах, с последующей трансплантацией стволовых клеток периферической крови. В конкретных аспектах после или одновременно с трансплантацией субъекты получают инфузию размноженных CAR T-клеток по настоящему изобретению. В дополнительном аспекте размноженные клетки вводят до или после хирургической операции.
Дозы вышеуказанных терапевтических препаратов, вводимых пациенту, будут варьироваться в зависимости от конкретного состояния, подвергаемого лечению, и реципиента, получающего лечение. Масштабирование доз для введения человеку можно проводить в соответствии с принятой в данной области практикой.
ПРИМЕРЫ
Пример 1: Материалы и методы для примеров 1-13.
Конструкты
Следующие конструкты, приведенные в Таблице 22, были использованы в примерах 1-13.
Следует отметить, что изобретение охватывает обе ориентации тяжелой и легкой цепи.
Таблица 22. Последовательности различных конструктов (используемый сигнальный пептид выделен жирным шрифтом; сайты расщепления фурина подчеркнуты)
FKBPmut_HA_Furin_CAR19
FKBPmut_HA_Furinmut_CAR19
DHFRmut_HA_Furin_CAR19
DHFRmut_HA_Furinmut_CAR19
ERmut_HA_FurinCAR19
ERmut_HA_FurinMmut_CAR19
FKBPmut_HA_noFurin_CAR19
ERmut_HA_noFurinCAR19
ERmut_noHa_FurinCAR19
ERmut_noHa_noFurin CAR19
Общие методы
Следующие общие материалы и методы были использованы для анализов, описанных в примерах 1-13.
Получение конструктов CAR
scFv, используемые в конструктах CAR, которые были оценены в примере 3, были независимо синтезированы на основании последовательности анти-CD19 scFv, приведенной выше. scFv клонировали в направлении от тяжелой к легкой цепи, с гибким линкером, соединяющим домены VH и VL (например, GGGGSGGGGSGGGGSGGGGS (SEQ ID NO: 29)), в каркас вектора, содержащий шарнирную область CD8 наряду с молекулой 4-1BB и молекулой CD3-дзета. В данный конструкт, выше scFv, добавляли N-концевой сайт расщепления фурина, слитый с доменом дестабилизации. Белки, используемые в конструктах фурин-дегрон, которые были оценены в примерах 4-5, были независимо синтезированы на основании общедоступных данных о последовательностях. В данный конструкт, выше последовательности белка, добавляли N-концевой сайт расщепления фурина, слитый с доменом дестабилизации.
Линии клеток и трансдукция клеток
Клетки Jurkat получали от ATCC и поддерживали в среде в соответствии с рекомендациями поставщика. Клетки линии Jurkat трансдуцировали путем спинокуляции лентивирусным супернатантом от клеток 293T, трансфицированных pELPS, с использованием регулируемой плазмидной ДНК белка-домена фурина.
Раковые клетки
Клетки линий NALM6 и K562 получали от ATCC и поддерживали в среде в соответствии с рекомендациями поставщика. Для получения биолюминесцентной модели для анализов на уничтожение T-клетками все клетки трансдуцировали лентивирусным конструктом для люциферазы и поддерживали путем отбора с антибиотиком.
Проточная цитометрия
Клетки выделяли из in vitro культуры, промывали один раз в PBS с добавлением 0,5% бычьего сывороточного альбумина и окрашивали на льду с использованием либо биотинилированного белка L, с последующей инкубацией с флуорохром-конъюгированным стрептавидиновым реагентом, либо антитела, узнающего конкретный антиген-мишень. Во всех анализах интересующую популяцию отбирали на основании характеристик прямого и бокового светорассеяния, с последующим отделением синглетов, и живые клетки отбирали. Проточную цитометрию проводили на четырехлазерной установке Fortessa (Becton-Dickinson).
Обработка соединениями
Во всех случаях либо 4-OHT, либо Shield-1, ресуспендировали в этаноле. Триметоприм (TMP) ресуспендировали в ДМСО. Во всех случаях, когда концентрации не указаны, соединения добавляли в общей сложности на 24 часа перед проведением анализа методом проточной цитометрии. Использовали 3 мкМ 4-OHT (ERα), 1 мкМ Shield-1 (FKBP) или 100 мкМ TMP (ecDHFR).
Анализ на уничтожение
Вкратце, трансдуцированные геном люциферазы клетки-мишени указанных линий инкубировали в указанных соотношениях с эффекторными CD19CAR или CD19CAR-FurON T-клетками в течение 18 часов. Остаточную люциферазную активность измеряли путем добавления Bright-Glo (Promega), на люминесцентном ридере (Envision). Процент уничтожения рассчитывали с использованием отрицательных контролей.
Секреция цитокинов
Эффекторные клетки и клетки-мишени инкубировали в соотношении 3:1 в среде RPMI, содержащей 10% ЭБС, в течение 18 часов. Супернатант анализировали с использованием 3-плексного набора в соответствии с инструкциями производителя (Invitrogen).
Пример 2: Фурин является наиболее высокоэкспрессируемой пропротеинконвертазой в первичных человеческих T-клетках
Литературные источники свидетельствуют о том, что фурин (FUR; PACE; PCSK3; SPC1) имеет широкий профиль экспрессии (Seidah, et al., Nature Reviews Drug Discovery 11, 367-383 (May 2012)). Экспрессию представителей семейства пропротеинконвертаз анализировали методом кОТ-ПЦР. РНК получали из нормальных донорских T-клеток в дни 0, 4 и 11 после стимуляции активирующими гранулами с анти-CD3/анти-CD28. В дополнительной группе в процессе культивирования добавляли 100 Ед/мл IL-2, и РНК собирали в день 11. Полученные данные показывают, что после активации гранулами с анти-CD3/анти-CD28 мРНК фурина экспрессируется на более высоком уровне, чем мРНК других представителей семейства пропротеинконвертаз (ФИГ. 1).
Пример 3: Экспрессия CD19 CAR, контролируемая добавлением соединения
T-клетки Jurkat трансдуцировали фуриновым дегрон-доменом (FKBPFD, ERαFD или DHFRFD), слитым с конструктом анти-CD19 scFv CAR, с последующей обработкой соответствующим соединением. FKBPFD-трансдуцированные клетки обрабатывали 1 мкМ раствором Shield-1. ERαFD-трансдуцированные клетки обрабатывали 1 мкМ раствором базедоксифена. DHFRFD-трансдуцированные клетки обрабатывали 1 мМ раствором TMP. Экспрессия анти-CD19 scFv индуцируется в присутствии соединения (ФИГ. 2). Черный цвет=НТ; серый цвет=конструкт, без соединения; белый цвет=конструкт, с соединением. Эти данные показывают, что несколько дегрон-доменов, при объединении с доменом расщепления фурина, приводят к четкой, зависимой от соединения регуляции экспрессии CAR 19.
Пример 4: Кинетика экспрессии CAR в клетках Jurkat после добавления соединения
T-клетки Jurkat трансдуцировали указанными фуриновыми дегрон-доменами (FKBPFD или ERαFD), слитыми с конструктом анти-CD19 scFv CAR. Эти клетки обрабатывали либо 1 мкМ раствором Shield-1, либо 1 мкМ раствором 4-OHT, в течение указанного периода времени, и экспрессию CAR определяли методом FACS. Полученные данные показывают, что индукция экспрессии при использовании CAR 19 с фуриновым дегроном происходит вскоре после добавления соединения и является стабильной в течение всего периода обработки соединением (ФИГ. 3).
Пример 5: Индуцируемая соединением экспрессия CAR в первичных человеческих T-клетках
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом ERα (доменом ERαFD), слитым с конструктом анти-CD19 scFv CAR. 100 Ед/мл IL-2 добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28. Базедоксифен добавляли в день 10, и экспрессию CAR определяли методом FACS в день 11. Полученные данные показывают, что фуриновый дегрон-домен (например, домен ERαFD) может регулировать экспрессию CAR 19 зависимым от соединения образом в первичных человеческих T-клетках (ФИГ. 4), и что стабилизация усиливается в присутствии IL-2 in vitro (ФИГ. 4).
Пример 6: Кинетика экспрессии CAR после вымывания соединения в первичных T-клетках
Первичные человеческие T-клетки трансдуцировали указанным фуриновым дегрон-доменом (FKBPFD или ERαFD), слитым с конструктом анти-CD19 scFv CAR. 100 Ед/мл IL-2 добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28. Базедоксифен добавляли в день 10, и T-клетки замораживали в день 11. T-клетки размораживали, обильно промывали и культивировали в течение указанного времени, с последующим определением экспрессии CAR методом FACS. Полученные данные показывают, что удаление соединения приводит к уменьшению экспрессии CAR 19 при использовании фуринового дегрон-домена (ФИГ. 5).
Пример 7: Несколько нацеленных на ER-альфа лекарственных средств стабилизируют ER-альфа FurON CART
T-клетки Jurkat трансдуцировали доменом деградации ERαFD, слитым с конструктом анти-CD19 scFv CAR, с последующей обработкой указанными соединениями в течение 24 часов. Соединения использовали в следующих концентрациях: 10 мкМ для 4-OHT, 1 мкМ для базедоксифена или 1 мкМ для лазофоксифена. Полученные данные показывают, что несколько нацеленных на ER-альфа соединений могут индуцировать экспрессию CAR19 при использовании системы фуринового дегрона (FurON) на основе рецептора эстрогена (ФИГ. 6).
Пример 8: Зависимость от дозы базедоксифена в человеческих T-клетках
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и культивировали с базедоксифеном в указанных концентрациях в течение 48 часов. Экспрессию CAR определяли методом FACS. Полученные данные показывают, что физиологически релевантные концентрации базедоксифена могут стабилизировать экспрессию CAR19 с фуриновым дегроном на уровне, аналогичном уровню в клетках с родительским CAR19 (ФИГ. 7).
Пример 9: Зависимое от соединения специфичное для мишени уничтожение клеток при помощи ER-альфа FurON CART
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и базедоксифен добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали в течение 20 часов с содержащими люциферазу клетками-мишенями указанных линий K562 (CD19-) или NALM6 (CD19+). Процент уничтожения определяли, анализируя остаточную люциферазную активность. Полученные данные показывают, что CAR19 с фуриновым дегрон-доменом на основе рецептора эстрогена вызывает специфическое уничтожение CD19+ клеток опухолей зависимым от соединения образом и не уступает по эффективности родительскому CAR19 (ФИГ. 8).
Пример 10: Зависимое от соединения специфичное для мишени уничтожение клеток при помощи FKBP FurON CART
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом FKBPFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и Shield-1 добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали в течение 20 часов с содержащими люциферазу клетками-мишенями указанных линий K562 (CD19-) или NALM6 (CD19+). Процент уничтожения определяли, анализируя остаточную люциферазную активность. Полученные данные показывают, что CAR19 с фуриновым дегрон-доменом на основе FKBP вызывает специфическое уничтожение CD19+ клеток опухолей зависимым от соединения образом и не уступает по эффективности родительскому CAR19 (ФИГ. 9).
Пример 11: Зависимое от соединения продуцирование цитокинов ER-альфа FurON CART
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и базедоксифен добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали в течение 20 часов с клетками-мишенями указанных линий. Супернатанты собирали и анализировали методом мультиплексного анализа цитокинов с микросферами. Полученные данные показывают, что CAR19 с фуриновым дегрон-доменом на основе рецептора эстрогена вызывает специфическое продуцирование цитокинов в присутствии CD19+ клеток опухолей зависимым от соединения образом и не уступает по эффективности родительскому CAR19 (ФИГ. 10).
Пример 12: Зависимая от соединения пролиферация ER-альфа FURON CART
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом ERαFD, слитым с конструктом анти-CD19 scFv CAR, или родительским конструктом CD19 CAR. 100 Ед/мл IL-2 и базедоксифен добавляли в день 9 после активации стимулирующими гранулами с анти-CD3/CD28, и T-клетки замораживали в день 11. T-клетки размораживали и инкубировали с клетками-мишенями указанных линий в течение 4 дней. Количество FurON-CAR T-клеток анализировали методом FACS. Полученные данные показывают, что CAR19 с фуриновым дегрон-доменом на основе рецептора эстрогена вызывает специфическую пролиферацию в присутствии CD19+ клеток опухолей зависимым от соединения образом и не уступает по эффективности родительскому CAR19 (ФИГ. 11).
Пример 13: материалы и методы для примеров 14-26.
Следующие общие материалы и методы были использованы для анализов, описанных в примерах 14-26.
Конструкты FurON
В некоторых вариантах осуществления слитый белок, описанный в настоящем документе, содержит фуриновый дегрон-домен (FurON), который включает два компонента: дегрон, или домен деградации, который представляет собой мутантный белковый домен, неспособный принимать правильную конформацию в отсутствие низкомолекулярного лиганда, и сайт расщепления фурина. Фуриновый дегрон-домен может быть слит с интересующим белком, который экспрессируется в эндоплазматическом ретикулуме. N- и/или C-конец интересующего белка могут быть использованы в качестве сайта слияния при условии, что фуриновый дегрон-домен направлен в сторону просвета эндоплазматического ретикулума. Интересующий белок может представлять собой либо мембранный белок (независимо от числа трансмембранных доменов), либо растворимый белок. Ориентация сайта расщепления фурина относительно дегрон-домена должна быть такой, чтобы расщепление приводило к разделению фуринового дегрон-домена и интересующего белка. В отсутствие низкомолекулярного лиганда или стабилизирующего соединения фуриновый дегрон-домен приводит к дестабилизации или деградации всего слитого белка. В присутствии низкомолекулярного лиганда или стабилизирующего соединения слитый белок не подвергается деградации. Фуриновый дегрон-домен мутирован таким образом, что аффинность для его естественного эндогенного лиганда устранена; аффинность для низкомолекулярного лиганда или стабилизирующего соединения сохранена; и белок становится нестабильным в отсутствие низкомолекулярного лиганда.
Несколько конструктов, имеющих разные мутации и разные сайты расщепления фурина в фуриновом дегрон-домене, были получены и слиты с N-концом анти-CD19 scFV CAR или анти-CD123 scFV CAR. Независимо от ориентации тяжелой и легкой цепей scFV, слияние фуринового дегрон-домена имеет место между лидерным сигнальным пептидом и scFV. Выбранный мутантный белок в фуриновом дегрон-домене представлял собой укороченный вариант рецептора эстрогена альфа. Низкомолекулярные лиганды, выбранные для стабилизации фуринового дегрон-домена, принадлежат к семейству избирательных модуляторов или ингибиторов рецептора эстрогена.
Эффективность фуринового дегрон-домена при дестабилизирующей или стабилизирующей структуре CAR оценивали в отсутствие или в присутствии низкомолекулярного лиганда. Проявление эффекторной функции CAR T-клетки со слитым фуриновым дегрон-доменом также оценивали в отсутствие или в присутствии низкомолекулярного лиганда и сравнивали с клеткой, содержащей родительский конструкт CAR19. Клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток, с добавлением не трансдуцированных T-клеток (НТ) из того же источника размноженных донорских T-клеток. Затем нормированные популяции использовали в анализах с совместным культивированием для измерения CAR-опосредованной цитолитической функции, продуцирования цитокинов и пролиферации.
Получение конструктов FurON CAR
scFv, используемые в конструктах CAR, которые были оценены в примерах, были независимо синтезированы на основании последовательностей анти-CD19 или анти-CD123 scFV, приведенных выше. scFv клонировали в направлении от легкой к тяжелой цепи (анти-CD19) или в направлении от тяжелой к легкой цепи (анти-CD123), с гибким линкером, соединяющим домены VH и VL (например, GGGGSGGGGSGGGGSGGGGS (SEQ ID NO: 29)), в каркас вектора, содержащий шарнирную область CD8 наряду с молекулой 4-1BB и молекулой CD3-дзета. В данный конструкт, выше scFv, добавляли N-концевой сайт расщепления фурина, слитый с доменом дестабилизации. Все конструкты получали в лентивирусном векторе. Последовательности различных конструктов FurON CAR и их компонентов приведены в Таблице 23.
Таблица 23. Последовательности конструктов FurON CAR и их компонентов
(305ак-549ак)
Линии клеток и трансдукция клеток
Клетки Jurkat получали от ATCC и поддерживали в среде в соответствии с рекомендациями поставщика. Клетки линии Jurkat трансдуцировали путем спинокуляции лентивирусным супернатантом от клеток 293T, трансфицированных различными плазмидными ДНК.
Раковые клетки
Клетки линий NALM6, K562, Molm13 получали от ATCC и поддерживали в среде в соответствии с рекомендациями поставщика. Для получения биолюминесцентной модели для анализов на уничтожение T-клетками все клетки трансдуцировали лентивирусным конструктом для люциферазы и поддерживали путем отбора с антибиотиком.
Обработка соединениями
4-гидрокситамоксифен (4-OHT) ресуспендировали в этаноле. Базедоксифен и ралоксифен ресуспендировали в ДМСО. Во всех случаях, когда концентрации не указаны, соединения добавляли в концентрации 1 мкМ на 24 часа перед проведением анализа методом проточной цитометрии.
Проточная цитометрия
Клетки выделяли из in vitro культуры, промывали один раз в PBS с добавлением 0,5% бычьего сывороточного альбумина и окрашивали на льду с использованием либо биотинилированного белка L, с последующей инкубацией с флуорохром-конъюгированным стрептавидиновым реагентом, либо антитела, узнающего конкретный антиген-мишень. Во всех анализах интересующую популяцию отбирали на основании характеристик прямого и бокового светорассеяния, с последующим отделением синглетов, и живые клетки отбирали. Проточную цитометрию проводили на четырехлазерной установке Fortessa (Becton-Dickinson).
Анализ на уничтожение клеток опухоли
Вкратце, трансдуцированные геном люциферазы клетки-мишени указанных линий совместно культивировали в указанных соотношениях с эффекторными CD19CAR, FurON-CD19CAR, CD123CAR, FurON-CD123 CAR T-клетками в течение 20 часов в присутствии или в отсутствие базедоксифена. Остаточную люциферазную активность измеряли путем добавления Bright-Glo (Promega) на люминесцентном ридере (Envision). Процент уничтожения рассчитывали с использованием отрицательных контролей.
Секреция цитокинов
Эффекторные клетки и трансдуцированные геном люциферазы клетки-мишени указанных линий совместно культивировали в соотношении 3:1 в среде RPMI, содержащей 10% ЭБС, в течение 20 часов в присутствии или в отсутствие базедоксифена. Супернатант анализировали с использованием 3-плексного набора в соответствии с инструкциями производителя (Invitrogen).
Анализ пролиферации
Эффекторные клетки и облученные клетки-мишени совместно культивировали в течение 4 дней в присутствии или в отсутствие базедоксифена. Затем клетки собирали, промывали и окрашивали с использованием анти-CD3 антитела и/или реагента белка L для обнаружения поверхностной экспрессии CAR. Затем клетки промывали, ресуспендировали в FACS буфере и фиксированный объем калиброванной суспензии микросфер Absolute Counting Beads добавляли к каждому образцу. Образцы анализировали на FACS анализаторе Fortessa, и одинаковые количества событий в дискриминационном окне для Counting Beads собирали для всех образцов.
Пример 14: Оценка разных сайтов расщепления фурина в фуриновом дегрон-домене в контексте CAR19 (анти-CD19 scFv CAR)
Генные фрагменты, содержащие фуриновый дегрон-домен, слитый с анти-CD19 scFv CAR и с предшествующим промотором T7, подвергали in vitro транскрипции/трансляции. Различия между генными фрагментами заключаются в созданных сайтах расщепления фурина, согласно аннотации. Синтезированные in vitro белки инкубировали с фурином, как указано, при 37°C в течение 1 часа. Образцы наносили на SDS-ПААГ в восстанавливающих условиях и анализировали методом иммуноблоттинга с использованием анти-CD3ζ антитела.
ФИГ. 12A-12B показывают степень расщепления фурином различных протестированных сайтов расщепления фурина в контексте CAR19. Протестированными сайтами расщепления фурина являются: № 105 - LQWLEQQVAKRRTKR (SEQ ID NO: 129); № 106 - GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); № 107 - GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); № 108 - GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); № 102 - SLNLTESHNSRKKR (SEQ ID NO: 135); № 103 - GTGAEDPRPSRKRR (SEQ ID NO: 127); № 104 - CKINGYPKRGRKRR (SEQ ID NO: 137); № 73 - RTKR (SEQ ID NO: 123). Генный фрагмент, полученный из родительского CAR19, использовали в качестве контроля (контроль) и не наблюдали никакого расщепления (ФИГ. 12A-12B).
Пример 15: Индуцируемая соединением экспрессия CAR в первичных человеческих T-клетках
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с конструктом анти-CD19 scFv CAR (конструкт № 106). Не трансдуцированные T-клетки (НТ) и родительский CAR19 использовали в качестве контролей. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, базедоксифен (BZA) добавляли в день 8. Перед замораживанием клеток определяли экспрессию CAR в день 10 методом FACS с использованием окрашивания белком L. Также оценивали количество, размер и жизнеспособность клеток.
Данные показали, что фуриновый дегрон-домен регулирует экспрессию CAR19 зависимым от стабилизирующего соединения образом в человеческих первичных T-клетках, при этом СИФ (средняя интенсивность флуоресценции) CAR является более низкой, чем в случае родительского конструкта CAR (ФИГ. 13). Кроме того, фуриновый дегрон-домен не оказывал влияние на жизнеспособность клеток и пролиферацию клеток (ФИГ. 13).
Пример 16: Зависимое от соединения FurON CAR-опосредованное уничтожение опухоли
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с анти-CD19 scFv CAR (конструкт № 106). Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR19 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, базедоксифен добавляли в день 8 (образцы CD19 CAR+ и FurON 106+) или не добавляли (образцы CD19 CAR и FurON 106). Клетки замораживали в день 10. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками-мишенями указанных линий (CD19+ NALM6 клетками или CD19- K562 клетками) и базедоксифеном в течение 20 часов. CAR T-клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток. Лизис опухоли в процентах определяли, анализируя остаточную люциферазную активность.
Полученные данные показали, что CAR19 с фуриновым дегрон-доменом вызывает уничтожение CD19+ клеток опухоли зависимым от дозы стабилизирующего соединения образом и не уступает по эффективности родительскому конструкту CAR (ФИГ. 14).
Пример 17: Зависимая от соединения и опухоли секреция цитокинов, вызываемая FurON CAR
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с анти-CD19 scFv CAR (конструкт 106). Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR19 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, базедоксифен (BAZ) добавляли в день 8 (образцы CD19 CAR+BAZ и FurON 106+BAZ) или не добавляли (образцы CD19 CAR и FurON 106). Клетки замораживали в день 10. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками линии NALM6, CD19+ клетками-мишенями, в течение 20 часов, и базедоксифеном, как указано. CAR T-клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток. Супернатанты собирали и оценивали на уровни IFNγ .
Полученные данные показали, что первичные человеческие T-клетки, экспрессирующие ERαFurON CAR19, секретируют IFNγ в присутствии CD19+ клеток опухоли зависимым от дозы стабилизирующего соединения образом и не уступают клеткам с родительским конструктом CAR19 (ФИГ. 15).
Пример 18: Зависимая от соединения и опухоли пролиферация клеток с FurON CAR
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с анти-CD19 scFv CAR (конструкт 106). Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR19 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, базедоксифен (Baz) добавляли в день 8 (образцы CD19 CAR+BAZ и FurON 106+BAZ) или не добавляли (образцы CD19 CAR и FurON 106). Клетки замораживали в день 10. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками-мишенями указанных линий (CD19+ клетками NALM6 или CD19- клетками K562) и базедоксифеном. CAR T-клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток. Через 4 дня образцы анализировали методом FACS, и 3000 событий в дискриминационном окне для Counting Beads собирали для всех образцов.
Полученные данные показали, что первичные человеческие T-клетки, экспрессирующие ERαFurON CAR19, пролиферируют в присутствии CD19+ клеток опухоли зависимым от стабилизирующего соединения образом и не уступают клеткам с родительским конструктом CAR19 (ФИГ. 16).
Пример 19: Индуцируемая соединением экспрессия CAR в T-клетках Jurkat
T-клетки Jurkat трансдуцировали одним из двух фуриновых дегрон-доменов, слитых с конструктами анти-CD19 scFv CAR. Два конструкта имеют одну и ту же последовательность расщепления фурина, но отличаются по числу мутаций в домене деградации (ERmut1 или ERmut2, приведенные в Таблице 23). Конструкт с большим количеством мутаций представлял собой FurON CART19 № 106 (с ERmut1); и конструкт с меньшим количеством мутаций представлял собой FurON CART19 № 130 (с ERmut2). Трансдуцированные клетки инкубировали с 4-OH тамоксифеном, базедоксифеном или ралоксифеном в указанных концентрациях в течение 42 часов. Экспрессию анти-CD19 scFv определяли методом FACS с использованием белка L.
Полученные данные показали, что протестированные фуриновые дегрон-домены могут регулировать экспрессию CAR19 зависимым от стабилизирующего соединения образом, независимо от числа мутаций; и никакой поверхностной экспрессии CAR не было обнаружено в отсутствие соединения (ФИГ. 17).
Пример 20: Индуцируемая соединением экспрессия CAR в человеческих первичных T-клетках
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с конструктом анти-CD19 scFv CAR (конструкт № 130). Не трансдуцированные T-клетки (НТ) и родительский CAR19 использовали в качестве контролей. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, или не добавляли, базедоксифен (BZA) добавляли в день 8. Перед замораживанием клеток определяли экспрессию CAR в день 10 методом FACS с использованием окрашивания белком L.
Полученные данные показали, что домен FurON - содержащий ограниченное число мутаций в дегрон-домене - регулирует экспрессию CAR19 зависимым от стабилизирующего соединения и IL-2 образом в человеческих первичных T-клетках (ФИГ. 18). Кроме того, никакой поверхностной экспрессии CAR не было обнаружено в отсутствие стабилизирующего соединения базедоксифена, когда фрагмент FurON был слит с CAR19 (ФИГ. 18).
Пример 21: Зависимое от соединения FurON CAR-опосредованное уничтожение опухоли
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с конструктом анти-CD19 scFv CAR (конструкт № 130). Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR19 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7. Базедоксифен (BZA) добавляли в день 8 к части образца FurON 130 BZA, таким образом, экспрессию CAR можно было определять в день 10 методом FACS с использованием окрашивания белком L, перед замораживанием клеток. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками-мишенями указанных линий (CD19+ клетками NALM6 или CD19- клетками K562) в течение 20 часов в присутствии или в отсутствие базедоксифена. Использовали разные соотношения CART («эффектора») и клеток-мишеней, как указано по оси x на ФИГ. 19A-19B. CAR T-клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток. Лизис опухоли в процентах определяли, анализируя остаточную люциферазную активность.
Полученные данные показали, что CAR T-клетки, экспрессирующие FurON CAR19, содержащий ограниченное число мутаций в дегрон-домене, уничтожают CD19+ клетки опухоли зависимым от стабилизирующего соединения и зависимым от мишени образом и не уступают по эффективности клеткам с родительским конструктом CAR (ФИГ. 19A-19B).
Пример 22: Зависимая от соединения и зависимая от опухоли секреция цитокинов, вызываемая FurON CAR
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с конструктом анти-CD19 scFv CAR (конструкт № 130). Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR19 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7. Базедоксифен (BZA) добавляли в день 8 к части образца FurON 130 BZA, таким образом, экспрессию CAR можно было определять в день 10 методом FACS с использованием окрашивания белком L, перед замораживанием клеток. Клетки замораживали в день 10. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками-мишенями указанной линии (CD19+ клетками NALM6) в течение 20 часов при соотношении эффектор:мишень, составляющем 5:1, в присутствии или в отсутствие базедоксифена. CAR T-клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток. Супернатант собирали и оценивали на уровни IFNγ.
Полученные данные показали, что CAR T-клетки, экспрессирующие FurON CAR19, содержащий ограниченное число мутаций в дегрон-домене, секретируют цитокины в присутствии CD19+ клеток опухоли зависимым от стабилизирующего соединения образом и не уступают клеткам с родительским конструктом CAR (ФИГ. 20).
Пример 23: Зависимая от соединения и зависимая от опухоли пролиферация T-клеток
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с анти-CD19 scFv CAR (конструкт № 130). Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR19 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7. Базедоксифен добавляли в день 8 к части образца FurON 130 BZA, таким образом, экспрессию CAR можно было определять в день 10 методом FACS с использованием окрашивания белком L, перед замораживанием клеток. Клетки замораживали в день 10. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками-мишенями указанных линий в течение 4 дней в присутствии или в отсутствие базедоксифена. CAR T-клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток. Через 4 дня образцы анализировали методом FACS, и 3000 событий в дискриминационном окне для Counting Beads собирали для всех образцов.
Полученные данные показали, что CD3+ T-клетки, содержащие FurON CAR19, пролиферируют в присутствии CD19+ клеток опухоли зависимым от стабилизирующего соединения образом и не уступают клеткам с родительским конструктом CAR (ФИГ. 21).
Пример 24: Индуцируемая соединением экспрессия CAR123 в первичных человеческих T-клетках
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с конструктом анти-CD123 scFv CAR. Не трансдуцированные T-клетки (НТ) и родительский CAR123 использовали в качестве контролей. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, базедоксифен (BZA) добавляли в день 8 (Furon123+BZA), или не добавляли (Furon123). Перед замораживанием клеток определяли экспрессию CAR в день 10 методом FACS с использованием окрашивания белком L.
Полученные данные показали, что домен FurON регулирует экспрессию CAR123 в первичных человеческих T-клетках зависимым от стабилизирующего соединения образом (ФИГ. 22).
Пример 25: Зависимое от соединения CAR123-опосредованное уничтожение опухоли
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с конструктом анти-CD123 scFv CAR. Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR123 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, базедоксифен (BZA) добавляли в день 8 (FurON123+ BZA), или не добавляли (FurON123). Перед замораживанием клеток определяли экспрессию CAR в день 10 методом FACS с использованием окрашивания белком L. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками-мишенями указанных линий в течение 20 часов в присутствии или в отсутствие базедоксифена. Molm13 представляет собой линию CD123+ клеток; очень низкая экспрессия CD123+ наблюдается в клетках K562. Использовали разные соотношения CART и клеток-мишеней, как указано по оси x (соотношения Э:М) на ФИГ. 25. CAR T-клетки нормировали к одному и тому же процентному содержанию CAR-экспрессирующих клеток. Лизис опухоли в процентах определяли, анализируя остаточную люциферазную активность.
Полученные данные показали, что CAR T-клетки, экспрессирующие FurON CAR123, уничтожают CD123+ клетки опухоли зависимым от стабилизирующего соединения и зависимым от мишени образом, и не уступают по эффективности клеткам с родительским конструктом CAR (ФИГ. 23).
Пример 26: Зависимая от соединения и зависимая от опухоли секреция цитокина IFNγ клетками с FurON CAR123
Первичные человеческие T-клетки трансдуцировали фуриновым дегрон-доменом, слитым с анти-CD123 scFv CAR. Не трансдуцированные T-клетки (НТ) использовали в качестве контроля. Родительский конструкт CAR123 включали в качестве эталона для полной функциональной активности CAR. Клетки размножали в течение 10 дней в присутствии стимулирующих гранул с анти-CD3/CD28. 100 Ед/мл IL-2 добавляли в день 7, базедоксифен (BZA) добавляли в день 8 (FurON123+ BZA), или не добавляли (FurON123). Клетки замораживали в день 10. T-клетки размораживали и совместно культивировали с содержащими люциферазу клетками-мишенями указанных линий в течение 20 часов при соотношении эффектора и мишени, составляющем 5:1, в присутствии или в отсутствие базедоксифена. Molm13 представляет собой CD123+ линию клеток; очень низкая экспрессия CD123+ наблюдается в клетках K562. Супернатант собирали и оценивали на уровни IFNγ.
Полученные данные показали, что CAR T-клетки, экспрессирующие FurON CAR123, секретируют цитокины в присутствии CD123+ клеток опухоли зависимым от стабилизирующего соединения образом и не уступают клеткам с родительским конструктом CAR (ФИГ. 24).
Пример 27: FurON CART19 эффективен против CD19+ клеток опухоли в животной модели лишь при введении базедоксифена
Линия клеток
NALM6 (RRID: CVCL_0092) представляет собой линию клеток человеческого лейкоза, которая получена из клеток периферической крови 19-летнего человека, страдающего острым лимфобластным лейкозом (ALL), при рецидиве в 1976 г. Клетки выращивали в среде RMPI, содержащей 10% эмбриональной бычьей сыворотки. Клетки этой линии растут в суспензии в колбах для культивирования тканей. Клетки данной линии персистируют и размножаются в организме мышей при внутривенной имплантации. Клетки NALM6 были модифицированы для экспрессии люциферазы, так что рост клеток опухоли также можно контролировать путем визуализации мышей.
Мыши
6-недельных мышей NSG (NOD.Cg-PrkdcscidIl2rgtm1Wjl/SzJ) получали из Jackson Laboratory. Животных оставляли для акклиматизации в помещении для содержания животных NIBR на по меньшей мере 3 дня до проведения эксперимента. С животными обращались в соответствии с правилами и руководящими принципами комиссии по содержанию и использованию лабораторных животных (ACUC) Novartis. Электронные транспондеры для идентификации животных были имплантированы животным в левый бок за один день до имплантации опухоли.
Имплантация опухоли
Клетки NALM6 в логарифмической фазе роста собирали и промывали в 50-мл пробирках Falcon при 1200 об/мин в течение 5 минут, один раз в ростовой среде, а затем два раза в холодном стерильном PBS. Клетки ресуспендировали в PBS в концентрации 5×106/мл, помещали на лед и немедленно вводили инъекцией мышам. Клетки опухоли вводили внутривенной инъекцией в объеме 200 мкл через хвостовую вену. Модельные клетки NALM6 эндогенно экспрессируют CD19 и, таким образом, могут быть использованы для тестирования in vivo эффективности CD19-нацеленных CAR T-клеток. В данной модели опухоль растет хорошо при внутривенной имплантации мышам и может быть визуализирована для определения опухолевой нагрузки.
Получение CART19 и FurON CART19 клеток для in vivo исследования
CAR T-клетки получали из аферезного материала крови здоровых доноров, чьи «необученные» T-клетки получали путем отрицательного отбора на T-клетки, CD4+ и CD8+ лимфоциты. Эти клетки активировали путем добавления гранул с анти-CD3/CD28 (Dynabeads® Human T-Expander CD3/CD28, Thermo Fisher Scientific) в соотношении 1:3 (T-клетки:гранулы) в среде для T-клеток (RPMI 1640, 10% инактивированной нагреванием эмбриональной телячьей сыворотки (ЭТС), 2 мМ L-глутамина, 1x смеси пенициллин/стрептомицин, 100 мкМ несущественных аминокислот, 1 мМ пирувата натрия, 10 мМ Hepes и 55 мкМ 2-меркаптоэтанола) при 37°C, 5% CO2. T-клетки культивировали при плотности 4×106 T-клеток (НТ) или 5×106 (CART19 и FurON CART19) в 1 мл среды в лунке 24-луночного планшета. Через 24 часа, когда T-клетки находились в стадии бластов, добавляли 0,5 мл неконцентрированного, или меньшие объемы концентрированного, вирусного супернатанта; T-клетки трансдуцировали с показателем множественности инфекции (MOI), равным 5. T-клетки начинали делиться логарифмически, что контролировали, измеряя количество клеток в мл, и T-клетки разбавляли свежей средой каждые два дня. В день 7 в культуры добавляли 100 Ед/мл IL2 (Peprotech, Rocky Hill, NJ) и 1 мкМ базедоксифена. В день 9 добавляли 1 мкМ базедоксифена. В день 10 клетки собирали, и количество, в процентах, трансдуцированных клеток (экспрессирующих CD19-специфический CAR на клеточной поверхности) определяли методом проточной цитометрии на FACS анализаторе Fortessa (BD). Результаты вирусной трансдукции показали сходную эффективность трансдукции; поверхностная экспрессия FurON CAR19 (средняя интенсивность флуоресценции, СИФ) была ниже, чем в случае CART19. Все CAR T-клетки были получены в условиях производства категории «для исследований» (то есть, не для клинического применения).
Лечение CART19 или FurON CART19 клетками
CD19+ клетки опухоли NALM6, экспрессирующие люциферазу, вводили инфузией мышам NSG. Через семь дней опухолевую нагрузку определяли методом биолюминесценции всего тела, животных рандомизировали в группы лечения (по 5 мышей в группе) и им вводили инфузией PBS (растворитель), CART19 (1×106 или 5×106 CAR+ T-клеток), FurON CART19 клетки (5×106 CAR+ T-клеток) или не трансдуцированные T-клетки (НТ), внутривенно через боковую хвостовую вену. Все животные получали одну и ту же дозу суммарных T-клеток (16,4×106 клеток/мышь). Животным в некоторых группах лечения вводили базедоксифен (BZA), базедоксифен плюс интерлейкин 2 (BZA/IL2) или растворитель, как указано. BZA вводили в течение 10 дней (одна доза 200 мг/кг; п/о). IL2 вводили в течение 5 дней, делали перерыв на два дня и вновь вводили в течение 3 дней (одна доза 18×106 МЕ/кг; в/б). Рост опухолей и состояние здоровья животных контролировали с течением времени. График средней интенсивности биолюминесценции для всех групп лечения приведен на ФИГ. 27; стрелка показывает, когда введение BZA и IL2 было прекращено.
Результаты
Как показано на ФИГ. 47, в то время как опухоль продолжала развиваться у мышей, используемых в качестве отрицательного контроля, и мышей, получавших только FurON CART19, рост опухоли ингибировался у мышей, получавших инфузию CART19, или получавших инфузию FurON CART19 и только BZA или BZA совместно с IL2. После прекращения введения базедоксифена и IL2 лишь конститутивно активные CART19 в самой высокой дозе были способны контролировать рост опухоли. Ранее было показано, что BZA не влияет на рост клеток опухоли NALM6 в тех же дозах и режимах дозирования (данные не представлены). Таким образом, FurON CART19 в присутствии базедоксифена продемонстрировали сопоставимую активность ингибирования опухоли, что и положительный контроль CART19.
Пример 28: Дополнительные последовательности FurON CAR
Таблица 24. Последовательности дополнительных конструктов FurON CAR и их компонентов
Пример 29: Временное контролируемое полное истощение B-клеток
Далее приведено описание материалов и методов, используемых в данных экспериментах.
Создание конструктов CAR, содержащих суицидные гены. Для конструктов с одноцепочечным вариабельным фрагментом (scFv) FMC63 (анти-CD19) использовали ранее описанный вектор (pRRLSIN.cPPT.интересующий ген-WPRE с промотором гена EF1-альфа человека), который был модифицирован для экспрессии каспазы-9 следующим образом:
1. Для экспрессии индуцируемой каспазы-9 в 3' положении от FMC63-bbz CAR трансмембранный домен и цитоплазматический «хвост» удаляли путем расщепления EcoRV и SalI и заменяли блоком генов (IDT), кодирующих такой же трансмембранный домен и цитоплазматический «хвост», за которыми следовал сайт 2A и FKBP12F36V, а затем короткий GS-линкер и домен промолекулы каспазы-9.
2. Для экспрессии индуцируемой каспазы-9 в 5' положении от FMC63-bbz CAR сигнальный пептид и часть FMC63 scFv удаляли путем расщепления XbaI и Tth111I и заменяли блоком генов (IDT), кодирующих такой же домен индуцируемой каспазы-9, как описано в 1, за которым следовал сайт 2A и последовательность, кодирующая ранее удаленную часть оригинальной плазмиды.
3. Для экспрессии обратимой каспазы-9 в 3' положении от FMC63-bbz CAR трансмембранный домен и цитоплазматический «хвост» удаляли путем расщепления EcoRV и SalI и заменяли блоком генов (geneart, Thermofisher), кодирующих такой же трансмембранный домен и цитоплазматический «хвост», за которыми следовал сайт 2A и 2 повтора FKBP12F36M, а затем короткий GS-линкер (SGGGS, SEQ ID NO:3036) и домен промолекулы каспазы-9.
4. Для экспрессии scFv для CD20 человека FMC63 scFv и шарнир CD8 удаляли из конструктов, описанных в 1-3, и заменяли кодон-оптимизированным блоком генов (IDT), кодирующих аминокислотную последовательность велтузумаба.
Создание конструктов CAR, содержащих домены условной агрегации. Для экспрессии доменов условной агрегации в 5' положении от FMC63-bbz CAR плазмиду разрезали BamHI между сигнальным пептидом и scFv, и вставляли блок генов (geneart), кодирующих 4 повтора FKBP12F36M, за которыми следовала последовательность узнавания фурина, между сигнальным пептидом и scFv.
Получение лентивирусов. Псевдотипированные лентивирусные частицы VSV-G получали с использованием упаковывающей системы 4-го поколения. Клетки 293T трансфицировали при конфлюэнтности 90% смесью pRRLSIN.cPPT.EF1α-интересующий ген.WPRE, оболочечной плазмиды pMD2.G (Addgene №12252), упаковывающих плазмид pRSVRev (Addgene №12253) и pMDLgm/pRRE (Addgene №12251) в комплексе с липофектамином 2000 (Life Technologies). Содержащий лентивирус супернатант собирали через 24 и 48 часов, фильтровали через 0,4-мкм PES мембрану, концентрировали при 12000 x g в течение 12 часов при 4°C и хранили при -80°C.
Стимуляция и размножение первичных человеческих T-клеток. Первичные человеческие T-клетки культивировали в RPMI 1640 с 10% ЭБС, 10 мМ HEPES, 1% смеси пенициллин/стрептомицин. Суммарные T-клетки (CD4+ и CD8+) стимулировали гранулами с анти-CD3 и анти-CD28 (Dynabeads, Life Technologies) при соотношении гранулы:клетки, составляющем 3:1. В культуральную среду добавляли 100 МЕ/мл интерлейкина 2. Через 24 часа после стимуляции 106 T-клеток трансдуцировали лентивирусными частицами, кодирующими разные конструкты CAR или контрольные конструкты, или ложно трансдуцировали. Размножение T-клеток контролировали в течение 8-12 дней путем измерения объема и концентрации клеток (счетчик Коултера, Beckman Coulter). Клеточную поверхностную экспрессию конструктов CAR подтверждали методом проточной цитометрии (BD LSRII) с поликлональными антителами против тяжелой и легкой цепей иммуноглобулинов человека или мыши. Проводили окрашивание CAR в течение 25 минут при комнатной температуре. Все процедуры окрашивания проводили в условиях насыщения. Для некоторых экспериментов трансдуцированные T-клетки предварительно замораживали в 90% ЭБС и 10% ДМСО. Эксперименты проводили, когда клетки находились в состоянии покоя после стимуляции (то есть, объем <450 фл).
Анализы in vitro цитотоксичности и продуцирования цитокинов. In vitro уничтожение клеток NALM6 тестировали в анализе с высвобождением 51Cr. 5×105 клеток-мишеней нагружали 50 мкКи Na251CrO4 (Perkin Elmer) в течение 90-120 минут, дважды промывали и ресуспендировали в среде, свободной от фенолового красного, с 5% ЭБС. Содержащие CAR, контрольный CAR или ложно трансдуцированные T-клетки (8-10 дней после начальной активации) совместно инкубировали с нагруженными клетками-мишенями в течение 4 часов при разных соотношениях эффектор:мишень (Э:М), и высвобождение хрома в супернатант измеряли в планшетном счетчике MicroBeta2 (Perkin Elmer). Спонтанное высвобождение из клеток-мишеней (без эффекторных клеток) анализировали в таком же объеме, и максимальное высвобождение определяли путем лизиса клеток-мишеней SDS в конечной концентрации 5%. Процент специфического лизиса=[(экспериментальное высвобождение - спонтанное высвобождение)/(максимальное высвобождение - спонтанное высвобождение)]*100. Все эксперименты проводили по меньшей мере в 3 репликах.
Элиминация CD19 CAR T-клеток. CD19 sCAR T-клетки инкубировали в присутствии указанных концентраций AP20187 в течение 16 часов при 37°C. Мертвые клетки обнаруживали с помощью фиолетового красителя для живых/мертвых клеток и количественно определяли методом проточной цитометрии.
CD19 sCAR T-клетки сохраняют биологическую эффективность in vivo. Мышам предварительно вводили IVIG (Privigen, CSL Behring) в дозе 600 мг/кг в/в в течение 2 дней для блокирования FcγR на моноцитах и нейтрофилах. Затем мышам NSG вводили инъекцией 1×106 CD19+ клеток NALM6, экспрессирующих люциферазу щелкунов, для обнаружения биолюминесценции. Через пять дней мышам вводили либо 5×106 CD19 CAR T-клеток, экспрессирующих индуцируемую каспазу-9, или не трансдуцированные контрольные T-клетки. Периферическую кровь собирали из ретроорбитального синуса, и присутствие B-клеток и приживление T-клеток определяли методом проточной цитометрии с использованием пробирок BD TruCOUNT (BD Biosciences) в соответствии с инструкциями производителя. Биолюминесценцию оценивали в день 5, 6, 7, 10, 13 и 18 после инъекции B-клеток, которую сочетали с внутрибрюшинным введением IVIG (600 мг/кг). Мышей подвергали эвтаназии для сбора органов в соответствии с правилами местной комиссии IACUC, и образцы костного мозга, селезенки и крови оценивали методом проточной цитометрии.
Далее следует описание результатов эксперимента.
Истощение B-клеток, если оно является 100%-м, должно приводить к исцелению обыкновенной пузырчатки (PV) и других опосредованных антителами заболеваний, поскольку патогенные B-клетки должны быть элиминированы и должен сформироваться совершенно новый репертуар B-клеток. Учитывая множество контрольных точек, предотвращающих аутоиммунитет, маловероятно, что аутореактивные B-клетки вновь появятся.
Преимущество подхода с CD19 CAR T-клетками заключается в том, что он представляет собой универсальный подход к лечению любых опосредованных B-клетками или антителами заболеваний и, как подтверждено в клинических испытаниях, является высокоэффективным для истощения CD19+ B-клеток. Таким образом, нет необходимости знать антиген-мишень в случае конкретного заболевания. Данный терапевтический подход может быть применен к любому заболеванию, при котором B-клетки или антитела, которые они продуцируют, приводит к аутоиммунному состоянию или заболеванию. Кроме того, можно использовать CD19 CAR для элиминации аллоантител к не собственным белкам, предотвращающих функциональное спасение при генетических заболеваниях, например антител против HLA или бета-2-микроглобулина вследствие трансплантации органов, антител против антигенов группы крови или Rh вследствие переливания крови или беременности, или против фактора VIII, α-L-идуронидазы и многих других белков, которые используют в клинике или разрабатывают для заместительной терапии.
CD19 CAR T-клетки продемонстрировали эффективность в истощении B-клеток в клинических испытаниях с участием людей, без существенной нецелевой цитотоксичности, хотя истощение B-клеток является постоянным, что приводит к пожизненной иммуносупрессии. CD20 также является клинической мишенью для истощения B-клеток. Таким образом, включение суицидного гена в конструкцию анти-CD19 или анти-CD20 CAR (sCAR), или избирательная активация функция CART (за счет обратимой суицидной кассеты или условной экспрессии CAR) позволит временно контролировать CAR-опосредованное истощение B-клеток в качестве важной меры безопасности.
Пример суицидного гена в sCAR включает слитый белок человеческой каспазы-9 с модифицированным человеческим FK-связывающим белком, который делает возможной условную димеризацию при воздействии синтетического димерирующего лекарственного средства, такого как AP1903. После димеризации каспаза-9 становится активированной, приводя к гибели клеток, экспрессирующих суицидный ген. Таким образом, инфузия CD19 sCAR T-клеток будет приводить к полному истощению B-клеток, следствием чего будет излечение опосредованного B-клетками или антителами заболевания. Последующая активация суицидного гена при помощи AP1903, AP20187 или аналогичного средства будет приводить к элиминации sCAR T-клеток, что позволит популяции B-клеток восстанавливаться, таким образом, будет восстановлена нормальная иммунная функция. Пример обратимого суицидного гена в revCAR включает слитый белок человеческой каспазы-9 с модифицированным человеческим FK-связывающим белком, который по умолчанию димеризуется и вызывает гибель клеток, экспрессирующих суицидный ген. При солюбилизации доменов димеризации активность каспазы-9 ингибируется и гибель клетки предотвращается, что позволяет CAR T-клетке выполнять свою функцию. Пример регуляторной системы on-CAR включает слитый белок CAR с модифицированными доменами человеческого FK-связывающего белка, который по умолчанию димеризуется и вызывает агрегацию и деградацию белков в секреторной системе клетки. Солюбилизация доменов димеризации делает возможным выход и процессинг CAR в секреторной системе клетки, включающий отщепление фурином CAR от доменов FKBP, что делает возможной функциональную клеточную поверхностную экспрессию CAR.
С целью оценки данных подходов для временного контроля функции CAR T-клетки были созданы несколько конструктов; для одного варианта осуществления один конструкт с суицидным геном перед CAR и один конструкт с суицидным геном после CAR (ФИГ. 27). Для другого варианта осуществления конструкт с обратимым суицидным геном (либо перед, либо после CAR) (ФИГ. 28). Для другого варианта осуществления регуляторный onCAR (ФИГ. 26). Было показано, что первичные человеческие T-клетки эффективно экспрессируют CD19 sCAR, CD19 revCAR и CD20 CAR (ФИГ. 29A-29F), и CD19 sCAR T-клетки демонстрировали специфическую цитотоксичность против их запланированных мишеней (ФИГ. 30). Кроме того, первичные человеческие T-клетки, экспрессирующие CD19 sCAR, были специфически уничтожены после активации переключения на самоуничтожение при помощи AP20187 in vitro, в то время как не трансдуцированные T-клетки не погибали после обработки AP20187 (ФИГ. 31). Кроме того, CD19 sCAR T-клетки оставались эффективными для элиминации CD19+ B-клеток в in vivo мышиной модели (ФИГ. 32) и хорошо приживались (ФИГ. 33).
Как видно из результатов анализа на уничтожение клеток на ФИГ. 34, CD20 sCAR, CD20 revCAR и CD20 onCAR демонстрировали эквивалентное и специфическое уничтожение CD20+ клеток-мишеней. On-CAR тестировали в присутствии 500 нМ Shield-1.
Как видно на ФИГ. 35, в отсутствие солюбилизирующего FKBP лиганда (например, shield-1) функция CAR ингибируется. При более низком соотношении Э:М функция On-CAR сильно ингибируется, если лиганд FKBP не присутствует.
Как видно на ФИГ. 36, поверхностная экспрессия CAR может быть модулирована при помощи лиганда FKBP Shield-1. Shield-1 вызывает зависимое от дозы увеличение экспрессии CAR, в то время как отсутствие Shield-1 приводит к ~60% уменьшению экспрессии CD20 on-CAR.
Как видно на ФИГ. 37, Shield-1 титровали в системе CD19rev CAR, и более низкие дозы Shield-1 приводили к более высокой активации каспазы-9 и возрастанию апоптоза.
Как видно на ФИГ. 38, in vivo оценка эффективности апоптоза в анти-CD19 revCAR T-клетках показала достаточный in vivo апоптоз revCAR T-клеток (ФИГ. 38). Также была оценена in vivo эффективность CD19 revCAR T-клеток (ФИГ. 39).
Как видно на ФИГ. 40, 41 и 42, активация суицидного гена приводила к периферическому истощению суицидных CAR T-клеток (например, истощению sCAR T-клеток в лимфоидных органах на ФИГ. 42).
Хронологическая последовательность действий для получения T-клетки по настоящему изобретению схематично изображена на ФИГ. 43, и хронологическая последовательность действий в дизайне in vivo эксперимента по настоящему изобретению схематично изображена на ФИГ. 44.
Как показано на ФИГ. 45, «универсальные» sCAR T-клетки могут приводить к истощению периферических B-клеток у не аутологичных мышей BT и человеческих B-клеток в нераковой гуманизированной мышиной модели. Кроме того, на ФИГ. 46 показано, что универсальные sCAR T-клетки могут быть истощены при воздействии AP1903.
Соответствующие последовательности для некоторых экспериментальных результатов, представленных в настоящем документе, приведены далее:
CD19 sCAR:
Суицидный ген, за которым следует CD19 CAR (нк)
Суицидный ген, за которым следует CD19 CAR (ак)
CD19 CAR, за которым следует суицидный ген (нк)
CD19 CAR, за которым следует суицидный ген (ак)
CD20 CAR и sCAR:
CD20bbz CAR (нк и ак)
CD20 CAR, за которым следует суицидный ген (нк и ак)
суицидный ген, за которым следует CD20 CAR (нк и ак)
CD19 revCAR:
CD19 CAR, за которым следует обратимая суицидная кассета (нк и ак)
CD19 onCAR:
CD19 on-CAR (нк и ак)
CD20 revCAR:
CD20 CAR, за которым следует обратимая суицидная кассета (нк и ак)
CD20 onCAR:
CD20 on-CAR (нк и ак)
Суицидный ген=индуцируемая каспаза-9 (активирует апоптоз при димеризации с низкомолекулярными активаторами)
Сайт 2A=сайт ухода с рибосомы
CD19 CAR, содержащий трансмембранный домен CD8, цитоплазматические сигнальные домены CD137 и CD3-дзета (CD3-дзета также называют CD247, в совокупности CD137-CD3-дзета также называют bbz)
Индуцируемая каспаза-9-2A-CD19bbz, нуклеотидная последовательность (SEQ ID NO: 3018)
ATGCTCGAGGGGGTTCAGGTGGAGACTATCAGCCCGGGCGACGGACGGACATTCCCAAAGCGCGGGCAGACGTGTGTGGTGCATTACACCGGGATGCTTGAGGACGGAAAGAAAGTGGACTCTTCCCGAGACCGAAATAAACCATTCAAGTTCATGTTGGGCAAGCAGGAGGTTATCAGAGGGTGGGAGGAGGGCGTCGCTCAGATGAGTGTCGGACAGAGGGCCAAGCTCACGATCTCCCCTGATTACGCCTACGGGGCAACTGGTCACCCCGGAATCATCCCCCCTCACGCAACCCTCGTGTTCGACGTCGAGCTGCTCAAACTGGAATCAGGCGGAGGCAGTGGCGCTAGCGGGTTTGGCGATGTCGGTGCCCTTGAAAGCTTGAGAGGAAATGCCGATCTCGCTTACATCTTGAGCATGGAGCCCTGTGGGCACTGTCTGATCATCAACAATGTTAACTTTTGCCGGGAGTCCGGCCTGCGCACACGCACAGGCTCCAACATTGACTGCGAAAAACTTCGAAGGAGGTTTAGCTCTCTGCATTTCATGGTAGAGGTGAAGGGGGATCTGACCGCCAAGAAAATGGTTCTCGCCCTTCTCGAGCTTGCGCAGCAGGACCATGGAGCGCTTGACTGTTGTGTCGTTGTGATACTGAGCCATGGCTGTCAGGCTTCCCATCTCCAGTTTCCAGGGGCCGTGTACGGAACCGATGGATGCCCTGTGTCAGTTGAAAAGATCGTAAACATCTTTAACGGAACATCTTGCCCGAGCCTCGGCGGTAAACCGAAGCTTTTTTTTATCCAGGCCTGCGGCGGTGAACAGAAAGATCATGGCTTCGAGGTTGCCAGTACCAGCCCTGAAGACGAATCCCCCGGGTCAAATCCTGAACCAGATGCGACCCCTTTCCAGGAAGGACTCCGCACTTTTGACCAGCTTGACGCCATTTCCTCCCTGCCAACACCTTCCGACATATTTGTAAGCTACTCCACCTTTCCAGGATTCGTGAGCTGGCGCGACCCAAAATCCGGCAGTTGGTATGTTGAAACCCTGGACGATATTTTCGAACAATGGGCCCACAGTGAGGACCTGCAGTCCCTTCTTCTGCGCGTAGCCAATGCCGTGTCAGTCAAAGGGATTTACAAGCAGATGCCAGGCTGCTTTAATTTCCTGCGCAAGAAACTGTTTTTTAAGACCAGTGGCTCCGGCGCAACAAATTTCTCCTTGCTGAAACAGGCAGGCGACGTTGAGGAAAATCCCGGCCCAATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGACATCCAGATGACACAGACTACATCCTCCCTGTCTGCCTCTCTGGGAGACAGAGTCACCATCAGTTGCAGGGCAAGTCAGGACATTAGTAAATATTTAAATTGGTATCAGCAGAAACCAGATGGAACTGTTAAACTCCTGATCTACCATACATCAAGATTACACTCAGGAGTCCCATCAAGGTTCAGTGGCAGTGGGTCTGGAACAGATTATTCTCTCACCATTAGCAACCTGGAGCAAGAAGATATTGCCACTTACTTTTGCCAACAGGGTAATACGCTTCCGTACACGTTCGGAGGGGGGACTAAGTTGGAAATAACAGGTGGCGGTGGCTCGGGCGGTGGTGGGTCGGGTGGCGGCGGATCTGAGGTGAAACTGCAGGAGTCAGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCGTCACATGCACTGTCTCAGGGGTCTCATTACCCGACTATGGTGTAAGCTGGATTCGCCAGCCTCCACGAAAGGGTCTGGAGTGGCTGGGAGTAATATGGGGTAGTGAAACCACATACTATAATTCAGCTCTCAAATCCAGACTGACCATCATCAAGGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTGCAAACTGATGACACAGCCATTTACTACTGTGCCAAACATTATTACTACGGTGGTAGCTATGCTATGGACTACTGGGGTCAAGGAACCTCAGTCACCGTCTCCTCAACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGCTAA
Индуцируемая каспаза-9-2A-CD19bbz, аминокислотная последовательность (SEQ ID NO: 3019)
MLEGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLESGGGSGASGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTSGSGATNFSLLKQAGDVEENPGPMALPVTALLLPLALLLHAARPDIQMTQTTSSLSASLGDRVTISCRASQDISKYLNWYQQKPDGTVKLLIYHTSRLHSGVPSRFSGSGSGTDYSLTISNLEQEDIATYFCQQGNTLPYTFGGGTKLEITGGGGSGGGGSGGGGSEVKLQESGPGLVAPSQSLSVTCTVSGVSLPDYGVSWIRQPPRKGLEWLGVIWGSETTYYNSALKSRLTIIKDNSKSQVFLKMNSLQTDDTAIYYCAKHYYYGGSYAMDYWGQGTSVTVSSTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
CD19bbz-2A-индуцируемая каспаза-9, нуклеотидная последовательность (SEQ ID NO: 3020)
ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGACATCCAGATGACACAGACTACATCCTCCCTGTCTGCCTCTCTGGGAGACAGAGTCACCATCAGTTGCAGGGCAAGTCAGGACATTAGTAAATATTTAAATTGGTATCAGCAGAAACCAGATGGAACTGTTAAACTCCTGATCTACCATACATCAAGATTACACTCAGGAGTCCCATCAAGGTTCAGTGGCAGTGGGTCTGGAACAGATTATTCTCTCACCATTAGCAACCTGGAGCAAGAAGATATTGCCACTTACTTTTGCCAACAGGGTAATACGCTTCCGTACACGTTCGGAGGGGGGACTAAGTTGGAAATAACAGGTGGCGGTGGCTCGGGCGGTGGTGGGTCGGGTGGCGGCGGATCTGAGGTGAAACTGCAGGAGTCAGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCGTCACATGCACTGTCTCAGGGGTCTCATTACCCGACTATGGTGTAAGCTGGATTCGCCAGCCTCCACGAAAGGGTCTGGAGTGGCTGGGAGTAATATGGGGTAGTGAAACCACATACTATAATTCAGCTCTCAAATCCAGACTGACCATCATCAAGGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTGCAAACTGATGACACAGCCATTTACTACTGTGCCAAACATTATTACTACGGTGGTAGCTATGCTATGGACTACTGGGGTCAAGGAACCTCAGTCACCGTCTCCTCAACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGCTCGGAAGCGACGGGGCTCCGGCGCAACAAATTTCTCCTTGCTGAAACAGGCAGGCGACGTTGAGGAAAATCCCGGCCCAGGGGTTCAGGTGGAGACTATCAGCCCGGGCGACGGACGGACATTCCCAAAGCGCGGGCAGACGTGTGTGGTGCATTACACCGGGATGCTTGAGGACGGAAAGAAAGTGGACTCTTCCCGAGACCGAAATAAACCATTCAAGTTCATGTTGGGCAAGCAGGAGGTTATCAGAGGGTGGGAGGAGGGCGTCGCTCAGATGAGTGTCGGACAGAGGGCCAAGCTCACGATCTCCCCTGATTACGCCTACGGGGCAACTGGTCACCCCGGAATCATCCCCCCTCACGCAACCCTCGTGTTCGACGTCGAGCTGCTCAAACTGGAATCAGGCGGAGGCAGTGGCGGGTTTGGCGATGTCGGTGCCCTTGAAAGCTTGAGAGGAAATGCCGATCTCGCTTACATCTTGAGCATGGAGCCCTGTGGGCACTGTCTGATCATCAACAATGTTAACTTTTGCCGGGAGTCCGGCCTGCGCACACGCACAGGCTCCAACATTGACTGCGAAAAACTTCGAAGGAGGTTTAGCTCTCTGCATTTCATGGTAGAGGTGAAGGGGGATCTGACCGCCAAGAAAATGGTTCTCGCCCTTCTCGAGCTTGCGCAGCAGGACCATGGAGCGCTTGACTGTTGTGTCGTTGTGATACTGAGCCATGGCTGTCAGGCTTCCCATCTCCAGTTTCCAGGGGCCGTGTACGGAACCGATGGATGCCCTGTGTCAGTTGAAAAGATCGTAAACATCTTTAACGGAACATCTTGCCCGAGCCTCGGCGGTAAACCGAAGCTTTTTTTTATCCAGGCCTGCGGCGGTGAACAGAAAGATCATGGCTTCGAGGTTGCCAGTACCAGCCCTGAAGACGAATCCCCCGGGTCAAATCCTGAACCAGATGCGACCCCTTTCCAGGAAGGACTCCGCACTTTTGACCAGCTTGACGCCATTTCCTCCCTGCCAACACCTTCCGACATATTTGTAAGCTACTCCACCTTTCCAGGATTCGTGAGCTGGCGCGACCCAAAATCCGGCAGTTGGTATGTTGAAACCCTGGACGATATCTTCGAACAATGGGCCCACAGTGAGGACCTGCAGTCCCTTCTTCTGCGCGTAGCCAATGCCGTGTCAGTCAAAGGGATTTACAAGCAGATGCCAGGCTGCTTTAATTTCCTGCGCAAGAAACTGTTTTTTAAGACCAGTTGAGTCGACGGAGGAGGAG
CD19bbz-2A-индуцируемая каспаза-9, аминокислотная последовательность (SEQ ID NO: 3021)
MALPVTALLLPLALLLHAARPDIQMTQTTSSLSASLGDRVTISCRASQDISKYLNWYQQKPDGTVKLLIYHTSRLHSGVPSRFSGSGSGTDYSLTISNLEQEDIATYFCQQGNTLPYTFGGGTKLEITGGGGSGGGGSGGGGSEVKLQESGPGLVAPSQSLSVTCTVSGVSLPDYGVSWIRQPPRKGLEWLGVIWGSETTYYNSALKSRLTIIKDNSKSQVFLKMNSLQTDDTAIYYCAKHYYYGGSYAMDYWGQGTSVTVSSTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRRKRRGSGATNFSLLKQAGDVEENPGPGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLESGGGSGGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS
Сигнальный пептид-анти-CD20 человека-шарнир CD8-трансмембранный CD8-CD137-CD247, нуклеотидная последовательность (SEQ ID NO:3022)
ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGGATCCGATATTCAACTTACACAGTCCCCTAGTTCCTTGTCCGCCTCCGTCGGCGACAGAGTTACCATGACTTGTCGAGCGTCTTCTAGCGTTTCCTACATTCATTGGTTCCAACAGAAGCCCGGAAAGGCACCAAAACCTTGGATCTACGCCACGTCCAATTTGGCTAGTGGTGTTCCGGTGCGATTTTCCGGGTCAGGTAGCGGGACGGACTATACTTTTACCATTTCAAGCCTTCAGCCTGAAGACATCGCGACGTACTATTGTCAGCAGTGGACCTCTAACCCTCCTACCTTTGGCGGTGGAACAAAGCTGGAGATCAAACGAGGCGGGGGTGGCTCTGGGGGAGGAGGTTCCGGTGGGGGAGGCTCTCAAGTACAACTGCAACAAAGTGGGGCTGAAGTGAAGAAGCCCGGTTCTTCAGTCAAAGTATCATGTAAGGCAAGTGGTTATACTTTTACGTCTTATAACATGCATTGGGTAAAGCAAGCCCCTGGTCAGGGCCTCGAGTGGATTGGTGCGATCTACCCTGGAATGGGTGATACGAGCTATAATCAGAAATTCAAGGGGAAAGCCACCTTGACTGCAGACGAATCTACGAACACGGCTTACATGGAGCTTAGCTCACTCAGATCAGAGGATACAGCCTTTTACTACTGCGCTAGATCAACTTATTACGGAGGAGACTGGTATTTTGATGTATGGGGTCAGGGGACCACAGTCACTGTTAGCTCTGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC
Сигнальный пептид-анти-CD20 человека-шарнир CD8-трансмембранный CD8-CD137-CD247, аминокислотная последовательность (SEQ ID NO: 3023)
MALPVTALLLPLALLLHAARPGSDIQLTQSPSSLSASVGDRVTMTCRASSSVSYIHWFQQKPGKAPKPWIYATSNLASGVPVRFSGSGSGTDYTFTISSLQPEDIATYYCQQWTSNPPTFGGGTKLEIKRGGGGSGGGGSGGGGSQVQLQQSGAEVKKPGSSVKVSCKASGYTFTSYNMHWVKQAPGQGLEWIGAIYPGMGDTSYNQKFKGKATLTADESTNTAYMELSSLRSEDTAFYYCARSTYYGGDWYFDVWGQGTTVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRZ
Анти-CD20 человека bbz-2A-iCasp9, нуклеотидная последовательность (SEQ ID NO: 3024)
ATGGCTCTGCCTGTGACAGCTCTGCTGCTGCCTCTGGCCCTGCTGCTGCATGCTGCCAGACCTGGCTCCGATATTCAACTTACACAGTCCCCTAGTTCCTTGTCCGCCTCCGTCGGCGACAGAGTTACCATGACTTGTCGAGCGTCTTCTAGCGTTTCCTACATTCATTGGTTCCAACAGAAGCCCGGAAAGGCACCAAAACCTTGGATCTACGCCACGTCCAATTTGGCTAGTGGTGTTCCGGTGCGATTTTCCGGGTCAGGTAGCGGGACGGACTATACTTTTACCATTTCAAGCCTTCAGCCTGAAGACATCGCGACGTACTATTGTCAGCAGTGGACCTCTAACCCTCCTACCTTTGGCGGTGGAACAAAGCTGGAGATCAAACGAGGCGGGGGTGGCTCTGGGGGAGGAGGTTCCGGTGGGGGAGGCTCTCAAGTACAACTGCAACAAAGTGGGGCTGAAGTGAAGAAGCCCGGTTCTTCAGTCAAAGTATCATGTAAGGCAAGTGGTTATACTTTTACGTCTTATAACATGCATTGGGTAAAGCAAGCCCCTGGTCAGGGCCTCGAGTGGATTGGTGCGATCTACCCTGGAATGGGTGATACGAGCTATAATCAGAAATTCAAGGGGAAAGCCACCTTGACTGCAGACGAATCTACGAACACGGCTTACATGGAGCTTAGCTCACTCAGATCAGAGGATACAGCCTTTTACTACTGCGCTAGATCAACTTATTACGGAGGAGACTGGTATTTTGATGTATGGGGTCAGGGGACCACAGTCACTGTTAGCTCTGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGCGGCTCCGGCGCAACAAATTTCTCCTTGCTGAAACAGGCAGGCGACGTTGAGGAAAATCCCGGCCCAGGGGTTCAGGTGGAGACTATCAGCCCGGGCGACGGACGGACATTCCCAAAGCGCGGGCAGACGTGTGTGGTGCATTACACCGGGATGCTTGAGGACGGAAAGAAAGTGGACTCTTCCCGAGACCGAAATAAACCATTCAAGTTCATGTTGGGCAAGCAGGAGGTTATCAGAGGGTGGGAGGAGGGCGTCGCTCAGATGAGTGTCGGACAGAGGGCCAAGCTCACGATCTCCCCTGATTACGCCTACGGGGCAACTGGTCACCCCGGAATCATCCCCCCTCACGCAACCCTCGTGTTCGACGTCGAGCTGCTCAAACTGGAATCAGGCGGAGGCAGTGGCGGGTTTGGCGATGTCGGTGCCCTTGAAAGCTTGAGAGGAAATGCCGATCTCGCTTACATCTTGAGCATGGAGCCCTGTGGGCACTGTCTGATCATCAACAATGTTAACTTTTGCCGGGAGTCCGGCCTGCGCACACGCACAGGCTCCAACATTGACTGCGAAAAACTTCGAAGGAGGTTTAGCTCTCTGCATTTCATGGTAGAGGTGAAGGGGGATCTGACCGCCAAGAAAATGGTTCTCGCCCTTCTCGAGCTTGCGCAGCAGGACCATGGAGCGCTTGACTGTTGTGTCGTTGTGATACTGAGCCATGGCTGTCAGGCTTCCCATCTCCAGTTTCCAGGGGCCGTGTACGGAACCGATGGATGCCCTGTGTCAGTTGAAAAGATCGTAAACATCTTTAACGGAACATCTTGCCCGAGCCTCGGCGGTAAACCGAAGCTTTTTTTTATCCAGGCCTGCGGCGGTGAACAGAAAGATCATGGCTTCGAGGTTGCCAGTACCAGCCCTGAAGACGAATCCCCCGGGTCAAATCCTGAACCAGATGCGACCCCTTTCCAGGAAGGACTCCGCACTTTTGACCAGCTTGACGCCATTTCCTCCCTGCCAACACCTTCCGACATATTTGTAAGCTACTCCACCTTTCCAGGATTCGTGAGCTGGCGCGACCCAAAATCCGGCAGTTGGTATGTTGAAACCCTGGACGATATCTTCGAACAATGGGCCCACAGTGAGGACCTGCAGTCCCTTCTTCTGCGCGTAGCCAATGCCGTGTCAGTCAAAGGGATTTACAAGCAGATGCCAGGCTGCTTTAATTTCCTGCGCAAGAAACTGTTTTTTAAGACCAGTTGA
Анти-CD20 человека bbz-2A-iCasp9, аминокислотная последовательность (SEQ ID NO: 3025)
MALPVTALLLPLALLLHAARPGSDIQLTQSPSSLSASVGDRVTMTCRASSSVSYIHWFQQKPGKAPKPWIYATSNLASGVPVRFSGSGSGTDYTFTISSLQPEDIATYYCQQWTSNPPTFGGGTKLEIKRGGGGSGGGGSGGGGSQVQLQQSGAEVKKPGSSVKVSCKASGYTFTSYNMHWVKQAPGQGLEWIGAIYPGMGDTSYNQKFKGKATLTADESTNTAYMELSSLRSEDTAFYYCARSTYYGGDWYFDVWGQGTTVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRGSGATNFSLLKQAGDVEENPGPGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLESGGGSGGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTSZ
iCasp9-2A-анти-CD20 человека bbz, нуклеотидная последовательность (SEQ ID NO: 3026)
ATGCTCGAGGGGGTTCAGGTGGAGACTATCAGCCCGGGCGACGGACGGACATTCCCAAAGCGCGGGCAGACGTGTGTGGTGCATTACACCGGGATGCTTGAGGACGGAAAGAAAGTGGACTCTTCCCGAGACCGAAATAAACCATTCAAGTTCATGTTGGGCAAGCAGGAGGTTATCAGAGGGTGGGAGGAGGGCGTCGCTCAGATGAGTGTCGGACAGAGGGCCAAGCTCACGATCTCCCCTGATTACGCCTACGGGGCAACTGGTCACCCCGGAATCATCCCCCCTCACGCAACCCTCGTGTTCGACGTCGAGCTGCTCAAACTGGAATCAGGCGGAGGCAGTGGCGCTAGCGGGTTTGGCGATGTCGGTGCCCTTGAAAGCTTGAGAGGAAATGCCGATCTCGCTTACATCTTGAGCATGGAGCCCTGTGGGCACTGTCTGATCATCAACAATGTTAACTTTTGCCGGGAGTCCGGCCTGCGCACACGCACAGGCTCCAACATTGACTGCGAAAAACTTCGAAGGAGGTTTAGCTCTCTGCATTTCATGGTAGAGGTGAAGGGGGATCTGACCGCCAAGAAAATGGTTCTCGCCCTTCTCGAGCTTGCGCAGCAGGACCATGGAGCGCTTGACTGTTGTGTCGTTGTGATACTGAGCCATGGCTGTCAGGCTTCCCATCTCCAGTTTCCAGGGGCCGTGTACGGAACCGATGGATGCCCTGTGTCAGTTGAAAAGATCGTAAACATCTTTAACGGAACATCTTGCCCGAGCCTCGGCGGTAAACCGAAGCTTTTTTTTATCCAGGCCTGCGGCGGTGAACAGAAAGATCATGGCTTCGAGGTTGCCAGTACCAGCCCTGAAGACGAATCCCCCGGGTCAAATCCTGAACCAGATGCGACCCCTTTCCAGGAAGGACTCCGCACTTTTGACCAGCTTGACGCCATTTCCTCCCTGCCAACACCTTCCGACATATTTGTAAGCTACTCCACCTTTCCAGGATTCGTGAGCTGGCGCGACCCAAAATCCGGCAGTTGGTATGTTGAAACCCTGGACGATATTTTCGAACAATGGGCCCACAGTGAGGACCTGCAGTCCCTTCTTCTGCGCGTAGCCAATGCCGTGTCAGTCAAAGGGATTTACAAGCAGATGCCAGGCTGCTTTAATTTCCTGCGCAAGAAACTGTTTTTTAAGACCAGTGGCTCCGGCGCAACAAATTTCTCCTTGCTGAAACAGGCAGGCGACGTTGAGGAAAATCCCGGCCCAATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGGATCCGATATTCAACTTACACAGTCCCCTAGTTCCTTGTCCGCCTCCGTCGGCGACAGAGTTACCATGACTTGTCGAGCGTCTTCTAGCGTTTCCTACATTCATTGGTTCCAACAGAAGCCCGGAAAGGCACCAAAACCTTGGATCTACGCCACGTCCAATTTGGCTAGTGGTGTTCCGGTGCGATTTTCCGGGTCAGGTAGCGGGACGGACTATACTTTTACCATTTCAAGCCTTCAGCCTGAAGACATCGCGACGTACTATTGTCAGCAGTGGACCTCTAACCCTCCTACCTTTGGCGGTGGAACAAAGCTGGAGATCAAACGAGGCGGGGGTGGCTCTGGGGGAGGAGGTTCCGGTGGGGGAGGCTCTCAAGTACAACTGCAACAAAGTGGGGCTGAAGTGAAGAAGCCCGGTTCTTCAGTCAAAGTATCATGTAAGGCAAGTGGTTATACTTTTACGTCTTATAACATGCATTGGGTAAAGCAAGCCCCTGGTCAGGGCCTCGAGTGGATTGGTGCGATCTACCCTGGAATGGGTGATACGAGCTATAATCAGAAATTCAAGGGGAAAGCCACCTTGACTGCAGACGAATCTACGAACACGGCTTACATGGAGCTTAGCTCACTCAGATCAGAGGATACAGCCTTTTACTACTGCGCTAGATCAACTTATTACGGAGGAGACTGGTATTTTGATGTATGGGGTCAGGGGACCACAGTCACTGTTAGCTCTGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC
iCasp9-2A-анти-CD20 человека bbz, аминокислотная последовательность (SEQ ID NO: 3027)
MLEGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKVDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLESGGGSGASGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTSGSGATNFSLLKQAGDVEENPGPMALPVTALLLPLALLLHAARPGSDIQLTQSPSSLSASVGDRVTMTCRASSSVSYIHWFQQKPGKAPKPWIYATSNLASGVPVRFSGSGSGTDYTFTISSLQPEDIATYYCQQWTSNPPTFGGGTKLEIKRGGGGSGGGGSGGGGSQVQLQQSGAEVKKPGSSVKVSCKASGYTFTSYNMHWVKQAPGQGLEWIGAIYPGMGDTSYNQKFKGKATLTADESTNTAYMELSSLRSEDTAFYYCARSTYYGGDWYFDVWGQGTTVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRZ
FMC63-bbz-2A-revCasp9, нуклеотидная последовательность (SEQ ID NO: 3028)
ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGGATCCGACATCCAGATGACACAGACTACATCCTCCCTGTCTGCCTCTCTGGGAGACAGAGTCACCATCAGTTGCAGGGCAAGTCAGGACATTAGTAAATATTTAAATTGGTATCAGCAGAAACCAGATGGAACTGTTAAACTCCTGATCTACCATACATCAAGATTACACTCAGGAGTCCCATCAAGGTTCAGTGGCAGTGGGTCTGGAACAGATTATTCTCTCACCATTAGCAACCTGGAGCAAGAAGATATTGCCACTTACTTTTGCCAACAGGGTAATACGCTTCCGTACACGTTCGGAGGGGGGACTAAGTTGGAAATAACAGGTGGCGGTGGCTCGGGCGGTGGTGGGTCGGGTGGCGGCGGATCTGAGGTGAAACTGCAGGAGTCAGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCGTCACATGCACTGTCTCAGGGGTCTCATTACCCGACTATGGTGTAAGCTGGATTCGCCAGCCTCCACGAAAGGGTCTGGAGTGGCTGGGAGTAATATGGGGTAGTGAAACCACATACTATAATTCAGCTCTCAAATCCAGACTGACCATCATCAAGGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTGCAAACTGATGACACAGCCATTTACTACTGTGCCAAACATTATTACTACGGTGGTAGCTATGCTATGGACTACTGGGGTCAAGGAACCTCAGTCACCGTCTCCTCAGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCCCCTCTGGCCGGCACCTGTGGCGTGCTGCTGCTGTCTCTCGTGATCACCCTGTACTGCAAGCGGGGCAGAAAGAAGCTGCTGTACATCTTCAAGCAGCCCTTCATGCGGCCCGTGCAGACCACCCAGGAAGAGGACGGCTGCTCCTGCAGATTCCCCGAGGAAGAAGAAGGCGGCTGCGAGCTGAGAGTGAAGTTCAGCAGAAGCGCCGACGCCCCTGCCTATCAGCAGGGCCAGAACCAGCTGTACAACGAGCTGAACCTGGGCAGACGGGAAGAGTACGACGTGCTGGACAAGCGGAGAGGCAGGGACCCTGAGATGGGCGGCAAGCCCAGAAGAAAGAACCCCCAGGAAGGCCTGTATAACGAACTGCAGAAAGACAAGATGGCCGAGGCCTACAGCGAGATCGGAATGAAGGGCGAGCGGAGAAGAGGCAAGGGCCACGATGGCCTGTACCAGGGCCTGAGCACCGCCACCAAGGACACCTATGACGCCCTGCACATGCAGGCCCTGCCTCCAAGAGGAAGCGGCGCCACCAATTTCAGCCTGCTGAAACAGGCCGGCGACGTGGAAGAGAACCCTGGCCCTAGAGGCGTGCAGGTGGAAACCATCTCTCCCGGCGACGGCAGAACCTTCCCTAAGAGGGGCCAGACCTGCGTGGTGCACTACACCGGCATGCTGGAAGATGGCAAGAAGATGGACAGCTCCCGGGACCGGAACAAGCCCTTCAAGTTCATGCTGGGCAAGCAGGAAGTGATCCGGGGCTGGGAAGAGGGCGTGGCACAGATGTCTGTGGGCCAGAGAGCCAAGCTGACCATCAGCCCCGATTACGCCTACGGCGCCACAGGCCACCCTGGCATCATTCCTCCACACGCCACACTGGTGTTCGATGTGGAACTGCTGAAGCTGGAAACCCGGGGAGTGCAGGTGGAAACAATCAGCCCTGGCGACGGCCGGACCTTTCCAAAACGGGGACAGACATGTGTGGTGCATTATACAGGGATGCTGGAAGATGGGAAAAAAATGGATAGCAGCCGCGACCGCAACAAACCTTTTAAGTTTATGCTGGGGAAACAGGAAGTGATTAGAGGCTGGGAAGAGGGGGTGGCACAGATGAGCGTGGGACAGCGGGCCAAACTGACAATCTCCCCCGACTATGCCTATGGGGCCACCGGACACCCCGGAATCATCCCACCTCATGCTACCCTGGTGTTTGACGTGGAACTGCTGAAACTGGAAACAAGCGGCGGAGGCAGCGGCGGCTTTGGAGATGTGGGAGCCCTGGAAAGCCTGCGGGGCAATGCCGATCTGGCCTACATCCTGAGCATGGAACCCTGCGGCCACTGCCTGATTATCAACAACGTGAACTTCTGCAGAGAGAGCGGCCTGCGGACCAGAACCGGCAGCAACATCGACTGCGAGAAGCTGCGGCGGAGATTCAGCAGCCTGCACTTCATGGTGGAAGTGAAGGGGGACCTGACCGCCAAGAAAATGGTGCTGGCTCTGCTGGAACTGGCCCAGCAGGATCATGGCGCCCTGGACTGTTGCGTGGTCGTGATCCTGAGCCACGGCTGCCAGGCCAGCCATCTGCAGTTTCCCGGCGCTGTGTATGGCACCGATGGCTGCCCTGTGTCCGTGGAAAAGATCGTGAATATCTTCAACGGCACCAGCTGCCCCAGCCTGGGCGGAAAGCCTAAGCTGTTCTTTATTCAAGCCTGTGGGGGCGAGCAGAAGGACCACGGATTTGAGGTGGCCAGCACCTCCCCCGAGGATGAGAGCCCTGGCAGCAACCCTGAGCCTGACGCCACCCCATTCCAGGAAGGACTGCGGACCTTCGACCAGCTGGACGCCATCTCTAGCCTGCCCACCCCCAGCGACATCTTCGTGTCCTACAGCACCTTCCCTGGCTTTGTGTCCTGGCGGGACCCCAAGTCCGGCTCTTGGTACGTGGAAACCCTGGACGACATCTTTGAGCAGTGGGCCCATAGCGAGGACCTGCAGAGCCTGCTGCTGAGGGTGGCCAATGCCGTGTCCGTGAAGGGCATCTACAAGCAGATGCCCGGCTGCTTCAACTTCCTGCGGAAGAAGCTGTTTTTCAAGACCAGC
FMC63-bbz-2A-revCasp9, аминокислотная последовательность (SEQ ID NO:3029)
MALPVTALLLPLALLLHAARPGSDIQMTQTTSSLSASLGDRVTISCRASQDISKYLNWYQQKPDGTVKLLIYHTSRLHSGVPSRFSGSGSGTDYSLTISNLEQEDIATYFCQQGNTLPYTFGGGTKLEITGGGGSGGGGSGGGGSEVKLQESGPGLVAPSQSLSVTCTVSGVSLPDYGVSWIRQPPRKGLEWLGVIWGSETTYYNSALKSRLTIIKDNSKSQVFLKMNSLQTDDTAIYYCAKHYYYGGSYAMDYWGQGTSVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRGSGATNFSLLKQAGDVEENPGPRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETSGGGSGGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS
CD19bbz on-CAR, нуклеотидная последовательность, CD19 on-CAR (SEQ ID NO: 977, также приведена ранее в настоящем документе)
Сигнальный пептид-домены условной агрегации (4 повтора)-сайт фурина-FMC63bbz
ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGGATCCCGGGGCGTGCAGGTTGAGACAATTTCCCCAGGAGATGGGCGAACGTTCCCCAAGCGCGGACAGACATGCGTTGTGCACTACACAGGAATGTTGGAGGACGGAAAGAAAATGGACAGTTCAAGAGATCGGAACAAACCATTCAAATTCATGTTGGGAAAACAGGAAGTGATACGGGGCTGGGAAGAGGGTGTAGCGCAAATGTCCGTTGGTCAACGAGCAAAACTCACGATAAGTCCCGATTATGCTTACGGCGCAACCGGTCACCCGGGCATCATACCGCCTCATGCGACTTTGGTCTTTGATGTGGAGCTGTTGAAACTTGAAACTCGCGGAGTACAGGTTGAAACAATATCACCCGGGGACGGGCGGACTTTTCCGAAGAGAGGTCAGACCTGCGTCGTCCATTATACCGGTATGCTGGAGGACGGAAAGAAAATGGACAGCTCACGGGACCGAAATAAACCATTCAAATTTATGTTGGGGAAACAAGAGGTTATCAGGGGCTGGGAGGAGGGTGTGGCCCAGATGTCTGTCGGTCAGCGCGCGAAACTCACAATCTCTCCGGATTATGCGTATGGGGCGACAGGGCATCCGGGAATTATCCCTCCCCACGCTACCTTGGTTTTCGATGTTGAGCTTCTGAAGTTGGAGACCAGAGGAGTTCAAGTGGAGACAATATCTCCTGGGGATGGACGGACGTTCCCCAAGCGCGGCCAGACCTGTGTAGTCCACTACACAGGGATGCTTGAAGACGGAAAAAAGATGGATAGCAGTAGAGATCGCAACAAACCATTTAAGTTCATGCTGGGGAAGCAGGAAGTAATACGCGGCTGGGAGGAAGGCGTGGCACAGATGAGTGTTGGTCAACGGGCCAAACTTACTATTTCTCCCGATTATGCGTATGGAGCCACCGGGCACCCTGGCATTATCCCACCCCATGCCACATTGGTTTTTGACGTTGAATTGCTTAAATTGGAGACCAGGGGAGTCCAAGTGGAAACAATATCACCGGGGGATGGTCGGACTTTTCCTAAAAGGGGCCAAACCTGTGTAGTCCATTATACCGGAATGCTCGAAGACGGAAAGAAAATGGACTCTTCTAGAGACCGCAATAAGCCCTTCAAGTTCATGTTGGGTAAGCAAGAGGTGATCCGGGGCTGGGAAGAGGGGGTCGCTCAAATGTCCGTCGGTCAGCGAGCTAAACTGACTATTTCCCCAGACTACGCATATGGAGCGACTGGCCACCCCGGTATTATTCCTCCCCATGCGACTCTCGTGTTCGACGTAGAACTCTTGAAATTGGAAACGTCAGCCCGGAACAGGCGGAAGAGAGGATCCGACATCCAGATGACACAGACTACATCCTCCCTGTCTGCCTCTCTGGGAGACAGAGTCACCATCAGTTGCAGGGCAAGTCAGGACATTAGTAAATATTTAAATTGGTATCAGCAGAAACCAGATGGAACTGTTAAACTCCTGATCTACCATACATCAAGATTACACTCAGGAGTCCCATCAAGGTTCAGTGGCAGTGGGTCTGGAACAGATTATTCTCTCACCATTAGCAACCTGGAGCAAGAAGATATTGCCACTTACTTTTGCCAACAGGGTAATACGCTTCCGTACACGTTCGGAGGGGGGACTAAGTTGGAAATAACAGGTGGCGGTGGCTCGGGCGGTGGTGGGTCGGGTGGCGGCGGATCTGAGGTGAAACTGCAGGAGTCAGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCGTCACATGCACTGTCTCAGGGGTCTCATTACCCGACTATGGTGTAAGCTGGATTCGCCAGCCTCCACGAAAGGGTCTGGAGTGGCTGGGAGTAATATGGGGTAGTGAAACCACATACTATAATTCAGCTCTCAAATCCAGACTGACCATCATCAAGGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTGCAAACTGATGACACAGCCATTTACTACTGTGCCAAACATTATTACTACGGTGGTAGCTATGCTATGGACTACTGGGGTCAAGGAACCTCAGTCACCGTCTCCTCAGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGCTAA
CD19bbz on-CAR, аминокислотная последовательность (SEQ ID NO: 978, также приведена ранее в настоящем документе)
Сигнальный пептид-домены условной агрегации (4 повтора)-сайт фурина-FMC63bbz
MALPVTALLLPLALLLHAARPGSRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETSARNRRKRGSDIQMTQTTSSLSASLGDRVTISCRASQDISKYLNWYQQKPDGTVKLLIYHTSRLHSGVPSRFSGSGSGTDYSLTISNLEQEDIATYFCQQGNTLPYTFGGGTKLEITGGGGSGGGGSGGGGSEVKLQESGPGLVAPSQSLSVTCTVSGVSLPDYGVSWIRQPPRKGLEWLGVIWGSETTYYNSALKSRLTIIKDNSKSQVFLKMNSLQTDDTAIYYCAKHYYYGGSYAMDYWGQGTSVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRZ
Сигнальный пептид-анти-CD20 человека-шарнир CD8-трансмембранный CD8-CD137-CD247-2A-revCasp9, нуклеотидная последовательность (SEQ ID NO: 3030)
ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGGATCCGATATTCAACTTACACAGTCCCCTAGTTCCTTGTCCGCCTCCGTCGGCGACAGAGTTACCATGACTTGTCGAGCGTCTTCTAGCGTTTCCTACATTCATTGGTTCCAACAGAAGCCCGGAAAGGCACCAAAACCTTGGATCTACGCCACGTCCAATTTGGCTAGTGGTGTTCCGGTGCGATTTTCCGGGTCAGGTAGCGGGACGGACTATACTTTTACCATTTCAAGCCTTCAGCCTGAAGACATCGCGACGTACTATTGTCAGCAGTGGACCTCTAACCCTCCTACCTTTGGCGGTGGAACAAAGCTGGAGATCAAACGAGGCGGGGGTGGCTCTGGGGGAGGAGGTTCCGGTGGGGGAGGCTCTCAAGTACAACTGCAACAAAGTGGGGCTGAAGTGAAGAAGCCCGGTTCTTCAGTCAAAGTATCATGTAAGGCAAGTGGTTATACTTTTACGTCTTATAACATGCATTGGGTAAAGCAAGCCCCTGGTCAGGGCCTCGAGTGGATTGGTGCGATCTACCCTGGAATGGGTGATACGAGCTATAATCAGAAATTCAAGGGGAAAGCCACCTTGACTGCAGACGAATCTACGAACACGGCTTACATGGAGCTTAGCTCACTCAGATCAGAGGATACAGCCTTTTACTACTGCGCTAGATCAACTTATTACGGAGGAGACTGGTATTTTGATGTATGGGGTCAGGGGACCACAGTCACTGTTAGCTCTGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGCGGAAGCGGCGCCACCAATTTCAGCCTGCTGAAACAGGCCGGCGACGTGGAAGAGAACCCTGGCCCTAGAGGCGTGCAGGTGGAAACCATCTCTCCCGGCGACGGCAGAACCTTCCCTAAGAGGGGCCAGACCTGCGTGGTGCACTACACCGGCATGCTGGAAGATGGCAAGAAGATGGACAGCTCCCGGGACCGGAACAAGCCCTTCAAGTTCATGCTGGGCAAGCAGGAAGTGATCCGGGGCTGGGAAGAGGGCGTGGCACAGATGTCTGTGGGCCAGAGAGCCAAGCTGACCATCAGCCCCGATTACGCCTACGGCGCCACAGGCCACCCTGGCATCATTCCTCCACACGCCACACTGGTGTTCGATGTGGAACTGCTGAAGCTGGAAACCCGGGGAGTGCAGGTGGAAACAATCAGCCCTGGCGACGGCCGGACCTTTCCAAAACGGGGACAGACATGTGTGGTGCATTATACAGGGATGCTGGAAGATGGGAAAAAAATGGATAGCAGCCGCGACCGCAACAAACCTTTTAAGTTTATGCTGGGGAAACAGGAAGTGATTAGAGGCTGGGAAGAGGGGGTGGCACAGATGAGCGTGGGACAGCGGGCCAAACTGACAATCTCCCCCGACTATGCCTATGGGGCCACCGGACACCCCGGAATCATCCCACCTCATGCTACCCTGGTGTTTGACGTGGAACTGCTGAAACTGGAAACAAGCGGCGGAGGCAGCGGCGGCTTTGGAGATGTGGGAGCCCTGGAAAGCCTGCGGGGCAATGCCGATCTGGCCTACATCCTGAGCATGGAACCCTGCGGCCACTGCCTGATTATCAACAACGTGAACTTCTGCAGAGAGAGCGGCCTGCGGACCAGAACCGGCAGCAACATCGACTGCGAGAAGCTGCGGCGGAGATTCAGCAGCCTGCACTTCATGGTGGAAGTGAAGGGGGACCTGACCGCCAAGAAAATGGTGCTGGCTCTGCTGGAACTGGCCCAGCAGGATCATGGCGCCCTGGACTGTTGCGTGGTCGTGATCCTGAGCCACGGCTGCCAGGCCAGCCATCTGCAGTTTCCCGGCGCTGTGTATGGCACCGATGGCTGCCCTGTGTCCGTGGAAAAGATCGTGAATATCTTCAACGGCACCAGCTGCCCCAGCCTGGGCGGAAAGCCTAAGCTGTTCTTTATTCAAGCCTGTGGGGGCGAGCAGAAGGACCACGGATTTGAGGTGGCCAGCACCTCCCCCGAGGATGAGAGCCCTGGCAGCAACCCTGAGCCTGACGCCACCCCATTCCAGGAAGGACTGCGGACCTTCGACCAGCTGGACGCCATCTCTAGCCTGCCCACCCCCAGCGACATCTTCGTGTCCTACAGCACCTTCCCTGGCTTTGTGTCCTGGCGGGACCCCAAGTCCGGCTCTTGGTACGTGGAAACCCTGGACGACATCTTTGAGCAGTGGGCCCATAGCGAGGACCTGCAGAGCCTGCTGCTGAGGGTGGCCAATGCCGTGTCCGTGAAGGGCATCTACAAGCAGATGCCCGGCTGCTTCAACTTCCTGCGGAAGAAGCTGTTTTTCAAGACCAGC
Сигнальный пептид-анти-CD20 человека-шарнир CD8-трансмембранный CD8-CD137-CD247-2A-revCasp9, аминокислотная последовательность (SEQ ID NO: 3031)
MALPVTALLLPLALLLHAARPGSDIQLTQSPSSLSASVGDRVTMTCRASSSVSYIHWFQQKPGKAPKPWIYATSNLASGVPVRFSGSGSGTDYTFTISSLQPEDIATYYCQQWTSNPPTFGGGTKLEIKRGGGGSGGGGSGGGGSQVQLQQSGAEVKKPGSSVKVSCKASGYTFTSYNMHWVKQAPGQGLEWIGAIYPGMGDTSYNQKFKGKATLTADESTNTAYMELSSLRSEDTAFYYCARSTYYGGDWYFDVWGQGTTVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPRGSGATNFSLLKQAGDVEENPGPRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETSGGGSGGFGDVGALESLRGNADLAYILSMEPCGHCLIINNVNFCRESGLRTRTGSNIDCEKLRRRFSSLHFMVEVKGDLTAKKMVLALLELAQQDHGALDCCVVVILSHGCQASHLQFPGAVYGTDGCPVSVEKIVNIFNGTSCPSLGGKPKLFFIQACGGEQKDHGFEVASTSPEDESPGSNPEPDATPFQEGLRTFDQLDAISSLPTPSDIFVSYSTFPGFVSWRDPKSGSWYVETLDDIFEQWAHSEDLQSLLLRVANAVSVKGIYKQMPGCFNFLRKKLFFKTS
CD20bbz on-CAR, нуклеотидная последовательность, CD20 on-CAR (SEQ ID NO: 3032)
Сигнальный пептид-домены условной агрегации (4 повтора)-сайт фурина-анти-CD20bbz
ATGGCCTTACCAGTGACCGCCTTGCTCCTGCCGCTGGCCTTGCTGCTCCACGCCGCCAGGCCGGGATCCCGGGGCGTGCAGGTTGAGACAATTTCCCCAGGAGATGGGCGAACGTTCCCCAAGCGCGGACAGACATGCGTTGTGCACTACACAGGAATGTTGGAGGACGGAAAGAAAATGGACAGTTCAAGAGATCGGAACAAACCATTCAAATTCATGTTGGGAAAACAGGAAGTGATACGGGGCTGGGAAGAGGGTGTAGCGCAAATGTCCGTTGGTCAACGAGCAAAACTCACGATAAGTCCCGATTATGCTTACGGCGCAACCGGTCACCCGGGCATCATACCGCCTCATGCGACTTTGGTCTTTGATGTGGAGCTGTTGAAACTTGAAACTCGCGGAGTACAGGTTGAAACAATATCACCCGGGGACGGGCGGACTTTTCCGAAGAGAGGTCAGACCTGCGTCGTCCATTATACCGGTATGCTGGAGGACGGAAAGAAAATGGACAGCTCACGGGACCGAAATAAACCATTCAAATTTATGTTGGGGAAACAAGAGGTTATCAGGGGCTGGGAGGAGGGTGTGGCCCAGATGTCTGTCGGTCAGCGCGCGAAACTCACAATCTCTCCGGATTATGCGTATGGGGCGACAGGGCATCCGGGAATTATCCCTCCCCACGCTACCTTGGTTTTCGATGTTGAGCTTCTGAAGTTGGAGACCAGAGGAGTTCAAGTGGAGACAATATCTCCTGGGGATGGACGGACGTTCCCCAAGCGCGGCCAGACCTGTGTAGTCCACTACACAGGGATGCTTGAAGACGGAAAAAAGATGGATAGCAGTAGAGATCGCAACAAACCATTTAAGTTCATGCTGGGGAAGCAGGAAGTAATACGCGGCTGGGAGGAAGGCGTGGCACAGATGAGTGTTGGTCAACGGGCCAAACTTACTATTTCTCCCGATTATGCGTATGGAGCCACCGGGCACCCTGGCATTATCCCACCCCATGCCACATTGGTTTTTGACGTTGAATTGCTTAAATTGGAGACCAGGGGAGTCCAAGTGGAAACAATATCACCGGGGGATGGTCGGACTTTTCCTAAAAGGGGCCAAACCTGTGTAGTCCATTATACCGGAATGCTCGAAGACGGAAAGAAAATGGACTCTTCTAGAGACCGCAATAAGCCCTTCAAGTTCATGTTGGGTAAGCAAGAGGTGATCCGGGGCTGGGAAGAGGGGGTCGCTCAAATGTCCGTCGGTCAGCGAGCTAAACTGACTATTTCCCCAGACTACGCATATGGAGCGACTGGCCACCCCGGTATTATTCCTCCCCATGCGACTCTCGTGTTCGACGTAGAACTCTTGAAATTGGAAACGTCAGCCCGGAACAGGCGGAAGAGAGATATTCAACTTACACAGTCCCCTAGTTCCTTGTCCGCCTCCGTCGGCGACAGAGTTACCATGACTTGTCGAGCGTCTTCTAGCGTTTCCTACATTCATTGGTTCCAACAGAAGCCCGGAAAGGCACCAAAACCTTGGATCTACGCCACGTCCAATTTGGCTAGTGGTGTTCCGGTGCGATTTTCCGGGTCAGGTAGCGGGACGGACTATACTTTTACCATTTCAAGCCTTCAGCCTGAAGACATCGCGACGTACTATTGTCAGCAGTGGACCTCTAACCCTCCTACCTTTGGCGGTGGAACAAAGCTGGAGATCAAACGAGGCGGGGGTGGCTCTGGGGGAGGAGGTTCCGGTGGGGGAGGCTCTCAAGTACAACTGCAACAAAGTGGGGCTGAAGTGAAGAAGCCCGGTTCTTCAGTCAAAGTATCATGTAAGGCAAGTGGTTATACTTTTACGTCTTATAACATGCATTGGGTAAAGCAAGCCCCTGGTCAGGGCCTCGAGTGGATTGGTGCGATCTACCCTGGAATGGGTGATACGAGCTATAATCAGAAATTCAAGGGGAAAGCCACCTTGACTGCAGACGAATCTACGAACACGGCTTACATGGAGCTTAGCTCACTCAGATCAGAGGATACAGCCTTTTACTACTGCGCTAGATCAACTTATTACGGAGGAGACTGGTATTTTGATGTATGGGGTCAGGGGACCACAGTCACTGTTAGCTCTGCTAGCACCACGACGCCAGCGCCGCGACCACCAACACCGGCGCCCACCATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATTCCGGAATCTACATCTGGGCGCCCTTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAACGGGGCAGAAAGAAACTCCTGTATATATTCAAACAACCATTTATGAGACCAGTACAAACTACTCAAGAGGAAGATGGCTGTAGCTGCCGATTTCCAGAAGAAGAAGAAGGAGGATGTGAACTGAGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGC
CD20bbz on-CAR, аминокислотная последовательность (SEQ ID NO: 3033)
Сигнальный пептид-домены условной агрегации (4 повтора)-сайт фурина-анти-CD20bbz
MALPVTALLLPLALLLHAARPGSRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETRGVQVETISPGDGRTFPKRGQTCVVHYTGMLEDGKKMDSSRDRNKPFKFMLGKQEVIRGWEEGVAQMSVGQRAKLTISPDYAYGATGHPGIIPPHATLVFDVELLKLETSARNRRKRGSDIQLTQSPSSLSASVGDRVTMTCRASSSVSYIHWFQQKPGKAPKPWIYATSNLASGVPVRFSGSGSGTDYTFTISSLQPEDIATYYCQQWTSNPPTFGGGTKLEIKRGGGGSGGGGSGGGGSQVQLQQSGAEVKKPGSSVKVSCKASGYTFTSYNMHWVKQAPGQGLEWIGAIYPGMGDTSYNQKFKGKATLTADESTNTAYMELSSLRSEDTAFYYCARSTYYGGDWYFDVWGQGTTVTVSSASTTTPAPRPPTPAPTIASQPLSLRPEACRPAAGGAVHTRGLDFACDSGIYIWAPLAGTCGVLLLSLVITLYCKRGRKKLLYIFKQPFMRPVQTTQEEDGCSCRFPEEEEGGCELRVKFSRSADAPAYQQGQNQLYNELNLGRREEYDVLDKRRGRDPEMGGKPRRKNPQEGLYNELQKDKMAEAYSEIGMKGERRRGKGHDGLYQGLSTATKDTYDALHMQALPPR
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Содержание каждого и всех патентов, патентных заявок и публикаций, цитированных в настоящем документе, включено в настоящий документ посредством ссылки в полном объеме. При том, что данное изобретение раскрыто со ссылкой на конкретные варианты осуществления, очевидно, что другие варианты осуществления и вариации данного изобретения могут быть разработаны специалистами в данной области без отклонения от истинной сущности и объема изобретения. Прилагаемую формулу изобретения следует толковать, как включающую все такие варианты осуществления и эквивалентные вариации.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NOVARTIS AG
THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA
<120> КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИЗБИРАТЕЛЬНОЙ ЭКСПРЕССИИ БЕЛКА
<130> N2067-7128WO
<140>
<141>
<150> 62/322,931
<151> 2016-04-15
<150> 62/481,094
<151> 2017-04-03
<160> 3036
<170> PatentIn version 3.5
<210> 1
<211> 1184
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1
cgtgaggctc cggtgcccgt cagtgggcag agcgcacatc gcccacagtc cccgagaagt
60
tggggggagg ggtcggcaat tgaaccggtg cctagagaag gtggcgcggg gtaaactggg
120
aaagtgatgt cgtgtactgg ctccgccttt ttcccgaggg tgggggagaa ccgtatataa
180
gtgcagtagt cgccgtgaac gttctttttc gcaacgggtt tgccgccaga acacaggtaa
240
gtgccgtgtg tggttcccgc gggcctggcc tctttacggg ttatggccct tgcgtgcctt
300
gaattacttc cacctggctg cagtacgtga ttcttgatcc cgagcttcgg gttggaagtg
360
ggtgggagag ttcgaggcct tgcgcttaag gagccccttc gcctcgtgct tgagttgagg
420
cctggcctgg gcgctggggc cgccgcgtgc gaatctggtg gcaccttcgc gcctgtctcg
480
ctgctttcga taagtctcta gccatttaaa atttttgatg acctgctgcg acgctttttt
540
tctggcaaga tagtcttgta aatgcgggcc aagatctgca cactggtatt tcggtttttg
600
gggccgcggg cggcgacggg gcccgtgcgt cccagcgcac atgttcggcg aggcggggcc
660
tgcgagcgcg gccaccgaga atcggacggg ggtagtctca agctggccgg cctgctctgg
720
tgcctggcct cgcgccgccg tgtatcgccc cgccctgggc ggcaaggctg gcccggtcgg
780
caccagttgc gtgagcggaa agatggccgc ttcccggccc tgctgcaggg agctcaaaat
840
ggaggacgcg gcgctcggga gagcgggcgg gtgagtcacc cacacaaagg aaaagggcct
900
ttccgtcctc agccgtcgct tcatgtgact ccacggagta ccgggcgccg tccaggcacc
960
tcgattagtt ctcgagcttt tggagtacgt cgtctttagg ttggggggag gggttttatg
1020
cgatggagtt tccccacact gagtgggtgg agactgaagt taggccagct tggcacttga
1080
tgtaattctc cttggaattt gccctttttg agtttggatc ttggttcatt ctcaagcctc
1140
agacagtggt tcaaagtttt tttcttccat ttcaggtgtc gtga
1184
<210> 2
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 2
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 3
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3
atggccctgc ctgtgacagc cctgctgctg cctctggctc tgctgctgca tgccgctaga
60
ccc
63
<210> 4
<211> 45
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 4
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 5
<211> 135
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 5
accacgacgc cagcgccgcg accaccaaca ccggcgccca ccatcgcgtc gcagcccctg
60
tccctgcgcc cagaggcgtg ccggccagcg gcggggggcg cagtgcacac gagggggctg
120
gacttcgcct gtgat
135
<210> 6
<211> 230
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 6
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys Met
225 230
<210> 7
<211> 690
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 7
gagagcaagt acggccctcc ctgcccccct tgccctgccc ccgagttcct gggcggaccc
60
agcgtgttcc tgttcccccc caagcccaag gacaccctga tgatcagccg gacccccgag
120
gtgacctgtg tggtggtgga cgtgtcccag gaggaccccg aggtccagtt caactggtac
180
gtggacggcg tggaggtgca caacgccaag accaagcccc gggaggagca gttcaatagc
240
acctaccggg tggtgtccgt gctgaccgtg ctgcaccagg actggctgaa cggcaaggaa
300
tacaagtgta aggtgtccaa caagggcctg cccagcagca tcgagaaaac catcagcaag
360
gccaagggcc agcctcggga gccccaggtg tacaccctgc cccctagcca agaggagatg
420
accaagaacc aggtgtccct gacctgcctg gtgaagggct tctaccccag cgacatcgcc
480
gtggagtggg agagcaacgg ccagcccgag aacaactaca agaccacccc ccctgtgctg
540
gacagcgacg gcagcttctt cctgtacagc cggctgaccg tggacaagag ccggtggcag
600
gagggcaacg tctttagctg ctccgtgatg cacgaggccc tgcacaacca ctacacccag
660
aagagcctga gcctgtccct gggcaagatg
690
<210> 8
<211> 282
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 8
Arg Trp Pro Glu Ser Pro Lys Ala Gln Ala Ser Ser Val Pro Thr Ala
1 5 10 15
Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala
20 25 30
Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys
35 40 45
Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
50 55 60
Ser His Thr Gln Pro Leu Gly Val Tyr Leu Leu Thr Pro Ala Val Gln
65 70 75 80
Asp Leu Trp Leu Arg Asp Lys Ala Thr Phe Thr Cys Phe Val Val Gly
85 90 95
Ser Asp Leu Lys Asp Ala His Leu Thr Trp Glu Val Ala Gly Lys Val
100 105 110
Pro Thr Gly Gly Val Glu Glu Gly Leu Leu Glu Arg His Ser Asn Gly
115 120 125
Ser Gln Ser Gln His Ser Arg Leu Thr Leu Pro Arg Ser Leu Trp Asn
130 135 140
Ala Gly Thr Ser Val Thr Cys Thr Leu Asn His Pro Ser Leu Pro Pro
145 150 155 160
Gln Arg Leu Met Ala Leu Arg Glu Pro Ala Ala Gln Ala Pro Val Lys
165 170 175
Leu Ser Leu Asn Leu Leu Ala Ser Ser Asp Pro Pro Glu Ala Ala Ser
180 185 190
Trp Leu Leu Cys Glu Val Ser Gly Phe Ser Pro Pro Asn Ile Leu Leu
195 200 205
Met Trp Leu Glu Asp Gln Arg Glu Val Asn Thr Ser Gly Phe Ala Pro
210 215 220
Ala Arg Pro Pro Pro Gln Pro Gly Ser Thr Thr Phe Trp Ala Trp Ser
225 230 235 240
Val Leu Arg Val Pro Ala Pro Pro Ser Pro Gln Pro Ala Thr Tyr Thr
245 250 255
Cys Val Val Ser His Glu Asp Ser Arg Thr Leu Leu Asn Ala Ser Arg
260 265 270
Ser Leu Glu Val Ser Tyr Val Thr Asp His
275 280
<210> 9
<211> 847
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 9
aggtggcccg aaagtcccaa ggcccaggca tctagtgttc ctactgcaca gccccaggca
60
gaaggcagcc tagccaaagc tactactgca cctgccacta cgcgcaatac tggccgtggc
120
ggggaggaga agaaaaagga gaaagagaaa gaagaacagg aagagaggga gaccaagacc
180
cctgaatgtc catcccatac ccagccgctg ggcgtctatc tcttgactcc cgcagtacag
240
gacttgtggc ttagagataa ggccaccttt acatgtttcg tcgtgggctc tgacctgaag
300
gatgcccatt tgacttggga ggttgccgga aaggtaccca cagggggggt tgaggaaggg
360
ttgctggagc gccattccaa tggctctcag agccagcact caagactcac ccttccgaga
420
tccctgtgga acgccgggac ctctgtcaca tgtactctaa atcatcctag cctgccccca
480
cagcgtctga tggcccttag agagccagcc gcccaggcac cagttaagct tagcctgaat
540
ctgctcgcca gtagtgatcc cccagaggcc gccagctggc tcttatgcga agtgtccggc
600
tttagcccgc ccaacatctt gctcatgtgg ctggaggacc agcgagaagt gaacaccagc
660
ggcttcgctc cagcccggcc cccaccccag ccgggttcta ccacattctg ggcctggagt
720
gtcttaaggg tcccagcacc acctagcccc cagccagcca catacacctg tgttgtgtcc
780
catgaagata gcaggaccct gctaaatgct tctaggagtc tggaggtttc ctacgtgact
840
gaccatt
847
<210> 10
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 10
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 11
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 11
ggtggcggag gttctggagg tggaggttcc
30
<210> 12
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 12
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr Leu Tyr Cys
20
<210> 13
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 13
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc
60
accctttact gc
72
<210> 14
<211> 42
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 14
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 15
<211> 126
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 15
aaacggggca gaaagaaact cctgtatata ttcaaacaac catttatgag accagtacaa
60
actactcaag aggaagatgg ctgtagctgc cgatttccag aagaagaaga aggaggatgt
120
gaactg
126
<210> 16
<211> 48
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 16
Gln Arg Arg Lys Tyr Arg Ser Asn Lys Gly Glu Ser Pro Val Glu Pro
1 5 10 15
Ala Glu Pro Cys Arg Tyr Ser Cys Pro Arg Glu Glu Glu Gly Ser Thr
20 25 30
Ile Pro Ile Gln Glu Asp Tyr Arg Lys Pro Glu Pro Ala Cys Ser Pro
35 40 45
<210> 17
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 17
aggagtaaga ggagcaggct cctgcacagt gactacatga acatgactcc ccgccgcccc
60
gggcccaccc gcaagcatta ccagccctat gccccaccac gcgacttcgc agcctatcgc
120
tcc
123
<210> 18
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 18
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 19
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 19
agagtgaagt tcagcaggag cgcagacgcc cccgcgtaca agcagggcca gaaccagctc
60
tataacgagc tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc
120
cgggaccctg agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgtacaat
180
gaactgcaga aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc
240
cggaggggca aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc
300
tacgacgccc ttcacatgca ggccctgccc cctcgc
336
<210> 20
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 20
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 21
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 21
agagtgaagt tcagcaggag cgcagacgcc cccgcgtacc agcagggcca gaaccagctc
60
tataacgagc tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc
120
cgggaccctg agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgtacaat
180
gaactgcaga aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc
240
cggaggggca aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc
300
tacgacgccc ttcacatgca ggccctgccc cctcgc
336
<210> 22
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 22
Gly Gly Gly Gly Ser
1 5
<210> 23
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 23
ggtggcggag gttctggagg tggaggttcc
30
<210> 24
<211> 150
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 24
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln Phe Gln Thr Leu Val
145 150
<210> 25
<211> 450
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 25
cccggatggt ttctggactc tccggatcgc ccgtggaatc ccccaacctt ctcaccggca
60
ctcttggttg tgactgaggg cgataatgcg accttcacgt gctcgttctc caacacctcc
120
gaatcattcg tgctgaactg gtaccgcatg agcccgtcaa accagaccga caagctcgcc
180
gcgtttccgg aagatcggtc gcaaccggga caggattgtc ggttccgcgt gactcaactg
240
ccgaatggca gagacttcca catgagcgtg gtccgcgcta ggcgaaacga ctccgggacc
300
tacctgtgcg gagccatctc gctggcgcct aaggcccaaa tcaaagagag cttgagggcc
360
gaactgagag tgaccgagcg cagagctgag gtgccaactg cacatccatc cccatcgcct
420
cggcctgcgg ggcagtttca gaccctggtc
450
<210> 26
<211> 394
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 26
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro
20 25 30
Trp Asn Pro Pro Thr Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly
35 40 45
Asp Asn Ala Thr Phe Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe
50 55 60
Val Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu
65 70 75 80
Ala Ala Phe Pro Glu Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe
85 90 95
Arg Val Thr Gln Leu Pro Asn Gly Arg Asp Phe His Met Ser Val Val
100 105 110
Arg Ala Arg Arg Asn Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser
115 120 125
Leu Ala Pro Lys Ala Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg
130 135 140
Val Thr Glu Arg Arg Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser
145 150 155 160
Pro Arg Pro Ala Gly Gln Phe Gln Thr Leu Val Thr Thr Thr Pro Ala
165 170 175
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
180 185 190
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
195 200 205
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
210 215 220
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
225 230 235 240
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
245 250 255
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
260 265 270
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
275 280 285
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
290 295 300
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
305 310 315 320
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
325 330 335
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
340 345 350
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
355 360 365
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
370 375 380
Ala Leu His Met Gln Ala Leu Pro Pro Arg
385 390
<210> 27
<211> 1182
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 27
atggccctcc ctgtcactgc cctgcttctc cccctcgcac tcctgctcca cgccgctaga
60
ccacccggat ggtttctgga ctctccggat cgcccgtgga atcccccaac cttctcaccg
120
gcactcttgg ttgtgactga gggcgataat gcgaccttca cgtgctcgtt ctccaacacc
180
tccgaatcat tcgtgctgaa ctggtaccgc atgagcccgt caaaccagac cgacaagctc
240
gccgcgtttc cggaagatcg gtcgcaaccg ggacaggatt gtcggttccg cgtgactcaa
300
ctgccgaatg gcagagactt ccacatgagc gtggtccgcg ctaggcgaaa cgactccggg
360
acctacctgt gcggagccat ctcgctggcg cctaaggccc aaatcaaaga gagcttgagg
420
gccgaactga gagtgaccga gcgcagagct gaggtgccaa ctgcacatcc atccccatcg
480
cctcggcctg cggggcagtt tcagaccctg gtcacgacca ctccggcgcc gcgcccaccg
540
actccggccc caactatcgc gagccagccc ctgtcgctga ggccggaagc atgccgccct
600
gccgccggag gtgctgtgca tacccgggga ttggacttcg catgcgacat ctacatttgg
660
gctcctctcg ccggaacttg tggcgtgctc cttctgtccc tggtcatcac cctgtactgc
720
aagcggggtc ggaaaaagct tctgtacatt ttcaagcagc ccttcatgag gcccgtgcaa
780
accacccagg aggaggacgg ttgctcctgc cggttccccg aagaggaaga aggaggttgc
840
gagctgcgcg tgaagttctc ccggagcgcc gacgcccccg cctataagca gggccagaac
900
cagctgtaca acgaactgaa cctgggacgg cgggaagagt acgatgtgct ggacaagcgg
960
cgcggccggg accccgaaat gggcgggaag cctagaagaa agaaccctca ggaaggcctg
1020
tataacgagc tgcagaagga caagatggcc gaggcctact ccgaaattgg gatgaaggga
1080
gagcggcgga ggggaaaggg gcacgacggc ctgtaccaag gactgtccac cgccaccaag
1140
gacacatacg atgccctgca catgcaggcc cttccccctc gc
1182
<210> 28
<211> 40
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(40)
<223> /примечание="Данная последовательность может включать 1-10
повторяющихся единиц ‘Gly Gly Gly Ser’"
<400> 28
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
20 25 30
Gly Gly Gly Ser Gly Gly Gly Ser
35 40
<210> 29
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 29
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 30
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 30
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 31
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 31
Gly Gly Gly Ser
1
<210> 32
<211> 5000
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(5000)
<223> /примечание="Данная последовательность может включать 50-5000
нуклеотидов"
<220>
<221> источник
<223> /примечание="Смотри спецификацию поданной заявки для подробного
описания
замен и предпочтительных вариантов осуществления"
<400> 32
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
60
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1980
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2040
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2100
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2160
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2220
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2280
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2340
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2400
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2460
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2520
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2580
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2640
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2700
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2760
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2820
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2880
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2940
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3000
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3060
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4980
aaaaaaaaaa aaaaaaaaaa
5000
<210> 33
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 33
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccc
63
<210> 34
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 34
atctacattt gggcccctct ggctggtact tgcggggtcc tgctgctttc actcgtgatc
60
actctttact gt
72
<210> 35
<211> 5
<212> БЕЛОК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность гранзима B"
<220>
<221> МОД_ОСТ
<222> (5)..(5)
<223> Любая аминокислота
<400> 35
Ile Glu Pro Asp Xaa
1 5
<210> 36
<211> 5
<212> БЕЛОК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность энтерокиназы"
<400> 36
Asp Asp Asp Asp Lys
1 5
<210> 37
<211> 6
<212> БЕЛОК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность гененазы"
<400> 37
Pro Gly Ala Ala His Tyr
1 5
<210> 38
<211> 7
<212> БЕЛОК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность PreScission протеазы"
<400> 38
Leu Glu Val Phe Gln Gly Pro
1 5
<210> 39
<211> 373
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 39
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln Phe Gln Thr Leu Val Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
145 150 155 160
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
165 170 175
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
180 185 190
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
195 200 205
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
210 215 220
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
225 230 235 240
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
245 250 255
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
260 265 270
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
275 280 285
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
290 295 300
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
305 310 315 320
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
325 330 335
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
340 345 350
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
355 360 365
Ala Leu Pro Pro Arg
370
<210> 40
<211> 6
<212> БЕЛОК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность тромбина"
<400> 40
Leu Val Pro Arg Gly Ser
1 5
<210> 41
<211> 7
<212> БЕЛОК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность TEV-протеазы"
<400> 41
Glu Asn Leu Tyr Phe Gln Gly
1 5
<210> 42
<211> 2
<212> БЕЛОК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
последовательность эластазы 1"
<220>
<221> ВАРИАНТ
<222> (1)..(1)
<223> /замена="Gly" или "Ser" или "Val"
<220>
<221> МОД_ОСТ
<222> (2)..(2)
<223> Любая аминокислота
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(2)
<223> /примечание="Остатки варианта, приведенные в
последовательности,
не являются предпочтительными относительно тех, которые приведены в
аннотациях
для положений варианта"
<400> 42
Ala Xaa
1
<210> 43
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 43
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro
20
<210> 44
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 44
Met Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1 5 10 15
Val Thr Asn Ser
20
<210> 45
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 45
Met Ala Gln Val Lys Leu Gln Glu Ser Gly Thr Glu Leu Ala Lys Pro
1 5 10 15
Gly Ala Ala Val Lys
20
<210> 46
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 46
Met Arg Phe Leu Ala Ala Thr Phe Leu Leu Leu Ala Leu Ser Thr Ala
1 5 10 15
Ala Gln Ala
<210> 47
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 47
Lys Asp Glu Leu
1
<210> 48
<211> 787
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 48
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
275 280 285
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
290 295 300
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
305 310 315 320
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
325 330 335
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
340 345 350
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
355 360 365
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
370 375 380
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
385 390 395 400
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
405 410 415
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
420 425 430
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
435 440 445
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
450 455 460
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
465 470 475 480
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
485 490 495
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
500 505 510
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
515 520 525
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
530 535 540
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
545 550 555 560
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
565 570 575
Cys Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Arg Asn
580 585 590
Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu His His
595 600 605
Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala Arg
610 615 620
Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His Glu
625 630 635 640
Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu Pro Leu
645 650 655
Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr Ser Phe
660 665 670
Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe Met Met
675 680 685
Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr Gln Val
690 695 700
Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys Arg Gln
705 710 715 720
Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu Met Gln
725 730 735
Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu Glu
740 745 750
Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu Leu His
755 760 765
Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser Tyr Leu
770 775 780
Asn Ala Ser
785
<210> 49
<211> 816
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 49
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaaga
816
<210> 50
<400> 50
000
<210> 51
<400> 51
000
<210> 52
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 52
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Arg Asn Leu Pro
1 5 10 15
Val
<210> 53
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 53
gtggtggcgg tggaagcggc ggtggcggaa gcggcggtgg cggcagcaga aacctccccg
60
tgg
63
<210> 54
<400> 54
000
<210> 55
<400> 55
000
<210> 56
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 56
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
1 5 10 15
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
20 25 30
Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
35 40 45
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
50 55 60
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
65 70 75 80
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
85 90 95
Leu Val Phe Asp Val Glu Leu Leu Lys Pro Glu
100 105
<210> 57
<211> 158
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 57
Ile Ser Leu Ile Ala Ala Leu Ala Val Asp Tyr Val Ile Gly Met Glu
1 5 10 15
Asn Ala Met Pro Trp Asn Leu Pro Ala Asp Leu Ala Trp Phe Lys Arg
20 25 30
Asn Thr Leu Asn Lys Pro Val Ile Met Gly Arg His Thr Trp Glu Ser
35 40 45
Ile Gly Arg Pro Leu Pro Gly Arg Lys Asn Ile Ile Leu Ser Ser Gln
50 55 60
Pro Ser Thr Asp Asp Arg Val Thr Trp Val Lys Ser Val Asp Glu Ala
65 70 75 80
Ile Ala Ala Cys Gly Asp Val Pro Glu Ile Met Val Ile Gly Gly Gly
85 90 95
Arg Val Ile Glu Gln Phe Leu Pro Lys Ala Gln Lys Leu Tyr Leu Thr
100 105 110
His Ile Asp Ala Glu Val Glu Gly Asp Thr His Phe Pro Asp Tyr Glu
115 120 125
Pro Asp Asp Trp Glu Ser Val Phe Ser Glu Phe His Asp Ala Asp Ala
130 135 140
Gln Asn Ser His Ser Tyr Cys Phe Glu Ile Leu Glu Arg Arg
145 150 155
<210> 58
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 58
Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met Val Ser Ala Leu Leu
1 5 10 15
Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr Asp Pro Thr Arg Pro
20 25 30
Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr Asn Leu Ala Asp Arg
35 40 45
Glu Leu Val His Met Ile Asn Trp Ala Lys Arg Val Pro Gly Phe Val
50 55 60
Asp Leu Ala Leu His Asp Gln Val His Leu Leu Glu Cys Ala Trp Met
65 70 75 80
Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser Met Glu His Pro Gly
85 90 95
Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp Arg Asn Gln Gly Lys
100 105 110
Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met Leu Leu Ala Thr Ser
115 120 125
Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu Phe Val Cys Leu
130 135 140
Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr Phe Leu Ser Ser
145 150 155 160
Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His Arg Val Leu Asp
165 170 175
Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys Ala Gly Leu Thr
180 185 190
Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser
195 200 205
His Ile Arg His Met Ser Ser Lys Arg Met Glu His Leu Tyr Ser Met
210 215 220
Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu Leu Leu Glu Met Leu
225 230 235 240
Asp Ala His Arg Leu
245
<210> 59
<211> 610
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 59
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp
20 25 30
Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr
35 40 45
Gly Met Leu Glu Asp Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn
50 55 60
Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp
65 70 75 80
Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr
85 90 95
Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile
100 105 110
Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Pro Glu
115 120 125
Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Phe Pro Val Asp Arg Thr Lys
130 135 140
Arg Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
145 150 155 160
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
165 170 175
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
180 185 190
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
210 215 220
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
225 230 235 240
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly
245 250 255
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln
260 265 270
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr
275 280 285
Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile
290 295 300
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly
305 310 315 320
Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile
325 330 335
Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val
340 345 350
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr
355 360 365
Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
370 375 380
Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
385 390 395 400
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
405 410 415
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
420 425 430
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
435 440 445
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
450 455 460
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
465 470 475 480
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
485 490 495
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys
500 505 510
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
515 520 525
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
530 535 540
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
545 550 555 560
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
565 570 575
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
580 585 590
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
595 600 605
Pro Arg
610
<210> 60
<211> 1830
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 60
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccggagtgc aggtggaaac catctcccca ggagacgggc gcaccttccc caagcgcggc
120
cagacctgtg tggtgcacta caccgggatg cttgaagatg gaaagaaagt cgattcctcc
180
cgggacagaa acaagccctt taagtttatg ctaggcaagc aggaggtgat ccgaggctgg
240
gaagaagggg ttgcccagat gagtgtgggt cagagagcca aactgactat atctccagat
300
tatgcctatg gtgccactgg gcacccaggc atcatcccac cacatgccac tctcgtcttc
360
gatgtggagc ttctaaaacc ggaataccct tatgatgttc ctgattatgc tttccccgtg
420
gatcgtacta aaagagaaat tgtgatgacc cagtcacccg ccactcttag cctttcaccc
480
ggtgagcgcg caaccctgtc ttgcagagcc tcccaagaca tctcaaaata ccttaattgg
540
tatcaacaga agcccggaca ggctcctcgc cttctgatct accacaccag ccggctccat
600
tctggaatcc ctgccaggtt cagcggtagc ggatctggga ccgactacac cctcactatc
660
agctcactgc agccagagga cttcgctgtc tatttctgtc agcaagggaa caccctgccc
720
tacacctttg gacagggcac caagctcgag attaaaggtg gaggtggcag cggaggaggt
780
gggtccggcg gtggaggaag ccaggtccaa ctccaagaaa gcggaccggg tcttgtgaag
840
ccatcagaaa ctctttcact gacttgtact gtgagcggag tgtctctccc cgattacggg
900
gtgtcttgga tcagacagcc accggggaag ggtctggaat ggattggagt gatttggggc
960
tctgagacta cttactactc ttcatccctc aagtcacgcg tcaccatctc aaaggacaac
1020
tctaagaatc aggtgtcact gaaactgtca tctgtgaccg cagccgacac cgccgtgtac
1080
tattgcgcta agcattacta ttatggcggg agctacgcaa tggattactg gggacagggt
1140
actctggtca ccgtgtccag caccactacc ccagcaccga ggccacccac cccggctcct
1200
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
1260
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
1320
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1380
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1440
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1500
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1560
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1620
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1680
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1740
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1800
gctcttcaca tgcaggccct gccgcctcgg
1830
<210> 61
<211> 610
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 61
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp
20 25 30
Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr
35 40 45
Gly Met Leu Glu Asp Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn
50 55 60
Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp
65 70 75 80
Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr
85 90 95
Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile
100 105 110
Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Pro Glu
115 120 125
Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Phe Pro Val Asp Ala Thr Lys
130 135 140
Arg Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
145 150 155 160
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
165 170 175
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
180 185 190
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
210 215 220
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
225 230 235 240
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly
245 250 255
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln
260 265 270
Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr
275 280 285
Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile
290 295 300
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly
305 310 315 320
Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile
325 330 335
Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val
340 345 350
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr
355 360 365
Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
370 375 380
Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
385 390 395 400
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
405 410 415
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
420 425 430
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
435 440 445
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
450 455 460
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
465 470 475 480
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
485 490 495
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys
500 505 510
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
515 520 525
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
530 535 540
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
545 550 555 560
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
565 570 575
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
580 585 590
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
595 600 605
Pro Arg
610
<210> 62
<211> 1830
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 62
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccggagtgc aggtggaaac catctcccca ggagacgggc gcaccttccc caagcgcggc
120
cagacctgtg tggtgcacta caccgggatg cttgaagatg gaaagaaagt cgattcctcc
180
cgggacagaa acaagccctt taagtttatg ctaggcaagc aggaggtgat ccgaggctgg
240
gaagaagggg ttgcccagat gagtgtgggt cagagagcca aactgactat atctccagat
300
tatgcctatg gtgccactgg gcacccaggc atcatcccac cacatgccac tctcgtcttc
360
gatgtggagc ttctaaaacc ggaataccct tatgatgttc ctgattatgc tttccccgtg
420
gatgctacta aaagagaaat tgtgatgacc cagtcacccg ccactcttag cctttcaccc
480
ggtgagcgcg caaccctgtc ttgcagagcc tcccaagaca tctcaaaata ccttaattgg
540
tatcaacaga agcccggaca ggctcctcgc cttctgatct accacaccag ccggctccat
600
tctggaatcc ctgccaggtt cagcggtagc ggatctggga ccgactacac cctcactatc
660
agctcactgc agccagagga cttcgctgtc tatttctgtc agcaagggaa caccctgccc
720
tacacctttg gacagggcac caagctcgag attaaaggtg gaggtggcag cggaggaggt
780
gggtccggcg gtggaggaag ccaggtccaa ctccaagaaa gcggaccggg tcttgtgaag
840
ccatcagaaa ctctttcact gacttgtact gtgagcggag tgtctctccc cgattacggg
900
gtgtcttgga tcagacagcc accggggaag ggtctggaat ggattggagt gatttggggc
960
tctgagacta cttactactc ttcatccctc aagtcacgcg tcaccatctc aaaggacaac
1020
tctaagaatc aggtgtcact gaaactgtca tctgtgaccg cagccgacac cgccgtgtac
1080
tattgcgcta agcattacta ttatggcggg agctacgcaa tggattactg gggacagggt
1140
actctggtca ccgtgtccag caccactacc ccagcaccga ggccacccac cccggctcct
1200
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
1260
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
1320
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1380
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1440
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1500
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1560
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1620
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1680
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1740
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1800
gctcttcaca tgcaggccct gccgcctcgg
1830
<210> 63
<211> 661
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 63
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ile Ser Leu Ile Ala Ala Leu Ala Val Asp Tyr
20 25 30
Val Ile Gly Met Glu Asn Ala Met Pro Trp Asn Leu Pro Ala Asp Leu
35 40 45
Ala Trp Phe Lys Arg Asn Thr Leu Asn Lys Pro Val Ile Met Gly Arg
50 55 60
His Thr Trp Glu Ser Ile Gly Arg Pro Leu Pro Gly Arg Lys Asn Ile
65 70 75 80
Ile Leu Ser Ser Gln Pro Ser Thr Asp Asp Arg Val Thr Trp Val Lys
85 90 95
Ser Val Asp Glu Ala Ile Ala Ala Cys Gly Asp Val Pro Glu Ile Met
100 105 110
Val Ile Gly Gly Gly Arg Val Ile Glu Gln Phe Leu Pro Lys Ala Gln
115 120 125
Lys Leu Tyr Leu Thr His Ile Asp Ala Glu Val Glu Gly Asp Thr His
130 135 140
Phe Pro Asp Tyr Glu Pro Asp Asp Trp Glu Ser Val Phe Ser Glu Phe
145 150 155 160
His Asp Ala Asp Ala Gln Asn Ser His Ser Tyr Cys Phe Glu Ile Leu
165 170 175
Glu Arg Arg Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Phe Pro Val Asp
180 185 190
Arg Thr Lys Arg Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser
195 200 205
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp
210 215 220
Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
225 230 235 240
Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala
245 250 255
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
260 265 270
Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn
275 280 285
Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly
290 295 300
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
305 310 315 320
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
325 330 335
Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val
340 345 350
Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val
355 360 365
Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg
370 375 380
Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu
385 390 395 400
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His
405 410 415
Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr
420 425 430
Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
435 440 445
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
450 455 460
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
465 470 475 480
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
485 490 495
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
500 505 510
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
515 520 525
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
530 535 540
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
545 550 555 560
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
565 570 575
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
580 585 590
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
595 600 605
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
610 615 620
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
625 630 635 640
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
645 650 655
Ala Leu Pro Pro Arg
660
<210> 64
<211> 1983
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 64
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccatctctc tgattgccgc tctggccgtg gactacgtga tcgggatgga aaacgctatg
120
ccatggaatc tgcccgccga tctggcttgg ttcaagagga acaccctgaa caagccagtg
180
atcatgggca gacacacttg ggagtccatt ggccggcccc tgcctggacg caagaacatc
240
attctgagct cccagccctc taccgacgac agggtgacat gggtgaaaag tgtggacgaa
300
gccattgccg cttgcggaga tgtgcccgag atcatggtca tcggcggagg gagagtgatc
360
gagcagttcc tgcctaaggc ccagaaactg tacctgactc acattgacgc tgaggtggaa
420
ggggacaccc attttcctga ttatgagcca gacgattggg aaagcgtgtt ctccgagttt
480
cacgacgccg atgctcagaa ctctcatagt tattgctttg agatcctgga aaggagatac
540
ccttatgatg ttcctgatta tgctttcccc gtggatcgta ctaaaagaga aattgtgatg
600
acccagtcac ccgccactct tagcctttca cccggtgagc gcgcaaccct gtcttgcaga
660
gcctcccaag acatctcaaa ataccttaat tggtatcaac agaagcccgg acaggctcct
720
cgccttctga tctaccacac cagccggctc cattctggaa tccctgccag gttcagcggt
780
agcggatctg ggaccgacta caccctcact atcagctcac tgcagccaga ggacttcgct
840
gtctatttct gtcagcaagg gaacaccctg ccctacacct ttggacaggg caccaagctc
900
gagattaaag gtggaggtgg cagcggagga ggtgggtccg gcggtggagg aagccaggtc
960
caactccaag aaagcggacc gggtcttgtg aagccatcag aaactctttc actgacttgt
1020
actgtgagcg gagtgtctct ccccgattac ggggtgtctt ggatcagaca gccaccgggg
1080
aagggtctgg aatggattgg agtgatttgg ggctctgaga ctacttacta ctcttcatcc
1140
ctcaagtcac gcgtcaccat ctcaaaggac aactctaaga atcaggtgtc actgaaactg
1200
tcatctgtga ccgcagccga caccgccgtg tactattgcg ctaagcatta ctattatggc
1260
gggagctacg caatggatta ctggggacag ggtactctgg tcaccgtgtc cagcaccact
1320
accccagcac cgaggccacc caccccggct cctaccatcg cctcccagcc tctgtccctg
1380
cgtccggagg catgtagacc cgcagctggt ggggccgtgc atacccgggg tcttgacttc
1440
gcctgcgata tctacatttg ggcccctctg gctggtactt gcggggtcct gctgctttca
1500
ctcgtgatca ctctttactg taagcgcggt cggaagaagc tgctgtacat ctttaagcaa
1560
cccttcatga ggcctgtgca gactactcaa gaggaggacg gctgttcatg ccggttccca
1620
gaggaggagg aaggcggctg cgaactgcgc gtgaaattca gccgcagcgc agatgctcca
1680
gcctacaagc aggggcagaa ccagctctac aacgaactca atcttggtcg gagagaggag
1740
tacgacgtgc tggacaagcg gagaggacgg gacccagaaa tgggcgggaa gccgcgcaga
1800
aagaatcccc aagagggcct gtacaacgag ctccaaaagg ataagatggc agaagcctat
1860
agcgagattg gtatgaaagg ggaacgcaga agaggcaaag gccacgacgg actgtaccag
1920
ggactcagca ccgccaccaa ggacacctat gacgctcttc acatgcaggc cctgccgcct
1980
cgg
1983
<210> 65
<211> 661
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 65
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ile Ser Leu Ile Ala Ala Leu Ala Val Asp Tyr
20 25 30
Val Ile Gly Met Glu Asn Ala Met Pro Trp Asn Leu Pro Ala Asp Leu
35 40 45
Ala Trp Phe Lys Arg Asn Thr Leu Asn Lys Pro Val Ile Met Gly Arg
50 55 60
His Thr Trp Glu Ser Ile Gly Arg Pro Leu Pro Gly Arg Lys Asn Ile
65 70 75 80
Ile Leu Ser Ser Gln Pro Ser Thr Asp Asp Arg Val Thr Trp Val Lys
85 90 95
Ser Val Asp Glu Ala Ile Ala Ala Cys Gly Asp Val Pro Glu Ile Met
100 105 110
Val Ile Gly Gly Gly Arg Val Ile Glu Gln Phe Leu Pro Lys Ala Gln
115 120 125
Lys Leu Tyr Leu Thr His Ile Asp Ala Glu Val Glu Gly Asp Thr His
130 135 140
Phe Pro Asp Tyr Glu Pro Asp Asp Trp Glu Ser Val Phe Ser Glu Phe
145 150 155 160
His Asp Ala Asp Ala Gln Asn Ser His Ser Tyr Cys Phe Glu Ile Leu
165 170 175
Glu Arg Arg Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Phe Pro Val Asp
180 185 190
Ala Thr Lys Arg Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser
195 200 205
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp
210 215 220
Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
225 230 235 240
Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala
245 250 255
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
260 265 270
Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn
275 280 285
Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly
290 295 300
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
305 310 315 320
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
325 330 335
Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val
340 345 350
Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val
355 360 365
Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg
370 375 380
Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu
385 390 395 400
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His
405 410 415
Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr
420 425 430
Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
435 440 445
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
450 455 460
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
465 470 475 480
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
485 490 495
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
500 505 510
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
515 520 525
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
530 535 540
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
545 550 555 560
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
565 570 575
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
580 585 590
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
595 600 605
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
610 615 620
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
625 630 635 640
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
645 650 655
Ala Leu Pro Pro Arg
660
<210> 66
<211> 1983
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 66
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccatctctc tgattgccgc tctggccgtg gactacgtga tcgggatgga aaacgctatg
120
ccatggaatc tgcccgccga tctggcttgg ttcaagagga acaccctgaa caagccagtg
180
atcatgggca gacacacttg ggagtccatt ggccggcccc tgcctggacg caagaacatc
240
attctgagct cccagccctc taccgacgac agggtgacat gggtgaaaag tgtggacgaa
300
gccattgccg cttgcggaga tgtgcccgag atcatggtca tcggcggagg gagagtgatc
360
gagcagttcc tgcctaaggc ccagaaactg tacctgactc acattgacgc tgaggtggaa
420
ggggacaccc attttcctga ttatgagcca gacgattggg aaagcgtgtt ctccgagttt
480
cacgacgccg atgctcagaa ctctcatagt tattgctttg agatcctgga aaggagatac
540
ccttatgatg ttcctgatta tgctttcccc gtggatgcta ctaaaagaga aattgtgatg
600
acccagtcac ccgccactct tagcctttca cccggtgagc gcgcaaccct gtcttgcaga
660
gcctcccaag acatctcaaa ataccttaat tggtatcaac agaagcccgg acaggctcct
720
cgccttctga tctaccacac cagccggctc cattctggaa tccctgccag gttcagcggt
780
agcggatctg ggaccgacta caccctcact atcagctcac tgcagccaga ggacttcgct
840
gtctatttct gtcagcaagg gaacaccctg ccctacacct ttggacaggg caccaagctc
900
gagattaaag gtggaggtgg cagcggagga ggtgggtccg gcggtggagg aagccaggtc
960
caactccaag aaagcggacc gggtcttgtg aagccatcag aaactctttc actgacttgt
1020
actgtgagcg gagtgtctct ccccgattac ggggtgtctt ggatcagaca gccaccgggg
1080
aagggtctgg aatggattgg agtgatttgg ggctctgaga ctacttacta ctcttcatcc
1140
ctcaagtcac gcgtcaccat ctcaaaggac aactctaaga atcaggtgtc actgaaactg
1200
tcatctgtga ccgcagccga caccgccgtg tactattgcg ctaagcatta ctattatggc
1260
gggagctacg caatggatta ctggggacag ggtactctgg tcaccgtgtc cagcaccact
1320
accccagcac cgaggccacc caccccggct cctaccatcg cctcccagcc tctgtccctg
1380
cgtccggagg catgtagacc cgcagctggt ggggccgtgc atacccgggg tcttgacttc
1440
gcctgcgata tctacatttg ggcccctctg gctggtactt gcggggtcct gctgctttca
1500
ctcgtgatca ctctttactg taagcgcggt cggaagaagc tgctgtacat ctttaagcaa
1560
cccttcatga ggcctgtgca gactactcaa gaggaggacg gctgttcatg ccggttccca
1620
gaggaggagg aaggcggctg cgaactgcgc gtgaaattca gccgcagcgc agatgctcca
1680
gcctacaagc aggggcagaa ccagctctac aacgaactca atcttggtcg gagagaggag
1740
tacgacgtgc tggacaagcg gagaggacgg gacccagaaa tgggcgggaa gccgcgcaga
1800
aagaatcccc aagagggcct gtacaacgag ctccaaaagg ataagatggc agaagcctat
1860
agcgagattg gtatgaaagg ggaacgcaga agaggcaaag gccacgacgg actgtaccag
1920
ggactcagca ccgccaccaa ggacacctat gacgctcttc acatgcaggc cctgccgcct
1980
cgg
1983
<210> 67
<211> 750
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 67
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Tyr Pro Tyr Asp
260 265 270
Val Pro Asp Tyr Ala Phe Pro Val Asp Arg Thr Lys Arg Glu Ile Val
275 280 285
Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
290 295 300
Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp
305 310 315 320
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr
325 330 335
Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
340 345 350
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
355 360 365
Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly
370 375 380
Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro
405 410 415
Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser
420 425 430
Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro
435 440 445
Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr
450 455 460
Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn
465 470 475 480
Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
485 490 495
Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr
500 505 510
Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr
515 520 525
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
530 535 540
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
545 550 555 560
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
565 570 575
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
580 585 590
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
595 600 605
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
610 615 620
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
625 630 635 640
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
645 650 655
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
660 665 670
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
675 680 685
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
690 695 700
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
705 710 715 720
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
725 730 735
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 68
<211> 2250
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 68
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actctaccct tatgatgttc ctgattatgc tttccccgtg
840
gatcgtacta aaagagaaat tgtgatgacc cagtcacccg ccactcttag cctttcaccc
900
ggtgagcgcg caaccctgtc ttgcagagcc tcccaagaca tctcaaaata ccttaattgg
960
tatcaacaga agcccggaca ggctcctcgc cttctgatct accacaccag ccggctccat
1020
tctggaatcc ctgccaggtt cagcggtagc ggatctggga ccgactacac cctcactatc
1080
agctcactgc agccagagga cttcgctgtc tatttctgtc agcaagggaa caccctgccc
1140
tacacctttg gacagggcac caagctcgag attaaaggtg gaggtggcag cggaggaggt
1200
gggtccggcg gtggaggaag ccaggtccaa ctccaagaaa gcggaccggg tcttgtgaag
1260
ccatcagaaa ctctttcact gacttgtact gtgagcggag tgtctctccc cgattacggg
1320
gtgtcttgga tcagacagcc accggggaag ggtctggaat ggattggagt gatttggggc
1380
tctgagacta cttactactc ttcatccctc aagtcacgcg tcaccatctc aaaggacaac
1440
tctaagaatc aggtgtcact gaaactgtca tctgtgaccg cagccgacac cgccgtgtac
1500
tattgcgcta agcattacta ttatggcggg agctacgcaa tggattactg gggacagggt
1560
actctggtca ccgtgtccag caccactacc ccagcaccga ggccacccac cccggctcct
1620
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
1680
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
1740
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1800
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1860
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1920
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1980
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
2040
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
2100
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
2160
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
2220
gctcttcaca tgcaggccct gccgcctcgg
2250
<210> 69
<211> 750
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 69
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Tyr Pro Tyr Asp
260 265 270
Val Pro Asp Tyr Ala Phe Pro Val Asp Ala Thr Lys Arg Glu Ile Val
275 280 285
Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
290 295 300
Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp
305 310 315 320
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr
325 330 335
Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
340 345 350
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
355 360 365
Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly
370 375 380
Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro
405 410 415
Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser
420 425 430
Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro
435 440 445
Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr
450 455 460
Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn
465 470 475 480
Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
485 490 495
Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr
500 505 510
Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr
515 520 525
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
530 535 540
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
545 550 555 560
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
565 570 575
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
580 585 590
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
595 600 605
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
610 615 620
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
625 630 635 640
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
645 650 655
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
660 665 670
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
675 680 685
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
690 695 700
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
705 710 715 720
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
725 730 735
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 70
<211> 2250
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 70
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actctaccct tatgatgttc ctgattatgc tttccccgtg
840
gatgctacta aaagagaaat tgtgatgacc cagtcacccg ccactcttag cctttcaccc
900
ggtgagcgcg caaccctgtc ttgcagagcc tcccaagaca tctcaaaata ccttaattgg
960
tatcaacaga agcccggaca ggctcctcgc cttctgatct accacaccag ccggctccat
1020
tctggaatcc ctgccaggtt cagcggtagc ggatctggga ccgactacac cctcactatc
1080
agctcactgc agccagagga cttcgctgtc tatttctgtc agcaagggaa caccctgccc
1140
tacacctttg gacagggcac caagctcgag attaaaggtg gaggtggcag cggaggaggt
1200
gggtccggcg gtggaggaag ccaggtccaa ctccaagaaa gcggaccggg tcttgtgaag
1260
ccatcagaaa ctctttcact gacttgtact gtgagcggag tgtctctccc cgattacggg
1320
gtgtcttgga tcagacagcc accggggaag ggtctggaat ggattggagt gatttggggc
1380
tctgagacta cttactactc ttcatccctc aagtcacgcg tcaccatctc aaaggacaac
1440
tctaagaatc aggtgtcact gaaactgtca tctgtgaccg cagccgacac cgccgtgtac
1500
tattgcgcta agcattacta ttatggcggg agctacgcaa tggattactg gggacagggt
1560
actctggtca ccgtgtccag caccactacc ccagcaccga ggccacccac cccggctcct
1620
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
1680
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
1740
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1800
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1860
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1920
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1980
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
2040
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
2100
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
2160
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
2220
gctcttcaca tgcaggccct gccgcctcgg
2250
<210> 71
<211> 606
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 71
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp
20 25 30
Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr
35 40 45
Gly Met Leu Glu Asp Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn
50 55 60
Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp
65 70 75 80
Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr
85 90 95
Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile
100 105 110
Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Pro Glu
115 120 125
Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Phe Pro Val Asp Glu Ile Val
130 135 140
Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr
180 185 190
Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly
245 250 255
Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro
260 265 270
Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser
275 280 285
Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro
290 295 300
Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr
305 310 315 320
Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn
325 330 335
Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
340 345 350
Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr
355 360 365
Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr
370 375 380
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
385 390 395 400
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
405 410 415
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
420 425 430
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
435 440 445
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
450 455 460
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
465 470 475 480
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
485 490 495
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
500 505 510
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
515 520 525
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
530 535 540
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
545 550 555 560
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
565 570 575
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
580 585 590
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
595 600 605
<210> 72
<211> 1818
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 72
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccggagtgc aggtggaaac catctcccca ggagacgggc gcaccttccc caagcgcggc
120
cagacctgtg tggtgcacta caccgggatg cttgaagatg gaaagaaagt cgattcctcc
180
cgggacagaa acaagccctt taagtttatg ctaggcaagc aggaggtgat ccgaggctgg
240
gaagaagggg ttgcccagat gagtgtgggt cagagagcca aactgactat atctccagat
300
tatgcctatg gtgccactgg gcacccaggc atcatcccac cacatgccac tctcgtcttc
360
gatgtggagc ttctaaaacc ggaataccct tatgatgttc ctgattatgc tttccccgtg
420
gatgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
480
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
540
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
600
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
660
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
720
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
780
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
840
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
900
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
960
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1020
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1080
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1140
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1200
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1260
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1320
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1380
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1440
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1500
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1560
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1620
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1680
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1740
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1800
caggccctgc cgcctcgg
1818
<210> 73
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 73
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Tyr Pro Tyr Asp
260 265 270
Val Pro Asp Tyr Ala Phe Pro Val Asp Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 74
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 74
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actctaccct tatgatgttc ctgattatgc tttccccgtg
840
gatgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 75
<211> 737
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 75
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
275 280 285
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
290 295 300
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
305 310 315 320
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
325 330 335
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
340 345 350
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
355 360 365
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
370 375 380
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
385 390 395 400
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
405 410 415
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
420 425 430
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
435 440 445
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
450 455 460
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
465 470 475 480
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
485 490 495
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
500 505 510
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
515 520 525
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
530 535 540
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
545 550 555 560
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
565 570 575
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
580 585 590
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
595 600 605
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
610 615 620
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
625 630 635 640
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
645 650 655
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
660 665 670
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
675 680 685
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
690 695 700
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
705 710 715 720
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
725 730 735
Arg
<210> 76
<211> 2211
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 76
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaagagaaa ttgtgatgac ccagtcaccc
840
gccactctta gcctttcacc cggtgagcgc gcaaccctgt cttgcagagc ctcccaagac
900
atctcaaaat accttaattg gtatcaacag aagcccggac aggctcctcg ccttctgatc
960
taccacacca gccggctcca ttctggaatc cctgccaggt tcagcggtag cggatctggg
1020
accgactaca ccctcactat cagctcactg cagccagagg acttcgctgt ctatttctgt
1080
cagcaaggga acaccctgcc ctacaccttt ggacagggca ccaagctcga gattaaaggt
1140
ggaggtggca gcggaggagg tgggtccggc ggtggaggaa gccaggtcca actccaagaa
1200
agcggaccgg gtcttgtgaa gccatcagaa actctttcac tgacttgtac tgtgagcgga
1260
gtgtctctcc ccgattacgg ggtgtcttgg atcagacagc caccggggaa gggtctggaa
1320
tggattggag tgatttgggg ctctgagact acttactact cttcatccct caagtcacgc
1380
gtcaccatct caaaggacaa ctctaagaat caggtgtcac tgaaactgtc atctgtgacc
1440
gcagccgaca ccgccgtgta ctattgcgct aagcattact attatggcgg gagctacgca
1500
atggattact ggggacaggg tactctggtc accgtgtcca gcaccactac cccagcaccg
1560
aggccaccca ccccggctcc taccatcgcc tcccagcctc tgtccctgcg tccggaggca
1620
tgtagacccg cagctggtgg ggccgtgcat acccggggtc ttgacttcgc ctgcgatatc
1680
tacatttggg cccctctggc tggtacttgc ggggtcctgc tgctttcact cgtgatcact
1740
ctttactgta agcgcggtcg gaagaagctg ctgtacatct ttaagcaacc cttcatgagg
1800
cctgtgcaga ctactcaaga ggaggacggc tgttcatgcc ggttcccaga ggaggaggaa
1860
ggcggctgcg aactgcgcgt gaaattcagc cgcagcgcag atgctccagc ctacaagcag
1920
gggcagaacc agctctacaa cgaactcaat cttggtcgga gagaggagta cgacgtgctg
1980
gacaagcgga gaggacggga cccagaaatg ggcgggaagc cgcgcagaaa gaatccccaa
2040
gagggcctgt acaacgagct ccaaaaggat aagatggcag aagcctatag cgagattggt
2100
atgaaagggg aacgcagaag aggcaaaggc cacgacggac tgtaccaggg actcagcacc
2160
gccaccaagg acacctatga cgctcttcac atgcaggccc tgccgcctcg g
2211
<210> 77
<211> 733
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 77
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Glu Ile Val Met
260 265 270
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
275 280 285
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
290 295 300
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
305 310 315 320
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
325 330 335
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
340 345 350
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
355 360 365
Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly
370 375 380
Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly
385 390 395 400
Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly
405 410 415
Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly
420 425 430
Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr
435 440 445
Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser
450 455 460
Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
465 470 475 480
Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala
485 490 495
Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr
500 505 510
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
515 520 525
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
530 535 540
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
545 550 555 560
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
565 570 575
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
580 585 590
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
595 600 605
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
610 615 620
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
625 630 635 640
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
645 650 655
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
660 665 670
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
675 680 685
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
690 695 700
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
705 710 715 720
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
725 730
<210> 78
<211> 2199
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 78
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgaaatt gtgatgaccc agtcacccgc cactcttagc
840
ctttcacccg gtgagcgcgc aaccctgtct tgcagagcct cccaagacat ctcaaaatac
900
cttaattggt atcaacagaa gcccggacag gctcctcgcc ttctgatcta ccacaccagc
960
cggctccatt ctggaatccc tgccaggttc agcggtagcg gatctgggac cgactacacc
1020
ctcactatca gctcactgca gccagaggac ttcgctgtct atttctgtca gcaagggaac
1080
accctgccct acacctttgg acagggcacc aagctcgaga ttaaaggtgg aggtggcagc
1140
ggaggaggtg ggtccggcgg tggaggaagc caggtccaac tccaagaaag cggaccgggt
1200
cttgtgaagc catcagaaac tctttcactg acttgtactg tgagcggagt gtctctcccc
1260
gattacgggg tgtcttggat cagacagcca ccggggaagg gtctggaatg gattggagtg
1320
atttggggct ctgagactac ttactactct tcatccctca agtcacgcgt caccatctca
1380
aaggacaact ctaagaatca ggtgtcactg aaactgtcat ctgtgaccgc agccgacacc
1440
gccgtgtact attgcgctaa gcattactat tatggcggga gctacgcaat ggattactgg
1500
ggacagggta ctctggtcac cgtgtccagc accactaccc cagcaccgag gccacccacc
1560
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1620
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1680
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1740
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1800
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1860
ctgcgcgtga aattcagccg cagcgcagat gctccagcct acaagcaggg gcagaaccag
1920
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
1980
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2040
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2100
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2160
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2199
<210> 79
<400> 79
000
<210> 80
<400> 80
000
<210> 81
<400> 81
000
<210> 82
<211> 5000
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(5000)
<223> /примечание="Данная последовательность может включать 100-5000
нуклеотидов"
<220>
<221> источник
<223> /примечание="Смотри спецификацию поданной заявки для подробного
описания
замен и предпочтительных вариантов осуществления"
<400> 82
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
60
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
1980
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2040
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2100
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2160
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2220
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2280
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2340
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2400
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2460
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2520
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2580
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2640
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2700
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2760
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2820
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2880
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
2940
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3000
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3060
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3420
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3480
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3540
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3600
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3660
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3720
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3780
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3840
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
3960
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4020
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4080
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4140
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4200
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4260
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4320
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4380
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4440
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4500
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4560
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4620
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4680
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4740
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4800
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4860
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4920
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
4980
aaaaaaaaaa aaaaaaaaaa
5000
<210> 83
<400> 83
000
<210> 84
<400> 84
000
<210> 85
<400> 85
000
<210> 86
<400> 86
000
<210> 87
<400> 87
000
<210> 88
<400> 88
000
<210> 89
<400> 89
000
<210> 90
<400> 90
000
<210> 91
<400> 91
000
<210> 92
<400> 92
000
<210> 93
<400> 93
000
<210> 94
<400> 94
000
<210> 95
<400> 95
000
<210> 96
<400> 96
000
<210> 97
<400> 97
000
<210> 98
<400> 98
000
<210> 99
<400> 99
000
<210> 100
<400> 100
000
<210> 101
<400> 101
000
<210> 102
<400> 102
000
<210> 103
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 103
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Ser Leu Asn Leu
260 265 270
Thr Glu Ser His Asn Ser Arg Lys Lys Arg Glu Ile Val Met Thr Gln
275 280 285
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
290 295 300
Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln
305 310 315 320
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu
325 330 335
His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
340 345 350
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr
355 360 365
Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr
370 375 380
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
405 410 415
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
420 425 430
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
435 440 445
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
450 455 460
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
465 470 475 480
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
485 490 495
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 104
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 104
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcagtctc aatttgactg agtcacacaa ttccaggaag
840
aaaagggaaa ttgtgatgac ccagtcaccc gccactctta gcctttcacc cggtgagcgc
900
gcaaccctgt cttgcagagc ctcccaagac atctcaaaat accttaattg gtatcaacag
960
aagcccggac aggctcctcg ccttctgatc taccacacca gccggctcca ttctggaatc
1020
cctgccaggt tcagcggtag cggatctggg accgactaca ccctcactat cagctcactg
1080
cagccagagg acttcgctgt ctatttctgt cagcaaggga acaccctgcc ctacaccttt
1140
ggacagggca ccaagctcga gattaaaggt ggaggtggca gcggaggagg tgggtccggc
1200
ggtggaggaa gccaggtcca actccaagaa agcggaccgg gtcttgtgaa gccatcagaa
1260
actctttcac tgacttgtac tgtgagcgga gtgtctctcc ccgattacgg ggtgtcttgg
1320
atcagacagc caccggggaa gggtctggaa tggattggag tgatttgggg ctctgagact
1380
acttactact cttcatccct caagtcacgc gtcaccatct caaaggacaa ctctaagaat
1440
caggtgtcac tgaaactgtc atctgtgacc gcagccgaca ccgccgtgta ctattgcgct
1500
aagcattact attatggcgg gagctacgca atggattact ggggacaggg tactctggtc
1560
accgtgtcca gcaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 105
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 105
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln
275 280 285
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
290 295 300
Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln
305 310 315 320
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu
325 330 335
His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
340 345 350
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr
355 360 365
Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr
370 375 380
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
405 410 415
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
420 425 430
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
435 440 445
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
450 455 460
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
465 470 475 480
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
485 490 495
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 106
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 106
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgagg atccacgacc cagcagaaag
840
cgacgggaaa ttgtgatgac ccagtcaccc gccactctta gcctttcacc cggtgagcgc
900
gcaaccctgt cttgcagagc ctcccaagac atctcaaaat accttaattg gtatcaacag
960
aagcccggac aggctcctcg ccttctgatc taccacacca gccggctcca ttctggaatc
1020
cctgccaggt tcagcggtag cggatctggg accgactaca ccctcactat cagctcactg
1080
cagccagagg acttcgctgt ctatttctgt cagcaaggga acaccctgcc ctacaccttt
1140
ggacagggca ccaagctcga gattaaaggt ggaggtggca gcggaggagg tgggtccggc
1200
ggtggaggaa gccaggtcca actccaagaa agcggaccgg gtcttgtgaa gccatcagaa
1260
actctttcac tgacttgtac tgtgagcgga gtgtctctcc ccgattacgg ggtgtcttgg
1320
atcagacagc caccggggaa gggtctggaa tggattggag tgatttgggg ctctgagact
1380
acttactact cttcatccct caagtcacgc gtcaccatct caaaggacaa ctctaagaat
1440
caggtgtcac tgaaactgtc atctgtgacc gcagccgaca ccgccgtgta ctattgcgct
1500
aagcattact attatggcgg gagctacgca atggattact ggggacaggg tactctggtc
1560
accgtgtcca gcaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 107
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 107
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Cys Lys Ile Asn
260 265 270
Gly Tyr Pro Lys Arg Gly Arg Lys Arg Arg Glu Ile Val Met Thr Gln
275 280 285
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
290 295 300
Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln
305 310 315 320
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu
325 330 335
His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
340 345 350
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr
355 360 365
Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr
370 375 380
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
405 410 415
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
420 425 430
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
435 440 445
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
450 455 460
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
465 470 475 480
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
485 490 495
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 108
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 108
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actctgcaag atcaacggct accctaagag gggcagaaag
840
cggcgggaaa ttgtgatgac ccagtcaccc gccactctta gcctttcacc cggtgagcgc
900
gcaaccctgt cttgcagagc ctcccaagac atctcaaaat accttaattg gtatcaacag
960
aagcccggac aggctcctcg ccttctgatc taccacacca gccggctcca ttctggaatc
1020
cctgccaggt tcagcggtag cggatctggg accgactaca ccctcactat cagctcactg
1080
cagccagagg acttcgctgt ctatttctgt cagcaaggga acaccctgcc ctacaccttt
1140
ggacagggca ccaagctcga gattaaaggt ggaggtggca gcggaggagg tgggtccggc
1200
ggtggaggaa gccaggtcca actccaagaa agcggaccgg gtcttgtgaa gccatcagaa
1260
actctttcac tgacttgtac tgtgagcgga gtgtctctcc ccgattacgg ggtgtcttgg
1320
atcagacagc caccggggaa gggtctggaa tggattggag tgatttgggg ctctgagact
1380
acttactact cttcatccct caagtcacgc gtcaccatct caaaggacaa ctctaagaat
1440
caggtgtcac tgaaactgtc atctgtgacc gcagccgaca ccgccgtgta ctattgcgct
1500
aagcattact attatggcgg gagctacgca atggattact ggggacaggg tactctggtc
1560
accgtgtcca gcaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 109
<211> 748
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 109
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Leu Gln Trp Leu
260 265 270
Glu Gln Gln Val Ala Lys Arg Arg Thr Lys Arg Glu Ile Val Met Thr
275 280 285
Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
290 295 300
Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln
305 310 315 320
Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg
325 330 335
Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr
340 345 350
Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val
355 360 365
Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly
370 375 380
Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
405 410 415
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
420 425 430
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
435 440 445
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
450 455 460
Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
465 470 475 480
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
485 490 495
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
500 505 510
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr
515 520 525
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
530 535 540
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
545 550 555 560
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
565 570 575
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
580 585 590
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
595 600 605
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
610 615 620
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
625 630 635 640
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
645 650 655
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
660 665 670
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
675 680 685
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
690 695 700
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
705 710 715 720
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
725 730 735
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 110
<211> 2244
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 110
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcctgcaa tggctggagc agcaggtggc gaagcggaga
840
actaagcggg aaattgtgat gacccagtca cccgccactc ttagcctttc acccggtgag
900
cgcgcaaccc tgtcttgcag agcctcccaa gacatctcaa aataccttaa ttggtatcaa
960
cagaagcccg gacaggctcc tcgccttctg atctaccaca ccagccggct ccattctgga
1020
atccctgcca ggttcagcgg tagcggatct gggaccgact acaccctcac tatcagctca
1080
ctgcagccag aggacttcgc tgtctatttc tgtcagcaag ggaacaccct gccctacacc
1140
tttggacagg gcaccaagct cgagattaaa ggtggaggtg gcagcggagg aggtgggtcc
1200
ggcggtggag gaagccaggt ccaactccaa gaaagcggac cgggtcttgt gaagccatca
1260
gaaactcttt cactgacttg tactgtgagc ggagtgtctc tccccgatta cggggtgtct
1320
tggatcagac agccaccggg gaagggtctg gaatggattg gagtgatttg gggctctgag
1380
actacttact actcttcatc cctcaagtca cgcgtcacca tctcaaagga caactctaag
1440
aatcaggtgt cactgaaact gtcatctgtg accgcagccg acaccgccgt gtactattgc
1500
gctaagcatt actattatgg cgggagctac gcaatggatt actggggaca gggtactctg
1560
gtcaccgtgt ccagcaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
1620
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
1680
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
1740
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1800
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1860
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1920
agccgcagcg cagatgctcc agcctacaag caggggcaga accagctcta caacgaactc
1980
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
2040
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
2100
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
2160
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
2220
cacatgcagg ccctgccgcc tcgg
2244
<210> 111
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 111
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 112
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 112
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtgaaatt gtgatgaccc agtcacccgc cactcttagc
900
ctttcacccg gtgagcgcgc aaccctgtct tgcagagcct cccaagacat ctcaaaatac
960
cttaattggt atcaacagaa gcccggacag gctcctcgcc ttctgatcta ccacaccagc
1020
cggctccatt ctggaatccc tgccaggttc agcggtagcg gatctgggac cgactacacc
1080
ctcactatca gctcactgca gccagaggac ttcgctgtct atttctgtca gcaagggaac
1140
accctgccct acacctttgg acagggcacc aagctcgaga ttaaaggtgg aggtggcagc
1200
ggaggaggtg ggtccggcgg tggaggaagc caggtccaac tccaagaaag cggaccgggt
1260
cttgtgaagc catcagaaac tctttcactg acttgtactg tgagcggagt gtctctcccc
1320
gattacgggg tgtcttggat cagacagcca ccggggaagg gtctggaatg gattggagtg
1380
atttggggct ctgagactac ttactactct tcatccctca agtcacgcgt caccatctca
1440
aaggacaact ctaagaatca ggtgtcactg aaactgtcat ctgtgaccgc agccgacacc
1500
gccgtgtact attgcgctaa gcattactat tatggcggga gctacgcaat ggattactgg
1560
ggacagggta ctctggtcac cgtgtccagc accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct acaagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 113
<211> 751
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 113
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Gly Glu Ile
275 280 285
Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
290 295 300
Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
305 310 315 320
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His
325 330 335
Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly
340 345 350
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
355 360 365
Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe
370 375 380
Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
405 410 415
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
420 425 430
Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro
435 440 445
Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr
450 455 460
Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp
465 470 475 480
Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala
485 490 495
Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser
500 505 510
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
515 520 525
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
530 535 540
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
545 550 555 560
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
565 570 575
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
580 585 590
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
595 600 605
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
610 615 620
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
625 630 635 640
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
645 650 655
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
660 665 670
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
675 680 685
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
690 695 700
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
705 710 715 720
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
725 730 735
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 114
<211> 2253
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 114
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggcaca ggtgccgagg accctcggcc aagccgcaaa
840
aggaggtcac ttggcggcga aattgtgatg acccagtcac ccgccactct tagcctttca
900
cccggtgagc gcgcaaccct gtcttgcaga gcctcccaag acatctcaaa ataccttaat
960
tggtatcaac agaagcccgg acaggctcct cgccttctga tctaccacac cagccggctc
1020
cattctggaa tccctgccag gttcagcggt agcggatctg ggaccgacta caccctcact
1080
atcagctcac tgcagccaga ggacttcgct gtctatttct gtcagcaagg gaacaccctg
1140
ccctacacct ttggacaggg caccaagctc gagattaaag gtggaggtgg cagcggagga
1200
ggtgggtccg gcggtggagg aagccaggtc caactccaag aaagcggacc gggtcttgtg
1260
aagccatcag aaactctttc actgacttgt actgtgagcg gagtgtctct ccccgattac
1320
ggggtgtctt ggatcagaca gccaccgggg aagggtctgg aatggattgg agtgatttgg
1380
ggctctgaga ctacttacta ctcttcatcc ctcaagtcac gcgtcaccat ctcaaaggac
1440
aactctaaga atcaggtgtc actgaaactg tcatctgtga ccgcagccga caccgccgtg
1500
tactattgcg ctaagcatta ctattatggc gggagctacg caatggatta ctggggacag
1560
ggtactctgg tcaccgtgtc cagcaccact accccagcac cgaggccacc caccccggct
1620
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
1680
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
1740
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1800
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1860
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1920
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1980
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
2040
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
2100
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
2160
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
2220
gacgctcttc acatgcaggc cctgccgcct cgg
2253
<210> 115
<211> 750
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 115
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Glu Ile Val
275 280 285
Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
290 295 300
Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp
305 310 315 320
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr
325 330 335
Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser
340 345 350
Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
355 360 365
Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly
370 375 380
Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro
405 410 415
Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser
420 425 430
Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro
435 440 445
Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr
450 455 460
Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn
465 470 475 480
Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
485 490 495
Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr
500 505 510
Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr
515 520 525
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
530 535 540
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
545 550 555 560
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
565 570 575
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
580 585 590
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
595 600 605
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
610 615 620
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
625 630 635 640
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
645 650 655
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
660 665 670
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
675 680 685
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
690 695 700
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
705 710 715 720
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
725 730 735
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 116
<211> 2250
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 116
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggagcagaag atcccagacc aagccggaaa
840
aggcggtccc tgggtgaaat tgtgatgacc cagtcacccg ccactcttag cctttcaccc
900
ggtgagcgcg caaccctgtc ttgcagagcc tcccaagaca tctcaaaata ccttaattgg
960
tatcaacaga agcccggaca ggctcctcgc cttctgatct accacaccag ccggctccat
1020
tctggaatcc ctgccaggtt cagcggtagc ggatctggga ccgactacac cctcactatc
1080
agctcactgc agccagagga cttcgctgtc tatttctgtc agcaagggaa caccctgccc
1140
tacacctttg gacagggcac caagctcgag attaaaggtg gaggtggcag cggaggaggt
1200
gggtccggcg gtggaggaag ccaggtccaa ctccaagaaa gcggaccggg tcttgtgaag
1260
ccatcagaaa ctctttcact gacttgtact gtgagcggag tgtctctccc cgattacggg
1320
gtgtcttgga tcagacagcc accggggaag ggtctggaat ggattggagt gatttggggc
1380
tctgagacta cttactactc ttcatccctc aagtcacgcg tcaccatctc aaaggacaac
1440
tctaagaatc aggtgtcact gaaactgtca tctgtgaccg cagccgacac cgccgtgtac
1500
tattgcgcta agcattacta ttatggcggg agctacgcaa tggattactg gggacagggt
1560
actctggtca ccgtgtccag caccactacc ccagcaccga ggccacccac cccggctcct
1620
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
1680
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
1740
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1800
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1860
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1920
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1980
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
2040
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
2100
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
2160
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
2220
gctcttcaca tgcaggccct gccgcctcgg
2250
<210> 117
<400> 117
000
<210> 118
<211> 126
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 118
aagcgcggtc ggaagaagct gctgtacatc tttaagcaac ccttcatgag gcctgtgcag
60
actactcaag aggaggacgg ctgttcatgc cggttcccag aggaggagga aggcggctgc
120
gaactg
126
<210> 119
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 119
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
60
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
120
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
180
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
240
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
300
tatgacgctc ttcacatgca ggccctgccg cctcgg
336
<210> 120
<211> 35
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 120
Thr Lys Lys Lys Tyr Ser Ser Ser Val His Asp Pro Asn Gly Glu Tyr
1 5 10 15
Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser Arg Leu Thr Asp
20 25 30
Val Thr Leu
35
<210> 121
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 121
Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met Val Ser Ala Leu Leu
1 5 10 15
Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr Asp Pro Thr Arg Pro
20 25 30
Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr Asn Leu Ala Asp Arg
35 40 45
Glu Leu Val His Met Ile Asn Trp Ala Lys Arg Val Pro Gly Phe Val
50 55 60
Asp Leu Thr Leu His Asp Gln Val His Leu Leu Glu Cys Ala Trp Met
65 70 75 80
Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser Met Glu His Pro Gly
85 90 95
Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp Arg Asn Gln Gly Lys
100 105 110
Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met Leu Leu Ala Thr Ser
115 120 125
Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu Phe Val Cys Leu
130 135 140
Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr Phe Leu Ser Ser
145 150 155 160
Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His Arg Val Leu Asp
165 170 175
Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys Ala Gly Leu Thr
180 185 190
Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser
195 200 205
His Ile Arg His Met Ser Asn Lys Arg Met Glu His Leu Tyr Ser Met
210 215 220
Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu Leu Leu Glu Met Leu
225 230 235 240
Asp Ala His Arg Leu
245
<210> 122
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 122
tcgttggcac tttccctgac tgccgaccag atggtgtccg cccttctgga cgccgagcct
60
ccaattctgt actcggagta cgatccgact cgcccgttct ccgaagccag catgatgggc
120
ctgttgacta acctggcgga ccgcgagttg gtgcacatga ttaactgggc taagcgggtg
180
ccgggcttcg tggacctgac cctgcacgac caagtgcacc tcctggaatg cgcctggatg
240
gaaatcctca tgatcggcct cgtgtggaga tccatggagc atcccggaaa gctcctgttt
300
gcacccaacc tcctgcttga tcgcaaccag ggaaaatgcg tggaaggggg tgtcgagatt
360
ttcgacatgc tgctcgccac ctcttcccgg ttccggatga tgaatctgca gggagaagag
420
ttcgtgtgtc tgaagtcaat catcctgctg aactccgggg tctatacctt cctgagctcg
480
accctcaagt cactggagga aaaagaccac atccatcgcg tgctcgataa gatcaccgac
540
acccttatcc atctcatggc gaaggctgga ctgaccctgc aacagcagca ccagaggctg
600
gcccagttgc tgctgattct gagccacatc cggcacatgt cgaacaagag gatggaacac
660
ctgtacagca tgaagtgcaa gaacgtcgtg cctctgtccg atctgctcct ggaaatgctg
720
gacgcgcaca gactc
735
<210> 123
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 123
Arg Thr Lys Arg
1
<210> 124
<211> 41
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 124
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 125
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 125
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu
1 5 10 15
Gly Asp Val Gly
20
<210> 126
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 126
ggaaccggcg cggaagaccc ccggccctcc aggaagcgaa ggtccctcgg agacgtgggt
60
<210> 127
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 127
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg
1 5 10
<210> 128
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 128
ggaaccggcg cggaagaccc ccggccctcc aggaagcgaa gg
42
<210> 129
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 129
Leu Gln Trp Leu Glu Gln Gln Val Ala Lys Arg Arg Thr Lys Arg
1 5 10 15
<210> 130
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 130
ctgcaatggc tggagcagca ggtggcgaag cggagaacta agcgg
45
<210> 131
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 131
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu
1 5 10 15
Gly Gly
<210> 132
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 132
ggcacaggtg ccgaggaccc tcggccaagc cgcaaaagga ggtcacttgg cggc
54
<210> 133
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 133
Gly Thr Gly Ala Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu
1 5 10 15
Gly
<210> 134
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 134
ggaaccggag cagaagatcc cagaccaagc cggaaaaggc ggtccctggg t
51
<210> 135
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 135
Ser Leu Asn Leu Thr Glu Ser His Asn Ser Arg Lys Lys Arg
1 5 10
<210> 136
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 136
agtctcaatt tgactgagtc acacaattcc aggaagaaaa gg
42
<210> 137
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 137
Cys Lys Ile Asn Gly Tyr Pro Lys Arg Gly Arg Lys Arg Arg
1 5 10
<210> 138
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 138
tgcaagatca acggctaccc taagaggggc agaaagcggc gg
42
<210> 139
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 139
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 140
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 140
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccc
63
<210> 141
<211> 737
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 141
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
275 280 285
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
290 295 300
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
305 310 315 320
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
325 330 335
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
340 345 350
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
355 360 365
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
370 375 380
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
385 390 395 400
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
405 410 415
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
420 425 430
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
435 440 445
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
450 455 460
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
465 470 475 480
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
485 490 495
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
500 505 510
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
515 520 525
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
530 535 540
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
545 550 555 560
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
565 570 575
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
580 585 590
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
595 600 605
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
610 615 620
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
625 630 635 640
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
645 650 655
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
660 665 670
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
675 680 685
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
690 695 700
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
705 710 715 720
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
725 730 735
Arg
<210> 142
<211> 2211
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 142
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaagagaaa ttgtgatgac ccagtcaccc
840
gccactctta gcctttcacc cggtgagcgc gcaaccctgt cttgcagagc ctcccaagac
900
atctcaaaat accttaattg gtatcaacag aagcccggac aggctcctcg ccttctgatc
960
taccacacca gccggctcca ttctggaatc cctgccaggt tcagcggtag cggatctggg
1020
accgactaca ccctcactat cagctcactg cagccagagg acttcgctgt ctatttctgt
1080
cagcaaggga acaccctgcc ctacaccttt ggacagggca ccaagctcga gattaaaggt
1140
ggaggtggca gcggaggagg tgggtccggc ggtggaggaa gccaggtcca actccaagaa
1200
agcggaccgg gtcttgtgaa gccatcagaa actctttcac tgacttgtac tgtgagcgga
1260
gtgtctctcc ccgattacgg ggtgtcttgg atcagacagc caccggggaa gggtctggaa
1320
tggattggag tgatttgggg ctctgagact acttactact cttcatccct caagtcacgc
1380
gtcaccatct caaaggacaa ctctaagaat caggtgtcac tgaaactgtc atctgtgacc
1440
gcagccgaca ccgccgtgta ctattgcgct aagcattact attatggcgg gagctacgca
1500
atggattact ggggacaggg tactctggtc accgtgtcca gcaccactac cccagcaccg
1560
aggccaccca ccccggctcc taccatcgcc tcccagcctc tgtccctgcg tccggaggca
1620
tgtagacccg cagctggtgg ggccgtgcat acccggggtc ttgacttcgc ctgcgatatc
1680
tacatttggg cccctctggc tggtacttgc ggggtcctgc tgctttcact cgtgatcact
1740
ctttactgta agcgcggtcg gaagaagctg ctgtacatct ttaagcaacc cttcatgagg
1800
cctgtgcaga ctactcaaga ggaggacggc tgttcatgcc ggttcccaga ggaggaggaa
1860
ggcggctgcg aactgcgcgt gaaattcagc cgcagcgcag atgctccagc ctacaagcag
1920
gggcagaacc agctctacaa cgaactcaat cttggtcgga gagaggagta cgacgtgctg
1980
gacaagcgga gaggacggga cccagaaatg ggcgggaagc cgcgcagaaa gaatccccaa
2040
gagggcctgt acaacgagct ccaaaaggat aagatggcag aagcctatag cgagattggt
2100
atgaaagggg aacgcagaag aggcaaaggc cacgacggac tgtaccaggg actcagcacc
2160
gccaccaagg acacctatga cgctcttcac atgcaggccc tgccgcctcg g
2211
<210> 143
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 143
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 144
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 144
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtgaaatt gtgatgaccc agtcacccgc cactcttagc
900
ctttcacccg gtgagcgcgc aaccctgtct tgcagagcct cccaagacat ctcaaaatac
960
cttaattggt atcaacagaa gcccggacag gctcctcgcc ttctgatcta ccacaccagc
1020
cggctccatt ctggaatccc tgccaggttc agcggtagcg gatctgggac cgactacacc
1080
ctcactatca gctcactgca gccagaggac ttcgctgtct atttctgtca gcaagggaac
1140
accctgccct acacctttgg acagggcacc aagctcgaga ttaaaggtgg aggtggcagc
1200
ggaggaggtg ggtccggcgg tggaggaagc caggtccaac tccaagaaag cggaccgggt
1260
cttgtgaagc catcagaaac tctttcactg acttgtactg tgagcggagt gtctctcccc
1320
gattacgggg tgtcttggat cagacagcca ccggggaagg gtctggaatg gattggagtg
1380
atttggggct ctgagactac ttactactct tcatccctca agtcacgcgt caccatctca
1440
aaggacaact ctaagaatca ggtgtcactg aaactgtcat ctgtgaccgc agccgacacc
1500
gccgtgtact attgcgctaa gcattactat tatggcggga gctacgcaat ggattactgg
1560
ggacagggta ctctggtcac cgtgtccagc accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct acaagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 145
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 145
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 146
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 146
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtgaaatt gtgatgaccc agtcacccgc cactcttagc
900
ctttcacccg gtgagcgcgc aaccctgtct tgcagagcct cccaagacat ctcaaaatac
960
cttaattggt atcaacagaa gcccggacag gctcctcgcc ttctgatcta ccacaccagc
1020
cggctccatt ctggaatccc tgccaggttc agcggtagcg gatctgggac cgactacacc
1080
ctcactatca gctcactgca gccagaggac ttcgctgtct atttctgtca gcaagggaac
1140
accctgccct acacctttgg acagggcacc aagctcgaga ttaaaggtgg aggtggcagc
1200
ggaggaggtg ggtccggcgg tggaggaagc caggtccaac tccaagaaag cggaccgggt
1260
cttgtgaagc catcagaaac tctttcactg acttgtactg tgagcggagt gtctctcccc
1320
gattacgggg tgtcttggat cagacagcca ccggggaagg gtctggaatg gattggagtg
1380
atttggggct ctgagactac ttactactct tcatccctca agtcacgcgt caccatctca
1440
aaggacaact ctaagaatca ggtgtcactg aaactgtcat ctgtgaccgc agccgacacc
1500
gccgtgtact attgcgctaa gcattactat tatggcggga gctacgcaat ggattactgg
1560
ggacagggta ctctggtcac cgtgtccagc accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 147
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 147
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln
275 280 285
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
290 295 300
Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln
305 310 315 320
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu
325 330 335
His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
340 345 350
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr
355 360 365
Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr
370 375 380
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
405 410 415
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
420 425 430
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
435 440 445
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
450 455 460
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
465 470 475 480
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
485 490 495
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 148
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 148
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgaag atccacgacc cagcagaaag
840
cgacgggaaa ttgtgatgac ccagtcaccc gccactctta gcctttcacc cggtgagcgc
900
gcaaccctgt cttgcagagc ctcccaagac atctcaaaat accttaattg gtatcaacag
960
aagcccggac aggctcctcg ccttctgatc taccacacca gccggctcca ttctggaatc
1020
cctgccaggt tcagcggtag cggatctggg accgactaca ccctcactat cagctcactg
1080
cagccagagg acttcgctgt ctatttctgt cagcaaggga acaccctgcc ctacaccttt
1140
ggacagggca ccaagctcga gattaaaggt ggaggtggca gcggaggagg tgggtccggc
1200
ggtggaggaa gccaggtcca actccaagaa agcggaccgg gtcttgtgaa gccatcagaa
1260
actctttcac tgacttgtac tgtgagcgga gtgtctctcc ccgattacgg ggtgtcttgg
1320
atcagacagc caccggggaa gggtctggaa tggattggag tgatttgggg ctctgagact
1380
acttactact cttcatccct caagtcacgc gtcaccatct caaaggacaa ctctaagaat
1440
caggtgtcac tgaaactgtc atctgtgacc gcagccgaca ccgccgtgta ctattgcgct
1500
aagcattact attatggcgg gagctacgca atggattact ggggacaggg tactctggtc
1560
accgtgtcca gcaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 149
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 149
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln
275 280 285
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
290 295 300
Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln
305 310 315 320
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu
325 330 335
His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
340 345 350
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr
355 360 365
Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr
370 375 380
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
405 410 415
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
420 425 430
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
435 440 445
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
450 455 460
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
465 470 475 480
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
485 490 495
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 150
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 150
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgaag atccacgacc cagcagaaag
840
cgacgggaaa ttgtgatgac ccagtcaccc gccactctta gcctttcacc cggtgagcgc
900
gcaaccctgt cttgcagagc ctcccaagac atctcaaaat accttaattg gtatcaacag
960
aagcccggac aggctcctcg ccttctgatc taccacacca gccggctcca ttctggaatc
1020
cctgccaggt tcagcggtag cggatctggg accgactaca ccctcactat cagctcactg
1080
cagccagagg acttcgctgt ctatttctgt cagcaaggga acaccctgcc ctacaccttt
1140
ggacagggca ccaagctcga gattaaaggt ggaggtggca gcggaggagg tgggtccggc
1200
ggtggaggaa gccaggtcca actccaagaa agcggaccgg gtcttgtgaa gccatcagaa
1260
actctttcac tgacttgtac tgtgagcgga gtgtctctcc ccgattacgg ggtgtcttgg
1320
atcagacagc caccggggaa gggtctggaa tggattggag tgatttgggg ctctgagact
1380
acttactact cttcatccct caagtcacgc gtcaccatct caaaggacaa ctctaagaat
1440
caggtgtcac tgaaactgtc atctgtgacc gcagccgaca ccgccgtgta ctattgcgct
1500
aagcattact attatggcgg gagctacgca atggattact ggggacaggg tactctggtc
1560
accgtgtcca gcaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 151
<211> 737
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 151
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
275 280 285
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
290 295 300
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
305 310 315 320
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
325 330 335
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
340 345 350
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
355 360 365
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
370 375 380
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
385 390 395 400
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
405 410 415
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
420 425 430
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
435 440 445
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
450 455 460
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
465 470 475 480
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
485 490 495
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
500 505 510
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
515 520 525
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
530 535 540
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
545 550 555 560
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
565 570 575
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
580 585 590
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
595 600 605
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
610 615 620
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
625 630 635 640
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
645 650 655
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
660 665 670
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
675 680 685
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
690 695 700
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
705 710 715 720
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
725 730 735
Arg
<210> 152
<211> 2211
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 152
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaagagaaa ttgtgatgac ccagtcaccc
840
gccactctta gcctttcacc cggtgagcgc gcaaccctgt cttgcagagc ctcccaagac
900
atctcaaaat accttaattg gtatcaacag aagcccggac aggctcctcg ccttctgatc
960
taccacacca gccggctcca ttctggaatc cctgccaggt tcagcggtag cggatctggg
1020
accgactaca ccctcactat cagctcactg cagccagagg acttcgctgt ctatttctgt
1080
cagcaaggga acaccctgcc ctacaccttt ggacagggca ccaagctcga gattaaaggt
1140
ggaggtggca gcggaggagg tgggtccggc ggtggaggaa gccaggtcca actccaagaa
1200
agcggaccgg gtcttgtgaa gccatcagaa actctttcac tgacttgtac tgtgagcgga
1260
gtgtctctcc ccgattacgg ggtgtcttgg atcagacagc caccggggaa gggtctggaa
1320
tggattggag tgatttgggg ctctgagact acttactact cttcatccct caagtcacgc
1380
gtcaccatct caaaggacaa ctctaagaat caggtgtcac tgaaactgtc atctgtgacc
1440
gcagccgaca ccgccgtgta ctattgcgct aagcattact attatggcgg gagctacgca
1500
atggattact ggggacaggg tactctggtc accgtgtcca gcaccactac cccagcaccg
1560
aggccaccca ccccggctcc taccatcgcc tcccagcctc tgtccctgcg tccggaggca
1620
tgtagacccg cagctggtgg ggccgtgcat acccggggtc ttgacttcgc ctgcgatatc
1680
tacatttggg cccctctggc tggtacttgc ggggtcctgc tgctttcact cgtgatcact
1740
ctttactgta agcgcggtcg gaagaagctg ctgtacatct ttaagcaacc cttcatgagg
1800
cctgtgcaga ctactcaaga ggaggacggc tgttcatgcc ggttcccaga ggaggaggaa
1860
ggcggctgcg aactgcgcgt gaaattcagc cgcagcgcag atgctccagc ctacaagcag
1920
gggcagaacc agctctacaa cgaactcaat cttggtcgga gagaggagta cgacgtgctg
1980
gacaagcgga gaggacggga cccagaaatg ggcgggaagc cgcgcagaaa gaatccccaa
2040
gagggcctgt acaacgagct ccaaaaggat aagatggcag aagcctatag cgagattggt
2100
atgaaagggg aacgcagaag aggcaaaggc cacgacggac tgtaccaggg actcagcacc
2160
gccaccaagg acacctatga cgctcttcac atgcaggccc tgccgcctcg g
2211
<210> 153
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 153
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 154
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 154
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtgaaatt gtgatgaccc agtcacccgc cactcttagc
900
ctttcacccg gtgagcgcgc aaccctgtct tgcagagcct cccaagacat ctcaaaatac
960
cttaattggt atcaacagaa gcccggacag gctcctcgcc ttctgatcta ccacaccagc
1020
cggctccatt ctggaatccc tgccaggttc agcggtagcg gatctgggac cgactacacc
1080
ctcactatca gctcactgca gccagaggac ttcgctgtct atttctgtca gcaagggaac
1140
accctgccct acacctttgg acagggcacc aagctcgaga ttaaaggtgg aggtggcagc
1200
ggaggaggtg ggtccggcgg tggaggaagc caggtccaac tccaagaaag cggaccgggt
1260
cttgtgaagc catcagaaac tctttcactg acttgtactg tgagcggagt gtctctcccc
1320
gattacgggg tgtcttggat cagacagcca ccggggaagg gtctggaatg gattggagtg
1380
atttggggct ctgagactac ttactactct tcatccctca agtcacgcgt caccatctca
1440
aaggacaact ctaagaatca ggtgtcactg aaactgtcat ctgtgaccgc agccgacacc
1500
gccgtgtact attgcgctaa gcattactat tatggcggga gctacgcaat ggattactgg
1560
ggacagggta ctctggtcac cgtgtccagc accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct acaagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 155
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 155
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
290 295 300
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
305 310 315 320
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
325 330 335
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
340 345 350
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
355 360 365
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
370 375 380
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
405 410 415
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
420 425 430
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
435 440 445
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
450 455 460
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
465 470 475 480
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
485 490 495
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
500 505 510
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
515 520 525
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 156
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 156
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtgaaatt gtgatgaccc agtcacccgc cactcttagc
900
ctttcacccg gtgagcgcgc aaccctgtct tgcagagcct cccaagacat ctcaaaatac
960
cttaattggt atcaacagaa gcccggacag gctcctcgcc ttctgatcta ccacaccagc
1020
cggctccatt ctggaatccc tgccaggttc agcggtagcg gatctgggac cgactacacc
1080
ctcactatca gctcactgca gccagaggac ttcgctgtct atttctgtca gcaagggaac
1140
accctgccct acacctttgg acagggcacc aagctcgaga ttaaaggtgg aggtggcagc
1200
ggaggaggtg ggtccggcgg tggaggaagc caggtccaac tccaagaaag cggaccgggt
1260
cttgtgaagc catcagaaac tctttcactg acttgtactg tgagcggagt gtctctcccc
1320
gattacgggg tgtcttggat cagacagcca ccggggaagg gtctggaatg gattggagtg
1380
atttggggct ctgagactac ttactactct tcatccctca agtcacgcgt caccatctca
1440
aaggacaact ctaagaatca ggtgtcactg aaactgtcat ctgtgaccgc agccgacacc
1500
gccgtgtact attgcgctaa gcattactat tatggcggga gctacgcaat ggattactgg
1560
ggacagggta ctctggtcac cgtgtccagc accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 157
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 157
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln
275 280 285
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
290 295 300
Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln
305 310 315 320
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu
325 330 335
His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
340 345 350
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr
355 360 365
Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr
370 375 380
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
405 410 415
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
420 425 430
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
435 440 445
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
450 455 460
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
465 470 475 480
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
485 490 495
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 158
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 158
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgaag atccacgacc cagcagaaag
840
cgacgggaaa ttgtgatgac ccagtcaccc gccactctta gcctttcacc cggtgagcgc
900
gcaaccctgt cttgcagagc ctcccaagac atctcaaaat accttaattg gtatcaacag
960
aagcccggac aggctcctcg ccttctgatc taccacacca gccggctcca ttctggaatc
1020
cctgccaggt tcagcggtag cggatctggg accgactaca ccctcactat cagctcactg
1080
cagccagagg acttcgctgt ctatttctgt cagcaaggga acaccctgcc ctacaccttt
1140
ggacagggca ccaagctcga gattaaaggt ggaggtggca gcggaggagg tgggtccggc
1200
ggtggaggaa gccaggtcca actccaagaa agcggaccgg gtcttgtgaa gccatcagaa
1260
actctttcac tgacttgtac tgtgagcgga gtgtctctcc ccgattacgg ggtgtcttgg
1320
atcagacagc caccggggaa gggtctggaa tggattggag tgatttgggg ctctgagact
1380
acttactact cttcatccct caagtcacgc gtcaccatct caaaggacaa ctctaagaat
1440
caggtgtcac tgaaactgtc atctgtgacc gcagccgaca ccgccgtgta ctattgcgct
1500
aagcattact attatggcgg gagctacgca atggattact ggggacaggg tactctggtc
1560
accgtgtcca gcaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 159
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 159
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln
275 280 285
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
290 295 300
Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln
305 310 315 320
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu
325 330 335
His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
340 345 350
Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr
355 360 365
Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr
370 375 380
Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
405 410 415
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
420 425 430
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
435 440 445
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
450 455 460
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
465 470 475 480
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
485 490 495
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
500 505 510
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 160
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 160
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgaag atccacgacc cagcagaaag
840
cgacgggaaa ttgtgatgac ccagtcaccc gccactctta gcctttcacc cggtgagcgc
900
gcaaccctgt cttgcagagc ctcccaagac atctcaaaat accttaattg gtatcaacag
960
aagcccggac aggctcctcg ccttctgatc taccacacca gccggctcca ttctggaatc
1020
cctgccaggt tcagcggtag cggatctggg accgactaca ccctcactat cagctcactg
1080
cagccagagg acttcgctgt ctatttctgt cagcaaggga acaccctgcc ctacaccttt
1140
ggacagggca ccaagctcga gattaaaggt ggaggtggca gcggaggagg tgggtccggc
1200
ggtggaggaa gccaggtcca actccaagaa agcggaccgg gtcttgtgaa gccatcagaa
1260
actctttcac tgacttgtac tgtgagcgga gtgtctctcc ccgattacgg ggtgtcttgg
1320
atcagacagc caccggggaa gggtctggaa tggattggag tgatttgggg ctctgagact
1380
acttactact cttcatccct caagtcacgc gtcaccatct caaaggacaa ctctaagaat
1440
caggtgtcac tgaaactgtc atctgtgacc gcagccgaca ccgccgtgta ctattgcgct
1500
aagcattact attatggcgg gagctacgca atggattact ggggacaggg tactctggtc
1560
accgtgtcca gcaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 161
<211> 738
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 161
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
275 280 285
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
290 295 300
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
305 310 315 320
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
325 330 335
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
340 345 350
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
355 360 365
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
370 375 380
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
405 410 415
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
420 425 430
Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
435 440 445
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser
450 455 460
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
465 470 475 480
Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
485 490 495
Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu
500 505 510
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
515 520 525
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
530 535 540
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
545 550 555 560
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
565 570 575
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
580 585 590
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
595 600 605
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
610 615 620
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
625 630 635 640
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
645 650 655
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
660 665 670
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
675 680 685
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
690 695 700
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
705 710 715 720
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
725 730 735
Pro Arg
<210> 162
<211> 2214
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 162
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaagacaag tgcaactcgt ccaaagcgga
840
gcggaagtca agaaacccgg agcgagcgtg aaagtgtcct gcaaagcctc cggctacacc
900
tttacgggct actacatgca ctgggtgcgc caggcaccag gacagggtct tgaatggatg
960
ggatggatca accctaattc gggcggaact aactacgcac agaagttcca ggggagagtg
1020
actctgactc gggatacctc catctcaact gtctacatgg aactctcccg cttgcggtca
1080
gatgatacgg cagtgtacta ctgcgcccgc gacatgaata tcctggctac cgtgccgttc
1140
gacatctggg gacaggggac tatggttact gtctcatcgg gcggtggagg ttcaggagga
1200
ggcggctcgg gaggcggagg ttcggacatt cagatgaccc agtccccatc ctctctgtcg
1260
gccagcgtcg gagatagggt gaccattacc tgtcgggcct cgcaaagcat ctcctcgtac
1320
ctcaactggt atcagcaaaa gccgggaaag gcgcctaagc tgctgatcta cgccgcttcg
1380
agcttgcaaa gcggggtgcc atccagattc tcgggatcag gctcaggaac cgacttcacc
1440
ctgaccgtga acagcctcca gccggaggac tttgccactt actactgcca gcagggagac
1500
tccgtgccgc ttactttcgg ggggggtacc cgcctggaga tcaagaccac taccccagca
1560
ccgaggccac ccaccccggc tcctaccatc gcctcccagc ctctgtccct gcgtccggag
1620
gcatgtagac ccgcagctgg tggggccgtg catacccggg gtcttgactt cgcctgcgat
1680
atctacattt gggcccctct ggctggtact tgcggggtcc tgctgctttc actcgtgatc
1740
actctttact gtaagcgcgg tcggaagaag ctgctgtaca tctttaagca acccttcatg
1800
aggcctgtgc agactactca agaggaggac ggctgttcat gccggttccc agaggaggag
1860
gaaggcggct gcgaactgcg cgtgaaattc agccgcagcg cagatgctcc agcctaccag
1920
caggggcaga accagctcta caacgaactc aatcttggtc ggagagagga gtacgacgtg
1980
ctggacaagc ggagaggacg ggacccagaa atgggcggga agccgcgcag aaagaatccc
2040
caagagggcc tgtacaacga gctccaaaag gataagatgg cagaagccta tagcgagatt
2100
ggtatgaaag gggaacgcag aagaggcaaa ggccacgacg gactgtacca gggactcagc
2160
accgccacca aggacaccta tgacgctctt cacatgcagg ccctgccgcc tcgg
2214
<210> 163
<211> 754
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 163
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
290 295 300
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
305 310 315 320
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
325 330 335
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
340 345 350
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
355 360 365
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
370 375 380
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
385 390 395 400
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
420 425 430
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
435 440 445
Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
450 455 460
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser
465 470 475 480
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
485 490 495
Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
500 505 510
Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu
515 520 525
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
530 535 540
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
545 550 555 560
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
565 570 575
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
580 585 590
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
595 600 605
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
610 615 620
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
625 630 635 640
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
645 650 655
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
660 665 670
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
675 680 685
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
690 695 700
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
705 710 715 720
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
725 730 735
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
740 745 750
Pro Arg
<210> 164
<211> 2262
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 164
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtcaagtg caactcgtcc aaagcggagc ggaagtcaag
900
aaacccggag cgagcgtgaa agtgtcctgc aaagcctccg gctacacctt tacgggctac
960
tacatgcact gggtgcgcca ggcaccagga cagggtcttg aatggatggg atggatcaac
1020
cctaattcgg gcggaactaa ctacgcacag aagttccagg ggagagtgac tctgactcgg
1080
gatacctcca tctcaactgt ctacatggaa ctctcccgct tgcggtcaga tgatacggca
1140
gtgtactact gcgcccgcga catgaatatc ctggctaccg tgccgttcga catctgggga
1200
caggggacta tggttactgt ctcatcgggc ggtggaggtt caggaggagg cggctcggga
1260
ggcggaggtt cggacattca gatgacccag tccccatcct ctctgtcggc cagcgtcgga
1320
gatagggtga ccattacctg tcgggcctcg caaagcatct cctcgtacct caactggtat
1380
cagcaaaagc cgggaaaggc gcctaagctg ctgatctacg ccgcttcgag cttgcaaagc
1440
ggggtgccat ccagattctc gggatcaggc tcaggaaccg acttcaccct gaccgtgaac
1500
agcctccagc cggaggactt tgccacttac tactgccagc agggagactc cgtgccgctt
1560
actttcgggg ggggtacccg cctggagatc aagaccacta ccccagcacc gaggccaccc
1620
accccggctc ctaccatcgc ctcccagcct ctgtccctgc gtccggaggc atgtagaccc
1680
gcagctggtg gggccgtgca tacccggggt cttgacttcg cctgcgatat ctacatttgg
1740
gcccctctgg ctggtacttg cggggtcctg ctgctttcac tcgtgatcac tctttactgt
1800
aagcgcggtc ggaagaagct gctgtacatc tttaagcaac ccttcatgag gcctgtgcag
1860
actactcaag aggaggacgg ctgttcatgc cggttcccag aggaggagga aggcggctgc
1920
gaactgcgcg tgaaattcag ccgcagcgca gatgctccag cctaccagca ggggcagaac
1980
cagctctaca acgaactcaa tcttggtcgg agagaggagt acgacgtgct ggacaagcgg
2040
agaggacggg acccagaaat gggcgggaag ccgcgcagaa agaatcccca agagggcctg
2100
tacaacgagc tccaaaagga taagatggca gaagcctata gcgagattgg tatgaaaggg
2160
gaacgcagaa gaggcaaagg ccacgacgga ctgtaccagg gactcagcac cgccaccaag
2220
gacacctatg acgctcttca catgcaggcc ctgccgcctc gg
2262
<210> 165
<211> 748
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 165
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln
275 280 285
Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys
290 295 300
Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn
325 330 335
Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu
340 345 350
Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu
355 360 365
Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile
370 375 380
Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
385 390 395 400
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
420 425 430
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
435 440 445
Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
450 455 460
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
465 470 475 480
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu
485 490 495
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val
500 505 510
Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr
515 520 525
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
530 535 540
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
545 550 555 560
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
565 570 575
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
580 585 590
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
595 600 605
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
610 615 620
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
625 630 635 640
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
645 650 655
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
660 665 670
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
675 680 685
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
690 695 700
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
705 710 715 720
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
725 730 735
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 166
<211> 2244
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 166
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggcaag tgcaactcgt ccaaagcgga gcggaagtca agaaacccgg agcgagcgtg
900
aaagtgtcct gcaaagcctc cggctacacc tttacgggct actacatgca ctgggtgcgc
960
caggcaccag gacagggtct tgaatggatg ggatggatca accctaattc gggcggaact
1020
aactacgcac agaagttcca ggggagagtg actctgactc gggatacctc catctcaact
1080
gtctacatgg aactctcccg cttgcggtca gatgatacgg cagtgtacta ctgcgcccgc
1140
gacatgaata tcctggctac cgtgccgttc gacatctggg gacaggggac tatggttact
1200
gtctcatcgg gcggtggagg ttcaggagga ggcggctcgg gaggcggagg ttcggacatt
1260
cagatgaccc agtccccatc ctctctgtcg gccagcgtcg gagatagggt gaccattacc
1320
tgtcgggcct cgcaaagcat ctcctcgtac ctcaactggt atcagcaaaa gccgggaaag
1380
gcgcctaagc tgctgatcta cgccgcttcg agcttgcaaa gcggggtgcc atccagattc
1440
tcgggatcag gctcaggaac cgacttcacc ctgaccgtga acagcctcca gccggaggac
1500
tttgccactt actactgcca gcagggagac tccgtgccgc ttactttcgg ggggggtacc
1560
cgcctggaga tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
1620
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
1680
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
1740
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1800
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1860
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1920
agccgcagcg cagatgctcc agcctaccag caggggcaga accagctcta caacgaactc
1980
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
2040
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
2100
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
2160
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
2220
cacatgcagg ccctgccgcc tcgg
2244
<210> 167
<211> 738
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 167
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
275 280 285
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
290 295 300
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
305 310 315 320
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
325 330 335
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
340 345 350
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
355 360 365
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
370 375 380
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
405 410 415
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
420 425 430
Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
435 440 445
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser
450 455 460
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
465 470 475 480
Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
485 490 495
Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu
500 505 510
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
515 520 525
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
530 535 540
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
545 550 555 560
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
565 570 575
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
580 585 590
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
595 600 605
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
610 615 620
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
625 630 635 640
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
645 650 655
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
660 665 670
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
675 680 685
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
690 695 700
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
705 710 715 720
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
725 730 735
Pro Arg
<210> 168
<211> 2214
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 168
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaagacaag tgcaactcgt ccaaagcgga
840
gcggaagtca agaaacccgg agcgagcgtg aaagtgtcct gcaaagcctc cggctacacc
900
tttacgggct actacatgca ctgggtgcgc caggcaccag gacagggtct tgaatggatg
960
ggatggatca accctaattc gggcggaact aactacgcac agaagttcca ggggagagtg
1020
actctgactc gggatacctc catctcaact gtctacatgg aactctcccg cttgcggtca
1080
gatgatacgg cagtgtacta ctgcgcccgc gacatgaata tcctggctac cgtgccgttc
1140
gacatctggg gacaggggac tatggttact gtctcatcgg gcggtggagg ttcaggagga
1200
ggcggctcgg gaggcggagg ttcggacatt cagatgaccc agtccccatc ctctctgtcg
1260
gccagcgtcg gagatagggt gaccattacc tgtcgggcct cgcaaagcat ctcctcgtac
1320
ctcaactggt atcagcaaaa gccgggaaag gcgcctaagc tgctgatcta cgccgcttcg
1380
agcttgcaaa gcggggtgcc atccagattc tcgggatcag gctcaggaac cgacttcacc
1440
ctgaccgtga acagcctcca gccggaggac tttgccactt actactgcca gcagggagac
1500
tccgtgccgc ttactttcgg ggggggtacc cgcctggaga tcaagaccac taccccagca
1560
ccgaggccac ccaccccggc tcctaccatc gcctcccagc ctctgtccct gcgtccggag
1620
gcatgtagac ccgcagctgg tggggccgtg catacccggg gtcttgactt cgcctgcgat
1680
atctacattt gggcccctct ggctggtact tgcggggtcc tgctgctttc actcgtgatc
1740
actctttact gtaagcgcgg tcggaagaag ctgctgtaca tctttaagca acccttcatg
1800
aggcctgtgc agactactca agaggaggac ggctgttcat gccggttccc agaggaggag
1860
gaaggcggct gcgaactgcg cgtgaaattc agccgcagcg cagatgctcc agcctaccag
1920
caggggcaga accagctcta caacgaactc aatcttggtc ggagagagga gtacgacgtg
1980
ctggacaagc ggagaggacg ggacccagaa atgggcggga agccgcgcag aaagaatccc
2040
caagagggcc tgtacaacga gctccaaaag gataagatgg cagaagccta tagcgagatt
2100
ggtatgaaag gggaacgcag aagaggcaaa ggccacgacg gactgtacca gggactcagc
2160
accgccacca aggacaccta tgacgctctt cacatgcagg ccctgccgcc tcgg
2214
<210> 169
<211> 754
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 169
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
290 295 300
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
305 310 315 320
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
325 330 335
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
340 345 350
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
355 360 365
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
370 375 380
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
385 390 395 400
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
405 410 415
Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro
420 425 430
Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg
435 440 445
Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
450 455 460
Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser
465 470 475 480
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
485 490 495
Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
500 505 510
Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu
515 520 525
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
530 535 540
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
545 550 555 560
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
565 570 575
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
580 585 590
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
595 600 605
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
610 615 620
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
625 630 635 640
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln
645 650 655
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
660 665 670
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
675 680 685
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
690 695 700
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
705 710 715 720
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
725 730 735
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
740 745 750
Pro Arg
<210> 170
<211> 2262
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 170
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtcaagtg caactcgtcc aaagcggagc ggaagtcaag
900
aaacccggag cgagcgtgaa agtgtcctgc aaagcctccg gctacacctt tacgggctac
960
tacatgcact gggtgcgcca ggcaccagga cagggtcttg aatggatggg atggatcaac
1020
cctaattcgg gcggaactaa ctacgcacag aagttccagg ggagagtgac tctgactcgg
1080
gatacctcca tctcaactgt ctacatggaa ctctcccgct tgcggtcaga tgatacggca
1140
gtgtactact gcgcccgcga catgaatatc ctggctaccg tgccgttcga catctgggga
1200
caggggacta tggttactgt ctcatcgggc ggtggaggtt caggaggagg cggctcggga
1260
ggcggaggtt cggacattca gatgacccag tccccatcct ctctgtcggc cagcgtcgga
1320
gatagggtga ccattacctg tcgggcctcg caaagcatct cctcgtacct caactggtat
1380
cagcaaaagc cgggaaaggc gcctaagctg ctgatctacg ccgcttcgag cttgcaaagc
1440
ggggtgccat ccagattctc gggatcaggc tcaggaaccg acttcaccct gaccgtgaac
1500
agcctccagc cggaggactt tgccacttac tactgccagc agggagactc cgtgccgctt
1560
actttcgggg ggggtacccg cctggagatc aagaccacta ccccagcacc gaggccaccc
1620
accccggctc ctaccatcgc ctcccagcct ctgtccctgc gtccggaggc atgtagaccc
1680
gcagctggtg gggccgtgca tacccggggt cttgacttcg cctgcgatat ctacatttgg
1740
gcccctctgg ctggtacttg cggggtcctg ctgctttcac tcgtgatcac tctttactgt
1800
aagcgcggtc ggaagaagct gctgtacatc tttaagcaac ccttcatgag gcctgtgcag
1860
actactcaag aggaggacgg ctgttcatgc cggttcccag aggaggagga aggcggctgc
1920
gaactgcgcg tgaaattcag ccgcagcgca gatgctccag cctaccagca ggggcagaac
1980
cagctctaca acgaactcaa tcttggtcgg agagaggagt acgacgtgct ggacaagcgg
2040
agaggacggg acccagaaat gggcgggaag ccgcgcagaa agaatcccca agagggcctg
2100
tacaacgagc tccaaaagga taagatggca gaagcctata gcgagattgg tatgaaaggg
2160
gaacgcagaa gaggcaaagg ccacgacgga ctgtaccagg gactcagcac cgccaccaag
2220
gacacctatg acgctcttca catgcaggcc ctgccgcctc gg
2262
<210> 171
<211> 748
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 171
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln
275 280 285
Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys
290 295 300
Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg
305 310 315 320
Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn
325 330 335
Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu
340 345 350
Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu
355 360 365
Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile
370 375 380
Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
385 390 395 400
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
420 425 430
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
435 440 445
Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
450 455 460
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
465 470 475 480
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu
485 490 495
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val
500 505 510
Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr
515 520 525
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
530 535 540
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
545 550 555 560
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
565 570 575
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
580 585 590
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
595 600 605
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
610 615 620
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
625 630 635 640
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
645 650 655
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
660 665 670
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
675 680 685
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
690 695 700
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
705 710 715 720
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
725 730 735
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 172
<211> 2244
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 172
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgaag atccacgacc cagcagaaag
840
cgacggcaag tgcaactcgt ccaaagcgga gcggaagtca agaaacccgg agcgagcgtg
900
aaagtgtcct gcaaagcctc cggctacacc tttacgggct actacatgca ctgggtgcgc
960
caggcaccag gacagggtct tgaatggatg ggatggatca accctaattc gggcggaact
1020
aactacgcac agaagttcca ggggagagtg actctgactc gggatacctc catctcaact
1080
gtctacatgg aactctcccg cttgcggtca gatgatacgg cagtgtacta ctgcgcccgc
1140
gacatgaata tcctggctac cgtgccgttc gacatctggg gacaggggac tatggttact
1200
gtctcatcgg gcggtggagg ttcaggagga ggcggctcgg gaggcggagg ttcggacatt
1260
cagatgaccc agtccccatc ctctctgtcg gccagcgtcg gagatagggt gaccattacc
1320
tgtcgggcct cgcaaagcat ctcctcgtac ctcaactggt atcagcaaaa gccgggaaag
1380
gcgcctaagc tgctgatcta cgccgcttcg agcttgcaaa gcggggtgcc atccagattc
1440
tcgggatcag gctcaggaac cgacttcacc ctgaccgtga acagcctcca gccggaggac
1500
tttgccactt actactgcca gcagggagac tccgtgccgc ttactttcgg ggggggtacc
1560
cgcctggaga tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
1620
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
1680
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
1740
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1800
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1860
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1920
agccgcagcg cagatgctcc agcctaccag caggggcaga accagctcta caacgaactc
1980
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
2040
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
2100
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
2160
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
2220
cacatgcagg ccctgccgcc tcgg
2244
<210> 173
<211> 734
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 173
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
275 280 285
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
290 295 300
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
305 310 315 320
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
325 330 335
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
340 345 350
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
355 360 365
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
370 375 380
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
385 390 395 400
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser
405 410 415
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
420 425 430
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
435 440 445
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
450 455 460
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
465 470 475 480
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
485 490 495
Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr
500 505 510
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
515 520 525
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
530 535 540
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
545 550 555 560
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
565 570 575
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
580 585 590
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
595 600 605
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
610 615 620
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
625 630 635 640
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
645 650 655
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
660 665 670
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
675 680 685
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
690 695 700
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
705 710 715 720
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
725 730
<210> 174
<211> 2202
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 174
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaagagaag tgcaattggt ggaatcaggg
840
ggaggacttg tgcagcctgg aggatcgctg agactgtcat gtgccgtgtc cggctttgcc
900
ctgtccaacc acgggatgtc ctgggtccgc cgcgcgcctg gaaagggcct cgaatgggtg
960
tcgggtattg tgtacagcgg tagcacctac tatgccgcat ccgtgaaggg gagattcacc
1020
atcagccggg acaactccag gaacactctg tacctccaaa tgaattcgct gaggccagag
1080
gacactgcca tctactactg ctccgcgcat ggcggagagt ccgacgtctg gggacagggg
1140
accaccgtga ccgtgtctag cgcgtccggc ggaggcggca gcgggggtcg ggcatcaggg
1200
ggcggcggat cggacatcca gctcacccag tccccgagct cgctgtccgc ctccgtggga
1260
gatcgggtca ccatcacgtg ccgcgccagc cagtcgattt cctcctacct gaactggtac
1320
caacagaagc ccggaaaagc cccgaagctt ctcatctacg ccgcctcgag cctgcagtca
1380
ggagtgccct cacggttctc cggctccggt tccggtactg atttcaccct gaccatttcc
1440
tccctgcaac cggaggactt cgctacttac tactgccagc agtcgtactc caccccctac
1500
actttcggac aaggcaccaa ggtcgaaatc aagaccacta ccccagcacc gaggccaccc
1560
accccggctc ctaccatcgc ctcccagcct ctgtccctgc gtccggaggc atgtagaccc
1620
gcagctggtg gggccgtgca tacccggggt cttgacttcg cctgcgatat ctacatttgg
1680
gcccctctgg ctggtacttg cggggtcctg ctgctttcac tcgtgatcac tctttactgt
1740
aagcgcggtc ggaagaagct gctgtacatc tttaagcaac ccttcatgag gcctgtgcag
1800
actactcaag aggaggacgg ctgttcatgc cggttcccag aggaggagga aggcggctgc
1860
gaactgcgcg tgaaattcag ccgcagcgca gatgctccag cctaccagca ggggcagaac
1920
cagctctaca acgaactcaa tcttggtcgg agagaggagt acgacgtgct ggacaagcgg
1980
agaggacggg acccagaaat gggcgggaag ccgcgcagaa agaatcccca agagggcctg
2040
tacaacgagc tccaaaagga taagatggca gaagcctata gcgagattgg tatgaaaggg
2100
gaacgcagaa gaggcaaagg ccacgacgga ctgtaccagg gactcagcac cgccaccaag
2160
gacacctatg acgctcttca catgcaggcc ctgccgcctc gg
2202
<210> 175
<211> 750
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 175
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
290 295 300
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
305 310 315 320
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
325 330 335
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
340 345 350
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
355 360 365
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
370 375 380
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
385 390 395 400
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
405 410 415
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser
420 425 430
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
435 440 445
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
450 455 460
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
465 470 475 480
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
485 490 495
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
500 505 510
Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr
515 520 525
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
530 535 540
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
545 550 555 560
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
565 570 575
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
580 585 590
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
595 600 605
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
610 615 620
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
625 630 635 640
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
645 650 655
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
660 665 670
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
675 680 685
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
690 695 700
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
705 710 715 720
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
725 730 735
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 176
<211> 2250
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 176
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtgaagtg caattggtgg aatcaggggg aggacttgtg
900
cagcctggag gatcgctgag actgtcatgt gccgtgtccg gctttgccct gtccaaccac
960
gggatgtcct gggtccgccg cgcgcctgga aagggcctcg aatgggtgtc gggtattgtg
1020
tacagcggta gcacctacta tgccgcatcc gtgaagggga gattcaccat cagccgggac
1080
aactccagga acactctgta cctccaaatg aattcgctga ggccagagga cactgccatc
1140
tactactgct ccgcgcatgg cggagagtcc gacgtctggg gacaggggac caccgtgacc
1200
gtgtctagcg cgtccggcgg aggcggcagc gggggtcggg catcaggggg cggcggatcg
1260
gacatccagc tcacccagtc cccgagctcg ctgtccgcct ccgtgggaga tcgggtcacc
1320
atcacgtgcc gcgccagcca gtcgatttcc tcctacctga actggtacca acagaagccc
1380
ggaaaagccc cgaagcttct catctacgcc gcctcgagcc tgcagtcagg agtgccctca
1440
cggttctccg gctccggttc cggtactgat ttcaccctga ccatttcctc cctgcaaccg
1500
gaggacttcg ctacttacta ctgccagcag tcgtactcca ccccctacac tttcggacaa
1560
ggcaccaagg tcgaaatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
1620
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
1680
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
1740
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1800
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1860
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1920
aaattcagcc gcagcgcaga tgctccagcc taccagcagg ggcagaacca gctctacaac
1980
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
2040
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
2100
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
2160
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
2220
gctcttcaca tgcaggccct gccgcctcgg
2250
<210> 177
<211> 744
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 177
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg
305 310 315 320
Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser
325 330 335
Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser
340 345 350
Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
355 360 365
Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser
370 375 380
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile
405 410 415
Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
420 425 430
Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
435 440 445
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala
450 455 460
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
465 470 475 480
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
485 490 495
Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe
500 505 510
Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
515 520 525
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
530 535 540
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
545 550 555 560
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
565 570 575
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
580 585 590
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
595 600 605
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
610 615 620
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
625 630 635 640
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
645 650 655
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
660 665 670
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
675 680 685
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
690 695 700
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
705 710 715 720
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
725 730 735
His Met Gln Ala Leu Pro Pro Arg
740
<210> 178
<211> 2232
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 178
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctggcc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gtccaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgaag atccacgacc cagcagaaag
840
cgacgggaag tgcaattggt ggaatcaggg ggaggacttg tgcagcctgg aggatcgctg
900
agactgtcat gtgccgtgtc cggctttgcc ctgtccaacc acgggatgtc ctgggtccgc
960
cgcgcgcctg gaaagggcct cgaatgggtg tcgggtattg tgtacagcgg tagcacctac
1020
tatgccgcat ccgtgaaggg gagattcacc atcagccggg acaactccag gaacactctg
1080
tacctccaaa tgaattcgct gaggccagag gacactgcca tctactactg ctccgcgcat
1140
ggcggagagt ccgacgtctg gggacagggg accaccgtga ccgtgtctag cgcgtccggc
1200
ggaggcggca gcgggggtcg ggcatcaggg ggcggcggat cggacatcca gctcacccag
1260
tccccgagct cgctgtccgc ctccgtggga gatcgggtca ccatcacgtg ccgcgccagc
1320
cagtcgattt cctcctacct gaactggtac caacagaagc ccggaaaagc cccgaagctt
1380
ctcatctacg ccgcctcgag cctgcagtca ggagtgccct cacggttctc cggctccggt
1440
tccggtactg atttcaccct gaccatttcc tccctgcaac cggaggactt cgctacttac
1500
tactgccagc agtcgtactc caccccctac actttcggac aaggcaccaa ggtcgaaatc
1560
aagaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
1620
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
1680
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
1740
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1800
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1860
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1920
gatgctccag cctaccagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1980
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
2040
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
2100
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
2160
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
2220
ctgccgcctc gg
2232
<210> 179
<211> 734
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 179
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Arg Thr Lys Arg
260 265 270
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
275 280 285
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
290 295 300
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
305 310 315 320
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
325 330 335
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
340 345 350
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
355 360 365
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
370 375 380
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
385 390 395 400
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser
405 410 415
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
420 425 430
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
435 440 445
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
450 455 460
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
465 470 475 480
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
485 490 495
Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr
500 505 510
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
515 520 525
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
530 535 540
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
545 550 555 560
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
565 570 575
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
580 585 590
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
595 600 605
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
610 615 620
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
625 630 635 640
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
645 650 655
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
660 665 670
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
675 680 685
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
690 695 700
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
705 710 715 720
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
725 730
<210> 180
<211> 2202
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 180
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actccgtact aaaagagaag tgcaattggt ggaatcaggg
840
ggaggacttg tgcagcctgg aggatcgctg agactgtcat gtgccgtgtc cggctttgcc
900
ctgtccaacc acgggatgtc ctgggtccgc cgcgcgcctg gaaagggcct cgaatgggtg
960
tcgggtattg tgtacagcgg tagcacctac tatgccgcat ccgtgaaggg gagattcacc
1020
atcagccggg acaactccag gaacactctg tacctccaaa tgaattcgct gaggccagag
1080
gacactgcca tctactactg ctccgcgcat ggcggagagt ccgacgtctg gggacagggg
1140
accaccgtga ccgtgtctag cgcgtccggc ggaggcggca gcgggggtcg ggcatcaggg
1200
ggcggcggat cggacatcca gctcacccag tccccgagct cgctgtccgc ctccgtggga
1260
gatcgggtca ccatcacgtg ccgcgccagc cagtcgattt cctcctacct gaactggtac
1320
caacagaagc ccggaaaagc cccgaagctt ctcatctacg ccgcctcgag cctgcagtca
1380
ggagtgccct cacggttctc cggctccggt tccggtactg atttcaccct gaccatttcc
1440
tccctgcaac cggaggactt cgctacttac tactgccagc agtcgtactc caccccctac
1500
actttcggac aaggcaccaa ggtcgaaatc aagaccacta ccccagcacc gaggccaccc
1560
accccggctc ctaccatcgc ctcccagcct ctgtccctgc gtccggaggc atgtagaccc
1620
gcagctggtg gggccgtgca tacccggggt cttgacttcg cctgcgatat ctacatttgg
1680
gcccctctgg ctggtacttg cggggtcctg ctgctttcac tcgtgatcac tctttactgt
1740
aagcgcggtc ggaagaagct gctgtacatc tttaagcaac ccttcatgag gcctgtgcag
1800
actactcaag aggaggacgg ctgttcatgc cggttcccag aggaggagga aggcggctgc
1860
gaactgcgcg tgaaattcag ccgcagcgca gatgctccag cctaccagca ggggcagaac
1920
cagctctaca acgaactcaa tcttggtcgg agagaggagt acgacgtgct ggacaagcgg
1980
agaggacggg acccagaaat gggcgggaag ccgcgcagaa agaatcccca agagggcctg
2040
tacaacgagc tccaaaagga taagatggca gaagcctata gcgagattgg tatgaaaggg
2100
gaacgcagaa gaggcaaagg ccacgacgga ctgtaccagg gactcagcac cgccaccaag
2160
gacacctatg acgctcttca catgcaggcc ctgccgcctc gg
2202
<210> 181
<211> 750
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 181
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly
275 280 285
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
290 295 300
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
305 310 315 320
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
325 330 335
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
340 345 350
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
355 360 365
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
370 375 380
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
385 390 395 400
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
405 410 415
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser
420 425 430
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
435 440 445
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
450 455 460
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
465 470 475 480
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
485 490 495
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
500 505 510
Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr
515 520 525
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
530 535 540
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
545 550 555 560
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
565 570 575
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
580 585 590
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
595 600 605
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
610 615 620
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
625 630 635 640
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
645 650 655
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
660 665 670
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
675 680 685
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
690 695 700
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
705 710 715 720
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
725 730 735
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 182
<211> 2250
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 182
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcggaacc ggcgcggaag acccccggcc ctccaggaag
840
cgaaggtccc tcggagacgt gggtgaagtg caattggtgg aatcaggggg aggacttgtg
900
cagcctggag gatcgctgag actgtcatgt gccgtgtccg gctttgccct gtccaaccac
960
gggatgtcct gggtccgccg cgcgcctgga aagggcctcg aatgggtgtc gggtattgtg
1020
tacagcggta gcacctacta tgccgcatcc gtgaagggga gattcaccat cagccgggac
1080
aactccagga acactctgta cctccaaatg aattcgctga ggccagagga cactgccatc
1140
tactactgct ccgcgcatgg cggagagtcc gacgtctggg gacaggggac caccgtgacc
1200
gtgtctagcg cgtccggcgg aggcggcagc gggggtcggg catcaggggg cggcggatcg
1260
gacatccagc tcacccagtc cccgagctcg ctgtccgcct ccgtgggaga tcgggtcacc
1320
atcacgtgcc gcgccagcca gtcgatttcc tcctacctga actggtacca acagaagccc
1380
ggaaaagccc cgaagcttct catctacgcc gcctcgagcc tgcagtcagg agtgccctca
1440
cggttctccg gctccggttc cggtactgat ttcaccctga ccatttcctc cctgcaaccg
1500
gaggacttcg ctacttacta ctgccagcag tcgtactcca ccccctacac tttcggacaa
1560
ggcaccaagg tcgaaatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
1620
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
1680
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
1740
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1800
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1860
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1920
aaattcagcc gcagcgcaga tgctccagcc taccagcagg ggcagaacca gctctacaac
1980
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
2040
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
2100
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
2160
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
2220
gctcttcaca tgcaggccct gccgcctcgg
2250
<210> 183
<211> 744
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 183
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp
20 25 30
Gln Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser
35 40 45
Glu Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu
50 55 60
Leu Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala
65 70 75 80
Lys Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His
85 90 95
Leu Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp
100 105 110
Arg Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu
115 120 125
Leu Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe
130 135 140
Asp Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln
145 150 155 160
Gly Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly
165 170 175
Val Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp
180 185 190
His Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu
195 200 205
Met Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala
210 215 220
Gln Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg
225 230 235 240
Met Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser
245 250 255
Asp Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala
260 265 270
Glu Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu
275 280 285
Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys
290 295 300
Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg
305 310 315 320
Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser
325 330 335
Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser
340 345 350
Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg
355 360 365
Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser
370 375 380
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile
405 410 415
Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
420 425 430
Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
435 440 445
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala
450 455 460
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
465 470 475 480
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
485 490 495
Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe
500 505 510
Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
515 520 525
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
530 535 540
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
545 550 555 560
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
565 570 575
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
580 585 590
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
595 600 605
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
610 615 620
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
625 630 635 640
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
645 650 655
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
660 665 670
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
675 680 685
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
690 695 700
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
705 710 715 720
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
725 730 735
His Met Gln Ala Leu Pro Pro Arg
740
<210> 184
<211> 2232
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 184
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccggtcgt cgttggcact ttccctgact gccgaccaga tggtgtccgc ccttctggac
120
gccgagcctc caattctgta ctcggagtac gatccgactc gcccgttctc cgaagccagc
180
atgatgggcc tgttgactaa cctggcggac cgcgagttgg tgcacatgat taactgggct
240
aagcgggtgc cgggcttcgt ggacctgacc ctgcacgacc aagtgcacct cctggaatgc
300
gcctggatgg aaatcctcat gatcggcctc gtgtggagat ccatggagca tcccggaaag
360
ctcctgtttg cacccaacct cctgcttgat cgcaaccagg gaaaatgcgt ggaagggggt
420
gtcgagattt tcgacatgct gctcgccacc tcttcccggt tccggatgat gaatctgcag
480
ggagaagagt tcgtgtgtct gaagtcaatc atcctgctga actccggggt ctataccttc
540
ctgagctcga ccctcaagtc actggaggaa aaagaccaca tccatcgcgt gctcgataag
600
atcaccgaca cccttatcca tctcatggcg aaggctggac tgaccctgca acagcagcac
660
cagaggctgg cccagttgct gctgattctg agccacatcc ggcacatgtc gaacaagagg
720
atggaacacc tgtacagcat gaagtgcaag aacgtcgtgc ctctgtccga tctgctcctg
780
gaaatgctgg acgcgcacag actcgggacg ggagctgaag atccacgacc cagcagaaag
840
cgacgggaag tgcaattggt ggaatcaggg ggaggacttg tgcagcctgg aggatcgctg
900
agactgtcat gtgccgtgtc cggctttgcc ctgtccaacc acgggatgtc ctgggtccgc
960
cgcgcgcctg gaaagggcct cgaatgggtg tcgggtattg tgtacagcgg tagcacctac
1020
tatgccgcat ccgtgaaggg gagattcacc atcagccggg acaactccag gaacactctg
1080
tacctccaaa tgaattcgct gaggccagag gacactgcca tctactactg ctccgcgcat
1140
ggcggagagt ccgacgtctg gggacagggg accaccgtga ccgtgtctag cgcgtccggc
1200
ggaggcggca gcgggggtcg ggcatcaggg ggcggcggat cggacatcca gctcacccag
1260
tccccgagct cgctgtccgc ctccgtggga gatcgggtca ccatcacgtg ccgcgccagc
1320
cagtcgattt cctcctacct gaactggtac caacagaagc ccggaaaagc cccgaagctt
1380
ctcatctacg ccgcctcgag cctgcagtca ggagtgccct cacggttctc cggctccggt
1440
tccggtactg atttcaccct gaccatttcc tccctgcaac cggaggactt cgctacttac
1500
tactgccagc agtcgtactc caccccctac actttcggac aaggcaccaa ggtcgaaatc
1560
aagaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
1620
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
1680
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
1740
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1800
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1860
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1920
gatgctccag cctaccagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1980
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
2040
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
2100
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
2160
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
2220
ctgccgcctc gg
2232
<210> 185
<211> 521
<212> ДНК
<213> Неизвестная
<220>
<221> источник
<223> /примечание="Описание неизвестной последовательности:
промотор PGK дикого типа"
<400> 185
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac gagggaccgc gacaggcaga
240
cgctcccatg atcactctgc acgccgaagg caaatagtgc aggccgtgcg gcgcttggcg
300
ttccttggaa gggctgaatc cccgcctcgt ccttcgcagc ggccccccgg gtgttcccat
360
cgccgcttct aggcccactg cgacgcttgc ctgcacttct tacacgctct gggtcccagc
420
cgcggcgacg caaagggcct tggtgcgggt ctcgtcggcg cagggacgcg tttgggtccc
480
gacggaacct tttccgcgtt ggggttgggg caccataagc t
521
<210> 186
<211> 118
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 186
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtg
118
<210> 187
<211> 221
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 187
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac g
221
<210> 188
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 188
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac gagggaccgc gacaggcaga
240
cgctcccatg atcactctgc acgccgaagg caaatagtgc aggccgtgcg gcgcttggcg
300
ttccttggaa gggctgaatc cccg
324
<210> 189
<211> 422
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 189
acccctctct ccagccacta agccagttgc tccctcggct gacggctgca cgcgaggcct
60
ccgaacgtct tacgccttgt ggcgcgcccg tccttgtccc gggtgtgatg gcggggtgtg
120
gggcggaggg cgtggcgggg aagggccggc gacgagagcc gcgcgggacg actcgtcggc
180
gataaccggt gtcgggtagc gccagccgcg cgacggtaac gagggaccgc gacaggcaga
240
cgctcccatg atcactctgc acgccgaagg caaatagtgc aggccgtgcg gcgcttggcg
300
ttccttggaa gggctgaatc cccgcctcgt ccttcgcagc ggccccccgg gtgttcccat
360
cgccgcttct aggcccactg cgacgcttgc ctgcacttct tacacgctct gggtcccagc
420
cg
422
<210> 190
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(21)
<223> /примечание="Остатки варианта, приведенные в
последовательности,
не являются предпочтительными относительно тех, которые приведены в
аннотациях
для положений варианта"
<400> 190
Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu
1 5 10 15
Glu Asn Pro Gly Pro
20
<210> 191
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(22)
<223> /примечание="Остатки варианта, приведенные в
последовательности,
не являются предпочтительными относительно тех, которые приведены в
аннотациях
для положений варианта"
<400> 191
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 192
<211> 23
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(23)
<223> /примечание="Остатки варианта, приведенные в
последовательности,
не являются предпочтительными относительно тех, которые приведены в
аннотациях
для положений варианта"
<400> 192
Gly Ser Gly Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp
1 5 10 15
Val Glu Ser Asn Pro Gly Pro
20
<210> 193
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<220>
<221> ВАРИАНТ
<222> (1)..(3)
<223> /замена=" "
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(25)
<223> /примечание="Остатки варианта, приведенные в
последовательности,
не являются предпочтительными относительно тех, которые приведены в
аннотациях
для положений варианта"
<400> 193
Gly Ser Gly Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala
1 5 10 15
Gly Asp Val Glu Ser Asn Pro Gly Pro
20 25
<210> 194
<400> 194
000
<210> 195
<400> 195
000
<210> 196
<400> 196
000
<210> 197
<400> 197
000
<210> 198
<400> 198
000
<210> 199
<400> 199
000
<210> 200
<400> 200
000
<210> 201
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 201
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser Ile Leu Gln Asn Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu
210 215 220
Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 202
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 202
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Asn Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Ile Arg Met Thr Gln Ser Pro Ser
130 135 140
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
145 150 155 160
Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser Ile Leu Gln Asn Gly
180 185 190
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu
210 215 220
Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 203
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 203
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe
50 55 60
Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser Pro Ala Ile
130 135 140
Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser
145 150 155 160
Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln Lys Ser Gly Thr Ser
165 170 175
Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro
180 185 190
Gly Arg Phe Ser Gly Ser Gly Ser Gly Asn Ser Tyr Ser Leu Thr Ile
195 200 205
Ser Ser Val Glu Ala Glu Asp Asp Ala Thr Tyr Tyr Cys Gln Gln Trp
210 215 220
Ser Gly Tyr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile
225 230 235
<210> 204
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 204
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Arg Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
130 135 140
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Ile Ser Cys
145 150 155 160
Arg Ala Ser Gln Ser Val Ser Ser Asn Phe Ala Trp Tyr Gln Gln Arg
165 170 175
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Asn Arg Ala
180 185 190
Thr Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Ala Tyr Tyr
210 215 220
Cys His Gln Arg Ser Asn Trp Leu Tyr Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Asp Ile Lys
<210> 205
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 205
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Arg Arg Thr Val Val Thr Pro Arg Ala Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser
145 150 155 160
Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser
165 170 175
Asn Ser Leu Asn Trp Tyr Gln Gln Lys Ala Gly Lys Ala Pro Lys Leu
180 185 190
Leu Ile Tyr Asp Ala Ser Thr Leu Glu Thr Gly Val Pro Ser Arg Phe
195 200 205
Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Phe Thr Ile Ser Ser Leu
210 215 220
Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln His Asp Asn Leu
225 230 235 240
Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
245 250
<210> 206
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 206
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Pro Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Glu Trp Asp Gly Ser Tyr Tyr Tyr Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Leu
130 135 140
Thr Gln Thr Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Thr Tyr Leu Asn Trp Tyr
165 170 175
Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser
180 185 190
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Thr Tyr Tyr Cys Gln Gln Ser Phe Ser Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 207
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 207
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Val Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asn Thr Asp Gly Ser Thr Thr Thr Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Gly Gly His Trp Ala Val Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Thr
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Asp Arg Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Val Tyr Tyr Cys Gln Gln
210 215 220
Tyr Gly His Leu Pro Met Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu
225 230 235 240
Ile Lys
<210> 208
<211> 252
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 208
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Arg Leu Ile Ala Val Ala Gly Asp Tyr Tyr Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ala Ser Val
145 150 155 160
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Val Gly Arg
165 170 175
Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Thr Ala Pro Lys Leu Leu
180 185 190
Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Leu Gln
210 215 220
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro
225 230 235 240
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
245 250
<210> 209
<211> 250
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 209
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Lys Val Ser Ser Ser Ser Pro Ala Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val
130 135 140
Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr Thr Lys Tyr Leu Gly
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp
180 185 190
Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro Leu Ile Thr
225 230 235 240
Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
245 250
<210> 210
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 210
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr Pro Phe Thr Gly Tyr
20 25 30
Ser Leu His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Gly Asn Ser Leu Phe Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr
130 135 140
Gln Ser Pro Ser Ser Ile Ser Ala Ser Val Gly Asp Thr Val Ser Ile
145 150 155 160
Thr Cys Arg Ala Ser Gln Asp Ser Gly Thr Trp Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Met Tyr Asp Ala Ser Thr
180 185 190
Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Ala Ser Gly Thr
195 200 205
Glu Phe Thr Leu Thr Val Asn Arg Leu Gln Pro Glu Asp Ser Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Asp Ile Lys
245
<210> 211
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 211
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Glu Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Gly Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val His
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Tyr Ser Ser Ser Ser Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
130 135 140
Met Thr Gln Ser Pro Pro Ser Leu Ser Ala Ser Val Gly Asp Arg Val
145 150 155 160
Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Ala Leu Ala Trp
165 170 175
Tyr Gln Gln Lys Pro Gly Thr Pro Pro Lys Leu Leu Ile Tyr Asp Ala
180 185 190
Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
195 200 205
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
210 215 220
Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Ser Tyr Pro Leu Thr Phe Gly
225 230 235 240
Gly Gly Thr Arg Leu Glu Ile Lys
245
<210> 212
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 212
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ala Gly Gly Ile Tyr Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Thr Ile Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Val Met Thr Gln Thr Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg
145 150 155 160
Ala Thr Ile Ser Cys Lys Ser Ser His Ser Val Leu Tyr Asn Arg Asn
165 170 175
Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
180 185 190
Lys Leu Leu Phe Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val Pro Asp
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Thr Gln
225 230 235 240
Thr Phe Pro Leu Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Asn
245 250 255
<210> 213
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 213
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Thr Thr Thr Ser Tyr Ala Phe Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln
130 135 140
Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Lys Ala Ser Thr Leu
180 185 190
Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Thr Tyr
210 215 220
Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 214
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 214
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe Ile Phe Ser Asp Tyr
20 25 30
Tyr Met Gly Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Gly Arg Ser Gly Ser Ser Met Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Phe Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ala Ser Pro Val Val Ala Ala Thr Glu Asp Phe Gln His Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val
130 135 140
Met Thr Gln Thr Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr Ser Asn Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Leu Phe Gly
180 185 190
Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Met Tyr Tyr Cys Gln Gln Tyr Gly Ser Ala Pro Val Thr Phe
225 230 235 240
Gly Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 215
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 215
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Ala Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Phe Thr Phe Arg Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Arg Ala Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Thr Ala Ser Cys Gly Gly Asp Cys Tyr Tyr Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Met Thr Gln Ser Pro Pro Thr Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val Asn Ile Trp Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys
180 185 190
Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser Tyr Pro Leu Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Asp Ile Lys
245
<210> 216
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 216
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Gly Ser Ser Ser Trp Ser Trp Gly Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu Thr Gln Asp
130 135 140
Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val Arg Thr Thr Cys Gln
145 150 155 160
Gly Asp Ala Leu Arg Ser Tyr Tyr Ala Ser Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Gln Ala Pro Met Leu Val Ile Tyr Gly Lys Asn Asn Arg Pro Ser
180 185 190
Gly Ile Pro Asp Arg Phe Ser Gly Ser Asp Ser Gly Asp Thr Ala Ser
195 200 205
Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys
210 215 220
Asn Ser Arg Asp Ser Ser Gly Tyr Pro Val Phe Gly Thr Gly Thr Lys
225 230 235 240
Val Thr Val Leu
<210> 217
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 217
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly Ser Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu Thr Gln
130 135 140
Glu Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val Arg Ile Thr Cys
145 150 155 160
Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ala Pro Val Leu Val Ile Phe Gly Arg Ser Arg Arg Pro
180 185 190
Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser Ser Gly Asn Thr Ala
195 200 205
Ser Leu Ile Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr
210 215 220
Cys Asn Ser Arg Asp Asn Thr Ala Asn His Tyr Val Phe Gly Thr Gly
225 230 235 240
Thr Lys Leu Thr Val Leu
245
<210> 218
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 218
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly Ser Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu Thr Gln
130 135 140
Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val Arg Ile Thr Cys
145 150 155 160
Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly Lys Asn Asn Arg Pro
180 185 190
Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser Ser Gly Asn Thr Ala
195 200 205
Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr
210 215 220
Cys Asn Ser Arg Gly Ser Ser Gly Asn His Tyr Val Phe Gly Thr Gly
225 230 235 240
Thr Lys Val Thr Val Leu
245
<210> 219
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 219
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Val Trp Val
35 40 45
Ser Arg Ile Asn Ser Asp Gly Ser Ser Thr Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Thr Gly Trp Val Gly Ser Tyr Tyr Tyr Tyr Met Asp Val Trp
100 105 110
Gly Lys Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
130 135 140
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
145 150 155 160
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Tyr Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Arg Leu Leu Ile Tyr
180 185 190
Asp Val Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly Gly
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu
210 215 220
Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro Trp
225 230 235 240
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
245 250
<210> 220
<211> 250
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 220
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Gly Tyr Ser Arg Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val
130 135 140
Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr Thr Lys Tyr Leu Gly
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp
180 185 190
Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro Leu Ile Thr
225 230 235 240
Phe Gly Gln Gly Thr Lys Val Asp Ile Lys
245 250
<210> 221
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 221
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Arg Glu Ala Ala Ala Gly His Asp Trp Tyr Phe Asp Leu Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Arg Val Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala
180 185 190
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Ile Pro Leu Thr Phe
225 230 235 240
Gly Gln Gly Thr Lys Val Glu Ile Lys
245
<210> 222
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 222
Gln Val Gln Leu Val Gln Ser Trp Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Asn Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Pro Arg Val Thr Thr Gly Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
130 135 140
Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser
180 185 190
Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala
210 215 220
Thr Tyr Tyr Cys Gln Gln Tyr Ser Ser Tyr Pro Leu Thr Phe Gly Gly
225 230 235 240
Gly Thr Arg Leu Glu Ile Lys
245
<210> 223
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 223
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Arg Ala Ser Gly Asp Thr Ser Thr Arg His
20 25 30
Tyr Ile His Trp Leu Arg Gln Ala Pro Gly Gln Gly Pro Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Thr Thr Gly Pro Ala Thr Gly Ser Pro Ala Tyr
50 55 60
Ala Gln Met Leu Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr
65 70 75 80
Arg Thr Val Tyr Met Glu Leu Arg Ser Leu Arg Phe Glu Asp Thr Ala
85 90 95
Val Tyr Tyr Cys Ala Arg Ser Val Val Gly Arg Ser Ala Pro Tyr Tyr
100 105 110
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
145 150 155 160
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser
165 170 175
Asp Tyr Ser Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
180 185 190
Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe
195 200 205
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Tyr Leu
210 215 220
Gln Ser Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Tyr
225 230 235 240
Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
245 250
<210> 224
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 224
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Tyr Thr Thr Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Leu Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ile Arg Ser Cys Gly Gly Asp Cys Tyr Tyr Phe Asp Asn Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
130 135 140
Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg
145 150 155 160
Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val Asn Ile Trp Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys
180 185 190
Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp
210 215 220
Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser Tyr Pro Leu Thr Phe
225 230 235 240
Gly Gly Gly Thr Lys Val Asp Ile Lys
245
<210> 225
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 225
Gln Ile Thr Leu Lys Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Ser Thr Ala
20 25 30
Gly Val His Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Leu Ile Ser Trp Ala Asp Asp Lys Arg Tyr Arg Pro Ser
50 55 60
Leu Arg Ser Arg Leu Asp Ile Thr Arg Val Thr Ser Lys Asp Gln Val
65 70 75 80
Val Leu Ser Met Thr Asn Met Gln Pro Glu Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Leu Gln Gly Phe Asp Gly Tyr Glu Ala Asn Trp Gly Pro Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr
130 135 140
Gln Ser Pro Ser Ser Leu Ser Ala Ser Ala Gly Asp Arg Val Thr Ile
145 150 155 160
Thr Cys Arg Ala Ser Arg Gly Ile Ser Ser Ala Leu Ala Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Lys Pro Pro Lys Leu Leu Ile Tyr Asp Ala Ser Ser
180 185 190
Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Asp Ser Leu Glu Pro Glu Asp Phe Ala Thr
210 215 220
Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Trp Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Asp Ile Lys
245
<210> 226
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 226
Gly Tyr Thr Phe Thr Asp Tyr Tyr Met His
1 5 10
<210> 227
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 227
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 228
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 228
Gly Trp Asp Phe Asp Tyr
1 5
<210> 229
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 229
Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His
1 5 10
<210> 230
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 230
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Asn Phe Gln
1 5 10 15
Gly
<210> 231
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 231
Gly Tyr Ser Phe Thr Gly Tyr Thr Met Asn
1 5 10
<210> 232
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 232
Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser Tyr Asn Gln Lys Phe Arg
1 5 10 15
Gly
<210> 233
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 233
Gly Gly Tyr Asp Gly Arg Gly Phe Asp Tyr
1 5 10
<210> 234
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 234
Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 235
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 235
Gly Arg Tyr Tyr Gly Met Asp Val
1 5
<210> 236
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 236
Asp Leu Arg Arg Thr Val Val Thr Pro Arg Ala Tyr Tyr Gly Met Asp
1 5 10 15
Val
<210> 237
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 237
Gly Glu Trp Asp Gly Ser Tyr Tyr Tyr Asp Tyr
1 5 10
<210> 238
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 238
Gly Phe Thr Phe Ser Ser Tyr Trp Met His
1 5 10
<210> 239
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 239
Arg Ile Asn Thr Asp Gly Ser Thr Thr Thr Tyr Ala Asp Ser Val Glu
1 5 10 15
Gly
<210> 240
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 240
Gly His Trp Ala Val
1 5
<210> 241
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 241
Gly Tyr Thr Phe Thr Ser Tyr Tyr Met His
1 5 10
<210> 242
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 242
Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
<210> 243
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 243
Tyr Arg Leu Ile Ala Val Ala Gly Asp Tyr Tyr Tyr Tyr Gly Met Asp
1 5 10 15
Val
<210> 244
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 244
Gly Phe Thr Phe Ser Ser Tyr Ala Met His
1 5 10
<210> 245
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 245
Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 246
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 246
Trp Lys Val Ser Ser Ser Ser Pro Ala Phe Asp Tyr
1 5 10
<210> 247
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 247
Gly Tyr Pro Phe Thr Gly Tyr Ser Leu His
1 5 10
<210> 248
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 248
Asp His Tyr Gly Gly Asn Ser Leu Phe Tyr
1 5 10
<210> 249
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 249
Ile Ile Asn Pro Ser Gly Gly Ser Thr Gly Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 250
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 250
Gly Gly Tyr Ser Ser Ser Ser Asp Ala Phe Asp Ile
1 5 10
<210> 251
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 251
Gly Tyr Thr Phe Thr Ser Tyr Gly Ile Ser
1 5 10
<210> 252
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 252
Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu Gln
1 5 10 15
<210> 253
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 253
Val Ala Gly Gly Ile Tyr Tyr Tyr Tyr Gly Met Asp Val
1 5 10
<210> 254
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 254
Thr Thr Thr Ser Tyr Ala Phe Asp Ile
1 5
<210> 255
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 255
Gly Phe Ile Phe Ser Asp Tyr Tyr Met Gly
1 5 10
<210> 256
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 256
Tyr Ile Gly Arg Ser Gly Ser Ser Met Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 257
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 257
Ser Pro Val Val Ala Ala Thr Glu Asp Phe Gln His
1 5 10
<210> 258
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 258
Gly Phe Thr Phe Arg Gly Tyr Tyr Ile His
1 5 10
<210> 259
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 259
Ile Ile Asn Pro Ser Gly Gly Ser Arg Ala Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 260
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 260
Thr Ala Ser Cys Gly Gly Asp Cys Tyr Tyr Leu Asp Tyr
1 5 10
<210> 261
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 261
Gly Phe Thr Phe Asp Asp Tyr Ala Met His
1 5 10
<210> 262
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 262
Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
<210> 263
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 263
Asp Gly Ser Ser Ser Trp Ser Trp Gly Tyr Phe Asp Tyr
1 5 10
<210> 264
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 264
Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 265
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 265
Asp Ser Ser Ser Trp Tyr Gly Gly Gly Ser Ala Phe Asp Ile
1 5 10
<210> 266
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 266
Arg Ile Asn Ser Asp Gly Ser Ser Thr Ser Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 267
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 267
Thr Gly Trp Val Gly Ser Tyr Tyr Tyr Tyr Met Asp Val
1 5 10
<210> 268
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 268
Gly Phe Thr Phe Ser Ser Tyr Gly Met His
1 5 10
<210> 269
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 269
Gly Tyr Ser Arg Tyr Tyr Tyr Tyr Gly Met Asp Val
1 5 10
<210> 270
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 270
Gly Phe Thr Phe Ser Ser Tyr Ala Met Ser
1 5 10
<210> 271
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 271
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 272
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 272
Arg Glu Ala Ala Ala Gly His Asp Trp Tyr Phe Asp Leu
1 5 10
<210> 273
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 273
Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 274
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 274
Ser Pro Arg Val Thr Thr Gly Tyr Phe Asp Tyr
1 5 10
<210> 275
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 275
Gly Asp Thr Ser Thr Arg His Tyr Ile His
1 5 10
<210> 276
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 276
Val Ile Asn Pro Thr Thr Gly Pro Ala Thr Gly Ser Pro Ala Tyr Ala
1 5 10 15
Gln Met Leu Gln Gly
20
<210> 277
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 277
Ser Val Val Gly Arg Ser Ala Pro Tyr Tyr Phe Asp Tyr
1 5 10
<210> 278
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 278
Gly Tyr Thr Phe Thr Asn Tyr Tyr Met His
1 5 10
<210> 279
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 279
Ile Ile Asn Pro Ser Gly Gly Tyr Thr Thr Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 280
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 280
Ile Arg Ser Cys Gly Gly Asp Cys Tyr Tyr Phe Asp Asn
1 5 10
<210> 281
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 281
Gly Phe Ser Leu Ser Thr Ala Gly Val His Val Gly
1 5 10
<210> 282
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 282
Leu Ile Ser Trp Ala Asp Asp Lys Arg Tyr Arg Pro Ser Leu Arg Ser
1 5 10 15
<210> 283
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 283
Gln Gly Phe Asp Gly Tyr Glu Ala Asn
1 5
<210> 284
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 284
Arg Ala Ser Gln Ser Ile Arg Tyr Tyr Leu Ser
1 5 10
<210> 285
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 285
Thr Ala Ser Ile Leu Gln Asn
1 5
<210> 286
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 286
Leu Gln Thr Tyr Thr Thr Pro Asp
1 5
<210> 287
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 287
Ser Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 288
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 288
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 289
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 289
Gln Gln Trp Ser Gly Tyr Pro Leu Thr
1 5
<210> 290
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 290
Arg Ala Ser Gln Ser Val Ser Ser Asn Phe Ala
1 5 10
<210> 291
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 291
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 292
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 292
His Gln Arg Ser Asn Trp Leu Tyr Thr
1 5
<210> 293
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 293
Gln Ala Ser Gln Asp Ile Ser Asn Ser Leu Asn
1 5 10
<210> 294
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 294
Asp Ala Ser Thr Leu Glu Thr
1 5
<210> 295
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 295
Gln Gln His Asp Asn Leu Pro Leu Thr
1 5
<210> 296
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 296
Arg Ala Ser Gln Ser Ile Asn Thr Tyr Leu Asn
1 5 10
<210> 297
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 297
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 298
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 298
Gln Gln Ser Phe Ser Pro Leu Thr
1 5
<210> 299
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 299
Arg Ala Ser Gln Ser Ile Ser Asp Arg Leu Ala
1 5 10
<210> 300
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 300
Lys Ala Ser Ser Leu Glu Ser
1 5
<210> 301
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 301
Gln Gln Tyr Gly His Leu Pro Met Tyr Thr
1 5 10
<210> 302
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 302
Arg Ala Ser Gln Gly Val Gly Arg Trp Leu Ala
1 5 10
<210> 303
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 303
Ala Ala Ser Thr Leu Gln Ser
1 5
<210> 304
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 304
Gln Gln Ala Asn Ser Phe Pro Leu Thr
1 5
<210> 305
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 305
Arg Ala Ser Gln Ser Val Tyr Thr Lys Tyr Leu Gly
1 5 10
<210> 306
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 306
Asp Ala Ser Thr Arg Ala Thr
1 5
<210> 307
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 307
Gln His Tyr Gly Gly Ser Pro Leu Ile Thr
1 5 10
<210> 308
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 308
Arg Ala Ser Gln Asp Ser Gly Thr Trp Leu Ala
1 5 10
<210> 309
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 309
Asp Ala Ser Thr Leu Glu Asp
1 5
<210> 310
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 310
Gln Gln Tyr Asn Ser Tyr Pro Leu Thr
1 5
<210> 311
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 311
Arg Ala Ser Gln Asp Ile Ser Ser Ala Leu Ala
1 5 10
<210> 312
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 312
Asp Ala Ser Ser Leu Glu Ser
1 5
<210> 313
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 313
Gln Gln Phe Ser Ser Tyr Pro Leu Thr
1 5
<210> 314
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 314
Lys Ser Ser His Ser Val Leu Tyr Asn Arg Asn Asn Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 315
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 315
Trp Ala Ser Thr Arg Lys Ser
1 5
<210> 316
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 316
Gln Gln Thr Gln Thr Phe Pro Leu Thr
1 5
<210> 317
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 317
Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu Ala
1 5 10
<210> 318
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 318
Lys Ala Ser Thr Leu Glu Ser
1 5
<210> 319
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 319
Gln Gln Tyr Asn Thr Tyr Ser Pro Tyr Thr
1 5 10
<210> 320
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 320
Arg Ala Ser Gln Ser Val Thr Ser Asn Tyr Leu Ala
1 5 10
<210> 321
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 321
Gly Ala Ser Thr Arg Ala Thr
1 5
<210> 322
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 322
Gln Gln Tyr Gly Ser Ala Pro Val Thr
1 5
<210> 323
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 323
Arg Ala Ser Glu Asn Val Asn Ile Trp Leu Ala
1 5 10
<210> 324
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 324
Lys Ser Ser Ser Leu Ala Ser
1 5
<210> 325
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 325
Gln Gln Tyr Gln Ser Tyr Pro Leu Thr
1 5
<210> 326
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 326
Gln Gly Asp Ala Leu Arg Ser Tyr Tyr Ala Ser
1 5 10
<210> 327
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 327
Gly Lys Asn Asn Arg Pro Ser
1 5
<210> 328
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 328
Asn Ser Arg Asp Ser Ser Gly Tyr Pro Val
1 5 10
<210> 329
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 329
Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser
1 5 10
<210> 330
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 330
Gly Arg Ser Arg Arg Pro Ser
1 5
<210> 331
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 331
Asn Ser Arg Asp Asn Thr Ala Asn His Tyr Val
1 5 10
<210> 332
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 332
Asn Ser Arg Gly Ser Ser Gly Asn His Tyr Val
1 5 10
<210> 333
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 333
Arg Ala Ser Gln Ser Val Ser Ser Asn Tyr Leu Ala
1 5 10
<210> 334
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 334
Asp Val Ser Thr Arg Ala Thr
1 5
<210> 335
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 335
Gln Gln Arg Ser Asn Trp Pro Pro Trp Thr
1 5 10
<210> 336
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 336
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 337
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 337
Gln Gln Ser Tyr Ser Ile Pro Leu Thr
1 5
<210> 338
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 338
Arg Ala Ser Gln Ser Ile Ser Ser Trp Leu Ala
1 5 10
<210> 339
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 339
Gln Gln Tyr Ser Ser Tyr Pro Leu Thr
1 5
<210> 340
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 340
Arg Ala Ser Gln Gly Ile Ser Asp Tyr Ser
1 5 10
<210> 341
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 341
Gln Gln Tyr Tyr Ser Tyr Pro Leu Thr
1 5
<210> 342
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 342
Arg Ala Ser Arg Gly Ile Ser Ser Ala Leu Ala
1 5 10
<210> 343
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 343
Gln Gln Ser Tyr Ser Thr Pro Trp Thr
1 5
<210> 344
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 344
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp Ser
130 135 140
Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 345
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 345
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro
35 40 45
Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr
195 200 205
Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
210 215 220
Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 346
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 346
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile Asn Thr Val Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 347
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 347
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile
195 200 205
Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
210 215 220
Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 348
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 348
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr Asn Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 349
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 349
Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile Asn Thr Val Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr Thr Val Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser Pro Asp Ser
130 135 140
Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser
145 150 155 160
Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln
165 170 175
Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys
180 185 190
Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val
210 215 220
Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 350
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 350
Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro
35 40 45
Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser Ile
195 200 205
Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
210 215 220
Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 351
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 351
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe Asn
145 150 155 160
Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr
180 185 190
Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser Thr
195 200 205
Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
210 215 220
Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly Thr
225 230 235 240
Thr Val Thr Val Ser Ser
245
<210> 352
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 352
Glu Ile Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Gly Ser Gly Phe Asn Ile Glu Asp Tyr
20 25 30
Tyr Ile His Trp Val Lys Gln Arg Thr Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys Tyr Gly Pro Ile Phe
50 55 60
Gln Gly Arg Ala Thr Ile Thr Ala Asp Thr Ser Ser Asn Thr Val Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Phe Arg Gly Gly Val Tyr Trp Gly Pro Gly Thr Thr Leu Thr Val
100 105 110
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser His Met Asp Val Val Met Thr Gln Ser Pro Leu Thr Leu Ser Val
130 135 140
Ala Ile Gly Gln Ser Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu
145 150 155 160
Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro
165 170 175
Gly Gln Ser Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu Asp Ser
180 185 190
Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Tyr Cys
210 215 220
Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 353
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 353
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Asn Leu Glu Trp Ile
35 40 45
Gly Leu Ile Asn Pro Tyr Asn Gly Gly Thr Ile Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Gly Phe Val Leu Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ile Val Leu Thr Gln Ser
130 135 140
Pro Ser Ile Met Ser Val Ser Pro Gly Glu Lys Val Thr Ile Thr Cys
145 150 155 160
Ser Ala Ser Ser Ser Val Ser Tyr Met His Trp Phe Gln Gln Lys Pro
165 170 175
Gly Thr Ser Pro Lys Leu Cys Ile Tyr Ser Thr Ser Asn Leu Ala Ser
180 185 190
Gly Val Pro Ala Arg Phe Ser Gly Arg Gly Ser Gly Thr Ser Tyr Ser
195 200 205
Leu Thr Ile Ser Arg Val Ala Ala Glu Asp Ala Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Arg Ser Asn Tyr Pro Pro Trp Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys
<210> 354
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 354
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Asn Leu Glu Trp Ile
35 40 45
Gly Leu Ile Asn Pro Tyr Asn Gly Gly Thr Ile Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Gly Phe Val Leu Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ile Val Leu Thr Gln Ser
130 135 140
Pro Ala Ile Met Ser Ala Ser Pro Gly Glu Lys Val Thr Ile Thr Cys
145 150 155 160
Ser Ala Ser Ser Ser Val Ser Tyr Leu His Trp Phe Gln Gln Lys Pro
165 170 175
Gly Thr Ser Pro Lys Leu Trp Val Tyr Ser Thr Ser Asn Leu Pro Ser
180 185 190
Gly Val Pro Ala Arg Phe Gly Gly Ser Gly Ser Gly Thr Ser Tyr Ser
195 200 205
Leu Thr Ile Ser Arg Met Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Arg Ser Ile Tyr Pro Pro Trp Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys
<210> 355
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 355
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Asn Leu Glu Trp Ile
35 40 45
Gly Leu Ile Asn Pro Tyr Asn Gly Gly Thr Ile Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Tyr Gly Phe Val Leu Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Ile Val Leu Thr Gln Ser
130 135 140
Pro Ser Ile Met Ser Val Ser Pro Gly Glu Lys Val Thr Ile Thr Cys
145 150 155 160
Ser Ala Ser Ser Ser Val Ser Tyr Met His Trp Phe Gln Gln Lys Pro
165 170 175
Gly Thr Ser Pro Lys Leu Gly Ile Tyr Ser Thr Ser Asn Leu Ala Ser
180 185 190
Gly Val Pro Ala Arg Phe Ser Gly Arg Gly Ser Gly Thr Ser Tyr Ser
195 200 205
Leu Thr Ile Ser Arg Val Ala Ala Glu Asp Ala Ala Thr Tyr Tyr Cys
210 215 220
Gln Gln Arg Ser Asn Tyr Pro Pro Trp Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys
<210> 356
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 356
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Lys Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser Val Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu Thr Ile Ile
180 185 190
Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln
195 200 205
Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
225 230 235 240
Ser Ser
<210> 357
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 357
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 358
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 358
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 359
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 359
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 360
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 360
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 361
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 361
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 362
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 362
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 363
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 363
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 364
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 364
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 365
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 365
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 366
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 366
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 367
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 367
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 368
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 368
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 369
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 369
Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
1 5 10
<210> 370
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 370
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 371
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 371
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
1 5 10
<210> 372
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 372
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
1 5 10 15
<210> 373
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 373
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
1 5 10 15
<210> 374
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 374
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
1 5 10 15
<210> 375
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 375
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
1 5 10
<210> 376
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 376
His Thr Ser Arg Leu His Ser
1 5
<210> 377
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 377
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 378
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 378
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 379
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 379
Gln Val Gln Leu Leu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Ser Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr
115
<210> 380
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 380
Glu Leu Val Leu Thr Gln Ser Pro Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Pro Leu Ile
35 40 45
Tyr Ser Ala Thr Tyr Arg Asn Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Lys Asp Leu Ala Asp Tyr Phe Tyr Phe Cys Gln Tyr Asn Arg Tyr Pro
85 90 95
Tyr Thr Ser Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Arg Ser
100 105 110
<210> 381
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 381
Gln Val Gln Leu Leu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Ser Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Gly Ser Thr Ser Gly Ser Gly Lys Pro
115 120 125
Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Leu Val Leu Thr Gln Ser
130 135 140
Pro Lys Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val Thr Cys
145 150 155 160
Lys Ala Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr Arg Asn
180 185 190
Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp Tyr Phe
210 215 220
Tyr Phe Cys Gln Tyr Asn Arg Tyr Pro Tyr Thr Ser Gly Gly Gly Thr
225 230 235 240
Lys Leu Glu Ile Lys Arg Arg Ser
245
<210> 382
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 382
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
210 215 220
Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 383
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 383
gaagtgcaat tggtggaatc agggggagga cttgtgcagc ctggaggatc gctgagactg
60
tcatgtgccg tgtccggctt tgccctgtcc aaccacggga tgtcctgggt ccgccgcgcg
120
cctggaaagg gcctcgaatg ggtgtcgggt attgtgtaca gcggtagcac ctactatgcc
180
gcatccgtga aggggagatt caccatcagc cgggacaact ccaggaacac tctgtacctc
240
caaatgaatt cgctgaggcc agaggacact gccatctact actgctccgc gcatggcgga
300
gagtccgacg tctggggaca ggggaccacc gtgaccgtgt ctagcgcgtc cggcggaggc
360
ggcagcgggg gtcgggcatc agggggcggc ggatcggaca tccagctcac ccagtccccg
420
agctcgctgt ccgcctccgt gggagatcgg gtcaccatca cgtgccgcgc cagccagtcg
480
atttcctcct acctgaactg gtaccaacag aagcccggaa aagccccgaa gcttctcatc
540
tacgccgcct cgagcctgca gtcaggagtg ccctcacggt tctccggctc cggttccggt
600
actgatttca ccctgaccat ttcctccctg caaccggagg acttcgctac ttactactgc
660
cagcagtcgt actccacccc ctacactttc ggacaaggca ccaaggtcga aatcaag
717
<210> 384
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 384
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 385
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 385
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 386
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 386
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Gly Trp Val
35 40 45
Ser Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Pro Ala His Tyr Tyr Gly Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser
130 135 140
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
145 150 155 160
Arg Ala Ser Gln Ser Ile Ser Ser Ser Phe Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Arg Arg
180 185 190
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Ser Ala Val Tyr
210 215 220
Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 387
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 387
caagtgcaac tcgtggaatc tggtggagga ctcgtgcaac ccggaagatc gcttagactg
60
tcgtgtgccg ccagcgggtt cactttctcg aactacgcga tgtcctgggt ccgccaggca
120
cccggaaagg gactcggttg ggtgtccggc atttcccggt ccggcgaaaa tacctactac
180
gccgactccg tgaagggccg cttcaccatc tcaagggaca acagcaaaaa caccctgtac
240
ttgcaaatga actccctgcg ggatgaagat acagccgtgt actattgcgc ccggtcgcct
300
gcccattact acggcggaat ggacgtctgg ggacagggaa ccactgtgac tgtcagcagc
360
gcgtcgggtg gcggcggctc agggggtcgg gcctccgggg ggggagggtc cgacatcgtg
420
ctgacccagt ccccgggaac cctgagcctg agcccgggag agcgcgcgac cctgtcatgc
480
cgggcatccc agagcattag ctcctccttt ctcgcctggt atcagcagaa gcccggacag
540
gccccgaggc tgctgatcta cggcgctagc agaagggcta ccggaatccc agaccggttc
600
tccggctccg gttccgggac cgatttcacc cttactatct cgcgcctgga acctgaggac
660
tccgccgtct actactgcca gcagtaccac tcatccccgt cgtggacgtt cggacagggc
720
accaagctgg agattaag
738
<210> 388
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 388
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Gly Trp Val
35 40 45
Ser Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Pro Ala His Tyr Tyr Gly Gly Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 389
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 389
Asp Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Arg Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 390
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 390
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ser Val His Ser Phe Leu Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro
130 135 140
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser
145 150 155 160
Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys
165 170 175
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala
180 185 190
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
210 215 220
Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Glu Ile Lys
<210> 391
<211> 732
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 391
caagtgcaac tcgtcgaatc cggtggaggt ctggtccaac ctggtagaag cctgagactg
60
tcgtgtgcgg ccagcggatt cacctttgat gactatgcta tgcactgggt gcggcaggcc
120
ccaggaaagg gcctggaatg ggtgtcggga attagctgga actccgggtc cattggctac
180
gccgactccg tgaagggccg cttcaccatc tcccgcgaca acgcaaagaa ctccctgtac
240
ttgcaaatga actcgctcag ggctgaggat accgcgctgt actactgctc cgtgcattcc
300
ttcctggcct actggggaca gggaactctg gtcaccgtgt cgagcgcctc cggcggcggg
360
ggctcgggtg gacgggcctc gggcggaggg gggtccgaca tcgtgatgac ccagaccccg
420
ctgagcttgc ccgtgactcc cggagagcct gcatccatct cctgccggtc atcccagtcc
480
cttctccact ccaacggata caactacctc gactggtacc tccagaagcc gggacagagc
540
cctcagcttc tgatctacct ggggtcaaat agagcctcag gagtgccgga tcggttcagc
600
ggatctggtt cgggaactga tttcactctg aagatttccc gcgtggaagc cgaggacgtg
660
ggcgtctact actgtatgca ggcgctgcag accccctata ccttcggcca agggacgaaa
720
gtggagatca ag
732
<210> 392
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 392
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ser Val His Ser Phe Leu Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser
115
<210> 393
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 393
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 394
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 394
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser
130 135 140
Val Thr Pro Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser
145 150 155 160
Leu Leu Arg Asn Asp Gly Lys Thr Pro Leu Tyr Trp Tyr Leu Gln Lys
165 170 175
Ala Gly Gln Pro Pro Gln Leu Leu Ile Tyr Glu Val Ser Asn Arg Phe
180 185 190
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Ala Tyr Tyr
210 215 220
Cys Met Gln Asn Ile Gln Phe Pro Ser Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 395
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 395
gaagtgcaat tgttggaatc tggaggagga cttgtgcagc ctggaggatc actgagactt
60
tcgtgtgcgg tgtcaggctt cgccctgagc aaccacggca tgagctgggt gcggagagcc
120
ccggggaagg gtctggaatg ggtgtccggg atcgtctact ccggttcaac ttactacgcc
180
gcaagcgtga agggtcgctt caccatttcc cgcgataact cccggaacac cctgtacctc
240
caaatgaact ccctgcggcc cgaggacacc gccatctact actgttccgc gcatggagga
300
gagtccgatg tctggggaca gggcactacc gtgaccgtgt cgagcgcctc ggggggagga
360
ggctccggcg gtcgcgcctc cggggggggt ggcagcgaca ttgtgatgac gcagactcca
420
ctctcgctgt ccgtgacccc gggacagccc gcgtccatct cgtgcaagag ctcccagagc
480
ctgctgagga acgacggaaa gactcctctg tattggtacc tccagaaggc tggacagccc
540
ccgcaactgc tcatctacga agtgtcaaat cgcttctccg gggtgccgga tcggttttcc
600
ggctcgggat cgggcaccga cttcaccctg aaaatctcca gggtcgaggc cgaggacgtg
660
ggagcctact actgcatgca aaacatccag ttcccttcct tcggcggcgg cacaaagctg
720
gagattaag
729
<210> 396
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 396
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 397
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 397
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Arg Asn
20 25 30
Asp Gly Lys Thr Pro Leu Tyr Trp Tyr Leu Gln Lys Ala Gly Gln Pro
35 40 45
Pro Gln Leu Leu Ile Tyr Glu Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Ala Tyr Tyr Cys Met Gln Asn
85 90 95
Ile Gln Phe Pro Ser Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 398
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 398
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Lys Thr Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Asp Asn Phe
20 25 30
Gly Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Val Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
130 135 140
Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys
145 150 155 160
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asn
165 170 175
Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu
180 185 190
Gly Ser Lys Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu His Ile Thr Arg Val Gly Ala Glu Asp
210 215 220
Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe
225 230 235 240
Gly Gln Gly Thr Lys Leu Glu Ile Lys
245
<210> 399
<211> 747
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 399
caagtccaac tcgtccagtc cggcgcagaa gtcagaaaaa ccggtgctag cgtgaaagtg
60
tcctgcaagg cctccggcta cattttcgat aacttcggaa tcaactgggt cagacaggcc
120
ccgggccagg ggctggaatg gatgggatgg atcaacccca agaacaacaa caccaactac
180
gcacagaagt tccagggccg cgtgactatc accgccgatg aatcgaccaa taccgcctac
240
atggaggtgt cctccctgcg gtcggaggac actgccgtgt attactgcgc gaggggccca
300
tactactacc aaagctacat ggacgtctgg ggacagggaa ccatggtgac cgtgtcatcc
360
gcctccggtg gtggaggctc cggggggcgg gcttcaggag gcggaggaag cgatattgtg
420
atgacccaga ctccgcttag cctgcccgtg actcctggag aaccggcctc catttcctgc
480
cggtcctcgc aatcactcct gcattccaac ggttacaact acctgaattg gtacctccag
540
aagcctggcc agtcgcccca gttgctgatc tatctgggct cgaagcgcgc ctccggggtg
600
cctgaccggt ttagcggatc tgggagcggc acggacttca ctctccacat cacccgcgtg
660
ggagcggagg acgtgggagt gtactactgt atgcaggcgc tgcagactcc gtacacattc
720
ggacagggca ccaagctgga gatcaag
747
<210> 400
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 400
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Arg Lys Thr Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Asp Asn Phe
20 25 30
Gly Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Val Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met Asp Val Trp Gly Gln
100 105 110
Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 401
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 401
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Lys Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu His Ile
65 70 75 80
Thr Arg Val Gly Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 402
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 402
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Asp
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala Arg Gly Pro Arg Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
130 135 140
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
145 150 155 160
Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser
180 185 190
Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr His Phe Thr Leu Thr Ile Asn Ser Leu Gln Ser Glu Asp Ser Ala
210 215 220
Thr Tyr Tyr Cys Gln Gln Ser Tyr Lys Arg Ala Ser Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 403
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 403
caagtgcaac ttcaagaatc aggcggagga ctcgtgcagc ccggaggatc attgcggctc
60
tcgtgcgccg cctcgggctt caccttctcg agcgacgcca tgacctgggt ccgccaggcc
120
ccggggaagg ggctggaatg ggtgtctgtg atttccggct ccgggggaac tacgtactac
180
gccgattccg tgaaaggtcg cttcactatc tcccgggaca acagcaagaa caccctttat
240
ctgcaaatga attccctccg cgccgaggac accgccgtgt actactgcgc caagctggac
300
tcctcgggct actactatgc ccggggtccg agatactggg gacagggaac cctcgtgacc
360
gtgtcctccg cgtccggcgg aggagggtcg ggagggcggg cctccggcgg cggcggttcg
420
gacatccagc tgacccagtc cccatcctca ctgagcgcaa gcgtgggcga cagagtcacc
480
attacatgca gggcgtccca gagcatcagc tcctacctga actggtacca acagaagcct
540
ggaaaggctc ctaagctgtt gatctacggg gcttcgaccc tggcatccgg ggtgcccgcg
600
aggtttagcg gaagcggtag cggcactcac ttcactctga ccattaacag cctccagtcc
660
gaggattcag ccacttacta ctgtcagcag tcctacaagc gggccagctt cggacagggc
720
actaaggtcg agatcaag
738
<210> 404
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 404
Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Asp
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala Arg Gly Pro Arg Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 405
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 405
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr His Phe Thr Leu Thr Ile Asn Ser Leu Gln Ser
65 70 75 80
Glu Asp Ser Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Lys Arg Ala Ser
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 406
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 406
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Asn Tyr
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asn Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Tyr Met Asp Val Trp Gly Lys Gly Thr
100 105 110
Met Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg
115 120 125
Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Leu
130 135 140
Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser
145 150 155 160
Ser Gln Ser Leu Leu Tyr Ser Asn Gly Tyr Asn Tyr Val Asp Trp Tyr
165 170 175
Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser
180 185 190
Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Lys Leu Gln Ile Ser Arg Val Glu Ala Glu Asp Val Gly
210 215 220
Ile Tyr Tyr Cys Met Gln Gly Arg Gln Phe Pro Tyr Ser Phe Gly Gln
225 230 235 240
Gly Thr Lys Val Glu Ile Lys
245
<210> 407
<211> 741
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 407
caagtccaac tggtccagag cggtgcagaa gtgaagaagc ccggagcgag cgtgaaagtg
60
tcctgcaagg cttccgggta caccttctcc aactacggca tcacttgggt gcgccaggcc
120
ccgggacagg gcctggaatg gatggggtgg atttccgcgt acaacggcaa tacgaactac
180
gctcagaagt tccagggtag agtgaccatg actaggaaca cctccatttc caccgcctac
240
atggaactgt cctccctgcg gagcgaggac accgccgtgt actattgcgc ccggggacca
300
tactactact acatggatgt ctgggggaag gggactatgg tcaccgtgtc atccgcctcg
360
ggaggcggcg gatcaggagg acgcgcctct ggtggtggag gatcggagat cgtgatgacc
420
cagagccctc tctccttgcc cgtgactcct ggggagcccg catccatttc atgccggagc
480
tcccagtcac ttctctactc caacggctat aactacgtgg attggtacct ccaaaagccg
540
ggccagagcc cgcagctgct gatctacctg ggctcgaaca gggccagcgg agtgcctgac
600
cggttctccg ggtcgggaag cgggaccgac ttcaagctgc aaatctcgag agtggaggcc
660
gaggacgtgg gaatctacta ctgtatgcag ggccgccagt ttccgtactc gttcggacag
720
ggcaccaaag tggaaatcaa g
741
<210> 408
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 408
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Asn Tyr
20 25 30
Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asn Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Pro Tyr Tyr Tyr Tyr Met Asp Val Trp Gly Lys Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 409
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 409
Glu Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Asn Gly Tyr Asn Tyr Val Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Lys Leu Gln Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Gly
85 90 95
Arg Gln Phe Pro Tyr Ser Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 410
<211> 238
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 410
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Val Ser Pro Gly Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Ser Ser Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
165 170 175
Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala Ser Gly Ile Pro Asp
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr Gly
210 215 220
Ser Ser Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 411
<211> 714
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 411
gaagtgcaat tgctcgaaac tggaggaggt ctggtgcaac ctggaggatc acttcgcctg
60
tcctgcgccg tgtcgggctt tgccctgtcc aaccatggaa tgagctgggt ccgccgcgcg
120
ccggggaagg gcctcgaatg ggtgtccggc atcgtctact ccggctccac ctactacgcc
180
gcgtccgtga agggccggtt cacgatttca cgggacaact cgcggaacac cctgtacctc
240
caaatgaatt cccttcggcc ggaggatact gccatctact actgctccgc ccacggtggc
300
gaatccgacg tctggggcca gggaaccacc gtgaccgtgt ccagcgcgtc cgggggagga
360
ggaagcgggg gtagagcatc gggtggaggc ggatcagaga tcgtgctgac ccagtccccc
420
gccaccttga gcgtgtcacc aggagagtcc gccaccctgt catgccgcgc cagccagtcc
480
gtgtcctcca acctggcttg gtaccagcag aagccggggc aggcccctag actcctgatc
540
tatggggcgt cgacccgggc atctggaatt cccgataggt tcagcggatc gggctcgggc
600
actgacttca ctctgaccat ctcctcgctg caagccgagg acgtggctgt gtactactgt
660
cagcagtacg gaagctccct gactttcggt ggcgggacca aagtcgagat taag
714
<210> 412
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 412
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 413
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 413
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Ser Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Leu Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 414
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 414
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Ser Ser Lys Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
165 170 175
Arg Leu Leu Met Tyr Gly Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly
210 215 220
Ser Ser Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 415
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 415
gaagtgcaat tggtggaaac tggaggagga cttgtgcaac ctggaggatc attgagactg
60
agctgcgcag tgtcgggatt cgccctgagc aaccatggaa tgtcctgggt cagaagggcc
120
cctggaaaag gcctcgaatg ggtgtcaggg atcgtgtact ccggttccac ttactacgcc
180
gcctccgtga aggggcgctt cactatctca cgggataact cccgcaatac cctgtacctc
240
caaatgaaca gcctgcggcc ggaggatacc gccatctact actgttccgc ccacggtgga
300
gagtctgacg tctggggcca gggaactacc gtgaccgtgt cctccgcgtc cggcggtgga
360
gggagcggcg gccgcgccag cggcggcgga ggctccgaga tcgtgatgac ccagagcccc
420
gctactctgt cggtgtcgcc cggagaaagg gcgaccctgt cctgccgggc gtcgcagtcc
480
gtgagcagca agctggcttg gtaccagcag aagccgggcc aggcaccacg cctgcttatg
540
tacggtgcct ccattcgggc caccggaatc ccggaccggt tctcggggtc ggggtccggt
600
accgagttca cactgaccat ttcctcgctc gagcccgagg actttgccgt ctattactgc
660
cagcagtacg gctcctcctc atggacgttc ggccagggga ccaaggtcga aatcaag
717
<210> 416
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 416
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 417
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 417
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Lys
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Met
35 40 45
Tyr Gly Ala Ser Ile Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Ser Trp
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 418
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 418
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser
130 135 140
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Gly Ser Thr Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Ile Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Gly Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr
210 215 220
Gly Ser Ser Pro Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 419
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 419
gaagtgcaat tggtggagac tggaggagga gtggtgcaac ctggaggaag cctgagactg
60
tcatgcgcgg tgtcgggctt cgccctctcc aaccacggaa tgtcctgggt ccgccgggcc
120
cctgggaaag gacttgaatg ggtgtccggc atcgtgtact cgggttccac ctactacgcg
180
gcctcagtga agggccggtt tactattagc cgcgacaact ccagaaacac actgtacctc
240
caaatgaact cgctgcggcc ggaagatacc gctatctact actgctccgc ccatggggga
300
gagtcggacg tctggggaca gggcaccact gtcactgtgt ccagcgcttc cggcggtggt
360
ggaagcgggg gacgggcctc aggaggcggt ggcagcgaga ttgtgctgac ccagtccccc
420
gggaccctga gcctgtcccc gggagaaagg gccaccctct cctgtcgggc atcccagtcc
480
gtggggtcta ctaaccttgc atggtaccag cagaagcccg gccaggcccc tcgcctgctg
540
atctacgacg cgtccaatag agccaccggc atcccggatc gcttcagcgg aggcggatcg
600
ggcaccgact tcaccctcac catttcaagg ctggaaccgg aggacttcgc cgtgtactac
660
tgccagcagt atggttcgtc cccaccctgg acgttcggcc aggggactaa ggtcgagatc
720
aag
723
<210> 420
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 420
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Val Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 421
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 421
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Thr
20 25 30
Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Gly Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Pro
85 90 95
Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 422
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 422
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Gly Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
130 135 140
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
145 150 155 160
Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
165 170 175
Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
180 185 190
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
210 215 220
Ser Tyr Thr Leu Ala Phe Gly Gln Gly Thr Lys Val Asp Ile Lys
225 230 235
<210> 423
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 423
caagtgcaac tcgtggaatc tggtggagga ctcgtgaaac ctggaggatc attgagactg
60
tcatgcgcgg cctcgggatt cacgttctcc gattactaca tgagctggat tcgccaggct
120
ccggggaagg gactggaatg ggtgtcctac atttcctcat ccggctccac catctactac
180
gcggactccg tgaaggggag attcaccatt agccgcgata acgccaagaa cagcctgtac
240
cttcagatga actccctgcg ggctgaagat actgccgtct actactgcgc aagggagagc
300
ggagatggga tggacgtctg gggacagggt accactgtga ccgtgtcgtc ggcctccggc
360
ggagggggtt cgggtggaag ggccagcggc ggcggaggca gcgacatcca gatgacccag
420
tccccctcat cgctgtccgc ctccgtgggc gaccgcgtca ccatcacatg ccgggcctca
480
cagtcgatct cctcctacct caattggtat cagcagaagc ccggaaaggc ccctaagctt
540
ctgatctacg cagcgtcctc cctgcaatcc ggggtcccat ctcggttctc cggctcgggc
600
agcggtaccg acttcactct gaccatctcg agcctgcagc cggaggactt cgccacttac
660
tactgtcagc aaagctacac cctcgcgttt ggccagggca ccaaagtgga catcaag
717
<210> 424
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 424
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Ser Gly Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 425
<211> 105
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 425
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Thr Leu Ala Phe
85 90 95
Gly Gln Gly Thr Lys Val Asp Ile Lys
100 105
<210> 426
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 426
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Met Val Arg Glu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala
115 120 125
Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser
145 150 155 160
Glu Ser Leu Val His Asn Ser Gly Lys Thr Tyr Leu Asn Trp Phe His
165 170 175
Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Tyr Glu Val Ser Asn
180 185 190
Arg Asp Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Met Gln Gly Thr His Trp Pro Gly Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 427
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 427
caagtgcaac tggtgcaaag cggaggagga ttggtcaaac ccggaggaag cctgagactg
60
tcatgcgcgg cctctggatt caccttctcc gattactaca tgtcatggat cagacaggcc
120
ccggggaagg gcctcgaatg ggtgtcctac atctcgtcct ccgggaacac catctactac
180
gccgacagcg tgaagggccg ctttaccatt tcccgcgaca acgcaaagaa ctcgctgtac
240
cttcagatga attccctgcg ggctgaagat accgcggtgt actattgcgc ccggtccact
300
atggtccggg aggactactg gggacagggc acactcgtga ccgtgtccag cgcgagcggg
360
ggtggaggca gcggtggacg cgcctccggc ggcggcggtt cagacatcgt gctgactcag
420
tcgcccctgt cgctgccggt caccctgggc caaccggcct caattagctg caagtcctcg
480
gagagcctgg tgcacaactc aggaaagact tacctgaact ggttccatca gcggcctgga
540
cagtccccac ggaggctcat ctatgaagtg tccaacaggg attcgggggt gcccgaccgc
600
ttcactggct ccgggtccgg caccgacttc accttgaaaa tctccagagt ggaagccgag
660
gacgtgggcg tgtactactg tatgcagggt acccactggc ctggaacctt tggacaagga
720
actaagctcg agattaag
738
<210> 428
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 428
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Thr Met Val Arg Glu Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 429
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 429
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Glu Ser Leu Val His Asn
20 25 30
Ser Gly Lys Thr Tyr Leu Asn Trp Phe His Gln Arg Pro Gly Gln Ser
35 40 45
Pro Arg Arg Leu Ile Tyr Glu Val Ser Asn Arg Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly
85 90 95
Thr His Trp Pro Gly Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 430
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 430
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Arg Leu Thr Gln Ser Pro Ser Pro Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Glu Asp
145 150 155 160
Ile Asn Lys Phe Leu Asn Trp Tyr His Gln Thr Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Asp Ala Ser Thr Leu Gln Thr Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
195 200 205
Ser Leu Gln Pro Glu Asp Ile Gly Thr Tyr Tyr Cys Gln Gln Tyr Glu
210 215 220
Ser Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
225 230 235
<210> 431
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 431
caagtgcaac tcgtggaatc tggtggagga ctcgtgcaac ccggtggaag ccttaggctg
60
tcgtgcgccg tcagcgggtt tgctctgagc aaccatggaa tgtcctgggt ccgccgggca
120
ccgggaaaag ggctggaatg ggtgtccggc atcgtgtaca gcgggtcaac ctattacgcc
180
gcgtccgtga agggcagatt cactatctca agagacaaca gccggaacac cctgtacttg
240
caaatgaatt ccctgcgccc cgaggacacc gccatctact actgctccgc ccacggagga
300
gagtcggacg tgtggggcca gggaacgact gtgactgtgt ccagcgcatc aggagggggt
360
ggttcgggcg gccgggcctc ggggggagga ggttccgaca ttcggctgac ccagtccccg
420
tccccactgt cggcctccgt cggcgaccgc gtgaccatca cttgtcaggc gtccgaggac
480
attaacaagt tcctgaactg gtaccaccag acccctggaa aggcccccaa gctgctgatc
540
tacgatgcct cgacccttca aactggagtg cctagccggt tctccgggtc cggctccggc
600
actgatttca ctctgaccat caactcattg cagccggaag atatcgggac ctactattgc
660
cagcagtacg aatccctccc gctcacattc ggcgggggaa ccaaggtcga gattaag
717
<210> 432
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 432
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 433
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 433
Asp Ile Arg Leu Thr Gln Ser Pro Ser Pro Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Glu Asp Ile Asn Lys Phe
20 25 30
Leu Asn Trp Tyr His Gln Thr Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Thr Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Gly Thr Tyr Tyr Cys Gln Gln Tyr Glu Ser Leu Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 434
<211> 240
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 434
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Thr Thr Leu Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Gly Ser Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Gly Pro
165 170 175
Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn
210 215 220
Asp Trp Leu Pro Val Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
225 230 235 240
<210> 435
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 435
gaagtgcaat tggtggaaac tggaggagga cttgtgcaac ctggaggatc attgcggctc
60
tcatgcgctg tctccggctt cgccctgtca aatcacggga tgtcgtgggt cagacgggcc
120
ccgggaaagg gtctggaatg ggtgtcgggg attgtgtaca gcggctccac ctactacgcc
180
gcttcggtca agggccgctt cactatttca cgggacaaca gccgcaacac cctctatctg
240
caaatgaact ctctccgccc ggaggatacc gccatctact actgctccgc acacggcggc
300
gaatccgacg tgtggggaca gggaaccact gtcaccgtgt cgtccgcatc cggtggcgga
360
ggatcgggtg gccgggcctc cgggggcggc ggcagcgaga ctaccctgac ccagtcccct
420
gccactctgt ccgtgagccc gggagagaga gccaccctta gctgccgggc cagccagagc
480
gtgggctcca acctggcctg gtaccagcag aagccaggac agggtcccag gctgctgatc
540
tacggagcct ccactcgcgc gaccggcatc cccgcgaggt tctccgggtc gggttccggg
600
accgagttca ccctgaccat ctcctccctc caaccggagg acttcgcggt gtactactgt
660
cagcagtaca acgattggct gcccgtgaca tttggacagg ggacgaaggt ggaaatcaaa
720
<210> 436
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 436
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 437
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 437
Glu Thr Thr Leu Thr Gln Ser Pro Ala Thr Leu Ser Val Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Gly Ser Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Gly Pro Arg Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Asn Asp Trp Leu Pro
85 90 95
Val Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 438
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 438
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser
130 135 140
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Gly Ser Ser Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Met Tyr Gly Ala Ser Ser Arg Ala Ser Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr
210 215 220
Ala Gly Ser Pro Pro Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile
225 230 235 240
Lys
<210> 439
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 439
gaagtgcaat tggtggaatc tggtggagga cttgtgcaac ctggaggatc actgagactg
60
tcatgcgcgg tgtccggttt tgccctgagc aatcatggga tgtcgtgggt ccggcgcgcc
120
cccggaaagg gtctggaatg ggtgtcgggt atcgtctact ccgggagcac ttactacgcc
180
gcgagcgtga agggccgctt caccatttcc cgcgataact cccgcaacac cctgtacttg
240
caaatgaact cgctccggcc tgaggacact gccatctact actgctccgc acacggagga
300
gaatccgacg tgtggggcca gggaactacc gtgaccgtca gcagcgcctc cggcggcggg
360
ggctcaggcg gacgggctag cggcggcggt ggctccgaga tcgtgctgac ccagtcgcct
420
ggcactctct cgctgagccc cggggaaagg gcaaccctgt cctgtcgggc cagccagtcc
480
attggatcat cctccctcgc ctggtatcag cagaaaccgg gacaggctcc gcggctgctt
540
atgtatgggg ccagctcaag agcctccggc attcccgacc ggttctccgg gtccggttcc
600
ggcaccgatt tcaccctgac tatctcgagg ctggagccag aggacttcgc cgtgtactac
660
tgccagcagt acgcggggtc cccgccgttc acgttcggac agggaaccaa ggtcgagatc
720
aag
723
<210> 440
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 440
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His
20 25 30
Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser
85 90 95
Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser
115
<210> 441
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 441
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Gly Ser Ser
20 25 30
Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Met Tyr Gly Ala Ser Ser Arg Ala Ser Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala Gly Ser Pro
85 90 95
Pro Phe Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 442
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 442
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Tyr Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Ala Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg His Trp Gln Glu Trp Pro Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Glu Thr Thr Leu Thr Gln Ser Pro
130 135 140
Ala Phe Met Ser Ala Thr Pro Gly Asp Lys Val Ile Ile Ser Cys Lys
145 150 155 160
Ala Ser Gln Asp Ile Asp Asp Ala Met Asn Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Glu Ala Pro Leu Phe Ile Ile Gln Ser Ala Thr Ser Pro Val Pro
180 185 190
Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly Phe Gly Thr Asp Phe Ser
195 200 205
Leu Thr Ile Asn Asn Ile Glu Ser Glu Asp Ala Ala Tyr Tyr Phe Cys
210 215 220
Leu Gln His Asp Asn Phe Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 443
<211> 729
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 443
caagtgcagc ttcaggaaag cggaccgggc ctggtcaagc catccgaaac tctctccctg
60
acttgcactg tgtctggcgg ttccatctca tcgtcgtact actactgggg ctggattagg
120
cagccgcccg gaaagggact ggagtggatc ggaagcatct actattccgg ctcggcgtac
180
tacaacccta gcctcaagtc gagagtgacc atctccgtgg atacctccaa gaaccagttt
240
tccctgcgcc tgagctccgt gaccgccgct gacaccgccg tgtactactg tgctcggcat
300
tggcaggaat ggcccgatgc cttcgacatt tggggccagg gcactatggt cactgtgtca
360
tccgggggtg gaggcagcgg gggaggaggg tccggggggg gaggttcaga gacaaccttg
420
acccagtcac ccgcattcat gtccgccact ccgggagaca aggtcatcat ctcgtgcaaa
480
gcgtcccagg atatcgacga tgccatgaat tggtaccagc agaagcctgg cgaagcgccg
540
ctgttcatta tccaatccgc aacctcgccc gtgcctggaa tcccaccgcg gttcagcggc
600
agcggtttcg gaaccgactt ttccctgacc attaacaaca ttgagtccga ggacgccgcc
660
tactacttct gcctgcaaca cgacaacttc cctctcacgt tcggccaggg aaccaagctg
720
gaaatcaag
729
<210> 444
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 444
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Tyr Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Ala Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg His Trp Gln Glu Trp Pro Asp Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 445
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 445
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Ile Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Ala
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Pro Leu Phe Ile Ile
35 40 45
Gln Ser Ala Thr Ser Pro Val Pro Gly Ile Pro Pro Arg Phe Ser Gly
50 55 60
Ser Gly Phe Gly Thr Asp Phe Ser Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 446
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 446
Gln Val Asn Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Arg Thr Ser
20 25 30
Gly Met Cys Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Arg Ile Asp Trp Asp Glu Asp Lys Phe Tyr Ser Thr Ser
50 55 60
Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Asp Asn Gln Val
65 70 75 80
Val Leu Arg Met Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ser Gly Ala Gly Gly Thr Ser Ala Thr Ala Phe Asp Ile
100 105 110
Trp Gly Pro Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
130 135 140
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Asp Ile Tyr Asn Asn Leu Ala Trp Phe Gln Leu
165 170 175
Lys Pro Gly Ser Ala Pro Arg Ser Leu Met Tyr Ala Ala Asn Lys Ser
180 185 190
Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Ala Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr
210 215 220
Tyr Cys Gln His Tyr Tyr Arg Phe Pro Tyr Ser Phe Gly Gln Gly Thr
225 230 235 240
Lys Leu Glu Ile Lys
245
<210> 447
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 447
caagtcaatc tgcgcgaatc cggccccgcc ttggtcaagc ctacccagac cctcactctg
60
acctgtactt tctccggctt ctccctgcgg acttccggga tgtgcgtgtc ctggatcaga
120
cagcctccgg gaaaggccct ggagtggctc gctcgcattg actgggatga ggacaagttc
180
tactccacct cactcaagac caggctgacc atcagcaaag atacctctga caaccaagtg
240
gtgctccgca tgaccaacat ggacccagcc gacactgcca cttactactg cgcgaggagc
300
ggagcgggcg gaacctccgc caccgccttc gatatttggg gcccgggtac catggtcacc
360
gtgtcaagcg gaggaggggg gtccgggggc ggcggttccg ggggaggcgg atcggacatt
420
cagatgactc agtcaccatc gtccctgagc gctagcgtgg gcgacagagt gacaatcact
480
tgccgggcat cccaggacat ctataacaac cttgcgtggt tccagctgaa gcctggttcc
540
gcaccgcggt cacttatgta cgccgccaac aagagccagt cgggagtgcc gtcccggttt
600
tccggttcgg cctcgggaac tgacttcacc ctgacgatct ccagcctgca acccgaggat
660
ttcgccacct actactgcca gcactactac cgctttccct actcgttcgg acagggaacc
720
aagctggaaa tcaag
735
<210> 448
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 448
Gln Val Asn Leu Arg Glu Ser Gly Pro Ala Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Arg Thr Ser
20 25 30
Gly Met Cys Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu
35 40 45
Trp Leu Ala Arg Ile Asp Trp Asp Glu Asp Lys Phe Tyr Ser Thr Ser
50 55 60
Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr Ser Asp Asn Gln Val
65 70 75 80
Val Leu Arg Met Thr Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Ser Gly Ala Gly Gly Thr Ser Ala Thr Ala Phe Asp Ile
100 105 110
Trp Gly Pro Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 449
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 449
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Tyr Asn Asn
20 25 30
Leu Ala Trp Phe Gln Leu Lys Pro Gly Ser Ala Pro Arg Ser Leu Met
35 40 45
Tyr Ala Ala Asn Lys Ser Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Ala Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Tyr Arg Phe Pro Tyr
85 90 95
Ser Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 450
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 450
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Thr Ile Ala Ala Val Tyr Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Leu Ser
130 135 140
Leu Pro Val Thr Pro Glu Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser
145 150 155 160
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu
165 170 175
Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn
180 185 190
Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val
210 215 220
Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys
245
<210> 451
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 451
gaagtgcagc ttgtcgaatc cgggggggga ctggtcaagc cgggcggatc actgagactg
60
tcctgcgccg cgagcggctt cacgttctcc tcctactcca tgaactgggt ccgccaagcc
120
cccgggaagg gactggaatg ggtgtcctct atctcctcgt cgtcgtccta catctactac
180
gccgactccg tgaagggaag attcaccatt tcccgcgaca acgcaaagaa ctcactgtac
240
ttgcaaatga actcactccg ggccgaagat actgctgtgt actattgcgc caagactatt
300
gccgccgtct acgctttcga catctggggc cagggaacca ccgtgactgt gtcgtccggt
360
ggtggtggct cgggcggagg aggaagcggc ggcggggggt ccgagattgt gctgacccag
420
tcgccactga gcctccctgt gacccccgag gaacccgcca gcatcagctg ccggtccagc
480
cagtccctgc tccactccaa cggatacaat tacctcgatt ggtaccttca gaagcctgga
540
caaagcccgc agctgctcat ctacttggga tcaaaccgcg cgtcaggagt gcctgaccgg
600
ttctccggct cgggcagcgg taccgatttc accctgaaaa tctccagggt ggaggcagag
660
gacgtgggag tgtattactg tatgcaggcg ctgcagactc cgtacacatt tgggcagggc
720
accaagctgg agatcaag
738
<210> 452
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 452
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Thr Ile Ala Ala Val Tyr Ala Phe Asp Ile Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 453
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 453
Glu Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Glu
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 454
<211> 240
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 454
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Arg Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Ser Pro Ser Val Ser Ala
130 135 140
Ala Pro Gly Tyr Thr Ala Thr Ile Ser Cys Gly Gly Asn Asn Ile Gly
145 150 155 160
Thr Lys Ser Val His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Leu
165 170 175
Leu Val Ile Arg Asp Asp Ser Val Arg Pro Ser Lys Ile Pro Gly Arg
180 185 190
Phe Ser Gly Ser Asn Ser Gly Asn Met Ala Thr Leu Thr Ile Ser Gly
195 200 205
Val Gln Ala Gly Asp Glu Ala Asp Phe Tyr Cys Gln Val Trp Asp Ser
210 215 220
Asp Ser Glu His Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
225 230 235 240
<210> 455
<211> 720
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 455
gaagtccagc tcgtggagtc cggcggaggc cttgtgaagc ctggaggttc gctgagactg
60
tcctgcgccg cctccggctt caccttctcc gactactaca tgtcctggat cagacaggcc
120
ccgggaaagg gcctggaatg ggtgtcctac atctcgtcat cgggcagcac tatctactac
180
gcggactcag tgaaggggcg gttcaccatt tcccgggata acgcgaagaa ctcgctgtat
240
ctgcaaatga actcactgag ggccgaggac accgccgtgt actactgcgc ccgcgatctc
300
cgcggggcat ttgacatctg gggacaggga accatggtca cagtgtccag cggaggggga
360
ggatcgggtg gcggaggttc cgggggtgga ggctcctcct acgtgctgac tcagagccca
420
agcgtcagcg ctgcgcccgg ttacacggca accatctcct gtggcggaaa caacattggg
480
accaagtctg tgcactggta tcagcagaag ccgggccaag ctcccctgtt ggtgatccgc
540
gatgactccg tgcggcctag caaaattccg ggacggttct ccggctccaa cagcggcaat
600
atggccactc tcaccatctc gggagtgcag gccggagatg aagccgactt ctactgccaa
660
gtctgggact cagactccga gcatgtggtg ttcgggggcg gaaccaagct gactgtgctc
720
<210> 456
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 456
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Arg Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met
100 105 110
Val Thr Val Ser Ser
115
<210> 457
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 457
Ser Tyr Val Leu Thr Gln Ser Pro Ser Val Ser Ala Ala Pro Gly Tyr
1 5 10 15
Thr Ala Thr Ile Ser Cys Gly Gly Asn Asn Ile Gly Thr Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Leu Leu Val Ile Arg
35 40 45
Asp Asp Ser Val Arg Pro Ser Lys Ile Pro Gly Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Met Ala Thr Leu Thr Ile Ser Gly Val Gln Ala Gly
65 70 75 80
Asp Glu Ala Asp Phe Tyr Cys Gln Val Trp Asp Ser Asp Ser Glu His
85 90 95
Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 458
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 458
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Pro Ser Gly Tyr Thr Val Thr Ser His
20 25 30
Tyr Ile His Trp Val Arg Arg Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asn Pro Ser Gly Gly Val Thr Ala Tyr Ser Gln Thr Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Ser Asp Thr Ser Ser Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Ser Gly Ser Gly Trp Tyr Phe Asp Phe Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Pro Pro Ser
130 135 140
Val Ser Val Ser Pro Gly Gln Thr Ala Ser Ile Thr Cys Ser Gly Asp
145 150 155 160
Gly Leu Ser Lys Lys Tyr Val Ser Trp Tyr Gln Gln Lys Ala Gly Gln
165 170 175
Ser Pro Val Val Leu Ile Ser Arg Asp Lys Glu Arg Pro Ser Gly Ile
180 185 190
Pro Asp Arg Phe Ser Gly Ser Asn Ser Ala Asp Thr Ala Thr Leu Thr
195 200 205
Ile Ser Gly Thr Gln Ala Met Asp Glu Ala Asp Tyr Tyr Cys Gln Ala
210 215 220
Trp Asp Asp Thr Thr Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val
225 230 235 240
Leu
<210> 459
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 459
caagtgcagc tggtgcagag cggggccgaa gtcaagaagc cgggagcctc cgtgaaagtg
60
tcctgcaagc cttcgggata caccgtgacc tcccactaca ttcattgggt ccgccgcgcc
120
cccggccaag gactcgagtg gatgggcatg atcaacccta gcggcggagt gaccgcgtac
180
agccagacgc tgcagggacg cgtgactatg acctcggata cctcctcctc caccgtctat
240
atggaactgt ccagcctgcg gtccgaggat accgccatgt actactgcgc ccgggaagga
300
tcaggctccg ggtggtattt cgacttctgg ggaagaggca ccctcgtgac tgtgtcatct
360
gggggagggg gttccggtgg tggcggatcg ggaggaggcg gttcatccta cgtgctgacc
420
cagccaccct ccgtgtccgt gagccccggc cagactgcat cgattacatg tagcggcgac
480
ggcctctcca agaaatacgt gtcgtggtac cagcagaagg ccggacagag cccggtggtg
540
ctgatctcaa gagataagga gcggcctagc ggaatcccgg acaggttctc gggttccaac
600
tccgcggaca ctgctactct gaccatctcg gggacccagg ctatggacga agccgattac
660
tactgccaag cctgggacga cactactgtc gtgtttggag ggggcaccaa gttgaccgtc
720
ctt
723
<210> 460
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 460
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Pro Ser Gly Tyr Thr Val Thr Ser His
20 25 30
Tyr Ile His Trp Val Arg Arg Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Met Ile Asn Pro Ser Gly Gly Val Thr Ala Tyr Ser Gln Thr Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Ser Asp Thr Ser Ser Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Glu Gly Ser Gly Ser Gly Trp Tyr Phe Asp Phe Trp Gly Arg
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 461
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 461
Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Ser Gly Asp Gly Leu Ser Lys Lys Tyr Val
20 25 30
Ser Trp Tyr Gln Gln Lys Ala Gly Gln Ser Pro Val Val Leu Ile Ser
35 40 45
Arg Asp Lys Glu Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser
50 55 60
Asn Ser Ala Asp Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp Asp Asp Thr Thr Val Val
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 462
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 462
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Ala Gly Ile Ala Ala Arg Leu Arg Gly Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln
130 135 140
Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg Val Ile Ile Thr
145 150 155 160
Cys Arg Ala Ser Gln Gly Ile Arg Asn Trp Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Ala Ala Ser Asn Leu
180 185 190
Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Ala Asp
195 200 205
Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr
210 215 220
Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Phe Thr Phe Gly Pro Gly Thr
225 230 235 240
Lys Val Asp Ile Lys
245
<210> 463
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 463
caagtgcagc ttcaggagag cggcccggga ctcgtgaagc cgtcccagac cctgtccctg
60
acttgcaccg tgtcgggagg aagcatctcg agcggaggct actattggtc gtggattcgg
120
cagcaccctg gaaagggcct ggaatggatc ggctacatct actactccgg ctcgacctac
180
tacaacccat cgctgaagtc cagagtgaca atctcagtgg acacgtccaa gaatcagttc
240
agcctgaagc tctcttccgt gactgcggcc gacaccgccg tgtactactg cgcacgcgct
300
ggaattgccg cccggctgag gggtgccttc gacatttggg gacagggcac catggtcacc
360
gtgtcctccg gcggcggagg ttccgggggt ggaggctcag gaggaggggg gtccgacatc
420
gtcatgactc agtcgccctc aagcgtcagc gcgtccgtcg gggacagagt gatcatcacc
480
tgtcgggcgt cccagggaat tcgcaactgg ctggcctggt atcagcagaa gcccggaaag
540
gcccccaacc tgttgatcta cgccgcctca aacctccaat ccggggtgcc gagccgcttc
600
agcggctccg gttcgggtgc cgatttcact ctgaccatct cctccctgca acctgaagat
660
gtggctacct actactgcca aaagtacaac tccgcacctt ttactttcgg accggggacc
720
aaagtggaca ttaag
735
<210> 464
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 464
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Gly
20 25 30
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Ala Gly Ile Ala Ala Arg Leu Arg Gly Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 465
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 465
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 466
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 466
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Gly Tyr Gln Leu Leu Arg Trp Asp Val Gly Leu Leu
100 105 110
Arg Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
145 150 155 160
Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Ser Val
165 170 175
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Leu Tyr
180 185 190
Gly Lys Asn Asn Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
195 200 205
Arg Ser Gly Thr Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu
210 215 220
Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Arg Asp Ser Ser Gly Asp His
225 230 235 240
Leu Arg Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
245 250
<210> 467
<211> 759
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 467
caagtgcagc tggtccagtc gggcgccgag gtcaagaagc ccgggagctc tgtgaaagtg
60
tcctgcaagg cctccggggg cacctttagc tcctacgcca tctcctgggt ccgccaagca
120
ccgggtcaag gcctggagtg gatgggggga attatcccta tcttcggcac tgccaactac
180
gcccagaagt tccagggacg cgtgaccatt accgcggacg aatccacctc caccgcttat
240
atggagctgt ccagcttgcg ctcggaagat accgccgtgt actactgcgc ccggaggggt
300
ggataccagc tgctgagatg ggacgtgggc ctcctgcggt cggcgttcga catctggggc
360
cagggcacta tggtcactgt gtccagcgga ggaggcggat cgggaggcgg cggatcaggg
420
ggaggcggtt ccagctacgt gcttactcaa cccccttcgg tgtccgtggc cccgggacag
480
accgccagaa tcacttgcgg aggaaacaac attgggtcca agagcgtgca ttggtaccag
540
cagaagccag gacaggcccc tgtgctggtg ctctacggga agaacaatcg gcccagcgga
600
gtgccggaca ggttctcggg ttcacgctcc ggtacaaccg cttcactgac tatcaccggg
660
gcccaggcag aggatgaagc ggactactac tgttcctccc gggattcatc cggcgaccac
720
ctccgggtgt tcggaaccgg aacgaaggtc accgtgctg
759
<210> 468
<211> 129
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 468
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Gly Gly Tyr Gln Leu Leu Arg Trp Asp Val Gly Leu Leu
100 105 110
Arg Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
115 120 125
Ser
<210> 469
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 469
Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Gly Gln
1 5 10 15
Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile Gly Ser Lys Ser Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Leu Tyr
35 40 45
Gly Lys Asn Asn Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
50 55 60
Arg Ser Gly Thr Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Arg Asp Ser Ser Gly Asp His
85 90 95
Leu Arg Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105
<210> 470
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 470
Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Ser Phe Tyr Ala
50 55 60
Ile Ser Leu Lys Ser Arg Ile Ile Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Lys Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Ser Ser Pro Glu Gly Leu Phe Leu Tyr Trp Phe
100 105 110
Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Asp
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser Glu Leu
130 135 140
Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Ile Arg Ile
145 150 155 160
Thr Cys Gln Gly Asp Ser Leu Gly Asn Tyr Tyr Ala Thr Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly Thr Asn Asn
180 185 190
Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Ala Ser Ser Ser Gly Asn
195 200 205
Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu Ala Asp
210 215 220
Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly His His Leu Leu Phe Gly
225 230 235 240
Thr Gly Thr Lys Val Thr Val Leu
245
<210> 471
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 471
gaagtgcagc tccaacagtc aggaccgggg ctcgtgaagc catcccagac cctgtccctg
60
acttgtgcca tctcgggaga tagcgtgtca tcgaactccg ccgcctggaa ctggattcgg
120
cagagcccgt cccgcggact ggagtggctt ggaaggacct actaccggtc caagtggtac
180
tctttctacg cgatctcgct gaagtcccgc attatcatta accctgatac ctccaagaat
240
cagttctccc tccaactgaa atccgtcacc cccgaggaca cagcagtgta ttactgcgca
300
cggagcagcc ccgaaggact gttcctgtat tggtttgacc cctggggcca ggggactctt
360
gtgaccgtgt cgagcggcgg agatgggtcc ggtggcggtg gttcgggggg cggcggatca
420
tcatccgaac tgacccagga cccggctgtg tccgtggcgc tgggacaaac catccgcatt
480
acgtgccagg gagactccct gggcaactac tacgccactt ggtaccagca gaagccgggc
540
caagcccctg tgttggtcat ctacgggacc aacaacagac cttccggcat ccccgaccgg
600
ttcagcgctt cgtcctccgg caacactgcc agcctgacca tcactggagc gcaggccgaa
660
gatgaggccg actactactg caacagcaga gactcctcgg gtcatcacct cttgttcgga
720
actggaacca aggtcaccgt gctg
744
<210> 472
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 472
Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Ser Phe Tyr Ala
50 55 60
Ile Ser Leu Lys Ser Arg Ile Ile Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Lys Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Ser Ser Pro Glu Gly Leu Phe Leu Tyr Trp Phe
100 105 110
Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 473
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 473
Ser Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln
1 5 10 15
Thr Ile Arg Ile Thr Cys Gln Gly Asp Ser Leu Gly Asn Tyr Tyr Ala
20 25 30
Thr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr
35 40 45
Gly Thr Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Ala Ser
50 55 60
Ser Ser Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly His His
85 90 95
Leu Leu Phe Gly Thr Gly Thr Lys Val Thr Val Leu
100 105
<210> 474
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 474
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Glu Gly Ser Gly Ser Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu
130 135 140
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
145 150 155 160
Ser Val Ser Ser Ala Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
165 170 175
Pro Pro Arg Leu Leu Ile Ser Gly Ala Ser Thr Arg Ala Thr Gly Ile
180 185 190
Pro Asp Arg Phe Gly Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His
210 215 220
Tyr Gly Ser Ser Phe Asn Gly Ser Ser Leu Phe Thr Phe Gly Gln Gly
225 230 235 240
Thr Arg Leu Glu Ile Lys
245
<210> 475
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 475
gaagtgcagc tcgtggagtc aggaggcggc ctggtccagc cgggagggtc ccttagactg
60
tcatgcgccg caagcggatt cactttctcc tcctatgcca tgagctgggt ccgccaagcc
120
cccggaaagg gactggaatg ggtgtccgcc atctcggggt ctggaggctc aacttactac
180
gctgactccg tgaagggacg gttcaccatt agccgcgaca actccaagaa caccctctac
240
ctccaaatga actccctgcg ggccgaggat accgccgtct actactgcgc caaagtggaa
300
ggttcaggat cgctggacta ctggggacag ggtactctcg tgaccgtgtc atcgggcgga
360
ggaggttccg gcggtggcgg ctccggcggc ggagggtcgg agatcgtgat gacccagagc
420
cctggtactc tgagcctttc gccgggagaa agggccaccc tgtcctgccg cgcttcccaa
480
tccgtgtcct ccgcgtactt ggcgtggtac cagcagaagc cgggacagcc ccctcggctg
540
ctgatcagcg gggccagcac ccgggcaacc ggaatcccag acagattcgg gggttccggc
600
agcggcacag atttcaccct gactatttcg aggttggagc ccgaggactt tgcggtgtat
660
tactgtcagc actacgggtc gtcctttaat ggctccagcc tgttcacgtt cggacagggg
720
acccgcctgg aaatcaag
738
<210> 476
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 476
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Glu Gly Ser Gly Ser Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 477
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 477
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ala
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Arg Leu Leu
35 40 45
Ile Ser Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg Phe Gly
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Ser Phe
85 90 95
Asn Gly Ser Ser Leu Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile
100 105 110
Lys
<210> 478
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 478
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Arg Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr Tyr Ala Asp Ser Ala
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Thr Arg Ala Gly Ser Glu Ala Ser Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu
130 135 140
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
145 150 155 160
Ser Val Ser Asn Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Phe
210 215 220
Gly Thr Ser Ser Gly Leu Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
225 230 235 240
Lys
<210> 479
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 479
gaagtgcaac tggtggaaac cggtggcggc ctggtgcagc ctggaggatc attgaggctg
60
tcatgcgcgg ccagcggtat taccttctcc cggtacccca tgtcctgggt cagacaggcc
120
ccggggaaag ggcttgaatg ggtgtccggg atctcggact ccggtgtcag cacttactac
180
gccgactccg ccaagggacg cttcaccatt tcccgggaca actcgaagaa caccctgttc
240
ctccaaatga gctccctccg ggacgaggat actgcagtgt actactgcgt gacccgcgcc
300
gggtccgagg cgtctgacat ttggggacag ggcactatgg tcaccgtgtc gtccggcgga
360
gggggctcgg gaggcggtgg cagcggagga ggagggtccg agatcgtgct gacccaatcc
420
ccggccaccc tctcgctgag ccctggagaa agggcaacct tgtcctgtcg cgcgagccag
480
tccgtgagca actccctggc ctggtaccag cagaagcccg gacaggctcc gagacttctg
540
atctacgacg cttcgagccg ggccactgga atccccgacc gcttttcggg gtccggctca
600
ggaaccgatt tcaccctgac aatctcacgg ctggagccag aggatttcgc catctattac
660
tgccagcagt tcggtacttc ctccggcctg actttcggag gcggcacgaa gctcgaaatc
720
aag
723
<210> 480
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 480
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Arg Tyr
20 25 30
Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr Tyr Ala Asp Ser Ala
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Thr Arg Ala Gly Ser Glu Ala Ser Asp Ile Trp Gly Gln Gly Thr
100 105 110
Met Val Thr Val Ser Ser
115
<210> 481
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 481
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Asn Ser
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Ile Tyr Tyr Cys Gln Gln Phe Gly Thr Ser Ser Gly
85 90 95
Leu Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 482
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 482
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr
130 135 140
Gln Ser Pro Gly Thr Val Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu
145 150 155 160
Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Phe Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser
180 185 190
Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Ser Ala
210 215 220
Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp Thr Phe Gly
225 230 235 240
Gln Gly Thr Arg Leu Glu Ile Lys
245
<210> 483
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 483
caagtgcagc tcgtggaatc gggtggcgga ctggtgcagc cggggggctc acttagactg
60
tcctgcgcgg ccagcggatt cactttctcc tcctacgcca tgtcctgggt cagacaggcc
120
cctggaaagg gcctggaatg ggtgtccgca atcagcggca gcggcggctc gacctattac
180
gcggattcag tgaagggcag attcaccatt tcccgggaca acgccaagaa ctccttgtac
240
cttcaaatga actccctccg cgcggaagat accgcaatct actactgcgc tcgggccact
300
tacaagaggg aactgcgcta ctactacggg atggacgtct ggggccaggg aaccatggtc
360
accgtgtcca gcggaggagg aggatcggga ggaggcggta gcgggggtgg agggtcggag
420
atcgtgatga cccagtcccc cggcactgtg tcgctgtccc ccggcgaacg ggccaccctg
480
tcatgtcggg ccagccagtc agtgtcgtca agcttcctcg cctggtacca gcagaaaccg
540
ggacaagctc cccgcctgct gatctacgga gccagcagcc gggccaccgg tattcctgac
600
cggttctccg gttcggggtc cgggaccgac tttactctga ctatctctcg cctcgagcca
660
gaggactccg ccgtgtatta ctgccagcag taccactcct ccccgtcctg gacgttcgga
720
cagggcacaa ggctggagat taag
744
<210> 484
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 484
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 485
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 485
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Val Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 486
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 486
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Thr Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
130 135 140
Gln Ser Pro Ser Thr Leu Ser Leu Ser Pro Gly Glu Ser Ala Thr Leu
145 150 155 160
Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Thr Phe Leu Ala Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ser Ser
180 185 190
Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu Pro Glu Asp Phe Ala
210 215 220
Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Val Glu Ile Lys
245
<210> 487
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 487
gaggtgcagc ttgtggaaac cggtggcgga ctggtgcagc ccggaggaag cctcaggctg
60
tcctgcgccg cgtccggctt caccttctcc tcgtacgcca tgtcctgggt ccgccaggcc
120
cccggaaagg gcctggaatg ggtgtccgcc atctctggaa gcggaggttc cacgtactac
180
gcggacagcg tcaagggaag gttcacaatc tcccgcgata attcgaagaa cactctgtac
240
cttcaaatga acaccctgaa ggccgaggac actgctgtgt actactgcgc acgggccacc
300
tacaagagag agctccggta ctactacgga atggacgtct ggggccaggg aactactgtg
360
accgtgtcct cgggaggggg tggctccggg gggggcggct ccggcggagg cggttccgag
420
attgtgctga cccagtcacc ttcaactctg tcgctgtccc cgggagagag cgctactctg
480
agctgccggg ccagccagtc cgtgtccacc accttcctcg cctggtatca gcagaagccg
540
gggcaggcac cacggctctt gatctacggg tcaagcaaca gagcgaccgg aattcctgac
600
cgcttctcgg ggagcggttc aggcaccgac ttcaccctga ctatccggcg cctggaaccc
660
gaagatttcg ccgtgtatta ctgtcaacag taccactcct cgccgtcctg gacctttggc
720
caaggaacca aagtggaaat caag
744
<210> 488
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 488
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Thr Leu Lys Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 489
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 489
Glu Ile Val Leu Thr Gln Ser Pro Ser Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Thr
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ser Ser Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 490
<211> 239
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 490
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Lys Ala Val Pro Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Ser Ser Leu Ser
130 135 140
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser
145 150 155 160
Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro
165 170 175
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
180 185 190
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
195 200 205
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr
210 215 220
Ser Thr Pro Tyr Ser Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
225 230 235
<210> 491
<211> 717
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 491
gaagtgcagc tcgtggaaac tggaggtgga ctcgtgcagc ctggacggtc gctgcggctg
60
agctgcgctg catccggctt caccttcgac gattatgcca tgcactgggt cagacaggcg
120
ccagggaagg gacttgagtg ggtgtccggt atcagctgga atagcggctc aatcggatac
180
gcggactccg tgaagggaag gttcaccatt tcccgcgaca acgccaagaa ctccctgtac
240
ttgcaaatga acagcctccg ggatgaggac actgccgtgt actactgcgc ccgcgtcgga
300
aaagctgtgc ccgacgtctg gggccaggga accactgtga ccgtgtccag cggcgggggt
360
ggatcgggcg gtggagggtc cggtggaggg ggctcagata ttgtgatgac ccagaccccc
420
tcgtccctgt ccgcctcggt cggcgaccgc gtgactatca catgtagagc ctcgcagagc
480
atctccagct acctgaactg gtatcagcag aagccgggga aggccccgaa gctcctgatc
540
tacgcggcat catcactgca atcgggagtg ccgagccggt tttccgggtc cggctccggc
600
accgacttca cgctgaccat ttcttccctg caacccgagg acttcgccac ttactactgc
660
cagcagtcct actccacccc ttactccttc ggccaaggaa ccaggctgga aatcaag
717
<210> 492
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 492
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Gly Lys Ala Val Pro Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 493
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 493
Asp Ile Val Met Thr Gln Thr Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr
85 90 95
Ser Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 494
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 494
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Arg Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala Tyr Gly Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser His Gln Gly Val Ala Tyr Tyr Asn Tyr Ala Met Asp Val Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
130 135 140
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
145 150 155 160
Arg Ala Thr Gln Ser Ile Gly Ser Ser Phe Leu Ala Trp Tyr Gln Gln
165 170 175
Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Gln Arg
180 185 190
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Arg Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Arg Val Glu Pro Glu Asp Ser Ala Val Tyr
210 215 220
Tyr Cys Gln His Tyr Glu Ser Ser Pro Ser Trp Thr Phe Gly Gln Gly
225 230 235 240
Thr Lys Val Glu Ile Lys
245
<210> 495
<211> 738
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 495
gaagtgcagc tcgtggagag cgggggagga ttggtgcagc ccggaaggtc cctgcggctc
60
tcctgcactg cgtctggctt caccttcgac gactacgcga tgcactgggt cagacagcgc
120
ccgggaaagg gcctggaatg ggtcgcctca atcaactgga agggaaactc cctggcctat
180
ggcgacagcg tgaagggccg cttcgccatt tcgcgcgaca acgccaagaa caccgtgttt
240
ctgcaaatga attccctgcg gaccgaggat accgctgtgt actactgcgc cagccaccag
300
ggcgtggcat actataacta cgccatggac gtgtggggaa gagggacgct cgtcaccgtg
360
tcctccgggg gcggtggatc gggtggagga ggaagcggtg gcgggggcag cgaaatcgtg
420
ctgactcaga gcccgggaac tctttcactg tccccgggag aacgggccac tctctcgtgc
480
cgggccaccc agtccatcgg ctcctccttc cttgcctggt accagcagag gccaggacag
540
gcgccccgcc tgctgatcta cggtgcttcc caacgcgcca ctggcattcc tgaccggttc
600
agcggcagag ggtcgggaac cgatttcaca ctgaccattt cccgggtgga gcccgaagat
660
tcggcagtct actactgtca gcattacgag tcctcccctt catggacctt cggtcaaggg
720
accaaagtgg agatcaag
738
<210> 496
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 496
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Arg Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala Tyr Gly Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser His Gln Gly Val Ala Tyr Tyr Asn Tyr Ala Met Asp Val Trp
100 105 110
Gly Arg Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 497
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 497
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Thr Gln Ser Ile Gly Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Gln Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Arg Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Val Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Glu Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 498
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 498
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Val Arg Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser
130 135 140
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
145 150 155 160
Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala
165 170 175
Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro
180 185 190
Asp Arg Phe Ser Gly Asn Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
195 200 205
Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr
210 215 220
Gly Ser Pro Pro Arg Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile
225 230 235 240
Lys
<210> 499
<211> 723
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 499
gaggtgcagt tggtcgaaag cgggggcggg cttgtgcagc ctggcggatc actgcggctg
60
tcctgcgcgg catcaggctt cacgttttct tcctacgcca tgtcctgggt gcgccaggcc
120
cctggaaagg gactggaatg ggtgtccgcg atttcggggt ccggcgggag cacctactac
180
gccgattccg tgaagggccg cttcactatc tcgcgggaca actccaagaa caccctctac
240
ctccaaatga atagcctgcg ggccgaggat accgccgtct actattgcgc taaggtcgtg
300
cgcgacggaa tggacgtgtg gggacagggt accaccgtga cagtgtcctc ggggggaggc
360
ggtagcggcg gaggaggaag cggtggtgga ggttccgaga ttgtgctgac tcaatcaccc
420
gcgaccctga gcctgtcccc cggcgaaagg gccactctgt cctgtcgggc cagccaatca
480
gtctcctcct cgtacctggc ctggtaccag cagaagccag gacaggctcc gagactcctt
540
atctatggcg catcctcccg cgccaccgga atcccggata ggttctcggg aaacggatcg
600
gggaccgact tcactctcac catctcccgg ctggaaccgg aggacttcgc cgtgtactac
660
tgccagcagt acggcagccc gcctagattc actttcggcc ccggcaccaa agtggacatc
720
aag
723
<210> 500
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 500
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Val Arg Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
100 105 110
Val Thr Val Ser Ser
115
<210> 501
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 501
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Asn Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Pro Pro
85 90 95
Arg Phe Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 502
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 502
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ile Pro Gln Thr Gly Thr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu
130 135 140
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
145 150 155 160
Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln
165 170 175
Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile
180 185 190
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
195 200 205
Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His
210 215 220
Tyr Gly Ser Ser Pro Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu
225 230 235 240
Ile Lys
<210> 503
<211> 726
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 503
gaagtgcagc tgctggagtc cggcggtgga ttggtgcaac cggggggatc gctcagactg
60
tcctgtgcgg cgtcaggctt caccttctcg agctacgcca tgtcatgggt cagacaggcc
120
cctggaaagg gtctggaatg ggtgtccgcc atttccggga gcgggggatc tacatactac
180
gccgatagcg tgaagggccg cttcaccatt tcccgggaca actccaagaa cactctctat
240
ctgcaaatga actccctccg cgctgaggac actgccgtgt actactgcgc caaaatccct
300
cagaccggca ccttcgacta ctggggacag gggactctgg tcaccgtcag cagcggtggc
360
ggaggttcgg ggggaggagg aagcggcggc ggagggtccg agattgtgct gacccagtca
420
cccggcactt tgtccctgtc gcctggagaa agggccaccc tttcctgccg ggcatcccaa
480
tccgtgtcct cctcgtacct ggcctggtac cagcagaggc ccggacaggc cccacggctt
540
ctgatctacg gagcaagcag ccgcgcgacc ggtatcccgg accggttttc gggctcgggc
600
tcaggaactg acttcaccct caccatctcc cgcctggaac ccgaagattt cgctgtgtat
660
tactgccagc actacggcag ctccccgtcc tggacgttcg gccagggaac tcggctggag
720
atcaag
726
<210> 504
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 504
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ile Pro Gln Thr Gly Thr Phe Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 505
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 505
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 506
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 506
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Met Ser Arg Glu Asn Asp Lys Asn Ser Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Gly Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr
130 135 140
Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Ser Ala Thr Leu
145 150 155 160
Ser Cys Arg Ala Ser Gln Arg Val Ala Ser Asn Tyr Leu Ala Trp Tyr
165 170 175
Gln His Lys Pro Gly Gln Ala Pro Ser Leu Leu Ile Ser Gly Ala Ser
180 185 190
Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Phe Thr Leu Ala Ile Ser Arg Leu Glu Pro Glu Asp Ser Ala
210 215 220
Val Tyr Tyr Cys Gln His Tyr Asp Ser Ser Pro Ser Trp Thr Phe Gly
225 230 235 240
Gln Gly Thr Lys Val Glu Ile Lys
245
<210> 507
<211> 744
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 507
gaagtgcaac tggtggaaac cggtggagga ctcgtgcagc ctggcggcag cctccggctg
60
agctgcgccg cttcgggatt caccttttcc tcctacgcga tgtcttgggt cagacaggcc
120
cccggaaagg ggctggaatg ggtgtcagcc atctccggct ccggcggatc aacgtactac
180
gccgactccg tgaaaggccg gttcaccatg tcgcgcgaga atgacaagaa ctccgtgttc
240
ctgcaaatga actccctgag ggtggaggac accggagtgt actattgtgc gcgcgccaac
300
tacaagagag agctgcggta ctactacgga atggacgtct ggggacaggg aactatggtg
360
accgtgtcat ccggtggagg gggaagcggc ggtggaggca gcgggggcgg gggttcagaa
420
attgtcatga cccagtcccc gggaactctt tccctctccc ccggggaatc cgcgactttg
480
tcctgccggg ccagccagcg cgtggcctcg aactacctcg catggtacca gcataagcca
540
ggccaagccc cttccctgct gatttccggg gctagcagcc gcgccactgg cgtgccggat
600
aggttctcgg gaagcggctc gggtaccgat ttcaccctgg caatctcgcg gctggaaccg
660
gaggattcgg ccgtgtacta ctgccagcac tatgactcat ccccctcctg gacattcgga
720
cagggcacca aggtcgagat caag
744
<210> 508
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 508
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Met Ser Arg Glu Asn Asp Lys Asn Ser Val Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Gly Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Asn Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 509
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 509
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ala Ser Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln His Lys Pro Gly Gln Ala Pro Ser Leu Leu
35 40 45
Ile Ser Gly Ala Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Ala Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Asp Ser Ser Pro
85 90 95
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 510
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 510
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ala Leu Val Gly Ala Thr Gly Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Ser Leu Ser Ser Asn Phe Leu Ala Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Gln Ala Pro Gly Leu Leu Ile Tyr Gly Ala Ser Asn Trp Ala Thr
180 185 190
Gly Thr Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
195 200 205
Leu Thr Ile Thr Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys
210 215 220
Gln Tyr Tyr Gly Thr Ser Pro Met Tyr Thr Phe Gly Gln Gly Thr Lys
225 230 235 240
Val Glu Ile Lys
<210> 511
<211> 732
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 511
gaagtgcagc tgctcgaaac cggtggaggg ctggtgcagc cagggggctc cctgaggctt
60
tcatgcgccg ctagcggatt ctccttctcc tcttacgcca tgtcgtgggt ccgccaagcc
120
cctggaaaag gcctggaatg ggtgtccgcg atttccggga gcggaggttc gacctattac
180
gccgactccg tgaagggccg ctttaccatc tcccgggata actccaagaa cactctgtac
240
ctccaaatga actcgctgag agccgaggac accgccgtgt attactgcgc gaaggcgctg
300
gtcggcgcga ctggggcatt cgacatctgg ggacagggaa ctcttgtgac cgtgtcgagc
360
ggaggcggcg gctccggcgg aggagggagc gggggcggtg gttccgaaat cgtgttgact
420
cagtccccgg gaaccctgag cttgtcaccc ggggagcggg ccactctctc ctgtcgcgcc
480
tcccaatcgc tctcatccaa tttcctggcc tggtaccagc agaagcccgg acaggccccg
540
ggcctgctca tctacggcgc ttcaaactgg gcaacgggaa cccctgatcg gttcagcgga
600
agcggatcgg gtactgactt taccctgacc atcaccagac tggaaccgga ggacttcgcc
660
gtgtactact gccagtacta cggcacctcc cccatgtaca cattcggaca gggtaccaag
720
gtcgagatta ag
732
<210> 512
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 512
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ala Leu Val Gly Ala Thr Gly Ala Phe Asp Ile Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 513
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 513
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Ser Ser Asn
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Gly Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Asn Trp Ala Thr Gly Thr Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Tyr Tyr Gly Thr Ser Pro
85 90 95
Met Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 514
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 514
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Trp Phe Gly Glu Gly Phe Asp Pro Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro
130 135 140
Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser
145 150 155 160
Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys
165 170 175
Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala
180 185 190
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
195 200 205
Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr
210 215 220
Cys Met Gln Ala Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Val Asp Ile Lys
<210> 515
<211> 733
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 515
gaagtgcagc tgcttgagag cggtggaggt ctggtgcagc ccgggggatc actgcgcctg
60
tcctgtgccg cgtccggttt cactttctcc tcgtacgcca tgtcgtgggt cagacaggca
120
ccgggaaagg gactggaatg ggtgtcagcc atttcgggtt cggggggcag cacctactac
180
gctgactccg tgaagggccg gttcaccatt tcccgcgaca actccaagaa caccttgtac
240
ctccaaatga actccctgcg ggccgaagat accgccgtgt attactgcgt gctgtggttc
300
ggagagggat tcgacccgtg gggacaagga acactcgtga ctgtgtcatc cggcggaggc
360
ggcagcggtg gcggcggttc cggcggcggc ggatctgaca tcgtgttgac ccagtcccct
420
ctgagcctgc cggtcactcc tggcgaacca gccagcatct cctgccggtc gagccagtcc
480
ctcctgcact ccaatgggta caactacctc gattggtatc tgcaaaagcc gggccagagc
540
ccccagctgc tgatctacct tgggtcaaac cgcgcttccg gggtgcctga tagattctcc
600
gggtccggga gcggaaccga ctttaccctg aaaatctcga gggtggaggc cgaggacgtc
660
ggagtgtact actgcatgca ggcgctccag actcccctga ccttcggagg aggaacgaag
720
gtcgacatca aga
733
<210> 516
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 516
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Leu Trp Phe Gly Glu Gly Phe Asp Pro Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 517
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 517
Asp Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105 110
<210> 518
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 518
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Gly Tyr Asp Ser Ser Gly Tyr Tyr Arg Asp Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val
130 135 140
Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala
145 150 155 160
Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
165 170 175
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly
180 185 190
Thr Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg Phe Ser Gly Ser Gly
195 200 205
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp
210 215 220
Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Asn Ser Pro Pro Lys Phe
225 230 235 240
Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
245 250
<210> 519
<211> 753
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 519
caagtgcagc tcgtggagtc aggcggagga ctggtgcagc ccgggggctc cctgagactt
60
tcctgcgcgg catcgggttt taccttctcc tcctatgcta tgtcctgggt gcgccaggcc
120
ccgggaaagg gactggaatg ggtgtccgca atcagcggta gcgggggctc aacatactac
180
gccgactccg tcaagggtcg cttcactatt tcccgggaca actccaagaa taccctgtac
240
ctccaaatga acagcctcag ggccgaggat actgccgtgt actactgcgc caaagtcgga
300
tacgatagct ccggttacta ccgggactac tacggaatgg acgtgtgggg acagggcacc
360
accgtgaccg tgtcaagcgg cggaggcggt tcaggagggg gaggctccgg cggtggaggg
420
tccgaaatcg tcctgactca gtcgcctggc actctgtcgt tgtccccggg ggagcgcgct
480
accctgtcgt gtcgggcgtc gcagtccgtg tcgagctcct acctcgcgtg gtaccagcag
540
aagcccggac aggcccctag acttctgatc tacggcactt cttcacgcgc caccgggatc
600
agcgacaggt tcagcggctc cggctccggg accgacttca ccctgaccat tagccggctg
660
gagcctgaag atttcgccgt gtattactgc caacactacg gaaactcgcc gccaaagttc
720
acgttcggac ccggaaccaa gctggaaatc aag
753
<210> 520
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 520
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Val Gly Tyr Asp Ser Ser Gly Tyr Tyr Arg Asp Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 521
<211> 110
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 521
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Thr Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Asn Ser Pro
85 90 95
Pro Lys Phe Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 522
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 522
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Met Gly Trp Ser Ser Gly Tyr Leu Gly Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
130 135 140
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
145 150 155 160
Arg Ala Ser Gln Ser Val Ala Ser Ser Phe Leu Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Gly Arg
180 185 190
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
210 215 220
Tyr Cys Gln His Tyr Gly Gly Ser Pro Arg Leu Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Val Asp Ile Lys
245
<210> 523
<211> 739
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 523
gaagtccaac tggtggagtc cgggggaggg ctcgtgcagc ccggaggcag ccttcggctg
60
tcgtgcgccg cctccgggtt cacgttctca tcctacgcga tgtcgtgggt cagacaggca
120
ccaggaaagg gactggaatg ggtgtccgcc attagcggct ccggcggtag cacctactat
180
gccgactcag tgaagggaag gttcactatc tcccgcgaca acagcaagaa caccctgtac
240
ctccaaatga actctctgcg ggccgaggat accgcggtgt actattgcgc caagatgggt
300
tggtccagcg gatacttggg agccttcgac atttggggac agggcactac tgtgaccgtg
360
tcctccgggg gtggcggatc gggaggcggc ggctcgggtg gagggggttc cgaaatcgtg
420
ttgacccagt caccgggaac cctctcgctg tccccgggag aacgggctac actgtcatgt
480
agagcgtccc agtccgtggc ttcctcgttc ctggcctggt accagcagaa gccgggacag
540
gcaccccgcc tgctcatcta cggagccagc ggccgggcga ccggcatccc tgaccgcttc
600
tccggttccg gctcgggcac cgactttact ctgaccatta gcaggcttga gcccgaggat
660
tttgccgtgt actactgcca acactacggg gggagccctc gcctgacctt cggaggcgga
720
actaaggtcg atatcaaaa
739
<210> 524
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 524
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Met Gly Trp Ser Ser Gly Tyr Leu Gly Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 525
<211> 109
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 525
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ala Ser Ser
20 25 30
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Gly Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro
85 90 95
Arg Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
100 105
<210> 526
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 526
Gln Ile Gln Leu Val Gln Ser Gly Pro Asp Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Phe
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Phe Lys Trp Met
35 40 45
Ala Trp Ile Asn Thr Tyr Thr Gly Glu Ser Tyr Phe Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Val Glu Thr Ser Ala Thr Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Thr Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Gly Glu Ile Tyr Tyr Gly Tyr Asp Gly Gly Phe Ala Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 527
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 527
Asp Val Val Met Thr Gln Ser His Arg Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Arg Ala Ser Gln Asp Val Asn Thr Ala
20 25 30
Val Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Phe Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Ala Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Asp Ile Lys
100 105
<210> 528
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 528
Gln Ile Gln Leu Val Gln Ser Gly Pro Asp Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Phe
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Phe Lys Trp Met
35 40 45
Ala Trp Ile Asn Thr Tyr Thr Gly Glu Ser Tyr Phe Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Val Glu Thr Ser Ala Thr Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Thr Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Gly Glu Ile Tyr Tyr Gly Tyr Asp Gly Gly Phe Ala Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr Gln Ser
130 135 140
His Arg Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Ile Thr Cys
145 150 155 160
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ser Trp Tyr Gln Gln Lys
165 170 175
Pro Gly Gln Ser Pro Lys Leu Leu Ile Phe Ser Ala Ser Tyr Arg Tyr
180 185 190
Thr Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Ala Asp Phe
195 200 205
Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr
210 215 220
Cys Gln Gln His Tyr Ser Thr Pro Trp Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Leu Asp Ile Lys
<210> 529
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 529
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile Asn Trp Val Lys Arg Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Arg Glu Pro Ala Tyr Ala Tyr Asp Phe
50 55 60
Arg Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Tyr Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Leu Asp Tyr Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
100 105 110
Val Thr Val Ser Ser
115
<210> 530
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 530
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Met Ser Leu Gly
1 5 10 15
Lys Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Ser Val Ile
20 25 30
Gly Ala His Leu Ile His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Leu Ala Ser Asn Leu Glu Thr Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Glu Glu Asp Asp Val Ala Ile Tyr Ser Cys Leu Gln Ser Arg
85 90 95
Ile Phe Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 531
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 531
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Ile Asn Trp Val Lys Arg Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Glu Thr Arg Glu Pro Ala Tyr Ala Tyr Asp Phe
50 55 60
Arg Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Tyr Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Leu Asp Tyr Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
100 105 110
Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys
130 135 140
Lys Pro Gly Glu Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr
145 150 155 160
Phe Thr Asp Tyr Ser Ile Asn Trp Val Lys Arg Ala Pro Gly Lys Gly
165 170 175
Leu Lys Trp Met Gly Trp Ile Asn Thr Glu Thr Arg Glu Pro Ala Tyr
180 185 190
Ala Tyr Asp Phe Arg Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala
195 200 205
Ser Thr Ala Tyr Leu Gln Ile Asn Asn Leu Lys Tyr Glu Asp Thr Ala
210 215 220
Thr Tyr Phe Cys Ala Leu Asp Tyr Ser Tyr Ala Met Asp Tyr Trp Gly
225 230 235 240
Gln Gly Thr Ser Val Thr Val Ser Ser
245
<210> 532
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 532
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Arg His Tyr
20 25 30
Ser Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Arg Ile Asn Thr Glu Ser Gly Val Pro Ile Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Val Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Val Ile Asn Asn Leu Lys Asp Glu Asp Thr Ala Ser Tyr Phe Cys
85 90 95
Ser Asn Asp Tyr Leu Tyr Ser Leu Asp Phe Trp Gly Gln Gly Thr Ala
100 105 110
Leu Thr Val Ser Ser
115
<210> 533
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 533
Asp Ile Val Leu Thr Gln Ser Pro Pro Ser Leu Ala Met Ser Leu Gly
1 5 10 15
Lys Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Thr Ile Leu
20 25 30
Gly Ser His Leu Ile Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Thr Leu Leu Ile Gln Leu Ala Ser Asn Val Gln Thr Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Glu Glu Asp Asp Val Ala Val Tyr Tyr Cys Leu Gln Ser Arg
85 90 95
Thr Ile Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 534
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 534
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Arg His Tyr
20 25 30
Ser Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Arg Ile Asn Thr Glu Ser Gly Val Pro Ile Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Val Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Val Ile Asn Asn Leu Lys Asp Glu Asp Thr Ala Ser Tyr Phe Cys
85 90 95
Ser Asn Asp Tyr Leu Tyr Ser Leu Asp Phe Trp Gly Gln Gly Thr Ala
100 105 110
Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Pro Ser Leu Ala
130 135 140
Met Ser Leu Gly Lys Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser
145 150 155 160
Val Thr Ile Leu Gly Ser His Leu Ile Tyr Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Gln Pro Pro Thr Leu Leu Ile Gln Leu Ala Ser Asn Val Gln Thr
180 185 190
Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr
195 200 205
Leu Thr Ile Asp Pro Val Glu Glu Asp Asp Val Ala Val Tyr Tyr Cys
210 215 220
Leu Gln Ser Arg Thr Ile Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 535
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 535
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Ser Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Arg Ile Asn Thr Glu Thr Gly Glu Pro Leu Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Val Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Phe Phe Cys
85 90 95
Ser Asn Asp Tyr Leu Tyr Ser Cys Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Leu Thr Val Ser Ser
115
<210> 536
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 536
Asp Ile Val Leu Thr Gln Ser Pro Pro Ser Leu Ala Met Ser Leu Gly
1 5 10 15
Lys Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Thr Ile Leu
20 25 30
Gly Ser His Leu Ile Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Thr Leu Leu Ile Gln Leu Ala Ser Asn Val Gln Thr Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr Leu Thr Ile Asp
65 70 75 80
Pro Val Glu Glu Asp Asp Val Ala Val Tyr Tyr Cys Leu Gln Ser Arg
85 90 95
Thr Ile Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 537
<211> 243
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 537
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr His Tyr
20 25 30
Ser Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Arg Ile Asn Thr Glu Thr Gly Glu Pro Leu Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Arg Phe Ala Phe Ser Leu Glu Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Leu Val Ile Asn Asn Leu Lys Asn Glu Asp Thr Ala Thr Phe Phe Cys
85 90 95
Ser Asn Asp Tyr Leu Tyr Ser Cys Asp Tyr Trp Gly Gln Gly Thr Thr
100 105 110
Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Pro Ser Leu Ala
130 135 140
Met Ser Leu Gly Lys Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser
145 150 155 160
Val Thr Ile Leu Gly Ser His Leu Ile Tyr Trp Tyr Gln Gln Lys Pro
165 170 175
Gly Gln Pro Pro Thr Leu Leu Ile Gln Leu Ala Ser Asn Val Gln Thr
180 185 190
Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Arg Thr Asp Phe Thr
195 200 205
Leu Thr Ile Asp Pro Val Glu Glu Asp Asp Val Ala Val Tyr Tyr Cys
210 215 220
Leu Gln Ser Arg Thr Ile Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu
225 230 235 240
Glu Ile Lys
<210> 538
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 538
Asn His Gly Met Ser
1 5
<210> 539
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 539
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
1 5 10 15
<210> 540
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 540
His Gly Gly Glu Ser Asp Val
1 5
<210> 541
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 541
Asn Tyr Ala Met Ser
1 5
<210> 542
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 542
Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 543
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 543
Ser Pro Ala His Tyr Tyr Gly Gly Met Asp Val
1 5 10
<210> 544
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 544
Asp Tyr Ala Met His
1 5
<210> 545
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 545
Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 546
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 546
His Ser Phe Leu Ala Tyr
1 5
<210> 547
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 547
Asn Phe Gly Ile Asn
1 5
<210> 548
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 548
Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 549
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 549
Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met Asp Val
1 5 10
<210> 550
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 550
Ser Asp Ala Met Thr
1 5
<210> 551
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 551
Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 552
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 552
Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala Arg Gly Pro Arg Tyr
1 5 10
<210> 553
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 553
Asn Tyr Gly Ile Thr
1 5
<210> 554
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 554
Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 555
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 555
Gly Pro Tyr Tyr Tyr Tyr Met Asp Val
1 5
<210> 556
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 556
Asp Tyr Tyr Met Ser
1 5
<210> 557
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 557
Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 558
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 558
Glu Ser Gly Asp Gly Met Asp Val
1 5
<210> 559
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 559
Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 560
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 560
Ser Thr Met Val Arg Glu Asp Tyr
1 5
<210> 561
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 561
Ser Ser Tyr Tyr Tyr Trp Gly
1 5
<210> 562
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 562
Ser Ile Tyr Tyr Ser Gly Ser Ala Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 563
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 563
His Trp Gln Glu Trp Pro Asp Ala Phe Asp Ile
1 5 10
<210> 564
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 564
Thr Ser Gly Met Cys Val Ser
1 5
<210> 565
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 565
Arg Ile Asp Trp Asp Glu Asp Lys Phe Tyr Ser Thr Ser Leu Lys Thr
1 5 10 15
<210> 566
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 566
Ser Gly Ala Gly Gly Thr Ser Ala Thr Ala Phe Asp Ile
1 5 10
<210> 567
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 567
Ser Tyr Ser Met Asn
1 5
<210> 568
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 568
Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 569
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 569
Thr Ile Ala Ala Val Tyr Ala Phe Asp Ile
1 5 10
<210> 570
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 570
Asp Leu Arg Gly Ala Phe Asp Ile
1 5
<210> 571
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 571
Ser His Tyr Ile His
1 5
<210> 572
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 572
Met Ile Asn Pro Ser Gly Gly Val Thr Ala Tyr Ser Gln Thr Leu Gln
1 5 10 15
Gly
<210> 573
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 573
Glu Gly Ser Gly Ser Gly Trp Tyr Phe Asp Phe
1 5 10
<210> 574
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 574
Ser Gly Gly Tyr Tyr Trp Ser
1 5
<210> 575
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 575
Tyr Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 576
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 576
Ala Gly Ile Ala Ala Arg Leu Arg Gly Ala Phe Asp Ile
1 5 10
<210> 577
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 577
Ser Tyr Ala Ile Ser
1 5
<210> 578
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 578
Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 579
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 579
Arg Gly Gly Tyr Gln Leu Leu Arg Trp Asp Val Gly Leu Leu Arg Ser
1 5 10 15
Ala Phe Asp Ile
20
<210> 580
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 580
Ser Asn Ser Ala Ala Trp Asn
1 5
<210> 581
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 581
Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Ser Phe Tyr Ala Ile Ser Leu
1 5 10 15
Lys Ser
<210> 582
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 582
Ser Ser Pro Glu Gly Leu Phe Leu Tyr Trp Phe Asp Pro
1 5 10
<210> 583
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 583
Ser Tyr Ala Met Ser
1 5
<210> 584
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 584
Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 585
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 585
Val Glu Gly Ser Gly Ser Leu Asp Tyr
1 5
<210> 586
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 586
Arg Tyr Pro Met Ser
1 5
<210> 587
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 587
Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr Tyr Ala Asp Ser Ala Lys
1 5 10 15
Gly
<210> 588
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 588
Arg Ala Gly Ser Glu Ala Ser Asp Ile
1 5
<210> 589
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 589
Ala Thr Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp Val
1 5 10 15
<210> 590
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 590
Val Gly Lys Ala Val Pro Asp Val
1 5
<210> 591
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 591
Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala Tyr Gly Asp Ser Val Lys
1 5 10 15
Gly
<210> 592
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 592
His Gln Gly Val Ala Tyr Tyr Asn Tyr Ala Met Asp Val
1 5 10
<210> 593
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 593
Val Val Arg Asp Gly Met Asp Val
1 5
<210> 594
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 594
Ile Pro Gln Thr Gly Thr Phe Asp Tyr
1 5
<210> 595
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 595
Ala Asn Tyr Lys Arg Glu Leu Arg Tyr Tyr Tyr Gly Met Asp Val
1 5 10 15
<210> 596
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 596
Ala Leu Val Gly Ala Thr Gly Ala Phe Asp Ile
1 5 10
<210> 597
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 597
Trp Phe Gly Glu Gly Phe Asp Pro
1 5
<210> 598
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 598
Val Gly Tyr Asp Ser Ser Gly Tyr Tyr Arg Asp Tyr Tyr Gly Met Asp
1 5 10 15
Val
<210> 599
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 599
Met Gly Trp Ser Ser Gly Tyr Leu Gly Ala Phe Asp Ile
1 5 10
<210> 600
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 600
Asn Phe Gly Met Asn
1 5
<210> 601
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 601
Trp Ile Asn Thr Tyr Thr Gly Glu Ser Tyr Phe Ala Asp Asp Phe Lys
1 5 10 15
Gly
<210> 602
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 602
Gly Glu Ile Tyr Tyr Gly Tyr Asp Gly Gly Phe Ala Tyr
1 5 10
<210> 603
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 603
Asp Tyr Ser Ile Asn
1 5
<210> 604
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 604
Trp Ile Asn Thr Glu Thr Arg Glu Pro Ala Tyr Ala Tyr Asp Phe Arg
1 5 10 15
Gly
<210> 605
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 605
Asp Tyr Ser Tyr Ala Met Asp Tyr
1 5
<210> 606
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 606
His Tyr Ser Met Asn
1 5
<210> 607
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 607
Arg Ile Asn Thr Glu Ser Gly Val Pro Ile Tyr Ala Asp Asp Phe Lys
1 5 10 15
Gly
<210> 608
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 608
Asp Tyr Leu Tyr Ser Leu Asp Phe
1 5
<210> 609
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 609
Arg Ile Asn Thr Glu Thr Gly Glu Pro Leu Tyr Ala Asp Asp Phe Lys
1 5 10 15
Gly
<210> 610
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 610
Asp Tyr Leu Tyr Ser Cys Asp Tyr
1 5
<210> 611
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 611
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 612
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 612
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 613
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 613
Gln Gln Ser Tyr Ser Thr Pro Tyr Thr
1 5
<210> 614
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 614
Arg Ala Ser Gln Ser Ile Ser Ser Ser Phe Leu Ala
1 5 10
<210> 615
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 615
Gly Ala Ser Arg Arg Ala Thr
1 5
<210> 616
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 616
Gln Gln Tyr His Ser Ser Pro Ser Trp Thr
1 5 10
<210> 617
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 617
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 618
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 618
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 619
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 619
Met Gln Ala Leu Gln Thr Pro Tyr Thr
1 5
<210> 620
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 620
Lys Ser Ser Gln Ser Leu Leu Arg Asn Asp Gly Lys Thr Pro Leu Tyr
1 5 10 15
<210> 621
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 621
Glu Val Ser Asn Arg Phe Ser
1 5
<210> 622
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 622
Met Gln Asn Ile Gln Phe Pro Ser
1 5
<210> 623
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 623
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asn
1 5 10 15
<210> 624
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 624
Leu Gly Ser Lys Arg Ala Ser
1 5
<210> 625
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 625
Gly Ala Ser Thr Leu Ala Ser
1 5
<210> 626
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 626
Gln Gln Ser Tyr Lys Arg Ala Ser
1 5
<210> 627
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 627
Arg Ser Ser Gln Ser Leu Leu Tyr Ser Asn Gly Tyr Asn Tyr Val Asp
1 5 10 15
<210> 628
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 628
Met Gln Gly Arg Gln Phe Pro Tyr Ser
1 5
<210> 629
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 629
Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala
1 5 10
<210> 630
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 630
Gly Ala Ser Thr Arg Ala Ser
1 5
<210> 631
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 631
Gln Gln Tyr Gly Ser Ser Leu Thr
1 5
<210> 632
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 632
Arg Ala Ser Gln Ser Val Ser Ser Lys Leu Ala
1 5 10
<210> 633
<400> 633
000
<210> 634
<400> 634
000
<210> 635
<400> 635
000
<210> 636
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 636
Gly Ala Ser Ile Arg Ala Thr
1 5
<210> 637
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 637
Gln Gln Tyr Gly Ser Ser Ser Trp Thr
1 5
<210> 638
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 638
Arg Ala Ser Gln Ser Val Gly Ser Thr Asn Leu Ala
1 5 10
<210> 639
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 639
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 640
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 640
Gln Gln Tyr Gly Ser Ser Pro Pro Trp Thr
1 5 10
<210> 641
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 641
Gln Gln Ser Tyr Thr Leu Ala
1 5
<210> 642
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 642
Lys Ser Ser Glu Ser Leu Val His Asn Ser Gly Lys Thr Tyr Leu Asn
1 5 10 15
<210> 643
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 643
Glu Val Ser Asn Arg Asp Ser
1 5
<210> 644
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 644
Met Gln Gly Thr His Trp Pro Gly Thr
1 5
<210> 645
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 645
Gln Ala Ser Glu Asp Ile Asn Lys Phe Leu Asn
1 5 10
<210> 646
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 646
Asp Ala Ser Thr Leu Gln Thr
1 5
<210> 647
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 647
Gln Gln Tyr Glu Ser Leu Pro Leu Thr
1 5
<210> 648
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 648
Arg Ala Ser Gln Ser Val Gly Ser Asn Leu Ala
1 5 10
<210> 649
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 649
Gly Ala Ser Thr Arg Ala Thr
1 5
<210> 650
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 650
Gln Gln Tyr Asn Asp Trp Leu Pro Val Thr
1 5 10
<210> 651
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 651
Arg Ala Ser Gln Ser Ile Gly Ser Ser Ser Leu Ala
1 5 10
<210> 652
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 652
Gly Ala Ser Ser Arg Ala Ser
1 5
<210> 653
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 653
Gln Gln Tyr Ala Gly Ser Pro Pro Phe Thr
1 5 10
<210> 654
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 654
Lys Ala Ser Gln Asp Ile Asp Asp Ala Met Asn
1 5 10
<210> 655
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 655
Ser Ala Thr Ser Pro Val Pro
1 5
<210> 656
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 656
Leu Gln His Asp Asn Phe Pro Leu Thr
1 5
<210> 657
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 657
Arg Ala Ser Gln Asp Ile Tyr Asn Asn Leu Ala
1 5 10
<210> 658
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 658
Ala Ala Asn Lys Ser Gln Ser
1 5
<210> 659
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 659
Gln His Tyr Tyr Arg Phe Pro Tyr Ser
1 5
<210> 660
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 660
Gly Gly Asn Asn Ile Gly Thr Lys Ser Val His
1 5 10
<210> 661
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 661
Asp Asp Ser Val Arg Pro Ser
1 5
<210> 662
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 662
Gln Val Trp Asp Ser Asp Ser Glu His Val Val
1 5 10
<210> 663
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 663
Ser Gly Asp Gly Leu Ser Lys Lys Tyr Val Ser
1 5 10
<210> 664
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 664
Arg Asp Lys Glu Arg Pro Ser
1 5
<210> 665
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 665
Gln Ala Trp Asp Asp Thr Thr Val Val
1 5
<210> 666
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 666
Arg Ala Ser Gln Gly Ile Arg Asn Trp Leu Ala
1 5 10
<210> 667
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 667
Ala Ala Ser Asn Leu Gln Ser
1 5
<210> 668
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 668
Gln Lys Tyr Asn Ser Ala Pro Phe Thr
1 5
<210> 669
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 669
Gly Gly Asn Asn Ile Gly Ser Lys Ser Val His
1 5 10
<210> 670
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 670
Gly Lys Asn Asn Arg Pro Ser
1 5
<210> 671
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 671
Ser Ser Arg Asp Ser Ser Gly Asp His Leu Arg Val
1 5 10
<210> 672
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 672
Gln Gly Asp Ser Leu Gly Asn Tyr Tyr Ala Thr
1 5 10
<210> 673
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 673
Gly Thr Asn Asn Arg Pro Ser
1 5
<210> 674
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 674
Asn Ser Arg Asp Ser Ser Gly His His Leu Leu
1 5 10
<210> 675
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 675
Arg Ala Ser Gln Ser Val Ser Ser Ala Tyr Leu Ala
1 5 10
<210> 676
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 676
Gln His Tyr Gly Ser Ser Phe Asn Gly Ser Ser Leu Phe Thr
1 5 10
<210> 677
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 677
Arg Ala Ser Gln Ser Val Ser Asn Ser Leu Ala
1 5 10
<210> 678
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 678
Asp Ala Ser Ser Arg Ala Thr
1 5
<210> 679
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 679
Gln Gln Phe Gly Thr Ser Ser Gly Leu Thr
1 5 10
<210> 680
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 680
Arg Ala Ser Gln Ser Val Ser Ser Ser Phe Leu Ala
1 5 10
<210> 681
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 681
Gly Ala Ser Ser Arg Ala Thr
1 5
<210> 682
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 682
Arg Ala Ser Gln Ser Val Ser Thr Thr Phe Leu Ala
1 5 10
<210> 683
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 683
Gly Ser Ser Asn Arg Ala Thr
1 5
<210> 684
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 684
Gln Gln Ser Tyr Ser Thr Pro Tyr Ser
1 5
<210> 685
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 685
Arg Ala Thr Gln Ser Ile Gly Ser Ser Phe Leu Ala
1 5 10
<210> 686
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 686
Gly Ala Ser Gln Arg Ala Thr
1 5
<210> 687
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 687
Gln His Tyr Glu Ser Ser Pro Ser Trp Thr
1 5 10
<210> 688
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 688
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala
1 5 10
<210> 689
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 689
Gln Gln Tyr Gly Ser Pro Pro Arg Phe Thr
1 5 10
<210> 690
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 690
Gln His Tyr Gly Ser Ser Pro Ser Trp Thr
1 5 10
<210> 691
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 691
Arg Ala Ser Gln Arg Val Ala Ser Asn Tyr Leu Ala
1 5 10
<210> 692
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 692
Gln His Tyr Asp Ser Ser Pro Ser Trp Thr
1 5 10
<210> 693
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 693
Arg Ala Ser Gln Ser Leu Ser Ser Asn Phe Leu Ala
1 5 10
<210> 694
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 694
Gly Ala Ser Asn Trp Ala Thr
1 5
<210> 695
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 695
Gln Tyr Tyr Gly Thr Ser Pro Met Tyr Thr
1 5 10
<210> 696
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 696
Met Gln Ala Leu Gln Thr Pro Leu Thr
1 5
<210> 697
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 697
Gly Thr Ser Ser Arg Ala Thr
1 5
<210> 698
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 698
Gln His Tyr Gly Asn Ser Pro Pro Lys Phe Thr
1 5 10
<210> 699
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 699
Arg Ala Ser Gln Ser Val Ala Ser Ser Phe Leu Ala
1 5 10
<210> 700
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 700
Gly Ala Ser Gly Arg Ala Thr
1 5
<210> 701
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 701
Gln His Tyr Gly Gly Ser Pro Arg Leu Thr
1 5 10
<210> 702
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 702
Arg Ala Ser Gln Asp Val Asn Thr Ala Val Ser
1 5 10
<210> 703
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 703
Ser Ala Ser Tyr Arg Tyr Thr
1 5
<210> 704
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 704
Gln Gln His Tyr Ser Thr Pro Trp Thr
1 5
<210> 705
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 705
Arg Ala Ser Glu Ser Val Ser Val Ile Gly Ala His Leu Ile His
1 5 10 15
<210> 706
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 706
Leu Ala Ser Asn Leu Glu Thr
1 5
<210> 707
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 707
Leu Gln Ser Arg Ile Phe Pro Arg Thr
1 5
<210> 708
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 708
Arg Ala Ser Glu Ser Val Thr Ile Leu Gly Ser His Leu Ile Tyr
1 5 10 15
<210> 709
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 709
Leu Ala Ser Asn Val Gln Thr
1 5
<210> 710
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 710
Leu Gln Ser Arg Thr Ile Pro Arg Thr
1 5
<210> 711
<400> 711
000
<210> 712
<400> 712
000
<210> 713
<400> 713
000
<210> 714
<400> 714
000
<210> 715
<400> 715
000
<210> 716
<400> 716
000
<210> 717
<400> 717
000
<210> 718
<400> 718
000
<210> 719
<400> 719
000
<210> 720
<400> 720
000
<210> 721
<400> 721
000
<210> 722
<400> 722
000
<210> 723
<400> 723
000
<210> 724
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 724
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Glu Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asp Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser
195 200 205
Ile Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Leu Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 725
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 725
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Asn Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Arg Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ser Gly Trp Asp Phe Asp Tyr Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Arg Met
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Ile Arg Tyr Tyr Leu Ser Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Thr Ala Ser
195 200 205
Ile Leu Gln Asn Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Thr Tyr Tyr Cys Leu Gln Thr Tyr Thr Thr Pro Asp Phe Gly Pro Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 726
<211> 383
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 726
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu
20 25 30
Glu Lys Pro Gly Ala Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ser Phe Thr Gly Tyr Thr Met Asn Trp Val Lys Gln Ser His Gly Lys
50 55 60
Ser Leu Glu Trp Ile Gly Leu Ile Thr Pro Tyr Asn Gly Ala Ser Ser
65 70 75 80
Tyr Asn Gln Lys Phe Arg Gly Lys Ala Thr Leu Thr Val Asp Lys Ser
85 90 95
Ser Ser Thr Ala Tyr Met Asp Leu Leu Ser Leu Thr Ser Glu Asp Ser
100 105 110
Ala Val Tyr Phe Cys Ala Arg Gly Gly Tyr Asp Gly Arg Gly Phe Asp
115 120 125
Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr
145 150 155 160
Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met
165 170 175
Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln
180 185 190
Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu
195 200 205
Ala Ser Gly Val Pro Gly Arg Phe Ser Gly Ser Gly Ser Gly Asn Ser
210 215 220
Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu Asp Asp Ala Thr Tyr
225 230 235 240
Tyr Cys Gln Gln Trp Ser Gly Tyr Pro Leu Thr Phe Gly Ala Gly Thr
245 250 255
Lys Leu Glu Ile Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
<210> 727
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 727
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Arg Tyr Tyr Gly Met Asp Val Trp
115 120 125
Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn Phe Ala
180 185 190
Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp
195 200 205
Ala Ser Asn Arg Ala Thr Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp
225 230 235 240
Phe Ala Ala Tyr Tyr Cys His Gln Arg Ser Asn Trp Leu Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 728
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 728
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Leu Arg Arg Thr Val Val Thr Pro
115 120 125
Arg Ala Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser
165 170 175
Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala
180 185 190
Ser Gln Asp Ile Ser Asn Ser Leu Asn Trp Tyr Gln Gln Lys Ala Gly
195 200 205
Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Thr Leu Glu Thr Gly
210 215 220
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Phe
225 230 235 240
Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln
245 250 255
Gln His Asp Asn Leu Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 729
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 729
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Pro Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Glu Trp Asp Gly Ser Tyr Tyr Tyr
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Val Leu Thr Gln Thr Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Thr
180 185 190
Tyr Leu Asn Trp Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Phe Ser Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 730
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 730
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Trp Met His Trp Val Arg Gln Val Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asn Thr Asp Gly Ser Thr Thr Thr
65 70 75 80
Tyr Ala Asp Ser Val Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Gly Gly His Trp Ala Val Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
145 150 155 160
Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
165 170 175
Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Arg Leu Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Lys Ala Ser Ser
195 200 205
Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln Gln Tyr Gly His Leu Pro Met Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 731
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 731
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Tyr Arg Leu Ile Ala Val Ala Gly Asp
115 120 125
Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
165 170 175
Ser Val Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
180 185 190
Ser Gln Gly Val Gly Arg Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly
195 200 205
Thr Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly
210 215 220
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
225 230 235 240
Thr Ile Asn Asn Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
245 250 255
Gln Ala Asn Ser Phe Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 732
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 732
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Trp Lys Val Ser Ser Ser Ser Pro Ala
115 120 125
Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr
180 185 190
Thr Lys Tyr Leu Gly Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Ile Tyr Asp Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly
245 250 255
Ser Pro Leu Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 733
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 733
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Thr Ser Gly Tyr
35 40 45
Pro Phe Thr Gly Tyr Ser Leu His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp His Tyr Gly Gly Asn Ser Leu Phe
115 120 125
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Ile Ser Ala Ser Val Gly
165 170 175
Asp Thr Val Ser Ile Thr Cys Arg Ala Ser Gln Asp Ser Gly Thr Trp
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Met
195 200 205
Tyr Asp Ala Ser Thr Leu Glu Asp Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Ala Ser Gly Thr Glu Phe Thr Leu Thr Val Asn Arg Leu Gln Pro
225 230 235 240
Glu Asp Ser Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 734
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 734
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Glu Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Gly
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val His Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Gly Tyr Ser Ser Ser Ser Asp Ala
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Pro Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser
180 185 190
Ser Ala Leu Ala Trp Tyr Gln Gln Lys Pro Gly Thr Pro Pro Lys Leu
195 200 205
Leu Ile Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Ser Ser Tyr
245 250 255
Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 735
<211> 499
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 735
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn
65 70 75 80
Tyr Ala Gln Lys Leu Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ala Gly Gly Ile Tyr Tyr Tyr Tyr
115 120 125
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Ile Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Val Met Thr Gln Thr Pro Asp Ser Leu Ala Val
165 170 175
Ser Leu Gly Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser His Ser Val
180 185 190
Leu Tyr Asn Arg Asn Asn Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys
195 200 205
Pro Gly Gln Pro Pro Lys Leu Leu Phe Tyr Trp Ala Ser Thr Arg Lys
210 215 220
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
225 230 235 240
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Phe
245 250 255
Cys Gln Gln Thr Gln Thr Phe Pro Leu Thr Phe Gly Gln Gly Thr Arg
260 265 270
Leu Glu Ile Asn Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
275 280 285
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
290 295 300
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
305 310 315 320
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
325 330 335
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
340 345 350
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
355 360 365
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
370 375 380
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
385 390 395 400
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
405 410 415
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
420 425 430
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
435 440 445
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
450 455 460
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
465 470 475 480
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
485 490 495
Pro Pro Arg
<210> 736
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 736
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Thr Thr Thr Ser Tyr Ala Phe Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr
195 200 205
Lys Ala Ser Thr Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Asp
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Thr Tyr Ser Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 737
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 737
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Glu Ala Ser Gly Phe
35 40 45
Ile Phe Ser Asp Tyr Tyr Met Gly Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Gly Arg Ser Gly Ser Ser Met Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Phe Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ala Ser Pro Val Val Ala Ala Thr Glu Asp
115 120 125
Phe Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asp Ile Val Met Thr Gln Thr Pro Ala Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Thr
180 185 190
Ser Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Leu Phe Gly Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Met Tyr Tyr Cys Gln Gln Tyr Gly Ser
245 250 255
Ala Pro Val Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 738
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 738
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Arg Ala Pro Gly Ala Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Phe
35 40 45
Thr Phe Arg Gly Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Arg Ala
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Thr Ala Ser Cys Gly Gly Asp Cys Tyr
115 120 125
Tyr Leu Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Pro Thr Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val
180 185 190
Asn Ile Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Lys Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser
245 250 255
Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 739
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 739
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Asp Gly Ser Ser Ser Trp Ser Trp Gly
115 120 125
Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Ser
145 150 155 160
Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr Val
165 170 175
Arg Thr Thr Cys Gln Gly Asp Ala Leu Arg Ser Tyr Tyr Ala Ser Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Met Leu Val Ile Tyr Gly Lys
195 200 205
Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Asp Ser
210 215 220
Gly Asp Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp Glu
225 230 235 240
Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly Tyr Pro Val Phe
245 250 255
Gly Thr Gly Thr Lys Val Thr Val Leu Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 740
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 740
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Leu Tyr Tyr Cys Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly
115 120 125
Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser
145 150 155 160
Ser Glu Leu Thr Gln Glu Pro Ala Val Ser Val Ala Leu Gly Gln Thr
165 170 175
Val Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser
180 185 190
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Phe Gly
195 200 205
Arg Ser Arg Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser
210 215 220
Ser Gly Asn Thr Ala Ser Leu Ile Ile Thr Gly Ala Gln Ala Glu Asp
225 230 235 240
Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Asn Thr Ala Asn His Tyr
245 250 255
Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 741
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 741
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Thr Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Leu Tyr Tyr Cys Ala Lys Asp Ser Ser Ser Trp Tyr Gly Gly Gly
115 120 125
Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser
145 150 155 160
Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly Gln Thr
165 170 175
Val Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Ser Tyr Tyr Ala Ser
180 185 190
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile Tyr Gly
195 200 205
Lys Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Ser
210 215 220
Ser Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala Glu Asp
225 230 235 240
Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Gly Ser Ser Gly Asn His Tyr
245 250 255
Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 742
<211> 495
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 742
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Trp Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Val Trp Val Ser Arg Ile Asn Ser Asp Gly Ser Ser Thr Ser
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Arg Thr Gly Trp Val Gly Ser Tyr Tyr Tyr
115 120 125
Tyr Met Asp Val Trp Gly Lys Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu
165 170 175
Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val
180 185 190
Ser Ser Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
195 200 205
Arg Leu Leu Ile Tyr Asp Val Ser Thr Arg Ala Thr Gly Ile Pro Ala
210 215 220
Arg Phe Ser Gly Gly Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
225 230 235 240
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser
245 250 255
Asn Trp Pro Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 743
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 743
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Gly Tyr Ser Arg Tyr Tyr Tyr Tyr Gly
115 120 125
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Ile Leu Ser Cys Arg Ala Ser Gln Ser Val Tyr
180 185 190
Thr Lys Tyr Leu Gly Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Ile Tyr Asp Ala Ser Thr Arg Ala Thr Gly Ile Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly
245 250 255
Ser Pro Leu Ile Thr Phe Gly Gln Gly Thr Lys Val Asp Ile Lys Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 744
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 744
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Arg Glu Ala Ala Ala Gly His Asp Trp
115 120 125
Tyr Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Arg Val Thr Gln Ser Pro Ser Ser Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
180 185 190
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
245 250 255
Ile Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 745
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 745
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Trp Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Asn Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Pro Arg Val Thr Thr Gly Tyr Phe
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
180 185 190
Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Lys Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Ser Tyr Pro
245 250 255
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 746
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 746
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Arg Arg Pro Gly Ala Ser Val Lys Ile Ser Cys Arg Ala Ser Gly Asp
35 40 45
Thr Ser Thr Arg His Tyr Ile His Trp Leu Arg Gln Ala Pro Gly Gln
50 55 60
Gly Pro Glu Trp Met Gly Val Ile Asn Pro Thr Thr Gly Pro Ala Thr
65 70 75 80
Gly Ser Pro Ala Tyr Ala Gln Met Leu Gln Gly Arg Val Thr Met Thr
85 90 95
Arg Asp Thr Ser Thr Arg Thr Val Tyr Met Glu Leu Arg Ser Leu Arg
100 105 110
Phe Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Val Val Gly Arg
115 120 125
Ser Ala Pro Tyr Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
165 170 175
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
180 185 190
Ser Gln Gly Ile Ser Asp Tyr Ser Ala Trp Tyr Gln Gln Lys Pro Gly
195 200 205
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Thr Leu Gln Ser Gly
210 215 220
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
225 230 235 240
Thr Ile Ser Tyr Leu Gln Ser Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
245 250 255
Gln Tyr Tyr Ser Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp
260 265 270
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 747
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 747
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asn Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Tyr Thr Thr
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Leu Thr Met Thr Arg Asp Thr Ser
85 90 95
Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ile Arg Ser Cys Gly Gly Asp Cys Tyr
115 120 125
Tyr Phe Asp Asn Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Thr Leu Ser Ala
165 170 175
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val
180 185 190
Asn Ile Trp Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
195 200 205
Leu Leu Ile Tyr Lys Ser Ser Ser Leu Ala Ser Gly Val Pro Ser Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Ala Glu Phe Thr Leu Thr Ile Ser Ser
225 230 235 240
Leu Gln Pro Asp Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Gln Ser
245 250 255
Tyr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 748
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 748
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ile Thr Leu Lys Glu Ser Gly Pro Ala Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Ser Thr Ala Gly Val His Val Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Leu Ile Ser Trp Ala Asp Asp Lys
65 70 75 80
Arg Tyr Arg Pro Ser Leu Arg Ser Arg Leu Asp Ile Thr Arg Val Thr
85 90 95
Ser Lys Asp Gln Val Val Leu Ser Met Thr Asn Met Gln Pro Glu Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Leu Gln Gly Phe Asp Gly Tyr Glu Ala
115 120 125
Asn Trp Gly Pro Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Ala Gly
165 170 175
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Arg Gly Ile Ser Ser Ala
180 185 190
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Ser Leu Glu Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Trp
245 250 255
Thr Phe Gly Gln Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 749
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 749
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
120
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
180
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
240
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
300
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
360
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
420
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
480
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
540
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
600
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
660
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
720
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
780
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 750
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 750
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 751
<211> 264
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 751
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Arg Leu Glu Ile Lys
260
<210> 752
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 752
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 753
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 753
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 754
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 754
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgttca atccggcgca gaagtcaaga agccaggagc atcagtgaaa
120
gtgtcctgca aagcctcagg ctacatcttc acgggatact acatccactg ggtgcgccag
180
gctccgggcc agggccttga gtggatgggc tggatcaacc ctaactctgg gggaaccaac
240
tacgctcaga agttccaggg gagggtcact atgactcgcg atacctccat ctccactgcg
300
tacatggaac tctcgggact gagatccgac gatcctgccg tgtactactg cgcccgggac
360
atgaacatct tggcgaccgt gccgtttgac atttggggac agggcaccct cgtcactgtg
420
tcgagcggtg gaggaggctc ggggggtggc ggatcaggag ggggaggaag cgacatccag
480
ctgactcaga gcccatcgtc gttgtccgcg tcggtggggg atagagtgac cattacttgc
540
cgcgccagcc agagcatctc atcatatctg aattggtacc agcagaagcc cggaaaggcc
600
ccaaaactgc tgatctacgc tgcaagcagc ctccaatcgg gagtgccgtc acggttctcc
660
gggtccggtt cgggaactga ctttaccctg accgtgaatt cgctgcaacc ggaggatttc
720
gccacgtact actgtcagca aggagactcc gtgccgctga ccttcggtgg aggcaccaag
780
gtcgaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 755
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 755
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ile Phe Thr Gly Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Pro
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 756
<211> 264
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 756
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ile Phe Thr Gly Tyr Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Pro
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Val Glu Ile Lys
260
<210> 757
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 757
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Gly Leu Arg Ser Asp Asp Pro Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 758
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 758
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 759
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 759
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactccaaca gtcaggcgca gaagtgaaaa agagcggtgc atcggtgaaa
120
gtgtcatgca aagcctcggg ctacaccttc actgactact atatgcactg gctgcggcag
180
gcaccgggac agggacttga gtggatggga tggatcaacc cgaattcagg ggacactaac
240
tacgcgcaga agttccaggg gagagtgacc ctgacgaggg acacctcaat ttcgaccgtc
300
tacatggaat tgtcgcgcct gagatcggac gatactgctg tgtactactg tgcccgcgac
360
atgaacatcc tcgcgactgt gccttttgat atctggggac aggggactat ggtcaccgtt
420
tcctccgctt ccggtggcgg aggctcggga ggccgggcct ccggtggagg aggcagcgac
480
atccagatga ctcagagccc ttcctcgctg agcgcctcag tgggagatcg cgtgaccatc
540
acttgccggg ccagccagtc catttcgtcc tacctcaatt ggtaccagca gaagccggga
600
aaggcgccca agctcttgat ctacgctgcg agctccctgc aaagcggggt gccgagccga
660
ttctcgggtt ccggctcggg aaccgacttc actctgacca tctcatccct gcaaccagag
720
gactttgcca cctactactg ccaacaagga gattctgtcc cactgacgtt cggcggagga
780
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
840
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
900
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
960
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1020
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1080
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1140
ttcagccgca gcgcagatgc tccagcctac aagcaggggc agaaccagct ctacaacgaa
1200
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
1260
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
1320
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
1380
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
1440
cttcacatgc aggccctgcc gcctcgg
1467
<210> 760
<211> 336
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 760
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Ser Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asp Tyr Tyr Met His Trp Leu Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu
180 185 190
Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
<210> 761
<211> 266
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 761
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Ser Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Asp Tyr Tyr Met His Trp Leu Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu
180 185 190
Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
260 265
<210> 762
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 762
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Ser Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Leu Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Asp Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 763
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 763
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 764
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 764
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtcaggagcg gaagtcaaga agcccggagc gtcagtcaaa
120
gtgtcatgca aagcctcggg ctacactttc actgggtact acatgcactg ggtgcgccag
180
gctccaggac agggactgga atggatggga tggatcaacc cgaactccgg tggcaccaat
240
tacgcccaga agttccaggg gagggtgacc atgactcgcg acacgtcgat cagcaccgca
300
tacatggagc tgtcaagact ccggtccgac gatactgccg tgtactactg cgcacgggac
360
atgaacattc tggccaccgt gccttttgac atctggggtc agggaactat ggttaccgtg
420
tcctctggtg gaggcggctc cggcgggggg ggaagcggag gcggtggaag cgacattcag
480
atgacccagt cgccttcatc cctttcggcg agcgtgggag atcgcgtcac tatcacttgt
540
cgggcctcgc agtccatctc cacctacctc aattggtacc agcagaagcc aggaaaagca
600
ccgaatctgc tgatctacgc cgcgttttcc ttgcaatcgg gagtgccaag cagattcagc
660
ggatcgggat caggcactga tttcaccctc accatcaact cgctgcaacc ggaggatttc
720
gctacgtact attgccaaca aggagacagc gtgccgctca ccttcggcgg agggactaag
780
ctggaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 765
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 765
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Ala Ala
195 200 205
Phe Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 766
<211> 264
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 766
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr Leu Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr Ala Ala
195 200 205
Phe Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu Thr Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys
260
<210> 767
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 767
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 768
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 768
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Thr Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Phe Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 769
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 769
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagatcc agctggtgca gtcgggagct gaagtcaaaa agcctggcgc aaccgtcaag
120
atctcgtgca aaggatcagg gttcaacatc gaggactact acatccattg ggtgcaacag
180
gcacccggaa aaggcctgga gtggatgggg aggattgacc cagaaaatga cgaaaccaag
240
tacggaccga tcttccaagg acgggtgacc atcacggctg acacttccac taacaccgtc
300
tacatggaac tctcgagcct tcgctcggaa gataccgcgg tgtactactg cgcctttaga
360
ggtggagtct actggggaca agggactacc gtcaccgtgt cgtcaggtgg cggaggatca
420
ggcggaggcg gctccggtgg aggaggaagc ggaggaggtg gctccgacgt ggtgatgacg
480
cagtcaccgg actccttggc ggtgagcctg ggtgaacgcg ccactatcaa ctgcaagagc
540
tcccagagct tgctggactc cgatggaaag acttatctca attggctgca acagaagcct
600
ggccagccgc caaagagact catctcactg gtgagcaagc tggatagcgg agtgccagat
660
cggttttcgg gatcgggctc aggcaccgac ttcaccctga ctatttcctc cctccaagcc
720
gaggatgtgg ccgtctacta ctgttggcag gggactcact tcccggggac cttcggtgga
780
ggcactaagg tggagatcaa aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 770
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 770
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser
85 90 95
Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile
165 170 175
Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
225 230 235 240
Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 771
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 771
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tcatgactca aagcccagat tccttggctg tctcccttgg agaaagagca
120
acgatcaatt gcaaaagctc gcagtccctg ttggactccg atggaaaaac ctacctcaac
180
tggctgcagc agaagccggg acaaccacca aagcggctga tttccctcgt gtccaagctg
240
gacagcggcg tgccggatcg cttctcgggc agcggctcgg gaaccgattt tactctcact
300
atttcgtcac tgcaagcgga ggacgtggcg gtgtattact gctggcaggg cactcacttc
360
ccgggtactt ttggtggagg taccaaagtc gaaatcaagg gtggaggcgg gagcggagga
420
ggcgggtcgg gaggaggagg atcgggtggc ggaggctcag aaatccagct ggtgcagtca
480
ggtgccgaag tgaagaagcc tggggccacg gtgaagatct cgtgcaaggg gagcggattc
540
aacatcgagg attactacat ccattgggtg caacaggccc ctggcaaagg gctggaatgg
600
atgggaagga tcgaccccga gaatgacgag actaagtacg gcccgatctt ccaaggacgg
660
gtgaccatca ctgcagacac ttcaaccaac accgtctaca tggaactctc ctcgctgcgc
720
tccgaggaca ccgccgtgta ctactgtgct ttcagaggag gagtctactg gggacaggga
780
acgaccgtga ccgtcagctc aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 772
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 772
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln
180 185 190
Ala Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr
210 215 220
Ala Asp Thr Ser Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg
225 230 235 240
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 773
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 773
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaatcc agctggtgca aagcggagcc gaggtgaaga agcccggaga atccctgcgc
120
atctcgtgta agggttccgg ctttaacatc gaggattact acatccactg ggtgagacag
180
atgccgggca aaggtctgga atggatgggc cgcatcgacc cggagaacga cgaaaccaaa
240
tacggaccaa tcttccaagg acatgtgact atttccgcgg atacctccat caacactgtc
300
tacttgcagt ggagctcgct caaggcgtcg gataccgcca tgtactactg cgcattcaga
360
ggaggtgtgt actggggcca gggcactacg gtcaccgtgt cctcgggagg tggagggtca
420
ggaggcggag gctcgggcgg tggaggatca ggcggaggag gaagcgatgt ggtcatgact
480
caatccccac tgtcactgcc tgtcactctg gggcaaccgg cttccatctc atgcaagtca
540
agccaatcgc tgctcgactc cgacggaaaa acctacctca attggcttca gcagcgccca
600
ggccagtcgc ctcggaggct gatctcactc gtgtcgaagc ttgactccgg ggtgccggat
660
cggtttagcg gaagcggatc ggggaccgac ttcacgttga agattagccg ggtggaagcc
720
gaggacgtgg gagtctatta ctgctggcag gggacccact tcccggggac tttcggagga
780
ggcaccaaag tcgagattaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 774
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 774
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser
85 90 95
Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 775
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 775
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtcg tcatgaccca atcccctctc tccctgccgg tcaccctggg tcagccggcg
120
tcgatctcat gcaaaagctc acagtccctg ctggattcgg acggaaaaac ctacttgaac
180
tggctccaac agaggccggg tcagtcccct cgcagactga tctcgctggt gagcaagctc
240
gactcgggtg tgccggatcg gttctccggg tcaggatcgg gcaccgactt tacgctcaag
300
atttcgagag tggaggccga ggatgtggga gtgtactatt gctggcaggg cacgcatttc
360
cccgggacct ttggaggcgg gactaaggtg gaaatcaagg gaggtggcgg atcaggcgga
420
ggaggcagcg gcggaggtgg atcaggaggc ggagggtcag agatccagct ggtccaaagc
480
ggagcagagg tgaagaagcc aggcgagtcc cttcgcattt cgtgcaaagg gagcggcttc
540
aacattgaag attactacat ccactgggtg cggcaaatgc caggaaaggg tctggaatgg
600
atgggacgga tcgacccaga aaatgatgaa actaagtacg gaccgatctt ccaaggacac
660
gtcactatct ccgcggacac ttcgatcaac accgtgtacc tccagtggag cagcttgaaa
720
gcctccgaca ccgctatgta ctactgtgcc ttccgcggag gagtctactg gggacagggg
780
actactgtga ccgtgtcgtc caccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 776
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 776
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu
20 25 30
Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln
180 185 190
Met Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser
210 215 220
Ala Asp Thr Ser Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys
225 230 235 240
Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 777
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 777
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaatcc agctcgtgca gagcggagcc gaggtcaaga aaccgggtgc taccgtgaag
120
atttcatgca agggatcggg cttcaacatc gaggattact acatccactg ggtgcagcag
180
gcaccaggaa aaggacttga atggatgggc cggatcgacc cggaaaatga cgagactaag
240
tacggcccta tcttccaagg acgggtgacg atcaccgcag acactagcac caacaccgtc
300
tatatggaac tctcgtccct gaggtccgaa gatactgccg tgtactactg tgcgtttcgc
360
ggaggtgtgt actggggaca gggtaccacc gtcaccgtgt catcgggcgg tggaggctcc
420
ggtggaggag ggtcaggagg cggtggaagc ggaggaggcg gcagcgacgt ggtcatgact
480
caatcgccgc tgtcgctgcc cgtcactctg ggacaacccg cgtccatcag ctgcaaatcc
540
tcgcagtcac tgcttgactc cgatggaaag acctacctca actggctgca gcaacgccca
600
ggccaatccc caagacgcct gatctcgttg gtgtcaaagc tggactcagg ggtgccggac
660
cggttctccg ggagcgggtc gggcacggat ttcactctca agatctccag agtggaagcc
720
gaggatgtgg gagtctacta ctgctggcag ggaacccatt tccctggaac ttttggcgga
780
ggaactaagg tcgagattaa aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 778
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 778
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Thr Ser
85 90 95
Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 779
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 779
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagattc agctcgtgca atcgggagcg gaagtcaaga agccaggaga gtccttgcgg
120
atctcatgca agggtagcgg ctttaacatc gaggattact acatccactg ggtgaggcag
180
atgccgggga agggactcga atggatggga cggatcgacc cagaaaacga cgaaactaag
240
tacggtccga tcttccaagg ccatgtgact attagcgccg atacttcaat caataccgtg
300
tatctgcaat ggtcctcatt gaaagcctca gataccgcga tgtactactg tgctttcaga
360
ggaggggtct actggggaca gggaactacc gtgactgtct cgtccggcgg aggcgggtca
420
ggaggtggcg gcagcggagg aggagggtcc ggcggaggtg ggtccgacgt cgtgatgacc
480
cagagccctg acagcctggc agtgagcctg ggcgaaagag ctaccattaa ctgcaaatcg
540
tcgcagagcc tgctggactc ggacggaaaa acgtacctca attggctgca gcaaaagcct
600
ggccagccac cgaagcgcct tatctcactg gtgtcgaagc tggattcggg agtgcccgat
660
cgcttctccg gctcgggatc gggtactgac ttcaccctca ctatctcctc gcttcaagca
720
gaggacgtgg ccgtctacta ctgctggcag ggaacccact ttccgggaac cttcggcgga
780
gggacgaaag tggagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 780
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 780
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln Met Pro Gly Lys
50 55 60
Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser Ala Asp Thr Ser
85 90 95
Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Gln Gly
115 120 125
Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Val Met Thr
145 150 155 160
Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu Arg Ala Thr Ile
165 170 175
Asn Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Leu Gln Gln Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile
195 200 205
Ser Leu Val Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
225 230 235 240
Glu Asp Val Ala Val Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 781
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 781
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgacgtgg tgatgactca gtcgcctgac tcgctggctg tgtcccttgg agagcgggcc
120
actatcaatt gcaagtcatc ccagtcgctg ctggattccg acgggaaaac ctacctcaat
180
tggctgcagc aaaaaccggg acagcctcca aagcggctca tcagcctggt gtccaagttg
240
gacagcggcg tgccagaccg cttctccggt tcgggaagcg gtactgattt cacgctgacc
300
atctcatccc tccaagcgga ggatgtggca gtctactact gttggcaggg cacgcatttt
360
ccgggcactt ttggaggagg gaccaaggtc gaaatcaagg gaggaggtgg ctcgggcgga
420
ggaggctcgg gaggaggagg atcaggaggc ggtggaagcg agattcaact ggtccagagc
480
ggcgcagaag tcaagaagcc gggtgaatcg ctcagaatct cgtgcaaagg atcgggattc
540
aacatcgagg actactacat tcactgggtc agacaaatgc cgggcaaagg gctggaatgg
600
atggggagga tcgaccccga aaacgatgaa accaagtacg gaccaatctt ccaagggcac
660
gtgaccattt cggcggacac ctcaatcaac actgtgtacc tccagtggag ctcacttaag
720
gccagcgata ccgccatgta ctattgcgct ttccgcggag gggtgtactg gggacagggc
780
actactgtga ccgtgtcatc caccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 782
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 782
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Lys Pro Gly Gln Pro Pro Lys Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Glu Ser Leu Arg Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Arg Gln
180 185 190
Met Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly His Val Thr Ile Ser
210 215 220
Ala Asp Thr Ser Ile Asn Thr Val Tyr Leu Gln Trp Ser Ser Leu Lys
225 230 235 240
Ala Ser Asp Thr Ala Met Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 783
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 783
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgatgtgg tcatgacgca gtcaccactg tccctccccg tgacccttgg acagccagcg
120
tcgattagct gcaagtcatc ccaatccctg ctcgattcgg atggaaagac ctatctcaac
180
tggctgcagc aaagacccgg tcagagccct aggagactca tctcgttggt gtcaaagctg
240
gacagcggag tgccggaccg gttttccggt tcgggatcgg ggacggactt cactctgaag
300
atttcacggg tggaagctga ggatgtggga gtgtactact gctggcaggg aacccatttc
360
cctggcactt ttggcggagg aactaaggtc gaaatcaagg gaggaggtgg ctcgggagga
420
ggcggatcgg gcggaggcgg gagcggcgga ggagggtccg aaatccaact tgtccagtca
480
ggagccgaag tgaagaaacc gggagccacc gtcaaaatca gctgtaaggg atcgggattc
540
aatatcgagg actactacat ccactgggtg cagcaagctc cgggcaaagg actggagtgg
600
atggggcgca tcgacccaga gaacgacgaa accaaatacg gcccgatctt ccaagggcgg
660
gtgaccatca ccgcggacac ctcaactaac actgtgtaca tggagctgag ctccctgcgc
720
tccgaagata ctgcagtcta ctactgcgcc ttccgcggtg gtgtgtactg gggacagggc
780
accactgtga ctgtcagctc gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 784
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 784
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu
20 25 30
Pro Val Thr Leu Gly Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp Leu Gln Gln
50 55 60
Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile Ser Leu Val Ser Lys Leu
65 70 75 80
Asp Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
100 105 110
Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly Gly Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Gln Leu Val Gln Ser
145 150 155 160
Gly Ala Glu Val Lys Lys Pro Gly Ala Thr Val Lys Ile Ser Cys Lys
165 170 175
Gly Ser Gly Phe Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Gln Gln
180 185 190
Ala Pro Gly Lys Gly Leu Glu Trp Met Gly Arg Ile Asp Pro Glu Asn
195 200 205
Asp Glu Thr Lys Tyr Gly Pro Ile Phe Gln Gly Arg Val Thr Ile Thr
210 215 220
Ala Asp Thr Ser Thr Asn Thr Val Tyr Met Glu Leu Ser Ser Leu Arg
225 230 235 240
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr
245 250 255
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 785
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 785
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagatcc agctccaaca gagcggagcc gaactggtca aaccgggagc gtcggtgaag
120
ttgtcatgca ctggatcggg cttcaacatc gaggattact acatccactg ggtcaagcaa
180
cgcaccgagc aggggctgga atggatcgga cggatcgacc ccgaaaacga tgaaaccaag
240
tacgggccta tcttccaagg acgggccacc attacggctg acacgtcaag caataccgtc
300
tacctccagc tttccagcct gacctccgag gacactgccg tgtactactg cgccttcaga
360
ggaggcgtgt actggggacc aggaaccact ttgaccgtgt ccagcggagg cggtggatca
420
ggaggaggag gctcaggcgg tggcggctcg cacatggacg tggtcatgac tcagtccccg
480
ctgaccctgt cggtggcaat tggacagagc gcatccatct cgtgcaagag ctcacagtcg
540
ctgctggatt ccgacggaaa gacttatctg aactggctgc tccaaagacc agggcaatca
600
ccgaaacgcc ttatctccct ggtgtcgaaa ctcgactcgg gtgtgccgga tcggtttacc
660
ggtagcgggt ccggcacgga cttcactctc cgcatttcga gggtggaagc ggaggatctc
720
gggatctact actgttggca gggaacccac ttccctggga cttttggagg cggaactaag
780
ctggaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 786
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 786
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Gln Leu Gln Gln Ser Gly Ala Glu Leu
20 25 30
Val Lys Pro Gly Ala Ser Val Lys Leu Ser Cys Thr Gly Ser Gly Phe
35 40 45
Asn Ile Glu Asp Tyr Tyr Ile His Trp Val Lys Gln Arg Thr Glu Gln
50 55 60
Gly Leu Glu Trp Ile Gly Arg Ile Asp Pro Glu Asn Asp Glu Thr Lys
65 70 75 80
Tyr Gly Pro Ile Phe Gln Gly Arg Ala Thr Ile Thr Ala Asp Thr Ser
85 90 95
Ser Asn Thr Val Tyr Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Phe Arg Gly Gly Val Tyr Trp Gly Pro Gly
115 120 125
Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser His Met Asp Val Val Met Thr Gln Ser Pro
145 150 155 160
Leu Thr Leu Ser Val Ala Ile Gly Gln Ser Ala Ser Ile Ser Cys Lys
165 170 175
Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn Trp
180 185 190
Leu Leu Gln Arg Pro Gly Gln Ser Pro Lys Arg Leu Ile Ser Leu Val
195 200 205
Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Leu
225 230 235 240
Gly Ile Tyr Tyr Cys Trp Gln Gly Thr His Phe Pro Gly Thr Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 787
<211> 1452
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 787
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgatatcc aaatgactca gagcccttca tccctgagcg ccagcgtcgg agacagggtg
120
accatcacgt gccgggcatc ccaaggcatt agaaataact tggcgtggta tcagcaaaaa
180
ccaggaaagg ccccgaagcg cctgatctac gcggcctcca accttcagtc aggagtgccc
240
tcgcgcttca ccgggagcgg tagcggaact gagtttaccc ttatcgtgtc gtccctgcag
300
ccagaggact tcgcgaccta ctactgcctc cagcatcact cgtacccgtt gacttcggga
360
ggcggaacca aggtcgaaat caaacgcact ggctcgacgt cagggtccgg taaaccggga
420
tcgggagaag gatcggaagt ccaagtgctg gagagcggag gcggactcgt gcaacctggc
480
gggtcgctgc ggctcagctg tgccgcgtcg ggttttactt tcagctcgta cgctatgtca
540
tgggtgcggc aggctccggg aaaggggctg gaatgggtgt ccgctatttc cggctcgggt
600
ggaagcacca attacgccga ctccgtgaag ggacgcttca ccatctcacg ggataactcc
660
aagaatactc tgtacctcca gatgaactcg ctgagagccg aggacaccgc agtgtactac
720
tgcgcagggt caagcggctg gtccgaatac tggggacagg gcaccctcgt cactgtcagc
780
tccaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
840
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
900
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
960
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1020
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1080
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1140
gatgctccag cctacaagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1200
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
1260
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
1320
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
1380
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
1440
ctgccgcctc gg
1452
<210> 788
<211> 484
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 788
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Gly Ile Arg Asn Asn Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Arg Leu Ile Tyr Ala Ala Ser Asn Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Thr Gly Ser Gly Ser Gly Thr Glu Phe Thr Leu Ile Val
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His
100 105 110
His Ser Tyr Pro Leu Thr Ser Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Arg Thr Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly
130 135 140
Ser Glu Val Gln Val Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly
145 150 155 160
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser
165 170 175
Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
180 185 190
Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Asn Tyr Ala Asp Ser
195 200 205
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu
210 215 220
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
225 230 235 240
Cys Ala Gly Ser Ser Gly Trp Ser Glu Tyr Trp Gly Gln Gly Thr Leu
245 250 255
Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
260 265 270
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
275 280 285
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
290 295 300
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
305 310 315 320
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 789
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 789
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser
145 150 155 160
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln
195 200 205
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 790
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 790
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
120
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
180
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
240
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
300
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
360
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
420
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
480
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
540
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
600
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
660
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
720
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 791
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 791
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Gly Trp Val Ser Gly Ile Ser Arg Ser Gly Glu Asn Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Pro Ala His Tyr Tyr Gly Gly Met
115 120 125
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Ile Ser Ser Ser Phe Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Arg Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu
225 230 235 240
Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro Ser Trp
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 792
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 792
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtgga atctggtgga ggactcgtgc aacccggaag atcgcttaga
120
ctgtcgtgtg ccgccagcgg gttcactttc tcgaactacg cgatgtcctg ggtccgccag
180
gcacccggaa agggactcgg ttgggtgtcc ggcatttccc ggtccggcga aaatacctac
240
tacgccgact ccgtgaaggg ccgcttcacc atctcaaggg acaacagcaa aaacaccctg
300
tacttgcaaa tgaactccct gcgggatgaa gatacagccg tgtactattg cgcccggtcg
360
cctgcccatt actacggcgg aatggacgtc tggggacagg gaaccactgt gactgtcagc
420
agcgcgtcgg gtggcggcgg ctcagggggt cgggcctccg gggggggagg gtccgacatc
480
gtgctgaccc agtccccggg aaccctgagc ctgagcccgg gagagcgcgc gaccctgtca
540
tgccgggcat cccagagcat tagctcctcc tttctcgcct ggtatcagca gaagcccgga
600
caggccccga ggctgctgat ctacggcgct agcagaaggg ctaccggaat cccagaccgg
660
ttctccggct ccggttccgg gaccgatttc acccttacta tctcgcgcct ggaacctgag
720
gactccgccg tctactactg ccagcagtac cactcatccc cgtcgtggac gttcggacag
780
ggcaccaagc tggagattaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 793
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 793
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Leu Tyr Tyr Cys Ser Val His Ser Phe Leu Ala Tyr Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
145 150 155 160
Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys
165 170 175
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
180 185 190
Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu
195 200 205
Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp
225 230 235 240
Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 794
<211> 1464
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 794
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtcga atccggtgga ggtctggtcc aacctggtag aagcctgaga
120
ctgtcgtgtg cggccagcgg attcaccttt gatgactatg ctatgcactg ggtgcggcag
180
gccccaggaa agggcctgga atgggtgtcg ggaattagct ggaactccgg gtccattggc
240
tacgccgact ccgtgaaggg ccgcttcacc atctcccgcg acaacgcaaa gaactccctg
300
tacttgcaaa tgaactcgct cagggctgag gataccgcgc tgtactactg ctccgtgcat
360
tccttcctgg cctactgggg acagggaact ctggtcaccg tgtcgagcgc ctccggcggc
420
gggggctcgg gtggacgggc ctcgggcgga ggggggtccg acatcgtgat gacccagacc
480
ccgctgagct tgcccgtgac tcccggagag cctgcatcca tctcctgccg gtcatcccag
540
tcccttctcc actccaacgg atacaactac ctcgactggt acctccagaa gccgggacag
600
agccctcagc ttctgatcta cctggggtca aatagagcct caggagtgcc ggatcggttc
660
agcggatctg gttcgggaac tgatttcact ctgaagattt cccgcgtgga agccgaggac
720
gtgggcgtct actactgtat gcaggcgctg cagaccccct ataccttcgg ccaagggacg
780
aaagtggaga tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
840
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
900
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
960
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1020
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1080
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1140
agccgcagcg cagatgctcc agcctacaag caggggcaga accagctcta caacgaactc
1200
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
1260
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
1320
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
1380
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
1440
cacatgcagg ccctgccgcc tcgg
1464
<210> 795
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 795
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
145 150 155 160
Pro Leu Ser Leu Ser Val Thr Pro Gly Gln Pro Ala Ser Ile Ser Cys
165 170 175
Lys Ser Ser Gln Ser Leu Leu Arg Asn Asp Gly Lys Thr Pro Leu Tyr
180 185 190
Trp Tyr Leu Gln Lys Ala Gly Gln Pro Pro Gln Leu Leu Ile Tyr Glu
195 200 205
Val Ser Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp
225 230 235 240
Val Gly Ala Tyr Tyr Cys Met Gln Asn Ile Gln Phe Pro Ser Phe Gly
245 250 255
Gly Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 796
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 796
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattgttgga atctggagga ggacttgtgc agcctggagg atcactgaga
120
ctttcgtgtg cggtgtcagg cttcgccctg agcaaccacg gcatgagctg ggtgcggaga
180
gccccgggga agggtctgga atgggtgtcc gggatcgtct actccggttc aacttactac
240
gccgcaagcg tgaagggtcg cttcaccatt tcccgcgata actcccggaa caccctgtac
300
ctccaaatga actccctgcg gcccgaggac accgccatct actactgttc cgcgcatgga
360
ggagagtccg atgtctgggg acagggcact accgtgaccg tgtcgagcgc ctcgggggga
420
ggaggctccg gcggtcgcgc ctccgggggg ggtggcagcg acattgtgat gacgcagact
480
ccactctcgc tgtccgtgac cccgggacag cccgcgtcca tctcgtgcaa gagctcccag
540
agcctgctga ggaacgacgg aaagactcct ctgtattggt acctccagaa ggctggacag
600
cccccgcaac tgctcatcta cgaagtgtca aatcgcttct ccggggtgcc ggatcggttt
660
tccggctcgg gatcgggcac cgacttcacc ctgaaaatct ccagggtcga ggccgaggac
720
gtgggagcct actactgcat gcaaaacatc cagttccctt ccttcggcgg cggcacaaag
780
ctggagatta agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 797
<211> 493
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 797
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Arg Lys Thr Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Ile Phe Asp Asn Phe Gly Ile Asn Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Lys Asn Asn Asn Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
85 90 95
Thr Asn Thr Ala Tyr Met Glu Val Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Pro Tyr Tyr Tyr Gln Ser Tyr Met
115 120 125
Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro
165 170 175
Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly
180 185 190
Tyr Asn Tyr Leu Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln
195 200 205
Leu Leu Ile Tyr Leu Gly Ser Lys Arg Ala Ser Gly Val Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu His Ile Thr Arg
225 230 235 240
Val Gly Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln
245 250 255
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 798
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 798
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactcgtcca gtccggcgca gaagtcagaa aaaccggtgc tagcgtgaaa
120
gtgtcctgca aggcctccgg ctacattttc gataacttcg gaatcaactg ggtcagacag
180
gccccgggcc aggggctgga atggatggga tggatcaacc ccaagaacaa caacaccaac
240
tacgcacaga agttccaggg ccgcgtgact atcaccgccg atgaatcgac caataccgcc
300
tacatggagg tgtcctccct gcggtcggag gacactgccg tgtattactg cgcgaggggc
360
ccatactact accaaagcta catggacgtc tggggacagg gaaccatggt gaccgtgtca
420
tccgcctccg gtggtggagg ctccgggggg cgggcttcag gaggcggagg aagcgatatt
480
gtgatgaccc agactccgct tagcctgccc gtgactcctg gagaaccggc ctccatttcc
540
tgccggtcct cgcaatcact cctgcattcc aacggttaca actacctgaa ttggtacctc
600
cagaagcctg gccagtcgcc ccagttgctg atctatctgg gctcgaagcg cgcctccggg
660
gtgcctgacc ggtttagcgg atctgggagc ggcacggact tcactctcca catcacccgc
720
gtgggagcgg aggacgtggg agtgtactac tgtatgcagg cgctgcagac tccgtacaca
780
ttcggacagg gcaccaagct ggagatcaag accactaccc cagcaccgag gccacccacc
840
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
900
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
960
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1020
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1080
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1140
ctgcgcgtga aattcagccg cagcgcagat gctccagcct acaagcaggg gcagaaccag
1200
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
1260
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
1320
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
1380
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
1440
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
1479
<210> 799
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 799
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Asp Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Val Ile Ser Gly Ser Gly Gly Thr Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Leu Asp Ser Ser Gly Tyr Tyr Tyr Ala
115 120 125
Arg Gly Pro Arg Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
130 135 140
Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
195 200 205
Ile Tyr Gly Ala Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr His Phe Thr Leu Thr Ile Asn Ser Leu Gln
225 230 235 240
Ser Glu Asp Ser Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Lys Arg Ala
245 250 255
Ser Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 800
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 800
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aacttcaaga atcaggcgga ggactcgtgc agcccggagg atcattgcgg
120
ctctcgtgcg ccgcctcggg cttcaccttc tcgagcgacg ccatgacctg ggtccgccag
180
gccccgggga aggggctgga atgggtgtct gtgatttccg gctccggggg aactacgtac
240
tacgccgatt ccgtgaaagg tcgcttcact atctcccggg acaacagcaa gaacaccctt
300
tatctgcaaa tgaattccct ccgcgccgag gacaccgccg tgtactactg cgccaagctg
360
gactcctcgg gctactacta tgcccggggt ccgagatact ggggacaggg aaccctcgtg
420
accgtgtcct ccgcgtccgg cggaggaggg tcgggagggc gggcctccgg cggcggcggt
480
tcggacatcc agctgaccca gtccccatcc tcactgagcg caagcgtggg cgacagagtc
540
accattacat gcagggcgtc ccagagcatc agctcctacc tgaactggta ccaacagaag
600
cctggaaagg ctcctaagct gttgatctac ggggcttcga ccctggcatc cggggtgccc
660
gcgaggttta gcggaagcgg tagcggcact cacttcactc tgaccattaa cagcctccag
720
tccgaggatt cagccactta ctactgtcag cagtcctaca agcgggccag cttcggacag
780
ggcactaagg tcgagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 801
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 801
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Ser Asn Tyr Gly Ile Thr Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asn Thr Ser
85 90 95
Ile Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Pro Tyr Tyr Tyr Tyr Met Asp Val
115 120 125
Trp Gly Lys Gly Thr Met Val Thr Val Ser Ser Ala Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser
165 170 175
Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Ser Asn Gly Tyr Asn
180 185 190
Tyr Val Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu
195 200 205
Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Lys Leu Gln Ile Ser Arg Val Glu
225 230 235 240
Ala Glu Asp Val Gly Ile Tyr Tyr Cys Met Gln Gly Arg Gln Phe Pro
245 250 255
Tyr Ser Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 802
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 802
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtcc aactggtcca gagcggtgca gaagtgaaga agcccggagc gagcgtgaaa
120
gtgtcctgca aggcttccgg gtacaccttc tccaactacg gcatcacttg ggtgcgccag
180
gccccgggac agggcctgga atggatgggg tggatttccg cgtacaacgg caatacgaac
240
tacgctcaga agttccaggg tagagtgacc atgactagga acacctccat ttccaccgcc
300
tacatggaac tgtcctccct gcggagcgag gacaccgccg tgtactattg cgcccgggga
360
ccatactact actacatgga tgtctggggg aaggggacta tggtcaccgt gtcatccgcc
420
tcgggaggcg gcggatcagg aggacgcgcc tctggtggtg gaggatcgga gatcgtgatg
480
acccagagcc ctctctcctt gcccgtgact cctggggagc ccgcatccat ttcatgccgg
540
agctcccagt cacttctcta ctccaacggc tataactacg tggattggta cctccaaaag
600
ccgggccaga gcccgcagct gctgatctac ctgggctcga acagggccag cggagtgcct
660
gaccggttct ccgggtcggg aagcgggacc gacttcaagc tgcaaatctc gagagtggag
720
gccgaggacg tgggaatcta ctactgtatg cagggccgcc agtttccgta ctcgttcgga
780
cagggcacca aagtggaaat caagaccact accccagcac cgaggccacc caccccggct
840
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 803
<211> 482
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 803
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Val Ser Pro Gly Glu Ser Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Ser Ser Asn Leu Ala Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala
195 200 205
Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Gly Ser Ser Leu Thr Phe Gly Gly Gly Thr Lys Val
245 250 255
Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro
260 265 270
Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro
275 280 285
Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
290 295 300
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
305 310 315 320
Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu
325 330 335
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
340 345 350
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
355 360 365
Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys
370 375 380
Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu
385 390 395 400
Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly
405 410 415
Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu
420 425 430
Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly
435 440 445
Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser
450 455 460
Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro
465 470 475 480
Pro Arg
<210> 804
<211> 1446
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 804
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattgctcga aactggagga ggtctggtgc aacctggagg atcacttcgc
120
ctgtcctgcg ccgtgtcggg ctttgccctg tccaaccatg gaatgagctg ggtccgccgc
180
gcgccgggga agggcctcga atgggtgtcc ggcatcgtct actccggctc cacctactac
240
gccgcgtccg tgaagggccg gttcacgatt tcacgggaca actcgcggaa caccctgtac
300
ctccaaatga attcccttcg gccggaggat actgccatct actactgctc cgcccacggt
360
ggcgaatccg acgtctgggg ccagggaacc accgtgaccg tgtccagcgc gtccggggga
420
ggaggaagcg ggggtagagc atcgggtgga ggcggatcag agatcgtgct gacccagtcc
480
cccgccacct tgagcgtgtc accaggagag tccgccaccc tgtcatgccg cgccagccag
540
tccgtgtcct ccaacctggc ttggtaccag cagaagccgg ggcaggcccc tagactcctg
600
atctatgggg cgtcgacccg ggcatctgga attcccgata ggttcagcgg atcgggctcg
660
ggcactgact tcactctgac catctcctcg ctgcaagccg aggacgtggc tgtgtactac
720
tgtcagcagt acggaagctc cctgactttc ggtggcggga ccaaagtcga gattaagacc
780
actaccccag caccgaggcc acccaccccg gctcctacca tcgcctccca gcctctgtcc
840
ctgcgtccgg aggcatgtag acccgcagct ggtggggccg tgcatacccg gggtcttgac
900
ttcgcctgcg atatctacat ttgggcccct ctggctggta cttgcggggt cctgctgctt
960
tcactcgtga tcactcttta ctgtaagcgc ggtcggaaga agctgctgta catctttaag
1020
caacccttca tgaggcctgt gcagactact caagaggagg acggctgttc atgccggttc
1080
ccagaggagg aggaaggcgg ctgcgaactg cgcgtgaaat tcagccgcag cgcagatgct
1140
ccagcctaca agcaggggca gaaccagctc tacaacgaac tcaatcttgg tcggagagag
1200
gagtacgacg tgctggacaa gcggagagga cgggacccag aaatgggcgg gaagccgcgc
1260
agaaagaatc cccaagaggg cctgtacaac gagctccaaa aggataagat ggcagaagcc
1320
tatagcgaga ttggtatgaa aggggaacgc agaagaggca aaggccacga cggactgtac
1380
cagggactca gcaccgccac caaggacacc tatgacgctc ttcacatgca ggccctgccg
1440
cctcgg
1446
<210> 805
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 805
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Ser Ser Lys Leu Ala Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Gln Ala Pro Arg Leu Leu Met Tyr Gly Ala Ser Ile Arg Ala
195 200 205
Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Gly Ser Ser Ser Trp Thr Phe Gly Gln Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 806
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 806
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga aactggagga ggacttgtgc aacctggagg atcattgaga
120
ctgagctgcg cagtgtcggg attcgccctg agcaaccatg gaatgtcctg ggtcagaagg
180
gcccctggaa aaggcctcga atgggtgtca gggatcgtgt actccggttc cacttactac
240
gccgcctccg tgaaggggcg cttcactatc tcacgggata actcccgcaa taccctgtac
300
ctccaaatga acagcctgcg gccggaggat accgccatct actactgttc cgcccacggt
360
ggagagtctg acgtctgggg ccagggaact accgtgaccg tgtcctccgc gtccggcggt
420
ggagggagcg gcggccgcgc cagcggcggc ggaggctccg agatcgtgat gacccagagc
480
cccgctactc tgtcggtgtc gcccggagaa agggcgaccc tgtcctgccg ggcgtcgcag
540
tccgtgagca gcaagctggc ttggtaccag cagaagccgg gccaggcacc acgcctgctt
600
atgtacggtg cctccattcg ggccaccgga atcccggacc ggttctcggg gtcggggtcc
660
ggtaccgagt tcacactgac catttcctcg ctcgagcccg aggactttgc cgtctattac
720
tgccagcagt acggctcctc ctcatggacg ttcggccagg ggaccaaggt cgaaatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 807
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 807
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Gly Ser Thr Asn Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Asn Arg
195 200 205
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Gly Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Gly Ser Ser Pro Pro Trp Thr Phe Gly Gln Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 808
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 808
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga gactggagga ggagtggtgc aacctggagg aagcctgaga
120
ctgtcatgcg cggtgtcggg cttcgccctc tccaaccacg gaatgtcctg ggtccgccgg
180
gcccctggga aaggacttga atgggtgtcc ggcatcgtgt actcgggttc cacctactac
240
gcggcctcag tgaagggccg gtttactatt agccgcgaca actccagaaa cacactgtac
300
ctccaaatga actcgctgcg gccggaagat accgctatct actactgctc cgcccatggg
360
ggagagtcgg acgtctgggg acagggcacc actgtcactg tgtccagcgc ttccggcggt
420
ggtggaagcg ggggacgggc ctcaggaggc ggtggcagcg agattgtgct gacccagtcc
480
cccgggaccc tgagcctgtc cccgggagaa agggccaccc tctcctgtcg ggcatcccag
540
tccgtggggt ctactaacct tgcatggtac cagcagaagc ccggccaggc ccctcgcctg
600
ctgatctacg acgcgtccaa tagagccacc ggcatcccgg atcgcttcag cggaggcgga
660
tcgggcaccg acttcaccct caccatttca aggctggaac cggaggactt cgccgtgtac
720
tactgccagc agtatggttc gtccccaccc tggacgttcg gccaggggac taaggtcgag
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 809
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 809
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Glu Ser Gly Asp Gly Met Asp Val Trp
115 120 125
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
145 150 155 160
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
165 170 175
Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser
195 200 205
Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr
225 230 235 240
Tyr Tyr Cys Gln Gln Ser Tyr Thr Leu Ala Phe Gly Gln Gly Thr Lys
245 250 255
Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 810
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 810
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtgga atctggtgga ggactcgtga aacctggagg atcattgaga
120
ctgtcatgcg cggcctcggg attcacgttc tccgattact acatgagctg gattcgccag
180
gctccgggga agggactgga atgggtgtcc tacatttcct catccggctc caccatctac
240
tacgcggact ccgtgaaggg gagattcacc attagccgcg ataacgccaa gaacagcctg
300
taccttcaga tgaactccct gcgggctgaa gatactgccg tctactactg cgcaagggag
360
agcggagatg ggatggacgt ctggggacag ggtaccactg tgaccgtgtc gtcggcctcc
420
ggcggagggg gttcgggtgg aagggccagc ggcggcggag gcagcgacat ccagatgacc
480
cagtccccct catcgctgtc cgcctccgtg ggcgaccgcg tcaccatcac atgccgggcc
540
tcacagtcga tctcctccta cctcaattgg tatcagcaga agcccggaaa ggcccctaag
600
cttctgatct acgcagcgtc ctccctgcaa tccggggtcc catctcggtt ctccggctcg
660
ggcagcggta ccgacttcac tctgaccatc tcgagcctgc agccggagga cttcgccact
720
tactactgtc agcaaagcta caccctcgcg tttggccagg gcaccaaagt ggacatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 811
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 811
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ser Thr Met Val Arg Glu Asp Tyr Trp
115 120 125
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Leu Gly Gln Pro Ala Ser Ile
165 170 175
Ser Cys Lys Ser Ser Glu Ser Leu Val His Asn Ser Gly Lys Thr Tyr
180 185 190
Leu Asn Trp Phe His Gln Arg Pro Gly Gln Ser Pro Arg Arg Leu Ile
195 200 205
Tyr Glu Val Ser Asn Arg Asp Ser Gly Val Pro Asp Arg Phe Thr Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Gly Thr His Trp Pro Gly
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 812
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 812
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactggtgca aagcggagga ggattggtca aacccggagg aagcctgaga
120
ctgtcatgcg cggcctctgg attcaccttc tccgattact acatgtcatg gatcagacag
180
gccccgggga agggcctcga atgggtgtcc tacatctcgt cctccgggaa caccatctac
240
tacgccgaca gcgtgaaggg ccgctttacc atttcccgcg acaacgcaaa gaactcgctg
300
taccttcaga tgaattccct gcgggctgaa gataccgcgg tgtactattg cgcccggtcc
360
actatggtcc gggaggacta ctggggacag ggcacactcg tgaccgtgtc cagcgcgagc
420
gggggtggag gcagcggtgg acgcgcctcc ggcggcggcg gttcagacat cgtgctgact
480
cagtcgcccc tgtcgctgcc ggtcaccctg ggccaaccgg cctcaattag ctgcaagtcc
540
tcggagagcc tggtgcacaa ctcaggaaag acttacctga actggttcca tcagcggcct
600
ggacagtccc cacggaggct catctatgaa gtgtccaaca gggattcggg ggtgcccgac
660
cgcttcactg gctccgggtc cggcaccgac ttcaccttga aaatctccag agtggaagcc
720
gaggacgtgg gcgtgtacta ctgtatgcag ggtacccact ggcctggaac ctttggacaa
780
ggaactaagc tcgagattaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 813
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 813
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Arg Leu Thr Gln Ser
145 150 155 160
Pro Ser Pro Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Gln Ala Ser Glu Asp Ile Asn Lys Phe Leu Asn Trp Tyr His Gln Thr
180 185 190
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Ser Thr Leu Gln
195 200 205
Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Asn Ser Leu Gln Pro Glu Asp Ile Gly Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Glu Ser Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys
245 250 255
Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 814
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 814
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc aactcgtgga atctggtgga ggactcgtgc aacccggtgg aagccttagg
120
ctgtcgtgcg ccgtcagcgg gtttgctctg agcaaccatg gaatgtcctg ggtccgccgg
180
gcaccgggaa aagggctgga atgggtgtcc ggcatcgtgt acagcgggtc aacctattac
240
gccgcgtccg tgaagggcag attcactatc tcaagagaca acagccggaa caccctgtac
300
ttgcaaatga attccctgcg ccccgaggac accgccatct actactgctc cgcccacgga
360
ggagagtcgg acgtgtgggg ccagggaacg actgtgactg tgtccagcgc atcaggaggg
420
ggtggttcgg gcggccgggc ctcgggggga ggaggttccg acattcggct gacccagtcc
480
ccgtccccac tgtcggcctc cgtcggcgac cgcgtgacca tcacttgtca ggcgtccgag
540
gacattaaca agttcctgaa ctggtaccac cagacccctg gaaaggcccc caagctgctg
600
atctacgatg cctcgaccct tcaaactgga gtgcctagcc ggttctccgg gtccggctcc
660
ggcactgatt tcactctgac catcaactca ttgcagccgg aagatatcgg gacctactat
720
tgccagcagt acgaatccct cccgctcaca ttcggcgggg gaaccaaggt cgagattaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 815
<211> 484
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 815
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Thr Thr Leu Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Val Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Gly Ser Asn Leu Ala Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Gln Gly Pro Arg Leu Leu Ile Tyr Gly Ala Ser Thr Arg Ala
195 200 205
Thr Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Glu Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Tyr
225 230 235 240
Cys Gln Gln Tyr Asn Asp Trp Leu Pro Val Thr Phe Gly Gln Gly Thr
245 250 255
Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
260 265 270
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
275 280 285
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
290 295 300
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
305 310 315 320
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 816
<211> 1452
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 816
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga aactggagga ggacttgtgc aacctggagg atcattgcgg
120
ctctcatgcg ctgtctccgg cttcgccctg tcaaatcacg ggatgtcgtg ggtcagacgg
180
gccccgggaa agggtctgga atgggtgtcg gggattgtgt acagcggctc cacctactac
240
gccgcttcgg tcaagggccg cttcactatt tcacgggaca acagccgcaa caccctctat
300
ctgcaaatga actctctccg cccggaggat accgccatct actactgctc cgcacacggc
360
ggcgaatccg acgtgtgggg acagggaacc actgtcaccg tgtcgtccgc atccggtggc
420
ggaggatcgg gtggccgggc ctccgggggc ggcggcagcg agactaccct gacccagtcc
480
cctgccactc tgtccgtgag cccgggagag agagccaccc ttagctgccg ggccagccag
540
agcgtgggct ccaacctggc ctggtaccag cagaagccag gacagggtcc caggctgctg
600
atctacggag cctccactcg cgcgaccggc atccccgcga ggttctccgg gtcgggttcc
660
gggaccgagt tcaccctgac catctcctcc ctccaaccgg aggacttcgc ggtgtactac
720
tgtcagcagt acaacgattg gctgcccgtg acatttggac aggggacgaa ggtggaaatc
780
aaaaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
840
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
900
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
960
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1020
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1080
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1140
gatgctccag cctacaagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1200
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
1260
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
1320
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
1380
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
1440
ctgccgcctc gg
1452
<210> 817
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 817
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Phe
35 40 45
Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr
65 70 75 80
Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg
85 90 95
Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala
100 105 110
Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val Trp Gly Gln
115 120 125
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Arg Ala Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Ile Gly Ser Ser Ser Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Met Tyr Gly Ala Ser Ser Arg
195 200 205
Ala Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Ala Gly Ser Pro Pro Phe Thr Phe Gly Gln Gly
245 250 255
Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 818
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 818
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aattggtgga atctggtgga ggacttgtgc aacctggagg atcactgaga
120
ctgtcatgcg cggtgtccgg ttttgccctg agcaatcatg ggatgtcgtg ggtccggcgc
180
gcccccggaa agggtctgga atgggtgtcg ggtatcgtct actccgggag cacttactac
240
gccgcgagcg tgaagggccg cttcaccatt tcccgcgata actcccgcaa caccctgtac
300
ttgcaaatga actcgctccg gcctgaggac actgccatct actactgctc cgcacacgga
360
ggagaatccg acgtgtgggg ccagggaact accgtgaccg tcagcagcgc ctccggcggc
420
gggggctcag gcggacgggc tagcggcggc ggtggctccg agatcgtgct gacccagtcg
480
cctggcactc tctcgctgag ccccggggaa agggcaaccc tgtcctgtcg ggccagccag
540
tccattggat catcctccct cgcctggtat cagcagaaac cgggacaggc tccgcggctg
600
cttatgtatg gggccagctc aagagcctcc ggcattcccg accggttctc cgggtccggt
660
tccggcaccg atttcaccct gactatctcg aggctggagc cagaggactt cgccgtgtac
720
tactgccagc agtacgcggg gtccccgccg ttcacgttcg gacagggaac caaggtcgag
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 819
<211> 487
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 819
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Tyr Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Ala
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg His Trp Gln Glu Trp Pro Asp Ala
115 120 125
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Thr Thr
145 150 155 160
Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly Asp Lys Val
165 170 175
Ile Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Ala Met Asn Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Glu Ala Pro Leu Phe Ile Ile Gln Ser Ala
195 200 205
Thr Ser Pro Val Pro Gly Ile Pro Pro Arg Phe Ser Gly Ser Gly Phe
210 215 220
Gly Thr Asp Phe Ser Leu Thr Ile Asn Asn Ile Glu Ser Glu Asp Ala
225 230 235 240
Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Leu Thr Phe Gly
245 250 255
Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
325 330 335
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
340 345 350
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
355 360 365
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
370 375 380
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
385 390 395 400
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
405 410 415
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
420 425 430
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
435 440 445
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
450 455 460
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
465 470 475 480
Met Gln Ala Leu Pro Pro Arg
485
<210> 820
<211> 1461
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 820
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agcttcagga aagcggaccg ggcctggtca agccatccga aactctctcc
120
ctgacttgca ctgtgtctgg cggttccatc tcatcgtcgt actactactg gggctggatt
180
aggcagccgc ccggaaaggg actggagtgg atcggaagca tctactattc cggctcggcg
240
tactacaacc ctagcctcaa gtcgagagtg accatctccg tggatacctc caagaaccag
300
ttttccctgc gcctgagctc cgtgaccgcc gctgacaccg ccgtgtacta ctgtgctcgg
360
cattggcagg aatggcccga tgccttcgac atttggggcc agggcactat ggtcactgtg
420
tcatccgggg gtggaggcag cgggggagga gggtccgggg ggggaggttc agagacaacc
480
ttgacccagt cacccgcatt catgtccgcc actccgggag acaaggtcat catctcgtgc
540
aaagcgtccc aggatatcga cgatgccatg aattggtacc agcagaagcc tggcgaagcg
600
ccgctgttca ttatccaatc cgcaacctcg cccgtgcctg gaatcccacc gcggttcagc
660
ggcagcggtt tcggaaccga cttttccctg accattaaca acattgagtc cgaggacgcc
720
gcctactact tctgcctgca acacgacaac ttccctctca cgttcggcca gggaaccaag
780
ctggaaatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
840
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
900
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
960
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1020
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1080
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1140
cgcagcgcag atgctccagc ctacaagcag gggcagaacc agctctacaa cgaactcaat
1200
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
1260
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
1320
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
1380
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
1440
atgcaggccc tgccgcctcg g
1461
<210> 821
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 821
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Asn Leu Arg Glu Ser Gly Pro Ala Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Arg Thr Ser Gly Met Cys Val Ser Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Arg Ile Asp Trp Asp Glu Asp Lys
65 70 75 80
Phe Tyr Ser Thr Ser Leu Lys Thr Arg Leu Thr Ile Ser Lys Asp Thr
85 90 95
Ser Asp Asn Gln Val Val Leu Arg Met Thr Asn Met Asp Pro Ala Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Ala Arg Ser Gly Ala Gly Gly Thr Ser Ala
115 120 125
Thr Ala Phe Asp Ile Trp Gly Pro Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Tyr Asn Asn Leu
180 185 190
Ala Trp Phe Gln Leu Lys Pro Gly Ser Ala Pro Arg Ser Leu Met Tyr
195 200 205
Ala Ala Asn Lys Ser Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Ala Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Phe Ala Thr Tyr Tyr Cys Gln His Tyr Tyr Arg Phe Pro Tyr Ser
245 250 255
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 822
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 822
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtca atctgcgcga atccggcccc gccttggtca agcctaccca gaccctcact
120
ctgacctgta ctttctccgg cttctccctg cggacttccg ggatgtgcgt gtcctggatc
180
agacagcctc cgggaaaggc cctggagtgg ctcgctcgca ttgactggga tgaggacaag
240
ttctactcca cctcactcaa gaccaggctg accatcagca aagatacctc tgacaaccaa
300
gtggtgctcc gcatgaccaa catggaccca gccgacactg ccacttacta ctgcgcgagg
360
agcggagcgg gcggaacctc cgccaccgcc ttcgatattt ggggcccggg taccatggtc
420
accgtgtcaa gcggaggagg ggggtccggg ggcggcggtt ccgggggagg cggatcggac
480
attcagatga ctcagtcacc atcgtccctg agcgctagcg tgggcgacag agtgacaatc
540
acttgccggg catcccagga catctataac aaccttgcgt ggttccagct gaagcctggt
600
tccgcaccgc ggtcacttat gtacgccgcc aacaagagcc agtcgggagt gccgtcccgg
660
ttttccggtt cggcctcggg aactgacttc accctgacga tctccagcct gcaacccgag
720
gatttcgcca cctactactg ccagcactac taccgctttc cctactcgtt cggacaggga
780
accaagctgg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
840
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
900
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
960
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1020
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1080
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1140
ttcagccgca gcgcagatgc tccagcctac aagcaggggc agaaccagct ctacaacgaa
1200
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
1260
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
1320
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
1380
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
1440
cttcacatgc aggccctgcc gcctcgg
1467
<210> 823
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 823
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ser Ile Ser Ser Ser Ser Ser Tyr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Thr Ile Ala Ala Val Tyr Ala Phe Asp
115 120 125
Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr
145 150 155 160
Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Glu Glu Pro Ala Ser Ile
165 170 175
Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
180 185 190
Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile
195 200 205
Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
225 230 235 240
Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 824
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 824
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agcttgtcga atccgggggg ggactggtca agccgggcgg atcactgaga
120
ctgtcctgcg ccgcgagcgg cttcacgttc tcctcctact ccatgaactg ggtccgccaa
180
gcccccggga agggactgga atgggtgtcc tctatctcct cgtcgtcgtc ctacatctac
240
tacgccgact ccgtgaaggg aagattcacc atttcccgcg acaacgcaaa gaactcactg
300
tacttgcaaa tgaactcact ccgggccgaa gatactgctg tgtactattg cgccaagact
360
attgccgccg tctacgcttt cgacatctgg ggccagggaa ccaccgtgac tgtgtcgtcc
420
ggtggtggtg gctcgggcgg aggaggaagc ggcggcgggg ggtccgagat tgtgctgacc
480
cagtcgccac tgagcctccc tgtgaccccc gaggaacccg ccagcatcag ctgccggtcc
540
agccagtccc tgctccactc caacggatac aattacctcg attggtacct tcagaagcct
600
ggacaaagcc cgcagctgct catctacttg ggatcaaacc gcgcgtcagg agtgcctgac
660
cggttctccg gctcgggcag cggtaccgat ttcaccctga aaatctccag ggtggaggca
720
gaggacgtgg gagtgtatta ctgtatgcag gcgctgcaga ctccgtacac atttgggcag
780
ggcaccaagc tggagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 825
<211> 484
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 825
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asp Tyr Tyr Met Ser Trp Ile Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Leu Arg Gly Ala Phe Asp Ile Trp
115 120 125
Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Ser
145 150 155 160
Pro Ser Val Ser Ala Ala Pro Gly Tyr Thr Ala Thr Ile Ser Cys Gly
165 170 175
Gly Asn Asn Ile Gly Thr Lys Ser Val His Trp Tyr Gln Gln Lys Pro
180 185 190
Gly Gln Ala Pro Leu Leu Val Ile Arg Asp Asp Ser Val Arg Pro Ser
195 200 205
Lys Ile Pro Gly Arg Phe Ser Gly Ser Asn Ser Gly Asn Met Ala Thr
210 215 220
Leu Thr Ile Ser Gly Val Gln Ala Gly Asp Glu Ala Asp Phe Tyr Cys
225 230 235 240
Gln Val Trp Asp Ser Asp Ser Glu His Val Val Phe Gly Gly Gly Thr
245 250 255
Lys Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
260 265 270
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
275 280 285
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
290 295 300
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
305 310 315 320
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
325 330 335
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
340 345 350
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
355 360 365
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
370 375 380
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
385 390 395 400
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
405 410 415
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
420 425 430
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
435 440 445
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
450 455 460
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
465 470 475 480
Leu Pro Pro Arg
<210> 826
<211> 1452
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 826
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtcc agctcgtgga gtccggcgga ggccttgtga agcctggagg ttcgctgaga
120
ctgtcctgcg ccgcctccgg cttcaccttc tccgactact acatgtcctg gatcagacag
180
gccccgggaa agggcctgga atgggtgtcc tacatctcgt catcgggcag cactatctac
240
tacgcggact cagtgaaggg gcggttcacc atttcccggg ataacgcgaa gaactcgctg
300
tatctgcaaa tgaactcact gagggccgag gacaccgccg tgtactactg cgcccgcgat
360
ctccgcgggg catttgacat ctggggacag ggaaccatgg tcacagtgtc cagcggaggg
420
ggaggatcgg gtggcggagg ttccgggggt ggaggctcct cctacgtgct gactcagagc
480
ccaagcgtca gcgctgcgcc cggttacacg gcaaccatct cctgtggcgg aaacaacatt
540
gggaccaagt ctgtgcactg gtatcagcag aagccgggcc aagctcccct gttggtgatc
600
cgcgatgact ccgtgcggcc tagcaaaatt ccgggacggt tctccggctc caacagcggc
660
aatatggcca ctctcaccat ctcgggagtg caggccggag atgaagccga cttctactgc
720
caagtctggg actcagactc cgagcatgtg gtgttcgggg gcggaaccaa gctgactgtg
780
ctcaccacta ccccagcacc gaggccaccc accccggctc ctaccatcgc ctcccagcct
840
ctgtccctgc gtccggaggc atgtagaccc gcagctggtg gggccgtgca tacccggggt
900
cttgacttcg cctgcgatat ctacatttgg gcccctctgg ctggtacttg cggggtcctg
960
ctgctttcac tcgtgatcac tctttactgt aagcgcggtc ggaagaagct gctgtacatc
1020
tttaagcaac ccttcatgag gcctgtgcag actactcaag aggaggacgg ctgttcatgc
1080
cggttcccag aggaggagga aggcggctgc gaactgcgcg tgaaattcag ccgcagcgca
1140
gatgctccag cctacaagca ggggcagaac cagctctaca acgaactcaa tcttggtcgg
1200
agagaggagt acgacgtgct ggacaagcgg agaggacggg acccagaaat gggcgggaag
1260
ccgcgcagaa agaatcccca agagggcctg tacaacgagc tccaaaagga taagatggca
1320
gaagcctata gcgagattgg tatgaaaggg gaacgcagaa gaggcaaagg ccacgacgga
1380
ctgtaccagg gactcagcac cgccaccaag gacacctatg acgctcttca catgcaggcc
1440
ctgccgcctc gg
1452
<210> 827
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 827
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Pro Ser Gly Tyr
35 40 45
Thr Val Thr Ser His Tyr Ile His Trp Val Arg Arg Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Met Ile Asn Pro Ser Gly Gly Val Thr Ala
65 70 75 80
Tyr Ser Gln Thr Leu Gln Gly Arg Val Thr Met Thr Ser Asp Thr Ser
85 90 95
Ser Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Met Tyr Tyr Cys Ala Arg Glu Gly Ser Gly Ser Gly Trp Tyr Phe
115 120 125
Asp Phe Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Tyr Val Leu
145 150 155 160
Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln Thr Ala Ser Ile
165 170 175
Thr Cys Ser Gly Asp Gly Leu Ser Lys Lys Tyr Val Ser Trp Tyr Gln
180 185 190
Gln Lys Ala Gly Gln Ser Pro Val Val Leu Ile Ser Arg Asp Lys Glu
195 200 205
Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Gly Ser Asn Ser Ala Asp
210 215 220
Thr Ala Thr Leu Thr Ile Ser Gly Thr Gln Ala Met Asp Glu Ala Asp
225 230 235 240
Tyr Tyr Cys Gln Ala Trp Asp Asp Thr Thr Val Val Phe Gly Gly Gly
245 250 255
Thr Lys Leu Thr Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 828
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 828
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtgca gagcggggcc gaagtcaaga agccgggagc ctccgtgaaa
120
gtgtcctgca agccttcggg atacaccgtg acctcccact acattcattg ggtccgccgc
180
gcccccggcc aaggactcga gtggatgggc atgatcaacc ctagcggcgg agtgaccgcg
240
tacagccaga cgctgcaggg acgcgtgact atgacctcgg atacctcctc ctccaccgtc
300
tatatggaac tgtccagcct gcggtccgag gataccgcca tgtactactg cgcccgggaa
360
ggatcaggct ccgggtggta tttcgacttc tggggaagag gcaccctcgt gactgtgtca
420
tctgggggag ggggttccgg tggtggcgga tcgggaggag gcggttcatc ctacgtgctg
480
acccagccac cctccgtgtc cgtgagcccc ggccagactg catcgattac atgtagcggc
540
gacggcctct ccaagaaata cgtgtcgtgg taccagcaga aggccggaca gagcccggtg
600
gtgctgatct caagagataa ggagcggcct agcggaatcc cggacaggtt ctcgggttcc
660
aactccgcgg acactgctac tctgaccatc tcggggaccc aggctatgga cgaagccgat
720
tactactgcc aagcctggga cgacactact gtcgtgtttg gagggggcac caagttgacc
780
gtccttacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 829
<211> 489
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 829
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Gly Gly Tyr Tyr Trp Ser Trp Ile Arg Gln His Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Tyr Ile Tyr Tyr Ser Gly Ser Thr
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Ala Gly Ile Ala Ala Arg Leu Arg
115 120 125
Gly Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Val Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp
165 170 175
Arg Val Ile Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Trp Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile Tyr
195 200 205
Ala Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Ala Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
225 230 235 240
Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Phe Thr
245 250 255
Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 830
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 830
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agcttcagga gagcggcccg ggactcgtga agccgtccca gaccctgtcc
120
ctgacttgca ccgtgtcggg aggaagcatc tcgagcggag gctactattg gtcgtggatt
180
cggcagcacc ctggaaaggg cctggaatgg atcggctaca tctactactc cggctcgacc
240
tactacaacc catcgctgaa gtccagagtg acaatctcag tggacacgtc caagaatcag
300
ttcagcctga agctctcttc cgtgactgcg gccgacaccg ccgtgtacta ctgcgcacgc
360
gctggaattg ccgcccggct gaggggtgcc ttcgacattt ggggacaggg caccatggtc
420
accgtgtcct ccggcggcgg aggttccggg ggtggaggct caggaggagg ggggtccgac
480
atcgtcatga ctcagtcgcc ctcaagcgtc agcgcgtccg tcggggacag agtgatcatc
540
acctgtcggg cgtcccaggg aattcgcaac tggctggcct ggtatcagca gaagcccgga
600
aaggccccca acctgttgat ctacgccgcc tcaaacctcc aatccggggt gccgagccgc
660
ttcagcggct ccggttcggg tgccgatttc actctgacca tctcctccct gcaacctgaa
720
gatgtggcta cctactactg ccaaaagtac aactccgcac cttttacttt cggaccgggg
780
accaaagtgg acattaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
840
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
900
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
960
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1020
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1080
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1140
ttcagccgca gcgcagatgc tccagcctac aagcaggggc agaaccagct ctacaacgaa
1200
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
1260
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
1320
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
1380
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
1440
cttcacatgc aggccctgcc gcctcgg
1467
<210> 831
<211> 497
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 831
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
35 40 45
Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn
65 70 75 80
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Arg Gly Gly Tyr Gln Leu Leu Arg Trp
115 120 125
Asp Val Gly Leu Leu Arg Ser Ala Phe Asp Ile Trp Gly Gln Gly Thr
130 135 140
Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Ser Tyr Val Leu Thr Gln Pro Pro Ser Val Ser
165 170 175
Val Ala Pro Gly Gln Thr Ala Arg Ile Thr Cys Gly Gly Asn Asn Ile
180 185 190
Gly Ser Lys Ser Val His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
195 200 205
Val Leu Val Leu Tyr Gly Lys Asn Asn Arg Pro Ser Gly Val Pro Asp
210 215 220
Arg Phe Ser Gly Ser Arg Ser Gly Thr Thr Ala Ser Leu Thr Ile Thr
225 230 235 240
Gly Ala Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Ser Ser Arg Asp
245 250 255
Ser Ser Gly Asp His Leu Arg Val Phe Gly Thr Gly Thr Lys Val Thr
260 265 270
Val Leu Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
275 280 285
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
290 295 300
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
305 310 315 320
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
325 330 335
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
340 345 350
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
355 360 365
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
370 375 380
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
385 390 395 400
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
405 410 415
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
420 425 430
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
435 440 445
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
450 455 460
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
465 470 475 480
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
485 490 495
Arg
<210> 832
<211> 1491
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 832
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctggtcca gtcgggcgcc gaggtcaaga agcccgggag ctctgtgaaa
120
gtgtcctgca aggcctccgg gggcaccttt agctcctacg ccatctcctg ggtccgccaa
180
gcaccgggtc aaggcctgga gtggatgggg ggaattatcc ctatcttcgg cactgccaac
240
tacgcccaga agttccaggg acgcgtgacc attaccgcgg acgaatccac ctccaccgct
300
tatatggagc tgtccagctt gcgctcggaa gataccgccg tgtactactg cgcccggagg
360
ggtggatacc agctgctgag atgggacgtg ggcctcctgc ggtcggcgtt cgacatctgg
420
ggccagggca ctatggtcac tgtgtccagc ggaggaggcg gatcgggagg cggcggatca
480
gggggaggcg gttccagcta cgtgcttact caaccccctt cggtgtccgt ggccccggga
540
cagaccgcca gaatcacttg cggaggaaac aacattgggt ccaagagcgt gcattggtac
600
cagcagaagc caggacaggc ccctgtgctg gtgctctacg ggaagaacaa tcggcccagc
660
ggagtgccgg acaggttctc gggttcacgc tccggtacaa ccgcttcact gactatcacc
720
ggggcccagg cagaggatga agcggactac tactgttcct cccgggattc atccggcgac
780
cacctccggg tgttcggaac cggaacgaag gtcaccgtgc tgaccactac cccagcaccg
840
aggccaccca ccccggctcc taccatcgcc tcccagcctc tgtccctgcg tccggaggca
900
tgtagacccg cagctggtgg ggccgtgcat acccggggtc ttgacttcgc ctgcgatatc
960
tacatttggg cccctctggc tggtacttgc ggggtcctgc tgctttcact cgtgatcact
1020
ctttactgta agcgcggtcg gaagaagctg ctgtacatct ttaagcaacc cttcatgagg
1080
cctgtgcaga ctactcaaga ggaggacggc tgttcatgcc ggttcccaga ggaggaggaa
1140
ggcggctgcg aactgcgcgt gaaattcagc cgcagcgcag atgctccagc ctacaagcag
1200
gggcagaacc agctctacaa cgaactcaat cttggtcgga gagaggagta cgacgtgctg
1260
gacaagcgga gaggacggga cccagaaatg ggcgggaagc cgcgcagaaa gaatccccaa
1320
gagggcctgt acaacgagct ccaaaaggat aagatggcag aagcctatag cgagattggt
1380
atgaaagggg aacgcagaag aggcaaaggc cacgacggac tgtaccaggg actcagcacc
1440
gccaccaagg acacctatga cgctcttcac atgcaggccc tgccgcctcg g
1491
<210> 833
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 833
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Gln Gln Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp
35 40 45
Ser Val Ser Ser Asn Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro
50 55 60
Ser Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp
65 70 75 80
Tyr Ser Phe Tyr Ala Ile Ser Leu Lys Ser Arg Ile Ile Ile Asn Pro
85 90 95
Asp Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Lys Ser Val Thr Pro
100 105 110
Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Ser Pro Glu Gly Leu
115 120 125
Phe Leu Tyr Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Val
130 135 140
Ser Ser Gly Gly Asp Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Ser Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu Gly
165 170 175
Gln Thr Ile Arg Ile Thr Cys Gln Gly Asp Ser Leu Gly Asn Tyr Tyr
180 185 190
Ala Thr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val Ile
195 200 205
Tyr Gly Thr Asn Asn Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser Ala
210 215 220
Ser Ser Ser Gly Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln Ala
225 230 235 240
Glu Asp Glu Ala Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Ser Gly His
245 250 255
His Leu Leu Phe Gly Thr Gly Thr Lys Val Thr Val Leu Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 834
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 834
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctccaaca gtcaggaccg gggctcgtga agccatccca gaccctgtcc
120
ctgacttgtg ccatctcggg agatagcgtg tcatcgaact ccgccgcctg gaactggatt
180
cggcagagcc cgtcccgcgg actggagtgg cttggaagga cctactaccg gtccaagtgg
240
tactctttct acgcgatctc gctgaagtcc cgcattatca ttaaccctga tacctccaag
300
aatcagttct ccctccaact gaaatccgtc acccccgagg acacagcagt gtattactgc
360
gcacggagca gccccgaagg actgttcctg tattggtttg acccctgggg ccaggggact
420
cttgtgaccg tgtcgagcgg cggagatggg tccggtggcg gtggttcggg gggcggcgga
480
tcatcatccg aactgaccca ggacccggct gtgtccgtgg cgctgggaca aaccatccgc
540
attacgtgcc agggagactc cctgggcaac tactacgcca cttggtacca gcagaagccg
600
ggccaagccc ctgtgttggt catctacggg accaacaaca gaccttccgg catccccgac
660
cggttcagcg cttcgtcctc cggcaacact gccagcctga ccatcactgg agcgcaggcc
720
gaagatgagg ccgactacta ctgcaacagc agagactcct cgggtcatca cctcttgttc
780
ggaactggaa ccaaggtcac cgtgctgacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 835
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 835
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Val Glu Gly Ser Gly Ser Leu Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln
145 150 155 160
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
165 170 175
Cys Arg Ala Ser Gln Ser Val Ser Ser Ala Tyr Leu Ala Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Gln Pro Pro Arg Leu Leu Ile Ser Gly Ala Ser Thr
195 200 205
Arg Ala Thr Gly Ile Pro Asp Arg Phe Gly Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln His Tyr Gly Ser Ser Phe Asn Gly Ser Ser Leu Phe
245 250 255
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 836
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 836
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtgga gtcaggaggc ggcctggtcc agccgggagg gtcccttaga
120
ctgtcatgcg ccgcaagcgg attcactttc tcctcctatg ccatgagctg ggtccgccaa
180
gcccccggaa agggactgga atgggtgtcc gccatctcgg ggtctggagg ctcaacttac
240
tacgctgact ccgtgaaggg acggttcacc attagccgcg acaactccaa gaacaccctc
300
tacctccaaa tgaactccct gcgggccgag gataccgccg tctactactg cgccaaagtg
360
gaaggttcag gatcgctgga ctactgggga cagggtactc tcgtgaccgt gtcatcgggc
420
ggaggaggtt ccggcggtgg cggctccggc ggcggagggt cggagatcgt gatgacccag
480
agccctggta ctctgagcct ttcgccggga gaaagggcca ccctgtcctg ccgcgcttcc
540
caatccgtgt cctccgcgta cttggcgtgg taccagcaga agccgggaca gccccctcgg
600
ctgctgatca gcggggccag cacccgggca accggaatcc cagacagatt cgggggttcc
660
ggcagcggca cagatttcac cctgactatt tcgaggttgg agcccgagga ctttgcggtg
720
tattactgtc agcactacgg gtcgtccttt aatggctcca gcctgttcac gttcggacag
780
gggacccgcc tggaaatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 837
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 837
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile
35 40 45
Thr Phe Ser Arg Tyr Pro Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Asp Ser Gly Val Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Ala Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Phe Leu Gln Met Ser Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Thr Arg Ala Gly Ser Glu Ala Ser Asp Ile
115 120 125
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
145 150 155 160
Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
165 170 175
Cys Arg Ala Ser Gln Ser Val Ser Asn Ser Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Asp Ala Ser Ser Arg
195 200 205
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Ile Tyr
225 230 235 240
Tyr Cys Gln Gln Phe Gly Thr Ser Ser Gly Leu Thr Phe Gly Gly Gly
245 250 255
Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 838
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 838
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aactggtgga aaccggtggc ggcctggtgc agcctggagg atcattgagg
120
ctgtcatgcg cggccagcgg tattaccttc tcccggtacc ccatgtcctg ggtcagacag
180
gccccgggga aagggcttga atgggtgtcc gggatctcgg actccggtgt cagcacttac
240
tacgccgact ccgccaaggg acgcttcacc atttcccggg acaactcgaa gaacaccctg
300
ttcctccaaa tgagctccct ccgggacgag gatactgcag tgtactactg cgtgacccgc
360
gccgggtccg aggcgtctga catttgggga cagggcacta tggtcaccgt gtcgtccggc
420
ggagggggct cgggaggcgg tggcagcgga ggaggagggt ccgagatcgt gctgacccaa
480
tccccggcca ccctctcgct gagccctgga gaaagggcaa ccttgtcctg tcgcgcgagc
540
cagtccgtga gcaactccct ggcctggtac cagcagaagc ccggacaggc tccgagactt
600
ctgatctacg acgcttcgag ccgggccact ggaatccccg accgcttttc ggggtccggc
660
tcaggaaccg atttcaccct gacaatctca cggctggagc cagaggattt cgccatctat
720
tactgccagc agttcggtac ttcctccggc ctgactttcg gaggcggcac gaagctcgaa
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 839
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 839
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Ile Tyr Tyr Cys Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Val Ser Leu Ser Pro Gly
165 170 175
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
180 185 190
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
225 230 235 240
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
245 250 255
Ser Trp Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 840
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 840
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctcgtgga atcgggtggc ggactggtgc agccgggggg ctcacttaga
120
ctgtcctgcg cggccagcgg attcactttc tcctcctacg ccatgtcctg ggtcagacag
180
gcccctggaa agggcctgga atgggtgtcc gcaatcagcg gcagcggcgg ctcgacctat
240
tacgcggatt cagtgaaggg cagattcacc atttcccggg acaacgccaa gaactccttg
300
taccttcaaa tgaactccct ccgcgcggaa gataccgcaa tctactactg cgctcgggcc
360
acttacaaga gggaactgcg ctactactac gggatggacg tctggggcca gggaaccatg
420
gtcaccgtgt ccagcggagg aggaggatcg ggaggaggcg gtagcggggg tggagggtcg
480
gagatcgtga tgacccagtc ccccggcact gtgtcgctgt cccccggcga acgggccacc
540
ctgtcatgtc gggccagcca gtcagtgtcg tcaagcttcc tcgcctggta ccagcagaaa
600
ccgggacaag ctccccgcct gctgatctac ggagccagca gccgggccac cggtattcct
660
gaccggttct ccggttcggg gtccgggacc gactttactc tgactatctc tcgcctcgag
720
ccagaggact ccgccgtgta ttactgccag cagtaccact cctccccgtc ctggacgttc
780
ggacagggca caaggctgga gattaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 841
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 841
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Thr Leu Lys Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Ala Thr Tyr Lys Arg Glu Leu Arg Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Ile Val Leu Thr Gln Ser Pro Ser Thr Leu Ser Leu Ser Pro Gly
165 170 175
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Thr
180 185 190
Phe Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr Gly Ser Ser Asn Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Arg Arg Leu Glu
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr His Ser Ser Pro
245 250 255
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 842
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 842
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agcttgtgga aaccggtggc ggactggtgc agcccggagg aagcctcagg
120
ctgtcctgcg ccgcgtccgg cttcaccttc tcctcgtacg ccatgtcctg ggtccgccag
180
gcccccggaa agggcctgga atgggtgtcc gccatctctg gaagcggagg ttccacgtac
240
tacgcggaca gcgtcaaggg aaggttcaca atctcccgcg ataattcgaa gaacactctg
300
taccttcaaa tgaacaccct gaaggccgag gacactgctg tgtactactg cgcacgggcc
360
acctacaaga gagagctccg gtactactac ggaatggacg tctggggcca gggaactact
420
gtgaccgtgt cctcgggagg gggtggctcc ggggggggcg gctccggcgg aggcggttcc
480
gagattgtgc tgacccagtc accttcaact ctgtcgctgt ccccgggaga gagcgctact
540
ctgagctgcc gggccagcca gtccgtgtcc accaccttcc tcgcctggta tcagcagaag
600
ccggggcagg caccacggct cttgatctac gggtcaagca acagagcgac cggaattcct
660
gaccgcttct cggggagcgg ttcaggcacc gacttcaccc tgactatccg gcgcctggaa
720
cccgaagatt tcgccgtgta ttactgtcaa cagtaccact cctcgccgtc ctggaccttt
780
ggccaaggaa ccaaagtgga aatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 843
<211> 483
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 843
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Gly Lys Ala Val Pro Asp Val Trp
115 120 125
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln Thr
145 150 155 160
Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys
165 170 175
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys
180 185 190
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln
195 200 205
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
210 215 220
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
225 230 235 240
Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Ser Phe Gly Gln Gly Thr Arg
245 250 255
Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala
260 265 270
Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg
275 280 285
Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys
290 295 300
Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
305 310 315 320
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
325 330 335
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
340 345 350
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
355 360 365
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
370 375 380
Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
385 390 395 400
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
405 410 415
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
420 425 430
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
435 440 445
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
450 455 460
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
465 470 475 480
Pro Pro Arg
<210> 844
<211> 1449
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 844
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtgga aactggaggt ggactcgtgc agcctggacg gtcgctgcgg
120
ctgagctgcg ctgcatccgg cttcaccttc gacgattatg ccatgcactg ggtcagacag
180
gcgccaggga agggacttga gtgggtgtcc ggtatcagct ggaatagcgg ctcaatcgga
240
tacgcggact ccgtgaaggg aaggttcacc atttcccgcg acaacgccaa gaactccctg
300
tacttgcaaa tgaacagcct ccgggatgag gacactgccg tgtactactg cgcccgcgtc
360
ggaaaagctg tgcccgacgt ctggggccag ggaaccactg tgaccgtgtc cagcggcggg
420
ggtggatcgg gcggtggagg gtccggtgga gggggctcag atattgtgat gacccagacc
480
ccctcgtccc tgtccgcctc ggtcggcgac cgcgtgacta tcacatgtag agcctcgcag
540
agcatctcca gctacctgaa ctggtatcag cagaagccgg ggaaggcccc gaagctcctg
600
atctacgcgg catcatcact gcaatcggga gtgccgagcc ggttttccgg gtccggctcc
660
ggcaccgact tcacgctgac catttcttcc ctgcaacccg aggacttcgc cacttactac
720
tgccagcagt cctactccac cccttactcc ttcggccaag gaaccaggct ggaaatcaag
780
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
840
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
900
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
960
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1020
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1080
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1140
gctccagcct acaagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1200
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
1260
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
1320
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
1380
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
1440
ccgcctcgg
1449
<210> 845
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 845
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe
35 40 45
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Arg Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Ser Ile Asn Trp Lys Gly Asn Ser Leu Ala
65 70 75 80
Tyr Gly Asp Ser Val Lys Gly Arg Phe Ala Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Thr Val Phe Leu Gln Met Asn Ser Leu Arg Thr Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Ser His Gln Gly Val Ala Tyr Tyr Asn Tyr
115 120 125
Ala Met Asp Val Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Leu Ser Cys Arg Ala Thr Gln Ser Ile Gly Ser Ser Phe Leu
180 185 190
Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Gln Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Arg
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Val Glu Pro Glu
225 230 235 240
Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Glu Ser Ser Pro Ser Trp
245 250 255
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 846
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 846
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctcgtgga gagcggggga ggattggtgc agcccggaag gtccctgcgg
120
ctctcctgca ctgcgtctgg cttcaccttc gacgactacg cgatgcactg ggtcagacag
180
cgcccgggaa agggcctgga atgggtcgcc tcaatcaact ggaagggaaa ctccctggcc
240
tatggcgaca gcgtgaaggg ccgcttcgcc atttcgcgcg acaacgccaa gaacaccgtg
300
tttctgcaaa tgaattccct gcggaccgag gataccgctg tgtactactg cgccagccac
360
cagggcgtgg catactataa ctacgccatg gacgtgtggg gaagagggac gctcgtcacc
420
gtgtcctccg ggggcggtgg atcgggtgga ggaggaagcg gtggcggggg cagcgaaatc
480
gtgctgactc agagcccggg aactctttca ctgtccccgg gagaacgggc cactctctcg
540
tgccgggcca cccagtccat cggctcctcc ttccttgcct ggtaccagca gaggccagga
600
caggcgcccc gcctgctgat ctacggtgct tcccaacgcg ccactggcat tcctgaccgg
660
ttcagcggca gagggtcggg aaccgatttc acactgacca tttcccgggt ggagcccgaa
720
gattcggcag tctactactg tcagcattac gagtcctccc cttcatggac cttcggtcaa
780
gggaccaaag tggagatcaa gaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 847
<211> 485
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 847
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Val Val Arg Asp Gly Met Asp Val Trp
115 120 125
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
165 170 175
Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln Gln
180 185 190
Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg
195 200 205
Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Asn Gly Ser Gly Thr Asp
210 215 220
Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr
225 230 235 240
Tyr Cys Gln Gln Tyr Gly Ser Pro Pro Arg Phe Thr Phe Gly Pro Gly
245 250 255
Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
260 265 270
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
275 280 285
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
290 295 300
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
305 310 315 320
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 848
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 848
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaggtgc agttggtcga aagcgggggc gggcttgtgc agcctggcgg atcactgcgg
120
ctgtcctgcg cggcatcagg cttcacgttt tcttcctacg ccatgtcctg ggtgcgccag
180
gcccctggaa agggactgga atgggtgtcc gcgatttcgg ggtccggcgg gagcacctac
240
tacgccgatt ccgtgaaggg ccgcttcact atctcgcggg acaactccaa gaacaccctc
300
tacctccaaa tgaatagcct gcgggccgag gataccgccg tctactattg cgctaaggtc
360
gtgcgcgacg gaatggacgt gtggggacag ggtaccaccg tgacagtgtc ctcgggggga
420
ggcggtagcg gcggaggagg aagcggtggt ggaggttccg agattgtgct gactcaatca
480
cccgcgaccc tgagcctgtc ccccggcgaa agggccactc tgtcctgtcg ggccagccaa
540
tcagtctcct cctcgtacct ggcctggtac cagcagaagc caggacaggc tccgagactc
600
cttatctatg gcgcatcctc ccgcgccacc ggaatcccgg ataggttctc gggaaacgga
660
tcggggaccg acttcactct caccatctcc cggctggaac cggaggactt cgccgtgtac
720
tactgccagc agtacggcag cccgcctaga ttcactttcg gccccggcac caaagtggac
780
atcaagacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
840
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
900
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
960
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1020
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1080
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1140
gcagatgctc cagcctacaa gcaggggcag aaccagctct acaacgaact caatcttggt
1200
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
1260
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
1320
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
1380
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
1440
gccctgccgc ctcgg
1455
<210> 849
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 849
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Ile Pro Gln Thr Gly Thr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
145 150 155 160
Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser
165 170 175
Cys Arg Ala Ser Gln Ser Val Ser Ser Ser Tyr Leu Ala Trp Tyr Gln
180 185 190
Gln Arg Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ser
195 200 205
Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu Asp Phe Ala Val
225 230 235 240
Tyr Tyr Cys Gln His Tyr Gly Ser Ser Pro Ser Trp Thr Phe Gly Gln
245 250 255
Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 850
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 850
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctgctgga gtccggcggt ggattggtgc aaccgggggg atcgctcaga
120
ctgtcctgtg cggcgtcagg cttcaccttc tcgagctacg ccatgtcatg ggtcagacag
180
gcccctggaa agggtctgga atgggtgtcc gccatttccg ggagcggggg atctacatac
240
tacgccgata gcgtgaaggg ccgcttcacc atttcccggg acaactccaa gaacactctc
300
tatctgcaaa tgaactccct ccgcgctgag gacactgccg tgtactactg cgccaaaatc
360
cctcagaccg gcaccttcga ctactgggga caggggactc tggtcaccgt cagcagcggt
420
ggcggaggtt cggggggagg aggaagcggc ggcggagggt ccgagattgt gctgacccag
480
tcacccggca ctttgtccct gtcgcctgga gaaagggcca ccctttcctg ccgggcatcc
540
caatccgtgt cctcctcgta cctggcctgg taccagcaga ggcccggaca ggccccacgg
600
cttctgatct acggagcaag cagccgcgcg accggtatcc cggaccggtt ttcgggctcg
660
ggctcaggaa ctgacttcac cctcaccatc tcccgcctgg aacccgaaga tttcgctgtg
720
tattactgcc agcactacgg cagctccccg tcctggacgt tcggccaggg aactcggctg
780
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 851
<211> 492
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 851
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Met Ser Arg Glu Asn Asp
85 90 95
Lys Asn Ser Val Phe Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr
100 105 110
Gly Val Tyr Tyr Cys Ala Arg Ala Asn Tyr Lys Arg Glu Leu Arg Tyr
115 120 125
Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Glu Ile Val Met Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
165 170 175
Glu Ser Ala Thr Leu Ser Cys Arg Ala Ser Gln Arg Val Ala Ser Asn
180 185 190
Tyr Leu Ala Trp Tyr Gln His Lys Pro Gly Gln Ala Pro Ser Leu Leu
195 200 205
Ile Ser Gly Ala Ser Ser Arg Ala Thr Gly Val Pro Asp Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Ala Ile Ser Arg Leu Glu
225 230 235 240
Pro Glu Asp Ser Ala Val Tyr Tyr Cys Gln His Tyr Asp Ser Ser Pro
245 250 255
Ser Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 852
<211> 1476
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 852
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc aactggtgga aaccggtgga ggactcgtgc agcctggcgg cagcctccgg
120
ctgagctgcg ccgcttcggg attcaccttt tcctcctacg cgatgtcttg ggtcagacag
180
gcccccggaa aggggctgga atgggtgtca gccatctccg gctccggcgg atcaacgtac
240
tacgccgact ccgtgaaagg ccggttcacc atgtcgcgcg agaatgacaa gaactccgtg
300
ttcctgcaaa tgaactccct gagggtggag gacaccggag tgtactattg tgcgcgcgcc
360
aactacaaga gagagctgcg gtactactac ggaatggacg tctggggaca gggaactatg
420
gtgaccgtgt catccggtgg agggggaagc ggcggtggag gcagcggggg cgggggttca
480
gaaattgtca tgacccagtc cccgggaact ctttccctct cccccgggga atccgcgact
540
ttgtcctgcc gggccagcca gcgcgtggcc tcgaactacc tcgcatggta ccagcataag
600
ccaggccaag ccccttccct gctgatttcc ggggctagca gccgcgccac tggcgtgccg
660
gataggttct cgggaagcgg ctcgggtacc gatttcaccc tggcaatctc gcggctggaa
720
ccggaggatt cggccgtgta ctactgccag cactatgact catccccctc ctggacattc
780
ggacagggca ccaaggtcga gatcaagacc actaccccag caccgaggcc acccaccccg
840
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
900
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
960
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1020
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1080
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1140
cgcgtgaaat tcagccgcag cgcagatgct ccagcctaca agcaggggca gaaccagctc
1200
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
1260
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
1320
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
1380
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
1440
tatgacgctc ttcacatgca ggccctgccg cctcgg
1476
<210> 853
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 853
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Ser Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Ala Leu Val Gly Ala Thr Gly Ala Phe
115 120 125
Asp Ile Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu
145 150 155 160
Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Ser Leu Ser Ser Asn Phe Leu Ala Trp
180 185 190
Tyr Gln Gln Lys Pro Gly Gln Ala Pro Gly Leu Leu Ile Tyr Gly Ala
195 200 205
Ser Asn Trp Ala Thr Gly Thr Pro Asp Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Ile Thr Arg Leu Glu Pro Glu Asp Phe
225 230 235 240
Ala Val Tyr Tyr Cys Gln Tyr Tyr Gly Thr Ser Pro Met Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 854
<211> 1464
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 854
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctgctcga aaccggtgga gggctggtgc agccaggggg ctccctgagg
120
ctttcatgcg ccgctagcgg attctccttc tcctcttacg ccatgtcgtg ggtccgccaa
180
gcccctggaa aaggcctgga atgggtgtcc gcgatttccg ggagcggagg ttcgacctat
240
tacgccgact ccgtgaaggg ccgctttacc atctcccggg ataactccaa gaacactctg
300
tacctccaaa tgaactcgct gagagccgag gacaccgccg tgtattactg cgcgaaggcg
360
ctggtcggcg cgactggggc attcgacatc tggggacagg gaactcttgt gaccgtgtcg
420
agcggaggcg gcggctccgg cggaggaggg agcgggggcg gtggttccga aatcgtgttg
480
actcagtccc cgggaaccct gagcttgtca cccggggagc gggccactct ctcctgtcgc
540
gcctcccaat cgctctcatc caatttcctg gcctggtacc agcagaagcc cggacaggcc
600
ccgggcctgc tcatctacgg cgcttcaaac tgggcaacgg gaacccctga tcggttcagc
660
ggaagcggat cgggtactga ctttaccctg accatcacca gactggaacc ggaggacttc
720
gccgtgtact actgccagta ctacggcacc tcccccatgt acacattcgg acagggtacc
780
aaggtcgaga ttaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
840
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
900
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
960
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1020
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1080
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1140
agccgcagcg cagatgctcc agcctacaag caggggcaga accagctcta caacgaactc
1200
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
1260
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
1320
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
1380
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
1440
cacatgcagg ccctgccgcc tcgg
1464
<210> 855
<211> 488
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 855
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Val Leu Trp Phe Gly Glu Gly Phe Asp Pro Trp
115 120 125
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser
145 150 155 160
Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys
165 170 175
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
180 185 190
Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Leu
195 200 205
Gly Ser Asn Arg Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp
225 230 235 240
Val Gly Val Tyr Tyr Cys Met Gln Ala Leu Gln Thr Pro Leu Thr Phe
245 250 255
Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg
325 330 335
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
340 345 350
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
355 360 365
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
370 375 380
Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
385 390 395 400
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
405 410 415
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
420 425 430
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
435 440 445
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
450 455 460
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
465 470 475 480
His Met Gln Ala Leu Pro Pro Arg
485
<210> 856
<211> 1464
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 856
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtgc agctgcttga gagcggtgga ggtctggtgc agcccggggg atcactgcgc
120
ctgtcctgtg ccgcgtccgg tttcactttc tcctcgtacg ccatgtcgtg ggtcagacag
180
gcaccgggaa agggactgga atgggtgtca gccatttcgg gttcgggggg cagcacctac
240
tacgctgact ccgtgaaggg ccggttcacc atttcccgcg acaactccaa gaacaccttg
300
tacctccaaa tgaactccct gcgggccgaa gataccgccg tgtattactg cgtgctgtgg
360
ttcggagagg gattcgaccc gtggggacaa ggaacactcg tgactgtgtc atccggcgga
420
ggcggcagcg gtggcggcgg ttccggcggc ggcggatctg acatcgtgtt gacccagtcc
480
cctctgagcc tgccggtcac tcctggcgaa ccagccagca tctcctgccg gtcgagccag
540
tccctcctgc actccaatgg gtacaactac ctcgattggt atctgcaaaa gccgggccag
600
agcccccagc tgctgatcta ccttgggtca aaccgcgctt ccggggtgcc tgatagattc
660
tccgggtccg ggagcggaac cgactttacc ctgaaaatct cgagggtgga ggccgaggac
720
gtcggagtgt actactgcat gcaggcgctc cagactcccc tgaccttcgg aggaggaacg
780
aaggtcgaca tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
840
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
900
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
960
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1020
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1080
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1140
agccgcagcg cagatgctcc agcctacaag caggggcaga accagctcta caacgaactc
1200
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
1260
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
1320
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
1380
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
1440
cacatgcagg ccctgccgcc tcgg
1464
<210> 857
<211> 495
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 857
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Val Gly Tyr Asp Ser Ser Gly Tyr Tyr
115 120 125
Arg Asp Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser
165 170 175
Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser
180 185 190
Ser Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg
195 200 205
Leu Leu Ile Tyr Gly Thr Ser Ser Arg Ala Thr Gly Ile Ser Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg
225 230 235 240
Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Asn
245 250 255
Ser Pro Pro Lys Phe Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 858
<211> 1485
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 858
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccaagtgc agctcgtgga gtcaggcgga ggactggtgc agcccggggg ctccctgaga
120
ctttcctgcg cggcatcggg ttttaccttc tcctcctatg ctatgtcctg ggtgcgccag
180
gccccgggaa agggactgga atgggtgtcc gcaatcagcg gtagcggggg ctcaacatac
240
tacgccgact ccgtcaaggg tcgcttcact atttcccggg acaactccaa gaataccctg
300
tacctccaaa tgaacagcct cagggccgag gatactgccg tgtactactg cgccaaagtc
360
ggatacgata gctccggtta ctaccgggac tactacggaa tggacgtgtg gggacagggc
420
accaccgtga ccgtgtcaag cggcggaggc ggttcaggag ggggaggctc cggcggtgga
480
gggtccgaaa tcgtcctgac tcagtcgcct ggcactctgt cgttgtcccc gggggagcgc
540
gctaccctgt cgtgtcgggc gtcgcagtcc gtgtcgagct cctacctcgc gtggtaccag
600
cagaagcccg gacaggcccc tagacttctg atctacggca cttcttcacg cgccaccggg
660
atcagcgaca ggttcagcgg ctccggctcc gggaccgact tcaccctgac cattagccgg
720
ctggagcctg aagatttcgc cgtgtattac tgccaacact acggaaactc gccgccaaag
780
ttcacgttcg gacccggaac caagctggaa atcaagacca ctaccccagc accgaggcca
840
cccaccccgg ctcctaccat cgcctcccag cctctgtccc tgcgtccgga ggcatgtaga
900
cccgcagctg gtggggccgt gcatacccgg ggtcttgact tcgcctgcga tatctacatt
960
tgggcccctc tggctggtac ttgcggggtc ctgctgcttt cactcgtgat cactctttac
1020
tgtaagcgcg gtcggaagaa gctgctgtac atctttaagc aacccttcat gaggcctgtg
1080
cagactactc aagaggagga cggctgttca tgccggttcc cagaggagga ggaaggcggc
1140
tgcgaactgc gcgtgaaatt cagccgcagc gcagatgctc cagcctacaa gcaggggcag
1200
aaccagctct acaacgaact caatcttggt cggagagagg agtacgacgt gctggacaag
1260
cggagaggac gggacccaga aatgggcggg aagccgcgca gaaagaatcc ccaagagggc
1320
ctgtacaacg agctccaaaa ggataagatg gcagaagcct atagcgagat tggtatgaaa
1380
ggggaacgca gaagaggcaa aggccacgac ggactgtacc agggactcag caccgccacc
1440
aaggacacct atgacgctct tcacatgcag gccctgccgc ctcgg
1485
<210> 859
<211> 490
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 859
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Lys Met Gly Trp Ser Ser Gly Tyr Leu Gly
115 120 125
Ala Phe Asp Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Arg
165 170 175
Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ala Ser Ser Phe Leu
180 185 190
Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
195 200 205
Gly Ala Ser Gly Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser Gly Ser
210 215 220
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro Glu
225 230 235 240
Asp Phe Ala Val Tyr Tyr Cys Gln His Tyr Gly Gly Ser Pro Arg Leu
245 250 255
Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 860
<211> 1470
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 860
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaagtcc aactggtgga gtccggggga gggctcgtgc agcccggagg cagccttcgg
120
ctgtcgtgcg ccgcctccgg gttcacgttc tcatcctacg cgatgtcgtg ggtcagacag
180
gcaccaggaa agggactgga atgggtgtcc gccattagcg gctccggcgg tagcacctac
240
tatgccgact cagtgaaggg aaggttcact atctcccgcg acaacagcaa gaacaccctg
300
tacctccaaa tgaactctct gcgggccgag gataccgcgg tgtactattg cgccaagatg
360
ggttggtcca gcggatactt gggagccttc gacatttggg gacagggcac tactgtgacc
420
gtgtcctccg ggggtggcgg atcgggaggc ggcggctcgg gtggaggggg ttccgaaatc
480
gtgttgaccc agtcaccggg aaccctctcg ctgtccccgg gagaacgggc tacactgtca
540
tgtagagcgt cccagtccgt ggcttcctcg ttcctggcct ggtaccagca gaagccggga
600
caggcacccc gcctgctcat ctacggagcc agcggccggg cgaccggcat ccctgaccgc
660
ttctccggtt ccggctcggg caccgacttt actctgacca ttagcaggct tgagcccgag
720
gattttgccg tgtactactg ccaacactac ggggggagcc ctcgcctgac cttcggaggc
780
ggaactaagg tcgatatcaa aaccactacc ccagcaccga ggccacccac cccggctcct
840
accatcgcct cccagcctct gtccctgcgt ccggaggcat gtagacccgc agctggtggg
900
gccgtgcata cccggggtct tgacttcgcc tgcgatatct acatttgggc ccctctggct
960
ggtacttgcg gggtcctgct gctttcactc gtgatcactc tttactgtaa gcgcggtcgg
1020
aagaagctgc tgtacatctt taagcaaccc ttcatgaggc ctgtgcagac tactcaagag
1080
gaggacggct gttcatgccg gttcccagag gaggaggaag gcggctgcga actgcgcgtg
1140
aaattcagcc gcagcgcaga tgctccagcc tacaagcagg ggcagaacca gctctacaac
1200
gaactcaatc ttggtcggag agaggagtac gacgtgctgg acaagcggag aggacgggac
1260
ccagaaatgg gcgggaagcc gcgcagaaag aatccccaag agggcctgta caacgagctc
1320
caaaaggata agatggcaga agcctatagc gagattggta tgaaagggga acgcagaaga
1380
ggcaaaggcc acgacggact gtaccaggga ctcagcaccg ccaccaagga cacctatgac
1440
gctcttcaca tgcaggccct gccgcctcgg
1470
<210> 861
<400> 861
000
<210> 862
<400> 862
000
<210> 863
<400> 863
000
<210> 864
<400> 864
000
<210> 865
<400> 865
000
<210> 866
<400> 866
000
<210> 867
<400> 867
000
<210> 868
<400> 868
000
<210> 869
<400> 869
000
<210> 870
<400> 870
000
<210> 871
<400> 871
000
<210> 872
<400> 872
000
<210> 873
<400> 873
000
<210> 874
<400> 874
000
<210> 875
<400> 875
000
<210> 876
<400> 876
000
<210> 877
<400> 877
000
<210> 878
<400> 878
000
<210> 879
<400> 879
000
<210> 880
<400> 880
000
<210> 881
<400> 881
000
<210> 882
<400> 882
000
<210> 883
<400> 883
000
<210> 884
<400> 884
000
<210> 885
<400> 885
000
<210> 886
<400> 886
000
<210> 887
<400> 887
000
<210> 888
<400> 888
000
<210> 889
<400> 889
000
<210> 890
<400> 890
000
<210> 891
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 891
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 892
<211> 465
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 892
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Lys Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser Val Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu Thr Ile Ile
180 185 190
Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln
195 200 205
Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
225 230 235 240
Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
245 250 255
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
260 265 270
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
275 280 285
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
290 295 300
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
305 310 315 320
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
325 330 335
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
340 345 350
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln
355 360 365
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
370 375 380
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
385 390 395 400
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
405 410 415
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
420 425 430
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
435 440 445
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
450 455 460
Arg
465
<210> 893
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 893
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 894
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 894
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagcc accaccatca tcaccatcac cat
813
<210> 895
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 895
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser His His His His His His His His
260 265 270
<210> 896
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 896
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 897
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 897
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 898
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 898
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 899
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 899
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactaccaat catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagcc accaccatca tcaccatcac cat
813
<210> 900
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 900
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser His His His His His His His His
260 265 270
<210> 901
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 901
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactaccaat catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 902
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 902
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 903
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 903
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 904
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 904
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
tcatcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccga aatcgtgatg
480
acccagagcc ctgcaaccct gtccctttct cccggggaac gggctaccct ttcttgtcgg
540
gcatcacaag atatctcaaa atacctcaat tggtatcaac agaagccggg acaggcccct
600
aggcttctta tctaccacac ctctcgcctg catagcggga ttcccgcacg ctttagcggg
660
tctggaagcg ggaccgacta cactctgacc atctcatctc tccagcccga ggacttcgcc
720
gtctacttct gccagcaggg taacaccctg ccgtacacct tcggccaggg caccaagctt
780
gagatcaaac atcaccacca tcatcaccat cac
813
<210> 905
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 905
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
195 200 205
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Leu Glu Ile Lys His His His His His His His His
260 265 270
<210> 906
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 906
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
tcatcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccga aatcgtgatg
480
acccagagcc ctgcaaccct gtccctttct cccggggaac gggctaccct ttcttgtcgg
540
gcatcacaag atatctcaaa atacctcaat tggtatcaac agaagccggg acaggcccct
600
aggcttctta tctaccacac ctctcgcctg catagcggga ttcccgcacg ctttagcggg
660
tctggaagcg ggaccgacta cactctgacc atctcatctc tccagcccga ggacttcgcc
720
gtctacttct gccagcaggg taacaccctg ccgtacacct tcggccaggg caccaagctt
780
gagatcaaaa ccactactcc cgctccaagg ccacccaccc ctgccccgac catcgcctct
840
cagccgcttt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 907
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 907
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
195 200 205
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 908
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 908
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 909
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 909
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
caatcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccga aatcgtgatg
480
acccagagcc ctgcaaccct gtccctttct cccggggaac gggctaccct ttcttgtcgg
540
gcatcacaag atatctcaaa atacctcaat tggtatcaac agaagccggg acaggcccct
600
aggcttctta tctaccacac ctctcgcctg catagcggga ttcccgcacg ctttagcggg
660
tctggaagcg ggaccgacta cactctgacc atctcatctc tccagcccga ggacttcgcc
720
gtctacttct gccagcaggg taacaccctg ccgtacacct tcggccaggg caccaagctt
780
gagatcaaac atcaccacca tcatcaccat cac
813
<210> 910
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 910
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
195 200 205
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Leu Glu Ile Lys His His His His His His His His
260 265 270
<210> 911
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 911
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
caatcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccga aatcgtgatg
480
acccagagcc ctgcaaccct gtccctttct cccggggaac gggctaccct ttcttgtcgg
540
gcatcacaag atatctcaaa atacctcaat tggtatcaac agaagccggg acaggcccct
600
aggcttctta tctaccacac ctctcgcctg catagcggga ttcccgcacg ctttagcggg
660
tctggaagcg ggaccgacta cactctgacc atctcatctc tccagcccga ggacttcgcc
720
gtctacttct gccagcaggg taacaccctg ccgtacacct tcggccaggg caccaagctt
780
gagatcaaaa ccactactcc cgctccaagg ccacccaccc ctgccccgac catcgcctct
840
cagccgcttt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 912
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 912
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
195 200 205
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 913
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 913
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 914
<211> 828
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 914
atggccctcc cagtgaccgc tctgctgctg cctctcgcac ttcttctcca tgccgctcgg
60
cctgagatcg tcatgaccca aagccccgct accctgtccc tgtcacccgg cgagagggca
120
accctttcat gcagggccag ccaggacatt tctaagtacc tcaactggta tcagcagaag
180
ccagggcagg ctcctcgcct gctgatctac cacaccagcc gcctccacag cggtatcccc
240
gccagatttt ccgggagcgg gtctggaacc gactacaccc tcaccatctc ttctctgcag
300
cccgaggatt tcgccgtcta tttctgccag caggggaata ctctgccgta caccttcggt
360
caaggtacca agctggaaat caagggaggc ggaggatcag gcggtggcgg aagcggagga
420
ggtggctccg gaggaggagg ttcccaagtg cagcttcaag aatcaggacc cggacttgtg
480
aagccatcag aaaccctctc cctgacttgt accgtgtccg gtgtgagcct ccccgactac
540
ggagtctctt ggattcgcca gcctccgggg aagggtcttg aatggattgg ggtgatttgg
600
ggatcagaga ctacttacta ctcttcatca cttaagtcac gggtcaccat cagcaaagat
660
aatagcaaga accaagtgtc acttaagctg tcatctgtga ccgccgctga caccgccgtg
720
tactattgtg ccaaacatta ctattacgga gggtcttatg ctatggacta ctggggacag
780
gggaccctgg tgactgtctc tagccatcac catcaccacc atcatcac
828
<210> 915
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 915
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser His His His His
260 265 270
His His His His
275
<210> 916
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 916
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcg gcggaggcgg gagccaggtc caactccaag aaagcggacc gggtcttgtg
480
aagccatcag aaactctttc actgacttgt actgtgagcg gagtgtctct ccccgattac
540
ggggtgtctt ggatcagaca gccaccgggg aagggtctgg aatggattgg agtgatttgg
600
ggctctgaga ctacttacta ctcttcatcc ctcaagtcac gcgtcaccat ctcaaaggac
660
aactctaaga atcaggtgtc actgaaactg tcatctgtga ccgcagccga caccgccgtg
720
tactattgcg ctaagcatta ctattatggc gggagctacg caatggatta ctggggacag
780
ggtactctgg tcaccgtgtc cagcaccact accccagcac cgaggccacc caccccggct
840
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 917
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 917
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 918
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 918
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 919
<211> 828
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 919
atggccctcc cagtgaccgc tctgctgctg cctctcgcac ttcttctcca tgccgctcgg
60
cctgagatcg tcatgaccca aagccccgct accctgtccc tgtcacccgg cgagagggca
120
accctttcat gcagggccag ccaggacatt tctaagtacc tcaactggta tcagcagaag
180
ccagggcagg ctcctcgcct gctgatctac cacaccagcc gcctccacag cggtatcccc
240
gccagatttt ccgggagcgg gtctggaacc gactacaccc tcaccatctc ttctctgcag
300
cccgaggatt tcgccgtcta tttctgccag caggggaata ctctgccgta caccttcggt
360
caaggtacca agctggaaat caagggaggc ggaggatcag gcggtggcgg aagcggagga
420
ggtggctccg gaggaggagg ttcccaagtg cagcttcaag aatcaggacc cggacttgtg
480
aagccatcag aaaccctctc cctgacttgt accgtgtccg gtgtgagcct ccccgactac
540
ggagtctctt ggattcgcca gcctccgggg aagggtcttg aatggattgg ggtgatttgg
600
ggatcagaga ctacttacta ccagtcatca cttaagtcac gggtcaccat cagcaaagat
660
aatagcaaga accaagtgtc acttaagctg tcatctgtga ccgccgctga caccgccgtg
720
tactattgtg ccaaacatta ctattacgga gggtcttatg ctatggacta ctggggacag
780
gggaccctgg tgactgtctc tagccatcac catcaccacc atcatcac
828
<210> 920
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 920
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser His His His His
260 265 270
His His His His
275
<210> 921
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 921
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcg gaggcggagg gagccaggtc caactccaag aaagcggacc gggtcttgtg
480
aagccatcag aaactctttc actgacttgt actgtgagcg gagtgtctct ccccgattac
540
ggggtgtctt ggatcagaca gccaccgggg aagggtctgg aatggattgg agtgatttgg
600
ggctctgaga ctacttacta ccaatcatcc ctcaagtcac gcgtcaccat ctcaaaggac
660
aactctaaga atcaggtgtc actgaaactg tcatctgtga ccgcagccga caccgccgtg
720
tactattgcg ctaagcatta ctattatggc gggagctacg caatggatta ctggggacag
780
ggtactctgg tcaccgtgtc cagcaccact accccagcac cgaggccacc caccccggct
840
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 922
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 922
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 923
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 923
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 924
<211> 828
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 924
atggcactgc ctgtcactgc cctcctgctg cctctggccc tccttctgca tgccgccagg
60
ccccaagtcc agctgcaaga gtcaggaccc ggactggtga agccgtctga gactctctca
120
ctgacttgta ccgtcagcgg cgtgtccctc cccgactacg gagtgtcatg gatccgccaa
180
cctcccggga aagggcttga atggattggt gtcatctggg gttctgaaac cacctactac
240
tcatcttccc tgaagtccag ggtgaccatc agcaaggata attccaagaa ccaggtcagc
300
cttaagctgt catctgtgac cgctgctgac accgccgtgt attactgcgc caagcactac
360
tattacggag gaagctacgc tatggactat tggggacagg gcactctcgt gactgtgagc
420
agcggcggtg gagggtctgg aggtggagga tccggtggtg gtgggtcagg cggaggaggg
480
agcgagattg tgatgactca gtcaccagcc accctttctc tttcacccgg cgagagagca
540
accctgagct gtagagccag ccaggacatt tctaagtacc tcaactggta tcagcaaaaa
600
ccggggcagg cccctcgcct cctgatctac catacctcac gccttcactc tggtatcccc
660
gctcggttta gcggatcagg atctggtacc gactacactc tgaccatttc cagcctgcag
720
ccagaagatt tcgcagtgta tttctgccag cagggcaata cccttcctta caccttcggt
780
cagggaacca agctcgaaat caagcaccat caccatcatc accaccat
828
<210> 925
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 925
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys His His His His
260 265 270
His His His His
275
<210> 926
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 926
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
tcatcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccgg aggtggcgga
480
agcgaaatcg tgatgaccca gagccctgca accctgtccc tttctcccgg ggaacgggct
540
accctttctt gtcgggcatc acaagatatc tcaaaatacc tcaattggta tcaacagaag
600
ccgggacagg cccctaggct tcttatctac cacacctctc gcctgcatag cgggattccc
660
gcacgcttta gcgggtctgg aagcgggacc gactacactc tgaccatctc atctctccag
720
cccgaggact tcgccgtcta cttctgccag cagggtaaca ccctgccgta caccttcggc
780
cagggcacca agcttgagat caaaaccact actcccgctc caaggccacc cacccctgcc
840
ccgaccatcg cctctcagcc gctttccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 927
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 927
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 928
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 928
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 929
<211> 828
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 929
atggcactgc ctgtcactgc cctcctgctg cctctggccc tccttctgca tgccgccagg
60
ccccaagtcc agctgcaaga gtcaggaccc ggactggtga agccgtctga gactctctca
120
ctgacttgta ccgtcagcgg cgtgtccctc cccgactacg gagtgtcatg gatccgccaa
180
cctcccggga aagggcttga atggattggt gtcatctggg gttctgaaac cacctactac
240
cagtcttccc tgaagtccag ggtgaccatc agcaaggata attccaagaa ccaggtcagc
300
cttaagctgt catctgtgac cgctgctgac accgccgtgt attactgcgc caagcactac
360
tattacggag gaagctacgc tatggactat tggggacagg gcactctcgt gactgtgagc
420
agcggcggtg gagggtctgg aggtggagga tccggtggtg gtgggtcagg cggaggaggg
480
agcgagattg tgatgactca gtcaccagcc accctttctc tttcacccgg cgagagagca
540
accctgagct gtagagccag ccaggacatt tctaagtacc tcaactggta tcagcaaaaa
600
ccggggcagg cccctcgcct cctgatctac catacctcac gccttcactc tggtatcccc
660
gctcggttta gcggatcagg atctggtacc gactacactc tgaccatttc cagcctgcag
720
ccagaagatt tcgcagtgta tttctgccag cagggcaata cccttcctta caccttcggt
780
cagggaacca agctcgaaat caagcaccat caccatcatc atcaccac
828
<210> 930
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 930
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys His His His His
260 265 270
His His His His
275
<210> 931
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 931
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
caatcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccgg aggcggtggg
480
tcagaaatcg tgatgaccca gagccctgca accctgtccc tttctcccgg ggaacgggct
540
accctttctt gtcgggcatc acaagatatc tcaaaatacc tcaattggta tcaacagaag
600
ccgggacagg cccctaggct tcttatctac cacacctctc gcctgcatag cgggattccc
660
gcacgcttta gcgggtctgg aagcgggacc gactacactc tgaccatctc atctctccag
720
cccgaggact tcgccgtcta cttctgccag cagggtaaca ccctgccgta caccttcggc
780
cagggcacca agcttgagat caaaaccact actcccgctc caaggccacc cacccctgcc
840
ccgaccatcg cctctcagcc gctttccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 932
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 932
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Gln Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 933
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 933
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
115 120 125
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
130 135 140
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
145 150 155 160
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
165 170 175
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
180 185 190
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
195 200 205
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
210 215 220
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 934
<211> 828
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 934
atggccctcc cagtgaccgc tctgctgctg cctctcgcac ttcttctcca tgccgctcgg
60
cctgagatcg tcatgaccca aagccccgct accctgtccc tgtcacccgg cgagagggca
120
accctttcat gcagggccag ccaggacatt tctaagtacc tcaactggta tcagcagaag
180
ccagggcagg ctcctcgcct gctgatctac cacaccagcc gcctccacag cggtatcccc
240
gccagatttt ccgggagcgg gtctggaacc gactacaccc tcaccatctc ttctctgcag
300
cccgaggatt tcgccgtcta tttctgccag caggggaata ctctgccgta caccttcggt
360
caaggtacca agctggaaat caagggaggc ggaggatcag gcggtggcgg aagcggagga
420
ggtggctccg gaggaggagg ttcccaagtg cagcttcaag aatcaggacc cggacttgtg
480
aagccatcag aaaccctctc cctgacttgt accgtgtccg gtgtgagcct ccccgactac
540
ggagtctctt ggattcgcca gcctccgggg aagggtcttg aatggattgg ggtgatttgg
600
ggatcagaga ctacttacta caattcatca cttaagtcac gggtcaccat cagcaaagat
660
aatagcaaga accaagtgtc acttaagctg tcatctgtga ccgccgctga caccgccgtg
720
tactattgtg ccaaacatta ctattacgga gggtcttatg ctatggacta ctggggacag
780
gggaccctgg tgactgtctc tagccatcac catcaccacc atcatcac
828
<210> 935
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 935
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser His His His His
260 265 270
His His His His
275
<210> 936
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 936
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcg gaggcggtgg gagccaggtc caactccaag aaagcggacc gggtcttgtg
480
aagccatcag aaactctttc actgacttgt actgtgagcg gagtgtctct ccccgattac
540
ggggtgtctt ggatcagaca gccaccgggg aagggtctgg aatggattgg agtgatttgg
600
ggctctgaga ctacttacta caactcatcc ctcaagtcac gcgtcaccat ctcaaaggac
660
aactctaaga atcaggtgtc actgaaactg tcatctgtga ccgcagccga caccgccgtg
720
tactattgcg ctaagcatta ctattatggc gggagctacg caatggatta ctggggacag
780
ggtactctgg tcaccgtgtc cagcaccact accccagcac cgaggccacc caccccggct
840
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 937
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 937
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 938
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 938
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
130 135 140
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
145 150 155 160
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
165 170 175
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
180 185 190
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
195 200 205
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
210 215 220
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
225 230 235 240
Gly Thr Lys Leu Glu Ile Lys
245
<210> 939
<211> 828
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 939
atggcactgc ctgtcactgc cctcctgctg cctctggccc tccttctgca tgccgccagg
60
ccccaagtcc agctgcaaga gtcaggaccc ggactggtga agccgtctga gactctctca
120
ctgacttgta ccgtcagcgg cgtgtccctc cccgactacg gagtgtcatg gatccgccaa
180
cctcccggga aagggcttga atggattggt gtcatctggg gttctgaaac cacctactac
240
aactcttccc tgaagtccag ggtgaccatc agcaaggata attccaagaa ccaggtcagc
300
cttaagctgt catctgtgac cgctgctgac accgccgtgt attactgcgc caagcactac
360
tattacggag gaagctacgc tatggactat tggggacagg gcactctcgt gactgtgagc
420
agcggcggtg gagggtctgg aggtggagga tccggtggtg gtgggtcagg cggaggaggg
480
agcgagattg tgatgactca gtcaccagcc accctttctc tttcacccgg cgagagagca
540
accctgagct gtagagccag ccaggacatt tctaagtacc tcaactggta tcagcaaaaa
600
ccggggcagg cccctcgcct cctgatctac catacctcac gccttcactc tggtatcccc
660
gctcggttta gcggatcagg atctggtacc gactacactc tgaccatttc cagcctgcag
720
ccagaagatt tcgcagtgta tttctgccag cagggcaata cccttcctta caccttcggt
780
cagggaacca agctcgaaat caagcaccat caccatcatc accaccat
828
<210> 940
<211> 276
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 940
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys His His His His
260 265 270
His His His His
275
<210> 941
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 941
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcg gaggcggtgg gagccaggtc caactccaag aaagcggacc gggtcttgtg
480
aagccatcag aaactctttc actgacttgt actgtgagcg gagtgtctct ccccgattac
540
ggggtgtctt ggatcagaca gccaccgggg aagggtctgg aatggattgg agtgatttgg
600
ggctctgaga ctacttacta caactcatcc ctcaagtcac gcgtcaccat ctcaaaggac
660
aactctaaga atcaggtgtc actgaaactg tcatctgtga ccgcagccga caccgccgtg
720
tactattgcg ctaagcatta ctattatggc gggagctacg caatggatta ctggggacag
780
ggtactctgg tcaccgtgtc cagcaccact accccagcac cgaggccacc caccccggct
840
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 942
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 942
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val
145 150 155 160
Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser
165 170 175
Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn
195 200 205
Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn
210 215 220
Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp
245 250 255
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 943
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 943
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser
180 185 190
Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr
195 200 205
Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
225 230 235 240
Ser Ser
<210> 944
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 944
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactacaatt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagcc accaccatca tcaccatcac cat
813
<210> 945
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 945
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser His His His His His His His His
260 265 270
<210> 946
<211> 1473
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 946
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
aactcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccgg aggtggcgga
480
agcgaaatcg tgatgaccca gagccctgca accctgtccc tttctcccgg ggaacgggct
540
accctttctt gtcgggcatc acaagatatc tcaaaatacc tcaattggta tcaacagaag
600
ccgggacagg cccctaggct tcttatctac cacacctctc gcctgcatag cgggattccc
660
gcacgcttta gcgggtctgg aagcgggacc gactacactc tgaccatctc atctctccag
720
cccgaggact tcgccgtcta cttctgccag cagggtaaca ccctgccgta caccttcggc
780
cagggcacca agcttgagat caaaaccact actcccgctc caaggccacc cacccctgcc
840
ccgaccatcg cctctcagcc gctttccctg cgtccggagg catgtagacc cgcagctggt
900
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
960
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1020
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1080
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1140
gtgaaattca gccgcagcgc agatgctcca gcctacaagc aggggcagaa ccagctctac
1200
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
1260
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
1320
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
1380
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
1440
gacgctcttc acatgcaggc cctgccgcct cgg
1473
<210> 947
<211> 491
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 947
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro
165 170 175
Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
195 200 205
Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro
245 250 255
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 948
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 948
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr
20 25 30
Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met Thr Gln Ser Pro Ala
130 135 140
Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala
145 150 155 160
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
180 185 190
Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu
195 200 205
Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln
210 215 220
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu
225 230 235 240
Ile Lys
<210> 949
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 949
atggctctgc ccgtgaccgc actcctcctg ccactggctc tgctgcttca cgccgctcgc
60
ccacaagtcc agcttcaaga atcagggcct ggtctggtga agccatctga gactctgtcc
120
ctcacttgca ccgtgagcgg agtgtccctc ccagactacg gagtgagctg gattagacag
180
cctcccggaa agggactgga gtggatcgga gtgatttggg gtagcgaaac cacttactat
240
aactcttccc tgaagtcacg ggtcaccatt tcaaaggata actcaaagaa tcaagtgagc
300
ctcaagctct catcagtcac cgccgctgac accgccgtgt attactgtgc caagcattac
360
tactatggag ggtcctacgc catggactac tggggccagg gaactctggt cactgtgtca
420
tctggtggag gaggtagcgg aggaggcggg agcggtggag gtggctccga aatcgtgatg
480
acccagagcc ctgcaaccct gtccctttct cccggggaac gggctaccct ttcttgtcgg
540
gcatcacaag atatctcaaa atacctcaat tggtatcaac agaagccggg acaggcccct
600
aggcttctta tctaccacac ctctcgcctg catagcggga ttcccgcacg ctttagcggg
660
tctggaagcg ggaccgacta cactctgacc atctcatctc tccagcccga ggacttcgcc
720
gtctacttct gccagcaggg taacaccctg ccgtacacct tcggccaggg caccaagctt
780
gagatcaaac atcaccacca tcatcaccat cac
813
<210> 950
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 950
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val
35 40 45
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
65 70 75 80
Asn Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys
85 90 95
Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
115 120 125
Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Met
145 150 155 160
Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr
165 170 175
Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr
180 185 190
Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser
195 200 205
Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly
210 215 220
Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
225 230 235 240
Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln
245 250 255
Gly Thr Lys Leu Glu Ile Lys His His His His His His His His
260 265 270
<210> 951
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 951
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
120
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
180
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
240
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
300
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
360
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
420
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
480
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
540
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
600
tactacaact catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
660
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
720
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
780
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
840
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
900
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
960
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1020
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1080
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1140
agcgcagatg ctccagccta caagcagggg cagaaccagc tctacaacga actcaatctt
1200
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
1260
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
1320
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
1380
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
1440
caggccctgc cgcctcgg
1458
<210> 952
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 952
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu
20 25 30
Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Ile Pro
65 70 75 80
Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 953
<211> 813
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 953
atggccctgc ccgtcaccgc tctgctgctg ccccttgctc tgcttcttca tgcagcaagg
60
ccggacatcc agatgaccca aaccacctca tccctctctg cctctcttgg agacagggtg
120
accatttctt gtcgcgccag ccaggacatc agcaagtatc tgaactggta tcagcagaag
180
ccggacggaa ccgtgaagct cctgatctac catacctctc gcctgcatag cggcgtgccc
240
tcacgcttct ctggaagcgg atcaggaacc gattattctc tcactatttc aaatcttgag
300
caggaagata ttgccaccta tttctgccag cagggtaata ccctgcccta caccttcgga
360
ggagggacca agctcgaaat caccggtgga ggaggcagcg gcggtggagg gtctggtgga
420
ggtggttctg aggtgaagct gcaagaatca ggccctggac ttgtggcccc ttcacagtcc
480
ctgagcgtga cttgcaccgt gtccggagtc tccctgcccg actacggagt gtcatggatc
540
agacaacctc cacggaaagg actggaatgg ctcggtgtca tctggggtag cgaaactact
600
tactacaatt cagccctcaa aagcaggctg actattatca aggacaacag caagtcccaa
660
gtctttctta agatgaactc actccagact gacgacaccg caatctacta ttgtgctaag
720
cactactact acggaggatc ctacgctatg gattactggg gacaaggtac ttccgtcact
780
gtctcttcac accatcatca ccatcaccat cac
813
<210> 954
<211> 271
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 954
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser His His His His His His His His
260 265 270
<210> 955
<211> 1458
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 955
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccggacatcc agatgacaca gactacatcc tccctgtctg cctctctggg agacagagtc
120
accatcagtt gcagggcaag tcaggacatt agtaaatatt taaattggta tcagcagaaa
180
ccagatggaa ctgttaaact cctgatctac catacatcaa gattacactc aggagtccca
240
tcaaggttca gtggcagtgg gtctggaaca gattattctc tcaccattag caacctggag
300
caagaagata ttgccactta cttttgccaa cagggtaata cgcttccgta cacgttcgga
360
ggggggacca agctggagat cacaggtggc ggtggctcgg gcggtggtgg gtcgggtggc
420
ggcggatctg aggtgaaact gcaggagtca ggacctggcc tggtggcgcc ctcacagagc
480
ctgtccgtca catgcactgt ctcaggggtc tcattacccg actatggtgt aagctggatt
540
cgccagcctc cacgaaaggg tctggagtgg ctgggagtaa tatggggtag tgaaaccaca
600
tactataatt cagctctcaa atccagactg accatcatca aggacaactc caagagccaa
660
gttttcttaa aaatgaacag tctgcaaact gatgacacag ccatttacta ctgtgccaaa
720
cattattact acggtggtag ctatgctatg gactactggg gccaaggaac ctcagtcacc
780
gtctcctcaa ccacgacgcc agcgccgcga ccaccaacac cggcgcccac catcgcgtcg
840
cagcccctgt ccctgcgccc agaggcgtgc cggccagcgg cggggggcgc agtgcacacg
900
agggggctgg acttcgcctg tgatatctac atctgggcgc ccttggccgg gacttgtggg
960
gtccttctcc tgtcactggt tatcaccctt tactgcaaac ggggcagaaa gaaactcctg
1020
tatatattca aacaaccatt tatgagacca gtacaaacta ctcaagagga agatggctgt
1080
agctgccgat ttccagaaga agaagaagga ggatgtgaac tgagagtgaa gttcagcagg
1140
agcgcagacg cccccgcgta caagcagggc cagaaccagc tctataacga gctcaatcta
1200
ggacgaagag aggagtacga tgttttggac aagagacgtg gccgggaccc tgagatgggg
1260
ggaaagccga gaaggaagaa ccctcaggaa ggcctgtaca atgaactgca gaaagataag
1320
atggcggagg cctacagtga gattgggatg aaaggcgagc gccggagggg caaggggcac
1380
gatggccttt accagggtct cagtacagcc accaaggaca cctacgacgc ccttcacatg
1440
caggccctgc cccctcgc
1458
<210> 956
<211> 486
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 956
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 957
<211> 242
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 957
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val Lys Leu Gln Glu
115 120 125
Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser Val Thr Cys
130 135 140
Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg
145 150 155 160
Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile Trp Gly Ser
165 170 175
Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu Thr Ile Ile
180 185 190
Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln
195 200 205
Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly
210 215 220
Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val
225 230 235 240
Ser Ser
<210> 958
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 958
Asp Tyr Gly Val Ser
1 5
<210> 959
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 959
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 960
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 960
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
1 5 10
<210> 961
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 961
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser
1 5 10 15
<210> 962
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 962
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Gln Ser Ser Leu Lys Ser
1 5 10 15
<210> 963
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 963
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ser Leu Lys Ser
1 5 10 15
<210> 964
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 964
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
1 5 10
<210> 965
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 965
His Thr Ser Arg Leu His Ser
1 5
<210> 966
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 966
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 967
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(30)
<223> /примечание="Данная последовательность может включать 1-6
повторяющихся единиц 'Gly Gly Gly Gly Ser'"
<400> 967
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25 30
<210> 968
<211> 100
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 968
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
60
tttttttttt tttttttttt tttttttttt tttttttttt
100
<210> 969
<211> 400
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(400)
<223> /примечание="Данная последовательность может включать 100-400
нуклеотидов"
<220>
<221> источник
<223> /примечание="Смотри спецификацию поданной заявки для подробного
описания
замен и предпочтительных вариантов осуществления"
<400> 969
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
60
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
120
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
180
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
240
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
300
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
360
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
400
<210> 970
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 970
Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met Val Ser Ala Leu Leu
1 5 10 15
Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr Asp Pro Thr Arg Pro
20 25 30
Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr Asn Leu Ala Asp Arg
35 40 45
Glu Leu Val His Met Ile Asn Trp Ala Lys Arg Val Pro Gly Phe Val
50 55 60
Asp Leu Thr Leu His Asp Gln Val His Leu Leu Glu Cys Ala Trp Leu
65 70 75 80
Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser Met Glu His Pro Gly
85 90 95
Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp Arg Asn Gln Gly Lys
100 105 110
Cys Val Glu Gly Met Val Glu Ile Phe Asp Met Leu Leu Ala Thr Ser
115 120 125
Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu Phe Val Cys Leu
130 135 140
Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr Phe Leu Ser Ser
145 150 155 160
Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His Arg Val Leu Asp
165 170 175
Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys Ala Gly Leu Thr
180 185 190
Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu Leu Ile Leu Ser
195 200 205
His Ile Arg His Met Ser Asn Lys Gly Met Glu His Leu Tyr Ser Met
210 215 220
Lys Cys Lys Asn Val Val Pro Leu Tyr Asp Leu Leu Leu Glu Met Leu
225 230 235 240
Asp Ala His Arg Leu
245
<210> 971
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 971
tcgttggcac tttccctgac tgccgaccag atggtgtccg cccttctgga cgccgagcct
60
ccaattctgt actcggagta cgatccgact cgcccgttct ccgaagccag catgatgggc
120
ctgttgacta acctggcgga ccgcgagttg gtgcacatga ttaactgggc taagcgggtg
180
ccgggcttcg tggacctgac tctgcacgac caagtgcacc tcctggaatg cgcctggctg
240
gaaatcctca tgatcggcct cgtgtggaga tccatggagc atcccggaaa gctcctgttt
300
gcacccaacc tcctgcttga tcgcaaccag ggaaaatgcg tggaagggat ggtcgagatt
360
ttcgacatgc tgctcgccac ctcttcccgg ttccggatga tgaatctgca gggagaagag
420
ttcgtgtgtc tgaagtcaat catcctgctg aactccgggg tctatacctt cctgagctcg
480
accctcaagt cactggagga aaaagaccac atccatcgcg tgctcgataa gatcaccgac
540
acccttatcc atctcatggc gaaggctgga ctgaccctgc aacagcagca ccagaggctg
600
gcccagttgc tgctgattct gagccacatc cggcacatgt cgaacaaggg gatggaacac
660
ctgtacagca tgaagtgcaa gaacgtcgtg cctctgtacg atctgctcct ggaaatgctg
720
gacgcgcaca gactc
735
<210> 972
<211> 69
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 972
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Phe Trp Leu
35 40 45
Pro Ile Gly Cys Ala Ala Phe Val Val Val Cys Ile Leu Gly Cys Ile
50 55 60
Leu Ile Cys Trp Leu
65
<210> 973
<211> 207
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 973
accacgacgc cagcgccgcg accaccaaca ccggcgccca ccatcgcgtc gcagcccctg
60
tccctgcgcc cagaggcgtg ccggccagcg gcggggggcg cagtgcacac gagggggctg
120
gacttcgcct gtgatttctg gttacccata ggatgtgcag cctttgttgt agtctgcatt
180
ttgggatgca tacttatttg ttggctt
207
<210> 974
<211> 5000
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(5000)
<223> /примечание="Данная последовательность может включать 50-5000
нуклеотидов"
<220>
<221> источник
<223> /примечание="Смотри спецификацию поданной заявки для подробного
описания
замен и предпочтительных вариантов осуществления"
<400> 974
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
60
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
120
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
180
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
240
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
300
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
360
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
420
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
480
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
540
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
600
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
660
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
720
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
780
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
840
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
900
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
960
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1020
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1080
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1140
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1200
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1260
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1320
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1380
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1440
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1500
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1560
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1620
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1680
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1740
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1800
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1860
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1920
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
1980
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2040
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2100
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2160
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2220
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2280
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2340
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2400
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2460
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2520
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2580
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2640
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2700
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2760
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2820
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2880
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
2940
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3000
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3060
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3120
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3180
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3240
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3300
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3360
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3420
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3480
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3540
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3600
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3660
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3720
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3780
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3840
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3900
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
3960
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4020
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4080
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4140
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4200
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4260
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4320
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4380
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4440
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4500
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4560
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4620
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4680
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4740
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4800
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4860
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4920
tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt tttttttttt
4980
tttttttttt tttttttttt
5000
<210> 975
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 975
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
1 5 10 15
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
20 25 30
Gly Lys Lys Phe Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
35 40 45
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
50 55 60
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
65 70 75 80
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
85 90 95
Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu
100 105
<210> 976
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 976
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
1 5 10 15
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
20 25 30
Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
35 40 45
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
50 55 60
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
65 70 75 80
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
85 90 95
Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu
100 105
<210> 977
<211> 2817
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 977
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccgggatccc ggggcgtgca ggttgagaca atttccccag gagatgggcg aacgttcccc
120
aagcgcggac agacatgcgt tgtgcactac acaggaatgt tggaggacgg aaagaaaatg
180
gacagttcaa gagatcggaa caaaccattc aaattcatgt tgggaaaaca ggaagtgata
240
cggggctggg aagagggtgt agcgcaaatg tccgttggtc aacgagcaaa actcacgata
300
agtcccgatt atgcttacgg cgcaaccggt cacccgggca tcataccgcc tcatgcgact
360
ttggtctttg atgtggagct gttgaaactt gaaactcgcg gagtacaggt tgaaacaata
420
tcacccgggg acgggcggac ttttccgaag agaggtcaga cctgcgtcgt ccattatacc
480
ggtatgctgg aggacggaaa gaaaatggac agctcacggg accgaaataa accattcaaa
540
tttatgttgg ggaaacaaga ggttatcagg ggctgggagg agggtgtggc ccagatgtct
600
gtcggtcagc gcgcgaaact cacaatctct ccggattatg cgtatggggc gacagggcat
660
ccgggaatta tccctcccca cgctaccttg gttttcgatg ttgagcttct gaagttggag
720
accagaggag ttcaagtgga gacaatatct cctggggatg gacggacgtt ccccaagcgc
780
ggccagacct gtgtagtcca ctacacaggg atgcttgaag acggaaaaaa gatggatagc
840
agtagagatc gcaacaaacc atttaagttc atgctgggga agcaggaagt aatacgcggc
900
tgggaggaag gcgtggcaca gatgagtgtt ggtcaacggg ccaaacttac tatttctccc
960
gattatgcgt atggagccac cgggcaccct ggcattatcc caccccatgc cacattggtt
1020
tttgacgttg aattgcttaa attggagacc aggggagtcc aagtggaaac aatatcaccg
1080
ggggatggtc ggacttttcc taaaaggggc caaacctgtg tagtccatta taccggaatg
1140
ctcgaagacg gaaagaaaat ggactcttct agagaccgca ataagccctt caagttcatg
1200
ttgggtaagc aagaggtgat ccggggctgg gaagaggggg tcgctcaaat gtccgtcggt
1260
cagcgagcta aactgactat ttccccagac tacgcatatg gagcgactgg ccaccccggt
1320
attattcctc cccatgcgac tctcgtgttc gacgtagaac tcttgaaatt ggaaacgtca
1380
gcccggaaca ggcggaagag aggatccgac atccagatga cacagactac atcctccctg
1440
tctgcctctc tgggagacag agtcaccatc agttgcaggg caagtcagga cattagtaaa
1500
tatttaaatt ggtatcagca gaaaccagat ggaactgtta aactcctgat ctaccataca
1560
tcaagattac actcaggagt cccatcaagg ttcagtggca gtgggtctgg aacagattat
1620
tctctcacca ttagcaacct ggagcaagaa gatattgcca cttacttttg ccaacagggt
1680
aatacgcttc cgtacacgtt cggagggggg actaagttgg aaataacagg tggcggtggc
1740
tcgggcggtg gtgggtcggg tggcggcgga tctgaggtga aactgcagga gtcaggacct
1800
ggcctggtgg cgccctcaca gagcctgtcc gtcacatgca ctgtctcagg ggtctcatta
1860
cccgactatg gtgtaagctg gattcgccag cctccacgaa agggtctgga gtggctggga
1920
gtaatatggg gtagtgaaac cacatactat aattcagctc tcaaatccag actgaccatc
1980
atcaaggaca actccaagag ccaagttttc ttaaaaatga acagtctgca aactgatgac
2040
acagccattt actactgtgc caaacattat tactacggtg gtagctatgc tatggactac
2100
tggggtcaag gaacctcagt caccgtctcc tcagctagca ccacgacgcc agcgccgcga
2160
ccaccaacac cggcgcccac catcgcgtcg cagcccctgt ccctgcgccc agaggcgtgc
2220
cggccagcgg cggggggcgc agtgcacacg agggggctgg acttcgcctg tgattccgga
2280
atctacatct gggcgccctt ggccgggact tgtggggtcc ttctcctgtc actggttatc
2340
accctttact gcaaacgggg cagaaagaaa ctcctgtata tattcaaaca accatttatg
2400
agaccagtac aaactactca agaggaagat ggctgtagct gccgatttcc agaagaagaa
2460
gaaggaggat gtgaactgag agtgaagttc agcaggagcg cagacgcccc cgcgtaccag
2520
cagggccaga accagctcta taacgagctc aatctaggac gaagagagga gtacgatgtt
2580
ttggacaaga gacgtggccg ggaccctgag atggggggaa agccgagaag gaagaaccct
2640
caggaaggcc tgtacaatga actgcagaaa gataagatgg cggaggccta cagtgagatt
2700
gggatgaaag gcgagcgccg gaggggcaag gggcacgatg gcctttacca gggtctcagt
2760
acagccacca aggacaccta cgacgccctt cacatgcagg ccctgccccc tcgctaa
2817
<210> 978
<211> 939
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 978
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Arg Gly Val Gln Val Glu Thr Ile Ser
20 25 30
Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val
35 40 45
His Tyr Thr Gly Met Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg
50 55 60
Asp Arg Asn Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile
65 70 75 80
Arg Gly Trp Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala
85 90 95
Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro
100 105 110
Gly Ile Ile Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu
115 120 125
Lys Leu Glu Thr Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp
130 135 140
Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr
145 150 155 160
Gly Met Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn
165 170 175
Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp
180 185 190
Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr
195 200 205
Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile
210 215 220
Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu
225 230 235 240
Thr Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr
245 250 255
Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu
260 265 270
Glu Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe
275 280 285
Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly
290 295 300
Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro
305 310 315 320
Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His
325 330 335
Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg Gly
340 345 350
Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro Lys
355 360 365
Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp Gly
370 375 380
Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe Met
385 390 395 400
Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala Gln
405 410 415
Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr Ala
420 425 430
Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr Leu
435 440 445
Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Ser Ala Arg Asn Arg
450 455 460
Arg Lys Arg Gly Ser Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
465 470 475 480
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
485 490 495
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
500 505 510
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
515 520 525
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
530 535 540
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
545 550 555 560
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
580 585 590
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
595 600 605
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
610 615 620
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
625 630 635 640
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
645 650 655
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
660 665 670
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
675 680 685
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
690 695 700
Thr Ser Val Thr Val Ser Ser Ala Ser Thr Thr Thr Pro Ala Pro Arg
705 710 715 720
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
725 730 735
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
740 745 750
Leu Asp Phe Ala Cys Asp Ser Gly Ile Tyr Ile Trp Ala Pro Leu Ala
755 760 765
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
770 775 780
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
785 790 795 800
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
805 810 815
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
820 825 830
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
835 840 845
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
850 855 860
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
865 870 875 880
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
885 890 895
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
900 905 910
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
915 920 925
Ala Leu His Met Gln Ala Leu Pro Pro Arg Glx
930 935
<210> 979
<211> 436
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 979
Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe
1 5 10 15
Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu
20 25 30
Asp Gly Lys Lys Phe Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys
35 40 45
Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val
50 55 60
Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp
65 70 75 80
Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala
85 90 95
Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg Gly Val
100 105 110
Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg
115 120 125
Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp Gly Lys
130 135 140
Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe Met Leu
145 150 155 160
Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala Gln Met
165 170 175
Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr
180 185 190
Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr Leu Val
195 200 205
Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg Gly Val Gln Val Glu
210 215 220
Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr
225 230 235 240
Cys Val Val His Tyr Thr Gly Met Leu Glu Asp Gly Lys Lys Met Asp
245 250 255
Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe Met Leu Gly Lys Gln
260 265 270
Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala Gln Met Ser Val Gly
275 280 285
Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr
290 295 300
Gly His Pro Gly Ile Ile Pro Pro His Ala Thr Leu Val Phe Asp Val
305 310 315 320
Glu Leu Leu Lys Leu Glu Thr Arg Gly Val Gln Val Glu Thr Ile Ser
325 330 335
Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val
340 345 350
His Tyr Thr Gly Met Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg
355 360 365
Asp Arg Asn Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile
370 375 380
Arg Gly Trp Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala
385 390 395 400
Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro
405 410 415
Gly Ile Ile Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu
420 425 430
Lys Leu Glu Thr
435
<210> 980
<211> 436
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 980
Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe
1 5 10 15
Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu
20 25 30
Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys
35 40 45
Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val
50 55 60
Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp
65 70 75 80
Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala
85 90 95
Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg Gly Val
100 105 110
Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg
115 120 125
Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp Gly Lys
130 135 140
Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe Met Leu
145 150 155 160
Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala Gln Met
165 170 175
Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr
180 185 190
Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr Leu Val
195 200 205
Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg Gly Val Gln Val Glu
210 215 220
Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr
225 230 235 240
Cys Val Val His Tyr Thr Gly Met Leu Glu Asp Gly Lys Lys Met Asp
245 250 255
Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe Met Leu Gly Lys Gln
260 265 270
Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala Gln Met Ser Val Gly
275 280 285
Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr
290 295 300
Gly His Pro Gly Ile Ile Pro Pro His Ala Thr Leu Val Phe Asp Val
305 310 315 320
Glu Leu Leu Lys Leu Glu Thr Arg Gly Val Gln Val Glu Thr Ile Ser
325 330 335
Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val
340 345 350
His Tyr Thr Gly Met Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg
355 360 365
Asp Arg Asn Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile
370 375 380
Arg Gly Trp Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala
385 390 395 400
Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro
405 410 415
Gly Ile Ile Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu
420 425 430
Lys Leu Glu Thr
435
<210> 981
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 981
Ser Ala Arg Asn Arg Gln Lys Arg
1 5
<210> 982
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 982
Arg Gly Asp Ser
1
<210> 983
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 983
Gln Val Gln Leu Leu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Ser Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Gly Gly Gly Ser Gly Gly Gly Ser Gly
115 120 125
Gly Gly Ser Gly Gly Gly Ser Glu Leu Val Leu Thr Gln Ser Pro Lys
130 135 140
Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val Thr Cys Lys Ala
145 150 155 160
Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr Arg Asn Ser Gly
180 185 190
Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp Tyr Phe Cys Gln
210 215 220
Tyr Asn Arg Tyr Pro Tyr Thr Ser Phe Phe Phe Thr Lys Leu Glu Ile
225 230 235 240
Lys Arg Arg Ser
<210> 984
<211> 464
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 984
Gln Val Gln Leu Leu Glu Ser Gly Ala Glu Leu Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Gly Asp Gly Asp Thr Asn Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Gln Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Ser Cys
85 90 95
Ala Arg Lys Thr Ile Ser Ser Val Val Asp Phe Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Gly Gly Gly Ser Gly Gly Gly Ser Gly
115 120 125
Gly Gly Ser Gly Gly Gly Ser Glu Leu Val Leu Thr Gln Ser Pro Lys
130 135 140
Phe Met Ser Thr Ser Val Gly Asp Arg Val Ser Val Thr Cys Lys Ala
145 150 155 160
Ser Gln Asn Val Gly Thr Asn Val Ala Trp Tyr Gln Gln Lys Pro Gly
165 170 175
Gln Ser Pro Lys Pro Leu Ile Tyr Ser Ala Thr Tyr Arg Asn Ser Gly
180 185 190
Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
195 200 205
Thr Ile Thr Asn Val Gln Ser Lys Asp Leu Ala Asp Tyr Phe Cys Gln
210 215 220
Tyr Asn Arg Tyr Pro Tyr Thr Ser Phe Phe Phe Thr Lys Leu Glu Ile
225 230 235 240
Lys Arg Arg Ser Lys Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp
245 250 255
Asn Glu Lys Ser Asn Gly Thr Ile Ile His Val Lys Gly Lys His Leu
260 265 270
Cys Pro Ser Pro Leu Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu
275 280 285
Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val
290 295 300
Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His
305 310 315 320
Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys
325 330 335
His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser
340 345 350
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
355 360 365
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
370 375 380
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
385 390 395 400
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
405 410 415
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
420 425 430
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
435 440 445
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
450 455 460
<210> 985
<211> 246
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 985
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Glu
245
<210> 986
<211> 439
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 986
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
245 250 255
Pro Met Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr
260 265 270
Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Lys Arg Gly
275 280 285
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
290 295 300
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Glu Glu Glu
305 310 315 320
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
325 330 335
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
340 345 350
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
355 360 365
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
370 375 380
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
385 390 395 400
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
405 410 415
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
420 425 430
Gln Ala Leu Pro Pro Arg Leu
435
<210> 987
<211> 819
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 987
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys
245 250 255
Pro Met Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr
260 265 270
Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Lys Arg Gly
275 280 285
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
290 295 300
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Glu Glu Glu
305 310 315 320
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
325 330 335
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
340 345 350
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
355 360 365
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
370 375 380
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
385 390 395 400
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
405 410 415
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
420 425 430
Gln Ala Leu Pro Pro Arg Leu Glu Gly Gly Gly Glu Gly Arg Gly Ser
435 440 445
Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro Gly Pro Arg Met Leu
450 455 460
Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro Ala Phe
465 470 475 480
Leu Leu Ile Pro Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe
485 490 495
Lys Asp Ser Leu Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn
500 505 510
Cys Thr Ser Ile Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg
515 520 525
Gly Asp Ser Phe Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp
530 535 540
Ile Leu Lys Thr Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala
545 550 555 560
Trp Pro Glu Asn Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile
565 570 575
Ile Arg Gly Arg Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val
580 585 590
Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser
595 600 605
Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn
610 615 620
Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys
625 630 635 640
Ile Ile Ser Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val
645 650 655
Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg
660 665 670
Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp
675 680 685
Lys Cys Asn Leu Leu Glu Gly Glu Pro Arg Glu Phe Val Glu Asn Ser
690 695 700
Glu Cys Ile Gln Cys His Pro Glu Cys Leu Pro Gln Ala Met Asn Ile
705 710 715 720
Thr Cys Thr Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr
725 730 735
Ile Asp Gly Pro His Cys Val Lys Thr Cys Pro Ala Gly Val Met Gly
740 745 750
Glu Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys
755 760 765
His Leu Cys His Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro Gly Leu
770 775 780
Glu Gly Cys Pro Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala Thr Gly
785 790 795 800
Met Val Gly Ala Leu Leu Leu Leu Leu Val Val Ala Leu Gly Ile Gly
805 810 815
Leu Phe Met
<210> 988
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 988
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser
245
<210> 989
<211> 467
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 989
Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile
35 40 45
Tyr His Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr Gly Ser Thr Ser Gly
100 105 110
Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr Lys Gly Glu Val Lys
115 120 125
Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser Leu Ser
130 135 140
Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser
145 150 155 160
Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly Val Ile
165 170 175
Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser Arg Leu
180 185 190
Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys Met Asn
195 200 205
Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys His Tyr
210 215 220
Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser
225 230 235 240
Val Thr Val Ser Ser Ala Ala Ala Ile Glu Val Met Tyr Pro Pro Pro
245 250 255
Tyr Leu Asp Asn Glu Lys Ser Asn Gly Thr Ile Ile His Val Lys Gly
260 265 270
Lys His Leu Cys Pro Ser Pro Leu Phe Pro Gly Pro Ser Lys Pro Phe
275 280 285
Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu Leu
290 295 300
Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser Lys Arg Ser Arg
305 310 315 320
Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro
325 330 335
Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala
340 345 350
Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
355 360 365
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
370 375 380
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
385 390 395 400
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
405 410 415
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
420 425 430
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
435 440 445
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
450 455 460
Pro Pro Arg
465
<210> 990
<211> 751
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 990
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu Ile
275 280 285
Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
290 295 300
Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
305 310 315 320
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His
325 330 335
Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly
340 345 350
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
355 360 365
Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe
370 375 380
Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
405 410 415
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
420 425 430
Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro
435 440 445
Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr
450 455 460
Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp
465 470 475 480
Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala
485 490 495
Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser
500 505 510
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
515 520 525
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
530 535 540
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
545 550 555 560
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
565 570 575
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
580 585 590
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
595 600 605
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
610 615 620
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
625 630 635 640
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
645 650 655
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
660 665 670
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
675 680 685
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
690 695 700
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
705 710 715 720
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
725 730 735
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 991
<211> 751
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 991
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu Ile
275 280 285
Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg
290 295 300
Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn
305 310 315 320
Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His
325 330 335
Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly
340 345 350
Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
355 360 365
Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe
370 375 380
Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly
405 410 415
Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val
420 425 430
Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro
435 440 445
Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr
450 455 460
Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp
465 470 475 480
Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala
485 490 495
Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser
500 505 510
Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
515 520 525
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
530 535 540
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
545 550 555 560
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
565 570 575
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
580 585 590
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
595 600 605
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
610 615 620
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
625 630 635 640
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
645 650 655
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
660 665 670
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
675 680 685
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
690 695 700
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
705 710 715 720
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
725 730 735
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 992
<211> 745
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 992
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser Pro
275 280 285
Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg
290 295 300
Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
305 310 315 320
Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser
325 330 335
Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
340 345 350
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys
355 360 365
Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu
370 375 380
Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro
405 410 415
Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro
420 425 430
Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
435 440 445
Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser
450 455 460
Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val
465 470 475 480
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
485 490 495
Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp
500 505 510
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro
515 520 525
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
530 535 540
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
545 550 555 560
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
565 570 575
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
580 585 590
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
595 600 605
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
610 615 620
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
625 630 635 640
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
645 650 655
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
660 665 670
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
675 680 685
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
690 695 700
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
705 710 715 720
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
725 730 735
Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 993
<211> 745
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 993
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser Pro
275 280 285
Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg
290 295 300
Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro
305 310 315 320
Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser
325 330 335
Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
340 345 350
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe Cys
355 360 365
Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu
370 375 380
Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
385 390 395 400
Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro
405 410 415
Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu Pro
420 425 430
Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
435 440 445
Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser Ser
450 455 460
Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln Val
465 470 475 480
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
485 490 495
Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp
500 505 510
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro
515 520 525
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
530 535 540
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
545 550 555 560
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
565 570 575
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
580 585 590
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
595 600 605
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
610 615 620
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
625 630 635 640
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
645 650 655
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
660 665 670
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
675 680 685
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
690 695 700
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
705 710 715 720
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
725 730 735
Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 994
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 994
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln Val
275 280 285
Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val
290 295 300
Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met
305 310 315 320
His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp
325 330 335
Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly
340 345 350
Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu
355 360 365
Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg
370 375 380
Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly
385 390 395 400
Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
420 425 430
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
435 440 445
Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
450 455 460
Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
465 470 475 480
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
485 490 495
Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
500 505 510
Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile
515 520 525
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 995
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 995
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln Val
275 280 285
Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val
290 295 300
Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met
305 310 315 320
His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp
325 330 335
Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly
340 345 350
Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu
355 360 365
Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg
370 375 380
Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly
385 390 395 400
Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser
420 425 430
Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser
435 440 445
Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys
450 455 460
Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val
465 470 475 480
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
485 490 495
Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln
500 505 510
Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile
515 520 525
Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 996
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 996
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser Gly
275 280 285
Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala
290 295 300
Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala
305 310 315 320
Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly
325 330 335
Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg
340 345 350
Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser
355 360 365
Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala
370 375 380
Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
385 390 395 400
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
405 410 415
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
420 425 430
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
435 440 445
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
450 455 460
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
465 470 475 480
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro
485 490 495
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
500 505 510
Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 997
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 997
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser Gly
275 280 285
Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala
290 295 300
Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln Ala
305 310 315 320
Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly
325 330 335
Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr Arg
340 345 350
Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg Ser
355 360 365
Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu Ala
370 375 380
Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser
385 390 395 400
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
405 410 415
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
420 425 430
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
435 440 445
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
450 455 460
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
465 470 475 480
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln Pro
485 490 495
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro Leu
500 505 510
Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 998
<211> 748
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 998
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu Val
275 280 285
Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
290 295 300
Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly Met
305 310 315 320
Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly
325 330 335
Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg
340 345 350
Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met
355 360 365
Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His
370 375 380
Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
385 390 395 400
Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly
405 410 415
Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
420 425 430
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
435 440 445
Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
450 455 460
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
465 470 475 480
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
485 490 495
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr
500 505 510
Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
515 520 525
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
530 535 540
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
545 550 555 560
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
565 570 575
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
580 585 590
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
595 600 605
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
610 615 620
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
625 630 635 640
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
645 650 655
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
660 665 670
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
675 680 685
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
690 695 700
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
705 710 715 720
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
725 730 735
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 999
<211> 748
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 999
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu Val
275 280 285
Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
290 295 300
Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly Met
305 310 315 320
Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly
325 330 335
Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg
340 345 350
Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met
355 360 365
Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His
370 375 380
Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser
385 390 395 400
Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly
405 410 415
Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
420 425 430
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser
435 440 445
Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu
450 455 460
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
465 470 475 480
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
485 490 495
Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr
500 505 510
Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr
515 520 525
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
530 535 540
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
545 550 555 560
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
565 570 575
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
580 585 590
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
595 600 605
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
610 615 620
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
625 630 635 640
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
645 650 655
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
660 665 670
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
675 680 685
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
690 695 700
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
705 710 715 720
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
725 730 735
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1000
<211> 742
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1000
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser Gly
275 280 285
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val
290 295 300
Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala
305 310 315 320
Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser
325 330 335
Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
340 345 350
Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu
355 360 365
Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val
370 375 380
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
405 410 415
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
420 425 430
Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr
435 440 445
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser
450 455 460
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
465 470 475 480
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
485 490 495
Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly Gln
500 505 510
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
515 520 525
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
530 535 540
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
545 550 555 560
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
565 570 575
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
580 585 590
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
595 600 605
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
610 615 620
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
625 630 635 640
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
645 650 655
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
660 665 670
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
675 680 685
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
690 695 700
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
705 710 715 720
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
725 730 735
Gln Ala Leu Pro Pro Arg
740
<210> 1001
<211> 742
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1001
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met
20 25 30
Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr
35 40 45
Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr
50 55 60
Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg
65 70 75 80
Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu Leu
85 90 95
Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser
100 105 110
Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp
115 120 125
Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met
130 135 140
Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu
145 150 155 160
Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr
165 170 175
Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile
180 185 190
His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala
195 200 205
Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu
210 215 220
Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met Glu
225 230 235 240
His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu
245 250 255
Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu Asp
260 265 270
Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser Gly
275 280 285
Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Val
290 295 300
Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg Ala
305 310 315 320
Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly Ser
325 330 335
Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp
340 345 350
Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu
355 360 365
Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp Val
370 375 380
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly Gly
385 390 395 400
Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
405 410 415
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
420 425 430
Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr
435 440 445
Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser
450 455 460
Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
465 470 475 480
Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
485 490 495
Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly Gln
500 505 510
Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro
515 520 525
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
530 535 540
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
545 550 555 560
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
565 570 575
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
580 585 590
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
595 600 605
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
610 615 620
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
625 630 635 640
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
645 650 655
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
660 665 670
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
675 680 685
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
690 695 700
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
705 710 715 720
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
725 730 735
Gln Ala Leu Pro Pro Arg
740
<210> 1002
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1002
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1003
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1003
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1004
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1004
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1005
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1005
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1006
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1006
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1007
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1007
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1008
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1008
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1009
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1009
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1010
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1010
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1011
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1011
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1012
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1012
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1013
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1013
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1014
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1014
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1015
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1015
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1016
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1016
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1017
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1017
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1018
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1018
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1019
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1019
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1020
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1020
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1021
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1021
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1022
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1022
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1023
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1023
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1024
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1024
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1025
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1025
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1026
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1026
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1027
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1027
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1028
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1028
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1029
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1029
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1030
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1030
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1031
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1031
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1032
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1032
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1033
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1033
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1034
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1034
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1035
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1035
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1036
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1036
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1037
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1037
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1038
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1038
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1039
<211> 752
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1039
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu
290 295 300
Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu
305 310 315 320
Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr
325 330 335
His Thr Ser Arg Leu His Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser
340 345 350
Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
355 360 365
Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr
370 375 380
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
385 390 395 400
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Glu Ser
405 410 415
Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr
420 425 430
Val Ser Gly Val Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln
435 440 445
Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Val Ile Trp Gly Ser Glu
450 455 460
Thr Thr Tyr Tyr Ser Ser Ser Leu Lys Ser Arg Val Thr Ile Ser Lys
465 470 475 480
Asp Asn Ser Lys Asn Gln Val Ser Leu Lys Leu Ser Ser Val Thr Ala
485 490 495
Ala Asp Thr Ala Val Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly
500 505 510
Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
515 520 525
Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
530 535 540
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
545 550 555 560
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
565 570 575
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
580 585 590
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
595 600 605
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
610 615 620
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
625 630 635 640
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
645 650 655
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
660 665 670
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
675 680 685
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
690 695 700
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
705 710 715 720
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
725 730 735
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745 750
<210> 1040
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1040
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1041
<211> 746
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1041
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Ile Val Met Thr Gln Ser
275 280 285
Pro Ala Thr Leu Ser Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys
290 295 300
Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys
305 310 315 320
Pro Gly Gln Ala Pro Arg Leu Leu Ile Tyr His Thr Ser Arg Leu His
325 330 335
Ser Gly Ile Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr
340 345 350
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Val Tyr Phe
355 360 365
Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gln Gly Thr Lys
370 375 380
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
385 390 395 400
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
405 410 415
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Val Ser Leu
420 425 430
Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu
435 440 445
Glu Trp Ile Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Ser Ser
450 455 460
Ser Leu Lys Ser Arg Val Thr Ile Ser Lys Asp Asn Ser Lys Asn Gln
465 470 475 480
Val Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr
485 490 495
Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr
500 505 510
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1042
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1042
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1043
<211> 753
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1043
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Gln
275 280 285
Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser
290 295 300
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr
305 310 315 320
Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly
325 330 335
Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln
340 345 350
Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ile Ser Thr Val Tyr Met
355 360 365
Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala
370 375 380
Arg Asp Met Asn Ile Leu Ala Thr Val Pro Phe Asp Ile Trp Gly Gln
385 390 395 400
Gly Thr Met Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly
405 410 415
Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser
420 425 430
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala
435 440 445
Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly
450 455 460
Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly
465 470 475 480
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu
485 490 495
Thr Val Asn Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln
500 505 510
Gln Gly Asp Ser Val Pro Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu
515 520 525
Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
530 535 540
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
545 550 555 560
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
565 570 575
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
580 585 590
Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr
595 600 605
Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu
610 615 620
Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu
625 630 635 640
Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln
645 650 655
Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu
660 665 670
Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly
675 680 685
Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln
690 695 700
Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu
705 710 715 720
Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr
725 730 735
Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro
740 745 750
Arg
<210> 1044
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1044
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1045
<211> 747
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1045
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Gln Val Gln Leu Val Gln Ser
275 280 285
Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys
290 295 300
Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg Gln
305 310 315 320
Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser
325 330 335
Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Leu Thr
340 345 350
Arg Asp Thr Ser Ile Ser Thr Val Tyr Met Glu Leu Ser Arg Leu Arg
355 360 365
Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Asp Met Asn Ile Leu
370 375 380
Ala Thr Val Pro Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val
385 390 395 400
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
405 410 415
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
420 425 430
Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser
435 440 445
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
450 455 460
Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser
465 470 475 480
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Asn Ser Leu Gln
485 490 495
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Gly Asp Ser Val Pro
500 505 510
Leu Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Thr Thr Thr Pro
515 520 525
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
530 535 540
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
545 550 555 560
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
565 570 575
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
580 585 590
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
595 600 605
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
610 615 620
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
625 630 635 640
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
645 650 655
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
660 665 670
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
675 680 685
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
690 695 700
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
705 710 715 720
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
725 730 735
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1046
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1046
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1047
<211> 749
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1047
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Ser Leu Gly Asp Val Gly Glu
275 280 285
Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser
290 295 300
Leu Arg Leu Ser Cys Ala Val Ser Gly Phe Ala Leu Ser Asn His Gly
305 310 315 320
Met Ser Trp Val Arg Arg Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
325 330 335
Gly Ile Val Tyr Ser Gly Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly
340 345 350
Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln
355 360 365
Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala
370 375 380
His Gly Gly Glu Ser Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
385 390 395 400
Ser Ser Ala Ser Gly Gly Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly
405 410 415
Gly Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala
420 425 430
Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile
435 440 445
Ser Ser Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys
450 455 460
Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg
465 470 475 480
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser
485 490 495
Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser
500 505 510
Thr Pro Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
515 520 525
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
530 535 540
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
545 550 555 560
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
565 570 575
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
580 585 590
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
595 600 605
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
610 615 620
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
625 630 635 640
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
645 650 655
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
660 665 670
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
675 680 685
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
690 695 700
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
705 710 715 720
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
725 730 735
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 1048
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1048
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1049
<211> 743
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1049
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln
20 25 30
Met Val Ser Ala Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu
35 40 45
Tyr Asp Pro Thr Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu
50 55 60
Thr Asn Leu Ala Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys
65 70 75 80
Arg Val Pro Gly Phe Val Asp Leu Thr Leu His Asp Gln Val His Leu
85 90 95
Leu Glu Cys Ala Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg
100 105 110
Ser Met Glu His Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu
115 120 125
Asp Arg Asn Gln Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp
130 135 140
Met Leu Leu Ala Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly
145 150 155 160
Glu Glu Phe Val Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val
165 170 175
Tyr Thr Phe Leu Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His
180 185 190
Ile His Arg Val Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met
195 200 205
Ala Lys Ala Gly Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln
210 215 220
Leu Leu Leu Ile Leu Ser His Ile Arg His Met Ser Asn Lys Arg Met
225 230 235 240
Glu His Leu Tyr Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp
245 250 255
Leu Leu Leu Glu Met Leu Asp Ala His Arg Leu Gly Thr Gly Ala Glu
260 265 270
Asp Pro Arg Pro Ser Arg Lys Arg Arg Glu Val Gln Leu Val Glu Ser
275 280 285
Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala
290 295 300
Val Ser Gly Phe Ala Leu Ser Asn His Gly Met Ser Trp Val Arg Arg
305 310 315 320
Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Gly Ile Val Tyr Ser Gly
325 330 335
Ser Thr Tyr Tyr Ala Ala Ser Val Lys Gly Arg Phe Thr Ile Ser Arg
340 345 350
Asp Asn Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Pro
355 360 365
Glu Asp Thr Ala Ile Tyr Tyr Cys Ser Ala His Gly Gly Glu Ser Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Gly Gly
385 390 395 400
Gly Gly Ser Gly Gly Arg Ala Ser Gly Gly Gly Gly Ser Asp Ile Gln
405 410 415
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
420 425 430
Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn Trp
435 440 445
Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
450 455 460
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
465 470 475 480
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
485 490 495
Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr Thr Phe Gly
500 505 510
Gln Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
515 520 525
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
530 535 540
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
545 550 555 560
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
565 570 575
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly
580 585 590
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
595 600 605
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
610 615 620
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
625 630 635 640
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
645 650 655
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
660 665 670
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
675 680 685
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
690 695 700
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
705 710 715 720
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
725 730 735
Met Gln Ala Leu Pro Pro Arg
740
<210> 1050
<211> 2253
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1050
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct ggccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgtccaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg aaccggcgcg gaagaccccc ggccctccag gaagcgaagg
840
tccctcggag acgtgggtga aattgtgatg acccagtcac ccgccactct tagcctttca
900
cccggtgagc gcgcaaccct gtcttgcaga gcctcccaag acatctcaaa ataccttaat
960
tggtatcaac agaagcccgg acaggctcct cgccttctga tctaccacac cagccggctc
1020
cattctggaa tccctgccag gttcagcggt agcggatctg ggaccgacta caccctcact
1080
atcagctcac tgcagccaga ggacttcgct gtctatttct gtcagcaagg gaacaccctg
1140
ccctacacct ttggacaggg caccaagctc gagattaaag gtggaggtgg cagcggagga
1200
ggtgggtccg gcggtggagg aagccaggtc caactccaag aaagcggacc gggtcttgtg
1260
aagccatcag aaactctttc actgacttgt actgtgagcg gagtgtctct ccccgattac
1320
ggggtgtctt ggatcagaca gccaccgggg aagggtctgg aatggattgg agtgatttgg
1380
ggctctgaga ctacttacta ctcttcatcc ctcaagtcac gcgtcaccat ctcaaaggac
1440
aactctaaga atcaggtgtc actgaaactg tcatctgtga ccgcagccga caccgccgtg
1500
tactattgcg ctaagcatta ctattatggc gggagctacg caatggatta ctggggacag
1560
ggtactctgg tcaccgtgtc cagcaccact accccagcac cgaggccacc caccccggct
1620
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
1680
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
1740
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1800
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1860
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1920
gtgaaattca gccgcagcgc agatgctcca gcctaccagc aggggcagaa ccagctctac
1980
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
2040
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
2100
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
2160
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
2220
gacgctcttc acatgcaggc cctgccgcct cgg
2253
<210> 1051
<211> 2253
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1051
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct gaccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgaacaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg aaccggcgcg gaagaccccc ggccctccag gaagcgaagg
840
tccctcggag acgtgggtga aattgtgatg acccagtcac ccgccactct tagcctttca
900
cccggtgagc gcgcaaccct gtcttgcaga gcctcccaag acatctcaaa ataccttaat
960
tggtatcaac agaagcccgg acaggctcct cgccttctga tctaccacac cagccggctc
1020
cattctggaa tccctgccag gttcagcggt agcggatctg ggaccgacta caccctcact
1080
atcagctcac tgcagccaga ggacttcgct gtctatttct gtcagcaagg gaacaccctg
1140
ccctacacct ttggacaggg caccaagctc gagattaaag gtggaggtgg cagcggagga
1200
ggtgggtccg gcggtggagg aagccaggtc caactccaag aaagcggacc gggtcttgtg
1260
aagccatcag aaactctttc actgacttgt actgtgagcg gagtgtctct ccccgattac
1320
ggggtgtctt ggatcagaca gccaccgggg aagggtctgg aatggattgg agtgatttgg
1380
ggctctgaga ctacttacta ctcttcatcc ctcaagtcac gcgtcaccat ctcaaaggac
1440
aactctaaga atcaggtgtc actgaaactg tcatctgtga ccgcagccga caccgccgtg
1500
tactattgcg ctaagcatta ctattatggc gggagctacg caatggatta ctggggacag
1560
ggtactctgg tcaccgtgtc cagcaccact accccagcac cgaggccacc caccccggct
1620
cctaccatcg cctcccagcc tctgtccctg cgtccggagg catgtagacc cgcagctggt
1680
ggggccgtgc atacccgggg tcttgacttc gcctgcgata tctacatttg ggcccctctg
1740
gctggtactt gcggggtcct gctgctttca ctcgtgatca ctctttactg taagcgcggt
1800
cggaagaagc tgctgtacat ctttaagcaa cccttcatga ggcctgtgca gactactcaa
1860
gaggaggacg gctgttcatg ccggttccca gaggaggagg aaggcggctg cgaactgcgc
1920
gtgaaattca gccgcagcgc agatgctcca gcctaccagc aggggcagaa ccagctctac
1980
aacgaactca atcttggtcg gagagaggag tacgacgtgc tggacaagcg gagaggacgg
2040
gacccagaaa tgggcgggaa gccgcgcaga aagaatcccc aagagggcct gtacaacgag
2100
ctccaaaagg ataagatggc agaagcctat agcgagattg gtatgaaagg ggaacgcaga
2160
agaggcaaag gccacgacgg actgtaccag ggactcagca ccgccaccaa ggacacctat
2220
gacgctcttc acatgcaggc cctgccgcct cgg
2253
<210> 1052
<211> 2235
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1052
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct ggccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgtccaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg gacgggagct gaagatccac gacccagcag aaagcgacgg
840
gaaattgtga tgacccagtc acccgccact cttagccttt cacccggtga gcgcgcaacc
900
ctgtcttgca gagcctccca agacatctca aaatacctta attggtatca acagaagccc
960
ggacaggctc ctcgccttct gatctaccac accagccggc tccattctgg aatccctgcc
1020
aggttcagcg gtagcggatc tgggaccgac tacaccctca ctatcagctc actgcagcca
1080
gaggacttcg ctgtctattt ctgtcagcaa gggaacaccc tgccctacac ctttggacag
1140
ggcaccaagc tcgagattaa aggtggaggt ggcagcggag gaggtgggtc cggcggtgga
1200
ggaagccagg tccaactcca agaaagcgga ccgggtcttg tgaagccatc agaaactctt
1260
tcactgactt gtactgtgag cggagtgtct ctccccgatt acggggtgtc ttggatcaga
1320
cagccaccgg ggaagggtct ggaatggatt ggagtgattt ggggctctga gactacttac
1380
tactcttcat ccctcaagtc acgcgtcacc atctcaaagg acaactctaa gaatcaggtg
1440
tcactgaaac tgtcatctgt gaccgcagcc gacaccgccg tgtactattg cgctaagcat
1500
tactattatg gcgggagcta cgcaatggat tactggggac agggtactct ggtcaccgtg
1560
tccagcacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
1620
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
1680
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
1740
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1800
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1860
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1920
gcagatgctc cagcctacca gcaggggcag aaccagctct acaacgaact caatcttggt
1980
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
2040
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
2100
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
2160
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
2220
gccctgccgc ctcgg
2235
<210> 1053
<211> 2235
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1053
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct gaccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgaacaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg gacgggagct gaagatccac gacccagcag aaagcgacgg
840
gaaattgtga tgacccagtc acccgccact cttagccttt cacccggtga gcgcgcaacc
900
ctgtcttgca gagcctccca agacatctca aaatacctta attggtatca acagaagccc
960
ggacaggctc ctcgccttct gatctaccac accagccggc tccattctgg aatccctgcc
1020
aggttcagcg gtagcggatc tgggaccgac tacaccctca ctatcagctc actgcagcca
1080
gaggacttcg ctgtctattt ctgtcagcaa gggaacaccc tgccctacac ctttggacag
1140
ggcaccaagc tcgagattaa aggtggaggt ggcagcggag gaggtgggtc cggcggtgga
1200
ggaagccagg tccaactcca agaaagcgga ccgggtcttg tgaagccatc agaaactctt
1260
tcactgactt gtactgtgag cggagtgtct ctccccgatt acggggtgtc ttggatcaga
1320
cagccaccgg ggaagggtct ggaatggatt ggagtgattt ggggctctga gactacttac
1380
tactcttcat ccctcaagtc acgcgtcacc atctcaaagg acaactctaa gaatcaggtg
1440
tcactgaaac tgtcatctgt gaccgcagcc gacaccgccg tgtactattg cgctaagcat
1500
tactattatg gcgggagcta cgcaatggat tactggggac agggtactct ggtcaccgtg
1560
tccagcacca ctaccccagc accgaggcca cccaccccgg ctcctaccat cgcctcccag
1620
cctctgtccc tgcgtccgga ggcatgtaga cccgcagctg gtggggccgt gcatacccgg
1680
ggtcttgact tcgcctgcga tatctacatt tgggcccctc tggctggtac ttgcggggtc
1740
ctgctgcttt cactcgtgat cactctttac tgtaagcgcg gtcggaagaa gctgctgtac
1800
atctttaagc aacccttcat gaggcctgtg cagactactc aagaggagga cggctgttca
1860
tgccggttcc cagaggagga ggaaggcggc tgcgaactgc gcgtgaaatt cagccgcagc
1920
gcagatgctc cagcctacca gcaggggcag aaccagctct acaacgaact caatcttggt
1980
cggagagagg agtacgacgt gctggacaag cggagaggac gggacccaga aatgggcggg
2040
aagccgcgca gaaagaatcc ccaagagggc ctgtacaacg agctccaaaa ggataagatg
2100
gcagaagcct atagcgagat tggtatgaaa ggggaacgca gaagaggcaa aggccacgac
2160
ggactgtacc agggactcag caccgccacc aaggacacct atgacgctct tcacatgcag
2220
gccctgccgc ctcgg
2235
<210> 1054
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1054
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct ggccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgtccaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg aaccggcgcg gaagaccccc ggccctccag gaagcgaagg
840
tccctcggag acgtgggtca agtgcaactc gtccaaagcg gagcggaagt caagaaaccc
900
ggagcgagcg tgaaagtgtc ctgcaaagcc tccggctaca cctttacggg ctactacatg
960
cactgggtgc gccaggcacc aggacagggt cttgaatgga tgggatggat caaccctaat
1020
tcgggcggaa ctaactacgc acagaagttc caggggagag tgactctgac tcgggatacc
1080
tccatctcaa ctgtctacat ggaactctcc cgcttgcggt cagatgatac ggcagtgtac
1140
tactgcgccc gcgacatgaa tatcctggct accgtgccgt tcgacatctg gggacagggg
1200
actatggtta ctgtctcatc gggcggtgga ggttcaggag gaggcggctc gggaggcgga
1260
ggttcggaca ttcagatgac ccagtcccca tcctctctgt cggccagcgt cggagatagg
1320
gtgaccatta cctgtcgggc ctcgcaaagc atctcctcgt acctcaactg gtatcagcaa
1380
aagccgggaa aggcgcctaa gctgctgatc tacgccgctt cgagcttgca aagcggggtg
1440
ccatccagat tctcgggatc aggctcagga accgacttca ccctgaccgt gaacagcctc
1500
cagccggagg actttgccac ttactactgc cagcagggag actccgtgcc gcttactttc
1560
ggggggggta cccgcctgga gatcaagacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1055
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1055
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct gaccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgaacaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg aaccggcgcg gaagaccccc ggccctccag gaagcgaagg
840
tccctcggag acgtgggtca agtgcaactc gtccaaagcg gagcggaagt caagaaaccc
900
ggagcgagcg tgaaagtgtc ctgcaaagcc tccggctaca cctttacggg ctactacatg
960
cactgggtgc gccaggcacc aggacagggt cttgaatgga tgggatggat caaccctaat
1020
tcgggcggaa ctaactacgc acagaagttc caggggagag tgactctgac tcgggatacc
1080
tccatctcaa ctgtctacat ggaactctcc cgcttgcggt cagatgatac ggcagtgtac
1140
tactgcgccc gcgacatgaa tatcctggct accgtgccgt tcgacatctg gggacagggg
1200
actatggtta ctgtctcatc gggcggtgga ggttcaggag gaggcggctc gggaggcgga
1260
ggttcggaca ttcagatgac ccagtcccca tcctctctgt cggccagcgt cggagatagg
1320
gtgaccatta cctgtcgggc ctcgcaaagc atctcctcgt acctcaactg gtatcagcaa
1380
aagccgggaa aggcgcctaa gctgctgatc tacgccgctt cgagcttgca aagcggggtg
1440
ccatccagat tctcgggatc aggctcagga accgacttca ccctgaccgt gaacagcctc
1500
cagccggagg actttgccac ttactactgc cagcagggag actccgtgcc gcttactttc
1560
ggggggggta cccgcctgga gatcaagacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1056
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1056
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct ggccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgtccaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg aaccggcgcg gaagaccccc ggccctccag gaagcgaagg
840
caagtgcaac tcgtccaaag cggagcggaa gtcaagaaac ccggagcgag cgtgaaagtg
900
tcctgcaaag cctccggcta cacctttacg ggctactaca tgcactgggt gcgccaggca
960
ccaggacagg gtcttgaatg gatgggatgg atcaacccta attcgggcgg aactaactac
1020
gcacagaagt tccaggggag agtgactctg actcgggata cctccatctc aactgtctac
1080
atggaactct cccgcttgcg gtcagatgat acggcagtgt actactgcgc ccgcgacatg
1140
aatatcctgg ctaccgtgcc gttcgacatc tggggacagg ggactatggt tactgtctca
1200
tcgggcggtg gaggttcagg aggaggcggc tcgggaggcg gaggttcgga cattcagatg
1260
acccagtccc catcctctct gtcggccagc gtcggagata gggtgaccat tacctgtcgg
1320
gcctcgcaaa gcatctcctc gtacctcaac tggtatcagc aaaagccggg aaaggcgcct
1380
aagctgctga tctacgccgc ttcgagcttg caaagcgggg tgccatccag attctcggga
1440
tcaggctcag gaaccgactt caccctgacc gtgaacagcc tccagccgga ggactttgcc
1500
acttactact gccagcaggg agactccgtg ccgcttactt tcgggggggg tacccgcctg
1560
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1057
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1057
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct gaccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgaacaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg gacgggagct gaagatccac gacccagcag aaagcgacgg
840
caagtgcaac tcgtccaaag cggagcggaa gtcaagaaac ccggagcgag cgtgaaagtg
900
tcctgcaaag cctccggcta cacctttacg ggctactaca tgcactgggt gcgccaggca
960
ccaggacagg gtcttgaatg gatgggatgg atcaacccta attcgggcgg aactaactac
1020
gcacagaagt tccaggggag agtgactctg actcgggata cctccatctc aactgtctac
1080
atggaactct cccgcttgcg gtcagatgat acggcagtgt actactgcgc ccgcgacatg
1140
aatatcctgg ctaccgtgcc gttcgacatc tggggacagg ggactatggt tactgtctca
1200
tcgggcggtg gaggttcagg aggaggcggc tcgggaggcg gaggttcgga cattcagatg
1260
acccagtccc catcctctct gtcggccagc gtcggagata gggtgaccat tacctgtcgg
1320
gcctcgcaaa gcatctcctc gtacctcaac tggtatcagc aaaagccggg aaaggcgcct
1380
aagctgctga tctacgccgc ttcgagcttg caaagcgggg tgccatccag attctcggga
1440
tcaggctcag gaaccgactt caccctgacc gtgaacagcc tccagccgga ggactttgcc
1500
acttactact gccagcaggg agactccgtg ccgcttactt tcgggggggg tacccgcctg
1560
gagatcaaga ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1058
<211> 2244
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1058
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct ggccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgtccaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg aaccggcgcg gaagaccccc ggccctccag gaagcgaagg
840
tccctcggag acgtgggtga agtgcaattg gtggaatcag ggggaggact tgtgcagcct
900
ggaggatcgc tgagactgtc atgtgccgtg tccggctttg ccctgtccaa ccacgggatg
960
tcctgggtcc gccgcgcgcc tggaaagggc ctcgaatggg tgtcgggtat tgtgtacagc
1020
ggtagcacct actatgccgc atccgtgaag gggagattca ccatcagccg ggacaactcc
1080
aggaacactc tgtacctcca aatgaattcg ctgaggccag aggacactgc catctactac
1140
tgctccgcgc atggcggaga gtccgacgtc tggggacagg ggaccaccgt gaccgtgtct
1200
agcgcgtccg gcggaggcgg cagcgggggt cgggcatcag ggggcggcgg atcggacatc
1260
cagctcaccc agtccccgag ctcgctgtcc gcctccgtgg gagatcgggt caccatcacg
1320
tgccgcgcca gccagtcgat ttcctcctac ctgaactggt accaacagaa gcccggaaaa
1380
gccccgaagc ttctcatcta cgccgcctcg agcctgcagt caggagtgcc ctcacggttc
1440
tccggctccg gttccggtac tgatttcacc ctgaccattt cctccctgca accggaggac
1500
ttcgctactt actactgcca gcagtcgtac tccaccccct acactttcgg acaaggcacc
1560
aaggtcgaaa tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
1620
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
1680
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
1740
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1800
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1860
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1920
agccgcagcg cagatgctcc agcctaccag caggggcaga accagctcta caacgaactc
1980
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
2040
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
2100
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
2160
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
2220
cacatgcagg ccctgccgcc tcgg
2244
<210> 1059
<211> 2244
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1059
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct gaccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgaacaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg aaccggcgcg gaagaccccc ggccctccag gaagcgaagg
840
tccctcggag acgtgggtga agtgcaattg gtggaatcag ggggaggact tgtgcagcct
900
ggaggatcgc tgagactgtc atgtgccgtg tccggctttg ccctgtccaa ccacgggatg
960
tcctgggtcc gccgcgcgcc tggaaagggc ctcgaatggg tgtcgggtat tgtgtacagc
1020
ggtagcacct actatgccgc atccgtgaag gggagattca ccatcagccg ggacaactcc
1080
aggaacactc tgtacctcca aatgaattcg ctgaggccag aggacactgc catctactac
1140
tgctccgcgc atggcggaga gtccgacgtc tggggacagg ggaccaccgt gaccgtgtct
1200
agcgcgtccg gcggaggcgg cagcgggggt cgggcatcag ggggcggcgg atcggacatc
1260
cagctcaccc agtccccgag ctcgctgtcc gcctccgtgg gagatcgggt caccatcacg
1320
tgccgcgcca gccagtcgat ttcctcctac ctgaactggt accaacagaa gcccggaaaa
1380
gccccgaagc ttctcatcta cgccgcctcg agcctgcagt caggagtgcc ctcacggttc
1440
tccggctccg gttccggtac tgatttcacc ctgaccattt cctccctgca accggaggac
1500
ttcgctactt actactgcca gcagtcgtac tccaccccct acactttcgg acaaggcacc
1560
aaggtcgaaa tcaagaccac taccccagca ccgaggccac ccaccccggc tcctaccatc
1620
gcctcccagc ctctgtccct gcgtccggag gcatgtagac ccgcagctgg tggggccgtg
1680
catacccggg gtcttgactt cgcctgcgat atctacattt gggcccctct ggctggtact
1740
tgcggggtcc tgctgctttc actcgtgatc actctttact gtaagcgcgg tcggaagaag
1800
ctgctgtaca tctttaagca acccttcatg aggcctgtgc agactactca agaggaggac
1860
ggctgttcat gccggttccc agaggaggag gaaggcggct gcgaactgcg cgtgaaattc
1920
agccgcagcg cagatgctcc agcctaccag caggggcaga accagctcta caacgaactc
1980
aatcttggtc ggagagagga gtacgacgtg ctggacaagc ggagaggacg ggacccagaa
2040
atgggcggga agccgcgcag aaagaatccc caagagggcc tgtacaacga gctccaaaag
2100
gataagatgg cagaagccta tagcgagatt ggtatgaaag gggaacgcag aagaggcaaa
2160
ggccacgacg gactgtacca gggactcagc accgccacca aggacaccta tgacgctctt
2220
cacatgcagg ccctgccgcc tcgg
2244
<210> 1060
<211> 2226
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1060
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct ggccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgtccaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg gacgggagct gaagatccac gacccagcag aaagcgacgg
840
gaagtgcaat tggtggaatc agggggagga cttgtgcagc ctggaggatc gctgagactg
900
tcatgtgccg tgtccggctt tgccctgtcc aaccacggga tgtcctgggt ccgccgcgcg
960
cctggaaagg gcctcgaatg ggtgtcgggt attgtgtaca gcggtagcac ctactatgcc
1020
gcatccgtga aggggagatt caccatcagc cgggacaact ccaggaacac tctgtacctc
1080
caaatgaatt cgctgaggcc agaggacact gccatctact actgctccgc gcatggcgga
1140
gagtccgacg tctggggaca ggggaccacc gtgaccgtgt ctagcgcgtc cggcggaggc
1200
ggcagcgggg gtcgggcatc agggggcggc ggatcggaca tccagctcac ccagtccccg
1260
agctcgctgt ccgcctccgt gggagatcgg gtcaccatca cgtgccgcgc cagccagtcg
1320
atttcctcct acctgaactg gtaccaacag aagcccggaa aagccccgaa gcttctcatc
1380
tacgccgcct cgagcctgca gtcaggagtg ccctcacggt tctccggctc cggttccggt
1440
actgatttca ccctgaccat ttcctccctg caaccggagg acttcgctac ttactactgc
1500
cagcagtcgt actccacccc ctacactttc ggacaaggca ccaaggtcga aatcaagacc
1560
actaccccag caccgaggcc acccaccccg gctcctacca tcgcctccca gcctctgtcc
1620
ctgcgtccgg aggcatgtag acccgcagct ggtggggccg tgcatacccg gggtcttgac
1680
ttcgcctgcg atatctacat ttgggcccct ctggctggta cttgcggggt cctgctgctt
1740
tcactcgtga tcactcttta ctgtaagcgc ggtcggaaga agctgctgta catctttaag
1800
caacccttca tgaggcctgt gcagactact caagaggagg acggctgttc atgccggttc
1860
ccagaggagg aggaaggcgg ctgcgaactg cgcgtgaaat tcagccgcag cgcagatgct
1920
ccagcctacc agcaggggca gaaccagctc tacaacgaac tcaatcttgg tcggagagag
1980
gagtacgacg tgctggacaa gcggagagga cgggacccag aaatgggcgg gaagccgcgc
2040
agaaagaatc cccaagaggg cctgtacaac gagctccaaa aggataagat ggcagaagcc
2100
tatagcgaga ttggtatgaa aggggaacgc agaagaggca aaggccacga cggactgtac
2160
cagggactca gcaccgccac caaggacacc tatgacgctc ttcacatgca ggccctgccg
2220
cctcgg
2226
<210> 1061
<211> 2226
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1061
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccctcgttgg cactttccct gactgccgac cagatggtgt ccgcccttct ggacgccgag
120
cctccaattc tgtactcgga gtacgatccg actcgcccgt tctccgaagc cagcatgatg
180
ggcctgttga ctaacctggc ggaccgcgag ttggtgcaca tgattaactg ggctaagcgg
240
gtgccgggct tcgtggacct gaccctgcac gaccaagtgc acctcctgga atgcgcctgg
300
atggaaatcc tcatgatcgg cctcgtgtgg agatccatgg agcatcccgg aaagctcctg
360
tttgcaccca acctcctgct tgatcgcaac cagggaaaat gcgtggaagg gggtgtcgag
420
attttcgaca tgctgctcgc cacctcttcc cggttccgga tgatgaatct gcagggagaa
480
gagttcgtgt gtctgaagtc aatcatcctg ctgaactccg gggtctatac cttcctgagc
540
tcgaccctca agtcactgga ggaaaaagac cacatccatc gcgtgctcga taagatcacc
600
gacaccctta tccatctcat ggcgaaggct ggactgaccc tgcaacagca gcaccagagg
660
ctggcccagt tgctgctgat tctgagccac atccggcaca tgtcgaacaa gaggatggaa
720
cacctgtaca gcatgaagtg caagaacgtc gtgcctctgt ccgatctgct cctggaaatg
780
ctggacgcgc acagactcgg gacgggagct gaagatccac gacccagcag aaagcgacgg
840
gaagtgcaat tggtggaatc agggggagga cttgtgcagc ctggaggatc gctgagactg
900
tcatgtgccg tgtccggctt tgccctgtcc aaccacggga tgtcctgggt ccgccgcgcg
960
cctggaaagg gcctcgaatg ggtgtcgggt attgtgtaca gcggtagcac ctactatgcc
1020
gcatccgtga aggggagatt caccatcagc cgggacaact ccaggaacac tctgtacctc
1080
caaatgaatt cgctgaggcc agaggacact gccatctact actgctccgc gcatggcgga
1140
gagtccgacg tctggggaca ggggaccacc gtgaccgtgt ctagcgcgtc cggcggaggc
1200
ggcagcgggg gtcgggcatc agggggcggc ggatcggaca tccagctcac ccagtccccg
1260
agctcgctgt ccgcctccgt gggagatcgg gtcaccatca cgtgccgcgc cagccagtcg
1320
atttcctcct acctgaactg gtaccaacag aagcccggaa aagccccgaa gcttctcatc
1380
tacgccgcct cgagcctgca gtcaggagtg ccctcacggt tctccggctc cggttccggt
1440
actgatttca ccctgaccat ttcctccctg caaccggagg acttcgctac ttactactgc
1500
cagcagtcgt actccacccc ctacactttc ggacaaggca ccaaggtcga aatcaagacc
1560
actaccccag caccgaggcc acccaccccg gctcctacca tcgcctccca gcctctgtcc
1620
ctgcgtccgg aggcatgtag acccgcagct ggtggggccg tgcatacccg gggtcttgac
1680
ttcgcctgcg atatctacat ttgggcccct ctggctggta cttgcggggt cctgctgctt
1740
tcactcgtga tcactcttta ctgtaagcgc ggtcggaaga agctgctgta catctttaag
1800
caacccttca tgaggcctgt gcagactact caagaggagg acggctgttc atgccggttc
1860
ccagaggagg aggaaggcgg ctgcgaactg cgcgtgaaat tcagccgcag cgcagatgct
1920
ccagcctacc agcaggggca gaaccagctc tacaacgaac tcaatcttgg tcggagagag
1980
gagtacgacg tgctggacaa gcggagagga cgggacccag aaatgggcgg gaagccgcgc
2040
agaaagaatc cccaagaggg cctgtacaac gagctccaaa aggataagat ggcagaagcc
2100
tatagcgaga ttggtatgaa aggggaacgc agaagaggca aaggccacga cggactgtac
2160
cagggactca gcaccgccac caaggacacc tatgacgctc ttcacatgca ggccctgccg
2220
cctcgg
2226
<210> 1062
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1062
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1063
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1063
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1064
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1064
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1065
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1065
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1066
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1066
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1067
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1067
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1068
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1068
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1069
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1069
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1070
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1070
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1071
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1071
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1072
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1072
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1073
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1073
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgattcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1074
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1074
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1075
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1075
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1076
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1076
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1077
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1077
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1078
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1078
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1079
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1079
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1080
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1080
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1081
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1081
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1082
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1082
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1083
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1083
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1084
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1084
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1085
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1085
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccaactcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1086
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1086
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1087
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1087
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1088
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1088
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1089
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1089
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1090
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1090
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1091
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1091
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1092
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1092
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1093
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1093
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1094
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1094
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1095
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1095
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1096
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1096
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1097
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1097
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
cccgagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1098
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1098
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1099
<211> 2256
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1099
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaaattgtg atgacccagt cacccgccac tcttagcctt
900
tcacccggtg agcgcgcaac cctgtcttgc agagcctccc aagacatctc aaaatacctt
960
aattggtatc aacagaagcc cggacaggct cctcgccttc tgatctacca caccagccgg
1020
ctccattctg gaatccctgc caggttcagc ggtagcggat ctgggaccga ctacaccctc
1080
actatcagct cactgcagcc agaggacttc gctgtctatt tctgtcagca agggaacacc
1140
ctgccctaca cctttggaca gggcaccaag ctcgagatta aaggtggagg tggcagcgga
1200
ggaggtgggt ccggcggtgg aggaagccag gtccaactcc aagaaagcgg accgggtctt
1260
gtgaagccat cagaaactct ttcactgact tgtactgtga gcggagtgtc tctccccgat
1320
tacggggtgt cttggatcag acagccaccg gggaagggtc tggaatggat tggagtgatt
1380
tggggctctg agactactta ctactcttca tccctcaagt cacgcgtcac catctcaaag
1440
gacaactcta agaatcaggt gtcactgaaa ctgtcatctg tgaccgcagc cgacaccgcc
1500
gtgtactatt gcgctaagca ttactattat ggcgggagct acgcaatgga ttactgggga
1560
cagggtactc tggtcaccgt gtccagcacc actaccccag caccgaggcc acccaccccg
1620
gctcctacca tcgcctccca gcctctgtcc ctgcgtccgg aggcatgtag acccgcagct
1680
ggtggggccg tgcatacccg gggtcttgac ttcgcctgcg atatctacat ttgggcccct
1740
ctggctggta cttgcggggt cctgctgctt tcactcgtga tcactcttta ctgtaagcgc
1800
ggtcggaaga agctgctgta catctttaag caacccttca tgaggcctgt gcagactact
1860
caagaggagg acggctgttc atgccggttc ccagaggagg aggaaggcgg ctgcgaactg
1920
cgcgtgaaat tcagccgcag cgcagatgct ccagcctacc agcaggggca gaaccagctc
1980
tacaacgaac tcaatcttgg tcggagagag gagtacgacg tgctggacaa gcggagagga
2040
cgggacccag aaatgggcgg gaagccgcgc agaaagaatc cccaagaggg cctgtacaac
2100
gagctccaaa aggataagat ggcagaagcc tatagcgaga ttggtatgaa aggggaacgc
2160
agaagaggca aaggccacga cggactgtac cagggactca gcaccgccac caaggacacc
2220
tatgacgctc ttcacatgca ggccctgccg cctcgg
2256
<210> 1100
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1100
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1101
<211> 2238
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1101
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaaattg tgatgaccca gtcacccgcc actcttagcc tttcacccgg tgagcgcgca
900
accctgtctt gcagagcctc ccaagacatc tcaaaatacc ttaattggta tcaacagaag
960
cccggacagg ctcctcgcct tctgatctac cacaccagcc ggctccattc tggaatccct
1020
gccaggttca gcggtagcgg atctgggacc gactacaccc tcactatcag ctcactgcag
1080
ccagaggact tcgctgtcta tttctgtcag caagggaaca ccctgcccta cacctttgga
1140
cagggcacca agctcgagat taaaggtgga ggtggcagcg gaggaggtgg gtccggcggt
1200
ggaggaagcc aggtccaact ccaagaaagc ggaccgggtc ttgtgaagcc atcagaaact
1260
ctttcactga cttgtactgt gagcggagtg tctctccccg attacggggt gtcttggatc
1320
agacagccac cggggaaggg tctggaatgg attggagtga tttggggctc tgagactact
1380
tactactctt catccctcaa gtcacgcgtc accatctcaa aggacaactc taagaatcag
1440
gtgtcactga aactgtcatc tgtgaccgca gccgacaccg ccgtgtacta ttgcgctaag
1500
cattactatt atggcgggag ctacgcaatg gattactggg gacagggtac tctggtcacc
1560
gtgtccagca ccactacccc agcaccgagg ccacccaccc cggctcctac catcgcctcc
1620
cagcctctgt ccctgcgtcc ggaggcatgt agacccgcag ctggtggggc cgtgcatacc
1680
cggggtcttg acttcgcctg cgatatctac atttgggccc ctctggctgg tacttgcggg
1740
gtcctgctgc tttcactcgt gatcactctt tactgtaagc gcggtcggaa gaagctgctg
1800
tacatcttta agcaaccctt catgaggcct gtgcagacta ctcaagagga ggacggctgt
1860
tcatgccggt tcccagagga ggaggaaggc ggctgcgaac tgcgcgtgaa attcagccgc
1920
agcgcagatg ctccagccta ccagcagggg cagaaccagc tctacaacga actcaatctt
1980
ggtcggagag aggagtacga cgtgctggac aagcggagag gacgggaccc agaaatgggc
2040
gggaagccgc gcagaaagaa tccccaagag ggcctgtaca acgagctcca aaaggataag
2100
atggcagaag cctatagcga gattggtatg aaaggggaac gcagaagagg caaaggccac
2160
gacggactgt accagggact cagcaccgcc accaaggaca cctatgacgc tcttcacatg
2220
caggccctgc cgcctcgg
2238
<210> 1102
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1102
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1103
<211> 2259
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1103
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tcaagtgcaa ctcgtccaaa gcggagcgga agtcaagaaa
900
cccggagcga gcgtgaaagt gtcctgcaaa gcctccggct acacctttac gggctactac
960
atgcactggg tgcgccaggc accaggacag ggtcttgaat ggatgggatg gatcaaccct
1020
aattcgggcg gaactaacta cgcacagaag ttccagggga gagtgactct gactcgggat
1080
acctccatct caactgtcta catggaactc tcccgcttgc ggtcagatga tacggcagtg
1140
tactactgcg cccgcgacat gaatatcctg gctaccgtgc cgttcgacat ctggggacag
1200
gggactatgg ttactgtctc atcgggcggt ggaggttcag gaggaggcgg ctcgggaggc
1260
ggaggttcgg acattcagat gacccagtcc ccatcctctc tgtcggccag cgtcggagat
1320
agggtgacca ttacctgtcg ggcctcgcaa agcatctcct cgtacctcaa ctggtatcag
1380
caaaagccgg gaaaggcgcc taagctgctg atctacgccg cttcgagctt gcaaagcggg
1440
gtgccatcca gattctcggg atcaggctca ggaaccgact tcaccctgac cgtgaacagc
1500
ctccagccgg aggactttgc cacttactac tgccagcagg gagactccgt gccgcttact
1560
ttcggggggg gtacccgcct ggagatcaag accactaccc cagcaccgag gccacccacc
1620
ccggctccta ccatcgcctc ccagcctctg tccctgcgtc cggaggcatg tagacccgca
1680
gctggtgggg ccgtgcatac ccggggtctt gacttcgcct gcgatatcta catttgggcc
1740
cctctggctg gtacttgcgg ggtcctgctg ctttcactcg tgatcactct ttactgtaag
1800
cgcggtcgga agaagctgct gtacatcttt aagcaaccct tcatgaggcc tgtgcagact
1860
actcaagagg aggacggctg ttcatgccgg ttcccagagg aggaggaagg cggctgcgaa
1920
ctgcgcgtga aattcagccg cagcgcagat gctccagcct accagcaggg gcagaaccag
1980
ctctacaacg aactcaatct tggtcggaga gaggagtacg acgtgctgga caagcggaga
2040
ggacgggacc cagaaatggg cgggaagccg cgcagaaaga atccccaaga gggcctgtac
2100
aacgagctcc aaaaggataa gatggcagaa gcctatagcg agattggtat gaaaggggaa
2160
cgcagaagag gcaaaggcca cgacggactg taccagggac tcagcaccgc caccaaggac
2220
acctatgacg ctcttcacat gcaggccctg ccgcctcgg
2259
<210> 1104
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1104
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1105
<211> 2241
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1105
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cggcaagtgc aactcgtcca aagcggagcg gaagtcaaga aacccggagc gagcgtgaaa
900
gtgtcctgca aagcctccgg ctacaccttt acgggctact acatgcactg ggtgcgccag
960
gcaccaggac agggtcttga atggatggga tggatcaacc ctaattcggg cggaactaac
1020
tacgcacaga agttccaggg gagagtgact ctgactcggg atacctccat ctcaactgtc
1080
tacatggaac tctcccgctt gcggtcagat gatacggcag tgtactactg cgcccgcgac
1140
atgaatatcc tggctaccgt gccgttcgac atctggggac aggggactat ggttactgtc
1200
tcatcgggcg gtggaggttc aggaggaggc ggctcgggag gcggaggttc ggacattcag
1260
atgacccagt ccccatcctc tctgtcggcc agcgtcggag atagggtgac cattacctgt
1320
cgggcctcgc aaagcatctc ctcgtacctc aactggtatc agcaaaagcc gggaaaggcg
1380
cctaagctgc tgatctacgc cgcttcgagc ttgcaaagcg gggtgccatc cagattctcg
1440
ggatcaggct caggaaccga cttcaccctg accgtgaaca gcctccagcc ggaggacttt
1500
gccacttact actgccagca gggagactcc gtgccgctta ctttcggggg gggtacccgc
1560
ctggagatca agaccactac cccagcaccg aggccaccca ccccggctcc taccatcgcc
1620
tcccagcctc tgtccctgcg tccggaggca tgtagacccg cagctggtgg ggccgtgcat
1680
acccggggtc ttgacttcgc ctgcgatatc tacatttggg cccctctggc tggtacttgc
1740
ggggtcctgc tgctttcact cgtgatcact ctttactgta agcgcggtcg gaagaagctg
1800
ctgtacatct ttaagcaacc cttcatgagg cctgtgcaga ctactcaaga ggaggacggc
1860
tgttcatgcc ggttcccaga ggaggaggaa ggcggctgcg aactgcgcgt gaaattcagc
1920
cgcagcgcag atgctccagc ctaccagcag gggcagaacc agctctacaa cgaactcaat
1980
cttggtcgga gagaggagta cgacgtgctg gacaagcgga gaggacggga cccagaaatg
2040
ggcgggaagc cgcgcagaaa gaatccccaa gagggcctgt acaacgagct ccaaaaggat
2100
aagatggcag aagcctatag cgagattggt atgaaagggg aacgcagaag aggcaaaggc
2160
cacgacggac tgtaccaggg actcagcacc gccaccaagg acacctatga cgctcttcac
2220
atgcaggccc tgccgcctcg g
2241
<210> 1106
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1106
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1107
<211> 2247
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1107
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cggaaccggc gcggaagacc cccggccctc caggaagcga
840
aggtccctcg gagacgtggg tgaagtgcaa ttggtggaat cagggggagg acttgtgcag
900
cctggaggat cgctgagact gtcatgtgcc gtgtccggct ttgccctgtc caaccacggg
960
atgtcctggg tccgccgcgc gcctggaaag ggcctcgaat gggtgtcggg tattgtgtac
1020
agcggtagca cctactatgc cgcatccgtg aaggggagat tcaccatcag ccgggacaac
1080
tccaggaaca ctctgtacct ccaaatgaat tcgctgaggc cagaggacac tgccatctac
1140
tactgctccg cgcatggcgg agagtccgac gtctggggac aggggaccac cgtgaccgtg
1200
tctagcgcgt ccggcggagg cggcagcggg ggtcgggcat cagggggcgg cggatcggac
1260
atccagctca cccagtcccc gagctcgctg tccgcctccg tgggagatcg ggtcaccatc
1320
acgtgccgcg ccagccagtc gatttcctcc tacctgaact ggtaccaaca gaagcccgga
1380
aaagccccga agcttctcat ctacgccgcc tcgagcctgc agtcaggagt gccctcacgg
1440
ttctccggct ccggttccgg tactgatttc accctgacca tttcctccct gcaaccggag
1500
gacttcgcta cttactactg ccagcagtcg tactccaccc cctacacttt cggacaaggc
1560
accaaggtcg aaatcaagac cactacccca gcaccgaggc cacccacccc ggctcctacc
1620
atcgcctccc agcctctgtc cctgcgtccg gaggcatgta gacccgcagc tggtggggcc
1680
gtgcataccc ggggtcttga cttcgcctgc gatatctaca tttgggcccc tctggctggt
1740
acttgcgggg tcctgctgct ttcactcgtg atcactcttt actgtaagcg cggtcggaag
1800
aagctgctgt acatctttaa gcaacccttc atgaggcctg tgcagactac tcaagaggag
1860
gacggctgtt catgccggtt cccagaggag gaggaaggcg gctgcgaact gcgcgtgaaa
1920
ttcagccgca gcgcagatgc tccagcctac cagcaggggc agaaccagct ctacaacgaa
1980
ctcaatcttg gtcggagaga ggagtacgac gtgctggaca agcggagagg acgggaccca
2040
gaaatgggcg ggaagccgcg cagaaagaat ccccaagagg gcctgtacaa cgagctccaa
2100
aaggataaga tggcagaagc ctatagcgag attggtatga aaggggaacg cagaagaggc
2160
aaaggccacg acggactgta ccagggactc agcaccgcca ccaaggacac ctatgacgct
2220
cttcacatgc aggccctgcc gcctcgg
2247
<210> 1108
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1108
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctggccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgtc caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1109
<211> 2229
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1109
atggccctcc ctgtcaccgc cctgctgctt ccgctggctc ttctgctcca cgccgctcgg
60
ccccagtcgt tggcactttc cctgactgcc gaccagatgg tgtccgccct tctggacgcc
120
gagcctccaa ttctgtactc ggagtacgat ccgactcgcc cgttctccga agccagcatg
180
atgggcctgt tgactaacct ggcggaccgc gagttggtgc acatgattaa ctgggctaag
240
cgggtgccgg gcttcgtgga cctgaccctg cacgaccaag tgcacctcct ggaatgcgcc
300
tggatggaaa tcctcatgat cggcctcgtg tggagatcca tggagcatcc cggaaagctc
360
ctgtttgcac ccaacctcct gcttgatcgc aaccagggaa aatgcgtgga agggggtgtc
420
gagattttcg acatgctgct cgccacctct tcccggttcc ggatgatgaa tctgcaggga
480
gaagagttcg tgtgtctgaa gtcaatcatc ctgctgaact ccggggtcta taccttcctg
540
agctcgaccc tcaagtcact ggaggaaaaa gaccacatcc atcgcgtgct cgataagatc
600
accgacaccc ttatccatct catggcgaag gctggactga ccctgcaaca gcagcaccag
660
aggctggccc agttgctgct gattctgagc cacatccggc acatgtcgaa caagaggatg
720
gaacacctgt acagcatgaa gtgcaagaac gtcgtgcctc tgtccgatct gctcctggaa
780
atgctggacg cgcacagact cgggacggga gctgaagatc cacgacccag cagaaagcga
840
cgggaagtgc aattggtgga atcaggggga ggacttgtgc agcctggagg atcgctgaga
900
ctgtcatgtg ccgtgtccgg ctttgccctg tccaaccacg ggatgtcctg ggtccgccgc
960
gcgcctggaa agggcctcga atgggtgtcg ggtattgtgt acagcggtag cacctactat
1020
gccgcatccg tgaaggggag attcaccatc agccgggaca actccaggaa cactctgtac
1080
ctccaaatga attcgctgag gccagaggac actgccatct actactgctc cgcgcatggc
1140
ggagagtccg acgtctgggg acaggggacc accgtgaccg tgtctagcgc gtccggcgga
1200
ggcggcagcg ggggtcgggc atcagggggc ggcggatcgg acatccagct cacccagtcc
1260
ccgagctcgc tgtccgcctc cgtgggagat cgggtcacca tcacgtgccg cgccagccag
1320
tcgatttcct cctacctgaa ctggtaccaa cagaagcccg gaaaagcccc gaagcttctc
1380
atctacgccg cctcgagcct gcagtcagga gtgccctcac ggttctccgg ctccggttcc
1440
ggtactgatt tcaccctgac catttcctcc ctgcaaccgg aggacttcgc tacttactac
1500
tgccagcagt cgtactccac cccctacact ttcggacaag gcaccaaggt cgaaatcaag
1560
accactaccc cagcaccgag gccacccacc ccggctccta ccatcgcctc ccagcctctg
1620
tccctgcgtc cggaggcatg tagacccgca gctggtgggg ccgtgcatac ccggggtctt
1680
gacttcgcct gcgatatcta catttgggcc cctctggctg gtacttgcgg ggtcctgctg
1740
ctttcactcg tgatcactct ttactgtaag cgcggtcgga agaagctgct gtacatcttt
1800
aagcaaccct tcatgaggcc tgtgcagact actcaagagg aggacggctg ttcatgccgg
1860
ttcccagagg aggaggaagg cggctgcgaa ctgcgcgtga aattcagccg cagcgcagat
1920
gctccagcct accagcaggg gcagaaccag ctctacaacg aactcaatct tggtcggaga
1980
gaggagtacg acgtgctgga caagcggaga ggacgggacc cagaaatggg cgggaagccg
2040
cgcagaaaga atccccaaga gggcctgtac aacgagctcc aaaaggataa gatggcagaa
2100
gcctatagcg agattggtat gaaaggggaa cgcagaagag gcaaaggcca cgacggactg
2160
taccagggac tcagcaccgc caccaaggac acctatgacg ctcttcacat gcaggccctg
2220
ccgcctcgg
2229
<210> 1110
<211> 735
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1110
tcgttggcac tttccctgac tgccgaccag atggtgtccg cccttctgga cgccgagcct
60
ccaattctgt actcggagta cgatccgact cgcccgttct ccgaagccag catgatgggc
120
ctgttgacta acctggcgga ccgcgagttg gtgcacatga ttaactgggc taagcgggtg
180
ccgggcttcg tggacctggc cctgcacgac caagtgcacc tcctggaatg cgcctggatg
240
gaaatcctca tgatcggcct cgtgtggaga tccatggagc atcccggaaa gctcctgttt
300
gcacccaacc tcctgcttga tcgcaaccag ggaaaatgcg tggaaggggg tgtcgagatt
360
ttcgacatgc tgctcgccac ctcttcccgg ttccggatga tgaatctgca gggagaagag
420
ttcgtgtgtc tgaagtcaat catcctgctg aactccgggg tctatacctt cctgagctcg
480
accctcaagt cactggagga aaaagaccac atccatcgcg tgctcgataa gatcaccgac
540
acccttatcc atctcatggc gaaggctgga ctgaccctgc aacagcagca ccagaggctg
600
gcccagttgc tgctgattct gagccacatc cggcacatgt cgtccaagag gatggaacac
660
ctgtacagca tgaagtgcaa gaacgtcgtg cctctgtccg atctgctcct ggaaatgctg
720
gacgcgcaca gactc
735
<210> 1111
<211> 105
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1111
acaaaaaaga agtattcatc cagtgtgcac gaccctaacg gtgaatacat gttcatgaga
60
gcagtgaaca cagccaaaaa atccagactc acagatgtga cccta
105
<210> 1112
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 1112
cgtactaaaa ga
12
<210> 1113
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 1113
aggagtaaga ggagcaggct cctgcacagt gactacatga acatgactcc ccgccgcccc
60
gggcccaccc gcaagcatta ccagccctat gccccaccac gcgacttcgc agcctatcgc
120
tcc
123
<210> 1114
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 1114
Met Gly Leu Leu Gln Leu Leu Ala Phe Ser Phe Leu Ala Leu Cys Arg
1 5 10 15
Ala Arg Val Arg Ala
20
<210> 1115
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 1115
Met Leu Leu Ala Trp Val Gln Ala Phe Leu Val Ser Asn Met Leu Leu
1 5 10 15
Ala Glu Ala Tyr Gly
20
<210> 1116
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 1116
Met Lys Phe Gln Gly Pro Leu Ala Cys Leu Leu Leu Ala Leu Cys Leu
1 5 10 15
Gly Ser Gly Glu Ala
20
<210> 1117
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 1117
Met Asp Ala Met Lys Arg Gly Leu Cys Cys Val Leu Leu Leu Cys Gly
1 5 10 15
Ala Val Phe Val Ser Pro
20
<210> 1118
<211> 35
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1118
Met Gly Thr Val Ser Ser Arg Arg Ser Trp Trp Pro Leu Pro Leu Leu
1 5 10 15
Leu Leu Leu Leu Leu Leu Leu Gly Pro Ala Gly Ala Arg Ala Gln Glu
20 25 30
Asp Glu Asp
35
<210> 1119
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 1119
Arg Ser Ser Leu Ala Leu Ser Leu Thr Ala Asp Gln Met Val Ser Ala
1 5 10 15
Leu Leu Asp Ala Glu Pro Pro Ile Leu Tyr Ser Glu Tyr Asp Pro Thr
20 25 30
Arg Pro Phe Ser Glu Ala Ser Met Met Gly Leu Leu Thr Asn Leu Ala
35 40 45
Asp Arg Glu Leu Val His Met Ile Asn Trp Ala Lys Arg Val Pro Gly
50 55 60
Phe Val Asp Leu Ala Leu His Asp Gln Val His Leu Leu Glu Cys Ala
65 70 75 80
Trp Met Glu Ile Leu Met Ile Gly Leu Val Trp Arg Ser Met Glu His
85 90 95
Pro Gly Lys Leu Leu Phe Ala Pro Asn Leu Leu Leu Asp Arg Asn Gln
100 105 110
Gly Lys Cys Val Glu Gly Gly Val Glu Ile Phe Asp Met Leu Leu Ala
115 120 125
Thr Ser Ser Arg Phe Arg Met Met Asn Leu Gln Gly Glu Glu Phe Val
130 135 140
Cys Leu Lys Ser Ile Ile Leu Leu Asn Ser Gly Val Tyr Thr Phe Leu
145 150 155 160
Ser Ser Thr Leu Lys Ser Leu Glu Glu Lys Asp His Ile His Arg Val
165 170 175
Leu Asp Lys Ile Thr Asp Thr Leu Ile His Leu Met Ala Lys Ala Gly
180 185 190
Leu Thr Leu Gln Gln Gln His Gln Arg Leu Ala Gln Leu Leu Leu Ile
195 200 205
Leu Ser His Ile Arg His Met Ser Ser Lys Arg Met Glu His Leu Tyr
210 215 220
Ser Met Lys Cys Lys Asn Val Val Pro Leu Ser Asp Leu Leu Leu Glu
225 230 235 240
Met Leu Asp Ala His Arg Leu
245
<210> 1120
<400> 1120
000
<210> 1121
<400> 1121
000
<210> 1122
<400> 1122
000
<210> 1123
<400> 1123
000
<210> 1124
<400> 1124
000
<210> 1125
<400> 1125
000
<210> 1126
<400> 1126
000
<210> 1127
<400> 1127
000
<210> 1128
<400> 1128
000
<210> 1129
<400> 1129
000
<210> 1130
<400> 1130
000
<210> 1131
<400> 1131
000
<210> 1132
<400> 1132
000
<210> 1133
<400> 1133
000
<210> 1134
<400> 1134
000
<210> 1135
<400> 1135
000
<210> 1136
<400> 1136
000
<210> 1137
<400> 1137
000
<210> 1138
<400> 1138
000
<210> 1139
<400> 1139
000
<210> 1140
<400> 1140
000
<210> 1141
<400> 1141
000
<210> 1142
<400> 1142
000
<210> 1143
<400> 1143
000
<210> 1144
<400> 1144
000
<210> 1145
<400> 1145
000
<210> 1146
<400> 1146
000
<210> 1147
<400> 1147
000
<210> 1148
<400> 1148
000
<210> 1149
<400> 1149
000
<210> 1150
<400> 1150
000
<210> 1151
<400> 1151
000
<210> 1152
<400> 1152
000
<210> 1153
<400> 1153
000
<210> 1154
<400> 1154
000
<210> 1155
<400> 1155
000
<210> 1156
<400> 1156
000
<210> 1157
<400> 1157
000
<210> 1158
<400> 1158
000
<210> 1159
<400> 1159
000
<210> 1160
<400> 1160
000
<210> 1161
<400> 1161
000
<210> 1162
<400> 1162
000
<210> 1163
<400> 1163
000
<210> 1164
<400> 1164
000
<210> 1165
<400> 1165
000
<210> 1166
<400> 1166
000
<210> 1167
<400> 1167
000
<210> 1168
<400> 1168
000
<210> 1169
<400> 1169
000
<210> 1170
<400> 1170
000
<210> 1171
<400> 1171
000
<210> 1172
<400> 1172
000
<210> 1173
<400> 1173
000
<210> 1174
<400> 1174
000
<210> 1175
<400> 1175
000
<210> 1176
<400> 1176
000
<210> 1177
<400> 1177
000
<210> 1178
<400> 1178
000
<210> 1179
<400> 1179
000
<210> 1180
<400> 1180
000
<210> 1181
<400> 1181
000
<210> 1182
<400> 1182
000
<210> 1183
<400> 1183
000
<210> 1184
<400> 1184
000
<210> 1185
<400> 1185
000
<210> 1186
<400> 1186
000
<210> 1187
<400> 1187
000
<210> 1188
<400> 1188
000
<210> 1189
<400> 1189
000
<210> 1190
<400> 1190
000
<210> 1191
<400> 1191
000
<210> 1192
<400> 1192
000
<210> 1193
<400> 1193
000
<210> 1194
<400> 1194
000
<210> 1195
<400> 1195
000
<210> 1196
<400> 1196
000
<210> 1197
<400> 1197
000
<210> 1198
<400> 1198
000
<210> 1199
<400> 1199
000
<210> 1200
<400> 1200
000
<210> 1201
<400> 1201
000
<210> 1202
<400> 1202
000
<210> 1203
<400> 1203
000
<210> 1204
<400> 1204
000
<210> 1205
<400> 1205
000
<210> 1206
<400> 1206
000
<210> 1207
<400> 1207
000
<210> 1208
<400> 1208
000
<210> 1209
<400> 1209
000
<210> 1210
<400> 1210
000
<210> 1211
<400> 1211
000
<210> 1212
<400> 1212
000
<210> 1213
<400> 1213
000
<210> 1214
<400> 1214
000
<210> 1215
<400> 1215
000
<210> 1216
<400> 1216
000
<210> 1217
<400> 1217
000
<210> 1218
<400> 1218
000
<210> 1219
<400> 1219
000
<210> 1220
<400> 1220
000
<210> 1221
<400> 1221
000
<210> 1222
<400> 1222
000
<210> 1223
<400> 1223
000
<210> 1224
<400> 1224
000
<210> 1225
<400> 1225
000
<210> 1226
<400> 1226
000
<210> 1227
<400> 1227
000
<210> 1228
<400> 1228
000
<210> 1229
<400> 1229
000
<210> 1230
<400> 1230
000
<210> 1231
<400> 1231
000
<210> 1232
<400> 1232
000
<210> 1233
<400> 1233
000
<210> 1234
<400> 1234
000
<210> 1235
<400> 1235
000
<210> 1236
<400> 1236
000
<210> 1237
<400> 1237
000
<210> 1238
<400> 1238
000
<210> 1239
<400> 1239
000
<210> 1240
<400> 1240
000
<210> 1241
<400> 1241
000
<210> 1242
<400> 1242
000
<210> 1243
<400> 1243
000
<210> 1244
<400> 1244
000
<210> 1245
<400> 1245
000
<210> 1246
<400> 1246
000
<210> 1247
<400> 1247
000
<210> 1248
<400> 1248
000
<210> 1249
<400> 1249
000
<210> 1250
<400> 1250
000
<210> 1251
<400> 1251
000
<210> 1252
<400> 1252
000
<210> 1253
<400> 1253
000
<210> 1254
<400> 1254
000
<210> 1255
<400> 1255
000
<210> 1256
<400> 1256
000
<210> 1257
<400> 1257
000
<210> 1258
<400> 1258
000
<210> 1259
<400> 1259
000
<210> 1260
<400> 1260
000
<210> 1261
<400> 1261
000
<210> 1262
<400> 1262
000
<210> 1263
<400> 1263
000
<210> 1264
<400> 1264
000
<210> 1265
<400> 1265
000
<210> 1266
<400> 1266
000
<210> 1267
<400> 1267
000
<210> 1268
<400> 1268
000
<210> 1269
<400> 1269
000
<210> 1270
<400> 1270
000
<210> 1271
<400> 1271
000
<210> 1272
<400> 1272
000
<210> 1273
<400> 1273
000
<210> 1274
<400> 1274
000
<210> 1275
<400> 1275
000
<210> 1276
<400> 1276
000
<210> 1277
<400> 1277
000
<210> 1278
<400> 1278
000
<210> 1279
<400> 1279
000
<210> 1280
<400> 1280
000
<210> 1281
<400> 1281
000
<210> 1282
<400> 1282
000
<210> 1283
<400> 1283
000
<210> 1284
<400> 1284
000
<210> 1285
<400> 1285
000
<210> 1286
<400> 1286
000
<210> 1287
<400> 1287
000
<210> 1288
<400> 1288
000
<210> 1289
<400> 1289
000
<210> 1290
<400> 1290
000
<210> 1291
<400> 1291
000
<210> 1292
<400> 1292
000
<210> 1293
<400> 1293
000
<210> 1294
<400> 1294
000
<210> 1295
<400> 1295
000
<210> 1296
<400> 1296
000
<210> 1297
<400> 1297
000
<210> 1298
<400> 1298
000
<210> 1299
<400> 1299
000
<210> 1300
<400> 1300
000
<210> 1301
<400> 1301
000
<210> 1302
<400> 1302
000
<210> 1303
<400> 1303
000
<210> 1304
<400> 1304
000
<210> 1305
<400> 1305
000
<210> 1306
<400> 1306
000
<210> 1307
<400> 1307
000
<210> 1308
<400> 1308
000
<210> 1309
<400> 1309
000
<210> 1310
<400> 1310
000
<210> 1311
<400> 1311
000
<210> 1312
<400> 1312
000
<210> 1313
<400> 1313
000
<210> 1314
<400> 1314
000
<210> 1315
<400> 1315
000
<210> 1316
<400> 1316
000
<210> 1317
<400> 1317
000
<210> 1318
<400> 1318
000
<210> 1319
<400> 1319
000
<210> 1320
<400> 1320
000
<210> 1321
<400> 1321
000
<210> 1322
<400> 1322
000
<210> 1323
<400> 1323
000
<210> 1324
<400> 1324
000
<210> 1325
<400> 1325
000
<210> 1326
<400> 1326
000
<210> 1327
<400> 1327
000
<210> 1328
<400> 1328
000
<210> 1329
<400> 1329
000
<210> 1330
<400> 1330
000
<210> 1331
<400> 1331
000
<210> 1332
<400> 1332
000
<210> 1333
<400> 1333
000
<210> 1334
<400> 1334
000
<210> 1335
<400> 1335
000
<210> 1336
<400> 1336
000
<210> 1337
<400> 1337
000
<210> 1338
<400> 1338
000
<210> 1339
<400> 1339
000
<210> 1340
<400> 1340
000
<210> 1341
<400> 1341
000
<210> 1342
<400> 1342
000
<210> 1343
<400> 1343
000
<210> 1344
<400> 1344
000
<210> 1345
<400> 1345
000
<210> 1346
<400> 1346
000
<210> 1347
<400> 1347
000
<210> 1348
<400> 1348
000
<210> 1349
<400> 1349
000
<210> 1350
<400> 1350
000
<210> 1351
<400> 1351
000
<210> 1352
<400> 1352
000
<210> 1353
<400> 1353
000
<210> 1354
<400> 1354
000
<210> 1355
<400> 1355
000
<210> 1356
<400> 1356
000
<210> 1357
<400> 1357
000
<210> 1358
<400> 1358
000
<210> 1359
<400> 1359
000
<210> 1360
<400> 1360
000
<210> 1361
<400> 1361
000
<210> 1362
<400> 1362
000
<210> 1363
<400> 1363
000
<210> 1364
<400> 1364
000
<210> 1365
<400> 1365
000
<210> 1366
<400> 1366
000
<210> 1367
<400> 1367
000
<210> 1368
<400> 1368
000
<210> 1369
<400> 1369
000
<210> 1370
<400> 1370
000
<210> 1371
<400> 1371
000
<210> 1372
<400> 1372
000
<210> 1373
<400> 1373
000
<210> 1374
<400> 1374
000
<210> 1375
<400> 1375
000
<210> 1376
<400> 1376
000
<210> 1377
<400> 1377
000
<210> 1378
<400> 1378
000
<210> 1379
<400> 1379
000
<210> 1380
<400> 1380
000
<210> 1381
<400> 1381
000
<210> 1382
<400> 1382
000
<210> 1383
<400> 1383
000
<210> 1384
<400> 1384
000
<210> 1385
<400> 1385
000
<210> 1386
<400> 1386
000
<210> 1387
<400> 1387
000
<210> 1388
<400> 1388
000
<210> 1389
<400> 1389
000
<210> 1390
<400> 1390
000
<210> 1391
<400> 1391
000
<210> 1392
<400> 1392
000
<210> 1393
<400> 1393
000
<210> 1394
<400> 1394
000
<210> 1395
<400> 1395
000
<210> 1396
<400> 1396
000
<210> 1397
<400> 1397
000
<210> 1398
<400> 1398
000
<210> 1399
<400> 1399
000
<210> 1400
<400> 1400
000
<210> 1401
<400> 1401
000
<210> 1402
<400> 1402
000
<210> 1403
<400> 1403
000
<210> 1404
<400> 1404
000
<210> 1405
<400> 1405
000
<210> 1406
<400> 1406
000
<210> 1407
<400> 1407
000
<210> 1408
<400> 1408
000
<210> 1409
<400> 1409
000
<210> 1410
<400> 1410
000
<210> 1411
<400> 1411
000
<210> 1412
<400> 1412
000
<210> 1413
<400> 1413
000
<210> 1414
<400> 1414
000
<210> 1415
<400> 1415
000
<210> 1416
<400> 1416
000
<210> 1417
<400> 1417
000
<210> 1418
<400> 1418
000
<210> 1419
<400> 1419
000
<210> 1420
<400> 1420
000
<210> 1421
<400> 1421
000
<210> 1422
<400> 1422
000
<210> 1423
<400> 1423
000
<210> 1424
<400> 1424
000
<210> 1425
<400> 1425
000
<210> 1426
<400> 1426
000
<210> 1427
<400> 1427
000
<210> 1428
<400> 1428
000
<210> 1429
<400> 1429
000
<210> 1430
<400> 1430
000
<210> 1431
<400> 1431
000
<210> 1432
<400> 1432
000
<210> 1433
<400> 1433
000
<210> 1434
<400> 1434
000
<210> 1435
<400> 1435
000
<210> 1436
<400> 1436
000
<210> 1437
<400> 1437
000
<210> 1438
<400> 1438
000
<210> 1439
<400> 1439
000
<210> 1440
<400> 1440
000
<210> 1441
<400> 1441
000
<210> 1442
<400> 1442
000
<210> 1443
<400> 1443
000
<210> 1444
<400> 1444
000
<210> 1445
<400> 1445
000
<210> 1446
<400> 1446
000
<210> 1447
<400> 1447
000
<210> 1448
<400> 1448
000
<210> 1449
<400> 1449
000
<210> 1450
<400> 1450
000
<210> 1451
<400> 1451
000
<210> 1452
<400> 1452
000
<210> 1453
<400> 1453
000
<210> 1454
<400> 1454
000
<210> 1455
<400> 1455
000
<210> 1456
<400> 1456
000
<210> 1457
<400> 1457
000
<210> 1458
<400> 1458
000
<210> 1459
<400> 1459
000
<210> 1460
<400> 1460
000
<210> 1461
<400> 1461
000
<210> 1462
<400> 1462
000
<210> 1463
<400> 1463
000
<210> 1464
<400> 1464
000
<210> 1465
<400> 1465
000
<210> 1466
<400> 1466
000
<210> 1467
<400> 1467
000
<210> 1468
<400> 1468
000
<210> 1469
<400> 1469
000
<210> 1470
<400> 1470
000
<210> 1471
<400> 1471
000
<210> 1472
<400> 1472
000
<210> 1473
<400> 1473
000
<210> 1474
<400> 1474
000
<210> 1475
<400> 1475
000
<210> 1476
<400> 1476
000
<210> 1477
<400> 1477
000
<210> 1478
<400> 1478
000
<210> 1479
<400> 1479
000
<210> 1480
<400> 1480
000
<210> 1481
<400> 1481
000
<210> 1482
<400> 1482
000
<210> 1483
<400> 1483
000
<210> 1484
<400> 1484
000
<210> 1485
<400> 1485
000
<210> 1486
<400> 1486
000
<210> 1487
<400> 1487
000
<210> 1488
<400> 1488
000
<210> 1489
<400> 1489
000
<210> 1490
<400> 1490
000
<210> 1491
<400> 1491
000
<210> 1492
<400> 1492
000
<210> 1493
<400> 1493
000
<210> 1494
<400> 1494
000
<210> 1495
<400> 1495
000
<210> 1496
<400> 1496
000
<210> 1497
<400> 1497
000
<210> 1498
<400> 1498
000
<210> 1499
<400> 1499
000
<210> 1500
<400> 1500
000
<210> 1501
<400> 1501
000
<210> 1502
<400> 1502
000
<210> 1503
<400> 1503
000
<210> 1504
<400> 1504
000
<210> 1505
<400> 1505
000
<210> 1506
<400> 1506
000
<210> 1507
<400> 1507
000
<210> 1508
<400> 1508
000
<210> 1509
<400> 1509
000
<210> 1510
<400> 1510
000
<210> 1511
<400> 1511
000
<210> 1512
<400> 1512
000
<210> 1513
<400> 1513
000
<210> 1514
<400> 1514
000
<210> 1515
<400> 1515
000
<210> 1516
<400> 1516
000
<210> 1517
<400> 1517
000
<210> 1518
<400> 1518
000
<210> 1519
<400> 1519
000
<210> 1520
<400> 1520
000
<210> 1521
<400> 1521
000
<210> 1522
<400> 1522
000
<210> 1523
<400> 1523
000
<210> 1524
<400> 1524
000
<210> 1525
<400> 1525
000
<210> 1526
<400> 1526
000
<210> 1527
<400> 1527
000
<210> 1528
<400> 1528
000
<210> 1529
<400> 1529
000
<210> 1530
<400> 1530
000
<210> 1531
<400> 1531
000
<210> 1532
<400> 1532
000
<210> 1533
<400> 1533
000
<210> 1534
<400> 1534
000
<210> 1535
<400> 1535
000
<210> 1536
<400> 1536
000
<210> 1537
<400> 1537
000
<210> 1538
<400> 1538
000
<210> 1539
<400> 1539
000
<210> 1540
<400> 1540
000
<210> 1541
<400> 1541
000
<210> 1542
<400> 1542
000
<210> 1543
<400> 1543
000
<210> 1544
<400> 1544
000
<210> 1545
<400> 1545
000
<210> 1546
<400> 1546
000
<210> 1547
<400> 1547
000
<210> 1548
<400> 1548
000
<210> 1549
<400> 1549
000
<210> 1550
<400> 1550
000
<210> 1551
<400> 1551
000
<210> 1552
<400> 1552
000
<210> 1553
<400> 1553
000
<210> 1554
<400> 1554
000
<210> 1555
<400> 1555
000
<210> 1556
<400> 1556
000
<210> 1557
<400> 1557
000
<210> 1558
<400> 1558
000
<210> 1559
<400> 1559
000
<210> 1560
<400> 1560
000
<210> 1561
<400> 1561
000
<210> 1562
<400> 1562
000
<210> 1563
<400> 1563
000
<210> 1564
<400> 1564
000
<210> 1565
<400> 1565
000
<210> 1566
<400> 1566
000
<210> 1567
<400> 1567
000
<210> 1568
<400> 1568
000
<210> 1569
<400> 1569
000
<210> 1570
<400> 1570
000
<210> 1571
<400> 1571
000
<210> 1572
<400> 1572
000
<210> 1573
<400> 1573
000
<210> 1574
<400> 1574
000
<210> 1575
<400> 1575
000
<210> 1576
<400> 1576
000
<210> 1577
<400> 1577
000
<210> 1578
<400> 1578
000
<210> 1579
<400> 1579
000
<210> 1580
<400> 1580
000
<210> 1581
<400> 1581
000
<210> 1582
<400> 1582
000
<210> 1583
<400> 1583
000
<210> 1584
<400> 1584
000
<210> 1585
<400> 1585
000
<210> 1586
<400> 1586
000
<210> 1587
<400> 1587
000
<210> 1588
<400> 1588
000
<210> 1589
<400> 1589
000
<210> 1590
<400> 1590
000
<210> 1591
<400> 1591
000
<210> 1592
<400> 1592
000
<210> 1593
<400> 1593
000
<210> 1594
<400> 1594
000
<210> 1595
<400> 1595
000
<210> 1596
<400> 1596
000
<210> 1597
<400> 1597
000
<210> 1598
<400> 1598
000
<210> 1599
<400> 1599
000
<210> 1600
<400> 1600
000
<210> 1601
<400> 1601
000
<210> 1602
<400> 1602
000
<210> 1603
<400> 1603
000
<210> 1604
<400> 1604
000
<210> 1605
<400> 1605
000
<210> 1606
<400> 1606
000
<210> 1607
<400> 1607
000
<210> 1608
<400> 1608
000
<210> 1609
<400> 1609
000
<210> 1610
<400> 1610
000
<210> 1611
<400> 1611
000
<210> 1612
<400> 1612
000
<210> 1613
<400> 1613
000
<210> 1614
<400> 1614
000
<210> 1615
<400> 1615
000
<210> 1616
<400> 1616
000
<210> 1617
<400> 1617
000
<210> 1618
<400> 1618
000
<210> 1619
<400> 1619
000
<210> 1620
<400> 1620
000
<210> 1621
<400> 1621
000
<210> 1622
<400> 1622
000
<210> 1623
<400> 1623
000
<210> 1624
<400> 1624
000
<210> 1625
<400> 1625
000
<210> 1626
<400> 1626
000
<210> 1627
<400> 1627
000
<210> 1628
<400> 1628
000
<210> 1629
<400> 1629
000
<210> 1630
<400> 1630
000
<210> 1631
<400> 1631
000
<210> 1632
<400> 1632
000
<210> 1633
<400> 1633
000
<210> 1634
<400> 1634
000
<210> 1635
<400> 1635
000
<210> 1636
<400> 1636
000
<210> 1637
<400> 1637
000
<210> 1638
<400> 1638
000
<210> 1639
<400> 1639
000
<210> 1640
<400> 1640
000
<210> 1641
<400> 1641
000
<210> 1642
<400> 1642
000
<210> 1643
<400> 1643
000
<210> 1644
<400> 1644
000
<210> 1645
<400> 1645
000
<210> 1646
<400> 1646
000
<210> 1647
<400> 1647
000
<210> 1648
<400> 1648
000
<210> 1649
<400> 1649
000
<210> 1650
<400> 1650
000
<210> 1651
<400> 1651
000
<210> 1652
<400> 1652
000
<210> 1653
<400> 1653
000
<210> 1654
<400> 1654
000
<210> 1655
<400> 1655
000
<210> 1656
<400> 1656
000
<210> 1657
<400> 1657
000
<210> 1658
<400> 1658
000
<210> 1659
<400> 1659
000
<210> 1660
<400> 1660
000
<210> 1661
<400> 1661
000
<210> 1662
<400> 1662
000
<210> 1663
<400> 1663
000
<210> 1664
<400> 1664
000
<210> 1665
<400> 1665
000
<210> 1666
<400> 1666
000
<210> 1667
<400> 1667
000
<210> 1668
<400> 1668
000
<210> 1669
<400> 1669
000
<210> 1670
<400> 1670
000
<210> 1671
<400> 1671
000
<210> 1672
<400> 1672
000
<210> 1673
<400> 1673
000
<210> 1674
<400> 1674
000
<210> 1675
<400> 1675
000
<210> 1676
<400> 1676
000
<210> 1677
<400> 1677
000
<210> 1678
<400> 1678
000
<210> 1679
<400> 1679
000
<210> 1680
<400> 1680
000
<210> 1681
<400> 1681
000
<210> 1682
<400> 1682
000
<210> 1683
<400> 1683
000
<210> 1684
<400> 1684
000
<210> 1685
<400> 1685
000
<210> 1686
<400> 1686
000
<210> 1687
<400> 1687
000
<210> 1688
<400> 1688
000
<210> 1689
<400> 1689
000
<210> 1690
<400> 1690
000
<210> 1691
<400> 1691
000
<210> 1692
<400> 1692
000
<210> 1693
<400> 1693
000
<210> 1694
<400> 1694
000
<210> 1695
<400> 1695
000
<210> 1696
<400> 1696
000
<210> 1697
<400> 1697
000
<210> 1698
<400> 1698
000
<210> 1699
<400> 1699
000
<210> 1700
<400> 1700
000
<210> 1701
<400> 1701
000
<210> 1702
<400> 1702
000
<210> 1703
<400> 1703
000
<210> 1704
<400> 1704
000
<210> 1705
<400> 1705
000
<210> 1706
<400> 1706
000
<210> 1707
<400> 1707
000
<210> 1708
<400> 1708
000
<210> 1709
<400> 1709
000
<210> 1710
<400> 1710
000
<210> 1711
<400> 1711
000
<210> 1712
<400> 1712
000
<210> 1713
<400> 1713
000
<210> 1714
<400> 1714
000
<210> 1715
<400> 1715
000
<210> 1716
<400> 1716
000
<210> 1717
<400> 1717
000
<210> 1718
<400> 1718
000
<210> 1719
<400> 1719
000
<210> 1720
<400> 1720
000
<210> 1721
<400> 1721
000
<210> 1722
<400> 1722
000
<210> 1723
<400> 1723
000
<210> 1724
<400> 1724
000
<210> 1725
<400> 1725
000
<210> 1726
<400> 1726
000
<210> 1727
<400> 1727
000
<210> 1728
<400> 1728
000
<210> 1729
<400> 1729
000
<210> 1730
<400> 1730
000
<210> 1731
<400> 1731
000
<210> 1732
<400> 1732
000
<210> 1733
<400> 1733
000
<210> 1734
<400> 1734
000
<210> 1735
<400> 1735
000
<210> 1736
<400> 1736
000
<210> 1737
<400> 1737
000
<210> 1738
<400> 1738
000
<210> 1739
<400> 1739
000
<210> 1740
<400> 1740
000
<210> 1741
<400> 1741
000
<210> 1742
<400> 1742
000
<210> 1743
<400> 1743
000
<210> 1744
<400> 1744
000
<210> 1745
<400> 1745
000
<210> 1746
<400> 1746
000
<210> 1747
<400> 1747
000
<210> 1748
<400> 1748
000
<210> 1749
<400> 1749
000
<210> 1750
<400> 1750
000
<210> 1751
<400> 1751
000
<210> 1752
<400> 1752
000
<210> 1753
<400> 1753
000
<210> 1754
<400> 1754
000
<210> 1755
<400> 1755
000
<210> 1756
<400> 1756
000
<210> 1757
<400> 1757
000
<210> 1758
<400> 1758
000
<210> 1759
<400> 1759
000
<210> 1760
<400> 1760
000
<210> 1761
<400> 1761
000
<210> 1762
<400> 1762
000
<210> 1763
<400> 1763
000
<210> 1764
<400> 1764
000
<210> 1765
<400> 1765
000
<210> 1766
<400> 1766
000
<210> 1767
<400> 1767
000
<210> 1768
<400> 1768
000
<210> 1769
<400> 1769
000
<210> 1770
<400> 1770
000
<210> 1771
<400> 1771
000
<210> 1772
<400> 1772
000
<210> 1773
<400> 1773
000
<210> 1774
<400> 1774
000
<210> 1775
<400> 1775
000
<210> 1776
<400> 1776
000
<210> 1777
<400> 1777
000
<210> 1778
<400> 1778
000
<210> 1779
<400> 1779
000
<210> 1780
<400> 1780
000
<210> 1781
<400> 1781
000
<210> 1782
<400> 1782
000
<210> 1783
<400> 1783
000
<210> 1784
<400> 1784
000
<210> 1785
<400> 1785
000
<210> 1786
<400> 1786
000
<210> 1787
<400> 1787
000
<210> 1788
<400> 1788
000
<210> 1789
<400> 1789
000
<210> 1790
<400> 1790
000
<210> 1791
<400> 1791
000
<210> 1792
<400> 1792
000
<210> 1793
<400> 1793
000
<210> 1794
<400> 1794
000
<210> 1795
<400> 1795
000
<210> 1796
<400> 1796
000
<210> 1797
<400> 1797
000
<210> 1798
<400> 1798
000
<210> 1799
<400> 1799
000
<210> 1800
<400> 1800
000
<210> 1801
<400> 1801
000
<210> 1802
<400> 1802
000
<210> 1803
<400> 1803
000
<210> 1804
<400> 1804
000
<210> 1805
<400> 1805
000
<210> 1806
<400> 1806
000
<210> 1807
<400> 1807
000
<210> 1808
<400> 1808
000
<210> 1809
<400> 1809
000
<210> 1810
<400> 1810
000
<210> 1811
<400> 1811
000
<210> 1812
<400> 1812
000
<210> 1813
<400> 1813
000
<210> 1814
<400> 1814
000
<210> 1815
<400> 1815
000
<210> 1816
<400> 1816
000
<210> 1817
<400> 1817
000
<210> 1818
<400> 1818
000
<210> 1819
<400> 1819
000
<210> 1820
<400> 1820
000
<210> 1821
<400> 1821
000
<210> 1822
<400> 1822
000
<210> 1823
<400> 1823
000
<210> 1824
<400> 1824
000
<210> 1825
<400> 1825
000
<210> 1826
<400> 1826
000
<210> 1827
<400> 1827
000
<210> 1828
<400> 1828
000
<210> 1829
<400> 1829
000
<210> 1830
<400> 1830
000
<210> 1831
<400> 1831
000
<210> 1832
<400> 1832
000
<210> 1833
<400> 1833
000
<210> 1834
<400> 1834
000
<210> 1835
<400> 1835
000
<210> 1836
<400> 1836
000
<210> 1837
<400> 1837
000
<210> 1838
<400> 1838
000
<210> 1839
<400> 1839
000
<210> 1840
<400> 1840
000
<210> 1841
<400> 1841
000
<210> 1842
<400> 1842
000
<210> 1843
<400> 1843
000
<210> 1844
<400> 1844
000
<210> 1845
<400> 1845
000
<210> 1846
<400> 1846
000
<210> 1847
<400> 1847
000
<210> 1848
<400> 1848
000
<210> 1849
<400> 1849
000
<210> 1850
<400> 1850
000
<210> 1851
<400> 1851
000
<210> 1852
<400> 1852
000
<210> 1853
<400> 1853
000
<210> 1854
<400> 1854
000
<210> 1855
<400> 1855
000
<210> 1856
<400> 1856
000
<210> 1857
<400> 1857
000
<210> 1858
<400> 1858
000
<210> 1859
<400> 1859
000
<210> 1860
<400> 1860
000
<210> 1861
<400> 1861
000
<210> 1862
<400> 1862
000
<210> 1863
<400> 1863
000
<210> 1864
<400> 1864
000
<210> 1865
<400> 1865
000
<210> 1866
<400> 1866
000
<210> 1867
<400> 1867
000
<210> 1868
<400> 1868
000
<210> 1869
<400> 1869
000
<210> 1870
<400> 1870
000
<210> 1871
<400> 1871
000
<210> 1872
<400> 1872
000
<210> 1873
<400> 1873
000
<210> 1874
<400> 1874
000
<210> 1875
<400> 1875
000
<210> 1876
<400> 1876
000
<210> 1877
<400> 1877
000
<210> 1878
<400> 1878
000
<210> 1879
<400> 1879
000
<210> 1880
<400> 1880
000
<210> 1881
<400> 1881
000
<210> 1882
<400> 1882
000
<210> 1883
<400> 1883
000
<210> 1884
<400> 1884
000
<210> 1885
<400> 1885
000
<210> 1886
<400> 1886
000
<210> 1887
<400> 1887
000
<210> 1888
<400> 1888
000
<210> 1889
<400> 1889
000
<210> 1890
<400> 1890
000
<210> 1891
<400> 1891
000
<210> 1892
<400> 1892
000
<210> 1893
<400> 1893
000
<210> 1894
<400> 1894
000
<210> 1895
<400> 1895
000
<210> 1896
<400> 1896
000
<210> 1897
<400> 1897
000
<210> 1898
<400> 1898
000
<210> 1899
<400> 1899
000
<210> 1900
<400> 1900
000
<210> 1901
<400> 1901
000
<210> 1902
<400> 1902
000
<210> 1903
<400> 1903
000
<210> 1904
<400> 1904
000
<210> 1905
<400> 1905
000
<210> 1906
<400> 1906
000
<210> 1907
<400> 1907
000
<210> 1908
<400> 1908
000
<210> 1909
<400> 1909
000
<210> 1910
<400> 1910
000
<210> 1911
<400> 1911
000
<210> 1912
<400> 1912
000
<210> 1913
<400> 1913
000
<210> 1914
<400> 1914
000
<210> 1915
<400> 1915
000
<210> 1916
<400> 1916
000
<210> 1917
<400> 1917
000
<210> 1918
<400> 1918
000
<210> 1919
<400> 1919
000
<210> 1920
<400> 1920
000
<210> 1921
<400> 1921
000
<210> 1922
<400> 1922
000
<210> 1923
<400> 1923
000
<210> 1924
<400> 1924
000
<210> 1925
<400> 1925
000
<210> 1926
<400> 1926
000
<210> 1927
<400> 1927
000
<210> 1928
<400> 1928
000
<210> 1929
<400> 1929
000
<210> 1930
<400> 1930
000
<210> 1931
<400> 1931
000
<210> 1932
<400> 1932
000
<210> 1933
<400> 1933
000
<210> 1934
<400> 1934
000
<210> 1935
<400> 1935
000
<210> 1936
<400> 1936
000
<210> 1937
<400> 1937
000
<210> 1938
<400> 1938
000
<210> 1939
<400> 1939
000
<210> 1940
<400> 1940
000
<210> 1941
<400> 1941
000
<210> 1942
<400> 1942
000
<210> 1943
<400> 1943
000
<210> 1944
<400> 1944
000
<210> 1945
<400> 1945
000
<210> 1946
<400> 1946
000
<210> 1947
<400> 1947
000
<210> 1948
<400> 1948
000
<210> 1949
<400> 1949
000
<210> 1950
<400> 1950
000
<210> 1951
<400> 1951
000
<210> 1952
<400> 1952
000
<210> 1953
<400> 1953
000
<210> 1954
<400> 1954
000
<210> 1955
<400> 1955
000
<210> 1956
<400> 1956
000
<210> 1957
<400> 1957
000
<210> 1958
<400> 1958
000
<210> 1959
<400> 1959
000
<210> 1960
<400> 1960
000
<210> 1961
<400> 1961
000
<210> 1962
<400> 1962
000
<210> 1963
<400> 1963
000
<210> 1964
<400> 1964
000
<210> 1965
<400> 1965
000
<210> 1966
<400> 1966
000
<210> 1967
<400> 1967
000
<210> 1968
<400> 1968
000
<210> 1969
<400> 1969
000
<210> 1970
<400> 1970
000
<210> 1971
<400> 1971
000
<210> 1972
<400> 1972
000
<210> 1973
<400> 1973
000
<210> 1974
<400> 1974
000
<210> 1975
<400> 1975
000
<210> 1976
<400> 1976
000
<210> 1977
<400> 1977
000
<210> 1978
<400> 1978
000
<210> 1979
<400> 1979
000
<210> 1980
<400> 1980
000
<210> 1981
<400> 1981
000
<210> 1982
<400> 1982
000
<210> 1983
<400> 1983
000
<210> 1984
<400> 1984
000
<210> 1985
<400> 1985
000
<210> 1986
<400> 1986
000
<210> 1987
<400> 1987
000
<210> 1988
<400> 1988
000
<210> 1989
<400> 1989
000
<210> 1990
<400> 1990
000
<210> 1991
<400> 1991
000
<210> 1992
<400> 1992
000
<210> 1993
<400> 1993
000
<210> 1994
<400> 1994
000
<210> 1995
<400> 1995
000
<210> 1996
<400> 1996
000
<210> 1997
<400> 1997
000
<210> 1998
<400> 1998
000
<210> 1999
<400> 1999
000
<210> 2000
<400> 2000
000
<210> 2001
<400> 2001
000
<210> 2002
<400> 2002
000
<210> 2003
<400> 2003
000
<210> 2004
<400> 2004
000
<210> 2005
<400> 2005
000
<210> 2006
<400> 2006
000
<210> 2007
<400> 2007
000
<210> 2008
<400> 2008
000
<210> 2009
<400> 2009
000
<210> 2010
<400> 2010
000
<210> 2011
<400> 2011
000
<210> 2012
<400> 2012
000
<210> 2013
<400> 2013
000
<210> 2014
<400> 2014
000
<210> 2015
<400> 2015
000
<210> 2016
<400> 2016
000
<210> 2017
<400> 2017
000
<210> 2018
<400> 2018
000
<210> 2019
<400> 2019
000
<210> 2020
<400> 2020
000
<210> 2021
<400> 2021
000
<210> 2022
<400> 2022
000
<210> 2023
<400> 2023
000
<210> 2024
<400> 2024
000
<210> 2025
<400> 2025
000
<210> 2026
<400> 2026
000
<210> 2027
<400> 2027
000
<210> 2028
<400> 2028
000
<210> 2029
<400> 2029
000
<210> 2030
<400> 2030
000
<210> 2031
<400> 2031
000
<210> 2032
<400> 2032
000
<210> 2033
<400> 2033
000
<210> 2034
<400> 2034
000
<210> 2035
<400> 2035
000
<210> 2036
<400> 2036
000
<210> 2037
<400> 2037
000
<210> 2038
<400> 2038
000
<210> 2039
<400> 2039
000
<210> 2040
<400> 2040
000
<210> 2041
<400> 2041
000
<210> 2042
<400> 2042
000
<210> 2043
<400> 2043
000
<210> 2044
<400> 2044
000
<210> 2045
<400> 2045
000
<210> 2046
<400> 2046
000
<210> 2047
<400> 2047
000
<210> 2048
<400> 2048
000
<210> 2049
<400> 2049
000
<210> 2050
<400> 2050
000
<210> 2051
<400> 2051
000
<210> 2052
<400> 2052
000
<210> 2053
<400> 2053
000
<210> 2054
<400> 2054
000
<210> 2055
<400> 2055
000
<210> 2056
<400> 2056
000
<210> 2057
<400> 2057
000
<210> 2058
<400> 2058
000
<210> 2059
<400> 2059
000
<210> 2060
<400> 2060
000
<210> 2061
<400> 2061
000
<210> 2062
<400> 2062
000
<210> 2063
<400> 2063
000
<210> 2064
<400> 2064
000
<210> 2065
<400> 2065
000
<210> 2066
<400> 2066
000
<210> 2067
<400> 2067
000
<210> 2068
<400> 2068
000
<210> 2069
<400> 2069
000
<210> 2070
<400> 2070
000
<210> 2071
<400> 2071
000
<210> 2072
<400> 2072
000
<210> 2073
<400> 2073
000
<210> 2074
<400> 2074
000
<210> 2075
<400> 2075
000
<210> 2076
<400> 2076
000
<210> 2077
<400> 2077
000
<210> 2078
<400> 2078
000
<210> 2079
<400> 2079
000
<210> 2080
<400> 2080
000
<210> 2081
<400> 2081
000
<210> 2082
<400> 2082
000
<210> 2083
<400> 2083
000
<210> 2084
<400> 2084
000
<210> 2085
<400> 2085
000
<210> 2086
<400> 2086
000
<210> 2087
<400> 2087
000
<210> 2088
<400> 2088
000
<210> 2089
<400> 2089
000
<210> 2090
<400> 2090
000
<210> 2091
<400> 2091
000
<210> 2092
<400> 2092
000
<210> 2093
<400> 2093
000
<210> 2094
<400> 2094
000
<210> 2095
<400> 2095
000
<210> 2096
<400> 2096
000
<210> 2097
<400> 2097
000
<210> 2098
<400> 2098
000
<210> 2099
<400> 2099
000
<210> 2100
<400> 2100
000
<210> 2101
<400> 2101
000
<210> 2102
<400> 2102
000
<210> 2103
<400> 2103
000
<210> 2104
<400> 2104
000
<210> 2105
<400> 2105
000
<210> 2106
<400> 2106
000
<210> 2107
<400> 2107
000
<210> 2108
<400> 2108
000
<210> 2109
<400> 2109
000
<210> 2110
<400> 2110
000
<210> 2111
<400> 2111
000
<210> 2112
<400> 2112
000
<210> 2113
<400> 2113
000
<210> 2114
<400> 2114
000
<210> 2115
<400> 2115
000
<210> 2116
<400> 2116
000
<210> 2117
<400> 2117
000
<210> 2118
<400> 2118
000
<210> 2119
<400> 2119
000
<210> 2120
<400> 2120
000
<210> 2121
<400> 2121
000
<210> 2122
<400> 2122
000
<210> 2123
<400> 2123
000
<210> 2124
<400> 2124
000
<210> 2125
<400> 2125
000
<210> 2126
<400> 2126
000
<210> 2127
<400> 2127
000
<210> 2128
<400> 2128
000
<210> 2129
<400> 2129
000
<210> 2130
<400> 2130
000
<210> 2131
<400> 2131
000
<210> 2132
<400> 2132
000
<210> 2133
<400> 2133
000
<210> 2134
<400> 2134
000
<210> 2135
<400> 2135
000
<210> 2136
<400> 2136
000
<210> 2137
<400> 2137
000
<210> 2138
<400> 2138
000
<210> 2139
<400> 2139
000
<210> 2140
<400> 2140
000
<210> 2141
<400> 2141
000
<210> 2142
<400> 2142
000
<210> 2143
<400> 2143
000
<210> 2144
<400> 2144
000
<210> 2145
<400> 2145
000
<210> 2146
<400> 2146
000
<210> 2147
<400> 2147
000
<210> 2148
<400> 2148
000
<210> 2149
<400> 2149
000
<210> 2150
<400> 2150
000
<210> 2151
<400> 2151
000
<210> 2152
<400> 2152
000
<210> 2153
<400> 2153
000
<210> 2154
<400> 2154
000
<210> 2155
<400> 2155
000
<210> 2156
<400> 2156
000
<210> 2157
<400> 2157
000
<210> 2158
<400> 2158
000
<210> 2159
<400> 2159
000
<210> 2160
<400> 2160
000
<210> 2161
<400> 2161
000
<210> 2162
<400> 2162
000
<210> 2163
<400> 2163
000
<210> 2164
<400> 2164
000
<210> 2165
<400> 2165
000
<210> 2166
<400> 2166
000
<210> 2167
<400> 2167
000
<210> 2168
<400> 2168
000
<210> 2169
<400> 2169
000
<210> 2170
<400> 2170
000
<210> 2171
<400> 2171
000
<210> 2172
<400> 2172
000
<210> 2173
<400> 2173
000
<210> 2174
<400> 2174
000
<210> 2175
<400> 2175
000
<210> 2176
<400> 2176
000
<210> 2177
<400> 2177
000
<210> 2178
<400> 2178
000
<210> 2179
<400> 2179
000
<210> 2180
<400> 2180
000
<210> 2181
<400> 2181
000
<210> 2182
<400> 2182
000
<210> 2183
<400> 2183
000
<210> 2184
<400> 2184
000
<210> 2185
<400> 2185
000
<210> 2186
<400> 2186
000
<210> 2187
<400> 2187
000
<210> 2188
<400> 2188
000
<210> 2189
<400> 2189
000
<210> 2190
<400> 2190
000
<210> 2191
<400> 2191
000
<210> 2192
<400> 2192
000
<210> 2193
<400> 2193
000
<210> 2194
<400> 2194
000
<210> 2195
<400> 2195
000
<210> 2196
<400> 2196
000
<210> 2197
<400> 2197
000
<210> 2198
<400> 2198
000
<210> 2199
<400> 2199
000
<210> 2200
<400> 2200
000
<210> 2201
<400> 2201
000
<210> 2202
<400> 2202
000
<210> 2203
<400> 2203
000
<210> 2204
<400> 2204
000
<210> 2205
<400> 2205
000
<210> 2206
<400> 2206
000
<210> 2207
<400> 2207
000
<210> 2208
<400> 2208
000
<210> 2209
<400> 2209
000
<210> 2210
<400> 2210
000
<210> 2211
<400> 2211
000
<210> 2212
<400> 2212
000
<210> 2213
<400> 2213
000
<210> 2214
<400> 2214
000
<210> 2215
<400> 2215
000
<210> 2216
<400> 2216
000
<210> 2217
<400> 2217
000
<210> 2218
<400> 2218
000
<210> 2219
<400> 2219
000
<210> 2220
<400> 2220
000
<210> 2221
<400> 2221
000
<210> 2222
<400> 2222
000
<210> 2223
<400> 2223
000
<210> 2224
<400> 2224
000
<210> 2225
<400> 2225
000
<210> 2226
<400> 2226
000
<210> 2227
<400> 2227
000
<210> 2228
<400> 2228
000
<210> 2229
<400> 2229
000
<210> 2230
<400> 2230
000
<210> 2231
<400> 2231
000
<210> 2232
<400> 2232
000
<210> 2233
<400> 2233
000
<210> 2234
<400> 2234
000
<210> 2235
<400> 2235
000
<210> 2236
<400> 2236
000
<210> 2237
<400> 2237
000
<210> 2238
<400> 2238
000
<210> 2239
<400> 2239
000
<210> 2240
<400> 2240
000
<210> 2241
<400> 2241
000
<210> 2242
<400> 2242
000
<210> 2243
<400> 2243
000
<210> 2244
<400> 2244
000
<210> 2245
<400> 2245
000
<210> 2246
<400> 2246
000
<210> 2247
<400> 2247
000
<210> 2248
<400> 2248
000
<210> 2249
<400> 2249
000
<210> 2250
<400> 2250
000
<210> 2251
<400> 2251
000
<210> 2252
<400> 2252
000
<210> 2253
<400> 2253
000
<210> 2254
<400> 2254
000
<210> 2255
<400> 2255
000
<210> 2256
<400> 2256
000
<210> 2257
<400> 2257
000
<210> 2258
<400> 2258
000
<210> 2259
<400> 2259
000
<210> 2260
<400> 2260
000
<210> 2261
<400> 2261
000
<210> 2262
<400> 2262
000
<210> 2263
<400> 2263
000
<210> 2264
<400> 2264
000
<210> 2265
<400> 2265
000
<210> 2266
<400> 2266
000
<210> 2267
<400> 2267
000
<210> 2268
<400> 2268
000
<210> 2269
<400> 2269
000
<210> 2270
<400> 2270
000
<210> 2271
<400> 2271
000
<210> 2272
<400> 2272
000
<210> 2273
<400> 2273
000
<210> 2274
<400> 2274
000
<210> 2275
<400> 2275
000
<210> 2276
<400> 2276
000
<210> 2277
<400> 2277
000
<210> 2278
<400> 2278
000
<210> 2279
<400> 2279
000
<210> 2280
<400> 2280
000
<210> 2281
<400> 2281
000
<210> 2282
<400> 2282
000
<210> 2283
<400> 2283
000
<210> 2284
<400> 2284
000
<210> 2285
<400> 2285
000
<210> 2286
<400> 2286
000
<210> 2287
<400> 2287
000
<210> 2288
<400> 2288
000
<210> 2289
<400> 2289
000
<210> 2290
<400> 2290
000
<210> 2291
<400> 2291
000
<210> 2292
<400> 2292
000
<210> 2293
<400> 2293
000
<210> 2294
<400> 2294
000
<210> 2295
<400> 2295
000
<210> 2296
<400> 2296
000
<210> 2297
<400> 2297
000
<210> 2298
<400> 2298
000
<210> 2299
<400> 2299
000
<210> 2300
<400> 2300
000
<210> 2301
<400> 2301
000
<210> 2302
<400> 2302
000
<210> 2303
<400> 2303
000
<210> 2304
<400> 2304
000
<210> 2305
<400> 2305
000
<210> 2306
<400> 2306
000
<210> 2307
<400> 2307
000
<210> 2308
<400> 2308
000
<210> 2309
<400> 2309
000
<210> 2310
<400> 2310
000
<210> 2311
<400> 2311
000
<210> 2312
<400> 2312
000
<210> 2313
<400> 2313
000
<210> 2314
<400> 2314
000
<210> 2315
<400> 2315
000
<210> 2316
<400> 2316
000
<210> 2317
<400> 2317
000
<210> 2318
<400> 2318
000
<210> 2319
<400> 2319
000
<210> 2320
<400> 2320
000
<210> 2321
<400> 2321
000
<210> 2322
<400> 2322
000
<210> 2323
<400> 2323
000
<210> 2324
<400> 2324
000
<210> 2325
<400> 2325
000
<210> 2326
<400> 2326
000
<210> 2327
<400> 2327
000
<210> 2328
<400> 2328
000
<210> 2329
<400> 2329
000
<210> 2330
<400> 2330
000
<210> 2331
<400> 2331
000
<210> 2332
<400> 2332
000
<210> 2333
<400> 2333
000
<210> 2334
<400> 2334
000
<210> 2335
<400> 2335
000
<210> 2336
<400> 2336
000
<210> 2337
<400> 2337
000
<210> 2338
<400> 2338
000
<210> 2339
<400> 2339
000
<210> 2340
<400> 2340
000
<210> 2341
<400> 2341
000
<210> 2342
<400> 2342
000
<210> 2343
<400> 2343
000
<210> 2344
<400> 2344
000
<210> 2345
<400> 2345
000
<210> 2346
<400> 2346
000
<210> 2347
<400> 2347
000
<210> 2348
<400> 2348
000
<210> 2349
<400> 2349
000
<210> 2350
<400> 2350
000
<210> 2351
<400> 2351
000
<210> 2352
<400> 2352
000
<210> 2353
<400> 2353
000
<210> 2354
<400> 2354
000
<210> 2355
<400> 2355
000
<210> 2356
<400> 2356
000
<210> 2357
<400> 2357
000
<210> 2358
<400> 2358
000
<210> 2359
<400> 2359
000
<210> 2360
<400> 2360
000
<210> 2361
<400> 2361
000
<210> 2362
<400> 2362
000
<210> 2363
<400> 2363
000
<210> 2364
<400> 2364
000
<210> 2365
<400> 2365
000
<210> 2366
<400> 2366
000
<210> 2367
<400> 2367
000
<210> 2368
<400> 2368
000
<210> 2369
<400> 2369
000
<210> 2370
<400> 2370
000
<210> 2371
<400> 2371
000
<210> 2372
<400> 2372
000
<210> 2373
<400> 2373
000
<210> 2374
<400> 2374
000
<210> 2375
<400> 2375
000
<210> 2376
<400> 2376
000
<210> 2377
<400> 2377
000
<210> 2378
<400> 2378
000
<210> 2379
<400> 2379
000
<210> 2380
<400> 2380
000
<210> 2381
<400> 2381
000
<210> 2382
<400> 2382
000
<210> 2383
<400> 2383
000
<210> 2384
<400> 2384
000
<210> 2385
<400> 2385
000
<210> 2386
<400> 2386
000
<210> 2387
<400> 2387
000
<210> 2388
<400> 2388
000
<210> 2389
<400> 2389
000
<210> 2390
<400> 2390
000
<210> 2391
<400> 2391
000
<210> 2392
<400> 2392
000
<210> 2393
<400> 2393
000
<210> 2394
<400> 2394
000
<210> 2395
<400> 2395
000
<210> 2396
<400> 2396
000
<210> 2397
<400> 2397
000
<210> 2398
<400> 2398
000
<210> 2399
<400> 2399
000
<210> 2400
<400> 2400
000
<210> 2401
<400> 2401
000
<210> 2402
<400> 2402
000
<210> 2403
<400> 2403
000
<210> 2404
<400> 2404
000
<210> 2405
<400> 2405
000
<210> 2406
<400> 2406
000
<210> 2407
<400> 2407
000
<210> 2408
<400> 2408
000
<210> 2409
<400> 2409
000
<210> 2410
<400> 2410
000
<210> 2411
<400> 2411
000
<210> 2412
<400> 2412
000
<210> 2413
<400> 2413
000
<210> 2414
<400> 2414
000
<210> 2415
<400> 2415
000
<210> 2416
<400> 2416
000
<210> 2417
<400> 2417
000
<210> 2418
<400> 2418
000
<210> 2419
<400> 2419
000
<210> 2420
<400> 2420
000
<210> 2421
<400> 2421
000
<210> 2422
<400> 2422
000
<210> 2423
<400> 2423
000
<210> 2424
<400> 2424
000
<210> 2425
<400> 2425
000
<210> 2426
<400> 2426
000
<210> 2427
<400> 2427
000
<210> 2428
<400> 2428
000
<210> 2429
<400> 2429
000
<210> 2430
<400> 2430
000
<210> 2431
<400> 2431
000
<210> 2432
<400> 2432
000
<210> 2433
<400> 2433
000
<210> 2434
<400> 2434
000
<210> 2435
<400> 2435
000
<210> 2436
<400> 2436
000
<210> 2437
<400> 2437
000
<210> 2438
<400> 2438
000
<210> 2439
<400> 2439
000
<210> 2440
<400> 2440
000
<210> 2441
<400> 2441
000
<210> 2442
<400> 2442
000
<210> 2443
<400> 2443
000
<210> 2444
<400> 2444
000
<210> 2445
<400> 2445
000
<210> 2446
<400> 2446
000
<210> 2447
<400> 2447
000
<210> 2448
<400> 2448
000
<210> 2449
<400> 2449
000
<210> 2450
<400> 2450
000
<210> 2451
<400> 2451
000
<210> 2452
<400> 2452
000
<210> 2453
<400> 2453
000
<210> 2454
<400> 2454
000
<210> 2455
<400> 2455
000
<210> 2456
<400> 2456
000
<210> 2457
<400> 2457
000
<210> 2458
<400> 2458
000
<210> 2459
<400> 2459
000
<210> 2460
<400> 2460
000
<210> 2461
<400> 2461
000
<210> 2462
<400> 2462
000
<210> 2463
<400> 2463
000
<210> 2464
<400> 2464
000
<210> 2465
<400> 2465
000
<210> 2466
<400> 2466
000
<210> 2467
<400> 2467
000
<210> 2468
<400> 2468
000
<210> 2469
<400> 2469
000
<210> 2470
<400> 2470
000
<210> 2471
<400> 2471
000
<210> 2472
<400> 2472
000
<210> 2473
<400> 2473
000
<210> 2474
<400> 2474
000
<210> 2475
<400> 2475
000
<210> 2476
<400> 2476
000
<210> 2477
<400> 2477
000
<210> 2478
<400> 2478
000
<210> 2479
<400> 2479
000
<210> 2480
<400> 2480
000
<210> 2481
<400> 2481
000
<210> 2482
<400> 2482
000
<210> 2483
<400> 2483
000
<210> 2484
<400> 2484
000
<210> 2485
<400> 2485
000
<210> 2486
<400> 2486
000
<210> 2487
<400> 2487
000
<210> 2488
<400> 2488
000
<210> 2489
<400> 2489
000
<210> 2490
<400> 2490
000
<210> 2491
<400> 2491
000
<210> 2492
<400> 2492
000
<210> 2493
<400> 2493
000
<210> 2494
<400> 2494
000
<210> 2495
<400> 2495
000
<210> 2496
<400> 2496
000
<210> 2497
<400> 2497
000
<210> 2498
<400> 2498
000
<210> 2499
<400> 2499
000
<210> 2500
<400> 2500
000
<210> 2501
<400> 2501
000
<210> 2502
<400> 2502
000
<210> 2503
<400> 2503
000
<210> 2504
<400> 2504
000
<210> 2505
<400> 2505
000
<210> 2506
<400> 2506
000
<210> 2507
<400> 2507
000
<210> 2508
<400> 2508
000
<210> 2509
<400> 2509
000
<210> 2510
<400> 2510
000
<210> 2511
<400> 2511
000
<210> 2512
<400> 2512
000
<210> 2513
<400> 2513
000
<210> 2514
<400> 2514
000
<210> 2515
<400> 2515
000
<210> 2516
<400> 2516
000
<210> 2517
<400> 2517
000
<210> 2518
<400> 2518
000
<210> 2519
<400> 2519
000
<210> 2520
<400> 2520
000
<210> 2521
<400> 2521
000
<210> 2522
<400> 2522
000
<210> 2523
<400> 2523
000
<210> 2524
<400> 2524
000
<210> 2525
<400> 2525
000
<210> 2526
<400> 2526
000
<210> 2527
<400> 2527
000
<210> 2528
<400> 2528
000
<210> 2529
<400> 2529
000
<210> 2530
<400> 2530
000
<210> 2531
<400> 2531
000
<210> 2532
<400> 2532
000
<210> 2533
<400> 2533
000
<210> 2534
<400> 2534
000
<210> 2535
<400> 2535
000
<210> 2536
<400> 2536
000
<210> 2537
<400> 2537
000
<210> 2538
<400> 2538
000
<210> 2539
<400> 2539
000
<210> 2540
<400> 2540
000
<210> 2541
<400> 2541
000
<210> 2542
<400> 2542
000
<210> 2543
<400> 2543
000
<210> 2544
<400> 2544
000
<210> 2545
<400> 2545
000
<210> 2546
<400> 2546
000
<210> 2547
<400> 2547
000
<210> 2548
<400> 2548
000
<210> 2549
<400> 2549
000
<210> 2550
<400> 2550
000
<210> 2551
<400> 2551
000
<210> 2552
<400> 2552
000
<210> 2553
<400> 2553
000
<210> 2554
<400> 2554
000
<210> 2555
<400> 2555
000
<210> 2556
<400> 2556
000
<210> 2557
<400> 2557
000
<210> 2558
<400> 2558
000
<210> 2559
<400> 2559
000
<210> 2560
<400> 2560
000
<210> 2561
<400> 2561
000
<210> 2562
<400> 2562
000
<210> 2563
<400> 2563
000
<210> 2564
<400> 2564
000
<210> 2565
<400> 2565
000
<210> 2566
<400> 2566
000
<210> 2567
<400> 2567
000
<210> 2568
<400> 2568
000
<210> 2569
<400> 2569
000
<210> 2570
<400> 2570
000
<210> 2571
<400> 2571
000
<210> 2572
<400> 2572
000
<210> 2573
<400> 2573
000
<210> 2574
<400> 2574
000
<210> 2575
<400> 2575
000
<210> 2576
<400> 2576
000
<210> 2577
<400> 2577
000
<210> 2578
<400> 2578
000
<210> 2579
<400> 2579
000
<210> 2580
<400> 2580
000
<210> 2581
<400> 2581
000
<210> 2582
<400> 2582
000
<210> 2583
<400> 2583
000
<210> 2584
<400> 2584
000
<210> 2585
<400> 2585
000
<210> 2586
<400> 2586
000
<210> 2587
<400> 2587
000
<210> 2588
<400> 2588
000
<210> 2589
<400> 2589
000
<210> 2590
<400> 2590
000
<210> 2591
<400> 2591
000
<210> 2592
<400> 2592
000
<210> 2593
<400> 2593
000
<210> 2594
<400> 2594
000
<210> 2595
<400> 2595
000
<210> 2596
<400> 2596
000
<210> 2597
<400> 2597
000
<210> 2598
<400> 2598
000
<210> 2599
<400> 2599
000
<210> 2600
<400> 2600
000
<210> 2601
<400> 2601
000
<210> 2602
<400> 2602
000
<210> 2603
<400> 2603
000
<210> 2604
<400> 2604
000
<210> 2605
<400> 2605
000
<210> 2606
<400> 2606
000
<210> 2607
<400> 2607
000
<210> 2608
<400> 2608
000
<210> 2609
<400> 2609
000
<210> 2610
<400> 2610
000
<210> 2611
<400> 2611
000
<210> 2612
<400> 2612
000
<210> 2613
<400> 2613
000
<210> 2614
<400> 2614
000
<210> 2615
<400> 2615
000
<210> 2616
<400> 2616
000
<210> 2617
<400> 2617
000
<210> 2618
<400> 2618
000
<210> 2619
<400> 2619
000
<210> 2620
<400> 2620
000
<210> 2621
<400> 2621
000
<210> 2622
<400> 2622
000
<210> 2623
<400> 2623
000
<210> 2624
<400> 2624
000
<210> 2625
<400> 2625
000
<210> 2626
<400> 2626
000
<210> 2627
<400> 2627
000
<210> 2628
<400> 2628
000
<210> 2629
<400> 2629
000
<210> 2630
<400> 2630
000
<210> 2631
<400> 2631
000
<210> 2632
<400> 2632
000
<210> 2633
<400> 2633
000
<210> 2634
<400> 2634
000
<210> 2635
<400> 2635
000
<210> 2636
<400> 2636
000
<210> 2637
<400> 2637
000
<210> 2638
<400> 2638
000
<210> 2639
<400> 2639
000
<210> 2640
<400> 2640
000
<210> 2641
<400> 2641
000
<210> 2642
<400> 2642
000
<210> 2643
<400> 2643
000
<210> 2644
<400> 2644
000
<210> 2645
<400> 2645
000
<210> 2646
<400> 2646
000
<210> 2647
<400> 2647
000
<210> 2648
<400> 2648
000
<210> 2649
<400> 2649
000
<210> 2650
<400> 2650
000
<210> 2651
<400> 2651
000
<210> 2652
<400> 2652
000
<210> 2653
<400> 2653
000
<210> 2654
<400> 2654
000
<210> 2655
<400> 2655
000
<210> 2656
<400> 2656
000
<210> 2657
<400> 2657
000
<210> 2658
<400> 2658
000
<210> 2659
<400> 2659
000
<210> 2660
<400> 2660
000
<210> 2661
<400> 2661
000
<210> 2662
<400> 2662
000
<210> 2663
<400> 2663
000
<210> 2664
<400> 2664
000
<210> 2665
<400> 2665
000
<210> 2666
<400> 2666
000
<210> 2667
<400> 2667
000
<210> 2668
<400> 2668
000
<210> 2669
<400> 2669
000
<210> 2670
<400> 2670
000
<210> 2671
<400> 2671
000
<210> 2672
<400> 2672
000
<210> 2673
<400> 2673
000
<210> 2674
<400> 2674
000
<210> 2675
<400> 2675
000
<210> 2676
<400> 2676
000
<210> 2677
<400> 2677
000
<210> 2678
<400> 2678
000
<210> 2679
<400> 2679
000
<210> 2680
<400> 2680
000
<210> 2681
<400> 2681
000
<210> 2682
<400> 2682
000
<210> 2683
<400> 2683
000
<210> 2684
<400> 2684
000
<210> 2685
<400> 2685
000
<210> 2686
<400> 2686
000
<210> 2687
<400> 2687
000
<210> 2688
<400> 2688
000
<210> 2689
<400> 2689
000
<210> 2690
<400> 2690
000
<210> 2691
<400> 2691
000
<210> 2692
<400> 2692
000
<210> 2693
<400> 2693
000
<210> 2694
<400> 2694
000
<210> 2695
<400> 2695
000
<210> 2696
<400> 2696
000
<210> 2697
<400> 2697
000
<210> 2698
<400> 2698
000
<210> 2699
<400> 2699
000
<210> 2700
<400> 2700
000
<210> 2701
<400> 2701
000
<210> 2702
<400> 2702
000
<210> 2703
<400> 2703
000
<210> 2704
<400> 2704
000
<210> 2705
<400> 2705
000
<210> 2706
<400> 2706
000
<210> 2707
<400> 2707
000
<210> 2708
<400> 2708
000
<210> 2709
<400> 2709
000
<210> 2710
<400> 2710
000
<210> 2711
<400> 2711
000
<210> 2712
<400> 2712
000
<210> 2713
<400> 2713
000
<210> 2714
<400> 2714
000
<210> 2715
<400> 2715
000
<210> 2716
<400> 2716
000
<210> 2717
<400> 2717
000
<210> 2718
<400> 2718
000
<210> 2719
<400> 2719
000
<210> 2720
<400> 2720
000
<210> 2721
<400> 2721
000
<210> 2722
<400> 2722
000
<210> 2723
<400> 2723
000
<210> 2724
<400> 2724
000
<210> 2725
<400> 2725
000
<210> 2726
<400> 2726
000
<210> 2727
<400> 2727
000
<210> 2728
<400> 2728
000
<210> 2729
<400> 2729
000
<210> 2730
<400> 2730
000
<210> 2731
<400> 2731
000
<210> 2732
<400> 2732
000
<210> 2733
<400> 2733
000
<210> 2734
<400> 2734
000
<210> 2735
<400> 2735
000
<210> 2736
<400> 2736
000
<210> 2737
<400> 2737
000
<210> 2738
<400> 2738
000
<210> 2739
<400> 2739
000
<210> 2740
<400> 2740
000
<210> 2741
<400> 2741
000
<210> 2742
<400> 2742
000
<210> 2743
<400> 2743
000
<210> 2744
<400> 2744
000
<210> 2745
<400> 2745
000
<210> 2746
<400> 2746
000
<210> 2747
<400> 2747
000
<210> 2748
<400> 2748
000
<210> 2749
<400> 2749
000
<210> 2750
<400> 2750
000
<210> 2751
<400> 2751
000
<210> 2752
<400> 2752
000
<210> 2753
<400> 2753
000
<210> 2754
<400> 2754
000
<210> 2755
<400> 2755
000
<210> 2756
<400> 2756
000
<210> 2757
<400> 2757
000
<210> 2758
<400> 2758
000
<210> 2759
<400> 2759
000
<210> 2760
<400> 2760
000
<210> 2761
<400> 2761
000
<210> 2762
<400> 2762
000
<210> 2763
<400> 2763
000
<210> 2764
<400> 2764
000
<210> 2765
<400> 2765
000
<210> 2766
<400> 2766
000
<210> 2767
<400> 2767
000
<210> 2768
<400> 2768
000
<210> 2769
<400> 2769
000
<210> 2770
<400> 2770
000
<210> 2771
<400> 2771
000
<210> 2772
<400> 2772
000
<210> 2773
<400> 2773
000
<210> 2774
<400> 2774
000
<210> 2775
<400> 2775
000
<210> 2776
<400> 2776
000
<210> 2777
<400> 2777
000
<210> 2778
<400> 2778
000
<210> 2779
<400> 2779
000
<210> 2780
<400> 2780
000
<210> 2781
<400> 2781
000
<210> 2782
<400> 2782
000
<210> 2783
<400> 2783
000
<210> 2784
<400> 2784
000
<210> 2785
<400> 2785
000
<210> 2786
<400> 2786
000
<210> 2787
<400> 2787
000
<210> 2788
<400> 2788
000
<210> 2789
<400> 2789
000
<210> 2790
<400> 2790
000
<210> 2791
<400> 2791
000
<210> 2792
<400> 2792
000
<210> 2793
<400> 2793
000
<210> 2794
<400> 2794
000
<210> 2795
<400> 2795
000
<210> 2796
<400> 2796
000
<210> 2797
<400> 2797
000
<210> 2798
<400> 2798
000
<210> 2799
<400> 2799
000
<210> 2800
<400> 2800
000
<210> 2801
<400> 2801
000
<210> 2802
<400> 2802
000
<210> 2803
<400> 2803
000
<210> 2804
<400> 2804
000
<210> 2805
<400> 2805
000
<210> 2806
<400> 2806
000
<210> 2807
<400> 2807
000
<210> 2808
<400> 2808
000
<210> 2809
<400> 2809
000
<210> 2810
<400> 2810
000
<210> 2811
<400> 2811
000
<210> 2812
<400> 2812
000
<210> 2813
<400> 2813
000
<210> 2814
<400> 2814
000
<210> 2815
<400> 2815
000
<210> 2816
<400> 2816
000
<210> 2817
<400> 2817
000
<210> 2818
<400> 2818
000
<210> 2819
<400> 2819
000
<210> 2820
<400> 2820
000
<210> 2821
<400> 2821
000
<210> 2822
<400> 2822
000
<210> 2823
<400> 2823
000
<210> 2824
<400> 2824
000
<210> 2825
<400> 2825
000
<210> 2826
<400> 2826
000
<210> 2827
<400> 2827
000
<210> 2828
<400> 2828
000
<210> 2829
<400> 2829
000
<210> 2830
<400> 2830
000
<210> 2831
<400> 2831
000
<210> 2832
<400> 2832
000
<210> 2833
<400> 2833
000
<210> 2834
<400> 2834
000
<210> 2835
<400> 2835
000
<210> 2836
<400> 2836
000
<210> 2837
<400> 2837
000
<210> 2838
<400> 2838
000
<210> 2839
<400> 2839
000
<210> 2840
<400> 2840
000
<210> 2841
<400> 2841
000
<210> 2842
<400> 2842
000
<210> 2843
<400> 2843
000
<210> 2844
<400> 2844
000
<210> 2845
<400> 2845
000
<210> 2846
<400> 2846
000
<210> 2847
<400> 2847
000
<210> 2848
<400> 2848
000
<210> 2849
<400> 2849
000
<210> 2850
<400> 2850
000
<210> 2851
<400> 2851
000
<210> 2852
<400> 2852
000
<210> 2853
<400> 2853
000
<210> 2854
<400> 2854
000
<210> 2855
<400> 2855
000
<210> 2856
<400> 2856
000
<210> 2857
<400> 2857
000
<210> 2858
<400> 2858
000
<210> 2859
<400> 2859
000
<210> 2860
<400> 2860
000
<210> 2861
<400> 2861
000
<210> 2862
<400> 2862
000
<210> 2863
<400> 2863
000
<210> 2864
<400> 2864
000
<210> 2865
<400> 2865
000
<210> 2866
<400> 2866
000
<210> 2867
<400> 2867
000
<210> 2868
<400> 2868
000
<210> 2869
<400> 2869
000
<210> 2870
<400> 2870
000
<210> 2871
<400> 2871
000
<210> 2872
<400> 2872
000
<210> 2873
<400> 2873
000
<210> 2874
<400> 2874
000
<210> 2875
<400> 2875
000
<210> 2876
<400> 2876
000
<210> 2877
<400> 2877
000
<210> 2878
<400> 2878
000
<210> 2879
<400> 2879
000
<210> 2880
<400> 2880
000
<210> 2881
<400> 2881
000
<210> 2882
<400> 2882
000
<210> 2883
<400> 2883
000
<210> 2884
<400> 2884
000
<210> 2885
<400> 2885
000
<210> 2886
<400> 2886
000
<210> 2887
<400> 2887
000
<210> 2888
<400> 2888
000
<210> 2889
<400> 2889
000
<210> 2890
<400> 2890
000
<210> 2891
<400> 2891
000
<210> 2892
<400> 2892
000
<210> 2893
<400> 2893
000
<210> 2894
<400> 2894
000
<210> 2895
<400> 2895
000
<210> 2896
<400> 2896
000
<210> 2897
<400> 2897
000
<210> 2898
<400> 2898
000
<210> 2899
<400> 2899
000
<210> 2900
<400> 2900
000
<210> 2901
<400> 2901
000
<210> 2902
<400> 2902
000
<210> 2903
<400> 2903
000
<210> 2904
<400> 2904
000
<210> 2905
<400> 2905
000
<210> 2906
<400> 2906
000
<210> 2907
<400> 2907
000
<210> 2908
<400> 2908
000
<210> 2909
<400> 2909
000
<210> 2910
<400> 2910
000
<210> 2911
<400> 2911
000
<210> 2912
<400> 2912
000
<210> 2913
<400> 2913
000
<210> 2914
<400> 2914
000
<210> 2915
<400> 2915
000
<210> 2916
<400> 2916
000
<210> 2917
<400> 2917
000
<210> 2918
<400> 2918
000
<210> 2919
<400> 2919
000
<210> 2920
<400> 2920
000
<210> 2921
<400> 2921
000
<210> 2922
<400> 2922
000
<210> 2923
<400> 2923
000
<210> 2924
<400> 2924
000
<210> 2925
<400> 2925
000
<210> 2926
<400> 2926
000
<210> 2927
<400> 2927
000
<210> 2928
<400> 2928
000
<210> 2929
<400> 2929
000
<210> 2930
<400> 2930
000
<210> 2931
<400> 2931
000
<210> 2932
<400> 2932
000
<210> 2933
<400> 2933
000
<210> 2934
<400> 2934
000
<210> 2935
<400> 2935
000
<210> 2936
<400> 2936
000
<210> 2937
<400> 2937
000
<210> 2938
<400> 2938
000
<210> 2939
<400> 2939
000
<210> 2940
<400> 2940
000
<210> 2941
<400> 2941
000
<210> 2942
<400> 2942
000
<210> 2943
<400> 2943
000
<210> 2944
<400> 2944
000
<210> 2945
<400> 2945
000
<210> 2946
<400> 2946
000
<210> 2947
<400> 2947
000
<210> 2948
<400> 2948
000
<210> 2949
<400> 2949
000
<210> 2950
<400> 2950
000
<210> 2951
<400> 2951
000
<210> 2952
<400> 2952
000
<210> 2953
<400> 2953
000
<210> 2954
<400> 2954
000
<210> 2955
<400> 2955
000
<210> 2956
<400> 2956
000
<210> 2957
<400> 2957
000
<210> 2958
<400> 2958
000
<210> 2959
<400> 2959
000
<210> 2960
<400> 2960
000
<210> 2961
<400> 2961
000
<210> 2962
<400> 2962
000
<210> 2963
<400> 2963
000
<210> 2964
<400> 2964
000
<210> 2965
<400> 2965
000
<210> 2966
<400> 2966
000
<210> 2967
<400> 2967
000
<210> 2968
<400> 2968
000
<210> 2969
<400> 2969
000
<210> 2970
<400> 2970
000
<210> 2971
<400> 2971
000
<210> 2972
<400> 2972
000
<210> 2973
<400> 2973
000
<210> 2974
<400> 2974
000
<210> 2975
<400> 2975
000
<210> 2976
<400> 2976
000
<210> 2977
<400> 2977
000
<210> 2978
<400> 2978
000
<210> 2979
<400> 2979
000
<210> 2980
<400> 2980
000
<210> 2981
<400> 2981
000
<210> 2982
<400> 2982
000
<210> 2983
<400> 2983
000
<210> 2984
<400> 2984
000
<210> 2985
<400> 2985
000
<210> 2986
<400> 2986
000
<210> 2987
<400> 2987
000
<210> 2988
<400> 2988
000
<210> 2989
<400> 2989
000
<210> 2990
<400> 2990
000
<210> 2991
<400> 2991
000
<210> 2992
<400> 2992
000
<210> 2993
<400> 2993
000
<210> 2994
<400> 2994
000
<210> 2995
<400> 2995
000
<210> 2996
<400> 2996
000
<210> 2997
<400> 2997
000
<210> 2998
<400> 2998
000
<210> 2999
<400> 2999
000
<210> 3000
<400> 3000
000
<210> 3001
<211> 1200
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3001
atgctcgagg gggttcaggt ggagactatc agcccgggcg acggacggac attcccaaag
60
cgcgggcaga cgtgtgtggt gcattacacc gggatgcttg aggacggaaa gaaagtggac
120
tcttcccgag accgaaataa accattcaag ttcatgttgg gcaagcagga ggttatcaga
180
gggtgggagg agggcgtcgc tcagatgagt gtcggacaga gggccaagct cacgatctcc
240
cctgattacg cctacggggc aactggtcac cccggaatca tcccccctca cgcaaccctc
300
gtgttcgacg tcgagctgct caaactggaa tcaggcggag gcagtggcgc tagcgggttt
360
ggcgatgtcg gtgcccttga aagcttgaga ggaaatgccg atctcgctta catcttgagc
420
atggagccct gtgggcactg tctgatcatc aacaatgtta acttttgccg ggagtccggc
480
ctgcgcacac gcacaggctc caacattgac tgcgaaaaac ttcgaaggag gtttagctct
540
ctgcatttca tggtagaggt gaagggggat ctgaccgcca agaaaatggt tctcgccctt
600
ctcgagcttg cgcagcagga ccatggagcg cttgactgtt gtgtcgttgt gatactgagc
660
catggctgtc aggcttccca tctccagttt ccaggggccg tgtacggaac cgatggatgc
720
cctgtgtcag ttgaaaagat cgtaaacatc tttaacggaa catcttgccc gagcctcggc
780
ggtaaaccga agcttttttt tatccaggcc tgcggcggtg aacagaaaga tcatggcttc
840
gaggttgcca gtaccagccc tgaagacgaa tcccccgggt caaatcctga accagatgcg
900
acccctttcc aggaaggact ccgcactttt gaccagcttg acgccatttc ctccctgcca
960
acaccttccg acatatttgt aagctactcc acctttccag gattcgtgag ctggcgcgac
1020
ccaaaatccg gcagttggta tgttgaaacc ctggacgata ttttcgaaca atgggcccac
1080
agtgaggacc tgcagtccct tcttctgcgc gtagccaatg ccgtgtcagt caaagggatt
1140
tacaagcaga tgccaggctg ctttaatttc ctgcgcaaga aactgttttt taagaccagt
1200
<210> 3002
<211> 1172
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3002
cggacggaca ttcccaaagc gcgggcagac gtgtgtggtg cattacaccg ggatgcttga
60
ggacggaaag aaagtggact cttcccgaga ccgaaataaa ccattcaagt tcatgttggg
120
caagcaggag gttatcagag ggtgggagga gggcgtcgct cagatgagtg tcggacagag
180
ggccaagctc acgatctccc ctgattacgc ctacggggca actggtcacc ccggaatcat
240
cccccctcac gcaaccctcg tgttcgacgt cgagctgctc aaactggaat caggcggagg
300
cagtggcggg tttggcgatg tcggtgccct tgaaagcttg agaggaaatg ccgatctcgc
360
ttacatcttg agcatggagc cctgtgggca ctgtctgatc atcaacaatg ttaacttttg
420
ccgggagtcc ggcctgcgca cacgcacagg ctccaacatt gactgcgaaa aacttcgaag
480
gaggtttagc tctctgcatt tcatggtaga ggtgaagggg gatctgaccg ccaagaaaat
540
ggttctcgcc cttctcgagc ttgcgcagca ggaccatgga gcgcttgact gttgtgtcgt
600
tgtgatactg agccatggct gtcaggcttc ccatctccag tttccagggg ccgtgtacgg
660
aaccgatgga tgccctgtgt cagttgaaaa gatcgtaaac atctttaacg gaacatcttg
720
cccgagcctc ggcggtaaac cgaagctttt ttttatccag gcctgcggcg gtgaacagaa
780
agatcatggc ttcgaggttg ccagtaccag ccctgaagac gaatcccccg ggtcaaatcc
840
tgaaccagat gcgacccctt tccaggaagg actccgcact tttgaccagc ttgacgccat
900
ttcctccctg ccaacacctt ccgacatatt tgtaagctac tccacctttc caggattcgt
960
gagctggcgc gacccaaaat ccggcagttg gtatgttgaa accctggacg atatcttcga
1020
acaatgggcc cacagtgagg acctgcagtc ccttcttctg cgcgtagcca atgccgtgtc
1080
agtcaaaggg atttacaagc agatgccagg ctgctttaat ttcctgcgca agaaactgtt
1140
ttttaagacc agttgagtcg acggaggagg ag
1172
<210> 3003
<211> 1188
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3003
ggggttcagg tggagactat cagcccgggc gacggacgga cattcccaaa gcgcgggcag
60
acgtgtgtgg tgcattacac cgggatgctt gaggacggaa agaaagtgga ctcttcccga
120
gaccgaaata aaccattcaa gttcatgttg ggcaagcagg aggttatcag agggtgggag
180
gagggcgtcg ctcagatgag tgtcggacag agggccaagc tcacgatctc ccctgattac
240
gcctacgggg caactggtca ccccggaatc atcccccctc acgcaaccct cgtgttcgac
300
gtcgagctgc tcaaactgga atcaggcgga ggcagtggcg ggtttggcga tgtcggtgcc
360
cttgaaagct tgagaggaaa tgccgatctc gcttacatct tgagcatgga gccctgtggg
420
cactgtctga tcatcaacaa tgttaacttt tgccgggagt ccggcctgcg cacacgcaca
480
ggctccaaca ttgactgcga aaaacttcga aggaggttta gctctctgca tttcatggta
540
gaggtgaagg gggatctgac cgccaagaaa atggttctcg cccttctcga gcttgcgcag
600
caggaccatg gagcgcttga ctgttgtgtc gttgtgatac tgagccatgg ctgtcaggct
660
tcccatctcc agtttccagg ggccgtgtac ggaaccgatg gatgccctgt gtcagttgaa
720
aagatcgtaa acatctttaa cggaacatct tgcccgagcc tcggcggtaa accgaagctt
780
ttttttatcc aggcctgcgg cggtgaacag aaagatcatg gcttcgaggt tgccagtacc
840
agccctgaag acgaatcccc cgggtcaaat cctgaaccag atgcgacccc tttccaggaa
900
ggactccgca cttttgacca gcttgacgcc atttcctccc tgccaacacc ttccgacata
960
tttgtaagct actccacctt tccaggattc gtgagctggc gcgacccaaa atccggcagt
1020
tggtatgttg aaaccctgga cgatatcttc gaacaatggg cccacagtga ggacctgcag
1080
tcccttcttc tgcgcgtagc caatgccgtg tcagtcaaag ggatttacaa gcagatgcca
1140
ggctgcttta atttcctgcg caagaaactg ttttttaaga ccagttga
1188
<210> 3004
<211> 1518
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3004
agaggcgtgc aggtggaaac catctctccc ggcgacggca gaaccttccc taagaggggc
60
cagacctgcg tggtgcacta caccggcatg ctggaagatg gcaagaagat ggacagctcc
120
cgggaccgga acaagccctt caagttcatg ctgggcaagc aggaagtgat ccggggctgg
180
gaagagggcg tggcacagat gtctgtgggc cagagagcca agctgaccat cagccccgat
240
tacgcctacg gcgccacagg ccaccctggc atcattcctc cacacgccac actggtgttc
300
gatgtggaac tgctgaagct ggaaacccgg ggagtgcagg tggaaacaat cagccctggc
360
gacggccgga cctttccaaa acggggacag acatgtgtgg tgcattatac agggatgctg
420
gaagatggga aaaaaatgga tagcagccgc gaccgcaaca aaccttttaa gtttatgctg
480
gggaaacagg aagtgattag aggctgggaa gagggggtgg cacagatgag cgtgggacag
540
cgggccaaac tgacaatctc ccccgactat gcctatgggg ccaccggaca ccccggaatc
600
atcccacctc atgctaccct ggtgtttgac gtggaactgc tgaaactgga aacaagcggc
660
ggaggcagcg gcggctttgg agatgtggga gccctggaaa gcctgcgggg caatgccgat
720
ctggcctaca tcctgagcat ggaaccctgc ggccactgcc tgattatcaa caacgtgaac
780
ttctgcagag agagcggcct gcggaccaga accggcagca acatcgactg cgagaagctg
840
cggcggagat tcagcagcct gcacttcatg gtggaagtga agggggacct gaccgccaag
900
aaaatggtgc tggctctgct ggaactggcc cagcaggatc atggcgccct ggactgttgc
960
gtggtcgtga tcctgagcca cggctgccag gccagccatc tgcagtttcc cggcgctgtg
1020
tatggcaccg atggctgccc tgtgtccgtg gaaaagatcg tgaatatctt caacggcacc
1080
agctgcccca gcctgggcgg aaagcctaag ctgttcttta ttcaagcctg tgggggcgag
1140
cagaaggacc acggatttga ggtggccagc acctcccccg aggatgagag ccctggcagc
1200
aaccctgagc ctgacgccac cccattccag gaaggactgc ggaccttcga ccagctggac
1260
gccatctcta gcctgcccac ccccagcgac atcttcgtgt cctacagcac cttccctggc
1320
tttgtgtcct ggcgggaccc caagtccggc tcttggtacg tggaaaccct ggacgacatc
1380
tttgagcagt gggcccatag cgaggacctg cagagcctgc tgctgagggt ggccaatgcc
1440
gtgtccgtga agggcatcta caagcagatg cccggctgct tcaacttcct gcggaagaag
1500
ctgtttttca agaccagc
1518
<210> 3005
<211> 400
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3005
Met Leu Glu Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg
1 5 10 15
Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met
20 25 30
Leu Glu Asp Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro
35 40 45
Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu
50 55 60
Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser
65 70 75 80
Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro
85 90 95
His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Ser Gly
100 105 110
Gly Gly Ser Gly Ala Ser Gly Phe Gly Asp Val Gly Ala Leu Glu Ser
115 120 125
Leu Arg Gly Asn Ala Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys
130 135 140
Gly His Cys Leu Ile Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly
145 150 155 160
Leu Arg Thr Arg Thr Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg
165 170 175
Arg Phe Ser Ser Leu His Phe Met Val Glu Val Lys Gly Asp Leu Thr
180 185 190
Ala Lys Lys Met Val Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His
195 200 205
Gly Ala Leu Asp Cys Cys Val Val Val Ile Leu Ser His Gly Cys Gln
210 215 220
Ala Ser His Leu Gln Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys
225 230 235 240
Pro Val Ser Val Glu Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys
245 250 255
Pro Ser Leu Gly Gly Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly
260 265 270
Gly Glu Gln Lys Asp His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu
275 280 285
Asp Glu Ser Pro Gly Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln
290 295 300
Glu Gly Leu Arg Thr Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro
305 310 315 320
Thr Pro Ser Asp Ile Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val
325 330 335
Ser Trp Arg Asp Pro Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp
340 345 350
Asp Ile Phe Glu Gln Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu
355 360 365
Leu Arg Val Ala Asn Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met
370 375 380
Pro Gly Cys Phe Asn Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
385 390 395 400
<210> 3006
<211> 395
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3006
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
1 5 10 15
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
20 25 30
Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
35 40 45
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
50 55 60
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
65 70 75 80
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
85 90 95
Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Ser Gly Gly Gly Ser
100 105 110
Gly Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg Gly Asn Ala
115 120 125
Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His Cys Leu Ile
130 135 140
Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg Thr Arg Thr
145 150 155 160
Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe Ser Ser Leu
165 170 175
His Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys Lys Met Val
180 185 190
Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala Leu Asp Cys
195 200 205
Cys Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser His Leu Gln
210 215 220
Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val Ser Val Glu
225 230 235 240
Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser Leu Gly Gly
245 250 255
Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu Gln Lys Asp
260 265 270
His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu Ser Pro Gly
275 280 285
Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly Leu Arg Thr
290 295 300
Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro Ser Asp Ile
305 310 315 320
Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp Arg Asp Pro
325 330 335
Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile Phe Glu Gln
340 345 350
Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg Val Ala Asn
355 360 365
Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly Cys Phe Asn
370 375 380
Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
385 390 395
<210> 3007
<211> 506
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3007
Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe
1 5 10 15
Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu
20 25 30
Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys
35 40 45
Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val
50 55 60
Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp
65 70 75 80
Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala
85 90 95
Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg Gly Val
100 105 110
Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg
115 120 125
Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp Gly Lys
130 135 140
Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe Met Leu
145 150 155 160
Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala Gln Met
165 170 175
Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr
180 185 190
Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr Leu Val
195 200 205
Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Ser Gly Gly Gly Ser Gly
210 215 220
Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg Gly Asn Ala Asp
225 230 235 240
Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His Cys Leu Ile Ile
245 250 255
Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg Thr Arg Thr Gly
260 265 270
Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe Ser Ser Leu His
275 280 285
Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys Lys Met Val Leu
290 295 300
Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala Leu Asp Cys Cys
305 310 315 320
Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser His Leu Gln Phe
325 330 335
Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val Ser Val Glu Lys
340 345 350
Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser Leu Gly Gly Lys
355 360 365
Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu Gln Lys Asp His
370 375 380
Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu Ser Pro Gly Ser
385 390 395 400
Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly Leu Arg Thr Phe
405 410 415
Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro Ser Asp Ile Phe
420 425 430
Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp Arg Asp Pro Lys
435 440 445
Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile Phe Glu Gln Trp
450 455 460
Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg Val Ala Asn Ala
465 470 475 480
Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly Cys Phe Asn Phe
485 490 495
Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
500 505
<210> 3008
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3008
ggaagcggcg ccaccaattt cagcctgctg aaacaggccg gcgacgtgga agagaaccct
60
ggccct
66
<210> 3009
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3009
agtggctccg gcgcaacaaa tttctccttg ctgaaacagg caggcgacgt tgaggaaaat
60
cccggccca
69
<210> 3010
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3010
ggctccggcg caacaaattt ctccttgctg aaacaggcag gcgacgttga ggaaaatccc
60
ggccca
66
<210> 3011
<211> 32
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3011
ggggttcagg tggagactat cagcccgggc ga
32
<210> 3012
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3012
ggctccggcg caacaaattt ctccttgctg aaacaggcag gcgacgttga ggaaaatccc
60
ggccca
66
<210> 3013
<211> 22
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 3013
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 3014
<211> 26
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 3014
Arg Lys Arg Arg Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln
1 5 10 15
Ala Gly Asp Val Glu Glu Asn Pro Gly Pro
20 25
<210> 3015
<211> 1308
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3015
cggggcgtgc aggttgagac aatttcccca ggagatgggc gaacgttccc caagcgcgga
60
cagacatgcg ttgtgcacta cacaggaatg ttggaggacg gaaagaaaat ggacagttca
120
agagatcgga acaaaccatt caaattcatg ttgggaaaac aggaagtgat acggggctgg
180
gaagagggtg tagcgcaaat gtccgttggt caacgagcaa aactcacgat aagtcccgat
240
tatgcttacg gcgcaaccgg tcacccgggc atcataccgc ctcatgcgac tttggtcttt
300
gatgtggagc tgttgaaact tgaaactcgc ggagtacagg ttgaaacaat atcacccggg
360
gacgggcgga cttttccgaa gagaggtcag acctgcgtcg tccattatac cggtatgctg
420
gaggacggaa agaaaatgga cagctcacgg gaccgaaata aaccattcaa atttatgttg
480
gggaaacaag aggttatcag gggctgggag gagggtgtgg cccagatgtc tgtcggtcag
540
cgcgcgaaac tcacaatctc tccggattat gcgtatgggg cgacagggca tccgggaatt
600
atccctcccc acgctacctt ggttttcgat gttgagcttc tgaagttgga gaccagagga
660
gttcaagtgg agacaatatc tcctggggat ggacggacgt tccccaagcg cggccagacc
720
tgtgtagtcc actacacagg gatgcttgaa gacggaaaaa agatggatag cagtagagat
780
cgcaacaaac catttaagtt catgctgggg aagcaggaag taatacgcgg ctgggaggaa
840
ggcgtggcac agatgagtgt tggtcaacgg gccaaactta ctatttctcc cgattatgcg
900
tatggagcca ccgggcaccc tggcattatc ccaccccatg ccacattggt ttttgacgtt
960
gaattgctta aattggagac caggggagtc caagtggaaa caatatcacc gggggatggt
1020
cggacttttc ctaaaagggg ccaaacctgt gtagtccatt ataccggaat gctcgaagac
1080
ggaaagaaaa tggactcttc tagagaccgc aataagccct tcaagttcat gttgggtaag
1140
caagaggtga tccggggctg ggaagagggg gtcgctcaaa tgtccgtcgg tcagcgagct
1200
aaactgacta tttccccaga ctacgcatat ggagcgactg gccaccccgg tattattcct
1260
ccccatgcga ctctcgtgtt cgacgtagaa ctcttgaaat tggaaacg
1308
<210> 3016
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3016
tcagcccgga acaggcggaa gaga
24
<210> 3017
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 3017
Ser Ala Arg Asn Arg Arg Lys Arg
1 5
<210> 3018
<211> 2727
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3018
atgctcgagg gggttcaggt ggagactatc agcccgggcg acggacggac attcccaaag
60
cgcgggcaga cgtgtgtggt gcattacacc gggatgcttg aggacggaaa gaaagtggac
120
tcttcccgag accgaaataa accattcaag ttcatgttgg gcaagcagga ggttatcaga
180
gggtgggagg agggcgtcgc tcagatgagt gtcggacaga gggccaagct cacgatctcc
240
cctgattacg cctacggggc aactggtcac cccggaatca tcccccctca cgcaaccctc
300
gtgttcgacg tcgagctgct caaactggaa tcaggcggag gcagtggcgc tagcgggttt
360
ggcgatgtcg gtgcccttga aagcttgaga ggaaatgccg atctcgctta catcttgagc
420
atggagccct gtgggcactg tctgatcatc aacaatgtta acttttgccg ggagtccggc
480
ctgcgcacac gcacaggctc caacattgac tgcgaaaaac ttcgaaggag gtttagctct
540
ctgcatttca tggtagaggt gaagggggat ctgaccgcca agaaaatggt tctcgccctt
600
ctcgagcttg cgcagcagga ccatggagcg cttgactgtt gtgtcgttgt gatactgagc
660
catggctgtc aggcttccca tctccagttt ccaggggccg tgtacggaac cgatggatgc
720
cctgtgtcag ttgaaaagat cgtaaacatc tttaacggaa catcttgccc gagcctcggc
780
ggtaaaccga agcttttttt tatccaggcc tgcggcggtg aacagaaaga tcatggcttc
840
gaggttgcca gtaccagccc tgaagacgaa tcccccgggt caaatcctga accagatgcg
900
acccctttcc aggaaggact ccgcactttt gaccagcttg acgccatttc ctccctgcca
960
acaccttccg acatatttgt aagctactcc acctttccag gattcgtgag ctggcgcgac
1020
ccaaaatccg gcagttggta tgttgaaacc ctggacgata ttttcgaaca atgggcccac
1080
agtgaggacc tgcagtccct tcttctgcgc gtagccaatg ccgtgtcagt caaagggatt
1140
tacaagcaga tgccaggctg ctttaatttc ctgcgcaaga aactgttttt taagaccagt
1200
ggctccggcg caacaaattt ctccttgctg aaacaggcag gcgacgttga ggaaaatccc
1260
ggcccaatgg ccttaccagt gaccgccttg ctcctgccgc tggccttgct gctccacgcc
1320
gccaggccgg acatccagat gacacagact acatcctccc tgtctgcctc tctgggagac
1380
agagtcacca tcagttgcag ggcaagtcag gacattagta aatatttaaa ttggtatcag
1440
cagaaaccag atggaactgt taaactcctg atctaccata catcaagatt acactcagga
1500
gtcccatcaa ggttcagtgg cagtgggtct ggaacagatt attctctcac cattagcaac
1560
ctggagcaag aagatattgc cacttacttt tgccaacagg gtaatacgct tccgtacacg
1620
ttcggagggg ggactaagtt ggaaataaca ggtggcggtg gctcgggcgg tggtgggtcg
1680
ggtggcggcg gatctgaggt gaaactgcag gagtcaggac ctggcctggt ggcgccctca
1740
cagagcctgt ccgtcacatg cactgtctca ggggtctcat tacccgacta tggtgtaagc
1800
tggattcgcc agcctccacg aaagggtctg gagtggctgg gagtaatatg gggtagtgaa
1860
accacatact ataattcagc tctcaaatcc agactgacca tcatcaagga caactccaag
1920
agccaagttt tcttaaaaat gaacagtctg caaactgatg acacagccat ttactactgt
1980
gccaaacatt attactacgg tggtagctat gctatggact actggggtca aggaacctca
2040
gtcaccgtct cctcaaccac gacgccagcg ccgcgaccac caacaccggc gcccaccatc
2100
gcgtcgcagc ccctgtccct gcgcccagag gcgtgccggc cagcggcggg gggcgcagtg
2160
cacacgaggg ggctggactt cgcctgtgat atctacatct gggcgccctt ggccgggact
2220
tgtggggtcc ttctcctgtc actggttatc accctttact gcaaacgggg cagaaagaaa
2280
ctcctgtata tattcaaaca accatttatg agaccagtac aaactactca agaggaagat
2340
ggctgtagct gccgatttcc agaagaagaa gaaggaggat gtgaactgag agtgaagttc
2400
agcaggagcg cagacgcccc cgcgtaccag cagggccaga accagctcta taacgagctc
2460
aatctaggac gaagagagga gtacgatgtt ttggacaaga gacgtggccg ggaccctgag
2520
atggggggaa agccgagaag gaagaaccct caggaaggcc tgtacaatga actgcagaaa
2580
gataagatgg cggaggccta cagtgagatt gggatgaaag gcgagcgccg gaggggcaag
2640
gggcacgatg gcctttacca gggtctcagt acagccacca aggacaccta cgacgccctt
2700
cacatgcagg ccctgccccc tcgctaa
2727
<210> 3019
<211> 908
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3019
Met Leu Glu Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg
1 5 10 15
Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met
20 25 30
Leu Glu Asp Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro
35 40 45
Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu
50 55 60
Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser
65 70 75 80
Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro
85 90 95
His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Ser Gly
100 105 110
Gly Gly Ser Gly Ala Ser Gly Phe Gly Asp Val Gly Ala Leu Glu Ser
115 120 125
Leu Arg Gly Asn Ala Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys
130 135 140
Gly His Cys Leu Ile Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly
145 150 155 160
Leu Arg Thr Arg Thr Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg
165 170 175
Arg Phe Ser Ser Leu His Phe Met Val Glu Val Lys Gly Asp Leu Thr
180 185 190
Ala Lys Lys Met Val Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His
195 200 205
Gly Ala Leu Asp Cys Cys Val Val Val Ile Leu Ser His Gly Cys Gln
210 215 220
Ala Ser His Leu Gln Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys
225 230 235 240
Pro Val Ser Val Glu Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys
245 250 255
Pro Ser Leu Gly Gly Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly
260 265 270
Gly Glu Gln Lys Asp His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu
275 280 285
Asp Glu Ser Pro Gly Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln
290 295 300
Glu Gly Leu Arg Thr Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro
305 310 315 320
Thr Pro Ser Asp Ile Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val
325 330 335
Ser Trp Arg Asp Pro Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp
340 345 350
Asp Ile Phe Glu Gln Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu
355 360 365
Leu Arg Val Ala Asn Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met
370 375 380
Pro Gly Cys Phe Asn Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
385 390 395 400
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
405 410 415
Glu Glu Asn Pro Gly Pro Met Ala Leu Pro Val Thr Ala Leu Leu Leu
420 425 430
Pro Leu Ala Leu Leu Leu His Ala Ala Arg Pro Asp Ile Gln Met Thr
435 440 445
Gln Thr Thr Ser Ser Leu Ser Ala Ser Leu Gly Asp Arg Val Thr Ile
450 455 460
Ser Cys Arg Ala Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln
465 470 475 480
Gln Lys Pro Asp Gly Thr Val Lys Leu Leu Ile Tyr His Thr Ser Arg
485 490 495
Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
500 505 510
Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr
515 520 525
Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly
530 535 540
Thr Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
545 550 555 560
Gly Gly Gly Gly Ser Glu Val Lys Leu Gln Glu Ser Gly Pro Gly Leu
565 570 575
Val Ala Pro Ser Gln Ser Leu Ser Val Thr Cys Thr Val Ser Gly Val
580 585 590
Ser Leu Pro Asp Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Arg Lys
595 600 605
Gly Leu Glu Trp Leu Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr
610 615 620
Asn Ser Ala Leu Lys Ser Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys
625 630 635 640
Ser Gln Val Phe Leu Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala
645 650 655
Ile Tyr Tyr Cys Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met
660 665 670
Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Thr Thr Thr
675 680 685
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
690 695 700
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
705 710 715 720
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
725 730 735
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
740 745 750
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
755 760 765
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
770 775 780
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
785 790 795 800
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
805 810 815
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
820 825 830
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
835 840 845
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
850 855 860
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
865 870 875 880
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
885 890 895
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
900 905
<210> 3020
<211> 2741
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3020
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccggacatcc agatgacaca gactacatcc tccctgtctg cctctctggg agacagagtc
120
accatcagtt gcagggcaag tcaggacatt agtaaatatt taaattggta tcagcagaaa
180
ccagatggaa ctgttaaact cctgatctac catacatcaa gattacactc aggagtccca
240
tcaaggttca gtggcagtgg gtctggaaca gattattctc tcaccattag caacctggag
300
caagaagata ttgccactta cttttgccaa cagggtaata cgcttccgta cacgttcgga
360
ggggggacta agttggaaat aacaggtggc ggtggctcgg gcggtggtgg gtcgggtggc
420
ggcggatctg aggtgaaact gcaggagtca ggacctggcc tggtggcgcc ctcacagagc
480
ctgtccgtca catgcactgt ctcaggggtc tcattacccg actatggtgt aagctggatt
540
cgccagcctc cacgaaaggg tctggagtgg ctgggagtaa tatggggtag tgaaaccaca
600
tactataatt cagctctcaa atccagactg accatcatca aggacaactc caagagccaa
660
gttttcttaa aaatgaacag tctgcaaact gatgacacag ccatttacta ctgtgccaaa
720
cattattact acggtggtag ctatgctatg gactactggg gtcaaggaac ctcagtcacc
780
gtctcctcaa ccacgacgcc agcgccgcga ccaccaacac cggcgcccac catcgcgtcg
840
cagcccctgt ccctgcgccc agaggcgtgc cggccagcgg cggggggcgc agtgcacacg
900
agggggctgg acttcgcctg tgatatctac atctgggcgc ccttggccgg gacttgtggg
960
gtccttctcc tgtcactggt tatcaccctt tactgcaaac ggggcagaaa gaaactcctg
1020
tatatattca aacaaccatt tatgagacca gtacaaacta ctcaagagga agatggctgt
1080
agctgccgat ttccagaaga agaagaagga ggatgtgaac tgagagtgaa gttcagcagg
1140
agcgcagacg cccccgcgta ccagcagggc cagaaccagc tctataacga gctcaatcta
1200
ggacgaagag aggagtacga tgttttggac aagagacgtg gccgggaccc tgagatgggg
1260
ggaaagccga gaaggaagaa ccctcaggaa ggcctgtaca atgaactgca gaaagataag
1320
atggcggagg cctacagtga gattgggatg aaaggcgagc gccggagggg caaggggcac
1380
gatggccttt accagggtct cagtacagcc accaaggaca cctacgacgc ccttcacatg
1440
caggccctgc cccctcgctc ggaagcgacg gggctccggc gcaacaaatt tctccttgct
1500
gaaacaggca ggcgacgttg aggaaaatcc cggcccaggg gttcaggtgg agactatcag
1560
cccgggcgac ggacggacat tcccaaagcg cgggcagacg tgtgtggtgc attacaccgg
1620
gatgcttgag gacggaaaga aagtggactc ttcccgagac cgaaataaac cattcaagtt
1680
catgttgggc aagcaggagg ttatcagagg gtgggaggag ggcgtcgctc agatgagtgt
1740
cggacagagg gccaagctca cgatctcccc tgattacgcc tacggggcaa ctggtcaccc
1800
cggaatcatc ccccctcacg caaccctcgt gttcgacgtc gagctgctca aactggaatc
1860
aggcggaggc agtggcgggt ttggcgatgt cggtgccctt gaaagcttga gaggaaatgc
1920
cgatctcgct tacatcttga gcatggagcc ctgtgggcac tgtctgatca tcaacaatgt
1980
taacttttgc cgggagtccg gcctgcgcac acgcacaggc tccaacattg actgcgaaaa
2040
acttcgaagg aggtttagct ctctgcattt catggtagag gtgaaggggg atctgaccgc
2100
caagaaaatg gttctcgccc ttctcgagct tgcgcagcag gaccatggag cgcttgactg
2160
ttgtgtcgtt gtgatactga gccatggctg tcaggcttcc catctccagt ttccaggggc
2220
cgtgtacgga accgatggat gccctgtgtc agttgaaaag atcgtaaaca tctttaacgg
2280
aacatcttgc ccgagcctcg gcggtaaacc gaagcttttt tttatccagg cctgcggcgg
2340
tgaacagaaa gatcatggct tcgaggttgc cagtaccagc cctgaagacg aatcccccgg
2400
gtcaaatcct gaaccagatg cgaccccttt ccaggaagga ctccgcactt ttgaccagct
2460
tgacgccatt tcctccctgc caacaccttc cgacatattt gtaagctact ccacctttcc
2520
aggattcgtg agctggcgcg acccaaaatc cggcagttgg tatgttgaaa ccctggacga
2580
tatcttcgaa caatgggccc acagtgagga cctgcagtcc cttcttctgc gcgtagccaa
2640
tgccgtgtca gtcaaaggga tttacaagca gatgccaggc tgctttaatt tcctgcgcaa
2700
gaaactgttt tttaagacca gttgagtcga cggaggagga g
2741
<210> 3021
<211> 907
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3021
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg Arg Lys Arg Arg Gly Ser Gly Ala Thr Asn
485 490 495
Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro
500 505 510
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
515 520 525
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
530 535 540
Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
545 550 555 560
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
565 570 575
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
580 585 590
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
595 600 605
Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Ser Gly Gly Gly Ser
610 615 620
Gly Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg Gly Asn Ala
625 630 635 640
Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His Cys Leu Ile
645 650 655
Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg Thr Arg Thr
660 665 670
Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe Ser Ser Leu
675 680 685
His Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys Lys Met Val
690 695 700
Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala Leu Asp Cys
705 710 715 720
Cys Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser His Leu Gln
725 730 735
Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val Ser Val Glu
740 745 750
Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser Leu Gly Gly
755 760 765
Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu Gln Lys Asp
770 775 780
His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu Ser Pro Gly
785 790 795 800
Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly Leu Arg Thr
805 810 815
Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro Ser Asp Ile
820 825 830
Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp Arg Asp Pro
835 840 845
Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile Phe Glu Gln
850 855 860
Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg Val Ala Asn
865 870 875 880
Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly Cys Phe Asn
885 890 895
Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
900 905
<210> 3022
<211> 1479
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3022
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccgggatccg atattcaact tacacagtcc cctagttcct tgtccgcctc cgtcggcgac
120
agagttacca tgacttgtcg agcgtcttct agcgtttcct acattcattg gttccaacag
180
aagcccggaa aggcaccaaa accttggatc tacgccacgt ccaatttggc tagtggtgtt
240
ccggtgcgat tttccgggtc aggtagcggg acggactata cttttaccat ttcaagcctt
300
cagcctgaag acatcgcgac gtactattgt cagcagtgga cctctaaccc tcctaccttt
360
ggcggtggaa caaagctgga gatcaaacga ggcgggggtg gctctggggg aggaggttcc
420
ggtgggggag gctctcaagt acaactgcaa caaagtgggg ctgaagtgaa gaagcccggt
480
tcttcagtca aagtatcatg taaggcaagt ggttatactt ttacgtctta taacatgcat
540
tgggtaaagc aagcccctgg tcagggcctc gagtggattg gtgcgatcta ccctggaatg
600
ggtgatacga gctataatca gaaattcaag gggaaagcca ccttgactgc agacgaatct
660
acgaacacgg cttacatgga gcttagctca ctcagatcag aggatacagc cttttactac
720
tgcgctagat caacttatta cggaggagac tggtattttg atgtatgggg tcaggggacc
780
acagtcactg ttagctctgc tagcaccacg acgccagcgc cgcgaccacc aacaccggcg
840
cccaccatcg cgtcgcagcc cctgtccctg cgcccagagg cgtgccggcc agcggcgggg
900
ggcgcagtgc acacgagggg gctggacttc gcctgtgatt ccggaatcta catctgggcg
960
cccttggccg ggacttgtgg ggtccttctc ctgtcactgg ttatcaccct ttactgcaaa
1020
cggggcagaa agaaactcct gtatatattc aaacaaccat ttatgagacc agtacaaact
1080
actcaagagg aagatggctg tagctgccga tttccagaag aagaagaagg aggatgtgaa
1140
ctgagagtga agttcagcag gagcgcagac gcccccgcgt accagcaggg ccagaaccag
1200
ctctataacg agctcaatct aggacgaaga gaggagtacg atgttttgga caagagacgt
1260
ggccgggacc ctgagatggg gggaaagccg agaaggaaga accctcagga aggcctgtac
1320
aatgaactgc agaaagataa gatggcggag gcctacagtg agattgggat gaaaggcgag
1380
cgccggaggg gcaaggggca cgatggcctt taccagggtc tcagtacagc caccaaggac
1440
acctacgacg cccttcacat gcaggccctg ccccctcgc
1479
<210> 3023
<211> 494
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3023
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser
20 25 30
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Met Thr Cys Arg Ala
35 40 45
Ser Ser Ser Val Ser Tyr Ile His Trp Phe Gln Gln Lys Pro Gly Lys
50 55 60
Ala Pro Lys Pro Trp Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val
65 70 75 80
Pro Val Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr
85 90 95
Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln
100 105 110
Trp Thr Ser Asn Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
115 120 125
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
145 150 155 160
Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
165 170 175
Tyr Asn Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp
180 185 190
Ile Gly Ala Ile Tyr Pro Gly Met Gly Asp Thr Ser Tyr Asn Gln Lys
195 200 205
Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Glu Ser Thr Asn Thr Ala
210 215 220
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Phe Tyr Tyr
225 230 235 240
Cys Ala Arg Ser Thr Tyr Tyr Gly Gly Asp Trp Tyr Phe Asp Val Trp
245 250 255
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ser Gly Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Glx
485 490
<210> 3024
<211> 2733
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3024
atggctctgc ctgtgacagc tctgctgctg cctctggccc tgctgctgca tgctgccaga
60
cctggctccg atattcaact tacacagtcc cctagttcct tgtccgcctc cgtcggcgac
120
agagttacca tgacttgtcg agcgtcttct agcgtttcct acattcattg gttccaacag
180
aagcccggaa aggcaccaaa accttggatc tacgccacgt ccaatttggc tagtggtgtt
240
ccggtgcgat tttccgggtc aggtagcggg acggactata cttttaccat ttcaagcctt
300
cagcctgaag acatcgcgac gtactattgt cagcagtgga cctctaaccc tcctaccttt
360
ggcggtggaa caaagctgga gatcaaacga ggcgggggtg gctctggggg aggaggttcc
420
ggtgggggag gctctcaagt acaactgcaa caaagtgggg ctgaagtgaa gaagcccggt
480
tcttcagtca aagtatcatg taaggcaagt ggttatactt ttacgtctta taacatgcat
540
tgggtaaagc aagcccctgg tcagggcctc gagtggattg gtgcgatcta ccctggaatg
600
ggtgatacga gctataatca gaaattcaag gggaaagcca ccttgactgc agacgaatct
660
acgaacacgg cttacatgga gcttagctca ctcagatcag aggatacagc cttttactac
720
tgcgctagat caacttatta cggaggagac tggtattttg atgtatgggg tcaggggacc
780
acagtcactg ttagctctgc tagcaccacg acgccagcgc cgcgaccacc aacaccggcg
840
cccaccatcg cgtcgcagcc cctgtccctg cgcccagagg cgtgccggcc agcggcgggg
900
ggcgcagtgc acacgagggg gctggacttc gcctgtgatt ccggaatcta catctgggcg
960
cccttggccg ggacttgtgg ggtccttctc ctgtcactgg ttatcaccct ttactgcaaa
1020
cggggcagaa agaaactcct gtatatattc aaacaaccat ttatgagacc agtacaaact
1080
actcaagagg aagatggctg tagctgccga tttccagaag aagaagaagg aggatgtgaa
1140
ctgagagtga agttcagcag gagcgcagac gcccccgcgt accagcaggg ccagaaccag
1200
ctctataacg agctcaatct aggacgaaga gaggagtacg atgttttgga caagagacgt
1260
ggccgggacc ctgagatggg gggaaagccg agaaggaaga accctcagga aggcctgtac
1320
aatgaactgc agaaagataa gatggcggag gcctacagtg agattgggat gaaaggcgag
1380
cgccggaggg gcaaggggca cgatggcctt taccagggtc tcagtacagc caccaaggac
1440
acctacgacg cccttcacat gcaggccctg ccccctcgcg gctccggcgc aacaaatttc
1500
tccttgctga aacaggcagg cgacgttgag gaaaatcccg gcccaggggt tcaggtggag
1560
actatcagcc cgggcgacgg acggacattc ccaaagcgcg ggcagacgtg tgtggtgcat
1620
tacaccggga tgcttgagga cggaaagaaa gtggactctt cccgagaccg aaataaacca
1680
ttcaagttca tgttgggcaa gcaggaggtt atcagagggt gggaggaggg cgtcgctcag
1740
atgagtgtcg gacagagggc caagctcacg atctcccctg attacgccta cggggcaact
1800
ggtcaccccg gaatcatccc ccctcacgca accctcgtgt tcgacgtcga gctgctcaaa
1860
ctggaatcag gcggaggcag tggcgggttt ggcgatgtcg gtgcccttga aagcttgaga
1920
ggaaatgccg atctcgctta catcttgagc atggagccct gtgggcactg tctgatcatc
1980
aacaatgtta acttttgccg ggagtccggc ctgcgcacac gcacaggctc caacattgac
2040
tgcgaaaaac ttcgaaggag gtttagctct ctgcatttca tggtagaggt gaagggggat
2100
ctgaccgcca agaaaatggt tctcgccctt ctcgagcttg cgcagcagga ccatggagcg
2160
cttgactgtt gtgtcgttgt gatactgagc catggctgtc aggcttccca tctccagttt
2220
ccaggggccg tgtacggaac cgatggatgc cctgtgtcag ttgaaaagat cgtaaacatc
2280
tttaacggaa catcttgccc gagcctcggc ggtaaaccga agcttttttt tatccaggcc
2340
tgcggcggtg aacagaaaga tcatggcttc gaggttgcca gtaccagccc tgaagacgaa
2400
tcccccgggt caaatcctga accagatgcg acccctttcc aggaaggact ccgcactttt
2460
gaccagcttg acgccatttc ctccctgcca acaccttccg acatatttgt aagctactcc
2520
acctttccag gattcgtgag ctggcgcgac ccaaaatccg gcagttggta tgttgaaacc
2580
ctggacgata tcttcgaaca atgggcccac agtgaggacc tgcagtccct tcttctgcgc
2640
gtagccaatg ccgtgtcagt caaagggatt tacaagcaga tgccaggctg ctttaatttc
2700
ctgcgcaaga aactgttttt taagaccagt tga
2733
<210> 3025
<211> 911
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3025
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser
20 25 30
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Met Thr Cys Arg Ala
35 40 45
Ser Ser Ser Val Ser Tyr Ile His Trp Phe Gln Gln Lys Pro Gly Lys
50 55 60
Ala Pro Lys Pro Trp Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val
65 70 75 80
Pro Val Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr
85 90 95
Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln
100 105 110
Trp Thr Ser Asn Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
115 120 125
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
145 150 155 160
Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
165 170 175
Tyr Asn Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp
180 185 190
Ile Gly Ala Ile Tyr Pro Gly Met Gly Asp Thr Ser Tyr Asn Gln Lys
195 200 205
Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Glu Ser Thr Asn Thr Ala
210 215 220
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Phe Tyr Tyr
225 230 235 240
Cys Ala Arg Ser Thr Tyr Tyr Gly Gly Asp Trp Tyr Phe Asp Val Trp
245 250 255
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ser Gly Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser Gly
485 490 495
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
500 505 510
Pro Gly Pro Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg
515 520 525
Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met
530 535 540
Leu Glu Asp Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro
545 550 555 560
Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu
565 570 575
Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser
580 585 590
Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro
595 600 605
His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Ser Gly
610 615 620
Gly Gly Ser Gly Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg
625 630 635 640
Gly Asn Ala Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His
645 650 655
Cys Leu Ile Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg
660 665 670
Thr Arg Thr Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe
675 680 685
Ser Ser Leu His Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys
690 695 700
Lys Met Val Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala
705 710 715 720
Leu Asp Cys Cys Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser
725 730 735
His Leu Gln Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val
740 745 750
Ser Val Glu Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser
755 760 765
Leu Gly Gly Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu
770 775 780
Gln Lys Asp His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu
785 790 795 800
Ser Pro Gly Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly
805 810 815
Leu Arg Thr Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro
820 825 830
Ser Asp Ile Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp
835 840 845
Arg Asp Pro Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile
850 855 860
Phe Glu Gln Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg
865 870 875 880
Val Ala Asn Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly
885 890 895
Cys Phe Asn Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser Glx
900 905 910
<210> 3026
<211> 2745
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3026
atgctcgagg gggttcaggt ggagactatc agcccgggcg acggacggac attcccaaag
60
cgcgggcaga cgtgtgtggt gcattacacc gggatgcttg aggacggaaa gaaagtggac
120
tcttcccgag accgaaataa accattcaag ttcatgttgg gcaagcagga ggttatcaga
180
gggtgggagg agggcgtcgc tcagatgagt gtcggacaga gggccaagct cacgatctcc
240
cctgattacg cctacggggc aactggtcac cccggaatca tcccccctca cgcaaccctc
300
gtgttcgacg tcgagctgct caaactggaa tcaggcggag gcagtggcgc tagcgggttt
360
ggcgatgtcg gtgcccttga aagcttgaga ggaaatgccg atctcgctta catcttgagc
420
atggagccct gtgggcactg tctgatcatc aacaatgtta acttttgccg ggagtccggc
480
ctgcgcacac gcacaggctc caacattgac tgcgaaaaac ttcgaaggag gtttagctct
540
ctgcatttca tggtagaggt gaagggggat ctgaccgcca agaaaatggt tctcgccctt
600
ctcgagcttg cgcagcagga ccatggagcg cttgactgtt gtgtcgttgt gatactgagc
660
catggctgtc aggcttccca tctccagttt ccaggggccg tgtacggaac cgatggatgc
720
cctgtgtcag ttgaaaagat cgtaaacatc tttaacggaa catcttgccc gagcctcggc
780
ggtaaaccga agcttttttt tatccaggcc tgcggcggtg aacagaaaga tcatggcttc
840
gaggttgcca gtaccagccc tgaagacgaa tcccccgggt caaatcctga accagatgcg
900
acccctttcc aggaaggact ccgcactttt gaccagcttg acgccatttc ctccctgcca
960
acaccttccg acatatttgt aagctactcc acctttccag gattcgtgag ctggcgcgac
1020
ccaaaatccg gcagttggta tgttgaaacc ctggacgata ttttcgaaca atgggcccac
1080
agtgaggacc tgcagtccct tcttctgcgc gtagccaatg ccgtgtcagt caaagggatt
1140
tacaagcaga tgccaggctg ctttaatttc ctgcgcaaga aactgttttt taagaccagt
1200
ggctccggcg caacaaattt ctccttgctg aaacaggcag gcgacgttga ggaaaatccc
1260
ggcccaatgg ccttaccagt gaccgccttg ctcctgccgc tggccttgct gctccacgcc
1320
gccaggccgg gatccgatat tcaacttaca cagtccccta gttccttgtc cgcctccgtc
1380
ggcgacagag ttaccatgac ttgtcgagcg tcttctagcg tttcctacat tcattggttc
1440
caacagaagc ccggaaaggc accaaaacct tggatctacg ccacgtccaa tttggctagt
1500
ggtgttccgg tgcgattttc cgggtcaggt agcgggacgg actatacttt taccatttca
1560
agccttcagc ctgaagacat cgcgacgtac tattgtcagc agtggacctc taaccctcct
1620
acctttggcg gtggaacaaa gctggagatc aaacgaggcg ggggtggctc tgggggagga
1680
ggttccggtg ggggaggctc tcaagtacaa ctgcaacaaa gtggggctga agtgaagaag
1740
cccggttctt cagtcaaagt atcatgtaag gcaagtggtt atacttttac gtcttataac
1800
atgcattggg taaagcaagc ccctggtcag ggcctcgagt ggattggtgc gatctaccct
1860
ggaatgggtg atacgagcta taatcagaaa ttcaagggga aagccacctt gactgcagac
1920
gaatctacga acacggctta catggagctt agctcactca gatcagagga tacagccttt
1980
tactactgcg ctagatcaac ttattacgga ggagactggt attttgatgt atggggtcag
2040
gggaccacag tcactgttag ctctgctagc accacgacgc cagcgccgcg accaccaaca
2100
ccggcgccca ccatcgcgtc gcagcccctg tccctgcgcc cagaggcgtg ccggccagcg
2160
gcggggggcg cagtgcacac gagggggctg gacttcgcct gtgattccgg aatctacatc
2220
tgggcgccct tggccgggac ttgtggggtc cttctcctgt cactggttat caccctttac
2280
tgcaaacggg gcagaaagaa actcctgtat atattcaaac aaccatttat gagaccagta
2340
caaactactc aagaggaaga tggctgtagc tgccgatttc cagaagaaga agaaggagga
2400
tgtgaactga gagtgaagtt cagcaggagc gcagacgccc ccgcgtacca gcagggccag
2460
aaccagctct ataacgagct caatctagga cgaagagagg agtacgatgt tttggacaag
2520
agacgtggcc gggaccctga gatgggggga aagccgagaa ggaagaaccc tcaggaaggc
2580
ctgtacaatg aactgcagaa agataagatg gcggaggcct acagtgagat tgggatgaaa
2640
ggcgagcgcc ggaggggcaa ggggcacgat ggcctttacc agggtctcag tacagccacc
2700
aaggacacct acgacgccct tcacatgcag gccctgcccc ctcgc
2745
<210> 3027
<211> 916
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3027
Met Leu Glu Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg
1 5 10 15
Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met
20 25 30
Leu Glu Asp Gly Lys Lys Val Asp Ser Ser Arg Asp Arg Asn Lys Pro
35 40 45
Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu
50 55 60
Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser
65 70 75 80
Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro
85 90 95
His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Ser Gly
100 105 110
Gly Gly Ser Gly Ala Ser Gly Phe Gly Asp Val Gly Ala Leu Glu Ser
115 120 125
Leu Arg Gly Asn Ala Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys
130 135 140
Gly His Cys Leu Ile Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly
145 150 155 160
Leu Arg Thr Arg Thr Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg
165 170 175
Arg Phe Ser Ser Leu His Phe Met Val Glu Val Lys Gly Asp Leu Thr
180 185 190
Ala Lys Lys Met Val Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His
195 200 205
Gly Ala Leu Asp Cys Cys Val Val Val Ile Leu Ser His Gly Cys Gln
210 215 220
Ala Ser His Leu Gln Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys
225 230 235 240
Pro Val Ser Val Glu Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys
245 250 255
Pro Ser Leu Gly Gly Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly
260 265 270
Gly Glu Gln Lys Asp His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu
275 280 285
Asp Glu Ser Pro Gly Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln
290 295 300
Glu Gly Leu Arg Thr Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro
305 310 315 320
Thr Pro Ser Asp Ile Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val
325 330 335
Ser Trp Arg Asp Pro Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp
340 345 350
Asp Ile Phe Glu Gln Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu
355 360 365
Leu Arg Val Ala Asn Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met
370 375 380
Pro Gly Cys Phe Asn Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
385 390 395 400
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
405 410 415
Glu Glu Asn Pro Gly Pro Met Ala Leu Pro Val Thr Ala Leu Leu Leu
420 425 430
Pro Leu Ala Leu Leu Leu His Ala Ala Arg Pro Gly Ser Asp Ile Gln
435 440 445
Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val
450 455 460
Thr Met Thr Cys Arg Ala Ser Ser Ser Val Ser Tyr Ile His Trp Phe
465 470 475 480
Gln Gln Lys Pro Gly Lys Ala Pro Lys Pro Trp Ile Tyr Ala Thr Ser
485 490 495
Asn Leu Ala Ser Gly Val Pro Val Arg Phe Ser Gly Ser Gly Ser Gly
500 505 510
Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala
515 520 525
Thr Tyr Tyr Cys Gln Gln Trp Thr Ser Asn Pro Pro Thr Phe Gly Gly
530 535 540
Gly Thr Lys Leu Glu Ile Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly
545 550 555 560
Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Ala
565 570 575
Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser
580 585 590
Gly Tyr Thr Phe Thr Ser Tyr Asn Met His Trp Val Lys Gln Ala Pro
595 600 605
Gly Gln Gly Leu Glu Trp Ile Gly Ala Ile Tyr Pro Gly Met Gly Asp
610 615 620
Thr Ser Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp
625 630 635 640
Glu Ser Thr Asn Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu
645 650 655
Asp Thr Ala Phe Tyr Tyr Cys Ala Arg Ser Thr Tyr Tyr Gly Gly Asp
660 665 670
Trp Tyr Phe Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
675 680 685
Ala Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
690 695 700
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
705 710 715 720
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ser
725 730 735
Gly Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu
740 745 750
Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu
755 760 765
Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln
770 775 780
Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly
785 790 795 800
Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
805 810 815
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
820 825 830
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
835 840 845
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
850 855 860
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
865 870 875 880
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
885 890 895
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
900 905 910
Pro Pro Arg Glx
915
<210> 3028
<211> 3060
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3028
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccgggatccg acatccagat gacacagact acatcctccc tgtctgcctc tctgggagac
120
agagtcacca tcagttgcag ggcaagtcag gacattagta aatatttaaa ttggtatcag
180
cagaaaccag atggaactgt taaactcctg atctaccata catcaagatt acactcagga
240
gtcccatcaa ggttcagtgg cagtgggtct ggaacagatt attctctcac cattagcaac
300
ctggagcaag aagatattgc cacttacttt tgccaacagg gtaatacgct tccgtacacg
360
ttcggagggg ggactaagtt ggaaataaca ggtggcggtg gctcgggcgg tggtgggtcg
420
ggtggcggcg gatctgaggt gaaactgcag gagtcaggac ctggcctggt ggcgccctca
480
cagagcctgt ccgtcacatg cactgtctca ggggtctcat tacccgacta tggtgtaagc
540
tggattcgcc agcctccacg aaagggtctg gagtggctgg gagtaatatg gggtagtgaa
600
accacatact ataattcagc tctcaaatcc agactgacca tcatcaagga caactccaag
660
agccaagttt tcttaaaaat gaacagtctg caaactgatg acacagccat ttactactgt
720
gccaaacatt attactacgg tggtagctat gctatggact actggggtca aggaacctca
780
gtcaccgtct cctcagctag caccacgacg ccagcgccgc gaccaccaac accggcgccc
840
accatcgcgt cgcagcccct gtccctgcgc ccagaggcgt gccggccagc ggcggggggc
900
gcagtgcaca cgagggggct ggacttcgcc tgtgattccg gaatctacat ctgggcccct
960
ctggccggca cctgtggcgt gctgctgctg tctctcgtga tcaccctgta ctgcaagcgg
1020
ggcagaaaga agctgctgta catcttcaag cagcccttca tgcggcccgt gcagaccacc
1080
caggaagagg acggctgctc ctgcagattc cccgaggaag aagaaggcgg ctgcgagctg
1140
agagtgaagt tcagcagaag cgccgacgcc cctgcctatc agcagggcca gaaccagctg
1200
tacaacgagc tgaacctggg cagacgggaa gagtacgacg tgctggacaa gcggagaggc
1260
agggaccctg agatgggcgg caagcccaga agaaagaacc cccaggaagg cctgtataac
1320
gaactgcaga aagacaagat ggccgaggcc tacagcgaga tcggaatgaa gggcgagcgg
1380
agaagaggca agggccacga tggcctgtac cagggcctga gcaccgccac caaggacacc
1440
tatgacgccc tgcacatgca ggccctgcct ccaagaggaa gcggcgccac caatttcagc
1500
ctgctgaaac aggccggcga cgtggaagag aaccctggcc ctagaggcgt gcaggtggaa
1560
accatctctc ccggcgacgg cagaaccttc cctaagaggg gccagacctg cgtggtgcac
1620
tacaccggca tgctggaaga tggcaagaag atggacagct cccgggaccg gaacaagccc
1680
ttcaagttca tgctgggcaa gcaggaagtg atccggggct gggaagaggg cgtggcacag
1740
atgtctgtgg gccagagagc caagctgacc atcagccccg attacgccta cggcgccaca
1800
ggccaccctg gcatcattcc tccacacgcc acactggtgt tcgatgtgga actgctgaag
1860
ctggaaaccc ggggagtgca ggtggaaaca atcagccctg gcgacggccg gacctttcca
1920
aaacggggac agacatgtgt ggtgcattat acagggatgc tggaagatgg gaaaaaaatg
1980
gatagcagcc gcgaccgcaa caaacctttt aagtttatgc tggggaaaca ggaagtgatt
2040
agaggctggg aagagggggt ggcacagatg agcgtgggac agcgggccaa actgacaatc
2100
tcccccgact atgcctatgg ggccaccgga caccccggaa tcatcccacc tcatgctacc
2160
ctggtgtttg acgtggaact gctgaaactg gaaacaagcg gcggaggcag cggcggcttt
2220
ggagatgtgg gagccctgga aagcctgcgg ggcaatgccg atctggccta catcctgagc
2280
atggaaccct gcggccactg cctgattatc aacaacgtga acttctgcag agagagcggc
2340
ctgcggacca gaaccggcag caacatcgac tgcgagaagc tgcggcggag attcagcagc
2400
ctgcacttca tggtggaagt gaagggggac ctgaccgcca agaaaatggt gctggctctg
2460
ctggaactgg cccagcagga tcatggcgcc ctggactgtt gcgtggtcgt gatcctgagc
2520
cacggctgcc aggccagcca tctgcagttt cccggcgctg tgtatggcac cgatggctgc
2580
cctgtgtccg tggaaaagat cgtgaatatc ttcaacggca ccagctgccc cagcctgggc
2640
ggaaagccta agctgttctt tattcaagcc tgtgggggcg agcagaagga ccacggattt
2700
gaggtggcca gcacctcccc cgaggatgag agccctggca gcaaccctga gcctgacgcc
2760
accccattcc aggaaggact gcggaccttc gaccagctgg acgccatctc tagcctgccc
2820
acccccagcg acatcttcgt gtcctacagc accttccctg gctttgtgtc ctggcgggac
2880
cccaagtccg gctcttggta cgtggaaacc ctggacgaca tctttgagca gtgggcccat
2940
agcgaggacc tgcagagcct gctgctgagg gtggccaatg ccgtgtccgt gaagggcatc
3000
tacaagcaga tgcccggctg cttcaacttc ctgcggaaga agctgttttt caagaccagc
3060
<210> 3029
<211> 1020
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3029
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Asp Ile Gln Met Thr Gln Thr Thr Ser
20 25 30
Ser Leu Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala
35 40 45
Ser Gln Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp
50 55 60
Gly Thr Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly
65 70 75 80
Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu
85 90 95
Thr Ile Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln
100 105 110
Gln Gly Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu
115 120 125
Ile Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Glu Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser
145 150 155 160
Gln Ser Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp
165 170 175
Tyr Gly Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp
180 185 190
Leu Gly Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu
195 200 205
Lys Ser Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe
210 215 220
Leu Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys
225 230 235 240
Ala Lys His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly
245 250 255
Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ser Gly Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser Gly Ala
485 490 495
Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro
500 505 510
Gly Pro Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg
515 520 525
Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met
530 535 540
Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro
545 550 555 560
Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu
565 570 575
Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser
580 585 590
Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro
595 600 605
His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg
610 615 620
Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro
625 630 635 640
Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp
645 650 655
Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe
660 665 670
Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala
675 680 685
Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr
690 695 700
Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr
705 710 715 720
Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Ser Gly Gly Gly
725 730 735
Ser Gly Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg Gly Asn
740 745 750
Ala Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His Cys Leu
755 760 765
Ile Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg Thr Arg
770 775 780
Thr Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe Ser Ser
785 790 795 800
Leu His Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys Lys Met
805 810 815
Val Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala Leu Asp
820 825 830
Cys Cys Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser His Leu
835 840 845
Gln Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val Ser Val
850 855 860
Glu Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser Leu Gly
865 870 875 880
Gly Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu Gln Lys
885 890 895
Asp His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu Ser Pro
900 905 910
Gly Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly Leu Arg
915 920 925
Thr Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro Ser Asp
930 935 940
Ile Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp Arg Asp
945 950 955 960
Pro Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile Phe Glu
965 970 975
Gln Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg Val Ala
980 985 990
Asn Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly Cys Phe
995 1000 1005
Asn Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
1010 1015 1020
<210> 3030
<211> 3063
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3030
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccgggatccg atattcaact tacacagtcc cctagttcct tgtccgcctc cgtcggcgac
120
agagttacca tgacttgtcg agcgtcttct agcgtttcct acattcattg gttccaacag
180
aagcccggaa aggcaccaaa accttggatc tacgccacgt ccaatttggc tagtggtgtt
240
ccggtgcgat tttccgggtc aggtagcggg acggactata cttttaccat ttcaagcctt
300
cagcctgaag acatcgcgac gtactattgt cagcagtgga cctctaaccc tcctaccttt
360
ggcggtggaa caaagctgga gatcaaacga ggcgggggtg gctctggggg aggaggttcc
420
ggtgggggag gctctcaagt acaactgcaa caaagtgggg ctgaagtgaa gaagcccggt
480
tcttcagtca aagtatcatg taaggcaagt ggttatactt ttacgtctta taacatgcat
540
tgggtaaagc aagcccctgg tcagggcctc gagtggattg gtgcgatcta ccctggaatg
600
ggtgatacga gctataatca gaaattcaag gggaaagcca ccttgactgc agacgaatct
660
acgaacacgg cttacatgga gcttagctca ctcagatcag aggatacagc cttttactac
720
tgcgctagat caacttatta cggaggagac tggtattttg atgtatgggg tcaggggacc
780
acagtcactg ttagctctgc tagcaccacg acgccagcgc cgcgaccacc aacaccggcg
840
cccaccatcg cgtcgcagcc cctgtccctg cgcccagagg cgtgccggcc agcggcgggg
900
ggcgcagtgc acacgagggg gctggacttc gcctgtgatt ccggaatcta catctgggcg
960
cccttggccg ggacttgtgg ggtccttctc ctgtcactgg ttatcaccct ttactgcaaa
1020
cggggcagaa agaaactcct gtatatattc aaacaaccat ttatgagacc agtacaaact
1080
actcaagagg aagatggctg tagctgccga tttccagaag aagaagaagg aggatgtgaa
1140
ctgagagtga agttcagcag gagcgcagac gcccccgcgt accagcaggg ccagaaccag
1200
ctctataacg agctcaatct aggacgaaga gaggagtacg atgttttgga caagagacgt
1260
ggccgggacc ctgagatggg gggaaagccg agaaggaaga accctcagga aggcctgtac
1320
aatgaactgc agaaagataa gatggcggag gcctacagtg agattgggat gaaaggcgag
1380
cgccggaggg gcaaggggca cgatggcctt taccagggtc tcagtacagc caccaaggac
1440
acctacgacg cccttcacat gcaggccctg ccccctcgcg gaagcggcgc caccaatttc
1500
agcctgctga aacaggccgg cgacgtggaa gagaaccctg gccctagagg cgtgcaggtg
1560
gaaaccatct ctcccggcga cggcagaacc ttccctaaga ggggccagac ctgcgtggtg
1620
cactacaccg gcatgctgga agatggcaag aagatggaca gctcccggga ccggaacaag
1680
cccttcaagt tcatgctggg caagcaggaa gtgatccggg gctgggaaga gggcgtggca
1740
cagatgtctg tgggccagag agccaagctg accatcagcc ccgattacgc ctacggcgcc
1800
acaggccacc ctggcatcat tcctccacac gccacactgg tgttcgatgt ggaactgctg
1860
aagctggaaa cccggggagt gcaggtggaa acaatcagcc ctggcgacgg ccggaccttt
1920
ccaaaacggg gacagacatg tgtggtgcat tatacaggga tgctggaaga tgggaaaaaa
1980
atggatagca gccgcgaccg caacaaacct tttaagttta tgctggggaa acaggaagtg
2040
attagaggct gggaagaggg ggtggcacag atgagcgtgg gacagcgggc caaactgaca
2100
atctcccccg actatgccta tggggccacc ggacaccccg gaatcatccc acctcatgct
2160
accctggtgt ttgacgtgga actgctgaaa ctggaaacaa gcggcggagg cagcggcggc
2220
tttggagatg tgggagccct ggaaagcctg cggggcaatg ccgatctggc ctacatcctg
2280
agcatggaac cctgcggcca ctgcctgatt atcaacaacg tgaacttctg cagagagagc
2340
ggcctgcgga ccagaaccgg cagcaacatc gactgcgaga agctgcggcg gagattcagc
2400
agcctgcact tcatggtgga agtgaagggg gacctgaccg ccaagaaaat ggtgctggct
2460
ctgctggaac tggcccagca ggatcatggc gccctggact gttgcgtggt cgtgatcctg
2520
agccacggct gccaggccag ccatctgcag tttcccggcg ctgtgtatgg caccgatggc
2580
tgccctgtgt ccgtggaaaa gatcgtgaat atcttcaacg gcaccagctg ccccagcctg
2640
ggcggaaagc ctaagctgtt ctttattcaa gcctgtgggg gcgagcagaa ggaccacgga
2700
tttgaggtgg ccagcacctc ccccgaggat gagagccctg gcagcaaccc tgagcctgac
2760
gccaccccat tccaggaagg actgcggacc ttcgaccagc tggacgccat ctctagcctg
2820
cccaccccca gcgacatctt cgtgtcctac agcaccttcc ctggctttgt gtcctggcgg
2880
gaccccaagt ccggctcttg gtacgtggaa accctggacg acatctttga gcagtgggcc
2940
catagcgagg acctgcagag cctgctgctg agggtggcca atgccgtgtc cgtgaagggc
3000
atctacaagc agatgcccgg ctgcttcaac ttcctgcgga agaagctgtt tttcaagacc
3060
agc
3063
<210> 3031
<211> 1021
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3031
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser
20 25 30
Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Met Thr Cys Arg Ala
35 40 45
Ser Ser Ser Val Ser Tyr Ile His Trp Phe Gln Gln Lys Pro Gly Lys
50 55 60
Ala Pro Lys Pro Trp Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val
65 70 75 80
Pro Val Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr
85 90 95
Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln
100 105 110
Trp Thr Ser Asn Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
115 120 125
Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
145 150 155 160
Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
165 170 175
Tyr Asn Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp
180 185 190
Ile Gly Ala Ile Tyr Pro Gly Met Gly Asp Thr Ser Tyr Asn Gln Lys
195 200 205
Phe Lys Gly Lys Ala Thr Leu Thr Ala Asp Glu Ser Thr Asn Thr Ala
210 215 220
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Phe Tyr Tyr
225 230 235 240
Cys Ala Arg Ser Thr Tyr Tyr Gly Gly Asp Trp Tyr Phe Asp Val Trp
245 250 255
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ser Gly Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser Gly
485 490 495
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
500 505 510
Pro Gly Pro Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly
515 520 525
Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly
530 535 540
Met Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys
545 550 555 560
Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu
565 570 575
Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile
580 585 590
Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro
595 600 605
Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr
610 615 620
Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe
625 630 635 640
Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu
645 650 655
Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys
660 665 670
Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val
675 680 685
Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp
690 695 700
Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala
705 710 715 720
Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Ser Gly Gly
725 730 735
Gly Ser Gly Gly Phe Gly Asp Val Gly Ala Leu Glu Ser Leu Arg Gly
740 745 750
Asn Ala Asp Leu Ala Tyr Ile Leu Ser Met Glu Pro Cys Gly His Cys
755 760 765
Leu Ile Ile Asn Asn Val Asn Phe Cys Arg Glu Ser Gly Leu Arg Thr
770 775 780
Arg Thr Gly Ser Asn Ile Asp Cys Glu Lys Leu Arg Arg Arg Phe Ser
785 790 795 800
Ser Leu His Phe Met Val Glu Val Lys Gly Asp Leu Thr Ala Lys Lys
805 810 815
Met Val Leu Ala Leu Leu Glu Leu Ala Gln Gln Asp His Gly Ala Leu
820 825 830
Asp Cys Cys Val Val Val Ile Leu Ser His Gly Cys Gln Ala Ser His
835 840 845
Leu Gln Phe Pro Gly Ala Val Tyr Gly Thr Asp Gly Cys Pro Val Ser
850 855 860
Val Glu Lys Ile Val Asn Ile Phe Asn Gly Thr Ser Cys Pro Ser Leu
865 870 875 880
Gly Gly Lys Pro Lys Leu Phe Phe Ile Gln Ala Cys Gly Gly Glu Gln
885 890 895
Lys Asp His Gly Phe Glu Val Ala Ser Thr Ser Pro Glu Asp Glu Ser
900 905 910
Pro Gly Ser Asn Pro Glu Pro Asp Ala Thr Pro Phe Gln Glu Gly Leu
915 920 925
Arg Thr Phe Asp Gln Leu Asp Ala Ile Ser Ser Leu Pro Thr Pro Ser
930 935 940
Asp Ile Phe Val Ser Tyr Ser Thr Phe Pro Gly Phe Val Ser Trp Arg
945 950 955 960
Asp Pro Lys Ser Gly Ser Trp Tyr Val Glu Thr Leu Asp Asp Ile Phe
965 970 975
Glu Gln Trp Ala His Ser Glu Asp Leu Gln Ser Leu Leu Leu Arg Val
980 985 990
Ala Asn Ala Val Ser Val Lys Gly Ile Tyr Lys Gln Met Pro Gly Cys
995 1000 1005
Phe Asn Phe Leu Arg Lys Lys Leu Phe Phe Lys Thr Ser
1010 1015 1020
<210> 3032
<211> 2811
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полинуклеотид"
<400> 3032
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccgggatccc ggggcgtgca ggttgagaca atttccccag gagatgggcg aacgttcccc
120
aagcgcggac agacatgcgt tgtgcactac acaggaatgt tggaggacgg aaagaaaatg
180
gacagttcaa gagatcggaa caaaccattc aaattcatgt tgggaaaaca ggaagtgata
240
cggggctggg aagagggtgt agcgcaaatg tccgttggtc aacgagcaaa actcacgata
300
agtcccgatt atgcttacgg cgcaaccggt cacccgggca tcataccgcc tcatgcgact
360
ttggtctttg atgtggagct gttgaaactt gaaactcgcg gagtacaggt tgaaacaata
420
tcacccgggg acgggcggac ttttccgaag agaggtcaga cctgcgtcgt ccattatacc
480
ggtatgctgg aggacggaaa gaaaatggac agctcacggg accgaaataa accattcaaa
540
tttatgttgg ggaaacaaga ggttatcagg ggctgggagg agggtgtggc ccagatgtct
600
gtcggtcagc gcgcgaaact cacaatctct ccggattatg cgtatggggc gacagggcat
660
ccgggaatta tccctcccca cgctaccttg gttttcgatg ttgagcttct gaagttggag
720
accagaggag ttcaagtgga gacaatatct cctggggatg gacggacgtt ccccaagcgc
780
ggccagacct gtgtagtcca ctacacaggg atgcttgaag acggaaaaaa gatggatagc
840
agtagagatc gcaacaaacc atttaagttc atgctgggga agcaggaagt aatacgcggc
900
tgggaggaag gcgtggcaca gatgagtgtt ggtcaacggg ccaaacttac tatttctccc
960
gattatgcgt atggagccac cgggcaccct ggcattatcc caccccatgc cacattggtt
1020
tttgacgttg aattgcttaa attggagacc aggggagtcc aagtggaaac aatatcaccg
1080
ggggatggtc ggacttttcc taaaaggggc caaacctgtg tagtccatta taccggaatg
1140
ctcgaagacg gaaagaaaat ggactcttct agagaccgca ataagccctt caagttcatg
1200
ttgggtaagc aagaggtgat ccggggctgg gaagaggggg tcgctcaaat gtccgtcggt
1260
cagcgagcta aactgactat ttccccagac tacgcatatg gagcgactgg ccaccccggt
1320
attattcctc cccatgcgac tctcgtgttc gacgtagaac tcttgaaatt ggaaacgtca
1380
gcccggaaca ggcggaagag agatattcaa cttacacagt cccctagttc cttgtccgcc
1440
tccgtcggcg acagagttac catgacttgt cgagcgtctt ctagcgtttc ctacattcat
1500
tggttccaac agaagcccgg aaaggcacca aaaccttgga tctacgccac gtccaatttg
1560
gctagtggtg ttccggtgcg attttccggg tcaggtagcg ggacggacta tacttttacc
1620
atttcaagcc ttcagcctga agacatcgcg acgtactatt gtcagcagtg gacctctaac
1680
cctcctacct ttggcggtgg aacaaagctg gagatcaaac gaggcggggg tggctctggg
1740
ggaggaggtt ccggtggggg aggctctcaa gtacaactgc aacaaagtgg ggctgaagtg
1800
aagaagcccg gttcttcagt caaagtatca tgtaaggcaa gtggttatac ttttacgtct
1860
tataacatgc attgggtaaa gcaagcccct ggtcagggcc tcgagtggat tggtgcgatc
1920
taccctggaa tgggtgatac gagctataat cagaaattca aggggaaagc caccttgact
1980
gcagacgaat ctacgaacac ggcttacatg gagcttagct cactcagatc agaggataca
2040
gccttttact actgcgctag atcaacttat tacggaggag actggtattt tgatgtatgg
2100
ggtcagggga ccacagtcac tgttagctct gctagcacca cgacgccagc gccgcgacca
2160
ccaacaccgg cgcccaccat cgcgtcgcag cccctgtccc tgcgcccaga ggcgtgccgg
2220
ccagcggcgg ggggcgcagt gcacacgagg gggctggact tcgcctgtga ttccggaatc
2280
tacatctggg cgcccttggc cgggacttgt ggggtccttc tcctgtcact ggttatcacc
2340
ctttactgca aacggggcag aaagaaactc ctgtatatat tcaaacaacc atttatgaga
2400
ccagtacaaa ctactcaaga ggaagatggc tgtagctgcc gatttccaga agaagaagaa
2460
ggaggatgtg aactgagagt gaagttcagc aggagcgcag acgcccccgc gtaccagcag
2520
ggccagaacc agctctataa cgagctcaat ctaggacgaa gagaggagta cgatgttttg
2580
gacaagagac gtggccggga ccctgagatg gggggaaagc cgagaaggaa gaaccctcag
2640
gaaggcctgt acaatgaact gcagaaagat aagatggcgg aggcctacag tgagattggg
2700
atgaaaggcg agcgccggag gggcaagggg cacgatggcc tttaccaggg tctcagtaca
2760
gccaccaagg acacctacga cgcccttcac atgcaggccc tgccccctcg c
2811
<210> 3033
<211> 939
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
полипептид"
<400> 3033
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gly Ser Arg Gly Val Gln Val Glu Thr Ile Ser
20 25 30
Pro Gly Asp Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val
35 40 45
His Tyr Thr Gly Met Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg
50 55 60
Asp Arg Asn Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile
65 70 75 80
Arg Gly Trp Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala
85 90 95
Lys Leu Thr Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro
100 105 110
Gly Ile Ile Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu
115 120 125
Lys Leu Glu Thr Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp
130 135 140
Gly Arg Thr Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr
145 150 155 160
Gly Met Leu Glu Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn
165 170 175
Lys Pro Phe Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp
180 185 190
Glu Glu Gly Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr
195 200 205
Ile Ser Pro Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile
210 215 220
Pro Pro His Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu
225 230 235 240
Thr Arg Gly Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr
245 250 255
Phe Pro Lys Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu
260 265 270
Glu Asp Gly Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe
275 280 285
Lys Phe Met Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly
290 295 300
Val Ala Gln Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro
305 310 315 320
Asp Tyr Ala Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His
325 330 335
Ala Thr Leu Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Arg Gly
340 345 350
Val Gln Val Glu Thr Ile Ser Pro Gly Asp Gly Arg Thr Phe Pro Lys
355 360 365
Arg Gly Gln Thr Cys Val Val His Tyr Thr Gly Met Leu Glu Asp Gly
370 375 380
Lys Lys Met Asp Ser Ser Arg Asp Arg Asn Lys Pro Phe Lys Phe Met
385 390 395 400
Leu Gly Lys Gln Glu Val Ile Arg Gly Trp Glu Glu Gly Val Ala Gln
405 410 415
Met Ser Val Gly Gln Arg Ala Lys Leu Thr Ile Ser Pro Asp Tyr Ala
420 425 430
Tyr Gly Ala Thr Gly His Pro Gly Ile Ile Pro Pro His Ala Thr Leu
435 440 445
Val Phe Asp Val Glu Leu Leu Lys Leu Glu Thr Ser Ala Arg Asn Arg
450 455 460
Arg Lys Arg Gly Ser Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu
465 470 475 480
Ser Ala Ser Val Gly Asp Arg Val Thr Met Thr Cys Arg Ala Ser Ser
485 490 495
Ser Val Ser Tyr Ile His Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro
500 505 510
Lys Pro Trp Ile Tyr Ala Thr Ser Asn Leu Ala Ser Gly Val Pro Val
515 520 525
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser
530 535 540
Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Trp Thr
545 550 555 560
Ser Asn Pro Pro Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
565 570 575
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
580 585 590
Val Gln Leu Gln Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser Ser
595 600 605
Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Asn
610 615 620
Met His Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly
625 630 635 640
Ala Ile Tyr Pro Gly Met Gly Asp Thr Ser Tyr Asn Gln Lys Phe Lys
645 650 655
Gly Lys Ala Thr Leu Thr Ala Asp Glu Ser Thr Asn Thr Ala Tyr Met
660 665 670
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Phe Tyr Tyr Cys Ala
675 680 685
Arg Ser Thr Tyr Tyr Gly Gly Asp Trp Tyr Phe Asp Val Trp Gly Gln
690 695 700
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Thr Thr Pro Ala Pro
705 710 715 720
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
725 730 735
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
740 745 750
Gly Leu Asp Phe Ala Cys Asp Ser Gly Ile Tyr Ile Trp Ala Pro Leu
755 760 765
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
770 775 780
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
785 790 795 800
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
805 810 815
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
820 825 830
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
835 840 845
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
850 855 860
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
865 870 875 880
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
885 890 895
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
900 905 910
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
915 920 925
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
930 935
<210> 3034
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
олигонуклеотид"
<400> 3034
atggccttac cagtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg
60
ccg
63
<210> 3035
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 3035
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 3036
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
Синтетический
пептид"
<400> 3036
Ser Gly Gly Gly Ser
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ РАКА С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО АНТИГЕНСПЕЦИФИЧЕСКОГО РЕЦЕПТОРА НА ОСНОВЕ ГУМАНИЗИРОВАННОГО АНТИТЕЛА ПРОТИВ EGFRvIII | 2014 |
|
RU2831418C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) ПРОТИВ CD123 ДЛЯ ИСПОЛЬЗОВАНИЯ В ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2015 |
|
RU2724999C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ЭКСПРЕССИРУЮЩИХ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР КЛЕТОК | 2015 |
|
RU2751362C2 |
| CD20 ТЕРАПИЯ, CD22 ТЕРАПИЯ И КОМБИНИРОВАННАЯ ТЕРАПИЯ КЛЕТКАМИ, ЭКСПРЕССИРУЮЩИМИ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) K CD19 | 2016 |
|
RU2752918C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
| ХИМЕРНЫЕ РЕЦЕПТОРЫ АНТИГЕНА ПРОТИВ МЕЗОТЕЛИНА ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2714902C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2017 |
|
RU2826270C2 |
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНЫХ АНТИГЕННЫХ РЕЦЕПТОРОВ И ИНГИБИТОРОВ PD-1 | 2017 |
|
RU2809160C2 |
| ЛЕЧЕНИЕ РАКА С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА CLL-1 | 2015 |
|
RU2741120C2 |
| МОДИФИЦИРОВАННЫЕ НЕПРИРОДНЫЕ ЛИГАНДЫ NKG2D, КОТОРЫЕ ИЗБИРАТЕЛЬНО ДОСТАВЛЯЮТ ПРИСОЕДИНЕННЫЕ ГЕТЕРОЛОГИЧНЫЕ МОЛЕКУЛЫ К НЕПРИРОДНЫМ РЕЦЕПТОРАМ NKG2D НА CAR-КЛЕТКАХ | 2020 |
|
RU2823728C2 |
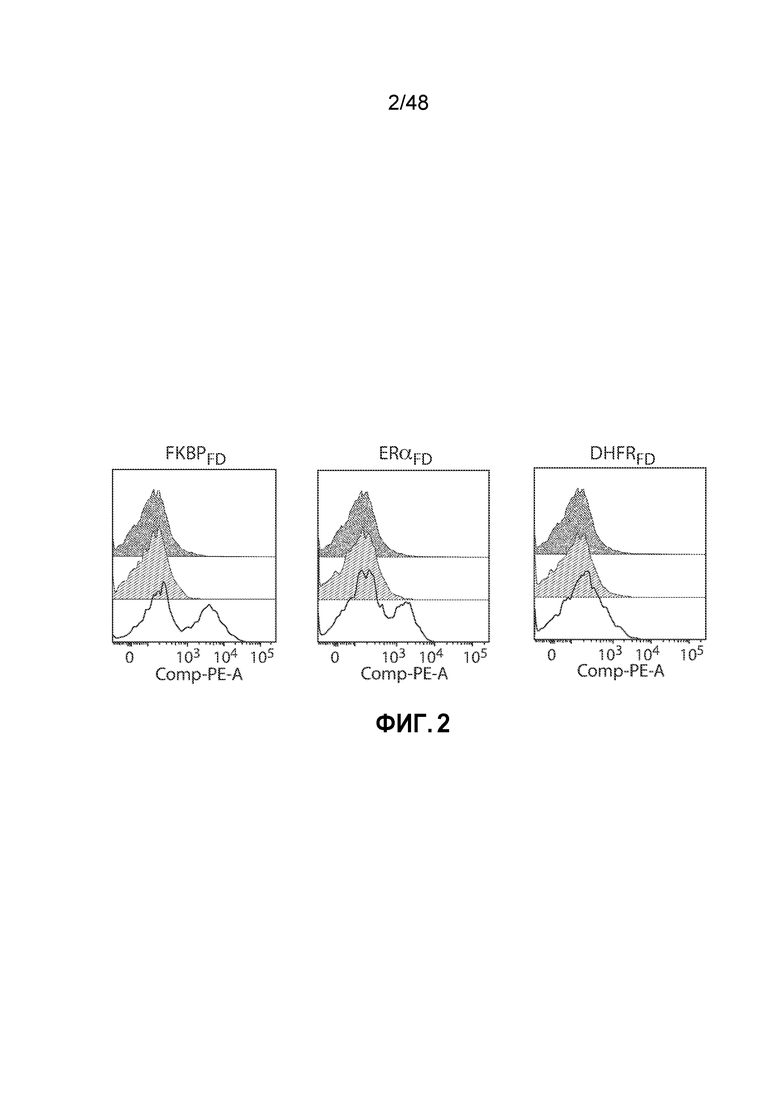
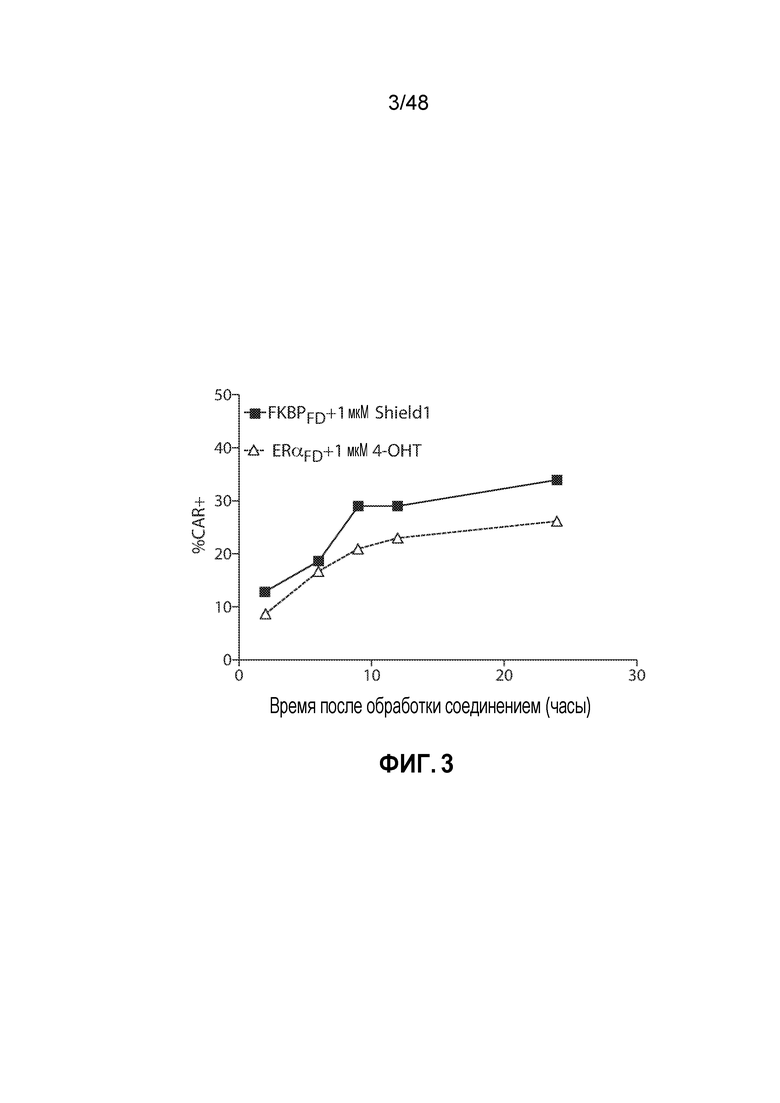

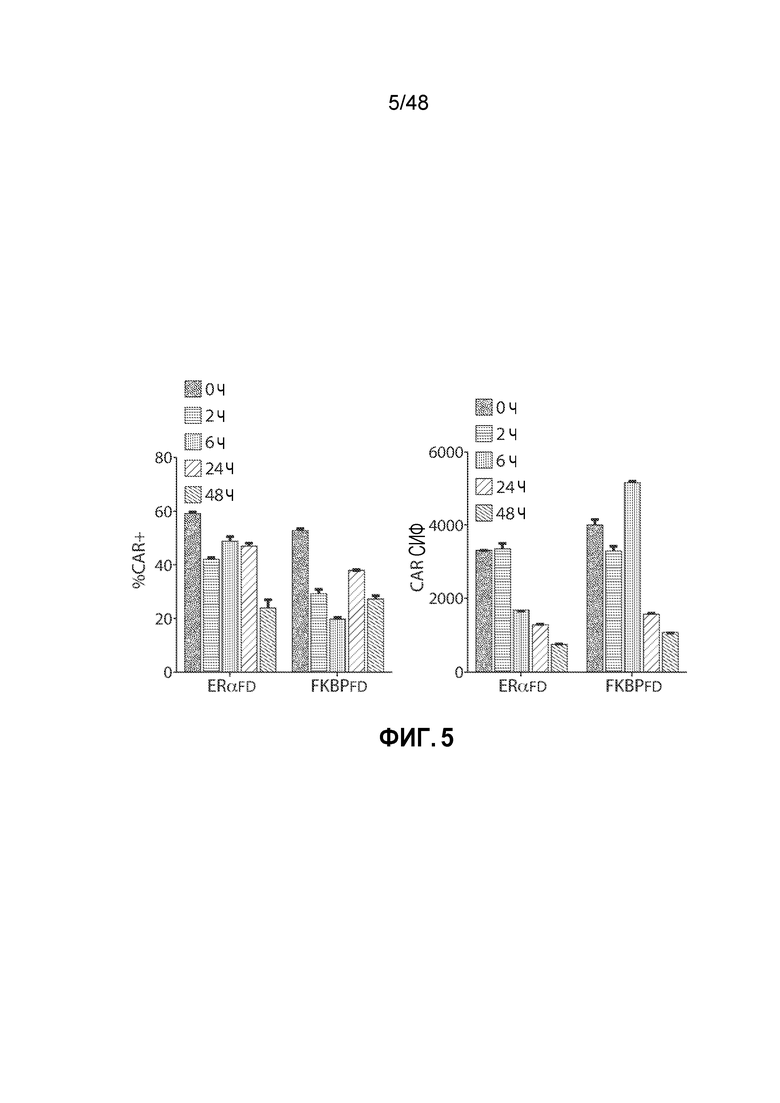
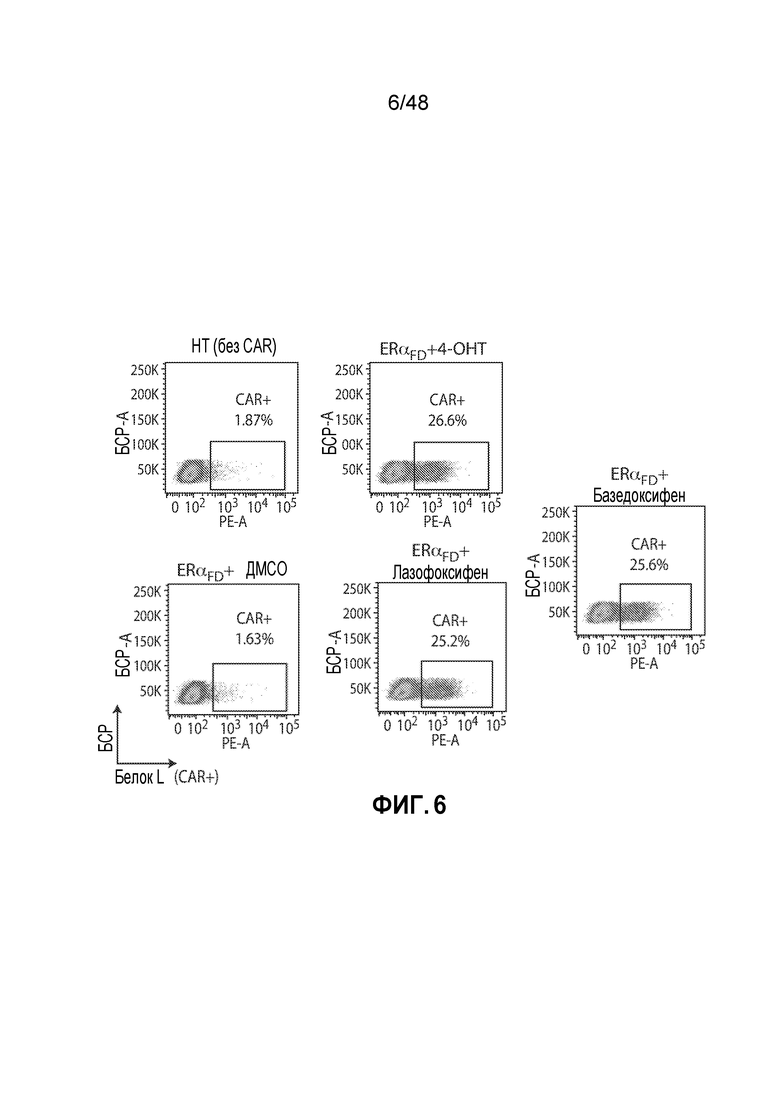

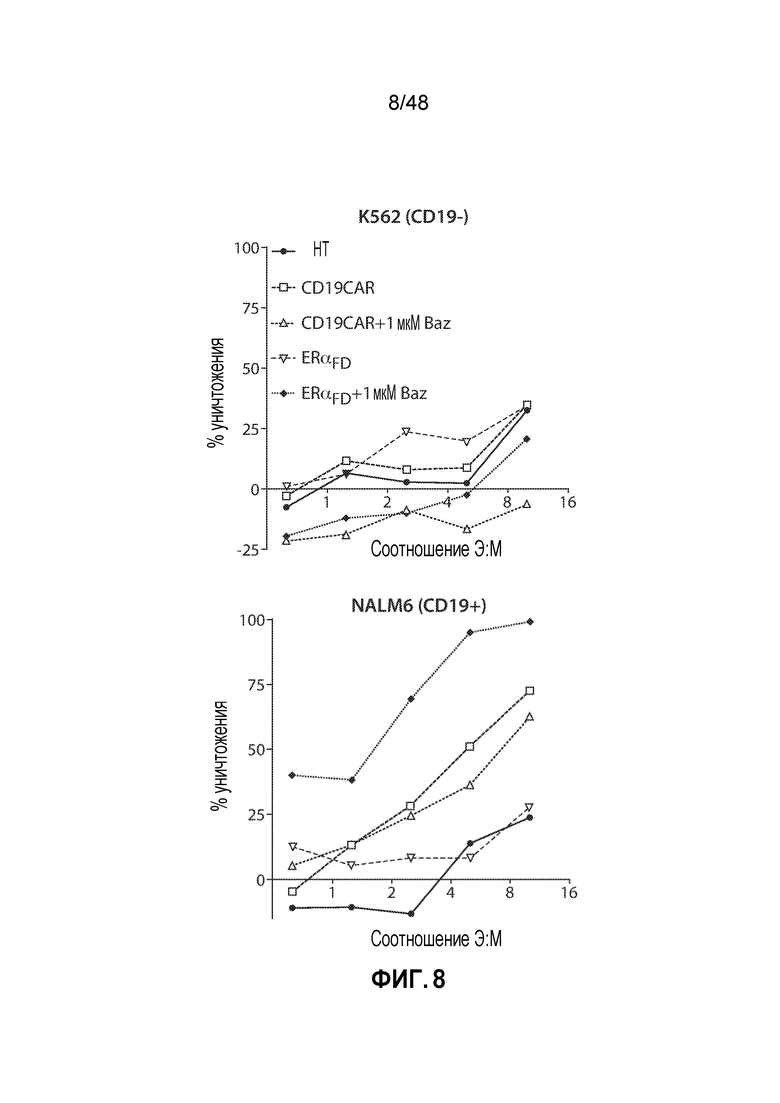

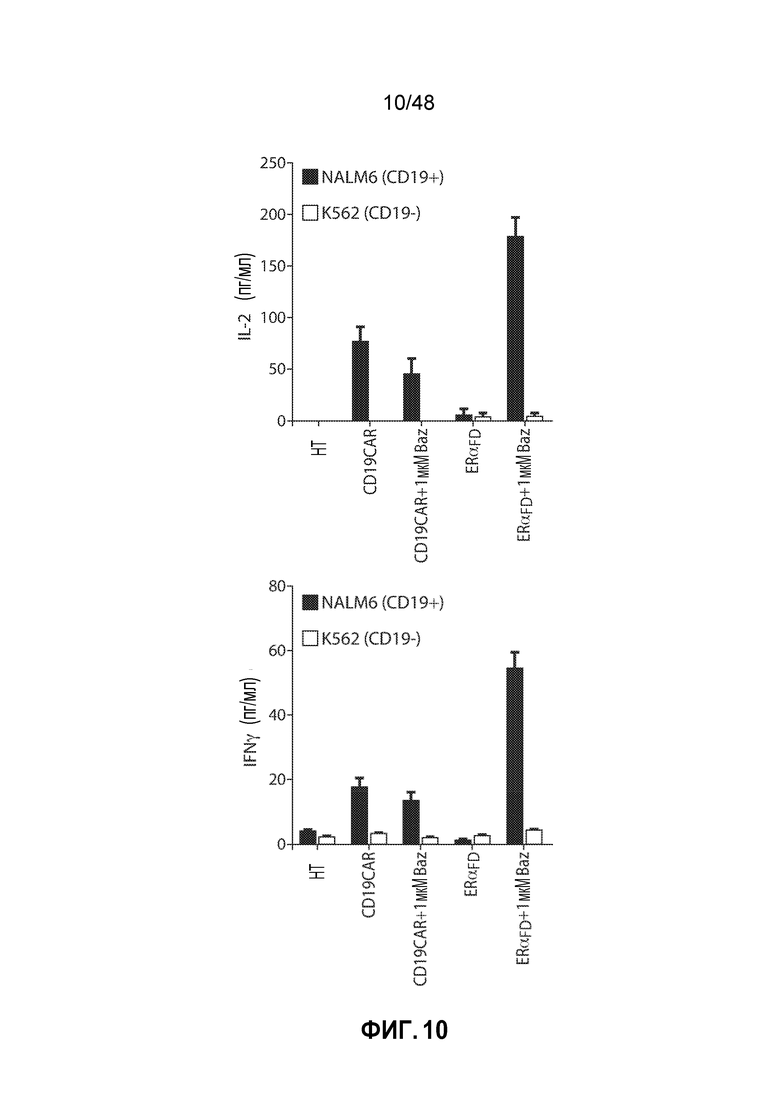
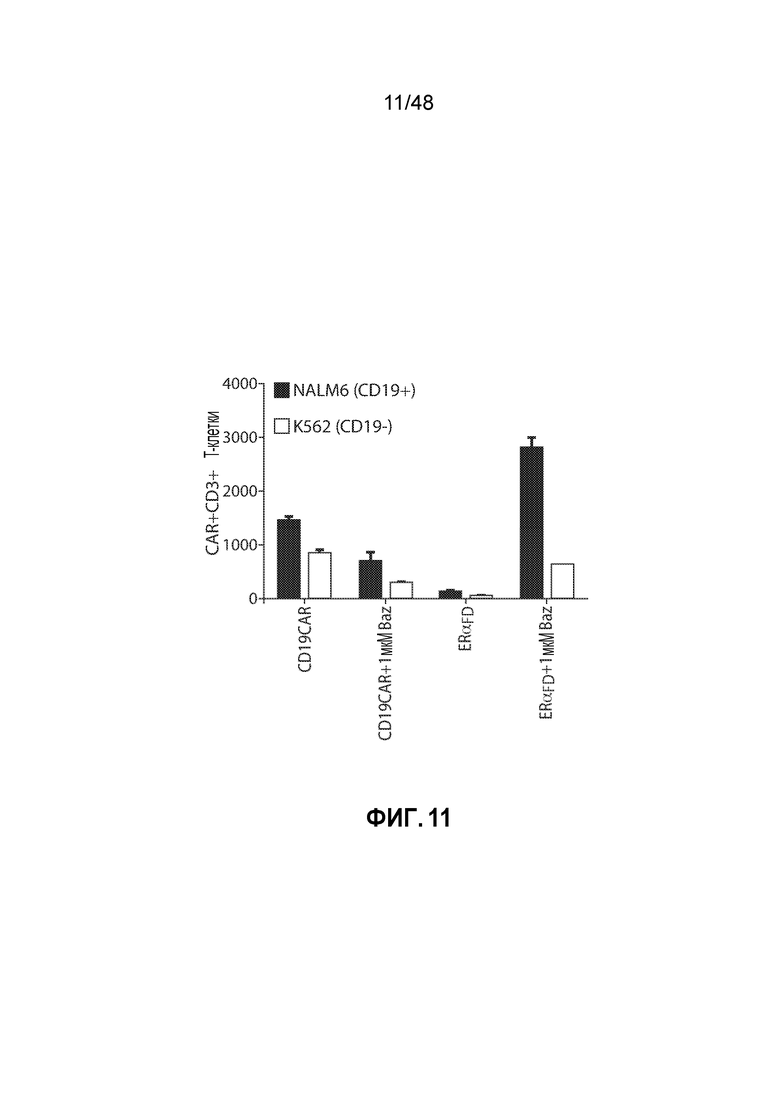
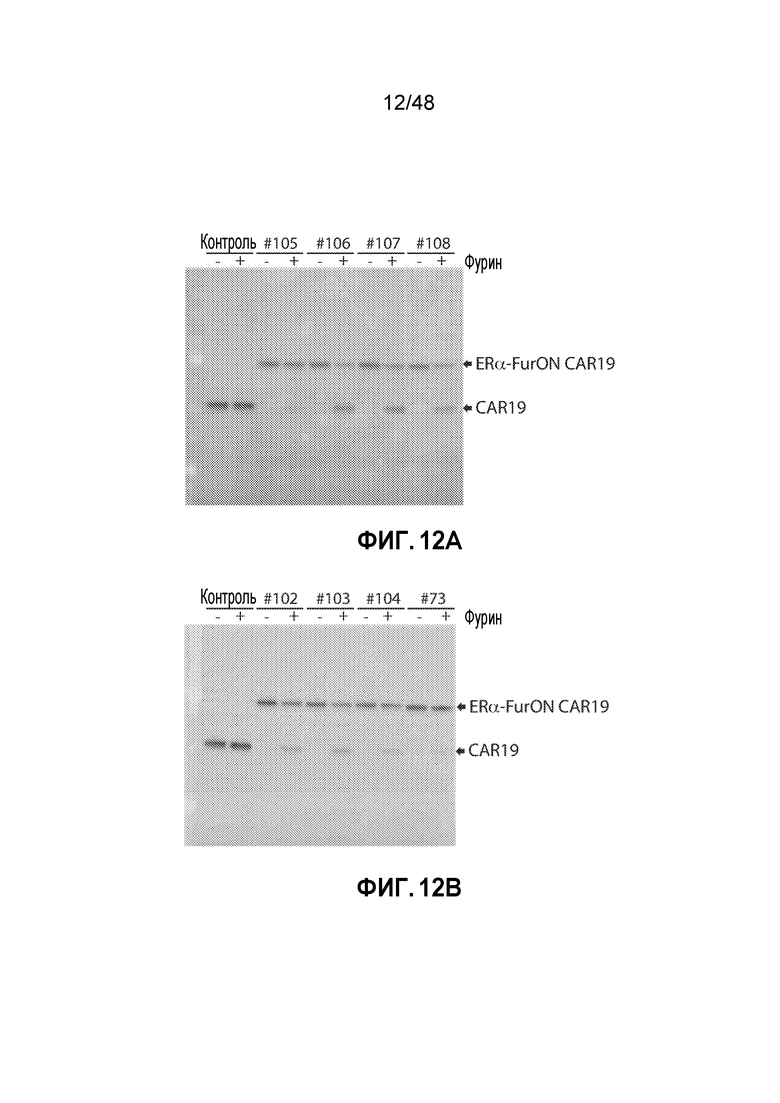
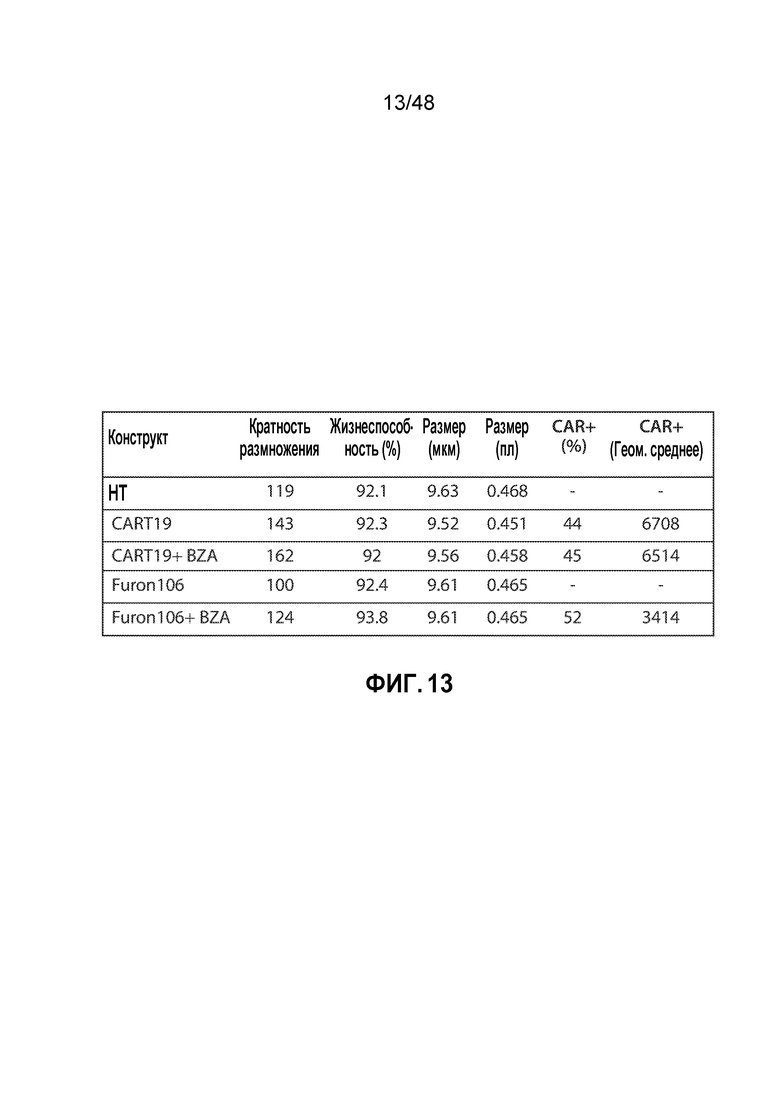
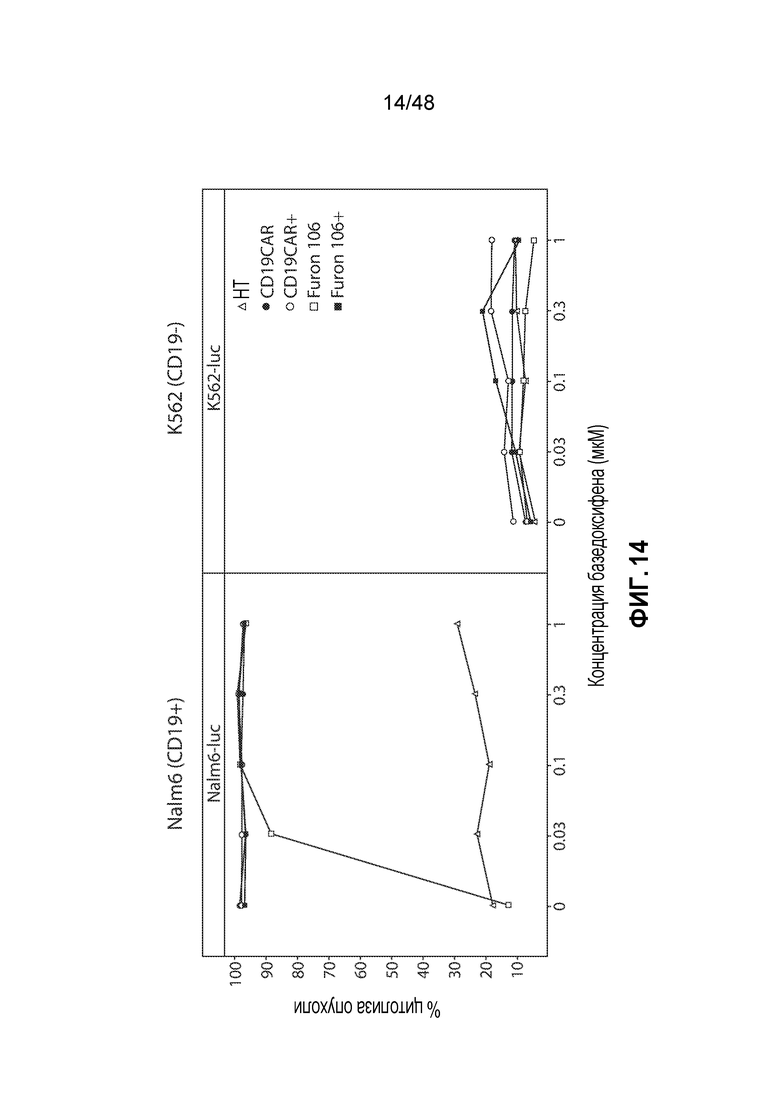
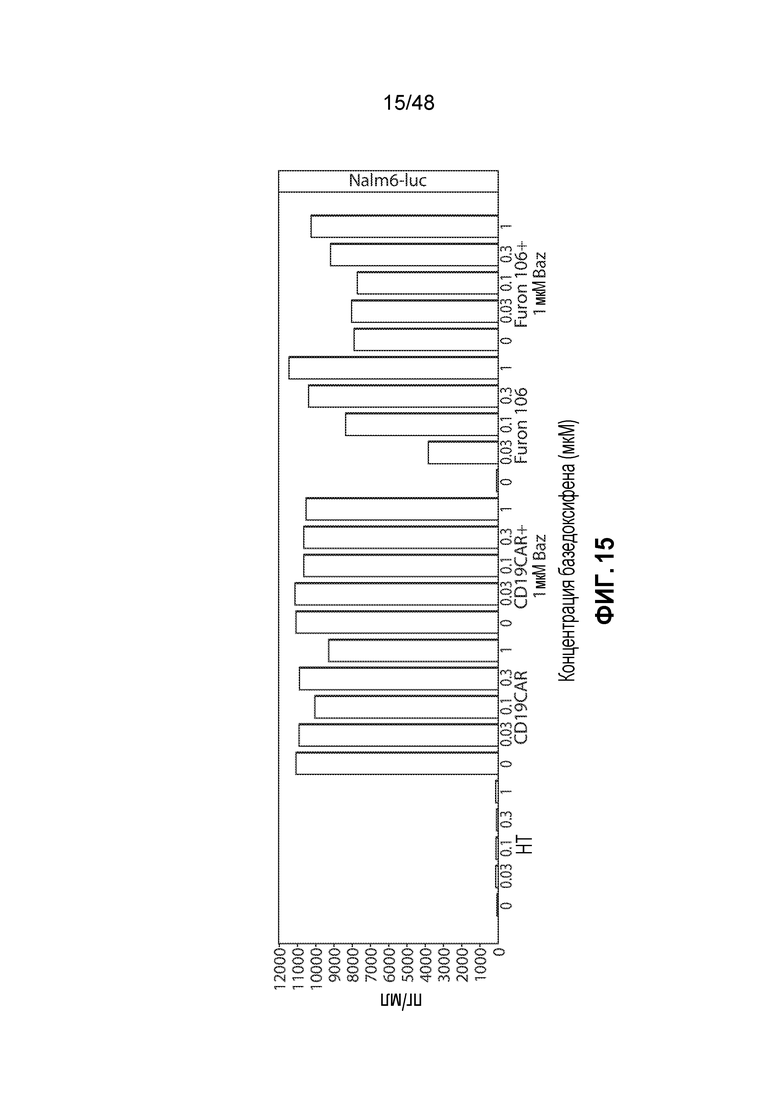

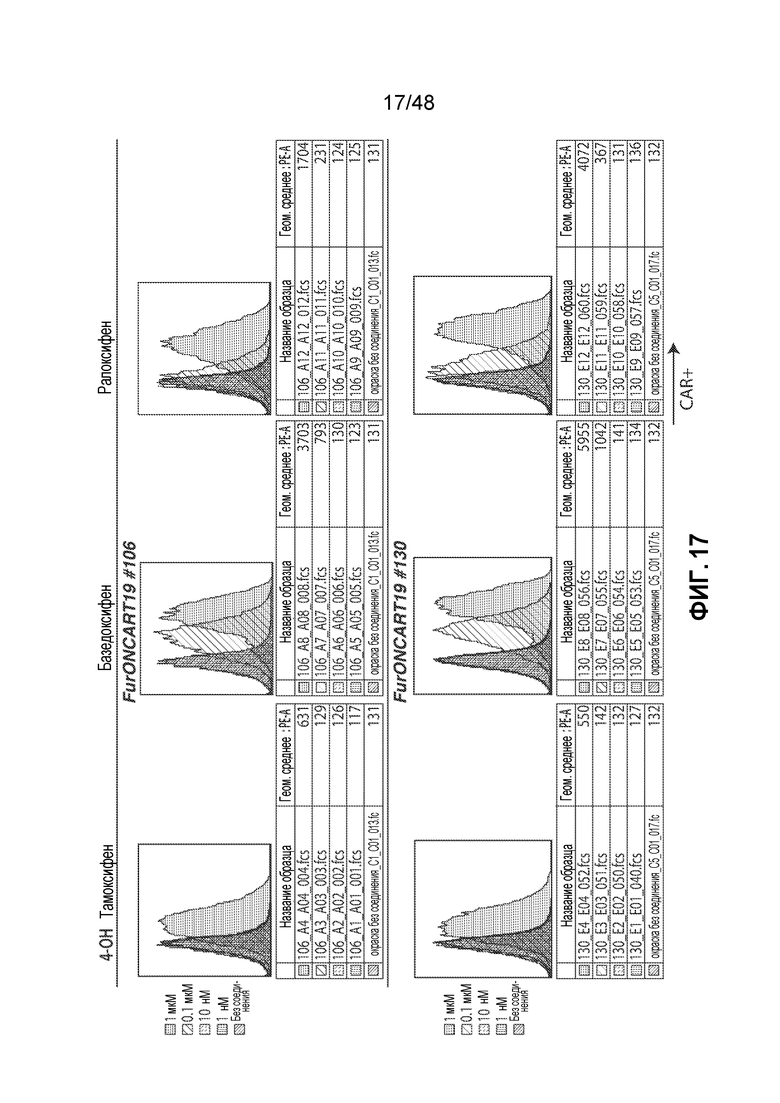
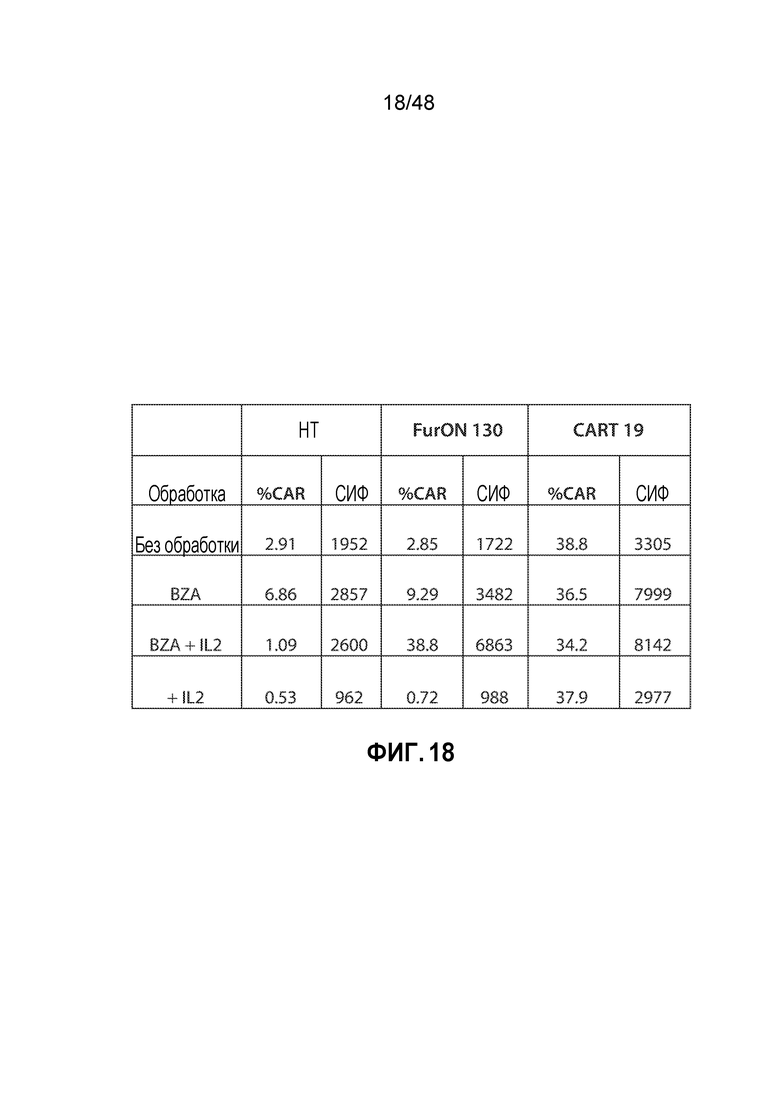
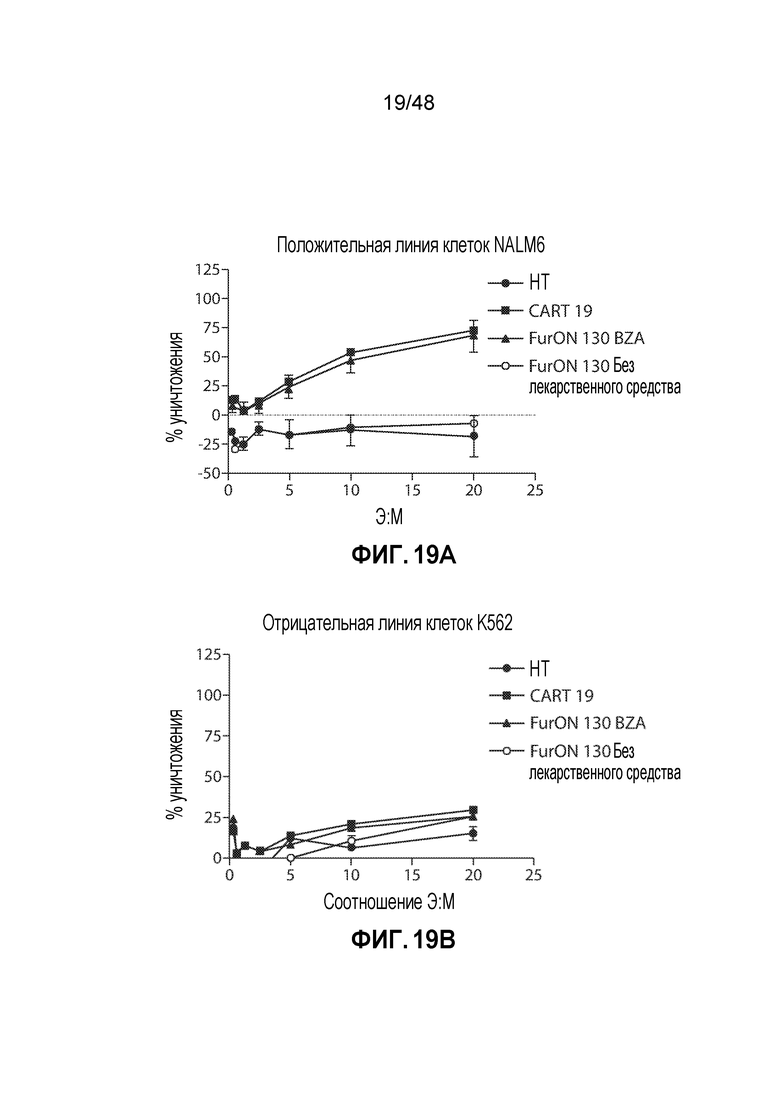
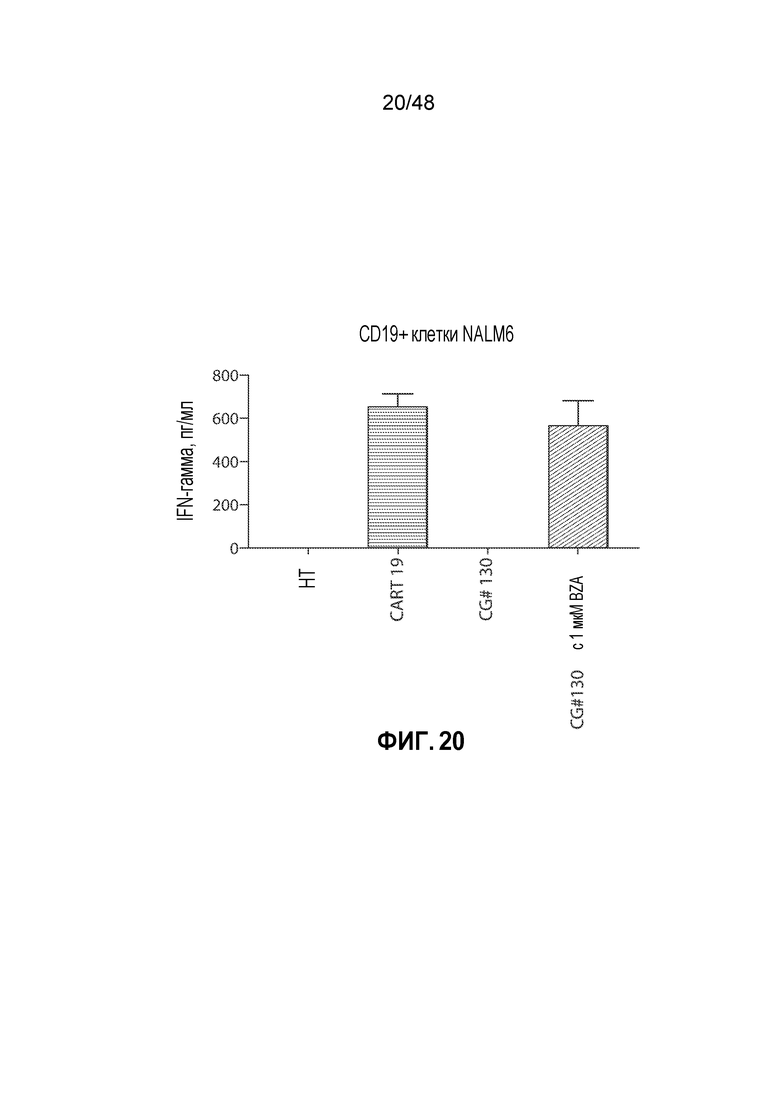
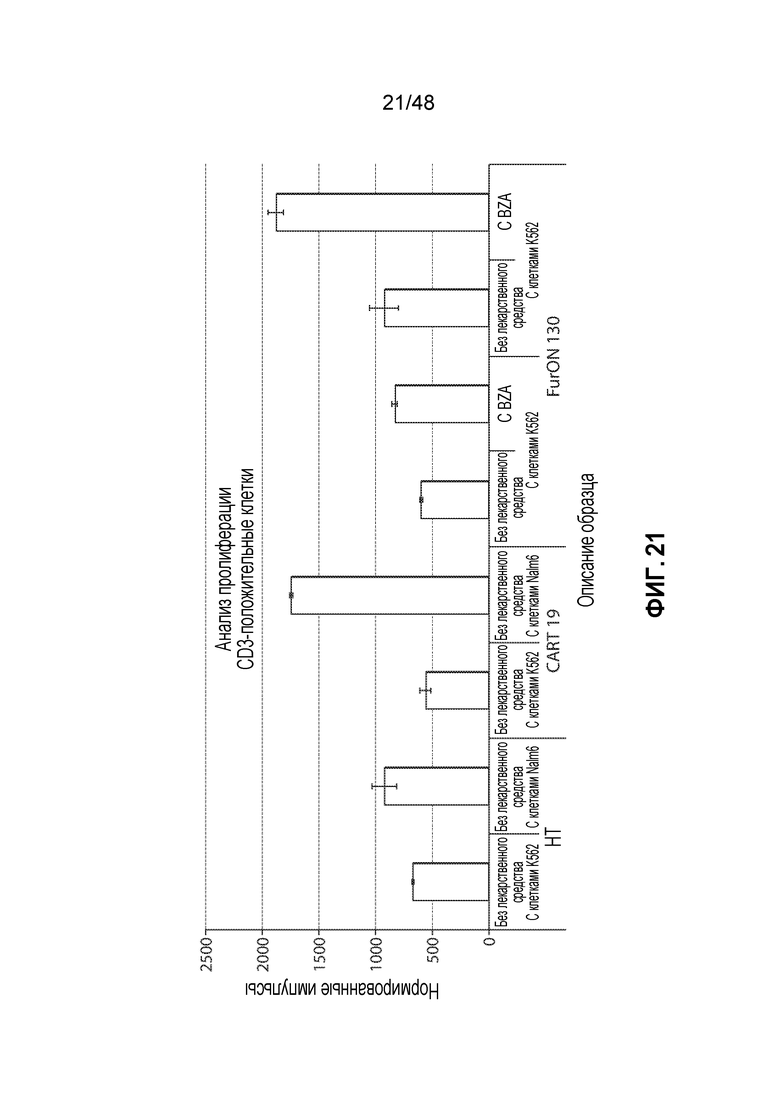

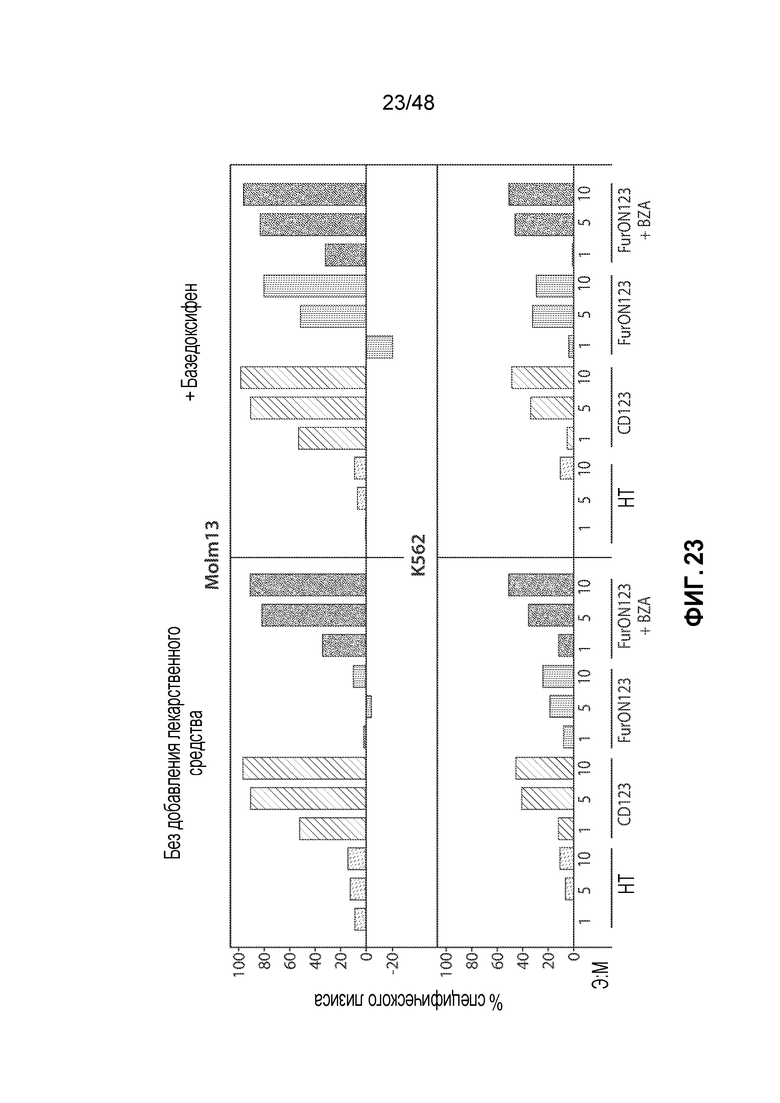
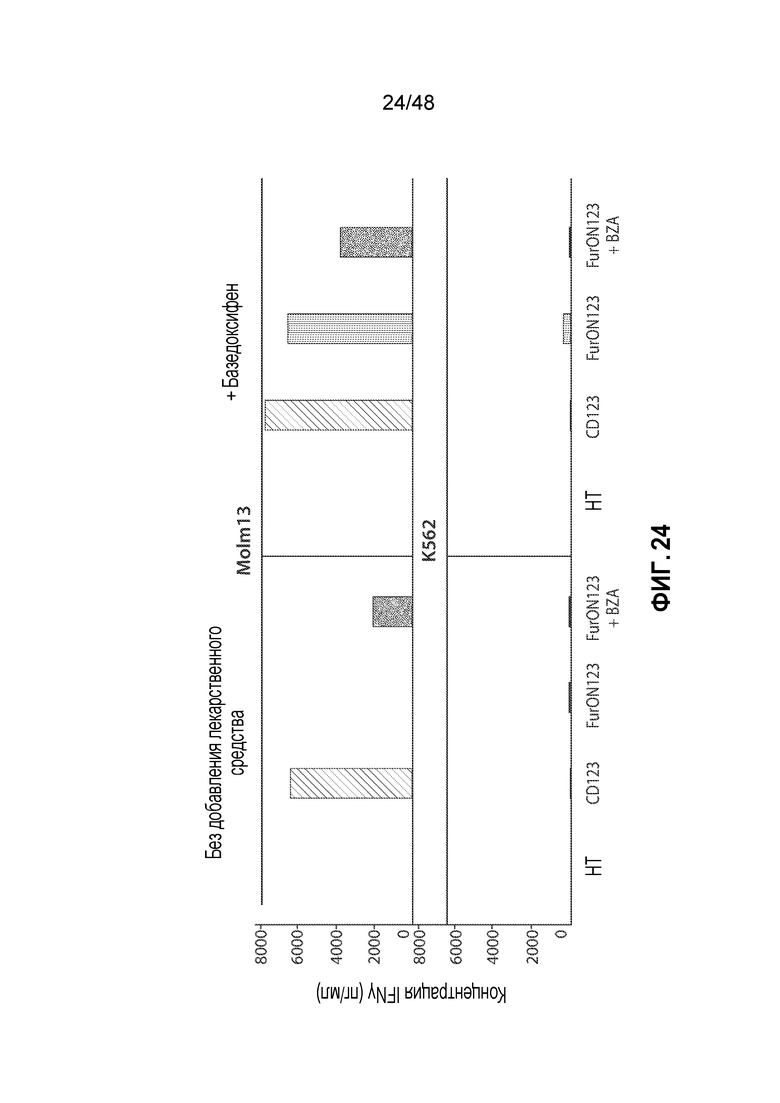


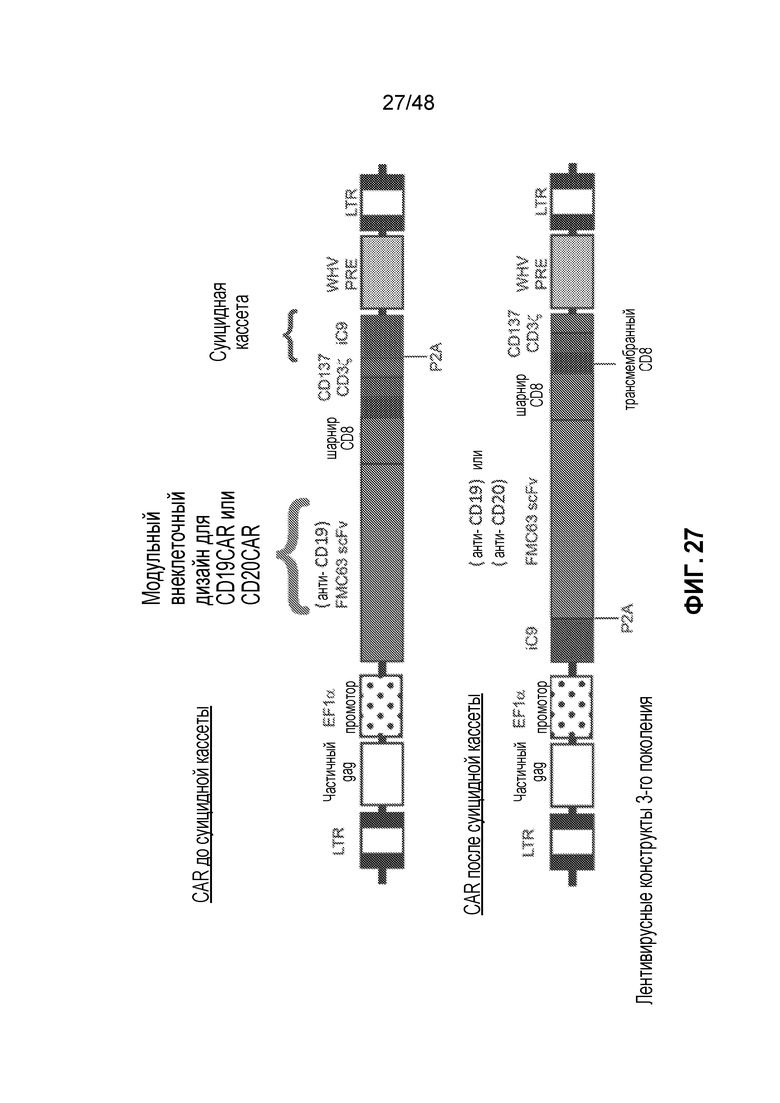
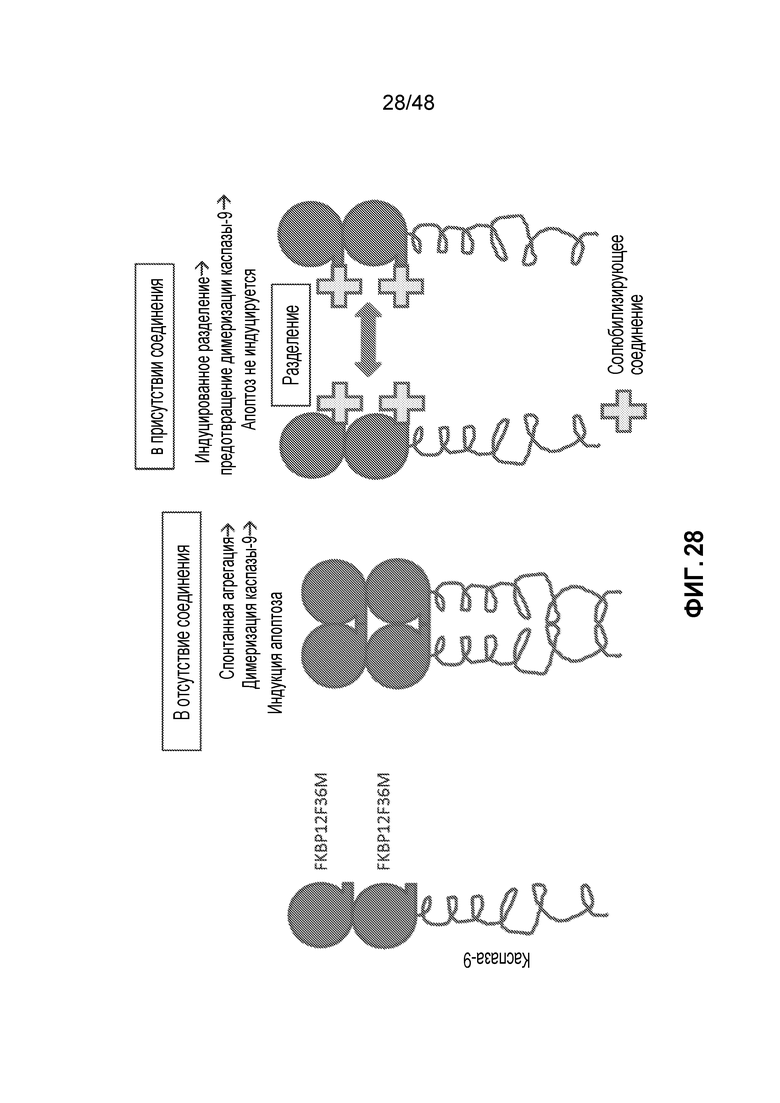
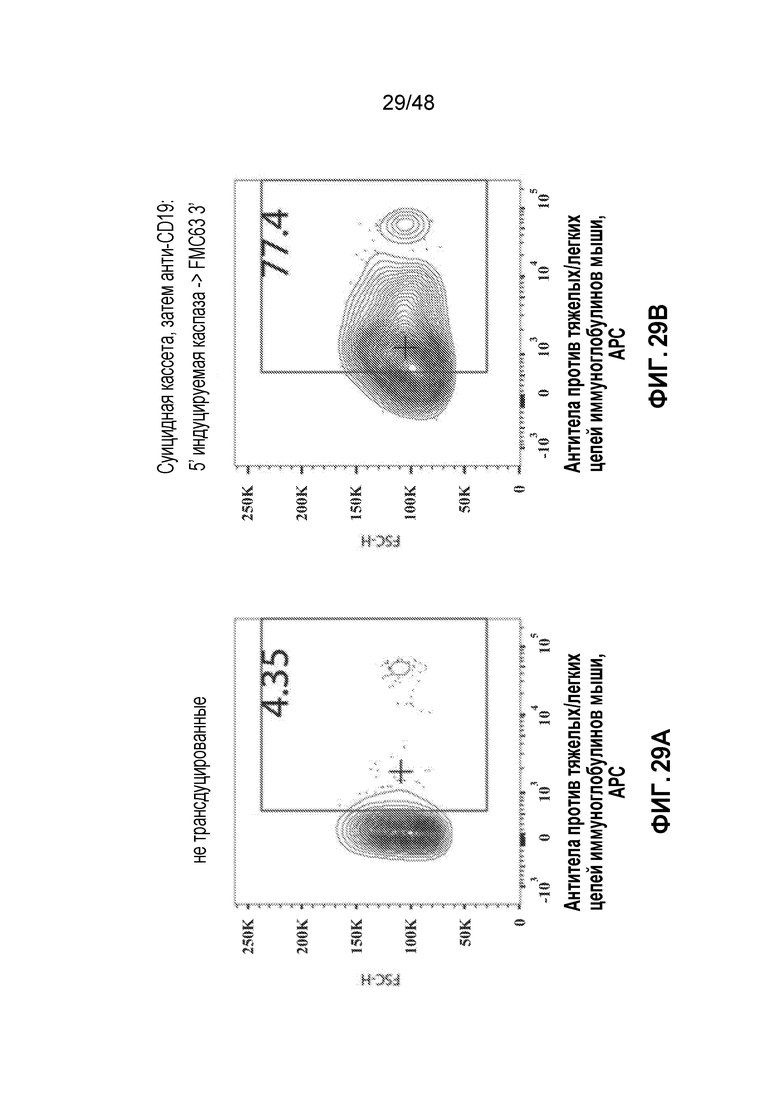
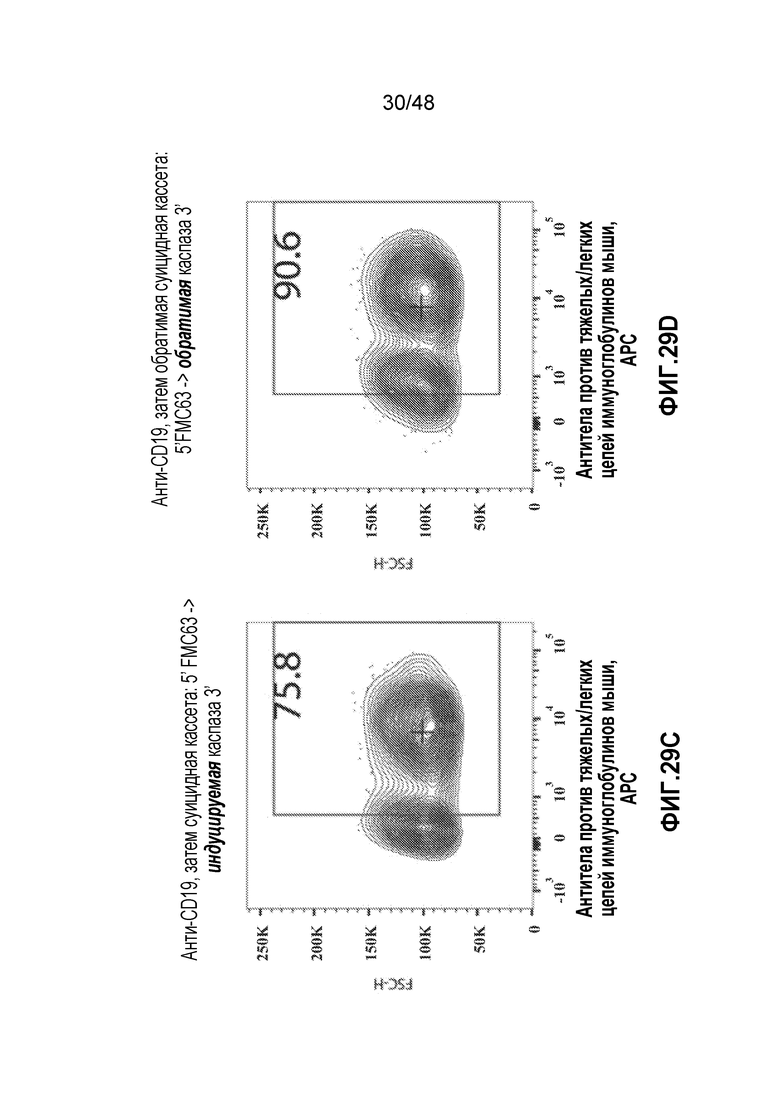
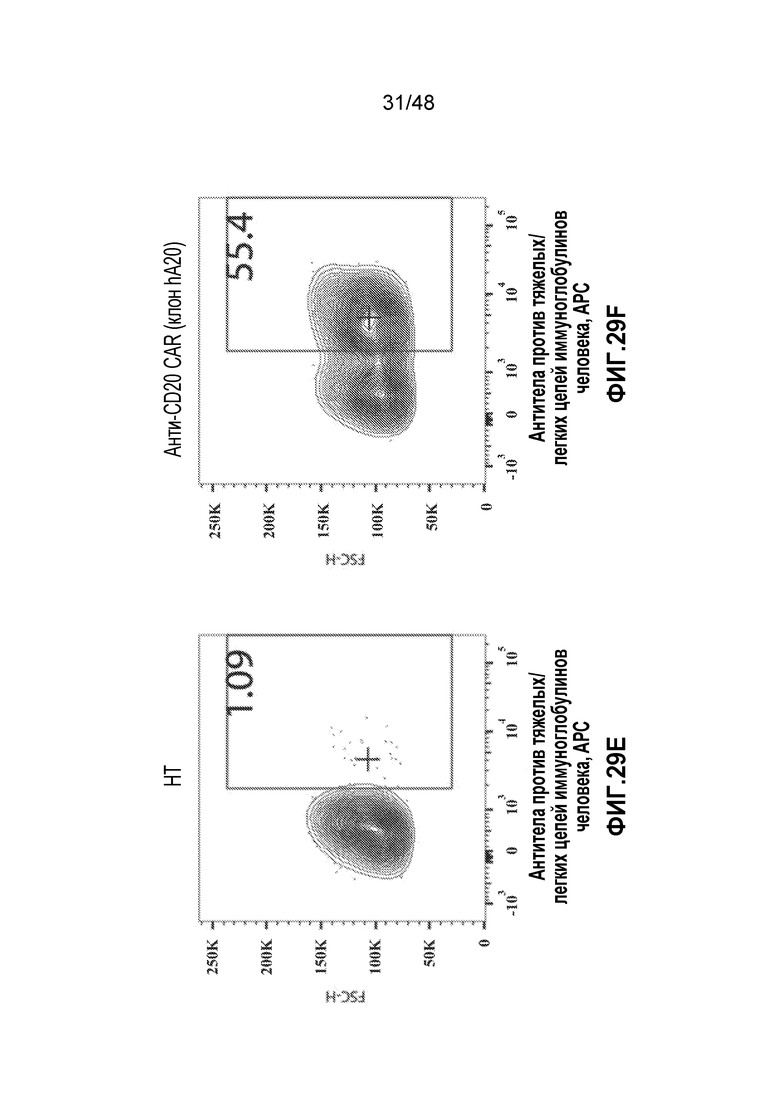
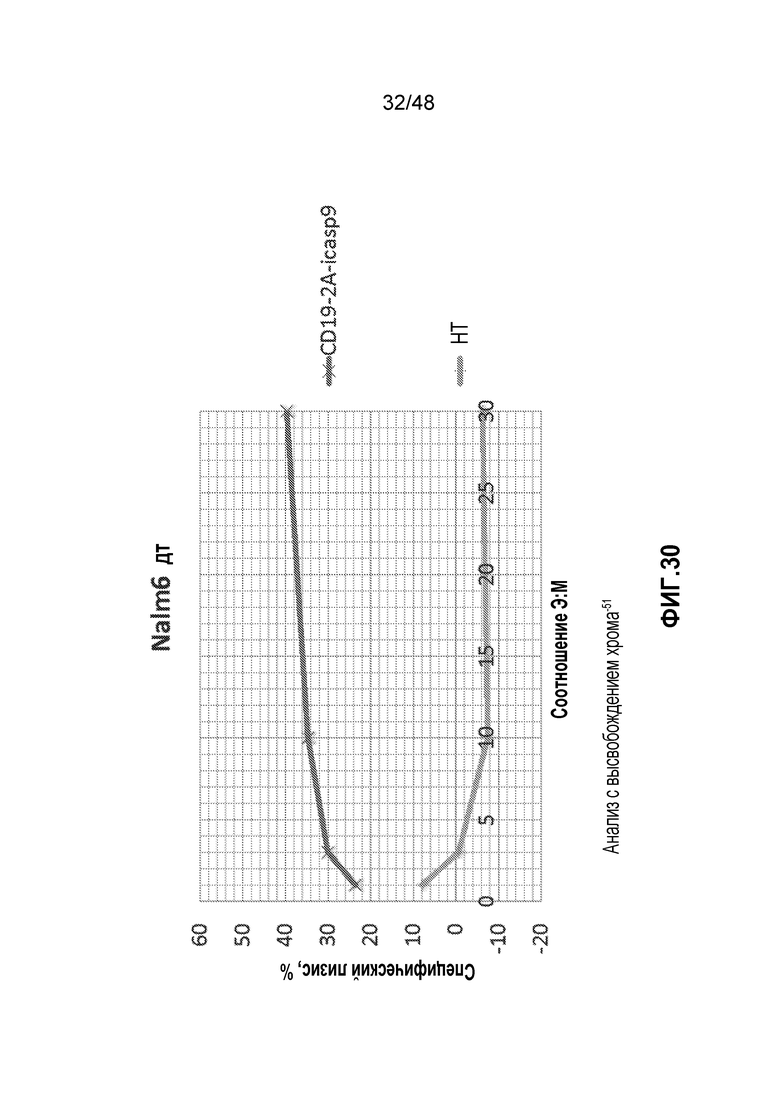

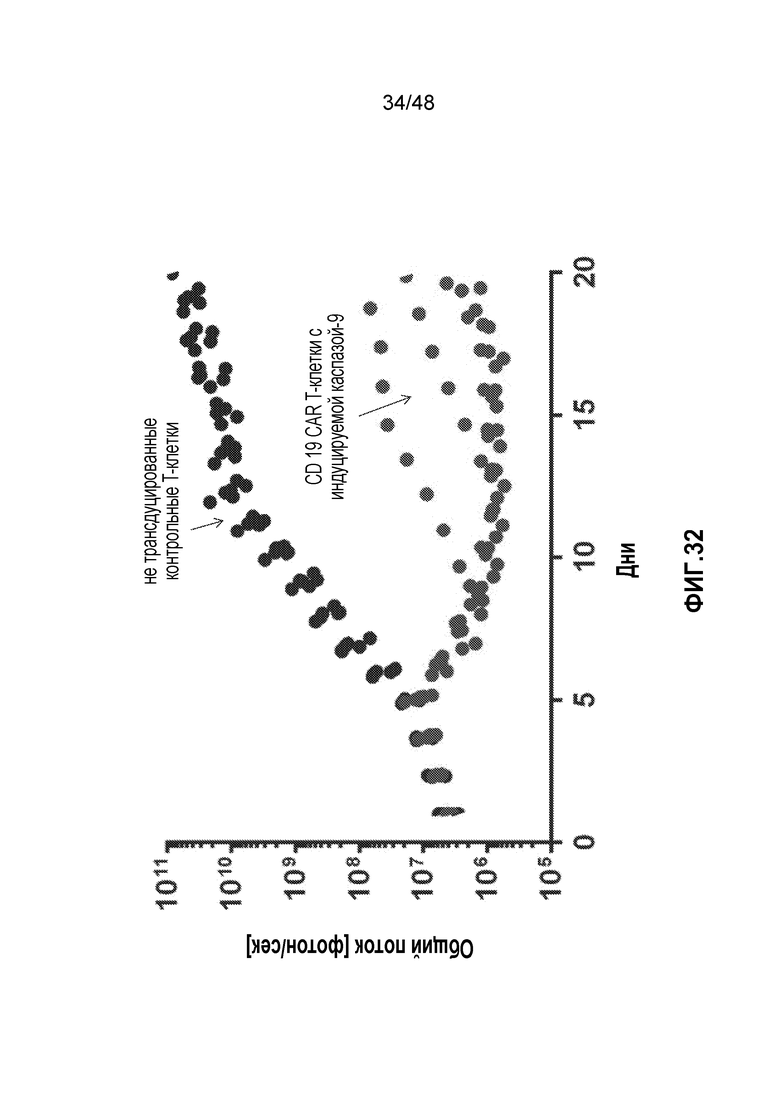

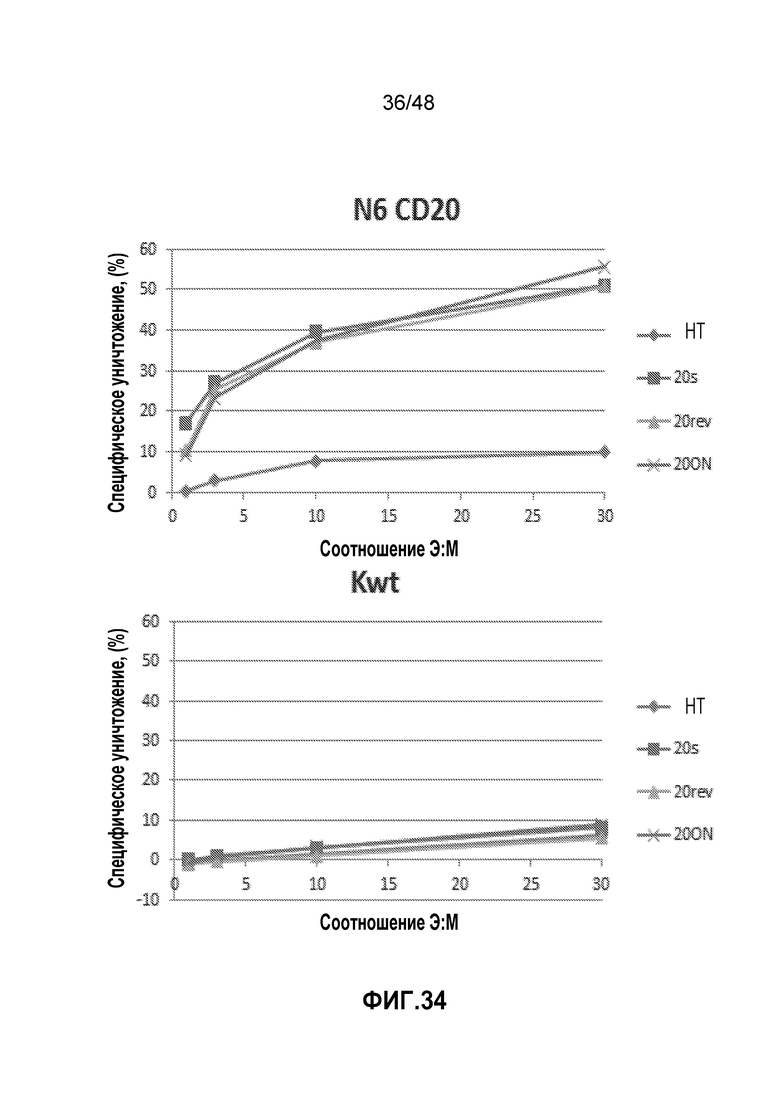
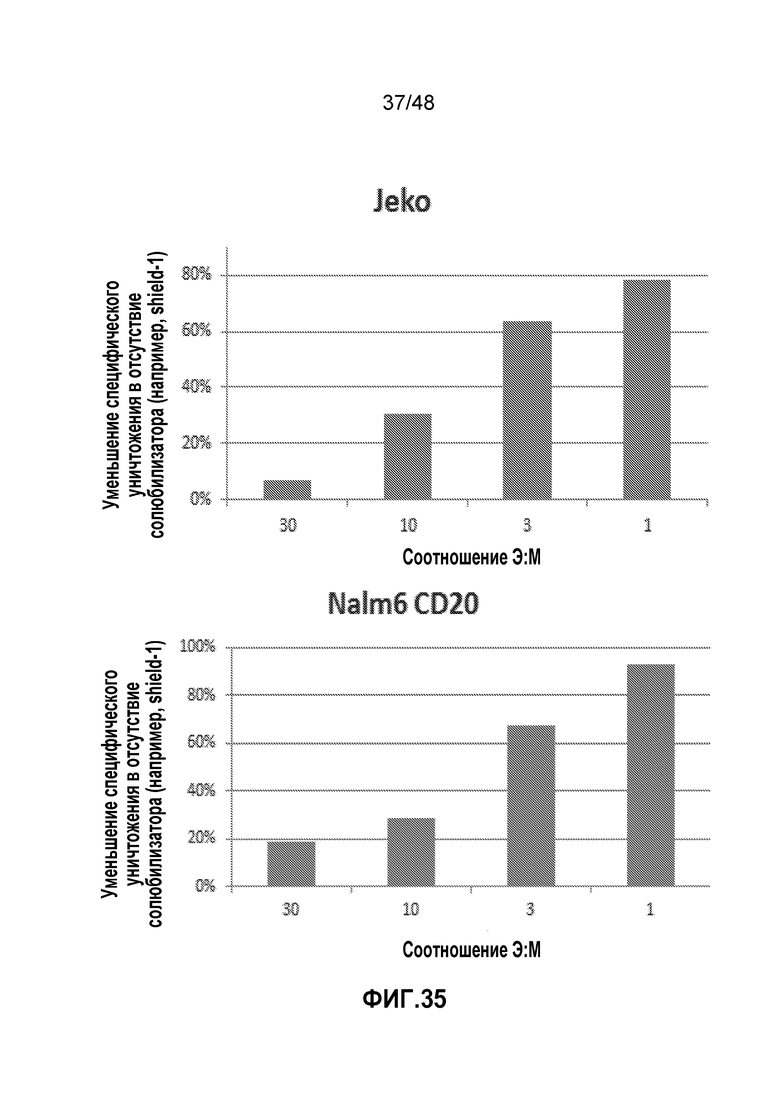
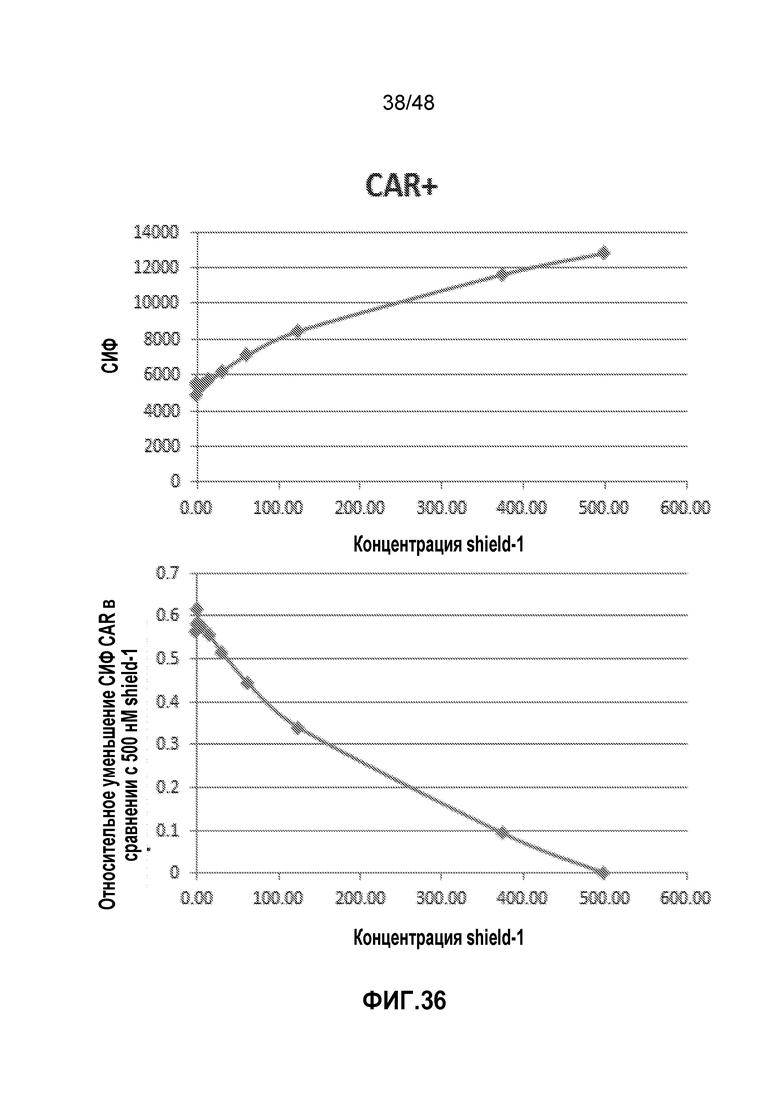

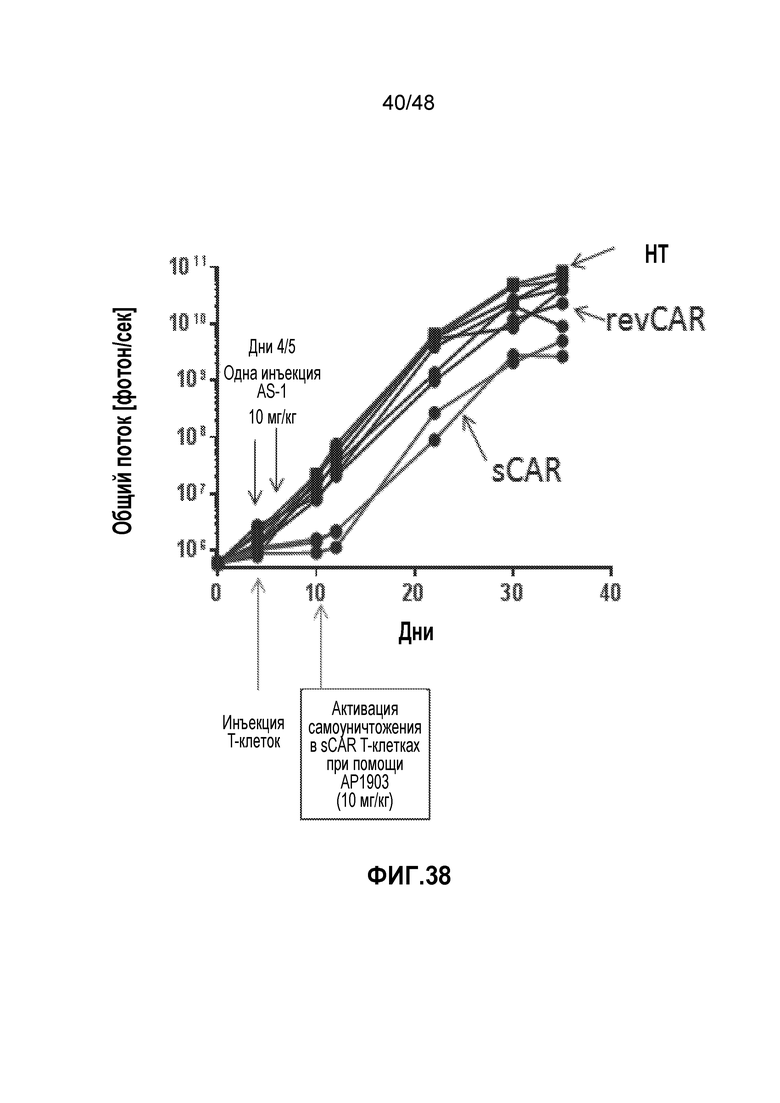
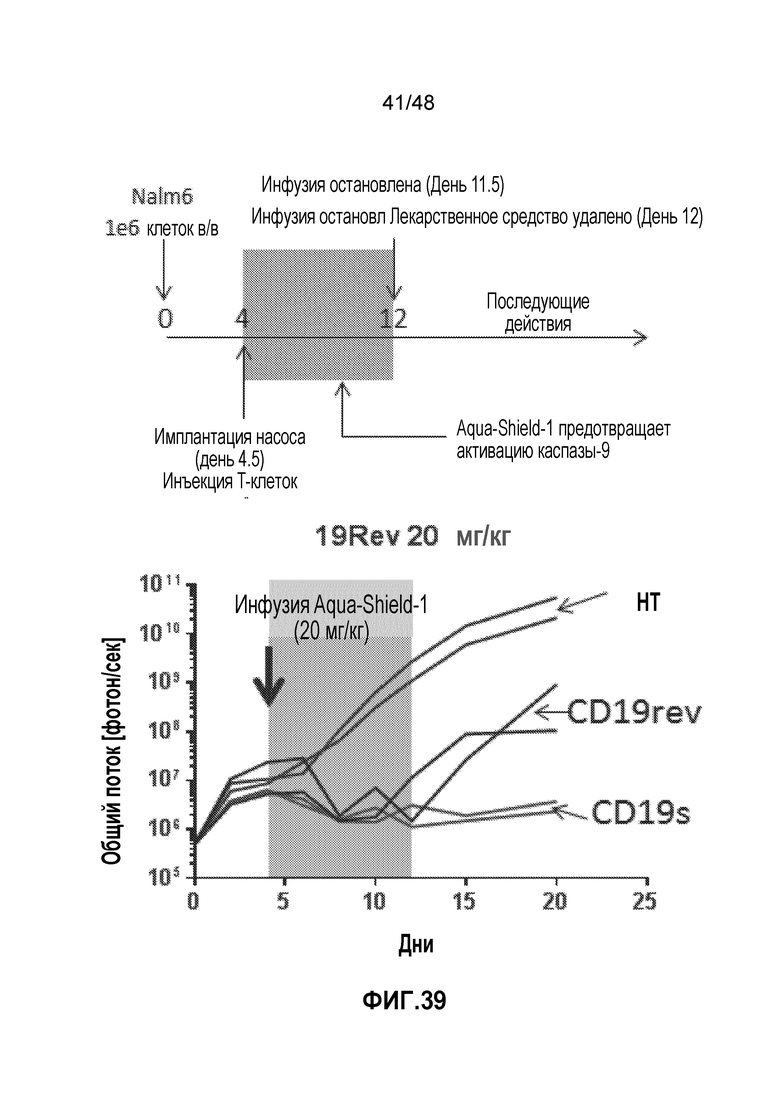




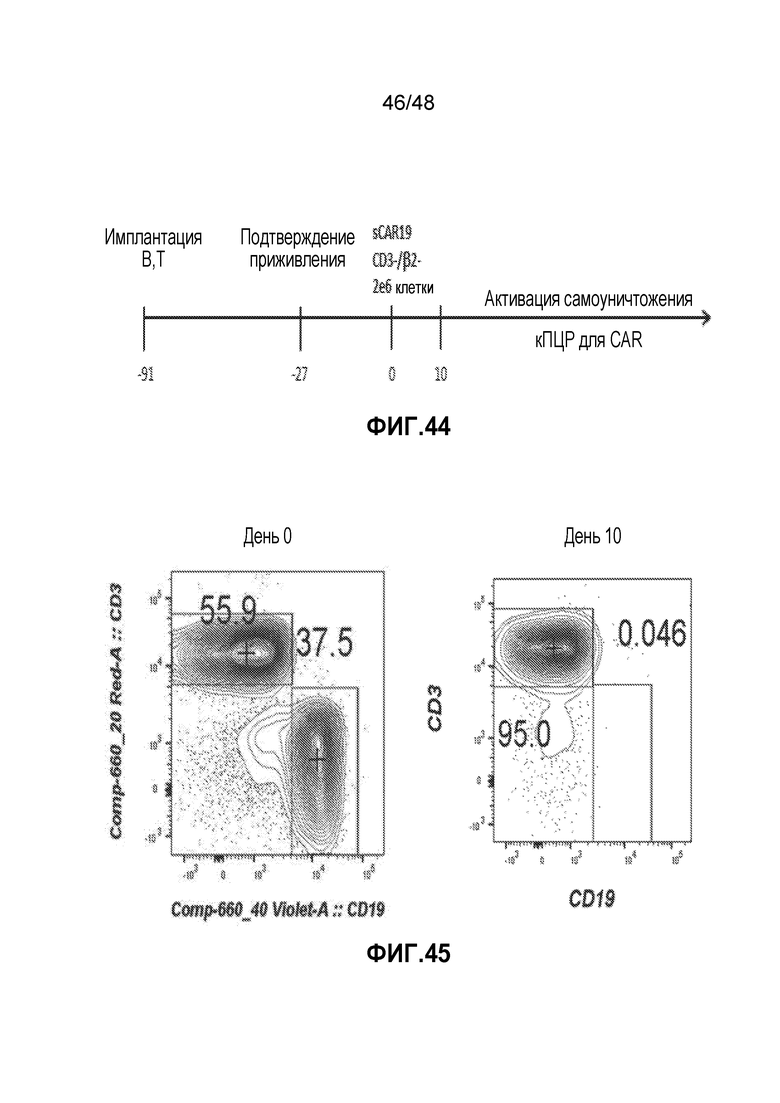
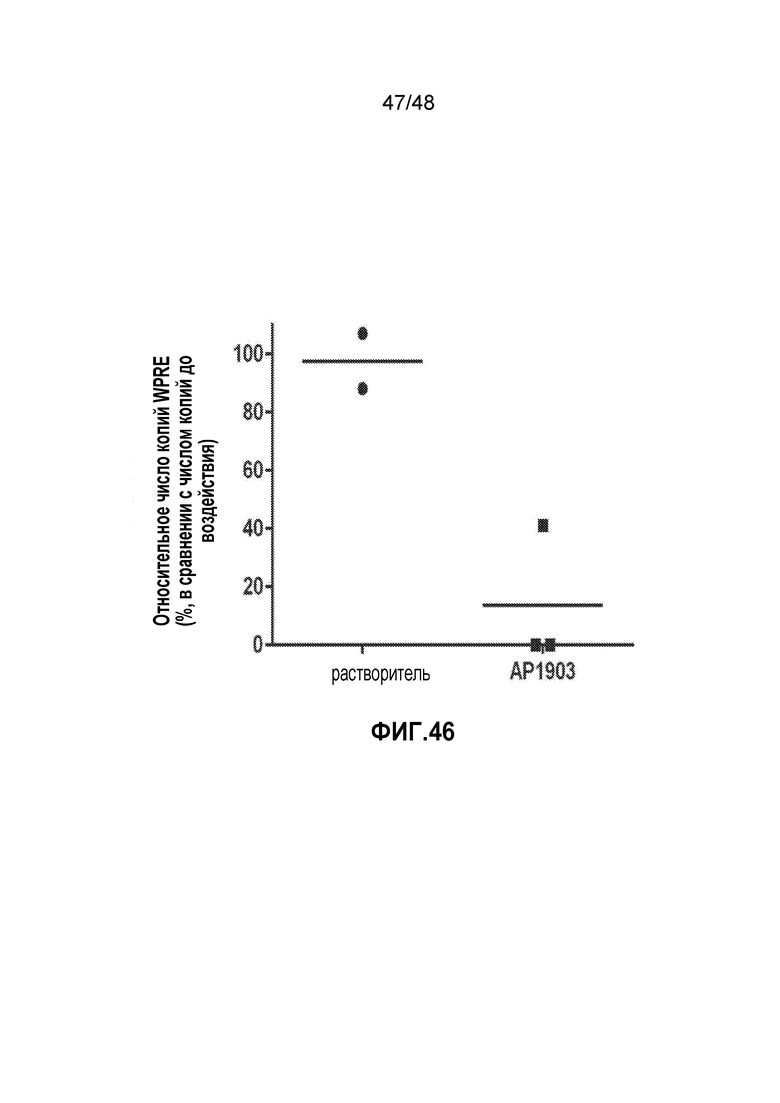
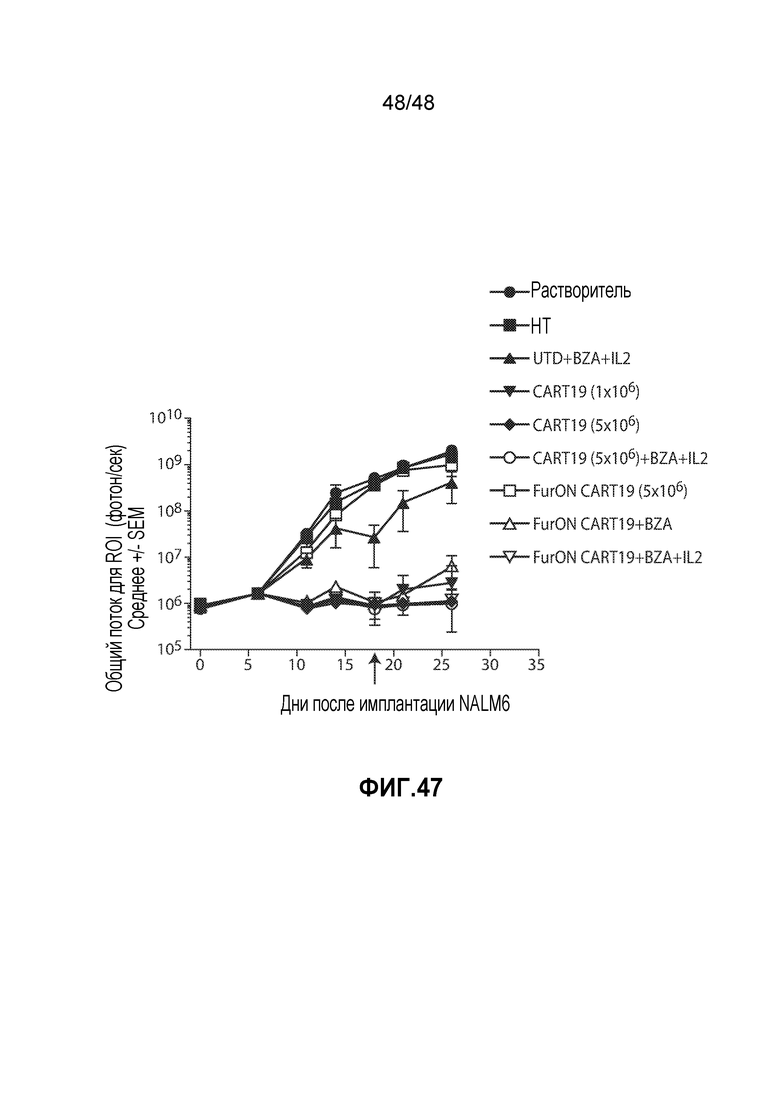
Изобретение относится к области биотехнологии, конкретно к получению слитых белков, и может быть использовано в медицине для лечения рака в присутствии стабилизирующего соединения. Рекомбинантным путем получают слитые белки, содержащие домен условной экспрессии, домен, содержащий интересующий белок, и расщепляемый протеазой домен, разделяющий эти два домена. Изобретение позволяет получить слитые белки, отличающиеся контролируемой экспрессией в зависимости от присутствия стабилизирующего соединения в среде. 9 н. и 59 з.п. ф-лы, 47 ил., 24 табл., 29 пр.
1. Слитый белок для использования в лечении cубъекта, имеющего рак, связанный с экспрессией опухолевого антигена, в присутствии стабилизирующего соединения, содержащий два белковых домена, разделенные сайтом расщепления фурина, где первый из указанных белковых доменов представляет собой домен деградации для регулируемой экспрессии указанного слитого белка и второй из указанных белковых доменов представляет собой химерный антигенный рецептор (CAR), где:
(i) домен деградации представляет собой домен рецептора эстрогена (ER); и
(ii) указанный CAR содержит антигенсвязывающий домен, который специфически связывает указанный опухолевый антиген, трансмембранный домен и один или более внутриклеточных сигнальных доменов.
2. Слитый белок для использования в лечении cубъекта, имеющего рак, связанный с экспрессией опухолевого антигена, в присутствии стабилизирующего соединения, содержащий два белковых домена, разделенные сайтом расщепления фурина, где первый из указанных белковых доменов представляет собой домен деградации для регулируемой экспрессии указанного слитого белка и второй из указанных белковых доменов представляет собой химерный антигенный рецептор (CAR), где:
(i) домен деградации представляет собой домен белка FKB (FKBP); и
(ii) указанный CAR содержит антигенсвязывающий домен, который специфически связывает указанный опухолевый антиген, трансмембранный домен и один или более внутриклеточных сигнальных доменов.
3. Слитый белок по п. 1, где домен деградации содержит аминокислотную последовательность, которая по меньшей мере на 90, 95, 97, 98, 99 или 100% идентична любой из SEQ ID NOs: 58 или 121.
4. Слитый белок по п. 2, где домен деградации содержит аминокислотную последовательность, которая по меньшей мере на 90, 95, 97, 98, 99 или 100% идентична SEQ ID NO: 56.
5. Слитый белок по любому из пп. 1-4, где домен деградации имеет первое состояние, связанное с первым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, и второе состояние, связанное со вторым уровнем поверхностной экспрессии и/или внеклеточной экспрессии слитого белка, где второй уровень повышен, например, по меньшей мере в 2, 3, 4, 5, 10, 20 или 30 раз относительно первого уровня, в присутствии стабилизирующего соединения.
6. Слитый белок по п. 1, где указанное стабилизирующее соединение выбирают из базедоксифена и 4-гидрокситамоксифена (4-OHT).
7. Слитый белок по п. 2, где указанное стабилизирующее соединение представляет собой Shield-1.
8. Слитый белок по любому из пп. 1-7, где указанный сайт расщепления фурина содержит полипептид, имеющий консенсусный мотив RX(K/R)R.
9. Слитый белок по любому из пп. 1-8, где указанный сайт расщепления фурина выбран из RTKR (SEQ ID NO: 123); GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125); GTGAEDPRPSRKRR (SEQ ID NO: 127); LQWLEQQVAKRRTKR (SEQ ID NO: 129); GTGAEDPRPSRKRRSLGG (SEQ ID NO: 131); GTGAEDPRPSRKRRSLG (SEQ ID NO: 133); SLNLTESHNSRKKR (SEQ ID NO: 135) или CKINGYPKRGRKRR (SEQ ID NO: 137).
10. Слитый белок по п. 9, где указанный сайт расщепления фурина представляет собой GTGAEDPRPSRKRRSLGDVG (SEQ ID NO: 125).
11. Слитый белок по п. 1, где указанный внутриклеточный сигнальный домен содержит один или более основных сигнальных доменов.
12. Слитый белок по п. 1, где указанный внутриклеточный сигнальный домен содержит один или более костимулирующих сигнальных доменов.
13. Слитый белок по п. 1, где указанный внутриклеточный сигнальный домен содержит один или более основных сигнальных доменов и один или более костимулирующих сигнальных доменов.
14. Слитый белок по п. 11 или 13, где один из указанных одного или более основных сигнальных доменов содержит стимулирующий домен CD3-дзета.
15. Слитый белок по п. 12 или 13, где указанный один или более из указанных костимулирующих сигнальных доменов представляет собой внутриклеточный домен из костимулирующего белка, выбранного из группы, состоящей из CD27, CD28, 4-1BB (CD137), OX40, GITR, CD30, CD40, ICOS, BAFFR, HVEM, ICAM-1, антигена 1, ассоциированного с функцией лимфоцитов (LFA-1), CD2, CDS, CD7, CD287, LIGHT, NKG2C, NKG2D, SLAMF7, NKp80, NKp30, NKp44, NKp46, CD160, B7-H3 или лиганда, который специфически связывает CD83.
16. Слитый белок по п. 15, где указанный один или более из указанных костимулирующих сигнальных доменов содержит костимулирующий домен 4-1BB.
17. Слитый белок по п. 15, где указанный один или более из указанных костимулирующих доменов содержит костимулирующий домен CD28.
18. Слитый белок по п. 1, где указанный антигенсвязывающий домен представляет собой scFv.
19. Слитый белок по п. 1, где указанный антигенсвязывающий домен связывает антиген, выбранный из группы, состоящей из CD19; CD123; CD22; CD30; CD171; CS-1; подобной лектину C-типа молекулы 1, CD33; рецептора варианта III эпидермального фактора роста (EGFRvIII); ганглиозида G2 (GD2); ганглиозида GD3; представителя семейства TNF-рецепторов, антигена созревания B-клеток (BCMA); Tn-антигена ((Tn Ag) или (GalNAcα-Ser/Thr)); простатического специфического мембранного антигена (PSMA); подобного рецепторной тирозинкиназе рецептора-сироты 1 (ROR1); Fms-подобной тирозинкиназы 3 (FLT3); опухоль-ассоциированного гликопротеина 72 (TAG72); CD38; CD44v6; канцероэмбрионального антигена (CEA); молекулы адгезии эпителиальных клеток (EPCAM); B7H3 (CD276); KIT (CD117); субъединицы альфа-2 рецептора интерлейкина-13; мезотелина; субъединицы альфа рецептора интерлейкина-11 (IL-11Ra); антигена простатических стволовых клеток (PSCA); сериновой протеазы 21; рецептора 2 фактора роста эндотелия сосудов (VEGFR2); Lewis(Y) антигена; CD24; рецептора бета фактора роста тромбоцитов (PDGFR-бета); стадиеспецифического эмбрионального антигена-4 (SSEA-4); CD20; фолатного рецептора альфа; рецепторной тирозин-специфической протеинкиназы ERBB2 (Her2/neu); муцина 1, связанного с клеточной поверхностью (MUC1); рецептора эпидермального фактора роста (EGFR); молекулы адгезии нейронов (NCAM); простазы; простатической кислой фосфатазы (PAP); мутантного фактора элонгации 2 (ELF2M); эфрина B2; белка альфа активации фибробластов (FAP); рецептора инсулиноподобного фактора роста 1 (рецептора IGF-I), карбоангидразы IX (CAIX); субъединицы протеасомы (просома, макропаин), типа бета, 9 (LMP2); гликопротеина 100 (gp100); онкогенного слитого белка, включающего область локализации сайта инициации реаранжировки (BCR) и гомолог 1 вирусного онкогена лейкоза мышей Абельсона (Abl) (bcr-abl); тирозиназы; рецептора эфрина A2 (EphA2); фукозила GM1; молекулы адгезии сиалил-Льюис (sLe); ганглиозида GM3; трансглутаминазы 5 (TGS5); высокомолекулярного меланома-ассоциированного антигена (HMWMAA); o-ацетил-GD2 ганглиозида (OAcGD2); фолатного рецептора бета; опухолевого эндотелиального маркера 1 (TEM1/CD248); антигена, родственного опухолевому эндотелиальному маркеру 7 (TEM7R); клаудина-6 (CLDN6); рецептора тиреостимулирующего гормона (TSHR); связанных с G-белками рецепторов класса C, группы 5, представителя D (GPRC5D); открытой рамки считывания 61 хромосомы X (CXORF61); CD97; CD179a; киназы анапластической лимфомы (ALK); полисиаловой кислоты; плацента-специфического белка 1 (PLAC1); гексасахаридной части гликоцерамида globoH (GloboH); дифференцировочного антигена молочной железы (NY-BR-1); уроплакина 2 (UPK2); клеточного рецептора 1 вируса гепатита A (HAVCR1); адренорецептора бета-3 (ADRB3); паннексина 3 (PANX3); связанного с G-белками рецептора 20 (GPR20); комплекса лимфоцитарного антигена 6, локуса K9 (LY6K); ольфакторного рецептора 51E2 (OR51E2); белка TCR-гамма с альтернативной рамкой считывания (TARP); белка опухоли Вильмса (WT1); антигена 1 рака яичка (NY-ESO-1); антигена 2 рака яичка (LAGE-1a); меланома-ассоциированного антигена 1 (MAGE-A1); транслокационного варианта 6 гена ETS, расположенного на хромосоме 12p (ETV6-AML); белка спермы 17 (SPA17); семейства X антигенов, представителя 1A (XAGE1); ангиопоэтин-связывающего клеточного поверхностного рецептора 2 (Tie 2); антигена 1 меланомы яичка (MAD-CT-1); антигена 2 меланомы яичка (MAD-CT-2); Fos-родственного антигена 1; опухолевого белка p53 (p53); мутанта p53; простеина; сурвивина; теломеразы; опухолевого антигена 1 карциномы предстательной железы, узнаваемого T-клетками антигена меланомы 1; мутанта белка вируса крысиной саркомы (Ras); обратной транскриптазы теломеразы человека (hTERT); точек разрыва при транслокации в случае саркомы; ингибитора апоптоза из клеток меланомы (ML-IAP); ERG (слитого гена трансмембранной сериновой протеазы 2 (TMPRSS2) и ETS); N-ацетилглюкозамин трансферазы V (NA17); белка парного бокса Pax-3 (PAX3); рецептора андрогена; циклина B1; полученного из нейробластомы гомолога онкогена v-myc вируса птичьего миелоцитоматоза (MYCN); представителя C семейства гомологов Ras (RhoC); родственного тирозиназе белка 2 (TRP-2); цитохрома P450 1B1 (CYP1B1); белка, подобного CCCTC-связывающему фактору (белку «цинковый палец»), узнаваемого T-клетками антигена плоскоклеточной карциномы 3 (SART3); белка парного бокса Pax-5 (PAX5); проакрозин-связывающего белка sp32 (OY-TES1); лимфоцит-специфической протеинтирозинкиназы (LCK); якорного белка 4 A-киназы (AKAP-4); точки разрыва 2 в X при синовиальной саркоме (SSX2); рецептора для конечных продуктов усиленного гликозилирования (RAGE-1); почечного убиквитарного белка 1 (RU1); почечного убиквитарного белка 2 (RU2); легумаина; белка E6 вируса папилломы человека (HPV E6); белка E7 вируса папилломы человека (HPV E7); кишечной карбоксилэстеразы; мутантного белка теплового шока 70-2 (mut hsp70-2); CD79a; CD79b; CD72; связанного с лейкоцитами иммуноглобулиноподобного рецептора 1 (LAIR1); Fc-фрагмента рецептора IgA (FCAR или CD89); иммуноглобулиноподобных рецепторов лейкоцитов, подсемейства A, представителя 2 (LILRA2); семейства белков, подобных молекуле CD300, представителя f (CD300LF); семейства 12 доменных лектинов C-типа, представителя A (CLEC12A); антигена 2 стромальных клеток костного мозга (BST2); белка 2, подобного EGF-подобный домен-содержащему муциноподобному гормональному рецептору (EMR2); лимфоцитарного антигена 75 (LY75); глипикана-3 (GPC3); Fc-рецептор-подобного белка 5 (FCRL5) или подобного цепи лямбда иммуноглобулина полипептида 1 (IGLL1).
20. Слитый белок по п. 19, где указанный антиген представляет собой CD19.
21. Слитый белок по п. 20, содержащий антигенсвязывающий домен, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 356-368 или 381.
22. Слитый белок по п. 20, содержащий химерный антигенный рецептор, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 897, 902, 907, 912, 917, 922, 927, 932, 937, 942, 947, 952 или 956.
23. Слитый белок по п. 19, где указанный антиген представляет собой CD123.
24. Слитый белок по п. 23, содержащий антигенсвязывающий домен, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 751, 756, 761 или 766.
25. Слитый белок по п. 23, содержащий химерный антигенный рецептор, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 750, 755, 760 или 765.
26. Слитый белок по п. 19, где указанный антиген представляет собой BCMA.
27. Слитый белок по п. 26, содержащий антигенсвязывающий домен, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 382, 386, 390, 394, 398, 402, 406, 410, 414, 418, 422, 426, 430, 434, 438, 442, 446, 450, 454, 458, 462, 466, 470, 474, 478, 482, 486, 490, 494, 498, 502, 506, 510, 514, 518, 522, 528, 531, 534 или 537.
28. Слитый белок по п. 26, содержащий химерный антигенный рецептор, содержащий аминокислотную последовательность, выбранную из любой из SEQ ID NOs: 789, 791, 793, 795, 797, 799, 801, 803, 805, 807, 809, 811, 813, 815, 817, 819, 821, 823, 825, 827, 829, 831, 833, 835, 837, 839, 841, 843, 845, 847, 849, 851, 853, 855, 857 или 859.
29. Слитый белок по п. 19, где указанный антиген представляет собой CD20.
30. Слитый белок по п. 29, содержащий антигенсвязывающий домен, содержащий аминокислотную последовательность, занимающую положения 470-712 или 470-939 в SEQ ID NO: 3033.
31. Слитый белок по п. 29, содержащий химерный антигенный рецептор, содержащий аминокислотную последовательность SEQ ID NO: 3033.
32. Слитый белок по п. 1, где домен деградации расположен в:
a) N-концевом направлении относительно указанного второго белкового домена; или
b) C-концевом направлении относительно указанного второго белкового домена.
33. Слитый белок по п. 1, дополнительно содержащий сигнальный пептид.
34. Слитый белок по п. 33, где указанный сигнальный пептид расположен в N-концевом направлении относительно указанного домена деградации.
35. Слитый белок по п. 33, дополнительно содержащий линкер, расположенный между сигнальным пептидом и другим доменом слитого белка.
36. Слитый белок по п. 35, где указанный линкер расположен между указанным сигнальным пептидом и указанным доменом деградации.
37. Слитый белок по п. 1, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 67, 69, 75, 103, 105, 107, 109, 111, 113, 115, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183 и 990-1049.
38. Слитый белок по п. 2, содержащий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 59 или 61.
39. Нуклеиновая кислота, кодирующая слитый белок по п. 37 или 38.
40. Экспрессионный вектор, содержащий нуклеиновую кислоту по п. 39.
41. Экспрессионный вектор по п. 40, представляющий собой вирусный вектор.
42. Экспрессионный вектор по п. 40, представляющий собой лентивирусный вектор.
43. Лентивирусная частица для получения слитого белка, содержащая экспрессионный вектор по любому из пп. 40-42.
44. Иммунная эффекторная клетка млекопитающего для регулируемой экспрессии слитого белка, содержащая экспрессионный вектор по любому из пп. 40-42.
45. Клетка млекопитающего по п. 44, где указанная человеческая эффекторная клетка представляет собой человеческую T-клетку или человеческую NK-клетку.
46. Клетка млекопитающего по п. 44, где указанная клетка дополнительно содержит фурин.
47. Клетка млекопитающего по п. 44, где в отсутствие указанного стабилизирующего соединения слитый белок деградирует в клеточных путях деградации.
48. Клетка млекопитающего по п. 47, где по меньшей мере 50%, 60%, 70%, 80%, 90% или более слитого белка деградирует.
49. Клетка млекопитающего по п. 44, в которой в присутствии указанного стабилизирующего соединения домен деградации принимает конформацию, более устойчивую к деградации в клетке, в присутствии стабилизирующего соединения, в сравнении с конформацией в отсутствие стабилизирующего соединения.
50. Клетка млекопитающего по п. 44, в которой в присутствии указанного стабилизирующего соединения конформация слитого белка является более подверженной расщеплению в сайте расщепления фурина в присутствии стабилизирующего соединения, в сравнении с конформацией в отсутствие стабилизирующего соединения.
51. Клетка млекопитающего по п. 44, в которой в присутствии указанного стабилизирующего соединения уровень клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка повышен по меньшей мере в 2, 3, 4, 5, 6, 7, 8, 9, 10, 20 или 30 раз относительно уровня клеточной поверхностной экспрессии или внеклеточной экспрессии слитого белка в клетке, не содержащей стабилизирующее соединение.
52. Способ лечения субъекта, имеющего рак, связанный с экспрессией опухолевого антигена, включающий введение субъекту эффективного количества клетки млекопитающего по п. 44 и указанного стабилизирующего соединения, где указанный CAR содержит, в направлении от N-конца к C-концу, антигенсвязывающий домен, трансмембранный домен и один или более внутриклеточных сигнальных доменов, и указанный антигенсвязывающий домен специфически связывает указанный опухолевый антиген.
53. Клетка млекопитающего по п. 44 для применения в лечении рака, связанного с экспрессией опухолевого антигена у субъекта.
54. Способ по п. 52, где указанная клетка млекопитающего является аутологичной для указанного субъекта.
55. Способ по п. 52, где указанная клетка млекопитающего является аллогенной для указанного субъекта.
56. Способ по п. 52, где указанное стабилизирующее соединение выбирают из базедоксифена или 4-гидрокситамоксифена (4-OHT), если слитый белок содержит домен деградации, полученный из рецептора эстрогена.
57. Способ по п. 52, где указанное стабилизирующее соединение представляет собой Shield-1, если слитый белок содержит домен деградации, полученный из белка FKB.
58. Способ по п. 52, где рак представляет собой мезотелиому, рак легкого, рак поджелудочной железы, аденокарциному пищевода, рак яичника, рак молочной железы, колоректальный рак, рак мочевого пузыря или любое их сочетание.
59. Способ по п. 58, где мезотелиома представляет собой злокачественную мезотелиому плевры.
60. Способ по п. 58, где рак легкого представляет собой немелкоклеточный рак легкого, мелкоклеточный рак легкого, плоскоклеточный рак легкого или крупноклеточный рак легкого.
61. Способ по п. 58, где рак поджелудочной железы представляет собой протоковую аденокарциному поджелудочной железы или метастатическую протоковую аденокарциному поджелудочной железы (PDA).
62. Способ по п. 58, где рак яичника представляет собой серозный эпителиальный рак яичника.
63. Способ по п. 52, где заболевание, связанное с экспрессией опухолевого антигена, представляет собой гематологический рак.
64. Способ по п. 63, где гематологический рак выбран из лейкоза и лимфомы.
65. Способ по п. 63, где гематологический рак выбирают из: хронического лимфоцитарного лейкоза (CLL), лимфомы из клеток мантийной зоны (MCL), множественной миеломы, острого лимфобластного лейкоза (ALL), лимфомы Ходжкина, B-клеточного острого лимфобластного лейкоза (BALL), T-клеточного острого лимфобластного лейкоза (TALL), мелкоклеточной лимфоцитарной лимфомы (SLL), B-клеточного пролимфоцитарного лейкоза, новообразования из бластных плазмацитоидных дендритных клеток, лимфомы Беркитта, диффузной крупноклеточной В-клеточной лимфомы (DLBCL), DLBCL, связанной с хроническим воспалением, хронического миелоидного лейкоза, миелопролиферативных новообразований, фолликулярной лимфомы, фолликулярной лимфомы у детей, волосатоклеточного лейкоза, мелкоклеточной или крупноклеточной фолликулярной лимфомы, злокачественных лимфопролиферативных состояний, лимфомы MALT-типа (экстранодальная лимфома маргинальной зоны, возникающая из лимфоидной ткани, ассоциированной со слизистыми оболочками), лимфомы маргинальной зоны, миелодисплазии, миелодиспластического синдрома, неходжскинской лимфомы, плазмабластной лимфомы, новообразования из плазмацитоидных дендритных клеток, макроглобулинемии Вальденстрема, лимфомы маргинальной зоны селезенки, лимфомы/лейкоза клеток селезенки, диффузной мелкоклеточной В-клеточной лимфомы красной пульпы селезенки, волосатоклеточного лейкоза - варианта, лимфоплазматической лимфомы, болезни тяжелых цепей, миеломы из плазматических клеток, одиночной плазмоцитомы кости, внекостной плазмоцитомы, нодальной лимфомы маргинальной зоны, нодальной лимфомы маргинальной зоны у детей, первичной кожной фолликулярной лимфомы, лимфогранулематоза, первичной медиастинальной крупноклеточной В-клеточной лимфомы (тимуса), внутрисосудистой крупноклеточной В-клеточной лимфомы, ALK+ крупноклеточной В-клеточной лимфомы, крупноклеточной В-клеточной лимфомы, возникающей при HHV8-ассоциированной многоочаговой болезни Кастлемана, первичной эффузионной лимфомы, В-клеточной лимфомы, острого миелоидного лейкоза (AML) или неподдающейся классификации лимфомы.
66. Способ по п. 65, где рак выбирают из MCL, CLL, ALL, лимфомы Ходжкина, AML и множественной миеломы.
67. Применение слитого белка по п. 1 или 2 в лечении рака, связанного с экспрессией опухолевого антигена, на который направлен антигенсвязывающий домен CAR в составе указанного слитого белка, где указанный слитый белок экспрессируется иммунной эффекторной клеткой млекопитающего в присутствии указанного стабилизирующего соединения.
68. Применение клетки млекопитающего по п. 44 в лечении рака, связанного с экспрессией опухолевого антигена, на который направлен антигенсвязывающий домен CAR в составе указанного слитого белка, в присутствии указанного стабилизирующего соединения.
| JENSEN M | |||
| C | |||
| et al., Design and implementation of adoptive therapy with chimeric antigen receptor‐modified T cells, Immunological reviews, 2014, V | |||
| Аппарат для нагревания окружающей его воды | 1920 |
|
SU257A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| SUN J | |||
| et al., The quest for spatio-temporal control of CAR T cells, Cell research, 2015, V | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| WO 2014012001 A2, 16.01.2014 | |||
| WO 2015134877 A1, 11.09.2015 | |||
Авторы
Даты
2023-05-03—Публикация
2017-04-14—Подача