Изобретение относится к области микробиологии и биотехнологии, в частности, к получению биологически активных веществ с помощью микроорганизмов.
Решение проблемы обеспечения безопасными, эффективными и качественными лекарствами требует проведения широкого поиска новых соединений с выраженным фармакологическим потенциалом, без токсических эффектов в соответствии с принципами "зеленой химии". При этом разработка новых лекарственных средств должна осуществляться не только с использованием неагрессивных условий и реагентов, с минимальным выходом побочных продуктов на каждом этапе, но и с учетом (прогнозированием) возможной экологической судьбы разрабатываемого препарата и его метаболитов. Этот тезис лежит в основе «зеленой» и устойчивой фармацевтики [ Pharmaceuticals in the environment. Annu. Rev. Environ. Resour. 2010. V. 35. P. 57-75; Daughton C, Ruhoy I. Green pharmacy and pharmEcovigilance: prescribing and the planet. Expert Rev. Clin. Pharmacol. 2014. V. 4. P. 211-232; Leder C, Rastogi T.,
Pharmaceuticals in the environment. Annu. Rev. Environ. Resour. 2010. V. 35. P. 57-75; Daughton C, Ruhoy I. Green pharmacy and pharmEcovigilance: prescribing and the planet. Expert Rev. Clin. Pharmacol. 2014. V. 4. P. 211-232; Leder C, Rastogi T.,  . Putting benign by design into practice-novel concepts for green and sustainable pharmacy: Designing green drag derivatives by non-targeted synthesis and screening for biodegradability. Sustain. Chem. Pharm. 2015. V. 2. P. 31-36].
. Putting benign by design into practice-novel concepts for green and sustainable pharmacy: Designing green drag derivatives by non-targeted synthesis and screening for biodegradability. Sustain. Chem. Pharm. 2015. V. 2. P. 31-36].
Одним из активно развивающихся направлений является синтез биологически активных веществ на основе растительных терпеноидов. Так, лекарственные средства, полученные на основе вторичных растительных метаболитов, составляют около четверти всего мирового рынка фармацевтических препаратов [Calixto J. The role of natural products in modern drag discovery. An. Acad. Bras. Cienc. 2019. V. 91. P. 1-7]. Интерес исследователей к нативным терпеноидам обусловлен их доступностью, а также широким спектром проявляемой данными природными соединениями биоактивности, включая противовирусную, противомикробную, противовоспалительную, противоопухолевую, нейропротекторную и др. [Luchnikova Ν.Α., Grishko V.V, Ivshina I.В. Biotransformation of oleanane and ursane triterpenic acids. Molecules. 2020. V. 25. P. 1-31; Salakhutdinov N. F., Volcho K.P., Yarovaya О.I. Monoterpenes as a renewable source of biologically active compounds. Pure Appl. Chem. 2017. V. 89. P. 1105-1117]. Вместе с тем молекулы терпеноидов характеризуются повышенной гидрофобностью, что значительно ограничивает их применение в качестве эффективных фармакологических агентов и обусловливает необходимость их модификации с целью получения более гидрофильных и биологически активных соединений.
Одним из широко используемых в синтезе биоактивных веществ терпеноидов является монотерпеновый спирт (-)-изопулегол ((1R,2S,5R)-5-метил-2-(проп-1-ен-2-ил)циклогексан-1-ол, С10Н18О, CAS No. 89-79-2). Низкая себестоимость, доступность и разнообразные биологические свойства (-)-изопулегола обусловливают повышенный интерес исследователей в области биотехнологии и фармакологии к данному соединению [Minh Le T., Szakonyi Ζ. Enantiomeric isopulegol as the chiral pool in the total synthesis of bioactive agents. Chem. Rec. 2022. V. 2. P. 1-32]. Проведение трансформации (-)-изопулегола с использованием химических методов позволило получить соединения с выраженной противовирусной [Ilyina I.V., Zarubaev V.V, Lavrentieva I.Ν, Shtro Α.Α., Esaulkova I.L., Korchagina D.V., Borisevich S.S., Volcho K.P., Salakhutdinov N.F. Highly potent activity of isopulegol-derived substituted octahydro-2H-chromen-4-ols against influenza A and В viruses. Bioorg. Med. Chem. Lett. 2018. V. 28. P. 2061-2067; Nazimova Ε.V, ShtroA. Α., Anikin V.В., Patrusheva O.S., Ilyina I.V, Korchagina D.V, Zarubaev V.V, Volcho K.P., Salakhutdinov N.F. Influenza antiviral activity of Br-containing [2R,4R(S),4aR,7R,8aR]-4-dimethyl-2-(thiophen-2-yl)oc ols prepared from (-)-isopulegol. Chem. Nat. Compd. 2017. V. 53. P. 260-264], обезболивающей [Li-Zhulanov N.S., Pavlova Α.V, Korchagina D.V, Gatilov Y.V., Volcho K.P., Tolstikova T.G., Salakhutdinov N.F. Synthesis of 1,3-oxazine derivatives based on (-)-isopulegol using the Ritter reaction and study of their analgesic activity. Chem. Heterocycl. Compd. 2020. V. 56. P. 936-941] и антипролиферативной активностью [Le Minh T.,  Szakonyi Z. Synthesis and transformation of (-)-isopulegol-based chiral β-aminolactones and β-aminoamides. Int. J. Mol. Sci. 2018. V. 19. P. 1-19].
Szakonyi Z. Synthesis and transformation of (-)-isopulegol-based chiral β-aminolactones and β-aminoamides. Int. J. Mol. Sci. 2018. V. 19. P. 1-19].
По сравнению с традиционным органическим синтезом, биокаталитические процессы на основе ферментов и целых клеток микроорганизмов для получения энантиомерно чистых соединений наиболее эффективны и технологически перспективны. Это обусловлено их исключительной хемо- и стереоселективностью, спецификой многоцелевых оксигеназных ферментных систем, широким кругом метаболизируемых субстратов, отсутствием проблемы минимизации побочных реакций или необходимости в многочисленных стадиях защиты/снятия защитных групп и, что немаловажно, устойчивой активностью в экстремальных условиях внешней среды.
В последние годы биокатализ становится все более востребованным, что связано, главным образом, с большей доступностью высококачественных биоресурсов мировых микробных коллекций, с возможностью использования достижений геномики, протеомики, а также синтетической биологии и биоинформационных инструментов. При этом стоит отметить явный недостаток исследований, посвященных микробной трансформации (-)-изопулегола. Недавно группой ученых из США и Греции были предприняты попытки биотрансформации (-)-изопулегола иммобилизованными кутиназами и липазами, выделенными из грибов Aspergillus oryzae, Humicola insolens и Thermomyces lanuginosus, Rhizomucor miehei соответственно [Su Α., Kiokekli S., Naviwala M., Shirke Α., Pavlidis L, Gross R. Cutinases as stereoselective catalysts: Specific activity and enantioselectivity of cutinases and lipases for menthol and its analogs. Enzyme Microb. Technol. 2020. V. 133. P. 1-8]. Ранее Shukla с соавт. (1987) продемонстрировали способность представителей Rhodococcus sp. использовать (-)-изопулегол в качестве единственного источника углерода, однако продуктов трансформации детектировано не было [Shukla О., Bartholomus R, Gunsalus I. Microbial transformation of menthol and menthane-3,4-diol. Can. J. Microbiol. 1987. V. 33. P. 489-497]. Кроме того, стоит отметить, что анализ информации, представленной в международных базах данных интеллектуальной собственности (ФИПС, WIPO Patentscope, Espacenet, J-PlatPat), не выявил наличие патентов по микробной трансформации (-)-изопулегола.
Таким образом, чрезвычайно актуален поиск биокатализаторов и инновационных технологий с целью получения новых производных (-)-изопулегола с потенциальной биологической активностью.
Одной из широко разрабатываемых в биотехнологии групп микроорганизмов являются актино бактерии рода Rhodococcus, характеризующиеся большим разнообразием трансформируемых труднодоступных гидрофобных органических соединений [Anteneh Y., Franco С. Whole cell actinobacteria as biocatalysts. Front. Microbiol. 2019. V. 10. P. 1-15; Busch H., Hagedoorn P., Hanefeld U. Rhodococcus as a versatile biocatalyst in organic synthesis. Int. J. Mol. Sci. 2019. V. 20. P. 1-36; Krivoruchko Α., Kuyukina M., Ivshina I. Advanced Rhodococcus biocatalysts for environmental biotechnologies. Catalysts. 2019. V. 9. P. 236; Shukla O., Bartholomus R, Gunsalus I. Microbial transformation of menthol and menthane-3,4-diol. Can. J. Microbiol. 1987. V. 33. P. 489-497].
Немицелиальный характер роста, способность к выработке биосурфактантов, политрофность и лабильность метаболических систем родококков обусловливают целесообразность поиска активных биотрансформаторов (-)-изопулегола среди представителей данной группы микроорганизмов. Кроме того, ранее авторами изобретения была показана способность Rhodococcus spp.к биотрансформации растительных трициклических дитерпеноидов и пентациклических тритерпеноидов с образованием биоактивных производных [Патент RU 2529365, 2014; Cheremnykh K.M., Luchnikova Ν.Α., Grishko V.V., Ivshina I.В. Bioconversion of ecotoxic dehydroabietic acid using Rhodococcus actinobacteria. J. Hazard. Mater. 2018. V. 346. P. 103-112; Grishko V. V., Tarasova Ε. V., Ivshina I. B. Biotransformation of betulin to betulone by growing and resting cells of the actinobacterium Rhodococcus rhodochrous IEGM 66. Process Biochem. 2013. V. 48. P. 1640-1644].
Задачей предлагаемого изобретения является выявление возможности использования представителей рода Rhodococcus в качестве биотрансформаторов (-)-изопулегола для получения соединений, потенциально обладающих биологической активностью, то есть выявление среди полученных соединений потенциально значимых фармакологических агентов.
Техническим результатом изобретения является получение новых потенциально биологически активных соединений вследствие биотрансформации (-)-изопулегола с помощью использования представителя рода Rhodococcus.
Технический результат изобретения достигается тем, что в способе используется культура R. rhodochrous ИЭГМ 1362, выделенная из верхних слоев торфа на Пальтинском месторождении торфа (Пермский край, Россия) и поддерживаемая в Региональной профилированной коллекции алканотрофных микроорганизмов (акроним коллекции ИЭГМ, номер 285 во Всемирной федерации коллекции культур, реестровый номер УНУ 73559; www.iegmcol.ra). Штамм депонирован в Национальный биоресурсный центр Всероссийская коллекция промышленных микроорганизмов НИЦ "Курчатовский институт" - ГосНИИгенетика под регистрационным номером ВКПМ Ас-2187.
Согласно изобретению предлагается способ микробной биотрансформации растительного монотерпеноида (-)-изопулегола, предусматривающий взаимодействие (-)-изопулегола с бактериальной суспензией штамма Rhodococcus rhodochrous ВКПМ Ас-2187 в минерально-солевой среде в условиях периодического культивирования в течение 5 суток с последующим подкислением реакционной среды и экстрагированием этилацетатом полученных производных - 10-гидрокси- и 10-карбоксипроизводных (-)-изопулегола, обладающих потенциальной биологической активностью.
Изобретение осуществляется следующим образом.
Бактериальные клетки штамма ВКПМ Ас-2187 выращивали в колбах Эрленмейера объемом 250 мл, содержащих 100 мл минерально-солевой среды RS (г/л: K2HPO4 - 2,0; KH2PO4 - 2,0; KNO3 - 1,0; (NH4)2SO4 - 2,0; NaCl - 1,0; MgSO4 - 0,2; CaCl2 - 0,02, FeCl3×7H2O - 0,001), в условиях периодического культивирования (5 сут) на орбитальном шейкере при 160 об/мин и температуре 28°С. В среду дополнительно вносили дрожжевой экстракт (0,1 г/л) и микроэлементы по Постгейту (0,1 об. %). (-)-Изопулегол (SigmaAldrich, США) добавляли в концентрации 0,025 об. %.
В качестве контролей использовали (1) стерильный раствор (-)-изопулегола в минеральной среде (абиотический контроль); (2) бактериальную суспензию в минерально-солевой среде (биотический контроль).
Для обнаружения остаточного (-)-изопулегола и его метаболитов ферментационную среду подкисляли 10% раствором HCl и трижды экстрагировали эквивалентным объемом этилацетата. Объединенные экстракты последовательно промывали 1% водным раствором NaHCO3 и дистиллированной водой (до рН 7.0). Этилацетатный экстракт обезвоживали над безводным Na2SO4. Растворитель удаляли с помощью роторного испарителя (Heidolph, Германия). Качественный анализ проводили методом тонкослойной хроматографии (ТСХ) на пластинках Alugram® Xtra SIL G/UV254 (Machery-Nagel, Германия) в системе н-гексан - этилацетат (1:1). Визуализацию хроматографических пластинок проводили в парах йода.
Разделение реакционной смеси проводили с помощью колоночной хроматографии на силикагеле (Macherey-Nagel, 60-200 мкм), элюент этилацетат в гексане, от 0 до 100%. Анализ фракций осуществляли методом газожидкостной хроматографии на приборе Agilent 7820А, кварцевая колонка НР-5 (сополимер 5%-дифенил-95%-диметоксисилоксан) длиной 30 м, внутренний диаметр 0,25 мм, толщина стационарной фазы 0,25 мкм, детектор пламенно-ионизационный, газ-носитель гелий (скорость потока 2 мл/мин, деление потока 99:1). Хромато-масс-спектры записывали на газовом хроматографе Hewlett-Packard 5890/11 с квадрупольным масс-спектрометром (HP MSD 5971) в качестве детектора, кварцевая колонка HP-5MS 30000'0,25 мм, газ-носитель гелий.
Спектры ЯМР 1H и 13С регистрировали на спектрометрах BrakerAvance-III 400 (Ή: 400,13 МГц, 13С: 100,61 МГц). В качестве внутреннего стандарта использовали сигналы хлороформа (δΗ 7,24, δC 76,90 м.д.). Строение полученных соединений устанавливали на основе анализа спектров ЯМР 1Н и с привлечением спектров двойного резонанса 1H - 1H (COSY, NOES Y), спектров ЯМР 13С, записанных в режиме J-модуляции (JMOD), двумерных спектров гетероядерной 13С - 1Н корреляции на прямых (С - H COSY и HSQC, 1JC,H 135 Гц и 145 Гц, соответственно) и дальних константах спин-спинового взаимодействия (COLOC и НМВС, 2,3J 10 и 7 Гц, соответственно). Элементный состав определяли по данным масс-спектров, зарегистрированных на DFS спектрометре Thermo Scientific в режиме полного сканирования в диапазоне 0-500 m/z, ионизация электронным ударом 70 эВ при прямом вводе образца. Удельное вращение определяли на поляриметре polAAr 3005 для растворов веществ в CHCl3
(1R,2S,5R)-5-(гидроксиметил)-2-(проп-1-ен-2-ил)циклогексанол (2). Белый порошок, Тш 67,8°С, 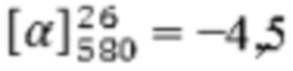 (с=5, CHCl3). Спектр ЯМР 1Н (400 МГц, CDCl3, δ, м.д, J/Гц): 0,90-1,05 (м, 2Н, 2-На, 6-Н), 1,26-1,39 (м, 1H, 5-На), 1,55-1,68 (м, 1Н, 1-На), 1,68-1,70 (м, 3Н, 9-Me), 1,69-1,82 (м, 2Н, 5-Не, 6-Н'), 1,86-1,95 (м, 1H, 4-На), 2,11 (д.м, 1Н, 2J 12,2, 2-Не), 3,43-3,54 (м, 3Н, 3-На, 10-Н, 10-H'), 4,82-4,86 (м, 1Н, 8-Н), 4,87-4,91 (м, 1H, 8-Н'). Спектр ЯМР 13С (100 МГц, CDCl3, δ, м.д): 39,1 (СН, С-1), 36,8 (СН2, С-2), 70,1 (СН, С-3), 54,3 (СН, С-4), 29,0 (СН2, С-5), 28,5 (СН2, С-6), 146,2 (С, С-7), 113,0 (СН2, С-8), 19,1 (СН3, С-9), 67,8 (СН2, С-10). Масс-спектр: найдено: m/z 170, 1299 [М]+, C10H18C2. Вычислено: 170, 1301.
(с=5, CHCl3). Спектр ЯМР 1Н (400 МГц, CDCl3, δ, м.д, J/Гц): 0,90-1,05 (м, 2Н, 2-На, 6-Н), 1,26-1,39 (м, 1H, 5-На), 1,55-1,68 (м, 1Н, 1-На), 1,68-1,70 (м, 3Н, 9-Me), 1,69-1,82 (м, 2Н, 5-Не, 6-Н'), 1,86-1,95 (м, 1H, 4-На), 2,11 (д.м, 1Н, 2J 12,2, 2-Не), 3,43-3,54 (м, 3Н, 3-На, 10-Н, 10-H'), 4,82-4,86 (м, 1Н, 8-Н), 4,87-4,91 (м, 1H, 8-Н'). Спектр ЯМР 13С (100 МГц, CDCl3, δ, м.д): 39,1 (СН, С-1), 36,8 (СН2, С-2), 70,1 (СН, С-3), 54,3 (СН, С-4), 29,0 (СН2, С-5), 28,5 (СН2, С-6), 146,2 (С, С-7), 113,0 (СН2, С-8), 19,1 (СН3, С-9), 67,8 (СН2, С-10). Масс-спектр: найдено: m/z 170, 1299 [М]+, C10H18C2. Вычислено: 170, 1301.
(1R,3R,4S)-3-гидроксн-4-(проп-1-ен -2-ил)циклогексанкарбоновая кислота (3). Белый порошок, Тш 121,2-121,9°С,  -9,1 (с=0,4, CHCl3). Спектр ЯМР 1Ή (400 МГц, CDCl3, δ, м.д): 1,28-1,51 (м, 3Н, 2-На, 5-На, 6-Н), 1,69 (ш.с, 3Н, 9-Me), 1,72-1,82 (м, 1H, 5-Не), 1,90-1,97 (м, 1H, 4-На), 1,95-2,04 (м, 1H, 6-H'), 2,30-2,47 (м, 2Н, 1-На, 2-Не), 3,44-3,55 (м, 1Н, 3-На), 4,84-4,87 (м, 1H, 8-Н), 4,89-4,92 (м, 1Н, 8-Н'). Спектр ЯМР 13С (100 МГц, CDCl3, δ, мд): 41,6 (СН, С-1), 35,6 (СН2, С-2), 69,6 (СН, С-3), 53,4 (СН, С-4), 28,7 (СН2, С-5), 27,9 (СН2, С-6), 145,6 (С, С-7), 113,5 (СН2, С-8), 19,0 (СН3, С-9), 180,5 (С, С-10). Масс-спектр: найдено: m/z 184,1096 [М]+, C10H16O3. Вычислено: 184, 1094.
-9,1 (с=0,4, CHCl3). Спектр ЯМР 1Ή (400 МГц, CDCl3, δ, м.д): 1,28-1,51 (м, 3Н, 2-На, 5-На, 6-Н), 1,69 (ш.с, 3Н, 9-Me), 1,72-1,82 (м, 1H, 5-Не), 1,90-1,97 (м, 1H, 4-На), 1,95-2,04 (м, 1H, 6-H'), 2,30-2,47 (м, 2Н, 1-На, 2-Не), 3,44-3,55 (м, 1Н, 3-На), 4,84-4,87 (м, 1H, 8-Н), 4,89-4,92 (м, 1Н, 8-Н'). Спектр ЯМР 13С (100 МГц, CDCl3, δ, мд): 41,6 (СН, С-1), 35,6 (СН2, С-2), 69,6 (СН, С-3), 53,4 (СН, С-4), 28,7 (СН2, С-5), 27,9 (СН2, С-6), 145,6 (С, С-7), 113,5 (СН2, С-8), 19,0 (СН3, С-9), 180,5 (С, С-10). Масс-спектр: найдено: m/z 184,1096 [М]+, C10H16O3. Вычислено: 184, 1094.
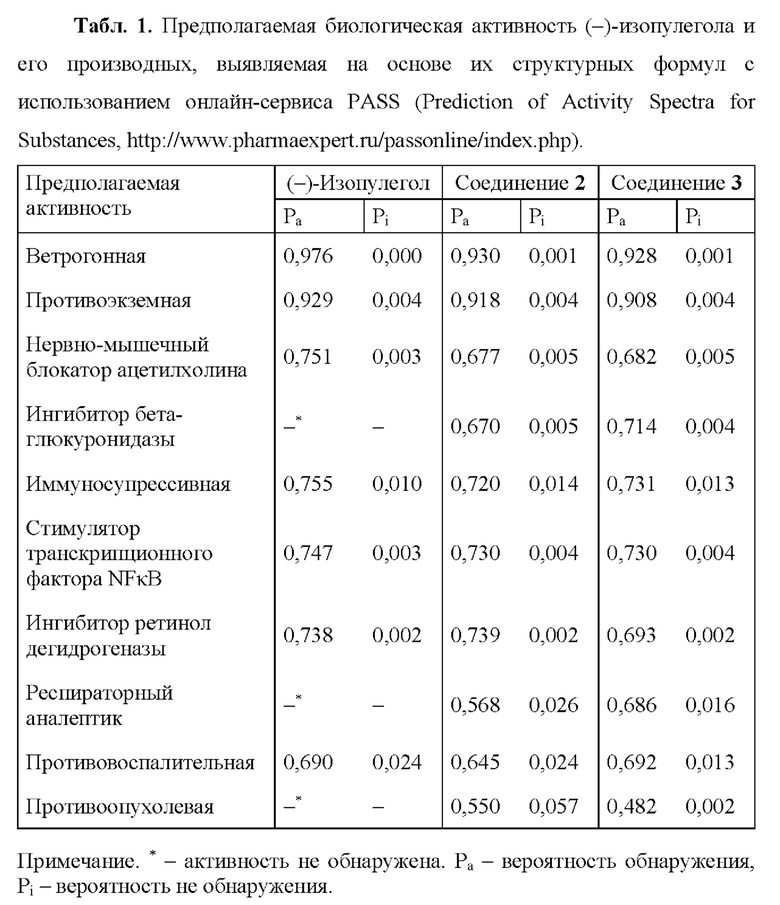
Оценку предполагаемой биологической активности полученных производных (-)-изопулегола прогнозировали на основе их структурных формул с использованием онлайн - сервис a PASS (Prediction of Activity Spectra for Substances, http://www.pharmaexpert.ru/passonline/index.php). Результат исследования биопотенциала веществ представлял собой список прогнозируемых видов биологической активности с оценкой вероятности обнаружения (Ра) и не обнаружения (Pi) последней. Наибольшая вероятность проявления биологической активности принималась за 1.
Изобретение поясняется следующим примером.
Пример.
Способ получения биологически активных производных (-)-изопулегола с использованием клеток Rhodococcus rhodochrous ВКПМ Ас-2187.
Биотрансформация 0,025 об. % (-)-изопулегола (1, 0,18 г) штаммом R. rhodochrous ВКПМ Ас-2187 протекала в течение 5 сут в 100 мл среды RS с добавлением дрожжевого экстракта (0,1 г/л) и микроэлементов по Постгейту (0,1 об. %) при температуре 28°С и постоянном перемешивании (160 об/мин) и сопровождалась образованием двух основных продуктов трансформации (2, 3) с выходом 8,5% (0,017 г) и 12,9% (0,028 г) соответственно. Идентификация производных с использованием ЯМР-спектрометрии (Bruker Avance-III 400, Германия) и рентгеноструктурного анализа (Bruker Kappa Apex II, Германия) позволила определить соединения как (1R,2S,5R)-5-(гидроксиметил)-2-(проп-1-ен-2-ил)циклогексанол (2) и (1R,3R,4S)-3-гидрокси-4-(проп-1-ен-2-ил)циклогексанкарбоновая кислота (3) (Фиг. 1).
На основе данных газовой хромато-масс спектрометрии (Hewlett-Packard 5890/11, США) предлагается схема превращения (-)-изопулегола в процессе трансформации штаммом R. rhodochrous ВКПМ Ас-2187 (Фиг. 2). По данным in silico анализа (онлайн-сервис PASS), оба соединения могут обладать противоопухолевой активностью, а также использоваться в качестве стимуляторов дыхания и агентов профилактики онкологических заболеваний (Табл. 1).
Изобретение поясняется нижеследующими материалами.
на Фиг. 1. приведены структурные формулы производных, полученных в процессе биотрансформации (-)-изопулегола штаммом R. rhodochrous ВКПМАс-2187, где
2-(1R,2S,5R)-5-(гидроксиметил)-2-(проп-1-ен-2-ил)циклогексанол, 3-(1R,3R,4S)-3-гидрокси-4-(проп-1-ен-2-ил)циклогексанкарбоновая кислота.
Нумерация атомов дана для удобства отнесения сигналов в спектрах ЯМР и не совпадает с нумерацией атомов в номенклатурном названии.
На Фиг. 2. приведена схема биоконверсии (-)-изопулегола с использованием клеток R. rhodochrous ВКПМ Ас-2187.
Схема биоконверсии (-)-изопулегола (1) с использованием клеток R. rhodochrous ВКПМ Ас-2187, где
2-(1R,2S,5R)-5-(гидроксиметил)-2-(проп-1-ен-2-ил)циклогексанол,
3-(1R,3R,4S)-3-гидрокси-4-(проп-1-ен-2-ил)циклогексанкарбоновая кислота.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 5α,22α-ДИГИДРОКСИ-ГИПСОГЕНОВОЙ КИСЛОТЫ С ИСПОЛЬЗОВАНИЕМ КЛЕТОК RHODOCOCCUS RHODOCHROUS | 2023 |
|
RU2810501C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕТУЛОНА | 2013 |
|
RU2529365C1 |
| СРЕДСТВО ДЛЯ БИОДЕСТРУКЦИИ КЕТОПРОФЕНА | 2023 |
|
RU2803338C1 |
| СПОСОБ БИОДЕСТРУКЦИИ ДЕГИДРОАБИЕТИНОВОЙ КИСЛОТЫ | 2022 |
|
RU2784816C1 |
| ШТАММ RHODOCOCCUS RUBER ИЭГМ 346 - БИОДЕСТРУКТОР ДИКЛОФЕНАКА НАТРИЯ | 2018 |
|
RU2707536C1 |
| Производные 7-гидроксикумарина, содержащие остатки монотерпеноидов, как ингибиторы репродукции респираторно-синцитиального вируса (РСВ) | 2022 |
|
RU2787352C1 |
| Биодеструктор ибупрофена | 2021 |
|
RU2762007C1 |
| Биотрансформация фенилметилового сульфида в (R)-сульфоксид с помощью иммобилизованных клеток Gordonia terrae ИЭГМ 136 | 2015 |
|
RU2607027C1 |
| Средство для ингибирования фермента тирозил-ДНК-фосфодиэстеразы 1 человека на основе фенилкумаринов, сенсибилизирующее опухоли к действию противоопухолевых агентов | 2019 |
|
RU2724878C1 |
| 1-Адамантил-3-(((1R,4aS,10aR)-7-изопропил-1,4а-диметил-1,2,3,4,4а,9,10,10а-октагидрофенантрен-1-ил)метил)мочевина, проявляющая ингибирующее действие в отношении фермента тирозил-ДНК-фосфодиэстеразы 1 человека и увеличивающая активность темозоломида в отношении клеток глиобластомы | 2019 |
|
RU2697409C1 |

Изобретение относится к области микробиологии и биотехнологии, в частности к получению биологически активных веществ с помощью микроорганизмов. Предложен способ биотрансформации (-)-изопулегола. Осуществляют взаимодействие штамма Rhodococcus rhodochrous ВКПМ Ас-2187 с (-)-изопулеголом в минерально-солевой среде в условиях периодического культивирования в течение 5 суток. Подкисляют реакционную среду. Экстрагируют этилацетатом полученные 10-гидрокси- и 10-карбоксипроизводные (-)-изопулегола. Изобретение позволяет получать новые потенциально биологически активные соединения: 2-(1R,2S,5R)-5-(гидроксиметил)-2-(проп-1-ен-2-ил)циклогексанол и 3-(1R,3R,4S)-3-гидрокси-4-(проп-1-ен-2-ил)циклогексанкарбоновую кислоту. 2 ил., 1 табл., 1 пр.
Способ микробной биотрансформации растительного монотерпеноида (-)-изопулегола, предусматривающий взаимодействие (-)-изопулегола с бактериальной суспензией штамма Rhodococcus rhodochrous ВКПМ Ас-2187 в минерально-солевой среде в условиях периодического культивирования в течение 5 суток с последующим подкислением реакционной среды и экстрагированием этилацетатом полученных производных – 10-гидрокси- и 10-карбоксипроизводных (-)-изопулегола.
| СПОСОБ ПОЛУЧЕНИЯ БЕТУЛОНА | 2013 |
|
RU2529365C1 |
| SHUKLA, O | |||
| P., et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Canadian Journal of Microbiology, 1987, v.33, no.6, p.489-497 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Переключатель | 1976 |
|
SU645218A1 |
| Предохранительная трубка для сосудов с огнеопасными жидкостями | 1923 |
|
SU1362A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| TARASOVA, E | |||
| V., et al | |||
Авторы
Даты
2023-05-29—Публикация
2022-10-14—Подача