Предшествующий уровень техники
Область техники, к которой относится изобретение
Настоящее изобретение относится к соединениям формулы (I) и их фармацевтически приемлемым солям, к фармацевтическим композициям, содержащим такие соединения и соли, и к их применению. Соединения, соли и композиции по настоящему изобретению могут быть полезны для лечения аномального роста клеток, такого как рак, у субъекта.
Описание предшествующего уровня техники
Циклинзависимые киназы (CDK) и родственные серин/треониновые протеинкиназы являются важными клеточными ферментами, которые выполняют важные функции в регуляции деления и пролиферации клеток. CDK 1-4, 6, 10, 11, как сообщается, играют непосредственную роль в прогрессировании клеточного цикла, в то время как CDK 3, 5 и 7-9 могут играть косвенную роль (например, через активацию других CDK, регуляцию транскрипции или нейрональные функции). Каталитические единицы CDK активируются путем связывания с регуляторными субъединицами, известными как циклины, с последующим фосфорилированием. Циклины можно разделить на четыре общих класса (G1, G1/S, S и M циклины), уровни экспрессии которых варьируются в разных точках клеточного цикла. Циклин B/CDK1, циклин A/CDK2, циклин E/CDK2, циклин D/CDK4, циклин D/CDK6 и, вероятно, другие гетеродины являются важными регуляторами развития клеточного цикла.
Сверхэкспрессия CDK2 связана с аномальной регуляцией клеточного цикла. Комплекс циклин E/CDK2 играет важную роль в регуляции перехода G1/S, биосинтеза гистонов и дублирования центросом. Прогрессирующее фосфорилирование ретинобластомы (Rb) с помощью циклин D/Cdk4/6 и циклин E/Cdk2 высвобождает фактор транскрипции G1, E2F, и способствует переходу в S-фазу. Активация циклин A/CDK2 во время ранней S-фазы способствует фосфорилированию эндогенных субстратов, которые обеспечивают репликацию ДНК и инактивацию E2F для завершения S-фазы. (Asghar et al. The history and future of targeting cyclin-dependent kinases in cancer therapy, Nat. Rev. Drug. Discov. 2015; 14(2): 130-146).
Циклин E, регуляторный циклин для CDK2, часто сверхэкспрессируется при раке. Амплификация или сверхэкспрессия циклина Е долгое время ассоциировалась с плохими исходами при раке молочной железы. (Keyomarsi et al., Cyclin E and survival in patients with breast cancer. N Engl J Med. (2002) 347:1566-75). Сверхэкспрессия циклина E2 (CCNE2) связана с эндокринной резистентностью в клетках рака молочной железы, и сообщалось, что ингибирование CDK2 восстанавливает чувствительность к тамоксифену или ингибиторам CDK4 в тамоксифен-резистентных и CCNE2 сверхэкспрессирующих клетках. (Caldon et al., Cyclin E2 overexpression is associated with endocrine resistance but not insensitivity to CDK2 inhibition in human breast cancer cells. Mol. Cancer Ther. (2012) 11:1488-99; Herrera-Abreu et al., Early Adaptation and Acquired Resistance to CDK4/6 Inhibition in Estrogen Receptor-Positive Breast Cancer, Cancer Res. (2016) 76: 2301-2313). Также сообщается, что амплификация циклина E способствует устойчивости к трастузумабу при раке молочной железы HER2+. (Scaltriti et al. Cyclin E amplification/overexpression is a mechanism of trastuzumab resistance in HER2+ breast cancer patients, Proc Natl Acad Sci. (2011) 108: 3761-6). Сообщалось также, что сверхэкспрессия циклина Е играет роль в базальноподобном и трижды негативном раке молочной железы (TNBC), а также в отечно-инфильтративном раке молочной железы. (Elsawaf & Sinn, Triple Negative Breast Cancer: Clinical and Histological Correlations, Breast Care (2011) 6:273-278; Alexander et al., Cyclin E overexpression as a biomarker for combination treatment strategies in inflammatory breast cancer, Oncotarget (2017) 8: 14897-14911.)
Амплификация или сверхэкспрессия циклина Е1 (CCNE1) также связана с плохими исходами при раке яичников, желудка, эндометрия и других типах рака. (Nakayama et al., Gene amplification CCNE1 is related to poor survival and potential therapeutic target in ovarian cancer, Cancer (2010) 116: 2621-34; Etemadmoghadam et al., Resistance to CDK2 Inhibitors Is Associated with Selection of Polyploid Cells in CCNE1-Amplified Ovarian Cancer, Clin Cancer Res (2013) 19: 5960-71; Au-Yeung et al., Selective Targeting of Cyclin E1-Amplified High-Grade Serous Ovarian Cancer by Cyclin-Dependent Kinase 2 and AKT Inhibition, Clin. Cancer Res. (2017) 23:1862-1874; Ayhan et al., CCNE1 copy-number gain and overexpression identify ovarian clear cell carcinoma with a poor prognosis, Modern Pathology (2017) 30: 297-303; Ooi et al., Gene amplification of CCNE1, CCND1, and CDK6 in gastric cancers detected by multiplex ligation-dependent probe amplification and fluorescence in situ hybridization, Hum Pathol. (2017) 61: 58-67; Noske et al., Detection of CCNE1/URI (19q12) amplification by in situ hybridisation is common in high grade and type II endometrial cancer, Oncotarget (2017) 8: 14794-14805).
Низкомолекулярный ингибитор, динациклиб (MK-7965) ингибирует CDK1, CDK2, CDK5 и CDK9 и в настоящее время находится в клинической разработке для рака молочной железы и гематологического рака. Селициклиб (росковитин или CYC202), который ингибирует CDK2, CDK7 и CDK9, был изучен при раке носоглотки и NSCLC, и в настоящее время исследуется в комбинации с сапацитабином у пациентов с мутациями BRCA. CYC065, который ингибирует CDK2 и CDK9, находится на ранней стадии клинической разработки. Несмотря на значительные усилия, на сегодняшний день нет одобренных средств, селективно нацеленных на CDK2. Cicenas et al. Highlights of the Latest Advances in Research on CDK Inhibitors. Cancers, (2014) 6:2224-2242.
По-прежнему существует потребность в обнаружении ингибиторов CDK с новыми профилями активности, таких как селективные ингибиторы CDK2, которые могут быть полезны для лечения рака или других пролиферативных заболеваний или состояний. В частности, ингибиторы CDK2 могут быть полезны при лечении CCNE1 или CCNE2 амплифицированных опухолей.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение частично относится к соединениям формулы (I) и их фармацевтически приемлемым солям. Такие соединения могут ингибировать активность CDK, включая CDK2, тем самым влияя на биологические функции. В некоторых вариантах осуществления изобретение относится к соединениям, селективным в отношении CDK2. Также представлены фармацевтические композиции и лекарственные средства, включающие соединения или соли по настоящему изобретению, отдельно или в комбинации с дополнительными противораковыми терапевтическими средствами.
Настоящее изобретение также относится, частично, к способам получения соединений, фармацевтически приемлемых солей и композиций по изобретению, и к способам применения вышеизложенного.
В одном аспекте изобретение относится к соединению формулы (I):
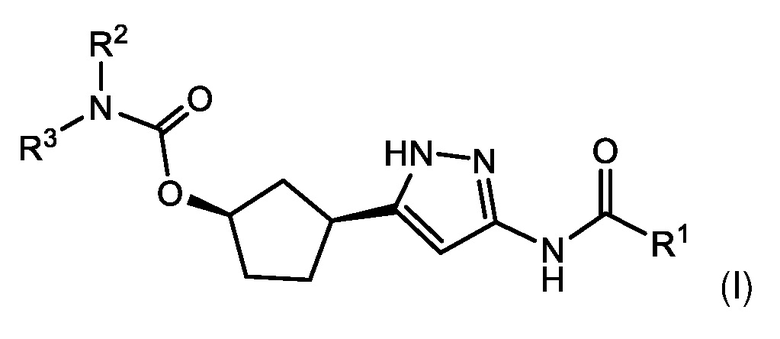
или его фармацевтически приемлемой соли, где:
R1 представляет собой -L1-(5-10-членный гетероарил) или -L1-(C6-C12 арил), где указанный 5-10-членный гетероарил или C6-C12 арил необязательно замещены одним или несколькими R4;
R2 и R3 независимо представляют собой H, C1-C6 алкил, C1-C6 фторалкил, -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил), где каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним или несколькими R5 и каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или несколькими R6; или
R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием 4-6-членного гетероциклила, необязательно содержащего дополнительный гетероатом, выбранный из O, N(R7) и S(O)q в качестве члена кольца, где указанный 4-6-членный гетероциклил необязательно замещен одним или несколькими R8;
каждый L1 и L2 независимо представляет собой связь или C1-C2 алкилен, необязательно замещенный одним или несколькими R9;
каждый R4 независимо представляет собой F, Cl, OH, CN, NR10R11, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси, C3-C8 циклоалкил, C(O)NR10R11, SO2R12, SO(=NH)R12 или SO2NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним или несколькими R13;
каждый R5 независимо представляет собой OH, C1-C4 алкокси или NR10R11;
каждый R6 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси или NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним или несколькими R13;
R7 представляет собой H, C1-C4 алкил или C(O)-C1-C4 алкил;
каждый R8 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 алкокси или CN;
каждый R9 независимо представляет собой F, OH или C1-C2 алкил;
каждый R10 и R11 независимо представляет собой H или C1-C4 алкил;
каждый R12 представляет собой C1-C4 алкил или C3-C6 циклоалкил;
каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15;
каждый R14 и R15 независимо представляет собой H или C1-C4 алкил; и
q имеет значение 0, 1 или 2.
В другом аспекте изобретение относится к соединению формулы (II):
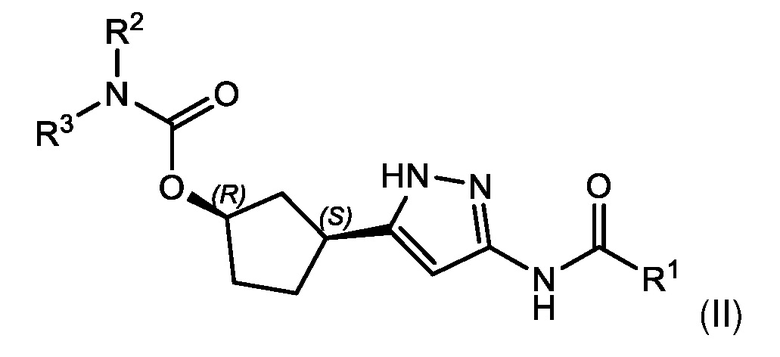
или его фармацевтически приемлемой соли, где:
R1, R2 и R3 имеют значения, определенные для формулы (I).
В другом аспекте изобретение относится к соединению формулы (III):
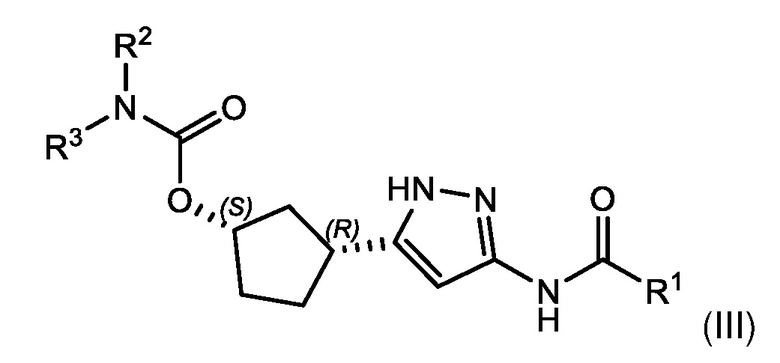
или его фармацевтически приемлемой соли, где:
R1, R2 и R3 имеют значения, определенные для формулы (I).
В другом аспекте изобретение относится к фармацевтической композиции, включающей соединение по изобретению согласно любой из формул, описанных в настоящем документе, или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или эксципиент. В некоторых вариантах осуществления фармацевтическая композиция включает два или несколько фармацевтически приемлемых носителей и/или эксципиентов.
Изобретение также предоставляет терапевтические способы и применения, включающие введение соединения по изобретению или его фармацевтически приемлемой соли, субъекту.
В одном аспекте изобретение относится к способу лечения аномального роста клеток, в частности рака, у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли. Соединения по настоящему изобретению можно вводить в виде отдельных средств или можно вводить в комбинации с другими противораковыми терапевтическими средствами, в частности, со стандартными средствами лечения, подходящими для конкретного вида рака.
В дополнительном аспекте изобретение относится к способу лечения аномального роста клеток, в частности рака, у субъекта, нуждающегося в этом, включающему введение субъекту количества соединения по настоящему изобретению или его фармацевтически приемлемой соли в комбинация с некоторым количеством дополнительного противоракового терапевтического средства, количества которых являются в совокупности эффективными при лечении указанного аномального роста клеток.
В другом аспекте изобретение относится к соединению по изобретению или его фармацевтически приемлемой соли для применения при лечении субъекта, нуждающегося в таком лечении. В некоторых вариантах осуществления, изобретение относится к соединению по изобретению или его фармацевтически приемлемой соли для применения при лечении аномального роста клеток, в частности рака, у субъекта.
В дополнительном аспекте изобретение относится к применению соединения по изобретению или его фармацевтически приемлемой соли для лечения аномального роста клеток, в частности рака, у субъекта.
В другом аспекте изобретение относится к фармацевтической композиции для применения при лечении аномального роста клеток, в частности рака, у субъекта, нуждающегося в этом, причем эта фармацевтическая композиция включает соединение по изобретению или его фармацевтически приемлемую соль, и фармацевтически приемлемый носитель или эксципиент.
В другом аспекте изобретение относится к соединению по изобретению или его фармацевтически приемлемой соли для применения в качестве лекарственного средства, в частности, лекарственного средства для лечения аномального роста клеток, такого как рак.
В еще одном аспекте изобретение относится к применению соединения по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для лечения аномального роста клеток, такого как рак, у субъекта.
В другом аспекте изобретение относится к способу лечения расстройства, опосредованного CDK2, у субъекта, включающему введение субъекту соединения по изобретению или его фармацевтически приемлемой соли в количестве, которое эффективно для лечения указанного расстройства, в частности, рака.
Каждый из вариантов осуществления соединений по настоящему изобретению, описанных ниже, может быть объединен с одним или несколькими другими вариантами осуществления соединений по настоящему изобретению, описанных в настоящем документе, не противоречащими варианту(ам) осуществления, с которым он объединен.
Кроме того, каждый из вариантов осуществления, описанных ниже, описывающих изобретение, предусматривает в пределах своего объема фармацевтически приемлемые соли соединений по изобретению. Соответственно, фраза “или его фармацевтически приемлемая соль” подразумевается в описании всех соединений, описанных в настоящем документе, если явно не указано иное.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На фиг. 1 показана монокристаллическая рентгеновская структура (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат моногидрата (форма 1).
На фиг. 2 показан спектр PXRD (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат моногидрата (форма 1).
Подробное описание изобретения
Настоящее изобретение может быть более легко понято посредством ссылки на следующее подробное описание предпочтительных вариантов осуществления изобретения и примеров, включенных в настоящее описание. Следует понимать, что используемая в настоящем описании терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения. Кроме того, следует понимать, что если специально не определено в настоящем документе, терминология, используемая в настоящем документе, должна иметь свое обычное значение, известное в соответствующей области техники.
Как используется в настоящем документе, формы единственного числа включают формы множественного числа, если не указано иное. Например, заместитель включает один или несколько заместителей.
Изобретение, описанное в настоящем документе, соответствующим образом может быть осуществлено на практике в отсутствие какого-либо элемента(-ов), конкретно не раскрытого в настоящем документе. Таким образом, например, в каждом случае в настоящем документе любой из терминов «включающий», «состоящий по существу из» и «состоящий из» может быть заменен любым из двух других терминов.
«Алкил» относится к насыщенному одновалентному алифатическому углеводородному радикалу, включая группы с прямой или разветвленной цепью, имеющие указанное число атомов углерода. Алкильные заместители обычно содержат 1-12 атомов углерода («C1-C12 алкил»), часто 1-8 атомов углерода («C1-C8 алкил»), или чаще 1-6 атомов углерода («C1-C6 алкил»), 1-5 атомов углерода («C1-C5 алкил»), 1-4 атомов углерода («C1-C4 алкил») или 1-2 атомов углерода («C1-C2 алкил»). Примеры алкильных групп включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, н-гептил, н-октил и тому подобное. Предпочтительные C1-C4 алкильные группы включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил. Предпочтительные C1-C6 алкильные группы включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изопентил, неопентил и н-гексил.
Алкильные группы, описанные в настоящем описании, как необязательно замещенные, могут быть замещены одной или несколькими группами заместителей, как дополнительно определено формулой изобретения в данном документе. Такие необязательные группы заместителей выбираются независимо, если не указано иное. Общее количество групп заместителей может равняться общему количеству атомов водорода в алкильном фрагменте, в той степени, в которой такое замещение имеет химический смысл. Необязательно замещенные алкильные группы обычно содержат от 1 до 6 необязательных заместителей, иногда от 1 до 5 необязательных заместителей, от 1 до 4 необязательных заместителей или предпочтительно от 1 до 3 необязательных заместителей.
Примеры групп заместителей в алкильных группах включают галоген, -OH, C1-C4 алкокси или NRxRy, где каждый Rx и Ry независимо представляет собой H или C1-C4 алкил. Следует понимать, что NRxRy используется в настоящем документе в общем для обозначения амино заместителей (например, NR10R11 как часть необязательного заместителя R5 или NR14R15 как часть необязательного заместителя R13) как определено в формуле изобретения. В некоторых случаях замещенные алкильные группы могут быть названы конкретно со ссылкой на группу-заместитель. Например, «галогеналкил» относится к алкильной группе, имеющей определенное число атомов углерода, которая замещена одним или несколькими галогеновыми заместителями, и обычно содержит 1-6 атомов углерода, 1-5 атомов углерода, 1-4 атомов углерода или 1-2 атома углерода и 1, 2 или 3 атомов галогена (т.е. “C1-C5 галогеналкил”, C1-C4 галогеналкил” или “C1-C2 галогеналкил”).
Более конкретно, фторированные алкильные группы могут конкретно упоминаться как «фторалкильные» группы (например, C1-C6, C1-C5, C1-C4 или C1-C2 фторалкильные группы), которые обычно замещены 1, 2 или 3 атомами фтора. Например, C1-C4 фторалкил включает трифторметил (-CF3), дифторметил (-CF2H), фторметил (-CFH2), дифторэтил (-CH2CF2H), и тому подобное. Такие группы могут быть дополнительно замещены необязательными группами заместителей, как дополнительно описано в настоящем документе. Аналогичным образом, алкильные группы, замещенные -OH, C1-C4 алкокси или NRxRy могут называться «гидроксиалкил», «алкоксиалкил» или «аминоалкил», в каждом случае имеющие указанное количество атомов углерода.
В некоторых вариантах осуществления настоящего изобретения алкильные и фторалкильные группы необязательно замещены одним или несколькими необязательными заместителями и предпочтительно от 1 до 4, от 1 до 3 или от 1 до 2 необязательных заместителей.
«Алкилен», используемый в настоящем документе, относится к двухвалентной гидрокарбильной группе, имеющей определенное количество атомов углерода, которая может связывать две другие группы вместе. Такие группы могут называться, например, C1-C6 алкиленом, C1-C4 алкиленом, C1-C2 алкиленом, и тому подобное. Если указано, алкилен также может быть замещен другими группами и может включать одну или несколько степеней ненасыщенности (т.е. алкениленовый или алкиниленовый фрагмент) или колец. Открытые валентности алкилена не обязательно должны находиться на противоположных концах цепи. Разветвленные алкиленовые группы могут включать -CH(Me)-, -CH2CH(Me)- и -C(Me)2-, также включены в объем термина алкилены. Если алкиленовая группа описана как необязательно замещенная, заместители включают те, которые описаны в настоящем документе. Например, C1-C2 алкилен может быть метиленом или этиленом.
«Алкокси» относится к одновалентной -O-алкильной группе, в которой алкильная часть имеет указанное количество атомов углерода. Алкоксигруппы обычно содержат от 1 до 8 атомов углерода (“C1-C8 алкокси”), или от 1 до 6 атомов углерода (“C1-C6 алкокси”), или от 1 до 4 атомов углерода (“C1-C4 алкокси”). Например, C1-C4 алкокси включает метокси, этокси, изопропокси, трет-бутилокси (т.е., -OCH3, -OCH2CH3, -OCH(CH3)2, -OC(CH3)3), и тому подобное. Алкоксигруппы могут быть необязательно замещены одним или несколькими атомами галогена, в частности одним или несколькими атомами фтора, вплоть до общего количества атомов водорода, присутствующих в алкильной части. Такие группы могут называться «галогеналкокси» (или, где фторированные, более конкретно, как «фторалкокси») группами, имеющими определенное число атомов углерода и замещенными одним или несколькими галогеновыми заместителями. Обычно такие группы содержат от 1 до 6 атомов углерода, предпочтительно от 1 до 4 атомов углерода, и иногда и от 1 до 2 атомов углерода, и 1, 2 или 3 атомов галогена (например, “C1-C6 галогеналкокси”, “C1-C4 галогеналкокси” или “C1-C2 галогеналкокси”). Более конкретно, фторированные алкильные группы могут конкретно упоминаться как «фторалкокси» группы, например, C1-C6, C1-C4 или C1-C2 фторалкоксигруппы, которые обычно замещены 1, 2 или 3 атомами фтора. Таким образом, C1-C4 фторалкокси включает, но не ограничивается ими, трифторметилокси (-OCF3), дифторметилокси (-OCF2H), фторметилокси (-OCFH2), дифторэтилокси (-OCH2CF2H), и тому подобное.
«Циклоалкил» относится к неароматической насыщенной карбоциклической кольцевой системе, содержащей конкретное количество атомов углерода, которая может быть моноциклической, спироциклической, мостиковой или конденсированной бициклической или полициклической кольцевой системой, которая связана с основной молекулой посредством атома углерода циклоалкильного кольца. Обычно циклоалкильные группы по изобретению содержат от 3 до 8 атомов углерода (“C3-C8 циклоалкил”), предпочтительно от 3 до 7 атомов углерода (“C3-C7 циклоалкил”) или от 3 до 6 атомов углерода (“C3-C6 циклоалкил”). Типичные примеры циклоалкильных колец включают, например, циклопропан, циклобутан, циклопентан, циклогексан, циклогептан и тому подобное. Циклоалкильные группы могут быть необязательно замещенными, незамещенными или замещены группами, описанными в настоящем документе.
Термины «гетероциклил» или «гетероциклический» могут использоваться взаимозаменяемо для обозначения неароматической насыщенной кольцевой системы, содержащей указанное количество кольцевых атомов, содержащей по меньшей мере один гетероатом, выбранный из N, O и S, в качестве кольцевых членов, где кольцевые атомы S необязательно замещены одной или двумя оксогруппами (т.е. S(O)q, где q имеет значение 0, 1 или 2), и где гетероциклическое кольцо связано с основной молекулой посредством кольцевого атома, которым может быть С или N. Если конкретно указано, такие гетероциклические кольца могут быть частично ненасыщенными. Гетероциклические кольца включают кольца, которые являются спироциклическими, мостиковыми или конденсированными с одним или несколькими другими гетероциклическими или карбоциклическими кольцами, где такие спироциклические, мостиковые или конденсированные кольца могут сами быть насыщенными, частично ненасыщенными или ароматическими в той степени, в которой ненасыщенность или ароматичность имеют химический смысл, при условии, что точка присоединения к основной молекуле представляет собой атом гетероциклической части кольцевой системы. Предпочтительно гетероциклические кольца содержат от 1 до 4 гетероатомов, выбранных из N, O, и S(O)q, в качестве кольцевых членов, и более предпочтительно от 1 до 2 кольцевых гетероатомов, при условии, что такие гетероциклические кольца не содержат двух смежных атомов кислорода.
Гетероциклильные группы являются незамещеными или замещены подходящими группами заместителей, как описано в настоящем документе. Такие заместители могут присутствовать в гетероциклическом кольце, присоединенном к основной молекуле, или на спироциклическом, мостиковом или конденсированном кольце, присоединенном к нему. Кроме того, кольцевые атомы N необязательно замещены группами, подходящими для амина, например, алкилом, ацилом, карбамоилом, сульфонилом и т.п.
Гетероциклы обычно включают 3-8-членные гетероциклильные группы и более предпочтительно 4-7- или 4-6-членные гетероциклильные группы в соответствии с определением в настоящем документе.
Иллюстративные примеры насыщенных гетероциклов включают, но не ограничиваются ими:
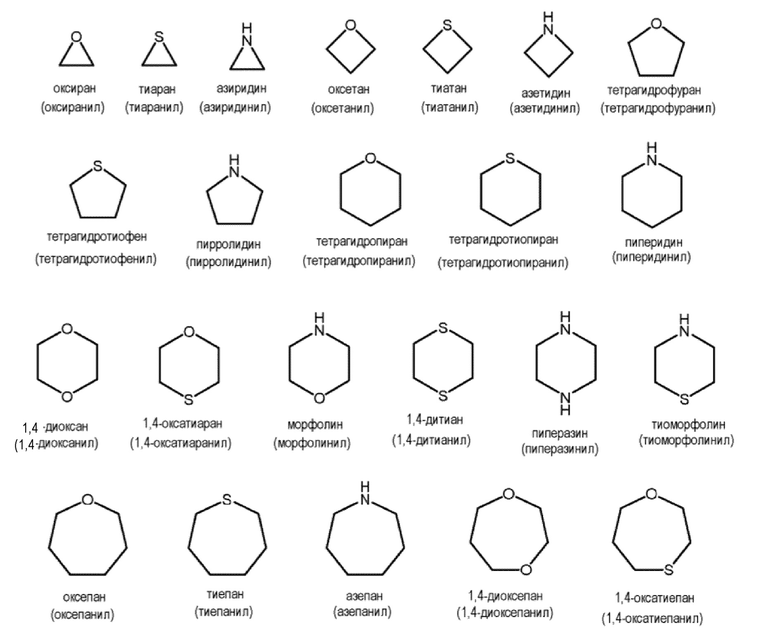
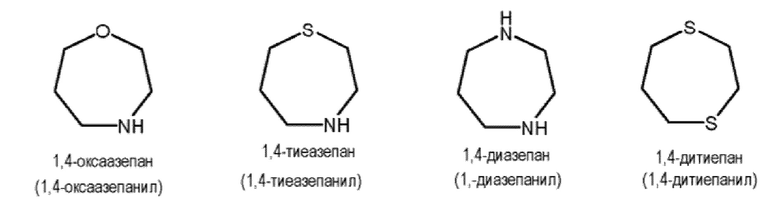
В некоторых вариантах осуществления, гетероциклические группы содержат 3-8 кольцевых членов, включая как атомы углерода, так и неуглеродные гетероатомы, и часто 4-7 или 4-6 кольцевых членов. В некоторых вариантах осуществления, группы-заместители, содержащие 4-7-членные гетероциклы выбраны из азетидинильного, пирролидинильного, пиперидинильного, пиперазинильного, азепанильного, диазепанильного, оксетанильного, тетрагидрофуранильного, тетрагидропиранильного, тетрагидротиопиранильного, морфолинильного и тиоморфолинильного колец, каждое из которых необязательно замещено, как описано в настоящем документе, если такое замещение имеет химический смысл.
В некоторых вариантах осуществления настоящего изобретения циклоалкильные и гетероциклильные группы необязательно замещены одним или несколькими необязательными заместителями, как описано в настоящем документе.
Следует понимать, что не более двух атомов N, О или S обычно соединены последовательно, за исключением случаев, когда оксогруппа присоединена к S с образованием сульфонильной группы, или в случае определенных гетероароматических колец, таких как триазол, тетразол, оксадиазол, тиадиазол, триазин и тому подобное.
«Арил» или «ароматический» относится к необязательно замещенной моноциклической или конденсированной бициклической или полициклической кольцевой системе, имеющей хорошо известные характеристики ароматичности, где по меньшей мере одно кольцо содержит полностью конъюгированную пи-электронную систему. Обычно арильные группы содержат от 6 до 20 атомов углерода ("C6-C20 арил") в качестве кольцевых членов, предпочтительно от 6 до 14 атомов углерода ("C6-C14 арил") или более предпочтительно от 6 до 12 атомов углерода ("C6-C12 арил"). Конденсированные арильные группы могут включать арильное кольцо (например, фенильное кольцо), конденсированное с другим арильным или гетероарильным кольцом, или конденсированное с насыщенным или частично ненасыщенным карбоциклическим или гетероциклическим кольцом, при условии, что точка присоединения к основной молекуле в таких конденсированных кольцевых системах представляет собой атом ароматической части кольцевой системы. Примеры, без ограничения, арильных групп включают фенил, бифенил, нафтил, антраценил, фенантренил, инданил, инденил и тетрагидронафтил. Арильная группа может быть незамещенной или замещена, как в дальнейшем раскрыто в настоящем описании.
Аналогично, "гетероарил" или "гетероароматический" относятся к моноциклическим или конденсированным бициклическим или полициклическим кольцевым системам, обладающим хорошо известными характеристиками ароматичности, которые содержат конкретное количество кольцевых атомов, как определено выше в разделе «арил», которые включают по меньшей мере один гетероатом, выбранный из N, О и S, в качестве кольцевого члена в ароматическом кольце. Включение гетероатома допускает ароматичность в 5-членных кольцах, а также в 6-членных кольцах. Обычно гетероарильные группы содержат от 5 до 12 кольцевых атомов ("5-12-членный гетероарил"), и более предпочтительно от 5 до 10 кольцевых атомов ("5-10-членный гетероарил"). Гетероарильные кольца присоединены к основной молекуле посредством кольцевого атома гетероароматического кольца, так что ароматичность сохраняется. Таким образом, 6-членные гетероарильные кольца могут быть присоединены к основной молекуле посредством кольцевого атома С, тогда как 5-членные гетероарильные кольца могут быть присоединены к основной молекуле посредством кольцевого атома С или N. Гетероарильные группы также могут быть конденсированы с другим арильным или гетероарильным кольцом или конденсированы с насыщенным или частично ненасыщенным карбоциклическим или гетероциклическим кольцом, при условии, что точка присоединения к основной молекуле в таких конденсированных кольцевых системах представляет собой атом гетероароматической части кольцевой системы. Примеры незамещенных гетероарильных групп включают, но не ограничиваются ими, пиразол, триазол, изоксазол, оксазол, тиазол, тиадиазол, имидазол, пиридин, пиразин, индазол и бензимидазол. Дополнительные гетероарильные группы включают пиррол, фуран, тиофен, оксадиазол, тетразол, пиридазин, пиримидин, бензофуран, бензотиофен, индол, хинолин, изохинолин, пурин, триазин, нафтриидин и карбазол. В частых вариантах осуществления 5- или 6-членные гетероарильные группы представляют собой пиразольные, триазольные, изоксазольные, оксазольные, тиазольные, тиадиазольные, имидазольные, пиридиновые или пиразиновые кольца. Гетероарильная группа может быть незамещенной или замещена, как в дальнейшем раскрыто в настоящем описании.
Арильные и гетероарильные фрагменты, описанные в настоящем документе как необязательно замещенные, могут быть замещены одной или несколькими группами заместителей, которые выбраны независимо, если не указано иное. Общее количество групп-заместителей может быть равно общему количеству атомов водорода в арильном, гетероарильном или гетероциклильном фрагменте в той степени, в которой такое замещение имеет химический смысл, и ароматичность сохраняется в случае арильных и гетероарильных колец. Необязательно замещенные арильные или гетероарильные группы обычно содержат от 1 до 5 необязательных заместителей, иногда от 1 до 4 необязательных заместителей, предпочтительно от 1 до 3 необязательных заместителей, или более предпочтительно от 1 до 2 необязательных заместителей, как описано в настоящем документе.
Примеры моноциклических гетероарильных групп включают, но не ограничиваются ими:
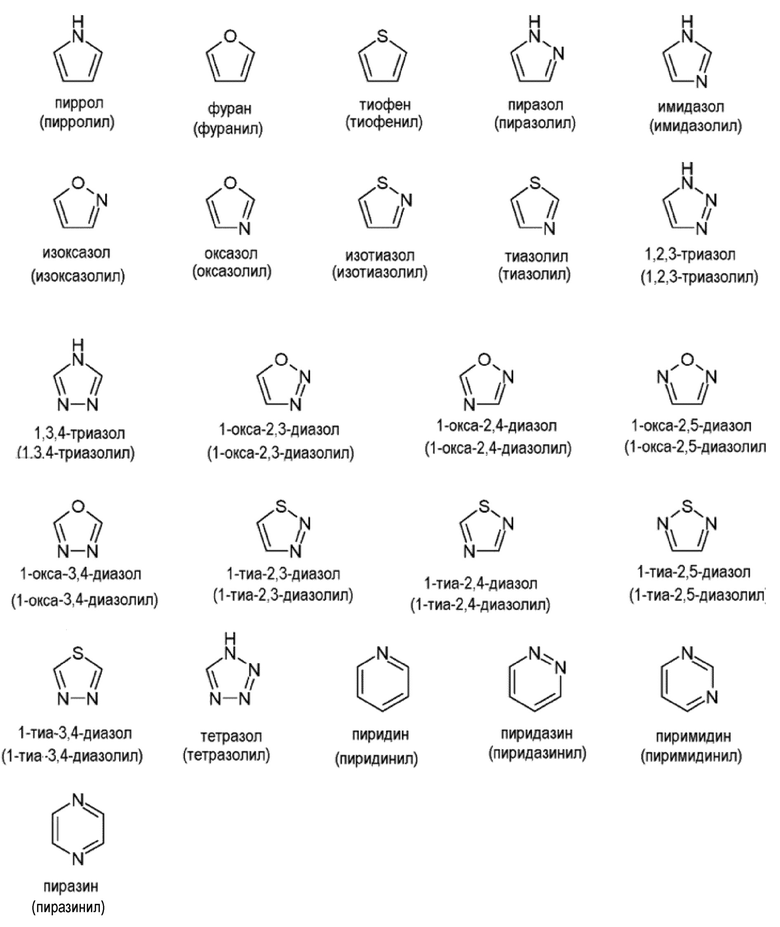
Иллюстративные примеры конденсированных гетероарильных групп включают, но не ограничиваются ими:
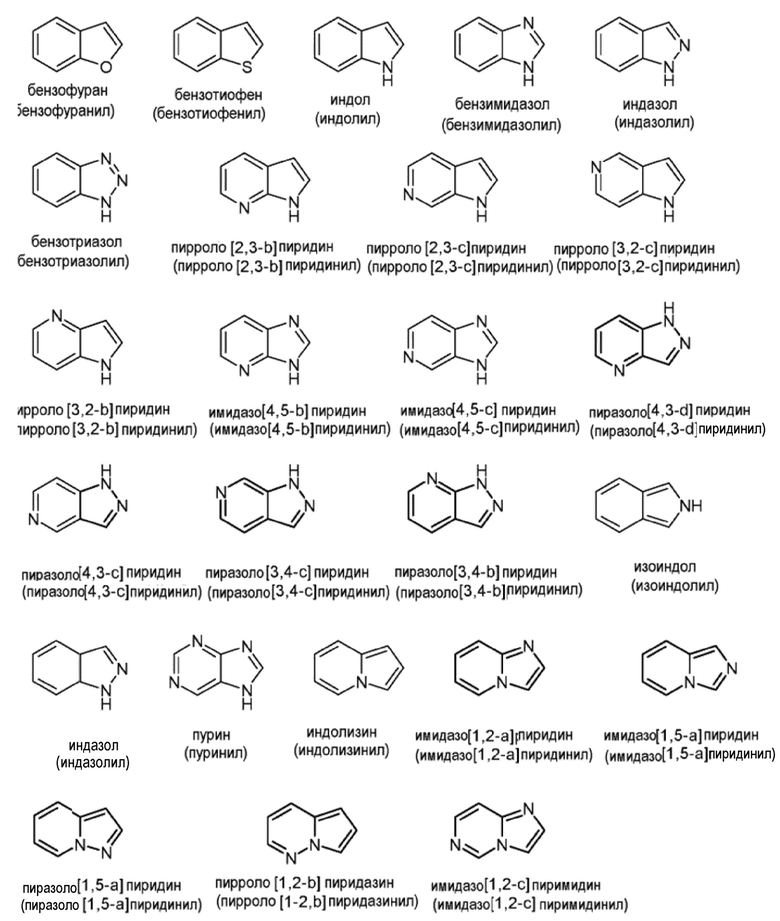
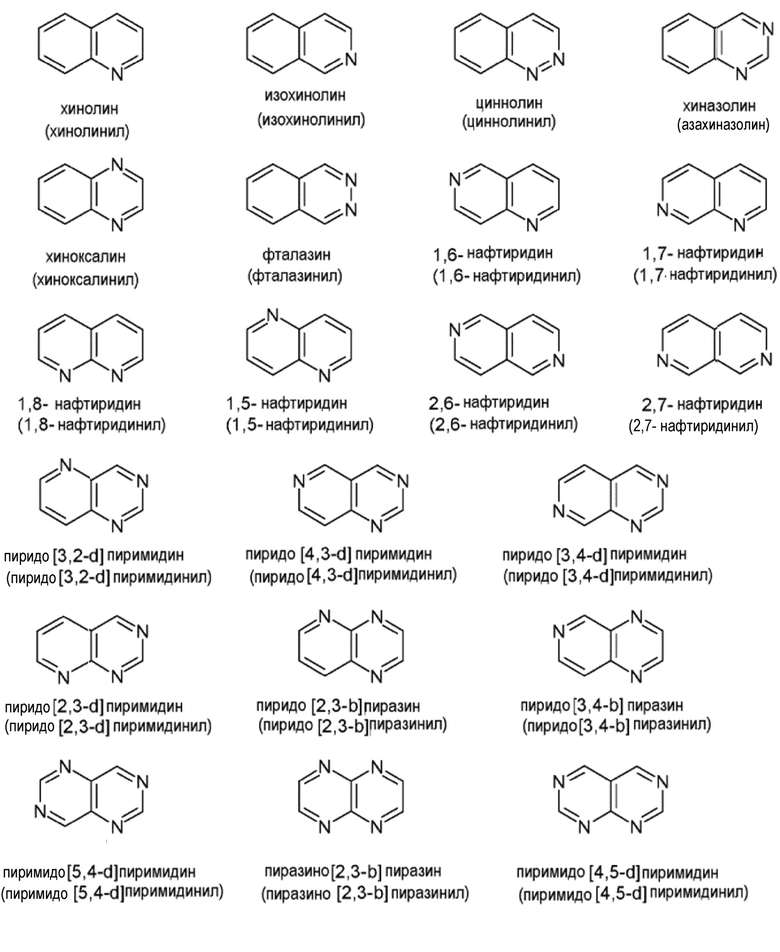
«Гидрокси» относится к группе ОН.
«Циано» относится к группе -C≡N.
"Незамещенный амино" относится к группе -NH2. Если амино описан как замещенный или необязательно замещенный, то термин включает группы вида -NRxRy, где каждый из Rx и Ry определены, как дополнительно описано в настоящем документе. Например, “алкиламино” относится к группе -NRxRy, где один из Rx и Ry представляет собой алкильную группу, а другой представляет собой H, и "диалкиламино" относится к -NRxRy, где оба из Rx и Ry представляют собой алкильные группы, где алкильные группы имеют конкретное количество атомов углерода (например, -NH-C1-C4 алкил или -N(C1-C4 алкил)2). Следует понимать, что NRxRy в общем используется для обозначения амино-заместителей (например, NR10R11 как часть необязательной группы заместителей R5 или NR14R15 как часть необязательной группы заместителей R13), как определено в формуле изобретения.
"Галоген" или "гало" относится к фтору, хлору, брому и йоду (F, Cl, Br, I). Предпочтительно галоген относится к фтору или хлору (F или Cl).
«Необязательный» или «необязательно» означает, что событие или условие, описанные потом, не обязательно могут происходить, и описание включает случаи, когда событие или условие происходит, и случаи, когда оно не происходит.
Термины "необязательно замещенный" и "замещенный или незамещенный" используются взаимозаменяемо для указания на то, что конкретная описываемая группа может не иметь неводородных заместителей (т.е. незамещенная), или эта группа может иметь один или более неводородных заместителей (т.е. замещенная). Если не указано иное, общее количество заместителей, которые могут присутствовать, равно количеству атомов Н, присутствующих в незамещенной форме описываемой группы. Если необязательный заместитель присоединен посредством двойной связи, такой как заместитель оксо (=O), то группа занимает две доступные валентности, так что суммарное количество других заместителей, которые могут быть включены, уменьшается на два. В случае, когда необязательные заместители независимо выбраны из списка альтернатив, выбранные группы могут быть одинаковыми или разными. На протяжении всего описания будет понятно, что количество и природа необязательных групп заместителей будут ограничены в той степени, в которой такие замены имеют химический смысл.
Часто группа, описанная в настоящем документе, как необязательно замещенная «одной или несколькими» группами заместителей, необязательно замещена от 1 до 4, предпочтительно необязательно замещена от 1 до 3 и более предпочтительно необязательно замещена от 1 до 2 таких заместителей. Упоминание в настоящем документе о том, что группа «необязательно замещена одним или несколькими» из списка необязательных заместителей, может быть заменена на «необязательно замещена 1-4», «необязательно замещена 1-3», «необязательно замещена 1-2», «необязательно замещенна одним, двумя, тремя или четырьмя», «необязательно замещена одним, двумя или тремя» или «необязательно замещена одним или двумя» из таких необязательных групп заместителей.
В одном аспекте изобретение относится к соединению формулы (I):

или его фармацевтически приемлемой соли, где:
R1 представляет собой -L1-(5-10-членный гетероарил) или -L1-(C6-C12 арил), где указанный 5-10-членный гетероарил или C6-C12 арил необязательно замещены одним или несколькими R4;
R2 и R3 независимо представляют собой H, C1-C6 алкил, C1-C6 фторалкил, -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил), где каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним или несколькими R5 и каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или несколькими R6; или
R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием 4-6-членного гетероциклила, необязательно содержащего дополнительный гетероатом, выбранный из O, N(R7) и S(O)q, в качестве члена кольца, где указанный 4-6-членный гетероциклил необязательно замещен одним или несколькими R8;
каждый L1 и L2 независимо представляет собой связь или C1-C2 алкилен, необязательно замещенный одним или несколькими R9;
каждый R4 независимо представляет собой F, Cl, OH, CN, NR10R11, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси, C3-C8 циклоалкил, C(O)NR10R11, SO2R12, SO(=NH)R12 или SO2NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним или несколькими R13;
каждый R5 независимо представляет собой OH, C1-C4 алкокси или NR10R11;
каждый R6 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси или NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним или несколькими R13;
R7 представляет собой H, C1-C4 алкил или C(O)-C1-C4 алкил;
каждый R8 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 алкокси или CN;
каждый R9 независимо представляет собой F, OH или C1-C2 алкил;
каждый R10 и R11 независимо представляет собой H или C1-C4 алкил;
каждый R12 представляет собой C1-C4 алкил или C3-C6 циклоалкил;
каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15;
каждый R14 и R15 независимо представляет собой H или C1-C4 алкил; и
q имеет значение 0, 1 или 2.
Соединения формулы (I) характеризуются син-зависимостью между группами заместителей в 1- и 3-положениях циклопентильного кольца. Соединения формулы (I) могут присутствовать в виде одного энантиомера, имеющего син-относительную конфигурацию в положениях 1 и 3 (т.е. (1R,3S) или (1S,3R)), или в виде смеси син-энантиомерных форм, например, рацемическая смесь (1R,3S) и (1S,3R).
В соединениях формулы (I), R1 представляет собой -L1-(5-10-членный гетероарил) или -L1-(C6-C12 арил), где указанный 5-10-членный гетероарил или C6-C12 арил необязательно замещены одним или несколькими R4.
В некоторых вариантах осуществления, R1 представляет собой -L1-(5-10-членный гетероарил), где указанный 5-10-членный гетероарил необязательно замещен одним или несколькими R4. В некоторых таких вариантах осуществления указанный 5-10-членный гетероарил представляет собой пиразолил, триазолил, изоксазолил, оксазолил, тиазолил, тиадиазолил, имидазолил, пиридинил, пиразинил, индазолил или бензимидазолил, где указанный 5-10-членный гетероарил необязательно замещен одним или несколькими R4. В некоторых вариантах осуществления указанный 5-10-членный гетероарил представляет собой пиразолил или триазолил, необязательно замещенный одним или несколькими R4. В конкретных вариантах осуществления указанный 5-10-членный гетероарил представляет собой пиразолил, необязательно замещенный одним или несколькими R4. В других вариантах осуществления указанный 5-10-членный гетероарил представляет собой триазолил, необязательно замещенный одним или несколькими R4. В других вариантах осуществления, указанный 5-10-членный гетероарил представляет собой изоксазолил, оксазолил, тиазолил, тиадиазолил, имидазолил, пиридинил, пиразинил, индазолил или бензимидазолил, где указанный 5-10-членный гетероарил необязательно замещен одним или несколькими R4. В некоторых вариантах осуществления указанный 5-10-членный гетероарил представляет собой изоксазолил или оксазолил, необязательно замещенный одним или несколькими R4. В конкретных вариантах осуществления указанный 5-10-членный гетероарил представляет собой изоксазолил, необязательно замещенный одним или несколькими R4. В других вариантах осуществления, указанный 5-10-членный гетероарил представляет собой тиазолил, тиадиазолил или имидазолил, где указанный 5-10-членный гетероарил необязательно замещен одним или несколькими R4. В еще других вариантах осуществления указанный 5-10-членный гетероарил представляет собой пиридинил, пиразинил, индазолил или бензимидазолил, где указанный 5-10-членный гетероарил необязательно замещен одним или несколькими R4. В некоторых вариантах осуществления каждого из вышеперечисленных, указанный 5-10-членный гетероарил необязательно замещен одним, двумя, тремя или четырьмя R4. В некоторых вариантах осуществления каждого из вышеперечисленных, указанный 5-10-членный гетероарил необязательно замещен одним или двумя R4.
В других вариантах осуществления, R1 представляет собой-L1-(C6-C12 арил), где указанный C6-C12 арил необязательно замещен одним или несколькими R4. В некоторых таких вариантах осуществления, указанный C6-C12 арил представляет собой фенил, необязательно замещенный одним или несколькими R4. В некоторых вариантах осуществления каждого из вышеперечисленных, указанный C6-C12 арил необязательно замещен одним, двумя, тремя или четырьмя R4. В некоторых вариантах осуществления каждого из вышеперечисленных, указанный C6-C12 арил необязательно замещен одним или двумя R4.
В соединениях формулы (I), L1 представляет собой связь или C1-C2 алкилен, необязательно замещенный одним или несколькими R9. В некоторых таких вариантах осуществления, указанный L1 представляет собой связь или C1-C2 алкилен, необязательно замещенный одним, двумя, тремя или четырьмя R9. В некоторых таких вариантах осуществления, L1 представляет собой связь или C1-C2 алкилен, необязательно замещенный одним или двумя R9. В некоторых таких вариантах осуществления, L1 представляет собой связь, метилен или этилен. В некоторых таких вариантах осуществления, L1 представляет собой связь или метилен. В некоторых вариантах осуществления каждого из вышеперечисленных, L1 представляет собой связь. В других вариантах осуществления каждого из вышеперечисленных, L1 представляет собой C1-C2 алкилен, необязательно замещенный одним или несколькими R9. В некоторых таких вариантах осуществления, указанный L1 представляет собой C1-C2 алкилен, необязательно замещенный одним, двумя, тремя или четырьмя R9. В некоторых таких вариантах осуществления, указанный L1 представляет собой C1-C2 алкилен, необязательно замещенный одним или двумя R9. В некоторых таких вариантах осуществления, L1 представляет собой метилен или этилен (т.е., -CH2 или -CH2CH2-). В некоторых вариантах осуществления L1 представляет собой метилен.
В соединениях формулы (I), R2 и R3 независимо представляют собой H, C1-C6 алкил, C1-C6 фторалкил, -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил), где каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним или несколькими R5 и, каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или несколькими R6; или R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием 4-6-членного гетероциклила, необязательно содержащего дополнительный гетероатом, выбранный из O, N(R7) и S(O)q, в качестве члена кольца, где указанный 4-6-членный гетероциклил необязательно замещен одним или несколькими R8.
В некоторых вариантах осуществления, R2 и R3 независимо представляют собой H, C1-C6 алкил, C1-C6 фторалкил, -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил), где каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним или несколькими R5 и, каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или несколькими R6. В некоторых таких вариантах осуществления, указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним, двумя, тремя или четырьмя R5 и, каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним, двумя, тремя или четырьмя R6. В некоторых таких вариантах осуществления, указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним или двумя R5 и, каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или двумя R6.
В некоторых вариантах осуществления, R2 и R3 независимо представляют собой H, C1-C6 алкил или C1-C6 фторалкил, где каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним или несколькими R5. В некоторых таких вариантах осуществления, каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним, двумя, тремя или четырьмя R5. В некоторых таких вариантах осуществления, каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним или двумя R5. В конкретных вариантах осуществления, R2 и R3 независимо представляют собой H, C1-C6 алкил или C1-C6 фторалкил. В конкретных вариантах осуществления, R2 представляет собой H и R3 представляет собой C1-C6 алкил или C1-C6 фторалкил. В конкретных вариантах осуществления, R2 представляет собой H и R3 представляет собой CH3, CH2CH3, CH2CH2CH3, CH(CH3)2, CH2CH2CH2CH3, CH(CH3)CH2CH3, CH2CH(CH3)2 или C(CH3)3.
В других вариантах осуществления, R2 и R3 независимо представляют собой H, -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил), где каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или несколькими R6. В некоторых таких вариантах осуществления, R2 представляет собой H и R3 представляет собой -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил), где каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или несколькими R6. В конкретных вариантах осуществления, R2 представляет собой H и R3 представляет собой -L2-(C3-C7 циклоалкил), где указанный C3-C7 циклоалкил необязательно замещен одним или несколькими R6. В некоторых вариантах осуществления каждого из вышеперечисленных, каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним, двумя, тремя или четырьмя R6. В некоторых вариантах осуществления каждого из вышеперечисленных, каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или двумя R6. В некоторых таких вариантах осуществления, каждый R6 представляет собой CH3.
В соединениях формулы (I), L2 представляет собой связь или C1-C2 алкилен, необязательно замещенный одним или несколькими R9. В некоторых таких вариантах осуществления, указанный L2 представляет собой связь или C1-C2 алкилен, необязательно замещенный одним, двумя, тремя или четырьмя R9. В некоторых таких вариантах осуществления, L2 представляет собой связь или C1-C2 алкилен, необязательно замещенный одним или двумя R9. В некоторых таких вариантах осуществления, L2 представляет собой связь, метилен или этилен. В некоторых таких вариантах осуществления, L2 представляет собой связь или метилен. В некоторых вариантах осуществления каждого из вышеперечисленных, L2 представляет собой связь. В других вариантах осуществления каждого из вышеперечисленных, L2 представляет собой C1-C2 алкилен, необязательно замещенный одним или несколькими R9. В некоторых таких вариантах осуществления L2 представляет собой C1-C2 алкилен, необязательно замещенный одним, двумя, тремя или четырьмя R9. В некоторых таких вариантах осуществления L2 представляет собой C1-C2 алкилен, необязательно замещенный одним или двумя R9. В некоторых таких вариантах осуществления, L2 представляет собой метилен или этилен (т.е., -CH2 или -CH2CH2-). В некоторых вариантах осуществления, L2 представляет собой метилен.
В некоторых вариантах осуществления, R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием 4-6-членного гетероциклила, необязательно содержащего дополнительный гетероатом, выбранный из O, N(R7) и S(O)q, в качестве члена кольца, где указанный 4-6-членный гетероциклил необязательно замещен одним или несколькими R8, и где q имеет значение 0, 1 или 2. В некоторых таких вариантах осуществления, указанный 4-6-членный гетероциклил необязательно замещен одним, двумя, тремя или четырьмя R8. В некоторых таких вариантах осуществления, указанный 4-6-членный гетероциклил необязательно замещен одним или двумя R8.
В некоторых таких вариантах осуществления, R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием необязательно замещенного 4-6-членного гетероциклила, необязательно содержащего дополнительный гетероатом, выбранный из O, N(R7) и S(O)q, в качестве члена кольца, где указанный 4-6-членный гетероциклил представляет собой азетидинил, пирролидинил, пиперидинил, пиперазинил, морфолинил или тиоморфолинил, каждый из которых необязательно замещен одним или несколькими R8. В некоторых таких вариантах осуществления, R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием азетидинила или пирролидинила, каждый из которых необязательно замещен одним или несколькими R8. В конкретных вариантах осуществления, R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием азетидинила, необязательно замещенного одним или несколькими R8. В некоторых вариантах осуществления, каждого из вышеперечисленных, указанный 4-6-членный гетероциклил необязательно замещен одним, двумя, тремя или четырьмя R8. В некоторых вариантах осуществления, каждого из вышеперечисленных, указанный 4-6-членный гетероциклил необязательно замещен одним или двумя R8. В некоторых таких вариантах осуществления, каждый R8 представляет собой CH3.
В соединениях формулы (I), каждый R4 независимо представляет собой F, Cl, OH, CN, NR10R11, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси, C3-C8 циклоалкил, C(O)NR10R11, SO2R12, SO(=NH)R12 или SO2NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним или несколькими R13. В некоторых вариантах осуществления, каждый R4 независимо представляет собой C1-C4 алкил или C1-C4 алкокси, где каждый C1-C4 алкил необязательно замещен одним или несколькими R13. В некоторых таких вариантах осуществления, каждый R13 представляет собой OCH3. В некоторых вариантах осуществления каждого из вышеперечисленных, каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним, двумя, тремя или четырьмя R13. В некоторых вариантах осуществления каждого из вышеперечисленных, каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним или двумя R13. В конкретных вариантах осуществления, каждый R4 (или R4, замещенный R13) независимо представляет собой CH3, OCH3 или CH2OCH3.
В соединениях формулы (I), каждый R5 независимо представляет собой OH, C1-C4 алкокси или NR10R11. В некоторых таких вариантах осуществления, каждый R5 независимо представляет собой OH, OCH3, NH2, NHCH3 или N(CH3)2.
В соединениях формулы (I), каждый R6 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси или NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним или несколькими R13. В некоторых вариантах осуществления, каждый R6 независимо представляет собой C1-C4 алкил или C1-C4 алкокси, где каждый C1-C4 алкил необязательно замещен одним или несколькими R13. В некоторых вариантах осуществления каждого из вышеперечисленных, каждый C1-C4 алкил необязательно замещен одним, двумя, тремя или четырьмя R13. В некоторых вариантах осуществления каждого из вышеперечисленных, каждый C1-C4 алкил необязательно замещен одним или двумя R13. В некоторых таких вариантах осуществления, R13 представляет собой CH3 или OCH3. В конкретных вариантах осуществления, каждый R6 независимо представляет собой CH3, OCH3 или CH2OCH3. В конкретных вариантах осуществления, каждый R6 независимо представляет собой CH3.
В соединениях формулы (I), R7 представляет собой H, C1-C4 алкил или C(O)-C1-C4 алкил. В некоторых вариантах осуществления, R7 представляет собой H, CH3 или C(O)CH3.
В соединениях формулы (I), каждый R8 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 алкокси или CN. В конкретных вариантах осуществления, каждый R8 независимо представляет собой F, OH, CH3, OCH3 или CN. В конкретных вариантах осуществления, каждый R8 представляет собой CH3.
В соединениях формулы (I), каждый R9 независимо представляет собой F, OH или C1-C2 алкил. В некоторых вариантах осуществления, R9 представляет собой F, OH или CH3. В конкретных вариантах осуществления, R9 представляет собой F, OH или CH3. В некоторых вариантах осуществления, L1 и L2 представляют собой связь или незамещенный C1-C2 алкилен, и R9 отсутствует.
В соединениях формулы (I), каждый R10 и R11 независимо представляет собой H или C1-C4 алкил. В конкретных вариантах осуществления, каждый R10 и R11 независимо представляет собой H или CH3.
В соединениях формулы (I), каждый R12 представляет собой C1-C4 алкил или C3-C6 циклоалкил. В конкретных вариантах осуществления, каждый R12 представляет собой CH3, CH2CH3, CH2CH2CH3, CH(CH3)2 или циклопропил.
В соединениях формулы (I), каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15. В конкретных вариантах осуществления, каждый R13 независимо представляет собой OH, OCH3 или NR14R15, где R14 и R15 независимо представляют собой H или CH3. В конкретных вариантах осуществления, каждый R13 независимо представляет собой OH, OCH3, NH2, NHCH3 или N(CH3)2.
В соединениях формулы (I), каждый R14 и R15 независимо представляет собой H или C1-C4 алкил. В конкретных вариантах осуществления, R14 и R15 независимо представляют собой H или CH3.
В некоторых вариантах осуществления, соединение формулы (I) имеет абсолютную стереохимию, как показано в формуле (II):
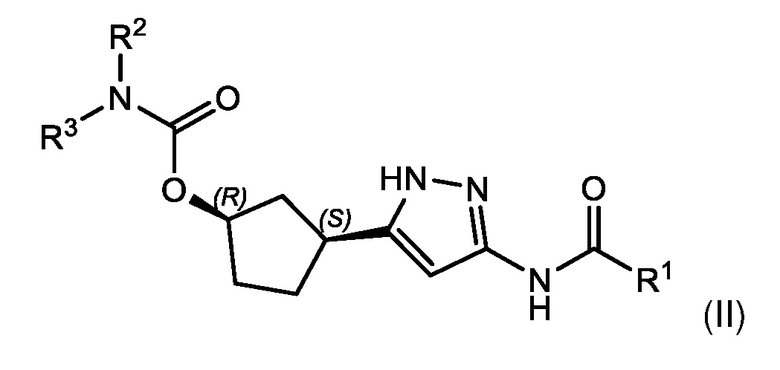
или его фармацевтически приемлемая соль, где:
R1, R2 и R3 имеют значения, определенные для формулы (I).
В некоторых вариантах осуществления, соединение формулы (I) имеет абсолютную стереохимию, как показано в формуле (III):
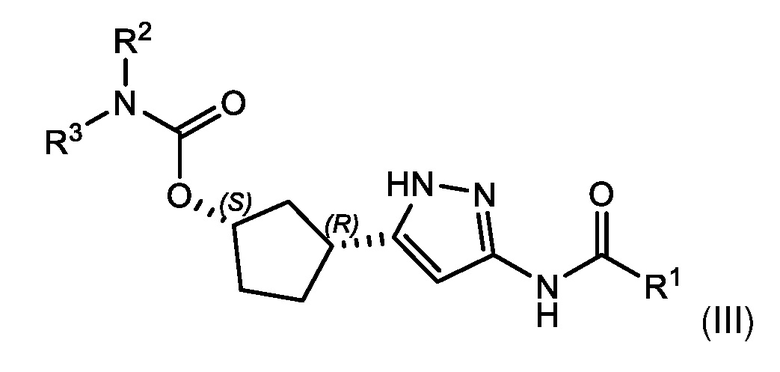
или его фармацевтически приемлемая соль, где:
R1, R2 и R3 имеют значения, определенные для формулы (I).
Соединения формул (II) и (III) поддерживают син-связь между группами заместителей в 1- и 3-положениях циклопентильного кольца, но присутствуют в виде энантиомера, указанного в основном в энантиомерно чистой форме.
Каждый из аспектов и вариантов осуществления, описанных в настоящем документе относительно формулы (I), также применим к соединениям формул (II) или (III).
В некоторых вариантах осуществления, изобретение относится к соединениям формулы (I), (II) или (III) или их фармацевтически приемлемым солям, где:
R1 представляет собой -L1-(5-10-членный гетероарил), необязательно замещенный одним или двумя R4;
R2 и R3 независимо представляют собой H, C1-C6 алкил, -L2-(C3-C7 циклоалкил), где указанный C3-C7 циклоалкил необязательно замещен одним R6;
каждый L1 и L2 независимо представляет собой связь или метилен;
каждый R4 независимо представляет собой F, Cl, OH, CN, NR10R11, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси, C3-C8 циклоалкил, C(O)NR10R11, SO2R12, SO(=NH)R12 или SO2NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним R13;
каждый R6 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси C1-C4 фторалкокси или NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним R13;
каждый R10 и R11 независимо представляет собой H или C1-C4 алкил;
каждый R12 представляет собой C1-C4 алкил или C3-C6 циклоалкил; и
каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15.
В других вариантах осуществления, изобретение относится к соединениям формулы (I), (II) или (III) или их фармацевтически приемлемым солям, где:
R1 представляет собой -L1-(5-10-членный гетероарил), необязательно замещенный одним или двумя R4;
R2 и R3 независимо представляют собой H, C1-C6 алкил или C3-C7 циклоалкил, необязательно замещенный одним C1-C4 алкилом;
L1 независимо представляет собой связь или метилен; и
каждый R4 независимо представляет собой C1-C4 алкил, необязательно замещенный OH или C1-C4 алкокси.
В дополнительных вариантах осуществления изобретение относится к соединениям формулы (I), (II) или (III) или их фармацевтически приемлемым солям, имеющим два или более из следующих признаков:
R1 представляет собой -L1-(5-10-членный гетероарил), где указанный 5-10-членный гетероарил необязательно замещен одним или несколькими R4;
R2 и R3 независимо представляют собой H или C1-C6 алкил;
L1 представляет собой связь или C1-C2 алкилен;
каждый R4 независимо представляет собой C1-C4 алкил, где каждый C1-C4 алкил необязательно замещен одним или несколькими R13;
каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15; и
каждый R14 и R15 независимо представляет собой H или C1-C4 алкил.
В некоторых таких вариантах осуществления изобретение относится к соединениям формулы (I), (II) или (III) или их фармацевтически приемлемым солям, имеющим два или более из следующих признаков:
R1 представляет собой -L1-(5-10-членный гетероарил), необязательно замещенный одним или несколькими R4, где указанный 5-10-членный гетероарил представляет собой пиразолил;
R2 представляет собой H;
R3 представляет собой C1-C6 алкил, предпочтительно C1-C4 алкил;
L1 представляет собой связь;
каждый R4 независимо представляет собой C1-C4 алкил, где каждый C1-C4 алкил необязательно замещен одним или несколькими R13;
каждый R13 независимо представляет собой OH, OCH3 или NR14R15; и
каждый R14 и R15 независимо представляет собой H или CH3.
В других вариантах осуществления, изобретение относится к соединениям формулы (I), (II) или (III) или их фармацевтически приемлемым солям, имеющим два или более из следующих признаков:
R1 представляет собой -L1-(5-10-членный гетероарил), где указанный 5-10-членный гетероарил необязательно замещен одним или несколькими R4;
R2 и R3 независимо представляют собой H или -L2-(C3-C7 циклоалкил), где указанный C3-C7 циклоалкил необязательно замещен одним или несколькими R6;
L1 представляет собой связь или C1-C2 алкилен;
L2 представляет собой связь или C1-C2 алкилен;
каждый R4 независимо представляет собой C1-C4 алкил, где каждый C1-C4 алкил необязательно замещен одним или несколькими R13;
каждый R6 независимо представляет собой F, OH, или C1-C4 алкил;
каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15; и
каждый R14 и R15 независимо представляет собой H или C1-C4 алкил.
В еще других вариантах осуществления, изобретение относится к соединениям формулы (I), (II) или (III) или их фармацевтически приемлемым солям, имеющим два или более из следующих признаков:
R1 представляет собой -L1-(5-10-членный гетероарил), необязательно замещенный одним или несколькими R4, где указанный 5-10-членный гетероарил представляет собой изоксазолил;
L1 представляет собой C1-C2 алкилен;
R2 представляет собой H;
R3 представляет собой -L2-(C3-C7 циклоалкил), необязательно замещенный одним или несколькими R6;
L2 представляет собой связь;
каждый R4 независимо представляет собой C1-C4 алкил, где каждый C1-C4 алкил необязательно замещен одним или несколькими R13;
каждый R6 независимо представляет собой F, OH, или C1-C4 алкил;
каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15; и
каждый R14 и R15 независимо представляет собой H или C1-C4 алкил.
В другом аспекте изобретение относится к соединению, выбранному из группы, состоящей из соединений, представленных в примерах с 1 по 649 включительно, или его фармацевтически приемлемой соли.
В другом аспекте изобретение относится к соединению, выбранному из группы, состоящей из:
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамата;
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамата;
(1R,3S)-3-(3-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил этилкарбамата;
(1R,3S)-3-(3-{[(1-метил-1H-1,2,3-триазол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамата;
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата;
(1R,3S)-3-(3-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата;
(1R,3S)-3-(3-{[(5-метил-1,2-оксазол-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата;
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (1-метилциклопропил)карбамата;
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамата (Изомер A);
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамата (Изомер B);
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамата;
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилата;
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамата;
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамата;
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата;
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамата;
(1R,3S)-3-{3-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-5-ил}циклопентил трет-бутилкарбамата; и
(1R,3S)-3-(3-{[(5-метил-1,3,4-тиадиазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклобутил)карбамата;
или его фармацевтически приемлемой соли.
В другом аспекте изобретение относится к соединению, выбранному из группы, состоящей из:
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамата; и
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамата;
или его фармацевтически приемлемой соли.
В другом аспекте изобретение предоставляет (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат, или его фармацевтически приемлемую соль.
В другом аспекте изобретение предоставляет (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат в форме свободного основания.
В другом аспекте изобретение предоставляет (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат в виде фармацевтически приемлемой соли.
В некоторых вариантах осуществления, изобретение предоставляет (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат моногидрат (форма 1). В некоторых таких вариантах осуществления, моногидрат (форма 1) характеризуется порошковой рентгеновской дифрактограммой (PXRD) (2θ), содержащей: (a) один, два, три, четыре, пять или более пяти пиков, выбранных из группы, состоящей из пиков в Таблице 1 в °2θ±0,2 °2θ; (b) один, два, три, четыре или пять пиков, выбранные из группы, состоящей из 10,4, 11,7, 12,9, 18,2 и 24,2 в °2θ±0,2 °2θ; (c) любые два пика, выбранные из группы, состоящей из 10,4, 11,7, 12,9, 18,2 и 24,2 в °2θ±,2 °2θ; (d) любые три пика, выбранные из группы, состоящей из 10,4, 11,7, 12,9, 18,2 и 24,2 в °2θ±0,2 °2θ; (e) любые четыре пика, выбранны из группы, состоящей из 10,4, 11,7, 12,9, 18,2 и 24,2 в °2θ±0,2 °2θ; (f) пики при 10,4, 11,7, 12,9, 18,2 и 24,2 в °2θ±0,2 °2θ; (g) пик при 10,4 и один, два, три или четыре пика, выбранные из группы, состоящей из 11,7, 12,9, 18,2 и 24,2 в °2θ±0,2 °2θ; (h) пик при 11,7, и один, два, три или четыре пика, выбранные из группы, состоящей из 10,4, 12,9, 18,2 и 24,2 в °2θ±0,2 °2θ; (i) пик при 12,9, и один, два, три или четыре пика, выбранные из группы, состоящей из 10,4, 11,7, 18,2 и 24,2 в °2θ±0,2 °2θ; (j) пик при 18,2, и один, два, три или четыре пика, выбранные из группы, состоящей из 10,4, 11,7, 12,9 и 24,2 в °2θ±0,2 °2θ; (k) пик при 24,2, и один, два, три или четыре пика, выбранные из группы, состоящей из 10,4, 11,7, 12,9, и 18,2 в °2θ±0,2 °2θ; или (l) пики при значениях 2θ по существу такие же, как показано на фиг. 2.
В другом варианте осуществления изобретение предоставляет (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат, или его фармацевтически приемлемую соль.
В другом варианте осуществления изобретение предоставляет (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат в форме свободного основания.
В другом варианте осуществления изобретение предоставляет (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат в виде фармацевтически приемлемой соли.
В конкретном варианте осуществления изобретение относится к соединению, имеющему структуру:
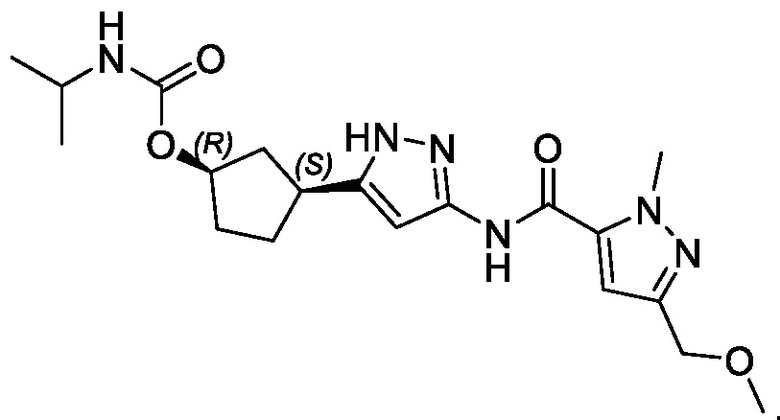 ,
,
или его фармацевтически приемлемой соли.
В другом конкретном варианте осуществления изобретение относится к соединению, имеющему структуру:
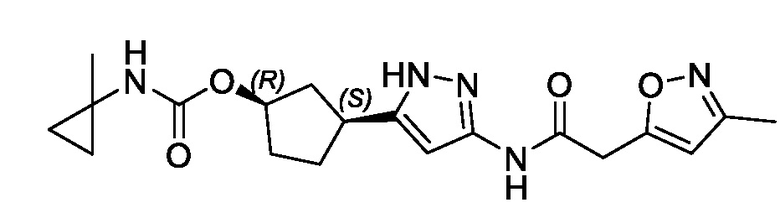 ,
,
или его фармацевтически приемлемой соли.
В предпочтительных вариантах осуществления соединения по изобретению являются селективными ингибиторами CDK2, т.е. они имеют более низкую константу ингибирования (например, Ki или IC50) в отношении CDK2 по сравнению с другими ферментативными мишенями. Новые данные предполагают, что ингибирование GSK3β может быть связано с желудочно-кишечной токсичностью, которая наблюдалась с некоторыми ингибиторами CDK. Соединения, которые являются селективными ингибиторами CDK2 по сравнению с GSK3β, могут обеспечивать улучшенный профиль безопасности, улучшенную схему введения доз (например, за счет уменьшения потребности в снижении дозы или перерывах в дозировании) и/или повышение общей эффективности из-за возможности более высоких доз, использования режима непрерывного введения доз и/или увеличения времени общего лечения. Точно так же селективные ингибиторы CDK2 могут иметь пониженный риск определенных гематологических токсических эффектов, которые, как сообщалось, связаны с ингибированием CDK6.
В некоторых вариантах осуществления, соединения по изобретению являются селективными в отношении CDK2 по сравнению с CDK1. В некоторых таких вариантах осуществления, соединения показали по меньшей мере 10-кратную селективность в отношении CDK2 по сравнению с CDK1. В других вариантах осуществления, соединения показали по меньшей мере 20-кратную селективность в отношении CDK2 по сравнению с CDK1. В конкретных вариантах осуществления, соединения показали по меньшей мере 30-кратную селективность в отношении CDK2 по сравнению с CDK1.
В некоторых вариантах осуществления соединения по изобретению являются селективными в отношении CDK2 по сравнению CDK4 и/или CDK6. В некоторых таких вариантах осуществления соединения показали по меньшей мере 10-кратную селективность в отношении CDK2 по сравнению CDK4 и/или CDK6. В других вариантах осуществления, соединения показали по меньшей мере 20-кратную селективность в отношении CDK2 по сравнению CDK4 и/или CDK6. В конкретных вариантах осуществления, соединения показали по меньшей мере 30-кратную селективность в отношении CDK2 по сравнению CDK4 и/или CDK6.
В некоторых вариантах осуществления, соединения по изобретению являются селективными в отношении CDK2 по сравнению GSK3β. В некоторых таких вариантах осуществления соединения показали по меньшей мере 10-кратную селективность в отношении CDK2 по сравнению с GSK3β. В других вариантах осуществления, соединения показали по меньшей мере 20-кратную селективность в отношении CDK2 по сравнению с GSK3β. В конкретных вариантах осуществления, соединения показали по меньшей мере 30-кратную селективность в отношении CDK2 по сравнению с GSK3β.
"Фармацевтическая композиция" относится к смеси одного или более чем одного соединения по настоящему изобретению, или его фармацевтически приемлемых соли, сольвата, гидрата или пролекарства в качестве активного ингредиента и по меньшей мере одного фармацевтически приемлемого носителя или эксципиента. В некоторых вариантах осуществления, фармацевтическая композиция включает два или несколько фармацевтически приемлемых носителей и/или эксципиентов. В других вариантах осуществления, фармацевтическая композиция дополнительно включает по меньшей мере одно дополнительное противораковое терапевтическое средство.
В одном аспекте изобретение относится к фармацевтической композиции, включающей соединение по изобретению, или его фармацевтически приемлемую соль, и фармацевтически приемлемый носитель или эксципиент. В некоторых вариантах осуществления, фармацевтическая композиция включает два или несколько фармацевтически приемлемых носителей и/или эксципиентов.
В некоторых вариантах осуществления, фармацевтическая композиция дополнительно включат по меньшей мере одно дополнительное противораковое терапевтическое средство. В некоторых таких вариантах осуществления, комбинация обеспечивает аддитивный, более чем аддитивный или синергетический противораковый эффект.
Термин «аддитивный» используется для обозначения того, что результат комбинации двух соединений, компонентов или целевых средств не превышает сумму каждого соединения, компонента или целевого средства по отдельности.
Термин «синергизм» или «синергетический эффект» используется для обозначения того, что результат комбинации двух соединений, компонентов или целевых средств больше, чем сумма каждого соединения, компонента или целевого агента по отдельности. Это улучшение заболевания, состояния или расстройства, которое лечат, является «синергетическим» эффектом. «Синергетическое количество» представляет собой количество комбинации двух соединений, компонентов или целевых средств, которое приводит к синергетическому эффекту, как в настоящем документе определено «синергетический».
Определение синергетического взаимодействия между одним или двумя компонентами, оптимальный диапазон для эффекта и диапазоны абсолютных доз каждого компонента для эффекта могут быть окончательно измерены путем введения компонентов в различных диапазонах доз и/или соотношениях доз пациентам, нуждающимся в лечении. Однако наблюдение синергизма на моделях in vitro или на моделях in vivo может быть предиктором эффекта у людей и других видов, и существуют модели in vitro или модели in vivo, как описано в настоящем документе, для определения синергетического эффекта. Результаты таких исследований также могут быть использованы для прогнозирования диапазонов эффективных доз и соотношений концентраций в плазме, а также абсолютных доз и концентраций в плазме, необходимых для людей и других видов животных, например, путем применения фармакокинетических и/или фармакодинамических методов.
Если не указано иное, все ссылки в настоящем документе на соединения по изобретению включают ссылки на их соли, сольваты, гидраты и комплексы, а также на их сольваты, гидраты и комплексы солей, включая полиморфы, стереоизомеры и их меченые изотопами версии.
Соединения по изобретению могут существовать в форме фармацевтически приемлемых солей, таких как, например, кислотно-аддитивные соли и основно-аддитивные соли соединений одной из формул, представленных в данном документе. Используемый в настоящем документе термин «фармацевтически приемлемая соль» относится к тем солям, которые сохраняют биологическую эффективность и свойства исходного соединения. Фраза «фармацевтически приемлемая(ые) соль(и)», используемая в настоящем описании, если не указано иное, включает соли кислотных или основных групп, которые могут присутствовать в соединениях формул, раскрытых в настоящем документе.
Например, соединения по изобретению, которые являются основными по своей природе, способны к образованию большого множества солей с различными неорганическими и органическими кислотами. Несмотря на то что такие соли должны быть фармацевтически приемлемыми для введения животным, часто на практике желательно сначала выделить соединение по настоящему изобретению из реакционной смеси в виде фармацевтически неприемлемой соли, а затем легко превратить последнюю обратно в соединение в виде свободного основания путем обработки щелочным реагентом, а впоследствии превратить это свободное основание в фармацевтически приемлемую соль присоединения кислоты. Кислотно-аддитивные соли основных соединений по этому изобретению могут быть получены путем обработки основного соединения по существу эквивалентным количеством выбранной неорганической или органической кислоты в водной среде-растворителе или в подходящем органическом растворителе, таком как метанол или этанол. После выпаривания растворителя получают желаемую твердую соль. Желаемую соль кислоты также можно осадить из раствора свободного основания в органическом растворителе путем добавления к раствору подходящей неорганической или органической кислоты.
Кислотами, которые могут быть использованы для получения фармацевтически приемлемых кислотно-аддитивных солей таких основных соединений, которые образуют нетоксичные кислотно-аддитивные соли, т.е. соли, содержащие фармакологически приемлемые анионы, такие как соли, представляющие собой гидрохлорид, гидробромид, гидройодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, ацетат, лактат, салицилат, цитрат, кислый цитрат, тартрат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкуронат, сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат и 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)] (т.е. памоат).
Примеры солей включают, но не ограничиваются ими, соли, представляющие собой ацетат, акрилат, бензолсульфонат, бензоат (такой как хлорбензоат, метилбензоат, динитробензоат, гидроксибензоат и метоксибензоат), бикарбонат, бисульфат, бисульфит, битартрат, борат, бромид, бутин-1,4-диоат, эдетат кальция, камсилат, карбонат, хлорид, капроат, каприлат, клавуланат, цитрат, деканоат, дигидрохлорид, дигидрогенфосфат, эдетат, эдизилат, эстолат, эзилат, этилсукцинат, формиат, фумарат, глюцептат, глюконат, глутамат, гликоллат, гликоллиларсанилат, гептаноат, гексин-1,6-диоат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, γ-гидроксибутират, йодид, изобутират, изотионат, лактат, лактобионат, лаурат, малат, малеат, малонат, манделят, мезилат, метафосфат, метан-сульфонат, метилсульфат, моногидрофосфат, мукат, напзилат, нафталин-1-сульфонат, нафталин-2-сульфонат, нитрат, олеат, оксалат, памоат (эмбонат), пальмитат, пантотенат, фенилацетаты, фенилбутират, фенилпропионат, фталат, фосфат/дифосфат, полигалактуронат, пропансульфонат, пропионат, пропиолат, пирофосфат, пиросульфат, салицилат, стеарат, субацетат, суберат, сукцинат, сульфат, сульфонат, сульфит, таннат, тартрат, теоклат, тозилат, триэтйодид и валерат.
Иллюстративные примеры подходящих солей включают органические соли, полученные из аминокислот, таких как глицин и аргинин, аммиака, первичных, вторичных и третичных аминов и циклических аминов, таких как пиперидин, морфолин и пиперазин, и неорганические соли, полученные из натрия, кальция, калия, магния, марганца, железа, меди, цинка, алюминия и лития.
Соединения по изобретению, которые включают основную группу, такую как аминогруппа, могут образовывать фармацевтически приемлемые соли с различными аминокислотами, помимо упомянутых выше кислот.
Альтернативно, полезные соединения, которые являются кислотными по своей природе, способны к образованию солей присоединения основания с различными фармакологически приемлемыми катионами. Примеры таких солей включают соли щелочных металлов или щелочно-земельных металлов, в частности, соли натрия и калия. Все эти соли получают по традиционным методикам. Химическими основаниями, которые используют в качестве реагентов для получения фармацевтически приемлемых солей присоединения основания по настоящему изобретению, являются основания, которые образуют нетоксичные соли основания с кислотными соединениями, описанными в настоящем документе. Эти соли могут быть получены любым подходящим способом, например, путем обработки свободной кислоты неорганическим или органическим основанием, таким как амин (первичный, вторичный или третичный), гидроксид щелочного металла или гидроксид щелочноземельного металла, или т.п. Эти соли также могут быть получены путем обработки соответствующих кислотных соединений водным раствором, содержащим желаемые фармакологически приемлемые катионы, а затем упаривания полученного раствора досуха, предпочтительно при пониженном давлении. Альтернативно, они также могут быть получены путем смешивания вместе растворов кислотных соединений в низших спиртах и желаемого алкоксида щелочного металла, а затем упаривания полученного раствора досуха таким же способом, как описано раньше. В любом случае для обеспечения полноты реакции и максимальных выходов целевого конечного продукта предпочтительно используют стехиометрические количества реагентов.
Химическими основаниями, которые могут быть использованы в качестве реагентов для получения фармацевтически приемлемых солей присоединения основания к соединениям по изобретению, являющимся кислотными по своей природе, являются такие, которые образуют нетоксичные соли присоединения основания с такими соединениями. Такие нетоксичные основные соли включают, но не ограничиваются ими, соли, полученные из таких фармакологически приемлемых катионов, таких как катионы щелочных металлов (например, калия и натрия) и катионы щелочно-земельных металлов (например, кальция и магния), соли аммония или водорастворимые соли присоединения амина, такого как N-метилглюкамин-(меглумин), и низшего алканоламмония и другие основные соли фармацевтически приемлемых органических аминов.
Также могут быть образованы гемисоли кислот и оснований, например, гемисульфат и гемикальциевые соли.
Для обзора подходящих солей, см. Handbook of Pharmaceutical Salts: Properties, Selection, and Use by Stahl and Wermuth (Wiley-VCH, 2002). Способы получения фармацевтически приемлемых солей соединений по изобретению и форм взаимопревращения солей и свободных оснований известны специалисту в данной области.
Соли по настоящему изобретению могут быть получены способами, известными специалистам в данной области техники. Фармацевтически приемлемая соль соединений по изобретению может быть легко получена путем смешивания вместе растворов соединения и желаемой кислоты или желаемого основания, в зависимости от конкретного случая. Соль может выпадать в осадок из раствора и ее можно собрать фильтрованием или можно извлечь путем выпаривания растворителя. Степень ионизации в соли может варьироваться от полностью ионизированной до почти неионизированной.
Специалистам в данной области техники будет понятно, что соединения по изобретению в форме свободного основания, имеющие основную функциональную группу, могут быть превращены в соли присоединения кислоты путем обработки стехиометрическим избытком подходящей кислоты. Кислотно-аддитивные соли соединений по изобретению могут быть преобразованы в соответствующее свободное основание путем обработки стехиометрическим избытком подходящего основания, такого как карбонат калия или гидроксид натрия, обычно в присутствии водного растворителя и при температуре между примерно 0° и 100°С. Форму свободного основания можно выделить традиционными способами, такими как экстракция органическим растворителем. Кроме того, кислотно-аддитивные соли соединений по настоящему изобретению можно подвергать взаимному обмену, используя преимущества, заключающиеся в разности растворимостей солей, летучестей или кислотностей кислот, или путем обработки подходящим образом нагруженной ионообменной смолой. Например, взаимный обмен можно осуществить путем взаимодействия соли соединений по изобретению со слегка стехиометрическим избытком кислоты при более низком рК, чем у кислотного компонента исходной соли. Это превращение обычно проводят при температуре от примерно 0°С до точки кипения растворителя, используемого в качестве среды для осуществления процедуры. Аналогичного типа замены возможны для солей присоединения основания, обычно путем посредничества формы свободного основания.
Соединения по изобретению могут существовать как в несольватированной, так и в сольватированной формах. Если растворитель или вода связаны крепко, то комплекс будет иметь вполне определенную стехиометрию независимо от влажности. Однако, если растворитель или вода связаны слабо, как в канальных сольватах и гигроскопичных соединениях, то содержание воды/растворителя будет зависеть от влажности и условий сушки. В таких случаях нестехиометрия будет нормой. Термин "сольват" используют в настоящем описании для описания молекулярного комплекса, включающего соединение по изобретению и одну или более чем одну молекулу фармацевтически приемлемого растворителя, например, этанола. Термин "гидрат" используют в тех случаях, когда растворителем является вода. Фармацевтически приемлемые сольваты по этому изобретению включают гидраты и сольваты, в которых растворитель кристаллизации может быть изотопно-замещенным, например, D2O, d6-ацетон, d6-DMSO.
Также включены в объем изобретения такие комплексы, как клатраты, комплексы включения лекарственное средство-хозяин, где в отличие от вышеупомянутых сольватов, лекарственное средство и хозяин присутствуют в стехиометрических или нестехиометрических количествах. Также включены комплексы лекарственного средства, включающие два или более чем два органических и/или неорганических компонента, которые могут быть в стехиометрических или нестехиометрических количествах. Полученные комплексы могут быть ионизированными, частично ионизированными или неионизированными. Обзор таких комплексов см. J Pharm Sci, 64 (8), 1269-1288 by Haleblian (August 1975), описание которого полностью включено в настоящее описание в качестве ссылки.
Изобретение также относится к пролекарствам соединений формул, предложенных в настоящем изобретении. Таким образом, некоторые производные соединений по изобретению, которые сами могут иметь небольшую фармакологическую активность или не иметь ее, могут при введении пациенту, превращаться в соединения по изобретению, например, путем гидролитического расщепления. Такие производные называют "пролекарствами". Дополнительную информацию, касающуюся применения пролекарств, можно обнаружить в 'Pro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T Higuchi and W Stella) and 'Bioreversible Carriers in Drug Design', Pergamon Press, 1987 (ed. E B Roche, American Pharmaceutical Association), раскрытия которых включены в настоящий документ в качестве ссылки во всей своей полноте.
Пролекарства по изобретению могут, например, быть получены путем замены подходящих функциональных групп, присутствующих в соединениях по изобретению, некоторыми группировками, которые известны специалистам в области техники в качестве "прогруппировок", как описано, например, в "Design of Prodrugs" by H Bundgaard (Elsevier, 1985), описание которого включено в настоящее описание путем ссылки во всей своей полноте.
Некоторые неограничивающие примеры пролекарств по изобретению включают:
(i) где соединение содержит функциональную группу карбоновой кислоты (-COOH), ее сложный эфир, например, с заменой водорода (C1-C8)алкилом;
(ii) где соединение содержит спиртовую функциональную группу (-ОН), его простой эфир, например, с заменой водорода (C1-C6)алканоилоксиметилом или группой фосфатного эфира; и
(iii) если соединение содержит первичную или вторичную функциональную аминогруппу (-NH2 или -NHR, R≠H), то его амид, например, с заменой одного или обоих атомов водорода подходящей метаболически неустойчивой группой, такой как амидная, карбаматная, мочевинная, фосфонатная, сульфонатная и т.д.
Дополнительные примеры замещающих групп в соответствии с приведенными выше примерами и примеры других типов пролекарств можно найти в вышеупомянутых ссылках. Наконец, некоторые соединения по изобретению могут сами действовать как пролекарства других соединений по изобретению.
В объем изобретения также включены метаболиты соединений формул, описанных в настоящем документе, то есть соединения, образованные in vivo после введения лекарственного средства.
В дополнение к син-взаимосвязи между группами заместителей в положениях 1 и 3 циклопентильного кольца в формулах (I), (II) и (III), соединения формул, представленных в данном документе, могут иметь дополнительные асимметричные атомы углерода, как часть групп заместителей, определенных как R1, R2 и R3, или необязательных заместителей, присоединенных к этим группам. В таких дополнительных асимметричных центрах сплошная линия используется для обозначения того, что включены все возможные стереоизомеры при таком атоме углерода, в то время как использовани сплошной или штриховой клиновидной линии указывает, что только указанный изомер предназначен для включения в такой стереоцентр, если не указано иное. Соединения приведенных в настоящем описании формул могут включать группы заместителей, содержащие цис- и транс-геометрические изомеры, поворотные изомеры, атропоизомеры, конформационные изомеры и таутомеры соединений по настоящему изобретению, включая соединения, проявляющие более одного типа изомерии.
Также включены соли присоединения кислоты или присоединения основания, где противоион является оптически активным, например, d-лактат или l-лизин, или рацемическим, например, dl-тартрат или dl-аргинин.
Если какой-либо рацемат кристаллизуется, то возможны кристаллы двух разных типов. Первым типом является вышеуказанное рацемическое соединение (истинный рацемат), где получена одна гомогенная форма кристалла, содержащая оба энантиомера в эквимолярных количествах. Вторым типом является рацемическая смесь или конгломерат, где получены две формы кристалла в эквимолярных количествах, каждая из которых содержит одиночный энантиомер.
Соединения по изобретению могут демонстрировать таутомерные эффекты и обладать структурной изомерией. Например, соединения могут существовать в нескольких таутомерных формах, включая енольную и иминную форму, и кето и енаминную форму, и геометрических изомерах и их смесях. Все такие таутомерные формы включены в объем, охватываемый соединениями по изобретению. Таутомеры существуют в виде смесей группы таутомеров в растворе. В твердой форме обычно преобладает один таутомер. Даже если один таутомер может быть описан, настоящее изобретение включает все таутомеры соединений приведенных формул.
Кроме того, некоторые соединения по изобретению могут образовывать атропизомеры (например, замещенные биарилы). Атропизомеры представляют собой конформационные стереоизомеры, которые встречаются, когда не допускается вращение вокруг одинарной связи в молекуле, или оно сильно замедлено в результате стерических взаимодействий с другими частями молекулы и заместители на обоих концах этой одинарной связи являются несимметричными. Взаимное превращение атропизомеров является достаточно слабым, чтобы предоставить возможность для разделения и выделения в заданных условиях. Энергетический барьер термической рацемизации может быть определен по стерическому затруднению в отношении свободного вращения одной или более связей, образующих хиральную ось.
Если соединение по изобретению содержит алкенильную или алкениленовую группу, то возможны геометрические цис/транс (или Z/E) изомеры. Цис/транс-изомеры могут быть разделены посредством традиционных методик, хорошо известных специалистам в данной области техники, например, хроматографией и фракционной кристаллизацией.
Традиционные методики получения/выделения индивидуальных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или расщепление рацемата (или рацемата соли или производного) с использованием, например, хиральной жидкостной хроматографии высокого давления (ВЭЖХ) или сверхкритической флюидной хроматографии (SFC).
Альтернативно, рацемат (или предшественник рацемата) может быть подвергнут взаимодействию с подходящим оптически активным соединением, например, спиртом, или в случае, когда соединение содержит кислотную или основную группу, с кислотой или основанием, такими как винная кислота или 1-фенилэтиламин. Полученная диастереомерная смесь может быть разделена хроматографией и/или фракционной кристаллизацией, и один или оба диастереоизомера могут быть превращены в соответствующий(е) чистый(е) энантиомер(ы) методами, хорошо известными специалисту в области техники.
Хиральные соединения по изобретению (и их хиральные предшественники) могут быть получены в энантиомерно-обогащенной форме с использованием хроматографии, обычно ВЭЖХ, на асимметричной смоле с подвижной фазой, состоящей из углеводорода, обычно гептана или гексана, содержащего от 0 до 50% изопропанола, обычно от 2 до 20%, и от 0 до 5% алкиламина, обычно 0,1% диэтиламина. Концентрирование элюата приводит к обогащенной смеси.
Стереоизомерные конгломераты могут быть разделены посредством традиционных методик, известным специалистам в области техники; см., например, “Stereochemistry of Organic Compounds” by E L Eliel (Wiley, New York, 1994), описание которого включено в настоящее описание путем ссылки во всей своей полноте.
Энантиомерная чистота соединений, описанных в настоящем документе, может быть описана в терминах энантиомерного избытка (ее), который указывает степень, в которой образец содержит один энантиомер в больших количествах, чем другой. Рацемическая смесь имеет ее 0%, в то время как один полностью чистый энантиомер имеет ее 100%. Аналогично, диастереомерная чистота может быть описана в терминах диастереомерного избытка (de). Используемые в настоящем описании термины «энантиомерно чистый» или «по существу энантиомерно чистый» означают соединение, которое включает один энантиомер соединения и по существу не содержит противоположного энантиомера соединения. Типичное энантиомерно чистое соединение включает более примерно 95% по массе одного энантиомера соединения и менее примерно 5% по массе противоположного энантиомера соединения, предпочтительно более примерно 97% по массе одного энантиомера соединения и менее примерно 3% по массе противоположного энантиомера соединения, более предпочтительно более примерно 98% по массе одного энантиомера соединения и менее примерно 2% по массе противоположного энантиомера соединения, и даже более предпочтительно более примерно 99% по массе одного энантиомера соединения и менее примерно 1% по массе противоположного энантиомера соединения.
Настоящее изобретение также включает меченные изотопом соединения, которые идентичны соединениям, изложенным в одной из предложенных формул, за исключением того, что один или несколько атомов заменены атомом, имеющим атомную массу или массовое число, отличающиеся от атомной массы или массового числа, обычно встречающихся в природе.
Меченные изотопом соединения по изобретению обычно могут быть получены традиционными методиками, известными специалистам в данной области техники, или способами, аналогичными способам, раскрытым в настоящем описании, с использованием подходящего меченного изотопом реагента вместо реагента, не меченного изотопом, используемого в других случаях.
Примеры изотопов, которые могут быть включены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как, но не ограничиваются ими, 2H, 3H, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F и 36Cl. Некоторые меченные изотопом соединения по изобретению, например, такие, в которые включены такие радиоактивные изотопы, такие 3H и 14C, являются полезными в анализах распределения лекарственного средства и/или субстрата в ткани. Тритированные, то есть 3Н и углерод-14, то есть 14С, изотопы являются особенно предпочтительными вследствие легкости их получения и обнаружения. Кроме того, замещение более тяжелыми изотопами, такими как дейтерии, т.е. 2H, может предоставить некоторые терапевтические преимущества, получаемые вследствие более высокой метаболической стабильности, например, повышенный период полураспада in vivo или пониженные требования к дозировкам, и, следовательно, могут быть предпочтительными в некоторых случаях. Меченные изотопом соединения по изобретению в основном могут быть получены посредством осуществления процедур, раскрытых на схемах и/или в примерах и получениях ниже, путем замены реагента, не меченного изотопом, на меченный изотопом реагент.
Соединения по изобретению, предназначенные для фармацевтического применения, можно вводить в виде кристаллических или аморфных продуктов или их смесей. Они могут быть получены, например, в виде твердых прессованных масс, порошков или пленок такими способами, как осаждение, кристаллизация, лиофильная сушка, сушка распылением или сушка выпариванием. Микроволновая или радиочастотная сушка могут быть использованы для этой цели.
Терапевтические способы и применения
Изобретение также предоставляет терапевтические способы и применения, включающие введение соединений по изобретению или их фармацевтически приемлемых солей, отдельно или в комбинации с другими терапевтическими средствами или паллиативными средствами.
В одном аспекте изобретение относится к способу лечения аномального клеточного роста у субъекта, нуждающегося в этом, включающему введение субъекту терапевтически эффективного количества соединения по изобретению или его фармацевтически приемлемой соли.
В другом аспекте изобретение относится к способу лечения аномального роста клеток у субъекта, нуждающегося в этом, включающему введение субъекту количества соединения по изобретению или его фармацевтически приемлемой соли в комбинации с количеством дополнительного терапевтического средства (например, противораковое терапевтическое средство), где эти количества совместно являются эффективными при лечении указанного аномального роста клеток.
В другом аспекте изобретение относится к соединению по изобретению или его фармацевтически приемлемой соли для применения при лечении аномального роста клеток у субъекта.
В дополнительном аспекте изобретение относится к применению соединения по изобретению или его фармацевтически приемлемой соли для лечения аномального роста клеток у субъекта.
В другом аспекте изобретение относится к фармацевтической композиции для применения при лечении аномального роста клеток у субъекта, нуждающегося в этом, причем фармацевтическая композиция включает соединение по изобретению или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или эксципиент.
В другом аспекте изобретение относится к соединению по изобретению или его фармацевтически приемлемой соли для применения в качестве лекарственного средства, в частности, лекарственного средства для лечения аномального роста клеток.
В еще одном аспекте изобретение относится к применению соединения по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для лечения аномального роста клеток у субъекта.
В частых вариантах осуществления способов, представленных в настоящем документе, аномальный рост клеток представляет собой рак. Соединения по настоящему изобретению можно вводить как отдельные средства или можно вводить в комбинации с другими противораковыми терапевтическими средствами, в частности, стандартными средствами для лечения, подходящими для конкретного типа рака.
В некоторых вариантах осуществления, представленные методы приводят к одному или нескольким из следующих эффектов: (1) ингибирование пролиферации раковых клеток; (2) подавление инвазивности раковых клеток; (3) индукция апоптоза раковых клеток; (4) ингибирование метастазирования раковых клеток; или (5) ингибирование ангиогенеза.
В другом аспекте изобретение относится к способу лечения расстройства, опосредованного CDK2, у субъекта, включающему введение субъекту соединения по изобретению или его фармацевтически приемлемой соли в количестве, которое эффективно для лечения указанного расстройства, в частности, рака.
В определенных аспектах и вариантах осуществления соединений, композиций, способов и применений, описанных в настоящем документе, соединения по настоящему изобретению являются селективными в отношении CDK2 по сравнению с другими CDK, в частности CDK1. В некоторых вариантах осуществления, соединения по изобретению являются селективными в отношении CDK2 по сравнению с CDK4 и/или CDK6. В других аспектах и вариантах осуществления соединения по изобретению являются селективными в отношении CDK2 по сравнению с гликоген-синтаза-киназа-3 бета (GSK3β). Соединения по изобретению включают соединения любой из формул, описанных в настоящем документе, или их фармацевтически приемлемые соли.
В другом аспекте изобретение относится к способу ингибирования пролиферации раковых клеток у субъекта, включающему введение субъекту соединения по изобретению или его фармацевтически приемлемой соли в количестве, эффективном для ингибирования пролиферации клеток.
В другом аспекте изобретение относится к способу ингибирования инвазивности раковых клеток у субъекта, включающему введение субъекту соединения по изобретению или его фармацевтически приемлемой соли в количестве, эффективном для ингибирования инвазивности клеток.
В другом аспекте изобретение относится к способу индукции апоптоза в раковых клетках у субъекта, включающему введение субъекту соединения по изобретению или его фармацевтически приемлемой соли в количестве, эффективном для индукции апоптоза.
В другом аспекте изобретение относится к способу ингибирования метастазирования раковых клеток у субъекта, включающему введение субъекту соединения по изобретению или его фармацевтически приемлемой соли в количестве, эффективном для ингибирования метастазирования клеток.
В другом аспекте изобретение относится к способу ингибирования ангиогенеза у субъекта, включающему введение субъекту соединения по изобретению или его фармацевтически приемлемой соли в количестве, эффективном для ингибирования ангиогенеза.
В частых вариантах осуществления способов, представленных в настоящем документе, аномальный рост клеток представляет собой рак. В некоторых таких вариантах осуществления, рак выбран из рака молочной железы, рака яичников, рака мочевого пузыря, рака матки, рака простаты, рака легкого (включая NSCLC, SCLC, плоскоклеточный рак или аденокарциному), рака пищевода, рака головы и шеи, колоректального рака, рака почки (включая RCC), рака печени (включая HCC), рака поджелудочной железы, рака желудка (то есть желудочно-кишечного тракта) и рака щитовидной железы. В других вариантах осуществления способов, представленных в настоящем документе, рак представляет собой рак молочной железы, рак яичников, рак мочевого пузыря, рак матки, рак простаты, рак легкого, рак пищевода, рак печени, рак поджелудочной железы или рак желудка.
В других вариантах осуществления, рак представляет собой рак молочной железы, включая, например, ER-положительный/HR-положительный, HER2-отрицательный рак молочной железы; ER-положительный/HR-положительный, HER2-положительный рак молочной железы; тройной негативный рак молочной железы (TNBC); или воспалительный рак молочной железы. В некоторых вариантах осуществления, рак молочной железы представляет собой эндокринно-резистентный рак молочной железы, резистентный к трастузумабу рак молочной железы или рак молочной железы, демонстрирующий первичную или приобретенную резистентность к ингибированию CDK4/CDK6. В некоторых вариантах осуществления, рак молочной железы представляет собой запущенный или метастатический рак молочной железы. В некоторых вариантах осуществления каждого из вышеперечисленных, рак молочной железы характеризуется амплификацией или сверхэкспрессией CCNE1 и/или CCNE2.
В некоторых вариантах осуществления способов, представленных в настоящем документе, аномальный рост клеток представляет собой рак, характеризующийся амплификацией или сверхэкспрессией CCNE1 и/или CCNE2. В некоторых вариантах осуществления способов, представленных в настоящем документе, у субъекта идентифицирован рак, характеризующийся амплификацией или сверхэкспрессией CCNE1 и/или CCNE2.
В некоторых вариантах осуществления, рак выбран из группы, состоящей из рака молочной железы и рака яичников. В некоторых таких вариантах осуществления, рак представляет собой рак молочной железы или рак яичников, характеризующийся амплификацией или сверхэкспрессией CCNE1 и/или CCNE2. В некоторых таких вариантах осуществления, рак представляет собой (a) рак молочной железы или рак яичников; (b) характеризуется амплификацией или сверхэкспрессией циклина E1 (CCNE1) или циклина E2 (CCNE2); или (c) оба (a) и (b). В некоторых вариантах осуществления, рак представляет собой рак яичников.
В некоторых вариантах осуществления, соединение по изобретению вводят в качестве терапии первой линии. В других вариантах осуществления, соединение по изобретению вводят в качестве терапии второй (или более поздней) линии. В некоторых вариантах осуществления, соединение по изобретению вводят в качестве терапии второй (или более поздней) линии после лечения гормональным терапевтическим средством и/или ингибитором CDK4/CDK6. В некоторых вариантах осуществления, соединение по изобретению вводят в качестве терапии второй (или более поздней) линии после лечения гормональным терапевтическим средством, например, ингибитором ароматазы, SERM или SERD. В некоторых вариантах осуществления, соединение по изобретению вводят в качестве терапии второй (или более поздней) линии после лечения ингибитором CDK4/CDK6. В некоторых вариантах осуществления, соединение по изобретению вводят в качестве терапии второй (или более поздней) линии после лечения одним или несколькими химиотерапевтическими режимами лечения, например, включая средства на основе таксана или платины. В некоторых вариантах осуществления, соединение по изобретению вводят в качестве терапии второй (или более поздней) линии после лечения средствами, нацеленными на HER2, например, трастузумабом.
Используемый в настоящем описании термин «эффективная доза» или «эффективное количество» лекарственного средства, соединения или фармацевтической композиции представляет собой количество, достаточное для воздействия на любой один или несколько полезных или желательных, включая биохимических, гистологических и/или поведенческих симптомов, заболевания, его осложнений и промежуточных патологических фенотипов, возникающих во время развития заболевания. Для терапевтического использования «терапевтически эффективное количество» относится к такому количеству вводимого соединения, которое будет ослаблять в некоторой степени один или несколько симптомов заболевания, которое лечат. При ссылке на лечение рака, терапевтически эффективное количество относится к такому количеству, которое обладает эффектом (1) уменьшения размера опухоли, (2) ингибирования (т.е. замедления в некоторой степени, предпочтительно останавку) метастазирования опухоли, (3) ингибирования в некоторой степени (т.е. замедления в некоторой степени, предпочтительно останавку) роста опухоли или инвазивности опухоли, и/или (4) ослабления в некоторой степени (или, предпочтительно, устранения) одного или нескольких признаков или симптомов, ассоциированных с раком, (5) уменьшения дозы других лекарственных средств, необходимых для лечения заболевания, и/или (6) усиления эффекта другого лекарственного средства, и/ или (7) задержки прогрессирования заболевания у пациента.
Эффективную дозу можно вводить за одно или несколько приемов. Для целей настоящего изобретения эффективная доза лекарственного средства, соединения или фармацевтической композиции представляет собой количество, достаточное для осуществления профилактического или терапевтического лечения прямо или косвенно. Как понимается в клиническом контексте, эффективная доза лекарственного средства, соединения или фармацевтической композиции может быть или не может быть достигнута в сочетании с другим лекарственным средством, соединением или фармацевтической композицией.
«Опухоль» применительно к субъекту, у которого диагностирован или подозревается рак, относится к злокачественному или потенциально злокачественному новообразованию или тканевой массе любого размера и включает первичные опухоли и вторичные новообразования. Солидная опухоль представляет собой аномальный рост или массу ткани, которая обычно не содержит кист или жидких участков. Примерами солидных опухолей являются саркомы, карциномы и лимфомы. Лейкемия (рак крови) обычно не образует солидных опухолей (National Cancer Institute, Dictionary of Cancer Terms).
«Масса опухоли» или «опухолевая нагрузка» относится к общему количеству опухолевого материала, распределенного по всему организму. Под опухолевой нагрузкой понимается общее количество раковых клеток или общий размер опухоли (опухолей) по всему организму, включая лимфатические узлы и костный мозг. Опухолевую нагрузку можно определить с помощью множества способов, известных в данной области, таких как, например, с помощью штангенциркуля, или при нахождении в организме с использованием методов визуализации, например, ультразвука, сканирования костей, компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ).
Термин «размер опухоли» относится к общему размеру опухоли, который можно измерить как длину и ширину опухоли. Размер опухоли может быть определен различными методами, известными в данной области, такими как, например, путем измерения размеров опухоли(ей) при удалении у субъекта, например, с помощью штангенциркуля, или во время нахождения в организме с использованием методов визуализации, например, сканирование костей, ультразвук, CR или МРТ.
Используемый в настоящем описании термин «субъект» относится к субъекту человека или животного. В определенных предпочтительных вариантах осуществления субъектом является человек.
Термин «лечить» или «лечение» рака, используемый в настоящем документе, означает введение соединения по настоящему изобретению субъекту, страдающему раком, или у кого диагностирован рак, для достижения по меньшей мере одного положительного терапевтического эффекта, такого как, например, снижение количество раковых клеток, уменьшение размера опухоли, снижение скорости инфильтрации раковых клеток в периферические органы или снижение скорости метастазов опухоли или роста опухоли, обращение вспять, облегчение, ингибирование прогрессирования или предотвращение расстройства или состояния, к которым применяется этот термин, или один или несколько симптомов такого расстройства или состояния. Термин "лечение", используемый в настоящем описании, если не указано иное, относится к акту процесса лечения как "процесса лечения", как он определен непосредственно выше. Термин "процесс лечения" также включает адъювантное и неоадъювантное лечение субъекта.
Для целей настоящего изобретения полезные или желаемые клинические результаты включают, но не ограничиваются ими, одно или несколько из следующего: уменьшение пролиферации (или разрушение) неопластических или раковых клеток; ингибирование метастазов или неопластических клеток; уменьшение или замедление размера опухоли; ремиссия рака; уменьшение симптомов, вызванных раком; повышение качества жизни больных раком; уменьшение дозы других лекарственных средств, необходимых для лечения рака; задержка прогрессирования рака; лечение рака; преодоление одного или нескольких механизмов резистентности рака; и/или продление выживаемости больных раком. Положительный терапевтический эффект при раке можно измерить несколькими путями (см., например, W. A. Weber, Assessing tumor response to therapy, J. Nucl. Med. 50 Suppl. 1:1S-10S (2009). Например, что касается ингибирования роста опухоли (T/C), согласно стандартам Национального института рака (NCI), T/C меньше или равное 42% является минимальным уровнем противоопухолевой активности. T/C<10% считается высоким уровнем противоопухолевой активности, где T/C (%) = средний объем опухоли, подвергнутой лечению/ средний объем опухоли в контроле x 100.
В некоторых вариантах осуществления, лечение, достигаемое соединением по изобретению, определяется ссылкой на любое из следующего: частичный ответ (PR), полный ответ (CR), общий ответ (OR), выживаемость без прогрессирования (PFS), выживаемость без признаков заболевания (DFS) и общая выживаемость (OS). PFS, также называемое «Время до прогрессирования опухоли», указывает продолжительность времени во время и после лечения, в течение которого рак не растет, и включает количество времени, в течение которого пациенты испытывали CR или PR, а также количество времени, в течение которого пациенты пережили стабилизацию заболевания (SD). DFS относится к промежутку времени во время и после лечения, в течение которого пациент остается свободным от заболевания. OS означает увеличение продолжительности жизни по сравнению с наивными субъектами или пациентами, или субъектами или пациентами, не получавшими лечение. В некоторых вариантах осуществления, ответ на комбинацию изобретения представляет собой любой из PR, CR, PFS, DFS, OR или OS, который оценивается с использованием критерией ответа Критерия оценки ответа солидных опухолей на лечение (RECIST) 1.1.
Схема лечения соединением по изобретению, которое эффективно для лечения больного раком, может варьироваться в зависимости от таких факторов, как состояние болезни, возраст и масса пациента, а также способности терапии вызывать противораковый ответ у субъекта. Хотя вариант осуществления любого из аспектов изобретения может быть неэффективным для достижения положительного терапевтического эффекта у каждого субъекта, он должен действовать в отношении статистически значимого числа субъектов, определяемого любым статистическим тестом, известным в данной области, таким как тест Стьюдента, критерий chi2, U-критерий Манна и Уитни, критерий Крускала-Уоллиса (H-критерий), критерий Джонкхиера-Терпстра и критерий Уилкона.
Термины «схема лечения», «протокол введения доз» и «схема введения доз» используются взаимозаменяемо для обозначения дозы и времени введения каждого соединения по изобретению, отдельно или в комбинации с другим терапевтическим средством.
«Улучшение» означает уменьшение или улучшение одного или нескольких симптомов после лечения комбинацией, описанной в настоящем документе, по сравнению с отсутствием введения комбинации. «Улучшение» также включает сокращение или уменьшение продолжительности симптома.
"Аномальный клеточный рост", используемый в настоящем описании, если не указано иное, относится к клеточному росту, который не зависит от нормальных регуляторных механизмов (например, потере контактного ингибирования). Аномальный клеточный рост может быть доброкачественным (нераковым) или злокачественным (раковым).
Аномальный клеточный рост включает аномальный рост: (1) опухолевых клеток (опухолей), которые демонстрируют повышенную экспрессию CDK2; (2) опухолей, которые пролиферируют вследствие аберрантной активации CDK2; (3) опухолей, характеризующихся амплификацией или сверхэкспрессией CCNE1 и/или CCNE2; и 4) опухолей, которые устойчивы к эндокринной терапии, антагонистам HER2 или ингибированию CDK4/6.
Термин «дополнительное противораковое терапевтическое средство» в контексте настоящего описания означает любое одно или несколько терапевтических средств, отличных от соединения по изобретению, которое используется или может быть использовано при лечении рака. В некоторых вариантах осуществления такие дополнительные противоопухолевые терапевтические средства включают соединения, полученные из следующих классов: ингибиторы митоза, алкилирующие средства, антиметаболиты, противоопухолевые антибиотики, средства против ангиогенеза, ингибиторы топоизомеразы I и II, растительные алкалоиды, гормональные средства и антагонисты, ингибиторы факторов роста, радиация, ингибиторы сигнальной трансдукции, такие как ингибиторы протеинтирозинкиназ и/или серин/треонинкиназ, ингибиторы клеточного цикла, модификаторы биологического ответа, ингибиторы ферментов, антисмысловые олигонуклеотиды или производные олигонуклеотидов, цитотоксические и иммуноонкологические средства и тому подобное.
В некоторых вариантах осуществления, дополнительное противораковое средство представляет собой гормональное средство, такое как ингибитор ароматазы, SERD или SERM.
В других вариантах осуществления, соединение по изобретению можно вводить в комбинации со стандартным средством для лечения. В некоторых вариантах осуществления, соединение по изобретению можно вводить в комбинации с гормональной терапией, например, с такими средствами, как летрозол, фулвестрант, тамоксифен, экземестан или анастрозол. В некоторых вариантах осуществления, соединение по изобретению можно вводить в комбинации с химиотерапевтическим средством, например, доцетакселом, паклитакселом, цисплатином, карбоплатином, капецитабином, гемцитабином или винорелбином. В других вариантах осуществления, соединение по изобретению можно вводить в комбинации со средством против HER2, например трастузумабом или пертузумабом.
В некоторых вариантах осуществления, дополнительное противораковое средство представляет собой средство против ангиогенеза, включая, например, ингибиторы VEGF, ингибиторы VEGFR, ингибиторы TIE-2, ингибиторы PDGFR, ингибиторы ангиопоэтина, ингибиторы PKCβ, ингибиторы COX-2 (циклооксигеназы II), интегрины (альфа-v/бета-3), ингибиторы MMP-2 (матриксной металлопротеиназы 2), и ингибиторы MMP-9 (матриксной металлопротеиназы 9). Предпочтительные средства против ангиогенеза включают сунитиниб (Sutent™), бевацизумаб (Avastin™), акситиниб (AG 13736), SU 14813 (Pfizer), и AG 13958 (Pfizer). Дополнительные средства против ангиогенеза включают ваталаниб (CGP 79787), сорафениб (Nexavar™), пегаптаниб октанатрий (Macugen™), вандетаниб (Zactima™), PF-0337210 (Pfizer), SU 14843 (Pfizer), AZD 2171 (AstraZeneca), ранибизумаб (Lucentis™), Neovastat™ (AE 941), тетратиомолибдат (Coprexa™), AMG 706 (Amgen), VEGF Trap (AVE 0005), CEP 7055 (Sanofi-Aventis), XL 880 (Exelixis), телатиниб (BAY 57-9352) и CP-868,596 (Pfizer). Другие средства против ангиогенеза включают энзастаурин (LY 317615), мидостаурин (CGP 41251), перифозин (KRX 0401), тепренон (Selbex™) и UCN 01 (Kyowa Hakko). Другие примеры средств против ангиогенеза включают целекоксиб (Celebrex™), парекоксиб (Dynastat™), деракоксиб (SC 59046), люмиракоксиб (Preige™), валдекоксиб (Bextra™), рофекоксиб (Vioxx™), игуратимод (Careram™), IP 751 (Invedus), SC-58125 (Pharmacia) и эторикоксиб (Arcoxia™). Еще дополнительные средства против ангиогенеза включают экзисулинд (Aptosyn™), салсалат (Amigesic™), дифлунизал (Dolobid™), ибупрофен (Motrin™), кетопрофен (Orudis™), набуметон (Relafen™), пироксикам (Feldene™), напроксен (Aleve™, Naprosyn™), диклофенак (Voltaren™), индометацин (Indocin™), сулиндак (Clinoril™), толметин (Tolectin™), этодолак (Lodine™), кеторолак (Toradol™), и оксапрозин (Daypro™). Еще дополнительные средства против ангиогенеза включают ABT 510 (Abbott), апратастат (TMI 005), AZD 8955 (AstraZeneca), инциклинид (Metastat™), и PCK 3145 (Procyon). Еще дополнительные средства против ангиогенеза включают ацитретин (Neotigason™), плитидепсин (aplidine™), циленгтид (EMD 121974), комбретастатин A4 (CA4P), фенретинид (4 HPR), галофугинон (Tempostatin™), Panzem™ (2-метоксиэстрадиол), PF-03446962 (Pfizer), ребимастат (BMS 275291), катумаксомаб (Removab™), леналидомид (Revlimid™), скваламин (EVIZON™), талидомид (Thalomid™), Ukrain™ (NSC 631570), Vitaxin™ (MEDI 522), и золедроновую кислоту (Zometa™).
В других вариантах осуществления, дополнительное противораковое средство представляет собой так называемый ингибитор сигнальной трансдукции (например, ингибирующий средства, с помощью которых регуляторные молекулы, которые управляют фундаментальными процессами роста, дифференцировки и выживания клеток, передаются внутри клетки). Ингибиторы сигнальной трансдукции включают малые молекулы, антитела и антисмысловые молекулы. Ингибиторы сигнальной трансдукции включают, например, ингибиторы киназы (например, ингибиторы тирозинкиназы или ингибиторы серин/треонинкиназы) и ингибиторы клеточного цикла. Более конкретно ингибиторы сигнальной трансдукции включают, например, ингибиторы фарнезил-протеинтрансферазы, ингибитор EGF, ErbB-1 (EGFR), ErbB-2, pan erb, ингибиторы IGF1R, MEK, ингибиторы c-Kit, ингибиторы FLT-3, ингибиторы K-Ras, ингибиторы киназы PI3, ингибиторы JAK, ингибиторы STAT, ингибиторы киназы Raf, ингибиторы Akt, ингибитор mTOR, ингибиторы киназы P70S6, ингибиторы пути WNT и так называемые многоцелевые ингибиторы киназ. Дополнительные примеры ингибиторов сигнальной трансдукции, которые можно использовать в сочетании с соединением по изобретению и фармацевтическими композициями, описанными в настоящем документе, включают BMS 214662 (Bristol-Myers Squibb), лонафарниб (Sarasar™), пелитрексол (AG 2037), матузумаб (EMD 7200), нимотузумаб (TheraCIM h-R3™), панитумумаб (Vectibix™), вандетаниб (Zactima™), пазопаниб (SB 786034), ALT 110 (Alteris Therapeutics), BIBW 2992 (Boehringer Ingelheim) и Cervene™ (TP 38). Другие примеры ингибиторов сигнальной трансдукции включают гефитиниб (Iressa™), цетуксимаб (Erbitux™), эрлотиниб (Tarceva™), трастузумаб (Herceptin™), сунитиниб (Sutent™), иматиниб (Gleevec™), кризотиниб (Pfizer), лорлатиниб (Pfizer), дакомитиниб (Pfizer), босутиниб (Pfizer), гедатолисиб (Pfizer), канертиниб (CI 1033), пертузумаб (Omnitarg™), лапатиниб (Tycerb™), пелитиниб (EKB 569), милтефозин (Miltefosin™), BMS 599626 (Bristol-Myers Squibb), Lapuleucel-T (Neuvenge™), NeuVax™ (E75 cancer vaccine), Osidem™ (IDM 1), мубритиниб (TAK-165), CP-724,714 (Pfizer), панитумумаб (Vectibix™), ARRY 142886 (Array Biopharm), эверолимус (Certican™), зотаролимус (Endeavor™), темсиролимус (Torisel™), AP 23573 (ARIAD), и VX 680 (Vertex), XL 647 (Exelixis), сорафениб (Nexavar™), LE-AON (Georgetown University), и GI-4000 (Globelmmune). Другие ингибиторы сигнальной трансдукции включают ABT 751 (Abbott), альвоцидиб (флавопиридол), BMS 387032 (Bristol Myers), EM 1421 (Erimos), индисулам (E 7070), селициклиб (CYC 200), BIO 112 (Onc Bio), BMS 387032 (Bristol-Myers Squibb), палбоциклиб (Pfizer), и AG 024322 (Pfizer).
В других вариантах осуществления, дополнительное противораковое средство представляет собой так называемое классическое противоопухолевое средство. Классические противоопухолевые средства включают, но не ограничиваются ими, гормональные модуляторы, такие как гормональные, противогормональные, андрогенные агонисты, андрогенные антагонисты и антиэстрогенные терапевтические средства, ингибиторы гистондеацетилазы (HDAC), ингибиторы ДНК-метилтрансферазы, средства сайленсинга или средства, активирующие гены, рибонуклеазы, протеосомики, ингибиторы топоизомеразы I, производные камптотецина, ингибиторы топоизомеразы II, алкилирующие средства, антиметаболиты, ингибитор поли(АДФ-рибоза) полимераза-1 (PARP-1) (такой как, например, талазопариб, олапарив, рукапариб, нирапариб, инипариб, велипариб), ингибиторы микротубулина, антибиотики, ингибиторы веретена растительного происхождения, соединения, координированные с платиной, генные терапевтические средства, антисмысловые олигонуклеотиды, агенты нацеливания на сосуды (VTA) и статины. Примеры классических противоопухолевых средств, используемых в комбинированной терапии с соединением по изобретению, необязательно с одним или несколькими другими средствами, включают, но не ограничиваются ими, глюкокортикоиды, такие как дексаметазон, преднизон, преднизолон, метилпреднизолон, гидрокортизон и прогестины, такие как медроксипрогестерон, мегестрола ацетат (Megace), мифепристон (RU-486), селективный модулятор рецепторов эстрогена (SERM; такие как тамоксифен, ралоксифен, лазофоксифен, афимоксифен, арзоксифен, базедоксифен, фиспемифен, ормелоксифен, оспемифен, тесмилифен, торемифен, трилостан и CHF 4227 (Cheisi), селективные ингибиторы эстрогеновых рецепторов (SERD; такие как фулвестрант), экземестан (аромазин), анастрозол (аримидекс), атаместан, фадрозол, летрозол (фемара), форместан; агонисты гонадотропин-высвобождающего гормона (GnRH; также обычно называемый гормон, высвобождающий лютеинизирующий гормон [LHRH]), такие как бусерелин (Suprefact), гозерелин (Zoladex), лейпрорелин (Lupron), и трипторелин (Trelstar), абареликс (Plenaxis), ципротерон, флутамид (Eulexin), мегестрол, нилутамид (Nilandron), и осатерон, дутастерид, эпристерид, финастерид, Serenoa repens, PHL 00801, абареликс, гозерелин, лейпрорелин, трипторелин, бикалутамид; антиандрогенные средства, такие как энзалутамид, абиратерона ацетат, бикалутамид (Casodex); и их комбинации. Другие примеры классических противоопухолевых средств, используемых в комбинации с соединением по изобретению, включают, но не ограничиваются ими, субероланилид гидроксамовую кислоту (SAHA, Merck Inc./Aton Pharmaceuticals), депсипептид (FR901228 или FK228), G2M-777, MS-275, пивалоилоксиметилбутират и PXD-101; Onconase (ранпирназа), PS-341 (MLN-341), Velcade (бортезомиб), 9-аминокамптотецин, белотекан, BN-80915 (Roche), camptothecin, дифломотекан, эдотекарин, экзатекан (Daiichi), гиматекан, 10-гидроксикамптотецин, иринотекан HCl (Camptosar), луртотекан, оратецин (рубитекан, Supergen), SN-38, топотекан, камптотецин, 10-гидроксикамптотецин, 9-аминокамптотецин, иринотекан, SN-38, эдотекарин, топотекан, акларубицин, адриамицин, амонафид, амрубицин, аннамицин, даунорубицин, доксорубицин, эльсамитруцин, эпирубицин, этопозид, идарубицин, галарубицин, гидроксикарбамид, неморубицин, новантрон (митоксантрон), пирарубицин, пиксантрон, прокарбазин, ребеккамицин, собузоксан, тафлупозид, валрубицин, Zinecard (дексразоксан), азотистый N-оксид-иприт, циклофосфамид, AMD-473, альтретамин, AP-5280, апазиквон, бросталлицин, бендамустин, бусульфан, карбоквон, кармустин, хлорамбуцил, дакарбазин, эстрамустин, фотемустин, глюфосфамид, ифосфамид, KW-2170, ломустин, мафосфамид, мехлорэтамин, мелфалан, митобронитол, митолактол, митомицин C, митоксатрон, нимустин, ранимустин, темозоломид, тиотепа, и координированные платиной алкилирующие соединения, такие как цисплатин, параплатин (карбоплатин), эптаплатин, лобаплатин, недаплатин, элоксатин (оксалиплатин, Sanofi), стрептозоцин, сатроплатин и их комбинации.
В еще других вариантах осуществления, дополнительным противораковым средством являются так называемые ингибиторы дигидрофолатредуктазы (такие как метотрексат и NeuTrexin (триметрезат глюкуронат)), антагонисты пурина (такие как 6-меркаптопурин рибозид, меркаптопурин, 6-тиогуанин, кладрибин, клофарабин (Clolar), флударабин, неларабин и ралтитрексед), антагонисты пиримидина (такие как 5-фторурацил (5-FU), Alimta (пеметрексед динатрия, LY231514, MTA), капецитабин (Xeloda™), цитозин арабинозид, Gemzar™ (гемцитабин, Eli Lilly), тегафур (UFT Orzel или Uforal и включая TS-1 комбинацию тегафура, гиместата и отостата), доксифлуридин, кармофур, цитарабин (включая окфосфат, стеарат фосфата, с замедленным высвобождением и липосомальные формы), эноцитабин, 5-азацитидин (видаза), децитабин и этинилцитидин) и другие антиметаболиты, такие как эфлорнитин, гидроксимочевина, лейковорин, нолатрексед (Thymitaq), триапин, триметрексат, N-(5-[N-(3,4-дигидро-2-метил-4-оксохиназолин-6-илметил)-N-метиламино]-2-теноил)-L-глутаминовая кислота, AG-014699 (Pfizer Inc.), ABT-472 (Abbott Laboratories), INO-1001 (Inotek Pharmaceuticals), KU-0687 (KuDOS Pharmaceuticals) и GPI 18180 (Guilford Pharm Inc) и их комбинации.
Другие примеры классических противоопухолевых цитотоксических средств включают, но не ограничиваются ими, абраксан (Abraxis BioScience, Inc.), батабулин (Amgen), EPO 906 (Novartis), винфлунин (Bristol-Myers Squibb Company), актиномицин D, блеомицин, митомицин C, неокарзиностатин (зиностатин), винбластин, винкристин, виндезин, винорелбин (навельбин), доцетаксел (таксотер), ортатаксел, паклитаксел (в том числе таксопрексин конъюгат DHA/пакилтаксел), цисплатин, карбоплатин, недаплатин, оксалиплатин (элоксатин), сатраплатин, камптозар, капецитабин (кселода), оксалиплатин (элоксатин), таксотер алитретиноин, канфосфамид (Telcyta™), DMXAA (Antisoma), ибандроновая кислота, L-аспарагиназа, пегаспаргаза (Oncaspar™), эфапроксирал (Efaproxyn™ - лучевая терапия), бексаротен (Targretin™), тесмилифен (DPPE - овышает эффективность цитотоксических средств), Theratope™ (Biomira), третиноин (Vesanoid™), тирапазамин (Trizaone™), мотексафин гадолиний (Xcytrin™) Cotara™ (mAb), и NBI-3001 (Protox Therapeutics), полиглутамат-паклитаксел (Xyotax™) и их комбинации. Дополнительные примеры классических противоопухолевых средств включают, но не ограничиваются ими, как адвексин (ING 201), TNFerade (GeneVec, соединение, которое экспрессирует TNF-альфа в ответ на лучевую терапию), RB94 (Baylor College of Medicine), Genasense (Oblimersen, Genta), комбретастатин A4P (CA4P), Oxi-4503, AVE-8062, ZD-6126, TZT-1027, аторвастатин (Lipitor, Pfizer Inc.), провастатин (Pravachol, Bristol-Myers Squibb), ловастатин (Mevacor, Merck Inc.), симвастатин (Zocor, Merck Inc.), флувастатин (Lescol, Novartis), церивастатин (Baycol, Bayer), розувастатин (Crestor, AstraZeneca), ловостатин, ниацин (Advicor, Kos Pharmaceuticals), Caduet, липитор, торцетрапиб, и их комбинации.
В других вариантах осуществления, дополнительное противораковое средство представляет собой эпигенетический модулятор, например, ингибитор или EZH2, SMARCA4, PBRM1, ARID1A, ARID2, ARID1B, DNMT3A, TET2, MLL1/2/3, NSD1/2, SETD2, BRD4, DOT1L, HKMTsanti, PRMT1-9, LSD1, UTX, IDH1/2 или BCL6.
В дополнительных вариантах осуществления дополнительное противораковое средство представляет собой иммуномодулирующее средство, такое как ингибитор CTLA-4, PD-1 или PD-L1 (например, пембролизумаб, ниволумаб или авелумаб), LAG-3, TIM-3, TIGIT, 4-1BB, OX40, GITR, CD40, или CAR-T-клеточная терапия.
Используемый в настоящем документе термин «рак» относится к любому злокачественному и/или инвазивному росту или опухоли, вызванному аномальным ростом клеток. Рак включает солидные опухоли, названные по типу клеток, которые их образуют, рак крови, костного мозга или лимфатической системы. Примеры солидных опухолей включают саркомы и карциномы. Рак крови включает, но не ограничивается ими, лейкемию, лимфому и миелому. Рак также включает первичный рак, который возникает в определенном месте организма, метастатический рак, который распространился из места, в котором он возник, в другие части организма, рецидив исходного первичного рака после ремиссии и второй первичный рак, который представляет собой новый первичный рак у человека с историей предыдущего рака другого типа, отличного от последнего.
В некоторых вариантах осуществления способов, представленных в настоящем документе, рак представляет собой рак молочной железы, рак яичников, рак мочевого пузыря, рак матки, рак простаты, рак легкого (включая SCLC или NSCLC), рак пищевода, рак печени, рак поджелудочной железы или рак желудка. В некоторых таких вариантах осуществления, рак характеризуется амплификацией или сверхэкспрессией CCNE1 и/или CCNE2.
Лекарственные формы и схемы введения
Введение соединений по изобретению можно осуществить любым способом, который делает возможной доставку соединений к месту действия. Эти способы включают пероральные пути, интрадуоденальные пути, парентеральную инъекцию (включая внутривенную, подкожную, внутримышечную, внутрисосудистую или инфузию), местное и ректальное введение.
Схемы введения доз можно скорректировать для обеспечения оптимального желаемого ответа. Например, можно вводить разовый болюс, можно вводить несколько доз, разделенных по времени, или дозу можно пропорциональным образом уменьшить или увеличить, как предписывает терапевтическая ситуация. Особенно полезно изготавливать парентеральные композиции в стандартной лекарственной форме для легкости введения и единообразия дозы. Стандартная лекарственная форма, как используется в настоящем описании, относится к физически дискретным единицам, пригодным в качестве единичных доз для млекопитающих, которых следует лечить; причем каждая единица содержит предварительно определенное количество активного соединения, рассчитанное для получения желаемого терапевтического эффекта вместе с желаемым фармацевтическим носителем. Подробное определение стандартных лекарственных форм по изобретению продиктовано и непосредственно зависит от (а) уникальных характеристик химиотерапевтического средства и конкретного терапевтического или профилактического эффекта, который следует достичь, и (b) ограничений, присущих в области приготовления лекарственных средств, таких как активное соединение для лечения чувствительности у индивидуумов.
Таким образом, специалисту будет понятно, что дозу и режим дозирования можно корректировать на основе предложенного описания в соответствии со способами, хорошо известными в области терапии. То есть можно легко установить максимально приемлемую дозу, также как и можно определить эффективное количество, обеспечивающее обнаруживаемую терапевтическую пользу для пациента, а также временные требования по введению каждого средства с обеспечением обнаруживаемой терапевтической пользы у пациента. Соответственно, несмотря на то, что в настоящем описании для некоторых доз и схем введения приведены примеры, эти примеры никоим образом не ограничивают дозу и схему введения, которые могут быть предложены пациенту при осуществлении настоящего изобретения на практике.
Следует отметить, что значения доз могут варьироваться в зависимости от типа и тяжести состояния, которое следует облегчить, и могут включать однократные или многократные дозы. Кроме того, следует понимать, что для любого конкретного субъекта конкретные схемы введения доз следует скорректировать в отношении времени в соответствии с индивидуальной потребностью и профессиональным суждением личности, осуществляющей введение и наблюдающей за введением композиций, и что изложенные в настоящем описании диапазоны доз являются только лишь типичными и не предназначены ограничивать объем или практическое использование заявленной композиции. Например, дозы можно скорректировать, исходя из фармакокинетических или фармакодинамических параметров, которые могут включать клинические эффекты, такие как токсические эффекты, и/или лабораторные значения. Таким образом, настоящее изобретение охватывает расширение диапазона доз для пациента, определяемое квалифицированным специалистом. Определение подходящих доз и схем введения химиотерапевтических средств хорошо известно в соответствующей области, и должно быть понятно специалисту в данной области после получения информации, раскрытой в настоящем описании.
Количество вводимого соединения по изобретению будет зависеть от субъекта, подлежащего лечению, тяжести расстройства или состояния, скорости введения, распределения соединения и усмотрения лечащего врача. Однако эффективная доза обычно находится в диапазоне от примерно 0,001 до примерно 100 мг на 1 кг массы тела в сутки, предпочтительно от примерно 1 до примерно 35 мг/кг/сутки, в однократной или разделенных дозах. Для человека с массой 70 кг, это количество могло бы составить от примерно 0,05 до примерно 7 г/сутки, предпочтительно от примерно 0,1 до примерно 2,5 г/сутки. В некоторых случаях уровни доз ниже нижнего предела вышеупомянутого диапазона могут быть более чем достаточными, в то время как в других случаях могут использоваться более большие дозы, не вызывая какого-либо опасного побочного эффекта, при условии, что такие большие дозы сначала делятся на несколько небольших доз для введения в течение суток.
Составы и способы введения
Используемый в настоящем описании "фармацевтически приемлемый носитель" относится к носителю или разбавителю, который не вызывает значительного раздражения организма и не отменяет биологическую активность и свойства вводимого соединения.
Фармацевтически приемлемый носитель может включать любой обычный фармацевтический носитель или эксципиент. Выбор носителя и/или эксципиента будет в большой степени зависеть от таких факторов, как конкретный путь введения, влияние носителя или эксципиента на растворимость и стабильность и природы лекарственной формы.
Подходящие фармацевтические носители включают инертные разбавители или наполнители, воду и различные органические растворители (например, гидраты и сольваты). Фармацевтические композиции могут, если желательно, содержать дополнительные ингредиенты, такие как корригенты, связующие вещества, эксципиенты и т.п. Таким образом, для перорального введения таблетки, содержащие различные эксципиенты, такие как лимонная кислота, можно применять вместе с различными разрыхлителями, такими как крахмал, альгиновая кислота и некоторые комплексные силикаты, и со связующими веществами, такими как сахароза, желатин и аравийская камедь. Примеры, без ограничения, эксципиентов включают карбонат кальция, фосфат кальция, различные сахара и виды крахмала, производные целлюлозы, желатин, растительные масла и полиэтиленгликоли. Кроме того, для целей таблетирования часто полезны смазывающие вещества, такие как стеарат магния, лаурилсульфат натрия и тальк. Твердые композиции подобного типа также можно применять в мягких и твердых наполненных желатиновых капсулах. Таким образом, неограничивающие примеры материалов включают лактозу или молочный сахар и высокомолекулярные полиэтиленгликоли. Когда для перорального введения желательны водные суспензии или эликсиры, активное соединение в них может быть объединено с различными подсластителями или ароматизаторами, красящими веществами или красками и, если желательно, эмульгаторами или суспендирующими средствами, вместе с разбавителями, такими как вода, этанол, пропиленгликоль, глицерин или их комбинации.
Фармацевтическая композиция может, например, находиться в форме, подходящей для перорального введения в виде таблетки, капсулы, пилюли, порошка, препаратов замедленного высвобождения, раствора, суспензии, для парентеральной инъекции в виде стерильного раствора, суспензии или эмульсии, для местного введения в виде мази или крема или для ректального введения в виде суппозитория.
Типичные формы для парентерального введения включают растворы или суспензии активных соединений в стерильных водных растворах, например, в водном пропиленгликолевом или декстрозном растворах. Если требуется, такие лекарственные формы могут быть подходящим образом буферизованы.
Фармацевтическая композиция может находиться в стандартных лекарственных формах, подходящих для однократного введения точных доз.
Фармацевтические композиции, подходящие для доставки соединений по изобретению, и способы их получения будут очевидны специалистам в данной области. Такие композиции и способы их получения можно обнаружить, например, в 'Remington's Pharmaceutical Sciences', 19th Edition (Mack Publishing Company, 1995), описание которого включено в настоящее описание путем ссылки во всей своей полноте.
Соединения по изобретению можно вводить перорально. Пероральное введение может включать глотание, так что соединение попадает в желудочно-кишечный тракт, или может быть использовано трансбуккальное или подъязычное введение, посредством которых соединение попадает в кровоток непосредственно изо рта.
Лекарственные формы, подходящие для перорального введения, включают твердые лекарственные формы, такие как таблетки, капсулы, содержащие частицы, жидкости или порошки, лепешки (включая заполненные жидкостью), жвачки, мульти- и наночастицы, гели, твердый раствор, липосому, пленки (включая мукоадгезивные), вагинальные суппозитории яйцевидной формы, спреи и жидкие композиции.
Жидкие композиции включают суспензии, растворы, сиропы и эликсиры. Такие композиции могут быть использованы в качестве наполнителей в мягких или твердых капсулах и обычно содержат носитель, например, воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу или подходящее масло, и один или несколько эмульгаторов и/или суспендирующих веществ. Жидкие композиции также могут быть приготовлены путем восстановления влагосодержания твердого вещества, например, из саше.
Соединения по изобретению также можно применять в быстрорастворимых, быстроразрушающихся лекарственных формах, таких как описанные в Expert Opinion in Therapeutic Patents, 11 (6), 981-986 by Liang and Chen (2001), описание которого включено в настоящее описание путем ссылки во всей своей полноте.
Для таблетированных лекарственных форм, в зависимости от дозы, лекарственное средство может составлять от 1% масс. до 80% масс. лекарственной формы, более типично от 5% масс. до 60% масс. лекарственной формы. В дополнение к лекарству таблетки обычно содержат разрыхлитель. Примеры разрыхлителей включают натрий крахмалгликолат, карбоксиметилцеллюлозу натрия, карбоксиметилцеллюлозу кальция, кроскармеллозу натрия, кросповидон, поливинилпирролидон, метилцеллюлозу, микрокристаллическую целлюлозу, низший алкилзамещенный гидроксипропил-целлюлозу, крахмал, прежелатинизированный крахмал и альгинат натрия. Обычно разрыхлитель будет составлять от 1% масс. до 25% масс., предпочтительно от 5% масс. до 20% масс. лекарственной формы.
Связующие вещества обычно используют для придания составу таблетки связующих качеств. Подходящие связующие вещества включают микрокристаллическую целлюлозу, желатин, сахара, полиэтиленгликоль, природные и синтетические смолы, поливинилпирролидон, прежелатинизированный крахмал, гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу. Таблетки также могут содержать разбавители, такие как лактоза (моногидрат, высушенный распылением моногидрат, безводный и т.п.), маннит, ксилит, декстрозу, сахарозу, сорбит, микрокристаллическую целлюлозу, крахмал и дигидрат двухосновного фосфата кальция.
Таблетки также необязательно могут содержать поверхностно-активные вещества, такие как лаурилсульфат натрия и полисорбат 80, и скользящие вещества, такие как диоксид кремния и тальк. Когда они присутствуют, поверхностно-активные вещества обычно находятся в количествах от 0,2% масс. до 5% масс. таблетки, и скользящие вещества обычно от 0,2% масс. до 1% масс. таблетки.
Таблетки также обычно содержат лубриканты, такие как стеарат магния, стеарат кальция, стеарат цинка, стеарилфумарат натрия и смеси стеарата магния с лаурилсульфатом натрия. Лубриканты обычно присутствуют в количествах от 0,25% масс. до 10% масс., предпочтительно от 0,5% масс. до 3% масс. таблетки.
Другие общепринятые ингредиенты включают антиоксиданты, красители, корригенты, консерванты и вещества, маскирующие вкус.
Типичные таблетки содержат вплоть до примерно 80% масс. лекарственного средства, от примерно 10% масс. до примерно 90% масс. связующего вещества, от примерно 0% масс. до примерно 85% масс. разбавителя, от примерно 2% масс. до примерно 10% масс. разрыхлителя и от примерно 0,25% масс. до примерно 10% масс. лубриканта.
Таблеточные смеси могут быть подвергнуты непосредственному прессованию или прессованию с помощью вращающегося цилиндра с формированием таблеток. Альтернативно, таблеточные смеси или части смесей могут быть подвергнуты влажному, сухому гранулированию или гранулированию из расплава, застыванию расплава или экструзии перед таблетированием. Конечная лекарственная форма может содержать один или более слоев и может быть покрытой или непокрытой, или инкапсулированной.
Получение таблеток подробно описано в “Pharmaceutical Dosage Forms: Tablets, Vol. 1”, by H. Lieberman and L. Lachman, Marcel Dekker, N.Y., N.Y., 1980 (ISBN 0-8247-6918-X), описание которого включено в настоящее описание путем ссылки во всей своей полноте.
Твердые лекарственные формы для перорального введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Лекарственные формы модифицированного высвобождения включают отсроченное, замедленное, прерывистое, контролируемое, направленное и программируемое высвобождение.
Подходящие лекарственные формы с модифицированным высвобождением описаны в патенте США No 6106864. Подробности других подходящих технологий высвобождения, таких как высокоэнергетические дисперсии и осмотические и покрытые частицы, можно обнаружить в Verma et al, Pharmaceutical Technology On-line, 25(2), 1-14 (2001). Использование жевательной резинки для достижения контролируемого высвобождения описано в WO 00/35298. Описания этих ссылок включены в настоящее описание путем ссылок во всей их полноте.
Соединения по изобретению также можно вводить непосредственно в кровоток, в мышцу или во внутренний орган. Подходящие способы парентерального введения включают внутривенное, внутриартериальное, внутрибрюшинное, интратекальное, внутрижелудочковое, интрауретральное, интрастернальное, интракраниальное, внутримышечное и подкожное. Подходящие устройства для парентерального введения включают игольчатые (в том числе микроигольчатые) инжекторы, безыгольные устройства для инъекций и оборудование для инфузии.
Парентеральные лекарственные формы обычно представляют собой водные растворы, которые могут содержать эксципиенты, такие как соли, углеводы и буферные вещества (предпочтительно до pH от 3 до 9), но в некоторых случаях они могут быть более подходящим образом изготовлены в виде стерильного неводного раствора или в виде сухой формы, которую следует использовать совместно с подходящим наполнителем, таким как стерильная апирогенная вода.
Приготовление парентеральных лекарственных форм в стерильных условиях, например, путем лиофилизации, может быть легко осуществлено с использованием стандартных фармацевтических методик, хорошо известных специалистам в данной области.
Растворимость соединений по изобретению, используемых при получении парентеральных растворов можно увеличить с помощью подходящих методик приготовления, таких как включение веществ, улучшающих растворимость.
Лекарственные формы для парентерального введения могут быть получены для немедленного и/или модифицированного высвобождения. Лекарственные формы модифицированного высвобождения включают отсроченное, замедленное, прерывистое, контролируемое, направленное и программируемое высвобождение. Таким образом, соединения по изобретению могут быть изготовлены в виде твердого вещества, полутвердого вещества или тиксотропной жидкости для введения в качестве имплантируемого депо, обеспечивающего модифицированное высвобождение активного соединения. Примеры таких лекарственных форм включают покрытые лекарством стенты и микросферы из PGLA.
Соединения по изобретению также можно вводить местно на кожу или слизистую оболочку, т.е. дермально или трансдермально. Типичные лекарственные формы для этой цели включают гели, гидрогели, лосьоны, растворы, кремы, мази, присыпки, перевязочные материалы, пены, пленки, кожные пластыри, пластины, имплантаты, губки, волокна, повязки и микроэмульсии. Также могут быть использованы липосомы. Типичные носители включают спирт, воду, минеральное масло, вазелиновое масло, медицинский вазелин, глицерин, полиэтиленгликоль и пропиленгликоль. Могут быть включены усилители проникновения; см., например, J Pharm Sci, 88 (10), 955-958 by Finnin and Morgan (October 1999). Другие средства для местного введения включают доставку электропорацией, ионтофорезом, фонофорезом, сонофорезом и микроигольчатой или безыгольчатой (например, Powderject™, Bioject™, и т.д.) инъекцией. Описания этих ссылок включены в настоящее описание путем ссылок во всей их полноте.
Лекарственные формы для местного введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Лекарственные формы модифицированного высвобождения включают отсроченное, замедленное, прерывистое, контролируемое, направленное и программируемое высвобождение.
Соединения по изобретению также можно вводить интраназально или ингаляцией, обычно в форме сухого порошка (либо отдельно, в виде смеси, например, сухой смеси с лактозой, или в виде частицы из смешанных компонентов, например, в смеси с фосфолипидами, такими как фосфатидилхолин) из ингалятора сухого порошка или в виде аэрозольного спрея из находящегося под давлением контейнера, насоса, разбрызгивателя, пульверизатора (предпочтительно пульверизатора, использующего электрогидродинамику для получения мелкодисперсного тумана) или небулайзера с использованием подходящего пропеллента, такого как 1,1,1,2-тетрафторэтан или 1,1,1,2,3,3,3-гептафторпропан, или без его использования. Для интраназального применения порошок может содержать биоадгезивные вещества, например хитозан или циклодекстрин.
Находящийся под давлением контейнер, насос, разбрызгиватель, пульверизатор или небулайзер содержит раствор или суспензию соединения(й) по изобретению, содержащую, например, этанол, водный этанол или подходящее альтернативное вещество для диспергирования, солюбилизации или удлинения высвобождения активного вещества, пропеллент(ы) в качестве растворителя и необязательное поверхностно-активное вещество, такое как сорбитантриолеат, олеиновая кислота или олигомолочная кислота.
Лекарственный продукт перед применением в препарате сухого порошка или суспензионном препарате подвергают микронизации до размера, подходящего для доставки ингаляцией (обычно менее чем 5 микрон). Этого можно достичь любым подходящим способом измельчения, таким как размол на спиральной струйной мельнице, размол на струйной мельнице с кипящим слоем, сверхкритической флюидной обработкой с образованием наночастиц, гомогенизацией при высоком давлении или сушкой распылением.
Капсулы (сделанные, например, из желатина или НРМС), блистеры и картриджи для применения в ингаляторе или инсуффляторе могут быть изготовлены таким образом, чтобы содержать порошковую смесь соединения по изобретению, подходящей порошковой основы, такой как лактоза или крахмал, и модификатора характеристик, такого как l-лейцин, маннит или стеарат магния. Лактоза может быть безводной или в форме моногидрата, предпочтительно в форме последнего. Другие подходящие эксципиенты включают декстран, глюкозу, мальтозу, сорбит, ксилит, фруктозу, сахарозу и трегалозу.
Подходящие композиции в форме раствора для применения в пульверизаторе, использующем электрогидродинамику для получения мелкодисперсного тумана, могут содержать от 1 мкг до 20 мг соединения по изобретению на одно включение, а объем активации может варьироваться от 1 до 100 мкл. Типичная композиция включает соединение по изобретению, пропиленгликоль, стерильную воду, этанол и хлорид натрия. Альтернативные растворители, которые могут быть использованы вместо пропиленгликоля, включают глицерин и полиэтиленгликоль.
Подходящие ароматизаторы, такие как ментол и левоментол, или подсластители, такие как сахарин или натрия сахарин, могут быть добавлены к таким композициям по изобретению, предназначенным для ингаляционного/интраназального введения.
Лекарственные формы для ингаляционного/интраназального введения могут быть изготовлены для немедленного и/или модифицированного высвобождения с использованием, например, поли(DL-молочная-согликолевая кислота) (PGLA). Лекарственные формы модифицированного высвобождения включают отсроченное, замедленное, прерывистое, контролируемое, направленное и программируемое высвобождение.
В случае ингаляторов сухого порошка и аэрозолей стандартную дозу определяют с помощью клапана, который доставляет отмеренное количество. Устройства в соответствии с изобретением типично оборудованы для введения отмеренной дозы или "вдоха", содержащего желаемое количество соединения по изобретению. Общую суточную дозу можно вводить в однократной дозе или чаще всего в виде разделенных доз на протяжении суток.
Соединения по изобретению можно вводить ректально или вагинально, например, в форме суппозитория, пессария или клизмы. Масло какао является традиционной основой для суппозиториев, но при необходимости можно использовать различные альтернативы.
Лекарственные формы для ректального/вагинального введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Лекарственные формы модифицированного высвобождения включают отсроченное, замедленное, прерывистое, контролируемое, направленное и программируемое высвобождение.
Соединения по изобретению также можно вводить непосредственно в глаз или в ухо, типично в форме капель состоящей из микрочастиц суспензии или раствора в изотоническом стерильном солевом растворе с установленным pH. Другие лекарственные формы, подходящие для глазного и ушного введения, включают мази, биоразлагаемые (например, гемостатические губки коллаген) и бионеразлагаемые (например, силиконовые) имплантаты, пластины, линзы и системы, состоящие из частиц или везикул, таких как ниосомы или липосомы. Полимер, такой как поперечно-сшитая полиакриловая кислота, поливиниловый спирт, гиалуроновая кислота, целлюлозный полимер, например, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза или метилцеллюлоза, или гетерополисахаридный полимер, например, гелановую камедь, можно включать вместе с консервантом, таким как хлорид бензалкония. Такие лекарственные формы можно также доставлять ионофорезом.
Лекарственные формы для глазного/ушного введения могут быть изготовлены для немедленного и/или модифицированного высвобождения. Лекарственные формы модифицированного высвобождения включают отсроченное, замедленное, прерывистое, контролируемое, направленное и программируемое высвобождение.
Другие технологии
Соединения по изобретению можно объединять с растворимыми макромолекулярными веществами, такими как циклодекстрин и его подходящие производные или полимеры, содержащие полиэтиленгликоль, в целях улучшения их растворимости, скорости растворения, маскирования вкуса, биодоступности и/или стабильности для применения при любом из вышеупомянутых путей введения.
Например, обнаружено, что комплексы лекарственное средство-циклодекстрин, в целом полезны для большинства лекарственных форм и путей введения. Могут быть использованы как комплексы включения, так и комплексы невключения. В качестве альтернативы непосредственному комплексообразованию с лекарством циклодекстрин можно использовать в качестве вспомогательной добавки, т.е. в качестве носителя, разбавителя или солюбилизатора. Чаще всего для этих целей используют альфа-, бета- и гаммациклодекстрины, примеры которых можно обнаружить в РСТ публикациях No WO 91/11172, WO 94/02518 и WO 98/55148, описания которых включены в настоящее описание путем ссылок во всей их полноте.
Дозы
Количество вводимого активного соединения будет зависеть от субъекта, получающего лечение, тяжести расстройства или состояния, скорости введения, распределения соединения и усмотрения лечащего врача. Однако эффективная доза обычно находится в диапазоне от примерно 0,001 до примерно 100 мг на 1 кг массы тела в сутки, предпочтительно от примерно 0,01 до примерно 35 мг/кг/сутки, в однократной или разделенных дозах. Для человека с массой 70 кг это количество могло бы составить от примерно 0,07 до примерно 7000 мг/сутки, предпочтительно от примерно 0,7 до примерно 2500 мг/сутки. В некоторых случаях уровни доз ниже нижнего предела вышеупомянутого диапазона могут быть более чем адекватными, тогда как в других случаях могут быть использованы даже большие дозы без вызывания какого-либо опасного побочного эффекта, где такие большие дозы обычно разделены на несколько меньших доз для введения в течение суток.
Набор из частей
Поскольку может быть желательным введение комбинации активных соединений, например, для лечения конкретного заболевания или состояния, в объем настоящего изобретения входят две или несколько фармацевтических композиций, по меньшей мере одна из которых содержит соединение по изобретению, можно удобно объединять в форме набора, подходящего для совместного введения композиций. Таким образом, набор по изобретению включает две или несколько отдельных фармацевтических композиций, по меньшей мере одна из которых включает соединение по изобретению, и средства для отдельного хранения указанных композиций, такие как контейнер, секционная бутыль или секционный пакет из фольги. Примером такого набора является знакомая блистерная упаковка, используемая для упаковки таблеток, капсул и тому подобного.
Набор по изобретению является особенно подходящим для введения различных лекарственных форм, например, пероральной и парентеральной, для введения отдельных композиций при различных интервалах дозирования или для титрования отдельных композиций друг против друга. Чтобы способствовать соблюдению пациентом режима и схемы лечения, набор обычно содержит инструкции по введению и может быть снабжен так называемой памяткой.
Комбинированная терапия
Используемый в настоящем описании термин "комбинированная терапия" относится к введению соединения по изобретению вместе по меньшей мере с одним дополнительным фармацевтическим или медицинским средством (например, противораковым средством) или последовательно, или одновременно.
Как отмечено выше, соединения по изобретению могут быть использованы в комбинации с одним или несколькими дополнительными противораковыми средствами. Эффективность соединений по настоящему изобретению в определенных опухолях может быть повышена путем комбинации с другими одобренными или экспериментальными методами лечения рака, например, облучением, хирургическим вмешательством, химиотерапевтическими средствами, направленными терапиями, средствами, которые ингибируют другие сигнальные пути, которые разрегулированы в опухолях, и другими усиливающими иммунитет средствами, такими как антагонисты PD-1 и тому подобное.
Когда используется комбинированная терапия, один или несколько дополнительных противораковых средств можно вводить последовательно или одновременно с соединением по изобретению. В одном варианте осуществления дополнительное противораковое средство вводят млекопитающему (например, человеку) до введения соединения по изобретению. В другом варианте осуществления дополнительное противораковое средство вводят млекопитающему после введения соединения по изобретению. В другом варианте осуществления дополнительное противораковое средство вводят млекопитающему (например, человеку) одновременно с введением соединения по изобретению.
Изобретение также относится к фармацевтической композиции для лечения аномального клеточного роста у млекопитающего, включая человека, включающей количество соединения по изобретению, определенного выше (включая гидраты, сольваты и полиморфы указанного соединения или его фармацевтически приемлемые соли), в комбинации с одним или несколькими (предпочтительно одним-тремя) дополнительными противораковыми терапевтическими средствами.
Способы синтеза
Соединения по изобретению получают в соответствии с иллюстративными процедурами, приведенными в настоящем описании, и их модификациями, известными специалистам в данной области.
Следующие аббревиатуры использованы в примерах: “Ac” означает ацетил, “AcO” или “OAc” означает ацетокси, “ACN” означает ацетонитрил, “водн” означает водный, “атм.” означает атмосфера(ы), “BOC”, “Boc” или “boc” означает N-трет-бутоксикарбонил, “Bn” означает бензил, “Bu” означает бутил, “nBu” означает нормальный бутил, “tBu” означает трет-бутил, “Cbz” означает бензилоксикарбонил, “DCM” (CH2Cl2) означает метиленхлорид/дихлорметан, “de” означает диастереомерный избыток, “DEA” означает диэтиламин, “DIPEA” означает диизопропилэтиламин, “DMA” означает N, N-диметилацетамид, “DMAP” означает 4-диметиламинопиридин, "DMF" означает N,N-диметилформамид, “DMSO" означает диметилсульфоксид,, “ee” означает энантиомерный избыток, “Et” означает этил, “EtOAc” означает этилацетат, “EtOH” означает этанол, “HATU” означает 1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридиния 3-оксид гексафторфосфат, “HOAc” или “AcOH” означает уксусную кислоту, “i-Pr” или “iPr” означает изопропил, “IPA” означает изопропиловый спирт, “Me” означает метил, “MeOH” означает метанол, “MS” означает масс-спектрометрию, "MTBE" означает метил трет-бутиловый эфир, “Ph” означает фенил, “насыщ.” означает насыщенный, “SFC” означает сверхкритическую флюидную хроматографию, “T3P” означает пропилфосфоновый ангидрид, “TFA” означает трифторуксусную кислоту, “THF” означает тетрагидрофуран, “TLC” означает тонкослойную хроматографию, “Rf” означает удерживаемую фракцию, “~” означает примерно, “rt” означает время удерживания, “ч” означает часы, “мин” означает минуты.
Примеры
Получение синтетических промежуточных соединений
Промежуточное соединение 1: бензил {1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}карбамат;
Промежуточное соединение 2: бензил {1-трет-бутил-3-[(1R,3S)-3-гидроксициклопентил]-1H-пиразол-5-ил}карбамат.
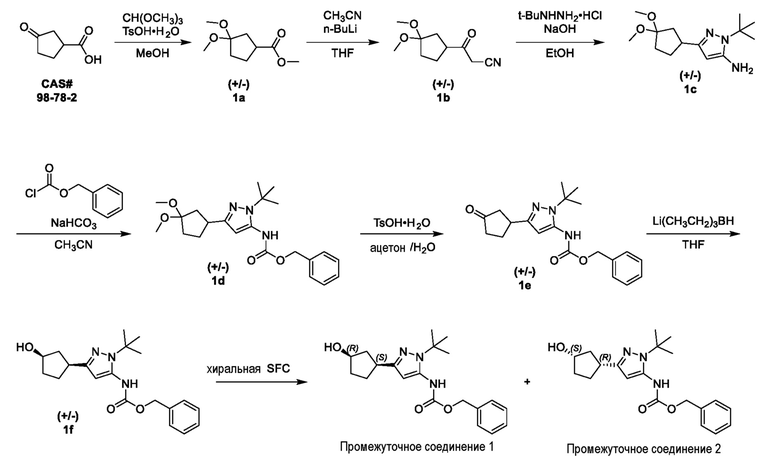
Две параллельные реакции, каждая из которых содержала раствор (±)-3-оксоциклопентанкарбоновой кислоты (CAS#98-78-2, 900 г, 7,02 моль) в метаноле (5 л) при 13°C, каждую обрабатывали триметилортоформиатом (4,47 кг, 42,15 моль, 4,62 л) и моногидратом 4-толуолсульфоновой кислоты (26,72 г, 140,5 ммоль). Смесь перемешивали при 13°C в течение 25 часов. Каждую партию отдельно гасили насыщ. водн. NaHCO3 (1 л), затем две партии объединяли и концентрировали под вакуумом для удаления большей части метанола. Остаток разбавляли этилацетатом (4 л), и слои разделяли. Водный слой дополнительно экстрагировали этилацетатом (2×1 л). Объединенные органические слои промывали насыщ. водн. NaCl (3×1 л), сушили над сульфатом магния, фильтровали, и концентрировали под вакуумом с получением (±)-метил 3,3-диметоксициклопентанкарбоксилата (1a, 2,5 кг, 13,28 моль, 94%) в виде светло-желтого масла. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=3,67 (с, 3H), 3,20 (с, 3H), 3,19 (с, 3H), 2,94-2,82 (м, 1H), 2,16-2,00 (м, 2H), 1,99-1,76 (м, 4H).
Раствор н-бутиллития (3,44 л 2,5 M раствора в гексане, 8,6 моль) добавляли в реактор, содержащий THF (3 л) при -65°C. По каплям добавляли безводный ацетонитрил (453 мл, 353 г, 8,61 моль), достаточно медленно, чтобы поддерживать внутреннюю температуру ниже -55°C. Смесь перемешивали в течение дополнительного 1 часа при -65°C. Раствор (±)-метил 3,3-диметоксициклопентанкарбоксилата (1a, 810 г, 4,30 моль) в THF (1 л) затем добавляли по каплям, достаточно медленно, чтобы поддерживать внутреннюю температуру ниже -50°C. После перемешивания в течение дополнительного часа при -65°C, реакцию гасили водой (4 л), нейтрализовали вод. HCl (1 M) до pH 7, и экстрагировали этилацетатом (3×3 л). Объединенные органические слои промывали насыщ. водн. NaCl (2×3 л), сушили над сульфатом магния, фильтровали, и концентрировали под вакуумом с получением неочищенного (±)-3-(3,3-диметоксициклопентил)-3-оксопропаннитрила (1b, 722 г, 3,66 моль, 85%) в виде красного масла, который использовали без дополнительной очистки.
Твердый гидроксид натрия (131,4 г, всего 3,29 моль) добавляли порциями к суспензии гидрохлорида трет-бутилгидразина (409,4 г, 3,29 моль) в этаноле (3 л) при 16-25°C. Перемешивание продолжали при 25°C в течение 1 часа. Раствор неочищенного (±)-3-(3,3-диметоксициклопентил)-3-оксопропаннитрила (1b, 540 г, 2,74 моль) в этаноле добавляли при 25°C, затем смесь нагревали до 75°C, внутренняя, в течение 30 часов. Реакционную смесь фильтровали и фильтрат концентрировали под вакуумом с получением неочищенного продукта в виде красного масла. Этот продукт объединяли с неочищенными продуктами из еще трех идентично полученных партий (каждая из которых начиналась с 540 г 1b; 2,16 кг, всего 10,96 моль для 4 партий), и очищали с помощью хроматографии на силикагеле (элюирование 0-35% этилацетатом в петролейном эфире), получая (±)-1-трет-бутил-3-(3,3-диметоксициклопентил)-1H-пиразол-5-амин (1c, 1,60 кг, 5,98 моль, 54% выход) в виде красного масла. 1H ЯМР (ХЛОРОФОРМ-d) δ=5,41 (с, 1H), 3,50 (шир.с, 2H), 3,22 (с, 3H), 3,20 (с, 3H), 3,13 (тт, J=7,9, 9,6 Гц, 1H), 2,25 (дд, J=8,0, 13,3 Гц, 1H), 2,09-2,00 (м, 1H), 1,99-1,91 (м, 1H), 1,83 (дд, J=10,8, 12,8 Гц, 2H), 1,78-1,68 (м, 1H), 1,60 (с, 9H).
Бензилхлорформиат (563,6 мл, 676,3 г, 3,96 моль) добавляли к охлажденному (0-5°C) раствору (±)-1-трет-бутил-3-(3,3-диметоксициклопентил)-1H-пиразол-5-амина (1c, 530 г, 1,98 моль) в ацетонитриле (3,5 L). Смесь перемешивали при 23°C в течение 2 часов, и затем порциями добавляли твердый гидрокарбонат натрия (532,9 г, 6,34 моль). Перемешивание продолжали при 23°C в течение 26 часов. Полученную суспензию фильтровали и фильтрат концентрировали под вакуумом с получением неочищенного (±)-бензил [1-трет-бутил-3-(3,3-диметоксициклопентил)-1H-пиразол-5-ил]карбамата (1d, 980 г, 1,98 моль макс) в виде красного масла, который использовали на следующей стадии без дополнительной очистки.
Раствор неочищенного (±)-бензил [1-трет-бутил-3-(3,3-диметоксициклопентил)-1H-пиразол-5-ил]карбамата (1d, 980 г, 1,98 моль макс) в ацетоне (2 л) и воде (2 л) при 18°C обрабатывали моногидратом 4-толуолсульфоновой кислоты (48,75 г, 256,3 ммоль). Смесь нагревали до 60°C, внутренняя, в течение 20 часов. После концентрирования в вакууме для удаления большей части ацетона водный остаток экстрагировали дихлорметаном (3×3 л). Объединенные органические экстракты сушили над сульфатом натрия, фильтровали, и концентрировали в вакууме до неочищенного красного масла. Этот неочищенный продукт объединяли с неочищенным продуктом из двух других идентично полученных партий (каждая получена из 1,98 моль 1c, всего 5,94 моль для 3 партий), и очищали с помощью хроматографии на силикагеле (элюирование 0-50% этилацетатом в петролейном эфире) с получением (±)-бензил [1-трет-бутил-3-(3-оксоциклопентил)-1H-пиразол-5-ил]карбамата (1e, 1,6 кг) в виде желтого твердого вещества. Это твердое вещество перемешивали в смеси петролейный эфир/этилацетат 10:1 (1,5 л) при 20°C в течение 18 часов. Полученную суспензию фильтровали, осадок на фильтре промывали петролейным эфиром (2×500 мл), и твердые вещества сушили под вакуумом с получением (±)-бензил [1-трет-бутил-3-(3-оксоциклопентил)-1H-пиразол-5-ил]карбамата (1e, 1,4 кг, 3,9 моль, 66% объединенные для трех партий). 1H ЯМР (DMSO-d6) δ=9,12 (шир.с, 1H), 7,56-7,13 (м, 5H), 6,03 (с, 1H), 5,12 (с, 2H), 3,41-3,27 (м, 1H), 2,48-2,39 (м, 1H), 2,34-2,10 (м, 4H), 1,98-1,81 (м, 1H), 1,48 (с, 9H).
Раствор (±)-бензил [1-трет-бутил-3-(3-оксоциклопентил)-1H-пиразол-5-ил]карбамата (1e, 320 г, 0,900 моль) в THF (1,5 л) дегазировали под вакуумом и продували сухим азотом (3 цикла), затем охлаждали до -65°C, внутренняя. По каплям добавляли раствор литий триэтилборгидрида (1,0 M в THF, 1,80 л, 1,80 моль) со скоростью, при которой внутренняя температура поддерживалась ниже -55°C, затем перемешивание продолжали при -65°C в течение 1,5 часов. Реакционную смесь гасили насыщ. водн. NaHCO3 (1,5 л) при от -40 до -30°C. К смеси по каплям добавляли перекись водорода (30% водный, 700 г), при этом внутреннюю температуру поддерживали от -10 до 0°C. Смесь перемешивали при 10°C в течение 1 часа, затем экстрагировали этилацетатом (3×2 л). Объединенные органические слои промывали насыщ. водн. Na2SO3 (2×1 л) и насыщ. водн. NaCl (2×1 л). Органические слои сушили над сульфатом магния, фильтровали, и концентрировали под вакуумом до неочищенного желтого масла. Неочищенный продукт из этой партии объединяли с неочищенным продуктом из трех других, идентично полученных партий (каждая, начиная с 0,900 моль 1e, всего 3,60 моль) для очистки. Перед хроматографией объединенная смесь показала соотношение цис/транс ~3,3:1 по данным ЯМР. Объединенный неочищенный продукт дважды очищали хроматографией на силикагеле, элюируя 0-50% этилацетатом в дихлорметане), получая (±)-транс-бензил [1-трет-бутил-3-(3-гидроксициклопентил)-1H-пиразол-5-ил]карбамат (1f, 960 г) в виде светло-желтого твердого вещества, которое дополнительно очищали растиранием, как описано ниже.
Предыдущую партию 1f получали в результате реакций меньшего масштаба, начиная с общего количества 120 г 1e (0,34 моль). Продукт из колонки из этой партии объединяли с продуктом из колонки из указанной выше партии (который был получен из 3,60 моль 1e, всего 3,94 моль 1e, использованных для всех объединенных партий), суспендирован в смеси дихлорметан/метанол 10:1 (1,5 л) и перемешивали при 20°C в течение 16 часов. Суспензию фильтровали, и осадок на фильтре промывали петролейным эфиром (2×500 мл). Твердые вещества сушили в вакууме, получая чистый (±)-транс-бензил [1-трет-бутил-3-(3-гидроксициклопентил)-1H-пиразол-5-ил]карбамат (1f, 840 г, 2,35 моль, общий выход 60% для всех объединенных партий) в виде белого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=9,07 (шир.с, 1H), 7,45-7,27 (м, 5H), 5,92 (с, 1H), 5,11 (с, 2H), 4,57 (д, J=4,5 Гц, 1H), 4,21-4,07 (м, 1H), 2,88 (квин, J=8,6 Гц, 1H), 2,24-2,13 (м, 1H), 1,92-1,78 (м, 1H), 1,78-1,62 (м, 2H), 1,61-1,53 (м, 1H), 1,47 (с, 9H), 1,52-1,43 (м, 1H). MS: 358 [M+H]+.
Энантиомеры (±)-транс-бензил [1-трет-бутил-3-(3-гидроксициклопентил)-1H-пиразол-5-ил]карбамата (1f, 700 г, 1,96 моль) разделяли с помощью хиральной SFC.
Продукт из пика первого элюированного энантиомера (310 г твердого вещества) суспендировали в смеси метанол/петролейный эфир (1:10, 1 л) и перемешивали при 25°C в течение 1 часа. Суспензию фильтровали, фильтрующий слой промывали петролейным эфиром (2×500 мл), и твердые вещества сушили под вакуумом с получением бензил {1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}карбамата (промежуточное соединение 1, 255 г, 713 ммоль, 36%, >99% ee) в виде белого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=9,08 (шир.с, 1H), 7,58-7,20 (м, 5H), 5,92 (с, 1H), 5,11 (с, 2H), 4,57 (д, J=4,4 Гц, 1H), 4,19-4,09 (м, 1H), 2,88 (квин, J=8,6 Гц, 1H), 2,24-2,13 (м, 1H), 1,91-1,79 (м, 1H), 1,79-1,61 (м, 2H), 1,61-1,53 (м, 1H), 1,47 (с, 9H), 1,52-1,44 (м, 1H). MS: 358 [M+H]+. Оптическое вращение [α]D +3,76 (c 1,0, MeOH). Хиральная чистота: >99% ee, время удерживания 3,371 мин. Хиральный SFC анализ проводили на колонке ChiralPak AD-3 150×4,6 мм ID, 3 мкм, нагретой до 40°C, элюирование подвижной фазой CO2 и градиентом 0-40% метанол+0,05%DEA в течение 5,5 мин, затем выдерживали при 40% в течение 3 мин; протекающей при 2,5 мл/мин.
Продукт из пика энантиомера второго элюирования (300 г твердого вещества) суспендировали в смеси метанол/петролейный эфир (1:10, 1 л) и перемешивали при 25°C в течение 1 часа. Суспензию фильтровали, фильтрующий слой промывали петролейным эфиром (2×500 мл), и твердые вещества сушили под вакуумом с получением бензил {1-трет-бутил-3-[(1R,3S)-3-гидроксициклопентил]-1H-пиразол-5-ил}карбамата (промежуточное соединение 2, 255 г, 713 ммоль, 36%, 94% ee) в виде белого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=9,08 (шир.с, 1H), 7,55-7,19 (м, 5H), 5,92 (с, 1H), 5,11 (с, 2H), 4,57 (д, J=4,4 Гц, 1H), 4,23-4,07 (м, 1H), 2,88 (квин, J=8,7 Гц, 1H), 2,23-2,14 (м, 1H), 1,90-1,79 (м, 1H), 1,77-1,61 (м, 2H), 1,61-1,53 (м, 1H), 1,47 (с, 9H), 1,52-1,44 (м, 1H). MS: 358 [M+H]+. Оптическое вращение [α]D -2,43 (c 1,0, MeOH). Хиральная чистота: 94% ee, время удерживания 3,608 мин. Хиральный SFC анализ проводили на колонке ChiralPak AD-3 150×4,6 мм ID, 3 мкм, нагретой до 40°C, элюирование подвижной фазой CO2 и градиентом 0-40% метанол+0,05%DEA в течение 5,5 мин, затем выдерживали при 40% в течение 3 мин; протекающей при 2,5 мл/мин.
Образец второго элюированного энантиомера из предыдущей партии с [α]D -3,1 (c 1,1, MeOH) и 96% ee кристаллизовали из дихлорэтана/пентана. Кристаллическую структуру получали с помощью рентгеновской кристаллографии малых молекул, которая показала (1R,3S) геометрию. Таким образом, абсолютная стереохимия промежуточного соединения 2 была определена (1R,3S) на основании его сопоставимого оптического вращения и порядка элюирования в аналитическом методе. Промежуточному соединению 1, энантиомеру промежуточного соединения 2, таким образом, была присвоена стереохимия (1S,3R).
Промежуточное соединение 3: (5-метил-1,3-оксазол-2-ил)уксусная кислота
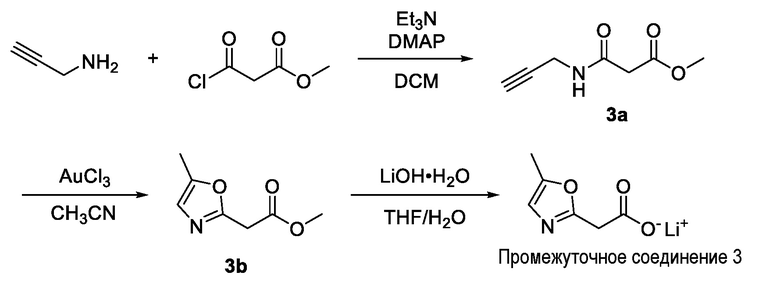
Раствор проп-2-ил-1-амина (25,0 г, 450 ммоль) в дихлорметане (500 мл) при 15°C обрабатывали триэтиламином (138 г, 1360 ммоль) и DMAP (5,55 г, 45,4 ммоль). Смесь охлаждали до 0°C и по каплям добавляли метил 3-хлор-3-оксопропаноат (74,4 г, 545 ммоль) в течение 30 минут. Полученный раствор перемешивали при 15°C в течение 16 часов, затем выдерживали при этой температуре в течение 2 дней. Полученную суспензию фильтровали, фильтрат концентрировали под вакуумом, и остаток очищали с помощью хроматографии на силикагеле (элюирование 60% EtOAc/петролейным эфиром) с получением метил 3-оксо-3-(проп-2-ин-1-иламино)пропаноата (3a, 47 г, 67%, 90% чистота по ЯМР) в виде светло-желтого масла. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=7,43 (шир.с, 1H), 4,09 (дд, J=2,6, 5,3 Гц, 2H), 3,76 (с, 3H), 3,36 (с, 2H), 2,25 (с, 1H).
Две параллельные партии получали в соответствии со следующей процедурой: Раствор метил 3-оксо-3-(проп-2-ин-1-иламино)пропаноата (3a, 23,5 г, 151 ммоль) в ацетонитриле (300 мл) обрабатывали трихлоридом золота (2,50 г, 8,24 ммоль) при комнатной температуре (20°C). Полученную смесь нагревали до 70°C в течение 16 часов в темноте. Затем две партии объединяли, фильтровали для удаления катализатора, и фильтрат концентрировали досуха. Остаток очищали с помощью хроматографии на силикагеле (элюирование 40% EtOAc/петролейным эфиром) с получением с получением метил (5-метил-1,3-оксазол-2-ил)ацетата (3b, 26,5 г, 56,5% для объединенных партий) в виде светло-желтого масла. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=6,68 (д, J=1,0 Гц, 1H), 3,80 (с, 2H), 3,75 (с, 3H), 2,30 (д, J=1,3 Гц, 3H).
Раствор метил (5-метил-1,3-оксазол-2-ил)ацетата (3b, 26,5 г, 170,8 ммоль) в THF (80 мл) и воде (20 мл) обрабатывали моногидратом гидроксида лития (7,17 г, 171 ммоль) и перемешивали при комнатной температуре (25°C) в течение 2 часов. Смесь концентрировали для удаления большей части THF, затем остаток разбавляли водой (25 мл) и экстрагировали дихлорметаном (2×30 мл). Водный слой концентрировали с получением неочищенного продукта (~26 г), который дополнительно очищали растиранием с EtOAc/MeOH (об/об 10/1) с получением литий (5-метил-1,3-оксазол-2-ил)ацетата (промежуточное соединение 3, 21,7 г, 90%) в виде светло-желтого твердого вещества. 1H ЯМР (400 МГц, ОКСИД ДЕЙТЕРИЯ) δ=6,63 (д, J=1,0 Гц, 1H), 3,59 (с, 2H), 2,22 (д, J=1,0 Гц, 3H).
Промежуточное соединение 4: Литий (5-метоксипиразин-2-ил)ацетат.
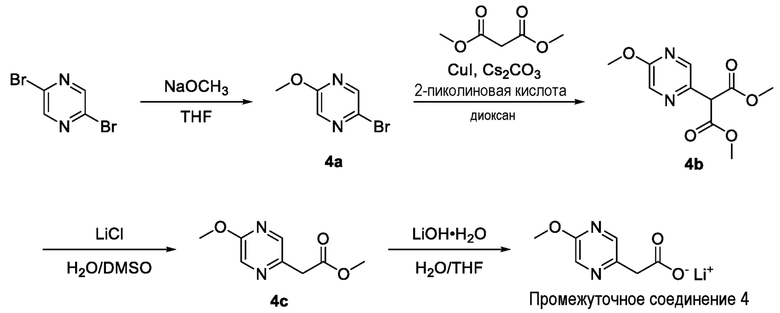
Раствор 2,5-дибромпиразина (30,0 г, 126 ммоль) в THF (252 мл) охлаждали до 0°C. По каплям добавляли метоксид натрия (25% масс. раствор в метаноле, 29,0 мл, 27,3 г, 126 ммоль) в течение 18 минут. Раствору давали нагреться до комнатной температуры и перемешивали в течение 37 часов. Суспензию фильтровали, колбу и фильтрпрессную лепешку промывали небольшим количеством THF, и фильтрат концентрировали под вакуумом с получением 2-бром-5-метоксипиразина (4a, 23,80 г, 100%) в виде твердого вещества. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=8,20 (д, J=1,2 Гц, 1H), 8,03 (д, J=1,2 Гц, 1H), 3,97 (с, 3H).
В продуваемую азотом колбу загружали йодид меди(I) (2,82 г, 14,8 ммоль), 2-пиколиновую кислоту (3,65 г, 29,6 ммоль), карбонат цезия (36,2 г, 111 ммоль), и 2-бром-5-метоксипиразин (4a, 7,00 г, 37,03 ммоль). Колбу снова продували азотом, затем шприцем вводили сухой диоксан (250 мл) и диметилмалонат (22 мл, 192 ммоль). Через раствор барботировали азот в течение 10 минут. Смесь нагревали при 100°C в течение 36 часов. После охлаждения до комнатной температуры, суспензию фильтровали, и фильтрат концентрировали до образования масла. Твердые вещества, оставшиеся в фильтрпрессной лепешке, суспендировали в воде (150 мл) и раствор медленно подкисляли 4M HCl (~17 мл). Этот раствор экстрагировали этилацетатом (2×150 мл). Этилацетатные экстракты объединяли с неочищенным маслом, полученным из фильтрата, и все промывали насыщ. водн. NH4Cl (50 мл), сушили над сульфатом натрия, фильтровали, и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (элюирование 0-50% этилацетатом в гептане) с получением диметил (5-метоксипиразин-2-ил)пропандиоата (4b, 5,94 г, 67%) в виде масла, который затвердевало при стоянии. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=8,23 (д, J=1,3 Гц, 1H), 8,18 (д, J=1,3 Гц, 1H), 4,90 (с, 1H), 3,97 (с, 3H), 3,79 (с, 6H).
Раствор диметил (5-метоксипиразин-2-ил)пропандиоата (4b, 7,30 г, 30,4 ммоль) в DMSO (51 мл) и воде (3,4 мл) охлаждали до 0°C. Добавляли твердый хлорид лития (5,15 г, 122 ммоль) и смесь нагревали до 100°C в течение 17 часов. Темно-красный раствор распределяли между этилацетатом (150 мл) и водой (300 мл). Водный слой дополнительно экстрагировали этилацетатом (3×50 мл). Объединенные органические слои промывали полунасыщенным водн. NaCl и насыщ. водн. NaCl, сушили над сульфатом натрия, фильтровали, и концентрировали. Неочищенный продукт очищали с помощью хроматографии на силикагеле (элюирование 0-60% этилацетатом в гептане), получая метил (5-метоксипиразин-2-ил)ацетат (4c, 3,86 г, 70%) в виде масла. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=8,18 (д, J=1,3 Гц, 1H), 8,06 (д, J=1,2 Гц, 1H), 3,96 (с, 3H), 3,79 (с, 2H), 3,73 (с, 3H).
Суспензию метил (5-метоксипиразин-2-ил)ацетата (4c, 3,86 г, 21,2 ммоль) и моногидрата гидроксида лития (889 мг, 21,2 ммоль) в THF (42 мл) и воде (42 мл) перемешивали при 25°C в течение 14 часов. Непрореагировавший сложный эфир все еще присутствовал по данным LCMS, поэтому добавляли дополнительное количество моногидрата гидроксида лития (50 мг, 1,2 ммоль) и перемешивание продолжали при 25°C в течение 6 часов. Конверсия все еще не была завершена, поэтому добавляли еще больше моногидрата гидроксида лития (110 мг, 2,62 ммоль; всего 1,049 г, 25 ммоль) и смесь нагревали до 30°C в течение 2 часов. THF удаляли в вакууме, и водный остаток лиофилизировали досуха, получая литий (5-метоксипиразин-2-ил)ацетат (промежуточное соединение 4, 4,272 г, 115% от теоретической массы 3,71 г), в виде смеси с гидроксидом лития. 1H ЯМР (400 МГц, ОКСИД ДЕЙТЕРИЯ) δ=8,14 (д, J=1,3 Гц, 1H), 8,01 (д, J=1,2 Гц, 1H), 3,93 (с, 3H), 3,64 (с, 2H).
Промежуточное соединение 5: Литий 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксилат.
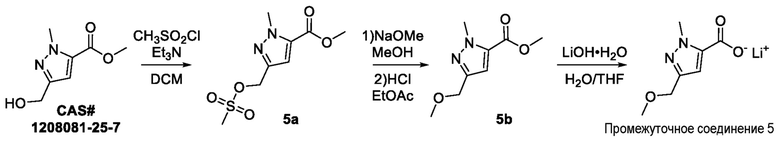
Раствор метансульфонилхлорида (11,32 г, 98,8 ммоль) в дихлорметане (50 мл) добавляли по каплям к охлажденной (0°C) смеси метил 3-(гидроксиметил)-1-метил-1H-пиразол-5-карбоксилата (CAS# 1208081-25-7, 15,0 г, 88,1 ммоль) и диизопропилэтиламина (14,8 г, 115 ммоль) в дихлорметане (250 мл). Смесь перемешивали при 0°C в течение 45 минут после завершения добавления. Реакционную смесь промывали насыщ. водн. NH4Cl, и органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением метил 1-метил-3-{[(метилсульфонил)окси]метил}-1H-пиразол-5-карбоксилата (5a, 22,6 г, >99%) в виде желтого масла, который использовали без дополнительной очистки. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=6,98 (с, 1H), 5,26 (с, 2H), 4,20 (с, 3H), 3,91 (с, 3H), 3,03 (с, 3H).
Раствор метил 1-метил-3-{[(метилсульфонил)окси]метил}-1H-пиразол-5-карбоксилата (5a, 22,6 г, 91,0 ммоль) в метаноле (200 мл) при комнатной температуре обрабатывали твердым метоксидом натрия (9,84 г, 182 ммоль) небольшими порциями. Реакционную смесь нагревали до 70°C в течение 30 минут. TLC показала частичный гидролиз сложного эфира, поэтому для повторной этерификации мутную смесь подкисляли 4M HCl в этилацетате (40 мл, 160 ммоль), и продолжали нагревание при 70°C в течение 5 часов. Смесь концентрировали досуха, оставляя белое твердое вещество. Это твердое вещество экстрагировали этилацетатом/петролейным эфиром (1/3, 3×200 мл). Объединенные экстракты концентрировали досуха, затем остаточное твердое вещество повторно экстрагировали этилацетатом/петролейным эфиром (1/3, 100 мл), сушили над сульфатом натрия, фильтровали, и концентрировали с получением метил 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксилата (5b, 14,5 г, 86%, 80% чистота по ЯМР) в виде светло-желтой жидкости, которая затвердевала при стоянии. Только основной компонент: 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=6,83 (с, 1H), 4,45 (с, 2H), 4,16 (с, 3H), 3,88 (с, 3H), 3,39 (с, 3H).
Раствор метил 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксилата (5b, 14,5 г, 78,7 ммоль) и моногидрата гидроксида лития (3,47 г, 82,7 ммоль) в THF (150 мл) и воде (50 мл) перемешивали при комнатной температуре в течение 16 часов. THF удаляли в вакууме, остаток растворяли в воде (100 мл) и экстрагировали дихлорметаном (3×30 мл). Органические слои отбрасывали. Водный слой концентрировали и сушили под вакуумом с получением литий 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксилата (промежуточное соединение 5, 12,85 г, 92%) в виде желтого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=6,37 (с, 1H), 4,24 (с, 2H), 4,01 (с, 3H), 3,20 (с, 3H). MS: 171 [M+H]+.
Общие способы и иллюстративные примеры
Способ A
Пример 1: (1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат
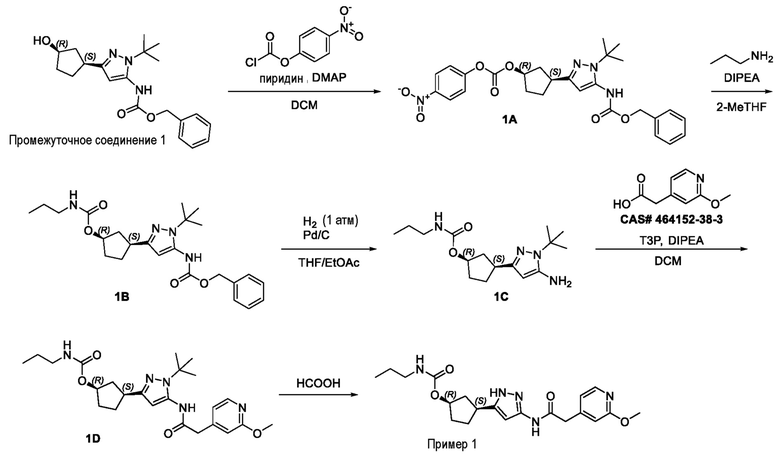
Раствор комнатной температуры бензил {1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}карбамата (промежуточное соединение 1, 5,00 г, 14,0 ммоль) и 4- нитрофенилхлорформиата (4,23 г, 21,0 ммоль) в безводном дихлорметане (50 мл) обрабатывали пиридином (3,40 мл, 42,0 ммоль) и 4-(диметиламино)пиридином (170 мг, 1,4 ммоль). После перемешивания при комнатной температуре в течение ночи, раствор концентрировали и очищали с помощью хроматографии на силикагеле (элюирование 0-100% этилацетатом в н-гептане) с получением (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 7,30 г, 100%) в виде твердой пены. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=8,24-8,14 (м, 2H), 7,36-7,22 (м, 7H), 6,21 (шир.с, 1H), 6,06 (шир.с, 1H), 5,25-5,15 (м, 1H), 5,12 (с, 2H), 3,15-2,97 (м, 1H), 2,58-2,47 (м, 1H), 2,09-1,78 (м, 5H), 1,51 (с, 9H). MS: 523 [M+H]+.
Раствор (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 36 г, 69 ммоль) в 2-метилтетрагидрофуране (300 мл) охлаждали до 10°C. Добавляли диизопропилэтиламин (26,7 г, 36 мл, 207 ммоль) и пропан-1-амин (6,11 г, 8,52 мл, 103 ммоль), и раствор перемешивали при 10°C в течение 16 часов. После концентрирования досуха остаток разбавляли этилацетатом (600 мл), промывали 1M NaOH (4×200 мл), и затем насыщ. водн. NaCl (100 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного бензил (1-трет-бутил-3-{(1S,3R)-3-[(пропилкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамата (1B, 30 г, 98%), который использовали без дополнительной очистки.
Суспензию комнатной температуры (20-25°C) Pd/C (50% H2O, 8 г) и неочищенного бензил (1-трет-бутил-3-{(1S,3R)-3-[(пропилкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамата (1B, 30 г, 68 ммоль) в этилацетате (300 мл) и THF (150 мл) дегазировали и продували водородом (3 цикла), затем перемешивали при комнатной температуре под водородным баллоном в течение 16 часов. Суспензию фильтровали, фильтрат концентрировали под вакуумом, и остаток кристаллизовали из этилацетата (50 мл) и петролейного эфира (300 мл), получая (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил пропилкарбамат (1C, 17,65 г, 84%) в виде белого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=7,00 (шир.т, J=5,6 Гц, 1H), 5,23 (с, 1H), 4,95 (шир.с, 1H), 4,82-4,58 (м, 2H), 2,91 (кв, J=6,6 Гц, 2H), 2,85-2,73 (м, 1H), 2,37-2,21 (м, 1H), 1,92-1,76 (м, 2H), 1,72-1,52 (м, 3H), 1,48 (с, 9H), 1,44-1,32 (м, 2H), 0,82 (т, J=7,4 Гц, 3H). MS: 309 [M+H]+. ]+. Оптическое вращение [α]D -4,04 (c 0,89, MeOH). Хиральная чистота: 98% ee с помощью хиральной аналитической SFC.
Охлажденную (10°C) смесь (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил пропилкарбамата (1C, 8,65 г, 28,05 ммоль), (2-метоксипиридин-4-ил)уксусной кислоты (CAS# 464152-38-3, 5,86 г, 33,7 ммоль) диизопропилэтиламина (14,7 мл, 84,1 ммоль) и пропилфосфонового ангидрида (T3P®, 50% масс. Раствора в EtOAc, 53,5 г, 84,1 ммоль) в дихлорметане (250 мл) перемешивали в течение 16 часов. Реакцию гасили насыщ. водн. Na2CO3 (20 мл) и экстрагировали дихлорметаном (100 мл). Органический слой промывали дополнительно насыщ. водн. Na2CO3 (2×200 мл) и насыщ. водн. NaCl (100 мл), сушили над безводным сульфатом натрия, фильтровали, и концентрировали досуха. Для очистки эту партию объединяли с двумя другими аналогично полученными партиями, полученными из 1,0 г и 8,0 г 1C (общий SM для трех партий=17,65 г, 57,23 ммоль 1C). Хроматография с силикагелем (элюирование 0-60% EtOAc/петролейным эфиром) дала (1R,3S)-3-(1-трет-бутил-5-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил пропилкарбамат (1D, 25 г, 95% выход для объединенных партий). MS: 458 [M+H]+.
Раствор (1R,3S)-3-(1-трет-бутил-5-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил пропилкарбамата (1D, 20,5 г, 44,8 ммоль) в муравьиной кислоте (50 мл) перемешивали при 75°C в течение 20 часов. Для очистки эту партию объединяли с меньшей партией (полученная из 4,50 г, 9,84 ммоль 1D, в общей сложности 25,0 г, 54,6 ммоль), концентрировали досуха, и очищали с помощью препаративной ВЭЖХ [колонка Phenomenex Gemini C18 250×50 мм x 10 мкм; элюирование с градиентом воды (0,05% гидроксид аммония об/об) в ACN в течение 15 минут; протекающей при 110 мл/мин]. Чистый (1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат (пример 1, 16,61 г, 76% выход для объединенных партий) в виде бледно-желтого твердого вещества. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=11,62-9,81 (м, 1H), 9,06 (шир.с, 1H), 8,06 (д, J=5,3 Гц, 1H), 6,79 (д, J=5,3 Гц, 1H), 6,66 (с, 1H), 6,50 (с, 1H), 5,24-4,94 (м, 2H), 3,88 (с, 3H), 3,58 (с, 2H), 3,19-2,83 (м, 3H), 2,54-2,28 (м, 1H), 2,04 (шир.с, 1H), 1,97-1,70 (м, 4H), 1,54-1,34 (м, 2H), 0,85 (шир.т, J=7,0 Гц, 3H). MS: 402 [M+H]+. Оптическое вращение [α]D +17,1 (c 1,06, MeOH). Хиральная чистота: 96% ee с помощью хиральной аналитической SFC.
Пример 2: (1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамат.
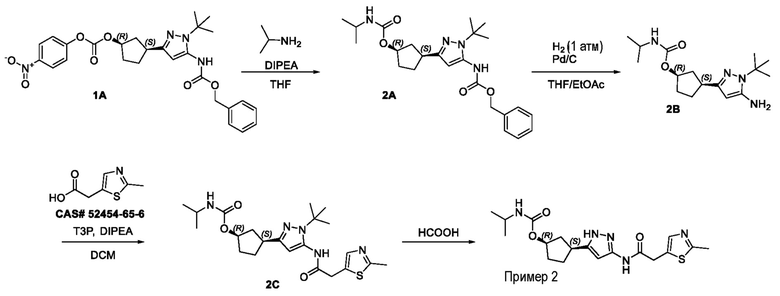
Раствор (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 2,00 г, 3,83 ммоль), изопропиламина (294 мг, 4,98 ммоль), и диизопропилэтиламина (3,33 мл, 19,1 ммоль) в THF (20 мл) перемешивали при 10°C в течение 4 часов. После концентрирования досуха, остаток разбавляли этилацетатом (100 мл), и раствор промывали 1M гидроксидом натрия (4×50 мл) и насыщ. водн. NaCl (30 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного бензил (1-трет-бутил-3-{(1S,3R)-3-[(пропан-2-илкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамата (2A, 1,8 г, 100% неочищенный).
Суспензию комнатной температуры (10°C) неочищенного бензил (1-трет-бутил-3-{(1S,3R)-3-[(пропан-2-илкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамата (2A, 1,8 г, 3,83 ммоль) и Pd/C (влажный, 200 мг) в этилацетате (10 мл) и THF (5 мл) дегазировали и продували водородом, затем перемешивали под водородным баллоном при 10°C в течение 16 часов. Катализатор удаляли фильтрацией, и фильтрат концентрировали досуха. Остаток очищали с помощью препаративной ВЭЖХ на колонке Phenomenex Gemini C18 250*50мм*10 мкм, элюируя 25-45% водой (0,05% гидроксид аммония об/об) в ацетонитриле. Лиофилизация фракций, содержащих продукт, дала (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил пропан-2-илкарбамат (2B, 1,0 г, 85%) в виде желтого масла. MS: 309 [M+H]+.
Добавляли пропилфосфоновый ангидрид (T3P®, 50% масс. раствор в EtOAc, 457,г. 0,718 ммоль) к охлажденному (0°C) раствору (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил пропан-2-илкарбамата (2B, 80 мг, 0,26 ммоль), диизопропилэтиламина (92,7 мг, 0,718 ммоль) и (2-метил-1,3-тиазол-5-ил)уксусной кислоты (CAS# 52454-65-6, 45,1 мг, 0,287 ммоль) в дихлорметане (3 мл). Смеси давали возможность перемешиваться при комнатной температуре (10°C) в течение 16 часов, затем разделяли между дихлорметаном (20 мл) и насыщ. водн. Na2CO3 (10 мл). Органический слой промывали насыщ. водн. NaCl (10 мл), сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного (1R,3S)-3-(1-трет-бутил-5-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил пропан-2-илкарбамата (2C, 120 мг, 100% неочищенный) в виде желтой камеди.
Неочищенный (1R,3S)-3-(1-трет-бутил-5-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил пропан-2-илкарбамат (2C, 120 мг, 0,26 ммоль) растворяли в муравьиной кислоте (5 мл) и перемешивали при 75°C в течение 20 часов. Летучие вещества удаляли под вакуумом, и остаток очищали с помощью препаративной ВЭЖХ на колонке Xtimate C18 150*25 мм*5 мкм, элюируя 12-52% воды (0,05% гидроксид аммония об/об) в ацетонитриле. Лиофилизация фракций, содержащих продукт, дала (1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамат (пример 2, 60,35 мг, 58%) в виде белого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=12,10 (с, 1H), 10,58 (с, 1H), 7,41 (с, 1H), 6,95 (шир.д, J=6,3 Гц, 1H), 6,29 (с, 1H), 4,98 (шир.с, 1H), 3,81 (с, 2H), 3,57 (шир.д, J=6,5 Гц, 1H), 3,03 (шир.с, 1H), 2,59 (с, 3H), 2,45 (шир.с, 1H), 2,07-1,81 (м, 2H), 1,78-1,44 (м, 3H), 1,03 (шир.д, J=6,5 Гц, 6H). MS: 392 [M+H]+. Хиральная чистота: 99% ee с помощью хиральной аналитической SFC.
Пример 3: (1R,3S)-3-(3-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил этилкарбамат
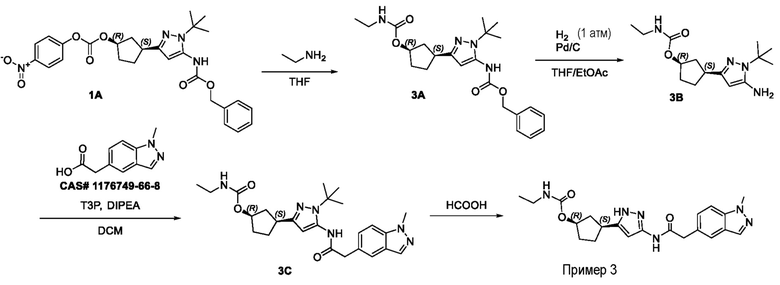
Раствор (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 2,5 г, 4,8 ммоль) и этиламина (1,08 г, 23,9 ммоль) в THF (20 мл) перемешивали при 30°C в течение 3 часов, концентрировали досуха, и остаток растворяли в дихлорметане (30 мл). Раствор промывали водн. NaOH до тех пор, пока органический слой не стал бесцветным (5×5 мл), затем промывали водой (5 мл) и насыщ. водн. NaCl (5 мл), сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного бензил (1-трет-бутил-3-{(1S,3R)-3-[(этилкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамата (3A, 2,0 г, 97%, >80% чистота по LCMS) в виде бесцветного масла. MS: 429 [M+H]+, 451 [M+Na]+.
Неочищенный бензил (1-трет-бутил-3-{(1S,3R)-3-[(этилкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамат (3A, 2,0 г, 4,7 ммоль) растворяли в этилацетате (30 мл) и THF (10 мл), раствор дегазировали, и добавляли катализатор 10%Pd/C (влажный, 200 мг). Суспензию перемешивали под водородным баллоном при комнатной температуре (10°C) в течение 2 часов. Катализатор удаляли фильтрацией, фильтрат концентрировали досуха, и остаток очищали с помощью хроматографии на силикагеле (элюирование 0-60% этилацетатом в петролейном эфире) с получением (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил этилкарбамата (3B, 1,15 г, 84%) в виде светло-желтой камеди, которая затвердевает при стоянии до светло-желтого твердого вещества. MS: 295 [M+H]+. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=5,43 (с, 1H), 5,13 (шир.с, 1H), 4,58 (шир.с, 1H), 3,50 (шир.с, 2H), 3,31-3,13 (м, 2H), 2,99 (квин, J=8,5 Гц, 1H), 2,53-2,39 (м, 1H), 2,04-1,96 (м, 1H), 1,95-1,87 (м, 1H), 1,87-1,68 (м, 3H), 1,62 (с, 9H), 1,14 (т, J=7,2 Гц, 3H). Хиральная чистота: >98% ee с помощью хиральной аналитической SFC.
Добавляли пропилфосфоновый ангидрид (T3P®, 50% масс. раствор в EtOAc, 0,485 мл, 0,815 ммоль) раствору комнатной температуры (10°C) (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил этилкарбамата (3B, 80,0 мг, 0,272 ммоль), 2-(1-метил-1H-индазол-5-ил)уксусной кислоты (CAS# 1176749-66-8, 59,1 мг, 0,311 ммоль), и диизопропилэтиламина (0,142 мл, 0,815 ммоль) в дихлорметане (5 мл). Смесь перемешивали в течение 3 часов, затем разделяли между дихлорметаном (5 мл) и водой (3 мл). Органический слой промывали насыщ. водн. Na2CO3 (2×3 мл), насыщ. водн. NH4Cl (2×3 мл), водой (2 мл), и насыщ. водн. NaCl (2 мл), затем сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного (1R,3S)-3-(1-трет-бутил-5-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил этилкарбамата (3C, 127 мг, 100% неочищенный) в виде светло-желтой камеди. MS: 489 [M+Na]+.
Раствор неочищенного (1R,3S)-3-(1-трет-бутил-5-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил этилкарбамата (3C, 127 мг, 0,272 ммоль) в муравьиной кислоте (6 мл) нагревали до 75°C в течение 18 часов. Реакционную смесь концентрировали досуха, затем очищали с помощью препаративной ВЭЖХ на колонке DuraShell 150*25 мм*5 мкм, элюируя 24-44% водой (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации фракций, содержащих продукт, (1R,3S)-3-(3-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил этилкарбамат (пример 3, 52,39 мг, 47%) получали в виде белого твердого вещества. MS: 411 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,05 (шир.с, 1H), 10,51 (с, 1H), 8,06-7,95 (м, 1H), 7,64 (с, 1H), 7,56 (д, J=8,5 Гц, 1H), 7,35 (дд, J=1,4, 8,7 Гц, 1H), 7,02 (шир.т, J=5,5 Гц, 1H), 6,27 (шир.с, 1H), 4,97 (шир.с, 1H), 4,04-3,95 (м, 3H), 3,66 (с, 2H), 3,10-2,85 (м, 3H), 2,43 (тд, J=6,9, 14,0 Гц, 1H), 2,04-1,92 (м, 1H), 1,91-1,80 (м, 1H), 1,74-1,49 (м, 3H), 0,97 (т, J=7,2 Гц, 3H). Хиральная чистота: 99% ee с помощью хиральной аналитической SFC.
Пример 4: (1R,3S)-3-(3-{[(1-метил-1H-1,2,3-триазол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
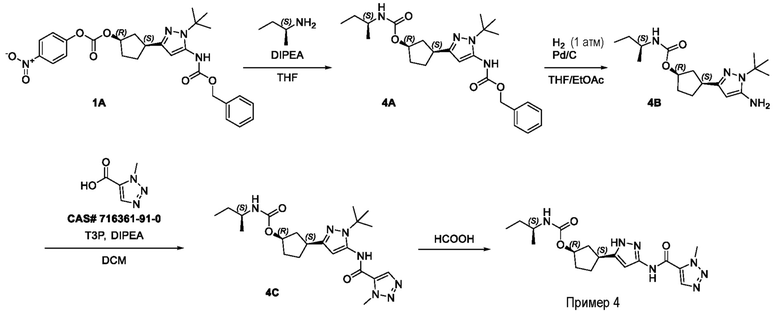
Раствор (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 22,0 г, 42,1 ммоль), (S)-(+)-втор-бутиламина (4,00 г, 54,7 ммоль), и диизопропилэтиламина (36,7 мл, 211 ммоль) в THF (300 мл) перемешивали при 10°C в течение 16 часов. Смесь концентрировали досуха, и остаток разбавляли этилацетатом (500 мл). Раствор промывали 1M вод. NaOH (4×200 мл) и насыщ. водн. NaCl (100 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного бензил {3-[(1S,3R)-3-{[(2S)-бутан-2-илкарбамоил]окси}циклопентил]-1-трет-бутил-1H-пиразол-5-ил}карбамата (4A, 18 г, 94%, ~80% чистота по LCMS). MS: 479 [M+Na]+.
Раствор комнатной температуры (10°C) неочищенного бензил {3-[(1S,3R)-3-{[(2S)-бутан-2-илкарбамоил]окси}циклопентил]-1-трет-бутил-1H-пиразол-5-ил}карбамата (4A, 18 г, 39 ммоль) в этилацетате (200 мл) и THF (100 мл) дегазировали и обрабатывали катализатором Pd/C (влажный, 5 г). Суспензию перемешивали под водородным баллоном в течение 16 часов. Смесь фильтровали для удаления катализатора, фильтрат концентрировали досуха. Для очистки эту партию объединяли со второй партией неочищенной, полученной тем же способом из 20 г 4A (всего для обеих партий: 38 г, 83 ммоль) и очищали с помощью препаративной ВЭЖХ на колонке Phenomenex Gemini C18 250*50 мм*10 мкм, элюируя 30-50% воды (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации, (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (2S)-бутан-2-илкарбамат (4B, 20,1 г, 75% для объединенных партий). MS: 323 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=6,86 (шир.д, J=8,3 Гц, 1H), 5,22 (с, 1H), 4,94 (шир.с, 1H), 4,82-4,49 (м, 2H), 3,46-3,36 (м, 1H), 2,90-2,71 (м, 1H), 2,38-2,24 (м, 1H), 1,91-1,75 (м, 2H), 1,74-1,53 (м, 3H), 1,52-1,46 (м, 9H), 1,43-1,27 (м, 2H), 1,01 (д, J=6,5 Гц, 3H), 0,81 (т, J=7,4 Гц, 3H). Оптическое вращение [α]D +4,0 (c 1,3, MeOH). Хиральная чистота: 98% de с помощью хиральной аналитической SFC.
Добавляли пропилфосфоновый ангидрид (T3P®, 50% масс. раствор в EtOAc, 592 мг, 0,93 ммоль) к охлажденному (0°C) раствору (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (2S)-бутан-2-илкарбамата (4B, 100 мг, 0,310 ммоль), 1-метил-1H-1,2,3-триазол-5-карбоновой кислоты (CAS# 716361-91-0, 59,1 мг, 0,465 ммоль), и диизопропилэтиламина (120 мг, 0,93 ммоль) в дихлорметане (5 мл). Смесь перемешивали при 10°C в течение 18 часов, затем промывали насыщ. водн. Na2CO3 и насыщ. водн. NaCl, сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного (1R,3S)-3-(1-трет-бутил-5-{[(1-метил-1H-1,2,3-триазол-5-ил)карбонил]амино}-1H-пиразол-3-ил)циклопентил (2S)-бутан-2-илкарбамата (4C, 130 мг, 97%) в виде желтой камеди. MS: 432 [M+H]+,454 [M+Na]+.
Раствор неочищенного (1R,3S)-3-(1-трет-бутил-5-{[(1-метил-1H-1,2,3-триазол-5-ил)карбонил]амино}-1H-пиразол-3-ил)циклопентил (2S)-бутан-2-илкарбамата (4C, 130 мг, 0,301 ммоль) в муравьиной кислоте (3 мл) перемешивали при 75°C в течение 6 дней. Смесь концентрировали досуха, и остаток очищали с помощью препаративной ВЭЖХ на колонке DuraShell 150*25 мм*5 мкм, элюируя 10-51% воды (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации, (1R,3S)-3-(3-{[(1-метил-1H-1,2,3-триазол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат (пример 4, 27,67 мг, 24%) получали в виде бледно-желтого твердого вещества. MS: 376 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,32 (шир.с, 1H), 11,14 (с, 1H), 8,46 (с, 1H), 6,90 (шир.д, J=8,0 Гц, 1H), 6,45 (шир.с, 1H), 5,00 (шир.д, J=3,8 Гц, 1H), 4,25 (с, 3H), 3,36 (шир.с, 2H), 3,29-2,99 (м, 1H), 2,09-2,01 (м, 1H), 1,95-1,84 (м, 1H), 1,81-1,56 (м, 3H), 1,44-1,27 (м, 2H), 1,01 (шир.д, J=6,5 Гц, 3H), 0,80 (шир.т, J=7,4 Гц, 3H). Хиральная чистота: >98% de с помощью хиральной аналитической SFC.
Пример 5: (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат
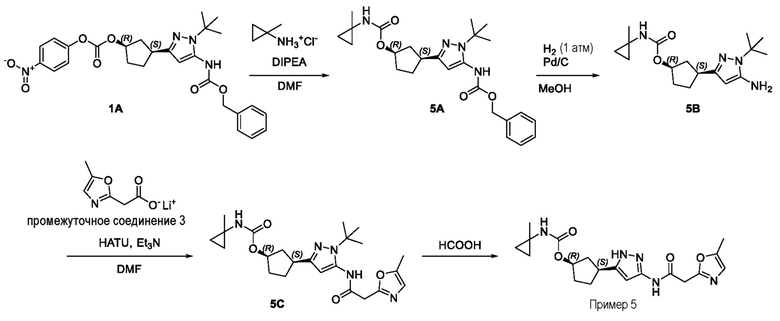
Раствор (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 9,50 г, 18,2 ммоль), 1-метилциклопропанамин гидрохлорида (2,93 г, 27,2 ммоль), и диизопропилэтиламина (10,0 мл, 58,2 ммоль) в DMF (80 мл) перемешивали при 60°C в течение 2 часов. После охлаждения до комнатной температуры, смесь разделяли между этилацетатом (300 мл) и водой (300 мл). Органический слой промывали водой (2×300 мл), 2M вод. Na2CO3 (300 мл), и насыщ. водн. NaCl (300 мл), затем сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 0-100% этилацетатом в гептане) с получением бензил {1-трет-бутил-3-[(1S,3R)-3-{[(1-метилциклопропил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамата (5A, 6,28 г, 76%) в виде твердого вещества. MS: 455 [M+H]+. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=7,45-7,30 (м, 5H), 6,30 (шир.с, 1H), 6,10 (шир.с, 1H), 5,20 (с, 2H), 5,15 (шир.с, 1H), 5,06 (шир.с, 1H), 3,08 (квин, J=8,3 Гц, 1H), 2,44 (шир.с, 1H), 2,12-1,97 (м, 1H), 1,96-1,75 (м, 4H), 1,58 (с, 9H), 1,35 (шир.с, 3H), 0,74 (шир.с, 2H), 0,58 (шир.с, 2H).
Смесь бензил {1-трет-бутил-3-[(1S,3R)-3-{[(1-метилциклопропил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамата (5A, 6,28 г, 13,8 ммоль) и 10%Pd/C (620 мг) в метаноле (200 мл) перемешивали при комнатной температуре (20°C) под водородным баллоном в течение 18 часов. Суспензию фильтровали через подушку из целита для удаления катализатора. Колбу и фильтрующую прокладку промывали дополнительным количеством метанола, затем объединенные фильтраты концентрировали с получением (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (5B, 4,42 г, 100% неочищенный) в виде пенообразного твердого вещества. MS: 321 [M+H]+. 1H ЯМР (400 МГц, МЕТАНОЛ-d4) δ=5,06 (шир.с, 1H), 3,14-2,97 (м, 1H), 2,58-2,37 (м, 1H), 2,14-2,00 (м, 1H), 2,00-1,69 (м, 4H), 1,69-1,54 (м, 10H), 1,31 (с, 3H), 0,74-0,66 (м, 2H), 0,60- 0,53 (м, 2H).
Раствор (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (5B, 4,00 г, 12,5 ммоль), литий (5-метил-1,3-оксазол-2-ил)ацетата (промежуточное соединение 3, 3,52 г, 24,9 ммоль), 1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридиния 3-оксид гексафторфосфата (HATU, 14,2 г, 37,3 ммоль), и триэтиламина (5,30 мл0, 38,0 ммоль) в DMF (100 мл) перемешивали при 60°C в течение 2 часов. После охлаждения до комнатной температуры, реакционную смесь разделяли между этилацетатом (200 мл) и водой (200 мл). Органическую фазу дополнительно промывали водой (2×200 мл) и насыщ. водн. NaCl (200 мл). Объединенные водные слои экстрагировали этилацетатом (200 мл). Объединенные органические экстракты сушили над сульфатом натрия, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 10-100% этилацетатом в гептане) с получением неочищенного продукта (5,50 г твердого вещества). Это неочищенное вещество повторно очищали с помощью хроматографии на силикагеле (элюирование 100% этилацетат) с получением чистого (1R,3S)-3-(1-трет-бутил-5-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (5C, 4,22 г, 76%) в виде твердого вещества. MS: 444 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=9,78 (с, 1H), 7,32 (шир.с, 1H), 6,78 (д, J=1,1 Гц, 1H), 5,93 (с, 1H), 4,97 (шир.с, 1H), 3,83 (с, 2H), 3,03-2,88 (м, 1H), 2,42-2,30 (м, 1H), 2,27 (д, J=1,1 Гц, 3H), 1,98-1,88 (м, 1H), 1,87-1,77 (м, 1H), 1,73-1,58 (м, 3H), 1,49 (с, 9H), 1,23 (с, 3H), 0,63-0,56 (м, 2H), 0,50-0,44 (м, 2H).
Раствор (1R,3S)-3-(1-трет-бутил-5-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (5C, 4,20 г, 9,47 ммоль) в муравьиной кислоте (50 мл) перемешивали при 100°C в течение 1 часа. После охлаждения до комнатной температуры реакционную смесь концентрировали для удаления большей части муравьиной кислоты. Остаток разделяли между этилацетатом (200 мл) и бикарбонатом натрия (200 мл). Водный слой экстрагировали снова этилацетатом (200 мл). Объединенные органические экстракты сушили над сульфатом натрия, фильтровали, и концентрировали досуха. Твердый остаток дважды растирали с этиловым эфиром (30 мл) с получением (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата (пример 5, 1,93 г, 53%) в виде твердого вещества. MS: 388 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,08 (шир.с, 1H), 10,59 (шир.с, 1H), 7,32 (шир.с, 1H), 6,74 (д, J=1,0 Гц, 1H), 6,27 (шир.с, 1H), 4,97 (шир.с, 1H), 3,79 (с, 2H), 3,14-2,93 (м, 1H), 2,44 (дд, J=14,1, 7,0 Гц, 1H), 2,26 (д, J=0,7 Гц, 3H), 1,99 (т, J=3,4 Гц, 1H), 1,93-1,81 (м, 1H), 1,68 (д, J=8,2 Гц, 2H), 1,60-1,46 (м, 1H), 1,22 (с, 3H), 0,58 (шир.с, 2H), 0,49- 0,42 (м, 2H).
Пример 6: (1R,3S)-3-(3-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат
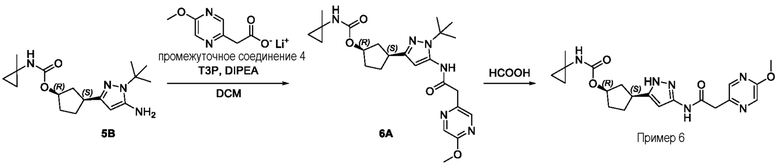
Раствор (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (5B, 150,0 мг, 0,468 ммоль), литий (5-метоксипиразин-2-ил)ацетата (промежуточное соединение 4, 118 мг, 0,702 ммоль), диизопропилэтиламина (182 мг, 1,40 ммоль), и пропилфосфонового ангидрида (T3P®, 50% масс. раствор в EtOAc, 447 мг, 0,702 ммоль) в дихлорметане (10,0 мл) перемешивали при 40°C в течение 30 часов. Реакцию гасили насыщ. водн. NaHCO3 (8 мл) и экстрагировали дихлорметаном (3×8 мл). Объединенные органические экстракты промывали насыщ. водн. NaCl (15 мл), концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 50% этилацетатом в петролейном эфире) с получением (1R,3S)-3-(1-трет-бутил-5-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (6A, 100 мг, 45%, 81% чистота по LCMS) в виде светло-желтой камеди. MS: 471 [M+H]+.
(1R,3S)-3-(1-трет-бутил-5-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамат (6A, 100 мг, 0,213 ммоль) растворяли в муравьиной кислоте (5 мл) и перемешивали при 75°C в течение 16 часов. Раствор концентрировали под вакуумом и остаток очищали с помощью препаративной ВЭЖХ на колонке DuraShell 150*25 мм*5 мкм, элюируя 26-46% воды (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации, (1R,3S)-3-(3-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат (пример 6, 15,55 мг, 18%) получали в виде белого твердого вещества. MS: 415 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,07 (шир.с, 1H), 10,54 (с, 1H), 8,23 (д, J=1,3 Гц, 1H), 8,16 (с, 1H), 7,35 (шир.с, 1H), 6,26 (шир.с, 1H), 4,96 (шир.с, 1H), 3,89 (с, 3H), 3,77 (с, 2H), 3,02 (шир.д, J=8,5 Гц, 1H), 2,47-2,39 (м, 1H), 1,97 (шир.д, J=9,3 Гц, 1H), 1,90-1,80 (м, 1H), 1,72-1,59 (м, 2H), 1,58-1,45 (м, 1H), 1,21 (с, 3H), 0,57 (шир.с, 2H), 0,48-0,40 (м, 2H). Хиральная чистота: 99% ee с помощью хиральной аналитической SFC.
Пример 7: (1R,3S)-3-(3-{[(5-метил-1,2-оксазол-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат
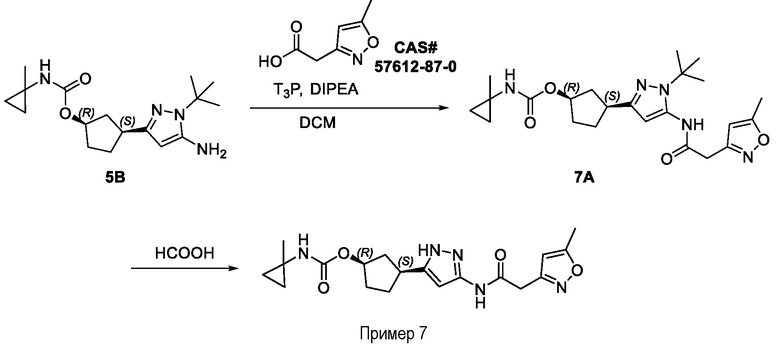
Раствор (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (5B, 78 мг, 0,24 ммоль), (5-метил-1,2-оксазол-3-ил)уксусной кислоты (CAS#57612-87-0, 51,5 мг, 0,365 ммоль), диизопропилэтиламина (0,130 мл, 0,730 ммоль), и пропилфосфонового ангидрида (T3P®, 50% масс. раствор в EtOAc, 0,435 мл, 0,730 ммоль) в дихлорметане (5,0 мл) перемешивали при 30-35°C в течение 18 часов. Раствор промывали насыщ. водн. NaHCO3 (5 мл) и насыщ. водн. NaCl (5 мл), сушили, фильтровали, и концентрировали, с получением неочищенного (1R,3S)-3-(1-трет-бутил-5-{[(5-метил-1,2-оксазол-3-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (7A, 95 мг, 88%) в виде камеди. MS: 444 [M+H]+.
Неочищенный (1R,3S)-3-(1-трет-бутил-5-{[(5-метил-1,2-оксазол-3-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамат (7A, 95 мг, 0,21 ммоль) растворяли в муравьиной кислоте (5,0 мл) и нагревали до 75°C в течение 15 часов. Образец концентрировали досуха, остаток растворяли в этилацетате (30 мл), промывали насыщ. водн. NaHCO3 (10 мл), сушили, фильтровали, и концентрировали. Неочищенный продукт очищали с помощью препаративной ВЭЖХ на колонке Agela Durashell C18 150*25 мм 5 мк, элюируя 18-58% воды (с 0,05% гидроксид аммония) в ацетонитриле, с получением (1R,3S)-3-(3-{[(5-метил-1,2-оксазол-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата (пример 7, 39,71 мг, 50%) в виде твердого вещества бежевого цвета. MS: 388 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,08 (шир.с, 1H), 10,59 (с, 1H), 7,34 (шир.с, 1H), 6,36-6,03 (м, 2H), 4,97 (шир.с, 1H), 3,64 (с, 2H), 3,15-2,87 (м, 1H), 2,46-2,40 (м, 1H), 2,37 (с, 3H), 1,98 (шир.д, J=9,0 Гц, 1H), 1,90-1,81 (м, 1H), 1,77-1,59 (м, 2H), 1,54 (шир.д, J=8,0 Гц, 1H), 1,22 (с, 3H), 0,58 (шир.с, 2H), 0,49-0,43 (м, 2H). Хиральная чистота: >99% ee с помощью хиральной аналитической SFC.
Пример 8: (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (1-метилциклопропил)карбамат
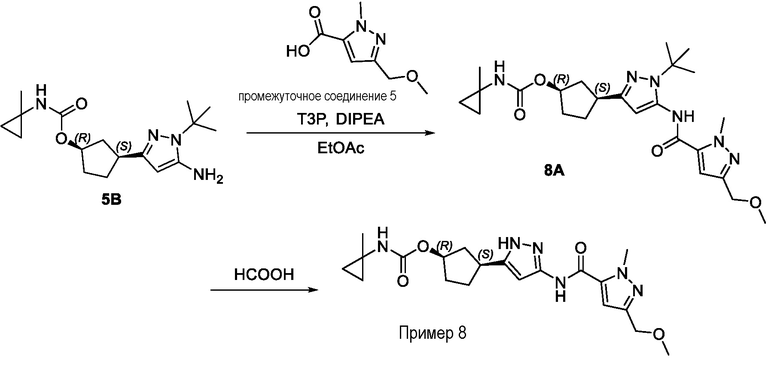
Раствор (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (5B, 5,47 г, 17,1 ммоль) и 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоновой кислоты (промежуточное соединение 5, 4,36 г, 25,6 ммоль) в этилацетате (80 мл) обрабатывали диизопропилэтиламином (9,00 мл, 52,4 ммоль) и пропилфосфоновым ангидридом (T3P®, 50% масс. раствор в EtOAc, 10,9 г, 10,0 мл, 31,4 ммоль) и перемешивали при комнатной температуре в течение ночи. Поскольку LCMS показала, что реакция не завершилась, смесь нагревали до 50°C в течение 3 часов, но LCMS по-прежнему показывала неполное превращение. После охлаждения до комнатной температуры, раствор разделяли между этилацетатом (100 мл) и деионизированной водой (200 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали. Остаток растворяли в этилацетате (80 мл). Дополнительно добавляли 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоновую кислоту (промежуточное соединение 5, 2,90 г, 17,1 ммоль), диизопропилэтиламин (9,00 мл, 52,4 ммоль), и T3P (10,0 мл, 33,6 ммоль), и реакционную смесь перемешивали при комнатной температуре в течение 4 часов. Раствор разбавляли этилацетатом (100 мл); промывали водой (200 мл), насыщ. водн. NaHCO3 (200 мл) и насыщ. водн. NaCl (200 мл); сушили над сульфатом натрия, фильтровали, и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (элюирование градиентом 0-100% этилацетатом в гептане), с получением (1R,3S)-3-[1-трет-бутил-5-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-3-ил]циклопентил (1-метилциклопропил)карбамата (8A, 4,83 г, 60%) в виде пенообразного твердого вещества. MS: 473 [M+H]+. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=7,71 (шир.с, 1 H), 6,68 (шир.с, 1 H), 6,23 (шир.с, 1 H), 5,12 (шир.с, 2 H), 4,47 (с, 2 H), 4,18 (с, 3 H), 3,43 (с, 3 H), 3,03-3,16 (м, 1 H), 2,41 (шир.с, 1 H), 1,97-2,11 (м, 1 H), 1,87 (м, J=5,9 Гц, 4 H), 1,63 (с, 9 H), 1,33 (с, 3 H), 0,73 (шир.с, 2 H), 0,52-0,61 (м, 2 H).
Раствор (1R,3S)-3-[1-трет-бутил-5-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-3-ил]циклопентил (1-метилциклопропил)карбамата (8A, 4,77 г, 10,1 ммоль) в муравьиной кислоте (50 мл) перемешивали при 100°C в течение 2 часов. После охлаждения до комнатной температуры, большую часть муравьиной кислоты удаляли под вакуумом, и остаток разделяли между этилацетатом (200 мл) и насыщ. водн. NaHCO3 (200 мл). Водный слой экстрагировали этилацетатом (200 мл). Объединенные органические экстракты сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 0-10% метанол в этилацетате) с получением белого твердого вещества (3,15 г). Это твердое вещество рекристаллизовывали из этилацетата/гептана с получением (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (1-метилциклопропил)карбамата (пример 8, 2,90 г, 69%) в виде твердого кристаллического вещества. MS: 417 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,20 (шир.с, 1 H), 10,69 (с, 1 H), 7,33 (шир.с, 1 H), 7,11 (с, 1 H), 6,41 (шир.с, 1 H), 4,99 (шир.с, 1 H), 4,33 (с, 2 H), 4,05 (с, 3 H), 3,27 (с, 3 H), 3,00-3,13 (м, 1 H), 2,41-2,49 (м, 1 H), 1,97-2,10 (м, 1 H), 1,83-1,95 (м, 1 H), 1,72 (шир.с, 2 H), 1,59 (шир.с, 1 H), 1,24 (с, 3 H), 0,60 (шир.с, 2 H), 0,47 (шир.с, 2 H)
Пример 9: (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Пример 10: (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
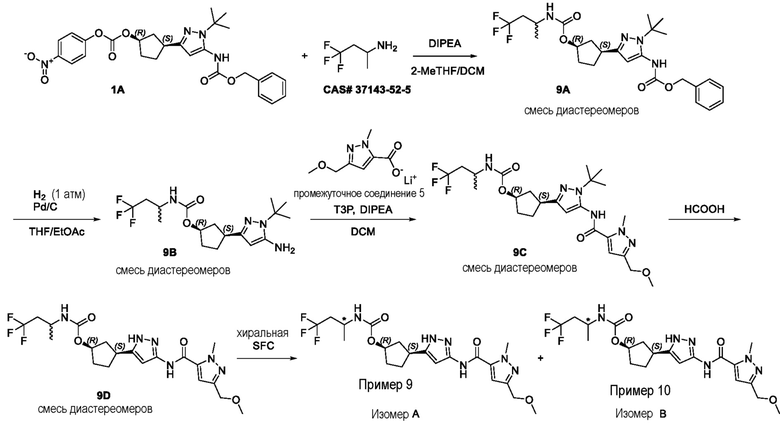
Раствор (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 2,5 г, 4,8 ммоль), 4,4,4-трифторбутан-2-амина (CAS# 37143-52-5, 900 мг, 5,5 ммоль), и диизопропилэтиламинома (4,17 мл, 23,9 ммоль) в 2-метилтетрагидрофуране (40 мл) и дихлорметане (20 мл) перемешивали при 40-50°C в течение 15 часов. Растворители удаляли под вакуумом, и остаток разделяли между этилацетатом (150 мл) и 1н вод. гидроксидом натрия (2×50 м). Органический слой промывали насыщ. водн. NaCl (60 мл), сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 15-30% этилацетатом в петролейном эфире), с получением бензил {1-трет-бутил-3-[(1S,3R)-3-{[(4,4,4-трифторбутан-2-ил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамата (9A, смесь диастереомеров, 2,0 г, 82%, 79% чистота по LCMS), в виде желтого масла. MS: 511 [M+H]+.
Бензил {1-трет-бутил-3-[(1S,3R)-3-{[(4,4,4-трифторбутан-2-ил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамат смесь (9A, 2,0 г, 3,9 ммоль) растворяли в этилацетате (20 мл) и THF (20 мл), и добавляли катализатор 10% Pd/C (50% влажный, 650 мг). Суспензию дегазировали, заполняли водородом из баллона и перемешивали при 20-25°C под водородным баллоном в течение 16 часов. Катализатор удаляли фильтрацией, и фильтровали концентрировали с получением неочищенного (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (4,4,4-трифторбутан-2-ил)карбамата (9B, смесь диастереомеров, 1,4 г, 95%, 76% чистота по LCMS) в виде желтого масла. MS: 377 [M+H]+.
Охлажденный (0°C) раствор неочищенного (1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил (4,4,4-трифторбутан-2-ил)карбамата (9B, 225 мг, 0,598 ммоль), 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксилата (промежуточное соединение 5, 173 мг, 0,897 ммоль), и диизопропилэтиламина (232 мг, 1,79 ммоль) в дихлорметане (10 мл) обрабатывали пропилфосфоновым ангидридом (T3P®, 50% масс. раствор в EtOAc, 1,14 г, 1,79 ммоль). Смесь нагревали до 20°C и перемешивали в течение 36 часов, затем нагревали до 40°C в течение 90 часов. Смесь разделяли между дихлорметаном и полунасыщенным Na2CO3. Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного (1R,3S)-3-[1-трет-бутил-5-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-3-ил]циклопентил (4,4,4-трифторбутан-2-ил)карбамата (9C, смесь диастереомеров, 300 мг, 95%) в виде желтой камеди. MS: 529 [M+H]+.
Раствор неочищенного (1R,3S)-3-[1-трет-бутил-5-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-3-ил]циклопентил (4,4,4-трифторбутан-2-ил)карбамата (9C, 300 мг, 0,57 ммоль) в муравьиной кислоте (10 мл) перемешивали при 80°C в течение 2 часов. Смесь концентрировали досуха и остаток очищали с помощью препаративной ВЭЖХ на колонке DuraShell 150*25 мм*5 мкм, элюируя 32% водой (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации, (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (4,4,4-трифторбутан-2-ил)карбамат (9D, смесь диастереомеров, 45 мг, 17%) получали в виде белого твердого вещества. MS: 473 [M+H]+.
Смесь диастереомеров 9D разделяли с помощью хиральной препаративной SFC на колонке Phenomenex-Amylose-1 250 мм*30 мм 5 мкм, элюируя 40% этанол (+0,1%NH3H2O) в CO2, получая пример 9 (пик 1, 12,26 мг, 27%, 99% de) и пример 10 (пик 2, 11,53 мг, 26%, 98% de) в виде белых твердых веществ. Абсолютная стереохимия хирального центра в 4,4,4-трифторбутан-2-ил]карбамате каждой молекулы не определялась.
Пример 9: (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A. 1H ЯМР (400 МГц, DMSO-d6) δ=12,25 (шир.с, 1H), 10,74 (с, 1H), 7,22 (шир.д, J=8,4 Гц, 1H), 7,12 (с, 1H), 6,43 (шир.с, 1H), 5,10-4,96 (м, 1H), 4,34 (с, 2H), 4,05 (с, 3H), 3,92-3,79 (м, 1H), 3,27 (с, 3H), 3,17-3,03 (м, 1H), 2,46 (шир.д, J=6,1 Гц, 1H), 2,43-2,31 (м, 2H), 2,12-1,85 (м, 2H), 1,80-1,57 (м, 3H), 1,13 (д, J=6,7 Гц, 3H). 19F ЯМР (377МГц, DMSO-d6) δ=-62,57 (с, 3F). MS: 473 [M+H]+. Оптическое вращение: [α]D -2 (c 0,1, MeOH). Хиральная чистота: 99% de. Хиральный SFC/MS-анализ выполняли на колонке Chiralpak AD-3 (150×4,6 мм I.D., 3 мкм), элюируя 40% этанолом (+0,05% DEA) в CO2, протекающей при 2,5 мл/мин, при 35°C, с давлением, установленным на 1500 фунтов на квадратный дюйм. В этих условиях время удерживания этого пика составляло 3,372 минут.
Пример 10: (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B. 1H ЯМР (400 МГц, DMSO-d6) δ=12,25 (шир.с, 1H), 10,74 (с, 1H), 7,24 (шир.д, J=8,3 Гц, 1H), 7,12 (с, 1H), 6,42 (шир.с, 1H), 5,16-4,91 (м, 1H), 4,34 (с, 2H), 4,05 (с, 3H), 3,84 (тд, J=7,0, 13,8 Гц, 1H), 3,27 (с, 3H), 3,16-3,01 (м, 1H), 2,50-2,46 (м, 1H), 2,45-2,29 (м, 2H), 2,12-1,99 (м, 1H), 1,95-1,85 (м, 1H), 1,80-1,53 (м, 3H), 1,13 (д, J=6,7 Гц, 3H). 19F ЯМР (377МГц, DMSO-d6) δ=-62,56 (с, 3F). MS: 473 [M+H]+. Оптическое вращение: [α]D +10 (c 0,1, MeOH). Хиральная чистота: 98% de. Хиральный SFC/MS-анализ выполняли на колонке Chiralpak AD-3 (150×4,6 мм I.D., 3 мкм), элюирование 40% этанол (+0,05% DEA) в CO2, протекающей при 2,5 мл/мин, при 35°C, с давлением, установленным на 1500 фунтов на квадратный дюйм. В этих условиях время удерживания этого пика составляло 4,123 минут.
Способ B
Пример 11: (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат.
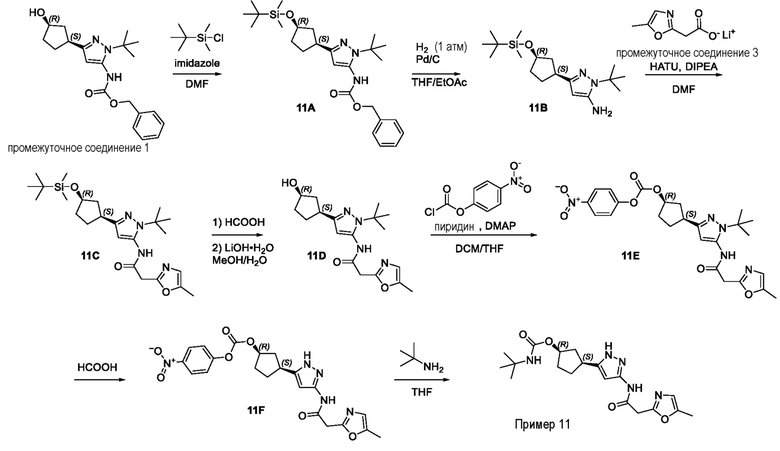
Бензил {1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}карбамат (промежуточное соединение 1, 20 г, 56 ммоль) и имидазол (5,71 г, 83,9 ммоль) растворяли в DMF (200 мл) с помощью ультразвуковой обработки. Пока раствор находился при комнатной температуре, порциями добавляли трет-бутилдиметилсилилхлорид (11,0 г, 72,7 ммоль). После завершения добавления прозрачный раствор перемешивали при 25°C в течение 1 часа. Растворители удаляли под вакуумом и остаток разделяли между этилацетатом (500 мл) и насыщ. водн. NaCl (200 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного бензил {1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-ил}карбамата (11A, 26 г, 99%) в виде бесцветного масла. MS: 472 [M+H]+.
Неочищенный бензил {1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-ил}карбамат (11A, 26 г, 55 ммоль) растворяли в этилацетате (100 мл) и THF (100 мл). Добавляли Pd/C (50% влажный, 4 г), дегазировали раствор, и перемешивали при 25°C под водородным баллоном в течение 2 часов. Смесь затем фильтровали, и фильтрат концентрировали под вакуумом с получением неочищенного 1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-амина (11B, 19 г, >99%) в виде светло-желтого масла. MS: 338 [M+H]+.
К раствору комнатной температуры (25°C) неочищенного 1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-амина (11B, 5,00 г, 14,8 ммоль), литий (5-метил-1,3-оксазол-2-ил)ацетата (промежуточное соединение 3, 3,14 г, 21,3 ммоль) и диизопропилэтиламина (5,74 г, 44,4 ммоль) в DMF (150 мл) добавляли 1-[бис(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридиния 3-оксид гексафторфосфат (HATU, 8,45 г, 22,2 ммоль). Смесь нагревали до 40°C в течение 1 часа, затем разбавляли этилацетатом (300 мл) и промывают последовательно водой (150 мл) и насыщ. водн. NaCl. Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (элюирование 30% этилацетатом в петролейном эфире) с получением N-{1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-ил}-2-(5-метил-1,3-оксазол-2-ил)ацетамида (11C, 5,5 г, 81%, 77% чистота по LCMS) в виде желтого масла. MS: 461 [M+H]+.
Раствор N-{1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}-циклопентил]-1H-пиразол-5-ил}-2-(5-метил-1,3-оксазол-2-ил)ацетамида (11C, 5,5 г, 11,9 ммоль) в муравьиной кислоте (50 мл) перемешивали при 25°C в течение 14 часов. Раствор концентрировали досуха и светло-желтый маслянистый остаток растворяли в метаноле (20 мл). К этому добавляли раствор моногидрата гидроксида лития (2,50 г, 59,7 ммоль) в воде (10 мл), и смесь перемешивали в течение 30 минут при 25°C. Раствор концентрировали досуха. Остаток растворяли в дихлорметане (30 мл), промывали водой (10 мл) и насыщ. водн. NaCl (10 мл), сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 3% метанолом в дихлорметане) с получением N-{1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}-2-(5-метил-1,3-оксазол-2-ил)ацетамида (11D, 3,8 г, 92%, 79% чистота по LCMS) в виде светло-желтого масла. MS: 347 [M+H]+.
Суспензию N-{1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}-2-(5-метил-1,3-оксазол-2-ил)ацетамида (11D, 3,8 г, 11 ммоль), DMAP (134 мг, 1,10 ммоль), пиридина (2,60 г, 32,9 ммоль) и 4-нитрофенилхлорформиата (4,42 г, 21,9 ммоль) в дихлорметане (40 мл) и THF (40 мл) перемешивали при 25°C в течение 2 часов. Растворители удаляли под вакуумом. Остаток растворяли в этилацетате (200 мл), промывали насыщ. водн. NH4Cl (100 мл) и насыщ. водн. NaCl, сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 50% этилацетатом в петролейном эфире) с получением (1R,3S)-3-(1-трет-бутил-5-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (11E, 5,0 г, 89%, 89% чистота по LCMS) в виде желтого масла. MS: 512 [M+H]+.
Раствор (1R,3S)-3-(1-трет-бутил-5-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (11E, 5,0 г, 9,8 ммоль) в муравьиной кислоте (30 мл) перемешивали при 75°C в течение 16 часов. Смесь концентрировали для удаления большей части муравьиной кислоты, затем остаток растворяли в дихлорметане (30 мл) и промывали насыщ. водн. NaHCO3 (2×15 мл), водой (15 мл), и насыщ. водн. NaCl (15 мл). Органический слой сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 80% этилацетатом в петролейном эфире) с получением (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 4-нитрофенилкарбоната (11F, 1,7 г, 38%) в виде светло-желтого твердого вещества. MS: 456 [M+H]+.
Раствор (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 4-нитрофенилкарбоната (11F, 4,00 г, 8,78 ммоль) и трет-бутиламина (6,42 г, 87,8 ммоль) в THF (30 мл) перемешивали при 25°C в течение 1 часа. Смесь концентрировали досуха, остаток растворяли в дихлорметане (80 мл), промывали 1M NaOH (2×20 мл) и насыщ. водн. NaCl (20 мл), сушили над сульфатом натрия, фильтровали, концентрировали и очищали с помощью хроматографии на силикагеле (элюирование 3% метанолом в дихлорметане с получением неочищенного (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамата (пример 11, 2,3 г, 67%, 73% чистота по ВЭЖХ). Вторую партию (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 4-нитрофенилкарбоната (11F, 1,50 г, 3,29 ммоль) растворяли в трет-бутиламине (10 мл) и перемешивали при 40°C в течение 1 часа. Эту реакционную смесь концентрировали досуха, и полученный таким образом неочищенный продукт объединяли с 2,3 г неочищенного продукта из первой партии, описанной выше, (всего 12,08 ммоль 11F израсходованной в обеих партиях) и дополнительно очищали с помощью препаративной ВЭЖХ на колонке Phenomenex Gemimi C18 250×50 мм, 10 мкм, элюируя 3-45% водой (+0,05%NH4OH) в ACN. Чистый (1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат (пример 11, 2,23 г, 47% для объединенных партий) получали в виде белого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=12,10 (с, 1H), 10,62 (с, 1H), 6,87-6,63 (м, 2H), 6,29 (д, J=1,8 Гц, 1H), 4,96 (шир.с, 1H), 3,79 (с, 2H), 3,03 (квин, J=8,6 Гц, 1H), 2,48-2,40 (м, 1H), 2,25 (д, J=1,1 Гц, 3H), 2,04-1,94 (м, 1H), 1,92-1,80 (м, 1H), 1,75-1,63 (м, 2H), 1,55 (шир.с, 1H), 1,19 (с, 9H). MS: 390 [M+H]+. Оптическое вращение [α]D +3,5 (c 0,8, MeOH). Хиральная чистота: 98% ee с помощью хиральной аналитической SFC.
Пример 12: (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилат
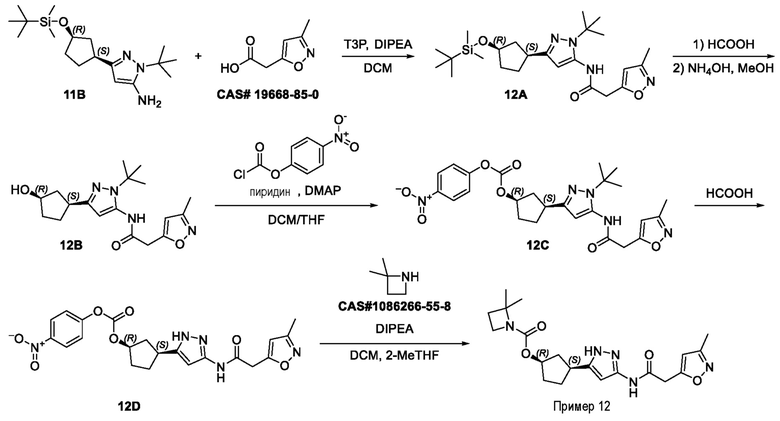
Добавляли пропилфосфоновый ангидрид (T3P®, 50% масс. раствор в EtOAc, 4,41 г, 6,93 ммоль) к охлажденному (0°C) раствору 1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-амина (11B, 780 мг, 2,31 ммоль), 3-метил-5-изоксазолуксусной кислоты (CAS# 19668-85-0, 489 мг, 3,47 ммоль) и диизопропилэтиламина (1,23 мл, 6,93 ммоль) в дихлорметане (10 мл). Смесь перемешивали при 30°C в течение 1 часа, затем разделяли между дихлорметаном и полунасыщенным Na2CO3. Органический слой промывали насыщ. водн. NaCl, сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 10-50% этилацетатом в петролейном эфире) с получением N-{1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-ил}-2-(3-метил-1,2-оксазол-5-ил)ацетамида (12A, 1,1 г) в виде бесцветного масла. MS: 461 [M+H]+.
Раствор N-{1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-ил}-2-(3-метил-1,2-оксазол-5-ил)ацетамида (12A, 1,1 г) в муравьиной кислоте (15 мл) перемешивали при 45°C в течение 1 часа, затем оставляли на ночь при комнатной температуре. Смесь концентрировали досуха, остаток растворяли в метаноле (30 мл) и водной NH4OH (10 мл), и раствор перемешивали при 20°C в течение 1 часа. Смесь концентрировали и очищали с помощью хроматографии на силикагеле (элюирование 1/10 метанол/дихлорметан) с получением N-{1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}-2-(3-метил-1,2-оксазол-5-ил)ацетамида (12B, 1,0 г) в виде светло-желтого масла. MS: 347 [M+H]+.
Раствор N-{1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}-2-(3-метил-1,2-оксазол-5-ил)ацетамида (12B, 1,0 г) в дихлорметане (30 мл) и THF (30 мл) обрабатывали DMAP (70,5 мг, 0,577 ммоль), пиридином (1,14 г, 14,4 ммоль), и 4-нитрофенилхлорформиатом (1,16 г, 5,77 ммоль). Полученную суспензию перемешивали при 20°C в течение 12 часов. Растворители удаляли под вакуумом, остаток растворяли в дихлорметане (30 мл), и раствор промывали последовательно насыщ. водн. NH4Cl (15 мл) и насыщ. водн. NaCl (15 мл). Органический слой сушили, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 50% этилацетатом в петролейном эфире) с получением (1R,3S)-3-(1-трет-бутил-5-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (12C, 1,3 г). MS: 512 [M+H]+.
Раствор (1R,3S)-3-(1-трет-бутил-5-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (12C, 1,3 г) в муравьиной кислоте (20 мл) нагревали до 75°C в течение 16 часов. Большую часть муравьиной кислоты удаляли под вакуумом, остаток растворяли в дихлорметане (30 мл), и раствор промывали последовательно насыщ. водн. NaHCO3 (2×15 мл), водой (15 мл), и насыщ. водн. NaCl (15 мл). Органический слой сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 80% этилацетатом в петролейном эфире) с получением (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 4-нитрофенилкарбоната (12D, 850 мг, 81% за 5 стадий на основе 11B) в виде белого твердого вещества. MS: 456 [M+H]+.
Раствор (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 4-нитрофенилкарбоната (12D, 60 мг, 0,13 ммоль), 2,2-диметилазетидина (CAS#1086266-55-8, 13,5 мг, 0,158 ммоль), и диизопропилэтиламина (102 мг, 0,79 ммоль) в дихлорметане (1 мл) и 2-метилтетрагидрофуране (1 мл) перемешивали при 15°C в течение 1 часа, затем концентрировали и остаток очищали с помощью препаративной ВЭЖХ (на колонке Xbridge 150*30 мм*10 мкм, элюируя 17-57% водой (0,05% гидроксид аммония об/об) в ацетонитриле). После лиофилизации, (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилат (пример 12, 28,21 мг, 53%) получали в виде белого твердого вещества. MS: 402 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,13 (шир.д, J=8,2 Гц, 1H), 10,62 (шир.с, 1H), 6,29 (с, 1H), 6,21 (с, 1H), 5,03-4,91 (м, 1H), 3,82 (с, 2H), 3,71 (шир.т, J=8,4 Гц, 1H), 3,64 (т, J=7,5 Гц, 1H), 3,12-3,01 (м, 1H), 2,41 (дт, J=6,7, 15,5 Гц, 1H), 2,19 (с, 3H), 2,04-1,97 (м, 1H), 1,96-1,89 (м, 2H), 1,87-1,79 (м, 1H), 1,77-1,57 (м, 3H), 1,37-1,27 (м, 6H). Хиральная чистота: 99% ee с помощью хиральной аналитической SFC.
Пример 13: (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат
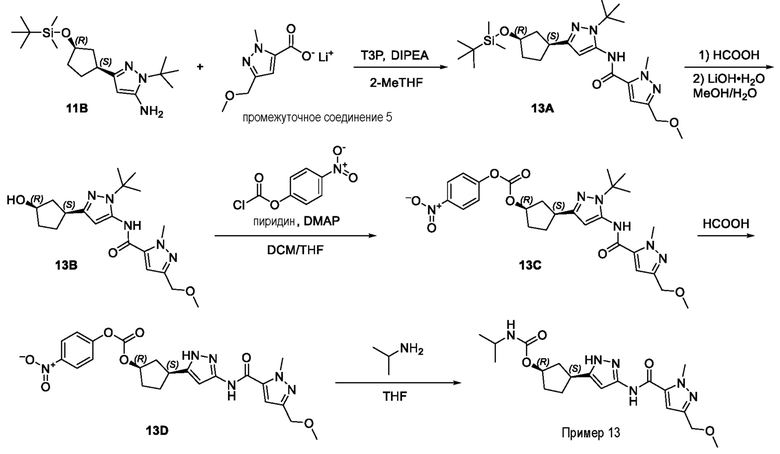
Добавляли пропилфосфоновый ангидрид (T3P®, 50% масс. раствор в EtOAc, 50,3 г, 79,1 ммоль) при комнатной температуре (26°C) раствор 1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-амина (11B, 8,90 г, 26,4 ммоль), литий 3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксилата (промежуточное соединение 5, 5,83 г, 34,3 ммоль), и диизопропилэтиламина (10,2 г, 79,1 ммоль) в 2-метилтетрагидрофуране (100,0 мл). Полученную смесь перемешивали при этой температуре в течение 18 часов. После концентрирования смеси досуха, остаток растворяли в дихлорметане (150 мл), и раствор промывали последовательно водой (2×30 мл), насыщ. водн. NaHCO3 (2×30 мл) и насыщ. водн. NaCl (30 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного N-{1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-ил}-3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксамида (13A, 12,9 г, 100%) в виде масла. MS: 490 [M+H]+.
Неочищенный N-{1-трет-бутил-3-[(1S,3R)-3-{[трет-бутил(диметил)силил]окси}циклопентил]-1H-пиразол-5-ил}-3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксамид (13A, 12,9 г, 26,3 ммоль) растворяли в муравьиной кислоте (80 мл) и перемешивали при комнатной температуре (27°C) в течение 30 минут. Смесь концентрировали досуха, и остаток растворяли в метаноле (80 мл). Добавляли раствор моногидрата гидроксида лития (3,43 г, 81,8 ммоль) в воде (15 мл), и смесь перемешивали при комнатной температуре (27°C) в течение 1 часа. Смесь концентрировали досуха, и остаток очищали с помощью хроматографии на силикагеле (элюирование 0-80% этилацетатом в петролейном эфире) с получением N-{1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}-3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксамида (13B, 8,0 г, 78%) в виде желтой камеди. MS: 376 [M+H]+.
Раствор N-{1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}-3-(метоксиметил)-1-метил-1H-пиразол-5-карбоксамида (13B, 8,0 г, 21 ммоль) в дихлорметане (80 мл) и THF (80 мл) обрабатывали DMAP (260 мг, 2,13 ммоль), пиридином (5,06 г, 63,9 ммоль), и 4-нитрофенилхлорформиатом (8,59 г, 42,6 ммоль). Полученную желтую суспензию перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь концентрировали досуха и очищали с помощью хроматографии на силикагеле (элюирование 0-45% этилацетатом в петролейном эфире) с получением (1R,3S)-3-[1-трет-бутил-5-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-3-ил]циклопентил 4-нитрофенилкарбоната (13C, 10,6 г, 92%) как светло-коричневой камеди. MS: 541 [M+H]+.
Раствор 1R,3S)-3-[1-трет-бутил-5-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-3-ил]циклопентил 4-нитрофенилкарбоната (13C, 10,6 г, 19,6 ммоль) в муравьиной кислоте (80 мл) перемешивали при 70°C в течение 18 часов. Раствор концентрировали досуха. Остаток растворяли в дихлорметане (150 мл) и раствор нейтрализовали насыщ. водн. NaHCO3. Органический слой промывали водой (30 мл) и насыщ. вод. NaCl (30 мл), сушили над карбонатом натрия, фильтровали, и концентрировали с получением неочищенного (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил 4-нитрофенилкарбоната (13D, 8,5 г, 90%, 86% чистота по LCMS) в виде светло-желтого стекла. MS: 485 [M+H]+.
Комнатной температуры (27°C) раствор неочищенного (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил 4-нитрофенилкарбоната (13D, 1,7 г, 3,5 ммоль) и 2-пропиламина (1,04 г, 17,5 ммоль) в THF (30 мл) перемешивали в течение 6 часов. Раствор концентрировали досуха, и остаток объединяли с остатком из второй партии, полученной из 1,7 г, 3,5 ммоль 13D (всего 6,27 ммоль 13D, израсходованных для двух объединенных партий) с получением 3,2 г неочищенного продукта. Продукт очищали с помощью препаративной ВЭЖХ на колонке Phenomenex Gemini C18 250*50мм*10 мкм, элюируя 15-45% водой (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации, (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат (пример 13, 2,06 г, 78%) получали в виде белого кристаллического твердого вещества, которое, как было установлено на основе элементного анализа, является моногидратом (форма 1). MS: 405 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,23 (шир.с, 1H), 10,73 (шир.с, 1H), 7,11 (с, 1H), 6,96 (шир.д, J=7,0 Гц, 1H), 6,41 (шир.с, 1H), 5,00 (шир.с, 1H), 4,33 (с, 2H), 4,04 (с, 3H), 3,57 (квд, J=6,6, 13,4 Гц, 1H), 3,26 (с, 3H), 3,17-2,96 (м, 1H), 2,48-2,39 (м, 1H), 2,03 (шир.д, J=6,8 Гц, 1H), 1,95-1,83 (м, 1H), 1,73 (шир.д, J=8,5 Гц, 2H), 1,61 (шир.с, 1H), 1,03 (шир.д, J=6,3 Гц, 6H). Оптическое вращение [α]D +4,8 (c 1,0, MeOH). Хиральная чистота: >99% ee с помощью хиральной аналитической SFC. Анал. Рассчитано для C19H28N6O4-H2O: C, 54,02; H, 7,16; N, 19,89. Найдено: C, 53,94; H, 7,22; N, 19,81. Белое кристаллическое твердое вещество, указанное выше (500 мг), рекристаллизовывали из 9: 1 H2O/CH3CN (2 мл) нагревая до растворения, а затем давая полученному раствору постоять при комнатной температуре в течение 18 ч. В течение 18 часов образовывались более крупные кристаллы моногидрата (Форма 1). Дифракция рентгеновских лучей на монокристалле выбранного кристалла из этого материала дала структуру, показанную на фиг. 1.
Кристаллическое твердое вещество, полученное выше в виде моногидрата (форма 1), дополнительно характеризовали с помощью порошковой рентгеновской дифракции (PXRD).
Инструментальная порошковая рентгеновская дифракция:
Анализ порошковой рентгеновской дифракцией проводили на дифрактометре Bruker AXS D8 Advance с источником излучения Cu. Дифрагированное излучение регистрировали детектором LYNXEYE_EX с моторизованными щелями. И первичный, и вторичный, снабжены 2,5-соллерными щелями. Напряжение и сила тока рентгеновской трубки были установлены на 40 кВ и 40 мА, соответственно. Данные собирали в гониометре Theta-Theta при сканировании заблокированной пары на длине волны Cu K-альфа от 3,0 до 40,0 градусов 2-тета с шагом 0,01 градуса, с использованием скорости сканирования 1,0 секунды за шаг. Образцы получали путем помещения в кремниевый низкофоновый образец. Данные собирали и анализировали с использованием программного обеспечения Bruker DIFFRAC Plus. Файл данных PXRD не обрабатывался до поиска пика. Алгоритм поиска пиков в программном обеспечении EVA был применен для предварительного назначения пиков с использованием порогового значения 1. Для обеспечения достоверности корректировки вносились вручную; результаты автоматических назначений были визуально проверены, и положения пиков были отрегулированы до максимума пика. Обычно выбирали пики с относительной интенсивностью ≥3%. Пики, которые не были разрешены или соответствовали шуму, не были выбраны. Типичная ошибка, связанная с положением пика PXRD, указанным в USP, составляет до +/- 0,2° 2-тета (USP-941).
PXRD-диаграмма моногидрата формы 1 примера 13 показана на фиг.2. Список пиков PXRD и данные относительной интенсивности для соединения примера 13, формы 1 моногидрата (2-тета°), представлены в таблице 1 ниже:
(%)
Пример 14: (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
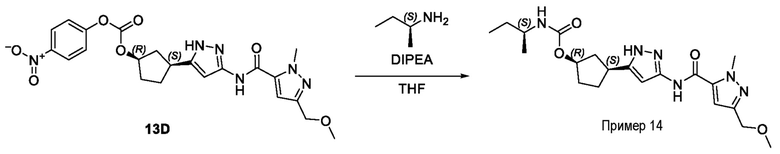
Раствор неочищенного (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил 4-нитрофенилкарбоната (13D, 5,5 г, 11 ммоль), (S)-(+)-втор-бутиламина (1,49 г, 13,6 ммоль), и диизопропилэтиламина (4,40 г, 34,1 ммоль) в THF (100 мл) перемешивали при комнатной температуре (30°C) в течение 18 часов. Реакционную смесь концентрировали досуха, и остаток очищали с помощью препаративной ВЭЖХ на колонке Phenomenex Gemini C18 250*50 мм*10 мкм, элюируя 25-45% водой (0,05% гидроксид аммония об/об) в ацетонитриле, с получением (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамата (пример 14, 3,50 г, 74%) в виде светло-желтого твердого вещества. MS: 419 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,23 (шир.с, 1H), 10,72 (с, 1H), 7,11 (с, 1H), 6,90 (шир.д, J=8,2 Гц, 1H), 6,42 (шир.с, 1H), 5,00 (шир.с, 1H), 4,33 (с, 2H), 4,04 (с, 3H), 3,43-3,37 (м, 1H), 3,26 (с, 3H), 3,14-2,98 (м, 1H), 2,45 (шир.с, 1H), 2,08-1,97 (м, 1H), 1,95-1,82 (м, 1H), 1,80-1,68 (м, 2H), 1,67-1,52 (м, 1H), 1,42-1,26 (м, 2H), 1,00 (д, J=6,5 Гц, 3H), 0,80 (т, J=7,4 Гц, 3H). Оптическое вращение [α]D +16,6 (c 2,05, MeOH). Хиральная чистота: >99% ee с помощью хиральной аналитической SFC.
Пример 15: (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат
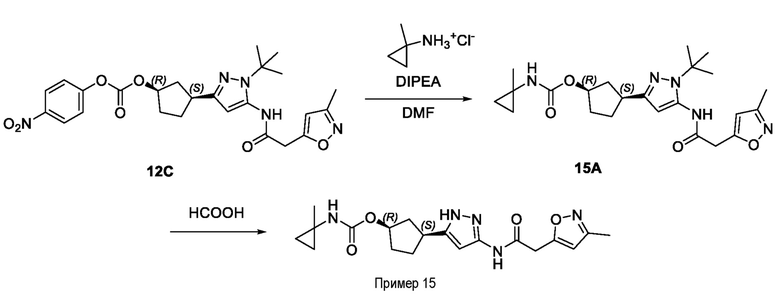
Раствор (1R,3S)-3-(1-трет-бутил-5-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (12C, 1,64 г, 3,2 ммоль) в DMF (10,7 мл) обрабатывали 1-метилциклопропан-1-амин гидрохлоридом (516 мг, 4,8 ммоль) и диизопропилэтиламином (1,7 мл, 9,6 ммоль). Смесь перемешивали в атмосфере азота в течение 2 часов при 60°C, затем при комнатной температуре в течение ночи. После разбавления этилацетатом (150 мл), раствор промывали деионизированной водой (20 мл), 2 M водн. Na2CO3 (20 мл), и насыщ. водн. NaCl (20 мл). Объединенные водные слои снова экстрагировали этилацетатом (30 мл). Объединенные органические экстракты сушили над сульфатом натрия, фильтровали, концентрировали и очищали с помощью хроматографии на силикагеле (элюирование 0-100% этилацетатом в гептане) с получением (1R,3S)-3-(1-трет-бутил-5-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (15A, 1,58 г, 82%) в виде масла.
Раствор 1R,3S)-3-(1-трет-бутил-5-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-3-ил)циклопентил (1-метилциклопропил)карбамата (15A, 1,50 г, 3,4 ммоль) в муравьиной кислоте (10 мл) нагревали на масляной бане при 100°C в течение 1 часа. Большую часть муравьиной кислоты удаляли под вакуумом. Остаток обрабатывали насыщ. водн. NaHCO3 (30 мл), затем экстрагировали этилацетатом (150 мл, затем 50 мл). Объединенные органические слои сушили над сульфатом магния, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 0-40% изопропанола в гептане) с получением белого твердого вещества (960 мг). Это твердое вещество растворяли в ацетонитриле (20 мл) и воде (10 мл), и раствор лиофилизировали в течение ночи с получением белого твердого вещества (796 мг). Лиофилизированный материал суспендировали в этилацетате (28 мл), перемешивали на масляной бане при 60°C в течение 1 часа, и давали остыть до комнатной температуры при перемешивании еще 3 часа. Твердое вещество собирали фильтрацией и сушили (50°C, 10 mmHg) с получением (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата (пример 15 565 мг, 41%) в виде белого твердого вещества. MS: 388 [M+H]+. 1H ЯМР (400 МГц, DMSO-d6) δ=12,10 (шир.с, 1H), 10,61 (с, 1H), 7,34 (шир.с, 1H), 6,28 (шир.с, 1H), 6,21 (с, 1H), 4,97 (шир.с, 1H), 3,82 (с, 2H), 3,14-2,94 (м, 1H), 2,48-2,39 (м, 1H), 2,20 (с, 3H), 1,99 (с, 1H), 1,93-1,80 (м, 1H), 1,78-1,60 (м, 2H), 1,54 (шир.с, 1H), 1,22 (с, 3H), 0,58 (шир.с, 2H), 0,49-0,42 (м, 2H). Оптическое вращение [α]D +10,0° (c 0,2, MeOH).
Способ C
Пример 16: (1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамат
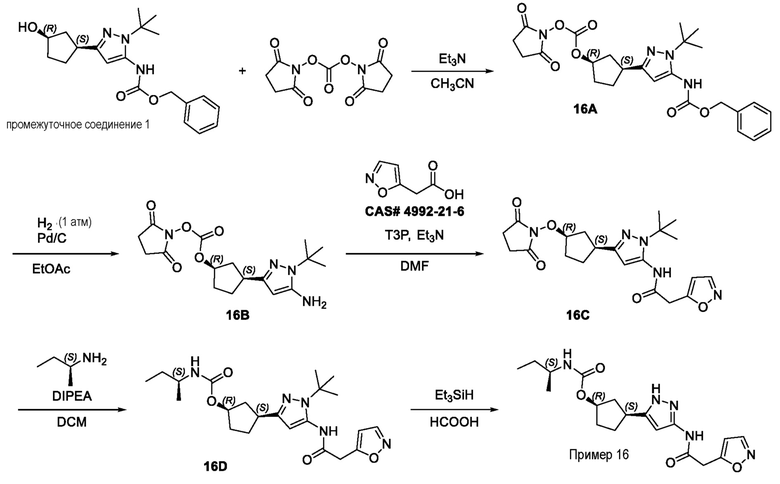
Триэтиламин (4,7 мл, 33,4 ммоль) добавляли к суспензии бензил {1-трет-бутил-3-[(1S,3R)-3-гидроксициклопентил]-1H-пиразол-5-ил}карбамата (промежуточное соединение 1, 5,97 г, 16,7 ммоль) в безводном ацетонитриле (50 мл). Раствор охлаждали до 0°C, затем добавляли N, N'-дисукцинимидилкарбонат (8,56 г, 33,4 ммоль). После перемешивания при 0°C в течение 10 минут, охлаждающую баню удаляли и смесь перемешивали при комнатной температуре (23°C) в течение 24 часов. LCMS показала, что непрореагировавший исходный спирт все еще присутствует, поэтому добавляли дополнительное количество N, N'-дисукцинимидилкарбоната (2,36 г; всего 10,92 г, 42,63 ммоль) и триэтиламина ((2,8 мл; всего 7,5 мл, 54 ммоль), и продолжали перемешивание при комнатной температуре в течение еще 5 часов. Растворители удаляли под вакуумом, и остаток разбавляли этилацетатом (150 мл) и деионизированной водой (100 мл). Полученную эмульсию фильтровали под вакуумом для удаления белого твердого вещества. Слои фильтрата разделяли. Осадок на фильтре промывали этилацетатом (2×100 мл), и те, которые промывали, использовали для дальнейшей экстракции водного слоя. Объединенные органические экстракты сушили над сульфатом магния, фильтровали, и концентрировали. Остаток очищали с помощью хроматографии на силикагеле (элюирование 20-70% этилацетатом в гептане), получая бензил {1-трет-бутил-3-[(1S,3R)-3-({[(2,5-диоксопирролидин-1-ил)окси]карбонил}окси)циклопентил]-1H-пиразол-5-ил}карбамат (16A, 4,5 г, 54%) в виде твердого вещества. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=7,42-7,34 (м, 5H), 6,24 (шир.с, 1H), 6,13 (шир.с, 1H), 5,30-5,22 (м, 1H), 5,20 (с, 2H), 3,21-3,12 (м, 1H), 2,82 (с, 4H), 2,57 (ддд, J=6,7, 8,4, 14,8 Гц, 1H), 2,15-2,05 (м, 2H), 2,04-1,87 (м, 3H), 1,59 (с, 9H). MS: 499 [M+H]+.
Раствор бензил {1-трет-бутил-3-[(1S,3R)-3-({[(2,5-диоксопирролидин-1-ил)окси]карбонил}окси)циклопентил]-1H-пиразол-5-ил}карбамата (16A, 3,5 г, 7,0 ммоль) и 10% Pd/C (1,2 г) в этилацетате (150 мл) перемешивали под водородным баллоном при комнатной температуре (23°C) в течение ночи. Смесь фильтровали через подушку из целита, фильтрующий слой промывали этилацетатом (3×30 мл), и объединенные фильтраты концентрировали с получением неочищенного 1-[({[(1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил]окси}карбонил)окси]пирролидин-2,5-диона (16B), который использовали непосредственно на следующей стадии. MS: 365 [M+H]+.
Неочищенный 1-[({[(1R,3S)-3-(5-амино-1-трет-бутил-1H-пиразол-3-ил)циклопентил]окси}карбонил)окси]пирролидин-2,5-дион (16B, 7,0 ммоль max) растворяли в DMF (20 мл), добавляли 1,2-оксазол-5-илуксусную кислоту (CAS# 4992-21-6, 1,4 г, 11 ммоль) и пропилфосфоновый ангидрид (T3P®, 11 мл 50% масс. раствор в EtOAc, 14 ммоль), и раствор охлаждали до 0°C в атмосфере азота. По каплям добавляли триэтиламин (3,5 мл, 25 ммоль) в течение 10 минут, достаточно медленно, чтобы поддерживать внутреннюю температуру ниже 20°C. Охлаждающую баню удаляли и смесь перемешивали при комнатной температуре в течение 1 часа. Реакцию гасили насыщ. водн. NaHCO3 и экстрагировали этилацетатом (3x). Объединенные органические слои промывали насыщ. водн. NaHCO3 (2x) и насыщ. водн. NaCl (1x), сушили над сульфатом магния, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 30-100% этилацетатом в гептане, получая N-(1-трет-бутил-3-{(1S,3R)-3-[(2,5-диоксопирролидин-1-ил)окси]циклопентил}-1H-пиразол-5-ил)-2-(1,2-оксазол-5-ил)ацетамид (16C, 2,46 г, 74%) в виде белой пены. 1H ЯМР (400 МГц, МЕТАНОЛ-d4) δ=8,35 (д, J=1,7 Гц, 1H), 6,42-6,37 (м, 1H), 6,05 (с, 1H), 5,33-5,23 (м, 1H), 3,98 (с, 2H), 3,16 (тд, J=8,8, 17,2 Гц, 1H), 2,82 (с, 4H), 2,63-2,51 (м, 1H), 2,16-2,02 (м, 3H), 2,00-1,80 (м, 3H), 1,56 (с, 9H). MS: 474 [M+H]+.
Раствор N-(1-трет-бутил-3-{(1S,3R)-3-[(2,5-диоксопирролидин-1-ил)окси]циклопентил}-1H-пиразол-5-ил)-2-(1,2-оксазол-5-ил)ацетамида (16C, 158 мг, 0,334 ммоль), диизопропилэтиламина (0,15 мл, 0,91 ммоль), и (S)-(+)-втор-бутиламина (50 мкл, 0,50 ммоль) в дихлорметане (3,5 мл) перемешивали при 20°C в течение 3 часов. Реакционную смесь разбавляли дихлорметан (10 мл) и промывали насыщ. водн. NaHCO3 (2×3 мл), деионизированной водой (3 мл), насыщ. водн. NH4Cl (3 мл) и насыщ. водн. NaCl (3 мл). Органический слой сушили над сульфатом магния, фильтровали, и концентрировали досуха, получая неочищенный (1R,3S)-3-{1-трет-бутил-5-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-3-ил}циклопентил (2S)-бутан-2-илкарбамат (16D, 115,0 мг, 80%) в виде желтого геля. 1H ЯМР (400 МГц, DMSO-d6) δ=9,79 (с, 1H), 8,50 (д, J=1,7 Гц, 1H), 6,85 (д, J=8,1 Гц, 1H), 6,40 (д, J=1,6 Гц, 1H), 5,93 (с, 1H), 4,97 (шир.с, 1H), 3,95 (с, 2H), 3,43-3,33 (м, 1H), 2,95 (квин, J=8,5 Гц, 1H), 2,40-2,31 (м, 1H), 1,99-1,77 (м, 2H), 1,76-1,57 (м, 3H), 1,47 (с, 9H), 1,39-1,30 (м, 2H), 1,00 (д, J=6,6 Гц, 3H), 0,79 (т, J=7,4 Гц, 3H). MS: 432 [M+H]+.
Неочищенный (1R,3S)-3-{1-трет-бутил-5-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-3-ил}циклопентил (2S)-бутан-2-илкарбамат (16D, 115,0 мг, 0,2665 ммоль) растворяли в муравьиной кислоте (6,0 мл) и триэтилсилане (1,5 мл) и перемешивали при 70°C в течение 18 часов. Слои полученной двухфазной смеси разделяли. Верхний слой триэтилсилана отбрасывали. Нижний кислотный слой концентрировали досуха, растворяли в ацетонитриле и снова концентрировали досуха. Остаток дополнительно сушили в вакууме с получением неочищенного продукта в виде воскообразного твердого вещества коричневого цвета (109,9 мг). Добавляли ацетонитрил (5 мл), и суспензию перемешивали при комнатной температуре в течение 1 часа. Полученный осадок собирали фильтрованием под вакуумом и сушили на воздухе с получением (1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамата (пример 16, 42,1 мг, 42%) в виде не совсем белого твердого вещества. 1H ЯМР (400 МГц, DMSO-d6) δ=12,11 (шир.с, 1H), 10,65 (с, 1H), 8,48 (д, J=1,7 Гц, 1H), 6,87 (д, J=8,1 Гц, 1H), 6,37 (д, J=1,5 Гц, 1H), 6,29 (шир.с, 1H), 4,98 (шир.с, 1H), 3,91 (с, 2H), 3,43-3,33 (м, 1H), 3,11-2,97 (м, 1H), 2,48-2,38 (м, 1H), 2,05-1,94 (м, 1H), 1,94-1,81 (м, 1H), 1,78-1,62 (м, 2H), 1,61-1,50 (м, 1H), 1,41-1,27 (м, 2H), 0,99 (д, J=6,6 Гц, 3H), 0,79 (т, J=7,4 Гц, 3H). MS: 376 [M+H]+.
Способ D
Пример 17: (1R,3S)-3-{3-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-5-ил}циклопентил трет-бутилкарбамат
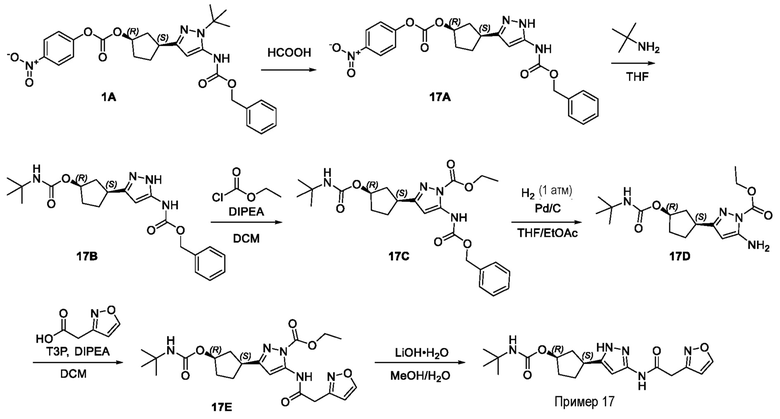
Раствор (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1-трет-бутил-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (1A, 5,00 г, 9,57 ммоль) в муравьиной кислоте (30 мл) перемешивали при 75°C в течение 20 часов. Смесь концентрировали досуха и остаток очищали с помощью хроматографии на силикагеле (элюирование 50-70% этилацетатом в петролейном эфире) с получением (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (17A, 3,6 г, 81%, 82% чистота по LCMS) в виде светло-желтого твердого вещества. MS: 467 [M+H]+.
Смесь (1R,3S)-3-(5-{[(бензилокси)карбонил]амино}-1H-пиразол-3-ил)циклопентил 4-нитрофенилкарбоната (17A, 2,2 г, 4,7 ммоль) и трет-бутиламина (1,38 г, 18,9 ммоль) в THF (40 мл) перемешивали при комнатной температуре (29°C) в течение 18 часов. Растворители удаляли под вакуумом, и остаток очищали с помощью хроматографии на силикагеле (элюирование 0-90% этилацетатом в петролейном эфире) с получением бензил (3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамата (17B, 1,5 г, 79%) в виде светло-желтого стекла. MS: 401 [M+H]+.
Добавляли этилхлорформиат (970 мг, 8,94 ммоль) частями к раствору комнатной температуры (29°C) бензил (3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-1H-пиразол-5-ил)карбамата (17B, 1,50 г, 3,75 ммоль) и диизопропилэтиламина (1,45 г, 11,2 ммоль) в дихлорметане (30 мл), затем смесь перемешивали при комнатной температуре в течение 18 часов. Раствор промывали насыщ. водн. NH4Cl (3×5 мл) и насыщ. водн. NaCl (5 мл), сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного этил 5-{[(бензилокси)карбонил]амино}-3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-1H-пиразол-1-карбоксилата (17C, 2,0 г, >99%) в виде светло-желтой камеди, который использовали без дополнительной очистки. MS: 473 [M+H]+.
Неочищенный этил 5-{[(бензилокси)карбонил]амино}-3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-1H-пиразол-1-карбоксилат (17C, 2,0 г, 4,2 ммоль если чистый) растворяли в этилацетате (15 мл) и THF (15 мл). Добавляли катализатор 10% Pd/C (200 мг), дегазировали и перемешивали под водородным баллоном при комнатной температуре (29°C) в течение 1,5 часов. Суспензию фильтровали для удаления катализатора, фильтрат концентрировали досуха, и остаток очищали с помощью хроматографии на силикагеле (элюирование 0-100% этилацетатом в петролейном эфире, затем 0-30% этилацетат в дихлорметане) с получением этил 5-амино-3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-1H-пиразол-1-карбоксилата (17D, 900 мг, 63%, 56% из 17A) в виде светло-желтой камеди. MS: 339 [M+H]+.
Раствор этил 5-амино-3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-1H-пиразол-1-карбоксилата (17D, 250 мг, 0,739 ммоль), диизопропилэтиламина (286 мг, 2,22 ммоль), и 1,2-оксазол-3-илуксусной кислоты (CAS# 57612-86-9, 113 мг, 0,887 ммоль) в дихлорметане (10 мл) при комнатной температуре (29°C) обрабатывали пропилфосфоновым ангидридом (T3P®, 50% масс. раствор в EtOAc, 1,41 г, 2,22 ммоль), затем перемешивали при комнатной температуре в течение 6 часов. Раствор разбавляли дихлорметаном (10 мл), затем промывали водой (5 мл), насыщ. водн. NaHCO3 (2×5 мл), насыщ. водн. NH4Cl (5 мл) и насыщ. водн. NaCl (5 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного этил 3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-5-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-1-карбоксилата (17E, 331 мг, 100%) в виде коричневой камеди. MS: 448 [M+H]+.
Этот неочищенный этил 3-{(1S,3R)-3-[(трет-бутилкарбамоил)окси]циклопентил}-5-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-1-карбоксилат (17E, 331 мг, 0,739 ммоль) растворяли в метаноле (5 мл), добавляли раствор моногидрата гидроксида лития (93,1 мг, 2,22 ммоль) в воде (1 мл) и смесь перемешивали при комнатной температуре (30°C) в течение 1 часа. Смеси давали постоять в течение ночи, затем концентрировали досуха. Остаток растворяли в метаноле (3 мл), фильтровали, и фильтрат очищали с помощью препаративной ВЭЖХ на колонке YMC-Actus Triart C18 150*30 5 мк, элюируя 20-50% водой (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации фракций, содержащих продукт, (1R,3S)-3-{3-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-5-ил}циклопентил трет-бутилкарбамат (пример 17, 74,84 мг, 27%, 99% ee с помощью хиральной аналитической SFC) получали в виде белого твердого вещества. 1H ЯМР (500 МГц, DMSO-d6) δ=12,09 (шир.с, 1H), 10,63 (с, 1H), 8,83 (с, 1H), 6,76 (шир.с, 1H), 6,53 (с, 1H), 6,29 (с, 1H), 4,96 (шир.с, 1H), 3,75 (с, 2H), 3,02 (квин, J=8,7 Гц, 1H), 2,47-2,41 (м, 1H), 2,04-1,93 (м, 1H), 1,92-1,79 (м, 1H), 1,78-1,61 (м, 2H), 1,55 (шир.с, 1H), 1,19 (с, 9H). MS: 376 [M+H]+.
Способ E
Пример 18: (1R,3S)-3-(3-{[(5-метил-1,3,4-тиадиазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклобутил)карбамат
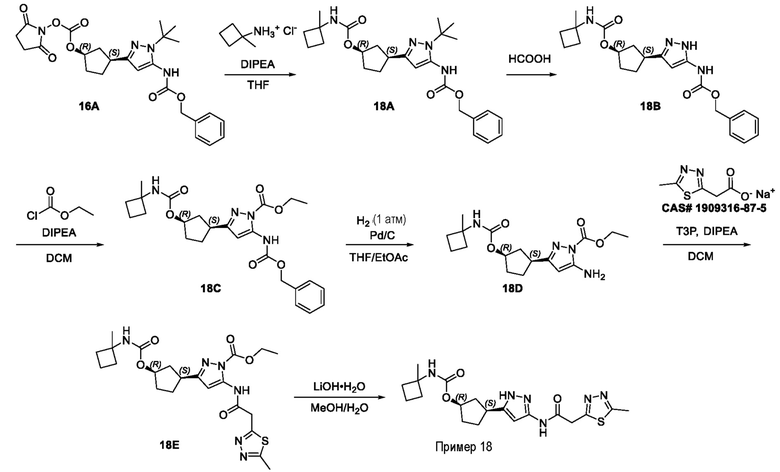
Раствор бензил {1-трет-бутил-3-[(1S,3R)-3-({[(2,5-диоксопирролидин-1-ил)окси]карбонил}окси)циклопентил]-1H-пиразол-5-ил}карбамата (16A, 1,20 г, 2,41 ммоль), 1-метилциклобутиламин гидрохлорида (CAS# 174886-05-6, 439 мг, 3,61 ммоль), и диизопропилэтиламина (1,56 г, 12,0 ммоль) в THF (15 мл) перемешивали при комнатной температуре (32°C) в течение 18 часов. Смесь концентрировали под вакуумом и остаток растворяли в дихлорметане (25 мл). Раствор промывали водой (2×5 мл), насыщ. водн. NH4Cl (5 мл) и насыщ. водн. NaCl (5 мл). Органический слой сушили над сульфатом натрия, фильтровали, концентрировали. Неочищенный продукт очищали с помощью хроматографии на силикагеле (элюирование 0-30% этилацетатом в петролейном эфире) с получением бензил {1-трет-бутил-3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамата (18A, 920 мг, 82%) в виде светло-желтой камеди. MS: 469 [M+H]+.
Бензил {1-трет-бутил-3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамат (18A, 920 мг, 1,96 ммоль) перемешивали в муравьиной кислоте (10 мл) при 75°C в течение 18 часов. Летучие вещества удаляли под вакуумом, и остаток разделяли между дихлорметаном (20 мл) и насыщ. водн. NaHCO3. Органический слой сушили над сульфатом натрия, фильтровали, концентрировали, и очищали с помощью хроматографии на силикагеле (элюирование 0-80% этилацетатом в петролейном эфире) с получением бензил {3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамата (18B, 500 мг, 62%) в виде светло-желтой камеди. MS: 435 [M+Na]+.
Добавляли этилхлорформиат (197 мг, 1,82 ммоль) по частям к раствору полученного бензил {3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-5-ил}карбамата (18B, 500 мг, 1,21 ммоль) и диизопропилэтиламина (470 мг, 3,64 ммоль) в дихлорметане (15 мл). Смесь перемешивали при комнатной температуре (35°C) в течение 4 часов, затем промывали насыщ. водн. NH4Cl (2×5 мл) и насыщ. водн. NaCl (5 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного этил 5-{[(бензилокси)карбонил]амино}-3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-1-карбоксилата (18C, 560 мг, 95%, 80% чистота по ЯМР) в виде светло-желтого стекла. 1H ЯМР (400 МГц, ХЛОРОФОРМ-d) δ=9,50 (с, 1H), 7,44-7,32 (м, 5H), 7,33-7,32 (м, 1H), 6,62 (шир.с, 1H), 5,22 (с, 2H), 5,17 (шир.с, 1H), 4,51 (кв, J=7,0 Гц, 2H), 3,25-3,13 (м, 1H), 2,51-2,30 (м, 2H), 2,14-2,03 (м, 1H), 2,00-1,73 (м, 8H), 1,47 (т, J=7,2 Гц, 4H), 1,44 (с, 3H). MS: 485 [M+H]+; 507 [M+Na]+.
Суспензию неочищенного этил 5-{[(бензилокси)карбонил]амино}-3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-1-карбоксилата (18C, 560 мг, 1,16 ммоль) и катализатора Pd/C (влажный, 50% масс., 150 мг) в этилацетате (10 мл) и THF (10 мл) дегазировали, заполняли водородом, затем перемешивали под водородным баллоном при комнатной температуре в течение 1 часа. Катализатор удаляли фильтрацией, и фильтрат концентрировали с получением неочищенного этил 5-амино-3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-1-карбоксилата (18D, 430 мг, 100% неочищенный) в виде светло-желтой камеди. MS: 351 [M+H]+; 373 [M+Na]+.
Неочищенный этил 5-амино-3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-1H-пиразол-1-карбоксилат (18D, 100,0 мг, 0,285 ммоль) и натрий 2-(5-метил-1,3,4-тиадиазол-2-ил)ацетат (CAS# 1909316-87-5, 77,6 мг, 0,428 ммоль) суспендировали в дихлорметане (10 мл) при комнатной температуре (35°C). Добавляли диизопропилэтиламин (184 мг, 1,43 ммоль) и пропилфосфоновый ангидрид (T3P®, 50% масс. раствор в EtOAc, 545 мг, 0,856 ммоль) и полученный раствор перемешивали при 35°C в течение 3 часов. Реакционную смесь промывали водой (3 мл), насыщ. водн. NH4Cl (2×3мл) и насыщ. вод. NaCl (3 мл). Органический слой сушили над сульфатом натрия, фильтровали, и концентрировали с получением неочищенного этил 3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-5-{[(5-метил-1,3,4-тиадиазол-2-ил)ацетил]амино}-1H-пиразол-1-карбоксилата (18E, 140 мг, 100% неочищенный) в виде светло-желтой камеди. MS: 513 [M+Na]+.
Смесь неочищенного этил 3-[(1S,3R)-3-{[(1-метилциклобутил)карбамоил]окси}циклопентил]-5-{[(5-метил-1,3,4-тиадиазол-2-ил)ацетил]амино}-1H-пиразол-1-карбоксилата (18E, 140 мг, 0,285 ммоль) и моногидрата гидроксида лития (35,9 мг, 0,856 ммоль) в метаноле (5 мл) и воде (1 мл) перемешивали при комнатной температуре (35°C) в течение 30 минут, затем оставляли стоять в течение ночи. Суспензию концентрировали до ~3 мл, твердые частицы удаляли фильтрацией, и фильтрат очищали с помощью препаративной ВЭЖХ на колонке DuraShell 150*25 мм*5 мкм, элюируя 27-47% водой (0,05% гидроксид аммония об/об) в ацетонитриле. После лиофилизации фракций, содержащих продукт, (1R,3S)-3-(3-{[(5-метил-1,3,4-тиадиазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклобутил)карбамат (пример 18, 30,89 мг, 26%, >99% ee с помощью хиральной аналитической SFC) получали в виде белого твердого вещества. 1H ЯМР (500 МГц, DMSO-d6) δ=12,14 (шир.с, 1H), 10,78 (с, 1H), 7,18 (шир.с, 1H), 6,30 (шир.с, 1H), 4,97 (шир.с, 1H), 4,19 (с, 2H), 3,13-2,95 (м, 1H), 2,69 (с, 3H), 2,48-2,40 (м, 1H), 2,21 (шир.с, 2H), 1,99 (шир.д, J=8,9 Гц, 1H), 1,92-1,83 (м, 1H), 1,82-1,75 (м, 2H), 1,74-1,63 (м, 4H), 1,57 (шир.с, 1H), 1,34-1,23 (м, 3H). MS: 419 [M+H]+.
Дополнительные соединения по изобретению получали с помощью модификаций способов, приведенных в настоящем документе в качестве примеров. Когда были доступны хиральные исходные реагенты, соединения получали и выделяли в виде отдельных стереоизомеров, имеющих известную абсолютную конфигурацию, как указано метками (R) и (S) на их структурах. Когда использовали рацемические исходные реагенты, соединения подвергали синтезу в виде смеси диастереомеров, и затем разделяли на отдельные стереоизомеры с помощью соответствующей хиральной препаративной ВЭЖХ или метода SFC перед характеристикой и тестированием. В этих случаях известные стереоцентры нарисованы клиновидными связями и помечены метками (R) и (S); неизвестные стереоцентры изображены в виде плоских связей, отмеченных звездочкой, и их объяснение включено в таблицу 2. В тех случаях, когда известна относительная, но не абсолютная стереохимия, структуры нарисованы с клиновидными связями, помеченными звездочкой, без меток (R) и/или (S), и объяснение включено в таблицу 2.
Выбранные соединения и соответствующие им характеристические данные представлены в Таблице 2 ниже.
(Способ)
(A)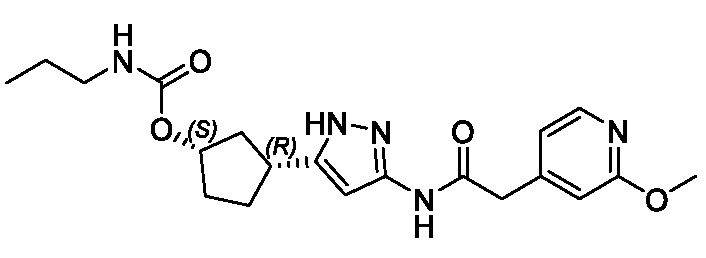
(1S,3R)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат
Все стереоцентры известны
(A)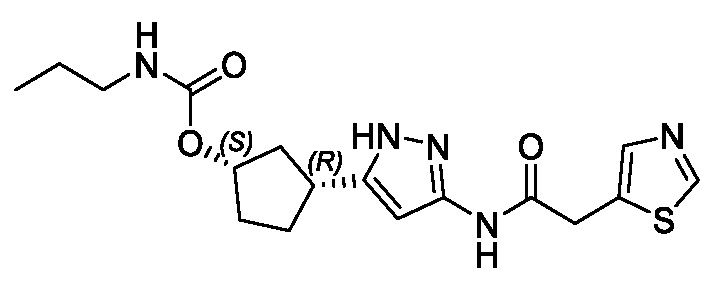 (1S,3R)-3-{3-[(1,3-тиазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил пропилкарбамат
(1S,3R)-3-{3-[(1,3-тиазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил пропилкарбамат
Все стереоцентры известны
(A)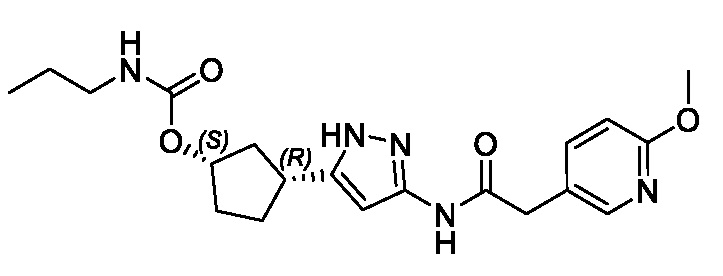
(1S,3R)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат
Все стереоцентры известны
(A)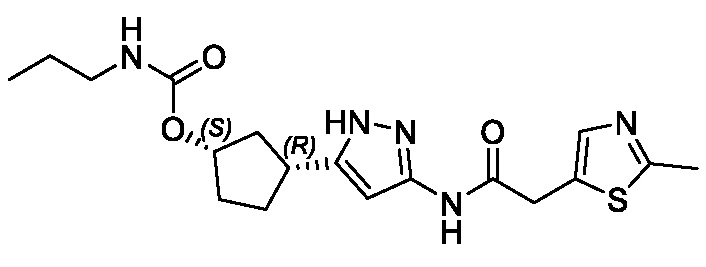
(1S,3R)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат
Все стереоцентры известны
(A)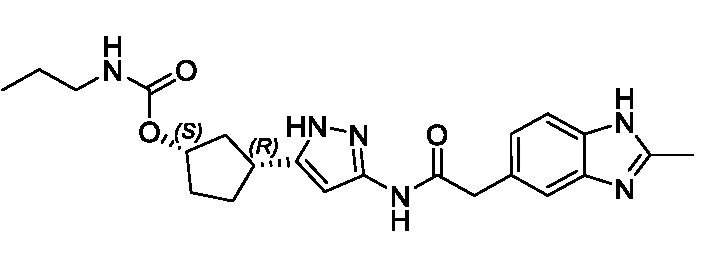
(1S,3R)-3-(3-{[(2-метил-1H-бензимидазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат
Все стереоцентры известны
(A)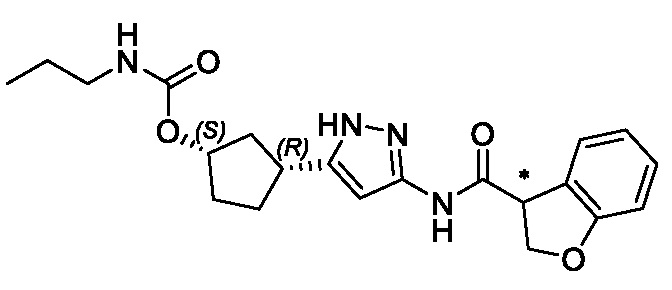
(1S,3R)-3-(3-{[(3ξ)-2,3-дигидро-1-бензофуран-3-илкарбонил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в дигидробензофуране не определена
[α]D25 -42,0 (c 0,1, MeOH)
Пик 1 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 40% IPA (0,1% NH3.H2O) в CO2; Скорость потока: 6,5 мл/мин Температура колонки 40°C
(A)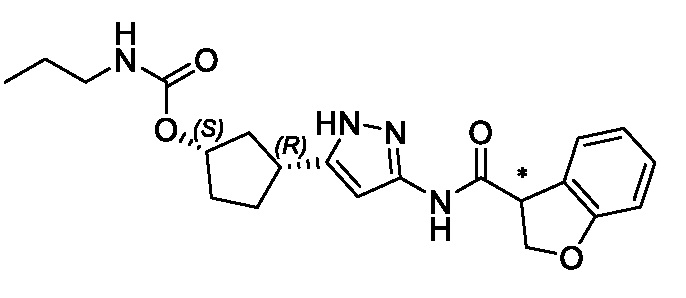
(1S,3R)-3-(3-{[(3ξ)-2,3-дигидро-1-бензофуран-3-илкарбонил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в дигидробензофуране не определена
[α]D25 +39,3 (c 0,1, MeOH)
Пик 2 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 40% IPA (0,1% NH3.H2O) в CO2; Скорость потока: 6,5 мл/мин Температура колонки 40°C
(A)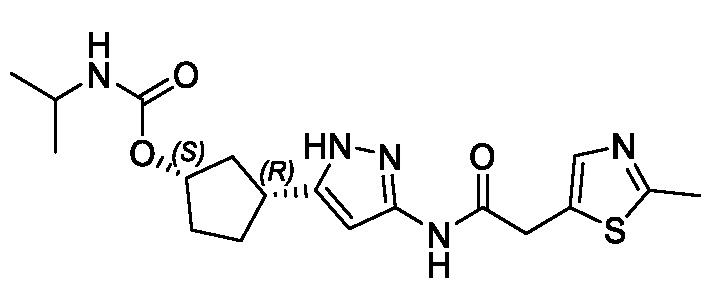
(1S,3R)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамат
Все стереоцентры известны
(B)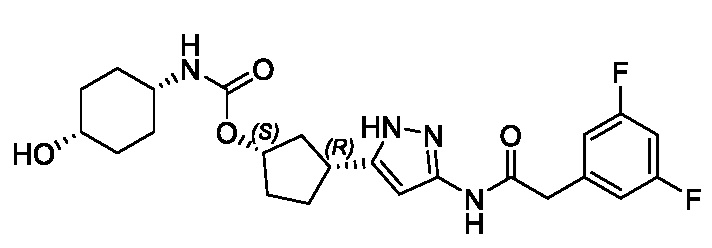
(1S,3R)-3-(3-{[(3,5-дифторфенил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (цис-4-гидроксициклогексил)карбамат
Все стереоцентры известны; циклогексильное кольцо представляет собой мезо- N, O-цис.
(B)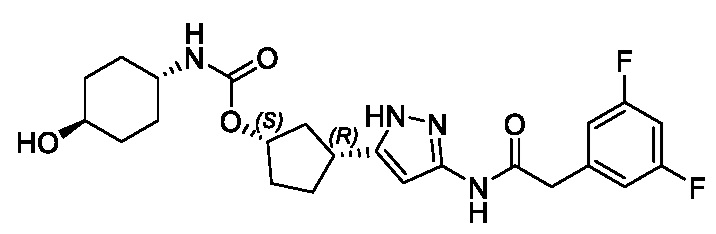
(1S,3R)-3-(3-{[(3,5-дифторфенил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (транс-4-гидроксициклогексил)карбамат
Все стереоцентры известны; циклогексильное кольцо представляет собой мезо- N, O-транс.
(C)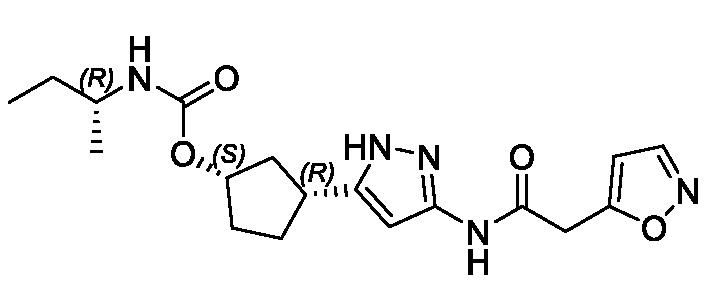
(1S,3R)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2R)-бутан-2-илкарбамат
Все стереоцентры известны
[α]D25 +3,6(c 0,11, MeOH)
(C)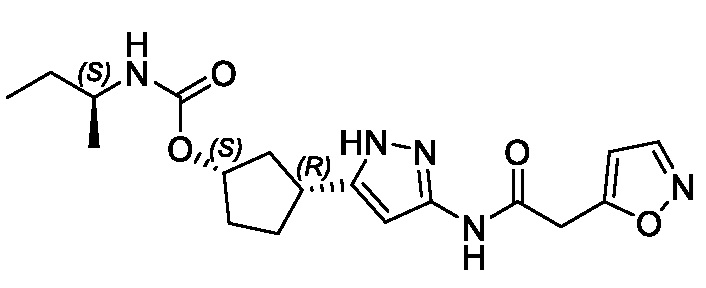
(1S,3R)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
[α]D25 -15,0 (c 0,11, MeOH)
(A)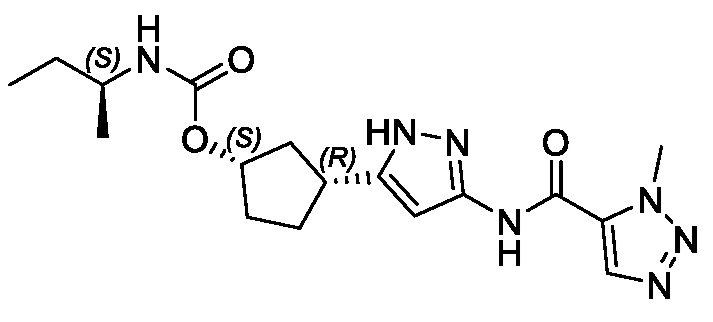
(1S,3R)-3-(3-{[(1-метил-1H-1,2,3-триазол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)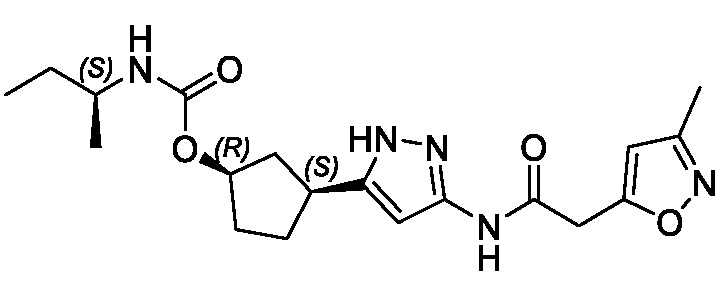
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)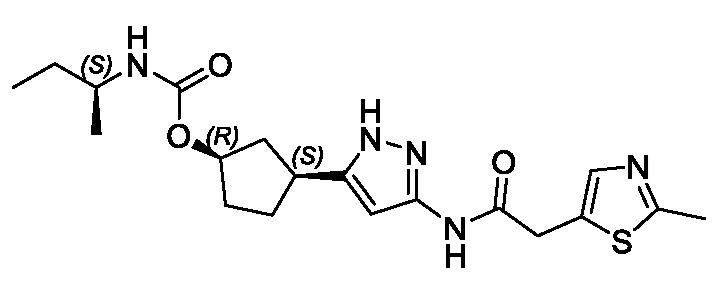
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)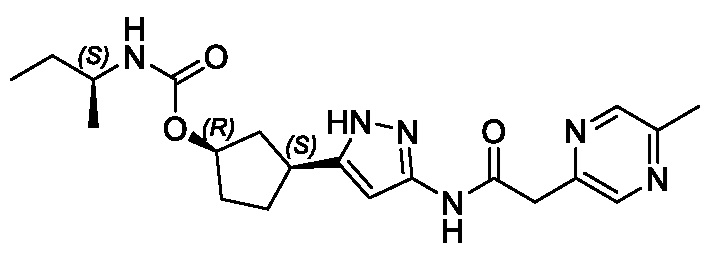
(1R,3S)-3-(3-{[(5-метилпиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)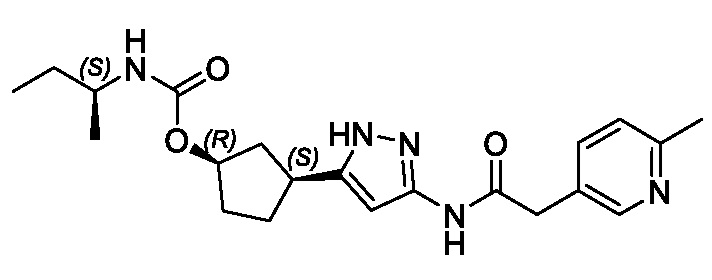
(1R,3S)-3-(3-{[(6-метилпиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)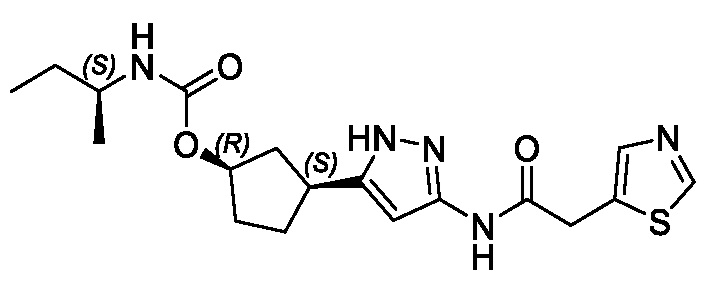
(1R,3S)-3-{3-[(1,3-тиазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)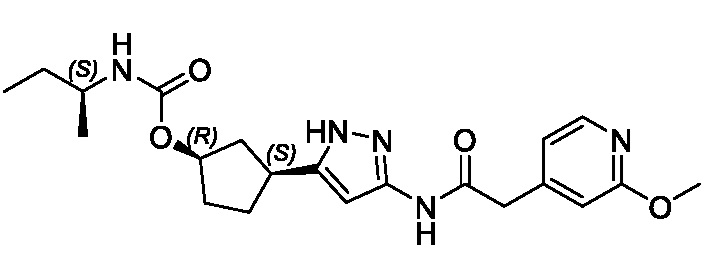
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)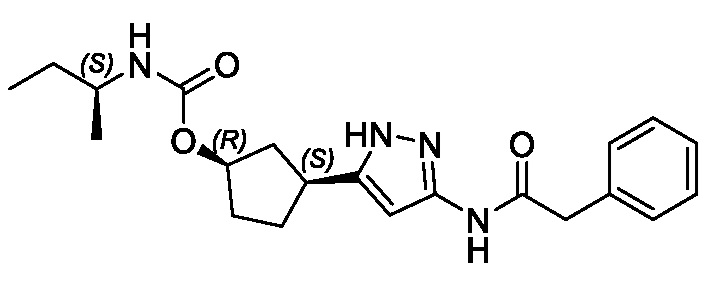
(1R,3S)-3-{3-[(фенилацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)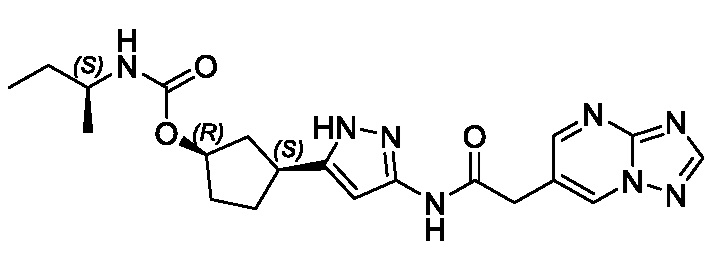
(1R,3S)-3-{3-[([1,2,4]триазоло[1,5-a]пиримидин-6-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)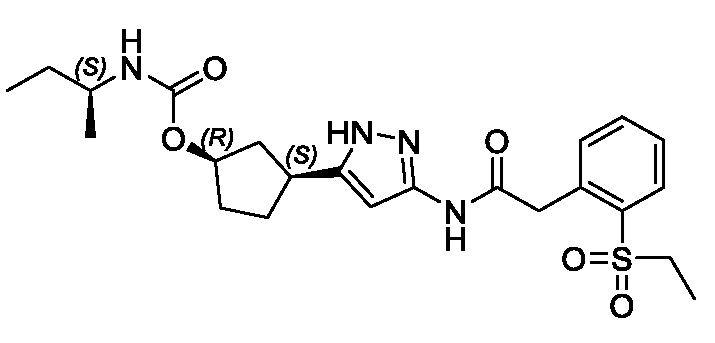
(1R,3S)-3-[3-({[2-(этилсульфонил)фенил]ацетил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны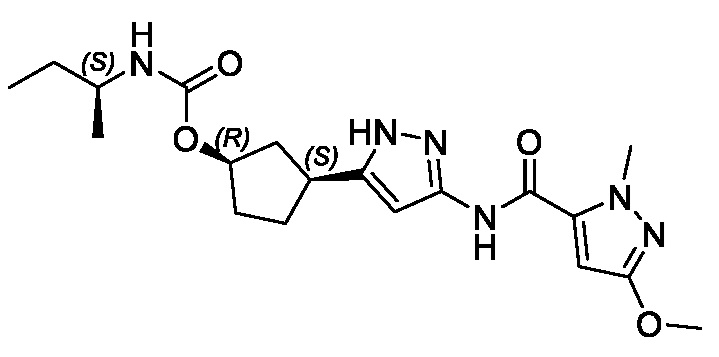
(1R,3S)-3-(3-{[(3-метокси-1-метил-1H-пиразол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)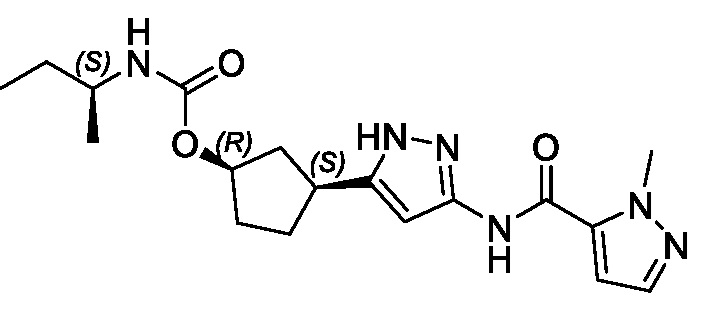
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(1R,3S)-3-{3-[([1,3]тиазоло[4,5-b]пиридин-7-илкарбонил)амино]-1H-пиразол-5-ил}циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)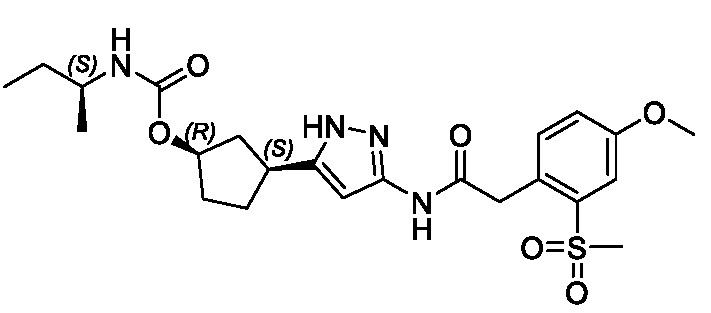
(1R,3S)-3-[3-({[4-метокси-2-(метилсульфонил)фенил]ацетил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)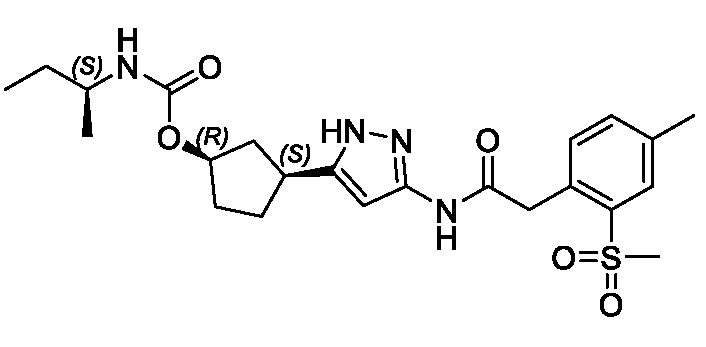
(1R,3S)-3-[3-({[4-метил-2-(метилсульфонил)фенил]ацетил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)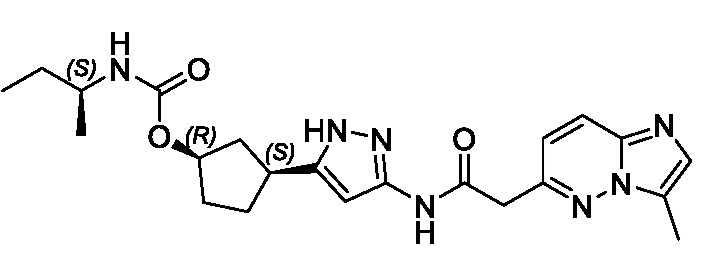
(1R,3S)-3-(3-{[(3-метилимидазо[1,2-b]пиридазин-6-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)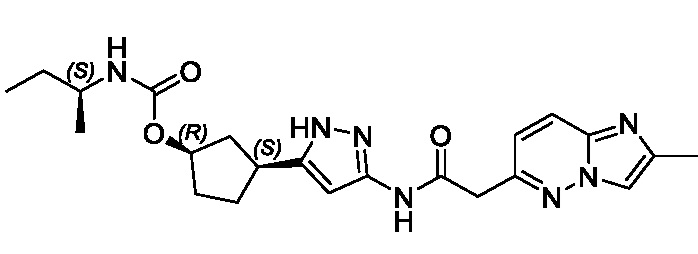
(1R,3S)-3-(3-{[(2-метилимидазо[1,2-b]пиридазин-6-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)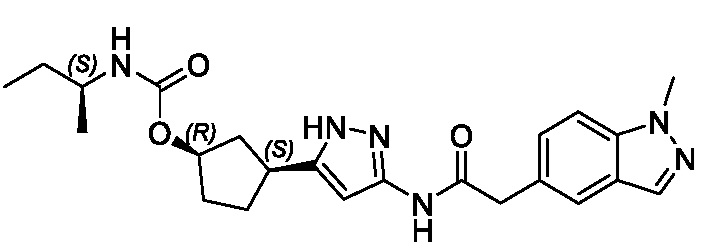
(1R,3S)-3-(3-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)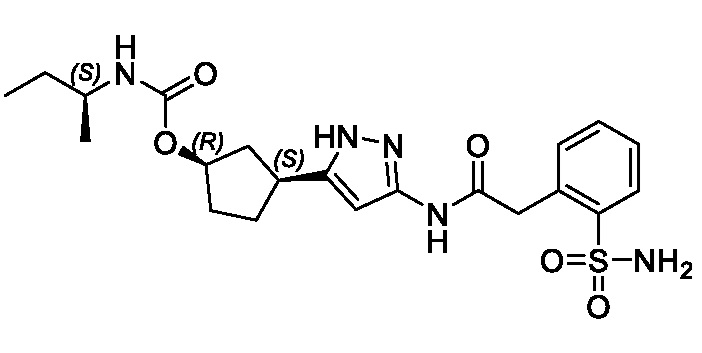
(1R,3S)-3-(3-{[(2-сульфамоилфенил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)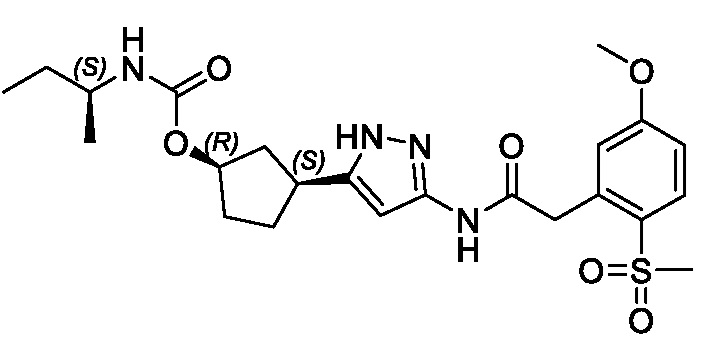
(1R,3S)-3-[3-({[5-метокси-2-(метилсульфонил)фенил]ацетил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)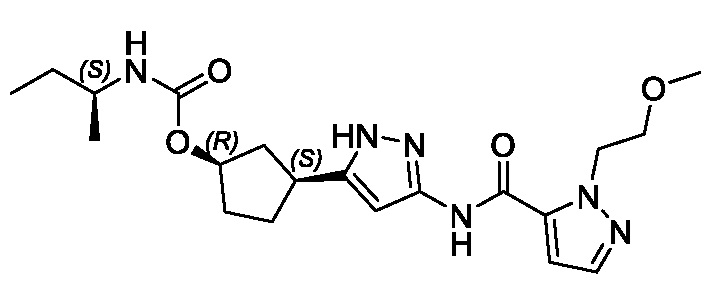
(1R,3S)-3-[3-({[1-(2-метоксиэтил)-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)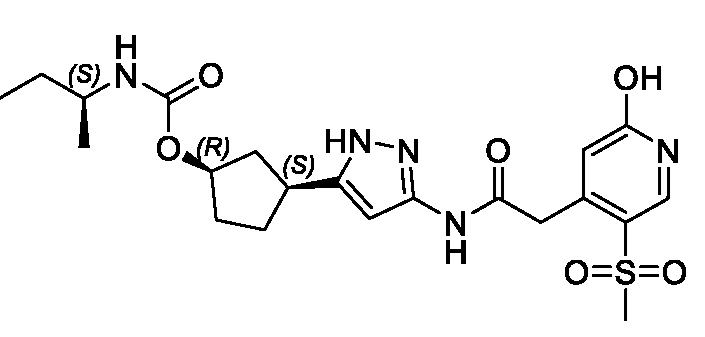
(1R,3S)-3-[3-({[2-гидрокси-5-(метилсульфонил)пиридин-4-ил]ацетил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)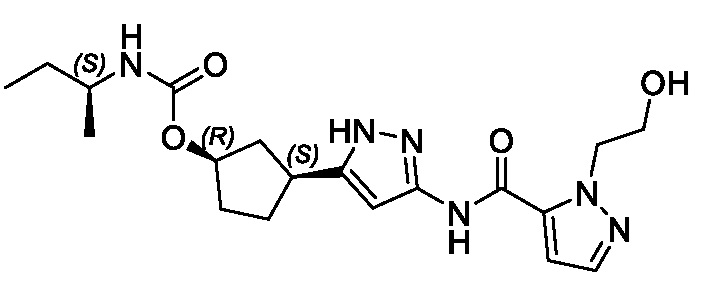
(1R,3S)-3-[3-({[1-(2-гидроксиэтил)-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (2S)-бутан-2-илкарбамат
Все стереоцентры известны
(A)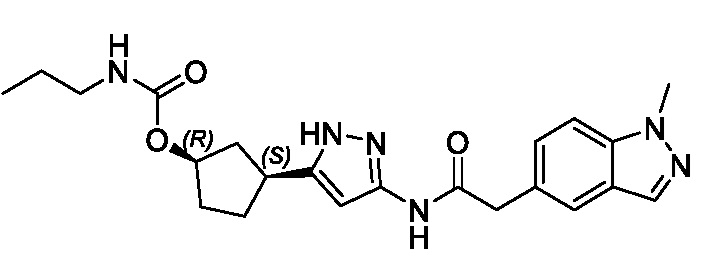
(1R,3S)-3-(3-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропилкарбамат
Все стереоцентры известны
(A)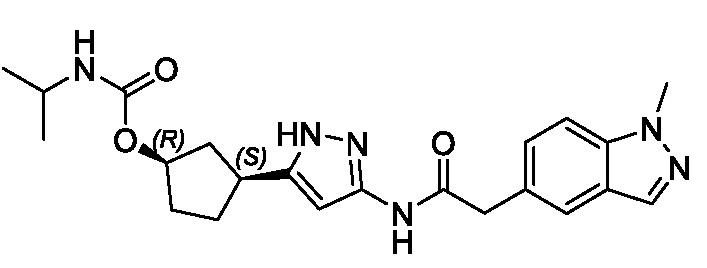
(1R,3S)-3-(3-{[(1-метил-1H-индазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамат
Все стереоцентры известны
(A)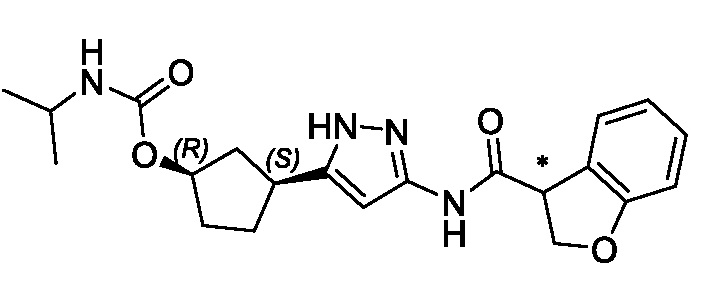
(1R,3S)-3-(3-{[(3ξ)-2,3-дигидро-1-бензофуран-3-илкарбонил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в дигидробензофуране не определена
[α]D25 -50 (c 0,12, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5 мл/мин; Температура колонки 35°C
(A)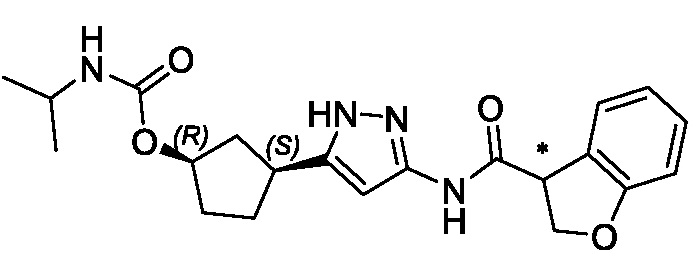
(1R,3S)-3-(3-{[(3ξ)-2,3-дигидро-1-бензофуран-3-илкарбонил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в дигидробензофуране не определена
[α]D25 +47 (c 0,4, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5 мл/мин; Температура колонки 35°C
(B)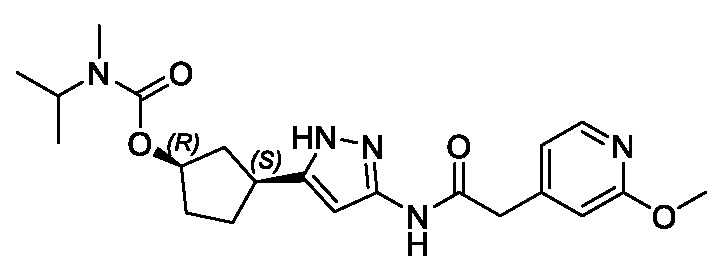
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил метил(пропан-2-ил)карбамат
Все стереоцентры известны
(B)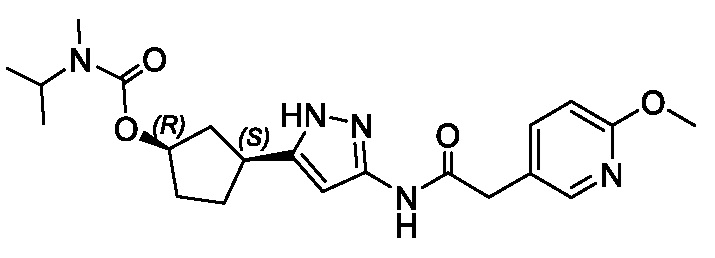
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил метил(пропан-2-ил)карбамат
Все стереоцентры известны
(A)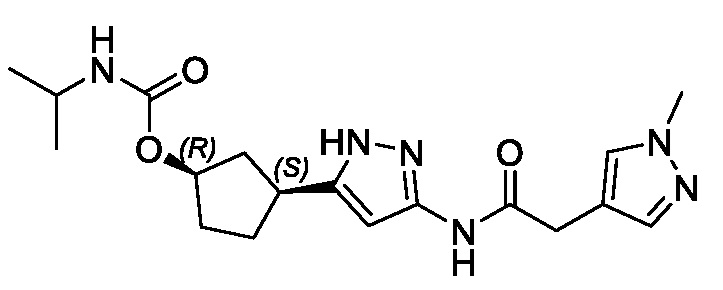
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил пропан-2-илкарбамат
Все стереоцентры известны
(B)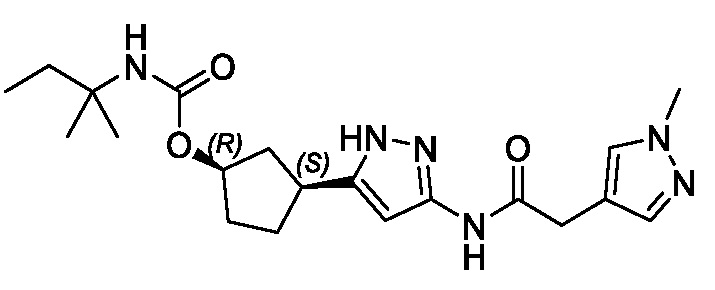
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2-метилбутан-2-ил)карбамат
Все стереоцентры известны
(B)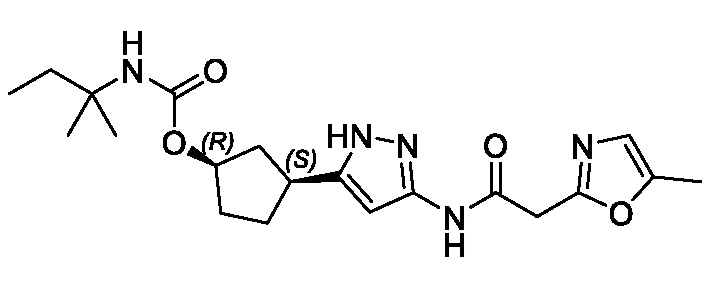
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2-метилбутан-2-ил)карбамат
Все стереоцентры известны
(A)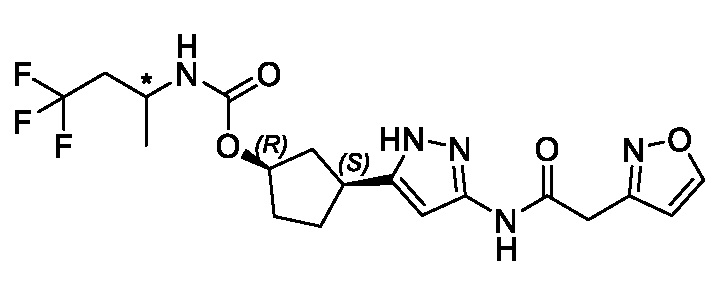
(1R,3S)-3-{3-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-5-ил}циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D20 -2,85 (c 0,117, MeOH)
Пик 1 из 2: Колонка: Xtimate C18 150*25 мм*5мкм; Подвижная фаза: от 22-52% CH3CN в воде (0,05% гидроксид аммиака об./об.); Скорость потока: 25мл/мин
(A)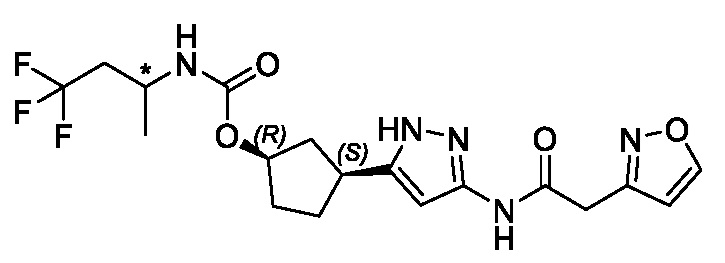
(1R,3S)-3-{3-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-5-ил}циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +8,12 (c 0,197, MeOH)
Пик 2 из 2: Колонка: Xtimate C18 150*25 мм*5 мкм; Подвижная фаза: из 22-52% CH3CN в воде (0,05% гидроксид аммиака об./об.); Скорость потока: 25мл/мин
(A)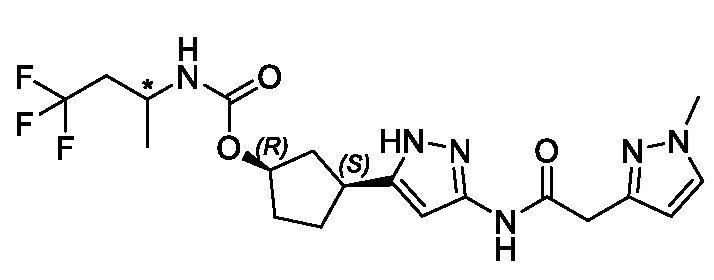
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -3,56 (c 0,15, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин
(A)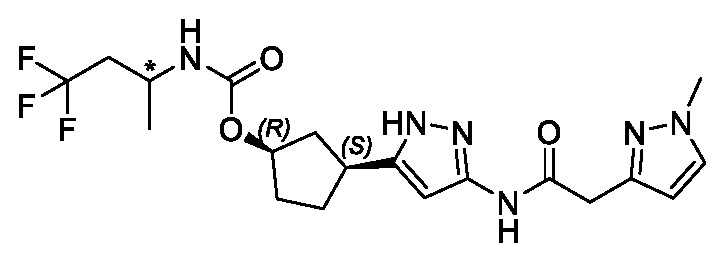
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +2,73 (c 0,22, MeOH);
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм x3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин
(A)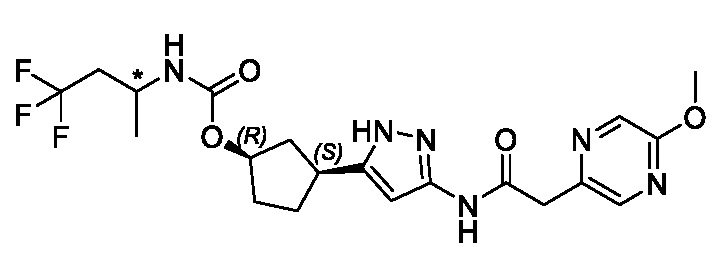
(1R,3S)-3-(3-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -1,67 (c 0,12, MeOH);
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм × 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2, Скорость потока: 2,5мл/мин
(A)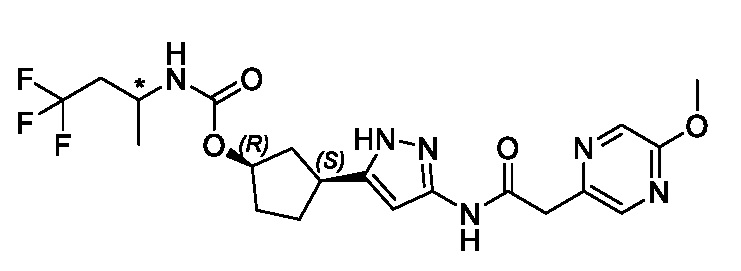
(1R,3S)-3-(3-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +6,67 (c 0,11, MeOH);
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм x3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2, Скорость потока: 2,5мл/мин
(A)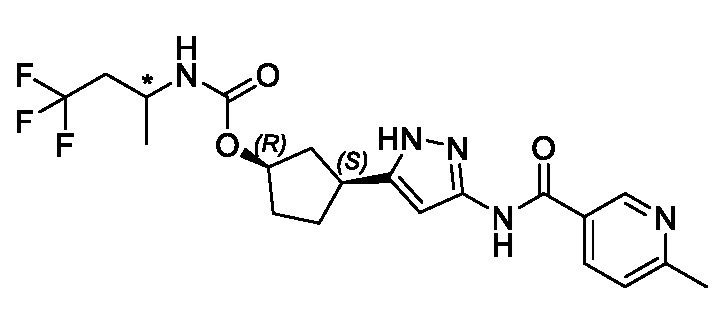
(1R,3S)-3-(3-{[(6-метилпиридин-3-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -2 (c 0,1, MeOH)
Пик 1 из 2: Колонка: ChiralPak AD-3 150×4,6 мм × 3 мкм; Градиент: 40% IPA (0,1% Этаноламин) в CO2; Скорость потока: 2,5мл/мин Температура колонки 40°C
(A)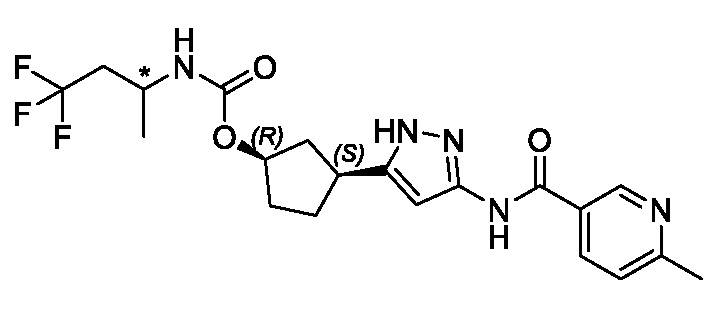
(1R,3S)-3-(3-{[(6-метилпиридин-3-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +8 (c 0,1, MeOH)
Пик 2 из 2: Колонка: ChiralPak AD-3 150×4,6 мм × 3 мкм; Градиент: 40% IPA (0,1% Этаноламин) в CO2; Скорость потока: 2,5мл/мин Температура колонки 40°C
(B)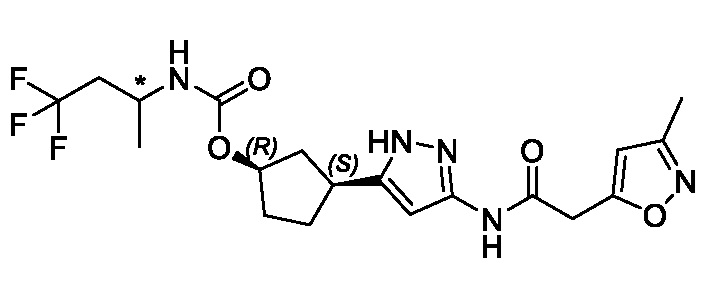
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -1,0 (c 0,2, MeOH)
Пик 1 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 35% IPA (0,1% NH3.H2O) в CO2; Скорость потока: 7мл/мин Температура колонки 40°C
(B)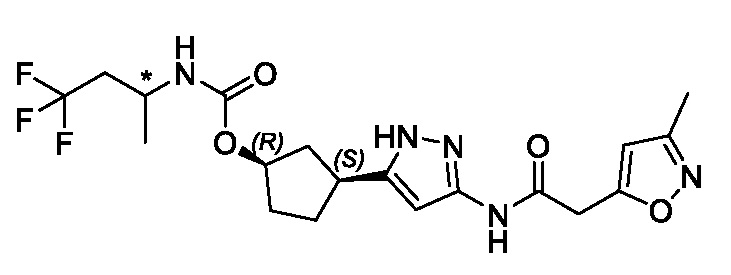
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +1,0 (c 0,2, MeOH)
Пик 2 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 35% IPA (0,1% NH3.H2O) в CO2; Скорость потока: 7мл/мин Температура колонки 40°C
(B)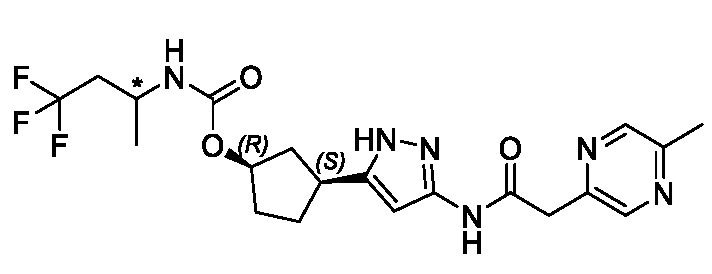
(1R,3S)-3-(3-{[(5-метилпиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -1,82° (c 0,11, MeOH)
Пик 1 из 2; Колонка: Chiralpak AD-3 50×3мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)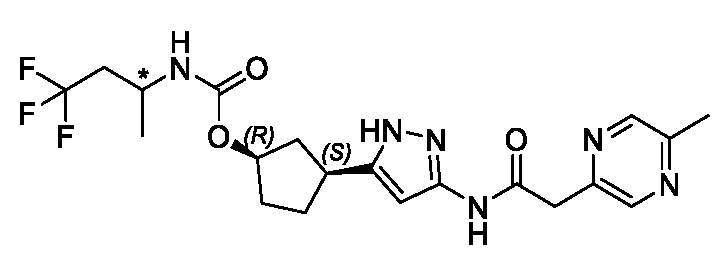
(1R,3S)-3-(3-{[(5-метилпиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +6,67 (c 0,12, MeOH)
Пик 2 из 2; Колонка: Chiralpak AD-3 50×3 мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)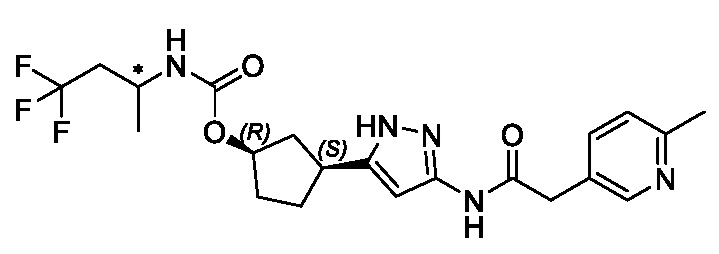
(1R,3S)-3-(3-{[(6-метилпиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +4,44 (c 0,120, MeOH)
Пик 1 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 35% EtOH (0,1% NH3.H2O) в CO2; Скорость потока: 7мл/мин; Температура колонки 40°C
(B)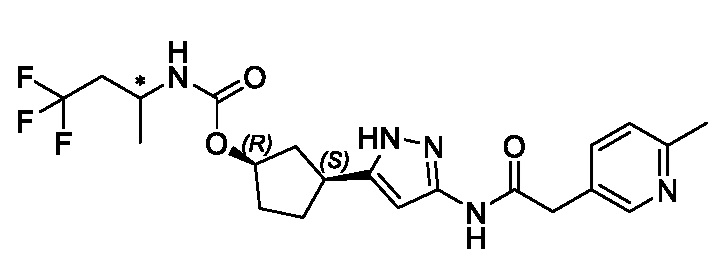
(1R,3S)-3-(3-{[(6-метилпиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +5,56 (c 0,108, MeOH)
Пик 2 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 35% EtOH (0,1% NH3.H2O) в CO2; Скорость потока: 7мл/мин; Температура колонки 40°C
(B)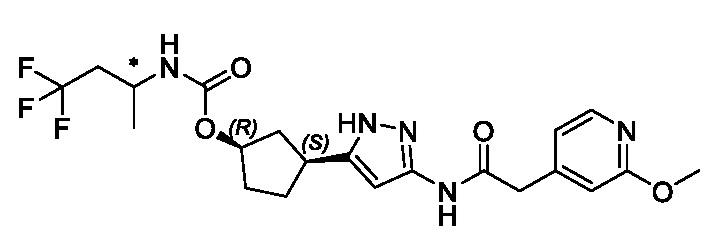
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +2,98 (c 0,134, MeOH)
Пик 1 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 35% IPA (0,1% NH3.H2O) в CO2; Скорость потока: 6,5мл/мин; Температура колонки 40°C
(B)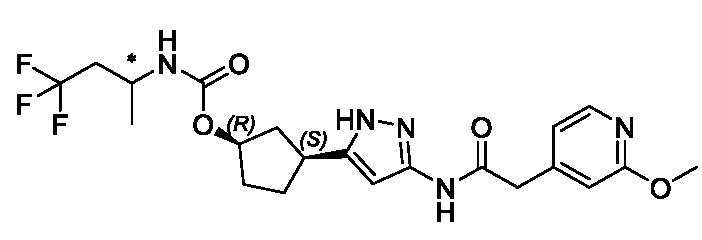
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +8,0 (c 0,1, MeOH)
Пик 2 из 2: Колонка: SS WHELK-O1 (250мм*50мм,10мкм); Подвижная фаза: 35% IPA (0,1% NH3.H2O) в CO2; Скорость потока: 6,5мл/мин; Температура колонки 40°C
(B)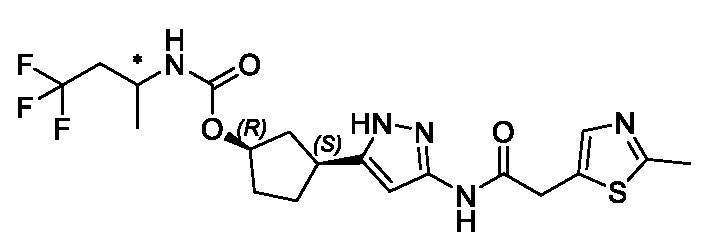
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
19F ЯМР (376МГц, DMSO-d6) δ=-62,57 (шир.с, 3F);
[α]D25 +3 (c 0,2, MeOH)
Пик 1 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 35% EtOH (0,1% NH3.H2O) в CO2; Скорость потока: 7мл/мин; Температура колонки 40 C
(B)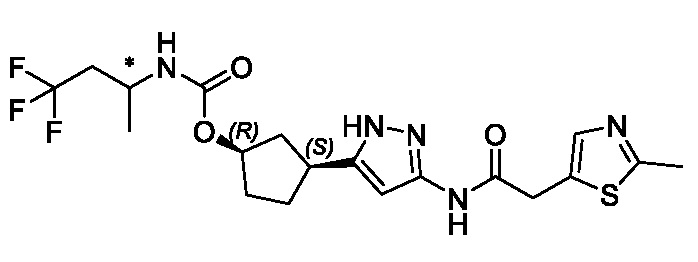
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
19F ЯМР (376МГц, DMSO-d6) δ=-62,55 (шир.с, 3F);
[α]D25 +12 (c 0,2, MeOH)
Пик 2 из 2: Колонка: SS WHELK-O1 (250 мм*50 мм,10 мкм); Подвижная фаза: 35% EtOH (0,1% NH3.H2O) в CO2; Скорость потока: 7мл/мин; Температура колонки 40°C
(A)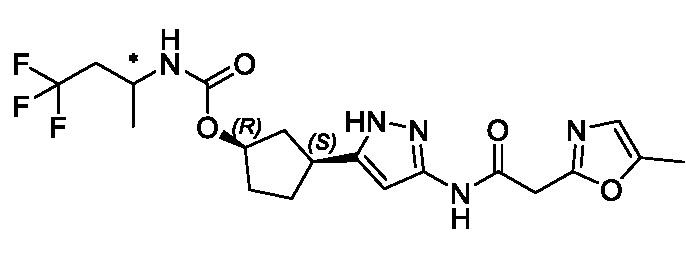
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -1,91 (c 0,115, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°С
(A)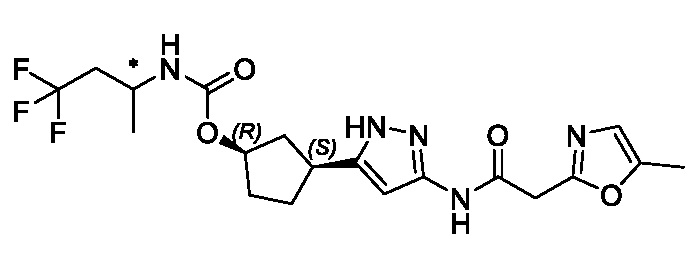
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +1,74 (c 0,115, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(A)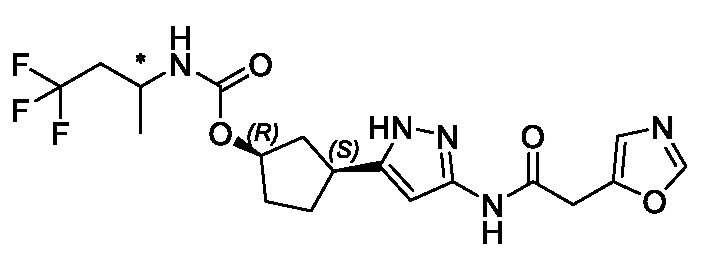
(1R,3S)-3-{3-[(1,3-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -1,82 (c 0,11, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(A)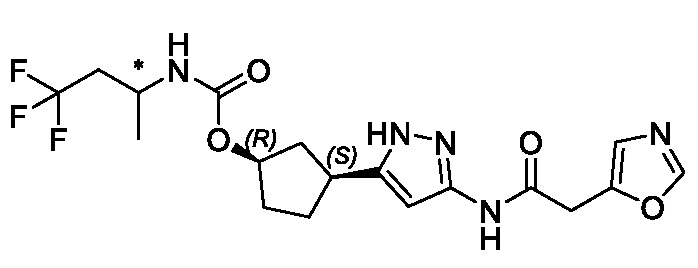
(1R,3S)-3-{3-[(1,3-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +8,60 (c 0,31, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(A)
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -4 (c 0,1, MeOH)
Пик 1 из 2; Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(A)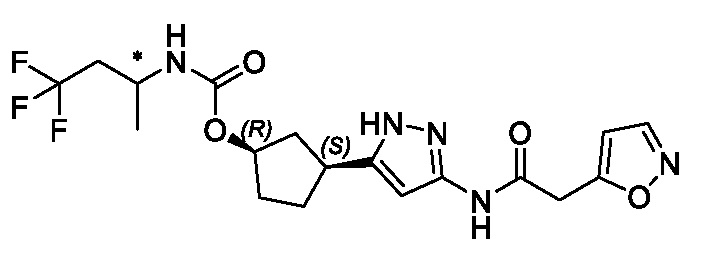
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +12 (c 0,1, MeOH)
Пик 2 из 2; Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(A)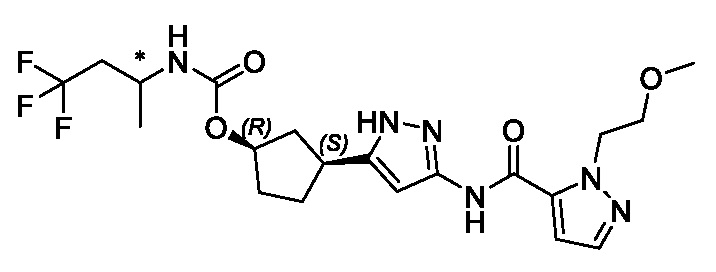
(1R,3S)-3-[3-({[1-(2-метоксиэтил)-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -7,27 (c 0,11, MeOH)
Пик 1 из 2: Колонка: ChiralPak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,1% Этаноламин) в CO2; Скорость потока: 2,5мл/мин Температура колонки 40°C
(A)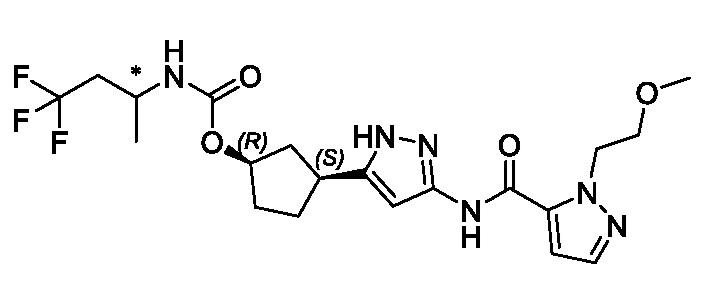
(1R,3S)-3-[3-({[1-(2-метоксиэтил)-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 +7,22 (c 0,12, MeOH);
Пик 2 из 2: Колонка: ChiralPak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,1% Этаноламин) в CO2; Скорость потока: 2,5мл/мин Температура колонки 40°C
(A)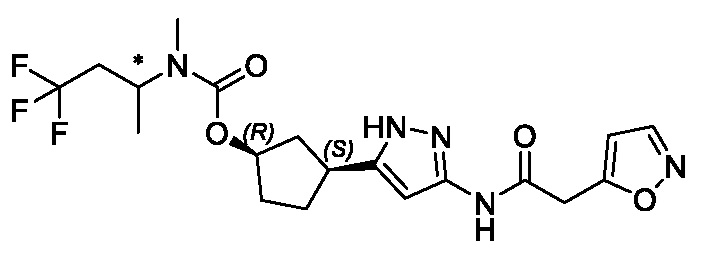
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил метил[(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -10 (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°С
(A)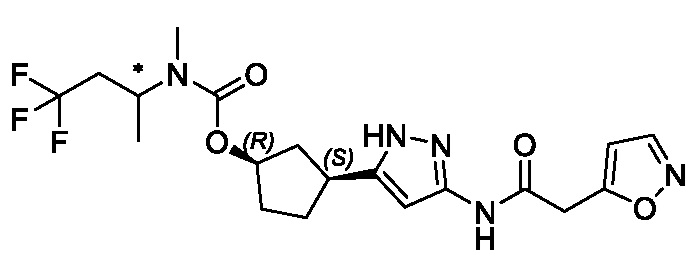
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил метил[(2ξ)-4,4,4-трифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4,4-трифторбутан-2-ил]карбамате не определена
[α]D25 -4 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°С
(B)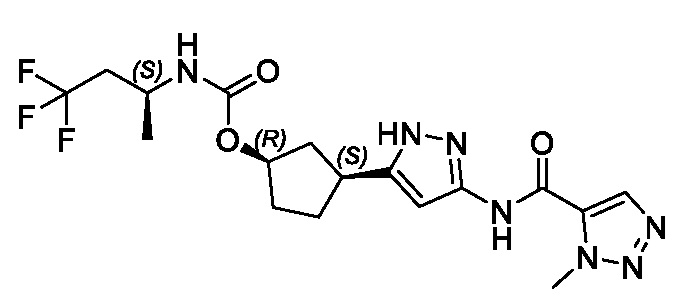
(1R,3S)-3-(3-{[(1-метил-1H-1,2,3-триазол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил [(2S)-4,4,4-трифторбутан-2-ил]карбамат
Все стереоцентры известны
19F ЯМР (376МГц, DMSO-d6) δ=-62,58 (с, 3F)
(A)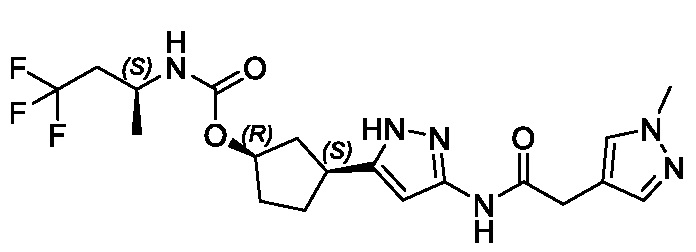
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2S)-4,4,4-трифторбутан-2-ил]карбамат
Все стереоцентры известны
[α]D22 +10,0 (c 0,3, MeOH)
(A)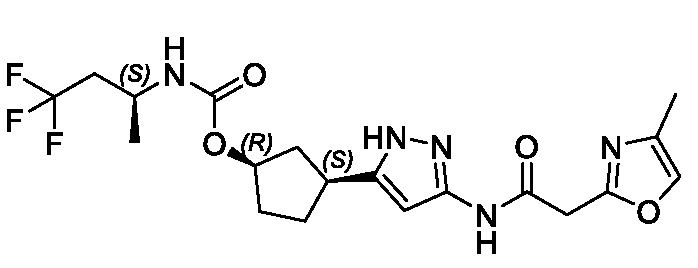
(1R,3S)-3-(3-{[(4-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2S)-4,4,4-трифторбутан-2-ил]карбамат
Все стереоцентры известны
[α]D25 +12,41 (c 0,145, MeOH);
(A)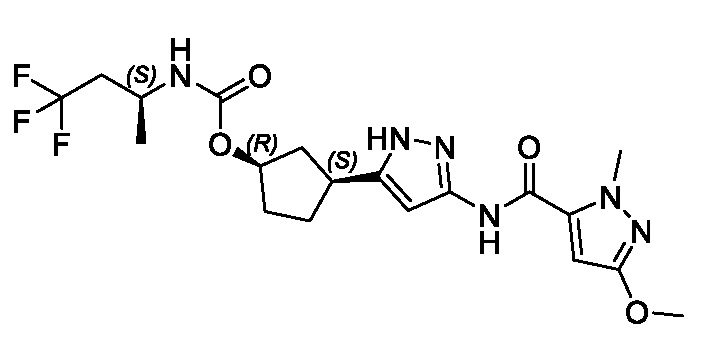
(1R,3S)-3-(3-{[(3-метокси-1-метил-1H-пиразол-5-ил)карбонил]амино}-1H-пиразол-5-ил)циклопентил [(2S)-4,4,4-трифторбутан-2-ил]карбамат
Все стереоцентры известны
(B)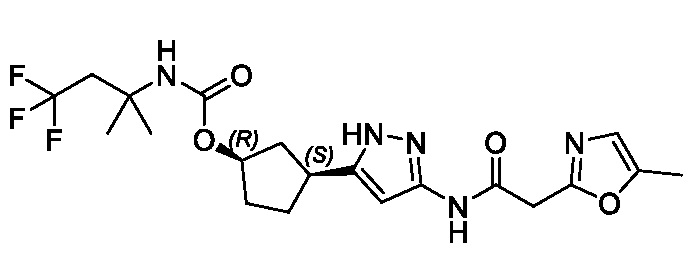
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (4,4,4-трифтор-2-метилбутан-2-ил)карбамат
Все стереоцентры известны
(B)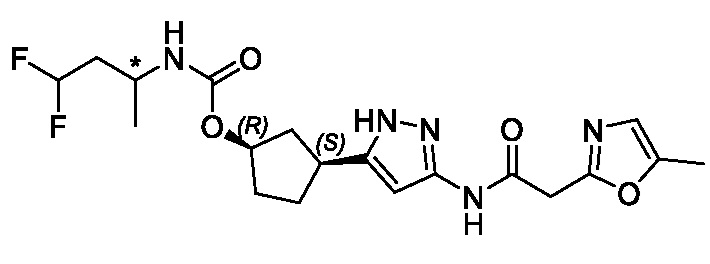
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4-дифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4-дифторбутан-2-ил]карбамате не определена
[α]D25 -4 (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 50×3 мм x3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)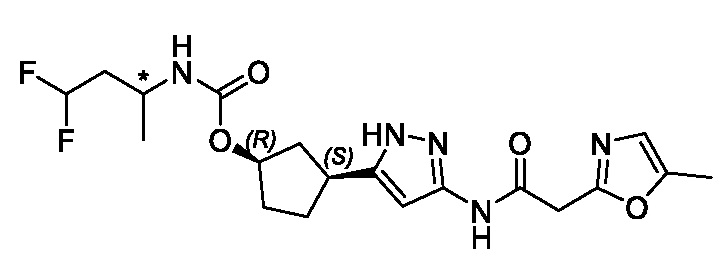
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4-дифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер, абсолютная конфигурация хирального центра в 4,4-дифторбутан-2-ил]карбамате не определена
[α]D25 +18 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 50×3 мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)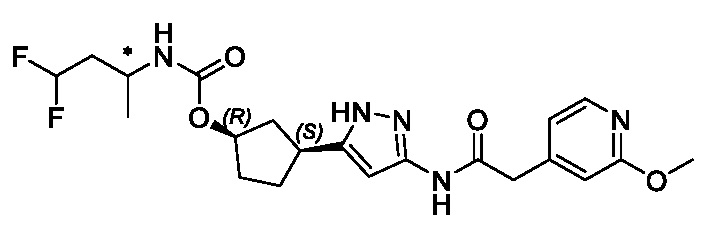
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4-дифторбутан-2-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4-дифторбутан-2-ил]карбамате не определена
[α]D25 -4° (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(B)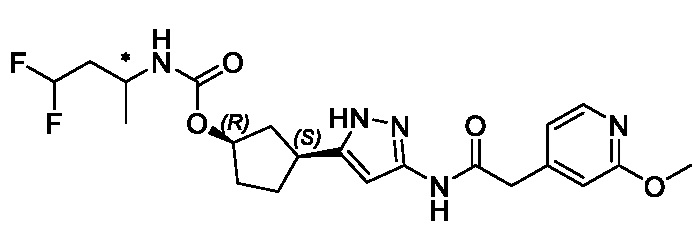
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2ξ)-4,4-дифторбутан-2-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 4,4-дифторбутан-2-ил]карбамате не определена
[α]D25 +18 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(B)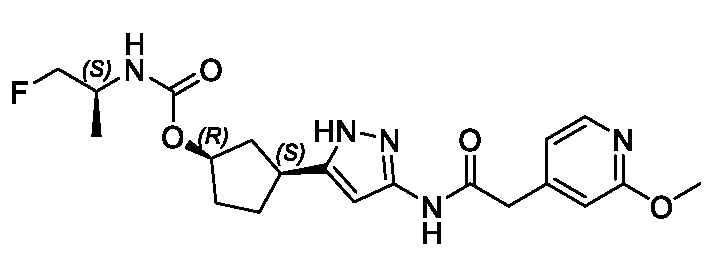
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2S)-1-фторпропан-2-ил]карбамат
Все стереоцентры известны
(B)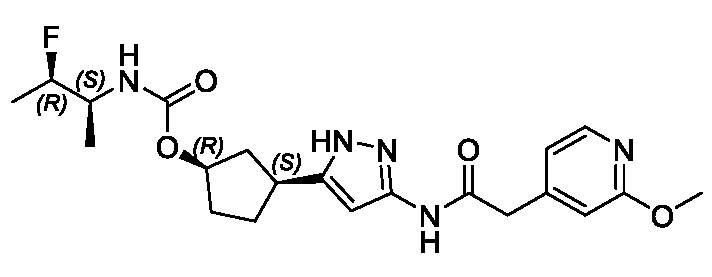
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(2S,3R)-3-фторбутан-2-ил]карбамат
Все стереоцентры известны
(B)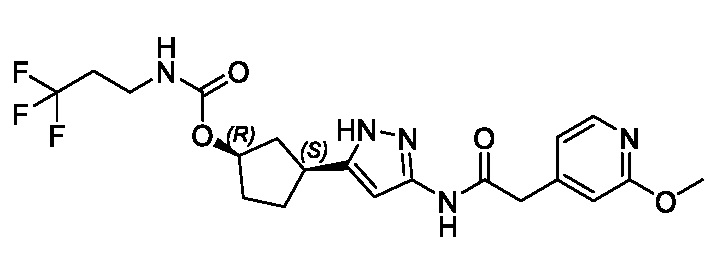
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (3,3,3-трифторпропил)карбамат
Все стереоцентры известны
(B)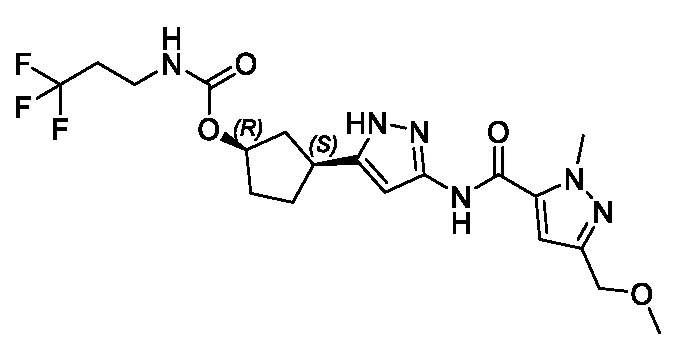
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил (3,3,3-трифторпропил)карбамат
Все стереоцентры известны
(B)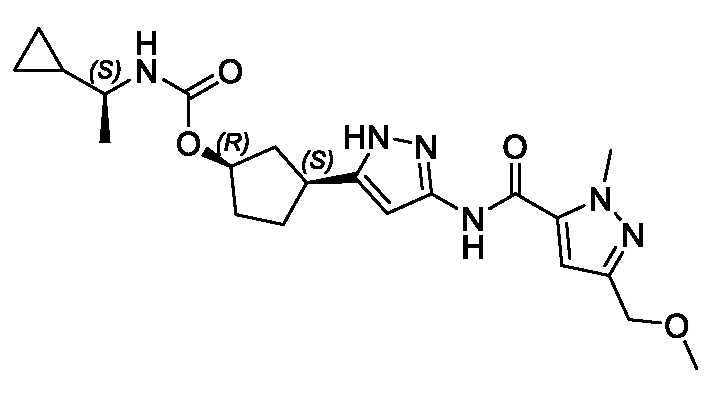
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(1S)-1-циклопропилэтил]карбамат
Все стереоцентры известны
(B)
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил [(1R)-1-циклопропилэтил]карбамат
Все стереоцентры известны
(B)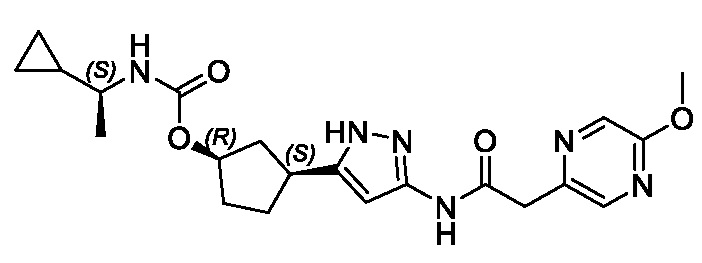
(1R,3S)-3-(3-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(1S)-1-циклопропилэтил]карбамат
Все стереоцентры известны
(D)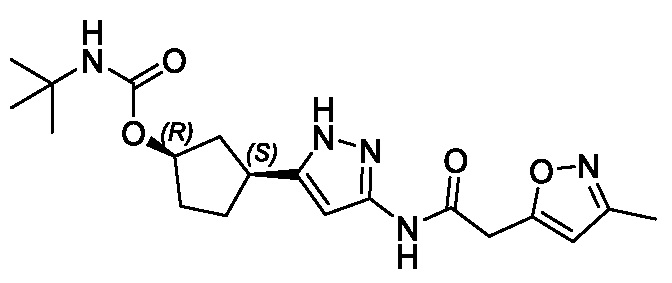
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат
Все стереоцентры известны
(D)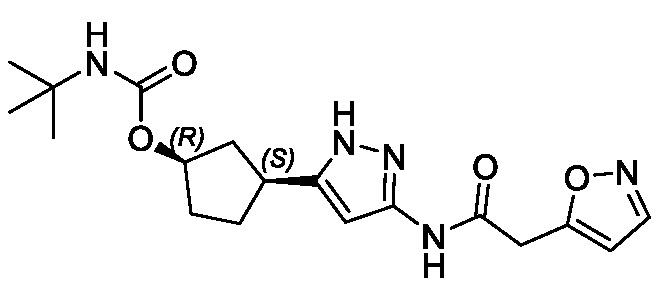
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил трет-бутилкарбамат
Все стереоцентры известны
[α]D25 +8,20 (c 0,13, MeOH);
(D)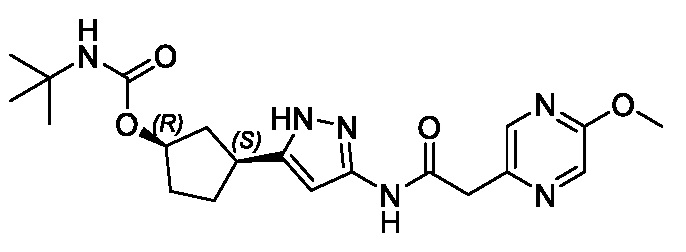
(1R,3S)-3-(3-{[(5-метоксипиразин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат
Все стереоцентры известны
(D)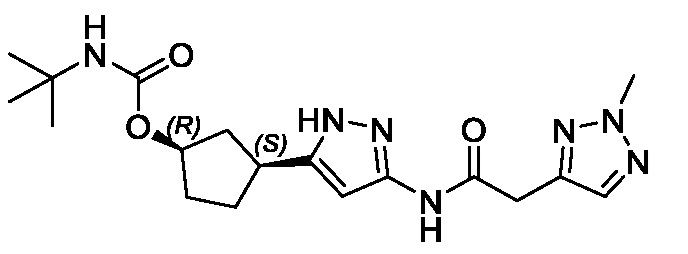
(1R,3S)-3-(3-{[(2-метил-2H-1,2,3-триазол-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат
Все стереоцентры известны
(B)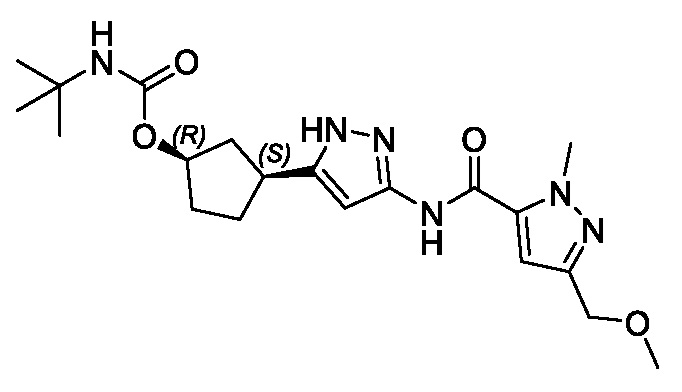
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил трет-бутилкарбамат
Все стереоцентры известны
(B)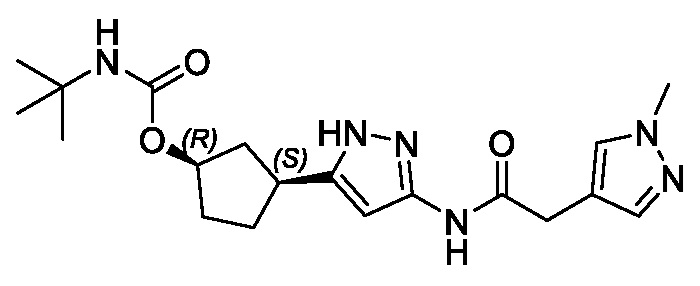
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат
Все стереоцентры известны
(B)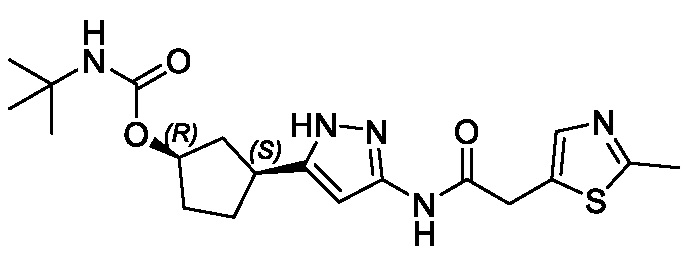
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат
Все стереоцентры известны
(B)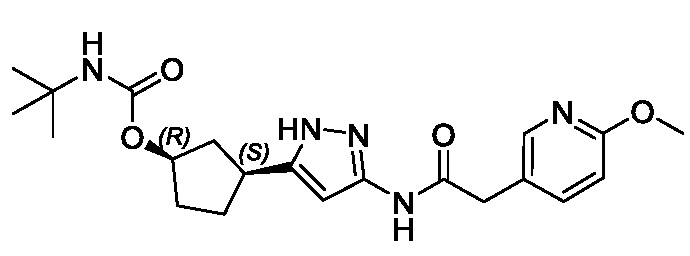
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат
Все стереоцентры известны
(D)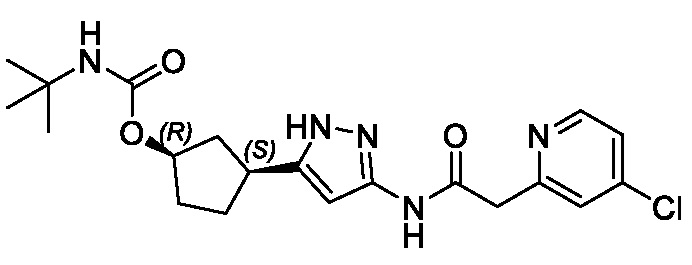
(1R,3S)-3-(3-{[(4-хлорпиридин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил трет-бутилкарбамат
Все стереоцентры известны
(B)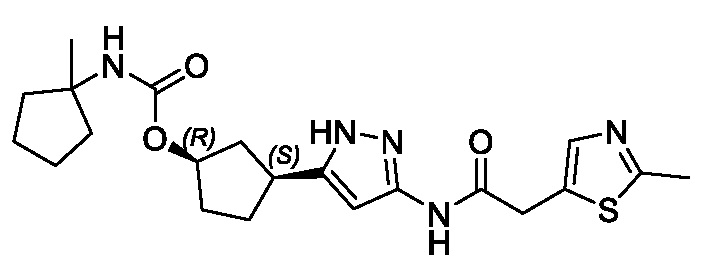
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопентил)-карбамат
Все стереоцентры известны
(B)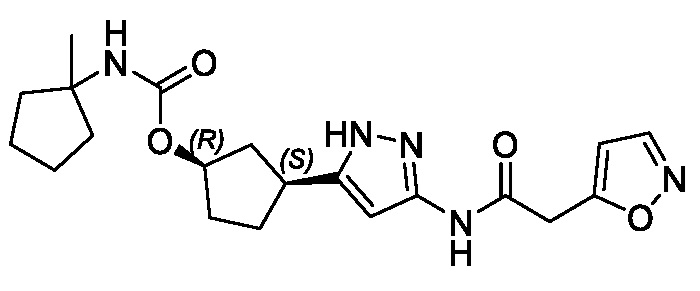
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (1-метилциклопентил)карбамат
Все стереоцентры известны
(B)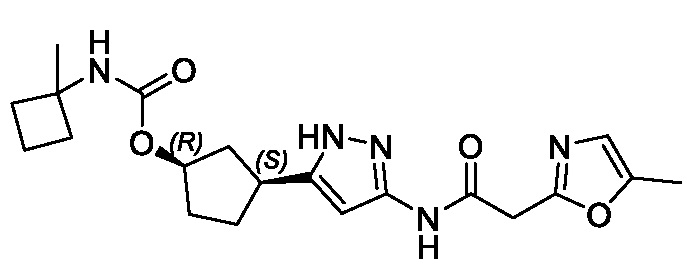
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклобутил)карбамат
Все стереоцентры известны
(B)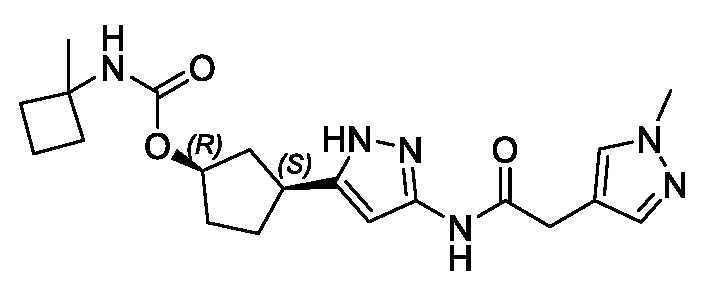
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклобутил)карбамат
Все стереоцентры известны
(B)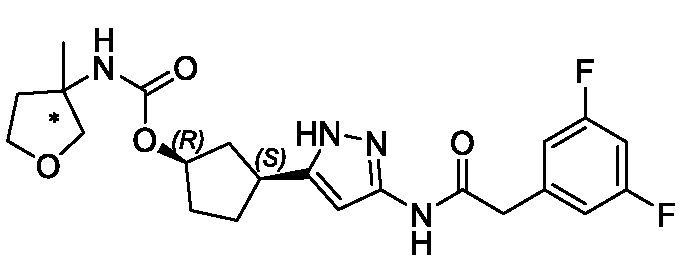
(1R,3S)-3-(3-{[(3,5-дифторфенил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
[α]D25 +16,67 (c 0,2, MeOH)
Пик 1 из 2: Колонка: Chiralpak IC-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°С
(B)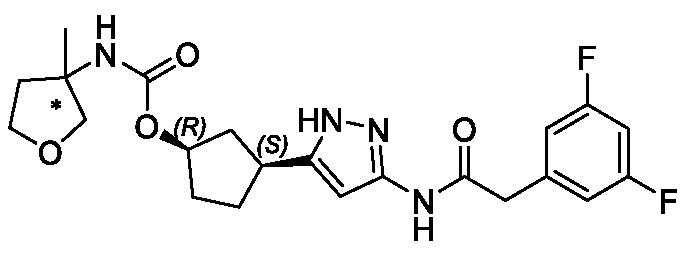
(1R,3S)-3-(3-{[(3,5-дифторфенил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
[α]D20 +12 (c 0,2, MeOH)
Пик 2 из 2: Колонка: Chiralpak IC-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(B)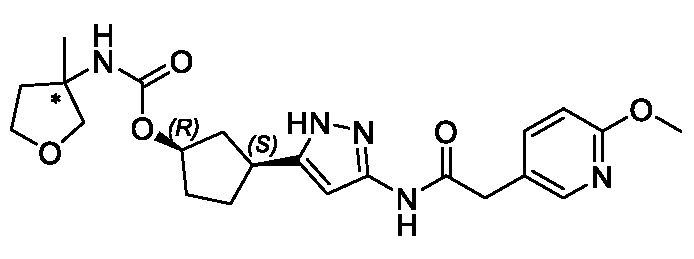
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
[α]D20 +17 (c 0,2, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C,
(B)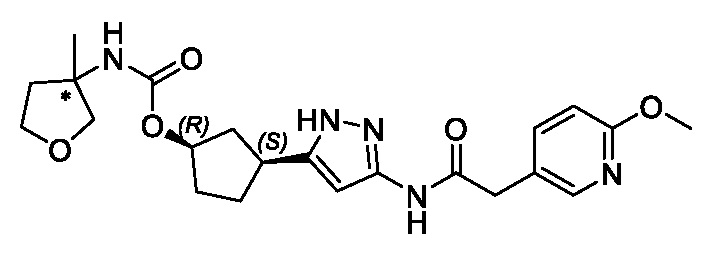
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
[α]D20 +11 (c 0,2, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C,
(A)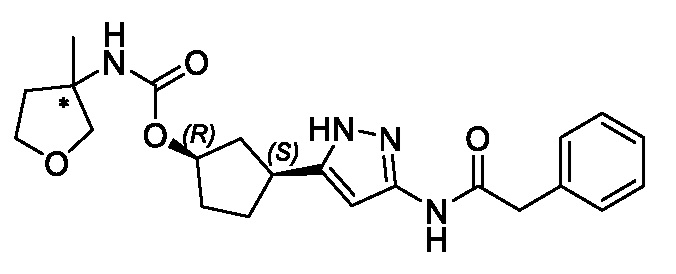
(1R,3S)-3-{3-[(фенилацетил)амино]-1H-пиразол-5-ил}циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
Пик 1 из 2: Колонка: ChiralPak AD-3 150×4,6 мм I.D., 3 мкм; Градиент: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин Температура колонки 40°C
(A)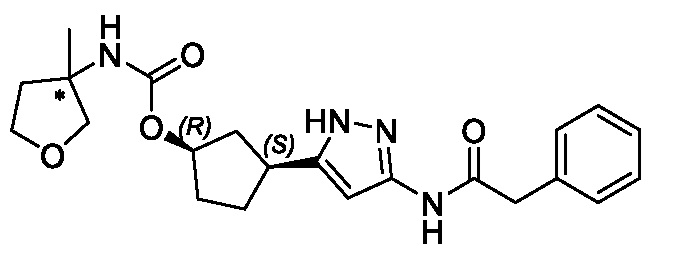
(1R,3S)-3-{3-[(фенилацетил)амино]-1H-пиразол-5-ил}циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
Пик 2 из 2: Колонка: ChiralPak AD-3 150×4,6 мм I.D., 3 мкм; Градиент: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин Температура колонки 40°C
(D)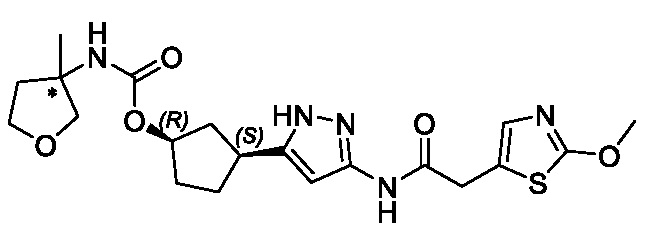
(1R,3S)-3-(3-{[(2-метокси-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
[α]D25 +4 (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak IC-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(D)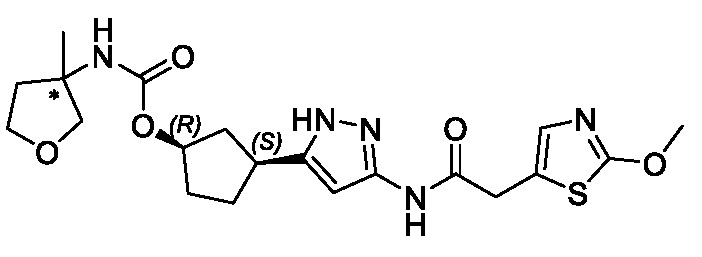
(1R,3S)-3-(3-{[(2-метокси-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил [(3ξ)-3-метилтетрагидрофуран-3-ил]карбамат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в метилтетрагидрофуране не определена
[α]D25 +6 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak IC-3 150×4,6 мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(A)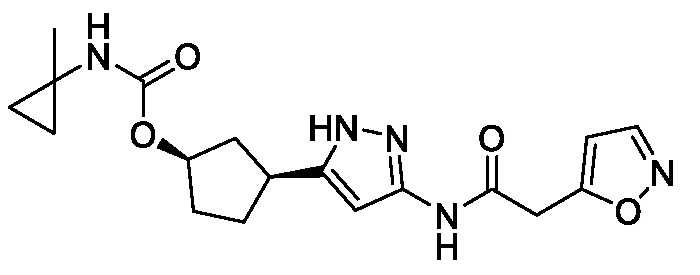
(1R,3S)-3-{3-[(1,2-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил (1-метилциклопропил)карбамат
Все стереоцентры известны
(A)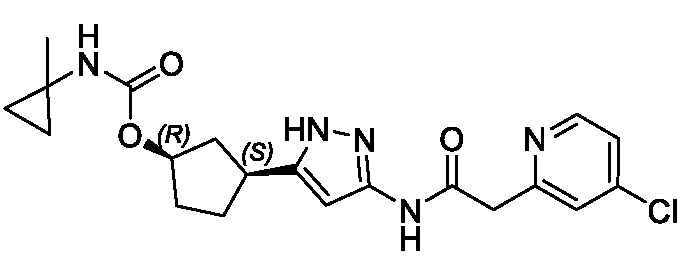
(1R,3S)-3-(3-{[(4-хлорпиридин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат
Все стереоцентры известны
(A)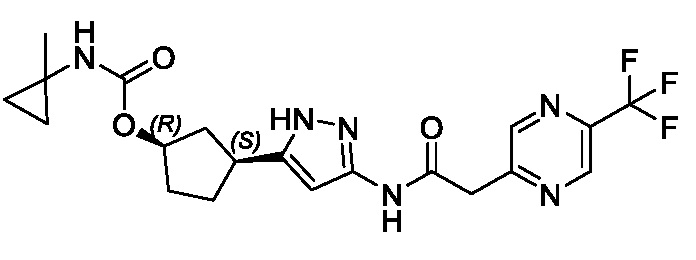
(1R,3S)-3-[3-({[5-(трифторметил)пиразин-2-ил]ацетил}амино)-1H-пиразол-5-ил]циклопентил (1-метилциклопропил)карбамат
Все стереоцентры известны
(A)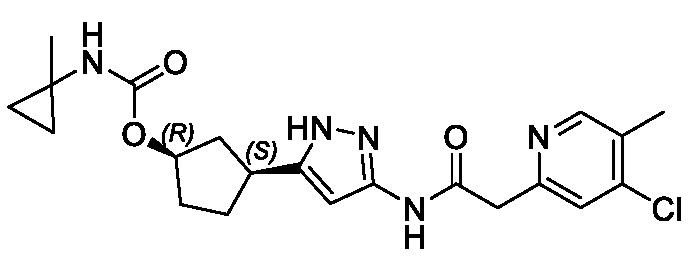
(1R,3S)-3-(3-{[(4-хлор-5-метилпиридин-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат
Все стереоцентры известны
(A)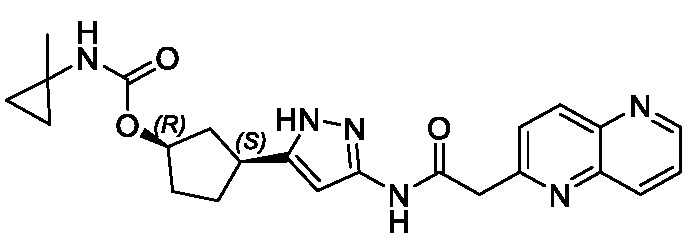
(1R,3S)-3-{3-[(1,5-нафтиридин-2-илацетил)амино]-1H-пиразол-5-ил}циклопентил (1-метилциклопропил)карбамат
Все стереоцентры известны
(A)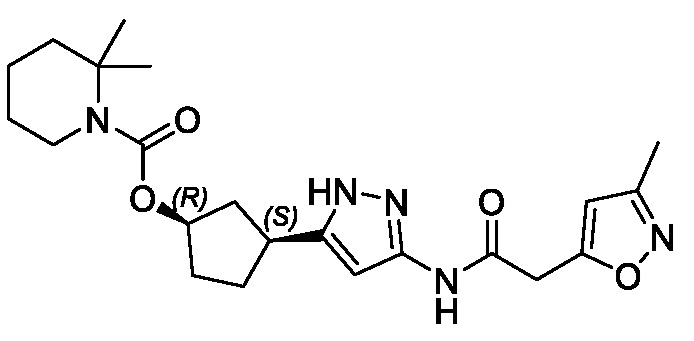
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилпиперидин-1-карбоксилат
Все стереоцентры известны
(B)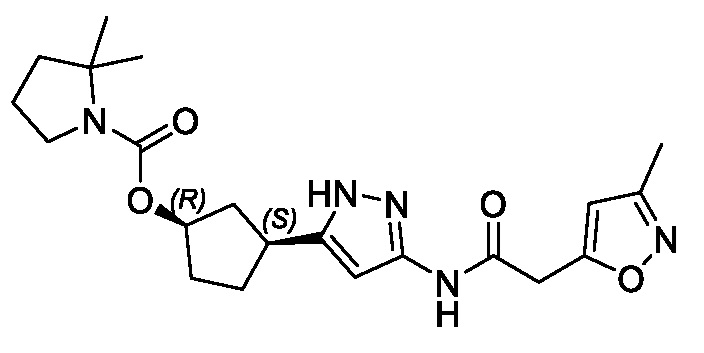
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилпирролидин-1-карбоксилат
Все стереоцентры известны
(A)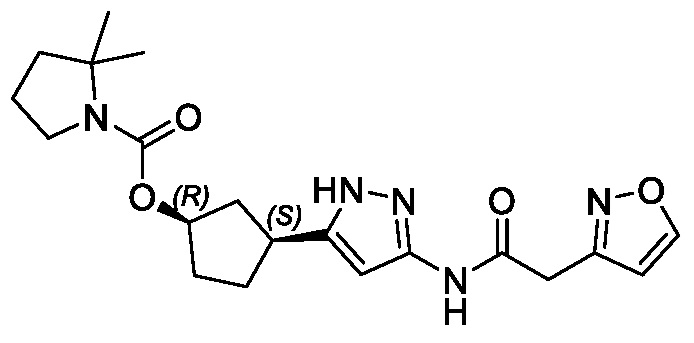
(1R,3S)-3-{3-[(1,2-оксазол-3-илацетил)амино]-1H-пиразол-5-ил}циклопентил 2,2-диметилпирролидин-1-карбоксилат
Все стереоцентры известны
(A)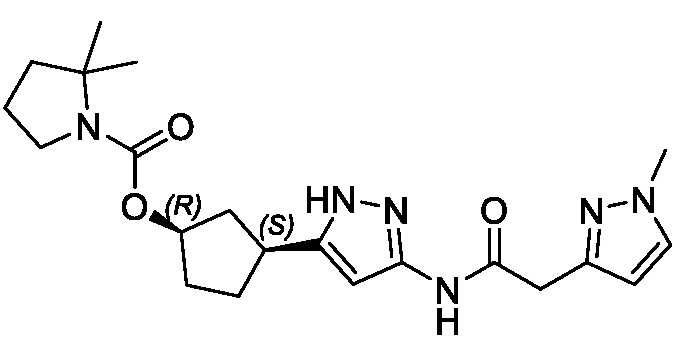
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилпирролидин-1-карбоксилат
Все стереоцентры известны
(A)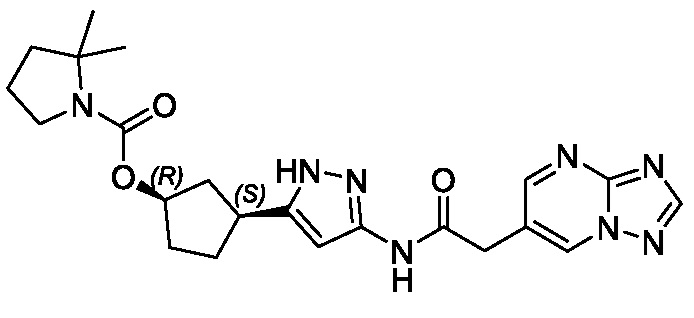
(1R,3S)-3-{3-[([1,2,4]триазоло[1,5-a]пиримидин-6-илацетил)амино]-1H-пиразол-5-ил}циклопентил 2,2-диметилпирролидин-1-карбоксилат
Все стереоцентры известны
(A)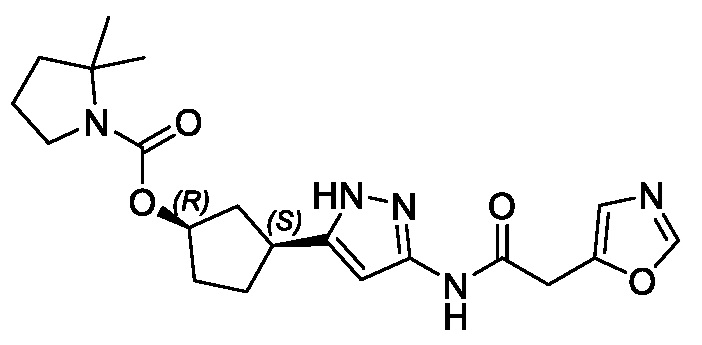
(1R,3S)-3-{3-[(1,3-оксазол-5-илацетил)амино]-1H-пиразол-5-ил}циклопентил 2,2-диметилпирролидин-1-карбоксилат
Все стереоцентры известны
(A)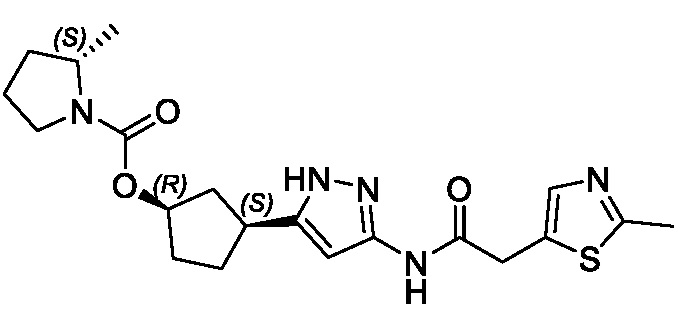
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-2-метилпирролидин-1-карбоксилат
Все стереоцентры известны
(A)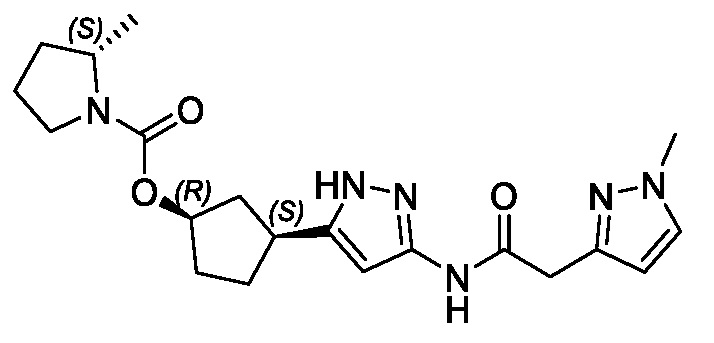
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S)-2-метилпирролидин-1-карбоксилат
Все стереоцентры известны
(A)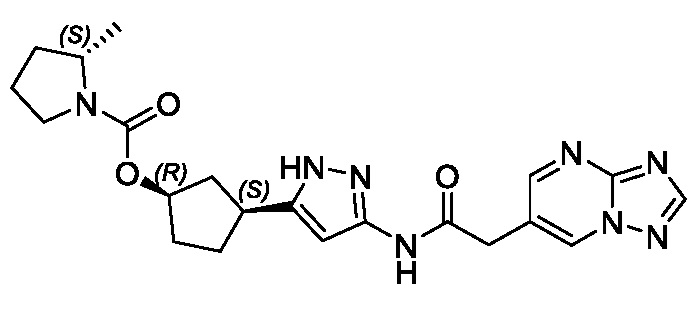
(1R,3S)-3-{3-[([1,2,4]триазоло[1,5-a]пиримидин-6-илацетил)амино]-1H-пиразол-5-ил}циклопентил (2S)-2-метилпирролидин-1-карбоксилат
Все стереоцентры известны
(B)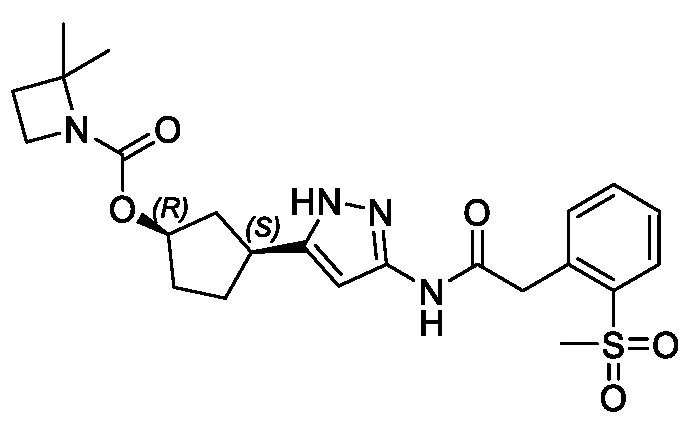
(1R,3S)-3-[3-({[2-(метилсульфонил)фенил]ацетил}амино)-1H-пиразол-5-ил]циклопентил 2,2-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)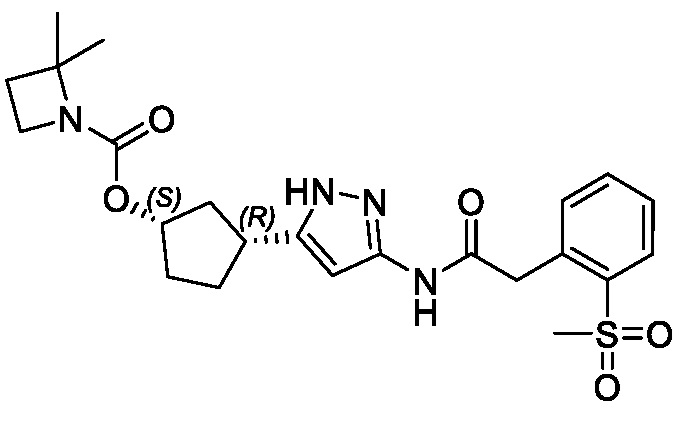
(1S,3R)-3-[3-({[2-(метилсульфонил)фенил]ацетил}амино)-1H-пиразол-5-ил]циклопентил 2,2-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)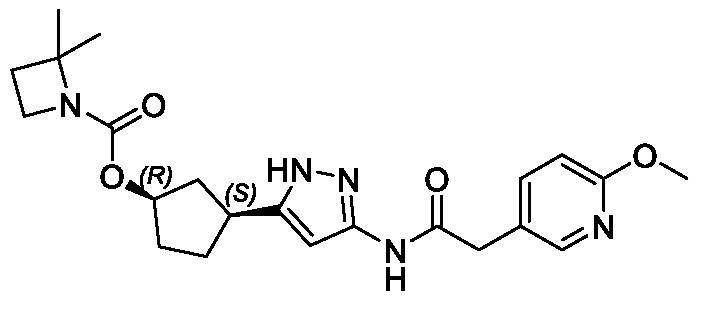
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)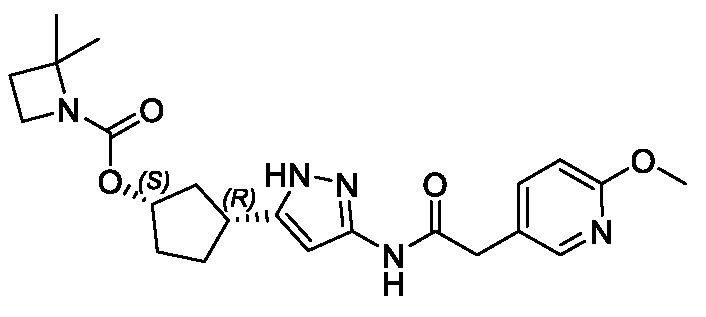
(1S,3R)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)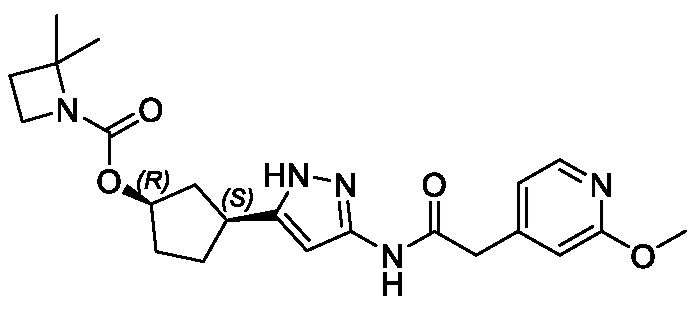
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)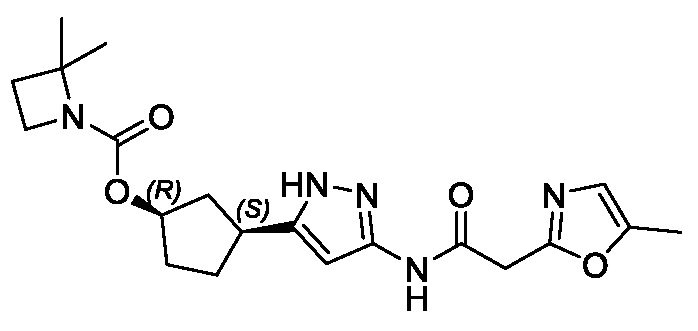
(1R,3S)-3-(3-{[(5-метил-1,3-оксазол-2-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)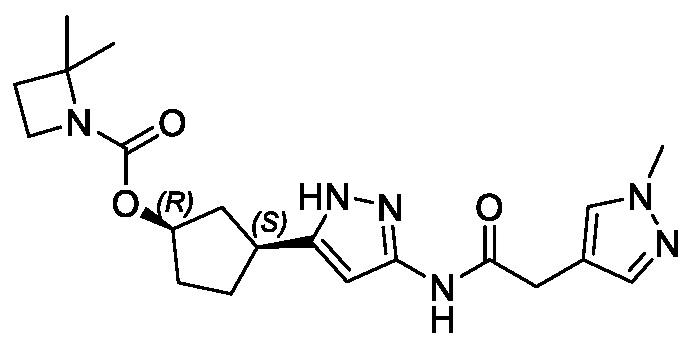
(1R,3S)-3-(3-{[(1-метил-1H-пиразол-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил 2,2-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)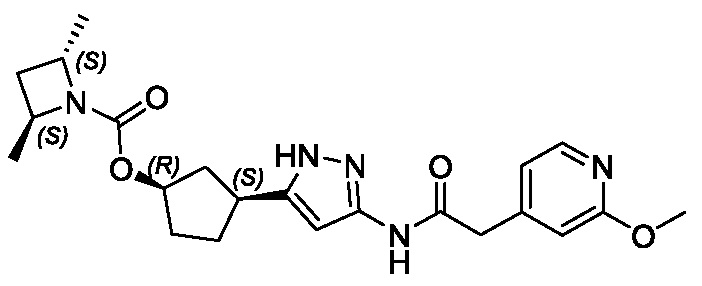
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S,4S)-2,4-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)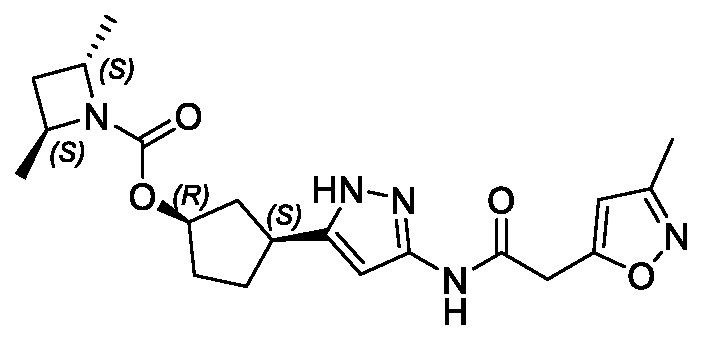
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S,4S)-2,4-диметилазетидин-1-карбоксилат
Все стереоцентры известны
(B)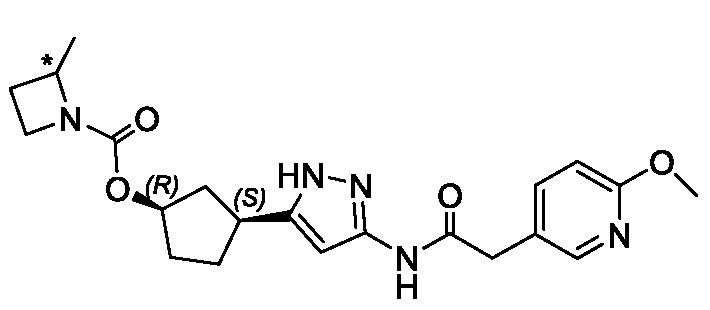
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2ξ)-2-метилазетидин-1-карбоксилат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 2-метилазетидине не определена
[α]D25 +15,0 (c 0,12, MeOH)
Пик 1 из 2 Колонка: Chiralpak AD-3 50×3 мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)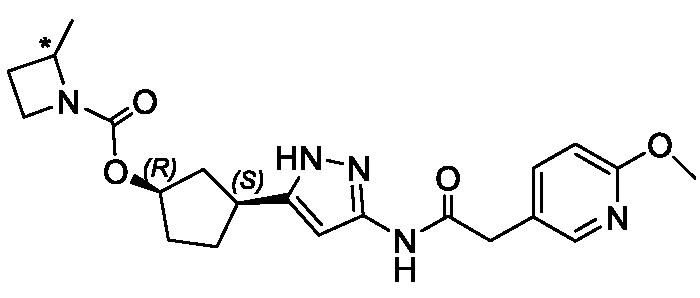
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2ξ)-2-метилазетидин-1-карбоксилат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 2-метилазетидине не определена
[α]D25 -21,15° (c 0,104, MeOH)
Пик 2 из 2 Колонка: Chiralpak AD-3 50×3 мм x3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)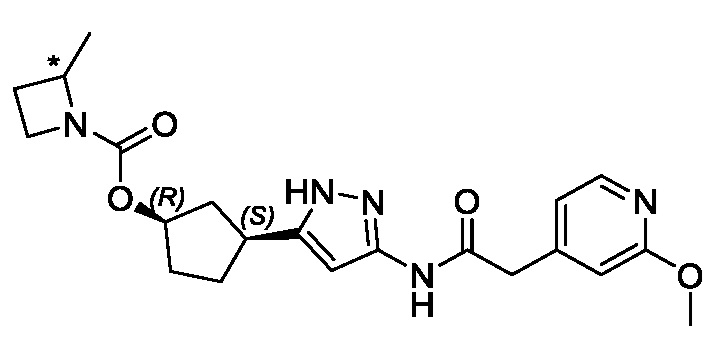
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2ξ)-2-метилазетидин-1-карбоксилат - Изомер A
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 2-метилазетидине не определена
[α]D25 +17,40 (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 50×3мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)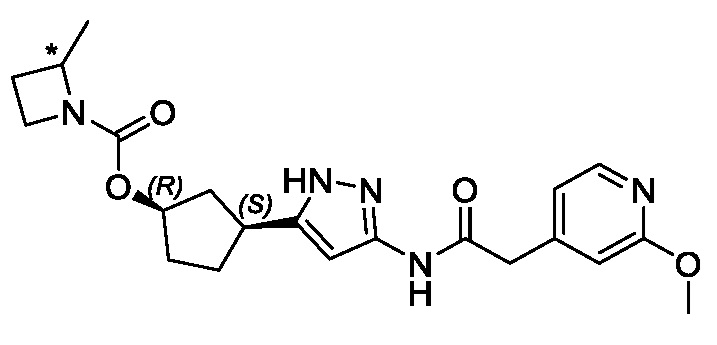
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2ξ)-2-метилазетидин-1-карбоксилат - Изомер B
Одиночный стереоизомер; абсолютная конфигурация хирального центра в 2-метилазетидине не определена
[α]D25 -33,15 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 50×3мм × 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин Температура колонки 40°C
(B)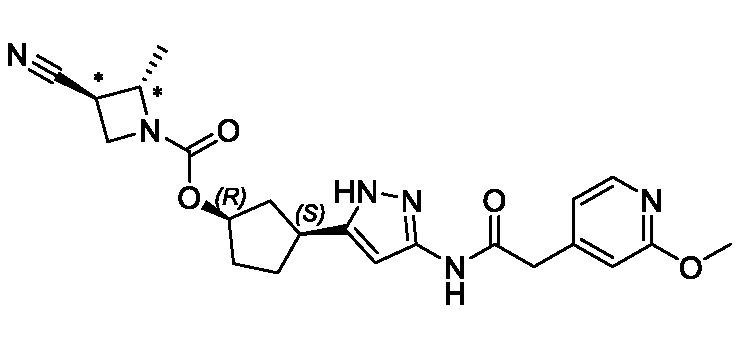
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2R*,3S*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер A
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[[α]D25 -10 (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 50×3 мм I.D., 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин; Температура колонки 40°C
(B)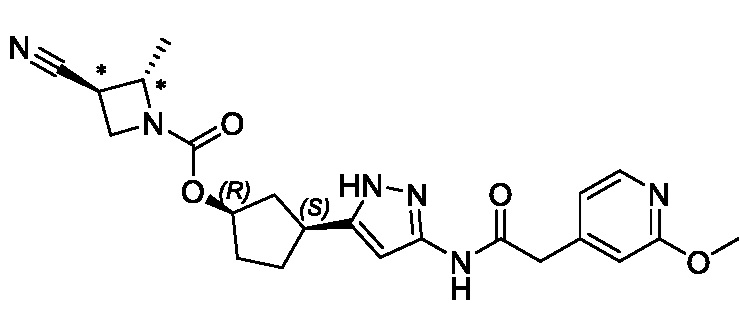
(1R,3S)-3-(3-{[(2-метоксипиридин-4-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2R*,3S*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер B
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[α]D25 -8 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 50×3мм I, D,, 3 мкм; Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 2мл/мин; Температура колонки 40°C
(B)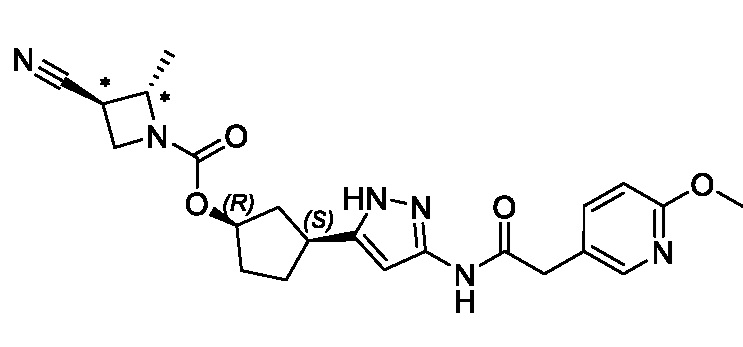
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S*,3R*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер A
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[α]D25 -8 (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak IC-3 150×4,6мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(B)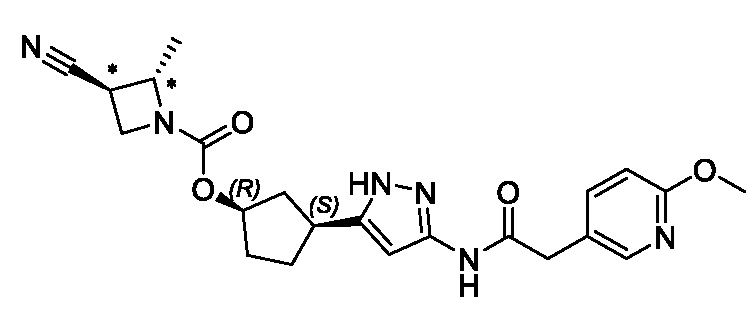
(1R,3S)-3-(3-{[(6-метоксипиридин-3-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S*,3R*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер B
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[α]D25 -10 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak IC-3 150×4,6мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(B)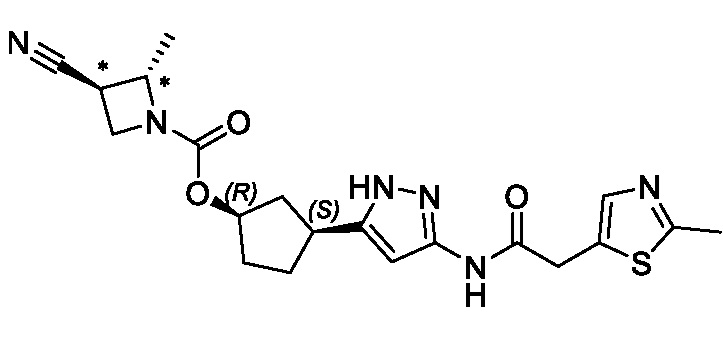
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S*,3R*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер A
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[α]D25 -6 (c 0,1, MeOH)
Пик 1 из 2: Колонка: Chiralpak IC-3 150×4,6мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(B)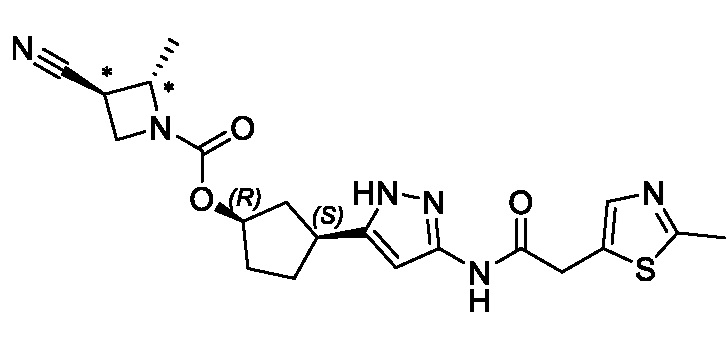
(1R,3S)-3-(3-{[(2-метил-1,3-тиазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (2S*,3R*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер B
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[α]D25 -10 (c 0,1, MeOH)
Пик 2 из 2: Колонка: Chiralpak IC-3 150×4,6мм I.D., 3 мкм; Подвижная фаза: 40% IPA (0,05% DEA) в CO2; Скорость потока: 2,5мл/мин; Температура колонки 35°C
(B)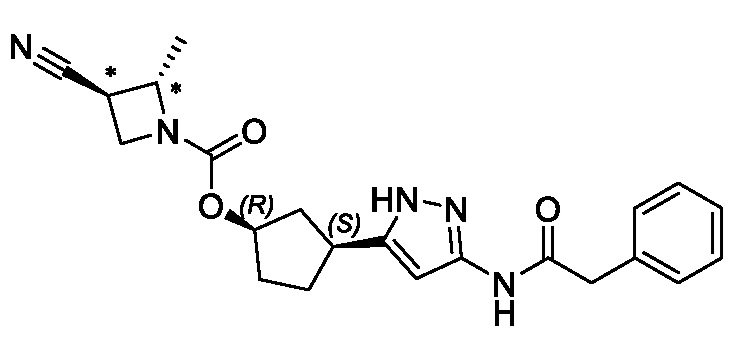
(1R,3S)-3-{3-[(фенилацетил)амино]-1H-пиразол-5-ил}циклопентил (2S*,3R*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер A
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[α]D25 -16,3 (c 0,11, MeOH)
Пик 1 из 2: Колонка: Chiralpak AD-3 50*4,6 мм I.D., 3 мкм: Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 4мл/мин; Температура колонки 40°C
(B)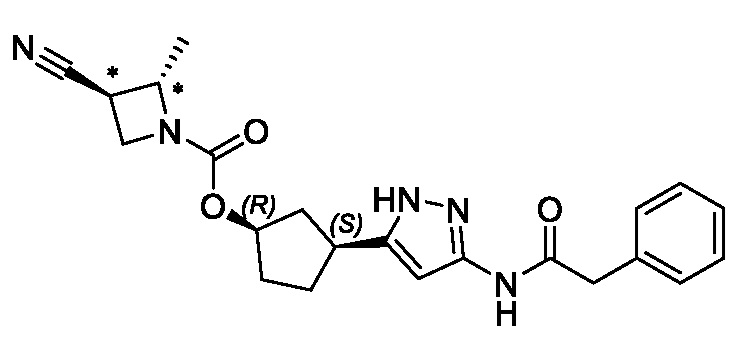
(1R,3S)-3-{3-[(фенилацетил)амино]-1H-пиразол-5-ил}циклопентил (2S*,3R*)-3-циано-2-метилазетидин-1-карбоксилат - Изомер B
Одиночный стереоизомер; метильные и цианогруппы на азетидиновом кольце являются транс, но абсолютная стереохимия этих групп не определена
[α]D25 -7,27 (c 0,12, MeOH)
Пик 2 из 2: Колонка: Chiralpak AD-3 50*4,6мм I.D., 3 мкм: Подвижная фаза: 40% EtOH (0,05% DEA) в CO2; Скорость потока: 4мл/мин; Температура колонки 40°C
Дополнительные соединения по изобретению получали модификациями способов, приведенных в настоящем документе в качестве примеров, и показаны в таблице 3.
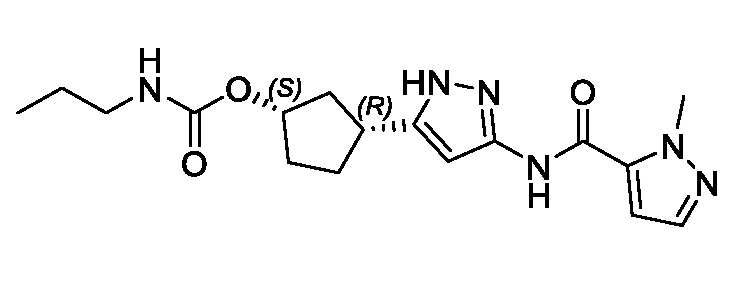
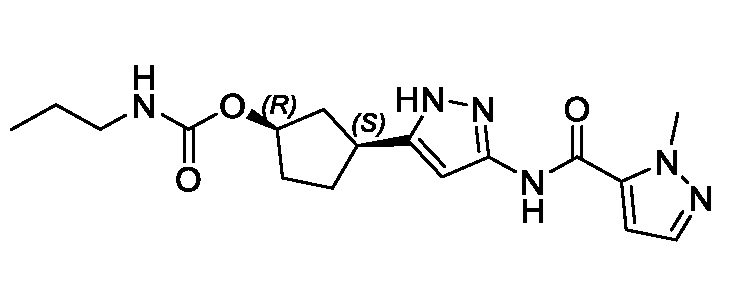
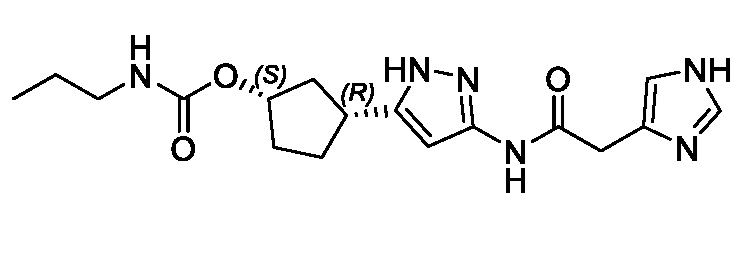
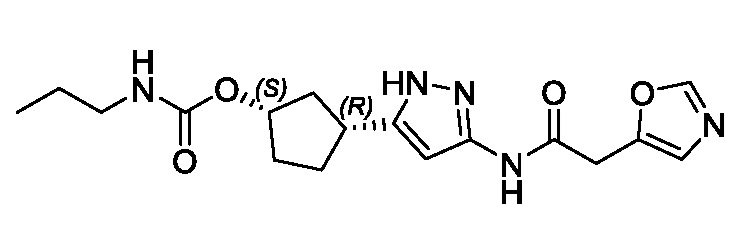
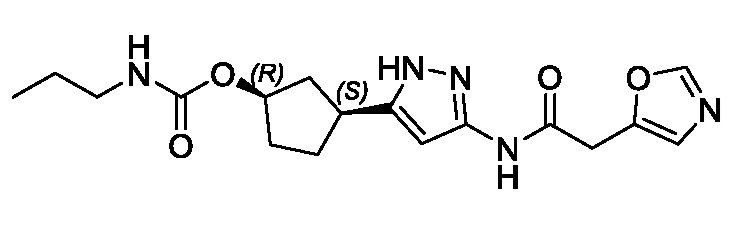
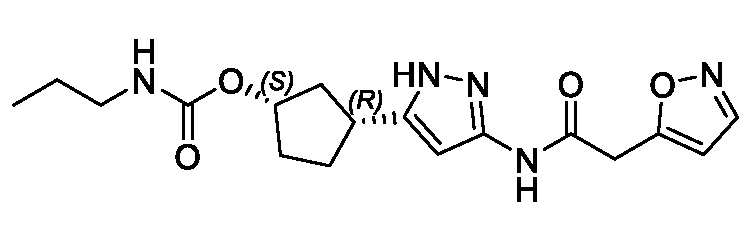
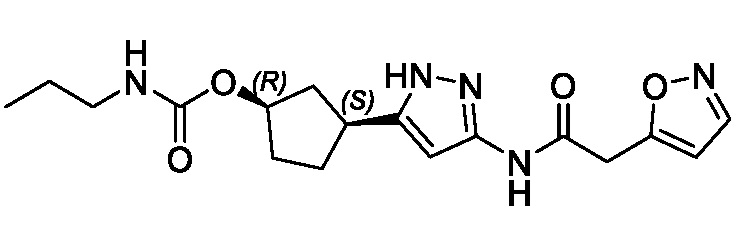
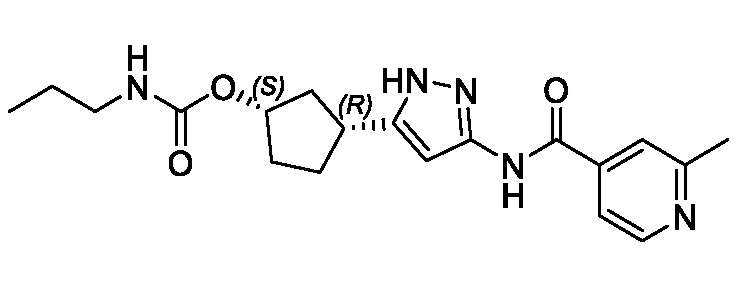
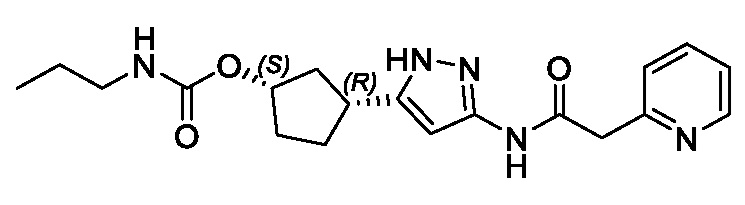
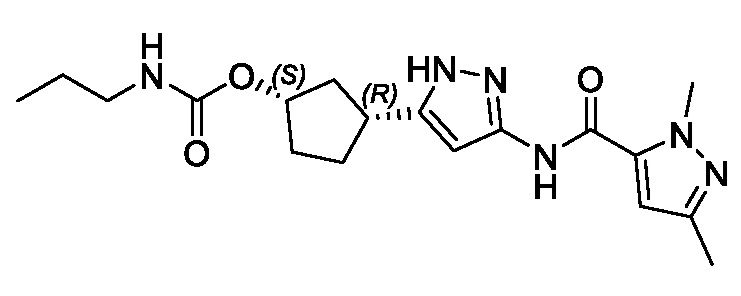
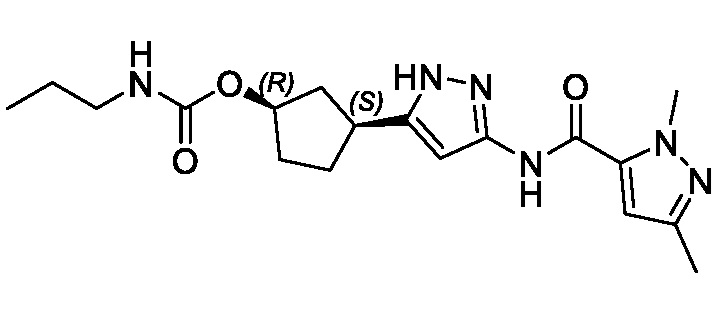
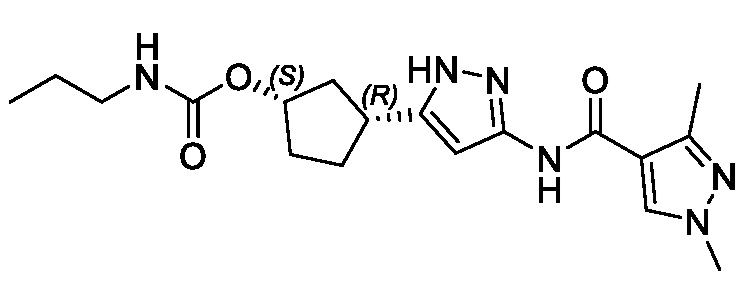
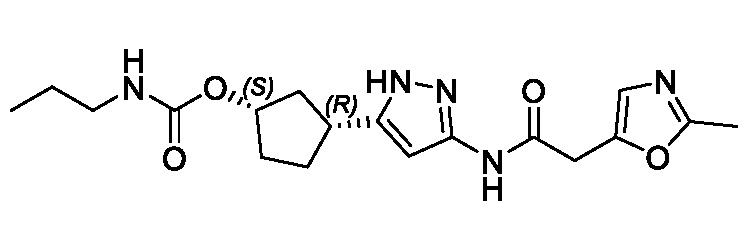
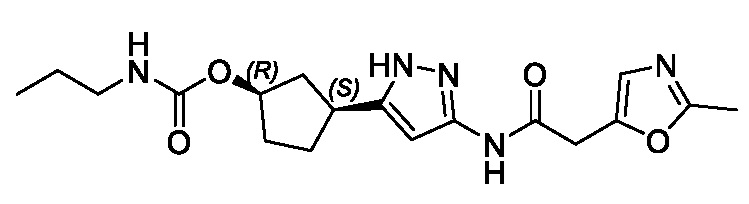
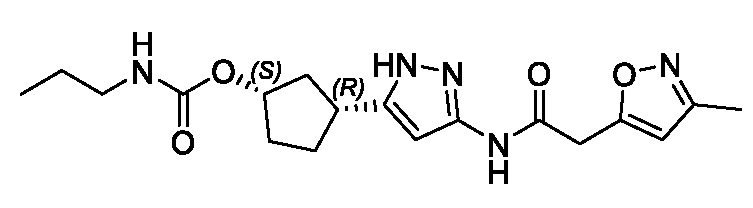
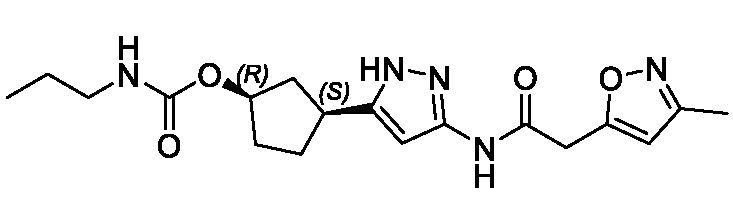
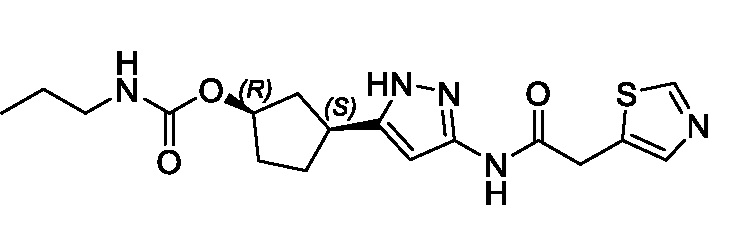
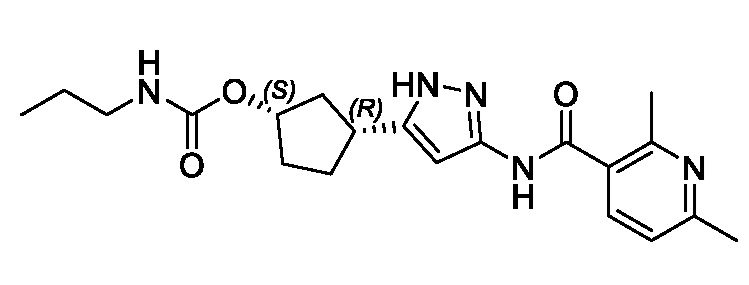
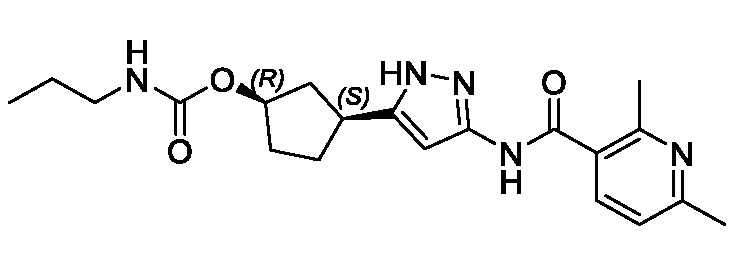
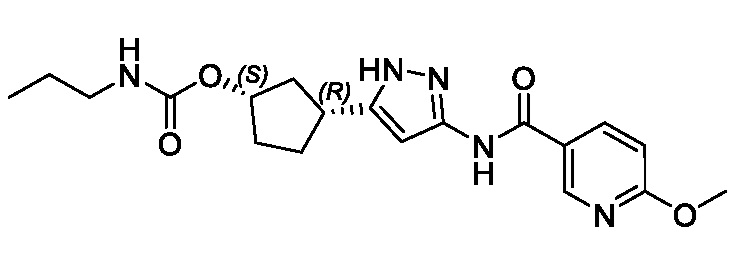
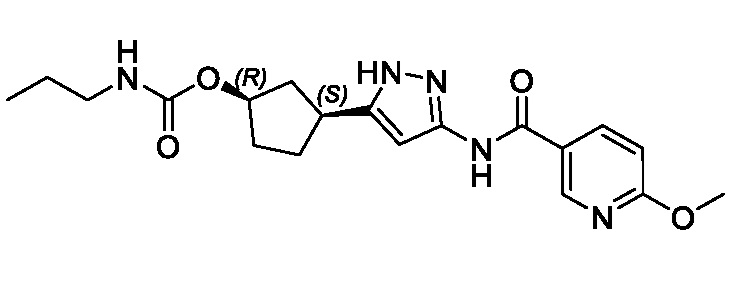
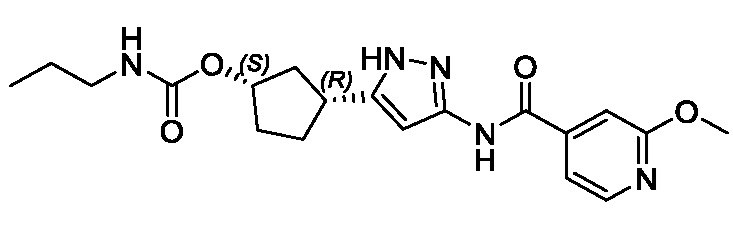
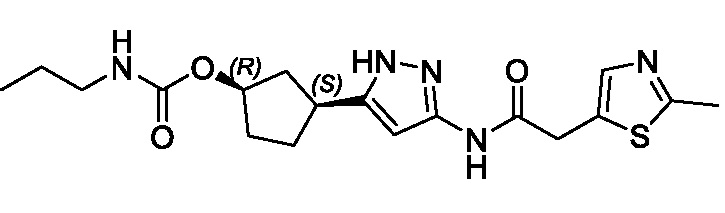
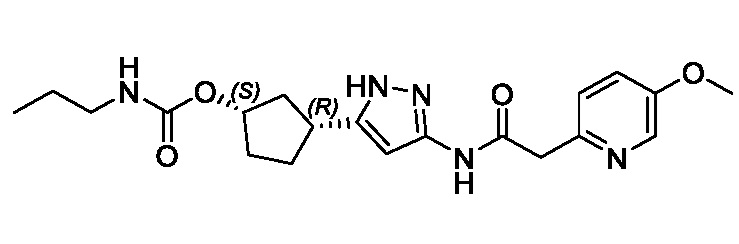
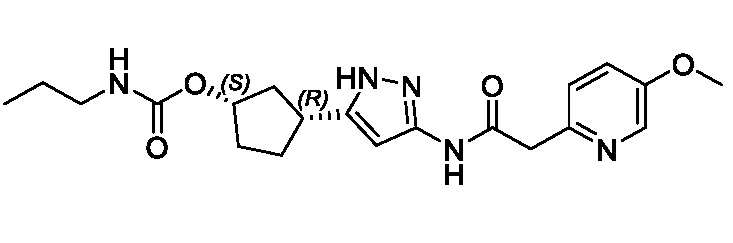
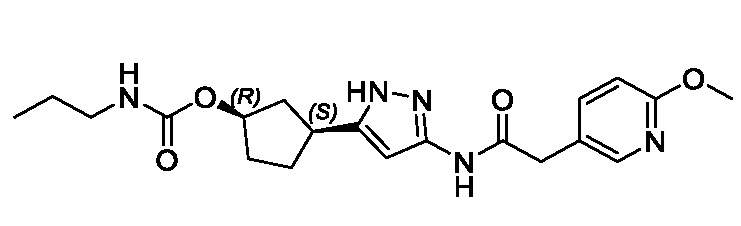
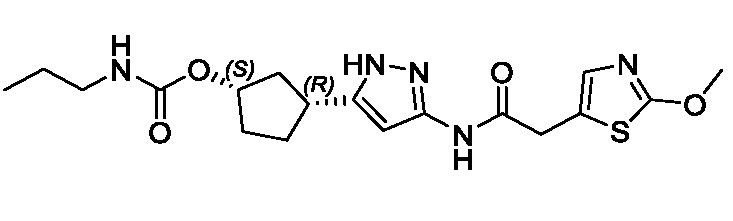
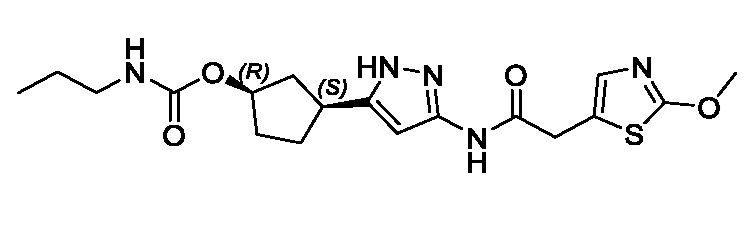
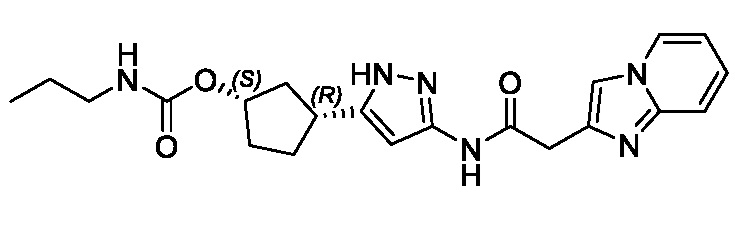
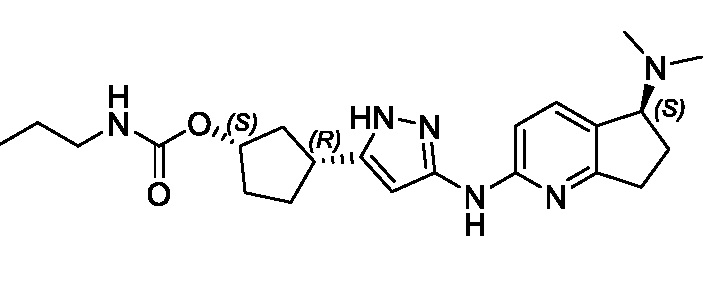
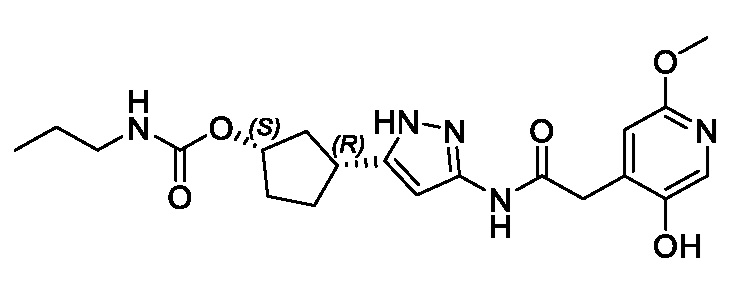
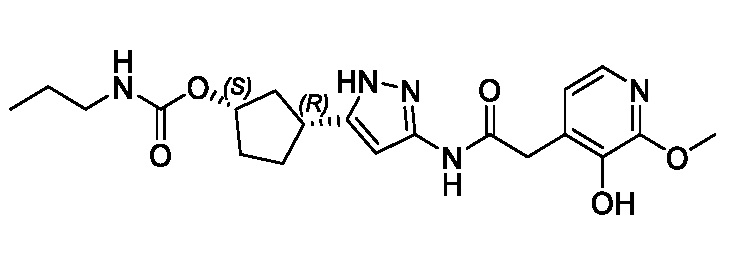
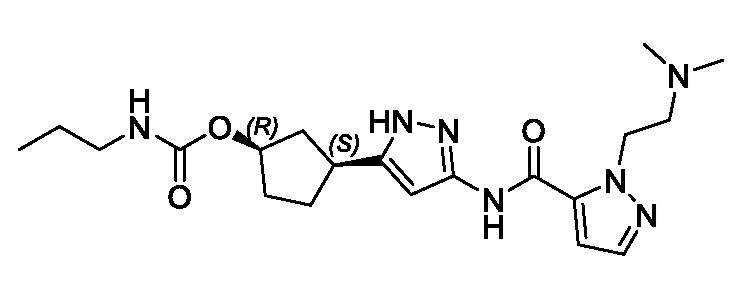
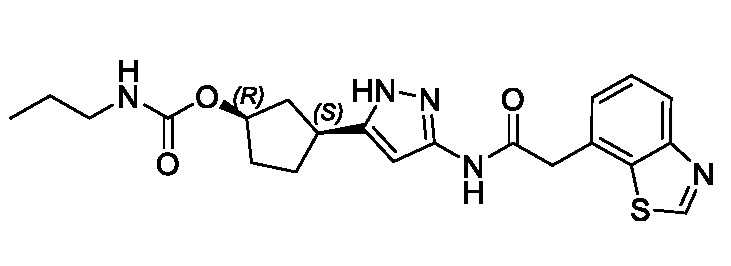
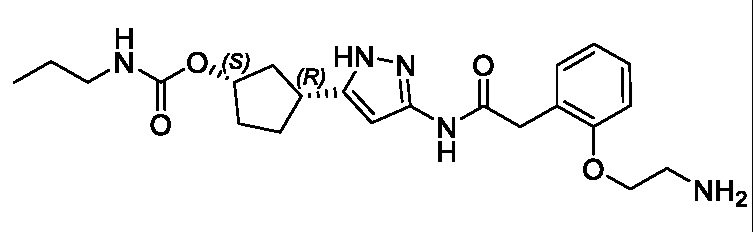
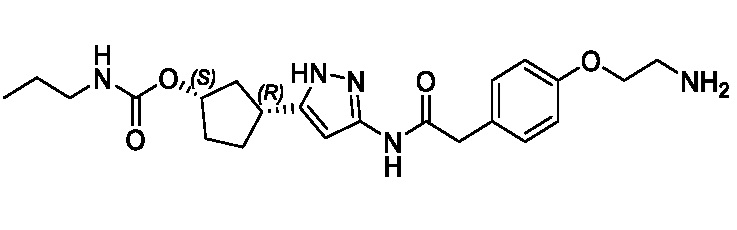
452,2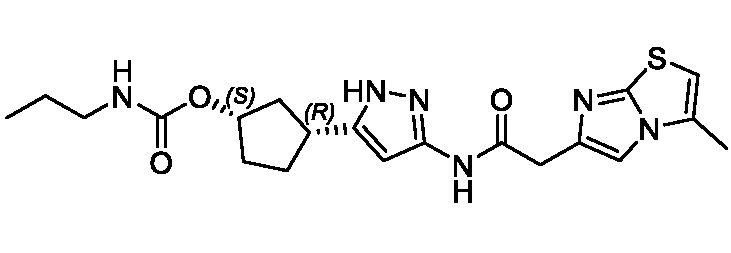
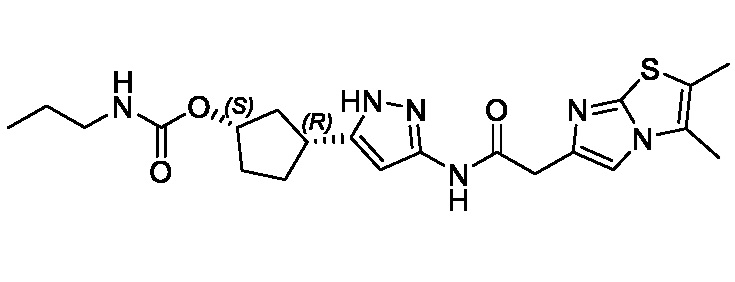
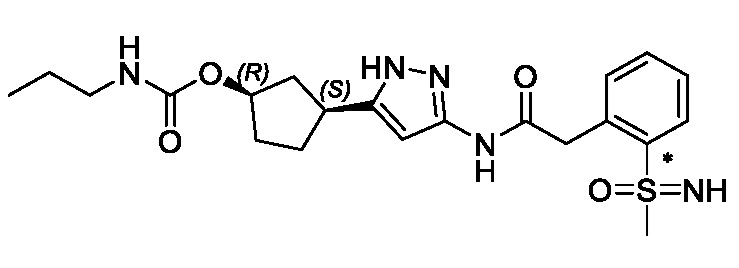
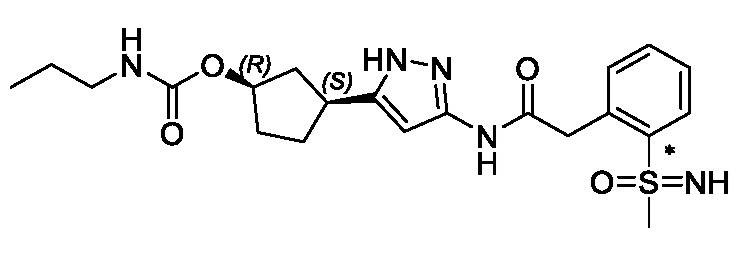
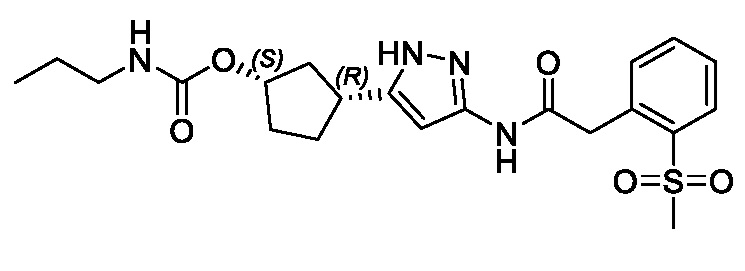
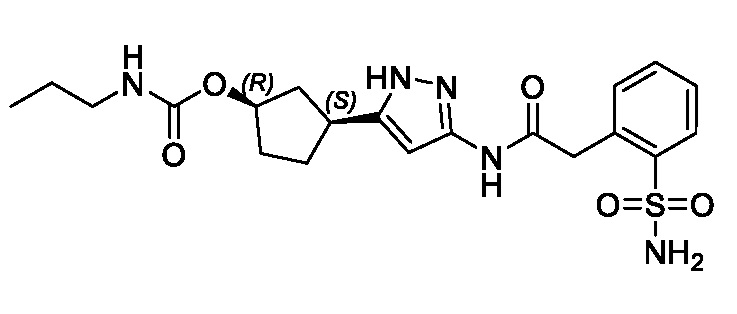
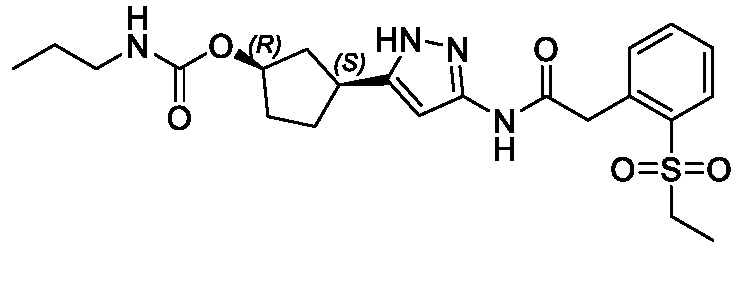
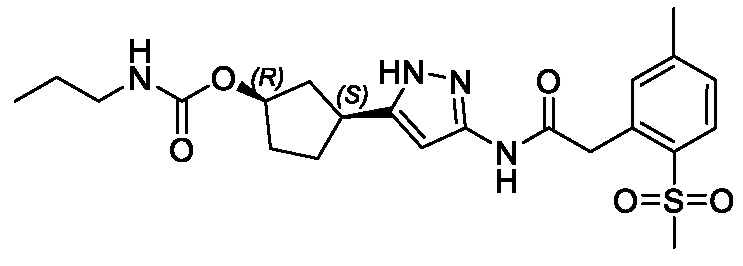
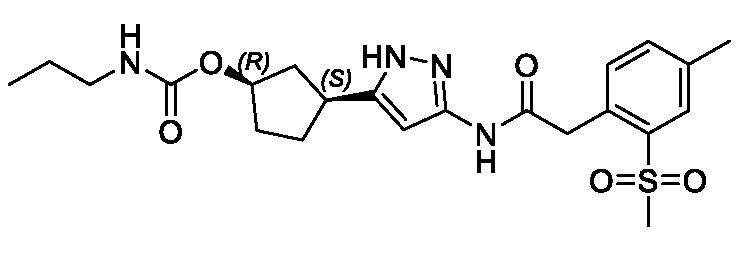
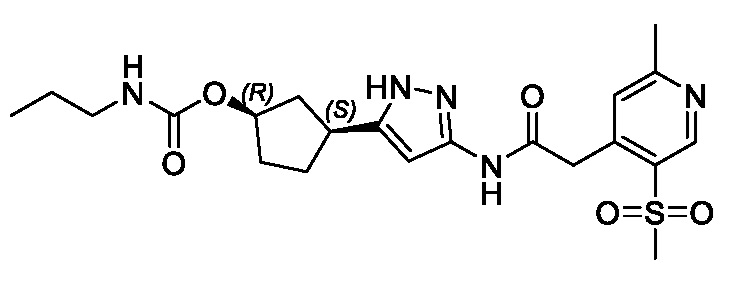
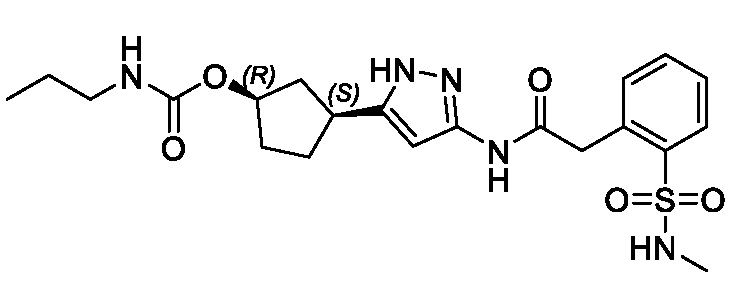
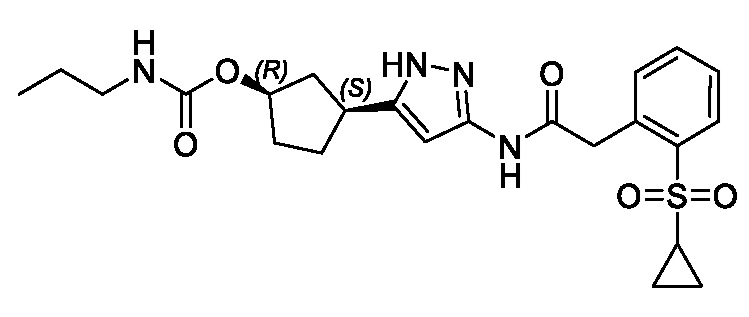
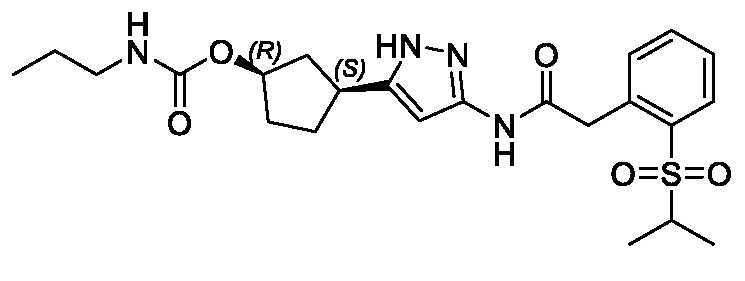
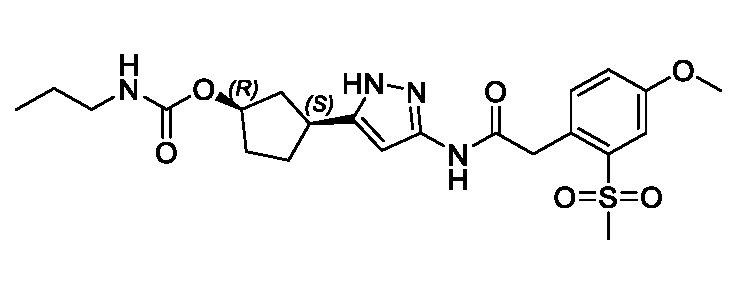
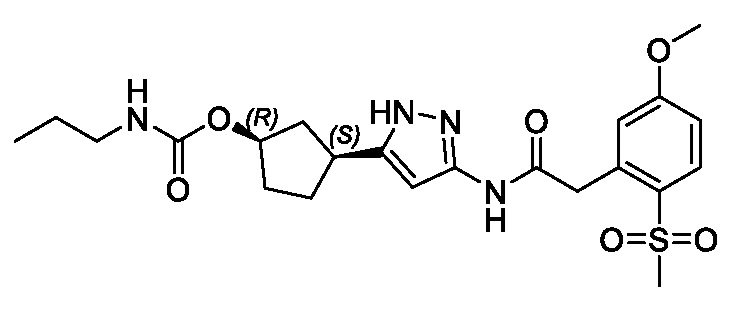
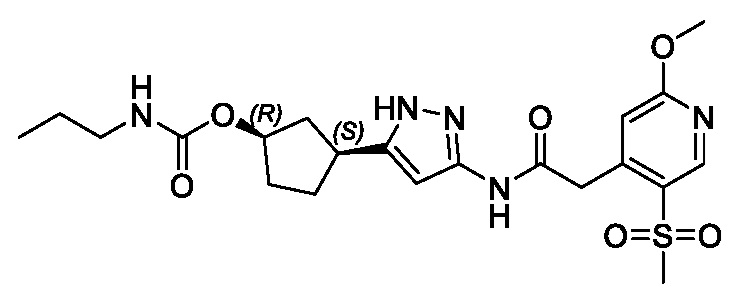
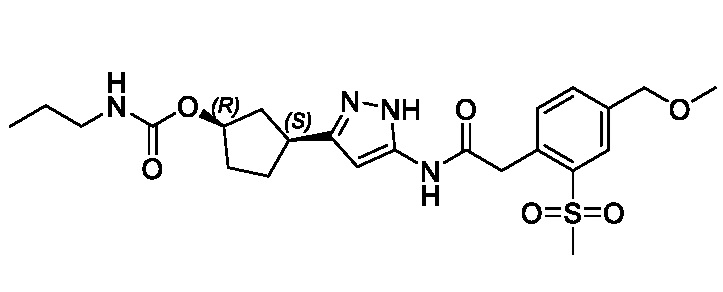
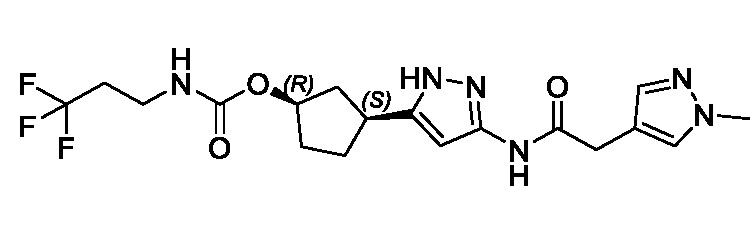
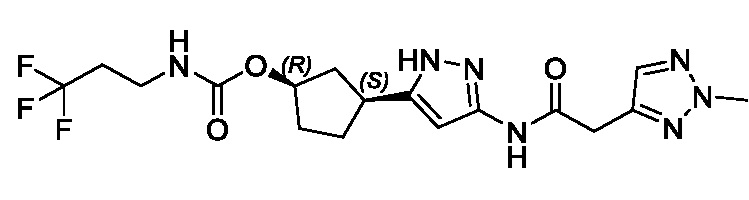
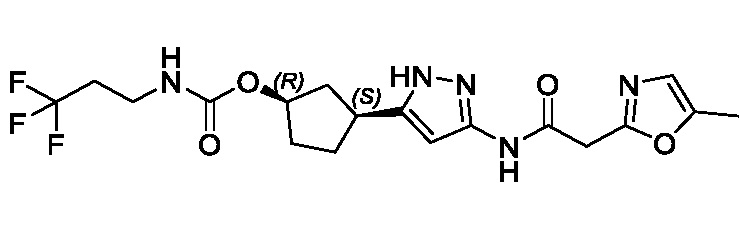
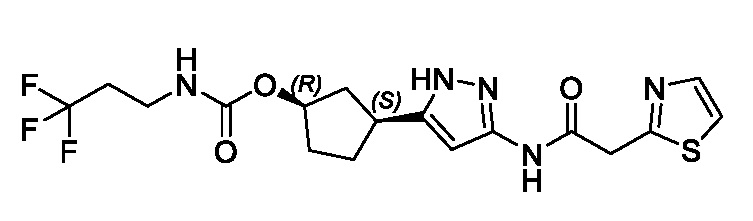
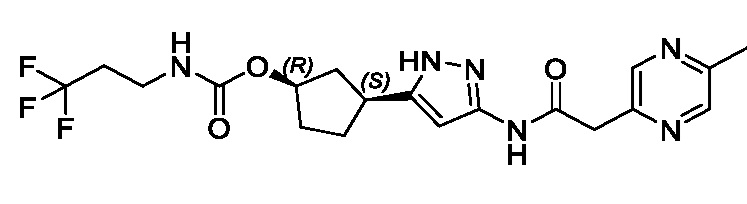
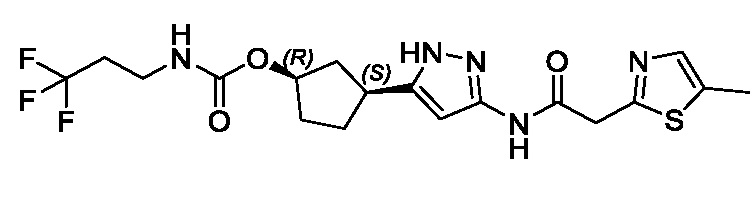
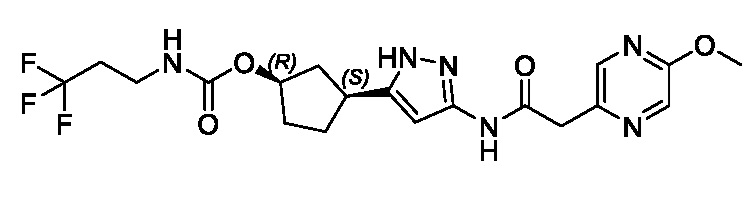
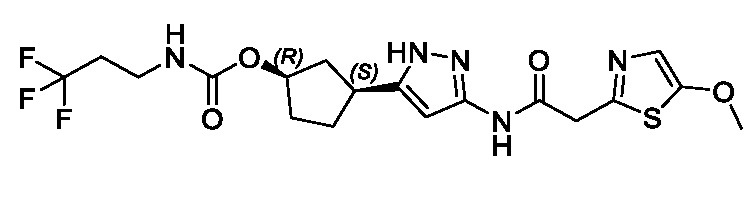
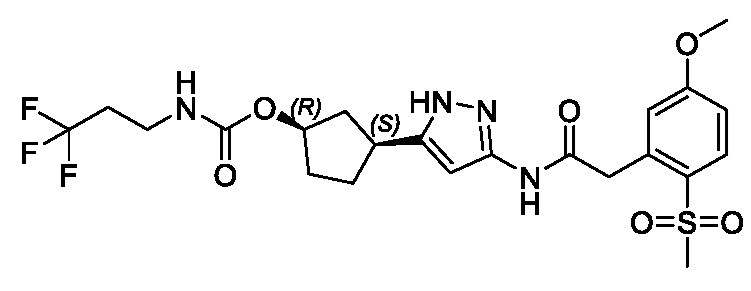
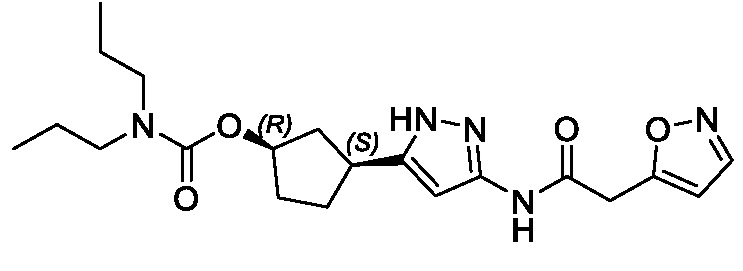
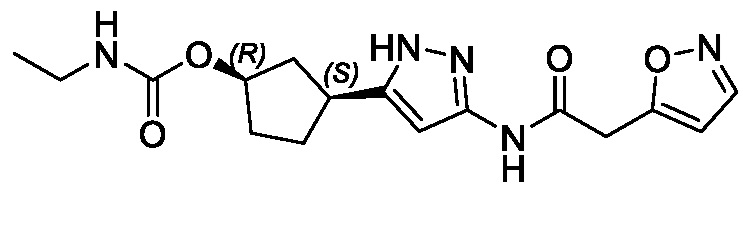
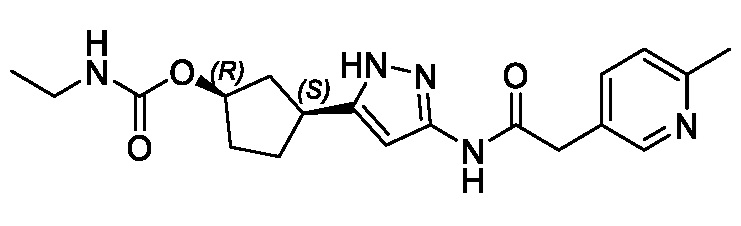
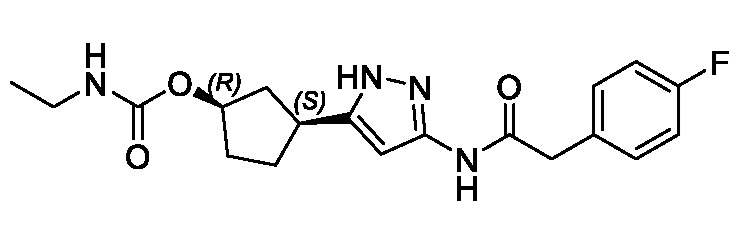
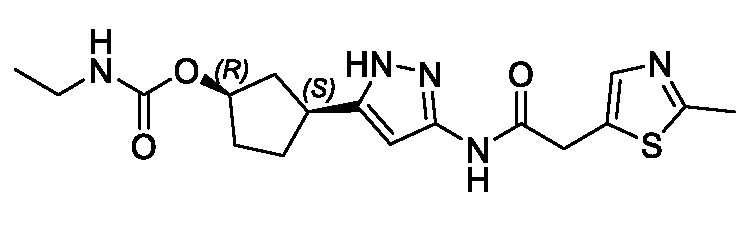
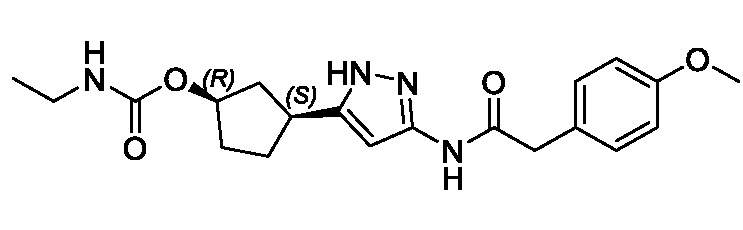
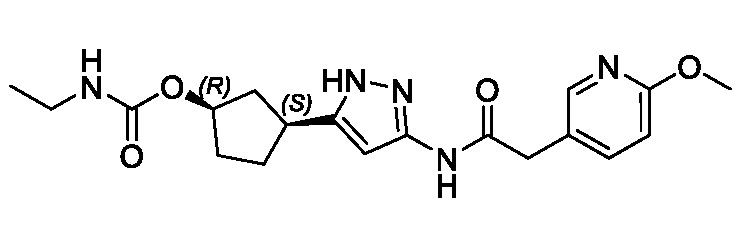
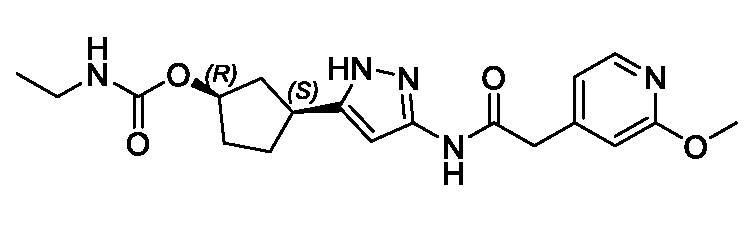
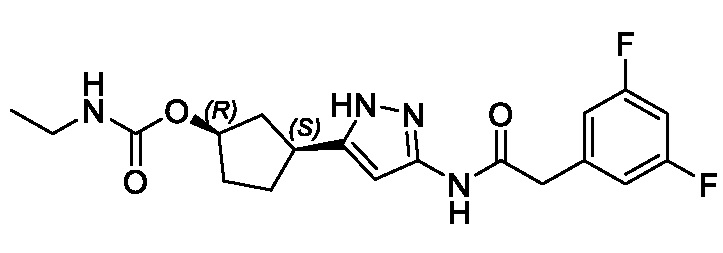
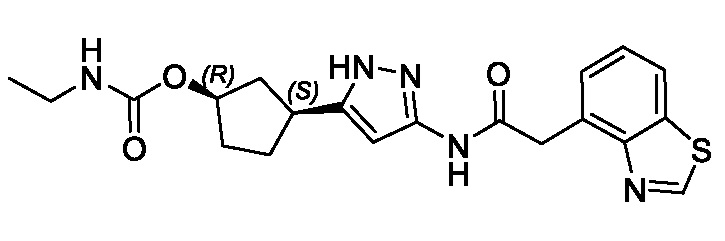
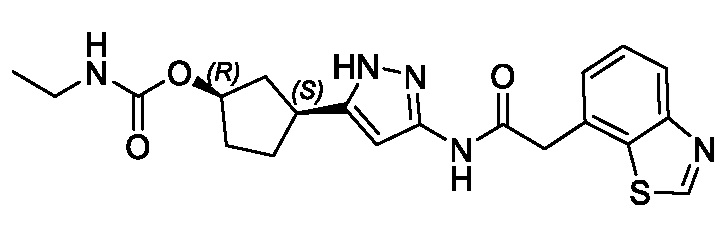
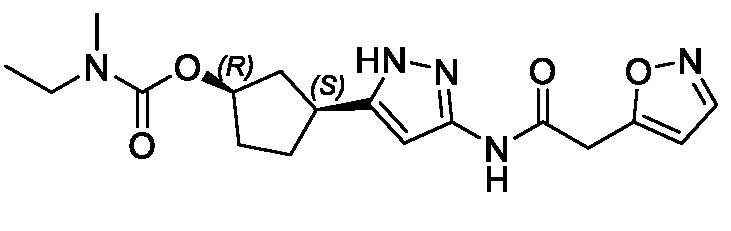
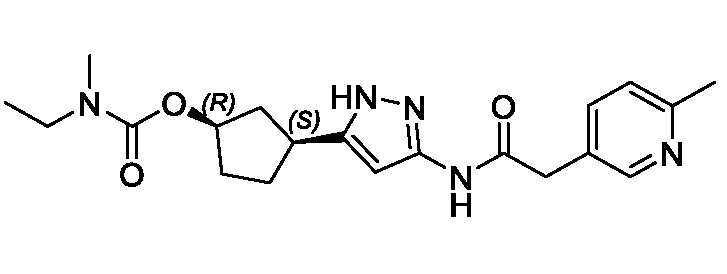
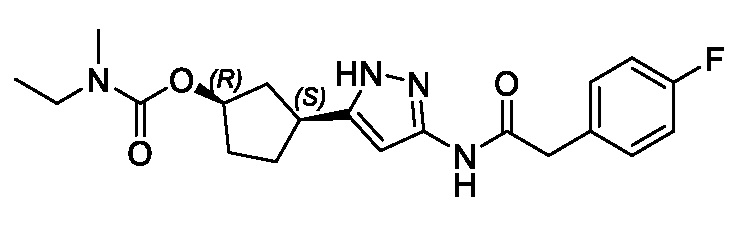
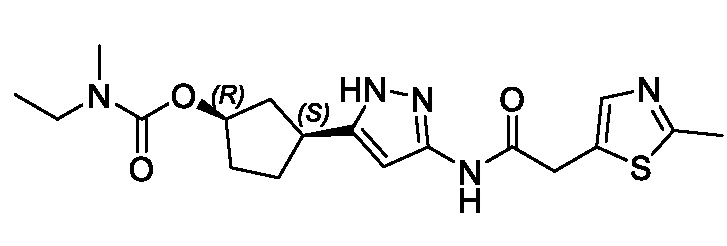
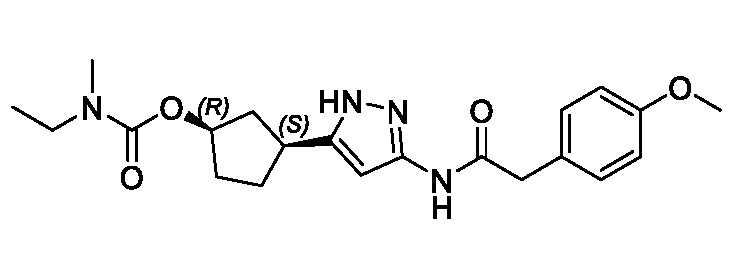
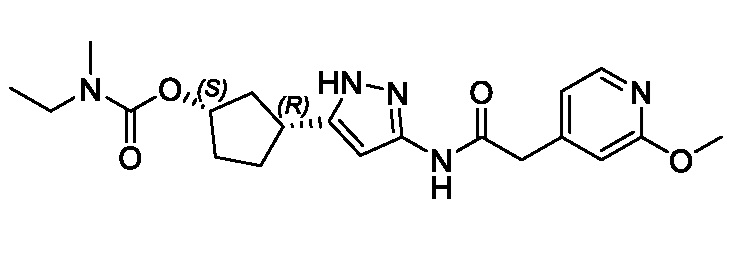
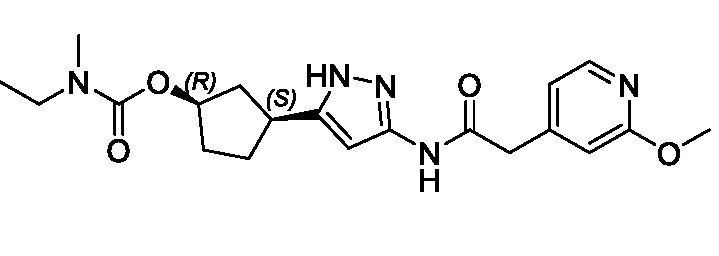
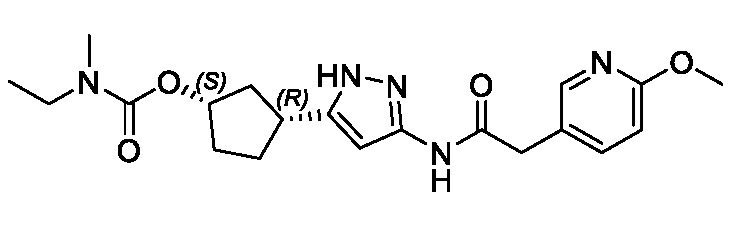
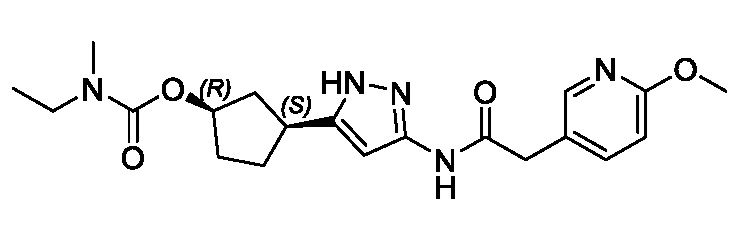
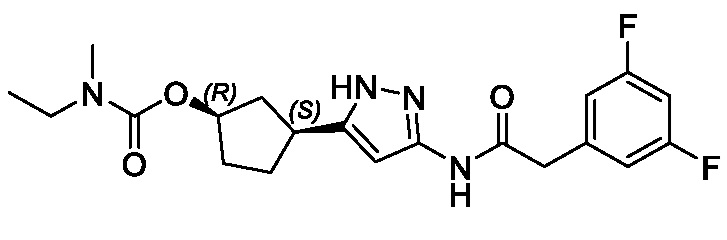
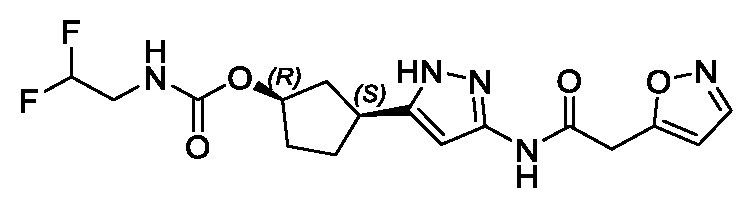
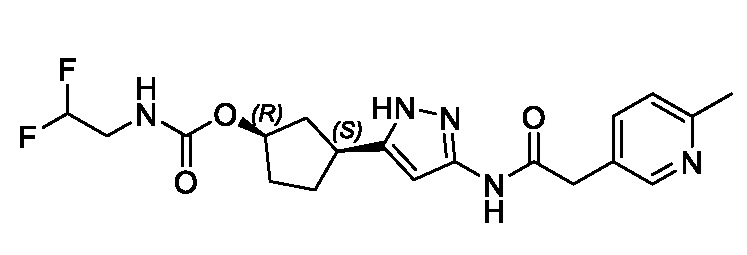
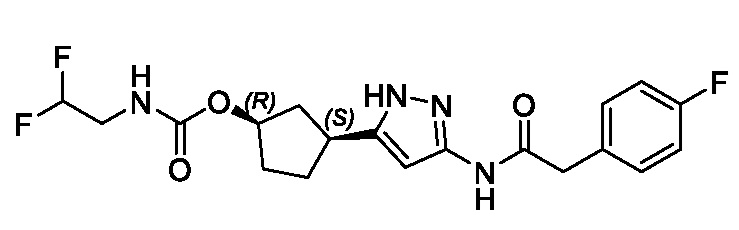
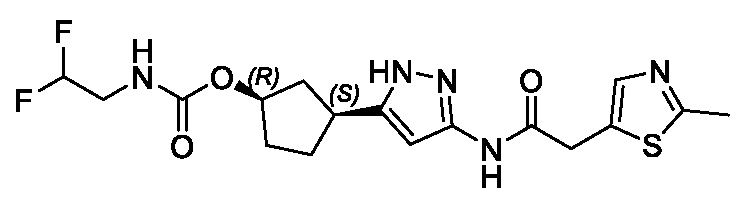
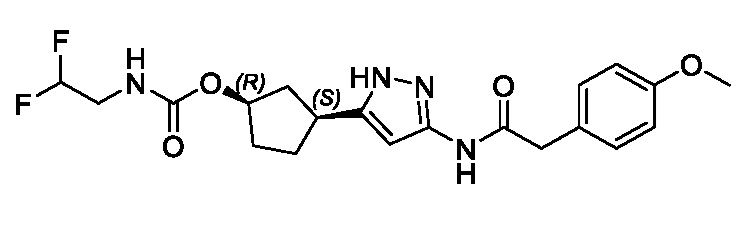
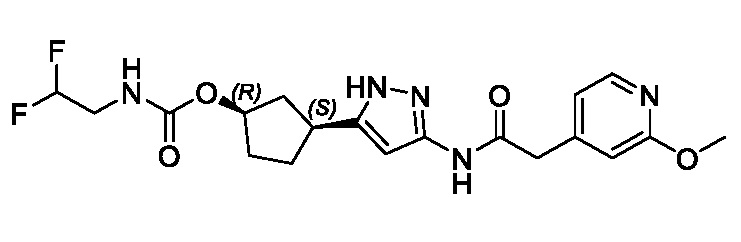
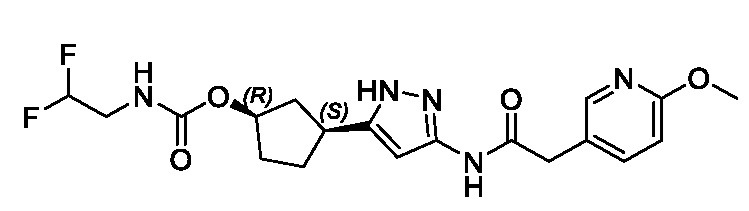
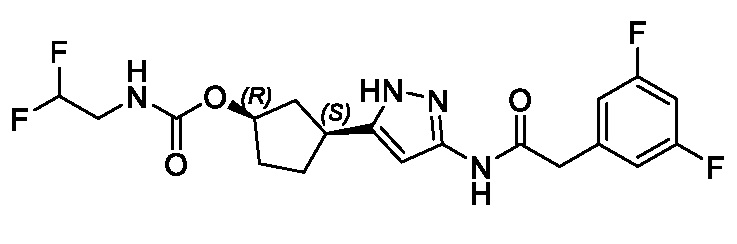
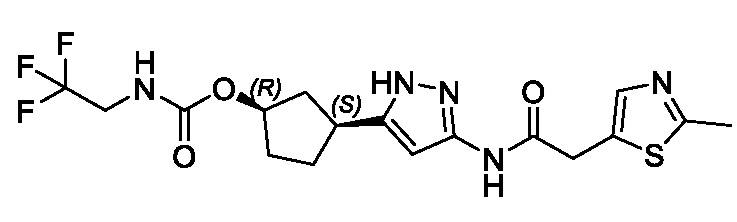
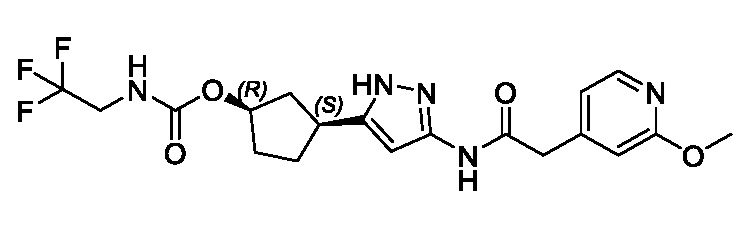
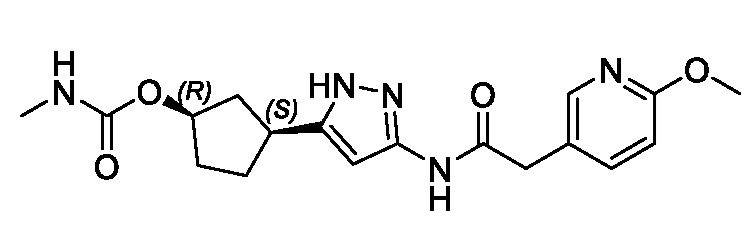
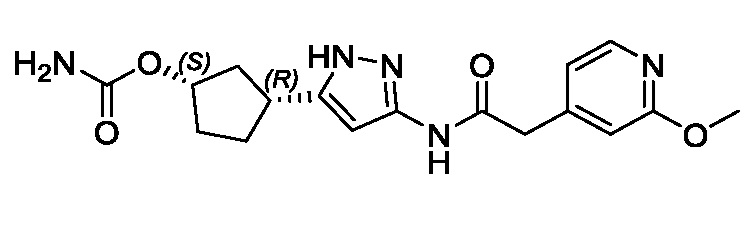
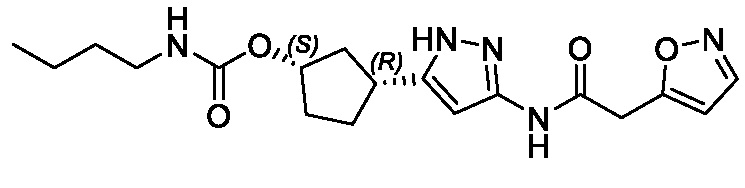
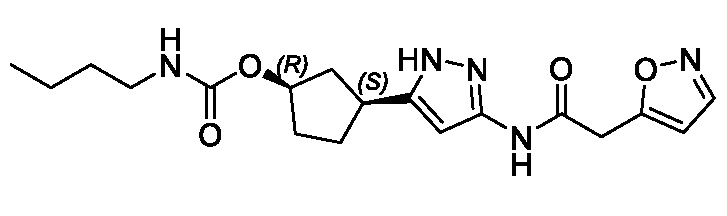
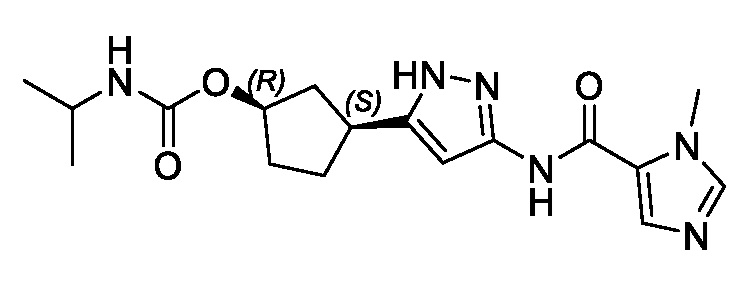
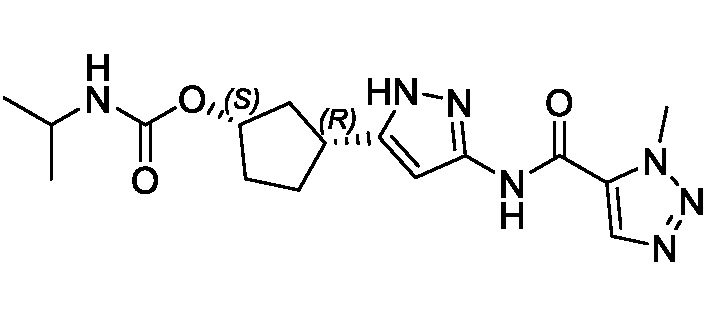
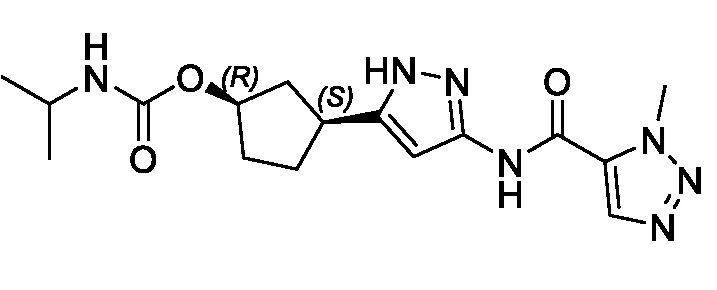
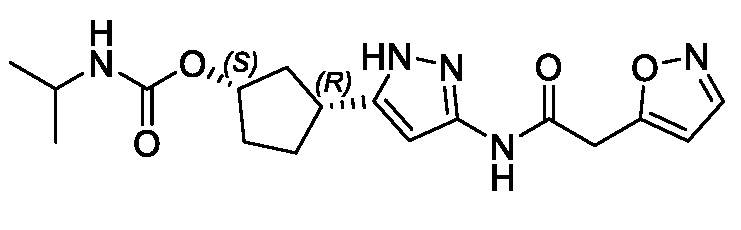
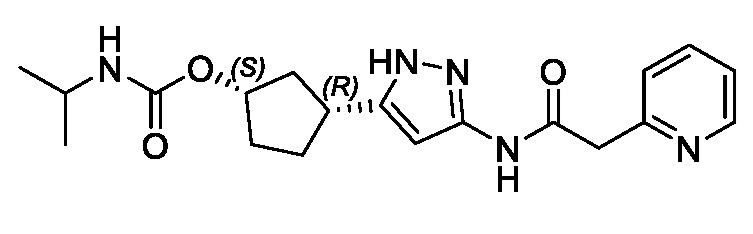
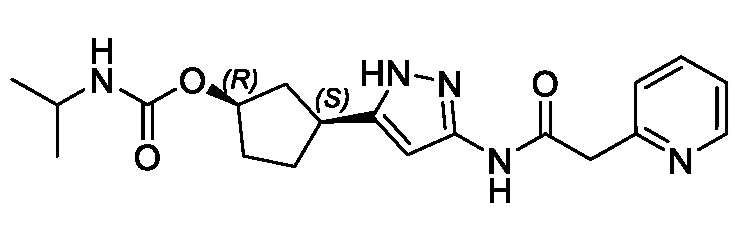
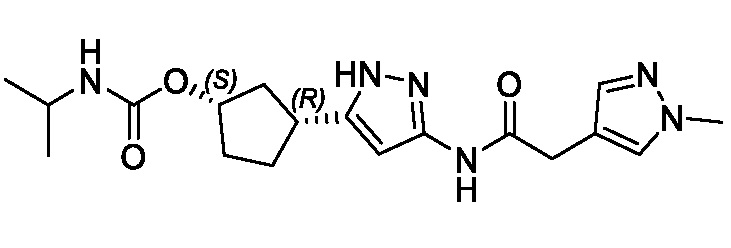
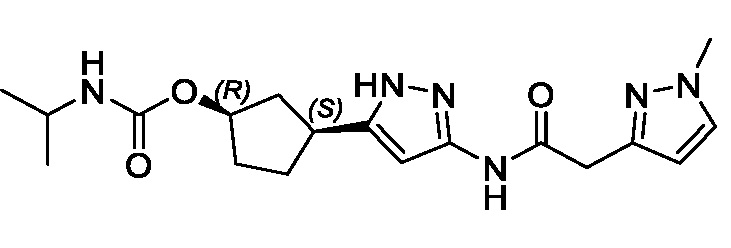
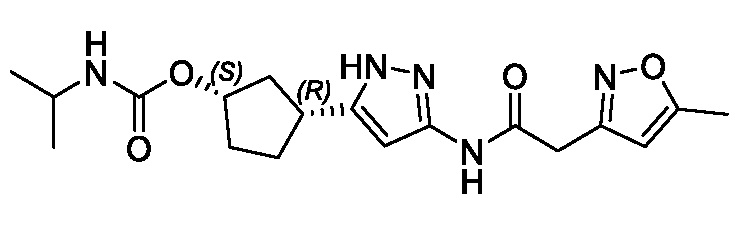
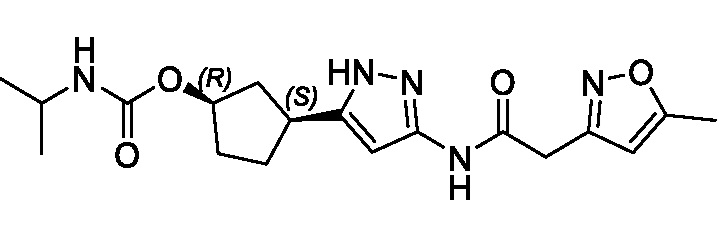

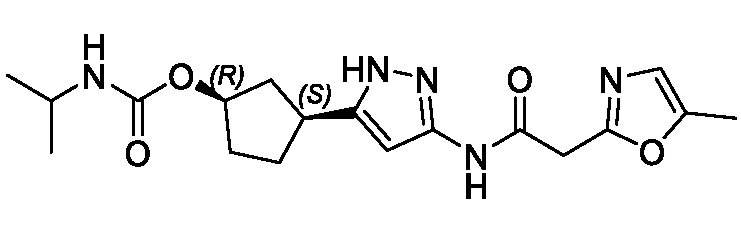
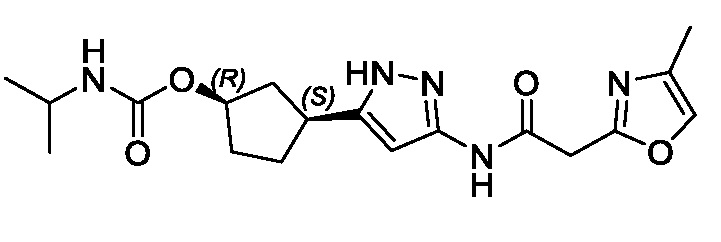
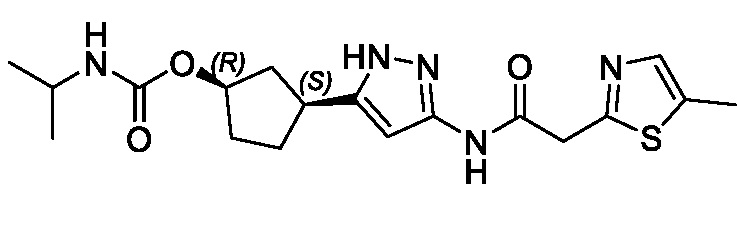
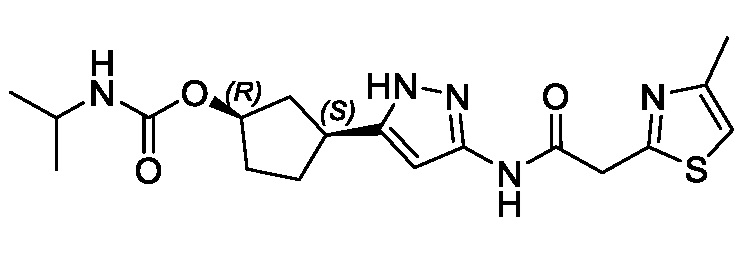
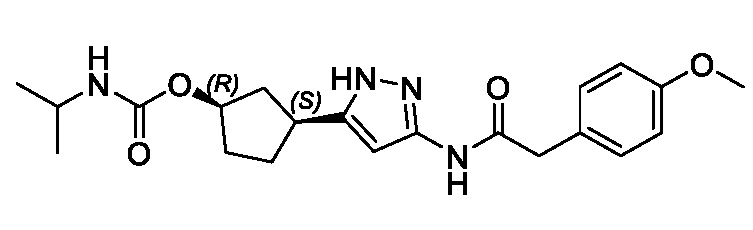
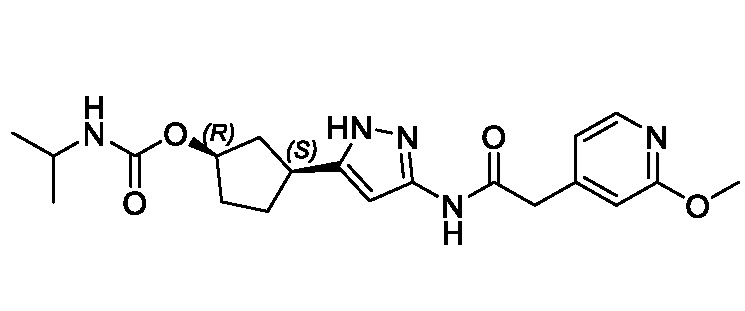
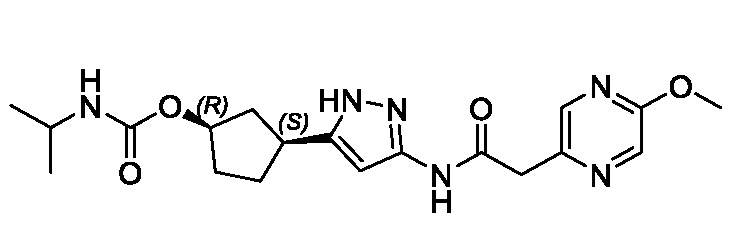
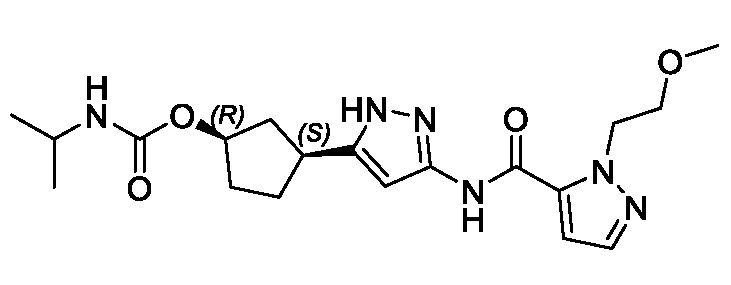
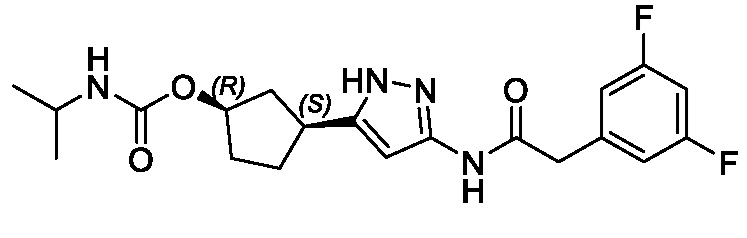
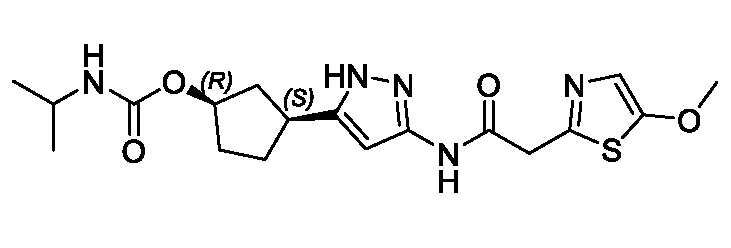
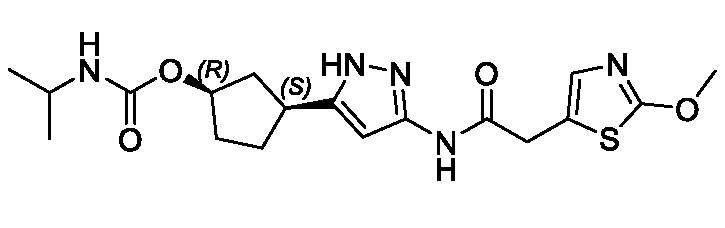
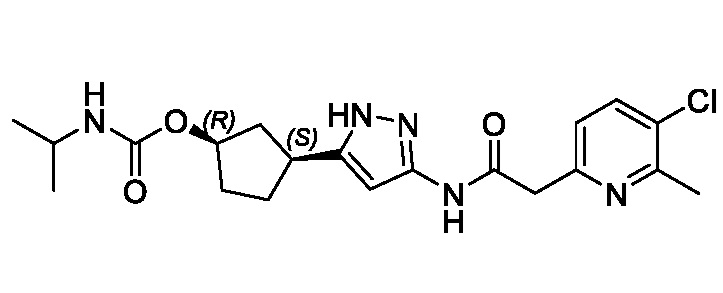
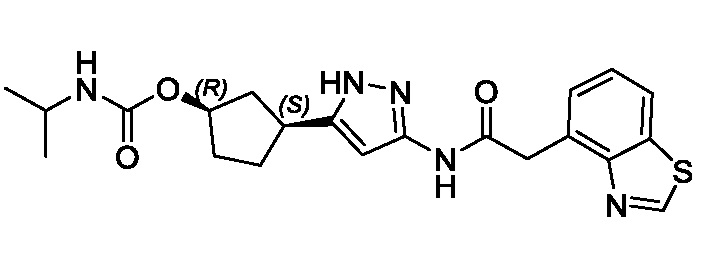
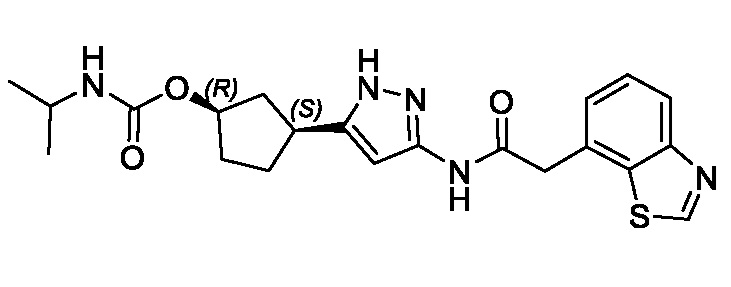
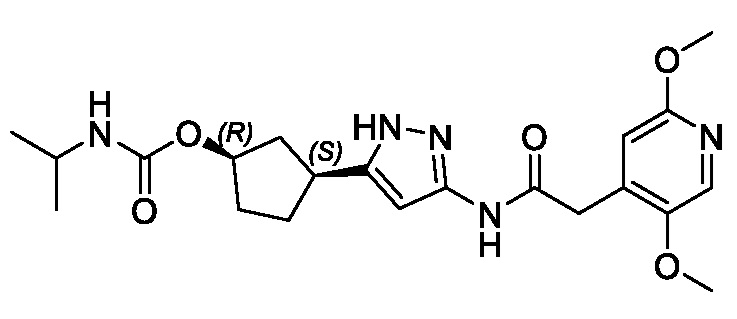
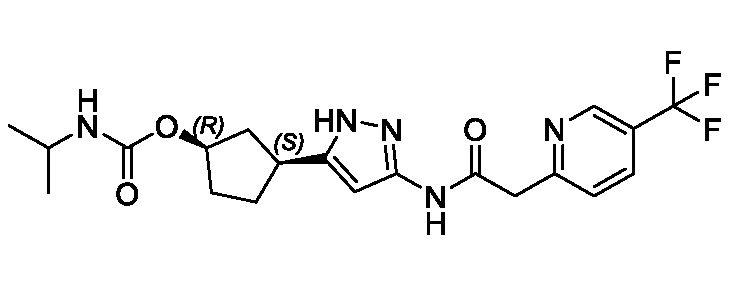
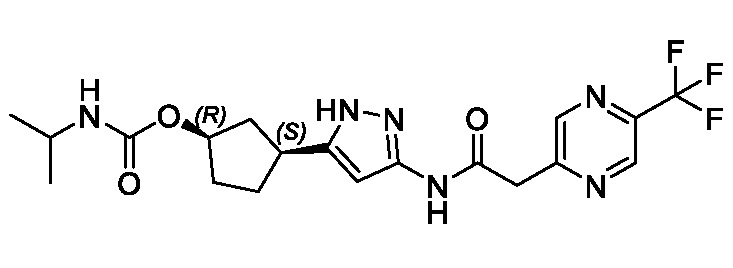
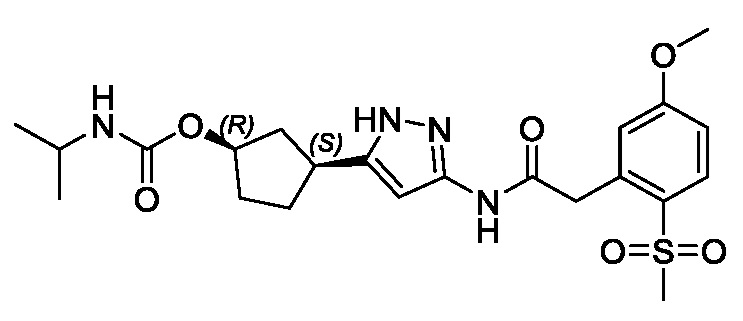
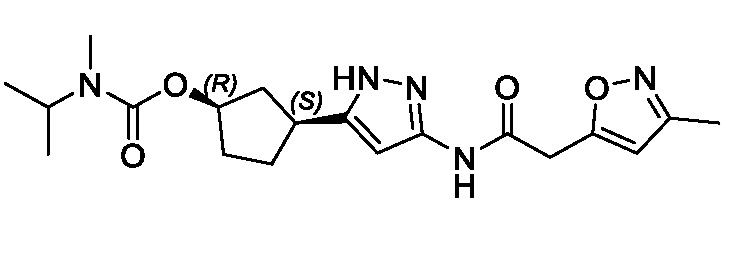
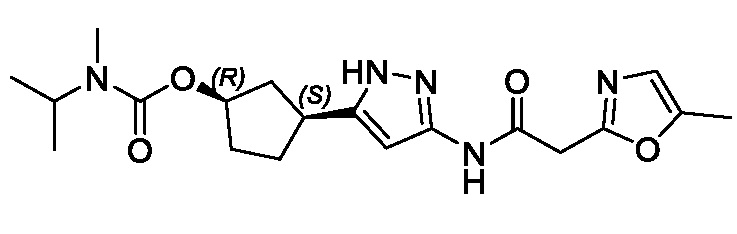
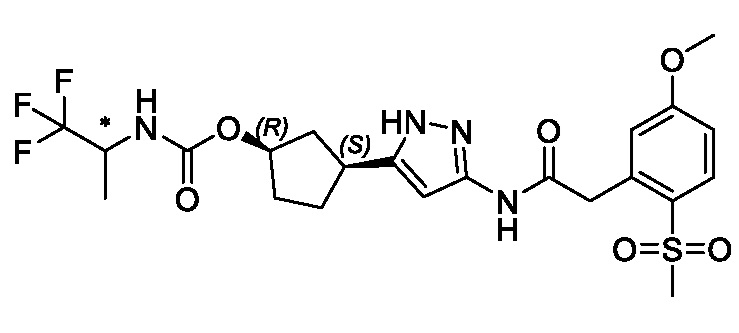
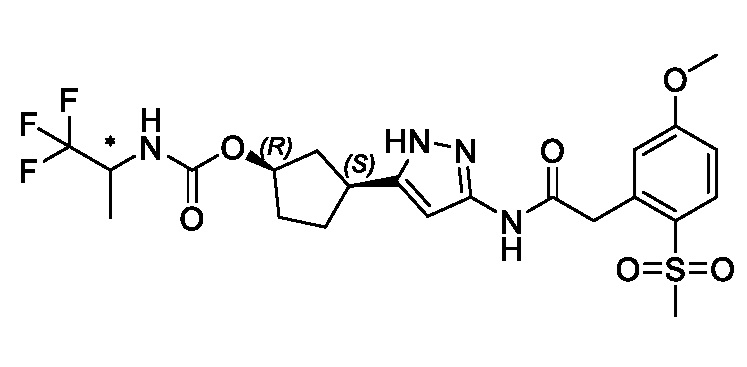
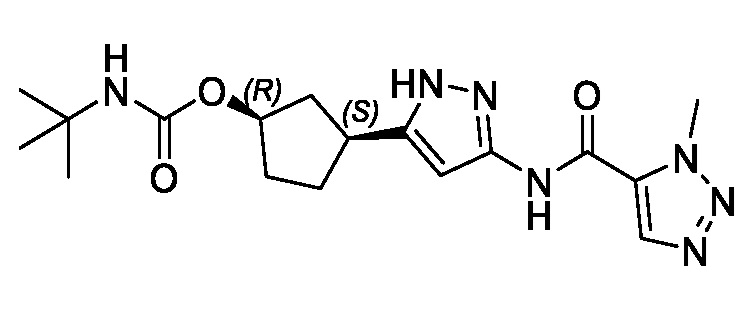
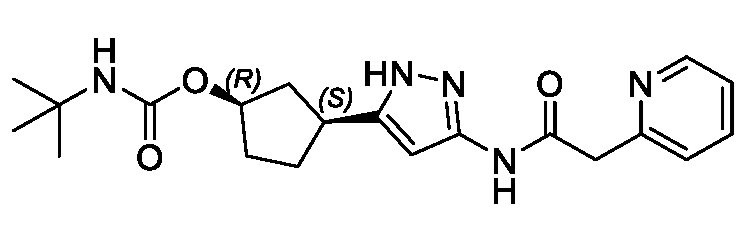
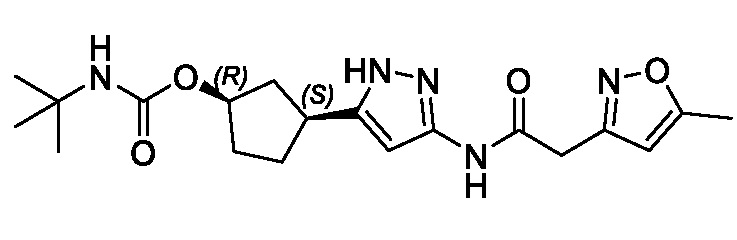
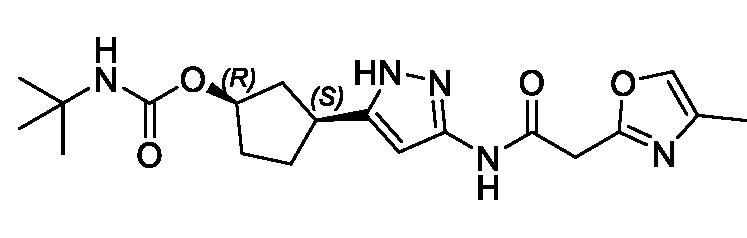
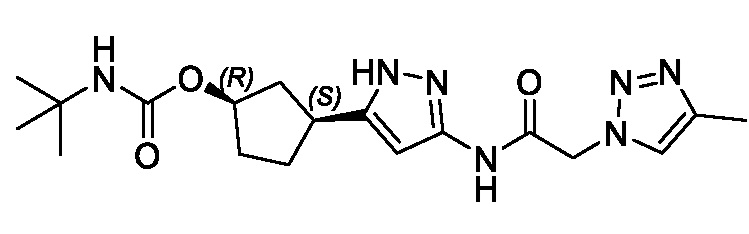
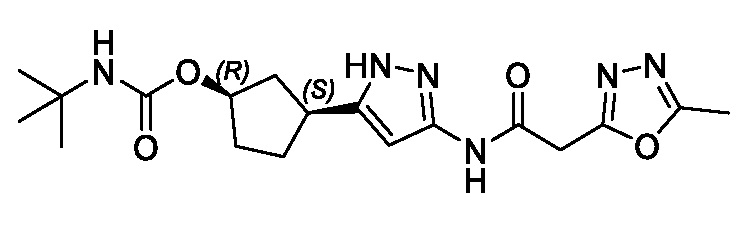
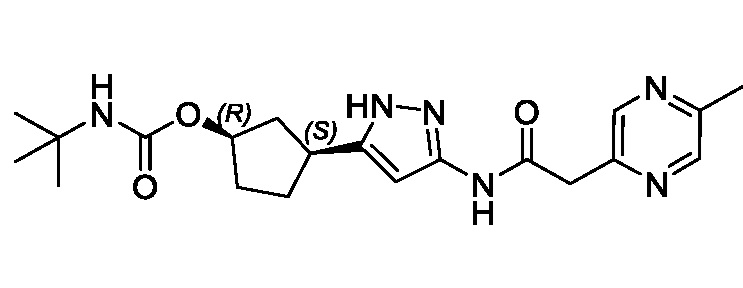
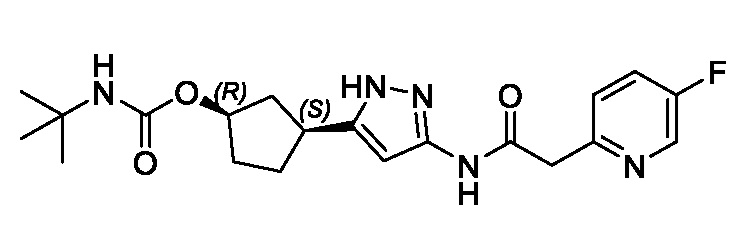
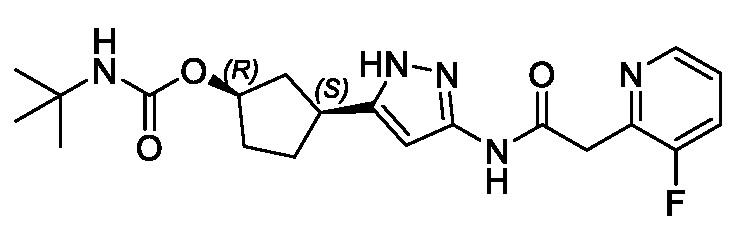
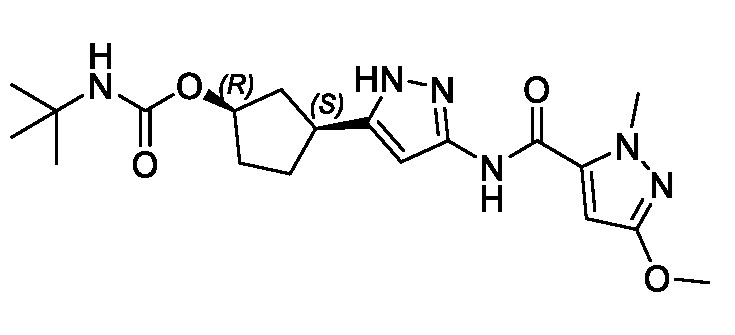
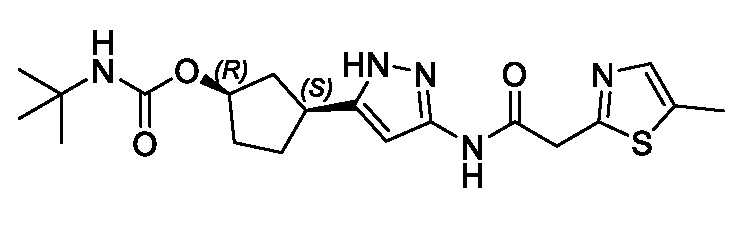
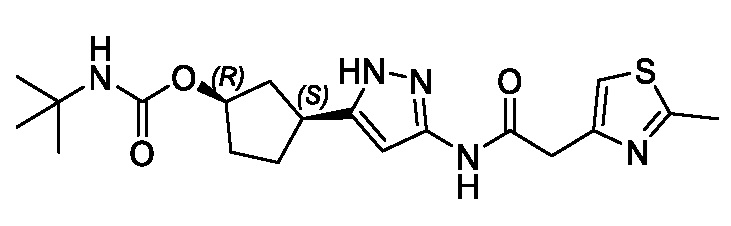
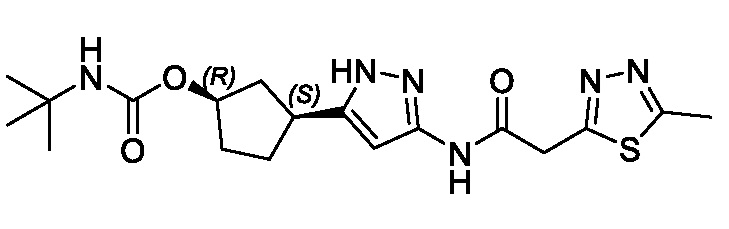
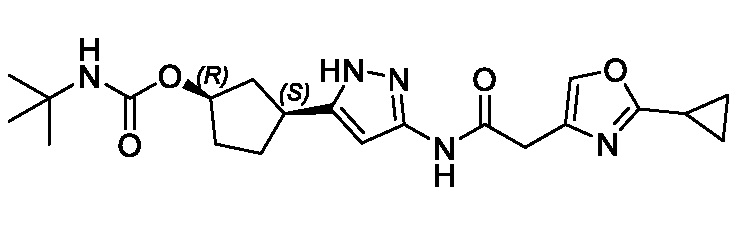
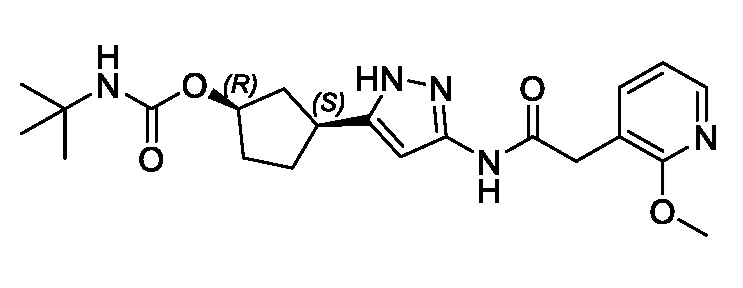
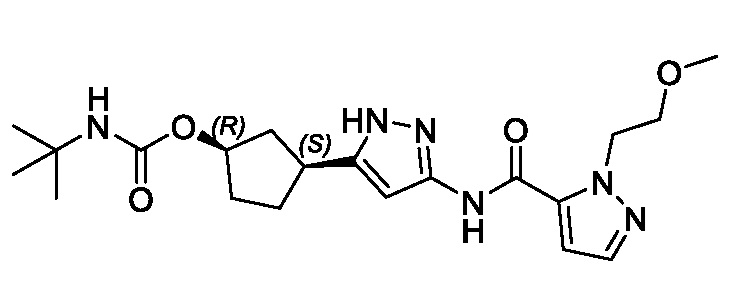
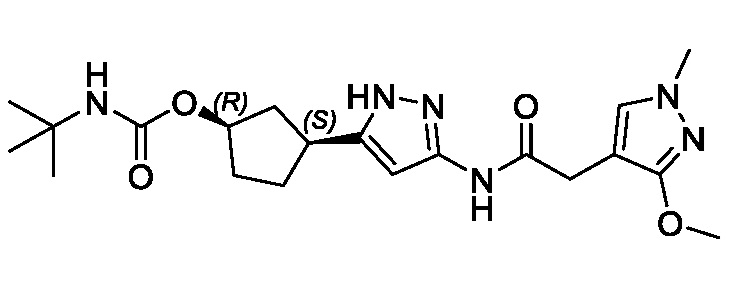
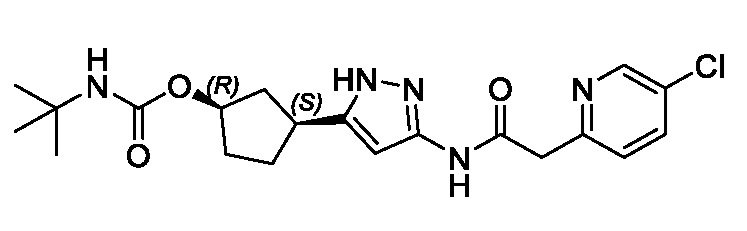
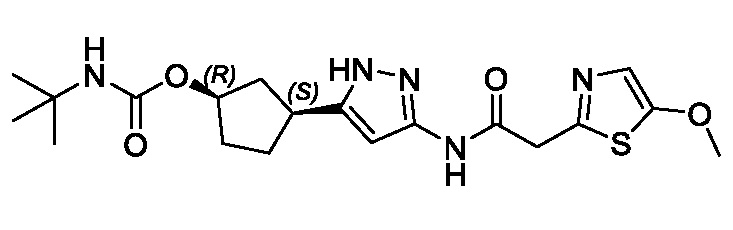
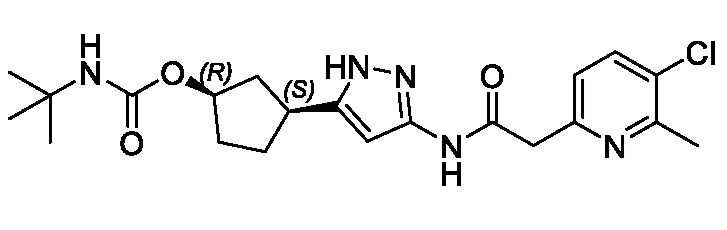
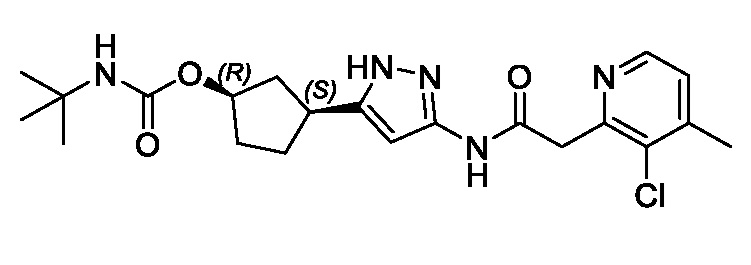
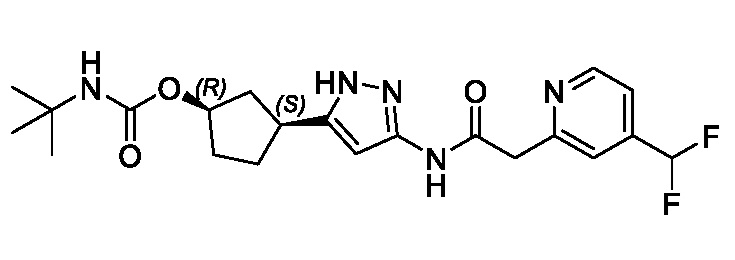
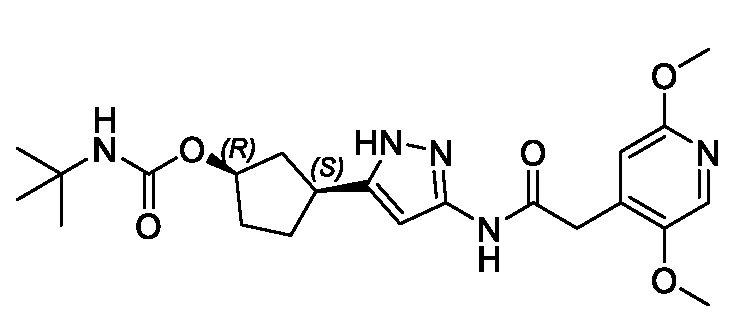
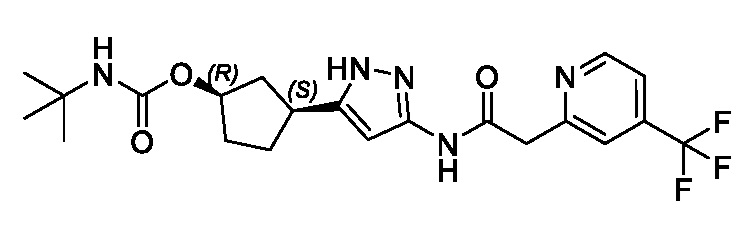
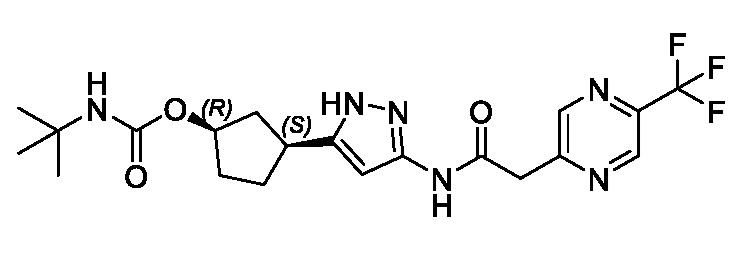
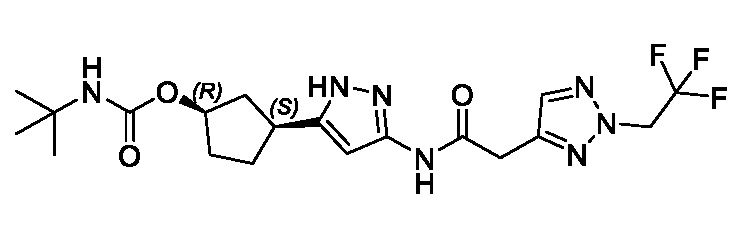
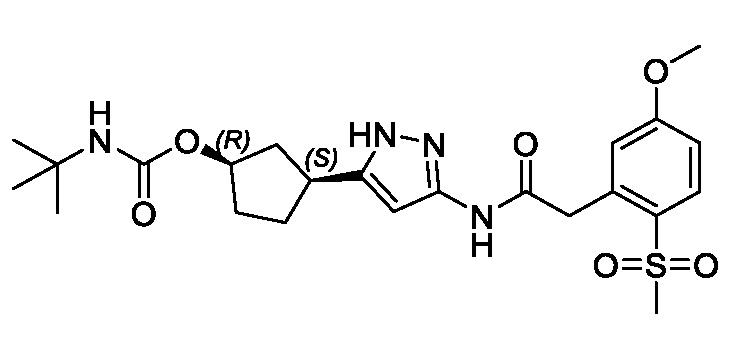
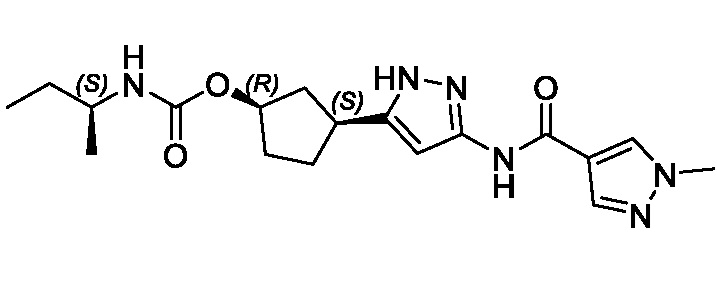
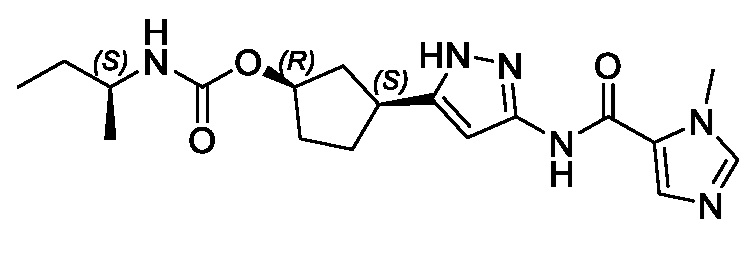
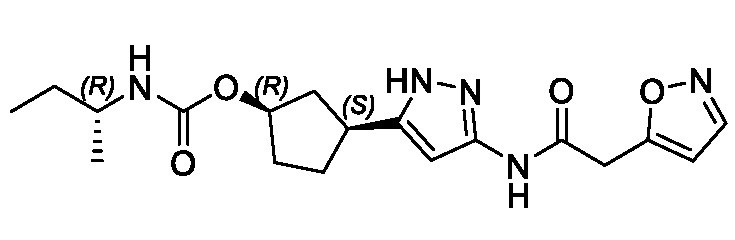
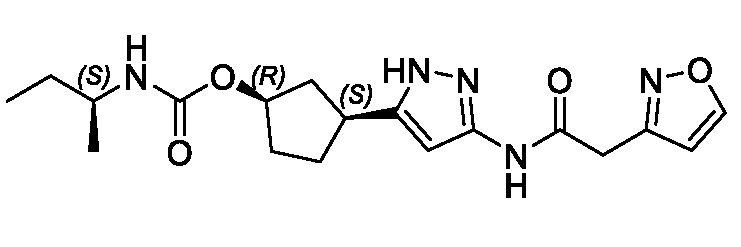
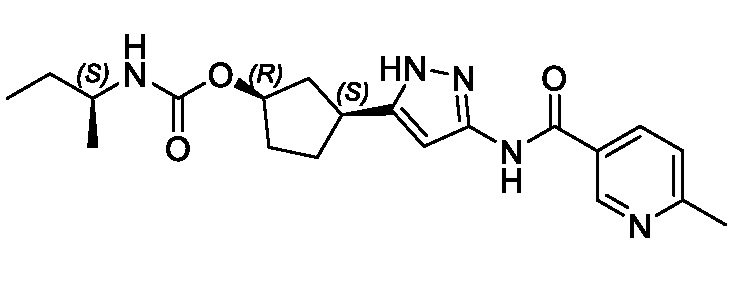
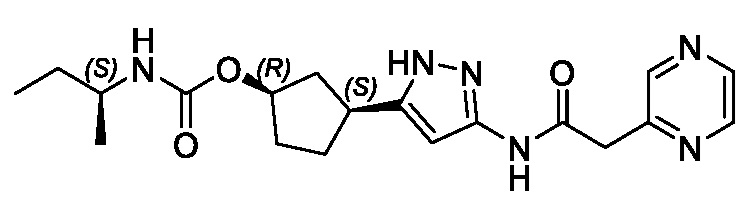
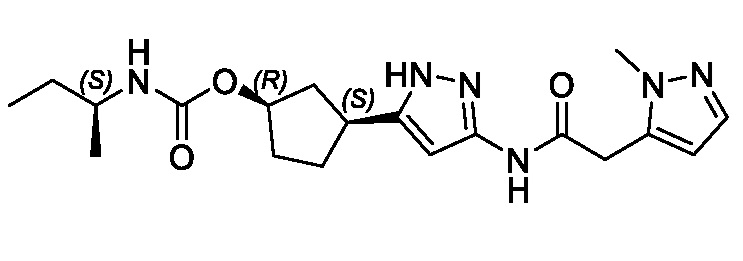
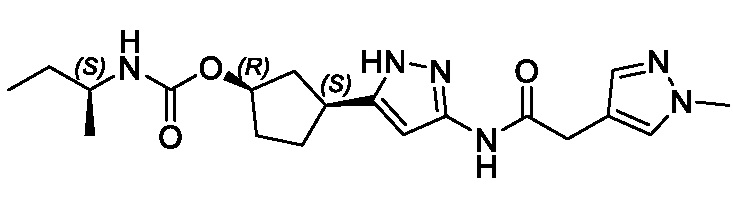
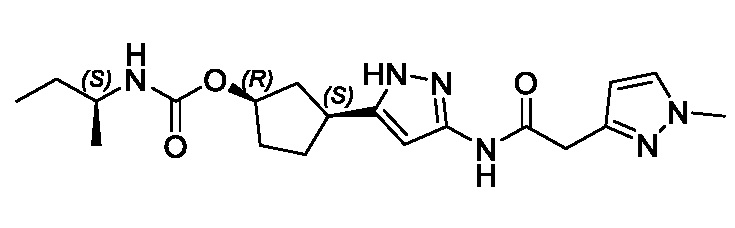
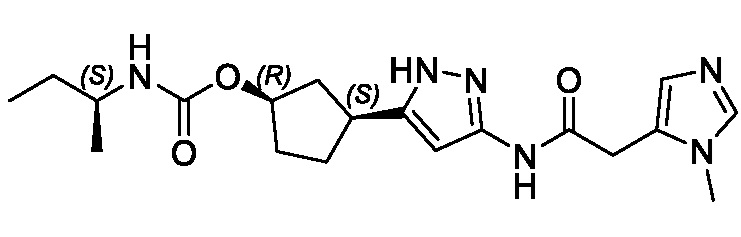
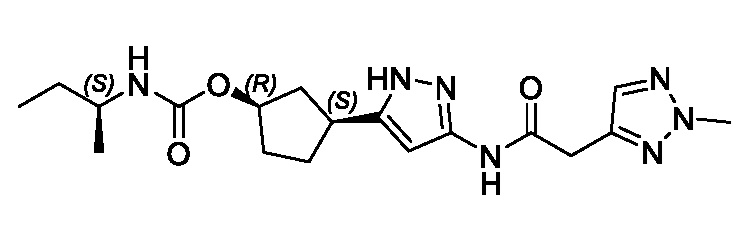

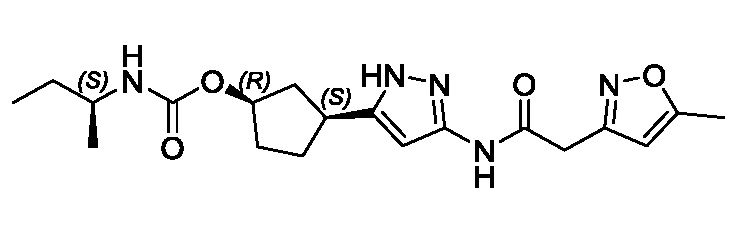
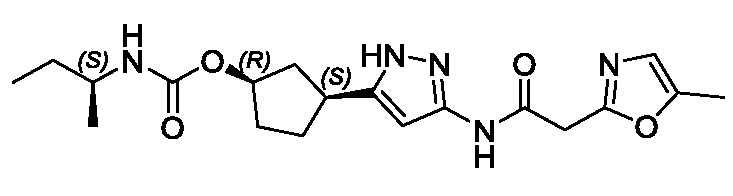
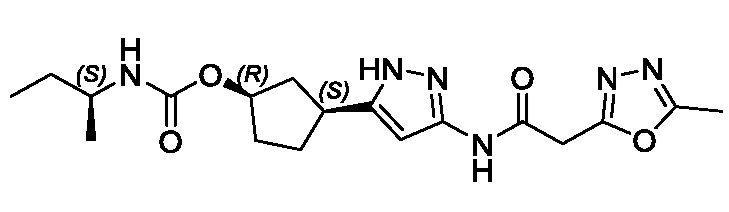
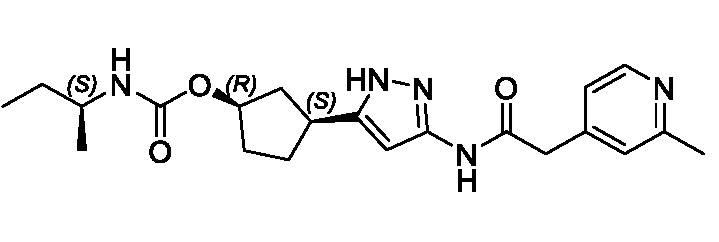
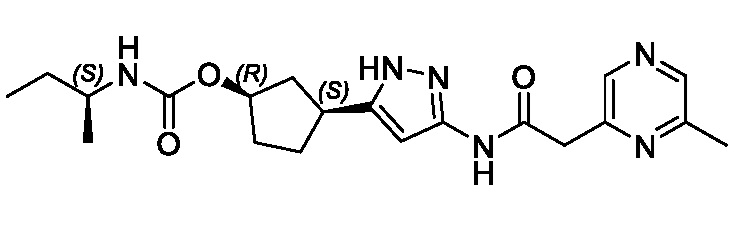
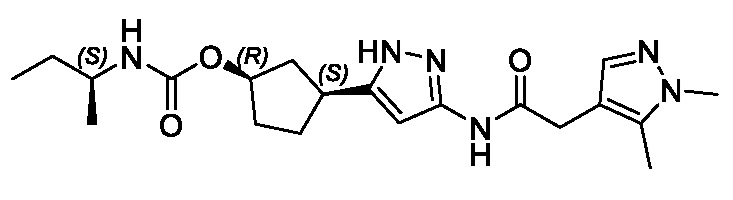
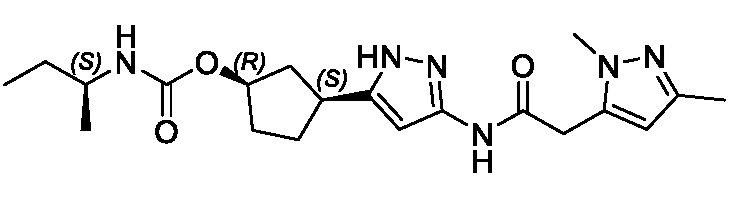
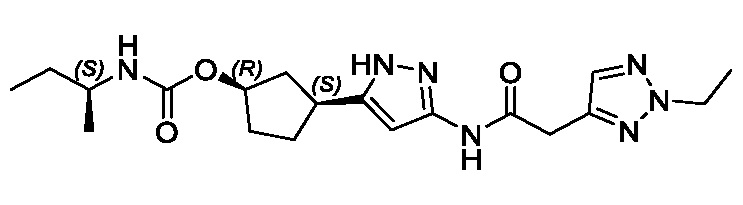
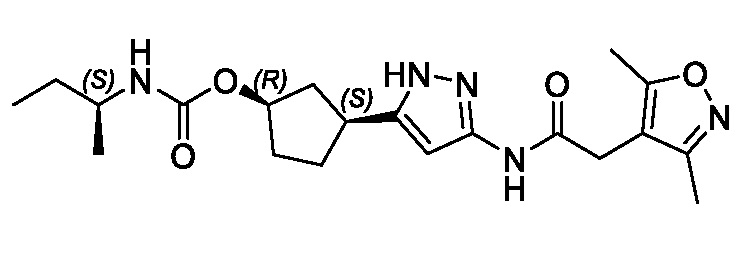
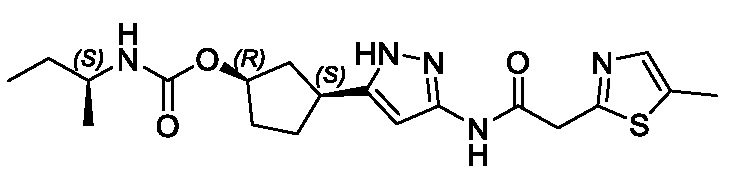
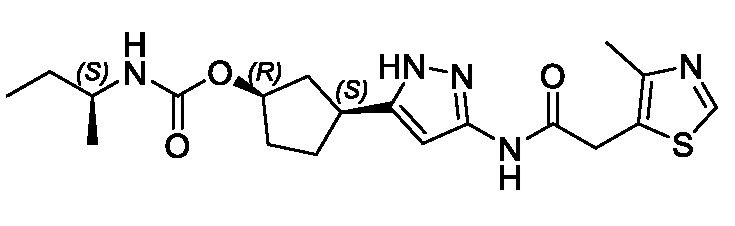
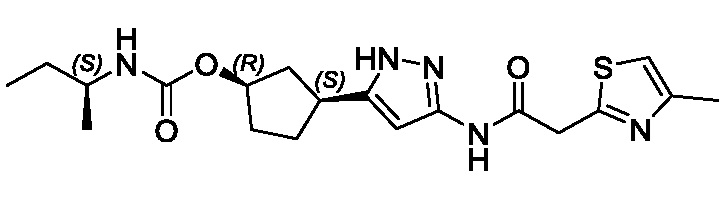
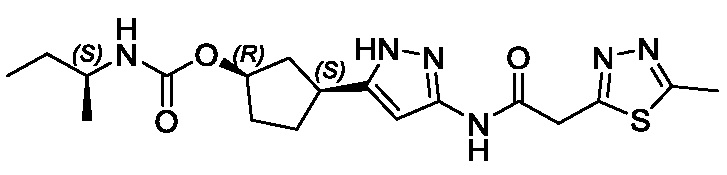
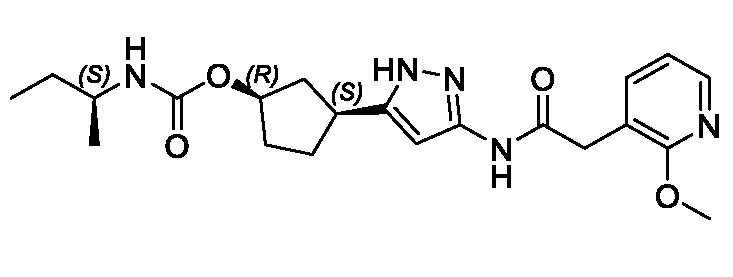
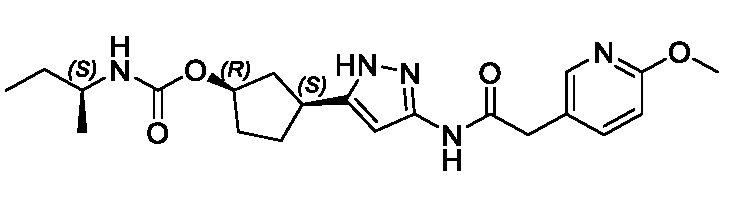
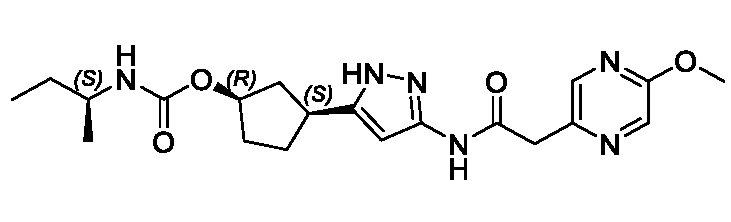
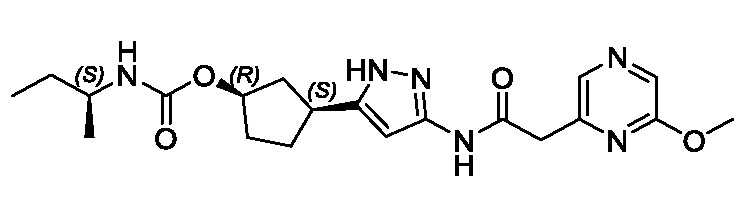
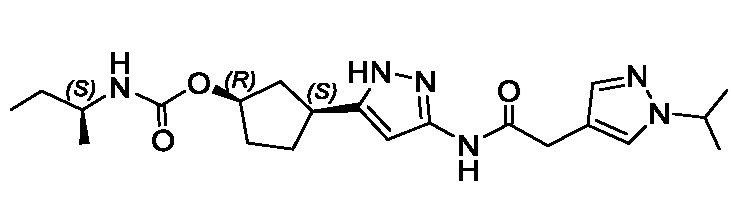
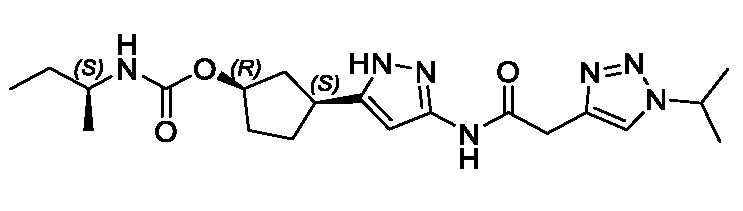
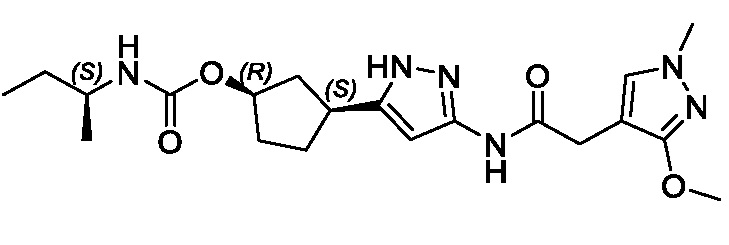
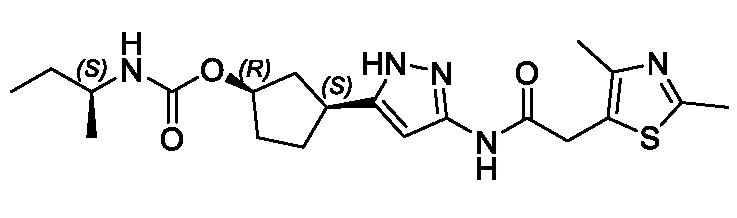
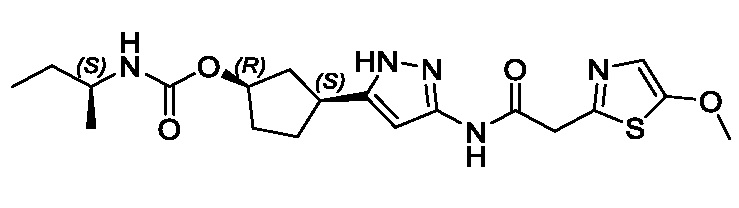
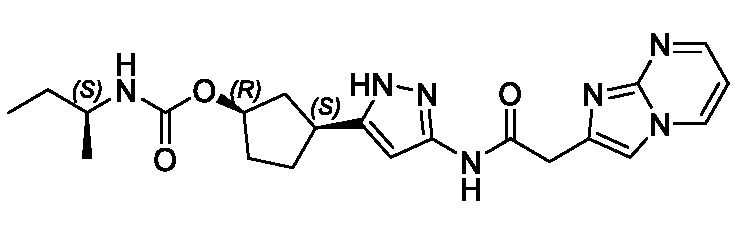
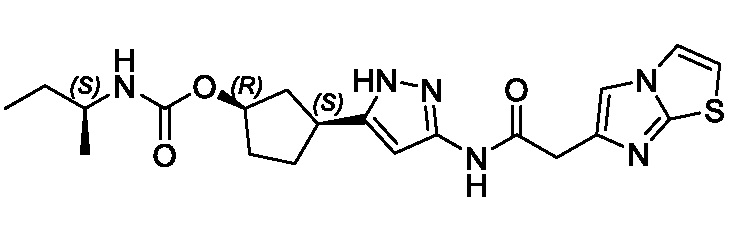
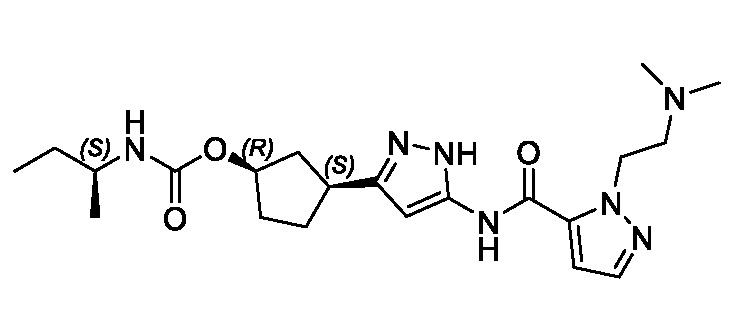
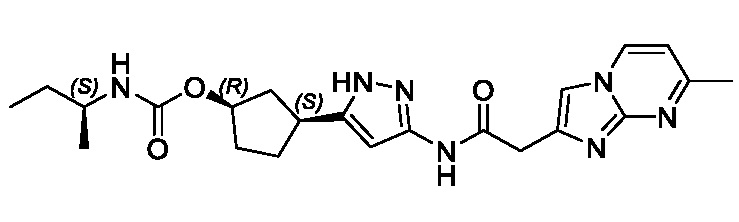
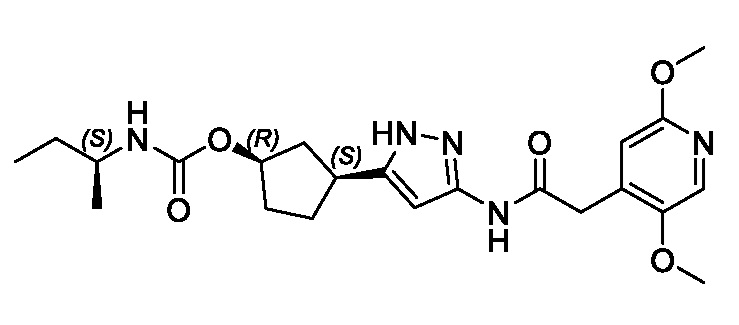
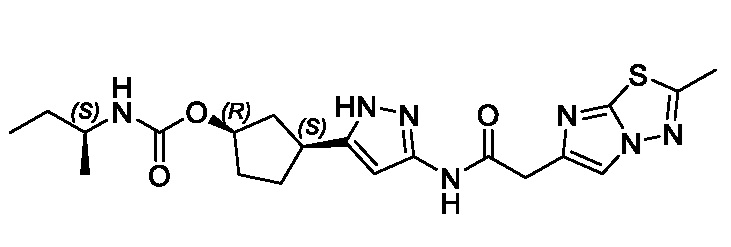
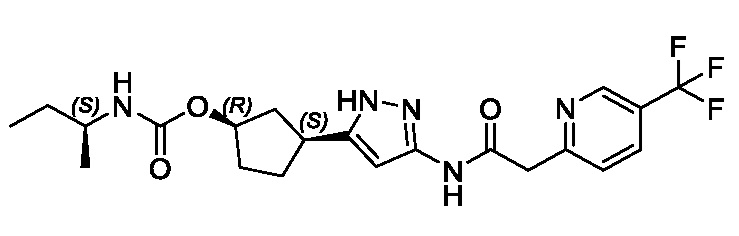
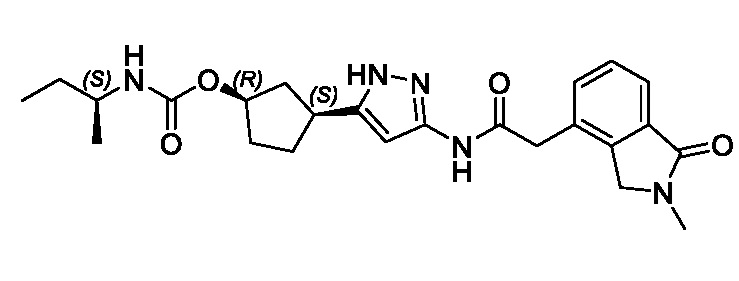
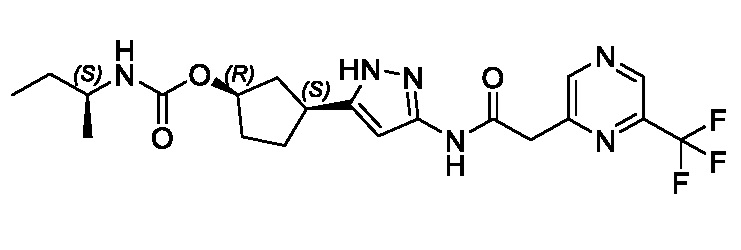
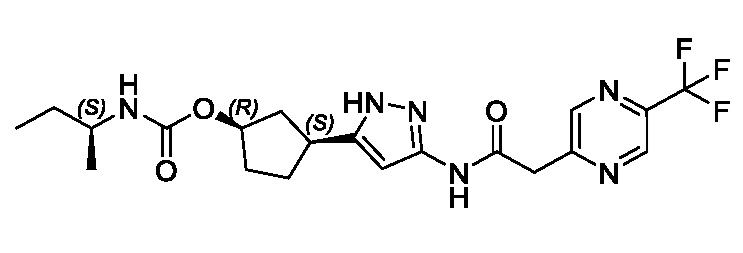
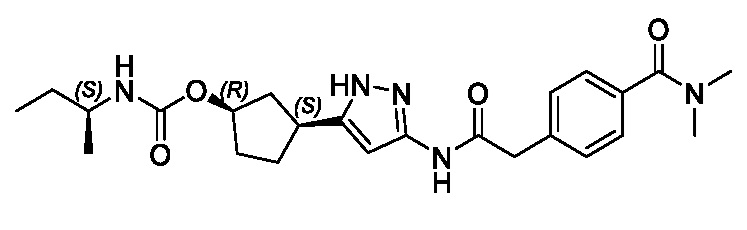
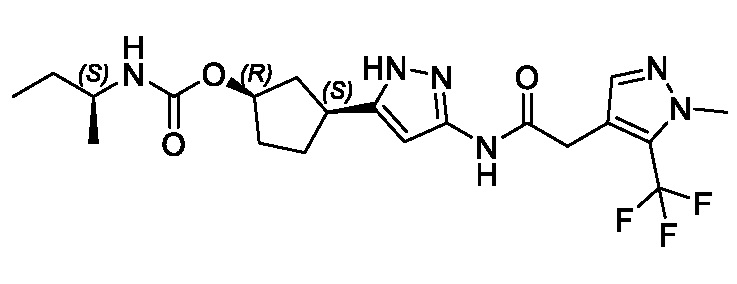
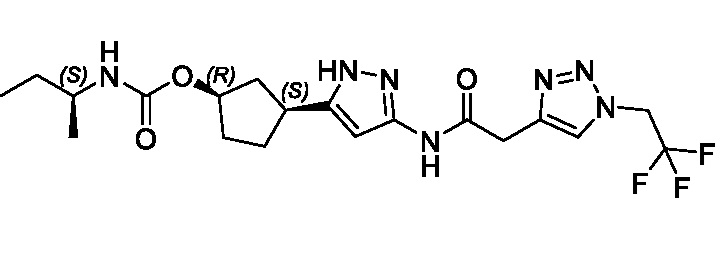
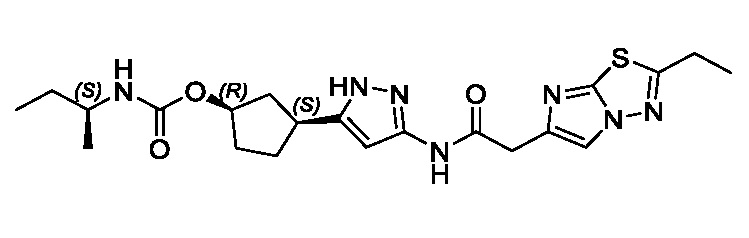
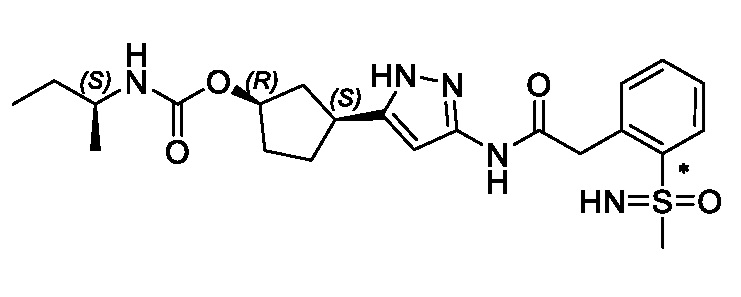
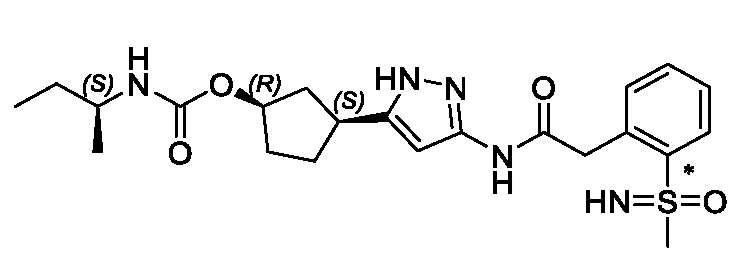
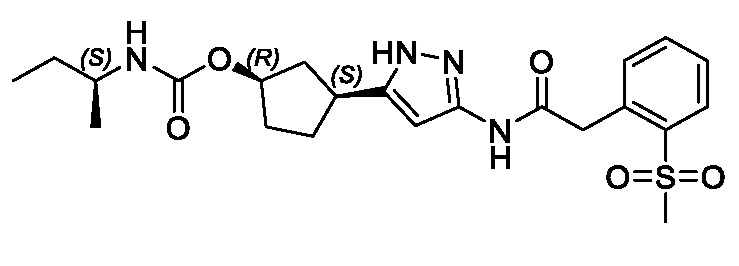
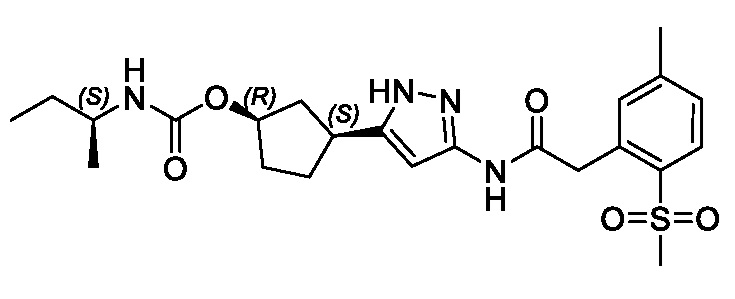
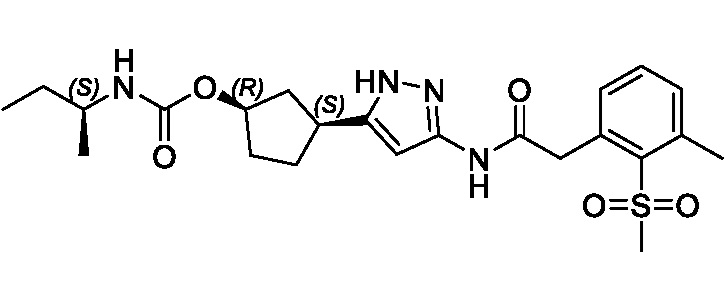
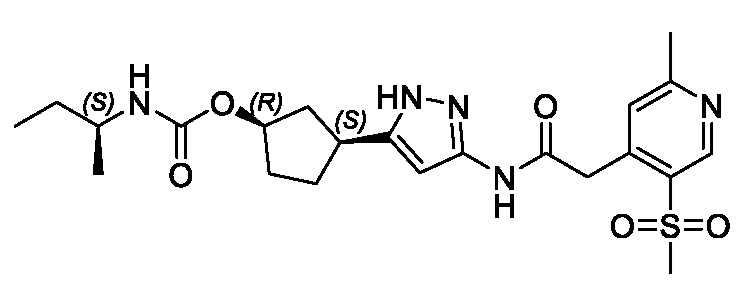
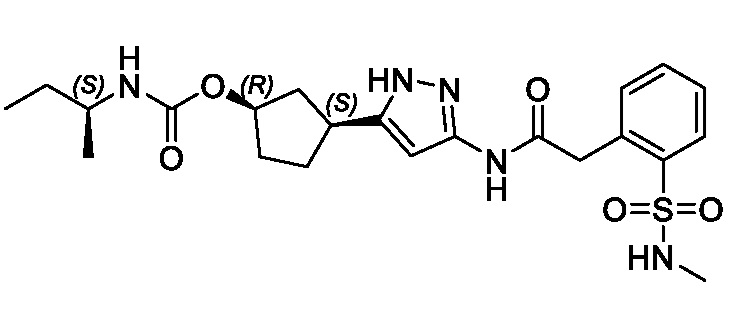
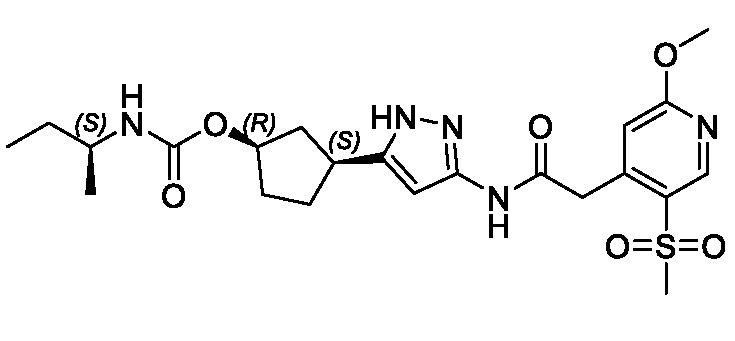
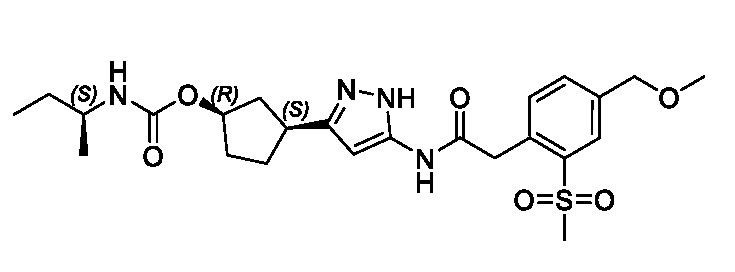
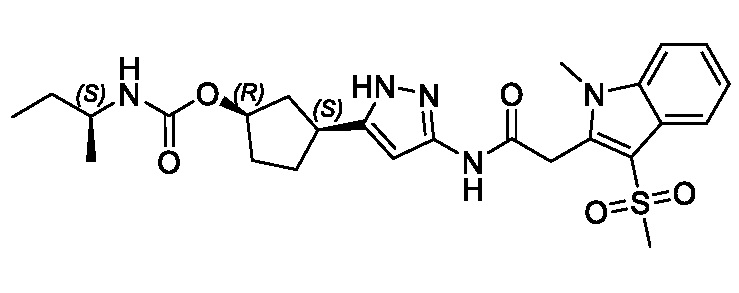
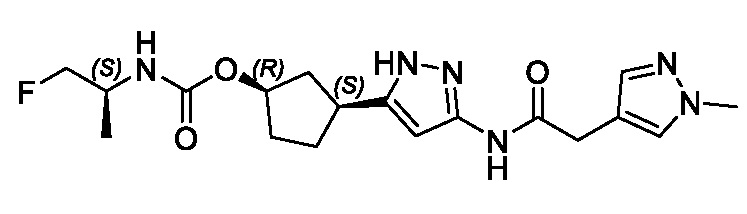
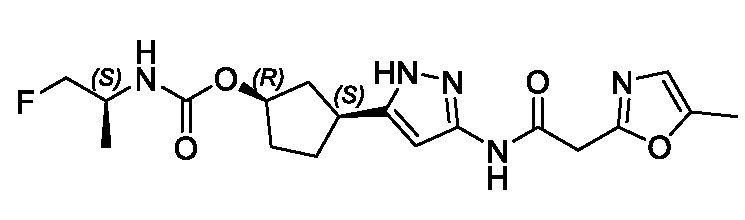
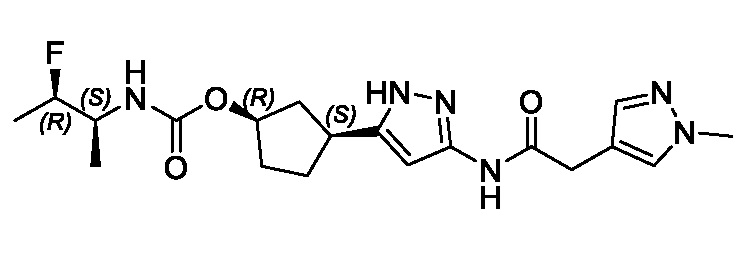
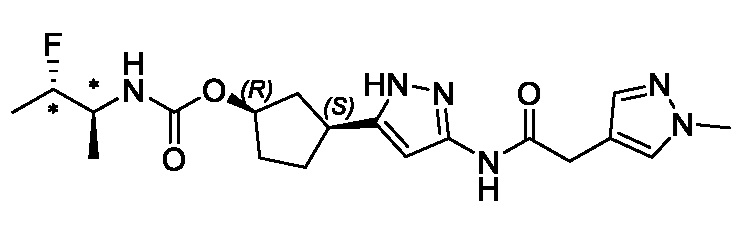
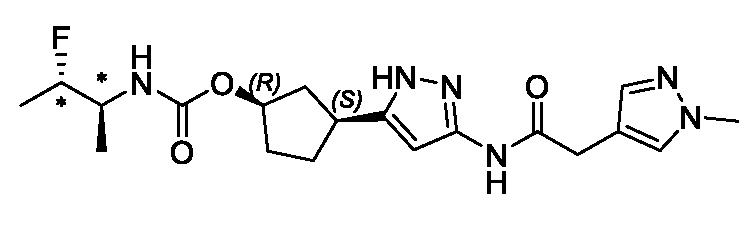
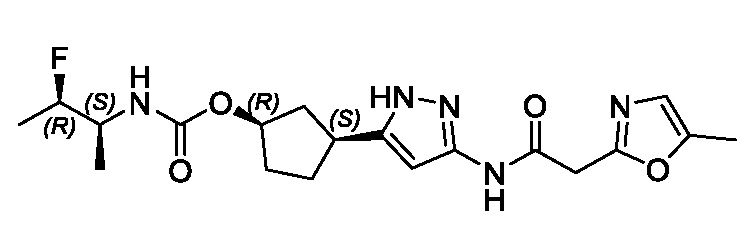
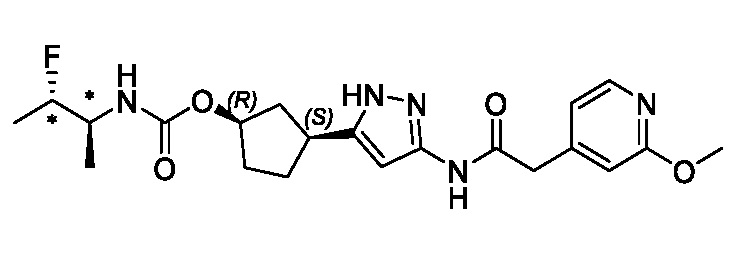
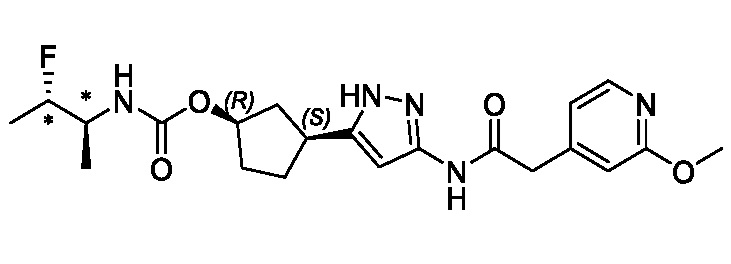
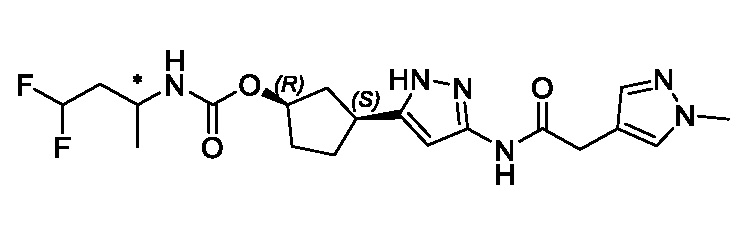
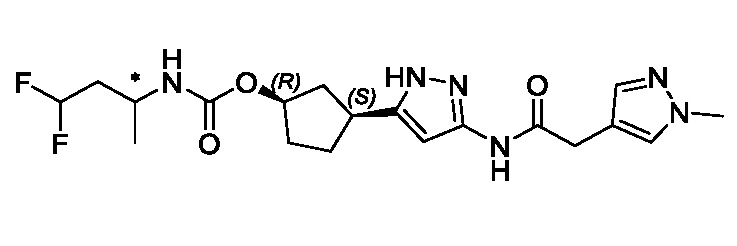
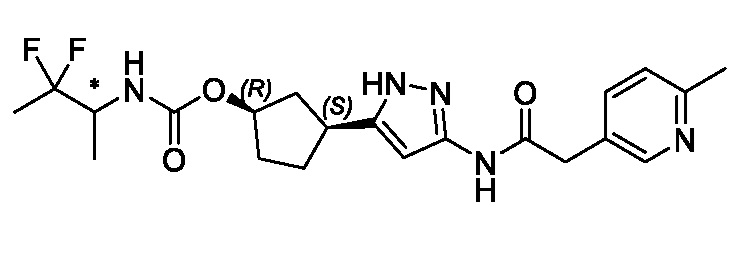
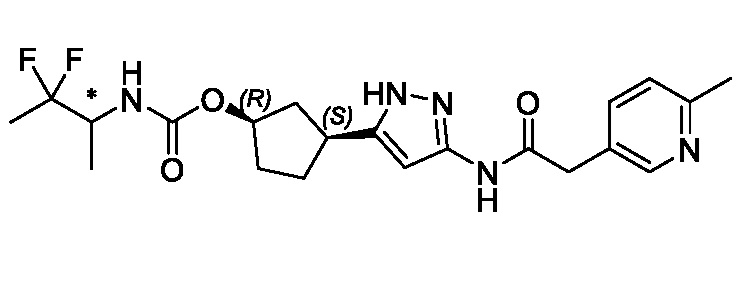
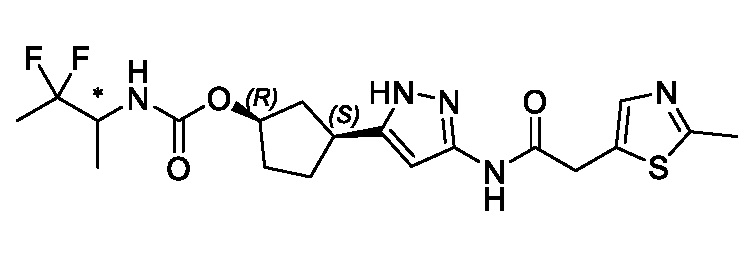
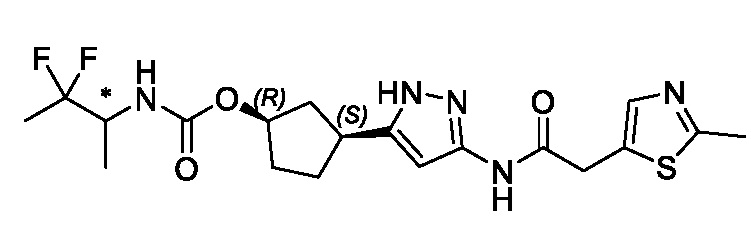
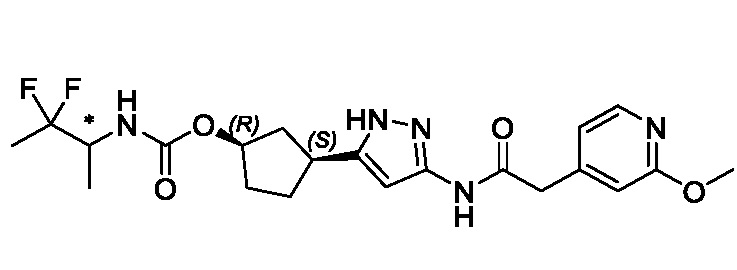
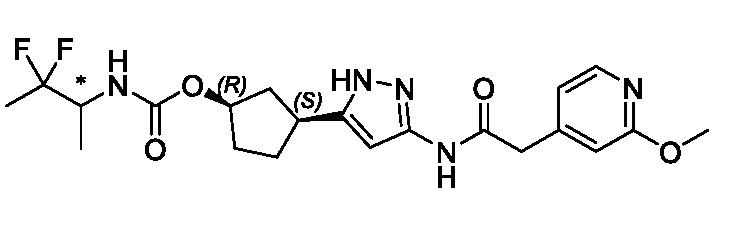
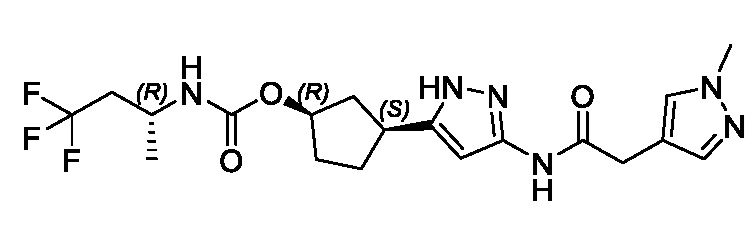
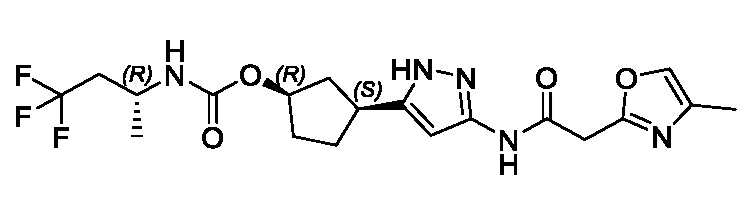
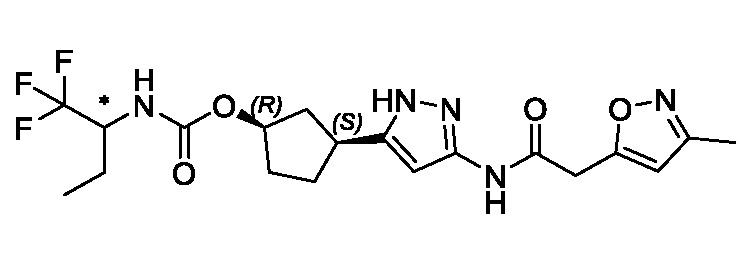
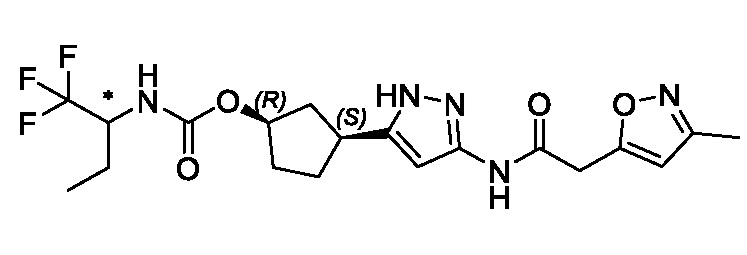
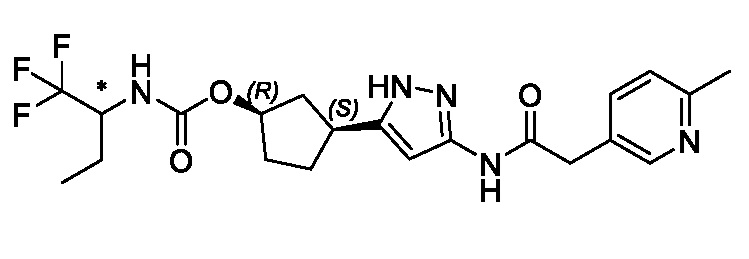
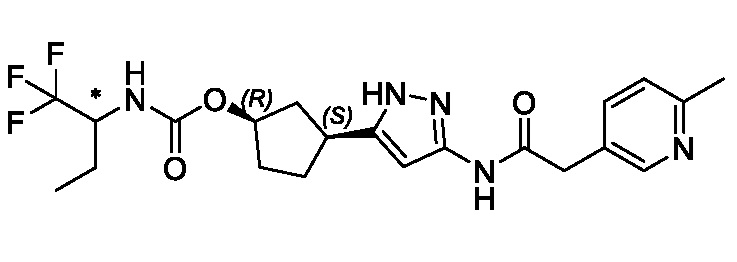
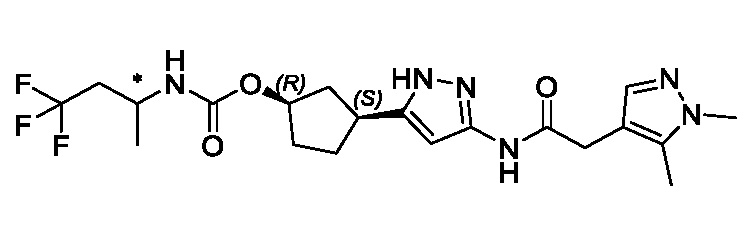
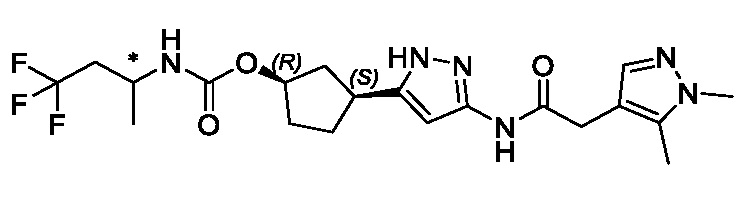
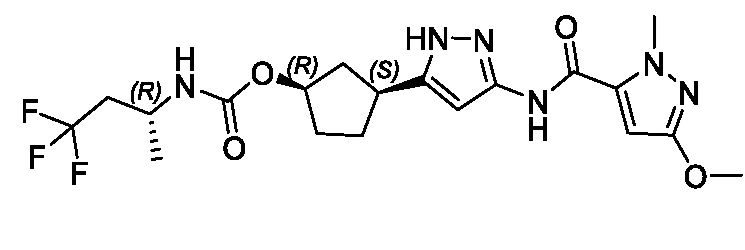
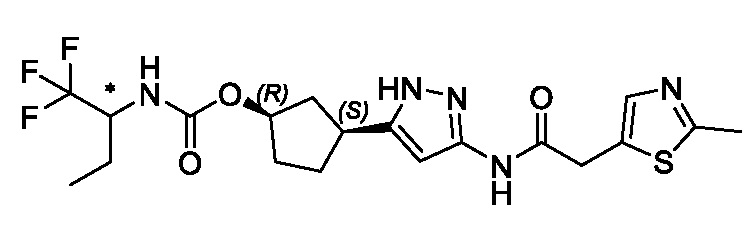
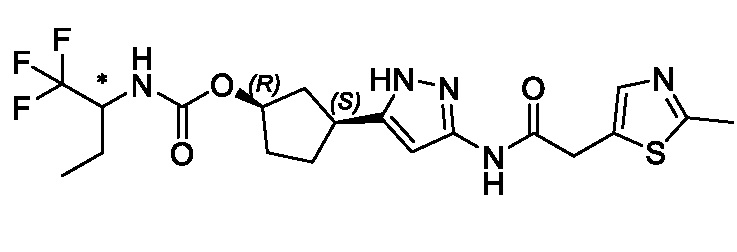
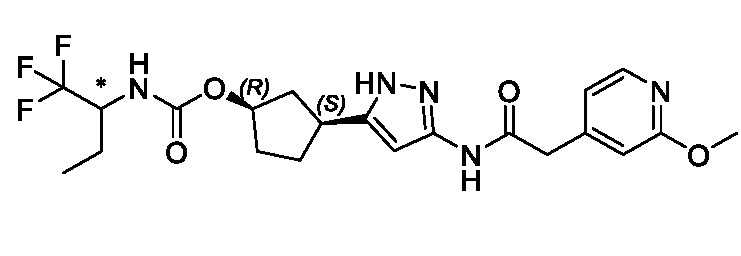
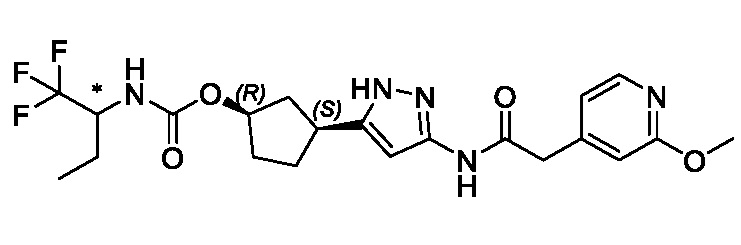
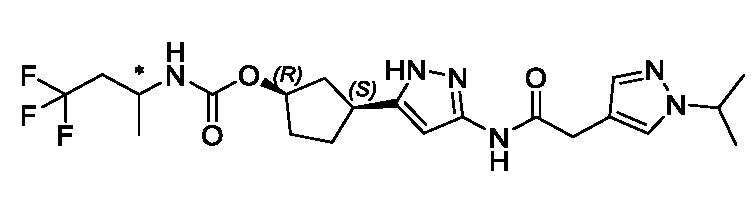
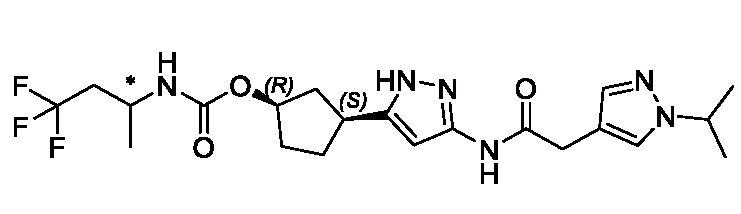
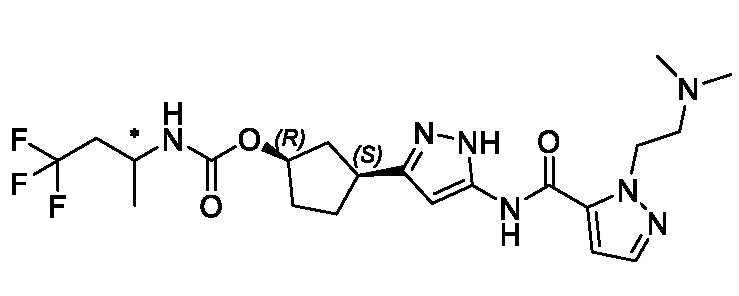
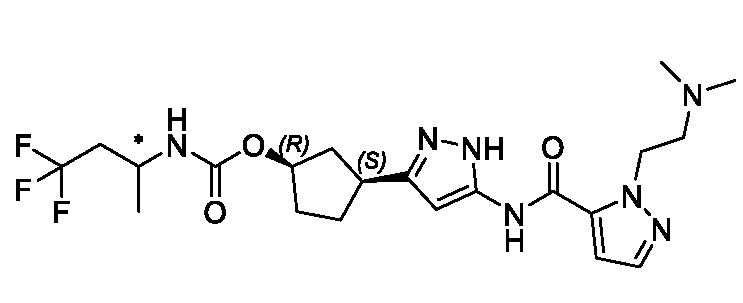
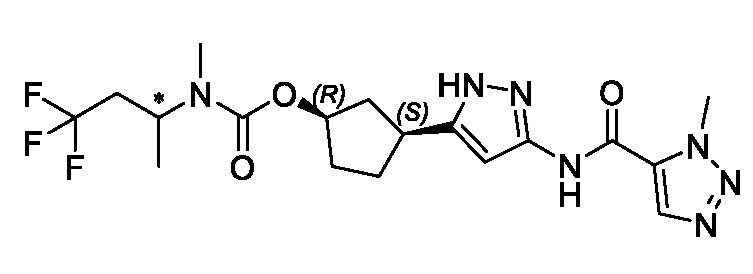
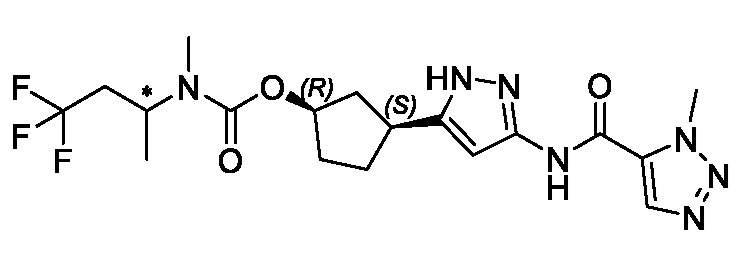
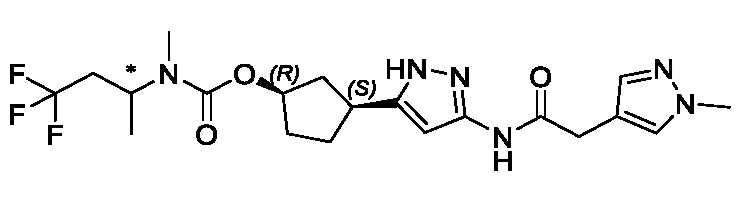
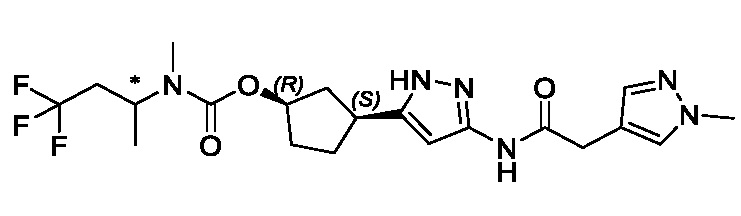
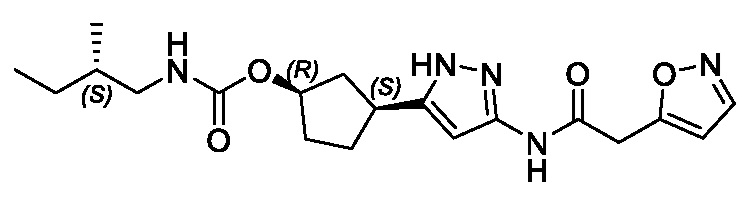
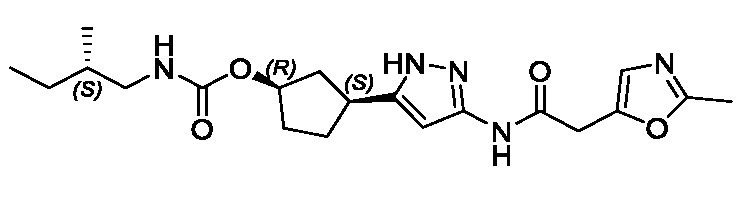
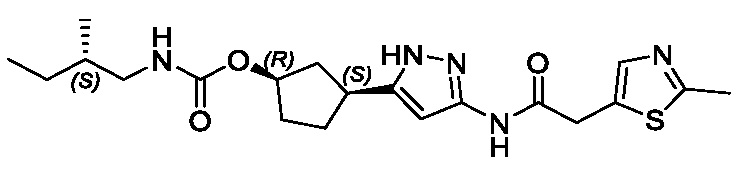
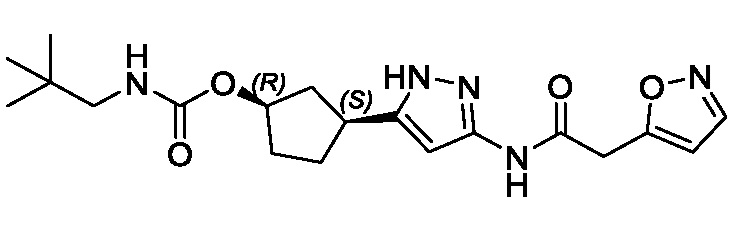
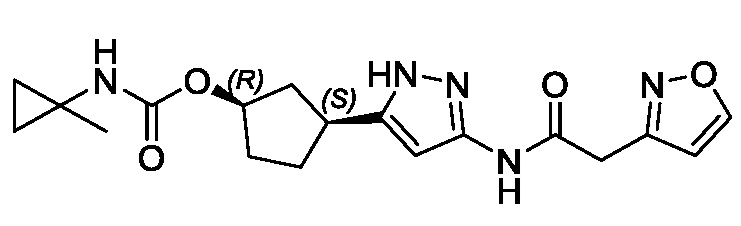
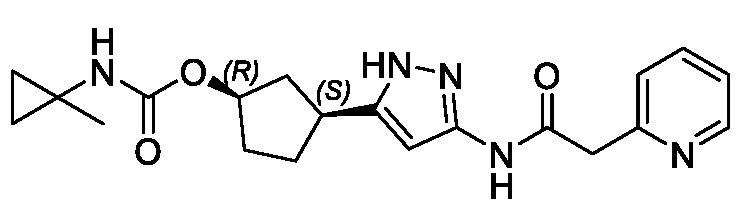
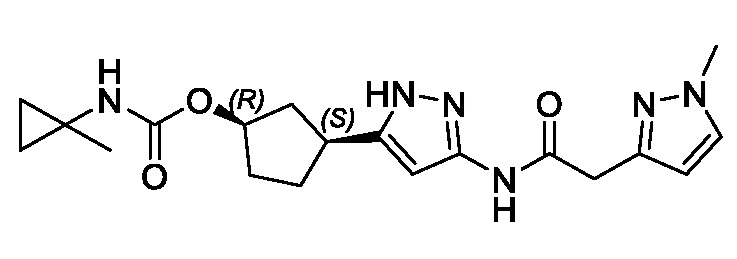
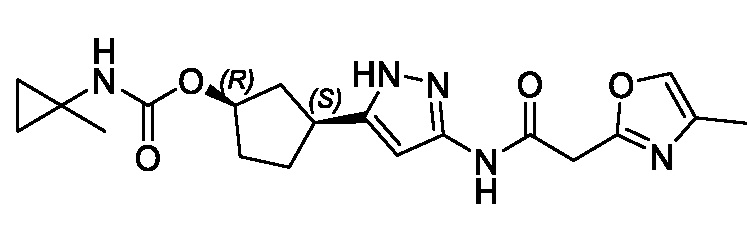
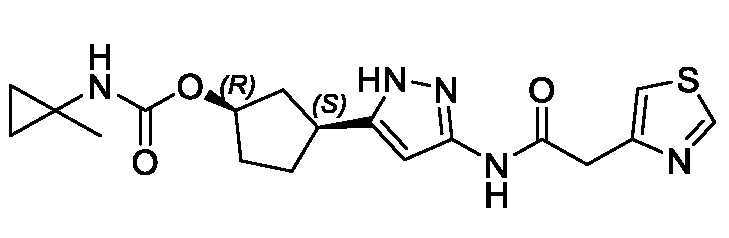
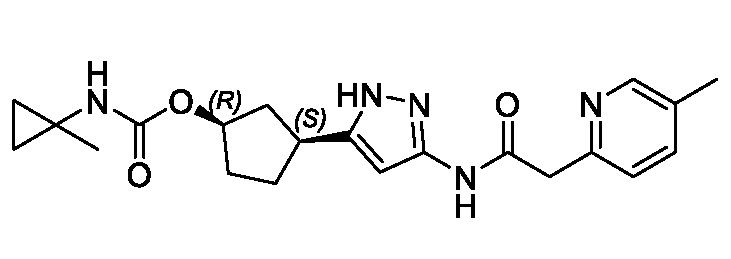
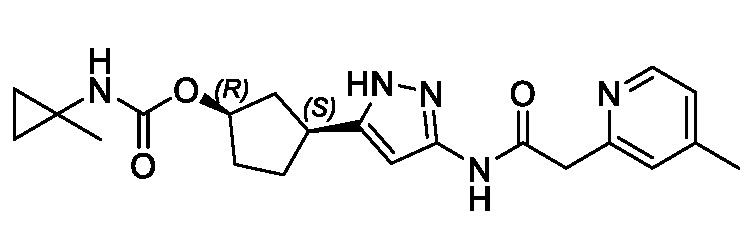
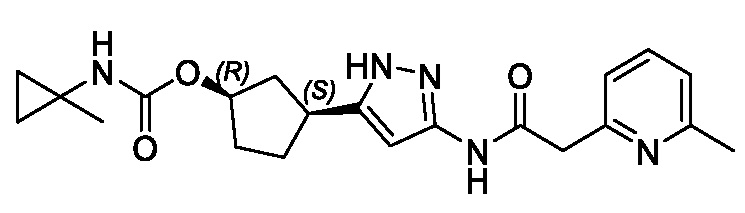


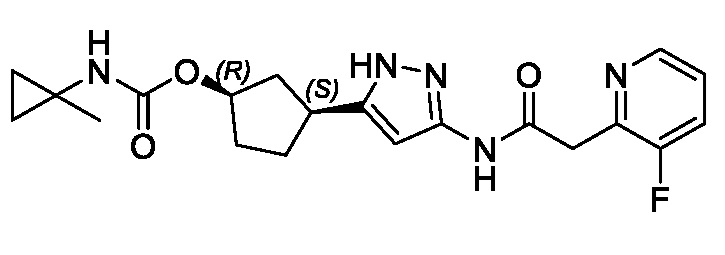
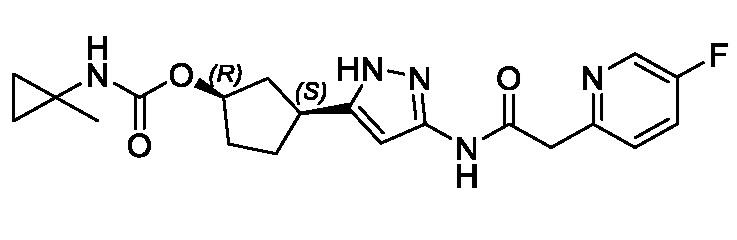
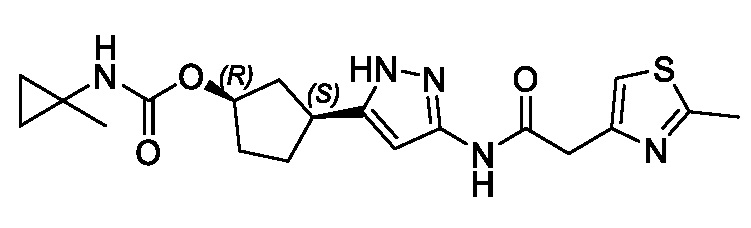
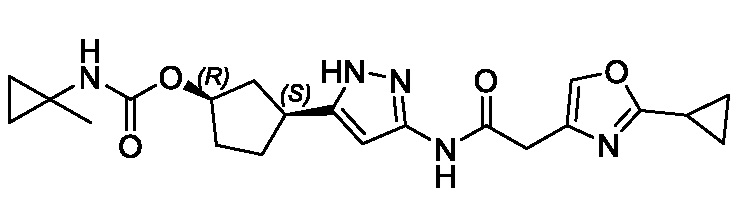
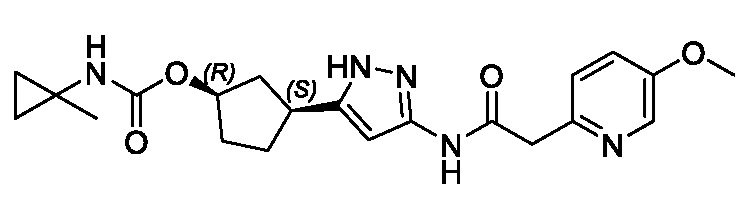
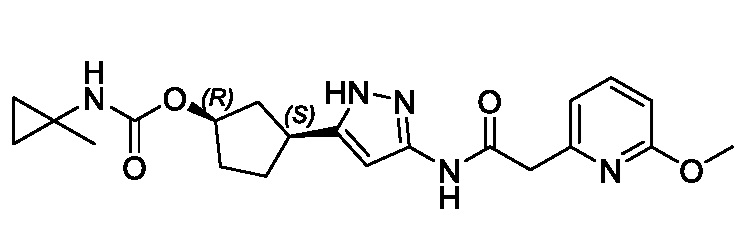
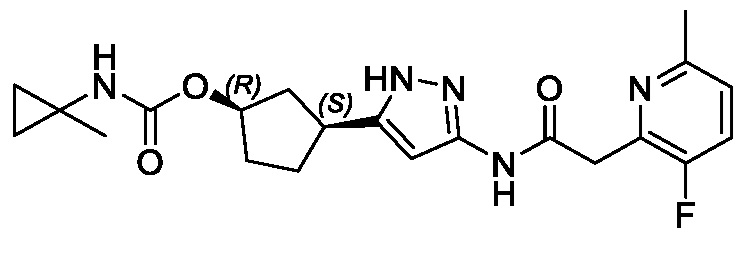
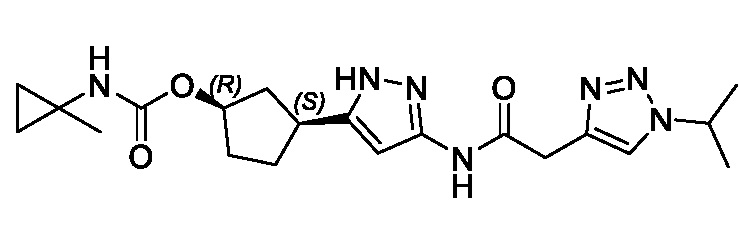
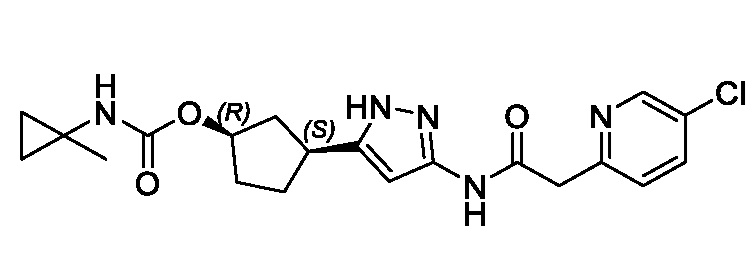
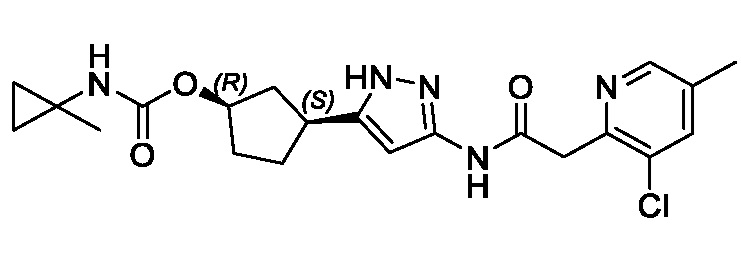
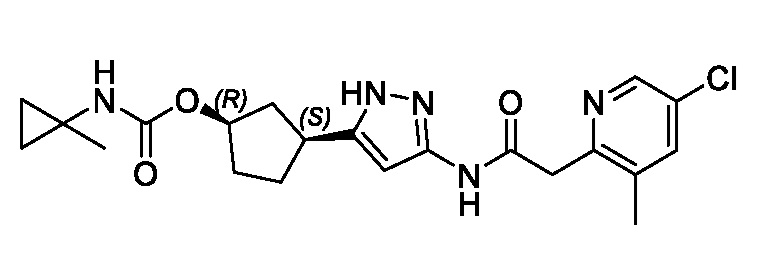
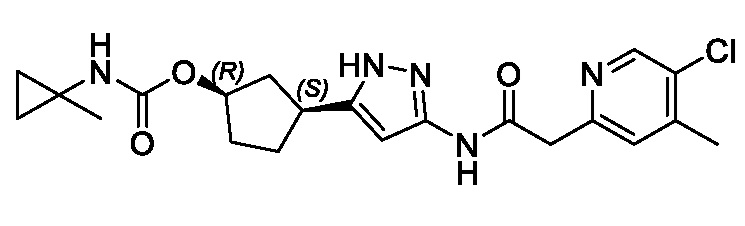
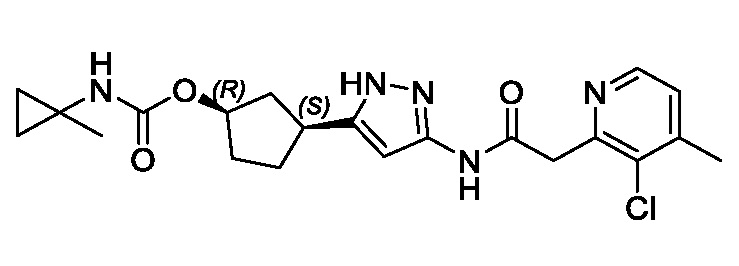
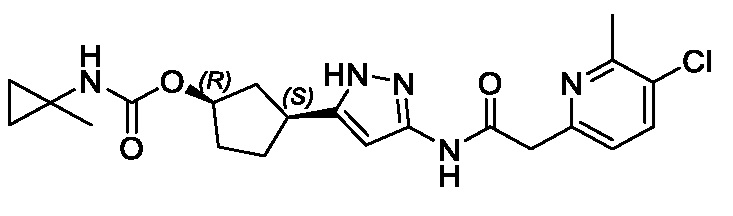
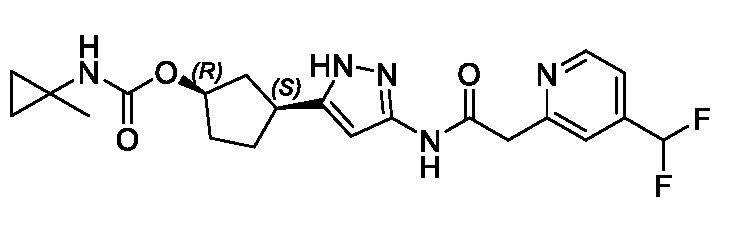
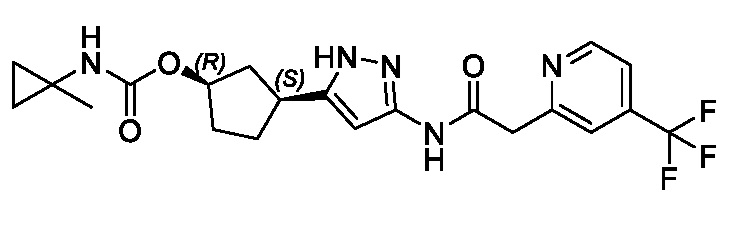
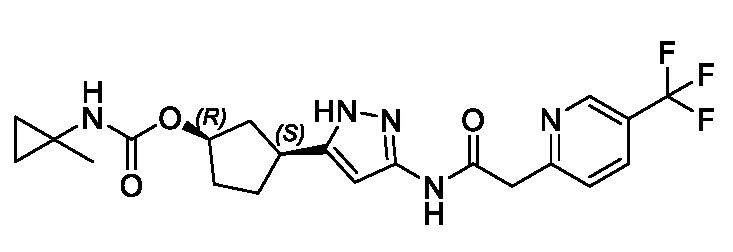
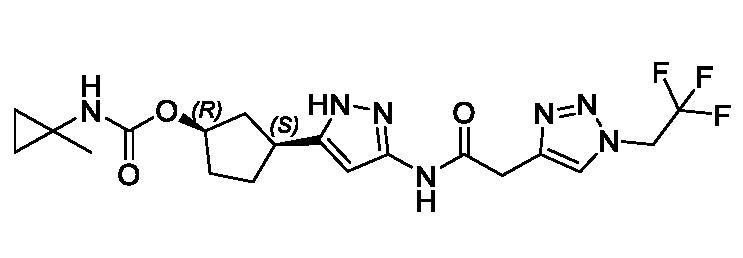
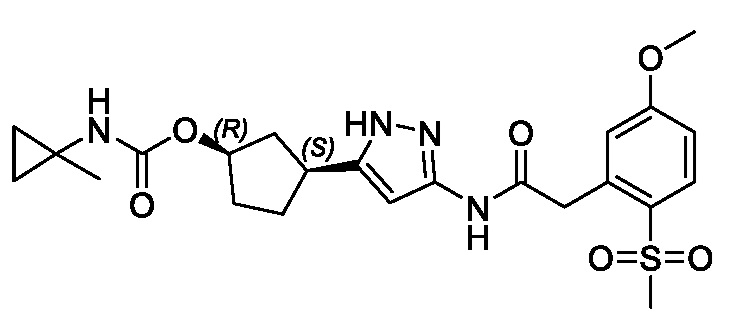
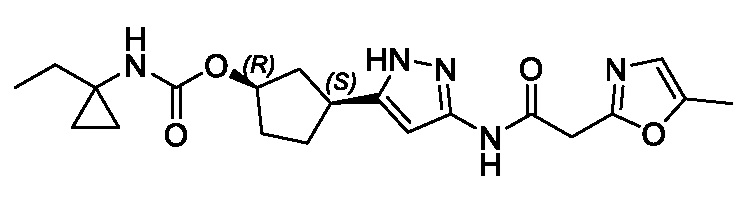
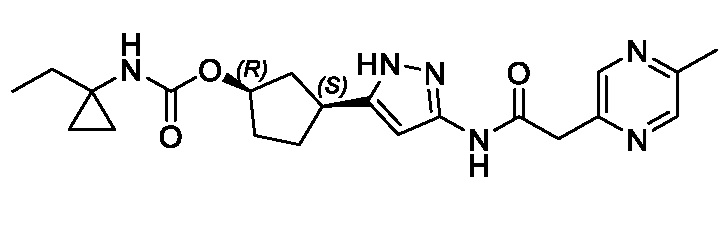
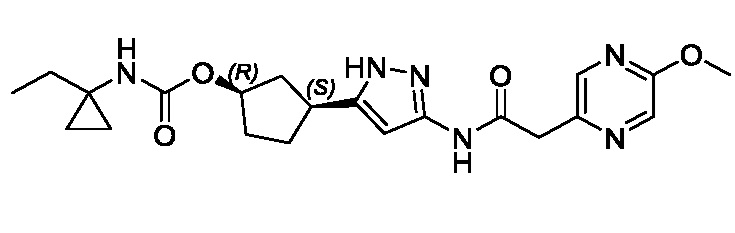
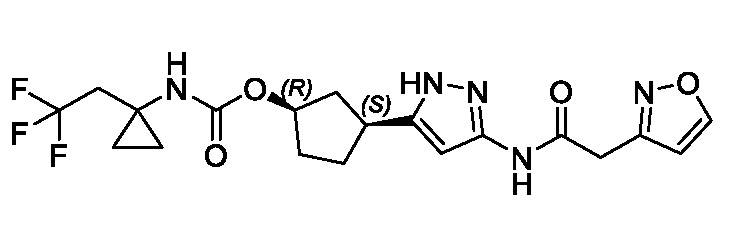
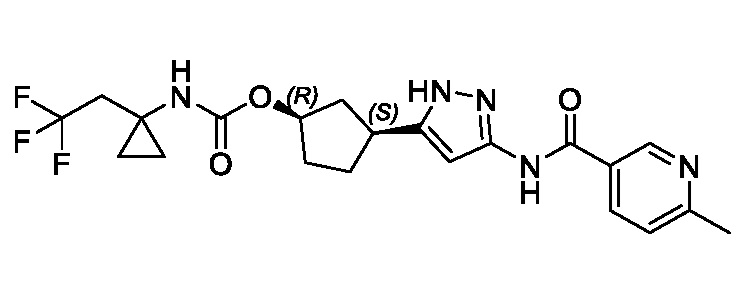
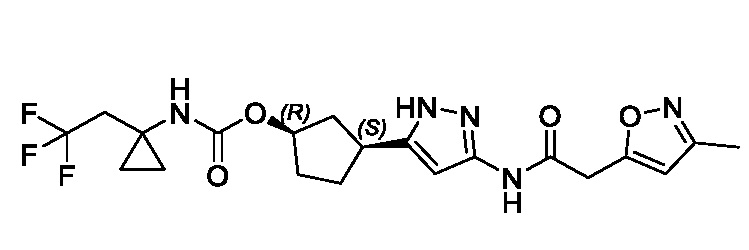
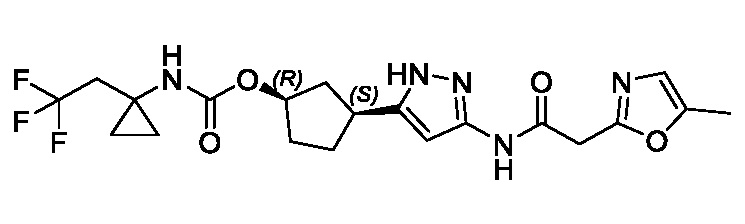
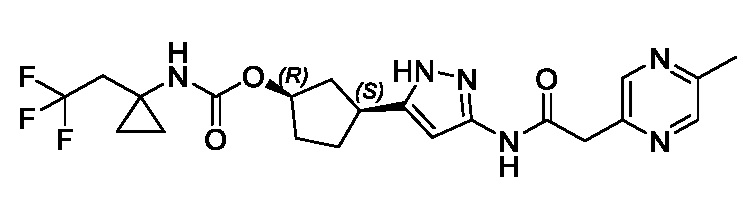
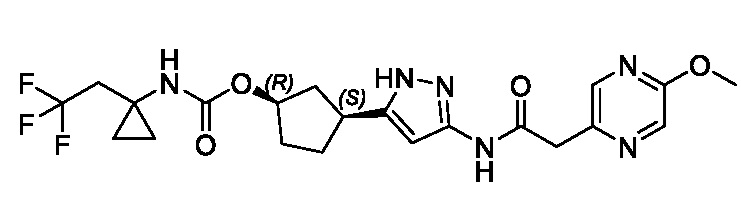
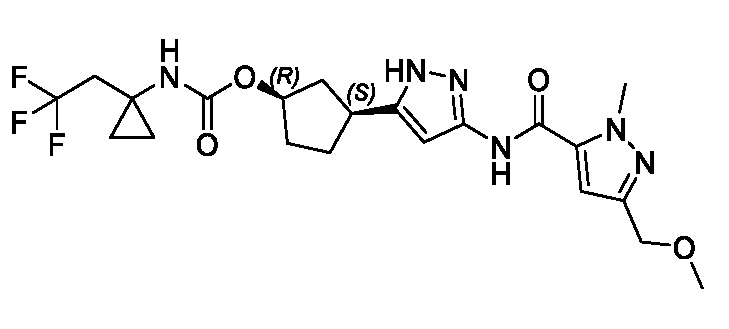
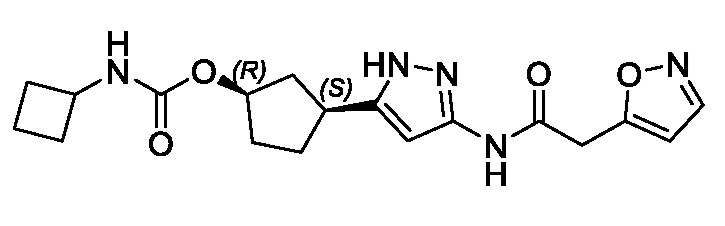
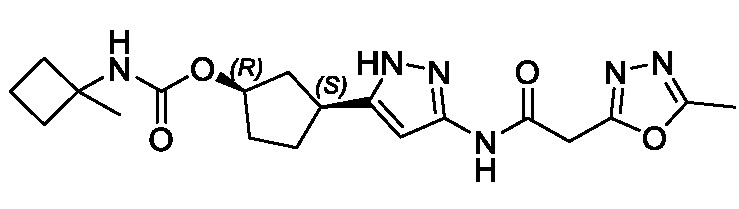
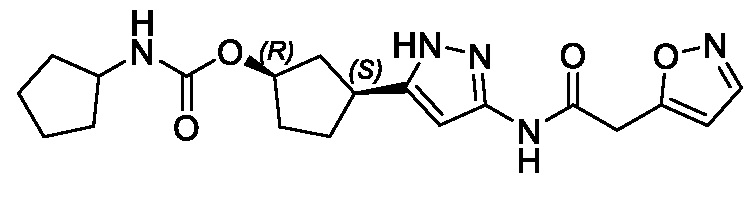
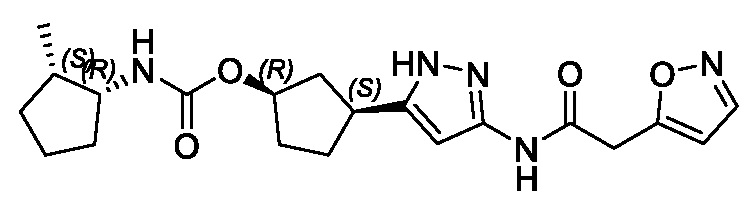
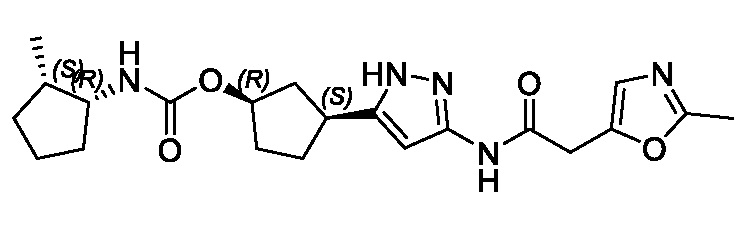
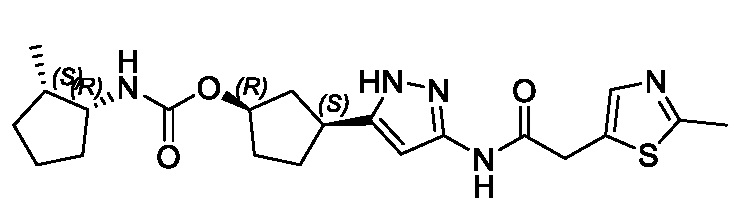
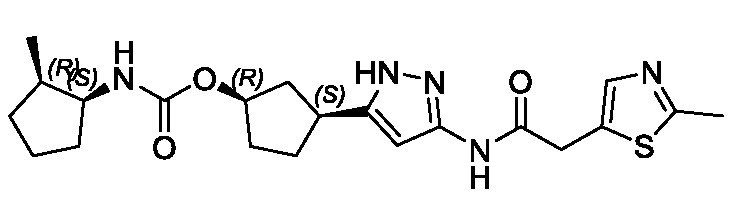
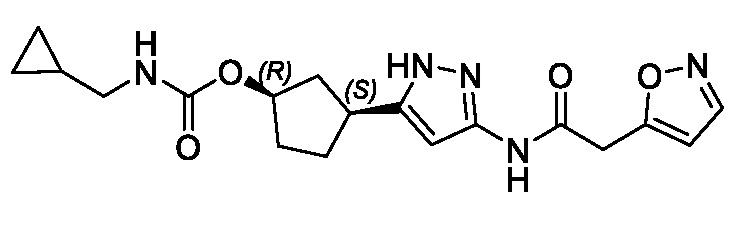
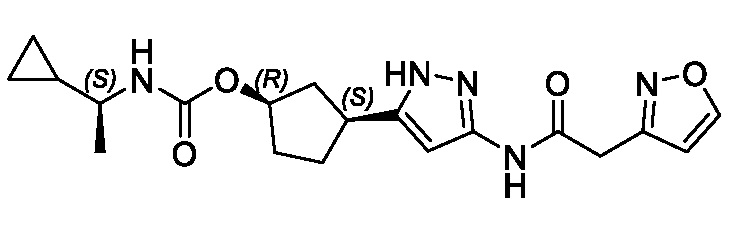
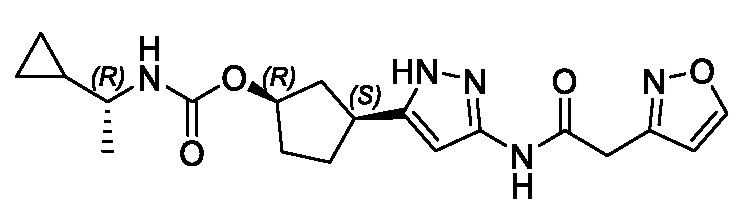
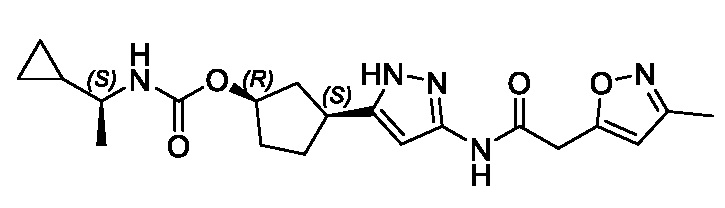
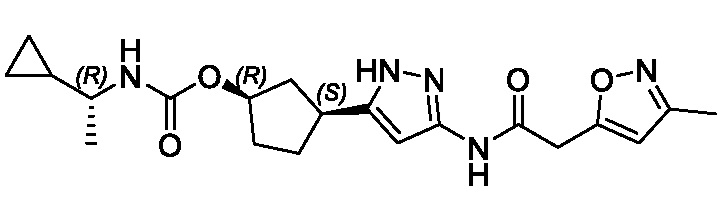
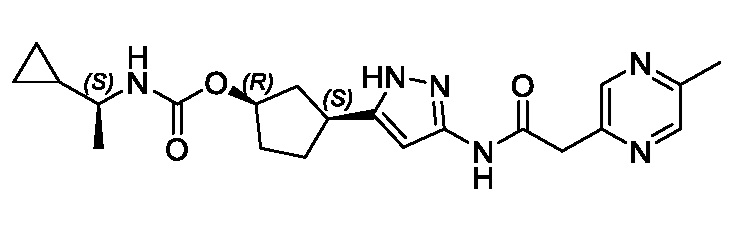
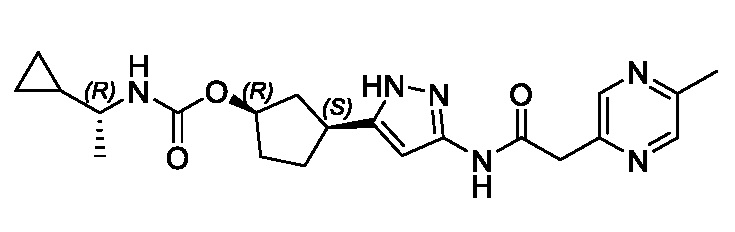
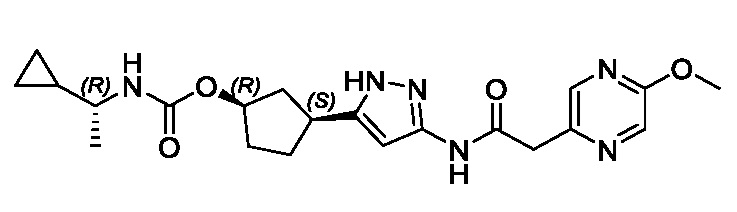
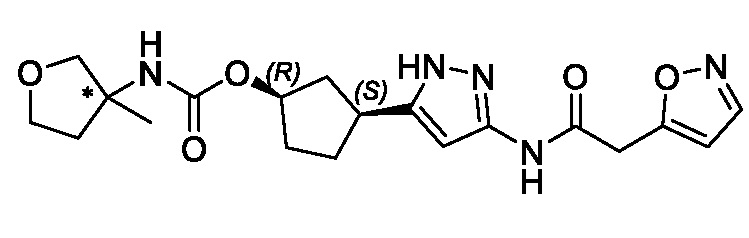
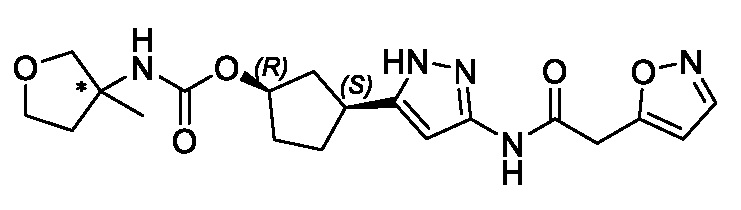
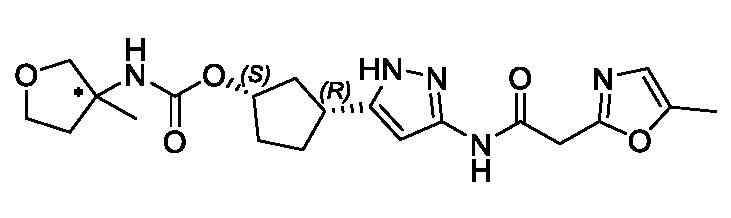
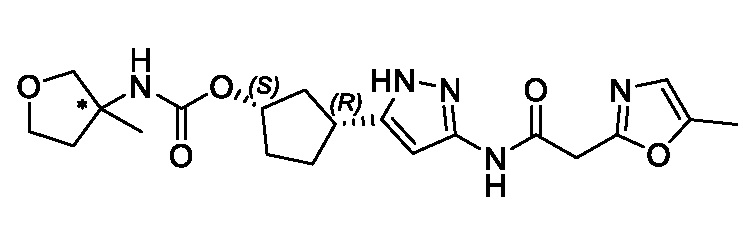
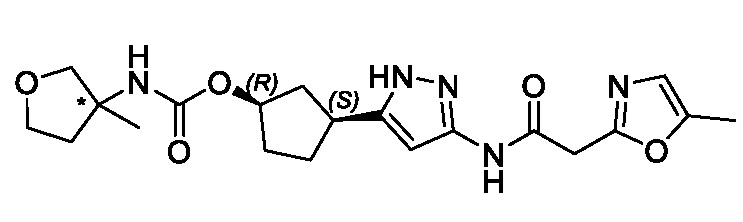
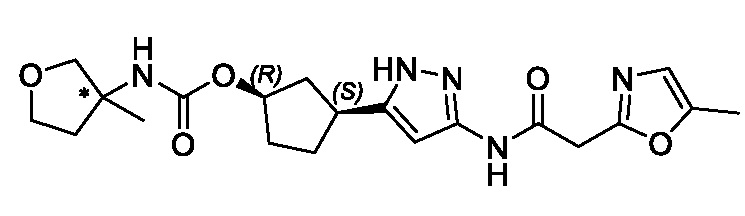
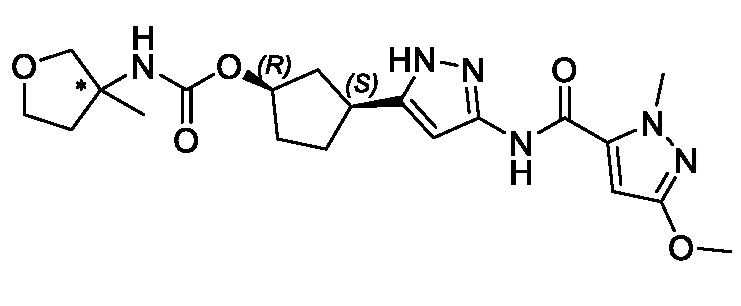
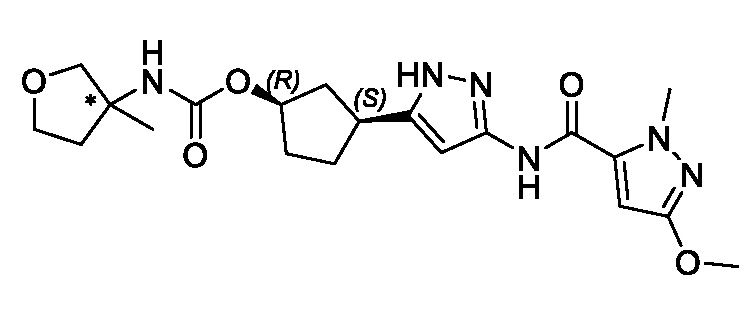
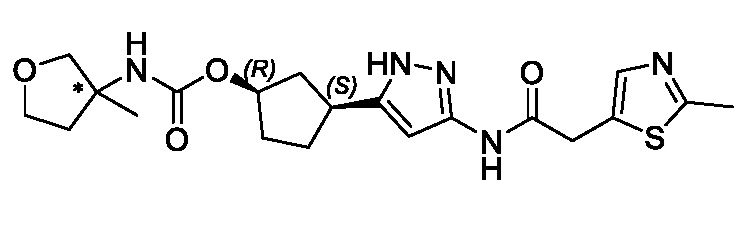
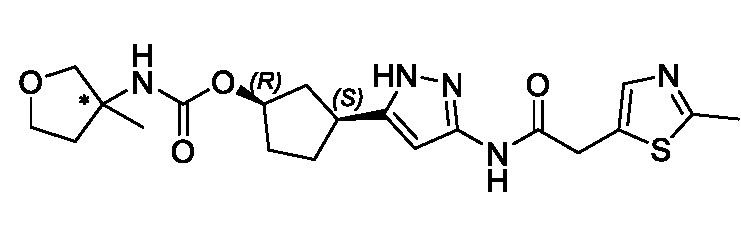
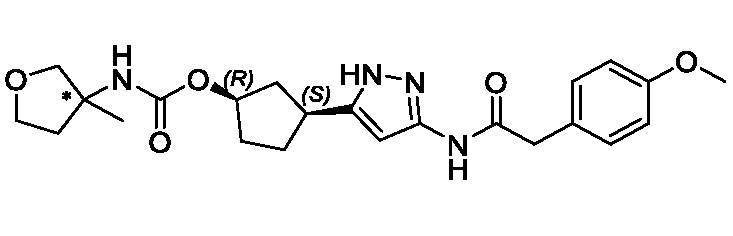
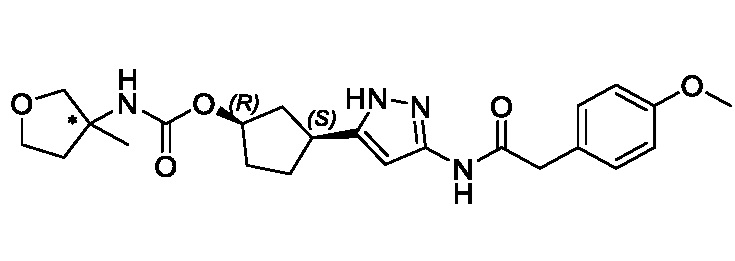
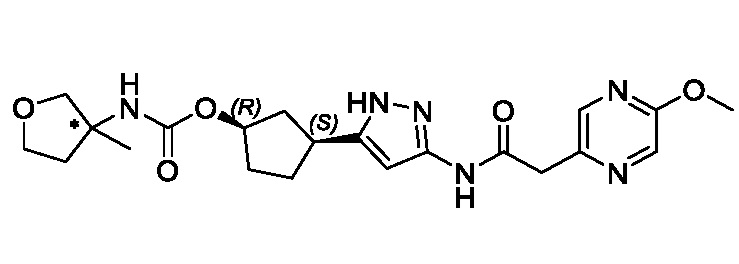
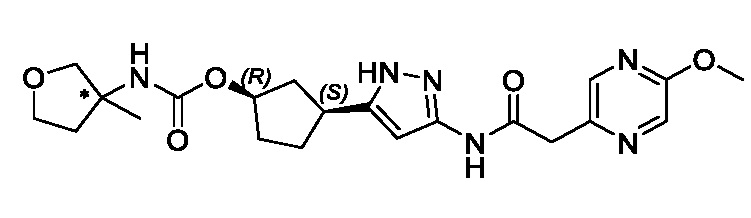
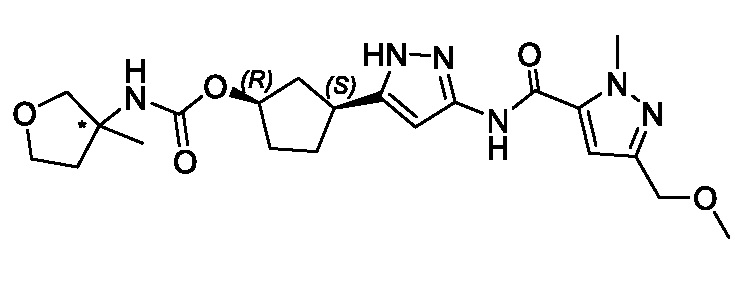
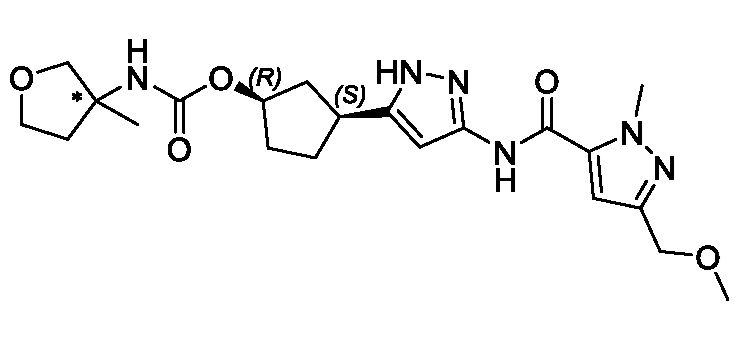
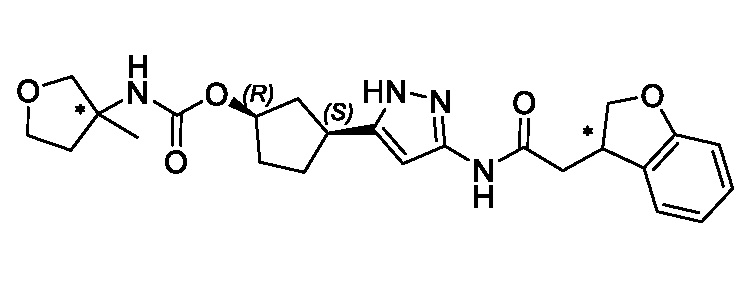
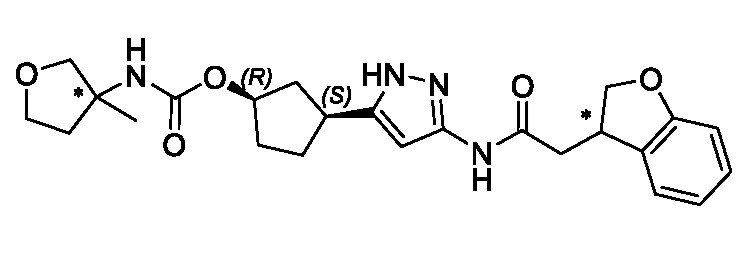
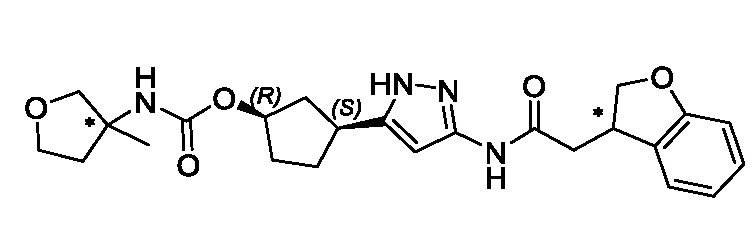
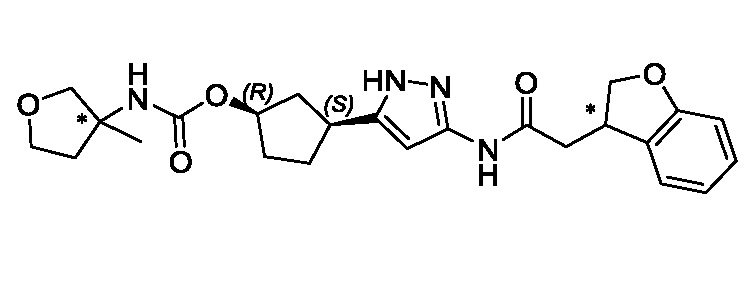
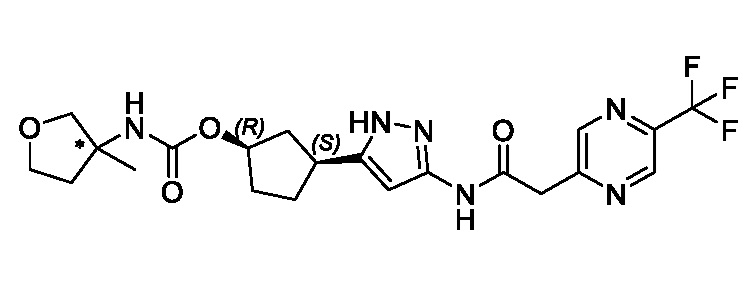
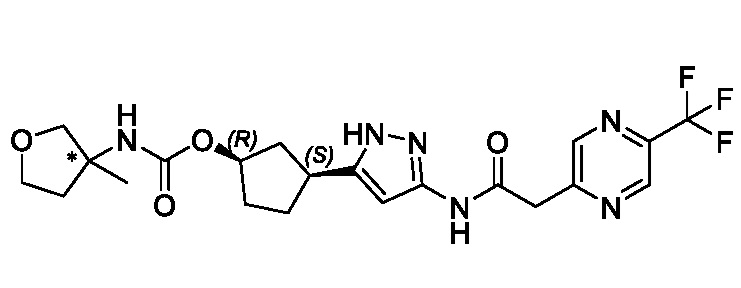
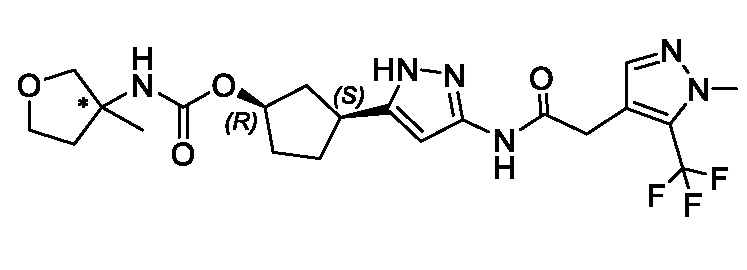
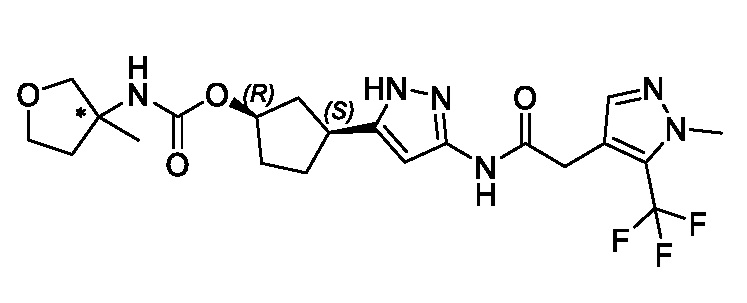
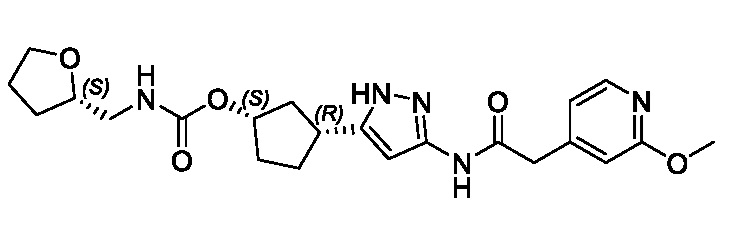
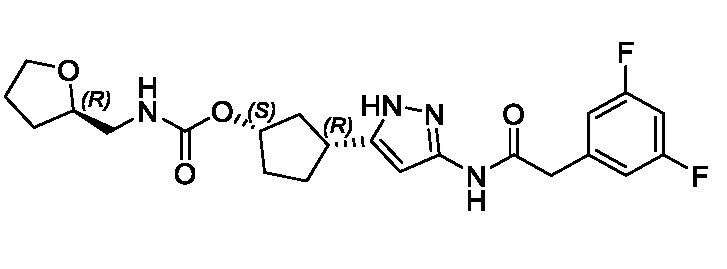
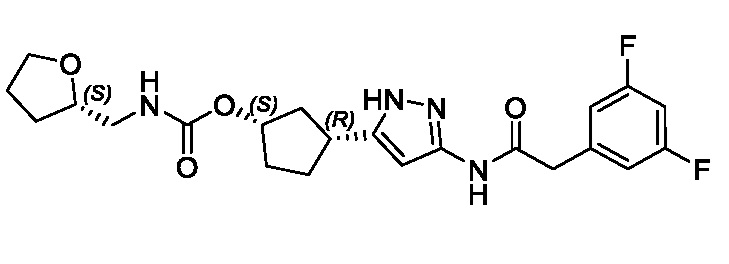
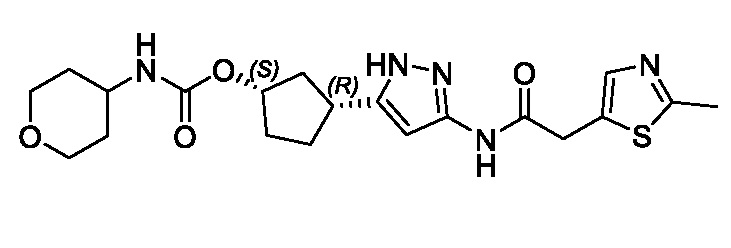
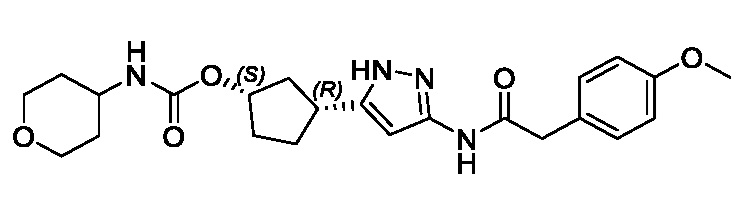
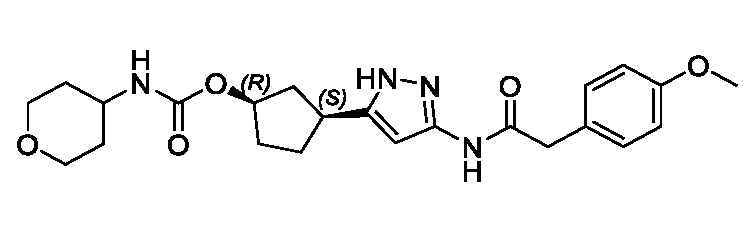
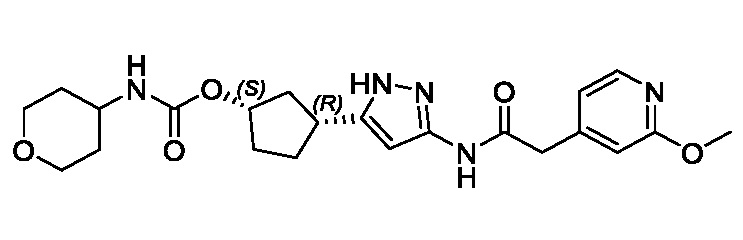
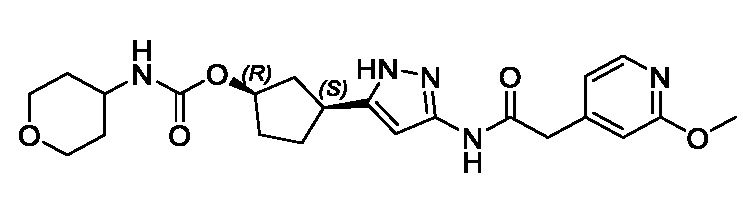
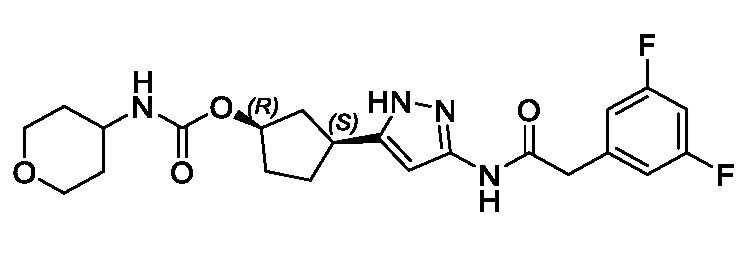
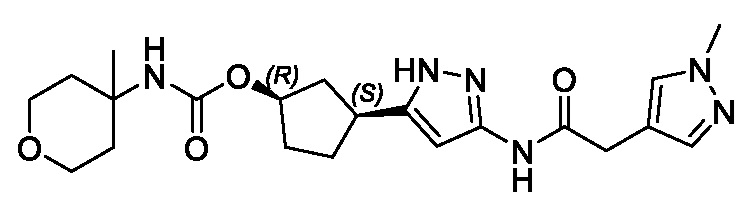
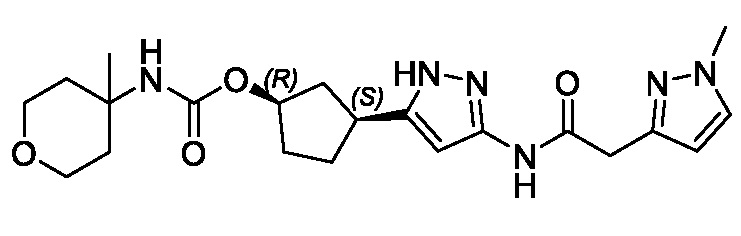
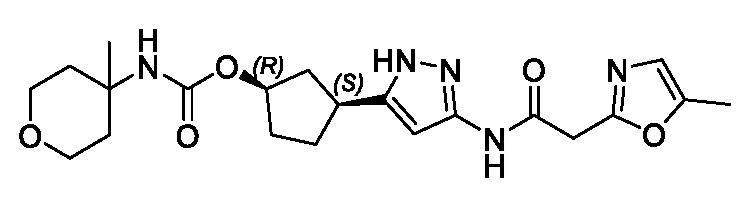
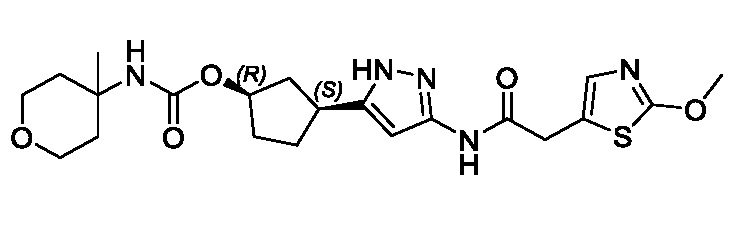
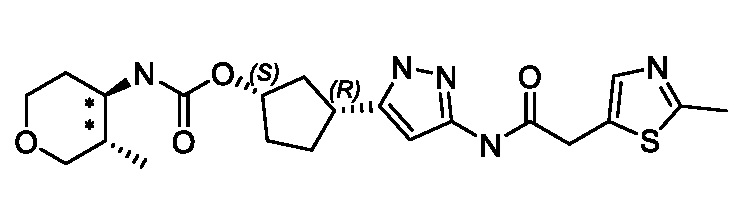
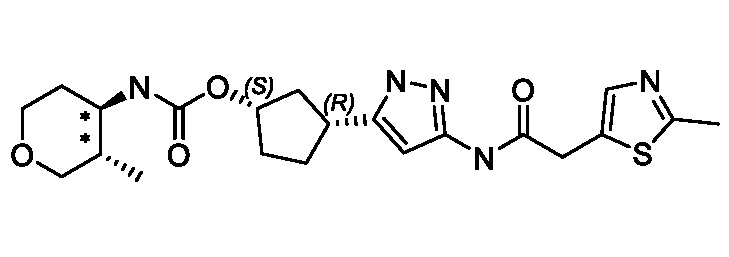
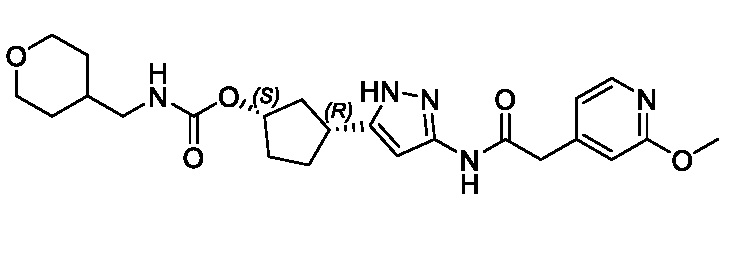
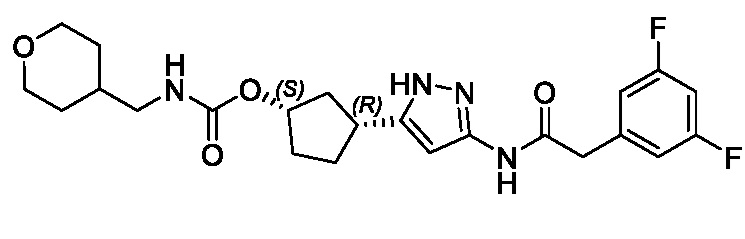
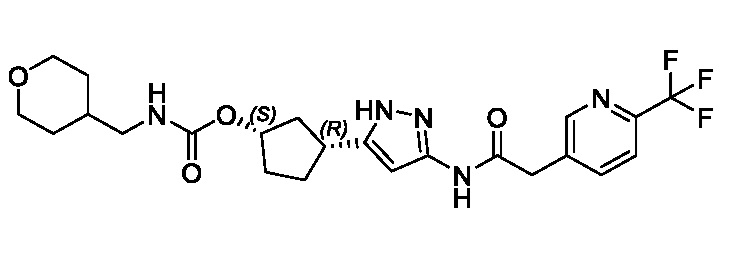
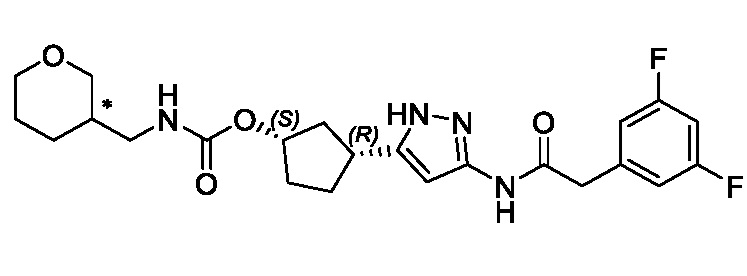
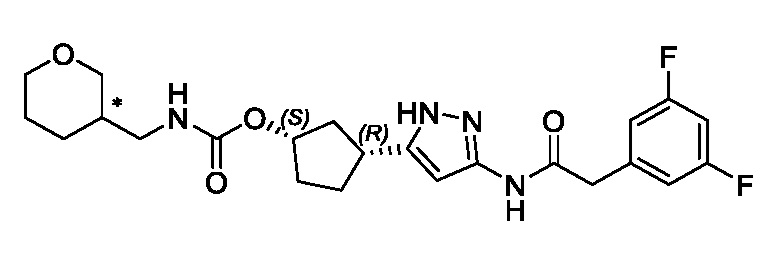
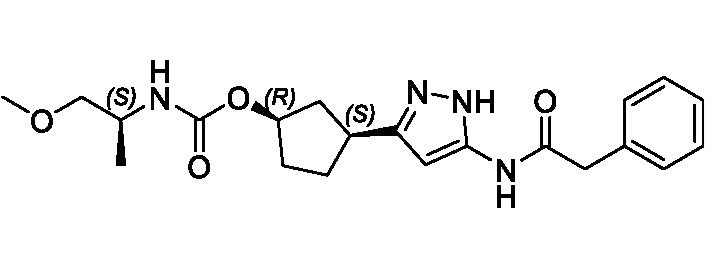
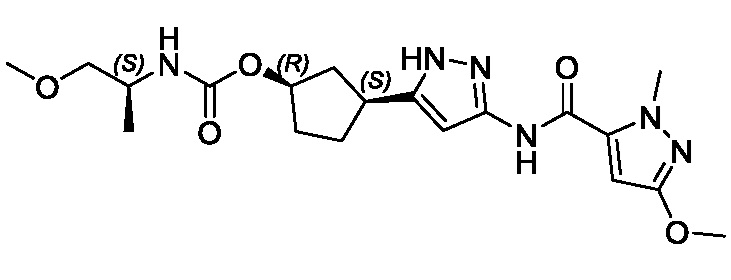
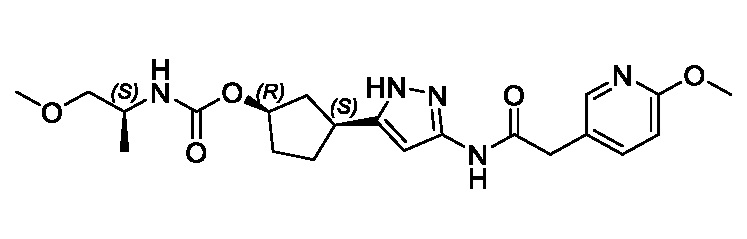
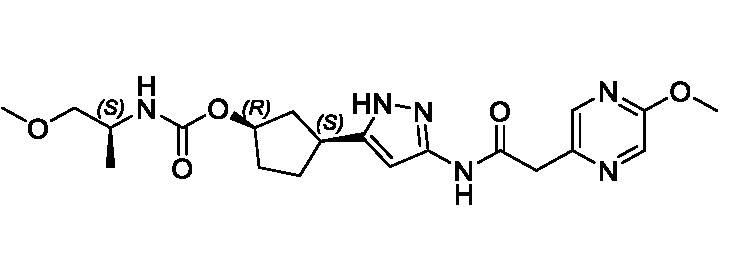
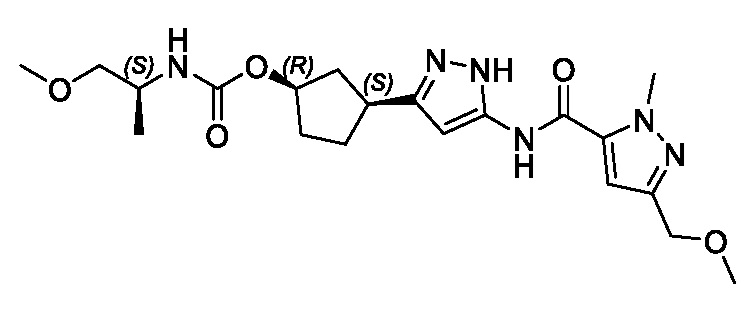
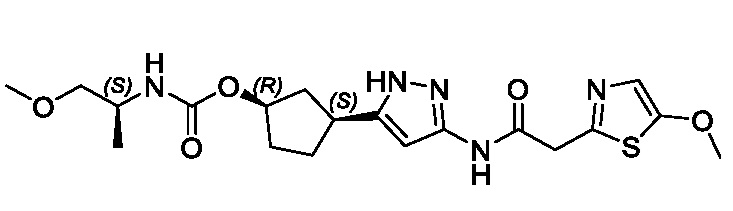
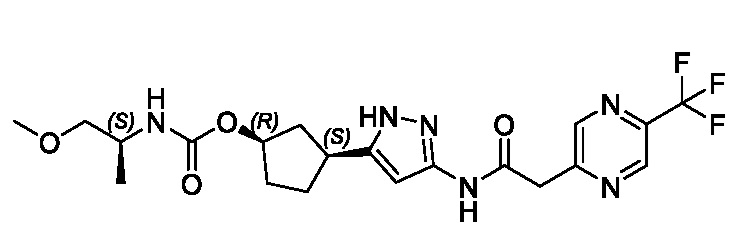
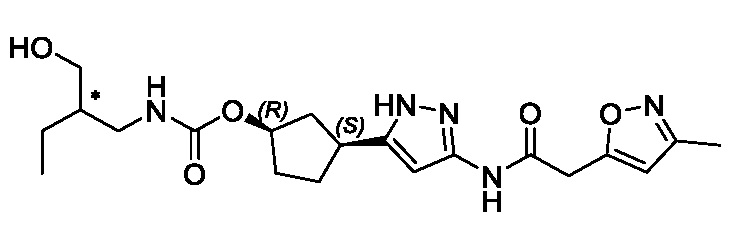
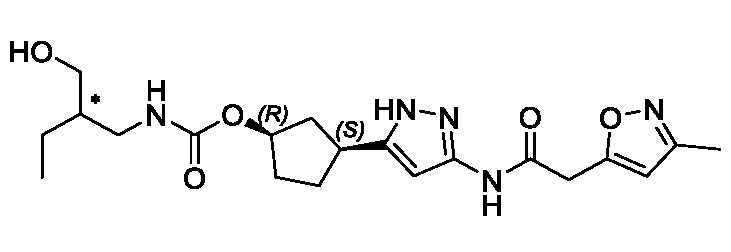
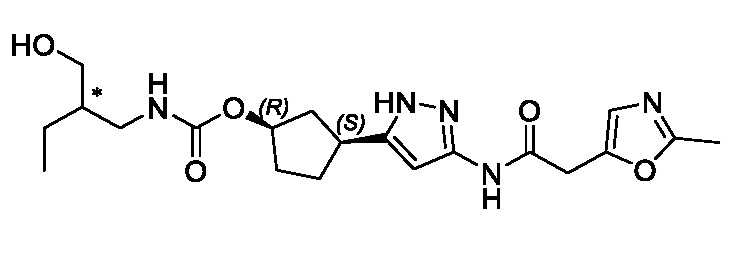
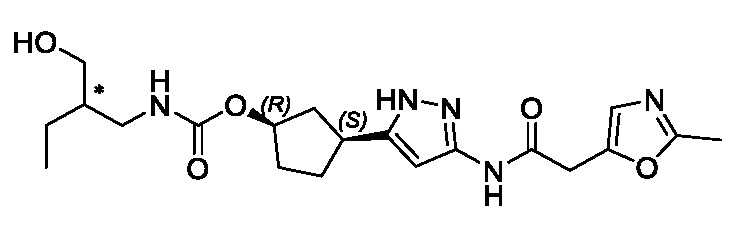
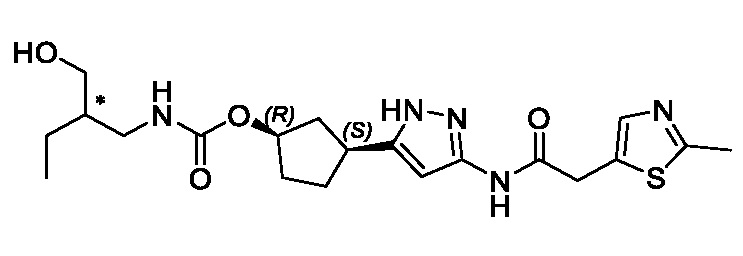
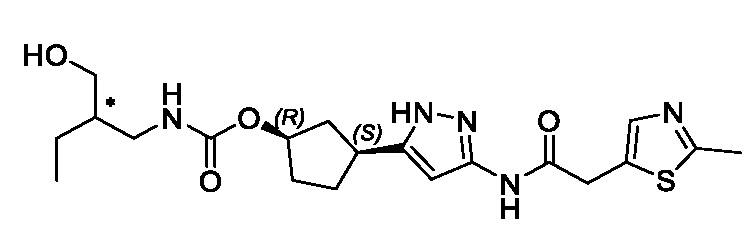
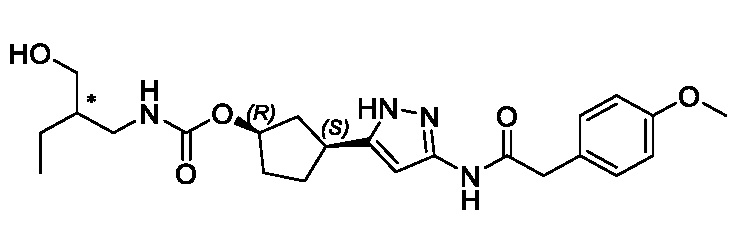
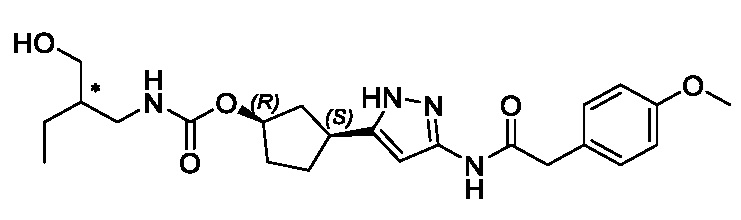
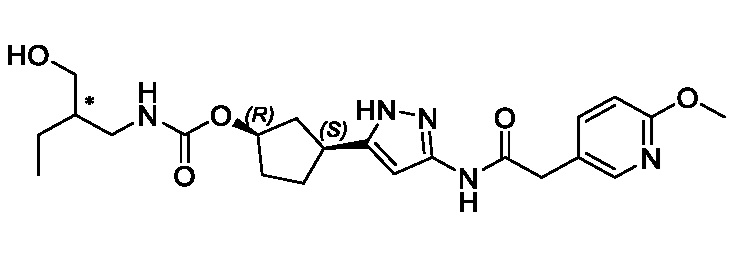
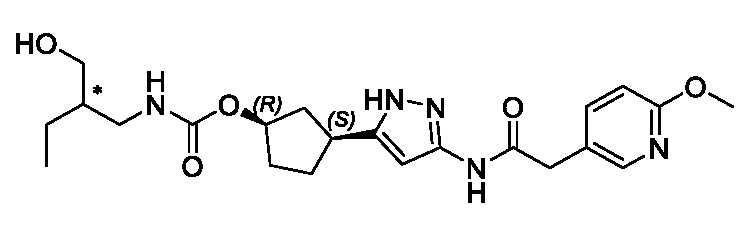
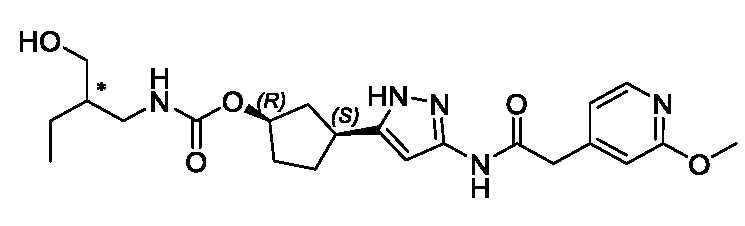
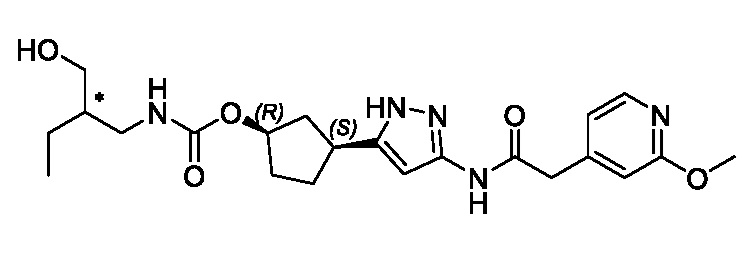
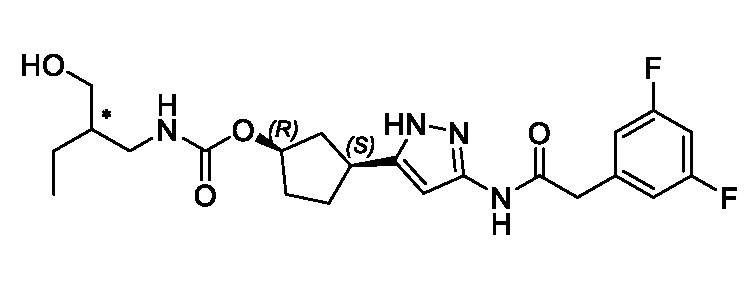
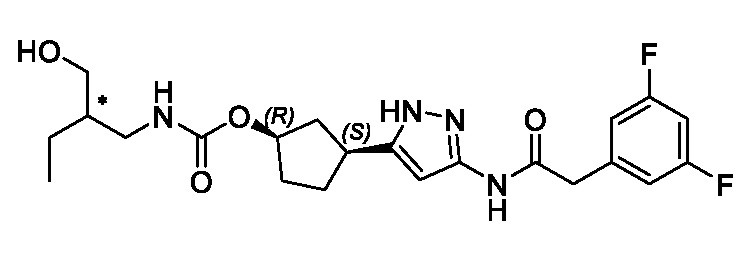
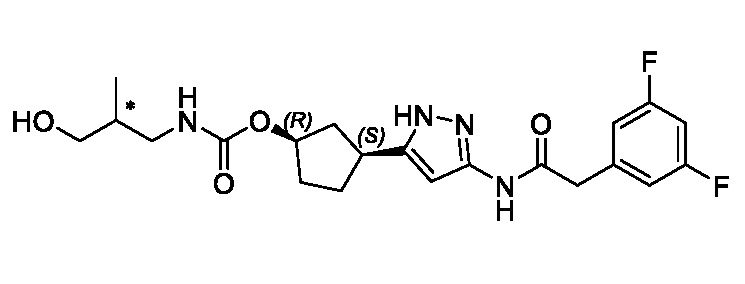
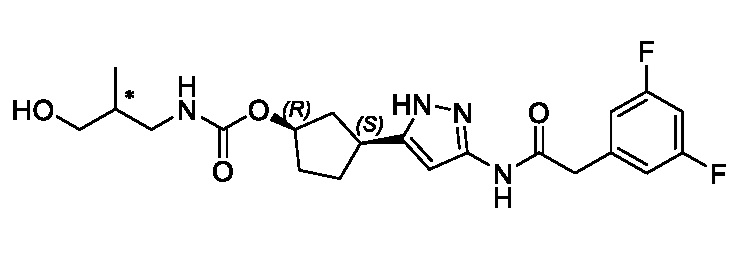
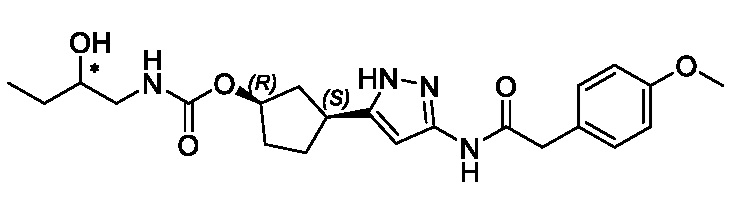
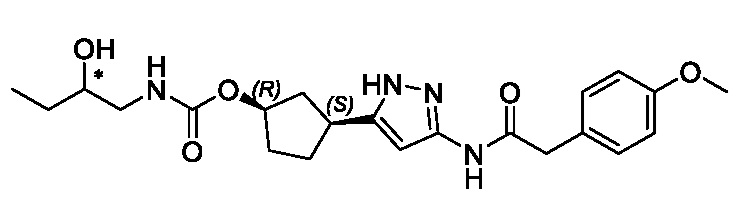
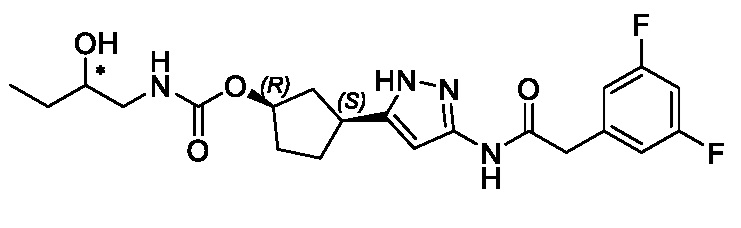
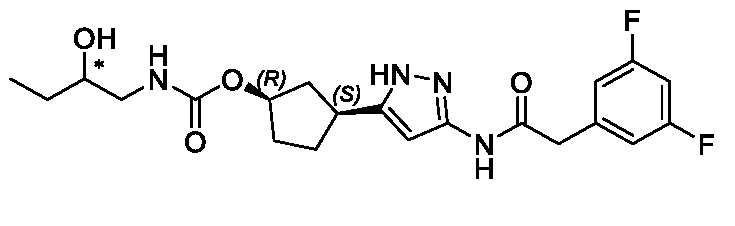
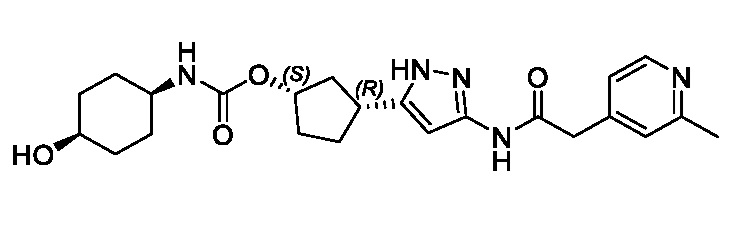
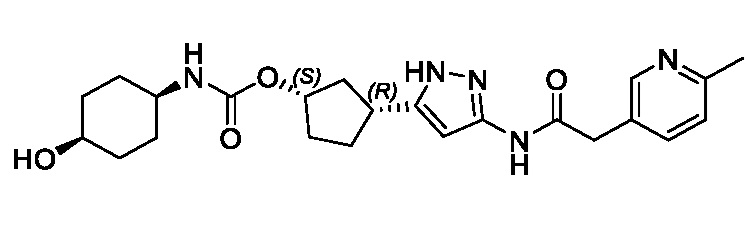
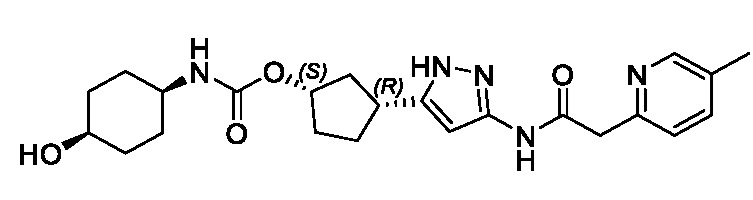
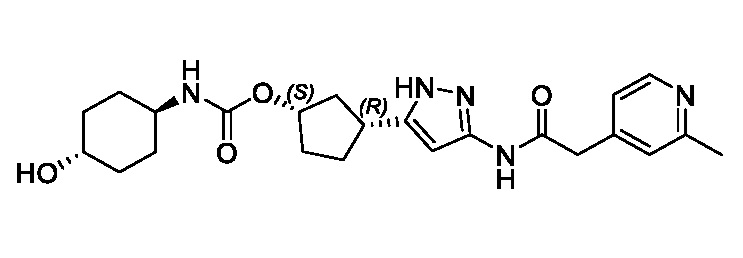
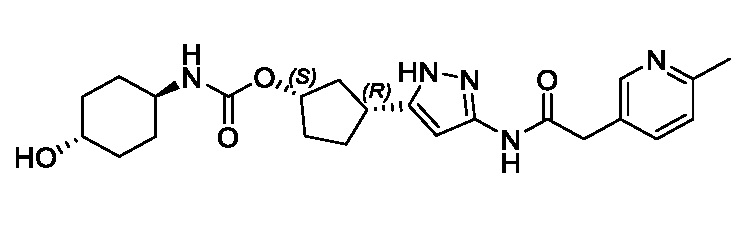
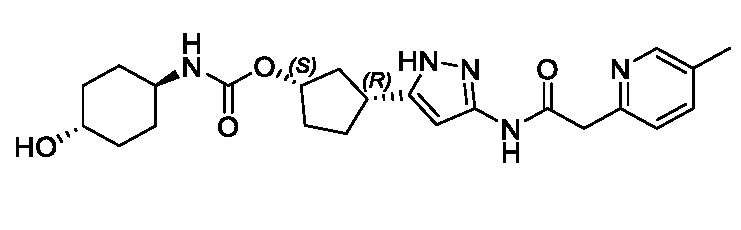
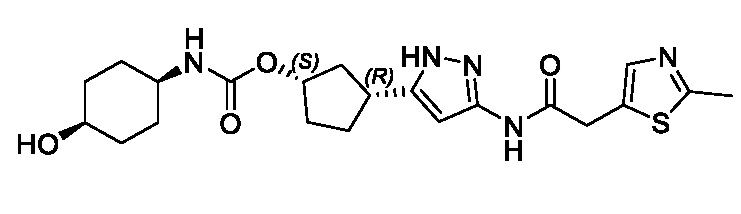
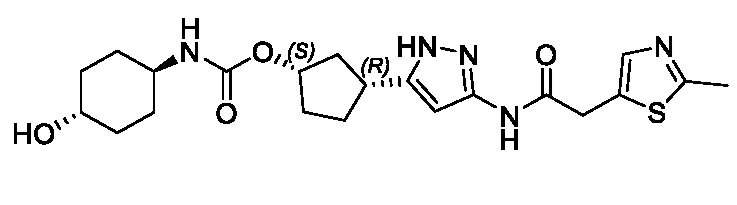
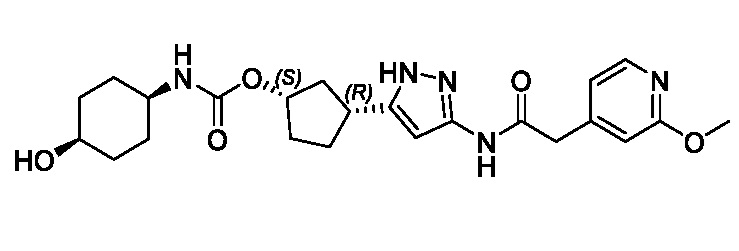
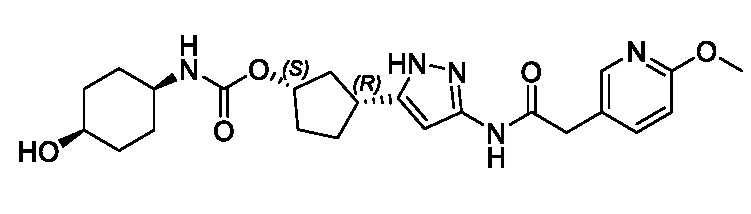
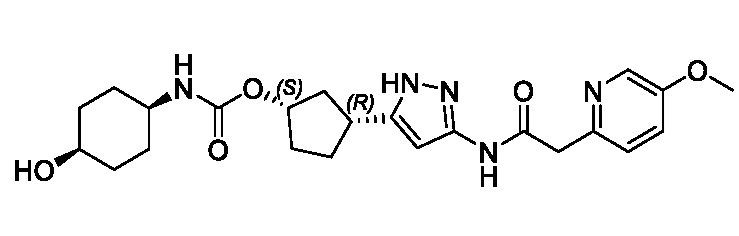

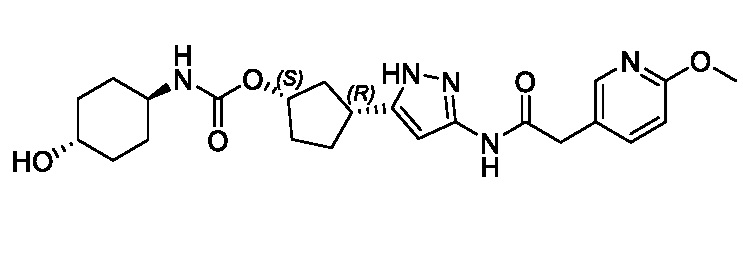
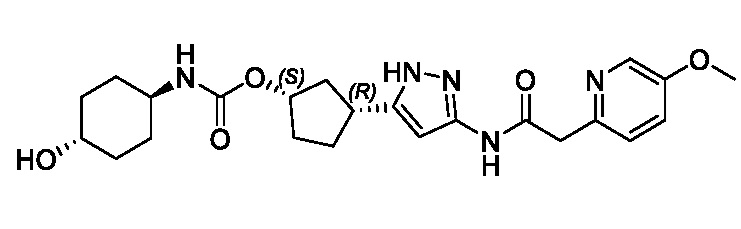
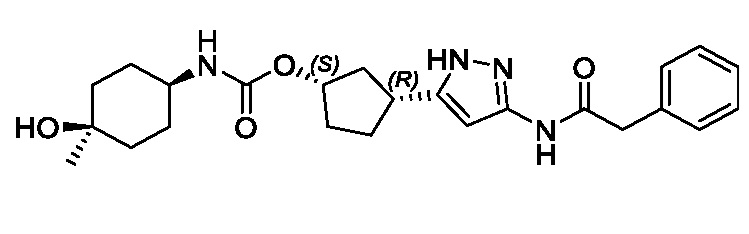
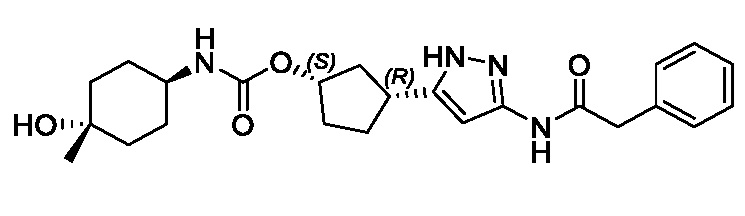
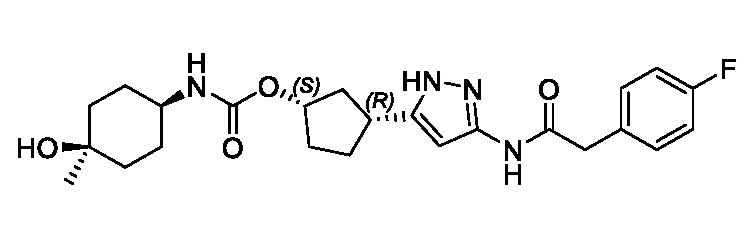
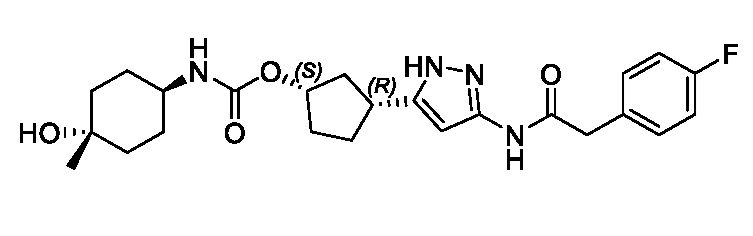
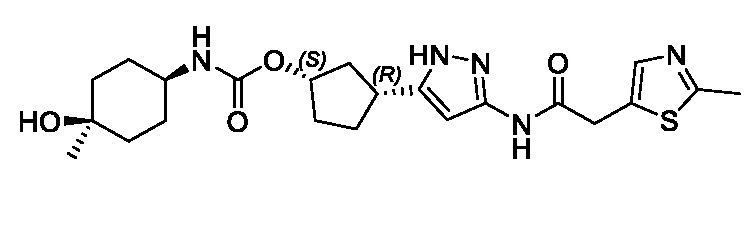
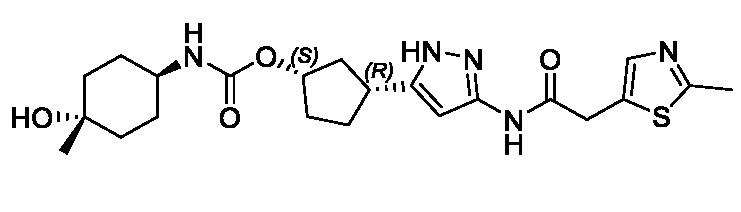
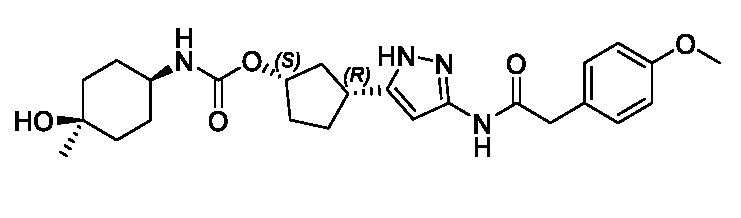
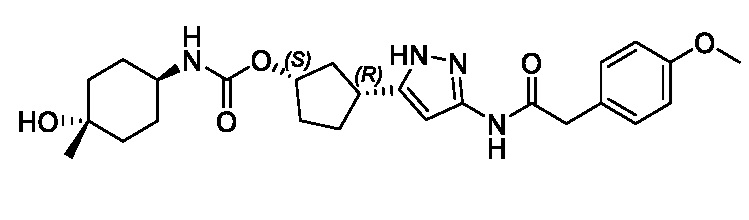
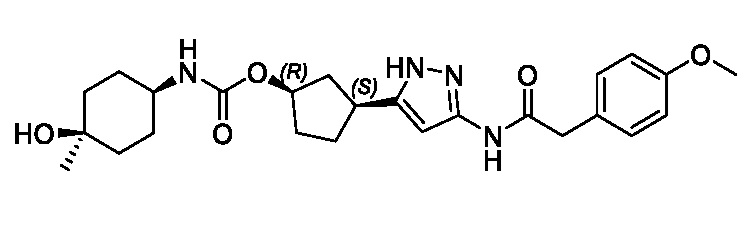
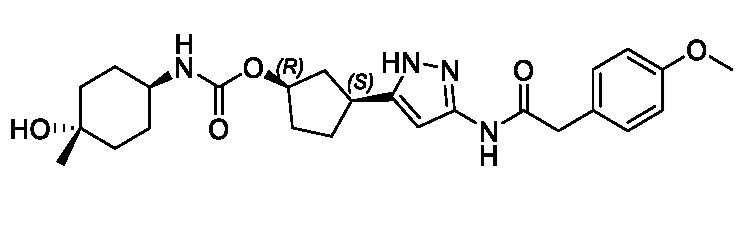
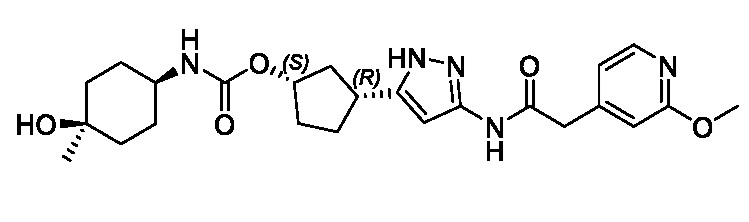
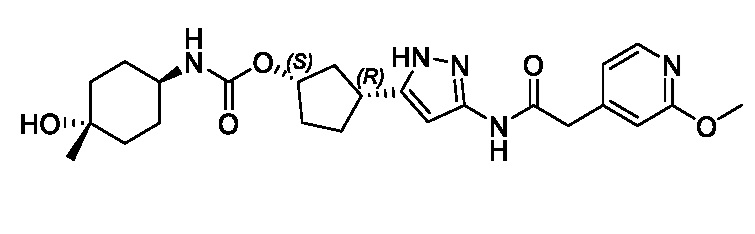
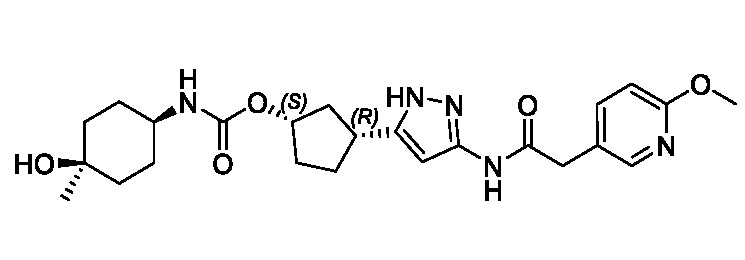
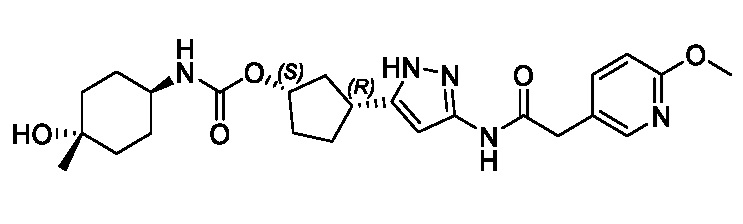
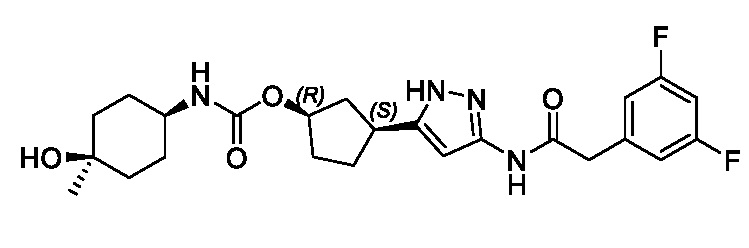
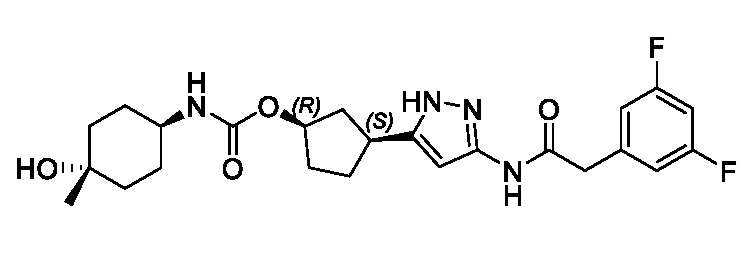
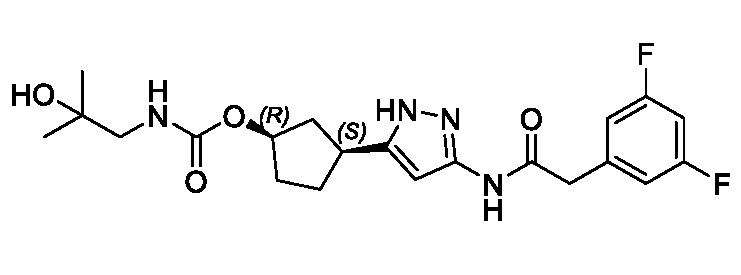
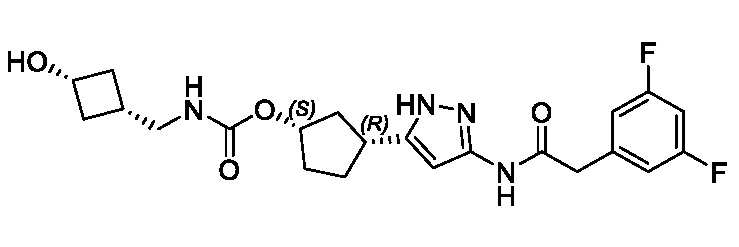
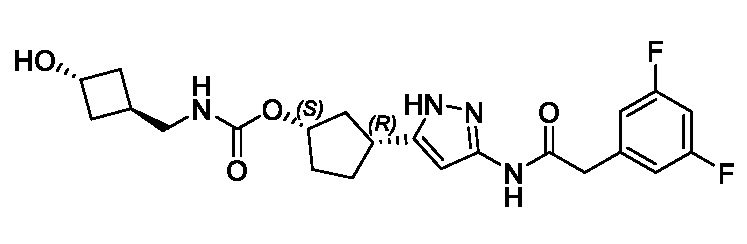
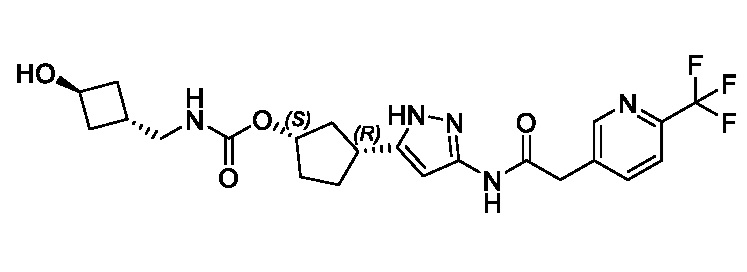
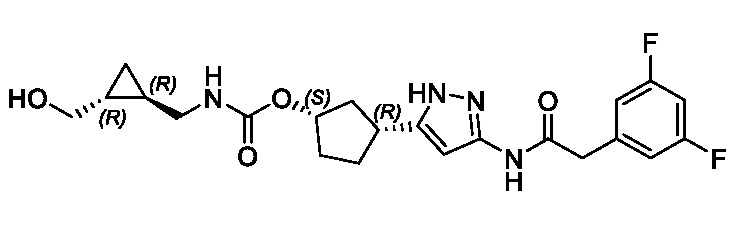

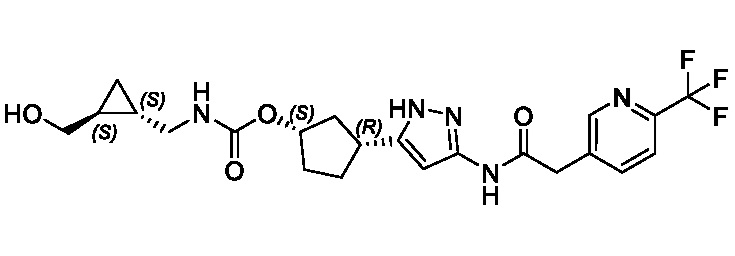
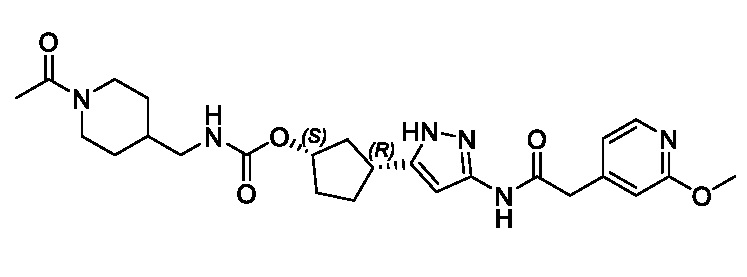
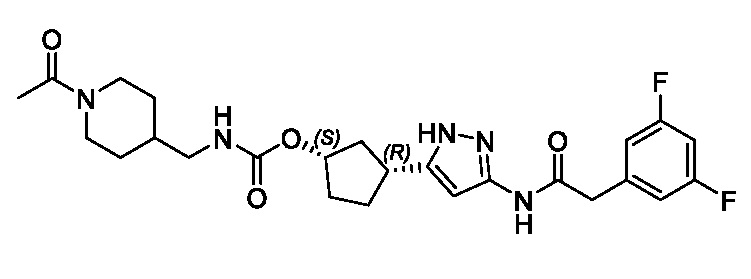
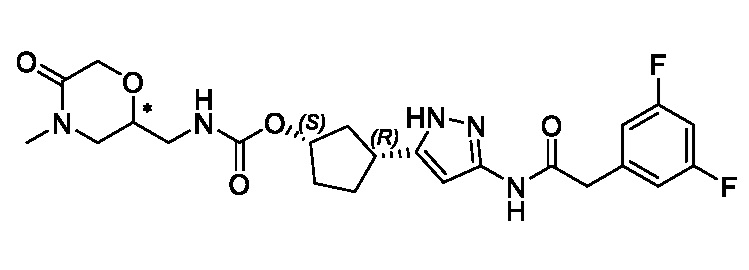
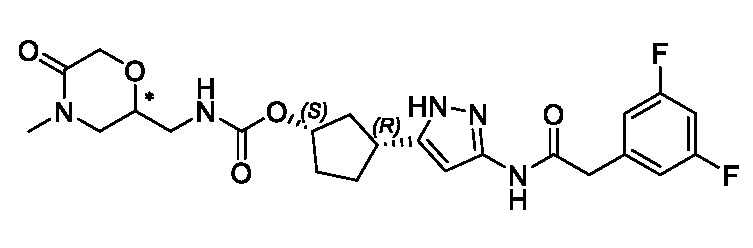
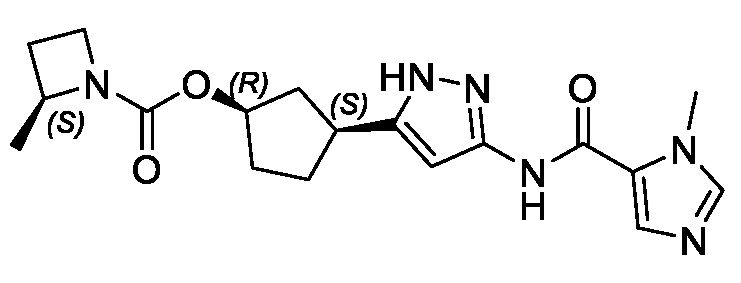
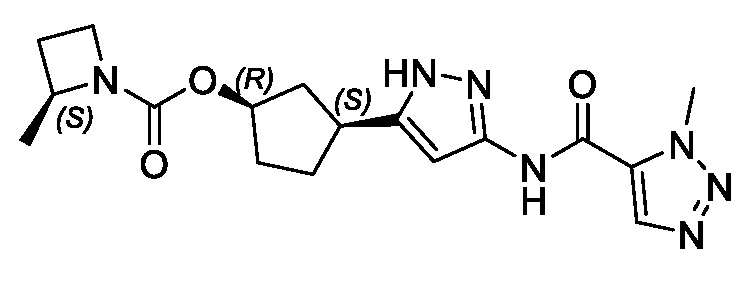
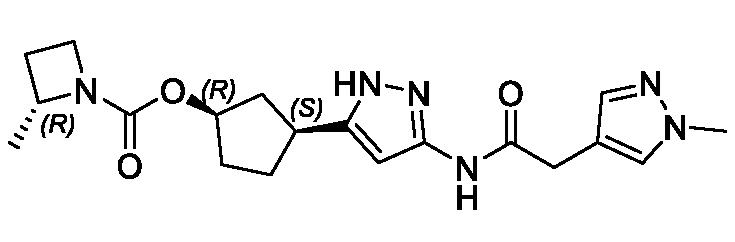
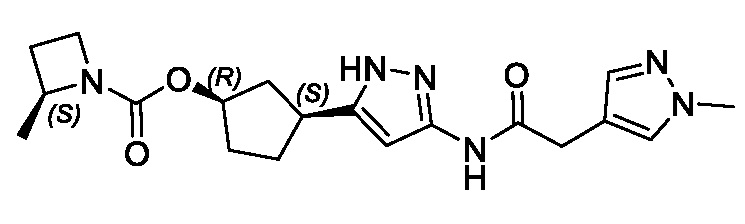
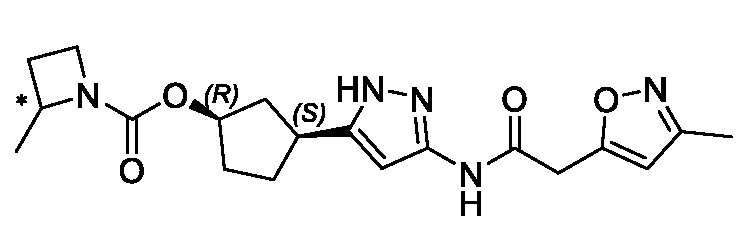
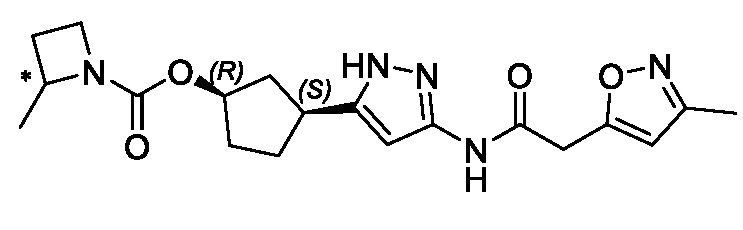
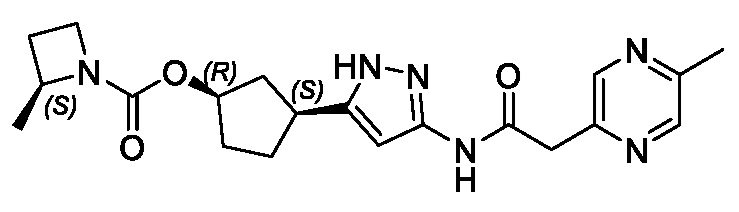
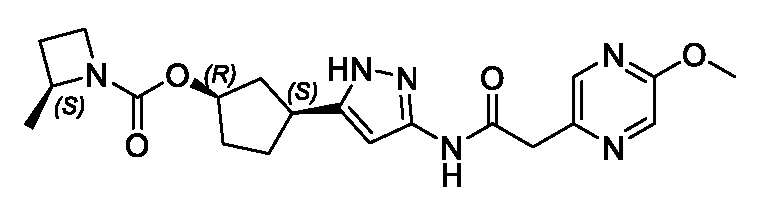
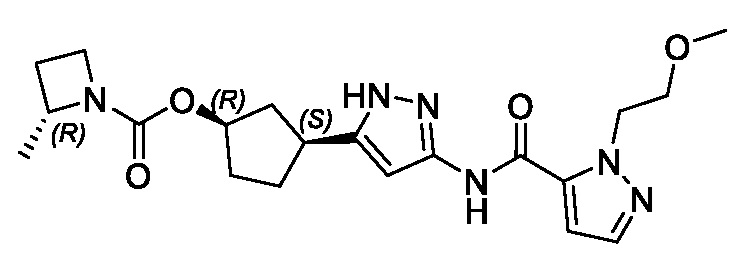
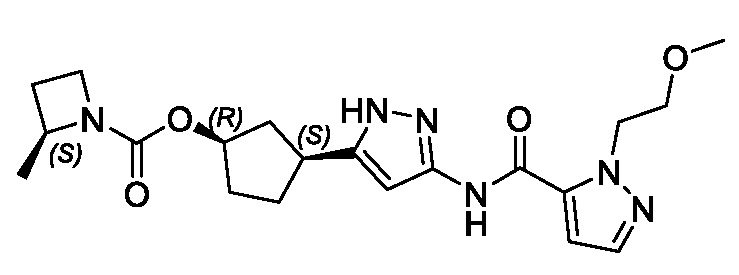
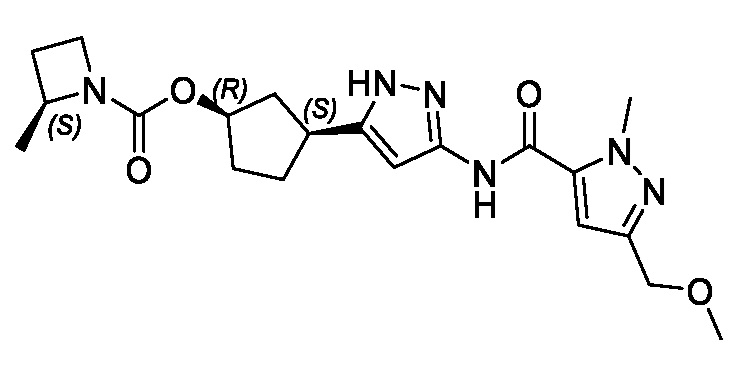
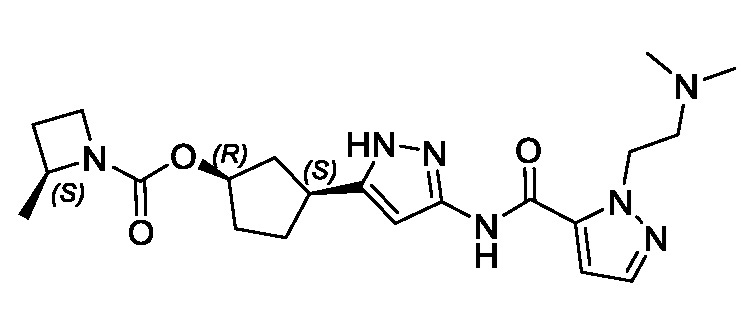
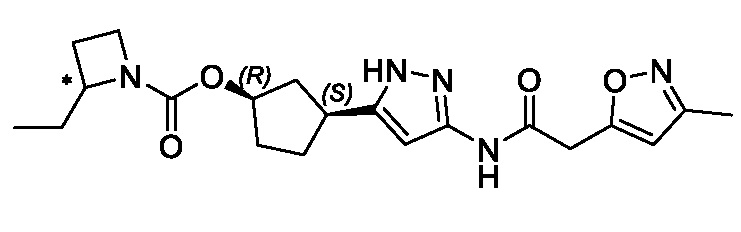
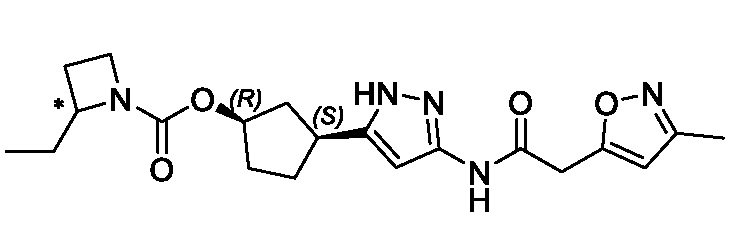
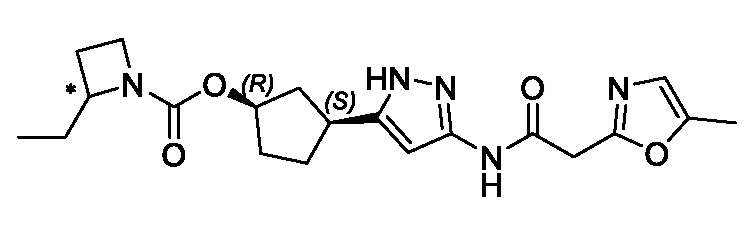
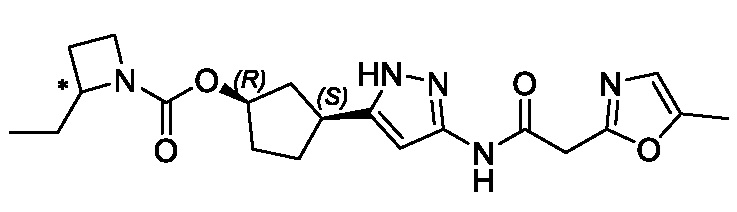
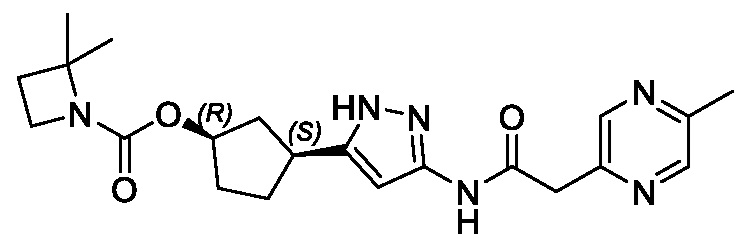
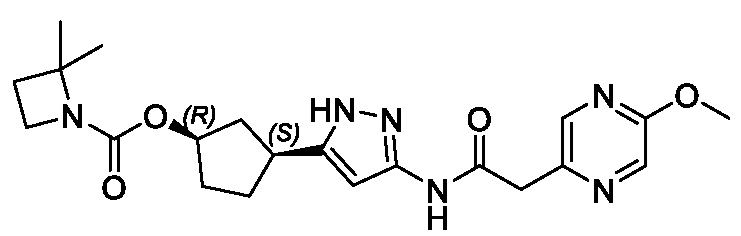
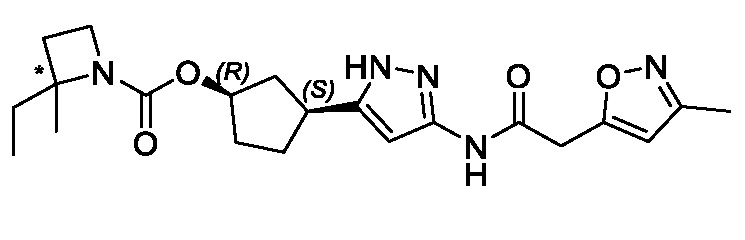
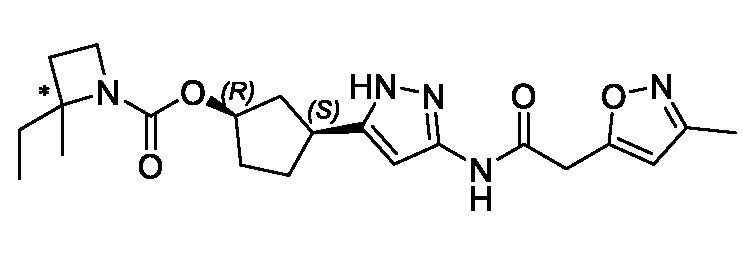
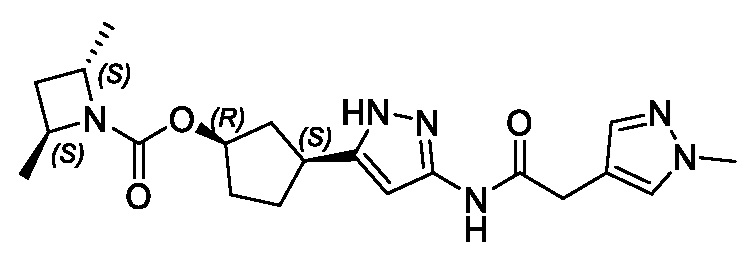
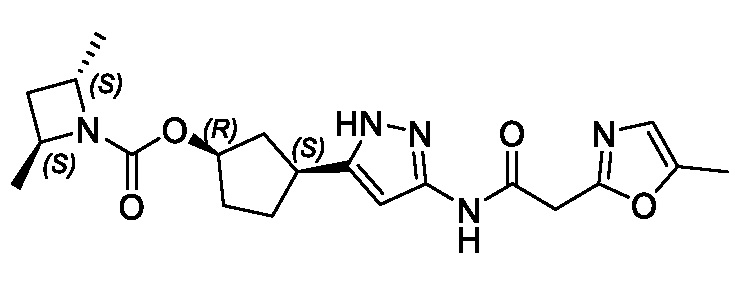
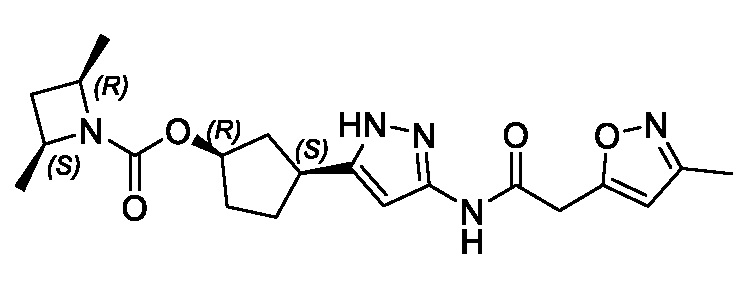
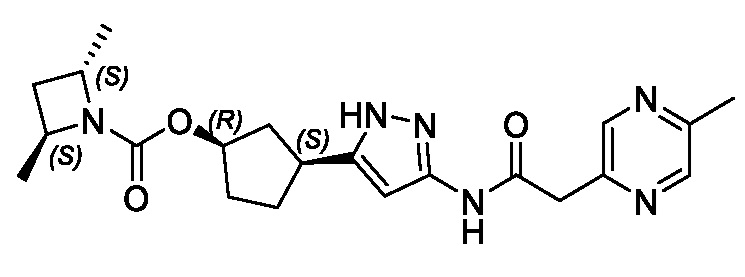
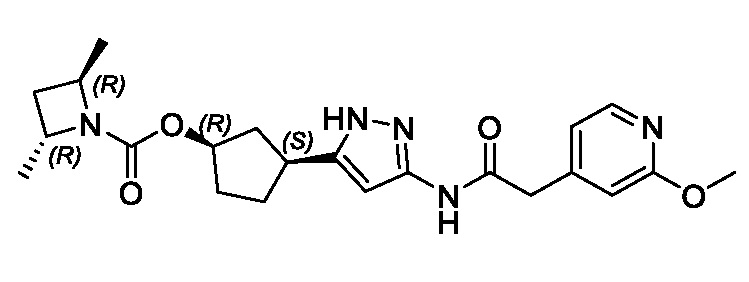
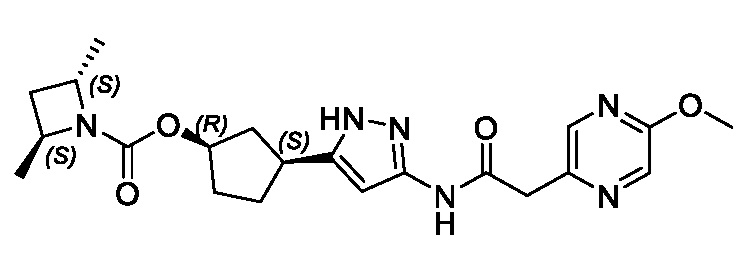
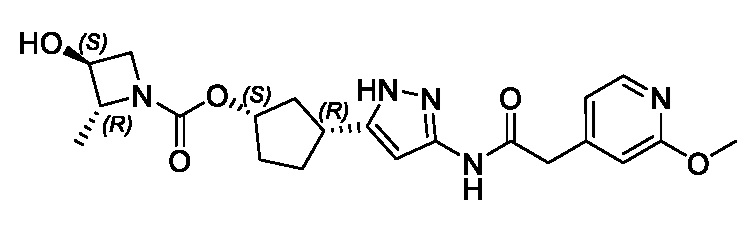
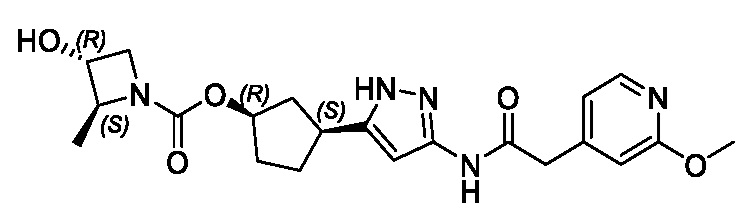
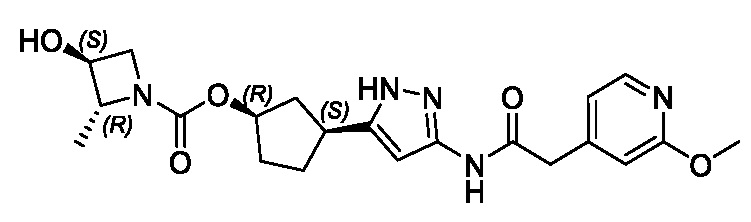
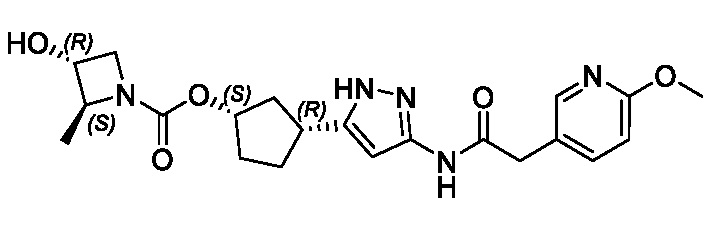
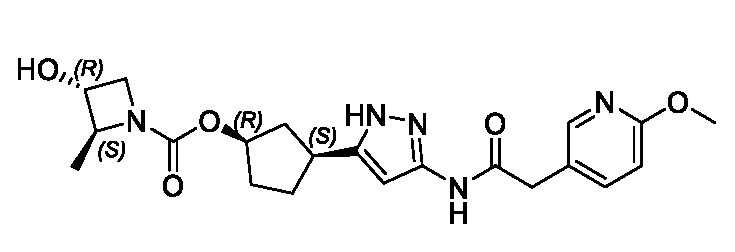
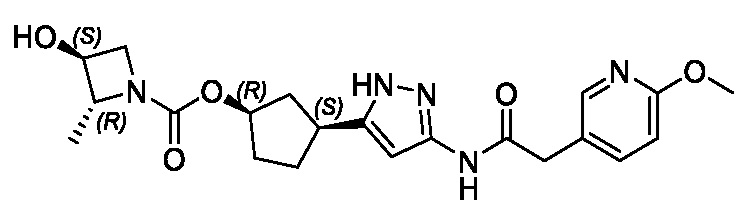
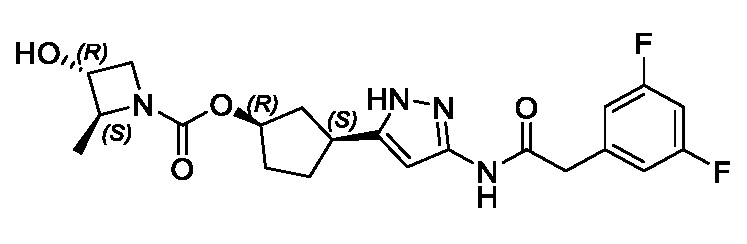
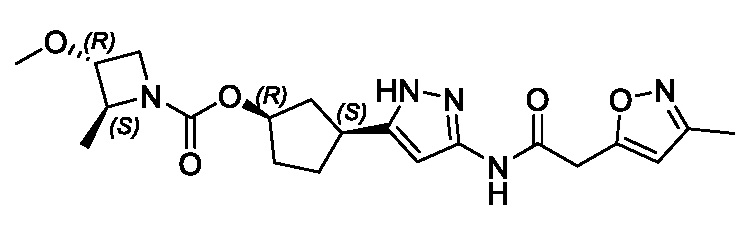
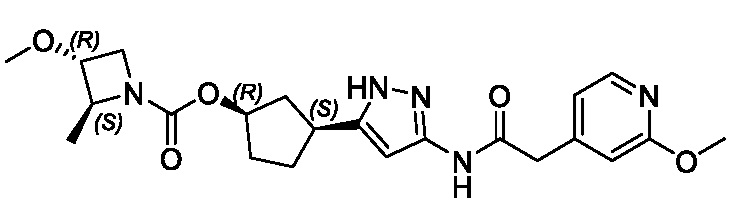
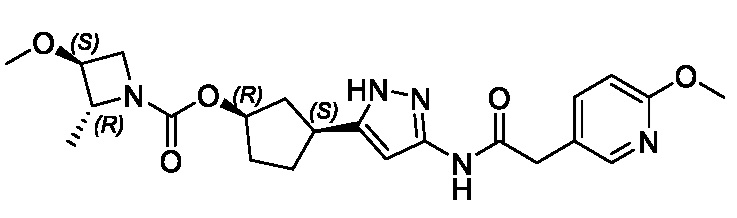
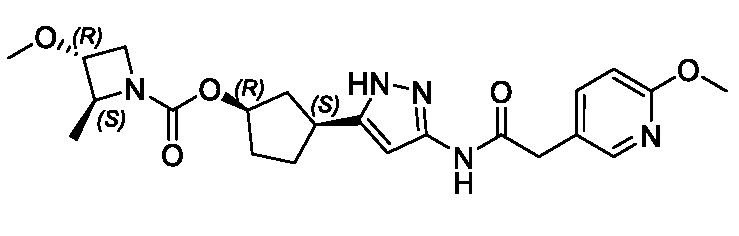
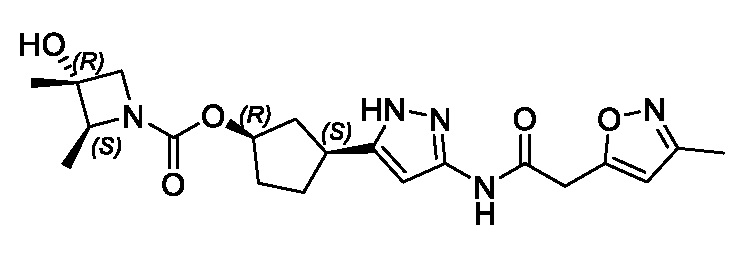
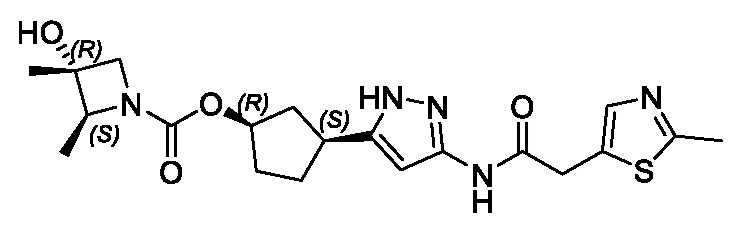
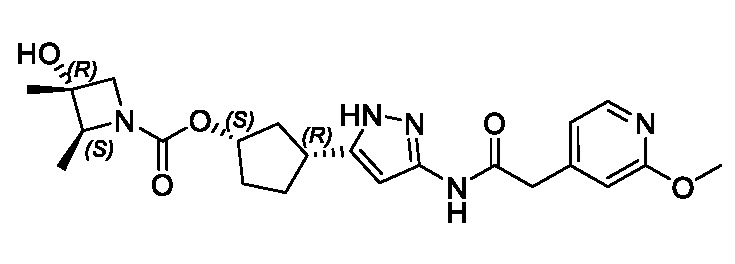
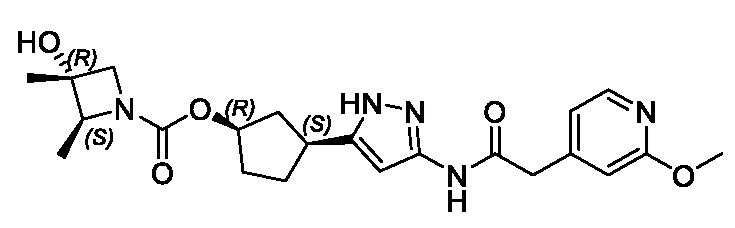
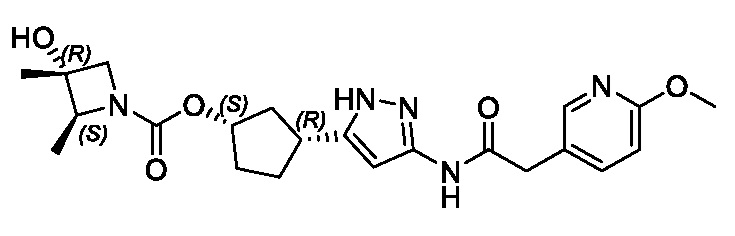
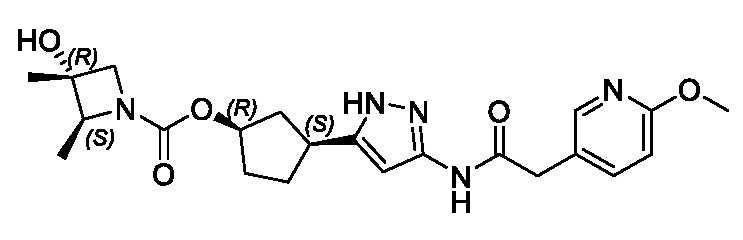
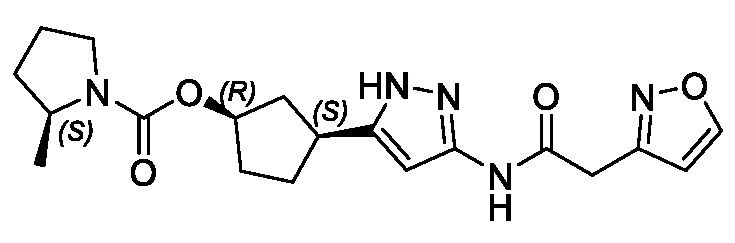
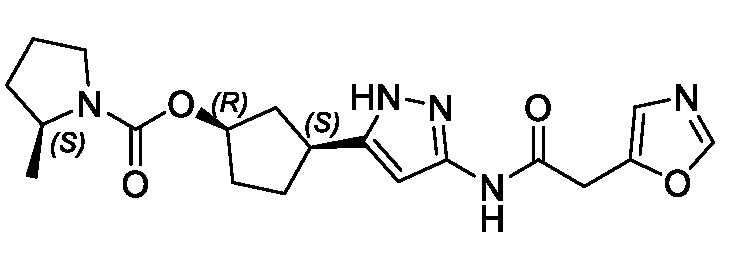
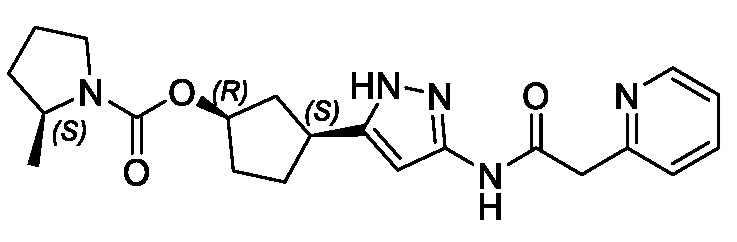
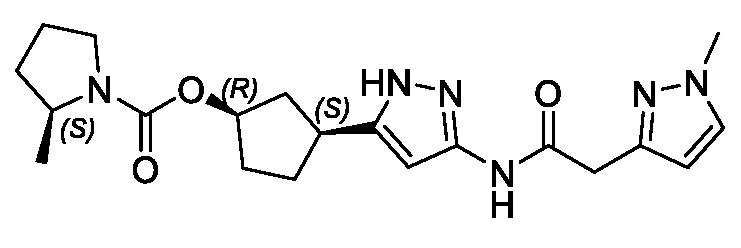
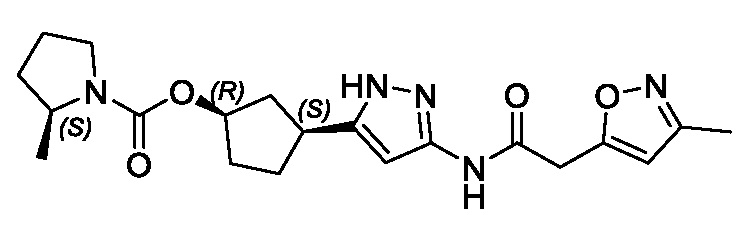
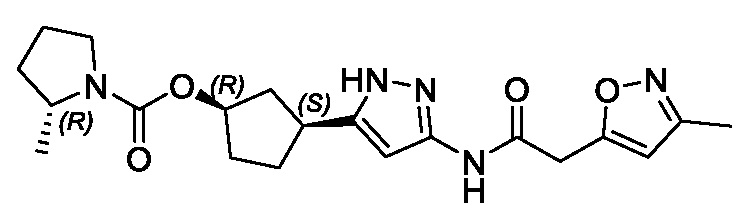
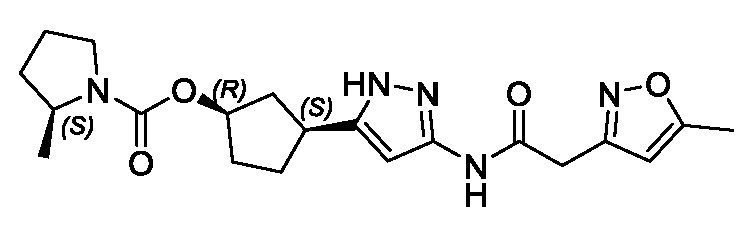
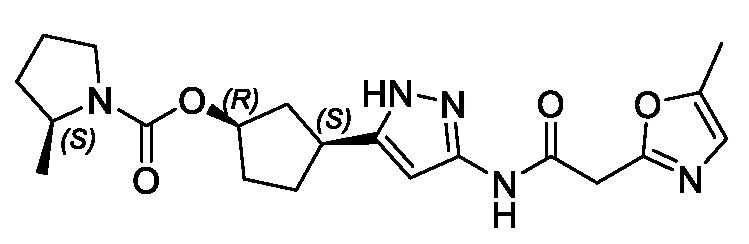
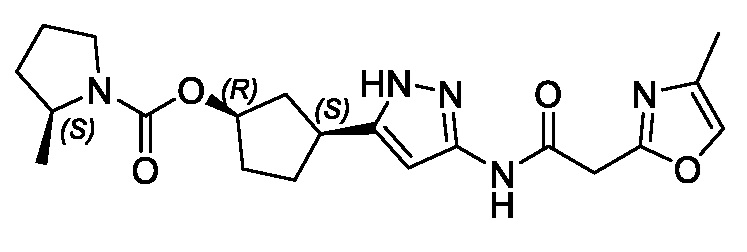
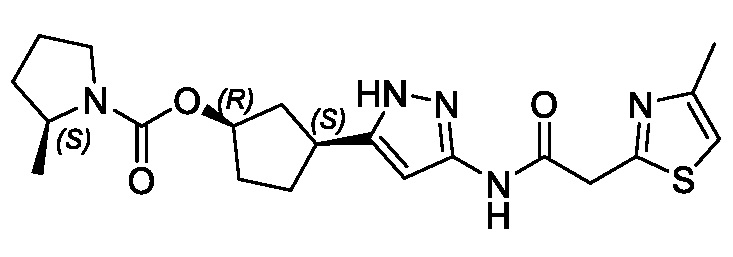
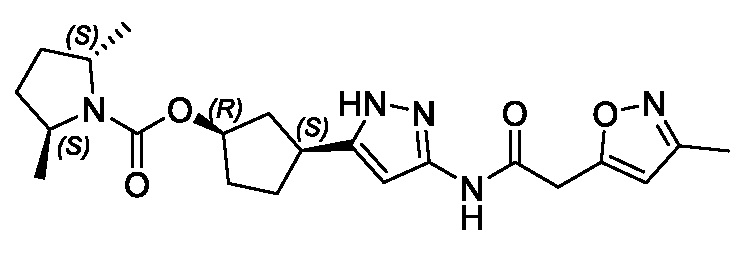
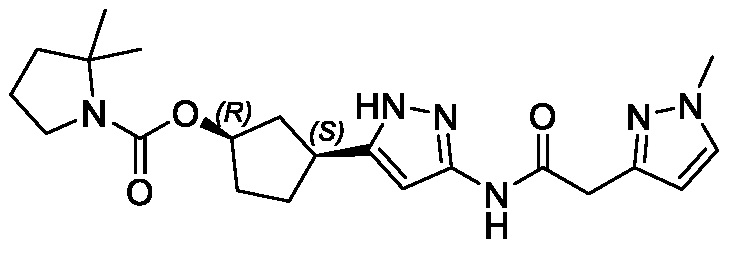
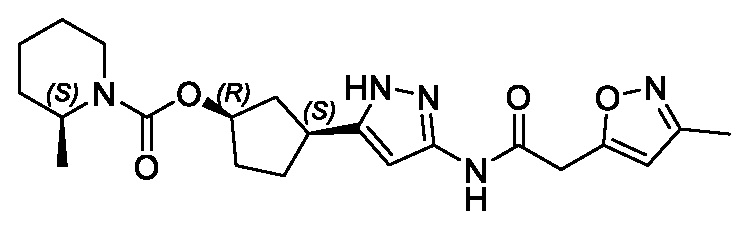
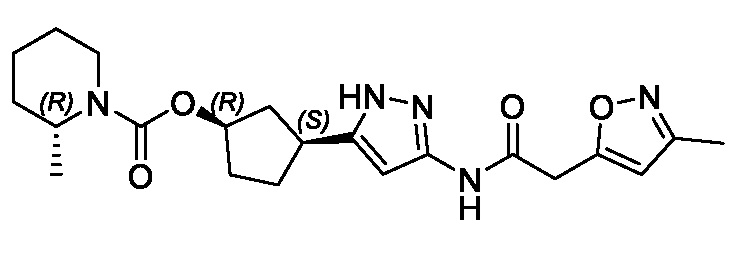
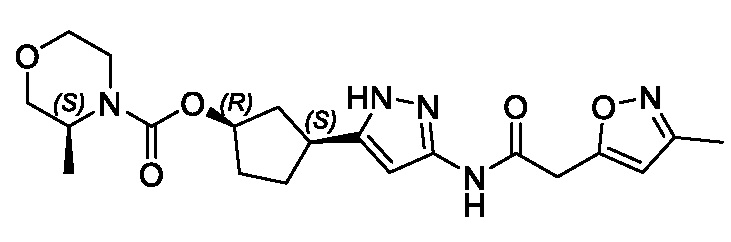
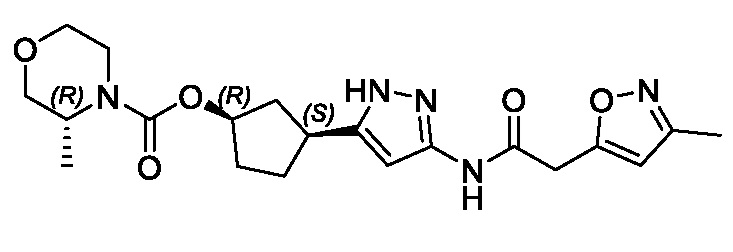
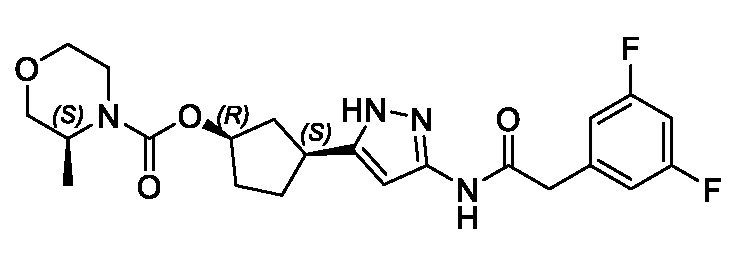
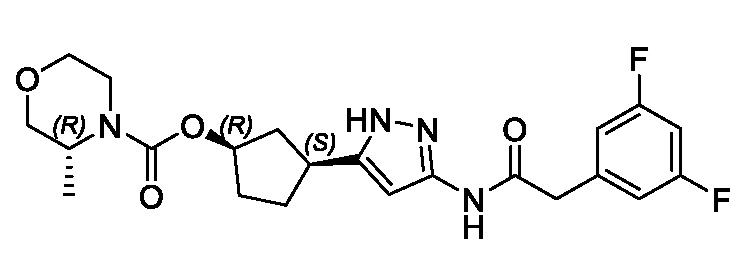
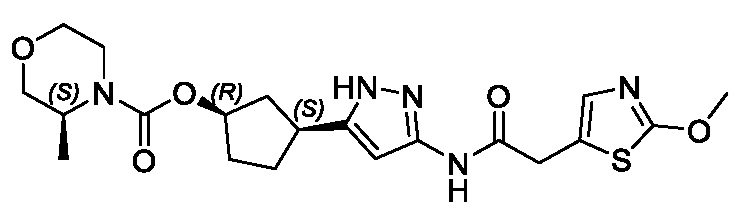
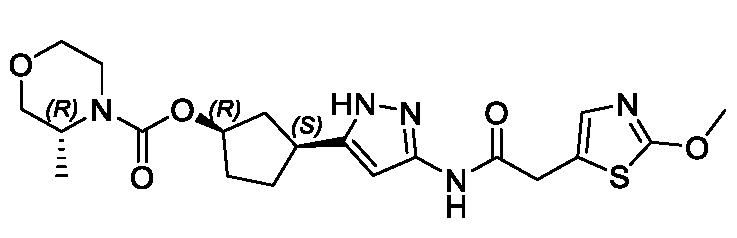

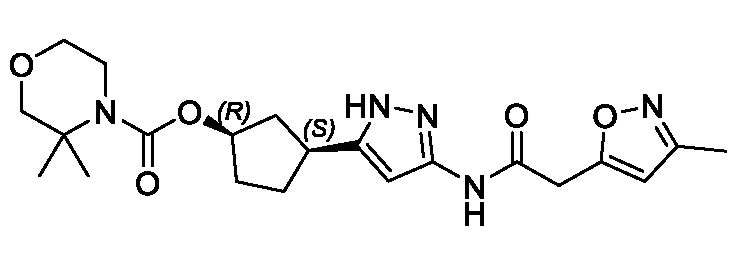
Биохимические анализы
Анализ изменения подвижности полноразмерной CDK2/циклин E1
Целью анализа CDK2/циклин E1 является оценка ингибирования (% ингибирования, значения Kiapp и Ki) низкомолекулярных ингибиторов с использованием анализа изменения микрофлюидной подвижности на основе флуоресценции. Полноразмерный CDK2/циклин E1 катализирует продуцирование ADP из ATP, которое сопровождает перенос фосфорила на пептидный субстрат FL-Пептид-18 (5-FAM-QSPKKG-CONH2, CPC Scientific, Sunnyvale, CA) (SEQ ID NO:1). Анализ изменения подвижности электрофоретически разделяет флуоресцентно меченные пептиды (субстрат и фосфорилированный продукт) после киназной реакции. Измеряют и субстрат, и продукт, и отношение этих значений используют для генерирования % конверсии субстрата в продукт с помощью ридера LabChip EZ. Комплекс ферментов дикого типа CDK2/дикого типа полноразмерного циклина E1 получали на месте (бакуловирусная экспрессия, LJIC-2080/LJIC-2103) и фосфорилировали комплексом ферментов CDK7/циклин H1/Mat1 с CDK2:CDK7 в соотношении 50:1 (концентрация мг/мл) в присутствии 10 мМ MgCl2 и 5 мМ ATP при комнатной температуре в течение одного часа. Типичные реакционные растворы (50 мкл конечного реакционного объема) содержали 2% DMSO (± ингибитор), 4 мМ MgCl2, 1 мМ DTT, 150 мкМ ATP (ATP Km=67,4 мкМ), 0,005% Tween-20, 3 мкМ FL-пептид-18, и 0,36 нМ (каталитически компетентный активный участок) комплекс ферментов фосфорилированный дикого типа полноразмерный CDK2/циклин E1 в 25 мМ HEPES буфере при pH 7,15. Анализ начинали с добавления ATP, после пятнадцатиминутной предварительной инкубации фермента и ингибитора при комнатной температуре в реакционной смеси. Реакцию останавливали через 45 минут при комнатной температуре путем добавления 50 мкл 80 мМ EDTA. Значение Ki определяли путем подгонки данных к уравнению сильной связи Моррисона для конкурентного ингибирования с концентрацией фермента в качестве переменной1, 2.
Анализ изменения подвижности GSK3бета (GSK3β)
Целью анализа GSK3β является оценка ингибирования (% ингибирования, значения Kiapp и Ki) низкомолекулярных ингибиторов с использованием анализа изменения микрофлюидной подвижности на основе флуоресценции. GSK3β катализирует продуцирование ADP из ATP, которое сопровождает перенос фосфорила на пептидный субстрат FL-Пептид-15 (5-FAM-KRREILSRRPpSYR-COOH, CPC Scientific, Sunnyvale, CA) (SEQ ID NO:2). Анализ изменения подвижности электрофоретически разделяет флуоресцентно меченные пептиды (субстрат и фосфорилированный продукт) после киназной реакции. Измеряют и субстрат, и продукт, и отношение этих значений используют для генерирования % конверсии субстрата в продукт с помощью ридера LabChip EZ. Активный GSK3β (H350L) приобретали в Upstate/Millipore. Типичные реакционные растворы (50 мкл конечного реакционного объема) содержали 2% DMSO (± ингибитор), 4 мМ MgCl2, 1 мМ DTT, 40 мкМ ATP (ATP Km=9,43 мкМ), 0,005% Tween-20, 2 мкМ FL-пептид-15, и 0,6 нМ GSK3β в 25 мМ HEPES буфере при pH 7,5. Анализ начинали с добавления ATP, после 15 минут предварительной инкубации фермента и ингибитора при комнатной температуре в реакционной смеси. Реакцию останавливали через 30 минут при комнатной температуре путем добавления 50 мкл 80 мМ EDTA. Значение Ki определяли путем подгонки данных к уравнению сильной связи Моррисона для конкурентного ингибирования с концентрацией фермента в качестве переменной. См. Morrison, J. F. (1969) Kinetics of the reversible inhibition of enzyme-catalysed reactions by tight-binding inhibitors, Biochimica et biophysica acta 185, 269-286; Murphy, D. J. (2004) Determination of accurate KI values for tight-binding enzyme inhibitors: an in silico study of experimental error and assay design, Analytical biochemistry 327, 61-67.
Анализ изменения подвижности CDK4/циклин D1
Целью анализа CDK4/циклин D1 является оценка ингибирования (% ингибирования, значения Kiapp и Ki) в присутствии низкомолекулярных ингибиторов с использованием анализа изменения микрофлюидной подвижности на основе флуоресценции. CDK4/циклин D3 катализирует продуцирование ADP из ATP, которое сопровождает перенос фосфорила на пептидный субстрат 5-FAM-Dyrktide (5-FAM-RRRFRPASPLRGPPK) (SEQ ID NO:3). Анализ изменения подвижности электрофоретически разделяет флуоресцентно меченные пептиды (субстрат и фосфорилированный продукт) после киназной реакции. Измеряют и субстрат, и продукт, и отношение этих значений используют для генерирования % конверсии субстрата в продукт с помощью ридера LabChip EZ. Типичные реакционные растворы содержали 2% DMSO (± ингибитор), 10 мМ MgCl2, 1 мМ DTT, 3,5 мМ ATP, 0,005% TW-20, 3 мкМ 5-FAM-Dyrktide, 3 нМ (активные участки) активированного CDK4/циклина D1 в 40 мМ HEPES буфере при pH 7,5.
Определения ингибитора Ki для активированного CDK4/циклин D1 (2007 E1/2008 +PO4) инициировали добавлением ATP (50 мкл конечного реакционного объема), после восемнадцатиминутной предварительной инкубации фермента и ингибитора при 22°С в реакционной смеси. Реакцию останавливали через 195 минут добавлением 50 мкл 30 мМ EDTA. Определения Ki были сделаны по графику дробной скорости как функции концентрации ингибитора, соответствующей уравнению Моррисона с концентрацией фермента в качестве переменной.
Анализ изменения подвижности CDK6/циклин D3
Целью анализа CDK6/циклин D3 является оценка ингибирования (% ингибирования, значения Kiapp и Ki) в присутствии низкомолекулярных ингибиторов с использованием анализа изменения микрофлюидной подвижности на основе флуоресценции. CDK6/циклин D3 катализирует продуцирование ADP из ATP, которое сопровождает перенос фосфорила на пептидный субстрат 5-FAM-Dyrktide (5-FAM-RRRFRPASPLRGPPK) (SEQ ID NO:3). Анализ изменения подвижности электрофоретически разделяет флуоресцентно меченные пептиды (субстрат и фосфорилированный продукт) после киназной реакции. Измеряют и субстрат, и продукт, и отношение этих значений используют для генерирования % конверсии субстрата в продукт с помощью ридера LabChip EZ. Типичные реакционные растворы содержали 2% DMSO (± ингибитор), 2% глицерин, 10 мМ MgCl2, 1 мМ DTT, 3,5 мМ ATP, 0,005% Tween 20 (TW-20), 3 мкМ 5-FAM-Dyrktide, 4 нМ (активные участки) активированного CDK6/циклин D3 в 40 мМ HEPES буфере при pH 7,5.
Определения ингибитора Ki для активированного CDK6/циклин D3 (LJIC-2009G1/2010 +PO4) инициировали добавлением ATP (50 мкл конечного реакционного объема), после восемнадцатиминутной предварительной инкубации фермента и ингибитора при 22°C в реакционной смеси. Реакцию останавливали через 95 минут добавлением 50 мкл 30 мМ EDTA. Определения Ki были сделаны по графику дробной скорости как функции концентрации ингибитора, соответствующей уравнению Моррисона с концентрацией фермента в качестве переменной.
Для подбора данных по ингибиторам сильного связывания, полученных с помощью анализов изменения подвижности CDK4 и CDK6, уравнения и принципы взяты из Morrison, J. F. (1969) Kinetics of the reversible inhibition of enzyme-catalysed reactions by tight-binding inhibitors, Biochimica et biophysica acta 185, 269-286; and Murphy, D. J. (2004) и Determination of accurate Ki values for tight-binding enzyme inhibitors: an in silico study of experimental error and assay design, Analytical biochemistry 327, 61-67.
Данные биологической активности
Данные биологической активности для репрезентативных соединений по изобретению представлены в таблице 4 ниже.
Дополнительные данные о биологической активности для выбранных соединений представлены в Таблице 5 ниже.
Все публикации и патентные заявки, процитированные в настоящем описании, включены в него посредством ссылки во всей их полноте. Специалистам в данной области техники будет очевидно, что в них могут быть сделаны определенные изменения и модификации без отклонения от сущности или объема прилагаемой формулы изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Pfizer Inc.
Behenna, Douglas C
Freeman-Cook, Kevin D
Hoffman, Robert L
Nagata, Asako
Ninkovic, Sacha
Sutton, Scott C
<120> ИНГИБИТОРЫ CDK2
<130> PC72484
<160> 3
<170> PatentIn version 3.5
<210> 1
<211> 6
<212> БЕЛОК
<213> Искусственный
<220>
<223> Синтетическая конструкция
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> 5-FAM меченый глутамин
<220>
<221> MOD_RES_AMIDATION
<222> (6)..(6)
<223> Амидирование глицина
<400> 1
Gln Ser Pro Lys Lys Gly
1 5
<210> 2
<211> 13
<212> БЕЛОК
<213> Искусственный
<220>
<223> Синтетическая конструкция
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> 5-FAM меченый лизин
<220>
<221> MOD_RES_PHOSPHORYLATION
<222> (11)..(11)
<223> Фосфорилированный по серину
<400> 2
Lys Arg Arg Glu Ile Leu Ser Arg Arg Pro Ser Tyr Arg
1 5 10
<210> 3
<211> 15
<212> БЕЛОК
<213> Искусственный
<220>
<223> Синтетическая конструкция
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> 5-FAM меченый аргинин
<400> 3
Arg Arg Arg Phe Arg Pro Ala Ser Pro Leu Arg Gly Pro Pro Lys
1 5 10 15
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ЦИКЛОАЛКАН-1,3-ДИАМИНОВОЕ ПРОИЗВОДНОЕ | 2019 |
|
RU2793247C2 |
| ПИРИДОПИРИМИДИНОВЫЕ ИНГИБИТОРЫ CDK2/4/6 | 2017 |
|
RU2726115C1 |
| ИНГИБИТОРЫ РЕЦЕПТОРА ФАКТОРА РОСТА ФИБРОБЛАСТОВ | 2014 |
|
RU2704112C2 |
| СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ПОВЫШЕНИЯ АКТИВНОСТИ CFTR | 2015 |
|
RU2767460C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СВЯЗАННЫХ С NTRK | 2016 |
|
RU2744974C2 |
| ИНГИБИТОРЫ ДИПЕПТИДИЛПЕПТИДАЗЫ IV | 2010 |
|
RU2574410C2 |
| НОВОЕ ПРОИЗВОДНОЕ НИКОТИНАМИДА ИЛИ ЕГО СОЛЬ | 2011 |
|
RU2576623C2 |
| НЕСТЕРОИДНЫЕ МОДУЛЯТОРЫ ГЛЮКОКОРТИОДИДНЫХ РЕЦЕПТОРОВ ДЛЯ МЕСТНОЙ ДОСТАВКИ ЛЕКАРСТВ | 2016 |
|
RU2731618C2 |
| АНТИПРОЛИФЕРАТИВНЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ PAH | 2020 |
|
RU2786588C1 |
| ПРОИЗВОДНЫЕ ДИАМИНОВ | 2002 |
|
RU2319699C2 |
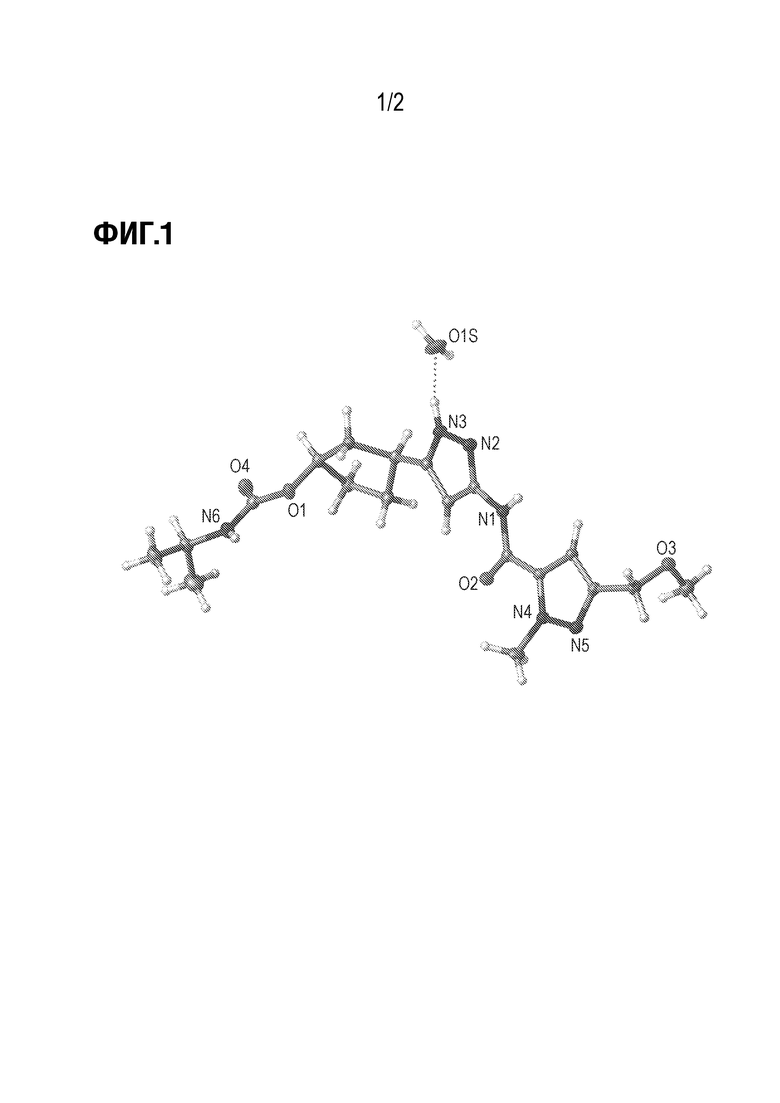
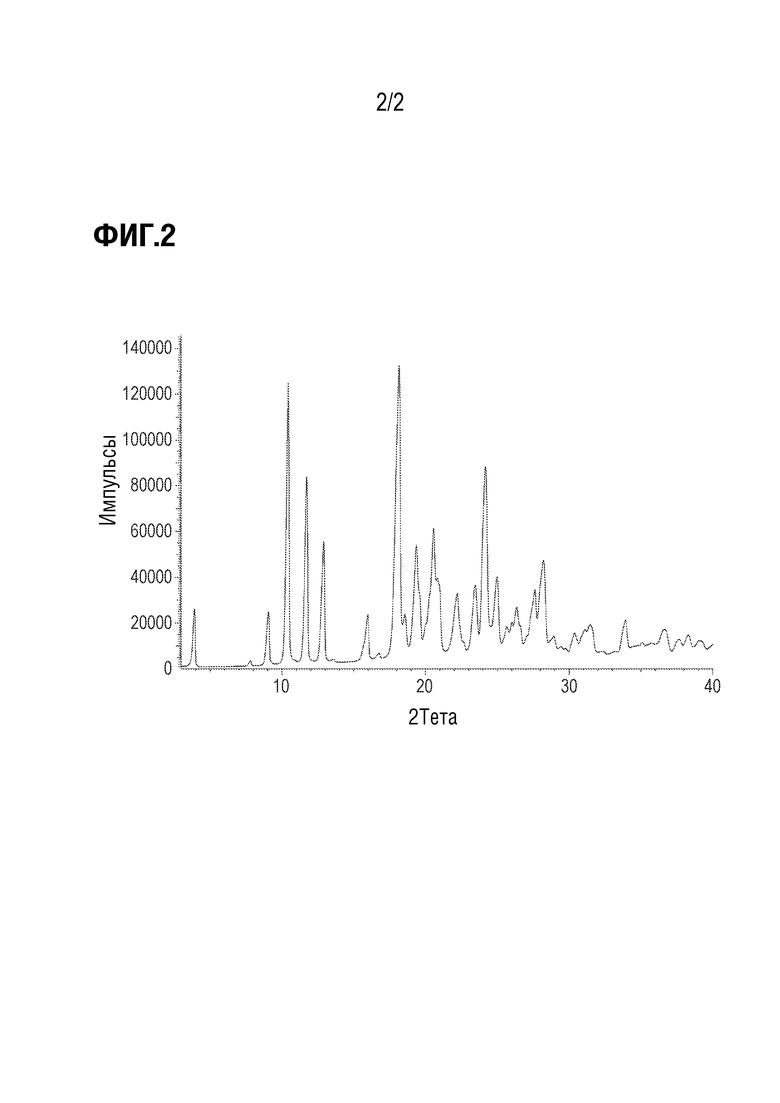
Группа изобретений относится к фармацевтической химии и включает соединение формулы (I), или его фармацевтически приемлемую соль, или сольват, (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат, (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат или их фармацевтически приемлемый сольват, фармацевтическую композицию и применение на основе указанных соединений, а также способ лечения рака, связанного с ингибированием активности CDK2. В формуле (I) R1 представляет собой -L1-(5-10-членный гетероарил, содержащий 1-4 гетероатома, каждый выбирают из N, O и S) или -L1-(C6-C12 арил), где указанный 5-10-членный гетероарил или C6-C12 арил необязательно замещены одним или двумя R4; R2 и R3 независимо представляют собой H, C1-C6 алкил, C1-C6 фторалкил, -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил, содержащий 1-2 гетероатома, каждый выбирают из N или O), где каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним R5 и каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или двумя R6; или R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием 4-6-членного гетероциклила, необязательно содержащего дополнительный гетероатом, который представляет собой O, в качестве члена кольца, где указанный 4-6-членный гетероциклил необязательно замещен одним-тремя R8; каждый L1 и L2 независимо представляет собой связь или C1-C2 алкилен; каждый R4 независимо представляет собой F, Cl, OH, CN, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси, C3-C8 циклоалкил, SO2R12, или SO2NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним R13; каждый R5 независимо представляет собой OH, C1-C4 алкокси или NR10R11; каждый R6 независимо представляет собой F, OH, C1-C4 алкил или C1-C4 фторалкил, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним R13; каждый R8 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 алкокси или CN; каждый R10 и R11 независимо представляет собой H или C1-C4 алкил; каждый R12 представляет собой C1-C4 алкил или C3-C6 циклоалкил; каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15; и каждый R14 и R15 независимо представляет собой H или C1-C4 алкил. Технический результат – соединения формулы (I), обладающие ингибирующей активностью в отношении CDK2. 7 н. и 13 з.п. ф-лы, 2 ил., 5 табл., 18 пр.
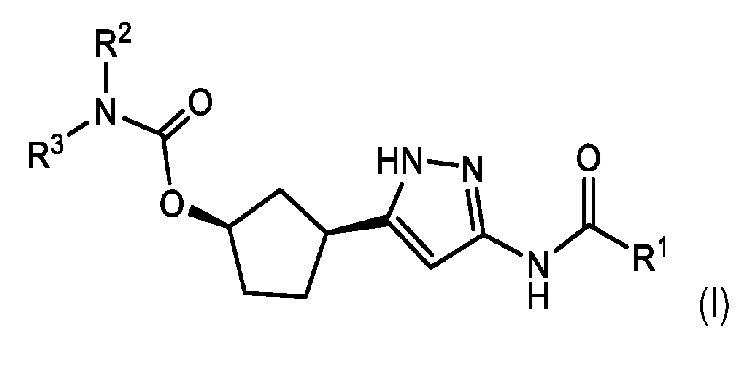
1. Соединение формулы (I):
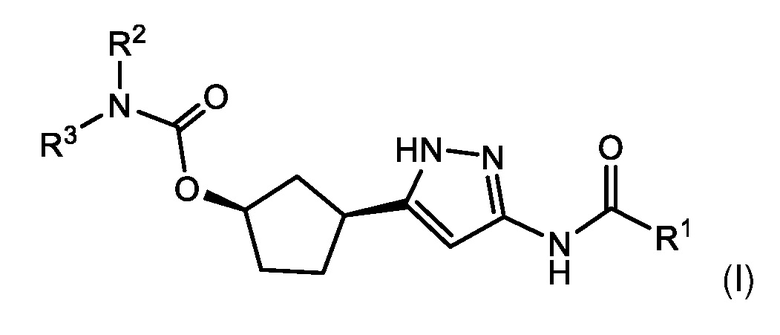
или его фармацевтически приемлемая соль или сольват, где:
R1 представляет собой -L1-(5-10-членный гетероарил, содержащий 1-4 гетероатома, каждый выбирают из N, O и S) или -L1-(C6-C12 арил), где указанный 5-10-членный гетероарил или C6-C12 арил необязательно замещены одним или двумя R4;
R2 и R3 независимо представляют собой H, C1-C6 алкил, C1-C6 фторалкил, -L2-(C3-C7 циклоалкил) или -L2-(4-7-членный гетероциклил, содержащий 1-2 гетероатома, каждый выбирают из N или O), где каждый указанный C1-C6 алкил и C1-C6 фторалкил необязательно замещен одним R5 и каждый указанный C3-C7 циклоалкил и 4-7-членный гетероциклил необязательно замещен одним или двумя R6; или
R2 и R3 взяты вместе с N-атомом, к которому они присоединены, с образованием 4-6-членного гетероциклила, необязательно содержащего дополнительный гетероатом, который представляет собой O, в качестве члена кольца, где указанный 4-6-членный гетероциклил необязательно замещен одним-тремя R8;
каждый L1 и L2 независимо представляет собой связь или C1-C2 алкилен;
каждый R4 независимо представляет собой F, Cl, OH, CN, C1-C4 алкил, C1-C4 фторалкил, C1-C4 алкокси, C1-C4 фторалкокси, C3-C8 циклоалкил, SO2R12, или SO2NR10R11, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним R13;
каждый R5 независимо представляет собой OH, C1-C4 алкокси или NR10R11;
каждый R6 независимо представляет собой F, OH, C1-C4 алкил или C1-C4 фторалкил, где каждый C1-C4 алкил и C1-C4 фторалкил необязательно замещен одним R13;
каждый R8 независимо представляет собой F, OH, C1-C4 алкил, C1-C4 алкокси или CN;
каждый R10 и R11 независимо представляет собой H или C1-C4 алкил;
каждый R12 представляет собой C1-C4 алкил или C3-C6 циклоалкил;
каждый R13 независимо представляет собой OH, C1-C4 алкокси или NR14R15; и
каждый R14 и R15 независимо представляет собой H или C1-C4 алкил.
2. Соединение по п. 1, имеющее формулу (II):
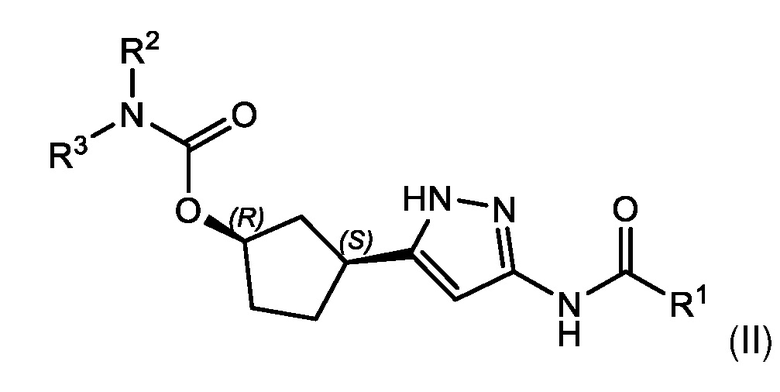
или его фармацевтически приемлемая соль или сольват.
3. Соединение по п. 1, имеющее формулу (III):
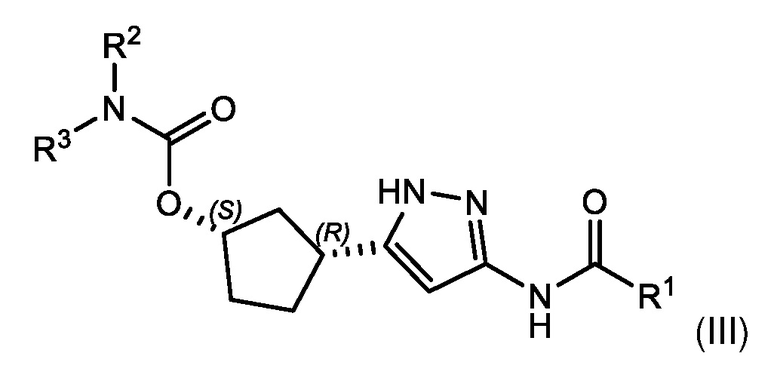
или его фармацевтически приемлемая соль или сольват.
4. Соединение по любому из п.п.1-3 или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -L1-(5-10-членный гетероарил, содержащий 1-4 гетероатома, каждый выбирают из N, O и S), где указанный 5-10-членный гетероарил необязательно замещен одним или двумя R4.
5. Соединение по п. 4 или его фармацевтически приемлемая соль или сольват, где указанный 5-10-членный гетероарил представляет собой пиразолил, триазолил, изоксазолил, оксазолил, тиазолил, тиадиазолил, имидазолил, пиридинил, пиразинил, индазолил или бензимидазолил, где указанный 5-10-членный гетероарил необязательно замещен одним или двумя R4.
6. Соединение по п. 5 или его фармацевтически приемлемая соль или сольват, где указанный 5-10-членный гетероарил представляет собой пиразолил, необязательно замещенный одним или двумя R4.
7. Соединение по п. 5 или его фармацевтически приемлемая соль или сольват, где указанный 5-10-членный гетероарил представляет собой изоксазолил, необязательно замещенный одним или двумя R4.
8. Соединение по любому из пп. 1-7 или его фармацевтически приемлемая соль или сольват, где L1 представляет собой связь или метилен.
9. Соединение по любому из пп. 1-8 или его фармацевтически приемлемая соль или сольват, где каждый R4 независимо представляет собой C1-C4 алкил или C1-C4 алкокси, где каждый C1-C4 алкил необязательно замещен одним R13.
10. Соединение по любому из пп. 1-9 или его фармацевтически приемлемая соль или сольват, где R2 представляет собой H и R3 представляет собой C1-C6 алкил.
11. Соединение по любому из пп. 1-9 или его фармацевтически приемлемая соль или сольват, где R2 представляет собой H и R3 представляет собой -L2-(C3-C7 циклоалкил), где указанный C3-C7 циклоалкил необязательно замещен одним или двумя R6.
12. Соединение по п. 11 или его фармацевтически приемлемая соль или сольват, где L2 представляет собой связь или метилен.
13. Соединение, выбранное из группы, состоящей из:
(1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамата; и
(1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамата.
14. Соединение по п. 13, которое представляет собой (1R,3S)-3-[3-({[3-(метоксиметил)-1-метил-1H-пиразол-5-ил]карбонил}амино)-1H-пиразол-5-ил]циклопентил пропан-2-илкарбамат.
15. Соединение по п. 13, которое представляет собой (1R,3S)-3-(3-{[(3-метил-1,2-оксазол-5-ил)ацетил]амино}-1H-пиразол-5-ил)циклопентил (1-метилциклопропил)карбамат.
16. Соединение, имеющее структуру:
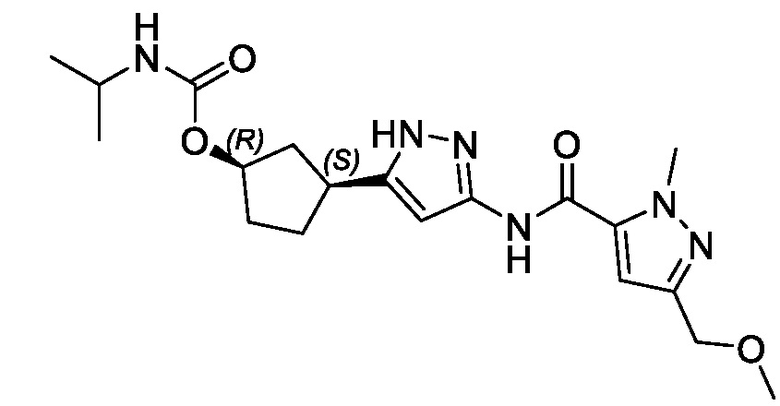 ,
,
или его фармацевтически приемлемый сольват.
17. Соединение, имеющее структуру:
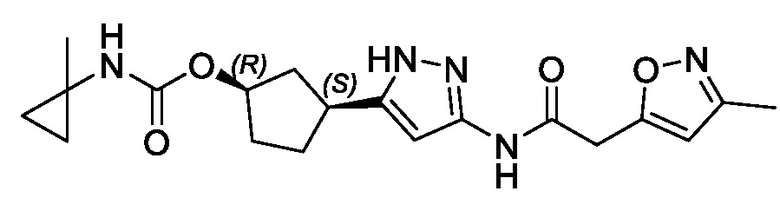 ,
,
или его фармацевтически приемлемый сольват.
18. Фармацевтическая композиция для ингибирования CDK2, содержащая эффективное количество соединения по любому из пп. 1-17 или его фармацевтически приемлемой соли или сольвата, и фармацевтически приемлемый носитель или эксципиент.
19. Способ лечения рака, связанного с ингибированием активности CDK2, у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества соединения по любому из пп.1-17, или его фармацевтически приемлемой соли или сольвата, где рак выбирают из рака молочной железы, рака яичников, рака мочевого пузыря, рака матки, рака простаты, рака легкого, рака пищевода, рака головы и шеи, колоректального рака, рака почки, рака печени, рака поджелудочной железы, рака желудка и рака щитовидной железы.
20. Применение соединения по любому из пп. 1-17 или его фармацевтически приемлемой соли или сольвата, для лечения рака, связанного с ингибированием активности CDK2, у субъекта, нуждающегося в этом, где рак выбирают из рака молочной железы, рака яичников, рака мочевого пузыря, рака матки, рака простаты, рака легкого, рака пищевода, рака головы и шеи, колоректального рака, рака почки, рака печени, рака поджелудочной железы, рака желудка и рака щитовидной железы.
| WO 2005051919 A1, 09.06.2005 | |||
| Mascarenhas N.M | |||
| et al., An efficient tool for identifying inhibitors based on 3D-QSAR and docking using feature-shape pharmacophore of biologically active conformation - a case study with CDK2/cyclina | |||
| European journal of medicinal chemistry, 2008, vol.43, no.12, pp.2807-2818 | |||
| НОВЫЕ СОЕДИНЕНИЯ | 2007 |
|
RU2458920C2 |
Авторы
Даты
2023-06-09—Публикация
2020-01-28—Подача