Гипергликемия является основным симптомом ряда метаболических нарушений, включая приобретший в последнее время характер эпидемии сахарный диабет 2 го типа [Roglic, G. WHO Global report on diabetes: A summary. Int. J. Non-Commun. Dis. 2016, 1, 3-8.]. Гипергликемия при сахарном диабете 2 го типа возникает при нарушении чувствительности инсулин-зависимых тканей (скелетные мышцы, жировая ткань и печень) к инсулину, что приводит к значительному уменьшению захвата ими глюкозы и гиперинсулинемии. По принципу обратной связи поджелудочная железа продуцирует большее количество инсулина для снижения концентрации глюкозы крови, что в более поздних стадиях заболевания приводит к истощению бета-клеток островков Лангерганса и нехватке инсулина. Зачастую нарушения углеводного обмена происходят параллельно с нарушением липидного обмена, характеризующимся дислипидемией с повышенными концентрациями липопротеинов низкой плотности и триглицеридов в крови. Такие нарушения обмена веществ вызывают быстрое прогрессирование атеросклероза и поражение нервной системы [Sonksen, P.; Sonksen, J. Insulin: Understanding its action in health and disease. Br. J. Anaesth. 2000, 85, 69-79.]. Осложнения являются основной причиной смерти и высокой инвалидности пациентов с сахарным диабетом. Для контроля гликемии и уровня липидов необходимы препараты гипогликемического действия [American Diabetes Association. 9. Pharmacologic approaches to glycemic treatment: Standards of medical care in diabetes-2019. Diabetes Care 2019, 42, 90-102].
В настоящее время не существует большого разнообразия терапевтических агентов для повышения чувствительности тканей к инсулину. Таким эффектом обладают лишь метформин и тиазолидиндионы, действие всех других используемых препаратов связано с увеличением секреции инсулина (производные сульфонилмочевины, ингибиторы DPP4), снижением всасывания глюкозы в желудочно-кишечном тракте (акарбоза) или с его повышенным выведением почками (ингибиторы SGLT2) [Pappachan, J.M.; Fernandez, C.J.; Chacko, E.C. Diabesity and antidiabetic drugs, Mol. Asp.Med. 2019, 66, 3-12, doi: 10.1016/j.mam.2018.10.004].
Основные побочные эффекты современных пероральных противодиабетических средств включают гипогликемию, лактат-ацидоз, задержку жидкости, остеопороз и сердечную недостаточность, что ограничивает их клиническое применение. Поэтому разработка новых соединений-кандидатов для контроля различных параметров метаболических нарушений (гипергликемия, гиперинсулинемия и гипертриглицеридемия) с минимизацией побочных эффектов остается первоочередной и наиболее важной задачей в лечении метаболических нарушений [Vieira, R.; Souto, S.B.; Sánchez-López, E.; Machado, A.L.; Severino, P.; Jose, S.; Santini, A.; Fortuna, A.; García, M.L.; Silva, A.M.; et al. Sugar-Lowering Drugs for Type 2 Diabetes Mellitus and Metabolic Syndrome-Review of Classical and New Compounds: Part-I. Pharmaceuticals 2019, 12, 152].
Изобретение относится к области органической химии и медицины, а именно, к гипогликемической активности соединений формулы 1.

Аналогами предлагаемого средства по фармакологическому действию являются гипогликемические фармацевтические препараты класса бигуанидов (метформин) и тиазолидиндионов (росиглитазон). Данные препараты зачастую обладают выраженными побочными действиями со стороны пищеварительной системы (боль в животе, тошнота, рвота, диарея), а также способны приводить к учащению заболеваемости инфекциями верхних дыхательных путей, мочевыводящей системы и др. Поскольку при длительной терапии пероральными препаратами может развиваться резистентность (состояние, при котором препараты уже не вызывают должного терапевтического ответа в организме, тем самым приводя к увеличению дозы для достижения желаемого терапевтического эффекта) или невозможность должного контроля углеводного обмена, необходимы принципиально новые препараты для лечения сахарного диабета 2 го типа.
Лекарственные препараты на основе природных соединений широко распространены на фармацевтическом рынке [Newman, D.J.; Cragg, G.M. Natural Products as Sources of New Drugs over the Nearly Four Decades from 01/1981 to 09/2019. J. Nat. Prod. 2020, 83, 770-803], часто имеют хороший профиль безопасности и более мягкое (часто пролонгированное) действие и обычно не вызывают серьезных побочных эффектов и переносимости лекарств. Природные соединения рассматриваются исследователями как потенциальные терапевтические агенты при сахарном диабете [Vieira, R.; Souto, S.B.; Sánchez-López, E.; Machado, A.L.; Severino, P.; Jose, S.; Santini, A.; Fortuna, A.; García, M.L.; Silva, A.M.; et al. Sugar-Lowering Drugs for Type 2 Diabetes Mellitus and Metabolic Syndrome-Review of Classical and New Compounds: Part-I. Pharmaceuticals 2019, 12, 152]; однако лишь небольшая часть опубликованных исследований в области гипогликемических средств связана с целенаправленной синтетической модификацией природных метаболитов.
Наиболее близким к заявляемому средству по фармакологическому действию - прототипом, является берберин.
Берберин 2 - это растительный алкалоид изохинолинового ряда. На протяжении веков берберин использовался в традиционной китайской медицине для лечения различных заболеваний, одна из его сильнейших особенностей - антидиабетическая активность. О клиническом применении берберина 2 при сахарном диабете 2 типа сообщалось с 1988 года, механизм его гипогликемического действия мультитаргетный [Advances in Structural Modifications and Biological Activities of Berberine: An Active Compound in Traditional Chinese Medicine Z.-J. Huang, Y. Zeng, P. Lan, P.-H. Sun and W.-M. Chen Mini-Reviews in Medicinal Chemistry, 2011, 11, 1122-1129].
Гипогликемический эффект берберина выражен, но эффективная доза берберина относительно высока (380 мг/кг). [Xia, X., Yan, J., Shen, Y., Tang, K., Yin, J., Zhang, Y., … Weng, J. (2011). Berberine Improves Glucose Metabolism in Diabetic Rats by Inhibition of Hepatic Gluconeogenesis. PLoS ONE, 6(2), e16556. doi:10.1371/journal.pone.0016556]. Основная причина в том, что биодоступность берберина крайне мала, не превышая 1% [An insight into the medicinal attributes of berberine derivatives: A review Sobhi Gaba, Anjali Saini, Gurpreet Singh, Vikramdeep Monga Bioorg. Med. Chem. 38 (2021) 116143].
В литературе описаны аналоги берберина, полученные путем его химической модификации, либо методом молекулярной сборки, которые на модели сахарного диабета, индуцированного аллоксаном, у мышей показали гипогликемический эффект в дозе 200 мг/кг (N-замещенное производное берберина 3) [Bian, X., He, L., & Yang, G. (2006). Synthesis and antihyperglycemic evaluation of various protoberberine derivatives. Bioorganic & Medicinal Chemistry Letters, 16(5), 1380-1383. doi:10.1016/j.bmcl.2005.11.045], на крысиной модели сахарного диабета, индуцированного стрептозотоцином, в дозе 100 мг/кг (8-оксоберберин 4) [Yaoxing Dou, Ronglei Huang, Qiaoping Li, Yuhong Liu, Yucui Li, Hanbin Chen, Gaoxiang Ai, Jianhui Xie, Huifang Zeng, Jiannan Chen, Chaodan Luo, Ziren Su Oxyberberine, an absorbed metabolite of berberine, possess su-perior hypoglycemic effect via regulating the PI3K/Akt and Nrf2 signaling pathways Biomedicine & Pharmacotherapy 137 (2021) 111312], на модели сахарного диабета мышей в концентрации 100 мг/кг (9-О-ацилпроизводное 5) [Berberine: a Promising Natural Isoquinoline Alkaloid for Development of Hypolipidemic Drug Article in Current Topics in Medicinal Chemistry · September 2020 DOI: 10.2174/1568026620666200908165913].
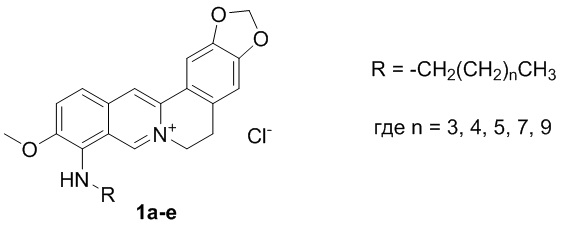
Задача, на решение которой направлено изобретение, заключается в создании нового эффективного средства на основе берберина, обладающего гипогликемической активностью. Поставленная задача решается путем использования в качестве гипогликемического средства соединений формулы 1, где R=н-пентил, н-гексил, н-гептил, н-децил, н-додецил..
Соединения 1a-e могут быть синтезированы в соответствии со схемой 1.

Схема 1
Для исследования соединений 1a-e использовали мышей C57BL/6, а также C57BL/6Ay (мыши AY), которые характеризуются наличием ожирения, гиперинсулинемией, нарушенной толерантностью к глюкозе и сопутствующей неалкогольной жировой болезнью печени [S. Kuranov, O. Luzina, M. Khvostov, D. Baev, D. Kuznetsova, N. Zhukova, P. Vassiliev, A. Kochetkov, T. Tolstikova, N. Salakhutdinov. Bornyl Derivatives of p-(Benzyloxy)Phenylpropionic Acid: In Vivo Evaluation of Antidiabetic Activity Pharma-ceuticals 2020, 13(11), 404]. В эксперименте на мышах AY в качестве положительного контроля был использован метформин (MF), эффективная доза которого у животных, согласно литературным данным, варьируется в диапазоне 200-250 мг/кг [Guo WR, Liu J, Cheng LD, Liu ZY, Zheng XB, Liang H, Xu F. Metformin Alleviates Steatohepatitis in Diet-Induced Obese Mice in a SIRT1-Dependent Way. Front Pharmacol. 2021 Aug 18;12:704112. doi: 10.3389/fphar.2021.704112.]. Введение соединения 1b в дозе 15 мг/кг в течение трех недель значительно повлияло на состояние мышей AY. Все основные маркеры метаболического синдрома, присущие данным животным, были нормализованы: снижена масса тела (фиг.1), уменьшены концентрации глюкозы (фиг.2 и 3) и инсулина (фиг.4) натощак, улучшена толерантность к глюкозе. Снижение массы тела произошло, в том числе, за счет снижения массы гонадного и межлопаточного жира, в том числе, и бурого (Таблица 1), что свидетельствует о повышении активности последнего [Carolline Santos Miranda, Flavia Silva-Veiga, Fabiane Ferreira Martins, Tamiris Lima Rachid, Carlos Alberto Mandarim-De-Lacerda, Vanessa Souza-Mello, PPAR-α activation counters brown adipose tissue whitening: a comparative study between high-fat- and high-fructose-fed mice, Nutrition, Volume 78, 2020, 110791]. При биохимическом исследовании (Таблица 2) было обнаружено снижение уровня лактата в крови животных, получавших соединение 1b. Это является дополнительным подтверждением улучшения чувствительности тканей мышей (печени, мышц, жира) к инсулину [J. Lovejoy, F.D. Newby, S.S.P. Gebhart, M. DiGirolamo, Insulin resistance in obesity is associated with elevated basal lactate levels and diminished lactate appearance following intravenous glucose and insulin, Metabolism, Volume 41, Issue 1, 1992, Pages 22-27]. Уровни триглицеридов и щелочной фосфатазы в группе мышей, получавших соединение 1b имеют некоторую тенденцию к снижению по сравнению с мышами AY в группе негативного контроля. Уровни общего холестерина, общего белка и аланинаминотрансферазы были такими же, как у мышей AY. Это свидетельствует об отсутствии гепатотоксичности у соединения 1b в дозе 15 мг/кг.
Изучение аналогов соединения 1b с более коротким (С5) и более длинным (С7, С10, С12) алифатическими фрагментами с целью определения их влияния на выраженность гипогликемического действия было проведено с использованием орального глюкозотолерантного теста (ОГТТ) на мышах C57BL/6, где в качестве положительного контроля использовали вилдаглиптин (VLD). Исследования были проведены в дозе 15 мг/кг.Было показано, что длина алифатического фрагмента влияет на выраженность гипогликемического эффекта, а именно, с уменьшением количества атомов углерода происходит его усиление, тогда как повышение длины цепочки приводит к его снижению (фиг.4-7).
Таким образом, производные берберина 9-(алкиламино)-2,3-метилендиокси-10-метоксипротоберберин хлорид 1a-e способны улучшать углеводный обмен в дозе 15 мг/кг и, таким образом, являются многообещающими кандидатами для терапии гипергликемии и метаболического синдрома.
Спектральные исследования выполнены в Химическом Сервисном Центре коллективного пользования СО РАН.
Изобретение иллюстрируется следующими примерами.
Пример 1. Синтез 9-(пентиламино)-2,3-метилендиокси-10-метоксипротоберберин хлорида 1a.
Берберин хлорид 2 сушили в печи в течение 2 часов при 95°C. К высушенному берберин хлориду 2 (2 г, 5.4 ммоль) добавляли 1-пентиламин (3.1 мл, 26.9 ммоль). Реакционную смесь нагревали до 125°C и перемешивали в течение 4 часов. К охлажденной до комнатной температуры реакционной смеси добавляли ацетон, образовавшийся осадок бордового цвета отфильтровывали. Осадок очищали колоночной хроматографией с получением соединения 1а (1.01 г, 44%) в виде твердого вещества бордового цвета.
1H NMR (400 MHz, DMSO-d6): δ 10.10 (s, 1H, H-8), 8.68 (s, 1H, H-13), 7.88 (d, J=8.6 Hz, 1H, H-9*), 7.75 (s, 1H, H-1), 7.46 (d, J=8.6 Hz, 1H, H-10*), 7.06 (s, 1H, H-4), 6.42 (t, J=5.8 Hz, 1H, NH), 6.15 (s, 2H, OCH2O), 4.79 (t, J=6.1 Hz, 2H, H-6), 3.95 (s, 3H, OCH3), 3.54-3.60 (m, 2H, NHCH2), 3.19 (t, J=5.9 Hz, 2H, H-5), 1.57-1.65 (m, 2H, NHCH2CH2), 1.27-1.35 (m, 4H, NHCH2CH2CH2CH2), 0.87 (t, J=6.9 Hz, 3H, CH2CH3). 13C NMR (100 MHz, DMSO-d6): δ 149.80, 147.93, 146.92, 137.56, 135.93, 133.34, (C-2, C-3, C-4a, C-10, C-12a, C-13a), 146.67 (C-8), 130.55, 120.91, 117.17 (C-8a, C-9, C-13b), 124.80 (C-13), 119.97 (C-12), 116.30 (C-11), 108.74 (C-4), 105.52 (C-1), 102.29 (OCH2O), 57.28 (OCH3), 55.13 (C-6), 47.60 (NHCH2), 30.49, 28.90, 26.96, 22.25 (NHCH2CH2CH2CH2, C-5), 14.28 (CH2CH3). MS (ESI): m/z (M+) calcd for C25H29N2O3, 391.202 found: 391.202.
Пример 2. Синтез 9-(гексиламино)-2,3-метилендиокси-10-метоксипротоберберин хлорида 1b.
Берберин хлорид 2 сушили в печи в течение 2 часов при 95°C. К высушенному берберин хлориду 2 (2 г, 5.4 ммоль) добавляли 1-гексиламин (2.5 мл, 19.0 ммоль). Реакционную смесь нагревали до 125°C и перемешивали в течение 4 часов. К охлажденной до комнатной температуры реакционной смеси добавляли ацетон, образовавшийся осадок бордового цвета отфильтровывали. Осадок очищали колоночной хроматографией с получением соединения 1b (1.23 г, 52%) в виде твердого вещества бордового цвета.
1H NMR (400 MHz, DMSO-d6): δ 10.10 (s, 1H, H-8), 8.68 (s, 1H, H-13), 7.88 (d, J=8.7 Hz, 1H, H-9*), 7.75 (s, 1H, H-1), 7.46 (d, J=8.7 Hz, 1H, H-10*), 7.06 (s, 1H, H-4), 6.40 (t, J=6.07 Hz, 1H, NH), 6.15 (s, 2H, OCH2O), 4.79 (t, J=6.1 Hz, 2H, H-6), 3.95 (s, 3H, OCH3), 3.54-3.60 (m, 2H, NHCH2), 3.18 (t, J=6.1 Hz, 2H, H-5), 1.57-1.64 (m, 2H, NHCH2CH2), 1.26-1.35 (m, 6H, NHCH2CH2CH2CH2CH2), 0.85 (t, J=6.9 Hz, 3H, CH2CH3). 13C NMR (100 MHz, DMSO-d6): δ 149.45, 147.58, 146.54, 137.24, 135.85, 133.00, (C-2, C-3, C-4a, C-10, C-12a, C-13a), 146.38 (C-8), 130.20, 120.57, 116.83 (C-8a, C-9, C-13b), 124.45 (C-13), 119.62 (C-12), 115.91 (C-11), 108.40 (C-4), 105.17 (C-1), 101.95 (OCH2O), 56.92 (OCH3), 54.74 (C-6), 47.24 (NHCH2), 31.03, 30.43, 26.62, 26.00, 22.04 (NHCH2CH2CH2CH2CH2, C-5), 13.88 (CH2CH3). MS (ESI): m/z (M+) calcd for C25H29N2O3, 405.217 found: 405.217.
Пример 3. Синтез 9-(гептиламино)-2,3-метилендиокси-10-метоксипротоберберин хлорида 1c.
Берберин хлорид 2 сушили в печи в течение 2 часов при 95°C. К высушенному берберин хлориду 2 (1.5 г, 4.0 ммоль) добавляли 1-гептиламин (2.98 мл, 20.1 ммоль). Реакционную смесь нагревали до 125°C и перемешивали в течение 4 часов. К охлажденной до комнатной температуры реакционной смеси добавляли ацетон, образовавшийся осадок бордового цвета отфильтровывали. Осадок очищали колоночной хроматографией с получением соединения 1c (0.5 г, 27%) в виде твердого вещества бордового цвета.
1H NMR (400 MHz, DMSO-d6): δ 10.17 (s, 1H, H-8), 8.68 (s, 1H, H-13), 7.88 (d, J=8.8 Hz, 1H, H-9*), 7.75 (s, 1H, H-1), 7.47 (d, J=8.8 Hz, 1H, H-10*), 7.07 (s, 1H, H-4), 6.48 (t, J=6.1 Hz, 1H, NH), 6.15 (s, 2H, OCH2O), 4.79 (t, J=6.0 Hz, 2H, H-6), 3.95 (s, 3H, OCH3), 3.53-3.61 (m, 2H, NHCH2), 3.18 (t, J=6.0 Hz, 2H, H-5), 1.55-1.65 (m, 2H, NHCH2CH2), 1.20-1.37 (m, 8H, NHCH2CH2CH2CH2CH2CH2), 0.83 (t, J=6.8 Hz, 3H, CH2CH3). 13C NMR (100 MHz, DMSO-d6): δ 149.78, 147.91, 146.83, 137.59, 135.90, 133.33, (C-2, C-3, C-4a, C-10, C-12a, C-13a), 146.74 (C-8), 130.53, 120.92, 117.16 (C-8a, C-9, C-13b), 124.80 (C-13), 119.94 (C-12), 116.18 (C-11), 108.74 (C-4), 105.51 (C-1), 102.29 (OCH2O), 57.24 (OCH3), 55.04 (C-6), 47.50 (NHCH2), 31.57, 30.82, 28.83, 26.96, 26.65, 22.39 (NHCH2CH2CH2CH2CH2CH2, C-5), 14.27 (CH2CH3). MS (ESI): m/z (M+) calcd for C25H29N2O3, 419.233 found: 419.233.
Пример 4. Синтез 9-(дециламино)-2,3-метилендиокси-10-метоксипротоберберин хлорида 1d.
Берберин хлорид 2 сушили в печи в течение 2 часов при 95°C. К высушенному берберин хлориду 2 (2 г, 5,4 ммоль) добавляли 1-дециламин (5.35 мл, 26.9 ммоль). Реакционную смесь нагревали до 125°C и перемешивали в течение 4 часов. К охлажденной до комнатной температуры реакционной смеси добавляли ацетон, образовавшийся осадок бордового цвета отфильтровывали. Осадок очищали колоночной хроматографией с получением соединения 1d (1,07 г, 40%) в виде твердого вещества бордового цвета.
1H NMR (400 MHz, DMSO-d6): δ 10.00 (s, 1H, H-8), 8.69 (s, 1H, H-13), 7.89 (d, J=8.6 Hz, 1H, H-9*), 7.76 (s, 1H, H-1), 7.47 (d, J=8.6 Hz, 1H, H-10*), 7.07 (s, 1H, H-4), 6.31 (t, J=6.1 Hz, 1H, NH), 6.15 (s, 2H, OCH2O), 4.78 (t, J=6.2 Hz, 2H, H-6), 3.96 (s, 3H, OCH3), 3.53-3.60 (m, 2H, NHCH2), 3.15-3.20 (t, J=6.2 Hz, 2H, H-5), 1.55-1.63 (m, 2H, NHCH2CH2), 1.18-1.34 (m, 14H, NHCH2CH2CH2CH2CH2CH2CH2CH2CH2), 0.83 (t, J=6.8 Hz, 3H, CH2CH3). 13C NMR (100 MHz, DMSO-d6): δ 149.76, 147.90, 146.92, 137.48, 135.89, 133.26 (C-2, C-3, C-4a, C-10, C-12a, C-13a), 146.68 (C-8), 130.52, 120.89, 117.10 (C-8a, C-9, C-13b), 124.59 (C-13), 119.98 (C-12), 116.30 (C-11), 108.73 (C-4), 105.49 (C-1), 102.28 (OCH2O), 57.19 (OCH3), 55.14 (C-6), 47.65 (NHCH2), 31.61, 30.75, 29.31, 29.25, 29.11, 29.02, 26.91, 26.61, 22.41 (NHCH2CH2CH2CH2CH2CH2CH2CH2CH2, C-5), 13.88 (CH2CH3). MS (ESI): m/z (M+) calcd for C25H29N2O3, 461.280 found: 461.280.
Пример 5. Синтез 9-(додециламино)-2,3-метилендиокси-10-метоксипротоберберин хлорида 1e.
Берберин хлорид 2 сушили в печи в течение 2 часов при 95°C. К высушенному берберин хлориду 2 (2 г, 5.4 ммоль) добавляли 1-додециламин (5 г, 26.9 ммоль). Реакционную смесь нагревали до 125°C и перемешивали в течение 4 часов. К охлажденной до комнатной температуры реакционной смеси добавляли ацетон, образовавшийся осадок бордового цвета отфильтровывали. Осадок очищали колоночной хроматографией с получением соединения 1e (0,96 г, 34%) в виде твердого вещества бордового цвета.
1H NMR (400 MHz, DMSO-d6): δ 10.00 (s, 1H, H-8), 8.70 (s, 1H, H-13), 7.89 (d, J=8.6 Hz, 1H, H-9*), 7.76 (s, 1H, H-1), 7.47 (d, J=8.6 Hz, 1H, H-10*), 7.07 (s, 1H, H-4), 6.32 (s, 1H, NH), 6.16 (s, 2H, OCH2O), 4.79 (t, J=5.9 Hz, 2H, H-6), 3.95 (s, 3H, OCH3), 3.54-3.59 (m, 2H, NHCH2), 3.17-3.21 (t, J=5.9 Hz, 2H, H-5), 1.57-1.62 (m, 2H, NHCH2CH2), 1.18-1.36 (m, 18H, NHCH2CH2CH2CH2CH2CH2CH2CH2CH2CH2CH2), 0.84 (t, J=6.9 Hz, 3H, CH2CH3). 13C NMR (100 MHz, DMSO-d6): δ 149.79, 147.92, 146.83, 137.60, 135.90, 133.34, (C-2, C-3, C-4a, C-10, C-12a, C-13a), 146.74 (C-8), 130.52, 120.92, 116.17 (C-8a, C-9, C-13b), 124.81 (C-13), 119.95 (C-12), 116.17 (C-11), 108.74 (C-4), 105.51 (C-1), 102.30 (OCH2O), 57.24 (OCH3), 55.04 (C-6), 47.48 (NHCH2), 31.62, 30.79, 29.38, 29.36, 29.32, 29.31, 29.13, 29.05, 26.96, 26.65, 22.42 (NHCH2CH2CH2CH2CH2CH2CH2CH2CH2CH2CH2, C-5), 14.29 (CH2CH3). MS (ESI): m/z (M+) calcd for C25H29N2O3, 489.311 found: 489.311.
Пример 6. Биологические испытания соединения 1b (9-(гексиламино)-2,3-метилендиокси-10-метоксипротоберберин хлорида).
Животные.
Самцы мышей AY массой 30-33 г и CD-1 массой 20-25 г были получены из SPF-вивария Института цитологии и генетики СО РАН. Животных содержали в стандартных условиях со свободным доступом к воде и корму в помещениях с регулируемой влажностью и температурой при цикле свет-темнота 12/12 ч. Все манипуляции с животными проводились в строгом соответствии с законодательством РФ, приказ Минздрава РФ от 25.07.2012 г.199n от 4 января 2016 г.и Директива 2010/63 / EU Европейского парламента и Совета Европейского Союза от 22 сентября 2010 г.о защите животных, используемых в научных целях.
Дизайн эксперимента на мышах AY
Мышей кормили стандартным гранулированным кормом с добавлением свиного сала и печенья ad libitum в течение 30 дней, пока они не набирали массу тела более 35 г.После этого были сформированы следующие группы: 1) мыши (n=5) AY+растворитель (вода+2 капли Tween 80), 2) мыши (n=5) AY+SHE-196 15 мг/кг, 3) мыши (n=5) AY+метформин (MF) 250 мг/кг и 4) мыши (n=5) C57BL/6+растворитель (вода+2 капли Tween 80). Каждая группа состояла из 6 животных. Диета оставалась неизменной до конца эксперимента. Все соединения вводили внутрижелудочно один раз в день. ОГТТ выполняли на 14-е сутки эксперимента. В конце эксперимента (22 дня) брали кровь для биохимического анализа и измерения инсулина.
Пероральный тест толерантности к глюкозе (ОГТТ).
Тест выполняли после 12-часового голодания. Пероральная нагрузка глюкозой (2,5 г/кг) выполнялась во всех группах мышей. Перед растворением в воде все соединения смешивали с двумя каплями Tween 80. Тестируемые соединения вводили через желудочный зонд за 30 минут до нагрузки глюкозой. Уровень глюкозы в крови определяли количественно с помощью глюкометра ONE TOUCH Select (LIFESCAN Inc., Милпитас, Калифорния, США) перед введением (точка 0) и через 30, 60, 90 и 120 минут после нагрузки глюкозой. Площадь под гликемической кривой рассчитывали с использованием модели Тай [Tai, M. A Mathematical Model for the Determination of Total Area Under Glucose Tolerance and Other Metabolic Curves. Diabetes Care, 1994, 17(2), 152-154].
Биохимические параметры
После 22 дней введения соединения 1b мышей декапитировали, собирали кровь и отделяли сыворотку центрифугированием при 1640 × g в течение 15 мин. Уровни общего холестерина, триглицеридов, общего белка, щелочной фосфатазы, аланинаминотрансферазы и лактата в сыворотке крови определяли количественно во всех группах с помощью стандартных диагностических наборов (Vector-Best, Новосибирск, Россия) и спектрофотометра Stat Fax 3300 (Awareness Technology Inc., США).
Оценка концентрации инсулина в крови после однократного введения.
Мышам CD-1 (n=5), голодавшим в течение 4 часов, вводили перорально (через желудочный зонд) однократно соединение 1b в дозе 15 мг/кг или воду с 2 каплями Твина 80. Эксперимент проводился на одних и тех же животных через день. Образцы крови объемом 0,1 мл отбирали из хвоста животных перед введением (0 мин) и через 30, 45 и 60 минут после введения. После коагуляции (не менее 30 мин) образцы крови центрифугировали 15 мин при 1640 × g в течение 15 мин для отделения сыворотки. Образцы сыворотки замораживали для дальнейшей оценки инсулина с помощью ИФА. Для анализа концентрации инсулина в сыворотке крови использовали набор ИФА для определения инсулина крыс/мышей (№по каталогу EZRMI-13K, Millipore). Подготовка образцов и все процедуры выполнялись в соответствии с руководством производителя. Для анализа использовали фотометр Multiscan Ascent (Thermo Labsystems, Финляндия).
Результаты:
В течение трех недель эксперимента отчетливо прослеживалась динамика снижения массы тела животных, которым вводили метформин и 1b (фиг 1).
Через две недели после начала эксперимента был проведен ОГТТ и было установлено выраженное гипогликемическое действие соединения 1b (фиг. 2 и 3).
Было показано, что соединение 1b в дозе 15 мг/кг после однократного перорального введения может повышать чувствительность тканей к инсулину, что отражается в снижении концентрации инсулина в крови (фиг.4).
Пример 7. Биологические испытания соединений 1a-e на мышах C57BL/6.
Животные.
Самцы мышей C57BL/6 массой 22-25 г были получены из SPF-вивария Института цитологии и генетики СО РАН. Животных содержали в стандартных условиях со свободным доступом к воде и корму в помещениях с регулируемой влажностью и температурой при цикле свет-темнота 12/12 ч. Все манипуляции с животными проводились в строгом соответствии с законодательством РФ, приказ Минздрава РФ от 25.07.2012 г.199n от 4 января 2016 г.и Директива 2010/63 / EU Европейского парламента и Совета Европейского Союза от 22 сентября 2010 г.о защите животных, используемых в научных целях.
Пероральный тест толерантности к глюкозе (ОГТТ).
Тест проводили на животных после 12-часового голодания (n=6 в каждой группе). Пероральная нагрузка глюкозой (2,5 г/кг) выполнялась во всех группах мышей. Перед растворением в воде все соединения смешивали с двумя каплями Tween 80. Таблетки положительного контроля вилдаглиптина (VLD) (Galvus, Novartis Far-maceutica SA, Барселона, Испания) растворяли в воде. Тестируемые соединения вводили через желудочный зонд за 30 минут до нагрузки глюкозой. Уровень глюкозы в крови определяли количественно с помощью глюкометра ONE TOUCH Select (LIFESCAN Inc., Милпитас, Калифорния, США) перед введением (точка 0) и через 30, 60, 90 и 120 минут после нагрузки глюкозой. Площадь под гликемической кривой рассчитывалась с использованием модели Тай [Tai, M. A Mathematical Model for the Determination of Total Area Under Glucose Tolerance and Other Metabolic Curves. Diabetes Care, 1994, 17(2), 152-154].
В результате проведенных исследований было обнаружено, что длина алифатического фрагмента, при введении соединений 1a-e в дозе 15 мг/кг, достоверно влияет на выраженность гипогликемического действия (Фиг.5-8), а именно, с уменьшением количества атомов углерода происходит его усиление, тогда как повышение длины цепочки приводит к его снижению.
Перечень фигур:
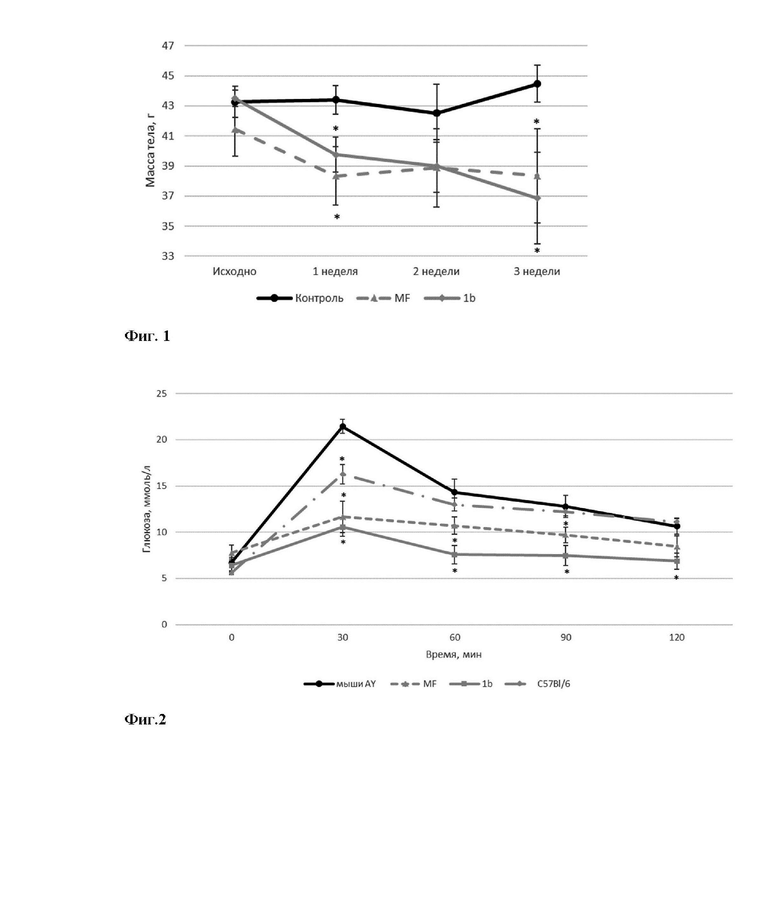
Фиг. 1. Изменение массы тела мышей AY в течение трех недель введения соединения 1b в дозе 15 мг/кг и метформина (MF) в дозе 250 мг/кг.*p<0.05 по сравнению с мышами AY (контроль).
Фиг. 2. ОГТТ выполняли после 2 недель введения соединения 1b в дозе 15 мг/кг и метформина (MF) в дозе 250 мг/кг.* p<0,05 по сравнению с мышами AY.
Фиг. 3. Площадь под гликемической кривой, рассчитанная по данным ОГТТ, после 2-недельного введения соединения 1b в дозе 15 мг / кг и метформина (MF) в дозе 250 мг / кг мышам AY. a, b, c: p<0,05 по сравнению с мышами AY; d: p<0,05 по сравнению с MF.
Фиг. 4. Изменение концентрации инсулина в крови после однократного перорального введения соединения 1b в дозе 15 мг/кг мышам CD-1. *p<0,05 по сравнению с контрольными животными.
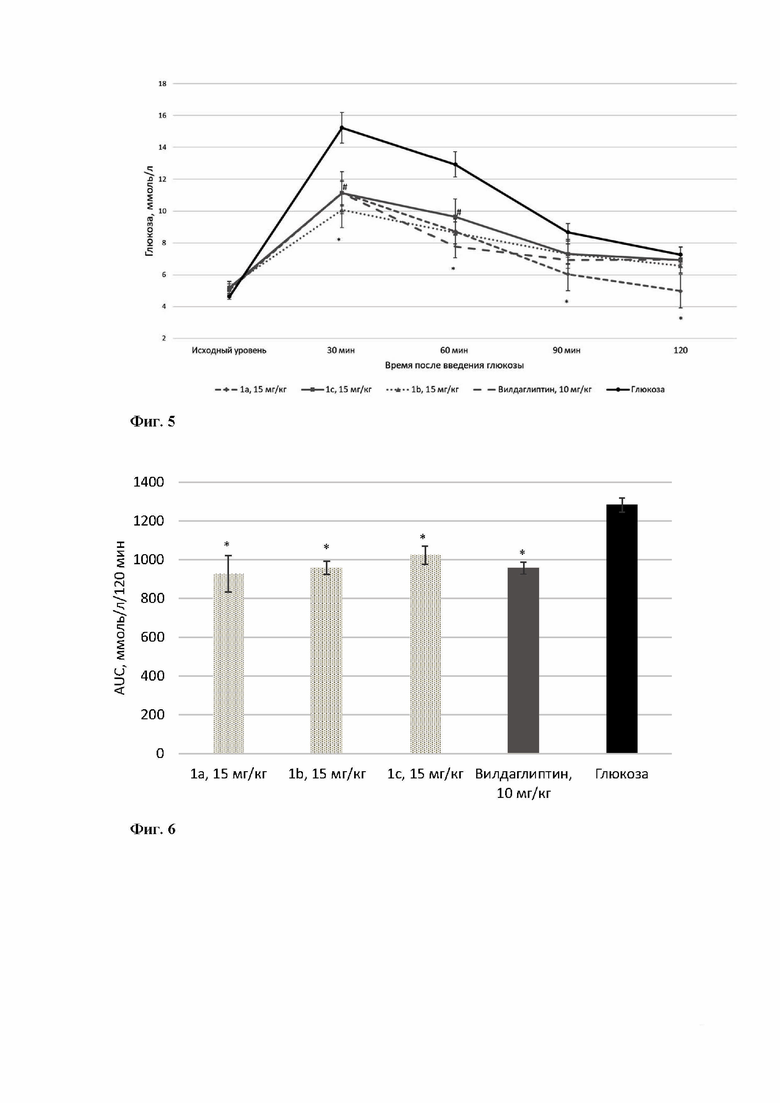
Фиг. 5. Результаты ОГТТ, 1a, 1b, 1c в дозе 15 мг/кг.*p<0,05 1а по отношению к глюкозе, #p<0,05 1b и 1c по отношению к глюкозе.
Фиг. 6. Результаты ОГТТ (площадь под гликемической кривой), 1a, 1b, 1c в дозе 15 мг/кг.*p<0,05 по отношению к глюкозе.
Фиг. 7. Результаты ОГТТ, 1e, 1d в дозе 15 мг/кг.*p<0,05 по отношению к глюкозе.
Фиг. 8. Результаты ОГТТ (площадь под гликемической кривой), 1e, 1d в дозе 15 мг/кг.*p<0,05 по отношению к глюкозе.
жир, г
бурый жир, г
*p<0.05 по сравнению с мышами AY.
ммоль/л
ЕД/л
ЕД/л
| название | год | авторы | номер документа |
|---|---|---|---|
| (2S)-3-(4-{ 2-[4-(2-{ [(1R,4aR,7S)-7-этинил-1,4a,7-триметил-1,2,3,4,4a,4b,5,6,7,8,10,10a-додекагидрофенантрен-1-ил]формамидо} этокси)фенил]этокси} фенил)-2-этокси-пропановая кислота для терапии и профилактики метаболического синдрома | 2023 |
|
RU2813464C1 |
| Монотерпензамещенные (S)-2-этокси-3-(4-(4-гидроксифенетокси)-фенил)-пропановые кислоты для терапии метаболического синдрома | 2024 |
|
RU2831554C1 |
| N-[3-ОКСОЛУП-28-ОИЛ]-2-(4-(2-(4-((S)-2-ЭТОКСИ-3-ПРОПАНОИЛ)ФЕНОКСИ)ЭТИЛ)ФЕНОКСИ)ЭТАНАМИД ДЛЯ ТЕРАПИИ И ПРОФИЛАКТИКИ МЕТАБОЛИЧЕСКОГО СИНДРОМА | 2021 |
|
RU2774591C1 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА | 1995 |
|
RU2137770C1 |
| ХИМИЧЕСКИЙ СИНТЕЗ И ПРОТИВООПУХОЛЕВЫЙ И ПРОТИВОМЕТАСТАТИЧЕСКИЙ ЭФФЕКТЫ КОНЪЮГАТА ДВОЙНОГО ДЕЙСТВИЯ | 2011 |
|
RU2729419C2 |
| ПРОИЗВОДНОЕ N-(1S)-1',2',3'-ТРИМЕТОКСИ-6,7-ДИГИДРО-1Н-БЕНЗО[5',6':5,4]ЦИКЛОГЕПТА-[3,2-F]БЕНЗОФУРАН-1-ИЛ)АЦЕТАМИДА И ЕГО ПРИМЕНЕНИЕ | 2013 |
|
RU2538982C1 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2011 |
|
RU2609018C2 |
| НОВЫЕ ГИДРОФИЛЬНЫЕ ПРОИЗВОДНЫЕ 2-АРИЛ-4-ХИНОЛОНОВ В КАЧЕСТВЕ ПРОТИВОРАКОВЫХ АГЕНТОВ | 2007 |
|
RU2424245C2 |
| АГОНИСТЫ РЕЦЕПТОРА GLP-1 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2769715C1 |
| ЗАМЕЩЕННЫЕ 2-МЕТИЛИДЕН-5-(ФЕНИЛАМИНО)-2,3-ДИГИДРОТИОФЕН-3-ОНЫ ДЛЯ ЛЕЧЕНИЯ ЛЕЙКОЗОВ С ТРАНСЛОКАЦИЯМИ MLL-ГЕНА И ДРУГИХ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2017 |
|
RU2656603C1 |


Изобретение относится к области органической химии и фармакологии и направлено на разработку новых средств для контроля метаболических нарушений. Раскрывается применение соединения 1a-e следующей структуры в качестве средства для повышения чувствительности тканей к инсулину при сахарном диабете 2-го типа. Изобретение обеспечивает эффективное повышение чувствительности тканей к инсулину при сахарном диабете 2-го типа. 8 ил., 2 табл., 7 пр.

Применение соединения 1a-e следующей структуры в качестве средства для повышения чувствительности тканей к инсулину при сахарном диабете 2-го типа
| National Center for Biotechnology Information, 2023, https://pubchem.ncbi.nlm.nih.gov/compound/137630200 | |||
| ZAGREBAEV et al | |||
| The Synthesis and Investigation of New Electroneutral Berberine Derivatives | |||
| Chemistry of Heterocyclic Compounds, 02.2022, vol | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
| EP 2070926 A1, 17.06.2009 | |||
| GLADKOVA E.D et al | |||
| The First Berberine-Based | |||
Авторы
Даты
2023-06-23—Публикация
2022-05-23—Подача