Область техники
Изобретение относится к области химической технологии получения неорганических соединений, а именно к способам получения карбоната кальция.
Уровень техники
Известен способ получения осажденного карбоната кальция обработкой отвального хлорида кальция от производства хлората калия содой в присутствии диоксида углерода [1]. По существу в 19 веке по этому способу первым производителем осажденного СаСО3 стала английская компания John Е. Sturge Ltd.
В России аналогом осажденного карбоната кальция (ОКК) является производство химически осажденного мела (ХОМ) на предприятии, размещенном в Саратовской области, которое использует традиционную технологию с использованием известняка в качестве исходного сырьевого источника и соды и углекислого газа в качестве реагента [2]. Существенным недостатком способа получения осажденного карбоната кальция, основанного на использовании известняка, является использование для этих целей только высококачественного известняка с минимальным содержанием примесей, а также использование дорогостоящего реагента кальцинированной соды.
Имеется предложение [3] использовать для получения ОКК в качестве источника кальция раствор хлорида кальция, который благодаря своей хорошей растворимости отделяют от нерастворимых примесей и далее карбонизируют в аммиачной среде, получая тонкодисперсный осадок карбоната кальция. Данный способ позволяет улучшить технико-экономические показатели способов, основанных на использовании известняка. Однако, существенным недостатком данного способа является то, что данный способ может быть реализован только на производствах, производящих хлористый кальций в качестве побочного продукта или в составе производственного отхода. Кроме того, для данного способа характерно зарастание контактных элементов абсорберов-карбонизаторов карбонатом кальция.
В патенте КНР [4] описан способ получения пористого сверхчистого осажденного карбоната кальция, основанный на взаимодействии водного раствора хлорида кальция с водным раствором гидрокарбоната аммония в присутствии СО2, исключающий необходимость применения абсорберов-карбонизаторов и связанным с этим зарастанием контактной поверхности оборудования карбонатом кальция.
По своей технической сущности и достигнутому результату данный способ получения осажденного карбоната кальция из сред, содержащих кальций, наиболее близок к заявляемому способу и поэтому он принят в качестве прототипа. Однако данный способ имеет недостатки.
Недостатками данного способа являются:
1) ограниченность номенклатуры сырьевых источников только чистыми растворами хлорида кальция;
2) неизбежность выделения углекислого газа в окружающую среду в процессе производства;
3) необходимость использования для получения осажденного СаСО3 только товарных реагентов в виде бикарбоната аммония и углекислого газа.
Указанные недостатки могут быть устранены реализацией следующих технических решений, положенных в основу заявляемого способа:
- использование для производства осажденного карбоната кальция очищенных от нефти, железа и марганца промысловых поликомпонентных рассолов нефтегазодобывающих предприятий, содержащих хлорид кальция;
- получение осадителя карбоната кальция в виде насыщенного раствора углеаммонийной соли с использованием водного раствора аммиака и содержащих углекислый газ различных газовых смесей;
- возможность использования для получения осажденного карбоната кальция водных растворов с низким содержанием кальция.
Реализация предлагаемых технических решений позволяет существенно расширить номенклатуру сырьевых источников, пригодных для получения осажденного карбоната кальция, исключить выброс углекислого газа в окружающую среду, обеспечив при этом получение насыщенного раствора углеаммонийной соли, являющейся эффективным осадителем карбоната кальция.
Сущность изобретения
Технический результат достигается тем, что в качестве раствора аммонийного осадителя используют раствор углеаммонийной соли, в качестве среды, содержащей хлорид кальция, используют промысловые поликомпонентные рассолы нефтегазодобывающих предприятий, которые подвергают очистке от нефти, железа и марганца и приводят в контакт или с оксидом кальция, или с гидроксидом кальция, или с газообразным аммиаком, образующийся в процессе контакта осадок гидроксида магния отделяют от промыслового рассола, освобожденный от магния промысловый рассол приводят в контакт с насыщенным раствором углеаммонийной соли, образующийся при этом осадок карбоната кальция отделяют от маточного промыслового рассола, промывают и сушат, а маточный промысловый рассол операции осаждения карбоната кальция используют в технологии нефтегазодобычи.
Технический результат достигается тем, что насыщенный раствор углеаммонийной соли получают абсорбцией углекислого газа насыщенным водным раствором аммиака, производимым в свою очередь абсорбцией газообразного аммиака водой.
Технический результат достигается тем, что в качестве источника углекислого газа используют содержащие СО2 газовые смеси, образующиеся при сжигании углеводородных материалов, таких как природный газ, нефть, мазут, каменный и бурый угли, древесина, а также углекислый газ, образующийся в результате паровой конверсии оксида углерода при очистке азотоводородной смеси в технологическом цикле производства аммиака.
Технический результат достигается тем, что при использовании в качестве источника углекислого газа высокотемпературные газовые смеси, содержащие СО2, их вначале охлаждают до температуры точки росы путем прямого контакта с рассолами или растворами, содержащими хлорид кальция, предельно насыщая при этом содержащие СО2 газовые смеси водяными парами и одновременно концентрируя рассолы или растворы до предельного их насыщения по хлориду кальция, далее предельно насыщенные водяными парами и содержащие СО2 газовые смеси охлаждают, получая и выводя из газовой фазы образующийся при охлаждении конденсат водяных паров и используют для получения насыщенного раствора углеаммонийной соли абсорбцией находящегося в составе газовых смесей углекислого газа насыщенным водным раствором аммиака.
Технический результат достигается тем, что в качестве осадителя кальция используют соду или раствор соды, при этом образующийся в процессе осаждения карбоната кальция из освобожденного от магния промыслового рассола маточный обогащенный хлоридом натрия промысловый рассол используют в технологии нефтедобычи, а образующийся в процессе осаждения карбоната кальция из насыщенного раствора хлорида кальция маточный раствор хлорида натрия используют либо в качестве товарного продукта в виде концентрированного раствора хлорида натрия, либо в качестве сырья для производства безводного хлорида натрия.
Технический результат достигается тем, что в качестве среды, содержащей хлорид кальция, используют промысловые поликомпонентные рассолы нефтегазодобывающих предприятий, которые подвергают очистке от нефти, железа и марганца и приводят в контакт или с оксидом кальция, или с гидроксидом кальция, или с газообразным аммиаком, образующийся в процессе контакта осадок гидроксида магния отделяют от промыслового рассола, освобожденный от магния промысловый рассол приводят в контакт с содой или раствором соды, образующийся при этом осадок карбоната кальция отделяют от маточного промыслового рассола, промывают и сушат, а маточный промысловый рассол операции осаждения карбоната кальция используют в технологии нефтегазодобычи.
Технический результат достигается тем, что используют оксид кальция и гидроксид кальция, полученные из карбоната кальция.
Пример 1. Образец промыслового рассола Ярактинского нефтегазоконденсатного месторождения ООО “ИНК” объемом 100 дм3, имеющего показатель рН=4,7 и содержащий (мг/дм3): железа - 98, нефтепродуктов - 115, марганца - 63, подщелачивали путем контакта с газообразным аммиаком до показателя рН=8,0-8,5 и аэрировали атмосферным воздухом до полного окисления Fe2+в Fe3+, далее в рассол дозировали при перемешивании концентрированный раствор NaOCl до полного окисления Mn2+в Mn4+, после дозирования в образцы рассола флокулянта и коагулянта образцы подвергали флотированию в радиальном флотаторе. После флотирования и контрольной фильтрации на нутч-фильтрах образец очищенного рассола с остаточным содержанием (мг/дм3): железа <5, нефтепродуктов <5, марганца <5 использовали для удаления магния путем осаждения его в виде Mg(OH)2 при контакте проб промыслового рассола объемом 80 дм3 с различными дозами газообразного аммиака. При подаче газообразного аммиака непосредственно в промысловый рассол абсорбированный аммиак, частично гидролизуясь, образует в составе рассола гидроксид аммония, который является эффективным осадителем магния. Состав исходных образцов промыслового рассола и составы образцов, образующихся после осаждения магния и отделения Mg(OH)2 фильтрацией маточных растворов представлены в таблице 1.
Из полученных результатов однозначно следует, что глубина осаждения магния из очищенного от железа, нефтепродуктов и марганца промыслового рассола зависит от исходного количества вводимого аммиака. При большом избытке аммиака (500% от стехиометрии) степень осаждения магния составляет 99%. Однако, при этом степень соосаждения кальция составляет 19%. Целесообразно ограничиться массовым избытком NH3 не более 150% от стехиометрии, так как можно обеспечить степень осаждения магния выше 90% при степени соосаждения кальция не более 10%. При этом длительность процесса осаждения Mg(OH)2 составляет не более 1 часа.
Пример 2. Промысловый раствор Ярактинского нефтегазоконденсатного месторождения (ЯНГКМ) очищали от нефти, железа и марганца по методике, описанной в примере 1. Очищенный рассол делили на равные порции. Порции подвергали очистке от магния по методике, описанной в примере 1, и из каждой очищенной от магния порции осаждали карбонат

кальция, используя в качестве осадителя раствор углеаммонийной соли различной концентрации при стехиометрическом массовом содержании (NH4)2CO3 в объемах осадителя. Использовали осадитель с концентрацией (NH4)2CO3 (г/дм3): 137,5; 202,0; 363,2 (насыщенный раствор). При этом выход СаСО3 в осадок составил соответственно (%): 86; 88; 96. Из полученных результатов следует, что насыщенный раствор осадителя приводит к минимальному разбавлению рассола, обеспечивая максимальный выход СаСО3 в осадок, исключая при этом соосаждение NH4Cl. Таким образом, в качестве осадителя целесообразно использовать насыщенный раствор углеаммонийной соли.
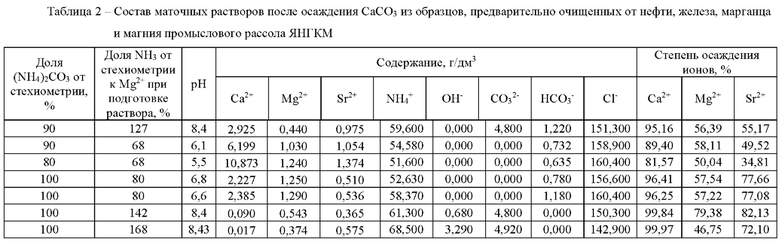
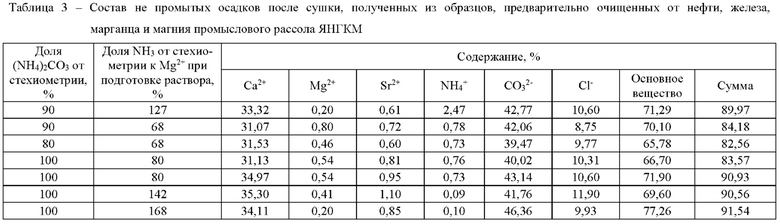
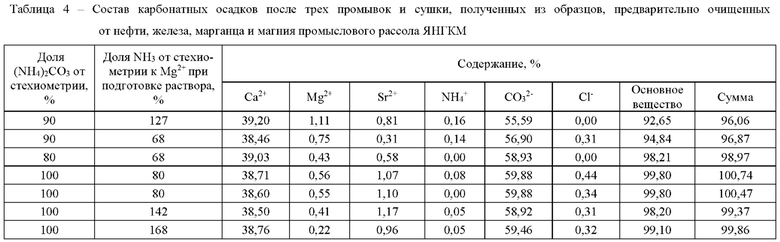
Пример 3. Промысловый рассол ЯНГКМ очищали от нефти, железа и марганца по методике, описанной в примере 1, делили на равные порции. Порции после очистки от магния приводили в контакт с насыщенными растворами углеаммонийной соли, содержащими различное массовое количество карбоната аммония, получая различные образцы осажденного карбоната кальция и маточные рассолы операций осаждения. Каждый из полученных образцов делили на две части. Одну часть образца сушили, не проводя промывку, другую часть образца вначале промывали водой, а затем сушили. Высушенные образцы анализировали на содержание основного вещества и содержание основных примесей. Полученные результаты приведены в таблицах 2, 3, 4.
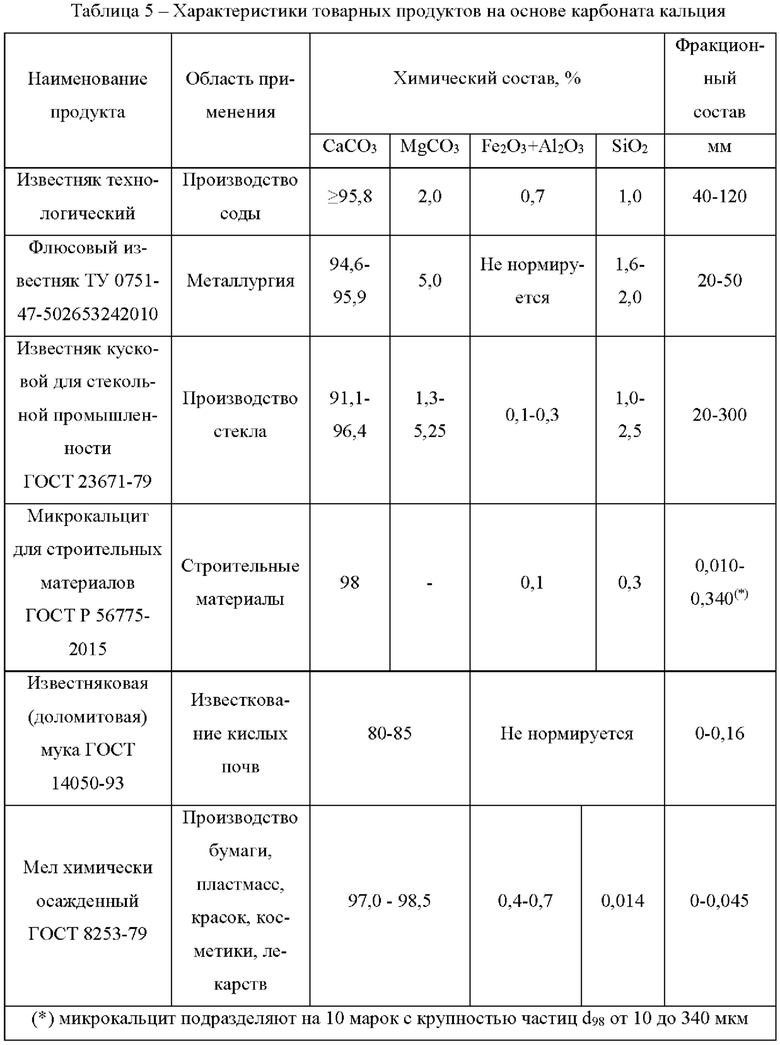
Из полученных результатов (таблица 2) следует, что степень осаждения кальция в виде СаСО3 карбонатом аммония при стехиометрическом его дозировании превышает 99%. При этом в случае отмывки образцов осажденного СаСО3 от маточного рассола высушенные осадки (таблица 4) по своему составу соответствуют требованиям, предъявляемым к товарным продуктам на основе карбоната кальция, представленным в таблице 5. При этом ситовой анализ полученных образцов показал их полное соответствие второму сорту химически осажденного СаСО3 (ГОСТ 8253-79). Остаток на сите 325 меш (0,045 мм) составил 0,5% при требовании 1%. Микроскопический анализ карбонатных осадков показал, что частицы исследованных образцов представляют собой агломерации мелкодисперсных кристаллических частиц размером менее 5 мкм.
Пример 4. Пластовый поликомпонентный пересыщенный по хлориду кальция природный рассол, добываемый на Знаменском месторождении рассолов Жигаловского района Иркутской области, откачиваемый из недр на поверхность с температурой 36-37°С элементного количественного состава (г/дм3): Li - 0,46; Na - 2,4; K - 4,3; Са - 143,3; Mg - 28,3; Cl - 347,9; Br -8,5, общей минерализацией 641 г/дм3, рН=5,3 и объемом 0,65 м3 охлаждали до 15°С, высаливая при этом 60,7 кг кристаллогидрата CaCl2⋅6Н2О. При этом содержание MgCl2⋅6Н2О, соосаждаемого с CaCl2⋅6Н2О в полученном осадке составило 3,8% мас.
Осадок кристаллогидрата нагревали до 45°С, получая расплав CaCl2⋅6Н2О, содержащий кристаллы MgCl2⋅6H2O. Кристаллы MgCl2⋅6H2O удаляли из расплава фильтрацией. Остаточное содержание магния в отфильтрованном расплаве не превышало 0,1% мас. Очищенный от магния расплав после затвердевания растворяли в воде, получая насыщенный раствор CaCl2. Образец насыщенного раствора CaCl2 смешивали с насыщенным раствором (NH4)2CO3 из расчета стехиометрического ввода в раствор карбонат-ионов по отношению к ионам кальция. Степень перевода кальция в СаСО3 в этом эксперименте составила 99,99%. Полученный осадок после трехкратной промывки сушили и анализировали на содержание основного вещества и размера частиц. Содержание основного вещества (СаСО3) составило 99,4%; размер частиц - в диапазоне 2-5 мкм.
Маточный раствор представляет собой концентрированный раствор NH4Cl, содержащий 1,7 г/дм3 (NH4)2CO3 в виде примеси.
Пример 5. На пилотной установке, включающей узел получения источника углекислого газа в виде содержащей СО2 газовой смеси с температурой 40°С, составом (% об.): N2 - 74,4; О2 - 15,13; СО2 - 2,33; Н2О - 7,28 и объемным расходом 3,73 м3/ч, два абсорбционных агрегата, содержащих тарельчатые абсорберы, емкости для циркуляции и перекачки абсорбента, циркуляционные насосы, узел приема отработанного абсорбента (насыщенного раствора углеаммонийной соли) и узел приготовления исходного абсорбента (насыщенный водный раствор аммиака) проводили экспериментальную проверку процесса получения раствора углеаммонийной соли путем абсорбции СО2 из газовой смеси аммиачным водным раствором. В установившемся режиме эксплуатации пилотной установки (постоянная подпитка исходным абсорбентом при постоянном отборе производимой углеаммонийной соли) при объемной подпитке исходным абсорбентом 1 дм3/ч, содержащим 116 г/дм3 растворенного в воде аммиака, производили 1 дм3/ч углеаммонийного раствора состава (г/дм3): 312,5 - (NH4)2CO3; 18,9 - NH4HCO3, имеющего показатель рН=9,4. Степень улавливания углекислого газа (двухступенчатая абсорбция) составляла 99,8%. Полученные результаты подтверждают возможность получения насыщенных растворов углеаммонийной соли абсорбцией углекислого газа из содержащих СО2 газовых смесей в условиях их контакта с насыщенным аммиаком водным раствором.
Пример 6. На пилотной установке, включающей узел получения высокотемпературной газовой смеси, содержащей углекислый газ, в теплогенераторе (циклонная топка, камера дожигания, камера охлаждения топочного газа смешением с атмосферным воздухом), узел форсированного охлаждения топочного газа до точки росы и предельного насыщения его парами воды путем прямого контакта с водным раствором в тарельчатой испарительной колонне была проведена экспериментальная проверка форсированного охлаждения газообразного теплоносителя, получаемого сжиганием в атмосферном воздухе природного легкого газа.
Исходный водный раствор, поступающий на форсированное охлаждение топочного газа и концентрирование, содержал в своем составе 116 г/дм3 CaCl2. В установившемся режиме на пилотной установке перерабатывали 50 дм3/ч исходного раствора CaCl2 и получали 15,3 дм3 концентрированного (близкого к насыщению) рассола с концентрацией CaCl2 379 г/дм3, при этом 34,7 кг/ч воды переходило в состав топочного газа. Объемный расход теплоносителя состава (% об.): N2 - 76,03; О2 - 15,47; СО2 - 2,48; Н2О 5,14 поступал на испарение при температуре 650°С с расходом 352,3 м3/ч. Объемный расход легкого газа состава (% об.): CH4 - 86,5600; С2Н6 - 9,1870; С3Н3 - 0,2171; Н2 - 0,0417; С4Н10 - 0,0025; N2 - 3,5950; Не - 0,2171 для получения теплоносителя составлял 2,6 м3/ч (поступал на сжигание при 21°С). Температура мокрого термометра (температура предельно увлажненного газа на выходе из испарительной колонны) составляла 72°С при составе увлажненного газового потока (% об.): N2 - 53,770; Н2О - 32,970; О2 - 10,794; СО2 - 0,175. При охлаждении увлажненного газового потока до 40°С в конденсаторе получили 32,4 кг/ч конденсата сокового пара. Объемный расход газовой смеси на выходе из конденсатора составлял 122,8 м3/ч и имел состав (% об.): N2 - 74,4; О2 - 15,13; Н2О - 7,28; СО2 - 2,4. Из полученных результатов однозначно следует, что содержащие в своем составе СО2 высокотемпературные топочные газы могут быть использованы для концентрирования содержащих CaCl2 растворов и рассолов, сопровождаемого получением обессоленной воды в виде конденсата сокового пара. При этом охлажденный и содержащий СО2 топочный газ является сырьевым источником для получения растворов углеаммонийной соли.
Пример 7. Пробу промыслового рассола одного из нефтяных месторождений в количестве 30 л очищали от нефти, железа и марганца и использовали для удаления магния с использованием в качестве осадителя СаО. Элементный состав очищенного промыслового рассола (г/дм3) составляет: Li - 0,174; Na - 22,5; K - 12,8; Cl - 74,5; Mg - 15,1; Cl - 220; В - 0,02; Br - 4,85; НСО3- - 0,37. Плотность рассола 1,25 кг/дм3, общая минерализация 356 г/дм3; рН=5,16. Остаточное содержание Fe <5,0 мг/дм3, нефти <5,0 мг/дм3, марганца <5,0 мг/дм3. В качестве осадителя использовали свежепрокаленный (t=900°C) оксид кальция с содержанием СаО 96,5% мас. Удаление магния проводили в две ступени. На второй ступени осуществляли глубокое осаждение магния путем контакта промыслового рассола, прошедшего первую ступень осаждения, с СаО, вводимым в стехиометрическом количестве по отношению к массовому содержанию магния в поступающем на первую ступень осаждения промыслового рассола. Полученный на второй ступени осаждения осадок (смесь Mg(OH)2 и СаО) использовали в качестве осадителя магния на первой ступени осаждения, обеспечивая тем самым достижение максимального значения степени полезного освоения осадителя при минимальном (стехиометрическом) его использовании. Полученные результаты представлены в таблице 6.
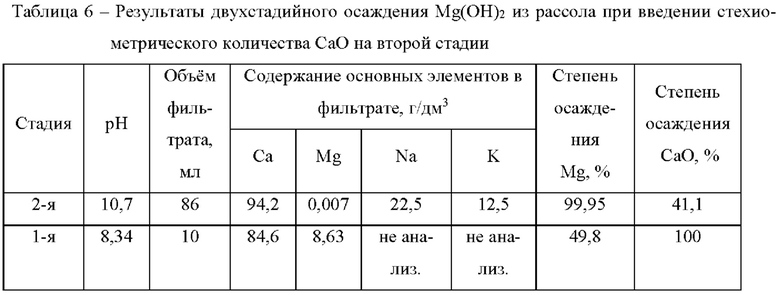
Из полученных результатов следует, что организация процесса осаждения магния в две стадии позволяет при стехиометрическом введении СаО обеспечить глубокое извлечение магния при 100%-ном значении степени полезного освоения осадителя. Содержание Mg(OH)2 в полученном осадке после его троекратной ступенчатой отмывки и сушки составило 98,7% при остаточном влагосодержании 0,6%.
Пример 8. Образец осадка СаСО3 массой 126 г, полученный в примере 3, содержащий 99,86% основного вещества прокаливали в муфеле при температуре 960°С до постоянного веса, который составил 69,63 г. Полученный после прокалки образец содержал 99,6% СаО.
Пример 9. Образец кристаллогидрата CaCl2⋅6H2O, произведенный охлаждением поликомпонентного и пересыщенного по хлориду кальция пластового рассола и очищенного от магния по методике, описанной в примере 4, растворяли в пресной воде, получив раствор хлорида кальция с концентрацией CaCl2 361 г/дм3. Раствор хлорида кальция объемом 1 дм3 смешивали с раствором NaCO3 концентрацией 297 г/дм3 объемом 2,16 дм3. Вес полученного осадка СаСО3 после его трехкратной промывки и сушки до постоянного веса составил 224,91 г, концентрация NaCl в маточном растворе осаждения составила 176,1 г/дм3. Из полученных результатов однозначно следует, что степень осаждения карбоната кальция из раствора CaCl2 содой превышает 99%. При этом образуется концентрированный раствор хлорида натрия, содержание NaCl в котором составило 271 г/дм3.
Источники информации
1. Информационный ресурс "Minerals technologies" [Электронный ресурс] -URL:https//www.mineralstech.com/bisines-segments/specialty-minerals/paper-pcc/precipitated calci-um-carbonate-(pcc), свободный. - Загл. С.Экрана- яз. англ. Дата обращения 02.12.2021.
2. Информационный ресурс "Коммерсантъ" [Электронный ресурс] URL: https//www.kommersant.ru/doc/402.5499, свободный.- Загл. С экрана.- Яз. рус. Дата обращения: 01.12.2021.
3. Патент US №9725330. Production of high purity precipitated calcium carbonate / Tavakkoli В., Sotemann J., Pohl. M., Schmolzer Т. Заяв. 23.02.2015, опуб. 02.07.2015.
4. CN №1757597A. Method for preparing porous super fine calcium carbonate. Shanghai Institute of Technology. Заяв. 25.10.2005, опуб. 12.04.2006.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения бромидных солей при комплексной переработке бромоносных поликомпонентных промысловых рассолов нефтегазодобывающих предприятий (варианты) | 2021 |
|
RU2780216C2 |
| КАЛЬЦИНАТНЫЙ СПОСОБ ПОЛУЧЕНИЯ КАРБОНАТА ЛИТИЯ ИЗ ЛИТИЕНОСНОГО СЫРЬЯ | 2013 |
|
RU2560359C2 |
| СПОСОБ ПОЛУЧЕНИЯ БРОМИДА АММОНИЯ | 2021 |
|
RU2789134C1 |
| Способ получения литиевого концентрата из литиеносных природных рассолов и его переработки в хлорид лития или карбонат лития | 2017 |
|
RU2659968C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИСТОГО КАЛЬЦИЯ ИЗ РАССОЛОВ ХЛОРКАЛЬЦИЕВОГО ТИПА | 2023 |
|
RU2819829C1 |
| Способ получения моногидрата гидроксида лития из рассолов | 2019 |
|
RU2713360C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИПОХЛОРИТА КАЛЬЦИЯ ПРИ КОМПЛЕКСНОЙ ПЕРЕРАБОТКЕ ПРИРОДНОГО ПОЛИКОМПОНЕНТНОГО ПЕРЕСЫЩЕННОГО РАССОЛА ХЛОРИДНОГО КАЛЬЦИЕВО-МАГНИЕВОГО ТИПА | 2016 |
|
RU2637694C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ГИДРОКСИДА МАГНИЯ ИЗ ПОЛИКОМПОНЕНТНОГО ГИДРОМИНЕРАЛЬНОГО СЫРЬЯ | 2023 |
|
RU2801733C1 |
| Способ получения оксида магния из природных рассолов и попутно добываемых вод нефтяных месторождений | 2021 |
|
RU2777082C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ РАССОЛОВ ХЛОРИДНОГО КАЛЬЦИЕВОГО И ХЛОРИДНОГО МАГНИЕВОГО ТИПОВ (ВАРИАНТЫ) | 2009 |
|
RU2436732C2 |
Изобретение относится к области химической технологии получения неорганических соединений, а именно к способам получения карбоната кальция. Способ включает осаждение карбоната кальция из сред, содержащих хлорид кальция. В качестве среды, содержащей кальций, используют промысловые поликомпонентные рассолы нефтегазодобывающих предприятий, которые подвергают очистке от нефти, железа и марганца и приводят в контакт с оксидом кальция, или с гидроксидом кальция, или с газообразным аммиаком. Образующийся в процессе контакта осадок гидроксида магния отделяют от промыслового рассола. Освобождённый от магния промысловый рассол приводят в контакт с насыщенным раствором углеаммонийной соли, или с содой, или раствором соды. Образующийся осадок карбоната кальция отделяют от маточного промыслового рассола, обогащённого хлоридом аммония или хлоридом натрия, промывают и сушат. Маточный обогащённый промысловый рассол операции осаждения карбоната кальция используют в технологии нефтедобычи. Обеспечивается расширение номенклатуры сырьевых источников, исключение выбросов углекислого газа. 2 н. и 4 з.п. ф-лы, 6 табл., 9 пр.
1. Способ получения осаждённого карбоната кальция из сред, содержащих хлорид кальция, включающий осаждение карбоната кальция из растворов аммонийными осадителями, отличающийся тем, что в качестве раствора аммонийного осадителя используют раствор углеаммонийной соли, в качестве среды, содержащей кальций, используют промысловые поликомпонентные рассолы нефтегазодобывающих предприятий, среду подвергают очистке от нефти, железа и марганца и приводят в контакт или с оксидом кальция, или с гидроксидом кальция, или с газообразным аммиаком, образующийся в процессе контакта осадок гидроксида магния отделяют от промыслового рассола, освобождённый от магния промысловый рассол приводят в контакт с насыщенным раствором углеаммонийной соли, образующийся при этом осадок карбоната кальция отделяют от маточного, обогащённого хлоридом аммония промыслового рассола, промывают и сушат, а маточный, обогащённый хлоридом аммония промысловый рассол операции осаждения карбоната кальция используют в технологии нефтедобычи.
2. Способ по п. 1, отличающийся тем, что насыщенный раствор углеаммонийной соли получают абсорбцией углекислого газа насыщенным водным раствором аммиака, производимым, в свою очередь, абсорбцией газообразного аммиака водой.
3. Способ по п. 2, отличающийся тем, что в качестве источников углекислого газа используют содержащие СО2 высокотемпературные газовые смеси, образующиеся при сжигании углеводородных материалов, таких как природный газ, нефть, мазут, каменный и бурый угли, древесина, а также углекислый газ, образующийся в результате реакции паровой конверсии оксида углерода при очистке азотоводородной смеси в технологическом цикле производства аммиака.
4. Способ по п. 3, отличающийся тем, что при использовании в качестве источника углекислого газа высокотемпературных газовых смесей, содержащих СО2, их вначале охлаждают до температуры точки росы путём прямого контакта с рассолами или растворами, содержащими хлорид кальция, предельно насыщая при этом содержащие СО2 охлаждённые до температуры точки росы газовые смеси водяными парами и одновременно концентрируя рассолы или растворы до достижения предельной концентрации в них хлорида кальция, далее предельно насыщенные водяными парами содержащие СО2 газовые смеси и имеющие температуру точки росы охлаждают, выводя из газовой фазы образующийся при охлаждении конденсат водяного пара, и используют в качестве источника углекислого газа для получения насыщенного раствора углеаммонийной соли абсорбцией находящегося в составе газовых смесей углекислого газа насыщенным водным раствором аммиака.
5. Способ получения осаждённого карбоната кальция из сред, содержащих хлорид кальция, включающий осаждение карбоната кальция из растворов, отличающийся тем, что в качестве среды, содержащей кальций, используют промысловые поликомпонентные рассолы нефтегазодобывающих предприятий, которые подвергают очистке от нефти, железа и марганца и приводят в контакт или с оксидом кальция, или с гидроксидом кальция, или с газообразным аммиаком, образующийся в процессе контакта осадок гидроксида магния отделяют от промыслового рассола, освобождённый от магния промысловый рассол приводят в контакт с содой или раствором соды, образующийся при этом осадок карбоната кальция отделяют от маточного, обогащённого хлоридом натрия, промыслового рассола, промывают и сушат, а обогащённый хлоридом натрия рассол используют в технологии нефтедобычи.
6. Способ по п. 1 или 5, отличающийся тем, что используют оксид кальция и гидроксид кальция, полученные из карбоната кальция.
| Способ изготовления обуви | 1990 |
|
SU1757597A1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ ПРИРОДНЫХ РАССОЛОВ ХЛОРИДНОГО КАЛЬЦИЕВО-МАГНИЕВОГО ТИПА | 2013 |
|
RU2543214C2 |
| CN 104386729 A, 04.03.2015 | |||
| ПОЛУЧЕНИЕ ОСАЖДЕННОГО КАРБОНАТА КАЛЬЦИЯ ВЫСОКОЙ ЧИСТОТЫ | 2011 |
|
RU2602140C2 |
| Способ комплексной переработки попутных вод нефтяных месторождений | 2020 |
|
RU2724779C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНАТА КАЛЬЦИЯ ВЫСОКОЙ ЧИСТОТЫ | 2009 |
|
RU2414425C1 |
| US 9138688 B2, 22.09.2015 | |||
| US 10604416 B2, 31.03.2020. | |||
Авторы
Даты
2023-07-05—Публикация
2022-03-03—Подача