Область техники, к которой относится изобретение
Настоящее изобретение относится к новому механохимическому способу получения кумаринов при помощи конденсации Пехмана.
Уровень техники
Конденсация Пехмана представляет собой удобный подход для синтеза кумаринового каркаса из фенолов и β-кетоэфиров в присутствии кислоты. Первоначально в реакции Пехмана использовались высокая температура и большой избыток кислотного катализатора (4-5 эквивалентов). Позже сообщалось о нескольких модификациях классической процедуры Пехмана, допускающих более удобные условия проведения реакции [см., например D1]. В частности, использование таких катализаторов, как метансульфоновая кислота (MsOH), MsOH на Al2O3, п-толуолсульфоновая кислота (p-TsOH), FeF3, поли(4-винилпиридин)-CuI, глутаминовая кислота [см., например D2-D7]. Однако все описанные модифицированные методы имеют ряд недостатков, например, использование по-прежнему высоких загрузок MsOH или p-TsOH (от 0,5 до 1,5 эквивалентов), что снижает экономичность процесса и увеличивает количество отходов. В то же время, описанные ранее методы имеют ограничения в различных замещенных субстратов: например, процедура с использованием MsOH на Al2O3 дает 4-алкилкумарины с хорошим выходом, в то время как 4-арил и 4-трифторметилкумарины не могут быть получены с удовлетворительными выходами.
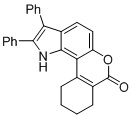
Например, иллюстративным примером этого подхода можно считать получение соединения с антитромбицитарными свойствами, описанное в D9 (Схема 1).

Схема 1
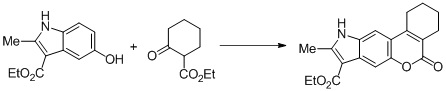
Еще одним примером использования реакции Пехмана является первая стадия синтеза аналога анти-ВИЧ препарата Каланолид А (Схема 2), описанная в D10.
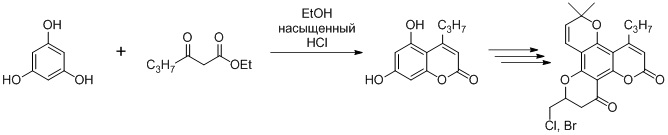
Схема 2
Таким образом, существует потребность в разработке экологически чистой и эффективной процедуры конденсации Пехмана для синтеза кумаринов и более сложных систем, содержащих кумариновый фрагмент.
Цитированные документы уровня техники
D1 M. Lončarić, D. Gašo-Sokač, S. Jokić, M. Molnar, Biomolecules, 2020, 10, 151.
D2 P. Kulkarni, Orient. J. Chem., 2015, 31, 447-451.
D3 H. Sharghi, M. Jokar, Heterocycles, 2007, 71, 2721-2733.
D4 T. Sugino, K. Tanaka, Chem. Lett., 2001, 30, 110-111.
D5 N. H. Jadhav, S. S. Sakate, N. K. Rasal, D. R. Shinde, R. A. Pawar, ACS Omega, 2019, 4, 8522-8527.
D6 V. Vahid, H. Farhad, Molecules, 2014, 19, 13093-13103.
D7 A. Jalal, S. Farhad, A. Jafar, A. Nezam, M. C. R. Tayebeh, C. R. Chim., 2013, 16, 407-411.
D8 S. Sabetpoor, F. Hatamjafari, Orient. J. Chem., 2014, 30, 863-865.
D9 A. A. Kathuria, N. Priya, K. Chand, P. Singh, A. Gupta, S. Jalal, S. Gupta, H. G. Raj, S. K. Sharma. Bioorg. Med. Chem., 2012, 20, 1624-1638.
D10 Ма, Т. et al. J. Med. 2008, 51, 1432-1446.
Раскрытие изобретения
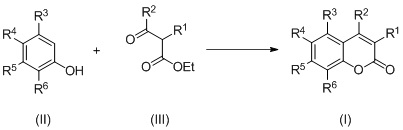
В первом аспекте настоящее изобретение относится к механохимическому способу получения соединений формулы (I), включающему взаимодействие исходного соединения формулы (II) с исходным соединением формулы (III):

где R1 и R2 каждый независимо представляет собой водород, галоген, необязательно замещенный С1-С6 алкил, необязательно замещенный С6-С10 арил, гетероарил или R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-необязательно замещенный С1-С6 алкил, и где n = 3-6;
R3-R6 каждый независимо представляет собой H, ОН, галоген, С1-С6 алкил, С1-С6 алкокси, NHCO2C1-С6 алкил, или два соседних R3-R6 объединены с образованием бензокольца или необязательно замещенного пиррольного кольца.
Необязательные заместители С1-С6 алкила выбраны из 1-3 атомов галогена и С6-С10 арила;
Необязательные заместители С6-С10 арила выбраны из 1-2 атомов галогена и С1-С6 алкокси;
Необязательные заместители пиррола выбраны из 1-2 групп С1-С6 алкила, С6-С10 арила, необязательно замещенного 1-3 С1-С6 алкоксигруппами, и CO2C1-С6 алкила;
где реакцию проводят при механической активации исходных соединений формулы (II) и формулы (III).
Реакцию можно проводить без растворителя или в присутствии инертного разбавителя, такого как гексан, диэтиловый эфир, этилацетат, этанол, ДМФА, HClO4, H3PO4.
Взаимодействие можно проводить в присутствии кислотного катализатора, в частности, HClO4, H2SO4, С1-С6 алкил-SO3H, С6-С10 арил-SO3H необязательно замещенный С1-С6 алкильной группой.
Полноту протекания реакции можно установить при помощи тонкослойной хроматографии (ТСХ), высокоэффективной жидкостной хроматографии (ВЭЖХ), спектроскопии ядерно-магнитного резонанса (ЯМР) или других известных методов. Как правило, реакция протекает полностью от 10 минут до 12 часов.
Температура проведения реакции не ограничивается особыми условиями, однако, с точки зрения технологии, предпочтительная температура составляет от 20 до 50°С, более предпочтительно от 20 до 40°С и наиболее предпочтительно является около 25°С.
Давление, при котором проводится реакция также не ограничивается специально, однако наиболее предпочтительным является использование атмосферного давления.
Определения
В настоящем описании С1-С6 алкил означает алкильную группу, содержащую от 1 до 6 атомов углерода. В предпочтительных вариантах С1-С6 алкил представляет собой С1-С3 алкил. Конкретные варианты алкила включают метил, этил, пропил (н-пропил, изо-пропил), бутил (н-бутил, изо-бутил, втор-бутил, трет-бутил), пентил (н-пентил, изо-пентил, втор-пентил, нео-пентил), гексил и т.д.
Алкокси означает алкильную группу, присоединенную через атом кислорода.
С6-С10 арил означает фенил или нафтил, в том числе 1-нафтил и 2-нафтил.
Галоген означает фтор, хлор, бром или йод.
Механическая активация (альтернативно также называемая здесь и далее механохимическая активация) включает все виды механического воздействия на исходные соединения формул (II) и (III), в том числе размол или истирание. С точки зрения аппаратуры для механохимической активации используются планетарные и струйные мельницы или дезинтеграторы.
Скорость вращения планетарной мельницы может составлять от 10 до 2000 оборотов в минуту. Предпочтительная скорость составляет от 100 до 1000 оборотов, наиболее предпочтительная скорость составляет около 500 оборотов в минуту (8.33 Гц).
Кислотный катализатор (или альтернативно просто катализатор) означает любую кислоту в рамках теории кислотности Бренстеда. Предпочтительными примерами кислотного катализатора являются протонные кислоты, в частности, органические или неорганические кислоты. Примерами протонных кислот являются галогенкарбоновые кислоты, HClO4, H2SO4, HCl, С1-С6 алкил-SO3H, необязательно замещенный галогенами, С6-С10 арил-SO3H, необязательно замещенный С1-С6 алкильной группой, нитрогруппой, атомами галогена или сульфогруппой. Конкретными примерами кислотного катализатора являются трифторуксусная кислота, метансульфоновая кислота, трифторметансульфоновая кислота, перфторбутансульфоновая кислота, серная кислота, фосфорная кислота, бензолсульфокислота, толуолсульфокислота (TsOH), о-, м-, п-нитробензолсульфикилота, 1- и 2-нафталинсульфокислота. Кислота может быть использована в виде раствора, такого как, например, раствор в протонном или апротонном растворителе. Предпочтительными примерами растворителей для кислот являются вода, этанол, метанол, этилацететат. В частности, может использоваться 70% раствор HClO4 в воде или 30% раствор HCl в воде.
Предпочтительные варианты осуществления:
В первом предпочтительном настоящее изобретение относится к способу синтеза соединения формулы (III) при взаимодействии с соединением формулы (II) с получением соединения формулы (I):

где R1 и R2 каждый независимо представляет собой водород, галоген, необязательно замещенный С1-С6 алкил, необязательно замещенный С6-С10 арил, тиофенил, или R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-необязательно замещенный С1-С6 алкил, и где n = 3, 4, 5 или 6;
R3-R6 каждый независимо представляет собой H, ОН, галоген, С1-С6 алкил, С1-С6 алкокси, NHCO2C1-С6 алкил, или два соседних R3-R6 объединены с образованием бензокольца или необязательно замещенного пиррольного кольца,
где необязательные заместители С1-С6 алкила выбраны из 1-3 атомов галогена и С6-С10 арила;
необязательные заместители С6-С10 арила выбраны из 1-2 атомов галогена и С1-С6 алкокси;
необязательные заместители пиррола выбраны из 1-2 группами С1-С6 алкила, С6-С10 арила, необязательно замещенного 1-3 С1-С6 алкоксигруппами, и CO2C1-С6 алкила;
где реакцию проводят без растворителя при истирании соединений (II) и (III) в шаровой мельнице;
в присутствии кислотного катализатора, в частности, HClO4, H2SO4, С1-С6 алкил-SO3H, необязательно замещенный галогеном, С6-С10 арил-SO3H, необязательно замещенный С1-С6 алкилом, предпочтительно С1-С6 алкил-SO3H, в особенности CH3SO3H.
В еще одном предпочтительном варианте
R1 представляют собой водород, галоген или необязательно замещенный С1-С6 алкил;
R2 представляют собой необязательно замещенный С1-С6 алкил, необязательно замещенный С6-С10 арил, или
R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-необязательно замещенный С1-С6 алкил, и где n = 3, 4, 5 или 6;
R3-R6 каждый независимо представляет собой атом водорода, ОН, галоген, С1-С6 алкил, С1-С6 алкокси, NHCO2C1-С6 алкил, или R5 и R6 объединены с образованием бензокольца или R4 и R5 объединены с образованием необязательно замещенного пиррольного кольца,
где необязательные заместители С1-С6 алкила выбраны из 1-3 атомов галогена и С6-С10 арила;
необязательные заместители С6-С10 арила выбраны из 1-2 атомов галогена, С1-С6 алкокси;
необязательные заместители пиррола выбраны из 1-2 С1-С6 алкила, С6-С10 арила, необязательно замещенного 1-3 С1-С6 алкоксигруппами, и CO2C1-С6 алкила;
В еще одном предпочтительном варианте
R1 представляют собой водород, галоген или необязательно замещенный С1-С6 алкил;
R2 представляют собой необязательно замещенный С1-С6 алкил, необязательно замещенный С6-С10 арил, или
R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-необязательно замещенный С1-С6 алкил, и где n = 3, 4, 5 или 6;
R3 представляет собой атом водорода или ОН;
R4 представляет собой атом водорода, галоген, С1-С6 алкокси или С1-С6 алкил;
R5 представляет собой ОН, С1-С6 алкокси, NHCO2C1-С6 алкил; или
R5 и R6 объединены с образованием бензокольца или
R4 и R5 объединены с образованием необязательно замещенного пиррольного кольца,
где необязательные заместители С1-С6 алкила выбраны из 1-3 атомов галогена и С6-С10 арила;
необязательные заместители С6-С10 арила выбраны из 1-2 атомов галогена, С1-С6 алкокси;
необязательные заместители пиррола выбраны из 1-2 С1-С6 алкила, С6-С10 арила, необязательно замещенного 1-3 С1-С6 алкоксигруппами, и CO2C1-С6 алкила.
В еще одном предпочтительном варианте
R1 представляет собой водород, галоген или необязательно замещенный С1-С6 алкил;
R2 представляет собой необязательно замещенный С1-С6 алкил, необязательно замещенный фенил, или
R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-необязательно замещенный С1-С6 алкил, и где n = 3, 4, 5 или 6;
R3 представляет собой атом водорода или ОН;
R4 представляет собой атом водорода, галоген, С1-С6 алкокси или С1-С6 алкил;
R5 представляет собой ОН, С1-С6 алкокси, NHCO2C1-С6 алкил; или
R5 и R6 объединены с образованием бензокольца или
R4 и R5 объединены с образованием необязательно замещенного пиррольного кольца,
где необязательные заместители С1-С6 алкила выбраны из 1-3 атомов галогена и фенила;
необязательные заместители фенила выбраны из 1-2 атомов галогена, С1-С6 алкокси;
необязательные заместители пиррола выбраны из 1-2 С1-С6 алкила, фенила, необязательно замещенного 1-3 С1-С6 алкоксигруппами, и CO2C1-С6 алкила.
В еще одном предпочтительном варианте
R1 представляет собой водород, галоген или необязательно замещенный С1-С6 алкил;
R2 представляет собой необязательно замещенный С1-С6 алкил, необязательно замещенный фенил, или
R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-необязательно замещенный С1-С6 алкил, и где n = 3, 4 или 5;
R3 представляет собой атом водорода или ОН;
R4 представляет собой атом водорода, галоген, С1-С6 алкокси или С1-С6 алкил;
R5 представляет собой ОН, С1-С6 алкокси, NHCO2C1-С6 алкил; или
R5 и R6 объединены с образованием бензокольца или
R4 и R5 объединены с образованием необязательно замещенного пиррольного кольца,
где необязательные заместители С1-С6 алкила выбраны из 1-3 атомов галогена и фенила;
необязательные заместители фенила выбраны из 1-2 атомов галогена, С1-С6 алкокси;
необязательные заместители пиррола выбраны из 1-2 С1-С6 алкила, фенила, необязательно замещенного 1-3 группами С1-С6 алкоксигруппами, и CO2C1-С6 алкила.
В еще одном предпочтительном варианте
R1 представляет собой водород, галоген, С1-С6 алкил, или С1-С6 алкил замещенный фенилом;
R2 представляет собой С1-С6 алкил, С1-С6 алкил замещенный 1-3 атомами галогена, фенил, фенил, замещенный галогеном или С1-С6 алкокси; или
R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-(фенил-С1-С6 алкил), и где n = 3, 4 или 5;
R3 представляет собой атом водорода или ОН;
R4 представляет собой атом водорода, галоген, С1-С6 алкокси или С1-С6 алкил;
R5 представляет собой ОН, С1-С6 алкокси, NHCO2C1-С6 алкил; или
R5 и R6 объединены с образованием бензокольца; или
R4 и R5 объединены с образованием пиррольного кольца, которое может быть замещено 1-2 группами С1-С6 алкила, фенила, необязательно замещенного 1-3 С1-С6 алкоксигруппами, и CO2C1-С6 алкила.
В еще одном предпочтительном варианте
R1 представляет собой водород, галоген, С1-С3 алкил или С1-С3 алкил замещенный фенилом;
R2 представляет собой С1-С3 алкил, С1-С3 алкил замещенный 1-3 атомами галогена, фенил, фенил, замещенный галогеном или С1-С6 алкокси; или
R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-(фенил-С1-С6 алкил), и где n = 3, 4 или 5;
R3 представляет собой атом водорода или ОН;
R4 представляет собой атом водорода, галоген, С1-С3 алкокси или С1-С6 алкил;
R5 представляет собой ОН, С1-С3 алкокси, NHCO2C1-С3 алкил; или
R5 и R6 объединены с образованием бензокольца или
R4 и R5 объединены с образованием пиррольного кольца, которое может быть замещено 1-2 группами С1-С3 алкила, фенила, необязательно замещенного 1-3 С1-С3 алкоксигруппами, и CO2C1-С3 алкила.
В еще одном предпочтительном варианте
R1 представляет собой водород, галоген, метил или бензил;
R2 представляет собой метил, пропил, трифторметил, фенил, орто-фторфенил, 3,4-диметоксифенил; или
R1 и R2 объединены с образованием необязательно замещенного (CH2)n, в котором одна группа CH2 заменена на NH-бензил, и где n = 3, 4 или 5;
R3 представляет собой атом водорода или ОН;
R4 представляет собой атом водорода, бром, метокси или гексил;
R5 представляет собой ОН, метокси, NHCO2C2H5; или
R5 и R6 объединены с образованием бензокольца или
R4 и R5 объединены с образованием пиррольного кольца, которое может быть замещено метилом и CO2C2H5, фенила, необязательно замещенного 1-3 метоксигруппами.
Таким образом, технический результат настоящего изобретения заключается в том, что предложен эффективный, масштабируемый, экологически чистый, механохимический синтез производных кумарина при температуре окружающей среды без использования растворителей, получаемых из фенолов и β-кетоэфиров.
Примеры
Примеры 1-11 Оптимизация условий реакции
Оптимизация была проведена на примере взаимодействия ацетоуксусного эфира с флороглюцином
Смесь флороглюцина, ацетоуксусного эфира и катализатора помещали в сосуд из нержавеющей стали объемом 10 мл. Добавляли десять шариков из нержавеющей стали диаметром 5 мм и смесь измельчали при частоте 8,33 Гц в течение 2 часов. После завершения полученное твердое вещество переносили в химический стакан на 30 мл с использованием 10-15 мл этанола и кристаллизовали.

В сравнительных примерах 10 (без механохимической активации) и 11 (без катализатора) не было получена продукта, или выход продукта был снижен.
Таким образом, для проведения реакции необходимо как добавление кислотного катализатора, так и механохимическая активация.
Представленные ниже примеры иллюстрируют некоторые предпочтительные варианты осуществления настоящего изобретения, но не ограничивают его.
Примеры 12-65 Промышленная применимость
Смесь фенола 1 (5,0 ммоль, 1,0 экв), β-кетоэфира 2 (5,5 ммоль, 1,1 экв) и MsOH (0,5 ммоль, 0,1 экв) помещали в сосуд из нержавеющей стали объемом 10 мл. Добавляли десять шариков из нержавеющей стали диаметром 5 мм и смесь измельчали при частоте 8,33 Гц в планетарной шаровой мельнице Retsch PM 100 течение 2 часов. После завершения полученную пасту или твердое вещество переносили в химический стакан на 30 мл с использованием 10-15 мл этанола (для примеров 1-44). Соединения примеров 45-53 кристаллизовали из ДМФА или смеси ДМФА-этанол (1:1).
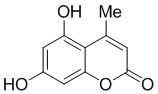
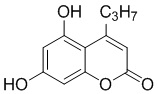
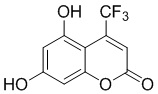
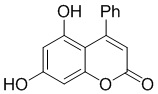
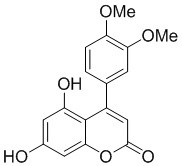
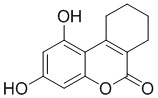
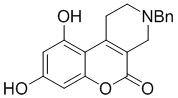
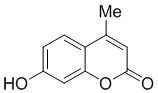
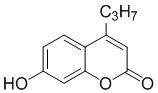
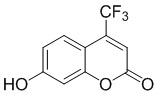
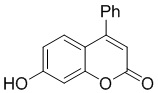
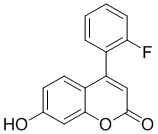
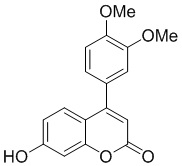

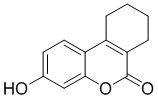
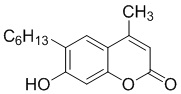
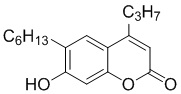
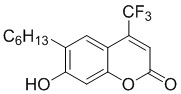
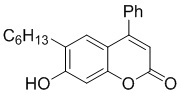
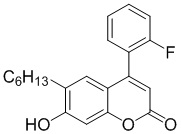
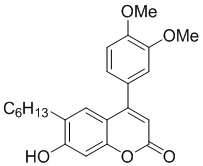
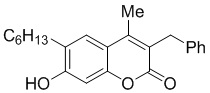
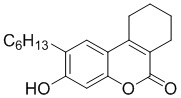
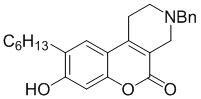
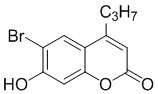
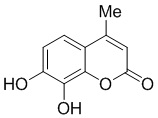
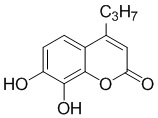
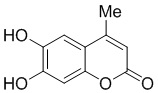
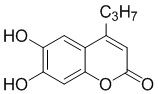
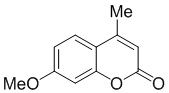
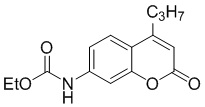
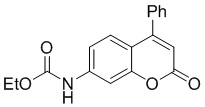
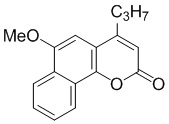
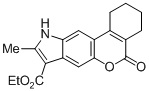

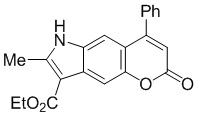
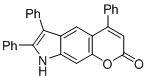
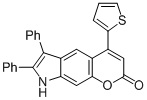
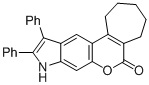
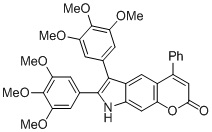
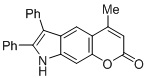
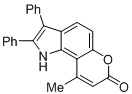
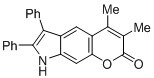
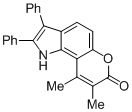
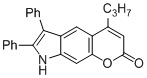
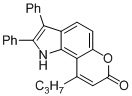
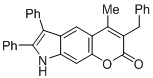
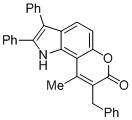
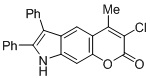
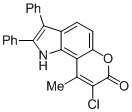
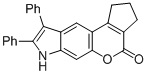
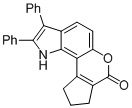
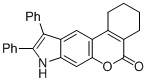
Примеры 66-69 Преимущество размалывания в шаровой мельнице перед обычным перемешиванием
Чтобы продемонстрировать технический эффект настоящего изобретения мы сравнили выходы при обычном перемешивании при помощи магнитной мешалки с размолом при помощи шаровой мельницы. В качестве иллюстративного примера использовали модификацию примера 45.
Реакция проводилась при перемешивании на мешалке IKA C-MAG HS7 при помощи тефлонового магнитного стержня в плоскодонном стакане объемом 50 мл или при размоле в планетарной шаровой мельнице (как указано для примеров 12-65 выше).
(300 об/мин)
(600 об/мин)
(600 об/мин)
(600 об/мин)
Таким образом, размол в мельнице позволяет достичь более высоких выходов продуктов по сравнению с обычным перемешиванием.
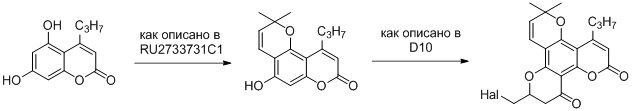
Пример 70
Соединение примера 13, полученного при помощи механохимического синтеза, использовалось для синтеза аналогов каланолида А.
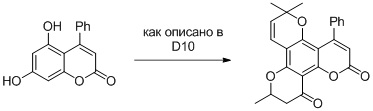
Пример 71
Соединение примера 15, полученного при помощи механохимического синтеза, использовалось для синтеза аналогов инофиллума.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ СЕЛЕКТИВНОГО ВВЕДЕНИЯ ЗАЩИТНЫХ ГРУПП В ПРОИЗВОДНЫЕ РЕЗОРЦИНА | 2019 |
|
RU2738408C1 |
| НОВЫЕ ЗАМЕЩЕННЫЕ 8-ГЕТЕРОАРИЛКСАНТИНЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2004 |
|
RU2357969C2 |
| СОЕДИНЕНИЯ ИНДОЛА И ИНДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРА НЕКРОЗА КЛЕТКИ | 2008 |
|
RU2437883C1 |
| ФОСФОИНДОЛЫ КАК ИНГИБИТОРЫ ВИЧ | 2005 |
|
RU2393163C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИНДОЛ-5-ОЛА И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2013 |
|
RU2674249C2 |
| ЗАМЕЩЕННЫЕ ИМИДАЗОПИРИДИНИЛ-АМИНОПИРИДИНОВЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ РАКА | 2010 |
|
RU2619463C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛОПИРИМИДИНЫ И ЗАМЕЩЕННЫЕ ПУРИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ УБИКВИТИН-СПЕЦИФИЧЕСКОЙ ПРОЦЕССИРУЮЩЕЙ ПРОТЕАЗЫ 1 (USP1) | 2019 |
|
RU2833222C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2001 |
|
RU2340611C2 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ BRD4 | 2016 |
|
RU2721120C2 |
| СПОСОБ СИНТЕЗИРОВАНИЯ НОВОГО ХИРАЛЬНОГО ЛИГАНДА, ХЕЛАТА МЕТАЛЛА, РАЗЛИЧНЫХ НЕПРИРОДНЫХ АМИНОКИСЛОТ, МАРАВИРОКА И ЕГО ОСНОВНЫХ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ | 2017 |
|
RU2727723C1 |
Изобретение относится к способу получения кумаринов формулы (I) механохимической активацией при истирании в шаровой мельнице соединения формулы (II) с соединением (III), где реакцию проводят без растворителя в присутствии 10 мол.% кислотного катализатора, где R1 представляет собой водород; R2 представляет собой С1-С6 алкил, С6 арил; R3 представляет собой H или ОН; R5 представляет собой ОН; R4 и R6 представляют собой H, и где кислотный катализатор представляет собой С1-С6 алкил-SO3H. Технический результат изобретения - эффективный, масштабируемый, экологически чистый, механохимический синтез производных кумарина из фенолов и β-кетоэфиров при температуре окружающей среды без использования растворителей. 5 з.п. ф-лы, 3 табл., 71 пр.
1. Способ получения кумаринов механохимической активацией синтеза соединения формулы (III) при взаимодействии с соединением формулы (II) с получением соединения формулы (I):
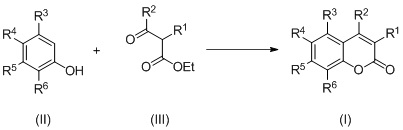
где R1 представляет собой водород;
R2 представляет собой С1-С6 алкил, С6 арил;
R3 представляет собой H или ОН;
R5 представляет собой ОН;
R4 и R6 представляют собой H;
где реакцию проводят без растворителя при истирании соединений (II) и (III) в шаровой мельнице;
в присутствии 10 мол.% кислотного катализатора, где кислотный катализатор представляет собой С1-С6 алкил-SO3H.
2. Способ по п.1, где R3 представляет собой OH.
3. Способ по п.1, где R3 представляет собой атом водорода.
4. Способ по любому из пп.1-3, где R2 представляет собой С1-С6 алкил.
5. Способ по любому из пп.1-3, где R2 представляет собой С6 арил.
6. Способ по любому из пп.1-5, где кислотный катализатор представляет собой CH3SO3H.
| Teizo Sugino and Koichi Tanaka "Solvent-Free Coumarin Synthesis", Chemistry Letters, 2001, рр | |||
| Прибор, автоматически записывающий пройденный путь | 1920 |
|
SU110A1 |
| Дж | |||
| Ли "Именные реакции | |||
| Механизмы органических реакций" | |||
| Пер | |||
| с англ | |||
| В.М | |||
| Демьянович, М., БИНОМ, Лаборатория знаний, 2006, 456 с., стр | |||
| Способ изготовления гибких труб для проведения жидкостей (пожарных рукавов и т.п.) | 1921 |
|
SU268A1 |
| Sarkar, A., Santra, S., Kundu, S | |||
| et al | |||
| "A decade update on solvent and catalyst-free organic neat | |||
Авторы
Даты
2023-07-06—Публикация
2022-05-12—Подача