Изобретение относится к органической химии, конкретно к синтезу пара-ацетиламинофенола (парацетамола, ацетаминофена, N-(4-гидроксифенил)ацетамида), который применяется в медицине в качестве анальгезирующего и жаропонижающего средства.
Пара-ацетиламинофенол (парацетамол, ацетаминофен) обычно получают ацетилированием пара-аминофенола - ключевого интермедиата в синтезе пара-ацетиламинофенола:
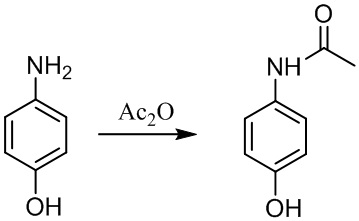
Пара-аминофенол в свою очередь может быть получен разными способами: восстановлением пара-нитрофенола, восстановлением пара-нитрозофенола.
Промышленный способ получения парацетамола заключается в восстановлении пара-нитрофенола до пара-аминофенола и ацетилировании последнего уксусным ангидридом. При этом пара-нитрофенол получают либо прямым нитрованием фенола [US 3663261 (1973), US 3517075 (1971), US 3510527 (1971)] либо последовательно нитрованием хлорбензола и щелочным гидролизом образующегося пара-нитрохлорбензола [US 3263011 (1966); M. Takasaki, Y. Motoyama, K. Higashi, S.-H.Yoon, I. Mochida, H. Nagashima, Org. Lett. 2008, 10, 1601-1604; M. Li, L. Hu, X. Cao, H. Hong, J. Lu and H. Gu, Chem. Eur. J. 2011, 17, 2763-2768]. Общими недостатками этих способов являются многостадийность, образование большого количества солей, а также неселективность реакции нитрования, приводящая к образованию смеси орто- и пара-нитрофенолов, требующая разделения орто- и пара-изомеров перегонкой с водяным паром.
Еще один способ получения пара-аминофенола - гидрирование нитробензола до фенилгидроксиламина, превращающегося в кислых условиях через перегруппировку Бамбергера в ключевой пара-аминофенол [C. V. Rode, M. J. Vaidya, R. Jaganathan and R. V.Chaudhari, Chem. Eng. Sci. 2001, 56, 1299-1304; J. M. Nadgeri, N. S. Biradar, P. B. Patil, S. T. Jadkar, A. C. Garade and C. V. Rode, Ind. Eng. Chem. Res. 2011, 50, 5478-5484.]. Недостатками этого способа являются образование большого количества сульфатных солей, а также побочного продукта - анилина.

Пара-аминофенол можно получить восстановлением пара-нитрозофенола в этилацетате в присутствии катализатора Pd/C при давлении водорода 2,0-4,- атм и температуре 20-50°С [RU 2461543 (2012)]. Недостатком способа метода является труднодоступность исходного пара-нитрозофенола, проведение процесса под давлением, использование дорогостоящего катализатора (Pd), а также экологически небезопасных растворов концентрированных кислот (HCl, HNO3) и щелочей.
Известен способ получения пара-аминофенола путем фотоокисления ароматических аминов кислородом при облучении видимым светом в водно-органическом растворителе в присутствии активных и стабильных фотосенсибилизаторов, представляющих собой замещенные фталоцианины [RU 2567552 (2015)]. Выход пара-аминофенола составляет 70%. Однако данный способ предполагает использование сложного специального оборудования - лазера или светодиодов.
Пара-ацетиламинофенол может быть получен амидированием гидрохинона ацетамидом [R. Joncour, N. Duguet, E.  , A. Ferreira, M. Lemaire. Amidation of phenol derivatives: a direct synthesis of paracetamol (acetaminophen) from hydroquinone. Green Chemistry, Royal Society of Chemistry, 2014, 16, pp.2997-3002.]. К недостаткам способа можно отнести высокую температуру процесса, длительность реакции, а также образование побочного пара-аминофенола.
, A. Ferreira, M. Lemaire. Amidation of phenol derivatives: a direct synthesis of paracetamol (acetaminophen) from hydroquinone. Green Chemistry, Royal Society of Chemistry, 2014, 16, pp.2997-3002.]. К недостаткам способа можно отнести высокую температуру процесса, длительность реакции, а также образование побочного пара-аминофенола.

Наиболее близким к заявляемому способом получения орто- и пара-аминофенолов является двухстадийный процесс, на первой стадии которого анилин окисляют персульфатом аммония в щелочной среде при 40-60°С, в присутствии 0,01-0,03 вес% фталоцианинового катализатора окисления (фталоцианина кобальта, железа (II), железа (III), марганца, никеля или цинка), с последующим охлаждением реакционной смеси, выделением промежуточных 4(2)-аминофенилсульфатов. При гидролизе последних в кислой среде при 85-95°С получают смесь орто- и пара-аминофенолов, из которой орто-аминофенол выделяют экстракцией хлороформом. Пара-аминофенол остается в водной фазе. В зависимости от продолжительности окисления анилина выход и соотношение образующихся орто- и пара-изомеров варьируется. Максимальный выход пара-аминофенола (72%) достигается при продолжительности окисления анилина 15 ч, при этом их реакционной смеси выделен также орто-аминофенол (13%) (Заявка на патент РФ №2021130569).

Задача, на решение которой направлено настоящее изобретение, заключается в увеличении выхода целевого соединения и упрощении технологии его получения.
Поставленная задача решается предлагаемым способом получения пара-аминофенола - ключевого соединения в синтезе пара-ацетиламинофенола. Анилин окисляют двумя окислителями - персульфатом аммония (ПСА) или калия (ПСК) или натрия (ПСН) и пероксидом водорода, в щелочной среде при мольном соотношении Анилин:NaOH:ПСА (ПСК, ПСН):Н2О2 равном 1:5:1,5:2 при 40-50°С в течение 10 ч при непрерывном барботировании воздухом через реакционную массу. Затем реакционную смесь охлаждают до комнатной температуры, гидролизуют соляной кислотой при 85-95°С и получают пара-аминофенол с выходом до 95 %.
Оптимальная продолжительность окисления анилина - 10-12 ч. При окислении менее 10 ч наблюдается уменьшение конверсии, образуется смесь орто- и пара-аминофенолов, При увеличении продолжительности окисления больше 12 ч выход пара-аминофенола также снижается, вероятно вследствие протекания побочных процессов.

Сущность заявленного технического решения подтверждается примерами конкретного выполнения.
Пример 1. Получение пара-аминофенола (табл. 1, п. 5)
В трехгорлой колбе, снабженной барботером, капельной воронкой, обратным холодильником и механической мешалкой, перемешивают 5 мл (0,055 моль) анилина в 30 мл дистиллированной воды при 40°С до полного растворения анилина, затем в реакционную смесь приливают раствор 11 г NaOH (0,275 моль) в 70 мл воды и прикапывают раствор 18,7 г (0,082 моль) персульфата аммония в 40 мл воды. После полного прибавления персульфата аммония прикапывают 10 мл 30%-ного пероксида водорода (0,11 моль) и начинают барботаж воздуха. Реакционную смесь перемешивают при температуре 40°С в течение 10 ч при непрерывном барботировании воздухом, охлаждают до комнатной температуры, экстрагируют этилацетатом (2×30 мл) для удаления непрореагировавшего анилина. В водную фракцию прикапывают 3,34 мл (0,11 моль) соляной кислоты, нагревают до 90°С и выдерживают при этой температуре при постоянном перемешивании в течение 3 ч, контролируя по ТСХ (элюент этанол:аммиак 4:1), охлаждают до комнатной температуры, подщелачивают раствором NaHCO3 до рН 7-8, экстрагируют хлороформом (3×20 мл), органический слой сушат MgSO4, после удаления растворителя получают 0% орто-аминофенола.
Водную фазу упаривают досуха, остаток растворяют в этиловом спирте, этанольный экстракт упаривают при пониженном давлении и получают 5,7 г (95%) пара-аминофенола в виде светло-коричневых кристаллов. В пересчете на исходный анилин выход пара-аминофенола составляет 95%.
Пара-аминофенол. Кристаллы светло-коричневого цвета. Тпл = 185-188 оС. Спектр ЯМР 1Н (DMSO-d6, δ, м.д.): 4.37 (2Н, уш. с, NH2), 6.37-6.44 (2Н, м, ArH), 6.44-6.50 (2Н, м, ArH), 8.33 (1Н, уш. с, ОН). Спектр ЯМР 13С (DMSO-d6, δ, м.д.): 115.90, 116.08 (4 СН, ArH), 140.97 (C-NH2), 148.80 (C-OH).
Пример 2. Ацилирование пара-аминофенола.
В круглодонную колбу, снабженную обратным холодильником, мешалкой и капельной воронкой, помещают 3,1 г (0,028 моль) пара-аминофенола, 10 мл воды и осторожно прикапывают 4 мл уксусного ангидрида. Реакционную смесь перемешивают до полного растворения пара-аминофенола, затем нагревают в течение 10 мин. Реакционную смесь охлаждают, (внешнее охлаждение, ледяная баня). Образовавшийся кристаллический осадок отфильтровывают, промывают небольшим количеством ледяной воды, сушат на воздухе. Получают 4,08 г (90%) пара-ацетиламинофенола.
Пара-ацетиламинофенол. Кристаллы белого цвета. Т пл 169-171°С. Спектр ЯМР 1Н (DMSO-d6, δ, м.д.): 1.98 (с, 3Н, СН3), 6.62 (д, 2Н, J=4.5 Гц), 7.30 (д, 2Н, J=4.5 Гц), 8.86 (с, 1Н, NH), 9.47 (с, 1Н, ОН) Спектр ЯМР 13С (DMSO-d6, δ, м.д.): 24.0 (СН3), 116.1, 123.0 (4 СН, ArH), 131.1 (C-NH), 154.1 (C-OH), 168.9 (С=О).
Суммарный выход пара-ацетиламинофенола (в пересчете на исходный анилин) - 85,5%.
Таким образом, предложен удобный способ получения пара-ацетиламинофенола (парацетамола), позволяющий существенно увеличить выход целевого соединения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Эффективный способ получения орто- и пара-аминофенолов | 2022 |
|
RU2800093C1 |
| Способ получения орто- и пара-аминофенолов | 2022 |
|
RU2793758C1 |
| Способ получения аминофенолов | 2022 |
|
RU2800099C1 |
| Способ получения орто- и пара-аминофенолов | 2021 |
|
RU2786515C1 |
| Способ получения 5-гидрокси-6-метилурацила | 2022 |
|
RU2806327C1 |
| Способ получения гидрохинона | 2022 |
|
RU2784427C1 |
| СПОСОБ ПОЛУЧЕНИЯ п-АЦЕТИЛАМИНОФЕНОЛА | 2012 |
|
RU2495865C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПАРАЦЕТАМОЛА | 2011 |
|
RU2461543C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПАРАЦЕТАМОЛА | 2014 |
|
RU2574733C1 |
| Способ получения 5-гидрокси-6-метилурацила | 2018 |
|
RU2700687C1 |
Изобретение относится к органической химии, конкретно к синтезу пара-ацетиламинофенола (парацетамола), применяемому в медицине в качестве анальгезирующего и жаропонижающего средства. Способ получения пара-ацетиламинофенола заключается в окислении анилина с последующим ацилированием образующегося пара-аминофенола и выделением целевого продукта, характеризуется тем, что для повышения выхода процесс окисления анилина персульфатом аммония (ПСА), или калия (ПСК), или натрия (ПСН) ведут в присутствии второго окислителя пероксида водорода при мольном соотношении анилин:ПСА (ПСК, ПСН):Н2О2 1:1,5:2 при 40-50°С в течение 10-12 ч при непрерывном барботировании реакционной смеси воздухом. Техническим результатом изобретения является увеличение выхода целевого соединения и упрощение технологии его получения. 3 табл., 2 пр.
Способ получения пара-ацетиламинофенола путем окисления анилина с последующим ацилированием образующегося пара-аминофенола и выделением целевого продукта, отличающийся тем, что для повышения выхода процесс окисления анилина персульфатом аммония (ПСА), или калия (ПСК), или натрия (ПСН) ведут в присутствии второго окислителя пероксида водорода при мольном соотношении Анилин:ПСА (ПСК, ПСН):Н2О2 1:1,5:2 при 40-50°С в течение 10-12 ч при непрерывном барботировании воздухом.
| E | |||
| Boyland, P | |||
| Sims | |||
| J | |||
| Chem., Soc, 1958, p.4198 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПАРА-АМИНОФЕНОЛОВ | 2014 |
|
RU2567552C1 |
| B | |||
| Marajanovic, I | |||
| Juranic, C | |||
| Ciric-Marjanovic Reply to "Comment on 'Revised Mechanism of Boyland-Sims Oxidation", journal Physical Chemistry, 2011, p.7865-7868 | |||
| N | |||
| Venkatasubramanian, A | |||
| Sabesan "Substituent effects in the reaction of aromatic amines and | |||
Авторы
Даты
2023-07-18—Публикация
2022-11-18—Подача