Область техники
Изобретение относится к области материаловедения, а именно к разработке подхода к получению фосфатов, оксофосфатов и фторидофосфатов ванадия с использованием органических восстановителей. Указанные соединения могут быть использованы как материалы для создания металл-ионных аккумуляторов.
Уровень техники
Развитие множества современных портативных устройств, электротранспорта, а также необходимость накопления электроэнергии на различных производствах и в частных домохозяйствах неразрывно связано с технологиями химических источников тока (ХИТ). На сегодняшний день для решения задач такого рода в подавляющем большинстве случаев используются литий-ионные аккумуляторы (ЛИА). Вместе с тем, нехватка ресурсов лития и ряд проблем, связанных с их неравномерным распределением, привели к развитию альтернативных технологий запасания энергии, таких как натрий- и калий- ионные аккумуляторы, далее НИА и КИА соответственно, которые в свою очередь классифицируются научным сообществом не как конкурентные, а как взаимодополняющие технологии [Tarascon, J.М. (2020). Na-ion versus Li-ion batteries: complementarity rather than competitiveness. Joule, 4(8), 1616-1620.], [Tian, Y., Zeng, G., Rutt, A., Shi, Т., Kim, H.,Wang, J., & Ceder, G. (2020). Promises and challenges of next-generation "beyond Li-ion" batteries for electric vehicles and grid decarbonization. Chemical reviews, 121(3), 1623-1669.]. Указанные группы накопителей имеют общий принцип работы: во всех случаях металл-ионный аккумулятор (МИА) состоит из положительного и отрицательного электродов (далее катод и анод соответственно), сепаратора, пропитанного электролитом, и герметичного корпуса.
Положительный электрод (катод) является основным компонентом МИА, ограничивающим его энергетические характеристики, главным образом, энергоемкость. [Abakumov, А.М., Fedotov, S.S., Antipov, Е.V., & Tarascon, J. М. (2020). Solid state chemistry for developing better metal-ion batteries. Nature Communications, 77(1), 1-14]. Каркасные соединения, содержащие фосфатную группу, в частности, фосфаты, оксо-, фторидо-фосфаты на сегодняшний день вызывают повышенное внимание исследователей, поскольку могут демонстрировать выдающиеся характеристики структурной стабильности и безопасности. Устойчивость кристаллической структуры позволяет обеспечить стабильное циклирование аккумулятора в течение тысяч циклов.
Одним из структурных типов, представляющим интерес для дизайна и создания материалов МИА нового поколения являются фосфаты, принадлежащие к семейству калий-титанил фосфата (далее «структура KTiOPO4» или «КТФ» или «структурный тип KTiOPO4»). Общая формула класса представляется как АМРО4Х (А=Li, Na, K, Rb, Ag, Cs, Tl или их смесь, М=V, Fe, Mn, Ti, Co, Cr, Al, Sc, Ga или их смесь, X=F, О или их смесь) [Fedotov, S.S., Samarin, A. S., & Antipov, Е. V. (2020). KTiOPO4-structured electrode materials for metal-ion batteries: A review. Journal of Power Sources, 480, 228840.]. Наибольший практический интерес из указанных составов и принадлежащих к структурному типу КТФ, представляют натриевые соединения (в качестве катодов МИА), синтез которых, как было показано ранее [Патент RU 2748159 С1 Электродный материал для натрий-ионных аккумуляторов, способ его получения, электрод и аккумулятор на основе электродного материала. Заявка от 11.12.2020, Опубл. 20.05.2021], [Shraer, S.D., Luchinin, N.D., Trussov, I.A., Aksyonov, D.A., Morozov, A.V., Ryazantsev, S.V., & Fedotov, S.S. (2022). Development of vanadium-based polyanion positive electrode active materials for high-voltage sodium-based batteries. Nature Communications, 73(1), 1-10.] прямыми методами невозможен. Кроме того, литиевые и калиевые соединения структурного типа КТФ также представляют интерес, в частности, углеродный композит на основе состава K0.15VPO4F демонстрирует стабильное циклирование ионов Li+при высоких плотностях тока с сохранением более 50% исходной емкости [Fedotov, S. S., Khasanova, N. R., Samarin, A. S., Drozhzhin, O. A., Batuk, D., Karakulina, О. M., Antipov, E. V. (2016). AVPO4F (A=Li, K): a 4 V cathode material for high-power rechargeable batteries. Chemistry of Materials, 28(2), 411-415.], [Патент Ru 2619600 C2 Электродный материал для металл-ионных аккумуляторов, способ его получения, электрод и аккумулятор на основе электродного материала. Заявка от 28.09.2015, Опубл. 17.05.2017]. Углеродные композиты на основе составов KA'PO4F (А'=Ti, V) являются примерами рекордно высоких величин рабочего потенциала соответствующей окислительно-восстановительной пары (Ti4+/Ti3+, V4+/V3+). Таким образом, емкостные и мощностные характеристики углеродных композитов на основе составов KMPO4X (X=О, F) позволяют рассматривать их как основу для создания прототипов высокомощных КИА [Fedotov, S. S., Luchinin, N. D., Aksyonov, D. A., Morozov, A. V., Ryazantsev, S. V., Gaboardi, M., Antipov, E. V. (2020). Titanium-based potassium-ion battery positive electrode with extraordinarily high redox potential. Nature communications, 11(1), 1-11.], Kim, H., Seo, D. H., Bianchini, M., Clement, R. J., Kim, H., Kim, J. C, Ceder, G. (2018). A New Strategy for High-Voltage Cathodes for K-lon Batteries: Stoichiometric KVPO4F. Advanced Energy Materials, 8(26), 1801591.], [Патент US 11145863 B2 Positive electrode active material for potassium ion battery, positive electrode for potassium ion battery, and potassium ion battery Опубл. 2021-10-12].
Вследствие невозможности синтеза большинства рассматриваемых составов прямыми химическими методами, зачастую проводят их двухэтапное получение через соединение прекурсора с нужным структурным типом. Метод получения аммонийсодержащего прекурсора, указанный в патенте [Патент RU 2748159 С1 Электродный материал для натрий-ионных аккумуляторов, способ его получения, электрод и аккумулятор на основе электродного материала. Заявка от 11.12.2020, Опубл. 20.05.2021], требует использования токсичных соединений азота, в частности, (NH2)2CNH, N2H6SO4, N2H5Cl, NH2OH, или N2H4⋅H2O. Кроме того, для синтеза аммоний-содержащего прекурсора требуется смесь двух фосфатов аммония (NH4H2PO4, (NH4)2HPO4) в определенном избытке относительно количеств ванадия. Это неизбежно приводит к потерям фосфат-анионов в процессе синтеза (соотношение переходный металл:фосфор в «аммоний-содержащем прекурсоре» составляет 1:1). Из близких по тематике работ, связанных с синтезом аммонийсодержащего прекурсора с целью дальнейшего получения материала МИА (в частности, НИА) можно отметить [Buyuker, I., Hidalgo, M.F.V., Zuba, М., Diamint, J., Zhou, H., Chernova, N. A., & Whittingham, M. S. (2021), Journal of The Electrochemical Society, 168, 050513], [Chernova, N. A., Hidalgo, M. F. V., Kaplan, C, Lee, K., Buyuker, I., Siu, C, Whittingham, M. S. (2020), Advanced Energy Materials, 10, 2002638.]. Аммоний-содержащий прекурсор - NH4VOPO4 (структурный тип КТФ) был получен гидротермальным методом. Для этого 0.455 г V2O5 (>98%) и 2.64 (NH4)2HPO4 (>99.0%) были внесены в 53.5 мл воды (соотношение V:P:H2O составляет 1:4:600). Далее было добавлено 9.5 мл этилового спирта. Смесь была перенесена в тефлоновый автоклав объемом 125 мл и выдерживалась в течение 72 часов при температуре 200°С. В результате был получен порошок коричневого цвета NH4VOPO4 (дополнительно промыт водой и спиртом). Ионный обмен катиона NH4+ на Na+ проводили в избытке NaBr в среде этиленгликоля или тетраэтиленгликоля в течение 24 часов, однако, по данным ИК-спектроскопии и порошковой рентгеновской дифракции этот метод не позволяет добиться количественного протекания реакции. Авторы работы связывают это с размером частиц (10-15 мкм).
Недостатком данного подхода является длительное время синтеза, необходимость использования 4-х кратного избытка фосфат-анинов по отношению к ионам ванадия, рост частиц сравнительного большого размера, что в дальнейшем будет негативно сказываться на электрохимических характеристиках конечного материала.
Синтез фторированного аналога указанного выше соединения - NH4VPO4F, за исключением методики, ссылка на которую была указана ранее [RU 2748159 С1], также является нецелесообразным с технологической точки зрения. Авторы работы [Alda, Е., Bazan, В., Mesa, J. L, Pizarro, J. L, Arriortua, M. I., & Rojo, T. (2003), Journal of solid state chemistry, 173, 101-108.] проводили обработку смеси V2O3, H3PO4 и HF в мольном соотношении 1:4:42 при рН=6.0 в водной среде в течение 120 часов при температуре 170°С в герметичной тефлоновой емкости объемом 30 мл при заполнении 75%. Оксид ванадия (III), V2O3, является дорогостоящими реагентом в сравнении с пентаоксидом (V2O5), использование 21-кратного избытка фторид-анионов является значительным препятствием с технологической точки зрения. Кроме того, плавиковая кислота является крайне токсичным и опасным реагентом. Длительность указанного синтеза неизбежно приводит к росту крупных частиц (в среднем длина достигает порядка 0.1 мм), что будет оказывать негативное влияние на мощностные свойства конечного материала, и не позволяет отнести данный метод к энергоэффективному [Feng S. Н., Li G. Н. Hydrothermal and solvothermal syntheses //Modern inorganic synthetic chemistry. - Elsevier, 2017. - C. 73-104].
Исходя из представленного обзора, можно заключить, что поиск новых методик синтеза, не требующих применения токсичных реагентов, и/или позволяющих уменьшить их количества, необходимые для получения однофазных образцов, оказывается актуальным. В частности, относительно указанных выше объектов, задача получения «аммонийсодержащего прекурсора» и конечного соединения без применения солей гидразина и/или гидроксиламина является новой и представляет значительный практический интерес.
Проведенный анализ уровня техники продемонстрировал, что заявленная совокупность существенных признаков, раскрывающих суть изобретения и изложенных в формуле изобретения, неизвестна. Это позволяет сделать вывод о ее соответствии критерию «новизна».
Раскрытие изобретения
Целью реализации данного изобретения является разработка группы методик получения высокоемких (удельная энергоемкость >450 Вт⋅ч⋅кг-1) электродных материалов для металл-ионного аккумулятора, отличающихся применением органических восстановителей вместо использования восстановителей на основе солей гидразина и/или гидроксиламина.
Техническим результатом изобретения является увеличение удельной емкости и снижение вредных выбросов в окружающую среду.
Ниже представлены способы реализации настоящего изобретения с указанием достигаемых технических результатов.
В соответствии с первым вариантом осуществления, заявленное изобретение относится к способу получения поликристаллического порошка активного электродного материала состава AV1-xMxPO4(F1-yOy), где А - по крайней мере один щелочной металл, выбранный из группы Li, Na, K, М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь, а 0≤х≤1 и 0≤у≤1.
Способ порошка активного электродного материала включает следующие стадии:
1) получение соединения-прекурсора, описываемого общей формулой (NH4)1-zAzV1-xMxPO4(F1-yOy), где А - по крайней мере один металл, выбранный из группы K, Са, Ва, М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь, a 0≤x≤1 и 0≤у≤1, гидро- или сольвотермальным способом, который включает в себя перемешивание в интервале температур 170-230°С в течение 10-20 часов раствора в деионизованной воде и/или в смеси вода-спирт, содержащего соль или оксид переходного металла М (MtOk, где t и к целые числа), дигидрофосфат аммония NH4H2PO4, органический восстановитель катионов ванадия и аммиак. В случае получения прекурсора с повышенной термической стабильностью раствор может содержать также соли калия, кальция или бария. При этом под понятием спирт подразумевается одно из следующих соединений: метиловый спирт (СН3ОН), этиловый спирт (С2Н5ОН), изопропиловый спирт (С3Н7ОН), бутиловый спирт (С4Н9ОН), этиленгликоль (НО-СН2-СН2-ОН), триэтиленгликоль (C6H14O4), тетраэтиленгликоль (C8H18O5). Объемное соотношение воды и спирта составляет от 50:50 до 99:1.
2) гомогенизация с помощью мельницы соединения прекурсора с солью лития, натрия, калия или их смесью с последующей термической обработкой (100-500°С) на воздухе или в инертной атмосфере.
В частном варианте реализации реакционная смесь, подвергаемая нагреву, находится в герметично закрытом реакторе, изготовленном из тефлона. Также герметичная вставка и/или реактор целиком могут быть изготовлены из инертной стали марки Inconel (в том числе, но не ограничиваясь Inconel 718) и/или Хастеллой (в том числе, но не ограничиваясь Хастеллой С-276). Использование герметичного реактора позволяет воздействовать на реакционную смесь повышенными давлениями при заданных температурах.
Смесь получения соединения-прекурсора дополнительно содержит компоненты из следующей группы: NH4F, NH4HF2, HF, Н2С2О4 (щавелевая кислота), Н2С2О4⋅2Н2О (дигидрат щавелевой кислоты), С6Н8О7 (лимонная кислота), С6Н8О7⋅Н2О (моногидрат лимонной кислоты), С6Н8О6 (аскорбиновая кислота), C6H7O6Na (аскорбат натрия), (NH4)2C2O4, Na3C6H5O7 (цитрат натрия), (NH4)3C6H5O7 (цитрат аммония), С3Н4О4 (пропандиовая кислота), С4Н6О4 (бутандиовая кислота). В качестве соли щелочного металла используется одна из солей из списка или их смесь: CH3COOLi (ацетат лития), LiBr (бромид лития), Li2C2O4 (оксалат лития), LiNO3 (нитрат лития), C6H7O6Li (аскорбат лития), Na2C2O4 (оксалат натрия), C5H8NO4Na (глутамат натрия), HCOONa (формиат натрия), HOCH2(CHOH)4COONa (глюконат натрия), C3H2Na2O4 (малонат натрия), CH3COOK (ацетат калия), KBr (бромид калия), K2CO3 (карбонат калия). В качестве источника катиона переходного металла используется оксид, алкоксид и/или соль соответствующего переходного металла.
Одним из вариантов осуществления изобретения, является синтез частиц активного электродного материала размером от 1 до 20 мкм, полученных способом согласно настоящему изобретению. Соединение описывается общей формулой (NH4)1-zAzV1-xMxPO4(F1-yOy), где А - по крайней мере один металл, выбранный из группы K, Са, Ва, М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь, a 0≤x≤1 и 0≤у≤1.
Еще одним вариантом изобретения является способ получения проводящего композитного активного электродного материала формулы AV1-xMxPO4(F1-yOy)/C, где А - по крайней мере один щелочной металл, выбранный из группы Li, Na, K, М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn, a 0≤x≤1 и 0≤y≤1, при этом способ включает следующие стадии:
a) получение аммонийсодержащего прекурсора AV1-xMxPO4(F1-yOy), где М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn; 0≤x≤1, 0≤y≤1, сольво- или гидротермальным способом при постоянном перемешивании исходных компонентов при температуре 150-250°С и давлении не более 60 атм в течение 1-48 часов, при этом в качестве исходных компонентов используют источник переходного металла - соль или оксид переходного металла; источника фосфора - по крайней мере один фосфат выбранный из группы: NH4H2PO4, (NH4)2HPO4 (NH4)3PO4; фторирующий агент - по крайней мере один фосфат выбранный из группы: HF, NH4F, NH4HF2; органическая кислота-восстановитель, выбранная из группы: H2C2O4, C6H8O7, С4Н6О6, СН2О2 или их гидраты; растворитель - дистиллированная вода или водно-спиртовой раствор, содержащий вышеуказанные соль или оксид переходного металла, источник фосфора, фторирующий агент, органическую кислоту-восстановитель;
b) получение материала формулы AV1-xMxPO4(F1-yOy), где А - по крайней мере один щелочной металл, выбранный из группы Li, Na, K, М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn, a 0≤x≤1 и 0≤y≤1, при смешивании полученного аммоний-содержащего прекурсора с по крайней мере одной легкоплавкой солью щелочного металла, выбранной из группы; ацетат лития, нитрат лития, бромид лития, оксалат лития, аскорбат лития, глутамат натрия, оксалат натрия, формиат натрия, малонат натрия, ацетат натрия, нитрат натрия, карбонат натрия, ацетат калия, бромид калия, карбонат калия, с последующим нагревом смеси при температуре 100-500°С в атмосфере воздуха или аргона;
с) смешивание полученного материала на стадии b) с углеродсодержащей добавкой, содержащей по крайней мере один компонент, выбранный из группы: полиакрилонитрил или его раствор в растворителе, выбранном из группы: ДМФА, ДМСО, N-метилпирролидоне, и/или по крайней мере один компонент, выбранный из группы глюкоза, сахароза, поливинилпирролидон.
Еще одним вариантом изобретения является электродная масса, состоящая из частиц заявленного электрохимически активного электродного материала или его проводящего композита с углеродом и вспомогательного компонента. В контексте настоящего изобретения под понятием «вспомогательный компонент» подразумевается смесь, состоящая из не менее чем одной электропроводящей добавки и связующего компонента. Суммарное содержание электропроводящего компонента может варьироваться в пределах от 0.5 до 30 масс.%. Суммарное содержание связующего компонента может варьироваться в пределах от 0.5 до 15 масс. %.
В соответствии с еще одним вариантом осуществления, заявленное изобретение представляет собой электрод для аккумулятора, нанесенный на металлический токосъемник.
В соответствии с еще одним вариантом осуществления, заявленное изобретение представляет собой металл-ионный аккумулятор, содержащий положительный и отрицательный электрод, при этом положительный электрод (далее - катод) содержит частицы, описанные в примерах реализации изобретения 1-9, а отрицательный электрод (далее - анод) выполнен из неграфитизируемого углерода и/или свинца, и/или олова, и/или висмута, и/или сурьмы, и/или их сплавов в различных мольных соотношениях.
Краткое описание чертежей
Сущность изобретения демонстрируется следующими фигурами:
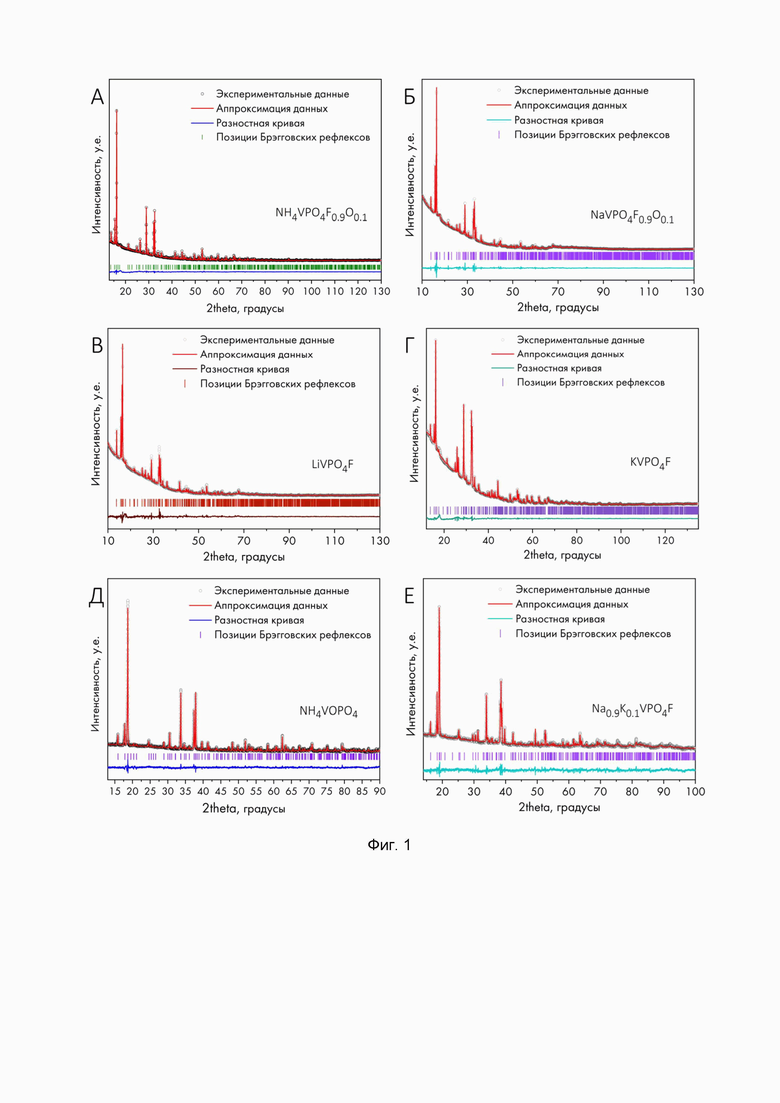
На фиг. 1 приведены дифрактограммы A) NH4VPO4F0.9O0.1; Б) NaVPO4F0.9O0.1, В) LiVPO4F, Г) KVPO4F (λ=1.5418 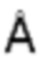 ), Д) NH4VOPO4F Е) Na0.9K0.1VPO4F (λ=1.78896
), Д) NH4VOPO4F Е) Na0.9K0.1VPO4F (λ=1.78896 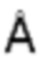 ), подтверждающие их однофазность.
), подтверждающие их однофазность.
На фиг. 2 приведены микрофотографии, полученные с помощью электронного микроскопа образцов A) NH4VPO4F0.9O0.1, Б) NaVPO4F0.9O0.1, В) NaVPO4F0.9O0.1/C, причем прекурсор NH4VPO4F0.9O0.1 был синтезирован при рН=6.8(±0.1).
На фиг. 3 приведены микрофотографии, полученные с помощью электронного микроскопа образцов A) NH4VPO4F0.75O0.25; Б) NaVPO4F0.75O0.25; причем прекурсор NH4VPO4F0.75O0.25 был синтезирован при рН=6.0(±0.1).
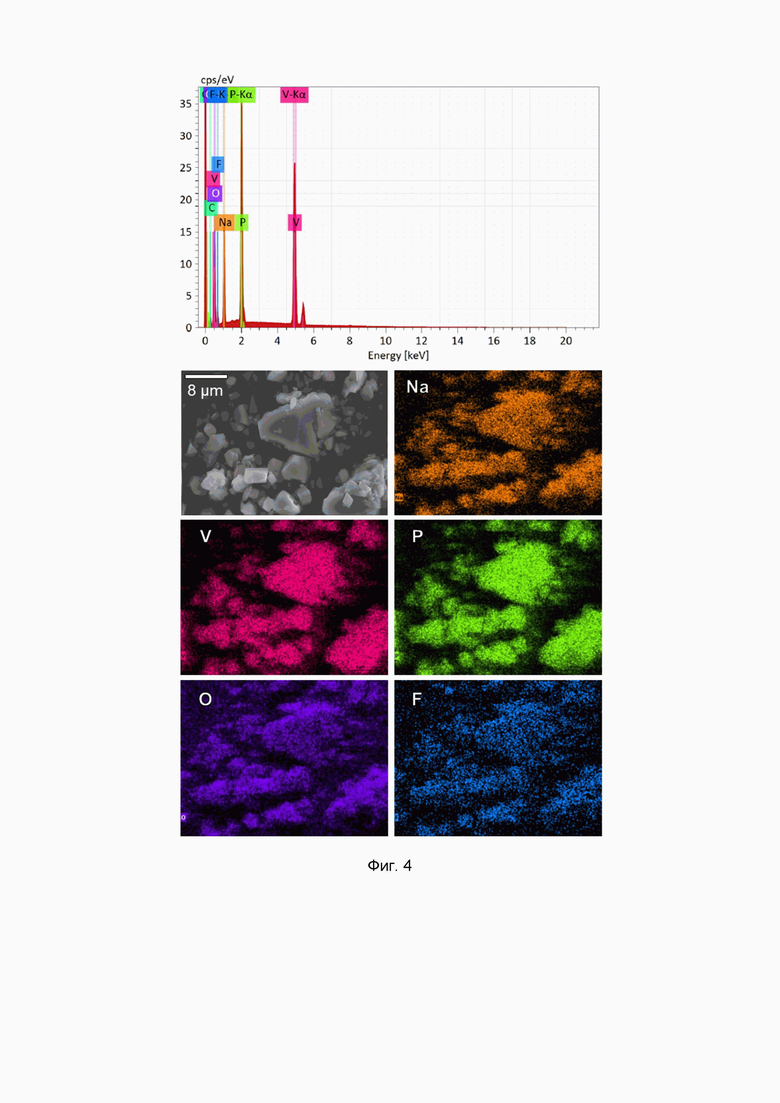
На фиг. 4 приведены данные локального рентгеноспектрального анализа (ЛРСМА) образца NaVPO4F0.9O0.1/C и результаты элементного картирования.
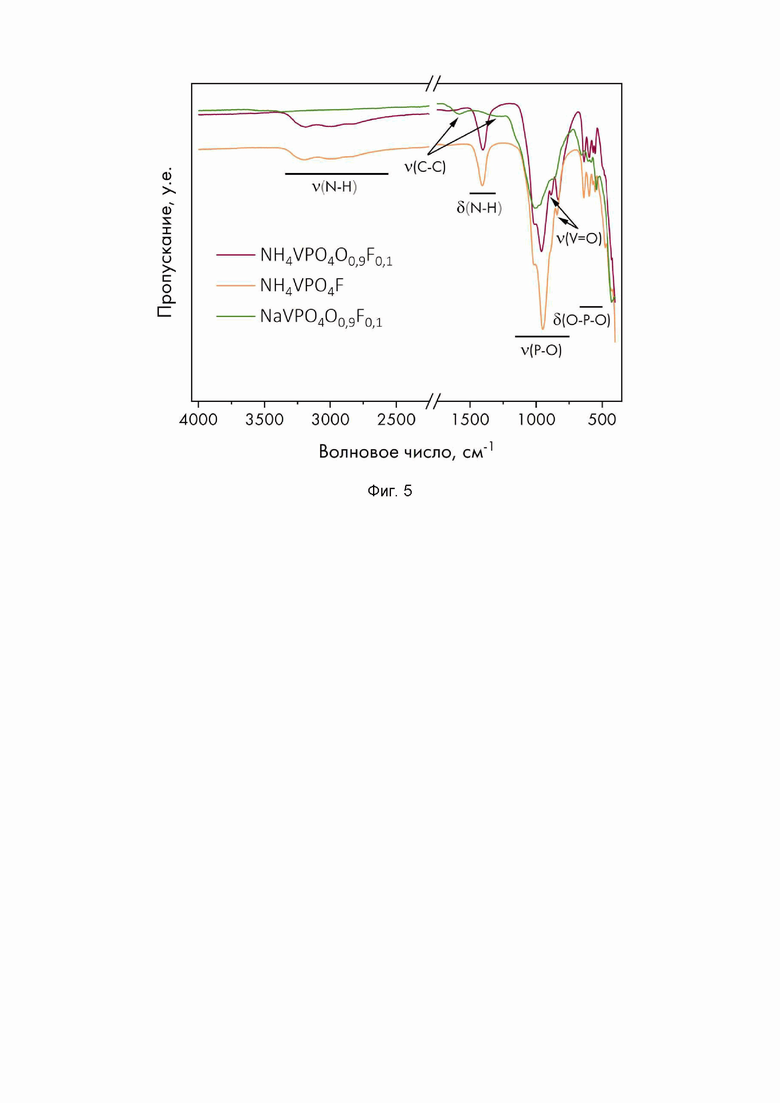
На фиг. 5 приведены ИК-спектры (режим нарушенного полного внутреннего отражения, НПВО) образцов NH4VPO4F0.9O0.1 и NaVPO4F0.9O0.1 полученных в соответствии с методикой примера 2. ИК-спектр NH4VPO4F приведен в качестве спектра сравнения.
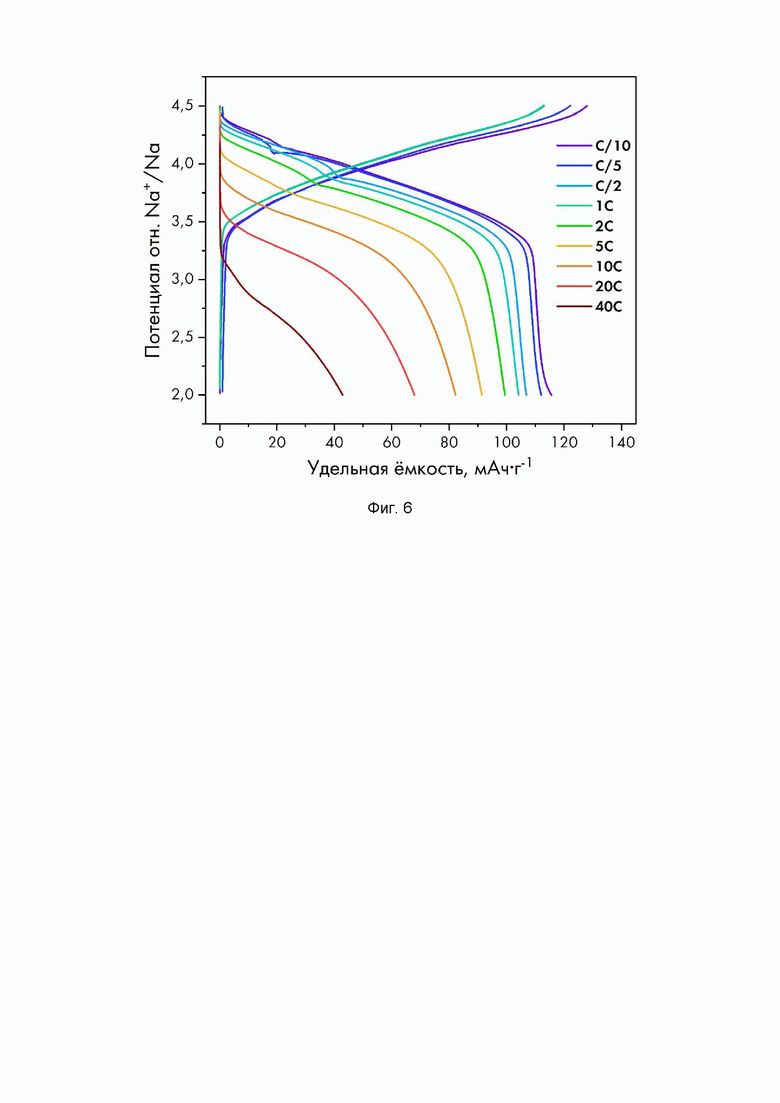
На фиг. 6 приведены данные циклирования композитного материала в гальваностатическом режиме в натриевой полуячейке в интервале потенциалов 2.0-4.5 В отн. Na+/Na (электролит - пропиленкарбонат (ПК): этиленкарбонат (ЭК)=1:1 с добавлением 5 об.% фторэтиленкарбоната (ФЭК), 1М NaPF6 чистотой не менее 99%) при комнатной температуре при различных скоростях циклирования от 0.1С (заряд/разряд за 10 часов) до 40С (заряд/разряд за 1.5 минуты), начиная со скорости 1С заряд проводился при скорости 0.5С (заряд за 2 часа).
Осуществление изобретения
В соответствии с заявленным изобретением в качестве электрохимически активного электродного материала выбраны соединения AV1-xMxPO4(F1-yOy), где А -по крайней мере один щелочной металл, выбранный из группы Li, Na, K, М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь, a 0≤x≤1 и 0≤у≤1. В качестве активного электродного композитного материала для натрий-ионных аккумуляторов рассматриваются составы AV1-xMxPO4(F1-yOy)/C, а 0≤х≤1 и 0≤у≤1. В указанных выше соединениях А - по крайней мере один щелочной металл, выбранный из группы Li, Na, K, М - по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь,). Рассматриваемые в рамках настоящего изобретения принадлежат к структурному типу «калий-титанил фосфат» (KTiOPO4, далее - КТФ). Кристаллическая структура орторомбического NaV1-xMxPO4(F1-yOy)/C (где М - по крайней мере один переходный металл, выбранный из группы Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь, a 0≤x≤1, 0≤x≤1) представляет собой цепочки из октаэдров MO4Y2 с общими вершинами, соединенные между собой узлами через тетраэдры PO4 в прочный трехмерный каркас. В полостях, образованных указанными полиэдрами, находятся ионы щелочного металла, в частности, Na+.
Синтез соединений, принадлежащих к данному структурному типу, проводится в две стадии, на первой проводится синтез аммониевого соединения (возможно также катионное легирование в позиции аммония) гидро-/сольво-термальным методом, на второй - ионный обмен катиона аммония (NH4+), на катион лития, натрия, калия или их смесь.
Структура и состав образцов описываемых составов исследованы необходимыми физико-химическими методами. Контроль полученной фазы осуществляли методом РФА на дифрактометре Bruker D8 Advance с использованием Cu-Kα излучения в интервале 2θ от 10 до 135°, а в ряде случаев с использованием камеры Гинье высокого разрешения Guinier Camera G670 производства компании Huber (Ge-монохроматор, Co-Kα1 излучение, интервал съемки 2θ 4-100°).
Степень замещения катиона аммония оценивали по данным ИК-спектров в режиме НПВО, которые регистрировали на автономном ИК-спектрометре-микроскопе LUMOS (Bruker), снабженном кристаллом германия и МСТ детектором, охлаждаемым жидким азотом.
Морфологию образцов исследовали при помощи РЭМ на сканирующем электронном микроскопе Quattro S (Thermo Fisher Scientific, катод LaB6, полевая эмиссия) в режиме детектирования вторичных электронов при ускоряющем напряжении 5-10 кВ. Анализ элементного состава проводился методом локального рентгеноспектрального микроанализа (ЛРСмА или ЛРСА) с помощью ЭДС-приставки Bruker (США) XFlash 6160 в указанном выше электронном микроскопе.
Для проведения электрохимических измерений готовилась однородная электродная паста, состоящая из 65-95 масс.% активного материала, 0.5-30 масс.% сажи (Carbon Super-C или Carbon Super Р), 0.5-5 масс.% промышленных углеродных нанотрубок (одностенные углеродные нанотрубки) и 0.5-15 масс.% полимерного связующего (раствор поливинилидендифторида в N-метилпирролидоне). Смесь равномерно наносится на алюминиевую фольгу (токосъемник), подвергается сушке и последующей прокатке на вальцах. Далее вырезались электроды диаметром 15 мм, измеряется их масса. Электроды подвергались сушке при пониженном давлении (10-2 атм.) при 100-120°С в течение 4-12 часов с целью удаления следовых количеств воды и/или органического растворителя. Исследования электрохимических свойств проводились в полуячейках (противоэлектродом является металлический литий, натрий или калий (для тестирования катодных материалов ЛИА, НИА или КИА, соответственно)) в органическом электролите: 1М NaPF6 или 1М NaClO4 (пропиленкарбонат (ПК):этиленкарбонат (ЭК)=1:1 с добавлением 0,5-10 об.% фторэтиленкарбоната (ФЭК)) при комнатной температуре, в качестве сепаратора используется боросиликатное стекло (glass fiber). В случае тестирования литиевой полуячейки используется электролит 1М LiPF6 (этиленкарбонат (ЭК):диэтилкарбонат(ДЭК) = 1:1 с добавлением 3% фторэтиленкарбоната (ФЭК)). В случае тестирования калиевой полуячейки используется электролит 0.5М KPF6 (пропиленкарбонат(ПК):этиленкарбонат = 1:1 с добавлением 3% фторэтиленкарбоната (ФЭК)). Сборку ячейки проводят в перчаточном боксе в атмосфере аргона (Ar) (рО2<0.1 ppm, pH2O<0.1 ppm, производства MBraun). Гальваностатическое циклирование проводится на потенциостате Biologic VMP-3 при помощи программного пакета EC-Lab.
Составы AMPC4O1-xFx (0≤х≤1) демонстрируют электрохимическую активность в интервале потенциалов 5.1-2.0 В отн. А+/А. В зависимости от выбора катиона переходного металла, а также величины × формулы, соединение может быть рассмотрено как материал положительного электрода (когда средний рабочий потенциал находится в области выше 3.0 В отн. А+/А), так и отрицательного (когда средний рабочий потенциал находится в области ниже 3.0 В отн. А+/А).
Электрохимические свойства составов продемонстрированы в серии последовательных измерений в гальваностатическом режиме с последовательным увеличением скорости циклирования от 0.1С (заряд/разряд за 10 часов) до 40С (заряд/разряд за 1.5 минуты).
В описании ниже приведен список реагентов и методов, которые могут быть использованы для осуществления настоящего изобретения, приведены примеры его реализации. Химические соединения и композиты на их основе, описываемые в рамках настоящего изобретения, являются продуктами химической промышленности и/или могут быть синтезированы с использованием коммерчески доступных реагентов.
В контексте настоящего изобретения термин «инертная атмосфера» подразумевает атмосферу газа - аргон, азот - и/или их смеси, которые не реагируют с веществами и/или продуктами их разложения, составляющими исходный материал.
Одним из частных вариантов реализации изобретения является двухстадийный синтез, первой стадией является получение «аммонийсодержащего прекурсора» путем обработки водного раствора реагентов при повышенных температурах (Т>100°С) и давлениях (р>1 атм). Возможно использование родственных методов, в частности сольвотермального и/или гидро-, сольво-термального с применением микроволнового излучения.
Реагенты, необходимые для получения «аммонийсодержащего прекурсора» являются многотоннажными продуктами химической промышленности. Для получения оксофосфатов используется соответствующее соединение переходного металла, стехиометрическое количество фосфат-анионов (в виде дигидрофосфата аммония, NH4H2PO4) и не менее чем 10-ти кратный избыток катионов аммония в реакционной смеси, который достигается путем добавления концентрированного раствора аммиака (NH3).
Все соединения в случае гидротермального метода растворяются в деионизованной воде при постоянном перемешивании и умеренном нагреве (от 70 до 100°С) и выдерживаются в герметичном автоклаве в течение 10-20 часов при повышенной температуре (190-250°С). Также возможно применение сольвотермального метода, в данной случае в качестве реакционной среды используется вода с добавлением определенного соотношения спирта, соотношение вода:спирт может варьироваться от 75:25 до 99:1.
Вторая стадия синтеза представляет собой обработку при повышенных температурах (от 150 до 400°С) смеси «аммонийсодержащего прекурсора» с солью лития, натрия или калия в течение 1-20 часов (CH3COOLi (ацетат лития), LiBr (бромид лития), Li2C2O4 (оксалат лития), LiNO3 (нитрат лития), C6H7O6Li (аскорбат лития), Na2C2O4 (оксалат натрия), C5H8NO4Na (глутамат натрия), HCOONa (формиат натрия), HOCH2(CHOH)4COONa (глюконат натрия), C3H2Na2O4 (малонат натрия), CH3COOK (ацетат калия), KBr (бромид калия), K2CO3 (карбонат калия)).
Получение углеродного композита на основе составов AV1-xMxPO4(F1-yOy)/C (0≤(х,у)≤1) проводится согласно методикам, описанным в изобретениях RU 2748159 С1, RU 2 732 368 С1.
Электродная масса на основе композитов AV1-xMxPO4(F1-yOy)/C подготавливается путем тщательного смешения электрохимически активного материала с полимерным связующим и проводящей добавкой и последующим диспергированием смеси в N-метилпироллидоне. Полученная паста наносится на алюминиевую фольгу, высушивается и подвергается прокатке на вальцах. Далее вырезаются заданного размера электроды, определяется масса электрохимически активного материала, электроды подвергаются сушке при пониженном давлении (р<10-2 атм) в течение 4-12 часов. Электролит представляет собой раствор с концентрацией соли от 0.5 до 1 моль/л (солью щелочного металла может являться гексафторфосфат, LiPF6/NaPF6/KPF6 или перхлорат, в частности LiClO4, NaClO4) в органических карбонатах (в том числе, но не ограничиваясь этилен-, пропилен-, диметил-карбонат), электролит может содержать от 0.1 до 5 об.% фторэтиленкарбоната (ФЭК). Измерения проводятся в полуячейках, в качестве противоэлектрода используется металлический литий, натрий или калий (для тестирования катодных материалов ЛИА, НИА или КИА, соответственно). Материалом сепаратора может являться боросиликатное стекло или полипропилен. Ячейки собираются в инертной атмосфере в перчаточном боксе, измерения проводятся в гальваностатическом режиме на потенциостате Biologic VMP-3 с установленным пакетом программного обеспечения EC-Lab при комнатной температуре.
В заявленном изобретении осуществлена замена восстановителей на основе соединений азота таких как соли гидроксиламина, гидразина, мочевины ((NH2)2CO, (NH2)2CNH, N2H6SO4, N2H5Cl, NH2OH, или N2H4⋅H2O) на соединения органических кислот и/или органические кислоты, список которых будет приведен выше в описании способа получения, в том числе, но не ограничиваясь щавелевой, лимонной, аскорбиновой, что оказывает меньшее отрицательное воздействие на окружающую среду.
Также в заявленном изобретении осуществлено уменьшение мольного соотношения используемых фосфатов по отношению к катионам ванадия. Как результат, отсутствие фосфат-анионов в маточном растворе, который неизбежно является побочным продуктом процесса, описанным в работе [Shraer, S. D., Luchinin, N. D., Trussov, I. A., Aksyonov, D. A., Morozov, A. V., Ryazantsev, S. V., & Fedotov, S. S. (2022). Development of vanadium-based polyanion positive electrode active materials for high-voltage sodium-based batteries. Nature Communications, 13(1), 1-10.], делает метод, описываемый в данном изобретении, более эффективным с точки зрения расхода реагентов.
Кроме того, в заявленном изобретении осуществлена возможность установки интервала кислотности среды исходного раствора, при котором образуются частицы AV1-xMxPO4(F1-yOy) различной морфологии.
В рамках заявленного изобретения обеспечивается возможность получения однофазного соединения с высоким уровнем кристалличности, что положительно сказывается на электрохимических свойствах материала, получаемого на следующей стадии.
Заявленное изобретение обеспечивает возможность варьирования доли органического растворителя в смеси, что позволяет синтезировать частицы различной морфологии.
В частном варианте реализации реакционная смесь, подвергаемая нагреву, находится в герметично закрытом реакторе, изготовленном из тефлона. Использование герметичного реактора позволяет воздействовать на реакционную смесь повышенными давлениями при заданных температурах.
Пример 1
Оксофторидофосфат натрия-ванадия (NaVPO4F0.5O0.5) со структурой титанил-фосфата калия получают в два этапа. На первом осуществляется синтез порошка прекурсора NH4VPO4F0.5O0.5 с использованием гидротермального метода. Для этого 5.46 г V2O5, 6.86 г NH4H2PO4, 18 г Н2С2О4 и 4.7 г NH4HF2 растворяют в 270 мл деионизованной воды при интенсивном перемешивании, рН раствора доводят до 6.8(±0.1) с помощью концентрированного раствора аммиака, добавляют объем деионизованной воды, необходимый для получения 300 мл раствора. Полученный раствор помещается в стальной гидротермальный реактор объемом 600 мл и плотно закрывается. Реакцию проводят при температуре Т=215°С в течение t=18 часов, после чего реактор охлаждается до комнатной температуры естественным образом. Полученный темно-фиолетовый порошок промывается несколько раз водой и ацетоном и высушивается при 75°С в течение 3 часов. На второй стадии, полученный NH4VPO4F0.5O0.5 тщательно смешивают с глутаматом натрия в массовом соотношении 1:4.5, при помощи ступки и пестика. Полученную смесь отжигают в муфельной печи при 200°С в течение 10 часов в атмосфере воздуха с последующим выделением вещества с помощью промывания на воронке с пористым дном.
Пример 2
Оксофторидофосфат натрия-ванадия (NaVPO4F0.9O0.1) со структурой титанил-фосфата синтезируют по схеме, описанной в п. 1, за исключением того, что вместо указанных навесок смешивают 5.46 г V2O5, 6.86 г. NH4H2PO4, 16.8 г. щавелевой кислоты и 4.41 г. NH4HF2.
Согласно данным ЛРСМА соотношение Na:V:P в продукте реакции составляет 1.00:1.01:1.01 (±0.06). Морфология частиц на всех стадиях получения материала изучена методом растровой электронной микроскопии (СЭМ), частицы материала представляют собой многогранники сложной формы размером от 10 до 20 мкм в длинном направлении (Фиг. 2А). В процессе ионного обмена и последующего нанесения углеродного покрытия при повышенных температурах в инертной атмосфере разрушения кристаллитов не наблюдается (Фиг. 2Б, 2В).
Кристаллическая структура состава NaVPO4F0.9O0.1 уточнена методом Ритвельда по данным порошковой рентгеновской дифракции. Соединение кристаллизуется в орторомбической сингонии и изоструктурно NaVPO4F (пр. гр. №34 Pna21, а=12.7340(7) 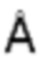 , b=6.2872(3)
, b=6.2872(3) 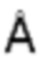 , с=10.6159(7)
, с=10.6159(7) 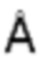 , V=849.93(8)
, V=849.93(8) 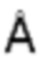 3, Rexp=0.97, Rp=1.92, GOF=3.01). Рассчитанные параметры ячейки указывают на отличие состава продукта от стехиометричного «NaVPO4F» в пользу. Эти данные подтверждаются расчетом суммы валентных усилий (ВУС, BVS - bond valence sum), на атомах ванадия, значение составляет 3.12. Количественное протекание реакции ионного обмена подтверждалось методом инфракрасной спектроскопии (Фиг. 5), данные которой также показывают отсутствие молекул адсорбированной воды, Н2О, а также структурных гидроксильных групп, -ОН. ИК спектр продукта реакции согласуется с составом NaVPO4F0.9O0.1, поскольку содержит максимумы поглощений при 844 и 886 см-1, отвечающих валентным колебаниям связи V=O.
3, Rexp=0.97, Rp=1.92, GOF=3.01). Рассчитанные параметры ячейки указывают на отличие состава продукта от стехиометричного «NaVPO4F» в пользу. Эти данные подтверждаются расчетом суммы валентных усилий (ВУС, BVS - bond valence sum), на атомах ванадия, значение составляет 3.12. Количественное протекание реакции ионного обмена подтверждалось методом инфракрасной спектроскопии (Фиг. 5), данные которой также показывают отсутствие молекул адсорбированной воды, Н2О, а также структурных гидроксильных групп, -ОН. ИК спектр продукта реакции согласуется с составом NaVPO4F0.9O0.1, поскольку содержит максимумы поглощений при 844 и 886 см-1, отвечающих валентным колебаниям связи V=O.
Пример 3
Оксофторидофосфат натрия-ванадия (NaVPO4F0.9O0.1) со структурой титанил-фосфата синтезируют по схеме, описанной в п. 2, за исключением того, что реакцию проводят при температуре Т=230°С в течение t=12 часов.
Пример 4
Для получения активного электродного материала NaVPO4F0.9O0.1/C один грамм NaVPO4F0.9O0.1, полученного по п. 2 смешивают с 0.110 г порошка полиакрилонитрила (ПАН) и при добавлении небольшого количества диметилформамида (ДМФА), необходимого для получения однородной густой суспензии. К суспензии добавляется избыток этилового спирта для ее коагуляции, избыток этилового спирта удаляется декантацией. Полученную пасту тщательно высушивают в вакууме при 60°С и затем отжигают при 525°С в течение 2 часов в атмосфере аргона с использованием мелкодисперсного порошка железа для поглощения остаточного кислорода. Остаточное содержание углерода в случае создания проводящего покрытия таким образом составляет 7 масс.%. Микрофотография полученного композита представлена на фиг.2В. Данные локального рентгеноспектрального анализа NaVPO4F0.9O0.1 и результаты элементного картирования показаны на фиг. 4.
Пример 5
Синтез KVOPO4 осуществляют в два этапа. В качестве прекурсора используют оксофосфат аммония-ванадия (NH4VOPO4) со структурой титан ил-фосфата калия, который синтезируют по схеме, описанной в п. 1, за исключением того, что не используется NH4HF2, а масса щавелевой кислоты (Н2С2О4) составляет 10.81 г. Дифрактограмма полученного прекурсора представлена на фиг.1Д. На второй стадии, полученный NH4VOPO4 тщательно смешивают с ацетатом калия в массовом соотношении 1:3, при помощи ступки и пестика. Полученную смесь отжигают в трубчатой печи при 320°С в течение 10 часов в атмосфере аргона с последующим выделением вещества с помощью промывания на воронке с пористым дном.
Пример 6
Синтез KVPO4F осуществляют в два этапа аналогично п. 4, за исключением того, что в качестве прекурсора используют фторидофосфат аммония-ванадия (NH4VPO4F) со структурой титанил-фосфата калия, который получают по методике описанной в п. 1, за исключением того, что используется 21.6 г. щавелевой кислоты и 6.96 г. NH4HF2, а также температура синтеза составляет 230°С. Дифрактограмма полученного KVPO4F приведена на фиг. 1Г.
Пример 7
Фторидофосфат натрия-ванадия (NaVPO4F0.5O0.5) со структурой титанилфосфата калия синтезируют по схеме, описанной в примере 1, за исключением того, что вместо навески щавелевой кислоты при подготовке раствора для гидротермальной обработки используется 1.6 г моногидрадата лимонной кислоты (С6Н8О7⋅Н2О).
Пример 8
Оксофторидофосфат натрия-калия-ванадия (Na0.9K0.1VPO4F) со структурой титанилфосфата калия синтезируют по схеме, описанной в примере 1, за исключением того, что при подготовке прекусора используются 5.46 г V2O5, 6.86 г NH4H2PO4, 0.33 г KH2PO4, 20 г Н2С2О4 и 5 г NH4HF2. Образцы (NH4)1-xKxVPO4F далее тщательно перетираются в ступке с пятикратным молярным избытком глутамата натрия. Смесь помещается в керамический тигель, после чего устанавливается в печь и выдерживается при 190°С в течение 10 часов (скорость нагрева 2°С/мин). После извлечения образцов из печи, порошки очищаются центрифугированием с дистиллированной водой 5 раз и один раз с ацетоном. После центрифугирования порошки высушиваются при 70°С. Дифрактограмма полученного Na0.9K0.9VPO4F представлена на фиг. 1Е и подтверждает его однофазность.
Пример 9
Оксофторидофосфат натрия-ванадия (NaVPO4F0.75O0.25) со структурой титанилфосфата калия синтезируют по схеме, описанной в п. 1, за исключением того, что вместо указанных навесок смешивают 5.46 г V2O5, 6.86 г NH4H2PO4, 15 г щавелевой кислоты (Н2С2О4) и 1.71 г NH4HF2, а также вместо рН=6.8(±0.1) при подготовке раствора для синтеза прекурсора используют рН=6.0(±0.1). Микрофотографии прекурсора NH4VPO4F0.75O0.25 и материала NaVPO4F0.75O0.25 представлены на фиг. 3А, Б.
Пример 10
Оксофторидофосфат натрия-ванадия-хрома со структурой титанил-фосфата калия (NaV0,9Cr0,1PO4F0.9O0.1) синтезируют по схеме, описанной в п. 1, за исключением того, что вместо навески V2O5 массой 5.46 г используют навески V2O5 массой 4.914 грамма и Cr(NO3)3⋅9H2O массой 1.2 грамма, а также используется 22 г щавелевой кислоты.
Пример 11
Фторидофосфат лития-ванадия (LiVPO4F) со структурой титанил-фосфата синтезируют по схеме, описанной в п. 5, за исключением того, в реакцию ионного обмена с прекурсором вступает ацетат лития, причем он берется 1.25-кратном в мольном избытке, а смесь перед реакцией предварительно прессуется в таблетки. Синтез проводится при температуре 330°С в течение 10 часов. После чего реакционную смесь вносят в дистиллированную воду, продукт реакции отделяется центрифугированием (не менее трех раз, 6000 об⋅мин-1) в течение 5 минут.
Пример 12
Оксофторидофосфат натрия-ванадия (NaVPO4F0.5O0.5) со структурой титанил-фосфата калия синтезируют по схеме, описанной в п. 1, за исключением того, что вместо глутамата натрия в реакции ионного обмена используется пятикратный мольный избыток оксалата натрия, Na2C2O4. При этом химическая реакция проводится в атмосфере аргона при температуре 300°С и времени выдержки 10 часов. После чего реакционную смесь вносят в деионизованную воде, продукт реакции отделяется центрифугированием (не менее трех раз, 6000 об мин-1) в течение 5 минут.
Пример 13
Для получения электрода электродную пасту готовят путем тщательного смешивания 80% NaVPO4F0.9O0.1)/C, полученного по примеру 3, с 10% проводящей сажи (Super Р) и 10% поливинилиденфторида (ПВдФ) в N-метилпирролидоне (НМП). Полученную пасту наносят на алюминиевую фольгу с графитовым покрытием по технологии нанесения ракелем с толщиной намазки 100 мкм. Электроды сушат под вакуумом при 110°С в течение 12 часов. Активная масса полученных электродов составляет около 4 мг см-2. Данные гальваностатического циклирования для изготовленных электродов приведены на фиг. 6. Удельная электрохимическая емкость при скорости заряда/разряда около 10 часов составляет более 115 мАч⋅г1 при среднем рабочем потенциале около 4.0 В отн. Na+/Na. Более того, активный материал электрода демонстрирует разрядную электрохимическую емкость около 100 мАч⋅г1 при увеличении скорости заряда до 1 часа, а разряда до 30 минут (фиг. 6).
Пример 14
Для получения электрода электродную пасту готовят по схеме из примера 12, за исключением того, что вместо сажи, частично используется суспензия одностенных углеродных нанотрубок в N-метилпирролидоне (НМП). Массовые доли веществ составляют 90% NaVPO4F0.9O0.1)/C с 3% проводящей сажи, 2% углеродных нанотрубок и 5% поливинилендифторида (ПВдФ).
Пример 15
Для получения электрода электродную пасту готовят по схеме из примера 12, за исключением того, что вместо сажи, используется суспензия одностенных углеродных нанотрубок в N-метилпирролидоне (НМП). Массовые доли веществ составляют 94% NaVPO4F0.9O0.1)/C 3% углеродных нанотрубок и 3% поливинилендифторида (ПВдФ).
Пример 16
Для получения электрода электродную пасту готовят по схеме из примера 12, за исключением того, что вместо NaVPO4F0.9O0.1)/C используется композитный электрохимически активный материал LiVPO4F/C.
Пример 17
Натрий-ионный аккумулятор изготавливают в герметичном корпусе, который содержит материал положительного электрода (электродная паста на фольге токосъемника), выполненный по схеме в примере 12, алюминиевые токосъемники, сепаратор из полипропилена или стекловолокна, материал отрицательного электрода из неграфитизируемого углерода и раствор электролита, которым выступает 1 М NaPF6 в смеси ЭК:ПК (50:50 по объему).
Пример 18
Натрий-ионный аккумулятор изготавливают по схеме в примере 15, за исключением того, что материал отрицательного электрода представляет собой частицы металла, в частности, свинца, олова или висмута, нанесенных на алюминиевую фольгу.
Пример 19
Натрий-ионный аккумулятор изготавливают в герметичном корпусе, который содержит материал положительного электрода, выполненный по схеме в примере 12, алюминиевые токосъемники, сепаратор из полипропилена или стекловолокна, материал отрицательного электрода из неграфитизируемого углерода и раствор электролита, которым выступает 1 М NaPF6 в смеси ЭК:ПК (50:50 по объему).
Пример 20
Литий-ионный аккумулятор изготавливают в герметичном корпусе, который содержит материал положительного электрода, выполненный по схеме в примере 14, алюминиевый и медный токосъемники, сепаратор из полипропилена или стекловолокна, материал отрицательного электрода из графита и раствор электролита, которым выступает 1 М LiPF6 в смеси ЭК:ДЭК (50:50 по объему).


Изобретение относится к области материаловедения, а именно, к технологии получения фосфатов, оксофосфатов и фторидофосфатов ванадия, которые могут быть использованы в качестве активных электродных материалов металл-ионных аккумуляторов. В роли электрохимических активных соединений рассматриваются составы AV1-xMxPO4(F1-yOy), а в качестве компонента электродной смеси композиты с углеродом на основе одноименных составов AV1-xMxPO4(F1-yOy)/C, где А=Li, Na, K или их смесь, М является одним из перечисленных металлов: Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь, причем 0≤х≤1, 0≤у≤1. Для получения указанных соединений используется двухэтапная химическая технология. Первый шаг включает подготовку прекурсора путем обработки реакционной смеси в гидротермальных или сольвотермальных условиях. На второй стадии проводится химическая реакция между полученным прекурсором и солью лития, натрия или калия при повышенных температурах. Технический результат заключается в повышении технологичности процесса, уменьшении нагрузки на окружающую среду и очистные сооружения, а также в возможности эффективного контроля морфологии частиц и соотношения фтор-кислород в процессе синтеза. 6 н. и 2 з.п. ф-лы, 6 ил., 20 пр.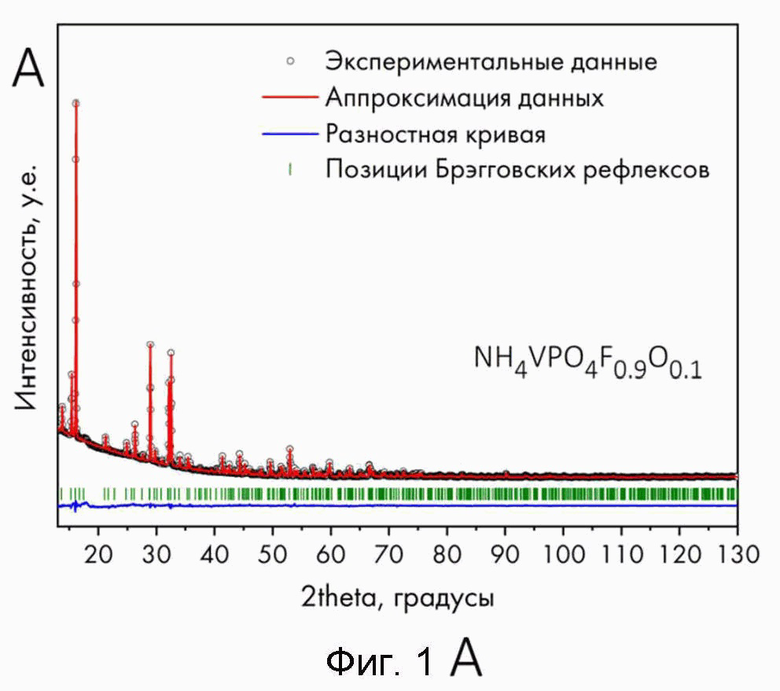
1. Способ получения порошка активного электродного материала положительного электрода с кристаллической структурой титанил-фосфата калия состава AV1-xMxPO4(F1-yOy), где A – щелочной металл, выбранный из группы Li, Na, K или их смесь, M – переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn или их смесь, а 0≤x≤1 и 0≤y≤1, при этом способ включает следующие этапы:
a) получение аммонийсодержащего прекурсора AV1-xMxPO4(F1-yOy), где M – по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn; 0≤x≤1, 0≤y≤1, сольво- или гидротермальным способом при постоянном перемешивании исходных компонентов при температуре 150-250°C и давлении не более 60 атм в течение 1-48 часов, при этом в качестве исходных компонентов используют источник переходного металла – соль или оксид переходного металла; источника фосфора – по крайней мере один фосфат выбранный из группы: NH4H2PO4, (NH4)2HPO4 (NH4)3PO4; фторирующий агент – по крайней мере один фосфат выбранный из группы: HF, NH4F, NH4HF2; органическая кислота-восстановитель, выбрана из группы: H2C2O4, C6H8O7, C4H6O6, CH2O2 или их гидраты; растворитель – дистиллированная вода или водно-спиртовой раствор, содержащий вышеуказанные соль или оксид переходного металла, источник фосфора, фторирующий агент, органическую кислоту-восстановитель;
b) смешивание полученного аммонийсодержащего прекурсора с по крайней мере одной легкоплавкой солью щелочного металла, выбранной из группы: ацетат лития, нитрат лития, бромид лития, оксалат лития, аскорбат лития, глутамат натрия, оксалат натрия, формиат натрия, малонат натрия, ацетат натрия, нитрат натрия, карбонат натрия, ацетат калия, бромид калия, карбонат калия, с последующим нагревом смеси при температуре 100-500°С в атмосфере воздуха или аргона.
2. Способ по п. 1, отличающийся тем, что в качестве соли переходного металла используют NH4VO3, VOSO4, TiOSO4, Ti2(SO4)3 (водный раствор), K2Cr2O7, CrCl3, Cr(NO3)3, MnCl2, Mn(NO3)2, KMnO4, NaMnO4, FeCl3, Fe(NO3)3, AlCl3, Al(NO3)3, SсCl3, Sc(CH3COO)3, ZnCl2, Zn(NO3)2 или гидраты указанных солей.
3. Способ получения проводящего композитного активного материала положительного электрода формулы AV1-xMxPO4(F1-yOy)/С, где A – по крайней мере один щелочной металл, выбранный из группы Li, Na, K, M – по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn, а 0≤x≤1 и 0≤y≤1, при этом способ включает следующие стадии:
a) получение аммонийсодержащего прекурсора AV1-xMxPO4(F1-yOy), где M – по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn; 0≤x≤1, 0≤y≤1, сольво- или гидротермальным способом при постоянном перемешивании исходных компонентов при температуре 150-250°C и давлении не более 60 атм в течение 1-48 часов, при этом в качестве исходных компонентов используют источник переходного металла – соль или оксид переходного металла; источника фосфора – по крайней мере один фосфат выбранный из группы: NH4H2PO4, (NH4)2HPO4 (NH4)3PO4; фторирующий агент – по крайней мере один фосфат выбранный из группы: HF, NH4F, NH4HF2; органическая кислота-восстановитель, выбранная из группы: H2C2O4, C6H8O7, C4H6O6, CH2O2 или их гидраты; растворитель – дистиллированная вода или водно-спиртовой раствор, содержащий вышеуказанные соль или оксид переходного металла, источник фосфора, фторирующий агент, органическую кислоту-восстановитель;
b) получение материала формулы AV1-xMxPO4(F1-yOy), где A – по крайней мере один щелочной металл, выбранный из группы Li, Na, K, M – по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn, а 0≤x≤1 и 0≤y≤1, при смешивании полученного аммонийсодержащего прекурсора с по крайней мере одной легкоплавкой солью щелочного металла, выбранной из группы; ацетат лития, нитрат лития, бромид лития, оксалат лития, аскорбат лития, глутамат натрия, оксалат натрия, формиат натрия, малонат натрия, ацетат натрия, нитрат натрия, карбонат натрия, ацетат калия, бромид калия, карбонат калия, с последующим нагревом смеси при температуре 100-500°С в атмосфере воздуха или аргона;
c) смешивание полученного материала на стадии b) с углеродсодержащей добавкой, содержащей по крайней мере один компонент, выбранный из группы: полиакрилонитрил или его раствор в растворителе, выбранном из группы: ДМФА (диметилформамид), ДМСО (диметилсульфоксид), N-метилпирролидоне, и/или по крайней мере один компонент, выбранный из группы глюкоза, сахароза, поливинилпирролидон.
4. Способ по п. 3, отличающийся тем, что в качестве соли переходного металла используют NH4VO3, VOSO4, TiOSO4, Ti2(SO4)3 (водный раствор), K2Cr2O7, CrCl3, Cr(NO3)3, MnCl2, Mn(NO3)2, KMnO4, NaMnO4, FeCl3, Fe(NO3)3, AlCl3, Al(NO3)3, SсCl3, Sc(CH3COO)3, ZnCl2, Zn(NO3)2 или гидраты указанных солей.
5. Активный электродный материал для металл-ионных аккумуляторов на основе состава AV1-xMxPO4(F1-yOy), полученный способом по любому из пп. 1-2, или его проводящий композит с углеродом формулы AV1-xMxPO4(F1-yOy)/С, полученный способом по любому из пп. 3-4, где A – по крайней мере один щелочной металл, выбранный из группы Li, Na, K, M – по крайней мере один переходный металл, выбранный из группы: Ti, Cr, Mn, Fe, Al, Sc, Zn, а 0≤x≤1 и 0≤y≤1), характеризующийся удельной электрохимической емкостью более 95 мАч·г-1 и рабочим потенциалом более 3.7 В отн. Na+/Na.
6. Электродная паста, содержащая активный электродный материал или его проводящий композит с углеродом по п. 5, электропроводящую добавку, содержащую сажу и/или по крайней мере один компонент, выбранный из группы: одностенные углеродные нанотрубки, нанолисты графена, полианилин, полипиролл, полиэтилендиокситиофени органическое связующее, и органическое связующего, содержащее поливиниленденфторид или по крайней мере один компонент, выбранный из группы: суспензия карбоксиметилцеллюлозы в воде, суспензия фторопласта в н-метилпирролидоне, суспензия тефлона в н-метилпирролидоне, при следующем соотношении компонентов в мас.%: активный электродный материал или его проводящий композит с углеродом – 70-99; электропроводящая добавка – 0.5-20 и органическое связующее – 0.5-10.
7. Электрод, содержащий ленту металлического токосъемника или ленту металлического токосъемника с проводящим углеродным покрытием, на поверхность которого нанесена электродная паста, полученная по п. 6, которая в дальнейшем подвержена горячей или холодной прокатке.
8. Металл-ионный аккумулятор, содержащий катод, выполненный из электрода по п. 7, а также металлический или углеродный анод.
| Электродный материал для натрий-ионных аккумуляторов, способ его получения, электрод и аккумулятор на основе электродного материала | 2020 |
|
RU2748159C1 |
| US 11145863 B2, 12.10.2021 | |||
| Электродная масса, электродный композитный материал, способ его получения и его применение металл-ионных аккумуляторах | 2020 |
|
RU2732368C1 |
| CN 110828793 A, 21.02.2020 | |||
| CN 113336277 B, 22.11.2022. | |||
Авторы
Даты
2023-09-26—Публикация
2023-03-07—Подача