ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к материалам положительного электрода (катода) на основе слоистых оксидов переходных металлов и может быть использовано для производства улучшенного активного катодного материала для высокоэнергоемких литий-ионных аккумуляторов, применяемых для питания портативных и стационарных электроприборов, а также для электротранспорта.
УРОВЕНЬ ТЕХНИКИ
Среди разнообразных электрохимических источников тока в последние годы большой импульс развития получили литий-ионные аккумуляторы (ЛИА), которые занимают все большую долю рынка и начинают доминировать среди автономных электрохимических источников энергии. ЛИА являются одними из наиболее широко используемых источников питания в электронных устройствах военного, медицинского, бытового и промышленного назначения. Это связано с рядом преимуществ, которыми обладают ЛИА, а именно, высокой энергоемкостью, устойчивостью к многократному циклированию, быстрым процессом заряда и отсутствием «эффекта памяти».
Как известно, такие электрохимические характеристики, как удельные энергетические и мощностные параметры ЛИА в значительной степени определяются свойствами материала положительного электрода (катода). В связи с этим, основной вектор научных исследований в области создания высокоэнергоемких аккумуляторов направлен на улучшение существующих и создание новых катодных материалов.
Материалом катода первого поколения в коммерческих ЛИА выступал LiCoO2, преимуществами которого являются относительная простота получения, возможность эксплуатации при высоких плотностях тока и др. Недостатки LiCoO2 связаны с его высокой стоимостью, токсичностью и ограниченной практически достижимой ёмкостью ~140-150 мАч/г при максимальном напряжении 4.2-4.3 В отн. Li/Li+ (что соответствует извлечению/внедрению примерно половины имеющегося в структуре лития). Последнее обстоятельство связано со структурной нестабильностью LiCoO2 при заряде выше 4.3 В и побочными реакциями материала катода с электролитом. Перечисленные недостатки положительного электрода на основе LiCoO2 способствовали поиску более дешевых, энергоемких и менее токсичных материалов. Одним из перспективных подходов является замена части кобальта на другие более дешевые переходные металлы, такие как никель и марганец. В результате этого подхода были получены изоструктурные LiCoO2 соединения состава LiNixMnyCozO2 (x + y + z = 1, обозначаемые также как NMCXYZ, где X:Y:Z - молярное соотношение Ni, Mn и Co). Огромный интерес представляют материалы NMC с повышенным содержанием никеля (x≥0.6) поскольку такие материалы могут обеспечить высокую удельную ёмкость (до 220 мАч/г) в одном и том же окне потенциалов за счет извлечения большего количества лития из структуры по сравнению с LiCoO2, а плотность энергии таких материалов может достигать 800 Втч/кг. Тем не менее практическое применение таких материалов ограничено ввиду возникновения проблем, связанных с безопасностью, и быстрого снижения удельной емкости в течение всего срока службы аккумуляторной батареи. Как правило, первая проблема связана с термодинамической нестабильностью полностью заряженного состояния (заряд при повышенных значениях потенциала) и при высокой температуре, вторая - связана с химическим, структурным и механическим разрушением катодного материала NMC. [S.S. Zhang, Problems and their origins of Ni-rich layered oxide cathode materials, Energy Storage Mater., 24, 247-254 (2020)]. Поскольку значительным структурным перестройкам подвергается в основном поверхность частиц положительного электрода, где происходит образование уплотненного слоя из-за частичной потери кислорода и образования неупорядоченных структур [M. Dixit, B. Markovsky, F. Schipper, D. Aurbach, D.T. Major, Origin of structural degradation during cycling and low thermal stability of Ni-rich layered transition metal based electrode materials, J. Phys. Chem., C 121, 22628-22636 (2017)], поверхностное модифицирование первичных частиц и вторичных агломератов представляется одним из наиболее перспективных и эффективных подходов, направленных на повышение стабильности и безопасности материалов на основе Ni-обогащенных NMC.
Одним из способов улучшения эксплуатационных характеристик катодного материала на основе NMC является модифицирование первичных и вторичных частиц материала с помощью литийсодержащих соединений, являющихся ионными проводниками по литию [US20170338471A1]. Благодаря этому увеличивается скорость интеркаляции/деинтеркаляции ионов лития на границе раздела электрод/электролит, а также формируется «защитный» слой, который препятствует взаимодействию катодного материала с HF, образующейся при использовании электролита на основе LiPF6 во время электрохимического циклирования. Указанными свойствами обладают простые и сложные серосодержащие соединения лития различного состава. Однако поскольку данные материалы для модификации частиц катодного материала демонстрируют низкие значения электронной проводимости, увеличение толщины покрытия может вызвать ухудшение электрохимических свойств вследствие повышения омического сопротивления.
Известен серосодержащий катодный материал и способ его получения, приведенные в патенте US 10090518 B2. Описанный в данном патенте материал получен путем «сухого» смешения коммерческого катодного материала состава Li1+a’M1-aO2, где a’<a, 0.95(1+a')/(1-a)≤1.15, M=Ni1-x-yM’xCoy, М’=Mn1-zAlz, 0≤z≤1, 0.1≤y≤0.4 и x+y = 0.5, Na2S2O8 и источника лития, преимущественно LiOH и Li2CO3, с последующей высокотемпературной обработкой в течение нескольких часов. В результате образуется композитный катодный материал, представляющий собой смесь слоистого оксида переходных металлов и LiNaSO4. Лучший приведенный образец состава NMC622 демонстрирует удельную разрядную емкость 179.9 мАч/г при скорости разряда 0.1С (плотность тока 16 мАч/г, 3.0-4.3 В отн. Li/Li+) с сохранением разрядной емкости от исходной за 100 циклов 98%. Недостатком предложенного способа является необходимость дополнительной стадии смешения исходных компонентов и высокотемпературной обработки. Еще один недостаток данного материала заключается в следующем. При заявленном подходе образующийся в результате твердофазного синтеза LiNaSO4 может формировать отдельные агломераты на поверхности вторичных частиц катодного материала. В таком случае диффузионная способность ионов лития на поверхности частиц катодного материала может быть затруднена, что приводит к значительному снижению удельной емкости и стабильности при многократном циклировании. Заявляемые в патенте составы катодного материала имеют достаточно узкий диапазон содержания никеля, в пределы которого не входят Ni-обогащенные NMC, которые характеризуются наиболее высокими показателями обратимой разрядной емкости.
Еще одним серьезным недостатком является присутствие в системе натрия, который может осаждаться на аноде в виде металла (натрий не интеркалируется в графитоподобные анодные материалы), а также встраиваться в структуру NMC, увеличивая изменение объема элементарной ячейки и приводя к возникновению механических напряжений.
Известен катодный материал, который представляет собой слоистый оксид состава LiNixMnyCozAvO2 (0.33≤x≤0.5, 0.20≤y≤0.33, 0.20≤z≤0.33, v≤0.05, x+y+z+v=1), а также его соединение-предшественник, представляющее собой гидроксид MOH или оксигидроксид MOOH, где М = NixMnyCozAv (0.33≤x≤0.5, 0.20≤y≤0.33, 0.20≤z≤0.33, A - легирующая добавка (Al, Mg, Zr, W, Ti, Cr, V) v≤0.05, x+y+z+v=1), с примесью серы, возникающей в связи с использованием сульфатов переходных металлов в качестве исходных реагентов [US 10547056 В2]. Синтез соединения-предшественника осуществлялся в проточном гидротермальном реакторе методом соосаждения смешанного гидроксида или оксигидроскида из сульфатов переходных металлов и источника гидроксид-ионов. Получение конечного продукта осуществлялось путем добавления к соединению-предшественнику источника лития, LiOH или Li2CO3, и отжига в температурном интервале 600°С-1100°С в течение более одного часа. Недостатком данного способа получения серосодержащего соединения-предшественника является высокая температура гидротермального синтеза, предпочтительно 120-170°С, что приводит к более высоким энергетических затратам, более быстрому изнашиванию оборудования и, как следствие, удорожанию материала. Также, гидротермальный синтез требует дорогостоящего оборудования для работы под повышенным давлением. Согласно предлагаемому изобретению, удельная площадь поверхности и содержание серы в соединении-предшественнике должны соответствовать приведенному в патенте неравенству:
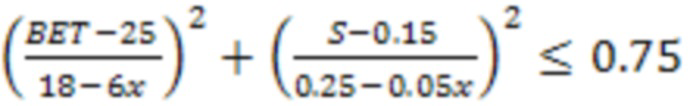 ,
,
где BET - это удельная площадь поверхности [ ], S - концентрация серы [масс. %].
], S - концентрация серы [масс. %].
Поскольку высокотемпературный отжиг оказывает существенное влияние на удельную площадь поверхности частиц, при варьировании условий высокотемпературной обработки из одного и того же соединения-предшественника могут быть получены материалы с различными значениями удельной площади поверхности. В связи с этим возможно возникновение проблемы контроля соответствия значений удельной площади поверхности и содержания серы, и, как следствие, сложности получения катодного материала с заданными электрохимическими показателями, что является критическим недостатком данного изобретения. Как и в патенте US 10090518 B2, заявленные составы катодного материала имеют узкий диапазон содержания никеля в NMC. В приведенном изобретении для заявленных катодных материалов приведены показатели зарядной емкости первого цикла без демонстрации экспериментальных данных, при этом не указаны данные о циклической устойчивости при многократном электрохимическом циклировании.
Известен также катодный материал Lia((Niz(Ni0.5Mn0.5)yCox)1-kAk)2-aO2, где x+y+z=1, 0.1≤x≤0.4, 0.36≤z≤0.50, A - легирующая добавка (B, Ca, Mn, Cr, V. Fe, Zr, S, F, P и Bi), 0≤k≤0.1 и 0.95≤a≤1.05, в состав которого входят растворимые основания, Li2CO3 и LiOH, где Li2CO3≥0.085 масс.% и Li2CO3/LiOH>0.2, а также его соединение-предшественник, представляющее собой смешанный оксигидроксид, полученный путем соосаждения из растворов сульфатов переходных металлов. Как и в предыдущем примере, данный катодный материал содержит примесь серы, которая возникает в связи с использованием сульфатов переходных металлов в качестве исходных реагентов [JP5660353B2]. Недостатками предложенного изобретения являются, во-первых, наличие литийсодержащих основных соединений, а именно, Li2CO3 и LiOH, поскольку они являются изоляторами, и их наличие отрицательно сказывается на электрохимических свойствах катодных материалов; во-вторых, согласно предлагаемому изобретению, удельная площадь поверхности катодного материала должна находиться в диапазоне от 0.22 до 0.40 м2/г, что не только затрудняет контроль соответствия значений удельной площади поверхности в процессе синтеза, но и является достаточно низким показателем для материалов заявляемых составов, в результате чего происходит уменьшение рабочей поверхности катода и, как следствие, снижение электрохимических эксплуатационных характеристик.
Также известен катодный материал на основе слоистых оксидов состава Li1+aM1-aO2±bM'kSm, где M - переходные металлы (не менее 95% Ni, Mn, Co и Ti), M' - Ca, Sr, Y, La, Ce и Zr, -0.033<a<0.06, b≈0, 0.0250<k≤0.1 масс.% и 0.15<m≤0.6 мол.%, получаемый из соединений-предшественников - гидроксида, оксигидроксида или карбоната - путем соосаждения из растворов сульфатов переходных металлов [US8303855B2]. Согласно данному изобретению, серосодержащая примесь отрицательно влияет на электрохимические свойства катодного материала, в связи с чем обязательным условием изготовления заявленного в данном изобретении материала является добавление дополнительного компонента M'. Добавление компонента может осуществляться путем добавления растворимой соли M' к исходному раствору сульфатов переходных металлов, или добавления металла M' на этапе высокотемпературного отжига или на этапе промывки, или добавления растворимой соли M' на этапе приготовления катодной смеси с последующей сушкой. Согласно примерам, иллюстрирующим данное изобретение, заявленные составы катодного материала, как и в предыдущих примерах, имеют узкий диапазон содержания никеля в NMC (≤0.67 масс.%), в пределы которого не входят Ni-обогащенные NMC, которые характеризуются наиболее высокими показателями обратимой разрядной емкости. Помимо этого, описанное в данной заявке изобретение обладает рядом существенных недостатков. Основным недостатком является необходимость введения дополнительного компонента M', предпочтительно кальция, в катодный материал для уменьшения отрицательного влияния серосодержащего компонента, причем концентрация легирующей добавки должна составлять предпочтительно 0.0250≤k≤0.0500, и соотношение серы и кальция должно изменяться в узком диапазоне, предпочтительно, их концентрации должны изменяться согласно следующему уравнению k=0.84*S. В то же время, как отмечают авторы данного изобретения, контроль содержания серосодержащего компонента затруднен в связи с его высокой растворимостью в воде и, как следствие, неконтролируемому снижению его содержания в катодном материале на этапе промывки, а избыточное добавление легирующей добавки может негативно сказаться на электрохимических свойствах катодного материала. Более того, введение легирующей добавки к катодному материалу требует добавления дополнительного операционного этапа синтеза, что приводит к удорожанию процесса производства материала.
Наиболее близким к заявляемому изобретению является решение по патенту US 8268198 B2. В данном изобретении раскрыто соединение-предшественник катодного материала, содержащее в своем составе два или более ионов переходных металлов, предпочтительно, NixCoyMn1-(x+y) 0.3≤x≤0.9, 0.1≤y≤0.6 и x+y≤1, и сульфат-ионы, оставшиеся после получения соединения-предшественника из сульфатов переходных металлов. Предлагаемое получение соединения-предшественника осуществляется с помощью метода соосаждения в течение достаточно большого период времени, а именно 20 часов, что приводит к удорожанию процесса изготовления и является недостатком данного технического решения. Поскольку в приведенном изобретении раскрыто только соединение-предшественник, содержащее сульфат-ионы, электрохимические данные для получаемого катодного материала из указанного соединения-предшественника носят иллюстративный характер без демонстрации показателей циклической устойчивости при длительном процессе заряда/разряда, циклируемости при различных плотностях тока и т.д.
Наиболее существенные отличия изобретений по патентам US 10547056 В2 и US 8268198 B2 от настоящего изобретения является тот факт, что из химических формул катодных материалов, получаемых из прекурсоров прямо следует отсутствие серы в составе катодных материалов, а в случае изобретений по патентам JP5660353 B2 и US8303855 B2, серосодержащий компонент является нежелательным побочным продуктом синтеза катодного материала, влияние которого стараются минимизировать с помощью различных подходов, что существенно отличает эти материалы от серосодержащих катодных материалов по настоящему изобретению, где аморфные серосодержащие соединения лития LidSbOc (0.001≤b≤2, 0≤c≤8, 0.001≤d≤2) образуют композит с электроактивными соединениями состава LiNixMnyCozAvO2∙(0.3≤x≤0.85, 0≤y≤0.3, 0≤z≤0.3, A - легирующая добавка (Al, Mg, Zr, W, Ti, Cr, V и др.), v≤0.1, x+y+z+v=1), являясь неотъемлемой частью активного катодного материала.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Задачей настоящего изобретения является разработка композитного активного катодного материала на основе NMC со слоистой структурой для литий-ионных аккумуляторов, обладающего улучшенными электрохимическими параметрами, в частности, высокими значениями удельной емкости при сохранении других основных параметров материала (высокой кулоновской эффективности, сохранении удельной емкости при увеличении плотности тока заряда/разряда) и высокими показателями сохранения емкости при большом количестве зарядно-разрядных циклов.
Технический результат, достигаемый заявляемым изобретением, заключается в улучшении эксплуатационных характеристик катодного материала, а именно в увеличении циклов заряда/разряда при сохранении высокой удельной емкости благодаря введению в состав активного катодного материала аморфного серосодержащего компонента - LidSbOc.
Поставленная задача и указанный технический результат достигаются за счет получения предлагаемого активного катодного материала, представляющего собой серосодержащий композитный материал, содержащий компонент в виде слоистых оксидов переходных металлов - LiNixMnyCozAvO2 и аморфный серосодержащий компонент - LidSbOc, при этом композитный материал представляет собой соединение формулы (1-a)LiNixMnyCozAvO2∙aLidSbOc, где 0.0001≤a≤0.02, 0.3≤x≤0.85, 0≤y≤0.3, 0≤z≤0.3, A - легирующая добавка (Al, Mg, Zr, W, Ti, Cr, V и др.), v≤0.1, x+y+z+v=1, 0.001≤b≤2 и 0≤c≤8, 0.001≤d≤2. Композитный материал получен из серосодержащего соединения-предшественника состава NixMnyCozOm(OH)2-2f(SbOc)f или NixMnyCoz(CO3)1-g(SbOc)g, где 0.3≤x≤0.85, 0≤y≤0.3, 0≤z≤0.3, 0≤m≤1, 0.001≤b≤2, 0≤c≤8, 0.0001≤f≤0.05 и 0.0001≤g≤0.02.
Указанный технический результат достигается также тем, что в способе получения серосодержащего композитного катодного материала отсутствуют дополнительные стадии введения серосодержащей добавки, что существенно сокращает время и затраты на подготовку готового композитного активного катодного материала. Соединения-предшественники могут быть получены с помощью следующих методов: соосаждение, гидротермальный и сольвотермальный синтез, включая активацию микроволновым излучением, золь-гель, и другие, так называемые, методы «мягкой» химии с использованием в качестве исходных солей переходных металлов и легирующих добавок не только сульфатов, но и различных других водорастворимых солей таких как, например, хлоридов, ацетатов, нитратов и др., а также их смесей, при условии добавления необходимого количества ионов-источников серы на стадии получения соединений-предшественников, например, путем введения серосодержащих ионов непосредственно в раствор осадителя. В качестве источников серосодержащих ионов, например, могут выступать H2SO4, (NH4)2SO4, Na2SO4, K2SO4 и другие. Композитный активный катодный материал получают смешиванием серосодержащего соединения-предшественника в виде карбоната или гидроксида, или их смеси, и источника лития, такого как LiOH, LiOH*H2O, Li2CO3, LiCH3COO, Li2C2O4, LiNO3 или их смеси, предпочтительно LiOH, LiOH*H2O, Li2CO3 или их смеси, и последующей высокотемпературной обработкой в течение нескольких часов.
Технический результат, достигаемый заявляемым изобретением, заключается в улучшении эксплуатационных характеристик активного катодного композитного материала состава (1-a)LiNixMnyCozAvO2∙aLidSbOc, где 0.0001≤a≤0.02, где 0.3≤x≤0.85, 0≤y≤0.3, 0≤z≤0.3, A - легирующая добавка (Al, Mg, Zr, W, Ti, Cr, V и др.), v≤0.1, x+y+z+v=1, где 0.001≤b≤2 и 0≤c≤8, 0.001≤d≤2, а именно в снижении скорости деградации емкости катодного материала при сохранении высоких значений удельной емкости при различных скоростях разряда, благодаря введению серосодержащего компонента. Указанный технический результат достигается тем, что катодный материал представляет собой композит, состоящий из двух компонентов: LiNixMnyCozAvO2 и LidSbOc, где компонент LidSbOc включает сульфат и/или пиросульфат и/или сульфит и/или сульфид и/или тиосульфат лития или их смесь, локализованный как на поверхности зерен электроактивного компонента LiNixMnyCozAvO2, преимущественно на границах зерен и в местах контакта зерен, так и распределенный по всему материалу. Аморфные серосодержащие соединения лития, распределенные по всему материалу, на поверхности зерен, на межзеренных границах и в местах контакта зерен компонента LiNixMnyCozAvO2, могут обеспечивать более высокую проводимость по ионам лития, создавать защитный слой на поверхности частиц компонента LiNixMnyCozAvO2, что препятствует их последующей химической и электрохимической деградации, а также обеспечивать связность зерен компонента LiNixMnyCozAvO2, препятствуя механической деградации композитного активного катодного материала.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Сущность изобретения поясняется графиками и чертежами.
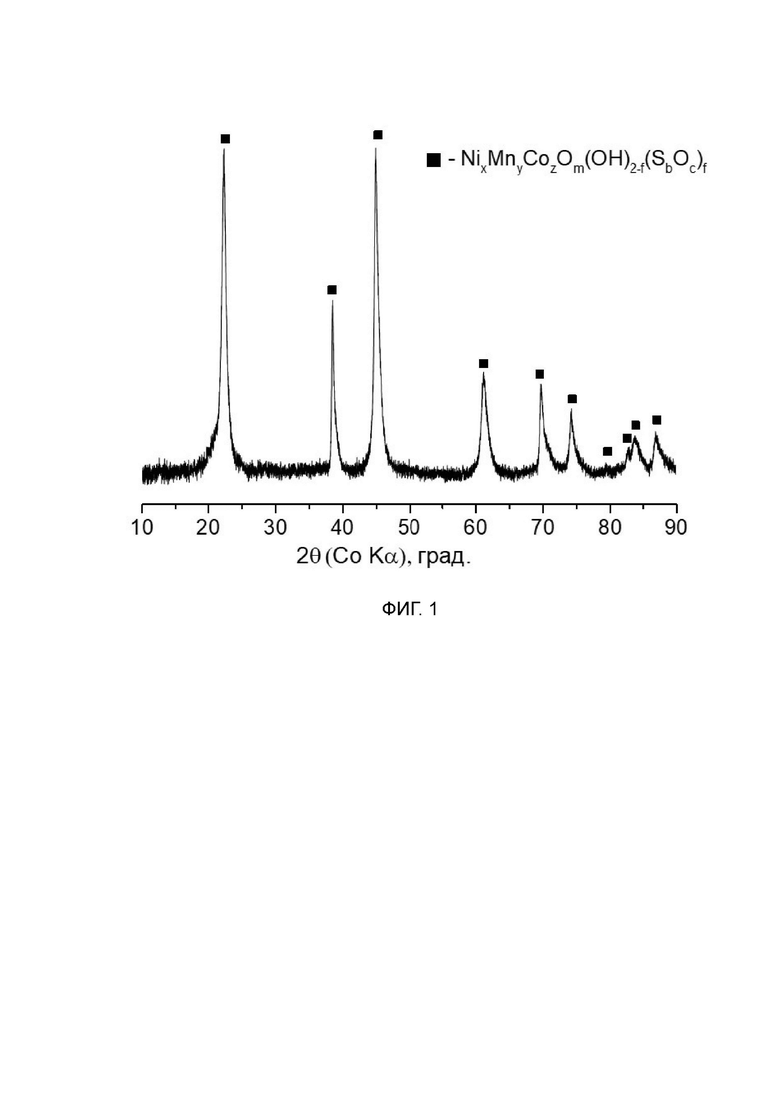
На фиг. 1 представлена рентгенограмма (рентгенограмма получена с использованием Co Кα1 излучения) однофазного соединения-предшественника, представляющего собой смешанный гидроксид или оксигидроксид Ni, Mn и Co со структурным типом β-Ni(OH)2, полученный согласно примеру 1. Рентгенограмма соединения-предшественника, полученного согласно примеру 4, имеет аналогичный профиль с рентгенограммой, представленной на фиг. 1, и свидетельствует о том, что соединение-предшественник по примеру 4 также представляет собой однофазный смешанный гидроксид или оксигидроксид Ni, Mn и Co со структурным типом β-Ni(OH)2.
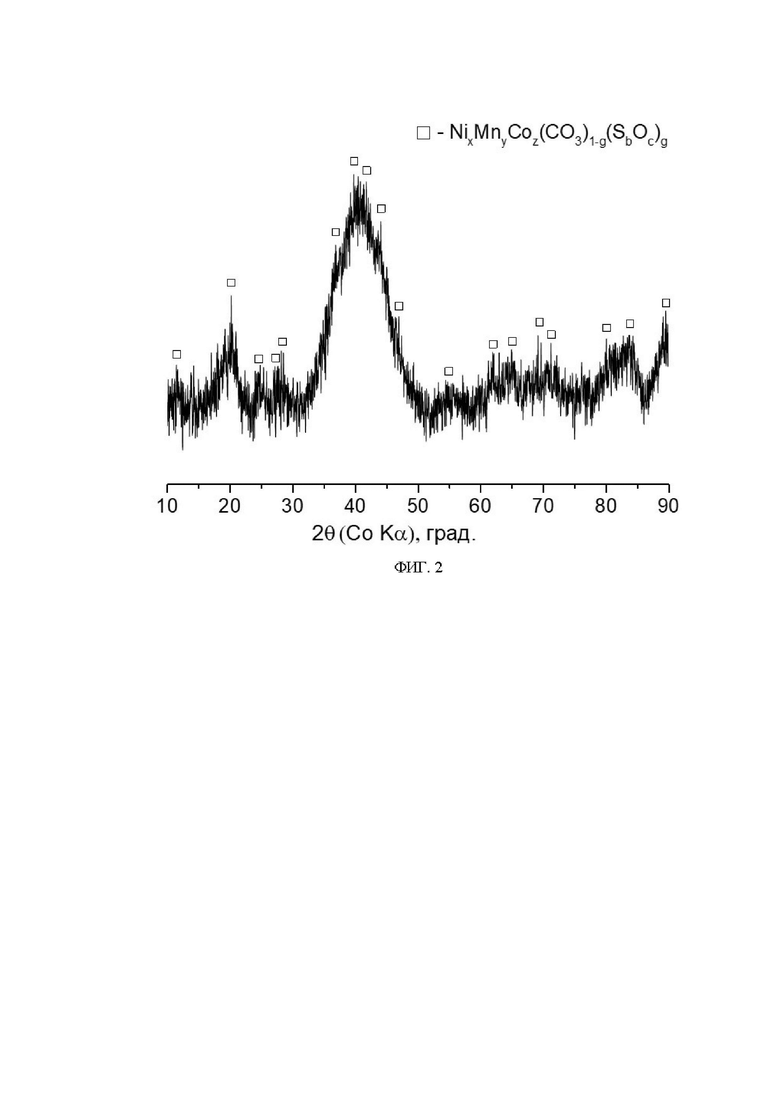
На фиг. 2 представлена рентгенограмма (рентгенограмма получена с использованием Co Кα1 излучения) однофазного соединения-предшественника, представляющего собой смешанный карбонат Ni, Mn и Co со структурным типом NiCO3∙H2O, полученный согласно примеру 3. Рентгенограмма соединения-предшественника, полученного согласно примеру 5, имеет аналогичный профиль с рентгенограммой, представленной на фиг. 2, и свидетельствует о том, что соединение-предшественник по примеру 5 также представляет собой однофазный смешанный карбонат Ni, Mn и Co со структурным типом NiCO3∙H2O.
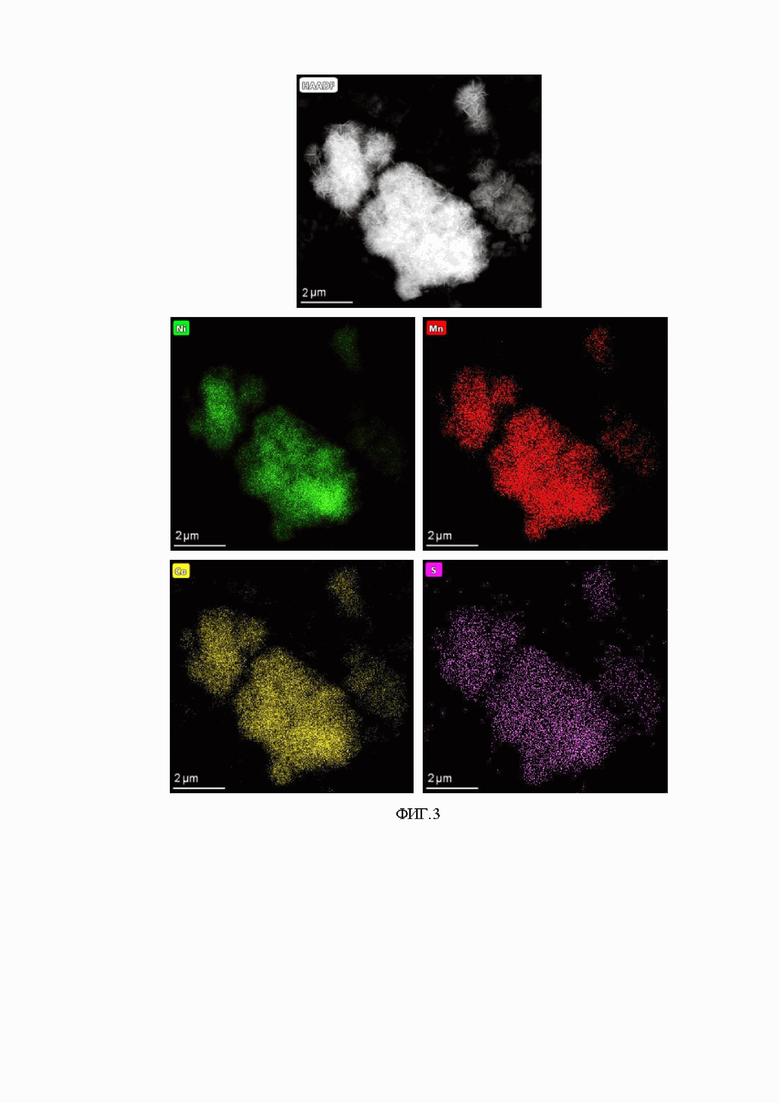
На фиг. 3 представлены карты распределения элементов, полученные с помощью энергодисперсионной рентгеновской спектроскопии (ЭДС), демонстрирующие пространственные распределения элементов Ni, Mn, Co и S для соединения-предшественника, полученного согласно примеру 1. Согласно полученным данным соотношение переходных металлов и серы в соединении-предшественнике составляет Ni:Mn:Co:S = (8.06±0.03): (0.9±0.01): (0.9±0.02): (0.05±0.03), все элементы, как переходные металлы Ni, Mn, Co, так и сера, распределены гомогенно.
На фиг. 4 представлены карты распределения элементов, полученные с помощью ЭДС, демонстрирующие пространственные распределения элементов Ni, Mn, Co и S для соединения-предшественника, полученного согласно примеру 2. Согласно полученным данным соотношение переходных металлов и серы в соединении-предшественнике составляет Ni:Mn:Co:S=(8.02±0.03):(0.85±0.03):(0.99±0.02):(0.02±0.01), все элементы, как переходные металлы Ni, Mn, Co, так и сера, распределены гомогенно.
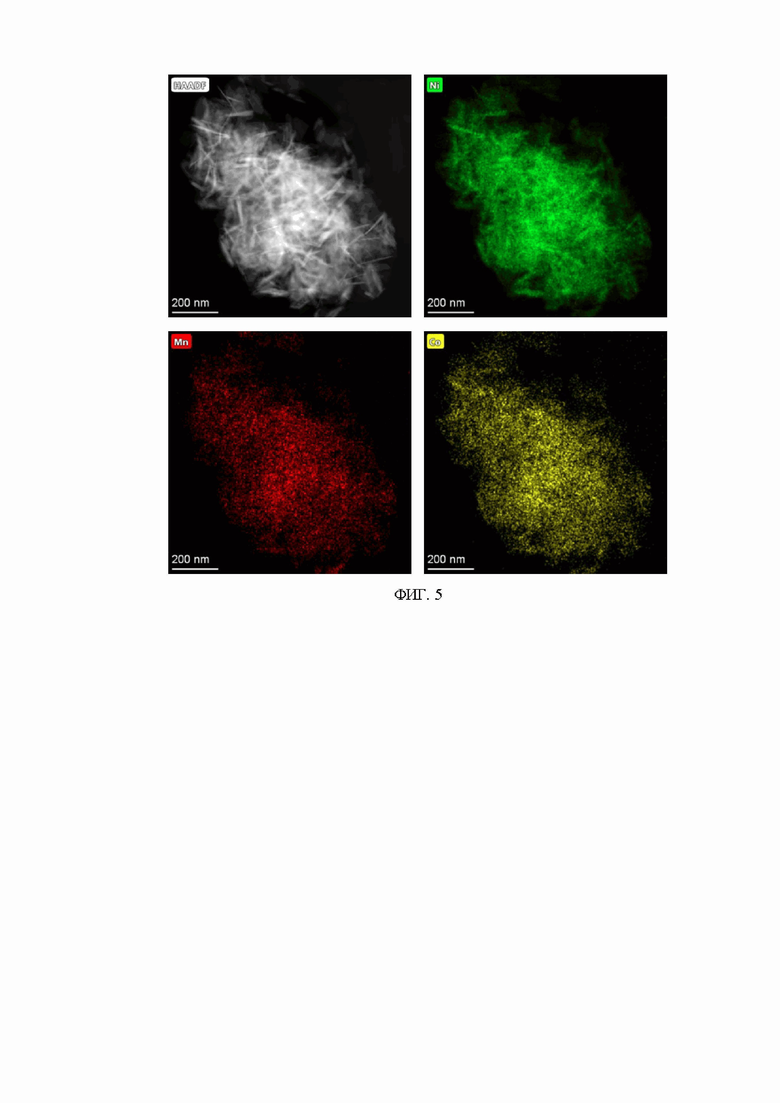
На фиг. 5 представлены карты распределения элементов, полученные с помощью ЭДС, демонстрирующие пространственные распределения элементов Ni, Mn, Co для соединения-предшественника, полученному согласно примеру 3, взятого в качестве образца сравнения для образца, полученного согласно примеру 1. Согласно полученным данным соотношение переходных металлов в соединении-предшественнике составляет Ni:Mn:Co=(8.34±0.49):(0.78±0.36):(0.88±0.14), все переходные металлы - Ni, Mn и Co - распределены гомогенно. В то же время в данном соединении-предшественнике не было обнаружено каких-либо посторонних примесей, в том числе серосодержащих соединений.
На фиг. 6 представлены карты распределения элементов, полученные с помощью ЭДС, демонстрирующие пространственные распределения элементов Ni, Mn и Co для соединения-предшественника, полученному согласно примеру 4, взятого в качестве образца сравнения для соединения-предшественника, полученного согласно примеру 2. Согласно полученным данным соотношение переходных металлов в соединении-предшественнике составляет Ni:Mn:Co=(7.96±0.55):(1.02±0.53):(1.02±0.05), все переходные металлы - Ni, Mn и Co - распределены гомогенно. В то же время в данном соединении-предшественнике не было обнаружено каких-либо посторонних примесей, в том числе серосодержащих соединений.
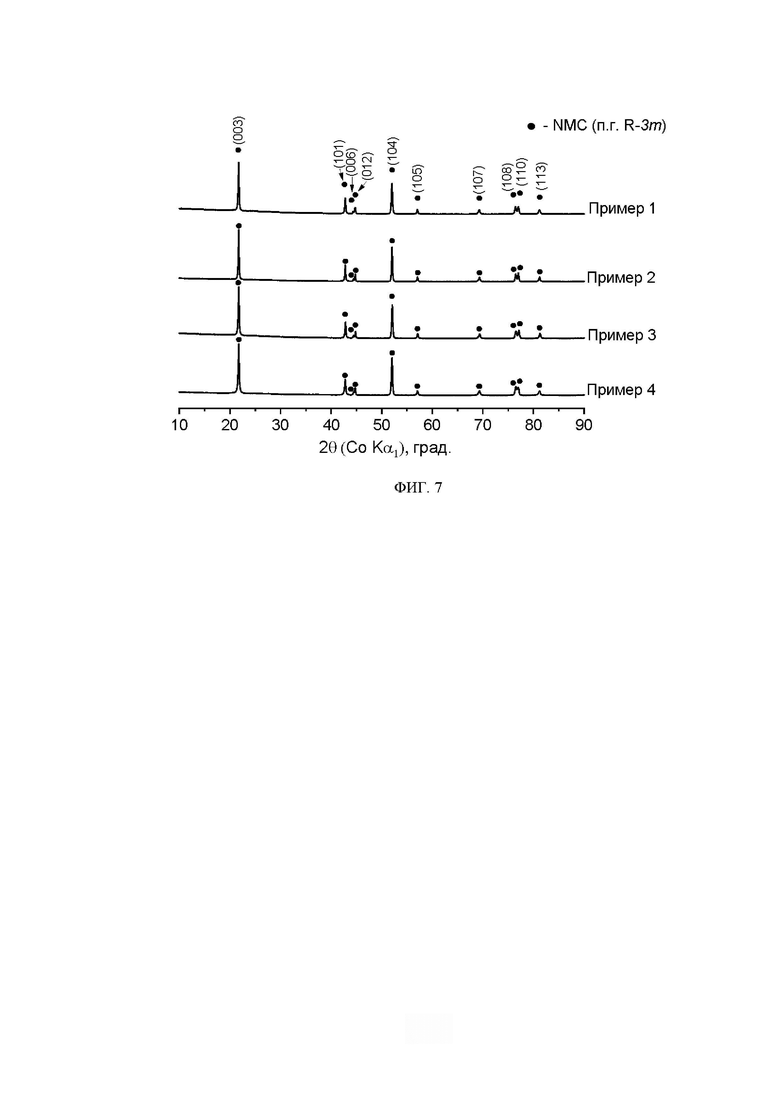
На фиг. 7 представлены рентгенограммы (рентгенограммы получены с использованием Co Кα1 излучения) композитных катодных материалов, полученных по примерам 1 и 2, а также рентгенограммы образцов сравнения, полученных по примерам 3 и 4. Согласно результатам рентгенофазового анализа, все полученные образцы представляют собой однофазные смешанные оксиды переходных металлов со слоистой структурой. Приведенные рентгенограммы были проиндицированы в соответствии с пространственной группой R-3m. Прочих кристаллических фаз, в том числе серосодержащих, не было обнаружено, что свидетельствует о том, что серосодержащий компонент представляет собой аморфную фазу.
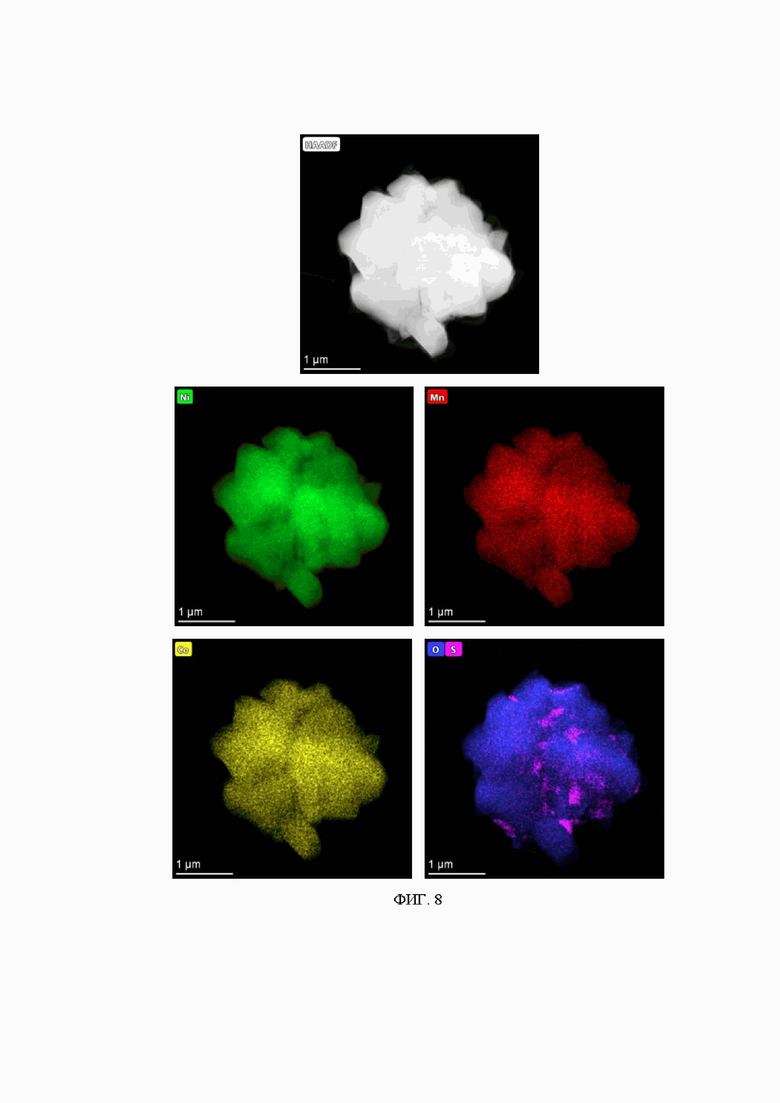
На фиг. 8 представлены карты распределения элементов, полученные с помощью ЭДС, демонстрирующие пространственные распределения элементов Ni, Mn, Co и S для композитного катодного материала, полученному согласно примеру 5, из соединения-предшественника, полученного согласно примеру 1. Согласно полученным данным соотношение переходных металлов и серы в композитном катодном материале составляет Ni:Mn:Co:S= =(7.92±0.37):(1.03±0.25):(0.99±0.15):(0.05±0.03), все переходные металлы - Ni, Mn и Co - распределены гомогенно. Карта распределения серы и кислорода для данного композитного катодного материала демонстрирует, что серосодержащий компонент композитного материала располагается как в объеме кристаллитов, так и на поверхности, особенно высокая локализация наблюдается на границах зерен.
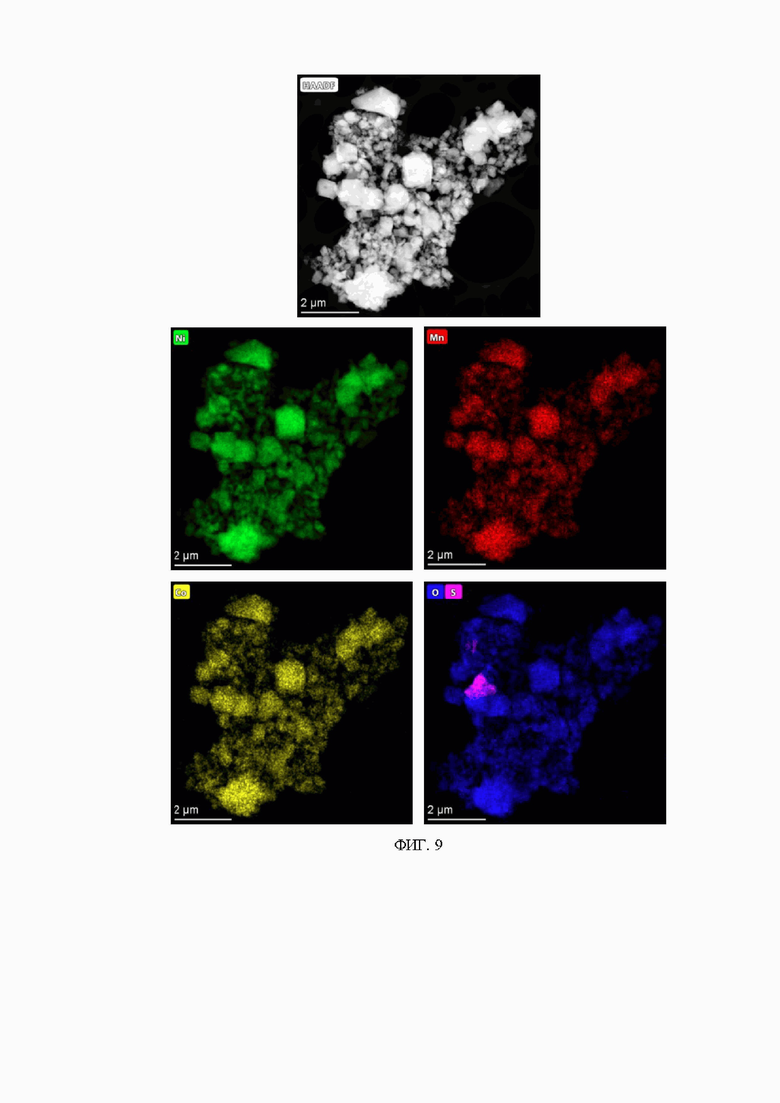
На фиг. 9 представлены карты распределения элементов, полученные с помощью ЭДС, демонстрирующие пространственные распределения элементов Ni, Mn, Co и S для композитного катодного материала, полученному согласно примеру 5 из соединения-предшественника, полученного согласно примеру 2. Согласно полученным данным соотношение переходных металлов и серы в композитном катодном материале составляет Ni:Mn:Co:S= (7.92±0.09):(0.99±0.04):(1.06±0.06):(0.03±0.02), все переходные металлы - Ni, Mn и Co - распределены гомогенно. Карта распределения серы и кислорода для данного композитного катодного материала демонстрирует, что серосодержащий компонент композитного материала располагается как в объеме кристаллов, так и на поверхности, особенно высокая локализация наблюдается на границах зерен.
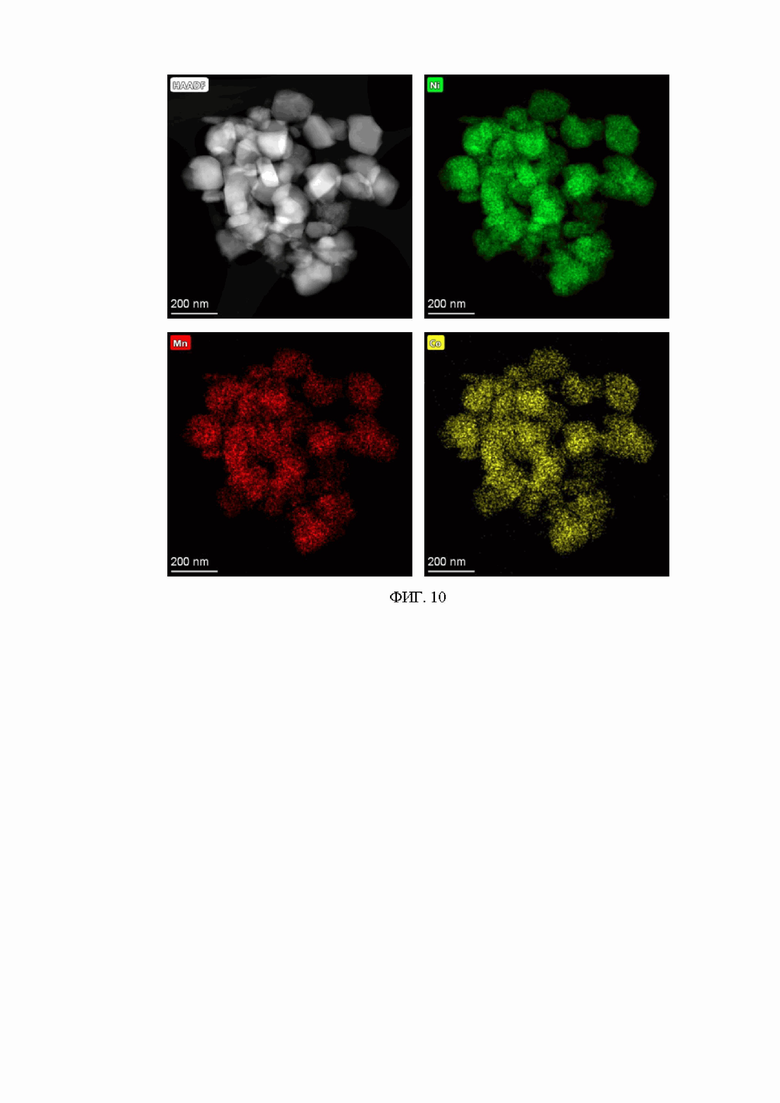
На фиг. 10 представлены карты распределения элементов, полученные с помощью ЭДС, демонстрирующие пространственные распределения элементов Ni, Mn и Co для катодного материала, полученному согласно примеру 5, из соединения-предшественника, полученного согласно примеру 4. Согласно полученным данным композитный катодный материал имеет состав LiNi0.8Mn0.1Co0.1O2, все переходные металлы - Ni, Mn и Co - распределены гомогенно. В то же время в данном соединении-предшественнике не обнаружено каких-либо посторонних примесей, в том числе серосодержащих.
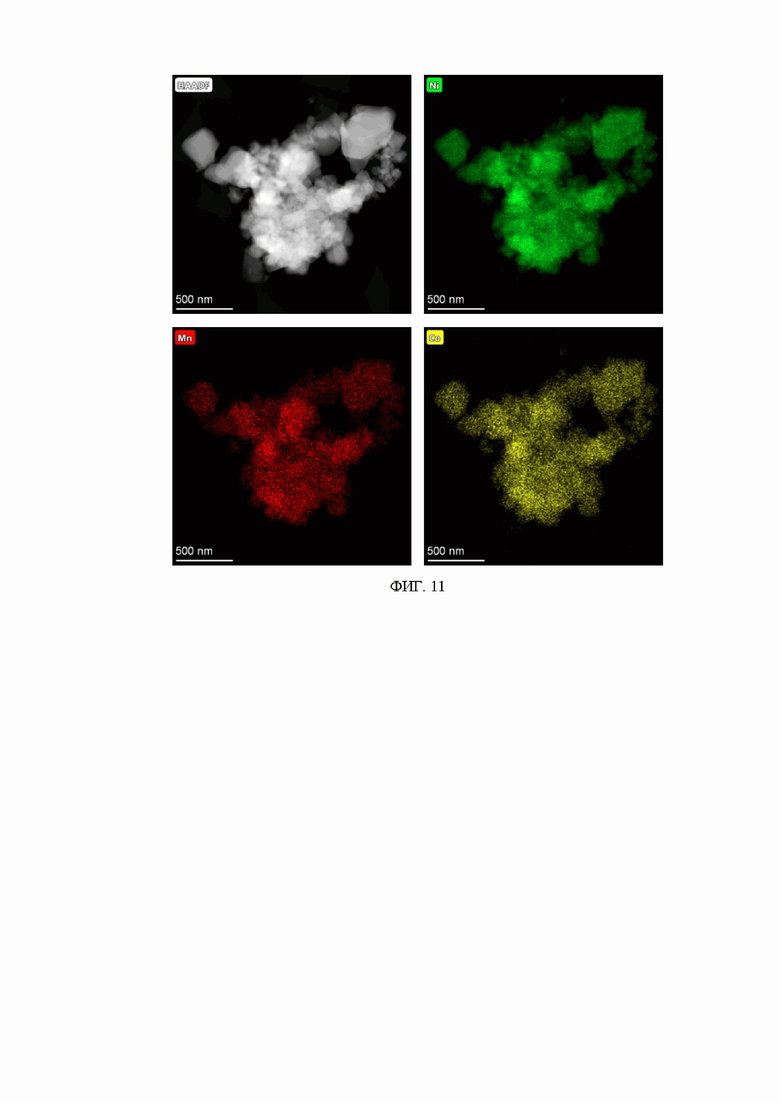
На фиг. 11 представлены карты распределения элементов, полученные с помощью ЭДС, демонстрирующие пространственные распределения элементов Ni, Mn и Co для катодного материала, полученному согласно примеру 5, из соединения-предшественника, полученного согласно примеру 4. Согласно полученным данным композитный катодный материал имеет состав LiNi0.8Mn0.1Co0.1O2, все переходные металлы - Ni, Mn и Co - распределены гомогенно. В то же время в данном соединении-предшественнике не обнаружено каких-либо посторонних примесей, в том числе серосодержащих.
На фиг. 12 представлен спектр характеристических потерь энергии электронов вблизи L края серы для катодного материала, полученного согласно примеру 5 из соединения-предшественника, полученного согласно примеру 1. Как видно, L край поглощения серы имеет сложную форму с тремя характерными особенностями со значениями энергии поглощения 174 эВ, 182 эВ и 197 эВ, которые соответствуют L2,3 переходами вблизи валентной зоны серы. Согласно работе [F. Hofer, P. Golob, New examples for near-edge fine structures in electron energy loss spectroscopy, Ultramicroscopy, 21, 379-384 (1987)], данная форма спектра характерна для серы в степени окисления +6 в тетраэдрическом окружении, что позволяет сделать вывод о том, что сера присутствует в данном композитном катодном материале в форме сульфат аниона SO42-.
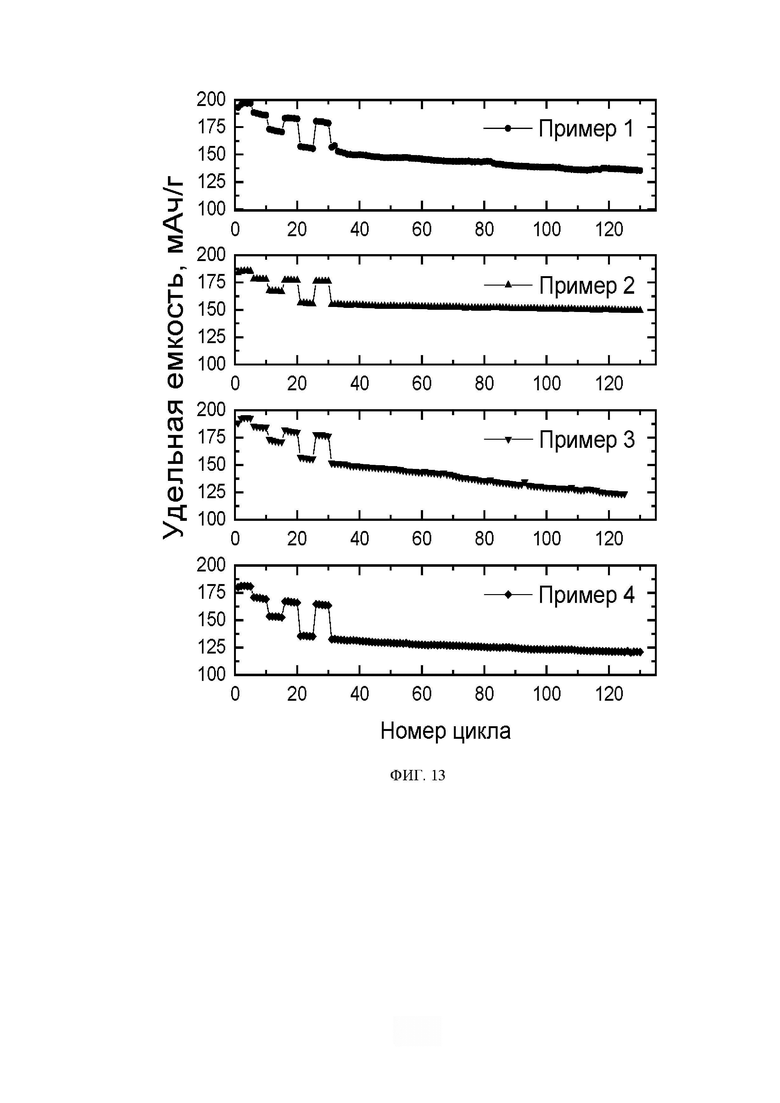
На фиг. 13 продемонстрированы зависимости удельной разрядной емкости катодных материалов, полученных согласно примеру 5 из соединения-предшественника, полученного согласно примерам 1-4, от номера цикла. Циклирование всех катодных материалов проводилось при различных скоростях в диапазоне потенциалов 2.5 - 4.3 В отн. Li/Li+ по следующей программе: 5 циклов - 0.1C, 5 циклов - 0.2C, 5 циклов - 0.5C, 5 циклов - 0.2C, 5 циклов - 1С, 5 циклов - 0.2C, 100 циклов - 1С, где С = 200 мА/г. Композитные катодные материалы, полученные согласно примеру 5, из соединений-предшественников, полученных согласно примерам 1 и 2, обладают более высокой удельной разрядной емкостью при различных скоростях, а также более высокой стабильностью при длительном циклировании по сравнению с катодными материалами, полученными из соединений-предшественников, полученных согласно примерам 3 и 4.
Осуществление изобретения
В нижеследующем описании приведены средства и методы, с помощью которых может быть осуществлено настоящее изобретение, а также приведены примеры его реализации.
Термин «активный катодный материал», используемый в настоящем описании, обозначает материал, который может входить в состав катода в электрохимических источниках тока и который способен к связыванию и высвобождению (интеркаляции и деинтеркаляции) носителей заряда при работе такого источника.
Получение активного катодного материала для литий-ионных аккумуляторов, представляющего собой серосодержащий композитный материал, содержащий компонент в виде слоистых оксидов переходных металлов - LiNixMnyCozAvO2 и аморфный серосодержащий компонент - LidSbOc , при этом композитный материал представляет собой соединение с формулой (1-a)LiNixMnyCozAvO2∙aLidSbOc, где 0.0001≤a≤0.02, 0.3≤x≤0.85, 0≤y≤0.3, 0≤z≤0.3, A - легирующая добавка (Al, Mg, Zr, W, Ti, Cr, V и др.), v≤0.1, x+y+z+v=1, 0.001≤b≤2 и 0≤c≤8, 0.001≤d≤2, состоит из двух последовательных этапов: синтез соединения-предшественника и высокотемпературный отжиг смеси соединения-предшественника и источника лития, представляющего собой литий содержащее соединение, например, LiOH, LiOH∙H2O, Li2CO3, LiCH3COO, Li2C2O4, LiNO3 или их смеси, предпочтительно LiOH, LiOH∙H2O, Li2CO3 или их смеси.
Соединение-предшественник, представляющее собой серосодержащий смешанный гидроксид или оксигидроксид состава NixMnyCozOm(OH)2-2f(SbOc)f или серосодержащий смешанный карбонат NixMnyCoz(CO3)1-g(SbOc)g (0.3≤x≤0.85, 0≤y≤0.3, 0≤z≤0.3, 0≤m≤1, 0.001≤b≤2, 0≤c≤8, 0.0001≤f≤0.05, 0.0001≤g≤0.02) может быть получено с помощью следующих методов: соосаждение, гидротермальный и сольвотермальный, включая активацию микроволновым излучением, золь-гель и другие, так называемые, методы «мягкой» химии. Далее будет более подробно приведено получение соединения-предшественника методом соосаждения.
Химические соединения для использования в настоящем изобретении являются коммерчески доступными или могут быть получены любыми известными способами из доступных реактивов.
В контексте настоящего изобретения под термином «инертная атмосфера» понимают атмосферу газа или смеси газов, которые по существу не реагируют с компонентами реакционной смеси. Примерами таких газов являются водород, азот, благородные газы, СО и/или их смеси. В качестве исходных реагентов могут быть использованы различные источники Ni, Mn и Co, обладающие высокой растворимостью в воде, для обеспечения высокой степени гомогенизации металлов в соединении-предшественнике. Для приготовления водного раствора солей переходных металлов с концентрацией от 0.1 до 2 М, содержащего также ионы-источники серы, необходимо взять хорошо растворимые в воде соли переходных металлов (Ni, Mn, Co), такие как, например, сульфаты, хлориды, ацетаты, нитраты и др. или их смесь. В случае использования солей переходных металлов, которые не содержат ионы-источники серы, к раствору переходных металлов необходимо добавить хорошо растворимые источники серосодержащих ионов, которые, в то же время не будут вступать в химические реакции с компонентами раствора переходных металлов, например, H2SO4, (NH4)2SO4, Na2SO4, K2SO4 и другие. Полученный раствор необходимо внести при постоянном перемешивании в реактор путем постепенного добавления реагентов с заданной скоростью, при этом одновременно с раствором-источником переходных металлов и серосодержащих ионов в реактор с той же скоростью должен вводится осадитель - водный или водно-аммиачный раствор гидроксида или карбоната щелочного металла, например, натрия, или калия, или цезия, предпочтительно, натрия или калия. Возможно введение серосодержащих ионов в раствор осадителя, при условии, что источник серосодержащих ионов хорошо растворим в воде и не взаимодействует с компонентами осадителя. В реакционном сосуде предварительно создана инертная атмосфера, предпочтительно с помощью аргона или азота, во избежание окисления составляющих компонентов реакционной смеси. На протяжении всего синтеза необходимо поддерживать постоянное значение pH от 7.3 до 12, предпочтительно, 10.5-11.5 в случае получения гидроксидного и/или оксигидроксидного соединения-предшественника и 7.3-9.0, предпочтительно 7.7-7.8, в случае получения карбонатного соединения-предшественника; значение температуры поддерживается на постоянном уровне 40-60°С, предпочтительно, 50-55°С. Перемешивание должно осуществляться непрерывно на протяжении всего синтеза соединения-предшественника. Непосредственное формирование частиц соединения-предшественника в процессе соосаждения может занимать от 20 минут до 5 часов, в зависимости от выбранных исходной концентрации раствора-источника переходных металлов и скоростей добавления этого раствора и раствора осадителя. Для «старения» частиц соединения-предшественника реакционную смесь оставляют перемешиваться на 2-12 часов с поддержанием инертной атмосферы, температуры и скорости перемешивания, после чего полученные частицы соединения-предшественника отделяют от раствора центрифугированием или фильтрованием, затем многократно промывают деионизированной водой и высушивают в динамическом вакууме в течение 8-12 часов при температуре 80-120°С, предпочтительно 85-95°С. Формирование соединения-предшественника устанавливают методом рентгенофазового анализа, а содержание серы в нем - с помощью энергодисперсионной рентгеновской спектроскопии.
Для получения серосодержащего композитного активного катодного материала полученное соединение-предшественник необходимо смешать с источником лития, взятого с избытком 0.01-10% от необходимого по стехиометрическому составу, предпочтительно, 3-6%, и подвергнуть высокотемпературной обработке на воздухе или в атмосфере кислорода, или в смеси азота и кислорода, или в смеси аргона и кислорода при температуре 500-1000°С, предпочтительно 750-950°С.
Образцы материалов были охарактеризованы необходимыми физико-химическими методами исследования. Фазовый состав образцов был установлен методом рентгенофазового анализа (дифрактометр Huber G670, Co Kα1 излучение). Локальный химический состав, анализ пространственного распределения элементов в объеме образцов и анализ координационного окружения и валентного состояния серы были изучены с помощью просвечивающей электронной микроскопии (микроскоп Titan Themis Z, ускоряющее напряжение 200 кВ, оборудованный приставкой Super-X для проведения элементного анализа с использованием энергодисперсионной рентгеновской спектроскопии (ЭДС) и приставкой для измерения спектров характеристических потерь энергии электронов (СХПЭЭ) Gatan Quantum ER965).
Согласно рентгенофазовому анализу, все полученные соединения-предшественники представляют собой однофазный смешанный гидроксид или оксигидроксид Ni, Mn и Co со структурным типом β-Ni(OH)2 (Фиг.1) или однофазный серосодержащий смешанный карбонат Ni, Mn и Co со структурным типом NiCO3∙H2O (Фиг.2). С помощью ЭДС было продемонстрировано, что как переходные металлы, Ni, Mn, Co (Фиг. 3-6), так и сера (Фиг. 3, 4) гомогенно распределены по всему объему соединений-предшественников. Таким образом, в соответствии с результатами проведенных измерений можно сделать вывод, что все соединения-предшественники, полученные из растворов сульфатов Ni, Mn и Co, являются серосодержащими смешанными гидроксидами или оксигидроксидами или карбонатами, причем введение серы не влияет на кристаллическую структуру соединений-предшественников.
С помощью данных методов был также изучен композитный материал, являющийся активным катодным материалом для литий-ионных аккумуляторов. Так, результаты рентгенофазового анализа (Фиг. 7) свидетельствуют об образовании кристаллического смешанного оксида лития и переходных металлов Ni, Mn и Co со слоистой структурой (пространственная группа R-3m). Присутствие прочих кристаллических фаз, в том числе серосодержащих, не было установлено с помощью данного метода, что связано с тем, что серосодержащий компонент представляет собой аморфную фазу. Для подтверждения присутствия серосодержащих компонентов в композиционных катодных материалах далее были использованы методы ЭДС и СХПЭЭ. Благодаря этим методам, а также картам, демонстрирующим распределение переходных металлов, серы и кислорода в случае композитных катодных материалов (Фиг. 8, 9, 12), было установлено, что заявляемый активный катодный материал представляет собой не что иное как композит на основе слоистого смешанного оксида переходных металлов LiNixMnyCozO2 и компонента LidSbOc на основе сульфат-аниона SO42-, локализованного на поверхности зерен, на межзеренных границах и в местах контакта зерен компонента LiNixMnyCozAvO2, так и распределенного по всему материалу.
Для приготовления электродной композиции (катодной массы) полученный активный катодный материал смешивают с одной или несколькими электропроводящими добавками и связующим веществом. В качестве электропроводящей добавки могут использоваться, например, различные формы углерода, в т.ч. графит, сажа, аморфный углерод, углеродные нанотрубки и фуллерены, проводящие полимерные материалы (на основе полианилина, полипиролла, полиэтилендиокситиофена) и т.п. Содержание электропроводящих добавок в электродной композиции по изобретению может варьироваться от 0.1 до 20 масс. %. В качестве связующего могут быть использованы, например, раствор поливинилиденфторида в N-метил-2-пирролидоне или суспензия перфторполиэтилена (фторопласт, тефлон) в воде. Содержание связующего в электродной композиции может варьироваться от 1 до 20% масс. %. Катод для литий-ионного аккумулятора может быть изготовлен из катодной массы известными в данной области техники методами. Для проведения электрохимических испытаний материалов методом гальваностатического циклирования собирали полуячейки диаметром 20 мм с анодом из металлического лития. В качестве электролита был взят 1М раствор LiPF6 в смеси органических растворителей этилен карбоната, пропилен карбоната и диметил карбоната, взятых в объемном соотношении 1:1:3, соответственно. В качестве сепаратора использовалось борсиликатное стекловолокно. Ячейки собирали в перчаточном боксе M-Braun с атмосферой аргона. К катодной смеси, состоящей из 80 масс.% активного катодного материала, 10 масс.% сажи Super-P и 10 масс.% поливинилиденфторида, добавляли 300-400 мкл N-метил-2-пирролидона и механически гомогенизировали до получения однородной суспензии. Полученную суспензию наносили на покрытую углеродом алюминиевую подложку (токосъемник) с помощью автоматического аппликатора Zehntner ZAA 2300, сушили и прокатывали на вальцах, затем вырезали электроды площадью 2 см2, которые взвешивали и окончательно высушивали при пониженном давлении (10-2 атм) при 120°С в течение 12 часов для удаления остаточной воды и растворителя (типичная массовая загрузка электродов 1.5 мг/см2).
Электрохимические испытания проводились с помощью гальваностатического циклирования при различных плотностях тока (0.1С, 0.2С, 0.5С и 1С, где 1С= 200 мА/г) в диапазоне потенциалов 2.7-4.3 В отн. Li/Li+ (Фиг. 13). С помощью данных измерений было установлено, что активные катодные материалы, представляющий собой композит состава (1-a)LiNixMnyCozAvO2∙aLidSbOc, изготовленные согласно примерам 1, 2 и 5, демонстрируют более высокий циклический ресурс, что выражается в более высоком показателе удержания емкости после 100 циклов при 1C, а также более высокие значения удельной разрядной емкости при разных плотностях тока по сравнению с катодными материалами сравнения, не включающими серосодержащего компонента, изготовленными согласно примерам 3, 4 и 5. Такое улучшение эксплуатационных характеристик катодных материалов обуславливается присутствием аморфного серосодержащего компонента, представляющего собой сульфат и/или пиросульфат и/или сульфит и/или сульфид и/или тиосульфат лития или их смесь. Так, для образцов, полученных из серосодержащего гидроксидного или оксигидроскидного соединения-предшественника, удержание емкости увеличилось примерно на 10% при длительном циклировании на скорости 1С, а для образцов, полученных из карбонатного соединения-предшественника - более чем на 5%.
Ниже представлены примеры конкретного осуществления изобретения, где в качестве электроактивного компонента LiNixMnyCozAvO2 использовали Ni-обогащенные NMC со слоистой структурой состава NMC811. С целью демонстрации преимуществ предлагаемого серосодержащего композитного активного катодного материала, также были получены NMC811 без серосодержащего компонента. Приведенные примеры иллюстрируют сущность изобретения, но никоим образом не ограничивают область его применения.
ПРИМЕР 1
Для синтеза соединения-предшественника Ni0.8Mn0.1Co0.1(OH)1.99(SO4)0.005, на основе кристаллогидратов сульфатов переходных металлов NiSO4∙6H2O, MnSO4∙2H2O и CoSO4∙6H2O, взятых в качестве исходных реагентов так, чтобы мольное соотношение металлов составляло Ni:Mn:Co= 8:1:1, было приготовлено 100 мл 2M водного раствора. Данный водный раствор, а также 100 мл 4M водно-аммиачного раствора NaOH, где аммиак был взят в качестве комплексообразующего агента, по каплям подавались в реактор общим объемом 500 мл при постоянном перемешивании. В реактор предварительно добавили 100 мл деионизированной воды, а также в реакторе была создана инертная атмосфера путем его заполнения аргоном во избежание окисления катионов переходных металлов. Скорость подачи растворов составляла 1 мл/мин. Температура реактора, которая поддерживалась на протяжении всего синтеза, составляла 50°С. Также в реакторе поддерживалось постоянное значение pH = 11.4-11.5. После полного введения растворов переходных металлов и NaOH в реактор, полученный осадок и маточный раствор были выдержаны в течении 12 часов при перемешивании и температуре 50°С. После этого полученный осадок был многократно промыт деионизированной водой и высушен в динамическом вакууме при 90°С в течение 12 ч. Согласно рентгенофазовому анализу (Фиг. 1) и энергодисперсионной рентгеновской спектроскопии (Фиг. 3), полученный осадок представляет собой соединение-предшественник, осажденное в виде смешанного гидроксида или оксигидроксида, с соотношением переходных металлов и серы Ni:Mn:Co:S=(8.06±0.03):(0.9±0.01):(0.9±0.02):(0.05±0.03).
ПРИМЕР 2
Для синтеза соединения-предшественника Ni0.8Mn0.1Co0.1(CO3)0.998(SO4)0.002, на основе кристаллогидратов сульфатов переходных металлов NiSO4∙6H2O, MnSO4∙2H2O и CoSO4∙6H2O, взятых в качестве исходных реагентов так, чтобы мольное соотношение металлов составляло Ni:Mn:Co= 8:1:1, было приготовлено 100 мл 2M водного раствора переходных металлов. Данный водный раствор, а также 100 мл 2M водно-аммиачного раствора Na2CO3, где аммиак был взят в качестве комплексообразующего агента, по каплям подавались в реактор общим объемом 500 мл, в который предварительно добавили 100 мл деионизированной воды. В реакторе была создана инертная атмосфера путем его заполнения аргоном во избежание окисления катионов переходных металлов. Скорость подачи растворов составляла 1 мл/мин. Температура реактора, которая поддерживалась на протяжении всего синтеза, составляла 56°С. Также в реакторе поддерживалось постоянное значение pH = 7.7-7.8. После полного вливания растворов переходных металлов и Na2CO3 в реактор, полученный осадок и маточный раствор были выдержаны в течении 12 часов при перемешивании и температуре 55°С. После этого полученный осадок был многократно промыт деионизированной водой и высушен в динамическом вакууме при 110°С в течение 12 ч. Согласно рентгенофазовому анализу и энергодисперсионной рентгеновской спектроскопии (Фиг. 4), полученный осадок представляет собой соединение-предшественник, осажденное в виде смешанного карбоната, с соотношением переходных металлов и серы Ni:Mn:Co:S=(8.02±0.03):(0.85±0.03):(0.99±0.02):(0.02±0.01).
ПРИМЕР 3 (сравнительный для гидроксидов)
Аналогичен примеру 1, отличие состоит в том, что в качестве исходных реагентов для синтеза соединения-предшественника Ni0.8Mn0.1Co0.1(OH)2 были использованы кристаллогидраты ацетатов Ni(CH3COO)2∙4H2O, Mn(CH3COO)2∙4H2O и Co(CH3COO)2∙2H2O, взятые так, чтобы мольное соотношение металлов составляло Ni:Mn:Co= 8:1:1, а концентрация водного раствора составляла 0.5M. Также отличие состоит в том, что концентрация водно-аммиачного раствора NaOH составляла 1М. Согласно рентгенофазовому анализу и энергодисперсионной рентгеновской спектроскопии (Фиг. 5), полученный осадок представляет собой соединение-предшественник, осажденное в виде не содержащего серу смешанного гидроксида или оксигидроксида, с соотношением переходных металлов Ni:Mn:Co=(8.34±0.49):(0.78±0.36):(0.88±0.14).
ПРИМЕР 4 (сравнительный для карбонатов)
Аналогичен примеру 3, отличие состоит в том, что в качестве исходных реагентов для синтеза соединения-предшественника Ni0.8Mn0.1Co0.1CO3 были использованы кристаллогидраты ацетатов Ni(CH3COO)2∙4H2O, Mn(CH3COO)2∙4H2O и Co(CH3COO)2∙2H2O, взятые так, чтобы мольное соотношение металлов составляло Ni:Mn:Co= 8:1:1, а концентрация водного раствора составляла 0.5M. Также отличие состоит в том, что концентрация водно-аммиачного раствора Na2CO3 составляла 0.5М. Согласно рентгенофазовому анализу и энергодисперсионной рентгеновской спектроскопии (Фиг. 6), полученный осадок представляет собой соединение-предшественник, осажденное в виде не содержащего серу смешанного карбоната, с соотношением переходных металлов Ni:Mn:Co=(7.96±0.55):(1.02±0.53):(1.02±0.05).
ПРИМЕР 5
Для синтеза активного катодного материала соединения-предшественники, полученные в примерах 1-4, были смешаны с LiOH∙H2O, взятого с 3 масс.% (в случае примеров 2 и 4) и 6 масс.% (в случае примеров 1 и 3) избытком от стехиометрии. Полученная смесь была механически гомогенизирована и отожжена при 750°С в токе кислорода в течение 12 ч, скорость нагрева составляла 5°С/мин. Согласно рентгенофазовому анализу (Фиг. 7), энергодисперсионной рентгеновской спектроскопии (Фиг. 8-11) и спектроскопии характеристических потерь энергии электронов (Фиг. 12), полученные порошки темно-серого или черного цвета представляют собой активные катодные материалы для литий-ионных батарей, являющиеся композитными материалами на основе компонента слоистых смешанных оксидов переходных металлов и аморфного серосодержащего компонента в случае примеров 1 и 2, соответственно: LiNi0.8Mn0.1Co0.1O2∙Li2S0.0050O1.015 и LiNi0.8Mn0.1Co0.1O2∙Li2S0.0027O1.0081, или слоистыми смешанными оксидами переходных металлов в случае примеров 3 и 4 состава LiNi0.8Mn0.1Co0.1O2.



Изобретение относится к электротехнической промышленности и может быть использовано для производства материала положительного электрода (катода) на основе слоистых оксидов переходных металлов для литий-ионных аккумуляторных батарей. Активный катодный серосодержащий композитный материал для литий-ионных аккумуляторов представляет собой соединение формулы (1-a)LiNixMnyCozAvO2⋅aLidSbOc, где LiNixMnyCozAvO2 - компонент, содержащий слоистые оксиды переходных металлов, LidSbOc - аморфный серосодержащий компонент, A - легирующая добавка, выбранная из группы: Al, Mg, Zr, W, Ti, Cr, V, v≤0,1, x+y+z+v=1, 0.3≤x≤0.85; 0≤y≤0.3; 0≤z≤0.3; 0.0001≤a≤0.02, 0.001≤b≤2; 0≤c≤8; 0.001≤d≤2, причем указанный композитный материал получен из серосодержащего соединения-предшественника формулы: NixMnyCozOm(OH)2-2f(SbOc)f или NixMnyCoz(CO3)1-g(SbOc)g, где 0.3≤x≤0.85; 0≤y≤0.3; 0≤z≤0.3, 0≤m≤1, 0.001≤b≤2, 0≤c≤8, 0.0001≤f≤0.05, 0.0001≤g≤0.02. Технический результат заключается в улучшении эксплуатационных характеристик катодного материала, а именно в увеличении циклов заряда/разряда при сохранении высокой удельной емкости благодаря введению в состав катода аморфного серосодержащего компонента - LidSbOc. 6 з.п. ф-лы, 13 ил., 4 пр., 1 табл.
1. Активный катодный серосодержащий композитный материал для литий-ионных аккумуляторов, представляющий собой соединение формулы (1-a)LiNixMnyCozAvO2∙aLidSbOc, где LiNixMnyCozAvO2 – компонент, содержащий слоистые оксиды переходных металлов, LidSbOc – аморфный серосодержащий компонент, A – легирующая добавка, выбранная из группы: Al, Mg, Zr, W, Ti, Cr, V, v≤0.1, x+y+z+v=1, 0.3≤x≤0.85; 0≤y≤0.3; 0≤z≤0.3; 0.0001≤a≤0.02, 0.001≤b≤2; 0≤c≤8; 0.001≤d≤2.
2. Активный катодный серосодержащий композитный катодный материал по п.1, характеризующийся тем, что LiNixMnyCozAvO2 присутствует в виде кристаллических зерен.
3. Активный катодный серосодержащий композитный материал по п.1, характеризующийся тем, что аморфный LidSbOc представляет собой по крайней мере одно соединение, выбранное из группы: сульфат, пиросульфат, сульфит, сульфид, тиосульфат лития.
4. Активный катодный серосодержащий композитный катодный материал по п.1, характеризующийся тем, что соединения серы распределены как на поверхности зерен, на межзеренных границах и в местах контакта зерен компонента LiNixMnyCozAvO2, так и по всему объему материала.
5. Активный катодный серосодержащий композитный материал по п.1, характеризующийся тем, что получен при взаимодействии с источником лития из состава серосодержащего соединения-предшественника формулы: NixMnyCozOm(OH)2-2f(SbOc)f или NixMnyCoz(CO3)1-g(SbOc)g, где 0.3≤x≤0.85; 0≤y≤0.3; 0≤z≤0.3, 0≤m≤1; 0.001≤b≤2; 0≤c≤8; 0.0001≤f≤0.05, 0.0001≤g≤0.02.
6. Активный катодный серосодержащий композитный катодный материал по п. 5, характеризующийся тем, что соединения-предшественники получены с помощью методов соосаждения, гидротермального и сольвотермального синтеза, включая активацию микроволновым излучением, золь-гель.
7. Активный катодный серосодержащий композитный катодный материал по п. 5, характеризующийся тем, что соединения-предшественники получены из водорастворимых солей переходных металлов, выбранных из группы: сульфаты, хлориды, ацетаты, нитраты или их смеси, содержащих ионы-источники серы.
| US 8268198 B2, 18.09.2012 | |||
| US 10547056 B2, 28.01.2020 | |||
| RU 2011148908 A, 10.06.2013 | |||
| Способ получения нанокомпозиционных катодов для литий-ионных аккумуляторов | 2015 |
|
RU2634306C2 |
Авторы
Даты
2021-05-31—Публикация
2020-12-11—Подача