[01] Область техники
[02] Изобретение относится к области фармакологии и хирургии, а именно к применению фосфолипидной эмульсии, содержащей дигидрокверцитин, (препарат «Фламена») для защиты тканей донорского органа, а также профилактики его отторжения, и может применяться в трансплантологии.
[03] Уровень техники
[04] Из уровня техники широко известна фосфолипидная эмульсия «Фламена», содержащая лецитин, дигидрокверцитин и глицин. Также известны возможности применения данного состава для лечения хронических эндометритов (см. патент РФ RU 2622024, 08.06.2018) и синдрома ишемии-реперфузии (см. патент РФ RU 2766681, 15.03.2022). Однако, известные способы применения данного препарата не направлены на защиту тканей донорских органов при трансплантации.
[05] Из уровня техники также известно применение составов в виде эмульсий для защиты донорского органа при трансплантации. В частности, в патенте РФ RU 2234503, 22.11.2004 (наиболее близкий аналог) раскрыта возможность применения фосфолипидной эмульсий, содержащей соединение - аналог витамина D (в частности, (Е)-7-[6-(3,4-Бис-гидроксиметил-феноксиметил)-пиридин-2-ил]-3-этил-нон-6-ен-3-ол), соевое масло, яичный фосфолипид и глицерин. Однако, указанный аналог не обеспечивает эффективное снижение скорости рассасывания трансплантируемой ткани.
[06] Технической проблемой, на решение которой направлено заявленное изобретение, является недостаточная эффективность защиты тканей донорского органа и профилактики его отторжения при трансплантации.
[07] Раскрытие сущности изобретения
[08] Технический результат изобретения заключается в увеличении времени отторжения трансплантируемой ткани, выражающемся в уменьшении скорости рассасывания трансплантата, снижении уровня окислительного стресса, предотвращении возникновении воспалительной реакции фагоцитов.
[09] Указанная задача решается, а приведенный технический результат достигается в заявленном изобретении за счет того, что для защиты- ткани при трансплантации применяют фосфолипидную эмульсию, содержащей эффективное количество дигидро-кверцетина (ДГК), причем эмульсия, содержит следующие компоненты в г на 100 мл: глицин - 3,5±0,5, яичный лецитин - 3,5±0,8, дигидрокверцетин - 0,35±0,1, вода - остальное.
[010] В частных случая реализации изобретения эмульсия может содержать фармацевтически приемлемые вспомогательные вещества При этом фосфолипидную эмульсию могут вводить перорально в суточной дозе для млекопитающих 0,29-18 мл на 1 кг массы (веса) пациента
[011] Краткое описание чертежей
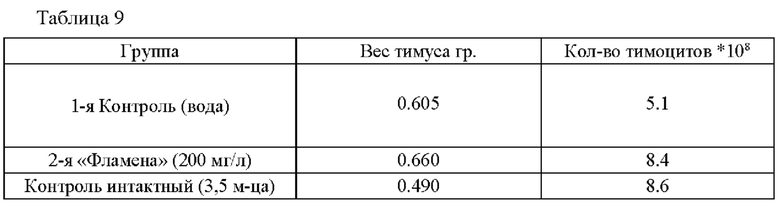
[012] Изобретение поясняется фигурами, где на фигуре 1 показано изменение АФК-генерирующей активности лейкоцитов крови в процессе трансплантации ткани с использованием заявленного изобретения, а на фигуре 2 - динамика изменения интенсивности хемилюминесцентного ответа фагоцитов крови после трансплантации печеночной ткани с использованием заявленного изобретения.
[013] Осуществление изобретения
[014] Заявленное изобретение предусматривает применение препарата «Фламена» в виде фосфолипидного комплекса, содержащего дигидрокверцетин (ДГК). При этом препарат также может дополнительно включать фармацевтически приемлемые вспомогательные вещества, например, загустители. Введение препарата осуществляется, предпочтительно, перорально. Также возможен вариант внутривенного введения препарата. Суточная доза препарата составляет от 0,29 до 18 мл эмульсии на 1 кг веса мелкопитающего. Возможно введение препарата как один раз в день, так и несколько раз (например, 3 раза) в день при условии соблюдения суточной дозировки.
[015] Для подтверждения эффективности заявленного изобретения проводили две серии исследований по изучению действия фосфолипидного комплекса на процесс трансплантации ткани. Изучение проводили на крысах самцах линии Вистар, полученных из питомника РАМН «Столбовая», после двухнедельного карантина в виварии института. Животных содержали в стандартных условиях со свободным доступом к корму и воде. Основу корма составляли специализированные брикетированные гранулированные корма фирмы «МЭСТ».
[016] Первая серия экспериментов
[017] В опытах использовали 60 крыс «Wistar» со средним весом 210 гр. (возраст 2 месяцев). Всех животных разбили на 3 группы: 1 - контроль, 2 и 3 - опытные по 20 шт. в каждой группе. Всем животным сделали подкожную трансплантацию тканей печени и легкого в область лопатки. Под уретановым наркозом (0,5 мл /100 гр. веса 20% раствора) у животных в области лопатки выстригали волосяной покров, делали небольшой разрез кожи (4-5 мм), через который тупой лопаточкой формировали подкожный карман, в который помещали кусочки ткани, и затем разрез зашивали.
[018] Донором ткани печени и легкого являлись 1-месячные крысы весом 100 гр. Под эфирным наркозом проводили декапитацию животного, отрезали кусочки печени, легкого и измельчали до размера 3 мм в растворе Хенкса. Каждой крысе в подкожный карман помещали 4 кусочка ткани печени и легкого весом по 80 мг (по 2 шт. каждой ткани). Операционное помещение в течение 2 час до трансплантации облучали ультрафиолетом, инструменты и операционное поле обрабатывали спиртом.
[019] Контрольную группу животных в течение всего эксперимента поили обычной водой.
[020] Второй группе животных в воду добавляли раствор препарата «Фламена» с исходной концентрацией дигидрокверцетина (ДГК) 4 г/л из расчета 12 мл/л, что составляло 48 мг/л, что соответствовало 1,6⋅10-4 М раствору ДГК.
[021] Третьей группе животных в воду добавляли 60 мл раствора препарата «Фламена» на литр раствора, что составляло 240 мг/л, что соответствовало 8⋅10-4 М раствору ДГК.
[022] Среднесуточное потребление воды составило в контрольной группе - 22 мл, во 2-ой - 40 мл, в 3-й - 35 мл на 100 г веса.
[023] Через 10 дней из каждой группы забивали по 5 крыс и извлекали трансплантаты для исследования.
[024] В таблице 1 показаны результаты исследований в разных группах
[025]
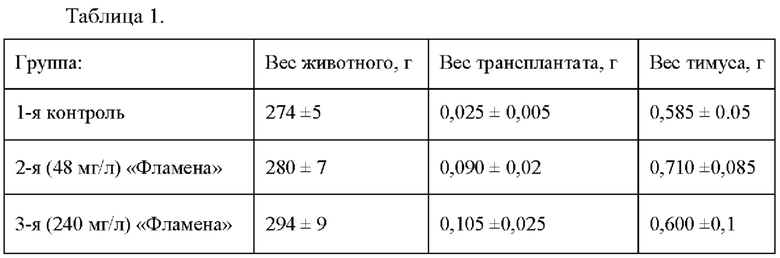
[026] Визуальный осмотр трансплантатов показал следующее
[027] 1 группа (контроль): трансплантат в виде горошины, темного цвета, похожий на ткань печени, других кусочков не обнаружено.
[028] 2-я группа (опыт), трансплантат в виде диска, диаметром 0,7-0,8 см, толщиной 0,5 см, из 2-х слоев. 1-й наружный темного цвета, напоминает ткань печени, 2-й внутренний светлый, более плотный.
[029] 3-я группа (опыт). Обнаруживался трансплантат в виде диска, диаметром 1,2 см, толщиной - 0,4 см. Наружный слой серо-розовый, мягкий по консистенции, внутренний слой светлый, более плотный, похожий на хрящевую ткань.
[030] Было проведено гистологическое исследование биологического материала
[031] Через 19 дней после начала опыта из каждой группы провели декапитацию 5 крыс и извлекли трансплантаты.
[032] Визуальный осмотр трансплантатов показал следующее
[033] 1-я группа (контроль): трансплантат был представлен в виде горошины размером 0,1-0,15 см3, расположен ближе к месту разреза, ткань красного цвета, плотная.
[034] 2-я группа (опыт): обнаружено 2 трансплантата размером 0,1 см3 и 0,3-0,4 см3, мягкие по консистенции, похожие на ткань печени.
[035] 3-я группа (опыт): обнаружено 2 трансплантата размером 0,3-0,4 см3, мягкий по консистенции, напоминает ткань печени.
[036] Через 26 дней после начала опыта провели декапитацию 5 крыс из каждой группы и извлекли трансплантаты.
[037] Визуальный осмотр трансплантатов показал следующее
[038] 1 группа (контроль): обнаружены еле заметные следовые количества трансплантата (меньше 0,1 см3) размер и вес которых измерить достоверно не представляло возможным.
[039] 2-я группа (опыт) - обнаружен трансплантат размером около 0,35 см3-0, 45 см3
[040] 3-я группа (опыт) - обнаружен трансплантат размером 0,35 см3-0,45 см3
[041] В таблице 2 показаны результаты исследований в разных группах через 26 дней после начала опыта
[042]
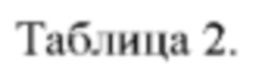
[043] Через 37 дней провели декапитацию оставшихся животных по 5 шт. из каждой группы.
[044] При визуальном осмотре трансплантаты в контрольной группе (1) не обнаружены. В экспериментальной (2) и (3) группе обнаружены диффузные множественные фрагменты ткани печени, измерение веса которых были затруднены.
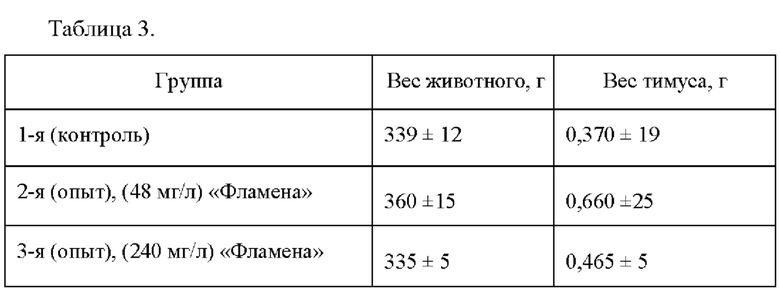
[045] В таблице 3 показаны результаты исследований в разных группах через 37 дней после начала опыта.
[046]
[047] АФК-генерирующую активность полиморфноядерных лейкоцитов и цельной крови определяли по интенсивности люминолзависимого хемилюминесцентного ответа при стимуляции ФМА (форбол-1,2 миристат-1,3 ацетат).
[048] На фигуре 1 показано изменение АФК-генерирующей активности лейкоцитов крови в процессе трансплантации ткани с использованием препарата «Фламена»
[049] На основании гистологических исследований установлено, что в ответ на аллогенную пересадку ткани печени происходила клеточная и тканевая реакция, направленная на ограничение инородного тела в виде ряда последовательных процессов, ведущих к формированию капсулы: от молодой грануляционной ткани - созревающей грануляционной ткани - фиброзной ткани. При этом ткань печени некротизируется с последующим рассасыванием.
[050] Что касается размеров трансплантированной ткани, то в начальный период трансплантат несколько увеличивался за счет отека и клеточных реакций. Далее наблюдали уменьшение отека, частичное рассасывание трансплантата, превращение грануляционной ткани в фиброзную с формированием в зоне трансплантата хронического продуктивного воспаления (фиброза, гранулем инородного тела, полей ксантомных клеток).
[051] Через 26-27 дней после трансплантации в контроле, практически, не было обнаружено ткани печени.
[052] В экспериментальных же группах животных, где использовали препарат «Фламена», обнаружены фрагменты ткани печени через 37 дней. Таким образом, были выявлены различия в динамике рассасывания ткани печени, трансплантированной в подкожный «карман» животного. Торможение процесса рассасывания ткани печени составляло 28-35% в группах животных, использующих перорально препарат «Фламена».
[053] Наиболее оптимальная концентрация препарата «Фламена», достаточная для увеличения времени отторжения трансплантата составила 20 мг/кг веса животного ежесуточно.
[054] Вторая серия экспериментов
[055] В опыт взяли 60 крыс «Wistar» со средним весом 210 гр. (возраст 2 месяцев). Всех животных разбили на 3 группы:
1. Контроль (20 шт.), животных в течение всего эксперимента поили обычной водой.
2. Опытные (20 шт.), в воду добавляли раствор препарата «Фламена» с исходной концентрацией дигидрокверцетина (ДГК) 4 гр/л из расчета 50 мл/л, т.е 200 мг/л.
[056] 3. Опытные (20 шт.). Животных поили 1% спиртовым раствором ДГК с концентрацией 200 мг/л.
[057] Всем животным сделали подкожную трансплантацию ткани печени в область лопатки. Под уретановым наркозом (0,5 мл /100 гр. веса 20% р-ра) у животных в области лопатки выстригали волосяной покров, делали небольшой разрез кожи (4-5 мм) через который тупой лопаточкой формировали подкожный карман, в который помещали кусочки ткани, и затем разрез зашивали. Через 8 дней швы снимали.
[058] Донором ткани печени являлась 1-месячная крыса весом 100 гр. Под эфирным наркозом животное забивали, отрезали печень и измельчали до размера 3 мм3 в растворе Хенкса. Каждой крысе в подкожный карман помещали 4 кусочка ткани печени. Операционное помещение в течение 2 час облучали ультрафиолетом, инструменты и операционное поле обрабатывали спиртом.
[059] Через 12 дней после трансплантации взяли на биохимию по 1 крысе из каждой группы и дополнительно сделали вскрытие 3 крысам из контрольной группы и по 3 крысы из 2 и 3 группы. Трансплантаты взвесили и сфотографировали.
[060] Результаты осмотра показали следующее.
[061] 1-я группа (контроль): 1-я крыса - трансплантат в виде отдельных точечных вкраплений; 2-я крыса - 2 небольших кусочка трансплантата общим весом - 0,025 г; 3-я крыса - трансплантат 1 кусочек, весом 0,180 г.
[062] 2-я группа (опытные): 1-я крыса - трансплантат 1 кусочек, весом 0,440 г; 2-я крыса - трансплантат 1 кусочек, весом 0,500 г; 3-я крыса - трансплантат 1 кусочек, весом 0,580 г.
[063] 3-я группа опытные: 1-я крыса - трансплантат 1 кусочек, весом 0,032 г; 2-я крыса, трансплантат 1 кусочек, весом 0,600 г; 3-я крыса - трансплантат 1 кусочек, весом 0,580 г.
[064] Через 19 дней взяли на биохимию по 1 крысе. Из каждой группы для анализа использовали по 3 животных.
[065] 1-я группа (контроль): 1-я крыса - трансплантат - 1 кусочек, весом 0,025 г; 2-я крыса - 1 кусочек трансплантата весом 0,020 г; 3-я крыса - 1 кусочек трансплантата общим весом 0,018 г.
[066] 2-я группа (опытные): 1-я крыса - 1 кусочек трансплантата весом 0,035 г. и несколько отдельных точечных вкраплений; 2-я крыса - 1 кусочек трансплантата весом 0,060 г; 3-я крыса - 2 кусочка трансплантата общим весом 0,055 г.
[067] 3-я группа опытные: 1-я крыса - 1 кусочек трансплантата весом 0,030 г; 2-я крыса, трансплантат 1 кусочек, весом 0,410 г; 3-я крыса - трансплантат 1 кусочек, весом 0,480 г.
[068] Через 27 дней взяли анализы на биохимию. Дополнительно от 2 животных из 2-ой группы и 3 группы взяли биоматериал на гистологию. У всех животных взяли тимус для определения тимоцитов.
[069] 1-я группа (контроль): трансплантат не обнаружен.
[070] 2-я группа (опытные): 1-я крыса - несколько отдельных точечных вкраплений размером 0,2-0,3 мм общим весом 0,060 г; 2-я крыса - 1 кусочек трансплантата весом 0,055 г; 3-я крыса - 1 кусочек трансплантата весом 0,047 гр.
[071] 3-я группа опытные: 1-я крыса - несколько отдельных точечных вкраплений размером 0,1-0,2 мм. 2-я крыса - 1 кусочек трансплантата весом 0,040 г; 3-я крыса - 1 кусочек трансплантата весом 0,035 г.
[072] Через 37 дней остался трансплантат только у опытных животных из 2-ой группы, которых поили препаратом «Фламена» (50 мл/л или 200 мг/л). Был обнаружен 1 кусочек, весом 0,035 г.
[073] В таблице 4 приведены показатели крови после трансплантации ткани печени в подкожный карман крыс через 3- 4 дня после трансплантации
[074]
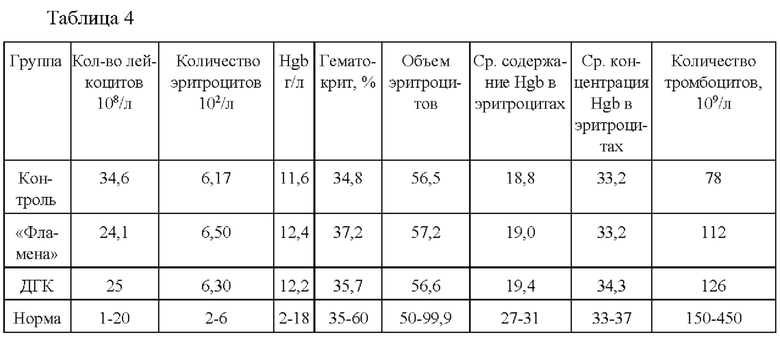
[075] В таблице 5 приведены показатели крови через 18 дней после трансплантации
[076]
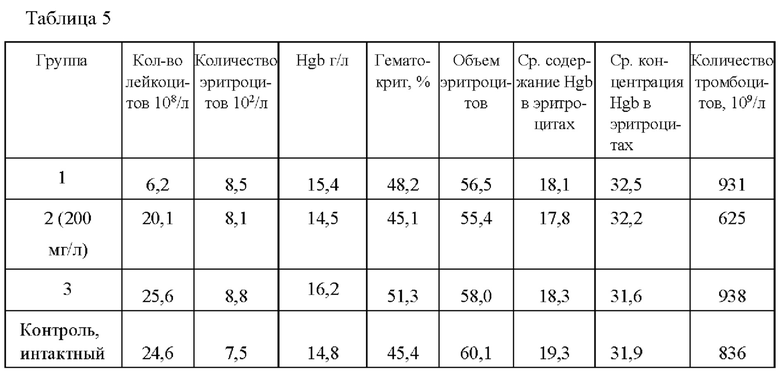
[077] В таблице 6 приведены показатели крови через 27 дней после трансплантации.
[078]
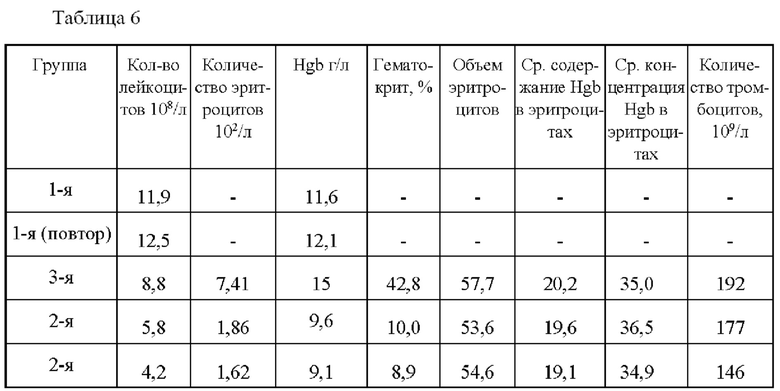
[079] В таблице 7 приведены показатели крови через 35 дней после трансплантации
[080]
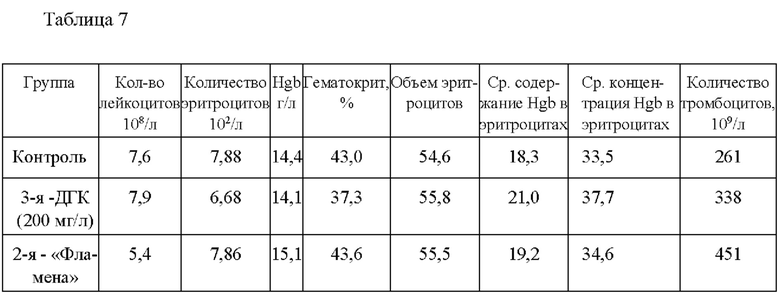
[081] Препарат «Фламена» не внес сбоя в систему в целом, что можно утверждать по достаточно стабильному состоянию показателей крови.
[082] В таблице 8 показаны результаты исследования количества тимоцитов через 27 дней после трансплантации ткани печени
[083]
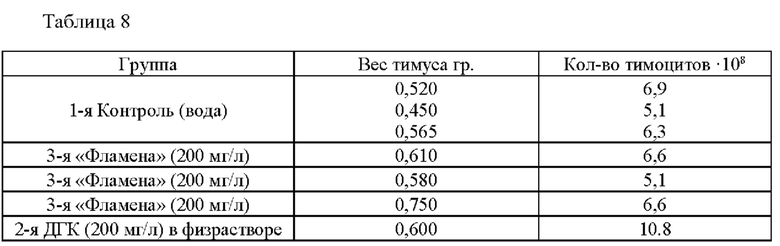
[084] В таблице 9 показаны результаты исследования количества тимоцитов через 37 дней после трансплантации ткани печени.
[085]
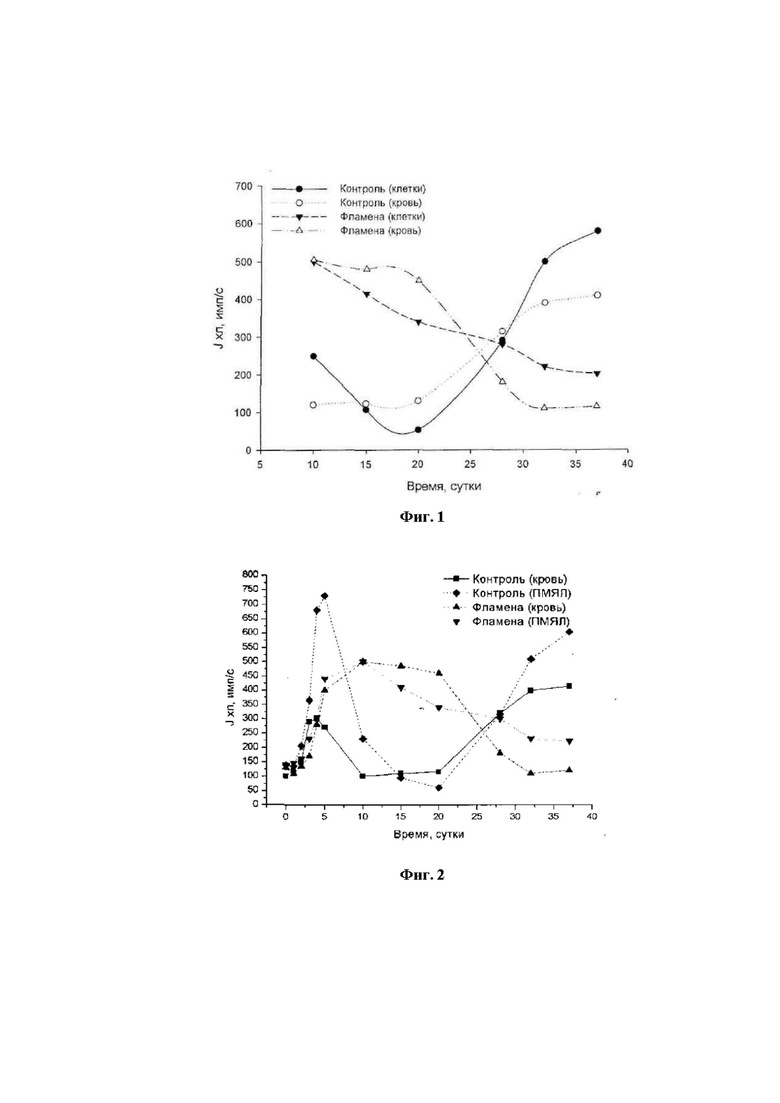
[086] На фигуре 2 показана динамика изменения интенсивности хемилюминесцентного ответа фагоцитов крови после трансплантации печеночной ткани с использованием препарата «Фламена». Как видно на фигуре, у контрольных животных после трансплантации ткани печени в подкожный карман в плазме крови развивается мощнейший окислительные стресс, в 7-8 раз превышающий уровень активных форм кислорода нормального животного. Через 10-20 дней состояние нормализуется. В дальнейшем, спустя 17-20 дней после операции, вновь возобновлялась активность фагоцитирующих клеток, характеризуя агрессивную реакцию организма. Таким образом, у контрольных животных было отмечено двухэтапное возрастание АФК-генерирующей активности фагоцитов, что, по-видимому, связано с развитием воспалительного процесса. У экспериментальной же группы животных после операции продукция активных форм кислорода была снижена (в 1,7-1,8 раз ниже по сравнению с контролем), что свидетельствует об ослаблении воспалительного процесса, интенсивность которого монотонно падала, приходя в норму к 37-40 суткам. Препарат «Фламена» позволил минимизировать воспалительные реакции организма, оказал иммунокоррегирующее действие, что позволило длительно сохранять трансплантированную ткань.
[087] Исследование применения фосфолипидного нанокомплекса «Фламена», состоящего из липосом, содержащих лецитин, дигидрокверцетин (ДГК) и глицин при суточном введении в дозе по ДГК 20-70 мг/кг после трансплантации ткани достоверно показало, что отторжение ткани происходила позже по сравнению с контролем. Трансплантаты в опыте жили по времени на 28-35% дольше. Рассасывание трансплантата в контроле сопряжено с превращением грануляционной ткани в фиброзную, и с формированием в зоне трансплантата хронического продуктивного воспаления (фиброза, гранулем инородного тела, полей ксантомных клеток). Применение препарата «Фламена» снижает уровень окислительного стресса и предотвращает вторичную воспалительную реакцию фагоцитов, что приводит к более длительному сохранению трансплантированной ткани.
[088] Также установлено, что в указанных концентрациях препарат «Фламена» не влияет на показатели крови. Применение заявленного изобретения является более эффективным в процессе сохранения трансплантата по сравнению с 1%-ным спиртовым раствором дигидрокверцетина аналогичной концентрации.
[089] Наиболее оптимальная доза препарата «Фламена», ведущая к увеличению времени отторжения трансплантата для крыс составила 50-70 мг/кг веса в сутки по ДГК, что соответствует 13-18 мл эмульсии на 1 кг веса для крысы. Для человека по причине иного метаболизма эффективная доза составляет от 0,29 до 5,7 мл эмульсии на 1 кг веса в сутки. Соответственно, для человека весом 70 кг суточная доза будет составлять 20,3-400 мл эмульсии, но наиболее оптимально вводить до 250 мл эмульсии в сутки.
[090] Применение нанокомплекса «Фламена», содержащего липосомальную форму фосфолипида, участвующего в структуре биомембран, ДГК антиоксиданта с высоким антиокислительным и антирадикальным потенциалом, а также аминокислотой, которая тормозит апоптоз клеток, обеспечивает иммунокоррегирующее действие на реакции врожденного иммунитета при его использовании в данных условиях трансплантации ткани печени.
[091] Несмотря на то, что результаты проведенных исследований относятся к защите тканей донорской печени и легкого, они также являются релевантными и по отношению к другим донорским органам. Так, специалисту в данной области техники будет очевидно, что описанные в настоящей заявке механизмы защиты трансплантируемой ткани являются универсальными. Следовательно заявленное изобретение может применяться для защиты трансплантируемых тканей и профилактики их отторжения по отношению к любому донорскому органу.
Настоящее изобретение относится к применению фосфолипидной эмульсии, содержащей эффективное количество дигидрокверцетина (ДГК), для защиты тканей донорского органа при трансплантации, при котором используют фосфолипидную эмульсию, содержащую следующие компоненты в г на 100 мл: глицин - 3,5±0,5; яичный лецитин - 3,5±0,8; дигидрокверцетин - 0,35±0,1; вода - остальное. Настоящее изобретение обеспечивает увеличение времени отторжения трансплантируемой ткани, выражающегося в уменьшении скорости рассасывания трансплантата, снижении уровня окислительного стресса, предотвращении возникновения воспалительной реакции фагоцитов. 3 з.п. ф-лы, 9 табл., 2 ил.
1. Применение фосфолипидной эмульсии, содержащей эффективное количество дигидрокверцетина (ДГК), для защиты тканей донорского органа при трансплантации, при котором используют фосфолипидную эмульсию, содержащую следующие компоненты в г на 100 мл:
2. Применение по п.1, в котором фосфолипидную эмульсию вводят перорально.
3. Применение по п.2, в котором фосфолипидную эмульсию вводят в суточной дозе 0,29-18 мл/кг массы для млекопитающих.
4. Применение по п.1, в котором используют фосфолипидную эмульсию, дополнительно содержащую фармацевтически приемлемые вспомогательные вещества.
| ФОСФОЛИПИДНАЯ ЭМУЛЬСИЯ, ВКЛЮЧАЮЩАЯ ДИГИДРОКВЕРЦЕТИН, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2007 |
|
RU2369383C2 |
| US 6676956 B1, 13.01.2004 | |||
| Применение фосфолипидной эмульсии, содержащей эффективное количество дигидрокверцетина, лецитин и глицин для лечения воспалительных заболеваний органов дыхания | 2021 |
|
RU2757360C1 |
| ПРИМЕНЕНИЕ ЛИПОСОМАЛЬНОЙ ЭМУЛЬСИИ С ДИГИДРОКВЕРЦЕТИНОМ "ФЛАМЕНА" ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЭНДОМЕТРИТОВ С АУТОИММУННЫМИ НАРУШЕНИЯМИ ПРИ БЕСПЛОДИИ | 2015 |
|
RU2622024C2 |
| О.С | |||
| Олифирова и др | |||
| Способ оптимизации лечения ран различного генеза / Тихоокеанский медицинский журнал, 2019, No | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
Авторы
Даты
2023-09-26—Публикация
2023-03-09—Подача