Изобретение относится к химико-фармацевтической промышленности, в частности, к производству лекарственных средств в виде субстанций и индивидуальных биологически активных соединений (БАС) и касается способа получения 4'-О-β-D-глюкопиранозида 3',4'-дигидроксибензилпротокатеховой кислоты (ореганола А) из травы душицы обыкновенной (Origanum vulgare L.), обладающего нефротропной и нейротропной активностью. Данное БАС возможно использовать в качестве мочегонного средства и средства для лечения тревожных состояний.
Трава душицы обыкновенной является перспективным растительным объектом ввиду богатого химического состава. Сырье душицы обыкновенной содержит эфирное масло (ведущая группа биологически активных веществ), флавоноиды, простые фенолы и фенилпропаноиды. Для травы душицы известно отхаркивающее, антибактериальное, противогрибковое, противовирусное, антиоксадантное действие (1-5). Сырье входит в состав многокомпонентного «Грудного сбора №1» и «Успокоительного сбора №3», а также фитопрепарата «Уролесан» (1, 6).
Известен способ выделения 4'-О-β-D-глюкопиранозида 3',4'-дигидроксибензилпротокатеховой кислоты из листьев душицы обыкновенной (Origanum vulgare L.) (4). Согласно данной методике: сырье душицы обыкновенной (100 г) экстрагируют 70% метанолом (около 3 л), фильтруют и концентрируют в вакууме примерно до 1 литра. Полученный экстракт разделяют между этилацетатом и водой. Водорастворимую фазу концентрируют при пониженном давлении. К полученному концентрированному экстракту добавляют 80% раствор этанола (1 л), и дают настояться при 25°C в течение 24 часов. Надосадочную жидкость и осадок отделяют фильтровальной бумагой, и раствор надосадочной жидкости подвергают дополнительной очистке. Раствор надосадочной жидкости концентрируют в вакууме, а полученный экстракт подвергают колоночной хроматографии на адсорбирующей смоле Diaion HP-20 (Mitsubishi Chem., 200 г). Адсорбент последовательно промывают водой и 70% метанолом. Экстракт из 70% метанола очищают с помощью сефадекса LH-20 на колоночной хроматографии. Колонку обрабатывают с 70% метанолом, а полученные фракции очищают методом жидкостной хроматографии при среднем давлении. Система (Tokyo Rikakiki) для этой очистки состояла из насоса EFC-1000 (длина хода 50; частота хода 70), ручного инжектора (SV-606010S) с петлей для отбора проб объемом 2,0 мл и детектора UV-D2 (A 254nm). Изократичная подвижная фаза представляла собой метанол:вода:уксусная кислота (50:50:0,1). Полученные фракции дополнительно очищают методом ВЭЖХ (движущаяся фаза: уксусная кислота: метанол (1:4); скорость тока: 5 мл/мин, A: 254 нм). В результате чего было получено соединение (270 мг), имеющее относительное время удерживания 12,4 минут. Данное соединение является 4'-О-β-D-глюкопиранозидом 3',4'-дигидроксибензилпротокатеховой кислоты (2).
Вышеуказанный метод взят нами в качестве прототипа.
Недостатками прототипа являются низкий выход целевого вещества - 4'-О-β-D-глюкопиранозид 3',4'-дигидроксибензилпротокатеховой кислоты, использование в больших количествах крайне опасного метанола (яд) не только в качестве экстрагента, но и в ходе колоночной хроматографии, многостадийность и длительность получения целевого вещества.
Таким образом, целью изобретения является разработка способа получения вещества, обладающего нефротропной и нейротропной активностью.
Техническим результатом является создание способа получения 4'-О-β-D-глюкопиранозида 3',4'-дигидроксибензилпротокатеховой кислоты (ореганола А) из травы душицы обыкновенной методом колоночной хроматографии.
Технический результат достигается тем, что извлечение получают из травы душицы обыкновенной экстракцией 70% этиловым спиртом в соотношении «сырье-экстрагент» 1:5, целевое вещество элюируют смесью хлороформ:этиловый спирт 96% в соотношении 70:30 с использованием колоночной хроматографии на силикагеле, а дальнейшую очистку осуществляют переосаждением в смеси ацетона и хлороформа.
Способ реализуется следующим образом.
Измельченное воздушно-сухое сырье травы душицы обыкновенной (100,0 г) экстрагируют 70% этиловым спиртом в соотношении 1:5 до полного истощения сырья методом дробной мацерации. Полученное объединенное водно-спиртовое извлечение упаривают на роторной вакуумной установке до густого экстракта, который затем смешивают с 70 г силикагеля L 40/100, высушивают и вносят на колонку (8 х 10 см), заполненную силикагелем в виде взвеси в хлороформе. Хроматографическую колонку промывают хороформом (0,25 л) и смесью хлороформ - этиловый спирт в соотношении 80:20 (1,0 л). Целевое вещество элюируют смесью хлороформ-этиловый спирт в соотношении 70:30 (1 л). Контроль за разделением веществ осуществляют хроматографированием на пластинках “Сорбфил ПТСХ-АФ-А-УФ-254” в системе растворителей: хлороформ-этиловый спирт-вода (26:16:3). Элюаты, содержащие 4'-О-β-D-глюкопиранозид 3',4'-дигидроксибензилпротокатеховой кислоты объединяют для последующего переосаждения в смеси ацетона и хлороформа. Полученное аморфное вещество представляет собой готовый продукт (4'-О-β-D-глюкопиранозид 3',4' дигидроксибензилпротокатеховой кислоты), имеющий степень чистоты 99,5%.
Предлагаемый способ поясняется следующим примером.
Пример 1.
Измельченное воздушно-сухое сырье травы душицы обыкновенной (100,0 г) экстрагируют 70% этиловым спиртом в соотношении 1:5 до полного истощения сырья методом дробной мацерации. Полученное объединенное водно-спиртовое извлечение упаривают на роторной вакуумной установке до густого экстракта, который затем смешивают с 70 г силикагеля L 40/100, высушивают и вносят на колонку (8 х 10 см), заполненную силикагелем в виде взвеси в хлороформе. Хроматографическую колонку промывают хороформом (0,25 л) и смесью хлороформ - этиловый спирт в соотношении 80:20 (1,0 л). Целевое вещество элюируют смесью хлороформ-этиловый спирт в соотношении 70:30 (1 л). Контроль за разделением веществ осуществляют хроматографированием на пластинках “Сорбфил ПТСХ-АФ-А-УФ-254” в системе растворителей: хлороформ-этиловый спирт-вода (26:16:3). Элюаты, содержащие 4'-О-β-D-глюкопиранозид 3',4'-дигидроксибензилпротокатеховой кислоты объединяют для последующего переосаждения в смеси ацетона и хлороформа. Получают 1,05 г вещества с выходом 1,05% от массы воздушно-сухого сырья и степенью чистоты 99,5%.
Химическая структура 4'-О-β-D-глюкопиранозида 3',4'-дигидроксибензилпротокатеховой кислоты представлена на Фиг. 1.
Спектральные и физико-химические свойства 4'-О-β-D-глюкопиранозида 3',4'-дигидроксибензилпротокатеховой кислоты. Аморфное вещество светло-желтого цвета состава С21Н24О11. УФ-спектр (EtOH, λmax, нм): 220, 263.
Спектр ЯМР 1Н (399.78 МГц, DMSO-d6, δ, м.д., J/Гц): 9.41 (1Н, уш.с, 3'-ОН-группа), 8.67 (1Н, с, 3'-ОН-группа),7.41 (1Н, дд, 2.0 и 9.0 Гц, Н-6), 7.34 (1Н, д, 2 Гц, Н-2), 7.07 (1Н, д, 9 Гц, Н-5'), 6.97 (1Н, д, 9 Гц, Н-5), 6.85 (1Н, д, 2 Гц, Н-2'), 6.77 (1Н, д, 2 и 9 Гц, Н-6'), 5.11 (2Н, c, Н-7'), 4.66 (д, J = 7.0, Н-1'' глюкопиранозы), 3.78 (3Н, с, СН3О), 3.22-3.66 (м, 6Н глюкопиранозы).
Спектр ЯМР 13С (100.52 МГц, DМSО-d6, δС, м.д.): 165.91 (С-7), 152.54 (С-4'), 147.27 (C-4), 146.82 (C-3'), 145.75 (C-3), 132.01 (C-2), 131.54 (C-6), 131.45 (C-5'), 122.45 (C-1), 122.13 (C-1'), 117.13 (C-5), 116.31 (C-2'), 116.22 (C-6'), 102.73 (С-1'' глюкозы), 77.74 (С-5’), 76.49 (С-3'''), 73.83 (С-2''), 70.34 (С-4''), 66.10 (C-7), 61.29 (С-6''), 56.17 (СН3О).
HR-ESI-MS, 180°С, m/z: 456.1500 [M+NH4]+, 461.1054 [M+Na]+, 477.0794 [M+К]+.
4'-О-β-D-глюкопиранозид 3',4'-дигидроксибензилпротокатеховой кислоты, полученный разработанным способом, исследовали на наличие нефротропной и нейтротропной активности.
Исследование нефротропной и нейтротропной активности проводили на белых беспородных крысах обоего пола массой 200-220 г. Животные содержались в условиях вивария на обычном рационе при свободном доступе к воде. Каждая группа состояла из десяти животных. Исследуемый препарат вводили внутрижелудочно через зонд в дозе 0,5 мг/кг. Контролем в изучении нейротропной активности служила вода очищенная. Препарат вводили однократно на фоне аналогичной водной нагрузки, эксперимент проводили через 2 часа после введения препарата (7). Исследование нейтротропной активности проводили с использованием теста Порсолта (8). При этом в течение пяти минут фиксировали индивидуальное время активных попыток животных выбраться из воды. Полученные данные обрабатывали статистически по критерию Манна-Уитни. Результаты исследования влияния на двигательную активность крыс в методике теста Порсолта представлены в таблице 1 - Фиг. 2.
Исходя из полученных результатов можно сделать вывод, что 4'-О-β-D-глюкопиранозида 3',4' дигидроксибензилпротокатеховой кислоты в дозе 0,5 мг/кг при однократном внутрижелудочном введении способствовал достоверному снижению двигательной активности животных в опытной группе на 47% по отношению к водному контролю.
Исследование нефротропной (диуретической) активности проводили следующим образом: контрольная группа животных получала 3% водную нагрузку внутрижелудочно, опытные животные - исследуемый препарат в дозе 0,5 мг/кг на фоне аналогичной водной нагрузки. После всех манипуляций животные рассаживались в обменные клетки на 24 ч. Пробы мочи собирались через 4 и 24 ч эксперимента. Определяли объем проб (диурез) и концентрацию креатинина. Креатининурез определялся методом колориметрии на КФК-3. Статистическую обработку полученных результатов проводили по методу Манна Уитни с поправкой Бонферрони.
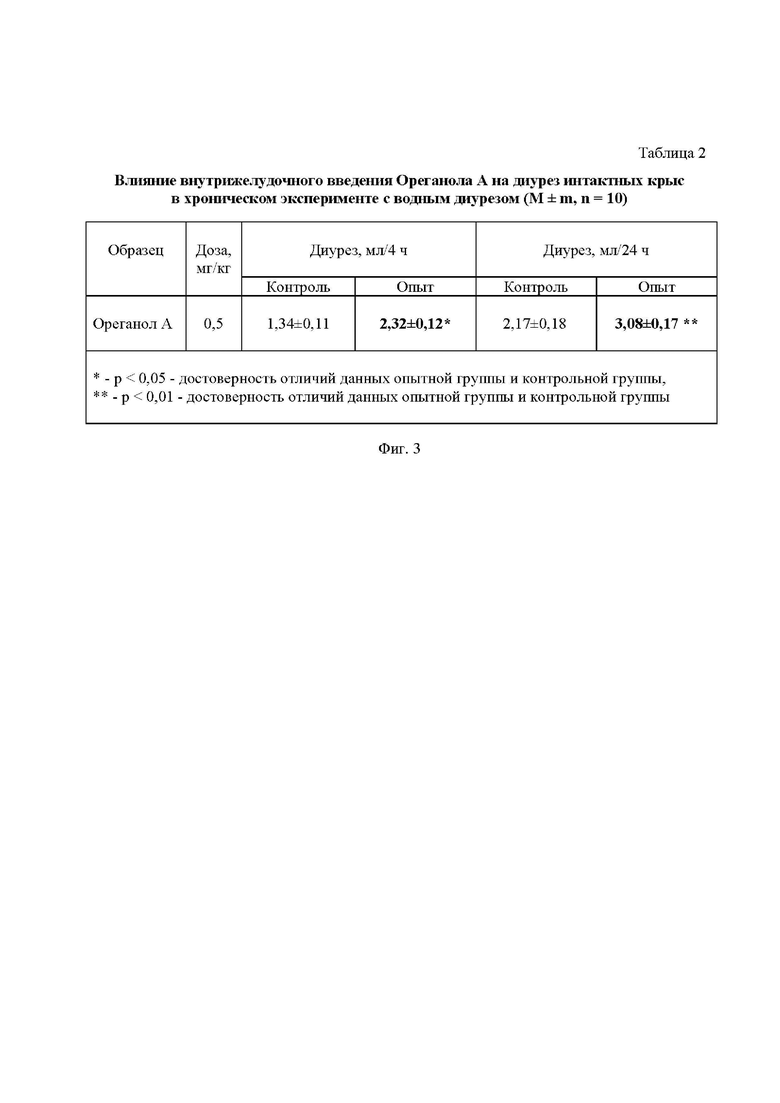
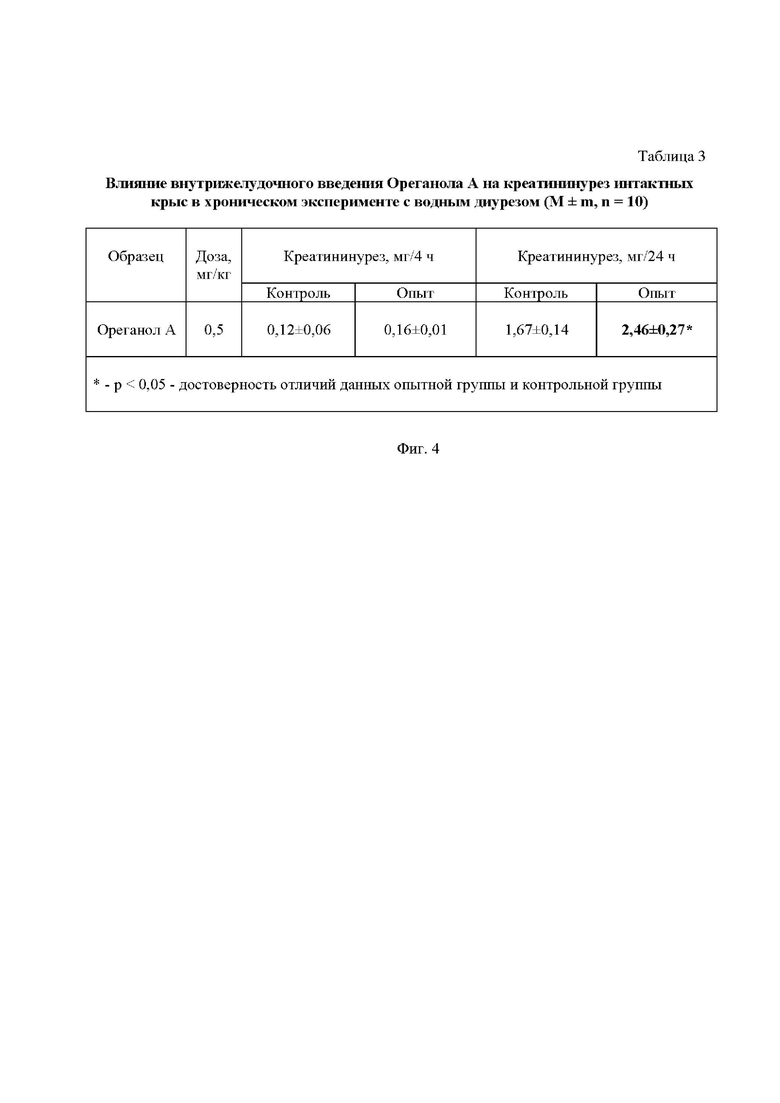
Результаты исследования влияния ореганола А на выделительную функцию почек представлены в таблице 2 - Фиг. 3 и таблице 3- Фиг. 4.
Исходя из полученных результатов можно сделать вывод, что 4'-О-β-D-глюкопиранозида 3',4' дигидроксибензилпротокатеховой кислоты в дозе 0,5 мг/кг при однократном внутрижелудочном введении способствовал достоверному увеличению диуреза (на 73% и 42%) за 4 и 24 ч опыта соответственно, а также креатининуреза (на 47%) за 24 ч эксперимента по отношению к водному контролю.
Таким образом, предлагаемый способ получения 4'-О-β-D-глюкопиранозида 3',4'-дигидроксибензилпротокатеховой кислоты из травы душицы обыкновенной методом колоночной хроматографии разработан впервые для данного вида сырья и обладает следующими преимуществами:
1. Разработанный способ позволяет получать более высокий выход вещества 4'-О-β-D-глюкопиранозида 3',4'-дигидроксибензилпротокатеховой кислоты - 1,05% вместо 0,27% у прототипа (4).
2. Разработанный способ менее трудоемок, поскольку включает три стадии получения целевого вещества: экстракция сырья этанолом, упаривание, хроматографическая очистка на силикагеле с использование элюента, представляющего собой смесь двух растворителей (хлороформ и этиловый спирт), вместо семи стадий в прототипе с использованием различных методов (колоночная хроматография и ВЭЖХ), сорбентов (адсорбирующая смола Diaion HP-20, сефадекс LH-20) и токсичного элюента - метанола (4).
3. Извлечение из сырья душицы получено с расходом небольшого количества нетоксичного экстрагента (1:5), по сравнению с прототипом, где соотношение «сырье-экстрагент» 1:30, а в качестве экстрагента применяется токсичный метанол (4).
4. Целевой продукт ореганол А, полученный разработанным способом, обладает нефротропной и нейтротропной активностью.
ИСТОЧНИКИ ИНФОРМАЦИИ:
1. Куркин В.А. Фармакогнозия: Учебник для студентов фармац. вузов - Изд. 4-е, перераб. и доп. - Самара: ООО «Офорт», ФГБОУ ВО СамГМУ Минздрава России. 2019. - 1278 с.
2. Мирович В. М. Фармакогностическое исследование представителей родов Origanum L. и Rhododendron L. флоры Восточной Сибири: автореф. дис. … д. фармац. н.: 14.04.02/ Мирович Вера Михайловна. - Улан-Удэ, 2010. - 41 с.
3. Knez Hrnčič M., Cör D., Simonovska J. et al. Extraction techniques and analytical methods for characterization of active compounds in Origanum species. Molecules, 2020; 25 (20): 4735.
4. Matsura H., Chiji H., Asakawa C. et al.. DPPH radical scavengers from dried leaves of Oregano (Origanum vulgare). Bioscience, Biotechnology, and Biochemistry, 2003; 67 (11): 2311-2316.
5. Fujie A., Yoshida K., Ôba K. et al. Antioxidative phenolic acids from Oregano (Origanum vulgare L.) leaves. Nippon Shokuhin Kagaku Kogaku Kaishi, 2003 50(9):404-410. DOI:10.3136/nskkk.50.404
6. Машковский М.Д. Лекарственные средства. 16-е изд., перераб., испр. и доп. Новая волна, 2020. - 1216 с.
7. Зайцева Е.Н., Зайцев А.Р., Дубищев А.В. Устройство для введения водной нагрузки лабораторным животным. Патент на ПМ 115651 Рос. Федерация. №2011138631/13; заявл. 20.09.11; опубл. 10.05.12, Бюл. №13. 2 с.
8. Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. Р.У. Хабриева. - 2-е изд., перераб. и доп. М.: ОАО Издательство «Медицина», 2005. - 832 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МИРИЦИТРИНА ИЗ КОРЫ ОРЕХА ЧЕРНОГО, ОБЛАДАЮЩЕГО НЕЙРОТРОПНОЙ АКТИВНОСТЬЮ | 2021 |
|
RU2776898C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛАВАНДОЗИДА | 2008 |
|
RU2367431C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-ГИДРОКСИАЦЕТОФЕНОН-4-О-БЕТА-D-ГЛЮКОПИРАНОЗИДА (ПИЦЕИНА) ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ | 2012 |
|
RU2532167C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО ПРОТИВОГРИБКОВОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2691997C1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИРЕОЗИДА, ОБЛАДАЮЩЕГО АНТИДЕПРЕССАНТНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2739191C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУММЫ ФЛАВОНОИДОВ, ОБЛАДАЮЩИХ ПРОТИВОВОСПАЛИТЕЛЬНЫМ И СПАЗМОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 1993 |
|
RU2095075C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЖЕНСКОЙ ПОЛОВОЙ СФЕРЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2217157C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ТРАВЕ ТЫСЯЧЕЛИСТНИКА ОБЫКНОВЕННОГО | 2022 |
|
RU2806035C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО НООТРОПНОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2288733C1 |
| Способ количественного определения сирингина в коре сирени обыкновенной | 2021 |
|
RU2782620C1 |


Изобретение относится к химико-фармацевтической промышленности, а именно к способу получения ореганола А, обладающего нефротропной и нейротропной активностью. Способ получения ореганола А, обладающего нефротропной и нейротропной активностью, с предварительным получением водно-спиртового извлечения из лекарственного растительного сырья с использованием метода хроматографии на сорбентах, согласно которому извлечение получают из травы душицы обыкновенной экстракцией 70% этиловым спиртом в соотношении «сырье-экстрагент» 1:5, экстракцию проводят методом дробной мацерации до полного истощения сырья, полученное объединенное водно-спиртовое извлечение упаривают до густого экстракта, который затем смешивают с силикагелем L 40/100, высушивают и вносят на колонку заполненную силикагелем в виде взвеси в хлороформе, целевое вещество элюируют смесью хлороформ:этиловый спирт 96% в соотношении 70:30 с использованием колоночной хроматографии на силикагеле, дальнейшую очистку осуществляют переосаждением в смеси ацетона и хлороформа с выходом вещества 1,05% и степенью чистоты 99,5%. Вышеописанный способ позволяет получить ореганол А, обладающий нефротропной и нейротропной активностью с выходом вещества 1,05% и степенью чистоты 99,5%. 4 ил., 1 пр.
Способ получения ореганола А, обладающего нефротропной и нейротропной активностью, с предварительным получением водно-спиртового извлечения из лекарственного растительного сырья с использованием метода хроматографии на сорбентах, отличающийся тем, что извлечение получают из травы душицы обыкновенной экстракцией 70% этиловым спиртом в соотношении «сырье-экстрагент» 1:5, экстракцию проводят методом дробной мацерации до полного истощения сырья, полученное объединенное водно-спиртовое извлечение упаривают до густого экстракта, который затем смешивают с силикагелем L 40/100, высушивают и вносят на колонку заполненную силикагелем в виде взвеси в хлороформе, целевое вещество элюируют смесью хлороформ:этиловый спирт 96% в соотношении 70:30 с использованием колоночной хроматографии на силикагеле, дальнейшую очистку осуществляют переосаждением в смеси ацетона и хлороформа с выходом вещества 1,05% и степенью чистоты 99,5%.
| Matsura H., Chiji H., Asakawa C | |||
| et al | |||
| DPPH radical scavengers from dried leaves of Oregano (Origanum vulgare) | |||
| Bioscience, Biotechnology, and Biochemistry, 2003; 67 (11): 2311-2316 | |||
| CN 113735922 A, 03.12.2021 | |||
| González MD et all.Polyphenolic profile of Origanum vulgare L | |||
| ssp | |||
| Пуговица | 0 |
|
SU83A1 |
| RU | |||
Авторы
Даты
2023-09-27—Публикация
2022-11-20—Подача