Изобретение относится к химико-фармацевтической промышленности, в частности к производству лекарственных средств в виде субстанций и индивидуальных биологически активных соединений (БАС), и касается способа получения лавандозида из цветков лаванды колосовой (Lavandula spica L., сем. Яснотковых - Lamiaceae).
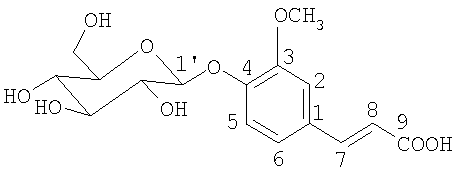
Лавандозид
Цветки лаванды колосовой (Lavandula spica L., сем. Lamiaceae) используются в Российской Федерации для производства бактерицидных препаратов «Ливиан» и «Лавандовый спирт» на основе эфирного масла, получаемого из свежих цветков лаванды [1, 2]. За рубежом это растение широко применяется в виде препаратов, обладающих седативными свойствами [3-6], среди которых «Нервофлюкс» зарегистрирован в РФ [2]. Для создания препаратов на основе цветков лаванды имеются объективные предпосылки в плане сырьевой базы, так как данное средиземноморское растение широко культивируется во многих странах мира, в том числе в Российской Федерации, в республиках бывшего СССР и в Марокко.
С использованием колоночной хроматографии на силикагеле, полиамиде и сефадексе марки LH-20 из цветков лаванды колосовой выделено новое природное соединение, названное нами лавандозидом.
Для установления химического строения данного соединения нами использованы методы 1Н-ЯМР-спектроскопии, УФ-спектроскопии и масс-спектрометрии, а также результаты химических превращений.
Лавандозид расщепляется под воздействием β-глюкозидазы («Fluka», Венгрия) на глюкозу и агликон, идентифицированный сравнением с достоверно известным образцом феруловой кислотой по некоторым физико-химическим и спектральным характеристикам, а также методом TCX.
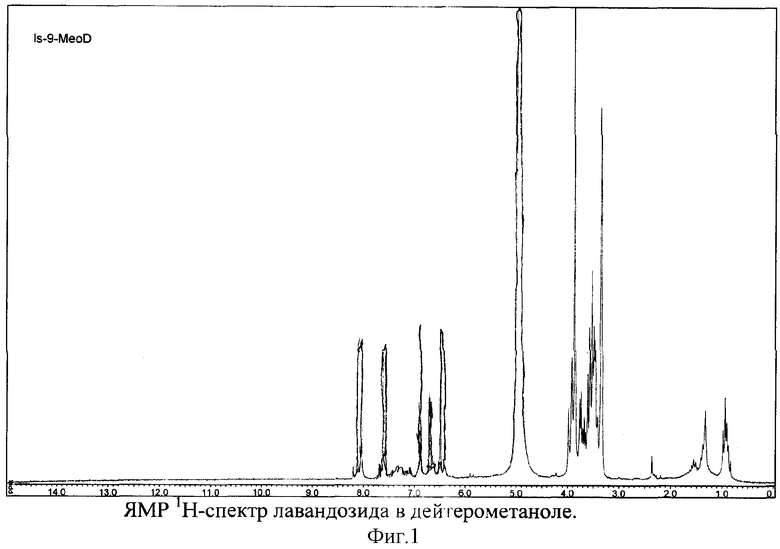
В ЯМР 1Н-спектре (фиг.1) при 8.08 и 6.44 м.д. присутствуют два однопротонных дублетных сигнала с константой спин-спинового взаимодействия (J) 16.05 Гц, отнесенные соответственно к протонам Н-7 и Н-8, что свидетельствует о наличии в молекуле фрагмента транскоричной кислоты (фенилпропаноид). Ароматическое кольцо лавандозида имеет характерное 3,4-замещение, так как в ЯМР 1Н-спектре (фиг.1) обнаружены характерные сигналы ароматических протонов при 7.60 (1Н, д, J=8.61, Н-5), 6.88 (1Н, J=2.33, Н-2) и 6.67 (1Н, дд, J=2.33 и J=8.61, Н-6). Наличие в молекуле ароматической метоксигруппы подтверждается трехпротонным синглетным сигналом при 3.86 м.д. (фиг.1).
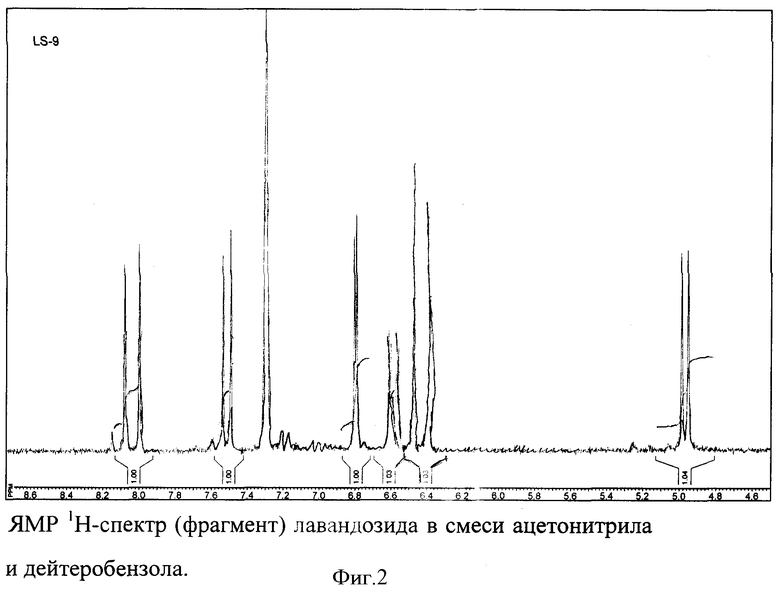
Сигналы углеводного фрагмента (глюкоза) обнаруживаются в ЯМР 1Н-спектре в виде мультиплета (6Н) и дублетного сигнала аномерного протона при 5.00 м.д. и при 4.98 м.д. с J=7.21, характерного для Н-11 β-D-глюкопиранозы (фиг.1, 2).
Отнесение глюкозы к 4-ОН-группе сделано на основании химического сдвига сигнала аномерного протона при 5.00 м.д., наблюдаемого в случае гликозилирования фенольной группы. Гликозилирование карбоксильной группы, т.е. образование ацилгликозидной связи, привело бы к смещению сигнала аномерного протона в более слабое поле - примерно до 6.0 м.д. [7].
Следует отметить, что ранее близкое по строение к лавандозиду было выделено из суспензионной культуры Chenopodium rubrum, однако, в данном фенилпропаноиде глюкоза присоединена к карбоксилу [8].
Таким образом, лавандозид, выделенный из цветков Lavandula spica, является новым природным соединением и имеет структуру 4-O-β-D-глюкопиранозида 4-гидрокси-3-метоксикоричной кислоты.
Известен способ получения вещества, обладающего нейротропной активностью [8, 9] - гиперфорина, выделенного из ацетонового экстракта зверобоя продырявленного. Полученный в виде масла гиперфорин ацилируют в бензоле и 3,5-динитробензоилхлорида пиридина 12 ч при 20°С и 1 ч при 80°С. Раствор промывают 5% НСl и 5% NаНСО3, концентрируют в вакууме и хроматографируют на колонке с силикагелем в течение 2 сут, вымывая бензолом и кристаллизуя 3,5-динитробензоат гиперфорина из смеси спирт-эфир (95:5) и из спирта. Далее полученную соль смешивают с 1 н. KOH, через 1,5 ч нейтрализуют 10% Н2SO4. Остаток растворяют в бензоле, промывают насыщенным раствором NаНСО3 и фильтруют через слой кремниевой кислоты. Полученный маслянистое вещество кристаллизуют из гексана, содержащего 0,05% ионола [8].
Однако выделение этого вещества осуществляется с использованием громоздкой и длительной (60 ч) технологии, заключающейся в использовании целого ряда реактивов (5% НСl, 5% NaHCO3, 1 н. KОН, 10% Н2SO4, ионол и др.).
Данный способ взят за прототип изобретения.
Целью изобретения является разработка способа получения лавандозида из цветков лаванды колосовой.
Заявляемый способ получения реализуется следующим образом. В качестве экстрагента используют 70…90% этиловый спирт, далее проводят хроматографическое разделение на силикагеле, полиамиде и сефадексе марки LH-20.
В ходе эксперимента использованы физико-химические методы анализа, такие как адсорбционная жидкостная колоночная хроматография, тонкослойная хроматография (хроматографические пластинки «Сорбфил ПТСХ-А-А-УФ»), а также сочетание экстракционных методов и перекристаллизации.
Нейротропную (седативную активность) активность лавандозида исследовали на модели хлоралгидратного сна: в опыте на мышах выявлено, что лавандозид в дозе 20 мг/кг увеличивает продолжительность хлоралгидратного сна с 21,6±1,1 мин до 32,3±1,5 (р<0,05) мин (на 49,5%).
Проведенный заявителем поиск по научно-техническим и патентным источникам информации и выбранный из перечня аналогов прототип [8] позволили выявить отличительные признаки в заявленном техническом решении. Следовательно, заявляемый способ получения удовлетворяет критерию изобретения "новизна" (табл.1).
Проведенный заявителем дополнительный поиск известных технических решений [8] с целью обнаружения в них признаков, сходных с признаками заявляемого способа получения, показал, что эти признаки отсутствуют, следовательно, заявляемое техническое решение удовлетворяет критерию "изобретательский уровень".
Заявляемый способ иллюстрируется следующим примером.
В качестве объекта исследования использовали цветки лаванды колосовой, собранные в Марокко, в долине Атласских гор (2006 г.).
Пример 1. Цветки лаванды колосовой подвергают исчерпывающему экстрагированию 70% этиловым спиртом, сочетая при этом способ мацерации (24 ч) с последующей термической экстракцией при температуре 65-70°С. Водно-спиртовые экстракты упаривают под вакуумом до густого остатка (около 50 мл). Сгущенный экстракт высушивают на силикагеле L 40/100 и полученный порошок (экстракт + силикагель) наносят на слой силикагеля, сформированный в хлороформе. Хроматографическую колонку элюируют хлороформом и смесью хлороформ-этанол в различных соотношениях (97:3; 95:5; 93:7; 90:10; 88:12; 85:15; 80:20; 70:30). Контроль за разделением осуществляют с помощью ТСХ-анализа.
Фракции, содержащие лавандозид, объединяют и наносят на полиамид «Wolem» с целью дальнейшей очистки. Сухой порошок (экстракт + полиамид) переносят в хроматографическую колонку (высота сорбента - 4,0 см, диаметр - 5 см). Хроматографическую колонку элюируют водой и водным раствором спирта этилового (20%; 40%; 70%; 96%). В результате проведенной очистки на колонках с полиамидом получают лавандозид (элюент - вода), дополнительную очистку которого осуществляют рехроматографией на сефадексе марки LH-20. При этом хроматографическую колонку элюируют хлороформом и смесью хлороформ-этанол в различных соотношениях (95:5; 93:7; 90:10; 88:12; 85:15; 80:20; 70:30). Выход лавандозида как целевого вещества составляет 0,95% от массы воздушно-сухого сырья.
УФ-спектры лавандозида регистрируют на спектрофотометре «Specord 40» (Analytik Jena). ЯМР 1Н-спектры лавандозида записывают на спектрометре «Bruker 250». Масс-спектры получают на спектрометре «Finnigan LXQ LC-MS/MS». Ферментативный гидролиз данного вещества осуществляют с использованием β-глюкозидазы («Fluka», Венгрия) при температуре 38°С в течение 12 ч.
Лавандозид, аморфное вещество светло-желтого цвета, С21H20О10, масс-спектр (m/z, %): 195,01 (М агликона +H)+ (24.71%), 176.98 (М агликона - Н2О+Н)+ (100.00), 152.97 (М агликона - COO+Н)+ (28.60). УФ-спектр (EtOH, λmax, нм): 281, 313. ЯМР 1Н-спектр (250 МГц, CD3OD, δ, м.д, J/Гц): 3.3-4.0 (6Н глюкозы), 3.86 (3Н, с, ОСН3), 5.00 (1Н, д, J=7.0, Н-11 глюкопиранозы), 6.44 (1Н, д, J=16.05, Н-8), 6.67 (1Н, дд, J=2.33 и J=8.61, Н-6), 6.88 (1Н, J=2.33, Н-2), 7.60 (1Н, д, J=8.61, Н-5), 8.08 (1Н, д, J=16.05, Н-7).
ЯМР 1Н-спектр (250 МГц, смесь ацетонитрила и С6D6, δ, м.д., J/Гц): 3.20-3.60 (4Н глюкозы), 3.64 (1Н, дд, J -5 и J=12, Н-61), 3.76 (ЗН, с, ОСН3), 3.84 (1Н, дд, J-1.86 и J=12.10, Н-61). 4.98 (1Н, д, J=7.21, Н-11 глюкопиранозы), 6.43 (1Н, д, J=16.05, Н-8), 6.57 (1Н, дд, J=2.33 и J=8.61, Н-6), 6.80 (1Н, J=2.33, Н-2), 7.52 (1Н, д, J-8.61, Н-5), 8.04 (1Н, д, J=16.05, Н-7).
Заявляемый способ позволяет в 50 раз увеличить выход целевого продукта из цветков лаванды колосовой по сравнению с прототипом (табл.2).
Кроме того, заявляемый способ позволяет в 1,8 раза сократить продолжительность технологического процесса, исключить из технологической схемы использование большого количества реактивов (5% НСl, 5% NаНСО3, 1 н. KОН, 10% Н3SO4, ионол и др.).
Полиамид
Сефадекс
Таким образом, использование заявляемого способа получения лавандозида дает следующие преимущества:
1. Использование в заявляемом способе 70%…90% этилового спирта позволяет исчерпывающе извлекать целевой продукт из цветков лаванды колосовой.
2. Заявляемый способ позволяет в 50 раз увеличить выход целевого продукта из цветков лаванды колосовой по сравнению с прототипом.
3. Заявляемый способ позволяет в 1,8 раз сократить продолжительность технологического процесса.
4. Заявляемый способ позволяет получить вещество, обладающее в дозе 20 мг/кг выраженной седативной активностью.
Источники информации
1. Куркин В.А. Фармакогнозия: Учебник для студентов фармацевтических вузов/В.А.Куркин. - 2-е изд., перераб. и доп. - Самара: ООО «Офорт», ГОУВПО «СамГМУ», 2007. - 1239 с.
2. Государственный реестр лекарственных средств. - T.1 (официальное издание по состоянию на 1 февраля 2003 г.). - М.: Минздрав РФ, 2004. - 1404 с.
3. А.Сежильмасси. Лекарственные растения в Марокко. - Касабланка. - 1995. - 145 с.
4. Nafysi, A.T. Review of Traditional Medicine in Iran, Isfahan University Publications, Isfahan. - 1989. - 122 p.
5. H. Wagner, Pharmazeutische Biologie. Drogen und ihre Inhaltsstoffe, Gustav Fischer Verlag, Stuttgart-New York. 1993. - 522 s.
6. J.B.Harborne. Comparative biochemistry of the flavonoids - phytochemical unit, the Hartley botanical laboratories, The University of Liverpool, England. - 1967. - 217 p.
7. Strack D., Bokem М. Metabolic activity of hydroxycinnamic acid glucose esters in cell suspension cultures of Chenipodium rubrum // Z.Naturforschung. - 1984. - Vol. 39 С. - №.9/10. - S.902-907.
8. Быстров Н.С. Химия гиперфорина VI. Общая химическая характеристика / Н.С.Быстров, В.Н.Добрынин, М.Н.Колосов, М.Н.Поправко, Б.К.Чернов // Биоорганическая химия. - 1978. - Т.4 - №6. - С.791-805.
9. Куркин, В.А. Исследование сырья и препаратов зверобоя // В.А.Куркин, О.Е.Правдивцева, А.В.Дубищев, Д.В.Кадацкая, Г.Г.Запесочная, И.П.Жданов // Фармация. - 2005. - Т. 53, №3. - С.23-25.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ 1-О-2-(3,4-ДИМЕТОКСИБЕНЗИЛ)-3-КАРБОКСИ-4-(3-МЕТОКСИ-4-ОКСИФЕНИЛ)-БУТИЛ-β-D-ГАЛАКТОПИРАНОЗЫ ИЗ Onopordum acanthium L. | 2006 |
|
RU2333914C1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИРЕОЗИДА, ОБЛАДАЮЩЕГО АНТИДЕПРЕССАНТНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2739191C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО ПРОТИВОГРИБКОВОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2691997C1 |
| НОВОЕ ПРИРОДНОЕ ВЕЩЕСТВО ИЗ ТРАВЫ ПЕРВОЦВЕТА ВЕСЕННЕГО | 2013 |
|
RU2539299C1 |
| Способ получения вещества, обладающего антибактериальной и противогрибковой активностью | 2017 |
|
RU2665167C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОРЕГАНОЛА А, ОБЛАДАЮЩЕГО НЕФРОТРОПНОЙ И НЕЙРОТРОПНОЙ АКТИВНОСТЬЮ | 2022 |
|
RU2804299C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО НООТРОПНОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2288733C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИРИЦИТРИНА ИЗ КОРЫ ОРЕХА ЧЕРНОГО, ОБЛАДАЮЩЕГО НЕЙРОТРОПНОЙ АКТИВНОСТЬЮ | 2021 |
|
RU2776898C1 |
| 3,6-ДИМЕТОКСИ-17-МЕТИЛ-7АЛЬФА-(ТРИФТОРАЦЕТИЛ)-4,5АЛЬФА-ЭПОКСИ-6АЛЬФА,14АЛЬФА-ЭТЕНОИЗОМОРФИНАН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2503677C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО АНТИОКСИДАНТНЫМ ДЕЙСТВИЕМ | 2002 |
|
RU2209063C1 |
Изобретение относится к химико-фармацевтической с промышленности. Проводят экстракцию цветков лаванды колосовой (Lavandula spica L., сем. Яснотковых - Lamiaceae) 70-90%-ным этиловым спиртом, сгущение полученного экстракта, высушивание, нанесение на силикагель, элюирование хлороформом и смесью хлороформ-этанол, объединение фракций, содержащих лавандозид, нанесение сухого экстракта на полиамид, элюирование лавандозида водой, нанесение на сефадекс, элюирование хлороформом и смесью хлороформ-этанол. Изобретение позволяет реализовать указанное назначение, увеличить выход продукта. 2 табл., 2 ил.
Способ получения лавандозида из цветков лаванды колосовой (Lavandula spica L., сем. Яснотковых - Lamiaceae), включающий экстракцию цветков лаванды 70-90%-ным этиловым спиртом, сгущение полученного экстракта, высушивание, нанесение на силикагель, элюирование хлороформом и смесью хлороформ-этанол, объединение фракций, содержащих лавандозид, нанесение сухого экстракта на полиамид, элюирование лавандозида водой, нанесение на сефадекс, элюирование хлороформом и смесью хлороформ-этанол.
| Государственный реестр лекарственных средств | |||
| - М.: Минздрав РФ, 2004, т.1, с.1404 | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ ОПРЕДЕЛЕНИЯ ЦЕНТРОВ ЦИЛИНДРИЧЕСКИХ ИЗДЕЛИЙ | 1933 |
|
SU37351A1 |
Авторы
Даты
2009-09-20—Публикация
2008-04-24—Подача