Фармакологическое соединение на основе 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата и применение его для коррекции и профилактики остеопороза.
Изобретение относится к медицине, области экспериментальной фармакологии, а именно к новым биологически активным соединениям, конкретно - фармакологическое соединение на основе 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата (ацексамат) и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, обеспечивающий коррекцию и профилактику остеопороза.
Постменопаузальный остеопороз - это системное метаболическое заболевание костей, которым страдают более 200 миллионов женщин во всем мире (Zhao K. et al., 2019). Постменопаузальный остеопороз, вызванный дисфункцией ремоделирования костей, вызывает низкую минеральную плотность костей и микроструктурные изменения, которые снижают прочность костей и увеличивают хрупкость костей, что приводит к увеличению риска переломов (Chen et al., 2018; Zhao X. et al., 2019). Известно, что у одной из трех женщин старше 50 лет возникает остеопоротический перелом, который существенно повлияет на повседневную деятельность и качество жизни пациентов, а также приведет к значительным экономическим затратам как для отдельных лиц, так и для общества в целом (Eriksen et al., 2014; Lin et al., 2016; An et al., 2019). Более того, остеопороз в постменопаузе еще больше увеличивается с возрастом населения.
Кортикостероиды широко используются в клинической практике при различных заболеваниях, включают заболевания соединительной ткани, астму, воспалительные заболевания кишечника, трансплантацию органов и др. Известно, что длительное применение кортикостероидов ускоряет потерю костной массы, что в конечном итоге приводит к остеопорозу и переломам (Ou et al., 2021).
Препараты для лечения постменопаузного и глюкокортикостероид - индуцированного остеопороза включают применение эстрогенов, кальцитонина, бифосфонаты, моноклональные антитела - современные лекарства несколько защищают от потери костной массы, однако имеют ряд нежелательных побочных эффектов увеличивая потенциальный риск рака груди, ишемии миокарда, тромбоэмболических заболеваний и атипичного изгиба бедренной кости (Eriksen et al., 2014; Black and Rosen, 2016; Compston et al., 2019; Чжао К. и др., 2019). Препараты моноклональных антител, Деносумаб, может ингибировать абсорбцию костной ткани, подавляя дифференцировку и активацию остеокластов, но кожная сыпь и инфекция возникают чаще, а влияние на метаболизм костной ткани быстро обратим после прекращения приема препарата (Compston et al., 2019).
Однако все имеющиеся препараты и поиски подходов к коррекции постменопаузного и стероид - индуцированного остеопороза являются недостаточно эффективными и показывают противоречивые и изменчивые результаты.
Поэтому поиск новых современных более эффективных и безопасных препаратов для лечения остеопороза является актуальной задачей современной фармакологии. Одним из таких препаратов является ацексамовая кислота (АК), производное аминокапроновой кислоты, способное ускорять очищение раневой поверхности от некротических масс, уменьшать экссудативные процессы, активировать рост грануляционной ткани, васкуляризацию (К. Saravana Ramasamy, 2016; Пахомов Д.В, 2020). Стимулирует образование костной мозоли, ускоряет срастание переломов костей. Предупреждает развитие келлоидных рубцов (RU № 2668966, публ. 05.10.2018).
Известен способ коррекции остеопороза и профилактики возникновения остеопоротических переломов лозартаном (RU № 2369391, публ. 10.10.2009), в котором остеопротективное действие лозартана оценивают по уровню микроциркуляции в костной ткани и ширине костных трабекул. Способ позволяет уменьшить признаки остеопороза после овариоэктомии путем блокирования рецепторов ангиотензина II, что обеспечивает улучшение микроциркуляции костной ткани.
Известен способ коррекции остеопороза и профилактики возникновения остеопоротических переломов резвератролом (RU № 2437161, публ. 20.12.2011), в котором оценивают остеопротективное действие резвератрола по уровню микроциркуляции в костной ткани и ширине костных трабекул. При выбранных дозе и режиме введения препарата способ обеспечивает улучшение кровообращения и микроархитектонику костной ткани при гипоэстрогенном состоянии. Исследование эффекта резвератрола проводят у самок крыс линии Wistar при моделировании остеопороза путем билатеральной овариэктомии. Для коррекции остеопороза резвератрол вводят животным внутрибрюшинно в течение восьми недель после овариэктомии ежедневно однократно в сутки в дозе 2 мг/кг.
Наиболее близким к заявленному решению является изобретение «Комплексные соли ацексамовой кислоты, стимулирующие регенерацию костной ткани, ускоряющие процессы репаративного остеогенеза, стимулирующие минерализацию костной ткани при остеопорозе» (патент RU № 2668966, публ. 05.10.2018), целью которого является синтез комплексные соли ацексамовой кислоты, стимулирующих регенерацию костной ткани, ускоряющих процессы рапаративного остеогенеза, стимулирующие минерализацию костной ткани при остеопорозе. Поставленная цель достигается синтезом N-ацетил-6-аминогексаноат серебра и 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноат.
Основными недостатками является то, что ряд предложенных композиций являются наиболее дорогостоящими, ряд соединений изучались на более мягких экспериментальных моделях остеопороза, это овариэктомии (первичный остеопороз) или вторичный (стероидный остеопороз), кроме того известные соединения не нашли применения в клинической практике.
Задачей предлагаемого изобретения является получение фармацевтического соединения на основе 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, обладающего остеопротекторной активностью и применение его для коррекции и профилактики остеопороза.
Технический результат заключается в новом эффективном фармацевтическом соединении на основе 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, обладающим остеопротекторной активностью его эффективном применении для коррекции и профилактики остеопороза.
Поставленная задача решается с помощью предлагаемого фармацевтического соединения, включающего 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата (АК) и дополнительно 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, полученного путем топохимического синтеза.
Пример 1.
Топохимический синтез нового фармацевтического соединения осуществляется гомогенизацией высушенных до постоянной массы при температуре 100 - 105 °С в течение 2-х часов и измельченных до 5-10 мкм 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата.
В гомогенизатор загружают 26,0 г (0,1 г/моль) 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, при перемешивании постепенно добавляют 93,2 г (0,3 г/моль) 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата. Массу гомогенизируют в течение 10-15 минут при скорости перемешивания 300-400 об/мин. Проверяют размер частиц полученного порошка, который должен составлять не более 10 мкм, при необходимости дополнительно гомогенизируют. Получают 119,0 г белого мелкокристаллического порошка с Тпл. = 139 - 143°С. Растворим в воде с легкой опалесценцией.
Найдено, %: С 62,48; Н 7,98; N 9,39 С62 Н94 N8О15 м.м. 1191,46
Вычислено, %: С 62,50; Н 7,95; N 9,41; O 20,14.
ИК-спектр (v, см-1): 3412 (OH) 3290 (NH), 2941 (СН), 2673 (N+), 1781 (С=N-), 1634 (C=C), 1561 (СОО-).
Масс-спектр протонированного нового фармацевтического соединения в режиме сканирования положительных ионов [M+H] +составляет, M/z: 1195,46, что соответствует м.м. 1191,46.
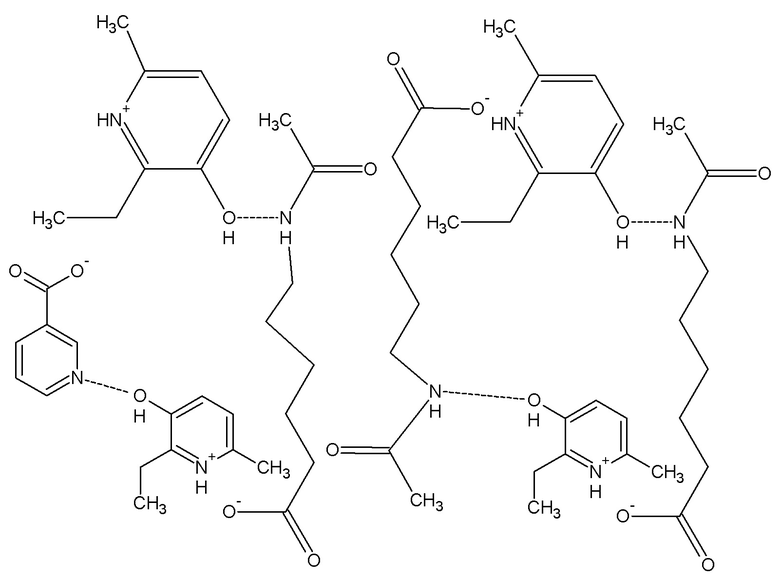
Соединение 1
полученное новое фармацевтическое соединение 1, в соотношении 1:3 способствует повышению остеопротекторной активности.
В предлагаемом изобретении выбрана более «жесткая модель» экспериментального остеопороза (гипо-эстроген-индуцированный +стероид-индуцированный остеопороз), где изучаемое фармакологического соединения, состоящее из 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата проявило не только выраженную остеопротекторную активность, выражающуюся в повышении плотности костной ткани, увеличении уровня микроциркуляции, снижении коэффициента эндотелиальной дисфункции и увеличении толщины костных трабекул в сравнении с группой контроля. Снижение среднего значения показателей малонового диальдегида в экспериментальной группе с введением фармакологического соединения, состоящего из 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата указывает на снижение активности остеокластов. А значительное повышение активности супероксиддисмутазы и глутатионпероксидазы, подчеркивает снижение оксидантного стресса. Кроме того, при анализе морфометрических исследований у изучаемого комплекса обнаружены выражение признаки остеобластической дифференцировки, остеогенной активности и структурного созревания новообразованной костной массы.
Поставленная задача достигается тем, что на фоне моделирования остеопороза в эксперименте с помощью билатеральной овариэктомии и введением глюкокортикостероида у крыс линии Wistar проводится его коррекция, в течение 56 суток, путем перорального введения фармацевтического соединения на основе 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в дозе 50 мг/кг, которое, обладая антиоксидантной, противовоспалительной и эндотелиотропной активностью, вызывает повышение кровоснабжения костной ткани и снижает развитие остеопороза.
СПОСОБ ОСУЩЕСТВЛЯЛСЯ СЛЕДУЮЩИМ ОБРАЗОМ
Опыты проводились на крысах-самках линии Wistar массой 220-280 г. Двухсторонняя овариэктомия проводилась под наркозом водного раствора хлоралгидрата в дозе 150 мг/кг и тилетамин в дозе 60 мг/кг внутрибрюшинно. Одновременно через 3 суток после овариэктомии производилось внутрибрюшинное введение метилпреднизолона в дозе 5 мг/кг каждые 3 суток эксперимента. Введение соединения 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в дозе 50 мг/кг, перорально вводили на следующий день после операции, один раз в сутки в течение 56 суток.
На 57 сутки крысы выводились из эксперимента с оценкой показателей рентгеновской денситометрии, где определялись такие показатели как:
Bone Column Density (BCD) - характеристика степени ослабления рентгеновского излучения на единицу глубины материала;
Bone Density (BD) - плотность кости с учетом глубины ткани и влияния этой глубины на плотность столбика CaPO4;
Bone Surface Density (BSD) - плотность поверхности кости независимо от плотности костного мозга с учетом геометрии изучаемого фрагмента кости.
Одновременно проводили измерение показателей микроциркуляции при помощи оборудования компании Biopac Systems, Inc. полиграфа МР150 с модулем лазерной допплеровской флоуметрии LDF100C и инвазивным датчиком TSD144, и программы AcqKnowledge версии 3.9. и оценку морфологических показателей (толщина костной трабекулы в проксимальном метафизе бедра) экспериментальных животных с коррекцией остеопорозом фармацевтического соединения 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в дозе 50 мг/кг и препарата сравнения алендроновой кислоты в дозе 2,5 мг/кг. Для оценки биохимических показателей после проведения сосудистых проб у всех животных экспериментальных групп проводился забор крови из хвостовой вены с последующим определением уровни супероксиддисмутазы (СОД), глутатионпероксидазы (ГП) и малонового диальдегида (МДА) (Nanjing Jiancheng Biological Engineering Research Institute, Китай) в соответствии с инструкциями производителя.
ПРИМЕР КОНКРЕТНОГО ВЫПОЛНЕНИЯ.
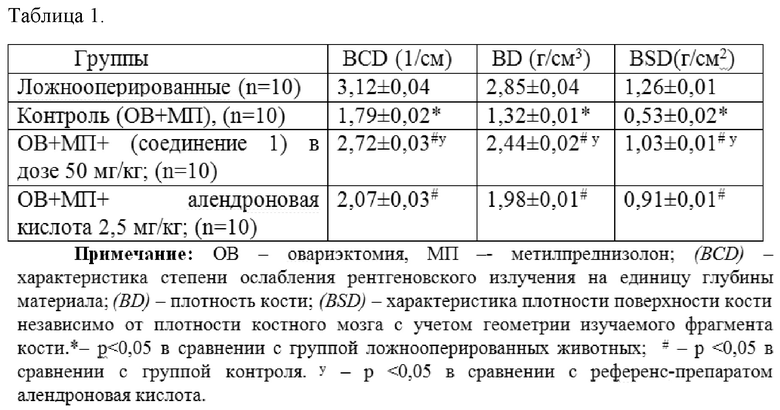
Изменения в костях скелета через 8 недель после овариэктомии и введения метилпреднизолона были подтверждены результатами денситометрии. Так в группе контроля на 57 сутки после начала эксперимента отмечалось значительное снижение выбранных показателей: BCD снизился на 47,7%; BD на 32,6%; а BSD на 34,1 % в сравнении с группой ложнооперированных животных, введение фармацевтического соединение 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в дозе 50 мг/кг способствовало ремоделированию костной ткани, достоверно повышая все показатели. Результаты денситометрии представлены в таблице 1.
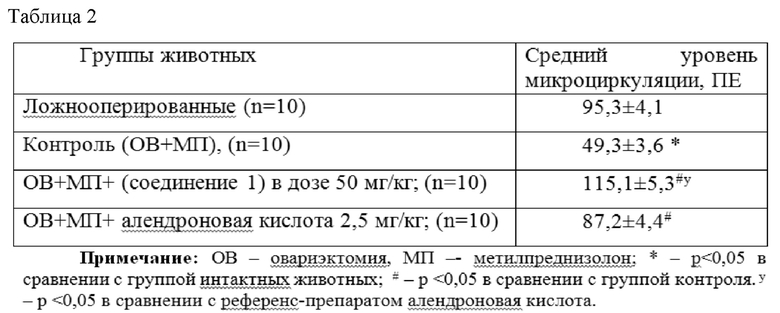
Средний уровень микроциркуляции в проксимальном метафизе бедра у ложнооперированных животных составлял 95,3±4,1 перфузионных единиц (НЕ). Проведение двухсторонней овариэктомии, при одновременном введении глюкокортикостероида метилпреднизолона в дозе 5 мг/кг каждые 3 дня эксперимента приводила у контрольных животных к достоверному снижению среднего уровня микроциркуляции по сравнению с интактными (ложнооперированными) крысами до значения 49,3±3,6 ПЕ. Одним из факторов уменьшения кровоснабжения в костной ткани является развитие остеопороза при гипоэстрогенном состоянии, приводящего в последствии к возникновению остеопоротических переломов. В группе животных, получавших в течение восьми недель после овариэктомии и введения метилпреднизолона 1 раз в 3 дня, ежедневное пероральное введение фармацевтического соединения 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в дозе 50 мг/кг и препарата сравнения алендроновой кислоты в дозе 2,5 мг/кг, приводило к достоверному повышению среднего уровня микроциркуляции в проксимальном метафизе бедра посравнению с контрольной группой до 115,1±5,3 ПЕ и 87,2±4,4 ПЕ соответственно, что подтверждает коррекцию развиваемого остеопороза при выбранной модели формирования остеопороза как фармацевтического соединения 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в дозе 50 мг/кг, так и препаратом сравнения алендроновой кислотой в дозе 2,5 мг/кг. Однако, как видно из результатов исследования препарат-референс, уступает по эффективности новому фармацевтическому соединению 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата. Динамика показателей среднего уровня микроциркуляции в проксимальном метафизе бедра при моделировании остеопороза и его коррекции новым фармацевтическим соединением 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в течение 56 суток представлена в таблице 2.
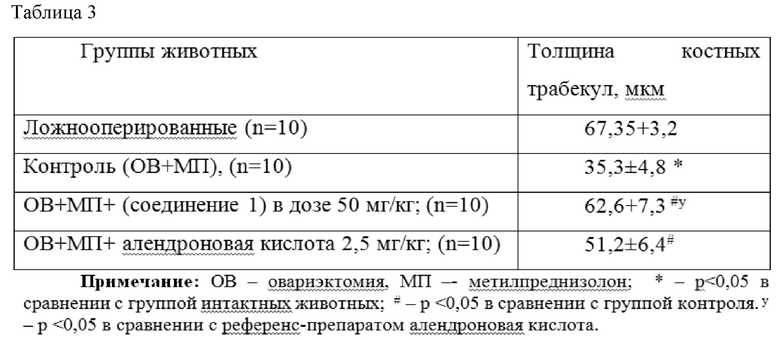
Результаты остеопротекторной активности нового фармацевтического соединения 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата подтвердили и гистоморфологические результаты исследования.
Результаты толщина костной трабекулы в проксимальном метафизе бедра при моделировании остеопороза и его коррекции новым фармацевтическим соединением 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в течение 56 суток представлены в таблице 3.
Показатели антиоксидантной активности нового фармацевтического соединения при моделировании остеопороза и его коррекции новым фармацевтическим соединением 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в течение 56 суток представлены в таблице 4.
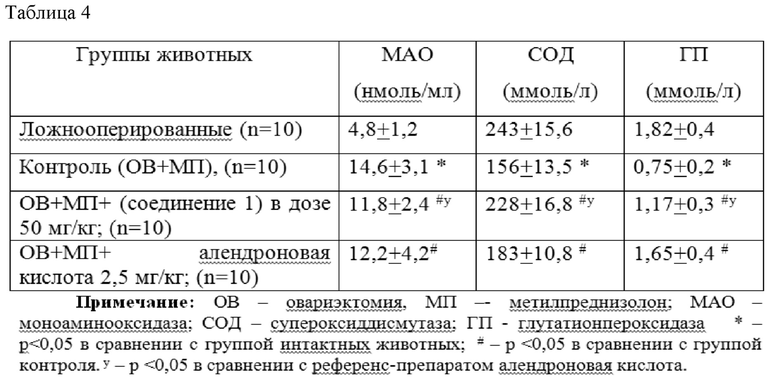
Таким образом, использование нового фармацевтического соединения1, состоящего из 2-этил-6-метил-3-гидроксипиридиния N -ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата в соотношении 1:3 (доза 50 мг/кг), на фоне остеопороза, вызванного билатеральной овариэктомией, и введением метилпреднизолона каждые 3 суток в течение 56 суток улучшало показатели денситометрии, предотвратило падение уровня микроциркуляции в проксимальном метафизе бедра, обеспечивая улучшение трофики костной ткани. Одновременно улучшались показатели гистоморфологических исследований, препятствуя снижению толщины костной трабекулы, улучшались показатели биохимических маркеров снижения оксидативного стресса, такие как супероксиддисмутаза и глутатионпероксидаза и снижался уровень моноаминооксидазы, что характеризует высокую антиоксидантную активность соединения 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ коррекции остеопороза и остеопоротических переломов 2-этил-6-метил-3-гидроксипиридинийгидроксибутандиоатом в эксперименте | 2021 |
|
RU2775439C1 |
| Способ коррекции остеопороза и остеопоротических переломов 3-гидрокси-2-этил-6-метилпиридиния никотинатом в эксперименте | 2021 |
|
RU2763011C1 |
| СПОСОБ КОРРЕКЦИИ ОСТЕОПОРОЗА И ПРОФИЛАКТИКИ ВОЗНИКНОВЕНИЯ ОСТЕОПОРОТИЧЕСКИХ ПЕРЕЛОМОВ РЕЗВЕРАТРОЛОМ | 2010 |
|
RU2437161C1 |
| СПОСОБ КОРРЕКЦИИ ОСТЕОПОРОЗА И ПРОФИЛАКТИКИ ВОЗНИКНОВЕНИЯ ОСТЕОПОРОТИЧЕСКИХ ПЕРЕЛОМОВ РЕЗВЕРАТРОЛОМ В КОМБИНАЦИИ С ЭНАЛАПРИЛОМ | 2010 |
|
RU2437160C1 |
| Комплексные соли ацексамовой кислоты, стимулирующие регенерацию костной ткани, ускоряющие процессы репаративного остеогенеза, стимулирующие минерализацию костной ткани при остеопорозе | 2018 |
|
RU2668966C1 |
| Способ коррекции микроциркуляторных нарушений 2-этил-6-метил-3-гидроксипиридиния 5-гидрокси-3-пиридинокарбоноатом при экспериментальной NMDA-опосредованной эксайтотоксичности в сетчатке | 2022 |
|
RU2784350C1 |
| Способ фармакологической коррекции оксидативных нарушений при переломах на фоне остеопороза в эксперименте хондроитином сульфатом | 2024 |
|
RU2832054C1 |
| СПОСОБ КОРРЕКЦИИ МИКРОЦИРКУЛЯЦИИ В КОСТНОЙ ТКАНИ ПРИ ЭКСПЕРИМЕНТАЛЬНОМ ОСТЕОПОРОЗЕ И ПЕРЕЛОМАХ НА ЕГО ФОНЕ КОМБИНАЦИЕЙ L-АРГИНИНА И ЛОЗАРТАНА | 2013 |
|
RU2542425C1 |
| СПОСОБ КОРРЕКЦИИ МИКРОЦИРКУЛЯЦИИ В КОСТНОЙ ТКАНИ ПРИ ЭКСПЕРИМЕНТАЛЬНОМ ОСТЕОПОРОЗЕ И ПЕРЕЛОМАХ НА ЕГО ФОНЕ РОЗУВАСТАТИНОМ | 2013 |
|
RU2538612C1 |
| СПОСОБ КОРРЕКЦИИ МИКРОЦИРКУЛЯЦИИ В КОСТНОЙ ТКАНИ ПРИ ЭКСПЕРИМЕНТАЛЬНОМ ОСТЕОПОРОЗЕ И ПЕРЕЛОМАХ НА ЕГО ФОНЕ КОМБИНАЦИЕЙ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА И РОЗУВАСТАТИНА | 2013 |
|
RU2541184C1 |
Группа изобретений относится к области органической химии, медицины и области экспериментальной фармакологии, а именно к новому соединению, обладающему остеопротекторной активностью. Раскрывается фармакологическое соединение 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, в соотношении 1:3, С62Н94N8О15, соединение 1, обладающее остеопротекторной активностью. Также раскрывается применение указанного выше фармакологического соединения 1, обеспечивающее эффективную коррекцию и профилактику остеопороза. Группа изобретений обеспечивает эффективную коррекцию и профилактику остеопороза. 2 н.п. ф-лы, 4 табл., 1 пр.
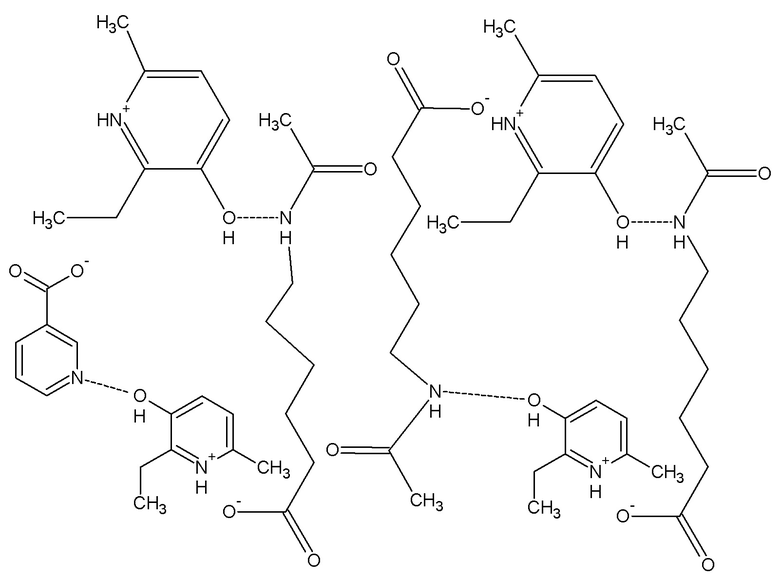
Соединение 1
1. Фармакологическое соединение 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, в соотношении 1:3, С62Н94N8О15,
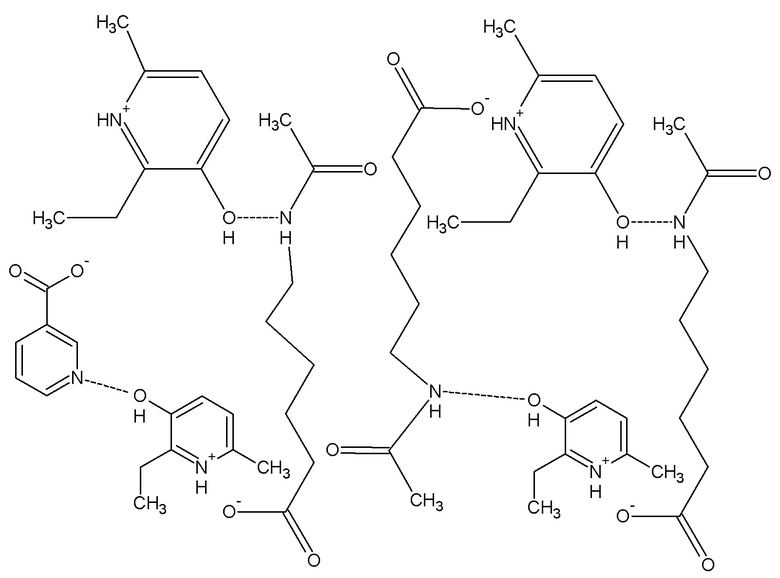
где
соединение 1, обладающее остеопротекторной активностью.
2. Применение фармакологического соединения 1, содержащего в качестве действующего вещества 2-этил-6-метил-3-гидроксипиридиния N-ацетил-6-аминогексаноата и 2-этил-6-метил-3-гидроксипиридиния 3-пиридинокарбоноата, в соотношении 1:3, обеспечивающее эффективную коррекцию и профилактику остеопороза.
| Комплексные соли ацексамовой кислоты, стимулирующие регенерацию костной ткани, ускоряющие процессы репаративного остеогенеза, стимулирующие минерализацию костной ткани при остеопорозе | 2018 |
|
RU2668966C1 |
| Способ коррекции остеопороза и остеопоротических переломов 2-этил-6-метил-3-гидроксипиридинийгидроксибутандиоатом в эксперименте | 2021 |
|
RU2775439C1 |
| КОМБИНАЦИЯ ХОНДРОПРОТЕКТОРНОГО СРЕДСТВА С НПВС | 2017 |
|
RU2742172C2 |
| Способ коррекции остеопороза и остеопоротических переломов 3-гидрокси-2-этил-6-метилпиридиния никотинатом в эксперименте | 2021 |
|
RU2763011C1 |
| ВОРОТНИКОВА С.Ю | |||
| и др | |||
| Золедроновая кислота в лечении остеопороза и других заболеваний скелета | |||
| Остеопороз и остеопатии, 2016, N 3, стр | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
Авторы
Даты
2023-10-26—Публикация
2023-02-06—Подача