Заявляемое изобретение относится к органической химии, а именно к химии гетероциклических соединений.
Лекарственный препарат сиднокарб (международное название, рекомендованное ВОЗ – mesocarb) – оригинальный отечественный психостимулятор [1-3], который являлся основным психостимулятором, применяемым в российской медицинской практике [1]. Сиднокарб эффективен при разных видах астенических состояний, протекающих с заторможенностью, вялостью, апатией, снижением работоспособности, при ипохондрии, повышенной сонливости. Препарат применялся при лечении алкоголизма, для снятия абстинентного синдрома. Сиднокарб также нашел применение в военной медицине. В связи с высокой эффективностью и хорошей переносимостью сиднокарб практически полностью заменил собой амфетамин [1] (в РФ выпускался под названием фенамин).
В молекуле N-фенилкарбамоил-3-(β-фенилизопропил)-сиднонимина (действующее вещество сиднокарба):
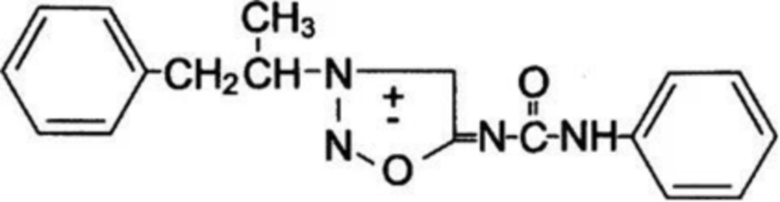
есть асимметрический атом углерода – атом, у которого все четыре заместителя различные (С6Н5СН2, СН3 и гетерокольцо), что позволяет говорить о существовании двух стереоизомеров. Сиднокарб – это рацемат, состоящий из равных частей D- и L-стереоизомеров.
Исследования [4, 6, 7] показали, что активным в препарате cиднокарб является левовращающий стереоизомер L-N-фенилкарбамоил-3(β-фенилизопропил)сиднонимин или L-cиднокарб, действующий в 2 раза эффективнее сиднокарба [4]:
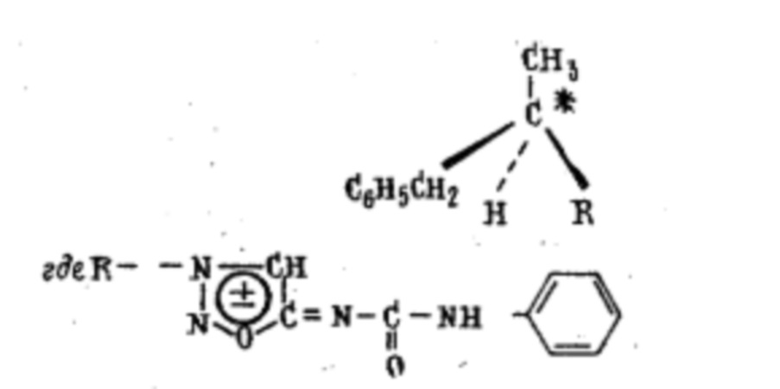
Правовращающий D-изомер сиднокарба практически не активен.
Из уровня техники известны два способа получения L-сиднокарба [4-5].
Первый способ [4] заключается в конденсации гидрохлорида L-3-(β-фенилизопропил)сиднонимина с фенилизоцианатом в среде изопропилового спирта в присутствии ацетата натрия или, в другой модификации метода, в добавлении фенилизоцианата к суспензии гидрохлорида L-3-(β-фенилизопропил)сиднонимина в бензоле в присутствии триэтиламина. Недостатком известного способа является низкий выход целевого продукта, порядка 66-68%, в расчете на исходное соединение.
В другом способе [5] L-сиднокарб получают при взаимодействии левовращающего изомера, L-N-нитрозо-N-(β-фенилизопропил)аминоацетонитрила, с фенилизоциантом в бензоле в присутствии триэтиламина.
Серьёзным недостатком указанных методов для практического применения является тот факт, что исходные соединения: левовращающие изомеры - гидрохлорид L-3-(β-фенилизопропил)сиднонимин и L-N-нитрозо-N-(β-фенилизопропил)аминоацетонитрил – и способы их получения не описаны в доступных источниках.
Однако поскольку химические свойства оптических изомеров и рацемата, как известно, абсолютно одинаковы, исходный для синтеза L-сиднокарба левовращающий изомер L-3-(β-фенилизопропил)сиднонимин можно в принципе получить таким же способом, как и его рацемат.
Описан [8, 9] многостадийный способ получения указанного рацемата гидрохлорида D,L-3-(β-фенилизопропил)сиднонимина в несколько ниже приведенных стадий исходя из рацемата соответствующего амина D,L-С6Н5СН2СН(СН3)-NH2:
• взаимодействием формальдегида с ацетонциангидрином в водной среде в присутствии поташа получают гликоленитрил (HOCH2CN, нитрил гликолевой кислоты), гликоленитрил при 10-12 °C вводят в реакцию с D,L-β-фенилизопропиламином, отделяют образовавшийся органический слой, который содержит продукт реакции - D,L-N-β-фенилизопропиламиноацетонитрил, ацетон, непрореагировавшие реагенты и др. примеси,
• отделенный органический слой растворяют в изопропаноле, постепенно добавляют раствор хлористого водорода в изопропаноле, отфильтровывают гидрохлорид D,L-N-β-фенилизопропиламиноацетонитрила, промывают и сушат;
• гидрохлорид D,L-N-β-фенилизопропиламиноацетонитрила растворяют в воде, добавляют этилацетат и нитрозируют действием раствора нитрита натрия при рН 1, отделяют органический слой, водный слой еще дважды экстрагируют этилацетатом;
• к объединенному экстракту добавляют при охлаждении раствор хлористого водорода в изопропаноле и отфильтровывают выпавший в осадок рацемат гидрохлорида D,L-3-(β-фенилизопропил)сиднонимина с выходом 42-53% в расчете на исходный амин D,L-С6Н5СН2СН(СН3)-NH2.
Аналогичным образом и с таким же выходом (42-53%) из левовращающего изомера L-С6Н5СН2СН(СН3)-NH2 можно получить гидрохлорид L-3-(β-фенилизопропил)сиднонимина и далее из него получить L-сиднокарб с выходом 66-68% согласно способу [4]. В результате этих многостадийных процессов с выделением промежуточных продуктов конечный выход целевого вещества, L-сиднокарба, составит менее 68%*53%=36% в расчете на исходный левовращающий изомер амина L-С6Н5СН2СН(СН3)-NH2.
Технический результат настоящего изобретения заключается в повышении выхода целевого вещества - L-N-фенилкарбамоил-3(β-фенилизопропил)сиднонимина, L-сиднокарба - из левовращающего изомера L-β-фенилизопропиламина и в упрощении получения целевого продукта путем проведения процесса в одну стадию без выделения промежуточных продуктов.
Указанный технический результат достигается следующим образом. К водному раствору ацетонциангидрина в слабощелочной среде добавляют соль или основание L-β-фенилизопропиламина, перемешивают, подкисляют и добавляют при охлаждении водный раствор нитрита натрия, после выдержки экстрагируют реакционную массу неполярным органическим растворителем, к полученному экстракту добавляют третичный амин и фенилизоцианат, перемешивают и после выдержки отфильтровывают выпавший в осадок целевой продукт - L-сиднокарб.
Выход целевого продукта при этом составляет 90-95% в расчете на исходный L-β-фенилизопропиламин.
Использовать основание L-β-фенилизопропиламина, представляющего собой маслянистую вязкую жидкость с неприятным запахом, менее удобно в производстве, чем соль в виде кристаллического порошка. При этом целесообразно использовать сульфат L-β-фенилизопропиламина ввиду отсутствия у него гигроскопичности.
В качестве неполярного органического растворителя можно использовать хлороформ, бензол, хлористый метилен, диэтиловый эфир или дихлорэтан, обычно применяемые в производстве.
В качестве третичного амина можно использовать один из триалкиламинов формулы R3N, где R одинаковые или разные, как правило, низшие алкилы: триметиламин, триэтиламин и др.
Пример 1. К раствору 11 г ацетонциангидрина в 100 мл воды при рН 7,5 – 8,0 добавляют 18,4 г сульфата L-β-фенилизопропиламина, перемешивают в течение 1 часа. При рН 2-3 и 10-12°С добавляют по каплям водный раствор 10 г нитрита натрия и перемешивают в течение 2 часов. Реакционную массу экстрагируют хлороформом (2 х 60 мл), к отделенному и высушенному экстракту добавляют при 20-22°С 10 мл триэтиламина и 14 г фенилизоцианата, перемешивают в течение 2 часов и отфильтровывают выпавший в осадок 29,6 г (выход 92% от теории в расчете на сульфат L-β-фенилизопропиламина) целевой продукт - L-N-фенилкарбамоил-3(β-фенилизопропил)сиднонимин, L-сиднокарб. Белый с желтовато-зеленоватым оттенком кристаллический порошок, практически нерастворимый в воде, температура плавления 152-154°С (с разложением). В УФ спектре (раствор в этаноле) имеет 3 максимума 204, 256, 340 нм. Удельное вращение αD20 - 233,3о (ацетон, С = 1)
C18H18N4O2
расчет: С – 67,06%, Н – 5,63%, N - 17,38%;
результат анализа: С – 67,12%, Н – 5,52%, N - 17,23%
Пример 2. Процесс проводят аналогично описанному в примере 1, но вместо сульфата L-β-фенилизопропиламина используют основание L-β-фенилизопропиламина. Выход L-N-фенилкарбамоил-3(β-фенилизопропил)сиднонимина, L-сиднокарба, 93% от теории в расчете на L-β-фенилизопропиламин.
Пример 3. Процесс проводят аналогично описанному в примере 1, но в качестве растворителя для экстракции вместо хлороформа используют бензол. Выход L-N-фенилкарбамоил-3(β-фенилизопропил)сиднонимина, L-сиднокарба, 92% от теории в расчете на сульфат L-β-фенилизопропиламин.
Цитируемые источники
1) Мезокарб / Википедия. URL: https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D0%B7%D0%BE%D0%BA%D0%B0%D1%80%D0%B1https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D0%B7%D0%BE%D0%BA%D0%B0%D1%80%D0%B1. Дата обращения 28.09.2023 г.
2) Холодов Л.Е. и соавт. Сиднокарб – новый стимулятор ЦНС, Хим. фарм. журнал, 1973, N1, с.50
3) 3-(β-фенилизопропил)-фенилкарбамоилсиднонимин, обладающий психостимулирующей активностью. Патенты: SU329890, DE2028880A1, CH542868A, GB1262830A
4) Холодов Л.Е. и др. L-3-(β-Фенилизопропил)- фенилкарбамоилсиднонимин, обладающий психостимулирующей активностью, Авт. Свид. СССР 715575
5) Kholodov L.E et al. Sydnonimine N-acyl derivatives and method for preparing, patent US4245100
6) Альтшулер Р.А., Машковский М.Д. Фармакол и токсикол. 4, 345 – 349 (1980).
7) Альтшулер Р.А., Сравнительная оценка сродства фенилэтиламинов. Хим-фарм. журнал, 39, No 4, с. 3-9 (1980).
8) Иозеп, А.А. и др. «Химическая технология фармацевтических субстанций». СПб. Издательство «Лань», 2016. С. 177-178
9) Самаренко В.Я. «Химическая технология лекарственных субстанций». СПб.: Санкт-Петербургская государственная химико-фармацевтическая академия (СПХФА). С. 107-109. URL: https://web.archive.org/web/20161213035135/http://www.fptl.ru/files/htls/psihostimulyatori.pdf
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения сиднонилинов | 1975 |
|
SU690008A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АРИЛКАРБАМОИЛСИДНОНИМИНОВ | 1968 |
|
SU222370A1 |
| 3-( -Фенилизопропил)- фенилкарбамоилсиднонимин,обладающий психостимулирующей активностью | 1976 |
|
SU715575A1 |
| ТРИАМИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 4-ФЕНИЛ-2- АМИНОТИАЗОЛОМ, ПРОЯВЛЯЮЩИЙ АНТИДЕПРЕССАНТНУЮ АКТИВНОСТЬ | 1990 |
|
SU1764303A1 |
| N-(ФЕНИЛИЗОПРОПИЛ)-3,3-ДИФЕНИЛ-2-ПРОПЕНИЛАМИН ИЛИ ЕГО СОЛИ, ОБЛАДАЮЩИЕ СИМПАТО- И АДРЕНОЛИТИЧЕСКИМИ СВОЙСТВАМИ | 1977 |
|
SU666787A1 |
| СПОСОБ ПОЛУЧЕНИЯ СИДНОНОВDLttUlUJn'')»ПАТПЛКО- TE:x:!R4ti^;.;sor'f,.''i'^-) -; [jA11 | 1965 |
|
SU173782A1 |
| СПОСОБ ПОЛУЧЕНИЯ (S)-2,6-ДИАМИНОГЕКСАНОВОЙ КИСЛОТЫ 3-МЕТИЛ-1,2,4- ТРИАЗОЛИЛ-5-ТИОАЦЕТАТА | 2012 |
|
RU2495874C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-ФТОР-L-ДОФА | 2023 |
|
RU2817082C1 |
| Способ получения замещенных сиднониминов или их солей | 1980 |
|
SU963469A3 |
| НОВЫЙ СПОСОБ ПОЛУЧЕНИЯ N-АЦЕТИЛ-(L)-4-ЦИАНОФЕНИЛАЛАНИНА АС-(L)-PHE(4-CN)-OH И N-АЦЕТИЛ-(L)-N-АМИДИНОФЕНИЛАЛАНИН-ЦИКЛОГЕКСИЛ-ГЛИЦИН-β-(3-N-МЕТИЛПИРИДИН ИЯ)-АЛАНИНА АС-(L)-PАPH-СHG-РAL МE(3)-NH | 1996 |
|
RU2170764C2 |
Изобретение относится к области химии и медицины, а именно к способу получения L-N-фенилкарбамоил-3(β-фенилизопропил)сиднонимина (L-сиднокарба) из L-β-фенилизопропиламина, отличающемуся тем, что к водному раствору ацетонциангидрина в слабощелочной среде добавляют основание или соль L-β-фенилизопропиламина, подкисляют и добавляют водный раствор нитрита натрия, после выдержки экстрагируют неполярным растворителем, к экстракту добавляют третичный амин и фенилизоцианат, перемешивают и после выдержки отфильтровывают выпавший в осадок целевой продукт L-сиднокарб. Технический результат заключается в повышении выхода целевого вещества из левовращающего изомера L-β-фенилизопропиламина и в упрощении получения целевого продукта путем проведения процесса в одну стадию без выделения промежуточных продуктов. 3 з.п. ф-лы, 3 пр.
1. Способ получения L-N-фенилкарбамоил-3(β-фенилизопропил)сиднонимина (L-сиднокарба) из L-β-фенилизопропиламина, отличающийся тем, что к водному раствору ацетонциангидрина в слабощелочной среде добавляют основание или соль L-β-фенилизопропиламина, подкисляют и добавляют водный раствор нитрита натрия, после выдержки экстрагируют неполярным растворителем, к экстракту добавляют третичный амин и фенилизоцианат, перемешивают и после выдержки отфильтровывают выпавший в осадок целевой продукт L-сиднокарб.
2. Способ по п. 1, отличающийся тем, что в качестве соли L-β-фенилизопропиламина используют сульфат L-β-фенилизопропиламина.
3. Способ по п. 1, отличающийся тем, что в качестве неполярного растворителя используют одно из следующих веществ: хлороформ, бензол, хлористый метилен, диэтиловый эфир или дихлорэтан.
4. Способ по п. 1, отличающийся тем, что в качестве третичного амина используют один из триалкиламинов формулы R3N, где R – одинаковые или разные низшие алкилы.
| 3-( -Фенилизопропил)- фенилкарбамоилсиднонимин,обладающий психостимулирующей активностью | 1976 |
|
SU715575A1 |
| US 4277609 A, 07.07.1981 | |||
| US 4301285 A, 17.11.1981 | |||
| Аппарат для ионизации воздуха | 1932 |
|
SU32064A1 |
Авторы
Даты
2023-11-14—Публикация
2023-10-06—Подача