Изобретение относится к области медицины, а именно к местным гемостатическим средствам и может применяться для остановки наружных кровотечений, а также при ранениях паренхиматозных органов и крупных сосудов.
На сегодняшний день местные гемостатические средства нашли широкое применение не только в хирургических клиниках, но и на догоспитальном этапе. Эти препараты удобны для интраоперационного гемостаза и при оказании первой помощи раненым. Во время оперативных вмешательств средства для локального гемостаза позволяют снизить или предотвратить интраоперационную кровопотерю. Топические гемостатики просты в применении и не способствуют дополнительной травматизации тканей, которая возможна при прошивании или перевязке источника кровотечения, применении диатермокоагуляции, лазерной фотокоагуляции и прочих физических методов гемостаза.
При кровотечениях из сосудов конечностей на этапе первой помощи эффективно наложение жгута, однако на переходных зонах и на туловище при оказании первой помощи раненым возможно использовать только местные гемостатические средства. На догоспитальном этапе специально разработанные кровоостанавливающие препараты позволяют обеспечить гемостаз до оказания квалифицированной помощи в условиях госпиталя или клиники.
В руководствах по оказанию помощи раненым во время боевых действий в Российской Федерации, США и странах НАТО рекомендовано использование местных гемостатических средств в порядке само- и взаимопомощи.
Современные материалы, используемые для производства местных гемостатических средств, отличаются по своей природе. По составу их можно подразделить на следующие группы:
- материалы на основе биологических факторов свертывания крови, полученных от животных или человека: коллаген, тромбин, фибрин, фибриноген, плазма и другие;
- материалы на основе производных целлюлозы;
- материалы на основе синтетических полимеров;
- материалы на основе неорганических соединений (цеолит, силикагель);
- материалы на основе экстрактов растений;
- материалы на основе хитозана и т.д
По форме выпуска существуют средства для гемостаза в виде марли, с нанесенным на нее действующим веществом, гемостатических губок, пластин, порошков и т.д.
Из патента RU2675631C1 известно местное гемостатическое средство, содержащее хитозан, карбоксиметилцеллюлозу и ципрофлоксацин. Препарат используется как средство первой помощи при наружных ранениях, позволяет профилактировать развитие инфекции в ране.
Бинт «ГЕМОФЛЕКС» (RU248770) создан на основе нановолокон хитозана. Он обладает большой удельной поверхностью, пористостью, воздухопроницаемостью и повышенными сорбционными свойствами.
К препаратам, производимым на территории Российской Федерации, относится также «ГЕПОГЛОС» (RU2635465), выпускаемый в форме бинта с нанесенным на него хитозаном. Действующее вещество - соль ацилированного хитозана, нанесено с двух сторон бинта. Бинт содержит также карбоксиметилкрахмал для увеличения сорбционной ёмкости и выполнен из нетканого материала "спанлейс", содержащего вискозу и полиэфир.
Известно гемостатическое средство «ГЕМОХИТ» (RU2681184C1), при изготовлении которого используется поперечно сшитый эпоксидной смолой хитозан, что обусловлено его более высокой поглотительной способностью по сравнению с несшитым хитозаном. Использование глицерина в качестве пластификатора (что обусловлено его высокими пластифицирующими свойствами) придает губке необходимые эластичность и прочность.
Корпорация HemCon Medical Technologies.Inc в США производит следующие гемостатические изделия: «HEMCON GUARDACARE PRO» US9205170B2 (покрытия для ран, содержащие хитозан) и «HEMCON BANDAGE PRO» (бинты с нанесённым на них хитозаном). Данный продукт широко применяется в условиях боевых действий при оказании помощи раненым.
Известен патент US5836970A: раневые повязки, содержащие хитозан и альгинат. Согласно патенту, данное медицинское изделие может быть произведено в виде порошка, пленки, геля, пены или их смесей.
Среди местных гемостатических средств, содержащих хитозан известен патент US20050123588A1, в котором представлен гемостатик, содержащий хитозановые волокна, на которые нанесены кровоостанавливающие микропористые полисахаридные микросферы и лекарственное средство или биологически активное вещество. Гемостатический материал рекомендован авторами для остановки активного кровотечения при ранениях артерий и вен, герметизации проколов бедренных артерий.
Известен также патент US20050203058A1, где описано гемостатическое средство, содержащее α- и β-хитозан и их производные.
В патенте под номером US6998509B1 представлено средство для лечения ран, содержащее хитозан. Хитозан в данном продукте находится в форме волокон, модифицированных обработкой кислотой в растворителе, который не способен растворять волокна хитозана, и путем обработки теплом.
Патент US8106030B2 описывает изобретение, в котором гемостатический порошок содержит соль хитозана вместе с по меньшей мере одним инертным материалом.
В патенте GB2393120A описана композитная повязка на рану, содержащая хитозан и окисленную целлюлозу. Препарат может иметь форму губки или раневой повязки.
Известно изобретение CN1833732A, где из хитозановых волокон путем химической модификации получены карбоксиметилхитозановые волокна. Его можно использовать для приготовления хирургической повязки для ран и ожогов, послеоперационных повязок.
В патенте WO2020021499A1 представлено изобретение, которое описывает гемостатическую гелевую повязку, содержащую хитозан в качестве полисахарида, желатин в качестве белка и крахмал в качестве углевода в одной фазе.
Известен патент CN105169459B в котором описан следующий способ приготовления кровоостанавливающего порошка: смешивание высоковязкого хитозана с высокой степенью деацетилирования с альдегидной кислотой, альгинатом натрия цинком.
Патент под номером CN105251036A представляет кровоостанавливающий материал, содержащий по массе 60-75 частей хитозанового волокна, 6-15 частей кератина, 10-25 частей натрия карбоксиметилцеллюлозы и 5-10 частей поливинилового спирта. Медицинский гемостатический материал обладает такими преимуществами, как быстрый гемостаз, превосходные механические свойства, хорошая биосовместимость и т.п.
В патенте КР101699924Б1 раскрыт способ изготовления медицинского волокна, содержащего кальций-карбоксиметилцеллюлозу и соединение хитозана.
Известен также патент CN104874011A описывающий кровоостанавливающее средство, которое представляет собой твердый препарат, полученный реакцией производного хитозана, гиалуроновой кислоты, хондроитинсульфата, альгиновой кислоты, карбомера, ксантановой камеди или производного целлюлозы и сшивающего агента Сшивающим агентом является формальдегид, метилглиоксаль, глутаровый альдегид. Гемостатик имеет преимущества, заключающиеся в быстром и эффективном гемостатическом эффекте, хорошей биологической совместимости и биологической разлагаемости.
В патенте RU2589840C1 описано изобретение гидрофильного геля для раневого покрытия, содержащий в качестве вспомогательных веществ сукцинат хитозана, воду и спирт этиловый. Технический результат - гидрофильный гель для раневого покрытия с улучшенными свойствами за счет повышения проникающей способности и заживления и обеззараживания и сохранения формы на ране.
К недостаткам всех аналогов относятся низкая адгезивность, что заключается в необходимости дополнительной фиксации препарата к ране, а также то, что действующее вещество, содержащее хитозан или его соли, при контакте с жидкостями организма теряет механическую прочность и постепенно размокает. Кроме того, все перечисленные аналоги рекомендованы к использованию только при наружных ранениях, их применение при внутриполостных ранениях не описано.
Среди аналогов, которые применимы для интраоперационного использования при работе с ранениями паренхиматозных органов и сосудов, необходимо упомянуть препараты на основе факторов свертывания. Они представляют собой комбинацию различных факторов свертывания. К ним относятся, например, «TACHOSIL» US9517287B2, который представляет собой коллагеновую губку, покрытую фибриногеном и тромбином, выделенными из крови человека. Этот препарат обладет быстрым и надежным гемостатическим эффектом.
«TACHOSIL» - является более совершенной модицикацией препарата «TACHOCOMB» (EP0059265B1). Последний изготовлен из лошадиного коллагена, бычьего тромбина, бычьего апротинина и человеческого фибриногена. «TACHOSIL» содержит только человеческий фибриноген с лошадиным коллагеном в качестве носителя. Он не содержит апротинина и других компонентов бычьего происхождения.
Суть работы подобных средств - имитация заключительных этапов коагуляции. Они обеспечивают достижение гемостаза за 3-5 минут. При контакте с кровоточащей поверхностью препарат становится активным, высвобождает активные факторы свертывания. Их биодеградация в организме длится около 12 недель.
Подобные кровоостанавливающие средства демонстрируют быстрый и надежный гемсоатический эффект, обладают биоадгезивностью, пригодны для внутриполостного использования. Однако эти препараты несут бо´льшую антигенную нагрузку, а также содержат белки крови человека, что влечет за собой риск заражения пациента вирусными инфекциями. Кроме того, они несомненно дороже, чем их синтетические аналоги на основе хитозана, каолина и т.д.
Наиболее близким к предлагаемому является гемостатическое средство «Haemostatic material», опубликованное в патенте US20110052665A1, торговое название «CELOX», которое выбрано нами в качестве прототипа.
В настоящее время прототип выпускается в виде гранул «CELOX GRANULES» или в аппликаторе «CELOX-A», а также в виде пленки. Наиболее удобны в использовании бинт с нанесенным на него действующим веществом «CELOX GAUZE» и комплект из гранул и повязки «CELOXPRO». Препарат способен останавливать даже массивные кровотечения, в том числе из бедренной артерии. В соответствии с изобретением предлагается гемостатический материал, включающий несущий слой и слой для контакта с раной, содержащий по меньшей мере один кровоостанавливающий агент в форме частиц, гранул, порошка или коротких волокон. Кровоостанавливающее средство может быть прикреплено к несущему слою с помощью клея, содержащего связующее вещество, которое может образовывать слой между кровоостанавливающим средством и несущим слоем.
Пленка диспергируется во влажном состоянии. Удаляемым слоем может быть любой лист или сетка, которые можно снять перед использованием. Кровоостанавливающее средство может быть приклеено под действием тепла и/или давления как к верхней, так и к нижней поверхностям несущего слоя. Это может быть растворимая пленка, изготовленная из полисахарида, такого как желатин или производное целлюлозы, или она может быть изготовлена из нерастворимого вещества, такого как поливинилацетат (ПВА) или поливиниловый спирт (ПВС). Препарат нетоксичен и обладает хорошей биосовместимостью. Изделие содержит соль хитозана - сукцинат в качестве основного гемостатического агента. Соль хитозана получают реакцией хитозана с соответствующей кислотой. Соль хитозана предпочтительно составляет по меньшей мере 5 мас.%.
В соответствии с другим вариантом осуществления изобретения, прототип может быть выполнен в виде компрессионной повязки или многокомпонентной повязки, в которой кровоостанавливающий листовой материал используется в качестве активной поверхности абсорбирующей повязки. Гемостатический материал позволит любой избыточной крови пройти через него, где она будет поглощена впитывающей повязкой сзади.
CELOX содержит также поверхностно-активные вещества: блок-сополимеры на основе этиленоксида и пропиленоксида (например, BASF Pluronics®), лауриновую кислоту, олеиновую кислоту, другие жирные кислоты и соли жирных кислот или поверхностно-активные вещества и эмульгаторы на основе силикона. Поверхностно-активное вещество составляет от 0,001 до 10% по весу.
Обнаружено, что свойства действующего вещества улучшаются при внесении в препарат инертных материалов. Например, хитин, хитозан или целлюлозу. Инертный материал может быть добавлен к порошку в количестве до 95% по массе от общей массы. Препарат имеет рН от 3,5 до 6,0. При создании гемостатический повязки препарат распыляют на марлю.
Несомненно, прототип доказал свою эффективность при остановке наружных кровотечений, однако он не лишен ряда недостатков. Предложенное авторами гемостатическое средство само по себе не обладает достаточными адгезивными свойствами. Для его фиксации необходимо применение дополнительных материалов: марлевой или другой циркулярной повязки, пластыря, одноразовой раневой повязки с клейкой поверхностью. Необходимо обязательно удалять гемостатическое средство, а также материал для его фиксации из раны при проведении первичной хирургической обработки. Это приводит к дополнительной травматизации раневой поверхности, а также доставляет пострадавшему болевые ощущения. Удаление варианта выполнения прототипа в виде гранулированного препарата, технически сложно выполнимо и может занимать значительное время. Также стоит отметить, что прототип во всех его вариантах исполнения не предназначен для остановки кровотечений из внутренних органов.
Таким образом, актуальной задачей на сегодняшний день является поиск наиболее эффективного решения проблемы остановки кровотечения как при наружных кровотечениях, так и при повреждении паренхиматозных органов.
Технический результат настоящего изобретения заключается в создании эффективного местного гемостатического средства с повышенной адгезией (в том числе к влажной раневой поверхности), не требующего дополнительных материалов для его фиксации.
Этот результат достигается тем, что создано местное гемостатическое средство, выполненное в виде пленки, содержащее несущий слой и слой для контакта с раной из соли хитозана, согласно изобретению, несущий слой содержит соль хитозана, глицерин и воду, а слой для контакта с раной дополнительно содержит таннин, воду и аргинин, или олигоаргинин, или полиаргинин, или протамина сульфата при следующем соотношении компонентов, масс. %:
Соль хитозана - 2-4,
Глицерин - 1,
Таннин - 1,
Аргинин - 1,
Олигоаргинин - 1,
Полиаргинин - 1,
Протамина сульфата - 1,
Вода - остальное.
Местное гемостатическое средство, выполненное в виде пленки по п. 1, согласно изобретению, для получения пленки несущий слой из соли хитозана, глицерина и воды высушивают на ровной поверхности в течение 48 часов при комнатной температуре в вытяжном шкафу, после чего на высушенный несущий слой наносят слой для контакта с раной, содержащий соль хитозана, аргинин, воду и таннин или олигоаргинин, или полиаргинин, или протамина сульфата, затем его также высушивают при комнатной температуре на ровной поверхности в течение 48 часов в вытяжном шкафу.
Хитозан - это природный полисахарид, выделяемый из панцирей ракообразных; положительный заряд -NH3 группы хитозана электростатически взаимодействует с анионами на поверхности эритроцитов, что приводит к интенсивной агрегации эритроцитов вокруг ранения с образованием тромбов, которые быстро останавливают кровотечение. Хитозан способствует активации тромбоцитов и усилению их адгезии. Кроме того, in vivo хитозан приводит к контактной активации факторов свертывания крови, укрепляя сгусток. Он биологически инертен и способен к биодеградации. Лизоцим является основным ферментом, ответственным за деградацию хитозана in vivo путем гидролиза ацетилированных остатков. Лизоцим содержится в том числе в крови (Овсянников В.Г., Торопкина Ю.Е., Краскевич В.В., Алексеев В.В., Бойченко А.Е., Алексеева Н.С., Краскевич Д.А. Лизоцим - грани возможного// Современные проблемы науки и образования. - 2020. - № 3.). Конечными продуктами деградации являются растворимые олигосахариды хитозана небольшой длины. Хитозан оказывает стимулирующее действие на макрофаги, а также является хемоаттрактантом для нейтрофилов, что способствует ускорению биодеградации хитозана. Хитозан обладает также неспецифической антимикробной активностью и способствует заживлению ран (Di Martino, A. Chitosan: a versatile biopolymer for orthopaedic tissue-engineering / A. Di Martino, M. Sittinger, M.V. Risbud // Biomaterials. -2005. - Vol. 26, № 30. - P. 5983-5990..), (Da Sacco, L. Chitin and chitosan as multipurpose natural polymers for groundwater arsenic removal and AS2O3 delivery in tumor therapy / L. Da Sacco, A. Masotti// Mar. Drugs. - 2010. - Vol. 8, № 5. - P. 1518-1525). Все эти свойства делают хитозан один из самых востребованных веществ для создания местных гемостатических средств и тканевых биоадгезивов.
В настоящем изобретении несущий слой также, как и активный содержит соль хитозана в качестве основы, что делает пленку биологически интертной и позволяет оставлять ее на ране после завершения операции на паренхиматозных органах и сосудах.
Для создания соли хитозана могут быть использованы органические и одноосновные неорганические кислоты, например, ацетат, лактат, сукцинат, малат, цитрат и им подобные. Хитозан при высыхании образует пленку, обладающую адгезивными свойствами, но которая при избытке жидкости набухает и переходит в желеобразное состояние.
Глицерин - органическое соединение, простейший представитель трёхатомных спиртов. Представляет собой вязкую прозрачную жидкость. Нетоксичен, в отличие, например, от простейших двухатомных спиртов (Титов, В. Н. Единение физико-химического и биологического действия спиртов глицерина и холестерина в поглощении клетками жирных кислот.// Клиническая лабораторная диагностика : журн. - 2013. - № 1.). Глицерин обеспечивает эластичность двухкомпонентной пленки после высыхания и делает нерастворимым несущий слой без использования сшивающих агентов, например, глутарового альдегида.
Вода используется в несущем и активном слоях в качестве растворителя при изготовлении раствора для высушивания.
В основе слоя для контакта с раной также применяется соль хитозана, для создания которой могут быть использованы органические и одноосновные неоргоганические кислоты, например, ацетат, лактат, сукцинат, малат, цитрат и им подобные.
Дополнительно активный слой пленки содержит аргинин -аминокислоту, имеющую в составе положительно заряженную гуанидиновую группу, благодаря которой потенцируются адгезивные и гемостатические свойства хитозана. Пленка Хитозан/Аргинин продемонстрировала подавление роста колоний E. Coli и S. Aureus. Более того, раствор хитозана и аргинина не проявлял цитотоксичности и способствовал клеточной пролиферации (Song J, Feng H, Wu M, Chen L, Xia W, Zhang W. Preparation and characterization of arginine-modified chitosan/hydroxypropyl methylcellose antibacterial film. Int J Biol Macromol. 2020 Feb 15;145:750-758. doi: 10.1016/j.ijbiomac.2019.12.141. Epub 2019 Dec 17. PMID: 31857168).
Адгезивные свойства пленки и устойчивость к размоканию во влажной среде усилены за счет добавления к слою для контакта с раной таннина - растительного полифенольного дубильного вещества. Хорошая адгезивность таннина обусловлена его химической реакцией с нуклеофильными группами, такими как -NH2 или -SH на поверхности ткани. Добавление таннина к раствору обеспечило значительную силу адгезии к влажной ткани и хорошую цитосовместимость (Guo J, Sun W, Kim JP, Lu X, Li Q, Lin M, Mrowczynski O, Rizk EB, Cheng J, Qian G, Yang J. Development of tannin-inspired antimicrobial bioadhesives. Acta Biomater. 2018 May; 72:35-44. doi: 10.1016/j.actbio.2018.03.008. Epub 2018 Mar 17. PMID: 29555464; PMCID: PMC6328059). Биологические адгезивы на основе таннина обладают антиоксидантными, противовоспалительными и антибактериальными свойствами. Таннин может связывать свободные радикалы, а также способствовать пролиферации клеток млекопитающих. Противовоспалительные свойства таннина обусловлены его способностью вызвать снижение экспрессии интерлейкина 1В и фактора некроза опухоли альфа (Wu K, Fu M, Zhao Y, Gerhard E, Li Y, Yang J, Guo J. Anti-oxidant anti-inflammatory and antibacterial tannin-crosslinked citrate-based mussel-inspired bioadhesives facilitate scarless wound healing. Bioact Mater. 2022 May 21;20:93-110. doi: 10.1016/j.bioactmat.2022.05.017. PMID: 35633874; PMCID: PMC9131258). Таннин не обладает токсичностью, что было изучено при применении повязок, содержащих таннин у больных с обширными ожогами (Chokotho L, van Hasselt E. The use of tannins in the local treatment of burn wounds - a pilot study. Malawi Med J. 2005 Jun;17(1):19-20. doi: 10.4314/mmj.v17i1.10866. PMID: 27528993; PMCID: PMC3346037).
Существует вариант изобретения, где в качестве добавки к хитозану и таннину в активном слое использован протимина сульфат - соединение, в котором 67% аминокислотного состава представлено аргинином, который делает его сильнощелочным поликатионным веществом с молекулярной массой 4,5 тыс. Да. Множественные положительно заряженные цепи протамина обеспечивают сильное электростатическое взаимодействие с отрицательно заряженными группами на клеточных мембранах.
Олигоаргинин - это пептид, содержащий участок аргинина и обладающий схожими с аргинином химическими свойствами (KASHEVEROV, I. E., KRYUKOVA, E. V., IVANOV, I. A., LEBEDEV, D. S., SPIROVA, E. N., EGOROVA, N. S., & TSETLIN, V. I. (2019). Oligo-arginine peptides as a new class of ligands of nicotinic acetylcholine receptors. Вестник Дальневосточного отделения Российской академии наук, (6s), 44.).
Полиаргинин представляет собой положительно заряженную синтетическую полиаминокислоту (Fuchs SM, Raines RT. Polyarginine as a multifunctional fusion tag. Protein Sci. 2005 Jun;14(6):1538-44).
Благодаря биологической интертности, способности к биодеградации препарат можно использовать при ранениях паренхиматозных органов, таких как печень, почки и селезенка, как средство временного или окончательного гемостаза. После операции препарат может быть оставлен в брюшной полости на ране.
При изготовлении пленки на ровной поверхности высушивается раствор солей хитозана и глицерина в течение 48 часов при комнатной температуре в вытяжном шкафу. Затем на высушенную подложку заливается раствор хитозана, аргинина и таннина. Он также высушивается при комнатной температуре на ровной поверхности в течение 48 часов. После высыхания пленка готова к использованию.
Сушка в вытяжном шкафу выбрана потому, что влажный гидрогель не обладает достаточной адгезией: в этом случае нет плотного контакта положительно заряженных групп с поверхностями клеток. Использование сухой пленки приводит к тому, что в месте ее контакта с кожей происходит локальная дегидратация поверхности ткани и образуется плотный контакт между функциональными группами компонентов пленки и клеточной мембраной.
Аппликация пленки производится стороной с нанесенным на нее раствором хитозана, аргинина и таннина на кровоточащую поверхность паренхиматозного органа, сосуда или наружного ранения. Далее осуществляется плотное прижатие пленки к раневой поверхности в течение 1 минуты. После чего пленка остается на поверхности повреждения на необходимый срок. В момент контакта с поверхностью раны происходит быстрая дегидратация ее поверхности и образование электростатических связей между положительно заряженными аминогруппами хитозана и гуаниновыми группами аргинина с отрицательно заряженными молекулами клеточных мембран, а также между тригидроксибензойными остатками таннинов с белками раневой поверхности.
Сущность поясняется примерами
Пример №1
Готовят несущий слой: получают 2 масс.% водный раствор ацетата хитозана (к 95 г деионизированной воды добавляют 2 г хитозана и 2 г ледяной уксусной кислоты). К полученному раствору добавляют 1 г глицерина при постоянном помешивании на магнитной мешалке. Перемешивают в течение 3-6 часов. После чего раствор высушивается на ровной поверхности в течение 48 часов при комнатной температуре в тяге. Состав и содержание компонентов, масс.%:
Ацетат хитозана - 2;
Глицерин - 1;
Вода - остальное.
Готовят слой для контакта с раной: к 94 г деионизированной воды добавляют 2 г хитозана и 2 г ледяной уксусной кислоты. Раствор перемешивают на магнитной мешалке при 20°С в течение 5-10 часов, затем к раствору добавляют 1 г аргинина, перемешивают на магнитной мешалке до полного растворения в течение примерно 2 часов. Полученный раствор нагревают до 60°C, после чего при постоянном помешивании на магнитной мешалке добавляют 1 г таннина, помешивая при температуре 60°C до полного растворения последнего в течение 2 часов. Раствор также высушивается при комнатной температуре на ровной поверхности в течение 48 часов. После высыхания пленка готова к использованию (Фиг.1). Состав и содержание компонентов, масс.%:
Хитозан - 2;
Уксусная кислота - 2;
Аргинин - 1;
Таннин - 1;
Вода - остальное.
Пример №2
Все стадии аналогичны примеру №1 (Фиг.2). Отличие состоит в том, что при изготовлении активного слоя используется 2 г соляной кислоты для образования соли хитозана. Состав и содержание компонентов в слое для контакта с раной, масс.%:
Хитозан - 2;
Соляная кислота - 2;
Аргинин - 1;
Таннин - 1;
Вода - остальное.
Пример №3
Все стадии аналогичны примеру №1 (Фиг.3). Отличие состоит в том, что при изготовлении активного слоя используется 4 г лимонной кислоты для образования соли хитозана. Состав и содержание компонентов в слое для контакта с раной, масс.%:
Хитозан - 2;
Лимонная кислота - 4;
Аргинин - 1;
Таннин - 1;
Вода - остальное.
Пример №4
Все стадии аналогичны примеру №1 (Фиг.4). Отличие состоит в том, что при изготовлении активного слоя используется 4 г молочной кислоты для образования соли хитозана. Состав и содержание компонентов в слое для контакта с раной, масс.%:
Хитозан - 2;
Молочная кислота - 4;
Аргинин - 1;
Таннин - 1;
Вода - остальное.
Пример №5
Все стадии аналогичны примеру №1 (Фиг.5). Отличие состоит в том, что при изготовлении активного слоя используется 2 г сукцината хитозана в готовом виде, растворенного в воде. Состав и содержание компонентов в слое для контакта с раной, масс.%:
Сукцинат хитозана - 2;
Аргинин - 1;
Таннин - 1;
Вода - остальное.
Пример №6
Все стадии аналогичны примеру №1 (Фиг.6). Отличие состоит в том, что при изготовлении активного слоя вместо аргинина используется 1 г протамина сульфата. Состав и содержание компонентов в слое для контакта с раной, масс.%:
Хитозан - 2;
Уксусная кислота - 2;
Протамина сульфат - 1;
Таннин - 1;
Вода - остальное.
Пример №7
Все стадии аналогичны примеру №1 (Фиг.7). Отличие состоит в том, что при изготовлении активного слоя вместо аргинина используется 1 г полиаргинина. Состав и содержание компонентов в слое для контакта с раной, масс.%:
Хитозан - 2;
Уксусная кислота - 2;
Полиаргинин - 1;
Таннин - 1;
Вода - остальное.
Пример №8
Все стадии аналогичны примеру №1 (Фиг.8). Отличие состоит в том, что при изготовлении активного слоя вместо аргинина используется 1 г олигоаргинина. Состав и содержание компонентов в слое для контакта с раной, масс.%:
Хитозан - 2;
Уксусная кислота - 2;
Олигоаргинин - 1;
Таннин - 1;
Вода - остальное.
Пример №9
Все стадии аналогичны примеру №1 (Фиг.9). Отличие состоит в том, что при изготовлении несущего слоя используется 4 г молочной кислоты для образования соли хитозана. Состав и содержание компонентов в несущем слое, масс.%:
Хитозан - 2;
Молочная кислота - 4;
Глицерин - 1;
Вода - остальное.
Пример №10
Все стадии аналогичны примеру №1 (Фиг.10). Отличие состоит в том, что при изготовлении несущего слоя используется 4 г лимонной кислоты для образования соли хитозана. Состав и содержание компонентов в несущем слое, масс.%:
Хитозан - 2;
Лимонная кислота - 4;
Глицерин - 1;
Вода - остальное.
Пример №11
Все стадии аналогичны примеру №1 (Фиг.11). Отличие состоит в том, что при изготовлении несущего слоя используется 2 г соляной кислоты для образования соли хитозана. Состав и содержание компонентов в несущем слое, масс.%:
Хитозан - 2;
Соляная кислота - 2;
Глицерин - 1;
Вода - остальное.
Пример №12
Все стадии аналогичны примеру №1 (Фиг.12). Отличие состоит в том, что при изготовлении несущего слоя используется 2 г сукцината хитозана в готовом виде, растворенного в воде. Состав и содержание компонентов в несущем слое, масс.%:
Сукцинат хитозана - 2;
Глицерин - 1;
Вода - остальное.
Таким образом, совокупность описанных выше компонентов в указанных количествах обеспечивает выраженный гемостатический эффект и повышенную адгезию средства при биологической инертности и способности к биодеградации, что позволяет использовать его без дополнительных фиксирующих материалов, а также обеспечивает универсальность его применения: изобретение может применяться как при наружных ранениях, так и при повреждениях паренхиматозных органов и сосудов, тогда как прототип применим только для наружных ранений.
Разработанная пленка за счет отличных адгезивных свойств позволяет использовать ее без фиксации с помощью повязки, а также при ранениях внутренних паренхиматозных органов и крупных сосудов.
При использовании препарата на наружных ранах его несомненным достоинством является легкость удаления пластины с раневой поверхности: пластина, в отличие от бинта, сохраняет свою эластичность после высыхания крови и удаляется одним движением, не причиняя значительных болезненных ощущений.
Заявленный препарат выгодно отличается от аналогов и прототипа универсальностью его применения:
- может использоваться интраоперационно при ранениях печени, почек и селезенки, крупных сосудов как средство временного или окончательного гемостаза
- применим в качестве раневого гемостатического адгезива при наружных ранах.
Внесение аргинина и таннина в препарат позволяет улучшить его благоприятные свойства, не увеличивая при этом количество побочных эффектов, а наличие несущего слоя увеличивает прочность пленки и ее устойчивость к размоканию во влажной среде.
Пример 13
Экспериментальное исследование разработанного нами гемостатического средства проводили на свиньях породы русская белая, на самцах, вес свиней 80-100 кг.
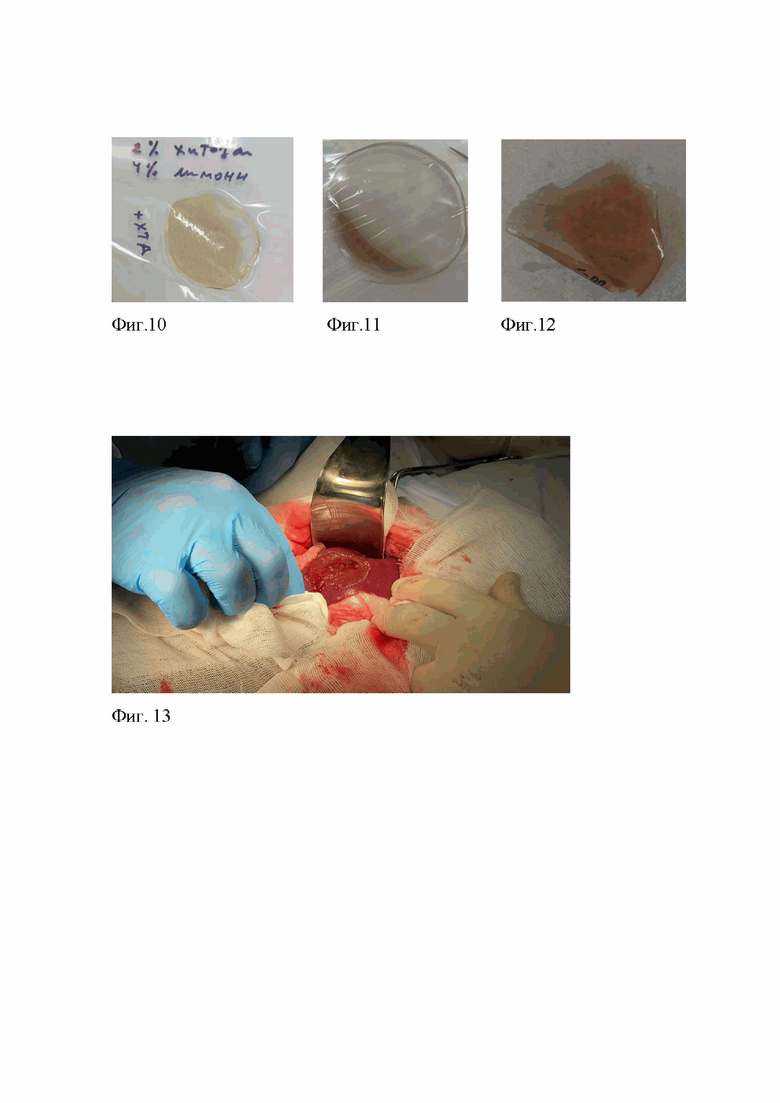
В условиях операционной, под наркозом выполнена лапаротомия. Правая доля печени выведена в рану на салфетках. Скальпелем иссечен участок правой доли размерами 2х2х0.5см. Дефект осушен салфеткой. Накрыт опытным образцом из Примера №1, диаметром 5см, прижат салфеткой. Экспозиция 20 секунд. Через 20 секунд отмечено плотное прилегание к ткани печени с хорошей адгезией по всей поверхности (Фиг.13). Кровотечения не наблюдается. Наблюдение в течение 3 минут 30 секунд для контроля гемостаза. На четвёртой минуте адгезия к ткани по-прежнему хорошая. Печень накрыта влажной салфеткой. Суммарно через 15 минут после аппликации наблюдается частичное размягчение образца, адгезия сохраняется. Кровотечения из дефекта печени не отмечено.
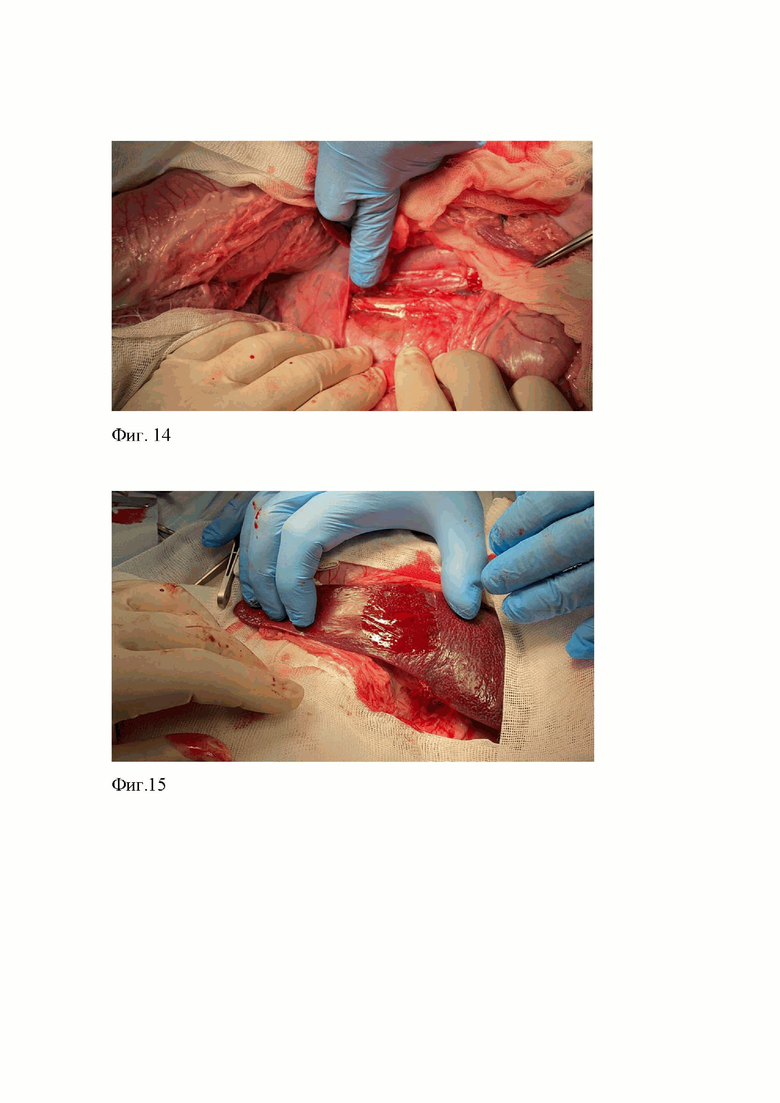
Брюшная аорта выделена на протяжении 6 см. На сосудистых зажимах пережата выше и ниже зоны доступа. Скальпелем произведена продольная аортотомия длина разреза 1 см. Рана осушена салфеткой. Дефект накрыт образцом из Примера №3 и прижат салфеткой (Фиг.14). Зажимы сняты. Через 30 с отмечено плотное приклеивание образца к аорте и парааортальным тканям. Гемостаз. Контроль систолического давления - 110 мм рт.ст.
Селезёнка выведена в рану, отграничена салфетками. Скальпелем в средней трети органа иссечен дефект размерами 2х1,5х0,5см. Наблюдается обильное кровотечение. Дефект осушен салфеткой, после чего сразу же накрыт образцом из Примера №7 диаметром около 5 см и прижат салфеткой (Фиг.15). Через 30 с наблюдается плотная адгезия по всей площади образца. Наблюдение в течение 20 минут. Кровотечение не продолжается. Адгезия сохраняется, подтекания крови не определяются.
Пример 14
Экспериментальное исследование разработанного гемостатического средства проводили на крысах линии Wistar.
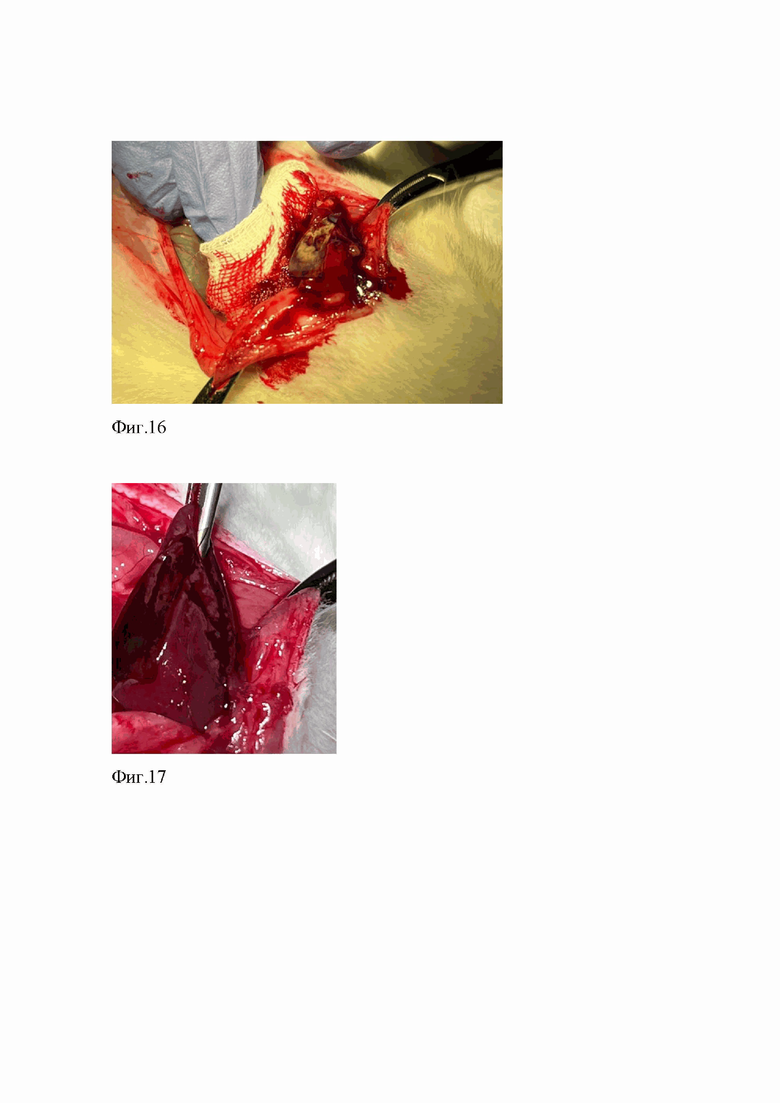
В условиях операционной, под наркозом выполнена лапаротомия крысе №1. Правая доля печени выведена в рану на салфетках. Скальпелем иссечен участок правой доли размерами 1,0х1,0х0,5см. Дефект осушен салфеткой. Накрыт опытным образцом из Примера №3 размерами 2,5х3,0 см, прижат салфеткой. Экспозиция 20 с. Через 20 секунд отмечено плотное прилегание к ткани печени с хорошей адгезией по всей поверхности (Фиг.16). Кровотечения не наблюдается. Наблюдение в течение 20 минут для контроля гемостаза и адгезии. На двадцать первой минуте гемостаз устойчивый, адгезия сохраняется.
В условиях операционной, под наркозом выполнена лапаротомия крысе №2. Правая доля печени выведена в рану на салфетках. Скальпелем высечен участок правой доли размерами 1,5х1,0х0,5см. Дефект осушен салфеткой. Накрыт опытным образцом из Примера №6, размерами 2,5х3,0 см, прижат салфеткой. Экспозиция 20 с. Через 20 с отмечено плотное прилегание к ткани печени с хорошей адгезией по всей поверхности (Фиг.17). Кровотечения не наблюдается. Наблюдение в течение 30 минут для контроля гемостаза и адгезии. На тридцать первой минуте гемостаз устойчивый, адгезия сохраняется.
Пример 15
Экспериментальное исследование разработанного нами гемостатического средства проводили на свинье породы белорусская черно-пестрая, самец, вес свиньи 90 кг.
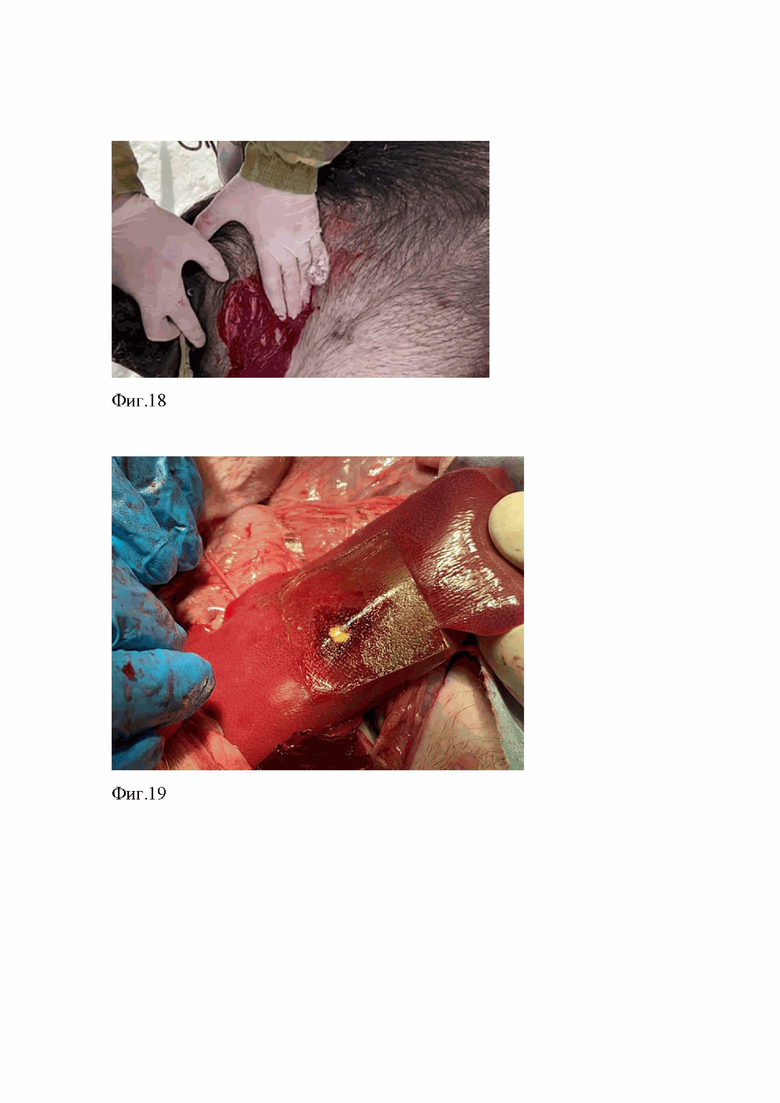
Под наркозом свинье нанесено сквозное ранение в область бедра по траектории снаружи внутрь. Из области раны наблюдалось обильное кровотечение. Рана осушена марлевой салфеткой, накрыта опытным образцом из Примера №10, диаметром 10 см, прижата салфеткой. Экспозиция 30 с. Через 30 с хорошая адгезия пленки к ране и поверхности кожи (Фиг.18). Кровотечения не наблюдается. Наблюдение в течение 10 минут для контроля гемостаза. На одиннадцатой минуте адгезия сохраняется без дополнительной фиксации пленки.
Пример 16
Экспериментальное исследование разработанного нами гемостатического средства проводили на свинье породы русская белая, самец, вес 70 кг.
В условиях операционной, под наркозом выполнена лапаротомия. Правая доля печени выведена в рану на салфетках. Скальпелем высечен участок правой доли размерами 2,5х2,5х0.5см. Дефект осушен салфеткой. Накрыт опытным образцом из Примера №4, размерами 7х7 см, прижат салфеткой. Экспозиция 10 с. Через 10 с отмечено плотное прилегание к ткани печени с хорошей адгезией по всей поверхности (Фиг.19). Кровотечения не наблюдается. Наблюдение в течение 15 минут для контроля гемостаза. На шестнадцатой минуте адгезия сохраняется, гемостаз устойчивый.
| название | год | авторы | номер документа |
|---|---|---|---|
| Гемостатическое средство | 2023 |
|
RU2826361C1 |
| Многослойное комбинированное гемостатическое средство местного действия | 2023 |
|
RU2826069C1 |
| Композиция для временной остановки кровотечений | 2023 |
|
RU2819603C1 |
| ГЕМОСТАТИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ ХИТОЗАНОВОГО АЭРОГЕЛЯ | 2020 |
|
RU2743425C1 |
| Способ остановки кровотечения с помощью модифицированного гиалуроната натрия с тромбином и мирамистином | 2024 |
|
RU2839473C1 |
| Гемостатическое средство на основе хитозана | 2023 |
|
RU2807862C1 |
| ГЕМОСТАТИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ ПОЛИВИНИЛПИРРОЛИДОНА И СПОСОБЫ ПОЛУЧЕНИЯ ЕГО ФАРМАКОЛОГИЧЕСКИХ ФОРМ | 2018 |
|
RU2705812C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСТАТИЧЕСКОГО СРЕДСТВА НА ОСНОВЕ ХИТОЗАНА | 2023 |
|
RU2806364C1 |
| Гемостатичекий гель однократного местного применения | 2023 |
|
RU2796161C1 |
| Способ изготовления гемостатического геля однократного местного применения | 2022 |
|
RU2789581C1 |

Изобретение относится к области медицины, а именно к местному гемостатическому средству. Местное гемостатическое средство, выполненное в виде пленки, содержащее несущий слой и слой для контакта с раной из соли хитозана, отличающийся тем, что несущий слой содержит соль хитозана, глицерин и воду, а слой для контакта с раной дополнительно содержит таннин, воду и аргинин или олигоаргинин, или полиаргинин, или протамина сульфат при следующем соотношении компонентов, масс. %: соль хитозана – 2-4, глицерин – 1, таннин – 1, аргинин, или олигоаргинин, или полиаргинин, или протамина сульфат – 1, вода – остальное. Вышеуказанное изобретение представляет собой эффективное местное гемостатическое средство с повышенной адгезией, в том числе к влажной раневой поверхности, не требующее дополнительных материалов для его фиксации. 1 з.п. ф-лы, 19 ил., 16 пр.
1. Местное гемостатическое средство, выполненное в виде пленки, содержащее несущий слой и слой для контакта с раной из соли хитозана, отличающийся тем, что несущий слой содержит соль хитозана, глицерин и воду, а слой для контакта с раной дополнительно содержит таннин, воду и аргинин, или олигоаргинин, или полиаргинин, или протамина сульфат при следующем соотношении компонентов, масс. %:
2. Местное гемостатическое средство, выполненное в виде пленки по п. 1, согласно изобретению, для получения пленки несущий слой из соли хитозана, глицерина и воды высушивают на ровной поверхности в течение 48 часов при комнатной температуре в вытяжном шкафу, после чего на высушенный несущий слой наносят слой для контакта с раной, содержащий соль хитозана, аргинин, воду и таннин или олигоаргинин, или полиаргинин, или протамина сульфата, затем его также высушивают при комнатной температуре на ровной поверхности в течение 48 часов в вытяжном шкафу.
| US 2011052665 A1, 03.03.2011 | |||
| Гемостатическое покрытие в форме губки или плёнки (варианты) | 2016 |
|
RU2639379C1 |
| БИОДЕГРАДИРУЕМОЕ РАНЕВОЕ ПОКРЫТИЕ И СПОСОБ ПОЛУЧЕНИЯ БИОДЕГРАДИРУЕМОГО РАНЕВОГО ПОКРЫТИЯ | 2013 |
|
RU2519158C1 |
| US 10179145 B2, 15.01.2019. | |||
Авторы
Даты
2023-11-21—Публикация
2023-03-28—Подача