Изобретение относится к области медицины, а именно к композициям с включением термочувствительных полимеров и предназначено для остановки кровотечений различной интенсивности, при оказании для как доврачебной, так и первой помощи, скорой медицинской и первичной медико-санитарной помощи, в полевых и в домашних условиях, в районах боевых действий, а также в условиях стационара для остановки кровотечения, в том числе из паренхиматозных органов, а также временной эмболизации кровеносных сосудов во время хирургических вмешательств.
В настоящее время актуальной задачей во всем мире является поиск способов остановки кровотечений при повреждениях кровеносных сосудов при травмах, ранениях, их перфорации во время оперативных вмешательств, повреждениях паренхиматозных органов, селезенки и т.д. Такая заинтересованность обусловлена также нарастанием количества вооруженных конфликтов в современном мире, и, как следствие, увеличением потребности в качественной медицинской обработки ран. От эффективности применяемых средств в боевых условиях зависит эффективность дальнейшего лечения, вследствие предупреждения возможных осложнений в результате оказания ненадлежащей первой помощи, а также снижается количество летальных исходов в процессе транспортировки раненых. Стоит отметить, что 10-15% всех смертей на поле боя происходит из-за невозможности адекватной остановки кровотечений [Современные методы остановки кровотечений при боевых ранениях. Международный студенческий научный вестник. - 2023].
Гемостатические средства (ГС) - это биохирургические материалы, обладающие кровоостанавливающим эффектом при непосредственном контакте с поврежденными тканями организма. Данная группа включает в себя широкий спектр препаратов с различным механизмом действия. Они бывают в виде гелей, порошков, губок и т.д.
Идеальные кровоостанавливающие средства как на поле боя и догоспитальном этапе, так и в медицинских учреждениях должны обладать следующими характеристиками [Нойффер М.К., Макдивитт Дж., Роуз Д., Кинг К., Клунан К.К., Вайер Дж. С. Кровоостанавливающие повязки для тех, кто оказывает первую помощь: обзор. Mil Med. 2004; 169(9):716-20. Пэн Т. Биоматериалы для контроля кровотечений. Тенденции биоматериализации искусственных органов. 2010; 24(1):27-68]:
1) быстрый и эффективный контроль кровотечения в широком диапазоне состояний и из различных ран в течение 2 минут, даже при нанесении на активно кровоточащий участок через лужу крови;
2) при использовании на поле боя продолжительность устойчивого гемостаза составляет несколько часов, что отражает задержку эвакуации;
3) простое удаление без остатков или отсутствие необходимости в удалении в результате биодеградации, готовность к применению без особых усилий и подготовки;
4) простое применение даже неспециалистом в суровых условиях;
5) простота изготовления и стерилизации и низкая стоимость;
6) простое хранение и длительное хранение; длительная стабильность (больше двухлетнего срока годности) даже при экстремальных условиях (-10 - +55°С);
7) хорошая биосовместимость без побочных эффектов на заживление и тромбоэмболических осложнений.
Однако ни одно из существующих гемостатических средств не отвечает всем требованиям. В связи с этим продолжаются усилия по разработке новых гемостатических средств доставки для остановки тяжелых кровотечений в военных условиях [Пэн Х.Т. Кровоостанавливающие средства для контроля кровотечений на догоспитальном этапе: описательный обзор. Военное медицинское издание 7, 13 (2020)].
В работе «Особенности применения гемостатических материалов местного действия в хирургии» (2016 г) авторы провели исследование механизмов обеспечения гемостаза, сравнительной эффективности и побочных известных эффектов современных кровоостанавливающих средств на основе желатина, целлюлозы, коллагена, крахмала. Было отмечено, что применение этих гемостатиков позволяет эффективно контролировать кровотечения при небольших повреждениях, например, во время микрохирургических вмешательств. Однако они обладают рядом существенных недостатков, таких как воспалительная реакция в зоне контакта гемостатика с раной, и, следовательно, задержка регенерации поврежденных тканей [Zacharias Т., Ferreira N. Carrier-bound fibrin sealant compared to oxidized cellulose application after liver resection.// HPB (Oxford). 2012; 14(12): P. 839-47], клинические проявления нейротоксической реакции: анорексия, тревожность, тошнота, ажитация, спутанность сознания, депрессия [The SURGIFLO® Hemostatic Matrix. Technical Report. SFL-0389-09-12/10. Ethicon, Inc. 2009], анафилактические реакции на белковые гемостатические материалы и т.д.
Основными типами местных гемостатических средств, используемых на сегодняшний день в полевых условиях, являются Боевая марля (Z-Medica Corporation, Уоллингфорд, Коннектикут, США), марля Celox (Medtrade Products Ltd., Крю, Великобритания;) и хитогауз (HemCon Medical Technologies, Портленд, Орегон, США;) [Gtiven НЕ. Актуальные гемостатические средства для контроля кровотечений на догоспитальном этапе - тогда и сейчас.Ulus Travma Acil Cerrahi Derg. 2017; 23(5):357-61]. Стоит отметить, что такие ГС применимы исключительно при наружных кровотечениях.
Существуют ГС на основе каолина. Препарат - QuickClot с основой на минеральных породах, при наложении на рану выделяет большое количества тепла. В итоге кровотечение останавливается не за счет свертывания, а за счет «прижигания», что приносит пострадавшему сильную боль и ожог.
Широко применяются гемостатические средства на основе хитозана. Хитозан является известным кровоостанавливающим материалом и представляет собой производное твердых отходов переработки раковинных моллюсков и ракообразных, а также может быть экстрагирован из культуры грибов. Он представляет собой катионный полимерный материал, который нерастворим в воде [патент РФ 2682712]. Гемостатические свойства хитозана широко известны: хитозан имеет свойство за счет наличия реакционноспособной аминогруппы деполяризовать гемовые группы гемоглобина, вызывая, таким образом, агглютинацию эритроцитов крови (Rao S.B., Sharma C.R "Use of chitosan as a biomaterial: studies on its safety and hemostatic potential" // J. Biomed. Mater. Res., 1997, vol. 34(1), pp. 21-28; Klokkevold P.R., Fukayama H., Sung E.C., Bertolami C.N. "The effect of chitosan (poly-N-acetyl glucosamine) on lingual hemostasis in heparinized rabbits" // J. Oral. Maxillofac. Surg., 1999, vol. 57(1), pp. 49-52; Pogorielov M., Kalinkevich O., Deineka V. et al. "Haemostatic chitosan coated gauze: in vitro interaction with human blood and in-vivo effectiveness" // Biomater. Res., 2015, 19:22). Сгустки из агглютинированных эритроцитов и других форменных элементов крови вызывают быстрое преобразование крови в гель, который существенно замедляет или полностью останавливает кровотечение, давая возможность естественным механизмам остановки кровотечения вступить в действие.
На основе гидролизата хитозана созданы гемостатические гранулы Celox. Кровоостанавливающий эффект достигается путем связывания положительно заряженных частиц Celox с отрицательно заряженными эритроцитами, путем смешивания и «склеивания» их между собой, образуя таким образом «псевдосгусток». Этот сгусток хорошо прилипает к влажным местам, позволяя буквально затыкать раневую поверхность. Подобный подход потенциально опасен из-за возможности тромбообразования за счет попадания препарата в кровеносную систему, кроме того возникает проблема извлечения псевдосгустка из раны после эвакуации пострадавшего. Так же отмечается недостаточный гемостатический эффект и слабая адгезионная способность при использовании средств на основе порошка или гранул хитозана. Недостатками препаратов этой группы являются кратковременность действия, невысокая специфическая активность и существующая потенциальная возможностью инфицирования раны в «полевых условиях» [патент РФ RU 2796161 C1].
Из патента РФ 2682717 С2 известна разлагаемая кровоостанавливающая композиция, содержащая хитозан, соль хитозана или производное хитозана и физиологически приемлемой кислоты.
Кровоостанавливающая композиция (КК) содержит хитозан, соль хитозана или производное хитозана и физиологически приемлемую кислоту в количестве от 20% до 70% от массы кровоостанавливающей композиции. КК способна полностью разлагаться в организме человека или животного в течение от примерно 1 суток до не более чем примерно 30 суток. Композицию изготавливают в виде гранул, порошка, листа, пены, геля, гидрогеля (в виде листов или аморфного) или ламината или комбинации любых двух или более вышеперечисленных форм. Физиологическая кислота в прототипе подразумевает применение муравьиной кислоты, уксусной кислоты, аскорбиновой кислоты, галогеноуксусных кислот, пропионовой кислоты, пропеновой кислоты, молочной кислоты, янтарной кислоты, акриловой кислоты, глиоксиловой кислоты, пировиноградной кислоты или оксипропионовой/масляной кислоты, серной кислоты, соляной кислоты и/или комбинаций любых двух или более из них.
Известны кровеостанавливающие гранулы «Кровестоп» на основе волокон хитозана. Они используются для оказания первой само и взаимопомощи при жизнеугрожающих массивных кровотечениях. ГС «Гемоспас М» представляет собой материал на основе крупнозернистого порошка гидросиликата кальция, «Гемоспас БИО» представляет собой материал на основе порошка лактата хитозана и йодоповидона, в основе ГС «ГЕПОГЛОС» лежит активное вещество - производное хитозана (соли ацилированного хитозана). В рамках гособоронзаказа было разработано линейка ГС «Гемохит» на основе модицфицированного хитозана в виде порошка и перевязочного средства.
Стоит отметить, что вышеперечисленные ГС доказали свою эффективность. Однако, с гемостатическими средствами в порошковой и гранулированной форме трудно работать в экстремальных условиях: загрязняется, сдувается ветром, просыпается мимо раны. Также все вышеперечисленные ГС должны быть удалены из раны для дальнейшей хирургической обработки [патент RU 2796161 C1].
Из патента RU 2607321 С2 известна саморасширяющаяся полиуретановая пена для остановки полостных кровотечений, полученной путем смешивания полиольного и изоцианатного компонентов непосредственно в устройстве для доставки пены в полость. При этом смешивание полиольного и изоцианатного компонентов осуществляют в соотношении от более 3,5:1 до 4,0:1 с добавлением гемостатических средств, полиольный компонент используют при следующем соотношении компонентов, в мас.ч.: пенорегулятор, содержащий высокомолекулярный полиол 100, вода 2,0-4,0, вспениватель 2,0-4,0, активатор уретанообразования 0,05-0,4, удлинитель цепи 0,2-1,5, пенооткрыватель 0,2-1,5, пеноотвердитель 0,2-1,5. В качестве изоцианатного компонента используют композицию на основе фенилметандиизоцианата с содержанием изоцианатных групп 26,0-32 мас. %, при этом пену вводят в полость в количестве, достаточном для создания в ней гемостатической компрессии. В качестве гемостатических средств в смесь полиольного и изоцианатного компонентов, предпочтительно, добавляют один или несколько компонентов, выбранных из группы, включающей танин, квасцы хлорного железа, хлорид цинка, сульфат меди, окисленную целлюлозу, полиангидроглюкоровую кислоту, полигексаметиленгуанидин гидрохлорид, железа полиакрилат. Полиуретан не является биодеградируемым материалом и требует последующего удаления. Фенилметандиизоцианат - относится к группе достаточно токсичных низкомолекулярных высокореактивных соединений, которые являются сильнодействующими респираторными и кожными сенсибилизаторами и являются частой причиной аллергического контактного дерматита и отравлений.
Таким образом, существует потребность в биосовместимой гемостатической композиции, которая может безопасно использоваться внутри организма человека, и которая может впоследствии оставаться в организме и безопасно рассасывается в течение определенного периода времени. Кроме того, гемостатические повязки (марли, бинты) на догоспитальном этапе предназначены в основном для наружного кровотечения и могут быть неэффективны при внутреннем или внутриполостном кровотечении.
Существует группа ГС на основе полимеров. Как правило, их гемостатические свойства обусловлены эффектом тампонады раневого канала.
Известно медицинское покрытие для закрытия ран различной этиологии «ОТРАН». Покрытие представляет собой двухкомпонентную пенополиуретановую композицию в упаковке из алюминизированного полиэтилена. Покрытие получается при смешении двух компонентов: - полиольного (с добавлением нанокристаллического бемита); - изоцианатного, Вспененная масса при нанесении на рану образует мелкопористое эластичное покрытие толщиной 0,8-1 см. Трудности применения его на поле боя также являются существенным недостатком, а также необходимость последующего удаления из раны.
Известны ГС на основе блок-сополимеров этиленоксида и пропиленоксида. Они представляют собой хорошо известные неионогенные поверхностно-активные вещества (полоксамеры, плюроники, полоксалены). Их амфифильный гидрофильно/гидрофобный характер объясняет широкий диапазон поверхностно-активных функций и фазовых переходов, а исключительная универсальность обусловила широкий спрос на различных рынках и в различных областях техники. Они разрешены к использованию в фармацевтике в качестве основы для гидрогелей (European Pharmacopoeia 5th edition, Order Code P2164030). Примечательно, что блок-сополимеры обладают уникальными поверхностно-активными свойствами и чрезвычайно низкой токсичностью и не иммуногенны. Применение указанного полимеров в медицине в качестве эмболизата известно, например, полимерный гель LeGoo на основе Pluronic-127 (Pluromed, Вобурн, США) [Winkler В, Miiller-Schweinitzer Е, Elezi F, Grussenmeyer T, Rueter F, Matt P, Konerding MA, Grapow MT, Eckstein FS. Effects of the novel polymer gel LeGoo on human internal thoracic arteries. Arm Thorac Surg. 2011]. Однако, все известные на сегодняшний день подобные гемостатические системы на основе как блок-сополимеров этиленоксида и пропиленоксида, так и других термочувствительных полимеров из-за низкой адгезии к стенке сосуда могут быть использованы только для окклюзии исключительно мелких сосудов и не пригодны для магистральных сосудов большего диаметра. Время устойчивого пребывания эмболизирующего геля LeGoo в сосуде составляет лишь 10-15 мин, после чего он растворяется.
Известен термочувствительный полимерный гель LeGoo (Pluromed, Вобурн, США) - на основе Poloxamer 407, который показал свою относительную эффективность при окклюзии мелких сосудов [Winkler В, Muller-Schweinitzer Е, Elezi F, Grussenmeyer Т, Rueter F, Matt P, Konerding MA, Grapow MT, Eckstein FS. Effects of the novel polymer gel LeGoo on human internal thoracic arteries. Ann Thorac Surg. 2011]. Гель представляет собой вязкую при комнатной температуре жидкость, которая немедленно затвердевает, когда ее нагревают до температуры тела. Следовательно, когда ее вводят в кровеносный сосуд при температуре тела, вязкая жидкость мгновенно превращается в закупоривающую пробку, которая сочетается с контурами тела, даже если просвет искажен артериальным заболеванием. Пробка сохраняет цилиндрическую форму целевого сосуда, что упрощает точное наложение швов, и ее можно легко проколоть хирургической иглой.
Пробка LeGoo самопроизвольно растворяется на месте через 10-20 минут, она может быть растворена по желанию путем введения в сосуд холодного физиологического раствора или с помощью инструмента для механического разрушения пробки. После растворения, LeGoo более не может образовывать новую пробку из-за слишком низкой концентрации полоксамера, который выводится из организма. В экспериментах показано, что раствор полоксамера не может образовывать гель при концентрации полимера ниже 12%. Также показано, что в дозах, достаточных для окклюзии мелких сосудов гель полоксамера не является нетоксичным. Таким образом, предлагаемая производителем концентрация геля Legoo - за счет слабой адгезии к стенке сосуда не способна обеспечить пристеночную герметизацию, что делает его неприменимым при повреждениях крупных сосудов, а также при массивных повреждениях. Также ограниченное время гемостаза (самопроизвольное растворение пробки через 10-20 минут) не позволяет добиться стойкой остановки кровотечения. Стоит также отметить, что гель LeGoo в виду крайне ограниченной области применения не нашел широкого использования на практике, а в РФ он даже не зарегистрирован.
В патенте СА2519946С «Temporary embolization using inverse thermosensitive polymers» раскрыта композиция на основе термочувствительных полимеров.
Предлагаемая авторами композиция выполнена на основе термочувствительного полимера. Термочувствительный полимер необходим для временной эмболизации участка сосуда у млекопитающего, где указанный обратный термочувствительный полимер обратимо превращается в гель при температуре перехода в сосудистой сети указанного млекопитающего, тем самым временно эмболизируя участок сосуда. При этом термочувствительный полимер представляет собой плюроник, колифор, лутрол, полоксамер или полоксамин, а именно плюроник 127, полоксамер 407, колифор Р 407, лутрол 127, полоксамер 338, полоксамер 188, полоксамин 1107 или полоксамин 1307. Термочувствительный полимер содержит агенты, усиливающие контраст из группы, состоящей из рентгеноконтрастных материалов, парамагнитных материалов, наночастиц тяжелых и переходных металлов, лантаноидов, актиноидов, красителей и материалов, содержащих радионуклиды, биологически активный агент, биологические активные агенты из группы противовоспалительных, противомикробных, анальгетических, антипролиферативных и химиотерапевтических средств. Предлагаемая композиция может вводиться в кровеносный сосуд при помощи катетера с охлаждением. Указанная временная эмболизация указанного участка сосуда заканчивается растворением обратного термочувствительного полимера или принудительным снижением температуры обратного термочувствительного полимера ниже температуры перехода в жидкое состояние.
Предложенная композиция доказала свою эффективность только при эмболизации мелких сосудов. Однако стоит отметить, что ее консистенция не позволяет полноценно заполнить все полости по ходу раневого канала при массивных повреждениях, что приводит к снижению сопротивления движению массы композиции к выходному отверстию раны, т.к. нет участков дополнительного крепления между раневой поверхностью и гелем.
Наиболее близким к предлагаемому является композиция на основе блок-сополимер этиленоксида и пропиленоксида, опубликованная в патенте № JP 6095675 В2 «Non-aqueous compositions for bone hemostasis and methods for using and manufacturing them», которая выбрана нами в качестве прототипа.
Предлагаемая композиция применяется в качестве костного кровоостанавливающего средства и содержит блок-сополимер полиоксиэтилена-полиоксипропилена присутствует в диапазоне от 40% до 80% по массе композиции, сополимер алкиленоксида в диапазоне от 20% до 50% по массе композиции. Согласно некоторым вариантам реализации, в композиции могут применяться дополнительно природные полимеры (сшитый или несшитый хитин, хитозан, желатин, коллаген), керамические частицы (карбонат кальция, гидроксиапатит, карбонатный гидроксиапатит, трикальцийфосфат, карбонатированный гидроксиапатит, трикальцийфосфат и гидроксиапатит в различных пропорциях, Si-замещенную керамику, Mg-замещенную керамику, Sr-замещенную керамику и т.п.), полимер оксазолина в качестве добавки для усиления адгезионных свойств композиции и т.д.
Несомненно, композиция, раскрытая в вышеуказанном изобретении, доказала свою эффективность, однако она имеет ряд существенных недостатков.
Во-первых, авторы указывают, что предлагаемую ими композицию применяют исключительно при костных кровотечениях. В патенте отсутствуют данные о возможности ее применения при повреждениях крупных сосудов (массивные кровотечения). Во-вторых, композиция выполняется в виде пасты или теста, что не позволяет заполнить всю раневую поверхность при глубоком ранении. Керамические частицы обычно применяются для заполнения костных дефектов в травматологии и ортопедии и не являются биодеградируемым материалом, поэтому при введении такой композиции в рану, требуется обязательное ее последующее удаление.
Таким образом, хотя к настоящему времени было испытано большое количество материалов для остановки кровотечений и, тем не менее, не найдено универсального средства, которое бы отвечало всем необходимым требованиям. Композиции на основе термочувствительных полимеров, доказали свою эффективность при кратковременной эмболизации мелких сосудов. Однако, применение их при обильных кровотечениях нами в литературе найдено не было. В связи с этим существует потребность для разработки разнообразных и более эффективных гемостатических технологий и биоматериалов для экстренных ситуаций не только в гражданских и военных травматических условиях, но и во время различных терапевтических и хирургических вмешательств.
Технический результат настоящего изобретения заключается в создании композиции для временной остановки кровотечений.
Указанный технический результат достигается за счет создания композиции на основе блок-сополимер этиленоксида и пропиленоксида, содержащей поли(этиленоксид) и воду, согласно изобретению, композиция дополнительно содержит полигексаметилен бигуанида гидрохлорид и хлористый натрий при следующем соотношении компонентов, мас. %:
Согласно предлагаемому решению, композиция выполнена на основе термочувствительных полимеров, где термочувствительный полимер представляет собой блок-сополимер этиленоксида и пропиленоксида, который, благодаря своим уникальным свойствам, при нагревании застывает и переходит в гелеобразное состояние, а при охлаждении он мгновенно превращаются в жидкий раствор. Он не токсичен и разрешен для применения в медицине и фармацевтике. Благодаря своим свойствам, композиции на основе термочувствительных полимеров легко удаляются из раневого отверстия и кровеносных сосудов, а также являются биоразлагаемыми. В качестве загустителя и адгезивного компонента в состав композиции входят неионогенные, высокомолекулярные, водорастворимые полимеры поли(этиленоксида), что позволяет гелю находиться в крупном сосуде или в раневом отверстии в течение нескольких часов. При этом, адгезивный полимер может представляет собой высокомолекулярные полиэтиленгликоль и поли(этиленоксид), а именно PEG 90М, Polyox WSR 301, Polyox WSR 303, Polyox WSR 308, Polyox WSR Coagulant. Полигексаметилен бигуанида гидрохлорид в предложенном соотношении проявляет бактерицидное и фунгицидное свойство.
В одном из частных вариантов осуществления изобретения, композиция может содержать двуокись углерода в количестве 5-10 мас. % в качестве пенообразователя. Двуокись углерода (CO2), как известно, применяют во время лапароскопических операций для наполнения брюшной полости пациента, чтобы хирурги получили больший простор для проведения манипуляций. Он применяется для повышения артериального давления благодаря свойству провоцировать учащение и углубление дыхания. Углекислый газ безопасен для внутрисосудистых инфузий. Он не вызывает эмболию дистального периферического русла, поскольку растворимость данного газа в жидкостях в 20 раз больше, чем у кислорода [Использование углекислого газа в качестве контрастного вещества при аортоартериографии / В.Н. Шиповский, В.Н. Золкин, Р.В. Курбанов [и др.] //. - 2011. - №6. - С. 16-20]. Мы попробовали растворить блок-сополимер этиленоксида и пропиленоксида в диоксиде углерода (5-10 мас. %) в качестве пропеллента. За счет того, что CO2 обладает низкой температурой кипения и достаточно высоким давлением насыщенных паров при условиях, в которых блок-сополимер используется, а давление в баллоне значительно выше атмосферного, композиция вскипает при выходе из баллона с образованием пузырьков. Таким образом, раствор, находящийся в баллоне, превращается в пену за счет вскипания пропеллента, растворенного в полимере. Диоксид углерода позволил также получить больший объем композиции для заполнения кровеносных сосудов. Так как блок-сополимер является биосовместимым полимером, то при переходе гелеобразной композиции в жидкое состояние внутри сосуда, у нас нет опасений, что это может быть токсично для пациента, а диоксид углерода, как указано выше, не вызывает эмболию дистального периферического русла. В данном варианте изобретения предложенная композиция может применяться при помощи баллона под давлением от 1,5 до 10 атм., что обеспечивает растворение углекислого газа в растворе блок-сополимер этиленоксида и пропиленоксида с последующим образованием стойкой пены для остановки массивных кровотечений.
В другом частном варианте композиция может содержать рентгеноконтрастное вещество йогексол или йодиксанол в количестве 20-30 мас. %. В таком варианте изобретения, предложенная композиция может применяться для остановки кровотечений из крупных и мелких кровеносных сосудов, а также при проведении хирургических манипуляций для временной эмболизации сосудов. При этом рентгеноконтрастные вещества (йогексол или йодиксанол) обеспечивают точную визуализацию окклюзированного сосуда.
Также композиция во всех вариантах осуществления может содержать поливинилпирролидон в количестве 5-20 мас. %, обычно называемый поливидоном или повидоном и представляющим собой водорастворимое полимерное соединение, полученное из мономера N-винилпирролидона. Он обеспечивает дополнительную вязкость и адгезию композиции.
В некоторых вариантах осуществления изобретения в композицию может быть добавлены водорастворимые соли хитозана, например, сукцинат хитозана. Его использование обеспечивает поливалентное действие предлагаемой композиции, т. е. совокупное проявление антимикробной, противовоспалительной, ранозаживляющей и т. п. биологической активности (патент РФ 2657826). Водорастворимая форма хитозана обеспечивает связывание микроорганизмов путем агглютинации, что создает высокий бактериостатический эффект. Взаимодействие кислотных остатков клеточных элементов крови с аминогруппами хитозана объясняет выраженные коагуляционные и гемостатические свойства полимера. Хитозан активизирует синтезирующую функцию фибробластов, что приводит к росту коллагеновых волокон и обеспечивает ускорение процессов регенерации эпителия (Хитин и хитозан. Получение, свойства и применение. / Под ред. Скрябина К.Г., Вихоревой Г.А., Варламова В.П. М.: Наука. 2002. С. 327-338).
В настоящее время композиций, содержащих предложенную совокупность компонентов заявляемых пределах их содержания, в научной и патентной литературе нами найдено не было.
Стоит отметить, что все компоненты предлагаемого изобретения во всех вариантах его осуществления являются нетоксичными для организма человека и животных, а также биоразлагаемыми. Композиция легко и удобно применима как для доврачебной, так и первой помощи, и самопомощи, скорой медицинской и первичной медико-санитарной помощи, в полевых и в домашних условиях, в районах боевых действий, а также в условиях стационара для остановки кровотечений, в том числе из паренхиматозных органов.
Способ получения композиции для временной остановки кровотечений осуществляют следующим образом.
Готовят водный раствор блок-сополимера этиленоксида и пропиленоксида в концентрации 15-30 мас. %. В полученный раствор вводят поли(этиленоксид) в концентрации 0,1-2,0 мас. % и полигексаметилен бигуанида гидрохлорид в концентрации 0,002 мас. %.
Смешение компонентов композиции проводят в при помощи верхнеприводной мешалки при температуре +4°С при непрерывном перемешивании до полного растворения ингредиентов и образования прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
При необходимости в полученную композицию дополнительно вводят поливинилпирролидон в количестве 5-20 мас. %, рентгеноконтрастные вещества в количестве 20-30 мас %, или водорастворимые соли хитозана в количестве 0,1-4,0 мас. %.
Также в композицию дополнительно можно ввести двуокись углерода в концентрации 5-10 мас. %. В таком варианте осуществления изобретения композицию применяют при помощи баллона под давлением от 1,5 до 10 атм. Для определения необходимого давления в баллоне, мы провели серию экспериментов. При давлении ниже 1,5 атм. получали более крупные пузырьки композиции, что препятствовало быстрому переходу ее из жидкого состояния в гель и не заполняло просвет раневого отверстия. При давлении в диапазоне 1,5-10 атм. нам удалось получить мелкодисперсную пену, что способствовало поддержанию объема композиции после перехода их жидкого состояния в гель и полного заполнения раневого канала. Благодаря тому, что выходящая из баллона пена в первые мгновения обладает высокой текучестью, она быстро заполняет раневой канал и не вызывает дополнительную деструкцию тканей, поскольку давление в пузырьках сразу же падает до атмосферного.
Сущность способа поясняется примерами.
Пример 1
Для приготовления 1 кг 15 мас. % композиции к 840 г воды добавляют навески 150 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 1 г поли(этиленоксида) и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 2
Для приготовления 1 кг 30 мас. % композиции к 671 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 20 г поли(этиленоксида) и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 3
Для приготовления 1 кг 30 мас. % композиции, содержащей 0,1 мас. % сукцината хитозана, к 690 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 1 г сукцината хитозана и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 4
Для приготовления 1 кг 15 мас. % композиции, содержащей 4 мас. % сукцината хитозана, к 800 г воды добавляют навески 150 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 40 г сукцината хитозана и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 5
Для приготовления 1 кг 30 мас. % композиции, содержащей 5 мас. % поливинилпирролидона, к 641 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 50 г поливинилпирролидона и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 6
Для приготовления 1 кг 30 мас. % композиции, содержащей 20 мас. % поливинилпирролидона, к 591 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 200 г поливинилпирролидона и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре+4°-+6°С.
Пример 7
Для приготовления 1 кг 20 мас. % рентгеноконтрастной композиции, содержащей к 671 г воды добавляют навески 200 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 20 г поли(этиленоксида) и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования прозрачного раствора. Затем к композиции добавляют 200 г йогексола и продолжают перемешивание при помощи верхнеприводной мешалки при температуре не выше +8°С до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 8
Для приготовления 1 кг 30 мас. % рентгеноконтрастной композиции к 671 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 20 г поли(этиленоксида) и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования прозрачного раствора. Затем к композиции добавляют 300 г йодиксанола и продолжают перемешивание при помощи верхнеприводной мешалки при температуре не выше +8°С до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 9
Для приготовления 1 кг 30 мас. % композиции в виде пены к 671 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 20 г поли(этиленоксида) и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную композицию выдерживают в статических условиях в течение одних суток, после чего переливают в металлический баллон типа сифона и впрыскивают 50 г двуокиси углерода под давлением. Готовую композицию в виде пены с двуокисью углерода в баллоне хранят в холодильной камере при температуре +4°-+6°С.
Пример 10
Для приготовления 1 кг 30 мас. % рентгеноконтрастной композиции, содержащей 5 мас. % поливинилпирролидона, к 641 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 50 г поливинилпирролидона и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования прозрачного раствора. Затем к композиции добавляют 300 г йогексола и продолжают перемешивание при помощи верхнеприводной мешалки при температуре не выше +8°С до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 11
Для приготовления 1 кг 30 мас. % рентгеноконтрастной композиции, содержащей 20 мас. % поливинилпирролидона, к 591 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 200 г поливинилпирролидона и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования прозрачного раствора. Затем к композиции добавляют 300 г йодиксанола и продолжают перемешивание при помощи верхнеприводной мешалки при температуре не выше +8°С до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную вязкую композицию выдерживают в статических условиях в течение одних суток. Все операции проводят с соблюдением санитарно-эпидемиологических требований. Готовую композицию хранят в холодильной камере при температуре +4°-+6°С.
Пример 12
Для приготовления 1 кг 30 мас. % композиции в виде пены, содержащей 0,1 мас. % сукцината хитозана, к 690 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 1 г сукцината хитозана и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную композицию выдерживают в статических условиях в течение одних суток, после чего переливают в металлический баллон типа сифона и впрыскивают 50 г двуокиси углерода под давлением. Готовую композицию в виде пены с двуокисью углерода в баллоне хранят в холодильной камере при температуре +4°-+6°С.
Пример 13
Для приготовления 1 кг 30 мас. % композиции в виде пены, содержащей 4 мас. % сукцината хитозана, к 650 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 40 г сукцината хитозана и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную композицию выдерживают в статических условиях в течение одних суток, после чего переливают в металлический баллон типа сифона и впрыскивают 50 г двуокиси углерода под давлением. Готовую композицию в виде пены с двуокисью углерода в баллоне хранят в холодильной камере при температуре +4°-+6°С.
Пример 14
Для приготовления 1 кг 30 мас. % композиции в виде пены, содержащей 5 мас. % поливинилпирролидона, к 641 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 50 г поливинилпирролидона и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную композицию выдерживают в статических условиях в течение одних суток, после чего переливают в металлический баллон типа сифона и впрыскивают 50 г двуокиси углерода под давлением. Готовую композицию в виде пены с двуокисью углерода в баллоне хранят в холодильной камере при температуре +4°-+6°С.
Пример 15
Для приготовления 1 кг 30 мас. % композиции в виде пены, содержащей 20 мас. % поливинилпирролидона, к 591 г воды добавляют навески 300 г блок-сополимера этиленоксида и пропиленоксида, 9 г хлористого натрия, 200 г поливинилпирролидона и 0,1 мл 20% раствора полигексаметилен бигуанида гидрохлорида. Смешение компонентов композиции проводят при помощи верхнеприводной мешалки при температуре не выше +8°С при непрерывном перемешивании до полного растворения ингредиентов и образования густого прозрачного раствора. Полученную композицию выдерживают в статических условиях в течение одних суток, после чего переливают в металлический баллон типа сифона и впрыскивают 50 г двуокиси углерода под давлением. Готовую композицию в виде пены с двуокисью углерода в баллоне хранят в холодильной камере при температуре +4°-+6°С.
Пример 16
Экспериментальные исследования композиции на крупных сосудах и при массивных повреждениях проводили на свиньях обоих полов. Все эксперименты проводили под наркозом. Животным моделировали травму мышцы с повреждением сосудистого пучка, проникающее ранение печени, селезенки и повреждение аорты. После чего выполняли заполнение раневых каналов предлагаемой композицией.
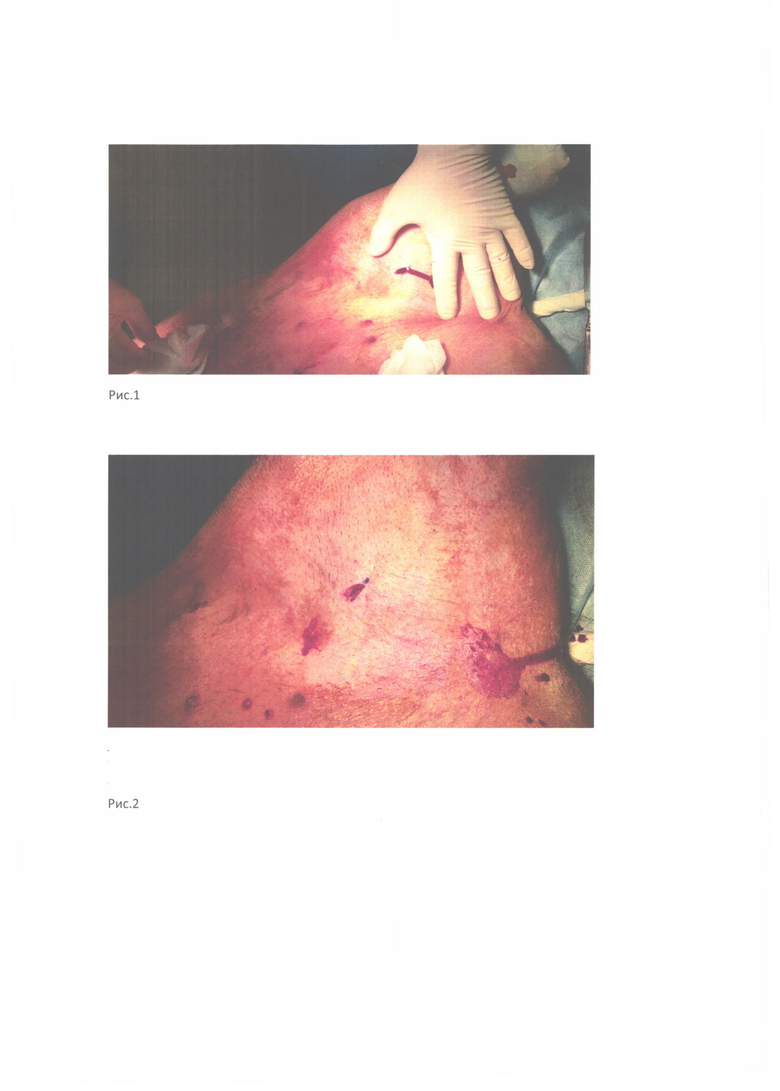
С внутренней поверхности левого бедра была нанесена колото-резаная рана при помощи среднего ампутационного ножа глубиной до 10 см сквозь подлежащий мышечный массив (рис. 1). Кровотечение умеренное. В рану введена композиция при помощи одноразового шприца объемом 20 мл. Гемостаз в течение 5-10 секунд (рис. 2).
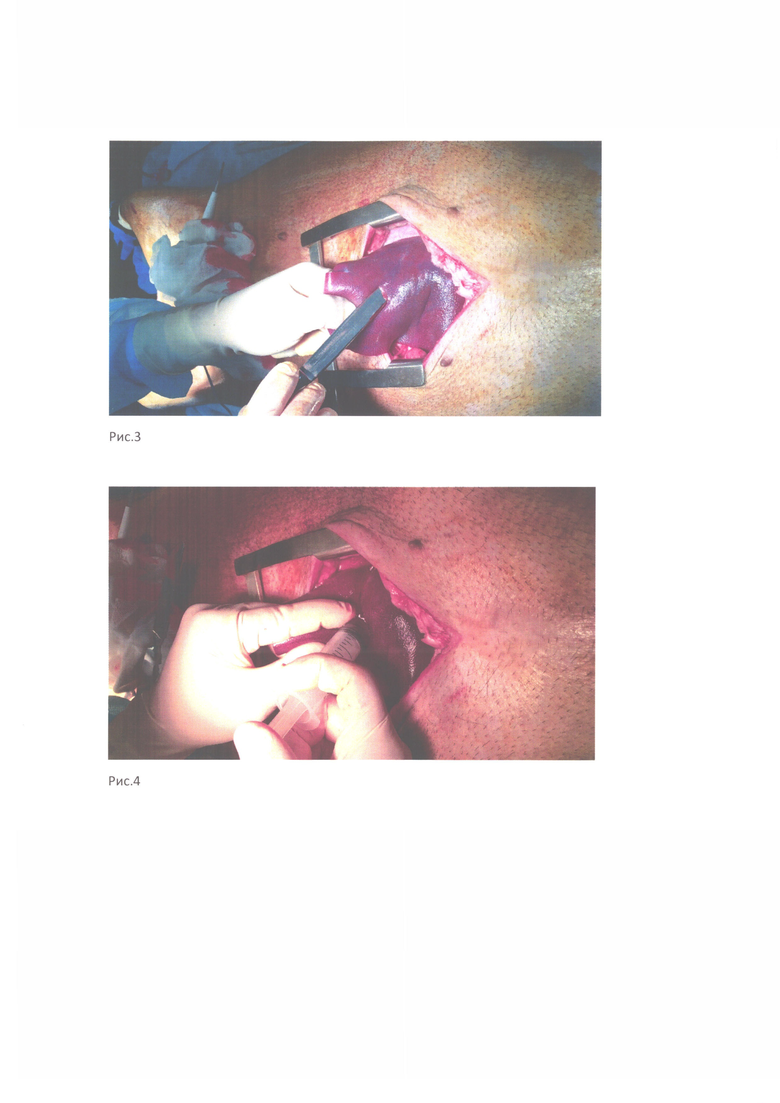
Лапаротомия верхне-срединная. В рану предлежит левая доля печени, вывихнута в рану. При помощи среднего ампутационного ножа в глубину паренхимы ткани печени на 10-12 см нанесена колото-резаная рана (рис. 3). Обильное кровотечение. В рану при помощи шприца объемом 20 мл введенакомпозиция (рис. 4). Гемостаз в течение 5-10 секунд. Наблюдение 5-10 минут. Кровотечения из раны печени нет (рис. 4).
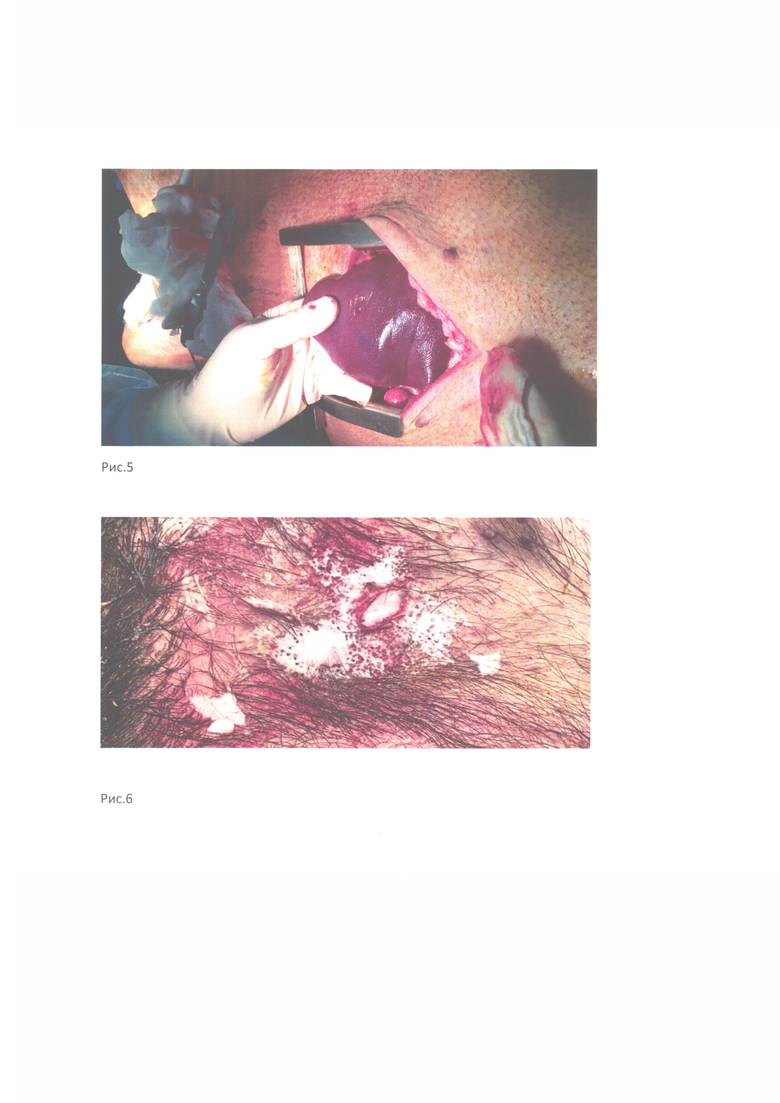
Для испытания композиции с добавлением двуокиси углерода, с внутренней поверхности левого бедра было нанесено огнестрельное ранение. Кровотечение обильное. В рану введена композиция с добавлением двуокиси углерода при помощи баллона под давлением. Гемостаз в течение 5-10 секунд (рис. 6).
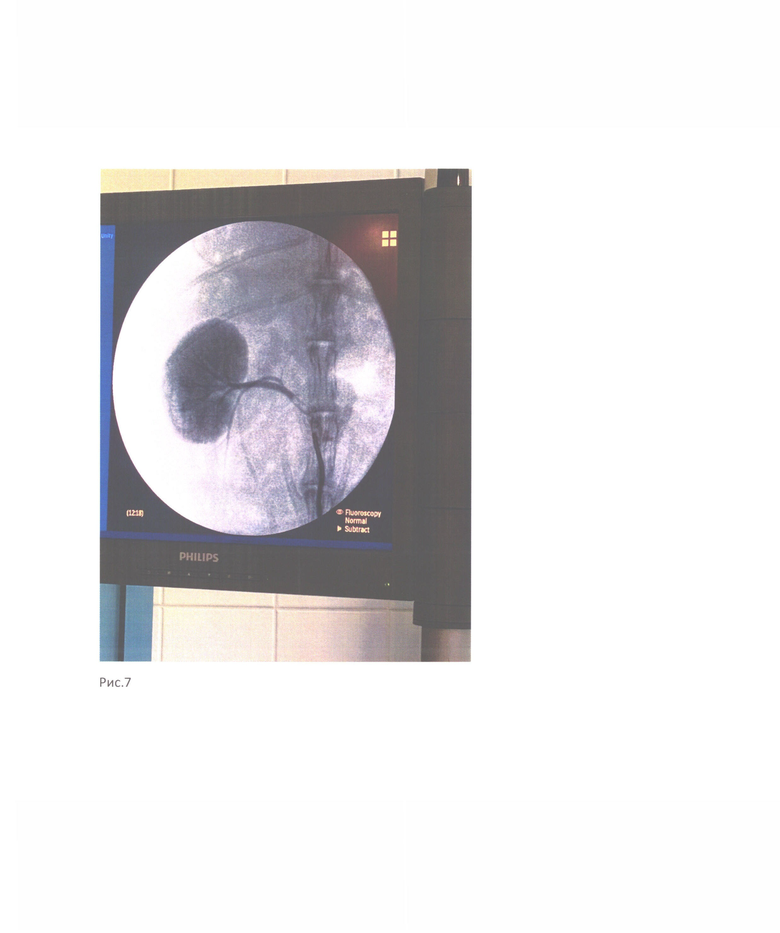
Экспериментальное исследование композиции с добавлением рентгеноконтрастных веществ проводили на кроликах породы шиншилла, самцы, вес 3,5-4,2 кг. Выполняли временную эмболизацию почечной артерии (ПА) под общей седацией с оперативным доступом через бедренную артерию. Композицию вводили путем медленной контролируемой инъекции через катетер в ПА под рентгеноскопическим контролем до полной остановки кровотока в левую почку (рис. 7). После введения в просвет сосуда, композиция застывала и создавала препятствие магистральному кровотоку. Для восстановления нормального кровообращения в этой зоне, мы вводили физраствор с температурой 4 градуса по Цельсию, в результате чего композиция растворялась и кровоток возобновлялся. Самопроизвольное рассасывание композиции в артерии полностью наступало через 1 час 45 минут.
Следует отметить, что во время экспериментов на животных, композиция во всех ее вариантах осуществления образовывала видимый тромб в месте ее введения, что способствовало остановке кровотечений из разных локализаций. В завершении всех экспериментов, мы растворяли образовавшуюся пробку при помощи охлажденного физиологического раствора для восстановления кровотока.
Таким образом, нам удалось создать композицию для временной остановки кровотечений из разных локализаций. Она обеспечивает остановку кровотечений не только из мелких сосудов, а также при повреждении крупных сосудов при травмах и ранениях, а также она может применяться для временной эмболизации целевого сосуда при проведении оперативных вмешательств.
| название | год | авторы | номер документа |
|---|---|---|---|
| Термоуправляемая композиция для временной остановки кровотечений | 2023 |
|
RU2810584C1 |
| Местное гемостатическое средство | 2023 |
|
RU2807892C1 |
| Гемостатическое средство | 2023 |
|
RU2826361C1 |
| Стент-графт для лечения аневризм и расслоения аорты | 2021 |
|
RU2764189C1 |
| ГЕМОСТАТИЧЕСКИЙ РАСТВОР, ГЕМОСТАТИЧЕСКОЕ ИЗДЕЛИЕ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2023 |
|
RU2827960C1 |
| Гемостатическая композиция (варианты) | 2022 |
|
RU2826621C2 |
| Способ деструкции эмбологенного матрикса в эксперименте. | 2020 |
|
RU2739669C1 |
| Способ протезирования магистральных ветвей аорты | 2023 |
|
RU2814372C1 |
| Многослойное комбинированное гемостатическое средство местного действия | 2023 |
|
RU2826069C1 |
| Способ формирования артериовенозной фистулы для профилактики нарушения проходимости магистральных артерий нижних конечностей | 2021 |
|
RU2780929C1 |
Изобретение относится к области медицины и предназначено для оказания как доврачебной, так и первой помощи, скорой медицинской и первичной медико-санитарной помощи, в полевых и домашних условиях, в районах боевых действий, а также в условиях стационара для остановки кровотечения, в том числе из паренхиматозных органов, а также временной эмболизации кровеносных сосудов во время хирургических вмешательств. Композиция для временной остановки кровотечений выполнена на основе блок-сополимера этиленоксида и пропиленоксида и содержит поли(этиленоксид), воду, полигексаметилен бигуанида гидрохлорид и хлористый натрий при следующем соотношении компонентов, мас. %: блок-сополимер этиленоксида и пропиленоксида - 15-30; поли(этиленоксид) - 0,1-2,0; полигексаметилен бигуанида гидрохлорид - 0,002; хлористый натрий - 0,9; вода - остальное. Изобретение обеспечивает временную остановку кровотечений. 5 з.п. ф-лы, 7 ил., 16 пр.
1. Композиция для временной остановки кровотечений, выполненная на основе блок-сополимера этиленоксида и пропиленоксида, содержащая поли(этиленоксид) и воду, отличающаяся тем, что композиция дополнительно содержит полигексаметилен бигуанида гидрохлорид и хлористый натрий при следующем соотношении компонентов, мас. %:
2. Композиция по п. 1, отличающаяся тем, что может дополнительно содержать двуокись углерода в количестве 5-10 мас. %.
3. Композиция по п. 1, отличающаяся тем, что может дополнительно содержать рентгеноконтрастное вещество йогексол или йодиксанол в количестве 20-30 мас %.
4. Композиция по любому из пп. 1-3, отличающаяся тем, что может дополнительно содержать поливинилпирролидон в количестве 5-20 мас. %.
5. Композиция по любому из пп. 1, 2, отличающаяся тем, что дополнительно может содержать водорастворимые соли хитозана в количестве 0,1-4,0 мас. %.
6. Композиция по п. 1, отличающаяся тем, что выполнена в виде геля или пены, или жидкости.
| JP 6095675 B2, 15.03.2017 | |||
| НАПРАВЛЯЮЩАЯ ДЛЯ ЛЫЖНОГО КРЕПЛЕНИЯ | 2012 |
|
RU2519946C2 |
| XIAOYAN AN et al | |||
| Antibacterial and superhydrophobic hemostatic properties of fluorinated random copolymer composite nanocoatings // Progress in Organic Coatings, 168 (2022), 106869, 1-10 | |||
| ПРОТИВОМИКРОБНОЕ, ГЕМОСТАТИЧЕСКОЕ И РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО | 2009 |
|
RU2414932C1 |
Авторы
Даты
2024-05-21—Публикация
2023-08-30—Подача