Область техники, к которой относится изобретение.
Изобретение относится к области биотехнологии, молекулярно-генетической диагностики, в частности к оценке однонуклеотидного полиморфизма rs10104 (A>G) гена C19orf53 молекулярно-генетическим методом исследования.
Уровень техники.
Ген C19orf53 (Gene ID: 28974) локализован на хромосоме 19p13.13. Однонуклеотидный полиморфизм rs10104, позиция chr19:13774670 (GRCh38.p14) [https://www.ncbi.nlm.nih.gov/snp/rs10104] представляет собой миссенс-мутацию и характеризуется заменой A>С,G. Однако, аллель C встречается популяциях мира с частотой менее 0,000001, в связи с чем именно полиморфизм A>G является актуальным для исследований многофакторных болезней человека. Генетический вариант rs10104 A>G приводит к замене аминокислоты лизина на аргинин. Согласно биоинформатическому ресурсу GTEx Portal, rs10104 влияет на уровень экспрессии C19orf53 в широком спектре различных тканей [https://gtexportal.org/home/snp/rs10104#eqtl-block]. Кроме того, данный SNP ассоциирован с модификациями гистонов во всех представленных ресурсом HaploReg v4.2 органах и тканях [https://pubs.broadinstitute.org/mammals/haploreg/detail_v4.2.php?query=&id=rs10104], влияет на связывание ДНК с факторами транскрипции. Установленная высокая функциональная значимость данного генетического варианта создает потребность в создании простого в исполнении, недорогого и доступного всем исследователям, работающим в области генетической эпидемиологии, метода идентификации таргетного полиморфного варианта rs10104 (A>G) гена C19orf53.
Известен способ анализа генетических вариаций в геноме человека методом секвенирования амплифицированных участков ДНК [Mardis E. R. DNA sequencing technologies: 2006-2016 //Nature protocols. - 2017. - Vol. 12. - №. 2. - P. 213-218]. Недостатками метода являются высокая стоимость оборудования и реагентов, что исключает широкое внедрение метода в экспериментальные исследования, особенно изучение многофакторных заболеваний, которые требуют большого размера выборок для обеспечения высокой мощности исследований.
Известен способ анализа генетических вариаций в геноме человека методом матричноактивированной лазерной десорбционно-ионизационной масс-спектрометрии (MALDI). Метод заключается в том, анализируемая ДНК переносится на подложку, где она кристаллизуется с матрицей. Затем кристаллизованные аналиты переносят, облучают лазером, вызывая десорбцию и ионизацию молекул в вакуумной камере. Положительно заряженные ионы ДНК ускоряются и мигрируют через вакуумную трубку к высокочувствительному детектору с разной скоростью в зависимости от массы ионов, что приводит к различному времени пролета. Используя время пролета отдельных ионизированных ДНК-аналитов, система определяет массу и отображает масс-спектр, идентифицирующий различные генетические мишени [Li D. et al. MALDI-TOF mass spectrometry in clinical analysis and research //ACS Measurement Science Au. - 2022. - Vol. 2. - №. 5. - P. 385-404]. Недостатками метода являются трудоемкость, высокая стоимость оборудования, высокая стоимость эксперимента, наличие высококвалифицированного персонала.
За прототип выбран коммерческий набор по генотипированию rs10104 (A/G) C19orf53 (C___2994058_10, каталог 4351379) компании ThermoFisher. Однако, генотипирование с использованием коммерческих наборов характеризуется высокой стоимостью, а информация о структуре необходимых для проведения ПЦР праймеров и аллель-специфических зондов является закрытой для исследователей, в связи с чем данная методика не может быть воспроизведена при наличии стандартного набора оборудования и реактивов.
Таким образом, существует реальная потребность в создании быстрого, недорогого и легко воспроизводимого способа идентификации полиморфизма rs10104 (A>G) гена C19orf53, с применением аллель-специфических зондов, который мог бы использоваться в качестве «рутинного» метода генотипирования в любой ПЦР-лаборатории.
Раскрытие сущности изобретения.
Техническим результатом данного изобретения является разработка простого в исполнении и экономически целесообразного способа генотипирования однонуклеотидного полиморфизма rs10104 (A>G), локализованного в позиции chr19:13774670 (GRCh38.p14) гена C19orf53 (Gene ID:28974) методом полимеразной цепной реакции в режиме «реального времени» с применением аллель-специфических сигнальных зондов, содержащие флуорофоры FAM и ROX.
Технический результат достигается тем, что идентификацию аллельных вариантов rs10104 (A>G) гена C19orf53 осуществляют с использованием прямого праймера rs10104 5′-TCACGTGAGCACATCTTTCC-3′ (SEQ ID NO 1), обратного праймера rs10104 5′-CTCCGGGCTCCATCTCTC-3′ (SEQ ID NO 2), rs10104-А-аллель-специфичного флуоресцентно-меченого зонда 5′-(FAM)TCGCTCCCAAGAAGGCGC(RTQ1)-3′ (SEQ ID NO 3), rs10104-G-аллель-специфичного флуоресцентно-меченого зонда 5′-(ROX)TCGCTCCCAGGAAGGCGC(BHQ2)-3′ (SEQ ID NO 4).
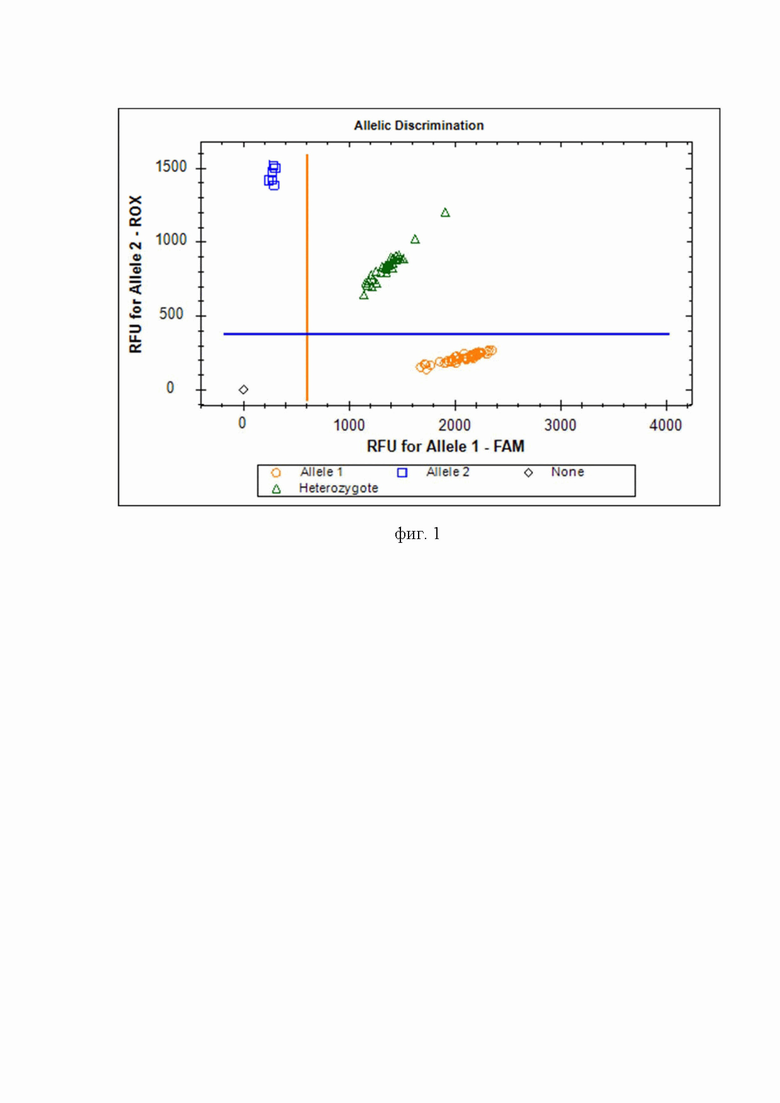
Изобретение поясняется следующей фигурой: дискриминация аллелей по локусу rs346157 гена C19orf53 при генотипировании методом ПЦР в режиме «реального времени» с применением аллель-специфических флуоресцентных зондов по данным величин RFU (относительные единицы флуоресценции) на амплификаторе CFX96: генотипы rs10104-A/A показаны оранжевыми кругами, генотипы rs10104-A/G показаны зелеными треугольниками, генотипы rs10104-G/G показаны голубыми квадратами; черным ромбом отмечен отрицательный контроль.
Работа над дизайном олигонуклеотидов включала несколько этапов:
1) С применением открытой базы данных Ensembl genome browser 109 [https://www.ensembl.org/index.html] выбран синвенс, фланкирующий искомую однонуклеотидную замену [A/G] rs346157 C19orf53, и затем с помощью доступного онлайн программного обеспечения Primer3web version 4.1.0 [https://primer3.ut.ee/] подобрана последовательность олигонуклеотидов, используемых для проведения ПЦР-реакции:
прямой общий праймер rs10104 5′-TCACGTGAGCACATCTTTCC-3′ (SEQ ID NO 1),
обратный общий праймер rs10104 5′-CTCCGGGCTCCATCTCTC-3′ (SEQ ID NO 2).
Размер амплифицируемого в ходе ПЦР фрагмента гена C19orf53 составляет 110 пар нуклеотидов
(TCACGTGAGCACATCTTTCCCCAGGTCGTGTTATCGCTCCCA[A/G]
GAAGGCGCGCGTCGTGCAGCAGCAAAAGCTCAAGAAGGTGTGCGGGGG
CGAGAGATGGAGCCCGGAG).
2) Для дизайна зондов пользовались практическими рекомендациями [Basu C. (ed.). PCR primer design. - New york : Humana Press, 2015]. В реакции использовались гидролизные зонды. Последовательность зонда подбирали таким образом, чтобы он отжигался на матрицу между прямым и обратным праймерами. Каждый зонд снабжали флуорофором и гасителем флуоресценции, спектр поглощения которого соответствует длинам волн спектра флуорофора. Для гашения флуоресценции FAM пользовались гасителем RTQ1; для гашения флуоресценции ROX - гасителем BHQ2.
На основании изложенных критериев и практических рекомендаций были подобраны зонды со следующей структурой:
rs10104-A-аллель-специфичный флуоресцентно-меченый зонд 5′-(FAM)TCGCTCCCAAGAAGGCGC(RTQ1)-3′ (SEQ ID NO 3),
rs10104-G-аллель-специфичный флуоресцентно-меченый зонд 5′-(ROX)TCGCTCCCAGGAAGGCGC(BHQ2)-3′ (SEQ ID NO 4).
3) Изготовление праймеров и зондов осуществлялось в сервисном центре НПК «Синтол», Москва.
4) С помощью практических экспериментов подобраны оптимальные условия для проведения генотипирования, которые включают следующие этапы: 50°C в течение 2 минут, 95°C в течение 10 минут, затем 39 циклов [95°C в течение 10 секунд и 61°C в течение 1 минуты].
5) Разработанный способ был апробирован в лаборатории геномных исследований на 200 образцах ДНК здоровых индивидуумов биобанка НИИ генетической и молекулярной эпидемиологии КГМУ. Генотипирование осуществляли по данным величин RFU (относительные единицы флуоресценции) зондов с флуоресцентными красителями. По результатам генотипирования rs10104 C19orf53 116 человек (58%) оказались гомозиготами по аллелю A (генотип А/А); 76 человек (38%) являлись гетерозиготами (генотип A/G), 8 человек (4%) индивидуумов оказались гомозиготами G/G.
6) Валидацию способа проводили методом масс-спектрометрического анализа на геномном времяпролетном масс-спектрометре MassArray analyzer 4 (Agena Bioscience). Результаты обоих способов генотипирования полностью (100% генотипов) совпали. Однако патентуемый способ генотипирования полиморфного локуса rs10104 (A>G) гена C19orf53 методом ПЦР в режиме «реального времени» с применением аллель-специфических зондов позволяет значительно (на 6 часов) сократить время проведения анализа, а также снижает себестоимость анализа (в 4-5 раз).
Осуществление изобретения.
Способ осуществляют следующим образом:
1. Выделение ДНК из периферической венозной крови. На первом этапе к 0,5 мл крови добавляли 0,5 мл PBS и центрифугировали 10 мин при 12 тыс. об/мин. Надосадочную жидкость сливали, добавляли 1 мл PBS и вновь центрифугировали при тех же условиях. Надосадочную жидкость сливали, добавляли 200 мкл ТЕ-буфера, пипетировали до растворения осадка и затем последовательно добавляли 10 мкл 1% раствора додецилсульфата натрия SDS и 5 мкл протеиназы К. Пробирки инкубировали в термостате при t=37°C 12 ч. В ходе второго этапа проводили четыре последовательных центрифугирования с фенолом и хлороформом согласно протоколу методики (10 мин, 8 тыс. об/мин), после чего ДНК осаждали ледяным раствором 95% этилового спирта и центрифугировали 10 мин при 14,3 тыс. об/мин. По испарении спирта ДНК растворяли в 100 мкл деионизированной дистиллированной воды. Получаемый раствор ДНК в воде имел чистоту в диапазоне А260/280=1,5-2,0 и среднюю концентрацию около 180-200 нг/мкл.
2. Подготовка образцов ДНК к генотипированию. Качество выделенной ДНК оценивали по степени чистоты и концентрации раствора на спектрофотометре NanoDrop (Thermo Fisher Scientific, США). Все анализируемые образцы ДНК были разведены деионизированной водой до концентрации 15-20 нг/мкл при А260/280=1,5-2,0.
3. Анализ полиморфизма rs10104 (A>G) гена C19orf53 с помощью полимеразной цепной реакции в реальном времени с использованием аллель-специфических зондов. Для генотипирования использовали два фланкирующих праймера, прямой (SEQ ID NO 1) и обратный (SEQ ID NO 2), а также аллель-специфические зонды: A-аллель-специфичный флуоресцентно-меченый зонд (SEQ ID NO 3), G-аллель-специфичный флуоресцентно-меченый зонд (SEQ ID NO 4).
ПЦР в «реальном времени» проводили в 25 мл реакционной смеси, содержащей 1,25 ЕД ДНК-полимеразы Hot Start Taq («Биолабмикс», Новосибирск, Россия), 20 нг ДНК, по 10 мкM каждого праймера, по 5 мкM каждого зонда, 0.03 мM каждого dNTP, 2,5 мМ MgCl2; 1xПЦР-буфер [67 мМ Tris-HCl, pH 8,8, 16,6 мМ (NH4)2SO4, 0,01% Tween-20]. Реакция амплификации состояла из стадии нагревания до 50°C в течение 2 минут, 95°C в течение 10 минут, затем 39 циклов [95°C в течение 10 секунд и 61°C в течение 1 минуты].
4. Генотипирование. При проведении ПЦР в амплификаторе с флуоресцентной детекцией (Bio-Rad CFX96 или аналогичном амплификаторе) генотипирование осуществляют по данным величин RFU (относительных единиц флуоресценции). Для rs10104 (A>G) гена C19orf53 зонд с флуоресцентным красителем FAM соответствует аллелю A, зонд с красителем ROX - аллелю G (фиг. 1). На фигуре видно четкое разделение образцов на кластеры, где черный ромб соответствуют отрицательному контролю, кластер оранжевых кругов - соответствует зонду с флуоресцентным красителем FAM и позволяет идентифицировать гомозигот A/A. Кластер синих квадратов соответствует зонду с красителем ROX и позволяет идентифицировать гомозигот G/G. Кластер зеленых треугольников позволяет идентифицировать гетерозигот A/G.
Резюме.
Таким образом, разработан эффективный и недорогой способ для экспресс-идентификации полиморфного варианта rs10104 (A>G) гена C19orf53 у человека методом ПЦР в режиме «реального времени» с применением аллель-специфических флуоресцентных зондов, который может быть использован в медицине при определении наследственной предрасположенности к развитию заболеваний, ассоциированных с носительством полиморфизмов гена C19orf53, а также в научных целях.
Изобретение относится к области биотехнологии. Описан способ генотипирования полиморфного локуса rs10104 (A>G) гена C19orf53 у человека методом ПЦР в режиме «реального времени» с применением аллель-специфических флуоресцентных зондов, предусматривающий проведение ПЦР с использованием специально подобранных праймеров и зондов c флуорофорами в амплификаторе с детекцией флуоресценции. Технический результат заключается в расширении арсенала средств генотипирования полиморфного локуса rs10104 (A>G) гена C19orf53 у человека. 1 ил.
Способ генотипирования полиморфного локуса rs10104 (A>G) гена C19orf53 у человека методом ПЦР в режиме «реального времени» с применением аллель-специфических флуоресцентных зондов, отличающийся тем, что идентификацию аллельных вариантов rs10104 (A>G) гена C19orf53 осуществляют с использованием прямого праймера rs10104 5′-TCACGTGAGCACATCTTTCC-3′ (SEQ ID NO: 1), обратного праймера rs10104 5′-CTCCGGGCTCCATCTCTC-3′ (SEQ ID NO: 2), rs10104-A-аллель-специфичного флуоресцентно-меченого зонда 5′-(FAM)TCGCTCCCAAGAAGGCGC(RTQ1)-3′ (SEQ ID NO: 3), rs10104-G-аллель-специфичного флуоресцентно-меченого зонда 5′-(ROX)TCGCTCCCAGGAAGGCGC(BHQ2)-3′ (SEQ ID NO: 4).
| US 20170342504 A1, 30.11.2017 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНЕТИЧЕСКОЙ ПРЕДРАСПОЛОЖЕННОСТИ К РАЗВИТИЮ ТУБЕРКУЛЕЗА С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ MYCOBACTERIUM TUBERCULOSIS ПРИ ВИЧ-ИНФЕКЦИИ | 2020 |
|
RU2750715C1 |
| Genes, encoding heat-resistant obscure (Hero) proteins: new players in ischemic stroke pathogenesis / O | |||
| Bushueva, V | |||
| Soldatov, A | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
Авторы
Даты
2023-12-05—Публикация
2023-10-16—Подача