Изобретение относится к области медицины, а именно к стоматологии, фармакологии и микробиологии и может быть применимо для диагностического исследования внутреннего содержимого раны в области дентального имплантата на этапе раскрытия дентального имплантата и может быть использовано для осуществления оценки микробной контаминации раны и, при необходимости, коррекции схемы антибактериальной терапии. На этапе установки формирователя десны, после обработки полости рта пациента раствором хлоргексидина биглюконата 0,05% в течении 1-й минуты, формируется слизисто-надкостничный лоскут для получения доступа к шахте дентального имплантата, в который ранее был установлен винт-заглушка. Производится замена винта-заглушки на формирователь десневой манжеты. Винт-заглушка упаковывается в стерильную транспортную систему и отправляется на микробиологическое исследование. Способ позволит оценить степень микробной контаминации внутреннего содержимого раны в области дентального имплантата.
Известен способ взятия проб материала для микробиологических исследований полости рта и устройство для его осуществления. Данный способ предполагает взятие проб микрофлоры с локальных участков слизистой оболочки в стерилизованные металлические гильзы с находящимися там различными питательными средами [1].
Недостатком данного метода является, что взятие образцов для микробиологического исследования проводится только с поверхности слизистой оболочки и не позволит оценить микробиологическую обсемененность более глубоких слоев раны, а именно участков под слизистой оболочкой полости рта, непосредственно в области костного ложа, где установлен дентальный имплантат.
Известен способ забора мазка-отпечатка и устройство для его осуществления. Метод позволяет дозировано осуществлять давление на слизистую оболочку с целью взятия клеток для цитологического исследования [2].
Недостатком метода является то, что взятие клеток происходит с поверхности слизистой оболочки и не окажется информативным при необходимости изучения внутреннего содержимого раны.
Известно устройство для забора биологической пробы со стенок полого органа. Устройство предполагает атравматичное получение биопробы за счет электрета с электрическим потенциалом 3-5 кВ, изготовленным из полимерного материала в форме круга с овальными краями, соединенного со стержнем гибкой ножкой [3].
Недостатком устройства является его поверхностное использование, без возможности получения биопробы из глубины раны.
Известен способ забора отделяемого из послеоперационной раны. Он предполагает использование капроновых лигатур, которые вводятся в дренажную трубку на этапе дренирования раны. По мере пропитывания лигатур внутренним содержимым раны, они извлекаются, от них отрезается конец, пропитанный содержимым раны, и отправляется на микробиологическое исследование. Способ позволяет осуществить мониторинг in vivo микрофлоры в послеоперационной ране [4].
Недостатком метода является невозможность его осуществления при герметичном ушивании раны, что необходимо при проведении операции дентальной имплантации.
Все перечисленные выше аналоги не позволяют дать характеристику качественного состава микробиома с использованием современных молекулярно-биологических методов, к которым может быть отнесена полимеразная цепная реакция (ПЦР) с праймерами пародонтопатогенных видов, которые в настоящее время считаются основными этиологическими факторами воспаления в пародонте и периимплантационных тканей [5, 8].
Предлагаемый метод предлагается осуществлять на основании получения информации о наличии микрозазора между имплантатом и винтом-заглушкой. Влияние микрозазора на уровень прилегающей костной ткани является предметом обсуждений среди врачей-стоматологов. Несмотря на то, что до этапа установки имплантата в полость рта, он является стерильным, во время операции неизбежно происходит попадание слюны и крови внутрь имплантата и в рану. При этом избежать контаминации и обеспечить абсолютную стерильность не представляется возможным. Кроме того, несмотря на сопоставление краев раны и накладывание швов, возможно подтекание слюны вглубь раны, что повышает число микроорганизмов и потенциально может сказаться неблагоприятно на процессе заживления. Вероятно, на этапе раскрытия имплантата может быть отмечена разница в степени контаминации внутреннего содержимого раны, сопоставление полученных данных с клиническими признаками заживления, а именно отсутствием или наличием гиперемии, отека слизистой оболочки в области установленного имплантата и/или наличия отделяемого в данной области.
Целью изобретения является получение достоверной информации относительно качественных и количественных показателей микробной контаминации внутреннего содержимого раны в области дентального имплантата на этапе его раскрытия.
Эта цель достигается тем, что после периода остеоинтеграции дентального имплантата, на этапе его раскрытия извлекается винт-заглушка и отправляется на бактериологическое и молекулярно-биологическое исследование с помощью ПЦР для выявления представителей пародонтопатогенных видов и их антибиотикорезистентных штаммов в исследуемом материале P. gingivalis, Agg. actinomycetemcomitans, P. intermedia, Т. denticola, Т. forsythia, F. nucleatum, S. sanguinis, S. mutans, C. albicans, C. Krusei, L. buccalis, F. alocis [6, 7, 9-12].
Способ микробиологической оценки внутрираневого содержимого на этапах операции дентальной имплантации заключается в следующем. После проведения операции дентальной имплантации, на этапе замены винта-заглушки на формирователь десневой манжеты, производят забор винта-заглушки непосредственно из дентального имплантата и транспортировку полученного винта в микробиологическую лабораторию с целью бактериологического и молекулярно-биологического исследования. Проводят обработку полости рта пациента раствором хлоргексидина биглюконата 0,05% в течении 1-й минуты, под местной анестезией, производят формирование слизисто-надкостничного лоскута в области дентального имплантата с целью получения доступа к нему. При помощи ручной отвертки выкручивается заглушка и упаковывается в стерильную транспортную среду. Производится антисептическая обработка внутренней поверхности имплантата раствором хлоргексидина 0.05%, установка формирователя десневой манжеты. Сформированный ранее лоскут смещается в новое положение и фиксируется швами. Полученную заглушку изучают бактериологическим и молекулярно-биологическим методами и производят клиническую оценку периода заживления раны после дентальной имплантации. Для исследования с помощью ПЦР используется набор праймеров, который позволяет диагностировать в исследуемом материале пародонтопатогенные виды бактерий и их антибиотикорезистентные штаммы P. gingivalis, Agg. actinomycetemcomitans, P. intermedia, Т. denticola, Т. forsythia, F. nucleatum, S. sanguinis, S. mutans, C. albicans, C. Krusei, L. buccalis, F. alocis [6, 7, 9-12].
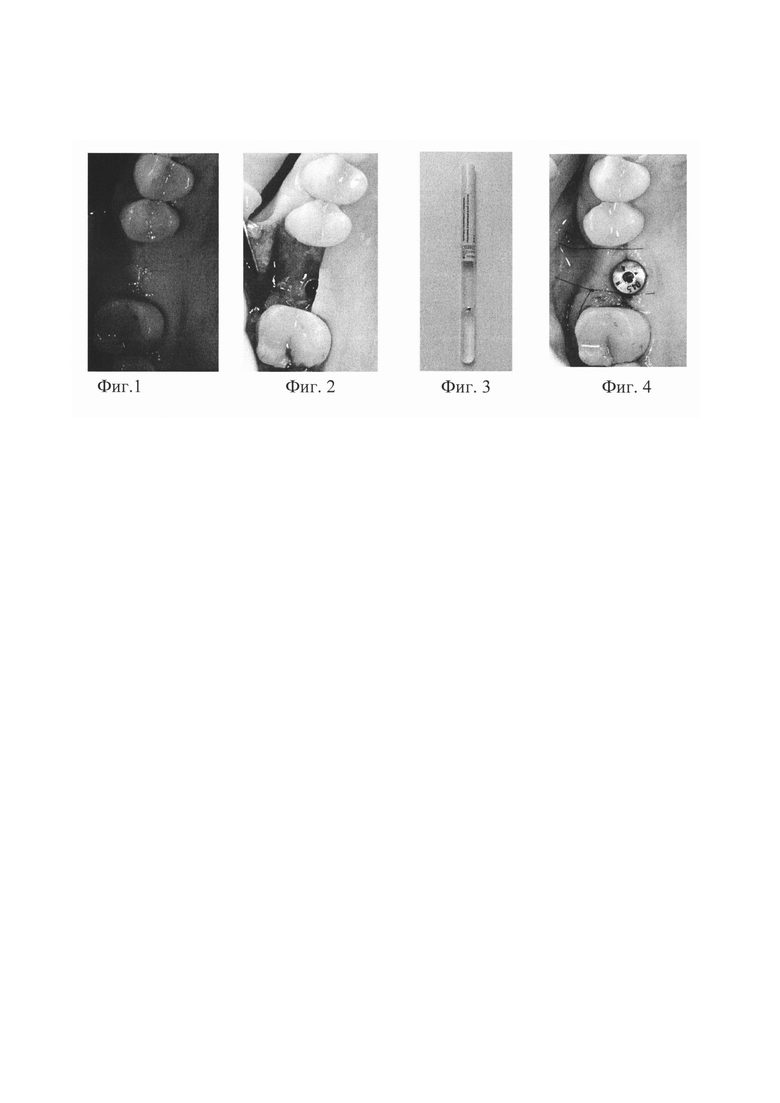
Способ микробиологической оценки внутрираневого содержимого на этапах операции дентальной имплантации был апробирован на пациенте П. (1986 года рождения), проходящем имплантологическое лечение. Пациент обратился с жалобами на отсутствие зуба 1.6. При осмотре отмечалось отсутствие зуба 1.6. Слизистая оболочка в данной области была бледно-розового цвета, умеренно увлажнена. В ходе клинико-рентгенологического обследования противопоказаний к дентальной имплантации отмечено не было. Была спланирована и под местной анестезией проведена операция установки дентального имплантата в области отсутствующего зуба 1.6 (Фиг. 1). Послеоперационный период протекал без особенностей. Осмотр пациента проводили на 1-е, 3-е и 7-е сутки после операции, при этом ни в один из дней наблюдения гиперемии, отека или наличия отделяемого отмечено не было. Снятие швов было проведено на 7-е сутки после операции установки дентального имплантата. Через 6 месяцев после установки дентального имплантата в области отсутствующего зуба 1.6 при осмотре определялась слизистая оболочка бледно-розового цвета, при клинико-рентгенологическом обследовании противопоказаний к дальнейшему лечению определено не было. Согласно плану лечения был спланирован этап установки формирователя десневой манжеты в области установленного ранее дентального имплантата 1.6. Непосредственно перед операцией установки формирователя десневой манжеты была проведена обработка полости рта пациента раствором хлоргексидина биглюконата 0,05% в течении 1-й минуты, под местной анестезией было проведено раскрытие винта-заглушки дентального имплантата 1.6 (Фиг. 2). Полученный винт-заглушка был помещен в транспортную среду для доставки образца в микробиологическую лабораторию для проведения исследования (Фиг. 3). На место винта-заглушки был установлен формирователь десневой манжеты, сопоставление краев раны и фиксация швами (Фиг. 4). Винт-заглушка в транспортной среде был передан в микробиологическую лабораторию. В результате были выделены представители пародонтопатогенной флоры: а-гемолитические стрептококки в ассоциации с F. nucleatum (3×102 КОЕ) и L. buccalis (1×101 КОЕ), пародонтопатогенные виды анаэробов, представленные преимущественно представителями I порядка: P. gingivalis (2×103), в ассоциации с родом Peptostreptococcus spp.в значительном количестве. Коррекция схемы антибактериальной терапии не потребовалась. При клинической оценке периода заживления на 1-е, 3-й, 7-е и 14-е сутки в области раны не было отмечено гиперемии, отека или наличия отделяемого. Снятие швов было проведено на 7-е сутки.
Данное исследование позволяет сделать вывод о том, что внутреннее содержимое имплантата после его установки является контаминированной поверхностью, а наличие высокого многообразия микроорганизмов является значимым фактором риска развития осложнений в послеоперационном периоде, что может требовать коррекции схемы антибактериальной терапии.
Список литературы:
1.Патент РФ RU2101692 С1, 18.06.1992
2. Патент РФ RU2111 473 С1, 18.10.1995
3. Патент РФ RU112019 U1, 28.07.2011
4. Патент РФ RU2337722 С1, 27.07.2007
5. Николаева, Е. Н., Пародонтопатогенные бактерии - индикаторы риска возникновения и развития пародонтита / Е. Н. Николаева, В. Н. Царев, Е. В. Ипполитов // Стоматология для всех. - 2011. - №4 (II ч.). - С. 4-7.
6. Ипполитов Е.В. Мониторинг формирования микробной биопленки и оптимизация диагностики воспалительных заболеваний пародонта // Автореф. дисс.канд. мед. наук. - Москва. - 2016.- 48 с.
7. Царев, В.Н. Оценка эффективности эндодонтической дезинфекции корневых каналов зуба с применением сканирующей электронной микроскопии микробной биопленки / В.Н. Царев, М.С. Подпорин, Е.В. Ипполитов // Бактериология. - 2017. - Т.2, №1. - С. 6-13.
8. Caton J.G., Armitage G., Berglundh Т. et al. A new classification scheme for periodontal and peri-implant diseases and conditions - Introduction and key changes from the 1999 classification // J Periodontol. 2018; 89 (Suppl 1):1-8.
9. Patent KR 20150129484 A publ. 2015-11-20. Primers and probes for detecting bacteria related to periodontal disease and method of detecting the same and use thereof. Inventors Shin E.S., Song K.H.; HUSTEPS INC, Korea.
10. Patent CA 2228836 A1 publ.-1999-08-04. Detection of periodontal pathogens including Bacteroides forsythus, Porphyromonas gingivalis, Prevotella intermedia and Prevotella nigrescens. Inventors Guillot E., Menard C, Mouton C; UNIV LAVAL, Canada.
11. Aruni A.W., Chioma O., Fletcher H.M. Filifactor alocis: The newly discovered kid on the block with special talents // J Dent Res. 2014; 93 (8): 725-732.
12. Wang Q., Wright C.J., Dingming H. et al. Oral community interactions of Filifactor alocis in vitro // PLoS One. 2013; 8 (10): e76271.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ предоперационной подготовки к реоперации дефекта нёба после уранопластики у детей с врождённой расщелиной нёба | 2022 |
|
RU2811300C2 |
| Способ оценки прогрессирования хронического пародонтита и набор реагентов для его осуществления | 2021 |
|
RU2777783C1 |
| СПОСОБ ОДНОМОМЕНТНОЙ ЭЛИМИНАЦИИ ПАРОДОНТОПАТОГЕНОВ В ЗАВИСИМОСТИ ОТ ИХ КЛИНИЧЕСКИ ЗНАЧИМЫХ ТИТРОВ И КЛИНИЧЕСКОГО СОСТОЯНИЯ ТКАНЕЙ ПАРОДОНТА | 2018 |
|
RU2679803C1 |
| СПОСОБ ИССЛЕДОВАНИЯ МИКРОБИОТЫ ПОЛОСТИ РТА В ЗАВИСИМОСТИ ОТ МАТЕРИАЛА НЕСЪЕМНЫХ ОРТОПЕДИЧЕСКИХ КОНСТРУКЦИЙ | 2023 |
|
RU2814756C1 |
| СПОСОБЫ УХОДА ЗА ПОЛОСТЬЮ РТА С ИСПОЛЬЗОВАНИЕМ САХАРИДА В КАЧЕСТВЕ ПРЕБИОТИКА | 2019 |
|
RU2741492C2 |
| Способ формирования смешанной биоплёнки пародонтопатогенных анаэробных бактерий в условиях текучих сред in vitro | 2015 |
|
RU2619169C1 |
| СПОСОБ ПЛАСТИКИ АЛЬВЕОЛЯРНОЙ КОСТИ АУТОТКАНЯМИ ЗУБОВ | 2021 |
|
RU2768970C1 |
| СПОСОБЫ УХОДА ЗА ПОЛОСТЬЮ РТА С ИСПОЛЬЗОВАНИЕМ САХАРИДА В КАЧЕСТВЕ ПРЕБИОТИКА | 2013 |
|
RU2691408C2 |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ИНДИВИДУАЛЬНОЙ ГИГИЕНЫ РТА У ПАЦИЕНТОВ С ДЕНТАЛЬНЫМИ ИМПЛАНТАТАМИ | 2022 |
|
RU2794828C2 |
| СРЕДСТВО "ГИАЛУДЕНТ" ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ПОЛОСТИ РТА | 2005 |
|
RU2286764C1 |
Изобретение относится к области медицины, а именно к стоматологии, фармакологии и микробиологии, и касается микробиологической оценки внутрираневого содержимого на этапах операции дентальной имплантации. Способ включает предварительную обработку полости рта пациента раствором хлоргексидина биглюконата 0,05% в течение 1-й минуты, создание доступа к ранее установленному имплантату, формирование и отслаивание слизисто-надкостничного лоскута, замену винта-заглушки на формирователь десневой манжеты, помещение винта-заглушки в стерильную транспортную систему, затем отправку на микробиологическое исследование. При этом в исследуемом материале с помощью ПЦР, используя набор праймеров, оценивают в исследуемом материале пародонтопатогенные виды бактерий и их антибиотикорезистентные штаммы P. gingivalis, Agg. actinomycetemcomitans, P. intermedia, T. denticola, Т. forsythia, F. nucleatum, S. sanguinis, mutans, S. mutans, C. albicans, C. krusei, L. buccalis, F. alocis. Изобретение позволяет определять качественные и количественные параметры микрофлоры внутрираневого содержимого в области дентального имплантата, включая пародонтопатогенные виды бактерий, что дает возможность судить о микробной контаминации данной области и в зависимости от этого проводить коррекцию схем антибактериальной терапии. 1 пр., 4 ил.
Способ микробиологической оценки внутрираневого содержимого на этапах операции дентальной имплантации, заключающийся в исследовании внутреннего содержимого раны в области дентального имплантата на этапе раскрытия дентального имплантата, осуществляемый путем предварительной обработки полости рта пациента раствором хлоргексидина биглюконата 0,05% в течение 1-й минуты, создания доступа к ранее установленному имплантату, формирования и отслаивания слизисто-надкостничного лоскута, замены винта-заглушки на формирователь десневой манжеты, помещения винта-заглушки в стерильную транспортную систему и отправки на микробиологическое исследование, где в исследуемом материале с помощью ПЦР, используя набор праймеров, оценивают в исследуемом материале пародонтопатогенные виды бактерий и их антибиотикорезистентные штаммы P. gingivalis, Agg. actinomycetemcomitans, P. intermedia, T. denticola, Т. forsythia, F. nucleatum, S. sanguinis, mutans, S. mutans, C. albicans, C. krusei, L. buccalis, F. alocis.
| СПОСОБ ЗАБОРА МАТЕРИАЛА ДЛЯ БАКТЕРИОЛОГИЧЕСКОГО ИССЛЕДОВАНИЯ ИЗ КОРНЕВОГО КАНАЛА И ПЕРИАПИКАЛЬНОЙ ОБЛАСТИ ЗУБА ПРИ ХРОНИЧЕСКИХ АПИКАЛЬНЫХ ПЕРИОДОНТИТАХ | 2012 |
|
RU2476185C1 |
| СПОСОБ ОЦЕНКИ ТЕЧЕНИЯ И ПРОГНОЗА РАЗВИТИЯ ГНОЙНЫХ РАН ПРИ ФЛЕГМОНАХ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2003 |
|
RU2233449C1 |
| Способ забора материала для бактериологического исследования из апикальной области корневого канала зуба при осложненных формах кариеса | 2016 |
|
RU2618645C1 |
| ДИСКОВАЯ ПИЛА | 2002 |
|
RU2228836C1 |
| Caton J.G., Armitage G., Berglundh Т | |||
| et al | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Wang | |||
Авторы
Даты
2023-12-12—Публикация
2022-08-11—Подача