ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к химерному антигенному рецептору (CAR), который связывается с антигеном-мишенью, имеющим низкую плотность, таким как антиген созревания B-клеток (BCMA).
УРОВЕНЬ ТЕХНИКИ
Множественная миелома
Множественная миелома (миелома) представляет собой злокачественное новообразование костного мозга из плазматических клеток. Популяции аномальных плазматических клеток накапливаются в костном мозге, где они препятствуют продукции нормальных клеток крови. Миелома является вторым по распространенности злокачественным заболеванием системы крови в США (после неходжкинской лимфомы), на нее приходится 13% злокачественных заболеваний системы крови и 1% всех случаев рака. Заболевание является обременительным относительно страданий пациентов и медицинских расходов, так как оно сопровождается патологическими переломами, восприимчивостью к инфекции, почечной недостаточностью и последующей недостаточностью костного мозга перед смертью.
В отличие от многих типов лимфомы, миелома на сегодняшний день неизлечима. Стандартные химиотерапевтические агенты, применяемые при лимфоме, в основном неэффективны при миеломе. Кроме того, из-за потери экспрессии CD20 на плазматических клетках при этом заболевании невозможно применять ритуксимаб. Новые агенты, такие как бортезомиб и ленолидомид частично эффективны, но не приводят к обеспечению продолжительной ремиссии.
Следовательно, существует потребность в альтернативных агентах для лечения миеломы, которые имели бы более высокую эффективность и улучшенные долгосрочные эффекты.
ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ (CAR)
Химерные антигенные рецепторы представляют собой белки, которые в своем обычном формате придают специфичность моноклонального антитела (МАТ) эффекторной функции Т-клетки. Их обычная форма представляет собой трансмембранный белок I типа с распознающим антиген амино-концом, спейсером и трансмембранным доменом, все из которых соединены с составным эндодоменом, передающим сигналы выживания и активации Т-клетки.
Наиболее распространенная форма этих молекул использует для распознавания антигена-мишени одноцепочечные вариабельные фрагменты (scFv), полученные из моноклональных антител. scFv соединяется с сигнальным эндодоменом через спейсер и трансмембранный домен. Такие молекулы вызывают активацию Т-клетки в ответ на распознавание scFv его мишени. Когда Т-клетки экспрессируют такой CAR, они распознают и убивают клетки-мишени, экспрессирующие антиген-мишень. Было разработано несколько CAR против опухолеассоциированных антигенов, а подходы адоптивного переноса таких экспрессирующих CAR Т-клеток в настоящее время проходят клинические исследования по лечению разных типов рака. Carpenter и соавт. (2013, Clin Cancer Res 19(8) 2048-60) описывают CAR, который содержит scFv против антигена созревания B-клеток (BCMA).
BCMA является трансмембранным белком, который преимущественно экспрессируется зрелыми лимфоцитами, то есть В-клетками памяти, плазмобластами и плазматическими клетками костного мозга. BCMA также экспрессируется на клетках множественной миеломы.
Carpenter и соавт. демонстрируют, что трансдуцированные Т-клетки, экспрессирующие CAR против BCMA, способны специфично убивать клетки миеломы, выделенные у пациента с плазмоцитомой или миеломой.
Несмотря на успехи, продемонстрированные подходами к применению CAR с использованием антител против BCMA, при нацеливании на этот антиген следует уделять особое внимание тому, что BCMA присутствует с очень низкой плотностью на клетках миеломы по сравнению, например, с экспрессией CD19 на клетках лимфомы. Несмотря на успех, продемонстрированный применением в клинике опосредованной CAR-Т-клетками терапии, направленной на распространенные антигены-мишени, такие как CD19 и GD2, имеются данные, что химерные антигенные рецепторы не способны формировать сигнал в ответ на антигены, имеющие очень низкую плотность.
Например, результаты исследования CAR-Т-клеток, нацеленных на киназу анапластической лимфомы (ALK), показали, что CAR-Т-клетки обладали ограниченной противоопухолевой эффективностью в двух ксенотрансплантатных моделях нейробластомы человека. Было показано, что продукция цитокинов в высокой степени зависела от плотности мишени (ALK), и что плотность мишени (ALK) на клетках линий нейробластомы была недостаточной для максимальной активации CAR-Т-клеток (Walker et al. (2017) Mol. Ther. 25, 2189-2201).
В другом исследовании CAR-Т-клетки против CD22 использовали для лечения рецидивирующего и/или рефрактерного лимфобластного лейкоза из В-клеток предшественников (В-ОЛЛ), несмотря на определенную наблюдаемую дозозависимую антилейкозную активность, в некоторых случаях имели место рецидивы. Рецидивы были ассоциированы со сниженной плотностью сайтов CD22, что считалось обуславливающими способность CD22+ клеток избегать уничтожения CD22-CAR-Т-клетками (Fry et al. (2017) Nat. Med. doi:10.1038/nm.4441).
В активации CAR-Т-клеток существует иерархия от уничтожения мишеней до высвобождения цитокинов и до пролиферации. CAR-Т-клетка может убить клетку-мишень, которая имеет низкую плотность антигена, но может не достичь при этом полной активации.
Следовательно, существует потребность в альтернативных подходах на основе CAR-Т-клеток, которые могли бы убивать клетки-мишени, экспрессирующие антиген-мишень, имеющий низкую плотность.
ОПИСАНИЕ ФИГУР
Фигура 1: Экспрессия BCMA у пациентов с множественной миеломой
Фигура 2: Разные форматы связывающего домена химерных антигенных рецепторов
(a) Fab CAR формат; (b) dAb CAR формат; (c) scFv CAR формат
Фигура 3: Схематичная диаграмма, иллюстрирующая взаимодействие классической CAR-Т-клетки и клетки-мишени, экспрессирующей антиген-мишень с низкой плотностью. (а) Мембрана CAR-Т-клетки в обычном состоянии; (b) мембрана CAR-Т-клетки формирует иммунный синапс с клеткой с высокой плотностью экспрессии мишени; (c) мембрана CAR-Т-клетки в ответ на клетку-мишень, которая имеет низкую плотность антигена.
Фигура 4: Схематичная диаграмма, иллюстрирующая конститутивно активный химерный антигенный рецептор. Химерный трансмембранный белок содержит домен димеризации и эндодомен рецептора цитокина. Представленный вариант реализации демонстрирует архитектуру типа «Fab», при которой домен димеризации содержит константные области тяжелой и легкой цепей по типу антитела. Стабильная димеризация этих двух доменов сближает общую γ-цепь рецептора интерлейкина-2 (ИЛ-2) с β-цепью рецептора ИЛ-2 или α-цепью рецептора ИЛ-7, что приводит к конститутивной передаче цитокиновых сигналов.
Фигура 5: Результаты теста на цитотоксичность, в котором сравнивали CAR против BCMA в форматах scFv и FabCAR. Клетки, экспрессирующие CAR, культивировали совместно с клетками-мишенями, не экспрессирующми BCMA (SupT1 NT), с низкой экспрессией BCMA (SupT1BCMAlow) или с очень низкой экспрессией BCMA (JeKo-1) в соотношении 1:4 (Фигура 5А) или 1:8 (Фигура 5В). В качестве положительного контроля применяли bb2121 - описанный ранее CAR против BCMA. Через 24 часа уничтожение клеток-мишеней оценивали методом проточной цитометрии (FACS), и количество клеток-мишеней нормализовали относительно количества Т-клеток, не подвергшихся трансфекции (NT).
Фигура 6: Результаты теста на цитотоксичность, в котором сравнивали CAR против BCMA в форматах scFv и FabCAR. Клетки, экспрессирующие CAR, культивировали совместно с клетками-мишенями, не экспрессирующими BCMA (SupT1 NT), с низкой экспрессией BCMA (SupT1BCMAlow) или с очень низкой экспрессией BCMA (JeKo-1) в соотношении 1:4 (Фигура 6А) или 1:8 (Фигура 6В). В качестве положительного контроля применяли bb2121 - описанный ранее CAR против BCMA. Через 72 часа уничтожение клеток-мишеней оценивали методом FACS, и количество клеток-мишеней нормализовали относительно количества Т-клеток, не подвергшихся трансфекции (NT).
Фигура 7: Продукция интерферона-γ (ИФН-γ) Т-клетками, экспрессирующими CAR против BCMA в форматах либо scFv, либо FabCAR, после совместного культивирования с клетками-мишенями.
Клетки, экспрессирующие CAR, культивировали совместно с клетками-мишенями не экспрессирующими BCMA (Фигура 7А) или с низкой экспрессией BCMA (Фигура 7В) в соотношении 1:4 или 1:8. В качестве положительного контроля применяли bb2121 - описанный ранее CAR против BCMA. Через 24 часа продукцию ИФН-γ оценивали методом иммуноферментного анализа (ИФА)
Фигура 8: Количество CD4 и CD8 Т-клеток, экспрессирующих CAR против BCMA в формате scFv или FabCAR, после совместного культивирования с клетками-мишенями.
Клетки, экспрессирующие CAR, культивировали совместно с клетками-мишенями, не экспрессирующими BCMA (SupT1 NT), с низкой экспрессией BCMA (SupT1BCMAlow) или с очень низкой экспрессией BCMA (JeKo-1), либо с клетками-мишенями MM.1s в соотношении 1:1 в течение 96 часов. Количество цельных CD4 (Фигура 8A) и CD8 (Фигура 8B) T-клеток оценивали гейтированием по CD3 и маркеру RQR8, затем по CD8+ или CD8-.
Фигура 9: Схематичная диаграмма, иллюстрирующая расщепляемый FabCAR
Расщепляемый FabCAR содержит два антигенсвязывающих домена: внешний (дистальный от мембраны) связывающий домен 1 и внутренний (проксимальный от мембраны) связывающий домен 2. Связывающие домены 1 и 2 соединены расщепляемым линкером. Расщепление линкера, например, матриксной металлопротеиназой (MMP) устраняет связывающий домен 1. Без расщепления, при интактном FabCAR, внутренний связывающий домен частично закрыт за счет присутствия внешнего домена из-за счет стерического препятствия. Внутренний домен активируется после расщепления тяжелой и легкой цепей.
Фигура 10: Схематичное изображение растворимого антитела, описанного в Примере 7
Растворимое антитело было сконструировано с двумя вариабельными доменами и внешним связывающим доменом против BCMA (анти-BCMA D8) и внутренним связывающим доменом против CD19 (анти-CD19 CAT). Расщепляемый MMP-9 линкер был встроен между VH доменами на одной цепи и VL доменами на другой цепи. Цепь, содержащая VH, также содержала Fc-часть антитела.
Фигура 11: На графике показано расщепление в процентах растворимого антитела (D8-MMP9-CAT19) с течением времени после инкубации в присутствии MMP-9. Эквивалентное антитело с рандомизированным линкером, который не содержит сайт расщепления MMP-9 (D8-рандомизированный-CAT19) использовали как отрицательный контроль.
Фигура 12: На графике показаны результаты оценки методом ИФА связывания CD19 растворимым антителом (D8-MMP9-CAT19) или отрицательным контролем с рандомизированным линкером (D8-рандомизированный-CAT19) без воздействия и после воздействия MMP-9.
Фигура 13: На графике показана кинетика связывания CD19 растворимым антителом без воздействия (D8-MMP9-CAT19) и после воздействия MMP-9 (D8-MMP9-CAT19 расщепленный). В качестве положительного контроля применяли моноклональное антитело к CD-19 (CAT19 IgG).
КРАТКОЕ ОПИСАНИЕ АСПЕКТОВ ИЗОБРЕТЕНИЯ
В настоящем изобретении авторами установлено, что при нацеливании CAR-Т-клеток на антиген-мишень, имеющий низкую плотность, применение CAR с антигенсвязывающим доменом Fab обеспечивает более эффективную опосредуемую CAR передачу сигналов.
Таким образом, в первом аспекте настоящего изобретения предложен химерный антигенный рецептор (CAR), который связывает антиген-мишень, имеющий низкую плотность, где указанный CAR содержит антигенсвязывающий домен Fab.
Антиген-мишень может экспрессироваться со средней плотностью менее 1500 копий на клетку-мишень.
Антиген-мишень может быть выбран из: ROR1, Tyrp-1, TACI, ALK и BCMA. Например, антиген-мишень может представлять собой BCMA.
В альтернативном варианте реализации первого аспекта настоящего изобретения антигенсвязывающий домен Fab может содержать первый связывающий домен, который связывается с первым антигеном-мишенью, и второй связывающий домен, который связывается со вторым антигеном-мишенью.
Первый антиген-мишень или второй антиген-мишень может представлять собой BCMA.
В настоящем варианте реализации FabCAR может содержать расщепляемый линкер между первым и вторым связывающими доменами.
Линкер может расщепляться под действием агента, такого как фермент. Например, линкер может расщепляться матриксной металлопротеиназой (MMP). Агент можно вводить субъекту до или после введения предложенных в рамках настоящего изобретения клеток, экспрессирующих CAR, для отщепления первого связывающего домена и высвобождения второго связывающего домена. В качестве альтернативы, расщепление может происходить в конкретной области организма естественным образом, если расщепляющий агент (напр., фермент) экспрессируется в этой области. Этой областью может быть, например, область воспаления или область опухоли.
Во втором аспекте настоящего изобретения предложена последовательность нуклеиновой кислоты, которая кодирует CAR согласно первому аспекту настоящего изобретения.
В третьем аспекте настоящего изобретения предложена конструкция нуклеиновой кислоты, которая кодирует CAR согласно первому аспекту настоящего изобретения и имеет одну из следующих общих структур:
VH-CH-spacer-TM-endo-coexpr-VL-CL;
VL-CL-coexpr-VH-CH-spacer-TM-endo;
VL-CL-spacer-TM-endo-coexpr-VH-CH; или
VH-CH-coexpr-VL-CL-spacer-TM-endo;
где:
VH является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи;
CH является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи;
spacer является нуклеиновой кислотой, кодирующей спейсер;
TM является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен;
endo является последовательностью нуклеиновой кислоты, кодирующей эндодомен;
coexpr является последовательностью нуклеиновой кислоты, обеспечивающей совместную экспрессию первого и второго полипептидов;
VL является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи; и
CL является последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи.
В альтернативном варианте реализации третьего аспекта настоящего изобретения конструкция нуклеиновой кислоты может иметь одну из следующих общих структур:
VH1-L1-VH2-CH-spacer-TM-endo-coexpr-VL1-L2-VL2-CL;
VL1-L1-VL2-CL-coexpr-VH1-L2-VH2-CH-spacer-TM-endo;
VL1-L1-VL2-CL-spacer-TM-endo-coexpr-VH1-L2-VH2-CH; или
VH1-L1-VH2-CH-coexpr-VL1-L2-VL2-CL-spacer-TM-endo;
где:
VH1 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи первого связывающего домена;
L1 и L2, которые могут быть одинаковыми или разными, являются расщепляемыми линкерами;
VH2 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи второго связывающего домена;
CH является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи;
spacer является нуклеиновой кислотой, кодирующей спейсер;
TM является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен;
endo является последовательностью нуклеиновой кислоты, кодирующей эндодомен;
coexpr является последовательностью нуклеиновой кислоты, обеспечивающей совместную экспрессию первого и второго полипептидов;
VL1 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи первого связывающего домена;
VL2 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи второго связывающего домена; и
CL является последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи.
Конструкция нуклеиновой кислоты также может кодировать второй химерный антигенный рецептор с антигенсвязывающим доменом, представляющим собой доменное антитело (dAb), scFv или Fab.
Второй химерный антигенный рецептор может связываться с одним из следующих антигенов: CD19, FcRL5 и TACI.
В четвертом аспекте настоящего изобретения предложен вектор, который содержит последовательность нуклеиновой кислоты согласно второму аспекту настоящего изобретения или конструкцию нуклеиновой кислоты согласно третьему аспекту настоящего изобретения.
В пятом аспекте настоящего изобретения предложена клетка, которая экспрессирует CAR согласно первому аспекту настоящего изобретения.
Клетка может экспрессировать CAR согласно первому аспекту настоящего изобретения и второй химерный антигенный рецептор, как определено выше.
Клетка также может экспрессировать конститутивно активный рецептор цитокина.
В шестом аспекте настоящего изобретения предложен способ получения клетки согласно пятому аспекту настоящего изобретения, который включает этап введения последовательности нуклеиновой кислоты согласно второму аспекту настоящего изобретения; конструкции нуклеиновой кислоты согласно третьему аспекту настоящего изобретения или вектора согласно четвертому аспекту настоящего изобретения внутрь клетки ex vivo.
В седьмом аспекте настоящего изобретения предложена фармацевтическая композиция, которая содержит множество клеток согласно пятому аспекту настоящего изобретения в комбинации с фармацевтически приемлемым носителем, разбавителем или вспомогательным веществом.
В восьмом аспекте настоящего изобретения предложен способ лечения рака, который включает этап введения субъекту фармацевтической композиции согласно седьмому аспекту настоящего изобретения.
Рак может представлять собой множественную миелому.
В девятом аспекте настоящего изобретения предложена фармацевтическая композиция согласно седьмому аспекту настоящего изобретения для применения в лечении рака.
В десятом аспекте настоящего изобретения предложено применение клетки согласно пятому аспекту настоящего изобретения в производстве фармацевтической композиции для лечения рака.
В настоящем изобретении предложены химерные антигенные рецепторы, которые демонстрируют улучшенную опосредуемую CAR передачу сигналов и более эффективное уничтожение клеток-мишеней при нацеливании на антигены, экспрессируемые с низкой плотностью на клетке-мишени. На такие антигены сложно нацеливать классические CAR, так как они формируют субоптимальные синапсы Т-клетка:клетка-мишень (Фигура 3).
Возможность нацеливания на такие антигены открывает совершенно новые возможности в области лечения рака. Многие потенциально полезные антигены-мишени рака, такие как ROR1, Tyrp-1, TACI, ALK и BCMA, имеют низкую плотность экспрессии на клетках-мишенях. В настоящем изобретении предложены усовершенствованные конструкции для воздействия на эти антигены, которые позволяют использовать их как отдельные мишени и, что важно, включать их в стратегии по нацеливанию на несколько антигенов для повышения эффективности и безопасности применения CAR-Т-клеток.
ДОПОЛНИТЕЛЬНЫЕ АСПЕКТЫ
В настоящем изобретении также предложены аспекты, кратко изложенные в пронумерованных абзацах ниже.
1. Химерный антигенный рецептор (CAR), который содержит антигенсвязывающий домен Fab, содержащий первый связывающий домен, который связывается с первым антигеном-мишенью, и второй связывающий домен, который связывается со вторым антигеном-мишенью.
2. CAR согласно абзацу 1, который содержит расщепляемый линкер между первым и вторым связывающими доменами.
3. CAR согласно абзацу 2, отличающийся тем, что линкер может расщепляться матриксной металлопротеиназой (MMP).
4. CAR согласно любому из предыдущих абзацев, отличающийся тем, что первый антиген-мишень экспрессируется в области опухоли, поэтому когда экспрессирующую CAR клетку вводят пациенту, имеющему рак, происходит хоуминг указанной клетки в область опухоли в организме субъекта.
5. CAR согласно любому из предыдущих абзацев, отличающийся тем, что второй антиген-мишень экспрессируется в области опухоли, а также в одной или нескольких нормальных тканях.
6. CAR согласно любому из предыдущих абзацев, отличающийся тем, что первый и/или второй антиген-мишень выбран из следующей группы: BCMA, ROR1, Tyrp-1, TACI, ALK, ErbB2, MUC1, CD33, CD123, PSMA, EpCAM, GD2, NCAM, белок, связывающий фолаты и MUC16.
7. CAR согласно любому из абзацев 1-5, отличающийся тем, что первый антиген-мишень/второй антиген-мишень выбраны из одной из следующих пар антигенов: ErbB2 и MUC1; CD33 и CD123; PSMA и EpCAM; GD2 и NCAM; белок, связывающий фолаты и MUC16.
8. CAR согласно абзацу 7, отличающийся тем, что первый антиген-мишень/второй антиген-мишень являются одной из пар антигенов, представленных в Таблице 2.
9. Последовательность нуклеиновой кислоты, которая кодирует CAR согласно любому из предыдущих абзацев.
10. Конструкция нуклеиновой кислоты, которая кодирует CAR согласно любому из абзацев 1-8 и имеет одну из следующих общих структур:
VH1-L1-VH2-CH-spacer-TM-endo-coexpr-VL1-L2-VL2-CL;
VL1-L1-VL2-CL-coexpr-VH1-L2-VH2-CH-spacer-TM-endo;
VL1-L1-VL2-CL-spacer-TM-endo-coexpr-VH1-L2-VH2-CH; или
VH1-L1-VH2-CH-coexpr-VL1-L2-VL2-CL-spacer-TM-endo,
где:
VH1 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи первого связывающего домена;
L1 и L2, которые могут быть одинаковыми или разными, являются расщепляемыми линкерами;
VH2 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи второго связывающего домена;
CH является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи;
spacer является нуклеиновой кислотой, кодирующей спейсер;
TM является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен;
endo является последовательностью нуклеиновой кислоты, кодирующей эндодомен;
coexpr является последовательностью нуклеиновой кислоты, обеспечивающей совместную экспрессию первого и второго полипептидов;
VL1 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи первого связывающего домена;
VL2 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи второго связывающего домена; и
CL является последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи.
11. Вектор, который содержит последовательность нуклеиновой кислоты согласно абзацу 9 или конструкцию нуклеиновой кислоты согласно абзацу 10.
12. Клетка, которая экспрессирует CAR согласно любому из абзацев 1-8.
13. Способ получения клетки согласно абзацу 12, который включает этап введения последовательности нуклеиновой кислоты согласно абзацу 9; конструкции нуклеиновой кислоты согласно абзацу 10 или вектора согласно абзацу 11 внутрь клетки ex vivo.
14. Фармацевтическая композиция, которая содержит множество клеток согласно абзацу 12 в комбинации с фармацевтически приемлемым носителем, разбавителем или вспомогательным веществом.
15. Способ лечения рака, который включает этап введения субъекту фармацевтической композиции согласно абзацу 14.
16. Фармацевтическая композиция согласно абзацу 14 для применения в лечении рака.
17. Применение клетки согласно абзацу 12 в производстве фармацевтической композиции для лечения рака.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ
Настоящее изобретение относится к химерному антигенному рецептору с антигенсвязывающим доменом Fab.
Классический химерный антигенный рецептор (CAR) является химерным трансмембранным белком I типа, который соединяет внеклеточный антигенраспознающий домен (связывающий элемент) с внутриклеточным сигнальным доменом (эндодомен). Связывающий элемент обычно является одноцепочечным вариабельным фрагментом (scFv), полученным из моноклонального антитела (МАТ), но в его основе могут быть другие форматы, содержащие антителоподобный антигенсвязывающий сайт. Спейсерный домен обычно необходим для изоляции связывающего элемента от мембраны для обеспечения его подходящей ориентации. В качестве спейсерного домена обычно используют Fc-фрагмент иммуноглобулина G1 (IgG1). В зависимости от антигена, могут подойти более компактные спейсеры, напр., «ствол» CD8α и даже только изолированная шарнирная область IgG1. Трансмембранный домен заякоривает белок в мембране клетки и соединяет спейсер с эндодоменом.
В ранних вариантах дизайна CAR эндодомены получали из внутриклеточных фрагментов γ-цепи FcεR1 или CD3ζ. Следовательно, эти рецепторы первого поколения передавали иммунологический сигнал 1, который был достаточен для запуска уничтожения когнатных клеток-мишеней Т-клетками, но не обеспечивал полную активацию Т-клеток, необходимую для их пролиферации и выживания. Для преодоления этого ограничения были разработаны составные эндодомены: слияние внутриклеточной части костимулирующей молекулы Т-клетки с таким же фрагментом CD3ζ легло в основу рецепторов второго поколения, которые после распознавания антигена могут одновременно передавать активирующий и костимулирующий сигналы. В качестве костимулирующего домена наиболее часто используют домен CD28. Это обеспечивает наиболее мощный костимулирующий сигнал, а именно иммунологический сигнал 2, который запускает пролиферацию Т-клеток. Также были описаны несколько рецепторов, которые содержат эндодомены семейства рецепторов фактора некроза опухоли (ФНО), такие как близкородственные OX40 и 41BB, которые передают сигналы выживания. На сегодняшний день описаны еще более мощные CAR третьего поколения, эндодомены которых способны передавать сигналы активации, пролиферации и выживания.
Когда CAR связывается с антигеном-мишенью, это приводит к передаче активирующего сигнала в Т-клетку, на которой он экспрессирован. Таким образом CAR обеспечивает специфичность и цитотоксичность Т-клетки в отношении клеток опухоли, экспрессирующих антиген-мишень.
Поэтому CAR обычно содержат: (i) антигенсвязывающий домен; (ii) спейсер; (iii) трансмембранный домен и (iii) внутриклеточный домен, который содержит сигнальный домен или связан с ним.
CAR может иметь общую структуру:
Антигенсвязывающий домен - спейсер - трансмембранный домен - внутриклеточный сигнальный домен (эндодомен).
Антигенсвязывающий домен
Антигенсвязывающий домен является частью химерного рецептора, распознающей антиген. В классическом CAR антигенсвязывающий домен содержит: одноцепочечный вариабельный фрагмент (scFv), полученный из моноклонального антитела (см. Фигуру 2с). Также были получены CAR с антигенсвязывающими доменами на основе доменного антитела (dAb) или VHH (см. Фигуру 2b).
В химерных антигенных рецепторах, предложенных в настоящем изобретении, антигенсвязывающий домен содержит Fab-фрагмент или, например, моноклональное антитело (см. Фигуру 2а). FabCAR содержит две цепи: одна из которых имеет антителоподобные вариабельную область (VL) и константную область (CL) легкой цепи; и вторая имеет вариабельную область (VH) и константную область (CH) тяжелой цепи. Одна цепь также содержит трансмембранный домен и внутриклеточный сигнальный домен. Ассоциация между CL и CH приводит к сборке рецептора.
Две цепи Fab CAR могут иметь общую структуру:
VH - CH - спейсер - трансмембранный домен - внутриклеточный сигнальный домен и
VL - CL
или
VL - CL - спейсер - трансмембранный домен - внутриклеточный сигнальный домен и
VH - CH
Для описанных в настоящей заявке химерных рецепторов типа Fab антигенсвязывающий домен состоит из VH одной полипептидной цепи и VL другой полипептидной цепи.
Полипептидные цепи могут содержать линкер между VH/VL доменом и CH/CL доменами. Линкер может быть гибким и обеспечивать пространственную сепарацию VH/VL домена от CH/CL доменов.
Гибкие линкеры могут состоять из небольших неполярных остатков, таких как глицин, треонин и серин. Линкер может содержать один или более повторов глицин-серинового линкера, такого как линкер (Gly4Ser)n (SEQ ID NO: 78), где n обозначает количество повторов. Такой или каждый линкер может иметь длину менее 50, 40, 30, 20 или 10 аминокислот.
В настоящем изобретении также предложены расщепляемые FabCAR, которые содержат первый антигенсвязывающий домен, связывающий первый антиген-мишень, и второй связывающий домен, связывающий второй антиген-мишень. Такой расщепляемый Fab CAR схематично изображен на Фигуре 9.
Расщепляемый Fab CAR может содержать расщепляемый линкер между первым и вторым связывающими доменами.
Две цепи расщепляемого Fab CAR могут иметь общую структуру:
VH1 - VH2 - CH - спейсер - трансмембранный домен - внутриклеточный сигнальный домен и
VL1 - VL2 - CL
или
VL1 - CL1 - спейсер - трансмембранный домен - внутриклеточный сигнальный домен и
VH2 - CH2
Для расщепляемого FabCAR характерна сниженная доступность проксимального к мембране связывающего домена (связывающего домена 2 на Фигуре 9) без расщепления за счет стерического препятствия из-за первого связывающего домена. После расщепления удаление связывающего домена 1 увеличивает доступность связывающего домена 2, что позволяет ему активироваться в присутствии своего антигена-мишени.
Расщепляемый линкер может расщепляться агентом, таким как малая молекула или фермент, например, протеаза. Агент можно вводить пациенту для расщепления линкера и активации или усиления передачи сигналов посредством второго связывающего домена. В качестве альтернативы, расщепляющий агент может естественным образом экспрессироваться in vivo, например, в области воспаления или роста опухоли/метастаза.
Матриксные металлопротеиназы (MMP) представляют собой группу ферментов, ответственных за расщепление большинства белков внеклеточного матрикса в процессе органогенеза и роста. Экспрессия и активность MMP в тканях взрослых обычно низкая, но значительно повышается при разных патологических состояниях, в том числе при воспалении и раке.
MMP являются кальций-зависимыми цинкосодержащими эндопептидазами с общей доменной структурой. Тремя общими доменами являются пропептид, каталитический домен и гемопексиноподобный С-концевой домен, который связан с каталитическим доменом гибкой шарнирной областью.
MMP присутствуют практически во всех типах рака человека; они могут экспрессироваться фибробластами прилегающей стромы, раково-ассоциированными фибробластами и/или отличными от фибробластов раковыми клетками. Таким образом, MMP могут оказывать влияние на окружение опухоли путем стимуляции ангиогенеза, роста опухоли и метастазирования. Соответственно, экспрессия MMP связана с агрессивностью и стадией опухоли, и с прогнозом для пациента.
Повышенная экспрессия MMP коррелирует с увеличенной пролиферацией раковых клеток и увеличением размера опухоли. Нарушения регуляции при разных типах рака человека было показано почти для каждого члена семейства MMP, наиболее часто этому подвержены MMP-1,-2,-7,-9,-13 и -14.
В расщепляемом FabCAR, предложенном в настоящем изобретении, линкер между первым и вторым антигенсвязывающими доменами может расщепляться MMP, в частности MMP, выбранной из MMP-1,-2,-7,-9,-13 и -14.
Известны различные последовательности, которые расщепляются ферментами MMP, например:
MMP-1: PLGLWA (SEQ ID NO: 85)
MMP-2: PAGLAG (SEQ ID NO: 86)
MMP-9: PLGLAG (SEQ ID NO: 87)
Последовательность расщепляемого линкера предложенного в настоящем изобретении расщепляемого FabCAR может содержать одну из последовательностей, представленных как SEQ ID NO: 85-87.
ДОМЕНЫ КОНСТАНТНОЙ ОБЛАСТИ
У человека существуют легкие цепи двух типов: каппа (κ) цепь и лямбда (λ) цепь. В тип лямбда входит 4 подтипа: λ1, λ2, λ3 и λ4. Константная область легкой цепи химерного рецептора типа Fab может быть получена из легкой цепи любого из этих типов.
Константная область легкой цепи химерного рецептора, предложенного в настоящем изобретении, может иметь последовательность SEQ ID NO: 1, которая является константным доменом каппа-цепи.
SEQ ID NO: 1
TVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
Существует пять типов тяжелых цепей иммуноглобулинов млекопитающих: γ, δ, α, μ и ε, которые определяют классы иммуноглобулинов IgG, IgD, IgA, IgM и IgE соответственно. Тяжелые цепи γ, δ и α имеют константный домен, состоящий из трех тандемных доменов Ig, и имеют шарнир участок для дополнительной гибкости. Тяжелые цепи μ и ε состоят из четырех доменов.
CH домен химерного рецептора типа Fab, предложенного в настоящем изобретении, может содержать последовательность SEQ ID NO: 2, которая получена из тяжелой γ-цепи иммуноглобулина.
SEQ ID NO: 2
STKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRV
СПЕЙСЕР
Классический CAR содержит спейсерную последовательность для соединения антигенсвязывающего домена с трансмембранным доменом и для пространственной сепарации антигенсвязывающего домена от эндодомена. Гибкий спейсер позволяет антигенсвязывающему домену располагаться в разных направлениях для облегчения связывания.
В FabCAR (Фигура 2а), как и в классическом химерном антигенном рецепторе (Фигура 2с) и в dAbCAR (Фигура 2С), спейсер может вызывать димеризацию двух полипептидных цепей. Две из полипептидных цепей могут содержать, например, один или более остатков цистеина для формирования дисульфидного мостика(ов). В этом отношении шарнирная область из IgG1 стабильна. Спейсер на основе шарнирной области IgG1 может иметь последовательность, представленную как SEQ ID. NO: 3.
SEQ ID NO: 3 (шарнирная область IgG1 человека):
AEPKSPDKTHTCPPCPKDPK
В качестве альтернативы, шарнирный спейсер может иметь последовательность SEQ ID. NO: 4.
SEQ ID NO: 4 (шарнирный спейсер)
EPKSCDKTHTCPPCP
ТРАНСМЕМБРАННЫЙ ДОМЕН
Трансмембранный домен является частью химерного рецептора, которая проходит через мембрану. Трансмембранный домен может иметь любую структуру белка, которая термодинамически стабильна в мембране. Обычно он является альфа-спиралью, содержащей несколько гидрофобных остатков. Трансмембранный домен любого трансмембранного белка можно использовать для обеспечения трансмембранной части химерного рецептора. Специалисты в данной области могут определить наличие трансмембранного домена белка и число прохождений через мембрану с помощью алгоритма TMHMM (http://www.cbs.dtu.dk/services/TMHMM-2.0/). В качестве альтернативы можно применять искусственно сконструированный трансмембранный (ТМ) домен.
ЭНДОДОМЕН
Эндодомен является частью химерного рецептора, передающей сигнал. Он может быть частью внутриклеточного домена химерного рецептора или может быть ассоциирован с ним. После распознавания антигена рецепторы группируются в кластеры, нативные CD45 и CD148 исключаются из синапса, и сигнал передается в клетку. Наиболее часто в качестве компонента-эндодомена используют эндодомен CD3-зета, который содержит 3 тирозиновых активирующих мотива иммунорецептора (ITAM). Он передает сигнал активации в Т-клетку после связывания антигена. CD3-зета может не обеспечивать полноценный сигнал активации, поэтому могут потребоваться дополнительные костимулирующие сигналы. Костимулирующие сигналы стимулируют пролиферацию и выживание Т-клеток. Существует два основных типа костимулирующих сигналов: принадлежащие семейству Ig (CD28, ICOS) и принадлежащие семейству ФНО (OX40, 41BB, CD27, GITR и др.). Например, химерные CD28 и OX40 можно применять с CD3-зета для передачи сигнала пролиферации/выживания, либо все три можно применять вместе.
Эндодомен может содержать:
(i) эндодомен, содержащий ITAM, такой как эндодомен из CD3-зета; и/или
(ii) костимулирующий эндодомен, такой как эндодомен из CD28 или ICOS; и/или
(iii) домен, который передает сигнал выживания, например, эндодомен семейства рецепторов ФНО, таких как OX-40, 4-1BB, CD27 или GITR.
Описано несколько систем, в которых часть, распознающая антиген, расположена не на части, передающей сигнал, а на отдельной молекуле, такие системы описаны в WO015/150771; WO2016/124930 и WO2016/030691. Таким образом, химерный рецептор, предложенный в настоящем изобретении, может содержать антигенсвязывающий компонент, содержащий антигенсвязывающий домен и трансмембранный домен; которые способны взаимодействовать с отдельным внутриклеточным сигнальным компонентом, содержащим сигнальный домен. Предложенный в настоящем изобретении вектор может экспрессировать сигнальную систему химерного рецептора, содержащую такой антигенсвязывающий компонент и внутриклеточный сигнальный компонент.
Химерный рецептор может содержать сигнальный пептид, поэтому когда он экспрессируется внутри клетки образующийся белок направляется в эндоплазматический ретикулум и, впоследствии, к поверхности клетки, в которой он экспрессируется. Сигнальный пептид может располагаться на аминоконце молекулы.
АНТИГЕН-МИШЕНЬ
«Антиген-мишень» является единицей, которая специфично распознается и связывается антигенсвязывающим доменом химерного рецептора, предложенного в настоящем изобретении.
Антиген-мишень может являться антигеном, присутствующим на раковой клетке, например, опухолеассоциированным антигеном.
Антиген-мишень для CAR может экспрессироваться на клетке-мишени с относительно низкой плотностью.
Клетка, предложенная в настоящем изобретении, может обладать способностью убивать клетки-мишени, такие как раковые клетки, которые имеют низкую плотность экспрессии антигена-мишени CAR. К примерам известных опухолеассоциированных антигенов, которые имеют низкую плотность экспрессии при определенных типах рака относятся, но не ограничиваются перечисленным, ROR1 при ХЛЛ, Typr-1 при меланоме, BCMA и TACI при миеломе и ALK при нейробластоме.
В Примере 1 описано исследование, в котором изучали экспрессию BCMA на клетках меланомы. Было установлено, что диапазон количества копий BCMA на поверхности клетки меланомы является низким: 348,7-4268,4 копий BCMA на клетку, со средним значением 1181 и медианой 1084,9 (Фигура 1).
Среднее количество копий антигена-мишени для CAR может быть меньше, чем приблизительно 10000; 5000; 3000; 2000; 1000 или 500 копий на клетку-мишень.
Среднее количество копий антигена на клетке, такой как раковая клетка, можно оценивать стандартными техниками, такими как применение меченных фикоэритрином (ФЭ) гранул Quantibrite, как описано в Примере 1.
Антиген-мишень для CAR может экспрессироваться на клетке-мишени со средним количеством копий 1500 копий на клетку или менее, либо 1000 копий на клетку или менее.
Антиген-мишень может, например, являться BCMA, ROR1, Tyrp-1, TACI или ALK.
BCMA
Мишень созревания В-клеток, также известная как BCMA; TR17_HUMAN, TNFRSF17 (UniProt Q02223) является трансмембранным белком, который экспрессируется зрелыми лимфоцитами, например, В-клетками памяти, плазмобластами и плазматическими клетками костного мозга. BCMA также экспрессируется на клетках миеломы. BCMA является негликозилированным трансмембранным белком III типа, который вовлечен в созревание, рост и выживание В-клеток.
Антигенсвязывающий домен CAR или TanCAR, который связывается с BCMA, может быть любым доменом, способным связываться с BCMA. Последовательности VH для VL четырнадцати антител против BCMA указаны ниже, последовательности участков, определяющих комплементарность (CDR), выделены жирным шрифтом с подчеркиванием.
SEQ ID NO: 5 (VH АТ 1 против BCMA)
QIQLVQSGPELVKPGSSVKLSCKTSGFTFSDSYMSWLKQVPGQSIEWIGNIYAGDGATHYHQKFKGKATLTVDTSSSTAYMDLSSLTSEDSALYFCARPLYTTAYYYVGGFAYWGQGTLVTVSS
SEQ ID NO: 6 (VL АТ 1 против BCMA)
DIVMTQSPSSLAVSAGETVTINCKSSQSLLSSGNQKNYLAWYQQKPGQSPKLLIYWASTRQSGVPDRFIGSGSGTDFTLTISSVQAEDLAIYYCQQYYDTPLTFGSGTKLEIK
SEQ ID NO: 7 (VH АТ 2 против BCMA)
EVKLVESGGGLVQPGRSLKLSCTASGFTFSNYDMAWVRQAPTKGLEWVASISTSGDTIYYRDSVKGRFTVSRDKAKSTLYLQMDSLRSEDTATYYCARHDYYDGYQSFAYWGQGTLVTVSS
SEQ ID NO: 8 (VL АТ 2 против BCMA)
NTVMTQSPTSMSISVGDRVTMNCKASQNVGNNIAWYQQKPGQSPKLLIYYASNRYTGVPDRFTGSGSGTDFTLTINSVQAEDAAFYYCQRIYNSALTFGSGTKLEIK
SEQ ID NO: 9 (VH АТ 3 против BCMA)
QVQLQQSGAALVKPGASVKMSCKASGYTFTDYWVSWVKQSHGKSLEWIGEIYPNSGPTNFNKKFKGKATLTVDKSTSTAYMELSRLTSEDSAIYYCTPRTVAPYNWFAYWGQGTLVTVSS
SEQ ID NO: 10 (VL АТ 3 против BCMA)
DIVLTQSPALAVSPGERVSISCRASESVSTRMHWYQQKPGQQPKLLIYGASNLESGVPARFSGSGSGTDFTLTIDPVEADDTATYFCQQSWNDPYTFGAGTKLELK
SEQ ID NO: 11 (VH АТ 4 против BCMA)
EVQLVESGGGLVQPGRSLKLSCSASGFIFSNFDMAWVRQAPRKGLEWVASITTSGGDTHYRDSVKGRFTVSRHNAKSTLYLQMDSLRSEDTATYYCARHVYYGLFWFFDFWGPGTMVTVSS
SEQ ID NO: 12 (VL АТ 4 против BCMA)
NTVMTQSPKSIFISVGDRVTVNCKASQNVGTNVDWYQQKTGQSPKLLIYGASNRYTGVPDRFTGSGSGTDFTFTISNMQAEDLAVYYCMQSNTNPFTFGAGTKLELKR
SEQ ID NO: 13 (VH АТ 5 против BCMA)
EVQLVESGGGLVQPGRSLKLSCTASGFTFSNYDMAWVRQAPTKGLEWVASISTSGDTIYYRDSVKGRFTVSRDKAKSTLYLQMDSLRSEDTATYYCARHDYYDGYQSFAYWGQGTLVTVSS
SEQ ID NO: 14 (VL АТ 5 против BCMA)
DIVMTQSPSTLPASLGERVTISCRASQSISNYLNWYQQKPDGTIKPLIYYTSNLQSGVPSRFSGSGSGTDYSLTISSLEPEDFAMYYCQQDASFPWTFGGGTKLELKR
SEQ ID NO: 15 (VH АТ 6 против BCMA)
EVQLQESGPGLVKPSQSLSLTCSVTGYPITNNYDWSWIRQFPGNKMEWMGYISDSGNTNYNPSLKSRISITRDTSKNQFFLQLNSVTTEDTATYYCASGYISYIPFAFWGQGTLVTVSS
SEQ ID NO: 16 (VL АТ 6 против BCMA)
DIVLTQSPALAVSLGQRATISCRASQSVSISSYNLMQWYQQKPGQQPKLLIYDASNLASGIPARFSGSGSGTDFTLTIDPVQADDIATYYCQQSKDDPNTFGAGTKLEIKR
SEQ ID NO: 17 (VH АТ 7 против BCMA)
EVQLQESGPGLVQPSQTLSLTCSVTGYPITNNYDWSWIRKFPGNKMEWMGYISDSGSTNYNPSLKSRISITRDTSKNQFFLQLNSVTTEDTATYYCASGYISYIPFGFWGQGTLVTVSS
SEQ ID NO: 18 (VL АТ 7 против BCMA)
DIVLTQSPALAVSPGERVTISCRASESVSTRMHWYQQKPGQQPKLLIYGASNLESGVPARFSGSGSGTDFTLTIDPVEADDTATYFCQQSWNDPPTFGSGTKLEIK
SEQ ID NO: 19 (VH АТ 8 против BCMA)
EVQLVESGGGLVQPGRSLKLSCTASGFTFSNYDMAWVRQAPTKGLEWVASISTSGDTIYYRDSVKGRFTVSRDKAKSTLYLQMDSLRSEDTATYYCARHDYYDGYQSFAYWGQGTLVTVSS
SEQ ID NO: 20 (VL АТ 8 против BCMA)
DIVMTQSPASQAVSAGEKVTMSCKSSQSLLYSGDQKNYLAWYQQKPGQSPKLLIYLASTRESGVPDRFIGSGSGTDFTLTISSVQAEDLADYYCQQHYSYPLTFGSGTKLEIK
SEQ ID NO: 21 (VH АТ 9 против BCMA)
EVQLVESGGGLVQPGRSLKLSCAASGFTFSNYDMAWVRQAPTKGLEWVASISTSGDTIYYRDSVKGRFTVSRDNAKSTLYLQMDSLRSEDTATYYCTRHGYYDGYQSFDYWGQGTLVTVSS
SEQ ID NO: 22 (VL АТ 9 против BCMA)
NTVMTQSPKSMSISVGDRVTMNCKASQNVGNNIAWYQQKPGQSPKLLIYYASNRYTGVPDRFTGGGYGTDFTLTINSVQAEDAATYYCQQWNYPSITFGSGTKLEIK
SEQ ID NO: 23 (VH АТ 10 против BCMA)
EVQLVESGGGLVQPGRSMKLSCAASGFTFSNYDMAWVRQAPTKGLEWVASISPSGGSTYYRDSVKGRFTVSRDNAKSSLYLQMDSLRSEDTATYYCTRGDYGYNYAYWFAYWGQGTLVTVSS
SEQ ID NO: 24 (VL АТ 10 против BCMA)
DIVMTQAPSSMPASLGERVTISCRASQGISNYLNWYQQKPDGTIKPLIYYTSNLQSGVPSRFSGSGSGTDYSLTISSLEPEDFAMYYCQQYDSSPLTFGAGTKLELK
SEQ ID NO: 25 (VH АТ 11 против BCMA)
EVQLVESGGGLVQPGRSLKLSCEASGFTFSNYDMAWVRQAPTKGLEWVASISTSGDSIYYRDSVKGRFTVSRDNVKSTLYLQMDSLRSEDTATYYCARHGYYDGYQSFDYWGQGTLVTVSS
SEQ ID NO: 26 (VL АТ 12 против BCMA)
DIVMTQSPSSLPASLGERVTISCRASQGISNNLNWYQQKPDGTIKPLIYYTSNLQSGVPSRFSGSGSGTDYSLTISSLEPEDFATYYCQQDETFPYTFGAGTKLELK
SEQ ID NO: 27 (VH АТ 13 против BCMA)
EVQLVESGGGLVQPGRSLKLSCAASGFTFSNYDMAWVRQAPTKGLEWVASISPSGGSTYYRDSVKGRFTISRDNAKSTLYLQMDSLRSEDTATYYCATHNYYDGSSLFAYWGQGTLVTVSS
SEQ ID NO: 28 (VL АТ 13 против BCMA)
DIVLTQSPALAVSPGERVTISCGANETVSTLVHWYQQKPGQQPKLLIYLASHLESGVPARFSGSGSGTDFTLTIDPVEADDTATYYCQQSWNDPPTFGGGTKLELK
SEQ ID NO: 29 (VH АТ 14 против BCMA)
EVQLVESGGGLVQPGRSLKLSCAASGFIFSDYNMAWVRQAPKKGLEWVATIIYDGSSTNHGDSVKGRFTISRDNAKSTLYLQMDSLRSEDTATYYCATRPGPFAYWGQGTLVTVS
SEQ ID NO: 30 (VL АТ 15 против BCMA)
DVVLTQTPPTLSATIGQSVSISCRSSQSLLHSNGNTYLHWLLQRPGQSPQFLIYLVSGLGSGVPNRFSGSGSGTDFTLKISGVEAEDLGIYYCVHGTHAWTVGGGTKLELK
Антигенсвязывающий домен CAR, связывающийся с BCMA, может содержать CDR из любого АТ 1-14 против BCMA, как описано выше.
Антигенсвязывающий домен CAR, связывающийся с BCMA, может содержать последовательность VH и/или VL из любого АТ 1-14 против BCMA, как описано выше, либо вариант этой последовательности, который имеет по меньшей мере 70, 80, 90 или 90 % идентичности с последовательностью, указанный вариант сохраняет способность связываться с BCMA.
В настоящем изобретении также предложены новые BCMA-связывающие антитела, обозначенные как АТ 1-14. Последовательности VH, VL и CDR АТ 1-14 указаны в или как SEQ ID NO: 5-30 выше.
BCMA-связывающее антитело АТ 1 демонстрирует особенно высокую эффективность в формате CAR. Например, АТ 1 в формате scFv CAR продемонстрировало улучшенное уничтожение клеток-мишеней, высвобождение ИЛ-2 и пролиферацию по сравнению с разными эквивалентными CAR с альтернативными BCMA-связывающими доменами (данные не предоставлены).
В настоящем изобретении также предложены аспекты, кратко изложенные в пронумерованных абзацах ниже.
1. Антигенсвязывающий домен, который содержит:
a) вариабельную область тяжелой цепи (VH), имеющую участки, определяющие комплементарность (CDR), с последовательностями, указанными в SEQ ID NO: 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27 или 29; и
b) вариабельную область легкой цепи (VL), имеющую участки, определяющие комплементарность (CDR), с последовательностями, указанными в SEQ ID NO: 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28 или 30.
2. Антигенсвязывающий домен, согласно абзацу 1, который содержит:
a) вариабельную область тяжелой цепи (VH), имеющую участки, определяющие комплементарность (CDR), со следующими последовательностями:
CDR1 - GFTFSDSY (SEQ ID NO: 68)
CDR2 - IYAGDGAT (SEQ ID NO: 69)
CDR3 - ARPLYTTAYYYVGGFAY (SEQ ID NO: 70) и
b) вариабельную область легкой цепи (VL), имеющую участки, определяющие комплементарность (CDR), со следующими последовательностями:
CDR1 - QSLLSSGNQKNY (SEQ ID NO: 71)
CDR2 - WAS (SEQ ID NO: 72)
CDR3 - QQYYDTPLT (SEQ ID NO: 73)
3. Антигенсвязывающий домен, согласно абзацу 1, который содержит:
a) вариабельную область тяжелой цепи (VH), имеющую участки, определяющие комплементарность (CDR), со следующими последовательностями:
CDR1 - GFIFSDYN (SEQ ID NO: 79)
CDR2 - IIYDGSST (SEQ ID NO: 80)
CDR3 - ATRPGPFAY (SEQ ID NO: 81) и
b) вариабельную область легкой цепи (VL), имеющую участки, определяющие комплементарность (CDR), со следующими последовательностями:
CDR1 - QSLLHSNGNTY (SEQ ID NO: 82)
CDR2 - LVS (SEQ ID NO: 83)
CDR3 - VHGTHAWT (SEQ ID NO: 84)
4. Антигенсвязывающий домен согласно абзацу 1, который содержит домен VH, имеющий одну из последовательностей SEQ ID NO: 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27 или 29; и домен VL, имеющий одну из последовательностей SEQ ID NO: 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28 или 30.
5. Антигенсвязывающий домен согласно абзацу 3, который содержит домен VH, имеющий последовательность SEQ ID NO: 5; и домен VL, имеющий последовательность SEQ ID NO: 6.
6. Антигенсвязывающий домен согласно абзацу 3, который содержит домен VH, имеющий последовательность SEQ ID NO: 29; и домен VL, имеющий последовательность SEQ ID NO: 30.
7. Антитело, которое содержит антигенсвязывающий домен согласно любому из предыдущих абзацев.
8. Конъюгат антитело-лекарственное средство (ADC) или биспецифичный рекрутер T-клеток (BiTE), который содержит антитело согласно абзацу 7.
9. Химерный антигенный рецептор (CAR), который содержит антигенсвязывающий домен согласно любому из абзацев 1-6.
10. CAR согласно абзацу 9, который является FabCAR.
11. Последовательность нуклеиновой кислоты, которая кодирует антигенсвязывающий домен согласно любому из абзацев 1-6, и антитело согласно абзацу 6, ADC или BiTE согласно абзацу 8 или CAR согласно абзацу 9 или 10.
12. Вектор, который содержит последовательность нуклеиновой кислоты согласно абзацу 11.
13. Клетка, которая экспрессирует CAR согласно абзацу 9 или 10.
14. Способ получения клетки согласно абзацу 13, который включает этап введения кодирующей CAR последовательности нуклеиновой кислоты согласно абзацу 11 в клетку.
15. Фармацевтическая композиция, которая содержит множество клеток согласно абзацу 13 совместно с фармацевтически приемлемым носителем, разбавителем или вспомогательным веществом.
16. Способ лечения рака, который включает этап введения субъекту фармацевтической композиции согласно абзацу 15.
17. Способ согласно абзацу 15, где рак является В-клеточным лейкозом или лимфомой.
18. Клетка согласно абзацу 13 для применения в лечении рака.
19. Применение клетки согласно абзацу 13 в производстве фармацевтической композиции для лечения рака.
Общие характеристики, например, химерных антигенных рецепторов, последовательностей и конструкций нуклеиновой кислоты, векторов, клеток, фармацевтических композиций и способов получения и применения клеток, описанных в предшествующем и следующем разделах, также распространяются на соответствующие компоненты, описанные в приведенных выше абзацах.
ROR1
Орфанный рецептор типа рецепторной тирозинкиназы-1 (ROR1), также известный как рецепторная нейротрофическая тирозинкиназа 1 (NTRKR1), является рецепторной тирозинкиназой, модулирующей рост аксонов в центральной нервной системе. Он представляет собой мембранный белок I типа и принадлежит к подсемейству ROR рецепторов клеточной поверхности.
Экспрессия ROR1 была показана на стволовых клетках рака яичников, на которых он, судя по всему, играет функциональную роль в стимуляции миграции/инвазии или формирования сфероидов in vitro и приживления опухоли у мышей с иммунодефицитом. Лечение гуманизированными МАТ, специфичными к ROR1, может подавлять способность клеток рака яичников к миграции, формированию сфероидов или приживлению у мышей с иммунодефицитом.
В WO2017/072361 описано несколько специфичных к ROR1 антител, пригодных для применения при создании CAR.
TACI
Трансмебранный активатор, а также партнер модулятора кальция и лиганда циклофилина (CAML) TACI (UniProtKB: O14836) является регулятором иммунных реакций и, также как BCMA, преимущественно экспрессируется зрелыми лимфоцитами, такими как CD27+ В-клетки памяти, в особенности В-клетками краевой зоны, плазматическими клетками костного мозга и клетками миеломы.
Помимо этого TACI экспрессируется на макрофагах и опосредует выживание макрофагов. TACI является специфичным для лимфоцитов членом суперсемейства рецепторов фактора некроза опухоли (ФНО), также известным как член 13В суперсемейства рецепторов фактора некроза опухоли (TNFRSF13B), он может отделяться с поверхности клетки и циркулировать в виде растворимой формы. В отличие от BCMA, TACI практически отсутствует в В-клетках зародышевого центра. Известно, что TACI функционирует как рецептор TNFSF13/APRIL и TNFSF13B/BAFF и связывается с обоими лигандами с высокой аффинностью. TACI ингибирует экспансию В-клеток и стимулирует дифференцировку и выживание плазматических клеток.
TACI является членом суперсемейства рецепторов фактора некроза опухоли (TNFR) и служит ключевым регулятором функции В-клеток. TACI с высокой аффиностью связывается с двумя лигандами, APRIL и BAFF, и его внеклеточная область содержит два богатых цистеином домена (CRD). Однако существует другая форма TACI, в которой CRD на N-конце удален в результате альтернативного сплайсинга. Было показано, что эта более короткая форма способна к индуцированной лигандом передаче сигнала, и что второй CRD (TACI_d2) сам обладает полноценной аффинностью к обоим лигандам (Hymowitz et al 2005 Am Soc. Biochem. And Mol. Biol. Inc 280(8) 7218-7227).
Структура кристаллаTACI_d2 была расшифрована одновременно со структурой сокристаллов комплексов APRILTACI_d2 и APRIL BCMA (Hymowitz и соавт. 2005, как указано выше).
CRD TACI и CRD других TNFR имеют общую особенность последовательности, так называемый мотив DXL, который состоит из консервативной последовательности из 6 остатков (Phe/Tyr/Trp)-Asp-Xaa-Leu-(Val/Thr)-(Arg/Gly) (SEQ ID NO: 74). Этот мотив необходим для связывания APRIL или BAFF. Рецепторный мотив связывается внутри гидрофобного кармана и взаимодействует с двумя консервативными остатками аргинина на поверхности BAFF.
Антигенсвязывающий домен CAR или tanCAR, который связывается с TACI, может быть любым доменом, способным связываться с TACI. Например, антигенсвязывающий домен может содержать связывающийся с TACI элемент, происходящий из одного из коммерчески доступных антител против TACI, перечисленных в Таблице 1.
Таблица 1
Антигенсвязывающий домен может содержать один из связывающихся с TACI элементов клонов 2H6, 2G2, 1G6 или 4B11.
Эти связывающиеся с TACI элементы имеют следующие последовательности:
2H6
ScFv:EVQLQQSGPELVKPGASVRMSCKASGYTFTNYVMHWVKQKPGQGLEWIGYINPSNDDTKYTEKFKGKATLTSDKSSSTAYMELSSLTSEDSAVYYCARGTHGDYYALDYWGQGTSVTVSSGGGGAGGGGSGGGGSDIVLTQSPASLAVSLGQSVTISCRASESVEYYGTSLMQWYQQKPGQAPKLLIYGASNVESGVPARFSGSGSGTDFSLNIHPVEEDDIAMYFCQQSRKVPWTFGGGTKLEIKR (SEQ ID NO: 31)
CDR H1: NYVMH (SEQ ID NO: 32)
CDR H2: YINPSNDDTKYTEKFKG (SEQ ID NO: 33)
CDR H3: GTHGDYYALDY (SEQ ID NO: 34)
CDR L1: RASESVEYYGTSLMQ (SEQ ID NO: 35)
CDR L2: GASNVES (SEQ ID NO: 36)
CDR L3: QQSRKVP (SEQ ID NO: 37)
2G2
ScFv:QVTLKESGPGMLQPSQTLSLTCSFSGFSLSTFGMGVGWIRQPSGKGLEWLAHIWWDDAQYSNPALRSRLTISKDTSKNQVFLKIANVDTADTATYYCSRIHSYYSYDEGFAYWGQGTLVTVSSGGGGSGGGGSGGGGSDIVMTQSQKFMSTTVGDRVSITCKASQNVGTAVAWYQQKPGQSPKLLIYSASNRYTGVPDRFTGSGSGTDFTLTISNMQSEDLADYFCQQYSSYRTFGGGTKLEIKR (SEQ ID No. 38)
CDR H1: TFGMGVG (SEQ ID NO: 39)
CDR H2: HIWWDDAQYSNPALRS (SEQ ID NO: 40)
CDR H3: RIHSYYSYDEGFAY (SEQ ID NO: 41)
CDR L1: KASQNVGTAVA (SEQ ID NO: 42)
CDR L2: SASNRYT (SEQ ID NO: 43)
CDR L3: QQYSSY (SEQ ID NO: 44)
1G6
VH:QVQLKQSGPGLVAPSQSLSITCTVSGFSLTSYGVDWVRQSPGKGLEWLGIIWGGGRTNYNSAFKSRLSISKDNSKSQVFLKMNSLQTDDTAMYYCASGDRAADYWGQGTSVTVSS (SEQ ID No. 45)
CDR H1: SYGVD (SEQ ID NO: 47)
CDR H2: IIWGGGRTNYNSAFKS (SEQ ID NO: 48)
CDR H3: GDRAADY (SEQ ID NO: 49)
VL:DIVMTQSQKFMSTTVGDRVTITCKASQNVGTAVAWYQQKPGQSPKLLIYSASNRYTGVPVRFTGSGSGTDFTLTINNMQSEDLADYFCQQYSSYPLTFGAGTKLELK (SEQ ID No. 46)
CDR L1: KASQNVGTAVA (SEQ ID NO: 50)
CDR L2: SASNRYT (SEQ ID NO: 51)
CDR L3: QQYSSYP (SEQ ID NO: 52)
4B11
VH:EVQLQQSVAELVRPGASVKLSCTASGFNIKNTYIHWVKQRPEQGLEWIGKIDPANGNSEYAPKFQGKATITADTSSNTAYLQLSSLTSEDTTIYYCTSGYGAYWGQGTTLTVSS (SEQ ID NO: 53)
CDR H1: NTYIH (SEQ ID NO: 55)
CDR H2: KIDPANGNSEYAPKFQG (SEQ ID NO: 56)
CDR H3: GYGAY (SEQ ID NO: 57)
VL:DIVLSQSPSSLAVSIGEKVTLSCKSSQSLLYSSNQKNYLAWFQQKPGQSLKLLIYWASTREFGVPDRFTGSGSGTDFTLTISSVKTEDLAVYYCQQYYTWTFGGGTKLEIK (SEQ ID NO: 54)
CDR L1: KSSQSLLYSSNQKNYLA (SEQ ID NO: 58)
CDR L2: WASTREF (SEQ ID NO: 59)
CDR L3: QQYYTW (SEQ ID NO: 60)
В настоящем изобретении предложен агент против TACI, такой как антитело, scFv, CAR или tanCAR, который содержит TACI-связывающий домен на основе домена одного из клонов: 2H6, 2G2, 1G6 или 4B11. Агент против TACI может содержать один или более CDR с последовательностями SEQ ID NO: 32-37; 39-44; 47-52; 55-60. Агент может содержать одну из следующих групп по шесть CDR: SEQ ID NO: 32-37; SEQ ID NO: 39-44; SEQ ID NO: 47-52 и 55-60.
Агент против TACI может содержать последовательности VH и/или VL с SEQ ID NO: 31 или 38 (VH расположен перед серин-глициновым линкером, VL расположен после серин-глицинового линкера), например, в формате Fab. Агент против TACI может содержать последовательность VH SEQ ID NO: 45 или 53 и/или последовательность VL SEQ ID NO: 46 или 54, например, в формате Fab. Агент против TACI может содержать scFv, представленный в SEQ ID NO: 31 или 38 или scFv, сформированный связыванием SEQ ID NO: 45 с SEQ ID NO: 46 или SEQ ID NO: 53 с SEQ ID NO: 54.
В случае всех перечисленных выше последовательностях агент против TACI может содержать последовательность, имеющую 80, 85, 90, 95 или 98% идентичности с указанной последовательностью, при условии, что вариант последовательности сохраняет способность связываться с TACI.
Tyrp-1
Tyrp1 является специфичным для меланоцитов продуктом гена, вовлеченным в синтез меланина. Тогда как Tyrp1 мыши обладает оксидазной активностью дигидроксииндолкарбоновой кислоты, его функция в меланоцитах человека менее ясна. Помимо роли в синтезе меланина, Tyrp1 вовлечен в стабилизацию белка тирозиназы и модулирование его каталитической активности. Tyrp1 также вовлечен в поддержание структуры меланосом и оказывает влияние на пролиферацию и гибель меланоцитов.
В WO2009114585 описаны несколько антител, которые связываются с Tyrp-1. Антитела против Tyrp-1 также коммерчески доступны, например, SAB1406566 и HPA000937 от Sigma-Aldrich.
ALK
Киназа анапластической лимфомы (ALK) является рецепторной тирозинкиназой, принадлежащей к суперсемейству рецепторов инсулина. Белок включает внеклеточный домен, гидрофобный протяженный участок, соответствующий трансмембранной области, однократно проходящей через мембрану, и внутриклеточный киназный домен. Последовательности ALK человека есть в открытом доступе, например, номера доступа в GENBANK®: NP_004295 (белок) и NM_004304 (нуклеиновая кислота), и в UniProt Acc.: No Q9UM73.
В WO2015069922 описаны несколько антигенсвязывающих доменов типа scFv, которые связываются с ALK.
Антигены-мишени для расщепляемого FabCAR
Fab CAR, предложенный в настоящем изобретении, может иметь два антигенсвязывающих домена, как схематично изображено на Фигуре 9.
В расщепляемом Fab CAR, предложенном в настоящем изобретении, первый и/или второй связывающий домен может связываться с антигеном, который экспрессирован на клетке-мишени с относительно низкой плотностью. Например, он может связываться с антигеном, выбранным из ROR1, Typr-1, BCMA, TACI и ALK. В частности, антиген-мишень для второго (проксимального от мембраны) связывающего домена может быть антигеном, экспрессированным на клетке-мишени с относительно низкой плотностью.
Связывание антигена-мишени с первым (дистальным от мембраны) связывающим доменом можно применять для обеспечения направленного воздействия CAR на опухоль. Расщепление линкера в опухоли обеспечивает возможность активации посредством связывания второго антигенсвязывающего домена со вторым антигеном-мишенью, что приводит к уничтожению опухолевой клетки. Однако следует отметить, что связывание первого антигена-мишени первым связывающим доменом также может запустить уничтожение клетки, но эффективность уничтожения может быть снижена (по сравнению с уничтожением, индуцированным связыванием антигена-мишени вторым связывающим доменом) из-за неэффективного формирования синапса.
Одним из преимуществ расщепляемого FabCAR является то, что внутренний связывающий домен (т.е. второй связывающий домен) в интактной молекуле частично скрыт за счет стерического препятствия. Это может повышать безопасность в случаях, когда второй антиген-мишень в определенной степени экспрессирован в одной или более здоровых тканях, так как воздействие второго связывающего домена на его антиген-мишень будет снижено до отщепления первого связывающего момента, что не может произойти до того как экспрессирующая CAR клетка достигнет опухоли.
Поэтому второй антиген может экспрессироваться с высокой плотностью на клетках опухоли и с низкой плотностью на клетках одной или более здоровых тканей.
Антиген-мишень для первого или второго связывающих доменов может быть выбран из одного из следующих: ErbB2, MUC1, CD33, CD123, PSMA, EpCAM, GD2, NCAM, белок, связывающий фолаты и MUC16.
В частности, расщепляемый FabCAR, предложенный в настоящем изобретении, может содержать связывающие домены, направленные против одной из следующих пар антигенов-мишеней: ErbB2 и MUC1; CD33 и CD123; PSMA и EpCAM; GD2 и NCAM; белок, связывающий фолаты и MUC16. В этих парах антигенов-мишеней связывающий домен 1 и связывающий домен 2 могут связываться с любым из антигенов, например, в паре антигенов-мишеней ErbB2 и MUC1 связывающий домен 1 может связываться с ErbB2, а связывающий домен 2 может связываться с MUC1, или связывающий домен 2 может связываться с ErbB2, а связывающий домен 1 может связываться с MUC1.
В частности, расщепляемый FabCAR, предложенный в настоящем изобретении, может содержать связывающие домены, направленные против одной из пар антигенов-мишеней, перечисленных в Таблице 2.
Таблица 2
ЛОГИЧЕСКИЕ ЭЛЕМЕНТЫ «ИЛИ»
CAR, предложенные в настоящем изобретении, можно применять в комбинации с одним или более других активирующих или ингибирующих химерных антигенных рецепторов. Например, их можно использовать в комбинации с одним или более других CAR в составе «логического элемента» - комбинации CAR, которая при экспрессии в клетке, такой как Т-клетка, способна выявлять определенный паттерн экспрессии по меньшей мере двух антигенов-мишеней. Если по меньшей мере два антигена-мишени произвольно обозначить как антиген А и антиген В, три возможных варианта являются следующими:
«ЭЛЕМЕНТ ИЛИ» - Т-клетка активируется когда на клетке-мишени присутствует антиген А или антиген В
«ЭЛЕМЕНТ И» - Т-клетка активируется только когда на клетке-мишени присутствуют оба антигена А и В
«ЭЛЕМЕНТ И-НЕ» - Т-клетка активируется, если на клетке-мишени присутствует только антиген А, но не активируется, если на клетке-мишени присутствуют оба антигена А и В
Сконструированные Т-клетки, экспрессирующие эти комбинации CAR, можно адаптировать так, что они будут исключительно специфичны к раковым клеткам на основании характерной для них экспрессии (или отсутствия экспрессии) двух или более маркеров.
Такие «логические элементы» описаны, например, в WO2015/075469, WO2015/075470 и WO2015/075470.
«Элемент ИЛИ» содержит два или более активирующих CAR, каждый из которых специфичен к отдельному антигену-мишени, экспрессируемому клеткой-мишенью. Достоинством элемента ИЛИ является то, что эффективное количество антигена-мишени на клетке-мишени повышается за счет того, что фактически он представляет собой комбинацию антигена А + антигена В. Это особенно важно для антигенов, экспрессируемых на клетке-мишени с вариабельной или низкой плотностью, так как плотность одного антигена может быть ниже порога, необходимого для эффективного нацеливания CAR-Т-клетки. Также это позволяет избежать феномена ускользания антигена. Например, некоторые лимфомы и лейкозы становятся CD19-отрицательными после нацеливания на CD19: применение элемента ИЛИ, который нацелен на CD19 в комбинации с другим антигеном, обеспечивает «запасной» антиген в случае такой ситуации.
FabCAR, предложенный в настоящем изобретении, можно применять в элементе ИЛИ в комбинации со вторым CAR против второго антигена-мишени, экспрессируемого клеткой-мишенью.
Для FabCAR против BCMA элемент ИЛИ может содержать CAR против второго антигена, экспрессируемого В-клетками или плазматическими клетками, такого как CD19, TACI или FcRL5.
Второй CAR может иметь любой подходящий антигенсвязывающий домен, например, связывающий домен на основе scFv, доменного антитела (dAb) или Fab.
Элемент ИЛИ может являться двойным FabCAR. В этом отношении клетка может экспрессировать два отдельных CAR с антигенсвязывающими доменами типа Fab. FabCAR могут быть направлены против, например, BCMA и TACI или BCMA и FcRL5.
В настоящем изобретении также предложен тройной элемент ИЛИ, содержащий три CAR, по меньшей мере один из которых является FabCAR согласно первому аспекту настоящего изобретения. Тройной элемент ИЛИ может, например, содержать BCMA FabCAR, CD19 CAR и FcRL5 CAR или FabCAR.
Второй CAR может содержать спейсер для пространственной сепарации антигенсвязывающего домена от трансмембранного домена и обеспечения определенной степени гибкости. В качестве спейсеров для CAR широко применяют множество последовательностей, например, Fc-область Ig G1, шарнирная область IgG1 (как описано выше) или «ствол» CD8 человека. Спейсер может содержать суперспиральный домен, например, как описано в WO2016/151315.
Второй CAR содержит активирующий эндодомен. Он может, например, содержать эндодомен из CD3ζ. Он может содержать один или более костимулирующих доменов, как описано выше. Например, он может содержать эндодомены из CD28, OX-40 или 4-1BB.
ЭЛЕМЕНТЫ, СВЯЗЫВАЮЩИЕ CD19
Ранее было описано несколько антител против CD19 в формате CAR, например, fmc63, 4G7, SJ25C1, CAT19 (как описано в WO2016/139487) и CD19ALAb (как описано в WO2016/102965).
CAR против CD19 для применения в двойном или тройном элементе ИЛИ, предложенном в настоящем изобретении, может содержать антигенсвязывающий домен, такой как антигенсвязывающий домен типа scFv, полученный из одного из этих антител против CD19.
CD19-связывающий домен может содержать:
a) вариабельную область тяжелой цепи (VH), имеющую участки, определяющие комплементарность (CDR), со следующими последовательностями:
CDR1 - GYAFSSS (SEQ ID NO: 61);
CDR2 - YPGDED (SEQ ID NO: 62)
CDR3 - SLLYGDYLDY (SEQ ID NO: 63) и
b) вариабельную область легкой цепи (VL), имеющую CDR со следующими последовательностями:
CDR1 - SASSSVSYMH (SEQ ID NO: 64);
CDR2 - DTSKLAS (SEQ ID NO: 65)
CDR3 - QQWNINPLT (SEQ ID NO: 66).
Существует возможность введения одной или более мутаций (замен, добавлений или делеций) в каждый CDR без отрицательного влияния на способность связывания CD19. Каждый CDR может, например, содержать одну, две или три мутации аминокислот.
CDR могут быть в формате одноцепочечного вариабельного фрагмента (scFv), который является белком слияния вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL) антитела, соединенных коротким линкерным пептидом длиной от 10 до приблизительно 25 аминокислот. scFv может иметь направление VH-VL, то есть VH расположен на аминоконце молекулы CAR, и домен VL соединен со спейсером и последовательно с трансмембранным доменом и эндодоменом.
CDR могут быть встроены (привиты) в каркас антитела или scFv человека. Например, CAR, предложенный в настоящем изобретении, может содержать CD19-связывающий домен, состоящий из одной из следующих последовательностей или содержащий ее.
CAR против CD19 может содержать следующую последовательность VH:
SEQ ID NO: 67 - последовательность VH из моноклонального антитела мыши
QVQLQQSGPELVKPGASVKISCKASGYAFSSSWMNWVKQRPGKGLEWIGRIYPGDEDTNYSGKFKDKATLTADKSSTTAYMQLSSLTSEDSAVYFCARSLLYGDYLDYWGQGTTLTVSS
CAR против CD19 может содержать следующую последовательность VL:
SEQ ID NO: 75 - последовательность VL из моноклонального антитела мыши
QIVLTQSPAIMSASPGEKVTMTCSASSSVSYMHWYQQKSGTSPKRWIYDTSKLASGVPDRFSGSGSGTSYFLTINNMEAEDAATYYCQQWNINPLTFGAGTKLELKR
CAR против CD19 может содержать следующую последовательность scFv:
SEQ ID NO: 76 - последовательность VH-VL scFv из моноклонального антитела мыши
QVQLQQSGPELVKPGASVKISCKASGYAFSSSWMNWVKQRPGKGLEWIGRIYPGDEDTNYSGKFKDKATLTADKSSTTAYMQLSSLTSEDSAVYFCARSLLYGDYLDYWGQGTTLTVSSGGGGSGGGGSGGGGSQIVLTQSPAIMSASPGEKVTMTCSASSSVSYMHWYQQKSGTSPKRWIYDTSKLASGVPDRFSGSGSGTSYFLTINNMEAEDAATYYCQQWNINPLTFGAGTKLELKR.
Процент идентичности двух полипептидных последовательностей можно легко определить с помощью программ, таких как BLAST, которая находится в свободном доступе на сайте: http://blast.ncbi.nlm.nih.gov.
FCRL5
Fc-рецептор-подобный белок-5 (FcRL5) является членом суперсемейства рецепторов иммуноглобулинов и семейства Fc-рецептор-подобных белков. FcRL5 является трансмембранным белком I типа, пронизывающим мембрану один раз, и содержит 8 иммуноглобулиноподобных доменов типа C2. Масса зрелого белка составляет 106 кДа.
FCRL5 имеет цитоплазматический хвост с двумя ингибирующими мотивами ITIM, передающими сигналы посредством фосфорилирования. Он ингибирует передачу сигналов от антигенного рецептора В-клетки за счет привлечения SHP1 после костимуляции антигенного рецептора В-клетки, что приводит к снижению притока кальция и фосфорилированию входящего в состав белка тирозина. Костимуляция FCRL5 и антигенного рецептора В-клетки стимулирует пролиферацию и дифференцировку наивных В-клеток. FCRL5 экспрессируется на зрелых В-клетках и на плазматических клетках, его экспрессия индуцируется белками вируса Эпштейна-Барра (ВЭБ). Его гиперэкспрессия характерна для злокачественных В-клеток пациентов с волосатоклеточным лейкозом, хроническим лимфоцитарным лейкозом, мантийноклеточной лимфомой и множественной миеломой.
Известны коммерчески доступные антитела против FcRL5, такие как CD307e (ThermoFisher) и REA391 (Miltenyi Biotec).
В WO2016090337 описаны несколько антигенсвязывающих доменов типа scFv, которые связываются с FcRL5.
В элементе ИЛИ, предложенном в настоящем изобретении, CAR против FcRL5 может содержать антигенсвязывающий домен на основе dAb, scFv или Fab. FcRL5 может содержать антигенсвязывающий домен на основе Fab.
КОНСТРУКЦИЯ НУКЛЕИНОВОЙ КИСЛОТЫ
В настоящем изобретении также предложена конструкция нуклеиновой кислоты, кодирующая химерный рецептор, предложенный в настоящем изобретении.
Конструкция нуклеиновой кислоты, кодирующая FabCAR (Фигура 2а) может иметь структуру:
VH-CH-spacer-TM-endo-coexpr-VL-CL или
VL-CL-spacer-TM-endo-coexpr-VH-CH
где:
VH является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи;
CH является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи;
spacer является нуклеиновой кислотой, кодирующей спейсер;
TM является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен;
endo является последовательностью нуклеиновой кислоты, кодирующей эндодомен;
coexpr является последовательностью нуклеиновой кислоты, обеспечивающей совместную экспрессию первого и второго полипептидов;
VL является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи; и
CL является последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи.
При двух указанных выше структурах последовательности нуклеиновой кислоты, кодирующие два полипептида, могут располагаться в конструкции в любом порядке.
Также предложена конструкция нуклеиновой кислоты, кодирующая элемент ИЛИ, который содержит два или более CAR, по меньшей мере один из которых является FabCAR согласно настоящему изобретению.
Конструкция нуклеиновой кислоты, кодирующая двойной элемент ИЛИ может иметь структуру:
VH-CH-spacer1-TM1-endo1-coexpr1-VL-CL-coexpr2-AgBD-spacer2-TM2-endo2; или
VL-CL-spacer-TM1-endo1-coexpr1-VH-CH-coexpr2-AgBD-spacer2-TM2-endo2,
где:
VH является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи первого CAR;
CH является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи первого CAR;
Spacer 1 является последовательностью нуклеиновой кислоты, кодирующей спейсер первого CAR;
TM1 является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен первого CAR;
Endo1 является последовательностью нуклеиновой кислоты, кодирующей эндодомен первого CAR;
Coexpr1 и coexpr2, которые могут быть одинаковыми или разными, являются последовательностями нуклеиновой кислоты, обеспечивающими совместную экспрессию первого и второго полипептидов первого CAR; а также первого и второго CAR;
VL является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи первого CAR;
CL является последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи первого CAR;
AgBD является последовательностью нуклеиновой кислоты, кодирующей антигенсвязывающий домен второго CAR;
Spacer2 является последовательностью нуклеиновой кислоты, кодирующей спейсер второго CAR;
TM2 является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен второго CAR; и
Endo2 является последовательностью нуклеиновой кислоты, кодирующей эндодомен второго CAR.
Антигенсвязывающий домен второго CAR может, например, являться scFv или dAb.
В обеих указанных выше структурах последовательности нуклеиновой кислоты, кодирующие два полипептида первого CAR, и последовательности нуклеиновой кислоты, кодирующие первый и второй CAR, могут располагаться в конструкции в любом порядке.
Конструкция нуклеиновой кислоты, кодирующая элемент ИЛИ двойного FabCAR, может иметь структуру:
VH1-CH1-spacer1-TM1-endo1-coexpr1-VL1-CL1-coexpr2-VH2-CH2-spacer2-TM2-endo2-coexpr3-VL2-CL2;
VH1-CH1-spacer1-TM1-endo1-coexpr1-VL1-CL1-coexpr2-VL2-CL2-spacer2-TM2-endo2-coexpr3-VH2-CH2;
VL1-CL1-spacer1-TM1-endo1-coexpr1-VH1-CH1-coexpr2-VL2-CL2-spacer2-TM2-endo2-coexpr3-VH2-CH2 или
VL1-CL1-spacer1-TM1-endo1-coexpr1-VH1-CH1-coexpr2-VH2-CH2-spacer2-TM2-endo2-coexpr3-VL2-CL2;
где:
VH1 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи первого CAR;
CH1 является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи первого CAR;
Spacer1 является последовательностью нуклеиновой кислоты, кодирующей спейсер первого CAR;
TM1 является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен первого CAR;
Endo1 является последовательностью нуклеиновой кислоты, кодирующей эндодомен первого CAR;
Coexpr1, coexpr2 и coexpr 3, которые могут быть одинаковыми или разными, являются последовательностями нуклеиновой кислоты, обеспечивающими совместную экспрессию первого и второго полипептидов первого CAR; и первого и второго полипептидов второго CAR;
VL2 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи второго CAR;
CL2 является последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи второго CAR;
VH2 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи второго CAR;
CH2 является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи второго CAR;
Spacer 2 является последовательностью нуклеиновой кислоты, кодирующей спейсер второго CAR;
TM2 является последовательностью нуклеиновой кислоты, кодирующей трансмембранный домен второго CAR;
Endo2 является последовательностью нуклеиновой кислоты, кодирующей эндодомен второго CAR;
VL2 является последовательностью нуклеиновой кислоты, кодирующей вариабельную область легкой цепи второго CAR;
CL2 является последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи второго CAR;
В настоящей заявке термины «полинуклеотид», «нуклеотид» и «нуклеиновая кислота» используются как синонимы.
Специалисту в данной области техники понятно, что из-за вырожденности генетического кода множество разных полинуклеотидов и нуклеиновых кислот могут кодировать один и тот же полипептид. Кроме того, следует понимать, что специалисты в данной области техники могут с помощью рутинных методик производить замены нуклеотидов, которые не оказывают влияния на последовательность полипептидов, кодированную полинуклеотидами, описанными в настоящей заявке, для того чтобы отразить частоту использования кодонов любым конкретным организмом-хозяином, в котором предполагается экспрессировать полипептиды.
Нуклеиновые кислоты согласно настоящему изобретению могут входить в состав ДНК или РНК. Они могут быть одноцепочечными или двухцепочечными. Они также могут являться полинуклеотидами, которые включают в себя синтетические или модифицированные нуклеотиды. В данной области техники известно несколько разных типов модификаций нуклеотидов. К ним относятся метилфосфонатный и фосфоротиоатный варианты остова, добавление акридиновой или полилизиновой цепи на 3' и/или 5' концах молекулы. Для применения с целью, описанной в настоящей заявке, следует понимать, что полинуклеотиды могут быть модифицированы любым из способов, доступных в данной области техники. Такие модификации можно осуществлять для увеличения активности или продолжительности жизни представляющих интерес полипептидов in vivo.
К терминам «вариант», «гомолог» или «производное» в отношении последовательности нуклеотидов относятся любые замены, вариации, модификации, замещения, делеции или добавления одной (или более) нуклеиновой кислоты из последовательности или в нее.
В описанной выше конструкции «coexpr» является последовательностью нуклеиновой кислоты, обеспечивающей совместную экспрессию двух полипептидов как отдельных единиц. Она может являться последовательностью, кодирующей сайт расщепления, что позволяет конструкции нуклеиновой кислоты продуцировать оба полипептида, объединенных сайтом(ами) расщепления. Сайт расщепления может быть саморасщепляющимся, благодаря чему после синтеза полипептида он мгновенно расщепляется на отдельные пептиды без необходимости внешнего расщепляющего воздействия.
Сайт расщепления может являться любой последовательностью, которая позволяет двум полипептидам разъединяться.
В настоящей заявке термин «расщепление» используют для удобства, тогда как сайт расщепления может обеспечивать разделение пептидов на отдельные единицы посредством механизма, отличного от классического расщепления. Например, для объяснения «расщепляющей» активности саморасщепляющегося пептида 2А вируса ящура (FMDV) (см. ниже) было предложено несколько моделей: протеолиз протеиназой клетки-хозяина, аутопротеолиз или трансляционный эффект (Donnelly et al (2001) J. Gen. Virol. 82:1027-1041). Точный механизм такого «расщепления» не важен для цели настоящего изобретения, при условии, что сайт расщепления, если он расположен между последовательностями нуклеиновых кислот, которые кодируют белки, обеспечивает экспрессию белков в виде отдельных единиц.
Сайт расщепления может, например, являться сайтом расщепления фурином, сайтом расщепления вируса гравировки табака (TEV) или кодировать саморасщепляющийся пептид.
«Саморасщепляющийся пептид» обозначает пептид, который функционирует таким образом, что после синтеза полипептида, содержащего белки и саморасщепляющийся пептид, он мгновенно «расщепляется» или разделяется на отдельные или индивидуальные первый и второй пептиды без необходимости внешнего расщепляющего воздействия.
Саморасщепляющийся пептид может являться 2А саморасщепляющимся пептидом афто- или кардиовирусов. Первичное расщепление 2A/2B афто- или кардиовирусов опосредуется «расщеплением» 2А на его собственном С-конце. У афтовирусов, таких как вирусы ящура (FMDV) и вирус ринита А лошадей, область 2А является коротким фрагментом приблизительно из 18 аминокислот, который вместе с N-концевым остатком белка 2В (консервативный остаток пролина) формирует автономный элемент, способный опосредовать «расщепление» на его собственном С-конце (Donelly и соавт. (2001), как указано выше).
«2А-подобные» последовательности были идентифицированы в пикорнавирусах, отличных от афто- и кардиовирусов, «пикорно-подобных» вирусах насекомых, ротавирусах типа С и повторяющихся последовательностях рода трипаносом и бактериальной последовательности (Donelly и соавт. (2001), как указано выше).
Сайт расщепления может содержать 2A-подобную последовательность, представленную в SEQ ID NO: 77 (RAEGRGSLLTCGDVEENPGP).
ХИМЕРНЫЙ РЕЦЕПТОР ЦИТОКИНА
Конструкция нуклеиновой кислоты, предложенная в настоящем изобретении, также может содержать одну или более последовательность(ей) нуклеиновой кислоты, кодирующую химерный рецептор цитокина.
Химерные рецепторы цитокинов описаны в WO2017/029512, которая включена в настоящую заявку посредством ссылки.
Химерный рецептор цитокина может содержать:
экзодомен, который связывается с лигандом, и
эндодомен рецептора цитокина.
Лиганд может являться, например, фактором, секретируемым опухолью, хемокином или антигеном клеточной поверхности.
Химерный рецептор цитокина содержит два полипептида:
(i) первый полипептид, который содержит:
(a) первый антигенсвязывающий домен, который связывается с первым эпитопом лиганда
(b) первую цепь эндодомена рецептора цитокина и
(ii) второй полипептид, который содержит:
(a) второй антигенсвязывающий домен, который связывается со вторым эпитопом лиганда (b) вторую цепь эндодомена рецептора цитокина.
В альтернативном варианте реализации химерный рецептор цитокина может содержать домен димеризации и эндодомен рецептора цитокина.
Димеризация может происходить спонтанно, в таком случае химерный трансмембранный белок будет конститутивно активен. В качестве альтернативы, димеризация может происходить только в присутствии химического индуктора димеризации (CID), в таком случае трансмембранный белок запускает передачу сигналов по цитокиновому типу только в присутствии CID.
Подходящие домены димеризации и CID описаны в WO2015/150771, материалы которой включены в настоящую заявку посредством ссылки.
Например, один домен димеризации может содержать рапамицин-связывающий домен FK-связывающего белка 12 (FKBP12), другой может содержать FKBP12-рапамицин-связывающий (FRB) домен mTOR; и CID может являться рапамицином или его производным.
В случаях, когда домен димеризации спонтанно гетеродимеризуется, он может быть основан на домене димеризации антитела. В частности, он может содержать часть, обеспечивающую димеризацию, константного домена тяжелой цепи (CH) и константного домена легкой цепи (CL). «Часть, обеспечивающая димеризацию» константного домена является частью последовательности, которая формирует дисульфидную связь между цепями.
Химерный рецептор цитокина может содержать Fab-часть антитела в качестве экзодомена, например, как схематично изображено на Фигуре 4.
Химерный рецептор цитокина может содержать два полипептида:
(i) первый полипептид, который содержит:
(a) первый домен димеризации и
(b) первую цепь эндодомена рецептора цитокина и
(ii) второй полипептид, который содержит:
(a) второй домен димеризации, который димеризуется с первым доменом димеризации, и
(b) вторую цепь эндодомена рецептора цитокина.
Химерный рецептор цитокина может содержать два полипептида:
(i) первый полипептид, который содержит:
(a) константный домен тяжелой цепи (CH)
(b) первую цепь эндодомена рецептора цитокина и
(ii) второй полипептид, который содержит:
(a) константный домен легкой цепи (CL)
(b) вторую цепь эндодомена рецептора цитокина.
Эндодомен рецептора цитокина может, например, содержать:
(i) эндодомен β-цепи рецептора ИЛ-2
(ii) эндодомен α-цепи рецептора ИЛ-7 или
(iii) эндодомен α-цепи рецептора ИЛ-15 и/или
(iv) общий эндодомен γ-цепи рецептора.
Конструкция нуклеиновой кислоты, кодирующая конститутивно активный химерный рецептор цитокина типа Fab, может иметь следующую общую структуру:
CH-CRE1-coexpr-CL-CRE2 или
CL-CRE2-coexpr-CH-CRE1
где:
CH является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи первого полипептида;
CRE1 является последовательностью нуклеиновой кислоты, кодирующей первую цепь эндодомена рецептора цитокина первого полипептида;
coexpr является последовательностью, обеспечивающей совместную экспрессию первого и второго полипептидов;
CH является последовательностью нуклеиновой кислоты, кодирующей константную область тяжелой цепи во втором полипептиде;
CRE2 является последовательностью нуклеиновой кислоты, кодирующей вторую цепь эндодомена рецептора цитокина во втором полипептиде;
Конструкция нуклеиновой кислоты, предложенная в настоящем изобретении, может кодировать FabCAR и химерный рецептор цитокина.
ВЕКТОР
В настоящем изобретении также предложен вектор или набор векторов, который содержит одну или более последовательностей нуклеиновой кислоты, кодирующих химерный рецептор согласно настоящему изобретению. Такой вектор можно использовать для введения последовательности(ей) нуклеиновой кислоты внутрь клетки-хозяина, таким образом, что она экспрессирует CAR согласно первому аспекту настоящего изобретения.
Также предложен вектор, содержащий конструкцию нуклеиновой кислоты из последовательностей нуклеиновой кислоты, кодирующих FabCAR и химерный рецептор цитокина.
Вектор может, например, являться плазмидой или вирусным вектором, таким как ретровирусный вектор, лентивирусный вектор, вектор на основе транспозона или синтетической иРНК.
Вектор может быть способен трансфицировать или трансдуцировать клетку, такую как Т-клетка или НК-клетка.
КЛЕТКА
В настоящем изобретении также предложена клетка, которая содержит химерный антигенный рецептор, предложенный в настоящем изобретении. Клетка может содержать два или более CAR, например, она может содержать двойной или тройной элемент ИЛИ, как описано выше.
Также предложена клетка, которая совместно экспрессирует FabCAR или элемент ИЛИ, предложенный в настоящем изобретении, и химерный рецептор цитокина.
Клетка может содержать нуклеиновую кислоту или вектор, предложенные в настоящем изобретении.
Клетка может являться цитолитической иммунной клеткой, такой как Т-клетка или НК-клетка.
Т-клетки или Т-лимфоциты являются типом лимфоцитов, который играет центральную роль в клеточно-опосредованном иммунитете. Их можно отличить от других лимфоцитов, таких как В-клетки и натуральные киллеры (НК-клетки), по наличию Т-клеточного рецептора (TCR) на поверхности клетки. Существуют разные типы Т-клеток, краткая информация о которых представлена ниже.
Т-хелперы (Тх-клетки) помогают другим лейкоцитам в иммунологических процессах, в том числе в созревании В-лимфоцитов в плазматические клетки и В-клетки памяти, а также в активации цитотоксических Т-клеток и макрофагов. Тх-клетки экспрессируют на своей поверхности CD4. Тх-клетки становятся активированными после презентации им пептидных антигенов молекулами MHC II класса на поверхности антигенпрезентирующих клеток (АПК). Эти клетки могут дифференцироваться в один из нескольких подтипов, в том числе в Tх1, Tх2, Tх3, Tх17, Tх9 или фолликулярные Т-хелперы (ФТх), которые секретируют разные цитокины для усиления иммунных реакций разных типов.
Цитолитические Т-клетки (или цитотоксические Т-клетки, CTL) разрушают клетки, инфицированные вирусами, и клетки опухолей, а также участвуют в отторжении трансплантата. CTL экспрессируют на своей поверхности CD8. Эти клетки распознают свои мишени путем связывания с антигеном, ассоциированным с молекулами MHC I класса, которые присутствуют на поверхности всех ядросодержащих клеток. Под действием ИЛ-10, аденозина и других молекул, секретируемых регуляторными Т-клетками, клетки CD8+ могут инактивироваться до состояния анергии, что предотвращает развитие аутоиммунных заболеваний, таких как экспериментальный аутоиммунный энцефаломиелит.
Т-клетки памяти являются субпопуляцией антигеноспецифичных Т-клеток, которые сохраняются в организме в течение продолжительного времени после разрешения инфекции. При повторном воздействии когнатного ими антигена происходит их быстрая экспансия с появлением большого количества эффекторных Т-клеток, что обеспечивает иммунную систему «памятью» о перенесенных инфекциях. Т-клетки памяти бывают трех подтипов: Т-клетки центральной памяти (TCM-клетки) и два типа Т-клеток эффекторной памяти (TEM-клетки и TEMRA-клетки). Клетки памяти могут быть CD4+ или CD8+. Т-клетки памяти обычно экспрессируют на своей поверхности белок CD45RO.
Регуляторные Т-клетки (Трег-клетки), ранее известные как Т-супрессоры, необходимы для поддержания иммунологической толерантности. Их основная функция заключается в подавлении опосредованного Т-клетками иммунитета в сторону завершения иммунной реакции и снижении активности аутореактивных Т-клеток, которые избежали процесса отрицательной селекции в тимусе.
Было описано два основных класса CD4+ Трег-клеток: естественные Трег-клетки и адаптивные Трег-клетки.
Естественные Трег-клетки (также известные как CD4+CD25+FoxP3+ Трег-клетки) появляются в тимусе, их связывают с взаимодействиями между развивающимися Т-клетками и миелоидными (CD11c+), а также плазмоцитоидными (CD123+) дендритными клетками, которые были активированы тимусным стромальным лимфопоэтином (TSLP). Естественные Трег-клетки можно отличить от других Т-клеток по наличию внутриклеточной молекулы FoxP3. Мутации гена FoxP3 могут предотвращать развитие регуляторных Т-клеток, что вызывает аутоиммунное заболевание со смертельным исходом - Х-сцепленный синдром иммунной дисрегуляции, полиэндокринопатии и энтеропатии (IPEX).
Адаптивные Трег-клетки (также известные как Трег1 или Трег3) могут появляться в ходе нормальной иммунной реакции.
Клетка может представлять собой клетку-натуральный киллер (или НК-клетку). НК-клетки формируют часть врожденной иммунной системы. НК-клетки обеспечивают быстрые реакции на характерные сигналы клеток, инфицированных вирусами, не зависимым от MHC образом.
НК-клетки (принадлежащие к группе лимфоидных клеток врожденного иммунитета) определяют как большие гранулярные лимфоциты (БГЛ) и являются третьим типом клеток, дифференцировавшихся из общего лимфоидного предшественника, дающего начало В- и Т-лимфоцитам. Известно, что НК-клетки дифференцируются и созревают в костном мозге, лимфатических узлах, селезенке, миндалинах и тимусе, откуда они выходят в кровоток.
Клетки, предложенные в настоящем изобретении, могут являться клетками любого из типов, указанных выше.
Клетки согласно настоящему изобретению могут быть получены либо ex vivo из периферической крови самого пациента (1-е лицо), либо при трансплантации гемопоэтических стволовых клеток из периферической крови донора (2-е лицо), либо из периферической крови стороннего донора (3-е лицо).
В качестве альтернативы, клетки могут быть получены в результате дифференцировки индуцируемых клеток-предшественников или эмбриональных клеток-предшественников ex vivo, например, в Т- или НК-клетки. В качестве альтернативы, можно применять иммортализованную линию Т-клеток, которые сохранили свою литическую функцию и могут выступать в роли лекарственного средства.
Во всех этих вариантах реализации химерные экспрессирующие полипептид клетки получают в результате введения в них ДНК или РНК, кодирующей химерный полипептид, одним из множества способов, в том числе трансдукцией вирусным вектором или трансфекцией ДНК или РНК.
Клетка, предложенная в настоящем изобретении, может являться ex vivo клеткой субъекта. Клетка может происходить из образца мононуклеарных клеток периферической крови (МКПК). Клетки могут быть активированы и/или подвергнуты экспансии перед их трансдукцией нуклеиновой кислотой, кодирующей молекулы, обеспечивающие синтез химерного полипептида согласно первому аспекту настоящего изобретения, например, подвергнуты воздействию моноклонального антитела против CD3.
Клетку, предложенную в настоящем изобретении, можно получить путем:
(i) выделения содержащего клетки образца от субъекта или из других перечисленных выше источников и
(ii) трансдукции или трансфекции клеток одной или более последовательностями нуклеиновой кислоты, кодирующими химерный полипептид.
После этого клетки могут быть очищены, например, путем селекции по экспрессии антигенсвязывающего домена антигенсвязывающего полипептида.
ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
Настоящее изобретение также относится к фармацевтической композиции, содержащей множество клеток согласно настоящему изобретению.
Фармацевтическая композиция может дополнительно содержать фармацевтически приемлемый носитель, разбавитель или вспомогательное вещество. Фармацевтическая композиция может необязательно содержать один или более дополнительных фармацевтически активных полипептидов и/или соединений. Такой состав, может, например, быть в форме, пригодной для внутривенной инфузии.
СПОСОБ ЛЕЧЕНИЯ
В настоящем изобретении предложен способ лечения заболевания, который включает этап введения субъекту клеток, предложенных в настоящем изобретении (например, в составе фармацевтической композиции, как описано выше).
Способ лечения заболевания относится к терапевтическому применению клеток, предложенных в настоящем изобретении. Согласно настоящей заявке, клетки можно вводить субъекту с заболеванием или состоянием для облегчения, смягчения или улучшения по меньшей мере одного симптома, связанного с заболеванием и/или для замедления, подавления или прекращения прогрессирования заболевания.
Способ профилактики заболевания относится к профилактическому применению клеток, предложенных в настоящем изобретении. Согласно настоящей заявке, клетки можно вводить субъекту, у которого еще не развилось заболевание, и/или у которого еще нет никаких симптомов заболевания, для предотвращения или устранения причины заболевания, либо для подавления или предотвращения возникновения по меньшей мере одного симптома, связанного с заболеванием. Субъект может иметь предрасположенность к заболеванию, либо может иметь риска развития заболевания.
Способ может содержать этапы:
(i) выделения содержащего клетки образца;
(ii) трансдукции или трансфекции таких клеток последовательностью нуклеиновой кислоты или вектором, предложенными в настоящем изобретении;
(iii) введения субъекту клеток из (ii).
Содержащий клетки образец может быть выделен у субъекта или из других источников, как описано выше.
В настоящем изобретении предложена клетка согласно настоящему изобретению для применения в лечении и/или профилактике заболевания.
Настоящее изобретение также относится к применению клетки, предложенной в настоящем изобретении, в производстве лекарственного препарата для лечения заболевания.
Заболевание, которое подлежит лечению способами, предложенными в настоящем изобретении, может являться онкологическим заболеванием, таким как рак мочевого пузыря, рак молочной железы, рак толстой кишки, рак эндометрия, рак почки (почечноклеточный), лейкоз, рак легкого, меланома, неходжкинская лимфома, рак поджелудочной железы, рак предстательной железы и рак щитовидной железы.
Заболевание может являться множественной миеломой (ММ), острым В-клеточным лимфобластным лейкозом (В-ОЛЛ), хроническим лимфоцитарным лейкозом (ХЛЛ), нейробластомой, острым Т-клеточным лимфобластным лейкозом (Т-ОЛЛ) или диффузной В-крупноклеточной лимфомой (ДВККЛ).
Заболевание может являться нарушением, связанным с плазматическими клетками, таким как плазмоцитома, плазмоклеточный лейкоз, множественная миелома, макроглобулинемия, амилоидоз, макроглобулинемия Вальденстрема, солитарная плазмоцитома кости, экстрамедуллярная плазмацитома, остеосклеротическая миелома, болезнь тяжелых цепей, моноклональная гаммапатия неясного значения или вялотекущая множественная миелома.
Клетки, предложенные в настоящем изобретении, могут обладать способностью уничтожать клетки-мишени, такие как раковые клетки. Для клетки-мишени может быть характерно наличие секретируемого опухолью лиганда или лиганда хемокина в непосредственной близости от клетки-мишени. Для клетки-мишени может быть характерно наличие растворимого лиганда, одновременно с экспрессией опухолеассоциированного антигена (ОАА) на поверхности клетки-мишени.
Клетки и фармацевтические композиции, предложенные в настоящем изобретении, можно применять для лечения и/или предотвращения заболеваний, описанных выше.
Настоящее изобретение будет далее описано с помощью Примеров, которые предназначены для того чтобы помочь среднему специалисту в данной области техники в реализации настоящего изобретения и никоим образом не предназначены для ограничения объема настоящего изобретения.
ПРИМЕРЫ
Пример 1 - Экспрессия BCMA на поверхности клеток множественной меланомы
Первичные клетки миеломы выделили иммуномагнитной селекцией по CD138 из свежих образцов костного мозга пациентов с множественной миеломой, имевших выраженное заболевание. Эти клетки пометили специфичным к BCMA МАТ J6MO (GSK), конъюгированным с ФЭ. Одновременно с этим, подготовили стандарт на основе гранул с известным количеством сайтов связывания с применением PE Quantibrite bead kit (Becton Dickenson), согласно инструкциям производителя. Количество копий BCMA на клетках миеломы определили путем сопоставления средней интенсивности флуоресценции клеток миеломы со стандартной кривой, полученной при анализе гранул. Было установлено, что диапазон количества копий BCMA на поверхности клетки меланомы является низким: 348,7-4268,4 копий BCMA на клетку, со средним значением 1181 и медианой 1084,9 (Фигура 1). Это значительно ниже, чем, например, для CD19 и GD2, являющихся классическими мишенями CAR.
Пример 2 - Конструирование FabCAR против BCMA и сравнение с scFvCAR против BCMA
Панель кодирующих CAR конструкций нуклеиновой кислоты создали, как представлено ниже:
RQR8-2A-aBCMAscFv-CD8STK-41BBZ - конструкция CAR на основе одноцепочечного Fv
RQR8-2A-aBCMAFAb-CD8STK-41BBZ - конструкция CAR на основе Fab
RQR8-2A-aBCMA_C11D5.3-CD8STK-41BB-z - bb2121, конструкция scFv CAR (положительный контроль)
scFv- и Fab-домены против BCMA содержали последовательности VH и VL для АТ1 против BCMA, описанного выше (SEQ ID NO: 5 и 6 соответственно). Все конструкции экспрессировали одновременно с геном-маркером самоубийства клетки RQR8, который описан в WO2013/153391, со связывающими BCMA фрагментами в обоих форматах scFv и Fab.
Пример 3 - Проверка экспрессии CAR
Для сравнения экспрессии CAR в разных форматах Т-клетки трансдуцировали scFv или FabCAR, после чего оценили наличие рецепторов на поверхности клеток методом проточной цитометрии. Экспрессию CAR определяли одновременным окрашиванием Т-клеток растворимыми BCMA-FC и QBEND10 (для выявления экспрессии RQR8).
Пример 4 - Тест на цитотоксичность на основе FACS (FBK)
Способность CAR-Т-клеток уничтожать клетки-мишени, экспрессирующие BCMA, оценивали с помощью теста на цитотоксичность на основе FACS. Т-клетки культивировали с клетками-мишенями в соотношениях (эффектор:мишень) 1:4 и 1:8. В качестве клеток-мишеней применяли клетки SupT1, которые в результате модификации экспрессировали физиологический уровень BCMA: в среднем 686 копий BCMA на клетку (SupT1-BCMA low). Также были созданы клетки-мишени, экспрессирующие очень низкий уровень BCMA: в среднем 81 копия BCMA на клетку (JeKo-1). Не подвергавшиеся модификации клетки SupT1 (SupT1-NT) применяли в качестве отрицательного контроля. Тесты проводили в 96-лучном планшете в общем объеме 0,2 мл, в каждую лунку вносили по 5x104 трансдуцированных клеток. Совместные культуры формировали после нормализации относительно эффективности трансдукции. Результаты FBK оценивали после 24 и 72 часов инкубации.
Результаты представлены на Фигурах 5 и 6. После 24 часов совместного культивирования (Фигура 5) BCMA scFvCAR и BCMA Fab CAR продемонстрировали успешное уничтожение клеток-мишеней, экспрессирующих на низком уровне антиген BCMA. Однако BCMA FabCAR продемонстрировал более высокую эффективность, чем эквивалентный scFvCAR, при уничтожении клеток-мишеней, экспрессирующих антиген BCMA на очень низком уровене (JeKo-1). BCMA FabCAR также продемонстрировал более эффективное уничтожение клеток-мишений по сравнению с другим BCMA scFvCAR - bb2121. Через 72 часа (Фигура 6) наблюдалась аналогичная картина. В соотношении 1:8 (Э:М) BCMA FabCAR обеспечил практически полное уничтожение клеток-мишеней с очень низкой экспрессией BCMA, тогда как scFvCAR с эквивалентным связывающим элементом продемонстрировал только частичное уничтожение клеток.
Пример 5 - Высвобождение цитокинов
Секрецию ИЛ-2 и интерферона-гамма (ИФН-γ) CAR-Т-клетками оценивали путем сбора супернатанта из совместных культур через 24 часа культивирования, как описано в Примере 4 при соотношениях эффектор:мишень 1:4 и 1:8. Продукцию ИЛ-2 и ИФН-γ определяли методом ИФА.
Результаты для ИФН-γ на Фигуре 7 показаны для совместных культур с клетками-мишенями без экспрессии антигена BCMA (Фигура 7А), и с клетками-мишенями, экспрессирующими низкие уровни BCMA (Фигура 7В). Т-клетки, экспрессирующие BCMA FabCAR, после совместного культивирования с клетками-мишенями с низкой экспрессией BCMA, продуцировали уровни ИФН-γ, сопоставимые с уровнями, продуцируемыми эквивалентными scFv CAR-Т-клетками. С нетрансдуцированными клетками-мишенями SupT1 наблюдали более высокий фон для bb2121 и эквивалентного scFvCAR, чем для FabCAR.
Пример 6 - Анализ пролиферации
Для оценки пролиферации ту же панель экспрессирующих CAR Т-клеток, описанную в Примере 4, пометили красителем Cell Trace Violet (CTV). Т-клетки инкубировали с CTV в течение 20 минут при температуре 37oC. После этого реакцию остановили добавлением 5 объемов полной среды. Через 5 минут инкубации Т-клетки отмыли и ресуспендировали в 2 мл полной среды. Дополнительную инкубацию в течение 10 минут при комнатной температуре провели для обеспечения гидролиза ацетата и удержания красителя. Меченные Т-клетки культивировали совместно с клетками-мишенями без экспрессии BCMA (SupT1 NT), с низкой экспрессией BCMA (SupT1BCMAlow), с очень низкой экспрессией BCMA (JeKo-1) или с клетками-мишенями MM.1s в соотношении 1:1 в течение 96 часов. Тест проводили в 96-лучном планшете в общем объеме 0,2 мл, в каждую лунку вносили по 5x104 трансдуцированных Т-клеток и такое же количество клеток-мишеней (соотношение 1:1). После совместного культивирования Т-клетки анализировали методом проточной цитометрии для измерения степени разведения CTV, которое происходит при делении Т-клеток.
Клетки также гейтировали по CD3 и маркеру RQR8, затем по CD8+ или CD8- для определения количества цельных CD4 и CD8 T-клеток. Результаты представлены на Фигуре 8. После культивирования со всеми тремя экспрессирующими BCMA клетками-мишенями (с низкой экспрессией, с очень низкой экспрессией и MM.1s) в культурах с BCMA FabCAR было выявлено большее количество CD8 клеток по сравнению с культурами с эквивалентным scFv CAR и bb2121, что отражает более сильную пролиферацию и/или более низкую гибель клеток (Фигура 8В). Следует отметить, что фоновая пролиферация CD4 клеток при применении bb2121 и scFvCAR была выше, чем при применении Fab CAR. Это может обеспечивать более высокую кажущуюся пролиферацию клеток-мишеней, но фактически отражает повышенную активацию CAR в отсутствие антигена.
Пример 7 - Дизайн и конструирование антител с двойными вариабельными доменами, эквивалентными антигенсвязывающему домену расщепляемого Fab CAR
Расщепляемый Fab CAR схематично изображен на Фигуре 9. Он содержит два антигенсвязывающих домена: внешний (дистальный от мембраны) связывающий домен 1 и внутренний (проксимальный от мембраны) связывающий домен 2. Связывающие домены 1 и 2 соединены расщепляемым линкером. Расщепление линкера, например, матриксной металлопротеиназой (MMP) устраняется связывающий домен 1 из CAR. Без расщепления, при интактном FabCAR, внутренний связывающий домен частично закрыт за счет присутствия внешнего домена из-за счет стерического препятствия. Внутренний домен активируется после расщепления тяжелой и легкой цепей.
Для того чтобы продемонстрировать возможность разработки молекулы с двумя связывающими доменами и активации внутреннего связывающего домена расщеплением внешнего связывающего домена ферментом, было разработано растворимое антитело, как показано на Фигуре 10.
Антитело содержало первый антигенсвязывающий домен, который связывается с BCMA и имеет последовательности VH и VL, представленные выше как SEQ ID NO: 29 и 30 соответственно. Второй антигенсвязывающий домен связывается с CD19 и имеет последовательности VH и VL, указанные выше как SEQ ID NO: 67 и 68 соответственно.
Расщепляемый MMP-9 линкер, имеющий последовательность PLGLAG (SEQ ID NO: 87), был добавлен между двумя доменами VL и между двумя доменами VH. В качестве отрицательного контроля применяли рандомизированную версию этой последовательности: LALGPG (SEQ ID NO: 88).
Конструкции были составлены следующим образом:
Плазмида 1: D8_MMP9_CAT19_HC_HuIgG1
Плазмида 2: D8_scrambled_CAT19_HC_HuIgG1
Плазмида 3: D8_MMP9_CAT19_LC
Плазмида 4: D8_scrambled_CAT19_LC
Клетки яичника китайского хомячка (CHO) одновременно трансфицировали Плазмидой 1 и Плазмидой 3, в результате чего они продуцировали антитело, изображенное на Фигуре 10, с расщепляемым MMP линкером; или одновременно трансфецировали Плазмидой 2 и Плазмидой 4, в результате чего они продуцировали эквивалентное антитело с рандомизированным линкером в цепи, содержащей VH, и в цепи, содержащей VL.
Пример 8 - Демонстрация возможности ферментативного расщепления внешнего связывающего домена антитела, имеющего два связывающих домена
Антитело, описанное в Примере 7, содержало расщепляемый MMP-9 линкер между доменами VH и доменами VL BCMA-связывающего домена и CD19-связывающего домена Для демонстрации возможности расщепления BCMA-связывающего домена ферментом MMP-9, провели тест на расщепление, как описано ниже.
Концентрацию MMP-9 человека в буфере для анализа довели до 100 мкг/мл. Для активации фермента добавили Р-аминофенилацетат ртути (APMA) в конечной концентрации 1 мМ, и инкубировали при температуре 37°C в течение 24 часов.
Для проведения тестов на расщепление 50 мкг антитела и 6 мкл активированного фермента смешали в конечном объеме буфера 200 мкл. Смеси для тестов на расщепление инкубировали при температуре 37°C и в разные моменты времени отбирали по 1 мкл раствора антител (4 мкл), отобранные пробы ресуспендировали в нагрузочном красителе NuPAGE, кипятили, замораживали, после чего проводили их электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия (ДНС-ПААГ). Процент расщепления оценивали методом денситометрии, результаты представлены на Фигуре 11.
Антитело, содержащее расщепляемый MMP-9 линкер, с течением времени расщеплялось под действием матриксной металлопротеиназы, приблизительно после 1 часа воздействия фермента процесс выходил на плато. Антитело с рандомизированным линкером не демонстрировало значимого усиления расщепления даже через 24 часа воздействия фермента.
Пример 9 - Изучение влияния расщепления внешнего связывающего домена на связывание антигена-мишени внутренним связывающим доменом
Для изучения активности внутреннего связывающего домена при удалении внешнего связывающего домена и без его удаления провели оценку связывания CD19 методом ИФА. Рекомбинантный CD19 нанесли на дно лунок 96-луночного планшета в концентрации 1 мкг/мл по 50 мкл/лунка. После блокирования в лунки на 30 минут внесли антитела в концентрации 15 мкл/мл, как описано в Примере 7 (содержащие линкер, расщепляемый MMP-9, или рандомизированный линкер, а также ранее подвергавшиеся и не подвергавшиеся воздействию MMP-9), после чего отмыли фосфатно-солевым буферным раствором (ФБР), содержащим 0,05 % твин 20. Вторичное антитело против Fc-фрагмента человека, конъюгированное с пероксидазой хрена (HRP), добавили в разведении 1:3000 и инкубировали в течение 1 часа. Сигнал регистрировали с помощью субстрата 1-Step Ultra TMB и блокировали 1 М раствором H2SO4. Результаты представлены на Фигуре 12. Растворимое антитело (D8-MMP-CAT19) продемонстрировало повышенное связывание с CD19 после расщепления MMP-9, тогда как предварительное воздействие MMP-9 не оказало влияния на связывание антитела с рандомизированным линкером (D8-scrambled-CAT19) с CD19.
Пример 10 - Изучение влияния расщепления внешнего связывающего домена на кинетику связывания CD19
Кинетику связывания CD19 анализировали с помощью биосенсора Biacore 8K путем регистрации антител на чипе, покрытом протеином А. Антитело, описанное в Примере 8, ранее подвергавшееся или не подвергавшееся воздействию MMP-9, а также антитело, выступавшее в роли положительного контроля (CAT19 IgG), регистрировали при 75 резонансных единицах (RU) для IgG и при 100 RU для конструкций с двумя связывающими доменами. Рекомбинантный CD19 подвергли диализу в буфере HBS-EP+, аналит проанализировали в концентрации 500 гМ при последовательном 2-кратном разведении. Результаты представлены на Фигуре 13. Анититело с расщепляемым MMP-9 линкером продемонстрировало более высокий максимальный наблюдаемый уровень связывания (Rmax) CD19 после расщепления MMP-9 (D8-MMP9-CAT19 расщепленное), чем эквивалентное антитело, не подвергавшееся воздействию MMP-9 (D8-MMP9-CAT19).
Все упомянутые в описании выше публикации включены в настоящую заявку посредством ссылок. Различные модификации и вариации описанных способов и систем, предложенных в настоящем изобретении, станут понятны для специалистов в данной области техники в пределах объема и сути изобретения. Несмотря на то, что настоящее изобретение описано в связи с конкретными предпочтительными вариантами реализации, следует понимать, что изобретение, как описано в настоящей заявке, не должно неоправданно ограничиваться такими конкретными вариантами реализации. В действительности, предполагается, что различные модификации описанных способов реализации настоящего изобретения, понятные для специалистов в молекулярной биологии и родственных областях, находятся в рамках объема следующей формулы изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Autolus Limited
<120> Химерный антигенный рецептор
<130> P116016PCT
<150> GB 1815775.0
<151> 27 сентября 2018 г.
<150> GB 1902021.3
<151> 14 февраля 2019 г.
<160> 88
<170> Версия PatentIn 3.5
<210> 1
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> константный домен каппа-цепи
<400> 1
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
1 5 10 15
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
20 25 30
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
35 40 45
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
50 55 60
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
65 70 75 80
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
85 90 95
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 2
<211> 97
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность из тяжелой гамма-цепи иммуноглобулина
<400> 2
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
1 5 10 15
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
20 25 30
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
35 40 45
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
50 55 60
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
65 70 75 80
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
85 90 95
Val
<210> 3
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> спейсер, шарнирная область Ig G1 человека
<400> 3
Ala Glu Pro Lys Ser Pro Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
Lys Asp Pro Lys
20
<210> 4
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> спейсер, шарнирный спенсер
<400> 4
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 5
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH (вариабельная область тяжелой цепи) АТ1 против BCMA
(антигена созревания
В-клеток)
<400> 5
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Thr Ser Gly Phe Thr Phe Ser Asp Ser
20 25 30
Tyr Met Ser Trp Leu Lys Gln Val Pro Gly Gln Ser Ile Glu Trp Ile
35 40 45
Gly Asn Ile Tyr Ala Gly Asp Gly Ala Thr His Tyr His Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Leu Tyr Phe Cys
85 90 95
Ala Arg Pro Leu Tyr Thr Thr Ala Tyr Tyr Tyr Val Gly Gly Phe Ala
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 6
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL (вариабельная область легкой цепи цепи) АТ1 против BCMA
<400> 6
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Thr Val Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Ser Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Ile Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asp Thr Pro Leu Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 7
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ2 против BCMA
<400> 7
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Thr Ser Gly Asp Thr Ile Tyr Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Lys Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg His Asp Tyr Tyr Asp Gly Tyr Gln Ser Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 8
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ2 против BCMA
<400> 8
Asn Thr Val Met Thr Gln Ser Pro Thr Ser Met Ser Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Gly Asn Asn
20 25 30
Ile Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Val Gln Ala
65 70 75 80
Glu Asp Ala Ala Phe Tyr Tyr Cys Gln Arg Ile Tyr Asn Ser Ala Leu
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 9
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ3 против BCMA
<400> 9
Gln Val Gln Leu Gln Gln Ser Gly Ala Ala Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Trp Val Ser Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Glu Ile Tyr Pro Asn Ser Gly Pro Thr Asn Phe Asn Lys Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Thr Ser Glu Asp Ser Ala Ile Tyr Tyr Cys
85 90 95
Thr Pro Arg Thr Val Ala Pro Tyr Asn Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 10
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ3 против BCMA
<400> 10
Asp Ile Val Leu Thr Gln Ser Pro Ala Leu Ala Val Ser Pro Gly Glu
1 5 10 15
Arg Val Ser Ile Ser Cys Arg Ala Ser Glu Ser Val Ser Thr Arg Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Gln Pro Lys Leu Leu Ile Tyr
35 40 45
Gly Ala Ser Asn Leu Glu Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Pro Val Glu Ala Asp
65 70 75 80
Asp Thr Ala Thr Tyr Phe Cys Gln Gln Ser Trp Asn Asp Pro Tyr Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 11
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ4 против BCMA
<400> 11
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ser Ala Ser Gly Phe Ile Phe Ser Asn Phe
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Arg Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Thr Thr Ser Gly Gly Asp Thr His Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg His Asn Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg His Val Tyr Tyr Gly Leu Phe Trp Phe Phe Asp Phe Trp Gly
100 105 110
Pro Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 12
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ4 против BCMA
<400> 12
Asn Thr Val Met Thr Gln Ser Pro Lys Ser Ile Phe Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Val Asn Cys Lys Ala Ser Gln Asn Val Gly Thr Asn
20 25 30
Val Asp Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Asn Met Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Met Gln Ser Asn Thr Asn Pro Phe
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg
100 105
<210> 13
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ5 против BCMA
<400> 13
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Thr Ser Gly Asp Thr Ile Tyr Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Lys Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg His Asp Tyr Tyr Asp Gly Tyr Gln Ser Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 14
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ5 против BCMA
<400> 14
Asp Ile Val Met Thr Gln Ser Pro Ser Thr Leu Pro Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Ser Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Ile Lys Pro Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Met Tyr Tyr Cys Gln Gln Asp Ala Ser Phe Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys Arg
100 105
<210> 15
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ6 против BCMA
<400> 15
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Pro Ile Thr Asn Asn
20 25 30
Tyr Asp Trp Ser Trp Ile Arg Gln Phe Pro Gly Asn Lys Met Glu Trp
35 40 45
Met Gly Tyr Ile Ser Asp Ser Gly Asn Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Gln Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Ser Gly Tyr Ile Ser Tyr Ile Pro Phe Ala Phe Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 16
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ6 против BCMA
<400> 16
Asp Ile Val Leu Thr Gln Ser Pro Ala Leu Ala Val Ser Leu Gly Gln
1 5 10 15
Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Ile Ser Ser
20 25 30
Tyr Asn Leu Met Gln Trp Tyr Gln Gln Lys Pro Gly Gln Gln Pro Lys
35 40 45
Leu Leu Ile Tyr Asp Ala Ser Asn Leu Ala Ser Gly Ile Pro Ala Arg
50 55 60
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Pro
65 70 75 80
Val Gln Ala Asp Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ser Lys Asp
85 90 95
Asp Pro Asn Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<210> 17
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ7 против BCMA
<400> 17
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Pro Ile Thr Asn Asn
20 25 30
Tyr Asp Trp Ser Trp Ile Arg Lys Phe Pro Gly Asn Lys Met Glu Trp
35 40 45
Met Gly Tyr Ile Ser Asp Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Gln Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Ser Gly Tyr Ile Ser Tyr Ile Pro Phe Gly Phe Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 18
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ7 против BCMA
<400> 18
Asp Ile Val Leu Thr Gln Ser Pro Ala Leu Ala Val Ser Pro Gly Glu
1 5 10 15
Arg Val Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Ser Thr Arg Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Gln Pro Lys Leu Leu Ile Tyr
35 40 45
Gly Ala Ser Asn Leu Glu Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Pro Val Glu Ala Asp
65 70 75 80
Asp Thr Ala Thr Tyr Phe Cys Gln Gln Ser Trp Asn Asp Pro Pro Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 19
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ8 против BCMA
<400> 19
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Thr Ser Gly Asp Thr Ile Tyr Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Lys Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg His Asp Tyr Tyr Asp Gly Tyr Gln Ser Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 20
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ8 против BCMA
<400> 20
Asp Ile Val Met Thr Gln Ser Pro Ala Ser Gln Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Gly Asp Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Leu Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ile Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Asp Tyr Tyr Cys Gln Gln
85 90 95
His Tyr Ser Tyr Pro Leu Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 21
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ9 против BCMA
<400> 21
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Thr Ser Gly Asp Thr Ile Tyr Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Thr Arg His Gly Tyr Tyr Asp Gly Tyr Gln Ser Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 22
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ9 против BCMA
<400> 22
Asn Thr Val Met Thr Gln Ser Pro Lys Ser Met Ser Ile Ser Val Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Gly Asn Asn
20 25 30
Ile Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Gly Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Ser Val Gln Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Asn Tyr Pro Ser Ile
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 23
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ10 против BCMA
<400> 23
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Met Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Pro Ser Gly Gly Ser Thr Tyr Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ala Lys Ser Ser Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Thr Arg Gly Asp Tyr Gly Tyr Asn Tyr Ala Tyr Trp Phe Ala Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 24
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ10 против BCMA
<400> 24
Asp Ile Val Met Thr Gln Ala Pro Ser Ser Met Pro Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Ile Lys Pro Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Met Tyr Tyr Cys Gln Gln Tyr Asp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 25
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ11 против BCMA
<400> 25
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Glu Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Thr Ser Gly Asp Ser Ile Tyr Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Val Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg His Gly Tyr Tyr Asp Gly Tyr Gln Ser Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 26
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ12 против BCMA
<400> 26
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Pro Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Ser Cys Arg Ala Ser Gln Gly Ile Ser Asn Asn
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr Ile Lys Pro Leu Ile
35 40 45
Tyr Tyr Thr Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Asp Glu Thr Phe Pro Tyr
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 27
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ13 против BCMA
<400> 27
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Asp Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Pro Ser Gly Gly Ser Thr Tyr Tyr Arg Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Thr His Asn Tyr Tyr Asp Gly Ser Ser Leu Phe Ala Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 28
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ13 против BCMA
<400> 28
Asp Ile Val Leu Thr Gln Ser Pro Ala Leu Ala Val Ser Pro Gly Glu
1 5 10 15
Arg Val Thr Ile Ser Cys Gly Ala Asn Glu Thr Val Ser Thr Leu Val
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Gln Gln Pro Lys Leu Leu Ile Tyr
35 40 45
Leu Ala Ser His Leu Glu Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Pro Val Glu Ala Asp
65 70 75 80
Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Ser Trp Asn Asp Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 29
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH АТ14 против BCMA
<400> 29
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Ser Asp Tyr
20 25 30
Asn Met Ala Trp Val Arg Gln Ala Pro Lys Lys Gly Leu Glu Trp Val
35 40 45
Ala Thr Ile Ile Tyr Asp Gly Ser Ser Thr Asn His Gly Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr Leu Tyr
65 70 75 80
Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Thr Arg Pro Gly Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser
115
<210> 30
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL АТ15 против BCMA
<400> 30
Asp Val Val Leu Thr Gln Thr Pro Pro Thr Leu Ser Ala Thr Ile Gly
1 5 10 15
Gln Ser Val Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Phe Leu Ile Tyr Leu Val Ser Gly Leu Gly Ser Gly Val Pro
50 55 60
Asn Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Gly Val Glu Ala Glu Asp Leu Gly Ile Tyr Tyr Cys Val His Gly
85 90 95
Thr His Ala Trp Thr Val Gly Gly Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 31
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> трансмебранный активатор, а также партнер модулятора кальция и
лиганда циклофилина (CAML) (TACI), 2H6 ScFv
<400> 31
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Arg Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Ser Asn Asp Asp Thr Lys Tyr Thr Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Thr His Gly Asp Tyr Tyr Ala Leu Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ala Gly Gly Gly
115 120 125
Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Leu Thr Gln Ser Pro Ala
130 135 140
Ser Leu Ala Val Ser Leu Gly Gln Ser Val Thr Ile Ser Cys Arg Ala
145 150 155 160
Ser Glu Ser Val Glu Tyr Tyr Gly Thr Ser Leu Met Gln Trp Tyr Gln
165 170 175
Gln Lys Pro Gly Gln Ala Pro Lys Leu Leu Ile Tyr Gly Ala Ser Asn
180 185 190
Val Glu Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr
195 200 205
Asp Phe Ser Leu Asn Ile His Pro Val Glu Glu Asp Asp Ile Ala Met
210 215 220
Tyr Phe Cys Gln Gln Ser Arg Lys Val Pro Trp Thr Phe Gly Gly Gly
225 230 235 240
Thr Lys Leu Glu Ile Lys Arg
245
<210> 32
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2H6, CDR H1
<400> 32
Asn Tyr Val Met His
1 5
<210> 33
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2H6, CDR H2
<400> 33
Tyr Ile Asn Pro Ser Asn Asp Asp Thr Lys Tyr Thr Glu Lys Phe Lys
1 5 10 15
Gly
<210> 34
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2H6, CDR H3
<400> 34
Gly Thr His Gly Asp Tyr Tyr Ala Leu Asp Tyr
1 5 10
<210> 35
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2H6, CDR L1
<400> 35
Arg Ala Ser Glu Ser Val Glu Tyr Tyr Gly Thr Ser Leu Met Gln
1 5 10 15
<210> 36
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2H6, CDR L2
<400> 36
Gly Ala Ser Asn Val Glu Ser
1 5
<210> 37
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2H6, CDR L3
<400> 37
Gln Gln Ser Arg Lys Val Pro
1 5
<210> 38
<211> 245
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI, 2G2 ScFv
<400> 38
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Met Leu Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Ser Thr Phe
20 25 30
Gly Met Gly Val Gly Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Ala His Ile Trp Trp Asp Asp Ala Gln Tyr Ser Asn Pro Ala
50 55 60
Leu Arg Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val
65 70 75 80
Phe Leu Lys Ile Ala Asn Val Asp Thr Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ser Arg Ile His Ser Tyr Tyr Ser Tyr Asp Glu Gly Phe Ala Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly Gly Ser
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Val Met Thr Gln
130 135 140
Ser Gln Lys Phe Met Ser Thr Thr Val Gly Asp Arg Val Ser Ile Thr
145 150 155 160
Cys Lys Ala Ser Gln Asn Val Gly Thr Ala Val Ala Trp Tyr Gln Gln
165 170 175
Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile Tyr Ser Ala Ser Asn Arg
180 185 190
Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp
195 200 205
Phe Thr Leu Thr Ile Ser Asn Met Gln Ser Glu Asp Leu Ala Asp Tyr
210 215 220
Phe Cys Gln Gln Tyr Ser Ser Tyr Arg Thr Phe Gly Gly Gly Thr Lys
225 230 235 240
Leu Glu Ile Lys Arg
245
<210> 39
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2G2, CDR H1
<400> 39
Thr Phe Gly Met Gly Val Gly
1 5
<210> 40
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2G2, CDR H2
<400> 40
His Ile Trp Trp Asp Asp Ala Gln Tyr Ser Asn Pro Ala Leu Arg Ser
1 5 10 15
<210> 41
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2G2, CDR H3
<400> 41
Arg Ile His Ser Tyr Tyr Ser Tyr Asp Glu Gly Phe Ala Tyr
1 5 10
<210> 42
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2G2, CDR L1
<400> 42
Lys Ala Ser Gln Asn Val Gly Thr Ala Val Ala
1 5 10
<210> 43
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2G2, CDR L2
<400> 43
Ser Ala Ser Asn Arg Tyr Thr
1 5
<210> 44
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 2G2, CDR L3
<400> 44
Gln Gln Tyr Ser Ser Tyr
1 5
<210> 45
<211> 115
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI, 1G6 VH
<400> 45
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val Asp Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Ile Ile Trp Gly Gly Gly Arg Thr Asn Tyr Asn Ser Ala Phe Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Ser Gly Asp Arg Ala Ala Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr
100 105 110
Val Ser Ser
115
<210> 46
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI, 1G6 VL
<400> 46
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Thr Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Thr Gly Val Pro Val Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Met Gln Ser
65 70 75 80
Glu Asp Leu Ala Asp Tyr Phe Cys Gln Gln Tyr Ser Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 47
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 1G6, CDR H1
<400> 47
Ser Tyr Gly Val Asp
1 5
<210> 48
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 1G6, CDR H2
<400> 48
Ile Ile Trp Gly Gly Gly Arg Thr Asn Tyr Asn Ser Ala Phe Lys Ser
1 5 10 15
<210> 49
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 1G6, CDR H3
<400> 49
Gly Asp Arg Ala Ala Asp Tyr
1 5
<210> 50
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 1G6, CDR L1
<400> 50
Lys Ala Ser Gln Asn Val Gly Thr Ala Val Ala
1 5 10
<210> 51
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 1G6, CDR L2
<400> 51
Ser Ala Ser Asn Arg Tyr Thr
1 5
<210> 52
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 1G6, CDR L3
<400> 52
Gln Gln Tyr Ser Ser Tyr Pro
1 5
<210> 53
<211> 114
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI, 4B11 VH
<400> 53
Glu Val Gln Leu Gln Gln Ser Val Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asn Thr
20 25 30
Tyr Ile His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Lys Ile Asp Pro Ala Asn Gly Asn Ser Glu Tyr Ala Pro Lys Phe
50 55 60
Gln Gly Lys Ala Thr Ile Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Thr Ile Tyr Tyr Cys
85 90 95
Thr Ser Gly Tyr Gly Ala Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val
100 105 110
Ser Ser
<210> 54
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI, 4B11 VL
<400> 54
Asp Ile Val Leu Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Ile Gly
1 5 10 15
Glu Lys Val Thr Leu Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Gln
35 40 45
Ser Leu Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Phe Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Lys Thr Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Thr Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 55
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 4B11, CDR H1
<400> 55
Asn Thr Tyr Ile His
1 5
<210> 56
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 4B11, CDR H2
<400> 56
Lys Ile Asp Pro Ala Asn Gly Asn Ser Glu Tyr Ala Pro Lys Phe Gln
1 5 10 15
Gly
<210> 57
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 4B11, CDR H3
<400> 57
Gly Tyr Gly Ala Tyr
1 5
<210> 58
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 4B11, CDR L1
<400> 58
Lys Ser Ser Gln Ser Leu Leu Tyr Ser Ser Asn Gln Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 59
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 4B11, CDR L2
<400> 59
Trp Ala Ser Thr Arg Glu Phe
1 5
<210> 60
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> домен, связывающий TACI 4B11, CDR L3
<400> 60
Gln Gln Tyr Tyr Thr Trp
1 5
<210> 61
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR VH CD19-связывающего домена, CDR1
<400> 61
Gly Tyr Ala Phe Ser Ser Ser
1 5
<210> 62
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR VH CD19-связывающего домена, CDR2
<400> 62
Tyr Pro Gly Asp Glu Asp
1 5
<210> 63
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR VH CD19-связывающего домена, CDR3
<400> 63
Ser Leu Leu Tyr Gly Asp Tyr Leu Asp Tyr
1 5 10
<210> 64
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR VL CD19-связывающего домена, CDR1
<400> 64
Ser Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 65
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR VL CD19-связывающего домена, CDR2
<400> 65
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 66
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> CDR VL CD19-связывающего домена, CDR3
<400> 66
Gln Gln Trp Asn Ile Asn Pro Leu Thr
1 5
<210> 67
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность VH моноклонального антитела мыши
<400> 67
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Ser
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Glu Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Ser Leu Leu Tyr Gly Asp Tyr Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 68
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR1
<400> 68
Gly Phe Thr Phe Ser Asp Ser Tyr
1 5
<210> 69
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR2
<400> 69
Ile Tyr Ala Gly Asp Gly Ala Thr
1 5
<210> 70
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR3
<400> 70
Ala Arg Pro Leu Tyr Thr Thr Ala Tyr Tyr Tyr Val Gly Gly Phe Ala
1 5 10 15
Tyr
<210> 71
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR1
<400> 71
Gln Ser Leu Leu Ser Ser Gly Asn Gln Lys Asn Tyr
1 5 10
<210> 72
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR2
<400> 72
Trp Ala Ser
1
<210> 73
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR3
<400> 73
Gln Gln Tyr Tyr Asp Thr Pro Leu Thr
1 5
<210> 74
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> мотив DXL богатого цистеином домена (CRD) TACI
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (1)..(1)
<223> Xaa может являться Phe, Tyr или Trp
<220>
<221> прочий_признак
<222> (3)..(3)
<223> Xaa может являться любой природной аминокислотой
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (5)..(5)
<223> Xaa может являться Val или Thr
<220>
<221> ПРОЧИЙ_ПРИЗНАК
<222> (6)..(6)
<223> Xaa может являться Arg или Gly
<400> 74
Xaa Asp Xaa Leu Xaa Xaa
1 5
<210> 75
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность VL моноклонального антитела мыши
<400> 75
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Asp Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Phe Leu Thr Ile Asn Asn Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Asn Ile Asn Pro Leu Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg
100 105
<210> 76
<211> 241
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> последовательность scFv моноклонального антитела мыши
<400> 76
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Ser Ser Ser
20 25 30
Trp Met Asn Trp Val Lys Gln Arg Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Tyr Pro Gly Asp Glu Asp Thr Asn Tyr Ser Gly Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Ser Leu Leu Tyr Gly Asp Tyr Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Gln Ile Val Leu Thr Gln Ser Pro Ala Ile
130 135 140
Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser
145 150 155 160
Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln Lys Ser Gly Thr Ser
165 170 175
Pro Lys Arg Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro
180 185 190
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Ser Tyr Phe Leu Thr Ile
195 200 205
Asn Asn Met Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp
210 215 220
Asn Ile Asn Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
225 230 235 240
Arg
<210> 77
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> сайт расщепления, 2A-подобная последовательность
<400> 77
Arg Ala Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu
1 5 10 15
Asn Pro Gly Pro
20
<210> 78
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> глицин-сериновый линкер
<400> 78
Gly Gly Gly Gly Ser
1 5
<210> 79
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR1
<400> 79
Gly Phe Ile Phe Ser Asp Tyr Asn
1 5
<210> 80
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR2
<400> 80
Ile Ile Tyr Asp Gly Ser Ser Thr
1 5
<210> 81
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VH CDR3
<400> 81
Ala Thr Arg Pro Gly Pro Phe Ala Tyr
1 5
<210> 82
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR1
<400> 82
Gln Ser Leu Leu His Ser Asn Gly Asn Thr Tyr
1 5 10
<210> 83
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR2
<400> 83
Leu Val Ser
1
<210> 84
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> VL CDR3
<400> 84
Val His Gly Thr His Ala Trp Thr
1 5
<210> 85
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> MMP-1, последовательность, расщепляемая ферментом MMP
<400> 85
Pro Leu Gly Leu Trp Ala
1 5
<210> 86
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> MMP-2, последовательность, расщепляемая ферментом MMP
<400> 86
Pro Ala Gly Leu Ala Gly
1 5
<210> 87
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> MMP-9, последовательность, расщепляемая ферментом MMP
<400> 87
Pro Leu Gly Leu Ala Gly
1 5
<210> 88
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> рандомизированный линкер, расщепляемый MMP-9 (отрицательный
контроль)
<400> 88
Leu Ala Leu Gly Pro Gly
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
| КЛЕТКА | 2014 |
|
RU2717984C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО К BCMA И BCMA-CAR-T-КЛЕТКИ | 2020 |
|
RU2762942C1 |
| КЛЕТКА | 2014 |
|
RU2732236C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2841244C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО К BCMA И BCMA-CAR-NK-КЛЕТКИ | 2020 |
|
RU2795443C2 |
| АНТИТЕЛО, НАЦЕЛЕННОЕ НА ВСМА, И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2799655C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ К BCMA | 2015 |
|
RU2747457C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2761632C2 |
| КЛЕТКА | 2015 |
|
RU2768019C2 |


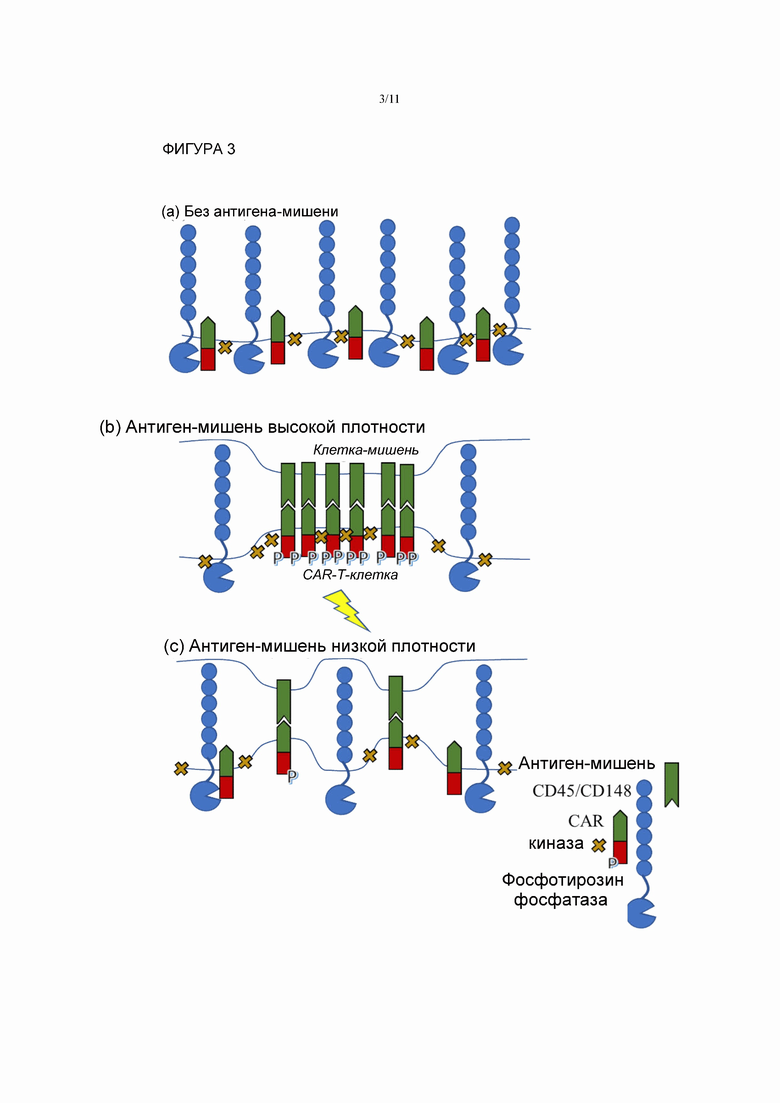
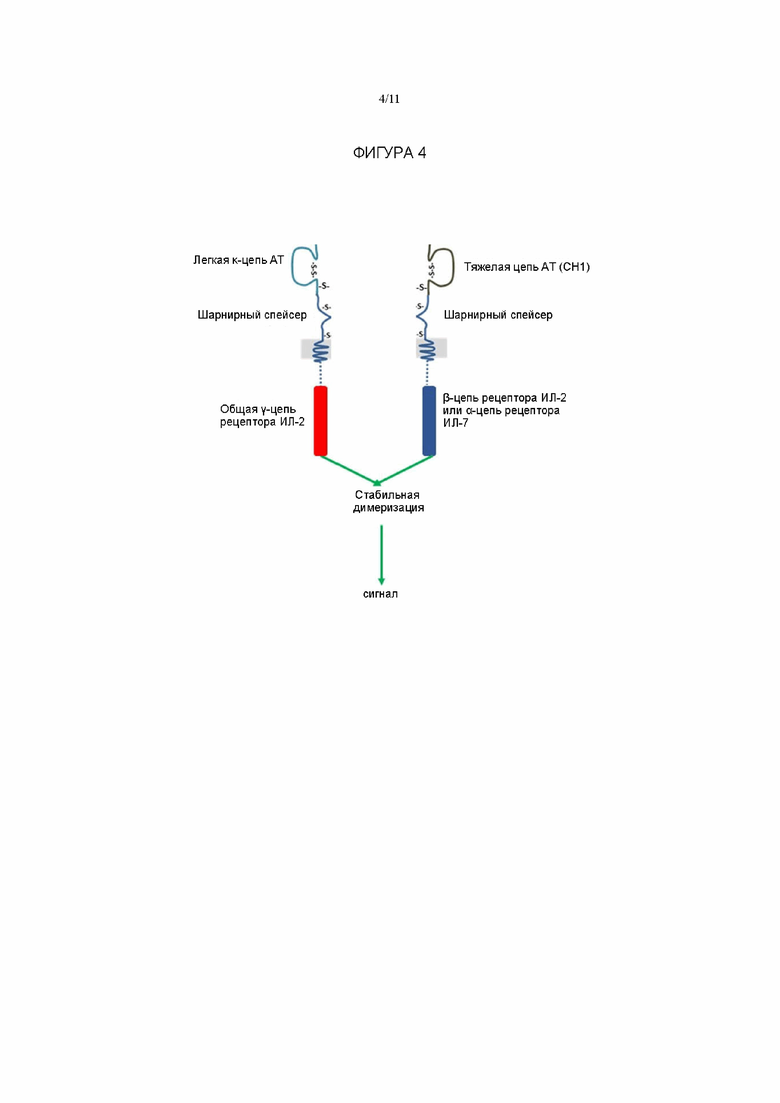







Изобретение относится к области биотехнологии, в частности к химерному антигенному рецептору (CAR), который связывает антиген созревания В-клеток (BCMA), а также к экспрессионной конструкции нуклеиновой кислоты и клетке, содержащим молекулу нуклеиновой кислоты, кодирующую указанный CAR. Также раскрыт вектор, содержащий вышеуказанную экспрессионную конструкцию. Изобретение также относится к способу получения цитолитической иммунной клетки, обладающей способностью убивать клетку-мишень, экспрессирующую BCMA, а также к композиции, содержащей вышеуказанную клетку. Изобретение эффективно для лечения рака. 11 н. и 3 з.п. ф-лы, 13 ил., 2 табл., 10 пр.
1. Химерный антигенный рецептор (CAR), который связывает антиген созревания В-клеток (BCMA), при этом указанный CAR содержит антигенсвязывающий домен Fab, причём указанный антигенсвязывающий домен Fab содержит:
a) вариабельную область тяжелой цепи (VH), имеющую участки, определяющие комплементарность (CDR), со следующими последовательностями:
CDR1 – GFIFSDYN (SEQ ID NO: 79),
CDR2 – IIYDGSST (SEQ ID NO: 80),
CDR3 – ATRPGPFAY (SEQ ID NO: 81), и
b) вариабельную область легкой цепи (VL), имеющую участки, определяющие комплементарность (CDR), со следующими последовательностями:
CDR1 – QSLLHSNGNTY (SEQ ID NO: 82),
CDR2 – LVS (SEQ ID NO: 83),
CDR3 – VHGTHAWT (SEQ ID NO: 84).
2. CAR по п. 1, отличающийся тем, что указанный антигенсвязывающий домен Fab содержит домен VH, имеющий последовательность SEQ ID NO: 29; и домен VL, имеющий последовательность SEQ ID NO: 30.
3. Экспрессионная конструкция нуклеиновой кислоты для обеспечения экспрессии CAR, которая содержит молекулу нуклеиновой кислоты, кодирующую CAR согласно п.1 или 2.
4. Экспрессионная конструкция нуклеиновой кислоты для обеспечения экспрессии CAR по п. 1 или 2, которая имеет одну из следующих общих структур:
VH-CH-spacer-TM-endo-coexpr-VL-CL;
VL-CL-coexpr-VH-CH-spacer-TM-endo;
VL-CL-spacer-TM-endo-coexpr-VH-CH или
VH-CH-coexpr-VL-CL-spacer-TM-endo;
где:
VH представляет собой последовательность нуклеиновой кислоты, кодирующую вариабельную область тяжелой цепи домена Fab CAR по п. 1 или 2;
CH представляет собой последовательность нуклеиновой кислоты, кодирующую константную область тяжелой цепи;
spacer представляет собой нуклеиновую кислоту, кодирующую спейсер;
TM представляет собой последовательность нуклеиновой кислоты, кодирующую трансмембранный домен;
endo представляет собой последовательность нуклеиновой кислоты, кодирующую эндодомен;
coexpr представляет собой последовательность нуклеиновой кислоты, обеспечивающую совместную экспрессию первого и второго полипептидов;
VL представляет собой последовательность нуклеиновой кислоты, кодирующую вариабельную область легкой цепи домена Fab CAR по п. 1 или 2; и
CL представляет собой последовательность нуклеиновой кислоты, кодирующую константную область легкой цепи.
5. Экспрессионная конструкция нуклеиновой кислоты для обеспечения экспрессии CAR по п. 1 или 2 и второго CAR, которая содержит первую молекулу нуклеиновой кислоты, кодирующую CAR согласно п.1 или 2, и вторую молекулу нуклеиновой кислоты, кодирующую второй CAR, который имеет антигенсвязывающий домен, представляющий собой доменное антитело (dAb), scFv или Fab.
6. Экспрессионная конструкция нуклеиновой кислоты по п. 5, отличающаяся тем, что указанный второй химерный антигенный рецептор связывается с одним из следующих антигенов: CD19, FcRL5 и TACI.
7. Вектор экспрессии для получения клетки, обладающей способностью убивать клетку-мишень, экспрессирующую BCMA, который содержит экспрессионную конструкцию нуклеиновой кислоты по любому из пп. 3-6.
8. Цитолитическая иммунная клетка, обладающая способностью убивать клетку-мишень, экспрессирующую BCMA, которая экспрессирует CAR по любому из пп. 1, 2, причём указанная клетка содержит нуклеиновую кислоту, кодирующую CAR по любому из пп. 1, 2.
9. Цитолитическая иммунная клетка, обладающая способностью убивать клетку-мишень, экспрессирующую BCMA, которая экспрессирует первый CAR по любому из пп. 1, 2 и второй химерный антигенный рецептор, который имеет антигенсвязывающий домен, представляющий собой доменное антитело (dAb), scFv или Fab, причём указанная клетка содержит нуклеиновую кислоту, кодирующую CAR по любому из пп. 1, 2.
10. Способ получения клетки по п. 8, который включает этап введения экспрессионной конструкции по п. 3 или 4 внутрь цитолитической иммунной клетки ex vivo.
11. Способ получения клетки по п. 9, который включает этап введения экспрессионной конструкции по п. 5 или 6 внутрь цитолитической иммунной клетки ex vivo.
12. Фармацевтическая композиция для лечения рака, который экспрессирует BCMA, которая содержит в эффективном количестве клетки по п. 8 или 9 совместно с фармацевтически приемлемым носителем, разбавителем или вспомогательным веществом.
13. Способ лечения рака, который экспрессирует BCMA, при этом указанный способ включает этап введения субъекту фармацевтической композиции по п. 12.
14. Способ по п. 13, отличающийся тем, что указанный рак представляет собой множественную миелому.
| WO 2016014789 A2, 28.01.2016 | |||
| WO 2016014565 A2, 28.01.2016 | |||
| WO 2016201300 A1, 15.12.2016 | |||
| HUANG X, PARK H, GREENE J, PAO J, MULVEY E, ZHOU SX, et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| RU 2016145968 A, 28.05.2018. | |||
Авторы
Даты
2023-12-21—Публикация
2019-09-26—Подача