ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет на основании предварительной патентной заявки США с серийным № 62/088309, поданной 5 декабря 2014 г., полное содержание которой включено в настоящий документ посредством ссылки и по отношению к которой испрашивается приоритет.
ВВЕДЕНИЕ
Настоящее изобретение относится к способам и композициям для лечения рака. Изобретение относится к химерным антигенным рецепторам (CAR), которые специфически нацелены на антиген созревания B-клеток (BCMA), иммунореактивным клеткам, содержащим такие CAR, и способам применения таких клеток для лечения рака (например, множественной миеломы).
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Клеточная иммунотерапия является терапией, обладающей потенциалом для излечения рака. T-клетки и другие иммунные клетки могут быть модифицированы для нацеливания на опухолевые антигены путем введения генетического материала, кодирующего искусственные или синтетические рецепторы для антигена, называемые химерными антигенными рецепторами (CAR), которые специфичны для выбранных антигенов. Недавно таргетированная T-клеточная терапия с использованием CAR зарекомендовала себя как клинически успешный подход к лечению злокачественных заболеваний крови.
Множественная миелома (MM) является вторым по распространенности злокачественным заболеванием крови8. Примерно 25% пациентов имеют цитогенетику с высокой степенью риска, что предвещает средний период выживания менее 2 лет9,10. Несмотря на достигнутый в последнее время прогресс, независимо от цитогенетики, заболевание по-прежнему считается неизлечимым, за исключением иммунотерапевтического эффекта «трансплантат против миеломы» (GvM) аллогенного трансплантата. Однако использование аллогенных трансплантатов ограничено несоответствием требованиям и высокой частотой связанной с трансплантацией заболеваемости и смертности11. Аналогично эффекту GvM, потенциально излечивающий эффект T-клеток может быть достигнут с минимальной токсичностью за счет аутологичной адоптивной T-клеточной терапии.
Миелома может быть идеальным заболеванием для тестирования адоптивной T-клеточной терапии. Во-первых, как указано выше, аллогенные трансплантаты продемонстрировали, что T-клетки могут быть средством радикального лечения, даже при минимальной сопутствующей химиотерапии, или без нее, например, после немиелоаблативной трансплантации или пост-трансплантационных инфузий донорских лимфоцитов. Во-вторых, кондиционирующая химиотерапия, возможно, через механизм истощения регуляторных T-клеток (Treg), повышает эффективность адоптивной T-клеточной терапии4,12, в силу этого период сразу после аутологичной трансплантации может быть оптимальным моментом для введения T-клеток, и миелома является одним из нескольких заболеваний, при которых аутологичная трансплантация стволовых клеток является стандартом лечения. В-третьих, иммуномодулирующее лекарственное средство леналидомид может повышать эффективность терапии на основе CAR, как было показано на мышах13, и леналидомид обычно используют для лечения MM. В-четвертых, адоптивная T-клеточная терапия лучше всего работает в случае заболеваний, поражающих преимущественно костный мозг, таких как ALL6,7, по сравнению с солидными опухолями или экстрамедуллярным CLL4, и аналогично ALL, миелома является заболеванием костного мозга.
Хотя есть множество причин ожидать, что адоптивная T-клеточная терапия может быть эффективной при MM, применение адоптивной T-клеточной терапии при миеломе также связано с особыми проблемами. В отличие от других B-клеточных злокачественных новообразований, экспрессия CD19 имеет место лишь у 2% пациентов с миеломой14. Более того, в отличие от CD19, все обычные внеклеточные иммунофенотипические маркеры при миеломе (CD138, CD38 и CD56) также экспрессируются на других важных типах клеток, и авторы изобретения прогнозируют, что CAR для любой из этих мишеней приводили бы к неприемлемой токсичности «внеопухолевых мишеней»6, которая может быть фатальной даже в случае мишеней, антитела к которым хорошо переносятся, как было в ситуации с нацеленными на HER2 CAR15. Соответственно, существует потребность в новых терапевтических стратегиях для конструирования CAR, нацеленных на антигены, которые на высоком уровне экспрессируются в клетках MM и ограниченно экспрессируются в нормальных тканях, для лечения множественной миеломы; стратегиях, которые могут приводить к эффективной эрадикации опухолей с минимальной токсичностью и иммуногенностью.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение, в целом, относится к химерным антигенным рецепторам (CAR), специфически нацеленным на антиген созревания B-клеток (BCMA), иммунореактивным клеткам, содержащим такие CAR, и применению таких CAR и иммунореактивных клеток для лечения множественной миеломы.
Настоящее изобретение относится к CAR. В одном неограничивающем примере CAR содержит внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен, при этом внеклеточный антигенсвязывающий домен представляет собой одноцепочечный вариабельный фрагмент (scFv) человеческого иммуноглобулина, специфически связывающийся с антигеном созревания B-клеток (BMCA). В конкретных вариантах осуществления человеческий scFv специфически связывается с BCMA с аффинностью связывания (KD), составляющей от примерно 1×10-9 M до примерно 3×10-6 M. В конкретных вариантах осуществления человеческий scFv специфически связывается с BCMA с аффинностью связывания (KD), составляющей от примерно 1×10-9 M до примерно 1×10-8 M.
В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, примерно 81%, примерно 82%, примерно 83%, примерно 84%, примерно 85%, примерно 86%, примерно 87%, примерно 88%, примерно 89%, примерно 90%, примерно 91%, примерно 92%, примерно 93%, примерно 94%, примерно 95%, примерно 96%, примерно 97%, примерно 98% или примерно 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65.
В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, примерно 81%, примерно 82%, примерно 83%, примерно 84%, примерно 85%, примерно 86%, примерно 87%, примерно 88%, примерно 89%, примерно 90%, примерно 91%, примерно 92%, примерно 93%, примерно 94%, примерно 95%, примерно 96%, примерно 97%, примерно 98% или примерно 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62 и 66.
В конкретных вариантах осуществления человеческий scFv содержит (a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, примерно 81%, примерно 82%, примерно 83%, примерно 84%, примерно 85%, примерно 86%, примерно 87%, примерно 88%, примерно 89%, примерно 90%, примерно 91%, примерно 92%, примерно 93%, примерно 94%, примерно 95%, примерно 96%, примерно 97%, примерно 98% или примерно 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65; и (b) вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, примерно 81%, примерно 82%, примерно 83%, примерно 84%, примерно 85%, примерно 86%, примерно 87%, примерно 88%, примерно 89%, примерно 90%, примерно 91%, примерно 92%, примерно 93%, примерно 94%, примерно 95%, примерно 96%, примерно 97%, примерно 98% или примерно 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62 и 66.
В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65, а также их консервативных модификаций.
В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62 и 66, а также их консервативных модификаций.
В конкретных вариантах осуществления человеческий scFv содержит (a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65, а также их консервативных модификаций, и (b) вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62 и 66, а также их консервативных модификаций.
В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из: SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из: SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62 и 66. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит (a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2; (b) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6; (c) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10; (d) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14; (e) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18; (f) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22; (g) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26; (h) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30; (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34; (j) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38; (k) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42; (l) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46; (m) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50; (n) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54; (o) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58; (p) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62; или (q) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21; и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53; и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57; и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61; и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62. В конкретных вариантах осуществления человеческий scFv содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65; и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66.
В конкретных неограничивающих вариантах осуществления человеческий scFv содержит обе из указанных тяжелой и легкой цепей, необязательно, с последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. Например, в конкретных неограничивающих вариантах осуществления человеческий scFv содержит (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и (ii) вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления человеческий scFv содержит (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и (ii) вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления человеческий scFv содержит (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и (ii) вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления человеческий scFv содержит (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и (ii) вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления человеческий scFv содержит (i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и (ii) вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи.
В конкретных вариантах осуществления человеческий scFv содержит (a) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 91, 97, 103, 109, 115, 121, 127, 133, 139, 145, 151, 157, 163, 169, 175, 181 и 187; и (b) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 94, 100, 106, 112, 118, 124, 130, 136, 142, 148, 154, 160, 166, 172, 178, 184 и 190.
В конкретных вариантах осуществления человеческий scFv содержит (a) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 90, 96, 102, 108, 114, 120, 126, 132, 138, 144, 150, 156, 162, 168, 174, 180 и 186, а также их консервативных модификаций; и (b) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 93, 99, 105, 111, 117, 123, 129, 135, 141, 147, 153, 159, 165, 171, 177, 183 и 189, а также их консервативных модификаций.
В конкретных вариантах осуществления человеческий scFv содержит (a) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 89, 95, 101, 107, 113, 119, 125, 131, 137, 143, 149, 155, 161, 167, 173, 179 и 185, а также их консервативных модификаций; и (b) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 92, 98, 104, 110, 116, 122, 128, 134, 140, 146, 152, 158, 164, 170, 176, 182 и 188, а также их консервативных модификаций. В конкретных вариантах осуществления человеческий scFv содержит: (a) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 89, 95, 101, 107, 113, 119, 125, 131, 137, 143, 149, 155, 161, 167, 173, 179 и 185; (b) CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 90, 96, 102, 108, 114, 120, 126, 132, 138, 144, 150, 156, 162, 168, 174, 180 и 186; (c) CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 91, 97, 103, 109, 115, 121, 127, 133, 139, 145, 151, 157, 163, 169, 175, 181 и 187; (d) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 92, 98, 104, 110, 116, 122, 128, 134, 140, 146, 152, 158, 164, 170, 176, 182 и 188; (e) CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 93, 99, 105, 111, 117, 123, 129, 135, 141, 147, 153, 159, 165, 171, 177, 183 и 189; и (f) CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 94, 100, 106, 112, 118, 124, 130, 136, 142, 148, 154, 160, 166, 172, 178, 184 и 190. В конкретных вариантах осуществления человеческий scFv содержит (a) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 91, или ее консервативные модификации; (b) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 95, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 96, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 97, или ее консервативные модификации; (c) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 101, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 102, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 103, или ее консервативные модификации; (d) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 107, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 108, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 109, или ее консервативные модификации; (e) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 113, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 114, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 115, или ее консервативные модификации; (f) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, или ее консервативные модификации; (g) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127, или ее консервативные модификации; (h) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133, или ее консервативные модификации; (i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139, или ее консервативные модификации; (j) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145, или ее консервативные модификации; (k) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151, или ее консервативные модификации; (l) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157, или ее консервативные модификации; (m) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163, или ее консервативные модификации; (n) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169, или ее консервативные модификации; (o) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175, или ее консервативные модификации; (p) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181, или ее консервативные модификации; или (q) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185, или ее консервативные модификации; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186, или ее консервативные модификации; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187, или ее консервативные модификации. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186; и CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187.
В конкретных вариантах осуществления человеческий scFv содержит (a) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 92, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94, или ее консервативные модификации; (b) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 98, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 99, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 100, или ее консервативные модификации; (c) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 104, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 105, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 106, или ее консервативные модификации; (d) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 110, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 111, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 112, или ее консервативные модификации; (e) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 116, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 117, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 118, или ее консервативные модификации; (f) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, или ее консервативные модификации; (g) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130, или ее консервативные модификации; (h) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136, или ее консервативные модификации; (i) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142, или ее консервативные модификации; (j) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148, или ее консервативные модификации; (k) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154, или ее консервативные модификации; (l) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160, или ее консервативные модификации; (m) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166, или ее консервативные модификации; (n) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172, или ее консервативные модификации; (o) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178, или ее консервативные модификации; (p) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184, или ее консервативные модификации; или (q) CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188, или ее консервативные модификации; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189, или ее консервативные модификации; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190, или ее консервативные модификации. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190.
В конкретных вариантах осуществления человеческий scFv содержит: (a) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 91; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 92; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94; (b) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 95; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 96; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 97; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 98; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 99; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 100; (c) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 101; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 102; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 103; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 104; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 105; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 106; (d) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 107; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 108; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 109; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 110; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 111; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 112; (e) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 113; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 114; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 115; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 116; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 117; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 118; (f) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124; (g) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130; (h) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136; (i) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142; (j) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SE ID NO: 147; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148; (k) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154; (l) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160; (m) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166; (n) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172; (o) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178; (p) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184; или (q) CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184. В конкретных вариантах осуществления человеческий scFv содержит: CDR1 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185; CDR2 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186; CDR3 вариабельной области тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187; CDR1 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188; CDR2 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189; и CDR3 вариабельной области легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190.
В конкретных вариантах осуществления BCMA содержит аминокислотную последовательность, приведенную в SEQ ID NO: 71. В конкретных вариантах осуществления человеческий scFv связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71. В конкретных вариантах осуществления человеческий scFv, который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22. В конкретных вариантах осуществления человеческий scFv, который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124.
В соответствии с настоящим изобретением, внеклеточный антигенсвязывающий домен ковалентно связан с трансмембранным доменом. Внеклеточный антигенсвязывающий домен может содержать сигнальный пептид, который ковалентно связан с 5'-концом внеклеточного антигенсвязывающего домена. В конкретных вариантах осуществления трансмембранный домен CAR содержит полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид CTLA-4, полипептид PD-1, полипептид LAG-3, полипептид 2B4, полипептид BTLA, синтетический пептид (не на основе белка, связанного с иммунным ответом) или их сочетание. В конкретных вариантах осуществления трансмембранный домен содержит полипептид CD8. В конкретных вариантах осуществления трансмембранный домен содержит полипептид CD28.
В соответствии с настоящим изобретением, внутриклеточный домен содержит полипептид CD3ζ. В конкретных вариантах осуществления внутриклеточный домен дополнительно содержит по меньшей мере одну сигнальную область. В конкретных вариантах осуществления по меньшей мере одна сигнальная область содержит полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10, полипептид PD-1, полипептид CTLA-4, полипептид LAG-3, полипептид 2B4, полипептид BTLA, синтетический пептид (не на основе белка, связанного с иммунным ответом) или их сочетание. В конкретных вариантах осуществления сигнальная область представляет собой костимулирующую сигнальную область. В конкретных вариантах осуществления костимулирующая сигнальная область содержит полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10 или их сочетание. В конкретных вариантах осуществления по меньшей мере одна костимулирующая сигнальная область содержит полипептид CD28. В конкретных вариантах осуществления по меньшей мере одна сигнальная область содержит полипептид 4-1BB. В одном конкретном неограничивающем варианте осуществления трансмембранный домен содержит полипептид CD28, внутриклеточный домен содержит полипептид CD3ζ и по меньшей мере один сигнальный домен содержит полипептид CD28.
В конкретных вариантах осуществления CAR экспрессируется рекомбинантно. CAR может экспрессироваться с вектора. В конкретных вариантах осуществления вектор представляет собой γ-ретровирусный вектор.
Настоящее изобретение также относится к выделенным иммунореактивным клеткам, содержащим вышеописанные CAR. В конкретных вариантах осуществления выделенная иммунореактивная клетка трансдуцирована CAR, например, CAR конститутивно экспрессируется на поверхности иммунореактивной клетки. В конкретных вариантах осуществления выделенная иммунореактивная клетка дополнительно трансдуцирована по меньшей мере одним костимулирующим лигандом, вследствие чего иммунореактивная клетка экспрессирует по меньшей мере один костимулирующий лиганд. В конкретных вариантах осуществления по меньшей мере один костимулирующий лиганд выбирают из группы, состоящей из 4-1BBL, CD80, CD86, CD70, OX40L, CD48, TNFRSF14, а также их сочетаний. В конкретных вариантах осуществления выделенная иммунореактивная клетка дополнительно трансдуцирована по меньшей мере одним цитокином, вследствие чего иммунореактивная клетка секретирует по меньшей мере один цитокин. В конкретных вариантах осуществления по меньшей мере один цитокин выбирают из группы, состоящей из IL-2, IL-3, IL-6, IL-7, IL-11, IL-12, IL-15, IL-17, IL-21, а также их сочетаний. В некоторых вариантах осуществления выделенную иммунореактивную клетку выбирают из группы, состоящей из T-клетки, клетки-естественного киллера (NK), цитотоксического T-лимфоцита (CTL), регуляторной T-клетки, человеческой эмбриональной стволовой клетки, лимфоидной клетки-предшественника, клетки-предшественника T-клетки и плюрипотентной стволовой клетки, из которой могут дифференцироваться лимфоидные клетки. В конкретных вариантах осуществления иммунореактивная клетка представляет собой T-клетку.
Настоящее изобретение также относится к молекулам нуклеиновой кислоты, кодирующим раскрытые в настоящем документе CAR, векторам, содержащим молекулы нуклеиновой кислоты, и клеткам-хозяевам, экспрессирующим такие молекулы нуклеиновой кислоты. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 207. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 208. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 209. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 229. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 230. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 231. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 232. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 233. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 234. В конкретных вариантах осуществления молекула нуклеиновой кислоты имеет нуклеотидную последовательность, приведенную в SEQ ID NO: 235. В конкретных вариантах осуществления вектор представляет собой γ-ретровирусный вектор. В конкретных вариантах осуществления клетка-хозяин представляет собой T-клетку.
Кроме того, настоящее изобретение относится к способам применения вышеописанной иммунореактивной клетки для уменьшения опухолевой нагрузки у субъекта. Например, настоящее изобретение относится к способу уменьшения опухолевой нагрузки у субъекта, включающему введение эффективного количества раскрытой в настоящем документе иммунореактивной клетки субъекту, в результате чего индуцируется гибель опухолевых клеток у субъекта. В конкретных вариантах осуществления способ приводит к уменьшению количества опухолевых клеток. В другом варианте осуществления способ приводит к уменьшению размера опухоли. В другом варианте осуществления способ приводит к уничтожению опухоли у субъекта. В конкретных вариантах осуществления опухоль выбирают из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема. В конкретных вариантах осуществления опухоль представляет собой множественную миелому. В конкретных вариантах осуществления субъект является человеком. В конкретных вариантах осуществления иммунореактивная клетка представляет собой T-клетку.
Кроме того, настоящее изобретение относится к способам применения вышеописанной иммунореактивной клетки для увеличения или продления срока выживания субъекта, имеющего неоплазию. Например, настоящее изобретение относится к способу увеличения или продления срока выживания субъекта, имеющего неоплазию, включающему введение эффективного количества раскрытой в настоящем документе иммунореактивной клетки субъекту, в результате чего увеличивается или продлевается срок выживания субъекта. В конкретных вариантах осуществления неоплазию выбирают из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема. В конкретных вариантах осуществления неоплазия представляет собой множественную миелому. В конкретных вариантах осуществления способ приводит к уменьшению или уничтожению опухолевой нагрузки у субъекта.
Настоящее изобретение также относится к способам получения иммунореактивной клетки, которая связывается с BCMA. В одном неограничивающем примере способ включает введение в иммунореактивную клетку нуклеотидной последовательности, кодирующей химерный антигенный рецептор (CAR), который содержит внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен, при этом внеклеточный антигенсвязывающий домен содержит человеческий scFv, который специфически связывается с BCMA.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим эффективное количество раскрытых в настоящем документе иммунореактивных клеток и фармацевтически приемлемый эксципиент. В конкретных вариантах осуществления фармацевтические композиции предназначены для лечения неоплазии. В конкретных вариантах осуществления неоплазию выбирают из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема. В конкретных вариантах осуществления неоплазия представляет собой множественную миелому.
Настоящее изобретение также относится к наборам для лечения неоплазии, включающим раскрытые в настоящем документе иммунореактивные клетки. В конкретных вариантах осуществления набор дополнительно включает письменные инструкции по применению иммунореактивной клетки для лечения неоплазии. В конкретных вариантах осуществления неоплазию выбирают из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема. В конкретных вариантах осуществления неоплазия представляет собой множественную миелому.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Следующее далее подробное описание, приведенное в качестве примера, но не предназначенное для ограничения изобретения конкретными описанными вариантами осуществления, может быть понятным в сочетании с сопроводительными чертежами.
На фигуре 1 представлен химерный антигенный рецептор, нацеленный на BCMA, в соответствии с одним неограничивающим вариантом осуществления настоящего изобретения.
На фигуре 2 показана экспрессия BCMA человека в нормальных тканях и линиях раковых клеток человека.
На фигуре 3 показана экспрессия раскрытого в настоящем документе BCMA CAR на T-клетках человека.
На фигуре 4 показана перекрестная реактивность человеческих scFv, нацеленных на BCMA человека, с BCMA мыши.
На фигуре 5 показана цитолитическая активность раскрытого в настоящем документе BCMA CAR в отношении клеток 3T3, избыточно экспрессирующих BCMA.
На фигуре 6 показана цитолитическая активность раскрытого в настоящем документе BCMA CAR в отношении линии клеток множественной миеломы человека.
На фигуре 7 представлен химерный антигенный рецептор, нацеленный на BCMA, в соответствии с одним неограничивающим вариантом осуществления настоящего изобретения.
На фигуре 8 представлена молекула нуклеиновой кислоты, кодирующая BCMA-нацеленный CAR в соответствии с одним неограничивающим вариантом осуществления настоящего изобретения.
На фигуре 9 представлена молекула нуклеиновой кислоты, кодирующая BCMA-нацеленный CAR в соответствии с одним неограничивающим вариантом осуществления настоящего изобретения.
На фигуре 10 представлена молекула нуклеиновой кислоты, кодирующая BCMA-нацеленный CAR в соответствии с одним неограничивающим вариантом осуществления настоящего изобретения.
На фигуре 11 представлена молекула нуклеиновой кислоты, кодирующая BCMA-нацеленный CAR в соответствии с одним неограничивающим вариантом осуществления настоящего изобретения.
На фигуре 12 представлена молекула нуклеиновой кислоты, кодирующая BCMA-нацеленный CAR в соответствии с одним неограничивающим вариантом осуществления настоящего изобретения.
На фигуре 13 показана цитотоксичность нацеленных на BCMA CAR T-клеток в отношении линий клеток множественной миеломы человека.
На фигуре 14 показана индукция секреции цитокинов BCMA-нацеленных CAR T-клеток.
На фигуре 15 показана противоопухолевая активность BCMA-нацеленных CAR T-клеток.
На фигурах 16A и 16B показана цитолитическая активность BCMA-нацеленных CAR T-клеток. (A) Показано процентное содержание GFP+ клеток опухолевой линии в момент времени 0. (B) Показан процент уничтожения GFP+ клеток опухолевой линии в момент времени 36 часов.
На фигуре 17 показано картирование эпитопов ET140-3.
На фигуре 18 показано картирование эпитопов ET140-24.
На фигуре 19 показано картирование эпитопов ET140-54.
На фигуре 20 показано картирование эпитопов ET140-3, ET140-24 и ET140-54.
На фигуре 21 представлены данные скрининга ET140-3, ET140-24, ET140-37, ET140-40 и ET140-54 методом ELISA.
На фигуре 22 представлены данные скрининга ET140-3, ET140-24, ET140-37, ET140-40 и ET140-54 методом FACS.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение, в целом, относится к химерным антигенным рецепторам (CAR), нацеленным на BCMA. В одном неограничивающем примере CAR содержит внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен, при этом внеклеточный антигенсвязывающий домен специфически связывается с BCMA. Настоящее изобретение также относится к иммунореактивным клеткам (например, T-клетке, клетке-естественному киллеру (NK), цитотоксическому T-лимфоциту (CTL), регуляторной T-клетке, человеческой эмбриональной стволовой клетке, лимфоидной клетке-предшественнику, клетке-предшественнику T-клетки и плюрипотентной стволовой клетке, из которой могут дифференцироваться лимфоидные клетки), экспрессирующим BCMA-нацеленные CAR, и способам применения таких иммунореактивных клеток для лечения опухоли, например, множественной миеломы.
I. Определения
Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют то значение, которое им обычно придают специалисты в области, к которой относится данное изобретение. В следующих литературных источниках специалист может найти определения многих терминов, используемых в рамках данного изобретения: Singleton et al., Dictionary of Microbiology and Molecular Biology (2-е издание, 1994); The Cambridge Dictionary of Science and Technology (Walker ed., 1988); The Glossary of Genetics, 5-е издание, R. Rieger et al. (eds.), Springer Verlag (1991); и Hale & Marham, The Harper Collins Dictionary of Biology (1991). Следующие термины, используемые в настоящем документе, имеют значения, определенные для них ниже, если не указано иное.
Используемый в настоящем документе термин «примерно» или «приблизительно» означает допустимый диапазон ошибки для конкретной величины, что может определять рядовой специалист в данной области; этот диапазон будет зависеть частично от того, каким образом величину определяют или измеряют, то есть, от ограничений системы измерения. Например, «примерно» может означать «в пределах 3 или более чем 3 стандартных отклонений», в соответствии с практикой в данной области. Альтернативно, «примерно» может означать «диапазон вплоть до 20%, предпочтительно до 10%, более предпочтительно до 5% и даже более предпочтительно до 1% от конкретной величины». Альтернативно, особенно в случае биологических систем или процессов, термин может означать «в пределах порядка величины», предпочтительно в пределах 5-кратного значения, и более предпочтительно, в пределах 2-двукратного значения величины.
Используемый в настоящем документе термин «популяция клеток» означает группу из по меньшей мере двух клеток, имеющих сходные или разные фенотипы. В неограничивающих примерах популяция клеток может включать по меньшей мере примерно 10, по меньшей мере примерно 100, по меньшей мере примерно 200, по меньшей мере примерно 300, по меньшей мере примерно 400, по меньшей мере примерно 500, по меньшей мере примерно 600, по меньшей мере примерно 700, по меньшей мере примерно 800, по меньшей мере примерно 900, по меньшей мере примерно 1000 клеток, имеющих сходные или разные фенотипы.
Используемый в настоящем документе термин «антитело» означает не только интактные молекулы антител, но также и фрагменты молекул антител, которые сохраняют способность связывать иммуноген. Такие фрагменты также хорошо известны в данной области и постоянно используются как in vitro, так и in vivo. Соответственно, используемый в настоящем документе термин «антитело» означает не только интактные молекулы иммуноглобулинов, но также и хорошо известные активные фрагменты F(ab')2 и Fab. Фрагменты F(ab')2 и Fab, которые лишены Fc-фрагмента интактного антитела, быстрее удаляются из системы циркуляции и могут отличаться меньшим неспецифическим связыванием с тканями, чем интактное антитело (Wahl et al., J. Nucl. Med. 24: 316-325 (1983)). Антитела по изобретению включают полноразмерные природные антитела, биспецифические антитела; химерные антитела; Fab, Fab', одноцепочечные фрагменты V-области (scFv), слитые полипептиды и необычные антитела.
Используемый в настоящем документе термин «одноцепочечный вариабельный фрагмент» или «scFv» означает слитый белок из вариабельных областей тяжелой (VH) и легкой (VL) цепей иммуноглобулина (например, мыши или человека), ковалентно связанных, с образованием VH::VL гетеродимера. Тяжелая (VH) и легкая (VL) цепи либо связаны напрямую, либо связаны с помощью закодированного пептидного линкера (например, длиной 10, 15, 20, 25 аминокислот), который соединяет N-конец VH с C-концом VL или C-конец VH с N-концом VL. Как правило, линкер бывает богат остатками глицина для гибкости, а также остатками серина или треонина для растворимости. Линкер может связывать вариабельную область тяжелой цепи и вариабельную область легкой цепи внеклеточного антигенсвязывающего домена. Неограничивающие примеры линкеров приведены в Shen et al., Anal. Chem. 80(6): 1910-1917 (2008) и WO 2014/087010, полное содержание которых включено в настоящий документ посредством ссылки. В конкретных вариантах осуществления линкер представляет собой линкер G4S.
В неограничивающем примере линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 210, которая представлена ниже.
GGGGSGGGGSGGGGS [SEQ ID NO: 210].
В конкретных вариантах осуществления нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 210, приведена в SEQ ID NO: 211, которая представлена ниже:
GGTGGAGGTGGATCAGGTGGAGGTGGATCTGGTGGAGGTGGATCT [SEQ ID NO: 211].
В одном неограничивающем примере линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69, которая представлена ниже.
SRGGGGSGGGGSGGGGSLEMA [SEQ ID NO: 69]
В конкретных вариантах осуществления нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 69, приведена в SEQ ID NO: 70, которая представлена ниже:
tctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggcc [SEQ ID NO: 70]
Несмотря на удаление константных областей и введение линкера, белки scFv сохраняют специфичность исходного иммуноглобулина. Антитела, представляющие собой одноцепочечный полипептид Fv, могут экспрессироваться с нуклеиновой кислоты, содержащей кодирующие VH и VL последовательности, как описано в Huston, et al. (Proc. Nat. Acad. Sci. USA, 85: 5879-5883, 1988). Смотри также патенты США №№ 5091513, 5132405 и 4956778; и публикации патентов США №№ 20050196754 и 20050196754. Описаны антагонистические scFv, обладающие ингибирующей активностью (смотри, например, Zhao et al., Hyrbidoma (Larchmt) 2008 27(6): 455-51; Peter et al., J Cachexia Sarcopenia Muscle 2012 August 12; Shieh et al., J Imunol 2009 183(4): 2277-85; Giomarelli et al., Thromb Haemost 2007 97(6): 955-63; Fife et al., J Clin Invst 2006 116(8): 2252-61; Brocks et al., Immunotechnology 1997 3(3): 173-84; Moosmayer et al., Ther Immunol 1995 2(10: 31-40). Описаны агонистические scFv, обладающие стимулирующей активностью (смотри, например, Peter et al., J Biol Chem 2003 25278(38): 36740-7; Xie et al., Nat Biotech 1997 15(8): 768-71; Ledbetter et al., Crit Rev Immunol1997 17(5-6): 427-55; Ho et al., BioChim Biophys Acta 2003 1638(3): 257-66).
Используемый в настоящем документе термин «F(ab)» означает фрагмент структуры антитела, который связывается с антигеном, но является одновалентным и не имеет Fc-части, например, при расщеплении антитела ферментом папаином образуются два F(ab)-фрагмента и Fc-фрагмент (например, константная область тяжелой (H) цепи; Fc-область, которая не связывается с антигеном).
Используемый в настоящем документе термин «F(ab')2» означает фрагменты антитела, получаемые при расщеплении пепсином целых IgG антител, причем данный фрагмент имеет две антигенсвязывающие области (ab') (двухвалентные), причем каждая (ab') область содержит две отдельные аминокислотные цепи, часть H-цепи и легкая (L) цепь соединены S-S связью для связывания антигена и при этом оставшиеся части H-цепей связаны вместе. «F(ab')2»-фрагмент может быть разделен на два отдельных Fab'-фрагмента.
Используемый в настоящем документе термин «вектор» означает любой генетический элемент, такой как плазмида, фаг, транспозон, космида, хромосома, вирус, вирион и так далее, который способен к репликации, будучи связан с правильными контрольными элементами, и который может переносить последовательности генов в клетки. Таким образом, термин охватывает клонирующие и экспрессионные векторы, а также вирусные векторы и плазмидные векторы.
Используемый в настоящем документе термин «экспрессионный вектор» означает рекомбинантную нуклеотидную последовательность, то есть, молекулу рекомбинантной ДНК, содержащую нужную кодирующую последовательность и соответствующие нуклеотидные последовательности, необходимые для экспрессии функционально связанной кодирующей последовательности в конкретном организме-хозяине. Нуклеотидные последовательности, необходимые для экспрессии в прокариотах, как правило, включают промотор, оператор (необязательно) и сайт связывания рибосомы, часто наряду с другими последовательностями. В эукариотических клетках, как известно, используются промоторы, энхансеры, а также последовательности терминации и сигналы полиаденилирования.
Используемый в настоящем документе термин «CDR» означает аминокислотные последовательности определяющей комплементарность области антитела, которые представляют собой гипервариабельные области тяжелых и легких цепей иммуноглобулинов. Смотри, например, Kabat et al., Sequences of Proteins of Immunological Interest, 4-е издание, U.S. Department of Health and Human Services, National Institutes of Health (1987). Как правило, антитела содержат по три области CDR, или CDR, в вариабельных областях тяжелой цепи и легкой цепи. CDR предоставляют большинство контактирующих остатков для связывания антитела с антигеном или эпитопом. В конкретных вариантах осуществления границы областей CDR определяют, используя систему Kabat (Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest, пятое издание, U.S. Department of Health и Human Services, NIH Publication No. 91-3242).
Используемый в настоящем документе термин «аффинность» означает меру силы связывания. Без привязки к конкретной теории, аффинность зависит от близости, создаваемой стереохимическим соответствием, между антигенсвязывающим центром антитела и антигенными детерминантами, от размера области контакта между ними и от распределения заряженных и гидрофобных групп. Аффинность также включает термин «авидность», который означает силу связи антиген-антитело после образования обратимых комплексов. Методы расчета аффинности антитела для антигена известны в данной области, они включают проведение экспериментов по связыванию для расчета аффинности. Активность антитела в функциональных анализах (например, в анализе методом проточной цитометрии) также является отражением аффинности антитела. Антитела и показатели аффинности можно фенотипически характеризовать и сравнивать с использованием функциональных анализов (например, анализа методом проточной цитометрии).
Молекулы нуклеиновой кислоты, полезные в способах по изобретению, включают любую молекулу нуклеиновой кислоты, которая кодирует полипептид по изобретению или его фрагмент. Такие молекулы нуклеиновой кислоты не обязательно должны быть на 100% идентичны эндогенной нуклеотидной последовательности, однако они, как правило, будут иметь существенную идентичность. Полинуклеотиды, имеющие «существенную идентичность» с эндогенной последовательностью, как правило, способны гибридизоваться с по меньшей мере одной цепью двухцепочечной молекулы нуклеиновой кислоты. «Гибридизация» означает спаривание, с образованием двухцепочечной молекулы, между комплементарными полинуклеотидными последовательностями (например, гена, описанного в настоящем документе) или их частями в разных условиях строгости. (Смотри, например, Wahl, G. M. and S. L. Berger (1987) Methods Enzymol. 152: 399; Kimmel, A. R. (1987) Methods Enzymol. 152: 507).
Например, концентрация соли в строгих условиях, как правило, будет составлять менее примерно 750 мМ NaCl и 75 мМ цитрата тринатрия, предпочтительно менее примерно 500 мМ NaCl и 50 мМ цитрата тринатрия, и более предпочтительно менее примерно 250 мМ NaCl и 25 мМ цитрата тринатрия. Низкую строгость условий гибридизации можно получать в отсутствие органических растворителей, например, формамида, в то время как высокую строгость условий гибридизации можно получать в присутствии по меньшей мере примерно 35% формамида, и более предпочтительно по меньшей мере примерно 50% формамида. Температура в строгих условиях, как правило, включает температуру по меньшей мере примерно 30°C, более предпочтительно по меньшей мере примерно 37°C и наиболее предпочтительно по меньшей мере примерно 42°C. Различные дополнительные параметры, такие как время гибридизации, концентрация детергента, например, додецилсульфата натрия (SDS), а также включение или исключение ДНК-носителя, хорошо известны специалистам в данной области. Комбинируя эти различные условия по мере необходимости, можно добиваться различных уровней строгости. В предпочтительном варианте осуществления гибридизация будет происходить при 30°C в растворе, содержащем 750 мМ NaCl, 75 мМ цитрата тринатрия и 1% SDS. В более предпочтительном варианте осуществления гибридизация будет происходить при 37°C в растворе, содержащем 500 мМ NaCl, 50 мМ цитрата тринатрия, 1% SDS, 35% формамида и 100 мкг/мл денатурированной ДНК спермы лосося (оцДНК). В наиболее предпочтительном варианте осуществления гибридизация будет происходить при 42°C в растворе, содержащем 250 мМ NaCl, 25 мМ цитрата тринатрия, 1% SDS, 50% формамида и 200 мкг/мл оцДНК. Полезные вариации этих условий будут очевидны для специалистов в данной области.
В большинстве случаев строгость условий на этапах промывания после гибридизации также будут варьироваться. Строгость условий при промывании может определяться концентрацией соли и температурой. Как описано выше, строгость условий при промывании можно повышать путем снижения концентрации соли или путем повышения температуры. Например, концентрация соли в строгих условиях на этапах промывания предпочтительно будет составлять менее примерно 30 мМ NaCl и 3 мМ цитрата тринатрия, и наиболее предпочтительно менее примерно 15 мМ NaCl и 1,5 мМ цитрата тринатрия. Температура в строгих условиях на этапах промывания, как правило, будет включать температуру по меньшей мере примерно 25°C, более предпочтительно по меньшей мере примерно 42°C, и еще более предпочтительно по меньшей мере примерно 68°C. В предпочтительном варианте осуществления этапы промывания будут проводиться при 25°C в растворе, содержащем 30 мМ NaCl, 3 мМ цитрата тринатрия и 0,1% SDS. В более предпочтительном варианте осуществления этапы промывания будут проводиться при 42°C в растворе, содержащем 15 мМ NaCl, 1,5 мМ цитрата тринатрия и 0,1% SDS. В более предпочтительном варианте осуществления этапы промывания будут проводиться при 68°C в растворе, содержащем 15 мМ NaCl, 1,5 мМ цитрата тринатрия и 0,1% SDS. Дополнительные вариации этих условий будут очевидны для специалистов в данной области. Методы гибридизации хорошо известны специалистам в данной области и описаны, например, в Benton and Davis (Science 196: 180, 1977); Grunstein and Rogness (Proc. Natl. Acad. Sci., USA 72: 3961, 1975); Ausubel et al. (Current Protocols in Molecular Biology, Wiley Interscience, New York, 2001); Berger and Kimmel (Guide to Molecular Cloning Techniques, 1987, Academic Press, New York); и Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, New York.
Выражение «по существу идентичны» означает, что полипептид или молекула нуклеиновой кислоты проявляет по меньшей мере 50% идентичности с эталонной аминокислотной последовательностью (например, любой из аминокислотных последовательностей, описанных в настоящем документе) или нуклеотидной последовательностью (например, например, любой из нуклеотидных последовательностей, описанных в настоящем документе). Предпочтительно, такая последовательность на по меньшей мере 60%, более предпочтительно 80% или 85%, и более предпочтительно 90%, 95% или даже 99% идентична на аминокислотном или нуклеотидном уровне последовательности, используемой для сравнения.
Идентичность последовательностей, как правило, определяют с использованием программ анализа последовательностей (например, пакета программ для анализа последовательностей от Genetics Computer Group, University of Wisconsin Biotechnology Center, 1710 University Avenue, Madison, Wis. 53705; программ BLAST, BESTFIT, GAP или PILEUP/PRETTYBOX). Такие программы сопоставляют идентичные или сходные последовательности путем присвоения степени гомологии в случае различных замен, делеций и/или других модификаций. В иллюстративном подходе для определения степени идентичности можно использовать программу BLAST с показателем вероятности от e-3 до e-100, указывающим на близкородственную последовательность.
Используемый в настоящем документе термин «аналог» означает структурно родственный полипептид или молекулу нуклеиновой кислоты, обладающие функцией эталонного полипептида или молекулы нуклеиновой кислоты.
Используемый в настоящем документе термин «лиганд» означает молекулу, которая связывается с рецептором. В частности, лиганд связывает рецептор на другой клетке, делая возможным межклеточное узнавание и/или взаимодействие.
Используемый в настоящем документе термин «заболевание» означает любое состояние или расстройство, которое нарушает или препятствует нормальному функционированию клетки, ткани или органа. Примеры заболеваний включают неоплазию или инфицирование патогенами клетки.
Используемый в настоящем документе термин «эффективное количество» означает количество, достаточное для достижения терапевтического эффекта. В конкретных вариантах осуществления «эффективное количество» представляет собой количество, достаточное для остановки, ослабления или ингибирования непрерывной пролиферации, роста или метастазирования (например, инвазии или миграции) неоплазии.
Используемый в настоящем документе термин «гетерологичные молекула нуклеиновой кислоты или полипептид» означает молекулу нуклеиновой кислоты (например, молекулу кДНК, ДНК или РНК) или полипептид, которые обычно не присутствуют в клетке или образце, полученном из клетки. Такая нуклеиновая кислота может быть из другого организма или она, например, может представлять собой молекулу мРНК, которая обычно не экспрессируется в клетке или образце.
Используемый в настоящем документе термин «иммунореактивная клетка» означает клетку, которая функционирует при иммунном ответе, либо ее предшественника или потомство.
Используемый в настоящем документе термин «модуляция» означает положительное или отрицательное изменение. Иллюстративная модуляция включает изменение на примерно 1%, примерно 2%, примерно 5%, примерно 10%, примерно 25%, примерно 50%, примерно 75% или примерно 100%.
Используемый в настоящем документе термин «увеличение» означает положительное изменение на по меньшей мере примерно 5%, включая, но без ограничения, положительное изменение на примерно 5%, на примерно 10%, на примерно 25%, на примерно 30%, на примерно 50%, на примерно 75% или на примерно 100%.
Используемый в настоящем документе термин «уменьшение» означает отрицательное изменение на по меньшей мере примерно 5%, включая, но без ограничения, отрицательное изменение на примерно 5%, на примерно 10%, на примерно 25%, на примерно 30%, на примерно 50%, на примерно 75% или на примерно 100%.
Используемый в настоящем документе термин «выделенная клетка» означает клетку, которая отделена от молекулярных и/или клеточных компонентов, которые обычно окружают клетку.
Используемый в настоящем документе термин «выделенный», «очищенный» или «биологически чистый» относится к материалу, который в разной степени свободен от компонентов, которые обычно окружают его в его естественном состоянии. «Выделенный» указывает на состояние отделенности от исходного источника или окружающей среды. «Очищенный» указывает на более высокую степень отделенности, чем при выделении. «Очищенный» или «биологически чистый» белок в достаточной степени свободен от других материалов, так что любые примеси существенно не влияют на биологические свойства белка или не вызывают другие неблагоприятные последствия. То есть, нуклеиновая кислота или пептид по данному изобретению являются очищенными, если они по существу свободны от клеточного материала, вирусного материала или культуральной среды в случае получения методами рекомбинантной ДНК, либо химических предшественников или других химических реагентов в случае химического синтеза. Чистоту и гомогенность, как правило, определяют методами аналитической химии, например, электрофорезом в полиакриламидном геле или высокоэффективной жидкостной хроматографией. Термин «очищенный» может указывать на то, что нуклеиновая кислота или белок образуют практически одну полосу в геле при электрофорезе. В случае белка, который может быть подвергнут модификациям, например, фосфорилированию или гликозилированию, различные модификации могут приводить к образованию разных выделенных белков, которые могут быть очищены отдельно.
Используемый в настоящем документе термин «секретируемый» относится к полипептиду, который высвобождается из клетки секреторным путем через эндоплазматический ретикулум, аппарат Гольджи и в виде везикула, который временно сливается с клеточной плазматической мембраной, выводя белки из клетки.
Используемый в настоящем документе термин «специфически связывает» или «специфически связывается с» или «специфически нацелен» означает, что полипептид или его фрагмент узнает и связывает интересующую биологическую молекулу (например, полипептид), но практически не узнает и не связывает другие молекулы в образце, например, биологическом образце, который естественным образом содержит полипептид по изобретению.
Используемый в настоящем документе термин «лечение» или «терапия» означает клиническое вмешательство в попытке изменить течение заболевания у индивидуума или клетки, которые подвергают лечению, и которое может производиться либо в профилактических целях, либо во время клинической патологии. Терапевтические эффекты лечения включают, но не ограничиваются ими, предотвращение возникновения или рецидива заболевания, ослабление симптомов, уменьшение любых прямых или косвенных патологических последствий заболевания, предотвращение метастазирования, снижение скорости прогрессирования заболевания, облегчение или ослабление болезненного состояния, а также достижение ремиссии или более благоприятного прогноза. В случае предотвращения заболевания или нарушения, лечение может предотвращать ухудшение состояния вследствие заболевания у субъекта с текущим или диагностированным заболеванием, или у субъекта, предположительно имеющего заболевание, однако лечение также способно предотвращать начало развития заболевания или симптома заболевания у субъекта, имеющего риск развития заболевания или предположительно имеющего заболевание.
Используемый в настоящем документе термин «субъект» означает любое животное (например, млекопитающее), включая, но без ограничения, людей, приматов, кроме человека, грызунов и тому подобное (например, которые будут получать конкретное лечение или от которых будут получены клетки).
II. Антиген созревания B-клеток (BCMA)
BCMA является идеальной мишенью для адоптивной T-клеточной терапии (например, терапии CAR), поскольку BCMA вовлечен в дифференциацию и сигнализацию B-клеток и, как известно, экспрессируется на незлокачественных дифференцированных B-клетках и плазматических клетках. Хотя может существовать риск индуцирования аплазии В-клеток, аплазия B-клеток, индуцируемая CD19 CAR, переносилась довольно легко. Несколько групп исследователей подтвердили экспрессию BCMA на поверхности клеток множественной миеломы (MM), при этом одна группа исследователей установила, что он может являться альтернативой CD138 в качестве FACS маркера для злокачественных плазматических клеток из свежих или замороженных образцов, полученных от пациента, с величиной средней относительной СИФ, составляющей 9-16 (n=35)1,2.
В конкретных неограничивающих вариантах осуществления BCMA представляет собой BCMA человека, имеющий аминокислотную последовательность, приведенную в SEQ ID NO: 71, или его фрагменты.
SEQ ID NO: 71 представлена ниже:
MLQMAGQCSQNEYFDSLLHACIPCQLRCSSNTPPLTCQRYCNASVTNSVKGTNAI
LWTCLGLSLIISLAVFVLMFLLRKINSEPLKDEFKNTGSGLLGMANIDLEKSRTGDE
IILPRGLEYTVEECTCEDCIKSKPKVDSDHCFPLPAMEEGATILVTTKTNDYCKSLPA
ALSATEIEKSISAR [SEQ ID NO: 71]
III. Химерный антигенный рецептор (CAR).
Химерные антигенные рецепторы (CAR) представляют собой сконструированные рецепторы, которые сообщают или придают интересующую специфичность иммунной эффекторной клетке. CAR можно использовать для придания специфичности моноклонального антитела T-клетке; при этом перенос их кодирующей последовательности осуществляют с помощью ретровирусных векторов.
Известно три поколения CAR. CAR «первого поколения», как правило, состоят из внеклеточного антигенсвязывающего домена (например, одноцепочечных вариабельных фрагментов (scFv)), слитого с трансмембранным доменом, слитым с цитоплазматическим/внутриклеточным доменом цепи T-клеточного рецептора. CAR «первого поколения», как правило, имеют внутриклеточный домен из CD3ξ-цепи, который является основным передатчиком сигналов от эндогенных TCR. CAR «первого поколения» могут обеспечивать узнавание de novo антигена и вызывать активацию как CD4+, так и CD8+ T-клеток через их сигнальный домен CD3ζ-цепи в одной слитой молекуле, независимо от опосредованного HLA представления антигена. В CAR «второго поколения» добавлены внутриклеточные домены из разных костимулирующих молекул (например, CD28, 4-1BB, ICOS, OX40) к цитоплазматическому хвосту CAR для обеспечения дополнительных сигналов для T-клетки. CAR «второго поколения» включают те, которые обеспечивают как костимуляцию (например, CD28 или 4-1BB), так и активацию (CD3ζ). Доклинические исследования показали, что CAR «второго поколения» способны повышать противоопухолевую активность T-клеток. Например, устойчивая эффективность T-клеток, модифицированных CAR «второго поколения», была продемонстрирована в клинических испытаниях по таргетированию молекулы CD19 у пациентов с хроническим лимфобластным лейкозом (CLL) и острым лимфобластным лейкозом (ALL). CAR «третьего поколения» включают те, которые обеспечивают множественную костимуляцию (например, CD28 и 4-1BB) и активацию (CD3ζ).
В соответствии с настоящим изобретением, CAR содержат внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен, при этом внеклеточный антигенсвязывающий домен связывается с BCMA. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой scFv. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой Fab, который, необязательно, является сшитым. В конкретных вариантах осуществления внеклеточный связывающий домен представляет собой F(ab)2. В конкретных вариантах осуществления любая из вышеуказанных молекул может находиться в слитом белке с гетерологичной последовательностью, образуя внеклеточный антигенсвязывающий домен. В одном конкретном неограничивающем варианте осуществления внеклеточный антигенсвязывающий домен содержит человеческий scFv, который специфически связывается с BCMA человека.
В конкретных неограничивающих вариантах осуществления внеклеточный антигенсвязывающий домен CAR имеет высокую специфичность связывания, а также высокую аффинность связывания с BCMA. Например, в таких вариантах осуществления внеклеточный антигенсвязывающий домен CAR (представляющий собой, например, человеческий scFv или его аналог) связывается с BCMA с константой диссоциации (KD), составляющей примерно 3×10-6 M или менее. В конкретных вариантах осуществления KD составляет примерно 1×10-6 M или менее, примерно 1×10-7 M или менее, примерно 1×10-8 M или менее, или примерно 1×10-9 M или менее, примерно 1×10-10 M или менее, или примерно 1×10-11 M или менее. В конкретных вариантах осуществления Kd составляет примерно 1×10-8 M или менее. В конкретных вариантах осуществления Kd составляет от примерно 1×10-11 M до примерно 3×10-6 M, например, от примерно 1×10-11 M до примерно 1×10-10 M, от примерно 1×10-10 M до примерно 1×10-9 M, от примерно 1×10-9 M до примерно 1×10-8 M, от примерно 1×10-8 M до примерно 1×10-7 M, или от примерно 1×10-7 M до примерно 1×10-6 M, или от примерно 1×10-6 M до примерно 3×10-6 M. В конкретных вариантах осуществления Kd составляет от примерно 1×10-9 M до примерно 1×10-8 M. В конкретных вариантах осуществления Kd составляет от примерно 1×10-9 M до примерно 1,5×10-9 M. В конкретных вариантах осуществления Kd составляет примерно 1,2×10-9 M. В конкретных вариантах осуществления Kd составляет от примерно 4×10-9 M до примерно 5×10-9 M. В конкретных вариантах осуществления Kd составляет примерно 5×10-9 M. В конкретных вариантах осуществления Kd составляет примерно 4,8×10-9 M. В конкретных вариантах осуществления Kd составляет от примерно 8×10-9 M до примерно 9×10-9 M. В конкретных вариантах осуществления Kd составляет примерно 8×10-9 M. В конкретных вариантах осуществления Kd составляет примерно 8,1×10-9 M.
Связывание внеклеточного антигенсвязывающего домена (представляющего собой, например, человеческий scFv или его аналог) раскрытого в настоящем документе CAR с BCMA можно подтверждать, например, твердофазным иммуноферментным анализом (ELISA), радиоиммунным анализом (RIA), FACS-анализом, биоанализом (например, ингибированием роста) или вестерн-блоттингом. Каждый из этих анализов, как правило, позволяет обнаруживать наличие конкретных интересующих комплексов белок-антитело за счет использования меченого реагента (например, антитела или scFv), специфичного для интересующего комплекса. Например, scFv можно метить радиоактивной меткой и использовать в радиоиммунном анализе (RIA) (смотри, например, публикацию Weintraub, B., Principles of Radioimmunoassays, Seventh Training Course on Radioligand Assay Techniques, The Endocrine Society, March, 1986, содержание которой включено в настоящий документ посредством ссылки). Радиоактивный изотоп можно обнаруживать, например, с помощью γ-счетчика или сцинтилляционного счетчика, или авторадиографии. В конкретных вариантах осуществления BCMA-нацеленный внеклеточный антигенсвязывающий домен мечен флуоресцентным маркером. Неограничивающие примеры флуоресцентных маркеров включают зеленый флуоресцентный белок (GFP), синий флуоресцентный белок (например, EBFP, EBFP2, азурит и mKa1ama1), циановый флуоресцентный белок (например, ECFP, лазурный и CyPet) и желтый флуоресцентный белок (например, YFP, цитрин, Венера и YPet). В конкретных вариантах осуществления BCMA-нацеленный человеческий scFv мечен GFP.
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен раскрытого в настоящем документе CAR содержит одноцепочечный вариабельный фрагмент (scFv). В одном конкретном неограничивающем варианте осуществления внеклеточный антигенсвязывающий домен раскрытого в настоящем документе CAR содержит человеческий scFv, который специфически связывается с BCMA человека. В конкретных вариантах осуществления scFv идентифицируют путем скрининга фаговой библиотеки scFv с использованием слитого белка BCMA-Fc.
Внеклеточный антигенсвязывающий домен CAR
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv) содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из: SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65. Нуклеотидными последовательностями, кодирующими аминокислотные последовательности SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65, являются SEQ ID NOS: 3, 7, 11, 15, 19, 23, 27, 31, 35, 39, 43, 47, 51, 55, 59, 63 и 67, соответственно. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv) содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62 и 66. Нуклеотидными последовательностями, кодирующими аминокислотные последовательности SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62 и 66, являются SEQ ID NOS: 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44, 48, 52, 56, 60, 64 и 68, соответственно. Последовательности SEQ ID NOS: 1-68 описаны в следующих далее таблицах 1-17.
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, scFv) содержит вариабельные области тяжелой и легкой цепи, содержащие аминокислотные последовательности, которые гомологичны аминокислотным последовательностям, описанным в настоящем документе и приведенным в таблицах 1-17. Например, и без ограничения, внеклеточный антигенсвязывающий домен (например, scFv) содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на примерно 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65.
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, scFv) содержит вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, и 66 are 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44, 48, 52, 56, 60, 64 и 68.
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, scFv) содержит (a) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 1, 5, 9, 13, 17, 21, 25, 29, 33, 37, 41, 45, 49, 53, 57, 61 и 65; и (b) вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOS: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, 50, 54, 58, 62, и 66 are 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44, 48, 52, 56, 60, 64 и 68.
Настоящее изобретение также относится к внеклеточным антигенсвязывающим доменам (например, scFv), которые содержат CDR вариабельной области тяжелой цепи и вариабельной области легкой цепи, например, CDR1, CDR2 и CDR3, приведенные в настоящем документе в таблицах 1-17. Границы областей CDR определены с использованием системы Kabat (Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest, пятое издание, U.S. Department of Health и Human Services, NIH Publication No. 91-3242). Настоящее изобретение также относится к внеклеточным антигенсвязывающим доменам (например, scFv), которые имеют консервативные модификации последовательностей антитела, раскрытых в настоящем документе. Например, и без ограничения, внеклеточные антигенсвязывающие домены (например, scFv) по настоящему изобретению содержат вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, при этом одна или более из этих последовательностей CDR содержат конкретные аминокислотные последовательности, раскрытые в настоящем документе, или их консервативные модификации, и при этом внеклеточные антигенсвязывающие домены сохраняют желательные функциональные свойства.
В конкретных вариантах осуществления настоящее изобретение относится к внеклеточному антигенсвязывающему домену (например, scFv), содержащему вариабельную область тяжелой цепи, при этом вариабельная область тяжелой цепи содержит: (a) CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 89, 95, 101, 107, 113, 119, 125, 131, 137, 143, 149, 155, 161, 167, 173, 179 и 185, а также их консервативных модификаций; (b) CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 90, 96, 102, 108, 114, 120, 126, 132, 138, 144, 150, 156, 162, 168, 174, 180 и 186, а также их консервативных модификаций; и (c) CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 91, 97, 103, 109, 115, 121, 127, 133, 139, 145, 151, 157, 163, 169, 175, 181 и 187, а также их консервативных модификаций.
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, scFv) содержит вариабельную область легкой цепи, при этом вариабельная область легкой цепи содержит: (a) CDR1, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 92, 98, 104, 110, 116, 122, 128, 134, 140, 146, 152, 158, 164, 170, 176, 182 и 188, а также их консервативных модификаций; (b) CDR2, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 93, 99, 105, 111, 117, 123, 129, 135, 141, 147, 153, 159, 165, 171, 177, 183 и 189, а также их консервативных модификаций; и (c) CDR3, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 94, 100, 106, 112, 118, 124, 130, 136, 142, 148, 154, 160, 166, 172, 178, 184 и 190, а также их консервативных модификаций.
Настоящее изобретение относится к внеклеточному антигенсвязывающему домену (например, scFv), содержащему вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, при этом: (a) CDR3 вариабельной области тяжелой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 91, 97, 103, 109, 115, 121, 127, 133, 139, 145, 151, 157, 163, 169, 175, 181 и 187, а также их консервативных модификаций; и (b) CDR3 вариабельной области легкой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 94, 100, 106, 112, 118, 124, 130, 136, 142, 148, 154, 160, 166, 172, 178, 184 и 190, а также их консервативных модификаций; при этом внеклеточный антигенсвязывающий домен специфически связывается с полипептидом BCMA (например, полипептидом BCMA человека). В конкретных вариантах осуществления CDR2 вариабельной области тяжелой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 125, 131, 137, 143, 149, 155, 161, 167, 173, 179, 185, 191, 197, 203, 209, 215, 221, 227, 233, 239, 245, 251, 257, 263, 305, 317, 329, 341, 353, 365, 377 и 389, а также их консервативных модификаций; и (b) CDR2 вариабельной области легкой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 93, 99, 105, 111, 117, 123, 129, 135, 141, 147, 153, 159, 165, 171, 177, 183 и 189, а также их консервативных модификаций; при этом внеклеточный антигенсвязывающий домен специфически связывается с полипептидом BCMA (например, полипептидом BCMA человека). В конкретных вариантах осуществления CDR1 вариабельной области тяжелой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 89, 95, 101, 107, 113, 119, 125, 131, 137, 143, 149, 155, 161, 167, 173, 179, и 185, а также их консервативных модификаций; и (b) CDR1 вариабельной области легкой цепи содержит аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NOS: 92, 98, 104, 110, 116, 122, 128, 134, 140, 146, 152, 158, 164, 170, 176, 182 и 188, а также их консервативных модификаций; при этом внеклеточный антигенсвязывающий домен специфически связывается с полипептидом BCMA (например, полипептидом BCMA человека).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 72 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-192 scFv (другое название «ET140-42 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 1, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 2, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 1, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 2, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 91, или ее консервативные модификации, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 92, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94, или ее консервативные модификации, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 91, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 92, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94, или ее консервативные модификации, смотри таблицу 1. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 89, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 90, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 91, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 92, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 93, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 94.
Таблица 1
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 73 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-197 scFv (другое название «ET140-47 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 5, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 6, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 5, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 6, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 95, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 96, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 97, или ее консервативные модификации, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 98, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 99, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 100, или ее консервативные модификации, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 95, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 96, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 97, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 98, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 99, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 100, или ее консервативные модификации, смотри таблицу 2. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 95, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 96, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 97, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 98, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 99, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 100.
Таблица 2
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 74 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-180 scFv (другое название «ET140-30 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 9, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 10, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 101, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 102, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 103, или ее консервативные модификации, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 104, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 105, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 106, или ее консервативные модификации, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 101, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 102, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 103, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 104, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 105, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 106, или ее консервативные модификации, смотри таблицу 3. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 101, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 102, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 103, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 104, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 105, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 106.
Таблица 3
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 75 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-172 scFv (другое название «ET140-22 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 13, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 14, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 13, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 14, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 107, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 108, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 109, или ее консервативные модификации, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 110, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 111, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 112, или ее консервативные модификации, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 107, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 108, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 109, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 110, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 111, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 112, или ее консервативные модификации, смотри таблицу 4. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 107, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 108, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 109, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 110, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 111, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 112.
Таблица 4
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 76 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-157 scFv (другое название «ET140-7 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 17, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 18, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 17, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 18, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 113, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 114, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 115, или ее консервативные модификации, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 116, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 117, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 118, или ее консервативные модификации, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 113, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 114, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 115, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 116, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 117, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 118, или ее консервативные модификации, смотри таблицу 5. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 113, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 114, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 115, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 116, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 117, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 118.
Таблица 5
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 77 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-153 scFv (другое название «ET140-3 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 21, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 22, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, или ее консервативные модификации, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, или ее консервативные модификации, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, или ее консервативные модификации, смотри таблицу 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124.
Таблица 6
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 78 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-201 scFv (другое название «ET140-51 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 25, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 26, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 25, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 26, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127, или ее консервативные модификации, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130, или ее консервативные модификации, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130, или ее консервативные модификации, смотри таблицу 7. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 125, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 126, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 127, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 128, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 129, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 130.
Таблица 7
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 79 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-167 scFv (другое название «ET140-17 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 29, смотри таблицу 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, смотри таблицу 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 30, смотри таблицу 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30, смотри таблицу 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 29, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 30, смотри таблицу 8. В конкретных вариантах осуществления анти-BCMA содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133, или ее консервативные модификации, смотри таблицу 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136, или ее консервативные модификации, смотри таблицу 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136, или ее консервативные модификации, смотри таблицу 8. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 131, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 132, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 133, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 134, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 135, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 136.
Таблица 8
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 80 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-163 scFv (другое название «ET140-13 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 33, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 34, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 33, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 34, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139, или ее консервативные модификации, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142, или ее консервативные модификации, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142, или ее консервативные модификации, смотри таблицу 9. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 137, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 138, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 139, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 140, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 141, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 142.
Таблица 9
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 81 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-207 scFv (другое название «ET140-57 scFv»).
В конкретном варианте осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 98. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 37, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 38, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 37, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 38, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145, или ее консервативные модификации, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148, или ее консервативные модификации, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148, или ее консервативные модификации, смотри таблицу 10. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 143, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 144, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 145, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 146, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 147, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 148.
Таблица 10
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 82 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-165 scFv (другое название «ET140-15 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 41, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 42, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 41, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 42, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151, или ее консервативные модификации, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154, или ее консервативные модификации, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154, или ее консервативные модификации, смотри таблицу 11. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 149, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 150, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 151, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 152, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 153, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 154.
Таблица 11
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 83 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-188 scFv (другое название «ET140-38 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 45, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 46, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 45, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 46, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157, или ее консервативные модификации, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160, или ее консервативные модификации, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160, или ее консервативные модификации, смотри таблицу 12. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 155, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 156, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 157, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 158, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 159, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 160.
Таблица 12
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 84 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-196 scFv (другое название «ET140-46 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 49, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 50, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 49, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 50, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163, или ее консервативные модификации, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166, или ее консервативные модификации, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166, или ее консервативные модификации, смотри таблицу 13. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 161, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 162, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 163, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 164, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 165, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 166.
Таблица 13
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 85 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-204 scFv (другое название «ET140-54 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 53, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 54, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169, или ее консервативные модификации, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172, или ее консервативные модификации, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172, или ее консервативные модификации, смотри таблицу 14. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 167, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 168, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 169, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 170, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 171, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 172.
Таблица 14
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 86 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-190 scFv (другое название «ET140-40 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 57, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 58, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175, или ее консервативные модификации, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178, или ее консервативные модификации, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178, или ее консервативные модификации, смотри таблицу 15. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 173, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 174, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 175, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 176, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 177, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 178.
Таблица 15
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 87 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-187 scFv (другое название «ET140-37 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 61, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 62, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181, или ее консервативные модификации, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184, или ее консервативные модификации, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184, или ее консервативные модификации, смотри таблицу 16. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 179, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 180, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 181, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 182, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 183, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 184.
Таблица 16
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит аминокислотную последовательность SEQ ID NO: 88 и специфически связывается с полипептидом BCMA (например, полипептидом BCMA, имеющим аминокислотную последовательность SEQ ID NO: 71, или его фрагментами), данный scFv обозначен ET140-174 scFv (другое название «ET140-24 scFv»).
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 65, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 66, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187, или ее консервативные модификации, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190, или ее консервативные модификации, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190, или ее консервативные модификации, смотри таблицу 17. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 185, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 186, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 187, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 188, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 189, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 190.
Таблица 17
Внеклеточный антигенсвязывающий домен (например, scFv), содержащий области VH и/или VL, имеющие высокую степень (то есть, 80% или более) гомологии с областями VH и VL последовательностей, приведенных выше, можно получать путем мутагенеза (например, сайт-направленного или ПЦР-опосредованного мутагенеза), с последующим тестированием закодированных измененных scFv на сохранение функции (то есть, аффинности связывания) с использованием анализов связывания, описанных в настоящем документе. В конкретных вариантах осуществления последовательность VH, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности, имеет замены (например, консервативные замены для получения консервативных модификаций последовательности), вставки или делеции относительно эталонной последовательности, однако внеклеточный антигенсвязывающий домен (например, scFv), содержащий данную последовательность, сохраняет способность связываться с полипептидом BCMA. В конкретных вариантах осуществления последовательность VL, имеющая по меньшей мере 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичности, имеет замены (например, консервативные замены для получения консервативных модификаций последовательности), вставки или делеции относительно эталонной последовательности, однако внеклеточный антигенсвязывающий домен (например, scFv), содержащий данную последовательность, сохраняет способность связываться с полипептидом BCMA. В конкретных вариантах осуществления в общей сложности от примерно 1 до примерно 10 аминокислот были заменены, вставлены и/или делетированы в раскрытых последовательностях. Например, и без ограничения, последовательность VH или последовательность VL может иметь до примерно одного, до примерно двух, до примерно трех, до примерно четырех, до примерно пяти, до примерно шести, до примерно семи, до примерно восьми, до примерно девяти или до примерно десяти аминокислотных остатков, которые модифицированы и/или заменены. Неограничивающие примеры консервативных модификаций приведены ниже, например, в таблице 18.
Используемый в настоящем документе термин «консервативные модификации последовательности» означает аминокислотные модификации, которые существенно не затрагивают или не изменяют характеристики связывания раскрытого в настоящем документе CAR (например, внеклеточного антигенсвязывающего домена), содержащего аминокислотную последовательность. Такие консервативные модификации включают аминокислотные замены, добавления и делеции. Модификации могут быть внесены в человеческий scFv по настоящему изобретению стандартными методами, известными в данной области, такими как сайт-направленный мутагенез и ПЦР-опосредованный мутагенез. Аминокислоты могут быть разделены на группы на основании их физико-химических свойств, таких как заряд и полярность. Консервативные аминокислотные замены являются такими заменами, при которых аминокислотный остаток заменен аминокислотой, относящейся к той же группе. Например, аминокислоты могут быть разделены на группы на основании заряда: положительно заряженные аминокислоты включают лизин, аргинин, гистидин; отрицательно заряженные аминокислоты включают аспарагиновую кислоту, глутаминовую кислоту; нейтральные аминокислоты включают аланин, аспарагин, цистеин, глутамин, глицин, изолейцин, лейцин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин и валин. Кроме того, аминокислоты могут быть разделены на группы на основании полярности: полярные аминокислоты включают аргинин (основная полярная), аспарагин, аспарагиновую кислоту (кислая полярная), глутаминовую кислоту (кислая полярная), глутамин, гистидин (основная полярная), лизин (основная полярная), серин, треонин и тирозин; неполярные аминокислоты включают аланин, цистеин, глицин, изолейцин, лейцин, метионин, фенилаланин, пролин, триптофан и валин. Таким образом, один или более аминокислотных остатков в области CDR можно заменять другими аминокислотными остатками из той же группы, и измененное антитело можно тестировать на сохранение функции (то есть, функций, описанных в пунктах (c)-(l), выше) в функциональных анализах, описанных в настоящем документе. В конкретных вариантах осуществления не более одного, не более двух, не более трех, не более четырех, не более пяти остатков в конкретной последовательности или области CDR изменены. Иллюстративные консервативные аминокислотные замены приведены в таблице 18.
Таблица 18
В конкретных неограничивающих вариантах осуществления внеклеточный антигенсвязывающий домен CAR может содержать линкер, соединяющий вариабельную область тяжелой цепи и вариабельную область легкой цепи внеклеточного антигенсвязывающего домена. Используемый в настоящем документе термин «линкер» означает функциональную группу (например, химическую группу или полипептид), которая ковалентно связывает два или более пептидов, или нуклеиновых кислот так, что они становятся связанными друг с другом. Используемый в настоящем документе термин «пептидный линкер» означает одну или более аминокислот, используемых для связывания между собой двух белков (например, для связывания доменов VH и VL). Неограничивающие примеры пептидных линкеров описаны в Shen et al., Anal. Chem. 80(6): 1910-1917 (2008) и WO 2014/087010.
В одном неограничивающем примере линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 69, приведена в SEQ ID NO: 70. В одном неограничивающем примере линкер представляет собой линкер G4S, который содержит аминокислотную последовательность, приведенную в SEQ ID NO: 210. В конкретных вариантах осуществления нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 98, приведена в SEQ ID NO: 211.
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 212, которая представлена ниже.
GGGGS [SEQ ID NO: 212].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 213, которая представлена ниже.
SGGSGGS [SEQ ID NO: 213].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 214, которая представлена ниже.
GGGGSGGGS [SEQ ID NO: 214].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 215, которая представлена ниже.
GGGGSGGGGS [SEQ ID NO: 215].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 216, которая представлена ниже.
GGGGSGGGGSGGGGGGGS [SEQ ID NO: 216].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 217, которая представлена ниже.
GGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 217].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 218, которая представлена ниже.
GGGGSGGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 218].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 219, которая представлена ниже.
GGGGSGGGGSGGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 219].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 220, которая представлена ниже.
GGGGSGGGGSGGGGSGGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 220].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 220, которая представлена ниже.
EPKSCDKTHTCPPCP [SEQ ID NO: 220].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 221, которая представлена ниже.
GGGGSGGGSEPKSCDKTHTCPPCP [SEQ ID NO: 222].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 223, которая представлена ниже.
ELKTPLGDTTHTCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCPRCP [SEQ ID NO: 223].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 224, которая представлена ниже.
GSGSGS [SEQ ID NO: 224].
В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 225, которая представлена ниже.
AAA [SEQ ID NO: 225].
Кроме того, внеклеточный антигенсвязывающий домен может содержать лидер или сигнальный пептид, который направляет образующийся белок в эндоплазматический ретикулум. Сигнальный пептид или лидер может быть необходим, если CAR должен быть гликозилирован и заякорен в клеточной мембране. Сигнальная последовательность или лидер может представлять собой пептидную последовательность (длиной примерно 5, примерно 10, примерно 15, примерно 20, примерно 25 или примерно 30 аминокислот), находящуюся на N-конце заново синтезированных белков, которая направляет их на путь секреции. В неограничивающих примерах сигнальный пептид ковалентно связан с 5'-концом внеклеточного антигенсвязывающего домена. В конкретных вариантах осуществления сигнальный пептид содержит полипептид CD8, содержащий аминокислотную последовательность, приведенную в SEQ ID NO: 191, которая представлена ниже.
MALPVTALLLPLALLLHAAR [SEQ ID NO: 191]
Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 191, приведена в SEQ ID NO: 192, которая представлена ниже:
ATGGCTCTCCCAGTGACTGCCCTACTGCTTCCCCTAGCGCTTCTCCTGCATGCAGCTCGT [SEQ ID NO: 192]
В другом варианте осуществления сигнальный пептид содержит аминокислотную последовательность, приведенную в SEQ ID NO: 205, которая представлена ниже.
METDTLLLWVLLLWVPGSTG [SEQ ID NO: 205]
Нуклеотидная последовательность, кодирующая аминокислотную последовательность SEQ ID NO: 205, приведена в SEQ ID NO: 206, которая представлена ниже:
ATGGAAACCGACACCCTGCTGCTGTGGGTGCTGCTGCTGTGGGTGCCAGGATCCACAGGA [SEQ ID NO: 206]
В конкретных вариантах осуществления scFv человека содержит вариабельную область тяжелой цепи, вариабельную область легкой цепи, пептидный линкер между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, а также His-метку и HA-метку. В конкретных вариантах осуществления аминокислотная последовательность His-метки и HA-метки содержит аминокислотную последовательность SEQ ID NO: 275, которая представлена ниже:
TSGQAGQHHHHHHGAYPYDVPDYAS [SEQ ID NO: 275]
Нуклеотидная последовательность, кодирующая SEQ ID NO: 275, приведена в SEQ ID NO: 276, которая представлена ниже:
ACTAGTGGCCAGGCCGGCCAGCACCATCACCATCACCATGGCGCATACCCGTACGACGTTCCGGACTACGCTTCT [SEQ ID NO: 276]
В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv) связывается с полипептидом BCMA человека, содержащим аминокислотную последовательность, приведенную в SEQ ID NO: 71. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv) связывается с одной или более областями аминокислотной последовательности, приведенной в SEQ ID NO: 71. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv) связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv) связывается с одной, двумя, тремя, четырьмя, пятью, шестью или семью областями эпитопа, выбранными из группы, состоящей из аминокислот 8-22, 9-23, 10-24, 11-25, 12-26, 13-27, 14-28 и 8-28 из SEQ ID NO: 71. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 9, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 10, необязательно, с (iii) последовательностью линкера, например, пептидного линкера, между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи. В конкретных вариантах осуществления линкер имеет аминокислотную последовательность, приведенную в SEQ ID NO: 69. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен, который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, представляет собой человеческий scFv с областями VH и VL или CDR, выбранными из таблицы 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен, который связывается с аминокислотами 14-22 из SEQ ID NO: 71, представляет собой слитый белок человеческий scFv-Fc или полноразмерный IgG человека с областями VH и VL или CDR, выбранными из таблицы 6. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 21. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VL, содержащую аминокислотную последовательность, которая по меньшей мере на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% гомологична аминокислотной последовательности, приведенной в SEQ ID NO: 22. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, и VL, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, или ее консервативные модификации, и VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, или ее консервативные модификации. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, или ее консервативные модификации. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, или ее консервативные модификации, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, или ее консервативные модификации, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, или ее консервативные модификации, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, или ее консервативные модификации, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, или ее консервативные модификации, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124, или ее консервативные модификации. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен (например, человеческий scFv), который связывается с областью эпитопа, содержащей аминокислоты 14-22 из SEQ ID NO: 71, содержит VH CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 119, VH CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 120, VH CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 121, VL CDR1, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 122, VL CDR2, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 123, и VL CDR3, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 124. В конкретных вариантах осуществления внеклеточный антигенсвязывающий домен представляет собой ET140-3 (или «ET140-153») scFv.
Трансмембранный домен CAR
В конкретных неограничивающих вариантах осуществления трансмембранный домен CAR содержит гидрофобную альфа-спираль, которая проходит через по меньшей мере часть мембраны. Разные трансмембранные домены приводят к разной стабильности рецепторов. После узнавания антигена происходит кластеризация рецепторов и сигнал передается клетке. В соответствии с настоящим изобретением, трансмембранный домен CAR может содержать полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид CTLA-4, полипептид PD-1, полипептид LAG-3, полипептид 2B4, полипептид BTLA, синтетический пептид (не на основе белка, связанного с иммунным ответом) или их сочетание.
В конкретных вариантах осуществления трансмембранный домен раскрытого в настоящем документе CAR содержит полипептид CD28. Полипептид CD28 может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или 100% гомологична последовательности, имеющей регистрационный № NCBI: P10747 или NP_006130 (SEQ ID NO: 193), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены. В неограничивающих вариантах осуществления полипептид CD28 может иметь аминокислотную последовательность, которая представляет собой непрерывный фрагмент из SEQ ID NO: 193, имеющий длину по меньшей мере 20 или по меньшей мере 30, или по меньшей мере 40, или по меньшей мере 50 и вплоть до 220 аминокислот. Альтернативно или дополнительно, в неограничивающих различных вариантах осуществления полипептид CD28 имеет аминокислотную последовательность из аминокислот 1-220, 1-50, 50-100, 100-150, 150-200 или 200-220 из SEQ ID NO: 193. В конкретных вариантах осуществления CAR, раскрытый в настоящем документе, содержит трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий костимулирующую сигнальную область, которая содержит полипептид CD28. В конкретных вариантах осуществления полипептид CD28, содержащийся в трансмембранном домене и внутриклеточном домене, имеет аминокислотную последовательность из аминокислот 114-220 из SEQ ID NO: 193.
SEQ ID NO: 193 представлена ниже:
1 MLRLLLALNL FPSIQVTGNK ILVKQSPMLV AYДНКVNLSC KYSYNLFSRE FRASLHKGLD
61 SAVEVCVVYG NYSQQLQVYS KTGFNCDGKL GNESVTFYLQ NLYVNQTDIY FCKIEVMYPP
121 PYLDNEKSNG TIIHVKGKHL CPSPLFPGPS KPFWVLVVVG GVLACYSLLV TVAFIIFWVR
181 SKRSRLLHSD YMNMTPRRPG PTRKHYQPYA PPRDFAAYRS [SEQ ID NO: 193]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты CD28» означает полинуклеотид, кодирующий полипептид CD28. В конкретных вариантах осуществления молекула нуклеиновой кислоты CD28, кодирующая полипептид CD28, содержащийся в трансмембранном домене и внутриклеточном домене (например, костимулирующей сигнальной области) раскрытого в настоящем документе CAR (аминокислоты 114-220 из SEQ ID NO: 193), содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 194, которая представлена ниже.
ATTGAAGTTATGTATCCTCCTCCTTACCTAGACAATGAGAAGAGCAATGGAACCATTATCCATGTGAAAGGGAAACACCTTTGTCCAAGTCCCCTATTTCCCGGACCTTCTAAGCCCTTTTGGGTGCTGGTGGTGGTTGGTGGAGTCCTGGCTTGCTATAGCTTGCTAGTAACAGTGGCCTTTATTATTTTCTGGGTGAGGAGTAAGAGGAGCAGGCTCCTGCACAGTGACTACATGAACATGACTCCCCGCCGCCCCGGGCCCACCCGCAAGCATTACCAGCCCTATGCCCCACCACGCGACTTCGCAGCCTATCGCTCC [SEQ ID NO: 194]
В конкретных вариантах осуществления трансмембранный домен раскрытого в настоящем документе CAR содержит полипептид CD8. Полипептид CD8 может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или 100% гомологична последовательности, имеющей регистрационный № NCBI: AAH25715 (SEQ ID NO: 226), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены. В неограничивающих вариантах осуществления полипептид CD8 может иметь аминокислотную последовательность, которая представляет собой непрерывный фрагмент из SEQ ID NO: 226, имеющий длину по меньшей мере 20 или по меньшей мере 30, или по меньшей мере 40, или по меньшей мере 50, или по меньшей мере 70, или по меньшей мере 100, или по меньшей мере 150, или по меньшей мере 200 и вплоть до 235 аминокислот. Альтернативно или дополнительно, в неограничивающих различных вариантах осуществления полипептид CD8 имеет аминокислотную последовательность из аминокислот 1-235, 1-50, 50-100, 100-150, 150-200, 130-210 или 200-235 из SEQ ID NO: 226. В конкретных вариантах осуществления полипептид CD8, содержащийся в трансмембранном домене, имеет аминокислотную последовательность из аминокислот 137-207 из SEQ ID NO: 226.
SEQ ID NO: 226 представлена ниже:
1 MALPVTALLL PLALLLHAAR PSQFRVSPLD RTWNLGETVE LKCQVLLSNP TSGCSWLFQP
61 RGAAASPTFL LYLSQNKPKA AEGLDTQRFS GKRLGDTFVL TLSDFRRENE GCYFCSALSN
121 SIMYFSHFVP VFLPAKPTTT PAPRPPTPAP TIASQPLSLR PEACRPAAGG AVHTRGLDFA
181 CDIYIWAPLA GTCGVLLLSL VITLYCNHRN RRRVCKCPRP VVKSGDKPSL SARYV [SEQ ID NO: 226].
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты CD8» означает полинуклеотид, кодирующий полипептид CD8. В конкретных вариантах осуществления молекула нуклеиновой кислоты CD8, кодирующая полипептид CD8, содержащийся в трансмембранном домене раскрытого в настоящем документе CAR (аминокислоты 137-207 из SEQ ID NO: 226), содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 227, которая представлена ниже.
CCCACCACGACGCCAGCGCCGCGACCACCAACCCCGGCGCCCACGATCGCGTCGCAGCCCCTGTCCCTGCGCCCAGAGGCGTGCCGGCCAGCGGCGGGGGGCGCAGTGCACACGAGGGGGCTGGACTTCGCCTGTGATATCTACATCTGGGCGCCCCTGGCCGGGACTTGTGGGGTCCTTCTCCTGTCACTGGTTATCACCCTTTACTGCAAC [SEQ ID NO: 227]
В конкретных неограничивающих вариантах осуществления CAR также может содержать область спейсера, который связывает внеклеточный антигенсвязывающий домен с трансмембранным доменом. Область спейсера может быть достаточно гибкой, чтобы позволять антигенсвязывающему домену ориентироваться в разных направлениях для облегчения узнавания антигена. Область спейсера может представлять собой шарнирную область из IgG1, либо область CH2CH3 иммуноглобулина и части CD3.
Внутриклеточный домен CAR
В конкретных неограничивающих вариантах осуществления внутриклеточный домен CAR может содержать полипептид CD3ζ, который может активировать или стимулировать клетку (например, клетку лимфоидной линии, например, T-клетку). CD3ζ содержит три ITAM и передает сигнал активации клетке (например, клетке лимфоидной линии, например, T-клетке) после связывания антигена. Полипептид CD3ζ может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или примерно 100% гомологична последовательности, приведенной в SEQ ID NO: 195, или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены. В неограничивающих вариантах осуществления полипептид CD3ζ может иметь аминокислотную последовательность, которая представляет собой непрерывный фрагмент из SEQ ID NO: 195, имеющий длину по меньшей мере 20, или по меньшей мере 30, или по меньшей мере 40, или по меньшей мере 50 и вплоть до 163 аминокислот. Альтернативно или дополнительно, в неограничивающих различных вариантах осуществления полипептид CD3ζ имеет аминокислотную последовательность из аминокислот 1-163, 1-50, 50-100, 100-150, или 150-163 из SEQ ID NO: 195. В конкретных вариантах осуществления полипептид CD3ζ, содержащийся в внутриклеточном домене раскрытого в настоящем документе CAR, имеет аминокислотную последовательность из аминокислот 52-163 из SEQ ID NO: 195.
SEQ ID NO: 195 представлена ниже:
1 MKWKALFTAA ILQAQLPITE AQSFGLLDPK LCYLLDGILF IYGVILTALF LRVKFSRSAD
61 APAYQQGQNQ LYNELNLGRR EEYDVLDKRR GRDPEMGGKP RRKNPQEGLY NELQKDKMAE
121 AYSEIGMKGE RRRGKGHDGL YQGLSTATKD TYDALHMQAL PPR [SEQ ID NO: 195]
В соответствии с настоящим изобретением «молекула нуклеиновой кислоты CD3ζ» означает полинуклеотид, кодирующий полипептид CD3ζ. В конкретных вариантах осуществления молекула нуклеиновой кислоты CD3ζ, кодирующая полипептид CD3ζ, содержащийся в внутриклеточном домене раскрытого в настоящем документе CAR (аминокислоты 52-163 из SEQ ID NO: 195), содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 196, которая представлена ниже.
AGAGTGAAGTTCAGCAGGAGCGCAGACGCCCCCGCGTACCAGCAGGGCCAGAACCAGCTCTATAACGAGCTCAATCTAGGACGAAGAGAGGAGTACGATGTTTTGGACAAGAGACGTGGCCGGGACCCTGAGATGGGGGGAAAGCCGAGAAGGAAGAACCCTCAGGAAGGCCTGTACAATGAACTGCAGAAAGATAAGATGGCGGAGGCCTACAGTGAGATTGGGATGAAAGGCGAGCGCCGGAGGGGCAAGGGGCACGATGGCCTTTACCAGGGTCTCAGTACAGCCACCAAGGACACCTACGACGCCCTTCACATGCAGGCCCTGCCCCCTCGCTAA [SEQ ID NO: 196]
В конкретных неограничивающих вариантах осуществления внутриклеточный домен CAR дополнительно содержит по меньшей мере одну сигнальную область. По меньшей мере одна сигнальная область может содержать полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10, полипептид PD-1, полипептид CTLA-4, полипептид LAG-3, полипептид 2B4, полипептид BTLA, синтетический пептид (не на основе белка, связанного с иммунным ответом) или их сочетание.
В конкретных вариантах осуществления сигнальная область представляет собой костимулирующую сигнальную область. В конкретных вариантах осуществления костимулирующая область содержит по меньшей мере одну костимулирующую молекулу, которая может обеспечивать оптимальную активацию лимфоцитов. Используемый в настоящем документе термин «костимулирующие молекулы» означает молекулы клеточной поверхности, отличные от антигенных рецепторов или их лигандов, которые необходимы для эффективного ответа лимфоцитов на антиген. По меньшей мере одна костимулирующая сигнальная область может содержать полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10 или их сочетание. Костимулирующая молекула может связываться с костимулирующим лигандом, представляющим собой белок, экспрессируемый на клеточной поверхности, который при связывании с его рецептором продуцирует костимулирующий ответ, то есть, внутриклеточный ответ, который влияет на стимуляцию, возникающую, когда антиген связывается с молекулой его CAR. Костимулирующие лиганды включают, но не ограничиваются ими, CD80, CD86, CD70, OX40L, 4-1BBL, CD48, TNFRSF14 и PD-L1. В качестве одного примера, лиганд 4-1BB (то есть, 4-1BBL) может связываться с 4-1BB (также известным как «CD137»), обеспечивая внутриклеточный сигнал, который в сочетании с сигналом CAR индуцирует эффекторную клеточную функцию CAR+ T-клетки. CAR, содержащие внутриклеточный домен, который содержит костимулирующую сигнальную область, содержащую 4-1BB, ICOS или DAP-10, описаны в патенте США 7446190 (например, нуклеотидная последовательность, кодирующая 4-1BB, приведена в SEQ ID NO: 15, нуклеотидная последовательность, кодирующая ICOS, приведена в SEQ ID NO: 16 и нуклеотидная последовательность, кодирующая DAP-10, приведена в SEQ ID NO: 17 в патенте США 7446190), полное содержание которого включено в настоящий документ посредством ссылки. В конкретных вариантах осуществления внутриклеточный домен CAR содержит костимулирующую сигнальную область, которая содержит полипептид CD28. В конкретных вариантах осуществления внутриклеточный домен CAR содержит костимулирующую сигнальную область, которая содержит две костимулирующие молекулы: CD28 и 4-1BB или CD28 и OX40.
4-1BB может действовать в качестве лиганда фактора некроза опухолей (TNF) и имеет стимулирующую активность. Полипептид 4-1BB может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или 100% гомологична последовательности, имеющей регистрационный № NCBI: P41273 или NP_001552 (SEQ ID NO: 197), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены. В конкретных вариантах осуществления полипептид 4-1BB, содержащийся в внутриклеточном домене раскрытого в настоящем документе CAR, имеет аминокислотную последовательность из аминокислот 214-255 из SEQ ID NO: 197.
SEQ ID NO: 197 представлена ниже:
1 MGNSCYNIVA TLLLVLNFER TRSLQDPCSN CPAGTFCDNN RNQICSPCPP NSFSSAGGQR
61 TCDICRQCKG VFRTRKECSS TSNAECDCTP GFHCLGAGCS MCEQDCKQGQ ELTKKGCKDC
121 CFGTFNDQKR GICRPWTNCS LDGKSVLVNG TKERDVVCGP SPADLSPGAS SVTPPAPARE
181 PGHSPQIISF FLALTSTALL FLLFFLTLRF SVVKRGRKKL LYIFKQPFMR PVQTTQEEDG
241 CSCRFPEEEE GGCEL [SEQ ID NO: 197]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты 4-1BB» означает полинуклеотид, кодирующий полипептид 4-1BB. В конкретных вариантах осуществления молекула нуклеиновой кислоты 4-1BB, кодирующая полипептид 4-1BB, содержащийся в внутриклеточном домене раскрытого в настоящем документе CAR (аминокислоты 214-255 из SEQ ID NO: 197), содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 228, которая представлена ниже.
aaacggggcagaaagaagctcctgtatatattcaaacaaccatttatgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaagaagaaggaggatgtgaactg [SEQ ID NO: 228]
Полипептид OX40 может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или 100% гомологична последовательности, имеющей регистрационный № NCBI: P43489 или NP_003318 (SEQ ID NO: 198), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены.
SEQ ID NO: 198 представлена ниже:
1 MCVGARRLGR GPCAALLLLG LGLSTVTGLH CVGDTYPSND RCCHECRPGN GMVSRCSRSQ
61 NTVCRPCGPG FYNDVVSSKP CKPCTWCNLR SGSERKQLCT ATQDTVCRCR AGTQPLDSYK
121 PGVDCAPCPP GHFSPGDNQA CKPWTNCTLA GKHTLQPASN SSDAICEDRD PPATQPQETQ
181 GPPARPITVQ PTEAWPRTSQ GPSTRPVEVP GGRAVAAILG LGLVLGLLGP LAILLALYLL
241 RRDQRLPPDA HKPPGGGSFR TPIQEEQADA HSTLAKI [SEQ ID NO: 198]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты OX40» означает полинуклеотид, кодирующий полипептид OX40.
Полипептид ICOS может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или 100% гомологична последовательности, имеющей регистрационный № NCBI: NP_036224 (SEQ ID NO: 199), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены.
SEQ ID NO: 199 представлена ниже:
1 MKSGLWYFFL FCLRIKVLTG EINGSANYEM FIFHNGGVQI LCKYPDIVQQ FKMQLLKGGQ
61 ILCDLTKTKG SGNTVSIKSL KFCHSQLSNN SVSFFLYNLD HSHANYYFCN LSIFDPPPFK
121 VTLTGGYLHI YESQLCCQLK FWLPIGCAAF VVVCILGCIL ICWLTKKKYS SSVHDPNGEY
181 MFMRAVNTAK KSRLTDVTL [SEQ ID NO: 199]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты ICOS» означает полинуклеотид, кодирующий полипептид ICOS.
CTLA-4 представляет собой ингибирующий рецептор, экспрессируемый активированными T-клетками, который при связывании с соответствующими ему лигандами (CD80 и CD86; B7-1 и B7-2, соответственно) опосредует ингибирование или анергию активированной T-клетки. Как в доклинических, так и в клинических исследованиях, блокирование CTLA-4 путем системной инфузии антител приводило к усилению эндогенного противоопухолевого ответа, хотя в клинических исследованиях сопровождалось значительной непредвиденной токсичностью.
CTLA-4 содержит внеклеточный V-домен, трансмембранный домен и цитоплазматический хвост. Были охарактеризованы альтернативно сплайсированные варианты, кодирующие разные изоформы. Мембраносвязанная изоформа функционирует в виде гомодимера, связанного дисульфидной связью, в то время как растворимая изоформа функционирует в виде мономера. Внутриклеточный домен аналогичен таковому у CD28 в том, что он не имеет собственной каталитической активности и содержит один мотив YVKM, способный связывать PI3K, PP2A и SHP-2, и один богатый остатками пролина мотив, способный связывать SH3-содержащие белки. Одна функция CTLA-4 в ингибировании T-клеточных ответов, судя по всему, осуществляется непосредственно через дефосфорилирование SHP-2 и PP2A TCR-проксимальных сигнальных белков, таких как CD3 и LAT. CTLA-4 также может влиять на сигнализацию опосредованно, за счет конкуренции с CD28 за связывание CD80/86. Также показано, что CTLA-4 связывается и/или взаимодействует с PI3K, CD80, AP2M1 и PPP2R5A.
В соответствии с настоящим изобретением, полипептид CTLA-4 может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или примерно 100% гомологична последовательности UniProtKB/Swiss-Prot с регистрационным №: P16410.3 (SEQ ID NO: 200) (гомологию между ними можно определять с использованием стандартных программ, таких как BLAST или FASTA), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены.
SEQ ID NO: 200 представлена ниже:
1 MACLGFQRHK AQLNLATRTW PCTLLFFLLF IPVFCKAMHV AQPAVVLASS RGIASFVCEY
61 ASPGKATEVR VTVLRQADSQ VTEVCAATYM MGNELTFLDD SICTGTSSGN QVNLTIQGLR
121 AMDTGLYICK VELMYPPPYY LGIGNGTQIY VIDPEPCPDS DFLLWILAAV SSGLFFYSFL
181 LTAVSLSKML KKRSPLTTGV YVKMPPTEPE CEKQFQPYFI PIN [SEQ ID NO: 200]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты CTLA-4» означает полинуклеотид, кодирующий полипептид CTLA-4.
PD-1 является отрицательным иммунорегулятором активированных T-клеток при взаимодействии с соответствующими ему лигандами PD-L1 и PD-L2, экспрессируемыми на эндогенных макрофагах и дендритных клетках. PD-1 представляет собой мембранный белок I типа из 268 аминокислот. PD-1 имеет два лиганда, PD-L1 и PD-L2, которые являются представителями семейства B7. Структура белка содержит внеклеточный домен IgV, за которым следует трансмембранная область и внутриклеточный хвост. Внутриклеточный хвост содержит два сайта фосфорилирования, находящиеся в тирозинсодержащем ингибиторном мотиве иммунорецепторов и тирозинсодержащем переключающем мотиве иммунорецепторов, PD-1 отрицательно регулирует сигналы TCR. SHP-I и SHP-2 фосфатазы связываются с цитоплазматическим хвостом PD-1 после связывания лиганда. Повышающая регуляция PD-L1 является одним из механизмов, позволяющих опухолевым клеткам ускользать от иммунной системы хозяина. В доклинических и клинических исследованиях блокирование PD-1 антагонистическими антителами индуцировало противоопухолевые ответы, опосредованные эндогенной иммунной системой хозяина.
В соответствии с настоящим изобретением, полипептид PD-1 может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или примерно 100% гомологична последовательности с регистрационным № NCBI: NP_005009.2 (SEQ ID NO: 201), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены.
SEQ ID NO: 201 представлена ниже:
1 MQIPQAPWPV VWAVLQLGWR PGWFLDSPDR PWNPPTFSPA LLVVTEGДНК TFTCSFSNTS
61 ESFVLNWYRM SPSNQTDKLA AFPEDRSQPG QDCRFRVTQL PNGRDFHMSV VRARRNDSGT
121 YLCGAISLAP KAQIKESLRA ELRVTERRAE VPTAHPSPSP RPAGQFQTLV VGVVGGLLGS
181 LVLLVWVLAV ICSRAARGTI GARRTGQPLK EDPSAVPVFS VDYGELDFQW REKTPEPPVP
241 CVPEQTEYAT IVFPSGMGTS SPARRGSADG PRSAQPLRPE DGHCSWPL [SEQ ID NO: 201]
В соответствии с настоящим изобретением «молекула нуклеиновой кислоты PD-1» означает полинуклеотид, кодирующий полипептид PD-1.
Белок активации лимфоцитов 3 (LAG-3) является отрицательным иммунорегулятором иммунных клеток. LAG-3 принадлежит к суперсемейству иммуноглобулинов (Ig) и содержит 4 внеклеточных Ig-подобных домена. Ген LAG3 содержит 8 экзонов. Данные относительно последовательности, организации экзонов/интронов и хромосомной локализации указывают на близкое родство LAG3 с CD4. LAG3 также имеет название CD223 (кластер дифференцировки 223).
В соответствии с настоящим изобретением, полипептид LAG-3 может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или примерно 100% гомологична последовательности UniProtKB/Swiss-Prot с регистрационным №: P18627.5 (SEQ ID NO: 202), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены.
SEQ ID NO: 202 представлена ниже:
1 MWEAQFLGLL FLQPLWVAPV KPLQPGAEVP VVWAQEGAPA QLPCSPTIPL QDLSLLRRAG
61 VTWQHQPDSG PPAAAPGHPL APGPHPAAPS SWGPRPRRYT VLSVGPGGLR SGRLPLQPRV
121 QLDERGRQRG DFSLWLRPAR RADAGEYRAVHLRDRALSC RLRLRLGQAS MTASPPGSLR
181 ASDWVILNCS FSRPDRPASV HWFRNRGQGR VPVRESPHHH LAESFLFLPQ VSPMDSGPWG
241 CILTYRDGFN VSIMYNLTVL GLEPPTPLTV YAGAGSRVGL PCRLPAGVGT RSFLTAKWTP
301 PGGGPDLLVT GDNGDFTLRL EDVSQAQAGT YTCHIHLQEQ QLNATVTLAI ITVTPKSFGS
361 PGSLGKLLCE VTPVSGQERF VWSSLDTPSQ RSFSGPWLEA QEAQLLSQPW QCQLYQGERL
421 LGAAVYFTEL SSPGAQRSGR APGALPAGHL LLFLILGVLS LLLLVTGAFG FHLWRRQWRP
481 RRFSALEQGI HPPQAQSKIE ELEQEPEPEP EPEPEPEPEP EPEQL [SEQ ID NO: 202]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты LAG-3» означает полинуклеотид, кодирующий полипептид LAG-3.
Рецептор 2B4 (2B4) клеток-естественных киллеров на NK-клетках и подмножествах T-клеток опосредует не рестриктированное по MHC уничтожение клеток. В настоящее время функцию 2B4 продолжают изучать, при этом считается, что изоформа 2B4-S является активирующим рецептором, а изоформа 2B4-L является отрицательным иммунорегулятором иммунных клеток. 2B4 блокируется при связывании его высокоаффинного лиганда, CD48. 2B4 содержит тирозинсодержащий переключающий мотив, молекулярный переключатель, позволяющий белку связываться с разными фосфатазами. 2B4 также имеет название CD244 (кластер дифференцировки 244).
В соответствии с настоящим изобретением, полипептид 2B4 может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или примерно 100% гомологична последовательности UniProtKB/Swiss-Prot с регистрационным №: Q9BZW8.2 (SEQ ID NO: 203), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены.
SEQ ID NO: 203 представлена ниже:
1 MLGQVVTLIL LLLLKVYQGK GCQGSADHVV SISGVPLQLQ PNSIQTKVDS IAWKKLLPSQ
61 NGFHHILKWE NGSLPSNTSN DRFSFIVKNL SLLIKAAQQQ DSGLYCLEVT SISGKVQTAT
121 FQVFVFESLL PDKVEKPRLQ GQGKILDRGR CQVALSCLVS RDGNVSYAWY RGSKLIQTAG
181 NLTYLDEEVD INGTHTYTCN VSNPVSWESH TLNLTQDCQN AHQEFRFWPF LVIIVILSAL
241 FLGTLACFCV WRRKRKEKQS ETSPKEFLTI YEDVKDLKTR RNHEQEQTFP GGGSTIYSMI
301 QSQSSAPTSQ EPAYTLYSLI QPSRKSGSRK RNHSPSFNST IYEVIGKSQP KAQNPARLSR
361 KELENFDVYS [SEQ ID NO: 203]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты 2B4» означает полинуклеотид, кодирующий полипептид 2B4.
Экспрессия аттенюатора B- и T-лимфоцитов (BTLA) индуцируется в процессе активации T-клеток, и BTLA остается экспрессированным на Th1 клетках, но не на Th2 клетках. Подобно PD1 и CTLA4, BTLA взаимодействует с гомологом B7, B7H4. Однако, в отличие от PD-1 и CTLA-4, BTLA вызывает ингибирование T-клеток при взаимодействии с представителями семейства рецепторов фактора некроза опухолей (TNF-R), а не только представителями семейства B7 рецепторов клеточной поверхности. BTLA является лигандом для представителя 14 суперсемейства (рецепторов) фактора некроза опухолей (TNFRSF14), также известного как медиатор проникновения вируса герпеса (HVEM). Комплексы BTLA-HVEM отрицательно регулируют T-клеточные иммунные ответы. Показано, что активация BTLA приводит к ингибированию функции специфичных в отношении рака человеческих CD8+ T-клеток. BTLA также имеет название CD272 (кластер дифференцировки 272).
В соответствии с настоящим изобретением, полипептид BTLA может иметь аминокислотную последовательность, которая по меньшей мере на примерно 85%, примерно 90%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или примерно 100% гомологична последовательности UniProtKB/Swiss-Prot с регистрационным №: Q7Z6A9.3 (SEQ ID NO: 204), или ее фрагментам, и/или может, необязательно, иметь одну, две или три консервативные аминокислотные замены.
SEQ ID NO: 204 представлена ниже:
1 MKTLPAMLGT GKLFWVFFLI PYLDIWNIHG KESCDVQLYI KRQSEHSILA GDPFELECPV
61 KYCANRPHVT WCKLNGTTCV KLEDRQTSWK EEKNISFFIL HFEPVLPNDN GSYRCSANFQ
121 SNLIESHSTT LYVTDVKSAS ERPSKDEMAS RPWLLYRLLP LGGLPLLITT CFCLFCCLRR
181 HQGKQNELSD TAGREINLVD AHLKSEQTEA STRQNSQVLL SETGIYDNDP DLCFRMQEGS
241 EVYSNPCLEE NKPGIVYASL NHSVIGPNSR LARNVKEAPT EYASICVRS [SEQ ID NO: 204]
В соответствии с настоящим изобретением, «молекула нуклеиновой кислоты BTLA» означает полинуклеотид, кодирующий полипептид BTLA.
В конкретных вариантах осуществления CAR содержит внеклеточную антигенсвязывающую область, содержащую человеческий scFv, который специфически связывается с BCMA человека, трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ζ и костимулирующую сигнальную область, которая содержит полипептид CD28, как показано на фигуре 1. Как показано на фигуре 1, CAR также содержит сигнальный пептид или лидер, ковалентно связанный с 5'-концом внеклеточного антигенсвязывающего домена. В конкретных вариантах осуществления сигнальный пептид содержит аминокислотную последовательность, приведенную SEQ ID NO: 205.
В конкретных вариантах осуществления CAR содержит внеклеточную антигенсвязывающую область, содержащую человеческий scFv, который специфически связывается с BCMA человека, трансмембранный домен, содержащий полипептид CD8, и внутриклеточный домен, содержащий полипептид CD3ζ и костимулирующую сигнальную область, которая содержит полипептид 4-1BB, как показано на фигуре 7. Как показано на фигуре 7, CAR также содержит сигнальный пептид или лидер, ковалентно связанный с 5'-концом внеклеточного антигенсвязывающего домена. В конкретных вариантах осуществления сигнальный пептид содержит аминокислотную последовательность, приведенную в SEQ ID NO: 205.
В конкретных вариантах осуществления CAR по настоящему изобретению может дополнительно содержать индуцируемый промотор для экспрессии нуклеотидных последовательностей в клетках человека. Промоторы, используемые для экспрессии генов CAR, могут быть конститутивными промоторами, такими как промотор гена убиквитина C (UbiC).
Настоящее изобретение также относится к выделенной молекуле нуклеиновой кислоты, кодирующей BCMA-нацеленный CAR, описанный в настоящем документе, или его функциональную часть. В конкретных вариантах осуществления выделенная молекула нуклеиновой кислоты кодирует раскрытый в настоящем документе BCMA-нацеленный CAR, содержащий человеческий scFv, который специфически связывается с BCMA человека, трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ξ и костимулирующую сигнальную область, содержащую полипептид CD28. В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 207, которая представлена ниже:
caatctgccctgactcagcctgcctccgtgtctgcgtctcctggacagtcgatcgccatctcctgcactggaaccagcagtgacgttggttggtatcaacagcacccaggcaaagcccccaaactcatgatttatgaggacagtaagcggccctcaggggtttctaatcgcttctctggctccaagtctggcaacacggcctccctgaccatctctgggctccaggctgaggacgaggctgattattactgcagctcaaatacaagaagcagcactttggtgttcggcggagggaccaagctgaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggccgaagtgcagctggtgcagtctggggctgagatgaagaagcctggggcctcactgaagctctcctgcaaggcttctggatacaccttcatcgactactatgtatactggatgcgacaggcccctggacaagggcttgagtccatgggatggatcaaccctaacagtggtggcacaaactatgcacagaagtttcagggcagggtcaccatgaccagggacacgtccatcagcacagcctacatggagctgagcaggctgagatctgacgacaccgccatgtattactgtgcgcgctcccagcgtgacggttacatggattactggggtcaaggtactctggtgaccgtctcctcagcggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgc [SEQ ID NO: 207]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 208, которая представлена ниже:
cagtctgtgctgacgcagccgccctcagtgtctggggccccagggcagagggtcaccatctcctgcactgggagcagctccaacatcggggcaggttttgatgtacactggtaccagcagcttccaggaacagcccccaaactcctcatctatggtaacagcaatcggccctcaggggtccctgaccgattctctggctccaagtctggcacctcagcctccctggccatcactgggctccaggctgaggatgaggctgattattactgccagtcctatgacagcagcctgagtggttatgtcttcggaactgggaccaaggtcaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggcccaggtccagctggtacagtctggggctgaggtgaagaagcctggggcctcagtgaaggtctcctgcaaggcttctggatacaccttcaccgactactatatgcactgggtgcgacaggcccctggacaacggcttgagtggatgggatggatcaaccctaacagtggtggcacaaactatgcacagaagtttcaggacaggatcaccgtgaccagggacacctccagcaacacaggctacatggagctgaccaggctgagatctgacgacacggccgtgtattactgtgcgcgctctccgtactctggtgttctggataaatggggtcaaggtactctggtgaccgtctcctcagcggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgc [SEQ ID NO: 208]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 209, которая представлена ниже:
tcctatgagctgactcagccaccctcagcgtctgggacccccgggcagagggtcaccatgtcttgttctggaaccagctccaacatcggaagtcactctgtaaactggtaccagcagctcccaggaacggcccccaaactcctcatctatactaataatcagcggccctcaggggtccctgaccgattctctggctccaagtctggcacctcagcctccctggccatcagtggcctccagtctgaggatgaggctgattattactgtgcagcatgggatggcagcctgaatggtctggtattcggcggagggaccaagctgaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggccgaggtgcagctggtgcagtctggagcagaggtgaaaaagcccggggagtctctgaagatctcctgtaagggttctggatacagctttaccagctactggatcggctgggtgcgccagatgcccgggaaaggcctggagtggatggggatcatctatcctggtgactctgataccagatacagcccgtccttccaaggccacgtcaccatctcagctgacaagtccatcagcactgcctacctgcagtggagcagcctgaaggcctcggacaccgccatgtattactgtgcgcgctactctggttctttcgataactggggtcaaggtactctggtgaccgtctcctcagcggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgc [SEQ ID NO: 209]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 229, которая представлена ниже:
CCTTCTCTAGGCGCCCCCATATGGCCATATGAGATCTTATATGGGGCACCCCCGCCCCTTGTAAACTTCCCTGACCCTGA
CATGACAAGAGTTACTAACAGCCCCTCTCTCCAAGCTCACTTACAGGCTCTCTACTTAGTCCAGCACGAAGTCTGGAGAC
CTCTGGCGGCAGCCTACCAAGAACAACTGGACCGACCGGTGCCGCCACCATGGAAACCGACACCCTGCTGCTGTGGGTGC
TGCTGCTGTGGGTGCCAGGATCCACAGGACTGCCTGTGCTGACTCAGCCACCCTCAGCGTCTGGGACCCCCGGGCAGAGG
GTCACCATCTCTTGTTCTGGACGCAGTTCCAACATCGGGAGTAATTCTGTTAACTGGTATCGACAACTCCCAGGAGCGGC
CCCCAAACTCCTCATCTATAGTAATAATCAGCGGCCCCCAGGGGTCCCTGTGCGATTCTCTGGCTCCAAGTCTGGCACCT
CAGCCTCCCTGGCCATCAGTGGGCTCCAGTCTGAAGATGAGGCCACTTATTACTGTGCAACATGGGATGACAATCTGAAT
GTTCACTATGTCTTCGGAACTGGGACCAAGGTCACCGTCCTAGGTTCTAGAGGTGGTGGTGGTAGCGGCGGCGGCGGCTC
TGGTGGTGGTGGATCCCTCGAGATGGCCCAGGTGCAGCTGGTGCAGTCTGGGGCTGAGGTGAAGAAGCCTGGGTCCTCGG
TGAAGGTCTCCTGCAAGGCTTCTGGAGGCACCTTCAGCAGCTATGCTATCAGCTGGGTGCGACAGGCCCCTGGACAAGGG
CTTGAGTGGATGGGAAGGATCATCCCTATCCTTGGTATAGCAAACTACGCACAGAAGTTCCAGGGCAGAGTCACGATTAC
CGCGGACAAATCCACGAGCACAGCCTACATGGAGCTGAGCAGCCTGAGATCTGAGGACACGGCCGTGTATTACTGTGCGC
GCGGTGGTTACTACTCTCATGACATGTGGTCTGAAGATTGGGGTCAAGGTACTCTGGTGACCGTCTCCTCAGCggccgca
cccaccacgacgccagcgccgcgaccaccaaccccggcgcccacgatcgcgtcgcagcccctgtccctgcgcccagaggc
gtgccggccagcggcggggggcgcagtgcacacgagggggctggacttcgcctgtgatatctacatctgggcgcccctgg
ccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaacaaacggggcagaaagaagctcctgtat
atattcaaacaaccatttatgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaaga
agaaggaggatgtgaactgagagtgaagttcagcaggagcgcagagccccccgcgtaccagcagggccagaaccagctct
ataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatgggggga
aagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagat
tgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacct
acgacgcccttcacatgcaggccctgccccctcgctaacagccactcgaggatccggattagtccaatttgttaaagaca
ggatatcagtggtccaggctctagttttgactcaacaatatcaccagctgaagcctatagagtacgagccatagataaaa
taaaagattttatttagtctccagaaaaaggggggaatgaaagaccccacctgtaggtttggcaagctagcttaagtaac
gccattttgcaaggcatggaaaaatacataactgagaatagagaagttcagatcaaggtcaggaacagatggaacagctg
aatatgggccaaacaggatatctgtggtaagcagttcctgccccggctcagggccaagaacagatggaacagctgaatat
gggccaaacaggatatctgtggtaagcagttcctgccccggctcagggccaagaacagatggtccccagatgcggtccag
ccctcagcagtttctagagaaccatcagatgtttccagggtgccccaaggacctgaaatgaccctgtgccttatttgaac
taaccaatcagttcgcttctcgcttctgttcgcgcgcttctgctccccgagctcaataaaagagcccacaacccctcact
cggggcgccagtcctccgattgactgagtcgcccgggtacccgtgtatccaataaaccctcttgcagttgcatccgactt
gtggtctcgctgttccttgggagggtctcctctgagtgattgactacccgtcagcgggggtctttcacacatgcagcatg
tatcaaaattaatttggttttttttcttaagtatttacattaaatggccatagtacttaaagttacattggcttccttga
aataaacatggagtattcagaatgtgtcataaatatttctaattttaagatagtatctccattggctttctactttttct
tttatttttttttgtcctctgtcttccatttgttgttgttgttgtttgtttgtttgtttgttggttggttggttaatttt
tttttaaagatcctacactatagttcaagctagactattagctactctgtaacccagggtgaccttgaagtcatgggtag
cctgctgttttagccttcccacatctaagattacaggtatgagctatcatttttggtatattgattgattgattgattga
tgtgtgtgtgtgtgattgtgtttgtgtgtgtgactgtgaaaatgtgtgtatgggtgtgtgtgaatgtgtgtatgtatgtg
tgtgtgtgagtgtgtgtgtgtgtgtgtgcatgtgtgtgtgtgtgactgtgtctatgtgtatgactgtgtgtgtgtgtgtg
tgtgtgtgtgtgtgtgtgtgtgtgtgtgtgttgtgaaaaaatattctatggtagtgagagccaacgctccggctcaggtg
tcaggttggtttttgagacagagtctttcacttagcttggAATTCACTGGCCGTCGTTTTACAACGTCGTGACTGGGAAA
ACCCTGGCGTTACCCAACTTAATCGCCTTGCAGCACATCCCCCTTTCGCCAGCTGGCGTAATAGCGAAGAGGCCCGCACC
GATCGCCCTTCCCAACAGTTGCGCAGCCTGAATGGCGAATGGCGCCTGATGCGGTATTTTCTCCTTACGCATCTGTGCGG
TATTTCACACCGCATATGGTGCACTCTCAGTACAATCTGCTCTGATGCCGCATAGTTAAGCCAGCCCCGACACCCGCCAA
CACCCGCTGACGCGCCCTGACGGGCTTGTCTGCTCCCGGCATCCGCTTACAGACAAGCTGTGACCGTCTCCGGGAGCTGC
ATGTGTCAGAGGTTTTCACCGTCATCACCGAAACGCGCGATGACGAAAGGGCCTCGTGATACGCCTATTTTTATAGGTTA
ATGTCATGATAATAATGGTTTCTTAGACGTCAGGTGGCACTTTTCGGGGAAATGTGCGCGGAACCCCTATTTGTTTATTT
TTCTAAATACATTCAAATATGTATCCGCTCATGAGACAATAACCCTGATAAATGCTTCAATAATATTGAAAAAGGAAGAG
TATGAGTATTCAACATTTCCGTGTCGCCCTTATTCCCTTTTTTGCGGCATTTTGCCTTCCTGTTTTTGCTCACCCAGAAA
CGCTGGTGAAAGTAAAAGATGCTGAAGATCAGTTGGGTGCACGAGTGGGTTACATCGAACTGGATCTCAACAGCGGTAAG
ATCCTTGAGAGTTTTCGCCCCGAAGAACGTTTTCCAATGATGAGCACTTTTAAAGTTCTGCTATGTGGCGCGGTATTATC
CCGTATTGACGCCGGGCAAGAGCAACTCGGTCGCCGCATACACTATTCTCAGAATGACTTGGTTGAGTACTCACCAGTCA
CAGAAAAGCATCTTACGGATGGCATGACAGTAAGAGAATTATGCAGTGCTGCCATAACCATGAGTGATAACACTGCGGCC
AACTTACTTCTGACAACGATCGGAGGACCGAAGGAGCTAACCGCTTTTTTGCACAACATGGGGGATCATGTAACTCGCCT
TGATCGTTGGGAACCGGAGCTGAATGAAGCCATACCAAACGACGAGCGTGACACCACGATGCCTGTAGCAATGGCAACAA
CGTTGCGCAAACTATTAACTGGCGAACTACTTACTCTAGCTTCCCGGCAACAATTAATAGACTGGATGGAGGCGGATAAA
GTTGCAGGACCACTTCTGCGCTCGGCCCTTCCGGCTGGCTGGTTTATTGCTGATAAATCTGGAGCCGGTGAGCGTGGGTC
TCGCGGTATCATTGCAGCACTGGGGCCAGATGGTAAGCCCTCCCGTATCGTAGTTATCTACACGACGGGGAGTCAGGCAA
CTATGGATGAACGAAATAGACAGATCGCTGAGATAGGTGCCTCACTGATTAAGCATTGGTAACTGTCAGACCAAGTTTAC
TCATATATACTTTAGATTGATTTAAAACTTCATTTTTAATTTAAAAGGATCTAGGTGAAGATCCTTTTTGATAATCTCAT
GACCAAAATCCCTTAACGTGAGTTTTCGTTCCACTGAGCGTCAGACCCCGTAGAAAAGATCAAAGGATCTTCTTGAGATC
CTTTTTTTCTGCGCGTAATCTGCTGCTTGCAAACAAAAAAACCACCGCTACCAGCGGTGGTTTGTTTGCCGGATCAAGAG
CTACCAACTCTTTTTCCGAAGGTAACTGGCTTCAGCAGAGCGCAGATACCAAATACTGTCCTTCTAGTGTAGCCGTAGTT
AGGCCACCACTTCAAGAACTCTGTAGCACCGCCTACATACCTCGCTCTGCTAATCCTGTTACCAGTGGCTGCTGCCAGTG
GCGATAAGTCGTGTCTTACCGGGTTGGACTCAAGACGATAGTTACCGGATAAGGCGCAGCGGTCGGGCTGAACGGGGGGT
TCGTGCACACAGCCCAGCTTGGAGCGAACGACCTACACCGAACTGAGATACCTACAGCGTGAGCATTGAGAAAGCGCCAC
GCTTCCCGAAGGGAGAAAGGCGGACAGGTATCCGGTAAGCGGCAGGGTCGGAACAGGAGAGCGCACGAGGGAGCTTCCAG
GGGGAAACGCCTGGTATCTTTATAGTCCTGTCGGGTTTCGCCACCTCTGACTTGAGCGTCGATTTTTGTGATGCTCGTCA
GGGGGGCGGAGCCTATGGAAAAACGCCAGCAACGCGGCCTTTTTACGGTTCCTGGCCTTTTGCTGGCCTTTTGCTCACAT
GTTCTTTCCTGCGTTATCCCCTGATTCTGTGGATAACCGTATTACCGCCTTTGAGTGAGCTGATACCGCTCGCCGCAGCC
GAACGACCGAGCGCAGCGAGTCAGTGAGCGAGGAAGCGGAAGAGCGCCCAATACGCAAACCGCCTCTCCCCGCGCGTTGG
CCGATTCATTAATGCAGCTGGCACGACAGGTTTCCCGACTGGAAAGCGGGCAGTGAGCGCAACGCAATTAATGTGAGTTA
GCTCACTCATTAGGCACCCCAGGCTTTACACTTTATGCTTCCGGCTCGTATGTTGTGTGGAATTGTGAGCGGATAACAAT
TTCACACAGGAAACAGCTATGACCATGATTACGCCAAGCTTTGCTCTTAGGAGTTTCCTAATACATCCCAAACTCAAATA
TATAAAGCATTTGACTTGTTCTATGCCCTAGGGGGCGGGGGGAAGCTAAGCCAGCTTTTTTTAACATTTAAAATGTTAAT
TCCATTTTAAATGCACAGATGTTTTTATTTCATAAGGGTTTCAATGTGCATGAATGCTGCAATATTCCTGTTACCAAAGC
TAGTATAAATAAAAATAGATAAACGTGGAAATTACTTAGAGTTTCTGTCATTAACGTTTCCTTCCTCAGTTGACAACATA
AATGCGCTGCTGAGCAAGCCAGTTTGCATCTGTCAGGATCAATTTCCCATTATGCCAGTCATATTAATTACTAGTCAATT
AGTTGATTTTTATTTTTGACATATACATGTGAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCA
TTTTGCAAGGCATGGAAAAATACATAACTGAGAATAGAAAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATA
TGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGC
CAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCT
CAGCAGTTTCTAGAGAACCATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAAC
CAATCAGTTCGCTTCTCGCTTCTGTTCGCGCGCTTATGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGG
GCGCCAGTCCTCCGATTGACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGG
TCTCGCTGTTCCTTGGGAGGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCATTTGGGGGCTCGTCCGG
GATCGGGAGACCCCTGCCCAGGGACCACCGACCCACCACCGGGAGGTAAGCTGGCCAGCAACTTATCTGTGTCTGTCCGA
TTGTCTAGTGTCTATGACTGATTTTATGCGCCTGCGTCGGTACTAGTTAGCTAACTAGCTCTGTATCTGGCGGACCCGTG
GTGGAACTGACGAGTTCGGAACACCCGGCCGCAACCCTGGGAGACGTCCCAGGGACTTCGGGGGCCGTTTTTGTGGCCCG
ACCTGAGTCCTAAAATCCCGATCGTTTAGGACTCTTTGGTGCACCCCCCTTAGAGGAGGGATATGTGGTTCTGGTAGGAG
ACGAGAACCTAAAACAGTTCCCGCCTCCGTCTGAATTTTTGCTTTCGGTTTGGGACCGAAGCCGCGCCGCGCGTCTTGTC
TGCTGCAGCATCGTTCTGTGTTGTCTCTGTCTGACTGTGTTTCTGTATTTGTCTGAAAATATGGGCCCGGGCTAGACTGT
TACCACTCCCTTAAGTTTGACCTTAGGTCACTGGAAAGATGTCGAGCGGATCGCTCACAACCAGTCGGTAGATGTCAAGA
AGAGACGTTGGGTTACCTTCTGCTCTGCAGAATGGCCAACCTTTAACGTCGGATGGCCGCGAGACGGCACCTTTAACCGA
GACCTCATCACCCAGGTTAAGATCAAGGTCTTTTCACCTGGCCCGCATGGACACCCAGACCAGGTCCCCTACATCGTGAC
CTGGGAAGCCTTGGCTTTTGACCCCCCTCCCTGGGTCAAGCCCTTTGTACACCCTAAGCCTCCGCCTCCTCTTCCTCCAT
CCGCCCCGTCTCTCCCCCTTGAACCTCCTCGTTCGACCCCGCCTCGATCCTCCCTTTATCCAGCCCTCACT [SEQ ID NO: 229]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 230, которая представлена ниже:
GGCCCTCTAGGCGCCCCCATATGGCCATATGAGATCTTATATGGGGCACCCCCGCCCCTTGTAAACTTCCCTGACCCTGA
CATGACAAGAGTTACTAACAGCCCCTCTCTCCAAGCTCACTTACAGGCTCTCTACTTAGTCCAGCACGAAGTCTGGAGAC
CTCTGGCGGCAGCCTACCAAGAACAACTGGACCGACCGGTGCCGCCACCATGGAAACCGACACCCTGCTGCTGTGGGTGC
TGCTGCTGTGGGTGCCAGGATCCACAGGAtcctatgagctgactcagccaccctcagcgtctgggacccccgggcagagg
gtcaccatgtcttgttctggaaccagctccaacatcggaagtcactctgtaaactggtaccagcagctcccaggaacggc
ccccaaactcctcatctatactaataatcagcggccctcaggggtccctgaccgattctctggctccaagtctggcacct
cagcctccctggccatcagtggcctccagtctgaggatgaggctgattattactgtgcagcatgggatggcagcctgaat
ggtctggtattcggcggagggaccaagctgaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctctgg
tggtggtggatccctcgagatggccgaggtgcagctggtgcagtctggagcagaggtgaaaaagcccggggagtctctga
agatctcctgtaagggttctggatacagctttaccagctactggatcggctgggtgcgccagatgcccgggaaaggcctg
gagtggatggggatcatctatcctggtgactctgataccagatacagcccgtccttccaaggccacgtcaccatctcagc
tgacaagtccatcagcactgcctacctgcagtggagcagcctgaaggcctcggacaccgccatgtattactgtgcgcgct
actctggttctttcgataactggggtcaaggtactctggtgaccgtctcctcagcggccgcacccaccacgacgccagcg
ccgcgaccaccaaccccggcgcccacgatcgcgtcgcagcccctgtccctgcgcccagaggcgtgccggccagcggcggg
gggcgcagtgcacacgagggggctggacttcgcctgtgatatctacatctgggcgcccctggccgggacttgtggggtcc
ttctcctgtcactggttatcaccctttactgcaacaaacggggcagaaagaagctcctgtatatattcaaacaaccattt
atgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaagaagaaggaggatgtgaact
gagagtgaagttcagcaggagcgcagagccccccgcgtaccagcagggccagaaccagctctataacgagctcaatctag
gacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaac
cctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcg
ccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgc
aggccctgccccctcgctaacagccactcgaggatccggattagtccaatttgttaaagacaggatatcagtggtccagg
ctctagttttgactcaacaatatcaccagctgaagcctatagagtacgagccatagataaaataaaagattttatttagt
ctccagaaaaaggggggaatgaaagaccccacctgtaggtttggcaagctagcttaagtaacgccattttgcaaggcatg
gaaaaatacataactgagaatagagaagttcagatcaaggtcaggaacagatggaacagctgaatatgggccaaacagga
tatctgtggtaagcagttcctgccccggctcagggccaagaacagatggaacagctgaatatgggccaaacaggatatct
gtggtaagcagttcctgccccggctcagggccaagaacagatggtccccagatgcggtccagccctcagcagtttctaga
gaaccatcagatgtttccagggtgccccaaggacctgaaatgaccctgtgccttatttgaactaaccaatcagttcgctt
ctcgcttctgttcgcgcgcttctgctccccgagctcaataaaagagcccacaacccctcactcggggcgccagtcctccg
attgactgagtcgcccgggtacccgtgtatccaataaaccctcttgcagttgcatccgacttgtggtctcgctgttcctt
gggagggtctcctctgagtgattgactacccgtcagcgggggtctttcacacatgcagcatgtatcaaaattaatttggt
tttttttcttaagtatttacattaaatggccatagtacttaaagttacattggcttccttgaaataaacatggagtattc
agaatgtgtcataaatatttctaattttaagatagtatctccattggctttctactttttcttttatttttttttgtcct
ctgtcttccatttgttgttgttgttgtttgtttgtttgtttgttggttggttggttaatttttttttaaagatcctacac
tatagttcaagctagactattagctactctgtaacccagggtgaccttgaagtcatgggtagcctgctgttttagccttc
ccacatctaagattacaggtatgagctatcatttttggtatattgattgattgattgattgatgtgtgtgtgtgtgattg
tgtttgtgtgtgtgactgtgaaaatgtgtgtatgggtgtgtgtgaatgtgtgtatgtatgtgtgtgtgtgagtgtgtgtg
tgtgtgtgtgcatgtgtgtgtgtgtgactgtgtctatgtgtatgactgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtg
tgtgtgtgtgtgttgtgaaaaaatattctatggtagtgagagccaacgctccggctcaggtgtcaggttggtttttgaga
cagagtctttcacttagcttggAATTCACTGGCCGTCGTTTTACAACGTCGTGACTGGGAAAACCCTGGCGTTACCCAAC
TTAATCGCCTTGCAGCACATCCCCCTTTCGCCAGCTGGCGTAATAGCGAAGAGGCCCGCACCGATCGCCCTTCCCAACAG
TTGCGCAGCCTGAATGGCGAATGGCGCCTGATGCGGTATTTTCTCCTTACGCATCTGTGCGGTATTTCACACCGCATATG
GTGCACTCTCAGTACAATCTGCTCTGATGCCGCATAGTTAAGCCAGCCCCGACACCCGCCAACACCCGCTGACGCGCCCT
GACGGGCTTGTCTGCTCCCGGCATCCGCTTACAGACAAGCTGTGACCGTCTCCGGGAGCTGCATGTGTCAGAGGTTTTCA
CCGTCATCACCGAAACGCGCGATGACGAAAGGGCCTCGTGATACGCCTATTTTTATAGGTTAATGTCATGATAATAATGG
TTTCTTAGACGTCAGGTGGCACTTTTCGGGGAAATGTGCGCGGAACCCCTATTTGTTTATTTTTCTAAATACATTCAAAT
ATGTATCCGCTCATGAGACAATAACCCTGATAAATGCTTCAATAATATTGAAAAAGGAAGAGTATGAGTATTCAACATTT
CCGTGTCGCCCTTATTCCCTTTTTTGCGGCATTTTGCCTTCCTGTTTTTGCTCACCCAGAAACGCTGGTGAAAGTAAAAG
ATGCTGAAGATCAGTTGGGTGCACGAGTGGGTTACATCGAACTGGATCTCAACAGCGGTAAGATCCTTGAGAGTTTTCGC
CCCGAAGAACGTTTTCCAATGATGAGCACTTTTAAAGTTCTGCTATGTGGCGCGGTATTATCCCGTATTGACGCCGGGCA
AGAGCAACTCGGTCGCCGCATACACTATTCTCAGAATGACTTGGTTGAGTACTCACCAGTCACAGAAAAGCATCTTACGG
ATGGCATGACAGTAAGAGAATTATGCAGTGCTGCCATAACCATGAGTGATAACACTGCGGCCAACTTACTTCTGACAACG
ATCGGAGGACCGAAGGAGCTAACCGCTTTTTTGCACAACATGGGGGATCATGTAACTCGCCTTGATCGTTGGGAACCGGA
GCTGAATGAAGCCATACCAAACGACGAGCGTGACACCACGATGCCTGTAGCAATGGCAACAACGTTGCGCAAACTATTAA
CTGGCGAACTACTTACTCTAGCTTCCCGGCAACAATTAATAGACTGGATGGAGGCGGATAAAGTTGCAGGACCACTTCTG
CGCTCGGCCCTTCCGGCTGGCTGGTTTATTGCTGATAAATCTGGAGCCGGTGAGCGTGGGTCTCGCGGTATCATTGCAGC
ACTGGGGCCAGATGGTAAGCCCTCCCGTATCGTAGTTATCTACACGACGGGGAGTCAGGCAACTATGGATGAACGAAATA
GACAGATCGCTGAGATAGGTGCCTCACTGATTAAGCATTGGTAACTGTCAGACCAAGTTTACTCATATATACTTTAGATT
GATTTAAAACTTCATTTTTAATTTAAAAGGATCTAGGTGAAGATCCTTTTTGATAATCTCATGACCAAAATCCCTTAACG
TGAGTTTTCGTTCCACTGAGCGTCAGACCCCGTAGAAAAGATCAAAGGATCTTCTTGAGATCCTTTTTTTCTGCGCGTAA
TCTGCTGCTTGCAAACAAAAAAACCACCGCTACCAGCGGTGGTTTGTTTGCCGGATCAAGAGCTACCAACTCTTTTTCCG
AAGGTAACTGGCTTCAGCAGAGCGCAGATACCAAATACTGTCCTTCTAGTGTAGCCGTAGTTAGGCCACCACTTCAAGAA
CTCTGTAGCACCGCCTACATACCTCGCTCTGCTAATCCTGTTACCAGTGGCTGCTGCCAGTGGCGATAAGTCGTGTCTTA
CCGGGTTGGACTCAAGACGATAGTTACCGGATAAGGCGCAGCGGTCGGGCTGAACGGGGGGTTCGTGCACACAGCCCAGC
TTGGAGCGAACGACCTACACCGAACTGAGATACCTACAGCGTGAGCATTGAGAAAGCGCCACGCTTCCCGAAGGGAGAAA
GGCGGACAGGTATCCGGTAAGCGGCAGGGTCGGAACAGGAGAGCGCACGAGGGAGCTTCCAGGGGGAAACGCCTGGTATC
TTTATAGTCCTGTCGGGTTTCGCCACCTCTGACTTGAGCGTCGATTTTTGTGATGCTCGTCAGGGGGGCGGAGCCTATGG
AAAAACGCCAGCAACGCGGCCTTTTTACGGTTCCTGGCCTTTTGCTGGCCTTTTGCTCACATGTTCTTTCCTGCGTTATC
CCCTGATTCTGTGGATAACCGTATTACCGCCTTTGAGTGAGCTGATACCGCTCGCCGCAGCCGAACGACCGAGCGCAGCG
AGTCAGTGAGCGAGGAAGCGGAAGAGCGCCCAATACGCAAACCGCCTCTCCCCGCGCGTTGGCCGATTCATTAATGCAGC
TGGCACGACAGGTTTCCCGACTGGAAAGCGGGCAGTGAGCGCAACGCAATTAATGTGAGTTAGCTCACTCATTAGGCACC
CCAGGCTTTACACTTTATGCTTCCGGCTCGTATGTTGTGTGGAATTGTGAGCGGATAACAATTTCACACAGGAAACAGCT
ATGACCATGATTACGCCAAGCTTTGCTCTTAGGAGTTTCCTAATACATCCCAAACTCAAATATATAAAGCATTTGACTTG
TTCTATGCCCTAGGGGGCGGGGGGAAGCTAAGCCAGCTTTTTTTAACATTTAAAATGTTAATTCCATTTTAAATGCACAG
ATGTTTTTATTTCATAAGGGTTTCAATGTGCATGAATGCTGCAATATTCCTGTTACCAAAGCTAGTATAAATAAAAATAG
ATAAACGTGGAAATTACTTAGAGTTTCTGTCATTAACGTTTCCTTCCTCAGTTGACAACATAAATGCGCTGCTGAGCAAG
CCAGTTTGCATCTGTCAGGATCAATTTCCCATTATGCCAGTCATATTAATTACTAGTCAATTAGTTGATTTTTATTTTTG
ACATATACATGTGAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTTTGCAAGGCATGGAAA
AATACATAACTGAGAATAGAAAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATC
TGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGG
TAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAGCAGTTTCTAGAGAAC
CATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAATCAGTTCGCTTCTCG
CTTCTGTTCGCGCGCTTATGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGGGCGCCAGTCCTCCGATTG
ACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCTCGCTGTTCCTTGGGA
GGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCATTTGGGGGCTCGTCCGGGATCGGGAGACCCCTGCC
CAGGGACCACCGACCCACCACCGGGAGGTAAGCTGGCCAGCAACTTATCTGTGTCTGTCCGATTGTCTAGTGTCTATGAC
TGATTTTATGCGCCTGCGTCGGTACTAGTTAGCTAACTAGCTCTGTATCTGGCGGACCCGTGGTGGAACTGACGAGTTCG
GAACACCCGGCCGCAACCCTGGGAGACGTCCCAGGGACTTCGGGGGCCGTTTTTGTGGCCCGACCTGAGTCCTAAAATCC
CGATCGTTTAGGACTCTTTGGTGCACCCCCCTTAGAGGAGGGATATGTGGTTCTGGTAGGAGACGAGAACCTAAAACAGT
TCCCGCCTCCGTCTGAATTTTTGCTTTCGGTTTGGGACCGAAGCCGCGCCGCGCGTCTTGTCTGCTGCAGCATCGTTCTG
TGTTGTCTCTGTCTGACTGTGTTTCTGTATTTGTCTGAAAATATGGGCCCGGGCTAGACTGTTACCACTCCCTTAAGTTT
GACCTTAGGTCACTGGAAAGATGTCGAGCGGATCGCTCACAACCAGTCGGTAGATGTCAAGAAGAGACGTTGGGTTACCT
TCTGCTCTGCAGAATGGCCAACCTTTAACGTCGGATGGCCGCGAGACGGCACCTTTAACCGAGACCTCATCACCCAGGTT
AAGATCAAGGTCTTTTCACCTGGCCCGCATGGACACCCAGACCAGGTCCCCTACATCGTGACCTGGGAAGCCTTGGCTTT
TGACCCCCCTCCCTGGGTCAAGCCCTTTGTACACCCTAAGCCTCCGCCTCCTCTTCCTCCATCCGCCCCGTCTCTCCCCC
TTGAACCTCCTCGTTCGACCCCGCCTCGATCCTCCCTTTATCCAGCCCTCACT [SEQ ID NO: 230]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 231, которая представлена ниже:
CCTTCTCTAGGCGCCCCCATATGGCCATATGAGATCTTATATGGGGCACCCCCGCCCCTTGTAAACTTCCCTGACCCTGA
CATGACAAGAGTTACTAACAGCCCCTCTCTCCAAGCTCACTTACAGGCTCTCTACTTAGTCCAGCACGAAGTCTGGAGAC
CTCTGGCGGCAGCCTACCAAGAACAACTGGACCGACCGGTGCCGCCACCATGGAAACCGACACCCTGCTGCTGTGGGTGC
TGCTGCTGTGGGTGCCAGGATCCACAGGACAGGCTGTGCTGACTCAGCCACCCTCAGCGTCTGGGACCCCCGGGCAGAGG
GTCACCATCTCTTGTTCTGGAAGCAGCTCCAACATCGGAAGTAATTACGTATTCTGGTACCAGCAGCTCCCAGGAACGGC
CCCCAAACTCCTCATCTATAGTAATAATCAGCGGCCCTCAGGGGTCCCTGACCGATTCTCTGGCTCCAAGTCTGGCACCT
CAGCCTCCCTGGCCATCAGTGGGCTCCGGTCCGAGGATGAGGCTGATTATTACTGTGCAGCATGGGATGACAGCCTGAGT
GCCTCTTATGTTTTCGGAACTGGGACCAAGGTCACCGTCCTAGGTTCTAGAGGTGGTGGTGGTAGCGGCGGCGGCGGCTC
TGGTGGTGGTGGATCCCTCGAGATGGCCCAGGTGCAGCTGGTGCAGTCTGGGGCTGAGGTGAAGAAGCCTGGGTCCTCGG
TGAAGGTCTCCTGCAAGGCTTCTGGAGGCACCTTCAGCAGCTATGCTATCAGCTGGGTGCGACAGGCCCCTGGACAAGGG
CTTGAGTGGATGGGAAGGATCATCCCTATCCTTGGTACAGCAAACTACGCACAGAAGTTCCAGGGCAGAGTCACGATTAC
CGCGGACGAATCCACGAGCACAGCCTACATGGAGCTGAGCAGCCTGAGATCTGAGGACACGGCCGTGTATTACTGTGCGC
GCTCTGGTTACGGTTCTTACCGTTGGGAAGATTCTTGGGGTCAAGGTACTCTGGTGACCGTCTCCTCAGCggccgcaccc
accacgacgccagcgccgcgaccaccaaccccggcgcccacgatcgcgtcgcagcccctgtccctgcgcccagaggcgtg
ccggccagcggcggggggcgcagtgcacacgagggggctggacttcgcctgtgatatctacatctgggcgcccctggccg
ggacttgtggggtccttctcctgtcactggttatcaccctttactgcaacaaacggggcagaaagaagctcctgtatata
ttcaaacaaccatttatgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaagaaga
aggaggatgtgaactgagagtgaagttcagcaggagcgcagagccccccgcgtaccagcagggccagaaccagctctata
acgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaag
ccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgg
gatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacg
acgcccttcacatgcaggccctgccccctcgctaacagccactcgaggatccggattagtccaatttgttaaagacagga
tatcagtggtccaggctctagttttgactcaacaatatcaccagctgaagcctatagagtacgagccatagataaaataa
aagattttatttagtctccagaaaaaggggggaatgaaagaccccacctgtaggtttggcaagctagcttaagtaacgcc
attttgcaaggcatggaaaaatacataactgagaatagagaagttcagatcaaggtcaggaacagatggaacagctgaat
atgggccaaacaggatatctgtggtaagcagttcctgccccggctcagggccaagaacagatggaacagctgaatatggg
ccaaacaggatatctgtggtaagcagttcctgccccggctcagggccaagaacagatggtccccagatgcggtccagccc
tcagcagtttctagagaaccatcagatgtttccagggtgccccaaggacctgaaatgaccctgtgccttatttgaactaa
ccaatcagttcgcttctcgcttctgttcgcgcgcttctgctccccgagctcaataaaagagcccacaacccctcactcgg
ggcgccagtcctccgattgactgagtcgcccgggtacccgtgtatccaataaaccctcttgcagttgcatccgacttgtg
gtctcgctgttccttgggagggtctcctctgagtgattgactacccgtcagcgggggtctttcacacatgcagcatgtat
caaaattaatttggttttttttcttaagtatttacattaaatggccatagtacttaaagttacattggcttccttgaaat
aaacatggagtattcagaatgtgtcataaatatttctaattttaagatagtatctccattggctttctactttttctttt
atttttttttgtcctctgtcttccatttgttgttgttgttgtttgtttgtttgtttgttggttggttggttaattttttt
ttaaagatcctacactatagttcaagctagactattagctactctgtaacccagggtgaccttgaagtcatgggtagcct
gctgttttagccttcccacatctaagattacaggtatgagctatcatttttggtatattgattgattgattgattgatgt
gtgtgtgtgtgattgtgtttgtgtgtgtgactgtgaaaatgtgtgtatgggtgtgtgtgaatgtgtgtatgtatgtgtgt
gtgtgagtgtgtgtgtgtgtgtgtgcatgtgtgtgtgtgtgactgtgtctatgtgtatgactgtgtgtgtgtgtgtgtgt
gtgtgtgtgtgtgtgtgtgtgtgtgtgttgtgaaaaaatattctatggtagtgagagccaacgctccggctcaggtgtca
ggttggtttttgagacagagtctttcacttagcttggAATTCACTGGCCGTCGTTTTACAACGTCGTGACTGGGAAAACC
CTGGCGTTACCCAACTTAATCGCCTTGCAGCACATCCCCCTTTCGCCAGCTGGCGTAATAGCGAAGAGGCCCGCACCGAT
CGCCCTTCCCAACAGTTGCGCAGCCTGAATGGCGAATGGCGCCTGATGCGGTATTTTCTCCTTACGCATCTGTGCGGTAT
TTCACACCGCATATGGTGCACTCTCAGTACAATCTGCTCTGATGCCGCATAGTTAAGCCAGCCCCGACACCCGCCAACAC
CCGCTGACGCGCCCTGACGGGCTTGTCTGCTCCCGGCATCCGCTTACAGACAAGCTGTGACCGTCTCCGGGAGCTGCATG
TGTCAGAGGTTTTCACCGTCATCACCGAAACGCGCGATGACGAAAGGGCCTCGTGATACGCCTATTTTTATAGGTTAATG
TCATGATAATAATGGTTTCTTAGACGTCAGGTGGCACTTTTCGGGGAAATGTGCGCGGAACCCCTATTTGTTTATTTTTC
TAAATACATTCAAATATGTATCCGCTCATGAGACAATAACCCTGATAAATGCTTCAATAATATTGAAAAAGGAAGAGTAT
GAGTATTCAACATTTCCGTGTCGCCCTTATTCCCTTTTTTGCGGCATTTTGCCTTCCTGTTTTTGCTCACCCAGAAACGC
TGGTGAAAGTAAAAGATGCTGAAGATCAGTTGGGTGCACGAGTGGGTTACATCGAACTGGATCTCAACAGCGGTAAGATC
CTTGAGAGTTTTCGCCCCGAAGAACGTTTTCCAATGATGAGCACTTTTAAAGTTCTGCTATGTGGCGCGGTATTATCCCG
TATTGACGCCGGGCAAGAGCAACTCGGTCGCCGCATACACTATTCTCAGAATGACTTGGTTGAGTACTCACCAGTCACAG
AAAAGCATCTTACGGATGGCATGACAGTAAGAGAATTATGCAGTGCTGCCATAACCATGAGTGATAACACTGCGGCCAAC
TTACTTCTGACAACGATCGGAGGACCGAAGGAGCTAACCGCTTTTTTGCACAACATGGGGGATCATGTAACTCGCCTTGA
TCGTTGGGAACCGGAGCTGAATGAAGCCATACCAAACGACGAGCGTGACACCACGATGCCTGTAGCAATGGCAACAACGT
TGCGCAAACTATTAACTGGCGAACTACTTACTCTAGCTTCCCGGCAACAATTAATAGACTGGATGGAGGCGGATAAAGTT
GCAGGACCACTTCTGCGCTCGGCCCTTCCGGCTGGCTGGTTTATTGCTGATAAATCTGGAGCCGGTGAGCGTGGGTCTCG
CGGTATCATTGCAGCACTGGGGCCAGATGGTAAGCCCTCCCGTATCGTAGTTATCTACACGACGGGGAGTCAGGCAACTA
TGGATGAACGAAATAGACAGATCGCTGAGATAGGTGCCTCACTGATTAAGCATTGGTAACTGTCAGACCAAGTTTACTCA
TATATACTTTAGATTGATTTAAAACTTCATTTTTAATTTAAAAGGATCTAGGTGAAGATCCTTTTTGATAATCTCATGAC
CAAAATCCCTTAACGTGAGTTTTCGTTCCACTGAGCGTCAGACCCCGTAGAAAAGATCAAAGGATCTTCTTGAGATCCTT
TTTTTCTGCGCGTAATCTGCTGCTTGCAAACAAAAAAACCACCGCTACCAGCGGTGGTTTGTTTGCCGGATCAAGAGCTA
CCAACTCTTTTTCCGAAGGTAACTGGCTTCAGCAGAGCGCAGATACCAAATACTGTCCTTCTAGTGTAGCCGTAGTTAGG
CCACCACTTCAAGAACTCTGTAGCACCGCCTACATACCTCGCTCTGCTAATCCTGTTACCAGTGGCTGCTGCCAGTGGCG
ATAAGTCGTGTCTTACCGGGTTGGACTCAAGACGATAGTTACCGGATAAGGCGCAGCGGTCGGGCTGAACGGGGGGTTCG
TGCACACAGCCCAGCTTGGAGCGAACGACCTACACCGAACTGAGATACCTACAGCGTGAGCATTGAGAAAGCGCCACGCT
TCCCGAAGGGAGAAAGGCGGACAGGTATCCGGTAAGCGGCAGGGTCGGAACAGGAGAGCGCACGAGGGAGCTTCCAGGGG
GAAACGCCTGGTATCTTTATAGTCCTGTCGGGTTTCGCCACCTCTGACTTGAGCGTCGATTTTTGTGATGCTCGTCAGGG
GGGCGGAGCCTATGGAAAAACGCCAGCAACGCGGCCTTTTTACGGTTCCTGGCCTTTTGCTGGCCTTTTGCTCACATGTT
CTTTCCTGCGTTATCCCCTGATTCTGTGGATAACCGTATTACCGCCTTTGAGTGAGCTGATACCGCTCGCCGCAGCCGAA
CGACCGAGCGCAGCGAGTCAGTGAGCGAGGAAGCGGAAGAGCGCCCAATACGCAAACCGCCTCTCCCCGCGCGTTGGCCG
ATTCATTAATGCAGCTGGCACGACAGGTTTCCCGACTGGAAAGCGGGCAGTGAGCGCAACGCAATTAATGTGAGTTAGCT
CACTCATTAGGCACCCCAGGCTTTACACTTTATGCTTCCGGCTCGTATGTTGTGTGGAATTGTGAGCGGATAACAATTTC
ACACAGGAAACAGCTATGACCATGATTACGCCAAGCTTTGCTCTTAGGAGTTTCCTAATACATCCCAAACTCAAATATAT
AAAGCATTTGACTTGTTCTATGCCCTAGGGGGCGGGGGGAAGCTAAGCCAGCTTTTTTTAACATTTAAAATGTTAATTCC
ATTTTAAATGCACAGATGTTTTTATTTCATAAGGGTTTCAATGTGCATGAATGCTGCAATATTCCTGTTACCAAAGCTAG
TATAAATAAAAATAGATAAACGTGGAAATTACTTAGAGTTTCTGTCATTAACGTTTCCTTCCTCAGTTGACAACATAAAT
GCGCTGCTGAGCAAGCCAGTTTGCATCTGTCAGGATCAATTTCCCATTATGCCAGTCATATTAATTACTAGTCAATTAGT
TGATTTTTATTTTTGACATATACATGTGAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTT
TGCAAGGCATGGAAAAATACATAACTGAGAATAGAAAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGG
GCCAAACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAA
ACAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAG
CAGTTTCTAGAGAACCATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAA
TCAGTTCGCTTCTCGCTTCTGTTCGCGCGCTTATGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGGGCG
CCAGTCCTCCGATTGACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCT
CGCTGTTCCTTGGGAGGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCATTTGGGGGCTCGTCCGGGAT
CGGGAGACCCCTGCCCAGGGACCACCGACCCACCACCGGGAGGTAAGCTGGCCAGCAACTTATCTGTGTCTGTCCGATTG
TCTAGTGTCTATGACTGATTTTATGCGCCTGCGTCGGTACTAGTTAGCTAACTAGCTCTGTATCTGGCGGACCCGTGGTG
GAACTGACGAGTTCGGAACACCCGGCCGCAACCCTGGGAGACGTCCCAGGGACTTCGGGGGCCGTTTTTGTGGCCCGACC
TGAGTCCTAAAATCCCGATCGTTTAGGACTCTTTGGTGCACCCCCCTTAGAGGAGGGATATGTGGTTCTGGTAGGAGACG
AGAACCTAAAACAGTTCCCGCCTCCGTCTGAATTTTTGCTTTCGGTTTGGGACCGAAGCCGCGCCGCGCGTCTTGTCTGC
TGCAGCATCGTTCTGTGTTGTCTCTGTCTGACTGTGTTTCTGTATTTGTCTGAAAATATGGGCCCGGGCTAGACTGTTAC
CACTCCCTTAAGTTTGACCTTAGGTCACTGGAAAGATGTCGAGCGGATCGCTCACAACCAGTCGGTAGATGTCAAGAAGA
GACGTTGGGTTACCTTCTGCTCTGCAGAATGGCCAACCTTTAACGTCGGATGGCCGCGAGACGGCACCTTTAACCGAGAC
CTCATCACCCAGGTTAAGATCAAGGTCTTTTCACCTGGCCCGCATGGACACCCAGACCAGGTCCCCTACATCGTGACCTG
GGAAGCCTTGGCTTTTGACCCCCCTCCCTGGGTCAAGCCCTTTGTACACCCTAAGCCTCCGCCTCCTCTTCCTCCATCCG
CCCCGTCTCTCCCCCTTGAACCTCCTCGTTCGACCCCGCCTCGATCCTCCCTTTATCCAGCCCTCACT [SEQ ID NO: 231]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 232, которая представлена ниже:
CCTTCTCTAGGCGCCCCCATATGGCCATATGAGATCTTATATGGGGCACCCCCGCCCCTTGTAAACTTCCCTGACCCTGA
CATGACAAGAGTTACTAACAGCCCCTCTCTCCAAGCTCACTTACAGGCTCTCTACTTAGTCCAGCACGAAGTCTGGAGAC
CTCTGGCGGCAGCCTACCAAGAACAACTGGACCGACCGGTGCCGCCACCATGGAAACCGACACCCTGCTGCTGTGGGTGC
TGCTGCTGTGGGTGCCAGGATCCACAGGAcagtctgtgctgacgcagccgccctcagtgtctggggccccagggcagagg
gtcaccatctcctgcactgggagcagctccaacatcggggcaggttttgatgtacactggtaccagcagcttccaggaac
agcccccaaactcctcatctatggtaacagcaatcggccctcaggggtccctgaccgattctctggctccaagtctggca
cctcagcctccctggccatcactgggctccaggctgaggatgaggctgattattactgccagtcctatgacagcagcctg
agtggttatgtcttcggaactgggaccaaggtcaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctc
tggtggtggtggatccctcgagatggcccaggtccagctggtacagtctggggctgaggtgaagaagcctggggcctcag
tgaaggtctcctgcaaggcttctggatacaccttcaccgactactatatgcactgggtgcgacaggcccctggacaacgg
cttgagtggatgggatggatcaaccctaacagtggtggcacaaactatgcacagaagtttcaggacaggatcaccgtgac
cagggacacctccagcaacacaggctacatggagctgaccaggctgagatctgacgacacggccgtgtattactgtgcgc
gctctccgtactctggtgttctggataaatggggtcaaggtactctggtgaccgtctcctcagcggccgcacccaccacg
acgccagcgccgcgaccaccaaccccggcgcccacgatcgcgtcgcagcccctgtccctgcgcccagaggcgtgccggcc
agcggcggggggcgcagtgcacacgagggggctggacttcgcctgtgatatctacatctgggcgcccctggccgggactt
gtggggtccttctcctgtcactggttatcaccctttactgcaacaaacggggcagaaagaagctcctgtatatattcaaa
caaccatttatgagaccagtacaaactactcaagaggaagatggctgtagctgccgatttccagaagaagaagaaggagg
atgtgaactgagagtgaagttcagcaggagcgcagagccccccgcgtaccagcagggccagaaccagctctataacgagc
tcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgaga
aggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaa
aggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgccc
ttcacatgcaggccctgccccctcgctaacagccactcgaggatccggattagtccaatttgttaaagacaggatatcag
tggtccaggctctagttttgactcaacaatatcaccagctgaagcctatagagtacgagccatagataaaataaaagatt
ttatttagtctccagaaaaaggggggaatgaaagaccccacctgtaggtttggcaagctagcttaagtaacgccattttg
caaggcatggaaaaatacataactgagaatagagaagttcagatcaaggtcaggaacagatggaacagctgaatatgggc
caaacaggatatctgtggtaagcagttcctgccccggctcagggccaagaacagatggaacagctgaatatgggccaaac
aggatatctgtggtaagcagttcctgccccggctcagggccaagaacagatggtccccagatgcggtccagccctcagca
gtttctagagaaccatcagatgtttccagggtgccccaaggacctgaaatgaccctgtgccttatttgaactaaccaatc
agttcgcttctcgcttctgttcgcgcgcttctgctccccgagctcaataaaagagcccacaacccctcactcggggcgcc
agtcctccgattgactgagtcgcccgggtacccgtgtatccaataaaccctcttgcagttgcatccgacttgtggtctcg
ctgttccttgggagggtctcctctgagtgattgactacccgtcagcgggggtctttcacacatgcagcatgtatcaaaat
taatttggttttttttcttaagtatttacattaaatggccatagtacttaaagttacattggcttccttgaaataaacat
ggagtattcagaatgtgtcataaatatttctaattttaagatagtatctccattggctttctactttttcttttattttt
ttttgtcctctgtcttccatttgttgttgttgttgtttgtttgtttgtttgttggttggttggttaatttttttttaaag
atcctacactatagttcaagctagactattagctactctgtaacccagggtgaccttgaagtcatgggtagcctgctgtt
ttagccttcccacatctaagattacaggtatgagctatcatttttggtatattgattgattgattgattgatgtgtgtgt
gtgtgattgtgtttgtgtgtgtgactgtgaaaatgtgtgtatgggtgtgtgtgaatgtgtgtatgtatgtgtgtgtgtga
gtgtgtgtgtgtgtgtgtgcatgtgtgtgtgtgtgactgtgtctatgtgtatgactgtgtgtgtgtgtgtgtgtgtgtgt
gtgtgtgtgtgtgtgtgtgtgttgtgaaaaaatattctatggtagtgagagccaacgctccggctcaggtgtcaggttgg
tttttgagacagagtctttcacttagcttggAATTCACTGGCCGTCGTTTTACAACGTCGTGACTGGGAAAACCCTGGCG
TTACCCAACTTAATCGCCTTGCAGCACATCCCCCTTTCGCCAGCTGGCGTAATAGCGAAGAGGCCCGCACCGATCGCCCT
TCCCAACAGTTGCGCAGCCTGAATGGCGAATGGCGCCTGATGCGGTATTTTCTCCTTACGCATCTGTGCGGTATTTCACA
CCGCATATGGTGCACTCTCAGTACAATCTGCTCTGATGCCGCATAGTTAAGCCAGCCCCGACACCCGCCAACACCCGCTG
ACGCGCCCTGACGGGCTTGTCTGCTCCCGGCATCCGCTTACAGACAAGCTGTGACCGTCTCCGGGAGCTGCATGTGTCAG
AGGTTTTCACCGTCATCACCGAAACGCGCGATGACGAAAGGGCCTCGTGATACGCCTATTTTTATAGGTTAATGTCATGA
TAATAATGGTTTCTTAGACGTCAGGTGGCACTTTTCGGGGAAATGTGCGCGGAACCCCTATTTGTTTATTTTTCTAAATA
CATTCAAATATGTATCCGCTCATGAGACAATAACCCTGATAAATGCTTCAATAATATTGAAAAAGGAAGAGTATGAGTAT
TCAACATTTCCGTGTCGCCCTTATTCCCTTTTTTGCGGCATTTTGCCTTCCTGTTTTTGCTCACCCAGAAACGCTGGTGA
AAGTAAAAGATGCTGAAGATCAGTTGGGTGCACGAGTGGGTTACATCGAACTGGATCTCAACAGCGGTAAGATCCTTGAG
AGTTTTCGCCCCGAAGAACGTTTTCCAATGATGAGCACTTTTAAAGTTCTGCTATGTGGCGCGGTATTATCCCGTATTGA
CGCCGGGCAAGAGCAACTCGGTCGCCGCATACACTATTCTCAGAATGACTTGGTTGAGTACTCACCAGTCACAGAAAAGC
ATCTTACGGATGGCATGACAGTAAGAGAATTATGCAGTGCTGCCATAACCATGAGTGATAACACTGCGGCCAACTTACTT
CTGACAACGATCGGAGGACCGAAGGAGCTAACCGCTTTTTTGCACAACATGGGGGATCATGTAACTCGCCTTGATCGTTG
GGAACCGGAGCTGAATGAAGCCATACCAAACGACGAGCGTGACACCACGATGCCTGTAGCAATGGCAACAACGTTGCGCA
AACTATTAACTGGCGAACTACTTACTCTAGCTTCCCGGCAACAATTAATAGACTGGATGGAGGCGGATAAAGTTGCAGGA
CCACTTCTGCGCTCGGCCCTTCCGGCTGGCTGGTTTATTGCTGATAAATCTGGAGCCGGTGAGCGTGGGTCTCGCGGTAT
CATTGCAGCACTGGGGCCAGATGGTAAGCCCTCCCGTATCGTAGTTATCTACACGACGGGGAGTCAGGCAACTATGGATG
AACGAAATAGACAGATCGCTGAGATAGGTGCCTCACTGATTAAGCATTGGTAACTGTCAGACCAAGTTTACTCATATATA
CTTTAGATTGATTTAAAACTTCATTTTTAATTTAAAAGGATCTAGGTGAAGATCCTTTTTGATAATCTCATGACCAAAAT
CCCTTAACGTGAGTTTTCGTTCCACTGAGCGTCAGACCCCGTAGAAAAGATCAAAGGATCTTCTTGAGATCCTTTTTTTC
TGCGCGTAATCTGCTGCTTGCAAACAAAAAAACCACCGCTACCAGCGGTGGTTTGTTTGCCGGATCAAGAGCTACCAACT
CTTTTTCCGAAGGTAACTGGCTTCAGCAGAGCGCAGATACCAAATACTGTCCTTCTAGTGTAGCCGTAGTTAGGCCACCA
CTTCAAGAACTCTGTAGCACCGCCTACATACCTCGCTCTGCTAATCCTGTTACCAGTGGCTGCTGCCAGTGGCGATAAGT
CGTGTCTTACCGGGTTGGACTCAAGACGATAGTTACCGGATAAGGCGCAGCGGTCGGGCTGAACGGGGGGTTCGTGCACA
CAGCCCAGCTTGGAGCGAACGACCTACACCGAACTGAGATACCTACAGCGTGAGCATTGAGAAAGCGCCACGCTTCCCGA
AGGGAGAAAGGCGGACAGGTATCCGGTAAGCGGCAGGGTCGGAACAGGAGAGCGCACGAGGGAGCTTCCAGGGGGAAACG
CCTGGTATCTTTATAGTCCTGTCGGGTTTCGCCACCTCTGACTTGAGCGTCGATTTTTGTGATGCTCGTCAGGGGGGCGG
AGCCTATGGAAAAACGCCAGCAACGCGGCCTTTTTACGGTTCCTGGCCTTTTGCTGGCCTTTTGCTCACATGTTCTTTCC
TGCGTTATCCCCTGATTCTGTGGATAACCGTATTACCGCCTTTGAGTGAGCTGATACCGCTCGCCGCAGCCGAACGACCG
AGCGCAGCGAGTCAGTGAGCGAGGAAGCGGAAGAGCGCCCAATACGCAAACCGCCTCTCCCCGCGCGTTGGCCGATTCAT
TAATGCAGCTGGCACGACAGGTTTCCCGACTGGAAAGCGGGCAGTGAGCGCAACGCAATTAATGTGAGTTAGCTCACTCA
TTAGGCACCCCAGGCTTTACACTTTATGCTTCCGGCTCGTATGTTGTGTGGAATTGTGAGCGGATAACAATTTCACACAG
GAAACAGCTATGACCATGATTACGCCAAGCTTTGCTCTTAGGAGTTTCCTAATACATCCCAAACTCAAATATATAAAGCA
TTTGACTTGTTCTATGCCCTAGGGGGCGGGGGGAAGCTAAGCCAGCTTTTTTTAACATTTAAAATGTTAATTCCATTTTA
AATGCACAGATGTTTTTATTTCATAAGGGTTTCAATGTGCATGAATGCTGCAATATTCCTGTTACCAAAGCTAGTATAAA
TAAAAATAGATAAACGTGGAAATTACTTAGAGTTTCTGTCATTAACGTTTCCTTCCTCAGTTGACAACATAAATGCGCTG
CTGAGCAAGCCAGTTTGCATCTGTCAGGATCAATTTCCCATTATGCCAGTCATATTAATTACTAGTCAATTAGTTGATTT
TTATTTTTGACATATACATGTGAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTTTGCAAG
GCATGGAAAAATACATAACTGAGAATAGAAAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGGGCCAAA
CAGGATATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAAACAGGA
TATCTGTGGTAAGCAGTTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAGCAGTTT
CTAGAGAACCATCAGATGTTTCCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAATCAGTT
CGCTTCTCGCTTCTGTTCGCGCGCTTATGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGGGCGCCAGTC
CTCCGATTGACTGAGTCGCCCGGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCTCGCTGT
TCCTTGGGAGGGTCTCCTCTGAGTGATTGACTACCCGTCAGCGGGGGTCTTTCATTTGGGGGCTCGTCCGGGATCGGGAG
ACCCCTGCCCAGGGACCACCGACCCACCACCGGGAGGTAAGCTGGCCAGCAACTTATCTGTGTCTGTCCGATTGTCTAGT
GTCTATGACTGATTTTATGCGCCTGCGTCGGTACTAGTTAGCTAACTAGCTCTGTATCTGGCGGACCCGTGGTGGAACTG
ACGAGTTCGGAACACCCGGCCGCAACCCTGGGAGACGTCCCAGGGACTTCGGGGGCCGTTTTTGTGGCCCGACCTGAGTC
CTAAAATCCCGATCGTTTAGGACTCTTTGGTGCACCCCCCTTAGAGGAGGGATATGTGGTTCTGGTAGGAGACGAGAACC
TAAAACAGTTCCCGCCTCCGTCTGAATTTTTGCTTTCGGTTTGGGACCGAAGCCGCGCCGCGCGTCTTGTCTGCTGCAGC
ATCGTTCTGTGTTGTCTCTGTCTGACTGTGTTTCTGTATTTGTCTGAAAATATGGGCCCGGGCTAGACTGTTACCACTCC
CTTAAGTTTGACCTTAGGTCACTGGAAAGATGTCGAGCGGATCGCTCACAACCAGTCGGTAGATGTCAAGAAGAGACGTT
GGGTTACCTTCTGCTCTGCAGAATGGCCAACCTTTAACGTCGGATGGCCGCGAGACGGCACCTTTAACCGAGACCTCATC
ACCCAGGTTAAGATCAAGGTCTTTTCACCTGGCCCGCATGGACACCCAGACCAGGTCCCCTACATCGTGACCTGGGAAGC
CTTGGCTTTTGACCCCCCTCCCTGGGTCAAGCCCTTTGTACACCCTAAGCCTCCGCCTCCTCTTCCTCCATCCGCCCCGT
CTCTCCCCCTTGAACCTCCTCGTTCGACCCCGCCTCGATCCTCCCTTTATCCAGCCCTCACT [SEQ ID NO: 232]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 233, которая представлена ниже:
CCTTCTCTAGGCGCCCCCATATGGCCATATGAGATCTTATATGGGGCACCCCCGCCCCTTGTAAACTTCCCTGACCCTGA
CATGACAAGAGTTACTAACAGCCCCTCTCTCCAAGCTCACTTACAGGCTCTCTACTTAGTCCAGCACGAAGTCTGGAGAC
CTCTGGCGGCAGCCTACCAAGAACAACTGGACCGACCGGTGCCGCCACCATGGAAACCGACACCCTGCTGCTGTGGGTGC
TGCTGCTGTGGGTGCCAGGATCCACAGGAcaatctgccctgactcagcctgcctccgtgtctgcgtctcctggacagtcg
atcgccatctcctgcactggaaccagcagtgacgttggttggtatcaacagcacccaggcaaagcccccaaactcatgat
ttatgaggacagtaagcggccctcaggggtttctaatcgcttctctggctccaagtctggcaacacggcctccctgacca
tctctgggctccaggctgaggacgaggctgattattactgcagctcaaatacaagaagcagcactttggtgttcggcgga
gggaccaagctgaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcga
gatggccgaagtgcagctggtgcagtctggggctgagatgaagaagcctggggcctcactgaagctctcctgcaaggctt
ctggatacaccttcatcgactactatgtatactggatgcgacaggcccctggacaagggcttgagtccatgggatggatc
aaccctaacagtggtggcacaaactatgcacagaagtttcagggcagggtcaccatgaccagggacacgtccatcagcac
agcctacatggagctgagcaggctgagatctgacgacaccgccatgtattactgtgcgcgctcccagcgtgacggttaca
tggattactggggtcaaggtactctggtgaccgtctcctcagcggccgcacccaccacgacgccagcgccgcgaccacca
accccggcgcccacgatcgcgtcgcagcccctgtccctgcgcccagaggcgtgccggccagcggcggggggcgcagtgca
cacgagggggctggacttcgcctgtgatatctacatctgggcgcccctggccgggacttgtggggtccttctcctgtcac
tggttatcaccctttactgcaacaaacggggcagaaagaagctcctgtatatattcaaacaaccatttatgagaccagta
caaactactcaagaggaagatggctgtagctgccgatttccagaagaagaagaaggaggatgtgaactgagagtgaagtt
cagcaggagcgcagagccccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagagg
agtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggc
ctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaa
ggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgcccc
ctcgctaacagccactcgaggatccggattagtccaatttgttaaagacaggatatcagtggtccaggctctagttttga
ctcaacaatatcaccagctgaagcctatagagtacgagccatagataaaataaaagattttatttagtctccagaaaaag
gggggaatgaaagaccccacctgtaggtttggcaagctagcttaagtaacgccattttgcaaggcatggaaaaatacata
actgagaatagagaagttcagatcaaggtcaggaacagatggaacagctgaatatgggccaaacaggatatctgtggtaa
gcagttcctgccccggctcagggccaagaacagatggaacagctgaatatgggccaaacaggatatctgtggtaagcagt
tcctgccccggctcagggccaagaacagatggtccccagatgcggtccagccctcagcagtttctagagaaccatcagat
gtttccagggtgccccaaggacctgaaatgaccctgtgccttatttgaactaaccaatcagttcgcttctcgcttctgtt
cgcgcgcttctgctccccgagctcaataaaagagcccacaacccctcactcggggcgccagtcctccgattgactgagtc
gcccgggtacccgtgtatccaataaaccctcttgcagttgcatccgacttgtggtctcgctgttccttgggagggtctcc
tctgagtgattgactacccgtcagcgggggtctttcacacatgcagcatgtatcaaaattaatttggttttttttcttaa
gtatttacattaaatggccatagtacttaaagttacattggcttccttgaaataaacatggagtattcagaatgtgtcat
aaatatttctaattttaagatagtatctccattggctttctactttttcttttatttttttttgtcctctgtcttccatt
tgttgttgttgttgtttgtttgtttgtttgttggttggttggttaatttttttttaaagatcctacactatagttcaagc
tagactattagctactctgtaacccagggtgaccttgaagtcatgggtagcctgctgttttagccttcccacatctaaga
ttacaggtatgagctatcatttttggtatattgattgattgattgattgatgtgtgtgtgtgtgattgtgtttgtgtgtg
tgactgtgaaaatgtgtgtatgggtgtgtgtgaatgtgtgtatgtatgtgtgtgtgtgagtgtgtgtgtgtgtgtgtgca
tgtgtgtgtgtgtgactgtgtctatgtgtatgactgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtgtg
ttgtgaaaaaatattctatggtagtgagagccaacgctccggctcaggtgtcaggttggtttttgagacagagtctttca
cttagcttggAATTCACTGGCCGTCGTTTTACAACGTCGTGACTGGGAAAACCCTGGCGTTACCCAACTTAATCGCCTTG
CAGCACATCCCCCTTTCGCCAGCTGGCGTAATAGCGAAGAGGCCCGCACCGATCGCCCTTCCCAACAGTTGCGCAGCCTG
AATGGCGAATGGCGCCTGATGCGGTATTTTCTCCTTACGCATCTGTGCGGTATTTCACACCGCATATGGTGCACTCTCAG
TACAATCTGCTCTGATGCCGCATAGTTAAGCCAGCCCCGACACCCGCCAACACCCGCTGACGCGCCCTGACGGGCTTGTC
TGCTCCCGGCATCCGCTTACAGACAAGCTGTGACCGTCTCCGGGAGCTGCATGTGTCAGAGGTTTTCACCGTCATCACCG
AAACGCGCGATGACGAAAGGGCCTCGTGATACGCCTATTTTTATAGGTTAATGTCATGATAATAATGGTTTCTTAGACGT
CAGGTGGCACTTTTCGGGGAAATGTGCGCGGAACCCCTATTTGTTTATTTTTCTAAATACATTCAAATATGTATCCGCTC
ATGAGACAATAACCCTGATAAATGCTTCAATAATATTGAAAAAGGAAGAGTATGAGTATTCAACATTTCCGTGTCGCCCT
TATTCCCTTTTTTGCGGCATTTTGCCTTCCTGTTTTTGCTCACCCAGAAACGCTGGTGAAAGTAAAAGATGCTGAAGATC
AGTTGGGTGCACGAGTGGGTTACATCGAACTGGATCTCAACAGCGGTAAGATCCTTGAGAGTTTTCGCCCCGAAGAACGT
TTTCCAATGATGAGCACTTTTAAAGTTCTGCTATGTGGCGCGGTATTATCCCGTATTGACGCCGGGCAAGAGCAACTCGG
TCGCCGCATACACTATTCTCAGAATGACTTGGTTGAGTACTCACCAGTCACAGAAAAGCATCTTACGGATGGCATGACAG
TAAGAGAATTATGCAGTGCTGCCATAACCATGAGTGATAACACTGCGGCCAACTTACTTCTGACAACGATCGGAGGACCG
AAGGAGCTAACCGCTTTTTTGCACAACATGGGGGATCATGTAACTCGCCTTGATCGTTGGGAACCGGAGCTGAATGAAGC
CATACCAAACGACGAGCGTGACACCACGATGCCTGTAGCAATGGCAACAACGTTGCGCAAACTATTAACTGGCGAACTAC
TTACTCTAGCTTCCCGGCAACAATTAATAGACTGGATGGAGGCGGATAAAGTTGCAGGACCACTTCTGCGCTCGGCCCTT
CCGGCTGGCTGGTTTATTGCTGATAAATCTGGAGCCGGTGAGCGTGGGTCTCGCGGTATCATTGCAGCACTGGGGCCAGA
TGGTAAGCCCTCCCGTATCGTAGTTATCTACACGACGGGGAGTCAGGCAACTATGGATGAACGAAATAGACAGATCGCTG
AGATAGGTGCCTCACTGATTAAGCATTGGTAACTGTCAGACCAAGTTTACTCATATATACTTTAGATTGATTTAAAACTT
CATTTTTAATTTAAAAGGATCTAGGTGAAGATCCTTTTTGATAATCTCATGACCAAAATCCCTTAACGTGAGTTTTCGTT
CCACTGAGCGTCAGACCCCGTAGAAAAGATCAAAGGATCTTCTTGAGATCCTTTTTTTCTGCGCGTAATCTGCTGCTTGC
AAACAAAAAAACCACCGCTACCAGCGGTGGTTTGTTTGCCGGATCAAGAGCTACCAACTCTTTTTCCGAAGGTAACTGGC
TTCAGCAGAGCGCAGATACCAAATACTGTCCTTCTAGTGTAGCCGTAGTTAGGCCACCACTTCAAGAACTCTGTAGCACC
GCCTACATACCTCGCTCTGCTAATCCTGTTACCAGTGGCTGCTGCCAGTGGCGATAAGTCGTGTCTTACCGGGTTGGACT
CAAGACGATAGTTACCGGATAAGGCGCAGCGGTCGGGCTGAACGGGGGGTTCGTGCACACAGCCCAGCTTGGAGCGAACG
ACCTACACCGAACTGAGATACCTACAGCGTGAGCATTGAGAAAGCGCCACGCTTCCCGAAGGGAGAAAGGCGGACAGGTA
TCCGGTAAGCGGCAGGGTCGGAACAGGAGAGCGCACGAGGGAGCTTCCAGGGGGAAACGCCTGGTATCTTTATAGTCCTG
TCGGGTTTCGCCACCTCTGACTTGAGCGTCGATTTTTGTGATGCTCGTCAGGGGGGCGGAGCCTATGGAAAAACGCCAGC
AACGCGGCCTTTTTACGGTTCCTGGCCTTTTGCTGGCCTTTTGCTCACATGTTCTTTCCTGCGTTATCCCCTGATTCTGT
GGATAACCGTATTACCGCCTTTGAGTGAGCTGATACCGCTCGCCGCAGCCGAACGACCGAGCGCAGCGAGTCAGTGAGCG
AGGAAGCGGAAGAGCGCCCAATACGCAAACCGCCTCTCCCCGCGCGTTGGCCGATTCATTAATGCAGCTGGCACGACAGG
TTTCCCGACTGGAAAGCGGGCAGTGAGCGCAACGCAATTAATGTGAGTTAGCTCACTCATTAGGCACCCCAGGCTTTACA
CTTTATGCTTCCGGCTCGTATGTTGTGTGGAATTGTGAGCGGATAACAATTTCACACAGGAAACAGCTATGACCATGATT
ACGCCAAGCTTTGCTCTTAGGAGTTTCCTAATACATCCCAAACTCAAATATATAAAGCATTTGACTTGTTCTATGCCCTA
GGGGGCGGGGGGAAGCTAAGCCAGCTTTTTTTAACATTTAAAATGTTAATTCCATTTTAAATGCACAGATGTTTTTATTT
CATAAGGGTTTCAATGTGCATGAATGCTGCAATATTCCTGTTACCAAAGCTAGTATAAATAAAAATAGATAAACGTGGAA
ATTACTTAGAGTTTCTGTCATTAACGTTTCCTTCCTCAGTTGACAACATAAATGCGCTGCTGAGCAAGCCAGTTTGCATC
TGTCAGGATCAATTTCCCATTATGCCAGTCATATTAATTACTAGTCAATTAGTTGATTTTTATTTTTGACATATACATGT
GAATGAAAGACCCCACCTGTAGGTTTGGCAAGCTAGCTTAAGTAACGCCATTTTGCAAGGCATGGAAAAATACATAACTG
AGAATAGAAAAGTTCAGATCAAGGTCAGGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAG
TTCCTGCCCCGGCTCAGGGCCAAGAACAGATGGAACAGCTGAATATGGGCCAAACAGGATATCTGTGGTAAGCAGTTCCT
GCCCCGGCTCAGGGCCAAGAACAGATGGTCCCCAGATGCGGTCCAGCCCTCAGCAGTTTCTAGAGAACCATCAGATGTTT
CCAGGGTGCCCCAAGGACCTGAAATGACCCTGTGCCTTATTTGAACTAACCAATCAGTTCGCTTCTCGCTTCTGTTCGCG
CGCTTATGCTCCCCGAGCTCAATAAAAGAGCCCACAACCCCTCACTCGGGGCGCCAGTCCTCCGATTGACTGAGTCGCCC
GGGTACCCGTGTATCCAATAAACCCTCTTGCAGTTGCATCCGACTTGTGGTCTCGCTGTTCCTTGGGAGGGTCTCCTCTG
AGTGATTGACTACCCGTCAGCGGGGGTCTTTCATTTGGGGGCTCGTCCGGGATCGGGAGACCCCTGCCCAGGGACCACCG
ACCCACCACCGGGAGGTAAGCTGGCCAGCAACTTATCTGTGTCTGTCCGATTGTCTAGTGTCTATGACTGATTTTATGCG
CCTGCGTCGGTACTAGTTAGCTAACTAGCTCTGTATCTGGCGGACCCGTGGTGGAACTGACGAGTTCGGAACACCCGGCC
GCAACCCTGGGAGACGTCCCAGGGACTTCGGGGGCCGTTTTTGTGGCCCGACCTGAGTCCTAAAATCCCGATCGTTTAGG
ACTCTTTGGTGCACCCCCCTTAGAGGAGGGATATGTGGTTCTGGTAGGAGACGAGAACCTAAAACAGTTCCCGCCTCCGT
CTGAATTTTTGCTTTCGGTTTGGGACCGAAGCCGCGCCGCGCGTCTTGTCTGCTGCAGCATCGTTCTGTGTTGTCTCTGT
CTGACTGTGTTTCTGTATTTGTCTGAAAATATGGGCCCGGGCTAGACTGTTACCACTCCCTTAAGTTTGACCTTAGGTCA
CTGGAAAGATGTCGAGCGGATCGCTCACAACCAGTCGGTAGATGTCAAGAAGAGACGTTGGGTTACCTTCTGCTCTGCAG
AATGGCCAACCTTTAACGTCGGATGGCCGCGAGACGGCACCTTTAACCGAGACCTCATCACCCAGGTTAAGATCAAGGTC
TTTTCACCTGGCCCGCATGGACACCCAGACCAGGTCCCCTACATCGTGACCTGGGAAGCCTTGGCTTTTGACCCCCCTCC
CTGGGTCAAGCCCTTTGTACACCCTAAGCCTCCGCCTCCTCTTCCTCCATCCGCCCCGTCTCTCCCCCTTGAACCTCCTC
GTTCGACCCCGCCTCGATCCTCCCTTTATCCAGCCCTCACT [SEQ ID NO: 233]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 234, которая представлена ниже:
atggaaaccgacaccctgctgctgtgggtgctgctgctgtgggtgccaggatccacaggactgcctgtgctgactcagccaccctcagcgtctgggacccccgggcagagggtcaccatctcttgttctggacgcagttccaacatcgggagtaattctgttaactggtatcgacaactcccaggagcggcccccaaactcctcatctatagtaataatcagcggcccccaggggtccctgtgcgattctctggctccaagtctggcacctcagcctccctggccatcagtgggctccagtctgaagatgaggccacttattactgtgcaacatgggatgacaatctgaatgttcactatgtcttcggaactgggaccaaggtcaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggcccaggtgcagctggtgcagtctggggctgaggtgaagaagcctgggtcctcggtgaaggtctcctgcaaggcttctggaggcaccttcagcagctatgctatcagctgggtgcgacaggcccctggacaagggcttgagtggatgggaaggatcatccctatccttggtatagcaaactacgcacagaagttccagggcagagtcacgattaccgcggacaaatccacgagcacagcctacatggagctgagcagcctgagatctgaggacacggccgtgtattactgtgcgcgcggtggttactactctcatgacatgtggtctgaagattggggtcaaggtactctggtgaccgtctcctcagcggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaa [SEQ ID NO: 234]
В одном конкретном неограничивающем примере выделенная молекула нуклеиновой кислоты содержит нуклеотидную последовательность, приведенную в SEQ ID NO: 235, которая представлена ниже:
atggaaaccgacaccctgctgctgtgggtgctgctgctgtgggtgccaggatccacaggacaggctgtgctgactcagccaccctcagcgtctgggacccccgggcagagggtcaccatctcttgttctggaagcagctccaacatcggaagtaattacgtattctggtaccagcagctcccaggaacggcccccaaactcctcatctatagtaataatcagcggccctcaggggtccctgaccgattctctggctccaagtctggcacctcagcctccctggccatcagtgggctccggtccgaggatgaggctgattattactgtgcagcatgggatgacagcctgagtgcctcttatgttttcggaactgggaccaaggtcaccgtcctaggttctagaggtggtggtggtagcggcggcggcggctctggtggtggtggatccctcgagatggcccaggtgcagctggtgcagtctggggctgaggtgaagaagcctgggtcctcggtgaaggtctcctgcaaggcttctggaggcaccttcagcagctatgctatcagctgggtgcgacaggcccctggacaagggcttgagtggatgggaaggatcatccctatccttggtacagcaaactacgcacagaagttccagggcagagtcacgattaccgcggacgaatccacgagcacagcctacatggagctgagcagcctgagatctgaggacacggccgtgtattactgtgcgcgctctggttacggttcttaccgttgggaagattcttggggtcaaggtactctggtgaccgtctcctcagcggccgcaattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaa [SEQ ID NO: 235]
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 207, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный 28z CAR54), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид CD28, при этом область CD28, содержащаяся в трансмембранном домене и костимулирующей сигнальной области, содержит аминокислоты 114-220 из SEQ ID NO: 193.
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 208, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный 28z CAR40), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид CD28, при этом область CD28, содержащаяся в трансмембранном домене и костимулирующей сигнальной области, содержит аминокислоты 114-220 из SEQ ID NO: 193.
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 209, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный 28z CAR24), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид CD28, при этом область CD28, содержащаяся в трансмембранном домене и костимулирующей сигнальной области, содержит аминокислоты 114-220 из SEQ ID NO: 193.
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 234, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный 28z CAR3), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид CD28, при этом область CD28, содержащаяся в трансмембранном домене и костимулирующей сигнальной области, содержит аминокислоты 114-220 из SEQ ID NO: 193.
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 235, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный 28z CAR37), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид CD28, при этом область CD28, содержащаяся в трансмембранном домене и костимулирующей сигнальной области, содержит аминокислоты 114-220 из SEQ ID NO: 193.
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 229, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный BBz CAR3), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 21, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 22, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD8, содержащий аминокислоты 137-207 из SEQ ID NO: 226, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид 4-1BB, содержащий аминокислоты 214-255 из SEQ ID NO: 197. Последовательность нуклеотидов 270-1031 из SEQ ID NO: 229 кодирует человеческий scFv. Последовательность нуклеотидов 1041-1253 из SEQ ID NO: 229 кодирует полипептид CD8, содержащийся в трансмембранном домене. Последовательность нуклеотидов 1254-1379 из SEQ ID NO: 229 кодирует полипептид 4-1BB, содержащийся в внутриклеточном домене. Последовательность нуклеотидов 1380-1718 из SEQ ID NO: 229 кодирует полипептид CD3дзета, содержащийся в внутриклеточном домене. Другие фрагменты SEQ ID NO: 229 приведены в таблице 19.
Таблица 19
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 230, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный BBz CAR24), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 65, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 66, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD8, содержащий аминокислоты 137-207 из SEQ ID NO: 226, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид 4-1BB, содержащий аминокислоты 214-255 из SEQ ID NO: 197. Последовательность нуклеотидов 270-1015 из SEQ ID NO: 230 кодирует человеческий scFv. Последовательность нуклеотидов 1023-1235 из SEQ ID NO: 230 кодирует полипептид CD8, содержащийся в трансмембранном домене. Последовательность нуклеотидов 1236-1361 из SEQ ID NO: 230 кодирует полипептид 4-1BB, содержащийся в внутриклеточном домене. Последовательность нуклеотидов 1362-1700 из SEQ ID NO: 230 кодирует полипептид CD3дзета, содержащийся в внутриклеточном домене. Другие фрагменты SEQ ID NO: 230 приведены в таблице 20.
Таблица 20
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 231, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный BBz CAR37), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 61, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 62, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD8, содержащий аминокислоты 137-207 из SEQ ID NO: 226, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид 4-1BB, содержащий аминокислоты 214-255 из SEQ ID NO: 197. Последовательность нуклеотидов 270-1028 из SEQ ID NO: 231 кодирует человеческий scFv. Последовательность нуклеотидов 1038-1250 из SEQ ID NO: 231 кодирует полипептид CD8, содержащийся в трансмембранном домене. Последовательность нуклеотидов 1251-1376 из SEQ ID NO: 231 кодирует полипептид 4-1BB, содержащийся в внутриклеточном домене. Последовательность нуклеотидов 1377-1715 из SEQ ID NO: 231 кодирует полипептид CD3дзета, содержащийся в внутриклеточном домене. Другие фрагменты SEQ ID NO: 231 приведены в таблице 21.
Таблица 21
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 232, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный BBz CAR40), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 57, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 58, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD8, содержащий аминокислоты 137-207 из SEQ ID NO: 226, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид 4-1BB, содержащий аминокислоты 214-255 из SEQ ID NO: 197. Последовательность нуклеотидов 270-1024 из SEQ ID NO: 232 кодирует человеческий scFv. Последовательность нуклеотидов 1032-1244 из SEQ ID NO: 232 кодирует полипептид CD8, содержащийся в трансмембранном домене. Последовательность нуклеотидов 1245-1370 из SEQ ID NO: 232 кодирует полипептид 4-1BB, содержащийся в внутриклеточном домене. Последовательность нуклеотидов 1371-1709 из SEQ ID NO: 232 кодирует полипептид CD3дзета, содержащийся в внутриклеточном домене. Другие фрагменты SEQ ID NO: 232 приведены в таблице 22.
Таблица 22
Выделенная молекула нуклеиновой кислоты, имеющая нуклеотидную последовательность SEQ ID NO: 233, кодирует BCMA-нацеленный CAR (обозначенный BCMA-нацеленный BBz CAR54), содержащий человеческий scFv, который содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 53, вариабельную область легкой цепи, содержащую аминокислотную последовательность, приведенную в SEQ ID NO: 54, и линкер, имеющий аминокислотную последовательность SEQ ID NO: 69, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи, трансмембранный домен, содержащий полипептид CD8, содержащий аминокислоты 137-207 из SEQ ID NO: 226, и внутриклеточный домен, содержащий полипептид CD3ξ, содержащий аминокислоты 52-163 из SEQ ID NO: 195, и костимулирующую сигнальную область, содержащую полипептид 4-1BB, содержащий аминокислоты 214-255 из SEQ ID NO: 197. Последовательность нуклеотидов 270-1003 из SEQ ID NO: 233 кодирует человеческий scFv. Последовательность нуклеотидов 1011-1223 из SEQ ID NO: 233 кодирует полипептид CD8, содержащийся в трансмембранном домене. Последовательность нуклеотидов 1224-1349 из SEQ ID NO: 233 кодирует полипептид 4-1BB, содержащийся в внутриклеточном домене. Последовательность нуклеотидов 1350-1688 из SEQ ID NO: 233 кодирует полипептид CD3дзета, содержащийся в внутриклеточном домене. Другие фрагменты SEQ ID NO: 233 приведены в таблице 23.
Таблица 23
В конкретных вариантах осуществления выделенная молекула нуклеиновой кислоты кодирует функциональную часть раскрытого в настоящем документе BCMA-нацеленного CAR. Используемый в настоящем документе термин «функциональная часть» означает любую часть, долю или фрагмент раскрытого в настоящем документе BCMA-нацеленного CAR, которые сохраняют биологическую активность BCMA-нацеленного CAR (исходного CAR). Например, функциональные части включают части, доли или фрагменты раскрытого в настоящем документе BCMA-нацеленного CAR, которые сохраняют способность узнавать клетку-мишень, лечить заболевание, например, множественную миелому, в аналогичной, такой же, или даже более высокой степени, что и исходный CAR. В конкретных вариантах осуществления выделенная молекула нуклеиновой кислоты, кодирующая функциональную часть раскрытого в настоящем документе BCMA-нацеленного CAR, может кодировать белок, содержащий, например, примерно 10%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% и 95%, или более, исходного CAR.
В фазе I одного клинического испытания (NCT02215967), проводимого Национальным институтом рака (NCI), были использованы T-клетки, трансдуцированные анти-BCMA CAR, для лечения множественной миеломы33,34. Анти-BCMA CAR, используемый в клиническом испытании, проводимом NCI, содержит мышиный scFv, связывающийся с BCMA человека. Использование мышиного антитела или мышиного scFv для лечения людей может приводить к иммунологическому ответу, направленному против мышиного антитела (HAMA), что может быть опасным для жизни. В отличие от клинического испытания NCI, в конкретных вариантах осуществления раскрытый в настоящем документе BCMA-нацеленный CAR содержит человеческий scFv и, таким образом, риск иммуногенности намного снижается по сравнению с CAR, содержащими мышиные антитела (смотри Maus et al., Cancer Immunol Res (2003); 1(1): 26-31), где сообщается, что потенциальная иммуногенность CAR, полученных из мышиных антител, может быть небезопасной для мРНК CAR).
III. Иммунореактивные клетки
Настоящее изобретение относится к иммунореактивным клеткам, экспрессирующим CAR, который содержит внеклеточный антигенсвязывающий домен, трансмембранный домен и внутриклеточный домен, при этом внеклеточный антигенсвязывающий домен специфически связывается с BCMA (например, BCMA человека), как описано выше. Иммунореактивные клетки могут быть трансдуцированы раскрытым в настоящем документе CAR, вследствие чего клетки экспрессируют CAR. Настоящее изобретение также относится к способам применения таких клеток для лечения опухоли, например, множественной миеломы (MM). Иммунореактивные клетки по настоящему изобретению могут представлять собой клетки лимфоидной линии. Клетки лимфоидной линии, включающие B, T-клетки и клетки-естественные киллеры (NK), обеспечивают продуцирование антител, регуляцию клеточной иммунной системы, обнаружение чужеродных агентов в крови, обнаружение клеток, чужеродных для хозяина, и тому подобное. Неограничивающие примеры иммунореактивных клеток лимфоидной линии включают T-клетки, клетки-естественные киллеры (NK), цитотоксические T-лимфоциты (CTL), регуляторные T-клетки, эмбриональные стволовые клетки и плюрипотентные стволовые клетки (например, те, из которых могут дифференцироваться лимфоидные клетки). T-клетки могут представлять собой лимфоциты, которые созревают в тимусе и несут основную ответственность за клеточно-опосредованный иммунитет. T-клетки являются частью адаптивной иммунной системы. T-клетки по настоящему изобретению могут быть T-клетками любого типа, включая, но без ограничения, T-хелперные клетки, цитотоксические T-клетки, T-клетки памяти (включая центральные T-клетки памяти, T-клетки памяти, подобные стволовым клеткам (или подобные стволовым клеткам T-клетки памяти), и два типа эффекторных T-клеток памяти: например, TEM клетки и TEMRA клетки), регуляторные T-клетки (также известные как супрессорные T-клетки), T-клетки - естественные киллеры, связанные со слизистой оболочкой инвариантные T-клетки и γδ-T-клетки. В конкретных вариантах осуществления CAR-экспрессирующие T-клетки экспрессируют Foxp3, что необходимо для достижения и поддержания фенотипа регуляторных T-клеток. Клетки-естественные киллеры (NK) могут представлять собой лимфоциты, являющиеся частью клеточно-опосредованного иммунитета и действующие в рамках врожденного иммунного ответа. NK-клетки не нуждаются в предварительной активации для оказания своего цитотоксического действия на клетки-мишени. Цитотоксические T-клетки (CTL или T-клетки-киллеры) относятся к подгруппе T-лимфоцитов, способных вызывать гибель инфицированных соматических или опухолевых клеток.
Иммунореактивные клетки по настоящему изобретению могут экспрессировать внеклеточный антигенсвязывающий домен (например, человеческий scFV, Fab, который, необязательно, является сшитым, или F(ab)2), который специфически связывается с BCMA (например, BCMA человека), для лечения множественной миеломы. Такие иммунореактивные клетки можно вводить субъекту (например, субъекту-человеку), который нуждается в этом, для лечения множественной миеломы. В конкретных вариантах осуществления иммунореактивная клетка представляет собой T-клетку. T-клетка может представлять собой CD4+ T-клетку или CD8+ T-клетку. В конкретных вариантах осуществления T-клетка представляет собой CD4+ T-клетку. В конкретных вариантах осуществления T-клетка представляет собой CD8+ T-клетку.
Раскрытая в настоящем документе иммунореактивная клетка может быть дополнительно трансдуцирована по меньшей мере одним костимулирующим лигандом, вследствие чего иммунореактивная клетка совместно экспрессирует или индуцируется для совместной экспрессии BCMA-нацеленного CAR и по меньшей мере одного костимулирующего лиганда. Взаимодействие между BCMA-нацеленным CAR и по меньшей мере одним костимулирующим лигандом обеспечивает не специфичный для антигена сигнал, важный для полной активации иммунореактивной клетки (например, T-клетки). Костимулирующие лиганды включают, но не ограничиваются ими, лиганды-представители суперсемейства факторов некроза опухолей (TNF) и суперсемейства иммуноглобулинов (Ig). TNF представляет собой цитокин, который вовлечен в системное воспаление и стимулирует реакции острой фазы. Его основная роль заключается в регуляции иммунных клеток. Представители суперсемейства TNF имеют целый ряд общих свойств. Большинство представителей суперсемейства TNF синтезируются как трансмембранные белки II типа (внеклеточный C-конец), содержащие короткий цитоплазматический сегмент и относительно длинную внеклеточную область. Представители суперсемейства TNF включают, но не ограничиваются ими, фактор роста нервов (NGF), CD40L (CD40L)/CD154, CD137L/4-1BBL, TNF-α, CD134L/OX40L/CD252, CD27L/CD70, Fas-лиганд (FasL), CD30L/CD153, фактор некроза опухолей-бета (TNFβ)/лимфотоксин-альфа (LTα), лимфотоксин-бета (LTβ), CD257/фактор активации B-клеток (BAFF)/Blys/THANK/Tall-1, глюкокортикоид-индуцируемый лиганд рецептора TNF (GITRL) и TNF-родственный апоптоз-индуцирующий лиганд (TRAIL), LIGHT (TNFSF14). Суперсемейство иммуноглобулинов (Ig) представляет собой большую группу белков клеточной поверхности и растворимых белков, которые вовлечены в процессы узнавания, связывания или адгезии клеток. Эти белки имеют общие структурные свойства с иммуноглобулинами - они имеют домен иммуноглобулинов (складку). Лиганды суперсемейства иммуноглобулинов включают, но не ограничиваются ими, CD80 и CD86, оба лиганда для CD28, PD-L1/(B7-H1), который является лигандом для PD-1. В некоторых вариантах осуществления по меньшей мере один костимулирующий лиганд выбирают из группы, состоящей из 4-1BBL, CD80, CD86, CD70, OX40L, CD48, TNFRSF14, PD-L1, а также их сочетаний. В конкретных вариантах осуществления иммунореактивная клетка трансдуцирована одним костимулирующим лигандом, который представляет собой 4-1BBL. В конкретных вариантах осуществления иммунореактивная клетка трансдуцирована двумя костимулирующими лигандами, которые представляют собой 4-1BBL и CD80. CAR, трансдуцированные по меньшей мере одним костимулирующим лигандом, описаны в патенте США № 8389282, полное содержание которого включено в настоящий документ посредством ссылки.
Кроме того, раскрытая в настоящем документе иммунореактивная клетка может быть дополнительно трансдуцирована по меньшей мере одним цитокином, вследствие чего иммунореактивная клетка секретирует по меньшей мере один цитокин, а также экспрессирует BCMA-нацеленный CAR. В конкретных вариантах осуществления по меньшей мере one цитокин выбирают из группы, состоящей из IL-2, IL-3, IL-6, IL-7, IL-11, IL-12, IL-15, IL-17 и IL-21. В конкретных вариантах осуществления цитокин представляет собой IL-12.
BCMA-специфичные или BCMA-нацеленные человеческие лимфоциты могут быть использованы в качестве периферических донорских лимфоцитов, например, таких, которые раскрыты в Sadelain, M., et al. 2003 Nat Rev Cancer 3: 35-45 (где описаны периферические донорские лимфоциты, генетически модифицированные для экспрессии CAR), в Morgan, R.A., et al. 2006 Science 314: 126-129 (где описаны периферические донорские лимфоциты, генетически модифицированные для экспрессии полноразмерного узнающего опухолевый антиген T-клеточного рецепторного комплекса, содержащего α и β гетеродимер), в Panelli, M.C., et al. 2000 J Immunol 164: 495-504; Panelli, M.C., et al. 2000 J Immunol 164: 4382-4392 (где описаны культуры лимфоцитов, полученные из инфильтрирующих опухоль лимфоцитов (TILs) в биопсиях опухолей), и в Dupont, J., et al. 2005 Cancer Res 65: 5417-5427; Papanicolaou, G.A., et al. 2003 Blood 102: 2498-2505 (где описаны селективно размноженные in vitro антигенспецифические лейкоциты периферической крови и использование искусственных антигенпредставляющих клеток (AAPC) или активированных дендритных клеток). Иммунореактивные клетки (например, T-клетки) могут быть аутологичными, не аутологичными (например, аллогенными) или полученными in vitro из генетически модифицированных предшественников или стволовых клеток.
В конкретных вариантах осуществления раскрытая в настоящем документе иммунореактивная клетка (например, T-клетка) экспрессирует от примерно 1 до примерно 4, от примерно 2 до примерно 4, от примерно 3 до примерно 4, от примерно 1 до примерно 2, от примерно 1 до примерно 3 или от примерно 2 до примерно 3 копий/клетку вектора для раскрытого в настоящем документе BCMA-нацеленного CAR.
Неочищенным источником CTL может быть любой известный в данной области источник, такой как костный мозг, источник эмбриональных, неонатальных или взрослых, либо других гемопоэтических клеток, например, эмбриональная печень, периферическая кровь или пуповинная кровь. Для разделения клеток можно использовать различные методы. Например, методы отрицательной селекции позволяют исходно удалять клетки, не являющиеся CTL. Моноклональные антитела особенно полезны для идентификации маркеров, ассоциированных с конкретными клеточными линиями дифференцировки и/или стадиями дифференцировки, как для положительной, так и для отрицательной селекции.
Большая часть терминально дифференцированных клеток может быть изначально удалена относительно грубым методом разделения. Например, сначала можно использовать разделение с помощью магнитных гранул для удаления большого числа ненужных клеток. Предпочтительно, по меньшей мере примерно 80%, как правило, по меньшей мере 70% всех гемопоэтических клеток будут удалены до выделения клеток.
Методы разделения включают, но не ограничиваются ими, центрифугирование в градиенте плотности; розеткообразование; связывание с частицами, изменяющими плотность клеток; магнитное разделение с помощью покрытых антителом магнитных гранул; аффинную хроматографию; цитотоксические средства, связанные с, или используемые в сочетании с мАт, включая, но без ограничения, комплемент и цитотоксины; а также пэннинг с помощью антител, закрепленных на твердой матрице, например, планшете, чипе; элютриацию или любой другой подходящий метод.
Методы разделения и анализа включают, но не ограничиваются ими, проточную цитометрию различной степени сложности, например, с использованием нескольких цветовых каналов, каналов для детекции низкоуглового и широкоуглового светорассеяния, импеденсных каналов.
Можно отбирать клетки среди мертвых клеток, используя красители, связывающиеся с мертвыми клетками, такие как пропидия иодид (PI). Предпочтительно, клетки собирают в среду, содержащую 2% эмбриональной телячьей сыворотки (ЭТС) или 0,2% бычьего сывороточного альбумина (БСА), или любую другую подходящую, предпочтительно стерильную, изотоническую среду.
IV. Векторы
Генетическую модификацию иммунореактивных клеток (например, T-клеток, CTL-клеток, NK-клеток) можно осуществлять, трансдуцируя по существу гомогенную композицию клеток рекомбинантным ДНК- или РНК-конструктом. Вектор может представлять собой ретровирусный вектор (например, гамма-ретровирусный), который используют для введения ДНК- или РНК-конструкта в геном клетки-хозяина. Например, полинуклеотид, кодирующий BCMA-нацеленный CAR, может быть клонирован в ретровирусный вектор, и экспрессия может управляться с его эндогенного промотора, с ретровирусного длинного концевого повтора или с альтернативного внутреннего промотора.
Также можно использовать невирусные векторы или РНК. Можно использовать случайную хромосомную интеграцию или направленную интеграцию (например, с использованием нуклеазы, подобных активатору транскрипции эффекторных нуклеаз (TALEN), нуклеаз «цинковых пальцев» (ZFN) и/или коротких палиндромных повторов, регулярно расположенных группами (CRISPR)), или трансгенную экспрессию (например, с использованием природной или химически модифицированной РНК).
Для начальной генетической модификации клеток с целью получения клеток, экспрессирующих BCMA-нацеленный CAR, как правило, для трансдукции используют ретровирусный вектор, однако можно использовать любую другую подходящую вирусную или невирусную систему доставки. Для последующей генетической модификации клеток с целью получения клеток, содержащих антигенпредставляющий комплекс, содержащий по меньшей мере два костимулирующих лиганда, ретровирусный перенос генов (трансдукция) также является эффективным. Также подходящими являются сочетания ретровирусного вектора и соответствующей упаковывающей линии клеток, при этом капсидные белки будут играть функциональную роль при инфицировании клеток человека. Известны различные амфотропные продуцирующие вирусы линии клеток, включая, но без ограничения, PA12 (Miller, et al. (1985) Mol. Cell. Biol. 5: 431-437); PA317 (Miller, et al. (1986) Mol. Cell. Biol. 6: 2895-2902) и CRIP (Danos, et al. (1988) Proc. Natl. Acad. Sci. USA 85: 6460-6464). Не амфотропные частицы также являются подходящими, например, частицы, псевдотипированные с оболочкой VSVG, RD114 или GALV, а также любые другие известные в данной области.
Возможные методы трансдукции также включают прямое совместное культивирование клеток с клетками-продуцентами, например, методом, описанным в Bregni, et al. (1992) Blood 80: 1418-1422, либо культивирование только с вирусным супернатантом или с концентрированными маточными растворами вектора с добавлением или без добавления соответствующих факторов роста и поликатионов, например, методом, описанным в Xu, et al. (1994) Exp. Hemat. 22: 223-230; и Hughes, et al. (1992) J. Clin. Invest. 89: 1817.
Трансдуцирующие вирусные векторы можно использовать для экспрессии костимулирующего лиганда (например, 4-1BBL и IL-12) в иммунореактивной клетке. Предпочтительно, выбранный вектор характеризуется высокой эффективностью инфицирования, а также стабильной интеграцией и экспрессией (смотри, например, Cayouette et al., Human Gene Therapy 8: 423-430, 1997; Kido et al., Current Eye Research 15: 833-844, 1996; Bloomer et al., Journal of Virology 71: 6641-6649, 1997; Naldini et al., Science 272: 263 267, 1996; и Miyoshi et al., Proc. Natl. Acad. Sci. U.S.A. 94: 10319, 1997). Другие вирусные векторы, которые можно использовать, включают, например, аденовирусные, лентивирусные и аденоассоциированные вирусные векторы, вирус осповакцины, вирус бычьей папилломы или вирус герпеса, например, вирус Эпштейна-Барр (также смотри, например, векторы, описанные в Miller, Human Gene Therapy 15-14, 1990; Friedman, Science 244: 1275-1281, 1989; Eglitis et al., BioTechniques 6: 608-614, 1988; Tolstoshev et al., Current Opinion in Biotechnology 1: 55-61, 1990; Sharp, The Lancet 337: 1277-1278, 1991; Cornetta et al., Nucleic Acid Research and Molecular Biology 36: 311-322, 1987; Anderson, Science 226: 401-409, 1984; Moen, Blood Cells 17: 407-416, 1991; Miller et al., Biotechnology 7: 980-990, 1989; Le Gal La Salle et al., Science 259: 988-990, 1993; и Johnson, Chest 107: 77S-83S, 1995). Ретровирусные векторы особенно хорошо разработаны и их используют в клинической практике (Rosenberg et al., N. Engl. J. Med 323: 370, 1990; Anderson et al., патент США № 5399346).
В конкретных неограничивающих вариантах осуществления вектор, экспрессирующий раскрытый в настоящем документе BCMA-нацеленный CAR, представляет собой ретровирусный вектор, например, ретровирусный вектор 293 galv9.
Для экспрессии белка в клетке также можно использовать подходы не на основе вирусов. Например, молекулу нуклеиновой кислоты можно вводить в клетку с помощью липофекции (Feigner et al., Proc. Natl. Acad. Sci. U.S.A. 84: 7413, 1987; Ono et al., Neuroscience Letters 17: 259, 1990; Brigham et al., Am. J. Med. Sci. 298: 278, 1989; Staubinger et al., Methods in Enzymology 101: 512, 1983), асиалооросомукоида-полилизина (Wu et al., Journal of Biological Chemistry 263: 14621, 1988; Wu et al., Journal of Biological Chemistry 264: 16985, 1989) или путем микроинъекции в хирургических условиях (Wolff et al., Science 247: 1465, 1990). Другие не вирусные методы переноса генов включают трансфекцию in vitro с использованием фосфата кальция, ДЭАЭ-декстрана, электропорацию и слияние протопластов. Липосомы также могут быть потенциально полезными для доставки ДНК в клетку. Трансплантацию нормальных генов в пораженные ткани субъекта также можно осуществлять путем переноса нормальной нуклеиновой кислоты в культивируемые клетки ex vivo (например, аутологичные или гетерологичные первичные клетки или их потомство), после чего клетки (или их потомство) инъецируют в целевую ткань или инъецируют системно. Рекомбинантные рецепторы также можно создавать или получать с использованием транспозаз или направленных нуклеаз (например, нуклеаз «цинковые пальцы», мегануклеаз или TALE нуклеаз). Временную экспрессию можно получать за счет введения РНК методом электропорации.
Экспрессия кДНК для использования в методах полинуклеотидной терапии может управляться с любого подходящего промотора (например, промоторов цитомегаловируса (CMV) человека, обезьяньего вируса 40 (SV40) или металлотионеина) и регулироваться любым подходящим регуляторным элементом или интроном млекопитающих (например, структурой энхансер/промотор/интрон фактора элонгации 1α). Например, при необходимости, для управления экспрессией нуклеиновой кислоты можно использовать энхансеры, которые, как известно, предпочтительно управляют экспрессией гена в клетках определенного типа. Используемые энхансеры могут включать, без ограничения, те, которые охарактеризованы как энхансеры, специфичные для ткани или типа клеток. Альтернативно, если геномный клон используют в качестве терапевтического конструкта, регуляция может быть опосредована когнатными регуляторными последовательностями или, в случае необходимости, регуляторными последовательностями, полученными из гетерологичного источника, в том числе, любым из промоторов или регуляторных элементов, описанных выше.
Полученные клетки можно выращивать в условиях, сходных с условиями для не модифицированных клеток, при этом модифицированные клетки можно размножать и использовать для разных целей.
V. Полипептиды, аналоги и полинуклеотиды
Настоящее изобретение также относится к внеклеточным антигенсвязывающим доменам, которые специфически связываются с BCMA (например, BCMA человека) (например, scFv (например, человеческий scFv), Fab или (Fab)2), полипептидам CD3ζ, CD8, CD28 и так далее, или их фрагментам, а также полинуклеотидам, кодирующим их, которые модифицированы способами, приводящими к усилению их противоопухолевой активности при экспрессии в иммунореактивной клетке. Настоящее изобретение относится к способам оптимизации аминокислотной последовательности или нуклеотидной последовательности за счет внесения изменений в последовательность. Такие изменения могут включать определенные мутации, делеции, вставки или посттрансляционные модификации. Настоящее изобретение также относится к аналогам любого природного полипептида по настоящему изобретению. Аналоги могут отличаться от природного полипептида по настоящему изобретению за счет различий в аминокислотной последовательности, за счет посттрансляционных модификаций или и того, и другого. Аналоги по настоящему изобретению, как правило, могут иметь по меньшей мере примерно 85%, примерно 90%, примерно 91%, примерно 92%, примерно 93%, примерно 94%, примерно 95%, примерно 96%, примерно 97%, примерно 98%, примерно 99% или более идентичности со всей или с частью природной аминокислотной последовательности по настоящему изобретению. Длина сравниваемых последовательностей составляет по меньшей мере 5, 10, 15, 20, 25, 50, 75, 100 или более аминокислотных остатков. Опять-таки, в иллюстративном подходе для определения степени идентичности можно использовать программу BLAST, с показателем вероятности от e-3 до e-100, указывающим на близкородственную последовательность. Модификации включают in vivo и in vitro химическую дериватизацию полипептидов, например, ацетилирование, карбоксилирование, фосфорилирование или гликозилирование; такие модификации могут происходить во время синтеза или процессинга полипептида, или после обработки выделенными модифицирующими ферментами. Аналоги также могут отличаться от природных полипептидов по настоящему изобретению за счет изменений в первичной последовательности. Сюда относятся генетические варианты, как природные, так и индуцированные (например, возникающие в результате случайного мутагенеза при облучении или воздействии этанметилсульфата, или в результате сайт-направленного мутагенеза, описанного в Sambrook, Fritsch and Maniatis, Molecular Cloning: A Laboratory Manual (2-е издание), CSH Press, 1989, или Ausubel et al., выше). Также включены циклизованные пептиды, молекулы и аналоги, которые содержат остатки, отличные от L-аминокислот, например, D-аминокислоты, либо неприродные или синтетические аминокислоты, например, бета (β) или гамма (γ) аминокислоты.
Помимо полноразмерных полипептидов, настоящее изобретение также относится к фрагментам любого из полипептидов или пептидных доменов по настоящему изобретению. Фрагмент может содержать по меньшей мере 5, 10, 13 или 15 аминокислот. В конкретных вариантах осуществления фрагмент содержит по меньшей мере 20 смежных аминокислот, по меньшей мере 30 смежных аминокислот или по меньшей мере 50 смежных аминокислот. В конкретных вариантах осуществления фрагмент содержит по меньшей мере 60-80, 100, 200, 300 или более смежных аминокислот. Фрагменты по настоящему изобретению могут быть получены методами, известными специалистам в данной области, или могут образовываться в результате обычного процессинга белка (например, удаления аминокислот из образующегося полипептида, которые не нужны для биологической активности, или удаления аминокислот в результате альтернативного сплайсинга мРНК или в результате альтернативного процессинга белка).
Небелковые аналоги имеют химическую структуру, разработанную для имитации функциональной активности белка по изобретению. Такие аналоги вводят способами по настоящему изобретению. Такие аналоги могут превосходить по физиологической активности исходный полипептид. Способы конструирования аналогов хорошо известны в данной области, и синтез аналогов можно выполнять такими способами, модифицируя химические структуры таким образом, что полученные аналоги превосходят по анти-неопластической активности исходный полипептид при экспрессии в иммунореактивной клетке. Такие химические модификации включают, но не ограничиваются ими, замещение альтернативных R-групп и варьирование степени насыщенности определенных атомов углерода эталонного полипептида. Белковые аналоги могут быть относительно устойчивы к деградации in vivo, результатом чего является более длительный терапевтический эффект после введения. Анализы для измерения функциональной активности включают, но не ограничиваются ими, те, которые описаны в разделе «Примеры», ниже.
В соответствии с настоящим изобретением, полинуклеотиды, кодирующие внеклеточный антигенсвязывающий домен, который специфически связывается с BCMA (например, BCMA человека) (например, scFv (например, человеческий scFv), Fab или (Fab)2), CD3ζ, CD8, CD28, могут быть модифицированы за счет оптимизации кодонов. Оптимизация кодонов может изменять как природные, так и рекомбинантные последовательности генов, для достижения максимально возможных уровней продуктивности в любой конкретной системе экспрессии. Факторы, играющие роль на разных стадиях экспрессии белка, включают адаптируемость кодонов, структуру мРНК и различные cis-элементы в транскрипции и трансляции. Можно использовать любые подходящие методы или технологии оптимизации кодонов, известные специалистам в данной области, для модификации полинуклеотидов по настоящему изобретению, включая, но без ограничения, OPTIMUMGENE™, Encor оптимизацию и Blue Heron.
VI. Введение
BCMA-нацеленные CAR и экспрессирующие их иммунореактивные клетки по настоящему изобретению можно предоставлять системно или непосредственно субъекту для лечения или предотвращения неоплазии. В конкретных вариантах осуществления BCMA-нацеленные CAR и экспрессирующие их иммунореактивные клетки напрямую инъецируют в интересующий орган (например, орган, затронутый неоплазией). Альтернативно или дополнительно, BCMA-нацеленные CAR и экспрессирующие их иммунореактивные клетки вводят опосредованно в интересующий орган, например, путем введения в систему циркуляции (например, сосудистую сеть опухоли). Средства для экспансии и дифференциации с целью увеличения продуцирования T-клеток in vitro или in vivo могут быть предоставлены до, в процессе или после введения клеток и композиций.
BCMA-нацеленные CAR и экспрессирующие их иммунореактивные клетки по настоящему изобретению можно вводить в любом физиологически приемлемом носителе, обычно внутрисосудистым введением, хотя их также можно вводить в кость или другой удобный участок тела, где клетки могут найти подходящее место для регенерации и дифференциации (например, тимус). Как правило, можно вводить по меньшей мере 1×105 клеток, в конечном итоге доводя количество до 1 x l010 или более. Клеточная популяция, содержащая иммунореактивные клетки, экспрессирующие BCMA-нацеленный CAR, может представлять собой очищенную популяцию клеток. Специалисты в данной области могут с легкостью определять процентную долю иммунореактивных клеток в клеточной популяции с использованием различных хорошо известных методов, таких как активированная флуоресценцией сортировка клеток (FACS). Степень чистоты клеточных популяций, содержащих генетически модифицированные иммунореактивные клетки, экспрессирующие BCMA-специфичный CAR, может составлять от примерно 50% до примерно 55%, от примерно 55% до примерно 60%, от примерно 65% до примерно 70%, от примерно 70% до примерно 75%, от примерно 75% до примерно 80%, от примерно 80% до примерно 85%, от примерно 85% до примерно 90%, от примерно 90% до примерно 95% или от примерно 95 до примерно 100%. Дозы могут с легкостью корректировать специалисты в данной области (например, при меньшей степени чистоты может потребоваться более высокая доза). Иммунореактивные клетки можно вводить путем инъекции, с помощью катетера или тому подобным образом. При необходимости, можно дополнительно включать факторы, в том числе, но без ограничения, интерлейкины, например, IL-2, IL-3, IL-6, IL-11, IL-7, IL-12, IL-15, IL-21, а также другие интерлейкины, колониестимулирующий факторы, такие как G-, M- и GM-CSF, интерфероны, например, γ-интерферон.
Композиции по настоящему изобретению включают фармацевтические композиции, содержащие иммунореактивные клетки, экспрессирующие BCMA-нацеленный CAR, и фармацевтически приемлемый носитель. Введение может быть аутологичным или не аутологичным. Например, иммунореактивные клетки, экспрессирующие BCMA-нацеленный CAR, и содержащие их композиции можно получать от одного субъекта, и вводить тому же субъекту или другому совместимому субъекту. Полученные из периферической крови T-клетки по настоящему изобретению или их потомство (например, полученное in vivo, ex vivo или in vitro) можно вводить локальной инъекцией, включая введение с помощью катетера, системной инъекцией, локализованной инъекцией, внутривенной инъекцией или парентеральным путем введения. Вводимая фармацевтическая композиция по настоящему изобретению (например, фармацевтическая композиция, содержащая иммунореактивные клетки, экспрессирующие BCMA-нацеленный CAR), может быть сформулирована в виде инъекционной стандартной дозы (раствора, суспензии, эмульсии).
VII. Препараты
Иммунореактивные клетки, экспрессирующие BCMA-нацеленный CAR, и содержащие их композиции по настоящему изобретению можно предоставлять в виде стерильных жидких препаратов, например, изотонических водных растворов, суспензий, эмульсий, дисперсий или вязких композиций, которые могут быть забуферены для достижения выбранного значения pH. Жидкие препараты, как правило, изготавливать легче, чем гели, другие вязкие композиции и твердые композиции. Кроме того, жидкие композиции удобнее вводить, особенно путем инъекции. Вязкие композиции, с другой стороны, могут быть сформулированы в пределах соответствующего диапазона вязкости для обеспечения более длительного контакта с определенными тканями. Жидкие или вязкие композиции могут содержать носители, которые могут представлять собой растворитель или дисперсионную среду, содержащие, например, воду, солевой раствор, фосфатно-солевой буфер, полиол (например, глицерин, пропиленгликоль, жидкий полиэтиленгликоль и тому подобное), а также их подходящие смеси.
Стерильные инъекционные растворы могут быть получены путем включения композиций, содержащих иммунореактивные клетки, экспрессирующие BCMA-нацеленный CAR, по настоящему изобретению в необходимое количество соответствующего растворителя с разными количествами других ингредиентов, по мере необходимости. Такие композиции могут находиться в смеси с соответствующим носителем, разбавителем или эксципиентом, таким как стерильная вода, физиологический солевой раствор, глюкоза, декстроза или тому подобное. Композиции также могут быть лиофилизированными. Композиции могут содержать вспомогательные вещества, такие как увлажняющие, диспергирующие средства или эмульгаторы (например, метилцеллюлоза), буферные реагенты для поддержания pH, гелеобразующие или повышающие вязкость добавки, консерванты, ароматизаторы, красители и тому подобное, в зависимости от пути введения и желательного препарата. Для получения соответствующих препаратов без излишнего экспериментирования можно руководствоваться стандартными литературными источниками, такими как «REMINGTON'S PHARMACEUTICAL SCIENCE», 17-е издание, 1985, содержание которого включено в настоящий документ посредством ссылки.
Можно вносить различные добавки, которые повышают стабильность и стерильность композиций, включая противомикробные консерванты, антиоксиданты, хелатирующие агенты и буферы. Предотвращать действие микроорганизмов можно с помощью различных антибактериальных и противогрибковых средств, например, парабенов, хлорбутанола, фенола, сорбиновой кислоты и тому подобного. Продолжительной абсорбции инъекционной фармацевтической формы можно добиваться за счет использования замедляющих абсорбцию средств, например, моностеарата алюминия и желатина. Однако в соответствии с настоящим изобретением, любые используемые растворители, разбавители или добавки должны быть совместимыми с иммунореактивными клетками, экспрессирующими BCMA-нацеленный CAR по настоящему изобретению.
Композиции могут быть изотоническими, то есть, они могут иметь такое же осмотическое давление, как у крови и слезной жидкости. Желательной изотоничности композиций по настоящему изобретению можно добиваться с помощью хлорида натрия или других фармацевтически приемлемых средств, таких как декстроза, борная кислота, натрия тартрат, пропиленгликоль или другие неорганические или органические растворенные вещества. Хлорид натрия является особенно предпочтительным для буферов, содержащих ионы натрия.
Вязкость композиций, при необходимости, можно поддерживать на желательном уровне с помощью фармацевтически приемлемого загустителя. Можно использовать метилцеллюлозу, поскольку она является легко доступной, недорогой и простой в обращении. Другие подходящие загустители включают, например, ксантановую камедь, карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, карбомер и тому подобное. Концентрация загустителя может зависеть от выбранного средства. Важным моментом является использование такого количества, которое позволит достичь желательной вязкости. Очевидно, что выбор соответствующих носителей и других добавок будет зависеть от конкретного пути введения и характера конкретной лекарственной формы, например, жидкой лекарственной формы (например, если композиция будет сформулирована в виде раствора, суспензии, геля или другой жидкой формы, такой как форма с замедленным высвобождением или заполненная жидкостью форма).
Специалисты в данной области понимают, что выбранные компоненты композиций должны быть химически инертными и не влиять на жизнеспособность или эффективность иммунореактивных клеток, описанных в настоящем документе. Это не будет являться проблемой для специалистов в области химии и фармацевтики, или проблем можно будет с легкостью избежать, обращаясь к стандартным руководствам или проводя простые эксперименты (без излишнего экспериментирования) на основании настоящего документа и приведенных в нем литературных источников.
Одним из соображений при терапевтическом применении иммунореактивных клеток по настоящему изобретению является количество клеток, необходимое для достижения оптимального эффекта. Количество вводимых клеток будет варьироваться для субъектов, получающих лечение. В конкретных вариантах осуществления субъекту вводят от примерно 104 до примерно 1010, от примерно 105 до примерно 109 или от примерно 106 до примерно 108 иммунореактивных клеток по настоящему изобретению. Более эффективные клетки можно вводить даже в меньших количествах. В некоторых вариантах осуществления субъекту-человеку вводят по меньшей мере примерно 1×108, примерно 2×108, примерно 3×108, примерно 4×108 и примерно 5×108 иммунореактивных клеток по настоящему изобретению. Точное определение того, что можно считать эффективной дозой, может быть основано на факторах, индивидуальных для каждого субъекта, включая размеры тела, возраст, пол, массу тела и состояние здоровья конкретного субъекта. Дозировки могут быть с легкостью определены специалистами в данной области на основании настоящего документа и общих знаний в данной области.
Квалифицированный специалист может с легкостью определять количество клеток, а также необязательные добавки, растворители, и/или носители в композициях, которые будут введены в соответствии со способами по настоящему изобретению. Как правило, любые добавки (в дополнение к активной клетке(ам) и/или средству(ам)) присутствуют в количестве от примерно 0,001% до примерно 50% по массе от массы раствора в фосфатно-солевом буфере, и активный ингредиент присутствует в количестве, порядок величины которого составляет от микрограмм до миллиграмм, например, от примерно 0,0001 масс% до примерно 5 масс%, от примерно 0,0001 масс% до примерно 1 масс%, от примерно 0,0001 масс% до примерно 0,05 масс%, от примерно 0,001 масс% до примерно 20 масс%, от примерно 0,01 масс% до примерно 10 масс%, или от примерно 0,05 масс% до примерно 5 масс%. Для любой композиции, которую предстоит вводить животному или человеку, и для любого конкретного способа введения следует определять параметры токсичности, например, путем определения летальной дозы (LD) и LD50 в соответствующей животной модели, например, на грызунах, таких как мышь; а также дозу композиции(ий), концентрацию компонентов в ней и сроки введения композиции(ий), которые приводят к подходящей ответной реакции. Такие определения не требуют излишнего экспериментирования и могут быть проведены на базе знаний квалифицированного специалиста, настоящего документа и документов, цитированных в нем. Время для последовательных введений также может быть установлено без излишнего экспериментирования.
VIII. Способы лечения
Микроокружение опухоли. Опухоли имеют микроокружение, враждебное для иммунной системы хозяина, с вовлечением целого ряда механизмов, с помощью которых злокачественные клетки защищаются от узнавания и уничтожения иммунными клетками. Это «враждебное микроокружение опухоли» включает различные иммуносупрессорные факторы, включая инфильтрирующие регуляторные CD4+ T-клетки (Treg), миелоидные супрессорные клетки (MDSC), опухоль-ассоциированные макрофаги (TAM), иммуносупрессорные цитокины, включая IL-10 и TGF-β, а также экспрессию лигандов для иммуносупрессорных рецепторов, экспрессируемых активированными T-клетками (CTLA-4 и PD-1). Эти механизмы иммуносупрессии участвуют в поддержании толерантности и подавлении неадекватных иммунных ответов, однако в микроокружении опухоли эти механизмы предотвращают эффективный противоопухолевый иммунный ответ. В совокупности эти иммуносупрессорные факторы могут вызывать либо заметную анергию, либо апоптоз адоптивно перенесенных модифицированных CAR T-клеток при встрече с целевыми опухолевыми клетками.
Проблемы иммунологии опухолей. Для эффективного противоопухолевого иммунитета необходимо узнавание опухолевых антигенов и беспрепятственное уничтожение опухоли эффекторными иммунными клетками. Опухолевые антигены должны содержать пептидные эпитопы, которые представляются опухолью и могут быть узнаны специфическими цитотоксическими T-лимфоцитами (CTL). Примированные CTL должны размножиться до достаточных количеств и мигрировать в участки опухоли, где они созревают до стадии эффекторов, чтобы выполнять свои функции, которые усиливаются за счет хелперных T-клеток и ослабляются за счет Treg и ингибирующих макрофагов.
Направленная T-клеточная терапия с помощью генетически модифицированных T-лимфоцитов. Генетическое модифицирование T-клеток является новаторской стратегией для потенциального устранения многих ранее выявленных недостатков ранних иммунотерапевтических подходов. В прошлом году исследователи сообщали о впечатляющей полной ремиссии при рецидивирующем16,17, не поддающемся химиотерапии лейкозе и метастатической меланоме18-20, достигнутой при использовании аутологичных T-клеток периферической крови, нацеленных на определенный антиген (CD19 и NY-ESO-1, соответственно).
Обоснование генетического подхода: Клеточную инженерию можно использовать для перенаправления T-клеток на опухолевые антигены и для усиления функции T-клеток. Одним из стимулов для генетической модификации T-клеток является потенциальная возможность повышения выживаемости и экспансии T-клеток и избегания гибели, анергии T-клеток и иммуносупрессии. Генетическое нацеливание T-клеток также может быть усовершенствовано для предотвращения нежелательного разрушения нормальных тканей.
Химерные антигенные рецепторы (CAR): Специфические для опухоли T-клетки могут быть получены путем переноса генов, кодирующих CAR21-26. CAR второго поколения содержат связывающий опухолевый антиген домен, слитый с внутриклеточным сигнальным доменом, способным активировать T-клетки, и костимулирующим доменом, разработанным для повышения эффективности и персистенции T-клеток27. Таким образом, конструкция CAR позволяет синхронизировать узнавание антигена и передачу сигнала, две функции, которые физиологически осуществляются двумя отдельными комплексами, гетеродимером TCR и комплексом CD3. Внеклеточный антигенсвязывающий домен в CAR, как правило, получают из мышиного моноклонального антитела (мАт), либо из рецепторов или их лигандов. Таким образом, узнавание антигена не рестриктировано MHC28,29 и, следовательно, возможно для любого пациента, в организме которого экспрессируется целевой антиген, с использованием одного и того же CAR. Связывание антигена с CAR запускает фосфорилирование активационных тирозинсодержащих мотивов иммунорецепторов (ITAM) во внутриклеточном домене, инициируя сигнальный каскад, необходимый для индукции цитолиза, секреции цитокинов и пролиферации. Поскольку рестриктирование по MHC при узнавании антигена отсутствует, на функцию CAR-направляемых T-клеток не влияет понижающая регуляция HLA или дефекты аппарата процессинга антигена.
Потребности T-клеток для экспансии и выживания: Пролиферация опухоль-специфических T-клеток необходима ex vivo и, возможно, желательна in vivo. Пролиферация T-клеток должна сопровождаться выживанием T-клеток для достижения абсолютной T-клеточной экспансии и персистенции. Для пролиферации в ответ на антиген T-клетки должны получать два сигнала. Один возникает при узнавании TCR комплексов антигенный пептид/MHC, экспонируемых на поверхности антигенпредставляющих клеток (APC)25. Другой сигнал обеспечивает T-клеточный костимулирующий рецептор, такой как рецепторы CD28 или 4-1BB. Хотя для цитолитической активности T-клеток нет необходимости в сопутствующей костимуляции, существует очень важная потребность в обеспечении костимулирующих сигналов для поддержания противоопухолевых функций адоптивно перенесенных T-клеток, как показано ранее23,27,30-32.
Иммунологический мониторинг: Лимфоциты являются многофункциональными «лекарственными средствами», которые проявляют динамично развивающиеся эффекты после инфузии. При встрече с антигеном опухоль-специфические T-клетки активируются и/или высвобождают различные белки, которые могут запускать уничтожение опухоли, T-клеточную пролиферацию, а также рекрутинг или иммуномодуляцию других иммунных клеток. Таким образом, определение того, какие белки секретируются из каких клеток, в каком количестве и в какой момент времени, дает глубокое понимание того, почему конкретный пациент отвечает или не отвечает на лечение, и обеспечивает очень важную обратную связь для разработки более эффективных испытаний. Такие системы анализа позволяют проводить непосредственные и значимые сравнения клинических подходов и, таким образом, помогают в разработке рациональных терапевтических стратегий следующего поколения.
Вводимое для лечения количество представляет собой количество, эффективное для достижения желательного результата. Эффективное количество может быть предоставлено одним введением или рядом введений. Эффективное количество может быть предоставлено болюсной инъекцией или непрерывной перфузией.
«Эффективное количество» (или «терапевтически эффективное количество») представляет собой количество, достаточное для достижения полезного или желательного клинического результата при лечении. Эффективное количество можно вводить субъекту в одной или более дозах. В случае лечения, эффективное количество представляет собой количество, достаточное для облегчения, ослабления, стабилизации, обращения вспять или замедления прогрессирования заболевания, либо иным образом уменьшения патологических последствий заболевания. Эффективное количество, как правило, определяет врач на индивидуальной основе, и его определение находится в пределах компетенции специалиста в данной области. Как правило, несколько факторов учитывают при определении соответствующей дозы для достижения эффективного количества. Такие факторы включают возраст, пол и массу тела субъекта, состояние, подвергаемое лечению, степень тяжести состояния, а также форму и эффективную концентрацию вводимых иммунореактивных клеток.
Для адоптивной иммунотерапии с использованием антигенспецифических T-клеток клетки в диапазоне доз от примерно 106 до примерно 1010 (например, примерно 109), как правило, вводят инфузией. После попадания иммунореактивных клеток в организм субъекта и последующей дифференциации индуцируются иммунореактивные клетки, которые специфически направлены против одного конкретного антигена (например, BCMA). «Индукция» T-клеток может включать инактивацию антигенспецифических T-клеток, например, за счет удаления или анергии. Инактивация особенно полезна для установления или повторного установления толерантности, как, например, при аутоиммунных заболеваниях. Иммунореактивные клетки по настоящему изобретению можно вводить любыми способами, известными в данной области, включая, но без ограничения, плевральное введение, внутривенное введение, подкожное введение, внутриузловое введение, внутриопухолевое введение, интратекальное введение, интраплевральное введение, внутрибрюшинное введение и прямое введение в тимус. В конкретных вариантах осуществления иммунореактивные клетки и содержащие их композиции внутривенно вводят субъекту, который нуждается в этом.
Настоящее изобретение относится к различным способам применения иммунореактивных клеток (например, T-клеток), экспрессирующих BCMA-нацеленный CAR. Например, настоящее изобретение относится к способам уменьшения опухолевой нагрузки у субъекта. В одном неограничивающем примере способ уменьшения опухолевой нагрузки включает введение эффективного количества раскрытой в настоящем документе иммунореактивной клетки субъекту, в результате чего индуцируется гибель опухолевых клеток у субъекта. Раскрытая в настоящем документе иммунореактивная клетка способна приводить к уменьшению количества опухолевых клеток, уменьшению размера опухоли и/или уничтожению опухоли у субъекта. Неограничивающие примеры соответствующей опухоли включают множественную миелому, неходжкинскую лимфому, лимфому Ходжкина, хронический лимфоцитарный лейкоз (CLL), глиобластому и макроглобулинемию Вальденстрема. В конкретных вариантах осуществления опухоль представляет собой множественную миелому.
Настоящее изобретение также относится к способам увеличения или продления срока выживания субъекта, имеющего неоплазию. В одном неограничивающем примере способ увеличения или продления срока выживания субъекта, имеющего неоплазию, включает введение эффективного количества раскрытой в настоящем документе иммунореактивной клетки субъекту, в результате чего увеличивается или продлевается срок выживания субъекта. Способ может приводить к уменьшению или уничтожению опухолевой нагрузки у субъекта. Настоящее изобретение также относится к способам лечения или предотвращения неоплазии у субъекта, включающим введение раскрытой в настоящем документе иммунореактивной клетки субъекту.
Используемый в настоящем документе термин «неоплазия» означает заболевание, характеризующееся патологической пролиферацией клетки или ткани и ее последующей миграцией или инвазией в другие ткани или органы. Неопластический рост, как правило, является неконтролируемым и прогрессирующим, и происходит в условиях, которые не вызвали бы, или вызвали бы прекращение, размножения нормальных клеток. Неоплазии могут поражать разные клетки, ткани или органы, включая, но без ограничения, орган, выбранный из группы, состоящей из мочевого пузыря, толстой кишки, кости, головного мозга, молочной железы, хряща, глии, пищевода, фаллопиевой трубы, желчного пузыря, сердца, кишечника, почки, печени, легких, лимфатических узлов, нервной ткани, яичников, плевры, поджелудочной железы, предстательной железы, скелетных мышц, кожи, спинного мозга, селезенки, желудка, яичек, тимуса, щитовидной железы, трахеи, урогенитального тракта, мочеточника, уретры, матки и влагалища, либо ткани или клеток из них. Неоплазии включают такие формы рака, как саркомы, карциномы или плазмацитомы (злокачественная опухоль плазматических клеток).
Раковые опухоли, рост которых можно ингибировать с использованием иммунореактивных клеток по настоящему изобретению, включают формы рака, как правило, отвечающие на иммунотерапию. Неограничивающие примеры рака, который можно лечить, включают множественную миелому, неходжкинскую лимфому, лимфому Ходжкина, хронический лимфоцитарный лейкоз (CLL), глиобластому и макроглобулинемию Вальденстрема. В конкретных вариантах осуществления опухоль представляет собой множественную миелому.
Кроме того, настоящее изобретение относится к способам повышения продуцирования иммуноактивирующих цитокинов в ответ на присутствие раковой клетки в организме субъекта. В одном неограничивающем примере способ включает введение раскрытой в настоящем документе иммунореактивной клетки субъекту. Иммуноактивирующий цитокин может представлять собой гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), IFN-α, IFN-β, IFN-γ, TNF-α, IL-2, IL-3, IL-6, IL-11, IL-7, IL-12, IL-15, IL-21, регуляторный фактор интерферона 7 (IRF7), а также их сочетания. В конкретных вариантах осуществления в иммунореактивных клетках, содержащих BCMA-специфичный CAR по настоящему изобретению, повышено продуцирование GM-CSF, IFN-γ и/или TNF-α.
Субъекты-люди, подходящие для терапии, как правило, составляют две группы лечения, которые различаются по клиническим критериям. Субъекты с «запущенным заболеванием» или «высокой опухолевой нагрузкой» являются субъектами, имеющими клинически определяемую опухоль (например, множественную миелому). Клиническими определяемая опухоль представляет собой опухоль, которую можно обнаружить по наличию опухолевой массы (например, при пальпации, на основании результатов КАТ-сканирования, сонограммы, маммограммы или рентгеновского снимка; наличия одних только биохимических или гистопатологических маркеров недостаточно для отнесения к этой популяции). Фармацевтическую композицию по настоящему изобретению вводят данным субъектам для инициации противоопухолевого ответа с целью облегчения их состояния. В идеале, результатом является уменьшение опухолевой массы, однако любое клиническое улучшение является полезным. Клиническое улучшение включает снижение риска или скорости прогрессирования, или уменьшение патологических последствий опухоли (например, множественной миеломы).
Вторая группа подходящих субъектов известна в данной области как «адъювантная группа». К этой группе относятся индивидуумы, которые имели в анамнезе неоплазию (например, множественную миелому), но ответили на другой вид терапии. Предшествующая терапия может включать, но без ограничения, хирургическую резекцию, радиотерапию и традиционную химиотерапию. В результате данные индивидуумы не имеют клинически определяемую опухоль. Однако они могут иметь риск прогрессирования заболевания, либо рядом с зоной исходной опухоли, либо вследствие метастазов. Эту группу можно дополнительно подразделять на подгруппы индивидуумов с высокой степенью риска и с низкой степенью риска. Это разделение проводят на основе признаков, наблюдаемых до или после первичного лечения. Эти особенности известны в клинической практике и соответствующим образом определены для каждой отдельной неоплазии. Признаками, типичными для подгрупп с высокой степенью риска, являются инвазия опухоли (например, множественной миеломы) в соседние ткани или признаки вовлечения лимфатических узлов. Индивидуумы другой группы имеют генетическую предрасположенность к неоплазии (например, множественной миеломе), однако у них пока не проявляются клинические признаки неоплазии (например, множественной миеломы). Например, женщины с положительными результатами теста на генетическую мутацию, связанную с раком молочной железы, но все-еще находящиеся в детородном возрасте, могут решить принимать один или более из антигенсвязывающих фрагментов, описанных в настоящем документе, в качестве профилактической меры для предотвращения развития неоплазии до тех пор, пока не наступит подходящее время для проведения превентивной хирургической операции.
Субъекты могут иметь запущенную форму заболевания (например, множественной миеломы), в этом случае цель лечения может включать облегчение или обращение вспять прогрессирования заболевания и/или ослабление побочных эффектов. Субъекты могут иметь в анамнезе состояние, для которого они уже получали лечение, в этом случае цель лечения, как правило, будет включать уменьшение риска или отсрочку рецидива.
Можно вносить дополнительные модификации в иммунореактивные клетки, экспрессирующие BCMA-нацеленный CAR (например, T-клетки), для предотвращения или минимизации риска иммунологических осложнений (известных как «злокачественная трансформация T-клеток»), например, реакции «трансплантат против хозяина» (GvHD), или в случае, когда здоровые ткани экспрессируют те же целевые антигены, что и клетки опухолей, что приводит к результатам, аналогичным GvHD. Потенциальным решением этой проблемы является введение генно-инженерными методами в CAR-экспрессирующие T-клетки гена самоубийства. Подходящие гены самоубийства включают, но не ограничиваются ими, ген тимидинкиназы вируса простого герпеса (hsv-tk), ген индуцируемой каспазы 9 (iCasp-9), а также ген укороченного полипептида рецептора эпидермального фактора роста (EGFRt) человека. В конкретных вариантах осуществления ген самоубийства представляет собой ген полипептида EGFRt. Полипептид EGFRt может вызывать элиминацию T-клеток при введении анти-EGFR моноклонального антитела (например, цетуксимаба). EGFRt может быть ковалентно связан с 3'-концом внутриклеточного домена BCMA-нацеленного CAR. Ген самоубийства можно включать в вектор, содержащий нуклеиновые кислоты, кодирующие раскрытый в настоящем документе BCMA-нацеленный CAR. В этой ситуации введение пролекарства, предназначенного для активации гена самоубийства (например, AP1903 для активации iCasp-9) в случае злокачественной трансформации T-клеток (например, GVHD), запускает апоптоз CAR-экспрессирующих T-клеток с активированным геном самоубийства.
IX. Наборы
Настоящее изобретение относится к наборам для лечения или предотвращения неоплазии (например, множественной миеломы). В конкретном варианте осуществления набор включает терапевтическую или профилактическую композицию, содержащую эффективное количество иммунореактивной клетки, содержащей BCMA-нацеленный CAR, в стандартной лекарственной форме. В конкретных вариантах осуществления клетки могут дополнительно экспрессировать по меньшей мере один костимулирующий лиганд. В конкретных вариантах осуществления набор включает стерильный контейнер, содержащий терапевтическую или профилактическую вакцину; такие контейнеры могут представлять собой коробки, ампулы, бутылки, флаконы, пробирки, мешки, пакеты, блистерные упаковки или другие подходящие формы контейнеров, известные в данной области. Такие контейнеры могут быть выполнены из пластика, стекла, ламинированной бумаги, металлической фольги или других материалов, подходящих для хранения лекарственных средств.
При необходимости, иммунореактивную клетку предоставляют совместно с инструкциями по введению клетки субъекту, имеющему, или имеющему риск развития неоплазии (например, множественной миеломы). Инструкции, как правило, будут содержать информацию об использовании композиции для лечения или предотвращения неоплазии (например, множественной миеломы). В других вариантах осуществления инструкции включают по меньшей мере одно из следующего: описание лекарственного средства; схему доз и режим введения для лечения или предотвращения неоплазии (например, множественной миеломы) или ее симптомов; меры предосторожности; предупреждения; показания; противопоказания; информацию о передозировке; побочные реакции; результаты фармакологических исследований на животных, клинических исследований и/или литературные источники. Инструкции могут быть напечатаны непосредственно на контейнере (при возможности), или представлять собой этикетку, прикрепленную к контейнеру, или представлять собой отдельный листок, брошюру, карточку или папку, которые предоставляют в контейнере или вместе с ним.
ПРИМЕРЫ
При осуществлении на практике настоящего изобретения, если нет иных указаний, используют общепринятые методы молекулярной биологии (включая рекомбинантные методы), микробиологии, клеточной биологии, биохимии и иммунологии, которые находятся в пределах компетенции специалиста в данной области. Такие методы подробно описаны в литературе, такой как «Molecular Cloning: A Laboratory Manual», второе издание (Sambrook, 1989); «Oligonucleotide Synthesis» (Gait, 1984); «Animal Cell Culture» (Freshney, 1987); «Methods in Enzymology»; «Handbook of Experimental Immunology» (Weir, 1996); «Gene Transfer Vectors for Mammalian Cells» (Miller and Calos, 1987); «Current Protocols in Molecular Biology» (Ausubel, 1987); «PCR: The Polymerase Chain Reaction», (Mullis, 1994); «Current Protocols in Immunology» (Coligan, 1991). Эти методы применимы для получения полинуклеотидов и полипептидов по изобретению и, следовательно, могут быть использованы при осуществлении на практике настоящего изобретения. Особенно полезные методы для конкретных вариантов осуществления будут описаны в следующих далее разделах.
Следующие примеры приведены, чтобы предоставить специалистам в данной области полное раскрытие и описание того, как выполнять и использовать анализ, скрининг и методы лечения по изобретению, и не предназначены для ограничения объема того, что авторы заявки считают своим изобретением.
Пример 1 - Экспрессия BCMA в различных тканях
Экспрессию BCMA человека оценивали в различных злокачественных и нормальных тканях путем изучения профилей экспрессии генов в базах данных, таких как энциклопедия линий раковых клеток и BioGPS. Как показано на фигуре 2, BCMA человека экспрессируется на высоком уровне в клетках лимфомы и множественной миеломы, но не в других злокачественных тканях. Нормальная экспрессия, судя по всему, ограничена B-клетками и плазматическими клетками. Потенциальное уничтожение BCMA-нацеленными CAR T-клетками нормальных клеток этого типа не может иметь существенные неблагоприятные последствия, о чем свидетельствует опыт с пациентом авторов изобретения при использовании нацеленных на CD19 CAR T-клеток. Любое отсутствие физиологического продуцирования антител может быть исправлено внутривенным введением иммуноглобулинов.
Пример 2 - Конструкт BCMA-специфичных 28z CAR
Было создано множество уникальных полностью человеческих scFv к BCMA и были получены CAR на основе этих scFv. Множество scFv было идентифицировано при скрининге фаговой библиотеки полностью человеческих scFv (> 6×1010 scFv) со слитым белком BCMA-Fc, а затем с клетками 3T3, экспрессирующими BCMA человека. После секвенирования было обнаружено 57 уникальных и положительных в отношении BCMA-Fc клонов из 79 секвенированных положительных клонов; показатель отбора уникальных клонов составил 72%. С помощью FACS-анализа фаговых клонов для антител против BCMA-3T3 и исходной линии клеток 3T3 было получено подтверждение для 25 уникальных положительных клонов.
ET140-153 scFv (или «ET140-3 scFv»), ET140-174 scFv (или «ET140-24 scFv»), ET140-187 scFv (или «ET140-37 scFv»), ET140-190 scFv (или «ET140-40 scFv») и ET140-204 scFv (или «ET140-54 scFv») были использованы для создания BCMA-нацеленных 28z CAR 3, 24, 37, 40 и 54, соответственно. Эти BCMA-нацеленные 28z CAR имели сходную структуру, например, каждый имел трансмембранный домен, содержащий полипептид CD28, и внутриклеточный домен, содержащий полипептид CD3ξ и костимулирующую сигнальную область, содержащую полипептид CD28, как показано на фигуре 1. Каждый из этих BCMA-нацеленных CAR клонировали в ретровирусный вектор. Эти вирусные векторы затем были трансдуцированы в клетки-упаковщики HEK 293 вирусов galv9 для создания стабильной упаковывающей линии для получения CAR+ T-клеток.
Человеческие T-клетки (неотобранные (CD4 и CD8) человеческие T-клетки от здорового донора) были трансдуцированы ретровирусом для экспрессии каждого из этих BCMA-нацеленных CAR, вследствие чего T-клетки экспрессировали эти BCMA-нацеленные 28z CAR. Экспрессию BCMA-нацеленных CAR на поверхности человеческих T-клеток оценивали по связыванию A647-конъюгированного слитого белка BCMA-Fc. Оценивали экспрессию на клеточной поверхности BCMA-нацеленного 28z CAR24, и обнаружение его на клеточной поверхности подтверждали методом проточной цитометрии, как показано на фигуре 3.
Оценивали перекрестную реактивность семнадцати человеческих scFv в отношении BCMA человека и BCMA мыши. Как показано на фигуре 4, некоторые scFv, например, ET140-153 scFv (или «ET140-3 scFv») и ET140-192 scFv (или «ET140-42 scFv») перекрестно реагировали с BCMA мыши, таким образом, эти scFv могут быть использованы для исследований на сингенных мышах.
Пример 3 - Активность BCMA-специфичных CAR
Оценивали противоопухолевую активность раскрытых в настоящем документе BCMA-специфичных 28z CAR. Данные in vitro показали, что BCMA-специфичные CAR специфически уничтожали BCMA-представляющие клетки, включая клетки линии MM. Например, как показано на фигуре 5, T-клетки, экспрессирующие BCMA-специфичный 28z CAR24, уничтожали клетки 3T3, избыточно экспрессирующие BCMA (но не контрольные клетки 3T3, избыточно экспрессирующие посторонний антиген). Как показано на фигуре 6, T-клетки, экспрессирующие BCMA-специфичные 28z CAR 24, 40 и 54, уничтожали клетки линии MM человека.
Пример 4 - Данные скрининга для анти-BCMA антител
ELISA-скрининг: На фигуре 21 представлены репрезентативные результаты белкового скрининга методом ELISA против антигена BCMA с использованием специфичных фаговых клонов scFv антител (ET140-3, ET140-24, ET140-37, ET140-40 и ET140-54). В лунки планшетов для ELISA вносили слитый белок ВКД BCMA человека-Fc, контроль-Fc слитый белок или только PBS в качестве пустой пробы, соответственно. Отдельные фаговые клоны из пулов библиотеки фагового дисплея, обогащенных путем пэннинга против слитого белка ВКД BCMA человека-Fc, инкубировали в покрытых лунках планшета. Связывание фаговых клонов обнаруживали с помощью HRP-конъюгированных анти-M13 антител и проводили окрашивание с использованием субстрата TMB. Поглощение определяли при 450 нм.
FACS-скрининг: На фигуре 22 представлены репрезентативные результаты FACS-анализа BCMA-специфичных фаговых клонов антител ET140-3, ET140-24, ET140-37, ET140-40 и ET140-54. Фаговые клоны инкубировали с клетками линии 3T3-BCMA, затем с анти-M13 мышиным антителом. В завершение, APC-меченое 2-е антитело против IgG мыши добавляли в реакционную смесь после промывания. Связывание измеряли методом FACS и выражали в единицах средней интенсивности флуоресценции (СИФ). Клетки, инкубированные только с 2-м антителом, M13 K07 хелперным фагом, и просто клетки использовали в качестве отрицательного контроля.
Пример 5 - Конструкт BCMA-специфичных BBz CAR
Было создано множество уникальных полностью человеческих scFv к BCMA, как описано в примере 2. ET140-153 scFv (или «ET140-3 scFv»), ET140-174 scFv (или «ET140-24 scFv»), ET140-187 scFv (или «ET140-37 scFv»), ET140-190 scFv (или «ET140-40 scFv») и ET140-204 scFv (или «ET140-54 scFv») были использованы для создания BCMA-нацеленных BBz CAR 3, 24, 37, 40 и 54, соответственно. Каждый из этих BCMA-нацеленных BBz CAR имеет трансмембранный домен, содержащий полипептид CD8, и внутриклеточный домен, содержащий полипептид CD3ξ и костимулирующую сигнальную область, содержащую полипептид 4-1BB, как показано на фигуре 7. Каждый из этих BCMA-нацеленных CAR клонировали в ретровирусный вектор SFG, в качестве примера, векторы с 4-1BB-содержащим CAR показаны на фигурах 8-12.
Пример 6 - Активность BCMA-нацеленных CAR T-клеток
Как показано на фигуре 13, BCMA-специфичный 28z CAR24 вызывал лизис клеток линий L363, NCL-H929 и U266 MM человека, в сравнении с нацеленными на постороннюю мишень MUC16-нацеленными 4h11-28z CAR T-клетками. Цитотоксичность, наблюдаемая в случае BCMA-специфичного 28z CAR24, была специфичной для BCMA, поскольку отсутствовал лизис BCMA-отрицательных CD19-положительных клеток линии Raji лимфомы Беркитта, как показано на фигуре 13.
Пример 7 - Индукция секреции цитокинов BCMA-нацеленными CAR T-клетками
Совместное культивирование BCMA-нацеленных 28z CAR24 T-клеток конкретно с клетками линии MM индуцировало секрецию цитокинов, профиль которой соответствовал профилю при активации T-клеток. На фигуре 14 показана секреция IL-2 после 24 ч совместного культивирования CAR T-клеток с клетками опухолевых линий человека (соотношение Э:М=1:1). В случае лимфоплазматической лимфомы (CD19+) с CD19-нацеленными CAR T-клетками (положительный контроль) и клеток линии MM с BCMA-нацеленными 28z CAR24 T-клетками наблюдали повышенное продуцирование цитокинов. Все из IFNγ, IL-6, TNFα, sCD40L, GM-CSF имели сходные профили секреции (данные не представлены).
Пример 8 - Противоопухолевая активность BCMA-нацеленных CAR T-клеток
BCMA-нацеленные 28z CAR54 T-клетки опосредовали иммунный ответ против миеломы. 1×107 клеток линии U266 миеломы человека вводили в/в инъекцией мышам NSG в день 0. В день 4 в/в инъекцией вводили 1×106 BCMA-нацеленных или CD19-нацеленных T-клеток с CAR второго поколения. Визуализация в день 11 (день 7 после инъекции CAR T-клеток) показала, что, в отличие от CAR T-клеток, нацеленных на постороннюю мишень (CD19), BCMA-нацеленные 28z CAR54 T-клетки были способны опосредовать противоопухолевый ответ. Смотри фигуру 15.
Пример 9 - Активность BCMA-нацеленных CAR T-клеток
Тестировали способность BCMA-нацеленных CAR T-клеток специфически лизировать клетки линии миеломы человека (HMCL). CD19-нацеленные CAR T-клетки или BCMA-нацеленные 28z CAR24 T-клетки инкубировали с экспрессирующими GFP клетками опухолевых линий SET2 (острый миелоидный лейкоз (AML), CD19-BCMA-); BCWM1 (лимфоплазматическая лимфома (LPL), CD19+BCMA-); L363 (множественная миелома (MM), CD19-BCMA+). В момент времени 0 процентная доля GFP+ опухолевых клеток показана на фигуре 16A. Через 36 ч используемые в качестве положительного контроля CD19-нацеленные CAR T-клетки специфически уничтожали GFP+ клетки линии LPL и, аналогично, BCMA-нацеленные 28z CAR24 T-клетки специфически уничтожали GFP+ клетки линии MM. Смотри фигуру 16B.
Пример 10 - Картирование эпитопов анти-BCMA антител
Пептиды BCMA были упорядочены на основании последовательности ВКД с N-концевым биотином+линкер SGSG+15 аминокислот с промежутком в 1 аминокислоту. Пептидная библиотека представлена в таблице 24.
Таблица 24

Пептиды наносили на покрытые стрептавидином планшеты в концентрации 2 мкг/мл в PBST (PBS+ 0,05% Tween-20). Затем промывали и блокировали 3% раствором БСА. После промывания ET140-3, ET140-24, ET140-54 или ET901 mIgG1 в концентрации 1 мкг/мл добавляли в лунки планшета, соответственно. «mIgG1» при использовании во всех примерах указывает на то, что вариабельная область является полностью человеческой, а Fc-часть происходит из IgG1 мыши. Затем в каждую лунку добавляли конъюгированное с HRP выявляющее антитело против IgG мыши. В завершение, при добавлении субстрата TMB развивалась окраска. Для анализа данных регистрировали поглощение при A450. Результаты показаны на фигурах 17-20. Как показано на фигурах 17 и 20, ET140-3 связывались с пептидами 7-13 (то есть, аминокислотами 8-22, 9-23, 10-24, 11-25, 12-26, 13-27 и 14-28) из SEQ ID NO: 71. Как показано на фигурах 18 и 19, для ET140-24 или ET140-54 не были обнаружены линейные эпитопы.
Выводы: 3 ET140 антитела (mIgG1) наряду с контрольным по изотипу ET901 mIgG1 тестировали на их связывающийся эпитоп против BCMA-ВКД. Пептидную библиотеку, состоящую из 39 пептидов (N-концевой биотин+линкер SGSG+15 аминокислот, со смещением в 1 аминокислоту), использовали для картирования эпитопов методом ELISA. Это позволяло производить поиск линейного связывающегося эпитопа BCMA-ВКД. ET901 mIgG1 использовали в качестве контрольного фона для каждого пептида. Только для ET140-3 удалось идентифицировать его область эпитопа: область, содержащую аминокислоты 14-22 из SEQ ID NO: 71, например, аминокислоты 8-28 из SEQ ID NO: 71.
В случае ET140-24 и ET140-54 не наблюдали никакого существенного связывания с пептидной библиотекой. Это указывало на то, что эти два антитела могут узнавать скорее конформационный эпитоп, а не линейный эпитоп в BCMA.
Пример 11 - Рекомбинантный антиген анти-BCMA антител методом поверхностного плазмонного резонанса
Кинетику взаимодействия между ET140-153 mIgG1 (или «ET140-3 mIgG1»), ET140-174 mIgG1 (или «ET140-24 mIgG1»), ET140-204 mIgG1 (или «ET140-54 mIgG1») и рекомбинантным антигеном BCMA определяли на приборе BIAcore X100. Вкратце, модифицированный стрептавидин в концентрации 50 мкг/мл иммобилизовали на улавливающем сенсорном чипе путем пропускания улавливающего биотин реагента через проточные ячейки со скоростью 2 мкл/мин в течение 5 минут. Биотинилированный белок BCMA-Fc в концентрации 10 мкг/мл загружали на проточную ячейку со скоростью 30 мкл/мин в течение 3 минут. В соответствии со стандартным протоколом определения кинетики выполняли серию инжекций ESK1 в концентрации от 0,6 до 15 мкг/мл, при этом каждый этап состоял из 3-минутной инжекции со скоростью 30 мкл/мин и 3-минутной диссоциации. Затем поверхность регенерировали в течение 2 минут раствором, состоящим из 75% (по объему) 8M гуанидина-HCl и 25% (по объему) 1M NaOH. Кинетические константы получали путем глобальной аппроксимации (модель Ленгмюра для связывания 1:1) с использованием оценочной программы BIAcore X100 (версия 2.0.1). Данные по аффинности связывания приведены в таблице 25.
Таблица 25
Хотя настоящее изобретение было описано в некоторых подробностях и проиллюстрировано примерами для ясности понимания, приведенное описание и примеры не должны быть истолкованы как ограничивающие объем настоящего изобретения. Содержание всех патентов и специальных литературных источников, цитированных в настоящем документе, специально включено в настоящий документ посредством ссылки.
Литература
1. Frigyesi, I., et al. Robustisolation of malignantplasma cells in multiplemyeloma. Blood 123, 1336-1340 (2014).
2. Tai, Y.T., et al. Novelafucosylate danti-B cellmaturation antigen-monomethylauristatin Fantibody-drugconjugate (GSK2857916) in ducespotent and selective anti-multiplemyeloma activity. Blood (2014).
3. Carpenter, R.O., et al. B-cell maturation antigenisapromising target for adoptive T-cell therapy of multiplemyeloma. Clinical cancer research: an official journal of the American Association for Cancer Research 19, 2048-2060 (2013).
4. Brentjens, R.J., et al. Safety and persistence of adoptively transferred autologous CD19-targeted T-клетки in patients with relapse dorchemo therapy refractory B-cell leukemias. Blood 118, 4817-4828 (2011).
5. Brentjens, R.J., et al. Eradication of systemic B-cell tumors by genetically targeted human T lymphocytes co-stimulated by CD80 and interleukin-15. Nature medicine 9,279-286 (2003).
6. Brentjens, R.J., et al. CD19-Targeted T-клетки Rapidly Induce Molecular Remissionsin Adults with Chemotherapy-Refractory Acute Lymphoblastic Leukemia. Science translational medicine 5,177 ra138 (2013).
7. Davila, M.L., et al. Efficacy and Toxicity Management of 19-28z CART Cell Therapyin B Cell Acute Lymphoblastic Leukemia. Science translational medicine 6,224 ra225 (2014).
8. Siegel, R., Naishadham, D. & Jemal, A. Cancerstatistics, 2013. CA: acancer journal for clinicians 63,11-30 (2013).
9. Boyd, K.D., et al. The clinical impact and molecular biology of del(17p) in multiple myeloma treated with conventional or thalidomide-based therapy. Genes, chromosomes & cancer 50,765-774 (2011).
10. Shaughnessy, J.D., Jr., et al. Avalidated gene expression model of high-risk multiplemyeloma is defined by deregulate dexpression of genes mapping to chromosome 1. Blood 109, 2276-2284 (2007).
11. Gahrton, G., et al. Allogeneic bone marrow transplantation in multiplemyeloma. European Groupfor Bone Marrow Transplantation. The New England journal of medicine 325, 1267-1273 (1991).
12. Pegram, H.J., etal. Tumor-targeted T-клетки modified to secrete IL-12 eradicate systemic tumors with outneed for prior conditioning. Blood 119, 4133-4141 (2012).
13. Sabrina Bertilaccio, M.T., et al. Low-Dose Lenalidomide Improves CAR-Based Immunotherapy In CLL By Reverting T-Cell Defects In Vivo. Blood 122, 4171 (2013).
14. Bataille, R., et al. The phenotype of normal, reactive and malignant plasma cells. Identification of "many and multiplemyelomas" and of new targets for myeloma therapy. Haematologica 91, 1234-1240 (2006).
15. Morgan, R.A., et al. Case report of a serious adverseevent following the administration of T-клетки transduced with a chimeric antigen receptor recognizing ERBB2. Molecular therapy: the journal of the American Society of Gene Therapy 18, 843-851 (2010).
16. Brentjens, R.J., et al. Safety and persistence of adoptively transferred autologous CD19-targeted T-клетки in patients with relapsed or chemotherapy refractory B-cell leukemias. Blood 118, 4817-4828 (2011).
17. Brentjens, R.J., et al. CD19-targeted T-клетки rapidly induce molecular remissions in adults with chemotherapy-refractory acute lymphoblastic leukemia. Science translational medicine 5, 177ra138 (2013).
18. Hunder, N.N., et al. Treatment of metastatic melanoma with autologous CD4+ T-клетки against NY-ESO-1. N.Engl.J.Med. 358, 2698-2703 (2008).
19. Rosenberg, S.A., Restifo, N.P., Yang, J.C., Morgan, R.A. & Dudley, M.E. Adoptive cell transfer: a clinical path to effective cancer immunotherapy. Nat.Rev.Cancer 8, 299-308 (2008).
20. Dudley, M.E., et al. Adoptive cell therapy for patients with metastatic melanoma: evaluation of intensive myeloablative chemoradiation preparative regimens. J Clin Oncol 26, 5233-5239 (2008).
21. Brentjens, R.J., et al. Genetically targeted T-клетки eradicate systemic acute lymphoblastic leukemia xenografts. Clin.Cancer Res. 13, 5426-5435 (2007).
22. Gade, T.P., et al. Targeted elimination of prostate cancer by genetically directed human T lymphocytes. Cancer Res. 65, 9080-9088 (2005).
23. Maher, J., Brentjens, R.J., Gunset, G., Riviere, I. & Sadelain, M. Human T-lymphocyte cytotoxicity and proliferation directed by a single chimeric TCRzeta /CD28 receptor. Nat.Biotechnol. 20, 70-75 (2002).
24. Kershaw, M.H., et al. Gene-engineered T-клетки as a superior adjuvant therapy for metastatic cancer. J Immunol 173, 2143-2150 (2004).
25. Sadelain, M., Brentjens, R. & Riviere, I. The promise and potential pitfalls of chimeric antigen receptors. Curr Opin Immunol (2009).
26. Hollyman, D., et al. Manufacturing validation of biologically functional T-клетки targeted to CD19 antigen for autologous adoptive cell therapy. J Immunother 32, 169-180 (2009).
27. Sadelain, M., Brentjens, R. & Riviere, I. The basic principles of chimeric antigen receptor design. Cancer discovery 3, 388-398 (2013).
28. Riviere, I., Sadelain, M. & Brentjens, R.J. Novel strategies for cancer therapy: the potential of genetically modified T lymphocytes. Curr Hematol Rep 3, 290-297 (2004).
29. Stephan, M.T., et al. T cell-encoded CD80 and 4-1BBL induce auto- and transco-stimulation, resulting in potent tumor rejection. Nat.Med. 13, 1440-1449 (2007).
30. Krause, A., et al. Antigen-dependent CD28 signaling selectively enhances survival and proliferation in genetically modified activated human primary T lymphocytes. J Exp Med 188, 619-626 (1998).
31. Gong, M.C., et al. Cancer patient T-клетки genetically targeted to prostate-specific membrane antigen specifically lyse prostate cancer cells and release cytokines in response to prostate-specific membrane antigen. Neoplasia. 1, 123-127 (1999).
32. Lyddane, C., et al. Cutting Edge: CD28 controls dominant regulatory T cell activity during active immunization. J.Immunol. 176, 3306-3310 (2006).
33. Carpenter et al., B-cell maturation antigen is a promising target for adoptive T-cell therapy of multiple myeloma. Clin Cancer Res. 2013 Apr 15;19(8):2048-60.
34. WO2013/154760
35. Maus et al., Cancer Immunol Res (2003);1(1):26-31
Из вышеприведенного описания будет понятно, что в изобретение, описанное в настоящем документе, могут быть внесены вариации и модификации, чтобы адаптировать его к разным вариантам применения и условиям. Такие варианты осуществления также входят в объем следующей далее формулы изобретения.
Все патенты и публикации, а также последовательности с указанными регистрационными или ссылочными номерами, упомянутые в данной спецификации, включены в настоящий документ посредством ссылки в такой же степени, как если было бы специально указано, что каждый отдельный патент или публикация, или последовательность индивидуально включены посредством ссылки.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> MEMORIAL SLOAN-KETTERING CANCER CENTER
EUREKA THERAPEUTICS, INC.
<120> ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ B-КЛЕТОК, И ИХ ПРИМЕНЕНИЕ
<130> 072734.0360
<140> PCT/US2015/064112
<141> 2015-12-04
<150> 62/088,309
<151> 2014-12-05
<160> 280
<170> PatentIn version 3.5
<210> 1
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 1
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Gln Gly Tyr Ser Tyr Tyr Gly Tyr Ser Asp Val
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 2
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 2
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly His Asn
20 25 30
Asp Val Ser Trp Tyr Gln His Leu Pro Gly Lys Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Phe Asp Asp Leu Leu Pro Ser Gly Val Ser Asp Arg Phe Ser
50 55 60
Ala Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Ala Phe Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 3
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 3
caggtacagc tgcagcagtc aggtccagga ctggtgaagc cctcgcagac cctctcactc 60
acctgtgcca tctccgggga cagtgtctct agcaacagtg ctgcttggaa ctggatcagg 120
cagtccccat cgagaggcct tgagtggctg ggaaggacat actacaggtc caagtggtat 180
aatgattatg cagtatctgt gaaaagtcga ataaccatca acccagacac atccaagaac 240
cagttctccc tgcagctgaa ctctgtgact cccgaggaca cggctgtgta ttactgtgcg 300
cgccagggtt actcttacta cggttactct gatgtttggg gtcaaggtac tctggtgacc 360
gtctcctca 369
<210> 4
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 4
cagtctgtgc tgactcagcc accctcggtg tctgtagccc ccaggcagag ggtcaccatc 60
tcgtgttctg gaagcagctc caacatcgga cataatgatg taagctggta ccagcatctc 120
ccagggaagg ctcccagact cctcatctat tttgatgacc tgctgccgtc aggggtctct 180
gaccgattct ctgcctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg gcagcctgaa tgcctttgtc 300
ttcggaactg ggaccaaggt caccgtccta ggt 333
<210> 5
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 5
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Tyr Gly Phe Ser Gly Ser Arg Phe Tyr Asp Thr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 6
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 6
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Phe Asp Asp Leu Leu Ser Ser Gly Val Ser Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 7
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 7
caggtacagc tgcagcagtc aggtccagga ctggtgaagc cctcgcagac cctctcactc 60
acctgtgcca tctccgggga cagtgtctct agcaacagtg ctgcttggaa ctggatcagg 120
cagtccccat cgagaggcct tgagtggctg ggaaggacat actacaggtc caagtggtat 180
aatgattatg cagtatctgt gaaaagtcga ataaccatca acccagacac atccaagaac 240
cagttctccc tgcagctgaa ctctgtgact cccgaggaca cggctgtgta ttactgtgcg 300
cgctacggtt tctctggttc tcgtttctac gatacttggg gtcaaggtac tctggtgacc 360
gtctcctca 369
<210> 8
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 8
cagcctgtgc tgactcagcc accctcggtg tctgaagccc ccaggcagag ggtcaccatc 60
tcctgttctg gaagcagctc caacatcgga aataatgctg taaactggta ccagcagctc 120
ccaggaaagg ctcccaaact cctcatctat tttgatgatc tgctgtcctc aggggtctct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaagatg aggctgatta ttactgtgca gcatgggatg acagcctgaa tggttatgtc 300
ttcggaactg ggaccaaggt caccgtccta ggt 333
<210> 9
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 9
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Ile Pro Ile Leu Gly Ile Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Glu Asp Thr Ser Thr Asp Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Tyr Ser Lys Ser Ile Val Ser Tyr Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 10
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 10
Leu Pro Val Leu Thr Gln Pro Pro Ser Thr Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Val Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Val Val Phe Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Val
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Val Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Ser Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 11
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 11
gaggtccagc tggtgcagtc tggagctgag gtgaagaagc ctgggtcctc ggtgaaggtc 60
tcctgcaagg cttctggagg caccttcagc agctatgcta tcagctgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggaagg atcatcccta tccttggtat agcaaactac 180
gcacagaagt tccagggcag agtcaccatg accgaggaca catctacaga cacagcctac 240
atggagctga gcagcctgag atctgaggac acggccgtgt attactgtgc gcgctctggt 300
tactctaaat ctatcgtttc ttacatggat tactggggtc aaggtactct ggtgaccgtc 360
tcctca 366
<210> 12
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 12
ctgcctgtgc tgactcagcc cccctccacg tctgggaccc ccgggcagag ggtcaccgtc 60
tcttgttctg gaagcagctc caacatcgga agtaatgttg tattctggta ccagcagctc 120
ccaggcacgg cccccaaact tgtcatctat aggaataatc aacggccctc aggggtccct 180
gaccgattct ctgtctccaa gtctggcacc tcagcctccc tggccatcag tgggctccgg 240
tccgaggacg aggctgatta ttattgtgca gcttgggatg acagcctgag tggttatgtc 300
ttcggaactg ggaccaaggt caccgtccta ggt 333
<210> 13
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 13
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gln Trp Gly Gly Val Leu Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 14
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 14
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ala Arg
20 25 30
Tyr Asp Val Gln Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Phe Gly Asn Asn Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Ser Ala Ser Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 15
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 15
gaggtccagc tggtacagtc tggggctgag gtgaagaagc ctggggcctc agtgaaggtt 60
tcctgcaagg catctggata caccttcacc agctactata tgcactgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggaata atcaacccta gtggtggtag cacaagctac 180
gcacagaagt tccagggcag agtcaccatg accagggaca cgtccacgag cacagtctac 240
atggagctga gcagcctgag atctgaggac acggccgtgt attactgtgc gcgctctcag 300
tggggtggtg ttctggatta ctggggtcaa ggtactctgg tgaccgtctc ctca 354
<210> 16
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 16
cagtctgtcg tgacgcagcc gccctcagtg tctggggccc cagggcagag ggtcaccatc 60
tcctgcagtg ggagcagctc caacatcggg gcacgttatg atgttcagtg gtaccagcag 120
cttccaggaa cagcccccaa actcctcatc tttggtaaca acaatcggcc ctcaggggtc 180
cctgaccgat tctctggctc caagtctggc acgtcagcct ccctggccat cactgggctc 240
caggctgagg atgaggctga ttattactgc cagtcctatg acagcagcct gagtgcttcg 300
gtgttcggcg gagggaccaa gctgaccgtc ctaggt 336
<210> 17
<211> 123
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 17
Gln Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Ile Pro Ile Leu Gly Ile Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Thr Gly Tyr Glu Ser Trp Gly Ser Tyr Glu Val Ile Asp Arg
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 18
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 18
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Arg Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 19
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 19
caggtgcagc tggtggagtc tggggctgag gtgaagaagc ctgggtcctc ggtgaaggtc 60
tcctgcaagg cttctggagg caccttcagc agctatgcta tcagctgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggaagg atcatcccta tccttggtat agcaaactac 180
gcacagaagt tccagggcag agtcacgatt accgcggacg aatccacgag cacagcctac 240
atggagctga gcagcctgag atctgaggac acggccgtat attactgtgc gcgcactggt 300
tacgaatctt ggggttctta cgaagttatc gatcgttggg gtcaaggtac tctggtgacc 360
gtctcctca 369
<210> 20
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 20
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agtaatactg taaactggta ccggcagctc 120
ccaggaacgg cccccaaact cctcatctat agtaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg acagcctgaa tggtgtggta 300
ttcggcggag ggaccaagct gaccgtccta ggt 333
<210> 21
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 21
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Ile Pro Ile Leu Gly Ile Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Tyr Tyr Ser His Asp Met Trp Ser Glu Asp Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 22
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 22
Leu Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Arg Ser Ser Asn Ile Gly Ser Asn
20 25 30
Ser Val Asn Trp Tyr Arg Gln Leu Pro Gly Ala Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Pro Gly Val Pro Val Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Thr Tyr Tyr Cys Ala Thr Trp Asp Asp Asn Leu
85 90 95
Asn Val His Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 23
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 23
caggtgcagc tggtgcagtc tggggctgag gtgaagaagc ctgggtcctc ggtgaaggtc 60
tcctgcaagg cttctggagg caccttcagc agctatgcta tcagctgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggaagg atcatcccta tccttggtat agcaaactac 180
gcacagaagt tccagggcag agtcacgatt accgcggaca aatccacgag cacagcctac 240
atggagctga gcagcctgag atctgaggac acggccgtgt attactgtgc gcgcggtggt 300
tactactctc atgacatgtg gtctgaagat tggggtcaag gtactctggt gaccgtctcc 360
tca 363
<210> 24
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 24
ctgcctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gacgcagttc caacatcggg agtaattctg ttaactggta tcgacaactc 120
ccaggagcgg cccccaaact cctcatctat agtaataatc agcggccccc aggggtccct 180
gtgcgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaagatg aggccactta ttactgtgca acatgggatg acaatctgaa tgttcactat 300
gtcttcggaa ctgggaccaa ggtcaccgtc ctaggt 336
<210> 25
<211> 125
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 25
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Gly Val Ser Gly Gly Ser Ile Ser Asn Ser
20 25 30
Asn Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Glu Ile Tyr His Ser Gly Ser Thr Lys Tyr Asn Pro Ser Leu
50 55 60
Arg Ser Arg Val Thr Ile Ser Val Asp Lys Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Asn Trp Lys Thr Pro Thr Thr Lys Ile Asp Gly Phe
100 105 110
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 26
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 26
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Ala Ser Leu Gly Ala
1 5 10 15
Ser Val Thr Leu Thr Cys Thr Leu Ser Ser Gly Tyr Ser Asn Tyr Lys
20 25 30
Val Asp Trp Tyr Gln Gln Arg Pro Gly Lys Gly Pro Arg Phe Val Met
35 40 45
Arg Val Gly Thr Gly Gly Ile Val Gly Ser Lys Gly Asp Gly Ile Pro
50 55 60
Asp Arg Phe Ser Val Leu Gly Ser Gly Leu Asn Arg Tyr Leu Thr Ile
65 70 75 80
Lys Asn Ile Gln Glu Glu Asp Glu Gly Asp Tyr His Cys Gly Ala Asp
85 90 95
His Gly Ser Gly Ser Asn Phe Val Tyr Val Phe Gly Thr Gly Thr Lys
100 105 110
Val Thr Val Leu Gly
115
<210> 27
<211> 375
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 27
caggtgcagc tgcaggagtc gggcccagga ctggtgaagc cttcggggac cctgtccctc 60
acctgcggtg tctctggtgg ctccatcagc aatagtaact ggtggagttg ggtccgccag 120
ccccccggga aggggctgga gtggattggg gaaatctatc atagtgggag caccaagtac 180
aacccgtccc tcaggagtcg agtcaccata tcagtagaca agtccaagaa ccagttctcc 240
ctaaaattga gctctgtgac cgccgcggac acggccgtat attactgtgc gagacgagat 300
aactggaaga cccccactac caaaattgat ggttttgata tctggggcca agggacaatg 360
gtcaccgtct cttca 375
<210> 28
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 28
cagcctgtgc tgactcagcc accttctgca tcagcctccc tgggagcctc ggtcacactc 60
acctgcaccc tgagcagcgg ctacagtaat tataaagtgg actggtacca gcagagacca 120
gggaagggcc cccggtttgt gatgcgagtg ggcactggtg ggattgtggg atccaagggg 180
gatggcatcc ctgatcgctt ctcagtcttg ggctcaggcc tgaatcggta cctgaccatc 240
aagaacatcc aggaagaaga tgagggtgac tatcactgtg gggcagacca tggcagtggg 300
agcaacttcg tgtatgtctt cggaactggg accaaggtca ccgtcctagg t 351
<210> 29
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 29
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gln Trp Gly Ser Ser Trp Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 30
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 30
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 31
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 31
caggtccagc tggtacagtc tggggctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggata caccttcacc ggctactata tgcactgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggatgg atcaacccta acagtggtgg cacaaactat 180
gcacagaagt ttcagggcag ggtcaccatg accagggaca cgtccatcag cacagcctac 240
atggagctga gcaggctgag atctgacgac acggccgtgt attactgtgc gcgctctcag 300
tggggttctt cttgggatta ctggggtcaa ggtactctgg tgaccgtctc ctca 354
<210> 32
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 32
gacatccagt tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc agctatttaa attggtatca gcagaaacca 120
gggaaagccc ctaagctcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagtg gcagtggatc tgggacagat ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agttacagta cccctccgac gttcggccaa 300
gggaccaagg tggagatcaa acgt 324
<210> 33
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 33
Glu Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Ser Tyr His Leu Tyr Gly Tyr Asp Ser Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 34
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 34
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Ala Ser Leu Gly Ala
1 5 10 15
Ser Val Thr Leu Thr Cys Thr Leu Ser Asn Asp Tyr Thr Asn Tyr Lys
20 25 30
Val Asp Trp Tyr Gln Gln Arg Pro Gly Lys Gly Pro Arg Phe Val Met
35 40 45
Arg Val Gly Pro Gly Gly Ile Val Gly Ser Lys Gly Asp Gly Ile Pro
50 55 60
Asp Arg Phe Ser Val Leu Gly Ser Gly Leu Asn Arg Tyr Leu Thr Ile
65 70 75 80
Lys Asn Ile Gln Glu Glu Asp Glu Ser Asp Tyr His Cys Gly Ala Asp
85 90 95
His Gly Thr Gly Ser Asn Phe Val Tyr Val Phe Gly Gly Gly Thr Lys
100 105 110
Leu Thr Val Leu Gly
115
<210> 35
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 35
gaggtgcagc tggtggagtc cggggctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggata caccttcacc ggctactata tgcactgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggatgg atcaacccta acagtggtgg cacaaactat 180
gcacagaagt ttcagggcag ggtcaccatg accagggaca cgtccatcag cacagcctac 240
atggagctga gcaggctgag atctgacgac acggccgtat attactgtgc gcgctcttct 300
taccatctgt acggttacga ttcttggggt caaggtactc tggtgaccgt ctcctca 357
<210> 36
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 36
cagcctgtgc tgactcagcc accttctgca tcagcctccc tgggagcctc ggtcactctc 60
acctgcaccc tgagcaacga ctacactaat tataaagtgg actggtacca gcagagacca 120
gggaagggcc cccggtttgt gatgcgagtg ggccctggtg ggattgtggg atccaagggg 180
gatggcatcc ctgatcgctt ctcagtcttg ggctcaggcc tgaatcgata cctgaccatc 240
aagaacatcc aggaggagga tgagagtgac taccactgtg gggcggacca tggcaccggg 300
agcaacttcg tgtacgtgtt cggcggaggg accaagctga ccgtcctagg t 351
<210> 37
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 37
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Ser Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Pro Trp Thr Trp Tyr Ser Pro Tyr Asp Gln Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 38
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 38
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Ala Ser Leu Gly Ala
1 5 10 15
Ser Val Thr Leu Thr Cys Thr Leu Ser Ser Gly Tyr Ser Asn Tyr Lys
20 25 30
Val Asp Trp Tyr Gln Gln Arg Pro Gly Lys Gly Pro Arg Phe Leu Met
35 40 45
Arg Val Asp Thr Gly Gly Ile Val Gly Ser Lys Gly Asp Gly Ile Pro
50 55 60
Asp Arg Phe Ser Val Ser Gly Ser Gly Leu Asn Arg Tyr Leu Thr Ile
65 70 75 80
Lys Asn Ile Gln Glu Glu Asp Glu Ser Asp Tyr His Cys Gly Ala Asp
85 90 95
His Gly Ser Gly Ser Asn Phe Val Trp Val Phe Gly Gly Gly Thr Lys
100 105 110
Leu Thr Val Leu Gly
115
<210> 39
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 39
caggtgcagc tggtgcagtc tggggctgag gtgaagaagc ctgggtcctc ggtgaaggtc 60
tcctgcaagg cttctggagg caccttcagc agctatgcta tcagctgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggaggg atcatcccta tctttagtac agcaaactac 180
gcacagaagt tccagggcag agtcaccatg accacagaca catccacgag cacagcctac 240
atggagctga ggagcctgag atctgacgac acggccgtgt attactgtgc gcgccagccg 300
tggacttggt actctccgta cgatcagtgg ggtcaaggta ctctggtgac cgtctcctca 360
<210> 40
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 40
cagcctgtgc tgactcagcc accttctgca tcagcctccc tgggagcctc ggtcacactc 60
acctgcaccc tgagcagcgg ctacagtaat tataaagtgg actggtatca acagagacca 120
gggaagggcc cccggtttct gatgcgagta gacaccggtg ggattgtggg atccaagggg 180
gatggcatcc ctgatcgctt ctcagtctcg ggctcaggtc tgaatcggta cctgaccatc 240
aagaacattc aggaagagga tgagagtgac taccactgtg gggcagacca tggcagtggg 300
agcaacttcg tgtgggtgtt cggcggaggg accaagctga ccgtcctagg t 351
<210> 41
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 41
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Thr Tyr
20 25 30
Ala Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Thr Pro Gly Gly Asp Arg Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Tyr Tyr Gly Tyr Met Ile Asp Met Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 42
<211> 113
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 42
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg
<210> 43
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 43
gaggtgcagc tggtggagac tgggggaggc ctggtacagc ctggggggtc cctgagactc 60
tcctgtgctg cctctggatt cacctttagc acctatgcca tgacctgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtctcagct attactcctg gtggtgatcg cacatactac 180
gcagactccg tgaagggccg tttcactatc tccagagaca attccaggaa cacgctgtat 240
ctgcaaatga acagcctgag agccgaggac acggccgtat attactgtgc gcgctactac 300
ggttacatga tcgatatgtg gggtcaaggt actctggtga ccgtctcctc a 351
<210> 44
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 44
gatgttgtga tgactcagtc tccactctcc ctgcccgtca cccctggaga gccggcctcc 60
atctcctgca ggtctagtca gagcctcctg catagtaatg gatacaacta tttggattgg 120
tacctgcaga agccagggca gtctccacag ctcctgatct atttgggttc taatcgggcc 180
tccggggtcc ctgacaggtt cagtggcagt ggatcaggca cagattttac actgaaaatc 240
agcagagtgg aggctgagga tgttggggtt tattactgca tgcaagctct acaaactcct 300
ctcactttcg gcggagggac caaggtggaa atcaaacgt 339
<210> 45
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 45
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Val His Trp Leu Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Asn Ala Gln Glu Phe
50 55 60
Gln Gly Arg Ile Thr Met Thr Arg Asp Thr Ser Ile Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gln Trp Gly Gly Thr Tyr Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 46
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 46
Ser Tyr Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Val Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Ala Ser Ala Ser Leu Ala Ile Ser Trp Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 47
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 47
cagatgcagc tggtgcagtc tggggctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggata caccttcacc ggctattatg tacactggtt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggttgg atcaacccta acagtggcgg cacaaacaat 180
gcacaggagt ttcaaggcag gatcaccatg accagggaca cgtccatcaa cacagcctac 240
atggagctga gcaggctgag atctgacgac acggccgtgt attactgtgc gcgctctcag 300
tggggtggta cttacgatta ctggggtcaa ggtactctgg tgaccgtctc ctca 354
<210> 48
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 48
tcctatgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agtaatactg taaactggta ccagcaggtc 120
ccaggaacgg cccccaaact cctcatctat agtaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcgcc tcagcctccc tggccatcag ttggctccag 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg acagcctgaa tggttgggtg 300
ttcggcggag ggaccaagct gaccgtccta ggt 333
<210> 49
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 49
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Asp Phe Thr Thr Tyr
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr Ser Pro Ser Val
50 55 60
Arg Gly Arg Val Thr Ile Ser Ala Asp Lys Ser Ile Asn Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Glu Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Met Trp Thr Phe Ser Gln Asp Gly Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 50
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 50
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Tyr
20 25 30
Thr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Phe Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 51
<211> 351
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 51
gaggtgcagc tggtgcagtc tggagcagag gtgaaaaagc cgggggagtc tctgaagatc 60
tcctgtaagg gttctggata tgactttacc acctactgga tcgggtgggt gcgccagatg 120
cccgggaagg gcctggagtg gatggggatc atctatcctg gtgactctga taccagatac 180
agcccgtccg tccgaggccg ggtcaccatc tcagccgaca agtccatcaa caccgcctat 240
ttgcagtgga gtagcctgga ggcctccgac accgccatgt attactgtgc gcgcatgtgg 300
actttctctc aggatggttg gggtcaaggt actctggtga ccgtctcctc a 351
<210> 52
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 52
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agttatactg taagctggta ccagcaactc 120
ccaggaacgg cccccaaatt cctcatctat tctaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 240
tctgaggatg aggctgatta ttactgtgct gcatgggatg acagcctgaa tggttatgtc 300
ttcggaactg ggaccaaggt caccgtccta ggt 333
<210> 53
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 53
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Met Lys Lys Pro Gly Ala
1 5 10 15
Ser Leu Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ile Asp Tyr
20 25 30
Tyr Val Tyr Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Ser Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Ser Gln Arg Asp Gly Tyr Met Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 54
<211> 105
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 54
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Ala Ser Pro Gly Gln
1 5 10 15
Ser Ile Ala Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Trp Tyr
20 25 30
Gln Gln His Pro Gly Lys Ala Pro Lys Leu Met Ile Tyr Glu Asp Ser
35 40 45
Lys Arg Pro Ser Gly Val Ser Asn Arg Phe Ser Gly Ser Lys Ser Gly
50 55 60
Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu Gln Ala Glu Asp Glu Ala
65 70 75 80
Asp Tyr Tyr Cys Ser Ser Asn Thr Arg Ser Ser Thr Leu Val Phe Gly
85 90 95
Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105
<210> 55
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 55
gaagtgcagc tggtgcagtc tggggctgag atgaagaagc ctggggcctc actgaagctc 60
tcctgcaagg cttctggata caccttcatc gactactatg tatactggat gcgacaggcc 120
cctggacaag ggcttgagtc catgggatgg atcaacccta acagtggtgg cacaaactat 180
gcacagaagt ttcagggcag ggtcaccatg accagggaca cgtccatcag cacagcctac 240
atggagctga gcaggctgag atctgacgac accgccatgt attactgtgc gcgctcccag 300
cgtgacggtt acatggatta ctggggtcaa ggtactctgg tgaccgtctc ctca 354
<210> 56
<211> 315
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 56
caatctgccc tgactcagcc tgcctccgtg tctgcgtctc ctggacagtc gatcgccatc 60
tcctgcactg gaaccagcag tgacgttggt tggtatcaac agcacccagg caaagccccc 120
aaactcatga tttatgagga cagtaagcgg ccctcagggg tttctaatcg cttctctggc 180
tccaagtctg gcaacacggc ctccctgacc atctctgggc tccaggctga ggacgaggct 240
gattattact gcagctcaaa tacaagaagc agcactttgg tgttcggcgg agggaccaag 300
ctgaccgtcc taggt 315
<210> 57
<211> 118
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 57
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Asp Arg Ile Thr Val Thr Arg Asp Thr Ser Ser Asn Thr Gly Tyr
65 70 75 80
Met Glu Leu Thr Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Pro Tyr Ser Gly Val Leu Asp Lys Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 58
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 58
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Phe Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Ser Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Ser Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 59
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 59
caggtccagc tggtacagtc tggggctgag gtgaagaagc ctggggcctc agtgaaggtc 60
tcctgcaagg cttctggata caccttcacc gactactata tgcactgggt gcgacaggcc 120
cctggacaac ggcttgagtg gatgggatgg atcaacccta acagtggtgg cacaaactat 180
gcacagaagt ttcaggacag gatcaccgtg accagggaca cctccagcaa cacaggctac 240
atggagctga ccaggctgag atctgacgac acggccgtgt attactgtgc gcgctctccg 300
tactctggtg ttctggataa atggggtcaa ggtactctgg tgaccgtctc ctca 354
<210> 60
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 60
cagtctgtgc tgacgcagcc gccctcagtg tctggggccc cagggcagag ggtcaccatc 60
tcctgcactg ggagcagctc caacatcggg gcaggttttg atgtacactg gtaccagcag 120
cttccaggaa cagcccccaa actcctcatc tatggtaaca gcaatcggcc ctcaggggtc 180
cctgaccgat tctctggctc caagtctggc acctcagcct ccctggccat cactgggctc 240
caggctgagg atgaggctga ttattactgc cagtcctatg acagcagcct gagtggttat 300
gtcttcggaa ctgggaccaa ggtcaccgtc ctaggt 336
<210> 61
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 61
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Ile Pro Ile Leu Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Gly Tyr Gly Ser Tyr Arg Trp Glu Asp Ser Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 62
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 62
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Tyr Val Phe Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Ser Ala Ser Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
<210> 63
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 63
caggtgcagc tggtgcagtc tggggctgag gtgaagaagc ctgggtcctc ggtgaaggtc 60
tcctgcaagg cttctggagg caccttcagc agctatgcta tcagctgggt gcgacaggcc 120
cctggacaag ggcttgagtg gatgggaagg atcatcccta tccttggtac agcaaactac 180
gcacagaagt tccagggcag agtcacgatt accgcggacg aatccacgag cacagcctac 240
atggagctga gcagcctgag atctgaggac acggccgtgt attactgtgc gcgctctggt 300
tacggttctt accgttggga agattcttgg ggtcaaggta ctctggtgac cgtctcctca 360
<210> 64
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 64
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 60
tcttgttctg gaagcagctc caacatcgga agtaattacg tattctggta ccagcagctc 120
ccaggaacgg cccccaaact cctcatctat agtaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccgg 240
tccgaggatg aggctgatta ttactgtgca gcatgggatg acagcctgag tgcctcttat 300
gttttcggaa ctgggaccaa ggtcaccgtc ctaggt 336
<210> 65
<211> 116
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 65
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Tyr Ser Gly Ser Phe Asp Asn Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 66
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 66
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Met Ser Cys Ser Gly Thr Ser Ser Asn Ile Gly Ser His
20 25 30
Ser Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
<210> 67
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 67
gaggtgcagc tggtgcagtc tggagcagag gtgaaaaagc ccggggagtc tctgaagatc 60
tcctgtaagg gttctggata cagctttacc agctactgga tcggctgggt gcgccagatg 120
cccgggaaag gcctggagtg gatggggatc atctatcctg gtgactctga taccagatac 180
agcccgtcct tccaaggcca cgtcaccatc tcagctgaca agtccatcag cactgcctac 240
ctgcagtgga gcagcctgaa ggcctcggac accgccatgt attactgtgc gcgctactct 300
ggttctttcg ataactgggg tcaaggtact ctggtgaccg tctcctca 348
<210> 68
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 68
tcctatgagc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatg 60
tcttgttctg gaaccagctc caacatcgga agtcactctg taaactggta ccagcagctc 120
ccaggaacgg cccccaaact cctcatctat actaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tggcctccag 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg gcagcctgaa tggtctggta 300
ttcggcggag ggaccaagct gaccgtccta ggt 333
<210> 69
<211> 21
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 69
Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
1 5 10 15
Ser Leu Glu Met Ala
20
<210> 70
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
олигонуклеотид
<400> 70
tctagaggtg gtggtggtag cggcggcggc ggctctggtg gtggtggatc cctcgagatg 60
gcc 63
<210> 71
<211> 184
<212> БЕЛОК
<213> Homo sapiens
<400> 71
Met Leu Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser
1 5 10 15
Leu Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr
20 25 30
Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser
35 40 45
Val Lys Gly Thr Asn Ala Ile Leu Trp Thr Cys Leu Gly Leu Ser Leu
50 55 60
Ile Ile Ser Leu Ala Val Phe Val Leu Met Phe Leu Leu Arg Lys Ile
65 70 75 80
Asn Ser Glu Pro Leu Lys Asp Glu Phe Lys Asn Thr Gly Ser Gly Leu
85 90 95
Leu Gly Met Ala Asn Ile Asp Leu Glu Lys Ser Arg Thr Gly Asp Glu
100 105 110
Ile Ile Leu Pro Arg Gly Leu Glu Tyr Thr Val Glu Glu Cys Thr Cys
115 120 125
Glu Asp Cys Ile Lys Ser Lys Pro Lys Val Asp Ser Asp His Cys Phe
130 135 140
Pro Leu Pro Ala Met Glu Glu Gly Ala Thr Ile Leu Val Thr Thr Lys
145 150 155 160
Thr Asn Asp Tyr Cys Lys Ser Leu Pro Ala Ala Leu Ser Ala Thr Glu
165 170 175
Ile Glu Lys Ser Ile Ser Ala Arg
180
<210> 72
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 72
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Val Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly His Asn
20 25 30
Asp Val Ser Trp Tyr Gln His Leu Pro Gly Lys Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Phe Asp Asp Leu Leu Pro Ser Gly Val Ser Asp Arg Phe Ser
50 55 60
Ala Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Ala Phe Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly Ser
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Glu Met Ala Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val
130 135 140
Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser
145 150 155 160
Val Ser Ser Asn Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser
165 170 175
Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr
180 185 190
Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp
195 200 205
Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu
210 215 220
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gln Gly Tyr Ser Tyr Tyr Gly
225 230 235 240
Tyr Ser Asp Val Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250 255
<210> 73
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 73
Gln Pro Val Leu Thr Gln Pro Pro Ser Val Ser Glu Ala Pro Arg Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Asn Asn
20 25 30
Ala Val Asn Trp Tyr Gln Gln Leu Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Phe Asp Asp Leu Leu Ser Ser Gly Val Ser Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly Ser
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Glu Met Ala Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val
130 135 140
Lys Pro Ser Gln Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser
145 150 155 160
Val Ser Ser Asn Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser
165 170 175
Arg Gly Leu Glu Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr
180 185 190
Asn Asp Tyr Ala Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp
195 200 205
Thr Ser Lys Asn Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu
210 215 220
Asp Thr Ala Val Tyr Tyr Cys Ala Arg Tyr Gly Phe Ser Gly Ser Arg
225 230 235 240
Phe Tyr Asp Thr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250 255
<210> 74
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 74
Leu Pro Val Leu Thr Gln Pro Pro Ser Thr Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Val Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Val Val Phe Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Val
35 40 45
Ile Tyr Arg Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Val Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Ser Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly Ser
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Glu Met Ala Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
145 150 155 160
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Ile Pro Ile Leu Gly Ile Ala Asn Tyr
180 185 190
Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Glu Asp Thr Ser Thr
195 200 205
Asp Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
210 215 220
Val Tyr Tyr Cys Ala Arg Ser Gly Tyr Ser Lys Ser Ile Val Ser Tyr
225 230 235 240
Met Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250
<210> 75
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 75
Gln Ser Val Val Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ala Arg
20 25 30
Tyr Asp Val Gln Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Phe Gly Asn Asn Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Ser Ala Ser Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly
100 105 110
Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Leu Glu Met Ala Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val
130 135 140
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
145 150 155 160
Thr Phe Thr Ser Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
165 170 175
Gly Leu Glu Trp Met Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser
180 185 190
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser
195 200 205
Thr Ser Thr Val Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ala Arg Ser Gln Trp Gly Gly Val Leu Asp Tyr
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250
<210> 76
<211> 255
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 76
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Arg Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Ser
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Glu Met Ala Gln Val Gln Leu Val Glu Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr
145 150 155 160
Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly
165 170 175
Leu Glu Trp Met Gly Arg Ile Ile Pro Ile Leu Gly Ile Ala Asn Tyr
180 185 190
Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr
195 200 205
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
210 215 220
Val Tyr Tyr Cys Ala Arg Thr Gly Tyr Glu Ser Trp Gly Ser Tyr Glu
225 230 235 240
Val Ile Asp Arg Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250 255
<210> 77
<211> 254
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 77
Leu Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Arg Ser Ser Asn Ile Gly Ser Asn
20 25 30
Ser Val Asn Trp Tyr Arg Gln Leu Pro Gly Ala Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Pro Gly Val Pro Val Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Thr Tyr Tyr Cys Ala Thr Trp Asp Asp Asn Leu
85 90 95
Asn Val His Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Leu Glu Met Ala Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
130 135 140
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
145 150 155 160
Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
165 170 175
Gly Leu Glu Trp Met Gly Arg Ile Ile Pro Ile Leu Gly Ile Ala Asn
180 185 190
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser
195 200 205
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ala Arg Gly Gly Tyr Tyr Ser His Asp Met Trp
225 230 235 240
Ser Glu Asp Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250
<210> 78
<211> 263
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 78
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Ala Ser Leu Gly Ala
1 5 10 15
Ser Val Thr Leu Thr Cys Thr Leu Ser Ser Gly Tyr Ser Asn Tyr Lys
20 25 30
Val Asp Trp Tyr Gln Gln Arg Pro Gly Lys Gly Pro Arg Phe Val Met
35 40 45
Arg Val Gly Thr Gly Gly Ile Val Gly Ser Lys Gly Asp Gly Ile Pro
50 55 60
Asp Arg Phe Ser Val Leu Gly Ser Gly Leu Asn Arg Tyr Leu Thr Ile
65 70 75 80
Lys Asn Ile Gln Glu Glu Asp Glu Gly Asp Tyr His Cys Gly Ala Asp
85 90 95
His Gly Ser Gly Ser Asn Phe Val Tyr Val Phe Gly Thr Gly Thr Lys
100 105 110
Val Thr Val Leu Gly Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Leu Glu Met Ala Gln Val Gln Leu Gln Glu
130 135 140
Ser Gly Pro Gly Leu Val Lys Pro Ser Gly Thr Leu Ser Leu Thr Cys
145 150 155 160
Gly Val Ser Gly Gly Ser Ile Ser Asn Ser Asn Trp Trp Ser Trp Val
165 170 175
Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Glu Ile Tyr His
180 185 190
Ser Gly Ser Thr Lys Tyr Asn Pro Ser Leu Arg Ser Arg Val Thr Ile
195 200 205
Ser Val Asp Lys Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val
210 215 220
Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Arg Asp Asn Trp
225 230 235 240
Lys Thr Pro Thr Thr Lys Ile Asp Gly Phe Asp Ile Trp Gly Gln Gly
245 250 255
Thr Met Val Thr Val Ser Ser
260
<210> 79
<211> 247
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 79
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Ser Arg Gly Gly
100 105 110
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Leu Glu Met
115 120 125
Ala Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
130 135 140
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly
145 150 155 160
Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
165 170 175
Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys
180 185 190
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala
195 200 205
Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr
210 215 220
Cys Ala Arg Ser Gln Trp Gly Ser Ser Trp Asp Tyr Trp Gly Gln Gly
225 230 235 240
Thr Leu Val Thr Val Ser Ser
245
<210> 80
<211> 257
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 80
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Ala Ser Leu Gly Ala
1 5 10 15
Ser Val Thr Leu Thr Cys Thr Leu Ser Asn Asp Tyr Thr Asn Tyr Lys
20 25 30
Val Asp Trp Tyr Gln Gln Arg Pro Gly Lys Gly Pro Arg Phe Val Met
35 40 45
Arg Val Gly Pro Gly Gly Ile Val Gly Ser Lys Gly Asp Gly Ile Pro
50 55 60
Asp Arg Phe Ser Val Leu Gly Ser Gly Leu Asn Arg Tyr Leu Thr Ile
65 70 75 80
Lys Asn Ile Gln Glu Glu Asp Glu Ser Asp Tyr His Cys Gly Ala Asp
85 90 95
His Gly Thr Gly Ser Asn Phe Val Tyr Val Phe Gly Gly Gly Thr Lys
100 105 110
Leu Thr Val Leu Gly Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Leu Glu Met Ala Glu Val Gln Leu Val Glu
130 135 140
Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys
145 150 155 160
Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Met His Trp Val Arg
165 170 175
Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn Pro Asn
180 185 190
Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met
195 200 205
Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr Met Glu Leu Ser Arg Leu
210 215 220
Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Ser Tyr His
225 230 235 240
Leu Tyr Gly Tyr Asp Ser Trp Gly Gln Gly Thr Leu Val Thr Val Ser
245 250 255
Ser
<210> 81
<211> 258
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 81
Gln Pro Val Leu Thr Gln Pro Pro Ser Ala Ser Ala Ser Leu Gly Ala
1 5 10 15
Ser Val Thr Leu Thr Cys Thr Leu Ser Ser Gly Tyr Ser Asn Tyr Lys
20 25 30
Val Asp Trp Tyr Gln Gln Arg Pro Gly Lys Gly Pro Arg Phe Leu Met
35 40 45
Arg Val Asp Thr Gly Gly Ile Val Gly Ser Lys Gly Asp Gly Ile Pro
50 55 60
Asp Arg Phe Ser Val Ser Gly Ser Gly Leu Asn Arg Tyr Leu Thr Ile
65 70 75 80
Lys Asn Ile Gln Glu Glu Asp Glu Ser Asp Tyr His Cys Gly Ala Asp
85 90 95
His Gly Ser Gly Ser Asn Phe Val Trp Val Phe Gly Gly Gly Thr Lys
100 105 110
Leu Thr Val Leu Gly Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Gly Gly Gly Gly Ser Leu Glu Met Ala Gln Val Gln Leu Val Gln
130 135 140
Ser Gly Ala Glu Val Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys
145 150 155 160
Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg
165 170 175
Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Ile Pro Ile
180 185 190
Phe Ser Thr Ala Asn Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Met
195 200 205
Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr Met Glu Leu Arg Ser Leu
210 215 220
Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys Ala Arg Gln Pro Trp Thr
225 230 235 240
Trp Tyr Ser Pro Tyr Asp Gln Trp Gly Gln Gly Thr Leu Val Thr Val
245 250 255
Ser Ser
<210> 82
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 82
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
115 120 125
Gly Ser Leu Glu Met Ala Glu Val Gln Leu Val Glu Thr Gly Gly Gly
130 135 140
Leu Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
145 150 155 160
Phe Thr Phe Ser Thr Tyr Ala Met Thr Trp Val Arg Gln Ala Pro Gly
165 170 175
Lys Gly Leu Glu Trp Val Ser Ala Ile Thr Pro Gly Gly Asp Arg Thr
180 185 190
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn
195 200 205
Ser Arg Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp
210 215 220
Thr Ala Val Tyr Tyr Cys Ala Arg Tyr Tyr Gly Tyr Met Ile Asp Met
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250
<210> 83
<211> 250
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 83
Ser Tyr Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Thr Val Asn Trp Tyr Gln Gln Val Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Ala Ser Ala Ser Leu Ala Ile Ser Trp Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Ser
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Glu Met Ala Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr
145 150 155 160
Phe Thr Gly Tyr Tyr Val His Trp Leu Arg Gln Ala Pro Gly Gln Gly
165 170 175
Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn Asn
180 185 190
Ala Gln Glu Phe Gln Gly Arg Ile Thr Met Thr Arg Asp Thr Ser Ile
195 200 205
Asn Thr Ala Tyr Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala
210 215 220
Val Tyr Tyr Cys Ala Arg Ser Gln Trp Gly Gly Thr Tyr Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250
<210> 84
<211> 249
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 84
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Tyr
20 25 30
Thr Val Ser Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Phe Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Asn Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly Ser
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Glu Met Ala Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Asp
145 150 155 160
Phe Thr Thr Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr
180 185 190
Ser Pro Ser Val Arg Gly Arg Val Thr Ile Ser Ala Asp Lys Ser Ile
195 200 205
Asn Thr Ala Tyr Leu Gln Trp Ser Ser Leu Glu Ala Ser Asp Thr Ala
210 215 220
Met Tyr Tyr Cys Ala Arg Met Trp Thr Phe Ser Gln Asp Gly Trp Gly
225 230 235 240
Gln Gly Thr Leu Val Thr Val Ser Ser
245
<210> 85
<211> 244
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 85
Gln Ser Ala Leu Thr Gln Pro Ala Ser Val Ser Ala Ser Pro Gly Gln
1 5 10 15
Ser Ile Ala Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Trp Tyr
20 25 30
Gln Gln His Pro Gly Lys Ala Pro Lys Leu Met Ile Tyr Glu Asp Ser
35 40 45
Lys Arg Pro Ser Gly Val Ser Asn Arg Phe Ser Gly Ser Lys Ser Gly
50 55 60
Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu Gln Ala Glu Asp Glu Ala
65 70 75 80
Asp Tyr Tyr Cys Ser Ser Asn Thr Arg Ser Ser Thr Leu Val Phe Gly
85 90 95
Gly Gly Thr Lys Leu Thr Val Leu Gly Ser Arg Gly Gly Gly Gly Ser
100 105 110
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Leu Glu Met Ala Glu Val
115 120 125
Gln Leu Val Gln Ser Gly Ala Glu Met Lys Lys Pro Gly Ala Ser Leu
130 135 140
Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ile Asp Tyr Tyr Val
145 150 155 160
Tyr Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Ser Met Gly Trp
165 170 175
Ile Asn Pro Asn Ser Gly Gly Thr Asn Tyr Ala Gln Lys Phe Gln Gly
180 185 190
Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr Met Glu
195 200 205
Leu Ser Arg Leu Arg Ser Asp Asp Thr Ala Met Tyr Tyr Cys Ala Arg
210 215 220
Ser Gln Arg Asp Gly Tyr Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
225 230 235 240
Thr Val Ser Ser
<210> 86
<211> 251
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 86
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly
20 25 30
Phe Asp Val His Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu
35 40 45
Leu Ile Tyr Gly Asn Ser Asn Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser Tyr Asp Ser Ser
85 90 95
Leu Ser Gly Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Leu Glu Met Ala Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
130 135 140
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
145 150 155 160
Thr Phe Thr Asp Tyr Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln
165 170 175
Arg Leu Glu Trp Met Gly Trp Ile Asn Pro Asn Ser Gly Gly Thr Asn
180 185 190
Tyr Ala Gln Lys Phe Gln Asp Arg Ile Thr Val Thr Arg Asp Thr Ser
195 200 205
Ser Asn Thr Gly Tyr Met Glu Leu Thr Arg Leu Arg Ser Asp Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ala Arg Ser Pro Tyr Ser Gly Val Leu Asp Lys
225 230 235 240
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250
<210> 87
<211> 253
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 87
Gln Ala Val Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ser Asn
20 25 30
Tyr Val Phe Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Arg
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Ser Leu
85 90 95
Ser Ala Ser Tyr Val Phe Gly Thr Gly Thr Lys Val Thr Val Leu Gly
100 105 110
Ser Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
115 120 125
Ser Leu Glu Met Ala Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
130 135 140
Lys Lys Pro Gly Ser Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly
145 150 155 160
Thr Phe Ser Ser Tyr Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
165 170 175
Gly Leu Glu Trp Met Gly Arg Ile Ile Pro Ile Leu Gly Thr Ala Asn
180 185 190
Tyr Ala Gln Lys Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser
195 200 205
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
210 215 220
Ala Val Tyr Tyr Cys Ala Arg Ser Gly Tyr Gly Ser Tyr Arg Trp Glu
225 230 235 240
Asp Ser Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
245 250
<210> 88
<211> 248
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 88
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Ala Ser Gly Thr Pro Gly Gln
1 5 10 15
Arg Val Thr Met Ser Cys Ser Gly Thr Ser Ser Asn Ile Gly Ser His
20 25 30
Ser Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Thr Asn Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser
50 55 60
Gly Ser Lys Ser Gly Thr Ser Ala Ser Leu Ala Ile Ser Gly Leu Gln
65 70 75 80
Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Gly Ser Leu
85 90 95
Asn Gly Leu Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Ser
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Glu Met Ala Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys
130 135 140
Lys Pro Gly Glu Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser
145 150 155 160
Phe Thr Ser Tyr Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly
165 170 175
Leu Glu Trp Met Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr
180 185 190
Ser Pro Ser Phe Gln Gly His Val Thr Ile Ser Ala Asp Lys Ser Ile
195 200 205
Ser Thr Ala Tyr Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala
210 215 220
Met Tyr Tyr Cys Ala Arg Tyr Ser Gly Ser Phe Asp Asn Trp Gly Gln
225 230 235 240
Gly Thr Leu Val Thr Val Ser Ser
245
<210> 89
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 89
Val Ser Ser Asn Ser Ala Ala Trp Asn
1 5
<210> 90
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 90
Tyr Arg Ser Lys Trp Tyr Asn
1 5
<210> 91
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 91
Ala Arg Gln Gly Tyr Ser Tyr Tyr Gly Tyr Ser Asp Val
1 5 10
<210> 92
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 92
Ser Ser Asn Ile Gly His Asn Asp
1 5
<210> 93
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 93
Phe Asp Asp
1
<210> 94
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 94
Ala Ala Trp Asp Gly Ser Leu Asn Ala Phe Val
1 5 10
<210> 95
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 95
Val Ser Ser Asn Ser Ala Ala Trp Asn
1 5
<210> 96
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 96
Tyr Arg Ser Lys Trp Tyr Asn
1 5
<210> 97
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 97
Ala Arg Tyr Gly Phe Ser Gly Ser Arg Phe Tyr Asp Thr
1 5 10
<210> 98
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 98
Ser Ser Asn Ile Gly Asn Asn Ala
1 5
<210> 99
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 99
Phe Asp Asp
1
<210> 100
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 100
Ala Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val
1 5 10
<210> 101
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 101
Gly Gly Thr Phe Ser Ser Tyr Ala
1 5
<210> 102
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 102
Ile Ile Pro Ile Leu Gly Ile Ala
1 5
<210> 103
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 103
Ala Arg Ser Gly Tyr Ser Lys Ser Ile Val Ser Tyr Met Asp Tyr
1 5 10 15
<210> 104
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 104
Ser Ser Asn Ile Gly Ser Asn Val
1 5
<210> 105
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 105
Arg Asn Asn
1
<210> 106
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 106
Ala Ala Trp Asp Asp Ser Leu Ser Gly Tyr Val
1 5 10
<210> 107
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 107
Gly Tyr Thr Phe Thr Ser Tyr Tyr
1 5
<210> 108
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 108
Ile Asn Pro Ser Gly Gly Ser Thr
1 5
<210> 109
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 109
Ala Arg Ser Gln Trp Gly Gly Val Leu Asp Tyr
1 5 10
<210> 110
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 110
Ser Ser Asn Ile Gly Ala Arg Tyr Asp
1 5
<210> 111
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 111
Gly Asn Asn
1
<210> 112
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 112
Gln Ser Tyr Asp Ser Ser Leu Ser Ala Ser Val
1 5 10
<210> 113
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 113
Gly Gly Thr Phe Ser Ser Tyr Ala
1 5
<210> 114
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 114
Ile Ile Pro Ile Leu Gly Ile Ala
1 5
<210> 115
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 115
Ala Arg Thr Gly Tyr Glu Ser Trp Gly Ser Tyr Glu Val Ile Asp Arg
1 5 10 15
<210> 116
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 116
Ser Ser Asn Ile Gly Ser Asn Thr
1 5
<210> 117
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 117
Ser Asn Asn
1
<210> 118
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 118
Ala Ala Trp Asp Asp Ser Leu Asn Gly Val Val
1 5 10
<210> 119
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 119
Gly Gly Thr Phe Ser Ser Tyr Ala
1 5
<210> 120
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 120
Ile Ile Pro Ile Leu Gly Ile Ala
1 5
<210> 121
<211> 14
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 121
Ala Arg Gly Gly Tyr Tyr Ser His Asp Met Trp Ser Glu Asp
1 5 10
<210> 122
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 122
Ser Ser Asn Ile Gly Ser Asn Ser
1 5
<210> 123
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 123
Ser Asn Asn
1
<210> 124
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 124
Ala Thr Trp Asp Asp Asn Leu Asn Val His Tyr Val
1 5 10
<210> 125
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 125
Gly Gly Ser Ile Ser Asn Ser Asn Trp
1 5
<210> 126
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 126
Ile Tyr His Ser Gly Ser Thr
1 5
<210> 127
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 127
Ala Arg Arg Asp Asn Trp Lys Thr Pro Thr Thr Lys Ile Asp Gly Phe
1 5 10 15
Asp Ile
<210> 128
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 128
Ser Gly Tyr Ser Asn Tyr Lys
1 5
<210> 129
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 129
Val Gly Thr Gly Gly Ile Val Gly
1 5
<210> 130
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 130
Gly Ala Asp His Gly Ser Gly Ser Asn Phe Val Tyr Val
1 5 10
<210> 131
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 131
Gly Tyr Thr Phe Thr Gly Tyr Tyr
1 5
<210> 132
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 132
Ile Asn Pro Asn Ser Gly Gly Thr
1 5
<210> 133
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 133
Ala Arg Ser Gln Trp Gly Ser Ser Trp Asp Tyr
1 5 10
<210> 134
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 134
Gln Ser Ile Ser Ser Tyr
1 5
<210> 135
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 135
Ala Ala Ser
1
<210> 136
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 136
Gln Gln Ser Tyr Ser Thr Pro Pro Thr
1 5
<210> 137
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 137
Gly Tyr Thr Phe Thr Gly Tyr Tyr
1 5
<210> 138
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 138
Ile Asn Pro Asn Ser Gly Gly Thr
1 5
<210> 139
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 139
Ala Arg Ser Ser Tyr His Leu Tyr Gly Tyr Asp Ser
1 5 10
<210> 140
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 140
Asn Asp Tyr Thr Asn Tyr Lys
1 5
<210> 141
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 141
Val Gly Pro Gly Gly Ile Val Gly
1 5
<210> 142
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 142
Gly Ala Asp His Gly Thr Gly Ser Asn Phe Val Tyr Val
1 5 10
<210> 143
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 143
Gly Gly Thr Phe Ser Ser Tyr Ala
1 5
<210> 144
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 144
Ile Ile Pro Ile Phe Ser Thr Ala
1 5
<210> 145
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 145
Ala Arg Gln Pro Trp Thr Trp Tyr Ser Pro Tyr Asp Gln
1 5 10
<210> 146
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 146
Ser Gly Tyr Ser Asn Tyr Lys
1 5
<210> 147
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 147
Val Asp Thr Gly Gly Ile Val Gly
1 5
<210> 148
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 148
Gly Ala Asp His Gly Ser Gly Ser Asn Phe Val Trp Val
1 5 10
<210> 149
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 149
Gly Phe Thr Phe Ser Thr Tyr Ala
1 5
<210> 150
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 150
Ile Thr Pro Gly Gly Asp Arg Thr
1 5
<210> 151
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 151
Ala Arg Tyr Tyr Gly Tyr Met Ile Asp Met
1 5 10
<210> 152
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 152
Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr
1 5 10
<210> 153
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 153
Leu Gly Ser
1
<210> 154
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 154
Met Gln Ala Leu Gln Thr Pro Leu Thr
1 5
<210> 155
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 155
Gly Tyr Thr Phe Thr Gly Tyr Tyr
1 5
<210> 156
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 156
Ile Asn Pro Asn Ser Gly Gly Thr
1 5
<210> 157
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 157
Ala Arg Ser Gln Trp Gly Gly Thr Tyr Asp Tyr
1 5 10
<210> 158
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 158
Ser Ser Asn Ile Gly Ser Asn Thr
1 5
<210> 159
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 159
Ser Asn Asn
1
<210> 160
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 160
Ala Ala Trp Asp Asp Ser Leu Asn Gly Trp Val
1 5 10
<210> 161
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 161
Gly Tyr Asp Phe Thr Thr Tyr Trp
1 5
<210> 162
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 162
Ile Tyr Pro Gly Asp Ser Asp Thr
1 5
<210> 163
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 163
Ala Arg Met Trp Thr Phe Ser Gln Asp Gly
1 5 10
<210> 164
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 164
Ser Ser Asn Ile Gly Ser Tyr Thr
1 5
<210> 165
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 165
Ser Asn Asn
1
<210> 166
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 166
Ala Ala Trp Asp Asp Ser Leu Asn Gly Tyr Val
1 5 10
<210> 167
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 167
Gly Tyr Thr Phe Ile Asp Tyr Tyr
1 5
<210> 168
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 168
Ile Asn Pro Asn Ser Gly Gly Thr
1 5
<210> 169
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 169
Ala Arg Ser Gln Arg Asp Gly Tyr Met Asp Tyr
1 5 10
<210> 170
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 170
Ile Ser Cys Thr Gly Thr Ser Ser Asp
1 5
<210> 171
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 171
Glu Asp Ser
1
<210> 172
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 172
Ser Ser Asn Thr Arg Ser Ser Thr Leu Val
1 5 10
<210> 173
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 173
Gly Tyr Thr Phe Thr Asp Tyr Tyr
1 5
<210> 174
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 174
Ile Asn Pro Asn Ser Gly Gly Thr
1 5
<210> 175
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 175
Ala Arg Ser Pro Tyr Ser Gly Val Leu Asp Lys
1 5 10
<210> 176
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 176
Ser Ser Asn Ile Gly Ala Gly Phe Asp
1 5
<210> 177
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 177
Gly Asn Ser
1
<210> 178
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 178
Gln Ser Tyr Asp Ser Ser Leu Ser Gly Tyr Val
1 5 10
<210> 179
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 179
Gly Gly Thr Phe Ser Ser Tyr Ala
1 5
<210> 180
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 180
Ile Ile Pro Ile Leu Gly Thr Ala
1 5
<210> 181
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 181
Ala Arg Ser Gly Tyr Gly Ser Tyr Arg Trp Glu Asp Ser
1 5 10
<210> 182
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 182
Ser Ser Asn Ile Gly Ser Asn Tyr
1 5
<210> 183
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 183
Ser Asn Asn
1
<210> 184
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 184
Ala Ala Trp Asp Asp Ser Leu Ser Ala Ser Tyr Val
1 5 10
<210> 185
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 185
Gly Tyr Ser Phe Thr Ser Tyr Trp
1 5
<210> 186
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 186
Ile Tyr Pro Gly Asp Ser Asp Thr
1 5
<210> 187
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 187
Ala Arg Tyr Ser Gly Ser Phe Asp Asn
1 5
<210> 188
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 188
Ser Ser Asn Ile Gly Ser His Ser
1 5
<210> 189
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 189
Thr Asn Asn
1
<210> 190
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 190
Ala Ala Trp Asp Gly Ser Leu Asn Gly Leu Val
1 5 10
<210> 191
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 191
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg
20
<210> 192
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
олигонуклеотид
<400> 192
atggctctcc cagtgactgc cctactgctt cccctagcgc ttctcctgca tgcagctcgt 60
<210> 193
<211> 220
<212> БЕЛОК
<213> Homo sapiens
<400> 193
Met Leu Arg Leu Leu Leu Ala Leu Asn Leu Phe Pro Ser Ile Gln Val
1 5 10 15
Thr Gly Asn Lys Ile Leu Val Lys Gln Ser Pro Met Leu Val Ala Tyr
20 25 30
Asp Asn Ala Val Asn Leu Ser Cys Lys Tyr Ser Tyr Asn Leu Phe Ser
35 40 45
Arg Glu Phe Arg Ala Ser Leu His Lys Gly Leu Asp Ser Ala Val Glu
50 55 60
Val Cys Val Val Tyr Gly Asn Tyr Ser Gln Gln Leu Gln Val Tyr Ser
65 70 75 80
Lys Thr Gly Phe Asn Cys Asp Gly Lys Leu Gly Asn Glu Ser Val Thr
85 90 95
Phe Tyr Leu Gln Asn Leu Tyr Val Asn Gln Thr Asp Ile Tyr Phe Cys
100 105 110
Lys Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser
115 120 125
Asn Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro
130 135 140
Leu Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly
145 150 155 160
Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile
165 170 175
Phe Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met
180 185 190
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
195 200 205
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser
210 215 220
<210> 194
<211> 321
<212> ДНК
<213> Homo sapiens
<400> 194
attgaagtta tgtatcctcc tccttaccta gacaatgaga agagcaatgg aaccattatc 60
catgtgaaag ggaaacacct ttgtccaagt cccctatttc ccggaccttc taagcccttt 120
tgggtgctgg tggtggttgg tggagtcctg gcttgctata gcttgctagt aacagtggcc 180
tttattattt tctgggtgag gagtaagagg agcaggctcc tgcacagtga ctacatgaac 240
atgactcccc gccgccccgg gcccacccgc aagcattacc agccctatgc cccaccacgc 300
gacttcgcag cctatcgctc c 321
<210> 195
<211> 163
<212> БЕЛОК
<213> Homo sapiens
<400> 195
Met Lys Trp Lys Ala Leu Phe Thr Ala Ala Ile Leu Gln Ala Gln Leu
1 5 10 15
Pro Ile Thr Glu Ala Gln Ser Phe Gly Leu Leu Asp Pro Lys Leu Cys
20 25 30
Tyr Leu Leu Asp Gly Ile Leu Phe Ile Tyr Gly Val Ile Leu Thr Ala
35 40 45
Leu Phe Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
50 55 60
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
65 70 75 80
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
85 90 95
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
100 105 110
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
115 120 125
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
130 135 140
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
145 150 155 160
Pro Pro Arg
<210> 196
<211> 339
<212> ДНК
<213> Homo sapiens
<400> 196
agagtgaagt tcagcaggag cgcagacgcc cccgcgtacc agcagggcca gaaccagctc 60
tataacgagc tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc 120
cgggaccctg agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgtacaat 180
gaactgcaga aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc 240
cggaggggca aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc 300
tacgacgccc ttcacatgca ggccctgccc cctcgctaa 339
<210> 197
<211> 255
<212> БЕЛОК
<213> Homo sapiens
<400> 197
Met Gly Asn Ser Cys Tyr Asn Ile Val Ala Thr Leu Leu Leu Val Leu
1 5 10 15
Asn Phe Glu Arg Thr Arg Ser Leu Gln Asp Pro Cys Ser Asn Cys Pro
20 25 30
Ala Gly Thr Phe Cys Asp Asn Asn Arg Asn Gln Ile Cys Ser Pro Cys
35 40 45
Pro Pro Asn Ser Phe Ser Ser Ala Gly Gly Gln Arg Thr Cys Asp Ile
50 55 60
Cys Arg Gln Cys Lys Gly Val Phe Arg Thr Arg Lys Glu Cys Ser Ser
65 70 75 80
Thr Ser Asn Ala Glu Cys Asp Cys Thr Pro Gly Phe His Cys Leu Gly
85 90 95
Ala Gly Cys Ser Met Cys Glu Gln Asp Cys Lys Gln Gly Gln Glu Leu
100 105 110
Thr Lys Lys Gly Cys Lys Asp Cys Cys Phe Gly Thr Phe Asn Asp Gln
115 120 125
Lys Arg Gly Ile Cys Arg Pro Trp Thr Asn Cys Ser Leu Asp Gly Lys
130 135 140
Ser Val Leu Val Asn Gly Thr Lys Glu Arg Asp Val Val Cys Gly Pro
145 150 155 160
Ser Pro Ala Asp Leu Ser Pro Gly Ala Ser Ser Val Thr Pro Pro Ala
165 170 175
Pro Ala Arg Glu Pro Gly His Ser Pro Gln Ile Ile Ser Phe Phe Leu
180 185 190
Ala Leu Thr Ser Thr Ala Leu Leu Phe Leu Leu Phe Phe Leu Thr Leu
195 200 205
Arg Phe Ser Val Val Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
210 215 220
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
225 230 235 240
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
245 250 255
<210> 198
<211> 277
<212> БЕЛОК
<213> Homo sapiens
<400> 198
Met Cys Val Gly Ala Arg Arg Leu Gly Arg Gly Pro Cys Ala Ala Leu
1 5 10 15
Leu Leu Leu Gly Leu Gly Leu Ser Thr Val Thr Gly Leu His Cys Val
20 25 30
Gly Asp Thr Tyr Pro Ser Asn Asp Arg Cys Cys His Glu Cys Arg Pro
35 40 45
Gly Asn Gly Met Val Ser Arg Cys Ser Arg Ser Gln Asn Thr Val Cys
50 55 60
Arg Pro Cys Gly Pro Gly Phe Tyr Asn Asp Val Val Ser Ser Lys Pro
65 70 75 80
Cys Lys Pro Cys Thr Trp Cys Asn Leu Arg Ser Gly Ser Glu Arg Lys
85 90 95
Gln Leu Cys Thr Ala Thr Gln Asp Thr Val Cys Arg Cys Arg Ala Gly
100 105 110
Thr Gln Pro Leu Asp Ser Tyr Lys Pro Gly Val Asp Cys Ala Pro Cys
115 120 125
Pro Pro Gly His Phe Ser Pro Gly Asp Asn Gln Ala Cys Lys Pro Trp
130 135 140
Thr Asn Cys Thr Leu Ala Gly Lys His Thr Leu Gln Pro Ala Ser Asn
145 150 155 160
Ser Ser Asp Ala Ile Cys Glu Asp Arg Asp Pro Pro Ala Thr Gln Pro
165 170 175
Gln Glu Thr Gln Gly Pro Pro Ala Arg Pro Ile Thr Val Gln Pro Thr
180 185 190
Glu Ala Trp Pro Arg Thr Ser Gln Gly Pro Ser Thr Arg Pro Val Glu
195 200 205
Val Pro Gly Gly Arg Ala Val Ala Ala Ile Leu Gly Leu Gly Leu Val
210 215 220
Leu Gly Leu Leu Gly Pro Leu Ala Ile Leu Leu Ala Leu Tyr Leu Leu
225 230 235 240
Arg Arg Asp Gln Arg Leu Pro Pro Asp Ala His Lys Pro Pro Gly Gly
245 250 255
Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala Asp Ala His Ser
260 265 270
Thr Leu Ala Lys Ile
275
<210> 199
<211> 199
<212> БЕЛОК
<213> Homo sapiens
<400> 199
Met Lys Ser Gly Leu Trp Tyr Phe Phe Leu Phe Cys Leu Arg Ile Lys
1 5 10 15
Val Leu Thr Gly Glu Ile Asn Gly Ser Ala Asn Tyr Glu Met Phe Ile
20 25 30
Phe His Asn Gly Gly Val Gln Ile Leu Cys Lys Tyr Pro Asp Ile Val
35 40 45
Gln Gln Phe Lys Met Gln Leu Leu Lys Gly Gly Gln Ile Leu Cys Asp
50 55 60
Leu Thr Lys Thr Lys Gly Ser Gly Asn Thr Val Ser Ile Lys Ser Leu
65 70 75 80
Lys Phe Cys His Ser Gln Leu Ser Asn Asn Ser Val Ser Phe Phe Leu
85 90 95
Tyr Asn Leu Asp His Ser His Ala Asn Tyr Tyr Phe Cys Asn Leu Ser
100 105 110
Ile Phe Asp Pro Pro Pro Phe Lys Val Thr Leu Thr Gly Gly Tyr Leu
115 120 125
His Ile Tyr Glu Ser Gln Leu Cys Cys Gln Leu Lys Phe Trp Leu Pro
130 135 140
Ile Gly Cys Ala Ala Phe Val Val Val Cys Ile Leu Gly Cys Ile Leu
145 150 155 160
Ile Cys Trp Leu Thr Lys Lys Lys Tyr Ser Ser Ser Val His Asp Pro
165 170 175
Asn Gly Glu Tyr Met Phe Met Arg Ala Val Asn Thr Ala Lys Lys Ser
180 185 190
Arg Leu Thr Asp Val Thr Leu
195
<210> 200
<211> 223
<212> БЕЛОК
<213> Homo sapiens
<400> 200
Met Ala Cys Leu Gly Phe Gln Arg His Lys Ala Gln Leu Asn Leu Ala
1 5 10 15
Thr Arg Thr Trp Pro Cys Thr Leu Leu Phe Phe Leu Leu Phe Ile Pro
20 25 30
Val Phe Cys Lys Ala Met His Val Ala Gln Pro Ala Val Val Leu Ala
35 40 45
Ser Ser Arg Gly Ile Ala Ser Phe Val Cys Glu Tyr Ala Ser Pro Gly
50 55 60
Lys Ala Thr Glu Val Arg Val Thr Val Leu Arg Gln Ala Asp Ser Gln
65 70 75 80
Val Thr Glu Val Cys Ala Ala Thr Tyr Met Met Gly Asn Glu Leu Thr
85 90 95
Phe Leu Asp Asp Ser Ile Cys Thr Gly Thr Ser Ser Gly Asn Gln Val
100 105 110
Asn Leu Thr Ile Gln Gly Leu Arg Ala Met Asp Thr Gly Leu Tyr Ile
115 120 125
Cys Lys Val Glu Leu Met Tyr Pro Pro Pro Tyr Tyr Leu Gly Ile Gly
130 135 140
Asn Gly Thr Gln Ile Tyr Val Ile Asp Pro Glu Pro Cys Pro Asp Ser
145 150 155 160
Asp Phe Leu Leu Trp Ile Leu Ala Ala Val Ser Ser Gly Leu Phe Phe
165 170 175
Tyr Ser Phe Leu Leu Thr Ala Val Ser Leu Ser Lys Met Leu Lys Lys
180 185 190
Arg Ser Pro Leu Thr Thr Gly Val Tyr Val Lys Met Pro Pro Thr Glu
195 200 205
Pro Glu Cys Glu Lys Gln Phe Gln Pro Tyr Phe Ile Pro Ile Asn
210 215 220
<210> 201
<211> 288
<212> БЕЛОК
<213> Homo sapiens
<400> 201
Met Gln Ile Pro Gln Ala Pro Trp Pro Val Val Trp Ala Val Leu Gln
1 5 10 15
Leu Gly Trp Arg Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp
20 25 30
Asn Pro Pro Thr Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp
35 40 45
Asn Ala Thr Phe Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val
50 55 60
Leu Asn Trp Tyr Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala
65 70 75 80
Ala Phe Pro Glu Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg
85 90 95
Val Thr Gln Leu Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg
100 105 110
Ala Arg Arg Asn Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu
115 120 125
Ala Pro Lys Ala Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val
130 135 140
Thr Glu Arg Arg Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro
145 150 155 160
Arg Pro Ala Gly Gln Phe Gln Thr Leu Val Val Gly Val Val Gly Gly
165 170 175
Leu Leu Gly Ser Leu Val Leu Leu Val Trp Val Leu Ala Val Ile Cys
180 185 190
Ser Arg Ala Ala Arg Gly Thr Ile Gly Ala Arg Arg Thr Gly Gln Pro
195 200 205
Leu Lys Glu Asp Pro Ser Ala Val Pro Val Phe Ser Val Asp Tyr Gly
210 215 220
Glu Leu Asp Phe Gln Trp Arg Glu Lys Thr Pro Glu Pro Pro Val Pro
225 230 235 240
Cys Val Pro Glu Gln Thr Glu Tyr Ala Thr Ile Val Phe Pro Ser Gly
245 250 255
Met Gly Thr Ser Ser Pro Ala Arg Arg Gly Ser Ala Asp Gly Pro Arg
260 265 270
Ser Ala Gln Pro Leu Arg Pro Glu Asp Gly His Cys Ser Trp Pro Leu
275 280 285
<210> 202
<211> 525
<212> БЕЛОК
<213> Homo sapiens
<400> 202
Met Trp Glu Ala Gln Phe Leu Gly Leu Leu Phe Leu Gln Pro Leu Trp
1 5 10 15
Val Ala Pro Val Lys Pro Leu Gln Pro Gly Ala Glu Val Pro Val Val
20 25 30
Trp Ala Gln Glu Gly Ala Pro Ala Gln Leu Pro Cys Ser Pro Thr Ile
35 40 45
Pro Leu Gln Asp Leu Ser Leu Leu Arg Arg Ala Gly Val Thr Trp Gln
50 55 60
His Gln Pro Asp Ser Gly Pro Pro Ala Ala Ala Pro Gly His Pro Leu
65 70 75 80
Ala Pro Gly Pro His Pro Ala Ala Pro Ser Ser Trp Gly Pro Arg Pro
85 90 95
Arg Arg Tyr Thr Val Leu Ser Val Gly Pro Gly Gly Leu Arg Ser Gly
100 105 110
Arg Leu Pro Leu Gln Pro Arg Val Gln Leu Asp Glu Arg Gly Arg Gln
115 120 125
Arg Gly Asp Phe Ser Leu Trp Leu Arg Pro Ala Arg Arg Ala Asp Ala
130 135 140
Gly Glu Tyr Arg Ala Ala Val His Leu Arg Asp Arg Ala Leu Ser Cys
145 150 155 160
Arg Leu Arg Leu Arg Leu Gly Gln Ala Ser Met Thr Ala Ser Pro Pro
165 170 175
Gly Ser Leu Arg Ala Ser Asp Trp Val Ile Leu Asn Cys Ser Phe Ser
180 185 190
Arg Pro Asp Arg Pro Ala Ser Val His Trp Phe Arg Asn Arg Gly Gln
195 200 205
Gly Arg Val Pro Val Arg Glu Ser Pro His His His Leu Ala Glu Ser
210 215 220
Phe Leu Phe Leu Pro Gln Val Ser Pro Met Asp Ser Gly Pro Trp Gly
225 230 235 240
Cys Ile Leu Thr Tyr Arg Asp Gly Phe Asn Val Ser Ile Met Tyr Asn
245 250 255
Leu Thr Val Leu Gly Leu Glu Pro Pro Thr Pro Leu Thr Val Tyr Ala
260 265 270
Gly Ala Gly Ser Arg Val Gly Leu Pro Cys Arg Leu Pro Ala Gly Val
275 280 285
Gly Thr Arg Ser Phe Leu Thr Ala Lys Trp Thr Pro Pro Gly Gly Gly
290 295 300
Pro Asp Leu Leu Val Thr Gly Asp Asn Gly Asp Phe Thr Leu Arg Leu
305 310 315 320
Glu Asp Val Ser Gln Ala Gln Ala Gly Thr Tyr Thr Cys His Ile His
325 330 335
Leu Gln Glu Gln Gln Leu Asn Ala Thr Val Thr Leu Ala Ile Ile Thr
340 345 350
Val Thr Pro Lys Ser Phe Gly Ser Pro Gly Ser Leu Gly Lys Leu Leu
355 360 365
Cys Glu Val Thr Pro Val Ser Gly Gln Glu Arg Phe Val Trp Ser Ser
370 375 380
Leu Asp Thr Pro Ser Gln Arg Ser Phe Ser Gly Pro Trp Leu Glu Ala
385 390 395 400
Gln Glu Ala Gln Leu Leu Ser Gln Pro Trp Gln Cys Gln Leu Tyr Gln
405 410 415
Gly Glu Arg Leu Leu Gly Ala Ala Val Tyr Phe Thr Glu Leu Ser Ser
420 425 430
Pro Gly Ala Gln Arg Ser Gly Arg Ala Pro Gly Ala Leu Pro Ala Gly
435 440 445
His Leu Leu Leu Phe Leu Ile Leu Gly Val Leu Ser Leu Leu Leu Leu
450 455 460
Val Thr Gly Ala Phe Gly Phe His Leu Trp Arg Arg Gln Trp Arg Pro
465 470 475 480
Arg Arg Phe Ser Ala Leu Glu Gln Gly Ile His Pro Pro Gln Ala Gln
485 490 495
Ser Lys Ile Glu Glu Leu Glu Gln Glu Pro Glu Pro Glu Pro Glu Pro
500 505 510
Glu Pro Glu Pro Glu Pro Glu Pro Glu Pro Glu Gln Leu
515 520 525
<210> 203
<211> 370
<212> БЕЛОК
<213> Homo sapiens
<400> 203
Met Leu Gly Gln Val Val Thr Leu Ile Leu Leu Leu Leu Leu Lys Val
1 5 10 15
Tyr Gln Gly Lys Gly Cys Gln Gly Ser Ala Asp His Val Val Ser Ile
20 25 30
Ser Gly Val Pro Leu Gln Leu Gln Pro Asn Ser Ile Gln Thr Lys Val
35 40 45
Asp Ser Ile Ala Trp Lys Lys Leu Leu Pro Ser Gln Asn Gly Phe His
50 55 60
His Ile Leu Lys Trp Glu Asn Gly Ser Leu Pro Ser Asn Thr Ser Asn
65 70 75 80
Asp Arg Phe Ser Phe Ile Val Lys Asn Leu Ser Leu Leu Ile Lys Ala
85 90 95
Ala Gln Gln Gln Asp Ser Gly Leu Tyr Cys Leu Glu Val Thr Ser Ile
100 105 110
Ser Gly Lys Val Gln Thr Ala Thr Phe Gln Val Phe Val Phe Glu Ser
115 120 125
Leu Leu Pro Asp Lys Val Glu Lys Pro Arg Leu Gln Gly Gln Gly Lys
130 135 140
Ile Leu Asp Arg Gly Arg Cys Gln Val Ala Leu Ser Cys Leu Val Ser
145 150 155 160
Arg Asp Gly Asn Val Ser Tyr Ala Trp Tyr Arg Gly Ser Lys Leu Ile
165 170 175
Gln Thr Ala Gly Asn Leu Thr Tyr Leu Asp Glu Glu Val Asp Ile Asn
180 185 190
Gly Thr His Thr Tyr Thr Cys Asn Val Ser Asn Pro Val Ser Trp Glu
195 200 205
Ser His Thr Leu Asn Leu Thr Gln Asp Cys Gln Asn Ala His Gln Glu
210 215 220
Phe Arg Phe Trp Pro Phe Leu Val Ile Ile Val Ile Leu Ser Ala Leu
225 230 235 240
Phe Leu Gly Thr Leu Ala Cys Phe Cys Val Trp Arg Arg Lys Arg Lys
245 250 255
Glu Lys Gln Ser Glu Thr Ser Pro Lys Glu Phe Leu Thr Ile Tyr Glu
260 265 270
Asp Val Lys Asp Leu Lys Thr Arg Arg Asn His Glu Gln Glu Gln Thr
275 280 285
Phe Pro Gly Gly Gly Ser Thr Ile Tyr Ser Met Ile Gln Ser Gln Ser
290 295 300
Ser Ala Pro Thr Ser Gln Glu Pro Ala Tyr Thr Leu Tyr Ser Leu Ile
305 310 315 320
Gln Pro Ser Arg Lys Ser Gly Ser Arg Lys Arg Asn His Ser Pro Ser
325 330 335
Phe Asn Ser Thr Ile Tyr Glu Val Ile Gly Lys Ser Gln Pro Lys Ala
340 345 350
Gln Asn Pro Ala Arg Leu Ser Arg Lys Glu Leu Glu Asn Phe Asp Val
355 360 365
Tyr Ser
370
<210> 204
<211> 289
<212> БЕЛОК
<213> Homo sapiens
<400> 204
Met Lys Thr Leu Pro Ala Met Leu Gly Thr Gly Lys Leu Phe Trp Val
1 5 10 15
Phe Phe Leu Ile Pro Tyr Leu Asp Ile Trp Asn Ile His Gly Lys Glu
20 25 30
Ser Cys Asp Val Gln Leu Tyr Ile Lys Arg Gln Ser Glu His Ser Ile
35 40 45
Leu Ala Gly Asp Pro Phe Glu Leu Glu Cys Pro Val Lys Tyr Cys Ala
50 55 60
Asn Arg Pro His Val Thr Trp Cys Lys Leu Asn Gly Thr Thr Cys Val
65 70 75 80
Lys Leu Glu Asp Arg Gln Thr Ser Trp Lys Glu Glu Lys Asn Ile Ser
85 90 95
Phe Phe Ile Leu His Phe Glu Pro Val Leu Pro Asn Asp Asn Gly Ser
100 105 110
Tyr Arg Cys Ser Ala Asn Phe Gln Ser Asn Leu Ile Glu Ser His Ser
115 120 125
Thr Thr Leu Tyr Val Thr Asp Val Lys Ser Ala Ser Glu Arg Pro Ser
130 135 140
Lys Asp Glu Met Ala Ser Arg Pro Trp Leu Leu Tyr Arg Leu Leu Pro
145 150 155 160
Leu Gly Gly Leu Pro Leu Leu Ile Thr Thr Cys Phe Cys Leu Phe Cys
165 170 175
Cys Leu Arg Arg His Gln Gly Lys Gln Asn Glu Leu Ser Asp Thr Ala
180 185 190
Gly Arg Glu Ile Asn Leu Val Asp Ala His Leu Lys Ser Glu Gln Thr
195 200 205
Glu Ala Ser Thr Arg Gln Asn Ser Gln Val Leu Leu Ser Glu Thr Gly
210 215 220
Ile Tyr Asp Asn Asp Pro Asp Leu Cys Phe Arg Met Gln Glu Gly Ser
225 230 235 240
Glu Val Tyr Ser Asn Pro Cys Leu Glu Glu Asn Lys Pro Gly Ile Val
245 250 255
Tyr Ala Ser Leu Asn His Ser Val Ile Gly Pro Asn Ser Arg Leu Ala
260 265 270
Arg Asn Val Lys Glu Ala Pro Thr Glu Tyr Ala Ser Ile Cys Val Arg
275 280 285
Ser
<210> 205
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 205
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly
20
<210> 206
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
олигонуклеотид
<400> 206
atggaaaccg acaccctgct gctgtgggtg ctgctgctgt gggtgccagg atccacagga 60
<210> 207
<211> 1398
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 207
caatctgccc tgactcagcc tgcctccgtg tctgcgtctc ctggacagtc gatcgccatc 60
tcctgcactg gaaccagcag tgacgttggt tggtatcaac agcacccagg caaagccccc 120
aaactcatga tttatgagga cagtaagcgg ccctcagggg tttctaatcg cttctctggc 180
tccaagtctg gcaacacggc ctccctgacc atctctgggc tccaggctga ggacgaggct 240
gattattact gcagctcaaa tacaagaagc agcactttgg tgttcggcgg agggaccaag 300
ctgaccgtcc taggttctag aggtggtggt ggtagcggcg gcggcggctc tggtggtggt 360
ggatccctcg agatggccga agtgcagctg gtgcagtctg gggctgagat gaagaagcct 420
ggggcctcac tgaagctctc ctgcaaggct tctggataca ccttcatcga ctactatgta 480
tactggatgc gacaggcccc tggacaaggg cttgagtcca tgggatggat caaccctaac 540
agtggtggca caaactatgc acagaagttt cagggcaggg tcaccatgac cagggacacg 600
tccatcagca cagcctacat ggagctgagc aggctgagat ctgacgacac cgccatgtat 660
tactgtgcgc gctcccagcg tgacggttac atggattact ggggtcaagg tactctggtg 720
accgtctcct cagcggccgc aattgaagtt atgtatcctc ctccttacct agacaatgag 780
aagagcaatg gaaccattat ccatgtgaaa gggaaacacc tttgtccaag tcccctattt 840
cccggacctt ctaagccctt ttgggtgctg gtggtggttg gtggagtcct ggcttgctat 900
agcttgctag taacagtggc ctttattatt ttctgggtga ggagtaagag gagcaggctc 960
ctgcacagtg actacatgaa catgactccc cgccgccccg ggcccacccg caagcattac 1020
cagccctatg ccccaccacg cgacttcgca gcctatcgct ccagagtgaa gttcagcagg 1080
agcgcagacg cccccgcgta ccagcagggc cagaaccagc tctataacga gctcaatcta 1140
ggacgaagag aggagtacga tgttttggac aagagacgtg gccgggaccc tgagatgggg 1200
ggaaagccga gaaggaagaa ccctcaggaa ggcctgtaca atgaactgca gaaagataag 1260
atggcggagg cctacagtga gattgggatg aaaggcgagc gccggagggg caaggggcac 1320
gatggccttt accagggtct cagtacagcc accaaggaca cctacgacgc ccttcacatg 1380
caggccctgc cccctcgc 1398
<210> 208
<211> 1419
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 208
cagtctgtgc tgacgcagcc gccctcagtg tctggggccc cagggcagag ggtcaccatc 60
tcctgcactg ggagcagctc caacatcggg gcaggttttg atgtacactg gtaccagcag 120
cttccaggaa cagcccccaa actcctcatc tatggtaaca gcaatcggcc ctcaggggtc 180
cctgaccgat tctctggctc caagtctggc acctcagcct ccctggccat cactgggctc 240
caggctgagg atgaggctga ttattactgc cagtcctatg acagcagcct gagtggttat 300
gtcttcggaa ctgggaccaa ggtcaccgtc ctaggttcta gaggtggtgg tggtagcggc 360
ggcggcggct ctggtggtgg tggatccctc gagatggccc aggtccagct ggtacagtct 420
ggggctgagg tgaagaagcc tggggcctca gtgaaggtct cctgcaaggc ttctggatac 480
accttcaccg actactatat gcactgggtg cgacaggccc ctggacaacg gcttgagtgg 540
atgggatgga tcaaccctaa cagtggtggc acaaactatg cacagaagtt tcaggacagg 600
atcaccgtga ccagggacac ctccagcaac acaggctaca tggagctgac caggctgaga 660
tctgacgaca cggccgtgta ttactgtgcg cgctctccgt actctggtgt tctggataaa 720
tggggtcaag gtactctggt gaccgtctcc tcagcggccg caattgaagt tatgtatcct 780
cctccttacc tagacaatga gaagagcaat ggaaccatta tccatgtgaa agggaaacac 840
ctttgtccaa gtcccctatt tcccggacct tctaagccct tttgggtgct ggtggtggtt 900
ggtggagtcc tggcttgcta tagcttgcta gtaacagtgg cctttattat tttctgggtg 960
aggagtaaga ggagcaggct cctgcacagt gactacatga acatgactcc ccgccgcccc 1020
gggcccaccc gcaagcatta ccagccctat gccccaccac gcgacttcgc agcctatcgc 1080
tccagagtga agttcagcag gagcgcagac gcccccgcgt accagcaggg ccagaaccag 1140
ctctataacg agctcaatct aggacgaaga gaggagtacg atgttttgga caagagacgt 1200
ggccgggacc ctgagatggg gggaaagccg agaaggaaga accctcagga aggcctgtac 1260
aatgaactgc agaaagataa gatggcggag gcctacagtg agattgggat gaaaggcgag 1320
cgccggaggg gcaaggggca cgatggcctt taccagggtc tcagtacagc caccaaggac 1380
acctacgacg cccttcacat gcaggccctg ccccctcgc 1419
<210> 209
<211> 1410
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 209
tcctatgagc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatg 60
tcttgttctg gaaccagctc caacatcgga agtcactctg taaactggta ccagcagctc 120
ccaggaacgg cccccaaact cctcatctat actaataatc agcggccctc aggggtccct 180
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tggcctccag 240
tctgaggatg aggctgatta ttactgtgca gcatgggatg gcagcctgaa tggtctggta 300
ttcggcggag ggaccaagct gaccgtccta ggttctagag gtggtggtgg tagcggcggc 360
ggcggctctg gtggtggtgg atccctcgag atggccgagg tgcagctggt gcagtctgga 420
gcagaggtga aaaagcccgg ggagtctctg aagatctcct gtaagggttc tggatacagc 480
tttaccagct actggatcgg ctgggtgcgc cagatgcccg ggaaaggcct ggagtggatg 540
gggatcatct atcctggtga ctctgatacc agatacagcc cgtccttcca aggccacgtc 600
accatctcag ctgacaagtc catcagcact gcctacctgc agtggagcag cctgaaggcc 660
tcggacaccg ccatgtatta ctgtgcgcgc tactctggtt ctttcgataa ctggggtcaa 720
ggtactctgg tgaccgtctc ctcagcggcc gcaattgaag ttatgtatcc tcctccttac 780
ctagacaatg agaagagcaa tggaaccatt atccatgtga aagggaaaca cctttgtcca 840
agtcccctat ttcccggacc ttctaagccc ttttgggtgc tggtggtggt tggtggagtc 900
ctggcttgct atagcttgct agtaacagtg gcctttatta ttttctgggt gaggagtaag 960
aggagcaggc tcctgcacag tgactacatg aacatgactc cccgccgccc cgggcccacc 1020
cgcaagcatt accagcccta tgccccacca cgcgacttcg cagcctatcg ctccagagtg 1080
aagttcagca ggagcgcaga cgcccccgcg taccagcagg gccagaacca gctctataac 1140
gagctcaatc taggacgaag agaggagtac gatgttttgg acaagagacg tggccgggac 1200
cctgagatgg ggggaaagcc gagaaggaag aaccctcagg aaggcctgta caatgaactg 1260
cagaaagata agatggcgga ggcctacagt gagattggga tgaaaggcga gcgccggagg 1320
ggcaaggggc acgatggcct ttaccagggt ctcagtacag ccaccaagga cacctacgac 1380
gcccttcaca tgcaggccct gccccctcgc 1410
<210> 210
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 210
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 211
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
олигонуклеотид
<400> 211
ggtggaggtg gatcaggtgg aggtggatct ggtggaggtg gatct 45
<210> 212
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 212
Gly Gly Gly Gly Ser
1 5
<210> 213
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 213
Ser Gly Gly Ser Gly Gly Ser
1 5
<210> 214
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 214
Gly Gly Gly Gly Ser Gly Gly Gly Ser
1 5
<210> 215
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 215
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 216
<211> 18
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 216
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly
1 5 10 15
Gly Ser
<210> 217
<211> 20
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 217
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 218
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 218
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 219
<211> 30
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 219
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25 30
<210> 220
<211> 35
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 220
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser
35
<210> 221
<211> 15
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 221
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 222
<211> 24
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 222
Gly Gly Gly Gly Ser Gly Gly Gly Ser Glu Pro Lys Ser Cys Asp Lys
1 5 10 15
Thr His Thr Cys Pro Pro Cys Pro
20
<210> 223
<211> 62
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 223
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 224
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 224
Gly Ser Gly Ser Gly Ser
1 5
<210> 225
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 225
Ala Ala Ala
1
<210> 226
<211> 235
<212> БЕЛОК
<213> Homo sapiens
<400> 226
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Gln Phe Arg Val Ser Pro Leu Asp Arg Thr
20 25 30
Trp Asn Leu Gly Glu Thr Val Glu Leu Lys Cys Gln Val Leu Leu Ser
35 40 45
Asn Pro Thr Ser Gly Cys Ser Trp Leu Phe Gln Pro Arg Gly Ala Ala
50 55 60
Ala Ser Pro Thr Phe Leu Leu Tyr Leu Ser Gln Asn Lys Pro Lys Ala
65 70 75 80
Ala Glu Gly Leu Asp Thr Gln Arg Phe Ser Gly Lys Arg Leu Gly Asp
85 90 95
Thr Phe Val Leu Thr Leu Ser Asp Phe Arg Arg Glu Asn Glu Gly Cys
100 105 110
Tyr Phe Cys Ser Ala Leu Ser Asn Ser Ile Met Tyr Phe Ser His Phe
115 120 125
Val Pro Val Phe Leu Pro Ala Lys Pro Thr Thr Thr Pro Ala Pro Arg
130 135 140
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
145 150 155 160
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
165 170 175
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
180 185 190
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn His
195 200 205
Arg Asn Arg Arg Arg Val Cys Lys Cys Pro Arg Pro Val Val Lys Ser
210 215 220
Gly Asp Lys Pro Ser Leu Ser Ala Arg Tyr Val
225 230 235
<210> 227
<211> 213
<212> ДНК
<213> Homo sapiens
<400> 227
cccaccacga cgccagcgcc gcgaccacca accccggcgc ccacgatcgc gtcgcagccc 60
ctgtccctgc gcccagaggc gtgccggcca gcggcggggg gcgcagtgca cacgaggggg 120
ctggacttcg cctgtgatat ctacatctgg gcgcccctgg ccgggacttg tggggtcctt 180
ctcctgtcac tggttatcac cctttactgc aac 213
<210> 228
<211> 126
<212> ДНК
<213> Homo sapiens
<400> 228
aaacggggca gaaagaagct cctgtatata ttcaaacaac catttatgag accagtacaa 60
actactcaag aggaagatgg ctgtagctgc cgatttccag aagaagaaga aggaggatgt 120
gaactg 126
<210> 229
<211> 7671
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 229
ccttctctag gcgcccccat atggccatat gagatcttat atggggcacc cccgcccctt 60
gtaaacttcc ctgaccctga catgacaaga gttactaaca gcccctctct ccaagctcac 120
ttacaggctc tctacttagt ccagcacgaa gtctggagac ctctggcggc agcctaccaa 180
gaacaactgg accgaccggt gccgccacca tggaaaccga caccctgctg ctgtgggtgc 240
tgctgctgtg ggtgccagga tccacaggac tgcctgtgct gactcagcca ccctcagcgt 300
ctgggacccc cgggcagagg gtcaccatct cttgttctgg acgcagttcc aacatcggga 360
gtaattctgt taactggtat cgacaactcc caggagcggc ccccaaactc ctcatctata 420
gtaataatca gcggccccca ggggtccctg tgcgattctc tggctccaag tctggcacct 480
cagcctccct ggccatcagt gggctccagt ctgaagatga ggccacttat tactgtgcaa 540
catgggatga caatctgaat gttcactatg tcttcggaac tgggaccaag gtcaccgtcc 600
taggttctag aggtggtggt ggtagcggcg gcggcggctc tggtggtggt ggatccctcg 660
agatggccca ggtgcagctg gtgcagtctg gggctgaggt gaagaagcct gggtcctcgg 720
tgaaggtctc ctgcaaggct tctggaggca ccttcagcag ctatgctatc agctgggtgc 780
gacaggcccc tggacaaggg cttgagtgga tgggaaggat catccctatc cttggtatag 840
caaactacgc acagaagttc cagggcagag tcacgattac cgcggacaaa tccacgagca 900
cagcctacat ggagctgagc agcctgagat ctgaggacac ggccgtgtat tactgtgcgc 960
gcggtggtta ctactctcat gacatgtggt ctgaagattg gggtcaaggt actctggtga 1020
ccgtctcctc agcggccgca cccaccacga cgccagcgcc gcgaccacca accccggcgc 1080
ccacgatcgc gtcgcagccc ctgtccctgc gcccagaggc gtgccggcca gcggcggggg 1140
gcgcagtgca cacgaggggg ctggacttcg cctgtgatat ctacatctgg gcgcccctgg 1200
ccgggacttg tggggtcctt ctcctgtcac tggttatcac cctttactgc aacaaacggg 1260
gcagaaagaa gctcctgtat atattcaaac aaccatttat gagaccagta caaactactc 1320
aagaggaaga tggctgtagc tgccgatttc cagaagaaga agaaggagga tgtgaactga 1380
gagtgaagtt cagcaggagc gcagagcccc ccgcgtacca gcagggccag aaccagctct 1440
ataacgagct caatctagga cgaagagagg agtacgatgt tttggacaag agacgtggcc 1500
gggaccctga gatgggggga aagccgagaa ggaagaaccc tcaggaaggc ctgtacaatg 1560
aactgcagaa agataagatg gcggaggcct acagtgagat tgggatgaaa ggcgagcgcc 1620
ggaggggcaa ggggcacgat ggcctttacc agggtctcag tacagccacc aaggacacct 1680
acgacgccct tcacatgcag gccctgcccc ctcgctaaca gccactcgag gatccggatt 1740
agtccaattt gttaaagaca ggatatcagt ggtccaggct ctagttttga ctcaacaata 1800
tcaccagctg aagcctatag agtacgagcc atagataaaa taaaagattt tatttagtct 1860
ccagaaaaag gggggaatga aagaccccac ctgtaggttt ggcaagctag cttaagtaac 1920
gccattttgc aaggcatgga aaaatacata actgagaata gagaagttca gatcaaggtc 1980
aggaacagat ggaacagctg aatatgggcc aaacaggata tctgtggtaa gcagttcctg 2040
ccccggctca gggccaagaa cagatggaac agctgaatat gggccaaaca ggatatctgt 2100
ggtaagcagt tcctgccccg gctcagggcc aagaacagat ggtccccaga tgcggtccag 2160
ccctcagcag tttctagaga accatcagat gtttccaggg tgccccaagg acctgaaatg 2220
accctgtgcc ttatttgaac taaccaatca gttcgcttct cgcttctgtt cgcgcgcttc 2280
tgctccccga gctcaataaa agagcccaca acccctcact cggggcgcca gtcctccgat 2340
tgactgagtc gcccgggtac ccgtgtatcc aataaaccct cttgcagttg catccgactt 2400
gtggtctcgc tgttccttgg gagggtctcc tctgagtgat tgactacccg tcagcggggg 2460
tctttcacac atgcagcatg tatcaaaatt aatttggttt tttttcttaa gtatttacat 2520
taaatggcca tagtacttaa agttacattg gcttccttga aataaacatg gagtattcag 2580
aatgtgtcat aaatatttct aattttaaga tagtatctcc attggctttc tactttttct 2640
tttatttttt tttgtcctct gtcttccatt tgttgttgtt gttgtttgtt tgtttgtttg 2700
ttggttggtt ggttaatttt tttttaaaga tcctacacta tagttcaagc tagactatta 2760
gctactctgt aacccagggt gaccttgaag tcatgggtag cctgctgttt tagccttccc 2820
acatctaaga ttacaggtat gagctatcat ttttggtata ttgattgatt gattgattga 2880
tgtgtgtgtg tgtgattgtg tttgtgtgtg tgactgtgaa aatgtgtgta tgggtgtgtg 2940
tgaatgtgtg tatgtatgtg tgtgtgtgag tgtgtgtgtg tgtgtgtgca tgtgtgtgtg 3000
tgtgactgtg tctatgtgta tgactgtgtg tgtgtgtgtg tgtgtgtgtg tgtgtgtgtg 3060
tgtgtgtgtg ttgtgaaaaa atattctatg gtagtgagag ccaacgctcc ggctcaggtg 3120
tcaggttggt ttttgagaca gagtctttca cttagcttgg aattcactgg ccgtcgtttt 3180
acaacgtcgt gactgggaaa accctggcgt tacccaactt aatcgccttg cagcacatcc 3240
ccctttcgcc agctggcgta atagcgaaga ggcccgcacc gatcgccctt cccaacagtt 3300
gcgcagcctg aatggcgaat ggcgcctgat gcggtatttt ctccttacgc atctgtgcgg 3360
tatttcacac cgcatatggt gcactctcag tacaatctgc tctgatgccg catagttaag 3420
ccagccccga cacccgccaa cacccgctga cgcgccctga cgggcttgtc tgctcccggc 3480
atccgcttac agacaagctg tgaccgtctc cgggagctgc atgtgtcaga ggttttcacc 3540
gtcatcaccg aaacgcgcga tgacgaaagg gcctcgtgat acgcctattt ttataggtta 3600
atgtcatgat aataatggtt tcttagacgt caggtggcac ttttcgggga aatgtgcgcg 3660
gaacccctat ttgtttattt ttctaaatac attcaaatat gtatccgctc atgagacaat 3720
aaccctgata aatgcttcaa taatattgaa aaaggaagag tatgagtatt caacatttcc 3780
gtgtcgccct tattcccttt tttgcggcat tttgccttcc tgtttttgct cacccagaaa 3840
cgctggtgaa agtaaaagat gctgaagatc agttgggtgc acgagtgggt tacatcgaac 3900
tggatctcaa cagcggtaag atccttgaga gttttcgccc cgaagaacgt tttccaatga 3960
tgagcacttt taaagttctg ctatgtggcg cggtattatc ccgtattgac gccgggcaag 4020
agcaactcgg tcgccgcata cactattctc agaatgactt ggttgagtac tcaccagtca 4080
cagaaaagca tcttacggat ggcatgacag taagagaatt atgcagtgct gccataacca 4140
tgagtgataa cactgcggcc aacttacttc tgacaacgat cggaggaccg aaggagctaa 4200
ccgctttttt gcacaacatg ggggatcatg taactcgcct tgatcgttgg gaaccggagc 4260
tgaatgaagc cataccaaac gacgagcgtg acaccacgat gcctgtagca atggcaacaa 4320
cgttgcgcaa actattaact ggcgaactac ttactctagc ttcccggcaa caattaatag 4380
actggatgga ggcggataaa gttgcaggac cacttctgcg ctcggccctt ccggctggct 4440
ggtttattgc tgataaatct ggagccggtg agcgtgggtc tcgcggtatc attgcagcac 4500
tggggccaga tggtaagccc tcccgtatcg tagttatcta cacgacgggg agtcaggcaa 4560
ctatggatga acgaaataga cagatcgctg agataggtgc ctcactgatt aagcattggt 4620
aactgtcaga ccaagtttac tcatatatac tttagattga tttaaaactt catttttaat 4680
ttaaaaggat ctaggtgaag atcctttttg ataatctcat gaccaaaatc ccttaacgtg 4740
agttttcgtt ccactgagcg tcagaccccg tagaaaagat caaaggatct tcttgagatc 4800
ctttttttct gcgcgtaatc tgctgcttgc aaacaaaaaa accaccgcta ccagcggtgg 4860
tttgtttgcc ggatcaagag ctaccaactc tttttccgaa ggtaactggc ttcagcagag 4920
cgcagatacc aaatactgtc cttctagtgt agccgtagtt aggccaccac ttcaagaact 4980
ctgtagcacc gcctacatac ctcgctctgc taatcctgtt accagtggct gctgccagtg 5040
gcgataagtc gtgtcttacc gggttggact caagacgata gttaccggat aaggcgcagc 5100
ggtcgggctg aacggggggt tcgtgcacac agcccagctt ggagcgaacg acctacaccg 5160
aactgagata cctacagcgt gagcattgag aaagcgccac gcttcccgaa gggagaaagg 5220
cggacaggta tccggtaagc ggcagggtcg gaacaggaga gcgcacgagg gagcttccag 5280
ggggaaacgc ctggtatctt tatagtcctg tcgggtttcg ccacctctga cttgagcgtc 5340
gatttttgtg atgctcgtca ggggggcgga gcctatggaa aaacgccagc aacgcggcct 5400
ttttacggtt cctggccttt tgctggcctt ttgctcacat gttctttcct gcgttatccc 5460
ctgattctgt ggataaccgt attaccgcct ttgagtgagc tgataccgct cgccgcagcc 5520
gaacgaccga gcgcagcgag tcagtgagcg aggaagcgga agagcgccca atacgcaaac 5580
cgcctctccc cgcgcgttgg ccgattcatt aatgcagctg gcacgacagg tttcccgact 5640
ggaaagcggg cagtgagcgc aacgcaatta atgtgagtta gctcactcat taggcacccc 5700
aggctttaca ctttatgctt ccggctcgta tgttgtgtgg aattgtgagc ggataacaat 5760
ttcacacagg aaacagctat gaccatgatt acgccaagct ttgctcttag gagtttccta 5820
atacatccca aactcaaata tataaagcat ttgacttgtt ctatgcccta gggggcgggg 5880
ggaagctaag ccagcttttt ttaacattta aaatgttaat tccattttaa atgcacagat 5940
gtttttattt cataagggtt tcaatgtgca tgaatgctgc aatattcctg ttaccaaagc 6000
tagtataaat aaaaatagat aaacgtggaa attacttaga gtttctgtca ttaacgtttc 6060
cttcctcagt tgacaacata aatgcgctgc tgagcaagcc agtttgcatc tgtcaggatc 6120
aatttcccat tatgccagtc atattaatta ctagtcaatt agttgatttt tatttttgac 6180
atatacatgt gaatgaaaga ccccacctgt aggtttggca agctagctta agtaacgcca 6240
ttttgcaagg catggaaaaa tacataactg agaatagaaa agttcagatc aaggtcagga 6300
acagatggaa cagctgaata tgggccaaac aggatatctg tggtaagcag ttcctgcccc 6360
ggctcagggc caagaacaga tggaacagct gaatatgggc caaacaggat atctgtggta 6420
agcagttcct gccccggctc agggccaaga acagatggtc cccagatgcg gtccagccct 6480
cagcagtttc tagagaacca tcagatgttt ccagggtgcc ccaaggacct gaaatgaccc 6540
tgtgccttat ttgaactaac caatcagttc gcttctcgct tctgttcgcg cgcttatgct 6600
ccccgagctc aataaaagag cccacaaccc ctcactcggg gcgccagtcc tccgattgac 6660
tgagtcgccc gggtacccgt gtatccaata aaccctcttg cagttgcatc cgacttgtgg 6720
tctcgctgtt ccttgggagg gtctcctctg agtgattgac tacccgtcag cgggggtctt 6780
tcatttgggg gctcgtccgg gatcgggaga cccctgccca gggaccaccg acccaccacc 6840
gggaggtaag ctggccagca acttatctgt gtctgtccga ttgtctagtg tctatgactg 6900
attttatgcg cctgcgtcgg tactagttag ctaactagct ctgtatctgg cggacccgtg 6960
gtggaactga cgagttcgga acacccggcc gcaaccctgg gagacgtccc agggacttcg 7020
ggggccgttt ttgtggcccg acctgagtcc taaaatcccg atcgtttagg actctttggt 7080
gcacccccct tagaggaggg atatgtggtt ctggtaggag acgagaacct aaaacagttc 7140
ccgcctccgt ctgaattttt gctttcggtt tgggaccgaa gccgcgccgc gcgtcttgtc 7200
tgctgcagca tcgttctgtg ttgtctctgt ctgactgtgt ttctgtattt gtctgaaaat 7260
atgggcccgg gctagactgt taccactccc ttaagtttga ccttaggtca ctggaaagat 7320
gtcgagcgga tcgctcacaa ccagtcggta gatgtcaaga agagacgttg ggttaccttc 7380
tgctctgcag aatggccaac ctttaacgtc ggatggccgc gagacggcac ctttaaccga 7440
gacctcatca cccaggttaa gatcaaggtc ttttcacctg gcccgcatgg acacccagac 7500
caggtcccct acatcgtgac ctgggaagcc ttggcttttg acccccctcc ctgggtcaag 7560
ccctttgtac accctaagcc tccgcctcct cttcctccat ccgccccgtc tctccccctt 7620
gaacctcctc gttcgacccc gcctcgatcc tccctttatc cagccctcac t 7671
<210> 230
<211> 7653
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 230
ggccctctag gcgcccccat atggccatat gagatcttat atggggcacc cccgcccctt 60
gtaaacttcc ctgaccctga catgacaaga gttactaaca gcccctctct ccaagctcac 120
ttacaggctc tctacttagt ccagcacgaa gtctggagac ctctggcggc agcctaccaa 180
gaacaactgg accgaccggt gccgccacca tggaaaccga caccctgctg ctgtgggtgc 240
tgctgctgtg ggtgccagga tccacaggat cctatgagct gactcagcca ccctcagcgt 300
ctgggacccc cgggcagagg gtcaccatgt cttgttctgg aaccagctcc aacatcggaa 360
gtcactctgt aaactggtac cagcagctcc caggaacggc ccccaaactc ctcatctata 420
ctaataatca gcggccctca ggggtccctg accgattctc tggctccaag tctggcacct 480
cagcctccct ggccatcagt ggcctccagt ctgaggatga ggctgattat tactgtgcag 540
catgggatgg cagcctgaat ggtctggtat tcggcggagg gaccaagctg accgtcctag 600
gttctagagg tggtggtggt agcggcggcg gcggctctgg tggtggtgga tccctcgaga 660
tggccgaggt gcagctggtg cagtctggag cagaggtgaa aaagcccggg gagtctctga 720
agatctcctg taagggttct ggatacagct ttaccagcta ctggatcggc tgggtgcgcc 780
agatgcccgg gaaaggcctg gagtggatgg ggatcatcta tcctggtgac tctgatacca 840
gatacagccc gtccttccaa ggccacgtca ccatctcagc tgacaagtcc atcagcactg 900
cctacctgca gtggagcagc ctgaaggcct cggacaccgc catgtattac tgtgcgcgct 960
actctggttc tttcgataac tggggtcaag gtactctggt gaccgtctcc tcagcggccg 1020
cacccaccac gacgccagcg ccgcgaccac caaccccggc gcccacgatc gcgtcgcagc 1080
ccctgtccct gcgcccagag gcgtgccggc cagcggcggg gggcgcagtg cacacgaggg 1140
ggctggactt cgcctgtgat atctacatct gggcgcccct ggccgggact tgtggggtcc 1200
ttctcctgtc actggttatc accctttact gcaacaaacg gggcagaaag aagctcctgt 1260
atatattcaa acaaccattt atgagaccag tacaaactac tcaagaggaa gatggctgta 1320
gctgccgatt tccagaagaa gaagaaggag gatgtgaact gagagtgaag ttcagcagga 1380
gcgcagagcc ccccgcgtac cagcagggcc agaaccagct ctataacgag ctcaatctag 1440
gacgaagaga ggagtacgat gttttggaca agagacgtgg ccgggaccct gagatggggg 1500
gaaagccgag aaggaagaac cctcaggaag gcctgtacaa tgaactgcag aaagataaga 1560
tggcggaggc ctacagtgag attgggatga aaggcgagcg ccggaggggc aaggggcacg 1620
atggccttta ccagggtctc agtacagcca ccaaggacac ctacgacgcc cttcacatgc 1680
aggccctgcc ccctcgctaa cagccactcg aggatccgga ttagtccaat ttgttaaaga 1740
caggatatca gtggtccagg ctctagtttt gactcaacaa tatcaccagc tgaagcctat 1800
agagtacgag ccatagataa aataaaagat tttatttagt ctccagaaaa aggggggaat 1860
gaaagacccc acctgtaggt ttggcaagct agcttaagta acgccatttt gcaaggcatg 1920
gaaaaataca taactgagaa tagagaagtt cagatcaagg tcaggaacag atggaacagc 1980
tgaatatggg ccaaacagga tatctgtggt aagcagttcc tgccccggct cagggccaag 2040
aacagatgga acagctgaat atgggccaaa caggatatct gtggtaagca gttcctgccc 2100
cggctcaggg ccaagaacag atggtcccca gatgcggtcc agccctcagc agtttctaga 2160
gaaccatcag atgtttccag ggtgccccaa ggacctgaaa tgaccctgtg ccttatttga 2220
actaaccaat cagttcgctt ctcgcttctg ttcgcgcgct tctgctcccc gagctcaata 2280
aaagagccca caacccctca ctcggggcgc cagtcctccg attgactgag tcgcccgggt 2340
acccgtgtat ccaataaacc ctcttgcagt tgcatccgac ttgtggtctc gctgttcctt 2400
gggagggtct cctctgagtg attgactacc cgtcagcggg ggtctttcac acatgcagca 2460
tgtatcaaaa ttaatttggt tttttttctt aagtatttac attaaatggc catagtactt 2520
aaagttacat tggcttcctt gaaataaaca tggagtattc agaatgtgtc ataaatattt 2580
ctaattttaa gatagtatct ccattggctt tctacttttt cttttatttt tttttgtcct 2640
ctgtcttcca tttgttgttg ttgttgtttg tttgtttgtt tgttggttgg ttggttaatt 2700
tttttttaaa gatcctacac tatagttcaa gctagactat tagctactct gtaacccagg 2760
gtgaccttga agtcatgggt agcctgctgt tttagccttc ccacatctaa gattacaggt 2820
atgagctatc atttttggta tattgattga ttgattgatt gatgtgtgtg tgtgtgattg 2880
tgtttgtgtg tgtgactgtg aaaatgtgtg tatgggtgtg tgtgaatgtg tgtatgtatg 2940
tgtgtgtgtg agtgtgtgtg tgtgtgtgtg catgtgtgtg tgtgtgactg tgtctatgtg 3000
tatgactgtg tgtgtgtgtg tgtgtgtgtg tgtgtgtgtg tgtgtgtgtg tgttgtgaaa 3060
aaatattcta tggtagtgag agccaacgct ccggctcagg tgtcaggttg gtttttgaga 3120
cagagtcttt cacttagctt ggaattcact ggccgtcgtt ttacaacgtc gtgactggga 3180
aaaccctggc gttacccaac ttaatcgcct tgcagcacat ccccctttcg ccagctggcg 3240
taatagcgaa gaggcccgca ccgatcgccc ttcccaacag ttgcgcagcc tgaatggcga 3300
atggcgcctg atgcggtatt ttctccttac gcatctgtgc ggtatttcac accgcatatg 3360
gtgcactctc agtacaatct gctctgatgc cgcatagtta agccagcccc gacacccgcc 3420
aacacccgct gacgcgccct gacgggcttg tctgctcccg gcatccgctt acagacaagc 3480
tgtgaccgtc tccgggagct gcatgtgtca gaggttttca ccgtcatcac cgaaacgcgc 3540
gatgacgaaa gggcctcgtg atacgcctat ttttataggt taatgtcatg ataataatgg 3600
tttcttagac gtcaggtggc acttttcggg gaaatgtgcg cggaacccct atttgtttat 3660
ttttctaaat acattcaaat atgtatccgc tcatgagaca ataaccctga taaatgcttc 3720
aataatattg aaaaaggaag agtatgagta ttcaacattt ccgtgtcgcc cttattccct 3780
tttttgcggc attttgcctt cctgtttttg ctcacccaga aacgctggtg aaagtaaaag 3840
atgctgaaga tcagttgggt gcacgagtgg gttacatcga actggatctc aacagcggta 3900
agatccttga gagttttcgc cccgaagaac gttttccaat gatgagcact tttaaagttc 3960
tgctatgtgg cgcggtatta tcccgtattg acgccgggca agagcaactc ggtcgccgca 4020
tacactattc tcagaatgac ttggttgagt actcaccagt cacagaaaag catcttacgg 4080
atggcatgac agtaagagaa ttatgcagtg ctgccataac catgagtgat aacactgcgg 4140
ccaacttact tctgacaacg atcggaggac cgaaggagct aaccgctttt ttgcacaaca 4200
tgggggatca tgtaactcgc cttgatcgtt gggaaccgga gctgaatgaa gccataccaa 4260
acgacgagcg tgacaccacg atgcctgtag caatggcaac aacgttgcgc aaactattaa 4320
ctggcgaact acttactcta gcttcccggc aacaattaat agactggatg gaggcggata 4380
aagttgcagg accacttctg cgctcggccc ttccggctgg ctggtttatt gctgataaat 4440
ctggagccgg tgagcgtggg tctcgcggta tcattgcagc actggggcca gatggtaagc 4500
cctcccgtat cgtagttatc tacacgacgg ggagtcaggc aactatggat gaacgaaata 4560
gacagatcgc tgagataggt gcctcactga ttaagcattg gtaactgtca gaccaagttt 4620
actcatatat actttagatt gatttaaaac ttcattttta atttaaaagg atctaggtga 4680
agatcctttt tgataatctc atgaccaaaa tcccttaacg tgagttttcg ttccactgag 4740
cgtcagaccc cgtagaaaag atcaaaggat cttcttgaga tccttttttt ctgcgcgtaa 4800
tctgctgctt gcaaacaaaa aaaccaccgc taccagcggt ggtttgtttg ccggatcaag 4860
agctaccaac tctttttccg aaggtaactg gcttcagcag agcgcagata ccaaatactg 4920
tccttctagt gtagccgtag ttaggccacc acttcaagaa ctctgtagca ccgcctacat 4980
acctcgctct gctaatcctg ttaccagtgg ctgctgccag tggcgataag tcgtgtctta 5040
ccgggttgga ctcaagacga tagttaccgg ataaggcgca gcggtcgggc tgaacggggg 5100
gttcgtgcac acagcccagc ttggagcgaa cgacctacac cgaactgaga tacctacagc 5160
gtgagcattg agaaagcgcc acgcttcccg aagggagaaa ggcggacagg tatccggtaa 5220
gcggcagggt cggaacagga gagcgcacga gggagcttcc agggggaaac gcctggtatc 5280
tttatagtcc tgtcgggttt cgccacctct gacttgagcg tcgatttttg tgatgctcgt 5340
caggggggcg gagcctatgg aaaaacgcca gcaacgcggc ctttttacgg ttcctggcct 5400
tttgctggcc ttttgctcac atgttctttc ctgcgttatc ccctgattct gtggataacc 5460
gtattaccgc ctttgagtga gctgataccg ctcgccgcag ccgaacgacc gagcgcagcg 5520
agtcagtgag cgaggaagcg gaagagcgcc caatacgcaa accgcctctc cccgcgcgtt 5580
ggccgattca ttaatgcagc tggcacgaca ggtttcccga ctggaaagcg ggcagtgagc 5640
gcaacgcaat taatgtgagt tagctcactc attaggcacc ccaggcttta cactttatgc 5700
ttccggctcg tatgttgtgt ggaattgtga gcggataaca atttcacaca ggaaacagct 5760
atgaccatga ttacgccaag ctttgctctt aggagtttcc taatacatcc caaactcaaa 5820
tatataaagc atttgacttg ttctatgccc tagggggcgg ggggaagcta agccagcttt 5880
ttttaacatt taaaatgtta attccatttt aaatgcacag atgtttttat ttcataaggg 5940
tttcaatgtg catgaatgct gcaatattcc tgttaccaaa gctagtataa ataaaaatag 6000
ataaacgtgg aaattactta gagtttctgt cattaacgtt tccttcctca gttgacaaca 6060
taaatgcgct gctgagcaag ccagtttgca tctgtcagga tcaatttccc attatgccag 6120
tcatattaat tactagtcaa ttagttgatt tttatttttg acatatacat gtgaatgaaa 6180
gaccccacct gtaggtttgg caagctagct taagtaacgc cattttgcaa ggcatggaaa 6240
aatacataac tgagaataga aaagttcaga tcaaggtcag gaacagatgg aacagctgaa 6300
tatgggccaa acaggatatc tgtggtaagc agttcctgcc ccggctcagg gccaagaaca 6360
gatggaacag ctgaatatgg gccaaacagg atatctgtgg taagcagttc ctgccccggc 6420
tcagggccaa gaacagatgg tccccagatg cggtccagcc ctcagcagtt tctagagaac 6480
catcagatgt ttccagggtg ccccaaggac ctgaaatgac cctgtgcctt atttgaacta 6540
accaatcagt tcgcttctcg cttctgttcg cgcgcttatg ctccccgagc tcaataaaag 6600
agcccacaac ccctcactcg gggcgccagt cctccgattg actgagtcgc ccgggtaccc 6660
gtgtatccaa taaaccctct tgcagttgca tccgacttgt ggtctcgctg ttccttggga 6720
gggtctcctc tgagtgattg actacccgtc agcgggggtc tttcatttgg gggctcgtcc 6780
gggatcggga gacccctgcc cagggaccac cgacccacca ccgggaggta agctggccag 6840
caacttatct gtgtctgtcc gattgtctag tgtctatgac tgattttatg cgcctgcgtc 6900
ggtactagtt agctaactag ctctgtatct ggcggacccg tggtggaact gacgagttcg 6960
gaacacccgg ccgcaaccct gggagacgtc ccagggactt cgggggccgt ttttgtggcc 7020
cgacctgagt cctaaaatcc cgatcgttta ggactctttg gtgcaccccc cttagaggag 7080
ggatatgtgg ttctggtagg agacgagaac ctaaaacagt tcccgcctcc gtctgaattt 7140
ttgctttcgg tttgggaccg aagccgcgcc gcgcgtcttg tctgctgcag catcgttctg 7200
tgttgtctct gtctgactgt gtttctgtat ttgtctgaaa atatgggccc gggctagact 7260
gttaccactc ccttaagttt gaccttaggt cactggaaag atgtcgagcg gatcgctcac 7320
aaccagtcgg tagatgtcaa gaagagacgt tgggttacct tctgctctgc agaatggcca 7380
acctttaacg tcggatggcc gcgagacggc acctttaacc gagacctcat cacccaggtt 7440
aagatcaagg tcttttcacc tggcccgcat ggacacccag accaggtccc ctacatcgtg 7500
acctgggaag ccttggcttt tgacccccct ccctgggtca agccctttgt acaccctaag 7560
cctccgcctc ctcttcctcc atccgccccg tctctccccc ttgaacctcc tcgttcgacc 7620
ccgcctcgat cctcccttta tccagccctc act 7653
<210> 231
<211> 7668
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 231
ccttctctag gcgcccccat atggccatat gagatcttat atggggcacc cccgcccctt 60
gtaaacttcc ctgaccctga catgacaaga gttactaaca gcccctctct ccaagctcac 120
ttacaggctc tctacttagt ccagcacgaa gtctggagac ctctggcggc agcctaccaa 180
gaacaactgg accgaccggt gccgccacca tggaaaccga caccctgctg ctgtgggtgc 240
tgctgctgtg ggtgccagga tccacaggac aggctgtgct gactcagcca ccctcagcgt 300
ctgggacccc cgggcagagg gtcaccatct cttgttctgg aagcagctcc aacatcggaa 360
gtaattacgt attctggtac cagcagctcc caggaacggc ccccaaactc ctcatctata 420
gtaataatca gcggccctca ggggtccctg accgattctc tggctccaag tctggcacct 480
cagcctccct ggccatcagt gggctccggt ccgaggatga ggctgattat tactgtgcag 540
catgggatga cagcctgagt gcctcttatg ttttcggaac tgggaccaag gtcaccgtcc 600
taggttctag aggtggtggt ggtagcggcg gcggcggctc tggtggtggt ggatccctcg 660
agatggccca ggtgcagctg gtgcagtctg gggctgaggt gaagaagcct gggtcctcgg 720
tgaaggtctc ctgcaaggct tctggaggca ccttcagcag ctatgctatc agctgggtgc 780
gacaggcccc tggacaaggg cttgagtgga tgggaaggat catccctatc cttggtacag 840
caaactacgc acagaagttc cagggcagag tcacgattac cgcggacgaa tccacgagca 900
cagcctacat ggagctgagc agcctgagat ctgaggacac ggccgtgtat tactgtgcgc 960
gctctggtta cggttcttac cgttgggaag attcttgggg tcaaggtact ctggtgaccg 1020
tctcctcagc ggccgcaccc accacgacgc cagcgccgcg accaccaacc ccggcgccca 1080
cgatcgcgtc gcagcccctg tccctgcgcc cagaggcgtg ccggccagcg gcggggggcg 1140
cagtgcacac gagggggctg gacttcgcct gtgatatcta catctgggcg cccctggccg 1200
ggacttgtgg ggtccttctc ctgtcactgg ttatcaccct ttactgcaac aaacggggca 1260
gaaagaagct cctgtatata ttcaaacaac catttatgag accagtacaa actactcaag 1320
aggaagatgg ctgtagctgc cgatttccag aagaagaaga aggaggatgt gaactgagag 1380
tgaagttcag caggagcgca gagccccccg cgtaccagca gggccagaac cagctctata 1440
acgagctcaa tctaggacga agagaggagt acgatgtttt ggacaagaga cgtggccggg 1500
accctgagat ggggggaaag ccgagaagga agaaccctca ggaaggcctg tacaatgaac 1560
tgcagaaaga taagatggcg gaggcctaca gtgagattgg gatgaaaggc gagcgccgga 1620
ggggcaaggg gcacgatggc ctttaccagg gtctcagtac agccaccaag gacacctacg 1680
acgcccttca catgcaggcc ctgccccctc gctaacagcc actcgaggat ccggattagt 1740
ccaatttgtt aaagacagga tatcagtggt ccaggctcta gttttgactc aacaatatca 1800
ccagctgaag cctatagagt acgagccata gataaaataa aagattttat ttagtctcca 1860
gaaaaagggg ggaatgaaag accccacctg taggtttggc aagctagctt aagtaacgcc 1920
attttgcaag gcatggaaaa atacataact gagaatagag aagttcagat caaggtcagg 1980
aacagatgga acagctgaat atgggccaaa caggatatct gtggtaagca gttcctgccc 2040
cggctcaggg ccaagaacag atggaacagc tgaatatggg ccaaacagga tatctgtggt 2100
aagcagttcc tgccccggct cagggccaag aacagatggt ccccagatgc ggtccagccc 2160
tcagcagttt ctagagaacc atcagatgtt tccagggtgc cccaaggacc tgaaatgacc 2220
ctgtgcctta tttgaactaa ccaatcagtt cgcttctcgc ttctgttcgc gcgcttctgc 2280
tccccgagct caataaaaga gcccacaacc cctcactcgg ggcgccagtc ctccgattga 2340
ctgagtcgcc cgggtacccg tgtatccaat aaaccctctt gcagttgcat ccgacttgtg 2400
gtctcgctgt tccttgggag ggtctcctct gagtgattga ctacccgtca gcgggggtct 2460
ttcacacatg cagcatgtat caaaattaat ttggtttttt ttcttaagta tttacattaa 2520
atggccatag tacttaaagt tacattggct tccttgaaat aaacatggag tattcagaat 2580
gtgtcataaa tatttctaat tttaagatag tatctccatt ggctttctac tttttctttt 2640
attttttttt gtcctctgtc ttccatttgt tgttgttgtt gtttgtttgt ttgtttgttg 2700
gttggttggt taattttttt ttaaagatcc tacactatag ttcaagctag actattagct 2760
actctgtaac ccagggtgac cttgaagtca tgggtagcct gctgttttag ccttcccaca 2820
tctaagatta caggtatgag ctatcatttt tggtatattg attgattgat tgattgatgt 2880
gtgtgtgtgt gattgtgttt gtgtgtgtga ctgtgaaaat gtgtgtatgg gtgtgtgtga 2940
atgtgtgtat gtatgtgtgt gtgtgagtgt gtgtgtgtgt gtgtgcatgt gtgtgtgtgt 3000
gactgtgtct atgtgtatga ctgtgtgtgt gtgtgtgtgt gtgtgtgtgt gtgtgtgtgt 3060
gtgtgtgttg tgaaaaaata ttctatggta gtgagagcca acgctccggc tcaggtgtca 3120
ggttggtttt tgagacagag tctttcactt agcttggaat tcactggccg tcgttttaca 3180
acgtcgtgac tgggaaaacc ctggcgttac ccaacttaat cgccttgcag cacatccccc 3240
tttcgccagc tggcgtaata gcgaagaggc ccgcaccgat cgcccttccc aacagttgcg 3300
cagcctgaat ggcgaatggc gcctgatgcg gtattttctc cttacgcatc tgtgcggtat 3360
ttcacaccgc atatggtgca ctctcagtac aatctgctct gatgccgcat agttaagcca 3420
gccccgacac ccgccaacac ccgctgacgc gccctgacgg gcttgtctgc tcccggcatc 3480
cgcttacaga caagctgtga ccgtctccgg gagctgcatg tgtcagaggt tttcaccgtc 3540
atcaccgaaa cgcgcgatga cgaaagggcc tcgtgatacg cctattttta taggttaatg 3600
tcatgataat aatggtttct tagacgtcag gtggcacttt tcggggaaat gtgcgcggaa 3660
cccctatttg tttatttttc taaatacatt caaatatgta tccgctcatg agacaataac 3720
cctgataaat gcttcaataa tattgaaaaa ggaagagtat gagtattcaa catttccgtg 3780
tcgcccttat tccctttttt gcggcatttt gccttcctgt ttttgctcac ccagaaacgc 3840
tggtgaaagt aaaagatgct gaagatcagt tgggtgcacg agtgggttac atcgaactgg 3900
atctcaacag cggtaagatc cttgagagtt ttcgccccga agaacgtttt ccaatgatga 3960
gcacttttaa agttctgcta tgtggcgcgg tattatcccg tattgacgcc gggcaagagc 4020
aactcggtcg ccgcatacac tattctcaga atgacttggt tgagtactca ccagtcacag 4080
aaaagcatct tacggatggc atgacagtaa gagaattatg cagtgctgcc ataaccatga 4140
gtgataacac tgcggccaac ttacttctga caacgatcgg aggaccgaag gagctaaccg 4200
cttttttgca caacatgggg gatcatgtaa ctcgccttga tcgttgggaa ccggagctga 4260
atgaagccat accaaacgac gagcgtgaca ccacgatgcc tgtagcaatg gcaacaacgt 4320
tgcgcaaact attaactggc gaactactta ctctagcttc ccggcaacaa ttaatagact 4380
ggatggaggc ggataaagtt gcaggaccac ttctgcgctc ggcccttccg gctggctggt 4440
ttattgctga taaatctgga gccggtgagc gtgggtctcg cggtatcatt gcagcactgg 4500
ggccagatgg taagccctcc cgtatcgtag ttatctacac gacggggagt caggcaacta 4560
tggatgaacg aaatagacag atcgctgaga taggtgcctc actgattaag cattggtaac 4620
tgtcagacca agtttactca tatatacttt agattgattt aaaacttcat ttttaattta 4680
aaaggatcta ggtgaagatc ctttttgata atctcatgac caaaatccct taacgtgagt 4740
tttcgttcca ctgagcgtca gaccccgtag aaaagatcaa aggatcttct tgagatcctt 4800
tttttctgcg cgtaatctgc tgcttgcaaa caaaaaaacc accgctacca gcggtggttt 4860
gtttgccgga tcaagagcta ccaactcttt ttccgaaggt aactggcttc agcagagcgc 4920
agataccaaa tactgtcctt ctagtgtagc cgtagttagg ccaccacttc aagaactctg 4980
tagcaccgcc tacatacctc gctctgctaa tcctgttacc agtggctgct gccagtggcg 5040
ataagtcgtg tcttaccggg ttggactcaa gacgatagtt accggataag gcgcagcggt 5100
cgggctgaac ggggggttcg tgcacacagc ccagcttgga gcgaacgacc tacaccgaac 5160
tgagatacct acagcgtgag cattgagaaa gcgccacgct tcccgaaggg agaaaggcgg 5220
acaggtatcc ggtaagcggc agggtcggaa caggagagcg cacgagggag cttccagggg 5280
gaaacgcctg gtatctttat agtcctgtcg ggtttcgcca cctctgactt gagcgtcgat 5340
ttttgtgatg ctcgtcaggg gggcggagcc tatggaaaaa cgccagcaac gcggcctttt 5400
tacggttcct ggccttttgc tggccttttg ctcacatgtt ctttcctgcg ttatcccctg 5460
attctgtgga taaccgtatt accgcctttg agtgagctga taccgctcgc cgcagccgaa 5520
cgaccgagcg cagcgagtca gtgagcgagg aagcggaaga gcgcccaata cgcaaaccgc 5580
ctctccccgc gcgttggccg attcattaat gcagctggca cgacaggttt cccgactgga 5640
aagcgggcag tgagcgcaac gcaattaatg tgagttagct cactcattag gcaccccagg 5700
ctttacactt tatgcttccg gctcgtatgt tgtgtggaat tgtgagcgga taacaatttc 5760
acacaggaaa cagctatgac catgattacg ccaagctttg ctcttaggag tttcctaata 5820
catcccaaac tcaaatatat aaagcatttg acttgttcta tgccctaggg ggcgggggga 5880
agctaagcca gcttttttta acatttaaaa tgttaattcc attttaaatg cacagatgtt 5940
tttatttcat aagggtttca atgtgcatga atgctgcaat attcctgtta ccaaagctag 6000
tataaataaa aatagataaa cgtggaaatt acttagagtt tctgtcatta acgtttcctt 6060
cctcagttga caacataaat gcgctgctga gcaagccagt ttgcatctgt caggatcaat 6120
ttcccattat gccagtcata ttaattacta gtcaattagt tgatttttat ttttgacata 6180
tacatgtgaa tgaaagaccc cacctgtagg tttggcaagc tagcttaagt aacgccattt 6240
tgcaaggcat ggaaaaatac ataactgaga atagaaaagt tcagatcaag gtcaggaaca 6300
gatggaacag ctgaatatgg gccaaacagg atatctgtgg taagcagttc ctgccccggc 6360
tcagggccaa gaacagatgg aacagctgaa tatgggccaa acaggatatc tgtggtaagc 6420
agttcctgcc ccggctcagg gccaagaaca gatggtcccc agatgcggtc cagccctcag 6480
cagtttctag agaaccatca gatgtttcca gggtgcccca aggacctgaa atgaccctgt 6540
gccttatttg aactaaccaa tcagttcgct tctcgcttct gttcgcgcgc ttatgctccc 6600
cgagctcaat aaaagagccc acaacccctc actcggggcg ccagtcctcc gattgactga 6660
gtcgcccggg tacccgtgta tccaataaac cctcttgcag ttgcatccga cttgtggtct 6720
cgctgttcct tgggagggtc tcctctgagt gattgactac ccgtcagcgg gggtctttca 6780
tttgggggct cgtccgggat cgggagaccc ctgcccaggg accaccgacc caccaccggg 6840
aggtaagctg gccagcaact tatctgtgtc tgtccgattg tctagtgtct atgactgatt 6900
ttatgcgcct gcgtcggtac tagttagcta actagctctg tatctggcgg acccgtggtg 6960
gaactgacga gttcggaaca cccggccgca accctgggag acgtcccagg gacttcgggg 7020
gccgtttttg tggcccgacc tgagtcctaa aatcccgatc gtttaggact ctttggtgca 7080
ccccccttag aggagggata tgtggttctg gtaggagacg agaacctaaa acagttcccg 7140
cctccgtctg aatttttgct ttcggtttgg gaccgaagcc gcgccgcgcg tcttgtctgc 7200
tgcagcatcg ttctgtgttg tctctgtctg actgtgtttc tgtatttgtc tgaaaatatg 7260
ggcccgggct agactgttac cactccctta agtttgacct taggtcactg gaaagatgtc 7320
gagcggatcg ctcacaacca gtcggtagat gtcaagaaga gacgttgggt taccttctgc 7380
tctgcagaat ggccaacctt taacgtcgga tggccgcgag acggcacctt taaccgagac 7440
ctcatcaccc aggttaagat caaggtcttt tcacctggcc cgcatggaca cccagaccag 7500
gtcccctaca tcgtgacctg ggaagccttg gcttttgacc cccctccctg ggtcaagccc 7560
tttgtacacc ctaagcctcc gcctcctctt cctccatccg ccccgtctct cccccttgaa 7620
cctcctcgtt cgaccccgcc tcgatcctcc ctttatccag ccctcact 7668
<210> 232
<211> 7662
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 232
ccttctctag gcgcccccat atggccatat gagatcttat atggggcacc cccgcccctt 60
gtaaacttcc ctgaccctga catgacaaga gttactaaca gcccctctct ccaagctcac 120
ttacaggctc tctacttagt ccagcacgaa gtctggagac ctctggcggc agcctaccaa 180
gaacaactgg accgaccggt gccgccacca tggaaaccga caccctgctg ctgtgggtgc 240
tgctgctgtg ggtgccagga tccacaggac agtctgtgct gacgcagccg ccctcagtgt 300
ctggggcccc agggcagagg gtcaccatct cctgcactgg gagcagctcc aacatcgggg 360
caggttttga tgtacactgg taccagcagc ttccaggaac agcccccaaa ctcctcatct 420
atggtaacag caatcggccc tcaggggtcc ctgaccgatt ctctggctcc aagtctggca 480
cctcagcctc cctggccatc actgggctcc aggctgagga tgaggctgat tattactgcc 540
agtcctatga cagcagcctg agtggttatg tcttcggaac tgggaccaag gtcaccgtcc 600
taggttctag aggtggtggt ggtagcggcg gcggcggctc tggtggtggt ggatccctcg 660
agatggccca ggtccagctg gtacagtctg gggctgaggt gaagaagcct ggggcctcag 720
tgaaggtctc ctgcaaggct tctggataca ccttcaccga ctactatatg cactgggtgc 780
gacaggcccc tggacaacgg cttgagtgga tgggatggat caaccctaac agtggtggca 840
caaactatgc acagaagttt caggacagga tcaccgtgac cagggacacc tccagcaaca 900
caggctacat ggagctgacc aggctgagat ctgacgacac ggccgtgtat tactgtgcgc 960
gctctccgta ctctggtgtt ctggataaat ggggtcaagg tactctggtg accgtctcct 1020
cagcggccgc acccaccacg acgccagcgc cgcgaccacc aaccccggcg cccacgatcg 1080
cgtcgcagcc cctgtccctg cgcccagagg cgtgccggcc agcggcgggg ggcgcagtgc 1140
acacgagggg gctggacttc gcctgtgata tctacatctg ggcgcccctg gccgggactt 1200
gtggggtcct tctcctgtca ctggttatca ccctttactg caacaaacgg ggcagaaaga 1260
agctcctgta tatattcaaa caaccattta tgagaccagt acaaactact caagaggaag 1320
atggctgtag ctgccgattt ccagaagaag aagaaggagg atgtgaactg agagtgaagt 1380
tcagcaggag cgcagagccc cccgcgtacc agcagggcca gaaccagctc tataacgagc 1440
tcaatctagg acgaagagag gagtacgatg ttttggacaa gagacgtggc cgggaccctg 1500
agatgggggg aaagccgaga aggaagaacc ctcaggaagg cctgtacaat gaactgcaga 1560
aagataagat ggcggaggcc tacagtgaga ttgggatgaa aggcgagcgc cggaggggca 1620
aggggcacga tggcctttac cagggtctca gtacagccac caaggacacc tacgacgccc 1680
ttcacatgca ggccctgccc cctcgctaac agccactcga ggatccggat tagtccaatt 1740
tgttaaagac aggatatcag tggtccaggc tctagttttg actcaacaat atcaccagct 1800
gaagcctata gagtacgagc catagataaa ataaaagatt ttatttagtc tccagaaaaa 1860
ggggggaatg aaagacccca cctgtaggtt tggcaagcta gcttaagtaa cgccattttg 1920
caaggcatgg aaaaatacat aactgagaat agagaagttc agatcaaggt caggaacaga 1980
tggaacagct gaatatgggc caaacaggat atctgtggta agcagttcct gccccggctc 2040
agggccaaga acagatggaa cagctgaata tgggccaaac aggatatctg tggtaagcag 2100
ttcctgcccc ggctcagggc caagaacaga tggtccccag atgcggtcca gccctcagca 2160
gtttctagag aaccatcaga tgtttccagg gtgccccaag gacctgaaat gaccctgtgc 2220
cttatttgaa ctaaccaatc agttcgcttc tcgcttctgt tcgcgcgctt ctgctccccg 2280
agctcaataa aagagcccac aacccctcac tcggggcgcc agtcctccga ttgactgagt 2340
cgcccgggta cccgtgtatc caataaaccc tcttgcagtt gcatccgact tgtggtctcg 2400
ctgttccttg ggagggtctc ctctgagtga ttgactaccc gtcagcgggg gtctttcaca 2460
catgcagcat gtatcaaaat taatttggtt ttttttctta agtatttaca ttaaatggcc 2520
atagtactta aagttacatt ggcttccttg aaataaacat ggagtattca gaatgtgtca 2580
taaatatttc taattttaag atagtatctc cattggcttt ctactttttc ttttattttt 2640
ttttgtcctc tgtcttccat ttgttgttgt tgttgtttgt ttgtttgttt gttggttggt 2700
tggttaattt ttttttaaag atcctacact atagttcaag ctagactatt agctactctg 2760
taacccaggg tgaccttgaa gtcatgggta gcctgctgtt ttagccttcc cacatctaag 2820
attacaggta tgagctatca tttttggtat attgattgat tgattgattg atgtgtgtgt 2880
gtgtgattgt gtttgtgtgt gtgactgtga aaatgtgtgt atgggtgtgt gtgaatgtgt 2940
gtatgtatgt gtgtgtgtga gtgtgtgtgt gtgtgtgtgc atgtgtgtgt gtgtgactgt 3000
gtctatgtgt atgactgtgt gtgtgtgtgt gtgtgtgtgt gtgtgtgtgt gtgtgtgtgt 3060
gttgtgaaaa aatattctat ggtagtgaga gccaacgctc cggctcaggt gtcaggttgg 3120
tttttgagac agagtctttc acttagcttg gaattcactg gccgtcgttt tacaacgtcg 3180
tgactgggaa aaccctggcg ttacccaact taatcgcctt gcagcacatc cccctttcgc 3240
cagctggcgt aatagcgaag aggcccgcac cgatcgccct tcccaacagt tgcgcagcct 3300
gaatggcgaa tggcgcctga tgcggtattt tctccttacg catctgtgcg gtatttcaca 3360
ccgcatatgg tgcactctca gtacaatctg ctctgatgcc gcatagttaa gccagccccg 3420
acacccgcca acacccgctg acgcgccctg acgggcttgt ctgctcccgg catccgctta 3480
cagacaagct gtgaccgtct ccgggagctg catgtgtcag aggttttcac cgtcatcacc 3540
gaaacgcgcg atgacgaaag ggcctcgtga tacgcctatt tttataggtt aatgtcatga 3600
taataatggt ttcttagacg tcaggtggca cttttcgggg aaatgtgcgc ggaaccccta 3660
tttgtttatt tttctaaata cattcaaata tgtatccgct catgagacaa taaccctgat 3720
aaatgcttca ataatattga aaaaggaaga gtatgagtat tcaacatttc cgtgtcgccc 3780
ttattccctt ttttgcggca ttttgccttc ctgtttttgc tcacccagaa acgctggtga 3840
aagtaaaaga tgctgaagat cagttgggtg cacgagtggg ttacatcgaa ctggatctca 3900
acagcggtaa gatccttgag agttttcgcc ccgaagaacg ttttccaatg atgagcactt 3960
ttaaagttct gctatgtggc gcggtattat cccgtattga cgccgggcaa gagcaactcg 4020
gtcgccgcat acactattct cagaatgact tggttgagta ctcaccagtc acagaaaagc 4080
atcttacgga tggcatgaca gtaagagaat tatgcagtgc tgccataacc atgagtgata 4140
acactgcggc caacttactt ctgacaacga tcggaggacc gaaggagcta accgcttttt 4200
tgcacaacat gggggatcat gtaactcgcc ttgatcgttg ggaaccggag ctgaatgaag 4260
ccataccaaa cgacgagcgt gacaccacga tgcctgtagc aatggcaaca acgttgcgca 4320
aactattaac tggcgaacta cttactctag cttcccggca acaattaata gactggatgg 4380
aggcggataa agttgcagga ccacttctgc gctcggccct tccggctggc tggtttattg 4440
ctgataaatc tggagccggt gagcgtgggt ctcgcggtat cattgcagca ctggggccag 4500
atggtaagcc ctcccgtatc gtagttatct acacgacggg gagtcaggca actatggatg 4560
aacgaaatag acagatcgct gagataggtg cctcactgat taagcattgg taactgtcag 4620
accaagttta ctcatatata ctttagattg atttaaaact tcatttttaa tttaaaagga 4680
tctaggtgaa gatccttttt gataatctca tgaccaaaat cccttaacgt gagttttcgt 4740
tccactgagc gtcagacccc gtagaaaaga tcaaaggatc ttcttgagat cctttttttc 4800
tgcgcgtaat ctgctgcttg caaacaaaaa aaccaccgct accagcggtg gtttgtttgc 4860
cggatcaaga gctaccaact ctttttccga aggtaactgg cttcagcaga gcgcagatac 4920
caaatactgt ccttctagtg tagccgtagt taggccacca cttcaagaac tctgtagcac 4980
cgcctacata cctcgctctg ctaatcctgt taccagtggc tgctgccagt ggcgataagt 5040
cgtgtcttac cgggttggac tcaagacgat agttaccgga taaggcgcag cggtcgggct 5100
gaacgggggg ttcgtgcaca cagcccagct tggagcgaac gacctacacc gaactgagat 5160
acctacagcg tgagcattga gaaagcgcca cgcttcccga agggagaaag gcggacaggt 5220
atccggtaag cggcagggtc ggaacaggag agcgcacgag ggagcttcca gggggaaacg 5280
cctggtatct ttatagtcct gtcgggtttc gccacctctg acttgagcgt cgatttttgt 5340
gatgctcgtc aggggggcgg agcctatgga aaaacgccag caacgcggcc tttttacggt 5400
tcctggcctt ttgctggcct tttgctcaca tgttctttcc tgcgttatcc cctgattctg 5460
tggataaccg tattaccgcc tttgagtgag ctgataccgc tcgccgcagc cgaacgaccg 5520
agcgcagcga gtcagtgagc gaggaagcgg aagagcgccc aatacgcaaa ccgcctctcc 5580
ccgcgcgttg gccgattcat taatgcagct ggcacgacag gtttcccgac tggaaagcgg 5640
gcagtgagcg caacgcaatt aatgtgagtt agctcactca ttaggcaccc caggctttac 5700
actttatgct tccggctcgt atgttgtgtg gaattgtgag cggataacaa tttcacacag 5760
gaaacagcta tgaccatgat tacgccaagc tttgctctta ggagtttcct aatacatccc 5820
aaactcaaat atataaagca tttgacttgt tctatgccct agggggcggg gggaagctaa 5880
gccagctttt tttaacattt aaaatgttaa ttccatttta aatgcacaga tgtttttatt 5940
tcataagggt ttcaatgtgc atgaatgctg caatattcct gttaccaaag ctagtataaa 6000
taaaaataga taaacgtgga aattacttag agtttctgtc attaacgttt ccttcctcag 6060
ttgacaacat aaatgcgctg ctgagcaagc cagtttgcat ctgtcaggat caatttccca 6120
ttatgccagt catattaatt actagtcaat tagttgattt ttatttttga catatacatg 6180
tgaatgaaag accccacctg taggtttggc aagctagctt aagtaacgcc attttgcaag 6240
gcatggaaaa atacataact gagaatagaa aagttcagat caaggtcagg aacagatgga 6300
acagctgaat atgggccaaa caggatatct gtggtaagca gttcctgccc cggctcaggg 6360
ccaagaacag atggaacagc tgaatatggg ccaaacagga tatctgtggt aagcagttcc 6420
tgccccggct cagggccaag aacagatggt ccccagatgc ggtccagccc tcagcagttt 6480
ctagagaacc atcagatgtt tccagggtgc cccaaggacc tgaaatgacc ctgtgcctta 6540
tttgaactaa ccaatcagtt cgcttctcgc ttctgttcgc gcgcttatgc tccccgagct 6600
caataaaaga gcccacaacc cctcactcgg ggcgccagtc ctccgattga ctgagtcgcc 6660
cgggtacccg tgtatccaat aaaccctctt gcagttgcat ccgacttgtg gtctcgctgt 6720
tccttgggag ggtctcctct gagtgattga ctacccgtca gcgggggtct ttcatttggg 6780
ggctcgtccg ggatcgggag acccctgccc agggaccacc gacccaccac cgggaggtaa 6840
gctggccagc aacttatctg tgtctgtccg attgtctagt gtctatgact gattttatgc 6900
gcctgcgtcg gtactagtta gctaactagc tctgtatctg gcggacccgt ggtggaactg 6960
acgagttcgg aacacccggc cgcaaccctg ggagacgtcc cagggacttc gggggccgtt 7020
tttgtggccc gacctgagtc ctaaaatccc gatcgtttag gactctttgg tgcacccccc 7080
ttagaggagg gatatgtggt tctggtagga gacgagaacc taaaacagtt cccgcctccg 7140
tctgaatttt tgctttcggt ttgggaccga agccgcgccg cgcgtcttgt ctgctgcagc 7200
atcgttctgt gttgtctctg tctgactgtg tttctgtatt tgtctgaaaa tatgggcccg 7260
ggctagactg ttaccactcc cttaagtttg accttaggtc actggaaaga tgtcgagcgg 7320
atcgctcaca accagtcggt agatgtcaag aagagacgtt gggttacctt ctgctctgca 7380
gaatggccaa cctttaacgt cggatggccg cgagacggca cctttaaccg agacctcatc 7440
acccaggtta agatcaaggt cttttcacct ggcccgcatg gacacccaga ccaggtcccc 7500
tacatcgtga cctgggaagc cttggctttt gacccccctc cctgggtcaa gccctttgta 7560
caccctaagc ctccgcctcc tcttcctcca tccgccccgt ctctccccct tgaacctcct 7620
cgttcgaccc cgcctcgatc ctccctttat ccagccctca ct 7662
<210> 233
<211> 7641
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 233
ccttctctag gcgcccccat atggccatat gagatcttat atggggcacc cccgcccctt 60
gtaaacttcc ctgaccctga catgacaaga gttactaaca gcccctctct ccaagctcac 120
ttacaggctc tctacttagt ccagcacgaa gtctggagac ctctggcggc agcctaccaa 180
gaacaactgg accgaccggt gccgccacca tggaaaccga caccctgctg ctgtgggtgc 240
tgctgctgtg ggtgccagga tccacaggac aatctgccct gactcagcct gcctccgtgt 300
ctgcgtctcc tggacagtcg atcgccatct cctgcactgg aaccagcagt gacgttggtt 360
ggtatcaaca gcacccaggc aaagccccca aactcatgat ttatgaggac agtaagcggc 420
cctcaggggt ttctaatcgc ttctctggct ccaagtctgg caacacggcc tccctgacca 480
tctctgggct ccaggctgag gacgaggctg attattactg cagctcaaat acaagaagca 540
gcactttggt gttcggcgga gggaccaagc tgaccgtcct aggttctaga ggtggtggtg 600
gtagcggcgg cggcggctct ggtggtggtg gatccctcga gatggccgaa gtgcagctgg 660
tgcagtctgg ggctgagatg aagaagcctg gggcctcact gaagctctcc tgcaaggctt 720
ctggatacac cttcatcgac tactatgtat actggatgcg acaggcccct ggacaagggc 780
ttgagtccat gggatggatc aaccctaaca gtggtggcac aaactatgca cagaagtttc 840
agggcagggt caccatgacc agggacacgt ccatcagcac agcctacatg gagctgagca 900
ggctgagatc tgacgacacc gccatgtatt actgtgcgcg ctcccagcgt gacggttaca 960
tggattactg gggtcaaggt actctggtga ccgtctcctc agcggccgca cccaccacga 1020
cgccagcgcc gcgaccacca accccggcgc ccacgatcgc gtcgcagccc ctgtccctgc 1080
gcccagaggc gtgccggcca gcggcggggg gcgcagtgca cacgaggggg ctggacttcg 1140
cctgtgatat ctacatctgg gcgcccctgg ccgggacttg tggggtcctt ctcctgtcac 1200
tggttatcac cctttactgc aacaaacggg gcagaaagaa gctcctgtat atattcaaac 1260
aaccatttat gagaccagta caaactactc aagaggaaga tggctgtagc tgccgatttc 1320
cagaagaaga agaaggagga tgtgaactga gagtgaagtt cagcaggagc gcagagcccc 1380
ccgcgtacca gcagggccag aaccagctct ataacgagct caatctagga cgaagagagg 1440
agtacgatgt tttggacaag agacgtggcc gggaccctga gatgggggga aagccgagaa 1500
ggaagaaccc tcaggaaggc ctgtacaatg aactgcagaa agataagatg gcggaggcct 1560
acagtgagat tgggatgaaa ggcgagcgcc ggaggggcaa ggggcacgat ggcctttacc 1620
agggtctcag tacagccacc aaggacacct acgacgccct tcacatgcag gccctgcccc 1680
ctcgctaaca gccactcgag gatccggatt agtccaattt gttaaagaca ggatatcagt 1740
ggtccaggct ctagttttga ctcaacaata tcaccagctg aagcctatag agtacgagcc 1800
atagataaaa taaaagattt tatttagtct ccagaaaaag gggggaatga aagaccccac 1860
ctgtaggttt ggcaagctag cttaagtaac gccattttgc aaggcatgga aaaatacata 1920
actgagaata gagaagttca gatcaaggtc aggaacagat ggaacagctg aatatgggcc 1980
aaacaggata tctgtggtaa gcagttcctg ccccggctca gggccaagaa cagatggaac 2040
agctgaatat gggccaaaca ggatatctgt ggtaagcagt tcctgccccg gctcagggcc 2100
aagaacagat ggtccccaga tgcggtccag ccctcagcag tttctagaga accatcagat 2160
gtttccaggg tgccccaagg acctgaaatg accctgtgcc ttatttgaac taaccaatca 2220
gttcgcttct cgcttctgtt cgcgcgcttc tgctccccga gctcaataaa agagcccaca 2280
acccctcact cggggcgcca gtcctccgat tgactgagtc gcccgggtac ccgtgtatcc 2340
aataaaccct cttgcagttg catccgactt gtggtctcgc tgttccttgg gagggtctcc 2400
tctgagtgat tgactacccg tcagcggggg tctttcacac atgcagcatg tatcaaaatt 2460
aatttggttt tttttcttaa gtatttacat taaatggcca tagtacttaa agttacattg 2520
gcttccttga aataaacatg gagtattcag aatgtgtcat aaatatttct aattttaaga 2580
tagtatctcc attggctttc tactttttct tttatttttt tttgtcctct gtcttccatt 2640
tgttgttgtt gttgtttgtt tgtttgtttg ttggttggtt ggttaatttt tttttaaaga 2700
tcctacacta tagttcaagc tagactatta gctactctgt aacccagggt gaccttgaag 2760
tcatgggtag cctgctgttt tagccttccc acatctaaga ttacaggtat gagctatcat 2820
ttttggtata ttgattgatt gattgattga tgtgtgtgtg tgtgattgtg tttgtgtgtg 2880
tgactgtgaa aatgtgtgta tgggtgtgtg tgaatgtgtg tatgtatgtg tgtgtgtgag 2940
tgtgtgtgtg tgtgtgtgca tgtgtgtgtg tgtgactgtg tctatgtgta tgactgtgtg 3000
tgtgtgtgtg tgtgtgtgtg tgtgtgtgtg tgtgtgtgtg ttgtgaaaaa atattctatg 3060
gtagtgagag ccaacgctcc ggctcaggtg tcaggttggt ttttgagaca gagtctttca 3120
cttagcttgg aattcactgg ccgtcgtttt acaacgtcgt gactgggaaa accctggcgt 3180
tacccaactt aatcgccttg cagcacatcc ccctttcgcc agctggcgta atagcgaaga 3240
ggcccgcacc gatcgccctt cccaacagtt gcgcagcctg aatggcgaat ggcgcctgat 3300
gcggtatttt ctccttacgc atctgtgcgg tatttcacac cgcatatggt gcactctcag 3360
tacaatctgc tctgatgccg catagttaag ccagccccga cacccgccaa cacccgctga 3420
cgcgccctga cgggcttgtc tgctcccggc atccgcttac agacaagctg tgaccgtctc 3480
cgggagctgc atgtgtcaga ggttttcacc gtcatcaccg aaacgcgcga tgacgaaagg 3540
gcctcgtgat acgcctattt ttataggtta atgtcatgat aataatggtt tcttagacgt 3600
caggtggcac ttttcgggga aatgtgcgcg gaacccctat ttgtttattt ttctaaatac 3660
attcaaatat gtatccgctc atgagacaat aaccctgata aatgcttcaa taatattgaa 3720
aaaggaagag tatgagtatt caacatttcc gtgtcgccct tattcccttt tttgcggcat 3780
tttgccttcc tgtttttgct cacccagaaa cgctggtgaa agtaaaagat gctgaagatc 3840
agttgggtgc acgagtgggt tacatcgaac tggatctcaa cagcggtaag atccttgaga 3900
gttttcgccc cgaagaacgt tttccaatga tgagcacttt taaagttctg ctatgtggcg 3960
cggtattatc ccgtattgac gccgggcaag agcaactcgg tcgccgcata cactattctc 4020
agaatgactt ggttgagtac tcaccagtca cagaaaagca tcttacggat ggcatgacag 4080
taagagaatt atgcagtgct gccataacca tgagtgataa cactgcggcc aacttacttc 4140
tgacaacgat cggaggaccg aaggagctaa ccgctttttt gcacaacatg ggggatcatg 4200
taactcgcct tgatcgttgg gaaccggagc tgaatgaagc cataccaaac gacgagcgtg 4260
acaccacgat gcctgtagca atggcaacaa cgttgcgcaa actattaact ggcgaactac 4320
ttactctagc ttcccggcaa caattaatag actggatgga ggcggataaa gttgcaggac 4380
cacttctgcg ctcggccctt ccggctggct ggtttattgc tgataaatct ggagccggtg 4440
agcgtgggtc tcgcggtatc attgcagcac tggggccaga tggtaagccc tcccgtatcg 4500
tagttatcta cacgacgggg agtcaggcaa ctatggatga acgaaataga cagatcgctg 4560
agataggtgc ctcactgatt aagcattggt aactgtcaga ccaagtttac tcatatatac 4620
tttagattga tttaaaactt catttttaat ttaaaaggat ctaggtgaag atcctttttg 4680
ataatctcat gaccaaaatc ccttaacgtg agttttcgtt ccactgagcg tcagaccccg 4740
tagaaaagat caaaggatct tcttgagatc ctttttttct gcgcgtaatc tgctgcttgc 4800
aaacaaaaaa accaccgcta ccagcggtgg tttgtttgcc ggatcaagag ctaccaactc 4860
tttttccgaa ggtaactggc ttcagcagag cgcagatacc aaatactgtc cttctagtgt 4920
agccgtagtt aggccaccac ttcaagaact ctgtagcacc gcctacatac ctcgctctgc 4980
taatcctgtt accagtggct gctgccagtg gcgataagtc gtgtcttacc gggttggact 5040
caagacgata gttaccggat aaggcgcagc ggtcgggctg aacggggggt tcgtgcacac 5100
agcccagctt ggagcgaacg acctacaccg aactgagata cctacagcgt gagcattgag 5160
aaagcgccac gcttcccgaa gggagaaagg cggacaggta tccggtaagc ggcagggtcg 5220
gaacaggaga gcgcacgagg gagcttccag ggggaaacgc ctggtatctt tatagtcctg 5280
tcgggtttcg ccacctctga cttgagcgtc gatttttgtg atgctcgtca ggggggcgga 5340
gcctatggaa aaacgccagc aacgcggcct ttttacggtt cctggccttt tgctggcctt 5400
ttgctcacat gttctttcct gcgttatccc ctgattctgt ggataaccgt attaccgcct 5460
ttgagtgagc tgataccgct cgccgcagcc gaacgaccga gcgcagcgag tcagtgagcg 5520
aggaagcgga agagcgccca atacgcaaac cgcctctccc cgcgcgttgg ccgattcatt 5580
aatgcagctg gcacgacagg tttcccgact ggaaagcggg cagtgagcgc aacgcaatta 5640
atgtgagtta gctcactcat taggcacccc aggctttaca ctttatgctt ccggctcgta 5700
tgttgtgtgg aattgtgagc ggataacaat ttcacacagg aaacagctat gaccatgatt 5760
acgccaagct ttgctcttag gagtttccta atacatccca aactcaaata tataaagcat 5820
ttgacttgtt ctatgcccta gggggcgggg ggaagctaag ccagcttttt ttaacattta 5880
aaatgttaat tccattttaa atgcacagat gtttttattt cataagggtt tcaatgtgca 5940
tgaatgctgc aatattcctg ttaccaaagc tagtataaat aaaaatagat aaacgtggaa 6000
attacttaga gtttctgtca ttaacgtttc cttcctcagt tgacaacata aatgcgctgc 6060
tgagcaagcc agtttgcatc tgtcaggatc aatttcccat tatgccagtc atattaatta 6120
ctagtcaatt agttgatttt tatttttgac atatacatgt gaatgaaaga ccccacctgt 6180
aggtttggca agctagctta agtaacgcca ttttgcaagg catggaaaaa tacataactg 6240
agaatagaaa agttcagatc aaggtcagga acagatggaa cagctgaata tgggccaaac 6300
aggatatctg tggtaagcag ttcctgcccc ggctcagggc caagaacaga tggaacagct 6360
gaatatgggc caaacaggat atctgtggta agcagttcct gccccggctc agggccaaga 6420
acagatggtc cccagatgcg gtccagccct cagcagtttc tagagaacca tcagatgttt 6480
ccagggtgcc ccaaggacct gaaatgaccc tgtgccttat ttgaactaac caatcagttc 6540
gcttctcgct tctgttcgcg cgcttatgct ccccgagctc aataaaagag cccacaaccc 6600
ctcactcggg gcgccagtcc tccgattgac tgagtcgccc gggtacccgt gtatccaata 6660
aaccctcttg cagttgcatc cgacttgtgg tctcgctgtt ccttgggagg gtctcctctg 6720
agtgattgac tacccgtcag cgggggtctt tcatttgggg gctcgtccgg gatcgggaga 6780
cccctgccca gggaccaccg acccaccacc gggaggtaag ctggccagca acttatctgt 6840
gtctgtccga ttgtctagtg tctatgactg attttatgcg cctgcgtcgg tactagttag 6900
ctaactagct ctgtatctgg cggacccgtg gtggaactga cgagttcgga acacccggcc 6960
gcaaccctgg gagacgtccc agggacttcg ggggccgttt ttgtggcccg acctgagtcc 7020
taaaatcccg atcgtttagg actctttggt gcacccccct tagaggaggg atatgtggtt 7080
ctggtaggag acgagaacct aaaacagttc ccgcctccgt ctgaattttt gctttcggtt 7140
tgggaccgaa gccgcgccgc gcgtcttgtc tgctgcagca tcgttctgtg ttgtctctgt 7200
ctgactgtgt ttctgtattt gtctgaaaat atgggcccgg gctagactgt taccactccc 7260
ttaagtttga ccttaggtca ctggaaagat gtcgagcgga tcgctcacaa ccagtcggta 7320
gatgtcaaga agagacgttg ggttaccttc tgctctgcag aatggccaac ctttaacgtc 7380
ggatggccgc gagacggcac ctttaaccga gacctcatca cccaggttaa gatcaaggtc 7440
ttttcacctg gcccgcatgg acacccagac caggtcccct acatcgtgac ctgggaagcc 7500
ttggcttttg acccccctcc ctgggtcaag ccctttgtac accctaagcc tccgcctcct 7560
cttcctccat ccgccccgtc tctccccctt gaacctcctc gttcgacccc gcctcgatcc 7620
tccctttatc cagccctcac t 7641
<210> 234
<211> 1491
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 234
atggaaaccg acaccctgct gctgtgggtg ctgctgctgt gggtgccagg atccacagga 60
ctgcctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 120
tcttgttctg gacgcagttc caacatcggg agtaattctg ttaactggta tcgacaactc 180
ccaggagcgg cccccaaact cctcatctat agtaataatc agcggccccc aggggtccct 240
gtgcgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccag 300
tctgaagatg aggccactta ttactgtgca acatgggatg acaatctgaa tgttcactat 360
gtcttcggaa ctgggaccaa ggtcaccgtc ctaggttcta gaggtggtgg tggtagcggc 420
ggcggcggct ctggtggtgg tggatccctc gagatggccc aggtgcagct ggtgcagtct 480
ggggctgagg tgaagaagcc tgggtcctcg gtgaaggtct cctgcaaggc ttctggaggc 540
accttcagca gctatgctat cagctgggtg cgacaggccc ctggacaagg gcttgagtgg 600
atgggaagga tcatccctat ccttggtata gcaaactacg cacagaagtt ccagggcaga 660
gtcacgatta ccgcggacaa atccacgagc acagcctaca tggagctgag cagcctgaga 720
tctgaggaca cggccgtgta ttactgtgcg cgcggtggtt actactctca tgacatgtgg 780
tctgaagatt ggggtcaagg tactctggtg accgtctcct cagcggccgc aattgaagtt 840
atgtatcctc ctccttacct agacaatgag aagagcaatg gaaccattat ccatgtgaaa 900
gggaaacacc tttgtccaag tcccctattt cccggacctt ctaagccctt ttgggtgctg 960
gtggtggttg gtggagtcct ggcttgctat agcttgctag taacagtggc ctttattatt 1020
ttctgggtga ggagtaagag gagcaggctc ctgcacagtg actacatgaa catgactccc 1080
cgccgccccg ggcccacccg caagcattac cagccctatg ccccaccacg cgacttcgca 1140
gcctatcgct ccagagtgaa gttcagcagg agcgcagacg cccccgcgta ccagcagggc 1200
cagaaccagc tctataacga gctcaatcta ggacgaagag aggagtacga tgttttggac 1260
aagagacgtg gccgggaccc tgagatgggg ggaaagccga gaaggaagaa ccctcaggaa 1320
ggcctgtaca atgaactgca gaaagataag atggcggagg cctacagtga gattgggatg 1380
aaaggcgagc gccggagggg caaggggcac gatggccttt accagggtct cagtacagcc 1440
accaaggaca cctacgacgc ccttcacatg caggccctgc cccctcgcta a 1491
<210> 235
<211> 1488
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полинуклеотид
<400> 235
atggaaaccg acaccctgct gctgtgggtg ctgctgctgt gggtgccagg atccacagga 60
caggctgtgc tgactcagcc accctcagcg tctgggaccc ccgggcagag ggtcaccatc 120
tcttgttctg gaagcagctc caacatcgga agtaattacg tattctggta ccagcagctc 180
ccaggaacgg cccccaaact cctcatctat agtaataatc agcggccctc aggggtccct 240
gaccgattct ctggctccaa gtctggcacc tcagcctccc tggccatcag tgggctccgg 300
tccgaggatg aggctgatta ttactgtgca gcatgggatg acagcctgag tgcctcttat 360
gttttcggaa ctgggaccaa ggtcaccgtc ctaggttcta gaggtggtgg tggtagcggc 420
ggcggcggct ctggtggtgg tggatccctc gagatggccc aggtgcagct ggtgcagtct 480
ggggctgagg tgaagaagcc tgggtcctcg gtgaaggtct cctgcaaggc ttctggaggc 540
accttcagca gctatgctat cagctgggtg cgacaggccc ctggacaagg gcttgagtgg 600
atgggaagga tcatccctat ccttggtaca gcaaactacg cacagaagtt ccagggcaga 660
gtcacgatta ccgcggacga atccacgagc acagcctaca tggagctgag cagcctgaga 720
tctgaggaca cggccgtgta ttactgtgcg cgctctggtt acggttctta ccgttgggaa 780
gattcttggg gtcaaggtac tctggtgacc gtctcctcag cggccgcaat tgaagttatg 840
tatcctcctc cttacctaga caatgagaag agcaatggaa ccattatcca tgtgaaaggg 900
aaacaccttt gtccaagtcc cctatttccc ggaccttcta agcccttttg ggtgctggtg 960
gtggttggtg gagtcctggc ttgctatagc ttgctagtaa cagtggcctt tattattttc 1020
tgggtgagga gtaagaggag caggctcctg cacagtgact acatgaacat gactccccgc 1080
cgccccgggc ccacccgcaa gcattaccag ccctatgccc caccacgcga cttcgcagcc 1140
tatcgctcca gagtgaagtt cagcaggagc gcagacgccc ccgcgtacca gcagggccag 1200
aaccagctct ataacgagct caatctagga cgaagagagg agtacgatgt tttggacaag 1260
agacgtggcc gggaccctga gatgggggga aagccgagaa ggaagaaccc tcaggaaggc 1320
ctgtacaatg aactgcagaa agataagatg gcggaggcct acagtgagat tgggatgaaa 1380
ggcgagcgcc ggaggggcaa ggggcacgat ggcctttacc agggtctcag tacagccacc 1440
aaggacacct acgacgccct tcacatgcag gccctgcccc ctcgctaa 1488
<210> 236
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 236
Ser Gly Ser Gly Leu Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr
1 5 10 15
Phe Asp Ser
<210> 237
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 237
Ser Gly Ser Gly Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe
1 5 10 15
Asp Ser Leu
<210> 238
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 238
Ser Gly Ser Gly Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp
1 5 10 15
Ser Leu Leu
<210> 239
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 239
Ser Gly Ser Gly Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser
1 5 10 15
Leu Leu His
<210> 240
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 240
Ser Gly Ser Gly Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser Leu
1 5 10 15
Leu His Ala
<210> 241
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 241
Ser Gly Ser Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser Leu Leu
1 5 10 15
His Ala Cys
<210> 242
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 242
Ser Gly Ser Gly Cys Ser Gln Asn Glu Tyr Phe Asp Ser Leu Leu His
1 5 10 15
Ala Cys Ile
<210> 243
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 243
Ser Gly Ser Gly Ser Gln Asn Glu Tyr Phe Asp Ser Leu Leu His Ala
1 5 10 15
Cys Ile Pro
<210> 244
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 244
Ser Gly Ser Gly Gln Asn Glu Tyr Phe Asp Ser Leu Leu His Ala Cys
1 5 10 15
Ile Pro Cys
<210> 245
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 245
Ser Gly Ser Gly Asn Glu Tyr Phe Asp Ser Leu Leu His Ala Cys Ile
1 5 10 15
Pro Cys Gln
<210> 246
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 246
Ser Gly Ser Gly Glu Tyr Phe Asp Ser Leu Leu His Ala Cys Ile Pro
1 5 10 15
Cys Gln Leu
<210> 247
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 247
Ser Gly Ser Gly Tyr Phe Asp Ser Leu Leu His Ala Cys Ile Pro Cys
1 5 10 15
Gln Leu Arg
<210> 248
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 248
Ser Gly Ser Gly Phe Asp Ser Leu Leu His Ala Cys Ile Pro Cys Gln
1 5 10 15
Leu Arg Cys
<210> 249
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 249
Ser Gly Ser Gly Asp Ser Leu Leu His Ala Cys Ile Pro Cys Gln Leu
1 5 10 15
Arg Cys Ser
<210> 250
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 250
Ser Gly Ser Gly Ser Leu Leu His Ala Cys Ile Pro Cys Gln Leu Arg
1 5 10 15
Cys Ser Ser
<210> 251
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 251
Ser Gly Ser Gly Leu Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys
1 5 10 15
Ser Ser Asn
<210> 252
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 252
Ser Gly Ser Gly Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser
1 5 10 15
Ser Asn Thr
<210> 253
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 253
Ser Gly Ser Gly His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser
1 5 10 15
Asn Thr Pro
<210> 254
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 254
Ser Gly Ser Gly Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn
1 5 10 15
Thr Pro Pro
<210> 255
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 255
Ser Gly Ser Gly Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr
1 5 10 15
Pro Pro Leu
<210> 256
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 256
Ser Gly Ser Gly Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr Pro
1 5 10 15
Pro Leu Thr
<210> 257
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 257
Ser Gly Ser Gly Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr Pro Pro
1 5 10 15
Leu Thr Cys
<210> 258
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 258
Ser Gly Ser Gly Cys Gln Leu Arg Cys Ser Ser Asn Thr Pro Pro Leu
1 5 10 15
Thr Cys Gln
<210> 259
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 259
Ser Gly Ser Gly Gln Leu Arg Cys Ser Ser Asn Thr Pro Pro Leu Thr
1 5 10 15
Cys Gln Arg
<210> 260
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 260
Ser Gly Ser Gly Leu Arg Cys Ser Ser Asn Thr Pro Pro Leu Thr Cys
1 5 10 15
Gln Arg Tyr
<210> 261
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 261
Ser Gly Ser Gly Arg Cys Ser Ser Asn Thr Pro Pro Leu Thr Cys Gln
1 5 10 15
Arg Tyr Cys
<210> 262
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 262
Ser Gly Ser Gly Cys Ser Ser Asn Thr Pro Pro Leu Thr Cys Gln Arg
1 5 10 15
Tyr Cys Asn
<210> 263
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 263
Ser Gly Ser Gly Ser Ser Asn Thr Pro Pro Leu Thr Cys Gln Arg Tyr
1 5 10 15
Cys Asn Ala
<210> 264
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 264
Ser Gly Ser Gly Ser Asn Thr Pro Pro Leu Thr Cys Gln Arg Tyr Cys
1 5 10 15
Asn Ala Ser
<210> 265
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 265
Ser Gly Ser Gly Asn Thr Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn
1 5 10 15
Ala Ser Val
<210> 266
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 266
Ser Gly Ser Gly Thr Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala
1 5 10 15
Ser Val Thr
<210> 267
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 267
Ser Gly Ser Gly Pro Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser
1 5 10 15
Val Thr Asn
<210> 268
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 268
Ser Gly Ser Gly Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val
1 5 10 15
Thr Asn Ser
<210> 269
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 269
Ser Gly Ser Gly Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr
1 5 10 15
Asn Ser Val
<210> 270
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 270
Ser Gly Ser Gly Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn
1 5 10 15
Ser Val Lys
<210> 271
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 271
Ser Gly Ser Gly Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser
1 5 10 15
Val Lys Gly
<210> 272
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 272
Ser Gly Ser Gly Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser Val
1 5 10 15
Lys Gly Thr
<210> 273
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 273
Ser Gly Ser Gly Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser Val Lys
1 5 10 15
Gly Thr Asn
<210> 274
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 274
Ser Gly Ser Gly Tyr Cys Asn Ala Ser Val Thr Asn Ser Val Lys Gly
1 5 10 15
Thr Asn Ala
<210> 275
<211> 25
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 275
Thr Ser Gly Gln Ala Gly Gln His His His His His His Gly Ala Tyr
1 5 10 15
Pro Tyr Asp Val Pro Asp Tyr Ala Ser
20 25
<210> 276
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
олигонуклеотид
<400> 276
actagtggcc aggccggcca gcaccatcac catcaccatg gcgcataccc gtacgacgtt 60
ccggactacg cttct 75
<210> 277
<211> 4
<212> БЕЛОК
<213> Homo sapiens
<400> 277
Tyr Val Lys Met
1
<210> 278
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 278
Ser Gly Ser Gly
1
<210> 279
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
пептид
<400> 279
Gly Ser Ser Ser Ser
1 5
<210> 280
<211> 53
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический
полипептид
<400> 280
Leu Gln Met Ala Gly Gln Cys Ser Gln Asn Glu Tyr Phe Asp Ser Leu
1 5 10 15
Leu His Ala Cys Ile Pro Cys Gln Leu Arg Cys Ser Ser Asn Thr Pro
20 25 30
Pro Leu Thr Cys Gln Arg Tyr Cys Asn Ala Ser Val Thr Asn Ser Val
35 40 45
Lys Gly Thr Asn Ala
50
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2766094C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОГО НОВООБРАЗОВАНИЯ С ИСПОЛЬЗОВАНИЕМ ГУМАНИЗИРОВАННОГО ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА ПРОТИВ ВСМА | 2015 |
|
RU2751660C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2841244C2 |
| Антитело к BCMA, его антигенсвязывающий фрагмент и их медицинское применение | 2020 |
|
RU2819660C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ ВСМА, NKG2D И CD16 | 2018 |
|
RU2805254C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО К BCMA И BCMA-CAR-T-КЛЕТКИ | 2020 |
|
RU2762942C1 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ К BCMA | 2015 |
|
RU2747457C2 |
| АНТИ-BCMA АНТИТЕЛА, СОДЕРЖАЩИЕ ТОЛЬКО ТЯЖЁЛУЮ ЦЕПЬ | 2017 |
|
RU2781301C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2019 |
|
RU2810092C2 |
| АНТИТЕЛО, НАЦЕЛЕННОЕ НА ВСМА, И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2799655C2 |
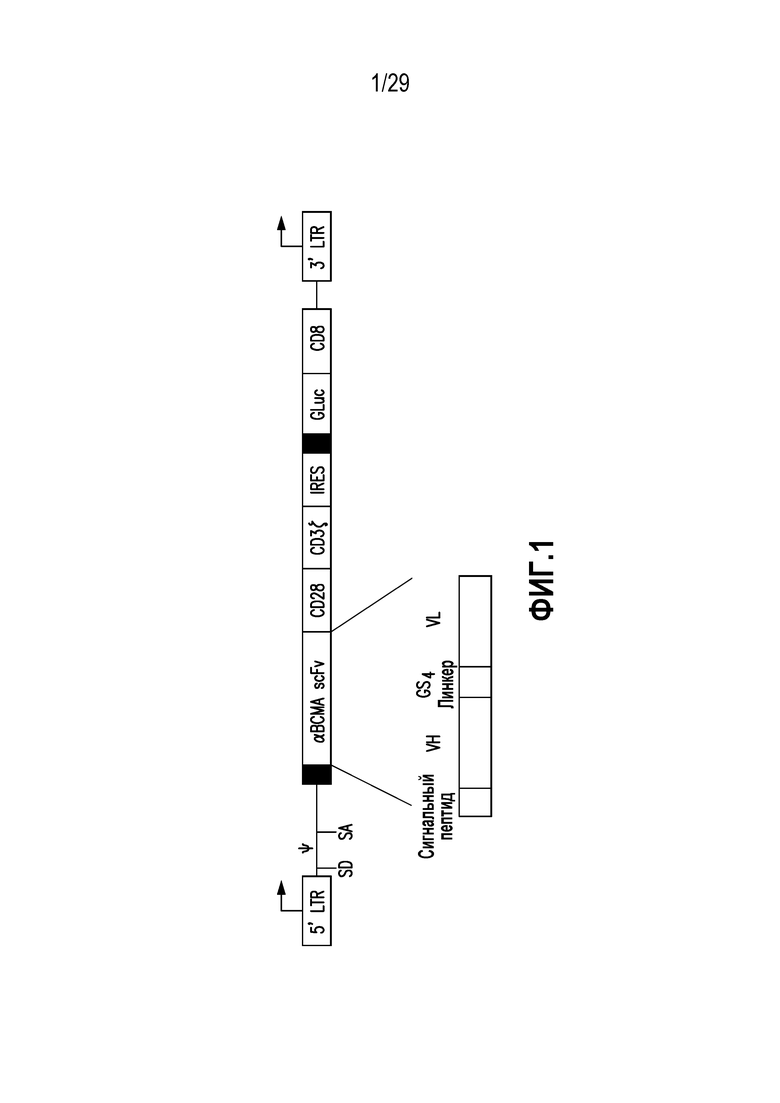
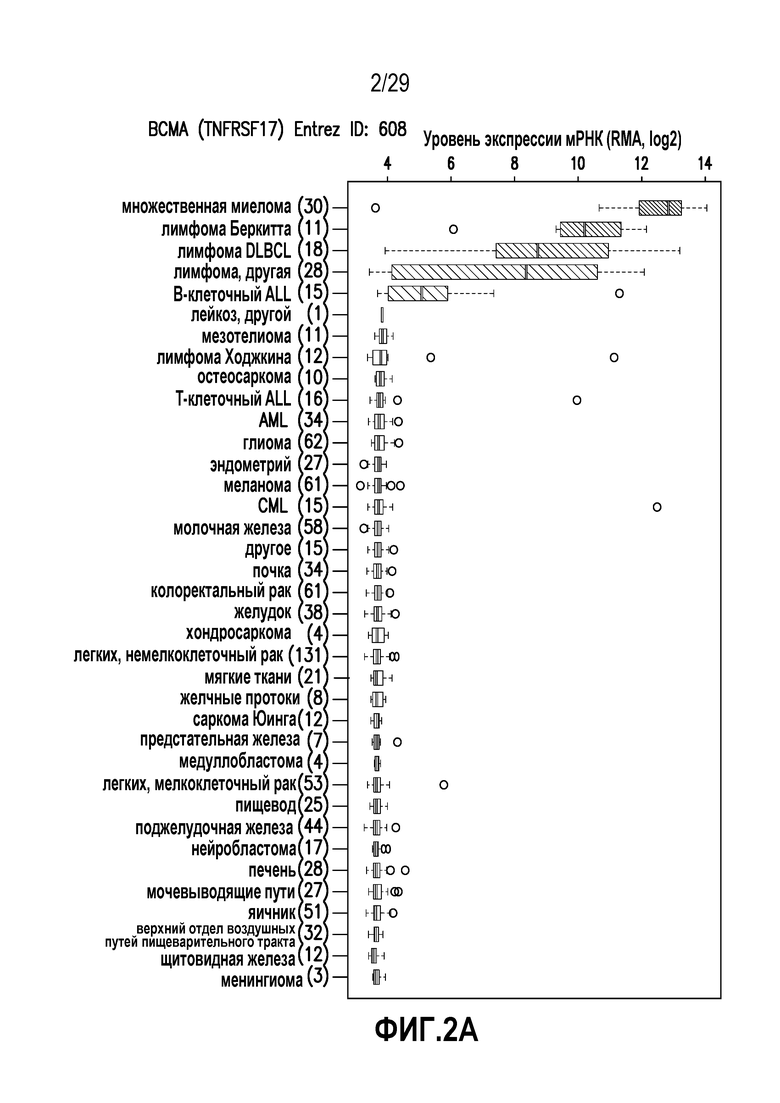


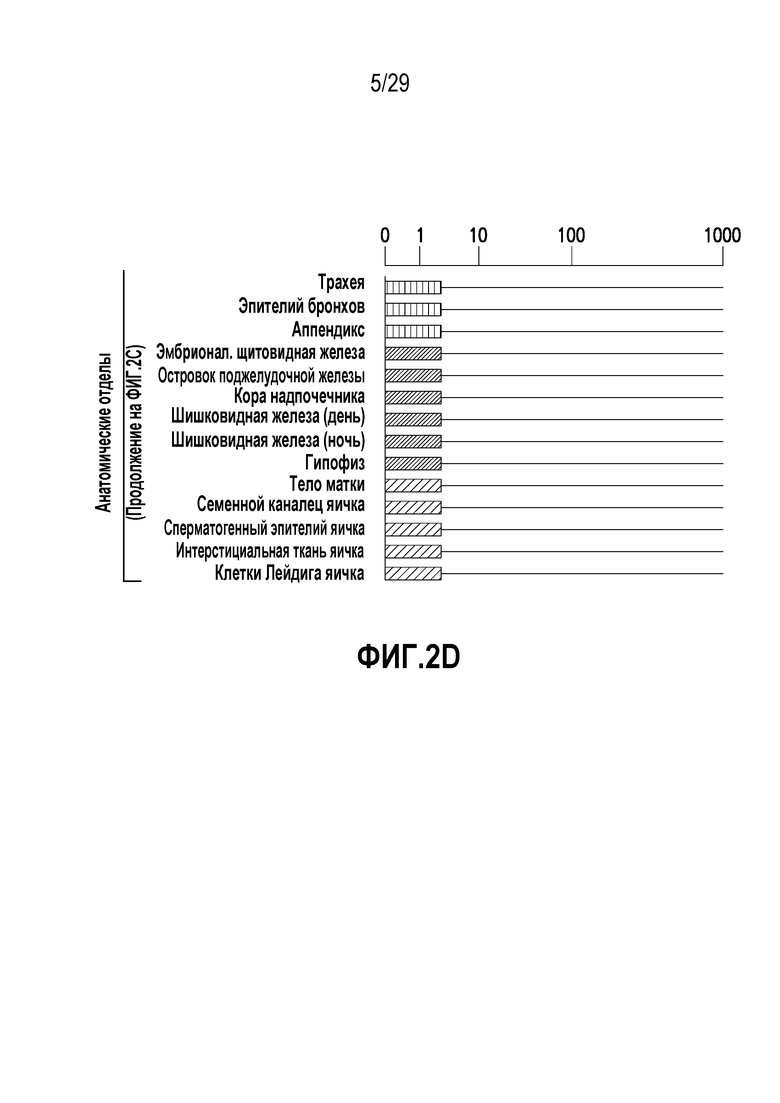
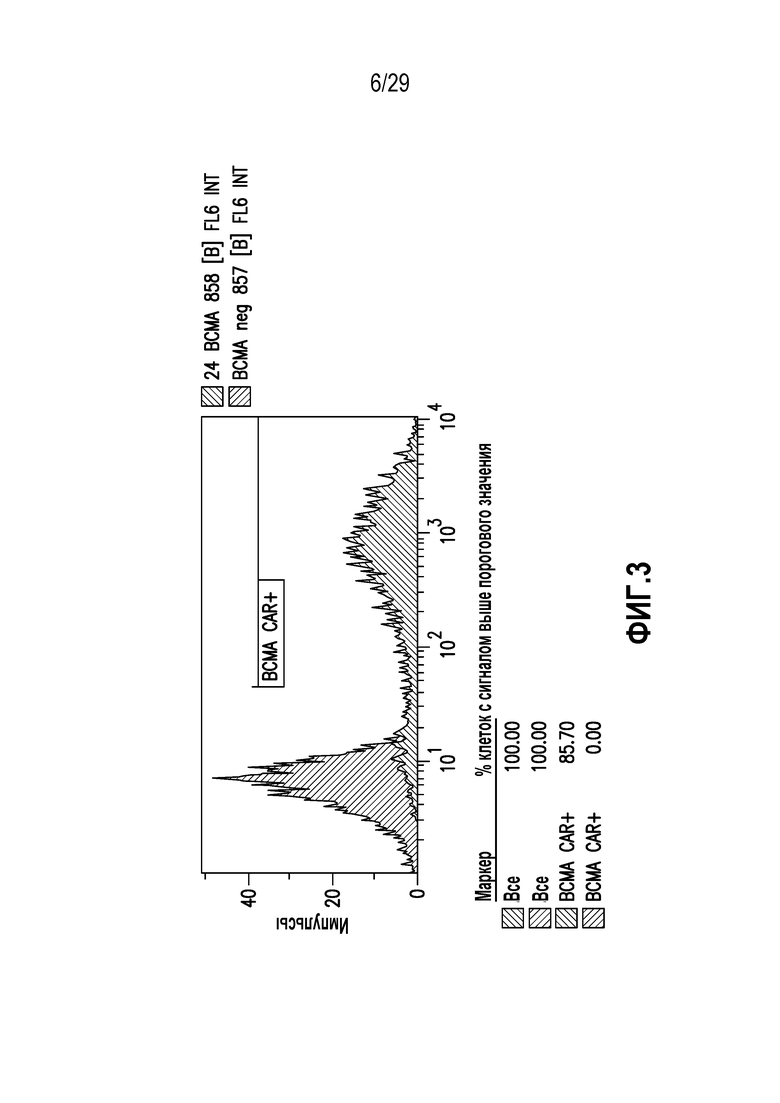
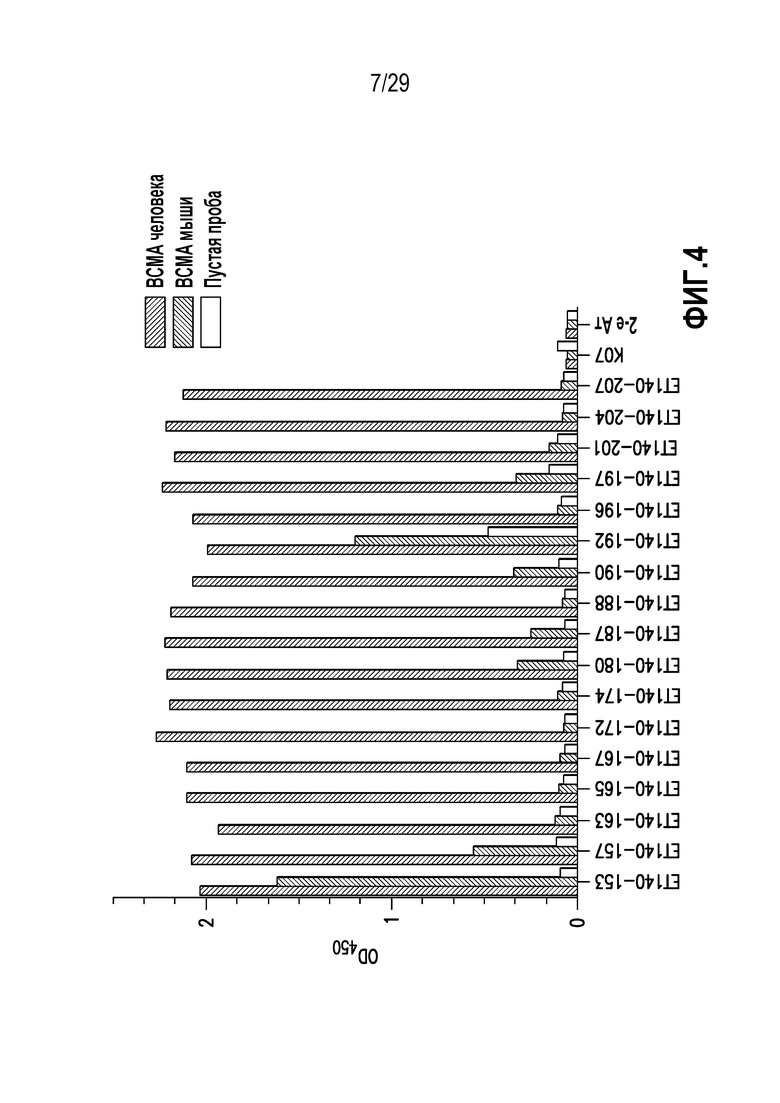

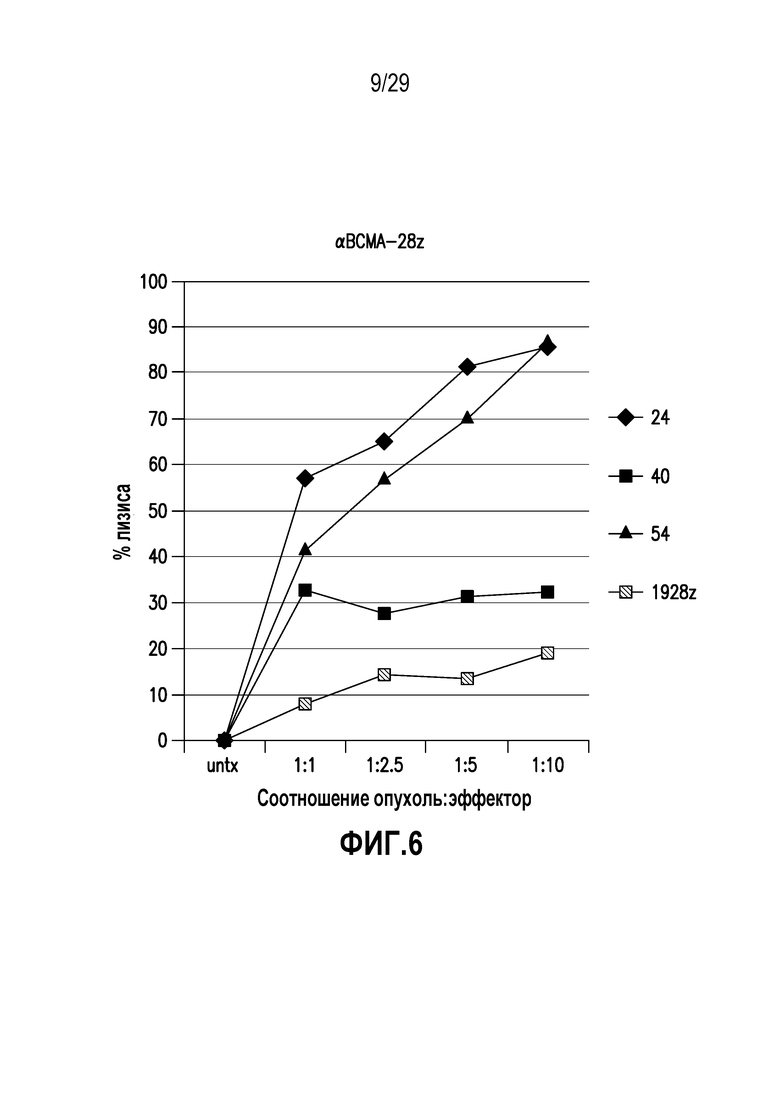
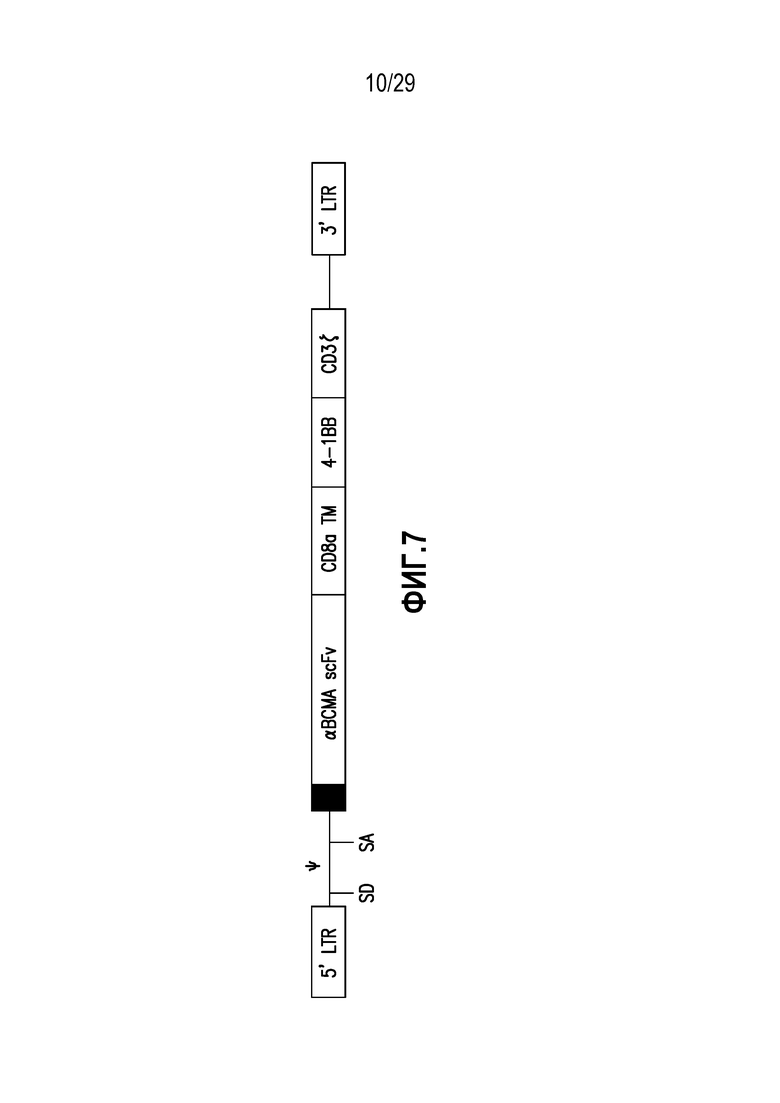
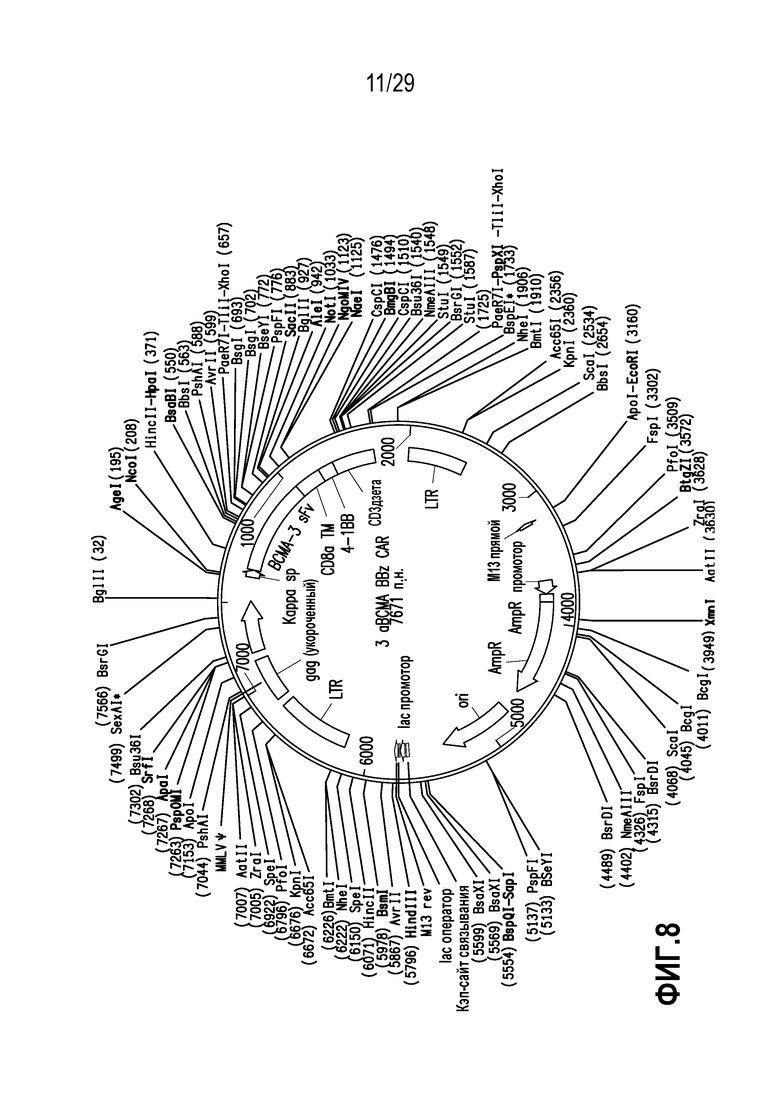
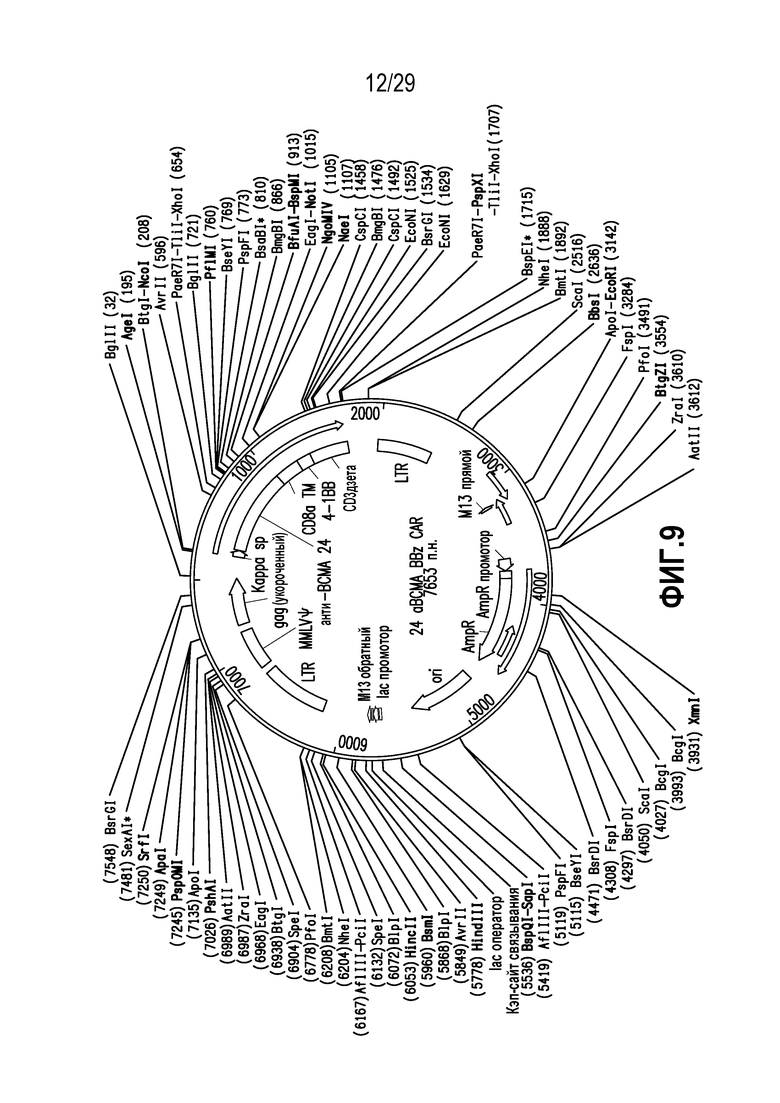
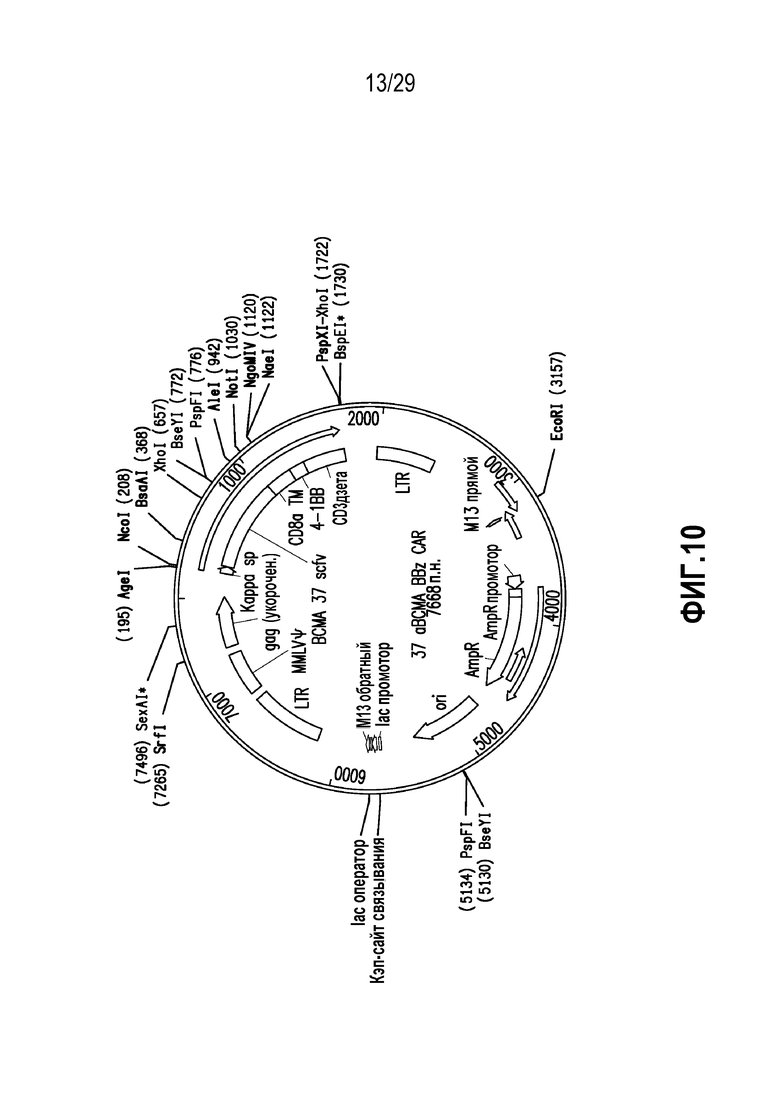
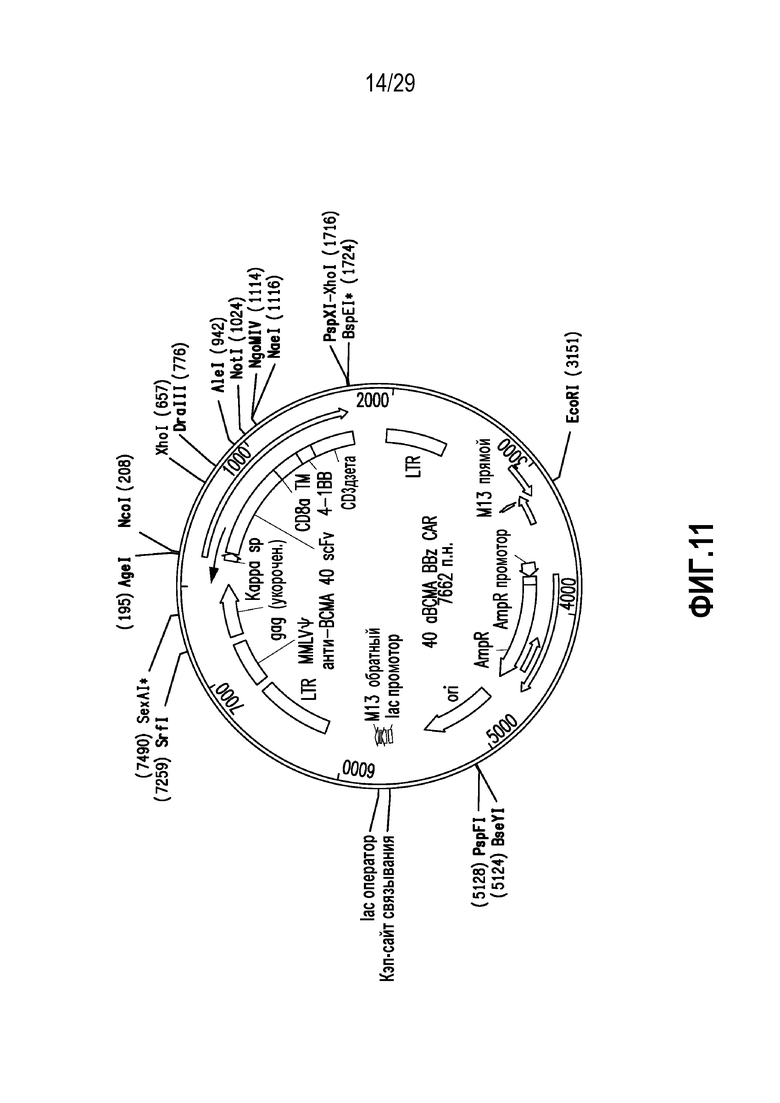
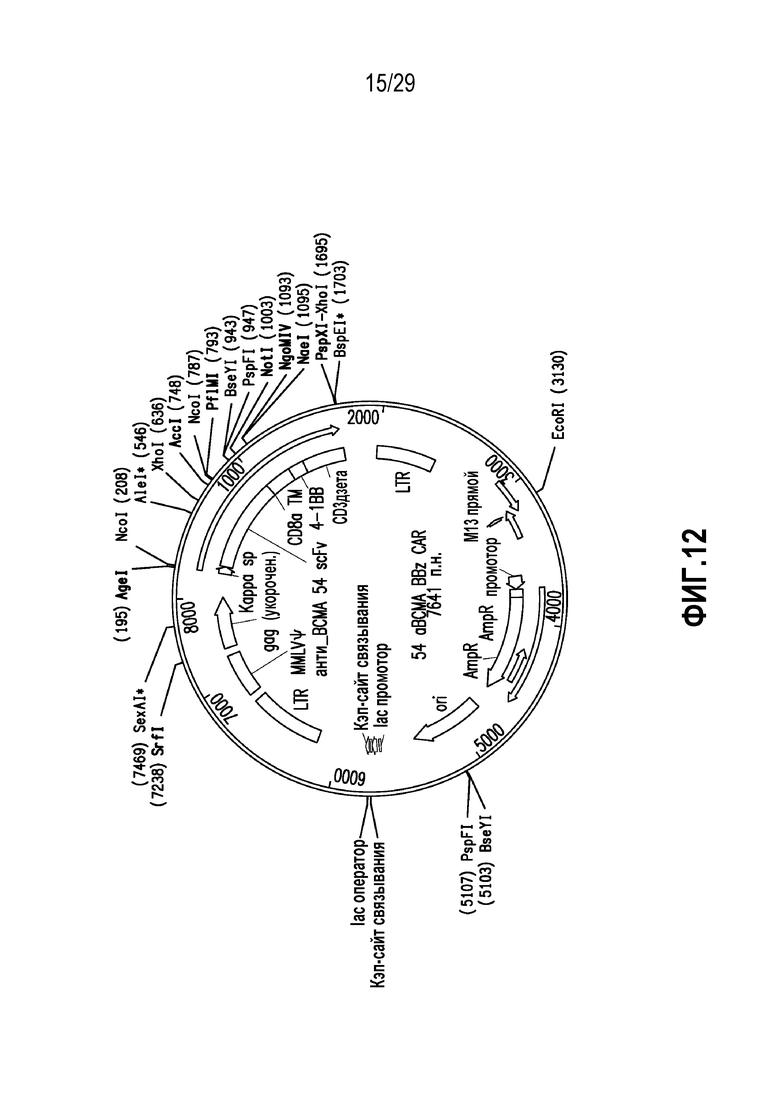
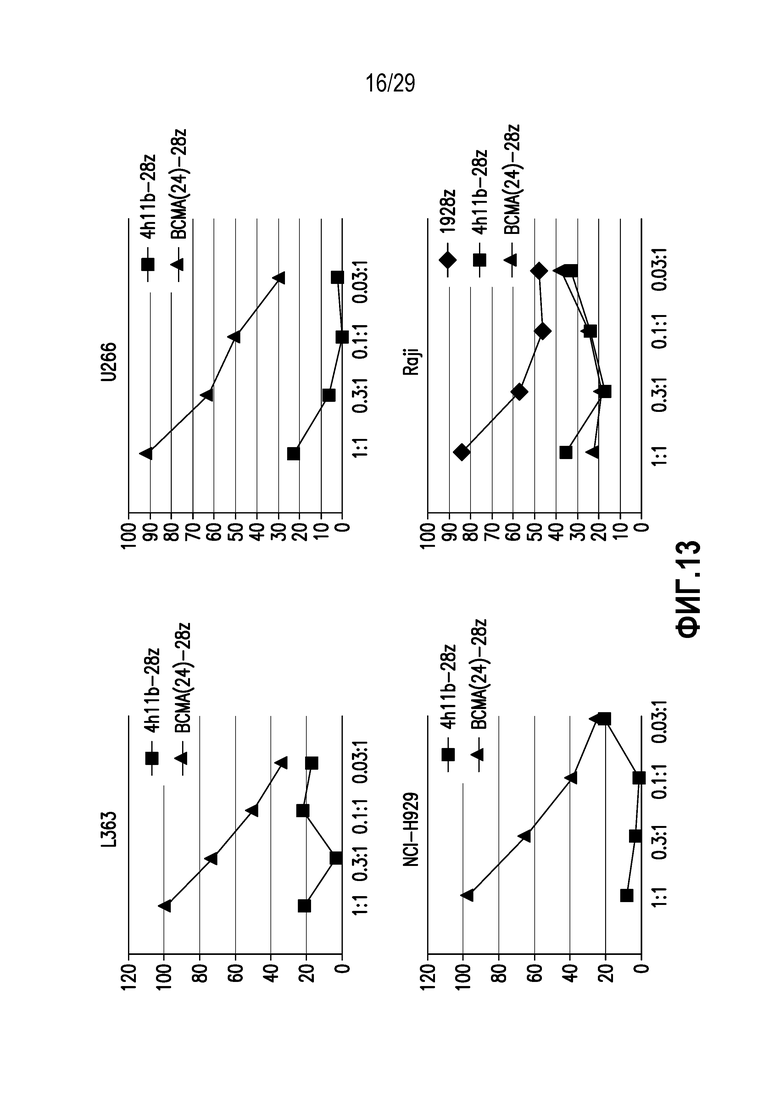
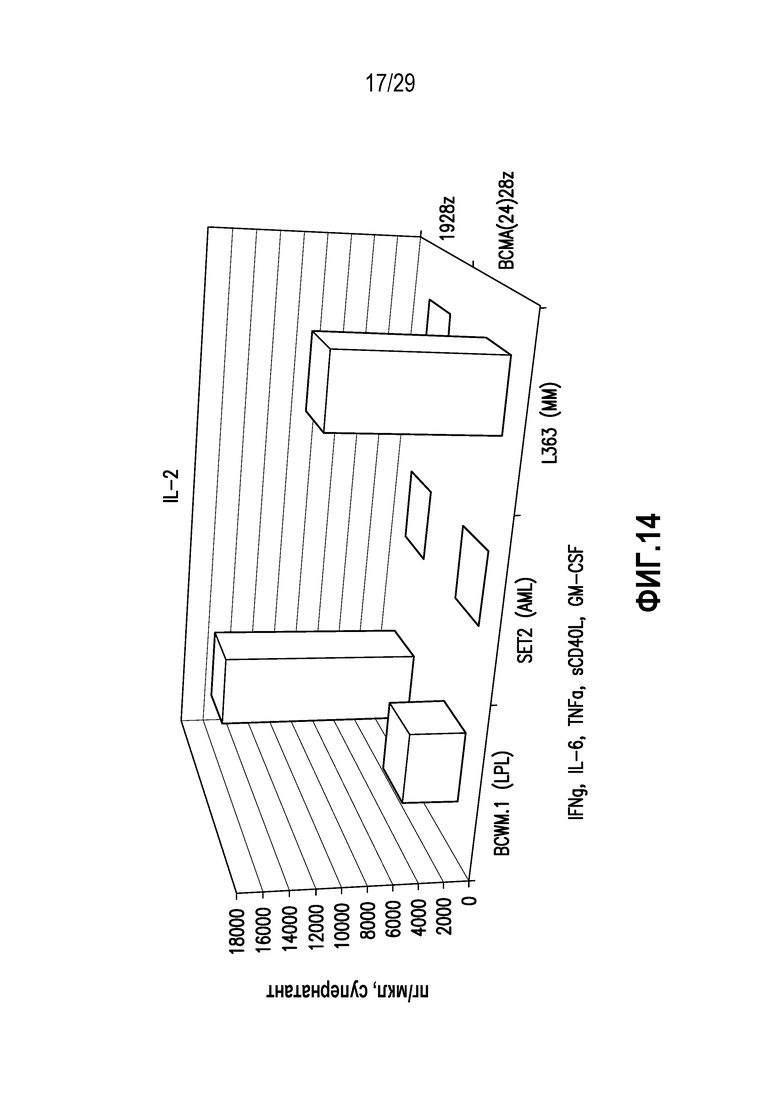
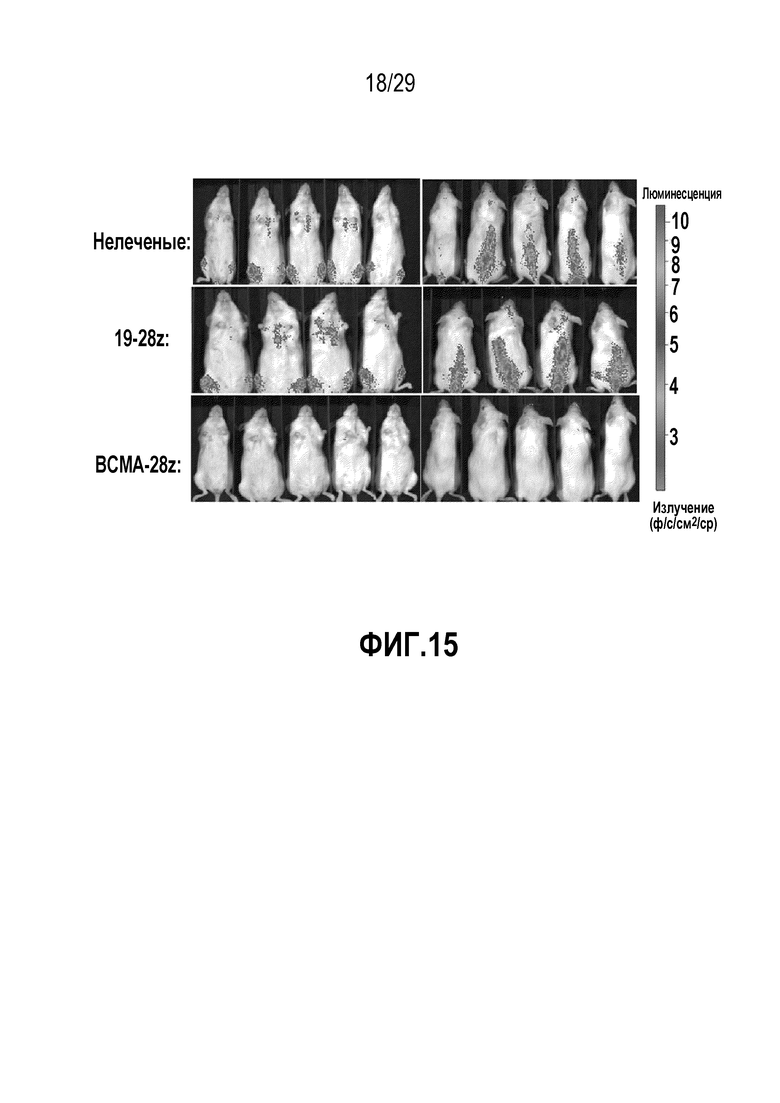
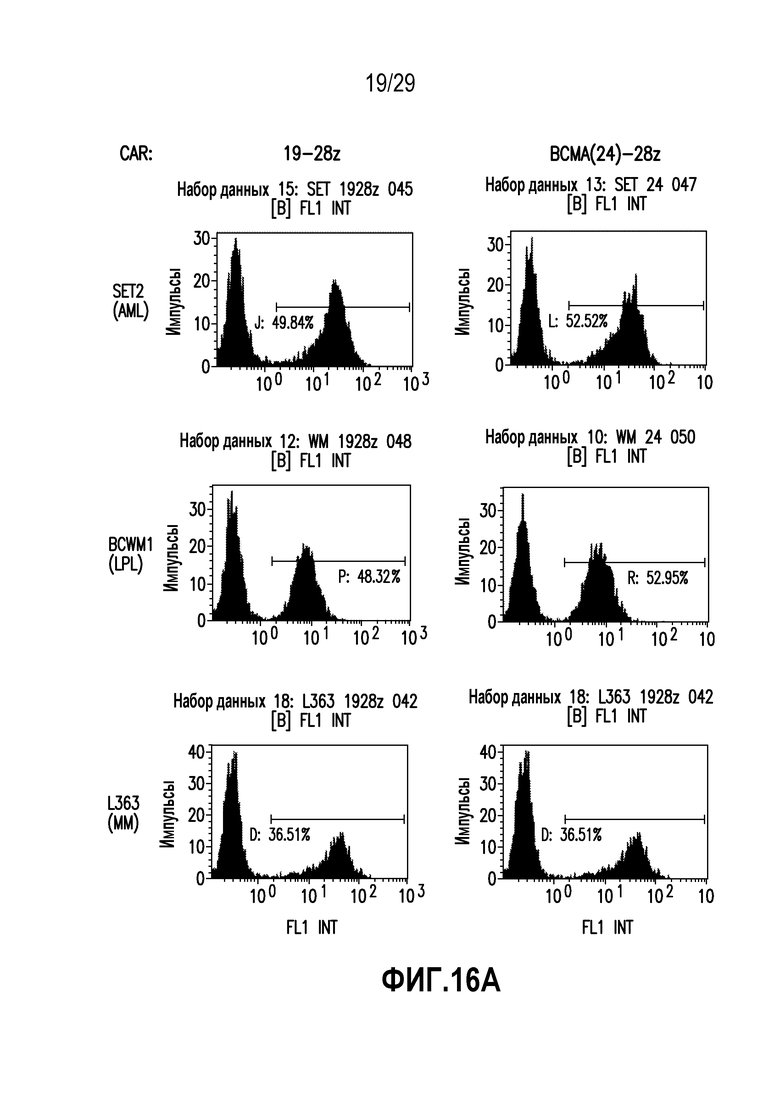
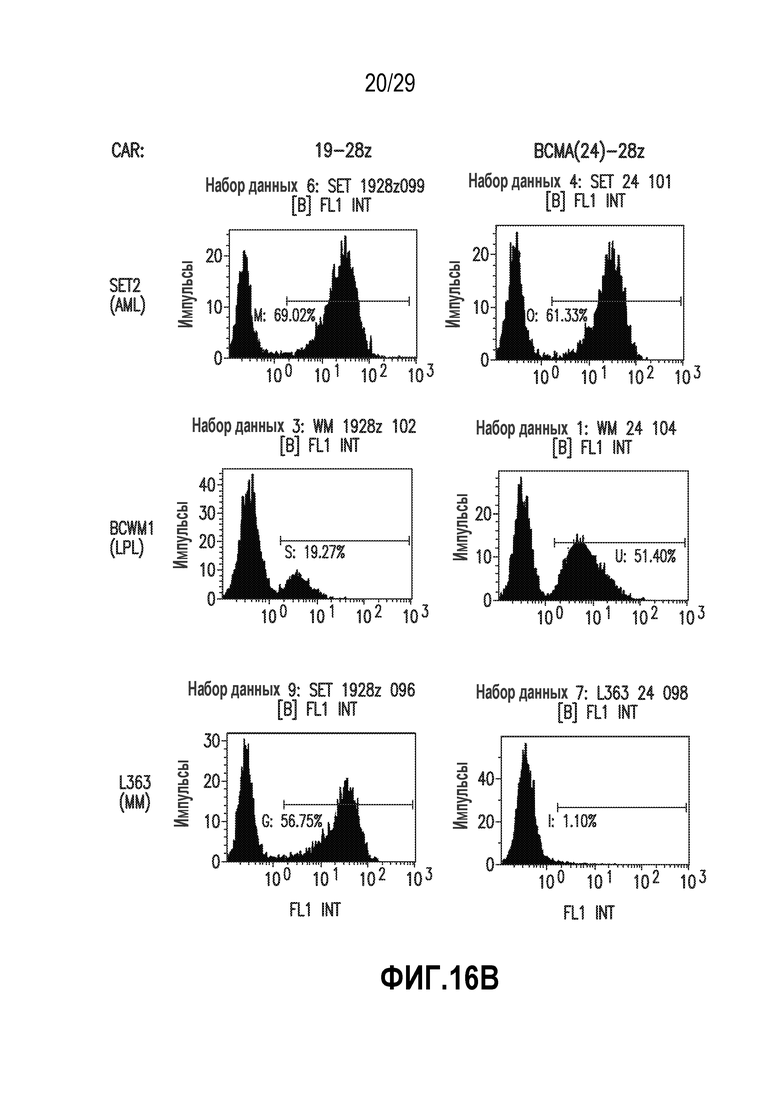
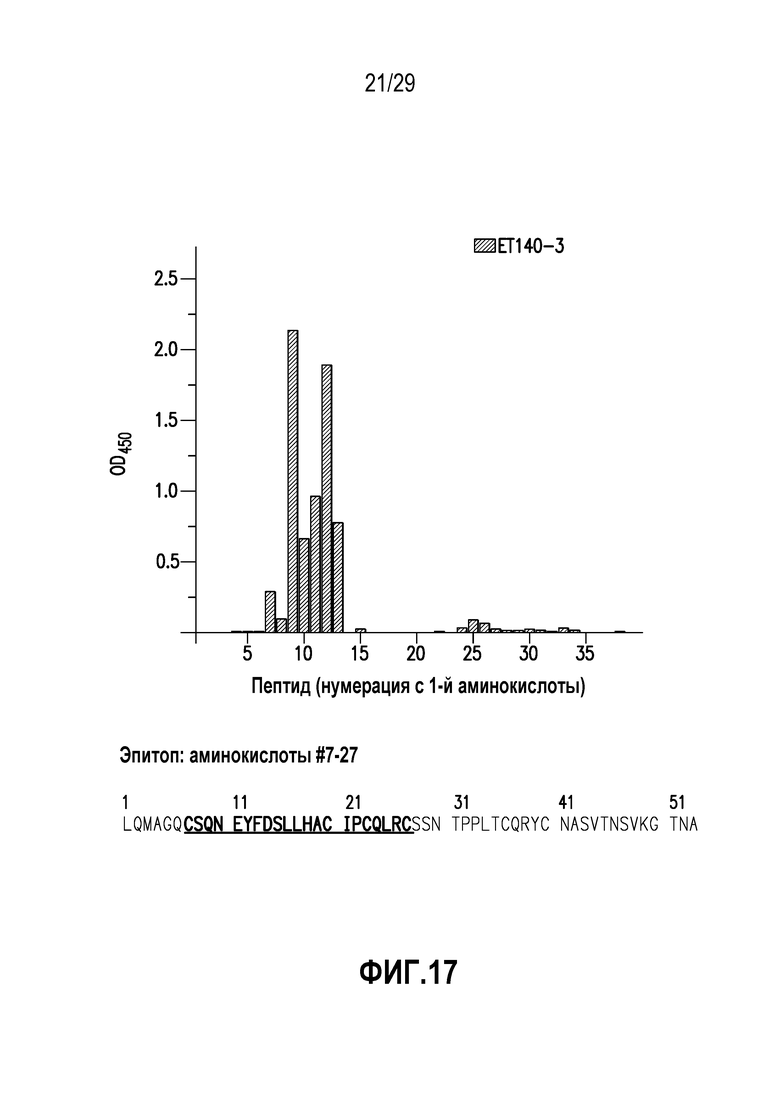
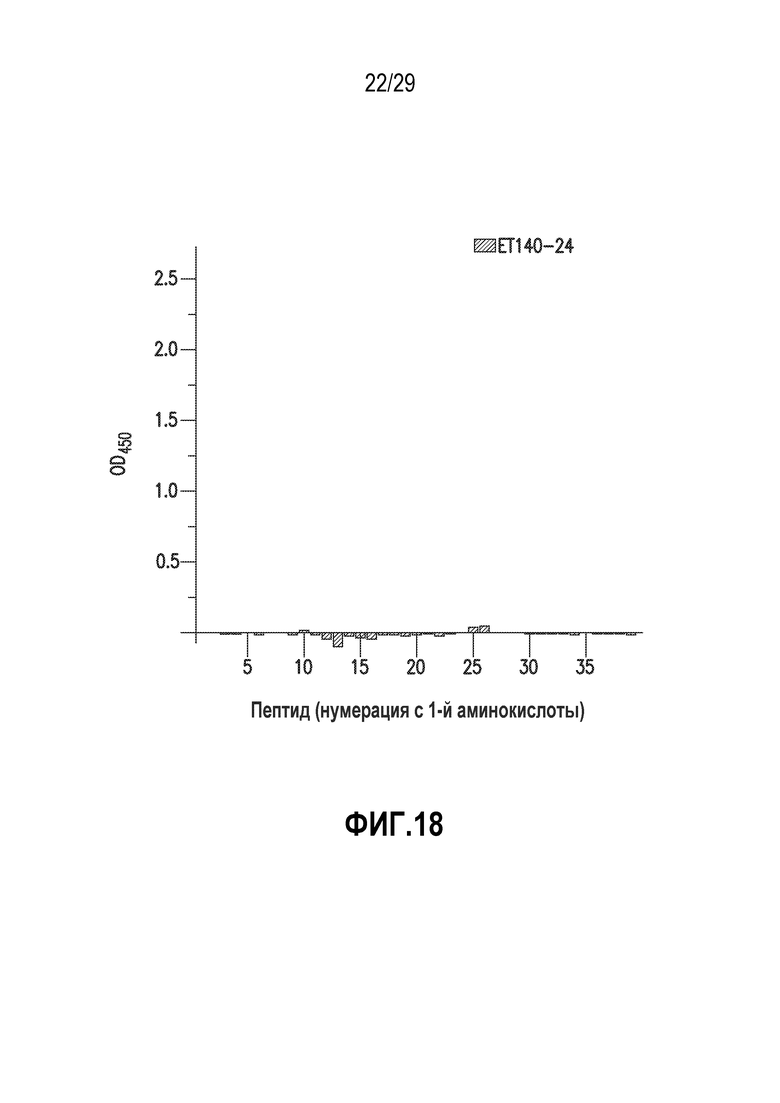
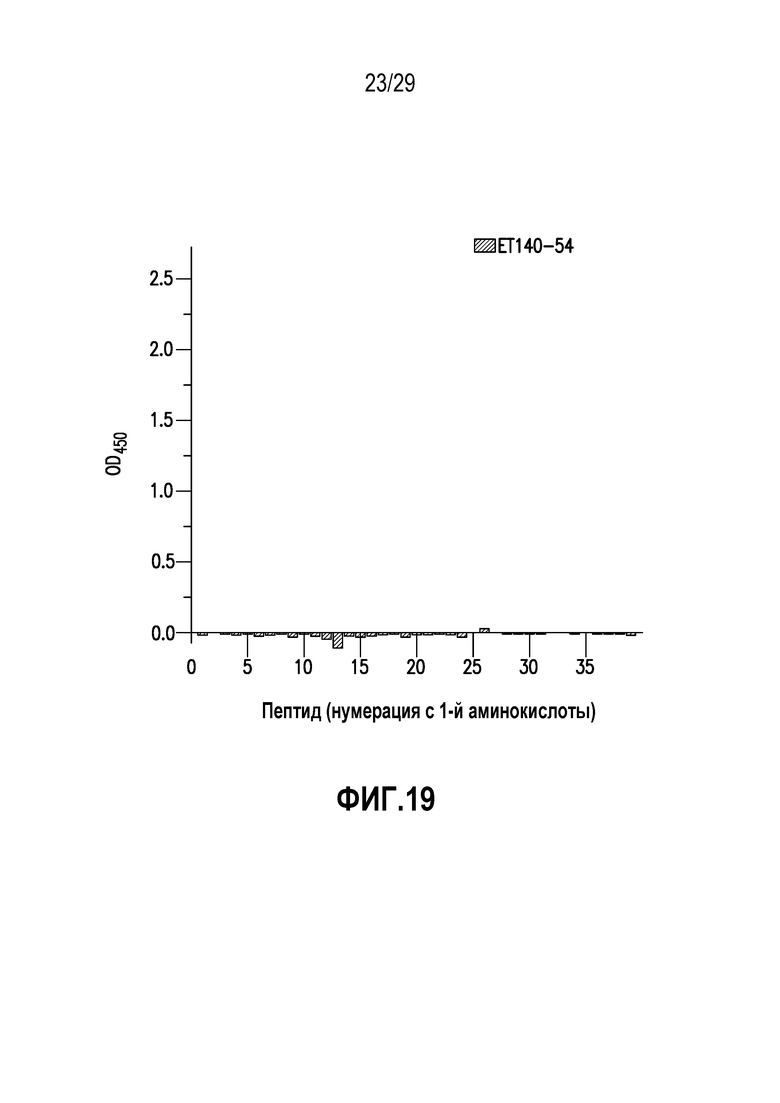

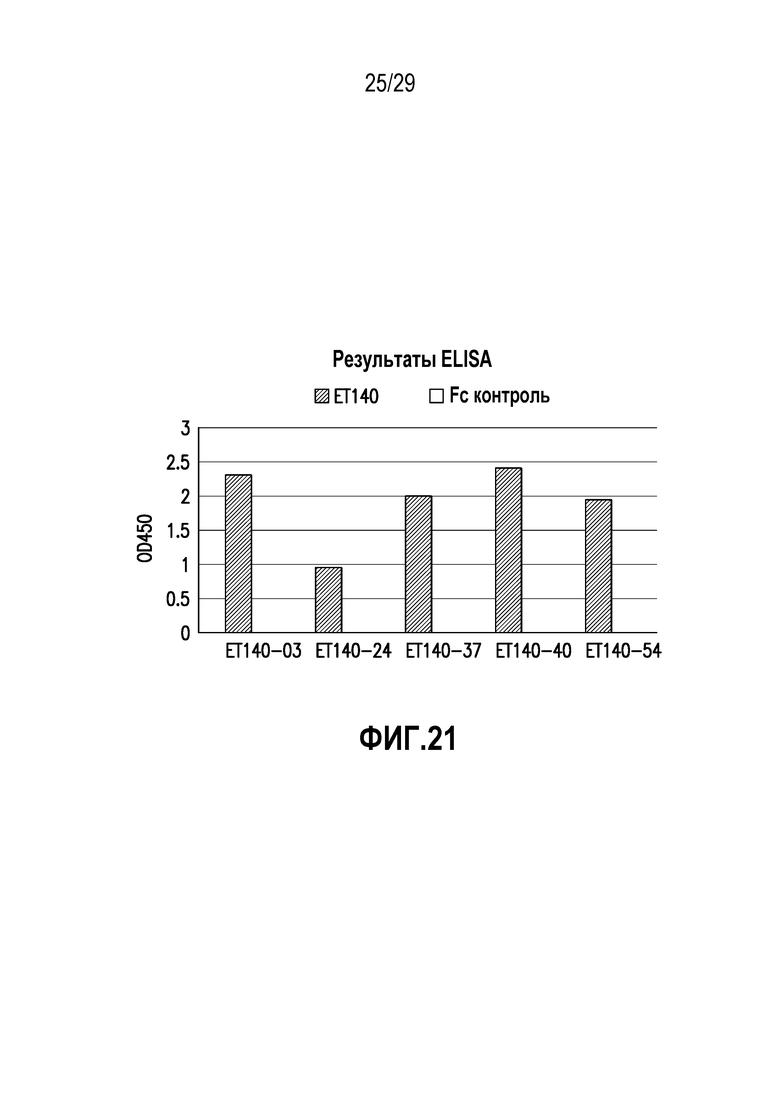
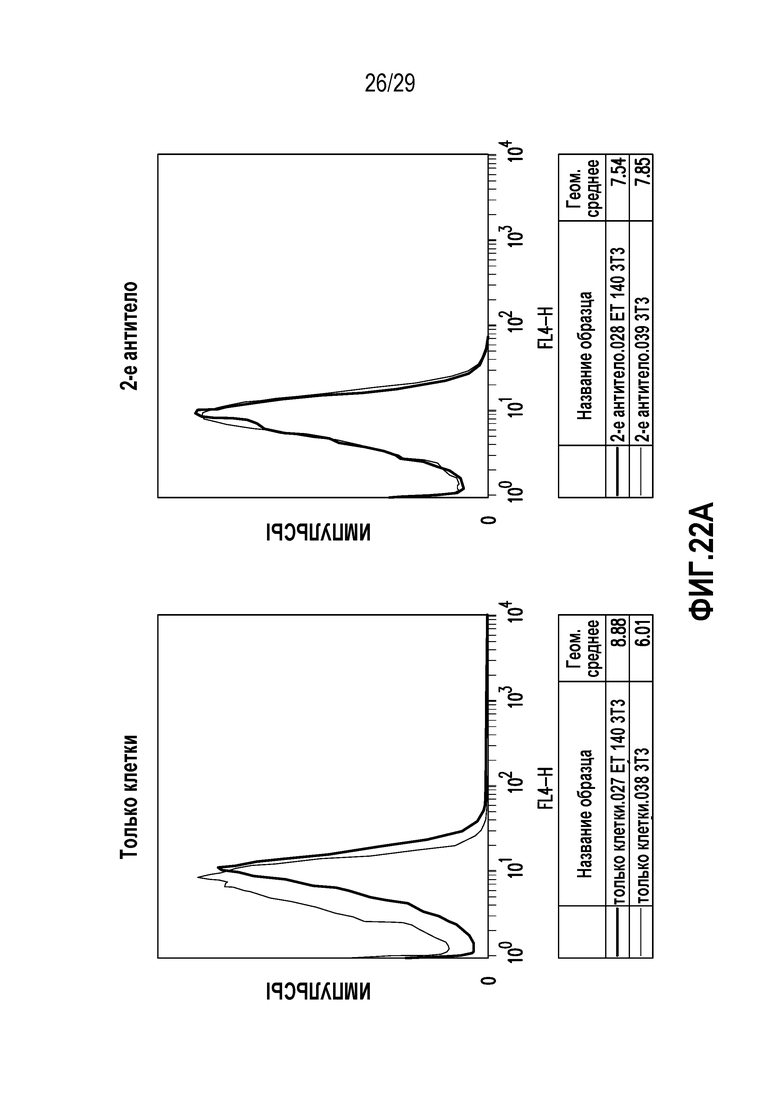
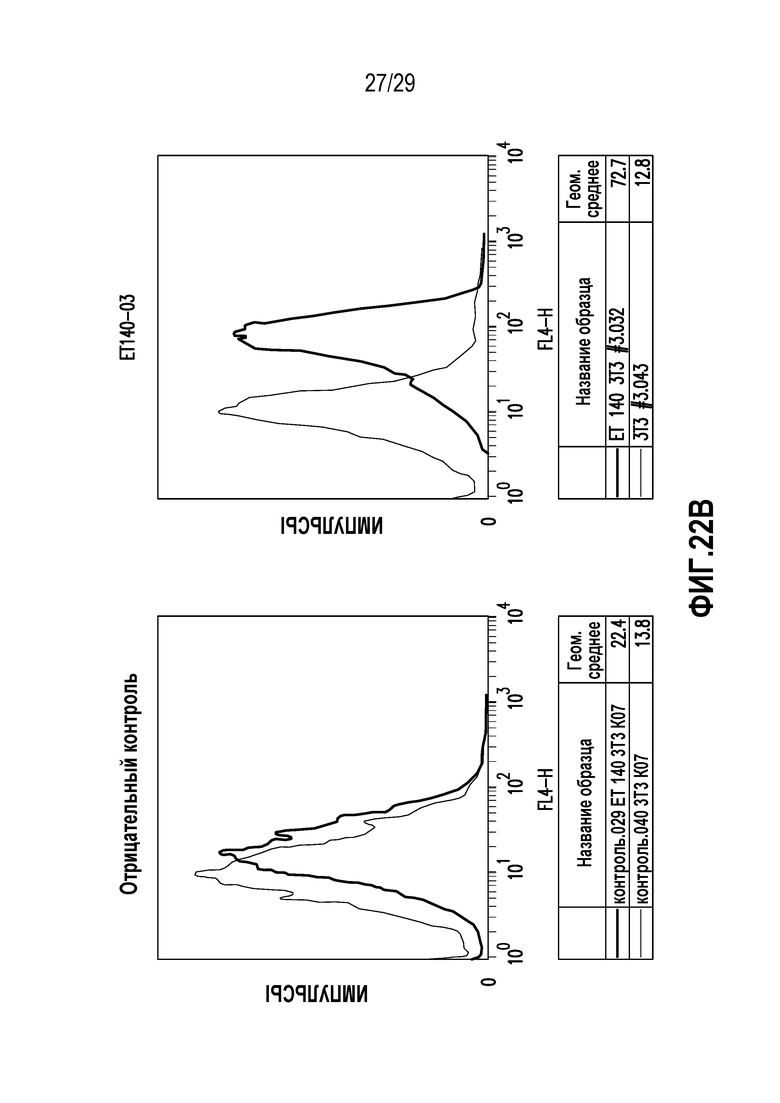
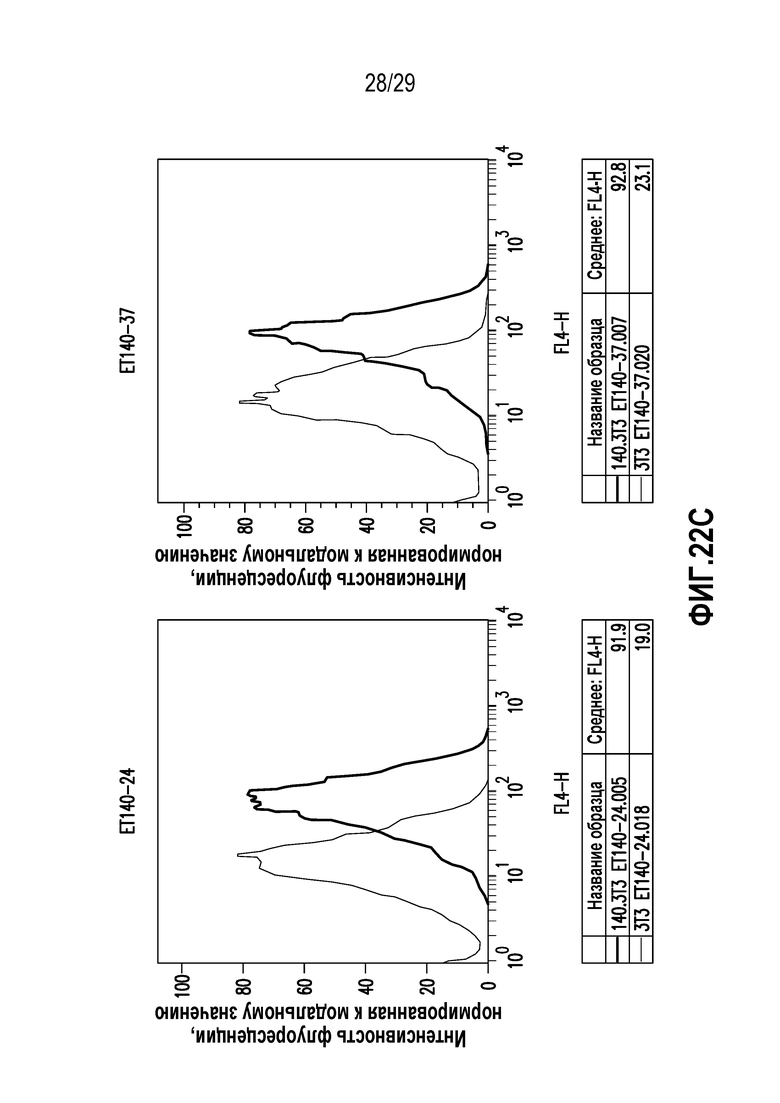
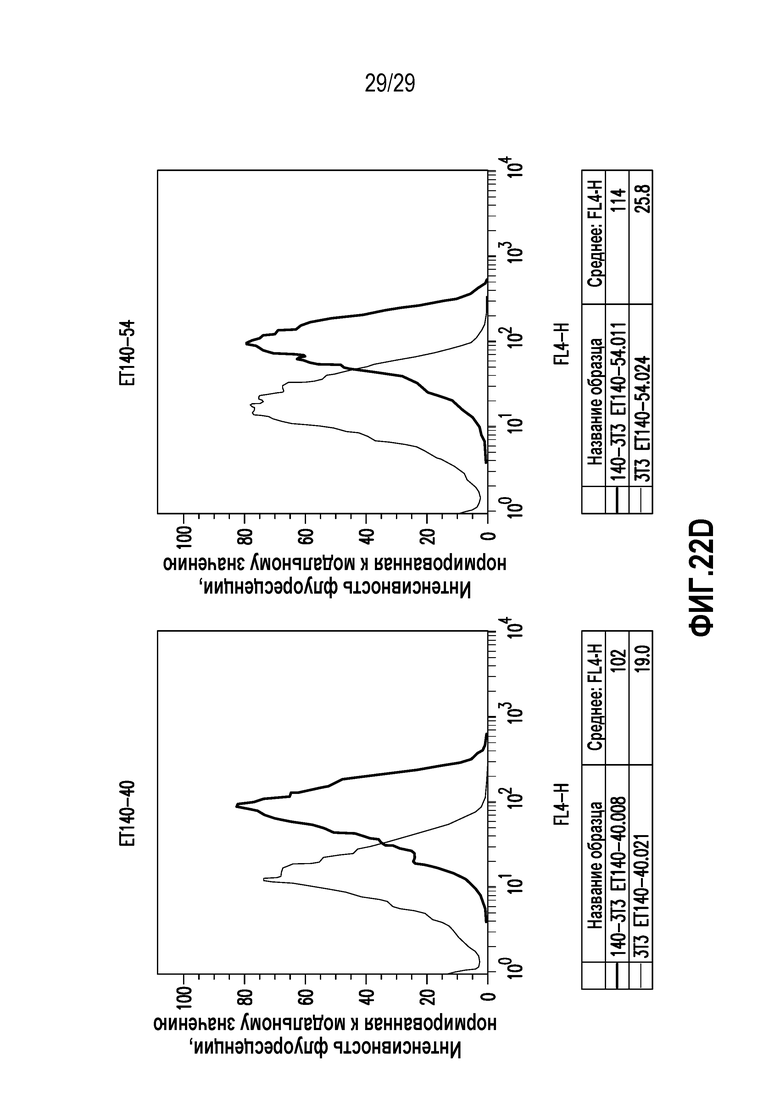
Настоящее изобретение относится к области иммунологии. Предложены химерные антигенные рецепторы (CAR) против антигена созревания В-клеток (ВСМА), иммунореактивные клетки, молекула нуклеиновой кислоты, экспрессионный вектор, Т-клетки. Кроме того, рассмотрены способ уменьшения опухолевой нагрузки, способы увеличения или продления срока выживания субъекта, способ получения иммунореактивной клетки, фармацевтические композиции, наборы для лечения опухоли. Данное изобретение может найти дальнейшее применение в терапии различных опухолей, экспрессирующих ВСМА. 16 н. и 73 з.п. ф-лы, 29 ил., 25 табл., 11 пр.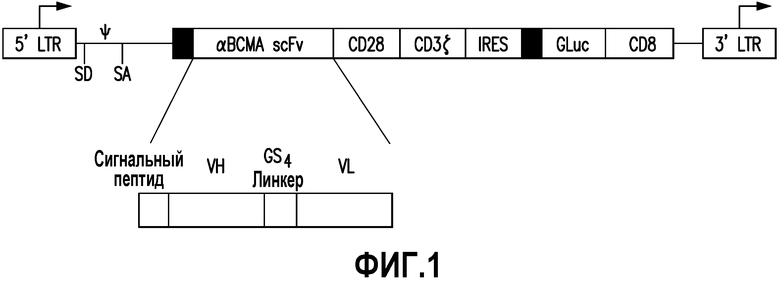
1. Химерный антигенный рецептор (CAR), содержащий внеклеточный антигенсвязывающий домен, который связывается с антигеном созревания B-клеток (BCMA), трансмембранный домен и внутриклеточный домен, где внеклеточный антигенсвязывающий домен содержит:
(a) вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 119, 120 и 121 соответственно, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 122, 123 и 124 соответственно;
(b) вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 185, 186 и 187 соответственно, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 188, 189 и 190 соответственно;
(c) вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 179, 180 и 181 соответственно, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 182, 183 и 184 соответственно;
(d) вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 173, 174 и 175 соответственно, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 176, 177 и 178 соответственно; или
(e) вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 167, 168 и 169 соответственно, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 170, 171 и 172 соответственно.
2. Химерный антигенный рецептор (CAR), содержащий внеклеточный антигенсвязывающий домен, который связывается с антигеном созревания B-клеток (BCMA), трансмембранный домен и внутриклеточный домен, где внеклеточный антигенсвязывающий домен содержит:
(a) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи, приведенной в SEQ ID NO: 21, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи, приведенной в SEQ ID NO: 22;
(b) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи, приведенной в SEQ ID NO: 65, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи, приведенной в SEQ ID NO: 66;
(c) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи, приведенной в SEQ ID NO: 61, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи, приведенной в SEQ ID NO: 62;
(d) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи, приведенной в SEQ ID NO: 57, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи, приведенной в SEQ ID NO: 58; или
(e) вариабельную область тяжелой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области тяжелой цепи, приведенной в SEQ ID NO: 53, и вариабельную область легкой цепи, содержащую CDR1, CDR2 и CDR3 последовательности вариабельной области легкой цепи, приведенной в SEQ ID NO: 54.
3. CAR по п. 1 или 2, где:
(a) вариабельная область тяжелой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 21, и вариабельная область легкой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 22;
(b) вариабельная область тяжелой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 65, и вариабельная область легкой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 66;
(c) вариабельная область тяжелой цепи содержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 61, и вариабельная область легкой цепи содержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 62;
(d) вариабельная область тяжелой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 57, и вариабельная область легкой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 58; или
(e) вариабельная область тяжелой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 53, и вариабельная область легкой цепи cодержит аминокислотную последовательность, которая имеет по меньшей мере приблизительно 90% идентичности аминокислотной последовательности, приведенной в SEQ ID NO: 54.
4. CAR по любому из пп. 1-3, где:
(a) вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 22;
(b) вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 66;
(c) вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 62;
(d) вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 58; или
(e) вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 54.
5. CAR по любому из пп. 1-3, где вариабельная область тяжелой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 119, 120 и 121 соответственно, и вариабельная область легкой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 122, 123 и 124 соответственно.
6. CAR по любому из пп. 1-3, где вариабельная область тяжелой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 185, 186 и 187 соответственно, и вариабельная область легкой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 188, 189 и 190 соответственно.
7. CAR по любому из пп. 1-3, где вариабельная область тяжелой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 179, 180 и 181 соответственно, и вариабельная область легкой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 182, 183 и 184 соответственно.
8. CAR по любому из пп. 1-3, где вариабельная область тяжелой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 173, 174 и 175 соответственно, и вариабельная область легкой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 176, 177 и 178 соответственно.
9. CAR по любому из пп. 1-3, где вариабельная область тяжелой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NO: 167, 168 и 169 соответственно, и вариабельная область легкой цепи содержит последовательности CDR1, CDR2 и CDR3, приведенные в SEQ ID NOs: 170, 171 и 172 соответственно.
10. CAR по любому из пп. 1-5, где вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 21, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 22.
11. CAR по любому из пп. 1-4 и 6, где вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 65, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 66.
12. CAR по любому из пп. 1-4 и 7, где вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 61, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 62.
13. CAR по любому из пп. 1-4 и 8, где вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 57, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 58.
14. CAR по любому из пп. 1-4 и 9, где вариабельная область тяжелой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 53, и вариабельная область легкой цепи содержит аминокислотную последовательность, приведенную в SEQ ID NO: 54.
15. CAR по любому из пп. 1-14, где внеклеточный антигенсвязывающий домен содержит линкер, расположенный между вариабельной областью тяжелой цепи и вариабельной областью легкой цепи.
16. CAR по любому из пп. 1-15, где внеклеточный антигенсвязывающий домен представляет собой одноцепочечный вариабельный фрагмент (scFv).
17. CAR по п. 16, где внеклеточный антигенсвязывающий домен представляет собой scFv человека.
18. CAR по любому из пп. 1-17, где внеклеточный антигенсвязывающий домен содержит аминокислотную последовательность, приведенную в SEQ ID NO: 77, SEQ ID NO: 88, SEQ ID NO: 87, SEQ ID NO: 86 или SEQ ID NO: 85.
19. CAR по любому из пп. 1-14, где внеклеточный антигенсвязывающий домен представляет собой Fab, который необязательно является поперечно сшитым.
20. CAR по любому из пп. 1-14 и 19, где внеклеточный антигенсвязывающий домен представляет собой F(ab’)2.
21. CAR по любому из пп. 1-14, где внеклеточный антигенсвязывающий домен содержит scFv, Fab или F(ab’)2 и указанный scFv, указанный Fab или указанный F(ab’)2 содержатся в слитом белке с гетерологичной последовательностью с образованием внеклеточного антигенсвязывающего домена.
22. CAR по любому из пп. 1-21, где внеклеточный антигенсвязывающий домен связывается с антигеном созревания B-клеток (BCMA) с аффинностью связывания (Kd), составляющей от примерно 1×10-9 M до примерно 3×10-6 M.
23. CAR по любому из пп. 1-22, где внеклеточный антигенсвязывающий домен связывается с антигеном созревания B-клеток (BCMA) с аффинностью связывания (Kd), составляющей от примерно 1×10-9 M до примерно 1×10-8 M.
24. CAR по любому из пп. 1-23, где внеклеточный антигенсвязывающий домен связывается с нелинейным эпитопом BCMA.
25. CAR по любому из пп. 1-24, где BCMA содержит аминокислотную последовательность, приведенную в SEQ ID NO: 71.
26. CAR по любому из пп. 1-25, где внеклеточный антигенсвязывающий домен связывается с областью эпитопа, содержащей остатки в пределах аминокислот 14-22 из SEQ ID NO: 71.
27. CAR по любому из пп. 1-26, где сигнальный пептид ковалентно связан с N-концом внеклеточного антигенсвязывающего домена.
28. CAR по любому из пп. 1-27, где трансмембранный домен содержит полипептид CD8, полипептид CD28, полипептид CD3ζ, полипептид CD4, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид CTLA-4, полипептид PD-1, полипептид LAG-3, полипептид 2B4, полипептид BTLA, синтетический пептид или их сочетание.
29. CAR по любому из пп. 1-28, где трансмембранный домен содержит полипептид CD8.
30. CAR по любому из пп. 1-28, где трансмембранный домен содержит полипептид CD28.
31. CAR по любому из пп. 1-30, где внутриклеточный домен содержит полипептид CD3ζ.
32. CAR по любому из пп. 1-31, где внутриклеточный домен дополнительно содержит по меньшей мере одну сигнальную область.
33. CAR по п. 32, где по меньшей мере одна сигнальная область содержит полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10, полипептид PD-1, полипептид CTLA-4, полипептид LAG-3, полипептид 2B4, полипептид BTLA, синтетический пептид или их сочетание.
34. CAR по п. 32 или 33, где по меньшей мере одна сигнальная область содержит по меньшей мере одну костимулирующую сигнальную область.
35. CAR по п. 34, где по меньшей мере одна костимулирующая сигнальная область содержит полипептид CD28, полипептид 4-1BB, полипептид OX40, полипептид ICOS, полипептид DAP-10 или их сочетание.
36. CAR по п. 34 или 35, где по меньшей мере одна костимулирующая сигнальная область содержит полипептид CD28.
37. CAR по п. 34 или 35, где по меньшей мере одна костимулирующая сигнальная область содержит полипептид 4-1BB.
38. CAR по любому из пп. 34-36, где трансмембранный домен содержит полипептид CD28, внутриклеточный домен содержит полипептид CD3ζ и по меньшей мере одна костимулирующая сигнальная область содержит полипептид CD28.
39. CAR по любому из пп. 34, 35 и 37, где трансмембранный домен содержит полипептид CD8, внутриклеточный домен содержит полипептид CD3ζ и по меньшей мере одна костимулирующая сигнальная область содержит полипептид 4-1BB.
40. CAR по любому из пп. 34, 35 и 37, где трансмембранный домен содержит полипептид CD28, внутриклеточный домен содержит полипептид CD3ζ и по меньшей мере одна костимулирующая сигнальная область содержит полипептид 4-1BB.
41. CAR по любому из пп. 1-40, который экспрессируется рекомбинантно.
42. CAR по любому из пп. 1-41, который экспрессируется с экспрессионного вектора.
43. CAR по п. 42, где экспрессионный вектор представляет собой γ-ретровирусный вектор.
44. CAR по п. 42, где экспрессионный вектор представляет собой лентивирусный вектор.
45. Иммунореактивная клетка для экспрессии химерного антигенного рецептора (CAR), содержащая CAR по любому из пп. 1-44, где указанная иммунореактивная клетка выбрана из группы, состоящей из T-клетки, клетки-естественного киллера (NK), цитотоксического T-лимфоцита (CTL), регуляторной T-клетки, лимфоидной клетки-предшественника, клетки-предшественника T-клетки и стволовой клетки, из которой могут дифференцироваться лимфоидные клетки.
46. Иммунореактивная клетка по п. 45, которая трансдуцирована молекулой нуклеиновой кислоты, кодирующей CAR.
47. Иммунореактивная клетка по п. 45 или 46, отличающаяся тем, что CAR конститутивно экспрессируется на поверхности иммунореактивной клетки.
48. Иммунореактивная клетка по любому из пп. 45-47, которая дополнительно трансдуцирована молекулой нуклеиновой кислоты, кодирующей по меньшей мере один костимулирующий лиганд, вследствие чего иммунореактивная клетка экспрессирует по меньшей мере один костимулирующий лиганд.
49. Иммунореактивная клетка по п. 48, отличающаяся тем, что по меньшей мере один костимулирующий лиганд выбирают из группы, состоящей из 4-1BBL, CD80, CD86, CD70, OX40L, CD48, TNFRSF14, а также их сочетаний.
50. Иммунореактивная клетка по любому из пп. 45-49, которая дополнительно трансдуцирована молекулой нуклеиновой кислоты, кодирующей по меньшей мере один цитокин, вследствие чего иммунореактивная клетка секретирует по меньшей мере один цитокин.
51. Иммунореактивная клетка по п. 50, отличающаяся тем, что по меньшей мере один цитокин выбирают из группы, состоящей из IL-2, IL-3, IL-6, IL-7, IL-11, IL-12, IL-15, IL-17, IL-21, а также их сочетаний.
52. Выделенная иммунореактивная клетка по любому из пп. 45-51, представляющая собой T-клетку.
53. Т-клетка для экспрессии химерного антигенного рецептора (CAR), содержащая CAR по любому из пп. 1-44.
54. Молекула нуклеиновой кислоты, кодирующая химерный антиген рецептор (CAR) по любому из пп. 1-44.
55. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 207.
56. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 208.
57. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 209.
58. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 229.
59. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 230.
60. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 231.
61. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 232.
62. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 233.
63. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 234.
64. Молекула нуклеиновой кислоты по п. 54, содержащая нуклеотидную последовательность, приведенную в SEQ ID NO: 235.
65. Экспрессионный вектор, содержащий молекулу нуклеиновой кислоты по любому из пп. 54-64.
66. Экспрессионный вектор по п. 65, представляющий собой γ-ретровирусный вектор.
67. Экспрессионный вектор по п. 65, представляющий собой лентивирусный вектор.
68. Иммунореактивная клетка для экспрессии химерного антигенного рецептора (CAR), содержащая молекулу нуклеиновой кислоты по любому из пп. 54-64, где указанная иммунореактивная клетка выбрана из группы, состоящей из T-клетки, клетки-естественного киллера (NK), цитотоксического T-лимфоцита (CTL), регуляторной T-клетки, лимфоидной клетки-предшественника, клетки-предшественника T-клетки и стволовой клетки, из которой могут дифференцироваться лимфоидные клетки.
69. Иммунореактивная клетка по п. 68, представляющая собой T-клетку.
70. Т-клетка для экспрессии химерного антигенного рецептора (CAR), содержащая молекулу нуклеиновой кислоты по любому из пп. 54-64.
71. Способ уменьшения опухолевой нагрузки у субъекта, включающий введение эффективного количества композиции, содержащей одну или более из иммунореактивной клетки по любому из пп. 45-53 или одну или более из Т-клетки по любому из пп. 68-70 субъекту, где:
указанная одна или более иммунореактивная клетка представляет собой клетку-естественного киллера (NK), CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит; или
указанная одна или более Т-клетка представляет собой CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит.
72. Способ по п. 71, приводящий к уменьшению количества опухолевых клеток.
73. Способ по п. 71, приводящий к уменьшению размера опухоли.
74. Способ по п. 71, приводящий к уничтожению опухоли у субъекта.
75. Способ по любому из пп. 71-74, где опухоль выбирают из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема.
76. Способ по п. 75, где опухоль представляет собой множественную миелому.
77. Способ по любому из пп. 71-76, где субъект является человеком.
78. Способ по любому из пп. 71-77, где иммунореактивная клетка представляет собой T-клетку.
79. Способ увеличения или продления срока выживания субъекта, имеющего опухоль, экспрессирующую антиген созревания B-клеток (BCMA), включающий введение эффективного количества композиции, содержащей одну или более из иммунореактивной клетки по любому из пп. 45-53 или одну или более из Т-клетки по любому из пп. 68-70 субъекту, где:
указанная одна или более иммунореактивная клетка представляет собой клетку-естественного киллера (NK), CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит; или
указанная одна или более Т-клетка представляет собой CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит.
80. Способ увеличения или продления срока выживания субъекта, имеющего опухоль, выбранную из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема, включающий введение эффективного количества композиции, содержащей одну или более из иммунореактивной клетки по любому из пп. 45-53 или одну или более из Т-клетки по любому из пп. 68-70 субъекту, где:
указанная одна или более иммунореактивная клетка представляет собой клетку-естественного киллера (NK), CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит; или
указанная одна или более Т-клетка представляет собой CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит.
81. Способ по п. 79 или 80, где неоплазия представляет собой множественную миелому.
82. Способ по любому из пп. 79-81, приводящий к уменьшению или уничтожению опухолевой нагрузки у субъекта.
83. Способ получения иммунореактивной клетки, которая связывается с антигеном созревания B-клеток (BMCA), включающий введение в иммунореактивную клетку молекулы нуклеиновой кислоты, кодирующей химерный антигенный рецептор (CAR) по любому из пп.1-44, где указанная иммунореактивная клетка выбрана из группы, состоящей из T-клетки, клетки-естественного киллера (NK), цитотоксического T-лимфоцита (CTL), регуляторной T-клетки, лимфоидной клетки-предшественника, клетки-предшественника T-клетки и стволовой клетки, из которой могут дифференцироваться лимфоидные клетки.
84. Фармацевтическая композиция для лечения опухоли, экспрессирующей антиген созревания B-клеток (BCMA), содержащая эффективное количество одной или более из иммунореактивной клетки по любому из пп. 45-53 или одной или более из Т-клетки по любому из пп. 68-70 и фармацевтически приемлемый эксципиент, где:
указанная одна или более иммунореактивная клетка представляет собой клетку-естественного киллера (NK), CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит; или
указанная одна или более Т-клетка представляет собой CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит.
85. Фармацевтическая композиция для лечения опухоли, выбранная из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема, содержащая эффективное количество одной или более из иммунореактивной клетки по любому из пп. 45-53 или одной или более из Т-клетки по любому из пп. 68-70 и фармацевтически приемлемый эксципиент, где:
указанная одна или более иммунореактивная клетка представляет собой клетку-естественного киллера (NK), CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит; или
указанная одна или более Т-клетка представляет собой CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит.
86. Фармацевтическая композиция по п. 84 или 85, где неоплазия представляет собой множественную миелому.
87. Набор для лечения опухоли, экспрессирующей антиген созревания B-клеток (BCMA), включающий одну или более из иммунореактивной клетки по любому из пп. 45-53 или одну или более из Т-клетки по любому из пп. 68-70 и письменные инструкции по применению указанной клетки для лечения субъекта, имеющего указанную опухоль, где:
указанная одна или более иммунореактивная клетка представляет собой клетку-естественного киллера (NK), CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит; или
указанная одна или более Т-клетка представляет собой CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит.
88. Набор для лечения опухоли, выбранной из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, хронического лимфоцитарного лейкоза (CLL), глиобластомы и макроглобулинемии Вальденстрема, включающий одну или более из иммунореактивной клетки по любому из пп. 45-53 или одну или более из Т-клетки по любому из пп. 68-70 и письменные инструкции по применению указанной клетки для лечения субъекта, имеющего указанную опухоль, где:
указанная одна или более иммунореактивная клетка представляет собой клетку-естественного киллера (NK), CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит; или
указанная одна или более Т-клетка представляет собой CD8+ цитотоксический T-лимфоцит (CTL) или CD8+ цитотоксический T-лимфоцит и CD4+ цитотоксический T-лимфоцит.
89. Набор по п. 87 или 88, где неоплазия представляет собой множественную миелому.
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| KOCHENDERFER JN et | |||
| al | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Способ получения бензидиновых оснований | 1921 |
|
SU116A1 |
| ПРЕДОХРАНИТЕЛЬНОЕ ПРИСПОСОБЛЕНИЕ ОТ КРАЖИ ИЛИ УТЕРИ БУМАЖНИКА | 1925 |
|
SU3875A1 |
| АПОПТОТИЧЕСКИЕ АНТИТЕЛА ПРОТИВ IgE | 2008 |
|
RU2500686C2 |
Авторы
Даты
2021-12-13—Публикация
2015-12-04—Подача