Изобретение относится к области органической химии, а именно к синтезу замещенных тетрагидрофуро[3,2-с]пиридинов.
Изобретение относится к разработке способа получения замещенных тетрагидрофуро[3,2-с]пиридинов общей формулы I, которые могут найти применение как вещества, обладающие потенциальной биологической активностью широкого спектра действия.
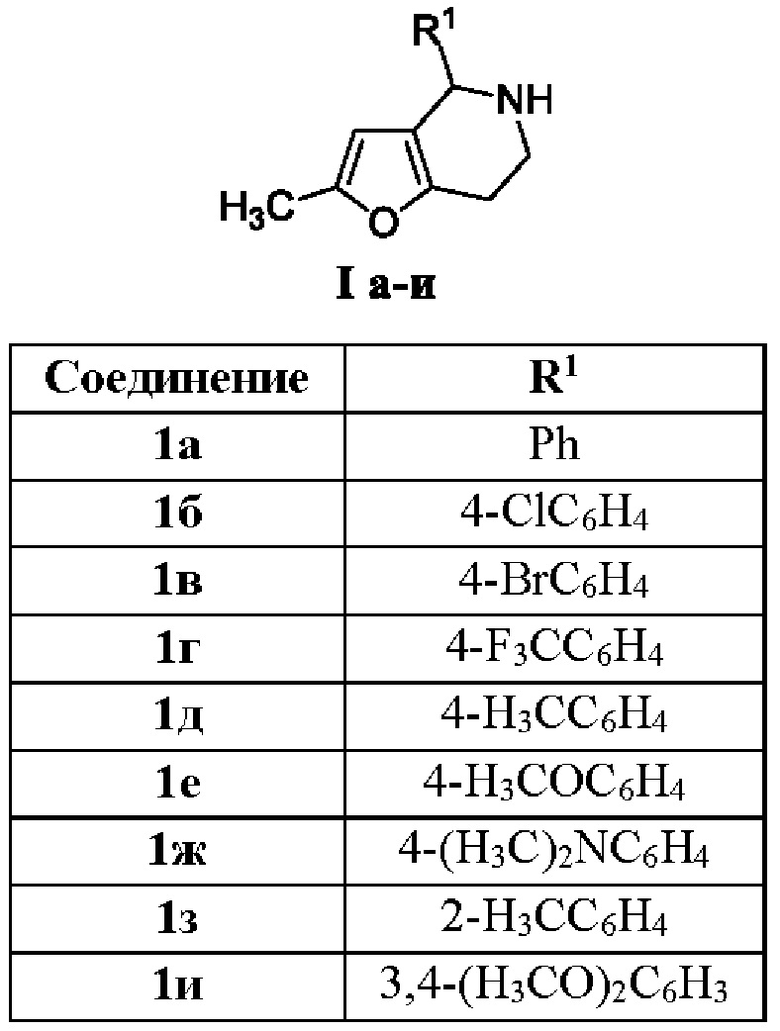
Несмотря на простоту тетрагидрофуро[3,2-с]пиридинового ядра, на сегодняшний день описаны лишь ограниченные подходы к синтезу этого класса с использованием производных фурана в качестве исходных соединений. Первая группа методов основана на использовании 3-замещенных фуранов. Например, внутримолекулярная реакция алкилирования Фриделя-Крафтса с использованием в качестве исходных веществ соответствующих спиртов [М.A. Schafroth, S.М. Rummelt, D. Sarlah, Е.М. Carreira, Org. Lett. 2017, 19, 3235-3238], алкенов [J.R. Fuchs, R.L. Funk, Org. Lett. 2001, 3, 3349-3351] или ацетиленов [Y. Sun, Xi. Tang, M. Shi, Chem. Commun. 2015, 51, 13937-13940]. К недостаткам этих подходов можно отнести немногочисленность изученных примеров алкилирования с использованием труднодоступных исходных 3-замещенных фуранов, а также частую перегруппировку образующегося бензилкарбокатиона в более стабильный катион бензгидрильного типа и образование изомерных продуктов.
В альтернативной группе методов в качестве исходных соединений используют более доступные 2-замещенные фураны. Например, описан двухстадийный подход к синтезу 4-замещенного тетрагидрофуро[3,2-с]пиридина циклоконденсацией Бишлера-Напиральского с последующим восстановлением [I. Kreituss, K.-Y. Chen, S.Н. Eitel, J.-M. Adam, G. Wuitschik, A. Fettes, J. W. Bode Angew. Chem. Int. Ed. 2015, 55, 1553-1556; K. Mohri, K. Isobe, M. Maeda, Takeda, Т.; Ohkubo, R.; Tsuda, Y.; Chem. Pharm. Bull. 1998, 46, 1872-1877; N.A. Tamayo, Y. Во, V. Gore, V. Ma, N. Nishimura, Ph. Tang, H. Deng, L. Klionsky, S.G. Lehto, W. Wang, B. Youngblood, J. Chen, T.L. Correll, M.D. Bartberger, N.R. Gavva, M.H. Norman, J. Med. Chem. 2012, 55, 1593-1611; W. Herz, S. Tocker, J. Am. Chem. Soc. 1955, 77, 3554-3556]. Несмотря на простоту такого подхода, следует отметить неустойчивость промежуточных дигидрофуро[3,2-с]пиридинов, осмоление реакционных смесей в кислых условиях и ограниченность изученных примеров циклизации. Другой путь конструирования тетрагидрофуро[3,2-с]пиридинов основан на реакции Пикте-Шпенглера. Наиболее изучен вариант этой циклизации, основанный на образовании ацилиминиевого катиона из соответствующих спиртов или алкенов, последующей атаке фуранового кольца и образовании аннелированных тетрагидрофуро[3,2-с]пиридинов. К недостатку данного подхода следует отнести труднодоступные исходные соединения и немногочисленные изученные примеры циклизации.
Наиболее близким к заявляемому методу синтеза является подход, который основан на взаимодействии гидрохлорида 2-(5-метилфуран-2-ил)этиламина с метилглиоксалатом в ацетонитриле при комнатной температуре в течение 3 часов [А. Naylor, D.В. Judd, D. I. С.Scopes, A.G. Hayes, P.J. Birch J. Med. Chem. 1994, 37), 2138-2144]. К недостатку последнего подхода следует отнести низкий выход целевого продукта, а также необходимость получения гидрохлорида 2-(5-метилфуран-2-ил)этиламина, который также был получен с невысоким выходом.
В основе заявляемого способа получения замещенных тетрагидрофуро[3,2-с]пиридинов Ia-и лежит кислотно-катализируемая реакция циклизации Пикте-Шпенглера N-арилиден-2-(5-метилфуран-2-ил)этиламинов, промежуточно образующихся в результате взаимодействия легкодоступного 2-(5-метилфуран-2-ил)этиламина и замещенных бензальдегидов.
Задача изобретения - разработка нового эффективного метода синтеза тетрагидрофуро[3,2-с]пиридинов Ia-и из замещенных бензальдегидов и легкодоступного 2-(5-метилфуран-2-ил)этиламина, позволяющего получать целевые бициклические соединения, содержащие разнообразные заместители, с целью поиска наиболее перспективных объектов для фармакологии, медицины и ветеринарии.
Техническим результатом является создание простого и эффективного метода синтеза замещенных тетрагидрофуро[3,2-с]пиридинов Ia-и, основанного на использовании легкодоступного 2-(5-метилфуран-2-ил)этиламина и замещенных бензальдегидов, позволяющего получать целевые продукты с хорошими выходами, а также варьировать заместители в 4-ом положении гетероциклического ядра.
Технический результат достигается осуществлением последовательных превращений, выполненных в однореакторном режиме. Первоначальная стадия заключается во взаимодействии легкодоступного 2-(5-метилфуран-2-ил)этиламина и замещенных бензальдегидов при кипячении в ацетонитриле с образованием соответствующих иминов. Вторая стадия заключается в циклизации полученных иминов в уксусной кислоте при 70°С в присутствии концентрированной соляной кислоты с последующей обработкой реакционной смеси раствором NaOH при комнатной температуре с образованием целевых тетрагидрофуро[3,2-c]пиридинов Ia-и.
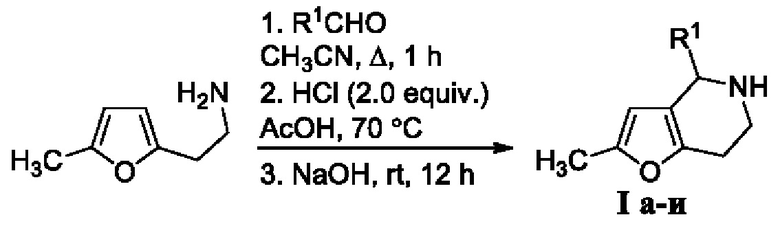
Полученный технический результат позволяет получать целевые продукты Ia-и с хорошими выходами в однореакторном режиме без выделения промежуточных продуктов. Метод имеет широкие границы применимости вследствие легкой доступности исходных компонентов и возможности широкого варьирования заместителей в исходных соединениях.
Таким образом, совокупность существенных признаков, изложенных в формуле изобретения, позволяет достичь желаемого технического результата.
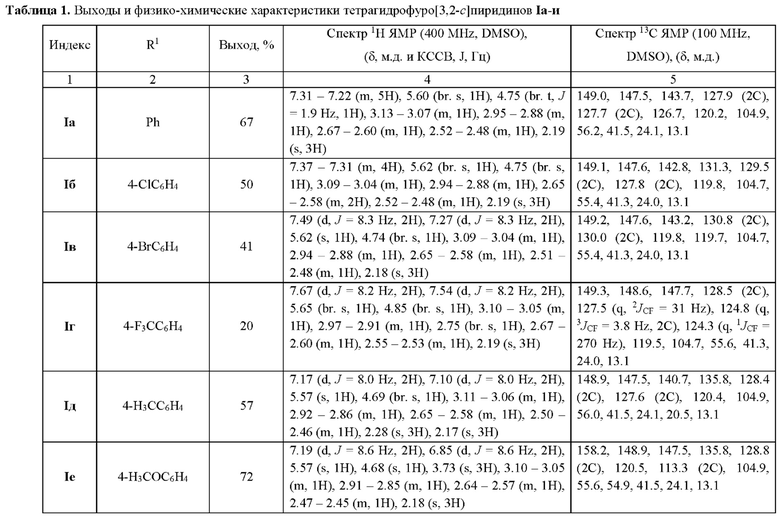
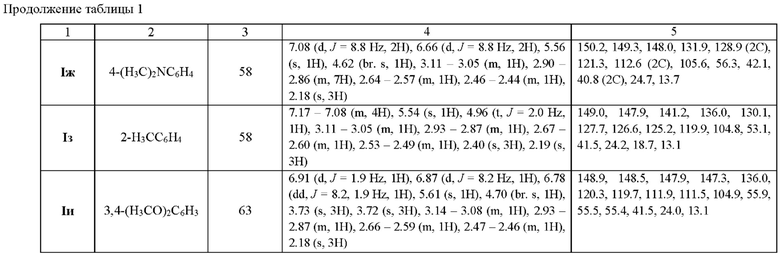
Индивидуальность и строение синтезированных соединений Ia-и подтверждены данными 1Н, 13С ЯМР - спектроскопии (таблица 1).
Примеры осуществления заявляемого способа получения 2-метил-4-фенил-4,5,6,7-тетрагидрофуро[3,2-с]пиридина (1а):
Пример 1.
К раствору бензадьдегида (1.0 ммоль) в сухом ацетонитриле (1 мл) добавляют 2-(5-метилфуран-2-ил)этиламин (1.0 ммоль, 0.125 мкл). Реакционную смесь кипятят в течение 1 ч (контроль ТСХ) и концентрируют досуха. К раствору имина в ледяной АсОН (650 мкл) добавляют конц. HCl (425 мкл). Реакционную смесь перемешивают при 70°С в течение 3.5 ч. Затем добавляют 10% водн. раствор NaOH и смесь перемешивают в течение ночи при комнатной температуре. Образовавшийся осадок отфильтровывают; фильтрат экстрагируют этилацетатом (3×10 мл). Объединенные органические слои промывают насыщенным водным раствором NaCl (3×10 мл), сушат над безводным Na2SO4 и концентрируют досуха. Остаток и осадок объединяют. Продукт очищают методом колоночной хроматографии на силикагеле, используя в качестве элюента смесь петролейного эфира и этилацетата (1:1).
Пример 2.
К раствору бензадьдегида (1.0 ммоль) в сухом ацетонитриле (1 мл) добавляют 2-(5-метилфуран-2-ил)этиламин (1.0 ммоль, 0.125 мкл). Реакционную смесь кипятят в течение 1 ч (контроль ТСХ) и концентрируют досуха. К раствору имина в ледяной АсОН (650 мкл) добавляют конц. HCl (425 мкл). Реакционную смесь перемешивают при 70°С в течение 1 ч. Затем добавляют 10% водн. раствор NaOH и смесь перемешивают в течение ночи при комнатной температуре. Образовавшийся осадок отфильтровывают; фильтрат экстрагируют этилацетатом (3×10 мл). Объединенные органические слои промывают насыщенным водным раствором NaCl (3×10 мл), сушат над безводным Na2SO4 и концентрируют досуха. Остаток и осадок объединяют. Продукт очищают методом колоночной хроматографии на силикагеле, используя в качестве элюента смесь петролейного эфира и этилацетата (1:1).
Пример 3.
К раствору бензадьдегида (1.0 ммоль) в сухом ацетонитриле (1 мл) добавляют 2-(5-метилфуран-2-ил)этиламин (1.0 ммоль, 0.125 мкл). Реакционную смесь кипятят в течение 1 ч (контроль ТСХ) и концентрируют досуха. К раствору имина в ледяной АсОН (650 мкл) добавляют конц. HCl (425 мкл). Реакционную смесь перемешивают при 70°С в течение 6.5 ч. Затем добавляют 10% водн. раствор NaOH и смесь перемешивают в течение ночи при комнатной температуре. Образовавшийся осадок отфильтровывают; фильтрат экстрагируют этилацетатом (3×10 мл). Объединенные органические слои промывают насыщенным водным раствором NaCl (3×10 мл), сушат над безводным Na2SO4 и концентрируют досуха. Остаток и осадок объединяют. Продукт очищают методом колоночной хроматографии на силикагеле, используя в качестве элюента смесь петролейного эфира и этилацетата (1:1).
Пример 4.
К раствору бензадьдегида (1.0 ммоль) в сухом ацетонитриле (1 мл) добавляют 2-(5-метилфуран-2-ил)этиламин (1.0 ммоль, 0.125 мкл). Реакционную смесь кипятят в течение 1 ч (контроль ТСХ) и концентрируют досуха. К раствору имина в ледяной АсОН (650 мкл) добавляют конц. HCl (425 мкл). Реакционную смесь перемешивают при комнатой температуре в течение 24 ч. Затем добавляют 10% водн. раствор NaOH и смесь перемешивают в течение ночи при комнатной температуре. Образовавшийся осадок отфильтровывают; фильтрат экстрагируют этилацетатом (3×10 мл). Объединенные органические слои промывают насыщенным водным раствором NaCl (3×10 мл), сушат над безводным Na2SO4 и концентрируют досуха. Остаток и осадок объединяют. Продукт очищают методом колоночной хроматографии на силикагеле, используя в качестве элюента смесь петролейного эфира и этилацетата (1:1).
Пример 5.
К раствору бензадьдегида (1.0 ммоль) в сухом ацетонитриле (1 мл) добавляют 2-(5-метилфуран-2-ил)этиламин (1.0 ммоль, 0.125 мкл). Реакционную смесь кипятят в течение 1 ч (контроль ТСХ) и концентрируют досуха. К раствору имина в ледяной АсОН (650 мкл) добавляют конц. HCl (425 мкл). Реакционную смесь перемешивают при 70°С в течение 5 ч. Затем добавляют 10% водн. раствор NaOH и смесь перемешивают в течение ночи при комнатной температуре. Образовавшийся осадок отфильтровывают; фильтрат экстрагируют этилацетатом (3×10 мл). Объединенные органические слои промывают насыщенным водным раствором NaCl (3×10 мл), сушат над безводным Na2SO4 и концентрируют досуха. Остаток и осадок объединяют. Продукт очищают методом колоночной хроматографии на силикагеле, используя в качестве элюента смесь петролейного эфира и этилацетата (1:1).
В таблице 2 приведены данные о влиянии времени и температуры заключительной стадии циклизации на выход целевого 2-метил-4-фенил-4,5,6,7-тетрагидрофуро[3,2-с]пиридина (1а) (примеры 1-5).
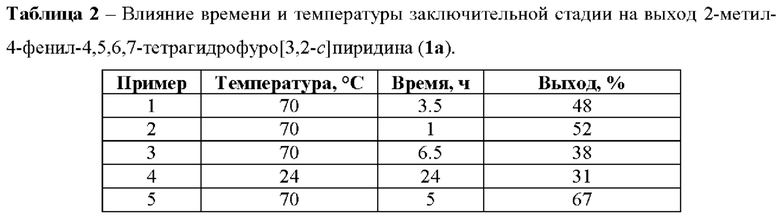
Как видно из таблицы 2, 2-метил-4-фенил-4,5,6,7-тетрагидрофуро[3,2-с]пиридин (1а) с наибольшим выходом был получен при нагревании (70°С) раствора промежуточного имина в уксусной кислоте в присутствии концентрированной соляной кислоты в течение 5 часов минут. Более длительное кипячение приводит к осмолению реакционной смеси, что сопровождается значительным снижением выхода целевого продукта 1а, а кратковременное кипячение приводит к неполной конверсии промежуточного имина и, как следствие, выход продукта 1а снижается до 52%. Проведение реакции циклизации амино-1,4-дикетона при комнатной температуре также не позволяет получить целевой продукт 1а с более высоким выходом. Таким образом, оптимальным условием проведения ключевой стадии циклизации промежуточного имина в синтезе 2-метил-4-фенил-4,5,6,7-тетрагидрофуро[3,2-c]пиридин является нагревание (70°С) раствора промежуточного имина в уксусной кислоте в присутствии концентрированной соляной кислоты в течение 5 часов, выход в данном случае составляет 67%. Заявляемым способом (Пример 5) получен ряд производных 2-метил-4-фенил-4,5,6,7-тетрагидрофуро[3,2-с]пиридина Ia-и с выходами 20-72%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 7-АЛКИЛ-2,3-ДИГИДРО-1Н-ПИРРОЛО[1,2-d][1,4]ДИАЗЕПИН-4(5Н)-ОНА | 2017 |
|
RU2659390C1 |
| НОВЫЕ АМИНОГЛИКОЗИДНЫЕ АНТИБИОТИКИ | 2007 |
|
RU2458931C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-АМИНО-5-ФТОР-3-ХЛОР-6-(ЗАМЕЩЕННЫХ)ПИКОЛИНАТОВ | 2013 |
|
RU2653855C2 |
| ЗАМЕЩЕННЫЕ ПИРИМИДИНТИОАЛКИЛЬНЫЕ ИЛИ АЛКИЛЭФИРНЫЕ СОЕДИНЕНИЯ И СПОСОБ ИНГИБИРОВАНИЯ ОБРАТНОЙ ТРАНСКРИПТАЗЫ ВИРУСОВ | 1996 |
|
RU2167155C2 |
| ТРИЦИКЛИЧЕСКИЕ ДИАЗЕПИНОВЫЕ АНТАГОНИСТЫ ВАЗОПРЕССИНА И АНТАГОНИСТЫ ОКСИТОЦИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 1994 |
|
RU2126006C1 |
| БИЦИКЛИЧЕСКИЕ 6-АЛКИЛИДЕНПЕНЕМЫ В КАЧЕСТВЕ ИНГИБИТОРОВ β-ЛАКТАМАЗ | 2003 |
|
RU2339640C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 6-АЛКИЛИДЕНПЕНЕМА | 2003 |
|
RU2317297C2 |
| АМИДОЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ КСАНТИНА, ОБЛАДАЮЩИЕ ИНГИБИРУЮЩИМ ДЕЙСТВИЕМ ФОСФОЕНОЛПИРУВАТКАРБОКСИКИНАЗЫ (ФЕПКК), СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ | 2003 |
|
RU2295525C2 |
| ПРОИЗВОДНОЕ 3-ОКСАДИАЗОЛИЛ-5,6,7,8-ТЕТРАГИДРО-1,6-НАФТИРИДИНА И ПРОИЗВОДНОЕ 5,6,7,8-ТЕТРАГИДРО-1,6-НАФТИРИДИНА | 1993 |
|
RU2107686C1 |
| 1-(АМИНОАЛКИЛ)-3-СУЛЬФОНИЛАЗАИНДОЛЫ В КАЧЕСТВЕ ЛИГАНДОВ 5-ГИДРОКСИТРИПТАМИНА-6 | 2003 |
|
RU2315048C2 |
Изобретение относится к области органической химии, а именно к способу получения замещенных тетрагидрофуро[3,2-с]пиридинов общей формулы I, которые могут найти применение как вещества, обладающие потенциальной биологической активностью широкого спектра действия. Способ осуществляется взаимодействием легкодоступного 2-(5-метилфуран-2-ил)этиламина и замещенных бензальдегидов при кипячении в ацетонитриле с образованием соответствующих иминов и последующей циклизацией полученных иминов в уксусной кислоте при 70°С в присутствии концентрированной соляной кислоты с последующей обработкой реакционной смеси раствором NaOH при комнатной температуре с образованием целевых тетрагидрофуро[3,2-с]пиридинов Ia-и. Технический результат изобретения заключается в создании простого и эффективного метода синтеза замещенных тетрагидрофуро[3,2-c]пиридинов формулы Iа-и, позволяющего получать целевые продукты с хорошими выходами, а также варьировать заместители в 4-м положении гетероциклического ядра. 2 табл., 5 пр.
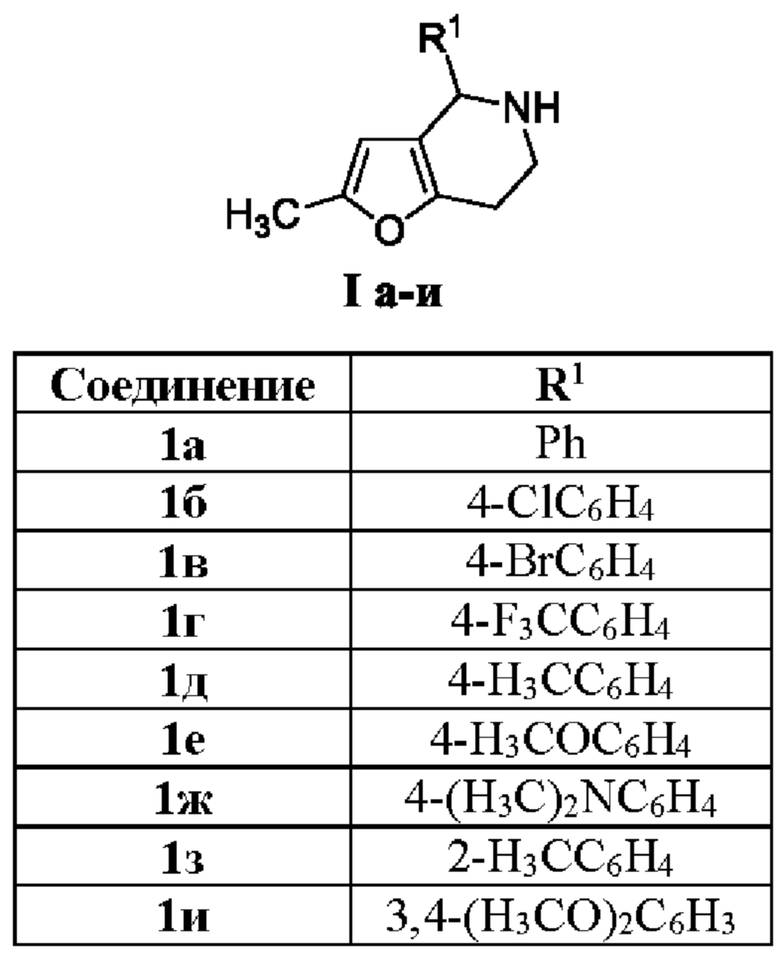
Способ получения замещенных тетрагидрофуро[3,2-с]пиридинов общей формулы I
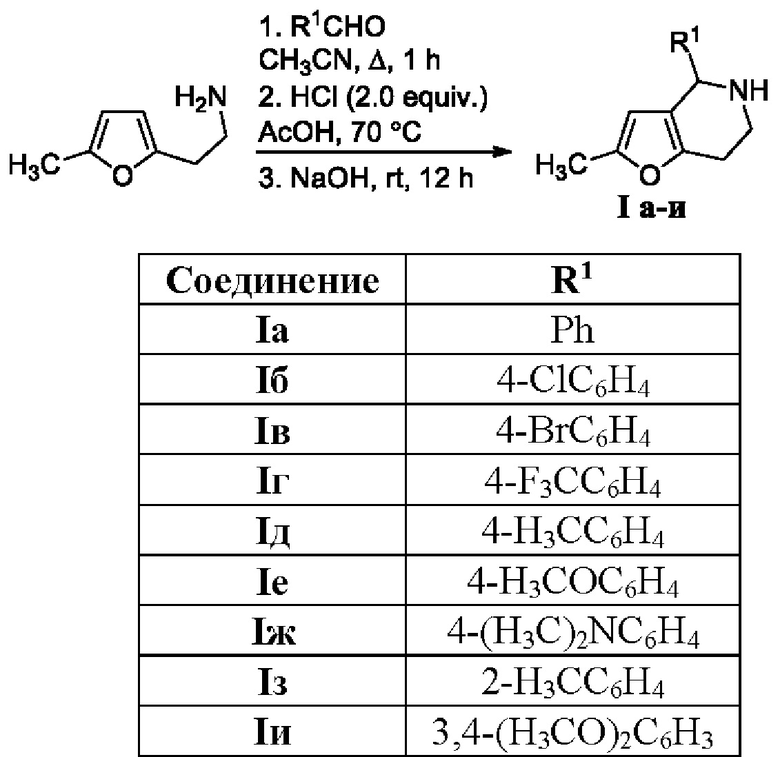
характеризующийся тем, что целевые тетрагидрофуро[3,2-с]пиридины образуются в результате взаимодействия легкодоступного 2-(5-метилфуран-2-ил)этиламина и замещенных бензальдегидов в соответствии с приведенной схемой.
| NAYLOR A | |||
| et al., 4-[(Alkylamino)methyl]furo[3,2-c]pyridines: A New Series of Selective K-Receptor Agonists, J | |||
| Med | |||
| Chem., 1994, vol.37, p.2138-2144 | |||
| MONHRI K | |||
| et al., Studies toward Total Synthesis of Non-Aromatic Erythrinan Alkaloids | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Synthesis of Cocculolidine Skeleton, Chem | |||
| Pharm | |||
| Bull., 1998, vol.46, no.12, p.1872-1877 | |||
| SCHAFROTH M.A | |||
Авторы
Даты
2023-12-25—Публикация
2023-03-22—Подача