Изобретение относится к области молекулярной биологии, в частности к генной инженерии, и может быть использовано для создания генетической конструкции с целью геномного редактирования предимплантационных эмбрионов для получения высокоценного племенного крупного рогатого скота молочного направления, устойчивого к лейкозу.
Изобретение обеспечивает эффективное встраивание генетической конструкции CRISPR/Cas9 в ДНК эмбриональной культуры клеток крупного рогатого скота при трансфекции.
Лейкоз крупного рогатого скота – вирусное заболевание, которое характеризуется злокачественным разрастанием лимфатической ткани. Возбудителем этого заболевания является вирус лейкоза крупного рогатого скота (ВЛКРС, BLV), который относится к семейству РНК-содержащих вирусов семейства Retroviridae, рода Deltaretrovirus. В настоящее время лейкоз крупного рогатого скота остается одним из самых распространенных карантинных заболеваний. По состоянию на март 2022 года 65 субъектов Российской Федерации являются неблагополучными по лейкозу крупного рогатого скота, что подтверждается официальной информацией Россельхознадзора (https://cerberus.vetrf.ru/cerberus/regionalization/pub), в т.ч. и Кемеровская область-Кузбасс.
Учитывая распространенность заболевания и отсутствия лечения, а также генетическую предрасположенность высокопродуктивных животных, необходим поиск принципиально новых методов профилактики данного заболевания, в т.ч. и с применением методов генной инженерии, что позволяет получать наиболее ценные по хозяйственным признакам животных, устойчивых к заражению ВЛКРС.
Патент РФ №2621146 «Способ профилактики постнатального заражения вирусом лейкоза крупного рогатого скота молодняка крупного рогатого скота», патент РФ № 2631607 «Средство для профилактики лейкоза крупного рогатого скота и способ его применения», описывают фармакологические методы профилактики заражения животных ВЛКРС. Недостатком методов является возможность заражения вирусом при отмене препаратов.
Ближайшим аналогом выбран патент РФ 2741092 «Генетическая конструкция для получения устойчивых к вирусу лейкоза эмбрионов крупного рогатого скота», описывающим генетическую конструкцию на основе плазмидного вектора, кодирующего последовательность направляющей РНК, а также ряд регуляторных последовательностей: промоторы CMV и U6, энхансеры, ген-репортер – GFP, вставку hSpCas9 (5400 п.н.), селективный ген (обеспечивающий резистентность к тем или иным антибиотикам), ген эндонуклеазы Cas9, сайты узнавания для различных рестриктаз. Несмотря на удобство применения плазмидного вектора с целью геномного редактирования эукариотических клеток, у данного метода имеется недостаток – несовпадение во времени деления эукариотических клеток редактируемого организма с транскрипцией гРНК и трансляцией Cas9, что приводит к получению химерного организма.
Техническим результатом настоящего изобретения является получение генетической конструкции, способной встраиваться в ДНК эмбриональной культуры клеток крупного рогатого скота, что обеспечивает модификацию генома с целью последующего получения генетически полноценных животных, устойчивых к вирусу лейкоза крупного рогатого скота.
Технический результат достигается тем, что готовый рибонуклеопротеиновый комплекс: смесь белка CAS9 и гРНК позволяет о проводить редактирование 2 экзона гена BoLA-DRB3 крупного рогатого скота за счет низкой неспецифической активности и редактирования сразу после встраивания в клетку.
Пример выполнения.
Для выявления генов, проводится сравнительный анализ нуклеотидных последовательностей крупного рогатого скота (представитель рода Bos Taurus), депонированных в генетическую базу данных (GenBank), в результате которого выявляется главный комплекс гистосовместимости крупного рогатого скота BoLA-DRB3, содержащий участок – экзон 2 гена BoLA-DRB3, содержащий нуклеотидную последовательность «GGAGTATTCTACGAGCGAGTGTCATTTCTTCAACGGGACCGAGCGGGTGCGGTACCTGGACAGATACTTCCATAATGGAGAAGAGTTCGTGCGCTTCGACAGCGACTGGGGCGAGTACCGGGCGGTGACCGAGCTAGGGCGGCGGTCCGCCGAGCAGTTGAACGGCCAGAAGGACACCCTGGAGCGGGAGCGGGCCTATGTGGACACGTACTGCAGACACAACTACGGGGTCGTTGA», кодирующих аминокислотную последовательность Val-Asp-Thr-Tir (VDTY) (фиг. 1), которая, ассоциирована с восприимчивостью к лейкозу, поскольку идентична участку аминокислотной цепи обратной транскриптазы вируса лейкоза.
Следующий этап работы заключается в разработке гРНК, с применением одного из веб-инструментов CHOP-CHOP (https://chopchop.cbu.uib.no/) для выбора целевых сайтов CRISPR/Cas9. Подбор включал в себя следующие этапы:
1. Введение нуклеотидной последовательности, полученной в результате анализа молекулярно-биологических программ (https://www.ncbi.nlm.nih.gov/) в веб-инструмент CHOP-CHOP;
2. Выбор видовой принадлежности редактируемого организма из предложенного списка. В нашем случае выбранным организмом является Bos Taurus;
3. Указание системы, с помощью которой планируется проводить редактирование. Свой выбор мы остановили на системе CRISPR/Cas9.
Для внесения двухцепочечного разрыва в геном крупного рогатого скота с применением системы редактирования CRISPR-Cas9 подбирается последовательность направляющей РНК с учетом следующих правил:
1. Оптимальным участком для внесения двуцепочечного разрыва ДНК с целью нокаутирования гена является участок экзонной области ДНК, расположенный на расстоянии около 150-300 п.н. после сарт-кодона.
2. Первым нуклеотидом, расположенным на 5′-конце гРНК (с которого будет начинаться синтез молекулы РНК), должен быть гуанин. Поэтому необходимо подбирать последовательности ДНК вида G(N)19 NGG.
3. Необходимо чтобы 17-м нуклеотидом протоспейсера, непосредственно прилегающего к месту разрыва, и наибольшим образом влияющий на исход репарации, являлся тимин или аденин. В этом случае с большей вероятностью произойдет инсерция-делеция со сдвигом рамки считывания.
4. Необходимо обеспечить исключение возникновения нецелевых мутаций при эффективном подборе целевых.
С учетом вышеуказанных требований была подобрана следующая гРНК: (5´- GACCGAGCGGGUGCGGUACCUGG -3´).
Для введения в клетки системы CAS применяется готовый рибонуклеопротеиновый комплекс: смесь белка CAS9 и гРНК с выбранной нуклеотидной последовательностью (5´- GACCGAGCGGGUGCGGUACCUGG -3´). Доставка системы CRISPR/CAS9 в виде готового рибонуклеопротеинового комплекса имеет ряд преимуществ, среди которых: высокая эффективность редактирования; низкая неспецифическая активность; редактирование сразу после встраивания в клетку; возможность быстрого скрининга эффективности направляющих РНК в пробирке.
Для исследования способности гРНК вносить двухцепочечный разрыв в выбранный участок редактируемого гена BoLA-DRB3 была проведена липофекция 9 эмбриональных клеточных культур крупного рогатого скота.
Полученные клеточные культуры культивировали при температуре 37 оС, в 5% СО2 в течение 40-48 часов. Через три дня культивирования из эмбриональных клеточных культур выделяют плазмидную ДНК, путем проведения денатурации и медленного отжига ПЦР-продуктов. При проведении отжига ампликоны фрагментов ds-DNA, расщепляли рестриктазой EarI. При исследовании ПЦР-продуктов на 2% агарозном геле с добавлением бромистого этидия и фиксируют системой гель-документации, имеющие различную длину нуклеотидные последовательности в агарозном геле появляются различными размерами фрагментов (табл. 1).
Таблица 1 – Генотипирование эмбрионых культур клеток крупного рогатого скота на наличие целевой модификации
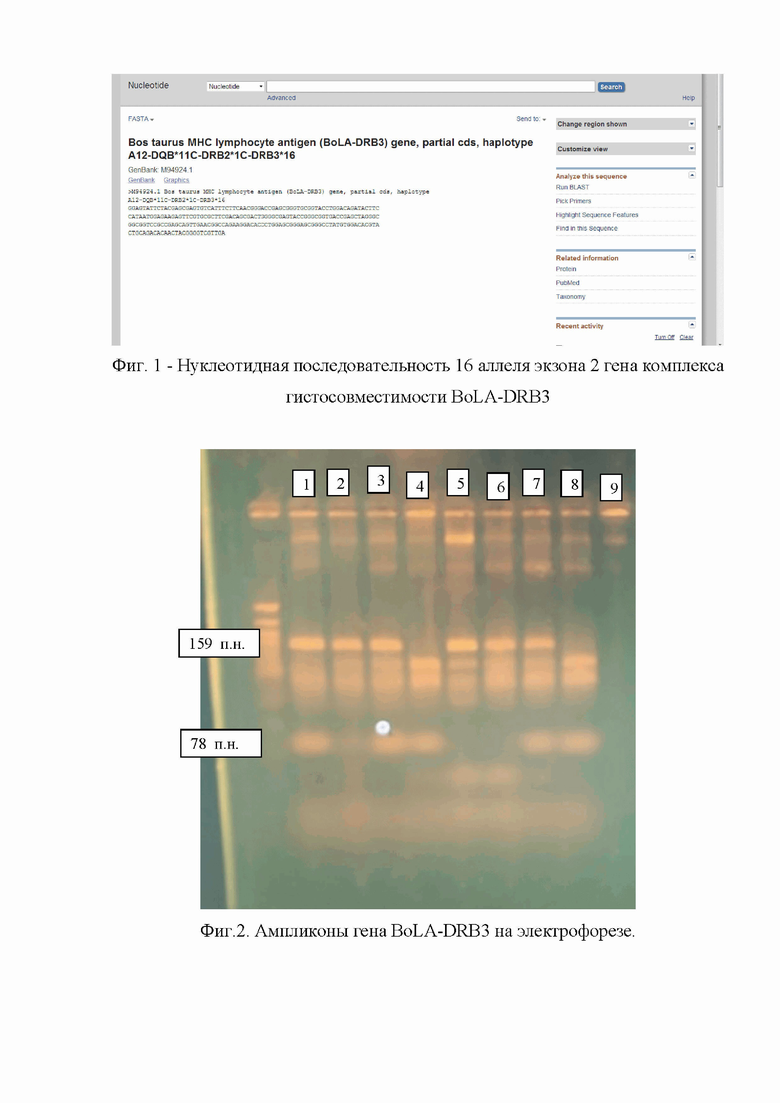
Визуализация менее ярких полос в 3 образцах, содержащих фрагменты рестрикции с меньшей молекулярной массой (159 п.н. и 78 п.н.) свидетельствует о наличии встроенной генетической конструкции (Фиг. 2).
Визуализация полос с данной молекулярной массой – является подтверждением эффективной интеграции целевой последовательности в геноме эмбриональных клеток.
На основании вышеизложенного, можно сделать вывод, что созданный рибонуклеопротеиновый комплекс: смесь белка CAS9 и гРНК 5´- GACCGAGCGGGUGCGGUACCUGG -3´ позволяет более эффективно проводить редактирование 2 экзона гена BoLA-DRB3 крупного рогатого скота за счет низкой неспецифической активности и редактирования сразу после встраивания в клетку. Определение эффективности встраивания геномной конструкции не требует высокоценного технологичного оборудования.
| название | год | авторы | номер документа |
|---|---|---|---|
| Генетическая конструкция для получения устойчивых к вирусу лейкоза эмбрионов крупного рогатого скота | 2020 |
|
RU2741092C1 |
| СИСТЕМА РЕДАКТИРОВАНИЯ ГЕНОМНОЙ ДНК ЭУКАРИОТИЧЕСКОЙ КЛЕТКИ НА ОСНОВЕ НУКЛЕОТИДНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ, КОДИРУЮЩЕЙ БЕЛОК SUCAS9NLS | 2022 |
|
RU2804422C1 |
| Способ редактирования генома вируса заразного узелкового дерматита крупного рогатого скота с помощью Overlap-ПЦР и CRISPR-Cas9 технологии | 2023 |
|
RU2825451C1 |
| СПОСОБ ДИАГНОСТИКИ УСТОЙЧИВОСТИ КРУПНОГО РОГАТОГО СКОТА К ВИРУСУ ЛЕЙКОЗА | 2010 |
|
RU2428485C1 |
| Способ получения генно-модифицированных кроликов с нокаутом гена LEPR с помощью системы CRISPR/Cas9 | 2023 |
|
RU2836438C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНЕТИЧЕСКОЙ УСТОЙЧИВОСТИ КРУПНОГО РОГАТОГО СКОТА К ВИРУСУ ЛЕЙКОЗА | 2022 |
|
RU2807575C1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ НАЦЕЛЕННЫХ ГЕНЕТИЧЕСКИХ МОДИФИКАЦИЙ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2771532C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ НАЦЕЛЕННОЙ ГЕНЕТИЧЕСКОЙ МОДИФИКАЦИИ С ИСПОЛЬЗОВАНИЕМ ПАРНЫХ ГИДОВЫХ РНК | 2015 |
|
RU2734770C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ МОДИФИКАЦИИ ЦЕЛЕВОГО ЛОКУСА | 2015 |
|
RU2704283C2 |
| Технология получения мышей с гуманизированным участком Gnao1 в области однонуклеотидного полиморфизма rs587777057 для тестирования РНК-терапии для GNAO1 c.607 G>A пациентов | 2021 |
|
RU2757121C1 |
Изобретение относится к области биотехнологии, а именно к рибонуклеопротеиновому комплексу для геномного редактирования восприимчивых к вирусу лейкоза крупного рогатого скота аллелей 2 экзона гена BOLA-DRB3, включающему белок CAS 9 и гРнк, характеризующаяся 5´- GACCGAGCGGGUGCGGUACCUGG -3. Изобретение эффективно для геномного редактирования для воспроизводства высокоценного племенного крупного рогатого скота молочного направления, устойчивого к вирусу лейкоза крупного рогатого скота. 2 ил., 1 табл.
Рибонуклеопротеиновый комплекс для геномного редактирования восприимчивых к вирусу лейкоза крупного рогатого скота аллелей 2 экзона гена BOLA-DRB3, включающий белок CAS 9 и гРнк, характеризующаяся 5´- GACCGAGCGGGUGCGGUACCUGG -3.
| МЕТЛЕВА А.С | |||
| И др., Отбор Grna для геномного редактирования чувствительных к вирусу лейкоза крупного рогатого скота аллелей экзона 2 гена Bola-DRB3 с помощью CRISPR/Cas9, Материалы IV Международной научно-практической конференции "Современная научно-техническая техника и проблемы сельского хозяйства" | |||
| Кемерово (Россия), 25 июня 2020 г., стр |
Авторы
Даты
2023-12-27—Публикация
2023-01-27—Подача