Изобретение относится к области молекулярной биологии, в частности к генетической инженерии, и может быть использовано для геномного редактирования предимплантационных эмбрионов для воспроизводства высокоценного племенного крупного рогатого скота молочного направления, устойчивого к лейкозу.
Изобретение обеспечивает эффективную экспрессию системы CRISPR/Cas9 при введении указанной конструкции в культуры клеток эмбрионов крупного рогатого скота.
В настоящее время лейкоз крупного рогатого скота остается одним из самых распространенных опасных заболеваний, приносящим большой экономический ущерб молочному и мясному скотоводству. Знания, основанные на изучении механизма заражения вирусом лейкоза, генетической предрасположенности животных, определяют поиск принципиально новых методов профилактики и лечения данного заболевания, что позволяет эффективно проводить отбор наиболее ценных по хозяйственным признакам животных, устойчивых к заражению вирусом лейкоза.
В последнее время интенсивное развитие методов генной инженерии и геномной терапии, основанных на применении технологии редактирования генома, позволило выявлять локусы генов, отвечающие за предрасположенность животного к тем или иным заболеваниям, а также проводить замену нуклеотидной последовательности в генах, повышая их резистентность (патент RU №2644673, опубл. 13.02.2018;патент RU №2687451, опубл.13.05.2019).
На сегодняшний день, несмотря на многообразие созданных генетических конструкций, применяемых для внесения в культуры клеток животных, до сих пор не разработана эффективная конструкция с помощью которой можно получать эмбрионы крупного рогатого скота, устойчивых к вирусу лейкоза.
Задачей настоящего изобретения является создание генетической конструкции, позволяющей более эффективно проводить редактирование генома крупного рогатого скота в культурах клеток эмбрионов для создания поголовья, устойчивого к вирусу лейкоза.
Задача решается новой генетической конструкцией, содержащей регуляторные элементы плазмидного вектора для трансфекции культуры клеток эмбрионов крупного рогатого скота, а также последовательностей, обеспечивающих экспрессию белков Cas9 и GFP, а также направляющей РНК под контролем промоторов.
Техническим результатом предлагаемого изобретения является обеспечение эффективной экспрессии белка Cas9 и направляющей РНК конструкцией, при введении которой в культуры клеток эмбрионов крупного рогатого скота, обеспечивается модификация экзона 2 гена BoLA-DRB3 с целью получения устойчивых к вирусу лейкоза эмбрионов крупного рогатого скота.
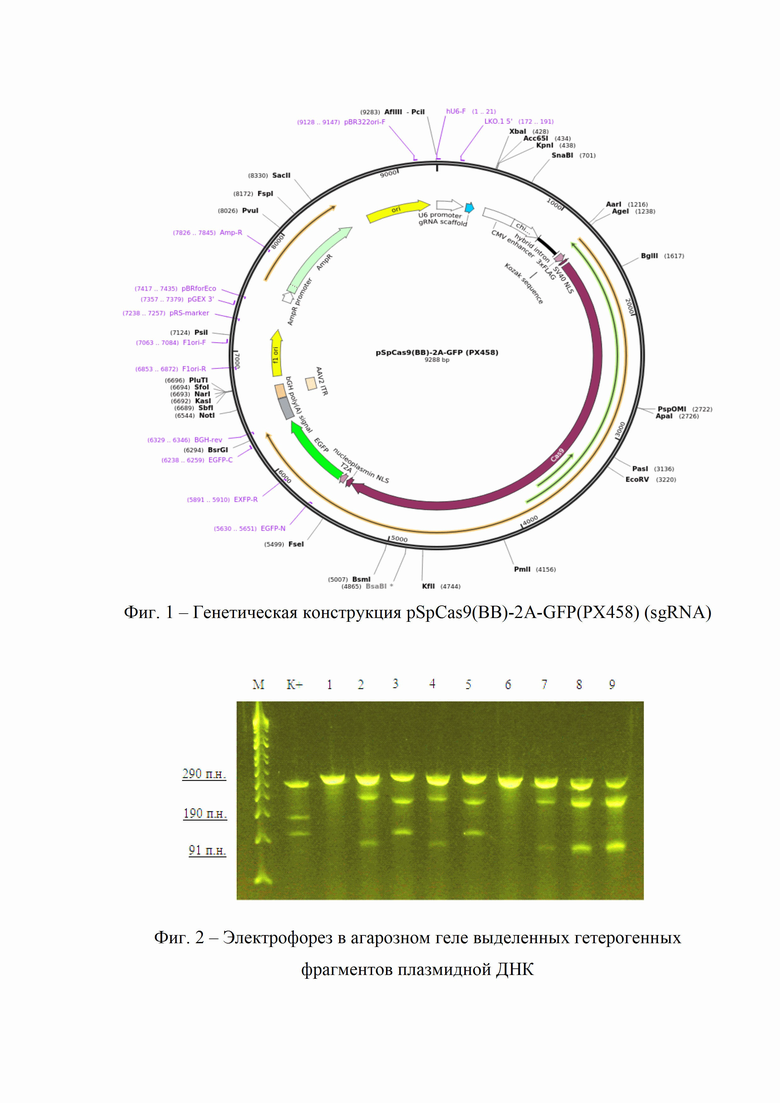
Объектом изобретения является генетическая конструкция на основе плазмидного вектора (фиг. 1), кодирующая последовательность направляющей РНК, а также ряд регуляторных последовательностей: промоторы CMV и U6, энхансеры, ген-репортер – GFP, вставку hSpCas9 (5400 п.н.), селективный ген (обеспечивающий резистентность к тем или иным антибиотикам), ген эндонуклеазы Cas9, сайты узнавания для различных рестриктаз.
Примеры выполнения
Пример 1. Подбор для редактирования генов, влияющих на формирование резистентности к вирусу лейкоза у эмбрионов крупного рогатого скота.
Для выявления генов, проводят сравнительный анализ нуклеотидных последовательностей крупного рогатого скота (представитель рода BosTaurus), депонированных в генетическую базу данных (GenBank), в результате которого выявляется главный комплекс гистосовместимости крупного рогатого скота BoLA-DRB3, содержащий участок – экзон 2 гена BoLA-DRB3.
Данный участок кодирует последовательность аминокислот Val-Asp-Thr-Tir (VDTY) в положении 75–78, которая ассоциирована с восприимчивостью к лейкозу, поскольку идентична участку аминокислотной цепи обратной транскриптазы вируса лейкоза.
Следовательно, при редактировании генома эмбрионов крупного рогатого скота для создания устойчивых к вирусу лейкоза линий, вносится двухцепочечный разрыв с последующей негомологичной репарацией в экзон 2 гена BoLA-DBR3 в результате которого участок, идентичный аминокислотной цепи обратной транскриптазы вируса лейкоза, теряет свою идентичность за счет изменения нуклеотидной последовательности.
Для внесения двухцепочечного разрыва в геном крупного рогатого скота с применением системы редактирования CRISPR-Cas9 с помощью программы CRISPOR (Version 4.95) подбирается последовательность направляющей РНК (5´-CGACTGGGGCGAGTACCGGG-3´) и проводится анализ ее специфичности.
Пример 2. Получение генетической конструкции.
В качестве основы для создания генетической конструкции, содержащей последовательности направляющей РНК, используют плазмидный вектор pSpCas9(BB)-2A-GFP(PX458).
В представленный вектор методом клонирования по сайтам рестрикции эндонуклеазами встраивают следующую нуклеотидную последовательность:
Последовательность направляющей РНК
5´-CGACTGGGGCGAGTACCGGG-3´.
Указанную последовательность вводят с 3'-конца от промотора U6. Вводимую последовательность направляющей РНК и специфические олигонуклеотиды (5´-CACCGCGACTGGGGCGAGTACCGGG-3´, 5´-AAAC CCCGGTACTCGCCCCAGTCG C-3´) синтезируют для вставки в плазмидный каркас.
Проводят перевод плазмиды в линейную форму расщеплением рестриктазой FastDigestBbsI, очистку расщепленной плазмиды в агарозном геле, фосфорилирование и отжиг каждого олигонуклеотида. Далее проводят лигирование последовательности направляющей РНК и экспрессионного вектора и обработку продукта лигированияэкзонуклеазой PlasmidSafe.
Проверку на наличие вставки направляющей последовательности РНК в плазмидную конструкцию проводят методом секвенирования с промотора U6 с использованием праймера U6-Fwd (TTT-ATG-GCG-AGG-CGG-CGG) с последующим сравнением результатов секвенирования с векторной последовательностью клонирования pSpCas9 (BB), чтобы убедиться, что 20-ти направляющая последовательность РНК вставлена между промотором U6 и оставшейся частью каркаса.
Предложена искусственно сконструированная генетическая конструкция с системой CRISPR/Cas9 для внесения двухцепочечного разрыва с последующей негомологичной репарацией в экзон 2 гена BoLA-DRB3, которая может быть использована для геномного редактирования предимплантационных эмбрионов для воспроизводства высокоценного племенного крупного рогатого скота молочного направления, устойчивого к лейкозу. Данная конструкция включает последовательности, кодирующие белки Cas9, GFP и экспрессирующие направляющую РНК. Генетическая конструкция содержит последовательность направляющей РНК для экспрессии под контролем промотора U6.
Указанная генетическая конструкция pSpCas9(BB)-2A-GFP(PX458) (sgRNA) содержит в себе все необходимые для экспрессии и функционирования компоненты: промоторы CMV и U6, вставку направляющей РНК (gRNA) (20 п.н.), энхансеры, ген-репортер – GFP, вставку hSpCas9 (5400 п.н.), селективный ген (обеспечивающий резистентность к тем или иным антибиотикам), ген эндонуклеазы Cas9, сайты узнавания для различных рестриктаз.
Пример 3. Проверка интеграции и экспрессии плазмидной ДНК в культурах клеток эмбрионов крупного рогатого скота,трансфицированныхплазмидой pSpCas9(BB)-2A-GFP(PX458)(sgRNA).
Для исследования влияния введения генетической конструкции на эффективность модификации экзона 2 гена BoLA-DRB3 было отобрано 9 инъецированных эмбрионов крупного рогатого скота, из которых были получены культуры клеток.
Для определения влияния введения генетической конструкции на эффективность модификации экзона 2 гена BoLA-DRB3, культуры клеток эмбрионов, трансфецированныеплазмидой pSpCas9(BB)-2A-GFP(PX458)(sgRNA), культивируют при температуре 37 оС, в 5% СО2 в течение 40-48 часов. Через три дня культивирования проверяют интеграцию и экспрессиюплазмидной ДНК путем проведения денатурации и медленного отжига ПЦР-продуктов. При проведении отжига ампликоны фрагментов ds-DNA, расщепленные рестриктазами AsuHPI / HphI, и имеющие различную длину нуклеотидные последовательности в агарозном геле появляются различными размерами фрагментов (Фиг. 2).
В результате образовывалась яркая одиночная полоса длиной 290 п.н. в образцах ПЦР (1 и 6), что говорит об отсутствии в данных клонах клеток целевой генетической модификации.
Визуализация менее ярких полос в 7 образцах, содержащих фрагменты рестрикции с меньшей молекулярной массой (190 п.н. и 91 п.н.) свидетельствует о наличии встроенной генетической конструкции, комплементарной ДНК клеток дикого типа.
Визуализация полос с меньшей молекулярной массой является подтверждением эффективной интеграции целевой последовательности в геноме клеток эмбрионов крупного рогатого скота (табл. 1).
Таблица 1 – Рестрикционный анализ эмбрионов крупного рогатого скота на наличие целевой модификации
амплификата, п.н.
На основании вышеизложенного, можно сделать вывод, что создание генетической конструкции с системой СRISPR/Cas9 позволяет провести эффективную генетическую модификацию участка экзона 2 гена BoLA-DRB3 за счет тщательно подобранных нуклеотидных последовательностей направляющих РНК, для получения эмбрионов крупного рогатого скота, устойчивых к вирусу лейкоза.
| название | год | авторы | номер документа |
|---|---|---|---|
| гРНК для геномного редактирования восприимчивых к вирусу лейкоза крупного рогатого скота аллелей 2 экзона гена BOLA-DRB3 | 2023 |
|
RU2810549C1 |
| СПОСОБ ДИАГНОСТИКИ УСТОЙЧИВОСТИ КРУПНОГО РОГАТОГО СКОТА К ВИРУСУ ЛЕЙКОЗА | 2010 |
|
RU2428485C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНЕТИЧЕСКОЙ УСТОЙЧИВОСТИ КРУПНОГО РОГАТОГО СКОТА К ВИРУСУ ЛЕЙКОЗА | 2022 |
|
RU2807575C1 |
| Способ редактирования генома вируса заразного узелкового дерматита крупного рогатого скота с помощью Overlap-ПЦР и CRISPR-Cas9 технологии | 2023 |
|
RU2825451C1 |
| Способ получения генно-модифицированных кроликов с нокаутом гена LEPR с помощью системы CRISPR/Cas9 | 2023 |
|
RU2836438C1 |
| Способ оценки устойчивости к лейкозу крупного рогатого скота | 2020 |
|
RU2737552C1 |
| РНК-НАПРАВЛЯЕМАЯ ИНЖЕНЕРИЯ ГЕНОМА ЧЕЛОВЕКА | 2013 |
|
RU2699523C2 |
| СПОСОБ ПОВЫШЕНИЯ ИММУННОЙ КОМПЕТЕНТНОСТИ ЖИВОТНЫХ В СТАДАХ КРУПНОГО РОГАТОГО СКОТА | 2010 |
|
RU2429598C1 |
| РНК-НАПРАВЛЯЕМАЯ ИНЖЕНЕРИЯ ГЕНОМА ЧЕЛОВЕКА | 2013 |
|
RU2766685C2 |
| Способ получения нокаута гена CD209 в эмбрионах Bos taurus путем трансдукции зигот адено-ассоциированными вирусами, кодирующими saCas9 и соответствующую гидовую РНК | 2022 |
|
RU2800917C1 |
Изобретение относится к области молекулярной биологии, в частности к генетической инженерии, и может быть использовано для геномного редактирования и получения эмбрионов крупного рогатого скота, устойчивых к вирусу лейкоза. Предложена генетическая конструкция для внесения двухцепочечного разрыва с последующей негомологичной репарацией в экзон 2 гена BoLA-DRB3, которая может быть использована для геномного редактирования предимплантационных эмбрионов для воспроизводства высокоценного племенного крупного рогатого скота молочного направления, устойчивого к лейкозу. 2 ил., 1 табл.
Генетическая конструкция для получения устойчивых к вирусу лейкоза эмбрионов крупного рогатого скота, включающая последовательности, кодирующие белки Cas9 и GFP, а также направляющую РНК, полученную на основе экспрессионного плазмидного вектора pSpCas9(BB)-2A-GFP(PX458) (sgRNA) структуры, указанной на Фиг. 1, включающего ряд регуляторных последовательностей: промоторы CMV и U6, вставку направляющей РНК (gRNA) (20 п.н.), энхансеры, ген-репортер – GFP, вставку hSpCas9 (5400 п.н.), селективный ген (обеспечивающий резистентность к тем или иным антибиотикам), ген эндонуклеазы Cas9, сайты узнавания для различных рестриктаз.
| WO 2019025984 A1, 07.02.2019 | |||
| CN 110835634 A, 25.02.2020 | |||
| СКОНСТРУИРОВАННАЯ СПОСОБАМИ ИНЖЕНЕРИИ ПЛАТФОРМА ДЛЯ ВСТРАИВАНИЯ ТРАНСГЕНА (ETIP) ДЛЯ НАЦЕЛИВАНИЯ ГЕНОВ И СТЭКИНГА ПРИЗНАКОВ | 2013 |
|
RU2666916C2 |
Авторы
Даты
2021-01-22—Публикация
2020-07-23—Подача