Область изобретения
[1] Настоящее изобретение относится к производной имидазопиридина и фармацевтическому препарату, содержащему ее в качестве активного ингредиента, и более конкретно, к производной имидазопиридина, которая ингибирует действие протеинкиназы и в таком качестве может использоваться для профилактики или лечения рака, нейродегенеративного заболевания, неалкогольного стеатогепатита, гриппа и т.п., а также к фармацевтическому препарату, содержащему ее в качестве активного ингредиента.
Предшествующий уровень техники
[2] Киназы запускают реакцию, в которой фосфатная группа из высокоактивных молекул, в частности, АТФ, перемещается в субстрат. Киназы стабилизируют фосфорно-ангидридные связи и располагают субстрат и фосфатную группу в определенном положении, в котором увеличивается скорость реакции. В большинстве случаев переходное состояние, возникающее в результате взаимодействия с фосфатной группой, имеющей отрицательный заряд, электростатически стабилизируется за счет окружающих аминокислот, имеющих положительный заряд, и некоторые киназы могут координироваться с фосфатной группой через металлический кофактор.
[3] В соответствии с субстратом и характеристиками, киназы могут классифицироваться, например, как протеинкиназы, липидкиназы и углеводные киназы. Протеины, липиды и углеводы могут варьироваться по своим активности, реактивности, способности связывать другие молекулы и т.п., в зависимости от состояния фосфорилирования. Киназы воздействуют на внутриклеточную передачу сигнала и регулируют сложные биологические механизмы внутри клеток. Благодаря фосфорилированию активность некоторых молекул может усиливаться или ослабляться, и их способность взаимодействовать с другими молекулами может контролироваться. Поскольку многие киназы реагируют на условия или сигналы среды, клетки могут контролировать внутриклеточные молекулы путем применения киназ, в зависимости от ситуации. В таком качестве киназы играют решающую роль в росте, дифференциации, разрастании, выживании, метаболизме, передаче сигналов, передаче ячеек, секреции клеток, a также многих других путей клеточных реакций.
[4] Протеинкиназы могут усиливать или ослаблять активность протеина, становиться маркером для стабилизации или деградации, помещать протеин в ту или иную ячейку клетки либо инициировать или препятствовать взаимодействиям протеина с другими протеинами. Известно, что большинство киназ представлены именно протеинкиназами, которые считаются важной целью исследований. Наряду с фосфатами, протеинами и энзимами, протеинкиназы регулируют также передачу сигналов клеток. Хотя протеины клеток подвержены многочисленным ковалентным связям, немногие из этих связей являются обратимыми. Соответственно, мы можем сказать, что фосфорилирование протеинов имеет регуляторную функцию. Протеинкиназы часто могут иметь несколько субстратов, и порой тот или иной протеин может выступать в качестве субстрата как минимум для одной киназы. По этой причине протеинкиназы получают наименования с использованием факторов, которые регулируют их виды деятельности. Например, кальмодулинзависимая протеинкиназа регулируется кальмодулином. В некоторых случаях могут классифицироваться как подгруппы. Например, циклические АМФ-зависимые протеинкиназы типа I и типа II включают в себя идентичные энзимные субъединицы, но их регуляторные субъединицы, связанные с циклическим АМФ, отличны друг от друга.
[5] Протеинкиназа - это энзим, который играет важную роль в процессе внутриклеточной передачи сигнала посредством фосфорилирования гидроксигруппы, присутствующей в тирозиновом, сериновом или треониновом остатках протеинов, а также играет важную роль в сигнализировании факторов роста, вызывающих рост, дифференциацию и быстрое разрастание клетки (И. Мельникова и др., Nature Reviews Drug Discovery [Обзор изысканий природных лекарственных средств], 3 (2004), 993).
[6] Баланс между “включенным” и “выключенным” состояниями пути внутриклеточного сигнализирования является важным для поддержания гомеостаза клетки. Когда обычный путь внутриклеточного сигнализирования, напр., по большей части продолжение “включенного” состояния внутриклеточных сигналов, прерывается из-за гиперэкспрессии или мутации той или иной протеинкиназы, это может приводить к началу различных заболеваний, таких как рак, воспалительные заболевания, нарушения метаболизма и болезни мозга. По оценкам, человеческий геном содержит 518 протеинкиназ, что составляет примерно 1,7% от всех человеческих генов. Протеинкиназы можно разделить в основном на тирозинпротеинкиназы (90 или более типов) и серин/треонинпротеинкиназы.
[7] Важные с точки зрения медицины серин/треонинкиназы включают в себя семейство митоген-активируемых протеинкиназ (MAPK), которые действуют в различных биологических процессах. МАPK активируется после фосфорилирования МАPK-киназами (MAP2K или MAPKK) при наличии определенных тирозиновых или треаниновых остатков, в то время как MAP2K активируется после фосфорилирования MAP2K-киназами (MAPKK, MAPKKK) при наличии сериновых и сериновых/ треониновых остатков. Семейство MAP3K включает в себя несколько МАPK, в том числе A/B/C-Raf, MEKK1/4, ASK1/2, MLK1/2/3, MEKK2/3 т.п. В активацию MAP3K в ответ на разнообразные внеклеточные раздражители, среди которых цитокины, факторы быстрого разрастания и внешние нагрузки, включаются несколько механизмов.
[8] Богатая лейцином повторная киназа-2 (LRRK2) - это протеин, относящийся к семейству богатых лейцином повторных киназ. Она состоит из последовательности 2 527 аминокислот с высокой степенью сходства между видами. В одном протеине LRRK2 имеет место активность ГТФ-гидролазы (гуанозинтрифосфатаза; ГТФаза) и серин/треонинкиназы. Отжатая LRRK2 наблюдалась в разных органах и тканях, в том числе в мозге, а на клеточном уровне она наличествует в цитоплазме или в клеточной мембране и наружной митохондриальной мембране.
[9] По сообщениям, LRRK2 имеет отношение к развитию умеренного когнитивного нарушения по типу болезни Альцгеймера, L-дофа-обусловленной дискинезии и расстройству ЦНС, обусловленному дифференциацией невральных клеток-предшественников. Кроме того, сообщалось, что G2019S-мутация LRRK2 увеличивает вероятность возникновения рака, отличного от рака кожи, например, острой миелоидной лейкемии (ОМЛ), рака почек, рака груди, рака легких, рака простаты и т.п. В частности, G2019S-мутация LRRK2 повышает каталитическую активность домена LRRK2-киназы. Кроме того, сообщалось, что LRRK2 также связана с амиотрофическим латеральным склерозом, ревматоидным артритом и анкилозирующим спондилитом.
[10] Данная несоответственно высокая активность протеинкиназы прямо или косвенно связана с рядом заболеваний, возникающих из-за ненормальной работы клеток. Соответственно делались попытки предотвратить или лечить это болезни путем селективного замедления активности протеинкиназы.
[11] Документы, использованные для экспертизы заявки
[12] Патентные документы
[13] (Патентный документ 1) Заявка на выдачу патента Кореи № 10-2018-0021255
[14] (Патентный документ 2) Международная патентная публикация № WO 2011/03857
Краткое раскрытие сущности изобретения
[15] Один аспект настоящего изобретения направлен на получение соединения производной имидазопиридина, способного замедлять активность протеинкиназы.
[16] Другой аспект настоящего изобретения направлен на получение фармацевтического препарата, содержащего соединение производной имидазопиридина в качестве активного ингредиента для профилактики или лечения рака, нейродегенеративного заболевания, неалкогольного стеатогепатита, гриппа и т.п., за счет замедления активности протеинкиназы.
[17] В соответствии с одним из вариантов осуществления настоящего изобретения, предлагается соединение, представленное Формулой 1 ниже, его стереоизомер, его сольват, его гидрат, или его приемлемая с точки зрения фармацевтики соль:
[18] [Формула 1]
[19] 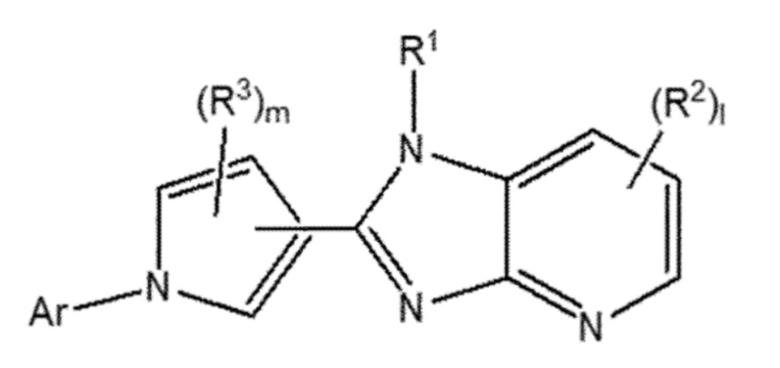
[20] в которой Ar - это C6-C20-арил или 5- - 20-членный гетероарил; R1, R2 и R3 каждый, независимо один от другого, выбраны из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C20 алкила, C1-C6 галоалкила, C1-C6 гидроксилалкила, C1-C6 алкоксилалкила, C1-C6 аминоалкила, C2-C20 алкенила, C2-C20 алкинила, C1-C8 алкокси, C3-C12 циклоалкила, C4-C12 циклоалкилалкила, 3-12-членного гетероциклила, 3-12-членного гетероциклилалкила, C6-C20-арила и 5-20-членного гетероарила; каждый из Ra, Rb и Rc независимо один от другого выбраны из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, C1-C20 алкила, C1-C6 галоалкила, C1-C6 гидроксилалкила, C1-C6 алкоксилалкила, C1-C6 аминоалкила, C2-C20 алкенила, C2-C20 алкинила, C1-C8 алкокси, C3-C12 циклоалкила, C4-C12 циклоалкилалкила, 3-12-членного гетероциклила, 3-12-членного гетероциклилалкила, C6-C20-арила и 5-20-членного гетероарила; «l» - целое число от 0 до 3; «m» - целое число от 0 до 3, при этом каждый из указанных компонентов: алкил, галоалкил, гидроксиалкил, алкоксиалкид, аминоалкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, гетероциклил, гетероциклилалкил, арил и гетероарил, могут замещаться один другим либо несколькими замещающими компонентами, выбранными из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкил, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксиалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероциклила, 3-10-членного гетероциклилалкила, C6-C12-арила и 5-12-членного гетероарила.
[21] В соответствии с другим вариантом осуществления настоящего изобретения, предлагается соединение, представленное Формулой 2 ниже, его стереоизомер, его сольват, его гидрат, или его приемлемая с точки зрения фармацевтики соль:
[22] [Формула 2]
[23] 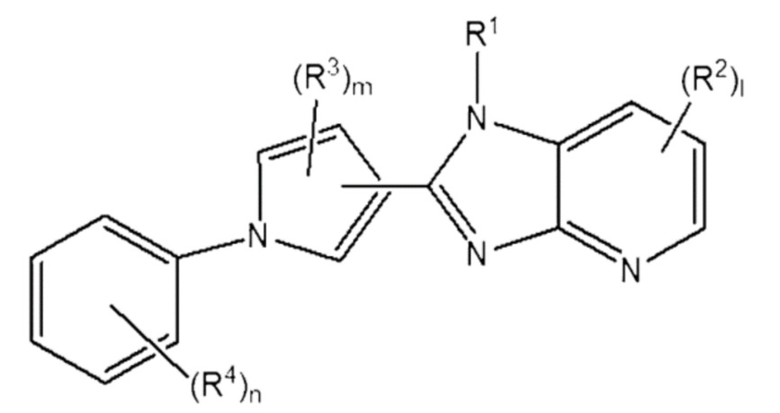
[24] в которой R1 - R3, l и m - те же самые, что определены в Формуле 1 выше, и R4 независимо один от другого выбраны из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкила, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксиалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероалкила, 3-10-членного гетероциклилалкила, C6-C12-арила, и 5-12-членного гетероарила, либо смежные группы могут связываться друг с другом с образованием кольца; «n» - это целое число от 0 до 5, при этом каждый из указанных компонентов: алкил, галоалкил, гидроксиалкил, алкоксиалкил, аминоалкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, гетероциклил, гетероциклилалкил, арил и гетероарил могут замещаться один другим либо несколькими замещающими компонентами, выбранными из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкила, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксиалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероциклилалкила, 3-10-членного гетероциклила, C6-C12-арила, и 5-12-членного гетероарила.
[25] В соответствии с еще одним вариантом осуществления настоящего изобретения, предлагается соединение, представленное Формулой 3 или Формулой 4 ниже, его стереоизомер, его сольват, его гидрат, или его приемлемая с точки зрения фармацевтики соль:
[26] [Формула 3]
[27] 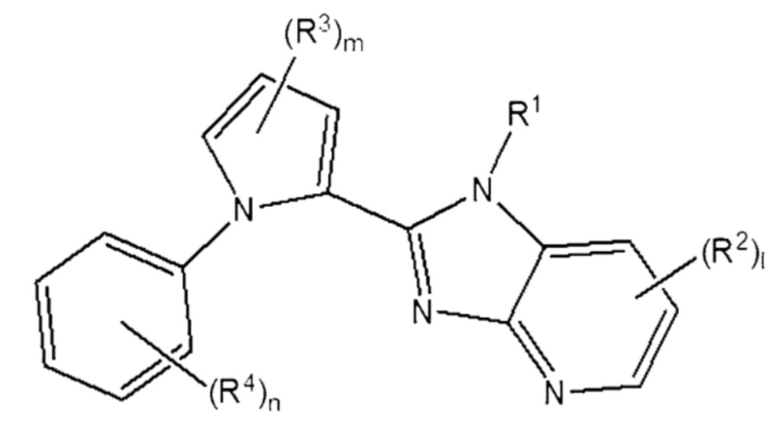
[28] [Формула 4]
[29] 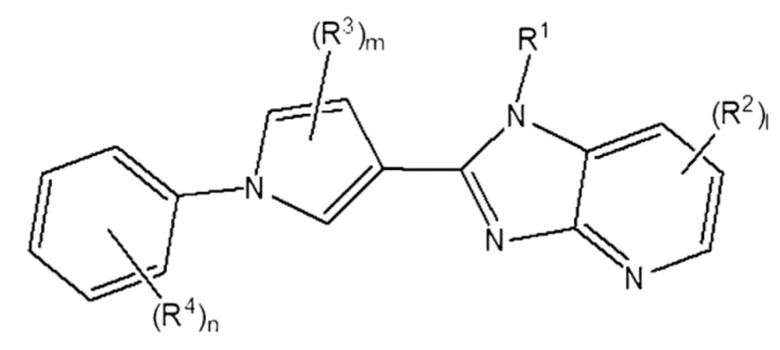
[30] в которой R1 - R4, l, m и n - те же самые, что определены в Формуле 2 выше.
[31] В соответствии с еще одним вариантом осуществления настоящего изобретения, предлагается соединение, представленное Формулой 5 ниже, его стереоизомер, его сольват, его гидрат, или его приемлемая с точки зрения фармацевтики соль:
[32] [Формула 5]
[33] 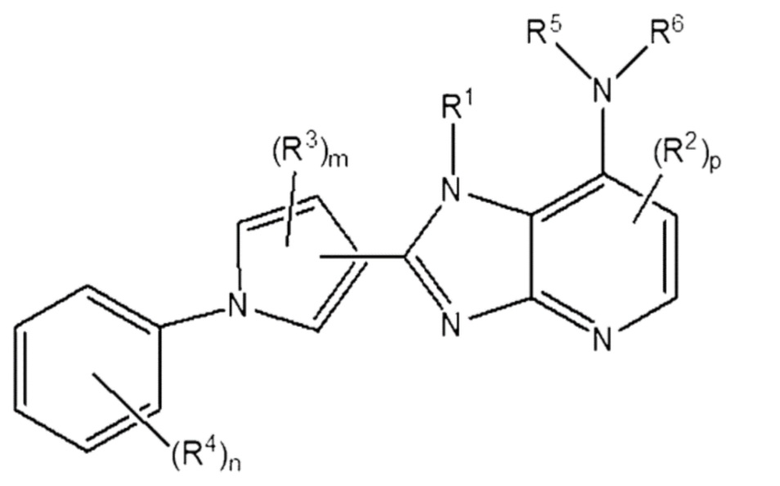
[34] в которой R1 - R4, l, m и n - те же самые, что определены в Формуле 2 выше; p - целое число от 0 до 2; R5 и R6 каждое независимо один от другого выбраны из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, C1-C20 алкила, C1-C6 галоалкила, C1-C6 гидроксиалкила, C1-C6 алкоксилалкила, C1-C6 аминоалкила, C2-C20 алкенила, C2-C20 алкинила, C1-C8 алкокси, C3-C12 циклоалкила, C4-C12 циклоалкилалкила, 3-12-членного гетероциклила, 3-12-членного гетероциклилалкила, C6-C20 арила и 5-20-членного гетероарила, при этом каждый из указанных компонентов: алкил, галоалкил, гидроксилалкил, алкоксилалкил, аминоалкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, гетероциклил, гетероциклилалкил, арил и гетероарил могут замещаться один другим либо несколькими замещающими компонентами, выбранными из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкила, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксилалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероциклила, 3-10-членного гетероциклилалкила, C6-C12 арила и 5-12-членного гетероарила.
[35] Может иметь место соединение, представленное Формулой 6 или Формулой 7 ниже, его стереоизомер, его сольват, его гидрат, или его приемлемая с точки зрения фармацевтики соль:
[36] [Формула 6]
[37] 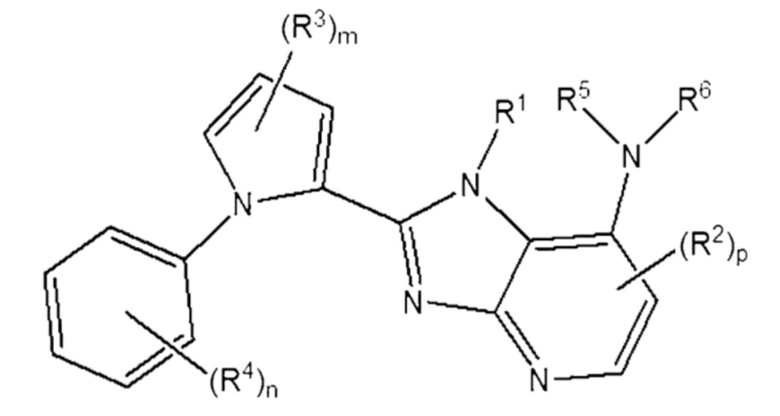
[38] [Формула 7]
[39] 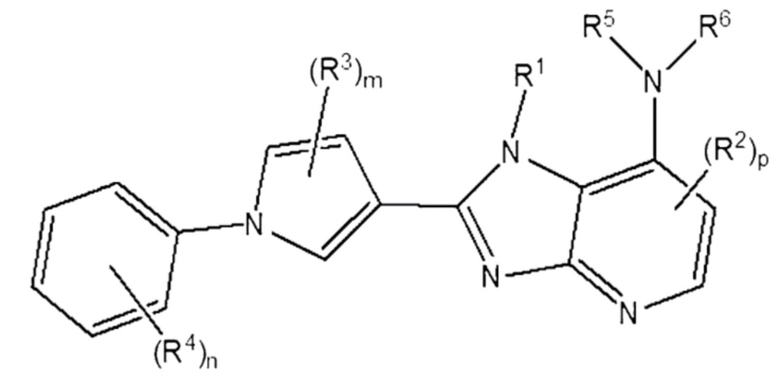
[40] В котором R1 - R6, m, n и p - те же самые, что определены в Формуле 5 выше.
[41] Соединение, представленное Формулой 1, может быть соединением, выбранным из группы, состоящей из следующих соединений, их стереоизомера, их сольвата, их гидрата, или их приемлемой с точки зрения фармацевтики соли:
[42] 1) (S)-6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[43] 2) (S)-6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[44] 3) (S)-6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[45] 4) (S)-6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[46] 5) (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
[47] 6) (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)( морфолино)метанон;
[48] 7) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
[49] 8) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3- метилфенил)метансульфонамид;
[50] 9) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2- метилфенил)метансульфонамид;
[51] 10) (S)-6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[52] 11) (S)-6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[53] 12) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)метансульфонамид;
[54] 13) (S)-6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[55] 14) 6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[56] 15) (S)-6-бромо-2-(1-(3,4-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[57] 16) 6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[58] 17) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-хлоробензолсульфонамид;
[59] 18) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-метилбензолсульфонамид;
[60] 19) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-этилбензолсульфонамид;
[61] 20) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензамид;
[62] 21) (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[63] 22) (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(4-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[64] 23) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[65] 24) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[66] 25) (S)-6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[67] 26) 3-((6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[68] 27) 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[69] 28) 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[70] 29) 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[71] 30) 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[72] 31) 3-((6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[73] 32) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-4-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[74] 33) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[75] 34) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-3-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[76] 35) 3-((6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[77] 36) 3-(3-(6-бромо-7-((3-сульфамилфенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пирролe-1-ил)-4-хлоробензолсульфонамид;
[78] 37) 3-((6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[79] 38) 3-((6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[80] 39) 3-((6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[81] 40) 3-((6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[82] 41) 3-((2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[83] 42) 3-((6-бромо-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[84] 43) 3-((6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[85] 44) 3-(3-(7-(бензо[d][1,3]диоксоль-5-ил-амино)-6-бромо-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[86] 45) 2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(4-(2-метоксиэтокси)фенил)-3H-имидазо[4,5-b]пиридин-7-амин;
[87] 46) 3-(3-(6-бромо-7-((4-(2-метоксиэтокси)фенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[88] 47) 3-((6-бромо-2-(2,5-диметил-1-(пиридин-3-ил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[89] 48) 3-((6-бромо-2-(2,5-диметил-1-(пиридин-4-илметил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[90] 49) (S)-2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[91] 50) N-(3-(3-(7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
[92] 51) N-(3-(3-(6-хлоро-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
[93] 52) (S)-6-хлоро-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[94] 53) (S)-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[95] 54) (S)-(3-(3-(6-хлоро-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
[96] 55) (S)-(3-(3-(7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
[97] 56) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид;
[98] 57) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид;
[99] 58) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота;
[100] 59) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота;
[101] 60) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-((диметиламино)метил)бензамид;
[102] 61) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид;
[103] 62) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)бензамид;
[104] 63) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид;
[105] 64) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(диметиламино)ацетамид;
[106] 65) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[107] 66) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-морфолиноацетамид;
[108] 67) (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон;
[109] 68) (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон;
[110] 69) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид;
[111] 70) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид;
[112] 71) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид;
[113] 72) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид;
[114] 73) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(диметиламино)ацетамид;
[115] 74) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид;
[116] 75) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[117] 76) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[118] 77) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-морфолиноацетамид;
[119] 78) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид;
[120] 79) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропанамид;
[121] 80) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-3-(диметиламино)пропанамид;
[122] 81) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(4-метилпиперазин-1-ил)метанон;
[123] 82) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-2-метилбензамид;
[124] 83) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(морфолино)метанон;
[125] 84) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(диметиламино)ацетамид;
[126] 85) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-морфолиноацетамид;
[127] 86) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропанамид;
[128] 87) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[129] 88) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид;
[130] 89) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[131] 90) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид;
[132] 91) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(морфолино)метанон;
[133] 92) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(4-метилпиперазин-1-ил)метанон;
[134] 93) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид;
[135] 94) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[136] 95) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(4-метилпиперазин-1-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[137] 96) 3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид;
[138] 97) (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(4-метилпиперазин-1-ил)метанон;
[139] 98) (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(морфолино)метанон.
[140] В соответствии с еще одним вариантом осуществления настоящего изобретения, предлагается фармацевтический препарат для профилактики или лечения болезней, выбранных из группы, включающей в себя рак, нейродегенеративное заболевание, неалкогольный стеатогепатит и грипп, в котором указанный фармацевтический препарат представлен Формулой 1, его стереоизомером, его сольватом, его гидратом, или его приемлемой с точки зрения фармацевтики солью в качестве активного ингредиента.
[141] Соединение может замедлять активность протеинкиназы.
[142] Протеинкиназа может быть как минимум одной выбранной из группы, включающей в себя MLK1, MLK2, MLK3, MLK4, DLK, LZK, ZAK и LRRK2.
[143] Рак может быть как минимум одним выбранным из группы, включающей в себя псевдомиксому, внутрипеченочную холангиокарциному, гепатобластому, рак печени, рак щитовидной железы, рак толстой кишки, рак яичек, миелодиспластический синдром, глиобластому, рак полости рта, рак губы, фунгоидный микоз, острую гранулоцитарную лейкемию, острую лимфоцитарную лейкемию, базальноклеточную эпителиому, эпителиальный рак яичников, карциному зародышевых клеток яичника, рак груди у мужчин, рак мозга, аденому гипофиза, миеломную болезнь, рак желчного пузыря, рак желчных протоков, рак толстой кишки, хроническую гранулоцитную лейкемию, хроническую лимфоцитную лейкемию, ретинобластому, хороидальную меланому, диффузную В-крупноклеточную лимфому, рак фатерова соска, рак мочевого пузыря, перитонеальный рак, рак паращитовидных желез, рак надпочечников, рак носовых пазух, немелкоклеточный рак легкого, неходжкинскую лимфому, рак языка, астроцитому, мелкоклеточный рак легкого, детский рак мозга, детскую лимфому, младенческую лейкемию, рак тонкого кишечника, менингиому, рак пищевода, глиому, нейробластому, рак почек, рак сердца, рак двенадцатиперстной кишки, злокачественную опухоль мягких тканей, злокачественный рак костей, злокачественную лимфому, злокачественную мезотелиому, злокачественную меланому, рак глаза, рак вульвы, рак уретры, злокачественную опухоль без выявленного первичного очага, желудочную лимфому, рак желудка, карциноид желудка, желудочно-кишечный стромальный рак, опухоль Вильмса, рак груди, саркому, рак полового члена, фарингальный рак, гестациозное трофобластичное заболевание, рак шейки матки, рак тела матки, саркому матки, рак простаты, рак костей с метастазами, рак мозга с метастазами, рак средостения, рак прямой кишки, карциноидную опухоль прямой кишки, рак вагины, рак позвоночника, невриному слухового нерва, рак поджелудочной железы, рак слюнных желез, саркому Капоши, болезнь Паджета, рак миндалевидной железы, плоскоклеточную карциному, аденокарциному легкого, рак легкого, плоскоклеточную карциному легкого, рак кожи, рак анального канала, рабдомиосаркому, рак гортани, рак плевры и рак вилочковой железы.
[144] Нейродегенеративное заболевание может быть как минимум одним выбранным из группы, включающей в себя болезнь Альцгеймера, синдром Дауна, болезнь Паркинсона, болезнь Лу Герига, деменцию, болезнь Хантингтона, рассеянный склероз, проксимальный латеральный склероз, апоплексию, инсульт и умеренное когнитивное расстройство.
[145] Неалкогольный стеатогепатит может быть как минимум одним выбранным из группы, включающей в себя неалкогольное жировое перерождение печени, неалкогольный стеатогепатит, цирроз и рак печени.
[146] Грипп может быть гриппом A или гриппом B.
Положительные эффекты
[147] Новое соединение производной имидазопиридина и его приемлемая с точки зрения фармацевтики соль в соответствии с настоящим изобретением обладает отличным действием против протеинкиназы. Соответственно, фармацевтический препарат, содержащий его в качестве активного ингредиента, может успешно применяться для профилактики или лечения болезней, связанных с протеинкиназой.
[148] В частности, оно может эффективно применяться для профилактики, лечения или получения положительной динамики при лечении рака, нейродегенеративного заболевания, неалкогольного стеатогепатита или гриппа.
Краткое описание чертежей
[149] ФИГ. 1 - фотография, показывающая результаты эксперимента по замедлению деятельности MLK3 с применением соединения в соответствии с осуществлением настоящего изобретения.
[150] ФИГ. 2 - диаграмма, показывающая результаты замедления активности разрастания раковой клетки сообразно концентрации соединения в соответствии с осуществлением настоящего изобретения.
[151] ФИГ. 3 - фотография, показывающая результаты замедления активности метастаз раковой клетки благодаря соединению в соответствии с осуществлением настоящего изобретения.
[152] ФИГ. 4 - диаграмма, показывающая сравнение результатов оценки аланиновой трансферазы аминопласта для группы животных в рамках экспериментального примера настоящего изобретения.
[153] ФИГ. 5 - диаграмма, показывающая сравнение результатов оценки аспартатаминотрансферазы для группы животных в рамках экспериментального примера настоящего изобретения.
[154] ФИГ. 6 - диаграмма, показывающая сравнение результатов оценки фиброзного участка для группы животных в рамках экспериментального примера настоящего изобретения.
[155] ФИГ. 7 - диаграмма, показывающая результаты замедления фосфорилирования LRRK2 для типового и сравнительного соединений настоящего изобретения.
[156] ФИГ. 8 - диаграмма, показывающая результаты защитного действия против нейронального повреждения для типового и сравнительного соединений настоящего изобретения.
[157] ФИГ. 9 - диаграмма, показывающая сравнение антивирусного воздействия отрицательной контрольной группы и примеров настоящего изобретения.
[158] ФИГ. 10 - диаграмма, показывающая сравнение антивирусного воздействия отрицательной контрольной группы и примеров настоящего изобретения.
[159] ФИГ. 11 - диаграмма, показывающая сравнение антивирусного воздействия отрицательной контрольной группы и примеров настоящего изобретения.
[160] ФИГ. 12 - диаграмма, показывающая сравнение антивирусного воздействия отрицательной контрольной группы и примеров настоящего изобретения.
[161] ФИГ. 13 - диаграмма, показывающая сравнение антивирусного воздействия отрицательной контрольной группы и примеров настоящего изобретения.
[162] ФИГ. 14 - диаграмма, показывающая сравнение антивирусного воздействия отрицательной контрольной группы и примеров настоящего изобретения.
[163] ФИГ. 15 - диаграмма, показывающая изменение веса тела в результате экспериментального применения антивирусного препарата в соответствии с осуществлением настоящего изобретения.
[164] ФИГ. 16 - диаграмма, показывающая коэффициент выживаемости в результате экспериментального применения антивирусного препарата в соответствии с осуществлением настоящего изобретения.
Примеры осуществления изобретения
[165] Настоящее изобретение можно лучше понять, обратившись к следующему детальному описанию предпочтительных осуществлений настоящего изобретения и включенных в них примеров. Следует понимать, что используемая здесь терминология предназначена только для описания конкретных осуществлений и не должна рассматриваться как ограничивающая. Далее, следует понимать, что используемая здесь терминология приводится в традиционном значении, известном в соответствующей области, если особо не оговаривается иное.
[166] В контексте данного документа форма единственного числа включает в себя ссылки на форму множественного числа, если не указывается иное. Например, “одна” замещающая группа включает в себя одну или более замещающую группу.
[167] Описанное здесь настоящее изобретение может адекватным образом использоваться в отсутствие любого элемента (любых элементов), не указанных здесь конкретно. Таким образом, например, в каждом примере данного документа любой из терминов “состоящий”, “состоящий в основном из”, и “состоящий из” может замещаться любым из двух других терминов.
[168] В контексте данного документа термин “гало” или “галоген” означает фтор (F), хлор (Cl), бром (Br) или йод (I), если особо не оговаривается иное.
[169] В контексте данного документа термин “алкил” означает насыщенный одновалентный алифатический углеводородный радикал, включая группы с прямой цепочкой и разветвленной цепочкой, имеющие определенное количество атомов углерода, если не оговаривается иное. Алкиловые группы обычно включают в себя от 1 до 20 атомов углерода (“C1-C20 алкил”), предпочтительно от 1 до 12 атомов углерода (“C1-C12 алкил”), более предпочтительно от 1 до 8 атомов углерода (“C1-C8 алкил”), или от 1 до 6 атомов углерода (“C1-C6 алкил”), или от 1 до 4 атомов углерода (“C1-C4 алкил”). Примеры алкиловых групп включают в себя метил, этил, n-пропил, изопропил, n-бутил, изобутил, третбутил, n-пентил, изопентил, неопентил, n-гексил, n-гептил, n-октил и т.п. Алкиловые группы могут замещаться или не замещаться. В частности, если не оговорено иное, алкиловые группы могут замещаться одной или более галогеновыми группами, до общего количества атомов водорода, присутствующих в алкиловом фрагменте молекулы. Соответственно, C1-C4 алкил включает в себя галогенизированные алкиловые группы и, например, фторированные алкиловые группы, имеющие от 1 до 4 атомов углерода, напр., трифторметил (-CF3) или дифторэтил (-CH2CHF2).
[170] Описанные здесь алкиловые группы, как необязательно замещаемые, могут замещаться одной или более замещающими группами, которые выбираются отдельно друг от друга, если не оговаривается иное. Общее количество замещающих групп может быть равно общему количеству атомов водорода в алкиловом фрагменте молекулы, в той степени, в какой такое замещение целесообразно с точки зрения химии. Как вариант, замещаемые алкиловые группы обычно включают в себя от 1 до 6 необязательных замещающих компонентов, иногда от 1 до 5 необязательных замещающих компонентов, предпочтительно от 1 до 4 необязательных замещающих компонентов, или более предпочтительно от 1 до 3 необязательных замещающих компонентов.
[171] Необязательные замещающие группы, подходящие для алкила, включают в себя, без ограничения, C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, 3-12-членный гетероциклил, C6-C12 арил и 5-12-членный гетероарил, гало, =O (оксо), =S (тионо), =N-CN, =N-ORx, =NR, -CN, -C(O)Rx, -CO2Rx, -C(O)NRxRy, -SRx, -SORx, -SO2Rx, -SO2NRxRy, -NO2, -NRxRy, -NRxC(O)Ry, -NRxC(O)NRxRy, -NRxC(O)ORx, -NRxSO2Ry, -NRxSO2NRxRy, -OR, -OC(O)Rx и -OC(O)NRxRy; где каждое из Rx и Ry является, отдельно друг от друга, водородом (H), C1-C8 алкилом, C1-C8 ацилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, 3-12-членным гетероциклилом, C6-C12 арилом или 5-12-членным гетероарилом, либо Rx и Ry могут оказываться вместе с атомом N, к которому они присоединены, с образованием 3-12-членного гетероциклила или 5-12-членного кольца гетероарила, каждый в качестве варианта включающий в себя 1, 2 или 3 дополнительных гетероатома, выбранных из O, N и S(O)q, где q это 0-2; каждое из Rx and Ry необязательно замещается замещающими компонентами в количестве от 1 до 3, отдельно друг от друга выбираемыми из группы, состоящей из гало, =O, =S, =N-CN, =N-OR′, =NR′, -CN, -C(O)R′, -CO2R′, -C(O)NR′2, -SOR′, -SO2R′, -SO2NR′2, -NO2, -NR′2, -NR′C(O)R′, -NR′C(O)NR′2, -NR′C(O)OR′, -NR′SO2R′, -NR′SO2NR′2, -OR′, -OC(O)R′ и -OC(O)NR′2, где любое R′ отдельно является водородом (H), C1-C8 алкилом, C1-C8 ацилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, 3-12-членным гетероциклилом, C6-C12 арилом, или C5-C12 гетероарилом, и где каждый из упомянутых C1-C8 алкила, C2-C8 алкенила, C2-C8 алкинила, C3-C8 циклоалкила, 3-12-членного гетероциклила, C6-C12 арила и 5-12-членного гетероарила являются необязательно замещаемыми, как будет определено здесь далее.
[172] Необязательно замещаемые алкиловые группы имеют конкретное наименование по замещающей группе.
[173] Например, В контексте данного документа термин “галоалкил” означает алкиловую группу, имеющую определенное количество атомов углерода, которые замещаются одним или более замещающих галогеновых компонентов и обычно включают в себя 1-6 атомов углерода, или предпочтительно 1-4 атома углерода или 1-2 атома углерода и 1, 2 или 3 атома галогена (т.e., “C1-C6 галоалкил”, C1-C4 галоалкил” или C1-C2 галоалкил”), если не оговаривается иное. Например, фторированные алкиловые группы могут иметь конкретное наименование по фторалкиловым группам, напр., C1-C6, C1-C4 или C1-C2 фторалкиловые группы, которые обычно замещаются 1, 2 или 3 атомами фтора. Соответственно, тот или иной C1-C4 фторалкил включает в себя трифторметил (-CF3), дифторметил (-CF2H), фторметил (-CFH2), дифторэтил (-CH2CF2H), и т.п.
[174] В контексте данного документа термин “гидроксиалкил” означает алкиловую группу, имеющую определенное количество атомов углерода, которые замещаются одним или более замещающих гидрокси-компонентов и обычно включают в себя 1-6 атомов углерода, предпочтительно 1-4 атома углерода, и 1, 2 или 3 гидрокси-компонентов (т.e., “C1-C6 гидроксиалкил”), если не оговаривается иное. Соответственно, C1-C6 гидроксиалкил включает в себя гидроксиметил (-CH2OH) и 2-гидроксиэтил (-CH2CH2OH).
[175] В контексте данного документа термин “алкоксиалкил” означает алкиловую группу, имеющую определенное количество атомов углерода, которое замещается одним или более замещающими алкокси-компонентами, если не оговаривается иное. Алкоксиалкиловые группы обычно содержат 1-6 атомов углерода в алкиловой части и замещаются 1, 2 или 3 C1-C4 замещающими алкокси-компонентами. Такие группы иногда описываются в настоящем документе как C1-C4 алкилокси-C1-C6 алкил.
[176] В контексте данного документа термин “аминоалкил” означает алкиловую группу, имеющую определенное количество атомов углерода, которое замещается одним или более замещаемыми или незамещаемыми аминогруппами, такими, как группы, определенные здесь далее, если не оговаривается иное. Аминоалкиловые группы обычно содержат 1-6 атомов углерода в алкиловой части и замещаются 1, 2 или 3 аминовыми замещающими компонентами. Соответственно, тот или иной C1-C6 аминоалкил включает в себя, например, аминометил (-CH2NH2), N,N-диметиламиноэтил (-CH2CH2N(CH3)2), 3-(N-циклопропиламино)пропил (-CH2CH2CH2NH-cPr) и N-пирролидинилэтил (-CH2CH2-N-пирролидинил).
[177] В контексте данного документа термин “алкенил” означает алкиловую группу, как она определяется здесь, состоящую как минимум из двух атомов углерода и как минимум из одной двойной связи «углерод-углерод», если не оговаривается иное. Обычно алкениловые группы имеют от 2 до 20 атомов углерода (“C2-C20 алкенил”), предпочтительно от 2 до 12 атомов углерода (“C2-C12 алкенил”), более предпочтительно от 2 до 8 атомов углерода (“C2-C8 алкенил”), или от 2 до 6 атомов углерода (“C2-C6 алкенил”), или от 2 до 4 атомов углерода (“C2-C4 алкенил”). Соответственно, алкенил включает в себя, например, этенил, 1-пропенил, 2-пропенил, 1-, 2-, или 3-бутенил, и т.п. Алкениловые группы являются незамещаемыми или замещаемыми теми же группами, что описаны здесь как подходящие для алкила.
[178] В контексте данного документа термин “алкинил” означает алкиловую группу, как она определяется здесь, состоящую из как минимум двух атомов углерода как минимум одной тройной связи «углерод-углерод», если не оговаривается иное. Алкиниловые группы имеют от 2 до 20 атомов углерода (“C2-C20 алкинил”), предпочтительно от 2 до 12 атомов углерода (“C2-C12 алкинил”), более предпочтительно от 2 до 8 атомов углерода (“C2-C8 алкинил”), или от 2 до 6 атомов углерода (“C2-C6 алкинил”), или от 2 до 4 атомов углерода (“C2-C4 алкинил”). Представительные примеры включают в себя, без ограничения, этинил, 1-пропинил, 2-пропинил, 1-, 2-, или 3-бутинил, и т.п. Алкиниловые группы являются незамещаемыми или замещаемыми теми же группами, что описаны здесь как подходящие для алкила.
[179] В контексте данного документа термин “алкилен” означает дивалентную гидрокарбиловую группу, имеющую определенное количество атомов углерода, которые могут связывать вместе две другие группы, если не оговаривается иное. Иногда он называется группой -(CH2)n- где n - число от 1 до 8, а предпочтительно n равно 1-4. Где это оговорено, тот ил иной алкилен может также замещаться другими группами и может включать в себя одну или более степеней ненасыщенности (т.e., фрагмент молекулы алкенилена или алкинилена) или кольца. Открытые валентности алкилена не должны быть на противоположных концах цепочки. Соответственно, ответвленные алкиленовые группы, такие как -CH(Me)-, -CH2CH(Me)- и -C(Me)2- также включаются в область термина “алкилены”, так как являются циклическими группами, такими как циклопропан-1,1-диил и ненасыщенными группами, такими как этилен (-CH=CH-) или пропилен (-CH2-CH=CH-). Алкиленовая группа является замещаемой или незамещаемой теми же группами, что описаны здесь как подходящие для алкила.
[180] В контексте данного документа термин “гетероалкилен” означает алкиленовую группу в соответствии с описанным выше, в которой один или более несмежных атомов углерода алкиленовой цепочки замещаются -N(R)-, -O- или -S(O)-, где R это водород (H) или подходящая замещающая группа, а x равно 0-2, если не оговаривается иное. Например, группа -O-(CH2)1-4- это ‘C2-C5’-гетероалкиленовая группа, где один из атомов углерода соответствующего алкилена заменяется на O. Гетероалкиленовая группа является замещаемой или незамещаемой теми же группами, что описаны здесь как подходящие для алкила является замещаемой или незамещаемой теми же группами, что описаны здесь как подходящие для алкила.
[181] В контексте данного документа термин “алкокси” означает -O-алкиловую группу, в которой алкиловая часть имеет определенное количество атомов углерода, если не оговаривается иное. Алкокси-группы обычно включают в себя от 1 до 8 атомов углерода (“C1-C8 алкокси”), или от 1 до 6 атомов углерода (“C1-C6 алкокси”), или от 1 до 4 атомов углерода (“C1-C4 алкокси”). Например, C1-C4 алкокси включает в себя метокси (-OCH3), этокси (-OCH2CH3), изопропокси (-OCH(CH3)2), трет-бутилoкси (-OC(CH3)3), и т.п. Алкокси-группы являются замещаемыми или незамещаемыми в алкиловой части теми же группами, что описаны здесь как подходящие для алкила. В частности, алкокси-группы могут необязательно замещаться одним или более атомами галогена, в частности, одним или более атомами фтора, до общего количества атомов водорода, присутствующих в алкиловой части. Такие группы называются “галоалкокси” (например, в случае фторирования - более конкретно как “фторалкокси”) группами, имеющими определенное количество атомов углерода и замещаемыми одним или более замещающими галогеновыми компонентами. Обычно такие группы содержат от 1до 6 атомов углерода, предпочтительно 1-4 атома углерода, иногда 1-2 атома углерода, и 1, 2 или 3 атома галогена (т.e., “C1-C6 галококси”, “C1-C4 галококси” или “C1-C2 галококси”). Более конкретно, фторированные алкиловые группы могут называться фторалкокси-группами, напр., C1-C6, C1-C4 или C1-C2 фторалкокси-группы, которые обычно замещаются 1, 2 или 3 атомами фтора. Соответственно, C1-C4 фторалкокси включает в себя трифторметилoкси (-OCF3), дифторметилoкси (-OCF2H), фторметилoкси (-OCFH2), дифторэтилoкси (-OCH2CF2H), и т.п.
[182] В контексте данного документа термин “тиоалкокси” означает одновалентную -S-алкиловую группу, в которой алкиловая часть имеет определенное количество атомов углерода, и необязательно замещается в алкиловой части теми же группами, которые описаны здесь как подходящие для алкила, если не оговаривается иное. Например, C1-C4 тиоалкокси включает в себя -SCH3 и -SCH2CH3.
[183] В контексте данного документа термин “циклоалкил” означает неароматическую, насыщенную или частично насыщенную карбоциклическую кольцевую систему, содержащую определенное количество атомов углерода, которые могут быть спироциклическими, соединенными мостиковой связью или конденсированными бициклическими или полициклическими кольцевыми системами, соединенными с основном молекулой через атом углерода циклоалкилового кольца, если не оговаривается иное. Обычно циклоалкиловые группы настоящего изобретения содержат от 3 до 12 атомов углерода (“C3-C12 циклоалкил”), предпочтительно от 3 до 8 атомов углерода (“C3-C8 циклоалкил”). Представительные примеры включают в себя, напр., циклопропан, циклобутан, циклопентан, циклопентен, циклогексан, циклогексен, циклогексадиен, циклогептан, циклогептатриен, адамантан, и т.п. Циклоалкиловые группы являются замещаемыми или незамещаемыми теми же группами, что описаны здесь как подходящие для алкила.
[184] В контексте данного документа термин “циклоалкилалкил” используется для описания циклоалкилового кольца, обычно C3-C8 циклоалкила, который соединен с основной молекулой алкиленовым линкером, обычно C1-C4 алкиленом. Иногда циклоалкилалкиловые группы описываются по общему количеству атомов углерода в карбоциклическом кольце и линкере, и обычно содержат от 4 до 12 атомов углерода (“C4-C12 циклоалкилалкил”), если не оговаривается иное. Соответственно, циклопропилметиловая группа - это C4-циклоалкилалкиловая группа, a циклогексилэтиловая группа - это C8-циклоалкилалкил. Циклоалкилалкиловые группы являются замещаемыми или незамещаемыми в циклоалкиловой и/или алкиленовой частях тех же групп, что описаны здесь как подходящие для алкиловых групп. Иногда циклоалкилалкиловые группы описываются здесь как -L-C3-C8-циклоалкил, где циклоалкиловая группа имеет указанное количество атомов углерода, а -L- означает алкиленовый линкер. Следует понимать, что когда -L- является химической связью, группа является циклоалкилом.
[185] В контексте данного документа термины “гетероциклил”, “гетероциклический” or “гетероалициклический” применяются как взаимозаменяемые и означают неароматическую, насыщенную либо частично ненасыщенную кольцевую систему, содержащую определенное количество атомных колец, включая как минимум один гетероатом, выбранный из N, O и S в качестве образующего кольцо атома, где кольцо из атомов S необязательно замещается одной или двумя оксо-группами (т.e., S(O), где x - это 0, 1 или 2) и где гетероциклическое кольцо связано с основной молекулой через атом кольца, который может быть C или N, если не оговаривается иное. Гетероциклические кольца включают в себя кольца, которые являются спироциклическими, соединенными мостиковой связью или конденсированными в одно или более других гетероциклических или карбоциклических колец, где спироциклические, соединенные мостиковой связью или конденсированные кольца могут насыщаться сами, быть частично насыщенными или ароматическими в той степени, в какой ненасыщенность или ароматичность является химически целесообразной, при условии, что точка присоединения к основной молекуле является атомом гетероциклической части системы кольца. Предпочтительно, гетероциклические кольца содержат от 1 до 4 гетероатомов, выбранных из N, O, и S(O)q в качестве членов кольца, и более предпочтительно от 1 до 2 гетероатомов кольца, при условии, что такие гетероциклические кольца не содержат два смежных атома кислорода. Гетероциклиловые группы являются незамещаемыми или замещаемыми подходящими замещающими группами, например, теми же группами, которые описаны здесь как подходящие для алкила, арила или гетероарила. Такие замещающие группы могут присутствовать в гетероциклическом кольце, присоединенном к основной молекуле, либо в присоединенном к ней спироциклическом, соединенном мостиковой связью или конденсированном кольце. Кроме того, атомы N кольца могут в необязательном порядке замещаться группами, подходящими для того или иного амина, напр., заместителей алкила, aцила, карбамила, сульфонила и т.п.
[186] Гетероциклы обычно включают в себя 3-12-членные гетероциклиловые группы, предпочтительно 3-10-членные гетероциклиловые группы, и более предпочтительно 5-6-членные гетероциклиловые группы, в соответствии с определенным здесь.
[187] В разных вариантах осуществления гетероциклические группы содержат 3-12 кольцевых членов, включая гетероатомы углерода и элементов, не являющихся углеродом, и предпочтительно 4-7 кольцевых членов. В отдельных предпочтительных вариантах осуществления замещающие группы, состоящие из 3-12-членных гетероциклов, выбираются из колец азетидинила, пирролидинила, пиперидинила, пиперазинилила, азепанила, диазепанила, тетрагидрофуранила, тетрагидропиранила, тетрагидротиофенила, тетранидротиопиранила, морфолинила и тиоморфолинила, каждое из которых может необязательно замещаться, как описано в отношении конкретной замещающей группы, в той степени, в какой это целесообразно с химической точки зрения.
[188] Здесь понимается, что не более чем два атома N, O или S обычно связаны последовательно, кроме случаев, когда оксо-группа присоединена к N или S с образованием нитро или сульфониловой группы, или в случае отдельных гетероароматических колец, например, триазина, триазола, тетразола, оксадиазола, тиадиазола, и т.п.
[189] В контексте данного документа термин “гетероциклилалкил” может использоваться для описания гетероциклической группы определенного размера, которая соединена с основной молекулой алкиленовым линкером определенной длины, если не оговаривается иное. Обычно такие группы содержат необязательно замещаемый 3-12-членный гетероцикл, соединенный с основной молекулой посредством C1-C4 алкиленового линкера. Где указано, такие группы необязательно замещаются в алкиленовой части теми же группами, которые описываются здесь как подходящие для алкиловой группы, а в гетероциклической части - группами, которые описываются как подходящие для гетероциклических колец. Иногда гетероциклилалкиловые группы описываются здесь как -L-гетероциклилалкил, где гетероциклилалкиловая группа имеет указанное число атомов кольца, a -L- означает алкиленовый линкер. Следует понимать, что когда -L- является химической связью, группа является гетероциклилом.
[190] В контексте данного документа термин “арил” или “ароматический” означает необязательно замещаемую моноциклическую или конденсированную бициклическую или полициклическую кольцевую систему, имеющую хорошо известные характеристики ароматичности, в которой как минимум одно кольцо содержит полностью сопряженную пи-электронную систему, если не оговаривается иное. Обычно ариловые группы содержат от 6 до 20 атомов углерода (“C5-C20 арил”) в качестве членов кольца, предпочтительно от 6 до 14 атомов углерода (“C6-C14 арил”) или более предпочтительно, от 6 до 12 атомов углерода (“C6-C12 арил”). Конденсированные ариловые группы могут включать в себя ариловое кольцо (напр., фениловое кольцо), которые конденсируются с другим ариловым или гетероариловым кольцом, либо конденсируются с насыщенным или частично ненасыщенным карбоциклическим или гетероциклическим кольцом, при условии, что точка присоединения к основной молекуле в таких конденсированных кольцевых системах является атомом ароматической части кольцевой системы. Например, ариловые группы включают в себя фенил, бифенил, нафтил, антраценил, фенантренил, инданил, инденил и тетрогидронафтил. Ариловая группа является незамещаемой или замещаемой, как описывается здесь в дальнейшем.
[191] В контексте данного документа термин “гетероарил” или “гетероароматический” означает моноциклические или конденсированные бициклические или полициклические кольцевые системы, имеющие хорошо известные характеристики ароматичности, которые содержат определенное количество атомов кольца и включают в себя как минимум один гетероатом, выбранный из N, O и S в качестве члена кольца в ароматическом кольце, если не оговаривается иное. Включение гетероатома обеспечивает ароматичность в 5-членных кольцах, а также в 6-членных кольцах. Обычно гетероариловые группы содержат от 5 до 20 атомов кольца (“5-20-членный гетероарил”), предпочтительно от 5 до 14 атомов кольца (“5-14-членный гетероарил”), и более предпочтительно от 5 до 12 атомов кольца (“5-12-членный гетероарил”). Гетероариловые кольца соединяются с основной молекулой посредством атома кольца гетероароматического кольца, с сохранением ароматичности. Соответственно, 6-членные гетероариловые кольца могут прикрепляться к основной молекуле посредством атома кольца C, в то время как 5-членные гетероариловые кольца могут прикрепляться к основной молекуле посредством атома кольца C или N. Гетероариловые группы могут также конденсироваться с другим ариловым или гетероариловым кольцом, либо конденсироваться с насыщенным или частично ненасыщенным карбоциклическим или гетероциклическим кольцом, при условии, что точка присоединения к основной молекуле в таких конденсированных кольцевых системах является атомом гетероароматической части кольцевой системы. Примеры незамещаемой гетероариловой группы включают в себя пиррол, фуран, тиофен, пиразол, имидазол, изоксазол, оксазол, изотиазол, тиазол, триазол, оксадиазол, тиадиазол, тетразол, пиридин, пиридазин, пиримидин, пиразин, бензофуран, бензотиофен, индол, бензимидазол, инедазол, хинолин, изохинолин, пурин, триазин, нафтиридин и карбазол. В разных вариантах осуществления 5- или 6-членные гетероариловые группы выбираются из группы, включающей в себя кольца пирролила, фуранила, тиофенила, пиразолила, имидазолила, изоксазолила, оксазолила, изотиазолила, тиазолила, триазолила, пиридинила и пиримидинила, пиразинила или пиридазинила. Гетероариловая группа является незамещаемой или замещаемой, как описывается здесь в дальнейшем.
[192] Фрагменты молекул арила, гетероарила и гетероциклила, описанные здесь как необязательно замещаемые, могут замещаться одной или более замещающими группами, которые выбираются отдельно друг от друга, если не оговорено иное. Общее количество замещающих групп может быть равно общему количеству атомов фрагментов молекул арила, гетероарила или гетероциклила, в той степени, в какой такое замещение химически целесообразно, при этом ароматичность сохраняется в случае ариловых и гетероариловых колец. Необязательно замещаемые ариловая, гетероариловая или гетероциклиловая группы обычно содержат от 1 до 5 необязательных замещающих групп, иногда от 1 до 4 необязательных замещающих групп, предпочтительно от 1 до 3 необязательных замещающих групп или более, предпочтительно от 1 до 2 необязательных замещающих групп.
[193] Необязательные замещающие группы, подходящие для колец арила, гетероарила и гетероциклила включают в себя, без ограничения, C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, 3-12-членный гетероциклил, C6-C12 арил и 5-12-членный гетероарил; и гало, =O (йод), =S (тионо), =N-CN, =N-ORx, =NRx, -CN, -C(O)Rx, -CO2Rx, -C(O)NRxRy, -SRx, -SORx, -SO2Rx, -SO2NRxRy, -NO2, -NRxRy, -NRxC(O)Ry, -NRxC(O)NRxRy, -NRxC(O)ORx, -NRxSO2Ry, -NRxSO2NRxRy, -ORx, -OC(O)Rx и -OC(O)NRxRy; где каждое из Rx и Ry являются отдельно водородом (H), C1-C8 алкилом, C1-C8 aцилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, 3-12-членным гетероциклилом, C6-C12 арилом, или 5-12-членным гетероарилом, или Rx и Ry могут браться вместе с атомом N, с которым они соединяются с образованием 3-12-членного гетероциклила или 5-12-членного гетероарила, каждый необязательно содержит 1, 2 или 3 дополнительных гетероатома, выбранных из O, N и S(O)q, где q равно от 0 до 2; каждое из Rx и Ry необязательно замещаются 1 - 3 замещающими группами, выбранными из группы, включающей в себя гало, =O, =S, =N-CN, =N-OR′, =NR′, -CN, -C(O)R′, -CO2R′, -C(O)NR′2, -SR′, -SOR′, -SO2R′, -SO2NR′2, -NO2, -NR′2, -NR′C(O)R′, -NR′C(O)NR′2, -NR′C(O)OR′, -NR′SO2R′, -NR′SO2NR′2, -OR′, -OC(O)R′ и -OC(O)NR′2, где каждое из R′ является отдельно (H), C1-C8 алкилом, C1-C8 aцилом, C2-C8 алкенилом, C2-C8 алкинилом, C3-C8 циклоалкилом, 3-12-членным гетероциклилом, C6-C12 арилом, или 5-12-членным гетероарилом; и каждый из упомянутых: C1-C8 алкил, C2-C8 алкенил, C2-C8 алкинил, C3-C8 циклоалкил, 3-12-членный гетероциклил, C6-C12 арил и 5-12-членный гетероарил является необязательно замещаемым, как определяется здесь в дальнейшем.
[194] В контексте данного документа термин “арилалкиловая” группа означает ариловую группу, в соответствии с описанным здесь, которая соединена с основной молекулой посредством алкиленового или аналогичного линкера. Арилалкиловые группы описываются по общему количеству атомов углерода в кольце и линкере. Соответственно, бензиловая группа - это C7-арилалкиловая группа, a фенилэтил - это C8-арилалкил. Обычно арилалкиловые группы содержат 7-16 атомов углерода (“C7-C16 арилалкил”), где ариловая часть содержит 6-12 атомов углерода и алкиленовая часть содержит 1-4 атома углерода. Такие группы могут быть также представлены как -C1-C4 алкилен-C6-C12 арил.
[195] В контексте данного документа термин “гетероарилалкил” означает гетероариловую группу, в соответствии с описанным выше, которая соединена с основной молекулой посредством алкиленового линкера и отличается от “арилалкила” тем, что как минимум одно кольцо атомов ароматического фрагмента молекулы - это гетероатом, выбранный из N, O и S. Гетероарилалкиловые группы иногда описываются здесь по общему количеству атомов, не являющихся атомами водорода (т.e., атомов C, N, S и O) совместно в кольце и линкере, исключая замещающие группы. Соответственно, например, пиридинилметил здесь может называться как “C7”-гетероарилалкил. Обычно незамещаемые гетероарилалкиловые группы содержат от 6 до 20 неводородных атомов (включая атомы C, N, S и O), в которых гетероариловая часть обычно содержит от 5 до 12 атомов, а алкиленовая часть обычно содержит от 1 до 4 атомов углерода. Такие группы могут также представляться как -C1-C4 алкилен-5-12-членный гетероарил. Иногда гетероарилалкиловые группы описываются здесь как -L- гетероарилалкил, где гетероарилалкиловая группа имеет указанное количество атомов кольца, а -L- означает алкиленовый линкер. Следует понимать, что когда -L- является химической связью, группа является гетероарилом.
[196] В контексте данного документа термины “арилалкокси” и “гетероарилалкокси” означают ариловую и гетероариловую группы, которая соединена с основной молекулой посредством гетероалкиленового линкера (т.e., -O-алкилен-), где группы описываются по общему количеству неводородных атомов (т.e., атомов C, N, S и O) совместно в кольце и линкере, если не оговаривается иное. Соответственно, -O-CH2-фениловая и -O-CH2-пиридиниловая группы будут называться C8-арилалкокси- и C8-гетероарилалкокси- группы, соответственно.
[197] В случаях, когда арилалкил, арилалкокси, гетероарилалкил или гетероарилалкокси описываются как необязательно замещаемые, замещающие группы могут быть либо в бивалентной части линкера, либо в ариловой или гетероариловой части группы. Замещающие группы, необязательно присутствующие в алкиленовой или гетероалкиленовой части, являются теми же, что описаны выше для алкиловой или алкокси группы в целом, в то время как замещающие группы, необязательно присутствующие в ариловой или гетероариловой части, являются теми же, что описаны выше ариловой или гетероариловой группы в целом.
[198] В контексте данного документа термин “гидрокси” означает -OH группу, если не оговаривается иное.
[199] В контексте данного документа термин “aцилокси” означает одновалентную группу -OC(O)алкил, где алкиловая часть имеет определенное количество атомов углерода (обычно C1-C8, предпочтительно C1-C6 или C1-C4), которые необязательно замещаются группами, подходящими для алкила, если не оговаривается иное. Соответственно, C1-C4 aцилокси включает в себя -OC(O)C1-C4 алкил замещающую группу, напр., -OC(O)CH3.
[200] В контексте данного документа термин “aцил” означает одновалентную группу -C(O)алкил, где алкиловая часть имеет определенное количество атомов углерода (обычно C1-C8, предпочтительно C1-C8 или C1-C4) и может необязательно замещаться группами, подходящими для алкила, напр., F, OH или алкокси, если не оговаривается иное. Соответственно, необязательно замещаемый -C(O)C1-C4 алкил включает в себя незамещаемые aциловые группы, такие как -C(O)CH3 (т.e., ацетил) и -C(O)CH2CH3 (т.e., пропионил), а также замещаемые aциловые группы, такие как -C(O)CF3 (трифторaцетил), -C(O)CH2OH (гидроксилацетил), -C(O)CH2OCH3 (метоксиацетил), -C(O)CF2H (дифторацетил), и т.п.
[201] В контексте данного документа термин “ациламино” означает одновалентную группу, -NHC(O)алкил или -NRC(O)алкил, где алкиловая часть имеет определенное количество атомов углерода (обычно C1-C8, предпочтительно C1-C6 or C1-C4 и является необязательно замещаемой группами, подходящими для алкила, если не оговаривается иное. Соответственно, C1-C4 aциламино включает в себя -NHC(O)C1-C4 алкиловую замещающую группу, напр., -NHC(O)CH3.
[202] В контексте данного документа термин “арилокси” или “гетероарилокси” означает необязательно замещаемые -O-арил или -O-гетероарил, где в каждом случае арил и гетероарил являются теми, как определяется здесь далее, если не оговаривается иное.
[203] В контексте данного документа термин “ариламино” или “гетероариламино” означают необязательно замещаемые -NH-арил, -NR-арил, -NH-гетероарил или -NR-гетероарил, где в каждом случае арил и гетероарил являются теми, как определяется здесь далее, а R означает замещающую группу, подходящую для того или иного амина, напр., алкиловую, aциловую, карбамoиловую или сульфониловую группу, или т.п., если не оговаривается иное.
[204] В контексте данного документа термин “циано” означает -C≡N группу, если не оговаривается иное.
[205] В контексте данного документа термин “незамещаемая амино” означает группу -NH2, если не оговаривается иное. В случае если амино описывается как замещаемая или необязательно замещаемая, термин включает в себя группы формы -NRxRy, где каждое из Rx и Ry является отдельно водородом (H), алкилом, алкенилом, алкинилом, циклоалкилом, гетероциклилом, aцилом, тиоaцилом, арилом, гетероарилом, циклоалкилалкилом, арилалкилом или гетероарилалкилом, в каждом случае имеющее определенное количество атомов и являющееся необязательно замещаемым, как описано здесь. Например, “алкиламино” означает группу -NRxRy, в которой одно из Rx и Ry является алкиловым фрагментом молекулы, другое H, а “диалкиламино” означает -NRxRy, где и Rx и Ry являются алкиловыми фрагментами молекулы, где алкиловые фрагменты молекул имеют определенное количество атомов углерода (напр., -NH-C1-C4 алкил или -N(C1-C4 алкил)2). Обычно алкиловые замещающие формы в аминах содержат от 1 до 8 атомов углерода, предпочтительно от 1 до 6 атомов углерода, или более предпочтительно от 1 до 4 атомов углерода. Этот термин включает в себя также формы, где Rx и Ry берутся вместе с атомом N, с которым они соединяются с образованием 3-12-членного гетероциклила или 5-12-членного гетероарилового кольца, каждый из которых может сам по себе быть необязательно замещаемым, в соответствии с описанным здесь для гетероциклилового или гетероарилового колец, и которые могут включать в себя от 1 до 3 дополнительных гетероатомов, выбранных из N, O и S(O)x, где x - это 0-2 членов кольца, при условии, что такие кольца не включают в себя два смежных атома кислорода.
[206] В контексте данного документа термин “необязательный” или “необязательно” означает, что далее описываемое событие или обстоятельство может, но не обязательно должно случаться, и описание включает в себя примеры, когда событие или обстоятельство происходит и примеры, когда оно не происходит.
[207] В контексте данного документа термины “необязательно замещаемые” и “замещаемые или незамещаемые” используются как взаимозаменяемые для указания того, что та или иная конкретная описываемая группа может не иметь неводородных замещаемых групп (т.e., быть не замещаемыми), либо группа может иметь одну или более неводородную замещающую группу (т.e., быть замещаемыми). Если не указывается иное, общее количество замещающих групп, которые могут присутствовать, равно количеству атомов H, присутствующих в незаменяемой форме описываемой группы. Если необязательная замещающая группа соединяется посредством двойной связи, пример, с помощью оксо (=O) замещающей группы, эта группа занимает две имеющиеся валентности, и общее количество других замещающих групп, которые сюда включены, уменьшается на две. В случае, когда необязательные замещающие группы выбираются отдельно от перечня альтернатив, выбранные группы будут теми же самыми или отличными. В рамках всего изобретения следует понимать, что количество и характер необязательной замещающей группы будут ограничиваться в той степени, в какой это будет химически целесообразно для таких замещающих групп.
[208]
[209] Осуществление настоящего изобретения позволяет получить соединение, представленное Формулой 1 ниже, или его приемлемую с точки зрения фармацевтики соль:
[210] [Формула 1]
[211] 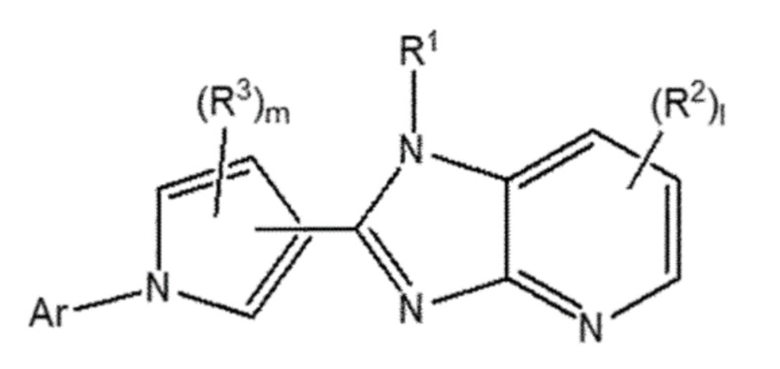
[212] в которой:
[213] Ar - это C6-C20 арил или 5-20-членный гетероарил;
[214] Каждое из R1, R2 и R3, независимо друг от друга, выбираются из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C20 алкила, C1-C6 галоалкила, C1-C6 гидроксиалкила, C1-C6 алкоксиалкила, C1-C6 аминоалкила, C2-C20 алкенила, C2-C20 алкинила, C1-C8 алкокси, C3-C12 циклоалкила, C4-C12 циклоалкилалкила, 3-12-членного гетероциклила, 3-12-членного гетероциклилалкила, C6-C20 арила, и 5-20-членного гетероарила;
[215] Каждое из Ra, Rb и Rc, независимо друг от друга, выбираются из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, C1-C20 алкила, C1-C6 галоалкила, C1-C6 гидроксиалкила, C1-C6 алкоксиалкила, C1-C6 аминоалкила, C2-C20 алкенила, C2-C20 алкинила, C1-C8 алкокси, C3-C12 циклоалкила, C4-C12 циклоалкилалкила, 3-12-членного гетероциклила, 3-12-членного гетероциклилалкила, C6-C20 арил, и 5-20-членного гетероарила;
[216] l является целым числом от 0 до 3; m является целым числом от 0 до 3,
[217] в которой каждое из следующего: алкил, галоалкил, гидроксиалкил, алкоксиалкил, аминоалкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, гетероциклил, гетероциклилалкил, арил и гетероарил могут замещаться одной или более замещающей группой, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкила, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксиалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероциклила, 3-10-членного гетероциклилалкила, C6-C12 арила, и 5-12-членного гетероарила.
[218] В частности, соединение, представленное Формулой 1 выше, может быть представлено Формулой 2 ниже.
[219] [Формула 2]
[220] 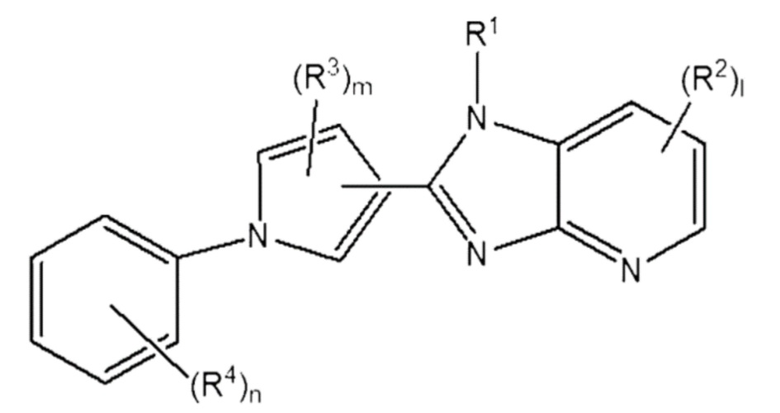
[221] в которой,
[222] R1 - R3, l и m - те же, что определены в Формуле 1 выше;
[223] R4 независимо одно от другого выбрано из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкила, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксиалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероциклила, 3-10-членного гетероциклилалкила, C6-C12 арила, и 5-12-членного гетероарила, либо смежные группы могут связываться друг с другом с образованием кольца; и
[224] n является целым числом от 0 до 5,
[225] в которой каждое из следующего: алкил, галоалкил, гидроксиалкил, алкоксиалкил, аминоалкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, гетероциклил, гетероциклилалкил, арил и гетероарил могут далее замещаться одной или более замещающей группой, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкила, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксиалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероциклила, 3-10-членного гетероциклилалкила, C6-C12 арила, и 5-12-членного гетероарила.
[226] Кроме того, в частности, соединение, представленное Формулой 2 выше, может быть представлено Формулой 3 или 4 ниже.
[227] [Формула 3]
[228] 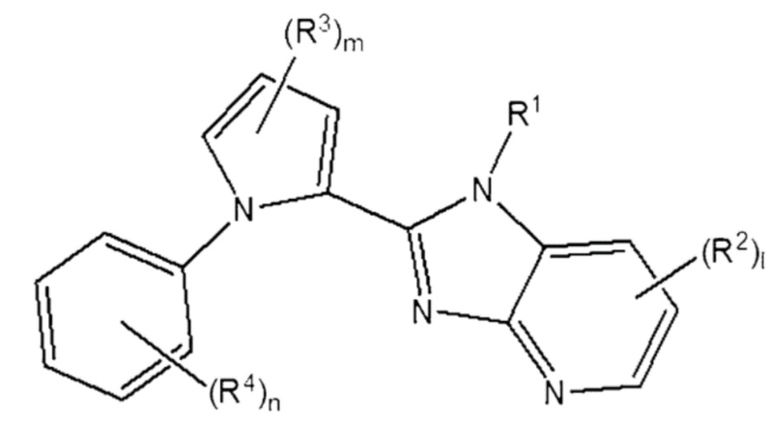
[229] [Формула 4]
[230] 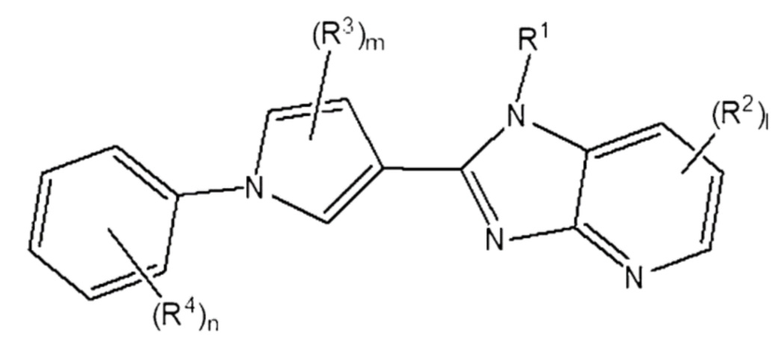
[231] в которой,
[232] R1 - R4, l и m - те же, что определены в Формуле 2 выше.
[233] Кроме того, в частности, соединение, представленное Формулой 2 выше, может быть представлено Формулой 5 ниже.
[234] [Формула 5]
[235] 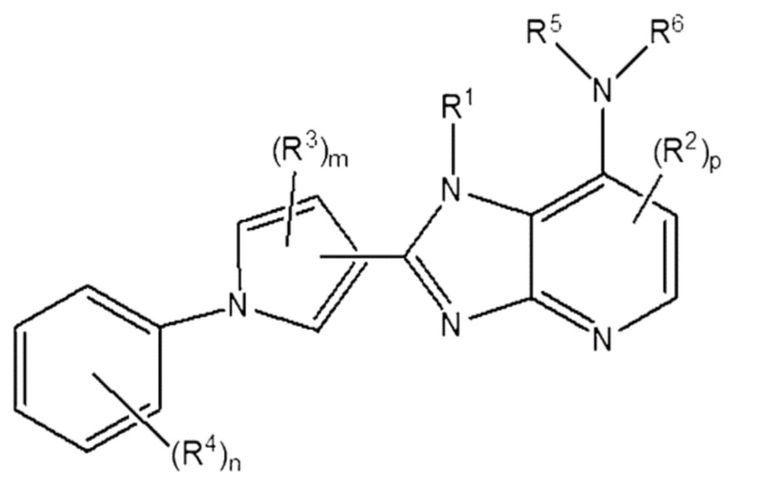
[236] в которой,
[237] R1 - R4, l, m и n - те же, что определены в Формуле 2 выше;
[238] p является целым числом от 0 до 2; и
[239] Каждое из R5 и R6, независимо друг от друга, выбирается из группы, состоящей из водорода, галогена, гидрокси, циано, нитро, C1-C20 алкила, C1-C6 галоалкила, C1-C6 гидроксиалкила, C1-C6 алкоксиалкила, C1-C6 аминоалкила, C2-C20 алкенила, C2-C20 алкинила, C1-C8 алкокси, C3-C12 циклоалкила, C4-C12 циклоалкилалкила, 3-12-членного гетероциклила, 3-12-членного гетероциклилалкила, C6-C20 арила и 5-20- членного гетероарила,
[240] в которой каждое из следующего: алкил, галоалкил, гидроксиалкил, алкоксиалкил, аминоалкил, алкенил, алкинил, алкокси, циклоалкил, циклоалкилалкил, гетероциклил, гетероциклилалкил, арил и гетероарил могут замещаться одной или более замещающей группой, состоящей из водорода, галогена, гидрокси, циано, нитро, -SRa, -S(=O)Ra, -S(=O)2Ra, -NRbRc, -CO2Rb, -CO-NRbRc, C1-C10 алкила, C1-C4 галоалкила, C1-C4 гидроксиалкила, C1-C4 алкоксиалкила, C1-C4 аминоалкила, C2-C10 алкенила, C2-C10 алкинила, C1-C4 алкокси, C3-C10 циклоалкила, C4-C10 циклоалкилалкила, 3-10-членного гетероциклила, 3-10-членного гетероциклилалкила, C6-C12 арила и 5-12-членного гетероарила.
[241] Кроме того, в частности, соединение, представленное Формулой 5 выше может быть представлено Формулой 6 или 7 ниже.
[242] [Формула 6]
[243] 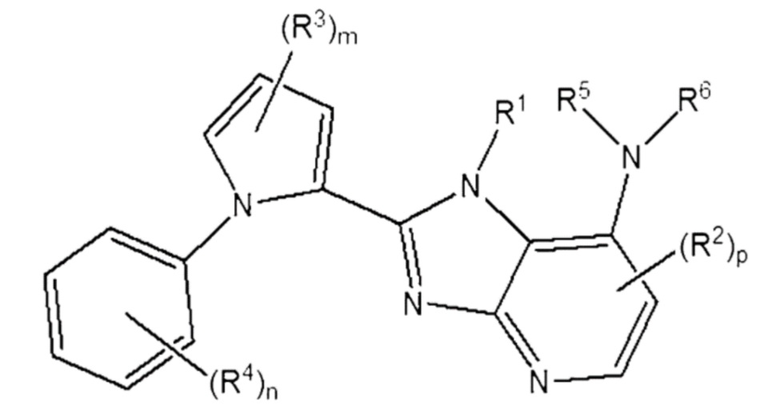
[244] [Формула 7]
[245] 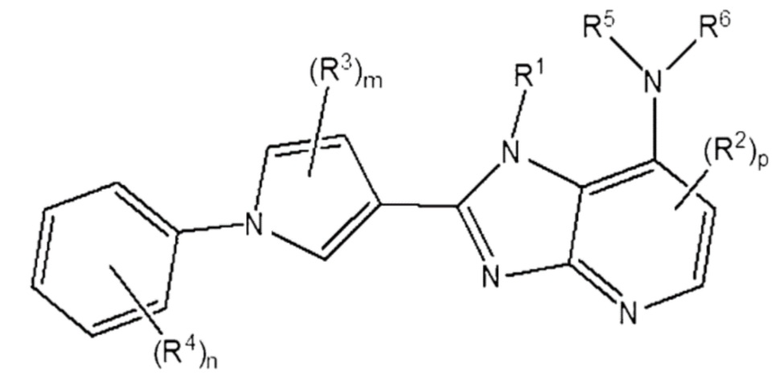
[246] в которой,
[247] R1 - R6, m, n и p - те же, что определены в Формуле 5 выше.
[248] Кроме того, в частности, соединение, представленное Формулой 1, может быть соединением, выбранным из группы, состоящей из следующих соединений, не ограничивающихся перечисленным.
[249] 1) (S)-6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[250] 2) (S)-6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[251] 3) (S)-6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[252] 4) (S)-6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[253] 5) (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
[254] 6) (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
[255] 7) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
[256] 8) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)метансульфонамид;
[257] 9) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)метансульфонамид;
[258] 10) (S)-6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[259] 11) (S)-6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[260] 12) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)метансульфонамид;
[261] 13) (S)-6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[262] 14) 6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[263] 15) (S)-6-бромо-2-(1-(3,4-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[264] 16) 6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[265] 17) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-хлоробензолсульфонамид;
[266] 18) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-метилбензолсульфонамид;
[267] 19) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-этилбензолсульфонамид;
[268] 20) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензамид;
[269] 21) (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[270] 22) (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(4-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[271] 23) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[272] 24) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[273] 25) (S)-6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[274] 26) 3-((6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[275] 27) 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[276] 28) 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[277] 29) 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[278] 30) 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[279] 31) 3-((6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[280] 32) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-4-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[281] 33) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[282] 34) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-3-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[283] 35) 3-((6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[284] 36) 3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пирролe-1-ил)-4-хлоробензолсульфонамид;
[285] 37) 3-((6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[286] 38) 3-((6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[287] 39) 3-((6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[288] 40) 3-((6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[289] 41) 3-((2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[290] 42) 3-((6-бромо-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[291] 43) 3-((6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[292] 44) 3-(3-(7-(бензо[d][1,3]диоксоль-5-ил-амино)-6-бромо-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[293] 45) 2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(4-(2-метоксиэтокси)фенил)-3H-имидазо[4,5-b]пиридин-7-амин;
[294] 46) 3-(3-(6-бромо-7-((4-(2-метоксиэтокси)фенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
[295] 47) 3-((6-бромо-2-(2,5-диметил-1-(пиридин-3-ил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[296] 48) 3-((6-бромо-2-(2,5-диметил-1-(пиридин-4-илметил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[297] 49) (S)-2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
[298] 50) N-(3-(3-(7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
[299] 51) N-(3-(3-(6-хлоро-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
[300] 52) (S)-6-хлоро-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[301] 53) (S)-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
[302] 54) (S)-(3-(3-(6-хлоро-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
[303] 55) (S)-(3-(3-(7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
[304] 56) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид;
[305] 57) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид;
[306] 58) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота;
[307] 59) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота;
[308] 60) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-((диметиламино)метил)бензамид;
[309] 61) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид;
[310] 62) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)бензамид;
[311] 63) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид;
[312] 64) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(диметиламино)ацетамид;
[313] 65) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[314] 66) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-морфолиноацетамид;
[315] 67) (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон;
[316] 68) (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон;
[317] 69) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид;
[318] 70) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид;
[319] 71) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид;
[320] 72) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид;
[321] 73) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(диметиламино)ацетамид;
[322] 74) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид;
[323] 75) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[324] 76) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[325] 77) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-морфолиноацетамид;
[326] 78) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид;
[327] 79) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропанамид;
[328] 80) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-3-(диметиламино)пропанамид;
[329] 81) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(4-метилпиперазин-1-ил)метанон;
[330] 82) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-2-метилбензамид;
[331] 83) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(морфолино)метанон;
[332] 84) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(диметиламино)ацетамид;
[333] 85) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-морфолиноацетамид;
[334] 86) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропанамид;
[335] 87) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[336] 88) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид;
[337] 89) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
[338] 90) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид;
[339] 91) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(морфолино)метанон;
[340] 92) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(4-метилпиперазин-1-ил)метанон;
[341] 93) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид;
[342] 94) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[343] 95) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(4-метилпиперазин-1-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
[344] 96) 3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид;
[345] 97) (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(4-метилпиперазин-1-ил)метанон;
[346] 98) (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(морфолино)метанон.
[347]
[348] Соединение, представленное Формулой 1 настоящего изобретения, может использоваться в форме приемлемой с точки зрения фармацевтики соли, в которой эта соль - предпочтительно соль присоединения кислоты, образованная приемлемыми с точки зрения фармацевтики свободными кислотами. Соль присоединения кислоты в данном случае может быть получена из неорганических кислот, например, из соляной кислоты, азотной кислоты, фосфорной кислоты, серной кислоты, бромистоводородной кислоты, йодистоводородной кислоты, азотистой кислоты и фосфористой кислоты; нетоксичных органических кислот, таких как алифатический моно/дикарбоксилaт, фенил-замещаемый алканоат, гидрокси-алканоат, алкандиоат, ароматические кислоты, и алифатические/ароматические сульфоновые кислоты; или органических кислот, таких как уксусная кислота, бензойная кислота, лимонная кислота, молочная кислота, малеиновая кислота, глюконовая кислота, метансульфоновая кислота, 4-толуолсульфоновая кислота, винная кислота и фумаровая кислота, в которых как минимум один галоген, выбранный из группы, состоящей из F, Cl, Br и I, является замещаемым или незамещаемым. Фармацевтически нетоксичные соли представлены такими примерами солей, как сульфат, пиросульфат, бисульфат, сульфит, бисульфит, нитрат, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, хлорид, бромид, иодид, фторид, ацетат, пропионат, деканоат, каприлат, акрилат, формат, изобутилат, капрат, гептаноат, пропиолат, оксалат, малонат, суккинат, суберат, кабакат, фумарат, малиат, бутен-1,4-диоат, гексан-1,6-диоат, бензоат, хлоробензоат, метилбензоат, динитробензоат, гидроксибензоат, метоксибензоат, фталат, терефталат, бензолсульфонат, толуолсульфонат, хлоробензолсульфонат, ксилолсульфонат, фенилацетат, фенилпропионат, фенилбутилат, цитрат, лактат, гидроксибутилат, гликолат, малат, тартат, метансульфонат, пропансульфонат, нафталол-1-сульфонат, нафталол-2-сульфонат и манделат.
[349] Соль присоединения кислоты в настоящем изобретении может быть приготовлена традиционным методом, известным для данной технологии. Например, соединение, представленное Формулой 1, растворяется в органическом соединителе, таком как метанол, этанол, ацетон, метиленхлорид или ацетонитрил, к которому добавляется органическая кислота или неорганическая кислота для того, чтобы вызвать осаждение. Затем осадок фильтруется и высушивается с образованием соли. Как вариант, растворитель и избыток кислоты дистиллируются под пониженным давлением и высушиваются с образованием соли. Как вариант, осадок кристаллизуется в органическом растворителе с образованием той же соли.
[350] Приемлемая с точки зрения фармацевтики соль металла может быть приготовлена с использованием основания. Соль щелочного металла или соль щелочноземельного металла получают в ходе следующего процесса: растворение соединения в избыточном растворе гидроксида щелочного металла или гидроксида щелочноземельного металла; фильтрование нерастворимой соли соединения; испарение оставшегося раствора и его высушивание. В этой связи соль металла предпочтительно готовится в фармацевтически приемлемой форме соли натрия, калия или кальция. Соответствующий раствор соли серебра готовится путем реакции соли щелочного металла или щелочноземельного металла с соответствующей солью серебра (например, нитратом серебра).
[351] Кроме того, настоящее изобретение включает в себя не только соединение, представленное Формулой 1, но также его приемлемую с точки зрения фармацевтики соль, a также сольват, стереоизомер или гидрат, которые могут быть полученными из нее.
[352] Термин “сольват” может включать в себя молекулярный комплекс, в том числе соединение согласно настоящему изобретению и как минимум одну молекулу приемлемого с точки зрения фармацевтики растворителя, напр., этанола или воды. Комплекс, в котором молекулой растворителя является вода, называется также “гидрат”.
[353] Соединения согласно настоящему изобретению могут существовать в форме стереоизомеров, например, таких как рацематы, энантиомеры или диастереоизомеры.
[354] Стереоизомеры соединений по Формуле данного документа могут включать в себя цис- и транс-изомеры, оптические изомеры, такие как (R) и (S) энантиомеры, диастереоизомеры, геометрические изомеры, поворотные изомеры, атропизмеры, конформационные изомеры и таутомеры соединений в соответствии с настоящим изобретением, включая соединения, демонстрирующие более одного типа изомерии, а также их смесь (например, рацематы и диастереоизомерные пары).
[355] При кристаллизации любого рацемата возможны кристаллы двух разных типов. Первый тип - это рацемическое соединение (истинный рацемат), упомянутое выше, в котором производится одна однородная форма кристалла, содержащая оба энантиомера в равномолярных количествах. Второй тип - это рацемическая смесь или конгломерат, в которой производятся две формы кристаллов в равномолярных количествах, каждая из которых включает в себя единичный энантиомер.
[356] Соединения согласно настоящему изобретению могут демонстрировать явление таутомерии и структурной изомерии. Например, соединения могут существовать в нескольких таутомерических формах, в том числе в форме энола и имина, в форме кето- и энамина и их геометрических изомеров и смесей. Все такие таутомерические формы включены в область соединений согласно настоящему изобретению. Таутомеры существуют как смеси таутомерического комплекса в растворе. В твердой форме превалирует обычно один таутомер. Даже если описывается только один таутомер, настоящее изобретение включает в себя все таутомеры соединений согласно представленной Формуле.
[357] Кроме того, некоторые из соединений согласно настоящему изобретению могут образовывать атропизомеры (напр., замещаемые биарилы). Атропоизомеры - это конформационные стереоизомеры, которые возникают, когда вращение вокруг единичной связи в молекуле не допускается или сильно замедляется в результате стерических взаимодействий с другими частями молекулы, а замещающие группы на обоих концах единичной связи несимметричны. Интерконверсия атропоизомеров слишком медленна для того, чтобы обеспечить разделение и изоляцию в предопределенных условиях. Энергетический барьер на пути термической рацемизации может определяться стерическим препятствованием свободному вращению одной или более связей, формирующих хиральную ось.
[358] В случае, если соединение в соответствии с настоящим изобретением содержит алкениловую или алкениленовую группу, возможны геометрические цис/транс (или Z/E) изомеры. Цис/транс изомеры могут разделяться обычными способами, хорошо известными специалистами в данной области, например, хроматографией и фракционной кристаллизацией.
[359] Обычные методы приготовления/изоляции тех или иных энантиомеров включают в себя хиральный синтез из подходящего оптически чистого прекурсора или разрешение рацемата (или рацемата соли или производного), с использованием, например, хиральной жидкостной хроматографии высокого давления (HPLC) или критической хроматографии сверхтекучей жидкости (SFC).
[360] В качестве альтернативы рацемат (или прекурсор рацемата) может реагировать с подходящим оптически активным соединением, например, спиртом, в случае, когда это соединение содержит кислый или основной фрагмент молекулы, кислоту или основание, например, винную кислоту или 1-фенилэтиламин. Образующаяся в результате диастереометрическая структура может отделяться хроматографией и/или фракционной кристаллизацией, и один или оба из диастереомеров преобразуются в соответствующий(е) чистый(е) энантиомер(ы) способами, хорошо известными специалистам в данной области.
[361] Настоящее изобретение включает в себя также изотопно меченые соединения, которые идентичны таковым, приведенным в одной из представленных Формул, но из-за того, что один или более атомов заменяются другим атомом (атомами), имеют атомную массу или массовое число, отличное от атомной массы или массового числа, которые обычно встречаются в естественном состоянии.
[362] Изотопно меченые соединения в соответствии с настоящим изобретением могут обычно приготавливаться традиционным методом, известным специалистам в данной технологии, или с использованием процессов, аналогичных описанным здесь, и использованием соответствующего изотопно меченого реагента вместо немеченого реагента, который используется в иных случаях.
[363] Далее, настоящее изобретение предлагает фармацевтический препарат, содержащий соединение, представленное Формулой 1, или его приемлемой с точки зрения фармацевтики солью в качестве активного ингредиента.
[364] Данный фармацевтический препарат может использоваться для профилактики или лечения болезней, выбранных из группы, включающей в себя рак, нейродегенеративное заболевание, неалкогольный стеатогепатит и грипп.
[365] Соединение, представленное Формулой 1, может замедлять активность протеинкиназы.
[366] Например, в отношении активности протеинкиназы, вариант MAPK включает в себя модуль ERK1/2, модуль JNK/p38, модуль ERK5 и т.п.
[367] В модуле ERK1/2, сигнальный каскад MAPK1/2 активируется связыванием лигандов с рецепторной тирозинкиназой (RTK); активированный рецептор производит заполнение и фосфорилирование адаптерных протеинов Grb2 и SOS, который в свою очередь взаимодействует с мембранносвязанной ГТФазой Ras и вызывает ее активацию. В такой активированной ГТФ-связанной форме Ras заполняет и активирует Raf киназы (A-Rf, B-Raf и C-Raf/Raf-1). Активированная Raf киназа активирует MAPK 1/2 (MKK1/2), которая в свою очередь катализирует фосфорилирование треониновых и тирозиновых остатков в цепочке активирования Thr-Glu-Tyr от ERK1/2.
[368] В модуле JNK/p38, киназы, расположенные выше MAP3K, такие как MEKK1/4, ASK1/2 и MLK1/2/3, активируют MAP2K3/6 (MKK3/6), MAP2K4 (MKK4) и MAP2K7 (MKK7). Эти MAP2K в свою очередь активируют JNK протеинкиназы, включая JNK1, JNK2 и JNK3, а также p38 α/β/γ/δ. Для выполнения своей функции JNK активируют несколько факторов транскрипции, включая c-Jun, ATF-2, NF-ATc1, HSF-1 и STAT1.
[369] В случае модуля ERK5 киназы, расположенные выше MAP2K5 (MKK5) - это MEKK2 и MEKK3.
[370] Соответственно, возможна профилактика или лечение соответствующих заболеваний путем замедления активности протеинкиназ, относящихся к MAP3K в пути MAPK, и блокирования расположенных выше киназ.
[371] С другой стороны, мутации LRRK2 или LRRK2 обнаруживаются у большинства пациентов с нейродегенеративным заболеванием. Мутации, имеющиеся в домене LRRK2 киназы, приводят увеличению активности LRRK2 киназы. В мозге человека экспрессия LRRK2 является самой высокой в том самом районе мозга, который поражен болезнью Паркинсона, и LRRK2 обнаруживается в тельцах Леви, характерном признаке болезни Паркинсона. Кроме того, мутации LRRK2, как оказалось, органически связаны с патологиями по типу болезни Альцгеймера, которые могут частично пересекаться с нейродегенеративными проявлениями в случаях обоих заболеваний - Альцгеймера и Паркинсона.
[372] Соответственно, возможна профилактика или лечение нейродегенеративных заболеваний, таких как болезнь Паркинсона или болезнь Альцгеймера, путем использования сильного ингибитора избирательного действия в отношении проникновения протеинкиназы в мозг для LRRK2.
[373] В настоящем изобретении протеинкиназа может относиться к семейству MLK (Mixed lineage kinase - киназы смешанного происхождения) или LRRK2, a семейство MLK может состоять из MLK1, MLK2, MLK3, MLK4, DLK, LZK или ZAK.
[374] Рак может быть как минимум одним выбранным из группы, включающей в себя псевдомиксому, внутрипеченочную холангиокарциному, гепатобластому, рак печени, рак щитовидной железы, рак толстой кишки, рак яичек, миелодиспластический синдром, глиобластому, рак полости рта, рак губы, фунгоидный микоз, острую гранулоцитарную лейкемию, острую лимфоцитарную лейкемию, базальноклеточную эпителиому, эпителиальный рак яичников, карциному зародышевых клеток яичника, рак груди у мужчин, рак мозга, аденому гипофиза, миеломную болезнь, рак желчного пузыря, рак желчных протоков, рак толстой кишки, хроническую гранулоцитную лейкемию, хроническую лимфоцитную лейкемию, ретинобластому, хороидальную меланому, диффузную В-крупноклеточную лимфому, рак фатерова соска, рак мочевого пузыря, перитонеальный рак, рак паращитовидных желез, рак надпочечников, рак носовых пазух, немелкоклеточный рак легкого, неходжкинскую лимфому, рак языка, астроцитому, мелкоклеточный рак легкого, детский рак мозга, детскую лимфому, младенческую лейкемию, рак тонкого кишечника, менингиому, рак пищевода, глиому, нейробластому, рак почек, рак сердца, рак двенадцатиперстной кишки, злокачественную опухоль мягких тканей, злокачественный рак костей, злокачественную лимфому, злокачественную мезотелиому, злокачественную меланому, рак глаза, рак вульвы, рак уретры, злокачественную опухоль без выявленного первичного очага, желудочную лимфому, рак желудка, карциноид желудка, желудочно-кишечный стромальный рак, опухоль Вильмса, рак груди, саркому, рак полового члена, фарингальный рак, гестациозное трофобластичное заболевание, рак шейки матки, рак тела матки, саркому матки, рак простаты, рак костей с метастазами, рак мозга с метастазами, рак средостения, рак прямой кишки, карциноидную опухоль прямой кишки, рак вагины, рак позвоночника, невриному слухового нерва, рак поджелудочной железы, рак слюнных желез, саркому Капоши, болезнь Паджета, рак миндалевидной железы, плоскоклеточную карциному, аденокарциному легкого, рак легкого, плоскоклеточную карциному легкого, рак кожи, рак анального канала, рабдомиосаркому, рак гортани, рак плевры и рак вилочковой железы.
[375] Нейродегенеративное заболевание может быть как минимум одним выбранным из группы, включающей в себя болезнь Альцгеймера, синдром Дауна, болезнь Паркинсона, болезнь Лу Герига, деменцию, болезнь Хантингтона, рассеянный склероз, проксимальный латеральный склероз, апоплексию, инсульт и умеренное когнитивное расстройство.
[376] Неалкогольный стеатогепатит может быть как минимум одним выбранным из группы, включающей в себя неалкогольное жировое перерождение печени, неалкогольный стеатогепатит, цирроз и рак печени.
[377] Грипп может быть гриппом A или гриппом B.
[378] Соединение, представленное Формулой 1 в соответствии с настоящим изобретением, может прописываться в разных формах для орального и парентерального приема во время клинического применения. В случае лекарственной формы она может быть приготовлена с использованием разбавителей или эксципиентов, таких как наполнители, сухие разбавители, связующие вещества, увлажнители, вещества для улучшения распадаемости, поверхностно-активные вещества и т.п., которые обычно используются.
[379] Твердые препараты для орального приема включают в себя таблетки, пилюли, порошки, гранулы, капсулы, пастилки и т.п., и могут приготовляться смешиванием одного или более эксципиентов, таких как крахмал, карбонат кальция, сахароза или лактоза, желатин и т.п., с соединениями в соответствии с настоящим изобретением. Кроме того, дополнительно к простым эксципиентам, могут использоваться также смазочные вещества, такие как стеарат магния, тальк и т.п. Примеры жидких препаратов для орального приема включают в себя взвеси, растворы, эмульсии и сиропы. Помимо воды и жидкого парафина, которые обычно используются, являясь простыми разбавителями, сюда же могут включаться различные эксципиенты, такие как увлажнители, подсластители, ароматизаторы, консерванты и т.п.
[380] Лекарственные формы для парентерального приема могут включать в себя стерилизованные водные растворы, неводные растворы, взвеси, эмульсии, лиофилизированные составы и суппозитории.
[381] Примеры неводного растворителя и растворителя в форме взвеси включают в себя полипропиленгликоль, полиэтиленгликоль, растительное масло, например, оливковое масло, и впрыскиваемый эфир, например, этилолеат. В качестве основы для суппозиториев могут использоваться витепсол, макрогол, tween 61, масло какао, лаурин, глицерогелатин и т.п.
[382] Далее, настоящее изобретение предлагает метод лечения рака, в котором данный метод включает в себя прописывание пациенту терапевтически эффективного количества соединения, его стереоизомера или его приемлемой с точки зрения фармацевтики соли.
[383] Терапевтически эффективным количеством называется количество, достаточное для смягчения симптомов или улучшения состояния пациента при приеме внутрь организма, в зависимости от способа приема. Кроме того, это количество может варьироваться в зависимости от веса, возраста, пола, состояния и наследственности лечащегося. Соответственно, метод лечения в настоящем изобретении может устанавливать разные дозы в соответствии с разными состояниями, в зависимости от пациента.
[384] “Эффективным количеством” называется количество, которого достаточно для лечения пролиферативных, воспалительных, инфекционных, неврологических или сердечно-сосудистых расстройств, или для лечения заболеваний. В другом конкретном осуществлении, “эффективным количеством” соединения называется, как минимум, минимальное количество, способное затормозить развитие заболевания.
[385] Соединение и состав в соответствии с методом настоящего изобретения могут прописываться в количестве эффективной дозы, определяемой методом подбора для лечения заболевания. Требуемое точное количество может варьироваться в зависимости от конкретного пациента, с учетом его расы, возраста и общего состояния здоровья, тяжести инфекции, конкретного вещества и его способа приема и т.п. Соединение в соответствии с настоящим изобретением может часто составляться в форме единицы дозы для облегчения приема и однородности дозирования. Термин “форма единицы дозы” означает физически независимую единицу лекарственной формы соединения, которая пригодна для лечения целевого объекта, в контексте данного документа. В то же время, здесь подразумевается, что совокупная ежедневная доза вещества и состав в соответствии с настоящим изобретением могут определяться врачом в рамках обоснованного врачебного решения. Конкретный эффективный уровень дозы для конкретного объекта или организма будет зависеть от ряда факторов, включая следующие.
[386] Термин “объект” в данном случае указывает на живое существо, например, млекопитающее, такое как человек.
[387] Фармацевтический препарат по настоящему изобретению может прописываться людям и другим животным системно или локально, орально или парентерально (назально, транспульмонально, внутривенно, ректально, подкожно, внутримышечно, наружно и т.п.), в зависимости от тяжести инфекции, подлежащей лечению.
[388] Чтобы получить желаемый лечебный эффект за счет использования фармацевтического препарата в соответствии с настоящим изобретением для конкретного лечения, дозировка соединения, представленного Формулой 1 настоящего изобретения как активный ингредиент, или его фармацевтически приемлемой формы соли, соответственно определяется с учетом возраста, пола, веса тела, болезни и глубины лечения пациента. Например, в случае орального приема в диапазоне приблизительно от 0,001 до 3000 мг/кг в день для взрослых (вес тела 60 кг), препарат можно нормально прописать весь сразу или разделить на несколько доз, и он может приниматься орально или парентерально один или несколько раз в течение двух дней, в неделю или в месяц. Доза для конкретного объекта или пациента должна определяться с учетом нескольких соответствующих факторов, таких как вес тела пациента, возраст, пол, состояние здоровья, диета, время приема, способ приема, тяжесть заболевания и т.п. Следует понимать, что величина дозы может соответственно регулироваться лечащим врачом. Здесь не предполагается, что доза будет ограничивать область настоящего изобретения в любых аспектах.
[389] Жидкая лекарственная форма для орального приема включает в себя фармацевтически приемлемые эмульсии, микроэмульсии, растворы, взвеси, сиропы и эликсиры, но не всегда ограничивается ими. В дополнение к активному соединению, жидкая лекарственная форма может также включать в себя инертные разбавители следующих примеров, обычно используемые в данной области: вода или другие растворители, солюбилизирующие компоненты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, растительное масло (например, хлопковое масло, арахисовое масло, кукурузное масло, масло бактерий, оливковое масло, касторовое масло, сезамовое масло), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоль, сложный эфир жирной кислоты сорбитана, а также их смеси. Помимо инертных разбавителей, лекарственная форма для орального приема может также включать в себя адъюванты, какие как увлажнители, эмульгаторы и суспендирующие агенты, подсластители и усилители вкуса.
[390] Инъекционные лекарственные препараты, например, стерильные инъекционные водные или липидные продуктивные взвеси могут создаваться путем использования соответствующих диспергентов или увлажнителей и суспендирующих агентов в соответствии с хорошо известной технологией. Стерильные инъекционные препараты могут быть также стерильными инъекционными растворами, взвесями или эмульсиями в нетоксичном парентерально принимаемом разбавителе или растворителе, например, в растворе 1,3-бутанэдиола. В качестве используемых носителей и растворителей можно выбрать воду, физиологический раствор (раствор Рингера), USP и изотонический раствор натрия хлорида. В качестве растворителя или дисперсионной среды обычно использовалось стерилизованное жирное масло. Для этой ели может использоваться произвольная смесь жирных масел, включая синтетический моно- или диглицерин. Кроме того, для приготовления инъекционных препаратов могут использоваться жирные кислоты, такие как олеиновая кислота.
[391] Инъекционные лекарственные препараты могут стерилизоваться путем фильтрации с использованием антибактериального фильтра или введением гермицида в качестве стерилизованной твердой формы, которая может растворяться или диспергироваться в стерилизованной воде или иной стерилизованной инъекционной среде.
[392] Для получения длительного эффекта от соединения в соответствии с настоящим изобретением часто бывает нужна замедленная абсорбция соединения от подкожной или внутримышечной инъекции. Такая замедленная абсорбция может быть достигнута за счет использования жидкой суспензии кристаллического или аморфного материала, плохо растворимого в воде.
[393] Скорость абсорбции соединения зависит от скорости растворения, на которую влияет размер кристалла и форма кристалла. В качестве альтернативы, можно добиться отложенной абсорбции парентерально принимаемого соединения путем растворения или образования взвеси соединения в масляном носителе. Лекарственная форма для внутримышечной инъекции может быть приготовлена путем создания микрокапсульной матрицы соединения в биоразлагаемом полимере, например в полилaктид-полигликолиде. В соответствии с соотношением «соединение-полимер» и характеристиками используемого здесь конкретного полимера, можно регулировать скорость выхода соединения. Примеры других биоразлагаемых полимеров включают в себя поли (ортоэфир) и поли (ангидрид). Лекарственная форма для внутримышечной инъекции можно приготовить также путем захвата соединения в липосому или микроэмульсию, совместимую с тканями тела.
[394] Препарат для ректального или вагинального приема, например, суппозиторий, который может быть приготовлен смешиванием соединения в соответствии с настоящим изобретением с подходящим нераздражающим эксципиентом или носителем, таким как масло какао, полиэтиленгликоль или воск для свечек. Данный суппозиторий является твердым при комнатной температуре, но становится жидким при температуре тела и соответственно тает в заднем проходе или вагине с выходом активного соединения.
[395] Твердые препараты для орального приема включают в себя капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых лекарственных формах для орального приема активное соединение смешивается как минимум с одним инертным, фармацевтически приемлемым эксципиентом или носителем, таким как цитрат натрия или дикальцийфосфат и/или a) наполнители или сухие разбавители, такие как крахмал, лактоза, сахароза, глюкоза, маннитол и кремниевая кислота, б) связующие вещества, такие как карбоксиметилцеллюлоза, альгинат, желатин, поливинилпирролидинон, сахароза и камедь, в) смачиватель, например, глицерин, г) разрыхлитель, например, агар, карбонат кальция, картофельный крахмал или крахмал тапиоки, альгиновая кислота, любой силикат и карбонат натрия, д) замедлители раствора, например, парафин, е) ускорители абсорбции, например, четвертичные соединения аммония, ж) смачиватели, например, цетиловый спирт и моностеарат глицерина, з) абсорбенты, например, каолин и бентонитовая глина, и) смазывающие вещества, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смесь. В случае капсул, таблеток и пилюль, лекарственные формы для приема могут содержать также буферные агенты.
[396] Твердые препараты аналогичного типа могут также применяться как наполнители в желатиновых капсулах с мягким и твердым наполнением, с использованием эксципиентов, таких как лактоза или молочный сахар, a также высокомолекулярный полиэтиленгликоль. Твердые лекарственные формы, такие как таблетки, драже, капсулы и гранулы могут быть приготовлены путем смешивания с материалами покрытий и оболочек, например, материалами кишечнорастворимых покрытий и другими материалами покрытий, хорошо известными в области технологии фармацевтических форм. Лекарственная форма может включать в себя опалесцирующий компонент. Лекарственная форма в соответствии с настоящим изобретением может представлять собой таковую, которая высвобождает только активный ингредиент (ингредиенты), например, в определенной части кишечного тракта с задержкой по времени. Используемая интегрируемая лекарственная форма может быть представлена примером полимерного вещества и воска. Твердые препараты аналогичного типа могут также применяться как наполнители в желатиновых капсулах с мягким и твердым наполнением, с использованием эксципиентов, таких как лактоза или молочный сахар, a также высокомолекулярный полиэтиленгликоль.
[397] Активное соединение может быть также в форме микрокапсул, с одним или более эксципиентами, как описано выше. Твердые лекарственные формы, такие как таблетки, драже, капсулы и гранулы, могут быть приготовлены путем смешивания с материалами покрытий и оболочек, например, материалами кишечнорастворимых покрытий и другими материалами покрытий, хорошо известными в области технологии фармацевтических форм. В таких твердых лекарственных формах активное соединение может смешиваться с одним или более инертным разбавителем, например, сахарозой, лактозой и крахмалом. Такие лекарственные формы для приема могут также содержать дополнительные вещества, отличные от инертных разбавителей, например, таблетировочные смазочные вещества и другие средства таблетирования, например, стеарат магния и микрокристаллическую целлюлозу. В случае капсул, таблеток и пилюль лекарственные формы для приема могут содержать также буферные агенты. Лекарственная форма может включать в себя опалесцирующий компонент. Лекарственная форма в соответствии с настоящим изобретением может представлять собой таковую, которая высвобождает только активный ингредиент (ингредиенты), например, в определенной части кишечного тракта с задержкой по времени. Используемая интегрируемая лекарственная форма может быть представлена примером полимерного вещества и воска.
[398] Лекарственные формы для местного или наружного применения в соответствии с настоящим изобретением включают в себя мази, пасты, кремы, лосьоны, гели, порошки, растворы, аэрозоли, средства для ингаляции или пластыри. Активный ингредиент смешивается с фармацевтически приемлемым носителем и любым нужным консервантом или буферным веществом, в стерильных условиях. Лекарственные формы для глаз, ушные капли и глазные капли также рассматриваются как входящие в область настоящего изобретения. Также, настоящее изобретение дополнительно включает в себя трансдермальные пластыри, которые имеют то преимущество, что обеспечивают контролируемое расслаивание соединения по телу. Такие лекарственные формулы могут быть приготовлены путем растворения или диспергирования соединения в соответствующей среде. Может быть также использован состав для повышения абсорбции, с целью увеличения потока соединения по коже. Скорость абсорбции может контролироваться за счет обеспечения регулирующей скорость мембраны или за счет диспергирования соединения в полимерной матрице или геле.
[399] В предпочтительном воплощении настоящего изобретения, соединение в соответствии с настоящим изобретением или фармацевтическая лекарственная форма, состоящая из него, может приниматься с противораковым средством. В настоящем изобретении термин “противораковое средство” означает любое средство, которое прописывается пациенту с раком в целях лечения рака.
[400] Комбинационная терапия включает в себя принятие лечебных средств параллельно или последовательно. В качестве альтернативы, лечебное средство может комбинироваться в один препарат, который прописывается пациенту.
[401] В предпочтительном воплощении настоящего изобретения, соединение в соответствии с настоящим изобретением применяется совместно с другими лечебными средствами. Соединение в соответствии с настоящим изобретением может приниматься без других лекарственных средств или в сочетании с цитотоксическими средствами, радиотерапией и иммунотерапией.
[402] Отдельно от комбинационной терапии могут приниматься дополнительные средства, обеспечиваемые как часть многократного введения дозы. В качестве альтернативы лекарственные средства могут быть частью формы однократного употребления, смешанного с соединением в соответствии с настоящим изобретением. При приеме как части комбинационной терапии, эти два лечебных средства могут приниматься одновременно, поочередно или с перерывами. Комбинационная терапия может использоваться для любых из описанных здесь симптомов. В предпочтительном воплощении настоящего изобретения комбинационная терапия проводится для лечения у пациента пролиферативного расстройства (например, рака).
[403] В другом аспекте настоящего изобретения, оно служит для замедления течения вышеназванного заболевания у биологического образца или объекта. Этот метод включает в себя прием соединения, представленного Формулой 1, или лекарственной формы, включающей в себя указанное соединение, либо контактирование биологического образца с указанным соединением. Термин “биологический образец” в данном случае включает в себя материалы in vivo, in vitro и ex vivo, и также включает в себя клеточные культуры или их экстракты; материалы биопсии, полученные от млекопитающего или их экстракты; a также кровь, слюну, мочу, фекалии, семенную жидкость, слезы или иные жидкости организма или их экстракты.
[404] Соединение или его приемлемая с фармацевтической точки зрения соль в соответствии с настоящим изобретением определяется за счет экспериментов как эффективное для профилактики или лечения рака, нейродегенеративного заболевания, неалкогольного стеатогепатита и гриппа.
[405] Для оценки ингибирующего действия соединения в соответствии с настоящим изобретением, был проведен эксперимент, в соответствии с пописанным в Экспериментальном примере 1 или 2 ниже. В результате было определено, что соединение в соответствии с примерами по настоящему изобретению обладало ингибирующим действием в отношении семейства MLK family, и что это соединение показало отличное ингибирующее действие на наномольном уровне. Соответственно, соединение в соответствии с настоящим изобретением может эффективно использоваться для профилактики или лечения не только заболеваний, связанных с перечисленными выше энзимами, но также вызываемыми ими видами рака.
[406] Кроме того, ингибирующее действие соединения по настоящему изобретению в отношении развития раковых клеток оценивалось для разных линий раковых клеток, как показано в Экспериментальных примерах 3 - 6 ниже. В результате ингибирующее действие в отношении развития раковых клеток определено как необычайно эффективное. Более того, как показано в Экспериментальном примере 7 ниже, было определено, что это соединение замедляло раковые метастазы и очень хорошо замедляло развитие раковых клеток (гибель раковых клеток). Соответственно, соединение по настоящему изобретению было определено как полезное для профилактики или лечения рака.
[407] Кроме того, в результате оценки действия по ингибированию фиброза, который является симптомом неалкогольного стеатогепатита, линии раковых клеток в печени человека, как в Экспериментальных примерах 8 и 9 ниже, соединение в соответствии с настоящим изобретением было определено как имеющее отличное антифиброзное действие и как повышающее индекс оценки для неалкогольного стеатогепатита, вызванного метионин-холин-дефицитной диетой, как показано в Экспериментальном примере 10 ниже. Соответственно, соединение в соответствии с настоящим изобретением было определено как полезное для профилактики или лечения неалкогольного стеатогепатита.
[408] Кроме того, соединение в соответствии с настоящим изобретением было определено как имеющее отличное ингибирующее действие на LRRK2, как показано в Экспериментальных примерах 11 - 13 ниже. Соответственно, соединение в соответствии с настоящим изобретением было определено как полезное в качестве лекарственного средства для профилактики или лечения неалкогольного стеатогепатита.
[409] Кроме того, соединение в соответствии с настоящим изобретением было определено как оказывающее отличное антивирусное воздействие, как показано в Экспериментальных примерах с 14 по 16 ниже. Соответственно, соединение по настоящему изобретению было определено как полезное в качестве лекарства для профилактики или лечения гриппа.
[410]
[411] Далее, настоящее изобретение будет детально описано с помощью Примеров и Экспериментальных примеров. При этом следующие Примеры и Экспериментальные примеры являются лишь иллюстрациями к настоящем изобретению, содержание которого не будет ограничиваться только ими.
[412]
[413] <Примеры>
[414] Соединение в соответствии с настоящим изобретением может быть приготовлено с помощью следующих Методов синтеза с 1 по 3 в качестве примеров.
[415] Для сведения, как в Методе синтеза 1 ниже, реакция может протекать после замещения атома галогена (X) в пиридиновом кольце при приготовлении Соединения B, а после завершения реакции может последовать удаление атома галогена (X), либо атом галогена (X) может не удаляться.
[416] Кроме того, как при приготовлении Соединения C по Методу синтеза 2 ниже, реакция может протекать без замещения атома галогена (X) в пиридиновом кольце.
[417] <Метод синтеза 1>
[418]
Нитрат церия аммония
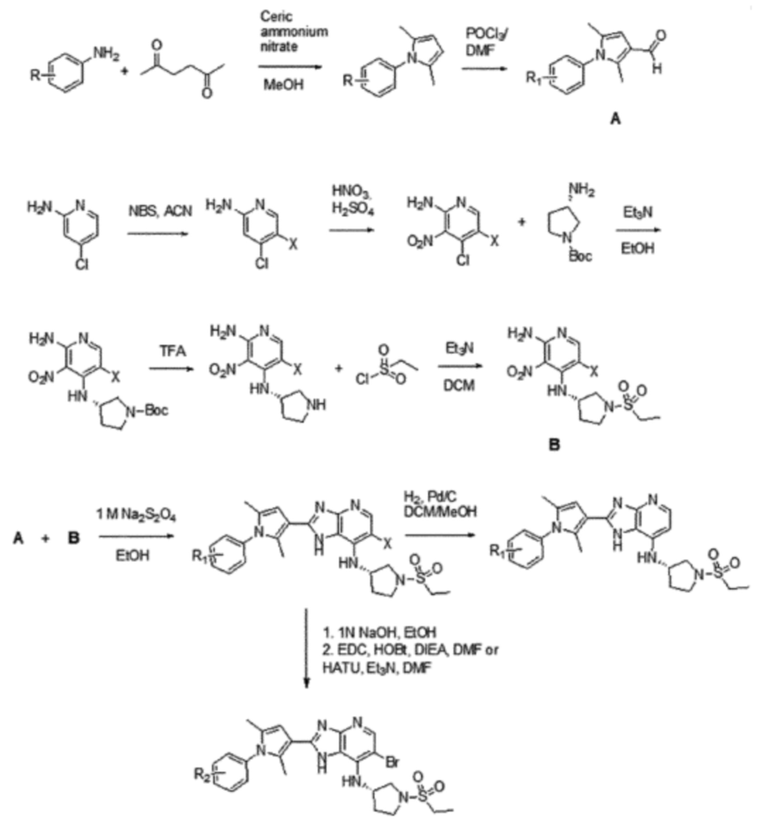
[419] <Метод синтеза 2>
[420]
Нитрат церия аммония
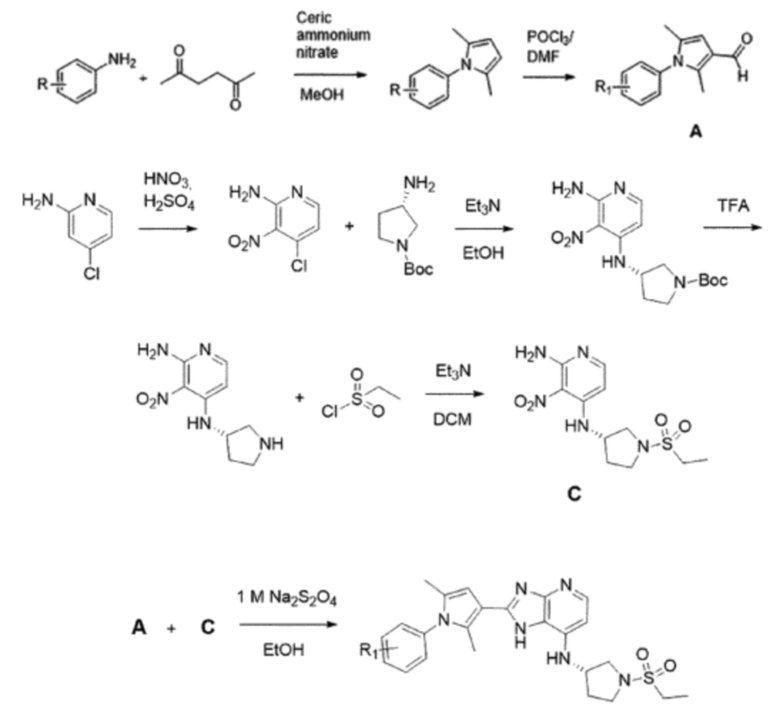
[421] <Метод синтеза 3>
[422]
Микроволна,
Нитрат церия аммония
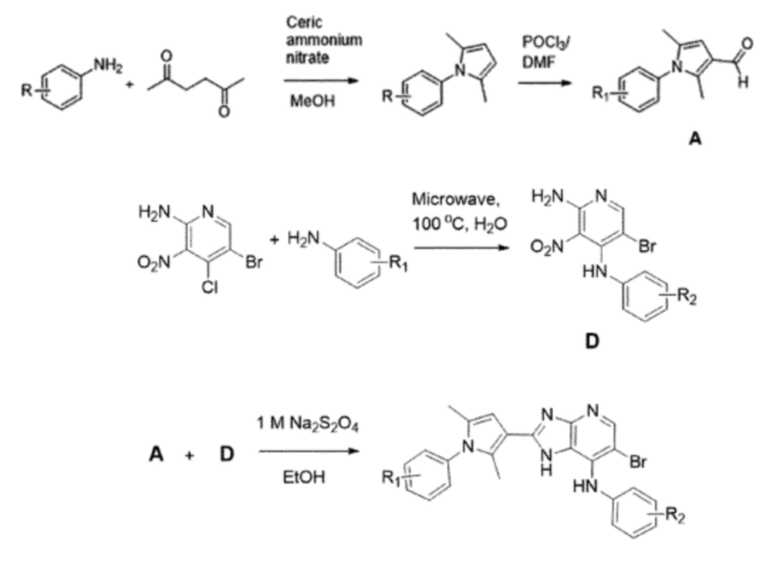
[423]
[424] Пример 1: (S)-6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[425] Соединение по Примеру 1 может быть приготовлено в соответствии с Методом синтеза 1, а именно в результате реакции, показанной на Схеме 1 ниже.
[426] [Реакция по Формуле 1]
[427]
Нитрат церия аммония
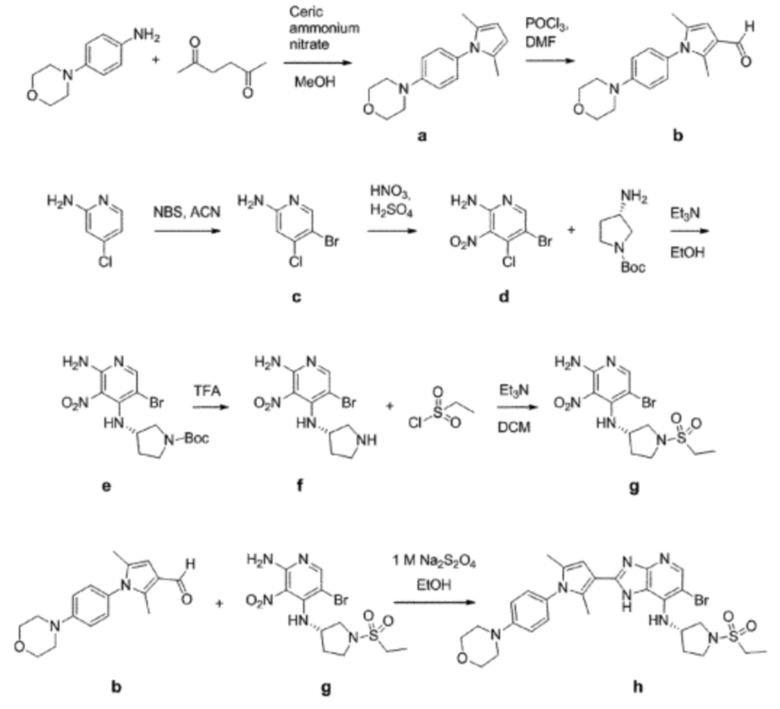
[428] 1-1. Синтез соединения b
[429] 4-морфолиноанилин (1 экв), гексан-2,5-дион (1 экв), MeOH и нитрат церия аммония (0,05 экв) были смешаны и перемешивались при комнатной температуре в течение 3 часов. Реакционная смесь подверглась концентрации под пониженным давлением. Сырой продукт был очищен методом колонной хроматографии (силикагель, гексан/EtOAc) для получения целевого соединения a (74%).
[430] Диметилформамид был помещен в каждый из двух контейнеров, температура была понижена до 0°C. Были добавлены и растворены соединение a (1 экв) и хлористый фосфорил (1,2 экв). Хлористый фосфорил (в ДМФ) медленно добавлялся к соединению a (в ДМФ) и перемешивался. По завершении реакции твердая фракция, полученная после доведения pH до 14 с использованием 20% NaOH, была отфильтрована, промыта водой и высушена для получения целевого соединения b (86%).
[431] 1-2. Синтез соединения g
[432] 4-хлоропиридин-2-амин (1 экв), N-бромосукцинимид (1,05 экв) и ацетонитрил были смешаны и перемешивались при комнатной температуре в течение 12 часов. Реакционная смесь подверглась концентрации под пониженным давлением, была разбавлена EtOAc, промыта 1N NaOH, водой и соляным раствором, высушена Na2SO4 и подверглась концентрации. Сырой продукт был рекристаллизирован (ДЦМ/Гексан) для получения целевого соединения c (70%).
[433] Соединение c (1 экв) и H2SO4 были смешаны при 0°C, была добавлена HNO3 (1,07 экв), все это нагрето до 55°C с перемешиванием в течение 1 часа. К реакционной смеси была добавлена ледяная крошка, pH был отрегулирован до 7 с помощью NaOH. Твердая фракция была отфильтрована, промыта водой и высушена для получения целевого соединения d (66%).
[434] Соединение d (1 экв), (s)-(-)-1-Бок-3-аминопирролидин (1,2 экв), триметиламин (4 экв) и EtOH были смешаны, нагреты до 80°C и перемешивались в течение 2 часов. Температура реакционной смеси была снижена до -20°C. Твердая фракция была отфильтрована, промыта водой и высушена для получения целевого соединения e (73 %).
[435] Соединение e (1 экв), ТФА (26,1 экв) и ДЦМ были смешаны и перемешивались при комнатной температуре в течение 3 часов. После добавления ДЦМ к реакционной смеси было выполнено повторное испарение, затем смесь высушили для получения соединения f.
[436] Соединение f (1 экв), этансульфонилхлорид (1,1 экв), триметиламин (5 экв) и дихлорметан были смешаны при -5°C и перемешивались в течение 1 часа. Реакционная смесь подверглась концентрации под пониженным давлением. Твердая фракция была отфильтрована, промыта водой и высушена для получения целевого соединения g (98%).
[437] 1-3. Синтез конечного продукта h
[438] Соединение b (1 экв), полученное в вышеприведенном примере синтеза, соединение g (1 экв), дитионит натрия (4,09 экв) и EtOH были смешаны и перемешивались в течение 2 дней. Реакционная смесь подверглась концентрации под пониженным давлением, разбавлена EtOAc, промыта водой и соляным раствором, высушена над Na2SO4 и подверглась концентрации. Сырой продукт был очищен методом колонной хроматографии (силикагель, гексан/EtOAc) для получения целевого соединения h (60%). 1H NMR (300 MHz, ДМСО-d6) δ 1.19 (t, J = 7.3 Hz, 3H), 1.98 (s, 3H), 2.10 (m, 1H), 2.31 (m, 1H), 2.37 (s, 3H), 3.09 (q, J = 7.5 Hz 2H), 3.20 (t, J = 4.4 Hz, 4H), 3.30 (m, 1H), 3.35 (m, 1H), 3.50(m, 1H), 3.68 (m, 1H), 3.75 (d, J= 4.4 Hz, 4H), 5.62 (m, 1H), 5.75 (d, J = 8.0 Hz, 1H), 6.54 (s, 1H), 7.07 (d, J = 9 Hz, 2H), 7.16 (d, J = 8.8 Hz, 2H), 7.96 (s, 1H), 12.66 (s, 1H)
[440] Далее, соединения по Примерам с 2 по 25 синтезировались в соответствии с репрезентативным методом синтеза 1.
[441] Пример 2: (S)-6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[442] 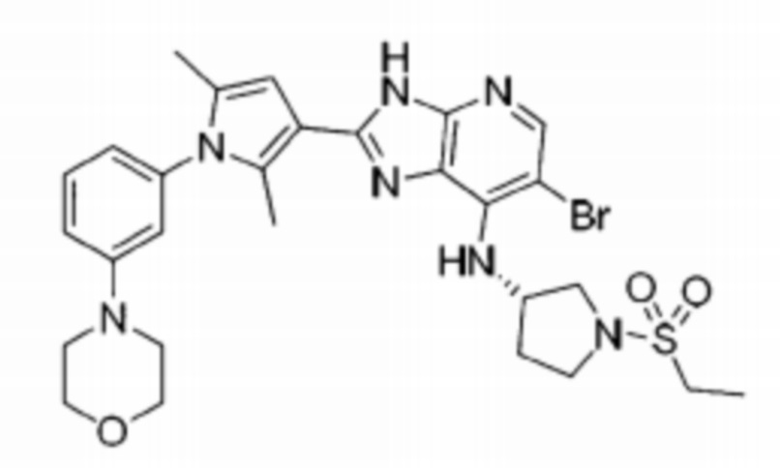
[443] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.40 Hz, 3H), 2.02 (m, 3 H), 2.12 (m, 1H), 2.31 (m, 1H), 2.41 (s, 3H), 3.09 (q, J=7.11 Hz, 2H), 3.18 (t, J=4.3 Hz, 4H), 3.28 (m, 1H), 3.35 (m, 1H), 3.49 (m, 1H), 3.67 (m, 1H), 3.74 (t, J=4.30 Hz, 4H), 5.63 (m, 1H), 5.76 (d, J=8.0 Hz, 1H), 6.56 (s, 1H), 6.72 (d, J=7.54 Hz, 1H), 6.85 (s, 1H), 7.05 (d, J=8.66 Hz, 1H), 7.39 (t, J=8.01 Hz, 1H), 7.97 (s, 1H), 12.68 (s, 1 H).
[444]
[445] Пример 3: (S)-6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин
[446] 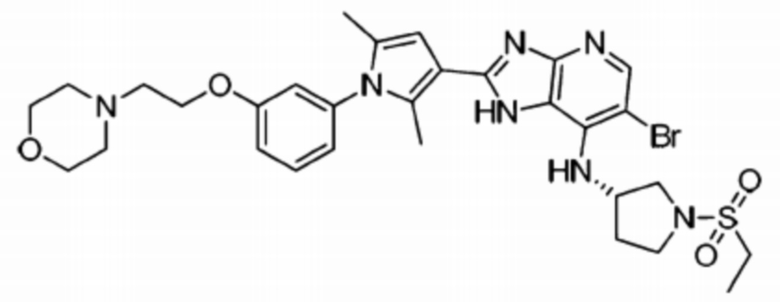
[447] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.5 Hz, 3H), 2.02 (s, 3H), 2.13 (m, 1H), 2.31 (m, 1H), 2.41 (s, 3H), 2.47(m, 4H), 2.70 (t, J=5.8 Hz, 2H), 3.09 (q, J=7.0 Hz, 2H), 2.28 (m, 1H), 3.36 (m, 1H), 3.5 (m, 1H), 3.57 (t, J=4.7 Hz, 4H), 3.68 (m, 1H), 4.15 (m, 2H), 5.61 (m, 1H), 5.77 (d, J=7.7 Hz, 1H), 6.57 (s, 1H), 6.91 (m, 2H), 7.08 (d, J=7.8, 1H), 7.45 (t, J=8.1, 1H), 7.97 (s, 1H), 12.70 (s, 1H).
[448]
[449] Пример 4: (S)-6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин
[450] 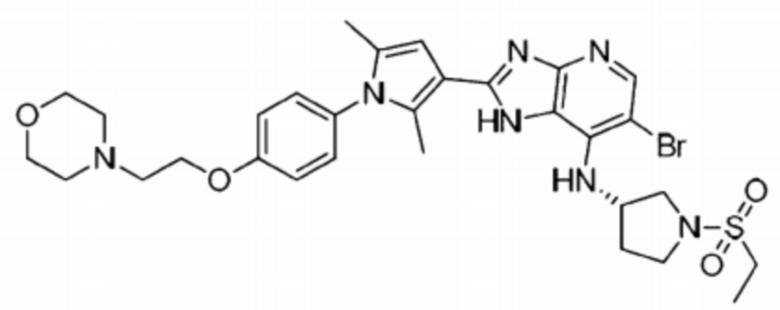
[451] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.4 Hz, 3H), 1.98 (s, 3H), 2.11 (m, 1H), 2.32 (m, 4H), 2.48 (m, 4H), 2.72 (t, J=5.5 Hz, 2H), 3.09 (q, J=7.4 Hz, 2H), 3.29 (m, 1H), 3.36 (m, 1H), 3.49 (m, 1H), 3.59 (m, 4H), 3.68 (m, 1H), 4.15 (t, J=5.6 Hz, 2H), 5.63 (m, 1H), 5.76 (m, 1H), 6.56 (s, 1H), 7.09 (d, J= 8.9 Hz, 2H), 7.24 (d, J=8.8 Hz, 2H), 7.97(s, 1H), 12.68 (s, 1H).
[452]
[453] Пример 5: (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон
[454] 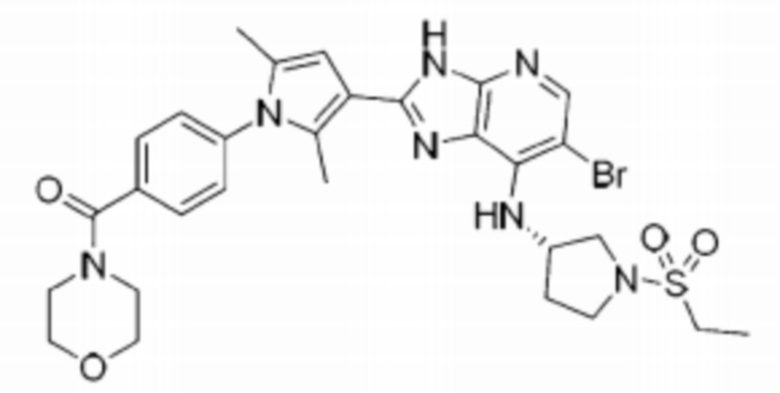
[455] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.3 Hz, 3H), 2.03 (s, 3H), 2.10 (m, 1H), 2.29 (m, 1H), 2.42 (s, 3H), 3.09 (q, J= 7.4 Hz, 2H), 3.30 (m,1H), 3.36 (m, 1H), 3.60 (m,10H), 5.63 (m, 1H), 5.78 (d, J=7.1 Hz, 1H), 6.60 (s, 1H), 7.44 (d, J= 8.5 Hz, 2H), 7.59 (d, J=8.4 Hz, 2H), 7.97 (s, 1H), 12.74 (s, 1H).
[456]
[457] Пример 6: (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон
[458] 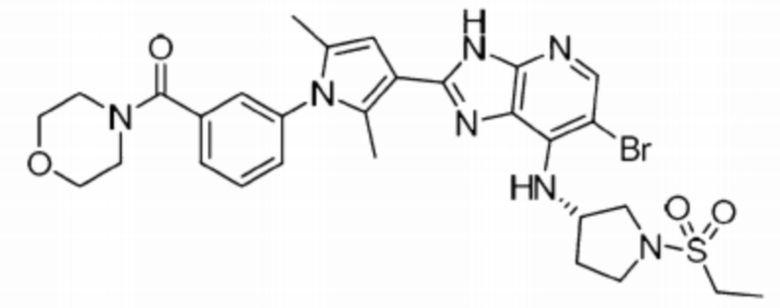
[459] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 ( t, J=7.3 Hz, 3H), 2.03 (s, 3H), 2.13 (m, 1H), 2.31 (m, 1H), 2.41 (s, 3H), 3.09 (m, 2H), 3.25 (m, 1H), 3.50 (m, 4H), 3.58 (m, 7H), 5.63 (m, 1H), 5.77 (m, 2H), 6.60 (s, 1H), 7.40 (s, 1H), 7.46 (d, J= 7.2 Hz, 1H), 7.54 (d, J=8.1, 1H), 7.66 (m, 1H), 7.98 (s, 1H), 12.74 (s, 1H).
[460]
[461] Пример 7: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид
[462] 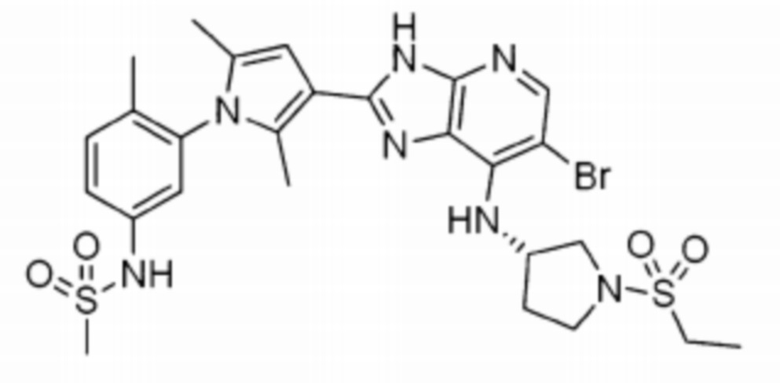
[463] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J = 7.3 Hz, 3H), 1.88 (s, 3H), 1.91(s, 3H), 2.13(m, 1H), 2.31 (m, 4H), 3.03 (s, 3H), 3.08 (q, J = 7.4 Hz, 2H), 3.30 (m, 1H), 3.35(m, 1H), 3.50 (m, 1H), 3.68 (m, 1H), 5.63 (m, 1H), 5.77 (d, J = 7.4 Hz, 1H), 6.62 (s, 1H), 7.03 (d, J = 2 Hz, 1H), 7.27 (d, J = 8 Hz, 1H), 7.43 (d, J = 8.4 Hz, 1H), 7.98 (s, 1H), 9.91 (s, 1H), 12.73 (s, 1H).
[464]
[465] Пример 8: N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)метансульфонамид
[466] 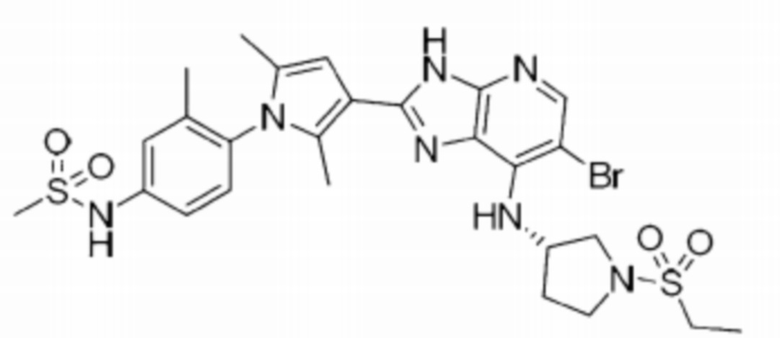
[467] 1H NMR (300 MHz, ДМСО- d 6) δ 1.18 (t, J = 7.4 Hz, 3H), 1.89 (s, 6H), 2.11 (m, 1H), 2.28 (m, 4H), 3.08 (m, 5H), 3.29 (m, 1H), 3.35 (m, 1H), 3.50 (m, 1H), 3.68 (m, 1H), 5.63 (m, 1H), 5.76 (d, J = 8.1 Hz, 1H), 6.60 (s, 1H), 7.21 (m, 3H), 7.97 (s, 1H), 10.00 (s, 1H), 12.70 (s, 1H).
[468]
[469] Пример 9: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)метансульфонамид
[470] 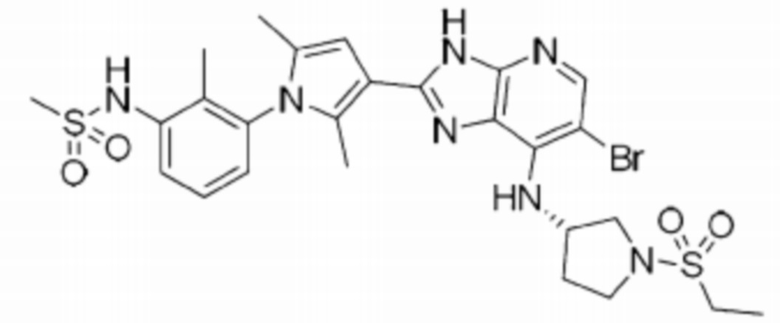
[471] 1H NMR (300 MHz, ДМСО- d 6) δ 1.18 (t, J = 7.3 Hz, 3H), 1.88 (d, J = 3.2 Hz, 6H), 2.12 (m, 1H), 2.28 (s, 3H), 2.35 (m, 1H), 3.05 (s, 3H), 3.08 (q, J = 7.2 Hz, 2H), 3.27 (m, 1H), 3.44 (m, 1H), 3.51 (m, 1H), 3.68 (m, 1H), 5.65 (m, 1H), 5.76 (d, J = 8.0 Hz, 1H), 6.62 (s, 1H), 7.2 (d, J = 8.4 Hz, 1H), 7.44 (m, 2H), 7.98 (s, 1H), 9.3 (s, 1H), 12.72 (s, 1H).
[472]
[473] Пример 10: (S)-6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[474] 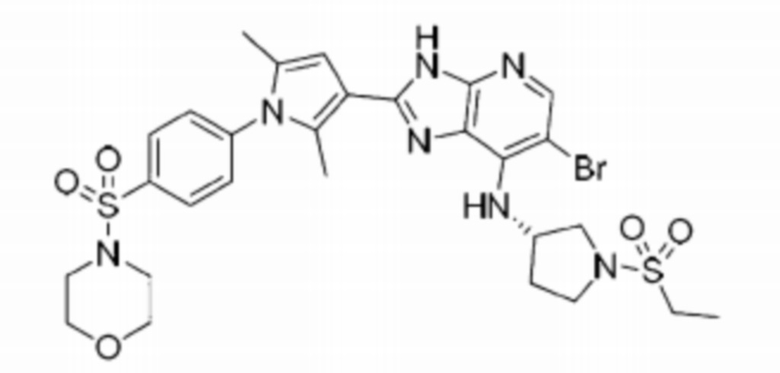
[475] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J= 7.4 Hz, 3H), 2.05 (s, 3H), 2.12 (m, 1H), 2.32 (m, 1H), 2.44 (s, 3H), 2.95 (t, J= 4.2 Hz, 4H), 3.10 (q, J= 7.5 Hz, 2H), 3.28 (m, 1H), 3.36 (m, 1H), 3.51 (m, 1H), 3.67 (m, 5H), 5.65 (m, 1H), 5.80 (d, J= 7.9 Hz, 1H), 6.64 (s, 1H), 7.69 (d, = 8.3 Hz, 2H), 7.91 (d, J= 8.3 Hz, 2H), 7.99 (s, 1H), 12.78 (s, 1H).
[476]
[477] Пример 11: (S)-6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[478] 
[479] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.4Hz, 3H), 2.04 (s, 3H), 2.14 (m, 1H), 2.32 (m, 1H), 2.43 (s, 3H), 2.95 (m, 4H), 3.09 (q, J=7.2 Hz, 2H), 3.28 (m, 1H), 3.36(m, 1H), 3.50 (m, 1H), 3.65 (m, 4H), 3.70 (m, 1H), 5.62 (m, 1H), 5.79 (m, 1H), 6.64 (s, 1H), 7.67 (s, 1H), 7.8 (m, 1H), 7.88 (d, J=4.9 Hz, 2H), 7.99 (s, 1H), 12.77 (s, 1H).
[480]
[481] Пример 12: (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)метансульфонамид
[482] 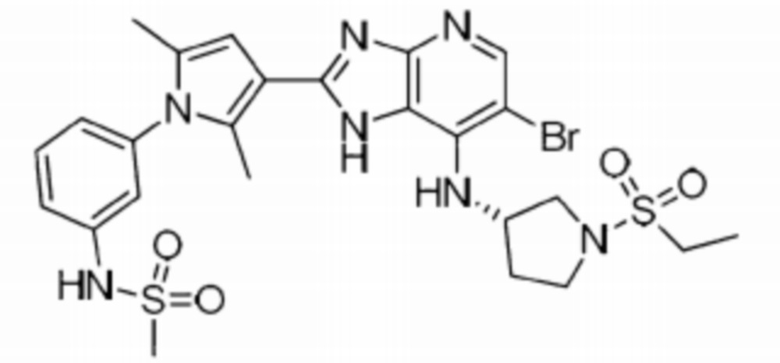
[483] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.3, 3H), 2.02 (s, 3H), 2.12 (m, 1H), 2.32 (m, 1H), 2.41 (s, 3H), 3.09 (m, 5H), 3.28 (m, 1H), 3.34 (m, 1H), 3.48 (m, 1H), 3.68 (m, 1H), 5.63 (m, 1H), 5.77 (d, J=8.4, 1H), 6.59 (s, 1H), 7.08 (m, 2H), 7.31 (d, J=6, 1H), 7.52 (m,1H), 7.98 (s, 1H), 10.04 (br. s., 1H), 12.71 (s, 1H).
[484]
[485] Пример 13: (S)-6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[486] 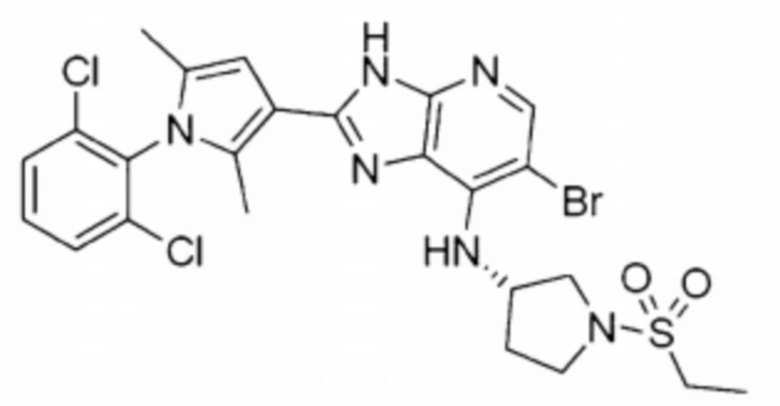
[487] 1H NMR (300 MHz, ДМСО- d 6) δ 1.18 (t, J = 7.4, 3H), 1.92 (s, 3H), 2.13 (m, 1H), 2.33 (m, 4H), 3.08 (q, J = 7.2 Hz, 2H), 3.30 (m, 1H), 3.36 (m, 1H), 3.50 (m, 1H), 3.70 (m, 1H), 5.63 (m, 1H), 5.79 (d, J = 7.7 Hz, 1H), 6.68 (s, 1H), 7.63 (m, 1H), 7.79 (d, J = 8.2 Hz, 2H), 7.99 (s, 1H), 12.78 (s, 1H).
[488]
[489] Пример 14: 6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[490] 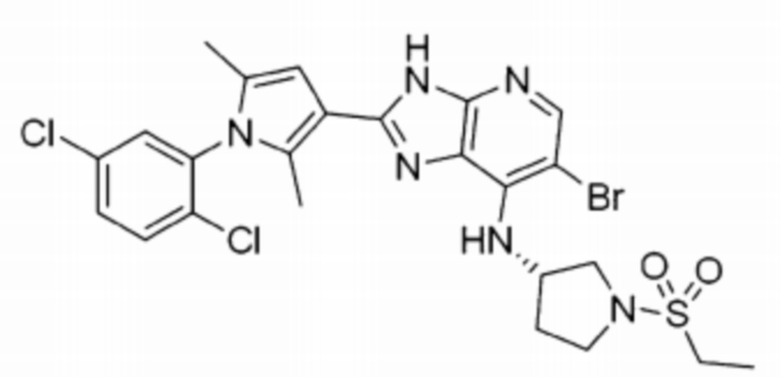
[491] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.3 Hz 3H), 1.95 (s, 3H), 2.12 (m, 1H), 2.29 (m, 1H), 2.34 (s, 3H), 3.09 (q, J= 7.2 Hz, 2H), 3.28 (m, 1H), 3.36 (m, 1H), 3.50 (m, 1H), 3.68 (m, 1H), 5.63 (m, 1H), 5.78 (m, 1H), 6.63 (s, 1H), 7.69 (m, 1H), 7.79 (m, 2H), 7.98 (s, 1H), 12.77 (s, 1H).
[492]
[493] Пример 15: (S)-6-бромо-2-(1-(3,4-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[494] 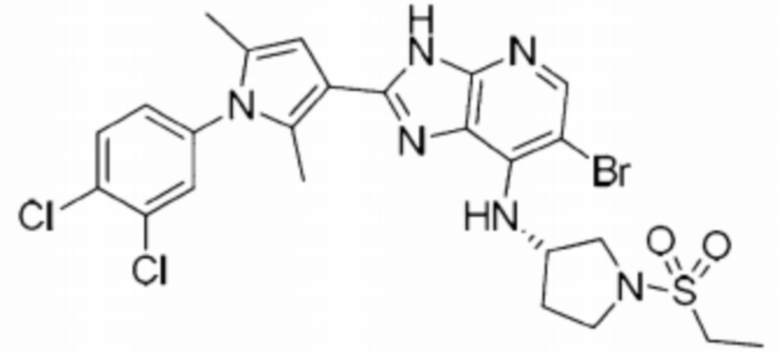
[495] 1H NMR (300 MHz, ДМСО- d 6) δ 1.20 (t, J=7.4 Hz, 3H), 2.03 (s, 3H), 2.13 (m, 1H), 2.31 (m, 1H), 2.43 (s, 3H), 3.09 (q, J=7.2 Hz, 2H), 3.28 (s, 1H), 3.35 (m, 1H), 3.51(m, 1H), 3.67(m, 1H), 5.62 (m, 1H), 5.79 (d, J=7.5 Hz, 1H), 6.60 (s, 1H), 7.42 (d, J=8.5 Hz, 1H), 7.83 (m, 2H), 7.98 (d, J=1.5, 1H), 12.75 (s, 1H).
[496]
[497] Пример 16: 6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[498] 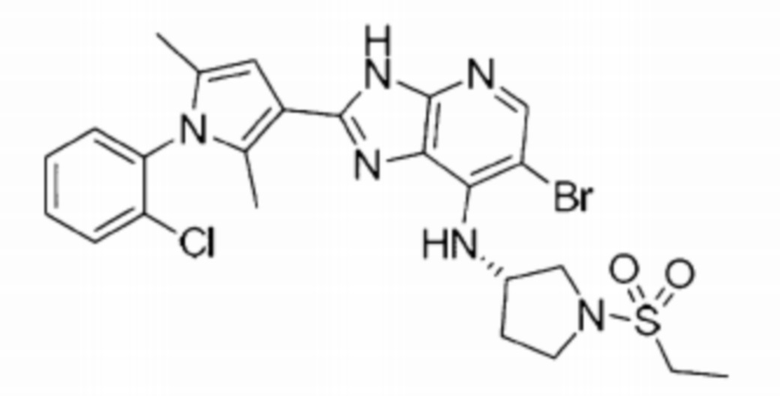
[499] 1H NMR (300 MHz, ДМСО- d 6) δ 1.18 (t, J = 7.3 Hz, 3H), 1.93 (s, 3H), 2.13 (m, 1H), 2.31 (m, 4H), 3.08 (q, J = 7.1 Hz, 2H), 3.30 (m, 1H), 3.35 (m, 1H), 3.50 (m, 1H), 3.68 (m, 1H), 5.63 (m, 1H), 5.77 (d, J = 7.5 Hz, 1H), 6.62 (s, 1H), 7.58 (m, 3H), 7.76 (m, 1H), 7.98 (s, 1H), 12.74 (s, 1H).
[500]
[501] Пример 17: 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-хлоробензолсульфонамид
[502] 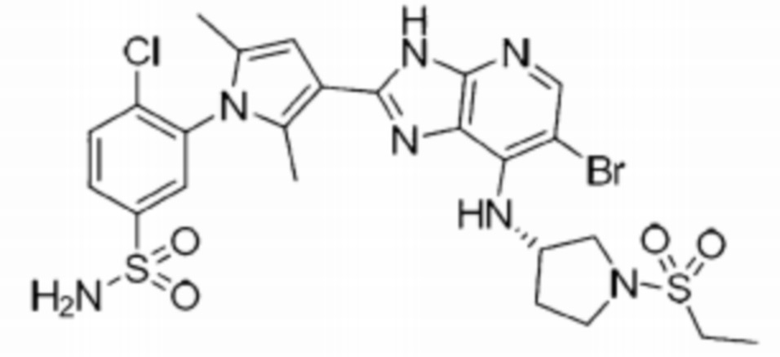
[503] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J = 7.1 Hz, 3H), 1.98 (s, 3H), 2.13 (m, 1H), 2.35 (m, 4H), 3.09 (q, J = 7.5 Hz, 2H), 3.29 (m, 1H), 3.36 (m, 1H), 3.49 (m, 1H), 3.69 (m, 1H), 5.63 (m, 1H), 5.80 (d, J = 7 Hz, 1H), 6.67 (s, 1H), 7.60 (s, 2H), 7.88 (m, 1H), 8.00 (s, 3H), 12.80 (s, 1H).
[504]
[505] Пример 18: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-метилбензолсульфонамид
[506] 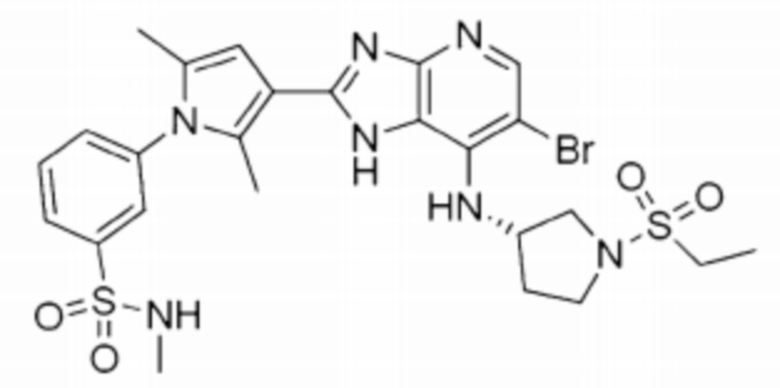
[507] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.30 Hz, 3H), 2.03 (s, 3H), 2.13 (m, 1H), 2.31 (m, 1H), 2.42 (s, 3H), 2.47 (s, 3H), 3.08 (q, J=7.26 Hz, 2 H), 3.29 (m, 1H), 3.36 (m, 1H,) 3.51 (m, 1H), 3.68 (m, 1H), 5.62 (m, 1H), 5.78 (d, J=7.92 Hz, 1H), 6.64 (s, 1H), 7.59 (br. s., 1H), 7.70 (m, 2H), 7.82 (t, J=7.68 Hz, 1H), 7.91 (m, 1H), 7.99 (s, 1H), 12.76 (br. s., 1H).
[508]
[509] Пример 19: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-этилбензолсульфонамид
[510] 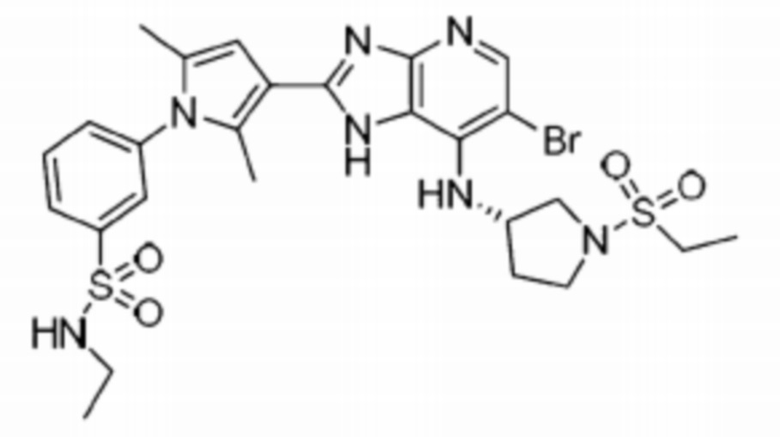
[511] 1H NMR (300 MHz, ДМСО- d 6) δ 0.97 (t, J=7.2, 3H), 1.18 (m, 3H), 2.03 (s, 3H), 2.13 (m, 1H), 2.31 (m, 1H), 2.42 (s, 3H), 2.85 (m, 2H), 3.08 (q, J=7.4 Hz, 2H), 3.28 (m, 1H), 3.36(m, 1H), 3.51 (m, 1H), 3.68 (m, 1H), 5.62 (m, 1H), 5.77 (m, 1H), 6.64 (s, 1H), 7.69 (m, 3H), 7.81 (t, J=7.8, 1H), 7.92 (d, J=7.7 Hz, 1H), 7.99 (s, 1H), 12.77 (br. s., 1H).
[512]
[513] Пример 20: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензамид
[514] 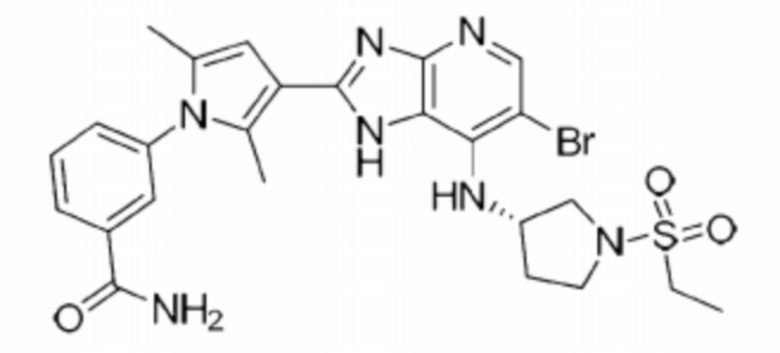
[515] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=6.5 Hz, 3H), 2.01 (s, 3H), 2.12 (m, 1H), 2.32 (m, 1H), 2.41 (s, 3H), 3.08 (q, J=7.4 Hz, 2H), 3.22 (m, 1H), 3.49 (m, 2H), 3.67 (m, 1H), 5.63 (d, J=5.3 Hz, 1H), 5.76 (d, J=7.2 Hz, 1H), 6.61 (s, 1H), 7.53 (m, 2H), 7.66 (t, 7.4 Hz, 1H), 7.83 (s, 1H), 8.01 (m, 2H), 8.11 (s, 1H), 12.77 (s, 1H).
[516]
[517] Пример 21: (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин
[518] 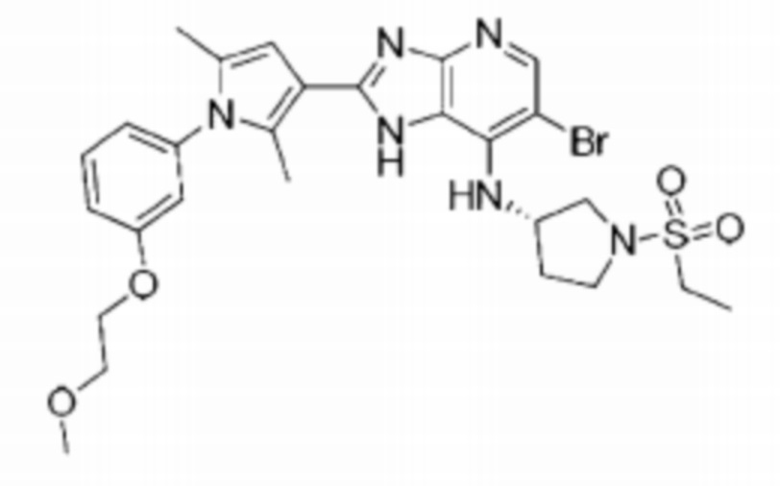
[519] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J = 7.4 Hz, 3H), 2.02 (s, 3H), 2.13 (m, 1H), 2.31 (m, 1H), 2.41 (s, 3H), 3.09 (q, J = 7.4 Hz, 2H), 3.28 (m, 1H), 3.36 (m, 1H), 3.50 (m, 1H), 3.68 (m, 3H), 4.16 (m, 2H), 5.62 (m, 1H), 5.76 (m, 1H), 6.57 (s, 1H), 6.9 (m, 2H), 7.08 (d, J = 8.6 Hz, 1H), 7.46 (m, 1H), 7.97 (s, 1H), 12.69 (s, 1H).
[520]
[521] Пример 22: (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(4-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин
[522] 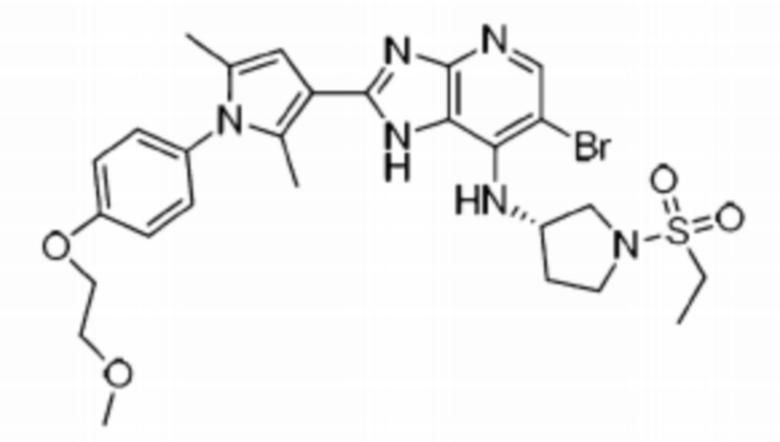
[523] 1H NMR (300 MHz, CDCl 3) δ 1.38 (t, J=7.4 Hz, 3H), 2.10 (m, 4H), 2.48 (m, 4H), 3.02 (m, 2H), 3.50 (s, 4H), 3.57 (m, 1H), 3.65 (m, 1H), 3.84 (m, 3H), 4.21 (m, 2H), 5.02 (d, J=8 Hz, 1H), 5.75 (m, 1H), 6.42 (s, 1H), 7.06 (d, J= 8.4, 2H), 7.18 (d, J=8.2 Hz, 2H), 8.18 (s, 1H), 12.26 (s, 1H).
[524]
[525] Пример 23: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид
[526] 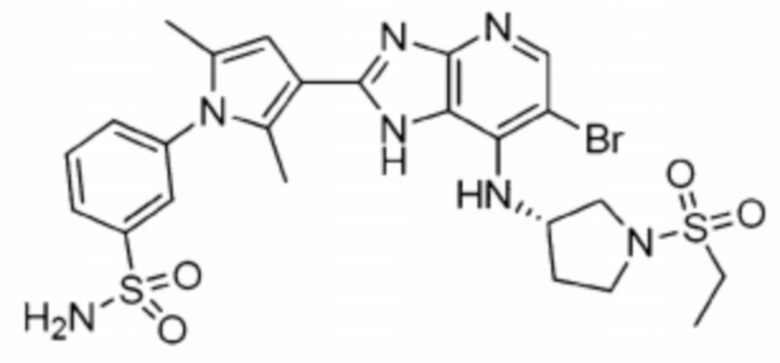
[527] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 ( t, J=7.1 Hz, 3H), 2.03 (s, 3H), 2.13 (m, 1H), 2.31 (m, 1H), 2.42 (s, 3H), 3.09 (q, J=7.2 Hz, 2H), 3.28 (m. 1H), 3.36 (m. 1H), 3.51 (m, 1H), 3.67 (m, 1H), 5.63 (m, 1H), 5.78 (d, J=7.6 Hz, 1H), 6.63 (s, 1H), 7.50 (br. s., 2H), 7.64 (d, J=8.7 Hz, 1H), 7.77 (m, 2H), 7.96 (m, 2H), 12.74 (s, 1H).
[528]
[529] Пример 24: (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид
[530] 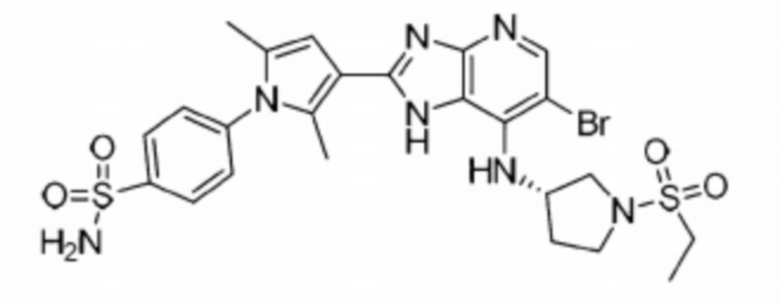
[531] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.3 Hz, 3H), 2.04 (s, 3H), 2.11 (m, 1H), 2.34 (m, 1H), 2.43 (s, 3H), 3.09 (m, 2H), 3.28 (m, 1H), 3.39 (m, 1H), 3.49 (m, 1H), 3.69 (m, 1H), 5.62 (m, 1H), 5.79 (d, J=7.9 Hz, 1H), 6.63 (s, 1H), 7.47(br. s., 2H), 7.6 (d, J=8.5 Hz, 2H), 8.00 (m, 3H), 12.43(br. s., 1H).
[532]
[533] Пример 25: (S)-6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[534] 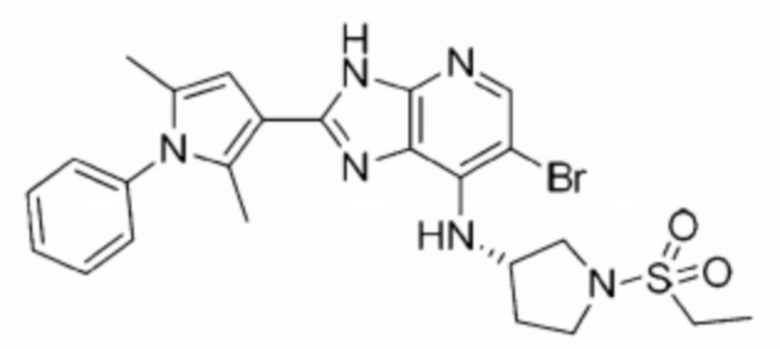
[535] 1H NMR (300 MHz, ДМСО- d 6) δ 1.19 (t, J=7.3 Hz, 3H), 2.00 (s, 3H), 2.15 (m, 1H), 2.32 (m, 1H), 2.39 (s, 3H), 3.08 (q, J=7.5 Hz, 2H), 3.28 (m, 1H), 3.38 (m, 1H), 3.51 (m, 1H), 3.68 (m, 1H), 5.64 (m, 1H), 5.77 (d, J = 7.6 Hz, 1H), 6.59 (s, 1H), 7.35 (d, J=7 Hz, 2H), 7.53 (m, 3H), 7.98 (s, 1H), 12.70 (s, 1H).
[536]
[537] Далее, соединения по Примерам с 26 по 48 синтезировались в соответствии с репрезентативным методом синтеза 3.
[538]
[539] Пример 26: 3-((6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[540] 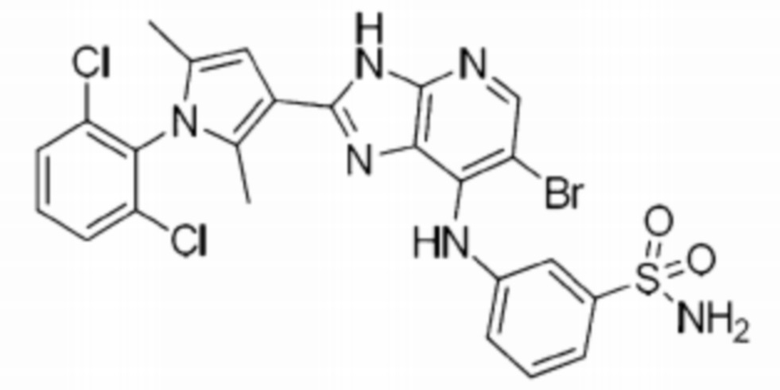
[541] 1H NMR (300 MHz, ДМСО- d 6) δ 1.89 (s, 3H), 1.97 (s, 3H), 6.64 (s, 1H), 7.21 (m, 3H), 7.33 (m, 2H), 7.6 (m, 2H), 7.75 (m, 2H), 8.21 (s, 1H), 8.54 (s, 1H), 12.91 (s, 1H).
[542]
[543] Пример 27: 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[544] 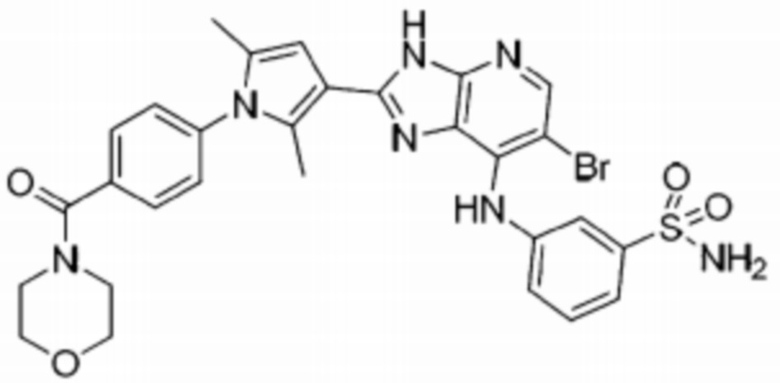
[545] 1H NMR (300 MHz, ДМСО- d 6) δ 2.00 (s, 3H), 2.09 (s, 3H), 3.44 (m, 2H), 3.63 (s, 6H), 6.60 (s, 1H), 7.19 (s, 3H), 7.34 (m, 4H), 7.57 (m, 3H), 8.20 (s, 1H), 8.52 (s, 1H), 12.85 (s, 1H).
[546]
[547] Пример 28: 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[548] 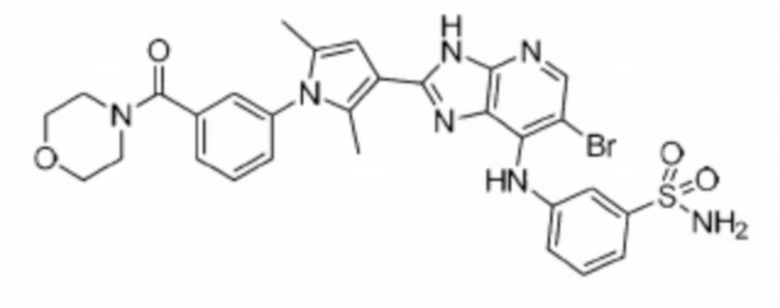
[549] 1H NMR (300 MHz, ДМСО- d 6) δ 2.00 (s, 3H), 2.15 (s, 3H), 3.62 (br. s., 8H), 6.58 (s, 1H), 7.16 (m, 2H), 7.33 (m, 5H), 7.58 (m, 4H), 8.19 (s, 1H) 12.85 (br. s., 1H).
[550]
[551] Пример 29: 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[552] 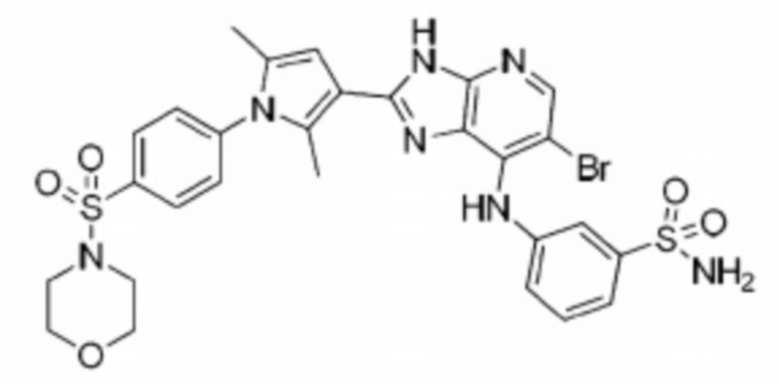
[553] 1H NMR (300 MHz, ДМСО- d 6) δ 2.02 (s, 3H), 2.13 (s, 3H), 2.95 (t, J= 4.2 Hz 4H), 3.67 (t, J=4.2 Hz, 4H), 6.64 (s, 1H), 7.20 (s, 3H), 7.32 (m, 2H), 7.55(s, 1H), 7.62 (d, J=8.5 Hz, 2H), 7.89 (d, J=8.5 Hz, 2H), 8.22 (s, 1H), 8.53 (s, 1H), 12.86 (s, 1H).
[554]
[555] Пример 30: 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[556] 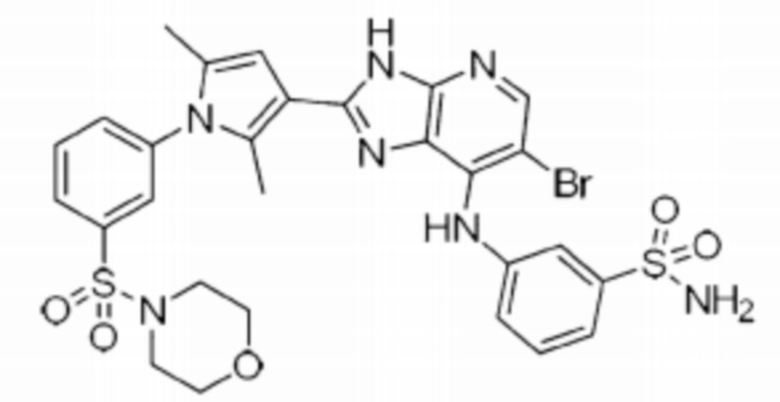
[557] 1H NMR (300 MHz, ДМСО- d 6) δ 2.01 (s, 3H), 2.09 (s, 3H), 2.93 (m, 4H), 3.65 (m, 4H), 6.63 (s, 1H), 7.19 (m, 3H), 7.32(m, 2H), 7.54 (s, 2H), 7.73 (m, 1H), 7.86 (m, 2H), 8.21 (s, 1H), 8.51 (s, 1H), 12.90 (s, 1H).
[558]
[559] Пример 31: 3-((6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[560] 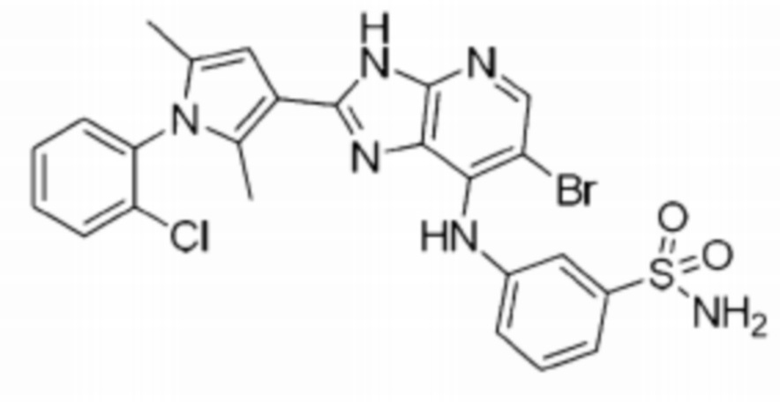
[561] 1H NMR (300 MHz, ДМСО- d 6) δ 1.9 (s, 3H), 1.98 (s, 3H), 6.6 (s, 1H), 7.19 (s, 3H), 7.32 (m, 2H), 7.46 (d, J = 6.1 Hz, 1H), 7.56 (m, 3H), 7.72 (m, 1H), 8.2 (s, 1H), 8.52 (s, 1H), 12.87 (s, 1H).
[562]
[563] Пример 32: 3-((6-бромо-2-(2,5-диметил-1-(2-метил-4-(метилсульфонамидо) фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[564] 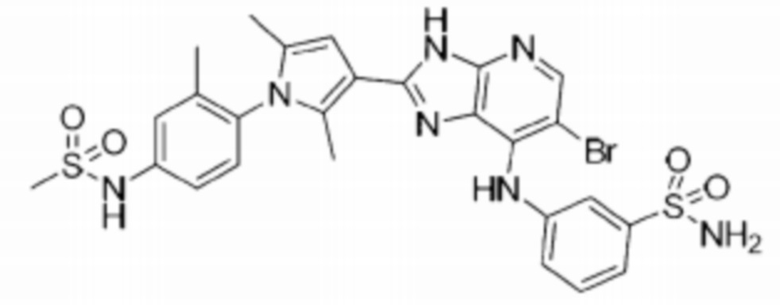
[565] 1H NMR (300 MHz, ДМСО- d 6) δ 1.84 (s, 3H), 1.87 (s, 3H), 1.96 (s, 3H), 3.01 (s, 3H), 6.59 (s, 1H), 6.96 (d, J = 2.1 Hz, 1H), 7.18 (s, 2H), 7.23 (s, 1H), 7.33 (m, 4H), 7.54 (s, 1H), 8.2 (s, 1H), 8.51 (s, 1H), 9.89 (s, 1H), 12.85 (s, 1H).
[566]
[567] Пример 33: 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(метилсульфонамидо) фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[568] 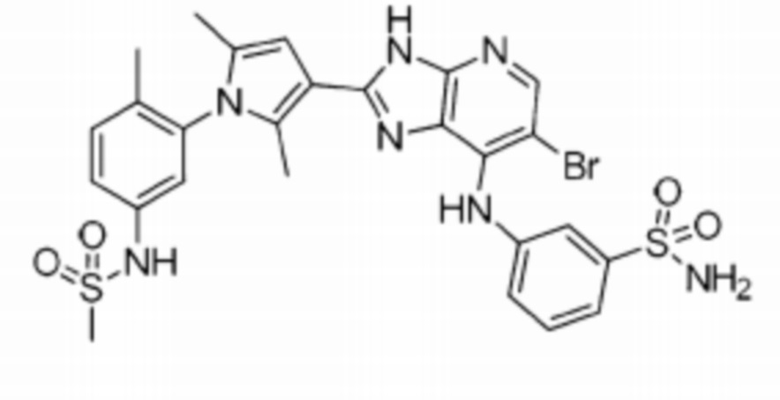
[569] 1H NMR (300 MHz, ДМСО- d 6) δ 1.82 (s, 3H), 1.88 (s, 3H), 1.96 (s, 3H), 3.01 (s, 3H), 6.59 (s, 1H), 6.96 (d, J = 2.1 Hz, 1H), 7.18 (s, 2H), 7.23 (s, 1H), 7.33 (m, 4H), 7.54 (s, 1H), 8.2 (s, 1H), 8.51 (s, 1H), 9.89 (s, 1H), 12.85 (s, 1H).
[570]
[571] Пример 34: 3-((6-бромо-2-(2,5-диметил-1-(2-метил-3-(метилсульфонамидо) фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[572] 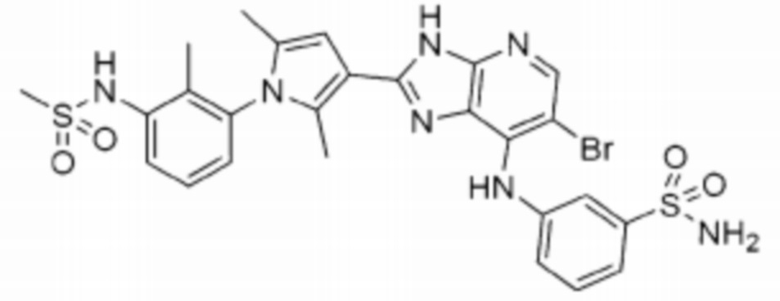
[573] 1H NMR (300 MHz, ДМСО- d 6) δ 1.82 (s, 3H), 1.86 (s, 3H), 1.95 (s, 3H), 3.04 (s, 3H), 6.60 (s, 1H), 7.16 (m, 4H), 7.38 (m, 4H), 7.54 (s, 1H), 8.2 (s, 1H), 8.51 (s, 1H), 9.28 (s, 1H), 12.85 (s, 1H).
[574]
[575] Пример 35: 3-((6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[576] 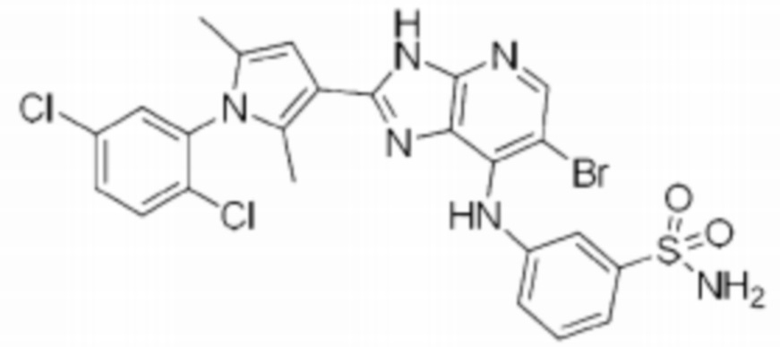
[577] 1H NMR (300 MHz, ДМСО- d 6) δ 1.92 (s, 3H), 2.00 (s, 3 H), 6.60 (s, 1H), 7.2 (m, 3H), 7.32 (m, 2H), 7.57(s, 1H), 7.68 (m, 2H), 7.77 (m, 1H), 8.21 (s, 1H), 8.53 (s, 1H), 12.88 (s, 1H).
[578]
[579] Пример 36: 3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пирролe-1-ил)-4-хлоробензолсульфонамид
[580] 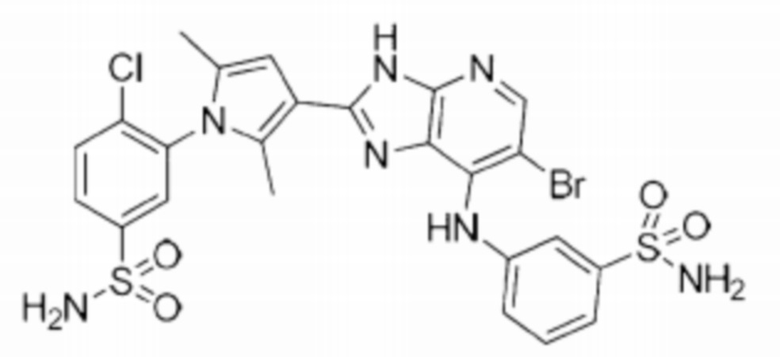
[581] 1H NMR (300 MHz, ДМСО- d 6) δ 1.93 (s, 3H), 2.01 (s, 3H), 6.64 (s, 1H), 7.20 (s, 3H), 7.32 (m, 3H), 7.56 (s, 2H), 7.81 (s, 1H), 7.97 (s, 2H), 8.22 (s., 1H), 8.53 (s, 1H) 12.86 (br. s., 1H).
[582]
[583] Пример 37: 3-((6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[584] 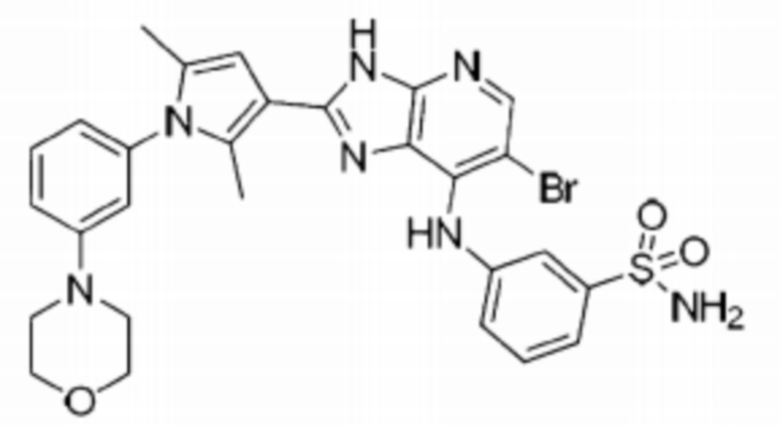
[585] 1H NMR (300 MHz, ДМСО- d 6) 1.99 (s, 3H), 2.07 (s, 3H), 3.16 (m, 4H), 3.73 (m, 4H), 6.54 (s, 1H), 6.65 (d, J=7.1 Hz, 1H), 6.77 (s, 1H), 7.03 (m, 1H), 7.20 (m, 3H), 7.35 (m, 3H), 7.55 (s, 1H), 8.19 (s, 1 H), 8.49 (s, 1H), 12.80 (s., 1H).
[586]
[587] Пример 38: 3-((6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[588] 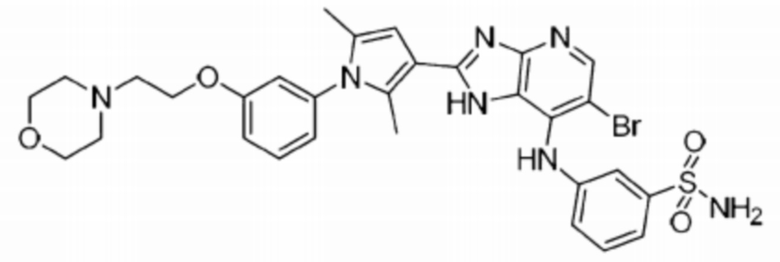
[589] 1H NMR (300 MHz, ДМСО- d 6) δ 1.99 (s, 3H), 2.07 (s, 3H), 2.46 (m, 4H), 2.69 (t, J=5.7 Hz, 2H), 3.57 ((t, J=4.7 Hz, 4H), 4.12 (t, J=5.9 Hz, 2H), 6.55 (s, 1H), 6.83 (m, 2H), 7.06 (d, J= 7.5 Hz, 1H), 7.20 (m, 3H), 7.32(m, 2H), 7.43 (t, J=8.1, 1H), 7.55 (s, 1H), 8.19 (s, 1H), 8.5 (s, 1H), 12.81 (s, 1H).
[590]
[591] Пример 39: 3-((6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[592] 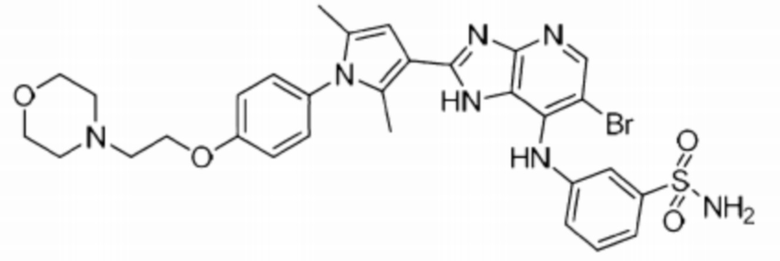
[593] 1H NMR (300 MHz, ДМСО-d 6) δ 1.95 (s, 3H), 2.04 (s, 3H), 2.47 (m, 4H), 2.72 (t, J=5.5 Hz, 2H), 3.59 (t, J=5.8 Hz, 4H), 4.14 (t, J=5.8 Hz, 2H), 6.54 (s, 1H), 7.07 (m, 2H), 7.18 (m, 5H), 7.3 (m, 2H), 7.54 (s, 1H), 8.19 (s, 1H), 8.5 (s, 1H), 12.8 (s, 1H).
[594]
[595] Пример 40: 3-((6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[596] 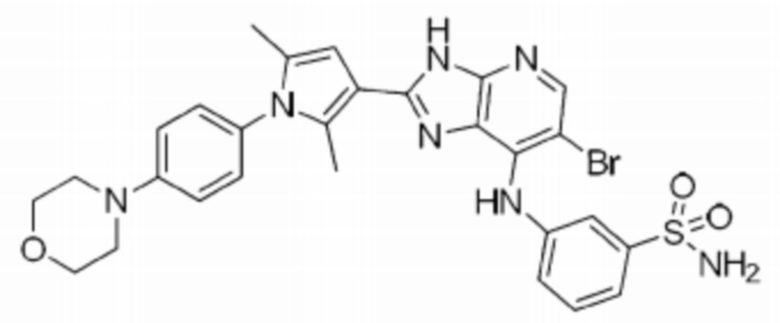
[597] 1H NMR (300 MHz, ДМСО- d 6) δ 1.96 (s, 3H), 2.04 (s, 3H), 3.19 (t, J=3.8 Hz, 4H), 3.76 (t, J = 3.8 Hz, 4H), 6.53 (s, 1H), 7.07 (q, J = 8.5 Hz, 4H), 7.19 (s, 3H), 7.3 (m, 2H), 7.54 (s, 1H), 8.19 (s, 1H), 8.5 (s, 1H), 12.78 (s, 1H).
[598]
[599] Пример 41: 3-((2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[600] 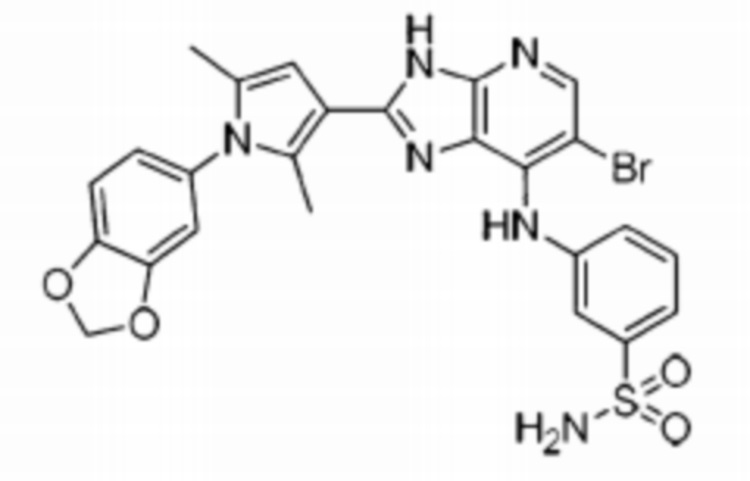
[601] 1H NMR (300 MHz, ДМСО- d 6) δ 1.98 (s, 3H), 2.07 (s, 3H), 6.14 (s, 2H), 6.53 (s, 1H), 6.72 (d, J=8.4 Hz, 1H), 6.91 (s, 1H), 7.04 (d, J=8.1 Hz, 1H), 7.19 (s, 3H), 7.32 (m, 2H), 7.54 (s, 1H), 8.19 (s, 1H), 8.50 (s, 1H), 12.81 (s, 1H).
[602]
[603] Пример 42: 3-((6-бромо-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[604] 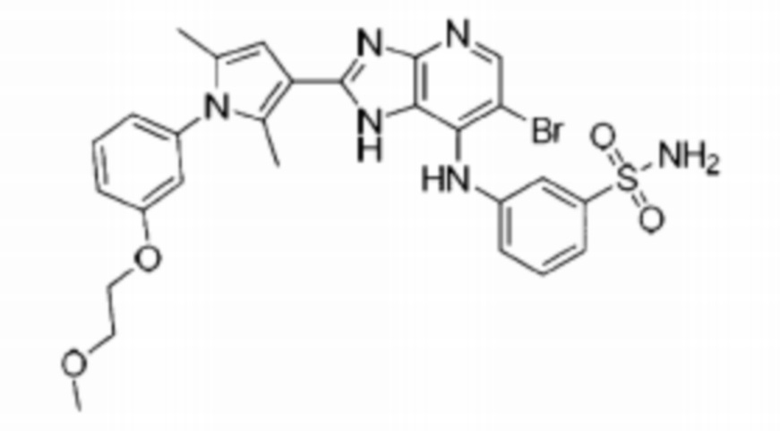
[605] 1H NMR (300 MHz, ДМСО- d 6) δ 1.99 (s, 3H), 2.08 (s, 3H), 3.31 (s, 3H), 3.66 (m, 2H), 4.14 (m, 2H), 6.55 (s, 1H), 6.83 (m, 2H), 7.06 (m, 1H), 7.26(m, 5H), 7.44 (m, 1H), 7.55 (m 1H), 8.19 (s, 1H), 8.5 (s, 1H), 12.82 (s, 1H).
[606]
[607] Пример 43: 3-((6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[608] 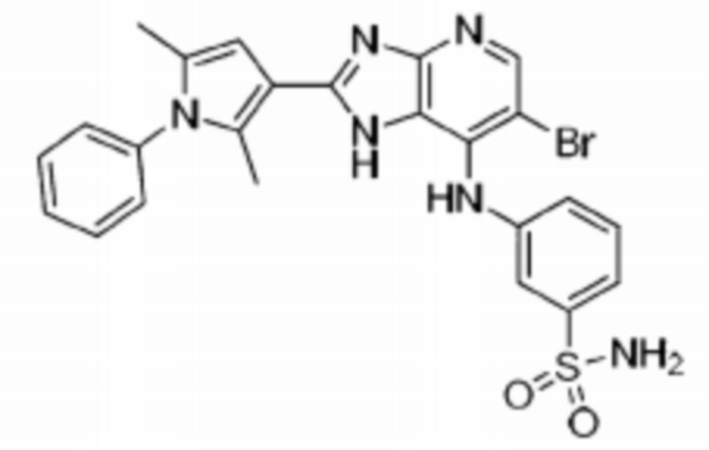
[609] 1H NMR (300 MHz, ДМСО- d 6) δ 1.97 (s, 3H), 2.06 (s, 3H), 6.57 (s, 1H), 7.18(m, 3H), 7.30 (m, 4H), 7.55 (m, 4H), 8.20 (s, 1H), 8.49 (s, 1H), 12.82 (br. s., 1H).
[610]
[611] Пример 44: 3-(3-(7-(бензо[d][1,3]диоксоль-5-ил-амино)-6-бромо-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид
[612] 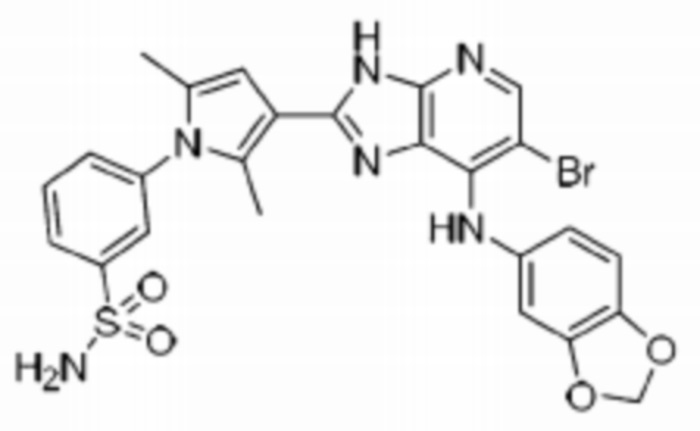
[613] 1H NMR (300 MHz, ДМСО- d 6) δ 2.00 (s, 3H), 2.11 (s, 3H), 5.88 (s, 2H), 6.59 (s, 1H), 6.67 (m, 1H), 6.76 (m, 2H), 7.52 (br. s., 2H), 7.60 (m, 1H), 7.68 (s, 1H), 7.76 (m, 1H), 7.92 (m, 2H), 8.10 (s, 1H) 12.72 (br. s., 1H).
[614]
[615] Пример 45: 2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(4-(2-метоксиэтокси)фенил)-3H-имидазо[4,5-b]пиридин-7-амин
[616] 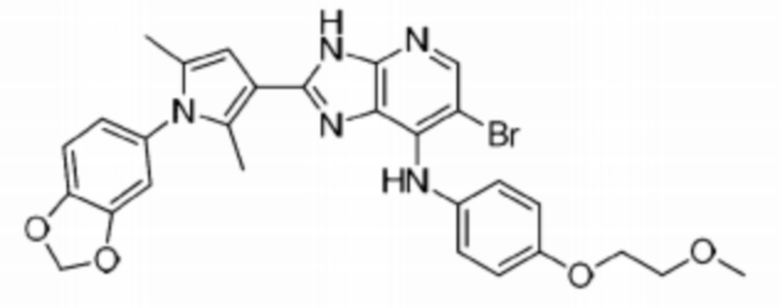
[617] 1H NMR (300 MHz, ДМСО- d 6) δ 1.97 (s, 3H), 2.02 (s, 3H), 3.23 (s, 3H), 3.59 (m, 2H), 4.00 (m, 2H), 6.14 (s, 2H), 6.49 (s, 1H), 6.71 (d, J=7.8 Hz, 1H), 6.81 (m, J=8.6 Hz, 2H), 6.91 (s, 1H), 7.04 (d, J=8.3 Hz, 1H), 7.11 (m, J=9Hz, 2H), 7.8 (s, 1H), 8.07 (s, 1H), 12.60 (s, 1H).
[618]
[619] Пример 46: 3-(3-(6-бромо-7-((4-(2-метоксиэтокси)фенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид
[620] 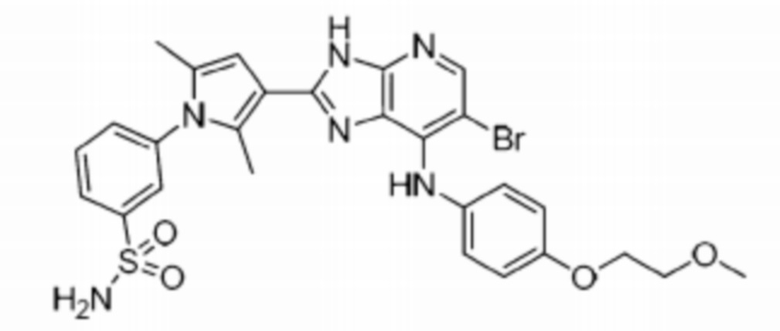
[621] 1H NMR (300 MHz, ДМСО- d 6) δ 1.99 (s, 3H), 2.04 (s, 3H), 3.19 (s, 3H), 3.57 (t, J=4.5 Hz, 2H), 3.98(m, 2H), 6.58 (s, 1H), 6.80 (d, J=9 Hz, 2H), 7.11 (d, J=8.8 Hz, 2H), 7.52 (s, 2H), 7.57(m, 1H), 7.66 (s, 1H), 7.75 (m, 1H), 7.83 (s, 1H), 7.91 (m, 1H), 8.08 (s, 1H), 12.68 (s, 1H).
[622]
[623] Пример 47: 3-((6-бромо-2-(2,5-диметил-1-(пиридин-3-ил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[624] 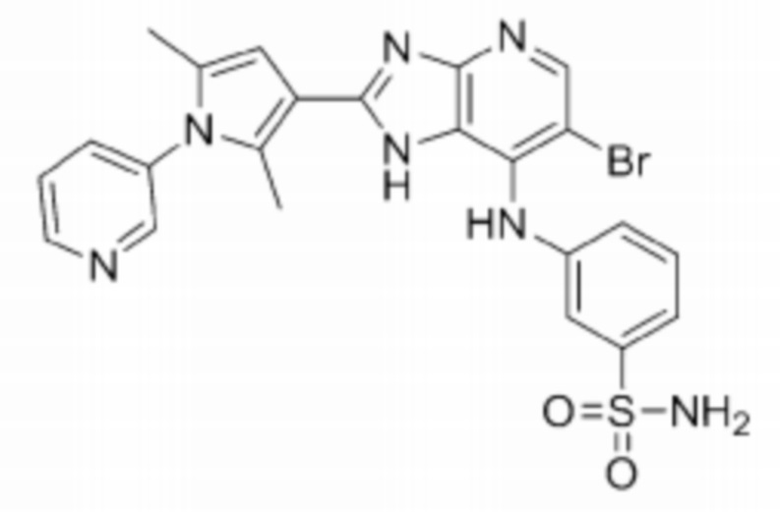
[625] 1H NMR (300 MHz, ДМСО-d 6) δ 1.99 (s, 3H), 2.08 (s, 3H), 6.62 (s, 1H), 7.2 (m, 4H), 7.32 (m, 2H), 7.58 (m, 2H), 7.81 (m, 1H), 8.21 (s, 1H), 8.53 (d, J=7.3, 2H), 8.69 (d, J=3.9, 1H), 12.87 (s, 1H).
[626]
[627] Пример 48: 3-((6-бромо-2-(2,5-диметил-1-(пиридин-4-илметил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[628] 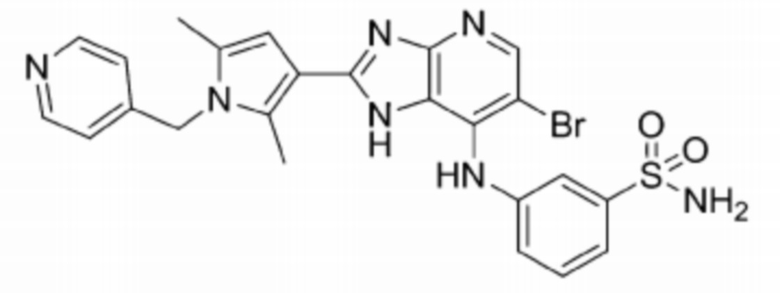
[629] 1H NMR (300 MHz, ДМСО-d 6) δ 2.09 (s, 3H), 2.22 (s, 3H), 5.16 (s, 2H), 6.53 (s, 1H), 6.87 (d, J=4.7, 2H), 7.19 (s, 3H), 7.31 (m, 2H), 7.54 (s, 1H), 8.19 (s, 1H), 8.49 (d, J=5.9, 3H), 12.8 (s, 1H).
[630]
[631] Далее, соединения по Примерам с 49 по 54 синтезировались в соответствии с репрезентативным методом синтеза 1.
[632]
[633] Пример 49: (S)-2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин
[634] 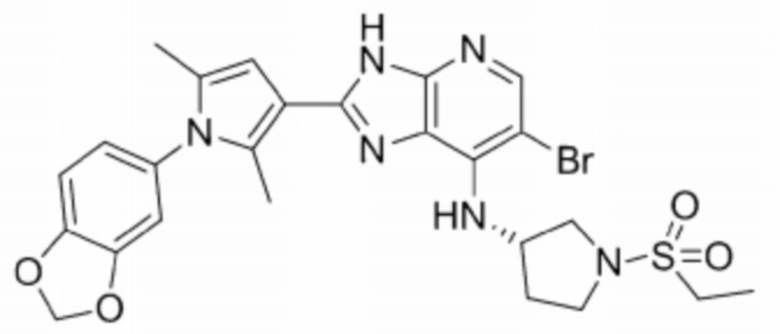
[635] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.36, 3 H), 2.11 (s, 4 H), 2.45 (s, 4 H), 3.03 (br. s., 2 H), 3.55 (m, 3 H), 3.85 (m, 1 H), 5.01 (d, J=8.47, 1 H), 5.74 (br. s., 1 H), 6.09 (s, 2 H), 6.36 (s, 1 H), 6.73 (m, 2 H), 6.92 (d, J=8.01, 1 H), 8.15 (s, 1 H), 11.56 (br. s., 1 H).
[636]
[637] Пример 50: N-(3-(3-(7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид
[638] 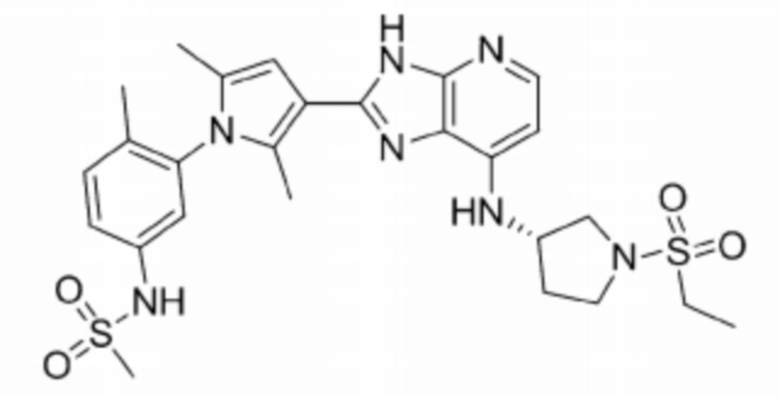
[639] 1H NMR (300 MHz, ДМСО-d 6) δ 1.19 (t, J=7.26, 3 H), 1.96 (m, 8 H), 2.28 (br. s., 1 H), 2.33 (s, 3 H), 3.03 (s, 3 H), 3.11 (m, 1 H), 3.25 (m, 1 H), 3.49 (m, 1 H), 3.67 (m, 3 H), 4.83 (br. s., 1 H), 6.34 (d, J=5.4, 1 H), 6.49 (d, J=6.98, 1 H), 6.59 (s, 1 H), 7.03 (s, 1 H), 7.27 (d, J=8.29, 1 H), 7.43 (d, J=8.38, 1 H), 7.77 (d, J=5.22 Hz, 1 H), 9.92 (br. s., 1 H), 12.46 (br. s., 1 H).
[640]
[641] Пример 51: N-(3-(3-(6-хлоро-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид
[642] 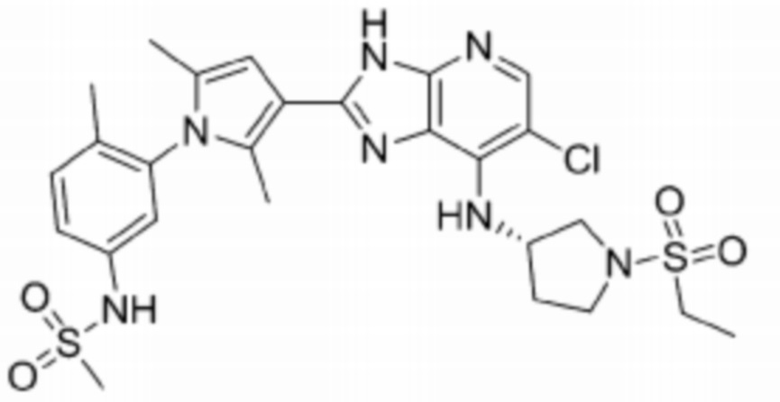
[643] 1H NMR (300 MHz, ДМСО-d 6) δ 1.88 (s, 3H), 1.9 (s, 3H), 2.3 (s, 3H), 3.02 (s, 3H), 5.62 (m, 1H), 6.04 (d, J=7.40, 1H), 6.61 (s, 1H), 7.02 (s, 1H), 7.26 (d, J=8.60, 1H), 7.42 (d, J=8.80 1H), 7.88 (s, 1H), 9.91 (s, 1H), 12.70 (s, 1H).
[644]
[645] Пример 52: (S)-6-хлоро-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин
[646] 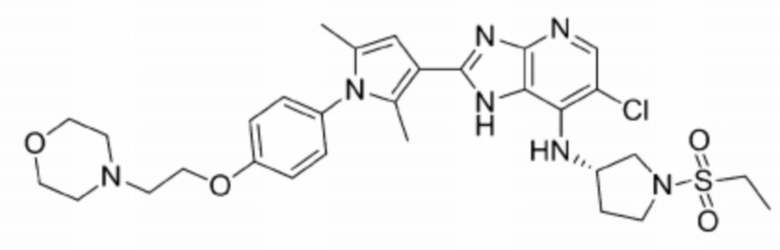
[647] 1H NMR (300 MHz, ДМСО-d 6) δ 1.19 (t, J=7.36, 3 H), 1.98 (s, 3 H), 2.14 (m, 1 H), 2.31 (m, 1 H), 2.38 (s, 3 H), 2.73 (t, J=5.70, 2 H), 3.09 (q, J=7.50, 2 H), 3.30 (m, 1 H), 3.33 (m,4H), 3.36 (m, 1 H), 3.54 (m, 5 H), 3.69 (m, 1 H), 4.16 (t, J=5.70, 2 H), 5.62 (m, 1 H), 6.05 (d, J=8.30, 1 H), 6.55 (s, 1 H), 7.10 (d, J=9.03, 2 H), 7.25 (d, J=8.94, 2 H), 7.88 (s, 1 H), 12.67 (s, 1 H).
[648]
[649] Пример 53: (S)-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин
[650] 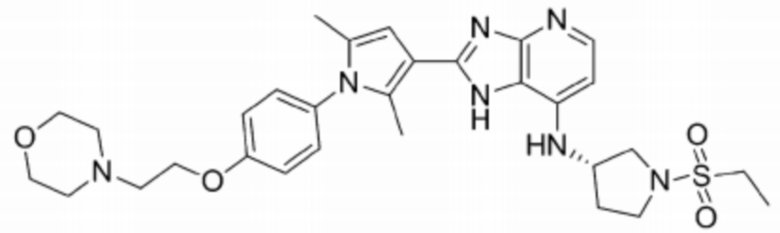
[651] 1H NMR (300 MHz, ДМСО-d 6) δ 1.19 (t, J=7.40, 3 H), 1.98 (s, 4H), 2.28 (br. s, 1H), 2.41 (s, 3H), 2.73 (t, J=5.80, 2H), 3.08 (m, 2H), 3.59 (m, 6H), 4.15 (m, 2H), 4.84 (s, 1H), 6.33 (d, J=5.8 Hz, 1H), 6.49 (m, 2H), 7.09 (d, J=8.5 Hz, 2H), 7.24 (d, J=9 Hz, 2H), 7.76 (d, J=5.3 Hz, 1H), 12.39 (s, 1H).
[652]
[653] Пример 54: (S)-(3-(3-(6-хлоро-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон
[654] 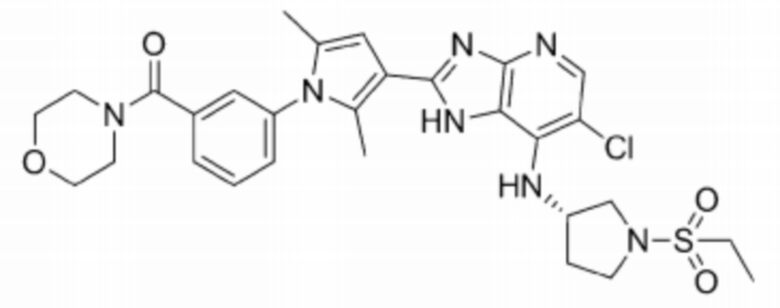
[655] 1H NMR (300 MHz, ДМСО-d 6) δ 1.19 (t, J=7.5, 3H), 2.03 (s, 3H), 2.15 (m, 1H), 2.5 (m, 4H), 3.33 (m, 1H), 2.42 (s, 3H), 3.08 (m, 2H), 3.68 (m, 8H), 6.06 (d, J=8.0, 1H), 6.61 (s, 1H), 7.41 (s, 1H), 7.46 (d, J=8.5, 1H), 7.54 (d, J=8.4, 1H), 7.65 (m, 1H), 7.89 (s, 1H), 12.72 (s, 1H).
[656]
[657] Далее, соединение по Примеру 55 было синтезировано в соответствии с репрезентативным методом синтеза 2.
[658]
[659] Пример 55: (S)-(3-(3-(7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон
[660] 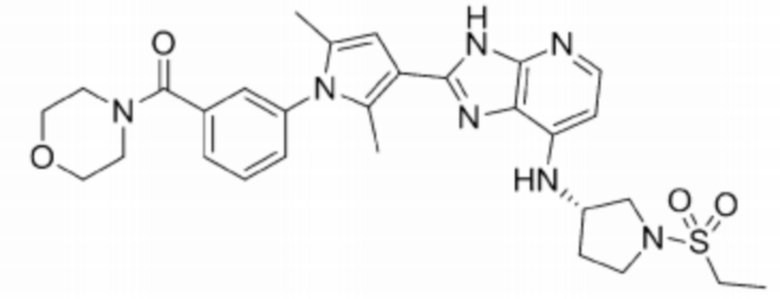
[661] 1H NMR (300 MHz, ДМСО-d 6) δ 1.19 (t, J=7.5, 3H), 2.03 (m, 4H), 2.29 (m, 1H), 2.46 (s, 3H), 3.09 (m, 2H), 2.5 (m, 4H), 3.68 (m, 8H), 4.85 (br. s, 1H), 6.35(s, 1H), 6.52 (s, 1H), 6.58 (s, 1H), 7.48 (m, 3H), 7.66 (m, 1H), 7.18 (br. s, 1H), 12.43 (br. s, 1H).
[662]
[663] Далее, соединение по Примерам с 56 по 87 синтезировались в соответствии с репрезентативным методом синтеза 1.
[664]
[665] Пример 56: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид
[666] 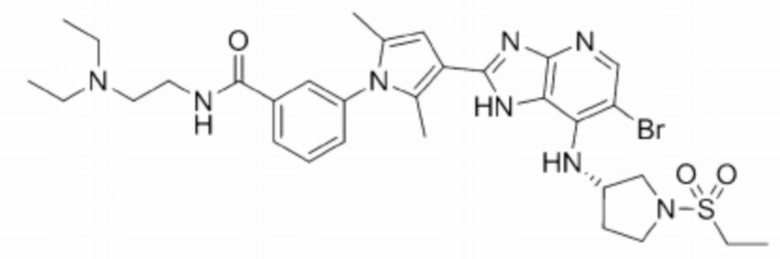
[667] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.27 (d, J=7.2, 6H), 1.38 (t, J=7.4, 7.4, 4H), 2.09 (m, 4H), 2.49 (m, 4H), 3.03 (m, 7H), 3.56 (m, 3H), 3.83 (m, 3H), 5.02 (d, J=7.9, 1H), 5.74 (br. s, 1H), 6.42 (s, 1H), 7.26 (m, 1H), 7.4 (d, J=7.5, 1H), 7.63 (t, J=7.8, 7.8, 1H), 7.92 (br. s, 1H), 8.13 (s, 2H), 11.39 (s, 1H).
[668]
[669] Пример 57: (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид
[670] 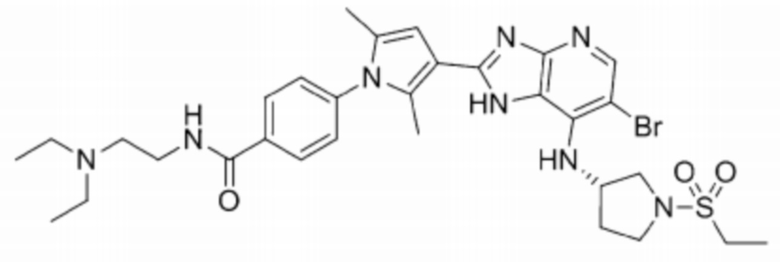
[671] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (m, 10H), 2.1 (s, 4H), 2.43 (m, 4H), 3.02 (m, 5H), 3.1 (br. s, 2H), 3.51 (m, 2H), 3.65 (m, 1H), 3.81 (m, 3H), 5.03 (d, J=8.2, 1H), 5.74 (br. s, 1H), 6.43 (s, 1H), 7.34 (d, J=8.2, 2H), 8.16 (m, 3H), 8.53 (br. s, 1H), 11.69 (br. s, 1H).
[672]
[673] Пример 58: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота
[674] 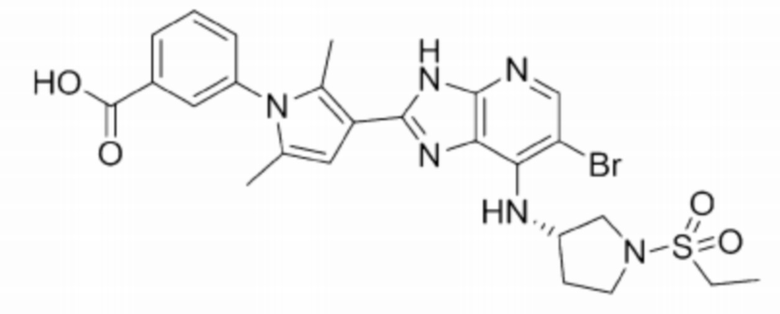
[675] 1H NMR (300 MHz, ДМСО-d 6) δ 1.18 (t, J=7.5, 7.5, 3H), 2 (br. s, 3H), 2.11 (br. s, 1 H), 2.31 (br. s, 1H), 2.39 (br. s, 3H), 3.1 (m, 3H), 3.3 (m, 2H), 3.5 (m, 1H), 3.67 (m, 1H), 5.63 (m, 1H), 5.78 (d, J=7.6, 1H), 6.61 (s, 1H), 7.57 (br. s, 1H), 7.65 (m, 1H), 7.77 (s, 1H), 7.98 (s, 1H), 8.05 (d, J=8.6, 1H), 12.75 (br. s, 1H).
[676]
[677] Пример 59: (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота
[678] 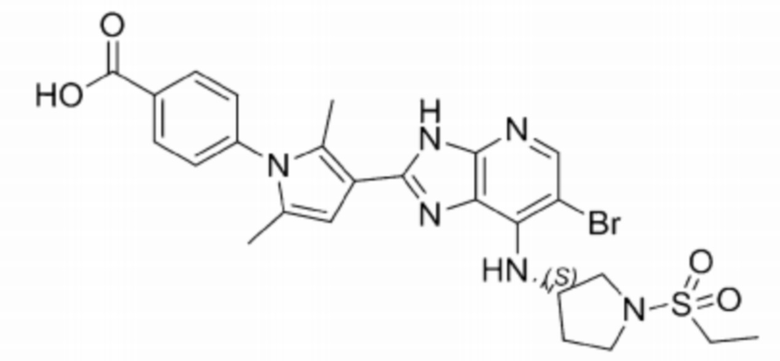
[679] 1H NMR (300 MHz, ДМСО-d 6) δ 1.19 (t, J=7.3, 7.3, 3H), 2.03 (s, 3H), 2.13 (m, 1H), 2.32 (m, 1H), 2.42 (s, 3H), 3.1 (m, 3H), 3.48 (m, 2H), 3.52 (m, 1H), 3.69 (m, 1H), 5.64 (m, 1H), 5.78 (d, J=8.4, 1H), 6.62 (s, 1H), 7.47 (d, J=8.3, 2H), 7.98 (s, 1H), 8.1 (d, J=8.4, 2H), 12.75 (s, 1H).
[680]
[681] Пример 60: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-((диметиламино)метил)бензамид
[682] 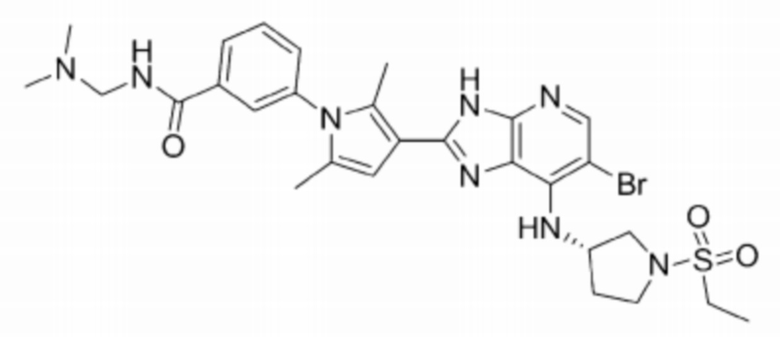
[683] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.4, 7.4; 3H), 2.09 (s, 4H), 2.38 (m, 6H), 2.44 (s, 3H), 2.49 (m, 1H), 2.68 (d, J=4.8; 2H), 3.03 (dt, J=11.5, 7.3, 7.3, 2H), 3.56 (m, 5H), 3.84 (dd, J=10.7,5.7; 1H), 5.02 (d, J=8.1; 1H), 5.73 (m, 1H), 6.41 (s, 1H), 7.26 (m, 1H), 7.39 (d, J=7.5; 1H), 7.6 (t, J=7.8, 7.8; 1H), 7.77 (s, 1H), 7.93 (d, J=7.5; 1H), 8.14 (s, 1H), 11.65 (br. s, 1H).
[684]
[685] Пример 61: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид
[686] 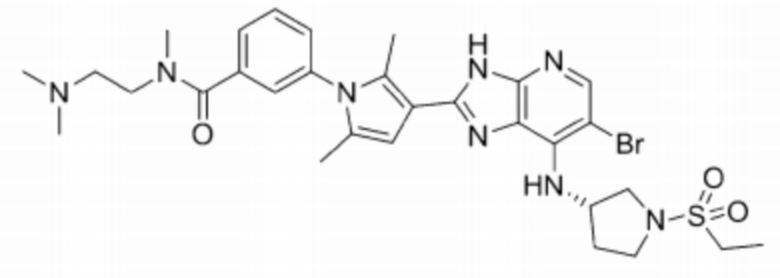
[687] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.4, 7.4, 3H),1.47 (br. s, 2H), 1.55 (m, 3H), 2.12(s, 4H), 2.47 (m, 4H), 2.51 (br. s, 3H), 3.03(m, 2H), 3.11(s, 3H), 3.56 (m, 4H), 3.84 (m, 2H), 5.03 (d, J=8.2, 1H), 5.74 (s, 1H), 6.42 (s, 1H), 7.33 (m, 2H), 7.59 (br. s, 2H), 8.15 (s, 1H), 11.82 (s, 1H).
[688]
[689] Пример 62: (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)бензамид
[690] 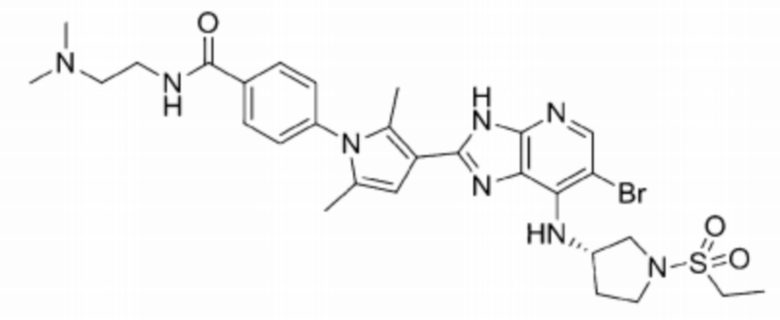
[691] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.5, 7.5, 3H), 2.11 (m, 4H), 2.34 (s, 6H), 2.48 (m, 4H), 2.61 (t, J=5.7, 5.7, 2H), 3.03 (m, 2H), 3.55 (m, 5H), 3.85 (dd, J=10.5, 5.6, 1H), 5.04 (d, J=7.7, 1H), 5.73 (br. s, 1H), 6.46 (s, 1H), 7.1 (br. s, 1H), 7.34 (d, J=8.2, 2H), 7.98 (d, J=8.2, 2H), 8.17 (s, 1H), 12.37(br. s, 1H).
[692]
[693] Пример 63: (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид
[694] 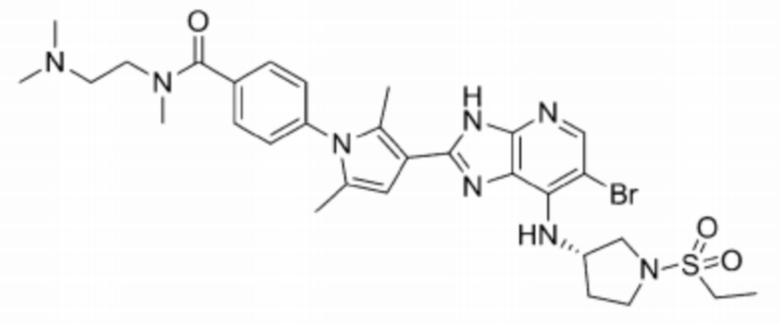
[695] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.4, 7.4; 3H), 2.12 (s, 7H), 2.46 (m, 8H), 2.67 (br. s; 1H), 3.03 (m, 5H), 3.57(m, 5H), 3.85 (dd, J=10.6, 5.7, 1H), 5.05 (d, J=7.9, 1H), 5.74 (m, 1H), 6.48 (s, 1H), 7.32 (m, J=8.0, 2H), 7.6 (m, J=7.9, 2H), 8.17 (s, 1H), 12.76 (br. s, 1H).
[696]
[697] Пример 64: (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(диметиламино)ацетамид
[698] 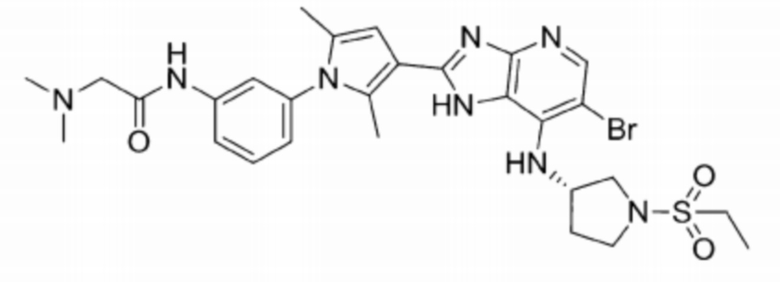
[699] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.5, 3 H), 2.10 (m, 1 H), 2.46 (m, 12 H), 3.03 (m, 2 H), 3.11 (s, 2 H), 3.54 (m, 4 H), 3.85 (m, 1 H), 5.02 (d, J=7.7, 1 H), 5.75 (m, 1 H), 6.41 (s, 1 H), 7.01 (d, J=8.0, 1 H), 7.47 (t, J=7.9, 1 H), 7.64 (m, 2 H), 8.16 (s, 1 H), 9.30 (s, 1 H), 12.11 (br. s., 1 H).
[700]
[701] Пример 65: (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(4-метилпиперазин-1-ил)ацетамид
[702] 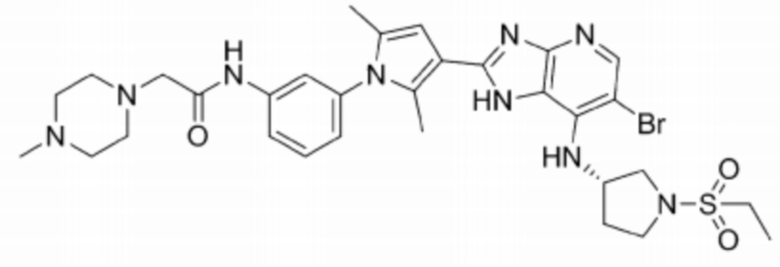
[703] 1H NMR (300 MHz, ДМСО-d 6) δ 1.19 (t, J=7.5, 3 H), 2.02 (s, 3 H), 2.13 (m, 1 H), 2.31 (m, 1 H), 2.40 (m, 6 H), 2.64 (m, 8 H), 3.09 (q, J=8.0, 2 H), 3.20 (s, 2 H), 3.27 (m, 1 H), 3.36 (m, 1 H), 3.51 (m, 1 H), 3.67 (m, 1 H), 5.64 (m, 1 H), 5.78 (d, J=8.0, 1 H), 6.59 (s, 1 H), 7.06 (d, J=8.0, 1 H), 7.50 (t, J=8.1, 1 H), 7.71 (m, 2 H), 7.98 (s, 1 H), 9.95 (s, 1 H), 12.72 (br. s., 1 H).
[704]
[705] Пример 66: (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-морфолиноацетамид
[706] 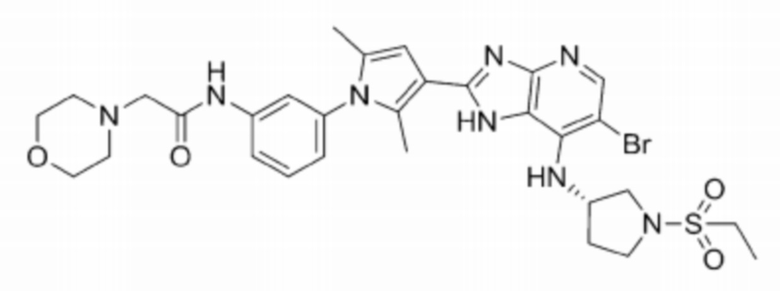
[707] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.38 (t, J=7.5, 3 H), 2.09 (m, 1 H), 2.16 (s, 3 H), 2.48 (m, 4 H), 2.67 (m, 4 H), 3.04 (m, 2 H), 3.20 (s, 2 H), 3.58 (m, 3 H), 3.81 (m, 4 H), 3.89 (m, 1 H), 5.04 (d, J=7.4, 1 H), 5.76 (m, 1 H), 6.45 (s, 1 H), 7.05 (d, J=7.5, 1 H), 7.50 (t, J=7.8, 1 H), 7.64 (m, 2 H), 8.19 (m, 1 H), 9.24 (m, 1 H), 12.38 (m, 1 H).
[708]
[709] Пример 67: (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон
[710] 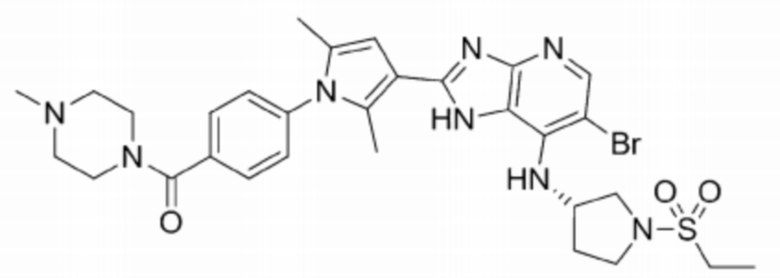
[711] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.39 (t, J=7.3, 7.3, 2.14 (s, 4H), 2.37 (s, 3H), 2.48 (br. s, 8H), 3.05 (m, 2H), 3.58 (m, 5H), 3.89 (m, 3H), 5.07 (m, 1H), 5.74 (br. s, 1H), 6.46 (s, 1H), 7.34 (m, 2H), 7.6 (d, J=7.5, 2H), 8.18 (s, 1H), 12.14 (m, 1H).
[712]
[713] Пример 68: (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон
[714] 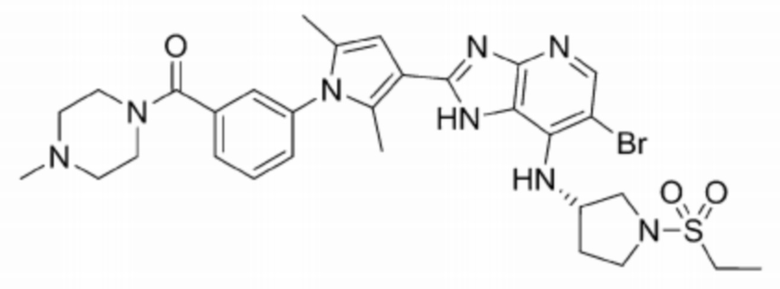
[715] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.38 (t, J=7.4, 7.4, 3H), 2.14 (s, 4H), 2.35 (s, 3H), 2.48 (m, 8H), 3.05 (m, 2H), 3.57 (m, 5H), 3.88 (m, 3H), 5.06 (d, J=7.5, 1H), 5.75 (br. s, 1H), 6.45 (s, 1H), 7.35 (m, 2H), 7.59 (m, 2H), 8.16 (s, 1H), 12.12 (br. s, 1H).
[716]
[717] Пример 69: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид
[718] 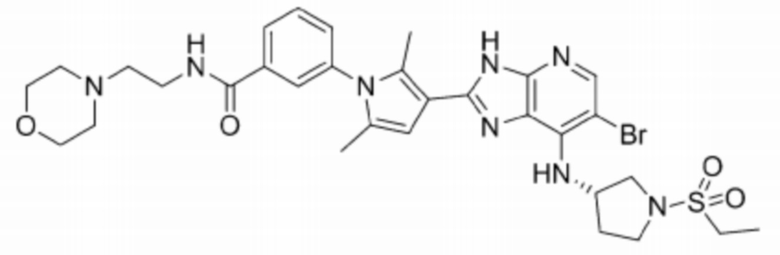
[719] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.0, 7.0, 3H), 2.11(m, 4H), 2.45(m, 4H), 2.53 (br. s, 4H), 2.64 (t, J=6.0, 6.0, 2H), 3.02(m, 2H), 3.47 (dd, J=10.3, 4.1, 1H), 3.63(m, 4H), 3.74 (t, J=4.3, 4.3, 4H), 3.86 (dd, J= 10.6, 5.9, 1H), 5.04 (d, J=8, 1H), 5.73 (br. s, 1H), 6.46 (s, 1H), 6.84 (br. s, 1H), 7.43 (d, J=7.8, 1H), 7.63 (t, J=7.8, 7.8, 1H), 7.74 (s, 1H), 7.86 (d, J=7.7, 1H), 8.17 (s, 1H), 12.18 (br. s, 1H).
[720]
[721] Пример 70: (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид
[722] 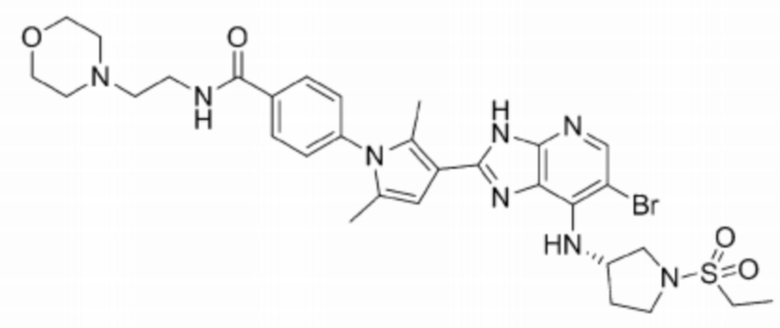
[723] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.5, 7.5, 3H), 2.09 (m, 4H), 2.47 (m, 4H), 2.56 (br. s, 4H), 2.68 (m, 2H), 3.03 (m, 2H), 3.48 (m, 1H), 3.61 (m, 4H), 3.77 (m, 4H), 3.87 (dd, J=10.4, 5.6, 1H), 5.04 (d, J=7.5, 1H), 5.72 (br. s, 1H), 6.46 (s, 1H), 6.9 (br. s, 1H), 7.36 (d, J=7.8, 2H), 7.95 (d, J=7.8, 2H), 8.17 (s, 1H), 12.22 (br. s, 1H).
[724]
[725] Пример 71: (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид
[726] 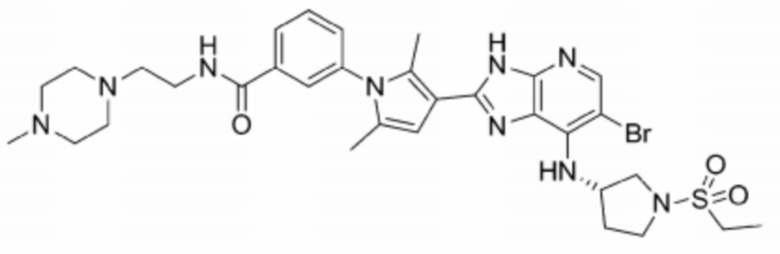
[727] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.4, 7.4, 3H), 2.1 (m, 4H), 2.36 (s, 3H), 2.46 (s, 4H), 2.6 (br. s, 4H), 2.72 (m, 6H), 3.02 (m, 2H), 3.48 (m, 1H), 3.6 (m, 4H), 3.86 (dd, J=10.8, 6.1, 1H), 5.03 (d, J=7.4, 1H) 5.74 (br. s, 1H), 6.44 (s, 1H), 7.13 (br. s, 1H), 7.41 (d, J=7.8, 1H), 7.62 (t, J=7.7, 7.7, 1H), 7.77 (s, 1H), 7.91 (d, J=7.2, 1H), 8.16 (s, 1H), 11.92 (s, 1H).
[728]
[729] Пример 72: (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид
[730] 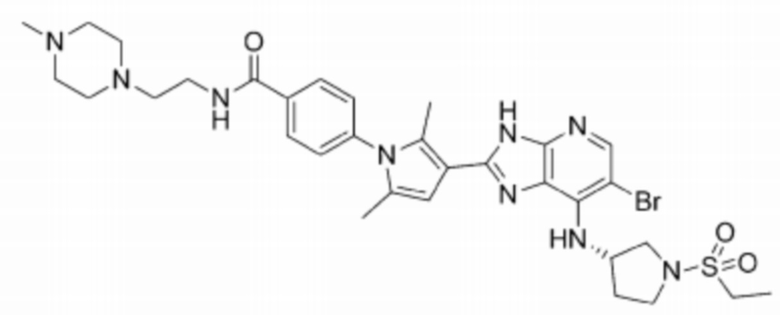
[731] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.3, 7.3, 3H), 2.14 (s, 4H), 2.33 (s, 3H), 2.48 (m, 8H), 2.63 (m, 6H), 3.04 (m, 2H), 3.5 (m, 1H), 3.61 (m, 4H), 3.87 (m, 1H), 5.07 (d, J=7.4, 1H) 5.74 (br. s, 1H), 6.48 (s, 1H), 6.96 (br. s, 1H), 7.37 (d, J=7.8, 2H), 7.96 (d, J=7.7, 2H), 8.18 (s, 1H), 12.39 (br. s, 1H).
[732]
[733] Пример 73: N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(диметиламино)ацетамид
[734] 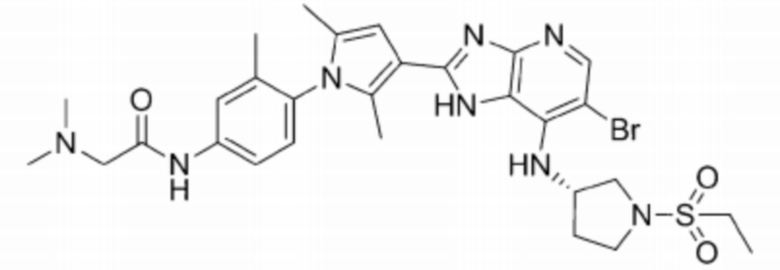
[735] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.4, 3 H), 2.02 (s, 6 H), 2.10 (m, 1 H), 2.36 (s, 3 H), 2.42 (s, 6 H), 2.48 (m, 1 H), 3.02 (m, 2 H), 3.13 (s, 2 H), 3.55 (m, 3 H), 3.84 (m, 1 H), 5.01 (d, J=7.7, 1 H), 5.76 (m, 1 H), 6.44 (s, 1 H), 7.16 (d, J=8.4, 1 H), 7.52 (m, 2 H), 8.16 (s, 1 H), 9.25 (s, 1 H), 12.05 (br. s, 1 H).
[736]
[737] Пример 74: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид
[738] 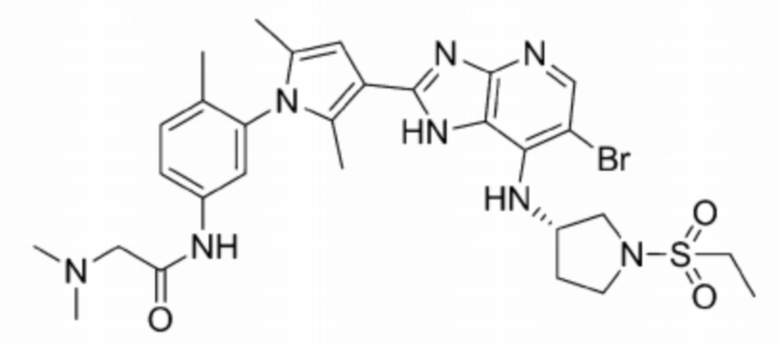
[739] 1H NMR (300 MHz, ДМСО-d 6) δ 1.18 (t, J=7.3, 3 H), 1.88 (s, 3 H), 1.91 (s, 3 H), 2.10 (m, 1 H), 2.27 (s, 6H), 2.29 (s, 3H), 2.33 (m, 1H), 3.08 (m, 4H), 3.29 (m, 1 H), 3.35 (m, 1H), 3.48 (m, 1H), 3.68 (m, 1H), 5.63 (m, 1H), 5.75 (m, 1H), 6.61 (s, 1H), 7.37 (d, J=8.1, 1H), 7.65 (m, 2 H), 7.97 (s, 1H), 9.88 (s, 1H), 12.71 (s, 1H).
[740]
[741] Пример 75: N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид
[742] 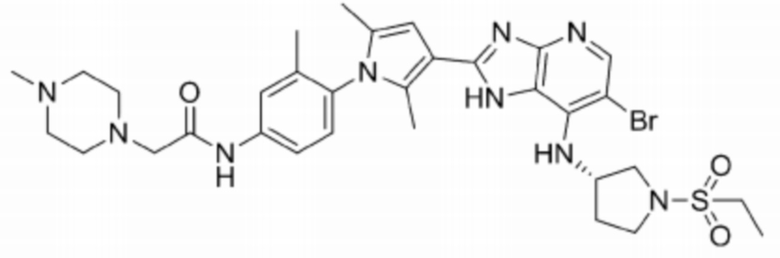
[743] 1H NMR (300 MHz, ДМСО-d 6) δ 1.18 (t, J=7.3, 3 H), 1.89 (m, 6 H), 2.10 (m, 1 H), 2.18 (s, 3 H), 2.29 (s, 3 H), 2.38 (m, 5 H), 2.53 (m, 4 H), 3.08 (q, J=7.2, 2 H), 3.14 (s, 2 H), 3.28 (m, 1 H), 3.30 (m, 1H), 3.49 (m, 1 H), 3.68 (m, 1 H), 5.65 (m, 1 H), 5.76 (d, J=7.5, 1 H), 6.60 (s, 1 H), 7.18 (d, J=8.1, 1 H), 7.68 (m, 2 H), 7.97 (s, 1 H), 9.85 (s, 1 H), 12.70 (s, 1 H).
[744]
[745] Пример 76: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид
[746] 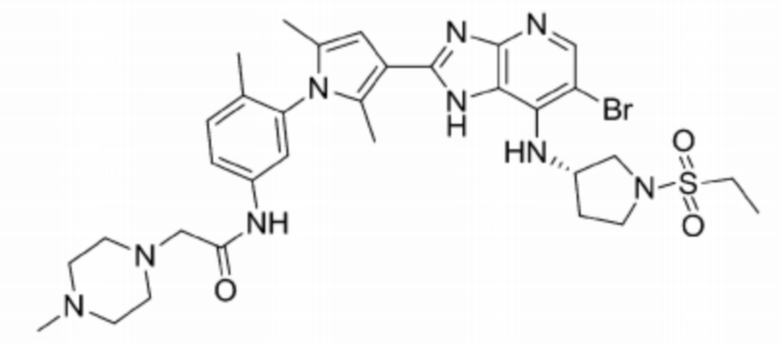
[747] 1H NMR (300 MHz, ДМСО-d 6) δ 1.18 (t, J=7.3, 3 H), 1.88 (s, 3 H), 1.91 (s, 3 H), 2.13 (m, 1 H), 2.29 (s, 3 H), 2.37 (m, 4 H), 2.62 (m, 8 H), 3.08 (q, J=7.2, 2 H), 3.18 (s, 2 H), 3.30 (m, 2H), 3.50 (m, 1 H), 3.69 (m, 1 H), 5.65 (m, 1 H), 5.76 (s, 1 H), 6.61 (s, 1 H), 7.39 (d, J=8.3, 1 H), 7.61 (m, 2 H), 7.97 (m, 1 H), 9.86 (s, 1 H), 12.72 (s, 1 H).
[748]
[749] Пример 77: N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-морфолиноацетамид
[750] 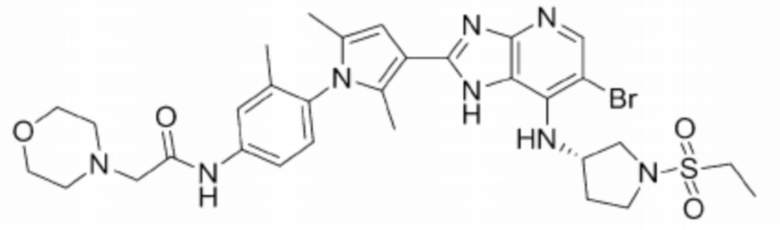
[751] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.3, 3 H), 2.01 (s, 3 H), 2.03 (s, 3 H), 2.10 (m, 1 H), 2.35 (s, 3 H), 2.48 (m, 1 H), 2.67 (t, J=4.9, 4 H), 3.02 (m, 2 H), 3.20 (s, 2 H), 3.55 (m, 3 H), 3.84 (m, 5 H), 5.01 (d, J=8.1, 1 H), 5.74 (m, 1 H), 6.42 (s, 1 H), 7.16 (d, J=8.3, 1 H), 7.59 (m, 2 H), 8.15 (s, 1 H), 9.19 (s, 1 H), 11.70 (br. s., 1 H).
[752]
[753] Пример 78: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид
[754] 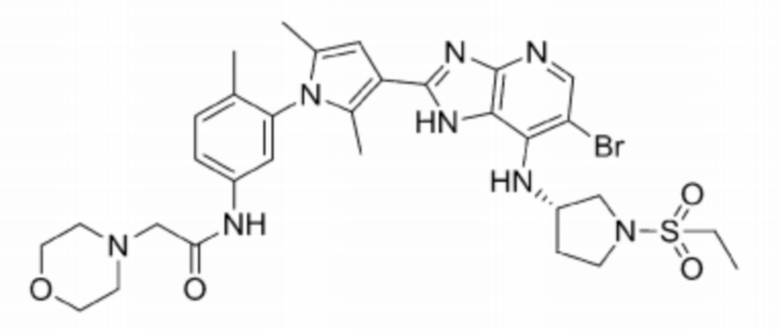
[755] 1H NMR (300 MHz, ДМСО-d 6) δ 1.18 (t, J=7.5, 3 H), 1.88 (s, 3 H), 1.91 (s, 3 H), 2.12 (m, 1 H), 2.31 (m, 4 H), 2.5 (m, 4H), 3.09 (m, 4 H), 3.2 (m, 2H), 3.47 (m, 1 H), 3.65 (m, 5 H), 5.64 (m, 1 H), 5.76 (d, J=8.1, 1 H), 6.61 (s, 1 H), 7.39 (d, J=8.1, 1 H), 7.63 (m, 2 H), 7.97 (s, 1 H), 9.87 (s, 1 H), 12.71 (br. s, 1 H).
[756]
[757] Пример 79: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропенамид
[758] 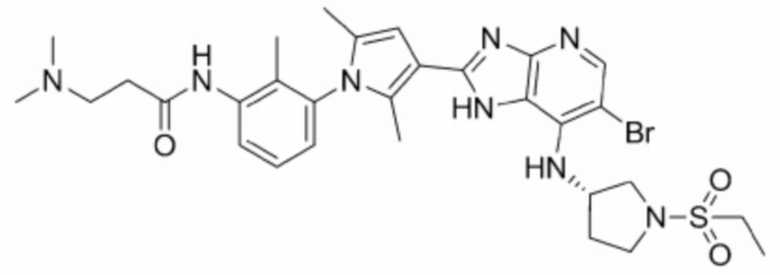
[759] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.4, 3 H), 2.01 (m, 6 H), 2.10 (m, 1 H), 2.35 (m, 3 H), 2.46 (m, 7 H), 2.54 (t, J=5.5, 2 H), 2.69 (t, J=5.5, 2 H), 3.03 (m, 2 H), 3.57 (m, 3 H), 3.84 (m, 1 H), 5.01 (d, J=7.7, 1 H), 5.75 (m, 1 H), 6.45 (s, 1 H), 7.12 (d, J=8.4, 1 H), 7.50 (m, 2 H), 8.17 (s, 1 H), 11.22 (s, 1 H), 12.17 (m, 1 H).
[760]
[761] Пример 80: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-3-(диметиламино)пропенамид
[762] 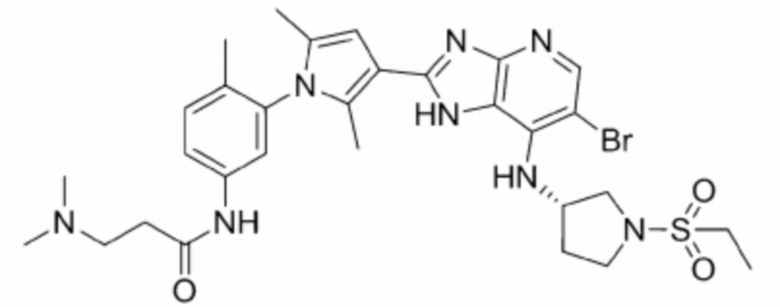
[763] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.5, 3 H), 1.96 (s, 3 H), 2.02 (s, 3 H), 2.06 (m, 1 H), 2.37 (s, 3 H), 2.44 (m, 7 H), 2.58 (t, J=5.5, 2 H), 2.76 (t, J=5.5, 2 H), 3.03 (m, 2 H), 3.54 (m, 3 H), 3.85 (m, 1 H), 5.00 (d, J=7.5, 1 H), 5.73 (m, 1H), 6.41 (s, 1 H), 7.29 (d, J=8.0, 1 H), 7.51 (m, 2 H), 8.14 (s, 1 H), 10.94 (s, 1 H), 11.41 (br. s, 1 H).
[764]
[765] Пример 81: (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(4-метилпиперазин-1-ил)метанон
[766] 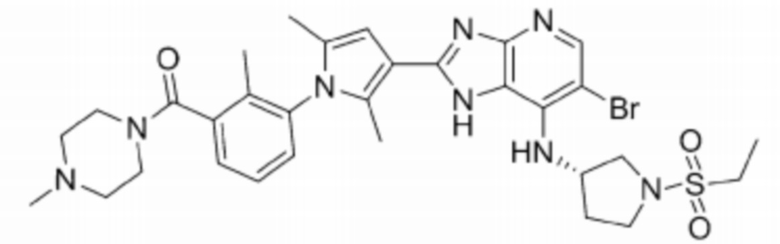
[767] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.5, 7.5, 3H), 1.97 (s, 3H), 2 (s, 1H), 2.03 (s, 2H), 2.09 (m, 1H), 2.35 (m, 9H), 2.51 (br. s, 3H), 3.02 (m, 2H), 3.28 (br. s, 2H), 3.54 (m, 3H), 3.88 (m, 3H), 5 (d, J=7.8, 1H), 5.74 (br. s, 1H), 6.47 (d, J=6.4, 1H), 7.34 (m, 1H), 7.41 (m, 1H), 8.17 (s, 1H), 12.07 (br. s, 1H).
[768]
[769] Пример 82: 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-2-метилбензамид
[770] 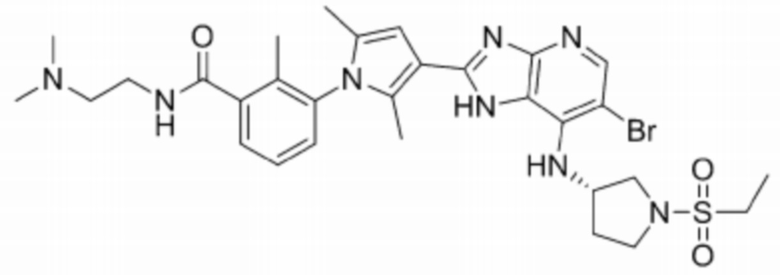
[771] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.4, 7.4, 3H), 2.01 (s, 3H), 2.1 (m, 4H), 2.34 (s, 5H), 2.36 (s, 3H), 2.47 (dd, J=12.8,7.2, 2H), 2.62 (t, J=5.6, 2H), 3.02 (m, 2H), 3.57 (m, 5H), 3.84 (dd, J=10.5, 6.0, 1H), 5.02 (d, J=8.0, 1H), 5.74 (d, J=11.9, 1H), 6.46 (s, 1H), 6.7 (br. s, 1H), 7.26 (m, 1H) 7.37(t, J=7.9, 7.9, 1H), 7.54 (d, J=7.7, 1H), 8.16 (s, 1H), 12.1 (br. s, 1H).
[772]
[773] Пример 83: (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(морфолино)метанон
[774] 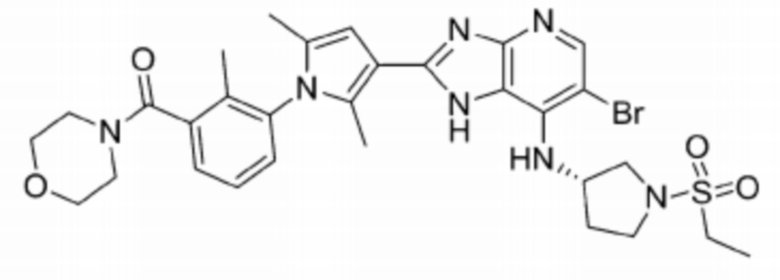
[775] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.4, 3H), 2.03 (m, 7H), 2.35 (m, 3H), 2.47 (m, 1H), 3.01 (m, 2H), 3.28 (br. s, 2H), 3.55 (m, 5H), 3.79 (br. s, 3H), 3.93 (m, 2H), 5.02 (m, 1H), 5.74 (br. s, 1H), 6.46 (m, 1H), 7.26 (m, 1H), 7.35 (m, 1H), 7.42 (m, 1H), 8.16 (s, 1H), 12.07 (br. s, 1H).
[776]
[777] Пример 84: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(диметиламино)ацетамид
[778] 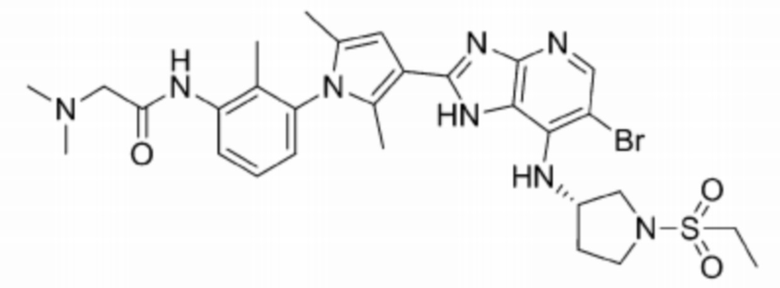
[779] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.3, 3 H), 1.92 (s, 3 H), 2.03 (s, 3 H), 2.11 (m, 1 H), 2.37 (s, 3 H), 2.46 (m, 7 H), 3.03 (m, 2 H), 3.17 (s, 2 H), 3.56 (m, 3 H), 3.85 (m, 1 H), 5.03 (d, J=7.9, 1 H), 5.76 (m, 1 H), 6.50 (s, 1 H), 7.02 (m, J=8.0, 1 H), 7.38 (t, J=7.5, 1 H), 8.19 (s, 1 H), 8.28 (t, J=7.50 Hz, 1 H), 9.43 (d, J=8.1, 1 H), 12.74 (s, 1 H).
[780]
[781] Пример 85: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-морфолиноацетамид
[782] 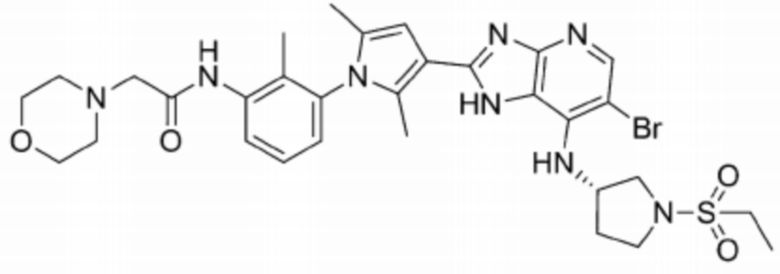
[783] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.5, 3 H), 1.93 (s, 3 H), 2.01 (s, 3 H), 2.12 (m, 1 H), 2.36 (s, 3 H), 2.47 (m, 1 H), 2.70 (t, J=5.0, 4 H), 3.02 (m, 2 H), 3.24 (s, 2 H), 3.46 (m, 1 H), 3.61 (m, 2 H), 3.77 (t, J=5.0, 4 H), 3.87 (m, 1 H), 5.01 (m, 1 H), 5.70 (m, 1 H), 6.43 (s, 1 H), 7.03 (m, 1 H), 7.39 (t, J=7.7, 1 H), 8.16 (s, 1 H), 8.34 (m, 1 H), 9.43 (d, J=6.7, 1 H), 11.57 (br. s, 1 H).
[784]
[785] Пример 86: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропанамид
[786] 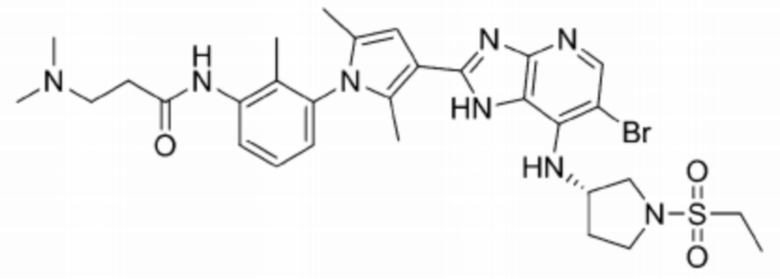
[787] 1H NMR (300 MHz, ДМСО-d 6) δ 1.18 (t, J=7.5, 3 H), 1.76 (s, 3 H), 1.89 (s, 3 H), 2.10 (m, 1 H), 2.22 (s, 6 H), 2.29 (m, 4 H), 2.50 (m, 2H), 2.59 (m, 2 H), 3.08 (m, 2 H), 3.29 (m, 1 H), 3.33(m, 1H), 3.48 (m, 1 H), 3.69 (m, 1 H), 5.64 (m, 1 H), 5.73 (m, J=1.1, 1 H), 6.61 (s, 1 H), 7.05 (d, J=8.1, 1 H), 7.36 (t, J=8.1, 1 H), 7.94 (m, 2 H), 10.27 (s, 1 H), 12.72 (br. s, 1 H).
[788]
[789] Пример 87: N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид
[790] 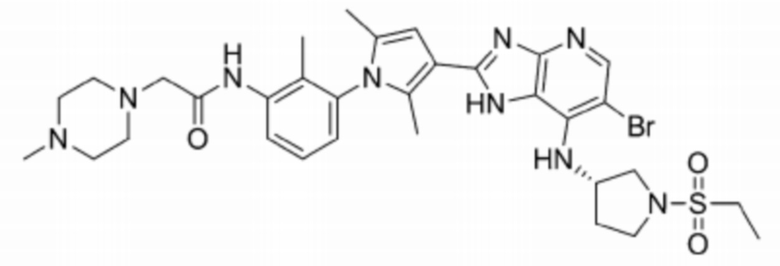
[791] 1H NMR (300 MHz, ДМСО-d 6) δ 1.18 (t, J=7.5, 3 H), 1.80 (s, 3 H), 1.90 (s, 3 H), 2.15 (m, 4 H), 2.33 (m, 8 H), 2.59 (m, 4 H), 3.09 (m, 2 H), 3.15 (s, 2 H), 3.26 (m, 1 H), 3.38 (m, 1 H), 3.48 (m, 1 H), 3.68 (m, 1 H), 5.64 (m, 1 H), 5.77 (d, J=7.5, 1 H), 6.62 (s, 1 H), 7.07 (m, 1 H), 7.39 (s, 1 H), 7.97 (m, 2 H), 9.58 (s, 1 H), 12.72 (s, 1 H).
[792]
[793] Далее, соединения по Примерам с 88 по 90 были синтезированы в соответствии с репрезентативным методом синтеза 3.
[794]
[795] Пример 88: N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид
[796] 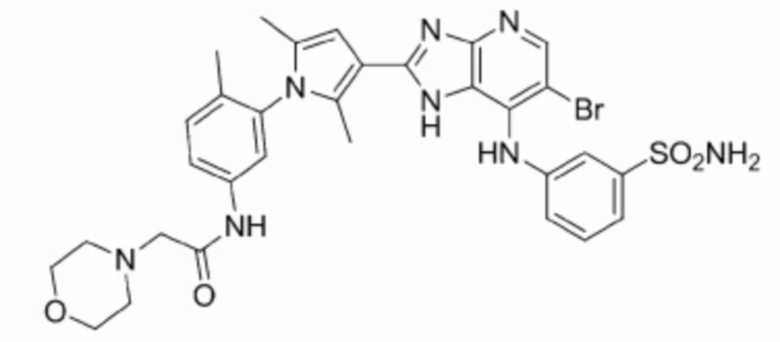
[797] 1H NMR (300 MHz, ДМСО-d 6) δ 1.82 (s, 3 H), 1.89 (s, 3 H), 1.97 (s, 3 H), 2.5 (m, 4H), 3.13 (s, 2 H), 3.64 (t, J=5.0, 4 H), 6.60 (s, 1 H), 7.18 (s, 2 H), 7.31 (m, 4 H), 7.55 (s, 2 H), 7.66 (m, 1 H), 8.20 (s, 1 H), 8.51 (s, 1 H), 9.87 (s, 1 H), 12.84 (br. s, 2H).
[798]
[799] Пример 89: N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид
[800] 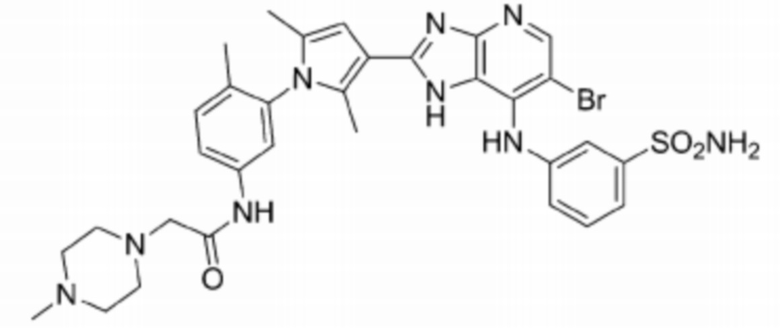
[801] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.90 (s, 3 H), 1.96 (s, 3 H), 2.02 (s, 3 H), 2.33 (s, 3 H), 2.52 (m, 4 H), 2.68 (m, 4 H), 3.17 (br. s., 2 H), 5.49 (br. s, 2 H), 6.19 (br. s, 1 H), 6.85 (br. s, 1 H), 7.40 (m, 7 H), 8.16 (s, 1 H), 9.23 (s, 1 H).
[802]
[803] Пример 90: N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид
[804] 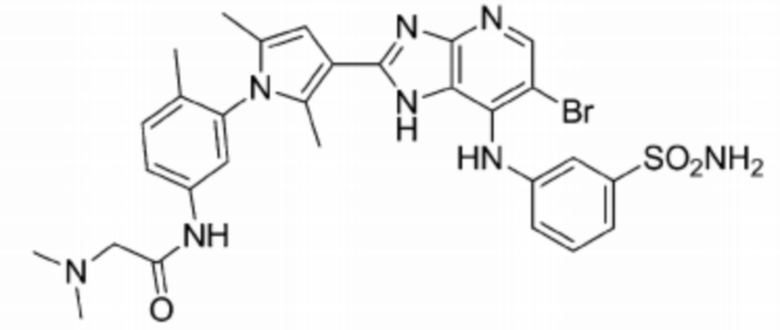
[805] 1H NMR (300 MHz, ДМСО-d 6) δ 1.81 (s, 3H), 1.87 (s, 3H), 2 (m, 3H), 2.27 (s, 6H), 3.07 (s, 2H), 6.58 (s, 1H), 7.18 (br. s, 2H), 7.3 (m, 3H), 7.57 (m, 2H), 7.65 (s, 1H), 7.72 (m, 1H), 8.17 (br. s, 1H), 8.53 (br. s, 1H), 9.88(s, 1H), 12.95 (br. s, 1H).
[806]
[807] Далее, соединения по Примерам с 91 по 93 были синтезированы в соответствии с репрезентативным методом синтеза 1.
[808]
[809] Пример 91: (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(морфолино)метанон
[810] 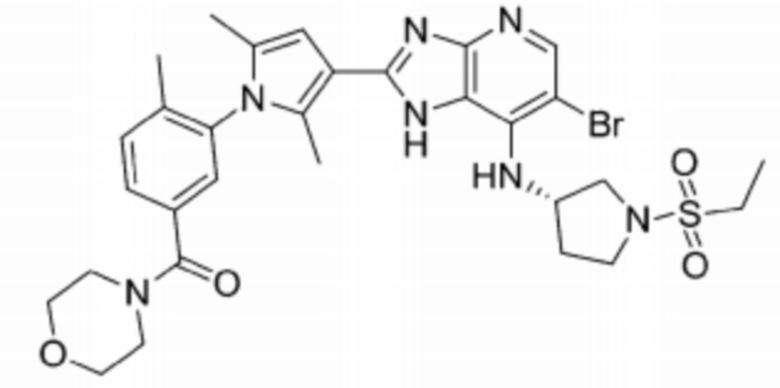
[811] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.38 (t, J=7.5, 3 H), 2.06 (m, 7 H), 2.39 (s, 3 H), 2.48 (m, 1 H), 3.03 (m, 2 H), 3.67 (m, 12 H), 5.05 (d, J=7.5, 1 H), 5.76 (m, 1 H), 6.53 (s, 1 H), 7.26 (m, 1H), 7.49 (m, 2 H), 8.20 (s, 1 H), 13.00 (s, 1 H).
[812]
[813] Пример 92: (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(4-метилпиперазин-1-ил)метанон
[814] 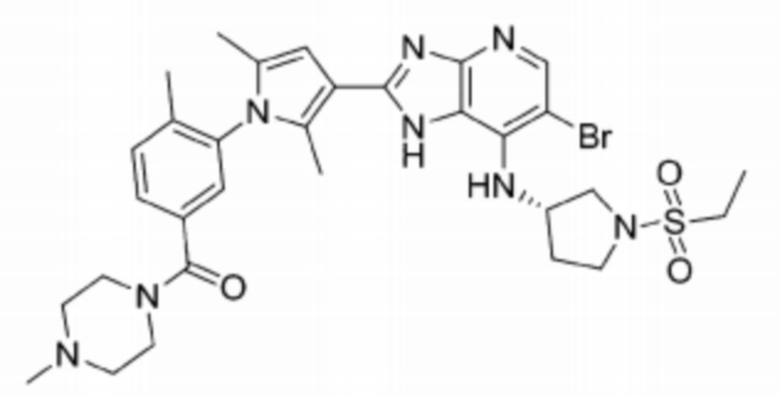
[815] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.5, 3 H), 2.06 (m, 7 H), 2.36 (m, 11 H), 3.02 (m, 2 H), 3.68 (m, 8 H), 5.03 (d, J=7.5, 1 H), 5.74 (m, 1 H), 6.48 (s, 1 H), 7.26 (m, 1H), 7.47 (m, 2 H), 8.17 (s, 1 H), 12.21 (br. s, 1 H).
[816]
[817] Пример 93: 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид
[818] 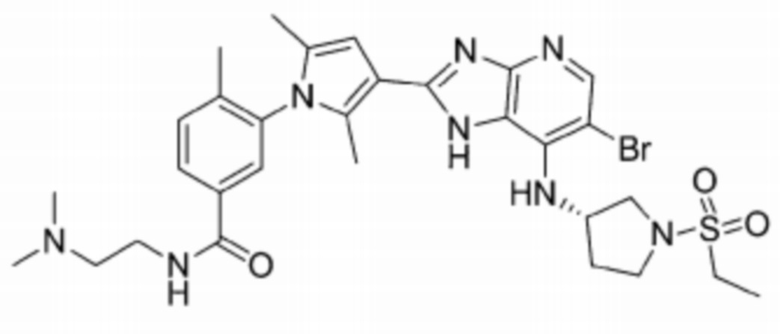
[819] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.36 (t, J=7.5, 3 H), 2.02 (s, 3 H), 2.07 (s, 3 H), 2.31 (m, 10 H), 2.47 (m, 1 H), 2.54 (m, 2 H), 3.03 (m, 2 H), 3.55 (m, 5 H), 3.84 (m, 1 H), 5.03 (d, J=7.5, 1 H), 5.75 (m, 1 H), 6.49 (s, 1 H), 6.88 (br. s., 1 H), 7.46 (d, J=8.20 Hz, 1 H), 7.65 (d, J=6.1, 1 H), 7.84 (t, J=7.26 Hz, 1 H), 8.18 (s, 1 H), 12.36 (br. s, 1 H).
[820]
[821] Далее, соединения по Примерам с 94 по 96 были синтезированы в соответствии с репрезентативным методом синтеза 3.
[822]
[823] Пример 94: 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[824] 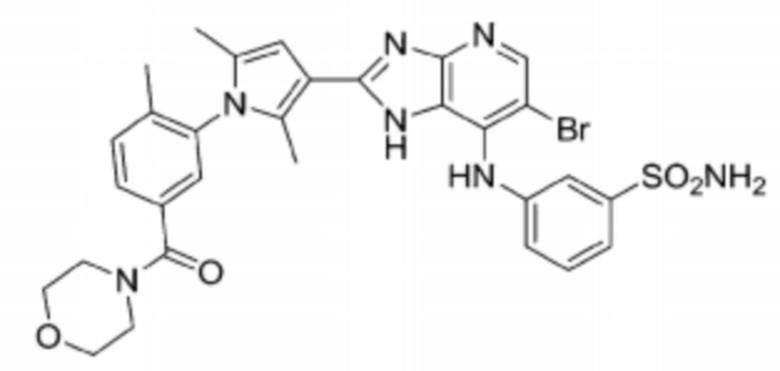
[825] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.92 (s, 3 H), 1.98 (s, 3 H), 2.05 (br. s, 3 H), 3.70 (m, 8 H), 5.62 (br. s, 2 H), 6.22 (br. s, 1 H), 6.81 (br. s, 1 H), 7.17 (br. s, 1 H), 7.41 (m, 4 H), 7.56 (br. s, 1 H), 7.80 (br. s, 1 H), 8.11 (br. s, 1 H).
[826]
[827] Пример 95: 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(4-метилпиперазин-1-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид
[828] 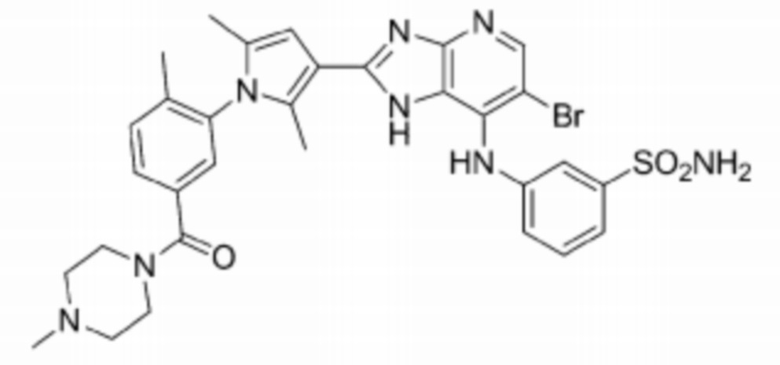
[829] 1H NMR (300 MHz, ДМСО-d 6) δ 1.87 (s, 3 H), 1.90 (s, 3 H), 2.00 (br. s, 3 H), 2.18 (m, 4 H), 2.31 (m, 4 H), 3.59 (br. s, 3 H), 6.60 (br. s, 1 H), 7.24 (m, 6 H), 7.49 (m, 3 H), 8.18 (s, 1 H), 8.50 (br. s, 1H), 12.79(br. s, 1H).
[830]
[831] Пример 96: 3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид
[832] 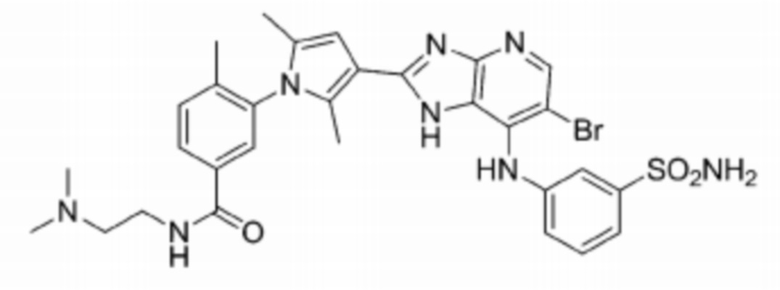
[833] 1H NMR (300 MHz, ДМСО-d 6) δ 1.88 (s, 3H), 1.93 (s, 3H), 2.01 (s, 3H), 2.16 (s, 6H), 2.38 (t, J=7.5, 2H), 3.2 (t, 2H), 6.61 (s, 1H), 7.15 (br. s, 2H), 7.31 (m, 3H), 7.52 (m, 2H), 7.68 (s, 1H), 7.90 (m, 1H), 8.19 (s, 1H), 8.48 (m, 2H), 12.87 (br. s, 1H).
[834]
[835] Далее, соединения по Примерам 97 и 98 были синтезированы в соответствии с репрезентативным методом синтеза 1.
[836]
[837] Пример 97: (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(4-метилпиперазин-1-ил)метанон
[838] 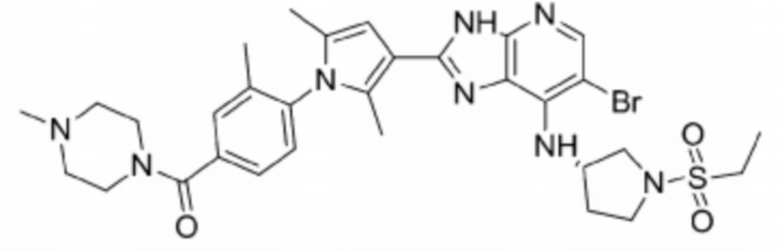
[839] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.3, 7.3, 3H), 2.01 (s, 3H), 2.05 (s, 3H), 2.36 (s, 7H), 2.47 (m, 6H), 3.03 (m, 2H), 3.55 (m, 5H, 3.85 (m, 3H), 5.01 (d, J=7.3, 1H), 5.73 (m, 1H), 6.53 (s, 1H), 7.22 (br. s, 1H), 7.37 (d, J=10, 1H), 7.46 (br. s, 1H), 8.15 (s, 1H), 11.46 (br. s, 1H).
[840]
[841] Пример 98: (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(морфолино)метанон
[842] 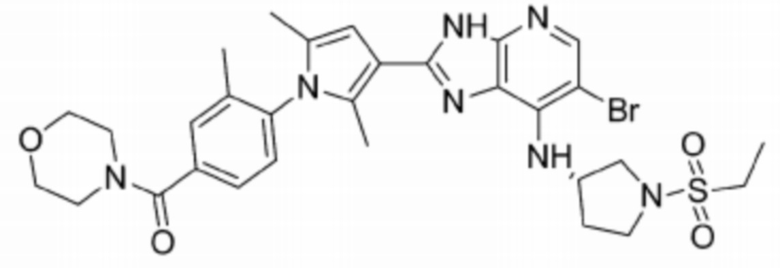
[843] 1H NMR (300 MHz, ХЛОРОФОРМ-d) δ 1.37 (t, J=7.6, 7.6, 3H), 2.01 (br. s, 3H), 2.06 (br. s, 4H) 2.37 (br. s, 3H), 2.46 (br. s, 1H), 3.02 (m, 2H), 3.45 (m, 1H), 3.61 (m, 3H), 3.78 (br. s, 5H), 3.89 (m, 2H), 5.01 (d, J=7.8, 1H), 5.72 (br. s, 1H), 6.45 (s, 1H) 7.22 (br. s, 1H), 7.26 (m, 1H), 7.36 (m, 1H), 7.47 (m, 1H), 8.17 (s, 1H), 11.92 (br. s, 1H).
[844]
[845] <Экспериментальный пример 1> Оценка ингибирующего действия ферментных единиц
[846] Чтобы измерить ингибирующее действие соединений из примеров выше на киназу, был проведен анализ в соответствии с протоколом для каждой киназы.
[847] (1) MLK1 (человек)
[848] Протеинкиназа MLK1 и соединения добавлялись в буферную систему, содержащую 8 мM MOPS pH 7.0, 0.2 мM ЭДТА, 2 мг/мл казеина, 10 мМ ацетата магния и [γ-33P]-ATФ, и затем в систему добавлялась смесь Mg/ATФ для инициирования реакции. После культивирования при комнатной температуре в течение 40 минут, добавляли 0,5% фосфорную кислоту для прекращения реакции. 10 μл реакционной смеси выкладывали на плоский фильтр P30 и промывали четыре раза в 0.425% фосфорной кислоте в течение общего времени 4 минуты. После однократной промывки в метаноле плоский фильтр высушивался и сцинтиллировался.
[849] (2) MLK2 (человек)
[850] Протеинкиназа MLK2 и соединения добавлялись в буферную систему, содержащую 8 мM МОПС pH 7.0, 0.2 мМ ЭДTA, 0.33 мг/мл основного белка миелина, 10 мМ ацетата магния и [γ-33P]-ATФ, и затем в систему добавлялась смесь Mg/ATФ для инициирования реакции. После культивирования при комнатной температуре в течение 40 минут, добавляли 0,5% фосфорную кислоту для прекращения реакции. 10 μл реакционной смеси выкладывали на плоский фильтр P30 и промывали четыре раза в 0.425% фосфорной кислоте в течение общего времени 4 минуты. После однократной промывки в метаноле плоский фильтр высушивался и сцинтиллировался.
[851] (3) MLK3 (человек)
[852] Протеинкиназа MLK3 и соединения добавлялись в буферную систему, содержащую 8 мM МОПС pH 7.0, 0.2 мМ ЭДTA, 0.33 мг/мл основного белка миелина, 5 мM ДTT, 10 мМ ацетата магния и [γ-33P]-ATФ, и затем в систему добавлялась смесь Mg/ATФ для инициирования реакции. После культивирования при комнатной температуре в течение 120 минут, добавляли 0,5% фосфорную кислоту для прекращения реакции. 10 μл реакционной смеси выкладывали на плоский фильтр P30 и промывали четыре раза в 0.425% фосфорной кислоте в течение общего времени 4 минуты. После однократной промывки в метаноле плоский фильтр высушивался и сцинтиллировался.
[853]
[854] Ингибирующие воздействия на MLK1, MLK2 и MLK3 соединений в соответствии с настоящим изобретением, приготовленных в примерах выше, были измерены, результаты показаны в Таблице 1 ниже. Для сведения: часть, помеченная "N.T.", означает "не проверялось (Not Tested)".
[856] В соответствии с результатами в Таблице 1 выше, подразумевается, что соединение по Формуле 1 в соответствии с настоящим изобретением обладало отличным ингибирующим воздействием на семейство MLK, в частности, на MLK3.
[857] <Экспериментальный пример 2> Идентификация механизма действия относительно ингибирования действия MLK3
[858] Чтобы идентифицировать механизм действия относительно ингибирования действия MLK3, обеспечиваемого данными соединениями, с использованием колонии клеток MDA-MB-231 рака груди человека, соединения по Примеру 7 подвергались обработке при концентрации 3 μM для определения схем фосфорилирования MKK3, p38, и паксиллина, которые являются белками-переносчиками субсигнала MLK3 с помощью белковых иммуноблотов. Результаты показаны на ФИГ. 1.
[859] Колония клеток наносилась на 6-луночный планшет с концентрацией 40 000 клеток на лунку, и по истечении 24 часов соединения из Примера 7 обрабатывались и культивировались в течение 60 часов. После этого культивированные клетки добавлялись в лизирующий буфер, раствор экстракта протеина (RIPA-буфер; Elpis Biotech), со смесью ингибиторов протеаз (каталожный № 88666) и со смесью ингибиторов фосфатазы (каталожный № A32957) от Pierce для растворения, далее производилось центрифугирование (14 000 об/мин) при 4°C в течение 15 минут для получения чистого протеина, остающегося в верхнем слое. Количество протеина определялось с использованием набора определения количества протеина с использованием BCA (бицинохиновой кислоты) (Bio-Rad); такое же количество протеина смешивалось с буфером для образца (Elpis Biotech), нагревалось при 100°C в течение 10 минут и отделялось от 10% ДСН-полиакриламидного геля. Последующая процедура основывалась на экспериментальном методе базового белкового иммуноблота, отделенный протеин переносился на ПВДФ-мембрану (Amersham Biosciences), a уровень экспрессии протеина с помощью микрофильтра ECL с использованием антител в рамках хемилюминесцентной системы визуализации Атто. Используемыми антителами были анти-MKK3 (8535), анти-фосфо-MKK3 (12280), анти-p38 (9212), анти-фосфо-p38 (9211), анти-паксиллин (2542), анти-фосфо-паксиллин (2541) от сигнальной системы клетки.
[860] В отношении ФИГ. 1, было определено, что соединения из примеров в соответствии с настоящим изобретением продемонстрировали эффект ингибирующего действия субпротеинов MLK3 путем ингибирования фосфорилирования of MLK3 и белков-переносчиков субсигнала MLK3.
[861]
[862] <Экспериментальный пример 3> Оценка 1 ингибирующего воздействия на развитие раковых клеток (фактор поражения раковых клеток)
[863] Чтобы определить, оказывает ли соединение противораковое воздействие, использовались колония клеток рака груди человека MDA-MB-231, колония клеток рака толстой и прямой кишки HT-29, колония клеток острой миелоидной лейкемии U937 и колония клеток рака хронической миелоидной лейкемии K562. Колония клеток была культивирована с использованием среды RPMI-1640, содержащей 10% сыворотку эмбриона теленка. В качестве среды использовалась продукция Welgene, сыворотка эмбриона теленка представляла продукцию Hyclone, и 1% антибиотиков для культуры клеток от Gibco использовались в качестве среды для культуры.
[864] Каждый набор клеток был нанесен на 96-луночный планшет с концентрацией 2000 клеток на лунку, и 10 μM каждого из соединений в соответствии с указанными примерами были обработаны по истечении 24 часов. Используемые соединения были приготовлены с 10 мM ДМСО и разбавлены в среде таким образом, чтобы конечная концентрация составила 10 μM, a конечная концентрация ДМСО была 0,1%. После 72 часов обработки соединениями противораковое действие измерялось с использованием CCK-8 (Dojindo). Метод измерения соответствовал экспериментальному методу, представленному в продукте, a поглощаемость при длине волны 450 нм измерялась микропланшетным ридером (Hidex) для определения наличия противоракового действия соединений. Когда поглощаемость лунок без клеток принимается за 0, поглощаемость группы отрицательного контроля, не обработанной соединениями, принимается за 100, а относительная процентная средняя величина принимается в качестве величины активности клетки (величина активности 100 клеток)%, это выражается как величина противоракового действия для оценки степени ингибирования активности клеток в сравнении с группой отрицательного контроля. Когда величина противоракового действия составляла 50% или более, она обозначалась '+++', когда она была более 10% и менее 50%, она обозначалась '++', и когда она была 10% или менее, она означалась '+.'
[865] Результаты вышеуказанных экспериментов показаны в Таблице 2 ниже.
[867] В отношении Таблицы 2 было определено, что соединения согласно примерам в соответствии с настоящим изобретением демонстрировали ингибирующее воздействие на развитие раковых клеток (фактор поражения раковых клеток) в отношении колоний клеток MDA-MB-231, HT-29, U937 и K562, которые являются колониями раковых клеток.
[868] <Экспериментальный пример 4> Оценка 2 ингибирующего воздействия на развитие раковых клеток (фактор поражения раковых клеток)
[869] Чтобы определить, оказывает ли соединение противораковое воздействие, использовались колония клеток острой лимфобластозной лейкемии Jurkat, колонии клеток рака желудка AGS, Hs76T и колония клеток рака легких человека A549. Колония клеток была культивирована с использованием среды RPMI-1640 (U937, Jurkat, AGS, A549) или среды DMEM (Hs746T), содержащей 10% сыворотку эмбриона теленка. В качестве среды использовалась продукция Welgene, сыворотка эмбриона теленка представляла продукцию Hyclone, и 1% антибиотиков для культуры клеток от Gibco использовались в качестве среды для культуры.
[870] Каждый набор клеток был нанесен на 96-луночный планшет с концентрацией 2000 клеток на лунку, и 10 μM каждого из соединений в соответствии с указанными примерами были обработаны по истечении 24 часов. Используемые соединения были приготовлены с 10 мM ДМСО и разбавлены в среде таким образом, чтобы конечная концентрация составила 10 μM, a конечная концентрация ДМСО была 0,1%. После 72 часов обработки соединениями противораковое действие измерялось с использованием CCK-8 (Dojindo). Метод измерения соответствовал экспериментальному методу, представленному в продукте, a поглощаемость при длине волны 450 нм измерялась микропланшетным ридером (Hidex) для определения наличия противоракового действия соединений. Когда поглощаемость лунок без клеток принимается за 0, поглощаемость группы отрицательного контроля, не обработанной соединениями, принимается за 100, а относительная процентная средняя величина принимается в качестве величины активности клетки (величина активности 100 клеток)%, это выражается как величина противоракового действия для оценки степени ингибирования активности клеток в сравнении с группой отрицательного контроля. Когда величина противоракового действия составляла 50% или более, она обозначалась '+++', когда она была более 10% и менее 50%, она обозначалась '++', и когда она была 10% или менее, она означалась '+.' Для сведения: часть, помеченная "N.T.", означает "не проверялось (Not Tested)".
[871] Результаты вышеуказанных экспериментов показаны в Таблице 3 ниже.
[873] В отношении Таблицы 3 следует понимать, что соединения из примеров в соответствии с настоящим изобретением демонстрировали ингибирующее воздействие на развитие раковых клеток (фактор поражения раковых клеток) в отношении колоний клеток U937, Jurkat, AGS, Hs746T и A549, которые являются колониями раковых клеток.
[874] <Экспериментальный пример 5> Оценка 2 ингибирующего воздействия на развитие раковых клеток (фактор поражения раковых клеток)
[875] Чтобы определить, оказывает ли соединение противораковое воздействие, использовались колония клеток рака груди человека MDA-MB-231 и колония клеток острой лимфобластозной лейкемии Jurkat, соединения по Примеру 7 использовались при концентрациях 0.1, 0.3, 1, 3, 10 и 30 μM. Противораковое действие оценивалось так же, как и в случае Экспериментального примера 3, а замедление концентрации на 50% рассчитывалось с помощью программы Excel и выражались как величина IC50.
[876] Результаты вышеназванных экспериментов показаны на ФИГ. 2.
[877] В отношении ФИГ. 2, было определено, что соединения по примерам в соответствии с настоящим изобретением демонстрировали отличное ингибирующее воздействие на развитие раковых клеток (фактор поражения раковых клеток) при концентрации в микромолях в отношении колоний клеток MDA-MB-231 и Jurkat, которые являются колониями раковых клеток.
[878]
[879] <Экспериментальный пример 6> Оценка 4 ингибирующего воздействия на развитие раковых клеток (фактор поражения раковых клеток)
[880] Чтобы определить противораковое воздействие концентрации соединения с использованием клеток рака желудка человека HS746T, соединения по примерам использовались при концентрациях 0.1, 0.3, 1, 3, 10 и 30 μM соответственно. Противораковое действие оценивалось так же, как и в случае Экспериментального примера 3, а замедление концентрации на 50% рассчитывалось с помощью программы Excel и выражались как величина IC50. Для сведения: часть, помеченная "N.T.", означает "не проверялось (Not Tested)".
[881] Результаты вышеуказанных экспериментов показаны в Таблице 4 ниже.
[883] В отношении Таблицы 4 было определено, что соединения из примеров в соответствии с настоящим изобретением демонстрировали отличное ингибирующее воздействие на развитие раковых клеток (фактор поражения раковых клеток) при концентрации в микромолях в отношении колонии клеток Hs746T, которая является колонией раковых клеток.
[884]
[885] <Экспериментальный пример 7> Оценка ингибирующего воздействия на метастазы раковых клеток
[886] Чтобы определить ингибирующее действие соединений на метастазы рака, использовалась колония клеток рака груди человека MDA-MB-231. После культивирования в течение 24 часов при концентрации 15 000 клеток на лунку в 96-луночном планшете ImageLock (Essen BioScience), она была заменена бессывороточной средой. При использовании 96-луночного приспособления для нанесения ранок (Essen BioScience) клетки равномерно соскребались в случае каждой лунки с образованием ранки, соединения использовались при концентрации от 1 до 3 μM соответственно, и каждые 12 часов оставшаяся длина ранки измерялась с использованием программы IncuCyte. Все эксперименты повторялись три раза, на ФИГ. 3 приводится фотография, на которой показаны результаты после 60 часов образования ранки.
[887] В отношении ФИГ. 3 было определено, что соединения из примеров в соответствии с настоящим изобретением демонстрировали отличное ингибирующее воздействие на метастазы раковых клеток при концентрации в микромолях в отношении колонии раковых клеток MDA-MB-231.
[888]
[889] <Экспериментальный пример 8> Оценка 1 ингибирования фиброза
[890] Чтобы определить, замедляют ли соединения симптомы неалкогольного стеатогепатита, использовалась колония клеток рака печени человека HepG2 от ATCC. Колония клеток культивировалась в среде 5% CO2 при 37°C с использованием DMEM (модификация среды Eagle от Dulbecco), к которой добавлялись FBS (сыворотка эмбриона теленка) от Gibco в концентрации 10%, пенициллин 100 ед./мл и стрептомицин 100 μг/мл.
[891] Чтобы вызвать фиброз, использовалась пальмитиновая кислота (сигма). 20 мM пальмитиновой кислоты и 0,001 N NaOH смешивались с DPBS (фосфатно-солевой буферный раствор от Dulbecco), с поддержанием температуры 70°C в течение 30 минут, для получения взвеси, и далее перемешивались с 5% раствором бычьего сывороточного альбумина без содержания жирных кислот в соотношении 1:3 (5 мM). Затем выполнялось связывание при 37°.
[892] Группа, которая не вызывала фиброз при обработке пальмитиновой кислотой, рассматривалась как невызывающая группа; группа, получающая обработку пальмитиновой кислотой, рассматривалась как группа отрицательного контроля, a группа, получающая обработку пальмитиновой кислотой и соединением, рассматривалась как экспериментальная группа.
[893] После культивирования клеток общая РНК изолировалась с помощью реагента Тризол (Trizol) (инвитроген) в соответствии с инструкциями производителя. 1 μг общей РНК, полученной таким образом, преобразовывалось в кДНК с помощью системы обратной транскрипции. Типы и последовательности праймеров, используемых в эксперименте, показаны в Таблице 5 ниже. Цепная реакция полимеразы в реальном времени была проведена в соответствии с методом, рекомендуемым производителем, с использованием зеленой мастер-микс ЦРП SYBR (SYBR Green PCR Master Mix) от Applied Biosystem, а относительные величины выражения гена количественно выражались на основе конститутивного гена β-actin. 10 μл 2 x SYBR Green PCR Master Mix, 9 μл кДНК, 0,2 μл праймера (смыслового), 0,2 μл праймера (антисмыслового) и 0,6 μл дистиллированной воды смешивались до общего объема 20 μл. Для начальной денатурации только первый цикл амплифицировался при 95°C в течение 10 минут, а остальные 40 циклов амплифицировались при 95°C в течение 15 секунд, а отжиг и вытягивание производились при 60°C в течение 1 минуты.
[894] Относительная степень замедления экспрессии (%) каждого гена - маркера фиброза соединениями из примеров рассчитывалась в соответствии с Уравнением 1 ниже.
[895] [Уравнение 1]

[897] Результаты приведенных выше экспериментов показаны в Таблице 6 ниже.
[899] В отношении Таблицы 6 было определено, что соединения из примеров в соответствии с настоящим изобретением ингибировали ген-маркер фиброза, вызываемого пальмитиновой кислотой в HepG2, колонии клеток рака печени, посредством которой определялось антифиброзное воздействие соединений в соответствии с настоящим изобретением.
[900]
[901] <Экспериментальный пример 9> Оценка 2 ингибирования фиброза
[902] Чтобы определить профилактическое и лечебное воздействие соединения в случае неалкогольного стеатогепатита, использовалась колония клеток рака печени человека HepG2 от ATCC. Колония клеток культивировалась в среде 5% CO2 при 37°C с использованием DMEM (модификация среды Eagle от Dulbecco), к которой добавлялись FBS (сыворотка эмбриона теленка) от Gibco в концентрации 10%, пенициллин 100 ед./мл и стрептомицин 100 μг/мл.
[903] Чтобы вызвать фиброз, использовалась пальмитиновая кислота (сигма). 20 мM пальмитиновой кислоты и 0,001 N NaOH смешивались с DPBS (фосфатно-солевой буферный раствор от Dulbecco), с поддержанием температуры 70°C в течение 30 минут, для получения взвеси, и далее перемешивались с 5% раствором бычьего сывороточного альбумина без содержания жирных кислот в соотношении 1:3 (5 мM). Затем выполнялось связывание при 37°.
[904] Группа, которая не вызывала фиброз при обработке пальмитиновой кислотой, рассматривалась как невызывающая группа; группа, получающая обработку пальмитиновой кислотой, рассматривалась как группа отрицательного контроля, a группа, получающая обработку пальмитиновой кислотой и соединением, рассматривалась как экспериментальная группа.
[905] После культивирования клеток общая РНК изолировалась с помощью реагента Тризол (Trizol) (инвитроген) в соответствии с инструкциями производителя. 1 μг общей РНК, полученной таким образом, преобразовывалось в кДНК с помощью системы обратной транскрипции. Типы и последовательности праймеров, используемых в эксперименте, показаны в Таблице 6 ниже. Цепная реакция полимеразы в реальном времени была проведена в соответствии с методом, рекомендуемым производителем, с использованием зеленой мастер-микс ЦРП SYBR (SYBR Green PCR Master Mix) от Applied Biosystem, а относительные величины выражения гена количественно выражались на основе конститутивного гена β-actin. 10 μл 2 x SYBR Green PCR Master Mix, 9 μл кДНК, 0,2 μл праймера (смыслового), 0,2 μл праймера (антисмыслового) и 0,6 μл дистиллированной воды смешивались до общего объема 20 μл. Для начальной денатурации только первый цикл амплифицировался при 95°C в течение 10 минут, а остальные 40 циклов амплифицировались при 95°C в течение 15 секунд, а отжиг и вытягивание производились при 60°C в течение 1 минуты.
[906] Относительная степень замедления экспрессии (%) каждого гена - маркера фиброза соединениями из примеров рассчитывалась в соответствии с Уравнением 1 выше.
[908] Результаты приведенных выше экспериментов показаны в Таблице 8 ниже.
[910] В отношении Таблицы 8 было определено, что соединения из примеров в соответствии с настоящим изобретением ингибировали ген-маркер фиброза, вызываемый пальмитиновой кислотой в HepG2, колонии клеток рака печени, посредством которой определялось антифиброзное воздействие соединений в соответствии с настоящим изобретением.
[911]
[912] <Экспериментальный пример 10> Оценка ингибирования неалкогольного стеатогепатита у животных моделей
[913] Чтобы определить воздействие соединений на неалкогольный стеатогепатит, использовались животные модели с неалкогольным стеатогепатитом, в качестве которых выступали 6-недельные мыши C57BL/6J; они получали метионин и были на метионин-холин-дефицитной диете (MCD). Группа на нормальной диете получала нормальное питание (Chow) без ограничения, а у группы MCD вызывался неалкогольный стеатогепатит путем содержания на диете MCD в течение 8 недель (Молекулы 2014, 19, 8189-8211). Животные содержались в хорошо вентилируемых помещениях с поддержанием температуры 23±2°C и относительной влажности 55±5%. Флуоресцентное освещение подавалось примерно 12 часов в сутки, отходы убирались раз в неделю.
[914] После 8 недель стандартной диеты или диеты MCD, животным, получавшим MCD, вводились внутрибрюшинно лекарства раз в день в течение 4 недель. Одновременно животные содержались на обычной диете. Среди животных на диете MCD "экспериментальная группа" получала 10 мг/кг соединения по Примеру 7, а "группа отрицательного контроля" получала носитель внутрибрюшинно раз в день в течение 4 недель. Конфигурация группы животных в этом экспериментальном примере показана в Таблице 9 ниже.
[916] Вес тела, прием пищи и питьевой воды измерялись раз в неделю, а по истечении 12 недель экспериментирования проводились оценки биохимических индикаторов сыворотки (ALT, AST, ALP, TG, глюкоза, альбумин) и гистопатологических индикаторов (оценка воздействия в баллах после закапывания красителя Сириус красный). Некоторые результаты показаны на ФИГ. 4 - 6. В отношении ФИГ. 4 - 6 было подтверждено, что соединения из примеров в соответствии с настоящим изобретением улучшали оценки индикаторов для неалкогольного стеатогепатита, вызываемого диетой MCD, благодаря чему были определены профилактическое и лечебное воздействия соединений в соответствии с настоящим изобретением в случае неалкогольного стеатогепатита.
[917]
[918] <Экспериментальный пример 11> Оценка ингибирующего действия против LRRK2
[919] Чтобы определить ингибирующее воздействие на киназы LRRK2 немутантного типа и LRRK2 мутантного типа (G2019S) примера соединения в соответствии с настоящим изобретением, бактерии кишечной палочки E. coli (E. coli) производные BL21 культивировались в 24-луночном планшете до фазы роста (фазы логарифмического роста). После культивирования бактериофаг T7, помеченный немутантным LRRK2 или мутантным LRRK2 (G2019S), использовался для множественного (MOI) при 0,4. После этого бактерии E. coli перемешивались при 32° в течение 90 - 150 минут для обеспечения растворения. Лизат бактерий E. coli подвергался центрифугированию (6 000 x g) и фильтрации (0,2 μм); полученный бактериофаг T7 был трансфектирован в клетки HEK293, и таким образом была получена протеинкиназа, помеченная ДНК (LRRK2 или LRRK2 G2019S).
[920] Магнитные шарики, покрытые стрептавидином, получали обработку бионилированными низкомолекулярными лигандами при комнатной температуре в течение 30 минут для приготовления аффиновой смолы. После блокирования бионилированного лиганда избытком биотина он промывался буферным раствором SeaBlock от Pierce (1 % БСА (бычьего сывороточного альбумина), 0,05% Tween 20, 1 мM ДTT) для удаления несвязанного лиганда и уменьшения неклассифицированного связывания. Реакция связывания проводилась путем смешивания магнитных шариков, полученных из клеток HEK293 с киназой и лигандовой связью и приводимым в примере соединением, содержащемся в буфере 1X.
[921] Соединение приготовлялось при концентрации 40X в 100% ДМСО и использовалось после разбавления, и все реакции связывания проводились в конечном объеме 0,02 мл в 384-луночном планшете. После перемешивания планшета в течение 1 часа при комнатной температуре магнитные шарики промывались промывочным буфером (1x полибутиленсукцинат, 0,05% Tween 20) и подвергались повторному суспендированию в элюирующем буфере (1x полибутиленсукцинат, 0,05% Tween 20, 0,5 μM небионилированного аффинного лиганда).
[922] Ингибирующее воздействие на киназы LRRK2 немутантного типа и LRRK2 мутантного типа (G2019S) примера соединений в соответствии с настоящим изобретением подвергалось измерению и показано в Таблице 10 ниже.
[924] В отношении Таблицы 10: в ней определено ингибирующее воздействие на активность киназы LRRK2 немутантного типа и LRRK2 мутантного типа (G2019S) примера соединений в соответствии с настоящим изобретением.
[925]
[926] <Экспериментальный пример 12> Оценка ингибирования фосфорилирования LRRK2
[927] Чтобы определить ингибирующее действие фосфорилирования на активность киназы LRRK2 примера соединений в соответствии с настоящим изобретением, использовалась колония клеток NIH-3T3, известная как экспрессирующая колония клеток LRRK2, a среда DMEM, к которой добавлялись 10% фетальная бычья сыворотка от Gibco и 1% пенициллина/стрептомицина, использовалась и культивировалась в среде of 5% CO2, при 37°C.
[928] После культивирования в 12-луночном планшете с 2 x 105 клеток, ингибиторы LRRK2 HG-10-102-01 и GNE0877 (сравнительные соединения 1 и 2 соответственно) и ингибитор MLK CEP1347 (сравнительное соединение 3) из Примера 7 обрабатывались концентрациями 5, 20, 100 и 1000 нM соответственно. После культивирования в течение 24 часов получали протеин, используя лизирующий буфер (50 мM Tris-HCl (pH7.5), 0,5% TX-100, 150 мM NaCl, 0.5 мM ЭДТA, смесь ингибиторов протеазы, 0.2 мM ПМСФ). Полученный протеин был проанализирован методом количественного определения с использованием набора BCA от Thermo Fisher Scientific; после нагревания при 75° в течение 5 минут выполнялось вестернблотирование. В качестве первичных антител LRRK2 использовались фосфо-LRRK2 и β-actin от Abcam; антитела LRRK2 и фосфо-LRRK2 вступали в реакцию в соотношении 1:1000, a антитело β-actin в соотношении 1:5000. Результаты вышеприведенных экспериментов показаны на ФИГ. 7.
[929] В отношении ФИГ. 7 было определено, что соединение из примера в соответствии с настоящим изобретением замедляли фосфорилирование LRRK2 на уровне, аналогичном уровню Сравнительных соединений 1 и 2, которые являются ингибиторами LRRK2, в колонии клеток NIH-3T3, которая является LRRK2-экспрессирующей колонией клеток.
[930]
[931] <Экспериментальный пример 13> Оценка защитного воздействия от повреждения нервных клеток
[932] Чтобы определить защитное действие соединения из примера в соответствии с настоящим изобретением в отношении повреждения нервов, у крысы был взят зародыш в 15-й день беременности, затем был извлечен участок корки головного мозга, который использовался в качестве первичных нейронов корки головного мозга. Клетки были разделены на аликвоты в 12-луночном планшете с 2 X 105 клетками и культивировались в течение 24 часов, а затем замещались средой Neurobasal от Gibco и культивировались. LRRK2 G22019S трансфектировались с использованием липофектамина и Opti-MEM от Invitrogen на 11-й день in vitro, a 6 часов спустя соединения из примеров или сравнительных примеров обрабатывались при концентрациях 0.01, 0.1 и 1 μM. После фиксации клеток обработкой 4% ПФА нейриты исследовались с помощью иммунного окрашивания с использованием антитела GFP от Abcam. Защитное воздействие каждого соединения против повреждений нервов оценивалось путем изменения длины неврита. Результаты приведенных выше экспериментов показаны на ФИГ. 8.
[933] В отношении FIG. 8 было определено, что соединение из примера в соответствии с настоящим изобретением оказывало защитное воздействие, в зависимости от дозы, от повреждений нейронов, вызванных повышенной экспрессией мутации LRRK2 G2019S.
[934]
[935] <Экспериментальный пример 14> Оценка антивирусного действия 1
[936] Чтобы определить ингибирующее действие соединения на активность гриппа, колония клеток MDCK (клеток Мадин-Дарби почек собак), выращенная в достаточном количестве в 96-луночном планшете, промывалась физиологическим раствором с фосфатным буфером (PBS), и далее в нее вводился вирус гриппа с 50-100 БОЕ (бляшкообразующими единицами) на лунку. Ее оставляли при 35°C примерно на 1 час для инфицирования клеток вирусами. После удаления среды культуры и промывания физиологическим раствором с фосфатным буфером, минимальная питательная среда культуры (MEM), содержащая 2 μг/мл TPCK-трипсина, в котором каждое соединение из примера разбавлялось до различных концентраций, добавлялась в каждую лунку. На третий день после инфицирования активность клеток оценивалась с помощью MTT (Sigma) [Jang YJ и др., (2014). Антивирусное средство Res 107:66-75.]. Путем измерения поглощающей способности при значениях длины волны 540 нм и 690 нм были рассчитаны 50% цитотоксическая концентрация (CC50) и 50% эффективная концентрация (EC50).
[937] Результаты вышеназванных экспериментов показаны в Таблице 11 ниже. Для сведения: ячейка с пометкой Н/Д означает "Нет данных".
[939] В отношении Таблицы 11 было определено, что соединения из примеров в соответствии с настоящим изобретением демонстрировали воздействие (антивирусное действие), замедляющее цитотоксичность, вызванную вирусной инфекцией, на уровне микромолярной концентрации в отношении колонии клеток MDCK, зараженной вирусной инфекцией.
[940]
[941] <Экспериментальный пример 15> Оценка антивирусного действия 2
[942] Чтобы определить ингибирующее действие соединения на активность гриппа, колония клеток А549 (колония клеток рака легких человека), выращенная в достаточном количестве в 24-луночном планшете, промывалась физиологическим раствором с фосфатным буфером (PBS), и далее в нее вводился вирус гриппа (A/PR8) с 14 000 БОЕ (бляшкообразующими единицами) на лунку. Далее она культивировалась при 35° в течение 1 часа с целью инфицирования клеток вирусом. После удаления среды культуры и промывания физиологическим раствором с фосфатным буфером, среда культуры RPMI-раствора, содержащая 0,1 μг/мл TPCK-трипсина, разбавленного до концентраций 11, 33 и 100 μM для каждого соединения из примеров, добавлялась в каждую лунку и культивировалась при 35°C.
[943] Чтобы измерить количество вирусов гриппа, присутствующих в среде культуры клетки, каждая среда культуры клетки собиралась после 2 дней культивирования, 10-кратно разбавлялась с 10-1 до 10-8 и инфицировались 100% выращенных клеток MDCK в 96-луночном планшете. Через три дня после инфицирования активность клеток измерялась с помощью MTT (Sigma), a 50% граничная точка вычислялась с использованием метода Рида-Мюнха (Reed-Muench) или Спирмена-Карбера (Spearman-Karber). Она была выражена как ЦПД50/мл (инфекционная доза в тканевой культуре 50%), которая является единицей, выражаемой как титр коэффициента разбавления, при котором клетки с привитым вирусом инфицировались на 50%. Группа отрицательного контроля была заражена вирусом, но не обрабатывалась соединением из примера.
[944] Результаты вышеназванных экспериментов показаны на ФИГ. 9 - 14.
[945] В отношении ФИГ. 9 - 14 было определено, что соединения из примеров в соответствии с настоящим изобретением демонстрировали ингибирующее воздействие (антивирусное воздействие) на цитотоксичность вследствие заражения вирусом гриппа.
[946]
[947] <Экспериментальный пример 16> Оценка антивирусного действия для животных моделей
[948] Чтобы определить ингибирующее воздействие соединения на активность гриппа у животных моделей, использовалась животная модель - мышь, зараженная адаптированным для мышей вирусом PR8 (далее в тексте - "maPR8"). Модель обеспечивалась путем инфицирования 7-недельных мышей Balb/c вирусом, соответствующим титру 3 MLD50 (доза половинной выживаемости мышей), через носовой проход. Чтобы наблюдать лечебный эффект, соединение по Примеру 4 вводилось за один день до заражения вирусом (день 0). В период проведения экспериментов с животными экспериментальная группа получала соединение по Примеру 4 раз в день с концентрацией 10 мг/кг/день в течение 9 дней. На одну группу приходилось три мыши, антивирусная эффективность измерялась через измерение веса. Объекты, чей вес тела уменьшался на 30% или более с начала эксперимента, умерщвлялись (в соответствии с правилами Комитета по экспериментированию с животными Корейского исследовательского института химических технологий) [Shin JS и др., (2017) J Microbiol. 55:979-983].
[949] Результаты вышеназванных экспериментов показаны на ФИГ. 15 и 16.
[950] В отношении ФИГ. 15 и 16 было определено, что в группе животных, получавших соединения из примеров в соответствии с настоящим изобретением, нормализовался вес тела у моделей - мышей, зараженных вирусом гриппа и повысилась выживаемость.
[951] Приведенное выше описание является чисто иллюстративным в отношении настоящего изобретения, и специалистам в той технической области, к какой относится настоящее изобретение, следует понимать, что настоящее изобретение может внедряться в модифицированной форме без отклонения от основных характеристик настоящего изобретения. Соответственно, описанные примеры и экспериментальные примеры должны рассматриваться скорее как иллюстративные, чем как ограничительная перспектива. Область действия настоящего изобретения указана в большей степени в формулах настоящего изобретения, чем в вышеприведенном описании, и все различия в его эквивалентной области должны рассматриваться как включенные в настоящее изобретение.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ ИМИДАЗОПИРИДИНИЛ-АМИНОПИРИДИНОВЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ РАКА | 2010 |
|
RU2619463C2 |
| ИНГИБИТОРЫ GCN2 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2811408C2 |
| АНТАГОНИСТЫ CXCR7 | 2013 |
|
RU2649004C2 |
| ИМИДАЗОПИРИДАЗИНЫ | 2012 |
|
RU2662443C2 |
| НОВЫЕ СОЕДИНЕНИЯ И ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2785126C2 |
| ИНГИБИТОРЫ БРОМДОМЕНА | 2012 |
|
RU2671571C1 |
| ИНГИБИТОРЫ GCN2 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2811403C2 |
| ПИРРОЛОПИРАЗИНОВЫЕ ИНГИБИТОРЫ КИНАЗЫ | 2012 |
|
RU2673064C2 |
| КОНДЕНСИРОВАННЫЕ ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПИРИДИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПРОИЗВОДСТВА И ПРИМЕНЕНИЕ | 2014 |
|
RU2668074C2 |
| ИНГИБИТОРЫ БРОМДОМЕНА | 2012 |
|
RU2647592C2 |

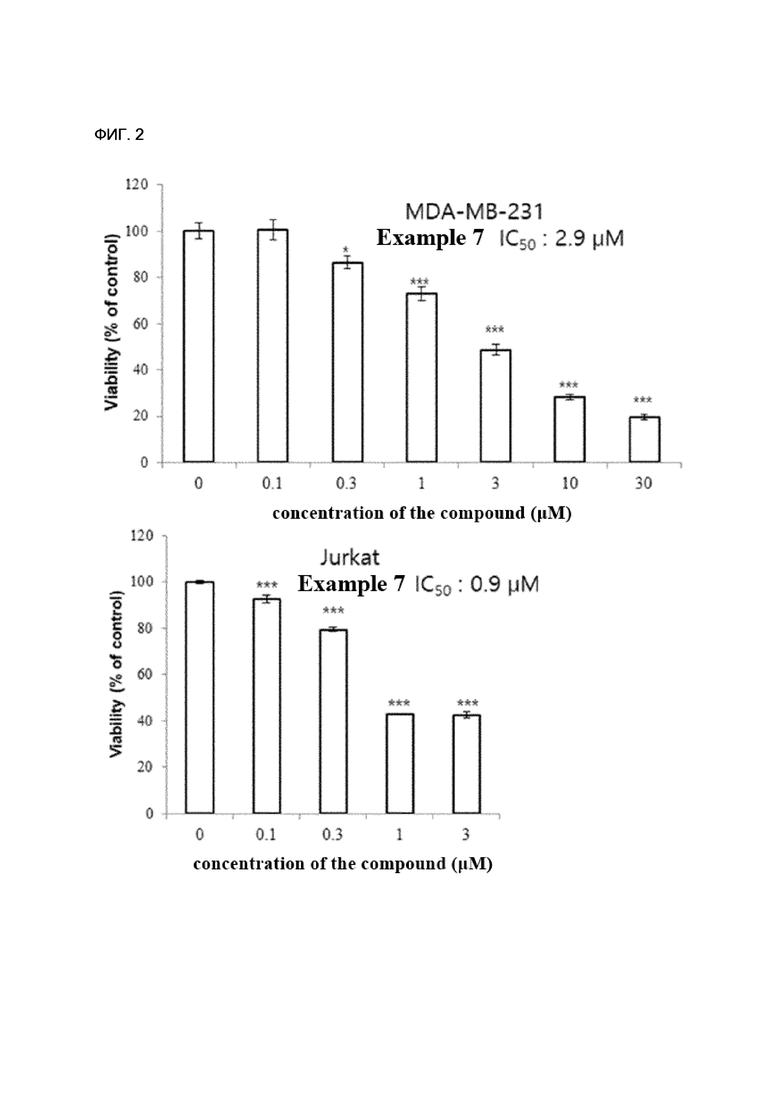

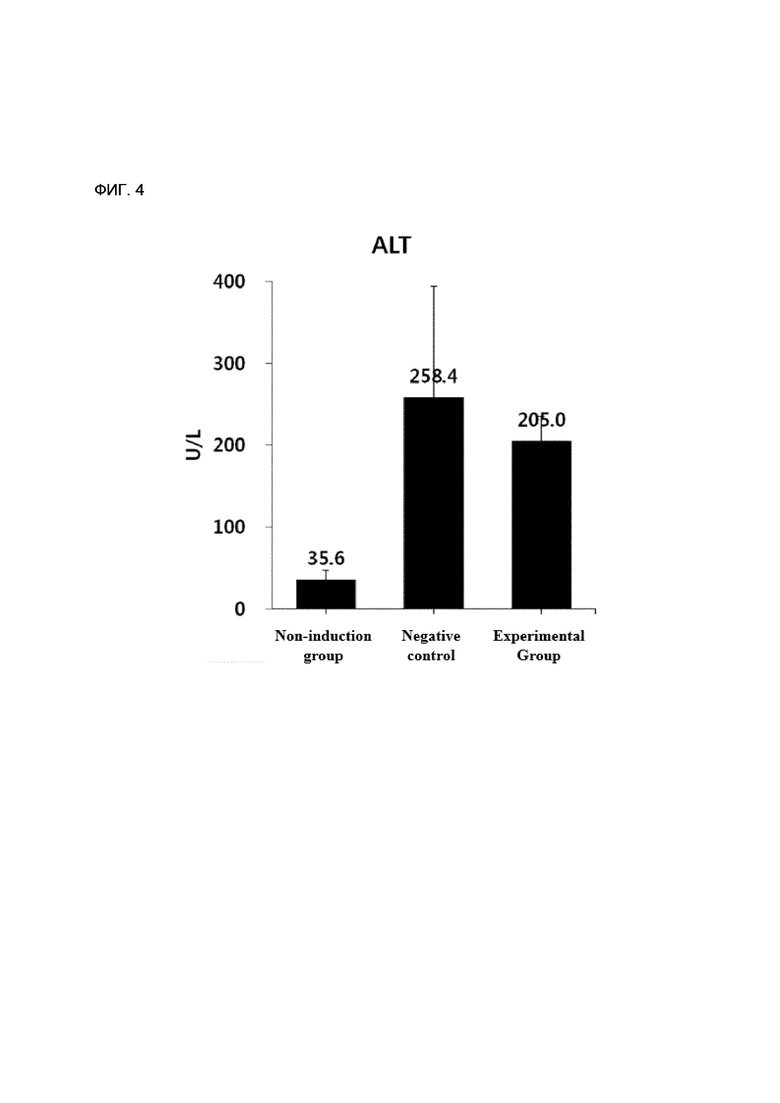
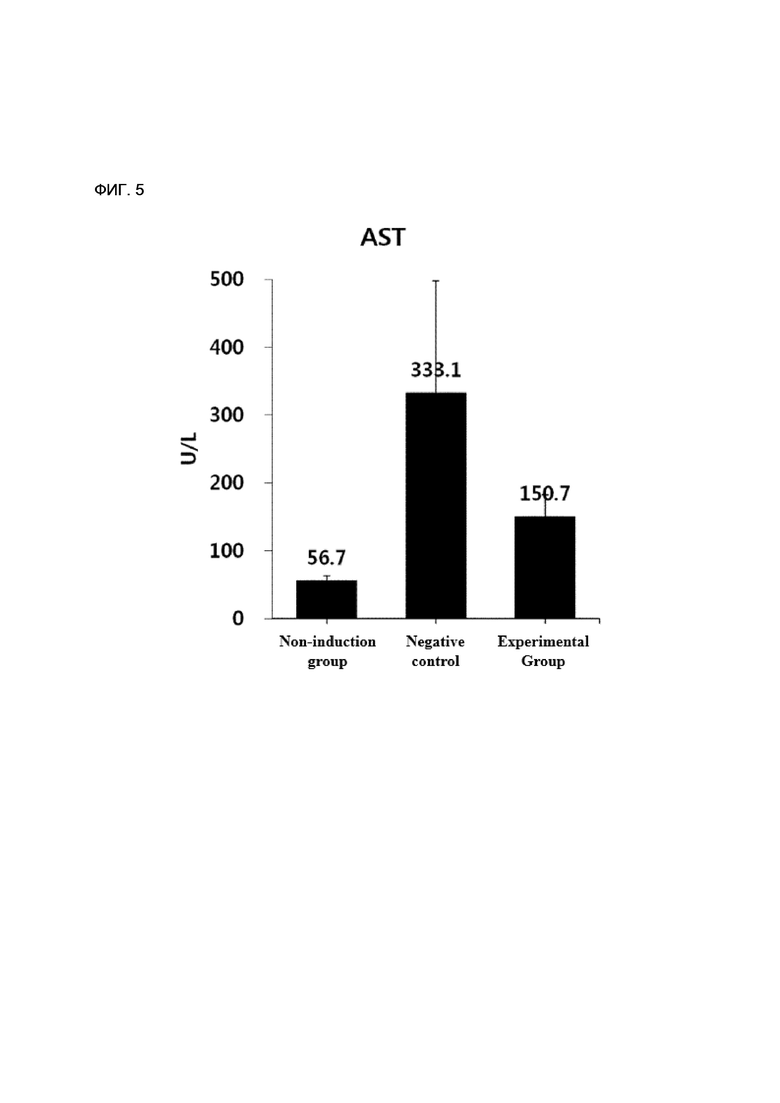
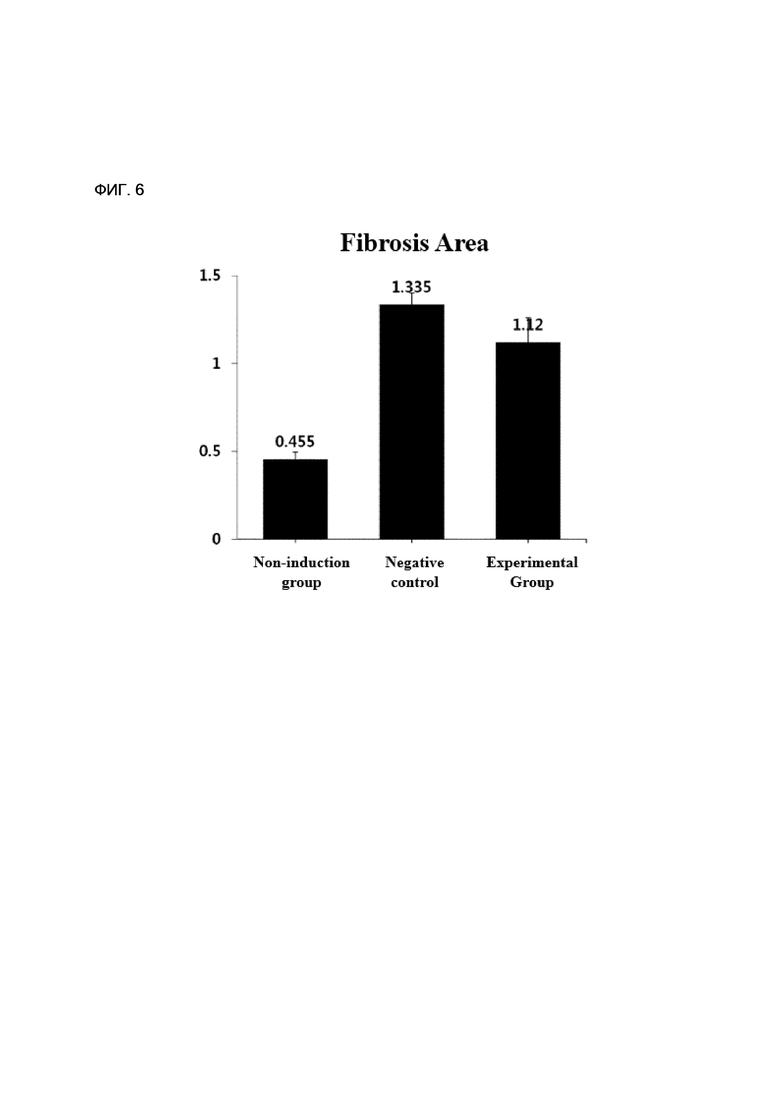

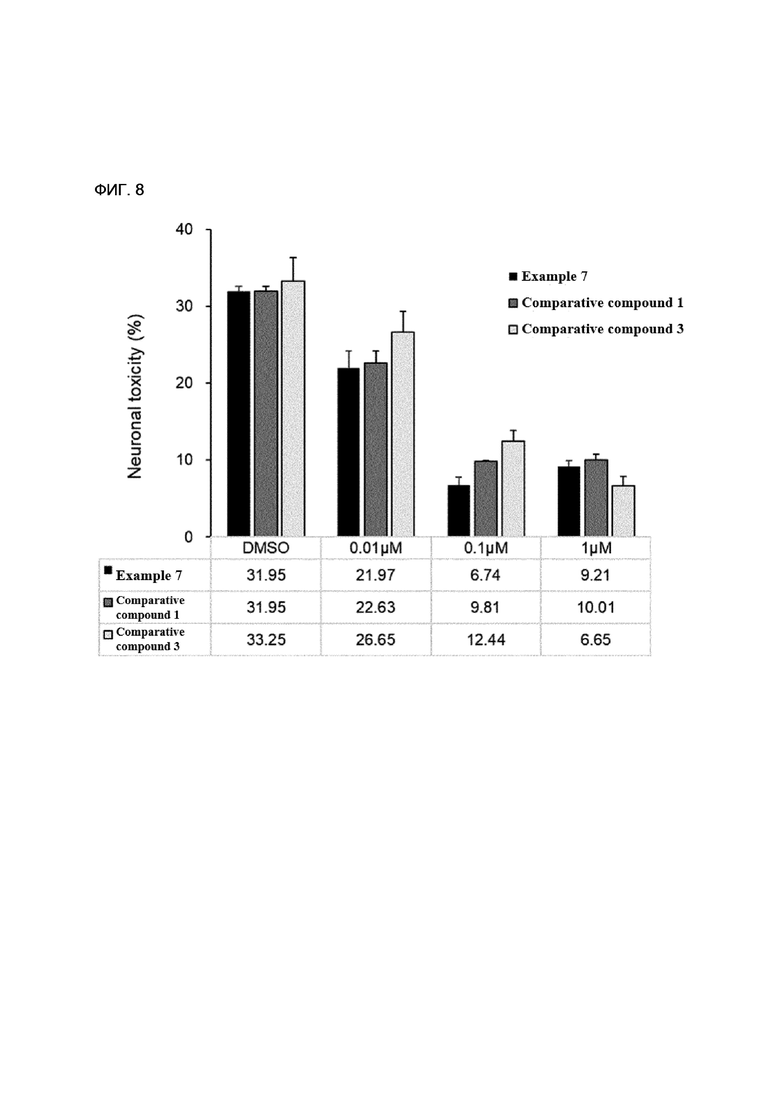
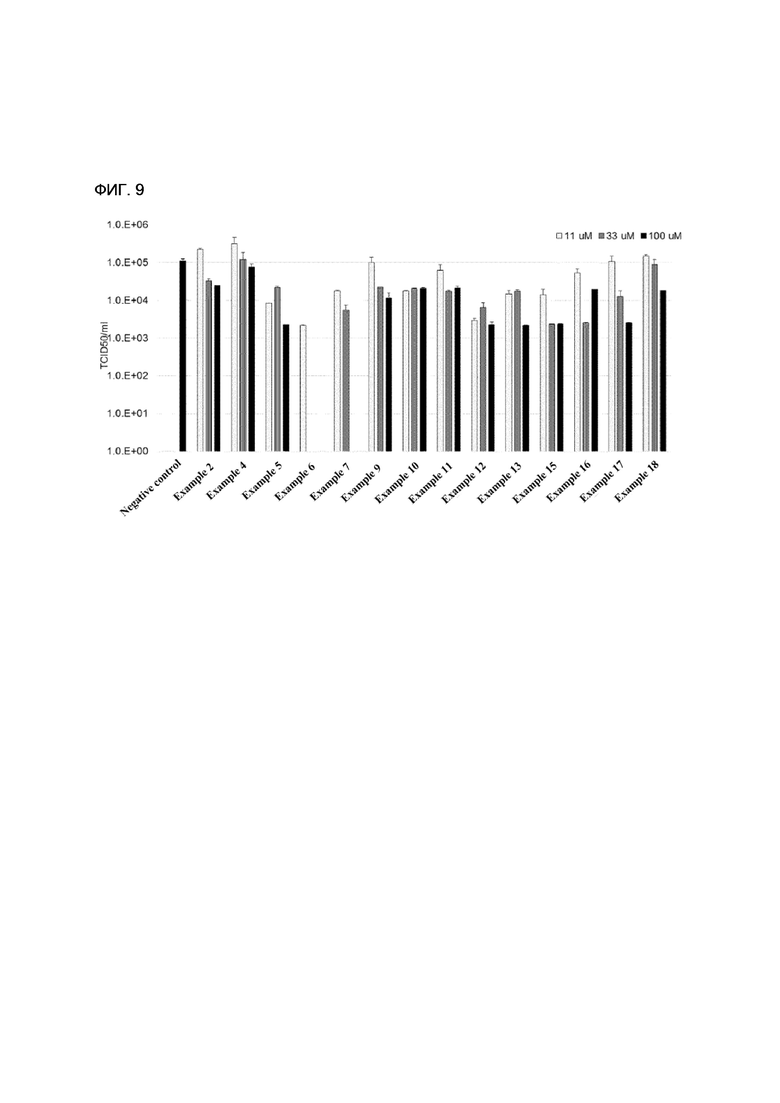
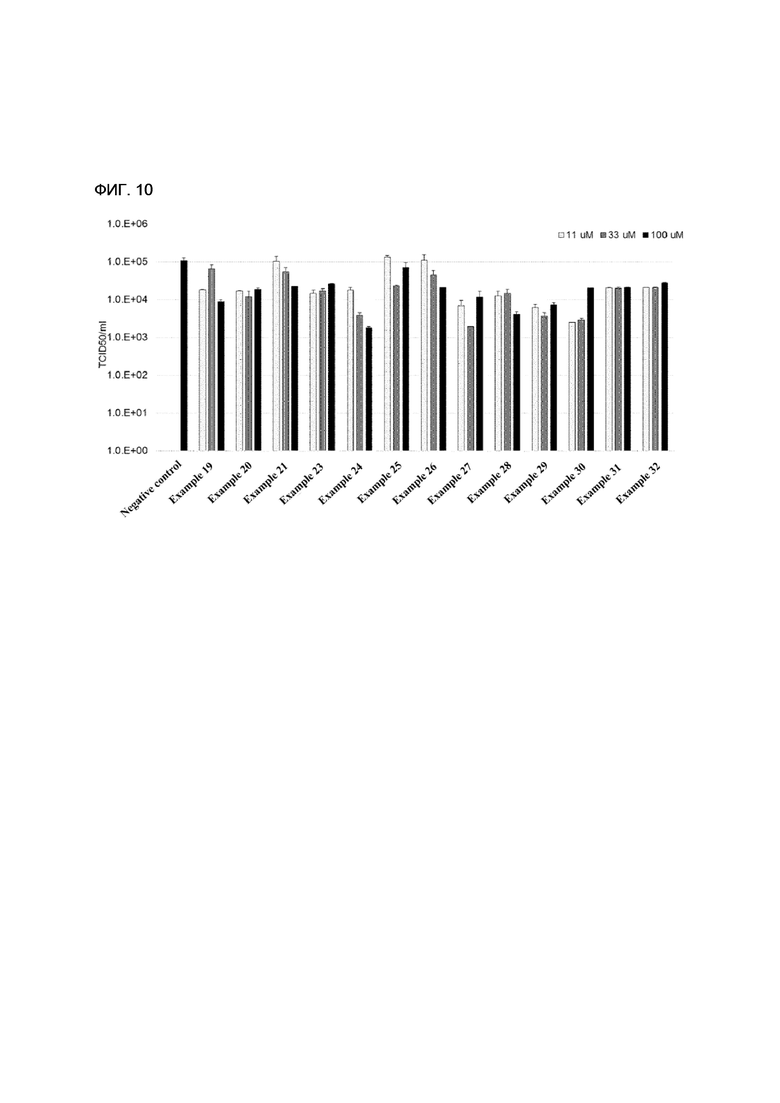
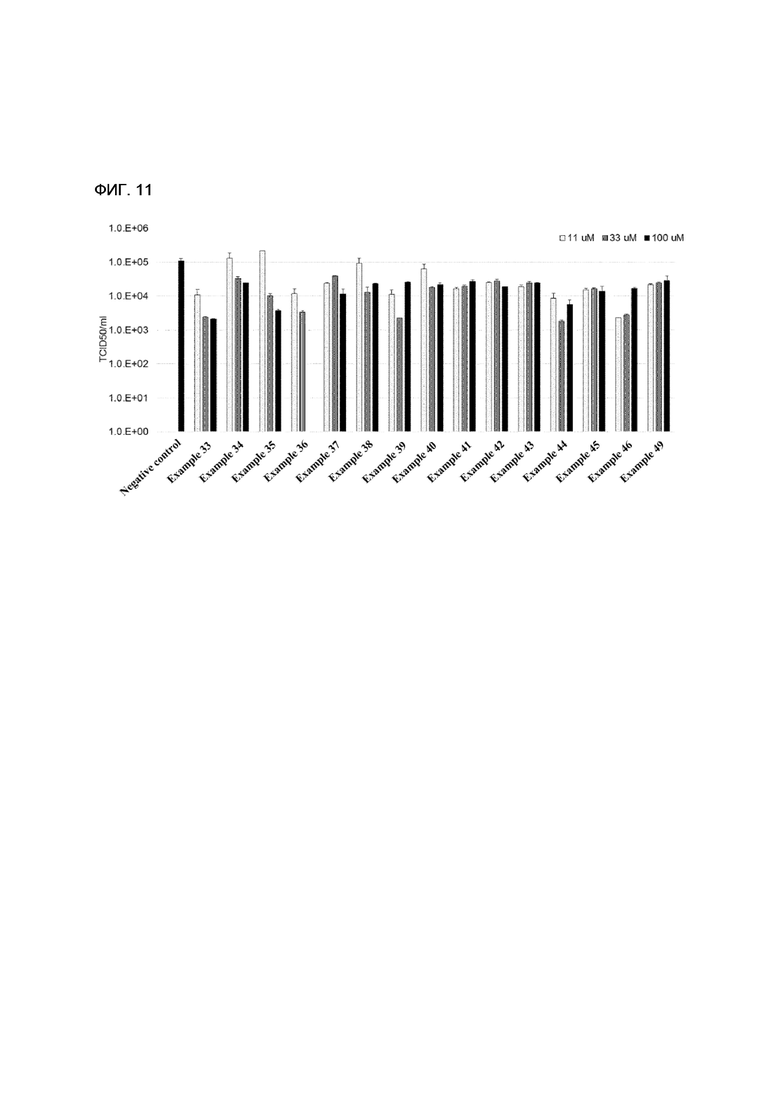
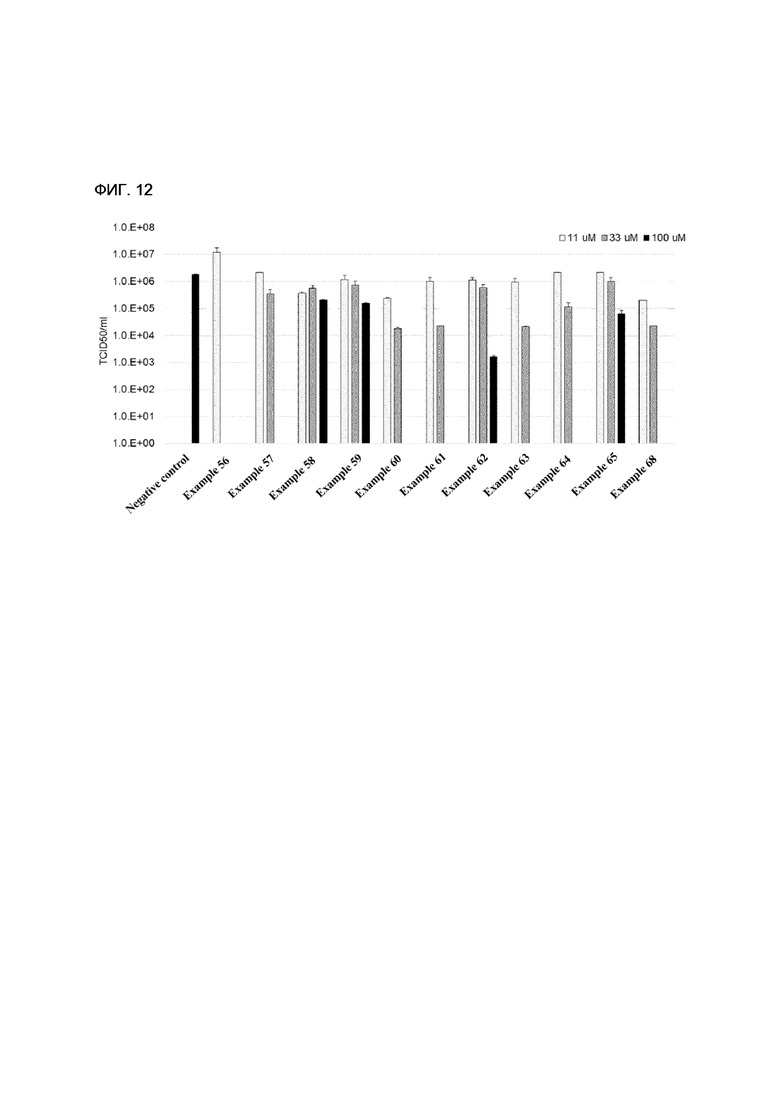
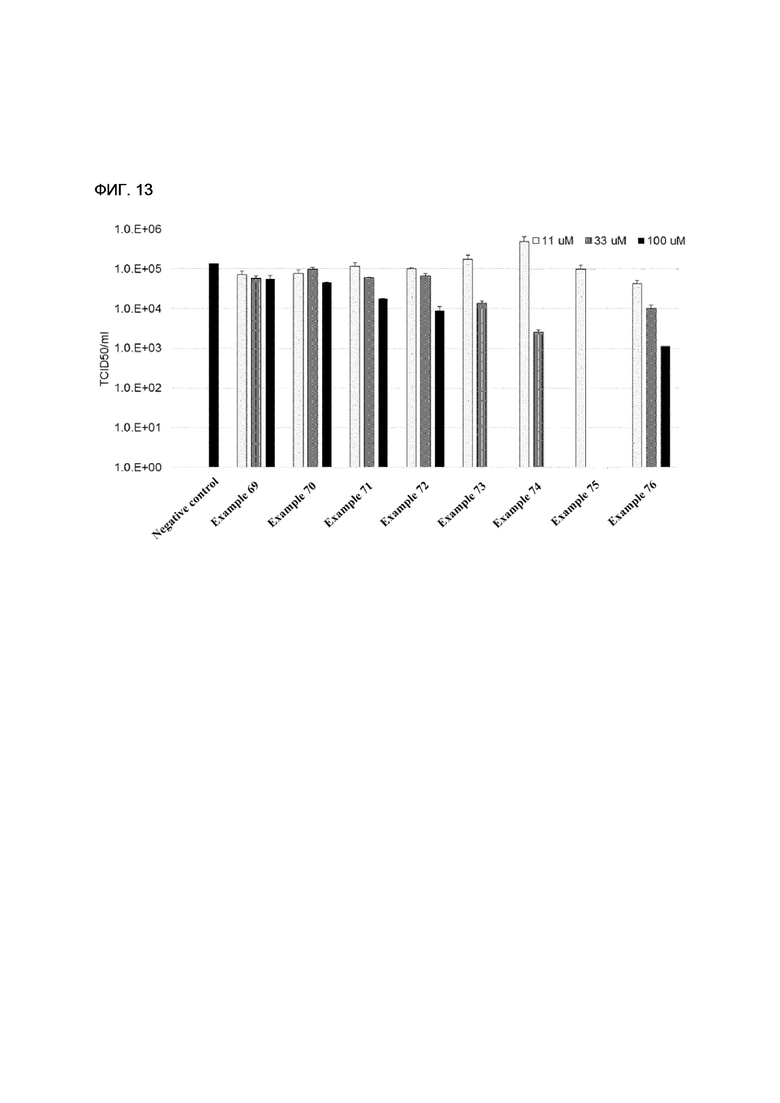
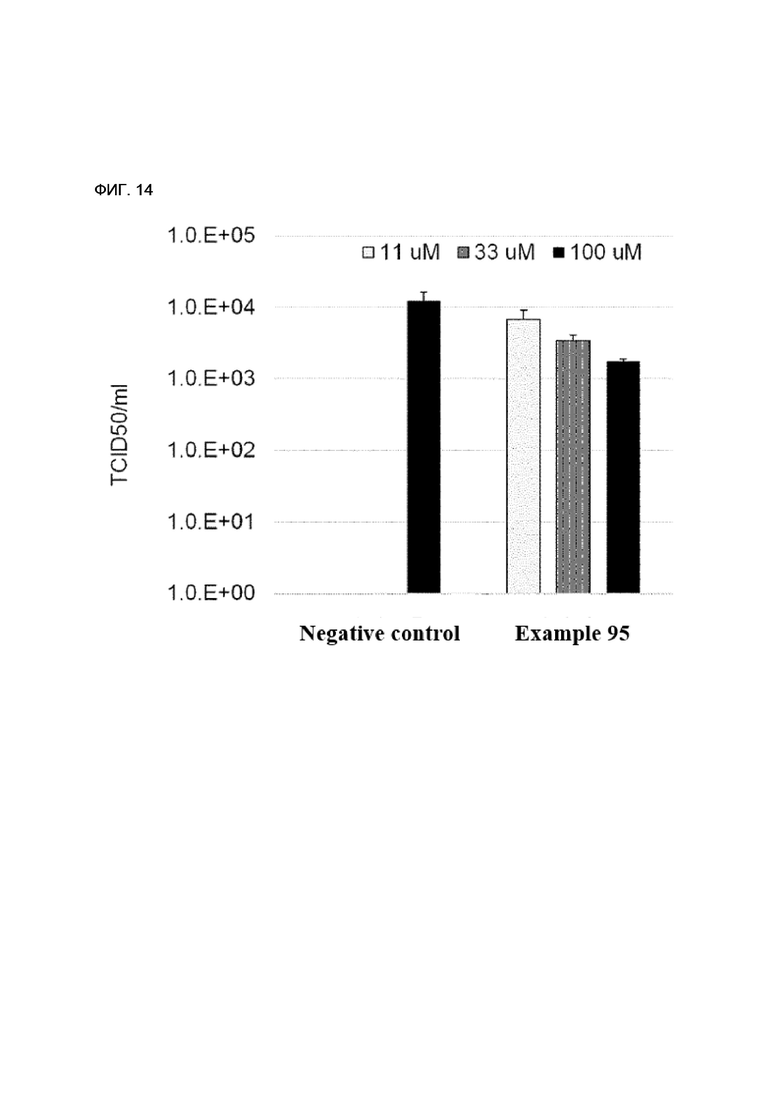
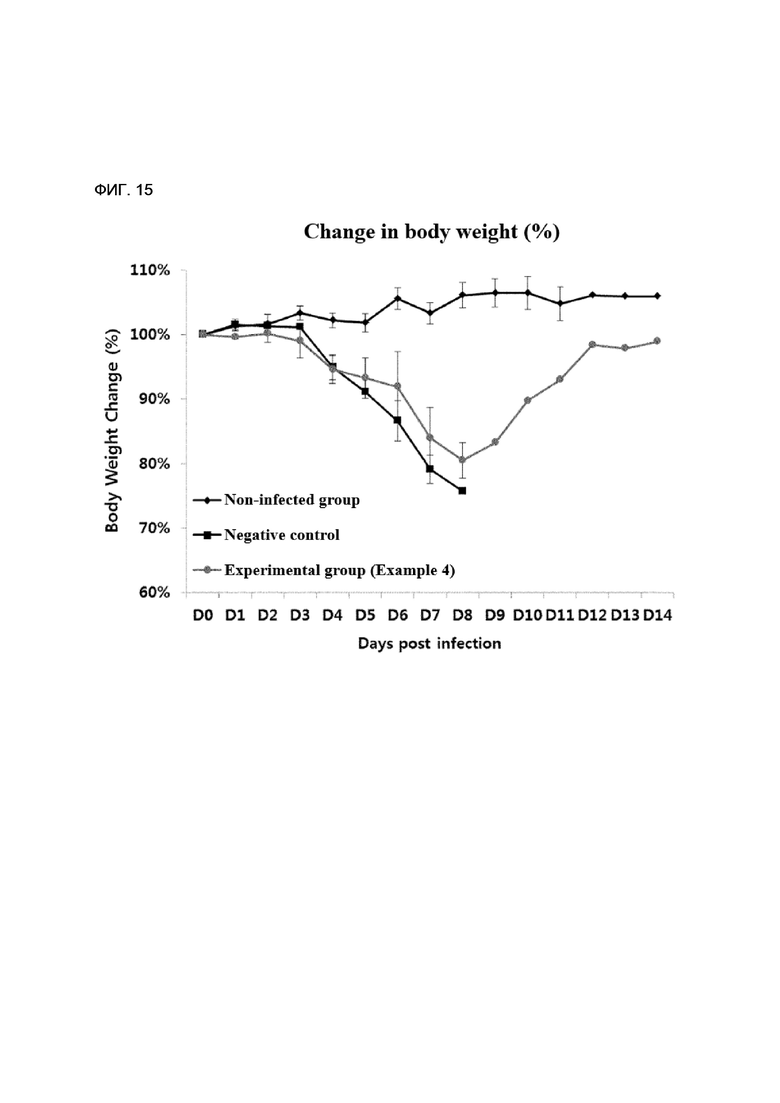
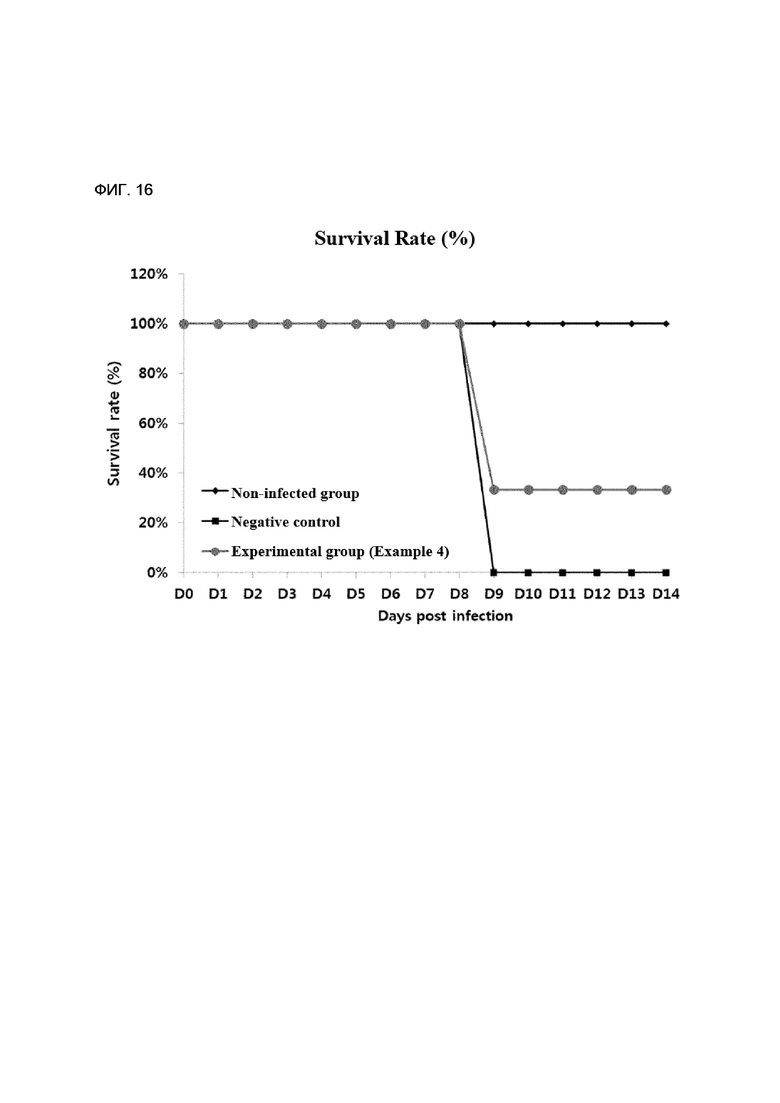
Изобретение относится к производным имидазопиридина, указанным в п. 1 формулы изобретения, которые ингибируют действие протеинкиназы, которая представляет собой по меньшей мере один фермент, выбранный из MLK1, MLK2, MLK3. Изобретение также относится к фармацевтическим препаратам, содержащим указанные производные в качестве активного ингредиента. Технический результат – получены новые соединения и фармацевтический препарат на их основе, которые могут найти применение в медицине для профилактики или лечения рака, нейродегенеративного заболевания, неалкогольного стеатогепатита и гриппа. 5 н. и 4 з.п. ф-лы, 16 ил., 11 табл., 98 пр.
1. Соединение, выбранное из группы, состоящей из следующих соединений, их стереоизомеров:
1) (S)-6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
2) (S)-6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
3) (S)-6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
4) (S)-6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
5) (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
6) (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
7) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
8) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)метансульфонамид;
9) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)метансульфонамид;
10) (S)-6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
11) (S)-6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
12) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)метансульфонамид;
13) (S)-6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
14) 6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
15) (S)-6-бромо-2-(1-(3,4-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
16) 6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-N-((S)-1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
17) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-хлоробензолсульфонамид;
18) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-метилбензолсульфонамид;
19) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-этилбензолсульфонамид;
20) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензамид;
21) (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
22) (S)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-2-(1-(4-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
23) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
24) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
25) (S)-6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
26) 3-((6-бромо-2-(1-(2,6-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
27) 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
28) 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
29) 3-((6-бромо-2-(2,5-диметил-1-(4-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
30) 3-((6-бромо-2-(2,5-диметил-1-(3-(морфолиносульфонил)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
31) 3-((6-бромо-2-(1-(2-хлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
32) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-4-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
33) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
34) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-3-(метилсульфонамидо)фенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
35) 3-((6-бромо-2-(1-(2,5-дихлорофенил)-2,5-диметил-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
36) 3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пирролe-1-ил)-4-хлоробензолсульфонамид;
37) 3-((6-бромо-2-(2,5-диметил-1-(3-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
38) 3-((6-бромо-2-(2,5-диметил-1-(3-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
39) 3-((6-бромо-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
40) 3-((6-бромо-2-(2,5-диметил-1-(4-морфолинофенил)-1H-пиррол-3-ил)-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
41) 3-((2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-3H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
42) 3-((6-бромо-2-(1-(3-(2-метоксиэтокси)фенил)-2,5-диметил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
43) 3-((6-бромо-2-(2,5-диметил-1-фенил-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
44) 3-(3-(7-(бензо[d][1,3]диоксоль-5-ил-амино)-6-бромо-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
45) 2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(4-(2-метоксиэтокси)фенил)-3H-имидазо[4,5-b]пиридин-7-амин;
46) 3-(3-(6-бромо-7-((4-(2-метоксиэтокси)фенил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензолсульфонамид;
47) 3-((6-бромо-2-(2,5-диметил-1-(пиридин-3-ил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
48) 3-((6-бромо-2-(2,5-диметил-1-(пиридин-4-илметил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
49) (S)-2-(1-(бензо[d][1,3]диоксоль-5-ил)-2,5-диметил-1H-пиррол-3-ил)-6-бромо-N-(1-(этилсульфонил)пирролидин-3-ил)-3H-имидазо[4,5-b]пиридин-7-амин;
50) N-(3-(3-(7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
51) N-(3-(3-(6-хлоро-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)метансульфонамид;
52) (S)-6-хлоро-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
53) (S)-2-(2,5-диметил-1-(4-(2-морфолиноэтокси)фенил)-1H-пиррол-3-ил)-N-(1-(этилсульфонил)пирролидин-3-ил)-1H-имидазо[4,5-b]пиридин-7-амин;
54) (S)-(3-(3-(6-хлоро-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
55) (S)-(3-(3-(7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(морфолино)метанон;
56) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид;
57) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диэтиламино)этил)бензамид;
58) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота;
59) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)бензойная кислота;
60) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-((диметиламино)метил)бензамид;
61) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид;
62) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)бензамид;
63) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-N-метилбензамид;
64) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(диметиламино)ацетамид;
65) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-(4-метилпиперазин-1-ил)ацетамид;
66) (S)-N-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)-2-морфолиноацетамид;
67) (S)-(4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон;
68) (S)-(3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)фенил)(4-метилпиперазин-1-ил)метанон;
69) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид;
70) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-морфолиноэтил)бензамид;
71) (S)-3-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид;
72) (S)-4-(3-(6-бромо-7-((1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(4-метилпиперазин-1-ил)этил)бензамид;
73) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(диметиламино)ацетамид;
74) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид;
75) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
76) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
77) N-(4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)-2-морфолиноацетамид;
78) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид;
79) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропанамид;
80) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-3-(диметиламино)пропанамид;
81) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(4-метилпиперазин-1-ил)метанон;
82) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-2-метилбензамид;
83) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)(морфолино)метанон;
84) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(диметиламино)ацетамид;
85) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-морфолиноацетамид;
86) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-3-(диметиламино)пропанамид;
87) N-(3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-2-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
88) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-морфолиноацетамид;
89) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(4-метилпиперазин-1-ил)ацетамид;
90) N-(3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)-2-(диметиламино)ацетамид;
91) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(морфолино)метанон;
92) (3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-4-метилфенил)(4-метилпиперазин-1-ил)метанон;
93) 3-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид;
94) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(морфолин-4-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
95) 3-((6-бромо-2-(2,5-диметил-1-(2-метил-5-(4-метилпиперазин-1-карбонил)фенил)-1H-пиррол-3-ил)-1H-имидазо[4,5-b]пиридин-7-ил)амино)бензолсульфонамид;
96) 3-(3-(6-бромо-7-((3-сульфамоилфенил)амино)-1H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-N-(2-(диметиламино)этил)-4-метилбензамид;
97) (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(4-метилпиперазин-1-ил)метанон;
98) (4-(3-(6-бромо-7-(((S)-1-(этилсульфонил)пирролидин-3-ил)амино)-3H-имидазо[4,5-b]пиридин-2-ил)-2,5-диметил-1H-пиррол-1-ил)-3-метилфенил)(морфолино)метанон.
2. Фармацевтический препарат, содержащий соединение для профилактики или лечения рака по п.1 или его стереоизомер в качестве активного ингредиента, при этом соединение замедляет активность протеинкиназы, которая представляет собой по меньшей мере один фермент, выбранный из группы, состоящей из MLK1, MLK2, MLK3.
3. Фармацевтический препарат по п. 2, отличающийся тем, что рак представляет собой по меньшей мере одно заболевание, выбранное из группы, включающей в себя острую гранулоцитарную лейкемию, острую лимфоцитарную лейкемию, рак толстой кишки, хроническую гранулоцитную лейкемию, хроническую лимфоцитную лейкемию, рак желудка, рак груди, рак простаты, рак поджелудочной железы и рак легкого.
4. Фармацевтический препарат для профилактики или лечения нейродегенеративного заболевания, содержащий соединение по п.1 или его стереоизомер в качестве активного ингредиента, при этом соединение замедляет активность протеинкиназы, которая представляет собой по меньшей мере один фермент, выбранный из группы, состоящей из MLK1, MLK2, MLK3.
5. Фармацевтический препарат по п. 4, отличающийся тем, что нейродегенеративным заболеванием является болезнь Паркинсона.
6. Фармацевтический препарат для профилактики или лечения неалкогольного стеатогепатита, содержащий соединение по п.1 или его стереоизомер в качестве активного ингредиента, при этом соединение замедляет активность протеинкиназы, которая представляет собой по меньшей мере один фермент, выбранный из группы, состоящей из MLK1, MLK2, MLK3.
7. Фармацевтический препарат по п. 6, отличающийся тем, что неалкогольный стеатогепатит является одним из выбранных из группы, включающей неалкогольный стеатогепатит и рак печени.
8. Фармацевтический препарат для профилактики или лечения гриппа, содержащий соединение по п.1 или его стереоизомер в качестве активного ингредиента, при этом соединение замедляет активность протеинкиназы, которая представляет собой по меньшей мере один фермент, выбранный из группы, состоящей из MLK1, MLK2, MLK3.
9. Фармацевтический препарат по п. 8, отличающийся тем, что грипп является гриппом A.
| WO 2007056155 A1, 18.05.2007 | |||
| СОЕДИНЕНИЯ И СПОСОБЫ МОДУЛИРОВАНИЯ КИНАЗ И ПОКАЗАНИЯ К ПРИМЕНЕНИЮ УКАЗАННЫХ СОЕДИНЕНИЙ И СПОСОБОВ | 2008 |
|
RU2487121C2 |
| Приспособление для улавливания соломы при промывке свеклы | 1930 |
|
SU20578A1 |
| WO 2009029609 A1, 05.03.2009 | |||
| WO 2013147711 А1, 03.10.2013. | |||
Авторы
Даты
2024-01-09—Публикация
2020-08-31—Подача