ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По настоящей заявке в соответствии с 35 U.S.C. §119(e) испрашивается приоритет по предварительной заявке U.S. № 62/623312, поданной 29 января 2018 г., содержание которой во всей его полноте включено в настоящее изобретение в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0002] Настоящее изобретение относится к соединениям и способам, применимых для ингибирования общей регулирующей содержание аминокислот киназы 2 с постоянной репрессией ("GCN2"). Настоящее изобретение также относится к фармацевтически приемлемым композициям, содержащим соединения, предлагаемые в настоящем изобретении, и способам применения указанных композиций для лечения разных нарушений.
УРОВЕНЬ ТЕХНИКИ
[0003] GCN2 (общая регулирующая содержание аминокислот киназа 2 с постоянной репрессией) представляет собой повсеместно экспрессирующуюся протеинкиназу, участвующую в клеточных ответах на недостаток аминокислот в эукариотах (Castilho et al., 2014). Недостаток одной или большего количества аминокислот в клетках приводит к накоплению незаряженных родственных транспортных RNAs (tRNAs), которые прямо связывает GCN2, что приводит к активации киназы и фосфорилированию эукариотного фактора инициирования 2 α (eIF2α) по серину 51 (Wek et al., 1989; Dong et al., 2000). Фосфорилирование eIF2α приводит к инициированию трансляции белка, что вызывает уменьшение трансляции большей части mRNAs, приводящему к уменьшению общего использования аминокислот. Одновременно фосфорилирование eIF2α усиливает трансляцию специфического поднабора mRNAs, содержащих некоторые открытые рамки считывания в обратном направлении в их 5’ нетранслированных областях (5’-UTRs), таких как фактор транскрипции ATF4 у млекопитающих (Vattem and Wek, 2004), который стимулирует восстановление гомеостаза белка. Поэтому GCN2 является критическим детерминантом гибели клеток в ответ на уменьшение содержания аминокислот.
[0004] Индуцирование клеточных ответов на недостаток аминокислот оказывается важным механизмом регуляции иммунной системы млекопитающего, в особенности при некоторых заболеваниях, включающих рак и аутоиммунитет. Сообщали, что разные типы иммуносупрессивных клеток, участвующих в регулировании иммунных ответов в этих случаях, включают толерогенные дендритные клетки, супрессорные клетки миелоидного происхождения (MDSCs), толерогенные/M2 макрофаги и сами раковые клетки, используют уменьшение содержания аминокислот для подавления T-клеточных ответов (Munn et al., 2004; Munn et al., 2005; Rodriguez et al., 2010; Whyte et al., 2011; Uyttenhove et al., 2003). Это осуществляется путем внутриклеточного транспорта аминокислот, связанного со сверхэкспрессией катаболизирующих аминокислоты ферментов в этих клетках, таких как катаболизирующие триптофан ферменты индоламин-2,3-диоксигеназа (IDO) и триптофан-2,3-диоксигеназа (TDO) и катаболизирующие аргинин ферменты аргиназа 1 и 2 (ARG1, ARG2). В результате в этих клетках могут уменьшаться локальные внутриклеточные концентрации конкретных аминокислот независимо от их местонахождения и поэтому антигенспецифическим образом индуцируется активность GCN2 в находящихся рядом T-клетках (Munn et al., 2004). Показано, что у мышей in vitro и in vivo уменьшение локальных концентрации триптофана или аргинина, например, с помощью экспрессирующих IDO- или ARG1 дендритных клеток, индуцирует пролиферативную блокировку и толерантность в T-клетках зависимым от GCN2 образом (Munn et al., 2005; Rodriguez et al., 2007; Fletcher et al., 2015). Кроме того, индуцирование и/или поддержание MDSCs и иммуносупрессивных регуляторных T-клеток (T-regs) также может зависеть от активности GCN2 при условиях уменьшения содержания аминокислот (Fletcher et al., 2015; Fallarino et al., 2006). Кроме того, в другой публикации указано на участие активации GCN2 посредством IDO в толерогенных макрофагах, как ключевой механизм подавления системных аутоиммунных ответов на апоптические клетки (Ravishankar et al., 2015). Эти данные показывают, что GCN2 является возможным ключевым эффектором иммуносупрессивных эффектов уменьшения содержания аминокислот, связанных с разными патологическими состояниями.
[0005] Для разрастания начинающихся раковых заболевании необходимо обойти противораковый иммунитет хозяина (Corthay, 2014). Это можно выполнить путем модуляции представления опухолевого антигена и/или путем использования механизмов ухода опухоли от иммунного надзора для активного подавления иммунной атаки. Значительную экспрессию катаболизирующих аминокислоту ферментов, таких как IDO и ARG1, наблюдали для значительной части пациентов с раком, у которых имелись опухоли разных типов, в самих раковых клетках и в типах иммуносупрессивных клеток хозяина, которые накапливаются в опухолях, дренирующих опухоль лимфатических узлах и/или периферическом кровотоке (Uyttenhove et al., 2003; Pilotte et al., 2012; Zea et al., 2005). Поэтому уменьшение содержания аминокислот может быть эффективным и распространенным механизмом ухода опухоли от иммунного надзора, при котором ограничивается противораковый иммунитет. Установлено, что уменьшение содержания аминокислот в опухолях и дренирующих опухоль лимфатических узлах является механизмом резистентности у имеющимся иммуноонкологическим средствам, включая антитела, блокирующие рецептор контрольных точек, в некоторых сингенных моделях опухолей на мышах (Holmgaard et al., 2013; Spranger et al., 2014). В связи с этим ингибиторы IDO и TDO в настоящее время все шире используются в клинических исследованиях рака и ингибиторы катаболазы дополнительной аминокислоты находятся в доклинической разработке. Соответственно, ингибиторы GCN2 также могут быть применимы для лечения рака путем разрушения узлового эффекторного сигнала при уменьшении содержания аминокислот в иммунной системе и для обеспечения противоракового иммунного ответа. Генетическая абляция GCN2 хорошо переносится мышами при стандартных условиях роста (Zhang et al., 2002) и ингибиторы GCN2 могут найти более широкое применение, чем ингибиторы катаболазы отдельной аминокислоты, поскольку GCN2 реагирует на уменьшение содержания некоторых разных аминокислот.
[0006] Кроме того, в отличие от нормальных тканей, в разных опухолях людей наблюдалась активация и сверхэкспрессия GCN2 (Ye et al., 2010; Wang et al., 2013). Уменьшение содержания GCN2 приводило к уменьшению роста эмбриональных фибробластов у мышей и раковых клеток у людей in vitro при условиях сильного уменьшения содержания аминокислот или глюкозы и блокировало рост ксенотрансплантатов опухолей людей у мышей (Ye et al., 2010). Поэтому ингибиторы GCN2 могут оказывать прямое противораковое воздействие вследствие частого нарушения подачи питательных веществ в микроокружение опухоли.
[0007] По этим причинам необходима разработка активных и селективных ингибиторов GCN2 для лечения рака, в виде от дельных средств или в комбинации, например, с антителами, блокирующими контрольные точки CTLA4 и PD1/PD-L1.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] Установлено, что соединения, предлагаемые в настоящем изобретении, и фармацевтически приемлемые содержащие их композиции, эффективны в качестве ингибиторов GCN2 киназы. Такие соединения обладают общей формулой I:
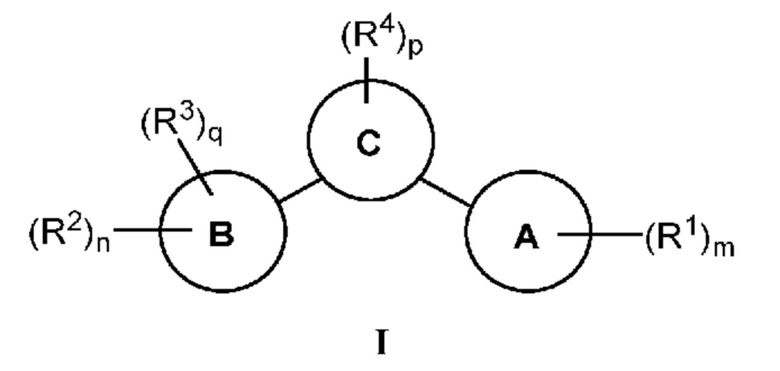
или их фармацевтически приемлемая соль, где каждая переменная является такой, как определено и описано в настоящем изобретении.
[0009] Соединения, предлагаемые в настоящем изобретении, и фармацевтически приемлемые содержащие их композиции, применимы для лечения различных заболеваний, нарушений или патологических состояний, связанных с регуляцией сигнальных путей с участием GCN2 киназы. Такие заболевания, нарушения или патологические состояния включают описанные в настоящем изобретении.
[0010] Соединения, предлагаемые в настоящем изобретении, также применимы для исследования фермента GCN2 в биологических и патологических явлениях; исследования путей внутриклеточной передачи сигналов в тканях организма; и сравнительного исследования новых ингибиторов GCN2 или других регуляторов киназ, путей передачи сигналов и содержания цитокина in vitro или in vivo.
ПОДРОБНОЕ ОПИСАНИЕ НЕКОТОРЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
1. Общее описание некоторых вариантов осуществления настоящего изобретения:
[0011] Соединения, предлагаемые в настоящем изобретении, и содержащие их композиции, применимы в качестве ингибиторов протеинкиназы GCN2. В некоторых вариантах осуществления предлагаемое соединение ингибирует GCN2.
[0012] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I:

или его фармацевтически приемлемой соли, в которой:
кольцо A выбрано из группы, включающей 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, необязательно сконденсировано с 5-6-членным ароматическим кольцом, содержащим 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное бициклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу, или
Het, где Het представляет собой 4-8-членное насыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное насыщенное спироциклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное насыщенное бициклическое гетероциклическое кольцо, содержащее 1-3 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 7-12-членное насыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
Кольцо B представляет собой
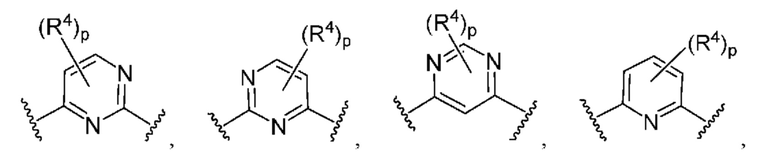
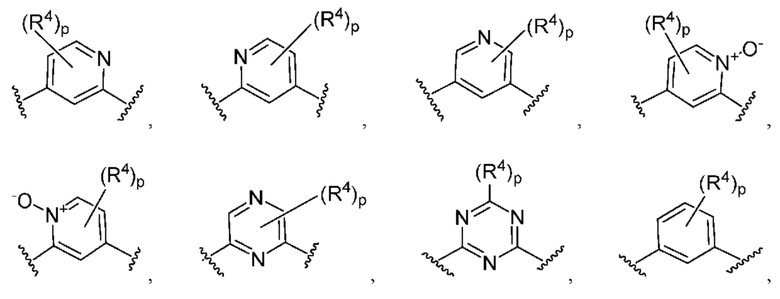
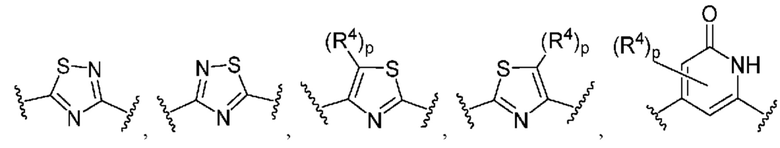
или 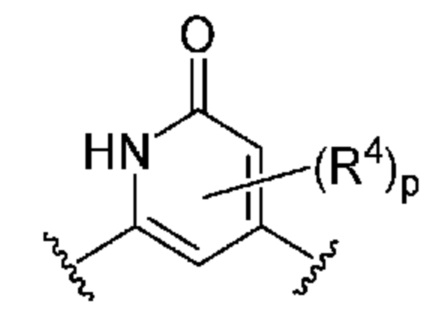 ;
;
каждый R независимо означает водород или необязательно замещенную группу, выбранную из группы, включающей C1-6 алифатическую группу, 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу; или
две группы R вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь;
две группы R необязательно вместе с находящимися между ними атомами образуют необязательно замещенное 3-7-членное насыщенное или частично ненасыщенное моноциклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
каждый R’ независимо означает водород или C1-3 алифатическую группу, необязательно замещенную галогеном;
каждый из R1 независимо означает водород, галоген, -CN, -NO2, -C(O)R, -C(O)OR, -C(O)NR2, -C(O)NRS(O)2R, -C(O)N=S(O)R2, -NR2, -NRC(O)R, -NRC(O)NR2, -NRC(O)OR, -NRS(O)2R, -NRS(O)2NR2, -OR, -ON(R)SO2R, -P(O)R2, -SR, -S(O)R, -S(O)2R, -S(O)(NH)R, -S(O)2N(R)2, -S(NH2)2(O)OH, -N=S(O)R2, -CH3, -CH2OH, -CH2NHSO2CH3, -CH3, -CH2OH, -CH2NHSO2CH3, -CD3, -CD2NRS(O)2R, или R; или:
две группы R1 вместе необязательно образуют =O, =NH или =NS(O)2R; или
две группы R1 вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь;
каждый из R2 независимо означает водород, галоген, -CN, -C(O)N(R’)2, -OR’, -N(R’)2, -S(O)2R, -S(O)2N(R)2, -O-фенил или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, фенил, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 4-8-членный насыщенный моноциклический гетероцикл, содержащий 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
R3 означает водород, галоген, -CN, -OR’, -N(R’)2 или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, фенил или 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
R4 означает водород, галоген, -CN, -OR, -N=S(O)R2, -N(R)2 или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 7-12-членное насыщенное или частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
m равно 0, 1, 2, 3, 4 или 5;
n равно 0, 1 или 2;
p равно 0 или 1; и
q равно 0 или 1.
2. Соединения и определения:
[0013] Соединения, предлагаемые в настоящем изобретении, включают описанные в целом в настоящем изобретении и они дополнительно иллюстрируются классами, подклассами и типами, раскрытыми в настоящем изобретении. При использовании в настоящем изобретении применимы следующие определения, если не указано иное. Для задач настоящего изобретения химические элементы описываются в соответствии с Периодической системой элементов, версия CAS, Handbook of Chemistry and Physics, 75th Ed. Кроме того, общие положения органической химии описаны в публикациях "Organic Chemistry", Thomas Sorrell, University Science Books, Sausalito: 1999, и "March’s Advanced Organic Chemistry", 5th Ed., Ed.: Smith, M.B. and March, J., John Wiley & Sons, New York: 2001, полные содержания которых включены в настоящее изобретение в качестве ссылки.
[0014] Термин "алифатический" или "алифатическая группа" при использовании в настоящем изобретении означает обладающую линейной цепью (т. е. неразветвленную) или разветвленную, замещенную или незамещенную углеводородную цепь, которая является полностью насыщенной или которая содержит одну или большее количество кратных связей, или моноциклический углеводород или бициклический углеводород, который является полностью насыщенным или который содержит одну или большее количество кратных связей, но не является ароматическим (также называющиеся в настоящем изобретении, как "карбоцикл", "циклоалифатический" или "циклоалкил"), который содержит одно положение присоединения к остальной части молекулы. Если не указано иное, алифатические группы содержат 1-6 алифатических атомов углерода. В некоторых вариантах осуществления алифатические группы содержат 1-5 алифатических атомов углерода. В других вариантах осуществления алифатические группы содержат 1-4 алифатических атомов углерода. В других вариантах осуществления алифатические группы содержат 1-3 алифатических атомов углерода и в других вариантах осуществления алифатические группы содержат 1-2 алифатических атомов углерода. В некоторых вариантах осуществления "циклоалифатический" (или "карбоцикл" или "циклоалкил") означает моноциклический C3-C6 углеводород, который является полностью насыщенным или который содержит одну или большее количество кратных связей, но не является ароматическим, который содержит одно положение присоединения к остальной части молекулы. Подходящие алифатические группы включают, но не ограничиваются только ими, линейные или разветвленные, замещенные или незамещенные алкильные, алкенильные, алкинильные группы и их гибриды, такие как (циклоалкил)алкил, (циклоалкенил)алкил или (циклоалкил)алкенил.
[0015] При использовании в настоящем изобретении термин "мостиковая бициклическая" означает любую бициклическую кольцевую систему, т. е. карбоциклическую или гетероциклическую, насыщенную или частично ненасыщенную, содержащую по меньшей мере один мостик. По определению IUPAC "мостик" представляет собой неразветвленную цепь атомов или атом, или валентную связь, соединяющую две головы мостика, где "головой мостика" является любой скелетный атом кольцевой системы, который связан с тремя или большим количеством скелетных атомов (исключая водород). В некоторых вариантах осуществления мостиковая бициклическая группа содержит 7-12 элементов кольца и 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. Такие мостиковые бициклические группы хорошо известны в данной области техники и включают группы, указанные ниже, где каждая группа присоединена к остальной части молекулы по любому способному к замещению атому углерода или азота. Если не указано иное, мостиковая бициклическая группа необязательно замещена одним или большим количеством заместителей, указанных для алифатических групп. Дополнительно или альтернативно, любой способный к замещению атом азота мостиковой бициклической группы необязательно является замещенным. Типичные мостиковые бициклические системы включают:
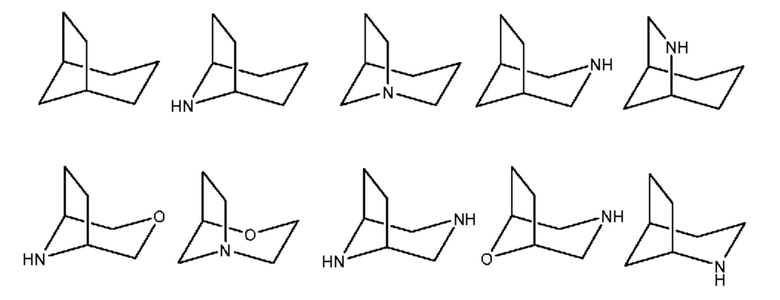
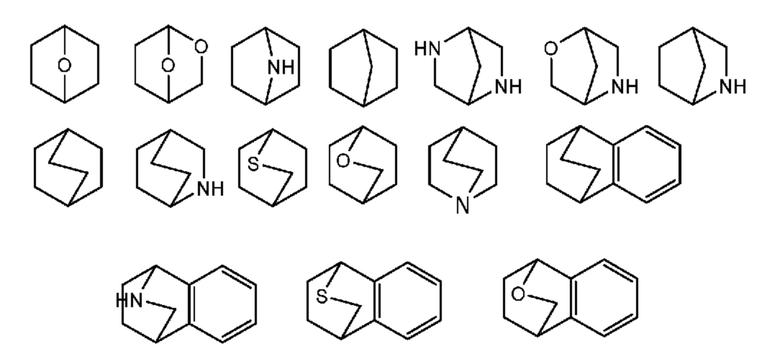
[0016] Термин "низший алкил" означает C1-4 линейную или разветвленную алкильную группу. Типичными низшими алкильными группами являются метил, этил, пропил, изопропил, бутил, изобутил и трет-бутил.
[0017] Термин "низший галогеналкил" означает C1-4 линейную или разветвленную алкильную группу, которая замещена одним или большим количеством атомов галогенов.
[0018] Термин "гетероатом" означает один или большее количество атомов кислорода, серы, азота, фосфора или кремния (включая любую окисленную форму азота, серы, фосфора или кремния; кватернизованную форму любого основного атома азота или; способный к замещению атом азота гетероциклического кольца, например, N (как в 3,4-дигидро-2H-пирролиле), NH (как в пирролидиниле) или NR+ (как в N-замещенном пирролидиниле)).
[0019] Термин "ненасыщенный" при использовании в настоящем изобретении означает, что фрагмент содержит одну или большее количество кратных связей.
[0020] При использовании в настоящем изобретении термин "двухвалентная C1-8 (или C1-6) насыщенная или ненасыщенная, линейная или разветвленная, углеводородная цепь" означает двухвалентные алкиленовые, алкениленовые и алкиниленовые цепи, которые являются линейными или разветвленными, как определено в настоящем изобретении.
[0021] Термин "алкилен" означает двухвалентную алкильную группу. "Алкиленовая цепь" представляет собой полиметиленовую группу, т. е. -(CH2)n-, где n является положительным целым числом, предпочтительно равным от 1 до 6, от 1 до 4, от 1 до 3, от 1 до 2 или от 2 до 3. Замещенная алкиленовая цепь представляет собой полиметиленовую группу, в которой один или большее количество метиленовых атомов водорода заменены заместителем. Подходящие заместители включают описанные ниже для замещенной алифатической группы.
[0022] Термин "алкенилен" означает двухвалентную алкенильную группу. Замещенная алкениленовая цепь представляет собой полиметиленовую группу, содержащую по меньшей мере одну двойную связь, в которой один или большее количество атомов водорода заменены заместителем. Подходящие заместители включают описанные ниже для замещенной алифатической группы.
[0023] При использовании в настоящем изобретении термин "циклопропиленил" означает двухвалентную циклопропильную группу следующей структуры: 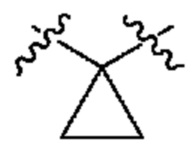 .
.
[0024] Термин "галоген" означает F, Cl, Br или I.
[0025] Термин "арил" при использовании по отдельности или в качестве части более крупного фрагмента, такого как "арилалкил", "арилалкоксигруппа" или "арилоксиалкил", означает моноциклические или бициклические кольцевые системы, содержащие всего от 5 до 14 элементов кольца, где по меньшей мере одно кольцо в системе является ароматическим и где каждое кольцо в системе содержит от 3 до 7 элементов кольца. Термин "арил" можно использовать взаимозаменяемым образом с термином "арильное кольцо". В некоторых вариантах осуществления настоящего изобретения, "арил" означает ароматическую кольцевую систему, которая включает, но не ограничивается только ими, фенил, бифенил, нафтил, антрацил и т. п., который может содержать один или большее количество заместителей. В объем термина "арил", как он используется в настоящем изобретении, также входит группа, в которой ароматическое кольцо сконденсировано с одним или большим количеством неароматических колец, такая как инданил, фталимидил, нафтимидил, фенантридинил или тетрагидронафтил и т. п.
[0026] Термины "гетероарил" и "гетероар-", при использовании по отдельности или в качестве части более крупного фрагмента, например, "гетероарилалкил" или "гетероарилалкоксигруппа", означают группы, содержащие от 5 до 10 кольцевых атомов, предпочтительно 5, 6 или 9 кольцевых атомов; содержащие 6, 10 или 14 π-электронов, обобщенных в циклической системе; и содержащие в дополнение к атомам углерода от 1 до 5 гетероатомов. Термин "гетероатом" означает азот, кислород или серу и включает любую окисленную форму азота или серы и любую кватернизованную форму основного атома азота. Гетероарильные группы включают, без наложения ограничений, тиенил, фуранил, пирролил, имидазолил, пиразолил, триазолил, тетразолил, оксазолил, изоксазолил, оксадиазолил, тиазолил, изотиазолил, тиадиазолил, пиридил, пиридазинил, пиримидинил, пиразинил, индолизинил, пуринил, нафтиридинил и птеридинил. Термины "гетероарил" и "гетероар-" при использовании в настоящем изобретении также включают группы, в которых гетероароматическое кольцо сконденсировано с одним или большим количеством арильных, циклоалифатических или гетероциклильных колец, где радикал или положение присоединения находится в гетероароматическом кольце. Неограничивающие примеры включают индолил, изоиндолил, бензотиенил, бензофуранил, дибензофуранил, индазолил, бензимидазолил, бензтиазолил, хинолил, изохинолил, циннолинил, фталазинил, хиназолинил, хиноксалинил, 4H-хинолизинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил, тетрагидрохинолинил, тетрагидроизохинолинил и пиридо[2,3-b]-1,4-оксазин-3(4H)-он. Гетероарильная группа может быть моно- или бициклической. Термин "гетероарил" можно использовать взаимозаменяемым образом с терминами "гетероарильное кольцо", "гетероарильная группа" или "гетероароматический", любой из этих терминов включают кольца, которые являются необязательно замещенными. Термин "гетероарилалкил" означает алкильную группу, замещенную гетероарилом, где алкильные и гетероарильные фрагменты независимо являются необязательно замещенными.
[0027] При использовании в настоящем изобретении термины "гетероцикл", "гетероциклил", "гетероциклический радикал" и "гетероциклическое кольцо" используют взаимозаменяемым образом и означают стабильный 5-7-членный моноциклический или 7-10-членный бициклический гетероциклический фрагмент, который является насыщенным или частично ненасыщенным и содержит в дополнение к атомам углерода один или большее количество, предпочтительно от 1 до 4 гетероатомов, определенных выше. При использовании применительно к кольцевому атому гетероцикла термин "азот" включает замещенный азот. В качестве примера в насыщенном или частично ненасыщенном кольце, содержащем 0-3 гетероатома, выбранных из группы, включающей кислород, серу или азот, азот может представлять собой N (как в 3,4-дигидро-2H-пирролиле), NH (как в пирролидиниле) или +NR (как в N-замещенном пирролидиниле).
[0028] Гетероциклическое кольцо может быть присоединено к своей боковой группе по любому гетероатому или атому углерода, если это приводит к стабильной структуре и любой из кольцевых атомов необязательно замещенным. Примеры таких насыщенных или частично ненасыщенных гетероциклических радикалов включают, без наложения ограничений, тетрагидрофуранил, тетрагидротиофенилпирролидинил, пиперидинил, пирролинил, тетрагидрохинолинил, тетрагидроизохинолинил, декагидрохинолинил, оксазолидинил, пиперазинил, диоксанил, диоксоланил, диазепинил, оксазепинил, тиазепинил, морфолинил и хинуклидинил. Термины "гетероцикл", "гетероциклил", "гетероциклильное кольцо", "гетероциклическая группа", "гетероциклический фрагмент" и "гетероциклический радикал" используют взаимозаменяемым образом в настоящем изобретении и также включают группы, в которых гетероциклильное кольцо сконденсировано с одним или большим количеством арильных, гетероарильных или циклоалифатических колец, такие как индолинил, 3H-индолил, хроманил, фенантридинил или тетрагидрохинолинил. Гетероциклильная группа может быть моно- или бициклической. Термин "гетероциклилалкил" означает алкильную группу, замещенную гетероциклилом, где алкильные и гетероциклильные фрагменты независимо являются необязательно замещенными.
[0029] При использовании в настоящем изобретении термин "частично ненасыщенный" означает кольцевой фрагмент, который включает по меньшей мере одну двойную или тройную связь. Термин "частично ненасыщенный" включает кольца, включающие несколько кратных связей, но не включает арильные или гетероарильные фрагменты, определенные в настоящем изобретении.
[0030] Как указано в настоящем изобретении, соединения, предлагаемые в настоящем изобретении, могут содержать "необязательно замещенные" фрагменты. Обычно термин "замещенный", независимо от того, находится ли перед ним термин "необязательно", означает, что один или большее количество атомов водорода указанного фрагмента заменены подходящим заместителем. Если не указано иное, "необязательно замещенная" группа может содержать подходящий заместитель в каждом способном к замещению положении группы и, если более, чем одно положение в любой данной структуре может быть замещено более, чем одним заместителем, выбранным из заданной группы, заместители в разных положениях могут быть одинаковыми или разными. Комбинациями заместителей, приведенных в настоящем изобретении, предпочтительно являются такими, которые приводят к образованию стабильных или химически возможных соединений. Термин "стабильное" при использовании в настоящем изобретении означает соединения, которые существенно не меняются при условиях, обеспечивающих их получение, обнаружение и, в некоторых вариантах осуществления их извлечение, очистку и применение для одной или большего количества задач, раскрытых в настоящем изобретении.
[0031] Подходящие одновалентные заместители по способному к замещению атому углерода "необязательно замещенной" группы независимо являются галоген; -(CH2)0-4R°; -(CH2)0-4OR°; -O(CH2)0-4Ro, -O-(CH2)0-4C(O)OR°; -(CH2)0-4CH(OR°)2; -(CH2)0-4SR°; -(CH2)0-4Ph, который может быть замещен группой R°; -(CH2)0-4O(CH2)0-1Ph, который может быть замещен группой R°; -CH=CHPh, который может быть замещен группой R°; -(CH2)0-4O(CH2)0-1-пиридил, который может быть замещен группой R°; -NO2; -CN; -N3; -(CH2)0-4N(R°)2; -(CH2)0-4N(R°)C(O)R°; -N(R°)C(S)R°; -(CH2)0-4N(R°)C(O)NR°2; -N(R°)C(S)NR°2; -(CH2)0-4N(R°)C(O)OR°; -N(R°)N(R°)C(O)R°; -N(R°)N(R°)C(O)NR°2; -N(R°)N(R°)C(O)OR°; -(CH2)0-4C(O)R°; -C(S)R°; -(CH2)0-4C(O)OR°; -(CH2)0-4C(O)SR°; -(CH2)0-4C(O)OSiR°3; -(CH2)0-4OC(O)R°; -OC(O)(CH2)0-4SR-, —SC(S)SR°; -(CH2)0-4SC(O)R°; -(CH2)0-4C(O)NR°2; -C(S)NR°2; -C(S)SR°; -(CH2)0-4OC(O)NR°2; -C(O)N(OR°)R°; -C(O)C(O)R°; -C(O)CH2C(O)R°; -C(NOR°)R°; -(CH2)0-4SSR°; -(CH2)0-4S(O)2R°; -(CH2)0-4S(O)2OR°; -(CH2)0-4OS(O)2R°; -S(O)2NR°2; -(CH2)0-4S(O)R°; -(CH2)0-4S(O)(NR°)R°; -N(R°)S(O)2NR°2; -N(R°)S(O)2R°; -N(R°)S(O)(NR°)R°2; -N(OR°)R°; -N=S(O)R°2; -N(OR°)SO2R°; -C(NH)NR°2; -P(O)2R°; -P(O)R°2; -OP(O)R°2; -OP(O)(OR°)2; -SiR°3; -(C1-4 линейный или разветвленный алкилен)O-N(R°)2; или -(C1-4 линейный или разветвленный алкилен)C(O)O-N(R°)2, где каждый R° может быть замещен, как определено ниже, и независимо означает водород, C1-6 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph, -CH2-(5-6-членное гетероарильное кольцо) или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или, независимо от приведенного выше определения, два независимо содержащихся R°, вместе с находящимся между ними атомом (атомами) образуют 3-12-членное насыщенное, частично ненасыщенное или арильное моно- или бициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, которое может быть замещенным, как определено ниже.
[0032] Подходящие одновалентные заместители у R° (или в кольце, образованном из двух независимо содержащихся R° вместе с находящимися между ними атомами), независимо означают галоген, -(CH2)0-2Rλ, -(галоген-Rλ), -(CH2)0-2OH, -(CH2)0-2ORλ, -(CH2)0-2CH(ORλ)2; -O(галоген-Rλ), -CN, -N3, -(CH2)0-2C(O)Rλ, -(CH2)0-2C(O)OH, -(CH2)0-2C(O)ORλ, -(CH2)0-2SRλ, -(CH2)0-2SH, -(CH2)0-2NH2, -(CH2)0-2NHRλ, -(CH2)0-2NRλ2, -NO2, -SiRλ3, -OSiRλ3, -C(O)SRλ, -(C1-4 линейный или разветвленный алкилен)C(O)ORλ или -SSRλ, где каждый Rλ является незамещенным или, если перед ним указан "галоген", замещен только одним или большим количеством галогенов и независимо выбран из группы, включающей C1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. Подходящие двухвалентные заместители у насыщенного атома углерода в R° включают =O и =S.
[0033] Подходящие двухвалентные заместители у насыщенного атома углерода в "необязательно замещенной" группе включают следующие: =O, =S, =NNR*2, =NNHC(O)R*, =NNHC(O)OR*, =NNHS(O)2R*, =NR*, =NOR*, -O(C(R*2))2-3O-, или -S(C(R*2))2-3S-, где в каждом независимом случае появления R* выбран из группы, включающей водород, C1-6 алифатическую группу которое может быть замещенным, как определено ниже, или незамещенное 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. Подходящие двухвалентные заместители, которые связаны с вицинальными способными к замещению атомами углерода "необязательно замещенной" группы включают: -O(CR*2)2-3O-, где в каждом независимом случае появления R* выбран из группы, включающей водород, C1-6 алифатическую группу которое может быть замещенным, как определено ниже, или незамещенное 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0034] Подходящие заместители алифатической группы в R* включают галоген, -Rλ, -(галоген-Rλ), -OH, -ORλ, -O(галоген-Rλ), -CN, -C(O)OH, -C(O)ORλ, -NH2, -NHRλ, -NRλ2, или -NO2, где каждый Rλ является незамещенным или, если перед ним указан "галоген", замещен только одним или большим количеством галогенов и независимо означает C1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0035] Подходящие заместители по способному к замещению атому азота в "необязательно замещенной" группе включают -R†, -NR†2, -C(O)R†, -C(O)OR†, -C(O)C(O)R†, -C(O)CH2C(O)R†, -S(O)2R†, -S(O)2NR†2, -C(S)NR†2, -C(NH)NR†2 или -N(R†)S(O)2R†; где каждый R† независимо означает водород, C1-6 алифатическую группу которое может быть замещенным, как определено ниже, незамещенный -OPh или незамещенное 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или, независимо от приведенного выше определения, два независимо содержащихся R† вместе с находящимся между ними атомом (атомами) образуют незамещенное 3-12-членное насыщенное, частично ненасыщенное или арильное моно- или бициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0036] Подходящие заместители алифатической группы в R† независимо означают галоген, -Rλ, -(галоген-Rλ), -OH, -ORλ, -O(галоген-Rλ), -CN, -C(O)OH, -C(O)ORλ, -NH2, -NHRλ, -NRλ2, или -NO2, где каждый Rλ является незамещенным или, если перед ним указан "галоген", замещен только одним или большим количеством галогенов и независимо означает C1-4 алифатическую группу, -CH2Ph, -O(CH2)0-1Ph или 5-6-членное насыщенное, частично ненасыщенное или арильное кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0037] При использовании в настоящем изобретении термин "фармацевтически приемлемая соль" означает соли, которые по результатам тщательной медицинской клинической оценки являются подходящими для соприкосновения с тканями людей и низших животных без нежелательной токсичности, раздражения, аллергической реакции и т. п. и соответствуют разумному отношению польза/риск. Фармацевтически приемлемые соли хорошо известны в данной области техники. Например, S. M. Berge et al., подробно описали фармацевтически приемлемые соли в публикации J. Pharmaceutical Sciences, 1977, 66, 1-19, которая включена в настоящее изобретение в качестве ссылки. Фармацевтически приемлемые соли соединений, предлагаемых в настоящем изобретении, включают образованные из подходящих неорганических и органических кислот и оснований. Примерами фармацевтически приемлемых, нетоксичных солей присоединения с кислотами являются соли амина, образованные с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и хлорная кислота, или с органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота или по другим методикам, использующимся в данной области техники, таким как ионный обмен. Другие фармацевтически приемлемые соли включают адипат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептаноат, гексаноат, гидройодид, 2-гидроксиэтансульфонат, лактобионат, лактат, лаурат, лаурилсульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат, ундеканоат, валерат и т. п.
[0038] Соли, образованные из подходящих оснований, включают соли щелочного металла, щелочноземельного металла, аммония и N+(C1-4алкил)4. Типичные соли щелочного или щелочноземельного металла l включают соли натрия, лития, калия, кальция, магния и т. п. Другие фармацевтически приемлемые соли включают, если они являются подходящими, нетоксичные соли аммониевого, четвертичного аммониевого и аминного катионов, образованные с противоионами, такими как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, низший алкилсульфонат и арилсульфонат.
[0039] Если не указано иное, структуры, приведенные в настоящем изобретении, также включают все изомерные (например, энантиомерные, диастереоизомерные и геометрические (или конформационные)) формы структуры; например, R и S конфигурации каждого асимметрического центра, Z и E изомеры относительно двойных связей и Z и E конформационные изомеры. Поэтому, отдельные стреохимические изомеры, а также энантиомерные, диастереоизомерные и геометрические (или конформационные) смеси соединений, предлагаемых в настоящем изобретении, входят в объем настоящего изобретения. Если не указано иное, все таутомерные формы соединений, предлагаемых в настоящем изобретении, входят в объем настоящего изобретения. Кроме того, если не указано иное, структуры, приведенные в настоящем изобретении, также включают соединения, которые различаются только присутствием одного или большего количества изотопно обогащенных атомов. Например, соединения, обладающие предлагаемыми структурами, включая в которых имеется замена водорода на дейтерий или тритий или замена углерода на 13C- или 14C-обогащенный углерод, входят в объем настоящего изобретения. Такие соединения применимы, например, в качестве аналитических средств, в качестве зондов в биологических исследованиях или в качестве терапевтических средств в соответствии с настоящим изобретением. В некоторых вариантах осуществления Rx в предлагаемом соединении включает один или большее количество атомов дейтерия.
[0040] При использовании в настоящем изобретении термин "ингибитор" определяется, как соединение, которое связывается с и/или ингибирует GCN2 с измеримым сродством. В некоторых вариантах осуществления ингибитор обладает значением IC50 и/или константы связывания, равным менее примерно 50 мкМ, менее примерно 1 мкМ, менее примерно 500 нМ, менее примерно 100 нМ, менее примерно 10 нМ или менее примерно 1 нМ.
[0041] Соединение, предлагаемое в настоящем изобретении, может быть привязано детектируемым фрагментом. Следует понимать, что такие соединения применимы в качестве визуализирующих средств. Специалист с общей подготовкой в данной области техники должен понимать, что детектируемый фрагмент может быть присоединен к предлагаемому соединению с помощью подходящего заместителя. При использовании в настоящем изобретении термин "подходящий заместитель" означает фрагмент, который способен к ковалентному присоединению к детектируемому фрагменту. Такие фрагменты хорошо известны специалисту с общей подготовкой в данной области техники и включают группы, содержащие, например, карбоксилатный фрагмент, аминный фрагмент, тиольный фрагмент или гидроксильный фрагмент, если указать только некоторые примеры. Следует понимать, что такие фрагменты могут быть прямо присоединены к предлагаемому соединению или через присоединенную группу, такую как двухвалентная насыщенная или ненасыщенная углеводородная цепь. В некоторых вариантах осуществления такие фрагменты могут быть присоединены с помощью клик-химии. В некоторых вариантах осуществления такие фрагменты могут быть присоединены посредством 1,3-циклоприсоединения азида к алкину, необязательно в присутствии медного катализатора. Методики использования клик-химии известны в данной области техники и включают описанные в публикации Rostovtsev et al., Angew. Chem. Int. Ed. 2002, 41, 2596-99 и Sun et al., Bioconjugate Chem., 2006, 17, 52-57.
[0042] При использовании в настоящем изобретении термин "детектируемый фрагмент" используется взаимозаменяемым образом с термином "метка" и относится к любому фрагменту, способному к детектированию, например, первичные метки и вторичные метки. Первичные метки, такие как радиоизотопы (например, тритий, 32P, 33P, 35S или 14C), масс-спектрометрические метки и флуоресцентные метки являются генерирующими сигналы репортерными группами, которые можно детектировать без дополнительных модификаций. Детектируемые фрагменты также включают люминесцентные и фосфоресцентные группы.
[0043] Термин "вторичная метка" при использовании в настоящем изобретении означает фрагменты, такие как биотин и разные антигены белков, в которых для выработки детектируемого сигнала необходимо наличие второго промежуточного продукта. Для биотина вторичный промежуточный продукт может включать конъюгаты стрептавидин-фермент. Для антигенных меток вторичные промежуточные продукты могут включать конъюгаты антитело-фермент. Некоторые флуоресцентные группы действуют, как вторичные метки, поскольку они переносят энергию к другой группе в процессе безызлучательного флуоресцентного резонансного переноса энергии (FRET) и вторая группа вырабатывает детектируемый сигнал.
[0044] Термины "флуоресцентная метка", "флуоресцентный краситель" и "флуорофор" при использовании в настоящем изобретении означают фрагменты, которые поглощают световую энергию при определенной длине волны возбуждения и испускают световую энергию при другой длине волны. Примеры флуоресцентных меток включают, но не ограничиваются только ими: красители Alexa Fluor (Alexa Fluor 350, Alexa Fluor 488, Alexa Fluor 532, Alexa Fluor 546, Alexa Fluor 568, Alexa Fluor 594, Alexa Fluor 633, Alexa Fluor 660 и Alexa Fluor 680), AMCA, AMCA-S, красители BODIPY (BODIPY FL, BODIPY R6G, BODIPY TMR, BODIPY TR, BODIPY 530/550, BODIPY 558/568, BODIPY 564/570, BODIPY 576/589, BODIPY 581/591, BODIPY 630/650, BODIPY 650/665), карбоксиродамин 6G, карбокси-X-родамин (ROX), Cascade Blue, Cascade Yellow, кумарин 343, цианиновые красители (Cy3, Cy5, Cy3,5, Cy5,5), Dansyl, Dapoxyl, диалкиламинокумарин, 4',5'-дихлор-2',7'-диметоксифлуоресцеин, DM-NERF, эозин, эритрозин, флуоресцеин, FAM, гидроксикумарин, красители IRD (IRD40, IRD 700, IRD 800), JOE, Lissamine родамин B, Marina Blue, метоксикумарин, нафтофлуоресцеин, Oregon Green 488, Oregon Green 500, Oregon Green 514, Pacific Blue, PyMPO, пирен, родамин B, родамин 6G, родамин Green, родамин Red, Rhodol Green, 2',4',5',7'-тетрабромульфонфлуоресцеин, тетраметилродамин (TMR), карбокситетраметилродамин (TAMRA), Texas Red, Texas Red-X.
[0045] Термин "масс-спектрометрическая метка" при использовании в настоящем изобретении означает любой фрагмент, который можно однозначно детектировать по его массе с использованием методик детектирования посредством масс-спектрометрии (MS). Примеры масс-спектрометрических меток включают высвобождающие электрофор метки, такие как N-[3-[4’-[(п-метокситетрафторбензил)окси]фенил]-3-метилглицеронил]изонипекотиновая кислота, 4’-[2,3,5,6-тетрафтор-4-(пентафторфенокси)]метилацетофенон и их производные. Синтез и использование этих масс-спектрометрических меток описаны в патентах U.S. 4650750, 4709016, 53608191, 5516931, 5602273, 5604104, 5610020 и 5650270. Другие примеры масс-спектрометрических меток включают, но не ограничиваются только ими, нуклеотиды, дидезоксинуклеотиды, олигонуклеотиды разной длины и основного состава, олигопептиды, олигосахариды и другие синтетические полимеры разной длины и с разным составом мономеров. В качестве масс-спектрометрических меток также можно использовать большое количество органических молекул, нейтральных и заряженных (биомолекулы или синтетические соединения) с подходящим диапазоном молекулярных масс (100-2000 Да).
[0046] Термины "измеримое сродство" и "измеримо ингибирование" при использовании в настоящем изобретении означает измеримое изменение активности протеинкиназы GCN2 при переходе от образца, содержащего соединение, предлагаемое в настоящем изобретении, или содержащую его композицию и протеинкиназу GCN2, к эквивалентному образцу, содержащему протеинкиназу GCN2, при отсутствии указанного соединения или содержащей его композиции.
3. Описание типичных вариантов осуществления:
[0047] Как указано выше, в некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I:
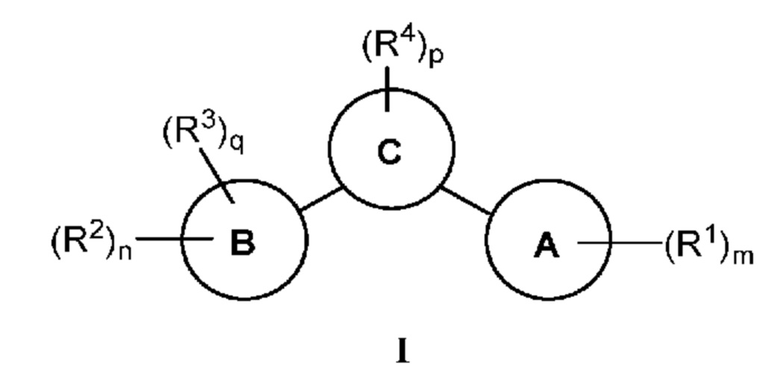
или его фармацевтически приемлемой соли, в которой:
кольцо A выбрано из группы, включающей 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, необязательно сконденсировано с 5-6-членным ароматическим кольцом, содержащим 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное бициклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу, или
Het, где Het представляет собой 4-8-членное насыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное насыщенное спироциклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное насыщенное бициклическое гетероциклическое кольцо, содержащее 1-3 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 7-12-членное насыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
Кольцо B представляет собой

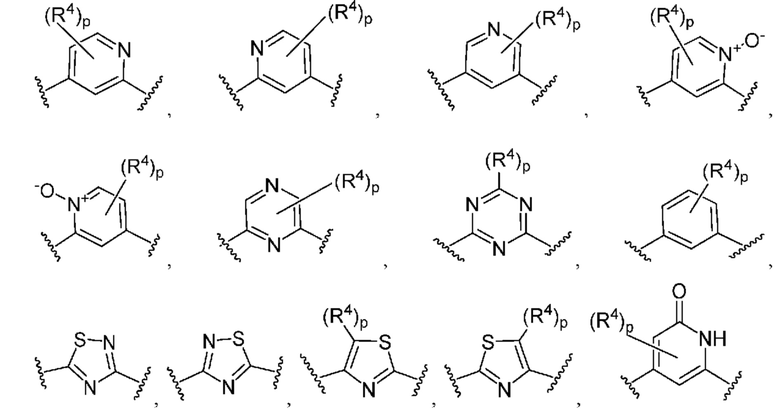
или 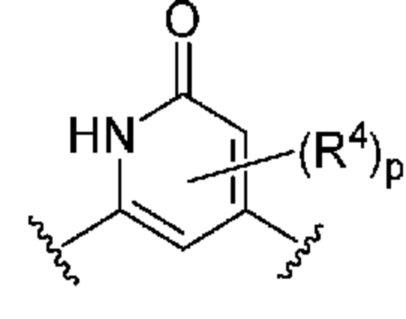 ;
;
каждый R независимо означает водород или необязательно замещенную группу, выбранную из группы, включающей C1-6 алифатическую группу, 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу; или
две группы R вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь;
две группы R необязательно вместе с находящимися между ними атомами образуют необязательно замещенное 3-7-членное насыщенное или частично ненасыщенное моноциклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
каждый R’ независимо означает водород или C1-3 алифатическую группу, необязательно замещенную галогеном;
каждый из R1 независимо означает водород, галоген, -CN, -NO2, -C(O)R, -C(O)OR, -C(O)NR2, -C(O)NRS(O)2R, -C(O)N=S(O)R2, -NR2, -NRC(O)R, -NRC(O)NR2, -NRC(O)OR, -NRS(O)2R, -NRS(O)2NR2, -OR, -ON(R)SO2R, -P(O)R2, -SR, -S(O)R, -S(O)2R, -S(O)(NH)R, -S(O)2N(R)2, -S(NH2)2(O)OH, -N=S(O)R2, -CH3, -CH2OH, -CH2NHSO2CH3, -CD3, -CD2NRS(O)2R, или R; или:
две группы R1 вместе необязательно образуют =O или =NH; или
две группы R1 вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь;
каждый из R2 независимо означает водород, галоген, -CN, -C(O)N(R’)2, -OR’, -N(R’)2, -S(O)2R, -S(O)2N(R)2, -O-фенил или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, фенил, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 4-8-членный насыщенный моноциклический гетероцикл, содержащий 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
R3 означает водород, галоген, -CN, -OR’, -N(R’)2 или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, фенил, или 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
R4 означает водород, галоген, -CN, -OR, -N=S(O)R2, -N(R)2 или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 7-12-членное насыщенное или частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
m равно 0, 1, 2, 3, 4 или 5;
n равно 0, 1 или 2;
p равно 0 или 1; и
q равно 0 или 1.
[0048] Как определено выше и указано в настоящем изобретении, кольцо A выбрано из группы, включающей 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, необязательно сконденсировано с 5-6-членным ароматическим кольцом, содержащим 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное бициклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное частично ненасыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу, или Het, где Het представляет собой 4-8-членное насыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное насыщенное спироциклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 7-12-членное насыщенное бициклическое гетероциклическое кольцо, содержащее 1-3 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 7-12-членное насыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0049] В некоторых вариантах осуществления кольцо A представляет собой 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо. В некоторых вариантах осуществления кольцо A представляет собой фенил. В некоторых вариантах осуществления кольцо A представляет собой 8-10-членное бициклическое ароматическое карбоциклическое кольцо. В некоторых вариантах осуществления кольцо A представляет собой 4-8-членное частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, необязательно сконденсировано с 5-6-членным ароматическим кольцом, содержащим 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 7-12-членное частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 7-12-членное частично ненасыщенное бициклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 7-12-членное частично ненасыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу.
[0050] В некоторых вариантах осуществления кольцо A представляет собой Het. В некоторых вариантах осуществления кольцо A представляет собой 4-8-членное насыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 7-12-членное насыщенное спироциклическое гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 7-12-членное насыщенное бициклическое гетероциклическое кольцо, содержащее 1-3 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления кольцо A представляет собой 7-12-членное насыщенное мостиковое бициклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0051] В некоторых вариантах осуществления кольцо A представляет собой 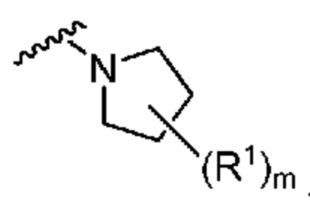 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 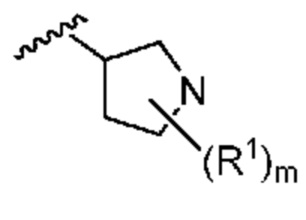 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 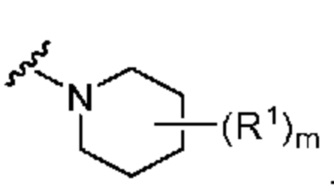 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 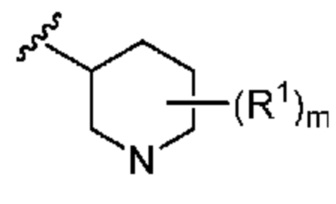 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 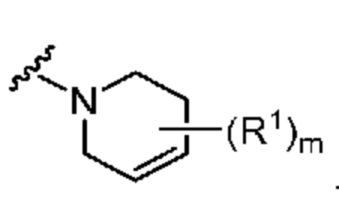 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 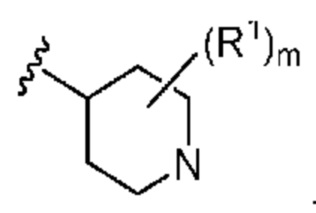 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 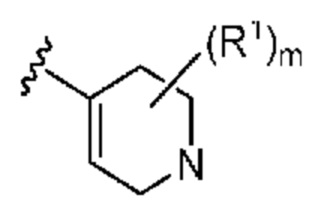 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 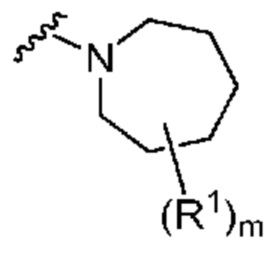 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 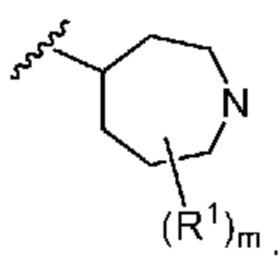 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 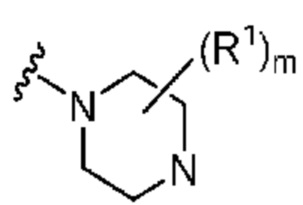 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 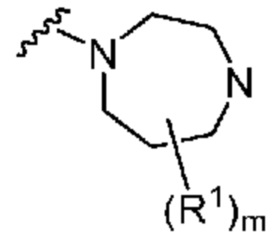 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 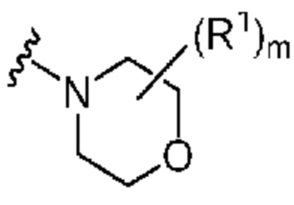 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 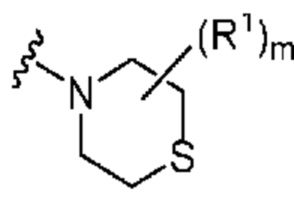 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 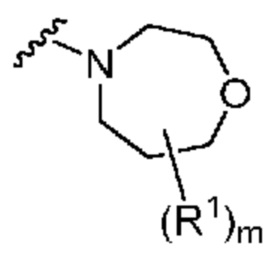 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 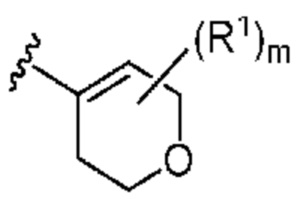 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 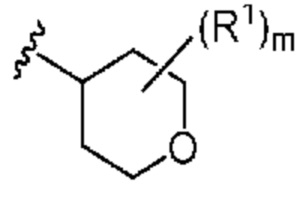 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 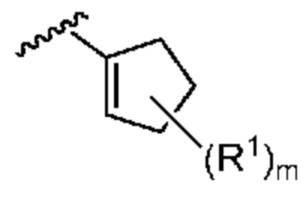 .
.
[0052] В некоторых вариантах осуществления кольцо A представляет собой 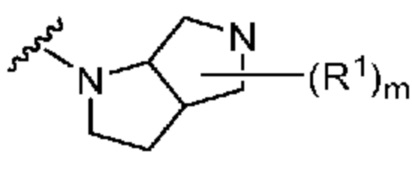 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 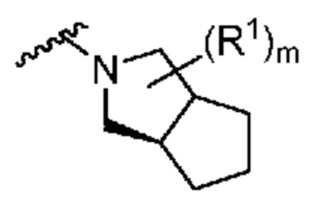 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 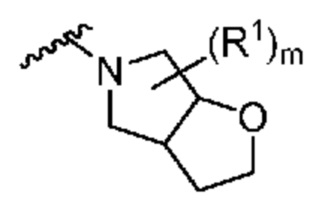 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 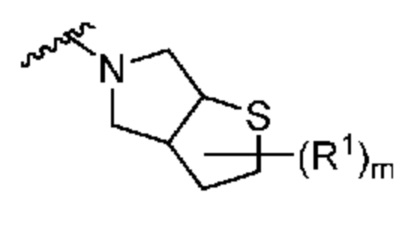 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 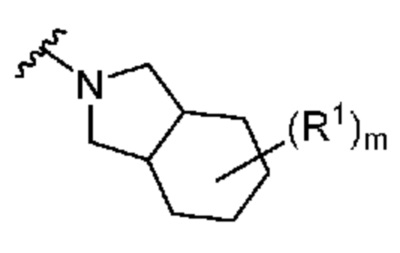 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 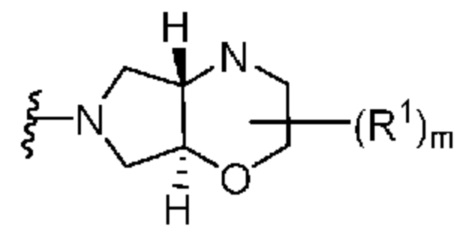 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 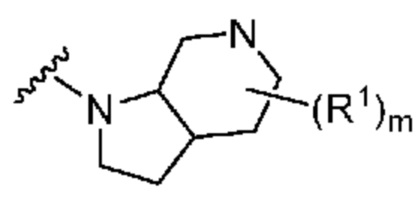 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 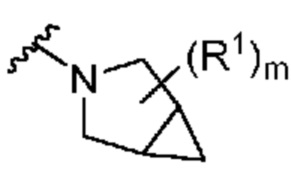 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 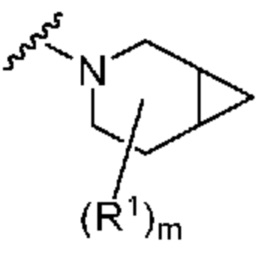 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 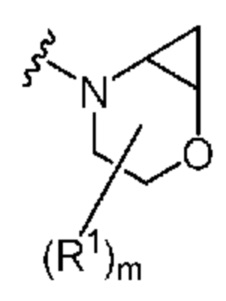 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 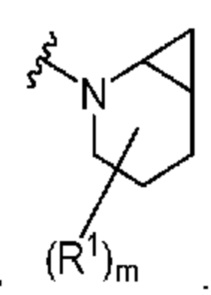 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 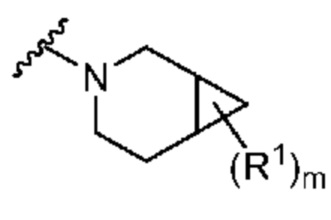 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 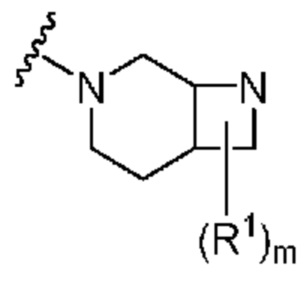 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 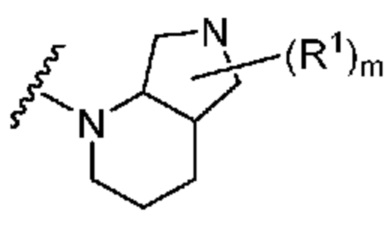 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 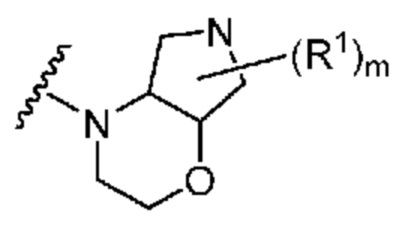 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 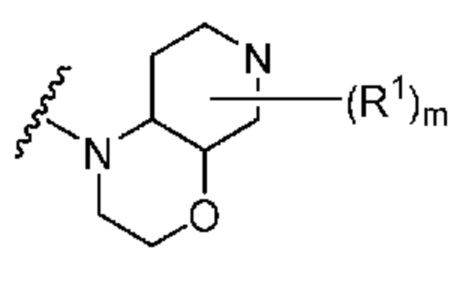 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 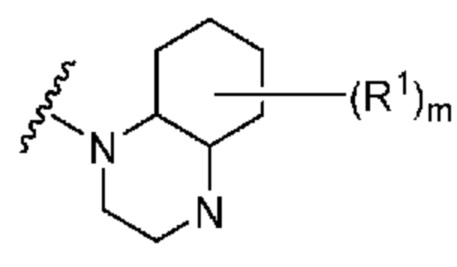 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 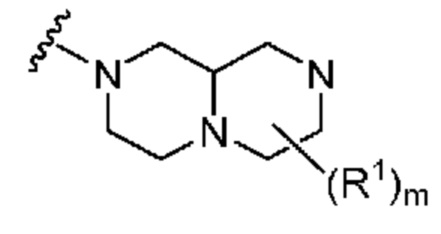 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 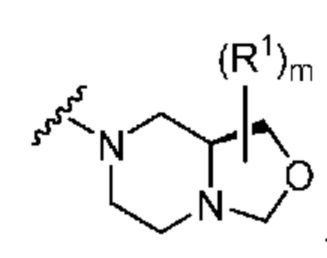 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 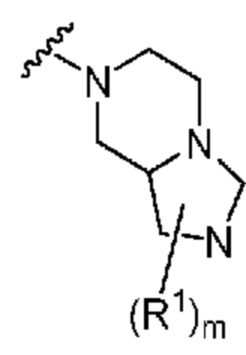 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 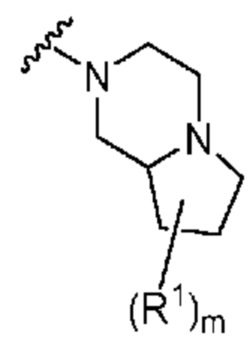 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 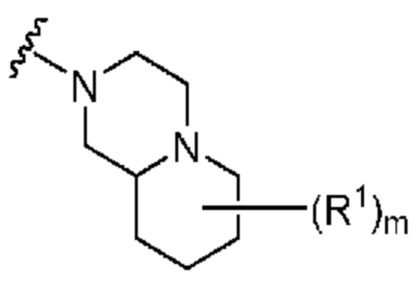 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 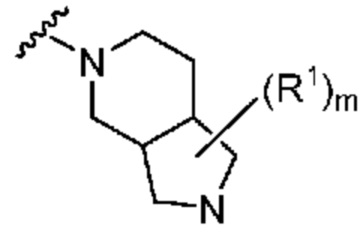 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 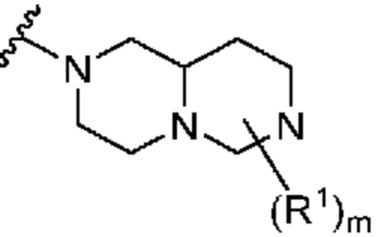 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 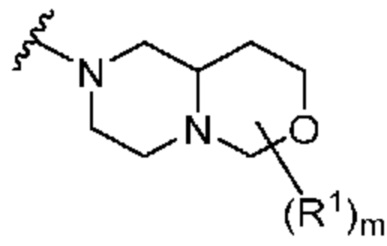 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 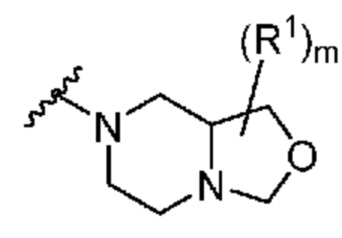 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 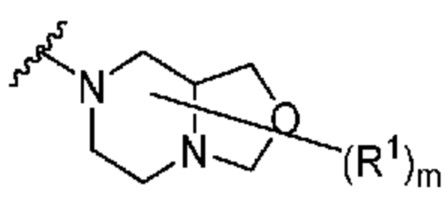 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 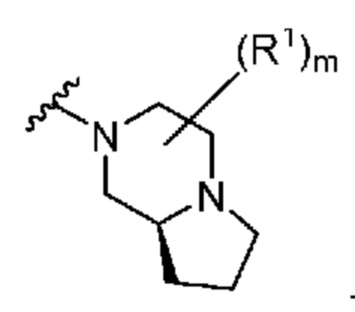 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 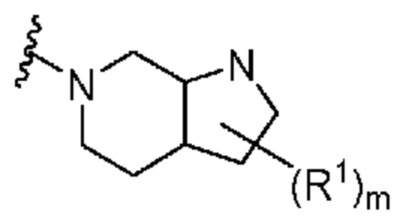 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 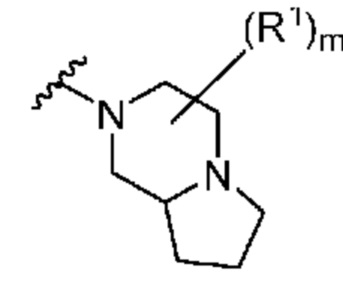 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 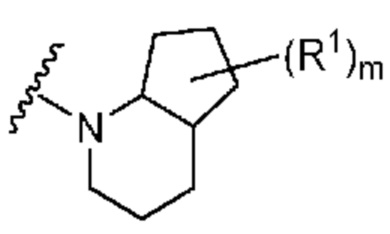 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 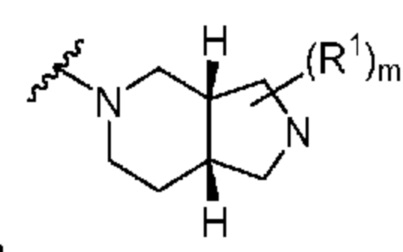 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 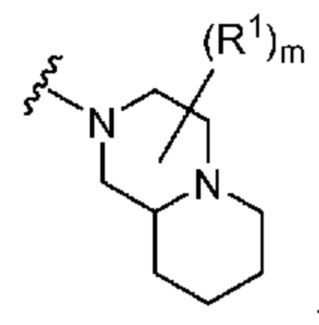 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 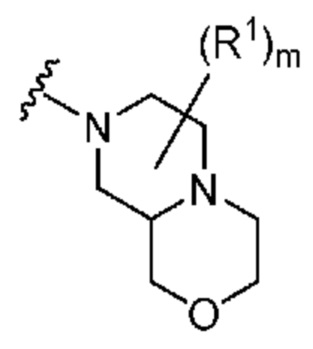 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 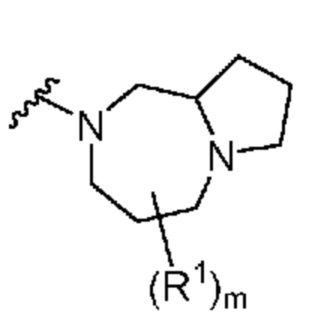 .
.
[0053] В некоторых вариантах осуществления кольцо A представляет собой 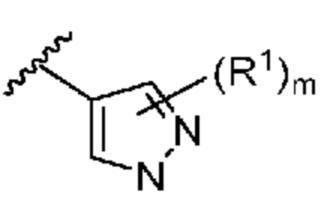 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 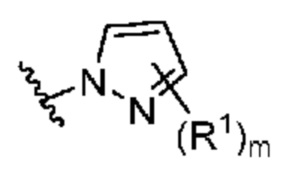 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 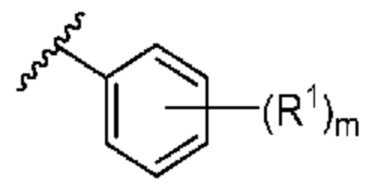 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 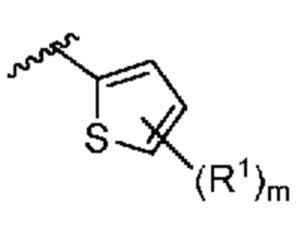 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 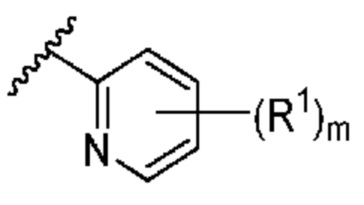 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 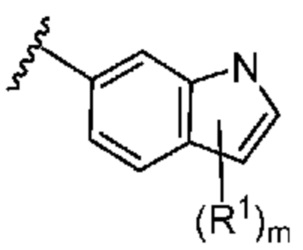 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 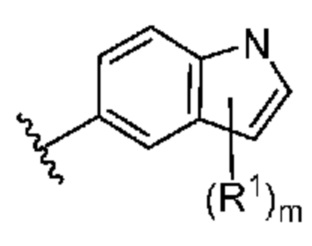 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 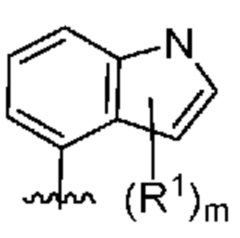 .
.
[0054] В некоторых вариантах осуществления кольцо A представляет собой 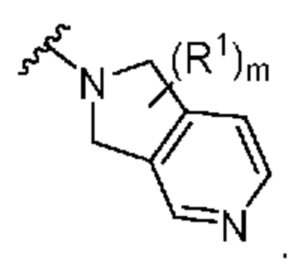 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 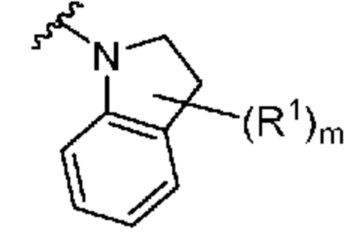 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 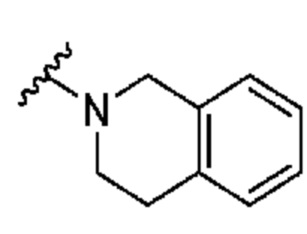 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 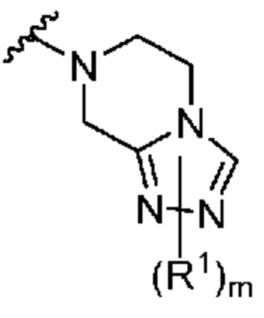 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 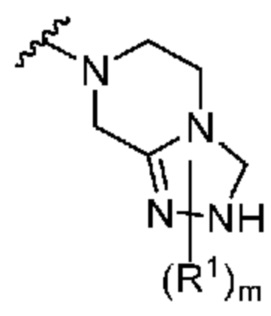 .
.
[0055] В некоторых вариантах осуществления кольцо A представляет собой 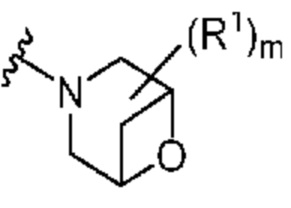 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 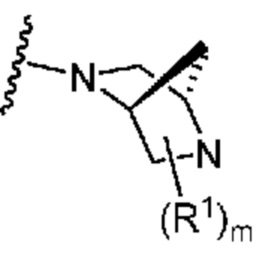 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 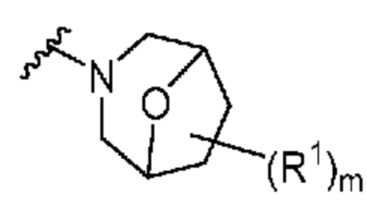 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 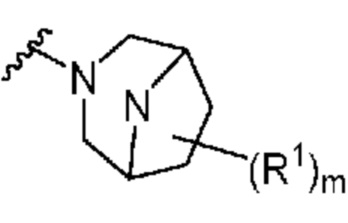 .
.
[0056] В некоторых вариантах осуществления кольцо A представляет собой 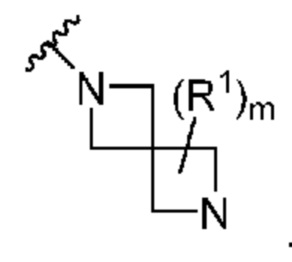 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 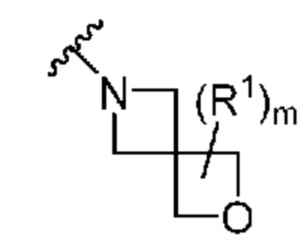 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 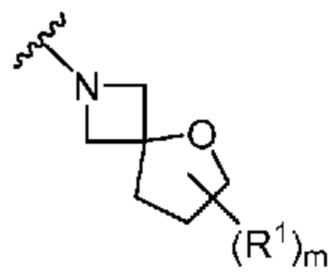 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 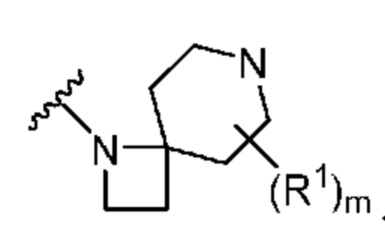 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 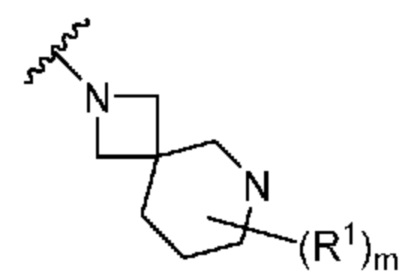 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 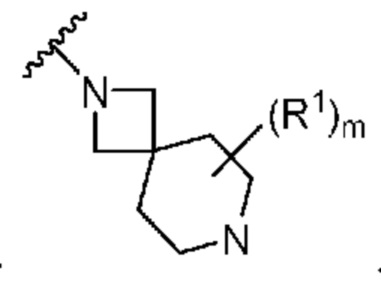 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 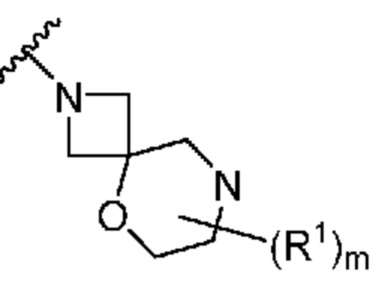 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 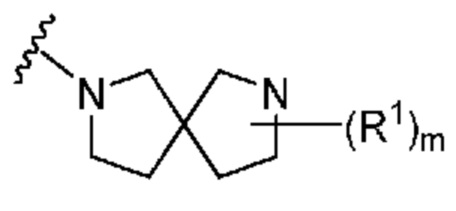 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 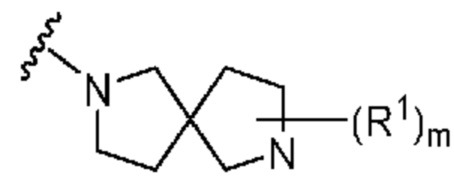 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 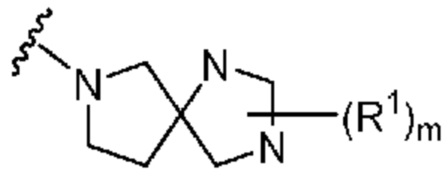 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 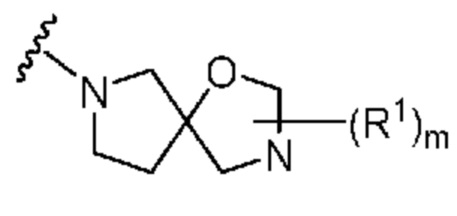 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 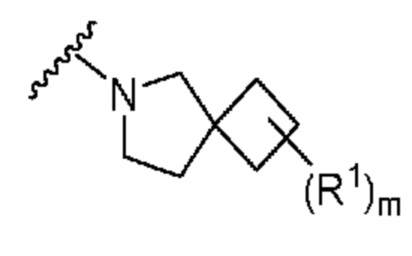 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 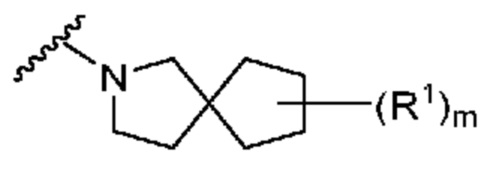 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 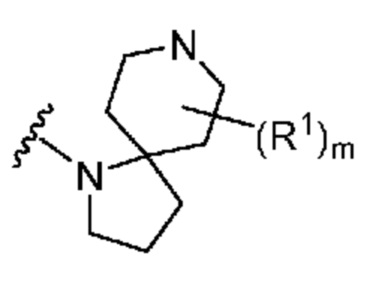 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 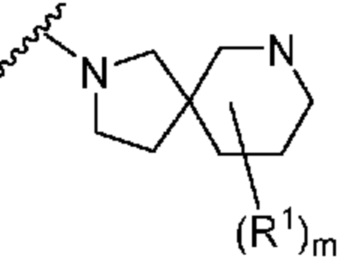 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 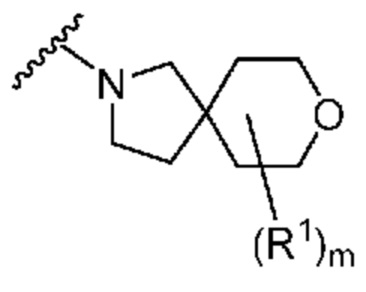 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 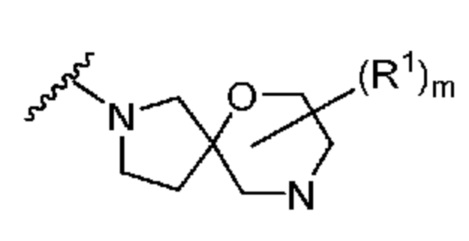 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 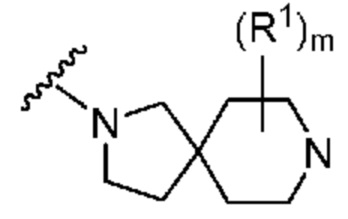 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 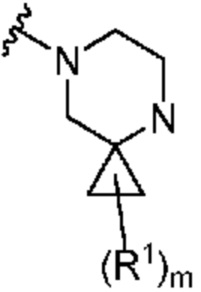 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 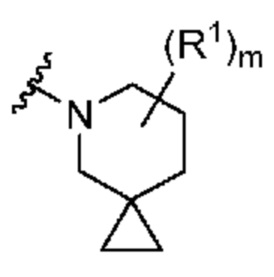 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 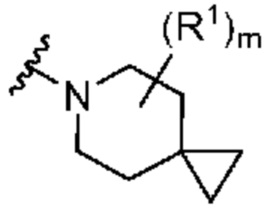 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 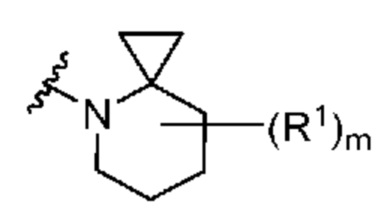 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 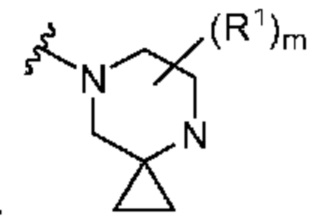 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 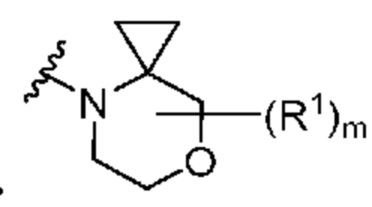 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 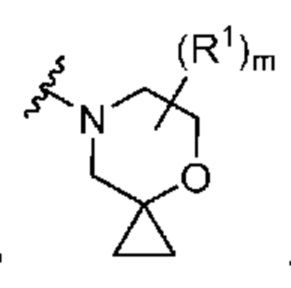 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 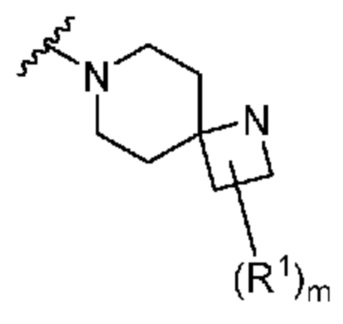 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 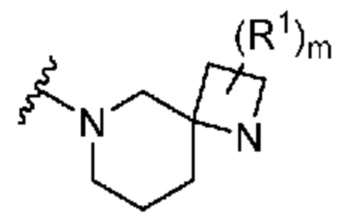 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 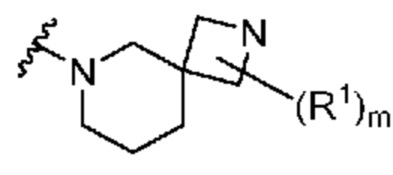 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 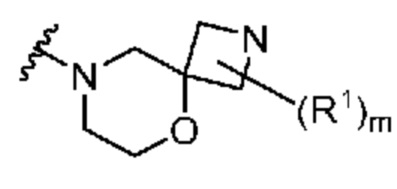 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 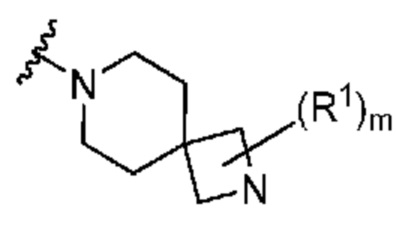 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 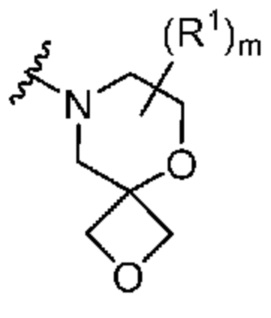 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 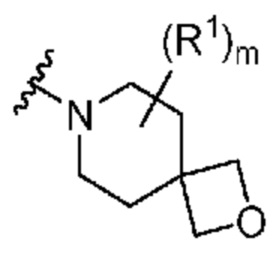 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 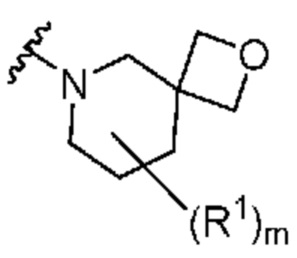 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 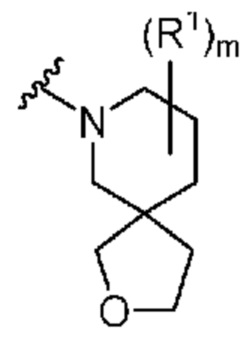 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 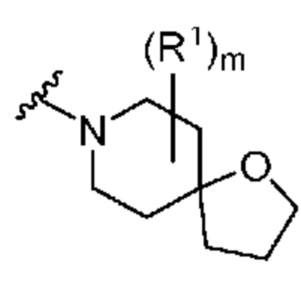 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 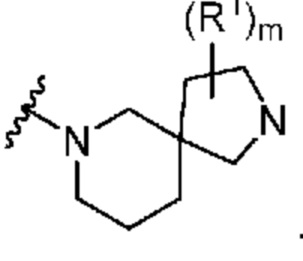 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 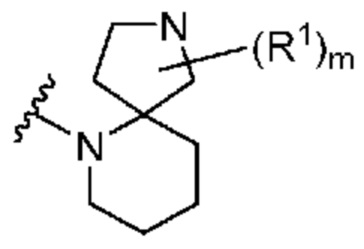 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 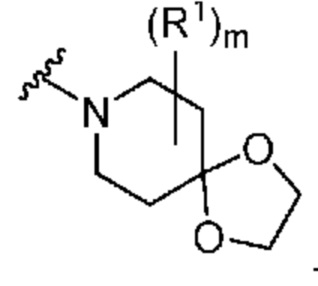 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 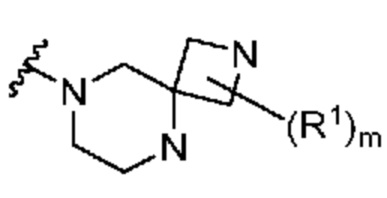 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 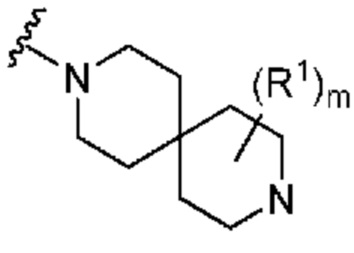 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 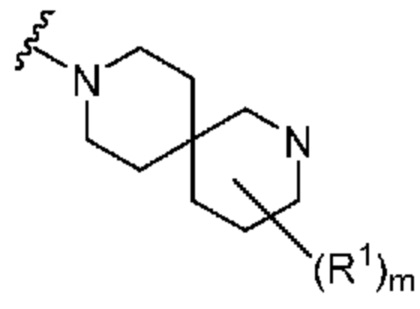 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 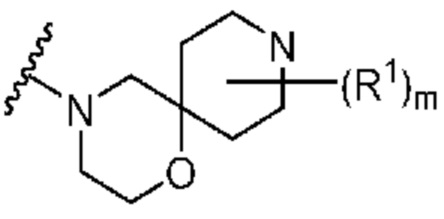 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 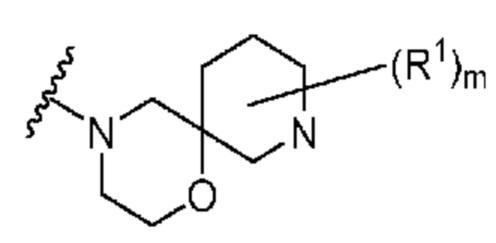 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 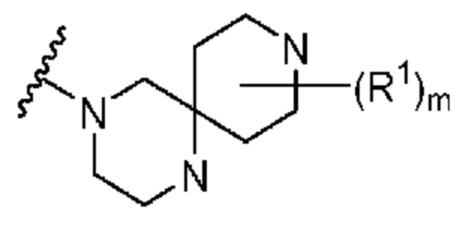 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 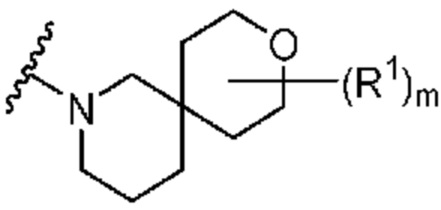 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 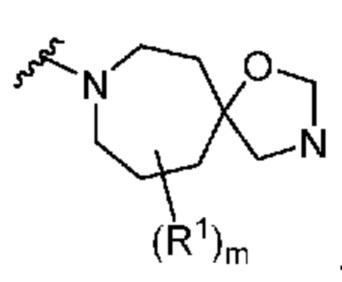 . В некоторых вариантах осуществления кольцо A представляет собой
. В некоторых вариантах осуществления кольцо A представляет собой 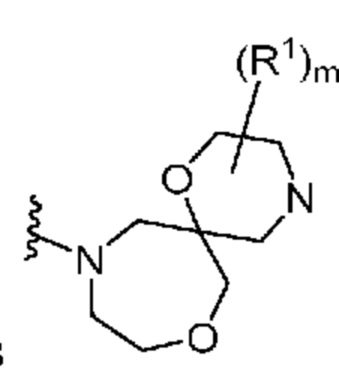 .
.
[0057] В некоторых вариантах осуществления кольцо A выбрано из числа структур, приведенных в таблице 1 ниже.
[0058] Как определено выше и указано в настоящем изобретении, кольцо B представляет собой



или  .
.
[0059] В некоторых вариантах осуществления кольцо B представляет собой 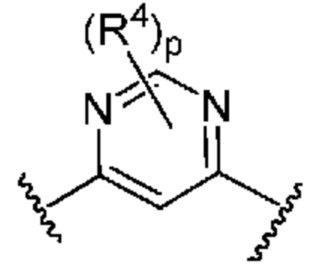 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 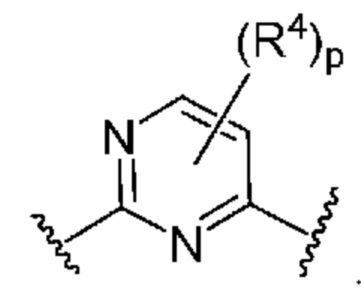 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 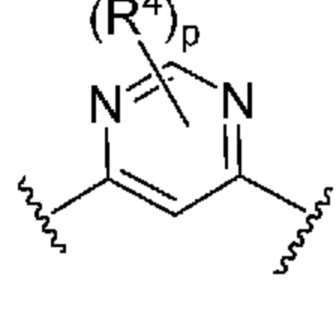 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 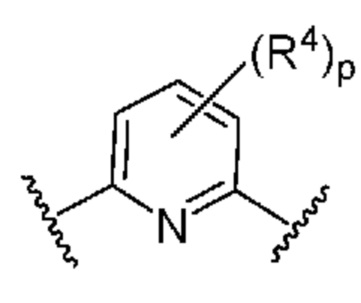 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 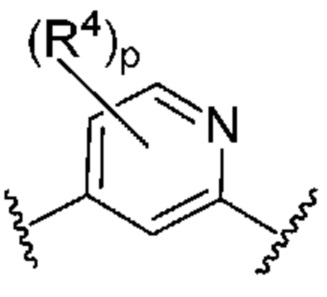 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 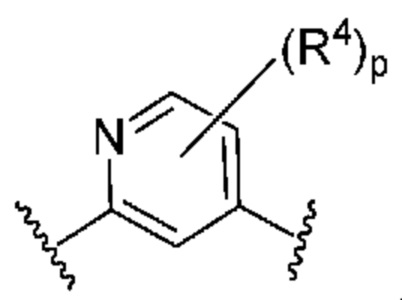 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 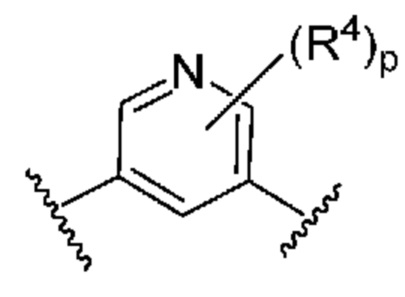 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 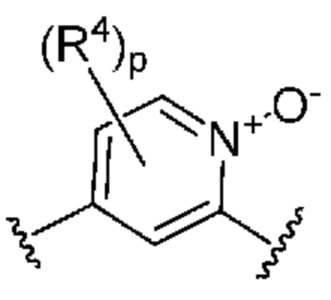 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 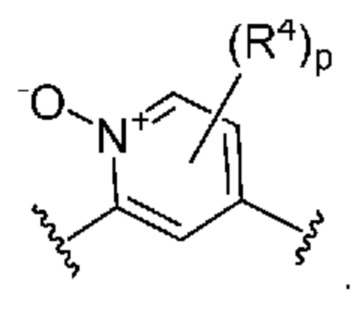 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 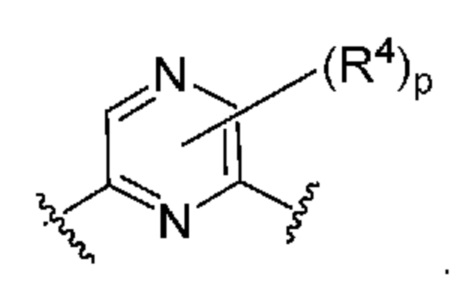 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 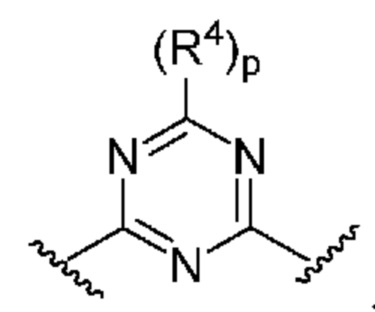 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 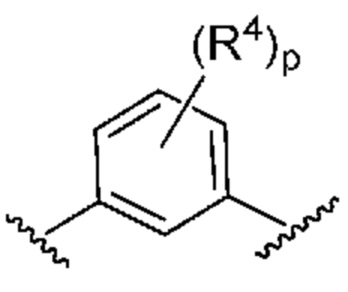 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 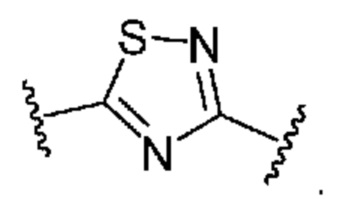 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 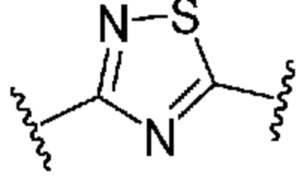 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 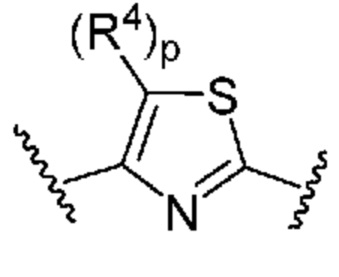 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 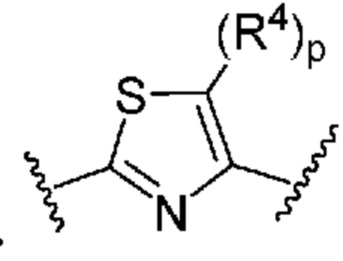 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 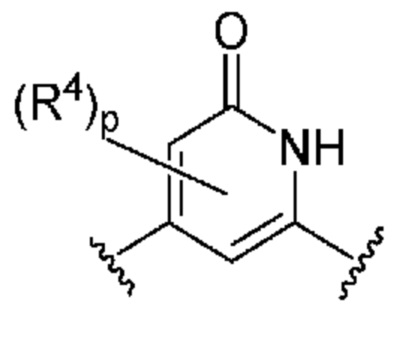 . В некоторых вариантах осуществления кольцо B представляет собой
. В некоторых вариантах осуществления кольцо B представляет собой 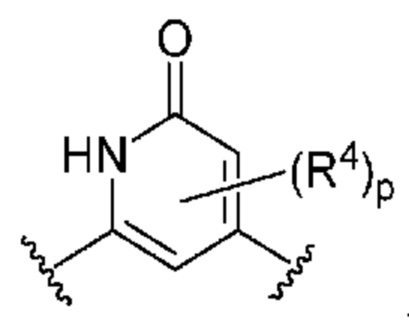 .
.
[0060] В некоторых вариантах осуществления кольцо B выбрано из числа структур, приведенных в таблице 1 ниже.
[0061] Как определено выше и указано в настоящем изобретении, каждый R независимо означает водород или необязательно замещенную группу, выбранную из группы, включающей C1-6 алифатическую группу, 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу; или две группы R вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь; или две группы R необязательно вместе с находящимися между ними атомами образуют необязательно замещенное 3-7-членное насыщенное или частично ненасыщенное моноциклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0062] В некоторых вариантах осуществления R означает водород. В некоторых вариантах осуществления R означает необязательно замещенную C1-6 алифатическую группу. В некоторых вариантах осуществления R означает необязательно замещенное 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо. В некоторых вариантах осуществления R означает необязательно замещенный фенил. В некоторых вариантах осуществления R означает необязательно замещенное 8-10-членное бициклическое ароматическое карбоциклическое кольцо. В некоторых вариантах осуществления R означает необязательно замещенное 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления R означает необязательно замещенное 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления R означает необязательно замещенное 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления две группы R вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь. В некоторых вариантах осуществления две группы R необязательно вместе с находящимися между ними атомами образуют необязательно замещенное 3-7-членное насыщенное или частично ненасыщенное моноциклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0063] В некоторых вариантах осуществления R выбран из числа структур, приведенных в таблице 1 ниже.
[0064] Как определено выше и указано в настоящем изобретении, каждый из R’ независимо означает водород или C1-3 алифатическую группу, необязательно замещенную галогеном.
[0065] В некоторых вариантах осуществления R’ означает водород. В некоторых вариантах осуществления R’ означает C1-3 алифатическую группу, необязательно замещенную галогеном.
[0066] В некоторых вариантах осуществления R’ выбран из числа структур, приведенных в таблице 1 ниже.
[0067] Как определено выше и указано в настоящем изобретении, каждый из R1 независимо означает водород, галоген, -CN, -NO2, -C(O)R, -C(O)OR, -C(O)NR2, -C(O)NRS(O)2R, -C(O)N=S(O)R2, -NR2, -NRC(O)R, -NRC(O)NR2, -NRC(O)OR, -NRS(O)2R, -NRS(O)2NR2, -OR, -ON(R)SO2R, -P(O)R2, -SR, -S(O)R, -S(O)2R, -S(O)(NH)R, -S(O)2N(R)2, -S(NH2)2(O)OH, -N=S(O)R2, -CH3, -CH2OH, -CH2NHSO2CH3, -CD3, -CD2NRS(O)2R, или R; или: две группы R1 вместе необязательно образуют =O или =NH; или две группы R1 вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь.
[0068] В некоторых вариантах осуществления R1 означает водород. В некоторых вариантах осуществления R1 означает галоген. В некоторых вариантах осуществления R1 означает -CN. В некоторых вариантах осуществления R1 означает -NO2. В некоторых вариантах осуществления R1 означает -C(O)R. В некоторых вариантах осуществления R1 означает -C(O)OR. В некоторых вариантах осуществления R1 означает -C(O)NR2. В некоторых вариантах осуществления R1 означает -C(O)NRS(O)2R. В некоторых вариантах осуществления R1 означает -C(O)N=S(O)R2. В некоторых вариантах осуществления R1 означает -NR2. В некоторых вариантах осуществления R1 означает -NRC(O)R. В некоторых вариантах осуществления R1 означает -NRC(O)NR2. В некоторых вариантах осуществления R1 означает -NRC(O)OR. В некоторых вариантах осуществления R1 означает -NRS(O)2R. В некоторых вариантах осуществления R1 означает -NRS(O)2NR2. В некоторых вариантах осуществления R1 означает -OR. В некоторых вариантах осуществления R1 означает -ON(R)SO2R. В некоторых вариантах осуществления R1 означает -P(O)R2. В некоторых вариантах осуществления R1 означает -SR. В некоторых вариантах осуществления R1 означает -S(O)R. В некоторых вариантах осуществления R1 означает -S(O)2R. В некоторых вариантах осуществления R1 означает -S(O)(NH)R. В некоторых вариантах осуществления R1 означает -S(O)2N(R)2. В некоторых вариантах осуществления R1 означает -S(NH2)2(O)OH. В некоторых вариантах осуществления R1 означает -N=S(O)R2. В некоторых вариантах осуществления R1 означает -CD3. В некоторых вариантах осуществления R1 означает -CD2NRS(O)2R. В некоторых вариантах осуществления R1 означает R. В некоторых вариантах осуществления две группы R1 вместе необязательно образуют =O или =NH. В некоторых вариантах осуществления две группы R1 вместе необязательно образуют двухвалентную C2-4 алкиленовую цепь.
[0069] В некоторых вариантах осуществления R1 означает фтор. В некоторых вариантах осуществления R1 означает хлор. В некоторых вариантах осуществления R1 означает метил. В некоторых вариантах осуществления R1 означает этил. В некоторых вариантах осуществления R1 означает -OH. В некоторых вариантах осуществления R1 означает -OCH3. В некоторых вариантах осуществления R1 означает -CH2OH. В некоторых вариантах осуществления R1 означает -CH2CN. В некоторых вариантах осуществления R1 означает -CF3. В некоторых вариантах осуществления R1 означает -CH2NH2. В некоторых вариантах осуществления R1 означает -COOH. В некоторых вариантах осуществления R1 означает -NH2.
[0070] В некоторых вариантах осуществления две группы R1 образуют =O. В некоторых вариантах осуществления две группы R1 образуют =NH. В некоторых вариантах осуществления две группы R1 образуют 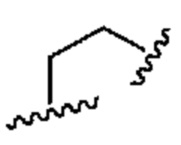 .
.
[0071] В некоторых вариантах осуществления R1 означает 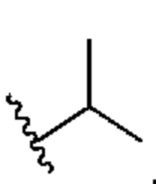 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 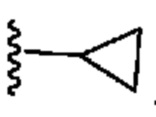 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 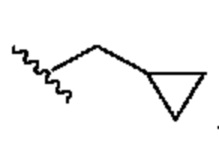 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает  . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 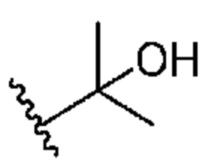 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 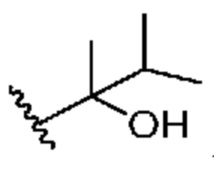 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 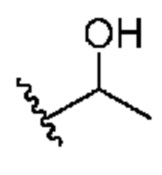 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 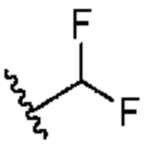 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 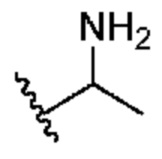 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 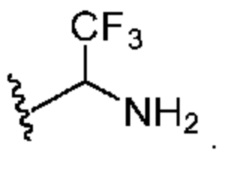 .
.
[0072] В некоторых вариантах осуществления R1 означает 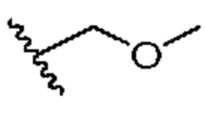 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 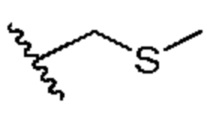 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 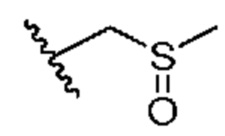 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 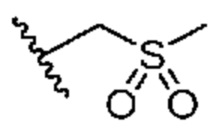 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 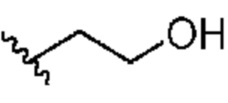 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает  . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 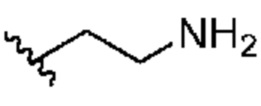 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 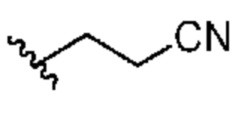 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 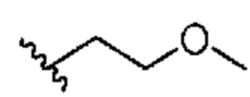 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 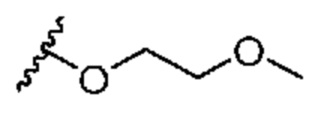 .
.
[0073] В некоторых вариантах осуществления R1 означает 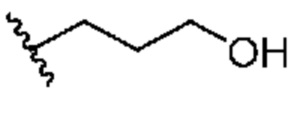 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 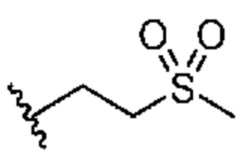 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 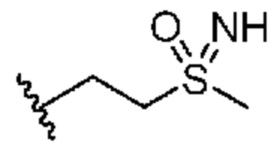 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 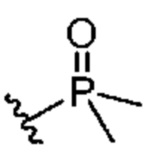 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 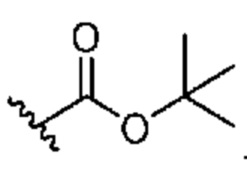 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 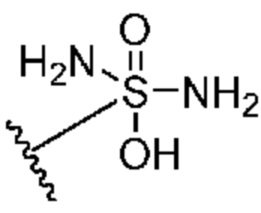 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 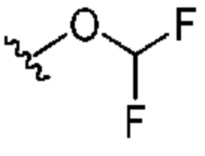 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 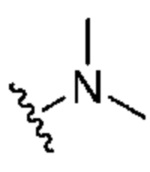 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 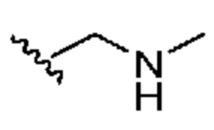 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 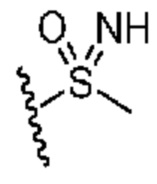 .
.
[0074] В некоторых вариантах осуществления R1 означает 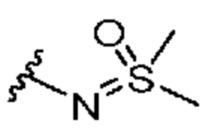 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 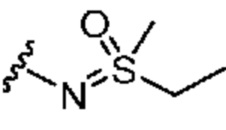 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 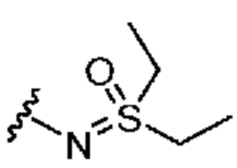 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 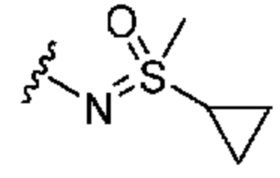 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 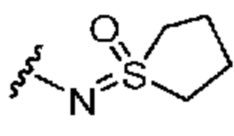 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 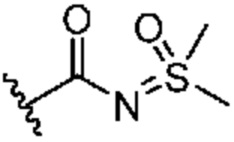 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 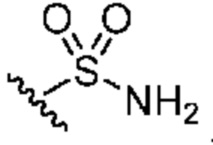 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 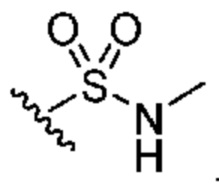 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 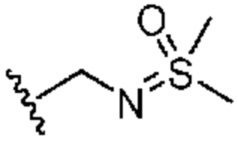 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 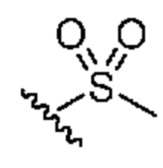 .
.
[0075] В некоторых вариантах осуществления R1 означает 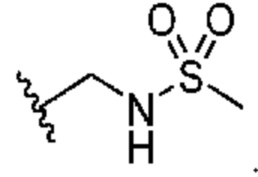 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 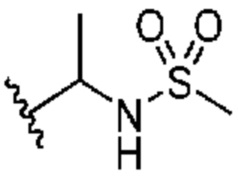 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 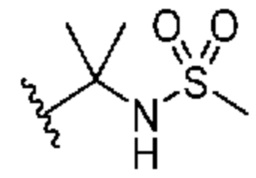 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 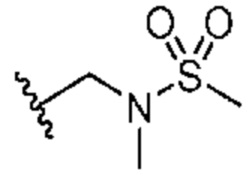 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 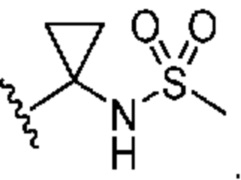 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 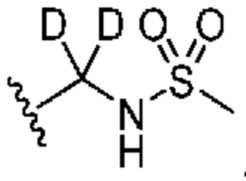 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 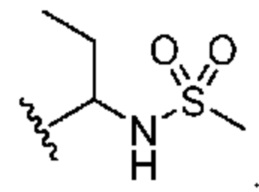 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 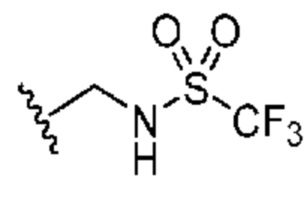 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 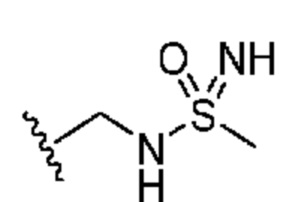 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 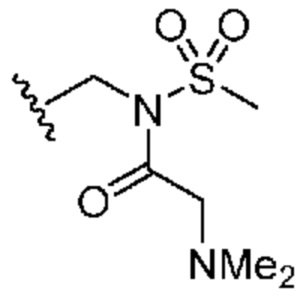 .
.
[0076] В некоторых вариантах осуществления R1 означает 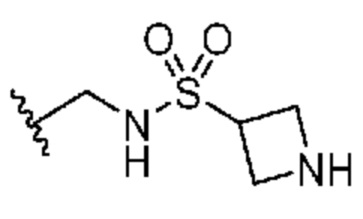 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 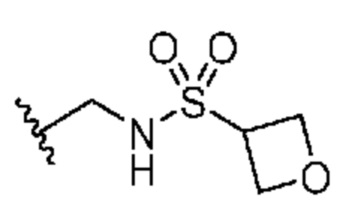 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 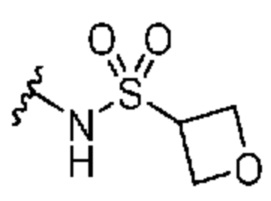 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 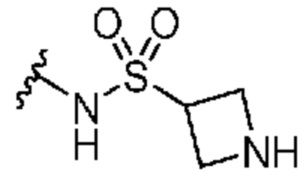 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 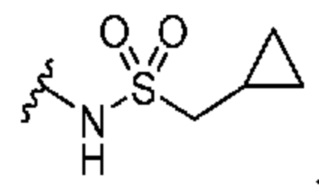 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 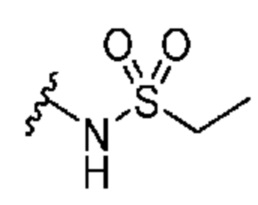 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 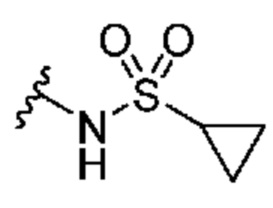 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 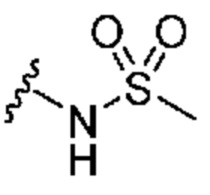 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 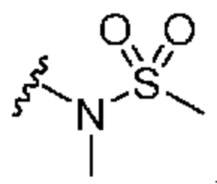 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 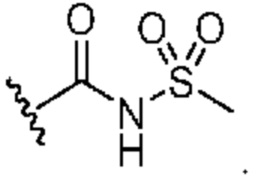 .
.
[0077] В некоторых вариантах осуществления R1 означает 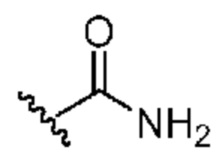 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 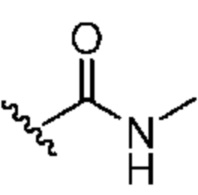 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 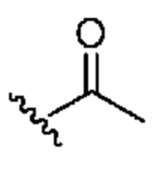 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 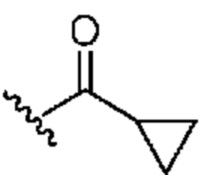 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 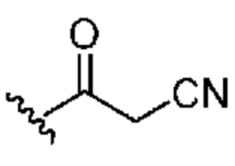 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 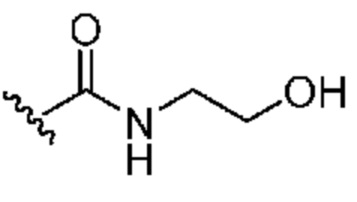 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 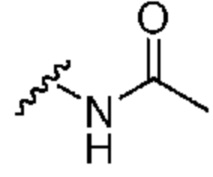 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 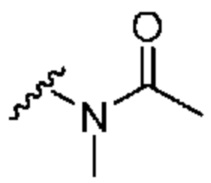 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 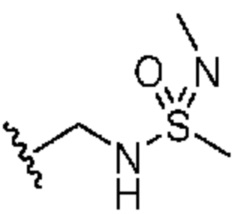 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 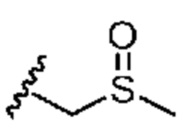 .
.
[0078] В некоторых вариантах осуществления R1 означает 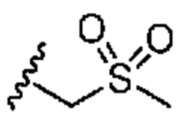 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает  . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 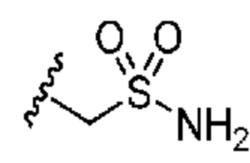 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 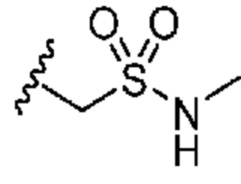 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 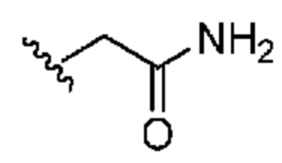 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 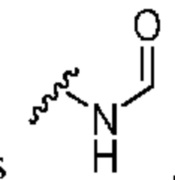 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 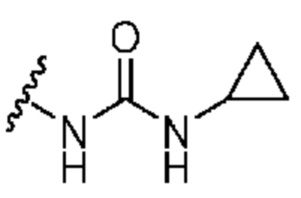 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 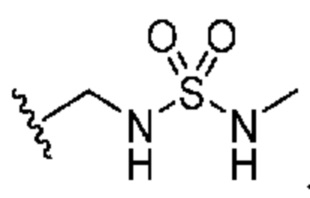 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 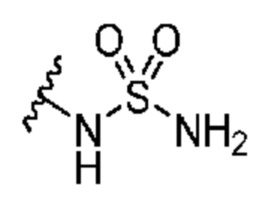 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 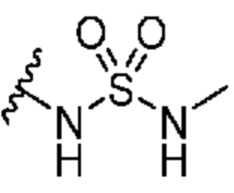 .
.
[0079] В некоторых вариантах осуществления R1 означает 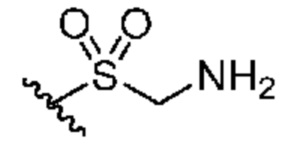 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 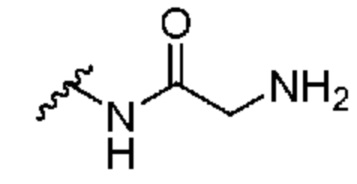 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 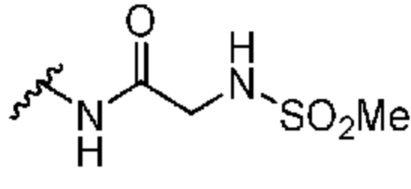 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 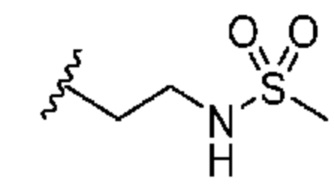 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 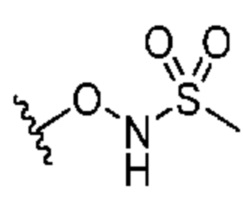 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 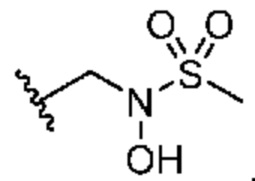 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 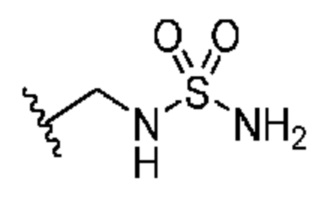 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 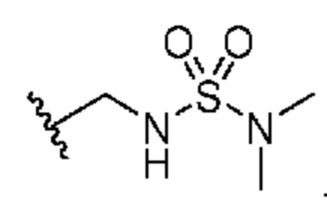 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 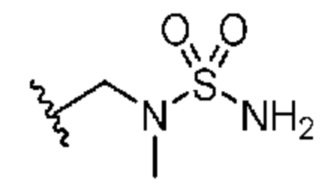 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 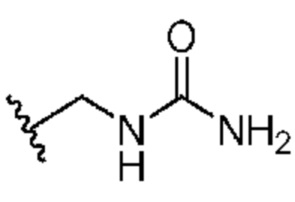 .
.
[0080] В некоторых вариантах осуществления R1 означает 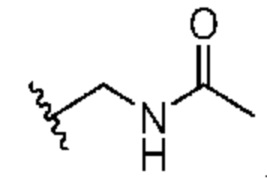 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 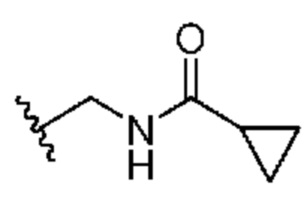 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает  . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 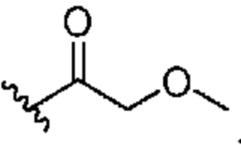 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 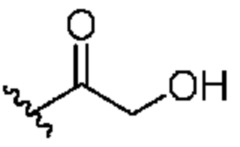 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 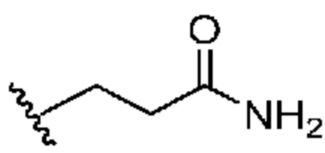 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 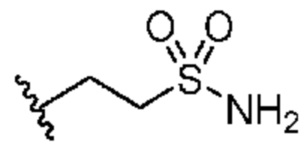 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 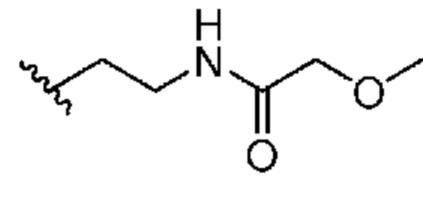 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 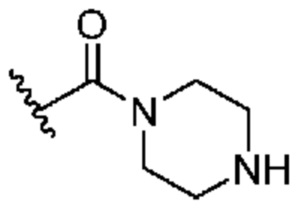 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 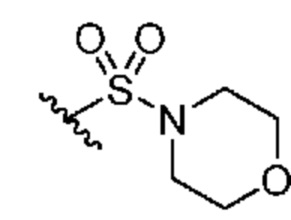 .
.
[0081] В некоторых вариантах осуществления R1 означает 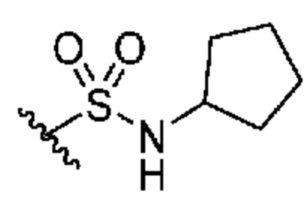 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 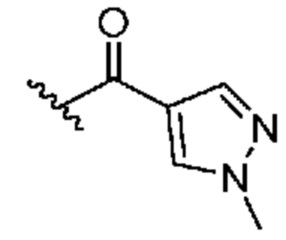 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 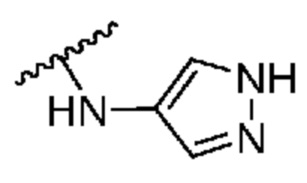 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 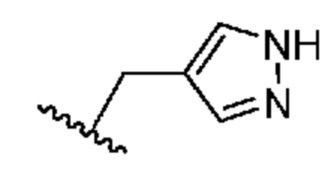 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 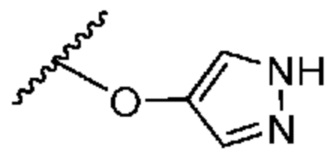 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 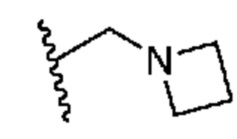 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 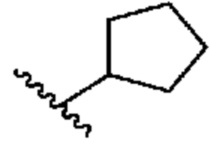 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 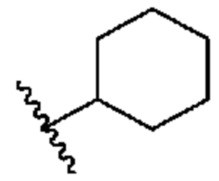 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 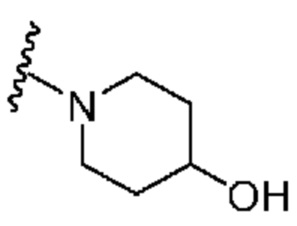 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 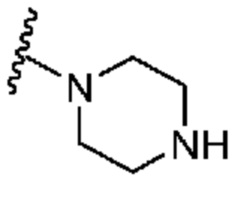 .
.
[0082] В некоторых вариантах осуществления R1 означает 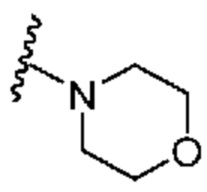 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 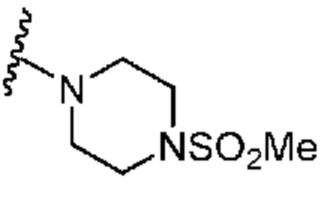 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 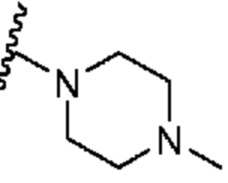 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 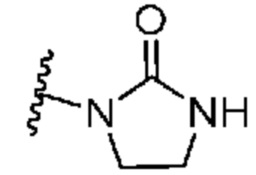 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 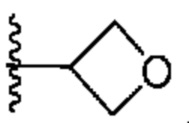 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 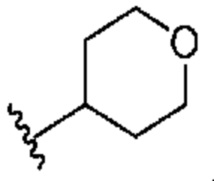 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 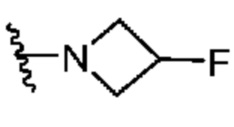 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 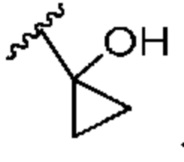 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 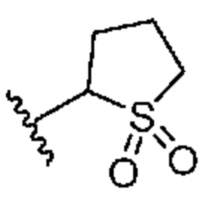 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 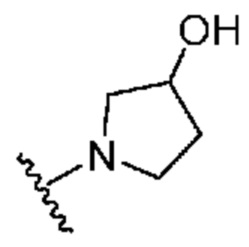 .
.
[0083] В некоторых вариантах осуществления R1 означает 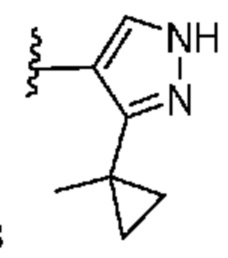 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 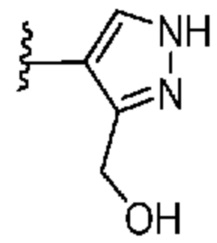 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 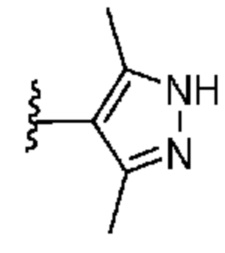 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 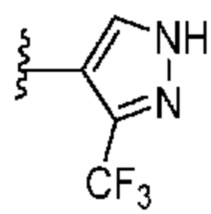 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 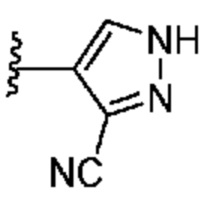 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 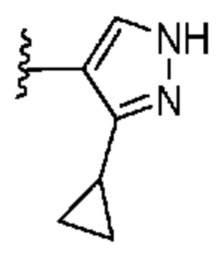 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 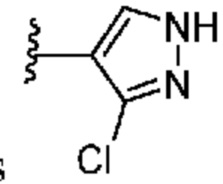 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 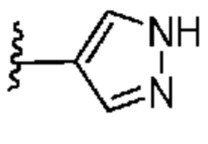 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 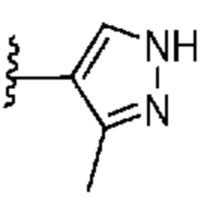 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 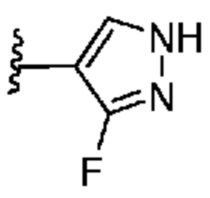 .
.
[0084] В некоторых вариантах осуществления R1 означает 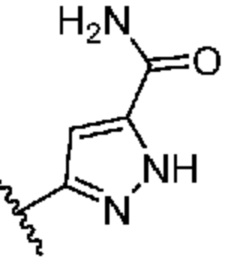 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 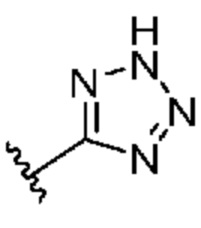 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 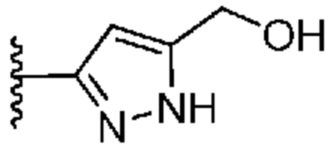 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает  . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 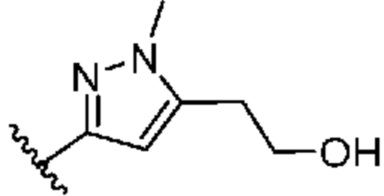 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 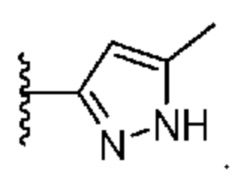 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 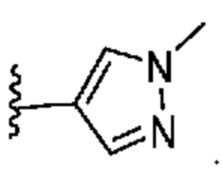 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 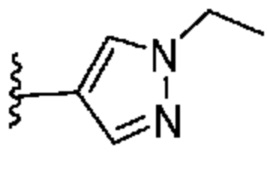 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 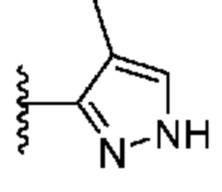 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 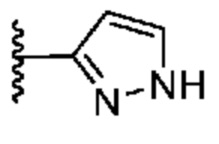 .
.
[0085] В некоторых вариантах осуществления R1 означает 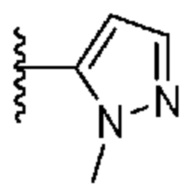 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 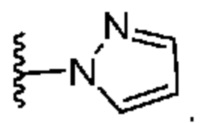 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 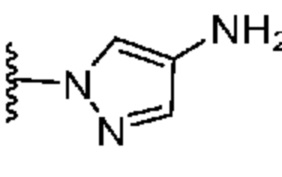 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 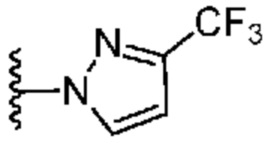 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 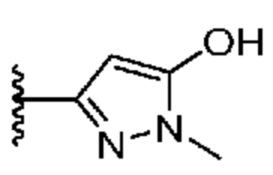 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 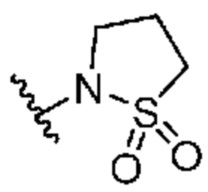 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 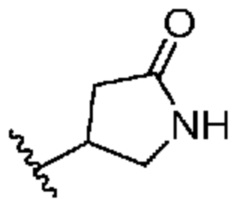 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 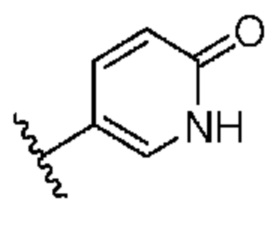 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 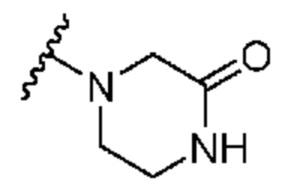 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 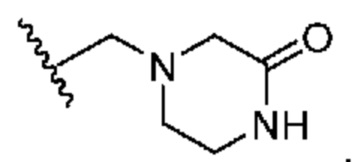 .
.
[0086] В некоторых вариантах осуществления R1 означает 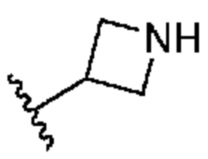 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 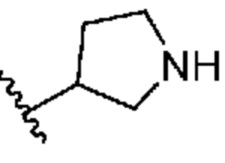 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 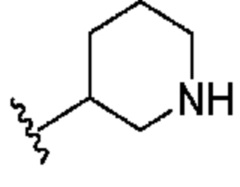 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 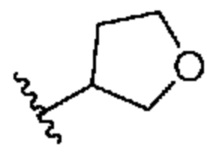 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 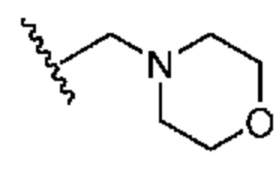 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 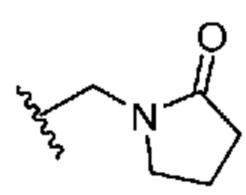 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 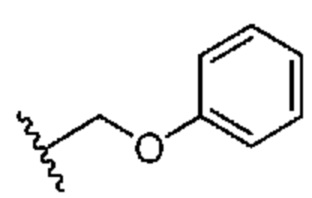 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 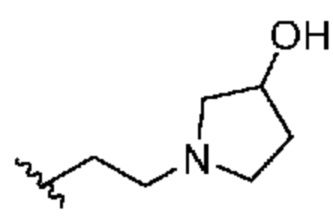 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 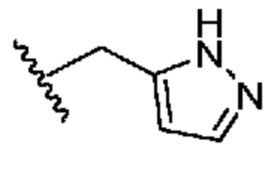 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 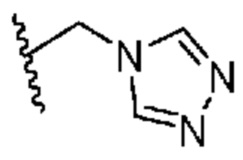 .
.
[0087] В некоторых вариантах осуществления R1 означает 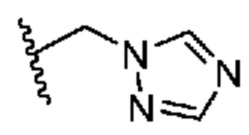 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 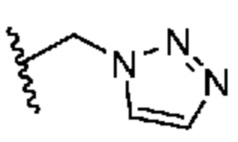 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 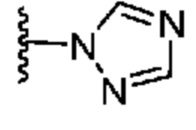 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 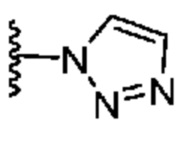 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 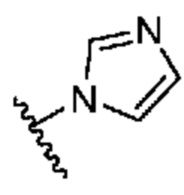 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 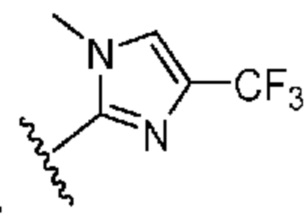 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 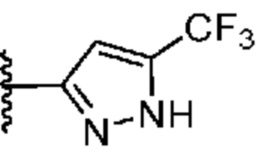 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 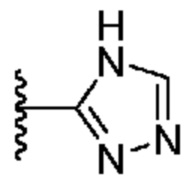 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 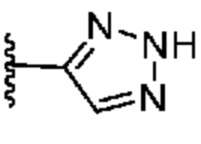 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 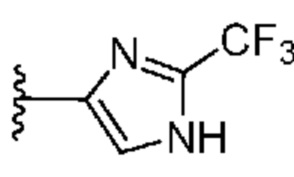 .
.
[0088] В некоторых вариантах осуществления R1 означает 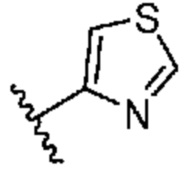 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 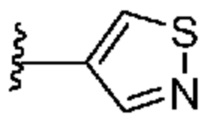 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 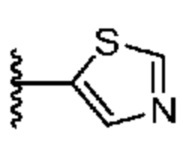 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 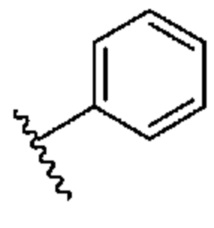 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 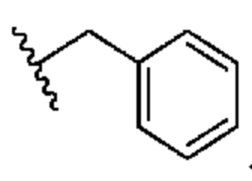 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 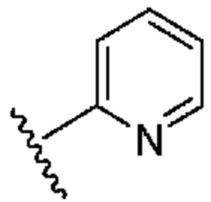 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 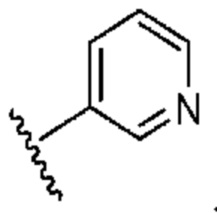 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 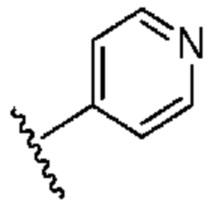 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 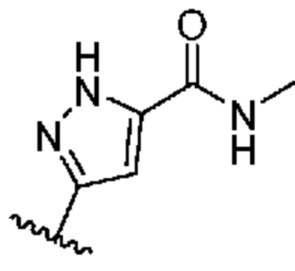 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 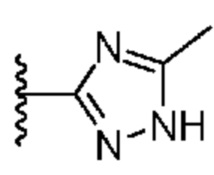 .
.
[0089] В некоторых вариантах осуществления R1 означает 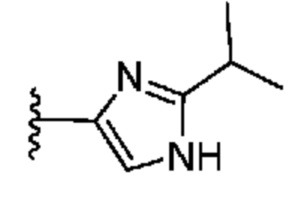 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 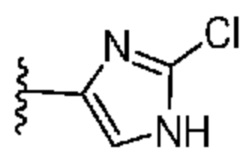 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 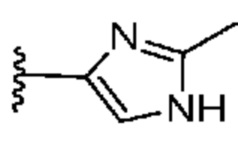 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 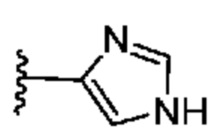 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 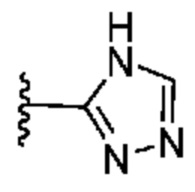 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 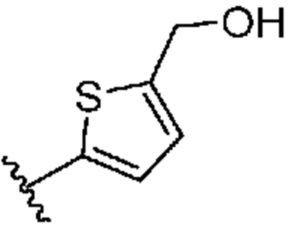 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 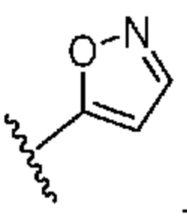 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 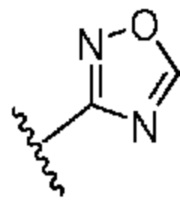 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 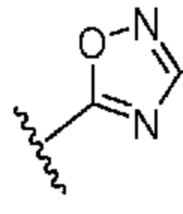 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 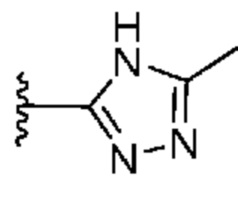 .
.
[0090] В некоторых вариантах осуществления R1 означает 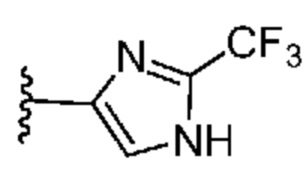 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 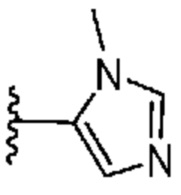 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 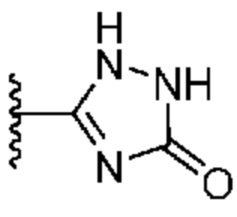 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 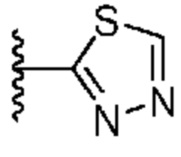 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 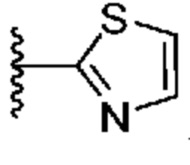 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 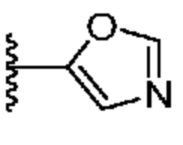 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 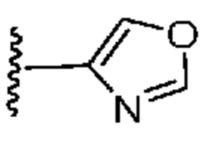 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 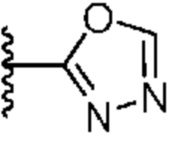 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 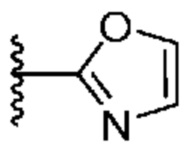 .
.
[0091] В некоторых вариантах осуществления R1 означает 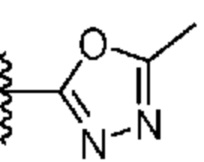 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 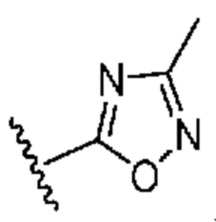 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 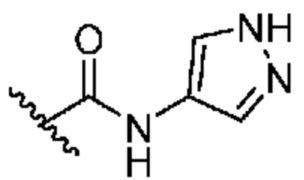 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 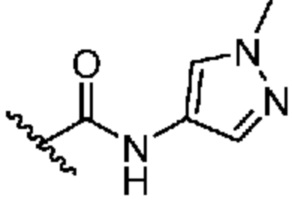 .
.
[0092] В некоторых вариантах осуществления R1 означает 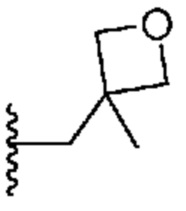 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 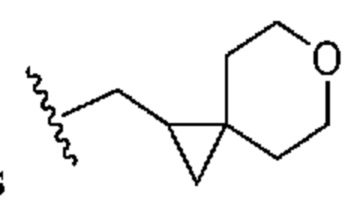 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 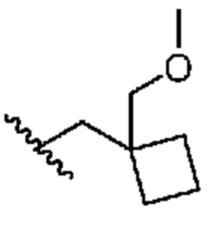 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 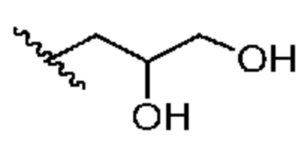 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 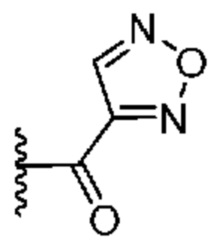 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 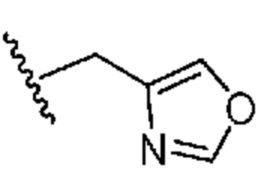 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 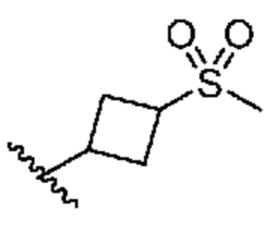 . В некоторых вариантах осуществления R1 означает
. В некоторых вариантах осуществления R1 означает 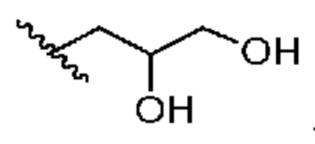 .
.
[0093] В некоторых вариантах осуществления R1 выбран из числа структур, приведенных в таблице 1 ниже.
[0094] Как определено выше и указано в настоящем изобретении, каждый из R2 означает каждый из R2 независимо означает водород, галоген, -CN, -C(O)N(R’)2, -OR’, -N(R’)2, -S(O)2R, -S(O)2N(R)2, -O-фенил или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, фенил, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 4-8-членный насыщенный моноциклический гетероцикл, содержащий 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0095] В некоторых вариантах осуществления R2 означает водород. В некоторых вариантах осуществления R2 означает галоген. В некоторых вариантах осуществления R2 означает -CN. В некоторых вариантах осуществления R2 означает -C(O)N(R’)2. В некоторых вариантах осуществления R2 означает -OR’. В некоторых вариантах осуществления R2 означает -N(R’)2. В некоторых вариантах осуществления R2 означает -S(O)2R. В некоторых вариантах осуществления R2 означает -S(O)2N(R)2. В некоторых вариантах осуществления R2 означает -O-фенил. В некоторых вариантах осуществления R2 означает необязательно замещенную C1-3 алифатическую группу. В некоторых вариантах осуществления R2 означает необязательно замещенный фенил. В некоторых вариантах осуществления R2 означает необязательно замещенное 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления R2 означает необязательно замещенный 4-8-членный насыщенный моноциклический гетероцикл, содержащий 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[0096] В некоторых вариантах осуществления R2 означает фтор. В некоторых вариантах осуществления R2 означает хлор. В некоторых вариантах осуществления R2 означает бром. В некоторых вариантах осуществления R2 означает метил. В некоторых вариантах осуществления R2 означает этил. В некоторых вариантах осуществления R2 означает -CF3. В некоторых вариантах осуществления R2 означает 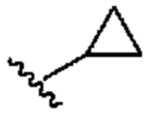 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 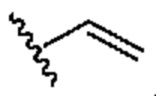 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 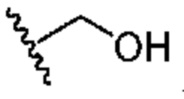 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 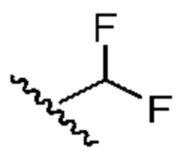 .
.
[0097] В некоторых вариантах осуществления R2 означает 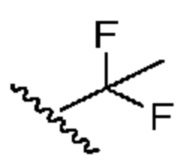 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 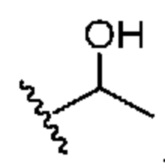 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 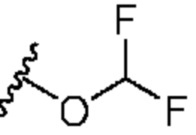 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 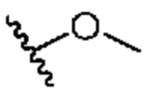 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 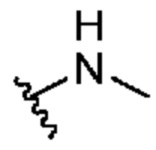 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 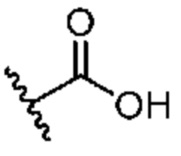 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 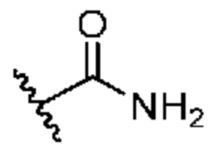 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 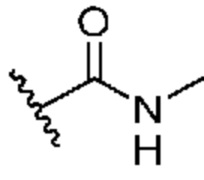 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 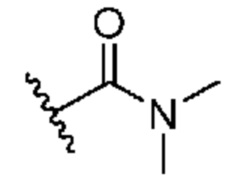 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает  . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 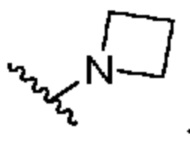 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 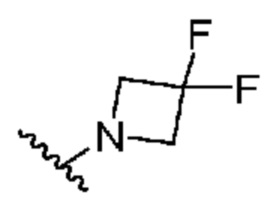 .
.
[0098] В некоторых вариантах осуществления R2 означает 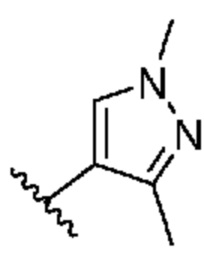 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 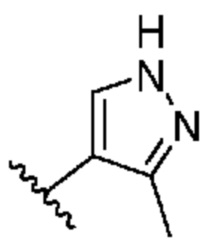 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 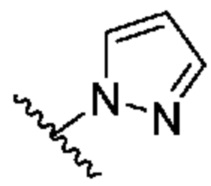 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 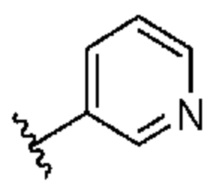 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 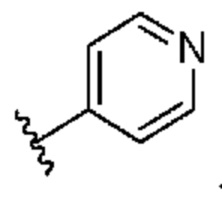 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 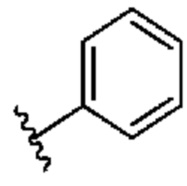 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 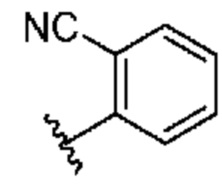 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 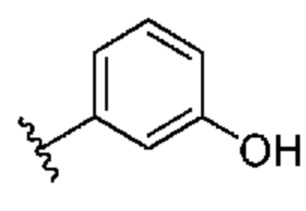 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 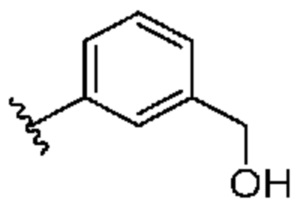 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 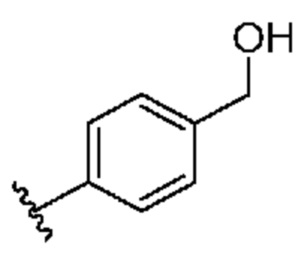 .
.
[0099] В некоторых вариантах осуществления R2 означает 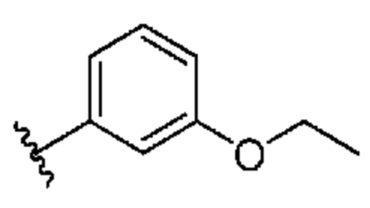 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 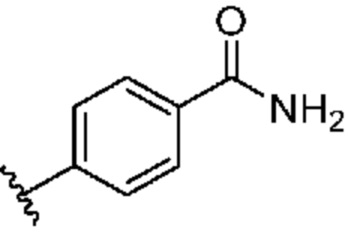 . В некоторых вариантах осуществления R2 означает
. В некоторых вариантах осуществления R2 означает 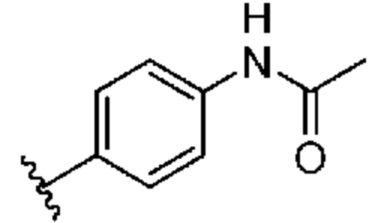 .
.
[00100] В некоторых вариантах осуществления R2 выбран из числа структур, приведенных в таблице 1 ниже.
[00101] Как определено выше и указано в настоящем изобретении, R3 означает водород, галоген, -CN, -OR’, -N(R’)2 или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, фенил или 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[00102] В некоторых вариантах осуществления R3 означает водород. В некоторых вариантах осуществления R3 означает галоген. В некоторых вариантах осуществления R3 означает -CN. В некоторых вариантах осуществления R3 означает -OR’. В некоторых вариантах осуществления R3 означает -N(R’)2. В некоторых вариантах осуществления R3 означает необязательно замещенную C1-3 алифатическую группу. В некоторых вариантах осуществления R3 означает необязательно замещенный фенил. В некоторых вариантах осуществления R3 означает необязательно замещенное 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[00103] В некоторых вариантах осуществления R3 выбран из числа структур, приведенных в таблице 1 ниже.
[00104] Как определено выше и указано в настоящем изобретении, R4 означает водород, галоген, -CN, -OR, -N=S(O)R2, -N(R)2 или необязательно замещенную группу, выбранную из группы, включающей C1-3 алифатическую группу, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 7-12-членное насыщенное или частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[00105] В некоторых вариантах осуществления R4 означает водород. В некоторых вариантах осуществления R4 означает галоген. В некоторых вариантах осуществления R4 означает -CN. В некоторых вариантах осуществления R4 означает -OR. В некоторых вариантах осуществления R4 означает -N=S(O)(R)2. В некоторых вариантах осуществления R4 означает -N(R)2. В некоторых вариантах осуществления R4 означает необязательно замещенную C1-3 алифатическую группу. В некоторых вариантах осуществления R4 означает необязательно замещенное 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу. В некоторых вариантах осуществления R4 означает необязательно замещенное 7-12-членное насыщенное или частично ненасыщенное спироциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
[00106] В некоторых вариантах осуществления R4 означает фтор. В некоторых вариантах осуществления R4 означает хлор. В некоторых вариантах осуществления R4 означает метил. В некоторых вариантах осуществления R4 означает -CF3. В некоторых вариантах осуществления R4 означает -OH. В некоторых вариантах осуществления R4 означает 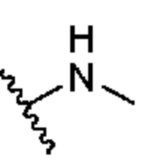 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 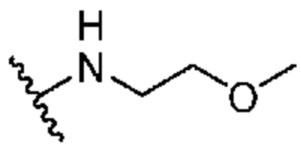 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 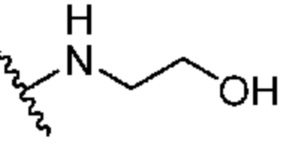 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 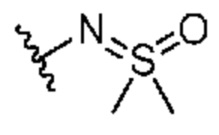 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 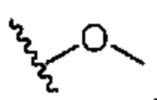 .
.
[00107] В некоторых вариантах осуществления R4 означает 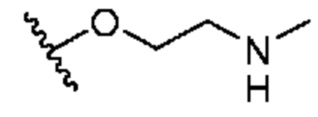 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 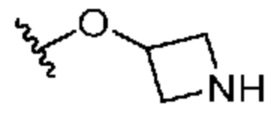 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 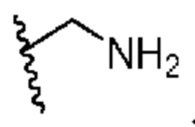 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 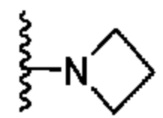 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 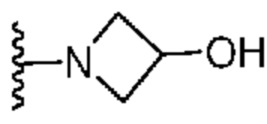 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 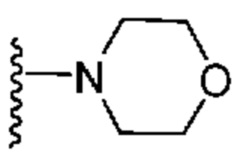 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 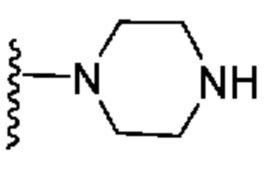 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 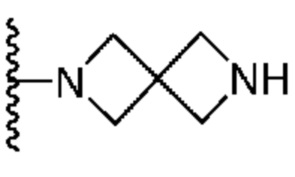 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 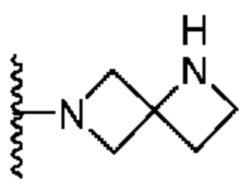 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 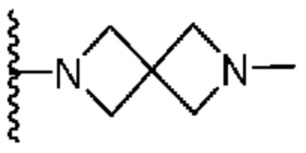 .
.
[00108] В некоторых вариантах осуществления R4 означает 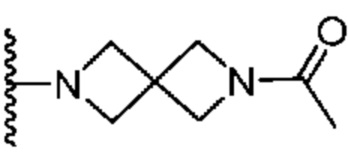 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 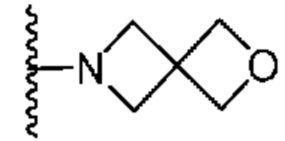 . В некоторых вариантах осуществления R4 означает
. В некоторых вариантах осуществления R4 означает 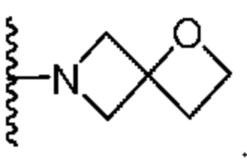 .
.
[00109] В некоторых вариантах осуществления R4 выбран из числа структур, приведенных в таблице 1 ниже.
[00110] Как определено выше и указано в настоящем изобретении, m равно 0, 1, 2, 3, 4 или 5.
[00111] В некоторых вариантах осуществления m равно 0. В некоторых вариантах осуществления m равно 1. В некоторых вариантах осуществления m равно 2. В некоторых вариантах осуществления m равно 3. В некоторых вариантах осуществления m равно 4. В некоторых вариантах осуществления m равно 5.
[00112] В некоторых вариантах осуществления m равно 1, 2 или 3.
[00113] В некоторых вариантах осуществления m выбран из числа структур, приведенных в таблице 1 ниже.
[00114] Как определено выше и указано в настоящем изобретении n равно 0, 1, или 2.
[00115] В некоторых вариантах осуществления n равно 0. В некоторых вариантах осуществления n равно 1. В некоторых вариантах осуществления n равно 2.
[00116] В некоторых вариантах осуществления n выбран из числа структур, приведенных в таблице 1 ниже.
[00117] Как определено выше и указано в настоящем изобретении p равно 0 или 1.
[00118] В некоторых вариантах осуществления p равно 0. В некоторых вариантах осуществления p равно 1.
[00119] В некоторых вариантах осуществления p выбран из числа структур, приведенных в таблице 1 ниже.
[00120] Как определено выше и указано в настоящем изобретении q равно 0 или 1.
[00121] В некоторых вариантах осуществления q равно 0. В некоторых вариантах осуществления q равно 1.
[00122] В некоторых вариантах осуществления q выбран из числа структур, приведенных в таблице 1 ниже.
[00123] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой Het и тем самым образует соединение формулы II:
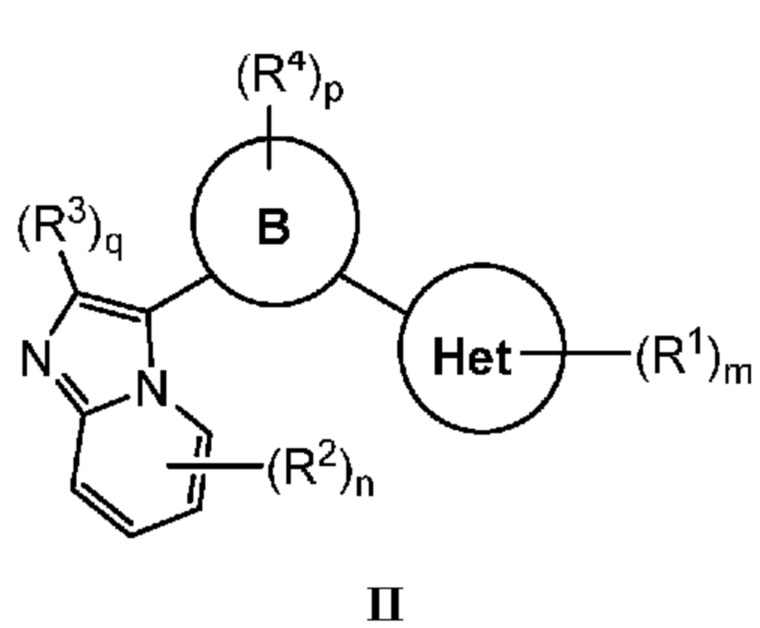
или его фармацевтически приемлемой соли, в которой каждое кольцо B, R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00124] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой Het и кольцо B представляет собой 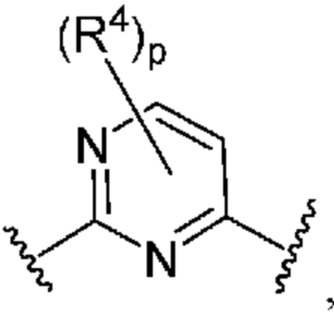 и тем самым образует соединение формулы III:
и тем самым образует соединение формулы III:
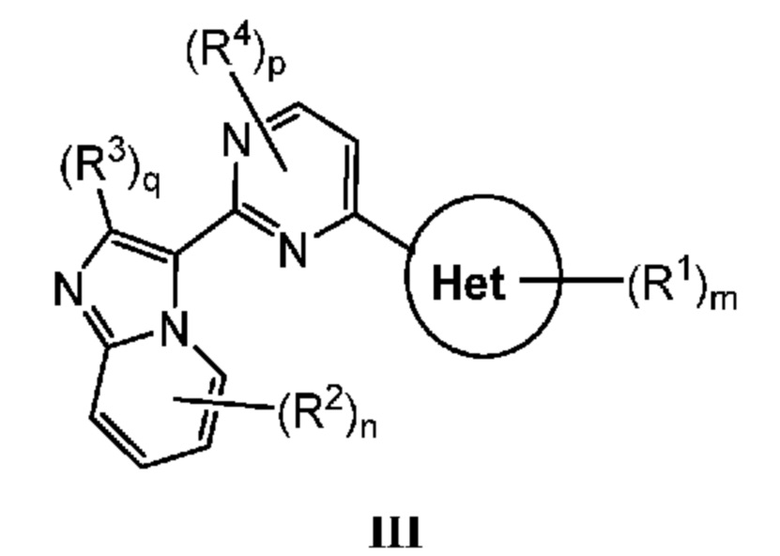
или его фармацевтически приемлемой соли, в которой каждый Het, R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00125] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы IV-a, IV-b или IV-c соответственно:
и тем самым образует соединение формулы IV-a, IV-b или IV-c соответственно:
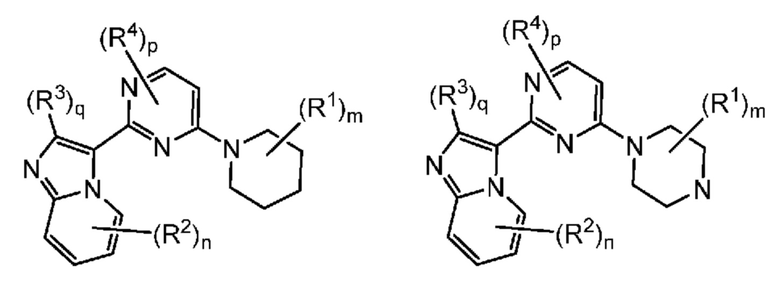
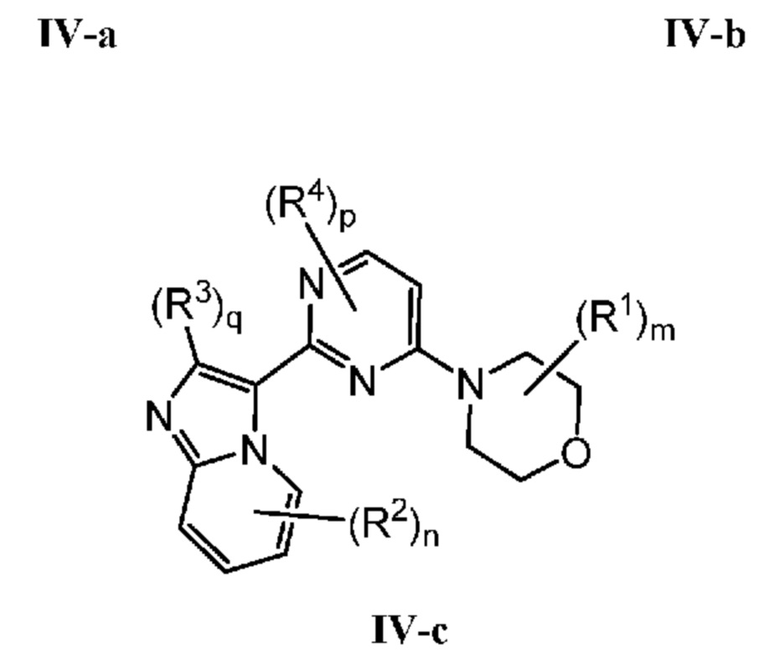
или его фармацевтически приемлемой соли, в которой каждый R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00126] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой Het и кольцо B представляет собой 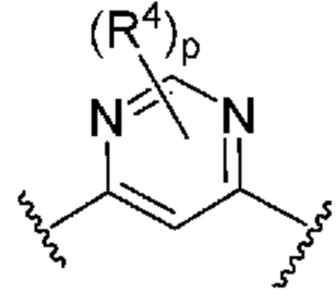 и тем самым образует соединение формулы V:
и тем самым образует соединение формулы V:
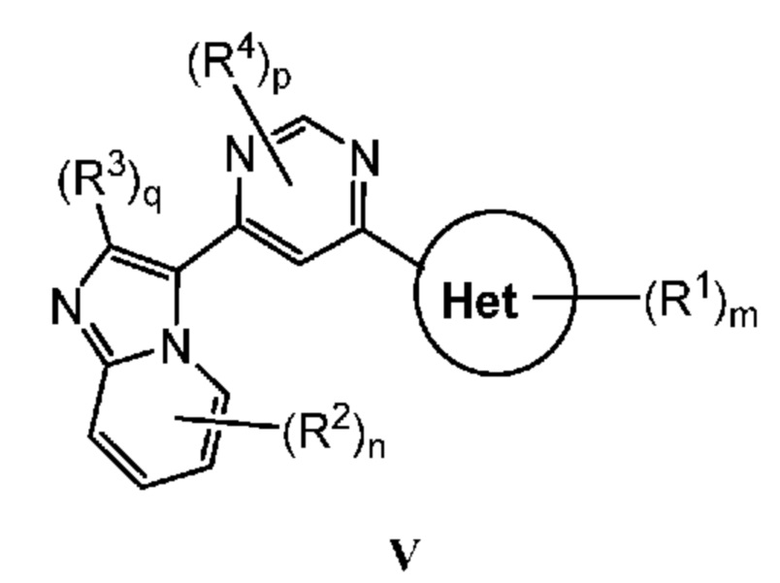
или его фармацевтически приемлемой соли, в которой каждый Het, R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00127] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы VI-a, VI-b или VI-c соответственно:
и тем самым образует соединение формулы VI-a, VI-b или VI-c соответственно:
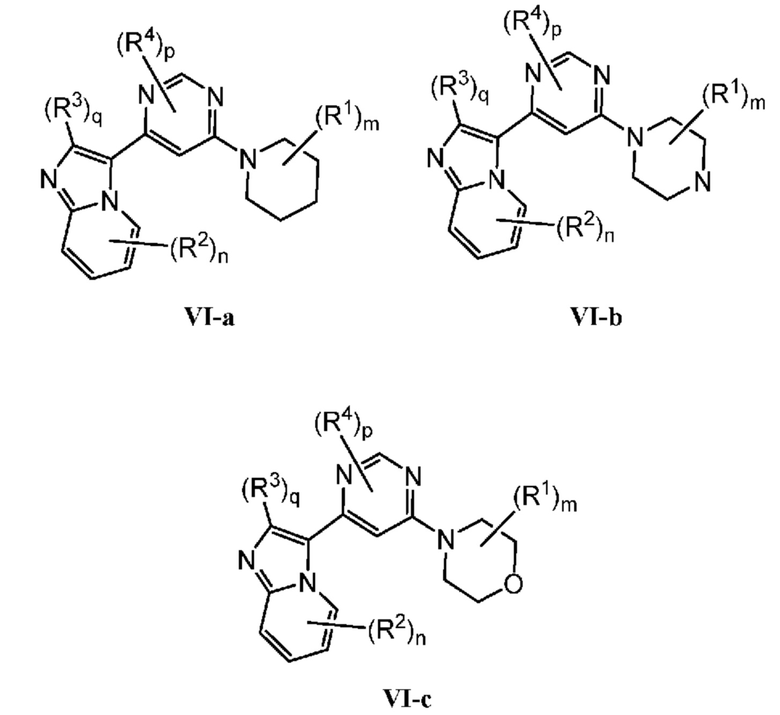
или его фармацевтически приемлемой соли, в которой каждый R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00128] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой Het и кольцо B представляет собой 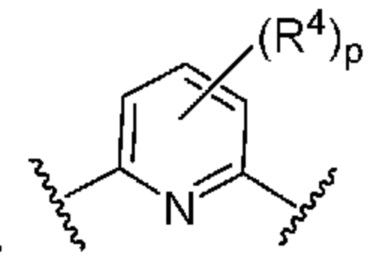 и тем самым образует соединение формулы VII:
и тем самым образует соединение формулы VII:
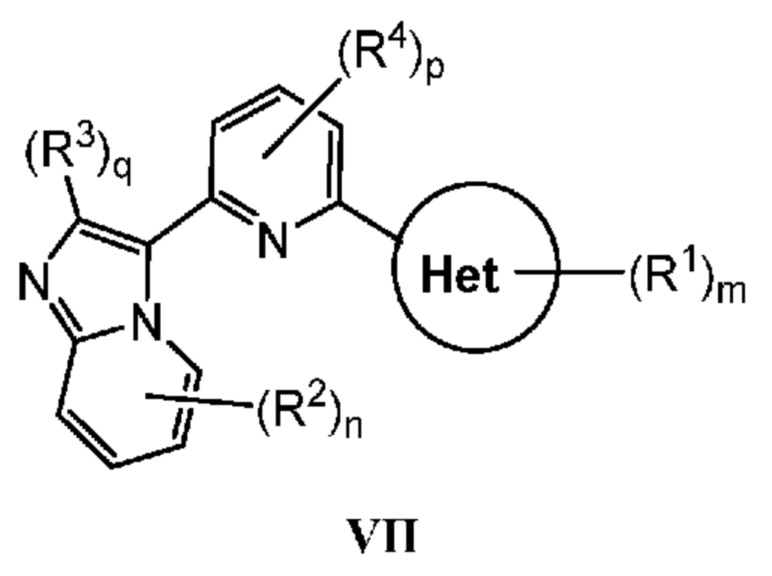
или его фармацевтически приемлемой соли, в которой каждый Het, R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00129] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы VIII-a, VIII-b или VIII-c соответственно:
и тем самым образует соединение формулы VIII-a, VIII-b или VIII-c соответственно:
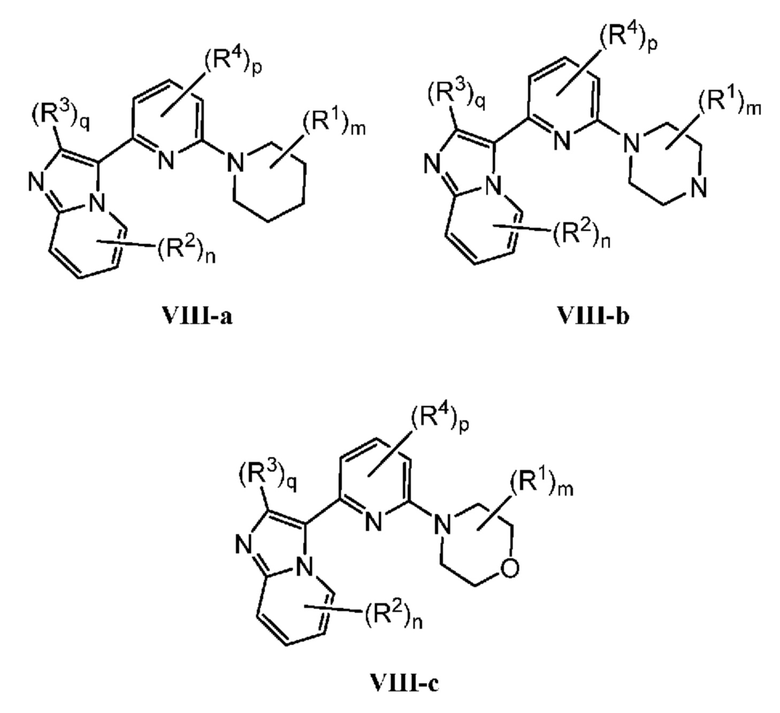
или его фармацевтически приемлемой соли, в которой каждый R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00130] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой Het и кольцо B представляет собой 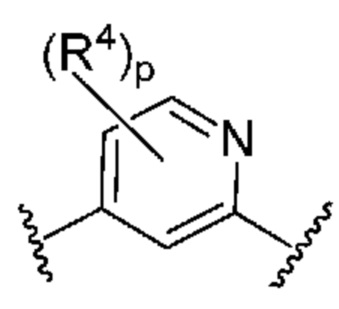 и тем самым образует соединение формулы IX:
и тем самым образует соединение формулы IX:
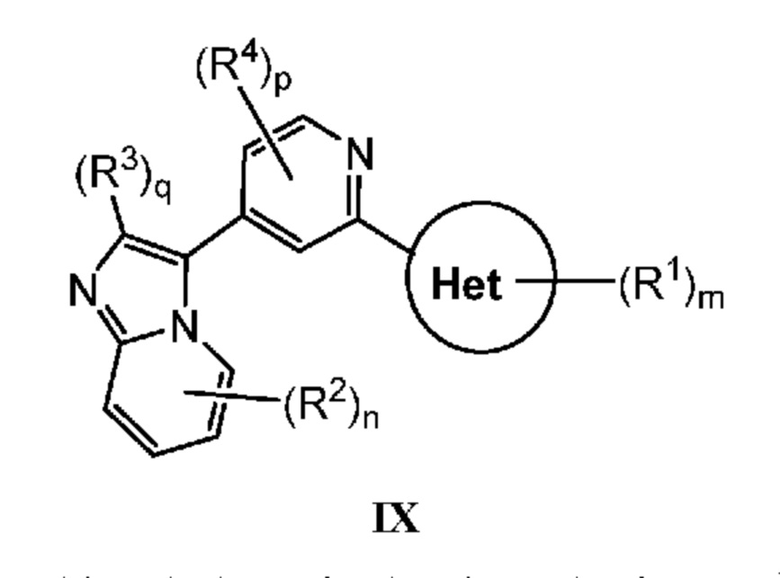
или его фармацевтически приемлемой соли, в которой каждый Het, R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00131] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы X-a, X-b или X-c соответственно:
и тем самым образует соединение формулы X-a, X-b или X-c соответственно:
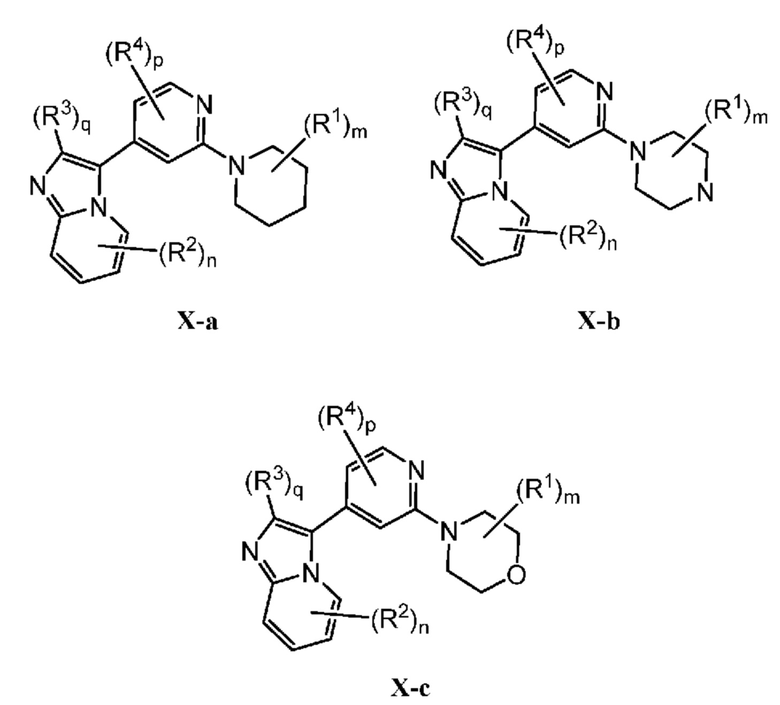
или его фармацевтически приемлемой соли, в которой каждый R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00132] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой Het и кольцо B представляет собой 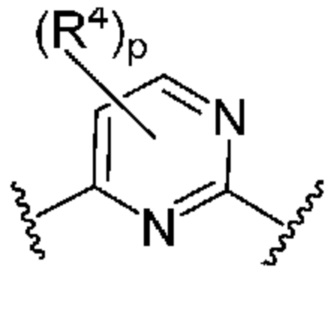 и тем самым образует соединение формулы XI:
и тем самым образует соединение формулы XI:
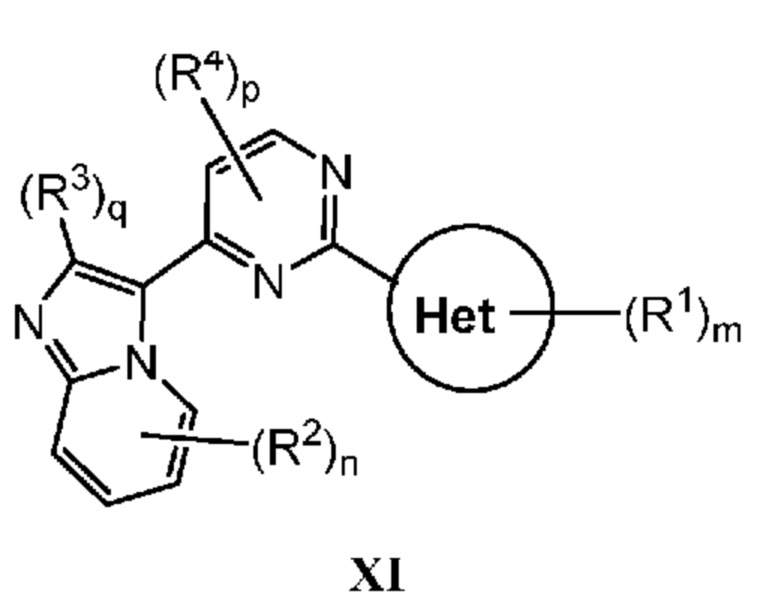
или его фармацевтически приемлемой соли, в которой каждый Het, R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00133] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы XII-a, XII-b или XII-c соответственно:
и тем самым образует соединение формулы XII-a, XII-b или XII-c соответственно:
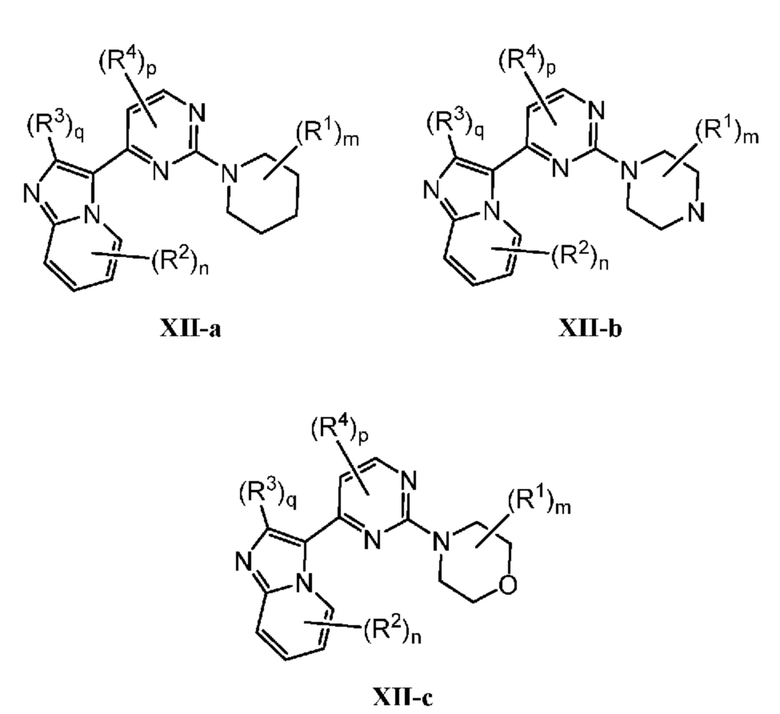
или его фармацевтически приемлемой соли, в которой каждый R1, R2, R3, R4, m, n, p и q является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00134] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает -CF3, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой 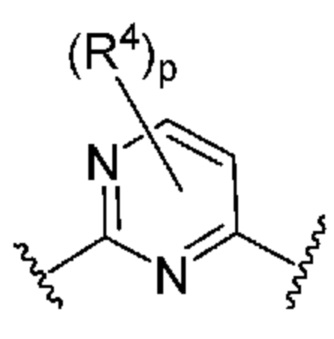 и тем самым образует соединение формулы XIII-a, XIII-b или XIII-c соответственно:
и тем самым образует соединение формулы XIII-a, XIII-b или XIII-c соответственно:
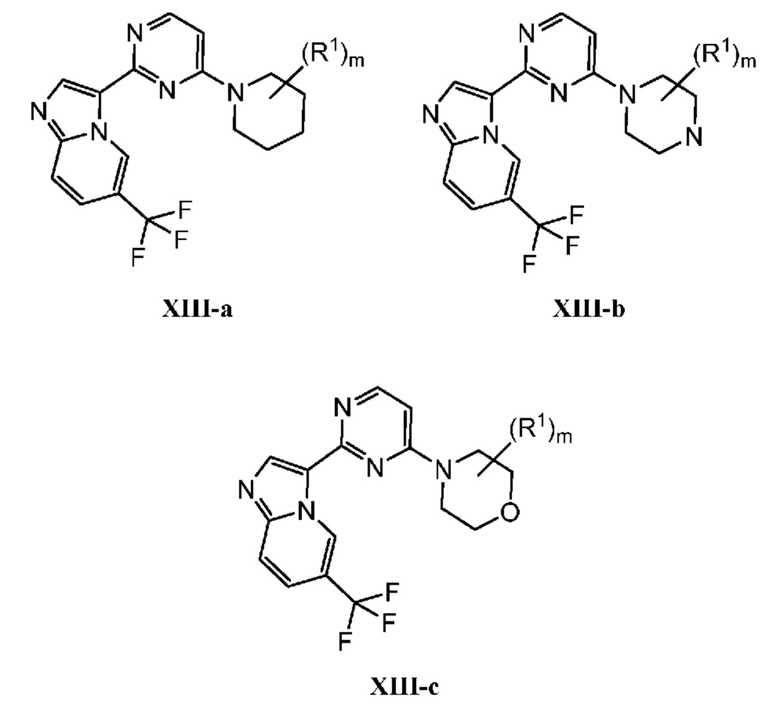
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00135] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает хлор, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы XIV-a, XIV-b или XIV-c соответственно:
и тем самым образует соединение формулы XIV-a, XIV-b или XIV-c соответственно:
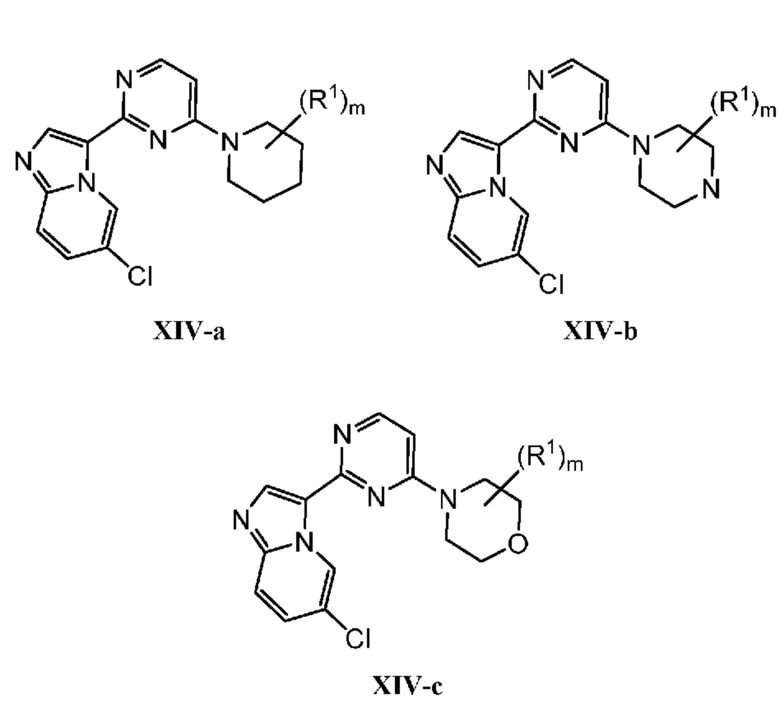
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00136] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает -CHF2, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой 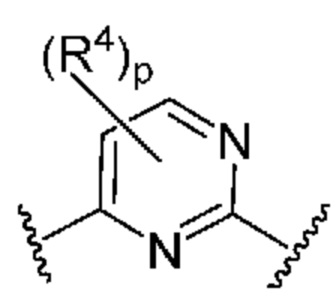 и тем самым образует соединение формулы XV-a, XV-b или XV-c соответственно:
и тем самым образует соединение формулы XV-a, XV-b или XV-c соответственно:
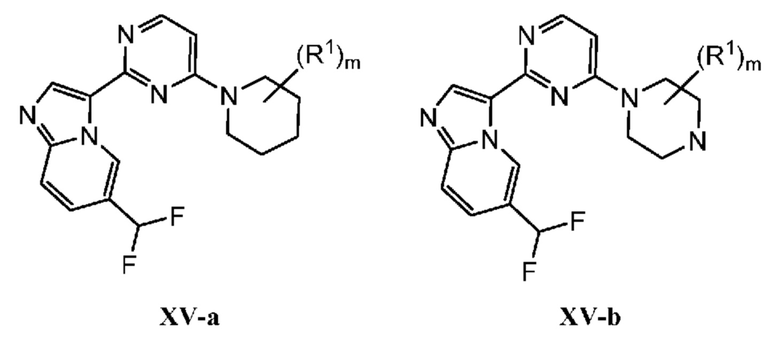
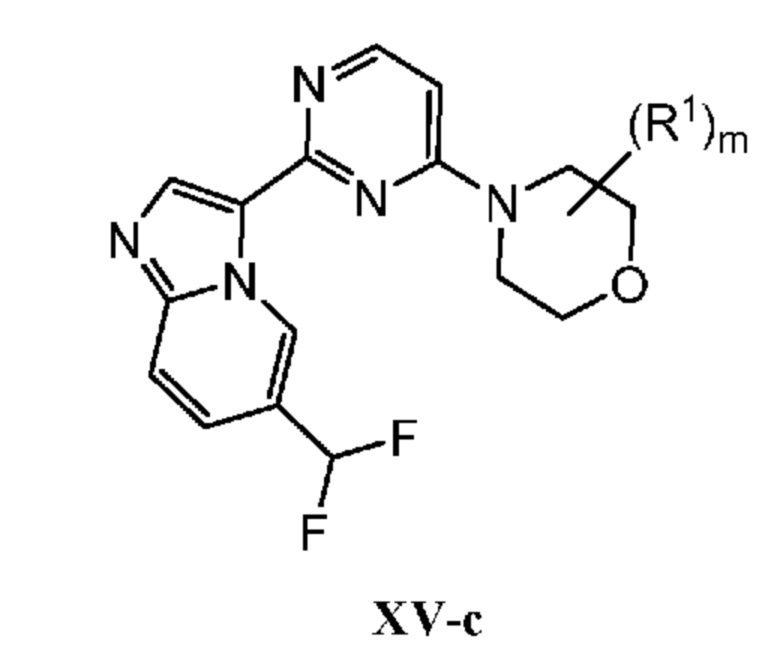
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00137] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает -CF3, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы XVI-a, XVI-b или XVI-c соответственно:
и тем самым образует соединение формулы XVI-a, XVI-b или XVI-c соответственно:
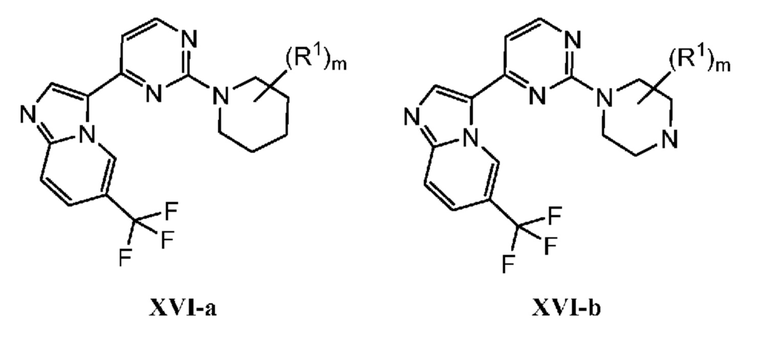
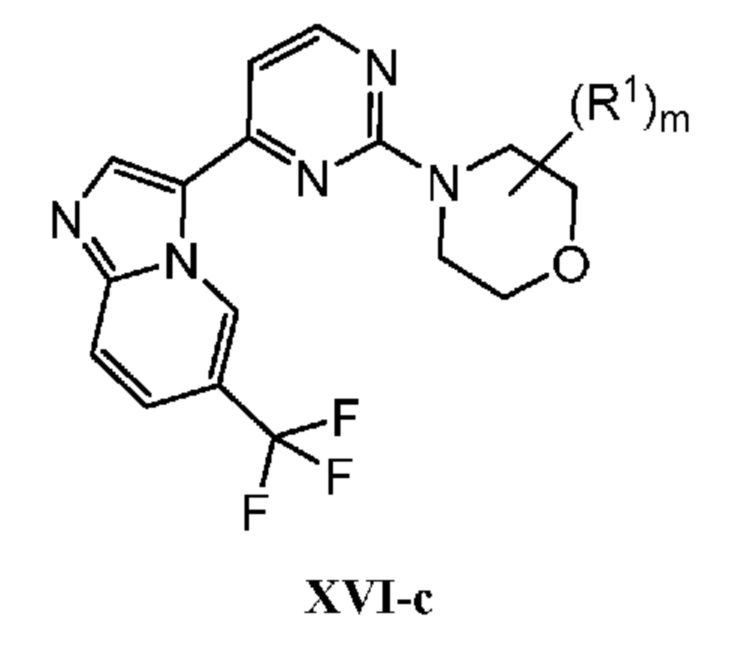
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00138] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает хлор, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой 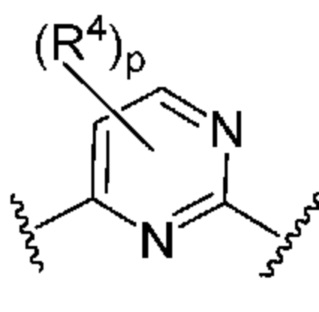 и тем самым образует соединение формулы XVII-a, XVII-b или XVII-c соответственно:
и тем самым образует соединение формулы XVII-a, XVII-b или XVII-c соответственно:
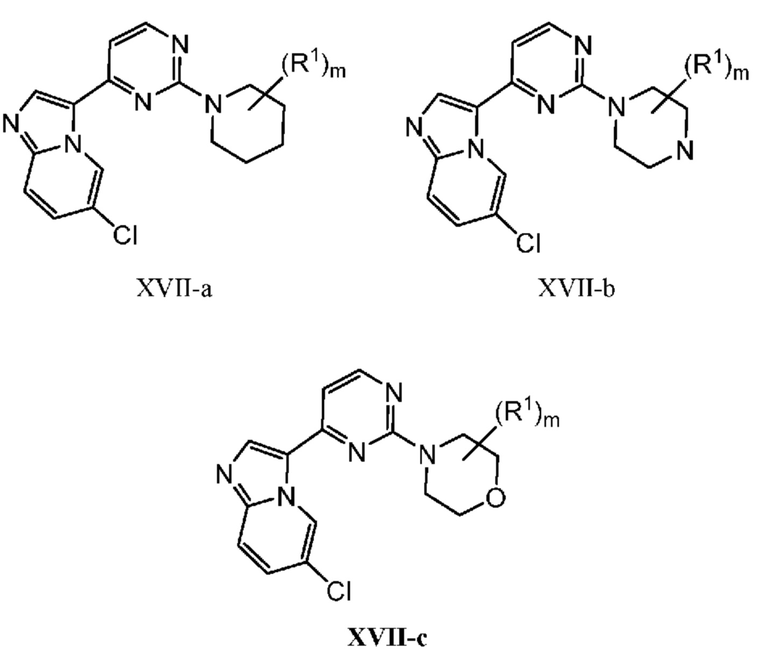
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00139] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает -CHF2, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы XVIII-a, XVIII-b или XVIII-c соответственно:
и тем самым образует соединение формулы XVIII-a, XVIII-b или XVIII-c соответственно:
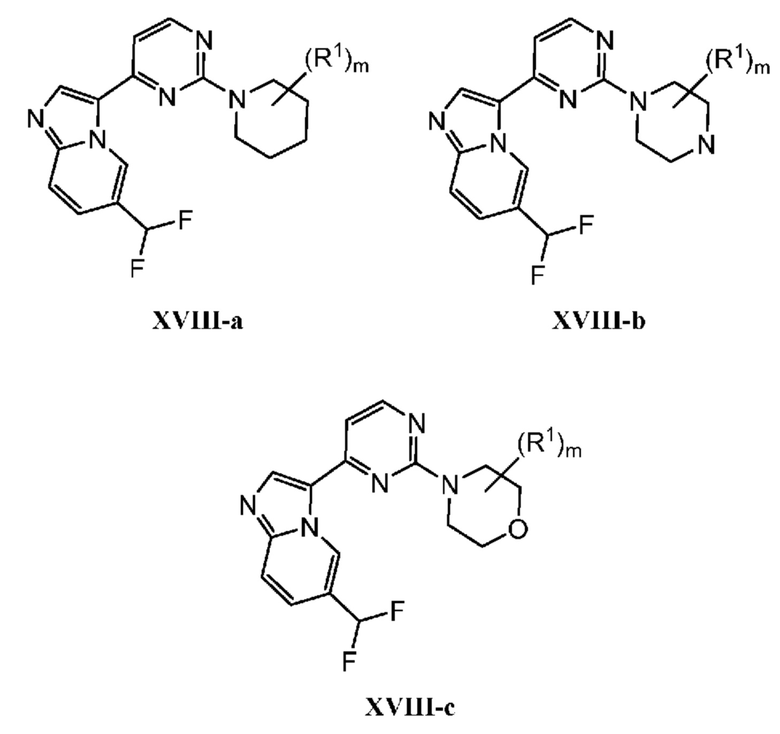
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00140] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает циклопропил, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы XIX-a, XIX-b или XIX-c соответственно:
и тем самым образует соединение формулы XIX-a, XIX-b или XIX-c соответственно:
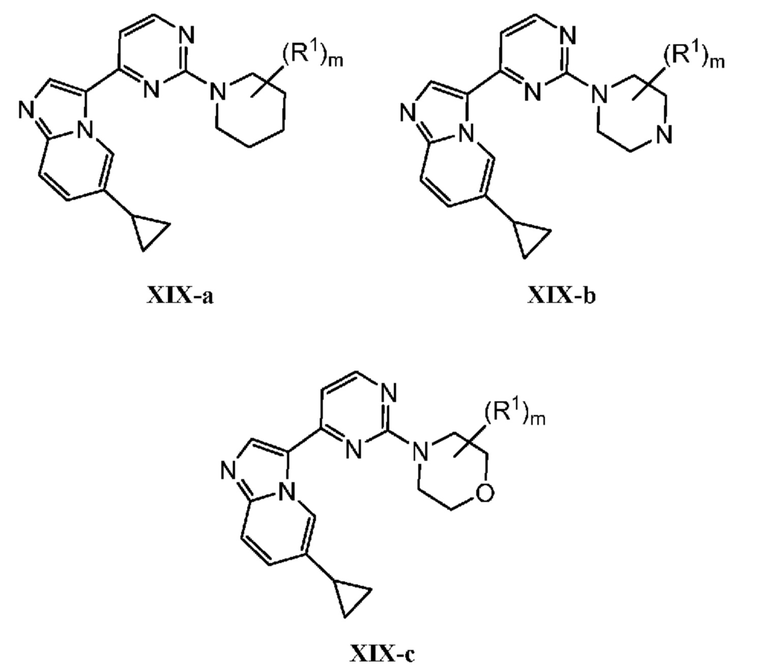
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00141] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает азетидинил, R3 означает водород, R4 означает водород, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы XX-a, XX-b или XX-c соответственно:
и тем самым образует соединение формулы XX-a, XX-b или XX-c соответственно:
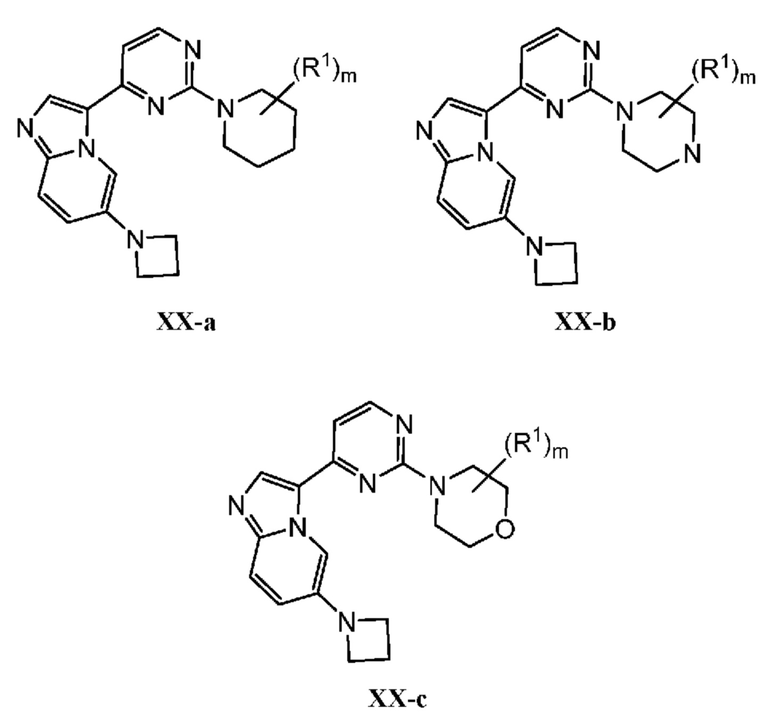
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00142] В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы I, в которой n равно 1, p равно 1, q равно 1, R2 означает 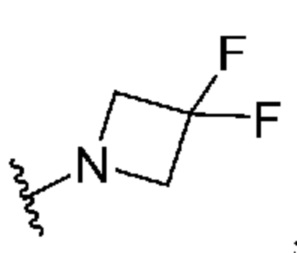 , R3 означает водород, R4 означает метил, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой
, R3 означает водород, R4 означает метил, кольцо A представляет собой пиперидинил, пиперазинил или морфолинил и кольцо B представляет собой  и тем самым образует соединение формулы XXI-a, XXI-b или XXI-c соответственно:
и тем самым образует соединение формулы XXI-a, XXI-b или XXI-c соответственно:
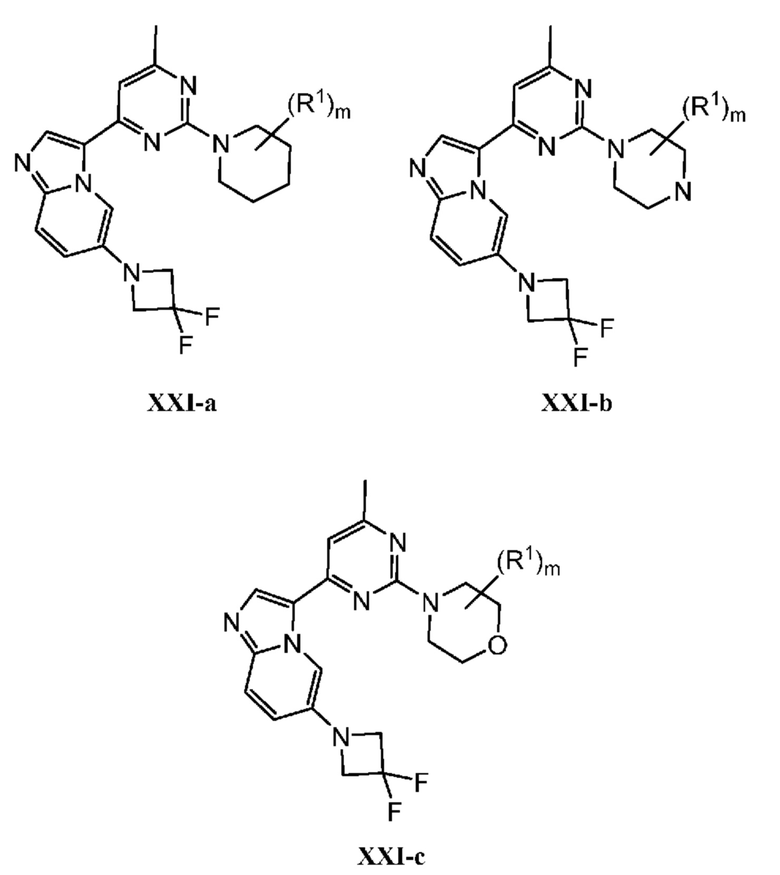
или его фармацевтически приемлемой соли, в которой каждый R1 и m является таким, как определено выше и описано в представленных вариантах осуществления, по отдельности и в комбинации.
[00143] Типичные соединения, предлагаемые в настоящем изобретении, приведены ниже в таблице 1.
Таблица 1. Типичные соединения формулы формулы I
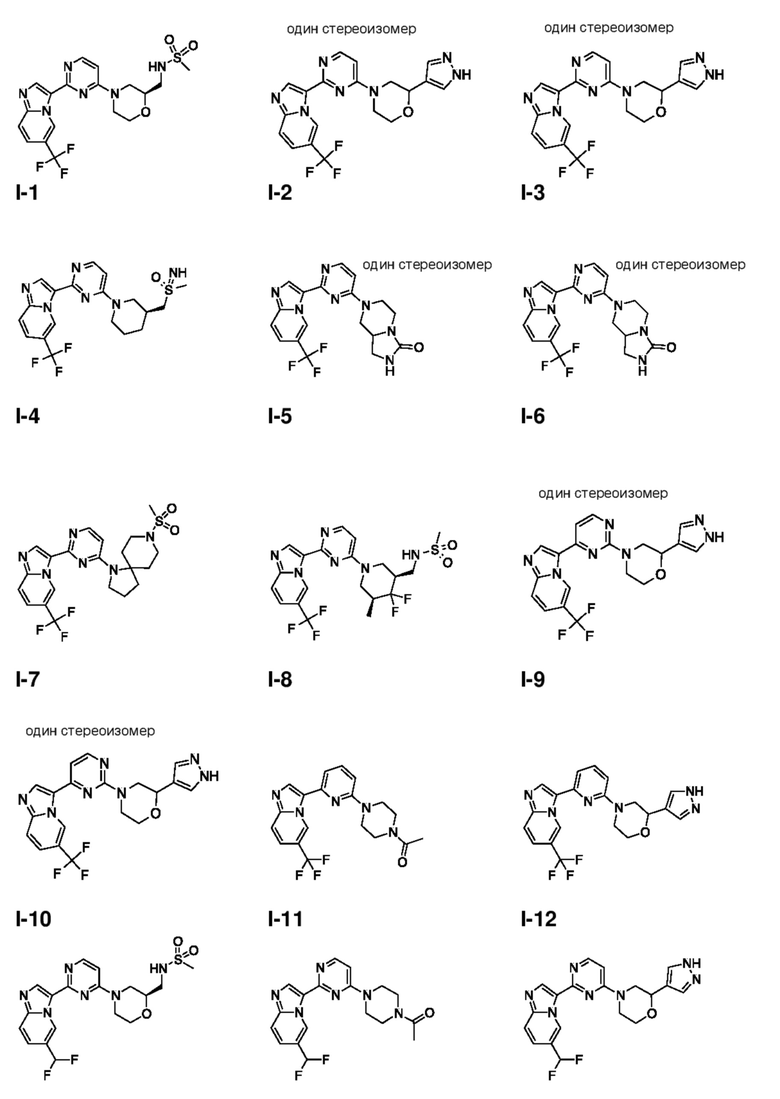
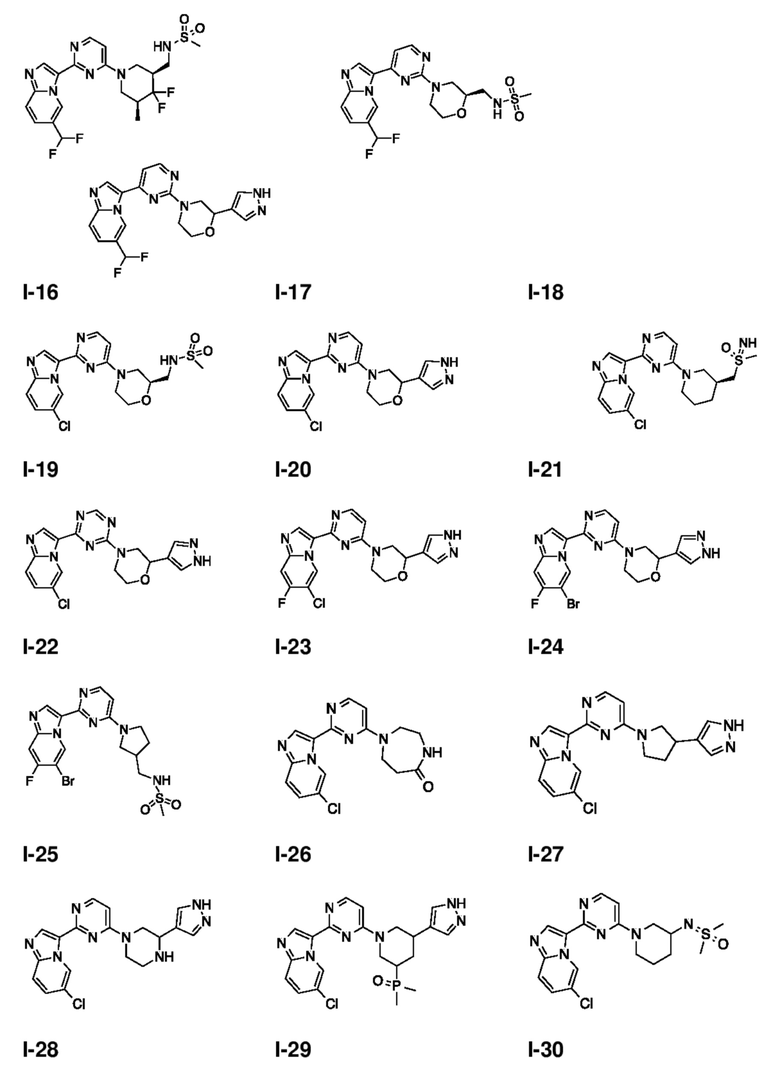
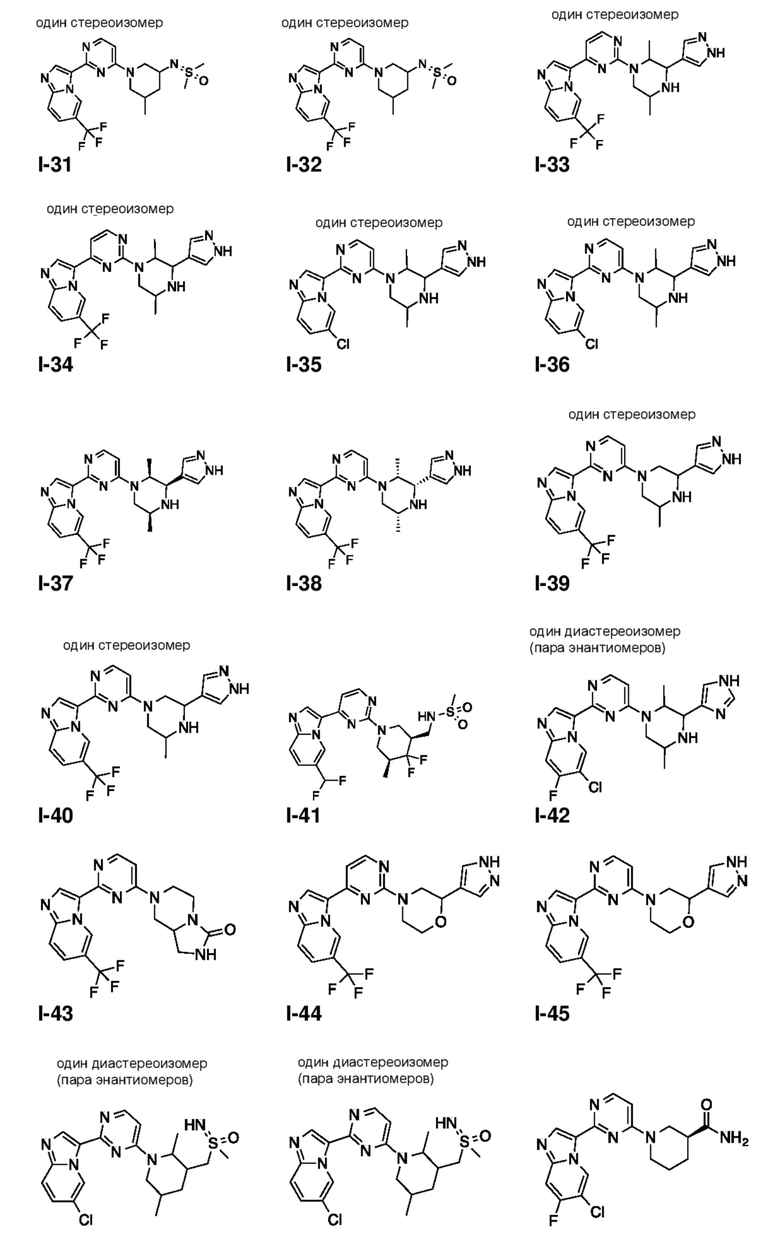
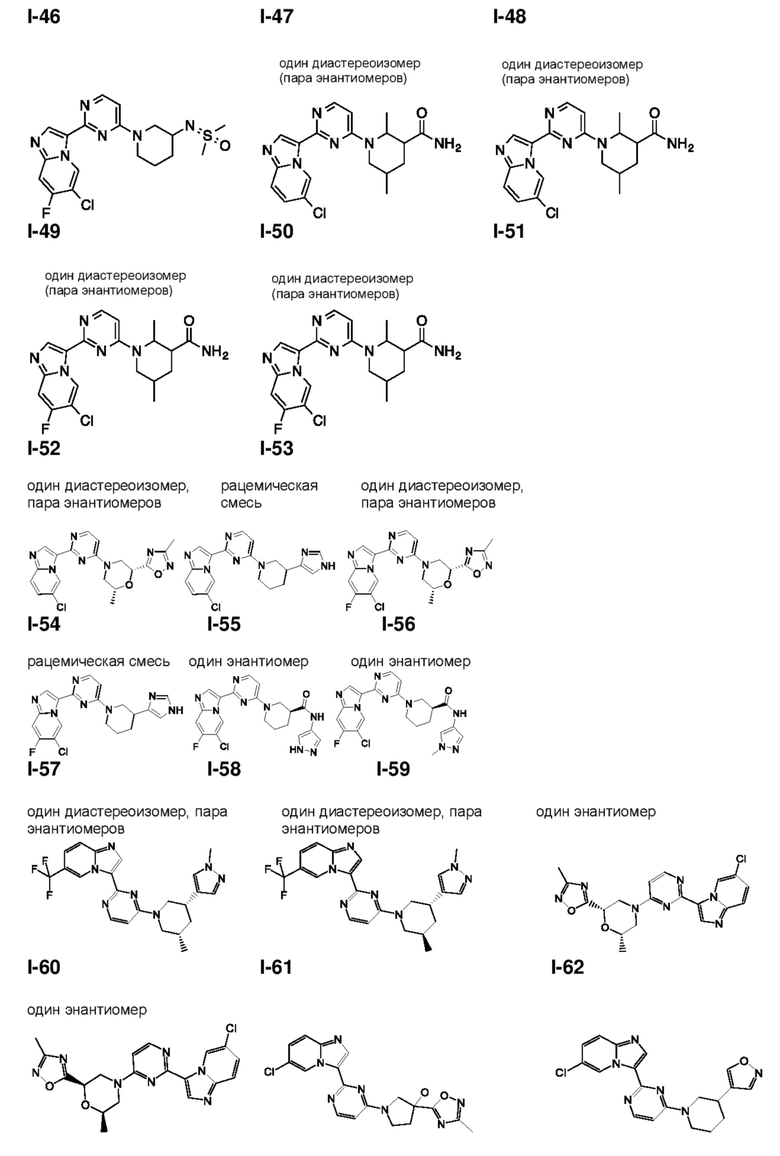
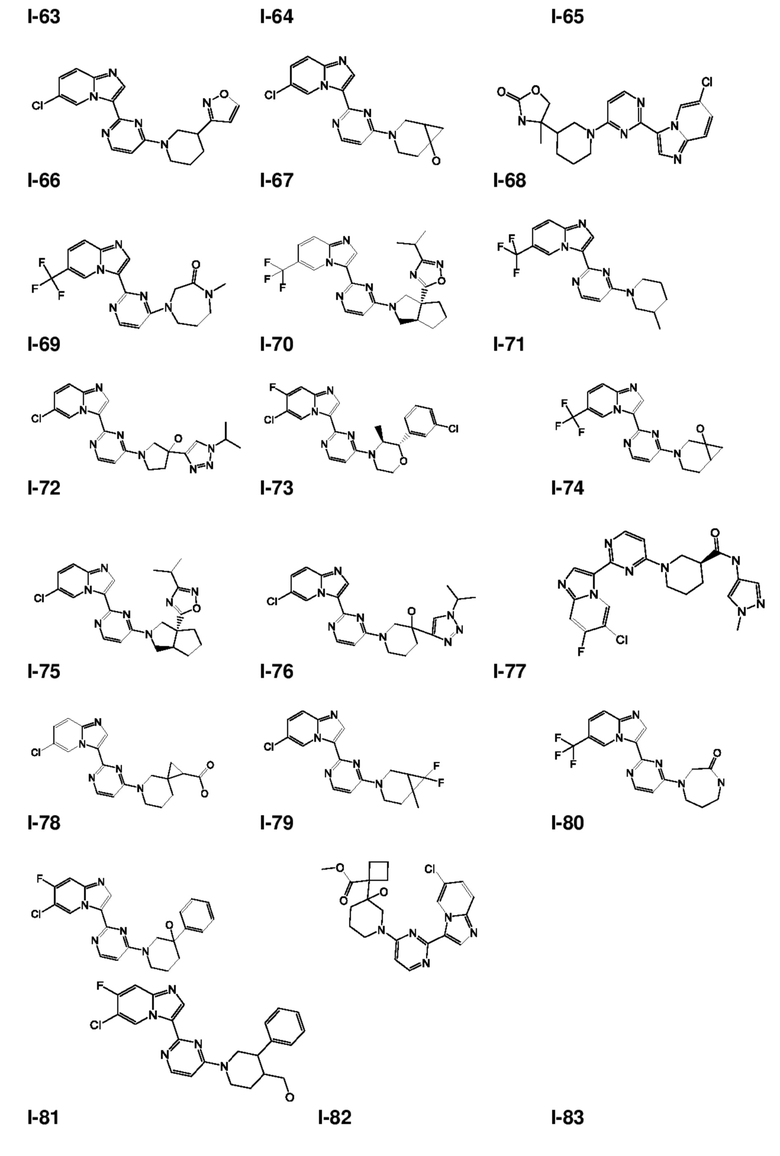
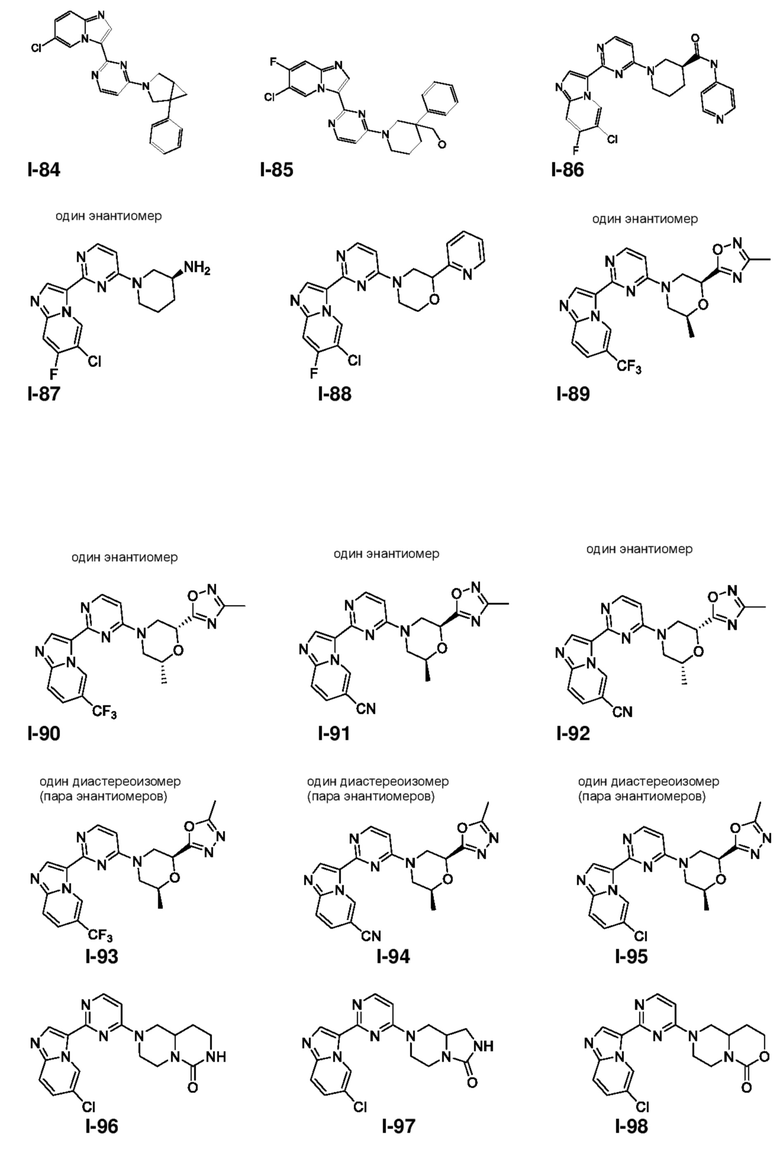
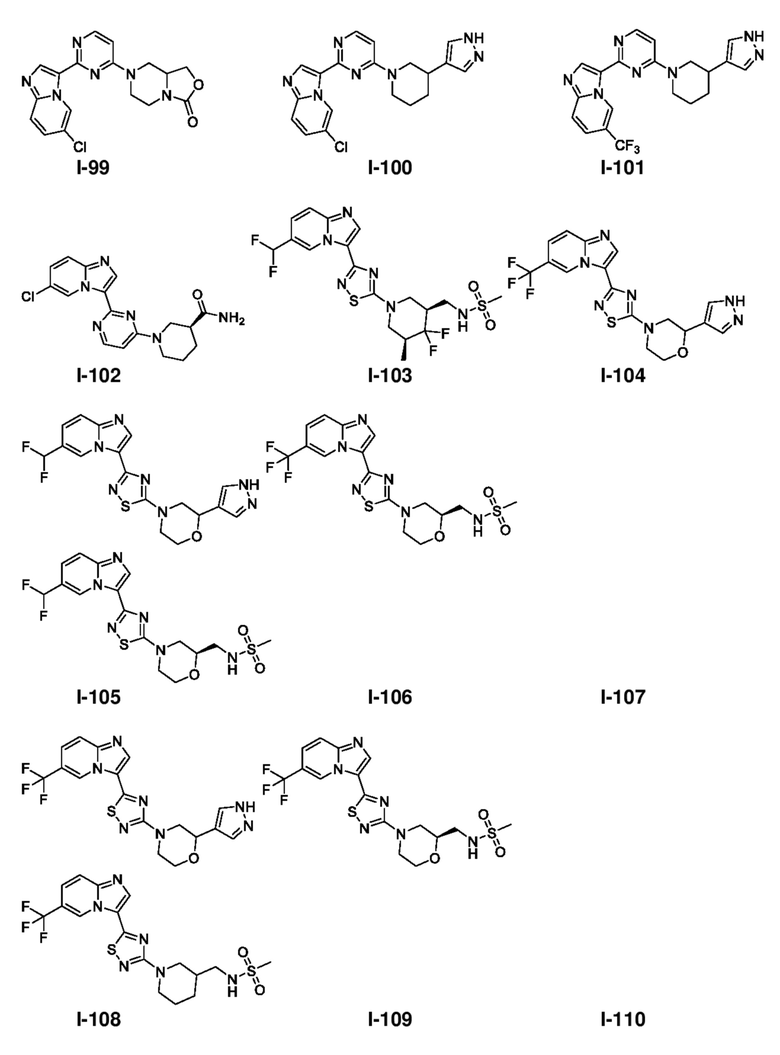
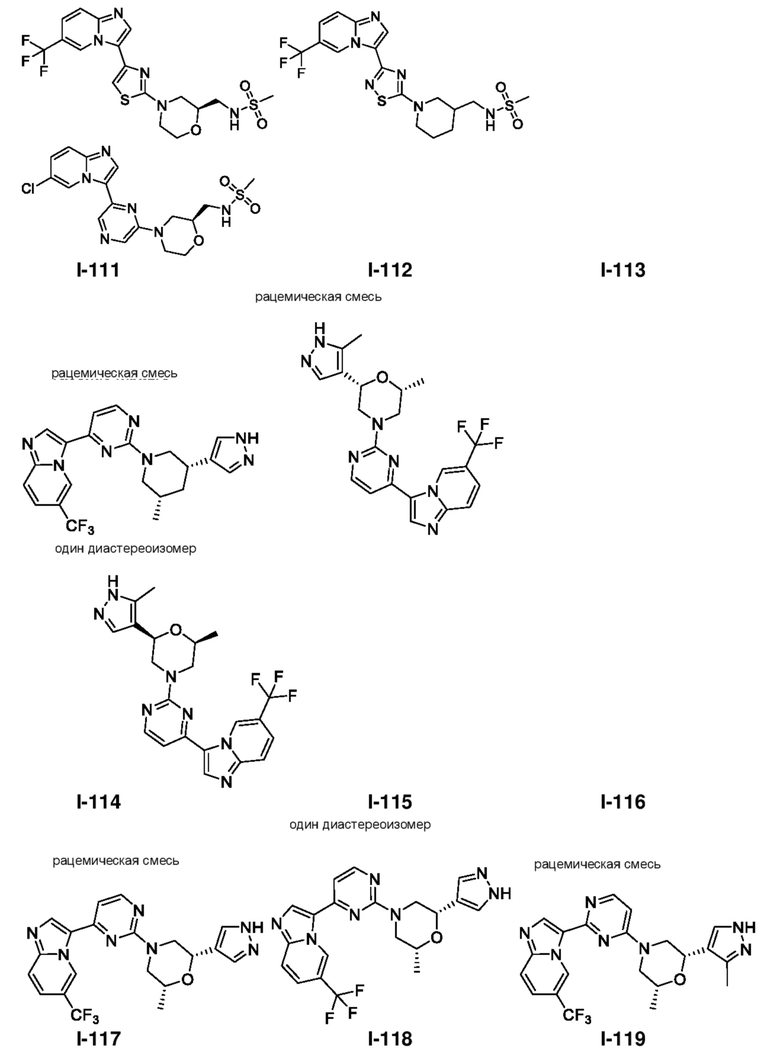
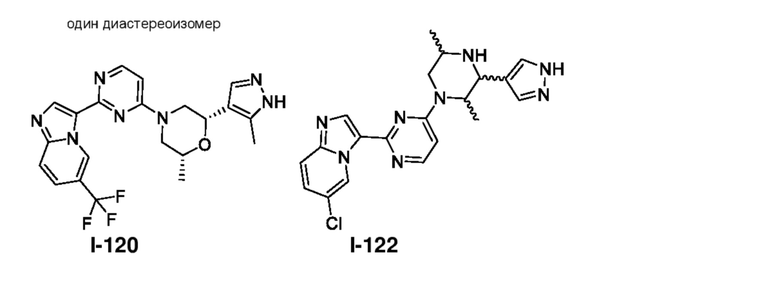
[00144] В некоторых вариантах осуществления настоящее изобретение относится к соединениям, приведенным выше в таблице 1, или их фармацевтически приемлемым солям.
[00145] В некоторых вариантах осуществления настоящее изобретение относится к комплексу, включающему GCN2 и ингибитор.
4. Общие методики получения соединений, предлагаемых в настоящем изобретении
[00146] Соединения, предлагаемые в настоящем изобретении, обычно можно получить или выделить по синтетическим и/или полусинтетическим методикам, известным специалистам в данной области техники для получения аналогичных соединений и по методикам, подробно описанным в примерах в настоящем изобретении.
[00147] На приведенных ниже схемах приведены конкретная защитная группа ("PG"), отщепляющаяся группа ("LG") или условия превращения и специалист с общей подготовкой в данной области техники должен понимать, что другие защитные группы, отщепляющиеся группы и условия превращения также являются подходящими и входят в объем настоящего изобретения. Такие группы и превращения подробно описаны с публикации March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, M. B. Smith and J. March, 5th Edition, John Wiley & Sons, 2001, Comprehensive Organic Transformations, R. C. Larock, 2nd Edition, John Wiley & Sons, 1999 и Protecting Groups in Organic Synthesis, T. W. Greene and P. G. M. Wuts, 3rd edition, John Wiley & Sons, 1999, которые во всей своей полноте включены в настоящее изобретение в качестве ссылки.
[00148] При использовании в настоящем изобретении выражение "отщепляющаяся группа" (LG) включает, но не ограничивается только ими, галогены (например, фторид, хлорид, бромид, йодид), сульфонаты (например, мезилат, тозилат, бензолсульфонат, брозилат, нозилат, трифлат), diazonium и т. п.
[00149] При использовании в настоящем изобретении выражение "защитная группа кислорода" включает, например, защитные группы карбонила, защитные группы гидроксила и т. п. Защитные группы гидроксила хорошо известны в данной области техники и включают подробно описанные в публикации Protecting Groups in Organic Synthesis, T. W. Greene and P. G. M. Wuts, 3rd edition, John Wiley & Sons, 1999, которая во всей своей полноте включена в настоящее изобретение в качестве ссылки. Примеры подходящих защитных групп гидроксила включают, но не ограничиваются только ими, сложноэфирные, простые аллилэфирные, простые эфирные, простые силилэфирные, простые алкилэфирные, простые арилалкилэфирные и простые алкоксиалкилэфирные. Примеры таких сложноэфирныех групп включают формиаты, ацетаты, карбонаты и сульфонаты. Конкретные примеры включают формиат, бензоилформиат, хлорацетат, трифторацетат, метоксиацетат, трифенилметоксиацетат, п-хлорфеноксиацетат, 3-фенилпропионат, 4-оксопентаноат, 4,4-(этилендитио)пентаноат, пивалат (триметилацетил), кротонат, 4-метокси-кротонат, бензоат, п-бензилбензоат, 2,4,6-триметилбензоат, карбонаты, такие как метил, 9-флуоренилметил, этил, 2,2,2-трихлорэтил, 2-(триметилсилил)этил, 2-(фенилсульфонил)этил, винил, аллил и п-нитробензил. Примеры таких силиловых простых эфирных групп включают триметилсилил, триэтилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, триизопропилсилил и другие триалкилсилиловые простые эфирные группы. Алкиловые простые эфирные группы включают метил, бензил, п-метоксибензил, 3,4-диметоксибензил, тритил, трет-бутил, аллил и аллилоксикарбониловые простые эфирные группы или производные. Алкоксиалкиловые простые эфирные группы включают ацетали, такие как метоксиметил, метилтиометил, (2-метоксиэтокси)метил, бензилоксиметил, бета-(триметилсилил)этоксиметил и тетрагидропираниловые простые эфирные группы. Примеры арилалкиловых простых эфирных групп включают бензил, п-метоксибензил-(MPM), 3,4-диметоксибензил, O-нитробензил, п-нитробензил, п-галогенбензил, 2,6-дихлорбензил, п-цианобензил и 2- и 4-пиколил.
[00150] Защитные группы аминогруппы хорошо известны в данной области техники и включают подробно описанные в публикации Protecting Groups in Organic Synthesis, T. W. Greene and P. G. M. Wuts, 3rd edition, John Wiley & Sons, 1999, которая во всей своей полноте включена в настоящее изобретение в качестве ссылки. Подходящие защитные группы аминогруппы включают, но не ограничиваются только ими, арилалкиламины, карбаматы, циклические имиды, аллиламины, амиды и т. п. Примеры таких групп включают трет-бутилоксикарбонил (BOC), этоксикарбонил, метилоксикарбонил, трихлорэтилоксикарбонил, аллилоксикарбонил (Alloc), бензилоксикарбонил (CBZ), аллил, фталимид, бензил-(Bn), флуоренилметилкарбонил (Fmoc), формил, ацетил, хлорацетил, дихлорацетил, трихлорацетил, фенилацетил, трифторацетил, бензоил и т. п.
[00151] Схема 1: Общая схема получения соединений формулы I, в которой кольцо B представляет собой пиримидин, связанный с бициклическим ядром в положении 2, R3 означает водород, R4 означает водород, p равно 1 и q равно 1.
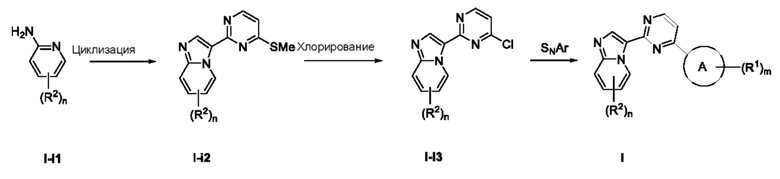
[00152] На приведенной выше схеме 1 каждое кольцо A, R1, R2, m и n является таким, как определено выше и ниже и в классах подклассах, описанных в настоящем изобретении.
[00153] Схема 2: Общая схема получения соединений формулы I, в которой кольцо B представляет собой пиримидин, связанный с бициклическим ядром в положении 2, R3 означает водород, R4 означает водород, n равно 1, p равно 1 и q равно 1.
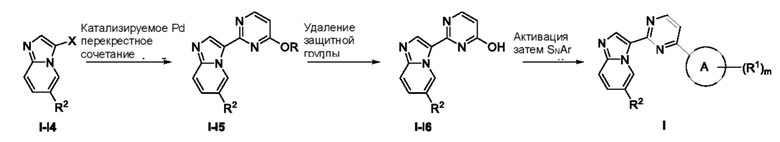
[00154] На приведенной выше схеме 2 каждое кольцо A, R1, R2, и m является таким, как определено выше и ниже и в классах подклассах, описанных в настоящем изобретении.
[00155] Схема 3: Общая схема получения соединений формулы I, в которой кольцо B представляет собой пиримидин, связанный с бициклическим ядром в положении 2, R3 означает водород, R4 означает водород, p равно 1 и q равно 1.
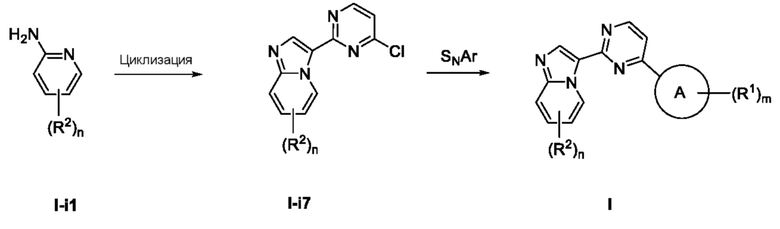
[00156] На приведенной выше схеме 3 каждое кольцо A, R1, R2, m и n является таким, как определено выше и ниже и в классах подклассах, описанных в настоящем изобретении.
[00157] Схема 4: Общая схема получения соединений формулы I, в которой кольцо B представляет собой пиримидин, связанный с бициклическим ядром в положении 4, R3 означает водород, R4 означает водород, n равно 1, p равно 1 и q равно 1.
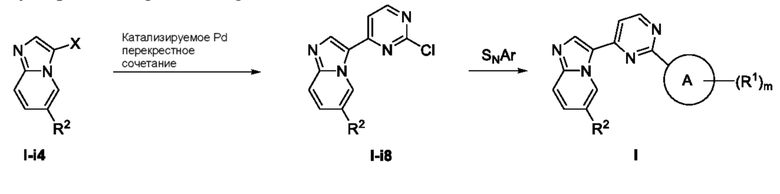
[00158]На приведенной выше схеме 4 каждое кольцо A, R1, R2, и m является таким, как определено выше и ниже и в классах подклассах, описанных в настоящем изобретении.
[00159] Специалист в данной области техники должен понимать, что соединения формулы I могут содержать один или большее количество стереоцентров и могут содержаться в виде рацемической смеси или смеси диастереоизомеров. Специалист в данной области техники также должен понимать, что в данной области техники известно много методик разделения изомеров и получения стереохимически обогащенных или стереохимически чистых изомеров этих соединений, включая, но не ограничиваясь только ими, HPLC, хиральную HPLC, фракционную кристаллизацию стереоизомерных солей, кинетическое ферментативное разделение (например, с помощью липазы или эстеразы, выделенной из грибов, бактерий или животных) и образование ковалентных диастереоизомерных производных с использованием энантиомерно обогащенного реагента.
[00160] Специалист в данной области техники должен понимать, что разные функциональные группы, содержащиеся в соединениях, предлагаемых в настоящем изобретении, такие как алифатические группы, спиртовые, карбоксильные, сложноэфирные, амидные, альдегидные, галогенидные и нитрильные можно подвергнуть взаимопревращению по методикам, хорошо известным в данной области техники, включая, но не ограничиваясь только ими восстановление, окисление, этерификацию, гидролиз, частичное окисление, частичное восстановление, галогенирование, дегидратацию, частичную гидратацию и гидрирование. "March’s Advanced Organic Chemistry", 5th Ed., Ed.: Smith, M.B. and March, J., John Wiley & Sons, New York: 2001, которая во всей своей полноте включена в настоящее изобретение в качестве ссылки. Для таких взаимопревращений может потребоваться одна или большее количество указанных выше методик и некоторые методики синтеза соединений, предлагаемых в настоящем изобретении, описаны ниже в разделе примеров.
5. Применение, приготовление и введение
a. Фармацевтически приемлемые композиции
[00161] В другом варианте осуществления настоящее изобретение относится к композиции, содержащей соединение, предлагаемое в настоящем изобретении, или его фармацевтически приемлемое производное и фармацевтически приемлемый носитель, вспомогательное вещество или разбавитель. Количество соединения в композициях, предлагаемых в настоящем изобретении, является таким, которое эффективно для измеримого ингибирования протеинкиназы GCN2 или ее мутанта в биологическом образце или у пациента. В некоторых вариантах осуществления количество соединения в композициях, предлагаемых в настоящем изобретении, является таким, которое эффективно для измеримого ингибирования протеинкиназы GCN2 или ее мутанта в биологическом образце или у пациента. В некоторых вариантах осуществления композицию, предлагаемую в настоящем изобретении, готовят для введения пациенту, нуждающемуся в такой композиции. В некоторых вариантах осуществления композицию, предлагаемую в настоящем изобретении, готовят для перорального введения пациенту.
[00162] Термин "пациент" при использовании в настоящем изобретении означает животное, предпочтительно млекопитающее и наиболее предпочтительно человека.
[00163] Термин "фармацевтически приемлемый носитель, вспомогательное вещество или разбавитель" означает нетоксичный носитель, вспомогательное вещество или разбавитель, который не нарушает фармакологическую активность соединения, с которым оно приготовлено. Фармацевтически приемлемые носители, вспомогательные вещества или разбавители, которые можно использовать в композициях, предлагаемых в настоящем изобретении, включают, но не ограничиваются только ими, ионообменники, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, смеси частичных глицеридов насыщенных растительных жирных кислот, вода, соли или электролиты, такие как сульфат протамина, динатрийгидрофосфат, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натриевая соль карбоксиметилцеллюлозы, полиакрилаты, воска, блок-сополимеры полиэтилен-полиоксипропилен, полиэтиленгликоль и ланолин.
[00164] "Фармацевтически приемлемое производное" означает любую нетоксичную соль, сложный эфир, соль сложного эфира или другое производное соединения, предлагаемого в настоящем изобретении, которое после введения реципиенту способно, прямо или косвенно, образовывать соединение, предлагаемое в настоящем изобретении, или его ингибирующий активный метаболит или остаток.
[00165] При использовании в настоящем изобретении термин "его ингибирующий активный метаболит или остаток" означает, что его метаболит или остаток также представляет собой ингибитор протеинкиназы GCN2 или его мутант.
[00166] Композиции, предлагаемые в настоящем изобретении, можно вводить перорально, парентерально, с помощью спрея для ингаляции, местно, ректально, назально, буккально, вагинально или с помощью имплантированного резервуара. Термин "парентеральный" при использовании в настоящем изобретении включает методики подкожной, внутривенной, внутримышечной, внутрисуставной, внутрисуставной, надчревной, интратекальной, внутрипеченочной, проводимой в пораженные ткани и внутричерепной инъекции или инфузии. Предпочтительно, если композиции вводят перорально, внутрибрюшинно или внутривенно. Стерильные формы для инъекции композиций, предлагаемых в настоящем изобретении, могут представлять собой водную или масляную суспензия. Эти суспензии можно готовить по методикам, известным в данной области техники, с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный препарат для инъекции также может представлять собой стерильный раствор или суспензию для инъекции в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. В число приемлемых разбавителей и растворителей, которые можно использовать, входят вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные, нелетучие масла обычно используют в качестве растворителя или суспендирующей среды.
[00167] Для этой цели можно использовать любое мягкое нелетучее масло, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицериды, применимы для приготовления форм для инъекции, как и натуральные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, их полиоксиэтилированные производные. Эти масляные растворы или суспензии также могут содержать обладающий длинной цепью спиртовый разбавитель или диспергирующее средство, такое как карбоксиметилцеллюлоза, или аналогичные диспергирующие агенты, которые обычно используют для приготовления фармацевтически приемлемых дозированных форм, включая эмульсии и суспензии. Другие обычно использующиеся поверхностно-активные вещества, такие как Tweens, Spans, и другие эмульгирующие агенты или усилители биодоступности, которые обычно используют для приготовления фармацевтически приемлемых твердых, жидких или других дозированных форм, также можно использовать для приготовления.
[00168] Фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, можно вводить перорально в любой перорально приемлемой дозированной форме, включая, но не ограничиваясь только ими, капсулы, таблетки, водные суспензии или растворы. В случае таблетки для перорального применения, обычно использующиеся носители включают лактозу и кукурузный крахмал. Также обычно добавляют смазывающие агенты, такие как стеарат магния. Для перорального введения в виде капсулы обычные разбавители включают лактозу и высушенный кукурузный крахмал. Если для перорального применения необходимы водные суспензии, активный ингредиент объединяют с эмульгирующими и суспендирующими агентами. При желании также можно добавлять некоторые подсластители, вкусовые или окрашивающие агенты.
[00169] Альтернативно, фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, можно вводить в виде суппозиториев для ректального введения. Их можно получить путем смешивания средства с подходящим нераздражающим инертным наполнителем, который является твердым при комнатной температуре, но жидким при температуре в прямой кишке и поэтому плавится в прямой кишке с высвобождением лекарственного средства. Такие материалы включают масло какао, пчелиный воск и полиэтиленгликоли.
[00170] Фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, также можно вводить местно, в особенности если мишень для лечения включает участки или органы, легко доступные с помощью местного применения, включая заболевания глаз, кожи или нижних отделов желудочно-кишечного тракта. Подходящие местные препараты легко приготовить для каждого из этих участков или органов.
[00171] Местное применение для нижних отделов желудочно-кишечного тракта можно провести с помощью препарата ректального суппозитория (см. выше) или подходящего препарата для клизмы. также можно использовать местные-чрескожные пластыри.
[00172] Для местного применения предложенные фармацевтически приемлемые композиции можно готовить в виде подходящей мази, содержащей активный компонент, суспендированный или растворенный в одном или большем количестве носителей. Носители для местного введения соединений, предлагаемых в настоящем изобретении, включают, но не ограничиваются только ими, минеральное масло, жидкое вазелиновое масло, белое вазелиновое масло, пропиленгликоль, полиоксиэтилен, полиоксипропилен, эмульгирующийся воск и воду. Альтернативно, предложенные фармацевтически приемлемые композиции можно готовить в виде подходящей примочки или крема, содержащего активные компоненты, суспендированные или растворенные в одном или большем количестве фармацевтически приемлемых носителей. Подходящие носители включают, но не ограничиваются только ими, минеральное масло, сорбитанмоностеарат, полисорбат 60, воск на основе цетиловых сложных эфиров, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
[00173] Для применения в офтальмологии предложенные фармацевтически приемлемые композиции можно готовить в виде микронизированных суспензий в изотоническом с отрегулированным pH стерильном физиологическом растворе или, предпочтительно, в виде растворов в изотоническом с отрегулированным pH стерильном физиологическом растворе с использованием или без использования консерванта, такого как бензилалконийхлорид. Альтернативно, для применения в офтальмологии фармацевтически приемлемые композиции можно готовить в виде мази, такой как на основе вазелинового масла.
[00174] Фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, также можно вводить с помощью назального аэрозоля или ингаляции. Такие композиции готовят по методикам, хорошо известным в области приготовления фармацевтических препаратов и их можно приготовить в виде растворов в физиологическом растворе, используя бензиловый спирт или других подходящие консерванты, стимуляторы всасывания для увеличения биодоступности, фторзамещенные углеводороды, и/или другие обычные солюбилизирующие или диспергирующие агенты.
[00175] Наиболее предпочтительно, фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, готовят для перорального введения. Такие препараты можно вводить с пищей или без пищи. В некоторых вариантах осуществления фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, вводят без пищи. В других вариантах осуществления фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, вводят с пищей.
[00176] Количество соединений, предлагаемых в настоящем изобретении, которое можно объединить с материалами носителя для получения композиции в виде одной дозированной формы меняется в зависимости от реципиента, подвергающегося лечению, конкретного режима введения. Предложенные композиции предпочтительно следует готовить так, чтобы пациенту, получающему эти композиции, можно было вводить дозу ингибитора, равную 0,01-100 мг/кг массы тела/сутки.
[00177] Также следует понимать, что конкретные доза и режим лечения любого конкретного пациента зависит от различных факторов, включая активность конкретного использующегося соединения, возраст, массу тела, общее состояние здоровья, пол, диету, время введения, скорость выведения, комбинации лекарственных средств и решение лечащего врача и тяжесть конкретного заболевания, подвергающегося лечению. Количество соединения, предлагаемого в настоящем изобретении, в композиции также зависит от конкретного соединения в композиции.
b. Применение соединений и фармацевтически приемлемых композиций
[00178] Соединения и композиции, описанные в настоящем изобретении, обычно применимы для ингибирования активности киназы GCN2.
[00179] Активность соединения, использующегося в настоящем изобретении, в качестве ингибитора GCN2 или ее мутанта можно исследовать in vitro, in vivo или с помощью линии клеток. Исследования in vitro включают исследования, в которых определяют ингибирование фосфорилирующей активности и/или последующие функциональные последствия или ATPase активность активированной GCN2 или ее мутанта. В альтернативных исследованиях in vitro количественно определяют способность ингибитора связываться с GCN2. Связывание ингибитора можно измерить путем введения в ингибитор радиоактивной метки до связывания, выделения комплекса ингибитор/GCN2 и определения количества связанной радиоактивной метки. Альтернативно, связывание ингибитора можно определить путем проведения сравнительного эксперимента, в котором новые ингибиторы инкубируют с GCN2, связанной с известными радиолигандами. Подробные условия исследования соединения, использующегося в настоящем изобретении, в качестве ингибитора GCN2 или ее мутанта приведены ниже в примерах.
[00180] При использовании в настоящем изобретении термины "лечение", "лечить" означают обращения, облегчения, задержки начала или подавления прогрессирования заболевания или нарушения или одного или большего количества его симптомов, описанных в настоящем изобретении. В некоторых вариантах осуществления лечение можно проводить после развития одного или большего количества симптомов. В других вариантах осуществления лечение можно проводить при отсутствии симптомов. Например, лечение можно проводить у восприимчивого индивидуума до начала симптомов (например, с учетом симптомов в анамнезе и/или с учетом генетических или других факторов восприимчивости). Лечение также можно продолжать после устранения симптомов, например, для предупреждения или задержки их рецидива.
[00181] Предложенные соединения являются ингибиторами одной или большего количества GCN2 и поэтому применимы для лечения одного или большего количества нарушений, связанных с активностью GCN2. Таким образом, в некоторых вариантах осуществления настоящее изобретение относится к способу лечения опосредуемого GCN2 нарушения, включающему стадию введения нуждающемуся в нем пациенту соединения, предлагаемого в настоящем изобретении, или содержащей его фармацевтически приемлемой композиции.
[00182] При использовании в настоящем изобретении термины "опосредуемые GCN2" нарушения, заболевания и/или патологические состояния при использовании в настоящем изобретении означает любое заболевание или другое болезнетворное патологическое состояние, для которого известно, что играют роль GCN2 или ее мутант. Соответственно, другой вариант осуществления настоящего изобретения относится к лечению или ослаблению тяжести одного или большего количества заболеваний, для которых известно, что играют роль GCN2 или ее мутант.
[00183] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения одного или большего количества нарушений, заболеваний и/или патологических состояний, где нарушение, заболевание или патологическое состояние выбрано из группы, включающей воспалительные патологические состояния, иммунологические патологические состояния, аутоиммунные патологические состояния, аллергические патологические состояния, ревматические патологические состояния, тромбические патологические состояния, рак, инфекции, нейродегенеративные заболевания, дегенеративные заболевания, нейровоспалительные заболевания, сердечно-сосудистые заболевания и метаболические патологические состояния.
[00184] В некоторых вариантах осуществления рак, подвергающийся лечению, представляет собой сóлидную опухоль или опухоль крови и иммунной системы.
[00185] В некоторых вариантах осуществления рак представляет собой сóлидную опухоль, где сóлидная опухоль происходит из группы опухолей эпителия, мочевого пузыря, желудка, почек, головы и шеи, пищевода, шейки матки, щитовидной железы, кишечника, печени, головного мозга, предстательной железы, мочеполового тракта, лимфатической системы, желудка, гортани, костей, включая хондросаркому и саркому Юинга, зародышевых клеток, включая опухоли эмбриональной ткани, и/или легких, выбранную из группы, включающей моноцитарный лейкоз, аденокарциному легких, мелкоклеточные карциномы легких, рак поджелудочной железы, глиобластому, нейрофиброму, ангиосаркому, карциному молочной железы и/или злокачественную меланому.
[00186] В некоторых вариантах осуществления аутоиммунным патологическим состоянием является ревматоидный артрит, системная волчанка, рассеянный склероз, псориаз, синдром Шегрена или отторжение трансплантата органа.
[00187] В некоторых вариантах осуществления метаболическим патологическим состоянием является диабет.
[00188] В некоторых вариантах осуществления дегенеративным заболеванием является остеоартрит.
[00189] В некоторых вариантах осуществления воспалительным патологическим состоянием является астма, воспалительная болезнь кишечника или гигантоклеточный артериит.
[00190] В некоторых вариантах осуществления сердечно-сосудистым заболеванием является ишемическое повреждение.
[00191] В некоторых вариантах осуществления нейродегенеративным заболеванием является болезнь Альцгеймера, синдром Дауна, наследственное кровоизлияние в головной мозг с амилоидозом голландского типа, амилоидная ангиопатия головного мозга, болезнь Крейтцфельда-Якоба, лобно-височные слабоумия, болезнь Гентингтона или болезнь Паркинсона.
[00192] В некоторых вариантах осуществления инфекция вызвана лейшманией, микобактериями, включая M. leprae, M. tuberculosis и/или M. avium, плазмодий, вирус иммунодефицита человека, вирус Эпштейна-Барра, вирус простого герпеса или вирус гепатита C.
[00193] Кроме того, настоящее изобретение относится к применению соединения, определенного в настоящем изобретении, или его фармацевтически приемлемой соли, или гидрата, или сольвата для приготовления лекарственного средства, предназначенного для лечения воспалительных патологических состояний, иммунологических патологических состояний, аутоиммунных патологических состояний, аллергических патологических состояний, ревматических патологических состояний, тромбических патологических состояний, рака, инфекций, нейродегенеративных заболеваний, дегенеративных заболеваний, нейровоспалительных заболеваний, сердечно-сосудистых заболеваний или метаболических патологических состояний.
c. Комбинированные терапевтические средства
[00194] В зависимости от конкретного патологического состояния или заболевания, подвергающегося лечению, дополнительные терапевтические средства, которые обычно вводят для лечения такого патологического состояния, можно вводить в комбинации с соединениями и композициями, предлагаемыми в настоящем изобретении. При использовании в настоящем изобретении дополнительные терапевтические средства, которые обычно вводят для лечения конкретного заболевания или патологического состояния, известны, как "подходящие для заболевания или патологического состояния, подвергающегося лечению".
[00195] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения раскрытого заболевания или патологического состояния, включающему введение нуждающемуся в нем пациенту эффективного количества соединения, раскрытого в настоящем изобретении, или его фармацевтически приемлемой соли и совместное введение, одновременно или последовательно, эффективного количества одного или большего количества дополнительных терапевтических средств, таких как описанные в настоящем изобретении. В некоторых вариантах осуществления способ включает совместное введение одного дополнительного терапевтического средства. В некоторых вариантах осуществления способ включает совместное введение двух дополнительных терапевтических средств. В некоторых вариантах осуществления комбинация раскрытого соединения и дополнительного терапевтического средства или средств действует синергетически.
[00196] Соединение, предлагаемое в настоящем изобретении, также можно использовать в сочетании с известными терапевтическими процедурами, например, введением гормонов или облучением. В некоторых вариантах осуществления предлагаемое соединение используют в качестве радиосенсибилизатора, в особенности для лечения опухолей, которые обладают низкой чувствительностью к радиотерапии.
[00197] Соединение, предлагаемое в настоящем изобретении, можно вводить по отдельности или в комбинации с одним или большим количеством других терапевтических соединений, возможное комбинированное терапевтическое средство имеет вид фиксированных комбинаций или введение соединения, предлагаемого в настоящем изобретении, и одного или большего количества других терапевтических соединений поочередно или независимо одно от другого, или объединенного введения фиксированных комбинаций и одного или большего количества других терапевтических соединений. Соединение, предлагаемое в настоящем изобретении, можно кроме этого или в дополнение вводить специально для противоопухолевой терапии в комбинации с химиотерапией, радиотерапией, иммунотерапией, фототерапией, хирургическим вмешательством или их комбинацией. Длительная терапия также возможна в качестве вспомогательной терапии в контексте других стратегий лечения, как описано выше. Другие возможные пути лечения представляют собой терапию для поддержания статуса пациента после регрессии опухоли или даже химиопревентивную терапию, например, у пациентов в группе риска.
[00198] В некоторых вариантах осуществления предложенную комбинацию или содержащую ее композицию вводят в комбинации с другим терапевтическим средством.
[00199] Примеры средств комбинаций, предлагаемых в настоящем изобретении, которые также можно объединять, включают без наложения ограничений: средства лечения болезни Альцгеймера, такие как арицепт® и экселон®; средства лечения HIV, такие как ритонавир; средства лечения болезни Паркинсона, такие как L-ДОПА/карбидопа, энтакапон, ропинрол, прамипексол, бромокриптин, перголид, тригексефендил и амантадин; средства лечения рассеянного склероза (MS), такие как бета-интерферон (например, авонекс® и ребиф®), копаксон® и митоксантрон; средства лечения астмы, такие как албутерол и сингуляр®; средства лечения шизофрении, такие как зипрекса, риспердал, сероквель и галоперидол; противовоспалительные средства, такие как кортикостероиды, блокаторы TNF, IL-1 RA, азатиоприн, циклофосфамид и сульфасалазин; иммуномодулирующие и иммуносупрессивные средства, такие как циклоспорин, такролимус, рапамицин, микофенолят мофетил, интерфероны, кортикостероиды, циклофосфамид, азатиоприн и сульфасалазин; нейротрофические факторы, такие как ингибиторы ацетилхолинэстеразы, ингибиторы MAO, интерфероны, противосудорожные средства, блокаторы ионных каналов, рилузол и антипаркинсонические средства; средства лечения сердечно-сосудистого заболевания, такие как бета-блокаторы, ингибиторы ACE, диуретики, нитраты, блокаторы кальциевых каналов и статины; средства лечения заболевание печени, такие как кортикостероиды, холестирамин, интерфероны и противовирусные средства; средства лечения нарушений крови, такие как кортикостероиды, противолейкозные средства и факторы роста; средства, которые пролонгируют или улучшают фармакокинетику, такие как ингибиторы цитохрома P450 (т. е. ингибиторы метаболического расщепления) и ингибиторы CYP3A4 (например, кетоконазол и ритонавир) и средства лечения иммунодефицитных нарушений, такие как гамма-глобулин.
[00200] В некоторых вариантах осуществления комбинацию терапевтических средств, предлагаемую в настоящем изобретении, или содержащую их фармацевтически приемлемую композицию вводят в комбинации с моноклональными антителами или терапевтической siRNA.
[00201] Эти дополнительные средства можно вводить отдельно от предложенного комбинированного терапевтического средства, в качестве части многодозового режима. Альтернативно, эти средства могут быть частью одной дозированной формы, смешанной с соединением, предлагаемым в настоящем изобретении, в единой композиции. Если вводят в качестве части многодозового режима, эти два активных средства могут быть введены одновременно, последовательно или с промежутком между ними, обычно равным не более 5 ч.
[00202] При использовании в настоящем изобретении термин "комбинированное", "объединенное" и родственные термины означают одновременное или последовательное введение терапевтических средств, предлагаемых в настоящем изобретении. Например, комбинацию, предлагаемую в настоящем изобретении, можно вводить с другим терапевтическим средством одновременно или последовательно в отдельны разовых дозированных формах или вместе в одной разовой дозированной форме.
[00203] Количество одного или большего количества дополнительных терапевтических средств, содержащихся в композициях, предлагаемых в настоящем изобретении, может быть не больше, чем количество, которое обычно вводят в композиции, содержащей это терапевтическое средство в качестве единственного активного средства. Предпочтительное количество одного или большего количества дополнительных терапевтических средств в раскрытых в настоящем изобретении композициях находится в диапазоне примерно от 50% до 100% от количества, обычно содержащегося в композиции, содержащей это средство в качестве единственного терапевтически активного средства. В некоторых вариантах осуществления одно или большее количество дополнительных терапевтических средств вводят в дозе, равной примерно 50%, примерно 55%, примерно 60%, примерно 65%, примерно 70%, примерно 75%, примерно 80%, примерно 85%, примерно 90% или примерно 95% от обычно количества вводимого количества этого средства. При использовании в настоящем изобретении выражение "обычно вводимое" означает утвержденное FDA для введения количество терапевтического средства, указанное в листке-вкладыше.
[00204] В одном варианте осуществления настоящее изобретение относится к композиции, содержащей соединение формулы I и одно или большее количество дополнительных терапевтических средств. Терапевтическое средство можно вводить вместе с соединением формулы I или можно вводить до или после введения соединения формулы I. Подходящие терапевтические средства подробно описаны ниже. В некоторых вариантах осуществления соединение формулы I можно вводить за 5 мин, 10 мин, 15 мин, 30 мин, 1 ч, 2 ч, 3 ч, 4 ч, 5, ч, 6 ч, 7 ч, 8 ч, 9 ч, 10 ч, 11 ч, 12 ч, 13 ч, 14 ч, 15 ч, 16 ч, 17 ч или 18 ч до терапевтического средства. В других вариантах осуществления соединение формулы I можно вводить через 5 мин, 10 мин, 15 мин, 30 мин, 1 ч, 2 ч, 3 ч, 4 ч, 5, ч, 6 ч, 7 ч, 8 ч, 9 ч, 10 ч, 11 ч, 12 ч, 13 ч, 14 ч, 15 ч, 16 ч, 17 ч или 18 ч после терапевтического средства.
[00205] В другом варианте осуществления настоящее изобретение относится к способу лечения воспалительного заболевания, нарушения или патологического состояния путем введения нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств. Такие дополнительные терапевтические средства могут представлять собой малые молекулы или рекомбинантные биологические средства и включают, например, ацетаминофен, нестероидные противовоспалительные лекарственные средства (NSAIDS), такие как аспирин, ибупрофен, напроксен, этодолак (лодин®) и целекоксиб, колхицин (колкрис®), кортикостероиды, такие как преднизон, преднизолон, метилпреднизолон, гидрокортизон и т. п., пробенецид, аллопуринол, фебуксостат (юлорик®), сульфасалазин (азульфидин®), противомалярийные средства, такие как гидроксихлорохин (плаквенил®) и хлорохин (арален®), метотрексат (ревматрекс®), соли золота, такие как тиоглюкозид золота (солганал®), тиомалат золота (миохризин®) и ауранофин (ридаура®), D-пеницилламин (депен® или купримин®), азатиоприн (имуран®), циклофосфамид (цитоксан®), хлорамбуцил (лейкеран®), циклоспорин (сандиммун®), лефлуномид (арава®) и "анти-TNF" средства, такие как этанерцепт (энбрел®), инфликсимаб (ремикаде®), голимумаб (симпони®), цертолизумаб пэгол (цимзия®) и адалимумаб (гумира®), "анти-IL-1" средства, такие как анакинра (кинерет®) и рилонацепт (аркалист®), канакинумаб (иларис®), ингибиторы анти-Jak, такие как тофацитиниб, антитела, такие как ритуксимаб (ритуксан®), "анти-T-клеточные" средства, такие как абатацепт (оренциа®), "анти-IL-6" средства, такие как тоцилизумаб (актемра®), диклофенак, кортизон, гиалуроновая кислота (синвиск® или гиалган®), моноклональные антитела, такие как танезумаб, антикоагулянты, такие как гепарин (кальцинпарин® или ликваемин®) и варфарин (кумадин®), противодиарейные средства, такие как дифеноксилат (ломотил®) и лоперамид (имодиум®), связывающие желчные кислоты средства, такие как холестирамин, алосетрон (лотронекс®), лубипростон (амитиза®), слабительные, такие как взвесь магнезии, полиэтиленгликоль (миралакс®), дулколакс®, корректол® и сенокот®, антихолинергетики или антиспазматические средства, такие как дицикломин (бентил®), сингуляр®, бета-2 агонисты, такие как албутерол (вентолин® HFA, провентил® HFA), левалбутерол (ксопенекс®), метапротеренол (алупент®), пирбутерол ацетат (максаир®), тербуталин сульфат (бретаир®), салметерол ксинафоат (серевент®) и формотерол (форадил®), антихолинергические средства, такие как ипратропийбромид (атровент®) и тиотропий (спирива®), кортикостероиды для ингаляции, такие как беклометазон дипропионат (бекловент®, квар® и ванцерил®), триамцинолон ацетонид (азмакорт®), мометазон (астманекс®), будесонид (пульмикорт®) и флунизолид (аэробид®), афвиар®, симбикорт®, дулера®, кромолин-натрий (интал®), метилксантины, такие как теофиллин (тео-дур®, теолаир®, слоу-бид®, юнифил®, тео-24®) и аминофиллин, антитела к IgE, такие как омализумаб (ксолаир®), ингибиторы нуклеозидной обратной транскриптазы, такие как зидовудин (ретровир®), абакавир (зиаген®), абакавир/ламивудин (эпзиком®), абакавир/ламивудин/зидовудин (тризивир®), диданозин (видекс®), эмтрицитабин (эмтрива®), ламивудин (эпивир®), ламивудин/зидовудин (комбивир®), ставудин (зерит®) и залцитабин (хивид®), ингибиторы ненуклеозидной обратной транскриптазы, такие как делавирдин (рескриптор®), эфавиренз (сустива®), невирапин (вирамун®) и этравирин (интеленс®), ингибиторы нуклеотидной обратной транскриптазы, такие как тенофовир (виреад®), ингибиторы протеазы, такие как ампренавир (агенераза®), атазанавир (реатаз®), дарунавир (презиста®), фосампренавир (лексива®), индинавир (криксиван®), лопинавир и ритонавир (калетра®), нелфинавир (вирацепт®), ритонавир (норвир®), саквинавир (фортоваза® или инвираза®) и типранавир (аптивус®), ингибиторы входа, такие как энфувиртид (фузеон®) и маравирок (селзентри®), ингибиторы интегразы, такие как ралтегравир (исентресс®), доксорубицин (гидродаунорубицин®), винкристин (онковин®), бортезомиб (велкаде®) и дексаметазон (декадрон®) в комбинации с леналидомид (ревлимид ®) или любую их комбинацию (комбинации).
[00206] В другом варианте осуществления настоящее изобретение относится к способу лечения подагры, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей нестероидные противовоспалительные лекарственные средства (NSAIDS), такие как аспирин, ибупрофен, напроксен, этодолак (лодин®) и целекоксиб, колхицин (колкрис®), кортикостероиды, такие как преднизон, преднизолон, метилпреднизолон, гидрокортизон и т. п., пробенецид, аллопуринол и фебуксостат (юлорик®).
[00207] В другом варианте осуществления настоящее изобретение относится к способу лечения ревматоидного артрита, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей нестероидные противовоспалительные лекарственные средства (NSAIDS), такие как аспирин, ибупрофен, напроксен, этодолак (лодин®) и целекоксиб, кортикостероиды, такие как преднизон, преднизолон, метилпреднизолон, гидрокортизон и т. п., сульфасалазин (азульфидин®), противомалярийные средства, такие как гидроксихлорохин (плаквенил®) и хлорохин (арален®), метотрексат (ревматрекс®), соли золота, такие как тиоглюкозид золота (солганал®), тиомалат золота (миохризин®) и ауранофин (ридаура®), D-пеницилламин (депен® или купримин®), азатиоприн (имуран®), циклофосфамид (цитоксан®), хлорамбуцил (лейкеран®), циклоспорин (сандиммун®), лефлуномид (арава®) и "анти-TNF" средства, такие как этанерцепт (энбрел®), инфликсимаб (ремикаде®), голимумаб (симпони®), цертолизумаб пэгол (цимзия®) и адалимумаб (гумира®), "анти-IL-1" средства, такие как анакинра (кинерет®) и рилонацепт (аркалист®), антитела, такие как ритуксимаб (ритуксан®), "анти-T-клеточные" средства, такие как абатацепт (оренциа®) и "анти-IL-6" средства, такие как тоцилизумаб (актемра®).
[00208] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения остеоартрита, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей ацетаминофен, нестероидные противовоспалительные лекарственные средства (NSAIDS), такие как аспирин, ибупрофен, напроксен, этодолак (лодин®) и целекоксиб, диклофенак, кортизон, гиалуроновая кислота (синвиск® или гиалган®) и моноклональные антитела, такие как танезумаб.
[00209] В некоторых вариантах осуществления настоящее изобретение относится к лечения волчанки, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей ацетаминофен, нестероидные противовоспалительные лекарственные средства (NSAIDS), такие как аспирин, ибупрофен, напроксен, этодолак (лодин®) и целекоксиб, кортикостероиды, такие как преднизон, преднизолон, метилпреднизолон, гидрокортизон и т. п., противомалярийные средства, такие как гидроксихлорохин (плаквенил®) и хлорохин (арален®), циклофосфамид (цитоксан®), метотрексат (ревматрекс®), азатиоприн (имуран®) и антикоагулянты, такие как гепарин (кальцинпарин® или ликваемин®) и варфарин (кумадин®).
[00210] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения воспалительной болезни кишечника, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей мезаламин (азакол®) сульфасалазин (азульфидин®), противодиарейные средства, такие как дифеноксилат (ломотил®) и лоперамид (имодиум®), связывающие желчные кислоты средства, такие как холестирамин, алосетрон (лотронекс®), лубипростон (амитиза®), слабительные, такие как взвесь магнезии, полиэтиленгликоль (миралакс®), дулколакс®, корректол® и сенокот® и антихолинергетики или антиспазматические средства, такие как дицикломин (бентил®), анти-TNF терапевтические средства, стероиды и антибиотики, такие как флагил или ципрофлоксацин.
[00211] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения астмы, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей сингуляр®, бета-2 агонисты, такие как албутерол (вентолин® HFA, провентил® HFA), левалбутерол (ксопенекс®), метапротеренол (алупент®), пирбутерол ацетат (максаир®), тербуталин сульфат (бретаир®), салметерол ксинафоат (серевент®) и формотерол (форадил®), антихолинергические средства, такие как ипратропийбромид (атровент®) и тиотропий (спирива®), кортикостероиды для ингаляции, такие как преднизон, преднизолон, беклометазон дипропионат (бекловент®, квар® и ванцерил®), триамцинолон ацетонид (азмакорт®), мометазон (астманекс®), будесонид (пульмикорт®), флунизолид (аэробид®), афвиар®, симбикорт® и дулера®, кромолин-натрий (интал®), метилксантины, такие как теофиллин (тео-дур®, теолаир®, слоу-бид®, юнифил®, тео-24®) и аминофиллин и антитела к IgE, такие как омализумаб (ксолаир®).
[00212] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения COPD, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей бета-2 агонисты, такие как албутерол (вентолин® HFA, провентил® HFA), левалбутерол (ксопенекс®), метапротеренол (алупент®), пирбутерол ацетат (максаир®), тербуталин сульфат (бретаир®), салметерол ксинафоат (серевент®) и формотерол (форадил®), антихолинергические средства, такие как ипратропийбромид (атровент®) и тиотропий (спирива®), метилксантины, такие как теофиллин (тео-дур®, теолаир®, слоу-бид®, юнифил®, тео-24®) и аминофиллин, кортикостероиды для ингаляции, такие как преднизон, преднизолон, беклометазон дипропионат (бекловент®, квар® и ванцерил®), триамцинолон ацетонид (азмакорт®), мометазон (астманекс®), будесонид (пульмикорт®), флунизолид (аэробид®), афвиар®, симбикорт® и дулера®.
[00213] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения HIV, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей ингибиторы нуклеозидной обратной транскриптазы, такие как зидовудин (ретровир®), абакавир (зиаген®), абакавир/ламивудин (эпзиком®), абакавир/ламивудин/зидовудин (тризивир®), диданозин (видекс®), эмтрицитабин (эмтрива®), ламивудин (эпивир®), ламивудин/зидовудин (комбивир®), ставудин (зерит®) и залцитабин (хивид®), ингибиторы ненуклеозидной обратной транскриптазы, такие как делавирдин (рескриптор®), эфавиренз (сустива®), невирапин (вирамун®) и этравирин (интеленс®), ингибиторы нуклеотидной обратной транскриптазы, такие как тенофовир (виреад®), ингибиторы протеазы, такие как ампренавир (агенераза®), атазанавир (реатаз®), дарунавир (презиста®), фосампренавир (лексива®), индинавир (криксиван®), лопинавир и ритонавир (калетра®), нелфинавир (вирацепт®), ритонавир (норвир®), саквинавир (фортоваза® или инвираза®) и типранавир (аптивус®), ингибиторы входа, такие как энфувиртид (фузеон®) и маравирок (селзентри®), ингибиторы интегразы, такие как ралтегравир (исентресс®) и их комбинации.
[00214] В другом варианте осуществления настоящее изобретение относится к способу лечения гемобластоза, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей ритуксимаб (ритуксан®), циклофосфамид (цитоксан®), доксорубицин (гидродаунорубицин®), винкристин (онковин®), преднизон, ингибитор передачи сигналов hedgehog, ингибитор BTK, ингибитор JAK/pan-JAK, ингибитор TYK2, ингибитор PI3K, ингибитор SYK и их комбинации.
[00215] В другом варианте осуществления настоящее изобретение относится к способу лечения сóлидной опухоли, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей ритуксимаб (ритуксан®), циклофосфамид (цитоксан®), доксорубицин (гидродаунорубицин®), винкристин (онковин®), преднизон, ингибитор передачи сигналов hedgehog, ингибитор BTK, ингибитор JAK/pan-JAK, ингибитор TYK2, ингибитор PI3K, ингибитор SYK и их комбинации.
[00216] В другом варианте осуществления настоящее изобретение относится к способу лечения гемобластоза, включающему введение нуждающемуся в нем пациенту соединения формулы I и ингибитор пути передачи сигналов Hedgehog (Hh). В некоторых вариантах осуществления гемобластоз представляет собой DLBCL (Ramirez et al "Defining causative factors contributing in the activation of hedgehog signaling in diffuse large B-cell lymphoma" Leuk. Res. (2012), published online July 17, и которая во всей своей полноте включена в настоящее изобретение в качестве ссылки).
[00217] В другом варианте осуществления настоящее изобретение относится к способу лечения диффузной крупноклеточной-В-клеточной лимфомы (DLBCL), включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей ритуксимаб (ритуксан®), циклофосфамид (цитоксан®), доксорубицин (гидродаунорубицин®), винкристин (онковин®), преднизон, ингибитор передачи сигналов hedgehog и их комбинации.
[00218] В другом варианте осуществления настоящее изобретение относится к способу лечения множественной миеломы, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей бортезомиб (велкаде®) и дексаметазон (декадрон®), ингибитор передачи сигналов hedgehog, ингибитор BTK, ингибитор JAK/pan-JAK, ингибитор TYK2, ингибитор PI3K, ингибитор SYK в комбинации с леналидомид (ревлимид®).
[00219] В другом варианте осуществления настоящее изобретение относится к способу лечения макроглобулинемии Вальденстрема, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей хлорамбуцил (лейкеран®), циклофосфамид (цитоксан®, неосар®), флударабин (флудара®), кладрибин (лейстатин®), ритуксимаб (ритуксан®), ингибитор передачи сигналов hedgehog, ингибитор BTK, ингибитор JAK/pan-JAK, ингибитор TYK2, ингибитор PI3K и ингибитор SYK.
[00220] В некоторых вариантах осуществления настоящее изобретение относится к способу лечения болезни Альцгеймера, включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей донепезил (арицепт®), ривастигмин (экселон®), галантамин (разадин®), такрин (когнекс®) и мемантин (наменда®).
[00221] В другом варианте осуществления настоящее изобретение относится к способу лечения отторжение трансплантата органа или реакции "трансплантат против хозяина", включающему введение нуждающемуся в нем пациенту соединения формулы I и одного или большего количества дополнительных терапевтических средств, выбранных из группы, включающей стероид, циклоспорин, FK506, рапамицин, ингибитор передачи сигналов hedgehog, ингибитор BTK, ингибитор JAK/pan-JAK, ингибитор TYK2, ингибитор PI3K и ингибитор SYK.
[00222] В другом варианте осуществления настоящее изобретение относится к способу лечения или ослабления тяжести заболевания, включающему введение нуждающемуся в нем пациенту соединения формулы I и ингибитор BTK, где заболевание выбрано из числа следующих: воспалительная болезнь кишечника, артрит, системная красная волчанка (SLE), васкулит, идиопатическая тромбоцитопеническая пурпура (ITP), ревматоидный артрит, псориатический артрит, остеоартрит, болезнь Стилла, ювенильный артрит, диабет, злокачественная миастения, тиреоидит Хашимото, тиреоидит Орда, болезнь Грейвса, аутоимунный тиреоидит, синдром Шегрена, рассеянный склероз, системный склероз, нейроборрелиоз Лайма, синдром Гийена-Барре, острый рассеянный энцефаломиелит, болезнь Аддисона, синдром опсоклонус-миоклонус, анкилозирующий спондилез, синдром антифосфолипидных антител, апластическая анемия, аутоиммунный гепатит, аутоиммунный гастрит, пернициозная анемия, целиакия, синдром Гудпасчера, идиопатическая тромбоцитопеническая пурпура, неврит зрительного нерва, склеродермия, первичный билиарный цирроз, синдром Рейтера, синдром Такаясу, височный артериит, тепловая аутоиммунная гемолитическая анемия, гранулематоз Вегенера, псориаз, генерализованная алопеция, болезнь Бехчета, хроническаяусталость, вегетативная дистония, мембранозная гломерулонефропатия, эндометриоз, интерстициальный цистит, обыкновенная пузырчатка, буллезный пемфигоид, нейромиотомия, склеродермия, вульводиния, гиперпролиферативное заболевание, отторжение трансплантированных органов или тканей, синдром приобретенного иммунодефицита (AIDS, также известный, как HIV), диабет типа 1, реакция "трансплантат против хозяина", трансплантация, трансфузия, анафилаксия, аллергии (например, аллергии на пыльцу растений, млечный сок, лекарственные средства, пищевые продукты, яды насекомых, шерсть животных, боязнь животных, клещи домашней пыли или чашевидные части тараканов), гиперчувствительность типа I, аллергический конъюнктивит, аллергический ринит и атопический дерматит, астма, аппендицит, атопический дерматит, астма, аллергия, блефарит, бронхиолит, бронхит, бурсит, цервицит, холангит, холецистит, хроническое отторжение трансплантата, колит, конъюнктивит, болезнь Крона, цистит, дакриоаденит, дерматит, дерматомиозит, энцефалит, эндокардит, эндометрит, энтерит, энтероколит, эпикондилит, эпидидимит, фасциит, фиброзит, гастрит, гастроэнтерит, пурпура Шенлейн-Геноха, гепатит, гнойный гидраденит, иммуноглобулин-A-нефропатия, интерстициальное заболевание легких, ларингит, мастит, менингит, миелит миокардит, миозит, нефрит, оофорит, орхит, остит, отит, панкреатит, паротит, перикардит, перитонит, фарингит, плеврит, флебит, пневмонит, пневмония, полимиозит, проктит, простатит, пиелонефрит, ринит, сальпингит, синусит, стоматит, синовит, тендинит, тонзиллит, язвенный колит, увеит, вагинит, васкулит или вульвит, B-пролиферативное клеточное нарушение, например, диффузная крупноклеточная В-клеточная лимфома, фолликулярная лимфома, хроническая лимфоцитарная лимфома, хронический лимфолейкоз, острый лимфолейкоз, пролимфоцитарный B-клеточный лейкоз, лимфоплазмоцитарная лимфома/макроглобулинемия Вальденстрема, селезеночная лимфома из клеток маргинальной зоны, множественная миелома (также известная, как плазмаклеточная миелома), неходжкинская лимфома, Ходжкинская лимфома, плазмоцитома, внеузловая B-клеточная лимфома из клеток маргинальной зоны, узловая B-клеточная лимфома из клеток маргинальной зоны, лимфома из клеток зоны мантии, средостенная (тимусная) крупноклеточная В-клеточная лимфома, внутрисосудистая крупноклеточная В-клеточная лимфома, первичная выпотная лимфома, лимфома Беркитта/лейкоз или лимфоматоидный гранулематоз, рак молочной железы, рак предстательной железы или рак тучных клеток (например, мастоцитома, тучноклеточный лейкоз, тучноклеточная саркома, системный мастоцитоз), рак кости, колоректальный рак, рак поджелудочной железы, заболевания костей и суставов включая, без наложения ограничений, ревматоидный артрит, серонегативные спондилоартропатии (включая анкилозирующий спондилит, псориатический артрит и болезнь Рейтера), болезнь Бехчета, синдром Шегрена, системный склероз, остеопороз, рак кости, метастазирование в кости, тромбоэмболическое нарушение (например, инфаркт миокарда, стенокардия, реокклюзия после ангиопластики, рестеноз после ангиопластики, реокклюзия после аортокоронарного шунтирования, рестеноз после аортокоронарного шунтирования, удар, транзиторная ишемия, окклюзионное нарушение периферических артерий, легочная эмболия, тромбоз глубоких вен), воспалительное заболевание таза, уретрит, солнечный ожогкожи, синусит, пневмонит, энцефалит, менингит, миокардит, нефрит, остеомиелит, миозит, гепатит, гастрит, энтерит, дерматит, гингивит, аппендицит, панкреатит, холецистит, агаммаглобулинемия, псориаз, аллергия, болезнь Крона, синдром раздраженной толстой кишки, язвенный колит, болезнь Шегрена, отторжение трансплантата ткани, сверхострое отторжение трансплантированных органов, астма, аллергический ринит, хроническое обструктивное заболевание легких (COPD), аутоиммунное плюригландулярное заболевание (также известное, как аутоиммунный плюригландулярный синдром), аутоиммунная алопеция, пернициозная анемия, гломерулонефрит, дерматомиозит, рассеянный склероз, склеродермия, васкулит, аутоиммунные гемолитические и тромбоцитопенические состояния, синдром Гудпасчера, атеросклероз, болезнь Аддисона, болезнь Паркинсона, болезнь Альцгеймера, диабет, септический шок, системная красная волчанка (SLE), ревматоидный артрит, псориатический артрит, ювенильный артрит, остеоартрит, хроническая идиопатическая тромбоцитопеническая пурпура, макроглобулинемия Вальденстрема, злокачественная миастения, тиреоидит Хашимото, атопический дерматит, дегенеративное заболевание сустава, витилиго, аутоиммунный гипопитуитаризм, синдром Гийена-Барре, болезнь Бехчета, склеродермия, грибовидный микоз, острые воспалительные ответы (такие как острый респираторный дистресс-синдром и ишемическое/реперфузионное поражение) и болезнь Грейвса.
[00223] В другом варианте осуществления настоящее изобретение относится к способу лечения или ослабления тяжести заболевания, включающему введение нуждающемуся в нем пациенту соединения формулы I и ингибитор PI3K, где заболевание выбрано из числа следующих: рак, нейродегенеративное нарушение, ангиогенное нарушение, вирусное заболевание, аутоиммунное заболевание, воспалительное нарушение, связанное с гормоном заболевание, патологические состояния, связанные с трансплантацией органа, иммунодефицитные состояния, деструктивное нарушение кости, пролиферативное нарушение, инфекционное заболевание, патологическое состояние, связанное с гибелью клеток, вызванная тромбином агрегация тромбоцитов, хронический миелолейкоз (CML), хронический лимфолейкоз (CLL), заболевание печени, патологические иммунные состояния, включающие активацию T-клеток, сердечно-сосудистое нарушение и нарушение CNS.
[00224] В другом варианте осуществления настоящее изобретение относится к способу лечения или ослабления тяжести заболевания, включающему введение нуждающемуся в нем пациенту соединения формулы I и ингибитор PI3K, где заболевание выбрано из числа следующих: доброкачественная или злокачественная опухоль, карцинома или сóлидная опухоль головного мозга, почек (например, почечноклеточная карцинома (RCC)), печени, надпочечника, мочевого пузыря, молочной железы, желудка, опухоли кишечника, яичников, толстой кишки, прямой кишки, предстательной железы, поджелудочной железы, легких, влагалища, эндометрия, шейки матки, яичек, мочеполового тракта, пищевода, гортани, кожи, кости или щитовидной железы, саркома, глиобластома, нейробластомы, множественная миелома или желудочно-кишечный рак, в особенности карцинома толстой кишки или колоректальная аденома или опухоль головы и шеи, гиперпролиферация эпидермиса, псориаз, гиперплазия предстательной железы, неоплазия, неоплазия эпителиального характера, аденома, аденокарцинома, кератоакантома, эпидермоидная карцинома, крупноклеточная карцинома, немелкоклеточная карцинома легких, лимфомы, (включая, например, неходжкинская лимфома (NHL) и ходжкинская лимфома (также называющаяся болезнью Ходжкина)), карцинома молочной железы, фолликулярная карцинома, недифференцированная карцинома, папиллярная карцинома, семинома, меланома или лейкоз, заболевания включают синдром Коудена, болезнь Лермитта-Дудоса и синдром Банаяна-Зонана или заболевания, в которых аберрантно активирован путь PI3K/PKB, астма любого типа или генеза включая наследственную (неаллергическую) астму и приобретенную (аллергическуюя) астму, слабую астму, астму средней тяжести, тяжелую астму, бронхиальную астму, астму напряжения, профессиональную астму и астму, вызванную бактериальной инфекцией, острое поражение легких (ALI), острый респираторный дистресс-синдром у взрослых (ARDS), хроническое обуструктивное легочное заболевание, заболевание дыхательных путей или легких (COPD, COAD или COLD), включая связанный с ними хронический бронхит или одышку, эмфизема, а также обострение гиперреактивности дыхательных путей после другого лекарственного средства, в частности, другого вдыхаемого лекарственного средства, бронхит любого типа или генеза, включая, но не ограничиваясь только ими, острый, арахиновый, катарральный, круппозный, хронический или гнойный туберкулезный бронхит, пневмокониоз (воспалительное, обычно профессиональное, заболевание легких, часто сопровождающееся обструкцией дыхательных путей, хроническое или острое и возникающее вследствие повторяющегося вдыхания пыли) любого типа или генеза, включая, например, алюминоз, антракоз, асбестоз, халикоз, птилоз, сидероз, силикоз, табакоз и биссиноз, синдром Леффлера, эозинофильная пневмония, заражение паразитами (в частности, многоклеточными) (включая тропическую эозинофилию), бронхолегочный аспергиллез, нодозный полиартериит (включая синдром Черджа-Штросса), эозинофильная гранулема и связанные с эозинофилом нарушения, влияющие на дыхательные пути, вызванные медикаментозной аллергией, псориаз, контактный дерматит, атопический дерматит, гнездная алопеция, полиморфная эритема, герпетиформный дерматит, склеродермия, витилиго, аллергический васкулит, крапивница, буллезный пемфигоид, красная волчанка, пузырчатка, приобретенный буллезный эпидермолиз, конъюнктивит, сухой кератоконъюнктивит и весенний конъюнктивит, заболевания, поражающие нос, включая аллергический ринит и воспалительное заболевание, в котором участвуют аутоиммунные реакции, или обладающее аутоиммунным компонентом или этиологией, включая аутоиммунные гематологические нарушения (например, гемолитическая анемия, апластическая анемия, истинная эритроцитарная анемия и идиопатическая тромбоцитопения), системная красная волчанка, ревматоидный артрит, полихондрия, склеродермия, гранулематоз Вегенера, дерматомиозит, хронический активный гепатит, злокачественная миастения, синдром Стивенса - Джонсона, идиопатическое спру, аутоиммунная воспалительная болезнь кишечника (например, язвенный колит и болезнь Крона), эндокринная офтальмопатия, болезнь Грейвса, саркоидоз, альвеолит, хронический гиперчувствительный пневмонит, рассеянный склероз, первичный билиарный цирроз, увеит (передний и задний), сухой кератоконъюнктивит и весенний кератоконъюнктивит, интерстициальный фиброз легких, псориатический артрит и гломерулонефрит (с нефротическим синдромом или без него, например, включая идиопатический нефротический синдром или нефропатию минимальных изменений), рестеноз, кардиомегалия, атеросклероз, инфаркт миокарда, ишемический удар и застойная сердечная недостаточность, болезнь Альцгеймера, болезнь Паркинсона, боковой амиотрофический склероз, болезнь Гентингтона и ишемия головного мозга и нейродегенеративное заболевание, вызванное травматическим поражением, глутаматная нейротоксичность и гипоксия.
[00225] Соединения и композиции, соответствующие способу, предлагаемому в настоящем изобретении, можно вводить в любом количестве и любым путем введения, эффективным для лечения или ослабления тяжести рака, аутоиммунного нарушения, пролиферативного нарушения, воспалительного нарушения, нейродегенеративного или неврологического нарушения, шизофрении, связанного с костями нарушения, заболевания печени или нарушения сердца. Точное необходимое количество меняется при переходе от субъекта к субъекту в зависимости от вида, возраста и общего состояния здоровья субъекта, тяжести инфекции, конкретного средства, режима его введения и т. п. Соединения, предлагаемые в настоящем изобретении, предпочтительно готовят в разовой дозированной форме для обеспечения легкости введения и равномерности дозировки. Выражение "разовая дозированная форма" при использовании в настоящем изобретении означает отдельную порцию средства, подходящую для пациента, подвергающегося лечению. Однако следует понимать, что полную суточную дозу соединений и композиций, предлагаемых в настоящем изобретении, определяет лечащий врач по результатам тщательной медицинской клинической оценки. Конкретная эффективная доза для любого конкретного пациента или организма зависит от различных факторов, включая нарушение, подвергающееся лечению, и тяжесть нарушения; активность конкретного использующегося соединения; конкретную использующуюся композицию; возраст, массу тела, общее состояние здоровья, пол и диету пациента; время введения, путь введения и скорость выведения конкретного использующегося соединения; длительность лечения; лекарственные средства, использующиеся в комбинации или вместе с конкретным используемым соединением, и аналогичные факторы, хорошо известные в медицине. Термин "пациент" при использовании в настоящем изобретении означает животное, предпочтительно млекопитающее и наиболее предпочтительно человека.
[00226] Фармацевтически приемлемые композиции, предлагаемые в настоящем изобретении, можно вводить людям и другим животным перорально, ректально, парентерально, интрацистернально, внутривагинально, внутрибрюшинно, местно (в виде порошков, мазей или капель), буккально, в виде перорального или назального спрея и т. п. в зависимости от тяжести инфекции, подвергающейся лечению. В некоторых вариантах осуществления соединения, предлагаемые в настоящем изобретении, можно вводить перорально или парентерально в дозах, равных от примерно 0,01 мг/кг до примерно 50 мг/кг и предпочтительно от примерно 1 мг/кг до примерно 25 мг/кг массы тела субъекту в сутки, один или большее количество раз в сутки, и обеспечивать желательный терапевтический эффект.
[00227] Жидкие дозированные формы для перорального введения включают, но не ограничиваются только ими, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активным соединениям жидкие дозированные формы могут содержать инертные разбавители, обычно использующиеся в данной области техники, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное, из зародышей, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и эфиры жирных кислот сорбитана и их смеси. Кроме инертных разбавителей пероральные композиции также могут включать вспомогательные вещества, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подсластители, вкусовые агенты и отдушки.
[00228] Препараты для инъекции, например, стерильные водные или масляные суспензии для инъекции можно готовить по известным в данной области техники методикам с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный препарат для инъекции также может представлять собой стерильный раствор для инъекции, суспензию или эмульсию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. В число приемлемых разбавителей и растворителей, которые можно использовать, входят вода, раствор Рингера U.S.P. и изотонический раствор хлорида натрия. Кроме того, стерильные, нелетучие масла обычно используют в качестве растворителя или суспендирующей среды. Для этой цели можно использовать любое мягкое нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, для приготовления форм для инъекции применимы жирные кислоты, такие как олеиновая кислота.
[00229] Препараты для инъекции можно стерилизовать, например, фильтрованием через удерживающий бактерии фильтр или путем включения стерилизующих агентов в форме стерильной твердой композиций, которую перед использованием можно растворить или диспергировать стерильной воде или другой стерильной среде для инъекции.
[00230] Для пролонгирования действия соединения, предлагаемого в настоящем изобретении, часто желательно замедлить всасывание соединения при подкожной или внутримышечной инъекции. Это можно обеспечить путем использования жидкой суспензии кристаллического или аморфного вещества, обладающего плохой растворимостью в воде. Тогда скорость всасывания соединения зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристалла и кристаллической формы. Альтернативно, замедленное всасывание парентерально введенной формы соединения обеспечивается путем растворения или суспендирования соединения в масляном разбавителе. Формы депо для инъекции готовят путем образования микрокапсулированных матриц соединения в биологически разлагающихся полимерах, такие как полилактид-полигликолид. В зависимости от отношения количества соединения к количеству полимера и природы конкретного использующегося полимера можно регулировать скорость высвобождения соединения. Примеры других биологически разлагающихся полимеров включают поли(ортоэфиры) и поли(ангидриды). Препараты депо для инъекции также готовят путем включения соединения в липосомы или микроэмульсии, которые совместимы с тканями организма.
[00231] Композициями для ректального или вагинального введения предпочтительно являются суппозитории, которые можно получить путем смешивания соединений, предлагаемых в настоящем изобретении, с подходящими нераздражающими инертными наполнителями или носителями, такими как масло какао, полиэтиленгликоль или воск для суппозиториев, которые являются твердыми при температуре окружающей среды, но жидкими при температуре тела, и поэтому плавятся в прямой кишке или полости влагалища и высвобождают активное соединение.
[00232] Твердые дозированные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах активное соединение смешано по меньшей мере с одним инертным фармацевтически приемлемым инертным наполнителем или носителем, таким как цитрат натрия или дикальцийфосфат и/или a) наполнителями или средствами, увеличивающими объем, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота, b) связующими, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и камедь акации, c) влагоудерживающими средствами, такими как глицерин, d) разрыхляющими агентами, такими как агар-агар, карбонат кальция, картофельный или маниоковый крахмал, альгиновая кислота, некоторые силикаты и карбонат натрия, e) замедляющими растворение агентами, такими как парафин, f) ускорителями всасывания, такими как четвертичные аммониевые соединения, g) смачивающими агентами, такими как, например, цетиловый спирт и глицеринмоностеарат, h) абсорбентами, такими как каолин и бентонитовая глина и i) смазывающими веществами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси. В случае капсул, таблеток и пилюль дозированная форма также может содержать буферные реагенты.
[00233] Твердые композиции аналогичного типа также можно использовать для наполнения капсул из мягкого и твердого желатин с использованием таких инертных наполнителей, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т. п. Твердые дозированные формы таблеток, драже, пилюль, пилюли и гранул можно приготовить с покрытиями или оболочками, такими как энтеросолюбильные покрытия и другие покрытия, хорошо известные в области приготовления фармацевтических препаратов. Они необязательно могут содержать замутняющие агенты и также могут представлять собой композицию, из которой высвобождается только активный ингредиент(ы) или предпочтительно в некоторой части кишечника, необязательно с задержкой. Примеры включающих составов, которые можно использовать, включают полимерные вещества и воска. Твердые композиции аналогичного типа также можно использовать для наполнения капсул из мягкого и твердого желатин с использованием таких инертных наполнителей, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и т. п.
[00234] Активные соединения также могут находиться в микрокапсулированной форме с одним или большим количеством инертных наполнителей, указанных выше. Твердые дозированные формы таблеток, драже, пилюль, пилюли и гранул можно приготовить с покрытиями или оболочками, такими как энтеросолюбильные покрытия и другие покрытия, хорошо известные в области приготовления фармацевтических препаратов. В таких твердых дозированных формах активное соединение можно смешать по меньшей мере с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие дозированные формы также могут содержать, что является обычной практикой, дополнительные вещества, не являющиеся инертными разбавителями, например, таблетирующие смазывающие вещества и другие таблетирующие средства, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль дозированные формы также могут содержать буферные реагенты. Они необязательно могут содержать замутняющие агенты и также могут представлять собой композицию, из которой высвобождается только активный ингредиент(ы) или предпочтительно в некоторой части кишечника, необязательно с задержкой. Примеры включающих составов, которые можно использовать, включают полимерные вещества и воска.
[00235] Дозированные формы для местного или чрескожного введения соединения, предлагаемого в настоящем изобретении, включают мази, пасты, кремы, примочки, гели, порошки, растворы, спреи, средства для ингаляции или пластыри. Активный компонент при стерильных условиях смешивают с фармацевтически приемлемым носителем и любыми необходимыми консервантами или буферами, которые могут потребоваться. Офтальмический препарат, ушные капли и глазные капли также считаются входящими в объем настоящего изобретения. Кроме того, настоящее изобретение включает применение чрескожных пластырей, которые обладают тем дополнительным преимуществом, что обеспечивают регулируемую доставку соединения в организм. Такие дозированные формы можно приготовить путем растворения или диспергирования соединения в надлежащей среде. Усилители всасывания также можно использовать для увеличения потока соединения через кожу. Скорость можно регулировать путем использования регулирующей скорость мембраны или путем диспергирования соединения в полимерной матрице или геле.
[00236] В одном варианте осуществления настоящее изобретение относится к способу ингибирования активности протеинкиназы в биологическом образце, включающему стадию взаимодействия указанного биологического образца с соединением, предлагаемым в настоящем изобретении, или с композицией, содержащей указанное соединение.
[00237] В другом варианте осуществления настоящее изобретение относится к способу ингибирования активности GCN2 или ее мутанта в биологическом образце, включающему стадию взаимодействия указанного биологического образца с соединением, предлагаемым в настоящем изобретении, или с композицией, содержащей указанное соединение.
[0100] Термин "биологический образец" при использовании в настоящем изобретении включает, без наложения ограничений, клеточные культуры или их экстракты; биоптический материал, полученный из млекопитающего или его экстрактов; и кровь, слюну, мочу, фекалии, сперму, слезы или другие жидкости организма или их экстракты.
[00238] Ингибирование активности протеинкиназы или протеинкиназы GCN2, или ее мутанта в биологическом образце применимо для множества целей, которые известны специалисту в данной области техники. Примеры таких целей включают, но не ограничиваются только ими, переливание крови, трансплантацию органа, хранение биологического образца и биологические исследования.
[00239] Другой вариант осуществления настоящего изобретения относится к способу ингибирования активности протеинкиназы у пациента, включающему стадию введения указанному пациенту соединения, предлагаемого в настоящем изобретении, или композиции, содержащей указанное соединение.
[00240] В другом варианте осуществления настоящее изобретение относится к способу ингибирования активности GCN2 или ее мутанта у пациента, включающему стадию введения указанному пациенту соединения, предлагаемого в настоящем изобретении, или композиции, содержащей указанное соединение. В других вариантах осуществления настоящее изобретение относится к способу лечения нарушения, опосредуемого GCN2, или ее мутантом у нуждающегося в нем пациента, включающему стадию введения указанному пациенту соединения, предлагаемого в настоящем изобретении, или содержащей его фармацевтически приемлемой композиции. Такие нарушения подробно описаны в настоящем изобретении.
[00241] В зависимости от конкретного патологического состояния или заболевания, подвергающегося лечению, дополнительные терапевтические средства, которые обычно вводят для лечения такого патологического состояния, могут также содержаться в композициях, предлагаемых в настоящем изобретении. При использовании в настоящем изобретении дополнительные терапевтические средства, которые обычно вводят для лечения конкретного заболевания или патологического состояния, известны, как "подходящие для заболевания или патологического состояния, подвергающегося лечению".
[00242] Соединение, предлагаемое в настоящем изобретении, также можно использовать для обеспечения преимущества в комбинации с другими антипролиферативными соединениями. Такие антипролиферативные соединения включают, но не ограничиваются только ими ингибиторы ароматазы; антиэстрогены; ингибиторы топоизомеразы I; ингибиторы топоизомеразы II; активные по отношению к микротрубочкам соединения; алкилирующие соединения; ингибиторы гистондезацетилазы; соединения, которые индуцируют процессы дифференциации клеток; ингибиторы циклооксигеназы; ингибиторы MMP; ингибиторы mTOR; противоопухолевые антиметаболиты; соединения платины; соединения, имеющие мишенью/уменьшающие активность протеин- или липидкиназы и дополнительные антиангиогенные соединения; соединения, которые имеют мишенью, уменьшают или ингибируют активность протеин- или липидфосфатазы; агонисты гонадорелина; анти-андрогены; ингибиторы метионинаминопептидазы; ингибиторы матричной металлопротеиназы; бисфосфонаты; модификаторы биологического ответа; антипролиферативные антитела; ингибиторы гепараназы; ингибиторы онкогенных изоформ Ras; ингибиторы теломеразы; ингибиторы протеасомы; соединения, применяющиеся для лечения злокачественных заболеваний крови; соединения, которые имеют мишенью, уменьшают или ингибируют активность Flt-3; ингибиторы Hsp90, такие как 17-AAG (17-аллиламиногелданамицин, NSC330507), 17-DMAG (17-диметиламиноэтиламино-17-деметокси-гелданамицин, NSC707545), IPI-504, CNF1010, CNF2024, CNF1010 фирмы Conforma Therapeutics; темозоломид (Темодал®); ингибиторы белка веретена деления кинезина, такие как SB715992 или SB743921 фирмы GlaxoSmithKline или пентамидин/хлорпромазин фирмы CombinatoRx; ингибиторы MEK, такие как ARRY142886 фирмы Array BioPharma, AZD6244 фирмы AstraZeneca, PD181461 фирмы Pfizer и лейковорин. Термин "ингибитор ароматазы" при использовании в настоящем изобретении относится к соединению, которое ингибирует продуцирование эстрогена, например, превращение субстратов андростендиона и тестостерона в эстрон и эстрадиол соответственно. Термин включает, но не ограничивается только ими, стероиды, предпочтительно атаместан, эксеместан и форместан и, в частности, нестероиды, предпочтительно аминоглутетимид, роглетимид, пироглютетимид, трилостан, тестолактон, кетоконазол, ворозол, фадрозол, анастрозол и летрозол. Эксеместан продается под торговым названием аромазин™. Форместан продается под торговым названием лентарон™. Фадрозол продается под торговым названием афема™. Анастрозол продается под торговым названием аримидекс™. Летрозол продается под торговыми названиями фемара™ или фемар™. Аминоглутетимид продается под торговым названием ориметен™. Комбинация, предлагаемая в настоящем изобретении, содержащая химиотерапевтическое средство, которое представляет собой ингибитор ароматазы, является особенно подходящей для лечения гормон-рецептор-положительных опухолей, таких как опухоли молочной железы.
[00243] Термин "антиэстроген" при использовании в настоящем изобретении относится к соединению, которое противодействует воздействию эстрогенов на уровне эстрогенного рецептора. Термин включает, но не ограничивается только ими тамоксифен, фулвестрант, ралоксифен и ралоксифен гидрохлорид. Тамоксифен продается под торговым названием нолвадекс™. Ралоксифен гидрохлорид продается под торговым названием эвиста™. Фулвестрант можно вводить под торговым названием фазлодекс™. Комбинация, предлагаемая в настоящем изобретении, содержащая химиотерапевтическое средство, которое представляет собой антиэстроген, является особенно подходящей для лечения эстроген-рецептор-положительных опухолей, таких как опухоли молочной железы.
[00244] Термин "антиандроген" при использовании в настоящем изобретении относится к любому веществу, которое способно ингибировать биологические воздействия адрогенных гормонов и включает, но не ограничивается только им, бикалутамид (касодекс™). Термин "агонист гонадорелина" при использовании в настоящем изобретении включает, но не ограничивается только ими абареликс, гозерелин и гозерелин ацетат. Гозерелин можно вводить под торговым названием золадекс™.
[00245] В некоторых вариантах осуществления одно или большее количество других терапевтических средств представляет собой ингибитор андрогенового рецептора. Утвержденные к применению ингибиторы андрогенового рецептора, применимые в настоящем изобретении, включают энзалутамид (кстанди®, Astellas/Medivation); утвержденные к применению ингибиторы синтеза андрогена включают абиратерон (зитига®, Centocor/Ortho); утвержденный к применению антагонист рецептора гонадотропин-рилизин гормона (GnRH) (дегараликс, фирмагон®, Ferring Pharmaceuticals).
[00246] В некоторых вариантах осуществления одно или большее количество других терапевтических средств представляют собой селективный модулятор эстрогенового рецептора (SERM), который препятствует синтезу или активности эстрогенов. Утвержденные к применению SERMs, применимые в настоящем изобретении, включают ралоксифен (эвиста®, Eli Lilly).
[00247] Термин "ингибитор топоизомеразы I" при использовании в настоящем изобретении включает, но не ограничивается только ими топотекан, гиматекан, иринотекан, камптотецин и его аналоги, 9-нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148. Иринотекан можно вводить, например, в форме, в которой он продается, например, под торговым названием камптосар™. Топотекан продается под торговым названием гикамптин™.
[00248] Термин "ингибитор топоизомеразы II" при использовании в настоящем изобретении включает, но не ограничивается только ими антрациклины, такие как доксорубицин (включая липосомный препарат, такой как каеликс™), даунорубицин, эпирубицин, идарубицин и неморубицин, антрахиноны митоксантрон и лосоксантрон и подофиллотоксины этопозид и тенипозид. Этопозид продается под торговым названием этопофос™. Тенипозид продается под торговым названием VM 26-Bristol. Доксорубицин продается под торговым названием акрибластин™ или адриамицин™. Эпирубицин продается под торговым названием фарморубицин™. Идарубицин продается под торговым названием заведос™. Митоксантрон продается под торговым названием новантрон.
[00249] Термин "активное по отношению к микротрубочкам средство" относится к стабилизирующим микротрубочки, дестабилизирующим микротрубочки соединениям и ингибиторам полимеризации микротубулина, включая, но не ограничиваясь только ими таксаны, такие как паклитаксел и доцетаксел; алкалоиды барвинка, такие как винбластин или винбластин сульфат, винкристин или винкристин сульфат и винорелбин; дискодермолиды; колхицин и эпотилоны и их производные. Паклитаксел продается под торговым названием таксол™. Доцетаксел продается под торговым названием таксотер™. Винбластин сульфат продается под торговым названием винбластин R.P™. Винкристин сульфат продается под торговым названием фармистин™.
[00250] Термин "алкилирующее средство" при использовании в настоящем изобретении включает, но не ограничивается только ими, циклофосфамид, ифосфамид, мелфалан или нитрозомочевина (BCNU или глиадел). Циклофосфамид продается под торговым названием циклостин™. Ифосфамид продается под торговым названием голоксан™.
[00251] Термин "ингибиторы гистондезацетилазы" или "ингибиторы HDAC" относится к соединениям, которые ингибируют гистондезацетилазу и которые обладают антипролиферативной активностью. Они включает, но не ограничивается только ими, субероиланилид гидроксамовой кислоты (SAHA).
[00252] Термин "противоопухолевый антиметаболит" включает, но не ограничивается только ими, 5-фторурацил или 5-FU, капецитабин, гемцитабин, деметилирующие DNA соединения, такие как 5-азацитидин и децитабин, метотрексат и эдатрексат и антагонисты фолиевой кислоты, такие как пеметрексед. Капецитабин продается под торговым названием кселода™. Гемцитабин продается под торговым названием гемзар™.
[00253] Термин "соединение платины" при использовании в настоящем изобретении включает, но не ограничивается только ими, карбоплатин, цисплатин, цисплатинум и оксалиплатин. Карбоплатин можно вводить, например, в форме, в которой он продается, например, под торговым названием карбоплат™. Оксалиплатин можно вводить, например, в форме, в которой он продается, например, под торговым названием элоксантин™.
[00254] Термин "соединения, имеющие мишенью/уменьшающие активность протеин- или липидкиназы; или активность протеин- или липидфосфатазы; или другие антиангиогенные соединения" при использовании в настоящем изобретении включает, но не ограничивается только ими, ингибиторы протеинтирозинкиназы и/или серин- и/или треонинкиназы или ингибиторы липидкиназы, такие как a) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецепторов тромбоцитарного фактора роста (PDGFR), такие как соединения, которые имеют мишенью, уменьшают или ингибируют активность PDGFR, предпочтительно соединения, которые ингибируют рецептор PDGF, такие как производное N-фенил-2-пиримидинамина, такое как иматиниб, SU101, SU6668 и GFB-111; b) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецепторов фактора роста фибробластов (FGFR); c) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецептора инсулиноподобного фактора роста I (IGF-IR), такие как соединения, которые имеют мишенью, уменьшают или ингибируют активность IGF-IR, предпочтительно соединения, которые ингибируют киназную активность рецептора IGF-I или антител, которые имеют мишенью внеклеточный домен рецептора IGF-I или его факторы роста; d) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецептора Trk семейства тирозинкиназ или ингибиторы эфрина B4; e) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецептора AxI семейства тирозинкиназ; f) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецептора Ret тирозинкиназы; g) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецептора Kit/SCFR тирозинкиназы, такие как иматиниб; h) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецептора C-kit тирозинкиназ, которые являются частью семейства PDGFR, такие как соединения, которые имеют мишенью, уменьшают или ингибируют активность рецептора c-Kit семейства тирозинкиназ, предпочтительно соединения, которые ингибируют рецептор c-Kit, такие как иматиниб; i) соединения, имеющие мишенью, уменьшающие или ингибирующие активность представителей семейства c-Abl, их продуктов слиния с генами (например, киназы BCR-Abl) и мутантов, такие как соединения, которые имеют мишенью, уменьшают или ингибируют активность представителей семейства c-Abl и их продуктов слиния с генами, такие как производное N-фенил-2-пиримидинамина, такие как иматиниб или нилотиниб (AMN107); PD180970; AG957; NSC 680410; PD173955 фирмы ParkeDavis; или дасатиниб (BMS-354825); j) соединения, имеющие мишенью, уменьшающие или ингибирующие активность представителей семейства протеинкиназы C (PKC) и Raf серин/треонинкиназ, представителей семейства MEK, SRC, JAK/pan-JAK, FAK, PDK1, PKB/Akt, Ras/MAPK, PI3K, SYK, TYK2, BTK и TEC, и/или представителей семейства циклин-зависимых киназ (CDK), включая производные стауроспорина, такие как мидостаурин; примеры дополнительных соединений включают UCN-01, сафингол, BAY 43-9006, бриостатин 1, перифозин; илмофозин; RO 318220 и RO 320432; GO 6976; lsis 3521; LY333531/LY379196; изохинолин соединения; FTIs; PD184352 или QAN697 (ингибитор P13K) или AT7519 (ингибитор CDK); k) соединения, имеющие мишенью, уменьшающие или ингибирующие активность ингибиторов протеинтирозинкиназы, такие как соединения, которые имеют мишенью, уменьшают или ингибируют активность ингибиторов протеинтирозинкиназы, включающие иматинибмезилат (глеевек™) или тирфостин, такой как тирфостин A23/RG-50810; AG 99; тирфостин AG 213; тирфостин AG 1748; тирфостин AG 490; тирфостин B44; тирфостин B44 (+) энантиомер; тирфостин AG 555; AG 494; тирфостин AG 556, AG957 и адафостин (адамантиловый эфир 4-{[(2,5- дигидроксифенил)метил]амино}-бензойной кислоты; NSC 680410, адафостин); l) соединения, имеющие мишенью, уменьшающие или ингибирующие активность семейства рецепторов эпидермального фактора роста тирозинкиназ (EGFR1 ErbB2, ErbB3, ErbB4 в виде гомо- или гетеродимеров) и их мутанты, такие как соединения, которые имеют мишенью, уменьшают или ингибируют активность семейства рецепторов эпидермального фактора роста, предпочтительно представляют собой соединения, белки или антитела, которые ингибируют представителей семейства EGF тирозинкиназ, таких как рецептор EGF, ErbB2, ErbB3 и ErbB4 или связываются с EGF или родственными EGF лигандами, CP 358774, ZD 1839, ZM 105180; трастузумаб (герцептин™), цетуксимаб (эрбутукс™), иресса, тарцева, OSI-774, Cl-1033, EKB-569, GW-2016, E1,1, E2,4, E2,5, E6,2, E6,4, E2,11, E6,3 или E7,6,3 и производные 7H-пирроло-[2,3-d]пиримидина; m) соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецептора c-Мет, такие как соединения, которые имеют мишенью, уменьшают или ингибируют активность c-Мет, предпочтительно соединения, которые ингибируют киназную активность рецептора c-Мет, или антитела, которые имеют мишенью внеклеточный домен рецептора c-Мет или связываются с HGF, n) соединения, имеющие мишенью, уменьшающие или ингибирующие киназную активность одного или большего количества JAK представителей семейства (JAK1/JAK2/JAK3/TYK2 и/или pan-JAK), включая, но не ограничиваясь только ими, PRT-062070, SB-1578, барицитиниб, пакритиниб, момелотиниб, VX-509, AZD-1480, TG-101348, тофацитиниб и руксолитиниб; o) соединения, имеющие мишенью, уменьшающие или ингибирующие киназную активность киназы PI3 (PI3K) включая, но не ограничиваясь только ими, ATU-027, SF-1126, DS-7423, PBI-05204, GSK-2126458, ZSTK-474, бупарлисиб, пиктрелисиб, PF-4691502, BYL-719, дактолизиб, XL-147, XL-765 и иделалисиб; и; и q) соединения, имеющие мишенью, уменьшающие или ингибирующие сигнальные эфекты белка hedgehog (Hh) или пути сглаженного рецептора (SMO), включая, но не ограничиваясь только ими, циклопамин, висмодегиб, итраконазол, эрисмодегиб и IPI-926 (саридгегиб).
[00255] Термин "ингибитор PI3K" при использовании в настоящем изобретении включает, но не ограничивается только ими соединения, обладающие ингибирующей активностью по отношению к одному или большему количеству ферментов семейства фосфатидилинозит-3-киназы, включая, но не ограничиваясь только ими PI3Kα, PI3Kγ, PI3Kδ, PI3Kβ, PI3K-C2α, PI3K-C2β, PI3K-C2γ, Vps34, p110-α, p110-β, p110-γ, p110-δ, p85-α, p85-β, p55-γ, p150, p101 и p87. Примеры ингибиторов PI3K, применимых в настоящем изобретении, включают, но не ограничиваются только ими, ATU-027, SF-1126, DS-7423, PBI-05204, GSK-2126458, ZSTK-474, бупарлисиб, пиктрелисиб, PF-4691502, BYL-719, дактолизиб, XL-147, XL-765 и иделалисиб.
[00256] Термин "ингибитор BTK" при использовании в настоящем изобретении включает, но не ограничивается только ими соединения, обладающие ингибирующей активностью по отношению к тирозинкиназе Брутона (BTK), включая, но не ограничиваясь только ими AVL-292 и ибрутиниб.
[00257] Термин "ингибитор SYK" при использовании в настоящем изобретении включает, но не ограничивается только ими соединения, обладающие ингибирующей активностью по отношению к тирозинкиназе селезенки (SYK), включая, но не ограничиваясь только ими, PRT-062070, R-343, R-333, эксцеллар, PRT-062607 и фостаматиниб.
[00258] Дополнительные примеры ингибирующих BTK соединений и патологических состояний, которые можно лечить такими соединениями в комбинации с соединениями, предлагаемыми в настоящем изобретении, приведены в WO2008039218 и WO2011090760, которые во всей своей полноте включены в настоящее изобретение в качестве ссылки.
[00259] Дополнительные примеры ингибирующих SYK соединений и патологических состояний, которые можно лечить такими соединениями в комбинации с соединениями, предлагаемыми в настоящем изобретении, приведены в WO2003063794, WO2005007623 и WO2006078846, которые во всей своей полноте включены в настоящее изобретение в качестве ссылки.
[00260] Дополнительные примеры игнибирующих PI3Ky соединений и патологических состояний, которые лечат такими соединениями в комбинации с соединениями, предлагаемыми в настоящем изобретении, приведены в WO2004019973, WO2004089925, WO2007016176, US8138347, WO2002088112, WO2007084786, WO2007129161, WO2006122806, WO2005113554 и WO2007044729, которые во всей своей полноте включены в настоящее изобретение в качестве ссылки.
[00261] Дополнительные примеры ингибирующих JAK соединений и патологических состояний, которые лечат такими соединениями в комбинации с соединениями, предлагаемыми в настоящем изобретении, приведены в WO2009114512, WO2008109943, WO2007053452, WO2000142246 и WO2007070514, которые во всей своей полноте включены в настоящее изобретение в качестве ссылки.
[00262] Другие антиангиогенные соединения включают соединения, обладающие другим механизмом активности, например, не связанные с ингибированием протеин- или липидкиназы, например, талидомид (Таломид™) и TNP-470.
[00263] Примеры ингибиторов протеасомы, применимых в комбинации с соединениями, предлагаемыми в настоящем изобретении, включают, но не ограничиваются только ими бортезомиб, дисульфирам, эпигаллокатехин-3-галлат (EGCG), салинспорамид A, карфилзомиб, ONX-0912, CEP-18770 и MLN9708.
[00264] Соединениями, которые имеют мишенью, уменьшают или ингибируют активность протеин- или липидфосфатазы являются, например, ингибиторы фосфатазы 1, фосфатазы 2A или CDC25, такие как окадаевая кислота или ее производное.
[00265] Соединения, которые индуцируют процессы дифференциации клеток включают, но не ограничиваются только ими, ретиноевую кислоту, α-, γ- или δ-токоферол или α-, γ- или δ-токотриенол.
[00266] Термин ингибитор циклооксигеназы при использовании в настоящем изобретении включает, но не ограничивается только ими, ингибиторы Cox-2, 5-алкилзамещенную 2-ариламинофенилуксусную кислоту и производные, такие как целекоксиб (целебрекс™), рофекоксиб (виокс™), эторикоксиб, валдекоксиб или 5-алкил-2- ариламинофенилуксусную кислоту, такую как 5-метил-2-(2'-хлор-6'-фторанилино)фенилуксусную кислоту, лумиракоксиб.
[00267] Термин "бисфосфонаты" при использовании в настоящем изобретении включает, но не ограничивается только ими, этридоновую, клодроновую, тилудроновую, памидроновую, алендроновую, ибандроновую, риседроновую и золендроновую кислоту. Этридроновая кислота продается под торговым названием дидронел™. Клодроновая кислота продается под торговым названием бонефос™. Тилудроновая кислота продается под торговым названием скелид™. Памидроновая кислота продается под торговым названием аредиа™. Алендроновая кислота продается под торговым названием фосамакс™. Ибандроновая кислота продается под торговым названием бондранат™. Риседроновая кислота продается под торговым названием актонел™. Золендроновая кислота продается под торговым названием зомета™. Термин "ингибиторы mTOR" относится к соединениям, которые ингибируют мишень воздействия рапамицина у млекопитающих (mTOR) и которые обладают антипролиферативной активностью, таким как сиролимус (рапамун®), эверолимус (цертикан™), CCI-779 и ABT578.
[00268] Термин "ингибитор гепараназы" при использовании в настоящем изобретении означает соединения, которые имеют мишенью, уменьшают или ингибируют разложение гепаринсульфата. Термин включает, но не ограничивается только ими, PI-88. Термин "модификатор биологического ответа" при использовании в настоящем изобретении означает лимфокин или интерфероны.
[00269] Термин "ингибитор онкогенных изоформ Ras", такой как H-Ras, K-Ras или N-Ras при использовании в настоящем изобретении означает соединения, которые имеют мишенью, уменьшают или ингибируют онкогенную активность Ras; например, "ингибитор фарнезилтрансферазы", такой как L-744832, DK8G557 или R115777 (зарнестра™). Термин "ингибитор теломеразы" при использовании в настоящем изобретении означает соединения, которые имеют мишенью, уменьшают или ингибируют активность теломеразы. Соединениями, которые имеют мишенью, уменьшают или ингибируют активность теломеразы, предпочтительно представляют собой соединения, которые ингибируют рецептор теломеразы, такие как теломестатин.
[00270] Термин "ингибитор метионинаминопептидазы" при использовании в настоящем изобретении означает соединения, которые имеют мишенью, уменьшают или ингибируют активность метионинаминопертидазы. Соединения, которые имеют мишенью, уменьшают или ингибируют активность метионинаминопертидазы включают, но не ограничиваются только ими, бенгамид или его производное.
[00271] Термин "ингибитор протеасомы" при использовании в настоящем изобретении означает соединения, которые имеют мишенью, уменьшают или ингибируют активность протеасомы. Соединения, которые имеют мишенью, уменьшают или ингибируют активность протеасомы включают, но не ограничиваются только ими, бортезомиб (велкаде™) и MLN 341.
[00272] Термин "ингибитор матричной металлопротеиназы" или (ингибитор "MMP") при использовании в настоящем изобретении включает, но не ограничивается только ими, пептидомиметические и непептидомиметические ингибиторы коллагена, производные тетрациклина, например, пептидомиметический гидроксаматный ингибитор батимастат и его перорально биодоступный аналог маримастат (BB-2516), приномастат (AG3340), метастат (NSC 683551) BMS-279251, BAY 12-9566, TAA211, MMI270B или AAJ996.
[00273] Термин "соединения, применяющиеся для лечения злокачественных заболеваний крови" при использовании в настоящем изобретении включает, но не ограничивается только ими, ингибиторы FMS-подобной тирозинкиназы, которые представляют собой соединения, имеющие мишенью, уменьшающие или ингибирующие активность рецепторов FMS-подобной тирозинкиназы (Flt-3R); интерферон, 1-β-D-арабинофуранзилцитозин (ara-c) и бисульфан; и ингибиторы ALK, которые представляют собой соединения, которые имеют мишенью, уменьшают или ингибируют киназу анапластической лимфомы.
[00274] Соединения, которые имеют мишенью, уменьшают или ингибируют активность рецепторов FMS-подобной тирозинкиназы (Flt-3R), предпочтительно представляют собой соединения, белки или антитела, которые ингибируют представителей семейства Flt-3R рецепторных киназ, такие как PKC412, мидостаурин, производное стауроспорина, SU11248 и MLN518.
[00275] Термин "ингибиторы HSP90" при использовании в настоящем изобретении включает, но не ограничивается только ими, соединения, имеющие мишенью, уменьшающие или ингибирующие собственную ATPase-ную активность HSP90; разрушающие, имеющие мишень, уменьшающие или ингибирующие клиентные белки HSP90 по убиквитин-протеосомному пути. Соединения, имеющие мишенью, уменьшающие или ингибирующие собственную ATPase-ную активность HSP90, предпочтительно представляют собой соединения, белки или антитела, которые ингибируют ATPase-ную активность HSP90, такие как 17-аллиламино-17-деметоксигелданамицин (17AAG), производное гелданамицина; другие родственные гелданамицину соединения; радицикол и ингибиторы HDAC.
[00276] Термин "антипролиферативные антитела" при использовании в настоящем изобретении включает, но не ограничивается только ими, трастузумаб (герцептин™), трастузумаб-DM1, эрбутукс, бевацизумаб (авастин™), ритуксимаб (ритуксан®), PRO64553 (анти-CD40) и антитела 2C4. Под антителами понимаются, например, интактные моноклональные антитела, поликлональные антитела, поливалентные антитела, сформированные по меньшей мере из двух интактных антител, и фрагменты антител, если они обладают необходимой биологической активностью.
[00276] Для лечения острого миелолейкоза (AML), соединения, предлагаемые в настоящем изобретении, можно использовать в комбинации со стандартными противолейкозными терапевтическими средствами, предпочтительно в комбинации с терапевтическими средствами used для лечения AML. В частности, соединения, предлагаемые в настоящем изобретении, можно вводить в комбинации, например, с ингибиторами фарнезилтрансферазы и/или другими лекарственными средствами, применяющимися для для лечения AML, такими как даунорубицин, адриамицин, Ara-C, VP-16, тенипозид, митоксантрон, идарубицин, карбоплатин и PKC412.
[00278] Другие противолейкозные соединения включают, например, Ara-C, аналог пиримидина, который представляет собой 2'-альфа-гидроксирибозное (арабинозид) производное дезоксицитидина. Также включен пуриновый аналог гипоксантина, 6-меркаптопурина (6-MP) и флударабинфосфата. Соединения, которые имеют мишенью, уменьшают или ингибируют активность ингибиторов гистондезацетилазы (HDAC), такие как бутират натрия и субероиланилид гидроксамовой кислоты (SAHA), ингибируют активность ферментов, известных, как гистондезацетилазы. Конкретные ингибиторы HDAC включают MS275, SAHA, FK228 (ранее FR901228), трихостатин A и соединения, раскрытые в US 6552065, включая, но не ограничиваясь только ими, N-гидрокси-3-[4-[[[2-(2-метил-1H-индол-3-ил)-этил]- амино]метил]фенил]-2E-2-пропенамид или его фармацевтически приемлемую соль и N-гидрокси-3-[4-[(2-гидроксиэтил){2-(1H-индол-3-ил)этил]-амино]метил]фенил]-2E-2- пропенамид или его фармацевтически приемлемую соль, предпочтительно лактат. Антагонисты соматостатинового рецептора при использовании в настоящем изобретении означают соединения, которые имеют мишенью, обрабатывают или ингибируют соматостатиновый рецептор, такие как октреотид и SOM230. Методики повреждения опухолевых клеток означют такие метдики, как исполльзующие ионизирующее излучение. Термин "ионизирующее излучение", указанное выше и ниже в настоящем изобретении означает ионизирующее излучение, которое проявляется в виде электромагнитного излучения (такого как рентгеновское излучение и гамма-излучение) или частиц (таких как альфа- и бета-частицы). Ионизирующее излучение используется, ное на ограничивается только ими, в лучевой терапии и известно в данной области техники. См. Hellman, Principles of Radiation Therapy, Cancer, in Principles and Practice of Oncology, Devita et al., Eds., 4th Edition, Vol. 1, pp. 248-275 (1993).
[00279] Также включены EDG связующие и ингибиторы рибонуклеотидредуктазы. Термин "EDG связующие" при использовании в настоящем изобретении означает класс иммуносупрессантов, которые модулируют рециркуляцию лимфоцитов, такие как FTY720. Термин "ингибиторы рибонуклеотидредуктазы" означает аналоги пиримидинового или пуринового нуклеозида, включая, но не ограничиваясь только ими, флударабин и/или цитозин арабинозид (ara-C), 6-тиогуанин, 5-фторурацил, кладрибин, 6-меркаптопурин (предпочтительно в комбинации с ara-C по отношению к ALL) и/или пентостатин. Ингибиторами рибонуклеотидредуктазы предпочтительно являются гидроксимочевина или производные 2-гидрокси-1H-изоиндол-1,3-диона.
[00280] Также включены в частности, соединения, белки или моноклональные антитела к VEGF, такие как 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин или его фармацевтически приемлемую соль, 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин сукцинат; ангиостатин™; эндостатин™; амиды антраниловых кислот; ZD4190; ZD6474; SU5416; SU6668; бевацизумаб; или антитела к VEGF или антитела к рецептору VEGF, такие как rhuMAb и RHUFab, аптамер VEGF, такой как макугон; ингибиторы FLT-4, ингибиторы FLT-3, VEGFR-2 IgGI антитела, ангиозим (RPI 4610) и бевацизумаб (авастин™).
[00281] Фотодинамическая терапия при использовании в настоящем изобретении означает терапию, в которой используются некоторые химикаты, известные, как фотосенсибилизирующие соединения для лечения или предупреждения раковых заболеваний. Примеры фотодинамической терапии включают лечение такими соединениями, как визудин™ и порфимер натрия.
[00282] Ангиостатические стероиды при использовании в настоящем изобретении означает соединения, которые блокируют или ингибируют ангиогенез, такие как, например, анекортав, триамцинолон, гидрокортизон, 11-α-эпигидрокортизол, кортексолон, 17α-гидроксипрогестерон, кортикостерон, дезоксикортикостерон, тестостерон, эстрон и дексаметазон.
[00283] Имплантаты, содержащие кортикостероиды, представляют собой соединения, такие как флуоцинолон и дексаметазон.
[00283] Другие химиотерапевтические соединения включают, но не ограничиваются только ими, растительные алкалоиды, гормональные соединения и антагонисты; модификаторы биологического ответа, предпочтительно лимфокины или интерфероны; антисмысловые олигонуклеотиды или производные олигонуклеотида; shRNA или siRNA; или разные соединения или соединения с другим или неизвестным механизмом действия.
[00285] Соединения, предлагаемые в настоящем изобретении, также применимы в качестве совместно использующихся терапевтических соединений для применения в комбинации с другими лекарственными веществами, такими как противовоспалительные, бронхорасширяющие или антигистаминные лекарственные вещества, в особенности для лечения обструктивных или воспалительных заболеваний дыхательных путей, таких как отмеченные выше в настоящем изобретении, например, в качестве усилителей терапевтической активности таких лекарственных средств или в качестве средств уменьшения необходимых доз или ослабления возможных побочных эффектов таких лекарственных средств. Соединение, предлагаемое в настоящем изобретении, можно смешать с другим лекарственным веществом в фиксированной фармацевтической композиции или его можно вводить отдельно, до, одновременно или после другого лекарственного вещества. Соответственно, настоящее изобретение включает комбинацию соединения, предлагаемого в настоящем изобретении, описанного выше в настоящем изобретении, с противовоспалительным, бронхорасширяющим, антигистаминным или противокашлевым лекарственным веществом, указанное соединение, предлагаемое в настоящем изобретении, и указанные лекарственные вещества находятся в одной или разных фармацевтических композициях.
[00286] Подходящие противовоспалительные лекарственные средства включают стероиды, в частности, глюкокортикостероиды, такие как будесонид, бекламетазон дипропионат, флутиказон пропионат, циклезонид или мометазон фуроат; антагонисты нестероидного глюкокортикоидного рецептора; антагонисты LTB4, такие как LY293111, CGS025019C, CP-195543, SC-53228, BIIL 284, ONO 4057, SB 209247; антагонисты LTD4, такие как монтелукаст и зафирлукаст; ингибиторы PDE4, такие как циломиласт (арифло® GlaxoSmithKline), рофлумиласт (Byk Gulden),V-11294A (Napp), BAY19-8004 (Bayer), SCH-351591 (Schering- Plough), арофиллин (Almirall Prodesfarma), PD189659/PD168787 (Parke-Davis), AWD-12- 281 (Asta Medica), CDC-801 (Celgene), SeICID(TM) CC-10004 (Celgene), VM554/UM565 (Vernalis), T-440 (Tanabe), KW-4490 (Kyowa Hakko Kogyo); агонисты A2a; антагонисты A2b; и агонисты бета-2 адренорецептора, такие как албутерол (сальбутамол), метапротеренол, тербуталин, салметерол фенотерол, прокатерол и предпочтительно, формотерол и его фармацевтически приемлемые соли. Подходящие бронхорасширяющие лекарственные средства включают антихолинергические или атимускариновые соединения, в частности, ипратропийбромид, окситропийбромид, соли тиотропия и CHF 4226 (Chiesi) и гликопирролат.
[00287] Подходящие антигистаминные лекарственные вещества включают цетиризингидрохлорид, ацетаминофен, клемастинфумарат, прометазин, лоратидин, деслоратидин, дифенгидрамин и фексофенадингидрохлорид, активастин, астемизол, азеластин, эбастин, эпинастин, мизоластин и тефенадин.
[00288] Другими применимыми комбинациями соединений, предлагаемых в настоящем изобретении, с противовоспалительными лекарственными средствами являются комбинации с антагонистами хемокиновых рецепторов, например, CCR-1, CCR-2, CCR-3, CCR-4, CCR-5, CCR-6, CCR-7, CCR-8, CCR-9 и CCR10, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, в особенности антагонисты CCR-5, такие как антагонисты фирмы Schering-Plough SC-351125, SCH- 55700 и SCH-D и антагонисты фирмы Takeda, такие как N-[[4-[[[6,7-дигидро-2-(4-метилфенил)-5H-бензоциклогептен-8-ил]карбонил]амино]фенил]-метил]тетрагидро-N, N-диметил-2H-пиран-4-аминийхлорид (TAK-770).
[00289] В некоторых вариантах осуществления одно или большее количество других терапевтических средств представляют собой ингибитор поли(ADP-рибозо)полимеразы (PARP). В некоторых вариантах осуществления ингибитор PARP выбран из группы, включающей олапариб (линпарза®, AstraZeneca); рукапариб (рубрака®, Clovis Oncology); нирапариб (зеджула®, Tesaro); талазопариб (MDV3800/BMN 673/LT00673, Medivation/Pfizer/Biomarin); велипариб (ABT-888, AbbVie); и BGB-290 (BeiGene, Inc.).
[00290] Термин "ингибитор Bcl-2" при использовании в настоящем изобретении включает, но не ограничивается только ими соединения, обладающие ингибирующей активностью по отношению к белку 2 B-клеточной лимфомы (Bcl-2), включая, но не ограничиваясь только ими, ABT-199, ABT-731, ABT-737, апогоссипол, ингибиторы Ascenta’s pan-Bcl-2, куркумин (и его аналоги), двойные ингибиторы Bcl-2/Bcl-xL (Infinity Pharmaceuticals/Novartis Pharmaceuticals), генасенсе (G3139), HA14-1 (и его аналоги; см. WO2008118802), навитоклакс (и его аналоги, см. US7390799), NH-1 (Shenayng Pharmaceutical University), обатоклакс (и его аналоги, см. WO2004106328), S-001 (Gloria Pharmaceuticals), соединения серии TW (Univ. of Michigan) и венетоклакс. В некоторых вариантах осуществления ингибитор Bcl-2 представляет собой терапевтическую малую молекулу. В некоторых вариантах осуществления ингибитор Bcl-2 представляет собой пептидомиметик.
[00291] В некоторых вариантах осуществления одно или большее количество других терапевтических средств представляют собой ингибитор антиапоптических белков, такой как BCL-2. Утвержденные к применению антиапоптические средства, которые можно использовать в настоящем изобретении, включают венетоклакс (венклекста®, AbbVie/Genentech); и блинатумомаб (блинцито®, Amgen). Другие терапевтические средства, имеющие мишенью апоптические белки, которые прошли клинические исследования и можно использовать в настоящем изобретении, включают навитоклакс (ABT-263, Abbott), ингибитор BCL-2 (NCT02079740).
[00292] Структура активных средств, у которых имеются кодовые номера, родовые или торговые названия, приведена в последнем издании стандартного справочника "The Merck Index" и в базах данных, например, Patents International, (например, IMS World Publications).
[00293] Соединение, предлагаемое в настоящем изобретении, также можно использовать в сочетании с известными терапевтическими процедурами, например, введением гормонов или облучением. В некоторых вариантах осуществления предлагаемое соединение используют в качестве радиосенсибилизатора, в особенности для лечения опухолей, которые обладают низкой чувствительностью к радиотерапии.
[00294] Соединение, предлагаемое в настоящем изобретении, можно вводить по отдельности или в комбинации с одним или большим количеством других терапевтических соединений, возможное комбинированное терапевтическое средство имеет вид фиксированных комбинаций или введение соединения, предлагаемого в настоящем изобретении, и одного или большего количества других терапевтических соединений поочередно или независимо одно от другого, или объединенного введения фиксированных комбинаций и одного или большего количества других терапевтических соединений. Соединение, предлагаемое в настоящем изобретении, можно кроме этого или в дополнение вводить специально для противоопухолевой терапии в комбинации с химиотерапией, радиотерапией, иммунотерапией, фототерапией, хирургическим вмешательством или их комбинацией. Длительная терапия также возможна в качестве вспомогательной терапии в контексте других стратегий лечения, как описано выше. Другие возможные пути лечения представляют собой терапию для поддержания статуса пациента после регрессии опухоли или даже химиопревентивную терапию, например, у пациентов в группе риска.
[00295] Эти дополнительные средства можно вводить отдельно из композиции, содержащей соединение, предлагаемое в настоящем изобретении, в качестве части многодозового режима. Альтернативно, эти средства могут быть частью одной дозированной формы, смешанной с соединением, предлагаемым в настоящем изобретении, в единой композиции. Если их вводят в качестве части многодозового режима, эти два активных средства можно введены одновременно, последовательно или с промежутком между ними, обычно равным не более 5 ч.
[00296] При использовании в настоящем изобретении термин "комбинированное", "объединенное" и родственные термины означают одновременное или последовательное введение терапевтических средств, предлагаемых в настоящем изобретении. Например, соединение, предлагаемое в настоящем изобретении, можно вводить с другим терапевтическим средством одновременно или последовательно в отдельны разовых дозированных формах или вместе в одной разовой дозированной форме. Соответственно, настоящее изобретение относится к одной разовой дозированной форме, содержащей соединение, предлагаемое в настоящем изобретении, дополнительное терапевтическое средство и фармацевтически приемлемый носитель, вспомогательное вещество или разбавитель.
[00297] Количество соединения, предлагаемого в настоящем изобретении, и дополнительного терапевтического средства (в этих композициях, которые содержат дополнительное терапевтическое средство, описанное выше), которое можно объединить с материалами носителя с получением одной дозированной формы, меняется в зависимости от реципиента, подвергающегося лечению, и конкретного режима введения. Композиции, предлагаемые в настоящем изобретении, предпочтительно следует готовить, чтобы можно было вводить дозу соединения, предлагаемого в настоящем изобретении, равную 0,01-100 мг/кг массы тела/сутки.
[00298] В таких композициях, которые содержат дополнительное терапевтическое средство, это дополнительное терапевтическое средство и соединение, предлагаемое в настоящем изобретении, могут действовать синергетически. Поэтому количество дополнительного терапевтического средства в таких композициях будет меньше, чем требуется для монотерапии с использованием только этого терапевтического средства. В таких композициях можно вводить дозу дополнительного терапевтического средства, равную 0,01-1,000 мкг/кг массы тела/сутки.
[00299] Количество дополнительного терапевтического средства, содержащегося в композициях, предлагаемых в настоящем изобретении, должно быть не больше, чем количество, которое обычно вводят в композиции, содержащей это терапевтическое средство в качестве единственного активного средства. Предпочтительное количество дополнительного терапевтического средства в раскрытых в настоящем изобретении композициях находится в диапазоне примерно от 50% до 100% от количества, обычно содержащегося в композиции, содержащей это средство в качестве единственного терапевтически активным средства.
[00300] Соединения, предлагаемые в настоящем изобретении, или содержащие их фармацевтические композиции также можно включать в композиции для нанесения на имплантируемое медицинское устройство, такое как протез, искусственный клапан, сосудистые трансплантаты, стенты и катетеры. Например, сосудистые стенты использовали для преодоления рестеноза (повторное сужение стенки сосуда после поражения). Однако у пациентов, использующих стенты или другие имплантируемые устройства имеется риск образования тромба или активации тромбоцитов. Эти нежелательные эффекты можно предупредить или ослабить путем предварительного нанесения на устройство фармацевтически приемлемой композиции, содержащей ингибитор киназы. Имплантируемые устройства с покрытием из соединения, предлагаемого в настоящем изобретении, являются другим вариантом осуществления настоящего изобретения.
Типичные иммуноонкологические средства
[00301] В некоторых вариантах осуществления одно или большее количество других терапевтических средств представляют собой иммуноонкологическое средство. При использовании в настоящем изобретении термин "иммуноонкологическое средство" означает средство, которое эффективно для усиления, стимулирования и/или повышающего регулирования иммунных ответов у субъекта. В некоторых вариантах осуществления введение иммуноонкологического средства с соединением, предлагаемым в настоящем изобретении, обладает синергетическим эффектом при лечении рака.
[00302] Иммуноонкологическое средство может представлять собой, например, лекарственную малую молекулу, антитела или биологическое средство или малую молекулу. Примеры биологических иммуноонкологических средств включают, но не ограничиваются только ими, противораковые вакцины, антитела и цитокины. В некоторых вариантах осуществления антитела представляют собой моноклональные антитела. В некоторых вариантах осуществления моноклональные антитела являются гуманизированными или человеческими.
[00303] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой (i) агонист стимулирующего (включая состимулирующий) рецептора или (ii) антагонист ингибирующего (включая соингибирующий) сигнала T-клеток, оба приводят к амплификации ответов антиген-специфических T-клеток.
[00304] Некоторые из стимулирующих и ингибирующих молекул являются представителями надсемейства иммуноглобулинов (IgSF). Одним важным семейством связанных с мембранами лигандов, которые связываются с состимулирующими или соингибирующими рецепторами, является семейство B7, которое включают B7-1, B7-2, B7-H1 (PD-L1), B7-DC (PD-L2), B7-H2 (ICOS-L), B7-H3, B7-H4, B7-H5 (VISTA) и B7-H6. Другим семейством связанных с мембранами лигандов, которые связываются с состимулирующими или соингибирующими рецепторами является семейство TNF молекул, которые связываются с представителями родственного семейства рецепторов TNF, которые включают CD40 и CD40L, OX-40, OX-40L, CD70, CD27L, CD30, CD30L, 4-1BBL, CD137 (4-1BB), TRAIL/Apo2-L, TRAILR1/DR4, TRAILR2/DR5, TRAILR3, TRAILR4, OPG, RANK, RANKL, TWEAKR/Fn14, TWEAK, BAFFR, EDAR, XEDAR, TACI, APRIL, BCMA, LTβR, LIGHT, DcR3, HVEM, VEGI/TL1A, TRAMP/DR3, EDAR, EDA1, XEDAR, EDA2, TNFR1, лимфотоксин α/TNFβ, TNFR2, TNFα, LTβR, лимфотоксин α1β2, FAS, FASL, RELT, DR6, TROY, NGFR.
[00305] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой цитокин, который ингибирует активацию T-клеток (например, IL-6, IL-10, TGF-β, VEGF и другие иммуносупрессивные цитокины), или цитокин, который стимулирует активацию T-клеток для стимулирования иммунного ответа.
[00306] В некоторых вариантах осуществления комбинация соединения, предлагаемого в настоящем изобретении, и иммуноонкологического средства может стимулировать ответы T-клеток. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой: (i) антагонист белка, который ингибирует активацию T-клеток (например, иммунные ингибиторы контрольных точек), такой как CTLA-4, PD-1, PD-L1, PD-L2, LAG-3, TIM-3, галектин 9, CEACAM-1, BTLA, CD69, галектин-1, TIGIT, CD113, GPR56, VISTA, 2B4, CD48, GARP, PD1H, LAIR1, TIM-1 и TIM-4; или (ii) агонист белка, который стимулирует активацию T-клеток, такой как B7-1, B7-2, CD28, 4-1BB (CD137), 4-1BBL, ICOS, ICOS-L, OX40, OX40L, GITR, GITRL, CD70, CD27, CD40, DR3 и CD28H.
[00307] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист ингибирующих рецепторов в клетках NK или агонисты активирующих рецепторов в клетках NK. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист KIR, такой как лирилумаб.
[00308] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой средство, которое ингибирует или уменьшает количество макрофагов или моноцитов, включая, но не ограничиваясь только ими, антагонисты CSF-1R, такие как антитела к антагонисту CSF-1R, включая RG7155 (WO11/70024, WO11/107553, WO11/131407, WO13/87699, WO13/119716, WO13/132044) или FPA-008 (WO11/140249; WO13169264; WO14/036357).
[00309] В некоторых вариантах осуществления иммуноонкологическое средство выбрано из группы, включающей агонистические средства, которые связываются с позитивными состимулирующими рецепторами, блокирующие средства, которые ослабляют передачу сигналов через ингибирующие рецепторы, антагонисты и одно или большее количество средств, которые системно увеличивают содержание противоопухолевых T-клеток, средства, которые преодолевают прямые иммунные супрессивные пути в микроокружении опухоли (например, блокируют ингибирующее воздействие рецептора (например, взаимодействия PD-L1/PD-1), устраняют или ингибируют Tregs (например, с использованием моноклональных антител к CD25 (например, даклизумаб) или путем ex vivo устранения антител к CD25), ингибируют метаболические ферменты, такие как IDO или обращают/предупреждают энергию или уменьшенние количества T-клеток) и средства, которые запускают врожденную иммунную активацию и/или воспаление в местах расположения опухолей.
[00310] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист CTLA-4. В некоторых вариантах осуществления антагонист CTLA-4 представляет собой антагонистические CTLA-4 антитела. В некоторых вариантах осуществления антагонистические CTLA-4 антитела представляют собой YERVOY (ипилимумаб) или тремелимумаб.
[00311] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист PD-1. В некоторых вариантах осуществления антагонист PD-1 вводят путем инфузии. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антитела или их связывающуюся с антигеном часть, которая специфически связывается с рецептором-1 программируемой гибели клеток (PD-1) и ингибирует активность PD-1. В некоторых вариантах осуществления антагонист PD-1 представляет собой антагонистические PD-1 антитела. В некоторых вариантах осуществления антагонистические PD-1 антитела представляют собой OPDIVO (ниволумаб), КЕЙТРУДА (пембролизумаб) или MEDI-0680 (AMP-514; WO2012/145493). В некоторых вариантах осуществления иммуноонкологическим средством может быть пидилизумаб (CT-011). В некоторых вариантах осуществления иммуноонкологическое средство представляет собой рекомбинантный белок, состоящий из внеклеточного домена PD-L2 (B7-DC), сконденсированного с Fc частью IgG1, называющийся AMP-224.
[00312] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист PD-L1. В некоторых вариантах осуществления антагонист PD-L1 представляет собой антагонистические PD-L1 антитела. В некоторых вариантах осуществления PD-L1 антитела представляют собой MPDL3280A (RG7446; WO2010/077634), дурвалумаб (MEDI4736), BMS-936559 (WO2007/005874) и MSB0010718C (WO2013/79174).
[00313] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист LAG-3. В некоторых вариантах осуществления антагонист LAG-3 представляет собой антагонистические LAG-3 антитела. В некоторых вариантах осуществления LAG3 антитела представляют собой BMS-986016 (WO10/19570, WO14/08218) или IMP-731 или IMP-321 (WO08/132601, WO009/44273).
[00314] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой агонист CD137 (4-1BB). В некоторых вариантах осуществления агонист CD137 (4-1BB) представляет собой агонистические CD137 антитела. В некоторых вариантах осуществления CD137 антитела представляют собой урелумаб или PF-05082566 (WO12/32433).
[00315] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой агонист GITR. В некоторых вариантах осуществления агонист GITR представляет собой агонистические GITR антитела. В некоторых вариантах осуществления антитела GITR представляют собой BMS-986153, BMS-986156, TRX-518 (WO006/105021, WO009/009116) или MK-4166 (WO11/028683).
[00316] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист индоламин-(2,3)-диоксигеназы (IDO). В некоторых вариантах осуществления антагонист IDO выбран из группы, включающей эпакадостат (INCB024360, Incyte); индоксимод (NLG-8189, NewLink Genetics Corporation); капманитиб (INC280, Novartis); GDC-0919 (Genentech/Roche); PF-06840003 (Pfizer); BMS:F001287 (Bristol-Myers Squibb); Phy906/KD108 (Phytoceutica); фермент, который разрушает кинуренин (Kynase, Kyn Therapeutics); и NLG-919 (WO09/73620, WO009/1156652, WO11/56652, WO12/142237).
[00317] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой агонист OX40. В некоторых вариантах осуществления агонист OX40 представляет собой агонистические OX40 антитела. В некоторых вариантах осуществления OX40 антитела представляют собой MEDI-6383 или MEDI-6469.
[00318] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист OX40L. В некоторых вариантах осуществления антагонист OX40L представляет собой антагонистические OX40 антитела. В некоторых вариантах осуществления антагонист OX40L представляет собой RG-7888 (WO06/029879).
[00319] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой агонист CD40. В некоторых вариантах осуществления агонист CD40 представляет собой агонистические CD40 антитела. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антагонист CD40. В некоторых вариантах осуществления антагонист CD40 представляет собой антагонистические CD40 антитела. В некоторых вариантах осуществления CD40 антитела представляют собой лукатумумаб или дацетузумаб.
[00320] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой агонист CD27. В некоторых вариантах осуществления агонист CD27 представляет собой агонистические CD27 антитела. В некоторых вариантах осуществления CD27 антитела представляют собой варилумаб.
[00321] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой MGA271 (к B7H3) (WO11/109400).
[00322] В некоторых вариантах осуществления иммуноонкологическим средством является абаговомаб, адекатумумаб, афутузумаб, алемтузумаб, анатумомаб мафенатокс, аполизумаб, атезолимаб, авелумаб, блинатумомаб, BMS-936559, катумаксомаб, дурвалумаб, эпакадостат, эпратузумаб, индоксимод, инотузумаб озогамицин, интелумумаб, ипилимумаб, изсатуксимам, ламбролизумаб, MED14736, MPDL3280A, ниволумаб, обинутузумаб, окаратузумаб, офатумумаб, олататумаб, пембролизумаб, пидилизумаб, ритуксимаб, тицилимумаб, самализумабили тремелимумаб.
[00323] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой иммуностимулирующее средство. Например, антитела, блокирующие ось ингибирования PD-1 и PD-L1, могут высвободить активированные опухоль-реактивные T-клетки и в клинических исследованиях было показано, что они индуцируют длительные противоопухолевые ответы в увеличиващемся количестве гистологических образцов опухолей, включая некоторые типы опухолей, которые обычно не считались чувствительными к иммунотерапии. См., например, Okazaki, T. et al. (2013) Nat. Immunol. 14, 1212-1218; Zou et al. (2016) Sci. Transl. Med. 8. Покзано, что антитела к PD-1 ниволумаб (опдиво®, Bristol-Myers Squibb, также известные, как ONO-4538, MDX1106 и BMS-936558) обладают способностью увеличивать общую выживаемость пациентов с RCC, у которые проявилось прогрессирование заболевания во время или после предварительной антиангиогенной терапии.
[00324] В некоторых вариантах осуществления иммуномодулирующее терапевтическое средство специфически индуцирует апоптоз опухолевых клеток. Утвержденные к применению иммуномодулирующие терапевтические средства, которые можно использовать в настоящем изобретении, включают помалидомид (помалист®, Celgene); леналидомид (ревлимид®, Celgene); ингенол мебутат (пикато®, LEO Pharma).
[00325] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой противораковую вакцину. В некоторых вариантах осуществления противораковая вакцина выбрана из группы, включающей сипулейцел-T (провенге®, Dendreon/Valeant Pharmaceuticals), который утвержден к применению для лечения асимптоматического или минимально симптоматического метастатического кастрационно-рефрактерного (устойчивого к гормонам) рака предстательной железы; и талимоген лагерпарепвек (имлигик®, BioVex/Amgen, ранее известный, как T-VEC), генетически модифицированное онколитические вирусное терапевтическое средство, утвержденное к применению для лечения нерезектабельных кожных, подкожных и узловых поражений при меланоме. В некоторых вариантах осуществления иммуноонкологическое средство выбрано из группы, включающей онколитические вирусное терапевтическое средство, такое как пексастимоген девацирепвек (PexaVec/JX-594, SillaJen/ранее Jennerex Biotherapeutics), дефицитная по тимидинкиназе- (TK-) вирусная вакцина, которой с помощью генной инженерии придана способность экспрессировать GM-CSF, для печеночно-клеточной карциномы (NCT02562755) и меланомы (NCT00429312); пелареореп (реолизин®, Oncolytics Biotech), вариант респираторного кишечного орфанного вируса (реовируса), который не реплицируется в клетках, которые не активированы посредством RAS-, в многочисленных раковых заболеваниях, включая колоректальный рак (NCT01622543); рак предстательной железы (NCT01619813); плоскоклеточный рак головы и шеи (NCT01166542); аденокарцинома поджелудочной железы (NCT00998322); и немелкоклеточный рак легких (NSCLC) (NCT 00861627); энаденотукирев (NG-348, PsiOxus, ранее известный, как ColoAd1), аденовирус, которому с помощью генной инженерии придана способность экспрессировать полноразмерный CD80, и фрагменты антител, специфичные для белка CD3 рецептора T-клеток, при раке яичников (NCT02028117); метастатических или запущенных эпителиальных опухолях, таких как колоректальный рак, рак мочевого пузыря, плоскоклеточная карцинома головы и шеи и рак слюнной железы (NCT02636036); ONCOS-102 (Targovax/ранее Oncos), аденовирус, которому с помощью генной инженерии придана способность экспрессировать GM-CSF, при меланоме (NCT03003676); и перитонеальном заболевании, колоректальном раке или раке яичников (NCT02963831); GL-ONC1 (GLV-1h68/GLV-1h153, Genelux GmbH), вирусные вакцины, которым с помощью генной инженерии придана способность экспрессировать бета-галактозидазу (бета-gal)/бета-глюкуронидазу или симпортер бета-gal/йодида натрия у человека (hNIS) соответственно, исследовали для перитонеального канцероматоза (NCT01443260); рак фаллопиевых труб, рак яичников (NCT 02759588); или CG0070 (Cold Genesys), аденовирус, которому с помощью генной инженерии придана способность экспрессировать GM-CSF, при раке мочевого пузыря (NCT02365818).
[00326] В некоторых вариантах осуществления иммуноонкологическое средство выбрано из группы, включающей JX-929 (SillaJen/ранее Jennerex Biotherapeutics), вирусные вакцины для TK- и дефицитной по фактору роста вакцинальной болезни, которым с помощью генной инженерии придана способность экспрессировать цитозиндезаминазу, которая способна превращать пролекарство 5-фторцитозин в цитотоксичный лекарственный 5-фторурацил; TG01 и TG02 (Targovax/ранее Oncos), иммунотерапевтические средства на основе пептидов, направленные на трудно поддающиеся лечению мутации RAS; и TILT-123 (TILT Biotherapeutics), полученный с помощью генной инженерии аденовирус, обозначенный, как: Ad5/3-E2F-delta24-hTNFα-IRES-hIL20; и VSV-GP (ViraTherapeutics) вирус везикулярного стоматита (VSV), которому с помощью генной инженерии придана способность экспрессировать гликопротеин (GP), вирус лимфоцитарного хориоменингита (LCMV), которому с помощью генной инженерии можно дополнительно придать способность экспрессировать антигены, предназначенные для усиления антигенспецифичного ответа CD8+ T-клетки.
[00327] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой T-клетки, которым с помощью генной инженерии придана способность экспрессировать химерный антиген рецептора или CAR. T-клетки, которым с помощью генной инженерии придана способность экспрессировать такой химерный антиген рецептора, называются CAR-T-клетками.
[00328] Получены CARs, которые состоят из связывающих доменов, которые можно получить из натуральных лигандов, одиночные цепочечные вариабельные фрагменты (scFv), полученные из моноклональных антител, специфических для антигенов поверхностей клеток, сконденсированных с эндодоменами, которые являются функциональным концом рецептора T-клетки (TCR), такими как the CD3-дзета сигнальный домен в TCRs, который способен генерировать сигнал активации в T-лимфоцитах. При связывании с антигеном такие CARs связываются с эндогенными сигнальными путями в эффекторных клетках и генерируют активирующие сигналы, аналогичные инициируемым комплексом TCR.
[00329] Например, в некоторых вариантах осуществления CAR-T-клетки являются одними из описанных в патенте U.S. 8906682 (June; во всей своей полноте включенный в настоящее изобретение в качестве ссылки), в котором раскрыты CAR-T-клетки, в которые с помощью генной инженерии включен внеклеточный домен, содержащий домен, связывающий антиген (такой как домен, который связывается с CD19), сконденсированный с внутриклеточным сигнальным доменом коплексной дзета цепи антигена рецептора T-клеток (такой как CD3 дзета). При экспрессировании в T-клетках CAR способен перенаправлять распозанвание антигена на основе специфичности связывания антигена. В случае CD19 антиген экспрессизуется в злокачественных B-клетках. В настоящее время проводится более 200 клинических исследований, в которых CAR-T исполькуется в широком диапазоне показаний. [https://clinicaltrials.gov/ct2/results?term=chimeric+antigen+receptors&pg=1].
[00330] В некоторых вариантах осуществления иммуностимулирующее средство представляет собой активатор рецептора ретиноевой кислоты-родственного орфанного рецептора γ (RORγt). RORγt представляет собой фактор трансрипции, который играет ключевую роль в дифференциации и поддержании типа 17 поднадора эффекторов CD4+ (Th17) и CD8+ (Tc17) T-клеток, а также дифференциации экспрессирующих IL-17 субпопуляций врожденных иммунных клеток, таких как NK клетки. В некоторых вариантах осуществления активатор RORγt представляет собой LYC-55716 (Lycera), который в настоящее время изучается в клинических исследованиях лечения сóлидных опухолей (NCT02929862).
[00331] В некоторых вариантах осуществления иммуностимулирующее средство представляет собой агонист или активатор toll-подобного рецептора (TLR). Подходящие активаторы TLRs включают агонист или активатор TLR9, такой как SD-101 (Dynavax). SD-101 представляет собой иммуностимулирующий CpG, который изучают для B-клеточных, фолликулярных и других лимфом (NCT02254772). Агонисты или активаторы TLR8, которые можно использовать в настоящем изобретении, включают мотолимод (VTX-2337, VentiRx Pharmaceuticals), который изучают для плоскоклеточного рака головы и шеи (NCT02124850) и рака яичников (NCT02431559).
[00332] Другие иммуноонкологические средства, которые можно использовать в настоящем изобретении, включают урелумаб (BMS-663513, Bristol-Myers Squibb), моноклональные антитела к CD137; варилумаб (CDX-1127, Celldex Therapeutics), моноклональные антитела к CD27; BMS-986178 (Bristol-Myers Squibb), моноклональные антитела к OX40; лирилумаб (IPH2102/BMS-986015, Innate Pharma, Bristol-Myers Squibb), моноклональные антитела к KIR; монализумаб (IPH2201, Innate Pharma, AstraZeneca) моноклональные антитела к NKG2A; андекаликсимаб (GS-5745, Gilead Sciences), антитела к MMP9; MK-4166 (Merck & Co.), моноклональные антитела к GITR.
[00333] В некоторых вариантах осуществления иммуностимулирующее средство выбрано из группы, включающей элотузумаб, мифамуртид, агонист или активатор toll-подобного рецептора и активатор RORγt.
[00334] В некоторых вариантах осуществления иммуностимулирующим терапевтическим средством является рекомбинантный интерлейкин человека 15 (rhIL-15). rhIL-15 исследовали в клинике в качестве терапевтического средства для меланома и почечноклеточной карцинома (NCT01021059 и NCT01369888) и лейкозов (NCT02689453). В некоторых вариантах осуществления иммуностимулирующее средство представляет собой рекомбинантный интерлейкин 12 человека (rhIL-12). В некоторых вариантах осуществления иммунотерапевтическим средством на основе IL-15 является гетеродимерный IL-15 (hetIL-15, Novartis/Admune), комплекс слияния, состоящий из синтетической формы эндогенного IL-15, образовавшего комплекс с растворимым связывающим белком IL-15 IL-15 рецептора альфа-цепи (IL15:sIL-15RA), который исследован в фазе 1 клинических исследований меланомы, почечноклеточной карциномы, немелкоклеточного рака легких и плоскоклеточной карциномы головы и шеи (NCT02452268). В некоторых вариантах осуществления рекомбинантный интерлейкин 12 человека (rhIL-12) представляет собой NM-IL-12 (Neumedicines, Inc.), NCT02544724 или NCT02542124.
[00335] В некоторых вариантах осуществления иммуноонкологическое средство выбрано из группы, включающей описанные в публикации Jerry L. Adams et al., "Big opportunities for small molecules in immuno-oncology", Cancer Therapy 2015, Vol. 14, pages 603-622, содержание которой во всей его полноте включено в настоящее изобретение в качестве ссылки. В некоторых вариантах осуществления иммуноонкологическое средство выбрано из группы, включающей примеры, описанные в таблице 1 в публикации Jerry L. Adams et al. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой малую молекулу, имеющую мишенью иммуноонкологическую мишень, выбранную из числа приведенных в таблице 2 в публикации Jerry L. Adams et al. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой малую молекулу средство, выбранную из числа приведенных в таблице 2 в публикации Jerry L. Adams et al.
[00336] В некоторых вариантах осуществления иммуноонкологическое средство выбрано из группы, включающей малую молекулу иммуноонкологического средства, описанную в публикации Peter L. Toogood, "Small molecule immuno-oncology therapeutic agents", Bioorganic & Medicinal Chemistry Letters 2018, Vol. 28, pages 319-329, содержание которой во всей его полноте включено в настоящее изобретение в качестве ссылки. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой средство, имеющее мишенью пути, описанные в публикации Peter L. Toogood.
[00337] В некоторых вариантах осуществления иммуноонкологическое средство выбрано из группы, включающей описанные в публикации Sandra L. Ross et al., "Bispecific T cell engager (BiTE® ) antibody constructs can mediate bystander tumor cell killing", PLoS ONE 12(8): e0183390, содержание которой во всей его полноте включено в настоящее изобретение в качестве ссылки. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой конструкцию биспецифических анител к активатору T-клеток (BiTE®). В некоторых вариантах осуществления конструкция биспецифических анител к активатору T-клеток (BiTE®) представляет собой конструкцию биспецифических анител к CD19/CD3. В некоторых вариантах осуществления конструкция биспецифических анител к активатору T-клеток (BiTE®) представляет собой конструкцию биспецифических анител к EGFR/CD3. В некоторых вариантах осуществления конструкция биспецифических анител к активатору T-клеток (BiTE®) activates T-клетки. В некоторых вариантах осуществления конструкция биспецифических анител к активатору T-клеток (BiTE®) активирует T-клетки, которые высвобождают цитокины, индуцирующую повышающую регуляцию молекулы 1 межклеточтой адгезии (ICAM-1) и FAS в находящихся рядом клетках. В некоторых вариантах осуществления конструкция биспецифических анител к активатору T-клеток (BiTE®) активирует T-клетки, что приводит к индуцированному лизису находящихся рядом клеток. В некоторых вариантах осуществления находящиеся рядом клетки расположены в сóлидных опухолях. В некоторых вариантах осуществления лизируемые находящиеся рядом клетки находятся вблизи от активированных посредством BiTE® T-клеток. В одном варианте осуществления находящиеся рядом клетки включают негативные по связанному с опухолью антигену (TAA) раковые клетки. В одном варианте осуществления находящиеся рядом клетки включают негативные по EGFR раковые клетки. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой антитела, которые блокируют ось PD-L1/PD1 и/или CTLA4. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой ex-vivo расширенные инфильтрующие в опухоль T-клетки. В некоторых вариантах осуществления иммуноонкологическое средство представляет собой конструкцию биспецифических анител или химерные антигены рецептора (CARs), которые прямо связывают T-клетки со связанными с опухолью антигенами поверхностей клеток (TAAs).
Типичные иммунные ингибиторы контрольных точек
[00338] В некоторых вариантах осуществления иммуноонкологическое средство представляет собой иммунный ингибитор контрольных точек, описанный в настоящем изобретении.
[00339] Термин "ингибитор контрольных точек" при использовании в настоящем изобретении относится к средствам, применимым для предупреждения попадания раковых клеток в иммунную систему пациента. Субверсия одного из главных механизмов противоопухолевого иммунитета, известна, как "истощение T-клеток", что обусловлено длительным воздействием антигенов, которые приводят к повышающей регуляции ингибирующих рецепторов. Эти ингибирующие рецепторы выступают в качестве иммунных контрольных точек для предупреждения неконтролируемых иммунных реакций.
[00340] PD-1 и соингибирующие рецепторы, такие как цитотоксический антиген 4 T-лимфоцитов (CTLA-4, аттенюатор B- и T-лимфоцитов (BTLA; CD272), иммуноглобулин T-клеток и домен-3 муцина (Tim-3), ген-3 активации лимфоцитов (Lag-3; CD223) и др., часто называют регуляторами контрольных точек. Они действуют, как молекулярные "диспетчеры", которые позволяют внеклеточной информации решать, будут ли протекать прогрессирование клеточного цикла и другие внутриклеточные сигнальные процессы.
[00341] В некоторых вариантах осуществления иммунный ингибитор контрольных точек представляет собой антитела к PD-1. PD-1 связвыается с рецептором 1 прогрвммированной гибели клеток (PD-1) для предупреждения связывания рецептора с ингибирующим лигандом PDL-1, таким образом корректируя возможность опухолей подавлять противоопухолевый иммунный ответа хозяина.
[00342] В одном объекте ингибитор контрольных точек представляет собой биологическое терапевтическое средство или малую молекулу. В другом объекте ингибитор контрольных точек представляет собой моноклональные антитела, гуманигированные антитела, полные антитела человека, белок слияния или их комбинацию. В другом объекте ингибитор контрольных точек ингибирует белок контрольной точки, выбранный из группы, включающей CTLA-4, PDLl, PDL2, PDl, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK 1, CHK2, A2aR, лиганды семейства B-7 или их комбинацию. В дополнительном объекте ингибитор контрольных точек взаимодействует с лигандом белка контрольной точки, выбранным из группы, включающей CTLA-4, PDLl, PDL2, PDl, B7-H3, B7-H4, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD160, CGEN-15049, CHK 1, CHK2, A2aR, лиганды семейства B-7 или их комбинацию. В одном объекте ингибитор контрольных точек представляет собой иммуностимулирующее средство, фактор роста T-клеток, интерлейкин, антитела, вакцину или их комбинацию. В другом объекте интерлейкин комбинацию IL-7 или IL-15. В предпочтительном объекте интерлейкин представляет собой гликозилированный IL-7. В дополнительном объекте вакцина представляет собой вакцину дендритных клеток (DC).
[00343] Ингибиторы контрольных точек включают любое средство, которое статистически значимым образом блокирует или ингибирует ингибирующие пути иммунной системы. Такие ингибиторы могут включать малые молекулы - ингибиторы или могут включать антитела или их связывающие антиген фрагменты, которые связываются с и блокируют или ингибируют рецепторы или антитела иммунных контрольных точек, которые связываются с и блокируют или ингибируют лиганды рецептора иммунного контрольных точек. Иллюстративные молекулы контрольных точек, которые можно направить на блокирование или ингибирование, включают, но не ограничиваются только ими, CTLA-4, PDL1, PDL2, PD1, B7-H3, B7-H4, BTLA, HVEM, GAL9, LAG3, TIM3, VISTA, KIR, 2B4 (относится к семейству молекул CD2 и экспрессируются во всех NK, γδ и CD8+ (αβ) T-клетках памяти), CD160 (также называющийся, как BY55), CGEN-15049, CHK 1 и CHK2 киназы, A2aR и разные лиганды семейства B-7. Лиганды семейства B7 включают, но не ограничиваются только ими, B7- 1, B7-2, B7-DC, B7-H1, B7-H2, B7-H3, B7-H4, B7-H5, B7-H6 и B7-H7. Ингибиторы контрольных точек включают антитела или их связывающие антиген фрагменты, другие связывающие белки, биологические терапевтические средства или малые молекулы, которые которые связываются с и блокируют или ингибируют активность одного или большего количества CTLA-4, PDL1, PDL2, PD1, BTLA, HVEM, TIM3, GAL9, LAG3, VISTA, KIR, 2B4, CD 160 и CGEN-15049. Иллюстративные иммунные ингибиторы контрольных точек включают тремелимумаб (блокирующие CTLA-4 антитела), анти-OX40, PD-Ll моноклональные антитела (антитела к B7-Hl; MEDI4736), MK-3475 (блокатор PD-1), ниволумаб (антитела к PDl ), CT-011 (антитела к PDl ), моноклональные антитела BY55, AMP224 (антитела к PDLl ), BMS-936559 (антитела к PDLl ), MPLDL3280A (антитела к PDLl ), MSB0010718C (антитела к PDLl ) и ипилимумаб (анти-CTLA-4 ингибитор контрольных точек). Лиганды белков контрольных точек включают, но не ограничиваются только ими PD-Ll, PD-L2, B7-H3, B7-H4, CD28, CD86 и TIM-3.
[00344] В некоторых вариантах осуществления иммунный ингибитор контрольных точек выбран из группы, включающей антагонист PD-1, антагонист PD-L1 и антагонист CTLA-4. В некоторых вариантах осуществления ингибитор контрольных точек выбран из группы, включающей ниволумаб (опдиво®), ипилимумаб (ервой®) и пембролизумаб (кейтруда®). В некоторых вариантах осуществления ингибитор контрольных точек выбран из группы, включающей ниволумаб (антитела к PD-1, опдиво®, Bristol-Myers Squibb); пембролизумаб (антитела к PD-1, кейтруда®, Merck); ипилимумаб (антитела к CTLA-4, ервой®, Bristol-Myers Squibb); дурвалумаб (антитела к PD-L1, имфинзи®, AstraZeneca); и атезолизумаб (антитела к PD-L1, тецентрик®, Genentech).
[00345] В некоторых вариантах осуществления ингибитор контрольных точек выбран из группы, включающей ламбролизумаб (MK-3475), ниволумаб (BMS-936558), пидилизумаб (CT-011), AMP-224, MDX-1105, MEDI4736, MPDL3280A, BMS-936559, ипилимумаб, лирлумаб, IPH2101, пембролизумаб (кейтруда®) и тремелимумаб.
[00346] В некоторых вариантах осуществления иммунный ингибитор контрольных точек представляет собой REGN2810 (Regeneron), антитела к PD-1, исследованные у пациентов, у которых имеется базально-клеточная карцинома (NCT03132636); NSCLC (NCT03088540); кожная плоскоклеточная карцинома (NCT02760498); лимфома (NCT02651662); и меланома (NCT03002376); пидилизумаб (CureTech), также известный, как CT-011, антитела, которые связываются с PD-1, изученные в клинических исследованиях диффузной крупноклеточной-В-клеточной лимфомы и множественной миеломы; авелумаб (бавенцио®, Pfizer/Merck KGaA), также известный, как MSB0010718C), полные антитела человека IgG1 к PD-L1, в клинических исследованиях, в которых изучали немелкоклеточный рак легких, карциному из клеток Меркеля, мезотелиома, сóлидные опухоли, рак почки, рак яичников, рак мочевого пузыря, рак головы и шеи и рак желудка; или PDR001 (Novartis), ингибирующие антитела, которые связываются с PD-1, в клинических исследованиях, в которых изучали немелкоклеточный рак легких, меланому, трижды негативный рак молочной железы и запущенные или метастатические сóлидные опухоли. Тремелимумаб (CP-675,206; Astrazeneca) представляет собой полные моноклональные антитела человека к CTLA-4, которые изучали в клинических исследованиях при ряде показаний, включая следующие: мезотелиома, колоректальный рак, рак почки, рак молочной железы, рак легких и немелкоклеточный рак легких, протоковая аденокарцинома поджелудочной железы, рак поджелудочной железы, рак зародышевых клеток, плоскоклеточный рак головы и шеи, печеночно-клеточная карцинома, рак предстательной железы, рак эндометрия, метастатический рак печени, рак печени, крупноклеточная В-клеточная лимфома, рак яичников, рак шейки матки, метастатический анапластический рак щитовидной железы, уротелиальный рак, рак фаллопиевых труб, множественная миелома, рак мочевого пузыря, саркома мягкой ткани и меланома. AGEN-1884 (Agenus) представляет собой антитела к CTLA4, которые изучают в фазе 1 клинических исследований запущенных сóлидных опухолей (NCT02694822).
[00347] В некоторых вариантах осуществления ингибитор контрольных точек представляет собой ингибитор T-клеточного иммуноглобулина муцина, содержащий белок-3 (TIM-3). Ингибиторы TIM-3, которые можно использовать в настоящем изобретении, включают TSR-022, LY3321367 и MBG453. TSR-022 (Tesaro) представляют собой антитела к TIM-3, которые изучают при сóлидных опухолях (NCT02817633). LY3321367 (Eli Lilly) представляют собой антитела к TIM-3, которые изучают при сóлидных опухолях (NCT03099109). MBG453 (Novartis) представляют собой антитела к TIM-3, которые изучают при запущенных злокачественных опухолях (NCT02608268).
[00348] В некоторых вариантах осуществления ингибитор контрольных точек представляет собой ингибитор иммунорецептора T-клеток с Ig и ITIM доменами или TIGIT, иммунного рецептора для некоторых T-клеток и NK клеток. Ингибиторы TIGIT, которые можно использовать в настоящем изобретении, включают BMS-986207 (Bristol-Myers Squibb), моноклональные антитела к TIGIT (NCT02913313); OMP-313M32 (Oncomed); и моноклональные антитела к TIGIT (NCT03119428).
[00349] В некоторых вариантах осуществления ингибитор контрольных точек представляет собой ингибитор гена-3 активации лимфоцитов (LAG-3). Ингибиторы LAG-3, которые можно использовать в настоящем изобретении, включают BMS-986016 и REGN3767 и IMP321. BMS-986016 (Bristol-Myers Squibb), антитела к LAG-3, изучают при глиобластоме и глиосаркоме (NCT02658981). REGN3767 (Regeneron), также представляет собой антитела к LAG-3 и его изучают при злокачественных опухолях (NCT03005782). IMP321 (Immutep S.A.) представляет собой белок слияния LAG-3-Ig и его изучают при n меланоме (NCT02676869); аденокарциноме (NCT02614833); и метастатическом раке молочной железы (NCT00349934).
[00350] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают агонисты OX40. Агонисты OX40, которые изучают в клинических исследованиях включают PF-04518600/PF-8600 (Pfizer), агонистические антитела к OX40 при метастатическом раке почки (NCT03092856) и запущенных раковых заболеваниях и неоплазии (NCT02554812; NCT05082566); GSK3174998 (Merck), агонистические антитела к OX40, в фазе 1 исследований рака (NCT02528357); MEDI0562 (Medimmune/AstraZeneca), агонистические антитела к OX40, при запущенных сóлидных опухолях (NCT02318394 и NCT02705482); MEDI6469, агонистические антитела к OX40 (Medimmune/AstraZeneca), у пациентов, у которых имеется колоректальный рак (NCT02559024), рак молочной железы (NCT01862900), рак головы и шеи (NCT02274155) и метастатический рак предстательной железы (NCT01303705); и BMS-986178 (Bristol-Myers Squibb) агонистические антитела к OX40, при запущенных раковых заболеваниях (NCT02737475).
[00351] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают агонисты CD137 (также называющиеся, как 4-1BB). Агонисты CD137, которые изучают в клинических исследованиях включают утомилумаб (PF-05082566, Pfizer) агонистические антитела к CD137, при диффузной крупноклеточной-В-клеточной лимфоме (NCT02951156) и i при запущенных раковых заболеваниях и неоплазии (NCT02554812 и NCT05082566); урелумаб (BMS-663513, Bristol-Myers Squibb), агонистические антитела к CD137, при меланоме и раке кожи (NCT02652455) и глиобластоме и глиосаркоме (NCT02658981).
[00352] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают агонисты CD27. Агонисты CD27, которые изучают в клинических исследованиях включают варилумаб (CDX-1127, Celldex Therapeutics) агонистические антитела к CD27, при плоскоклеточном раке головы и шеи, карциноме яичников, колоректальном раке, почечноклеточном раке и глиобластоме (NCT02335918); лимфомах (NCT01460134); и глиоме и астроцитоме (NCT02924038).
[00353] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают агонисты рецептора индуцированного глюкокортикоидом фактора некроза опухоли (GITR). Агонисты GITR, которые изучают в клинических исследованиях включают TRX518 (Leap Therapeutics), агонистические антитела к GITR, при злокачественной меланоме и других злокачественных сóлидных опухолях (NCT01239134 и NCT02628574); GWN323 (Novartis), агонистические антитела к GITR, при сóлидных опухолях и лимфоме (NCT 02740270); INCAGN01876 (Incyte/Agenus), агонистические антитела к GITR, при запущенных раковых заболеваниях (NCT02697591 и NCT03126110); MK-4166 (Merck), агонистические антитела к GITR, при сóлидных опухолях (NCT02132754) и MEDI1873 (Medimmune/AstraZeneca), агонистическая гексамерная молекула GITR-лиганда с доменом IgG1 Fc человека, при запущенных сóлидных опухолях (NCT02583165).
[00354] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают индуцируемый состимулятор T-клеток (ICOS, также известный, как агонисты CD278). Агонисты ICOS, которые изучают в клинических исследованиях включают MEDI-570 (Medimmune), агонистические антитела к ICOS, при лимфомах (NCT02520791); GSK3359609 (Merck), агонистические антитела к ICOS в фазе 1 (NCT02723955); JTX-2011 (Jounce Therapeutics), агонистические антитела к ICOS в фазе 1 (NCT02904226).
[00355] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают ингибиторы килерного IgG-подобного рецептора (KIR). Ингибиторы KIR, которые изучают в клинических исследованиях включают лирилумаб (IPH2102/BMS-986015, Innate Pharma/Bristol-Myers Squibb), антитела к KIR, при лейкозах (NCT01687387, NCT02399917, NCT02481297, NCT02599649), множественной миеломе (NCT02252263) и лимфоме (NCT01592370); IPH2101 (1-7F9, Innate Pharma) при миеломе (NCT01222286 и NCT01217203); и IPH4102 (Innate Pharma), антитела к KIR, которые связываются с тремя доменами длинного цитоплазматического хвоста (KIR3DL2), при лимфоме (NCT02593045).
[00356] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают CD47 ингибиторы взаимодействия между CD47 и сигнальным регуляторным белком альфа (SIRPa). Ингибиторы CD47/SIRPa, которые изучают в клинических исследованиях включают ALX-148 (Alexo Therapeutics), антагонистический вариант (SIRPa), которые связываются с CD47 и предупреждают опосредуемую CD47/SIRPa передачу сигналов, в фазе 1 (NCT03013218); TTI-621 (SIRPa-Fc, Trillium Therapeutics), растворимый рекомбинантный белок слияния, образованный связыванием N-концевого CD47-связывающего домена SIRPa с Fc доменом IgG1 человека, действует путем связывания CD47 человека и предупреждения вырабоки сигнала "не уничтожать" макрофагам, используется в клинических исследованиях в фазе 1 (NCT02890368 и NCT02663518); CC-90002 (Celgene), антитела к CD47, при лейкозах (NCT02641002); и Hu5F9-G4 (Forty Seven, Inc.), при колоректальной неоплазии и сóлидных опухолях (NCT02953782), остром миелолейкозе (NCT02678338) и лимфоме (NCT02953509).
[00357] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают ингибиторы CD73. Ингибиторы CD73, которые изучают в клинических исследованиях включают MEDI9447 (Medimmune), антитела к CD73, при сóлидных опухолях (NCT02503774); и BMS-986179 (Bristol-Myers Squibb), антитела к CD73, при сóлидных опухолях (NCT02754141).
[00358] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают агонисты белка стимулятора генов интерферона (STING, также известный, как трансмембранный белок 173 или TMEM173). Агонисты STING, которые изучают в клинических исследованиях включают MK-1454 (Merck), агонистический синтетический циклический динуклеотид, при лимфоме (NCT03010176); и ADU-S100 (MIW815, Aduro Biotech/Novartis), агонистический синтетический циклический динуклеотид, в фазе 1 (NCT02675439 и NCT03172936).
[00359] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают ингибиторы CSF1R. Ингибиторы CSF1R, которые изучают в клинических исследованиях включают пексидартиниб (PLX3397, Plexxikon), ингибитор CSF1R малой молекулы при колоректальном раке, раке поджелудочной железы, метастатических и запущенных раковых заболеваниях (NCT02777710) и меланоме, немелкоклеточном раке легких, плоскоклеточном раке головы и шеи, желудочно-кишечной стромальной опухоли (GIST) и раке яичников (NCT02452424); и IMC-CS4 (LY3022855, Lilly), антитела к CSF-1R, при раке поджелудочной железы (NCT03153410), меланоме (NCT03101254) и сóлидных опухолях (NCT02718911); и BLZ945 (метиламид 4-[2((1R,2R)-2-гидроксициклогексиламино)-бензотиазол-6-илокси]-пиридин-2-карбоновой кислоты, Novartis), перорально доступный ингибитор CSF1R, при запущенных сóлидных опухолях (NCT02829723).
[00360] Ингибиторы контрольных точек, которые можно использовать в настоящем изобретении, включают ингибиторы рецептора NKG2A. Ингибиторы рецептора NKG2A, которые изучают в клинических исследованиях включают монализумаб (IPH2201, Innate Pharma), антитела к NKG2A, при неоплазии головы и шеи (NCT02643550) и хроническом лимфолейкозе (NCT02557516).
[00361] В некоторых вариантах осуществления иммунный ингибитор контрольных точек выбран из группы, включающей ниволумаб, пембролизумаб, ипилимумаб, авелумаб, дурвалумаб, атезолизумаб или пидилизумаб.
ПРИМЕРЫ
[00362] Как показана в приведенных ниже примерах, в некоторых типичных вариантах осуществления соединения получают в соответствии с приведенными ниже общими методиками. Следует понимать, что, хотя в общих методиках описан синтез некоторых соединения, предлагаемых в настоящем изобретении, приведенные ниже общие методики и другие методики, известные специалисту с общей подготовкой в данной области техники, можно использовать для всех соединений и подклассов и типов каждого из этих соединений, описанных в настоящем изобретении.
Синтез 1: 3-(4-Метилсульфанилпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин
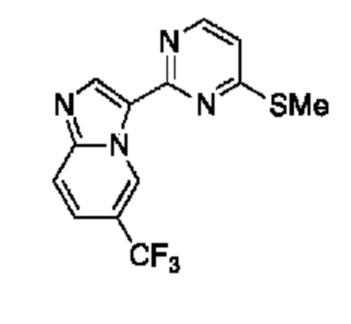
[00363] NBS (165,2 мг, 0,928 ммоля) добавляли к раствору 2-[(E)-2-этоксивинил]-4-метилсульфанилпиримидина (181,4 мг, 0,924 ммоля) в 1,4-диоксане (5,5 мл) и воде (2 мл) и реакционную смесь перемешивали при температуре окружающей среды в течение 15 мин. 5-(Трифторметил)пиридин-2-амин (150 мг, 0,925 ммоля) добавляли и реакционную смесь нагревали при 65-75°C в течение 7 ч. Смесь охлаждали до температуры окружающей среды и разбавляли насыщенным водным раствором NaHCO3 и экстрагировали с помощью DCM. Объединенные органические экстракты сушили (MgSO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (диоксид кремния, EtOAc/петролейный эфир, в градиентном режиме) и получали 3-(4-метилсульфанилпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин (165 мг, 58%); ESV-MS m/z 311,1 (M+H).
[00364] Следующие соединения получали по методологии, аналогичной описанной в синтезе 1:
6-Хлор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридин с использованием 5-хлорпиридин-2-амин;
6-Хлор-7-фтор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридин с использованием 5-хлор-4-фторпиридин-2-амин;
6-Бром-7-фтор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридин с использованием 5-бром-4-фторпиридин-2-амин;
6-Хлор-7-фтор-3-(4-(метилтио)пиримидин-2-ил)имидазо[1,2-a]пиридин с использованием 5-хлор-4-фторпиридин-2-амин.
Синтез 2: 3-(4-Хлорпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин
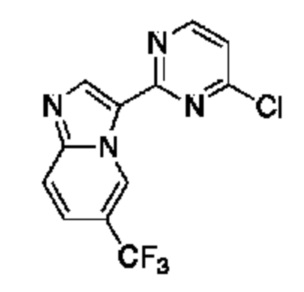
[00365] Сульфурилхлорид (174,9 мкл, 2,160 ммоля) добавляли к раствору 3-(4-метилсульфанилпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридина (165 мг, 0,532 ммоля) и концентрированной HCl (47,1 мкл 37% мас./мас., 0,860 ммоля) в MeCN (13 мл) и реакционную смесь перемешивали в течение 5 мин. По каплям добавляли охлажденный насыщенный водный раствор NaHCO3 и смесь перемешивали в течение 10 мин. Полученный осадок выделяли фильтрованием, промывали водой и сушили и получали 3-(4-хлорпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин (125 мг, 79%).
[00366] Следующие соединения получали по методологии, аналогичной описанной в синтезе 2:
6-Хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридин с использованием 6-хлор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридина;
6-Хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридин с использованием 6-хлор-7-фтор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридина;
6-Бром-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридин с использованием 6-бром-7-фтор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридина;
6-Хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридин с использованием 6-хлор-7-фтор-3-(4-(метилтио)пиримидин-2-ил)имидазо[1,2-a]пиридина.
4-Хлор-2-{6-феноксиимидазо[1,2-a]пиридин-3-ил}пиримидин
4-Хлор-2-{6-метансульфонилимидазо[1,2-a]пиридин-3-ил}пиримидин
3-(4-Хлорпиримидин-2-ил)-N-циклопропилимидазо[1,2-a]пиридин-6-сульфонамид
3-(4-Хлорпиримидин-2-ил)имидазо[1,2-a]пиридин-6-сульфонамид
Синтез 3: 3-Бром-6-(дифторметил)имидазо[1,2-a]пиридин
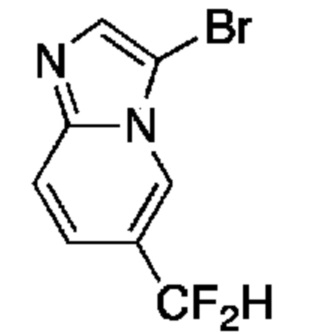
[00367] (Диэтиламино)трифторид серы (528,5 мкл, 4,00 ммоля) по каплям добавляли к 3-бромимидазо[1,2-a]пиридин-6-карбальдегиду (450 мг, 2,00 ммоля) в DCM (4,5 мл) при 0°C. Через 2,5 ч дополнительно добавляли (диэтиламино)трифторид серы (150 мкл, 1,135 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Неочищенную смесь разбавляли метанолом и очищали с помощью ионообменного картриджа SCX-2 и получали 3-бром-6-(дифторметил)имидазо[1,2-a]пиридин (310 мг, 63%); ESV-MS m/z 247,0 (M+H).
Синтез 4: 2-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ол
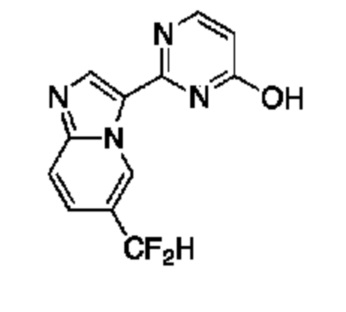
Стадия 1: 6-(Дифторметил)-3-(4-метоксипиримидин-2-ил)имидазо[1,2-a]пиридин
[00368] 3-Бром-6-(дифторметил)имидазо[1,2-a]пиридин (120 мг, 0,486 ммоля), трибутил-(4-метоксипиримидин-2-ил)станнан (200 мкл, 0,583 ммоля) и PdCl2(PPh3)2 (102,3 мг, 0,146 ммоля) объединяли в DMF (4 мл) и дегазировали азотом и нагревали при 120°C в течение 16 ч. Смеси давали охладиться, фильтровали и затем очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,05% TFA в качестве элюента) и получали трифторацетат 6-(дифторметил)-3-(4-метоксипиримидин-2-ил)имидазо[1,2-a]пиридина (97 мг, 72%); ESV-MS m/z 277,1 (M+H).
Стадия 2: 2-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ол
[00369] Хлортриметилсилан (267 мкл, 2,107 ммоля) добавляли к раствору 6-(дифторметил)-3-(4-метоксипиримидин-2-ил)имидазо[1,2-a]пиридина (97 мг, 0,351 ммоля) и NaI (315,8 мг, 2,107 ммоля) в MeCN (4 мл) и смесь нагревали при 80°C в течение 16 ч. Реакционную смесь охлаждали до комнатной температуры и растворитель удаляли при пониженном давлении. Остаток суспендировали в воде и промывали насыщенным водным раствором тиосульфата натрия. Твердое вещество отфильтровывали, промывали водой и сушили в вакууме и получали 2-[6-(дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ол (75 мг, 81%); ESV-MS m/z 263,1 (M+H). Вещество использовали без дополнительной очистки.
Синтез 5: 3-(2-Хлорпиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин
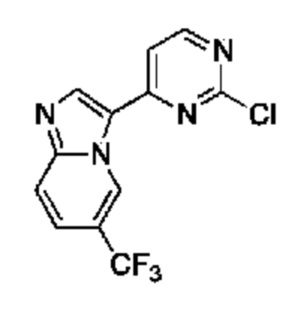
[00370] NBS (241 мг, 1,354 ммоля) добавляли к раствору 2-хлор-4-(2-этоксивинил)пиримидина (250 мг, 1,354 ммоля) в смеси 1,4-диоксан (8 мл)/вода (3 мл) и реакционную смесь перемешивали в течение 15 мин. Добавляли 5-(трифторметил)пиридин-2-амин (220 мг, 1,357 ммоля) и реакционную смесь нагревали при 80°C в течение 3 ч. Смесь охлаждали до комнатной температуры и разбавляли насыщенным водным раствором NaHCO3 и экстрагировали с помощью DCM. Объединенные органические экстракты сушили (MgSO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной флэш-хроматографии (диоксид кремния, EtOAc/петролейный эфир, в градиентном режиме, затем MeOH/DCM, в градиентном режиме) и получали 3-(2-хлорпиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин (234,5 мг, 58%) в виде бежевого твердого вещества.; 1H NMR (500 MHz, DMSO-d6) δ 10,26 (s, 1H), 8,95 (s, 1H), 8,78 (d, 1H), 8,19 (d, 1H), 8,05 (d, 1H), 7,84 (dd, 1H); 19F NMR (471 MHz, DMSO-d6) δ -60,86; ESV-MS m/z 299,1 (M+H).
Синтез 6: N-[[(2S)-Морфолин-2-ил]метил]метансульфонамид
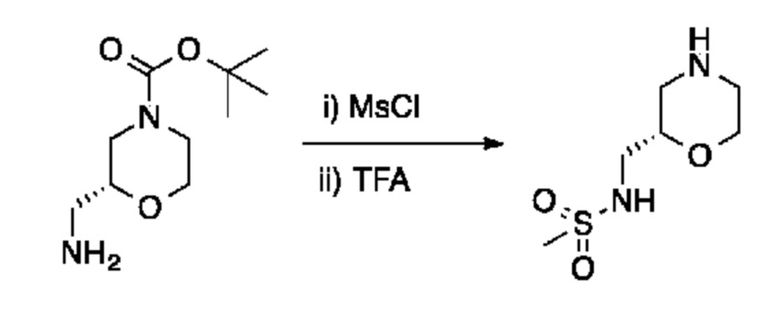
Стадия 1: трет-Бутил-(S)-2-(метилсульфонамидометил)морфолин-4-карбоксилат
[00371] В круглодонную колбу добавляли трет-бутил-(2R)-2-(аминометил)морфолин-4-карбоксилат (5 г, 23 ммоля) и Et3N (16,1 мл, 115 ммоля), затем добавляли THF (100 мл). DCM (50 мл) и смесь охлаждали до 0°C. По каплям добавляли метансульфонилхлорид (2,4 мл, 30,5 ммоля) и смесь перемешивали в течение 0,5 ч, затем выдерживали при температуре окружающей среды в течение 16 ч в атмосфере N2. Реакцию останавливали насыщенным водным раствором NaHCO3 (100 мл) и большую часть летучих веществ удаляли в вакууме. Водный слой экстрагировали этилацетатом (3×50 мл). Объединенные органические вещества сушили над Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния; 70-100% EtOAc/петролейный эфир элюирование в градиентном режиме). Фракции продукта объединяли и концентрировали в вакууме. Остаток сушили в течение ночи в вакууме и получали трет-бутил-(S)-2-(метилсульфонамидометил)морфолин-4-карбоксилат (3,61 г, 53%) в виде белого твердого вещества; 1H NMR (500 MHz, хлороформ-d) δ 4,71-4,59 (m, 1H), 3,98-3,82 (m, 2H), 3,63-3,49 (m, 2H), 3,38-3,24 (m, 1H), 3,20-3,11 (m, 1H), 3,04-2,90 (m, 4H), 2,73 (s, 1H), 1,49 (s, 9H).
Стадия 2: N-[[(2S)-Морфолин-2-ил]метил]метансульфонамид
[00372] TFA (9 мл, 115 ммоля) при перемешивании добавляли к раствору трет-бутил-(2S)-2-(метансульфонамидометил)морфолин-4-карбоксилата (3,6 г, 12 ммоля) в DCM (60 мл) и реакционную смесь перемешивали при температуре окружающей среды в течение 6 ч. Растворитель удаляли в вакууме и остаток подвергали азеотропной перегонке с DCM (×2) и диэтиловым эфиром (×2). Остаток переносили в метанол и пропускали через ионообменный картридж при элюировании метанолом (отбрасывали), затем 2 M метанольным раствором аммиака. Фильтрат концентрировали в вакууме и получали N-[[(2S)-морфолин-2-ил]метил]метансульфонамид (2,3 г, 97%); 1H NMR (500 MHz, хлороформ-d) δ 4,73 (s, 1H), 3,90-3,87 (m, 1H), 3,65-3,60 (m, 2H), 3,26 (dd, 1H), 3,09 (dd, 1H), 2,99 (s, 3H), 2,92-2,84 (m, 3H), 2,66 (dd, 1H); MS m/z: 195 (M+H)+.
Синтез 7: 2-(1H-Пиразол-4-ил)морфолин
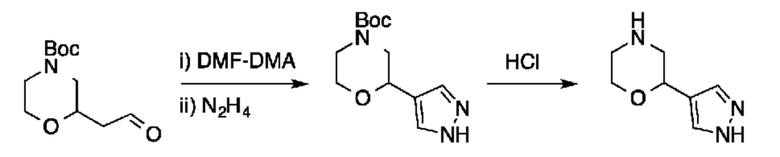
Стадия 1: трет-Бутил-2-(1H-пиразол-4-ил)морфолин-4-карбоксилат
[00373] Смесь трет-бутил-2-(2-оксоэтил)морфолин-4-карбоксилата (5,77 г, 25 ммоля) и DMF-DMA (6,7 мл, 50 ммоля) в DMF (50 мл) перемешивали при 80°C в течение 17 ч. Реакционную смесь охлаждали до температуры окружающей среды и растворитель удаляли в вакууме. Остаток переносили в EtOH (100 мл) и при перемешивании добавляли гидразингидрат (1,3 мл, 26,5 ммоля) при температуре окружающей среды. Через 3 ч растворитель удаляли в вакууме и остаток очищали с помощью хроматографии (диоксид кремния, PE/EtOAc элюирование в градиентном режиме), и получали трет-бутил-2-(1H-пиразол-4-ил)морфолин-4-карбоксилат (2,35 г, 37%) в виде желтого твердого вещества. 1H NMR (500 MHz, хлороформ-d) δ 7,63 (s, 2H), 4,52 (dd, 1H), 4,12 (br s, 1H), 3,97-3,90 (m, 2H), 3,68 (td, 1H), 3,05 (d, 2H), 1,51 (s, 9H); MS m/z: 254,1 (M+H)+.
Стадия 2: 2-(1H-Пиразол-4-ил)морфолин
[00374] 3M HCl в метаноле (45 мл 3M, 135 ммоля) при перемешивании добавляли к раствору трет-бутил-2-(1H-пиразол-4-ил)морфолин-4-карбоксилата (2,35 г, 9,3 ммоля) в DCM (75 мл) и реакционную смесь кипятили с обратным холодильником в течение 5 ч. Реакционную смесь охлаждали до температуры окружающей среды и растворитель удаляли в вакууме. Остаток растворяли в минимальном количестве DCM/MeOH и загружали в ионообменный картридж. Картридж промывали смесями MeOH/DCM, которые отбрасывали. Продукт элюировали путем промывки с помощью 2M NH3 в MeOH/DCM. Растворитель удаляли в вакууме и получали 2-(1H-пиразол-4-ил)морфолин (1,27 г, 89%) в виде оранжевого твердого вещества, которое использовали в следующей реакции без дополнительной очистки; 1H NMR (500 MHz, хлороформ-d) δ 7,60 (s, 2H), 4,56 (dd, 1H), 3,98 (ddd, 1H), 3,77 (td, 1H), 3,11 (dd, 1H), 3,00 (td, 1H), 2x,93-2,88 (m, 2H); MS m/z: 154,2 [M+H]+.
Синтез 8: 2-Метил-6-(1H-пиразол-4-ил)морфолин.
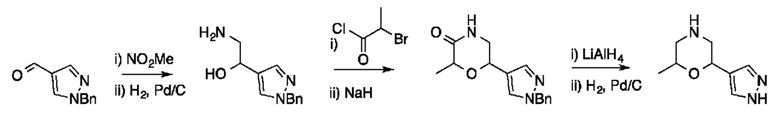
[00375] К раствору 1-бензилпиразол-4-карбальдегида (2 г, 10,7 ммоля) и нитрометана (7 мл, 129 ммоля), охлажденному в бане со льдом, добавляли Et3N (150 мкл, 1,1 ммоля). Смесь перемешивали при охлаждении в течение 15 мин, затем при температуре окружающей среды в течение 18 ч. Реакционную смесь концентрировали в вакууме и остаток очищали с помощью хроматографии (диоксид кремния, EtOAc/петролейный эфир элюирование в градиентном режиме). Соответствующие фракции объединяли и концентрировали в вакууме и получали бесцветное масло (1 г, 37%); MS m/z: 248 (M+H)+. Это вещество сразу использовали в следующей реакции.
[00376] Смесь 1-(1-бензилпиразол-4-ил)-2-нитроэтанола (100 мг, 0,4 ммоля), Pd на C, влажного, Degussa (20 мг, 0,2 ммоля) в метаноле (4 мл) перемешивали при температуре окружающей среды в течение 18 ч в атмосфере H2 при давлении 1 атм.. Реакционную смесь фильтровали и фильтрат концентрировали в вакууме и получали бесцветное смолообразное вещество (90 мг); MS m/z: 218 (M+H)+. Это вещество сразу использовали в следующей реакции.
[00377] 2-Бромпропаноилбромид (114 мг, 0,5 ммоля) добавляли к охлажденному льдом раствору 2-амино-1-(1-бензилпиразол-4-ил)этанола (100 мг, 0,5 ммоля) и Et3N (83 мкл, 0,6 ммоля) в DCM (4 мл) в атмосфере N2. Реакционную смесь перемешивали при температуре окружающей среды в течение 1 ч. Реакционную смесь разбавляли с помощью DCM, промывали 2M водным раствором HCl, насыщенным водным раствором NaHCO3 и рассолом. Органическую фазу сушили над сульфатом натрия, фильтровали и концентрировали в вакууме и получали бесцветное масло. Это вещество переносили в THF (3 мл) и раствор охлаждали в бане со льдом. Добавляли гидрид натрия (37 мг 60% дисперсии в минеральном масле, 0,9 ммоля) и полученную суспензию перемешивали при температуре окружающей среды в течение 2 ч. Реакцию останавливали метанолом затем разбавляли с помощью EtOAc, промывали насыщенным водным раствором бикарбоната натрия и рассолом. Органическую фазу сушили над MgSO4, фильтровали и концентрировали в вакууме и получали бледно-желтое смолообразное вещество (100 мг), MS m/z: 272 (M+H)+, которое сразу использовали в следующей реакции без очистки.
[00378] Смесь 6-(1-бензилпиразол-4-ил)-2-метилморфолин-3-она (100 мг, 0,4 ммоля) и LiAlH4 (184 мкл 2M, 0,4 ммоля) в THF (3 мл) перемешивали при 60°C в течение 1 ч. Полученную суспензию нейтрализовывали с помощью гранул Na2SO4.10H2O и перемешивали в течение 30 мин, затем фильтровали. Фильтрат концентрировали в вакууме и остаток переносили в метанол (2 мл). К раствору добавляли три капли концентрированной HCl и Pd на C, влажный, Degussa (20 мг, 0,02 ммоля). Реакционную смесь перемешивали при температуре окружающей среды в атмосфере H2 при давлении 1 атм. в течение 18 ч. Реакционную смесь выливали в ионообменный картридж и элюировали метанолом (фильтрат отбрасывали), затем 2 M метанольным раствором NH3. Фильтрат концентрировали в вакууме и получали 2-метил-6-(1H-пиразол-4-ил)морфолин (23 мг), MS m/z: 168 (M+H)+. Это вещество сразу использовали в следующей реакции.
Синтез 9: Имино(метил)(пиперидин-3-илметил)-λ6-сульфанон
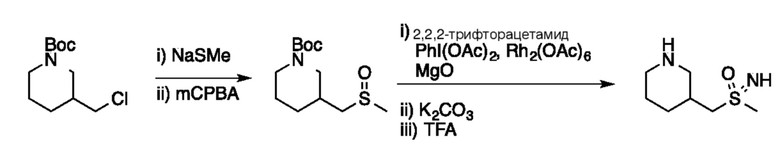
[00379] Смесь трет-бутил-3-(хлорметил)пиперидин-1-карбоксилата (500 мг, 2,14 ммоля), NaSMe (3 мл 20% мас./об., 8,56 ммоля), KI (355 мг, 2,14 ммоля) в этаноле (10 мл) перемешивали при 80°C в течение 22 ч. Реакционную смесь охлаждали до температуры окружающей среды затем концентрировали в вакууме. Остаток подвергали распределению между EtOAc и насыщенным водным раствором бикарбоната натрия. Органическую фазу промывали рассолом, сушили (MgSO4), фильтровали и концентрировали в вакууме и получали продукт в виде бледно-коричневого масла (460 мг 88%), которое использовали на следующей стадии без дополнительной очистки или исследования.
[00380] m-CPBA (324 мг, 1,88 ммоля) добавляли к охлажденному льдом раствору трет-бутил-3-(метилсульфанилметил)пиперидин-1-карбоксилата (460 мг, 1,88 ммоля) в DCM (7 мл) в атмосфере N2. Реакционную смесь перемешивали в течение 20 ч и температура повышалась до температуры окружающей среды. Реакционную смесь разбавляли с помощью DCM, промывали насыщенным водным раствором бикарбоната натрия и рассолом. Органическую фазу сушили над MgSO4, фильтровали и концентрировали в вакууме и получали бледно-коричневое масло (460 мг); MS m/z: 262 (M+H)+, которое использовали на следующей стадии без дополнительной очистки или исследования. трет-Бутил-3-(метилсульфинилметил)пиперидин-1-карбоксилат (5,5 г, 21,0 ммоля), 2,2,2-трифторацетамид (5,2 г, 46,3 ммоля), диацетоксийодбензол (10,2 г, 31,6 ммоля) и MgO (3,39 г, 84,2 ммоля) объединяли в DCM (250 мл) в атмосфере N2. Добавляли Rh2(OAc)6 (0,9 г, 2,0 ммоля) и реакционную смесь перемешивали при комнатной температуре в течение 16 ч. Смесь фильтровали через целит, промывали метанолом и DCM. Фильтрат концентрировали в вакууме и остаток переносили в метанол (5 мл) и добавляли смесь MeCN/вода (3:1) (5 мл). K2CO3 (17,4 г, 126,0 ммоля) и смесь перемешивали при 90°C в течение 2 ч. Смесь разбавляли с помощью EtOAc и промывали насыщенным водным раствором бикарбоната натрия и рассолом. Органическую фазу сушили (Na2SO4), фильтровали и концентрировали в вакууме и получали трет-бутил-3-[(метилсульфонимидоил)метил]пиперидин-1-карбоксилат (5,96 г, количественный выход) в виде масла янтарного цвета; MS m/z: 277 (M+H)+, которое сразу использовали в следующей реакции.
[00381] трет-Бутил-3-[(метилсульфонимидоил)метил]пиперидин-1-карбоксилат (600 мг, 2,17 ммоля) в DCM (3 мл) обрабатывали с помощью TFA (1,7 мл, 21,7 ммоля). Смесь перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь концентрировали в вакууме. Остаток переносили в метанол и загружали в ионообменный картридж. Картридж элюировали MeOH/DCM (фильтрат отбрасывали), затем метанольным раствором аммиака. Фильтрат концентрировали в вакууме и получали имино(метил)(пиперидин-3-илметил)-λ6-сульфанон (250 мг, 65%); 1H NMR (500 MHz, метанол-d4) δ 3,34-3,24 (m, 1H), 3,19-3,10 (m, 2H), 3,10-3,07 (m, 3H), 3,05-2,97 (m, 1H), 2,60 (ddd, 1H), 2,52-2,43 (m, 1H), 2,30-2,18 (m, 1H), 2,08 (ddtd, 1H), 1,75 (dq, 1H), 1,61 (dtq, 1H), 1,37 (dtd, 1H).
Синтез 10: Имино(метил)(пиперидин-3-илметил)-λ6-сульфанон
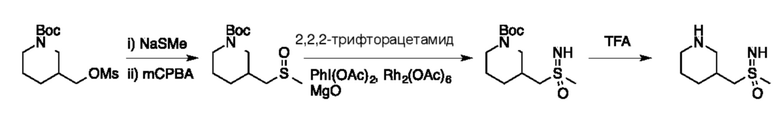
[00382] Тиометоксид натрия (4,06 г, 58 ммоля) добавляли к раствору трет-бутил-3-(метилсульфонилоксиметил)пиперидин-1-карбоксилата (8,5 г, 29 ммоля) в этаноле (170 мл). Смесь перемешивали при температуре окружающей среды в течение 6 ч затем концентрировали в вакууме. Остаток подвергали распределению между DCM и насыщенным водным раствором NaHCO3. Органическую фазу сушили и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния, MeOH/DCM элюирование в градиентном режиме) и получали бледно-желтое масло (6,9 г). Это вещество растворяли в DCM (100 мл) и раствор охлаждали в бане со льдом. Порциями добавляли m-CPBA (6,93 г, чистота 70% мас./мас., 28 ммоля). После завершения добавления реакционную смесь перемешивали в течение 10 мин, затем подвергали распределению между DCM, насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором тиосульфата натрия. Органическую фазу сушили и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния, DCM/MeOH элюирование в градиентном режиме) и получали продукт в виде бесцветного масла.
[00383] трет-Бутил-3-((метилсульфинил)метил)пиперидин-1-карбоксилат (5,5 г, 21,0 ммоля), 2,2,2-трифторацетамид (5,23 г, 46,3 ммоля), (диацетоксийодо)бензол (10,17 г, 31,6 ммоля) и оксид магния (3,39 г, 84,2 ммоля) растворяли в DCM (250 мл) и добавляли диацетокси(диацетоксиродио)родий (0,9 г, 2,04 ммоля). Смесь перемешивали при температуре окружающей среды в течение ночи, затем фильтровали через целит и концентрировали в вакууме. Остаток растворяли в метаноле (50 мл) и воде (10 мл) и добавляли K2CO3 (17,44 г, 126,2 ммоля). Смесь перемешивали при температуре окружающей среды в течение 3 ч, затем нагревали при 50°C в течение 3 дней. Смесь концентрировали в вакууме и остаток растворяли в метаноле (5 мл) и ацетонитрил/вода (3:1 смесь, 5 мл). Через 1,5 ч при 90°C смесь охлаждали, разбавляли в EtOAc и промывали рассолом и насыщенным водным раствором NaHCO3. Органический слой сушили (Na2SO4) и концентрировали в вакууме и получали трет-бутил-3-((S-метилсульфонимидоил)метил)пиперидин-1-карбоксилат (5,96 г) в виде масла янтарного цвета, которое использовали без дополнительной очистки.
[00384] Раствор трет-бутил-3-[(метилсульфонимидоил)метил]пиперидин-1-карбоксилата (600 мг, 2,17 ммоля) и TFA (1,67 мл, 21,71 ммоля) в DCM (3 мл) перемешивали при температуре окружающей среды в течение 16 ч, затем концентрировали в вакууме и остаток пропускали через картридж SCX-2. Продукт элюировали метанольным раствором аммиака и получали имино(метил)(пиперидин-3-илметил)-λ6-сульфанон (250 мг, 65%); 1H NMR (500 MHz, метанол-d4) δ 3,34-3,24 (m, 1H), 3,19-3,10 (m, 2H), 3,10-3,07 (m, 3H), 3,05-2,97 (m, 1H), 2,60 (ddd, J=12,4, 11,5, 3,1 Hz, 1H), 2,52-2,43 (m, 1H), 2,30-2,18 (m, 1H), 2,08 (ddtd, J=30,1, 10,9, 3,8, 1,8 Hz, 1H), 1,75 (dq, J=13,8, 3,3 Hz, 1H), 1,61 (dtq, J=13,6, 11,5, 3,8 Hz, 1H), 1,37 (dtd, J=12,8, 11,3, 3,9 Hz, 1H).
Синтез 11: 2,5-Диметил-3-((метилсульфинил)метил)пиперидин
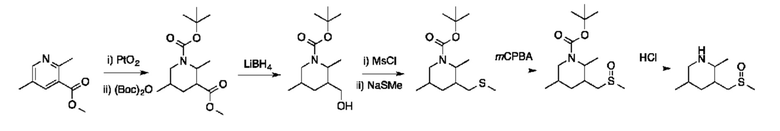
Стадия 1: 1-(трет-Бутил) 3-метил-2,5-диметилпиперидин-1,3-дикарбоксилат
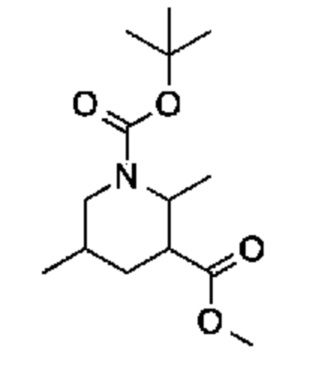
[00385] Смесь метил-2,5-диметилпиридин-3-карбоксилата (2,6 г, 15,74 ммоля) и PtO2 (713 мг, 3,14 ммоля) в HCl (57 мл 3M раствора в MeOH, 171,1 ммоля) перемешивали с подачей H2 из баллона. Реакционную смесь перемешивали в течение 16 ч при температуре окружающей среды, затем фильтровали через целит и фильтрат концентрировали в вакууме. Остаток растворяли в THF (27 мл) и последовательно добавляли триэтиламин (6,6 мл, 47,3 ммоля), DMAP (96 мг, 0,79 ммоля) и ди-трет-бутилдикарбонат (17,4 мл 1M раствора в THF, 17,4 ммоля). Реакционную смесь перемешивали в течение 16 ч, затем подвергали распределению между EtOAc и водой. Органический слой отделяли и промывали раствором NH4Cl, водой (1×), рассолом (1×), затем сушили (MgSO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния, 0-10% EtOAc/петролейный эфир элюирование в градиентном режиме) и получали 1-(трет-бутил) 3-метил-2,5-диметилпиперидин-1,3-дикарбоксилат (1,4 г, 33%) в виде бесцветного масла, содержащего смесь диастереоизомеров; 1H NMR (400 MHz, метанол-d4) δ 4,80-4,62 (m, 1H), 3,95-3,78 (m, 1H), 3,71 (d, 3H), 2,71 (dq, 1H), 2,46 (dt, 1H), 1,89-1,77 (m, 1H), 1,48 (q, 10H), 1,10-0,92 (m, 7H).
Стадия 2: трет-Бутил-3-(гидроксиметил)-2,5-диметилпиперидин-1-карбоксилат
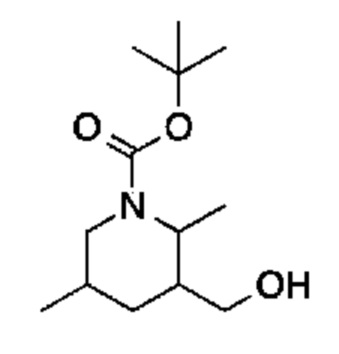
[00386] O1-трет-Бутил-O3-метил-2,5-диметилпиперидин-1,3-дикарбоксилат (1,40 г, 5,16 ммоля) растворяли в THF (42 мл) и охлаждали до 0°C. Добавляли борогидрид лития (10,3 мл 2M раствора в THF, 20,6 ммоля) и реакционной смеси давали нагреться до температуры окружающей среды. Через 30 мин реакционную смесь нагревали при 50°C и перемешивали в течение 16 ч. Реакционную смесь охлаждали до температуры окружающей среды затем реакцию останавливали водой. Смесь экстрагировали с помощью EtOAc (×3). Объединенные органические вещества сушили и концентрировали в вакууме и получали трет-бутил-3-(гидроксиметил)-2,5-диметилпиперидин-1-карбоксилат (1,25 г, 100%) в виде бесцветного масла, которое сразу использовали в следующей реакции без дополнительной очистки; 1H NMR (400 MHz, метанол-d4) δ 4,42-4,27 (m, 1H), 3,82-3,68 (m, 1H), 3,34-3,23 (m, 2H), 2,33 (dt, 1H), 1,91 (s, 1H), 1,82-1,68 (m, 1H), 1,54-1,37 (m, 2H), 1,35 (s, 9H), 0,95-0,87 (m, 3H), 0,86-0,76 (m, 4H).
Стадия 3: трет-Бутил-2,5-диметил-3-(((метилсульфонил)окси)метил)пиперидин-1-карбоксилат
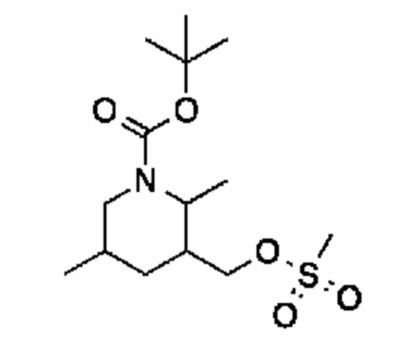
[00387] Метансульфонилхлорид (2,77 мл, 35,7 ммоля) добавляли к раствору трет-бутил-3-(гидроксиметил)-2,5-диметилпиперидин-1-карбоксилата (5,80 г, 23,8 ммоля) и триэтиламина (6,64 мл, 47,7 ммоля) в DCM (116 мл) и перемешивали при 0°C. Через 30 мин реакцию останавливали насыщенным водным раствором NaHCO3, перемешивали в течение 5 мин и затем слои разделяли с помощью картриджа для разделения фаз. Органическую фазу выпаривали в вакууме и получали трет-бутил-2,5-диметил-3-(((метилсульфонил)окси)метил)пиперидин-1-карбоксилат (7,6 г), который сразу использовали на следующей стадии без дополнительной очистки.
Стадия 4: трет-Бутил-2,5-диметил-3-((метилтио)метил)пиперидин-1-карбоксилат
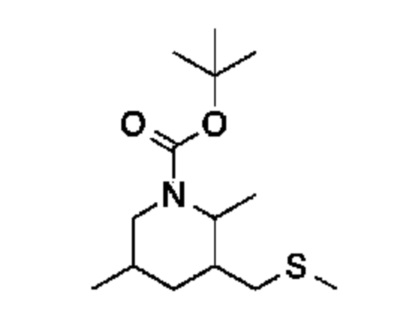
[00388] Тиометоксид натрия (9,94 г, 141,8 ммоля) добавляли к раствору трет-бутил-2,5-диметил-3-(((метилсульфонил)окси)метил)пиперидин-1-карбоксилата (7,6 г, 23,6 ммоля) в EtOH (100 мл), перемешивали при 0°C. После добавления охлаждение прекращали и реакционную смесь нагревали при 60°C в течение 16 ч. Реакционную смесь охлаждали до температуры окружающей среды, концентрировали в вакууме и очищали с помощью колоночной хроматографии (диоксид кремния, при элюировании с помощью 0-12,5% MeOH в DCM, в градиентном режиме) и получали трет-бутил-2,5-диметил-3-((метилтио)метил)пиперидин-1-карбоксилат (3,4 г, 66%) в виде бесцветного масла; 1H NMR (500 MHz, метанол-d4) δ 4,53-4,43 (m, 1H), 3,86 (td, J=13,3, 4,4 Hz, 1H), 2,53-2,31 (m, 3H), 2,10 (s, 3H), 1,91-1,81 (m, 1H), 1,74-1,63 (m, 1H), 1,61-1,50 (m, 1H), 1,48 (s, 9H), 1,10-0,99 (m, 4H), 0,93 (t, J=6,4 Hz, 3H).
Стадия 5: трет-Бутил-2,5-диметил-3-((метилсульфинил)метил)пиперидин-1-карбоксилат
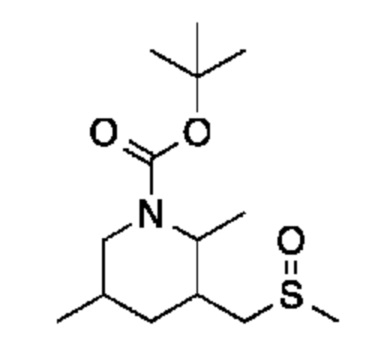
[00389] трет-Бутил-2,5-диметил-3-((метилтио)метил)пиперидин-1-карбоксилат (2 г, 7,31 ммоля) растворяли в DCM (73 мл) и раствор охлаждали до 0°C. Порциями добавляли m-CPBA (1,80 г, 7,31 ммоля) в течение 5 мин и реакционную смесь перемешивали в течение еще 5 мин, затем реакцию останавливали путем добавления насыщенного водного раствора тиосульфата натрия (40 мл) и перемешивали в течение 5 мин, затем экстрагировали с помощью DCM (3×50 мл). Объединенные органические вещества промывали насыщенным водным раствором NaHCO3 (2×40 мл), фильтровали через картридж для разделения фаз и концентрировали в вакууме и получали трет-бутил-2,5-диметил-3-((метилсульфинил)метил)пиперидин-1-карбоксилат (2,1 г, 100%) в виде бесцветного масла, которое использовали без дополнительной очистки.
Стадия 6: 2,5-Диметил-3-((метилсульфинил)метил)пиперидин
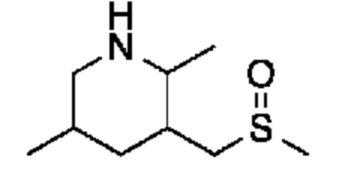
[00390] трет-Бутил-2,5-диметил-3-((метилсульфинил)метил)пиперидин-1-карбоксилат (2,1 г, 7,26 ммоля) растворяли в метаноле (36 мл) и добавляли 4M HCl в диоксане (9,1 мл, 36,3 ммоля). Реакционную смесь перемешивали в течение 16 ч при температуре окружающей среды, затем концентрировали в вакууме и получали 2,5-диметил-3-((метилсульфинил)метил)пиперидин (1,85 г, 97%) в виде белого твердого вещества; MS m/z: 190,1 (M+H)+.
Синтез 12: 2-(1H-Пиразол-4-ил)пиперазин
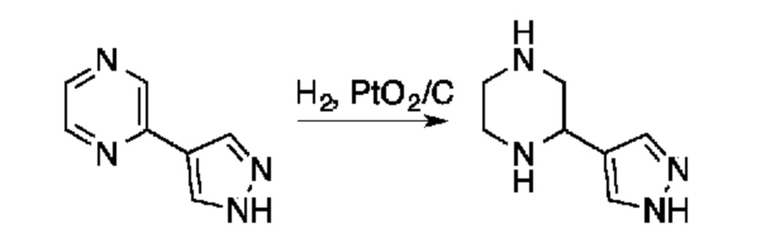
[00391] Смесь 2-(1H-пиразол-4-ил)пиразина (400 мг, 2,7 ммоля) , PtO2 (100 мг, 0,4 ммоля) в метаноле (15 мл) встряхивали при температуре окружающей среды при давлении H2, равном 60 фунт-сила/дюйм2, в течение 18 ч. Реакционную смесь фильтровали и фильтрат концентрировали в вакууме и получали 2-(1H-пиразол-4-ил)пиперазин в виде бесцветного масла, которое сразу использовали в следующей реакции без очистки; MS m/z: 153 (M+H)+.
Синтез 13: 2,5-Диметил-3-(1H-пиразол-4-ил)пиперазин
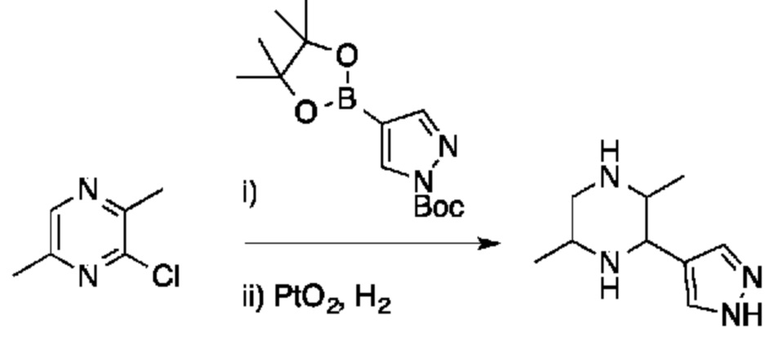
[00392] В 3-горлую колбу, снабженную обратным холодильником и термометром, помещали 3-хлор-2,5-диметилпиразин (5 мл, 40 ммоля), трет-бутил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразол-1-карбоксилат (10 г, 34 ммоля) в 1,4-диоксане (100 мл). Pd(PPh3)4 (2 г, 2 ммоля), и Na2CO3 (60 мл 2M, 100 ммоля) добавляли и раствор откачивали и повторно заполняли с помощью N2 (×2). Раствор нагревали при 100°C и перемешивали в течение ночи. Реакционную смесь охлаждали до температуры окружающей среды и фильтровали, промывали диэтиловым эфиром. Фильтрат концентрировали в вакууме и остаток очищали с помощью хроматографии (диоксид кремния, 0-100% [EtOAc+2% 2M метанольным раствор аммиака]-петролейный эфир элюирование в градиентном режиме). Фракции продукта объединяли и концентрировали в вакууме и получали 2,5-диметил-3-(1H-пиразол-4-ил)пиразин в виде белого твердого вещества (4,5 г, 64%); MS m/z: 175 (M+H)+.
[00393] Смесь 2,5-диметил-3-(1H-пиразол-4-ил)пиразина (4,5 г, 26 ммоля), PtO2 (1 г, 4 ммоля) и HCl (60 мл 3M раствора в MeOH, 200 ммоля) встряхивали в гидрогенизаторе Парра в течение 24 ч при давлении H2, равном 60 фунт-сила/дюйм2. Реакционную смесь фильтровали и фильтрат концентрировали в вакууме и получали продукт 2,5-диметил-3-(1H-пиразол-4-ил)пиперазин в виде почти белого твердого вещества (4,0 г, 61%); MS m/z: 181 (M+H)+. Это вещество использовали в следующей реакции при допущении о выделении дигидрохлорида.
[00394] Следующие соединения получали по методологии, аналогичной описанной в синтезе 213:
2-Метил-6-(1H-пиразол-4-ил)пиперазин;
3-(1H-Имидазол-4-ил)-2,5-диметилпиперазин.
Синтез 14: Диметил((5-метилпиперидин-3-ил)имино)-λ6-сульфанон
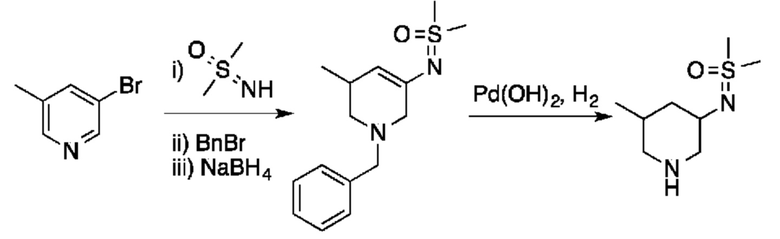
Стадия 1: Диметил((5-метилпиридин-3-ил)имино)-λ6-сульфанон
[00395] 3-Бром-5-метилпиридин (250 г, 1,439 моля), иминодиметил-λ6-сульфан (142,6 г, 1,454 моля), Xantphos (24,976 г, 43,16 ммоля), K2CO3 (218,8 г, 1,583 моля) и трис(бензилиденацетон)дипалладий(0) (19,76 г, 21,58 ммоля) суспендировали в 1,4-диоксане (2,4 л). Реакционную смесь дегазировали (3 цикла вакуум/азот) и перемешивали при кипячении с обратным холодильником при 125°C в течение 16 ч. Реакционной смеси давали охладиться до температуры окружающей среды затем фильтровали через целит, промывали с помощью EtOAc. Масло разбавляли небольшим количеством MTBE (достаточным для обнаружения небольшого осаждения; ~150 мл), засевали несколькими кристаллами аутентичного образца и перемешивали при температуре окружающей среды в течение 2 ч. Твердое вещество отфильтровывали и промывали минимальным количеством MTBE и получали светло-розовое твердое вещество, которое сушили при 30°C в вакуумном шкафу и получали искомый продукт (105,9 г, 40%). Маточные растворы концентрировали в вакууме и получали 247,4 г темно-коричневого масла. 247,4 г Неочищенной смеси очищали с помощью колоночной хроматографии (колонка с 3 кг диоксида кремния; продукт адсорбировали в слое из 350 г диоксида кремния; от 0 до 10% MeOH в EtOAc). Содержащие продукт фракции объединяли и концентрировали в вакууме и после растирания с диэтиловым эфиром получали продукт (106,4 г 40%). Полный выход 212,3 г (80%); 1H NMR (400 MHz, DMSO-d6) δ 7,97 (d, J=2,4 Hz, 1H), 7,92 (dd, J=1,9, 0,9 Hz, 1H), 7,13 (dq, J=2,8, 0,9 Hz, 1H), 3,25 (s, 6H), 2,22 (d, J=0,8 Hz, 3H); ESV-MS m/z 185,0 (M+1)+.
Стадия 2: 1-Бензил-3-((диметил(оксо)-λ6-сульфанилиден)амино)-5-метилпиридин-1-ийбромид
[00396] К раствору диметил((5-метилпиридин-3-ил)имино)-λ6-сульфанона (105,9 г, 574,73 ммоля) в MeCN (900 мл) добавляли BnBr (69 мл, 580 ммоля). Смесь перемешивали при 100°C в течение 4 ч. Реакционной смеси давали охладиться до температуры окружающей среды и полученный осадок собирали фильтрованием, промывали холодным MeCN. Продукт получали в виде почти белого твердого вещества (158,8 г, 78%); 1H NMR (400 MHz, DMSO-d6) δ 8,55 (s, 1H), 8,48 (t, J=1,8 Hz, 1H), 7,87 (t, J=1,5 Hz, 1H), 7,58-7,49 (m, 2H), 7,49-7,37 (m, 3H), 5,67 (s, 2H), 3,44 (s, 6H), 2,41 (s, 3H). ESV-MS m/z 275,1 (M+1)+.
Стадия 3: ((1-бензил-, 5-метил-1,2,5,6-тетрагидропиридин-3-ил)имино)диметил-λ6-сульфанон
[00397] Раствор NaBH4 (43 г, 1,137 моля) в гидроксиде натрия (1,6 л 0,01 M 16,00 ммоля) в течение 2 ч шприцевым насосом по каплям добавляли к раствору 1-бензил-3-((диметил(оксо)-λ6-сульфанилиден)амино)-5-метилпиридин-1-ийбромида (200 г, 562,9 ммоля) в смеси этанол (600 мл)/вода (600 мл) при 0°C в атмосфере N2. Смесь экстрагировали с помощью MTBE (3×1,6 л), органические вещества объединяли и промывали рассолом (1×600 мл), сушили (MgSO4), фильтровали и концентрировали в вакууме и получали искомый продукт (142 г , 91%); 1H NMR (400 MHz, хлороформ-d) δ 7,40-7,17 (m, 5H), 5,18-5,10 (m, 1H), 3,58 (s, 2H), 3,08 (d, J=1,9 Hz, 6H), 3,04-2,93 (m, 1H), 2,86-2,68 (m, 3H), 2,55-2,40 (m, 1H), 1,92 (dd, J=11,0, 8,2 Hz, 1H), 0,95 (d, J=6,9 Hz, 3H).ESV-MS m/z 279,1 (M+1)+.
Стадия 4: Диметил((5-метилпиперидин-3-ил)имино)-λ6-сульфанон
[00398] Pd(OH)2, (59 г, 20% мас./мас., Degussa, 84,03 ммоля) переносили в заполненный азотом и флакон откачивали и повторно заполняли азотом. Затем добавляли раствор ((1-бензил-,5-метил-1,2,5,6-тетрагидропиридин-3-ил)имино)диметил-λ6-сульфанона (117 г, 420,2 ммоля) в метаноле (700 мл) и полученный раствор дегазировали с помощью циклов вакуум/азот (×3). Атмосферу заменяли с помощью циклов вакуум/водород и реакционную смесь встряхивали в гидрогенизаторе Парра в течение 16 ч. Реакционную смесь охлаждали до температуры окружающей среды затем фильтровали через целит и концентрировали в вакууме и получали оранжевое масло, которое анализировали и устанавливали, что реакция не завершилась. Продукт повторно растворяли в метаноле (700 мл) и добавляли во флакон Парра, содержащий дигидроксипалладий (59 г 20% мас./мас., 84,03 ммоля). Затем смесь встряхивали при 50°C и при давлении молекулярного водорода, равном 30 фунт-сила/дюйм2, в течение ночи. Реакционную смесь охлаждали до температуры окружающей среды затем фильтровали через целит и фильтрат концентрировали в вакууме и получали оранжевое масло, которое анализировали с помощью UPLC-MS и устанавливали, что реакция не завершилась. Смесь повторно растворяли в метаноле (700 мл) и добавляли во флакон Парра, содержащий дигидроксипалладий (59 г 20% мас./мас., 84,03 ммоля). Смесь встряхивали при 50°C и при давлении молекулярного водорода, равном 30 фунт-сила/дюйм2, в гидрогенизаторе Парра в течение ночи. Смесь охлаждали до температуры окружающей среды затем фильтровали через целит, затем концентрировали в вакууме и получали диметил((5-метилпиперидин-3-ил)имино)-λ6-сульфанон (56,7 г, 71%); 1H NMR (500 MHz, DMSO-d6) δ 3,54 (замаскированный сигнал, 1H), 3,09 (tt, J=10,8, 4,4 Hz, 1H), 2,95 (s, 6H), 2,89-2,74 (m, 2H), 2,11 (dd, J=12,0, 10,3 Hz, 1H), 1,92 (dd, J=12,1, 11,0 Hz, 1H), 1,84-1,73 (m, 1H), 1,58-1,44 (m, 1H), 0,89 (d, J=12,4 Hz, 1H), 0,77 (d, J=6,6 Hz, 3H).
[00399] Следующее соединение получали по методологии, аналогичной описанной в синтезе 214:
Диметил((пиперидин-3-ил)имино)-λ6-сульфанон.
Синтез 15: 2,5-Диметилпиперидин-3-карбоксамид
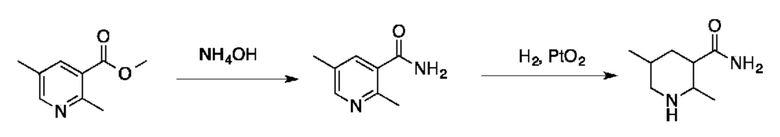
Стадия 1: 2,5-Диметилникотинамид
[00400] Метил-2,5-диметилпиридин-3-карбоксилат (100 мг, 0,61 ммоля) растворяли в гидроксиде аммония (480 мкл, 12,3 ммоля) и смесь нагревали при 70°C в герметизированной пробирке. Через 16 ч реакционную смесь разбавляли в воде и смесь концентрировали в вакууме и получали 2,5-диметилпиридин-3-карбоксамид (91 мг, 100%) в виде белого твердого вещества; MS m/z: 151,0 (M+H)+.
Стадия 2: 2,5-Диметилпиперидин-3-карбоксамид
[00401] 2,5-Диметилникотинамид (99 мг, 0,66 ммоля) и PtO2 (30,4 мг, 0,13 ммоля) растворяли в метаноле (3 мл) и 3M HCl (1,1 мл, 3,30 ммоля). Смесь дегазировали и перемешивали с подачей H2 из баллона в течение 90 мин, затем пропускали через целит и фильтрат концентрировали в вакууме и получали 2,5-диметилпиперидин-3-карбоксамид (дигидрохлорид) (150 мг, 99%); MS m/z: 157,0 (M+H)+.
Синтез 16: N-(((3S,5S)-4,4-Дифтор-5-метилпиперидин-3-ил)метил)метансульфонамид
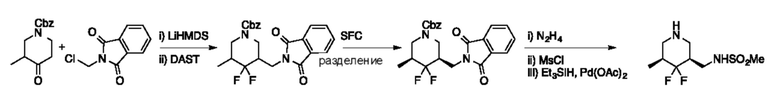
Стадия 1: Бензил-3-((1,3-диоксоизоиндолин-2-ил)метил)-5-метил-4-оксопиперидин-1-карбоксилат
[00402] Бензил-3-метил-4-оксопиперидин-1-карбоксилат (20 г, 0,08 моля) растворяли в THF (300 мл) в атмосфере N2. Раствор охлаждали до -78°C и по каплям добавляли LiHMDS (1M в THF, 101,1 мл, 0,1 моля) в течение 20 мин, поддерживая температуру ниже -70°C. После перемешивания при -78°C в течение 90 мин по каплям добавляли раствор 2-(хлорметил)изоиндолин-1,3-диона (23,7 г, 0,12 моля) в THF (200 мл) в течение 25 мин, поддерживая температуру ниже -70°C. Реакционную смесь перемешивали при -78°C в течение 1 ч, затем реакцию останавливали при -78°C, добавляя насыщенный водный раствор хлорида аммония (65 мл) и смеси давали нагреться до температуры окружающей среды. Реакцию повторяли и две полученные смеси объединяли и экстрагировали с помощью EtOAc (300 мл). Органическую фазу промывали насыщенным водным раствором бикарбоната натрия (300 мл) и рассолом (300 мл), сушили (Na2SO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния, элюирование смесью EtOAc/петролейный эфир). Фракции продукта объединяли и концентрировали в вакууме и остаток перекристаллизовывали из EtOAc и получали продукт в виде белого твердого вещества (7,56 г, 23%).
Стадия 2: Бензил-(3R,5S)-3-[(1,3-Диоксоизоиндолин-2-ил)метил]-4,4-дифтор-5-метилпиперидин-1-карбоксилат
[00403] В колбу помещали бензил-3-((1,3-диоксоизоиндолин-2-ил)метил)-5-метил-4-оксопиперидин-1-карбоксилат (60 г, 0,15 моля) и охлаждали в бане лед/вода. Одной порцией добавляли DAST (325 мл, 2,5 моля) и смесь перемешивали при температуре окружающей среды в течение 3 дней. Полученный желтый раствор разбавляли с помощью DCM (1 л) и медленно добавляли к смеси лед/вода и твердого бикарбоната натрия при перемешивании верхним смесителем. Температура оставалась равной ниже 0°C и дополнительно добавляли бикарбонат натрия для поддержания pH, равного 7-8. Смесь нагревали до температуры окружающей среды и слои разделяли. Водную фазу экстрагировали с помощью DCM (2 л). Объединенные органические вещества промывали рассолом, сушили (Na2SO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния, элюирование смесью EtOAc/петролейный эфир). Фракции продукта объединяли и концентрировали в вакууме. Продукт, бензил-3-((1,3-диоксоизоиндолин-2-ил)метил)-4,4-дифтор-5-метилпиперидин-1-карбоксилат, получал в виде стеклообразного вещества (32,5 г, 51%); 1H NMR (400 MHz, хлороформ-d) δ 7,89-7,64 (4H, m), 7,42-7,11 (5H, m), 5,15-5,03 (2H, m), 4,39-4,07 (3H, m), 3,83-3,66 (1H, m), 2,97-2,60 (2H, m), 2,56-2,31 (1H, m), 2,08-1,89 (1H, m), 1,05 (3H, d) в виде смеси изомеров.
[00404] Препаративную хиральную надкритическую жидкостную хроматографию (условия: Chiralpak®IC 5 мкм, CO2/iPrOH 90/10, 230 нм) использовали для выделения одного энантиомера бензил-(3R,5S)-3-[(1,3-диоксоизоиндолин-2-ил)метил]-4,4-дифтор-5-метилпиперидин-1-карбоксилата (98,7% ee).
Стадия 3: Бензил-(3R,5S)-3-(аминометил)-4,4-дифтор-5-метилпиперидин-1-карбоксилат
[00405] К суспензии бензил-(3R,5S)-3-[(1,3-диоксоизоиндолин-2-ил)метил]-4,4-дифтор-5-метилпиперидин-1-карбоксилата (9,6 г, 22,4 ммоля) в этаноле (144 мл) добавляли гидразингидрат (8,5 мл, 112 ммоля). Реакционную смесь кипятили с обратным холодильником в течение 5 ч, затем ей давали охладиться до температуры окружающей среды в течение ночи. Полученную суспензию фильтровали и осадок промывали с помощью EtOH (×2). Фильтрат загружали в ионообменные картриджи (50 г×10). Картриджи промывали смесями MeOH/DCM (фильтраты отбрасывали), затем 2 M метанольным раствором аммиака. Фильтраты объединяли и концентрировали в вакууме. Остаток переносили в метанол и концентрировали в вакууме (×2), затем обрабатывали гептаном и концентрировали в вакууме. Полученное желтое масло сушили в вакууме в течение ночи и получали продукт в виде твердого вещества (6,77 г), которое сразу использовали в следующей реакции; 1H NMR (400 MHz, DMSO-d6) δ 7,48-7,17 (m, 5H), 5,11 (s, 2H), 4,41 (ddt, 1H), 4,02 (d, 1H), 2,98 (dd, 1H), 2,64 (s, 2H), 2,41 (dd, 1H), 2,15-1,78 (m, 2H), 1,50 (s, 2H), 0,93 (d, 3H); MS m/z: 299 (M+H)+.
Стадия 4: Бензил-(3S,5S)-4,4-дифтор-3-(метансульфонамидометил)-5-метилпиперидин-1-карбоксилат
[00406] Бензил-(3R,5S)-3-(аминометил)-4,4-дифтор-5-метилпиперидин-1-карбоксилат (6,6 г, 22 ммоля) растворяли в DCM (66 мл) и охлаждали в бане со льдом. Внутренняя температура достигала 3°C. При перемешивании добавляли Et3N (3,4 мл, 24 ммоля). Метансульфонилхлорид (1,88 мл, 24 ммоля) добавляли в течение 5 мин с такой скоростью, чтобы внутренняя температура оставалась равной ниже 10°C. Через 30 мин баню со льдом удаляли. Раствор нагревали до температуры окружающей среды и реакцию останавливали насыщенным водным раствором NaHCO3 (66 мл). Слои разделяли и водную фазу экстрагировали с помощью DCM (33 мл). Объединенные органические вещества сушили над MgSO4, фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния; от 0 до 100% EtOAc/петролейный эфир элюирование в градиентном режиме). Фракции продукта объединяли и концентрировали в вакууме. Остаток сушили в течение ночи в вакууме и получали белое твердое вещество (7,92 г; 95%); 1H NMR (400 MHz, DMSO-d6) δ 7,45-7,31 (m, 5H), 7,31-7,19 (m, 1H), 5,12 (s, 2H), 4,37 (d, 1H), 4,18-3,94 (m, 1H), 3,38 (ddd, 1H), 3,00-2,80 (m, 4H), 2,68 (s, 2H), 2,15 (s, 2H), 0,95 (d, 3H); MS m/z: 377 (M+H)+.
Стадия 5: N-(((3S,5S)-4,4-Дифтор-5-метилпиперидин-3-ил)метил)метансульфонамид
[00407] К раствору бензил-(3S,5S)-4,4-дифтор-3-(метансульфонамидометил)-5-метилпиперидин-1-карбоксилата (7,54 г, 20 ммоля) в DCM (113 мл) добавляли Et3N (8,38 мл, 60 ммоля), затем Pd(OAc)2 (1,799 г, 8 ммоля). Добавляли Et3SiH (19,20 мл, 120 ммоля) в течение 5 мин. Раствор перемешивали при температуре окружающей среды в течение 1 ч, затем разделяли на 6 одинаковых порций и загружали в ионообменные картриджи (50 г). Картриджи промывали с помощью DCM, 1:1 MeOH:DCM и метанолом. Фильтраты отбрасывали. Картриджи промывали 2 M метанольным раствором аммиака. Фильтраты объединяли и концентрировали в вакууме. Остаток подвергали азеотропной перегонке с DCM, затем переносили в метанол (45 мл) и перемешивали с SPM32 (3-меркаптопропилэтилсульфид-диоксид кремния) в течение 2 ч при температуре окружающей среды, затем при 50°C в течение 1 ч. Смесь охлаждали и фильтровали через целит и фильтрат концентрировали в вакууме. Остаток переносили в DCM и концентрировали в вакууме. Остаток сушили в течение ночи в вакууме и получали N-(((3S,5S)-4,4-дифтор-5-метилпиперидин-3-ил)метил)метансульфонамид в виде белого твердого вещества (4,40 г, 91%); 1H NMR (400 MHz, DMSO-d6) δ 7,10 (t, 1H), 3,43-3,33 (m, 1H), 3,26-3,10 (m, 1H), 2,93-2,88 (m, 4H), 2,79 (dtd, 1H), 2,38-2,20 (m, 2H), 2,13-1,78 (m, 2H), 0,89 (d, 3H); MS m/z: 243,0 (M+H)+.
Синтез 17: N-(Пирролидин-3-илметил)метансульфонамид
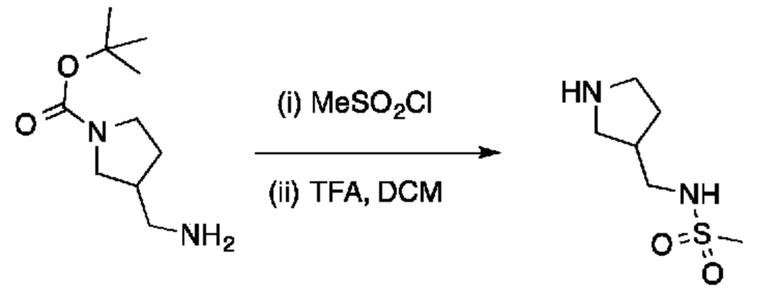
Стадия 1: трет-Бутил-3-(метансульфонамидометил)пирролидин-1-карбоксилат
[00408] Метансульфонилхлорид (222 мг, 150 мкл, 1,938 ммоля) при перемешивании добавляли к раствору трет-бутил-3-(аминометил)пирролидин-1-карбоксилата (300 мг, 1,498 ммоля) и триэтиламина (232,3 мг, 320 мкл, 2,296 ммоля) в THF (10 мл) в атмосфере азота и реакционную смесь перемешивали при температуре окружающей среды в течение 1,5 ч. Реакционную смесь разбавляли с помощью DCM и насыщенным водным раствором NaHCO3 и смесь перемешивали в течение 10 мин. Слои разделяли и водный слой экстрагировали с помощью DCM (×2). Объединенные органические экстракты сушили (MgSO4), фильтровали и концентрировали в вакууме и получали трет-бутил-3-(метансульфонамидометил)пирролидин-1-карбоксилат в виде бледно-желтого масла, из которого удаляли защитную группу при допущении о 100% выходе и чистоте; 1H NMR (500 MHz, DMSO-d6) δ 7,11 (t, J=6,2 Hz, 1H), 3,40-3,35 (m, 1H), 3,32-3,28 (m, 1H), 3,23-3,15 (m, 1H), 2,95-2,93 (m, 3H), 2,89 (s, 3H), 2,31-2,26 (m, 1H), 1,93-1,88 (m, 1H), 1,65-1,52 (m, 1H), 1,40 (s, 9H); ESV-MS m/z рассчитано 278,13004, найдено 223,1 (M+1)+.
Стадия 2: N-(Пирролидин-3-илметил)метансульфонамид
[00409] TFA (2,960 г, 2 мл, 25,96 ммоля) при перемешивании добавляли к раствору трет-бутил-3-(метансульфонамидометил)пирролидин-1-карбоксилата (417 мг, 1,498 ммоля) в DCM (20 мл) и реакционную смесь перемешивали при температуре окружающей среды в течение 15 ч. Растворитель удаляли в вакууме и остаток подвергали азеотропной перегонке с DCM (×2) и диэтиловым эфиром (×2). Остаток пропускали через 10 г картридж SCX-2 и промывали смесями MeOH/DCM. Продукт элюировали путем промывки картриджа смесями 2M NH3 в MeOH/DCM. Растворитель удаляли в вакууме и получали N-(пирролидин-3-илметил)метансульфонамид (227,4 мг, 85%) в виде бледно-желтого твердого вещества; 1H NMR (500 MHz, хлороформ-d) δ 3,16 (qd, J=12,3, 6,5 Hz, 2H), 3,09-3,03 (m, 2H), 2,98 (s, 3H), 2,94-2,89 (m, 1H), 2,75 (dd, J=10,7, 5,0 Hz, 1H), 2,40-2,32 (m, 1H), 2,04-1,96 (m, 1H), 1,55-1,48 (m, 1H). ; ESV-MS m/z 179,2 (M+1) +.
Синтез 18: 4-Пирролидин-3-ил-1H-пиразол
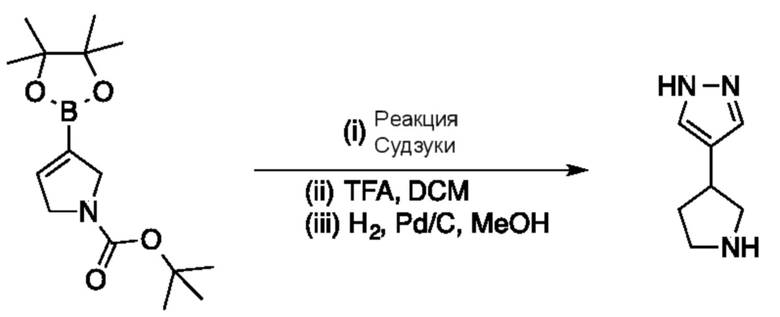
Стадия 1: трет-Бутил-3-(1H-пиразол-4-ил)-2,5-дигидропиррол-1-карбоксилат
[00410] трет-Бутил-4-бромпиразол-1-карбоксилат (230 мг, 0,931 ммоля) , трет-бутил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2,5-дигидропиррол-1-карбоксилат (250 мг, 0,847 ммоля) и карбонат калия (1,3 мл 2M, 2,60 ммоля) объединяли в диоксане (3 мл) и смесь дегазировали (×2 цикла вакуума). Добавляли Pd(dppf)Cl2.DCM (70 мг, 0,086 ммоля) и смесь дегазировали (×2 цикла вакуума), затем нагревали при 90°C в течение ночи. Реакционную смесь подвергали распределению между EtOAc и водой. Органическую фазу сушили (Na2SO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью хроматографии (диоксид кремния, 0-100% EtOAc/петролейный эфир элюирование в градиентном режиме). Фракции продукта объединяли и концентрировали и получали продукт в виде бледно-желтого пленкообразного вещества (65 мг, 33%), которое использовали в следующей реакции. ESV-MS m/z 236,0 (M+1) +.
Стадии 2 и 3: 4-Пирролидин-3-ил-1H-пиразол
[00411] трет-Бутил-3-(1H-пиразол-4-ил)-2,5-дигидропиррол-1-карбоксилат (550 мг, 2,338 ммоля) растворяли в DCM (10 мл) и добавляли TFA. Через 1 ч реакционную смесь концентрировали в вакууме и остаток подвергали азеотропной перегонке с DCM (×2). Остаток переносили в метанол (10 мл) и раствор дегазировали (×3 цикла вакуум - N2). Добавляли Pd на C, влажный, Degussa (200 мг 10% мас./мас., 0,188 ммоля) и смесь дегазировали (×3 цикла). Атмосферу N2 заменяли на водород (×3 цикла) и смесь перемешивали при температуре окружающей среды. Через 90 мин реакционную смесь фильтровали через целит, промывали метанолом. Фильтрат концентрировали в вакууме (холодная водяная баня) и получали неочищенный 4-пирролидин-3-ил-1H-пиразол (трифторацетат) (600 мг, количественный выход); ESV-MS m/z 136,0 (M+1) +.
Синтез 19: (E)-2-(2-Этоксивинил)-4-(метилтио)пиримидин
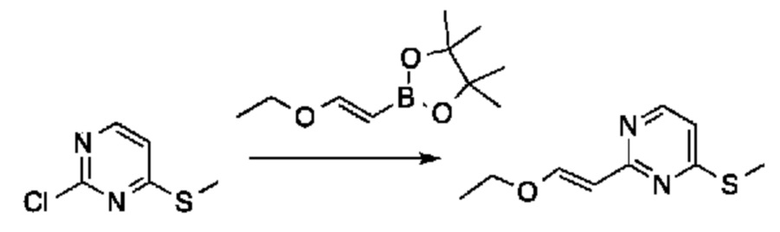
[00412] К суспензии 2-хлор-4-(метилтио)пиримидина (56,1 г, 349,3 ммоля) и 2 M водного раствора Na2CO3 (524 мл, 1,05 моля) в 1,2-диметоксиэтане (730 мл) добавляли 2-[(E)-2-этоксивинил]-4,4,5,5-тетраметил-1,3,2-диоксаборолан (76,1 г, 384 ммоля). Добавляли Pd(PPh3)4 (20,2 г, 17,5 ммоля) и смесь дегазировали. Реакционную смесь помещали в атмосферу азота и кипятили с обратным холодильником в течение 4 ч. Смесь охлаждали до температуры окружающей среды и подвергали распределению между EtOAc (1,1 л) и водой (560 мл). Органический слой промывали водой (2×560 мл), объединенные органические слои повторно экстрагировали с помощью EtOAc (280 мл) и объединенные органические фазы промывали рассолом (×1), сушили (MgSO4), фильтровали и концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии (диоксид кремния, при элюировании с помощью от 0 до 25% EtOAc/петролейный эфир) и получали (E)-2-(2-этоксивинил)-4-(метилтио)пиримидин в виде бледно-желтого кристаллического твердого вещества (62,4 г, 91%); 1H NMR (500 MHz, хлороформ-d) δ 8,18 (d, J=5,5 Hz, 1H), 7,95 (d, J=12,6 Hz, 1H), 6,85 (d, J=5,5 Hz, 1H), 5,91 (d, J=12,6 Hz, 1H), 4,02 (q, J=7,0 Hz, 2H), 2,56 (s, 3H), 1,40 (t, J=7,0 Hz, 3H); ES+ [M+H]= 197,1.
Синтез 20: 2-хлор-4-{6-циклопропилимидазо[1,2-a]пиридин-3-ил}пиримидин
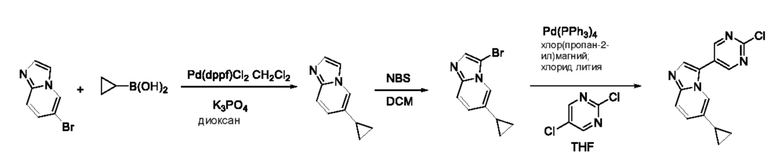
[00413] Стадия 1: 6-Циклопропилимидазо[1,2-a]пиридин. В круглодонную колбу объемом 150 мл помещали 6-бромимидазо[1,2-a]пиридин (5 г, 22,84 ммоля, 1 экв., 90%), циклопропилбороновую кислоту (3,1 г, 34,26 ммоля, 1,50 экв., 95%), Pd(dppf)Cl2.CH2Cl2 (2,0 г, 2,33 ммоля, 0,10 экв., 95%), диоксан (20 мл, 224,28 ммоля, 9,82 экв., 95%), K3PO4 (10,2 г, 45,68 ммоля, 2,00 экв., 95%). Полученный раствор перемешивали в течение в течение ночи при 100°C на масляной бане. Полученную смесь концентрировали. Остаток вводили в колонку с силикагелем, этилацетат/петролейный эфир (1/5). Это давало 3,6 г (89,67%) 6-циклопропилимидазо[1,2-a]пиридина в виде белого твердого вещества.
[00414] Стадия 2: 3-Бром-6-циклопропилимидазо[1,2-a]пиридин. В круглодонную колбу объемом 150 мл помещали 6-циклопропилимидазо[1,2-a]пиридин (3,6 г, 20,48 ммоля, 1 экв., 90%), NBS (3,8 г, 20,28 ммоля, 0,99 экв., 95%), DCM (20 мл, 298,87 ммоля, 14,59 экв., 95%). Полученный раствор перемешивали в течение 3 ч при 25°C. Полученную смесь концентрировали. Остаток вводили в колонку с силикагелем, этилацетат/петролейный эфир (1/5). Это давало 4,3 г (79,70%) 3-бром-6-циклопропилимидазо[1,2-a]пиридина в виде белого твердого вещества.
[00415] Стадия 3: 2-Хлор-4-{6-циклопропилимидазо[1,2-a]пиридин-3-ил}пиримидин. При перемешивании к раствору 3-бром-6-циклопропилимидазо[1,2-a]пиридина (1,5 г, 5,694 ммоля, 1 экв., 90%) в THF (10 мл, 117,259 ммоля, 21,0 экв., 95%) по каплям при -10°C в атмосфере азота добавляли iPrMgCl.LiCl (1,74 г, 11,388 ммоля, 2 экв., 95%). Полученную смесь перемешивали в течение 2 ч при 0°C в атмосфере азота. Полученную выше смесь при перемешивании добавляли к смеси 2,4-дихлорпиримидина (1,07 г, 6,824 ммоля, 1,20 экв., 95%) и Pd(PPh3)4 (0,35 г, 0,285 ммоля, 0,05 экв., 95%) в THF (10 мл, 117,259 ммоля, 21,0 экв., 95%) при комнатной температуре. Полученную смесь перемешивали в течение еще 4 ч при 70°C. Полученную смесь концентрировали. Остаток вводили в колонку с силикагелем, этилацетат/петролейный эфир (1/10). Это давало 1 г (58,39%) 2-хлор-4-[6-циклопропилимидазо[1,2-a]пиридин-3-ил]пиримидина в виде белого твердого вещества.
[00416] Следующие соединения получали по методологии, аналогичной описанной в синтезе 20:
2-Хлор-4-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин
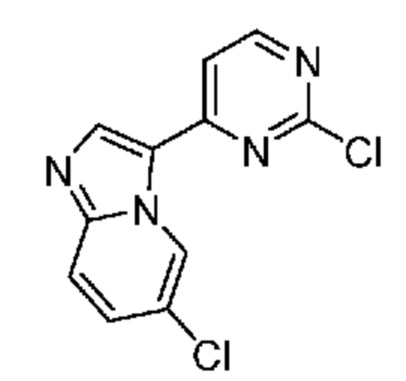
Синтез 21: 2-хлор-4-[(E)-2-этоксиэтенил]-6-метилпиримидин
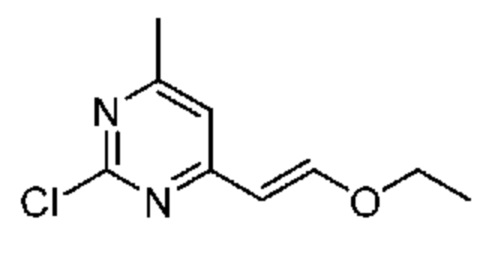
[00417] При перемешивании к раствору 2,4-дихлор-6-метилпиримидина (246,88 мг, 1,439 ммоля, 1,20 экв., 95%), 2-[(E)-2-этоксиэтенил]-4,4,5,5-тетраметил-1,3,2-диоксаборолана (250 мг, 1,199 ммоля, 1 экв., 95%) и K3PO4 (535,84 мг, 2,398 ммоля, 2,00 экв., 95%) в MeCN (12,45 мл, 303,230 ммоля, 187,63 экв., 95%) и H2O (4 мл, 210,932 ммоля, 364,96 экв., 95%) добавляли SPhos (36,27 мг, 0,084 ммоля, 0,07 экв., 95%) и Pd(AcO)2 (8,50 мг, 0,036 ммоля, 0,03 экв., 95%) при комнатной температуре в атмосфере азота. Полученную смесь перемешивали в течение в течение ночи при комнатной температуре в атмосфере азота. Полученную смесь концентрировали до небольшого объема. Полученную смесь разбавляли рассолом (20 мл). Полученную смесь экстрагировали с помощью EtOAc (3×50 мл). Объединенные органические слои промывали рассолом (2×20 мл), сушили над безводным MgSO4. После фильтрования фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью PE/EtOAc (5:1) и получали 2-хлор-4-[(E)-2-этоксиэтенил]-6-метилпиримидин(100 мг,37,78%) в виде светло-желтого масла.
Синтез 22: 2-хлор-4-[6-(3,3-дифторазетидин-1-ил)имидазо[1,2-a]пиридин-3-ил]-6-метилпиримидин
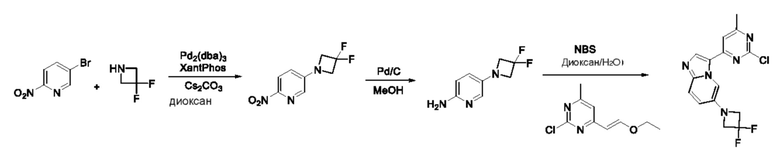
[00418] Стадия 1: 5-(3,3-дифторазетидин-1-ил)-2-нитропиридин. При перемешивании к раствору 5-бром-2-нитропиридина (500 мг, 2,340 ммоля, 1 экв., 95%), 3,3-дифторазетидингидрохлорида (350,95 мг, 2,574 ммоля, 1,1 экв., 95%) и Cs2CO3 (4012,66 мг, 11,700 ммоля, 5,00 экв., 95%) в диоксане (37,50 мл, 425,622 ммоля, 179,71 экв., 95%) добавляли Pd2(dba)3 (112,78 мг, 0,117 ммоля, 0,05 экв., 95%) и XantPhos (142,52 мг, 0,234 ммоля, 0,10 экв., 95%) при комнатной температуре в атмосфере азота. Полученную смесь перемешивали в течение 3 ч при 100°C в атмосфере азота. Полученную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью PE/EtOAc (1:1) и получали 5-(3,3-дифторазетидин-1-ил)-2-нитропиридин (200 мг, 27,81%) в виде светло-желтого твердого вещества.
[00419] Стадия 2: 5-(3,3-дифторазетидин-1-ил)пиридин-2-амин. При перемешивании к раствору 5-(3,3-дифторазетидин-1-ил)-2-нитропиридина (175 мг, 0,569 ммоля, 1 экв., 70%) в MeOH (56,00 мл, 1747,713 ммоля, 2307,89 экв., 95%) порциями при комнатной температуре в атмосфере азота добавляли Pd/C (318,89 мг, 2,847 ммоля, 5 экв., 95%). Полученную смесь перемешивали в течение в течение ночи при комнатной температуре в атмосфере водорода. Полученную смесь фильтровали, осадок на фильтре промывали с помощью MeOH (3×30 мл). Фильтрат концентрировали при пониженном давлении. Неочищенный продукт/полученную смесь использовали на следующей стадии без обработки без дополнительной очистки.
[00420] Стадия 3: 2-хлор-4-[6-(3,3-дифторазетидин-1-ил)имидазо[1,2-a]пиридин-3-ил]-6-метилпиримидин. При перемешивании к раствору 2-хлор-4-[(E)-2-этоксиэтенил]-6-метилпиримидина (550 мг, 2,630 ммоля, 1 экв., 95%) в H2O (18 мл, 999,151 ммоля, 379,87 экв., 9%) и H2O (18 мл, 999,151 ммоля, 379,87 экв., 9%) при комнатной температуре добавляли NBS (492,78 мг, 2,630 ммоля, 1 экв., 95%). Полученную смесь перемешивали в течение 1 ч при комнатной температуре. К полученной выше смеси добавляли 5-(3,3-дифторазетидин-1-ил)пиридин-2-амин (666,51 мг, 3,419 ммоля, 1,3 экв., 95%). Полученную смесь перемешивали в течение еще 2,5 ч при 85°C. Полученную смесь разбавляли с помощью EtOAc (20 мл). Смесь нейтрализовывали до pH 7 насыщенным раствором Na2CO3 (водным). Полученную смесь экстрагировали с помощью EtOAc (3×30 мл). Объединенные органические слои промывали рассолом (2×50 мл), сушили над безводным MgSO4. После фильтрования, фильтрат концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью CH2Cl2/MeOH (20:1). Это давало 2-хлор-4-[6-(3,3-дифторазетидин-1-ил)имидазо[1,2-a]пиридин-3-ил]-6-метилпиримидин(290 мг, 31,85%) в виде светло-желтого твердого вещества.
[00421] Следующие соединения получали по методологии, аналогичной описанной в синтезе 22:
2-Хлор-4-[6-(3-фторазетидин-1-ил)имидазо[1,2-a]пиридин-3-ил]пиримидин
Синтез 23: 5-[6-(азетидин-1-ил)имидазо[1,2-a]пиридин-3-ил]-2-хлорпиримидин
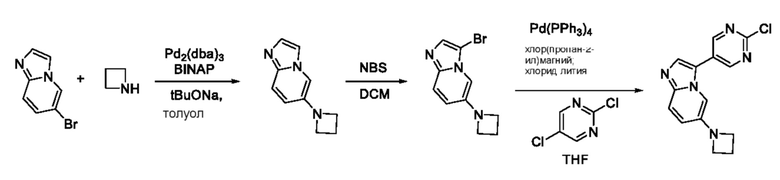
[00422] Стадия 1: 1-{имидазо[1,2-a]пиридин-6-ил}азетидин. В круглодонную колбу объемом 500 мл при комнатной температуре добавляли 6-бромимидазо[1,2-a]пиридин (3,5 г, 15,99 ммоля, 1 экв., 90%), азетидин (1441,3 мг, 23,98 ммоля, 1,50 экв., 95%), толуол (300 мл, 2678,69 ммоля, 167,55 экв., 95%), BINAP (1047,9 мг, 1,60 ммоля, 0,10 экв., 95%) и t-BuONa(3234,5 мг, 31,97 ммоля, 2,00 экв., 95%). Полученную смесь перемешивали в течение ночи при 100°C в атмосфере азота. Полученную смесь концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью PE/EtOAc (5:1) и получали 1-[имидазо[1,2-a]пиридин-6-ил]азетидин(2,5g,78,72%) в виде зеленого твердого вещества.
[00423] Стадия 2: 1-{3-бромимидазо[1,2-a]пиридин-6-ил}азетидин. В круглодонную колбу объемом 25 мл при комнатной температуре добавляли 1-[имидазо[1,2-a]пиридин-6-ил]азетидин (1 г, 5,03 ммоля, 1 экв., 87,2%), NBS(896,0 мг, 4,78 ммоля, 0,95 экв., 95%) и DCM (60 мл, 896,61 ммоля, 178,11 экв., 95%). Полученную смесь перемешивали в течение в течение ночи при комнатной температуре в атмосфере азота. Полученную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью PE/EtOAc (5:1) и получали 1-[3-бромимидазо[1,2-a]пиридин-6-ил]азетидин(1,1 г, 56,25%) в виде зеленого твердого вещества.
[00424] Стадия 3: 5-[6-(азетидин-1-ил)имидазо[1,2-a]пиридин-3-ил]-2-хлорпиримидин. При перемешивании к раствору 1-[3-бромимидазо[1,2-a]пиридин-6-ил]азетидина (200 мг, 0,777 ммоля, 1 экв., 98%) в THF(20 мл, 234,517 ммоля, 301,66 экв., 95%) по каплям при -10°C в атмосфере N2 добавляли хлор(пропан-2-ил)магнийхлорлитий (1 мл, 1,084 ммоля, 1,39 экв., 17,5%). Полученную смесь перемешивали в течение 2 ч при 0°C в атмосфере N2. Полученную выше смесь при перемешивании добавляли к смеси 2,4-дихлорпиримидина (182,86 мг, 1,166 ммоля, 1,50 экв., 95%) и Pd(PPh3)4 (47,28 мг, 0,039 ммоля, 0,05 экв., 95%) в THF при комнатной температуре. Полученную смесь перемешивали в течение еще 4 ч при 80°C. Реакцию останавливали насыщенным раствором NH4Cl (водным) при комнатной температуре. Водный слой экстрагировали с помощью EtOAc (3×20 мл). Полученную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью EA:PE (1:1) и получали 4-[6-(азетидин-1-ил)имидазо[1,2-a]пиридин-3-ил]-2-хлорпиримидин (120 мг, 19,61%) в виде зеленого твердого вещества.
Синтез 24: 5-(3-метил-1H-пиразол-4-ил)пиперидин-3-ол
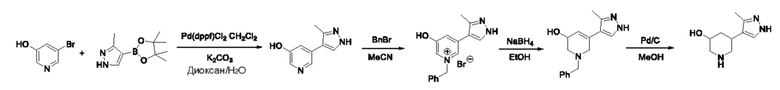
[00425] Стадия 1: 5-(3-Метил-1H-пиразол-4-ил)пиридин-3-ол. Смесь 5-бромпиридин-3-ола (10 г, 54,599 ммоля, 1 экв., 95%), Pd(dppf)Cl2.CH2Cl2 (2,35 г, 2,730 ммоля, 0,05 экв., 95%), K2CO3 (11,91 г, 81,898 ммоля, 1,50 экв., 95%) и 3-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиразола (14,35 г, 65,518 ммоля, 1,2 экв., 95%) в диоксане (150,01 мл, 1682,194 ммоля, 30,81 экв., 95%) и H2O (29,99 мл, 1664,971 ммоля, 28,97 экв., 95%) перемешивали в течение в течение ночи при 100°C в атмосфере азота. Полученную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью CH2Cl2/MeOH (10:1) и получали 5-(3-метил-1H-пиразол-4-ил)пиридин-3-ол (6,5g,61,16%) в виде коричневого твердого вещества.
[00426] Стадия 2: 1-Бензил-3-гидрокси-5-(3-метил-1H-пиразол-4-ил)пиридин-1-ийбромид. Смесь 5-(3-метил-1H-пиразол-4-ил)пиридин-3-ола (6,2 г, 31,851 ммоля, 1 экв., 90%) и BnBr (6,88 г, 0,038 ммоля, 1,2 экв., 95%) в MeCN (300,00 мл, 6942,365 ммоля, 170,23 экв., 95%) перемешивали в течение в течение ночи при 60°C в атмосфере водорода. Полученную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью CH2Cl2/MeOH (85:15) и получали 1-бензил-3-гидрокси-5-(3-метил-1H-пиразол-4-ил)пиридин-1-ийбромид (9 г, 73,45%) в виде коричневого твердого вещества.
[00427] Стадия 3: 1-Бензил-5-(3-метил-1H-пиразол-4-ил)-1,2,3,6-тетрагидропиридин-3-ол. Смесь 1-бензил-3-гидрокси-5-(3-метил-1H-пиразол-4-ил)пиридин-1-ийбромида (6,5 г, 16,896 ммоля, 1 экв., 90%) и NaBH4 (2,68 г, 67,296 ммоля, 3,98 экв., 95%) в EtOH (260,00 мл, 5643,864 ммоля, 251,64 экв., 95%) перемешивали в течение в течение ночи при комнатной температуре в атмосфере азота. Реакцию останавливали насыщенным раствором NH4Cl (водным) при комнатной температуре. Полученную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью CH2Cl2/MeOH (10:1) и получали 1-бензил-5-(3-метил-1H-пиразол-4-ил)-1,2,3,6-тетрагидропиридин-3-ол (5 г, 98,88%) в виде желтого масла.
[00428] Стадия 4: 5-(3-Метил-1H-пиразол-4-ил)пиперидин-3-ол. Смесь 1-бензил-5-(3-метил-1H-пиразол-4-ил)-1,2,3,6-тетрагидропиридин-3-ола (3,2 г, 10,692 ммоля, 1 экв., 90%) и Pd/C (1137,89 мг, 1,069 ммоля, 0,10 экв., 10%) в MeOH (200,00 мл, 5929,777 ммоля, 438,89 экв., 95%) перемешивали в течение 4 ч при комнатной температуре в атмосфере водорода. Полученную смесь фильтровали, осадок на фильтре промывали с помощью MeOH (3×5 мл). Фильтрат концентрировали при пониженном давлении и получали 5-(3-метил-1H-пиразол-4-ил)пиперидин-3-ол (2 г,92,88%) в виде бесцветного полужидкого вещества.
[00429] Следующие соединения получали по методологии, аналогичной описанной в синтезе 24:
3-(3-Фтор-1H-пиразол-4-ил)-5-метилпиперидин
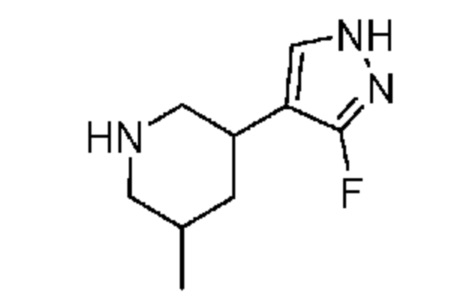
Пример 1: 3-(4-(3-((S-Метилсульфонимидоил)метил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-4
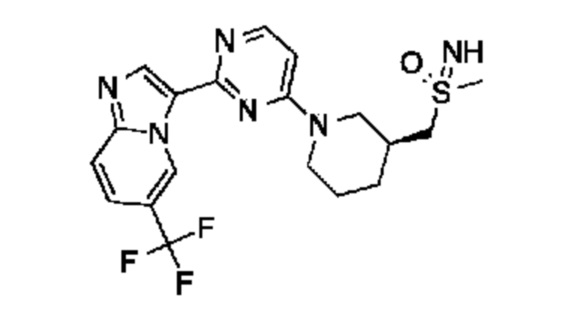
[00430] 3-(4-Хлорпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин (13,2 мг, 0,05 ммоля), 3-((S-метилсульфонимидоил)метил)пиперидин (8 мг, 0,045 ммоля), диизопропилэтиламин (8 мкл, 0,045 ммоля) в DMF нагревали при 80°C. Через 20 мин реакционную смесь охлаждали до комнатной температуры и смесь фильтровали и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,05% TFA в качестве элюента) и получали трифторацетат 3-(4-(3-((S-метилсульфонимидоил)метил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридина (12,7 мг, 40%).
[00431] Следующие соединения получали по методологии, аналогичной описанной в примере 1:
8-Метилсульфонил-1-[2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]-1,8-диазаспиро[4.5]декан, I-7
N-[[-4,4-Дифтор-5-метил-1-[2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]-3-пиперидил]метил]метансульфонамид, I-8
N-[[(2S)-4-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]морфолин-2-ил]метил]метансульфонамид, I-19 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
4-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-2-(1H-пиразол-4-ил)морфолин, I-20 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
6-Хлор-3-(4-(3-((метилсульфонимидоил)метил)пиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-21 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
4-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-2-(1H-пиразол-4-ил)морфолин, I-23 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридина)
4-[2-(6-Бром-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-2-(1H-пиразол-4-ил)морфолин, I-24 (с использованием 6-бром-7-фтор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридина)
N-[[1-[2-(6-Бром-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]пирролидин-3-ил]метил]метансульфонамид I-25 (с использованием 6-бром-7-фтор-3-(4-метилсульфанилпиримидин-2-ил)имидазо[1,2-a]пиридина)
1-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-1,4-диазепан-5-он I-26 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина);
6-Хлор-3-[4-[3-(1H-пиразол-4-ил)пирролидин-1-ил]пиримидин-2-ил]имидазо[1,2-a]пиридин I-27 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
6-Хлор-3-[4-[3-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-2-ил]имидазо[1,2-a]пиридин I-28 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
6-Хлор-3-[4-[3-диметилфосфорил-5-(1H-пиразол-4-ил)-1-пиперидил]пиримидин-2-ил]имидазо[1,2-a]пиридин I-29 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
((1-(2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)диметил-λ6-сульфанон I-30 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
N-[[-1-[4-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил]-4,4-дифтор-5-метил-3-пиперидил]метил]метансульфонамид, I-41 (с использованием 3-(2-хлорпиримидин-4-ил)-6-(дифторметил)имидазо[1,2-a]пиридина);
6-Хлор-7-фтор-3-[4-[3-(1H-имидазол-4-ил)-2,5-диметилпиперазин-1-ил]пиримидин-2-ил]имидазо[1,2-a]пиридин I-42 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридина)
7-[2-[6-(Трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]-1,2,5,6,8,8a-гексагидроимидазо[1,5-a]пиразин-3-он I-43 (с использованием 3-(4-хлорпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридина)
2-(1H-Пиразол-4-ил)-4-[4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил]морфолин I-44 (с использованием 3-(2-хлорпиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридина)
(3S)-1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]пиперидин-3-карбоксамид I-48 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридина)
((1-(2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)диметил-λ6-сульфанон I-49 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридина)
1-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-2,5-диметилпиперидин-3-карбоксамид I-50 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина);
1-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-2,5-диметилпиперидин-3-карбоксамид I-51 (с использованием 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина)
1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-2,5-диметилпиперидин-3-карбоксамид I-52 и 1-[2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил]-2,5-диметилпиперидин-3-карбоксамид I-53
Пример 2: 1H-Пиразол-4-ил-4-[2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]морфолин и 1H-пиразол-4-ил-4-[2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]морфолин, I-2 и I-3
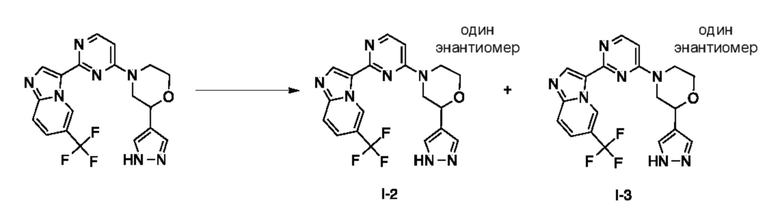
[00432] Рацемическую смесь 2-(1H-пиразол-4-ил)-4-[2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]морфолина (получали по методологии, аналогичной описанной в примере 107) разделяли с помощью хиральной надкритической жидкостной хроматографии (условия: OD-H, 45% MeOH, 20 мМ NH3, 290 нм). Первым элюирующимся соединением было соединение I-2 (99,3% ee); ESV-MS m/z 416,8 (M+H). Вторым элюирующимся соединением было соединение I-3 (98,2% ee); ESV-MS m/z 416,4 (M+H).
[00433] Следующие соединения получали по методологии, аналогичной описанной в примере 2:
7-(2-(6-(Трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)гексагидроимидазо[1,5-a]пиразин-3(2H)-он I-5
7-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)гексагидроимидазо[1,5-a]пиразин-3(2H)-он, I-6
2-(1H-Пиразол-4-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-9
2-(1H-пиразол-4-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-10
Диметил((5-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон I-31 и диметил((5-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон I-32
3-[2-[2,5-Диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-4-ил]-6-(трифторметил)имидазо[1,2-a]пиридин I-33 и 3-[2-[2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-4-ил]-6-(трифторметил)имидазо[1,2-a]пиридин I-34
6-Хлор-3-[4-[2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-2-ил]имидазо[1,2-a]пиридин I-35 и 6-хлор-3-[4-[2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-2-ил]имидазо[1,2-a]пиридин I-36
3-[4-[2,5-Диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-2-ил]-6-(трифторметил)имидазо[1,2-a]пиридин I-37 и 3-[4-[2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-2-ил]-6-(трифторметил)имидазо[1,2-a]пиридин I-38
3-[4-[3-Метил-5-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-2-ил]-6-(трифторметил)имидазо[1,2-a]пиридин I-39 и 3-[4-[3-метил-5-(1H-пиразол-4-ил)пиперазин-1-ил]пиримидин-2-ил]-6-(трифторметил)имидазо[1,2-a]пиридин I-40
Пример 3: N-[[(2S)-4-[2-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]морфолин-2-ил]метил]метансульфонамид, I-13
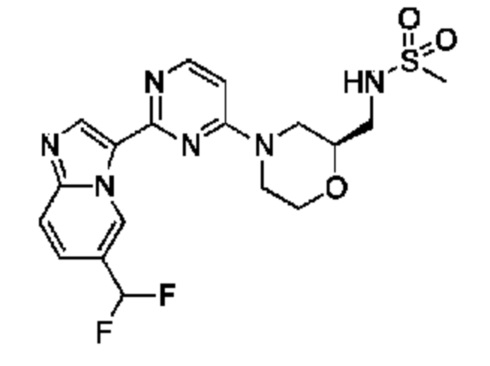
[00434] DBU (79,8 мкл, 0,534 ммоля) и PyBroP (124,5 мг, 0,267 ммоля) добавляли к раствору 2-[6-(дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ола (35 мг, 0,134 ммоля) в MeCN (700 мкл). Через 5 мин добавляли N-[[(2S)-морфолин-2-ил]метил]метансульфонамид (31,1 мг, 0,160 ммоля) и смесь нагревали при 40°C. Через 2 ч реакционную смесь охлаждали до комнатной температуры и смесь фильтровали и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,05% TFA в качестве элюента) и получали трифторацетат N-[[(2S)-4-[2-[6-(дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]морфолин-2-ил]метил]метансульфонамида (28,2 мг, 45%).
[00435] Следующие соединения получали по методологии, аналогичной описанной в примере 3:
N-[[(2S)-4-[2-[6-(Трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]морфолин-2-ил]метил]метансульфонамид, I-1 (с использованием 2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]-1H-пиримидин-6-она)
1-[4-[2-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]пиперазин-1-ил]этанон, I-14
4-[2-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил]-2-(1H-пиразол-4-ил)морфолин, I-15
N-(((3S,5S)-1-(2-(6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-4,4-дифтор-5-метилпиперидин-3-ил)метил)метансульфонамид, I-16
2-(1H-Пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-45
Пример 4: N-[[(2S)-4-[4-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил]морфолин-2-ил]метил]метансульфонамид, I-17
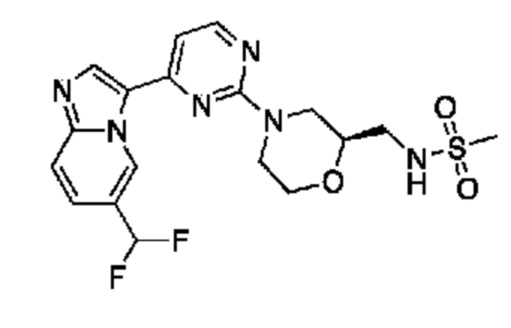
[00436] 3-Бром-6-(дифторметил)имидазо[1,2-a]пиридин (70 мг, 0,283 ммоля), трибутил-(2-хлорпиримидин-4-ил)станнан (137,3 мг, 0,340 ммоля) и PdCl2(PPh3)2 (59,7 мг, 0,085 ммоля) объединяли в DMF (2,1 мл) и дегазировали азотом, затем нагревали при 120°C. К смеси добавляли N-[[(2S)-морфолин-2-ил]метил]метансульфонамид (27,7 мг, 0,143 ммоля) и диизопропилэтиламин (49,6 мкл, 0,285 ммоля) и реакционную смесь нагревали при 150°C. Через 16 ч реакционную смесь охлаждали до комнатной температуры и смесь фильтровали и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,05% TFA в качестве элюента) и получали трифторацетат N-[[(2S)-4-[4-[6-(дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил]морфолин-2-ил]метил]метансульфонамида (6,5 мг, 5%).
[00437] Следующее соединение получали по методологии, аналогичной описанной в примере 4:
4-[4-[6-(Дифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил]-2-(1H-пиразол-4-ил)морфолин, I-18
Пример 5: 1-[4-[6-[6-(Трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]пиперазин-1-ил]этанон, I-11
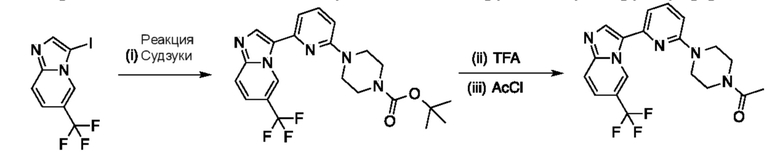
Стадия 1: трет-Бутил-4-[6-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]пиперазин-1-карбоксилат
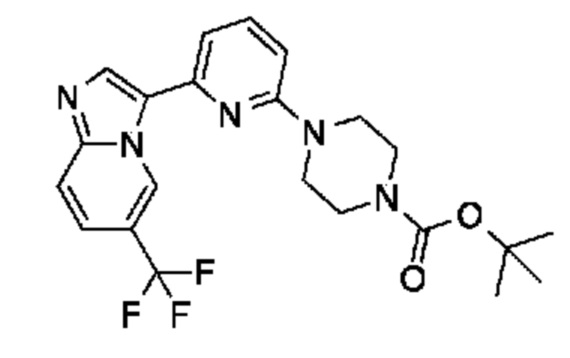
[00438] Смесь 3-йод-6-(трифторметил)имидазо[1,2-a]пиридина (50 мг, 0,160 ммоля), трет-бутил-4-[6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]пиперазин-1-карбоксилата (62,4 мг, 0,160 ммоля), dppf (8,8 мг, 0,016 ммоля), Pd(OAc)2 (1,8 мг, 0,008 ммоля), CuCl (15,9 мг, 0,160 ммоля) и Cs2CO3 (156,6 мг, 0,481 ммоля) в DMF (1 мл) дегазировали азотом и нагревали при 90°C в течение 16 ч. Реакционную смесь охлаждали до температуры окружающей среды, фильтровали через слой силикагеля и концентрировали при пониженном давлении и получали трет-бутил-4-[6-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]пиперазин-1-карбоксилат; ESV-MS m/z 448,2 (M+H). Вещество использовали без дополнительной очистки.
Стадия 2: 3-(6-Пиперазин-1-ил-2-пиридил)-6-(трифторметил)имидазо[1,2-a]пиридин
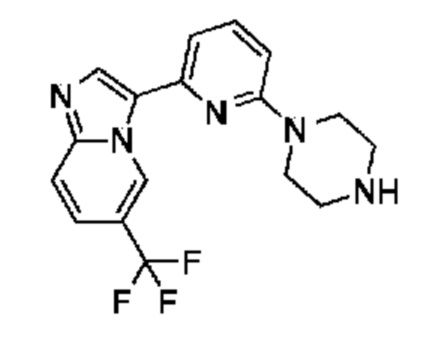
[00439] трет-Бутил-4-[6-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]пиперазин-1-карбоксилат растворяли в DCM (2 мл) и добавляли TFA (1 мл, 12,98 ммоля). Смесь перемешивали в течение 1 ч и затем концентрировали при пониженном давлении. Остаток растворяли в метаноле и очищали с помощью ионообменного картриджа SCX-2 и получали 3-(6-пиперазин-1-ил-2-пиридил)-6-(трифторметил)имидазо[1,2-a]пиридин; ESV-MS m/z 348,1 (M+H).
Стадия 3: 1-[4-[6-[6-(Трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]пиперазин-1-ил]этанон
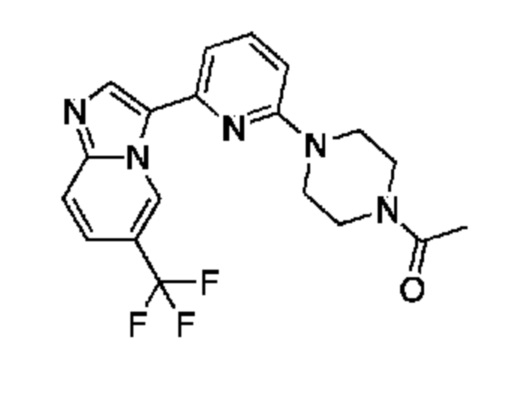
[00440] Ацетилхлорид (15 мкл, 0,208 ммоля) и триэтиламин (67 мкл, 0,481 ммоля) добавляли к раствору 3-(6-пиперазин-1-ил-2-пиридил)-6-(трифторметил)имидазо[1,2-a]пиридина в CH2Cl2 (1 мл) и перемешивали в течение 20 мин. Смесь концентрировали и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,05% TFA в качестве элюента) и получали трифторацетат 1-[4-[6-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]пиперазин-1-ил]этанона (5,5 мг, 5%).
Пример 6: 2-(1H-Пиразол-4-ил)-4-[6-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]морфолин, I-12
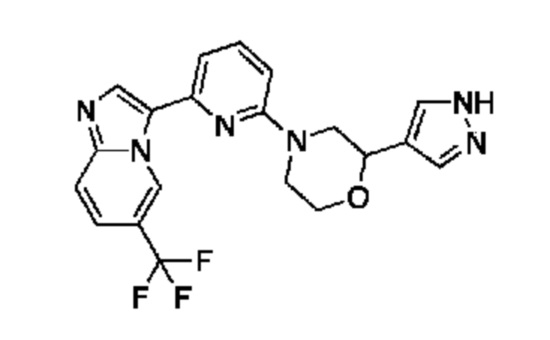
[00441] 3-Бром-6-(трифторметил)имидазо[1,2-a]пиридин (100 мг, 0,377 ммоля), 2-фтор-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (84,2 мг, 0,377 ммоля), dppf (20,6 мг, 0,038 ммоля), Pd(OAc)2 (4,2 мг, 0,0189 ммоля), CuCl (37,4 мг, 0,377 ммоля) и Cs2CO3 (368,8 мг, 1,132 ммоля) в DMF (2 мл) дегазировали азотом и нагревали при 90°C в течение 16 ч. Реакционную смесь охлаждали до температуры окружающей среды и фильтровали через слой силикагеля. Диизопропилэтиламин (48,8 мг, 66 мкл, 0,377 ммоля) и 2-(1H-пиразол-4-ил)морфолин (57,8 мг, 0,377 ммоля) добавляли прямо в фильтрат и смесь нагревали при 120°C в течение 16 ч. Реакционную смесь охлаждали до температуры окружающей среды, фильтровали и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,05% TFA в качестве элюента) и получали трифторацетат 2-(1H-пиразол-4-ил)-4-[6-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]-2-пиридил]морфолина (3,1 мг, 2%).
Пример 7: 4-[4-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-1,3,5-триазин-2-ил]-2-(1H-пиразол-4-ил)морфолин, I-22
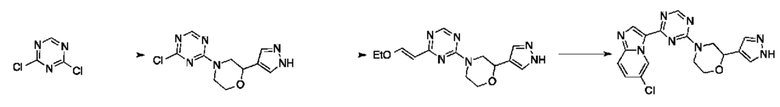
Стадия 1: 4-(4-Хлор-1,3,5-триазин-2-ил)-2-(1H-пиразол-4-ил)морфолин
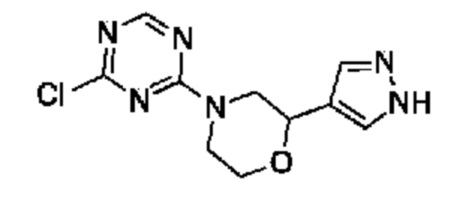
[00442] К раствору 2,4-дихлор-1,3,5-триазина (50 мг, 0,333 ммоля) и диизопропилэтиламина (128 мкл, 0,734 ммоля) в 1,4-диоксане (500 мкл) добавляли 2-(1H-пиразол-4-ил)морфолин (51,1 мг, 0,333 ммоля). Реакционную смесь перемешивали в течение 90 мин и затем подвергали распределению между DCM и водой, органические вещества экстрагировали, сушили (MgSO4), фильтровали и концентрировали и получали 4-(4-хлор-1,3,5-триазин-2-ил)-2-(1H-пиразол-4-ил)морфолин; ESV-MS m/z 267,1 (M+H). Вещество использовали без дополнительной очистки.
Стадия 2: 4-[4-[(E)-2-Этоксивинил]-1,3,5-триазин-2-ил]-2-(1H-пиразол-4-ил)морфолин
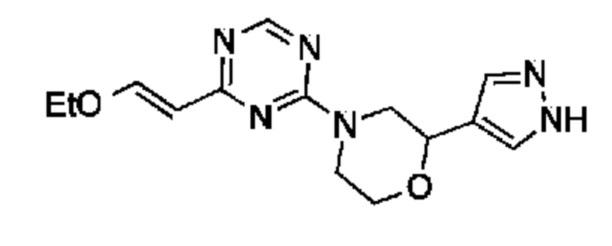
[00443] 4-(4-Хлор-1,3,5-триазин-2-ил)-2-(1H-пиразол-4-ил)морфолин растворяли в DME (750 мкл) и 2-(2-этоксивинил)-4,4,5,5-тетраметил-1,3,2-диоксаборолан (99 мг, 0,5 ммоля) и Na2CO3 (500 мкл 2M, 1 ммоля) добавляли. Смесь дегазировали с помощью циклов вакуум/азот (×3), затем Pd(PPh3)4 (38,5 мг, 0,033 ммоля) добавляли и смесь повторно дегазировали с помощью циклов вакуум/азот (×3). Смесь нагревали при 40°C в течение 2 ч. Реакционную смесь очищали с помощью колоночной хроматографии (диоксид кремния, EtOAc/петролейный эфир, в градиентном режиме) и получали 4-[4-[(E)-2-этоксивинил]-1,3,5-триазин-2-ил]-2-(1H-пиразол-4-ил)морфолин; ESV-MS m/z 303,2 (M+H).
Стадия 3: 4-[4-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-1,3,5-триазин-2-ил]-2-(1H-пиразол-4-ил)морфолин
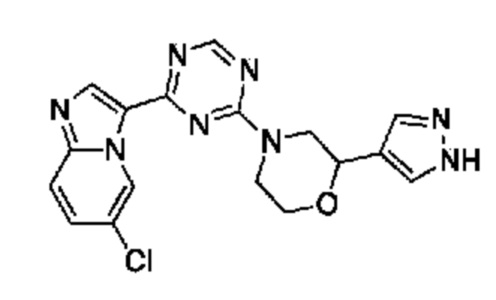
[00444] NBS (5,9 мг, 0,033 ммоля) добавляли к раствору 4-[4-[(E)-2-этоксивинил]-1,3,5-триазин-2-ил]-2-(1H-пиразол-4-ил)морфолин (10 мг, 0,033 ммоля) в 1,4-диоксане (300 мкл)/вода (100 мкл) и реакционную смесь перемешивали в течение 15 мин. 5-Хлорпиридин-2-амин (5,1 мг, 0,040 ммоля) затем добавляли и реакционную смесь нагревали при 65°C. Через 16 ч реакционную смесь охлаждали до температуры окружающей среды, фильтровали и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,05% TFA в качестве элюента) и получали трифторацетат 4-[4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-1,3,5-триазин-2-ил]-2-(1H-пиразол-4-ил)морфолина (4,9 мг, 26%).
Пример 8: ((1-(2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,5-диметилпиперидин-3-ил)метил)(имино)(метил)-λ6-сульфанон (транс-диастереоизомер), I-46
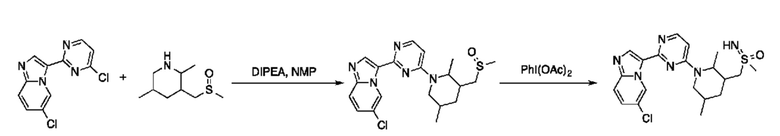
Стадия 1: 6-Хлор-3-[4-[2,5-диметил-3-(метилсульфинилметил)-1-пиперидил]пиримидин-2-ил]имидазо[1,2-a]пиридин (транс-диастереоизомер)
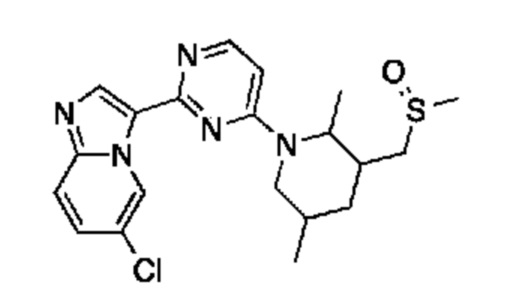
[00445] В сосуд для микроволновой печи помещали 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридин (30 мг, 0,113 ммоля), 2,5-диметил-3-(метилсульфинилметил)пиперидин (дигидрохлорид) (42 мг, 0,160 ммоля) , DIPEA (60 мкл, 0,345 ммоля) и NMP (900 мкл), затем герметизировали и нагревали при 100°C в течение 16 ч. Реакционной смеси давали охладиться, затем очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода - 0,1% гидроксид аммония в качестве элюента) и получали 6-хлор-3-[4-[2,5-диметил-3-(метилсульфинилметил)-1-пиперидил]пиримидин-2-ил]имидазо[1,2-a]пиридин (11 мг, 45%).
Стадия 2: ((1-(2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,5-диметилпиперидин-3-ил)метил)(имино)(метил)- λ6-сульфанон (транс-диастереоизомер)
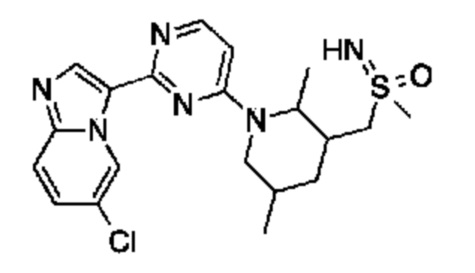
[00446] Метанол (375 мкл) добавляли к смеси 6-хлор-3-[4-[2,5-диметил-3-(метилсульфинилметил)-1-пиперидил]пиримидин-2-ил]имидазо[1,2-a]пиридина (11,2 мг, 0,144 ммоля) и (диацетоксийодо)бензола (34,7 мг, 0,108 ммоля), затем добавляли DCM (375 мкл). Реакционную смесь перемешивали при температуре окружающей среды в течение 3 ч. Неочищенную реакционную смесь фильтровали, затем очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода - 0,1% гидроксид аммония в качестве элюента) и получали ((1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,5-диметилпиперидин-3-ил)метил)(имино)(метил)- λ6-сульфанон (3 мг, 19%, транс-диастереоизомер) I-46.
[00447] Следующее соединение получали по методологии, аналогичной описанной в примере 8:
((1-(2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,5-диметилпиперидин-3-ил)метил)(имино)(метил)- λ6-сульфанон (цис-диастереоизомер), I-47
Пример 9: 6-хлор-3-{4-цис-2-метил-6-(3-метил-[1,2,4]оксадиазол-5-ил)-морфолин-4-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин, I-54
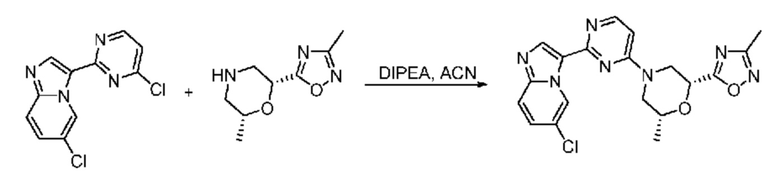
[00448] В сосуд для микроволновой печи, содержащий 6-хлор-3-(4-хлорпиримидин-2-ил)-имидазо[1,2-a]пиридин (50,00 мг; 0,19 ммоля; 1,00 экв.) и рац-(2r,6r)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)морфолингидрохлорид (41,43 мг; 0,19 ммоля; 1,00 экв.), добавляли DIPEA (0,11 мл; 0,66 ммоля; 3,50 экв.) и ацетонитрил (2,00 мл). Реакционную смесь перемешивали при 85°C в течение 2 ч, затем смесь разбавляли в 5 мл DMSO (частичное растворение), фильтровали и очищали в щелочной среде с помощью препаративной HPLC (C18,10-90% ACN/H2O/0,1% NH4OH в качестве элюента) и получали 6-хлор-3-{4-цис-2-метил-6-(3-метил-[1,2,4]оксадиазол-5-ил)-морфолин-4-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин (5,0 мг, 6,4%)
[00449] Следующие соединения получали по методологии, аналогичной описанной в примере 9:
6-Хлор-3-{4-[3-(1H-имидазол-4-ил)-пиперидин-1-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин, I-55
3-(2-((3R,5R)-3-Метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-136 (после хирального разделения)
3-(2-((3S,5S)-3-Метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-137 (после хирального разделения)
амид 5-метил-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты, I-149
амид (S)-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты, I-154
метиловый эфир 5,5-дифтор-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты, I-570
[00450] 2-[(3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил]-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин I-136 и 3-(2-((3S,5S)-3-Метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-137 очищали с помощью препаративной хиральной HPLC, как описано ниже:
[00451] (2-[(3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил]-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин (200 мг, 0,42 ммоля, 1 экв., 90%) очищали с помощью препаративной хиральной HPLC при следующих условиях (Колонка: Chiralpak IA, 2*25 см, 5 мкм; Подвижная фаза A: Гекс(8 ммоль/л NH3.MeOH)--HPLC, Подвижная фаза B: IPA--HPLC; Скорость потока: 20 мл/мин; Градиентный режим: от 20 B до 20 B за 25 мин; 254/220 нм; RT1:11,829). Это давало 116,2 мг (63,86%) 2-[(3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил]-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина I-136 в виде белого твердого вещества.
[00452] 2-[(3S,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил]-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин 200 мг, 0,42 ммоля, 1 экв., 90%) очищали с помощью препаративной хиральной HPLC при следующих условиях (Колонка: Chiralpak IA, 2*25 см, 5 мкм; Подвижная фаза A: Гекс(8 ммоль/л NH3.MeOH)--HPLC, Подвижная фаза B: IPA--HPLC; Скорость потока: 20 мл/мин; Градиентный режим: от 20 B до 20 B за 25 мин; 254/220 нм; RT2:19,149). Это давало 117,8 мг 2-[(3S,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил]-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин I-137 в виде белого твердого вещества
Пример 10: 6-Хлор-7-фтор-3-{4-[цис-2-метил-6-(3-метил-[1,2,4]оксадиазол-5-ил)-морфолин-4-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин, I-56
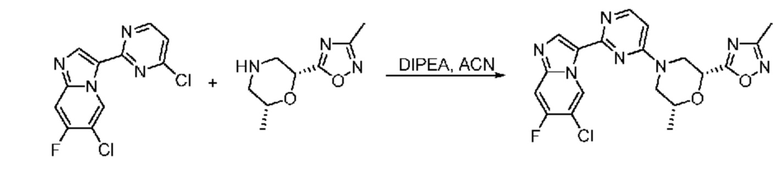
[00453] В сосуд для микроволновой печи, содержащий 6-хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридин (50,00 мг; 0,18 ммоля; 1,00 экв.) и рац-(2r,6r)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил) морфолингидрохлорид (38,80 мг; 0,18 ммоля; 1,00 экв.), добавляли DIPEA (0,10 мл; 0,62 ммоля; 3,50 экв.) и ацетонитрил (2,00 мл). Реакционную смесь перемешивали при 85°C в течение 2 ч. Белый осадок отфильтровывали, промывали с помощью H2O (2 мл×2), сушили и получали 6-хлор-7-фтор-3-{4-[цис-2-метил-6-(3-метил-[1,2,4]оксадиазол-5-ил)-морфолин-4-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин (75,9 мг, 79,2%).
[00454] Следующие соединения получали по методологии, аналогичной описанной в примере 10:
6-Хлор-7-фтор-3-{4-[3-(1H-имидазол-4-ил)-пиперидин-1-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин, I-57
3-{4-[(3S,5S)-3-Метил-5-(1-метил-1H-пиразол-4-ил)-пиперидин-1-ил]-пиримидин-2-ил}-6-трифторметилимидазо[1,2-a]пиридин (рацемическая смесь), I-60
3-{4-[(3R,5S)-3-Метил-5-(1-метил-1H-пиразол-4-ил)-пиперидин-1-ил]-пиримидин-2-ил}-6-трифторметилимидазо[1,2-a]пиридин (рацемическая смесь), I-61
1-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-(3-метил-[1,2,4]оксадиазол-5-ил)-пирролидин-3-ол, I-64
6-Хлор-3-[4-(3-изоксазол-4-илпиперидин-1-ил)-пиримидин-2-ил]-имидазо[1,2-a]пиридин, I-65
6-Хлор-3-[4-(3-изоксазол-3-илпиперидин-1-ил)-пиримидин-2-ил]-имидазо[1,2-a]пиридин, I-66
3-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-азабицикло[4.1.0]гептан-6-ол, I-67
4-{1-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-ил}-4-метилоксазолидин-2-он, I-68
1-Метил-4-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-[1,4]диазепан-2-он, I-69
3-{4-[(3aR,6aR)-3a-(3-Изопропил-[1,2,4]оксадиазол-5-ил)-гексагидроциклопента[c]пиррол-2-ил]-пиримидин-2-ил}-6-трифторметилимидазо[1,2-a]пиридин, I-70
3-[4-(3-Метилпиперидин-1-ил)-пиримидин-2-ил]-6-трифторметилимидазо[1,2-a]пиридин, I-71
1-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-(1-изопропил-1H-[1,2,3]триазол-4-ил)-пирролидин-3-ол, I-72
6-Хлор-3-{4-[(2S,3S)-2-(3-хлорфенил)-3-метилморфолин-4-ил]-пиримидин-2-ил}-7-фторимидазо[1,2-a]пиридин (рацемическая смесь), I-73
3-[2-(6-Трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-азабицикло[4.1.0]гептан-1-ол, I-74
6-Хлор-3-{4-[(3aR,6aR)-3a-(3-изопропил-[1,2,4]оксадиазол-5-ил)-гексагидроциклопента[c]пиррол-2-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин (рацемическая смесь), I-75
1-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-(1-изопропил-1H-[1,2,3]триазол-4-ил)-пиперидин-3-ол, I-76
(S)-1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты (1-метил-1H-пиразол-4-ил)-амид, I-77
5-[2-(6-Хлоримидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-5-азаспиро2.5]октан-1-карбоновая кислота, I-78
6-Хлор-3-[4-(7,7-дифтор-6-метил-3-азабицикло[4.1.0]гепт-3-ил)-пиримидин-2-ил]-имидазо[1,2-a]пиридин, I-79
4-[2-(6-Трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-[1,4]диазепан-2-он, I-80
1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-фенилпиперидин-3-ол, I-81
метиловый эфир 1-{1-[2-(6-хлоримидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-гидроксипиперидин-3-ил}-циклобутанкарбоновой кислоты, I-82
{1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-фенилпиперидин-4-ил}-метанол, I-83
6-Хлор-3-[4-(1-фенил-3-азабицикло[3.1.0]гекс-3-ил)-пиримидин-2-ил]-имидазо[1,2-a]пиридин, I-84
{1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-3-фенилпиперидин-3-ил}-метанол, I-85
Пример 11: (S)-1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновая кислота, I-58
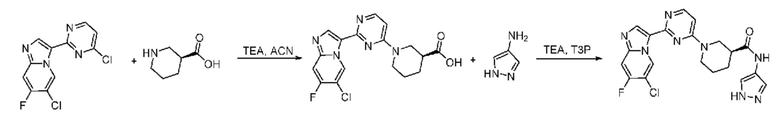
Стадия 1: (S)-1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновая кислота
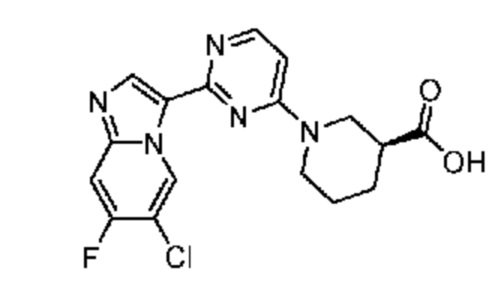
[00455] К раствору 6-Хлор-3-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридина (120,00 мг; 0,42 ммоля; 1,00 экв.) и (R)-(-)-нипеникотиновой кислоты (54,75 мг; 0,42 ммоля; 1,00 экв.) в ацетонитриле (2,00 мл) добавляли TEA (0,15 мл; 1,06 ммоля; 2,50 экв.) и перемешивали при 85°C в течение 3 ч. Белый осадок сушили и использовали на следующей стадии.
Стадия 2: (1H-Пиразол-4-ил)-амид (S)-1-[2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты
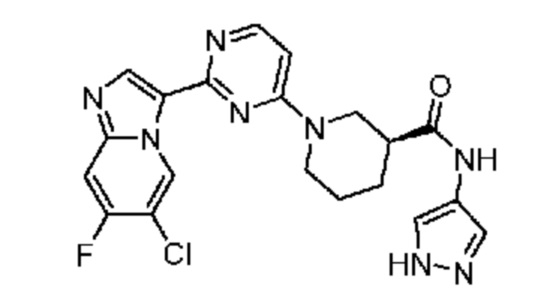
[00456] В круглодонную колбу, содержащую (S)-1-[2-(6-Хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновую кислоту (50,00 мг; 0,10 ммоля; 1,00 экв.) и 1H-пиразол-4-иламин (8,27 мг; 0,10 ммоля; 1,00 экв.) в DCM (2,00 мл) добавляли TEA (0,03 мл; 0,22 ммоля; 2,20 экв.). После перемешивания при КТ в течение 2 мин двумя порциями добавляли 1-пропанфосфоновый ангидрид (63,37 мг; 0,20 ммоля; 2,00 экв.). Реакционную смесь перемешивали при КТ в течение 15 мин, затем ее концентрировали, разбавляли смесью 2 мл MeOH/1 мл DMSO, фильтровали и очищали в щелочной среде с помощью препаративной HPLC (10-90% I/H2O/0,1% NH4OH в качестве элюента) и получали (1H-пиразол-4-ил)-амид (S)-1-[2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты (43,9 мг, 15,6%).
[00457] Следующие соединения получали по методологии, аналогичной описанной в примере 11:
(1-метил-1H-пиразол-4-ил)-амид (S)-1-[2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты, I-59
пиридин-4-иламид (S)-1-[2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты, I-86
Пример 12: (3S)-1-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)пиперидин-3-амин, I-87
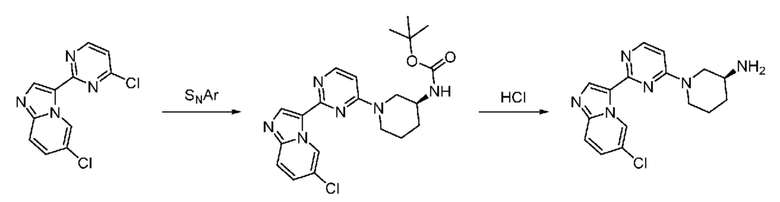
Стадия 1: трет-бутил-N-[(3S)-1-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)пиперидин-3-ил]карбамат
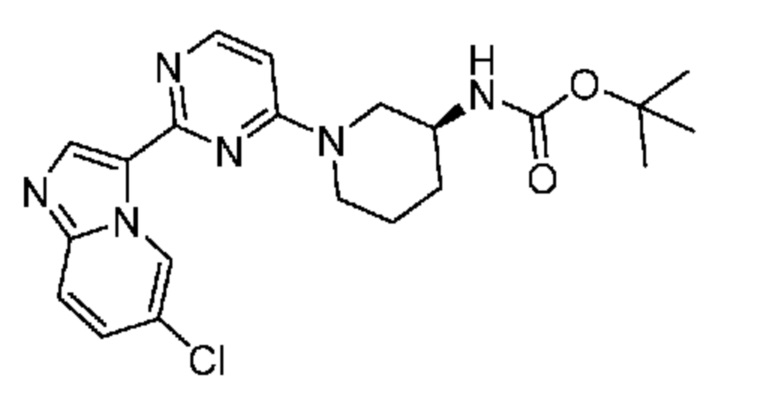
[00458] К смеси трет-бутил-N-[(3S)-пиперидин-3-ил]карбамата (195,3 мг, 0,98 ммоля) и 6-хлор-3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридина (198,8 мг, 0,75 ммоля) в DCM (3,75 мл) добавляли триэтиламин (0,21 мл, 1,50 ммоля). После перемешивания в течение ночи при комнатной температуре реакцию останавливали водой (3 мл) и экстрагировали с помощью DCM (2×5 мл). Объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и растворитель удаляли в вакууме и получали трет-бутил-N-[(3S)-1-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)пиперидин-3-ил]карбамат; ESI-MS m/z 429,2 (M+H). Вещество использовали без дополнительной очистки.
Стадия 2: (3S)-1-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)пиперидин-3-амин
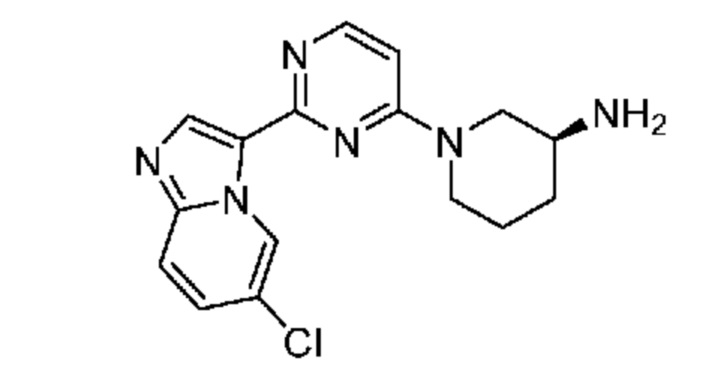
[00459] N-[(3S)-1-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)пиперидин-3-ил]карбамат растворяли в 1,4-диоксане (3 мл) и добавляли 4 н. HCl в 1,4-диоксане (3 мл, 35,2 ммоля). Смесь перемешивали в течение 1 ч при 40°C и затем концентрировали при пониженном давлении. Остаток растворяли в DMSO и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,01% NH4OH в качестве элюента) и получали (3S)-1-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)пиперидин-3-амин (72,7 мг, 29%).
Пример 13: 6-Хлор-7-фтор-3-[4-(2-пиридин-2-илморфолин-4-ил)-пиримидин-2-ил]-имидазо[1,2-a]пиридин, I-88
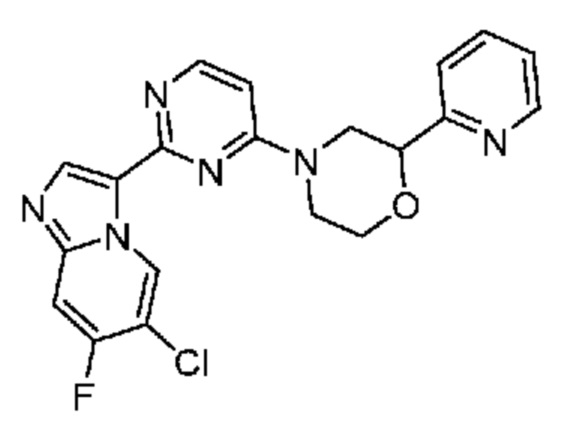
[00460] 6-Хлор-4-(4-хлорпиримидин-2-ил)-7-фторимидазо[1,2-a]пиридин (50,0 мг, 0,18 ммоля), 2-(пиридин-2-ил)морфолин (35,0 мг, 0,21 ммоля), триэтиламин (20 мкл, 0,18 ммоля) в DMF (1,0 мл) нагревали при 80°C. Через 14 ч реакционную смесь охлаждали до комнатной температуры и смесь фильтровали и очищали с помощью хроматографии с обращенной фазой (C18; MeCN/вода/0,01% NH4OH в качестве элюента) и получали 6-хлор-7-фтор-3-[4-(2-пиридин-2-илморфолин-4-ил)-пиримидин-2-ил]-имидазо[1,2-a]пиридин (11,1 мг, 16%).
[00461] Следующие соединения получали по методологии, аналогичной описанной в примере 13:
цис-2-метил-6-(5-метил-1,3,4-оксадиазол-2-ил)-4-{2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил}морфолин, I-93 (с использованием 3-(4-хХлорпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридина)
3-{4-[цис-2-метил-6-(5-метил-1,3,4-оксадиазол-2-ил)морфолин-4-ил]пиримидин-2-ил}имидазо[1,2-a]пиридин-6-карбонитрил, I-94 (с использованием 3-(4-хлорпиримидин-2-ил)имидазо[1,2-a]пиридин-6-карбонитрила)
цис-4-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-2-метил-6-(5-метил-1,3,4-оксадиазол-2-ил)морфолин, I-95 (с использованием 4-хлор-2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидина)
2-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-октагидро-1H-пиразино[1,2-c]пиримидин-6-он, I-96 (с использованием 4-хлор-2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидина)
7-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-октагидроимидазо[1,5-a]пиразин-3-он, I-97 (с использованием 4-хлор-2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидина)
2-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-октагидропиразино[1,2-c][1,3]оксазин-6-он, I-98 (с использованием 4-хлор-2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидина)
7-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-гексагидро-1H-[1,3]оксазоло[3,4-a]пиразин-3-он, I-99 (с использованием 4-хлор-2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидина)
2-{6-хлоримидазо[1,2-a]пиридин-3-ил}-4-[3-(1H-пиразол-4-ил)пиперидин-1-ил]пиримидин, I-100 (с использованием 4-хлор-2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидина)
4-[3-(1H-пиразол-4-ил)пиперидин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин, I-101 (с использованием 3-(4-Хлорпиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридина)
Пример 14: 2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)-4-{2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил}морфолин , I-89 и I-90
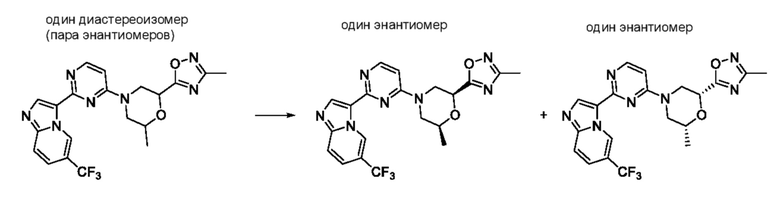
[00462] Рацемическую смесь цис-(2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)-4-{2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил}морфолина (получали по методологии, аналогичной описанной в примере 1) разделяли с помощью хиральной надкритической жидкостной хроматографии (условия: IA-H, MeOH+0,5% DMEA, 2 мл/мин, 220 нм). Первым элюирующимся соединением было соединение I-89 (98% ee); ESI-MS m/z 446,2 (M+H). Вторым элюирующимся соединением было соединение I-90 (98% ee); ESI-MS m/z 446,2 (M+H).
[00463] Следующие соединения получали по методологии, аналогичной описанной в примере 14:
3-{4-[(2S,6S)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)морфолин-4-ил]пиримидин-2-ил}имидазо[1,2-a]пиридин-6-карбонитрил, I-91 и 3-{4-[(2R,6R)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)морфолин-4-ил]пиримидин-2-ил}имидазо[1,2-a]пиридин-6-карбонитрил, I-92
Пример 15: Типичные соединения I-102 - I-113.
[00464] Дополнительные соединения получали по методологиям, аналогичным описанным выше в примерах 1-14:
(S)-1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-102
N-(((3S,5S)-1-(3-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-5-ил)-4,4-дифтор-5-метилпиперидин-3-ил)метил)метансульфонамид, I-103
2-(1H-пиразол-4-ил)-4-(3-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-5-ил)морфолин, I-104
4-(3-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-5-ил)-2-(1H-пиразол-4-ил)морфолин, I-105
(S)-N-((4-(3-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-5-ил)морфолин-2-ил)метил)метансульфонамид, I-106
(S)-N-((4-(3-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-5-ил)морфолин-2-ил)метил)метансульфонамид, I-107
2-(1H-пиразол-4-ил)-4-(5-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-3-ил)морфолин, I-108
(S)-N-((4-(5-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-3-ил)морфолин-2-ил)метил)метансульфонамид, I-109
N-((1-(5-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-3-ил)пиперидин-3-ил)метил)метансульфонамид, I-110
(S)-N-((4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)тиазол-2-ил)морфолин-2-ил)метил)метансульфонамид, I-111
N-((1-(3-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)-1,2,4-тиадиазол-5-ил)пиперидин-3-ил)метил)метансульфонамид, I-112
(S)-N-((4-(6-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиразин-2-ил)морфолин-2-ил)метил)метансульфонамид, I-113
Пример 16: 6-хлор-3-{4-цис-2-метил-6-(3-метил-[1,2,4]оксадиазол-5-ил)-морфолин-4-ил]-пиримидин-2-ил}-имидазо[1,2-a]пиридин, I-114
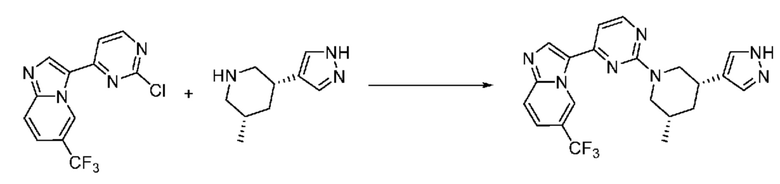
[00465] В герметизированную пробирку объемом 25 мл помещали 2-хлор-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин (200,000 мг, 0,60 ммоля, 1,00 экв., 90%), 3-метил-5-(1H-пиразол-4-ил)пиперидин (110,658 мг, 0,60 ммоля, 1,00 экв., 90%), DIEA (163,993 мг, 1,21 ммоля, 2,00 экв., 95%), изопропанол (10,000 мл, 124,30 ммоля, 206,24 экв., 95%). Полученный раствор перемешивали в течение в течение ночи при 100°C. Полученную смесь концентрировали в вакууме. Неочищенный продукт (300 мг) очищали с помощью препаративной HPLC при следующих условиях (Prep-HPLC-015): Колонка, XBridge Shield RP18 OBD Колонка, 30*150 мм, 5 мкм; подвижная фаза, вода (10 ммоль/л NH4HCO3+0,1%NH3.H2O) и ACN (от 43,0% ACN до 47,0% за 9 мин); Детектор, uv 254 нм. Это давало 23,9 мг (9%) 2-[3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил]-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина I-114 в виде белого твердого вещества.
[00466] Следующие соединения получали по методологии, аналогичной описанной в примере 16:
цис-2-Метил-6-(3-метил-1H-пиразол-4-ил)-4-{4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил}морфолин, I-115
цис-2-Метил-6-(1H-пиразол-4-ил)-4-{4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил}морфолин, I-117
3-{4-[цис-2-Метил-6-(3-метил-1H-пиразол-4-ил)-морфолин-4-ил]-пиримидин-2-ил}-6-трифторметилимидазо[1,2-a]пиридин, I-119
Таблица 2: Данные анализа соединений формулы I
[00467] Чистоту и время удерживания соединений, предлагаемых в настоящем изобретении, определяли с помощью HPLC.
[00468] Методика HPLC: аналитическую UPLC-MS с обращенной фазой проводили с помощью системы Waters Acquity UPLC-MS, снабженной колонкой с обращенной фазой Waters BEH 1,7 мм C-18 (2,1 мм×50 мм, 1,7 мкм). Подвижными фазами были ацетонитрил и вода/ацетонитрил (95:5 с добавлением 10 мМ формиата аммония, pH 9). Продолжительность исследования 5 мин
10,16 (m, 1H), 8,47 (s, 1H), 8,25 (d, 1H), 7,79 (d, 1H), 7,50 (d, 1H), 7,31 (m, 4H), 7,24 (m, 1H), 6,5 (m, 1H), 4,07 (m, 1H), 2,22 (m, 1H), 1,25 (m, 1H), 1,0 (m, 1H). Несколько пиков перекрываются с пиком растворителя.
Пример 17: Исследование ингибирования фермента GCN2
[00469] Скрининг способности соединений ингибировать активность GCN2 киназы проводили помощью анализа поляризации флуоресценции Transcreener® ADP2, при котором определяются содержания ADP (BellBrook Labs, WI). Исследования проводили в буфере, содержащем 25 мМ Tris-HCl (pH 7,5), 50 мМ NaCl, 10 мМ MgCl2 и 1 мМ DTT. Конечные концентрации субстрата равнялись 280 мкМ ATP и 200 мкМ пептидного субстрата (H-Gly-Arg-Ser-Arg-Ser-Arg-Ser-Arg-Ser-Arg-Ser-Arg-Ser-Arg-Ser-Arg-OH [(RS)7], Bachem, Switzerland). Исследования проводили при 25°C в присутствии GCN2 киназы в (типичной) конечной концентрации, равной 4 нМ.
[00470] Готовили буфер для анализа, содержащий GCN2 киназу и (RS)7. По 4,7 мкл этого исходного раствора помещали в лунки черного малообъемного 384-луночного планшета для микротитрования (например, catalogue number 3676, Corning Inc., NY). К этому добавляли 0,65 мкМ содержащих DMSO серийных разведений исследуемого соединения (типичные конечные концентрации исследуемого соединения равнялись от 0 до 8 мкМ). Планшет инкубировали в течение 10 мин при 25°C и затем добавляли 4,7 мкл ATP исходного буферного раствора для инициирования реакции фермента. Реакции давали протекать в течение 1 ч при 25°C, затем добавляли 10 мкл детектирующего буфера (содержащего в подходящих концентрациях ADP2 антитела и ADP Alexa633 меченое соединение в 1×стоп и детектирующий буфер, поставляемый фирмой BellBrook Labs). Реакционную смесь выдерживали для инкубирования в течение 1 ч при 25°C, затем для каждой лунки измеряли сигнал поляризации флуоресценции (mP) с помощью считывающего устройства PHERAstar FS (BMG Labtech, Germany).
[00471] Значения для поляризации флуоресценции нормировали на калибровочную зависимость для планшета для разных отношений количества ATP к количеству ADP в буфере для анализа до конечной полной концентрации, равной 280 мкМ. В планшет добавляли 9,4 мкл буфера при каждом отношении ATP:ADP и 0,65 мкл DMSO до добавления детектирующего буфера для имитации объемов и условий исследования. Калибровочную кривую использовали для пересчета значений mP, полученных для лунок с исследуемым веществом, в выраженную в процентах долю ATP, превратившегося в ADP. Затем для дозы каждого соединения рассчитывали выраженную в процентах степень ингибирования активности фермента. Значения IC50 и Ki(app) (с использованием известных параметров анализа и кинетических параметров) рассчитывали по данными степени ингибирования в процентах с использованием нелинейного алгоритма сильной связи. Все данные анализа обрабатывали с помощью программного обеспечения Screener® (Genedata, Switzerland).
Таблица 3: Активность по отношению к ферментам соединений формулы I
[00472] +++ для Ki<10 нМ; ++ для Ki в диапазоне 10 нМ-100 нМ; и+для Ki 100 нМ-1 мкМ.
Таблица 4: Активность по отношению к ферментам соединений формулы I
[00473] +++ для IC50 <10 нМ; ++ для IC50 в диапазоне 10 нМ-100 нМ; + для IC50 100 нМ-1 мкМ.
Пример 18: Исследование ингибирования GCN2 в клетках
[00474] Можно провести скрининг способности соединений ингибировать внутриклеточную GCN2 помощью анализа AlphaScreen (Perkin Elmer) для регистрации фосфорилирования субстрата eIF2α для GCN2 в обработанных боррелидином клетках. Клетки U2OS помещали в планшет по 5000 клеток/лунка в 384-луночные белые планшеты из полистирола (Corning 3570) в средах McCoy’s 5A (GIBCO 26600-023) с добавкой 10% фетальной бычьей сыворотки (SAFC 12103C), раствора пенициллин/стрептомицин, разведенного в отношении 1:100 (Sigma P0781) и 2 мМ L-глутамин (Sigma G7513) и давали слипаться в течение ночи при 37°C в 5% CO2. Соединения, затем добавляли к клеточным средам от конечной концентрации, равной 40 мкМ, в 4-кратных серийных разведениях. Боррелидин (FluoroChem M01440) сразу добавляли в лунки до конечной концентрации, равной 10 мкМ, и клетки инкубировали в течение 1 ч при 37°C в 5% CO2. После обработки боррелидином в течение 1 ч среды удаляли и клетки лизировали в литическом буфере (TGR BioSceinces TGRLB) при температуре окружающей среды.
[00475] Набор для анализа AlphaScreen SureFire P-eIF2α (Ser51) (Perkin Elmer TGREIF2S) использовали для определения содержания eIF2α, фосфорилированного по серину 51. Антифосфорилированные eIF2α Ser51 связанные с антителами акцепторные шарики (TGR BioScience 6760617) добавляли к гомогенизату клеток (разведение 1:250 в смеси активатора (TGR BioScience TGRAB) и реакционного буфера (TGR BioScience TGREIF2S), приготовленной непосредственно перед использованием). Затем планшет инкубировали в течение 2 ч при температуре окружающей среды в темноте. Затем добавляли связанные с антителами к eIF2α донорные шарики (TGR BioScience 6760617) (разводили 1:100 в буфере для разведения (TGR BioScience TGRDB), приготовленные непосредственно перед использованием). Затем планшет инкубировали в течение ночи при температуре окружающей среды в темноте.
[00476] Затем планшеты исследовали с помощью совместимого с Alpha Technology считывающего стройства для планшета PHERAstar FS (BMG Labtech Version 1.14) для количественного определения содержания фосфорилированного eIF2α Ser51. Выраженную в процентах степень ингибирования фосфорилированного eIF2α рассчитывали на основе сопоставления с контрольными лунками, стимулированными только боррелидином. Построены зависимости этих данных от концентрации соединения и IC50 определяли с помощью программного обеспечения Genedata Analyzer (Genedata AG Version 12.0.3).
Таблица 5: Активность по отношению к клеткам соединений формулы II (анализ биомаркера)
[00477] +++ для IC50<0,5 мкМ; ++ для IC50 в диапазоне 0,5 мкМ-5 мкМ; и+для IC50 >5 мкМ.
Пример 19: 4-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид, I-484
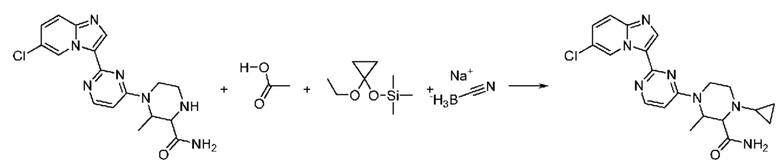
[00478] К раствору 4-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид I-451 (49,00 мг; 0,13 ммоля; 1,00 экв.) и 1-ethoxycyclopropoxy)триметилсилан (0,13 мл; 0,66 ммоля; 5,00 экв.) в метаноле (2,50 мл; 61,72 ммоля; 468,32 экв.) добавляли уксусную кислоту (0,06 мл; 1,05 ммоля; 8,00 экв.) и затем цианоборогидрид натрия (66,25 мг; 1,05 ммоля; 8,00 экв.). Реакционную смесь перемешивали в течение ночи при 70°C и очищали с помощью препаративной HPLC (10-90% ACN/NH4OH-H2O за 12 мин) и получали 4-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид (17,6 мг, 31%) в виде белого твердого вещества.
Пример 20: 5,5-Дифтор-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты амид, I-202
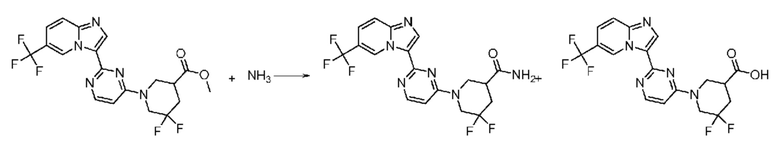
[00479] В сосуд для микроволновой печи, содержащий метиловый эфир 5,5-дифтор-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты (118,23 мг; 0,27 ммоля; 1,00 экв.), добавляли аммиак 7 н. в MeOH (2,00 мл). Реакционную смесь перемешивали при 100°C в течение 72 ч, затем ее очищали с помощью препаративной HPLC (10-90% ACN/0,1%NH4OH-H2O за 12 мин) и получали амид 5,5-дифтор-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты (2,2 мг, 1,9%) в виде белого твердого вещества.
Пример 21: 3-{2-[(2R,6S)-2-Метил-6-(1H-пиразол-4-ил)-морфолин-4-ил]-пиримидин-4-ил}-6-трифторметилимидазо[1,2-a]пиридин I-127 и (2S,6R)-2-метил-6-(1H-пиразол-4-ил)-4-{4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил}морфолин I-126
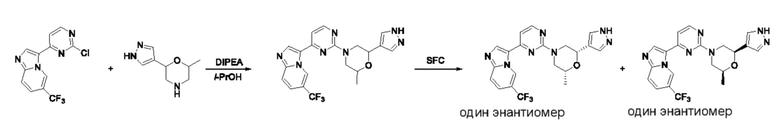
[00480] Стадия 1: 2-Метил-6-(1H-пиразол-4-ил)-4-{4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил}морфолин. Раствор 2-хлор-4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина (200 мг, 0,60 ммоля, 1 экв., 90%), 2-метил-6-(1H-пиразол-4-ил)морфолина (112,0 мг, 0,60 ммоля, 1 экв., 90%) и DIPEA (155,8 мг, 1,21 ммоля, 2 экв., 95%) в i-PrOH (10 мл, 124,30 ммоля, 206,24 экв., 95%) перемешивали в течение 16 ч при 100°C в атмосфере азота. Полученную смесь концентрировали в вакууме. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали смесью гексан/EtOAc (1:1) и получали 2-метил-6-(1H-пиразол-4-ил)-4-[4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил]морфолин (100 мг, 34,77%) в виде белого твердого вещества.
[00481] Стадия 2: 3-{2-[(2R,6S)-2-Метил-6-(1H-пиразол-4-ил)-морфолин-4-ил]-пиримидин-4-ил}-6-трифторметилимидазо[1,2-a]пиридин и (2S,6R)-2-метил-6-(1H-пиразол-4-ил)-4-{4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил}морфолин. Рацемическую смесь 2-метил-6-(1H-пиразол-4-ил)-4-[4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил]морфолина очищали с помощью хиральной препаративной HPLC при следующих условиях (Prep-HPLC-032): Колонка, Chiralpak IA, 2*25 см, 20 мкм; подвижная фаза, Гекс(8 ммоль/л NH3.MeOH)--HPLC и IPA--HPLC (15% IPA--HPLC в течение 29 мин); Детектор, UV 254/220 нм. Получали два чистых соединения: пик 1 3-{2-[(2R,6S)-2-Метил-6-(1H-пиразол-4-ил)-морфолин-4-ил]-пиримидин-4-ил}-6-трифторметилимидазо[1,2-a]пиридин I-127, время удерживания =18,029 мин, 10,6 мг (22%), белое твердое вещество; пик 2 (2S,6R)-2-метил-6-(1H-пиразол-4-ил)-4-{4-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-2-ил}морфолин I-126, время удерживания=25,76 мин, 12,3 мг (25%), белое твердое вещество.
Пример 22: 3-{4-[(S)-4-(3-Метансульфонилциклобутил)-3-(1H-пиразол-4-ил)-пиперазин-1-ил]-пиримидин-2-ил}-6-трифторметилимидазо[1,2-a]пиридин I-495 и 3-{4-[(R)-4-(3-Метансульфонилциклобутил)-3-(1H-пиразол-4-ил)-пиперазин-1-ил]-пиримидин-2-ил}-6-трифторметилимидазо[1,2-a]пиридин I-490
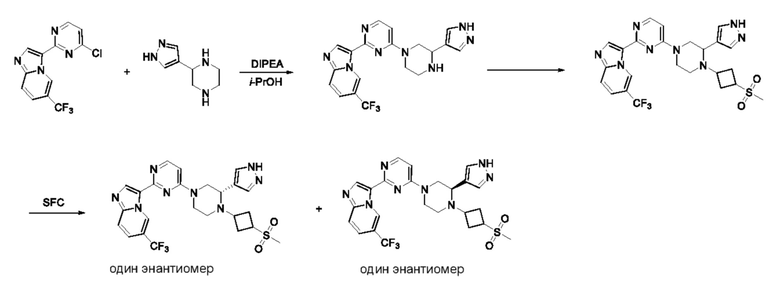
[00482] Стадия 1: 4-[3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин. При перемешивании к смеси 4-хлор-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина (600,00 мг, 1,808 ммоля, 1,00 экв., 90%) и 2-(1H-пиразол-4-ил)пиперазина (458,67 мг, 2,712 ммоля, 1,50 экв., 90%) в i-PrOH (15,00 мл, 245,293 ммоля, 271,32 экв., 95%) по каплям при комнатной температуре в атмосфере азота добавляли DIEA (491,98 мг, 3,616 ммоля, 2,00 экв., 95%). Полученную смесь перемешивали в течение 3 ч при 100°C в атмосфере азота. Искомый продукт можно было обнаружить с помощью LCMS. Полученную смесь концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, элюировали с помощью CH2Cl2/MeOH (8:1) и получали 4-[3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин (510 мг, 61,26%) в виде светло-желтого масла.
[00483] Стадия 2: 4-[4-(3-метансульфонилциклобутил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин. При перемешивании к смеси 4-[3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина (100,00 мг, 0,217 ммоля, 1,00 экв., 90%) и 3-метаносульфонилциклобутан-1-она (169,38 мг, 1,086 ммоля, 5,00 экв., 95%) в MeOH (2,50 мл, 74,121 ммоля, 270,09 экв., 95%) порциями при комнатной температуре в атмосфере азота добавляли CH3COOH (109,83 мг, 1,737 ммоля, 8,00 экв., 95%) и NaBH3CN (57,47 мг, 0,869 ммоля, 4,00 экв., 95%). Полученную смесь перемешивали в течение 3 ч при 70°C в атмосфере азота. Искомый продукт можно было обнаружить с помощью LCMS. Неочищенный продукт (110 мг ) очищали с помощью препаративной HPLC при следующих условиях (2#SHIMADZU (HPLC-01)): Колонка, XBridge Shield RP18 OBD Колонка, 30*150 мм, 5 мкм; подвижная фаза, вода (10 ммоль/л NH4HCO3+0,1%NH3.H2O) и ACN (от 30% фазы B до 35% за 8 мин); Детектор, UV 254 нм. Получали 80 мг рацемического продукта. Рацемический продукт (80) мг разделяли с помощью хиральной препаративной HPLC при следующих условиях (Prep-HPLC-032): Колонка, CHIRAL ART Cellulose -SB, 2*25 см, 5 мкм; подвижная фаза, Гекс(8 ммоль/л NH3.MeOH)- и EtOH- (50% EtOH- в течение 17 мин); Детектор, UV 254 нм. Это давало пик 1: 4-[(3S)-4-(3-метансульфонилциклобутил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина (11,0 мг 9,08%) в виде белого твердого вещества, время удерживания=4,501 мин, ee:99; пик 2: 4-[(3R)-4-(3-метансульфонилциклобутил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина (12,1 мг, 9,17%) в виде белого твердого вещества, время удерживания=5,529 мин, ee:98.
Пример 23: 4-[4-({6-оксаспиро2.5]октан-1-ил}метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин I-476
[00484] В сосуд для микроволновой печи, содержащий раствор 4-[3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина (50,00 мг; 0,12 ммоля; 1,00 экв.) и 6-оксаспиро2.5]октан-1-карбальдегида (84,57 мг; 0,60 ммоля; 5,00 экв.) в метаноле (2,50 мл; 61,72 ммоля; 640,56 экв.), добавляли уксусную кислоту (0,01 мл; 0,24 ммоля; 2,00 экв.) и затем цианоборогидрид натрия (30,33 мг; 0,48 ммоля; 4,00 экв.). Реакционную смесь перемешивали в течение ночи при 70C. LCMS-3 обнаруживала массу искомого продукта при полном превращении. Реакционной смеси давали охладиться, затем разбавляли с помощью DCM. Затем реакционную смесь по каплям добавляли к насыщенному раствору NaHCO3 и 3 раза промывали с помощью NaHCO3 и дважды рассолом. Органический слой сушили над безводным Na2SO4, фильтровали и концентрировали в вакууме. Неочищенное вещество растворяли в DMSO, затем очищали с помощью PuriFlash PF-C18HP 15 мкл 10-90% MeCN в воде (0,1% муравьиная кислота) 14 мин градиентный режим, затем 90% в течение 3 мин. Чистые фракции объединяли и лиофилизировали и получали продукт: 4-[4-({6-оксаспиро2.5]октан-1-ил}метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин (46,60 мг; 0,09 ммоля)
[00485] Пример 24: 4-[2-метил-4-(оксетан-3-ил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил) имидазо[1,2-a]пиридин-3-ил]пиримидин, I-322
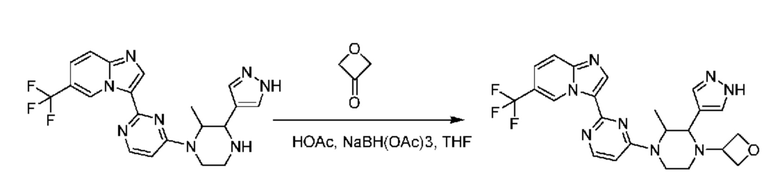
[00486] Раствор 4-[2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидина (150,00 мг; 0,35 ммоля; 1,00 экв.), оксетан-3-она (30,28 мг; 0,42 ммоля; 1,20 экв.) и уксусной кислоты (210,26 мг; 3,50 ммоля; 10,00 экв.) в THF (3 мл) обрабатывали триацетоксиборогидридом натрия (742,07 мг; 3,50 ммоля; 10,00 экв.) и смесь перемешивали при комнатной температуре в течение ночи. LCMS-3 показывала наличие искомого продукта. Неочищенный продукт загружали в HPLC с обращенной фазой и очищали с помощью 20% ACN в воде, содержащей от 0,1% NH4OH до 100% ACN за 10 мин при скорости потока, равной 60 мл/мин, и получали продукт, 4-[2-метил-4-(оксетан-3-ил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил) имидазо[1,2-a]пиридин-3-ил]пиримидин с выходом 16%. M/z (M+H): 485; H NMR (DMSO-d6): 12,70 (1H), 10,06 (1H), 8,46 (1H), 8,31 (1H), 7,80 (2H), 7,57 (1H), 7,46 (1H), 6,84 (1H), 3,82 (1H), 2,83 (2H), 2,58 (2H), 2,42 (1H), 1,13 (3H)
Пример 25: Типичные соединения I-122 - I-563.
[00487] Дополнительные соединения получали по методологиям, аналогичным описанным в приведенных выше примерах:
6-Хлор-3-(4-(2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-122
Диметил(((3R,5S)-5-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон, I-123
3-{4-[(2S,6R)-2-Метил-6-(3-метил-1H-пиразол-4-ил)-морфолин-4-ил]-пиримидин-2-ил}-6-трифторметилимидазо[1,2-a]пиридин, I-124
(2R,6S)-2-метил-6-(5-метил-1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-125
(((3R,5S)-1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил- λ6-сульфанон, I-128
(2R,6S)-6-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбоксамид, I-129
N, N-диметил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-130
пирролидин-1-ил(1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)метанон, I-131
5-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-азаспиро2.5]октан-1-карбоксамид, I-132
метил 5-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-азаспиро2.5]октан-1-карбоксилат, I-133
(2S,6S)-2-метил-6-(1H-пиразол-4-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-134
(2R,6R)-2-метил-6-(1H-пиразол-4-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-135
3-(2-((3R,5R)-3-Метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-136 (после хирального разделения)
3-(2-((3S,5S)-3-Метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-137 (после хирального разделения)
(2S,6R)-2-метил-6-(1H-пиразол-3-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-138
3-(2-((3R,5S)-3-(1,3-диметил-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-139
3-(2-((3S,5R)-3-(1,3-диметил-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-140
3-(2-((3S,5S)-3-(1,3-диметил-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-141
3-(2-((3R,5R)-3-(1,3-диметил-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-142
3-(2-((3R,5R)-3-(1-(2-метоксиэтил)-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-143
3-(2-((3R,5S)-3-(1-(2-метоксиэтил)-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-144
3-(2-((3S,5R)-3-(1-(2-метоксиэтил)-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-145
3-(2-((3S,5S)-3-(1-(2-метоксиэтил)-1H-пиразол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-146
(2S,6S)-2-метил-6-(5-метил-1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-147
(3R,5S)-5-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-148
5-Метил-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты амид, I-149
(S)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбоксамид, I-150
(R)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбоксамид, I-151
(R)-1-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперидин-3-карбоксамид, I-152
(S)-1-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперидин-3-карбоксамид, I-153
амид (S)-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновой кислоты, I-154
(2R,6R)-2-(1,3-диметил-1H-пиразол-4-ил)-6-метил-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-155
(2S,6S)-2-(1,3-диметил-1H-пиразол-4-ил)-6-метил-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-156
(2R,6S)-2-(1,3-диметил-1H-пиразол-4-ил)-6-метил-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-157
(2S,6R)-2-(1,3-диметил-1H-пиразол-4-ил)-6-метил-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-158
(((3R,5S)-1-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-159
4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(3-метил-1H-пиразол-4-ил)морфолин, I-160
2-(1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)уксусная кислота, I-161
2-(1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)ацетамид, I-162
4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбоксамид, I-163
(R)-1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-164
2-(1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)уксусная кислота, I-165
2-(1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)ацетамид, I-166
(((3S,5R)-1-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-5-метилпиримидин-2-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-167
(((3S,5R)-1-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-6-метилпиримидин-2-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-168
диметил(((3S,5R)-5-метил-1-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперидин-3-ил)имино)-λ6-сульфанон, I-169
3-(2-((2S,5S)-2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-170
3-(2-((2R,5R)-2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-171
3-(2-((2S, 5S)-2,5-диметил-3-(5-метил-1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-172
3-(2-((2R, 5R)-2,5-диметил-3-(5-метил-1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-173
(S)-1-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-5-метилпиримидин-2-ил)пиперидин-3-карбоксамид, I-174
(2S,6S)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-(5-фтор-1H-пиразол-4-ил)-6-метилморфолин, I-175
(2R,6S)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-(5-фтор-1H-пиразол-4-ил)-6-метилморфолин, I-176
(2S,6R)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-6-метилморфолин-2-карбоксамид, I-177
(2R,6R)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-6-метилморфолин-2-карбоксамид, I-178
(2S,6R)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-179
(2R,6S)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-180
(2S,6S)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-181
(2R,6R)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-182
(S)-1-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперидин-3-карбоксамид, I-183
6-хлор-3-(5-метил-2-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-184
6-хлор-3-(5-метил-2-((3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-185
6-хлор-3-(5-метил-2-((3S,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-186
N-(1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)ацетамид, I-187
4-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-4-карбоксамид, I-188
(2S,6S)-2-метил-6-(2H-тетразол-5-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-189
(2R,6R)-2-метил-6-(2H-тетразол-5-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)морфолин, I-190
(((3S,5R)-1-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-191
3-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-192
3-(4-(2-(5-(дифторметил)-1H-пиразол-4-ил)морфолино)пиримидин-2-ил)имидазо[1,2-a]пиридин-6-карбонитрил, I-193
6-хлор-3-(2-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-195
6-хлор-3-(2-((3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-196
6-хлор-3-(5-метил-2-((3S,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-197
6-хлор-3-(2-((3S,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-198
6-хлор-3-(2-((3S,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-199
6-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-200
6-метил-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоновая кислота, I-201
(2S,6R)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-5-метилпиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-203
(2R,6S)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-5-метилпиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-204
5,5-Дифтор-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновая кислота, I-205
5-фтор-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-карбоновая кислота, I-206
трет-бутил-2-карбамоил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-карбоксилат, I-207
6-хлор-3-(6-метил-2-((3S,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-208
6-хлор-3-(6-метил-2-((3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-209
6-хлор-3-(6-метил-2-((3S,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-210
6-хлор-3-(6-метил-2-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-211
трет-бутил-3-гидрокси-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксилат, I-212
3-гидрокси-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-213
3-гидрокси-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоновая кислота, I-214
4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-217
(2R,6R)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-6-метилпиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-218
(S)-1-(5-фтор-4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперидин-3-карбоксамид, I-219
(2S,6S)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-6-метилпиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-220
(2S,6R)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-6-метилпиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-221
(2R,6S)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)-6-метилпиримидин-2-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-222
(R)-1-(5-фтор-4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперидин-3-карбоксамид, I-223
3-(4-(3,3-дифторпиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-224
2-(дифторметил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-225
3-(4-(3-фтор-3-метилпиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-226
(S)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбонитрил, I-227
1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)азетидин-3-карбоксамид, I-228
5-фтор-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-229
2-(1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)азетидин-3-ил)ацетамид, I-230
3-(4-(3,5-диметилпиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-231
(S)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбонитрил, I-232
(S)-6-(трифторметил)-3-(4-(3-(трифторметил)пиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-233
3-(4-(3,5-диметил-4-(оксетан-3-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-234
6-циклопропил-3-(2-((3S,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-235
6-циклопропил-3-(2-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-236
трет-бутил-((3S,5S)-5-гидрокси-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)карбамат, I-237
(3R,5S)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3,5-диол, I-238
(3S,5S)-5-амино-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ол, I-239
3-(4-((3R,4R)-3-фтор-4-метилпиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-240
3-(гидроксиметил)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-4-ол, I-241
1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-сульфонамид, I-242
трет-бутил-((3R,4R)-1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-4-гидроксипиперидин-3-ил)карбамат, I-243
(((3S,5R)-1-(4-(6,7-дихлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-244
4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-(3,3,3-трифторпропил)пиперазин-2-карбоксамид, I-245
(2S,6S)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-246
6-Хлор-3-{2-[(2S,6R)-2-метил-6-(1H-пиразол-4-ил)-морфолин-4-ил]-пиримидин-4-ил}-имидазо[1,2-a]пиридин, I-247
6-Хлор-3-{2-[(2R,6S)-2-метил-6-(1H-пиразол-4-ил)-морфолин-4-ил]-пиримидин-4-ил}-имидазо[1,2-a]пиридин, I-248
6-Циклопропил-3-{2-[(3R,5R)-3-метил-5-(1H-пиразол-4-ил)-пиперидин-1-ил]-пиримидин-4-ил}-имидазо[1,2-a]пиридин, I-249
6-Циклопропил-3-{2-[(3S,5S)-3-метил-5-(1H-пиразол-4-ил)-пиперидин-1-ил]-пиримидин-4-ил}-имидазо[1,2-a]пиридин, I-250
(2R,6R)-4-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-251
трет-бутил-((3R,5R)-1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)карбамат, I-252
2-гидрокси-N-((3S,5S)-5-гидрокси-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)ацетамид, I-253
2-гидрокси-N-((3S,5S)-5-гидрокси-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)пропанамид, I-254
(3R,4R)-3-амино-1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-4-ол, I-255
(3R,5R)-1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-амин, I-256
N-((3S,5S)-5-гидрокси-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)-1H-пиразол-4-карбоксамид, I-257
1-(2-метоксиэтил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-258
6-(3,3-дифторазетидин-1-ил)-3-(2-((3S,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-259
(R)-1-(3-фтор-6-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиридин-2-ил)пиперидин-3-карбоксамид, I-260
6-(3,3-дифторазетидин-1-ил)-3-(2-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-261
3-(4-((3S,5R)-3-((диметил(оксо)-λ6-сульфанилиден)амино)-5-метилпиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин-6-карбонитрил, I-262
1-(оксетан-3-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-263
(2S,6S)-6-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбоксамид, I-264
(2S,6R)-6-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбоксамид, I-265
6-хлор-3-(4-(3-метил-5-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-266
6-хлор-3-(4-(3-метил-5-(5-метил-1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-267
6-хлор-3-(4-(3-метил-5-(5-метил-1H-пиразол-4-ил)-4-(метилсульфонил)пиперазин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-268
(((3S,5R)-1-(2-(6,7-дихлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-269
(2S,6R)-4-(4-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-270
6-(азетидин-1-ил)-3-(2-((3S,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-271
6-(азетидин-1-ил)-3-(2-((3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-272
(2R,6S)-4-(4-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-273
(2R,6R)-4-(4-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-274
(2S,6S)-4-(4-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-275
1-(4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(3-метил-1H-пиразол-4-ил)пиперазин-1-ил)этан-1-он, I-276
1-(4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(1H-пиразол-4-ил)пиперазин-1-ил)этан-1-он, I-277
(S)-1-(5-фтор-2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-278
6-хлор-3-(6-метокси-2-((3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-279
6-хлор-3-(6-метокси-2-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-280
6-хлор-3-(6-метокси-2-((3S,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-281
(S)-1-(5-фтор-2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-282
N-((1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)метил)-N-метилметансульфонамид, I-283
2-(1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)-2-метилпропановая кислота, I-284
трет-бутил 6-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,6-диазаспиро[3.5]нонан-2-карбоксилат, I-285
4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропилпиперазин-2-карбоксамид, I-286
6-(3,3-дифторазетидин-1-ил)-3-(6-метил-2-((3S,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-287
6-(3,3-дифторазетидин-1-ил)-3-(6-метил-2-((3R,5R)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-4-ил)имидазо[1,2-a]пиридин, I-288
(((3S,5R)-1-(2-(6-бромимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-289
диметил(((3S,5R)-5-метил-1-(2-(6-(трифторметокси)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон, I-290
диметил(((3S,5R)-5-метил-1-(2-(6-(дифторметокси)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон, I-291
трет-бутил 6,6-диметил-8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-окса-2,8-диазаспиро[3.5]нонан-2-карбоксилат, I-292
(2R,6S)-2-метил-6-(1H-пиразол-4-ил)-4-(2-(6-(трифторметокси)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-293
6,6-диметил-8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-окса-2,8-диазаспиро[3.5]нонан, I-294
(R)-6-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,6-диазаспиро[3.5]нонан-1-он, I-295
(S)-6-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,6-диазаспиро[3.5]нонан-1-он, I-296
1-(1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)циклопропан-1-карбоновая кислота, I-297
2-(4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-ил)уксусная кислота, I-298
6-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,6-диазаспиро[3.5]нонан, I-299
(((3S,5R)-1-(2-(6-циклопропилимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-300
6-хлор-3-(4-(3-метил-4-(метилсульфонил)-5-(1-(метилсульфонил)-1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-301
1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-(3-метил-1H-пиразол-4-ил)пиперидин-3-ол, I-302
1-(1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)циклопропан-1-карбоксамид, I-303
6,6-диметил-2-(метилсульфонил)-8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-окса-2,8-диазаспиро[3.5]нонан, I-304
2-((6,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-ил)метокси)-N, N-диметилацетамид, I-305
(3S,5R)-5-(5-метил-1H-пиразол-4-ил)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ол, I-307
(3R,5S)-5-(5-метил-1H-пиразол-4-ил)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ол, I-308
2-(1-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)-2-метилпропанамид, I-309
3-(4-((3R)-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-310
1-циклопропил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-311
диметил(((3R,5S)-5-метил-1-(2-(6-(метилсульфонил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон, I-312
3-(4-(3-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)-6-(метилсульфонил)имидазо[1,2-a]пиридин, I-313
(3S,5S)-5-(3-Метил-1H-пиразол-4-ил)-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-ол I-314
(3R,5R)-5-(3-Метил-1H-пиразол-4-ил)-1-[2-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-4-ил]-пиперидин-3-ол I-315
(3S,5S)-1-(4-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-5-гидроксипиперидин-3-карбоксамид, I-316
(((3S,5R)-1-(2-(6-бром-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-317
3-(4-(3-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)-N-циклопропилимидазо[1,2-a]пиридин-6-сульфонамид, I-318
N-циклопропил-3-(4-((3R,5S)-3-((диметил(оксо)-λ6-сульфанилиден)амино)-5-метилпиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин-6-сульфонамид, I-319,
3-(4-(3-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин-6-сульфонамид, I-320
3-(4-(2-метил-3-(5-метил-1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-321
(R)-1-циклопропил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-323
(S)-1-циклопропил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-324
диметил({[(3S,5R)-5-метил-1-(2-{6-феноксиимидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)пиперидин-3-ил]имино})-λ6-сульфанон I-325
3-(4-(3-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)-6-бром-7-фторимидазо[1,2-a]пиридин, I-326
N-(1-(4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-ил)этил)метансульфонамид, I-327
3-(4-((3R,5S)-3-((диметил(оксо)-λ6-сульфанилиден)амино)-5-метилпиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин-6-сульфонамид, I-328
2-{6-феноксиимидазо[1,2-a]пиридин-3-ил}-4-[3-(1H-пиразол-4-ил)пиперидин-1-ил]пиримидин I-329
(((3S,5R)-1-(2-(6-(3-фторазетидин-1-ил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-330
6-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбонитрил, I-331
3-метил-5-(1-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)-1,2,4-оксадиазол, I-332
3-(4-(3,3-диметил-4-(2,2,2-трифторэтил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-333
3-(4-(3,3-диметилпиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-334
3-(4-(4-(2-метоксиэтил)-3,5-диметилпиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-335
1-(2,2-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)этан-1-он, I-336
3-(4-(3-(5-метил-4H-1,2,4-триазол-3-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-337
8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)октагидропиразино[2,1-c][1,4]тиазин 2,2-диоксид, I-338
3-(4-(3,3-диметил-4-(метилсульфонил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-339
(((3S,5R)-1-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-340
(2S,6S)-4-(2-(6-циклопропил-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)морфолин, I-341
диметил(((3R,5R)-5-(5-метил-1H-пиразол-4-ил)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон, I-342
(2R,6R)-2-метил-6-(5-метилизоксазол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-343
диметил(((3S,5R)-5-(5-метил-1H-пиразол-4-ил)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)имино)-λ6-сульфанон, I-344
(2S,6S)-2-метил-6-(5-метилизоксазол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-345
(2S,6R)-2-метил-6-(5-метилизоксазол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-346
(2R,6S)-2-метил-6-(5-метилизоксазол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-347
3-(4-(4-(1-этоксициклопропил)-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-348
(R)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропилпиперазин-2-карбоксамид, I-349
(s)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропилпиперазин-2-карбоксамид, I-350
3-(4-(3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-351
3-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)пропан-1,2-диол, I-352
4-((2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метил)оксазол, I-353
3-(4-(3-(1H-пиразол-4-ил)-4-((тетрагидро-2H-пиран-4-ил)метил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-354
6-(трифторметил)-3-(4-(3-(3-(трифторметил)-1H-пиразол-1-ил)пиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-355
3-(4-(3-(1H-1,2,4-триазол-1-ил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-356
3-(4-(3-фтор-5-(3-метил-1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-357
2-метил-6-(3-метил-1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-358
(2S,6R)-4-(2-(7-хлор-6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(3-метил-1H-пиразол-4-ил)морфолин, I-359
(2R,6R)-4-(2-(7-хлор-6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(3-метил-1H-пиразол-4-ил)морфолин, I-360
3-(4-((2S,3R)-2-метил-4-(оксетан-3-ил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-361
4-[(2R,3S)-2-метил-4-(оксетан-3-ил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин, I-362
3-(4-((2R,3R)-2-метил-4-(оксетан-3-ил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-363
3-(4-((2S,3S)-2-метил-4-(оксетан-3-ил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-364
3-(4-(2S,3R)-2-метил-3-(5-метил-1H-пиразол-4-ил)-4-(оксетан-3-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-365
3-(4-(2R,3S)-2-метил-3-(5-метил-1H-пиразол-4-ил)-4-(оксетан-3-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-366
3-(4-(2S,3S)-2-метил-3-(5-метил-1H-пиразол-4-ил)-4-(оксетан-3-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-367
3-(4-(2R,3R)-2-метил-3-(5-метил-1H-пиразол-4-ил)-4-(оксетан-3-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-368
4-[4-(циклопропилметил)-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин, I-369
3-(4-(4-((3-оксабицикло[3.1.0]гексан-6-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-370
3-(4-(4-((1H-имидазол-2-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-371
3-(4-(4-((2-метил-1H-имидазол-5-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-372
3-(4-(4-((2-(трет-бутил)-1H-имидазол-5-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-373
3-(4-(4-(оксетан-3-илметил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-374
(2R,6R)-4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)морфолин, I-375
(((3S,5R)-1-(2-(6-циклопропил-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-376
6-циклопропил-7-фтор-3-(4-(3-фтор-5-(5-метил-1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-377
4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид, I-378
3-(4-(3-метил-4-(1H-пиразол-1-ил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-379
3-метил-4-{2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин-4-ил}пиперазин-2-карбоксамид, I-380
(1-(1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)-1H-1,2,3-триазол-4-ил)метанол, I-382
3-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)циклобутан-1-ол, I-383
3-(4-(4-((1-метил-1H-пиразол-4-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-384
3-(4-(4-((1H-имидазол-5-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-385
трет-бутил 8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-окса-2,8-диазаспиро[3.5]нонан-2-карбоксилат, I-386
трет-бутил 6-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,6-диазаспиро[3.5]нонан-2-карбоксилат, I-387
трет-бутил 9,9-диметил-8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-окса-2,8-диазаспиро[3.5]нонан-2-карбоксилат, I -388
4-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропилпиперазин-2-карбоксамид, I-389
(3-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)циклобутил)метанол, I-390
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-изопропил-1H-пиразол-4-ил)метанон, I-391
3-(4-(4-циклопропил-3,5-диметилпиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-392
2-(2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)ацетонитрил, I-393
N-(((1R,4S)-2-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-азабицикло[2.2.2]октан-6-ил)метил)метансульфонамид, I-394
6-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-(метилсульфонил)-2,6-диазаспиро[3.5]нонан, I-395
8-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-6,6-диметил-2-(метилсульфонил)-5-окса-2,8-диазаспиро[3.5]нонан, I-396
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(циклопропил)метанон, I-397
2-{6-феноксиимидазо[1,2-a]пиридин-3-ил}-4-[(3R)-3-(1H-пиразол-4-ил)пиперидин-1-ил]пиримидин I-398
2-{6-феноксиимидазо[1,2-a]пиридин-3-ил}-4-[(3S)-3-(1H-пиразол-4-ил)пиперидин-1-ил]пиримидин I-399
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(2,2-дифторциклопропил)метанон, I-400
(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-изопропил-1H-пиразол-3-ил)метанон, I-401
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(3,3-дифторциклобутил)метанон, I-402
циклопропил(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метанон, I-403
N-((R)-1-((S)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-ил)этил)метансульфонамид, I-404
N-((S)-1-((R)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-ил)этил)метансульфонамид, I-405
N-((R)-1-((R)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-ил)этил)метансульфонамид, I-406
N-((S)-1-((S)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-ил)этил)метансульфонамид, I-407
3-(4-((3R,5S)-3-метил-5-(5-метил-2H-1,2,3-триазол-4-ил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-408
3-(4-((3S,5R)-3-метил-5-(5-метил-2H-1,2,3-триазол-4-ил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-409
3-(4-(цис-3,5-диметил-4-(2,2,2-трифторэтил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-410
трет-бутил-3-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3,9-диазабицикло[3.3.1]нонан-9-карбоксилат, I-411
8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-окса-2,8-диазаспиро[3.5]нонан, I-412
6-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,6-диазаспиро[3.5]нонан, I-413
1-(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)этан-1-он, I-414
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-(2-гидроксиэтил)-1H-пиразол-4-ил)метанон, I-415
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-(2-метоксиэтил)-1H-пиразол-4-ил)метанон, I-416
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-(оксетан-3-ил)-1H-пиразол-4-ил)метанон, I-417
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-метил-1H-пиразол-4-ил)метанон, I-418
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-метил-1H-пиразол-5-ил)метанон, I-419
1-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-2-гидроксипропан-1-он, I-420
1-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-2-гидроксиэтан-1-он, I-421
1-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-3-(1H-имидазол-1-ил)пропан-1-он, I-422
1-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-3-(3,5-диметил-1H-пиразол-1-ил)пропан-1-он, I-423
(S)-4-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропилпиперазин-2-карбоксамид, I-424
(R)-4-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропилпиперазин-2-карбоксамид, I-425
6-хлор-7-фтор-3-(4-(3-фтор-5-(5-метил-1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-426
4-(2-(6-циклопропил-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид, I-427
(2S,6S)-4-(2-(6-циклопропил-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-428
(2S,6R)-4-(2-(6-циклопропил-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-429
1-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-карбонил)циклопропан-1-карбонитрил, I-432
(R)-1-(4-(4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)-1H-пиразол-1-карбонил)циклопропан-1-карбонитрил, I-433
(2R,3R)-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-434
(2S,3S)-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-карбоксамид, I-435
N-(((2R,3S)-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)метил)метансульфонамид, I-436
(3,3-дифторциклобутил)(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метанон, I-437
(2,2-дифторциклопропил)(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метанон, I-438
3-(4-(цис-3,5-диметил-4-(метилсульфонил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-439
(1-циклопропил-1H-пиразол-3-ил)(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метанон, I-440
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1,2,5-оксадиазол-3-ил)метанон, I-441
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(2H-1,2,3-триазол-4-ил)метанон, I-442
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(оксазол-4-ил)метанон, I-443
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(изоксазол-4-ил)метанон, I-444
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1H-имидазол-4-ил)метанон, I-445
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-метил-1H-имидазол-4-ил)метанон, I-446
2-(метилсульфонил)-8-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-окса-2,8-диазаспиро[3.5]нонан, I-447
2-(метилсульфонил)-6-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2,6-диазаспиро[3.5]нонан, I-448
3-(4-(3-(1H-пиразол-4-ил)-4-(3,3,3-трифторпропил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-449
3-(4-(4-(3,4-дифторбензил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-450
4-(2-{6-хлоримидазо[1,2-a]пиридин-3-ил}пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид, I-451
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(2-метоксипиридин-4-ил)метанон, I-452
(2R,3S)-4-(2-(6-циклопропил-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид, I-454
4-(2-(6-циклопропил-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метилпиперазин-2-карбоксамид, I-455
3-(4-(3-(1H-пиразол-4-ил)-4-(тетрагидро-2H-пиран-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-456
3-(4-(4-(4-фторбензил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-457
3-(4-(4-(3-фторбензил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-458
3-(4-(4-(2-фторбензил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-459
3-(4-(4-(4,4-дифторциклогексил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-460
4-{4-[(1,2,5-оксадиазол-3-ил)метил]-3-(1H-пиразол-4-ил)пиперазин-1-ил}-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин, I-461
3-(4-(цис-3,5-диметил-4-((тетрагидро-2H-пиран-4-ил)метил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-462
3-(2-((3R,5S)-3-(3,5-диметил-4H-1,2,4-триазол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-463
1-(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-2-(тетрагидро-2H-пиран-4-ил)этан-1-он, I-464
3-(2-((3S,5S)-3-(3,5-диметил-4H-1,2,4-триазол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-465
3-(2-((3S,5R)-3-(3,5-диметил-4H-1,2,4-триазол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-466
3-(2-((3R,5R)-3-(3,5-диметил-4H-1,2,4-триазол-4-ил)-5-метилпиперидин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-467
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(спиро[2.2]пентан-1-ил)метанон, I-468
5-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-карбонил)пирролидин-2-он, I-469
3-(4-(4-((2,2-дифторциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-470
N-(((2S,3S)-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)метил)метансульфонамид, I-471
N-((1-циклопропил-4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метилпиперазин-2-ил)метил)метансульфонамид, I-472
3-(4-(4-((2-метилциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-473
(S)-6-((S)-2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-карбонил)пиперидин-2-он, I-474
3-(4-(3-(1H-пиразол-4-ил)-4-(спиро[2.2]пентан-1-илметил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-475
3-(4-(4-((2,2-диметилциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-477
N-(5-(трифторметил)-1-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-ил)метансульфонамид, I-478
(R)-(1,3-диметил-1H-пиразол-4-ил)(2-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метанон, I-479
(S)-(1,3-диметил-1H-пиразол-4-ил)(2-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метанон, I-480
3-(4-((2S,3R)-2-метил-4-((3-метилоксетан-3-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-481
3-(4-((2S,3S)-2-метил-4-((3-метилоксетан-3-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-482
(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(пиридин-4-ил)метанон, I-483
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)((1R,2R)-2-фторциклопропил)метанон, I-485
(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-метилциклопропил)метанон, I-486
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(тетрагидро-2H-пиран-4-ил)метанон, I-487
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(1-(дифторметил)циклопропил)метанон, I-488
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)((1R,2R)-2-фторциклопропил)метанон, I-489
N-(((2R,3S,6S)-1-циклопропил-3,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)метил)метансульфонамид, I-491
4-(2,2-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-карбонил)циклогексан-1-он, I-492
N-(((2R,3R,6R)-1-циклопропил-3,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)метил)метансульфонамид, I-493
N-(((2S,3R,6R)-1-циклопропил-3,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)метил)метансульфонамид, I-494
N-((4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-(трифторметил)пиперазин-2-ил)метил)метансульфонамид, I-496
(2R,6R)-4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)морфолин, I-497
(2S,6S)-4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(3-метил-1,2,4-оксадиазол-5-ил)морфолин, I-498
(((3S,5R)-1-(4-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-499
N-((S)-1-((2S,3S)-1-циклопропил-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)этил)метансульфонамид, I-500
1-(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-2-(оксетан-3-ил)этан-1-он, I-501
(S)-3-(4-(3-(1H-пиразол-4-ил)-4-(2-оксаспиро[3.3]гептан-6-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-502
(R)-3-(4-(4-циклопропил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-503
(R)-3-(4-(3-(1H-пиразол-4-ил)-4-(2-оксаспиро[3.3]гептан-6-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-504
N-((R)-1-((2R,3R)-1-циклопропил-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)этил)метансульфонамид, I-505
N-((R)-1-((2S,3S)-1-циклопропил-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)этил)метансульфонамид, I-506
N-((S)-1-((2R,3R)-1-циклопропил-3-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-2-ил)этил)метансульфонамид, I-507
3-{2-[(R)-4-Циклопропил-3-(1H-пиразол-4-ил)-пиперазин-1-ил]-пиримидин-4-ил}-6-трифторметилимидазо[1,2-a]пиридин, I-508,
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(3-гидрокси-3-метилциклобутил)метанон, I-509
3-(4-(4-((1-метилциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-510
4-[(2R,3S)-4-{[1-(метоксиметил)циклобутил]метил}-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин, I-511
4-[(2S,3S)-4-{[1-(метоксиметил)циклобутил]метил}-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин, I-512
(6,7-дигидро-4H-пиразоло[5,1-c][1,4]оксазин-2-ил)(цис-2,6-диметил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)метанон, I-513
1-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-2-гидрокси-2-метилпропан-1-он, I-514
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(5-метилизоксазол-4-ил)метанон, I-515
N-(((2R,3S)-1-циклопропил-4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метилпиперазин-2-ил)метил)метансульфонамид, I-516
N-(((2S,3R)-1-циклопропил-4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метилпиперазин-2-ил)метил)метансульфонамид, I-517
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(4-метил-1,2,5-оксадиазол-3-ил)метанон, I-518
(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(3,5-диметилизоксазол-4-ил)метанон, I-519
3-(4-((R)-4-(((R)-6-оксаспиро2.5]октан-1-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-520
3-(4-((S)-4-(((S)-6-оксаспиро2.5]октан-1-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-521
3-(4-((S)-4-(((R)-6-оксаспиро2.5]октан-1-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-522
3-(4-((R)-4-(((S)-6-оксаспиро2.5]октан-1-ил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-523
((2S,6S)-4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-6-метилморфолин-2-ил)метанол, I-524
N-(1-(4-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)-5-(трифторметил)пиперидин-3-ил)метансульфонамид, I-525
3-(4-((R)-4-(((R)-2,2-диметилциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-526
3-(4-((S)-4-(((S)-2,2-диметилциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-527
3-(4-((S)-4-(((R)-2,2-диметилциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-528
3-(4-((R)-4-(((S)-2,2-диметилциклопропил)метил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-529
N-((4-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-3-метил-1-(оксетан-3-ил)пиперазин-2-ил)метил)метансульфонамид, I-530
N-(1-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-(трифторметил)пиперидин-3-ил)метансульфонамид, I-531
(R)-3-(4-(3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-532
(S)-3-(4-(3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-533
3-(4-((2S,3R)-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-534
3-(4-((2S,3S)-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-535
3-(4-((2R,3R)-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-536
4-[(2R,3S)-2-метил-3-(1H-пиразол-4-ил)пиперазин-1-ил]-2-[6-(трифторметил)имидазо[1,2-a]пиридин-3-ил]пиримидин, I-537
(2R,6R)-4-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-538
(2S,6S)-4-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-539
(2R,6S)-4-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-540
N-(((2R,3S)-1-циклопропил-3-метил-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперазин-2-ил)метил)метансульфонамид, I-541
3-(2-((S)-3-(1H-пиразол-4-ил)-4-(((R)-тетрагидро-2H-пиран-3-ил)метил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-542
N-{(2S,3R)-1-Циклопропил-3-метил-4-[4-(6-трифторметилимидазо[1,2-a]пиридин-3-ил)-пиримидин-2-ил]-пиперазин-2-илметил}-метансульфонамид, I-543
3-(2-((R)-3-(1H-пиразол-4-ил)-4-(((S)-тетрагидро-2H-пиран-3-ил)метил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-544
3-(2-((R)-3-(1H-пиразол-4-ил)-4-(((R)-тетрагидро-2H-пиран-3-ил)метил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-545
3-(2-((S)-3-(1H-пиразол-4-ил)-4-(((S)-тетрагидро-2H-пиран-3-ил)метил)пиперазин-1-ил)пиримидин-4-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-546
(2R,3R)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропил-3-метилпиперазин-2-карбоксамид, I-547
(2S,3S)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-1-циклопропил-3-метилпиперазин-2-карбоксамид, I-548
(S)-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(5-метилизоксазол-4-ил)метанон, I-549
(R)-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)(5-метилизоксазол-4-ил)метанон, I-550
1-(2-(1H-пиразол-4-ил)-4-(4-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-2-ил)пиперазин-1-карбонил)циклопропан-1-карбонитрил, I-551
3-(4-((R)-3-(1H-пиразол-4-ил)-4-(((R)-спиро[2.2]пентан-1-ил)метил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-552
3-(4-((S)-3-(1H-пиразол-4-ил)-4-(((S)-спиро[2.2]пентан-1-ил)метил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-553
3-(4-((S)-3-(1H-пиразол-4-ил)-4-(((R)-спиро[2.2]пентан-1-ил)метил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-554
3-(4-((R)-3-(1H-пиразол-4-ил)-4-(((S)-спиро[2.2]пентан-1-ил)метил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-555
(S)-6-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-2-тиаспиро[3.3]гептан 2,2-диоксид, I-556
(R)-6-(2-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперазин-1-ил)-2-тиаспиро[3.3]гептан 2,2-диоксид, I-557
(S)-1-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)пиперидин-3-карбоксамид, I-558
6-хлор-3-(4-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-559
(2S,6R)-2-метил-6-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-560
(2R,6S)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(5-метил-1H-пиразол-4-ил)морфолин, I-561
(2S,6S)-6-метил-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин-2-карбоксамид, I-562
6-хлор-3-(4-((2S,3R,5S)-2,5-диметил-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)имидазо[1,2-a]пиридин, I-563
(2R,6S)-2-метил-6-(1H-пиразол-4-ил)-4-(2-(6-(трифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)морфолин, I-564
3-(4-((2R,3S)-2-метил-4-(оксетан-3-ил)-3-(1H-пиразол-4-ил)пиперазин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-565
(2R,6S)-4-(2-(6-хлоримидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-566
3-(4-((3R,5S)-3-метил-5-(1H-пиразол-4-ил)пиперидин-1-ил)пиримидин-2-ил)-6-(трифторметил)имидазо[1,2-a]пиридин, I-567
(2S,6R)-4-(2-(6-хлор-7-фторимидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-2-метил-6-(1H-пиразол-4-ил)морфолин, I-568
(((3R,5R)-1-(2-(6-(дифторметил)имидазо[1,2-a]пиридин-3-ил)пиримидин-4-ил)-5-метилпиперидин-3-ил)имино)диметил-λ6-сульфанон, I-569
Пример 26: Исследование ингибирования GCN2 посредством IL-2 человека
[00488] Микроокружение опухоли является сильно иммуносупрессивным. Это можно приписать уменьшению содержания аминокислот (таких как аргинин и триптофан), что запускает активацию GCN2 в иммунных клетках, включая T-клетки и миелоидные клетки. В T-клетках активация GCN2 приводит к ослаблению эффекторных функций CD8 T-клеток и индуцированию и/или поддержанию иммуносупрессивных T-regs. Ингибирование этого иммуносупрессивного ответа ингибиторами GCN2 обеспечивает противораковый иммунный ответ путем активации эффекторных T-клеток. В настоящем изобретении описана система in-vitro, разработанная авторами с использованием T-клеток человека, стимулированных при условиях низкого содержания аминокислот, для проявления биологических характеристик GCN2. Описанная методика включает модулирования содержания IL-2, секретированного T-клетками человека в ответна ингибиторы GCN2, раскрытые в настоящем изобретении.
[00489] Не содержащую аминокислоты среду RPMI восстанавливали при наличии всех аминокислот кроме одной, находящейся в стандартной RMPI (например, аргинин, триптофан), добавляли 10% очищенную древесным углем фетальную бычью сыворотку, 100 Ед/мл пенициллин и 0,1 мг/мл стрептомицин. Первичные пан-T-клетки человека выделяли с помощью набора Pan T Cell Isolation для человека (MACS Miltenyi biotech Cat# Order no. 130-096-535) из конусов для аферезиса и 5×104 пан-T-клеток/лунка. Очищенные T-клетки высевали в 96-луночные круглодонные изготовленные из полистирола планшеты для микротитрования Nunc™ 96-Well (клетки выдерживали в не содержащих TRP средах в пробирке Falcon объемом 15 мл в инкубаторе в течение 30-45 мин и в это время провдили титрование триптофана и ингибирующих GCN2 соединений). Разработана матрица для планшета для титрования ингибитора GCN2 и исследуемой аминокислоты в диапазоне от "нет аминокислоты" вплоть до концентрации, обнаруженной в стандартных средах RPMI (20 мкМ для TRP и 950 мкМ для аргинина). Клетки инкубировали в течение 30 мин при 37°C с ингибитором GCN2 и затем стимулировали с помощью 5×104 анти-CD3/CD28 dynabeads® на лунку. После 96 ч инкубации содержание IL-2 в надосадочной жидкости измеряли с помощью ELISA (R&D systems Cat# DY202 (IL-2 DuoSet ELISA человека). Зависимость для данных строили с помощью программного обеспечения GraphPad Prism и рассчитывали EC50.
Таблица 6. Значения EC50, основанные на секреции IL-2 T-клетками
[00490] +++ для EC50 <100 нМ; ++ для EC50 в диапазоне 100-500 нМ; + для EC50 >500 нМ; и "-" для неактивных
[00491] Хотя описан целый ряд вариантов осуществления настоящего изобретения, очевидно, что приведенные основные примеры можно изменить и получить другие варианты осуществления, в которые используются соединения и способы, предлагаемые в настоящем изобретении. Поэтому следует понимать, что объем настоящего изобретения определяется прилагаемой формулой изобретения, а не конкретными вариантами осуществления, которые приведены в качестве примера.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ GCN2 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2811408C2 |
| НОВЫЕ СОЕДИНЕНИЯ И КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ NAMPT | 2011 |
|
RU2617988C2 |
| КОНДЕНСИРОВАННЫЕ ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПИРИДИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПРОИЗВОДСТВА И ПРИМЕНЕНИЕ | 2014 |
|
RU2668074C2 |
| КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА И ПИРАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2686117C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ PRMT5 | 2018 |
|
RU2797822C2 |
| КОНДЕНСИРОВАННЫЕ С ГЕТЕРОАРИЛКЕТОНАМИ АЗАДЕКАЛИНЫ - МОДУЛЯТОРЫ ГЛЮКОКОРТИКОИДНЫХ РЕЦЕПТОРОВ | 2013 |
|
RU2639867C2 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО ЦИАНОЕНОНА КАК МОДУЛЯТОРЫ KEAP1 | 2021 |
|
RU2822828C1 |
| ТИАЗОЛИНО-2-ПИРИДОНЫ С КОНДЕНСИРОВАННЫМИ ЦИКЛАМИ В КОМБИНАЦИИ С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ ПРОТИВ ТУБЕРКУЛЕЗА | 2018 |
|
RU2791467C2 |
| 4-(ИМИДАЗО[1,2-а]ПИРИДИН-3-ИЛ)-ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2822388C2 |
| ЗАМЕЩЕННЫЕ 1,2-ДИГИДРО-3Н-ПИРАЗОЛО[3,4-D]ПИРИМИДИН-3-ОНЫ | 2019 |
|
RU2812726C2 |
Группа изобретений относится к области органической химии и фармацевтики, а именно к соединениям, применимым для ингибирования общей регулирующей содержание аминокислот киназы 2 с постоянной репрессией (GCN2). Раскрыто соединение одной из формул XV-a, XV-b или XV-c или его фармацевтически приемлемая соль, где значения радикалов R1, R такие как представлено в н.п.1 формулы. Кроме того, раскрыто конкретное соединение, выбранное из группы, фармацевтическая композиция, обладающая ингибирующей общей регулирующей содержание аминокислот киназы 2 с постоянной репрессией (GCN2) активностью на основе раскрытых соединений, а кроме того, применение указанных соединений или фармацевтической композиции для ингибирования GCN2 в биологическом образце и для получения лекарственного средства для лечения опосредуемого GCN2 нарушения, заболевания или патологического состояния у пациента. Группа изобретений обеспечивает эффективное ингибирование GCN2. 5 н. и 34 з.п. ф-лы, 6 табл., 26 пр.
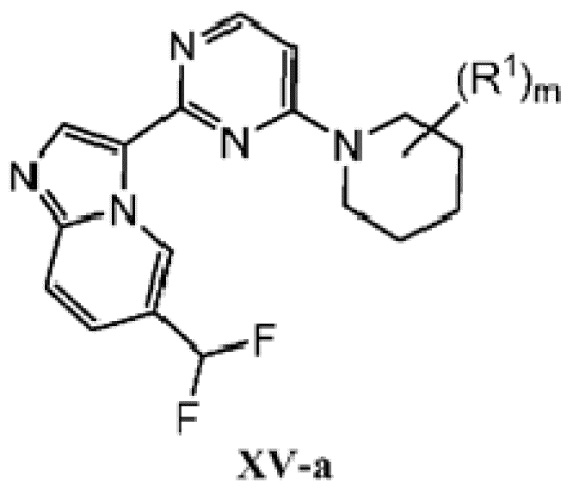
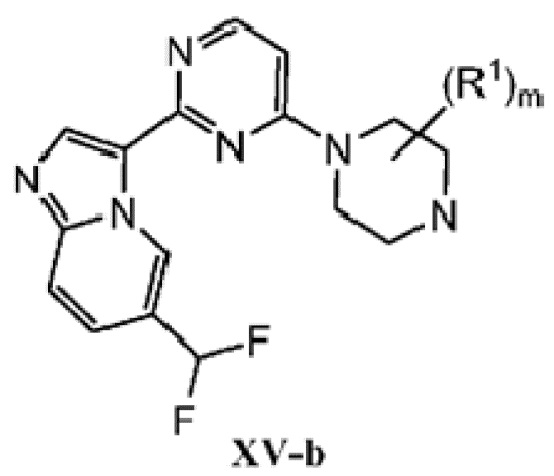
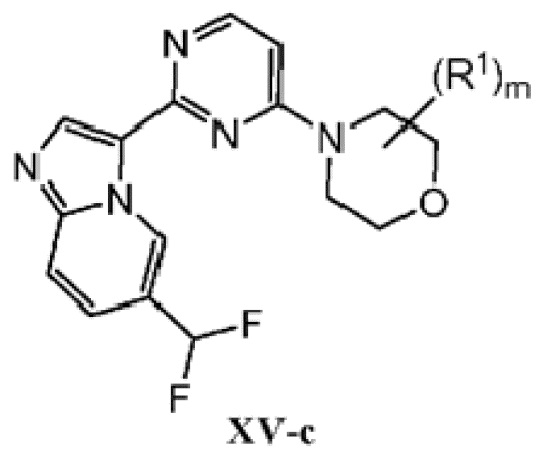
1. Соединение одной из формул XV-a, XV-b или XV-c:
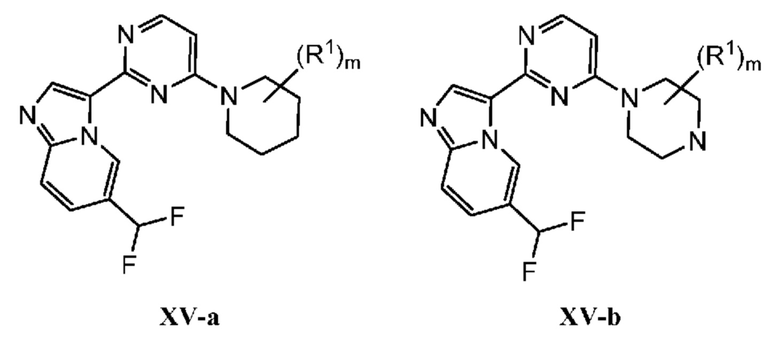
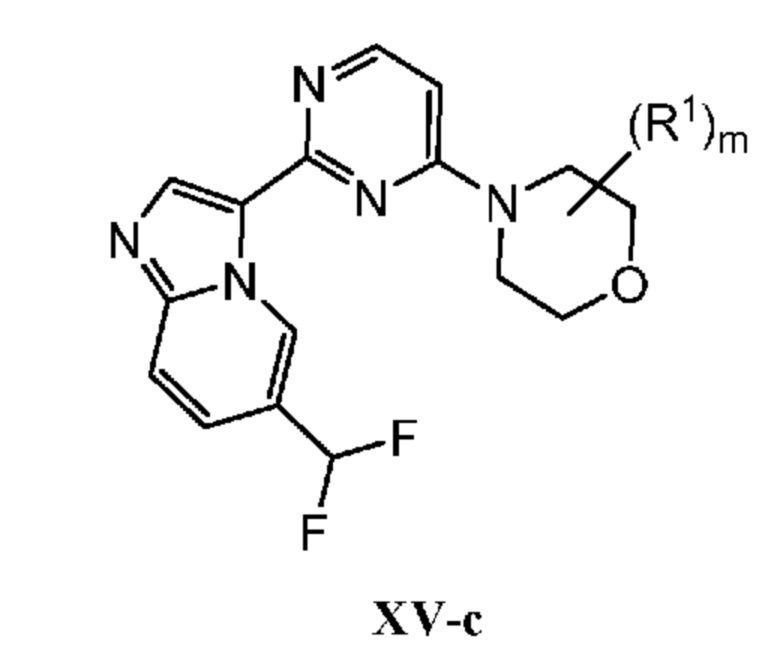
или его фармацевтически приемлемая соль,
где каждый из R1 независимо означает водород, галоген, -CN, -NO2, -C(O)R, -C(O)OR, -C(O)NR2, -C(O)NRS(O)2R, -C(O)N=S(O)R2, -NR2, -NRC(O)R, -NRC(O)NR2, -NRC(O)OR, -NRS(O)2R, -NRS(O)2NR2, -OR, -ON(R)SO2R, -P(O)R2, -SR, -S(O)R, -S(O)2R, -S(O)(NH)R, -S(O)2N(R)2, -S(NH2)2(O)OH, -N=S(O)R2, -CH3, -CH2OH, -CH2NHSO2CH3, -CD3, -CD2NRS(O)2R, или R; или:
две группы R1 вместе образуют =O или =NH; или
две группы R1 вместе образуют двухвалентную C2-4 алкиленовую цепь;
или каждый из R1 независимо выбран из группы, состоящей из:
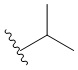 ,
, 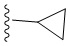 ,
, 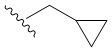 ,
, 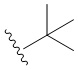 ,
, 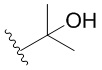 ,
, 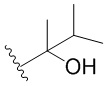 ,
, 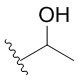 ,
, 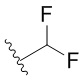 ,
, 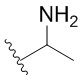 ,
, 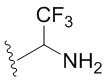 ,
, 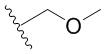 ,
, 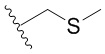 ,
, 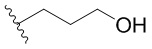 ,
, 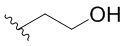 ,
, 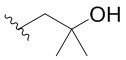 ,
, 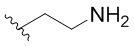 ,
, 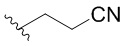 ,
, 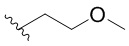 ,
, 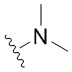 ,
, 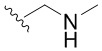 ,
, 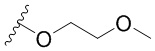 ,
, 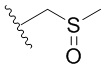 ,
, 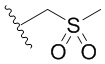 ,
, 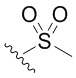 ,
, 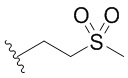 ,
, 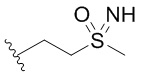 ,
, 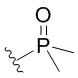 ,
, 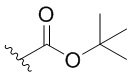 ,
, 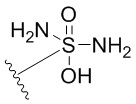 ,
,  ,
, 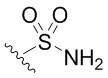 ,
, 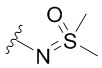 ,
, 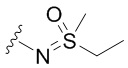 ,
, 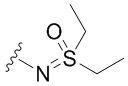 ,
, 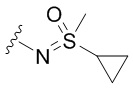 ,
, 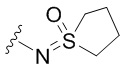 ,
, 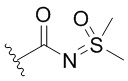 ,
, 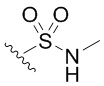 ,
, 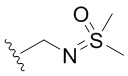 ,
, 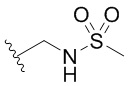 ,
,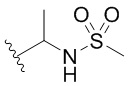 ,
, 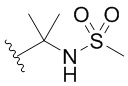 ,
, 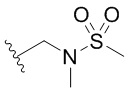 ,
, 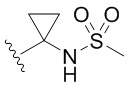 ,
, 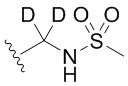 ,
, 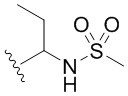 ,
, 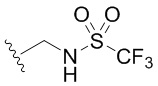 ,
, 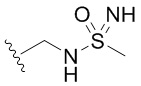 ,
, 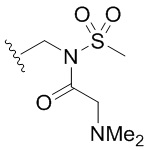 ,
, 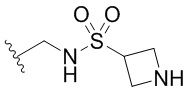 ,
,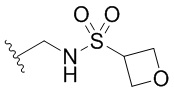 ,
, 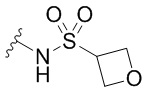 ,
, 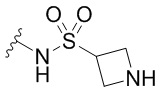 ,
, 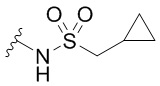 ,
, 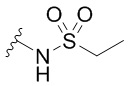 ,
, 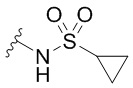 ,
, 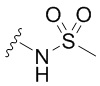 ,
, 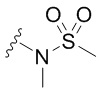 ,
, 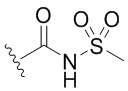 ,
, 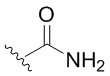 ,
, 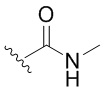 ,
, 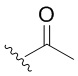 ,
, 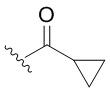 ,
, 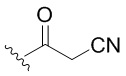 ,
, 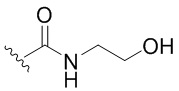 ,
, 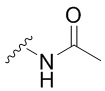 ,
, 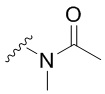 ,
, 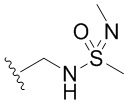 ,
, 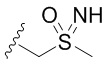 ,
, 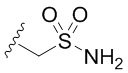 ,
, 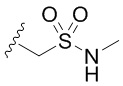 ,
, 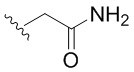 ,
, 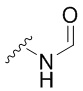 ,
, 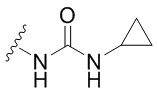 ,
, 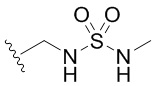 ,
, 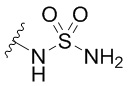 ,
, 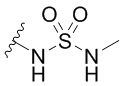 ,
, 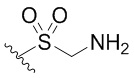 ,
, 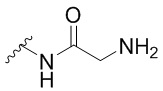 ,
, 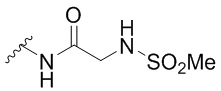 ,
, 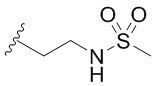 ,
,  ,
, 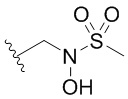 ,
, 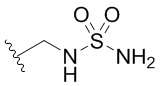 ,
, 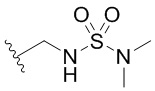 ,
, 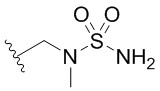 ,
, 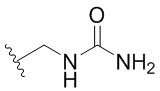 ,
,  ,
, 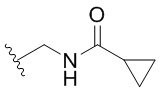 ,
, 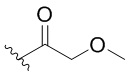 ,
, 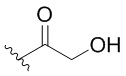 ,
, 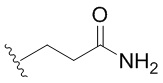 ,
, 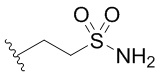 ,
, 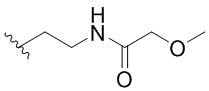 ,
, 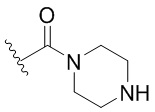 ,
, 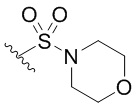 ,
, 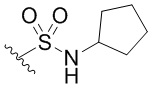 ,
, 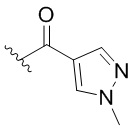 ,
, 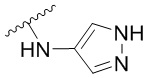 ,
, 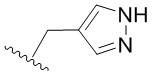 ,
, 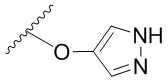 ,
, 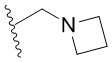 ,
, 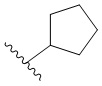 ,
, 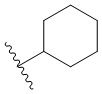 ,
, 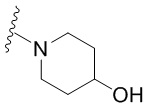 ,
, 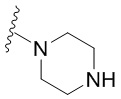 ,
, 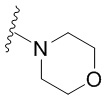 ,
, 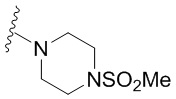 ,
, 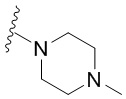 ,
, 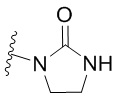 ,
, 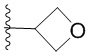 ,
, 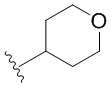 ,
, 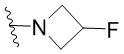 ,
, 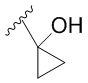 ,
, 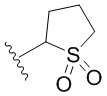 ,
, 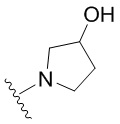 ,
, 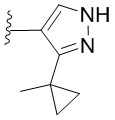 ,
, 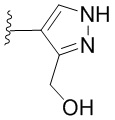 ,
, 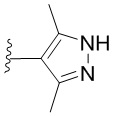 ,
, 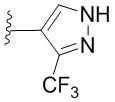 ,
, 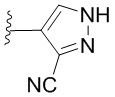 ,
, 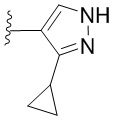 ,
, 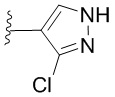 ,
, 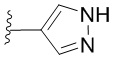 ,
, 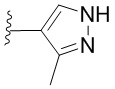 ,
, 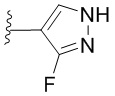 ,
, 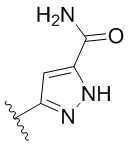 ,
, 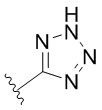 ,
, 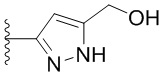 ,
, 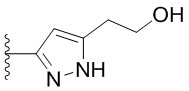 ,
, 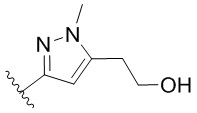 ,
, 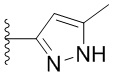 ,
, 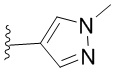 ,
, 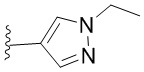 ,
, 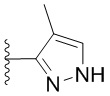 ,
, 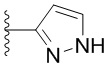 ,
, 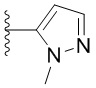 ,
, 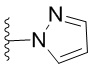 ,
, 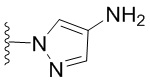 ,
, 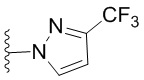 ,
, 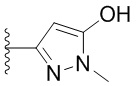 ,
, 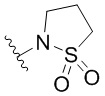 ,
, 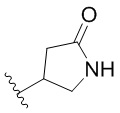 ,
, 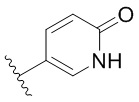 ,
, 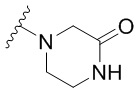 ,
, 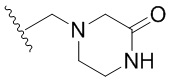 ,
, 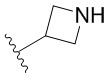 ,
, 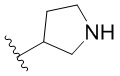 ,
, 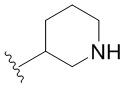 ,
, 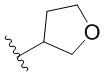 ,
, 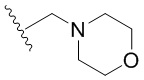 ,
, 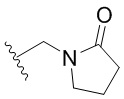 ,
, 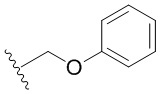 ,
, 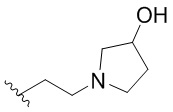 ,
, 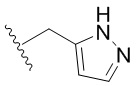 ,
, 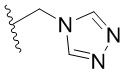 ,
, 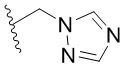 ,
, 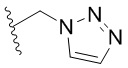 ,
, 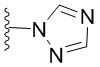 ,
, 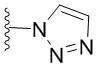 ,
, 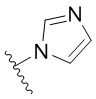 ,
, 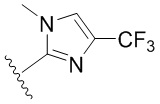 ,
, 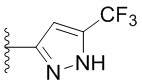 ,
, 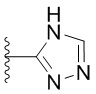 ,
, 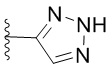 ,
, 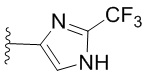 ,
, 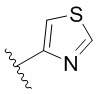 ,
, 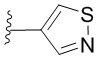 ,
,  ,
, 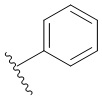 ,
, 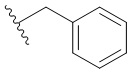 ,
,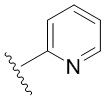 ,
, 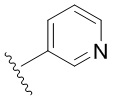 ,
, 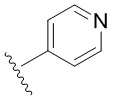 ,
, 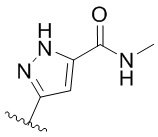 ,
, 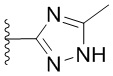 ,
, 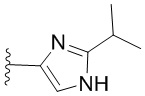 ,
, 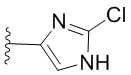 ,
, 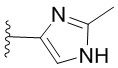 ,
, 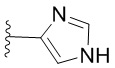 ,
, 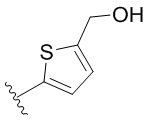 ,
, 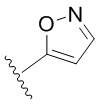 ,
, 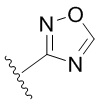 ,
, 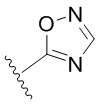 ,
, 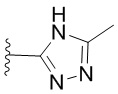 ,
, 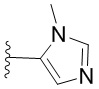 ,
, 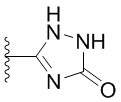 ,
, 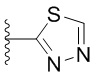 ,
, 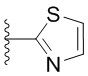 ,
, 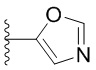 ,
, 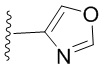 ,
, 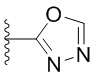 ,
, 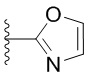 ,
, 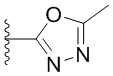 ,
, 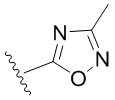 ,
, 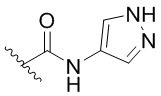 ,
, 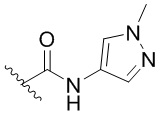 ,
, 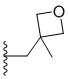 ,
, 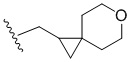 ,
, 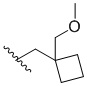 ,
, 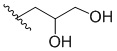 ,
, 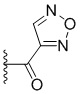 ,
, 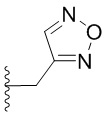 ,
, 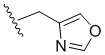 и
и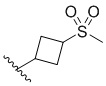 ;
;
каждый R независимо означает водород или группу, выбранную из группы, включающей C1-6 алифатическую группу, 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу; или
две группы R вместе образуют двухвалентную C2-4 алкиленовую цепь;
две группы R вместе с находящимися между ними атомами образуют 3-7-членное насыщенное или частично ненасыщенное моноциклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу;
m равно 0, 1, 2, 3, 4 или 5.
2. Соединение по п. 1, где R1 представляет собой водород, галоген, –CN, –C(O)R, –C(O)OR, –C(O)NR2, –C(O)NRS(O)2R, –C(O)N=S(O)R2, –NR2, –NRC(O)R, –NRC(O)NR2, –NRC(O)OR, –NRS(O)2R, –NRS(O)2NR2, –OR, –ON(R)SO2R, –P(O)R2, –SR, –S(O)R, –S(O)2R, –S(O)(NH)R, –S(O)2N(R)2, –S(NH2)2(O)OH, –N=S(O)R2, -CH3, -CH2OH, -CH2NHSO2CH3, –CD3, –CD2NRS(O)2R или R.
3. Соединение по п. 1, где две группы R1 вместе образуют двухвалентную C2-4 алкиленовую цепь.
4. Соединение по п.1, где две группы R1 вместе образуют =O или =NH.
5. Соединение по любому из пп. 1-4, в котором m равно 1, 2, 3, 4 или 5, предпочтительно 1, 2 или 3.
6. Соединение по п. 2, где каждый R независимо означает водород или группу, выбранную из группы, включающей C1-6 алифатическую группу, 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо, фенил, 8-10-членное бициклическое ароматическое карбоциклическое кольцо, 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу, или 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу.
7. Соединение по п. 2, где R представляет собой водород.
8. Соединение по п. 2, где R представляет собой C1-6 алифатическую группу.
9. Соединение по п. 2, где R представляет собой 3-8-членное насыщенное или частично ненасыщенное моноциклическое карбоциклическое кольцо.
10. Соединение по п. 2, где R представляет собой фенил.
11. Соединение по п. 2, где R представляет собой 8-10-членное бициклическое ароматическое карбоциклическое кольцо.
12. Соединение по п. 2, где R представляет собой 4-8-членное насыщенное или частично ненасыщенное моноциклическое гетероциклическое кольцо, содержащее 1-2 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
13. Соединение по п. 2, где R представляет собой 5-6-членное моноциклическое гетероароматическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
14. Соединение по п. 2, где R представляет собой 8-10-членное бициклическое гетероароматическое кольцо, содержащее 1-5 гетероатомов, независимо выбранных из группы, включающей азот, кислород или серу.
15. Соединение по п. 2, где две группы R вместе образуют двухвалентную C2-4 алкиленовую цепь.
16. Соединение по п. 2, где две группы R вместе с находящимися между ними атомами образуют 3-7-членное насыщенное или частично ненасыщенное моноциклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из группы, включающей азот, кислород или серу.
17. Соединение по п. 1, где R1 выбран из группы, состоящей из фтора, хлора, метила, этила, –OH, –OCH3, –CH2OH, –CH2CN, –CF3, –CH2NH2, –COOH, –NH2,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
18. Соединение по п. 1, где R1 выбран из группы, состоящей из:
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
19. Соединение по п. 1, где R1 выбран из группы, состоящей из:
 ,
, ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
20. Соединение по п. 1, где R1 выбран из группы, состоящей из:
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 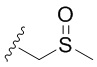 ,
, 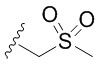 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 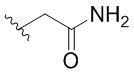 ,
,  ,
,  ,
,  ,
,  и
и  .
.
21. Соединение по п. 1, где R1 выбран из группы, состоящей из:
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
22. Соединение по п. 1, где R1 выбран из группы, состоящей из:
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
23. Соединение по п. 1, где R1 выбран из группы, состоящей из:
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, ,
,  ,
,  ,
,  и
и  .
.
24. Соединение по п. 1, где R1 выбран из группы, состоящей из:
 ,
,  ,
,  ,
,  ,
, 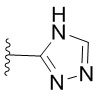 ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 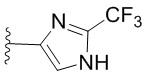 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
25. Соединение по п. 1, выбранное из группы, состоящей из:
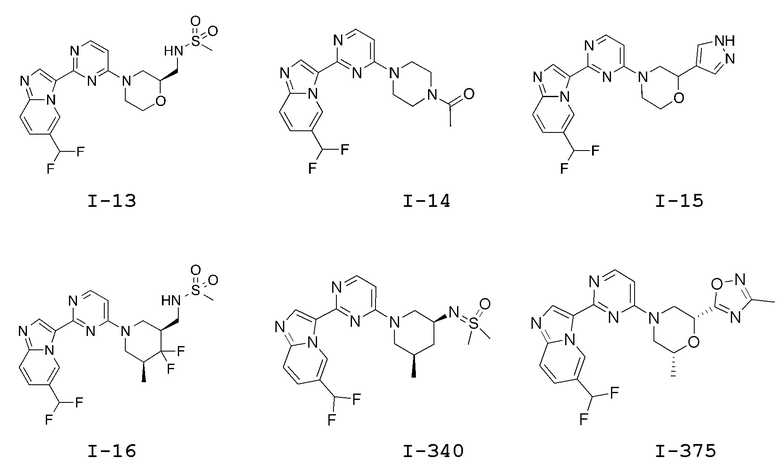
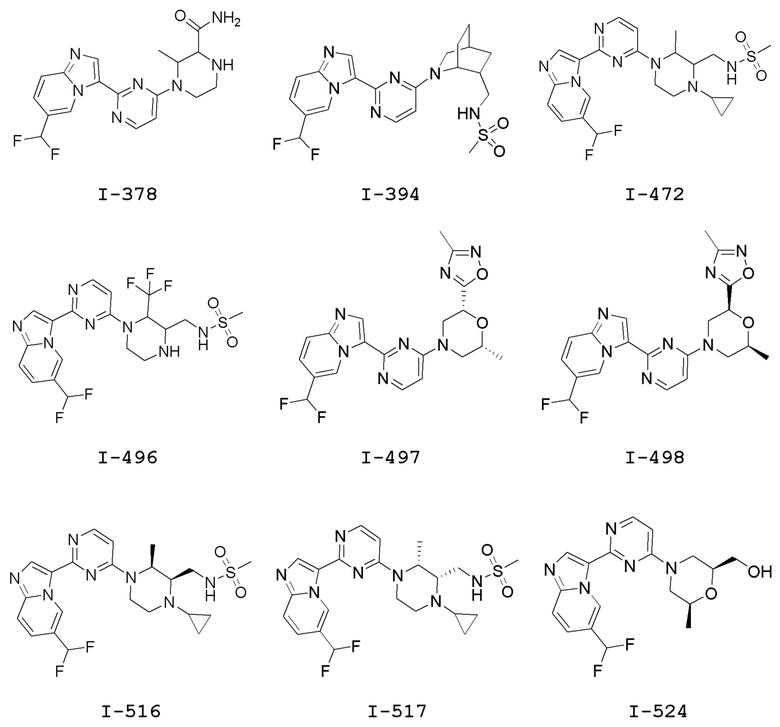
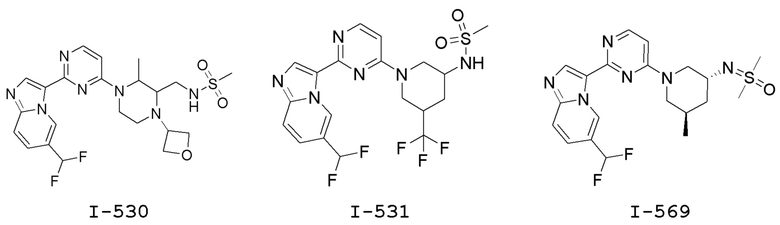
или его фармацевтически приемлемая соль.
26. Соединение, выбранное из группы, состоящей из:
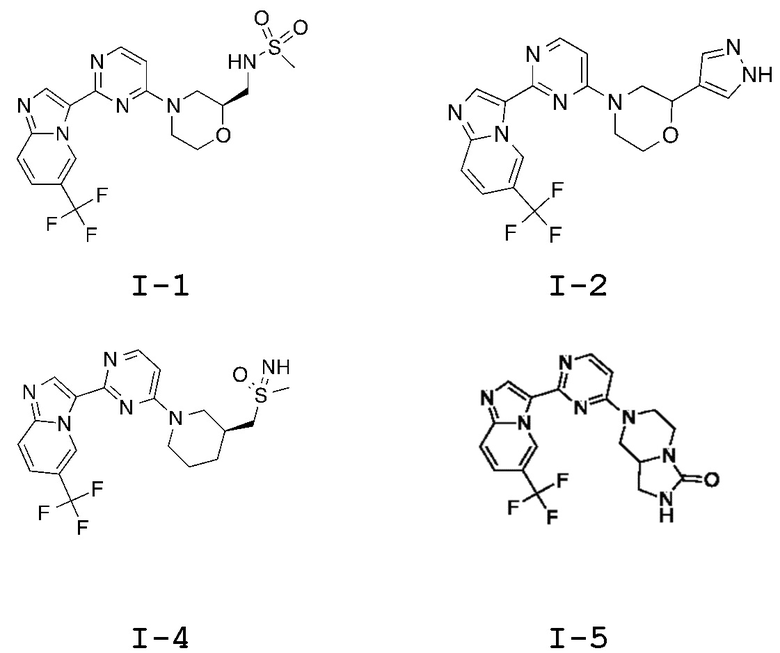
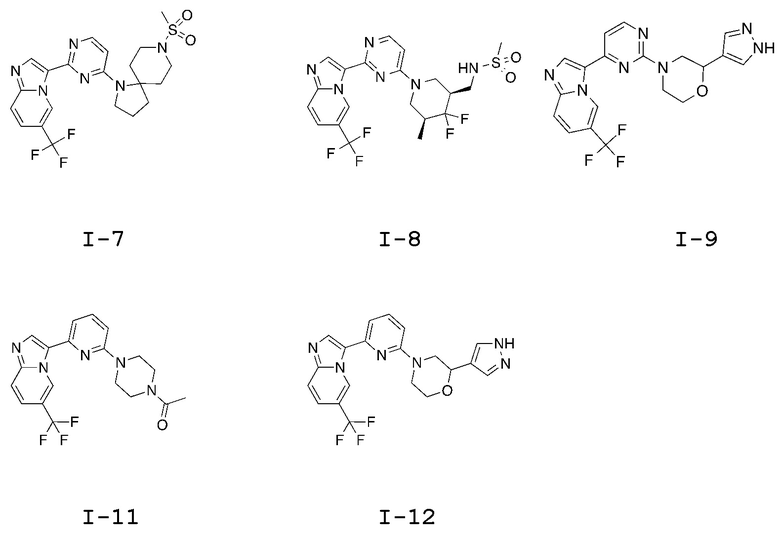
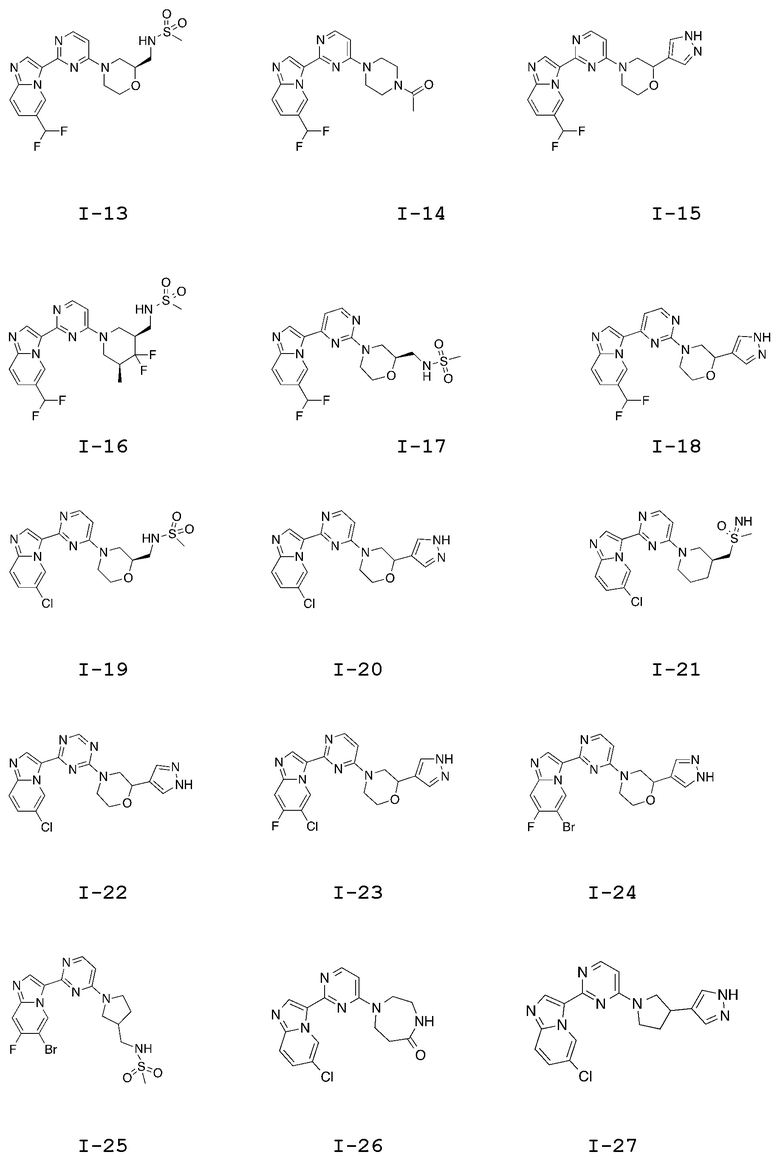
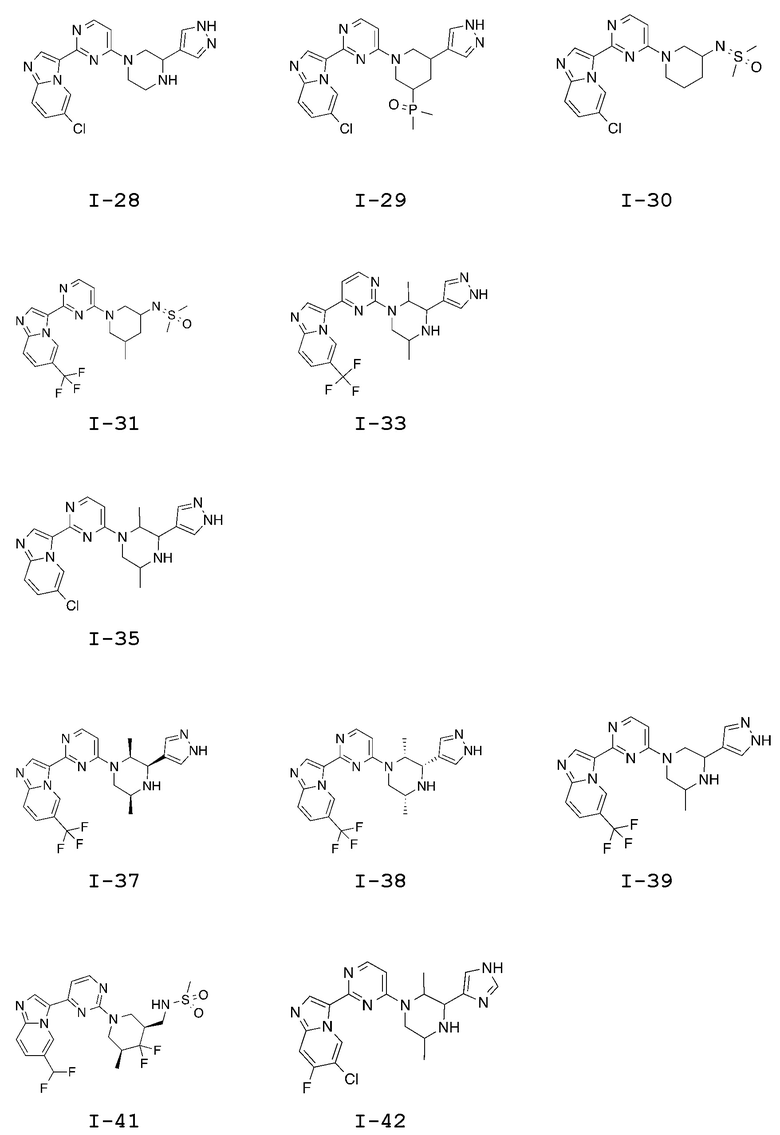
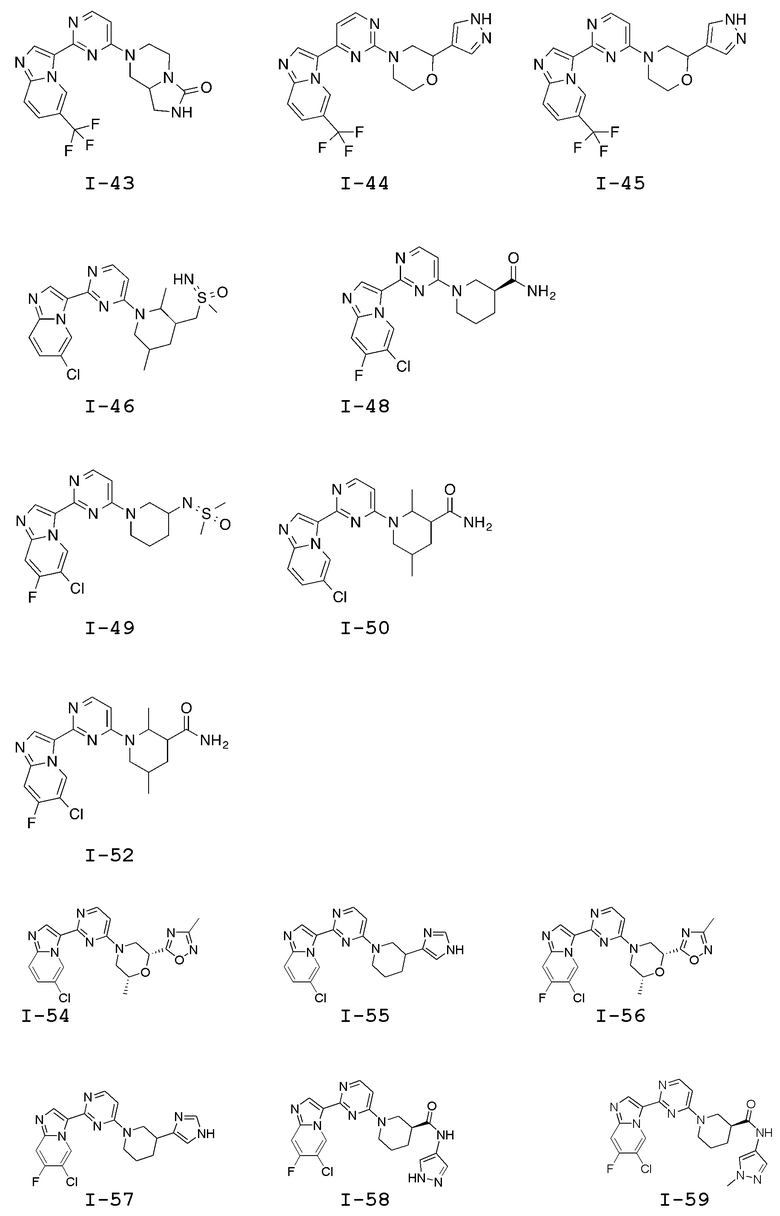
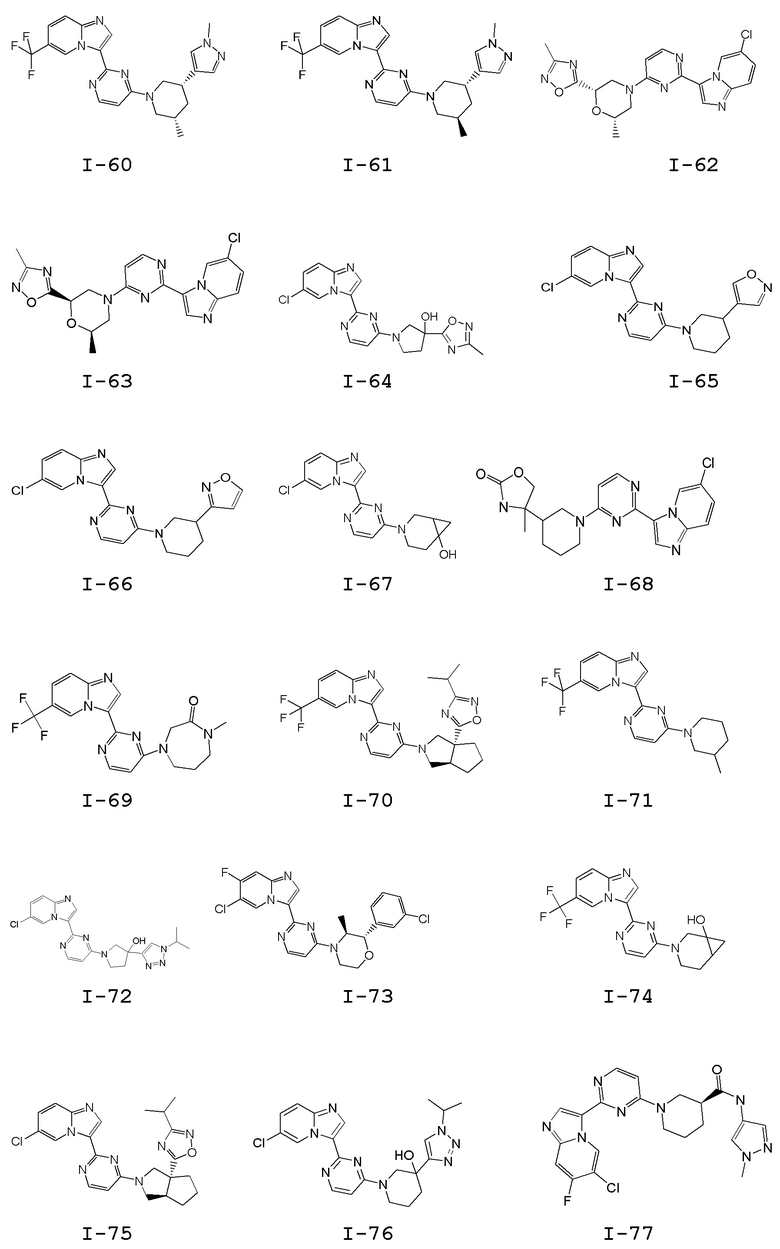
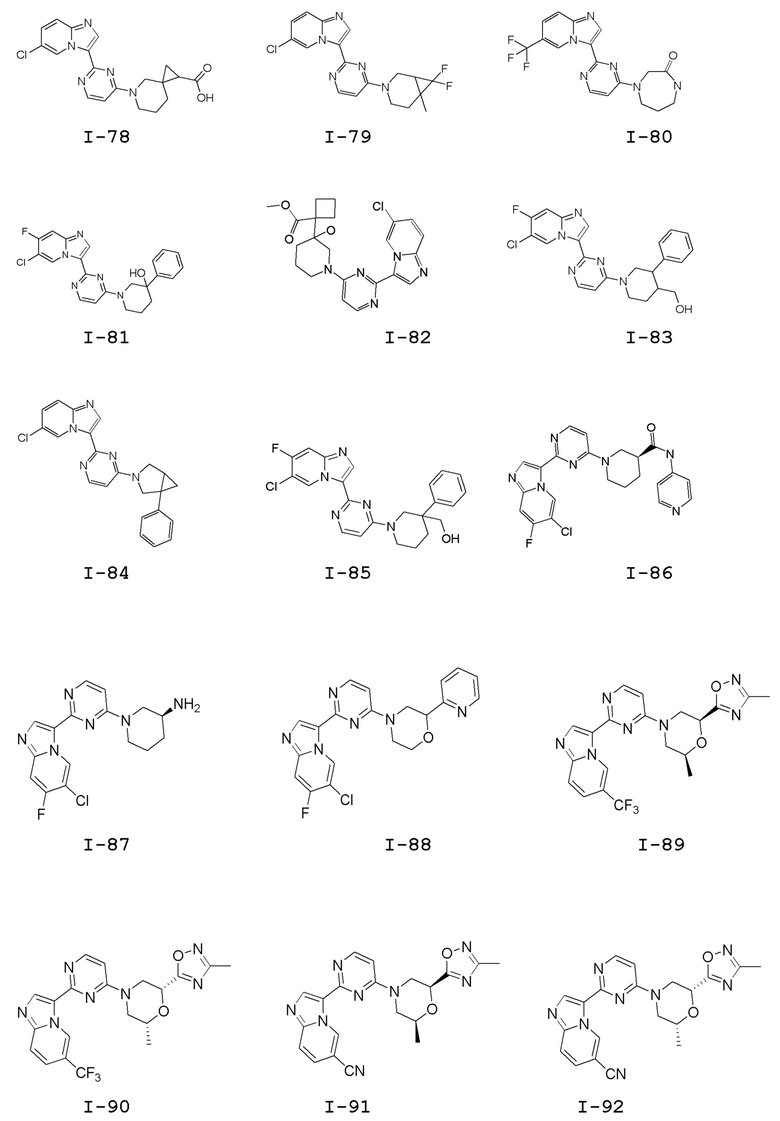
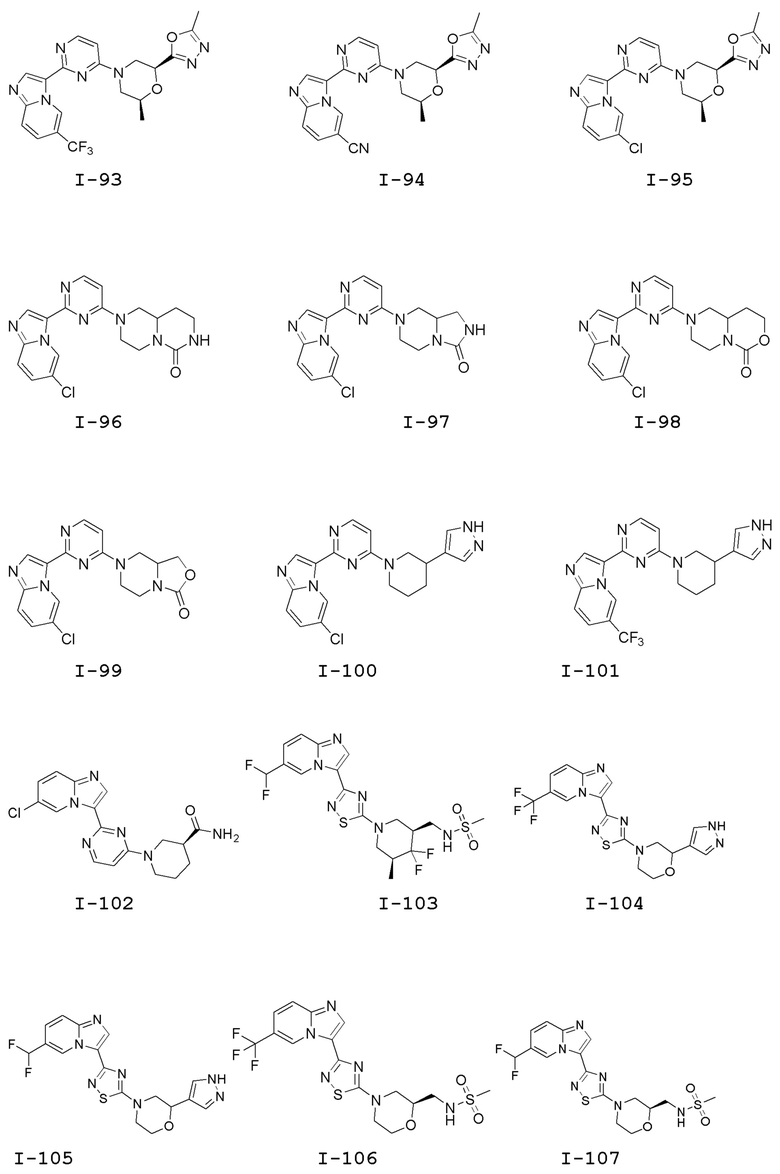
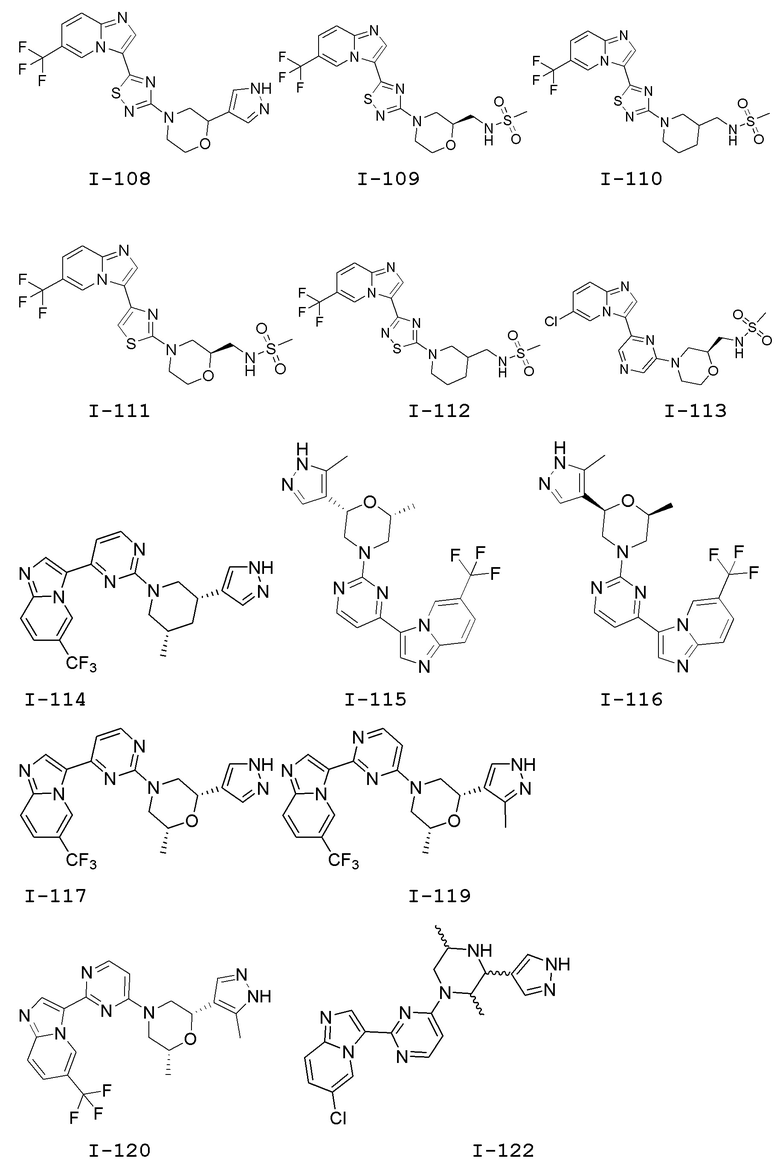
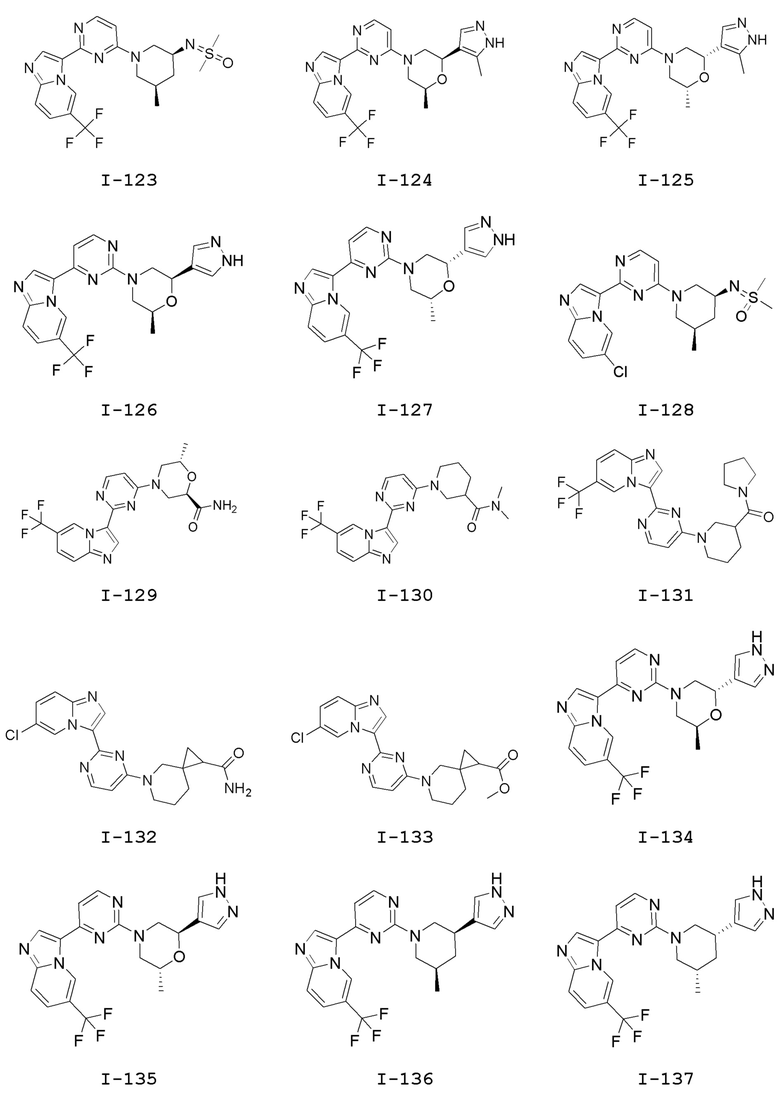
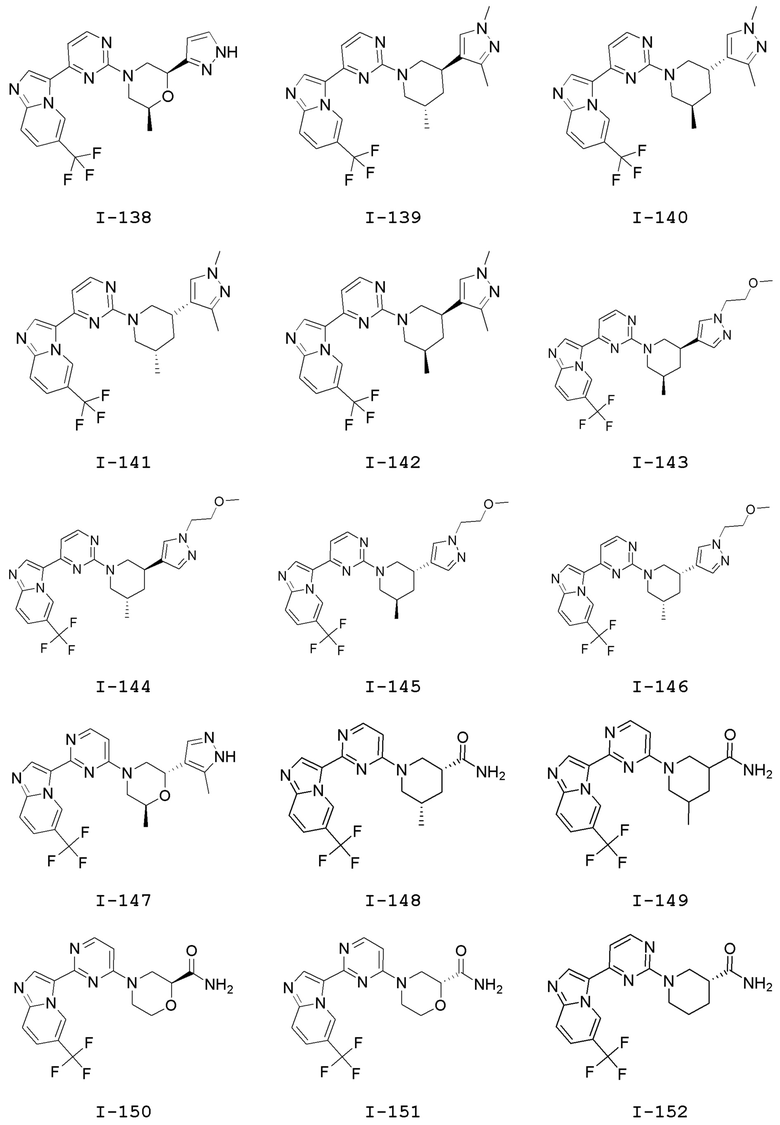
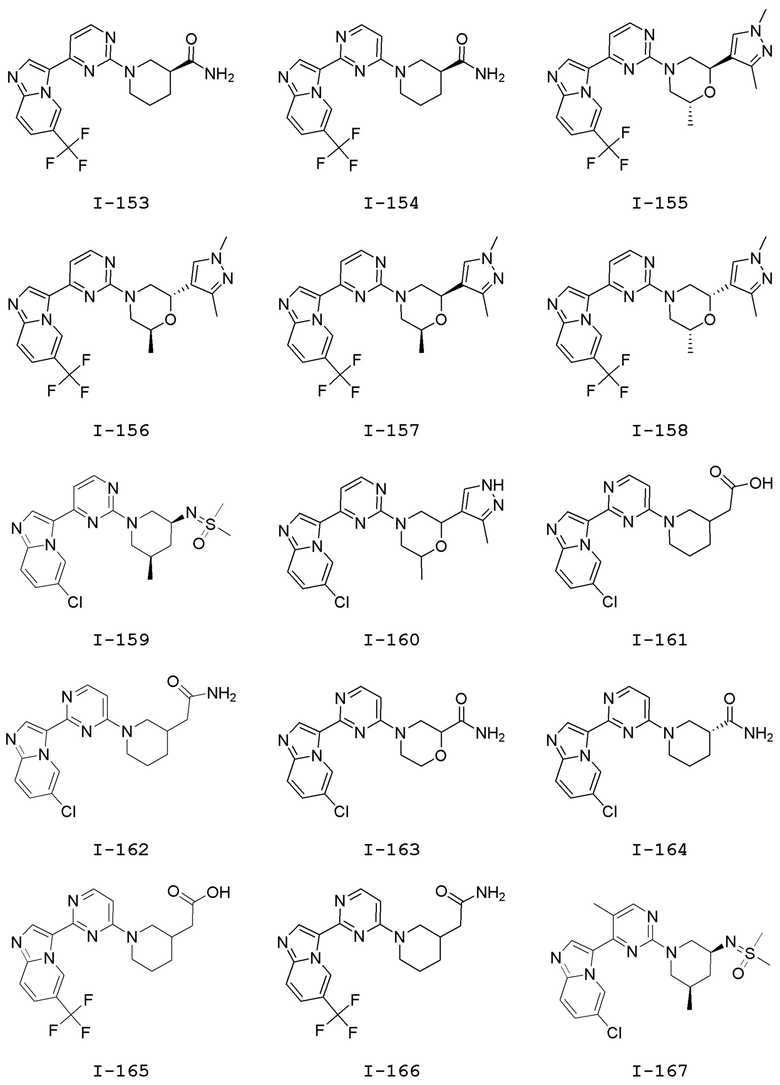
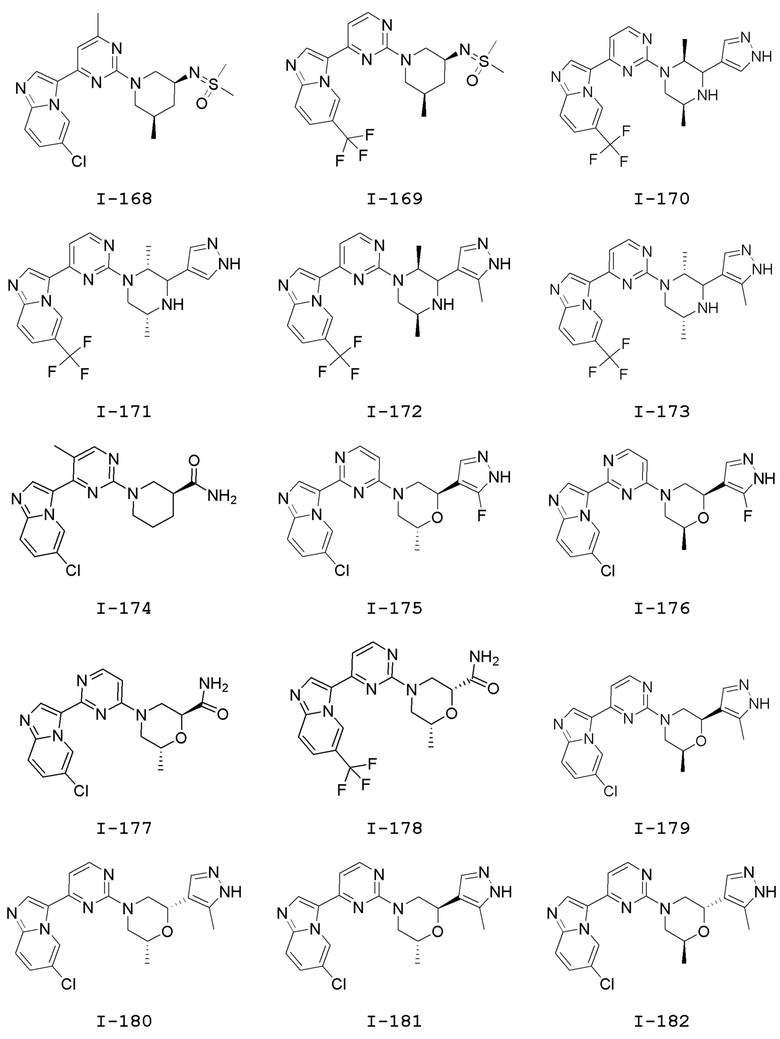
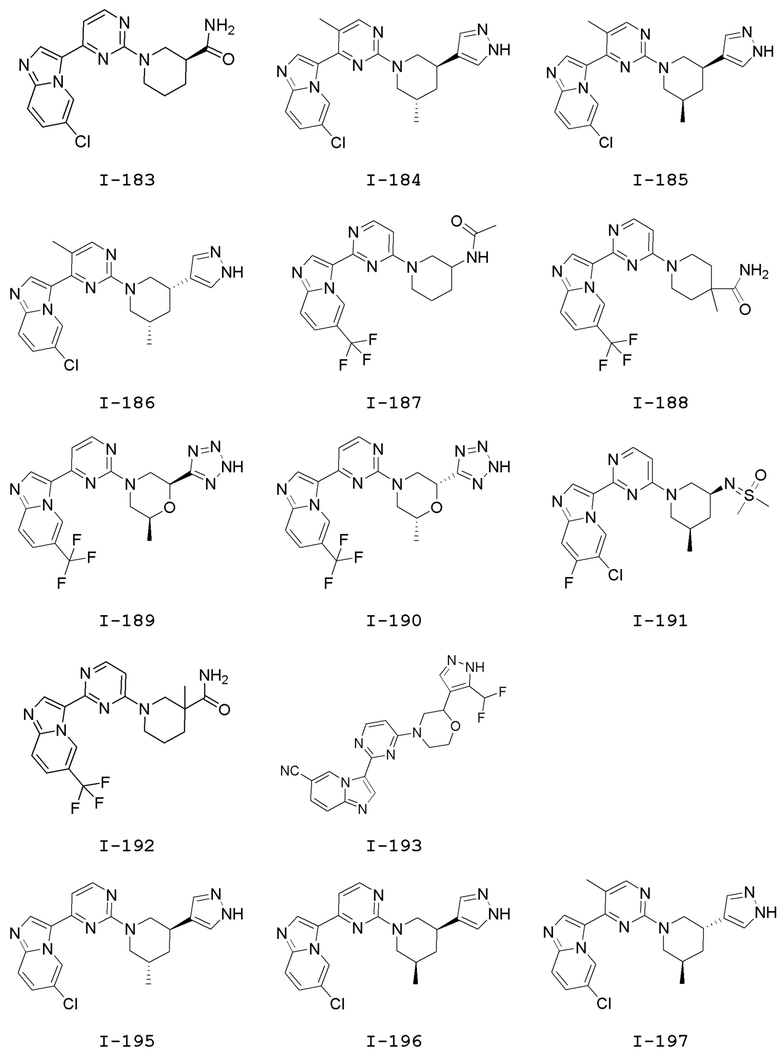
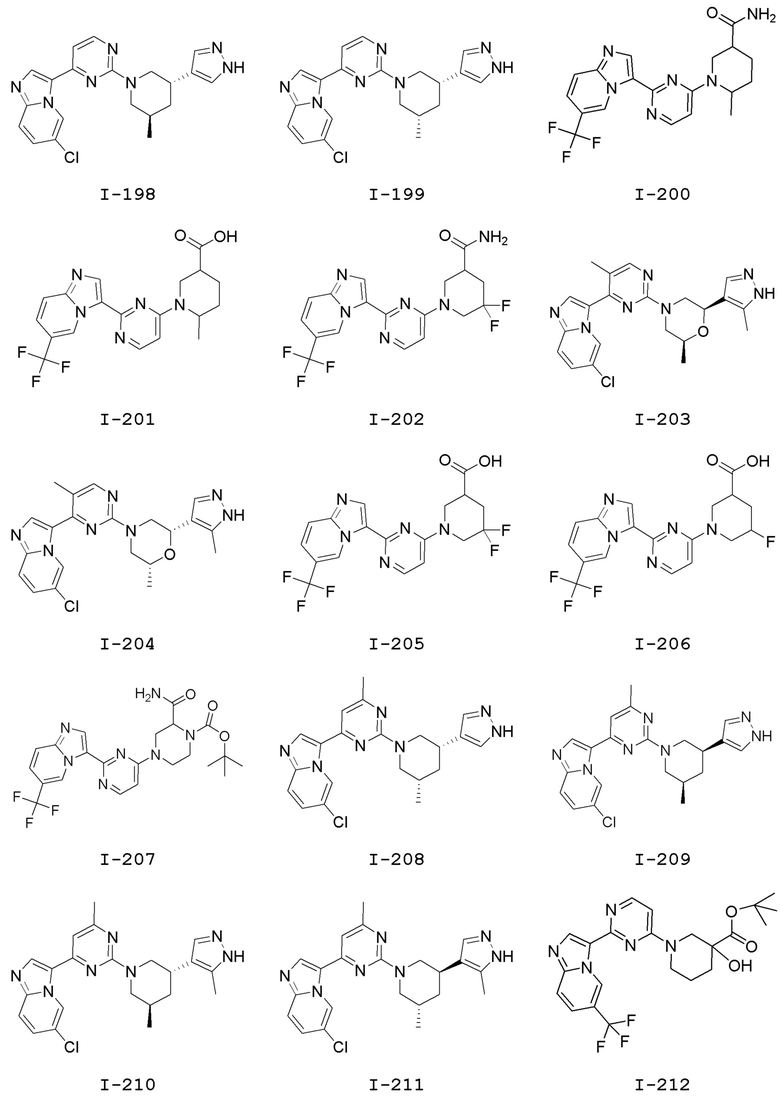
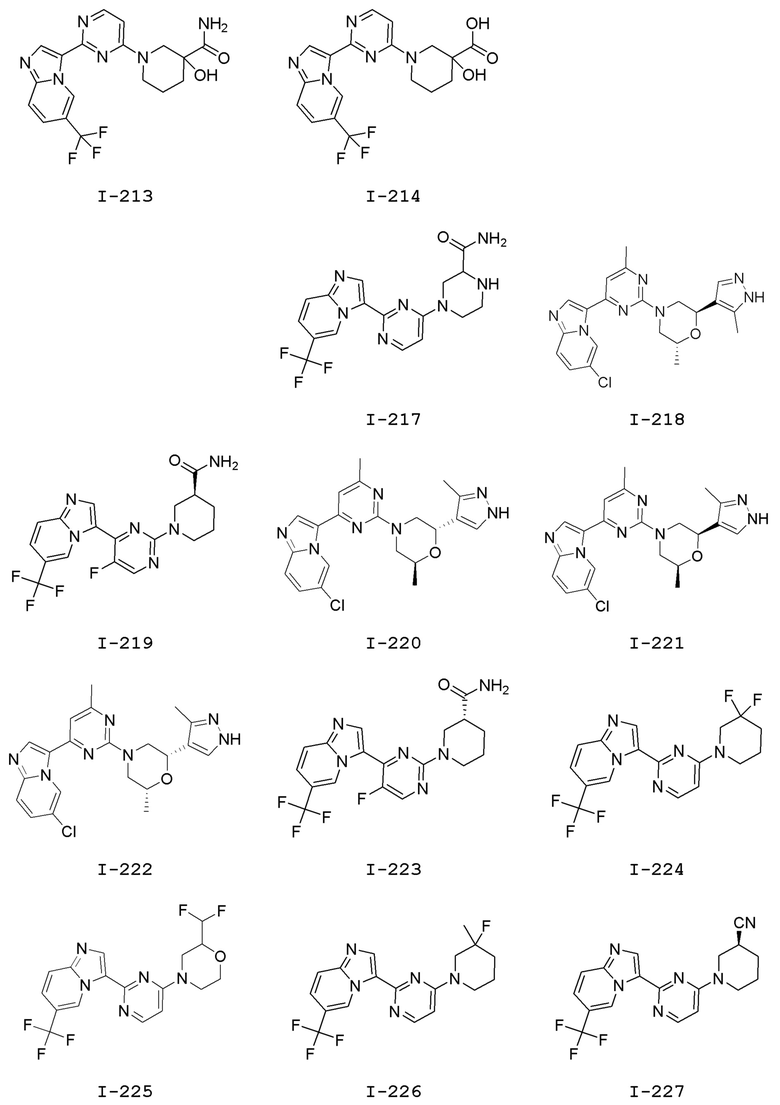
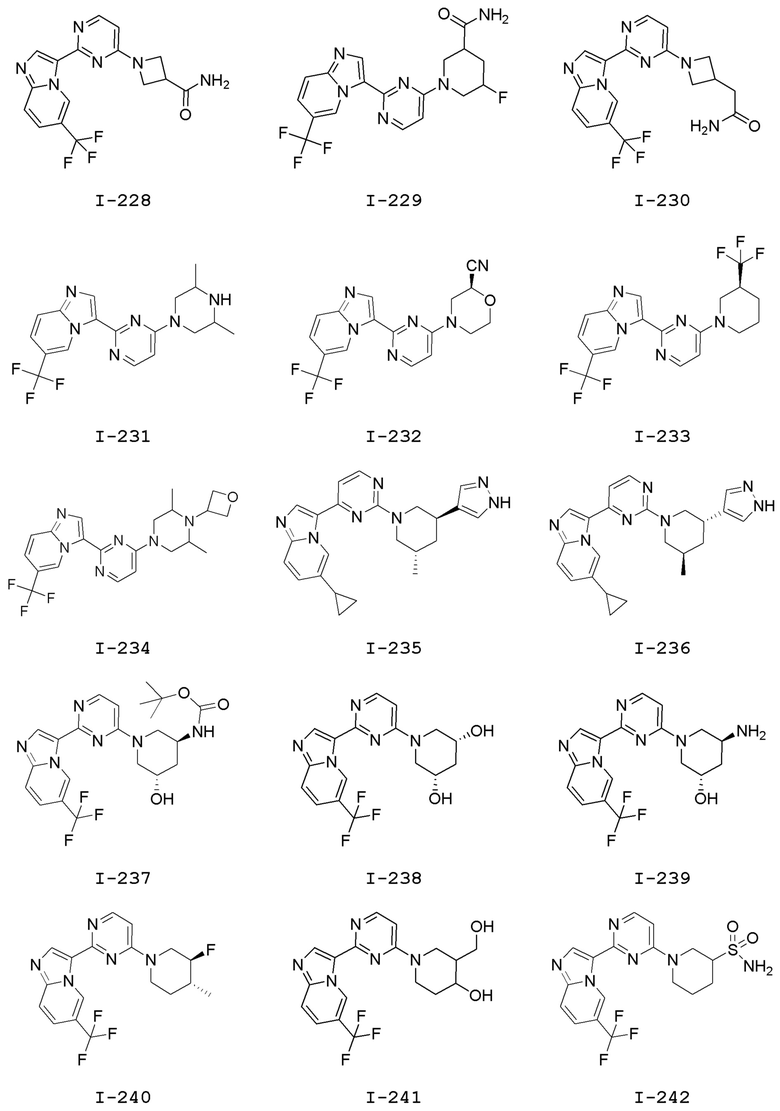
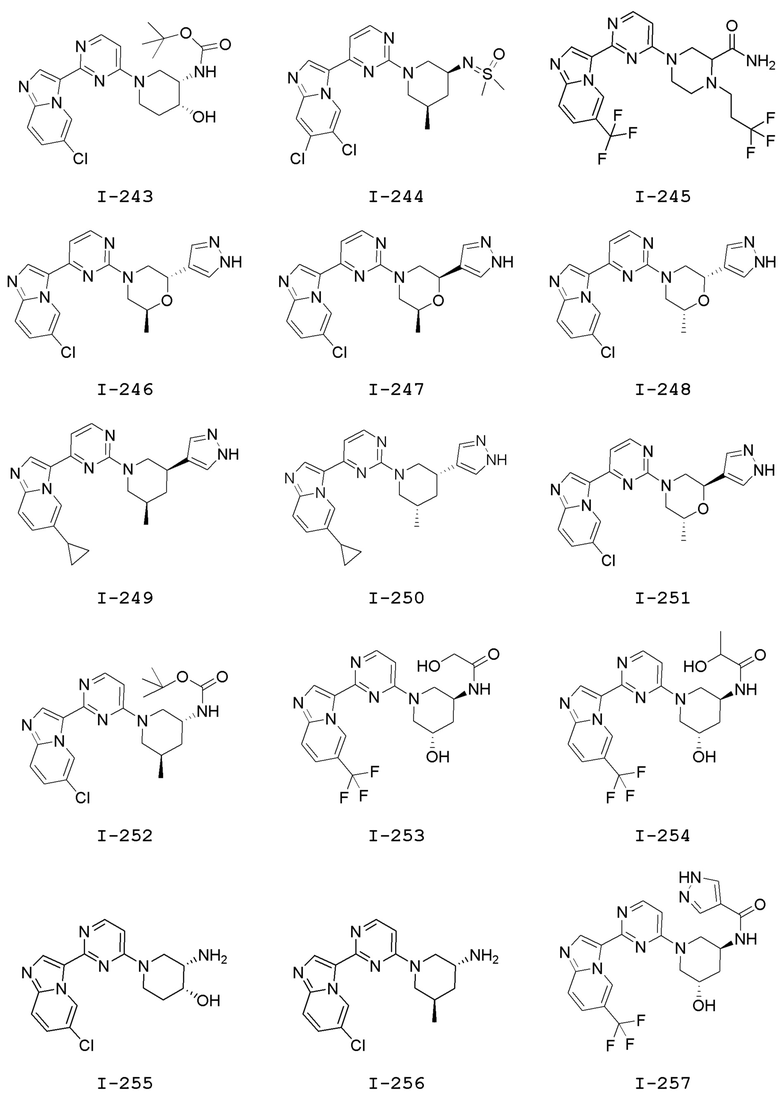
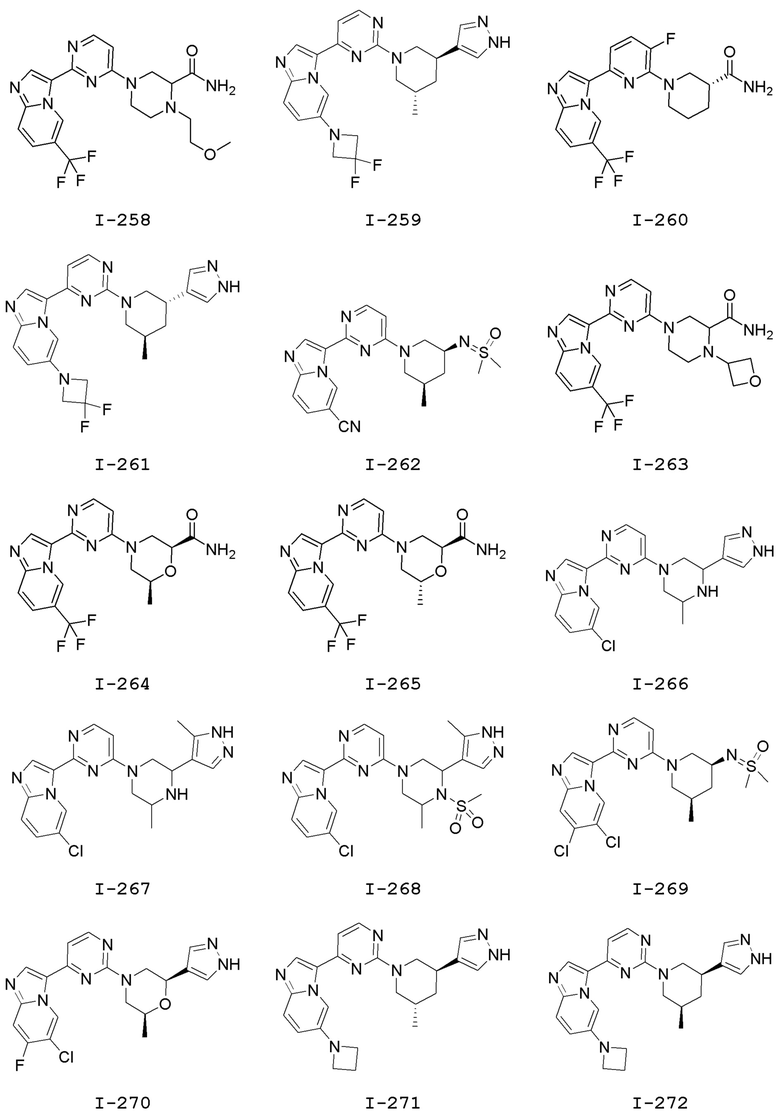
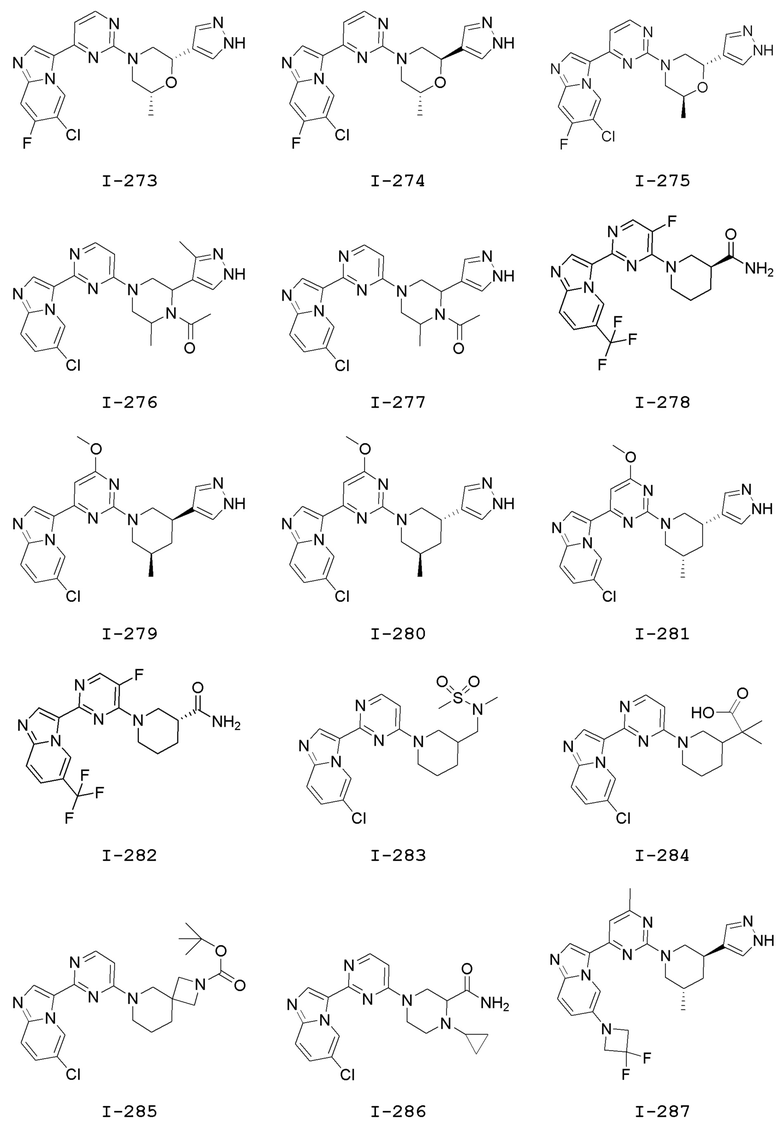
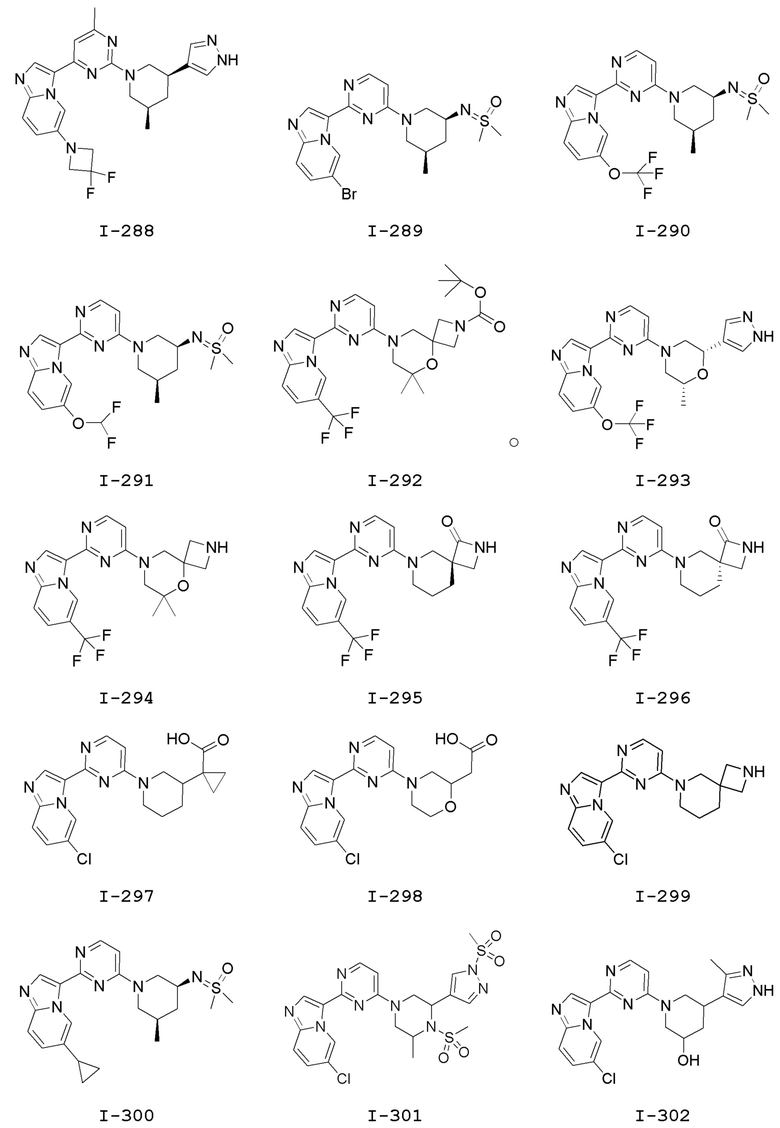
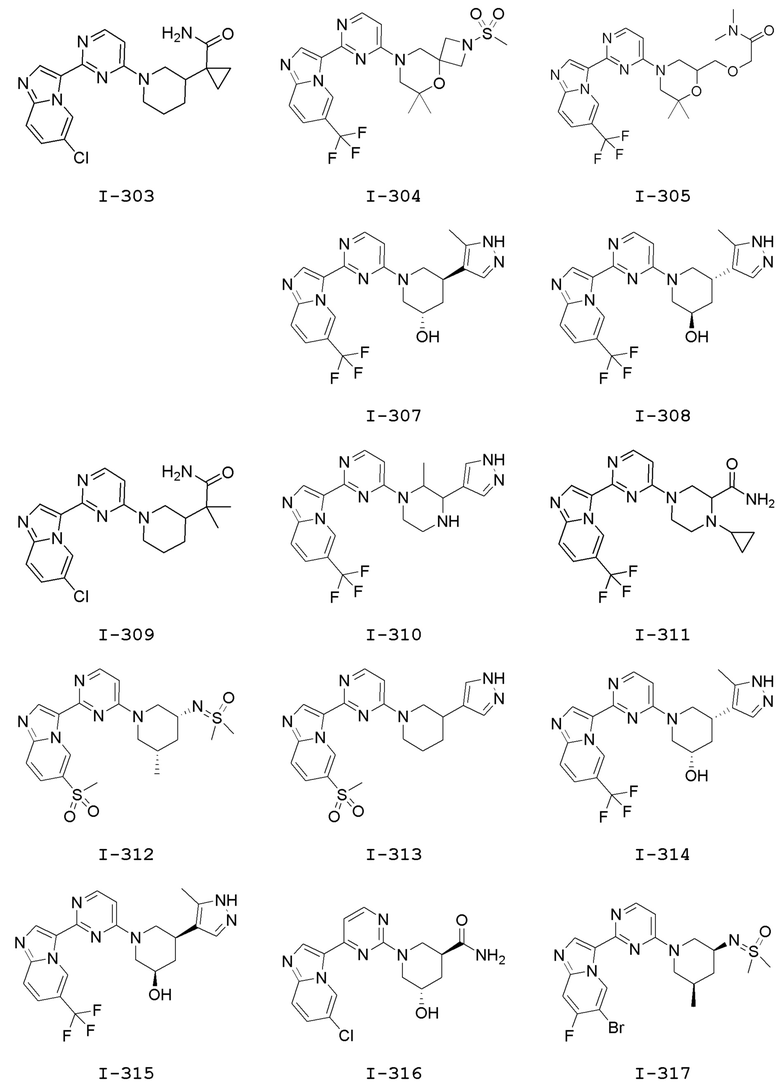
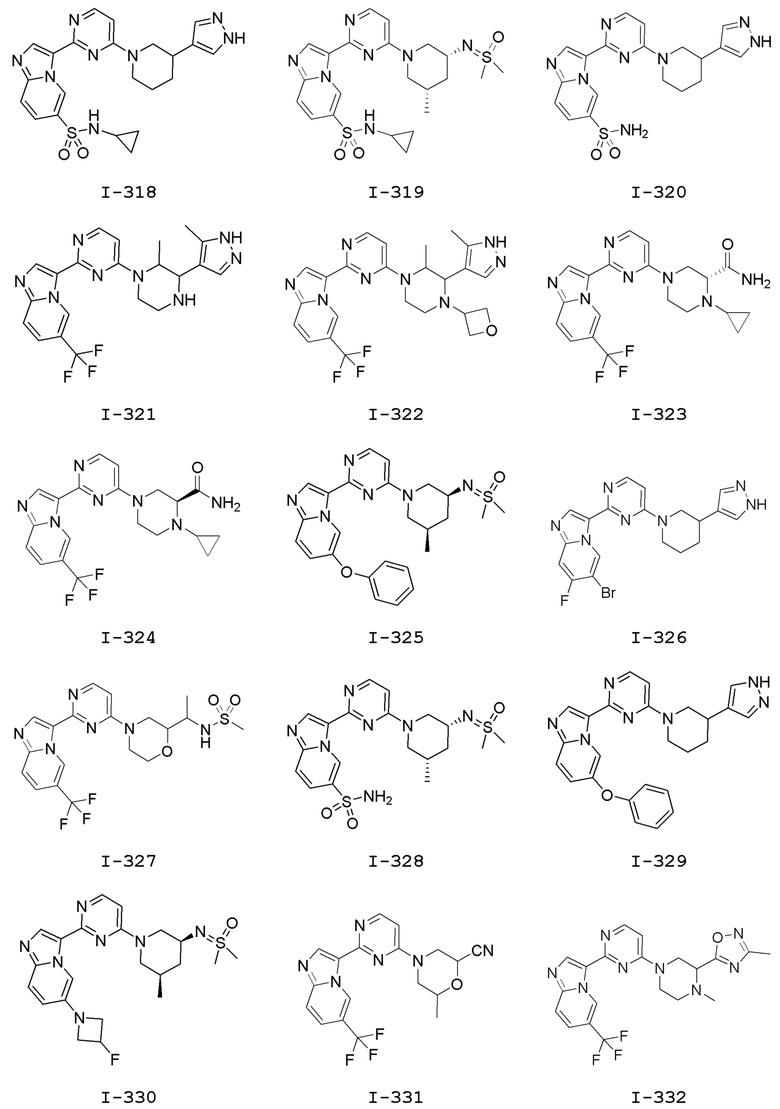
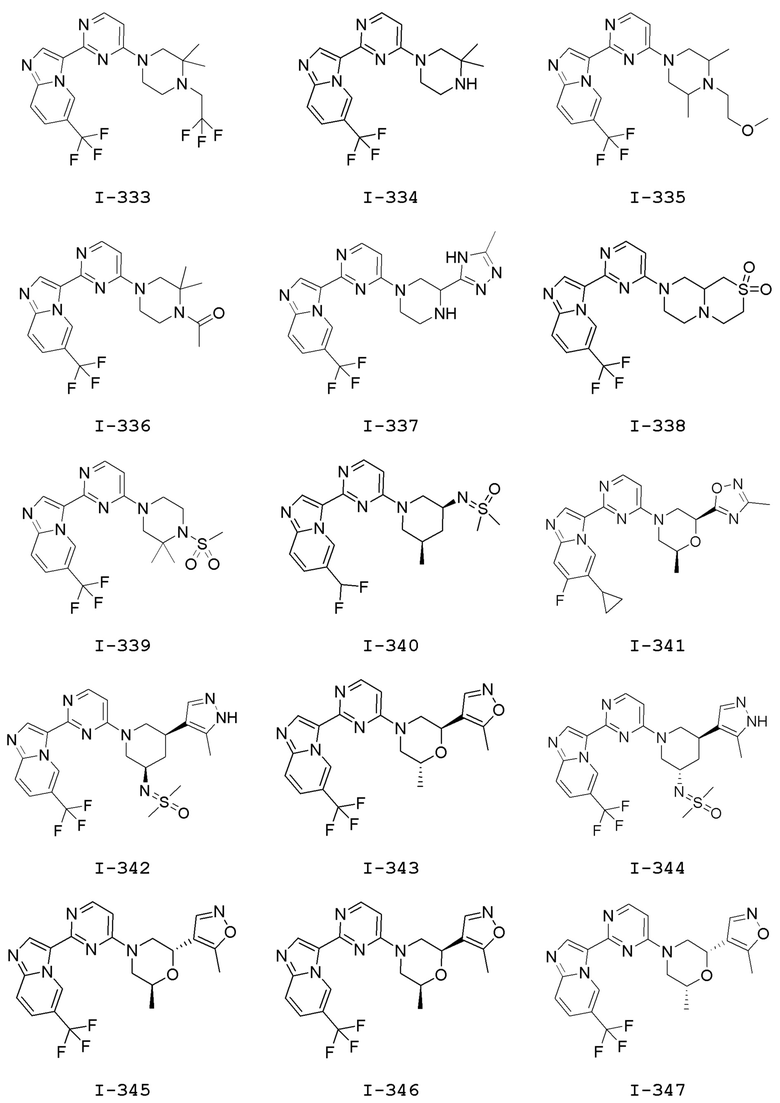
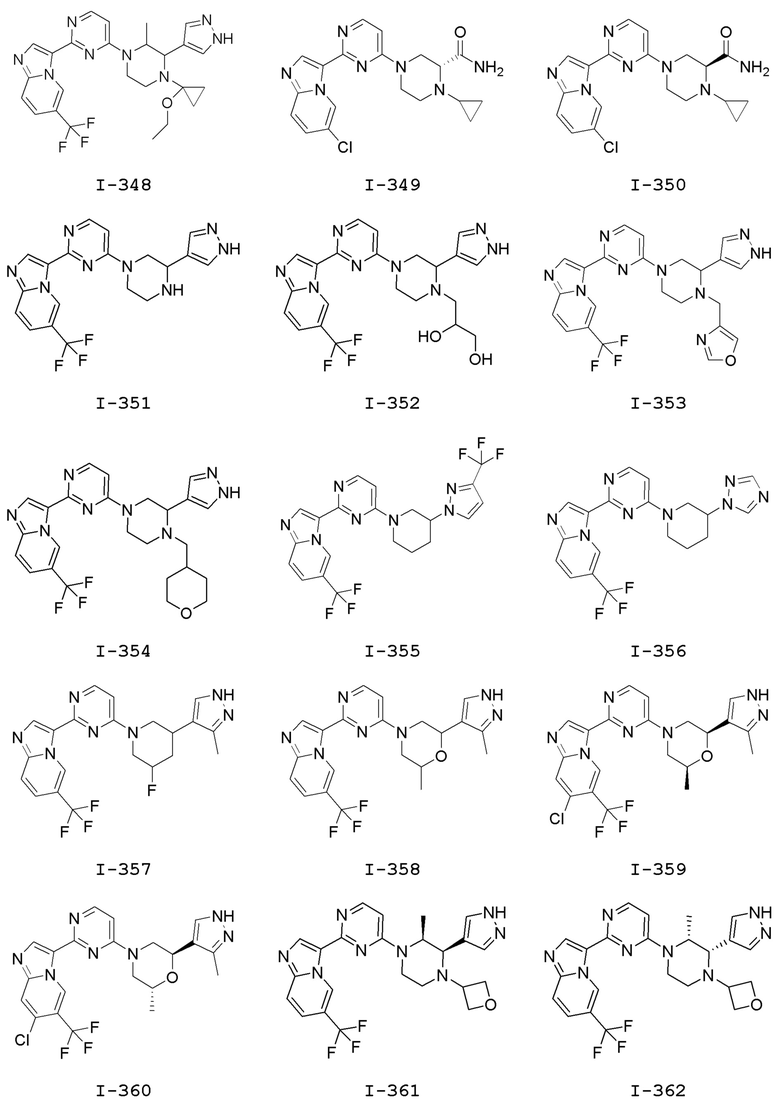
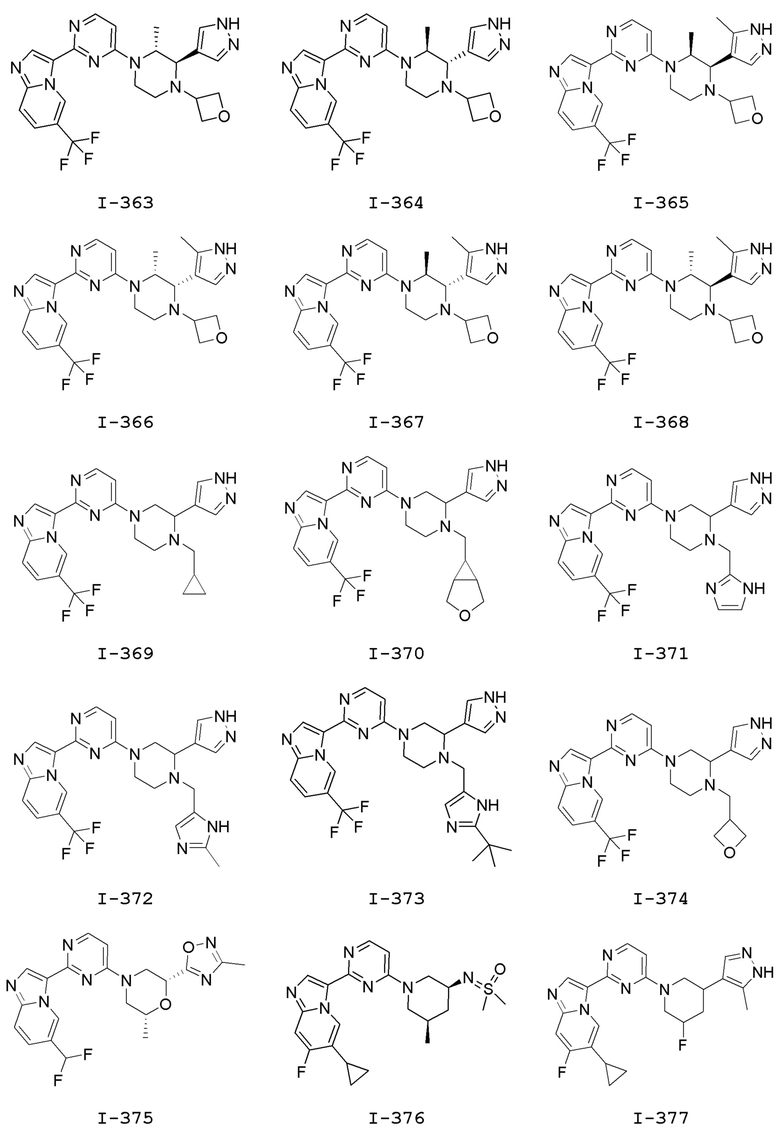
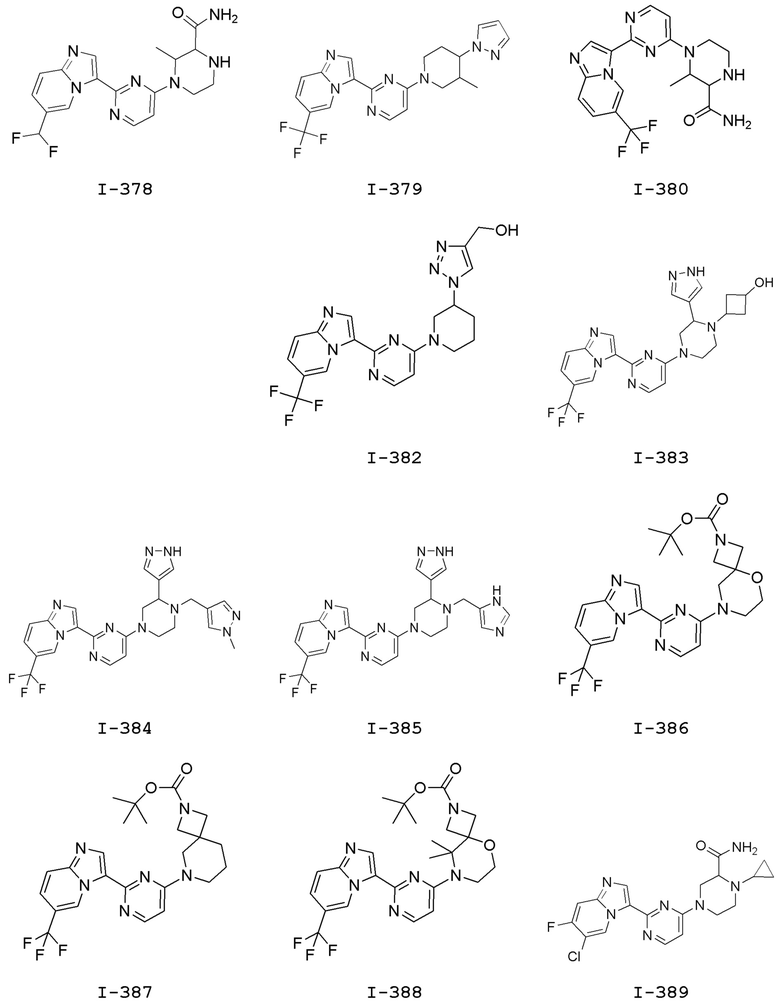
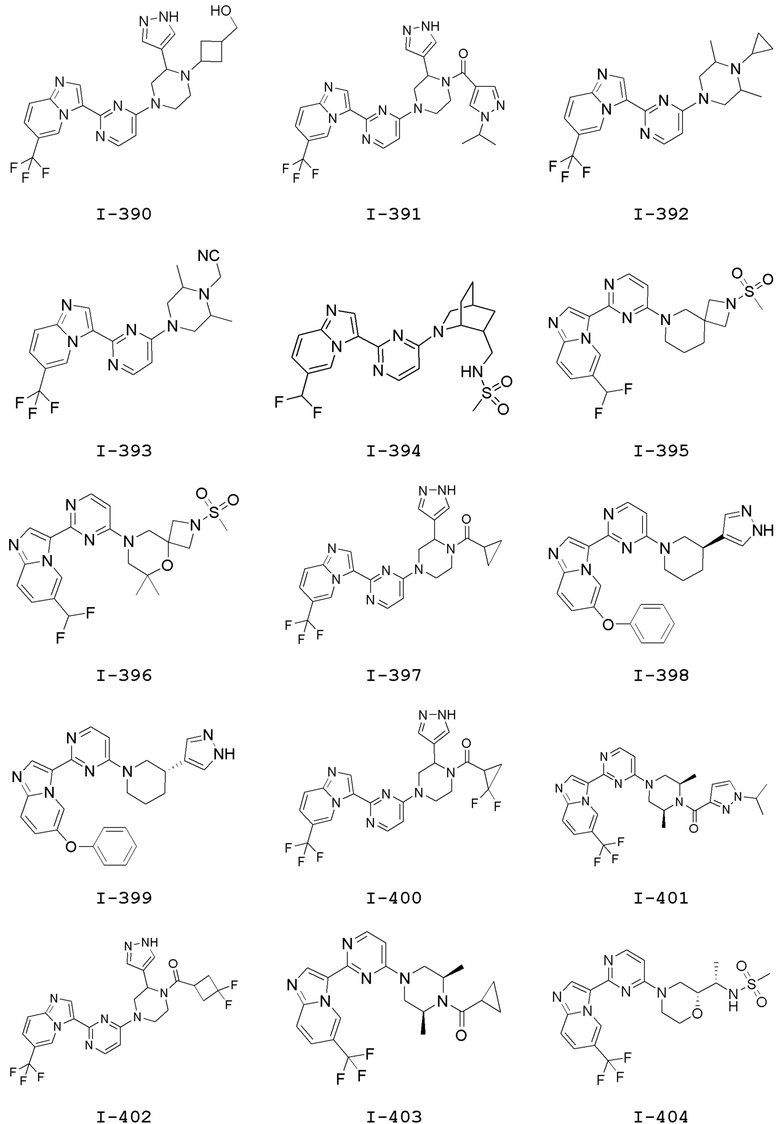
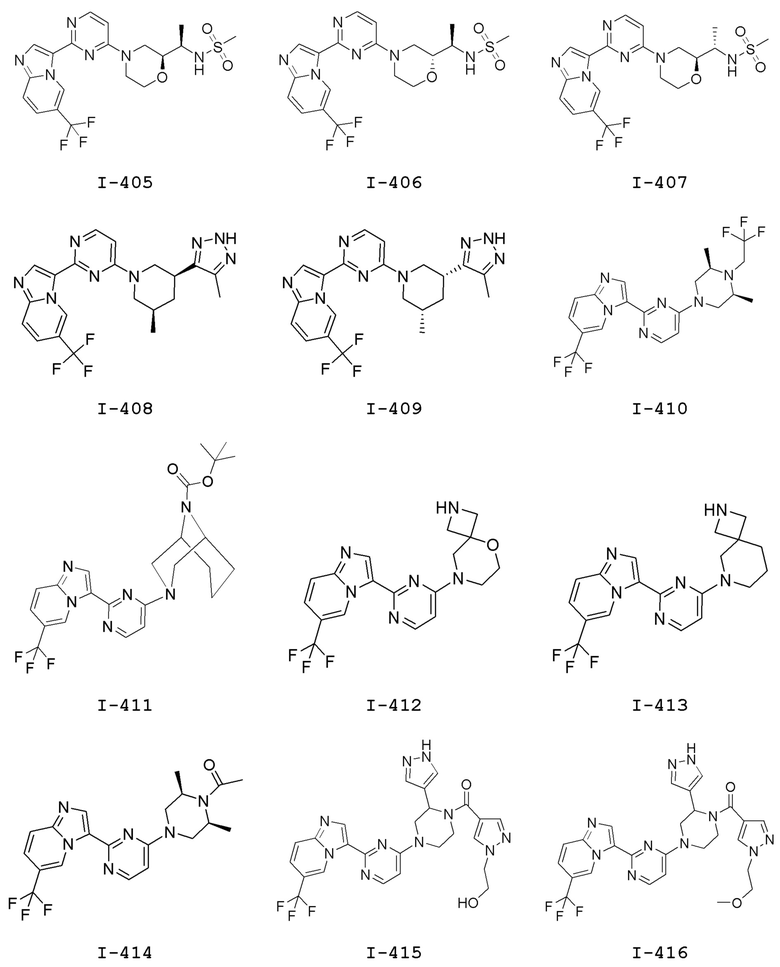
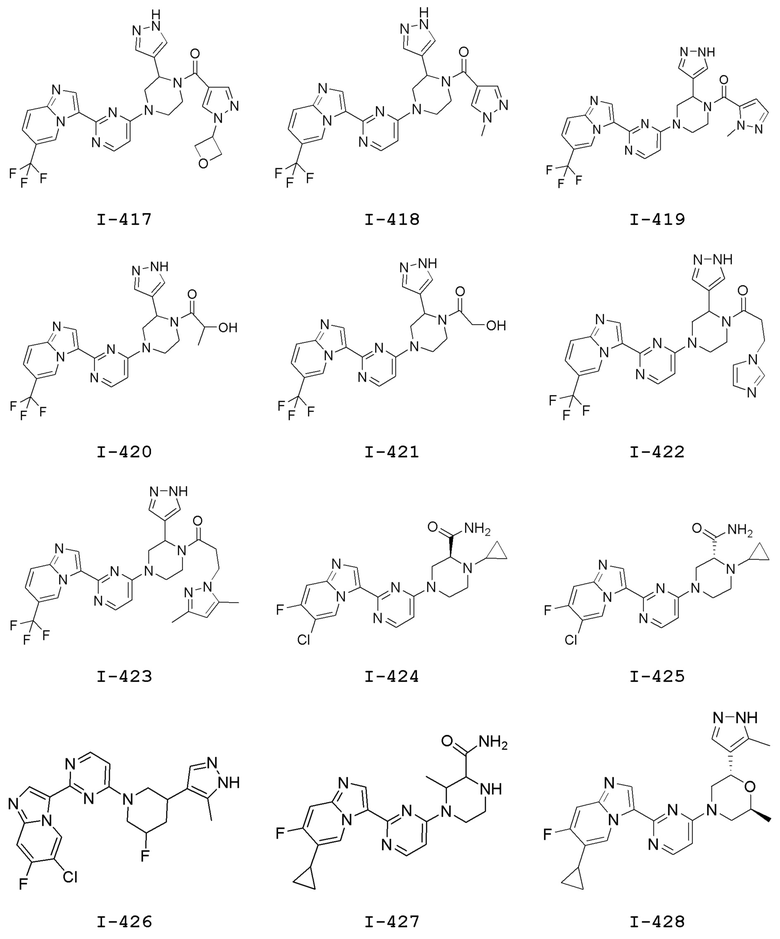
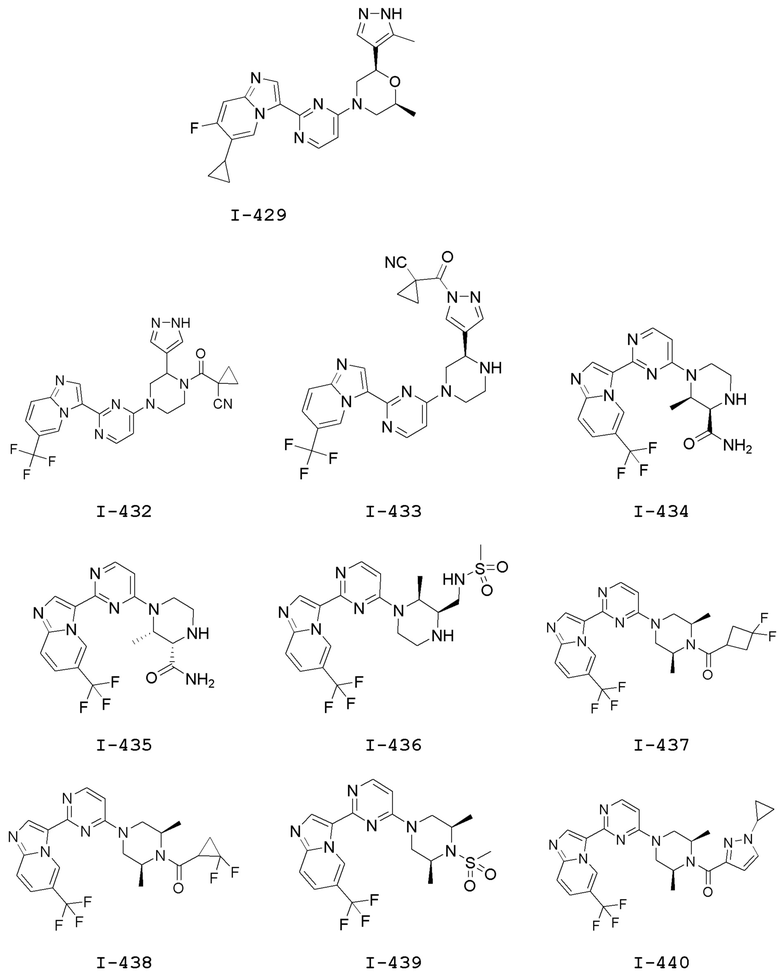
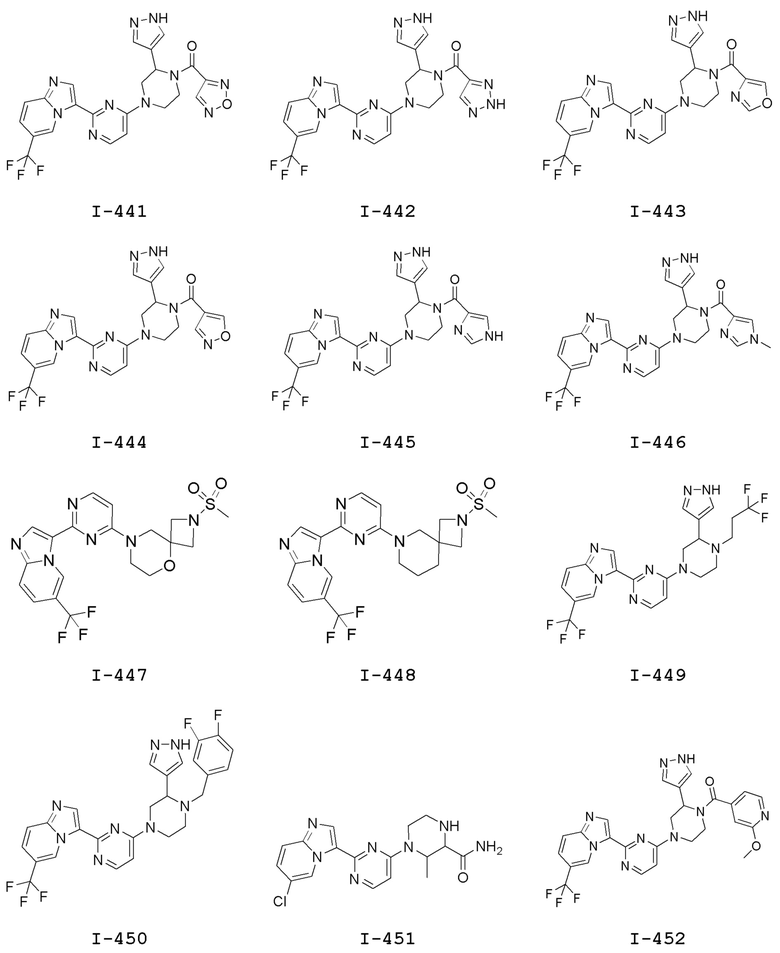
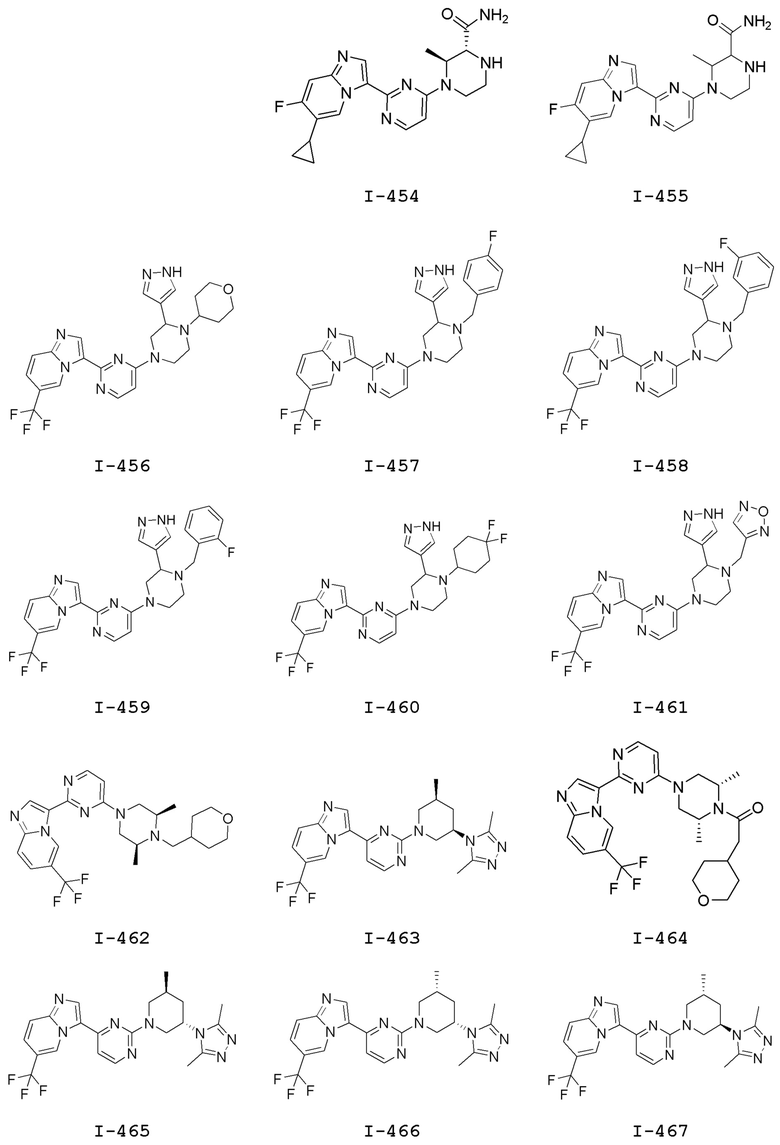
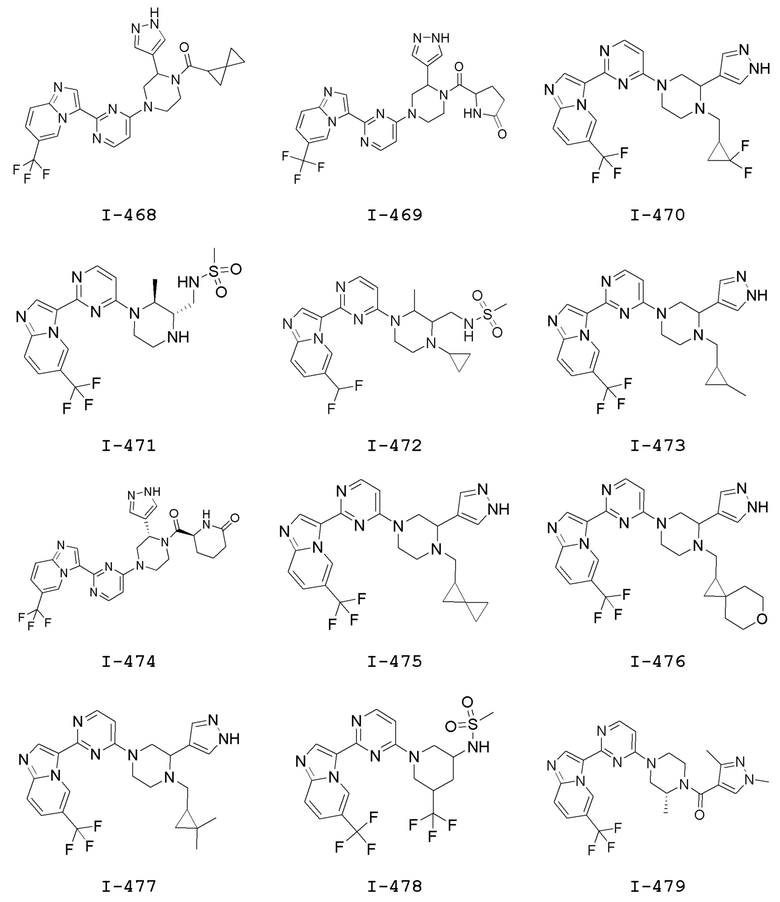
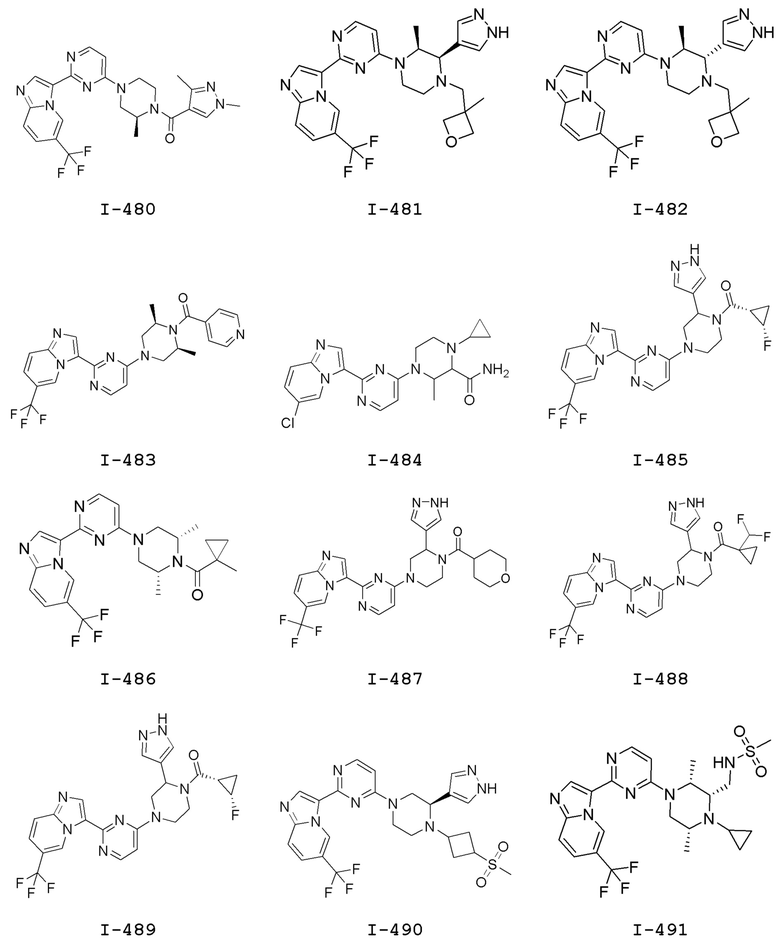
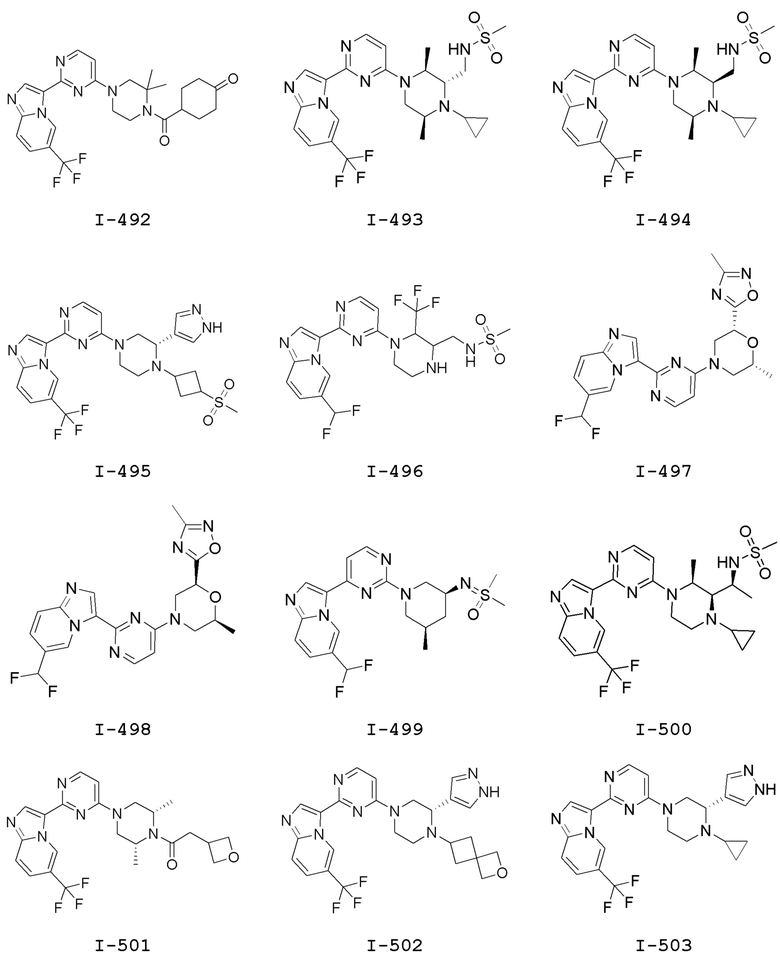
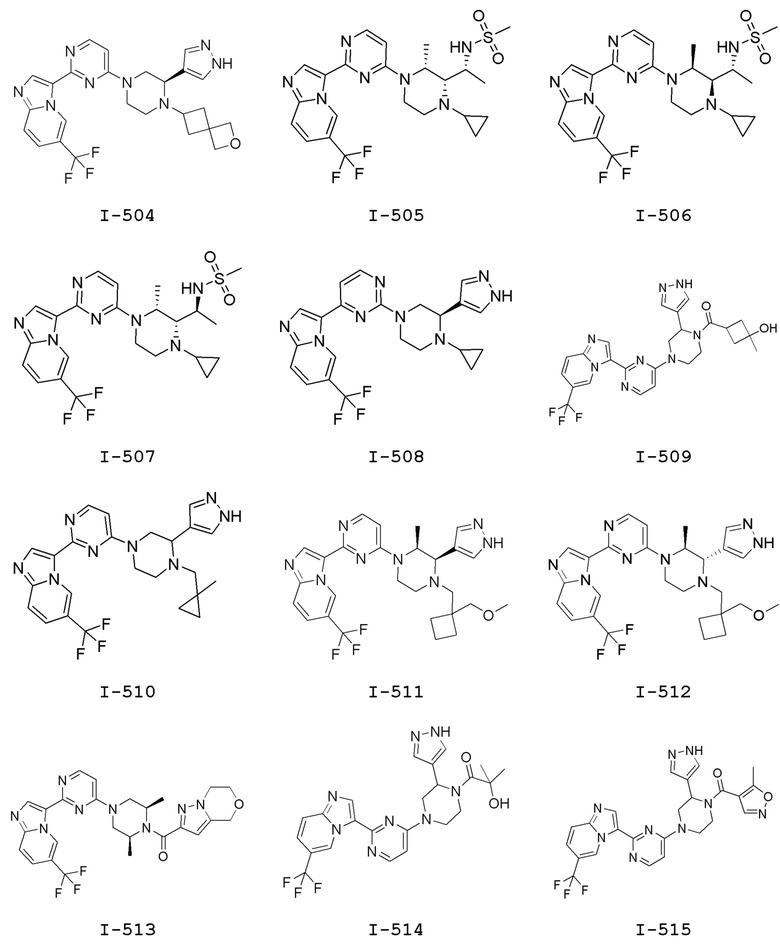
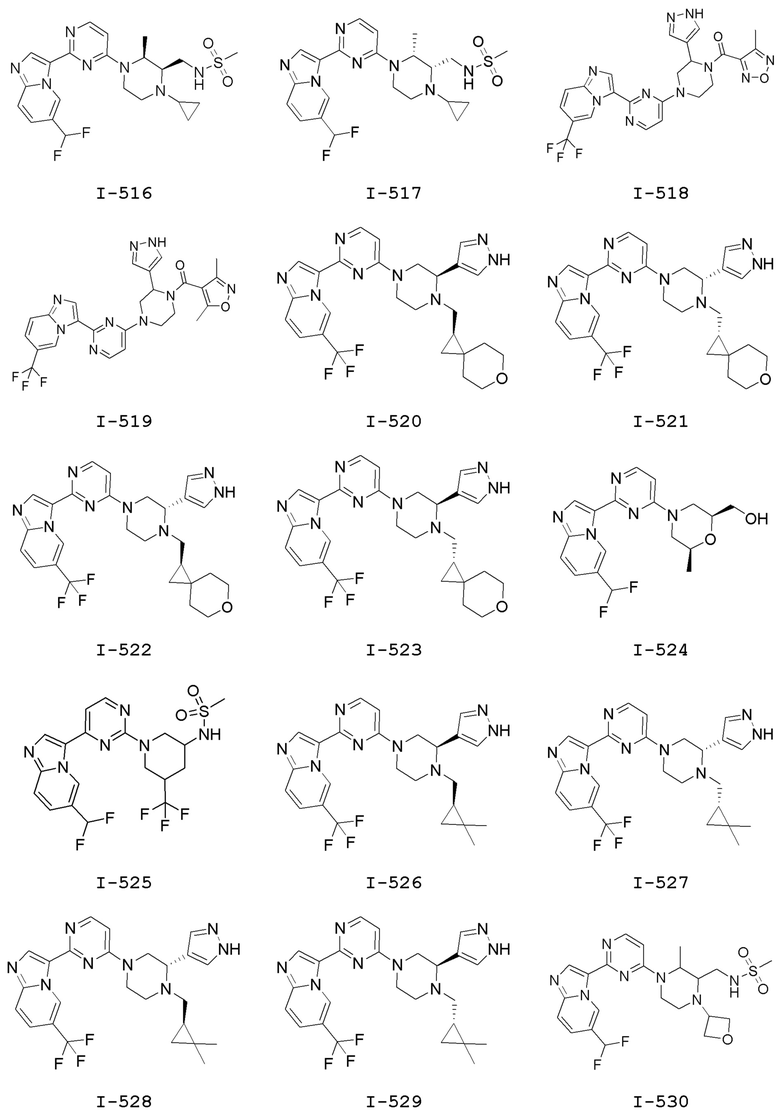
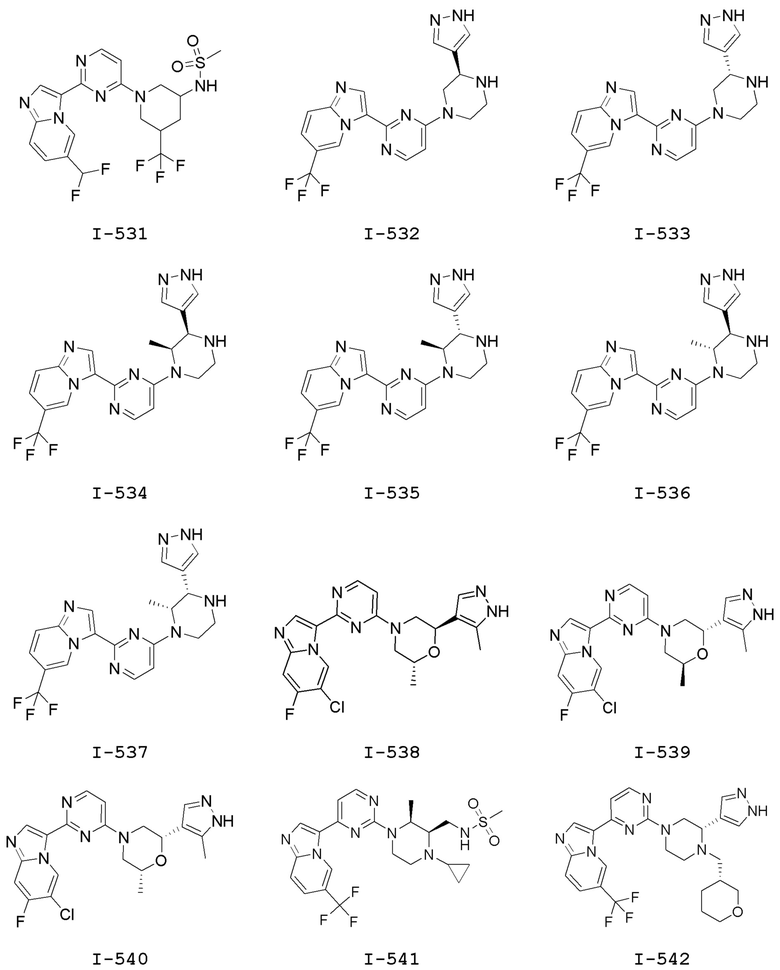
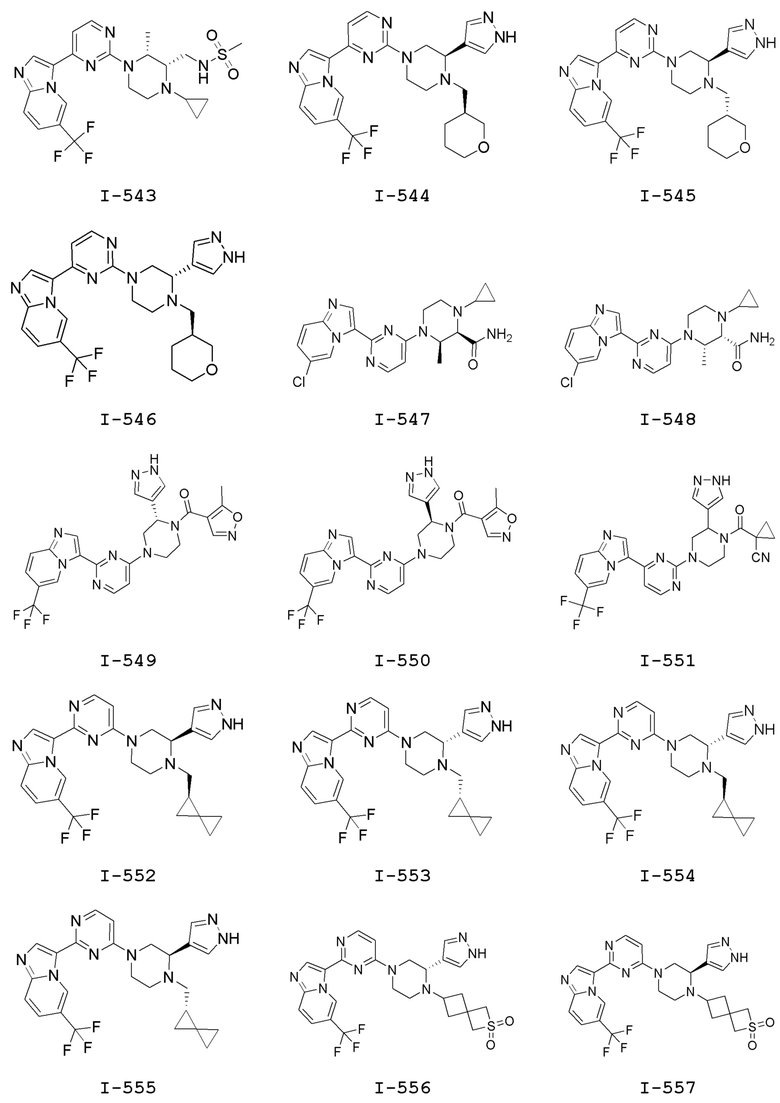
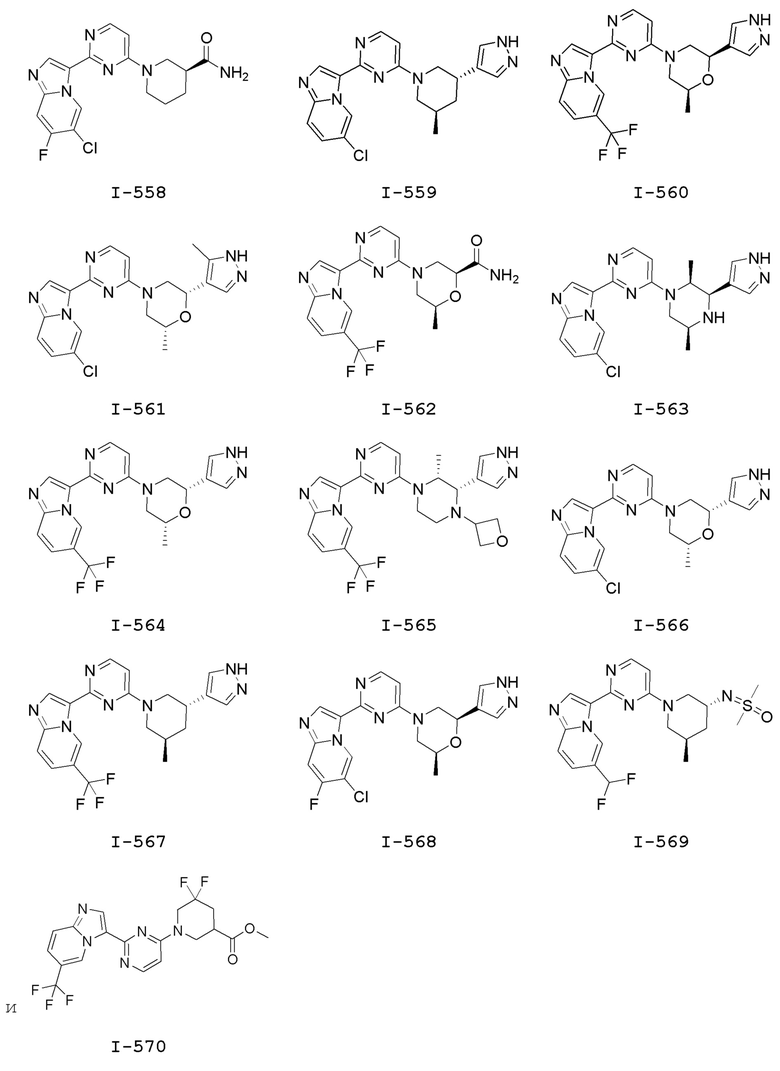
или его фармацевтически приемлемая соль.
27. Фармацевтическая композиция, обладающая ингибирующей общей регулирующей содержание аминокислот киназы 2 с постоянной репрессией (GCN2) активностью, содержащая эффективное количество соединения по любому из пп. 1-26 и фармацевтически приемлемый носитель, вспомогательное вещество или разбавитель.
28. Применение соединения по любому из пп. 1-26 или содержащей его фармацевтической композиции для ингибирования GCN2 в биологическом образце.
29. Применение соединения по любому из пп. 1-26 или содержащей его фармацевтической композиции для получения лекарственного средства для лечения опосредуемого GCN2 нарушения, заболевания или патологического состояния у пациента.
30. Применение по п. 29, где опосредуемое GCN2 нарушение, заболевание или патологическое состояние выбрано из группы, включающей воспалительные патологические состояния, иммунологические патологические состояния, аутоиммунные патологические состояния, аллергические патологические состояния, ревматические патологические состояния, тромбические патологические состояния, рак, инфекции, нейродегенеративные заболевания, дегенеративные заболевания, нейровоспалительные заболевания, сердечно-сосудистые заболевания и метаболические патологические состояния.
31. Применение по п. 30, где рак выбран из группы, включающей солидную опухоль, где солидная опухоль происходит из группы опухолей эпителия, мочевого пузыря, желудка, почек, головы и шеи, пищевода, шейки матки, щитовидной железы, кишечника, печени, головного мозга, предстательной железы, мочеполового тракта, лимфатической системы, желудка, гортани, костей, включая хондросаркому и саркому Юинга, зародышевых клеток, включая опухоли эмбриональной ткани, и/или легких, выбранную из группы, включающей моноцитарный лейкоз, аденокарциному легких, мелкоклеточные карциномы легких, рак поджелудочной железы, глиобластому, нейрофиброму, ангиосаркому, карциному молочной железы и/или злокачественную меланому и опухоль крови и иммунной системы.
32. Применение по п. 30, где аутоиммунным патологическим состоянием является ревматоидный артрит, системная волчанка, рассеянный склероз, псориаз, синдром Шегрена или отторжение трансплантата органа.
33. Применение по п. 30, где метаболическим патологическим состоянием является диабет.
34. Применение по п. 30, где дегенеративным заболеванием является остеоартрит.
35. Применение по п. 30, в котором воспалительным патологическим состоянием является астма, воспалительная болезнь кишечника или гигантоклеточный артериит.
36. Применение по п. 30, где сердечно-сосудистым заболеванием является ишемическое повреждение.
37. Применение по п. 30, где нейродегенеративным заболеванием является болезнь Альцгеймера, синдром Дауна, наследственное кровоизлияние в головной мозг с амилоидозом голландского типа, амилоидная ангиопатия головного мозга, болезнь Крейтцфельда - Якоба, лобно-височные слабоумия, болезнь Гентингтона или болезнь Паркинсона.
38. Применение по п. 29, где инфекция вызвана лейшманией, микобактериями, включая M. leprae, M. tuberculosis и/или M. avium, плазмодий, вирус иммунодефицита человека, вирус Эпштейна - Барр, вирус простого герпеса или вирус гепатита C.
39. Применение по п. 29, где опосредуемое GCN2 нарушение, заболевание или патологическое состояние представляет собой рак и способ дополнительно включает введение второго средства для лечения рака.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| WO 2013131609 A1, 12.09.2013 | |||
| WO 2003099817 A1, 04.12.2003 | |||
| DAVIS MI et al | |||
| Comprehensive analysis of kinase inhibitor selectivity | |||
| Nat Biotechnol | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| СПОСОБ ВПАИВАНИЯ СТЕКЛЯННОЙ ТРУБКИ ДЛЯ ОТВОДА ВОЗДУХА ИЛИ ИНОГО ГАЗА, ОТКАЧИВАЕМОГО ИЗ КОЛБ ЭЛЕКТРИЧЕСКИХ ЛАМП НАКАЛИВАНИЯ И КАТОДНЫХ | 1924 |
|
SU1046A1 |
| RU 2002107128 A, 27.09.2003. | |||
Авторы
Даты
2024-01-11—Публикация
2019-01-28—Подача