Изобретение относится к биотехнологической промышленности, а именно к способу получения биомассы метанокисляющих бактерий при непрерывном культивировании, и может быть использовано в кормовой, пищевой и химической промышленности.
Производство биомассы микроорганизмов - самое крупное микробиологическое производство. Микробная биомасса служит белково-витаминным компонентом в кормах для домашних животных, птиц и рыб. Большое значение микробиологических технологий в производстве белковых добавок определяется рядом факторов: высокая скорость биосинтеза протеина в клетках микроорганизмов, которая в десятки раз выше, чем в растениях. Кроме того, устойчивый уровень производства белковых добавок возможен вне зависимости от климатических и природных условий. Производство микробной биомассы особенно важно для стран, не выращивающих крупнотоннажно сою (соевую муку используют как традиционную белковую добавку к кормам). Продуктами для получения микробного белка являются растительные отходы, парафины, спирты, природный газ. Следовательно, такое производство является эффективным и высокорентабельным.
Особое значение для нашей страны имеет развитие производства кормового белка из природного газа. Главные достоинства природного газа - доступность, относительно низкая стоимость, высокие показатели преобразования в биомассу метанокисляющими микроорганизмами. существенное содержание в биомассе белка, сбалансированного по аминокислотному составу. Многие бактерии, растущие на метане, хорошо выдерживают кислые среды и высокие температуры. Однако реализация технологии получения кормового белка из метанокисляющих микроорганизмов осложнена многофакторностью процесса культивирования: обеспечение клеток необходимым газообразным питанием при низкой растворимости газов в жидкостях, оптимизация макро- и микроэлементного состава минеральных сред во избежание лимитирования и ингибирования роста микроорганизмов.
Известен способ получения биомассы метанокисляющих микроорганизмов и линия для ее производства (патент РФ №2755539, С12Р 21/00, опубл. 17.09.2021), который включает выращивание биомассы с использованием отработанной среды после концентрирования биомассы и ее сушку. После концентрирования биомассы отработанную среду отделяют и охлаждают, подвергают аэробной ферментации с последующим разделением на биомассу сопутствующей микрофлоры и жидкую фазу. Жидкую фазу возвращают в питательную среду для выращивания биомассы. Изобретение обеспечивает увеличение эффективности и продуктивности промышленного производства биопротеина при снижении потребления очищенной воды на единицу готовой продукции. Реализация предложенного технического решения напрямую связана с увеличением эффективности и продуктивности промышленного производства, с одновременным снижением себестоимости целевого продукта, благодаря введению в технологическую линию контура возврата отработанной среды через блок аэробной ферментации в блок промышленного выращивания метанокисляющих микроорганизмов.
Недостатком данного способа является усложнение технологического процесса получения биомассы метанокисляющих бактерий путем введения контура, содержащего дополнительные блок охлаждения отработанной культуральной жидкости, реактор для асептического культивирования сопутствующей микрофлоры и блок разделения. В описании известного решения не отражено насколько введение дополнительного контура повышает производительность процесса. Кроме того, указанный способ усложняется дополнительными блоками для разделения воздуха на азот и кислород, используемыми для аэрирования блока промышленного ферментера.
Известен способ получения микробного белка на основе углеводородного сырья (патент RU №2720121, C12N 1/20, опубл. 24.04.2020) на основе метанокисляющих бактерий Methylococcus capsulatus ГБС-15, предусматривающий приготовление питательной среды, состоящей из калия, магния, железа (II), меди, марганца, цинка, кобальта и молибдата натрия заданной концентрации с добавлением фосфорной кислоты, ферментацию бактериальных культур с постоянной подачей культуральной жидкости, раствора аммиака и газовой смеси при температуре 40-45°С в непрерывном протоке 0,2-0,3 объема ферментера в час. Затем осуществляют сепарацию с получением готового продукта. При этом отработанную культуральную жидкость после сепарации возвращают через накопительную емкость на стадию ферментации в объеме от 10 до 95% от общего количества используемой воды, обогащают недостающими минеральными солями до заданных концентраций в культуральной жидкости с последующим продолжением ферментации бактериальной культуры. Изобретение позволяет повысить выход готового продукта.
Недостатком данного способа является отсутствие в питательной среде для выращивания микроорганизмов источника азота. На лаг-фазе культивирования в период медленного роста, когда клетки адаптируются к среде, богатой питательными веществами, и готовятся к быстрому росту, происходит интенсивный синтез белков. На данном этапе закисление культуральной жидкости культурой микроорганизмов замедляется, либо вообще отсутствует, и, следовательно, подтитровка аммиачной водой, которая используется в качестве источника азота, будет идти с низкой скоростью, либо отсутствовать. Для синтеза клеток аминокислот, нуклеиновых кислот и белков необходим азот. В данном случае при его отсутствии или при его низких концентрациях рост метанокисляющих микроорганизмов может не начаться, либо же лаг-фаза культивирования с низкой скоростью роста может растянуться на очень длительное время.
Наиболее близким к предлагаемому способу (прототипом) является способ (патент RU №2768401, C12N 1/26, опубл. 24.03.2022) культивирования аэробных метанассимилирующих микроорганизмов Methylococcus capsulatus ВКПМ В-13554 в проточном режиме с постоянной скоростью отбора культуральной жидкости и скоростью протока минеральной среды от 0,25 до 0,35 ч-1 при 41-44°С, рН 5,4-5,8 и скорости потока газовоздушной смеси метан: воздух - 1:3. В состав питательной среды дополнительно вводят никель и до 10% воды заменяют на фугат культуральной жидкости; концентрацию компонентов минерального питания устанавливают в зависимости от заданной скорости протока среды D и планируемой продуктивности процесса культивирования Y по формуле:
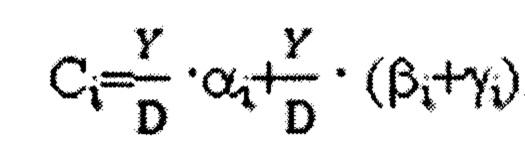 ,
,
где Ci - концентрация i-го компонента в питательной среде, мг/л;
Y - продуктивность процесса культивирования, г/л⋅ч;
D - скорость протока среды, ч-1;
αi - усредненная концентрация i-го компонента в биомассе, которая зависит от биологических особенностей штамма-продуцента и принята постоянной, мг/г;
βi - удельная концентрация i-го компонента во внеклеточных продуктах метаболизма, в пересчете на концентрацию биомассы в культуральной жидкости, мг/г;
γi - удельная остаточная концентрация i-го компонента в пересчете на концентрацию биомассы в культуральной жидкости, мг/г.
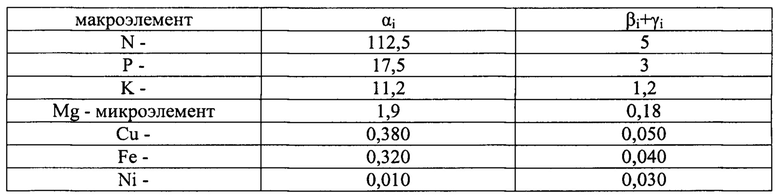
Значения «αi» и «βi+γi» для компонентов минерального питания установлены экспериментально:
αi - для отмытой от внеклеточных компонентов биомассы;
(βi+γi) - в микрофильтрате культуральной жидкости.
Данное изобретение обеспечивает повышение продуктивности процесса синтеза биомассы в биореакторах с различными массообменными характеристиками при масштабировании процесса длительного культивирования.
В известном способе культивирования используют фосфаты в виде солей аммония и солей макроэлементов К, Mg, что позволяет избежать применения концентрированных растворов фосфорной кислоты для приготовления питательных сред, снизить затраты на дорогостоящее оборудование для ее транспортирования, хранения и передачи и снизить содержание неассимилируемых сульфат-ионов в питательной среде. Однако использование солей фосфатов в питательной среде приводит к образованию буфера. Использование буферных систем питательных минеральных сред предпочтительнее при периодическом культивировании. Таким образом, на начальных этапах культивирования до определенного момента накопления биомассы в культуральной жидкости буферная система будет сохраняться, закисление среды не будет происходить, и, следовательно, не будет идти подтитровка аммиачным раствором, что приведет к разбалансированию питательной среды по азоту. Кроме того, для приготовления питательных сред обычно используют растворы концентратов минеральных солей, не все соли микроэлементов хорошо растворимы при нейтральном рН, для лучшего растворения солей микроэлементов добавляют кислоты. Поэтому для исключения буферности системы питательной минеральной среды, а также для растворения солей микроэлементов предпочтительнее использовать фосфорную кислоту.
Также в указанном способе заявлено, что определяющим фактором, который влияет на выход целевого продукта, является состав питательной среды, при этом акцентируя внимание на таких элементах как азот, фосфор, калий, магний, медь, железо, никель. В известном способе уделяют внимание тому, что медь, железо и никель - основные микроэлементы, которые определяют эффективность ассимиляции метана метанотрофными микроорганизмами, в связи с тем, что они входят в состав важнейших металлопротеиназ и пептидов, регулирующих этот процесс. Ассимиляция углерода является определяющей для жизнедеятельности клетки, однако стоит учитывать все метаболические процессы, протекающие в микроорганизмах. Минеральные соли, содержащие микро- и макроэлементы, оказывают влияние на активность всех метаболических путей, протекающих в клетках. Потребность метанокисляющих микроорганизмов в этих компонентах зависит от фазы развития культуры, скорости ее роста и от плотности микробной популяции. При этом необходимо учитывать остаточные концентрации минеральных солей в культуральной жидкости, но так, чтобы в конечном продукте зольность не превышала допустимых показателей. Поэтому важно сбалансировать всю питательную минеральную систему для получения продукта с высокой продуктивностью, отвечающего требованиям, предъявляемым к характеристикам белково-витаминных концентратов.
Задачей, на решение которой направлено предлагаемое изобретение, является разработка способа непрерывного промышленного культивирования метанокисляющих микроорганизмов в ферментерах различного объема с различными массообменными характеристиками.
Техническим результатом, на достижение которого направлено предлагаемое изобретение, является повышение продуктивности культивирования метанокисляющих микроорганизмов путем поддержания стабильного прироста биомассы за счет оптимизации состава питательной среды.
Указанный технический результат достигается за счет того, что в способе культивирования метанокисляющих микроорганизмов Methylococcus capsulatus в непрерывном режиме со скоростью протока питательной минеральной среды 0,26-0,38 ч-1, при температуре термостатирования 41-43°С, рН 5,4-5,8, при аэрировании газовоздушной смесью метан: воздух в соотношении 1:3, соответственно, включающем приготовление питательной среды, содержащей азот, фосфор, магний, калий, натрий, медь, железо (II), марганец, цинк, кобальт, молибден, никель, в условиях экспоненциальной стадии роста биомассы микроорганизмов концентрацию питательной среды, сбалансированной по всем компонентам, увеличивают дискретно по 20%, прямо пропорционально концентрации биомассы микроорганизмов и удельной скорости роста микроорганизмов. При этом непрерывно контролируют и поддерживают постоянными значения остаточных концентраций фосфора, азота и растворенного кислорода в культуральной жидкости.
Предлагаемый способ осуществляют следующим образом:
- приготавливают концентрированный раствор солей микроэлементов путем дозирования расчетного количества готовых индивидуальных навесок минеральных солей микроэлементов, фосфорной кислоты и подготовленной воды;
- приготавливают концентрированный раствор питательной минеральной среды путем дозирования расчетного количества готовых индивидуальных навесок минеральных солей макроэлементов, расчетного количества концентрата минеральных солей микроэлементов и подготовленной воды;
- приготавливают раствор питательной минеральной среды путем дозирования расчетного количества концентрата питательной минеральной среды, расчетного количества навески сульфата аммония и подготовленной воды;
- осуществляют подготовку воды путем очистки ее от механических примесей, отдельных микро- и макрокомпонентов, микроорганизмов;
- подготовленные растворы подают в ферментер;
производят засев ферментера суспензией метанокисляющих микроорганизмов Methylococcus capsulatus, например, Methylococcus capsulatus ВКПМ-13479, в которой содержание основной культуры-продуцента кормового белка составляет не менее 95%. Подготовку инокулята осуществляют непосредственно перед засевом в ферментер. Если посевной материал - культуральная жидкость, содержащая биомассу микроорганизмов, ее без подготовки заливают в ферментер с уже подготовленной питательной средой с рН 5,4-5,8. Если посевной материал - сгущенная паста микроорганизмов, то ее ресуспендируют в подготовленной нейтрализованной минеральной среде, слитой из ферментера, с рН 5,4-5,8 и заливают в ферментер. Засев ферментера суспензией микроорганизмов производят из расчета получения начальной концентрации в ферментере 0,5-2,5 гАСБ/л. Начальную концентрацию питательной минеральной среды в ферментере устанавливают таким образом, чтобы она соответствовала концентрации биомассы в культуральной жидкости 3 г/л при удельной скорости роста микроорганизмов 0,3 ч-1, и дополнительно вносят сульфат аммония в концентрации 100 мг/л. Удельная скорость роста микроорганизмов (μ) - показатель, характеризующий скорость роста единицы биомассы: увеличение концентрации единицы биомассы dX за промежуток времени dt.

С учетом скорости протока D, которая в свою очередь показывает скорость разбавления минеральной средой (Vпр) рабочего объема культуральной жидкости (Vpa6) в ферментере, удельную скорость роста рассчитывают по формуле:
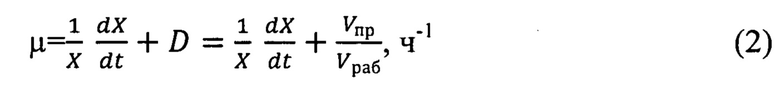
После интегрирования получаем формулу для определения удельной скорости роста (ч-1):

где x1 и x2 - концентрация биомассы в аппарате (г/л) в моменты времени t1 и t2 (ч), соответственно;
- осуществляют процесс ферментации при перемешивании с непрерывной подачей газовой смеси, при автоматическом поддержании рН 5,4-5,8 при температуре 41-43°С. Момент начала роста культуры оценивают по снижению рН в ферментере, а далее - по началу автоматического титрования раствором аммиачной воды. Метанокисляющие микроорганизмы характеризуются газообразным типом питания. Для аэробного окисления газообразного углеводорода необходимым компонентом газовой среды является кислород. При активном росте культуры процесс ферментации лимитируется по кислороду. Потребность микроорганизмов в кислороде превышает потребность в метане в 2-3 раза. О дыхательной активности культуры судят по снижению показаний растворенного кислорода в культуральной жидкости. При снижении показаний растворенного кислорода удельная скорость роста микроорганизмов сохраняется, но остаточная концентрация фосфора становится ниже оптимальной, увеличивается потребление клетками фосфора, что приводит к увеличению клеток в размерах за счет увеличения фосфолипидов в мембранах. Все это в свою очередь приводит к тому, что клетки становятся легче, и концентрация биомассы, исходя из пересчета оптической плотности, не соответствует реальному накоплению биомассы в культуральной жидкости. Также увеличивается закисление культуральной жидкости, за счет чего увеличивается подача титранта - аммиачной воды. Все это ведет к разбалансированию питательной среды, и в конечном итоге приводит к снижению ростовых характеристик. При увеличении показаний растворенного кислорода выше оптимальных удельная скорость роста микроорганизмов снижается, остаточные концентрации фосфора и азота и других макро- и микроэлементов в культуральной жидкости увеличиваются, что приводит к дальнейшему ингибированию метаболизма микроорганизмов;
- показатели растворенного кислорода в культуральной жидкости в диапазоне 0,2-0,4 мгО2/л поддерживают путем регулирования скорости вращения мешалок, либо регулируя расход подаваемого газа метан: воздух в соотношении 1:3, соответственно, либо регулируя избыточное давление в ферментере (если позволяет конструкция ферментера);
- далее процесс ведут с непрерывной подачей раствора минеральных солей в протоке со скоростью 0,26-0,38 ч-1, поддерживая таким образом на низком уровне концентрацию ингибирующих рост продуктов метаболизма микроорганизмов, а также ограничивая рост сопутствующей микрофлоры в условиях нестерильного процесса культивирования. Ежечасно отслеживают прирост микроорганизмов по увеличению оптической плотности культуральной жидкости или по увеличению абсолютно сухого веса биомассы в культуральной жидкости, а также регистрируют остаточные концентрации фосфора и азота в культуральной жидкости. Количество вносимого в питательную среду сульфата аммония варьируют отдельно, в зависимости от остаточного содержания аммонийного азота в культуральной жидкости, которое поддерживают в диапазоне 20-25 мг/л;
- в момент времени, когда значение концентрации биомассы достигает 3 г/л, а значение остаточной концентрации фосфора в культуральной жидкости достигает оптимального и начинает снижаться, концентрацию подаваемой питательной среды увеличивают на 20%;
- и далее, когда накопление биомассы увеличивается на 20%, концентрацию подаваемой минеральной среды вновь увеличивают на 20% от первоначальной;
- выходом на стационарный режим культивирования считают момент времени, когда при увеличении концентрации подаваемой питательной среды не происходит пропорционального увеличения накопления биомассы микроорганизмов, и при этом увеличиваются остаточные концентрации всех компонентов питательной среды в культуральной жидкости. В этот момент времени снижают концентрацию подаваемой минеральной среды на 20% и далее ведут процесс культивирования, поддерживая оптимальными остаточные концентрации фосфора, азота и показания растворенного кислорода в культуральной жидкости.
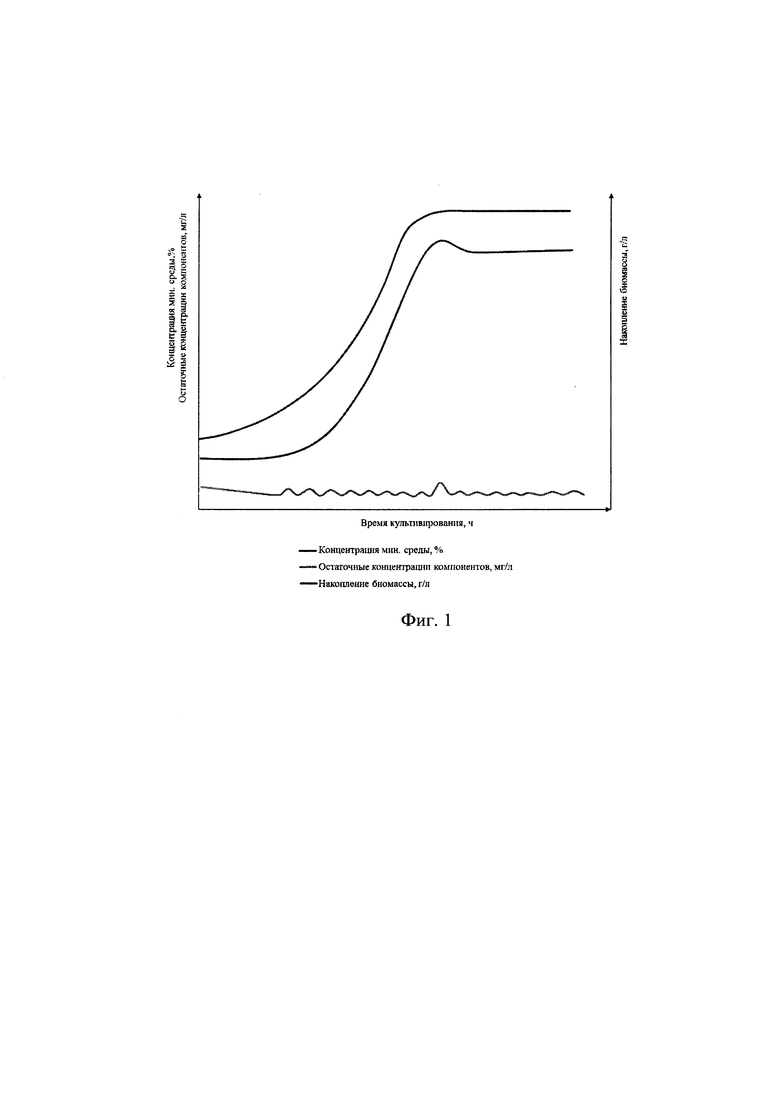
На чертеже изображен графически процесс культивирования метанокисляющих микроорганизмов предложенным способом.
В ходе проведения экспериментальных исследований был подобран оптимальный состав питательной минеральной среды (100%-ой) из расчета накопления биомассы в культуральной жидкости 1 г/л таким образом, что при дискретном увеличении концентрации питательной среды с учетом удельной скорости роста метанокисляющих микроорганизмов концентрация биомассы увеличивается пропорционально, а остаточные концентрации компонентов в культуральной жидкости поддерживаются постоянными (таблица 1).
Экспериментально было установлено, что при поддержании остаточных концентраций фосфора в пределах 7-13 мг/л, остаточных концентраций азота в пределах 20-25 мг/л и при поддержании показаний растворенного кислорода в культуральной жидкости в пределах 0,2- 0,4 мгО2/л достигается стабильный прирост биомассы со скоростью роста 0,27-0,34 ч-1.
Пример 1.
Проводили культивирование Methylococcus capsulatus ВКПМ-13479 в непрерывном режиме в течение 30 дней в емкостном ферментере с лопастными мешалками, общим объемом 10 л при рабочем объеме 5 л, при постоянном перемешивании, с коэффициентом массопереноса по сульфитному методу 1250 ч-1 с протоком питательной минеральной среды 1300-1900 мл/час. Концентрацию среды увеличивали дискретно с шагом 20%, при термостатировании (41-43°С), при аэрировании метано-воздушной смесью в соотношении 1:3, соответственно, при расходе 2,5-5 л/мин при атмосферном давлении, поддерживая показания растворенного кислорода 0,2-0,4 мгО2/л, и при рН-статировании, поддерживая рН в диапазоне 5,4-5,8 Титрование осуществляли 2,5%-ым раствором аммиачной воды. Ежечасно выполняли контроль накопления биомассы в культуральной жидкости по оптической плотности (раз в 4 часа - по сухому весу), и остаточных внеклеточных концентраций азота и фосфора.
При достижении концентрации подаваемой питательной минеральной среды 220%, при расходе метано-воздушной смеси 5 л/мин, при поддержании показаний растворенного кислорода в диапазоне 0,2-0,4 мгО2/л процесс культивирования перешел в стационарную фазу роста со скоростью протока 0,26-0,28 ч-1, и продуктивность составила 2,1-2,3 г/(л ч).
Остаточные концентрации макро- и микроэлементов в культуральной жидкости после отделения биомассы (отработанная культуральная жидкость, ОКЖ) микроорганизмов приведены в таблице 2. Химическое потребление кислорода, отражающее количество органических веществ в ОКЖ, составило 100-250 мгО2/л. Содержание сырого протеина в высушенном образце биомассы составляло 74%.
Пример 2.
Культивирование Methylococcus capsulatus ВКПМ-13479 проводили в непрерывном режиме в течение 30 дней в емкостном ферментере с лопастными мешалками общим объемом 50 л, при рабочем объеме 30 л, при постоянном перемешивании, с коэффициентом массопереноса по сульфитному методу 1150 ч-1, с протоком питательной минеральной среды 7,8-11,4 л/час. Концентрацию среды увеличивали дискретно с шагом 20%, при термостатировании (41-43°С), при аэрировании метано-воздушной смесью в соотношении 1:3, соответственно, при расходе 8-52 л/мин при избыточном давлении в аппарате, поддерживая показания растворенного кислорода 0,2-0,4 мгО2/л, и при рН-статировании, поддерживая рН в диапазоне 5,4-5,8. Титрование осуществляли 4%-ым раствором аммиачной воды. Ежечасно выполняли контроль накопления биомассы в культуральной жидкости по оптической плотности (раз в 4 часа - по сухому весу), и остаточных внеклеточных концентраций азота и фосфора.
При достижении концентрации подаваемой питательной минеральной среды 400% при расходе метано-воздушной смеси 52 л/мин, при избыточном давлении в аппарате 2,5 бар, при поддержании показания растворенного кислорода в диапазоне 0,2-0,4 мгО2/л процесс культивирования перешел в стационарную фазу роста со скоростью протока 0,26-0,28 ч-1, и продуктивность составила 3,8-4,0 г/(л ч).
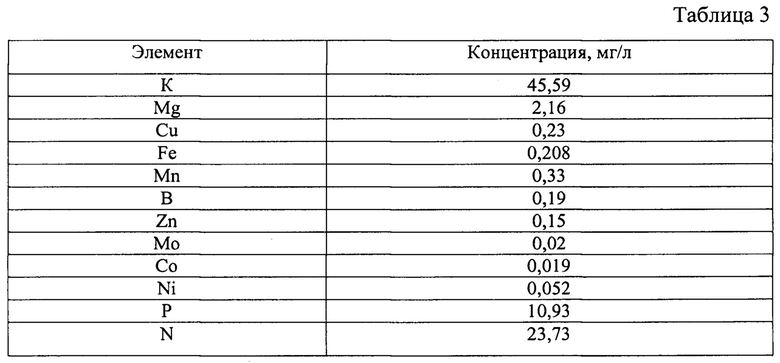
Остаточные концентрации макро- и микроэлементов в ОКЖ приведены в таблице 3. Химическое потребление кислорода составило 100-300 мгО2/л. Содержание сырого протеина в высушенном образце биомассы - 73%.
Качество получаемого продукта соответствует всем требованиям, предъявляемым к микробному белку.
Экспериментально полученные данные при отработке процесса культивирования метанокисляющих микроорганизмов подтверждают, что результатом реализации предлагаемого способа культивирования метанокисляющих микроорганизмов является высокая продуктивность стабильного получения биомассы в ферментерах различного объема с различными массообменными характеристиками.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ культивирования аэробных метанассимилирующих микроорганизмов | 2021 |
|
RU2768401C1 |
| Штамм Methylococcus capsulatus - продуцент высокобелковой биомассы | 2022 |
|
RU2787202C1 |
| СПОСОБ ВЫРАЩИВАНИЯ МЕТАНОКИСЛЯЮЩИХ МИКРООРГАНИЗМОВ | 1989 |
|
RU2032737C1 |
| Способ получения биомассы | 1979 |
|
SU908085A1 |
| Штамм бактерий Methylococcus capsulatus CONCEPT-8 - продуцент белковой биомассы | 2018 |
|
RU2706074C1 |
| Способ получения биомассы метанокисляющих микроорганизмов и линия для ее производства | 2020 |
|
RU2755539C1 |
| Штамм Methylococcus capsulatus ВКПМ В-13479 - продуцент микробной белковой массы, устойчивый к агрессивной среде | 2019 |
|
RU2728345C1 |
| Способ получения биомассы метанокисляющих бактерий | 2022 |
|
RU2807059C1 |
| Способ получения биомассы метанокисляющих бактерий с добавлением формиата натрия | 2021 |
|
RU2777669C1 |
| Штамм метанокисляющих бактерий Methylococcus capsulatus BF19-07 - продуцент для получения микробной белковой массы | 2020 |
|
RU2745093C1 |
Изобретение относится к области биотехнологии. Предложен способ культивирования метанокисляющих микроорганизмов в непрерывном режиме со скоростью подачи питательной минеральной среды 0,26-0,38 ч-1 при термостатировании 41-43°С, при рН 5,8-5,4, аэрировании метано-воздушной средой в соотношении 1:3 соответственно. В условиях экспоненциальной стадии роста концентрацию питательной среды, сбалансированной по всем компонентам, увеличивают дискретно по 20%, прямо пропорционально концентрации биомассы и удельной скорости роста микроорганизмов. При этом непрерывно контролируют и поддерживают постоянными остаточные концентрации фосфора, азота и показания растворенного кислорода в культуральной жидкости. Изобретение обеспечивает стабильное получение продукта с высокой продуктивностью в ферментерах различного объема с различными массообменными характеристиками. 1 ил., 3 табл., 2 пр.
Способ культивирования метанокисляющих микроорганизмов Methylococcus capsulatus ВКПМ-13479 в непрерывном режиме со скоростью протока питательной минеральной среды 0,26-0,38 ч-1, при температуре термостатирования 41-43°С, рН 5,4-5,8, при аэрировании газовоздушной смесью метан:воздух в соотношении 1:3 соответственно, включающий приготовление питательной среды, содержащей азот, фосфор, магний, калий, натрий, медь, железо (II), марганец, цинк, кобальт, молибден, никель, отличающийся тем, что в условиях экспоненциальной стадии роста биомассы микроорганизмов концентрацию питательной среды, сбалансированной по всем компонентам, увеличивают дискретно по 20%, прямо пропорционально концентрации биомассы микроорганизмов и удельной скорости роста микроорганизмов, при этом непрерывно контролируют и поддерживают постоянными значения остаточных концентраций фосфора, азота и растворенного кислорода в культуральной жидкости.
| Способ культивирования аэробных метанассимилирующих микроорганизмов | 2021 |
|
RU2768401C1 |
| Способ получения микробного белка на основе углеводородного сырья | 2019 |
|
RU2720121C1 |
| Способ получения биомассы метанокисляющих микроорганизмов и линия для ее производства | 2020 |
|
RU2755539C1 |
| Штамм Methylococcus capsulatus ВКПМ В-13479 - продуцент микробной белковой массы, устойчивый к агрессивной среде | 2019 |
|
RU2728345C1 |
| WO 2014060778 A1, 24.04.2014. | |||
Авторы
Даты
2024-01-11—Публикация
2023-04-10—Подача