Изобретение относится к области органической химии и химии люминесцентных излучателей, а именно к гетероциклическому соединению 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридину, а также к способу его получения.
Соединение может быть использовано в качестве полупроводниковых слоев для создания устройств органической электроники.
В литературе описаны замещенные 2,4,6-трифенилпиридины, содержащие электронодонорные гетероариленовые заместители, такие как карбазольные, дигидроакридиновые, феназиновые, феноксазиновые или фенотиазиновые фрагменты. Известно, что соединения такого типа используются в качестве светоизлучающих материалов (патент WO2015016200A1, C07D 401/08, опубл. 05.02.2015).
В рамках данного изобретения к тризамещенным 2,4,6-трифенилпиридинам относится органическое соединение, которое содержит в качестве электронодонорных заместителей одну 4-N,N-дифениламиногруппу и два карбазольных фрагмента, связанные через π-сопряженный фениленовый спейсер (π-спейсер) с электроноакцепторным пиридиновым ядром.
Наиболее близкими по строению к заявляемому тризамещенному 2,4,6-трифенилпиридину можно отнести схожие соединения, отличающиеся тем, что в п-положениях фенильных колец при втором, четвертом и шестом атомах пиридинового кольца содержатся электронодонорные заместители – карбазольные фрагменты (соединение № 1) или 4-N,N-дифениламиногруппы (соединение № 2).
В патенте CN107417668A, C07D 401/14, опубл. 01.12.2017 раскрывается схожий тризамещенный 2,4,6-трифенилпиридин, но содержащий вместо карбазольных заместителей при втором и шестом атомах пиридинового кольца 2-фенилбензимидазольные фрагменты (соединение № 3).
Как правило, синтез таких соединений основан на проведении реакции кросс-сочетания Сузуки с использованием 2,4,6-тригалогензамещенных пиридинов и соответствующих борных кислот или сложных эфиров борной кислоты (Synthesis and characterization of highly stable and efficient star-molecules. Huang H. F., Xu S. H., He Y. B., Zhu C. C., Fan H. L., Zhou X. H., Gao X.-C., Dai Y. F. Dyes Pigm., 2013, 96 (3), 705-713. doi: 10.1016/j.dyepig.2012.11.014; патент CN107417668A, C07D 401/14, опубл. 01.12.2017):
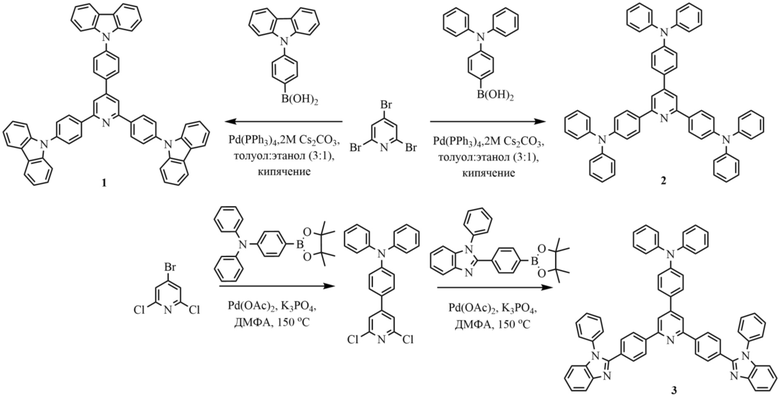
Однако методам присущи недостатки, связанные с длительностью синтеза и с трудоемкостью обработки продуктов реакции, а также с применением дорогостоящих палладиевых катализаторов. Так, в работе (Synthesis and characterization of highly stable and efficient star-molecules. Huang H. F., Xu S. H., He Y. B., Zhu C. C., Fan H. L., Zhou X. H., Gao X.-C., Dai Y. F. Dyes Pigm., 2013, 96 (3), 705-713. doi: 10.1016/j.dyepig.2012.11.014) авторы используют катализатор Pd(PPh3)4 в количестве 0.05 эквивалента. В патенте CN107417668A, C07D 401/14, опубл. 01.12.2017 для синтеза 2,4,6-трифенилпиримидина используют Pd(OAc)2 в количестве до 2 массовых процентов.
Задачей изобретения является разработка простого способа синтеза неописанного в литературе 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина, проявляющего флуоресцентные свойства.
Поставленная задача решается путем взаимодействия 4-(N,N-дифениламино)бензальдегида (соединение № 4), 4-(9-карбазолил)фенилэтанона (соединение № 5) и ацетата аммония в присутствии трифторметансульфокислоты по схеме:
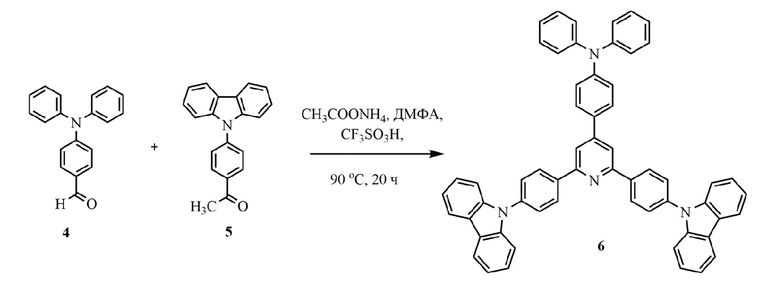
Процесс ведут при температуре 90 °С, в качестве растворителя используют диметилформамид.
В таблице 1 приведены данные о влиянии температуры и растворителя на выход целевого 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина.
Таблица 1 – Влияние температуры и растворителя на выход 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина
Как видно из таблицы 1 с наибольшим выходом был получен 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин (соединение № 6) при нагревании реакционной массы при температуре 90 °С в диметилформамиде. Проведение реакции при температуре ниже 90 °С снижает выход целевого продукта вследствие неполной конверсии 4-(N,N-дифениламино)бензальдегида (соединение № 4) и 4-(9-карбазолил)фенилэтанона (соединение № 5). Проведение реакции при температуре выше 90 °С также не позволяет получить целевой продукт с более высоким выходом. Таким образом, оптимальным условием проведения синтеза 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина (срединение № 6) является нагревание реакционной смеси при температуре 90 °С в среде диметилформамида, выход в данном случае составляет 84 %.
Из патентной и технической литературы не были выявлены способы получения 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина, в котором в п-положении фенильных колец при втором и шестом атомах пиридинового кольца расположены два карбазольных заместителя, а в п-положении фенильного кольца при четвертом атоме пиридинового цикла – N,N-дифениламиногруппа, имеющие сходные признаки с заявленным способом, а именно, не использовались исходные продукты, растворитель, в котором проходит реакция, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Пример. Синтез 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина (соединение № 6).
Раствор 14 мг (0.5 ммоль) 4-(N,N-дифениламино)бензальдегида (соединение № 4), 29 мг (1 ммоль) 4-(9-карбазолил)фенилэтанона (соединение № 5), 15 мг (2 ммоль) ацетата аммония и 0.6 мг (0.04 ммоль) трифторметансульфокислоты в 10 мл диметилформамида нагревали при 90° С в течение 20 часов. Реакцию контролировали с помощью тонкослойной хроматографии. После завершения реакции реакционную смесь охлаждали, растворитель упаривали досуха, остаток очищали препаративной колоночной хроматографией в адсорбционном режиме (силикагель, элюент: гексан:дихлорметан (1:1)). Выход 34 мг (84 %). Соединение C59H40N4. Найдено, %: 88.07 С, 5.06 H, 6.87 N. Вычислено, %: С 88.03, H 5.01, N 6.96.
Соединение № 6 – белое кристаллическое вещество, легкорастворимое в дихлорметане, диметилфорамиде, диметилсульфоксиде, не растворимое в воде. Устойчиво при хранении в обычных условиях.
В спектре ПМР 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина (соединение № 6), снятого в растворе CHCl3-d, кроме сигналов 4-N,N-дифениламиногруппы при 7.09 м.д. (т, 2H), 7.19 м.д. (д, 4H), 7.30 м.д. (д, 4H) и карбазольных фрагментов при 7.29-7.32 м.д. (м, 6H), 7.43 м.д. (т, 4H), 7.70 м.д. (д, 2H), 8.46 м.д. (д, 4H) присутствуют сигналы протонов фениленовых спейсеров при 7.50 м.д. (д, 4H), 7.74 м.д. (д. 4H), 8.15 м.д. (д, 4H), а также синглет двух протонов пиридинового цикла при 8.01 м.д.
Предлагаемый способ прост в осуществлении и позволяет получить неописанный в литературе 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин с высоким выходом.
УФ спектры синтезированного соединения записаны на спектрофотометре Shimadzu UV-2600, размер кюветы 10×10 мм, растворитель – абсолютизированный хлороформ, концентрация 2·10–5 моль/литр. Спектры флуоресценции записаны на спектрофлуориметре Shimadzu RF-5301, размер кюветы 10×10 мм, растворитель – абсолютизированный хлороформ, концентрация соединения 2·10–5 моль/литр. На основе полученных спектров поглощения и флуоресценции согласно методике, описанной в работе (Synthesis of new, highly luminescent bis (2, 2’-bithiophen-5-yl) substituted 1, 3, 4-oxadiazole, 1, 3, 4-thiadiazole and 1, 2, 4-triazole. Kostyuchenko A. S., Yurpalov V. L., Kurowska A., Domagala W., Pron A., Fisyuk A. S. Beilstein J. Org. Chem. 2014, 10 (1), 1596-1602. doi: 10.3762/bjoc.10.165), рассчитан квантовый выход флуоресценции (ФF) соединения № 6. На основе полученных спектров поглощения согласно методике, описанной в работе (Spectrophotometric studies of proton transfer complexes between 2-amino-4-methoxy-6-methyl-pyrimidine and 2-amino-4, 6-dimethyl-pyrimidine with 2, 6-dichloro-4-nitrophenol in acetonitrile. Habeeb M. M., Al-Attas A. S., Basha M. T. J. Mol. Liq. 2009, 150 (1-3), 56-61. doi: 10.1016/j.molliq.2009.09.013), рассчитан коэффициент молярного поглощения (ε).
Отличительной особенностью заявленного соединения (соединение № 6) является интенсивная флуоресценция в синей области спектра с максимумом испускания 445 нм (ФF = 89 %), а также эффективное поглощение в диапазоне от 300 до 420 нм (ε = 47600 л⋅моль-1⋅см-1). Представленные характеристики позволяют использовать 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин в индивидуальном виде в качестве полупроводниковых слоев при создании устройств органической электроники.
| название | год | авторы | номер документа |
|---|---|---|---|
| 4,6-бис-(4-N,N-диметиламинофенил)-2-фенилпиримидин, проявляющий флуоресцентные свойства, и способ его получения | 2022 |
|
RU2806025C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-[2-(МОРФОЛИН-4-ИЛ)ЭТИЛ]-4-ХЛОРБЕНЗАМИДА (ВАРИАНТЫ) | 2014 |
|
RU2570898C2 |
| ЛЮМИНОФОРЫ НА ОСНОВЕ 2,6-БИС(АМИНОВИНИЛ)-4-МЕТИЛЕН-1,4-ДИГИДРОПИРИДИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2023 |
|
RU2824353C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(4-ФЕНИЛАМИНОФЕНИЛ)МАЛЕИНИМИДА | 2013 |
|
RU2547727C2 |
| N,N-ЗАМЕЩЕННЫЕ 3-АМИНОПИРРОЛИДИНОВЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОВТОРНОГО ПОГЛОЩЕНИЯ МОНОАМИНОВ | 2006 |
|
RU2574406C2 |
| 4-(4-ПИРИДИЛ)БУТИЛОВЫЙ ЭФИР N-СУЛЬФОНИЛТИРОЗИНА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБ ПОЛУЧЕНИЯ 4-(4-ПИПЕРИДИЛ)БУТИЛОВОГО ЭФИРА N-СУЛЬФОНИЛТИРОЗИНА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1993 |
|
RU2114105C1 |
| СОЕДИНЕНИЯ ГЕТЕРОАРИЛА В КАЧЕСТВЕ ИНГИБИТОРОВ ТКБ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2742122C2 |
| N, N-ЗАМЕЩЕННЫЕ 3-АМИНОПИРРОЛИДИНОВЫЕ СОЕДИНЕНИЯ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОВТОРНОГО ПОГЛОЩЕНИЯ МОНОАМИНОВ | 2006 |
|
RU2414454C2 |
| СИНТЕТИЧЕСКИЕ ПОЛИСАХАРИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2167163C2 |
| Применение монозамещенных пиразинов, содержащих трифениламиновый заместитель, в качестве мономолекулярных сенсоров для обнаружения нитроароматических соединений | 2019 |
|
RU2723243C1 |
Изобретение относится к области органической химии и химии люминесцентных излучателей, а именно к новому гетероциклическому соединению, применяемому в качестве полупроводниковых слоев для создания устройств органической электроники. Соединение по изобретению представляет собой 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин. Также изобретение относится к способу получения соединения по изобретению, которое осуществляется путем перемешивания 4-(N,N-дифениламино)бензальдегида и 4-(9-карбазолил)фенилэтанона в присутствии ацетата аммония и трифторметансульфокислоты при 90°С в среде диметилформамида с последующим выделением целевого продукта. Технический результат - 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин для применения в качестве полупроводниковых слоев для создания устройств органической электроники. 2 н.п. ф-лы, 1 табл., 8 пр.
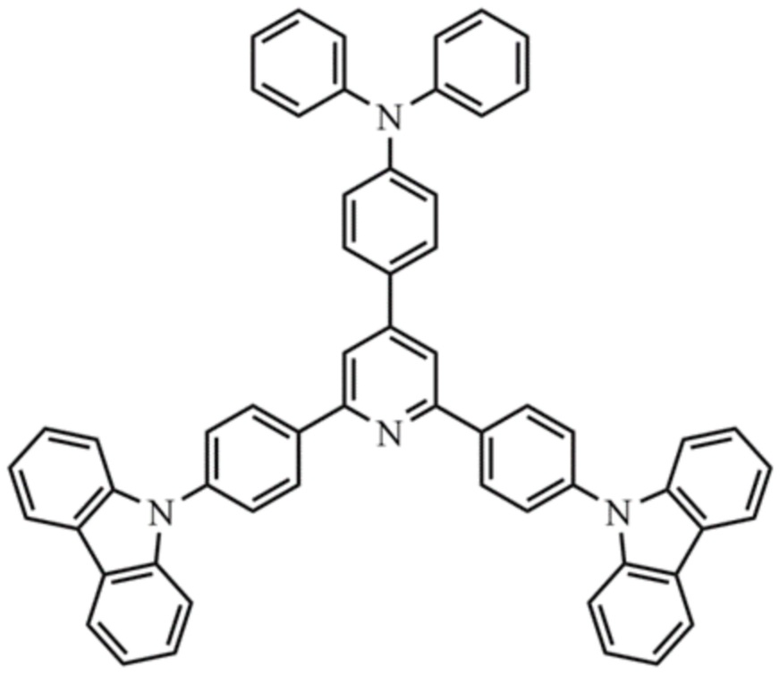
1. 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин формулы
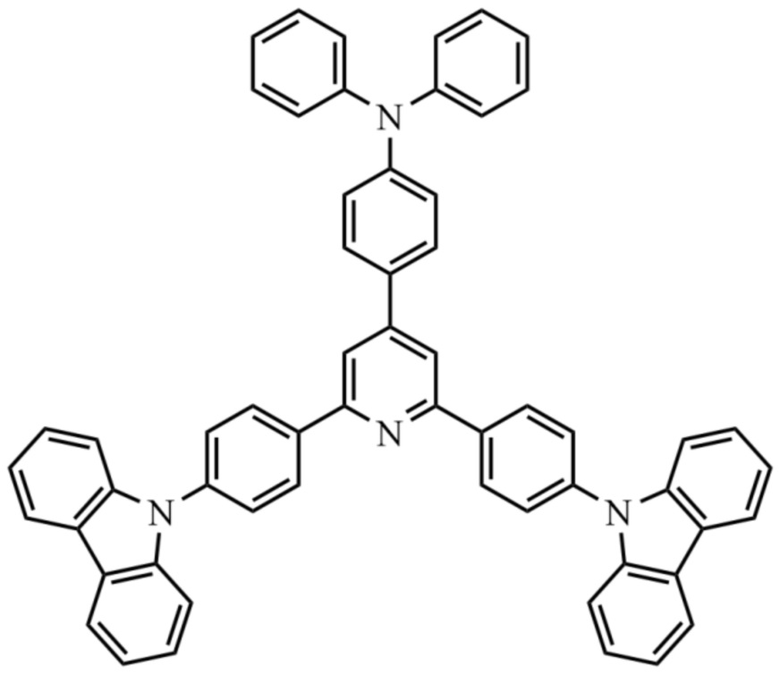
проявляющий флуоресцентные свойства.
2. Способ получения 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридина, отличающийся тем, что 4-(N,N-дифениламино)бензальдегид, 4-(9-карбазолил)фенилэтанон в присутствии ацетата аммония и трифторметансульфокислоты перемешивают при 90°С в среде диметилформамида с последующим выделением целевого продукта.
| WO 2015016200 A1, 05.02.2015 | |||
| CN 107417668 A, 01.12.2017 | |||
| US 20110291081 A1, 01.12.2011 | |||
| HUANG, H.-F | |||
| et al | |||
| Synthesis and characterization of highly stable and efficient star-molecules | |||
| Dyes and Pigments, 2013, 96(3), p.705-713 | |||
| СОЕДИНЕНИЯ ДЛЯ ОРГАНИЧЕСКИХ ЭЛЕКТРОННЫХ УСТРОЙСТВ | 2006 |
|
RU2419648C2 |
Авторы
Даты
2024-01-30—Публикация
2023-11-20—Подача