Изобретение относится к области фитохимии, к применению биологически активных соединений природного происхождения - класса флаванонов, а именно 5,7-дигидрокси-6,8-диметилфлаванона формулы (1):
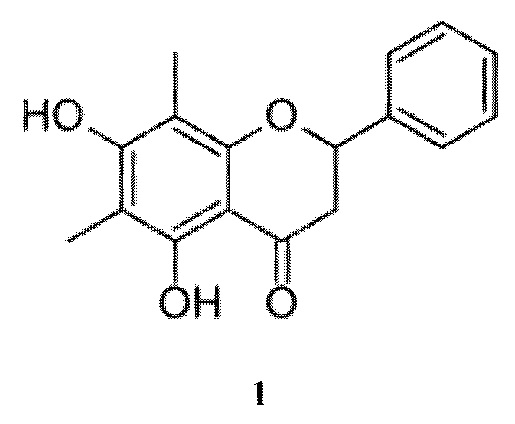
обладающему антиагрегационной активностью, что позволяет предложить его использование в фармакологии и медицине в качестве антиагреганта.
Существуют два основных способа получения флавононов, известные из уровня техники - выделение из природных источников и химический синтез.
Известны структурные аналоги к заявляемому соединению, проявляющие антиагрегационное действие
Антиагрегационная активность заявляемого соединения - 5,7-дигидрокси-6,8-диметилфлаванона ранее не была исследована.
Задачей изобретения является изыскание новых соединений, обладающих антиагрегационной активностью, и расширение арсенала средств воздействия на живой организм.
Поставленная задача решается тем, что соединение 5,7-дигидрокси-6,8-диметилфлаванон (1) проявляет высокую антиагрегационную активность при низкой токсичности.
Получают заявляемое соединение путем выделения из надземной части водяники черной Empetrum nigrum L.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение заявляемого соединения (1).
Проводилась экстракция высушенного сырья – побеги Водяники черной (масса – 10 гр.) н-гексаном (V = 200 мл). Экстракция проводилась до полного истощения сырья. Полученное извлечение выпаривалось на вакуумно-ротационном испарителе марки Heidolph при 60°C досуха и перерастворялась в 25 мл 96% этиловом спирте. Анализ полученных фракций и индивидуальных соединений проводили на аналитическом ВЭЖХ компании Shimadzu. Выделение индивидуального соединения проводили на препаративном ВЭЖХ компании Knauer.
Характеристика метода аналитического ВЭЖХ:
Хроматографическая колонка «SUPELCOSIL» LC-18, 25см x 4.6 мм, 5 мкм. Температура анализа - 40°C. Элюент: вода (компонент А), ацетонитрил (компонент В) с содержанием ТФУ 0,1%.
Время удерживания: 33,054 мин.
Характеристика метода препаративного ВЭЖХ:
Хроматографическая колонка «Kromasil» 100-5C18, 250 x 30 мм. Скорость потока 40 мл/мин. Элюент: вода (компонент А), ацетонитрил (компонент В) с содержанием ТФУ 0,1%.
Заявляемое соединение (1) представляет собой бледно-желтое кристаллическое вещество, имеющее два максимума поглощения в УФ-спектре (λmax) при 296 и 347 нм. Спектр HR-ESIMS имеет пик псевдомолекулярного иона [M+H]+ при m/z 285.1124 (расч. 285.1127), что соответствует молекулярной формуле C17H16O4.
Данные 1Н ЯМР-спектров соединения 1.
При установлении структуры соединения 1 применяли спектральные методы анализа. УФ-спектроскопию (СФ-2000, ОКБ Спектр, Россия), ЯМР-спектроскопию (Bruker Avance III 400 NMR Spectrometer, США) и масс-спектрометрию высокого разрешения (Bruker Micromass Q-TOF spectrometer, США).
Пример 2. Исследование влияние заявляемого соединения (I) на процессы активации и агрегации тромбоцитов.
Оценка влияние соединения I на функциональную активность тромбоцитов проводилась в условиях in vitro следующим образом. Эксперименты выполнены на крови здоровых доноров-мужчин в возрасте 18-24 лет. Общее количество доноров составило 12 человек. Забор крови проводился из кубитальной вены с использованием систем вакуумного забора крови BD Vacutainer® (Becton Dickinson and Company, США). В качестве стабилизатора венозной крови использовался 3,8% раствор цитрата натрия в соотношении 9:1.
Все тесты проводились на обогащенной и обедненной тромбоцитами плазмах. Образцы богатой тромбоцитами плазмы получали центрифугированием цитратной крови при 1000 об/мин в течение 10 минут, бестромбоцитарной плазмы - при 3000 об/мин в течение 20 минут. В работе использовалась центрифуга ОПН-3.02 (ОАО ТНК "ДАСТАН", Киргизия).
Исследование влияния на процесс агрегации тромбоцитов проводили по методу Born (Born G.G.V.Nature (London).-1962 .-V.194.) на агрегометре "АТ-02” (НПФ "Медтех", Россия). Определение антиагрегационной активности исследуемых веществ и препаратов сравнения проводили в конечной концентрации 1×10-3 моль/л. В качестве препарата сравнения использовали ацетилсалициловую кислоту («Ацетилсалициловая кислота», Фармацевтическая фабрика Шандонг Ксинхуа Фармасьютикал Ко., ЛТД, Китай). В качестве индукторов агрегации использовали аденозиндифосфат (АДФ) в концентрации 20 мкг/мл и коллаген в концентрации 5 мг/мл производства “Технология-Стандарт” (Россия, г. Барнаул).
В качестве маркера активации тромбоцитов измеряли экспрессию Р- селектина на поверхности тромбоцитов. Цитофлуориметрический анализ проводили на приборе BD FACSCanto II (США), используя оригинальное программное обеспечение. Измеряли связывание с тромбоцитами крови здоровых доноров флюорисцентно- меченых антител против СD62. Для этого образцы богатой тромбоцитами плазмы разводили в 100 раз 0,15 М фосфатно-солевым буферным раствором (рН 7,0-7,5), вносили исследуемые препараты и инкубировали в течение 5 минут. Для активации тромбоцитов в пробы вносили АДФ до конечной концентрации 20 мкг/мл и перемешивали. Активацию проводили в течение 15 минут, после чего клетки фиксировали добавлением 1% раствора формалина. После инкубации образцы богатой тромбоцитами плазмы окрашивали 20 минут при комнатной температуре мышиными моноклональными антителами CD62, меченными APC (алофикоцианином) (Becton Dickinson, США) согласно рекомендациям производителя. Параметры настройки прибора были одинаковы для всех измерений. Для каждой пробы собирали не менее 10000 событий. «Тромбоцитарное окно» выделяли по параметрам прямого (FCS) и малоугольного (SSC) светорассеяний в логарифмической шкале координат. Оценивали количество позитивных клеток (%) по СD62.
Результаты исследования обработаны с применением статистического пакета Statistica 10,0 (StatSoft Inc, США). Проверку на нормальность распределения фактических данных выполняли с помощью критерия Шапиро-Уилка. Выявлено, что вид распределения полученных данных отличается от нормального, поэтому при дальнейшей работе использовались непараметрические методы. Данные представлены в виде медианы, 25 и 75 процентилей. Дисперсионный анализ проводили с помощью критерия Краскела-Уоллиса. Критический уровень значимости р для статистических критериев принимали равным 0,05.
По результатам исследования установлено, что ацетилсалициловая кислота в скрининговой концентрации 1×10-3 моль/л проявила выраженную антиагрегационную активность, подавляя агрегацию тромбоцитов на 13,7% относительно контроля. При этом следует отметить, что ацетилсалициловая кислота не оказывает влияние на процессы реакции высвобождения тромбоцитов (латентный период) (таблица 1) и процессы активации тромбоцитов (таблица 2).
Таблица 1. Влияние соединения I и ацетилсалициловой кислоты на показатели агрегации тромбоцитов, Ме (0,25-0,75)
Примечание: *р≤0.05, **р≤0.001 - в сравнении с контролем; #р≤0.05, ##р≤0.001 - в сравнении с ацетилсалициловой кислотой; n=6.
Таблица 2. Экспрессия CD62 тромбоцитов в присутствии соединения I и ацетилсалициловой кислоты, Ме (0,25-0,75)
Примечание: Уровень статистической значимости различий признаков в сравнении с контролем: * - p>0,05, ** - p≤0,05; уровень статистической значимости различий признаков групп после активации АДФ: ‡ - p>0,05, ‡‡ - p≤0,05. CD62АДФ- - экспрессия CD62 до воздействия АДФ, CD62АДФ+ - экспрессия CD62 после воздействия АДФ.
Соединение I в эквимолярной концентрации подавляло АДФ-индуцированную агрегацию тромбоцитов в среднем на 19,5%, что превышает показатели активности ацетилсалициловой кислоты. Однако соединение I эффективнее ацетилсалициловой кислоты удлиняет реакцию высвобождения тромбоцитов на 23,6% и полностью ингибирует активацию тромбоцитов (экспрессия Р-селектина).
Таким образом, соединение I оказывает выраженную антиагрегационную активность, превосходящую по уровню и спектру аналоговый препарат - ацетилсалициловую кислоту.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ 1-(3,5-ДИГИДРОКСИ-4-МЕТОКСИФЕНИЛ)-2-(3-ГИДРОКСИФЕНИЛ)-ЭТАНА В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2806331C1 |
| ПРИМЕНЕНИЕ 4-O-α-АРАБИНОФУРАНОЗИЛЭЛЛАГОВОЙ КИСЛОТЫ В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2811240C1 |
| ПРИМЕНЕНИЕ 2,3,4-ТРИМЕТОКСИ-5-ГИДРОКСИ-9,10-ДИГИДРОФЕНАНТРЕНА В КАЧЕСТВЕ СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2808460C1 |
| 2-(1S,2R,5S)-6,6-ДИМЕТИЛБИЦИКЛО[3.1.1]ГЕПТ-2ИЛ]МЕТИЛ}СУЛЬФИНИЛ)ЭТАНОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ АНТИАГРЕГАЦИОННЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2522198C2 |
| Средство, проявляющее антиагрегационную активность | 2019 |
|
RU2727508C1 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ И АНТИТРОМБОГЕННУЮ АКТИВНОСТИ | 2010 |
|
RU2453312C1 |
| СПОСОБ ПЕРСОНИФИЦИРОВАННОГО ПОДБОРА АНТИАГРЕГАНТНЫХ ПРЕПАРАТОВ БОЛЬНЫМ, НУЖДАЮЩИМСЯ В ПОДОБНОМ ЛЕЧЕНИИ | 2012 |
|
RU2499261C1 |
| Производные триазола, проявляющие антиагрегационную активность | 2021 |
|
RU2770405C1 |
| Антиагрегационное и антиоксидантное средство | 2023 |
|
RU2808474C1 |
| Способ получения антиагрегационного и антиоксидантного средства | 2023 |
|
RU2819387C1 |
Изобретение относится к области фитохимии, к применению биологически активных соединений природного происхождения класса флаванонов, а именно к применению 5,7-дигидрокси-6,8-диметилфлаванона формулы (1) в качестве средства, обладающего антиагрегационной активностью. Технический результат изобретения заключается в проявлении 5,7-дигидрокси-6,8-диметилфлаваноном антиагрегационной активности, что может быть использовано в фармакологии и медицине при создании антиагрегационного лекарственного средства. 2 табл., 2 пр.
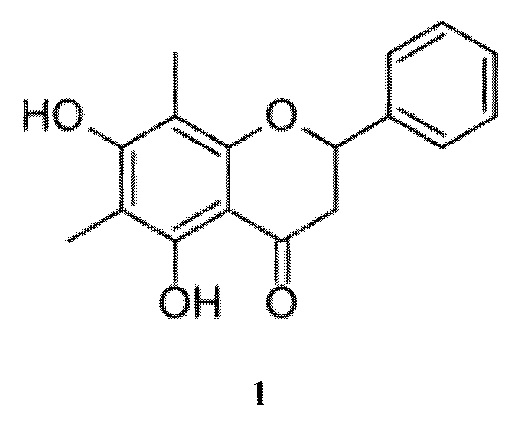
Применение 5,7-дигидрокси-6,8-диметилфлаванона (1):
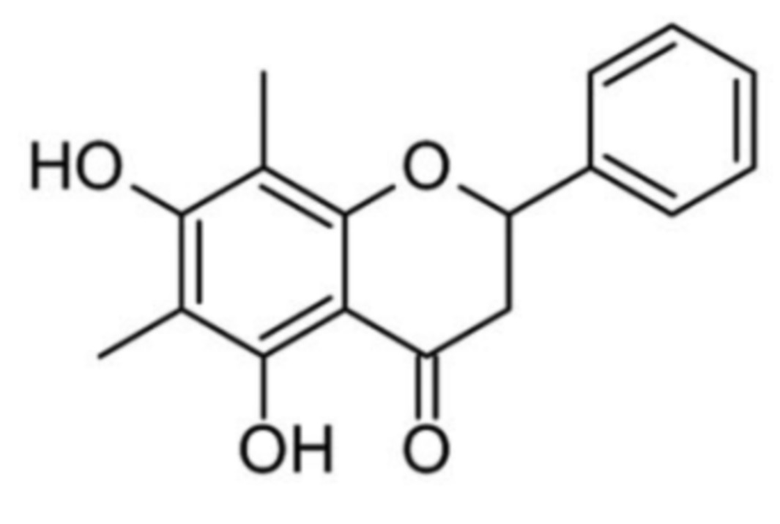
1
в качестве средства, обладающего антиагрегационной активностью.
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ АКТИВНОСТЬ | 2011 |
|
RU2486182C2 |
| СРЕДСТВО, ПРОЯВЛЯЮЩЕЕ АНТИАГРЕГАНТНУЮ И АНТИТРОМБОГЕННУЮ АКТИВНОСТИ | 2010 |
|
RU2453312C1 |
| CN 106045957 A, 26.10.2016 | |||
| BUDIONO B | |||
| et al | |||
| Antioxidant Activity of Syzygium samarangense L | |||
| and Their Endophytic Fungi, Molekul, 2019, vol.14, no.1, p.48-55 | |||
| INSANU M | |||
| et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2024-01-30—Публикация
2023-05-17—Подача