В соответствии с настоящим изобретением предложены продукты и композиции, а также варианты их применения. В частности, настоящее изобретение относится к продуктам нуклеиновых кислот, которые препятствуют экспрессии гена-мишени или ингибируют экспрессию гена-мишени, а также к вариантам терапевтического применения таких продуктов.
Уровень техники
Было показано, что двухцепочечная РНК (дцРНК), способная комплементарно связывать экспрессированную мРНК, способна блокировать экспрессию генов (Fire et al., 1998 и Elbashir et al., 2001) с помощью механизма, который был назван РНК-интерференцией (РНКи). Короткие дцРНК направляют геноспецифичный посттранскрипционный сайленсинг (подавление, «silencing») у многих организмов, включая позвоночных, и такие молекулы стали полезным инструментом для изучения функции генов. РНКи опосредуется РНК-индуцированным сайленсинг-комплексом (RISC), специфичной в отношении последовательности многокомпонентной нуклеазой, которая разрушает матричные РНК, гомологичные инициирующему фактору сайленсинга, загруженному в комплекс RISC. Интерферирующие РНК (называемые в настоящей заявке иРНК), такие как миРНК, антисмысловая РНК и микроРНК, представляют собой олигонуклеотиды, которые предотвращают образование белков путем сайленсинга генов, т.е. ингибируют трансляцию гена белка за счет разрушения молекул мРНК. Агенты, вызывающие сайленсинг гена, приобретают все большее значение для терапевтических приложений в медицине.
Согласно Watts and Corey в Journal of Pathology (2012; Vol 226, p 365-379), существуют алгоритмы, которые можно применять для конструирования нуклеиновых кислот, однако все они имеют недостатки. Для идентификации эффективных миРНК могут потребоваться различные экспериментальные способы, поскольку алгоритмы не учитывают такие факторы как третичная структура или участие РНК-связывающих белков. Таким образом, обнаружение эффективной нуклеиновой кислоты с минимальными нецелевыми эффектами является сложным процессом. Для фармацевтической разработки этих потенциально очень опасных молекул необходимо, чтобы их синтез был экономически выгодным, они распределялись по тканям-мишеням, проникали в клетки и функционировали в приемлемых пределах токсичности.
Однако доставка нуклеиновых кислот, таких как РНК, в клетки, без разрушения клеточными нуклеазами и при поддержании эффективности и специфичности в отношении мишени, оказалась сложной задачей для тех, кто занимается разработкой молекул нуклеиновых кислот для терапевтического применения.
Таким образом, средства для эффективной доставки олигонуклеотидов, в частности, двухцепочечных миРНК, в клетки в условиях in vivo приобретают все большее значение и требуют специфичного нацеливания и существенной защиты от внеклеточной среды, в частности, белков сыворотки. Одним из способов достижения специфичного нацеливания является конъюгация нацеливающей группы с дуплексным агентом РНКи. Нацеливающая группа помогает нацеливать дуплексный агент РНКи на требуемый целевой сайт, и существует потребность в конструировании подходящих нацеливающих групп для целевых рецепторных сайтов для конъюгированных молекул, которые будут поглощаться клетками, например, с помощью эндоцитоза.
Однако разработанные к настоящему времени нацеливающие лиганды не всегда могут быть применены в условиях in vivo, и существует явная потребность в более эффективных дуплексных агентах РНКи, конъюгированных со специфичным в отношении рецептора лигандом, а также способах их получения для доставки олигонуклеотидных терапевтических средств, нуклеиновых кислот и двухцепочечных миРНК в условиях in vivo.
Настоящее изобретение относится не столько к липидной системе доставки по отдельности, сколько к структуре самой нуклеиновой кислоты. Неожиданно было обнаружено, что нуклеиновая кислота в соответствии с настоящим изобретением обладает повышенной стабильностью, что предотвращает разрушение нуклеиновой кислоты до того, как она проникнет в клетку.
Сущность изобретения
Согласно настоящему изобретению предложена нуклеиновая кислота для ингибирования экспрессии гена-мишени в клетке, содержащая по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, при этом указанные первая и/или вторая цепи содержат фосфодитиоатную связь между по меньшей мере двумя нуклеотидами. Первая цепь может не содержать фосфодитиоатную связь между любыми из двух, трех или четырех концевых нуклеотидов на 5'-конце.
Первая и/или вторая цепи могут содержать фосфодитиоатную связь между по меньшей мере двумя концевыми 3' нуклеотидами и/или вторая цепь может содержать фосфодитиоатную связь между по меньшей мере двумя концевыми 5' нуклеотидами.
Нуклеиновая кислота может содержать фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 3'-конце первой цепи. Нуклеиновая кислота может содержать фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 3'-конце второй цепи. Нуклеиновая кислота может содержать фосфотиоатную или фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 5'-конце второй цепи.
Нуклеиновая кислота согласно настоящему изобретению также может содержать фосфотиоатную связь между каждым из трех концевых 3' нуклеотидов и/или между каждым из трех концевых 5' нуклеотидов на первой цепи, и/или между каждым из трех концевых 3' нуклеотидов и/или между каждым из трех 5' нуклеотидов второй цепи, если на этом конце отсутствует фосфодитиоатная связь.
Первая цепь и вторая цепь нуклеиновой кислоты могут представлять собой отдельные цепи. Нуклеиновая кислота может содержать одну цепь, которая содержит первую цепь и вторую цепь.
Первая цепь и/или указанная вторая цепь каждая могут содержать 17-35 нуклеотидов в длину, и по меньшей мере одна дуплексная область может состоять из 17-25 пар нуклеотидных оснований.
Нуклеиновая кислота может: а) иметь тупые концы на обоих концах; b) содержать липкий конец на одном конце и тупой конец на другом; или с) содержать липкие концы на обоих концах.
Один или более нуклеотидов на первой и/или второй цепях могут быть модифицированы с образованием модифицированных нуклеотидов. Один или более из нуклеотидов в нечетных положениях первой цепи могут быть модифицированы. Один или более из нуклеотидов в четных положениях первой цепи могут быть модифицированы с применением по меньшей мере второй модификации, причем указанная по меньшей мере вторая модификация отличается от модификации на одном или более нуклеотидах в нечетных положениях. По меньшей мере один из одного или более модифицированных нуклеотидов в четных положениях может быть смежным с по меньшей мере одним из одного или более модифицированных нуклеотидов в нечетных положениях.
Множество нуклеотидов в нечетных положениях могут быть модифицированы в нуклеиновой кислоте согласно настоящему изобретению. Множество нуклеотидов в четных положениях могут быть модифицированы с применением второй модификации. Первая цепь может содержать смежные нуклеотиды, которые модифицированы с применением общей модификации. Первая цепь также может содержать смежные нуклеотиды, которые модифицированы с применением второй отличающейся модификации.
Один или более из нуклеотидов в нечетных положениях второй цепи могут быть модифицированы с применением модификации, которая отличается от модификации на нуклеотидах в нечетных положениях первой цепи, и/или один или более из нуклеотидов в четных положениях второй цепи могут быть модифицированы с применением модификации, которая аналогична таковой на нуклеотидах в нечетных положениях первой цепи. По меньшей мере один из одного или более модифицированных нуклеотидов в четных положениях второй цепи может быть смежным с одним или более модифицированными нуклеотидами в нечетных положениях. Множество нуклеотидов в нечетных положениях второй цепи могут быть модифицированы с применением общей модификации, и/или множество нуклеотидов в четных положениях могут быть модифицированы с применением модификации, аналогичной той, которая присутствует на нуклеотидах в нечетных положениях первой цепи. Множество нуклеотидов в нечетных положениях могут быть модифицированы с применением второй модификации, причем указанная вторая модификация отличается от модификации на нуклеотидах в нечетных положениях первой цепи.
Вторая цепь может содержать смежные нуклеотиды, которые модифицированы с применением общей модификации, которая может представлять собой вторую модификацию, которая отличается от модификации на нуклеотидах в нечетных положениях первой цепи.
В нуклеиновой кислоте согласно настоящему изобретению каждый из нуклеотидов в нечетных положениях в первой цепи и каждый из нуклеотидов в четных положениях во второй цепи может быть модифицирован с применением общей модификации, а каждый из нуклеотидов в четных положениях в первой цепи может быть модифицирован с применением второй модификации, и каждый из нуклеотидов в нечетных положениях второй цепи может быть модифицирован с применением второй модификации.
В нуклеиновой кислоте согласно настоящему изобретению модифицированные нуклеотиды первой цепи могут быть сдвинуты по меньшей мере на один нуклеотид относительно немодифицированных или по-разному модифицированных нуклеотидов второй цепи.
Первая цепь может содержать последовательность SEQ ID NO: 1 и/или вторая цепь может содержать последовательность SEQ ID NO: 2.
Модификация и/или модификации могут быть выбраны по отдельности и независимо из группы, состоящей из 3'-концевого дезокситимина, 2'-O-метила, 2'-дезокси-модификации, 2'-амино-модификации, 2'-алкил-модификации, морфолино-модификации, фосфоамидатной модификации, модификации 5'-фосфотиоатной группой, модификации 5'-фосфатом или миметиком 5'-фосфата, а также модификации производным холестерина или группой бисдециламида додекановой кислоты, и/или модифицированный нуклеотид может представлять собой любой из закрытого нуклеотида, лишенного азотистого основания нуклеотида или содержащего неприродное основание нуклеотида. По меньшей мере одна модификация может представлять собой 2'-О-метил и/или по меньшей мере одна модификация может представлять собой 2'-F.
Нуклеиновая кислота согласно настоящему изобретению может быть конъюгирована с лигандом.
Нуклеиновая кислота согласно настоящему изобретению может содержать фосфотиоатную связь между одним, двумя или тремя концевыми 3' нуклеотидами и/или 5' нуклеотидами первой и/или второй цепей, в дополнение к фосфодитиоатной связи на этом (й) же самом (й) или на другом (ой) конце или цепи.
Согласно настоящему изобретению предложена, в качестве второго аспекта, нуклеиновая кислота для ингибирования экспрессии гена-мишени в клетке, содержащая по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, при этом указанные первая и/или вторая цепи содержат фосфодитиоатную связь между по меньшей мере двумя концевыми 3' нуклеотидами, и/или вторая цепь содержит фосфодитиоатную связь между по меньшей мере двумя концевыми 5' нуклеотидами, и при этом молекула нуклеиновой кислоты конъюгирована с лигандом.
Лиганд для применения в настоящем изобретении, таким образом, может содержать (i) одну или более групп N-ацетилгалактозамина (GalNAc) и их производных, и (ii) линкер, причем с помощью указанного линкера конъюгируют группы GalNAc с последовательностью, определенной в любых предшествующих аспектах. Линкер может иметь двухвалентную, трехвалентную или четырехвалентную разветвленную структуру. Нуклеотиды могут быть модифицированы, как определено в настоящей заявке. Лиганд может содержать формулу I:
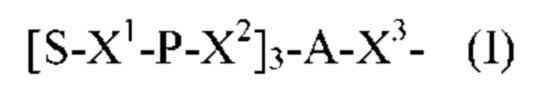
в которой:
S представляет собой сахарид, причем указанный сахарид представляет собой N-ацетилгалактозамин;
X1 представляет собой С3-С6 алкилен или (-СН2-СН2-O)m(-СН2)2-, где m равно 1, 2 или 3;
Р представляет собой фосфат или модифицированный фосфат (предпочтительно тиофосфат);
X2 представляет собой алкилен или простой алкиленовый эфир формулы (-СН2)n-O-СН2-, где n=1-6;
А представляет собой блок разветвления; X3 представляет собой мостиковый блок;
при этом нуклеиновая кислота в соответствии с настоящим изобретением конъюгирована с X3 за счет фосфата или модифицированного фосфата (предпочтительно тиофосфата).
Таким образом, согласно настоящему изобретению дополнительно предложена конъюгированная нуклеиновая кислота, имеющая одну из следующих структур:
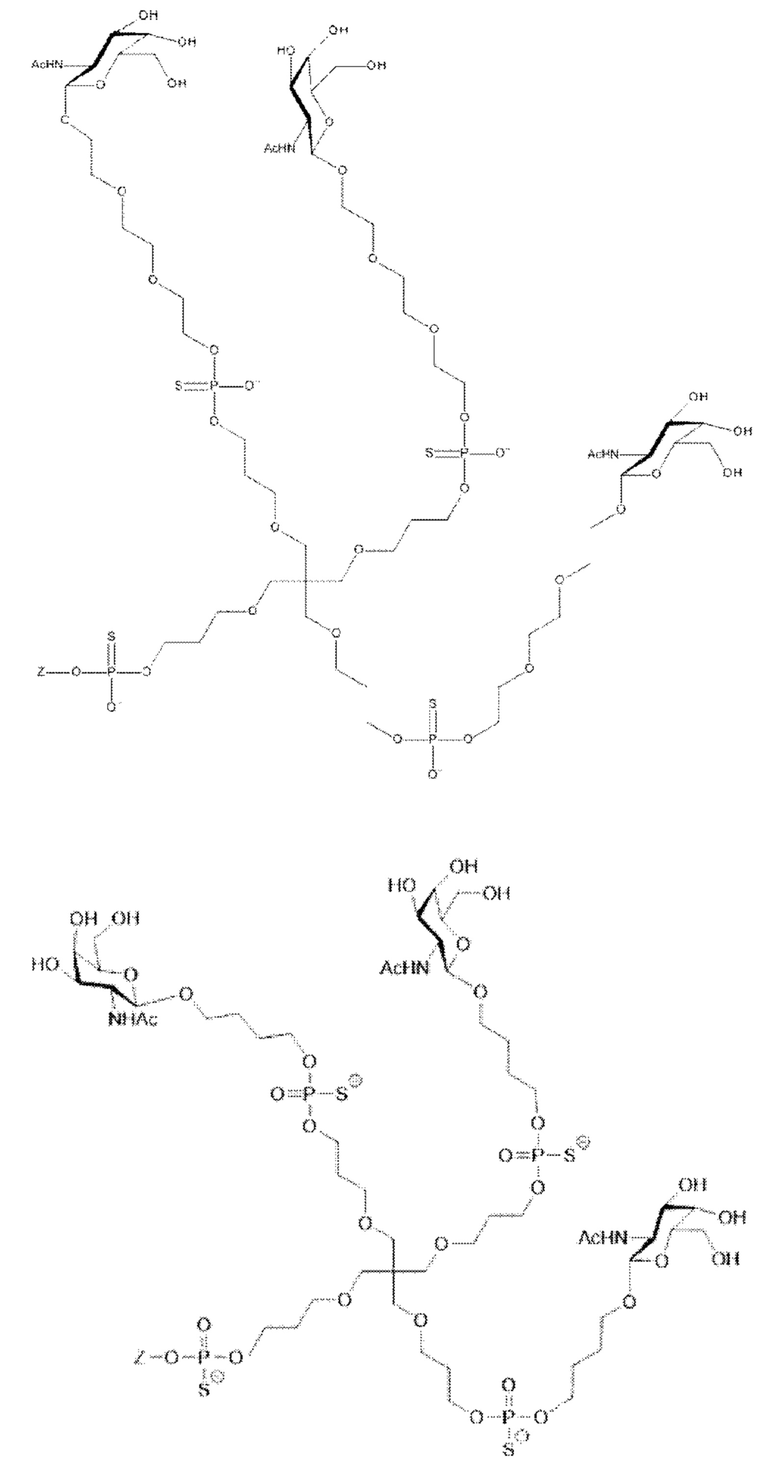
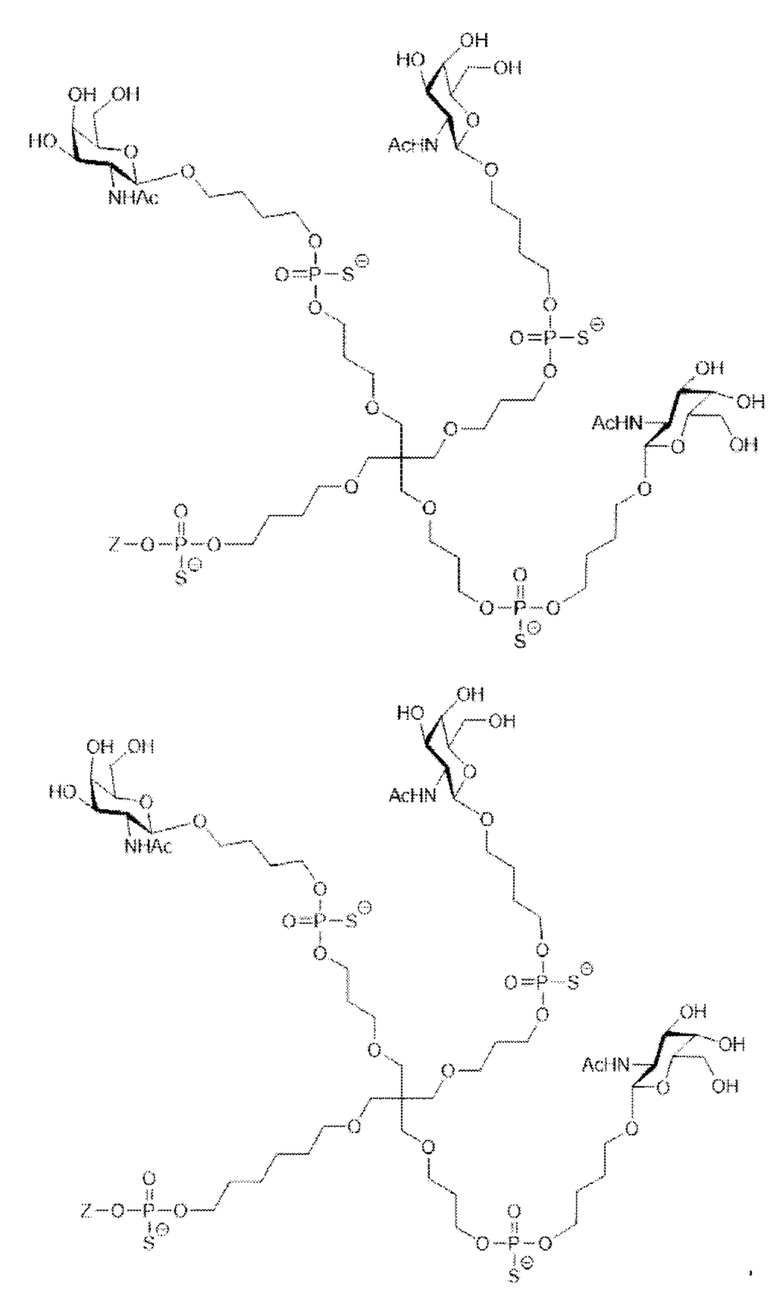
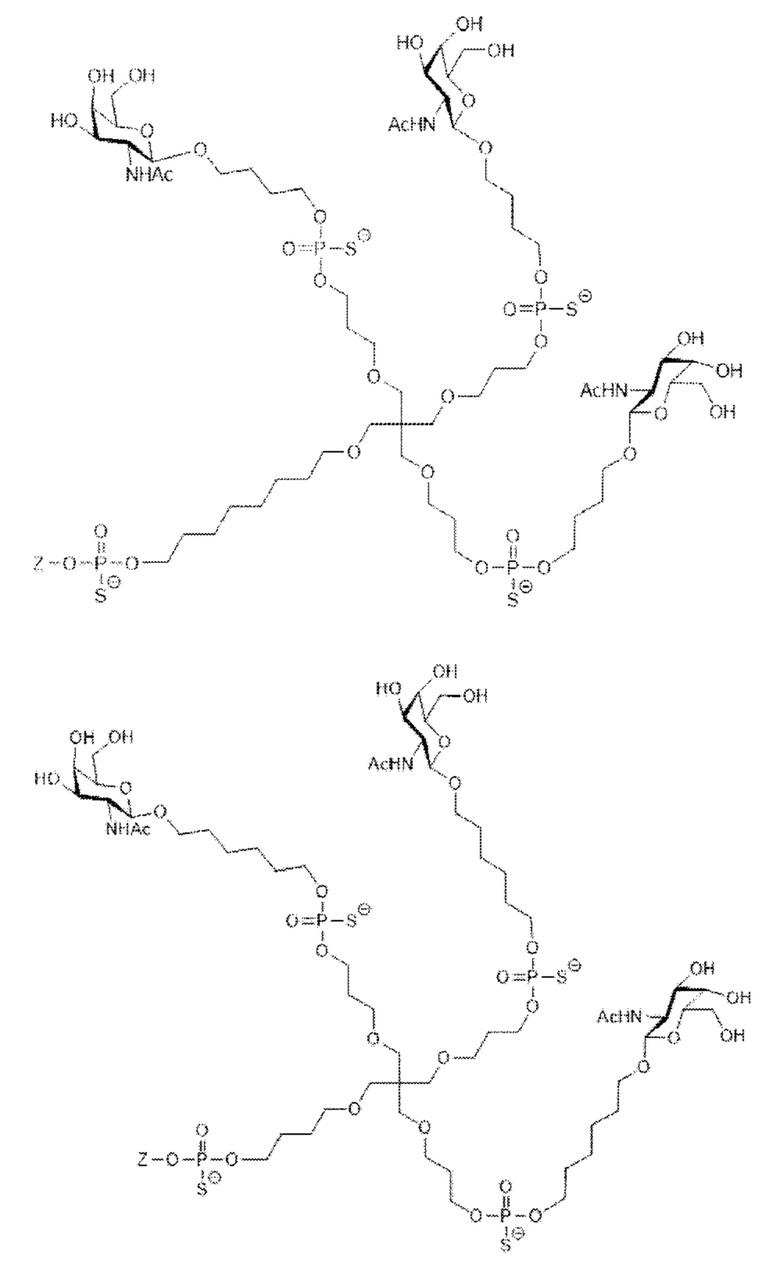
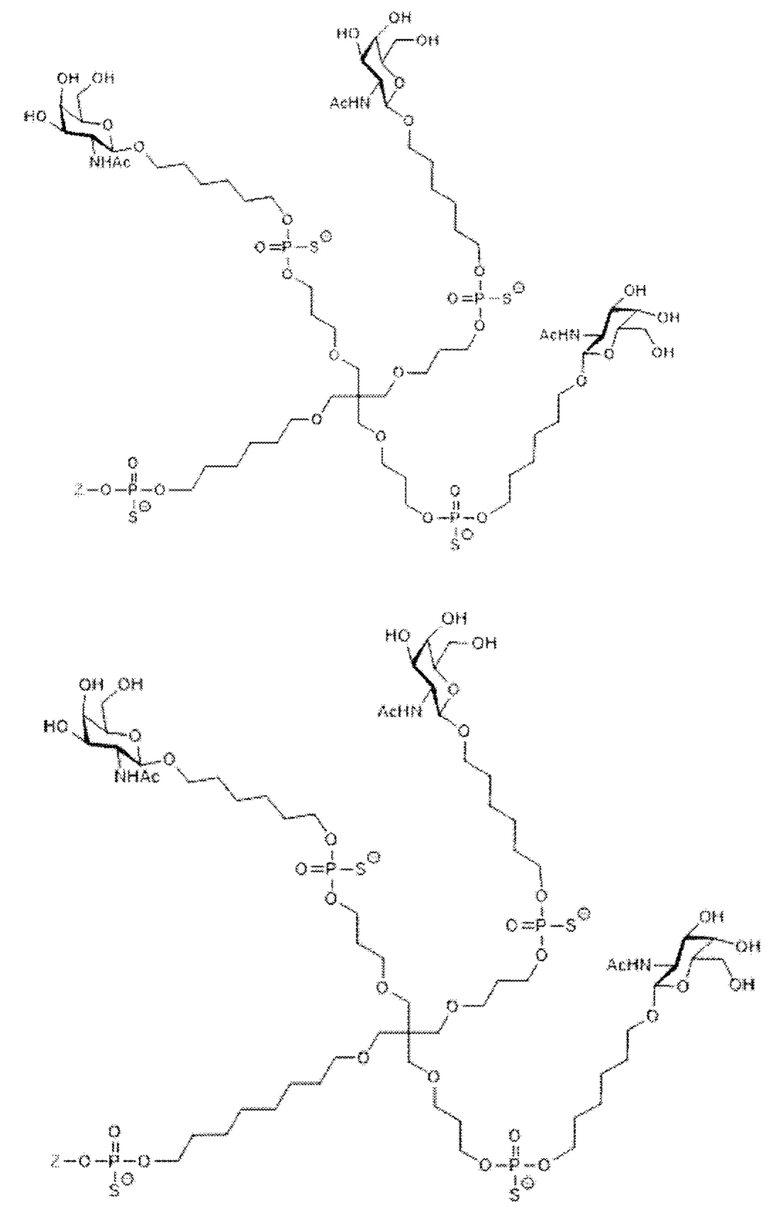
в которых Z представляет собой нуклеиновую кислоту, определенную в настоящей заявке выше.
Лиганд может содержать:
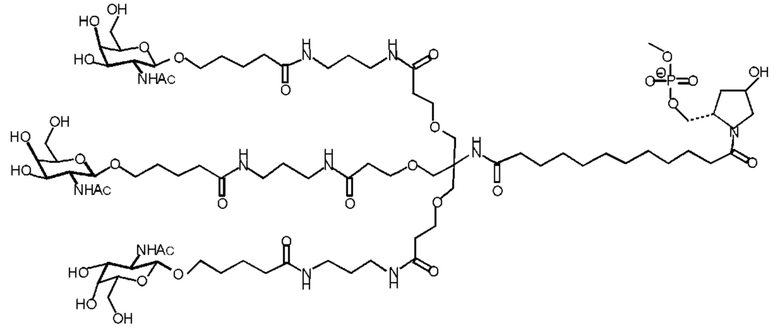
Согласно настоящему изобретению также предложена композиция, содержащая нуклеиновую кислоту или конъюгированную нуклеиновую кислоту, определенные в настоящей заявке, и одно или более физиологически приемлемых вспомогательных веществ. Вспомогательное (ые) вещество (а) может (могут) представлять собой:
i) катионный липид или его фармацевтически приемлемую соль;
ii) стероид;
iii) фосфолипид фосфатидилэтаноламин;
iv) пегилированный липид.
Содержание компонента катионного липида в композиции может составлять от приблизительно 55 мол.% до приблизительно 65 мол.% от общего содержания липидов липидного состава, предпочтительно приблизительно 59 мол.% от общего содержания липидов липидной композиции.
Композиция может содержать;
катионный липид, имеющий структуру;
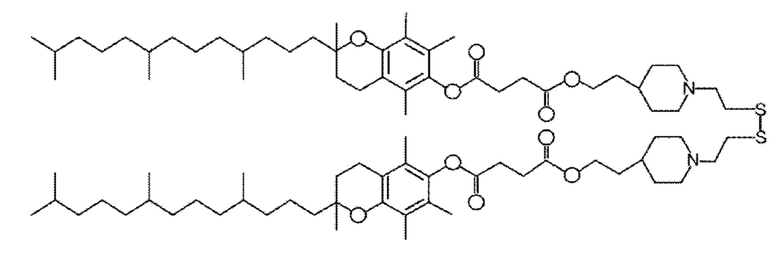
стероид, имеющий структуру;
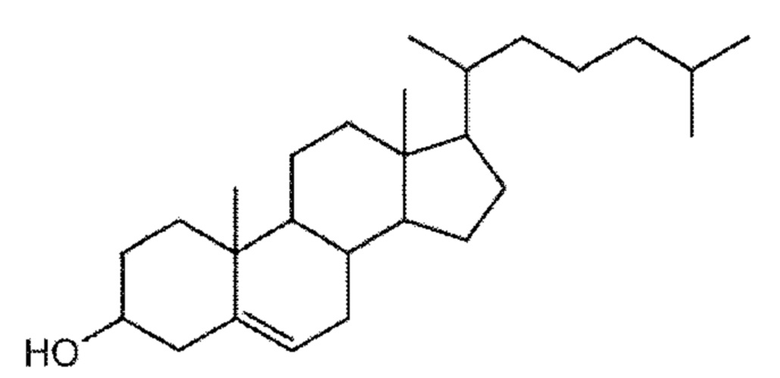
холестерин
фосфолипид фосфатидилэтаноламин, имеющий структуру;
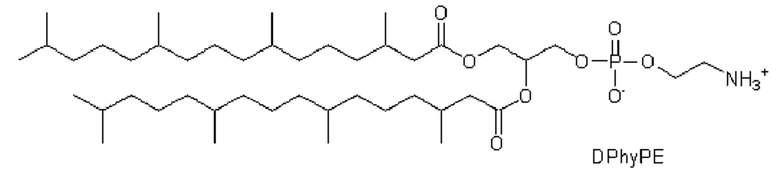
и пегилированный липид, имеющий структуру;
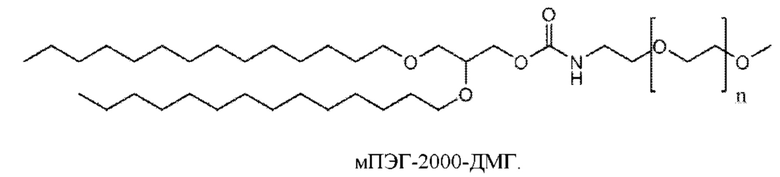
Также предложена нуклеиновая кислота или конъюгированная нуклеиновая кислота в соответствии с любым аспектом настоящего изобретения для применения при лечении или предотвращении заболевания или нарушения и/или при изготовлении лекарственного средства для лечения или предотвращения заболевания или нарушения.
Согласно настоящему изобретению предложен способ лечения или предотвращения заболевания или нарушения, включающий введение композиции, содержащей нуклеиновую кислоту или конъюгированную нуклеиновую кислоту в соответствии с любым аспектом настоящего изобретения, индивидууму, нуждающемуся в лечении. Нуклеиновую кислоту или конъюгированную нуклеиновую кислоту можно вводить субъекту подкожно, внутривенно или с использованием любых других путей применения, таких как пероральный, ректальный или внутрибрюшинный.
Также включен способ получения нуклеиновой кислоты или конъюгированной нуклеиновой кислоты согласно настоящему изобретению.
Подробное описание изобретения
Настоящее изобретение относится к нуклеиновой кислоте, которая является двухцепочечной и направлена к экспрессированному РНК-транскрипту гена-мишени, а также к ее композициям. Эти нуклеиновые кислоты можно применять при лечении различных заболеваний и нарушений, при которых целевым является снижение экспрессии продуктов гена-мишени.
Первый аспект настоящего изобретения относится к нуклеиновой кислоте для ингибирования экспрессии гена-мишени в клетке, содержащей по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, подлежащего ингибированию, и при этом указанные первая и/или вторая цепи содержат фосфодитиоатную связь между по меньшей мере двумя нуклеотидами.
Необязательно первая и/или вторая цепи могут содержать фосфодитиоатную связь между по меньшей мере двумя концевыми 3' нуклеотидами и/или вторая цепь может содержать фосфодитиоатную связь между по меньшей мере двумя концевыми 5' нуклеотидами.
Необязательно первая цепь не содержит фосфодитиоатную связь между любыми из двух, трех или четырех концевых нуклеотидов на 5'-конце, иными словами, она содержит связь, отличную от фосфодитиоатной связи, между любыми из двух, трех или четырех концевых нуклеотидов на 5'-конце.
Родственный аспект представляет собой нуклеиновую кислоту для ингибирования экспрессии гена-мишени в клетке, содержащую по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, при этом нуклеиновая кислота содержит фосфодитиоатные связи между двумя концевыми нуклеотидами на 3'-конце первой цепи, при этом нуклеиновая кислота содержит фосфодитиоатную связь, каждая из которых находится между двумя концевыми нуклеотидами на 3'-конце и между двумя концевыми нуклеотидами на 5'-конце второй цепи, и при этом первая цепь содержит связь, отличную от фосфодитиоатной связи, между двумя, тремя или четырьмя концевыми нуклеотидами на 5'-конце. Предпочтительно эта связь, отличная от фосфодитиоатной связи, представляет собой фосфат или фосфотиоат, более предпочтительно (незамещенный) фосфат. Предпочтительно все связи между нуклеотидами обеих цепей, которые отличаются от связи между двумя концевыми нуклеотидами на 3'-конце первой цепи и связей между двумя концевыми нуклеотидами на 3'-конце и на 5'-конце второй цепи, представляют собой незамещенные фосфатные связи.
Под нуклеиновой кислотой подразумевают нуклеиновую кислоту, содержащую две цепи, содержащие нуклеотиды, которая способна препятствовать экспрессии генов. Ингибирование может быть полным или частичным и приводит к снижению экспрессии генов нацеленным образом. Нуклеиновая кислота содержит две отдельные полинуклеотидные цепи; первую цепь, которая также может быть направляющей цепью; и вторую цепь, которая также может быть пассажирской цепью. Первая цепь и вторая цепь могут быть частью одной и той же полинуклеотидной молекулы, являющейся самокомплементарной, которая «складывается» с образованием двухцепочечной молекулы. Нуклеиновая кислота может представлять собой молекулу миРНК.
Нуклеиновая кислота может содержать рибонуклеотиды, модифицированные рибонуклеотиды, дезоксинуклеотиды, дезоксирибонуклеотиды или аналоги нуклеотидов. Нуклеиновая кислота может дополнительно содержать двухцепочечную часть нуклеиновой кислоты или дуплексную область, образованную всей первой цепью или ее частью (также известной в данной области техники как направляющая цепь) и всей второй цепью или ее частью (также известной в данной области техники как пассажирская цепь). Дуплексная область определяется как область, начинающаяся с первой пары оснований, образованной между первой цепью и второй цепью, и заканчивающаяся последней парой оснований, образованной между первой цепью и второй цепью, включительно.
Под дуплексной областью подразумевают область в двух комплементарных или по существу комплементарных олигонуклеотидах, которые образуют пары оснований друг с другом, либо путем спаривания оснований по Уотсону-Крику, либо любым другим способом, который обеспечивает образование дуплекса между олигонуклеотидными цепями, которые являются комплементарными или по существу комплементарными. Например, олигонуклеотидная цепь, содержащая 21 нуклеотидный блок, может спариваться с другим олигонуклеотидом из 21 нуклеотидного блока, но только 19 нуклеотидов на каждой цепи являются комплементарными или по существу комплементарными так, что «дуплексная область» состоит из 19 пар оснований. Оставшиеся пары оснований могут существовать в виде 5'- и 3'-липких концов или в виде одноцепочечных областей. Кроме того, в дуплексной области не требуется 100% комплементарность; в дуплексной области допустима существенная комплементарность. Существенная комплементарность относится к такой комплементарности между цепями, что они способны ренатурировать в биологических условиях. Методики, позволяющие эмпирически определить, способны ли две цепи ренатурировать в биологических условиях, хорошо известны в данной области техники. Согласно другому варианту две цепи могут быть синтезированы и добавлены вместе в биологических условиях, чтобы определить, ренатурируют ли они друг с другом.
Части первой цепи и второй цепи, которые образуют по меньшей мере одну дуплексную область, могут быть полностью комплементарны и по меньшей мере частично комплементарны друг другу.
В зависимости от длины нуклеиновой кислоты не обязательно требуется идеальное соответствие между первой цепью и второй цепью с точки зрения комплементарности оснований. Однако первая и вторая цепи должны быть способны гибридизоваться в физиологических условиях.
Комплементарность между первой цепью и второй цепью по меньшей мере в одной дуплексной области может быть идеальной в том, что в любой цепи отсутствуют несоответствия нуклеотидов или дополнительные/удаленные нуклеотиды. Согласно другому варианту комплементарность может быть неидеальной. Комплементарность может составлять по меньшей мере 70%, 75%, 80%, 85%, 90% или 95%.
Каждая из первой цепи и второй цепи может содержать область комплементарности, которая содержит по меньшей мере 15 смежных нуклеотидов.
Нуклеиновая кислота включает образование дуплексной области между всей первой цепь или ее частью и частью нуклеиновой кислоты-мишени. Часть нуклеиновой кислоты-мишени, которая образует дуплексную область с первой цепью, определяемую как область, которая начинается с первой пары оснований, образованной между первой цепью и последовательностью-мишенью, и заканчивается последней парой оснований, образованной между первой цепью и последовательностью-мишенью, включительно, представляет собой последовательность нуклеиновой кислоты-мишени или просто последовательность-мишень. Дуплексная область, образованная между первой цепью и второй цепью, необязательно должна быть аналогична дуплексной области, образованной между первой цепью и последовательностью-мишенью. Это означает, что вторая цепь может иметь последовательность, отличающуюся от последовательности-мишени, однако первая цепь должна быть способна образовывать дуплексную структуру с обеими второй цепью и последовательностью-мишенью.
Комплементарность между первой цепью и последовательностью-мишенью может быть идеальной (в каждой нуклеиновой кислоте отсутствуют несовпадения нуклеотидов или дополнительные/удаленные нуклеотиды).
Комплементарность между первой цепью и последовательностью-мишенью может быть неидеальной. Комплементарность может составлять от приблизительно 70% до приблизительно 100%. Более конкретно, комплементарность может составлять по меньшей мере 70%, 80%, 85%, 90% или 95% или промежуточное значение.
Идентичность между первой цепью и комплементарной последовательностью последовательности-мишени может составлять от приблизительно 75% до приблизительно 100%. Более конкретно, комплементарность может составлять по меньшей мере 75%, 80%, 85%, 90% или 95% или промежуточное значение, при условии, что нуклеиновая кислота способна уменьшать или ингибировать экспрессию гена-мишени.
Нуклеиновая кислота, имеющая менее чем 100% комплементарность между первой цепью и последовательностью-мишенью, может быть способна уменьшить экспрессию гена-мишени до того же уровня, как и нуклеиновая кислота с идеальной комплементарностью между первой цепью и последовательностью-мишенью. Согласно другому варианту она может быть способна уменьшить экспрессию гена-мишени до уровня, который составляет 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% от уровня экспрессии, достигнутого с помощью нуклеиновой кислоты с идеальной комплементарностью.
Согласно дополнительному аспекту нуклеиновая кислота, описанная в настоящей заявке, может уменьшить экспрессию гена-мишени в клетке на по меньшей мере 10% по сравнению с уровнем, наблюдаемым в отсутствие ингибитора, который может представлять собой нуклеиновую кислоту. Все предпочтительные признаки любого из предшествующих аспектов также применимы к этому аспекту. В частности, экспрессия гена-мишени в клетке может быть уменьшена до 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, 15% или менее, а также промежуточных значений, по сравнению с экспрессией, которая наблюдается в отсутствие ингибитора (который может представлять собой нуклеиновую кислоту).
Нуклеиновая кислота может содержать первую цепь и вторую цепь, каждая из которых содержит 19-25 нуклеотидов в длину. Первая цепь и вторая цепь могут иметь разную длину.
Нуклеиновая кислота может содержать 15-25 пар нуклеотидов в длину. Нуклеиновая кислота может содержать 17-23 пары нуклеотидов в длину. Нуклеиновая кислота может содержать 17-25 пар нуклеотидов в длину. Нуклеиновая кислота может содержать 23-24 пары нуклеотидов в длину. Нуклеиновая кислота может содержать 19-21 пару нуклеотидов в длину. Нуклеиновая кислота может содержать 21-23 пары нуклеотидов в длину.
Нуклеиновая кислота может содержать дуплексную область, которая состоит из 19-25 пар нуклеотидных оснований. Дуплексная область может состоять из 17, 18, 19, 20, 21, 22, 23, 24 или 25 пар оснований, которые могут быть смежными.
Предпочтительно нуклеиновая кислота опосредует РНК-интерференцию.
Согласно дополнительному аспекту описанная нуклеиновая кислота или конъюгированная нуклеиновая кислота может уменьшать экспрессию своего транскрипта-мишени на по меньшей мере 15% по сравнению с экспрессией, наблюдаемой в отсутствие нуклеиновой кислоты или конъюгированной нуклеиновой кислоты. Все предпочтительные признаки любого из предшествующих аспектов также применимы к этому аспекту. В частности, экспрессия транскрипта-мишени может быть уменьшена по меньшей мере до следующих заданных процентных значений (%) или до менее чем 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, 15% или менее, а также промежуточных значений, относительно экспрессии, которая наблюдалась в отсутствие нуклеиновой кислоты или конъюгированной нуклеиновой кислоты или в присутствии не вызывающего сайленсинг контроля.
Применение фосфодитиоатной связи в нуклеиновой кислоте согласно настоящему изобретению уменьшает варьирование стереохимии популяции молекул нуклеиновой кислоты, которое может быть вызвано фосфотиоатной связью, имеющей хиральный центр, и отсутствием возможности контроля того, какой несоединяющий атом кислорода замещен серой. Применение фосфодитиоата обеспечивает отсутствие в этой связи хирального центра, и, таким образом, уменьшает или устраняет любое варьирование в популяции молекул нуклеиновой кислоты в зависимости от количества фосфодитиоатных и фосфотиоатных связей, применяемых в молекуле нуклеиновой кислоты.
Кроме того, безотносительно к какой-либо теории, может оказаться, что вместо двух фосфотиоатных связей можно применять одну фосфодитиоатную связь и уменьшить таким образом количество «неприродных» связей внутри нуклеиновой кислоты согласно настоящему изобретению.
Нуклеиновая кислота может содержать фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 3'-конце первой цепи. Нуклеиновая кислота может содержать фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 3'-конце второй цепи. Нуклеиновая кислота может содержать фосфотиоатную или фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 5'-конце второй цепи.
Нуклеиновая кислота согласно настоящему изобретению также может содержать фосфотиоатную связь между каждым из трех концевых 3' нуклеотидов и/или между каждым из трех концевых 5' нуклеотидов на первой цепи, и/или между каждым из трех 3'-концевых нуклеотидов и/или между каждым из трех 5'-концевых нуклеотидов второй цепи, если на этом конце отсутствует фосфодитиоатная связь.
Нуклеиновая кислота согласно настоящему изобретению может содержать смесь фосфотиоатных и фосфодитиоатных связей, примеры которых приведены в настоящей заявке. Нуклеиновая кислота согласно настоящему изобретению может содержать фосфодитиоат на 3'-конце каждой из первой цепи и второй цепи.
Нуклеиновая кислота может содержать тупые концы на обоих концах; может содержать липкий конец на одном конце и тупой конец на другом конце; или содержит липкий конец на обоих концах.
В настоящей заявке «липкий конец ("overhang")» имеет свое обычное и принятое значение в данной области техники, т.е. одноцепочечная часть нуклеиновой кислоты, которая простирается за пределы концевого нуклеотида комплементарной цепи в двухцепочечной нуклеиновой кислоте. Термин «тупой конец» включает двухцепочечные нуклеиновые кислоты, в которых обе цепи оканчиваются в одном и том же положении, независимо от того, спарен (ы) ли концевой (ые) нуклеотид (ы). Концевой нуклеотид первой цепи и второй цепи на тупом конце может быть спаренным. Концевой нуклеотид первой цепи и второй цепи на тупом конце может быть неспаренным. Два концевых нуклеотида первой цепи и второй цепи на тупом конце могут быть спаренными. Два концевых нуклеотида первой цепи и второй цепи на тупом конце могут быть неспаренными.
В настоящей заявке термин «незамещенный фосфат» обозначает обычный фосфат, который обычно обнаруживается между двумя нуклеотидами в природе, например, в природных молекулах ДНК или РНК. Такой фосфат может быть обозначен в настоящей заявке просто как «фосфат», «незамещенный фосфат» или «фосфодиэфир».
Нуклеиновая кислота может содержать липкий конец на одном конце и тупой конец на другом. Нуклеиновая кислота может содержать липкий конец на обоих концах. Нуклеиновая кислота может содержать тупые концы на обоих концах. Нуклеиновая кислота может иметь тупой конец на конце с 5'-концом первой цепи и 3'-концом второй цепи или на 3'-конце первой цепи и 5'-конце второй цепи.
Нуклеиновая кислота может содержать липкий конец на 3'- или 5'-конце. Нуклеиновая кислота может содержать 3'-липкий конец на первой цепи. Нуклеиновая кислота может содержать 3'-липкий конец на второй цепи. Нуклеиновая кислота может содержать 5'-липкий конец на первой цепи. Нуклеиновая кислота может содержать 5'-липкий конец на второй цепи. Нуклеиновая кислота может содержать липкий конец как на 5'-конце, так и на 3'-конце первой цепи. Нуклеиновая кислота может содержать липкий конец как на 5'-конце, так и на 3'-конце второй цепи. Нуклеиновая кислота может содержать 5'-липкий конец на первой цепи и 3'-липкий конец на второй цепи. Нуклеиновая кислота может содержать 3'-липкий конец на первой цепи и 5'-липкий конец на второй цепи. Нуклеиновая кислота может содержать 3'-липкий конец на первой цепи и 3'-липкий конец на второй цепи. Нуклеиновая кислота может содержать 5'-липкий конец на первой цепи и 5'-липкий конец на второй цепи.
Липкий конец на 3'-конце или 5'-конце второй цепи или первой цепи может быть выбран из 1, 2, 3, 4 и 5 нуклеотидов в длину. Необязательно липкий конец может состоять из 1 или 2 нуклеотидов, которые могут быть модифицированы, но необязательно.
Немодифицированные полинуклеотиды, в частности, рибонуклеотиды, могут быть подвержены разрушению клеточными нуклеазами, и, как таковые, модификации/модифицированные нуклеотиды могут быть включены в нуклеиновую кислоту согласно настоящему изобретению. Такие модификации могут помочь стабилизировать нуклеиновую кислоту, делая ее более устойчивой к нуклеазам. Улучшенная устойчивость обеспечивает активность нуклеиновых кислот в качестве посредников РНК-интерференции в течение более длительных периодов времени и особенно желательна, если нуклеиновые кислоты должны применяться для лечения.
Один или более нуклеотидов на второй цепи и/или первой цепи нуклеиновой кислоты согласно настоящему изобретению могут быть модифицированы.
Модификации нуклеиновой кислоты согласно настоящему изобретению обычно обеспечивают эффективный инструмент для преодоления потенциальных ограничений, включая, но не ограничиваясь этим, стабильность и биодоступность в условиях in vitro и в условиях in vivo, присущие природным молекулам РНК. Нуклеиновая кислота в соответствии с настоящим изобретением может быть модифицирована с помощью химических модификаций. Модифицированная нуклеиновая кислота также может свести к минимуму возможность индукции активности интерферона у человека. Модификация может дополнительно усиливать функциональную доставку нуклеиновой кислоты к клетке-мишени. Модифицированная нуклеиновая кислота согласно настоящему изобретению может содержать один или более химически модифицированных рибонуклеотидов любой или обеих из первой цепи или второй цепи. Рибонуклеотид может содержать химическую модификацию основания, сахара или фосфатных групп. Рибонуклеиновая кислота может быть модифицирована путем замены или вставки аналогов нуклеиновых кислот или оснований.
Один или более нуклеотидов нуклеиновой кислоты согласно настоящему изобретению могут быть модифицированы. Нуклеиновая кислота может содержать по меньшей мере один модифицированный нуклеотид. Модифицированный нуклеотид может находиться на первой цепи. Модифицированный нуклеотид может находиться во второй цепи. Модифицированный нуклеотид может находиться в дуплексной области. Модифицированный нуклеотид может находиться за пределами дуплексной области, т.е. в одноцепочечной области. Модифицированный нуклеотид может находиться на первой цепи и может находиться за пределами дуплексной области. Модифицированный нуклеотид может находиться на второй цепи и может находиться за пределами дуплексной области. 3'-концевой нуклеотид первой цепи может представлять собой модифицированный нуклеотид. 3'-концевой нуклеотид второй цепи может представлять собой модифицированный нуклеотид. 5'-концевой нуклеотид первой цепи может представлять собой модифицированный нуклеотид. 5'-концевой нуклеотид второй цепи может представлять собой модифицированный нуклеотид.
Нуклеиновая кислота согласно настоящему изобретению может содержать 1 модифицированный нуклеотид или нуклеиновая кислота согласно настоящему изобретению может содержать приблизительно 2-4 модифицированных нуклеотида, или нуклеиновая кислота может содержать приблизительно 4-6 модифицированных нуклеотидов, приблизительно 6-8 модифицированных нуклеотидов, приблизительно 8-10 модифицированных нуклеотидов, приблизительно 10-12 модифицированных нуклеотидов, приблизительно 12-14 модифицированных нуклеотидов, приблизительно 14-16 модифицированных нуклеотидов, приблизительно 16-18 модифицированных нуклеотидов, приблизительно 18-20 модифицированных нуклеотидов, приблизительно 20-22 модифицированных нуклеотида, приблизительно 22-24 модифицированных нуклеотида, 24-26 модифицированных нуклеотидов или приблизительно 26-28 модифицированных нуклеотидов. В каждом случае нуклеиновая кислота, содержащая указанные модифицированные нуклеотиды, сохраняет по меньшей мере 50% своей активности по сравнению с этой же нуклеиновой кислотой, но без указанных модифицированных нуклеотидов. Нуклеиновая кислота может сохранять 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% или промежуточное значение своей активности по сравнению с этой же нуклеиновой кислотой, но без указанных модифицированных нуклеотидов, или может иметь более 100% активности этого же нуклеотида без указанных модифицированных нуклеотидов.
Модифицированный нуклеотид может представлять собой пурин или пиримидин. По меньшей мере половина пуринов может быть модифицирована. По меньшей мере половина пиримидинов может быть модифицирована. Все из пуринов могут быть модифицированы. Все из пиримидинов могут быть модифицированы. Модифицированные нуклеотиды могут быть выбраны из группы, состоящей из 3'-концевого дезокситиминового (dT) нуклеотида, 2'-O-метил-модифицированного нуклеотида, 2'-модифицированного нуклеотида, 2'-дезокси-модифицированного нуклеотида, закрытого нуклеотида, лишенного азотистого основания нуклеотида, 2'-амино-модифицированного нуклеотида, 2'-алкил-модифицированного нуклеотида, морфолино-нуклеотида, фосфоамидата, содержащего неприродное основание нуклеотида, нуклеотида, содержащего 5'-фосфотиоатную группу, нуклеотида, содержащего 5'-фосфат или миметик 5'-фосфата, и концевого нуклеотида, соединенного с производным холестерина или группой бисдециламида додекановой кислоты.
Нуклеиновая кислота может содержать нуклеотид, содержащий модифицированный нуклеотид, причем основание выбрано из 2-аминоаденозина, 2,6-диаминопурина, инозина, пиридин-4-она, пиридин-2-она, фенила, псевдоурацила, 2,4,6-триметоксибензола, 3-метилурацила, дигидроуридина, нафтила, аминофенила, 5-алкилцитидина (например, 5-метилцитидина), 5-алкилуридина (например, риботимидина), 5-галоуридина (например, 5-бромуридина), 6-азапиримидина, 6-алкилпиримидина (например, 6-метилуридина), пропина, квеуозина, 2-тиоуридина, 4-тиоуридина, вайбутозина, вайбутоксозина, 4-ацетилцитидина, 5-(карбоксигидроксиметил)уридина, 5'-карбоксиметиламинометил-2-тиоуридина, 5-карбоксиметиламинометилуридина, бета-О-галактозилквеуозина, 1-метиладенозина, 1-метилинозина, 2,2-диметилгуанозина, 3-метилцитидина, 2-метиладенозина, 2-метилгуанозина, N6-метиладенозина, 7-метилгуанозина, 5-метоксиаминометил-2-тиоуридина, 5-метиламинометилуридина, 5-метилкарбонилметилуридина, 5-метилоксиуридина, 5-метил-2-тиоуридина, 2-метилтио-N6-изопентениладенозина, бета-О-маннозилквеуозина, уридин-5-оксиуксусной кислоты и 2-тиоцитидина. Основание может представлять собой 2,6-диамнопуринрибозид, пиридин-4-он-рибозид, пиридин-2-он-рибозид, фенилрибозид, 2,4,6-триметоксибензолрибозид, аминофенилрибозид, 6-азапиримидинрибозид, пропинрибозид.
Нуклеиновые кислоты, обсуждаемые в настоящей заявке, включают немодифицированную РНК, а также РНК, которая была модифицирована, например, для улучшения эффективности, и полимеры нуклеозидных суррогатов. Немодифицированная РНК относится к молекуле, в которой компоненты нуклеиновой кислоты, а именно сахара, основания и фосфатные группы, являются такими же или по существу такими же, как и те, которые встречаются в природе, например, которые встречаются в природе в организме человека. В настоящей заявке модифицированный нуклеотид относится к нуклеотиду, в котором один или более из компонентов нуклеотидов, а именно сахара, основания и фосфатные группы, отличаются от тех, которые встречаются в природе. Несмотря на то, что модифицированные нуклеотиды так называются из-за своей модификации, они также включают молекулы, которые не являются нуклеотидами, например, полинуклеотидные молекулы, в которых рибофосфатный остов заменен нерибофосфатной конструкцией, которая обеспечивает гибридизацию между цепями, т.е. модифицированные нуклеотиды имитируют рибофосфатный остов.
Многие из описанных ниже модификаций, которые встречаются в нуклеиновой кислоте, будут повторены в полинуклеотидной молекуле, например, модификация основания или фосфатной группы, или несоединяющего О из фосфатной группы. В некоторых случаях модификация будет встречаться во всех из возможных положений/нуклеотидов в полинуклеотиде, но во многих случаях не будет встречаться. Модификация может встречаться только в 3'- или 5'-концевом положении, может встречаться только в концевых областях, например, в положении на концевом нуклеотиде или в последних 2, 3, 4, 5 или 10 нуклеотидах цепи. Модификация может встречаться в двухцепочечной области, одноцепочечной области или в обеих. Модификация может встречаться только в двухцепочечной области нуклеиновой кислоты согласно настоящему изобретению или может встречаться только в одноцепочечной области нуклеиновой кислоты согласно настоящему изобретению. Фосфотиоатная модификация в положении несоединяющего О может встречаться только на одном или обоих концах, может встречаться только в концевой области, например, в положении на концевом нуклеотиде или в последних 2, 3, 4 или 5 нуклеотидах цепи или может встречаться в дуплексе и/или в одноцепочечных областях, в частности, на концах. 5'-конец или 3'-конец могут быть фосфорилированы.
Стабильность нуклеиновой кислоты согласно настоящему изобретению может быть повышена путем включения конкретных оснований в липких концах или включения модифицированных нуклеотидов, в одноцепочечных липких концах, например, в 5' или 3'-липком конце или в обоих. В липкие концы могут быть включены пуриновые нуклеотиды. Все или некоторые из оснований в 3'- или 5'-липком конце могут быть модифицированы. Модификации могут включать применение модификаций в группе 2'-ОН рибозного сахара, применение дезоксирибонуклеотидов вместо рибонуклеотидов и модификации в фосфатной группе, такие как фосфотиоатные модификации. Липкие концы необязательно должны быть гомологичны последовательности-мишени.
5'- или 3'-липкие концы в смысловой цепи, антисмысловой цепи или обеих цепях дцРНК-агента согласно настоящему изобретению могут быть фосфорилированы. Согласно некоторым вариантам реализации настоящего изобретения область липкого конца содержит два нуклеотида, содержащих фосфотиоат между двумя нуклеотидами, причем два нуклеотида могут быть одинаковыми или разными. Согласно одному варианту реализации настоящего изобретения липкий конец присутствует на 3'-конце смысловой цепи, антисмысловой цепи или обеих цепей. Согласно одному варианту реализации настоящего изобретения 3'-липкий конец присутствует в антисмысловой цепи. Согласно одному варианту реализации настоящего изобретения 3'-липкий конец присутствует в смысловой цепи.
Нуклеазы могут гидролизовать фосфодиэфирные связи нуклеиновых кислот. Однако химические модификации нуклеиновых кислот могут придавать улучшенные свойства и могут сделать олигорибонуклеотиды более устойчивыми к нуклеазам.
В настоящей заявке модифицированные нуклеиновые кислоты могут включать одно или более из следующего:
(i) изменение, например, замещение одного или обоих из несоединяющих атомов кислорода фосфата и/или одного или более из соединяющих атомов кислорода фосфата (упоминается как событие соединения, даже если происходит на 5'- и 3'-конце нуклеиновой кислоты согласно настоящему изобретению);
(ii) изменение, например, замещение компонента рибозного сахара, например, 2'-гидроксила на рибозном сахаре;
(iii) замещение фосфатной группы «дефосфо» линкерами;
(iv) модификация или замещение природного основания;
(v) замещение или модификация рибозофосфатного остова;
(vi) модификация 3'-конца или 5'-конца РНК, например, удаление, модификация или замещение концевой фосфатной группы или конъюгация группы, например, флуоресцентномеченой группы, с 3'- или 5'-концом РНК.
Термины замещение, модификация, изменение указывают на отличие от природной молекулы.
Конкретные модификации более подробно обсуждаются ниже.
Примеры модифицированных фосфатных групп включают фосфотиоат, фосфоселенаты, боранофосфаты, сложные эфиры боранофосфата, фосфонаты водорода, фосфоамидаты, алкил или арилфосфонаты и фосфотриэфиры. В фосфодитиоатах оба несоединяющих атома кислорода замещены серой. Один, каждый или оба несоединяющих атома кислорода в фосфатной группе могут быть независимо замещены любым из S, Se, В, С, Н, N или OR (R представляет собой алкил или арил).
Фосфатный линкер также можно модифицировать путем замещения соединяющего атома кислорода азотом (мостиковые фосфоамидаты), серой (мостиковые фосфотиоаты) и углеродом (мостиковые метиленфосфонаты). Замещение может происходить у концевого кислорода. Возможно замещение несоединяющих атомов кислорода азотом.
Модифицированный нуклеотид может содержать модификацию сахарных групп.2'-гидроксильная группа (ОН) может быть модифицирована или замещена рядом различных «окси» или «дезокси» заместителей.
Примеры модификаций «окси»-2'-гидроксильная группа включают алкокси или арилокси (OR, например, R=H, алкил, циклоалкил, арил, аралкил, гетероарил или сахар); полиэтиленгликоли (ПЭГ), O(CH2CH2O)nCH2CH2OR; «закрытые» нуклеиновые кислоты (LNA), в которых 2'-гидроксил соединен, например, метиленовым мостиком, с 4'-углеродом этого же рибозного сахара; О-АМИН (АМИН=NH2; алкиламино, диалкиламино, гетероциклил, ариламино, диариламино, гетероариламино или дигетероариламино, этилендиамин, полиамино) и аминоалкокси, O(СН2)пАМИН, (например, АМИН=NH2; алкиламино, диалкиламино, гетероциклил, ариламино, диариламино, гетероариламино или дигетероариламино, этилендиамин, полиамино).
«Дезокси» модификации включают водород, галоген, амино (например, NH2; алкиламино, диалкиламино, гетероциклил, ариламино, диариламино, гетероариламино, дигетероариламино или аминокислоту); NH(CH2CH2NH)nCH2CH2-АМИН (АМИН=NH2; алкиламино, диалкиламино, гетероциклил, ариламино, диариламино, гетероариламино или дигетероариламино), -NHC(O)R (R=алкил, циклоалкил, арил, аралкил, гетероарил или сахар), циано; меркапто; алкил-тио-алкил; тиоалкокси; и алкил, циклоалкил, арил, алкенил и алкинил, которые могут быть необязательно замещены, например, функциональной аминогруппой. Другие заместители из определенных вариантов реализации включают 2'-метоксиэтил, 2'-ОСН3, 2'-O-аллил, 2'-С-аллил и 2'-фтор.
Сахарная группа также может содержать один или более атомов углерода, которые имеют стереохимическую конфигурацию, противоположную той, которая имеется у соответствующего углерода в рибозе. Таким образом, модифицированные нуклеотиды могут содержать сахар, такой как арабиноза.
Модифицированные нуклеотиды также могут содержать «лишенные азотистого основания» сахара, в которых отсутствует нуклеиновое основание у С-1***. Эти лишенные азотистого основания сахара могут дополнительно содержать модификации у одного или более из атомов, составляющих сахар.
2'-модификации можно применять в комбинации с одной или более модификациями фосфатного линкера (например, фосфотиоат).
Фосфатные группы могут быть индивидуально замещены соединителями, не содержащими фосфор.
Примеры групп, которые могут замещать фосфатную группу, включают силоксан, карбонат, карбоксиметил, карбамат, амид, простой тиоэфир, этиленоксидный линкер, сульфонат, сульфонамид, тиоформацеталь, формацеталь, оксим, метиленимино, метиленметилимино, метиленгидразо, метилендиметилгидразо и метиленоксиметилимино. Согласно определенным вариантам реализации настоящего изобретения замещения могут включать метиленкарбониламино- и метиленметилиминогруппы.
Фосфатный линкер и рибозный сахар могут быть замещены устойчивыми к нуклеазе нуклеотидами.
Примеры включают такие суррогаты нуклеозидов как морфолино, циклобутил, пирролидин и пептидная нуклеиновая кислота (ПНК). В определенных вариантах реализации могут применяться ПНК-суррогаты.
3'- и 5'-концы олигонуклеотида могут быть модифицированы. Такие модификации могут быть на 3'-конце или 5'-конце или на обоих концах молекулы. Они могут включать модификацию или замещение всего концевого фосфата или одного или более из атомов фосфатной группы. Например, 3'- и 5'-концы олигонуклеотида могут быть конъюгированы с другими функциональными молекулярными группами, такими как группы, представляющие собой метки, например, флуорофоры (например, пирен, TAMRA, флуоресцеин, красители Су3 или Су5), или защитные группы (например, на основе серы, кремния, бора или сложного эфира). Функциональные молекулярные группы могут быть присоединены к сахару за счет фосфатной группы и/или линкера. Концевой атом линкера может соединяться или замещать соединяющий атом фосфатной группы или С-3' или С-5' О, N, S или С группы сахара. Согласно другому варианту линкер может соединяться с концевым атомом суррогата нуклеотида (например, ПНК) или замещать его. Эти спейсеры или линкеры могут включать, например, -(СН2)n-, -(CH2)nN-, - (CH2)nO-, -(CH2)nS-, -O(CH2CH2O)nCH2CH2O- (например, n=3 или 6), лишенные азотистого основания сахара, амид, карбокси, амин, оксиамин, оксиимин, простой тиоэфир, дисульфид, тиомочевину, сульфонамид или морфолино, или биотин и флуоресцеиновые реагенты. 3'-конец может представлять собой группу -ОН.
Другие примеры концевых модификаций включают красители, интеркалирующие агенты (например, акридины), сшивающие агенты (например, псорален, митомицин С), порфирины (ТРРС4, тексафирин, сапфирин), полициклические ароматические углеводороды (например, феназин, дигидрофеназин), искусственные эндонуклеазы, ЭДТА, липофильные носители (например, холестерин, желчную кислоту, адамантануксусную кислоту, 1-пиренмасляную кислоту, дигидротестостерон, 1,3-бис-О-(гексадецил)глицерин, геранилоксигексильную группу, гексадецилглицерин, борнеол, ментол, 1,3-пропандиол, гептадецильную группу, пальмитиновую кислоту, миристиновую кислоту, O3-(олеоил)литохолевую кислоту, O3-(олеоил)холеновую кислоту, диметокситритил или феноксазин) и пептидные конъюгаты (например, пептид Antennapedia, пептид Tat), алкилирующие агенты, фосфат, амино, меркапто, ПЭГ (например, ПЭГ-40К), MPEG, [MPEG]2, полиамино, алкил, замещенный алкил, радиомеченые маркеры, ферменты, гаптены (например, биотин), стимуляторы транспорта/абсорбции (например, аспирин, витамин Е, фолиевую кислоту), синтетические рибонуклеазы (например, имидазол, бисимидазол, гистамин, кластеры имидазола, конъюгаты акридин-имидазол, комплексы Eu3+ и тетраазамакроциклов).
Концевые модификации могут быть добавлены по ряду причин, включая модуляцию активности или модуляцию устойчивости к разрушению. Концевые модификации, которые можно применять для модулирования активности, включают модификацию 5'-конца фосфатом или аналогами фосфата. Нуклеиновые кислоты согласно настоящему изобретению могут быть 5'-фосфорилированы на первой или второй цепях или могут содержать фосфор ильный аналог на 5'-конце. Модификации 5'-фосфатом включают модификации, которые совместимы с RISC-опосредуемым сайленсингом генов. Подходящие модификации включают: 5'-монофосфат ((НО)2(O)Р-O-5'); 5'-дифосфат ((НО)2(O)Р-О-Р(НО)(O)-O-5'); 5'-трифосфат ((НО)2(O)Р-О-(НО)(O)Р-О- Р(НО)(O)-O-5'); 5'-гуанозиновый кэп (7-метилированный или неметилированный) (7m-G-O-5'-(НО)(O)Р-О-(НО)(O)Р-О-Р(НО)(O)-O-5'); 5'-аденозиновый кэп (Аррр) и любую кэп-структуру модифицированного или немодифицированного нуклеотида (N-О-5'-(HO)(O)Р-О-(НО)(O)Р-О-Р(НО)(O)-O-5'); 5'-монотиофосфат (фосфотиоат; (HO)2(S)P-O-5'); 5'-монодитиофосфат (фосфодитиоат; (HO)(HS)(S)P-O-5'), 5'-фосфотиолат ((HO)2(O)Р-S-5'); любую дополнительную комбинацию монофосфата, дифосфата и трифосфатов, в которых кислород замещен серой (например, 5'-альфа тиотрифосфат, 5'-гамма-тиотрифосфат и т.д.), 5'-фосфоамидаты ((НО)2(O)Р-NH-5', (HO)(NH2)(O)P-O-5'), 5'-алкилфосфонаты (R=алкил=метил, этил, изопропил, пропил и т.д., например, RP(OH)(O)-O-5'-, (ОН)2(O)Р-5'-СН2-), 5'-винилфосфонат, 5'-алкилэфирфосфонаты (R=алкилэфир=метоксиметил (МеОСН2-), этоксиметил и т.д., например, RP(OH)(O)-O-5'-).
Нуклеиновая кислота согласно настоящему изобретению может содержать одну или более фосфотиоатных модификаций на одном или более концевых участках первой и/или второй цепей. Необязательно каждый или любой конец первой цепи может содержать один, два или три модифицированных фосфотиоатом нуклеотида. Необязательно каждый или любой конец второй цепи может содержать один, два или три модифицированных фосфотиоатом нуклеотида. Необязательно оба конца первой цепи и 5'-конец второй цепи могут содержать два модифицированных фосфотиоатом нуклеотида. Под нуклеотидом, модифицированным фосфотиоатом, подразумевают, что связь между нуклеотидом и смежным нуклеотидом содержит фосфотиоатную группу вместо стандартной фосфатной группы.
Концевые модификации также можно применять для мониторинга распределения, и в таких случаях группы, которые будут добавлены, могут включать флуорофоры, например, флуоресцеин или краситель Alexa. Концевые модификации также можно применять для усиления поглощения, подходящие для этого модификации включают холестерин. Концевые модификации также можно применять для поперечной сшивки РНК-агента с другой группой.
Аденин, гуанин, цитозин и урацил являются наиболее распространенными основаниями, обнаруженными в РНК. Эти основания могут быть модифицированы или замещены для обеспечения РНК, имеющих улучшенные свойства. Например, устойчивые к нуклеазе олигорибонуклеотиды могут быть получены с применением этих оснований или синтетических и природных нуклеиновых оснований (например, инозина, тимина, ксантина, гипоксантина, нубуларина, изогуанизина или туберцидина) и любой одной из указанных выше модификаций. Согласно другому варианту можно применять замещенные или модифицированные аналоги любого из вышеуказанных оснований и «универсальных оснований». Примеры включают 2-аминоаденин, 6-метил и другие алкильные производные аденина и гуанина, 2-пропил и другие алкильные производные аденина и гуанина, 5-галоурацил и цитозин, 5-пропинилурацил и цитозин, 6-азоурацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацил, 5-галоурацил, 5-(2-аминопропил)урацил, 5-аминоаллилурацил, 8-галоген, амино, тиол, тиоалкил, гидроксил и другие 8-замещенные аденины и гуанины, 5-трифторметил и другие 5-замещенные урацилы и цитозины, 7-метилгуанин, 5-замещенные пиримидины, 6-азапиримидины и N-2, N-6 и О-6-замещенные пурины, включая 2-аминопропиладенин, 5-пропинилурацил и 5-пропинилцитозин, дигидроурацил, 3-деаза-5-азацитозин, 2-аминопурин, 5-алкилурацил, 7-алкилгуанин, 5-алкилцитозин, 7-деазааденин, N6,N6-диметиладенин, 2,6-диаминопурин, 5-аминоаллилурацил, N3-метилурацил, замещенные 1,2,4-триазолы, 2-пиридинон, 5-нитроиндол, 3-нитропиррол, 5-метоксиурацил, урацил-5-оксиуксусную кислоту, 5-метоксикарбонилметилурацил, 5-метил-2-тиоурацил, 5-метоксикарбонилметил-2-тиоурацил, 5-метиламинометил-2-тиоурацил, 3-(3-амино-3-карбоксипропил)урацил, 3-метилцитозин, 5-метилцитозин, N<4>-ацетилцитозин, 2-тиоцитозин, N6-метиладенин, N6-изопентиладенин, 2-метилтио-N6-изопентениладенин, N-метилгуанины или О-алкилированные основания.
В настоящей заявке термин «неспаривающийся аналог нуклеотида» означает аналог нуклеотида, который содержит неспаривающуюся с основанием группу, включая, но не ограничиваясь ими: 6-дезаминоаденозин (небуларин), 4-Ме-индол, 3-нитропиррол, 5-нитроиндол, Ds, Pa, N3-Me рибоU, N3-Me рибоТ, N3-Me dC, N3-Me-dT, N1-Me-dG, N1-Me-dA, N3-этил-dC, N3-Me dC. Согласно некоторым вариантам реализации настоящего изобретения неспаривающийся с основанием аналог нуклеотида представляет собой рибонуклеотид. Согласно другим вариантам реализации настоящего изобретения он представляет собой дезоксирибонуклеотид.
В настоящей заявке термин «концевая функциональная группа» включает, но не ограничивается ими, галогеновые, спиртовые, аминные, карбоновые, сложноэфирные, амидные, альдегидные, кетоновые, простые эфирные группы.
Определенные группы могут быть соединены с 5'-концом первой цепи или второй цепи и включают лишенную азотистого основания рибозную группу, лишенную азотистого основания дезоксирибозную группу, модификации лишенной азотистого основания рибозной группы и лишенной азотистого основания дезоксирибозной группы, включая 2'-алкильные модификации; инвертированные лишенные азотистого основания рибозные группы и лишенные азотистого основания дезоксирибозные группы и их модификации, С6-имино-Pi; зеркальный нуклеотид, включая L-ДНК и L-PHK; 5'-ОМе-нуклеотид; и аналоги нуклеотидов, включая 4',5'-метиленнуклеотид; 1-β-D-эритрофуранозилнуклеотид; 4'-тионуклеотид, карбоциклический нуклеотид; 5'-аминоалкилфосфат; 1,3-диамино-2-пропилфосфат, 3-аминопропилфосфат; 6-аминогексилфосфат; 12-аминододецилфосфат; гидроксипропилфосфат; 1,5-ангидрогекситолнуклеотид; альфа-нуклеотид; треопентофуранозилнуклеотид; ациклический 3',4'-секонуклеотид; 3,4-дигидроксибутилнуклеотид; 3,5 дигидроксипентилнуклеотид, 5'-5'-инвертированную лишенную азотистого основания группу; 1,4-бутандиолфосфат; 5'-амино; и мостиковые или немостиковые метилфосфонатные и 5'-меркапто группы.
Нуклеиновые кислоты согласно настоящему изобретению могут быть включены как один или более инвертированных нуклеотидов, например, инвертированный тимидин или инвертированный аденин (например, см. Takei, et al., 2002. JBC 277 (26):23800-06).
В настоящей заявке термин «ингибировать», «подавлять» или «уменьшать» в отношении экспрессии гена означает, что экспрессия гена или уровень молекул РНК или эквивалентных молекул РНК, кодирующих один или более белков или субъединиц белков (например, мРНК), или активность одного или более белков или субъединиц белков, или пептидов уменьшается ниже уровня, наблюдаемого в отсутствие нуклеиновой кислоты согласно настоящему изобретению, или по отношению к молекуле миРНК без известной гомологии с транскриптами человека (в настоящей заявке называется не вызывающий сайленсинг контроль). Такой контроль может быть конъюгирован и модифицирован аналогичным образом, как и молекула согласно настоящему изобретению, и доставлен в клетку-мишень аналогичным путем; например, экспрессия может быть уменьшена до 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20%, 15% или до меньшего значения, чем то, которое наблюдается в отсутствие ингибитора (который может представлять собой нуклеиновую кислоту) или в присутствии не вызывающего сайленсинг контроля (который может представлять собой нуклеиновую кислоту, которая не является комплементарной последовательности-мишени).
Нуклеиновая кислота согласно настоящему изобретению может содержать лишенный азотистого основания нуклеотид. В настоящей заявке термин «лишенный азотистого основания» относится к группам, не содержащим основание или имеющим другие химические группы вместо основания в положении Г, например, 3',3'-соединенное или 5',5'-соединенное производное лишенной азотистого основания дезоксирибозы.
Нуклеиновая кислота может содержать один или более нуклеотидов на второй и/или первой цепях, которые модифицированы. Чередующиеся нуклеотиды могут быть модифицированы с образованием модифицированных нуклеотидов.
Чередование, описанное в настоящей заявке, означает, что оно происходит один за другим на регулярной основе. Другими словами, чередование означает повторение по очереди. Например, если один нуклеотид модифицирован, следующий смежный нуклеотид не модифицирован, а следующий смежный нуклеотид модифицирован и так далее. Один нуклеотид может быть модифицирован с применением первой модификации, следующий смежный нуклеотид может быть модифицирован с применением второй модификации, а следующий смежный нуклеотид модифицирован с применением первой модификации и так далее, при этом первая и вторая модификации отличаются.
Один или более из нуклеотидов в нечетных положениях первой цепи нуклеиновой кислоты согласно настоящему изобретению могут быть модифицированы, причем первая цепь пронумерована от 5' к 3', самый крайний 5'-нуклеотид представляет собой нуклеотид номер 1 первой цепи. Термин «в нечетном положении», описанный в настоящей заявке, означает число, неделимое на два. Примерами нечетных чисел являются 1, 3, 5, 7, 9, 11 и так далее. Один или более из нуклеотидов в четных положениях первой цепи нуклеиновой кислоты согласно настоящему изобретению могут быть модифицированы, причем первая цепь пронумерована от 5' к 3'. Термин «в четном положении», описанный в настоящей заявке, означает число, которое поровну делится на два. Примерами четных чисел являются 2, 4, 6, 8, 10, 12, 14 и так далее. Один или более из нуклеотидов в нечетных положениях второй цепи нуклеиновой кислоты согласно настоящему изобретению могут быть модифицированы, при этом вторая цепь пронумерована от 3' к 5', причем наиболее 3'-концевой нуклеотид представляет собой нуклеотид номер 1 второй цепи. Один или более из нуклеотидов в четных положениях второй цепи нуклеиновой кислоты согласно настоящему изобретению могут быть модифицированы, причем вторая цепь пронумерована от 3' к 5'.
Один или более нуклеотидов на первой и/или второй цепях могут быть модифицированы с образованием модифицированных нуклеотидов. Один или более из нуклеотидов в нечетных положениях первой цепи могут быть модифицированы. Один или более из нуклеотидов в четных положениях первой цепи могут быть модифицированы с применением по меньшей мере второй модификации, причем по меньшей мере вторая модификация отличается от модификации на одном или более нуклеотидах в нечетных положениях. По меньшей мере один из одного или более модифицированных нуклеотидов в четных положениях может быть смежным с по меньшей мере одним из одного или более модифицированных нуклеотидов в нечетных положениях.
Множество нуклеотидов в нечетных положениях в первой цепи могут быть модифицированы в нуклеиновой кислоте согласно настоящему изобретению. Множество нуклеотидов в четных положениях первой цепи могут быть модифицированы с применением второй модификации. Первая цепь может содержать смежные нуклеотиды, которые модифицированы с применением общей модификации. Первая цепь также может содержать смежные нуклеотиды, которые модифицированы с применением второй отличающейся модификации.
Один или более из нуклеотидов в нечетных положениях второй цепи могут быть модифицированы с применением модификации, которая отличается от модификации нуклеотидов в нечетных положениях на первой цепи, и/или один или более из нуклеотидов в четных положениях второй цепи могут быть модифицированы с применением модификации, аналогичной таковой для нуклеотидов в нечетных положениях первой цепи. По меньшей мере один из одного или более модифицированных нуклеотидов в четных положениях второй цепи может быть смежным с одним или более модифицированными нуклеотидами в нечетных положениях. Множество нуклеотидов в нечетных положениях второй цепи могут быть модифицированы с применением общей модификации, и/или множество нуклеотидов в четных положениях могут быть модифицированы с применением модификации, которая аналогична присутствующей на нуклеотидах в нечетных положениях первой цепи. Множество нуклеотидов в нечетных положениях на второй цепи могут быть модифицированы с применением второй модификации, причем вторая модификация отличается от модификации нуклеотидов в нечетных положениях первой цепи.
Вторая цепь может содержать смежные нуклеотиды, которые модифицированы с применением общей модификации, которая может представлять собой вторую модификацию, которая отличается от модификации нуклеотидов в нечетных положениях первой цепи.
В нуклеиновой кислоте согласно настоящему изобретению каждый из нуклеотидов в нечетных положениях в первой цепи и каждый из нуклеотидов в четных положениях во второй цепи может быть модифицирован с применением общей модификации, и каждый из нуклеотидов в четных положениях в первой цепи может быть модифицирован с применением второй модификации, и каждый из нуклеотидов в нечетных положениях во второй цепи может быть модифицирован с применением второй модификации.
Модифицированные нуклеотиды первой цепи нуклеиновой кислоты согласно настоящему изобретению могут быть сдвинуты по меньшей мере на один нуклеотид относительно немодифицированных или по-разному модифицированных нуклеотидов второй цепи.
Один или более или каждый из нуклеотидов в нечетных положениях могут быть модифицированы в первой цепи, и один или более или каждый из нуклеотидов в четных положениях могут быть модифицированы во второй цепи. Один или более или каждый из чередующихся нуклеотидов на любой или обеих цепях могут быть модифицированы с применением второй модификации. Один или более или каждый из нуклеотидов в четных положениях могут быть модифицированы в первой цепи, и один или более или каждый из нуклеотидов в четных положениях могут быть модифицированы во второй цепи. Один или более или каждый из чередующихся нуклеотидов на любой или обеих цепях могут быть модифицированы с применением второй модификации. Один или более или каждый из нуклеотидов в нечетных положениях могут быть модифицированы в первой цепи и один или более из нуклеотидов в нечетных положениях могут быть модифицированы во второй цепи с применением общей модификации. Один или более или каждый из чередующихся нуклеотидов на любой или обеих цепях могут быть модифицированы с применением второй модификации. Один или более или каждый из нуклеотидов в четных положениях могут быть модифицированы в первой цепи и один или более или каждый из нуклеотидов в нечетных положениях могут быть модифицированы во второй цепи с применением общей модификации. Один или более или каждый из чередующихся нуклеотидов на любой или обеих цепях могут быть модифицированы с применением второй модификации.
Нуклеиновая кислота согласно настоящему изобретению может содержать одноцепочечные или двухцепочечные конструкции, которые содержат по меньшей мере две области чередующихся модификаций в одной или обеих цепях. Эти чередующиеся области могут содержать до приблизительно 12 нуклеотидов, но предпочтительно содержат от приблизительно 3 до приблизительно 10 нуклеотидов. Области чередующихся нуклеотидов могут быть расположены на концах одной или обеих цепей нуклеиновой кислоты согласно настоящему изобретению. Нуклеиновая кислота может содержать от 4 до приблизительно 10 чередующихся нуклеотидов на каждом конце (3' и 5'), и эти области могут быть отделены с помощью от приблизительно 5 до приблизительно 12 смежных немодифицированных или по-разному модифицированных или модифицированных с применением общей модификации нуклеотидов.
Нуклеотиды в нечетном положении первой цепи могут быть модифицированы и нуклеотиды в четном положении могут быть модифицированы с применением второй модификации. Вторая цепь может содержать смежные нуклеотиды, которые модифицированы с применением общей модификации, которая может быть аналогична модификации нуклеотидов в нечетных положениях первой цепи. Один или более нуклеотидов второй цепи также могут быть модифицированы с применением второй модификации. Один или более нуклеотидов со второй модификацией могут быть смежными друг с другом и с нуклеотидами, содержащими модификацию, которая аналогична модификации нуклеотидов в нечетных положениях первой цепи. Первая цепь также может содержать фосфотиоатные связи между двумя нуклеотидами на 3'-конце и на 5'-конце. Вторая цепь может содержать фосфотиоатную связь между двумя нуклеотидами на 5'-конце. Вторая цепь также может быть конъюгирована с лигандом на 5'-конце.
Нуклеиновая кислота согласно настоящему изобретению может содержать первую цепь, содержащую смежные нуклеотиды, которые модифицированы с применением общей модификации. Один или более таких нуклеотидов могут быть смежными с одним или более нуклеотидами, которые могут быть модифицированы с применением второй модификации. Один или более нуклеотидов со второй модификацией могут быть смежными. Вторая цепь может содержать смежные нуклеотиды, которые модифицированы с применением общей модификации, которая может быть аналогична одной из модификаций одного или более нуклеотидов первой цепи. Один или более нуклеотидов второй цепи также могут быть модифицированы с применением второй модификации. Один или более нуклеотидов со второй модификацией могут быть смежными. Первая цепь также может содержать фосфотиоатные связи между двумя нуклеотидами на 5'-конце и на 3'-конце. Вторая цепь может содержать фосфотиоатную связь между двумя нуклеотидами на 3'-конце. Вторая цепь также может быть конъюгирована с лигандом на 5'-конце.
Нуклеотиды, пронумерованные (от 5' к 3' на первой цепи и от 3' к 5' на второй цепи) 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23 и 25, могут быть модифицированы с применением модификации на первой цепи. Нуклеотиды, пронумерованные 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22 и 24, могут быть модифицированы с применением второй модификации на первой цепи. Нуклеотиды, пронумерованные 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, могут быть модифицированы с применением модификации на второй цепи. Нуклеотиды, пронумерованные 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22 и 24, могут быть модифицированы с применением второй модификации на второй цепи. В отношении нуклеиновой кислоты согласно настоящему изобретению нуклеотиды пронумерованы от 5' к 3' на первой цепи и от 3' к 5' на второй цепи.
Нуклеотиды, пронумерованные 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22 и 24, могут быть модифицированы с применением модификации на первой цепи. Нуклеотиды, пронумерованные 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, могут быть модифицированы с применением второй модификации на первой цепи. Нуклеотиды, пронумерованные 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, могут быть модифицированы с применением модификации на второй цепи. Нуклеотиды, пронумерованные 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22 и 24, могут быть модифицированы с применением второй модификации на второй цепи.
Понятно, что если первая и/или вторая цепи короче чем 25 нуклеотидов в длину, например, 19 нуклеотидов в длину, то нуклеотиды с номерами 20, 21, 22, 23, 24 и 25, подлежащие модификации, отсутствуют. Специалист поймет приведенное выше описание для применения к более коротким цепям, соответственно.
Один или более модифицированных нуклеотидов на первой цепи могут быть спарены с модифицированными нуклеотидами на второй цепи, имеющими общую модификацию. Один или более модифицированных нуклеотидов на первой цепи могут быть спарены с модифицированными нуклеотидами на второй цепи, имеющими другую модификацию. Один или более модифицированных нуклеотидов на первой цепи могут быть спарены с немодифицированными нуклеотидами на второй цепи. Один или более модифицированных нуклеотидов на второй цепи могут быть спарены с немодифицированными нуклеотидами на первой цепи. Другими словами, чередующиеся нуклеотиды могут быть выравнены на двух цепях таким образом, что, например, все модификации в чередующихся областях второй цепи спарены с идентичными модификациями в первой цепи или, согласно другому варианту, модификации могут быть компенсированы одним нуклеотидом с общими модификациями в чередующихся областях одной цепи, спаренным с отличающимися модификациями (т.е. второй или дополнительной модификацией) в другой цепи. Другой вариант заключается в наличии разных модификаций в каждой из цепей.
Модификации на первой цепи могут быть сдвинуты на один нуклеотид относительно модифицированных нуклеотидов на второй цепи так, что нуклеотиды с общей модификацией не спариваются друг с другом.
Модификация и/или модификации могут быть по отдельности и независимо выбраны из группы, состоящей из 3'-концевого дезокситимина, 2'-O-метила, 2'-дезокси-модификации, 2'-амино-модификации, 2'-алкил-модификации, морфолино-модификации, модификации фосфоамидатом, модификации 5'-фосфотиоатной группой, модификации 5'-фосфатом или миметиком 5'-фосфата, а также модификации производным холестерина или группой бисдециламида додекановой кислоты, и/или модифицированный нуклеотид может представлять собой любой из закрытого нуклеотида, лишенного азотистого основания нуклеотида или содержащего неприродное основание нуклеотида.
По меньшей мере одна модификация может представлять собой 2'-O-метил и/или по меньшей мере одна модификация может представлять собой 2'-F. Дополнительные модификации, описанные в настоящей заявке, могут присутствовать на первой и/или второй цепях.
Нуклеиновая кислота согласно настоящему изобретению может содержать инвертированный РНК-нуклеотид на одном или нескольких концах цепи. Такие инвертированные нуклеотиды обеспечивают стабильность нуклеиновой кислоты. Предпочтительно нуклеиновая кислота содержит по меньшей мере инвертированный нуклеотид на одном или нескольких из 3'-конца по меньшей мере одной из цепей и/или на 5'-конце второй цепи. Более предпочтительно нуклеиновая кислота содержит инвертированный нуклеотид на 3'-конце второй цепи. Наиболее предпочтительно нуклеиновая кислота содержит инвертированный РНК-нуклеотид на 3'-конце второй цепи, и этот нуклеотид предпочтительно представляет собой инвертированный А. Инвертированный нуклеотид предпочтительно присутствует на конце цепи не в виде липкого конца, а напротив соответствующего нуклеотида в другой цепи. Нуклеиновая кислота с такой модификацией является стабильной и легко синтезируется.
В описании настоящего изобретения «аналогичная или общая модификация» означает одну и ту же модификацию для любого нуклеотида, будь то A, G, С или U, модифицированного с применением группы, такой как метальная группа или фторгруппа. Это не подразумевает аналогичное добавление на одном и том же нуклеотиде. Например, 2'-F-dU, 2'-F-dA, 2'-F-dC, 2'-F-dG все считаются аналогичными или общими модификациями, так же как и 2'-OMe-rU, 2'-OMe-rA; 2'-OMe-rC; 2'-OMe-rG. Модификация 2'-F представляет собой модификацию, отличную от модификации 2'-ОМе.
Некоторые типичные модифицированные последовательности нуклеиновых кислот согласно настоящему изобретению показаны в примерах. Подразумевается, что эти примеры являются типичными, а не ограничивающими.
Предпочтительно нуклеиновая кислота может содержать модификацию и вторую или дополнительную модификацию, которые по отдельности и независимо выбраны из группы, включающей 2'-O-метил-модификацию и 2'-F-модификацию. Нуклеиновая кислота может содержать модификацию, которая представляет собой 2'-O-метил (2'-ОМе), который может представлять собой первую модификацию, и вторую модификацию, которая представляет собой 2'-F. Нуклеиновая кислота согласно настоящему изобретению также может содержать фосфотиоатную модификацию и/или дезокси-модификацию, которая может присутствовать на 1, 2 или 3 концевых нуклеотидах или между ними каждого или любого конца каждой или обеих цепей.
Нуклеиновая кислота согласно настоящему изобретению может быть конъюгирована с лигандом с образованием конъюгата.
Некоторые лиганды могут обладать эндосомолитическими свойствами. Эндосомолитические лиганды способствуют лизису эндосомы и/или транспорту композиции согласно настоящему изобретению или ее компонентов из эндосомы в цитоплазму клетки. Эндосомолитический лиганд может представлять собой полианионный пептид или миметик пептида, который проявляет рН-зависимую активность в отношении мембраны и способность к слиянию. Эндосомолитический компонент может содержать химическую группу, которая претерпевает изменение заряда или протонирования в ответ на изменение рН. Эндосомолитический компонент может быть линейным или разветвленным.
Лиганды могут включать терапевтические модификаторы, например, для усиления поглощения; диагностические соединения или репортерные группы, например, для мониторинга распространения; сшивающие агенты; и группы, придающие устойчивость к нуклеазам. Общие примеры включают липиды, стероиды, витамины, сахара, белки, пептиды, полиамины и миметики пептидов. Лиганды могут включать природное вещество, такое как белок, углевод или липид. Лиганд может представлять собой рекомбинантную или синтетическую молекулу.
Лиганды также могут включать нацеливающие группы, например, нацеливающий на клетки или ткани агент. Нацеливающий лиганд может представлять собой лектин, гликопротеин, липид или белок.
Другие примеры лигандов включают красители, интеркалирующие агенты, сшивающие агенты, порфирины, полициклические ароматические углеводороды, искусственные эндонуклеазы или хелатор, липофильные молекулы, алкилирующие агенты, фосфат, амино, меркапто, ПЭГ, мПЭГ, алкил, замещенный алкил, радиомеченые маркеры, ферменты, гаптены, стимуляторы транспорта/абсорбции, синтетические рибонуклеазы или кластеры имидазола.
Лиганды могут представлять собой белки, например, гликопротеины или пептиды. Лиганды также могут представлять собой гормоны или рецепторы гормонов. Они могут также включать непептидные молекулы, такие как липиды, лектины, углеводы, витамины или кофакторы.
Лиганд может представлять собой вещество, такое как лекарственное средство, которое может увеличить поглощение нуклеиновой кислоты в клетку, например, путем разрушения цитоскелета клетки.
Лиганд может увеличивать поглощение нуклеиновой кислоты в клетку, активируя воспалительный ответ. Такие лиганды включают фактор некроза опухоли альфа (TNF-альфа), интерлейкин-1 бета или гамма-интерферон.
Лиганд может представлять собой липид или молекулу на основе липида. Липид или молекула на основе липида предпочтительно связывает белок сыворотки. Предпочтительно лиганд на основе липида связывает сывороточный альбумин человека (САЧ). Липид или молекула на основе липида может повышать устойчивость к разрушению конъюгата, усиливать нацеливание или транспорт в клетку-мишень и/или может регулировать связывание с белком сыворотки. Лиганд на основе липида можно применять для модуляции связывания конъюгата с тканью-мишенью.
Лиганд может представлять собой стероид. Предпочтительно лиганд представляет собой холестерин или производное холестерина.
Лиганд может представлять собой группу, например, витамин, которая поглощается клеткой-мишенью. Примерные витамины включают витамины А, Е, К, а также витамины группы В. Витамины могут поглощаться пролиферирующими клетками, это можно применять для доставки нуклеиновой кислоты в клетки, такие как злокачественные или незлокачественные опухолевые клетки.
Лиганд может представлять собой агент для проникновения в клетку, такой как спиральный агент для проникновения в клетку. Предпочтительно такой агент является амфипатическим.
Лиганд может представлять собой пептид или миметик пептида. Миметик пептида представляет собой молекулу, способную складываться в определенную трехмерную структуру, сходную с природным пептидом. Пептидный или пептидомиметический лиганд может включать природные или модифицированные пептиды или и те, и другие. Пептид или миметик пептида может представлять собой пептид для проникновения в клетки, катионный пептид, амфипатический пептид или гидрофобный пептид. Пептидная группа может представлять собой дендримерный пептид, ограниченный пептид или сшитый пептид. Пептидная группа может содержать гидрофобную последовательность для транслокации через мембрану. Пептидная группа может представлять собой пептид, способный переносить большие полярные молекулы, такие как пептиды, олигонуклеотиды и белки, через клеточные мембраны, например, последовательности из белка Tat ВИЧ (GRKKRRQRRRPPQ) и белка Antennapedia Drosophila (RQIKIWFQNRRMKWKK). Предпочтительно пептид или миметик пептида представляет собой пептид, нацеливающий на клетку, например, пептид аргинин-глицин-аспарагиновая кислота (RGD).
Лиганд может представлять собой пептид для проникновения в клетку, который способен проникать, например, в микробную клетку или клетку млекопитающего.
Лиганд может представлять собой модулятор фармакокинетики (ФК). Модулятор фармакокинетики может представлять собой липофильные агенты, желчные кислоты, стероиды, аналоги фосфолипидов, пептиды, связывающие белки агенты, ПЭГ, витамины и т.д.
Если присутствуют два или более лигандов, все лиганды могут иметь одинаковые свойства, все имеют разные свойства, или некоторые лиганды имеют одинаковые свойства, в то время как другие имеют отличающиеся свойства. Например, лиганд может обладать нацеливающими свойствами, может обладать эндосомолитической активностью или модулирующими ФК свойствами. В предпочтительном варианте все лиганды имеют разные свойства.
Лиганды могут быть связаны с нуклеиновой кислотой на 3'-конце, 5'-конце и/или во внутреннем положении. Предпочтительно лиганд связан с нуклеиновой кислотой за счет промежуточного соединителя или линкера.
Согласно некоторым вариантам реализации настоящего изобретения нуклеиновая кислота представляет собой двухцепочечную нуклеиновую кислоту. В двухцепочечной нуклеиновой кислоте лиганд может быть присоединен к одной или обеим цепям. Согласно некоторым вариантам реализации настоящего изобретения двухцепочечная нуклеиновая кислота содержит лиганд, конъюгированный со смысловой цепью. Согласно другим вариантам реализации настоящего изобретения двухцепочечная нуклеиновая кислота содержит лиганд, конъюгированный с антисмысловой цепью.
Лиганды могут быть конъюгированы с нуклеиновыми основаниями, сахарными группами или межнуклеозидными связями молекул нуклеиновой кислоты. Конъюгация с пуриновыми нуклеиновыми основаниями или их производными может происходить в любом положении, включая эндоциклические и экзоциклические атомы. Конъюгация с пиримидиновыми нуклеотидами или их производными также может происходить в любом положении. Конъюгация с сахарными группами нуклеозидов может происходить у любого атома углерода. Конъюгация с межнуклеозидными связями может происходить у атома фосфора фосфоросодержащей связи или у атома кислорода, азота или серы, связанного с атомом фосфора. Для амино- или амидосодержащих межнуклеозидных связей конъюгация может происходить у атома азота амина или амида или у смежного атома углерода.
Лиганд, как правило, представляет собой углевод, например, моносахарид, дисахарид, трисахарид, тетрасахарид или полисахарид. Лиганд может быть конъюгирован с нуклеиновой кислотой с помощью линкера. Линкер может представлять собой одновалентный, двухвалентный или трехвалентный разветвленный линкер.
Средства для эффективной доставки олигонуклеотидов, в частности, двухцепочечных нуклеиновых кислот согласно настоящему изобретению, в клетки в условиях in vivo имеют большое значение и требуют специфичного нацеливания и существенной защиты от внеклеточной среды, в частности, белков сыворотки. Одним из способов осуществления специфичного нацеливания является конъюгация нацеливающей группы или лиганда с нуклеиновой кислотой. Нацеливающая группа помогает нацеливать нуклеиновую кислоту на требуемый сайт-мишень, и существует потребность в конъюгации подходящих нацеливающих групп для целевых рецепторных сайтов для конъюгированных молекул, которые будут поглощаться клетками, например, с помощью эндоцитоза. Нацеливающая группа или лиганд могут представлять собой любую группу или лиганд, которые способны нацеливать на конкретный рецептор.
Например, рецептор асиалогликопротеина (ASGP-R) представляет собой высокоэффективный рецептор, который широко распространен на гепатоцитах. Одно из первых раскрытий трехантенных кластерных гликозидов было представлено в патенте США US 5885968. Конъюгаты, содержащие три лиганда GalNAc и содержащие фосфатные группы, известны и описаны в Dubber et al. (2003). ASGP-R проявляет в 50 раз более высокую аффинность в отношении N-ацетил-D-галактозиламина (GalNAc), чем в отношении D-Gal.
Гепатоциты, экспрессирующие лектин (рецептор асиалогликопротеина; ASGPR), который специфично распознает концевые β-галактозильные субъединицы гликозилированных белков или других олигосахаридов (P.Н. Weigel et. al., 2002,), можно применять для нацеливания лекарственного средства на печень путем ковалентного связывания галактозы или галактозамина с лекарственным веществом (Ishibashi,S.; et. al., J Biol. Chem. 1994 Nov 11;269(45):27803-6). Кроме того, аффинность связывания может быть значительно повышена за счет поливалентного эффекта, который достигается с помощью повторения нацеливающего блока (Biessen ЕА, et al., J Med Chem. 1995 Apr 28;38(9): 1538-46).
ASGPR выступает посредником для активного эндосомального транспорта гликопротеинов, содержащих концевой β-галактозил, поэтому ASGPR является очень подходящим для нацеленной доставки лекарственных средств-кандидатов, таких как нуклеиновые кислоты, которые должны быть доставлены в клетку (Akinc et al.).
Сахарид, который также может упоминаться как лиганд, может быть выбран так, чтобы обладать аффинностью в отношении по меньшей мере одного типа рецептора на клетке-мишени. В частности, рецептор находится на поверхности клетки печени млекопитающего, например, печеночный рецептор асиалогликопротеина (ASGP-R).
Сахарид может быть выбран из N-ацетилгалактозамина, маннозы, галактозы, глюкозы, глюкозамина и фукозы. Сахарид может представлять собой N-ацетилгалактозамин (GalNAc).
Лиганд может содержать (i) одну или более групп N-ацетилгалактозамина (GalNAc) и их производных, и (ii) линкер, причем указанный линкер конъюгирует группы GalNAc с нуклеиновой кислотой, определенной в любых предшествующих аспектах. Линкер может представлять собой двухвалентную, трехвалентную или четырехвалентную разветвленную структуру. Нуклеотиды могут быть модифицированы, как определено в настоящей заявке.
«GalNAc» относится к 2-ацетиламино-2-дезокси-D-галактопиранозе, обычно называемой в литературе N-ацетилгалактозамином. Ссылка на «GalNAc» или «N-ацетилгалактозамин» включает обе β-форму, 2-ацетиламино-2-дезокси-β-D-галактопиранозу, и α-форму, 2-ацетиламино-2-дезокси-α-D-галактопиранозу. Обе β-форма, 2-ацетиламино-2-дезокси-β-D-галактопираноза, и α-форма, 2-ацетиламино-2-дезокси-α-D-галактопираноза, могут использоваться взаимозаменяемо. Предпочтительно соединения согласно настоящему изобретению содержат β-форму, 2-ацетиламино-2-дезокси-β-D-галактопиранозу.
Лиганд может содержать GalNAc.
Лиганд может содержать соединение формулы I:
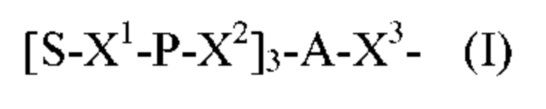
в которой:
S представляет собой сахарид, причем указанный сахарид представляет собой N-ацетилгалактозамин;
X1 представляет собой С3-С6 алкилен или (-СН2-СН2-O)m(-СН2)2-, где m равно 1, 2 или 3;
Р представляет собой фосфат или модифицированный фосфат (предпочтительно тиофосфат);
X2 представляет собой алкилен или простой алкиленовый эфир формулы (-СН2)n-O-СН2-, где n=1-6;
А представляет собой блок разветвления; X3 представляет собой мостиковый блок;
при этом нуклеиновая кислота в соответствии с настоящим изобретением конъюгирована с X3 за счет фосфата или модифицированного фосфата (предпочтительно тиофосфата).
В формуле I блок разветвления «А» разветвляется на три для размещения трех сахаридных лигандов. Блок разветвления ковалентно присоединен к лигандам и нуклеиновой кислоте. Блок разветвления может содержать разветвленную алифатическую группу, содержащую группы, выбранные из алкильной, амидной, дисульфидной, полиэтиленгликолевой, простой эфирной, простой тиоэфирной и гидроксиаминной групп. Блок разветвления может содержать группы, выбранные из алкильной и простой эфирной групп.
Блок разветвления А может иметь структуру, выбранную из:
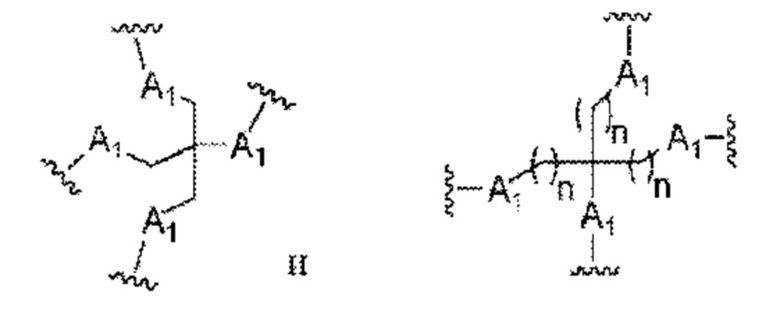
в которой каждый A1 независимо представляет собой О, S, С=O или NH; и каждый п независимо представляет собой целое число от 1 до 20. Блок разветвления может иметь структуру, выбранную из:
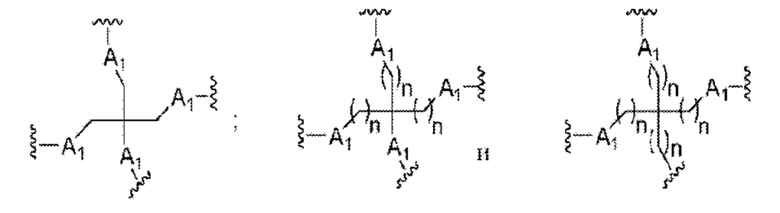
в которой каждый A1 независимо представляет собой О, S, С=O или NH; и каждый n независимо представляет собой целое число от 1 до 20. Блок разветвления может иметь структуру, выбранную из:
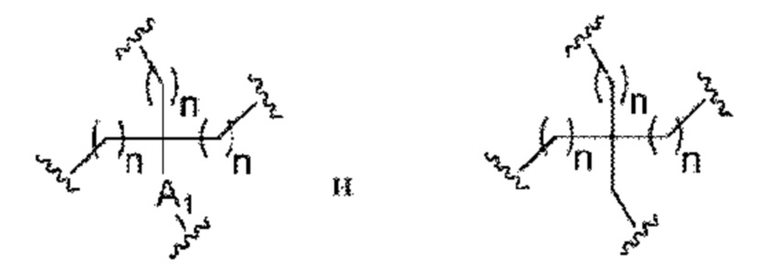
в которой A1 представляет собой О, S, С=O или NH; и
каждый n независимо представляет собой целое число от 1 до 20.
Блок разветвления может иметь структуру:
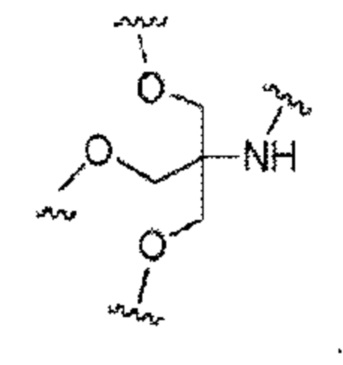
Блок разветвления может иметь структуру:
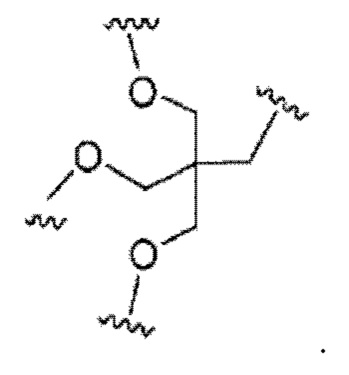
Блок разветвления может иметь структуру:
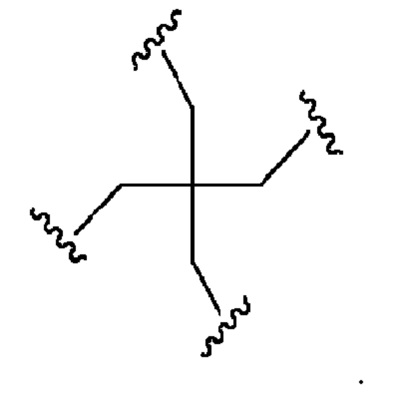
Необязательно блок разветвления состоит только из атома углерода.
Часть «X3» представляет собой мостиковый блок. Мостиковый блок является линейным и ковалентно связан с блоком разветвления и нуклеиновой кислотой.
X3 может быть выбран из -С1-С20 алкилен-, -С2-С20 алкенилен-, простого алкиленового эфира формулы -(С1-С20 алкилен)-O-(С1-С20 алкилен)-, -C(O)-С1-С20 алкилен-, -С0-С4 алкилен(Су)С0-С4 алкилен-, где Су представляет собой замещенное или незамещенное 5 или 6-членное циклоалкиленовое, ариленовое, гетероциклиленовое или гетероариленовое кольцо, -С1-С4 алкилен-NHC(O)-С1-С4-алкилен-, -С1-С4 алкилен-С(O)NH-С1-С4-алкилен-, -С1-С4 алкилен-SC(O)-С1-С4-алкилен-, -С1-С4 алкилен-С(O)S-С1-С4 алкилен-, -С1-С4 алкилен-ОС(O)-С1-С4 алкилен-, -С1-С4 алкилен-С(O)O-С1-С4 алкилен- и -C1-С6 алкилен-S-S-С1-С6 алкилен-.
X3 может представлять собой простой алкиленовый эфир формулы -(С1-С20 алкилен)-O-(С1-С2о алкилен)-. X3 может представлять собой простой алкиленовый эфир формулы -(С1-С20 алкилен)-O-(С4-С20 алкилен)-, причем указанный (С4-С20 алкилен) соединен с Z. X3 может быть выбран из группы, состоящей из -CH2-О-С3Н6-, -CH2-О-С4Н8-, -CH2-O-C6H12- и -CH2-O-C8H16-, в частности, -CH2-O-С4Н8-, -CH2-O-C6H12- и -CH2-O-C8H16-, где в каждом случае группа -CH2- соединена с А.
Лиганд может содержать соединение формулы (II):
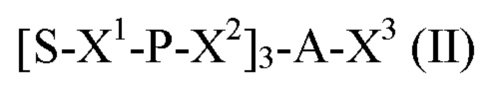
в которой:
S представляет собой сахарид;
X1 представляет собой С3-С6 алкилен или этиленгликолевую цепь (-CH2-CH2-O)m(-СН2)2-, где m равно 1, 2 или 3;
Р представляет собой фосфат или модифицированный фосфат (предпочтительно тиофосфат);
X2 представляет собой C1-C8 алкилен;
А представляет собой блок разветвления, выбранный из:
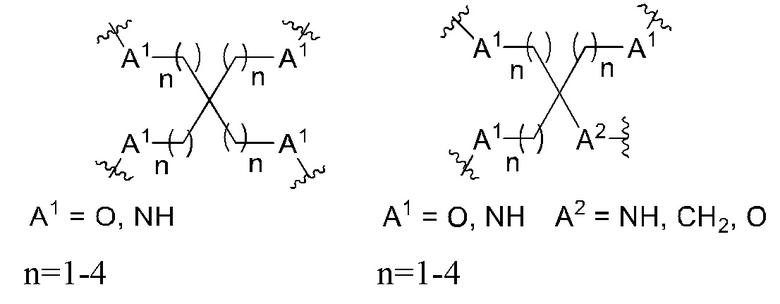
X3 представляет собой мостиковый блок;
при этом нуклеиновая кислота в соответствии с настоящим изобретением конъюгирована с X3 за счет фосфата или модифицированного фосфата (предпочтительно тиофосфата).
Блок разветвления А может иметь структуру:
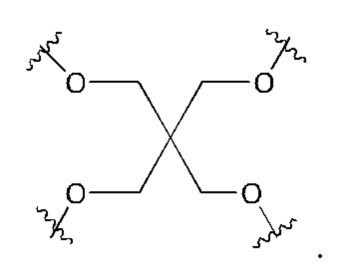
Блок разветвления А может иметь структуру:
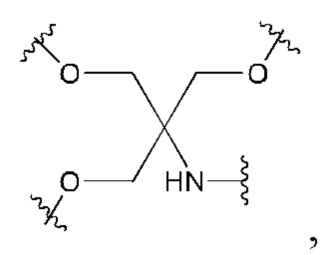
в которой X3 присоединен к атому азота.
X3 может представлять собой С1-С20 алкилен. Предпочтительно X3 выбран из группы, состоящей из -С3Н6-, -C4H8-, -C6H12- и -C8H16-, в частности, -C4H8-, -C6H12- и - C8H16-.
Лиганд может содержать соединение формулы (III):
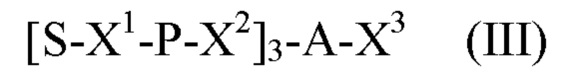
в которой:
S представляет собой сахарид;
X1 представляет собой С3-С6 алкилен или этиленгликолевую цепь (-CH2-CH2-O)m(-СН2)2-, где m равно 1, 2 или 3;
Р представляет собой фосфат или модифицированный фосфат (предпочтительно тиофосфат);
X2 представляет собой простой алкиленовый эфир формулы -С3Н6-O-CH2-;
А представляет собой блок разветвления;
X3 представляет собой простой алкиленовый эфир формулы, выбранной из группы,
состоящей из -CH2-O-CH2-, -CH2-O-С2Н4-, -CH2-O-С3Н6-, -CH2-O-С4Н8-, -CH2-O-С5Н10-, -СН2-O-С6Н12-, -CH2-О-С7Н14- и -CH2-O-C8H16-, при этом в каждом случае группа -CH2- соединена с А,
и при этом нуклеиновая кислота в соответствии с настоящим изобретением конъюгирована с X3 за счет фосфата или модифицированного фосфата (предпочтительно тиофосфата).
Блок разветвления может содержать углерод. Предпочтительно блок разветвления представляет собой углерод.
X3 может быть выбран из группы, состоящей из -CH2-О-С4Н8-, -CH2-О-С5Н10-, -CH2-O-С6Н12-, -CH2-О-С7Н14- и -CH2-О-С8Н16-. Предпочтительно X3 выбран из группы, состоящей из -CH2-O-С4Н8-, -CH2-O-C6H12- и -CH2-O-C8H16.
Для любого из вышеуказанных аспектов Р представляет собой модифицированную фосфатную группу. Р может быть представлен как:
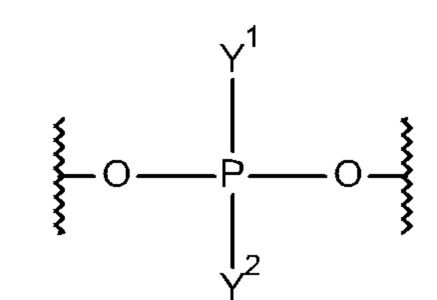
где Y1 и Y2 каждый независимо представляют собой =O, =S, -О-, -ОН, -SH, -ВН3, -ОСН2СО2, -OCH2CO2Rx, -OCH2C(S)ORx и -ORx, где Rx представляет собой C1-C6 алкил и где  указывает на присоединение к остальной части соединения.
указывает на присоединение к остальной части соединения.
Под модифицированным фосфатом подразумевается фосфатная группа, в которой один или более из атомов кислорода замещены. Примеры модифицированных фосфатных групп включают фосфотиоат, фосфоселенаты, боранофосфаты, сложные эфиры боранофосфата, фосфонаты водорода, фосфоамидаты, алкил или арилфосфонаты и сложные фосфотриэфиры. В фосфодитиоатах оба несоединяющих атома кислорода замещены серой. Один, каждый или оба несоединяющих атома кислорода в фосфатной группе могут независимо представлять собой любой из S, Se, В, С, Н, N или OR (R представляет собой алкил или арил).
Фосфатный линкер также может быть модифицирован путем замещения соединяющего атома кислорода азотом (мостиковые фосфоамидаты), серой (мостиковые фосфотиоаты) и углеродом (мостиковые метиленфосфонаты). Замещение может происходить на концевом атоме кислорода. Возможно замещение несоединяющих атомов кислорода азотом.
Например, Y1 может представлять -ОН, a Y2 может представлять =O или =S; или
Y1 может представлять -О-, a Y2 может представлять =O или =S;
Y1 может представлять =O, a Y2 может представлять -СН3, -SH, -ORx или -ВН3;
Y1 может представлять =S, a Y2 может представлять -СН3, ORx или -SH.
Специалист в данной области техники поймет, что в определенных случаях будет делокализация между Y1 и Y2.
Предпочтительно модифицированная фосфатная группа представляет собой тиофосфатную группу. Тиофосфатные группы включают битиофосфат (т.е. где Y1 представляет =S и Y2 представляет -S-) и монотиофосфат (т.е. где Y1 представляет -О- и Y2 представляет =S, или где Y1 представляет =O и Y2 представляет -S-). Предпочтительно Р представляет собой монотиофосфат. Авторы настоящего изобретения обнаружили, что конъюгаты, имеющие тиофосфатные группы вместо фосфатных групп, обладают улучшенной активностью и продолжительностью действия в условиях in vivo.
Р также может представлять собой этилфосфат (т.е. где Y1 представляет собой =O и Y2 представляет собой ОСН2СН3).
Сахарид, который также может упоминаться как лиганд, может быть выбран так, чтобы обладать аффинностью в отношении по меньшей мере одного типа рецептора на клетке-мишени. В частности, рецептор находится на поверхности клетки печени млекопитающего, например, печеночный рецептор асиалогликопротеина (ASGP-R).
Для любого из вышеуказанных аспектов сахарид может быть выбран из N-ацетила с одним или более из галактозамина, маннозы, галактозы, глюкозы, глюкозамина и фруктозы. Предпочтительно сахарид представляет собой две молекулы N-ацетилгалактозамина (GalNAc). Предпочтительно соединения согласно настоящему изобретению могут содержать 3 лиганда, каждый из которых предпочтительно представляет собой N-ацетилгалактозамин. «GalNAc» относится к 2-ацетиламино-2-дезокси-O-галактопиранозе, обычно называемой в литературе N-ацетилгалактозамином. Ссылка на «GalNAc» или «N-ацетилгалактозамин» включает обе β-форму, 2-ацетиламино-2-дезокси-β-D-галактопиранозу, и α-форму, 2-ацетиламино-2-дезокси-α-D-галактопиранозу. Согласно определенным вариантам реализации настоящего изобретения β-форма, 2-ацетиламино-2- дезокси-β-D-галактопираноза, и α-форма, 2-ацетиламино-2-дезокси-α-D-галактопираноза, могут использоваться взаимозаменяемо. Предпочтительно соединения согласно настоящему изобретению содержат β-форму, 2-ацетиламино-2-дезокси-β-D-галактопиранозу.
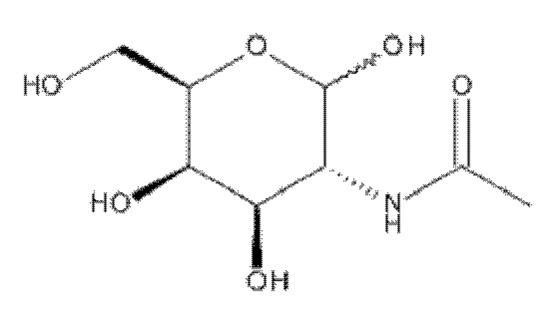
2-ацетиламино-2-дезокси-D-галактопираноза
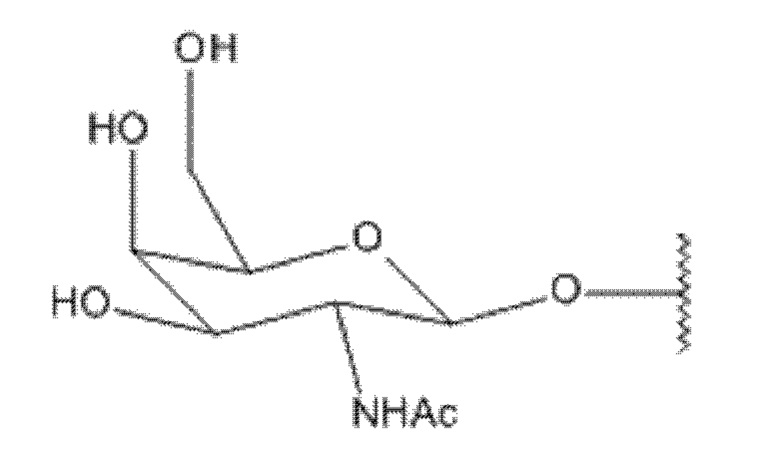
2-ацетиламино-2-дезокси-β-D-галактопираноза
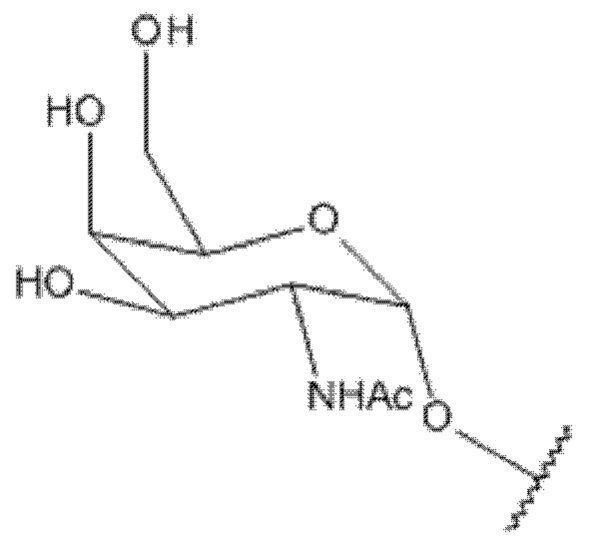
2-ацетиламино-2-дезокси-α-D-галактопираноза.
Для любого из вышеуказанных соединений формулы (III) X1 может представлять собой этиленгликолевую цепь (-CH2-CH2-O)m(-CH2)2-, где m равен 1, 2 или 3. X1 может представлять собой (-CH2-CH2-O)(-CH2)2-. X1 может представлять собой (-CH2-CH2-O)2(-СН2)2-. X1 может представлять собой (-CH2-CH2-O)3(-CH2)2-. Предпочтительно X1 представляет собой (-CH2-CH2-O)2(-CH2)2-. Согласно другому варианту X1 представляет собой С3-С6 алкилен. X1 может представлять собой пропилен. X1 может представлять собой бутилен. X1 может представлять собой пентилен. X1 может представлять собой гексилен. Предпочтительно алкил представляет собой линейный алкилен. В частности, X1 может представлять собой бутилен.
Для соединений формулы (III) X2 представляет собой простой алкиленовый эфир формулы -С3Н6-O-CH2-, т.е. С3 алкоксиметилен, или -CH2CH2CH2OCH2-.
Таким образом, согласно настоящему изобретению дополнительно предложена конъюгированная нуклеиновая кислота, имеющая одну из следующих структур:
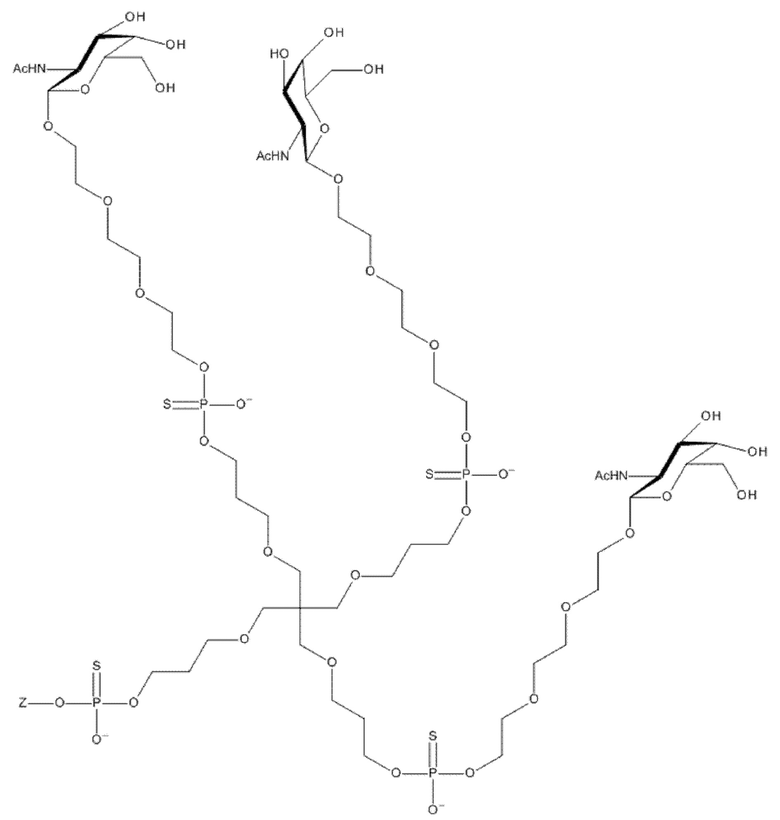
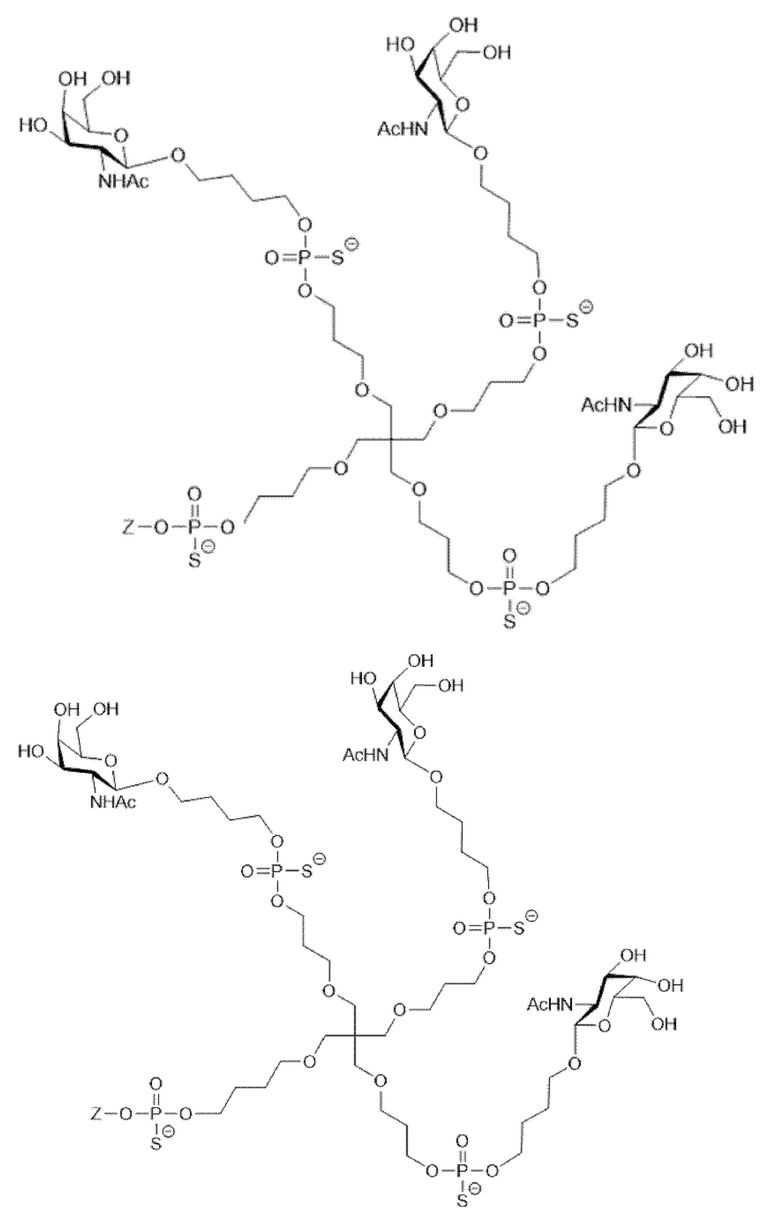
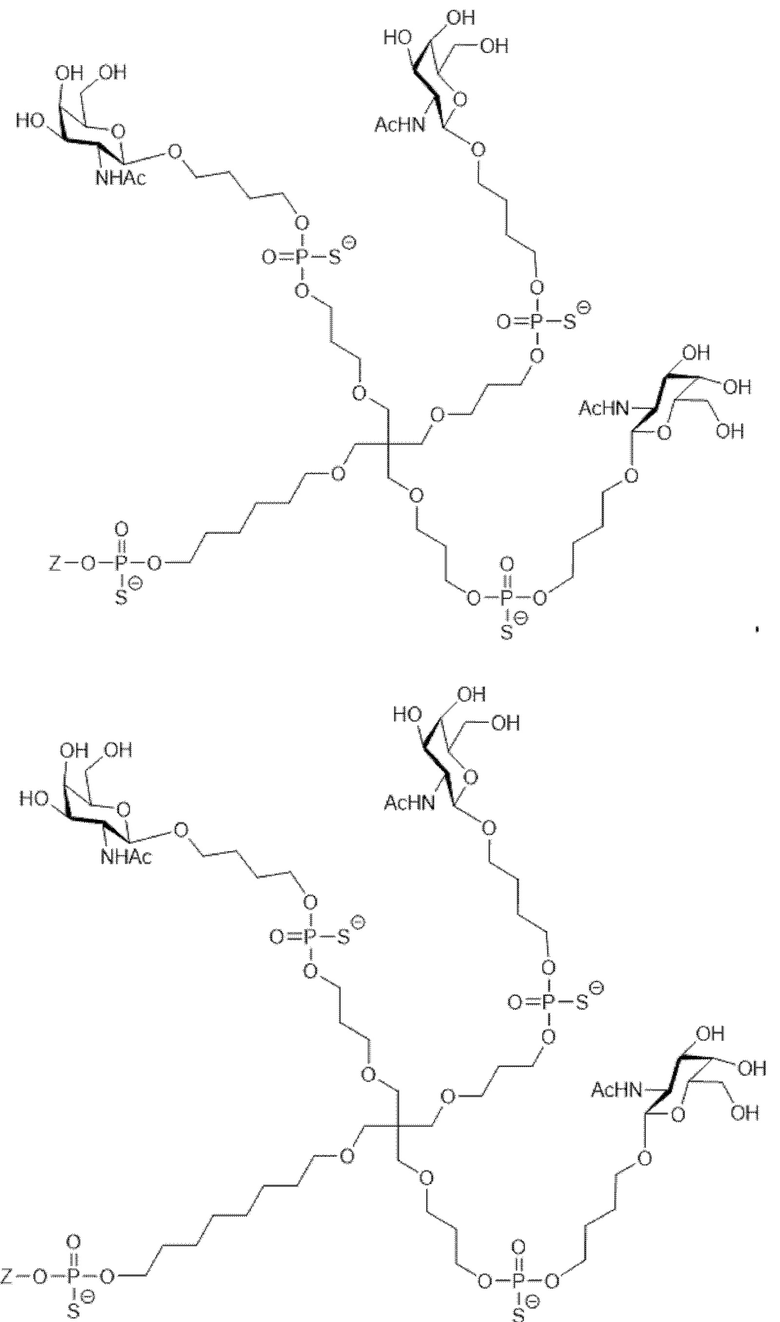
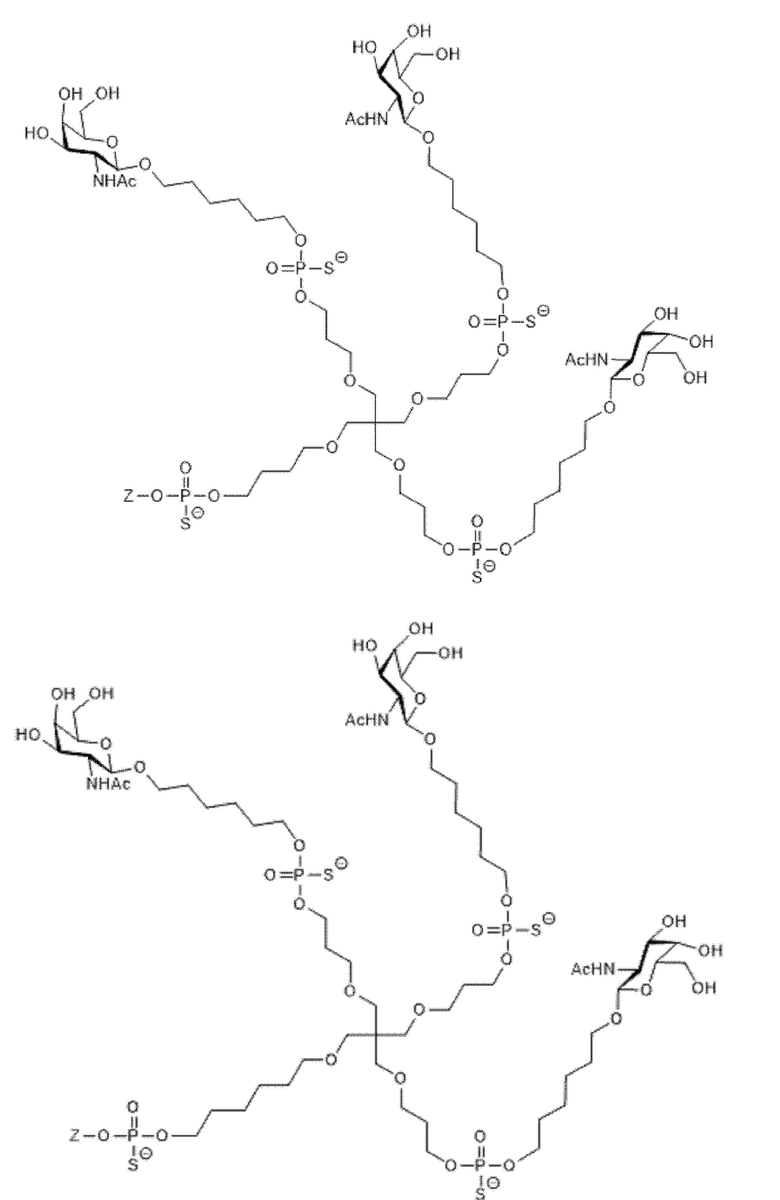
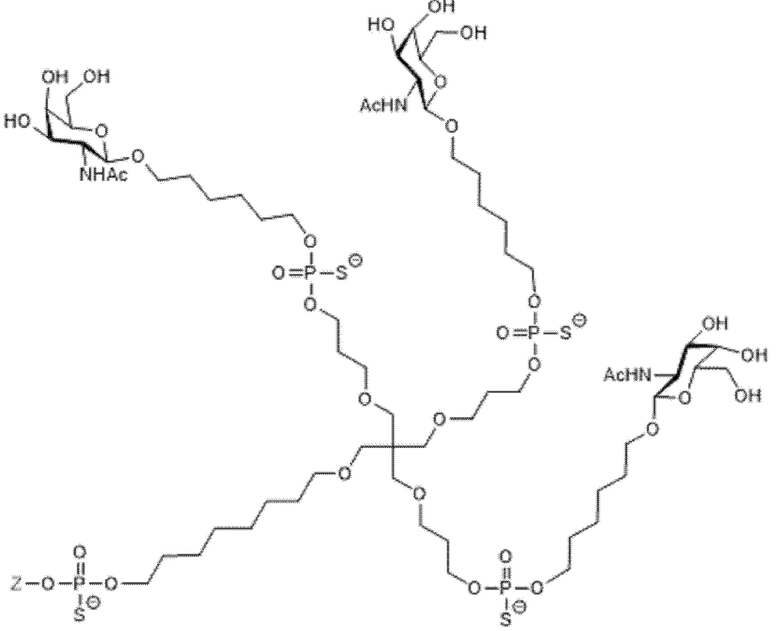
в которых Z представляет собой нуклеиновую кислоту, определенную в настоящей заявке ранее.
Лиганд формулы (I), (II) или (III) может быть присоединен на 3'-конце первой (антисмысловой) цепи и/или на любом из 3'- и/или 5'-конца второй (смысловой) цепи. Нуклеиновая кислота может содержать более одного лиганд а формулы (I), (II) или (III). Однако предпочтительным является один лиганд формулы (I), (II) или (III), поскольку одного такого лиганда достаточно для эффективного нацеливания нуклеиновой кислоты на клетки-мишени.
Предпочтительно 5'-конец первой (антисмысловой) цепи не присоединен к лиганду формулы (I), (II) или (III), поскольку лиганд в этом положении потенциально может препятствовать биологической активности нуклеиновой кислоты.
Нуклеиновая кислота с одним лигандом формулы (I), (II) или (III) на 5'-конце цепи имеет более простую структуру и, следовательно, ее дешевле синтезировать, чем аналогичную нуклеиновую кислоту с аналогичным лигандом на 3'-конце. Таким образом, предпочтительно один лиганд любой из формул (I), (II) или (III) ковалентно присоединен (конъюгирован с ним) к 5'-концу второй цепи нуклеиновой кислоты.
Согласно одному варианту реализации настоящего изобретения нуклеиновая кислота конъюгирована с лигандом, который содержит липид, и более предпочтительно с лигандом, который содержит холестерин.
Конъюгат согласно настоящему изобретению может содержать любую нуклеиновую кислоту, раскрытую в настоящей заявке, конъюгированную с любым лигандом или лигандами, раскрытыми в настоящей заявке.
Настоящее изобретение также относится к конъюгату для ингибирования экспрессии гена-мишени в клетке, причем указанный конъюгат содержит часть нуклеиновой кислоты, содержащую нуклеиновую кислоту согласно любому аспекту настоящего изобретения, и по меньшей мере одну часть лиганда, причем указанная по меньшей мере одна часть лиганда содержит линкерную группу, предпочтительно линкерную группу, происходящую из серинола, а также нацеливающий лиганд для нацеливания в условиях in vivo на клетки и конъюгированный исключительно с 3' и/или 5'-концами одной или обеих цепей РНК, причем 5'-конец первой цепи РНК не конъюгирован, при этом:
(i) вторая цепь РНК конъюгирована на 5'-конце с нацеливающим лигандом, и при этом (а) вторая цепь РНК также конъюгирована на 3 '-конце с нацеливающим лигандом и 3'-конец первой цепи РНК не конъюгирован; или (b) первая цепь РНК конъюгирована на 3'-конце с нацеливающим лигандом и 3'-конец второй цепи РНК не конъюгирован; или (с) обе вторая цепь РНК и первая цепь РНК также конъюгированы на 3'-концах с нацеливающим лигандом; или
(ii) обе вторая цепь РНК и первая цепь РНК конъюгированы на 3'-концах с нацеливающим лигандом и 5'-конец второй цепи РНК не конъюгирован.
Согласно варианту реализации настоящего изобретения вторая цепь РНК (т.е. смысловая цепь) конъюгирована на 5'-конце с нацеливающим лигандом, первая цепь РНК (т.е. антисмысловая цепь) конъюгирована на 3'-конце с нацеливающим лигандом и 3'-конец второй цепи РНК (т.е. смысловой цепи) не конъюгирован, так, что образуется конъюгат со схематической структурой, представленной на Фигуре 16А.
Согласно варианту реализации настоящего изобретения вторая цепь РНК (т.е. смысловая цепь) конъюгирована на 5'-конце с нацеливающим лигандом, вторая цепь РНК (т.е. смысловая цепь) также конъюгирована на 3'-конце с нацеливающим лигандом и 3'-конец первой цепи РНК (т.е. антисмысловой цепи) не конъюгирован, так, что образуется конъюгат со схематической структурой, представленной на Фигуре 16В.
Согласно варианту реализации настоящего изобретения обе вторая цепь РНК (т.е. смысловая цепь) и первая цепь РНК (т.е. антисмысловая цепь) конъюгированы на 3'-концах с нацеливающим лигандом, и 5'-конец второй цепи РНК (т.е. смысловой цепи) не конъюгирован, так, что образуется конъюгат со схематической структурой, представленной на Фигуре 16С.
Согласно варианту реализации настоящего изобретения вторая цепь РНК (т.е. смысловая цепь) конъюгирована на 5'-конце с нацеливающим лигандом, и обе вторая цепь РНК (т.е. смысловая цепь) и первая цепь РНК (т.е. антисмысловая цепь) также конъюгированы на 3'-концах с нацеливающим лигандом, так, что образуется конъюгат со схематической структурой, представленной на Фигуре 16D.
В любом из приведенных выше вариантов реализации  указывает на линкер, с помощью которого лиганд конъюгирован с концами части нуклеиновой кислоты; лиганд может представлять собой группу GalNAc, такую как GalNAc; и схематическая структура, представленная на Фигуре 16Е, представляет часть нуклеиновой кислоты.
указывает на линкер, с помощью которого лиганд конъюгирован с концами части нуклеиновой кислоты; лиганд может представлять собой группу GalNAc, такую как GalNAc; и схематическая структура, представленная на Фигуре 16Е, представляет часть нуклеиновой кислоты.
Эти схематические диаграммы не предназначены для ограничения количества нуклеотидов в первой или второй цепях, а также диаграммы не представляют собой какое-либо ограничение комплементарности оснований или какое-либо другое ограничение.
Лиганды могут быть мономерными или мультимерными (например, димерными, тримерными и т.д.).
Является приемлемым, когда лиганды являются мономерными и, соответственно, содержат одну группу нацеливающего лиганда, например, одну группу GalNAc.
Согласно другому варианту лиганды могут представлять собой димерные лиганды, в которых части лигандов содержат две линкерные группы, такие как линкерные группы, происходящие из серинола, или линкерные группы, отличные от серинола, каждая из которых соединена с одной группой нацеливающего лиганда.
Лиганды могут представлять собой тримерные лиганды, в которых части лигандов содержат три линкерные группы, такие как линкерные группы, происходящие из серинола, или линкерные группы, отличные от серинола, каждая из которых соединена с одной группой нацеливающего лиганда.
Две или три линкерные группы, происходящие из серинола, могут быть соединены последовательно, например, как показано ниже:
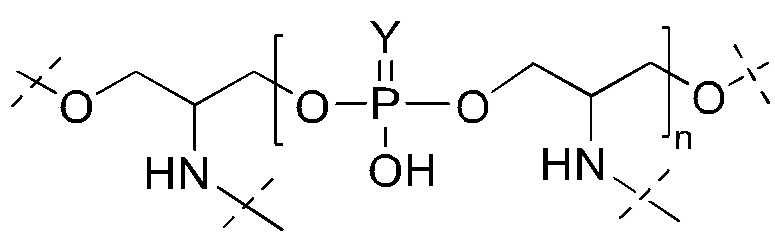
где n равно 1 или 2, a Y представляет собой S или О.
Предпочтительно лиганды являются мономерными.
Является приемлемым, когда конъюгированные цепи РНК конъюгируют с нацеливающим лигандом за счет линкерной группы, включая дополнительный линкер, причем указанный дополнительный линкер представляет собой или содержит насыщенную, неразветвленную или разветвленную C1-15 алкильную цепь, при этом необязательно один или более атомов углерода (например, 1, 2 или 3 атома углерода, является приемлемым, когда 1 или 2, в частности, 1), замещен(ы) гетероатомом, выбранным из О, N, S(O)p, где р равно 0, 1 или 2 (например, группа СН2 замещена О или NH, или S, или SO2, или группа -СН3 на конце цепи или на ветви замещена ОН или NH2), причем указанная цепь необязательно замещена одной или более оксогруппами (например, 1-3, например, 1 группой).
Является приемлемым, когда линкерная группа представляет собой линкерную группу, происходящую из серинола.
Является более приемлемым, когда дополнительный линкер содержит насыщенную неразветвленную С1-15 алкильную цепь, в которой один или более атомов углерода (например, 1, 2 или 3 атома углерода, является приемлемым, когда 1 или 2, в частности, 1) замещен (ы) атомом кислорода.
Является более приемлемым, когда дополнительный линкер содержит ПЭГ-цепь.
Является более приемлемым, когда дополнительный линкер содержит насыщенную неразветвленную C1-15 алкильную цепь.
Является более приемлемым, когда дополнительный линкер содержит насыщенную неразветвленную С1-6 алкильную цепь.
Является более приемлемым, когда дополнительный линкер содержит насыщенную неразветвленную С4 или С6 алкильную цепь, например, С4 алкильную цепь.
Согласно варианту реализации настоящего изобретения  представляет собой соединяющую группу формулы (V):
представляет собой соединяющую группу формулы (V):
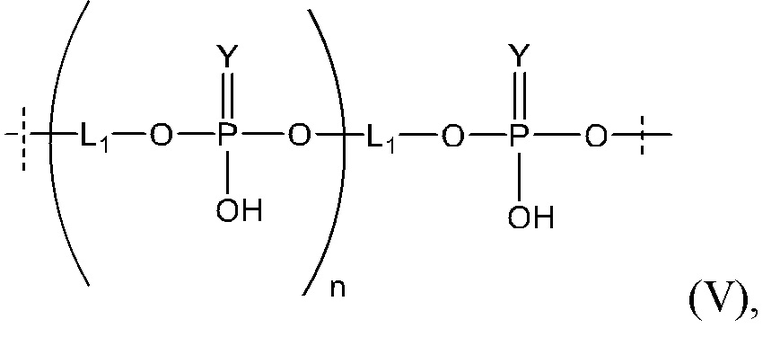
в которой n, Y и L1 определены ниже, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Таким образом, в варианте реализации часть нацеливающего лиганда представляет собой соединяющую группу формулы (VI):
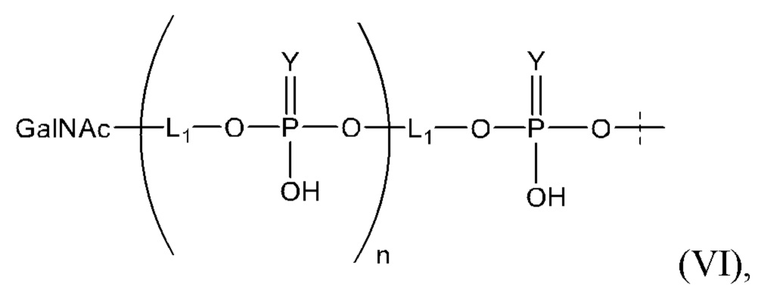
в которой n, Y и L1 определены ниже, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Является приемлемым, когда  представляет собой соединяющую группу формулы (XIV):
представляет собой соединяющую группу формулы (XIV):
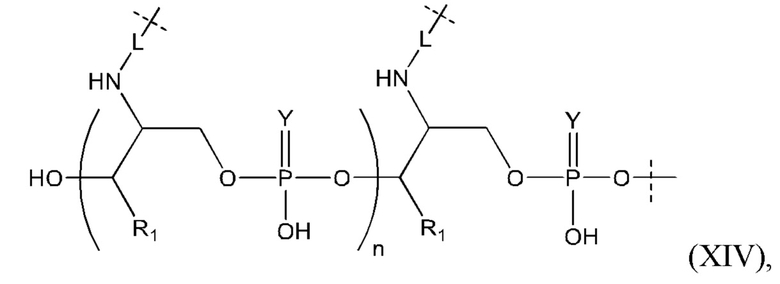
в которой n, Y, R1 и L определены ниже, L соединен с нацеливающим лигандом, например, GalNAc, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Является приемлемым, когда часть нацеливающего лиганда представляет собой соединяющую группу формулы (IV):
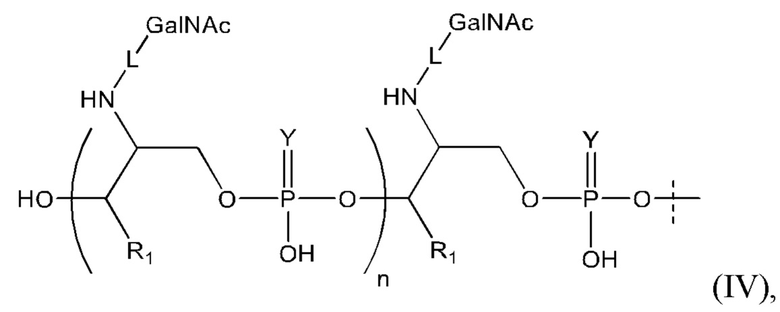
в которой n, Y, R1 и L определены ниже, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Является приемлемым, когда  представляет собой соединяющую группу формулы (VII):
представляет собой соединяющую группу формулы (VII):
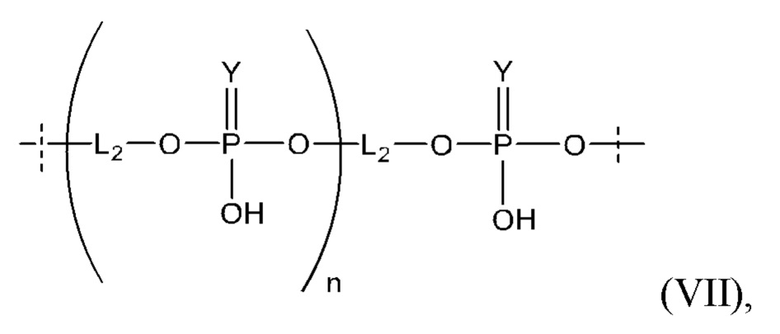
в которой n, Y и L2 определены ниже, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Является приемлемым, когда часть нацеливающего лиганда представляет собой соединяющую группу формулы (VIII):
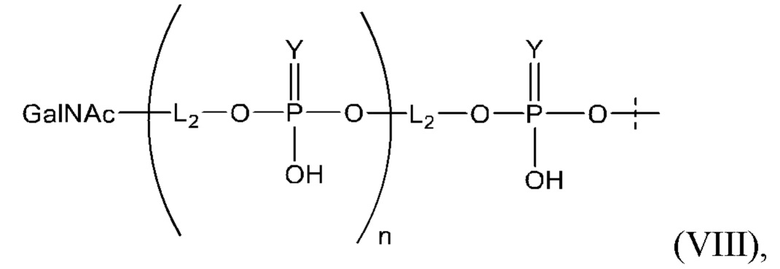
в которой n, Y и L2 определены ниже, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Является приемлемым, когда  представляет собой соединяющую группу формулы (IX):
представляет собой соединяющую группу формулы (IX):
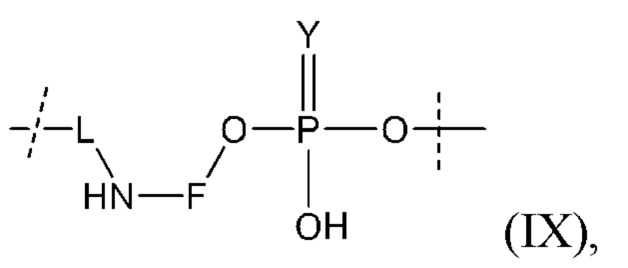
в которой F, Y и L определены ниже, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Является приемлемым, когда часть нацеливающего лиганда представляет собой соединяющую группу формулы (IXa):
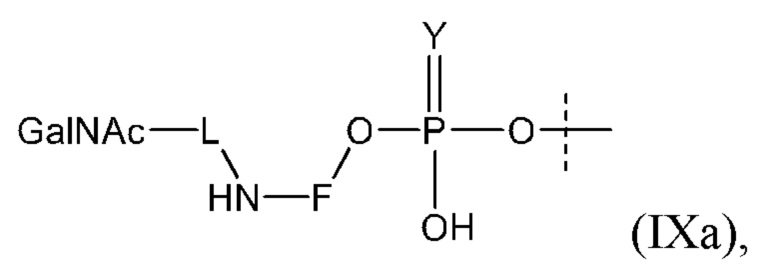
в которой F, Y и L определены ниже, и О фосфогруппы присоединен к концевому олигонуклеозиду цепей РНК.
Является приемлемым, когда L представляет собой:
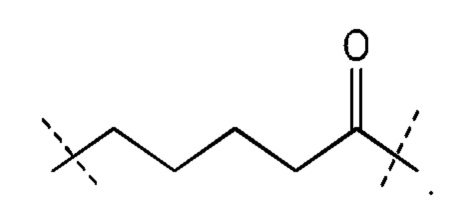
В любой из вышеуказанных структур приемлемо, когда лиганды выбраны из групп GalNAc и галактозы, в частности, групп GalNAc. Согласно другому варианту GalNAc может быть замещен другим нацеливающим лигандом, например, сахаридом.
Согласно варианту реализации настоящего изобретения первая цепь РНК представляет собой соединение формулы (X):
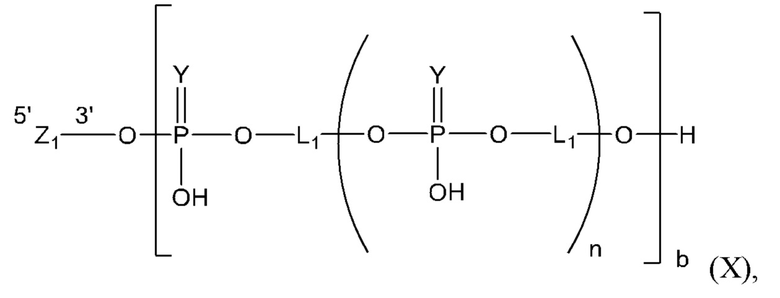
в которой b равно 0 или 1; и
вторая цепь РНК представляет собой соединение формулы (XI):
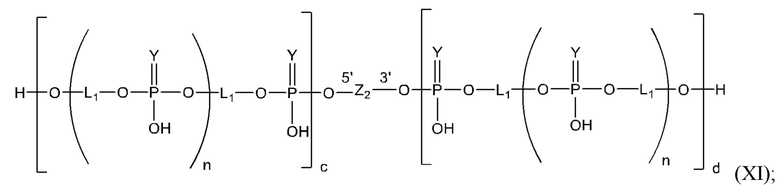
в которой:
c и d независимо равны 0 или 1;
Z1 и Z2 представляют собой части РНК первой и второй цепей РНК, соответственно;
Y представляет собой О или S;
n равно 0, 1, 2 или 3; и
L1 представляет собой линкер, к которому присоединен лиганд;
и при этом b+с+d равно 2 или 3.
Является приемлемым, когда первая цепь РНК представляет собой соединение формулы (XV)
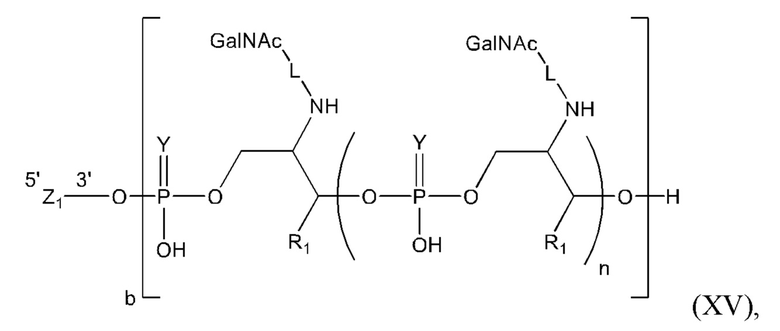
в которой b равно 0 или 1; и
вторая цепь РНК представляет собой соединение формулы (XVI):
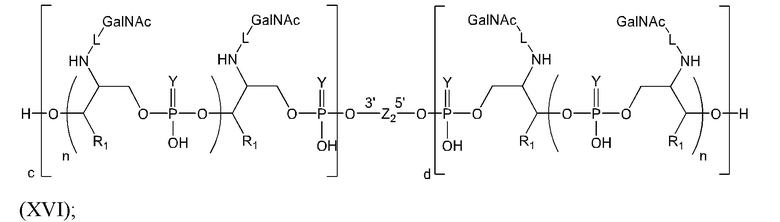
в которой
c и d независимо равны 0 или 1;
в которой:
Z1 и Z2 представляют собой части РНК первой и второй цепей РНК, соответственно;
Y представляет собой О или S;
R1 представляет собой Н или метил;
n равно 0, 1, 2 или 3; и
L является одинаковым или различным в формулах (XV) и (XVI) и выбран из группы, состоящей из:
-(СН2)r-С(O)-, где r=2-12;
-(CH2-CH2-O)s-CH2-C(O)-, где s=1-5;
-(CH2)t-CO-NH-(CH2)t-NH-C(O)-, где t независимо представляет собой 1-5;
-(CH2)u-CO-NH-(CH2)u-C(O)-, где и независимо представляет собой 1-5; и
-(CH2)v-NH-C(O)-, где v представляет собой 2-12; и
причем концевой С(О) (если он присутствует) присоединен к группе NH;
и при этом b+с+d равно 2 или 3.
Является приемлемым, когда первая цепь РНК представляет собой соединение формулы (XII):
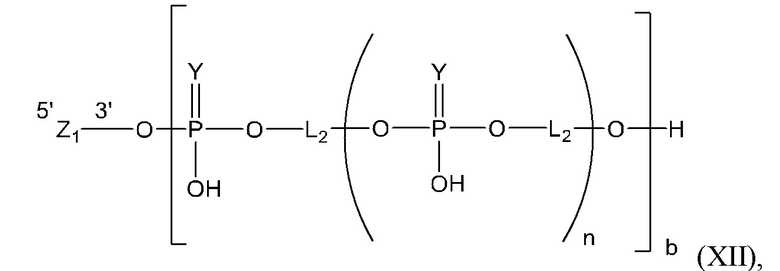
в которой b равно 0 или 1; и
вторая цепь РНК представляет собой соединение формулы (XIII):
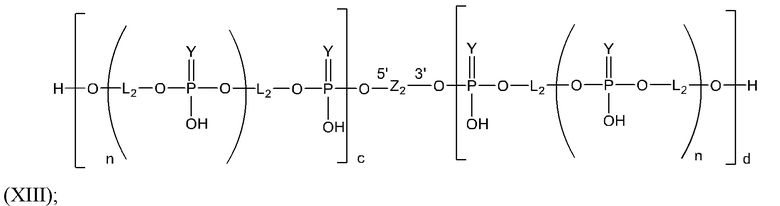
в которой:
c и d независимо равны 0 или 1;
Z1 и Z2 представляют собой части РНК первой и второй цепей РНК, соответственно;
Y представляет собой О или S;
n равно 0, 1, 2 или 3; и
L2 является одинаковым или различным в формулах (XII) и (XIII) и одинаковым или различным в группах, заключенных в скобки с индексом b, с и d, и выбран из группы, состоящей из:
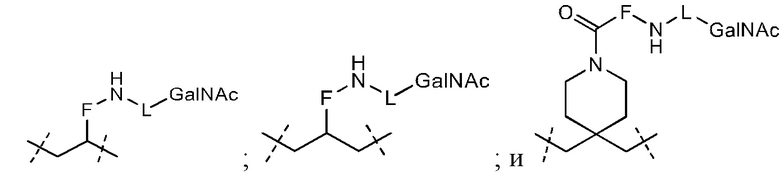
или
n равно 0 и L2 представляет собой:
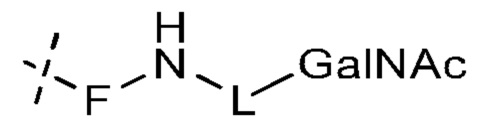
и концевая группа ОН отсутствует, так, что образуется следующая группа:
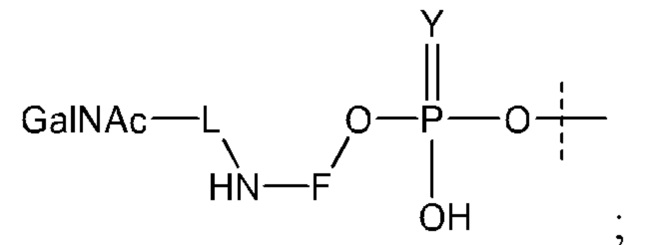
где
F представляет собой насыщенную разветвленную или неразветвленную (например, неразветвленную) C1-8 алкильную (например, С1-6 алкильную) цепь, в которой один из атомов углерода необязательно замещен атомом кислорода, при условии, что указанный атом кислорода отделен от другого гетероатома (например, атома О или N) по меньшей мере 2 атомами углерода;
L является одинаковым или различным в формулах (XII) и (XIII) и выбран из группы, состоящей из:
-(СН2)r-С(O)-, где r=2-12;
-(CH2-CH2-O)s-CH2-C(O)-, где s=1-5;
-(CH2)t-CO-NH-(CH2)t-NH-C(O)-, где t независимо представляет собой 1-5;
-(CH2)u-CO-NH-(CH2)u-C(O)-, где и независимо представляет собой 1-5; и
-(CH2)v-NH-C(O)-, где v представляет собой 2-12; и
причем концевой С(О) (если он присутствует) присоединен к группе NH;
и при этом b+с+d равно 2 или 3.
В любой из приведенных выше формул, в которых присутствует GalNAc, GalNAc может быть заменен любым другим нацеливающим лигандом, таким как те, которые упомянуты в настоящей заявке.
Является приемлемым, когда b равно 0, с равно 1 и d равно 1; b равно 1, с равно 0 и d равно 1; b равно 1, с равно 1 и d равно 0; или b равно 1, с равно 1 и d равно 1.
Является более приемлемым, когда b равно 0, с равно 1 и d равно 1; b равно 1, с равно 0 и d равно 1; или b равно 1, с равно 1 и d равно 1.
Является наиболее приемлемым, когда b равно 0, с равно 1 и d равно 1.
Согласно одному варианту реализации настоящего изобретения Y представляет собой О. В другом варианте Y представляет собой S.
Согласно одному варианту реализации настоящего изобретения R1 представляет собой Н или метил. Согласно одному варианту реализации настоящего изобретения R1 представляет собой Н. Согласно другому варианту реализации настоящего изобретения R1 представляет собой метил.
Согласно одному варианту реализации настоящего изобретения n равно 0, 1, 2 или 3. Является приемлемым, когда n равно 0.
Согласно одному варианту реализации настоящего изобретения L выбран из группы,
состоящей из:
-(СН2)r-С(O)-, где r=2-12;
-(CH2-CH2-O)s-CH2-C(O)-, где s=1-5;
-(CH2)t-CO-NH-(CH2)t-NH-C(O)-, где t независимо представляет собой 1-5;
-(CH2)u-CO-NH-(CH2)u-C(O)-, где u независимо представляет собой 1-5; и
-(CH2)v-NH-C(O)-, где v представляет собой 2-12;
при этом концевой С(О) присоединен к группе NH.
Является приемлемым, когда L представляет собой -(СН2)r-С(O)-, где r=2-12. Является приемлемым, когда r=2-6. Является более приемлемым, когда r=4 или 6, например, 4.
Является приемлемым, когда L представляет собой:
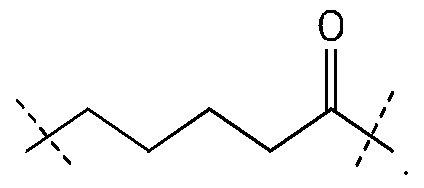
Примерные группы F включают (CH2)1-6, например, (CH2)1-4, например, СН2, (СН2)4, (СН2)5 или (СН2)6, или CH2O(СН2)2-3, например, CH2O(СН2)СН3.
Является приемлемым, когда L2 представляет собой:
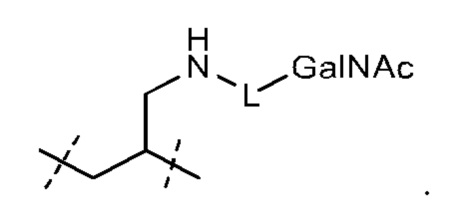
Является приемлемым, когда L2 представляет собой:
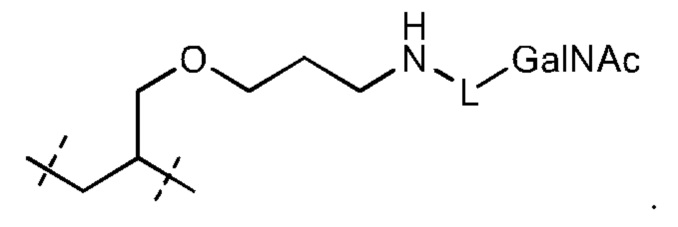
Является приемлемым, когда L2 представляет собой:
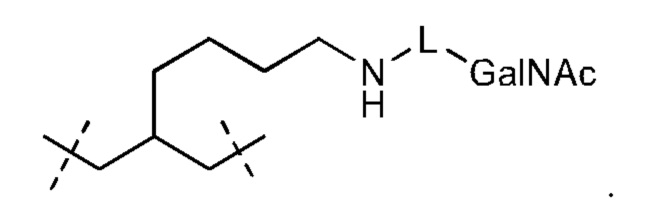
Является приемлемым, когда L2 представляет собой:
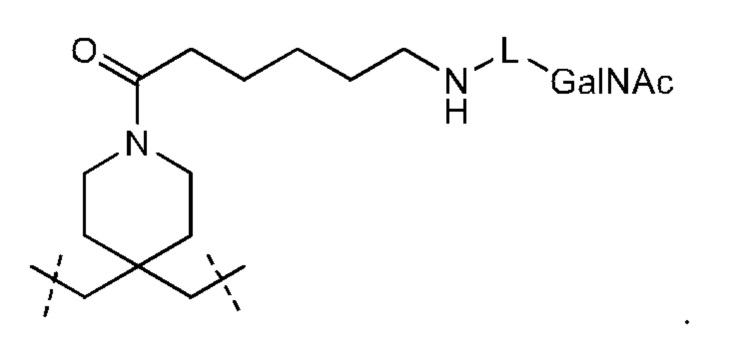
Является приемлемым, когда n равно 0 и L2 представляет собой:
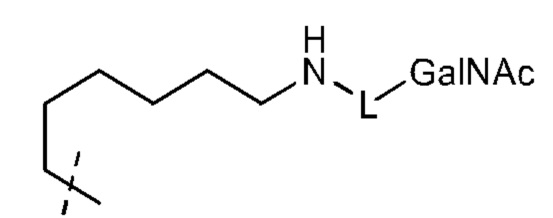
и концевая группа ОН отсутствует, так, что образуется следующая группа:
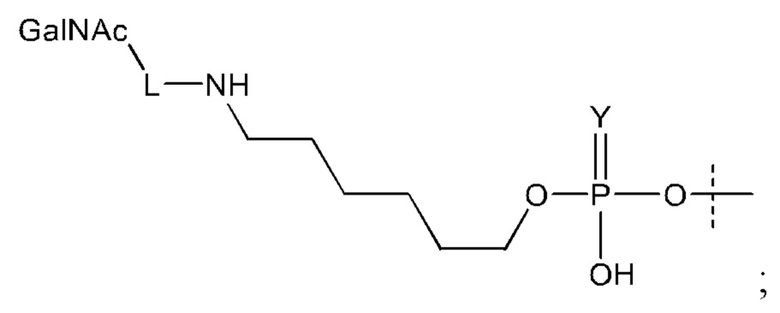
где Y определен в другом месте в настоящей заявке.
Как правило, L2 внутри группы, заключенной в скобки с индексом b, с и d, является одинаковым. L2 может быть одинаковым или различным в группах, заключенных в скобки с индексами b, с и d. В варианте реализации L2 в группе, заключенной в скобки с индексом с, аналогичен L2 в группе, заключенной в скобки с индексом d. Согласно варианту реализации настоящего изобретения L2 в группе, заключенной в скобки с индексом с, отличается от L2 в группе, заключенной в скобки с индексом d. Согласно варианту реализации настоящего изобретения L2 в группе, заключенной в скобки с индексами b, с и d, является одинаковым, например, когда линкерная группа представляет собой линкерную группу, происходящую из серинола.
Линкерные группы, происходящие из серинола, могут быть основаны на сериноле с любой стереохимией, т.е. происходят из изомера L-серина, изомера D-серина, рацемического серина или другой комбинации изомеров. В предпочтительном аспекте настоящего изобретения группа серинол-GalNAc (SerGN) имеет следующую стереохимию:
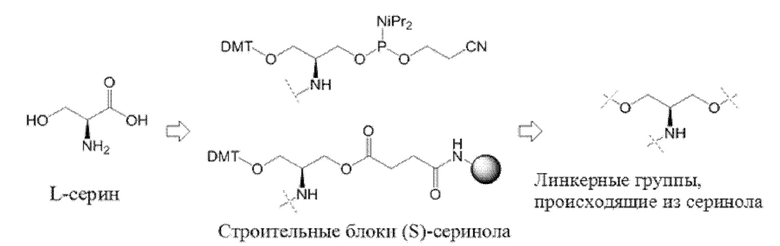
т.е. основан на (S)-сериноламидитном или (S)-серинолсукцинатном твердом поддерживаемом строительном блоке, полученном из изомера L-серина.
Согласно одному варианту реализации настоящего изобретения клетки-мишени представляют собой гепатоциты.
Согласно настоящему изобретению в качестве дополнительного аспекта предложена нуклеиновая кислота для ингибирования экспрессии гена-мишени в клетке, содержащая по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, подлежащего ингибированию, и при этом указанные первая и/или вторая цепи содержат фосфодитиоатную связь между по меньшей мере двумя концевыми 3'-нуклеотидами, и/или вторая цепь содержит фосфодитиоатную связь между по меньшей мере двумя концевыми 5'-нуклеотидами, и при этом молекула нуклеиновой кислоты непосредственно или косвенно конъюгирована с лигандом за счет линкера.
Нуклеиновая кислота может быть конъюгирована с лигандом, как описано в настоящей заявке. Нуклеотиды первой и/или второй цепей могут быть модифицированы, как описано в настоящей заявке.
Лиганд может представлять собой GalNAc.
Расщепляемая соединяющая группа представляет собой линкер, который стабилен за пределами клетки, но расщепляется при попадании в клетку-мишень. Расщепление высвобождает две части, которые удерживаются вместе линкером.
Согласно предпочтительному варианту реализации настоящего изобретения нуклеиновая кислота согласно настоящему изобретению содержит расщепляемую соединяющую группу, которая расщепляется по меньшей мере в 10 раз или более, предпочтительно по меньшей мере в 100 раз быстрее в клетке-мишени или при первом эталонном условии (которое может быть выбрано, например, чтобы имитировать или представлять внутриклеточные условия), чем в крови субъекта, или при втором эталонном условии (которое может быть выбрано, например, чтобы имитировать или представлять условия, обнаруженные в крови или сыворотке).
Расщепляемые соединяющие группы чувствительны к расщепляющим агентам, например, рН, окислительно-восстановительному потенциалу или присутствию разрушающих молекул. Разрушающие молекулы включают окисляющие или восстанавливающие ферменты, восстанавливающие агенты (такие как меркаптаны), эстеразы, эндосомы или агенты, которые могут создавать кислую среду, ферменты, которые могут гидролизовать или разрушать расщепляемую кислотой соединяющую группу, действуя как обычная кислота, пептидазы и фосфатазы.
Расщепляемая соединяющая группа может представлять собой дисульфидную связь, которая чувствительна к рН.
Линкер может содержать расщепляемую соединяющую группу, которая может быть расщеплена конкретным ферментом. Тип расщепляемой соединяющей группы, встроенной в линкер, может зависеть от клетки-мишени. Например, линкер, который содержит сложноэфирную группу, является предпочтительным, если мишенью является клетка печени. Линкеры, которые содержат пептидные связи, можно применять при нацеливании на клетки, богатые пептидазами, такие как клетки печени и синовиоциты.
В целом, пригодность расщепляемой соединяющей группы-кандидата можно оценить путем тестирования способности разрушающего агента (или условия) расщеплять соединяющую группу-кандидата. Также желательным будет тестирование способности расщепляемой соединяющей группы-кандидата быть устойчивой к расщеплению в крови или при контакте с другой нецелевой тканью. Согласно предпочтительным вариантам реализации настоящего изобретения подходящие соединения-кандидаты расщепляются по меньшей мере в 2, 4, 10 или 100 раз быстрее в клетке (или в условиях in vitro, выбранных для имитации внутриклеточных условий) по сравнению с кровью или сывороткой (или в условиях in vitro, выбранных для имитации внеклеточных условий).
Согласно одному аспекту расщепляемая соединяющая группа может представлять собой окислительно-восстановительную соединяющую группу. Окислительно-восстановительная расщепляемая соединяющая группа может представлять собой дисульфидную соединяющую группу.
Согласно одному аспекту соединяющая группа может представлять собой расщепляемую соединяющую группу на основе фосфата. Предпочтительные варианты реализации представляют собой -O-Р(O)(ОН)-O-, -O-P(S)(OH)-O-, -O-P(S)(SH)-O-, -S-Р(O)(ОН)-O-, -O-P(O)(OH)-S-, -S-P(O)(OH)-S-, -O-P(S)(OH)-S-, -S-P(S)(OH)-O-, -O-P(O)(H)-O-, -O-P(S)(H)-O-, -S-P(O)(H)-O-, -S-P(S)(H)-O-, -S-P(O)(H)-S-, -O-P(S)(H)-S-. Предпочтительные варианты реализации представляют собой -O-Р(O)(ОН)-O-.
Согласно одному аспекту расщепляемая соединяющая группа может представлять собой расщепляемую кислотой соединяющую группу. Предпочтительно расщепляемая кислотой соединяющая группа расщепляется в средах, в которых рН равно 6,5 или ниже, или расщепляется агентами, такими как ферменты, которые могут действовать как обычная кислота. Примеры расщепляемых кислотой соединяющих групп включают, но не ограничиваются ими, гидразоны, сложные эфиры и сложные эфиры аминокислот. Расщепляемые кислотой группы могут иметь общую формулу C=NN-; С(O)O или -ОС(О). Предпочтительный вариант реализации представляет собой соединяющую группу, в которой углерод, присоединенный к атому кислорода сложного эфира (алкоксигруппа), представляет собой арильную группу, замещенную алкильную группу или третичную алкильную группу, такую как диметилпентил или трет-бутил.
Согласно одному варианту реализации настоящего изобретения расщепляемая соединяющая группа может представлять собой расщепляемую соединяющую группу на основе сложного эфира. Примеры расщепляемых соединяющих групп на основе сложных эфиров включают, но не ограничиваются ими, сложные эфиры алкиленовых, алкениленовых и алкиниленовых групп.
Согласно одному варианту реализации настоящего изобретения расщепляемая соединяющая группа может представлять собой расщепляемую соединяющую группу на основе пептида. Расщепляемые соединяющие группы на основе пептидов представляют собой пептидные связи, образованные между аминокислотами с получением олигопептидов (например, дипептидов, трипептидов и т.д.) и полипептидов. Расщепляемая соединяющая группа на основе пептида обычно ограничена пептидной связью (то есть амидной связью), образованной между аминокислотами, образующими пептиды и белки, и не включает всю амидную функциональную группу. Расщепляемые соединяющие группы на основе пептидов имеют общую формулу - NHCHRAC(O)NHCHRBC(O)-, где RA и RB представляют собой группы R двух смежных аминокислот.
Синтез одиночных цепей
Примерные соединения можно синтезировать в соответствии со способами, описанными ниже и известными специалисту в данной области техники. Сборку олигонуклеотидной цепи и линкерных строительных блоков можно выполнять, например, с помощью твердофазного синтеза с применением фосфоамидитной методологии. Твердофазный синтез можно начинать с основания или модифицированного строительного блока, загруженного на lcaa CPG. Цикл связывания фосфоамидитного синтеза состоит из 1) удаления DMT, 2) удлинения цепи с применением необходимого DMT-замаскированного фосфоамидита и активатора, который может представлять собой бензилтиотетразол (БТТ), 3) кэппирования неудлиненных олигонуклеотидных цепей с последующим окислением Р(III) до P(V) либо с помощью йода (если требуется фосфодиэфирная связь), либо EDITH (если требуется фосфотиоатная или фосфодитиоатная связь) и затем повторного кэппирования (Сар/Ох/Сар или Cap/Thio/Сар). В случае если целевой является фосфодитиоатная связь, цикл связывания фосфоамидитного синтеза состоит из 1) удаления DMT, 2) удлинения цепи с применением требуемого DMT-замаскированного тиофосфоамидита, 3) кэппирования неудлиненных олигонуклеотидных цепей с последующим окислением Р(III) до P(V) с помощью EDITH и повторного кэппирования (Cap/Thio/Сар). Для конъюгации на колонке трехвалентного древовидного кластера GalNAc применяли аналогичный цикл фосфоамидитного синтеза с применением необходимого трехвалентного разветвляющего амидита ST41-phos, за которым следовал другой раунд цикла синтеза с применением GalNAc амидита ST23-phos. Необходимые строительные блоки доступны коммерчески или синтез описан ниже.
Все готовые одноцепочечные продукты анализировали с помощью АХ-ВЭЖХ для подтверждения их чистоты. Чистота представлена в % FLP (% полноразмерного продукта), который представляет собой процент УФ-площади под сигналом заданного продукта на УФ-кривой анализа готового продукта методом АХ-ВЭЖХ. Идентичность соответствующих одноцепочечных продуктов подтверждали с помощью анализа методом ЖХ/МС.
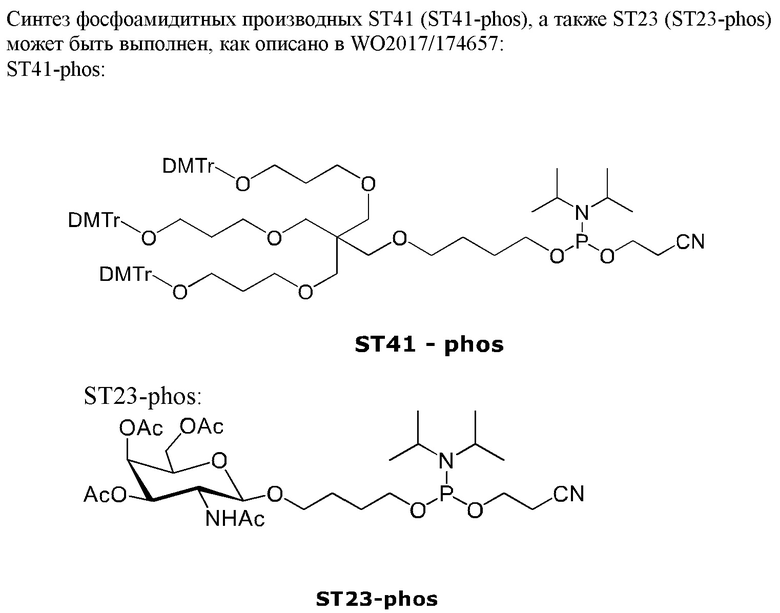
Синтез двойных цепей
Чтобы получить двухцепочечные конъюгаты, необходимые отдельные одиночные цепи растворяют в концентрации 60 OD/мл в Н2О. Оба раствора отдельных олигонуклеотидов могут быть добавлены вместе в реакционный сосуд. Для более легкого мониторинга реакции можно выполнять титрование. Первую цепь добавляют с 25% избытком по сравнению со второй цепью, что определяется по УФ-поглощению при 260 нм. Реакционную смесь нагревают, например, до 80°С в течение 5 минут, а затем медленно охлаждают до комнатной температуры. Образование двойной цепи можно контролировать по образованию ионных пар с помощью ВЭЖХ с обращенной фазой. На основании УФ-области остаточной одиночной цепи можно рассчитать необходимое количество второй цепи и добавить его в реакционную смесь. Реакционную смесь снова нагревают, например, до 80°С, и медленно охлаждают до комнатной температуры. Эту процедуру можно повторять до тех пор, пока не будет обнаружено менее 10% остаточной одиночной цепи.
Нуклеиновая кислота, описанная в настоящей заявке, может быть изготовлена с липидом в форме липосомы. Такой состав может быть описан в данной области техники как липоплекс. Композицию с липидом/липосомой можно применять для облегчения доставки нуклеиновой кислоты согласно настоящему изобретению в клетки-мишени. Липидную систему доставки, описанную в настоящей заявке, можно применять в качестве альтернативы конъюгированному лиганду. Модификации, описанные в настоящей заявке, могут присутствовать при применении нуклеиновой кислоты согласно настоящему изобретению с липидной системой доставки или с системой доставки на основе конъюгата лиганда.
Такой липоплекс может содержать липидную композицию, содержащую:
i) катионный липид или его фармацевтически приемлемую соль;
ii) стероид;
iii) фосфолипид фосфатидилэтаноламин;
iv) пегилированный липид.
Катионный липид может представлять собой аминокатионный липид.
Катионный липид может иметь формулу (XIX):
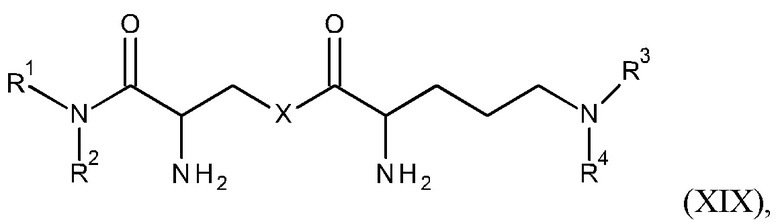
или его фармацевтически приемлемая соль, в которой:
X представляет собой О, S или NH;
R1 и R2 каждый независимо представляет собой С4-С22 линейную или разветвленную алкильную цепь или С4-С22 линейную или разветвленную алкенильную цепь с одной или более двойными связями, причем алкильная или алкенильная цепь необязательно содержит промежуточный сложный эфир, амид или дисульфид;
если X представляет собой S или NH, R3 и R4 каждый независимо представляет собой водород, метил, этил, моно- или полиаминную группу, или R3 и R4 вместе образуют гетероциклильное кольцо;
если X представляет собой О, R3 и R4 каждый независимо представляет собой водород, метил, этил, моно- или полиаминную группу, или R3 и R4 вместе образуют гетероциклильное кольцо, или R3 представляет собой водород и R4 представляет собой C(NH)(NH2).
Катионный липид может иметь формулу (XIXA):
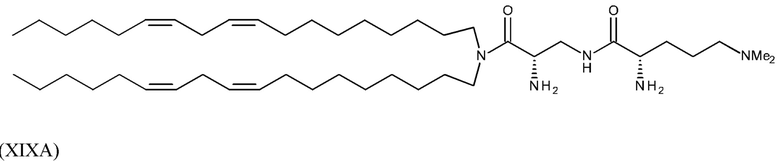
или его фармацевтически приемлемая соль.
Катионный липид может иметь формулу (XIXB):
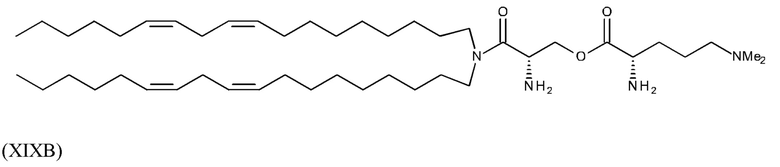
или его фармацевтически приемлемая соль.
Содержание компонента катионного липида может составлять от приблизительно 55 мол.% до приблизительно 65 мол.% от общего содержания липидов композиции. В частности, компонент катионного липида составляет приблизительно 59 мол.% от общего содержания липидов композиции.
Композиции могут дополнительно содержать стероид. Стероид может представлять собой холестерин. Содержание стероида может составлять от приблизительно 26 мол.% до приблизительно 35 мол.% от общего содержания липидов липидной композиции. Более конкретно, содержание стероида может составлять приблизительно 30 мол.% от общего содержания липидов липидной композиции.
Фосфолипид фосфатидилэтаноламин может быть выбран из группы, состоящей из 1,2-дифитаноил-sn-глицеро-3-фосфоэтаноламина (DPhyPE), 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламина (DOPE), 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина (DSPE), 1,2-дилауроил-sn-глицеро-3-фосфоэтаноламина (DLPE), 1,2-димиристоил-sn-глицеро-3- фосфоэтаноламина (DMPE), 1,2-дипальмитоил-sn-глицеро-3-фосфоэтаноламина (DPPE), 1,2-дилинолеоил-sn-глицеро-3-фосфоэтаноламина (DLoPE), 1-пальмитоил-2-олеоил-sn-глицеро-3-фосфоэтаноламина (POPE), 1,2-диэрукоил-sn-глицеро-3-фосфоэтаноламина (DEPE), 1,2-дисквалеоил-sn-глицеро-3-фосфоэтаноламина (DSQPE) и 1-стеароил-2-линолеоил-sn-глицеро-3-фосфоэтаноламина (SLPE). Содержание фосфолипида может составлять приблизительно 10 мол.% от общего содержания липидов композиции.
Пегилированный липид может быть выбран из группы, состоящей из 1,2-димиристоил-sn-глицерина, метоксиполиэтиленгликоля (DMG-PEG) и С16-церамид-ПЭГ.
Содержание пегилированного липида может составлять от приблизительно 1 до 5 мол.% от общего содержания липидов композиции.
Содержание компонента катионного липида в композиции может составлять от приблизительно 55 мол.% до приблизительно 65 мол.% от общего содержания липидов липидной композиции, предпочтительно приблизительно 59 мол.% от общего содержания липидов липидной композиции.
Композиция может иметь молярное соотношение компонентов i):ii):iii):iv), выбранное из 55:34:10:1; 56:33:10:1; 57:32:10:1; 58:31:10:1; 59:30:10:1; 60:29:10:1; 61:28:10:1; 62:27:10:1; 63:26:10:1; 64:25:10:1; и 65:24:10:1.
Композиция может содержать катионный липид, имеющий структуру
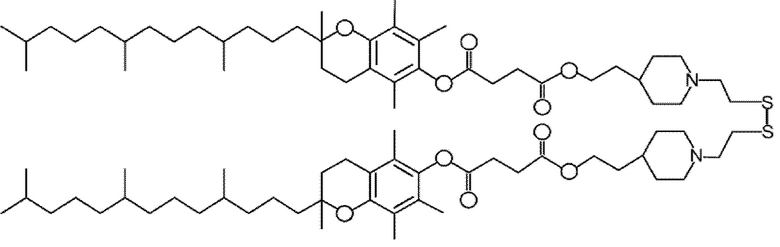
стероид, имеющий структуру
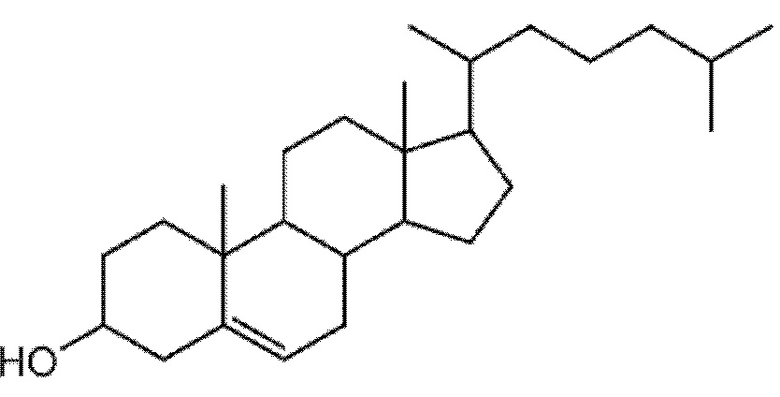 холестерин
холестерин
фосфолипид фосфатидилэтаноламин, имеющий структуру
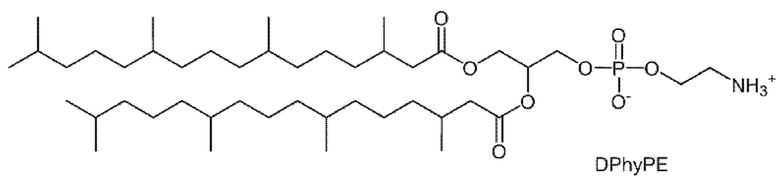
и пегилированный липид, имеющий структуру
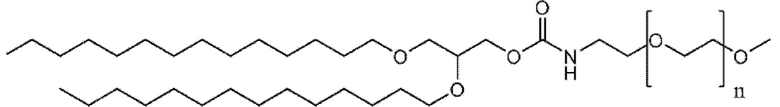
мПЭГ-2000-ДМГ
Нейтральные липосомные композиции могут быть образованы, например, из димиристоилфосфатидилхолина (DMPC) или дипальмитоилфосфатидилхолина (DPPC). Анионные липосомные композиции могут быть образованы из димиристоилфосфатидилглицерина, в то время как анионные липосомы, способные к слиянию, могут быть образованы главным образом из диолеоилфосфатидилэтаноламина (DOPE). Другой тип липосомальной композиции может быть образован из фосфатидилхолина (ФХ), такого как, например, ФХ соевых бобов и ФХ яиц. Другой тип образован из смесей фосфолипида и/или фосфатидилхолина и/или холестерина.
Положительно заряженный синтетический катионный липид, хлорид N-[1-(2,3- диолеилокси)пропил]-N,N,N-триметиламмония (DOTMA), можно применять для образования небольших липосом, которые спонтанно взаимодействуют с нуклеиновой кислотой с образованием комплексов липид-нуклеиновая кислота, которые способны сливаться с отрицательно заряженными липидами клеточных мембран клеток тканевой культуры. Для образования липосом также можно применять аналоги DOTMA.
Для образования липосом также можно применять производные и аналоги липидов, описанных в настоящей заявке.
Липосома, содержащая нуклеиновую кислоту, может быть получена с помощью различных способов. В одном примере липидный компонент липосомы растворяют в детергенте так, что образуются мицеллы с липидным компонентом. Например, липидный компонент может представлять собой амфипатический катионный липид или липидный конъюгат. Детергент может иметь высокую критическую концентрацию мицеллообразования и может быть неионогенным. Примерные детергенты включают холат, CHAPS, октилглюкозид, дезоксихолат и лауроилсаркозин. Препарат нуклеиновой кислоты затем добавляют к мицеллам, которые содержат липидный компонент. Катионные группы на липиде взаимодействуют с нуклеиновой кислотой и конденсируются вокруг нуклеиновой кислоты с образованием липосомы. После конденсации детергент удаляют, например, с помощью диализа, чтобы получить липосомальный препарат нуклеиновой кислоты.
При необходимости транспортирующее соединение, которое способствует конденсации, может быть добавлено во время реакции конденсации, например, путем контролируемого добавления. Например, транспортирующее соединение может представлять собой полимер, отличный от нуклеиновой кислоты (например, спермин или спермидин). рН также можно корректировать, чтобы способствовать конденсации.
Составы нуклеиновых кислот могут включать поверхностно-активное вещество. Согласно одному варианту реализации настоящего изобретения нуклеиновая кислота изготовлена в виде эмульсии, которая содержит поверхностно-активное вещество.
Поверхностно-активное вещество, которое не является ионизированным, представляет собой неионное поверхностно-активное вещество. Примеры включают неионные сложные эфиры, такие как сложные эфиры этиленгликоля, сложные эфиры пропиленгликоля, сложные эфиры глицерина и т.д., неионные алканоламиды и простые эфиры, такие как этоксилаты алифатических спиртов, пропоксилированные спирты и этоксилированные/пропоксилированные блок-полимеры.
Поверхностно-активное вещество, которое несет отрицательный заряд при растворении или диспергировании в воде, представляет собой анионное поверхностно-активное вещество. Примеры включают карбоксилаты, такие как мыла, ациллактилаты, ациламиды аминокислот, сложные эфиры серной кислоты, такие как алкилсульфаты, и этоксилированные алкилсульфаты, сульфонаты, такие как алкилбензолсульфонаты, ацилизетионаты, ацилтаураты и сульфосукцинаты, а также фосфаты.
Поверхностно-активное вещество, которое несет положительный заряд при растворении или диспергировании в воде, представляет собой катионное поверхностно-активное вещество. Примеры включают соли четвертичного аммония и этоксилированные амины.
Поверхностно-активное вещество, которое обладает способностью нести как положительный, так и отрицательный заряд, представляет собой амфотерное поверхностно-активное вещество. Примеры включают производные акриловой кислоты, замещенные алкиламиды, N-алкилбетаины и фосфатиды.
«Мицеллы» определены в настоящей заявке как конкретный тип молекулярной сборки, в которой амфипатические молекулы расположены в сферической структуре так, что все гидрофобные части молекул направлены внутрь, оставляя гидрофильные части в контакте с окружающей водной фазой. Обратное расположение существует, если среда является гидрофобной. Мицелла может быть образована путем смешивания водного раствора нуклеиновой кислоты, алкилсульфата щелочного металла и по меньшей мере одного мицеллообразующего соединения.
Примерные мицеллообразующие соединения включают лецитин, гиалуроновую кислоту, фармацевтически приемлемые соли гиалуроновой кислоты, гликолевую кислоту, молочную кислоту, экстракт ромашки, экстракт огурца, олеиновую кислоту, линолевую кислоту, линоленовую кислоту, моноолеин, моноолеаты, монолаураты, масло семян бурачника, масло примулы вечерней, ментол, тригидроксиоксохоланилглицин и его фармацевтически приемлемые соли, глицерин, полиглицерин, лизин, полилизин, триолеин, простые полиоксиэтиленовые эфиры и их аналоги, простые алкильные эфиры полидоканола и их аналоги, хенодезоксихолат, дезоксихолат и их смеси.
Фенол и/или м-крезол могут быть добавлены к смешанной мицеллярной композиции в качестве стабилизатора и консерванта. Может быть добавлен изотонический агент, такой как глицерин.
Препарат нуклеиновой кислоты может быть встроен в частицу, такую как микрочастица. Микрочастицы могут быть получены с помощью распылительной сушки, лиофилизации, испарения, сушки в псевдоожиженном слое, вакуумной сушки или комбинации этих способов.
Согласно настоящему изобретению также предложены фармацевтические композиции, содержащие нуклеиновую кислоту или конъюгированную нуклеиновую кислоту согласно настоящему изобретению. Фармацевтические композиции можно применять в качестве лекарственных средств или в качестве диагностических агентов, по отдельности или в комбинации с другими агентами. Например, нуклеиновую кислоту или конъюгированную нуклеиновую кислоту согласно настоящему изобретению можно комбинировать с носителем для доставки (например, липосомами) и вспомогательными веществами, такими как носители, разбавители. Также могут быть добавлены другие агенты, такие как консерванты и стабилизаторы. Способы доставки нуклеиновой кислоты или конъюгированной нуклеиновой кислоты известны в данной области техники и известны специалисту в данной области техники.
Нуклеиновую кислоту или конъюгированную нуклеиновую кислоту согласно настоящему изобретению также можно вводить в комбинации с другими терапевтическими соединениями, либо вводить по отдельности, либо одновременно, например, в виде комбинированной стандартной дозы. Настоящее изобретение также включает фармацевтическую композицию, содержащую нуклеиновую кислоту или конъюгированную нуклеиновую кислоту согласно настоящему изобретению в физиологически/фармацевтически приемлемом вспомогательном веществе, таком как стабилизатор, консервант, разбавитель, буфер и тому подобное.
Фармацевтическая композиция может быть специально изготовлена для введения в твердой или жидкой форме. Композиция может быть изготовлена для перорального введения, парентерального введения (включая, например, подкожную, внутримышечную, внутривенную или эпидуральную инъекцию), местного применения, интравагинального или интраректального введения, подъязычного введения, глазного введения, трансдермального введения или назального введения. Предпочтительной является доставка с применением подкожных или внутривенных способов.
Уровни дозировки для лекарственного средства и фармацевтических композиций согласно настоящему изобретению могут быть определены специалистами в данной области техники с помощью обычных экспериментов. Согласно одному варианту реализации настоящего изобретения стандартная доза может содержать от приблизительно 0,01 мг/кг до приблизительно 100 мг/кг массы тела нуклеиновой кислоты. Согласно другому варианту доза может составлять от 10 мг/кг до 25 мг/кг массы тела, или от 1 мг/кг до 10 мг/кг массы тела, или от 0,05 мг/кг до 5 мг/кг массы тела, или 0,1 мг/кг до 5 мг/кг массы тела, или от 0,1 мг/кг до 1 мг/кг массы тела, или от 0,1 мг/кг до 0,5 мг/кг массы тела, или от 0,5 мг/кг до 1 мг/кг массы тела. Уровни дозировки также могут быть рассчитаны с помощью других параметров, таких как, например, площадь поверхности тела.
Фармацевтическая композиция может представлять собой стерильную инъецируемую водную суспензию или раствор или может быть в лиофилизированной форме. Согласно одному варианту реализации настоящего изобретения фармацевтическая композиция может содержать лиофилизированные липоплексы или водную суспензию липоплексов. Липоплексы предпочтительно содержат нуклеиновую кислоту согласно настоящему изобретению. Такие липоплексы можно применять для доставки нуклеиновой кислоты согласно настоящему изобретению в клетку-мишень как в условиях in vitro, так и в условиях in vivo.
Фармацевтические композиции и лекарственные средства согласно настоящему изобретению можно вводить субъекту-млекопитающему в фармацевтически эффективной дозе. Млекопитающее может быть выбрано из человека, собак, кошек, лошадей, крупного рогатого скота, свиньи, козы, овцы, мыши, крысы, хомяка и морской свинки.
Дополнительный аспект настоящего изобретения относится к нуклеиновой кислоте или конъюгированной нуклеиновой кислоте согласно настоящему изобретению или фармацевтической композиции, содержащей вышеуказанное, для применения при лечении или предотвращении заболевания или нарушения. Настоящее изобретение включает фармацевтическую композицию, содержащую одну или более молекул для РНК-интерференции согласно настоящему изобретению в физиологически/фармацевтически приемлемом вспомогательном веществе, таком как стабилизатор, консервант, разбавитель, буфер и тому подобное.
Фармацевтическая композиция может представлять собой стерильную инъецируемую водную суспензию или раствор или может быть в лиофилизированной форме.
Фармацевтически приемлемые композиции могут содержать терапевтически эффективное количество одной или более нуклеиновых кислот в любом варианте реализации в соответствии с настоящим изобретением, взятых по отдельности или изготовленных в виде одного или более фармацевтически приемлемых носителей, вспомогательного вещества и/или разбавителей.
Примеры материалов, которые могут служить в качестве фармацевтически приемлемых носителей, включают: (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмалы, такие как кукурузный крахмал и картофельный крахмал; (3) целлюлозу и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; (4) порошкообразный трагакант; (5) солод; (6) желатин; (7) смазывающие агенты, такие как стеарат магния, лаурилсульфат натрия и тальк; (8) вспомогательные вещества, такие как масло какао и воски для суппозиториев; (9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль; (11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) буферные агенты, такие как гидроксид магния и гидроксид алюминия; (15) альгиновую кислоту; (16) апирогенную воду; (17) изотонический солевой раствор; (18) раствор Рингера; (19) этиловый спирт; (20) рН буферные растворы; (21) сложные полиэфиры, поликарбонаты и/или полиангидриды; (22) наполняющие агенты, такие как полипептиды и аминокислоты; (23) сывороточный компонент, такой как сывороточный альбумин, ЛПВП и ЛПНП; и (22) другие нетоксичные совместимые вещества, применяемые в фармацевтических составах.
Стабилизаторы могут представлять собой агенты, которые стабилизируют нуклеиновую кислоту-агент, например, белок, который может образовывать комплекс с нуклеиновой кислотой, хелаторы (например, ЭДТА), соли, ингибиторы РНКазы и ингибиторы ДНКазы.
В некоторых случаях желательно замедлить всасывание лекарственного средства при подкожной или внутримышечной инъекции, чтобы продлить действие лекарственного средства. Это можно осуществлять путем применения жидкой суспензии кристаллического или аморфного материала, имеющего слабую растворимость в воде.
Скорость всасывания лекарственного средства затем зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристалла и кристаллической формы.
Согласно другому варианту отсроченное всасывание лекарственной формы, вводимой парентерально, осуществляется за счет растворения или суспендирования лекарственного средства в масляном носителе.
Нуклеиновая кислота, описанная в настоящей заявке, может быть способна ингибировать экспрессию гена-мишени в клетке. Нуклеиновая кислота, описанная в настоящей заявке, может быть способна частично ингибировать экспрессию гена-мишени в клетке. Ингибирование может быть полным, т.е. 0% от уровня экспрессии гена-мишени в отсутствие нуклеиновой кислоты согласно настоящему изобретению. Ингибирование экспрессии гена-мишени может быть частичным, т.е. оно может составлять 15%, 20%, 30%, 40%, 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95% от экспрессии гена-мишени в отсутствие нуклеиновой кислоты согласно настоящему изобретению. Ингибирование может длиться 4 недели, 5 недель, 6 недель, 7 недель, 8 недель, 10 недель, 11 недель, 12 недель, 13 недель, 14 недель или до 3 месяцев при применении у субъекта, такого как субъект-человек. Нуклеиновую кислоту или композицию, содержащую композицию нуклеиновой кислоты, можно применять однократно, каждую неделю, каждые две недели, каждые три недели, каждые четыре недели, каждые пять недель, каждые шесть недель, каждые семь недель или каждые восемь недель. Нуклеиновую кислоту можно применять для подкожного, внутривенного или любых других путей применения, таких как пероральный, ректальный или внутрибрюшинный.
В клетках и/или у субъектов, обработанных или получающих нуклеиновую кислоту согласно настоящему изобретению, экспрессия гена-мишени может быть ингибирована по сравнению с необработанными клетками и/или субъектами по меньшей мере приблизительно на 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 98% или 100%. Уровень ингибирования может обеспечить лечение заболевания, ассоциированного с экспрессией или сверхэкспрессией гена-мишени, или может обеспечить дальнейшее изучение функций продукта гена-мишени.
Ген-мишень может представлять собой фактор VII, Eg5, PCSK9, ТРХ2, ароВ, SAA, TTR, RSV, ген PDGF бета, ген Erb-B, ген Src, ген CRK, ген GRB2, ген RAS, ген MEKK, ген INK, ген RAF, ген Erkl/2, ген PCNA(p21), ген MYB, ген JU, ген FOS, ген BCL-2, гепцидин, активированный белок С, ген циклина D, ген VEGF, ген EGFR, ген циклина А, ген циклина Е, ген WNT-1, ген бета-катенина, ген с-МЕТ, ген РКС, ген NFKB, ген STAT3, ген сурвивина, ген Her2/Neu, ген топоизомеразы I, ген топоизомеразы II альфа, мутации в гене р73, мутации в гене p21(WAF I/CIPI), мутации в гене р27(К1Р1), мутации в гене РРМ ID, мутации в гене RAS, мутации в гене кавеолина I, мутации в гене МТВ I, мутации в гене MTAI, мутации в гене М68, мутации в генах-супрессорах опухолей и мутации в гене-супрессоре опухоли р53.
Другой аспект настоящего изобретения относится к нуклеиновой кислоте или конъюгированной нуклеиновой кислоте согласно настоящему изобретению при изготовлении лекарственного средства для лечения или предотвращения заболевания или нарушения.
Также в настоящее изобретение включен способ лечения или предотвращения заболевания или нарушения, включающий введение фармацевтической композиции, содержащей нуклеиновую кислоту или конъюгированную нуклеиновую кислоту, описанные в настоящей заявке, индивидууму, нуждающемуся в лечении. Композицию нуклеиновой кислоты можно вводить два раза в неделю, один раз в неделю, каждые две недели, каждые три недели, каждые четыре недели, каждые пять недель, каждые шесть недель, каждые семь недель или каждые восемь недель. Нуклеиновую кислоту можно вводить субъекту подкожно, внутривенно или с применением любых других путей применения, таких как пероральный, ректальный или внутрибрюшинный.
Согласно одному варианту реализации настоящего изобретения субъекту вводят начальную дозу и одну или более поддерживающих доз нуклеиновой кислоты-агента. Поддерживающая доза или дозы могут быть такими же или ниже, чем начальная доза, например, наполовину меньше начальной дозы. Поддерживающие дозы вводят, например, не чаще одного раза в 2, 5, 10 или 30 дней. Схема лечения может длиться в течение периода времени, который будет варьироваться в зависимости от характера конкретного заболевания, его степени тяжести и общего состояния пациента.
Согласно одному варианту реализации настоящего изобретения композиция включает множество молекул нуклеиновой кислоты-агента. Согласно другому варианту реализации настоящего изобретения молекула нуклеиновой кислоты-агента имеет последовательности, которые не перекрываются и не являются смежными с другой молекулой в отношении природной последовательности-мишени. Согласно другому варианту реализации настоящего изобретения множество молекул нуклеиновой кислоты-агента являются специфичными в отношении различных природных генов-мишеней. Согласно другому варианту реализации настоящего изобретения нуклеиновая кислота-агент является специфичной в отношении аллеля.
Нуклеиновую кислоту или конъюгированную нуклеиновую кислоту согласно настоящему изобретению также можно вводить или применять в комбинации с другими терапевтическими соединениями, либо вводить по отдельности, либо одновременно, например, в виде комбинированной стандартной дозы.
Нуклеиновую кислоту или конъюгированную нуклеиновую кислоту согласно настоящему изобретению можно получить с применением обычных способов в данной области техники, включая химический синтез или экспрессию нуклеиновой кислоты как в условиях in vitro (например, с помощью прерванной транскрипции), так и в условиях in vivo. Например, применяя твердофазный химический синтез или применяя вектор экспрессии. Согласно одному варианту реализации настоящего изобретения вектор экспрессии может продуцировать нуклеиновую кислоту согласно настоящему изобретению в клетке-мишени.
Способы синтеза нуклеиновой кислоты, описанные в настоящей заявке, известны специалистам в данной области техники.
Примерные соединения синтезировали в соответствии со способами, известными специалисту в данной области техники. Сборку олигонуклеотидной цепи и линкерных строительных блоков можно выполнять с помощью твердофазного синтеза с применением фосфоамидитной методологии. На схеме 1 показан утроительный амидит C4xlt-phos и GalNAc-амидит (ST23-phos), необходимые для сборки трехвалентного древовидного кластера GalNAc во время твердофазного синтеза олигонуклеотидов. Синтез C4XLT-phos, а также ST23-phos можно осуществлять, как описано в WO2017/174657.
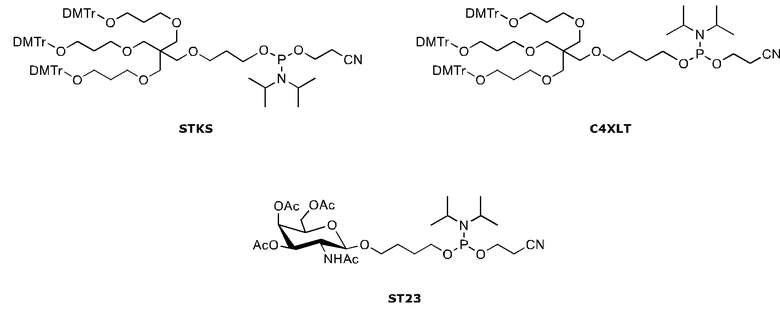
Схема 1: Структуры утроительных амидитов и GalNAc-амидитов, применяемые для конъюгации трехвалентных древовидных кластеров GalNAc на колонке.
Синтез олигонуклеотидов миРНК, конъюгированной с древовидным кластером GalNAc, представлен на схеме 2, показанной на Фигуре 11.
Сборку олигонуклеотидной цепи можно начинать с применением подложки, загруженной основанием, например, 5'DMT-2'FdU-сукцинат-lcaa-СРО, как в примерном соединении А0149 (STS12009V15L4B). Для введения первой фосфодитиоатной связи цикл связывания фосфоамидитного синтеза состоит из 1) удаления DMT, 2) удлинения цепи с применением необходимого DMT-замаскированного тиофосфоамидита, 3) кэппирования неудлиненных олигонуклеотидных цепей с последующим окислением Р(III) до P(V) с помощью EDITH и повторным кэппированием (Cap/Thio/Сар). После этого цикл синтеза можно повторять с применением стандартных DMT-фосфоамидитов и Сар/Ох/Сар или Cap/Thio/Сар в зависимости от того, желательна ли фосфодиэфирная или фосфотиоатная связь, пока не будет достигнута полная длина продукта. Для конъюгации на колонке трехвалентного древовидного кластера GalNAc можно применять аналогичный цикл синтеза с применением необходимого трехвалентного разветвляющего амидита C4XLT, за которым следует другой раунд цикла синтеза с применением GalNAc амидита ST23. По завершении этого последнего этапа в синтезаторе олигонуклеотид может быть отщеплен от твердой подложки и освобожден от дополнительных защитных групп с помощью обработки метиламином (в присутствии 20 мМ DTT, если присутствуют фосфодитиоатные связи). Затем неочищенный продукт может быть очищен с помощью АХ-ВЭЖХ с применением градиента NaCl. Избыток соли после очистки методом ИХ удаляли с помощью гель-проникающей хроматографии (SEC) для получения готового продукта.
Все готовые одноцепочечные продукты анализировали с помощью АХ-ВЭЖХ для подтверждения их чистоты. Чистота может быть представлена в % FLP (% полноразмерного продукта), который представляет собой процент УФ-площади под сигналом заданного продукта на УФ-кривой анализа готового продукта методом АХ-ВЭЖХ. Идентичность соответствующих одноцепочечных продуктов (немодифицированных или GalNAc-конъюгированных олигонуклеотидов) подтверждали с помощью анализа методом ЖХ/МС.
Образование дуплекса двухцепочечной миРНК можно осуществлять путем эквимолярного добавления соответствующих одиночных цепей и нагревания до 80°С. Медленное охлаждение до комнатной температуры может привести к образованию полной двойной цепи. После образования дуплекса можно выполнять ИП-ОФ-ВЭЖХ (обращенно-фазовая ВЭЖХ с образованием ионных пар). Чистота двойной цепи может быть представлена в % двойной цепи, который представляет собой процент УФ-площади под сигналом заданного продукта на УФ-кривой анализа методом ИП-ОФ-ВЭЖХ.
Согласно настоящему изобретению также предложена нуклеиновая кислота в соответствии с любым аспектом настоящего изобретения, описанным в настоящей заявке, в которой первая цепь РНК имеет концевой 5'-(Е)-винилфосфонатный нуклеотид, и концевой 5'-(Е)-винилфосфонатный нуклеотид предпочтительно соединен со вторым нуклеотидом в первой цепи с помощью фосфодиэфирной связи.
Согласно одному варианту реализации настоящего изобретения первая цепь может содержать более 1 фосфодиэфирной связи.
Согласно одному варианту реализации настоящего изобретения первая цепь может содержать фосфодиэфирные связи между по меньшей мере тремя концевыми 5'-нуклеотидами.
Согласно одному варианту реализации настоящего изобретения первая цепь может содержать фосфодиэфирные связи между по меньшей мере четырьмя концевыми 5'-нуклеотидами.
Согласно одному варианту реализации настоящего изобретения первая цепь может содержать формулу (XVII):
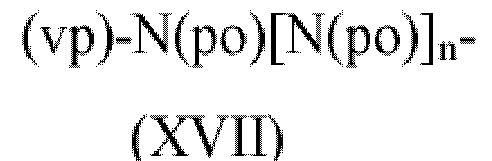
в которой «(vp)-» представляет собой 5'-(Е)-винилфосфонат, «N» представляет собой нуклеотид, «ро» представляет собой фосфодиэфирную связь, а n составляет от 1 до (общее количество нуклеотидов в первой цепи -2), при этом предпочтительно n составляет от 1 до (общее количество нуклеотидов в первой цепи -3), при этом более предпочтительно n составляет от 1 до (общее количество нуклеотидов в первой цепи -4).
Согласно одному варианту реализации настоящего изобретения первая цепь может содержать по меньшей мере одну фосфотиоатную (ps) связь.
Согласно одному варианту реализации настоящего изобретения первая цепь может дополнительно содержать фосфотиоатную связь между двумя концевыми 3'-нуклеотидами или фосфотиоатные связи между тремя концевыми 3'-нуклеотидами.
Согласно одному варианту реализации настоящего изобретения связи между другими нуклеотидами в первой цепи представляют собой фосфодиэфирные связи.
Согласно одному варианту реализации настоящего изобретения первая цепь может содержать более 1 фосфотиоатной связи.
Согласно дополнительному варианту реализации вторая цепь может содержать фосфотиоатную связь между двумя концевыми 3'-нуклеотидами или фосфотиоатные связи между тремя концевыми 3'-нуклеотидами.
Согласно другому дополнительному варианту реализации вторая цепь может содержать фосфотиоатную связь между двумя концевыми 5'-нуклеотидами или фосфотиоатные связи между тремя концевыми 5'-нуклеотидами.
Согласно варианту реализации настоящего изобретения концевой 5'-(E)-винилфосфонатный нуклеотид представляет собой РНК-нуклеотид.
Концевой 5'-(Е)-винилфосфонатный нуклеотид представляет собой нуклеотид, в котором природная фосфатная группа на 5'-конце замещена Е-винилфосфонатом, в котором мостиковый 5'-атом кислорода концевого нуклеотида 5'-фосфорилированной цепи замещен метинильной (-СН=) группой:
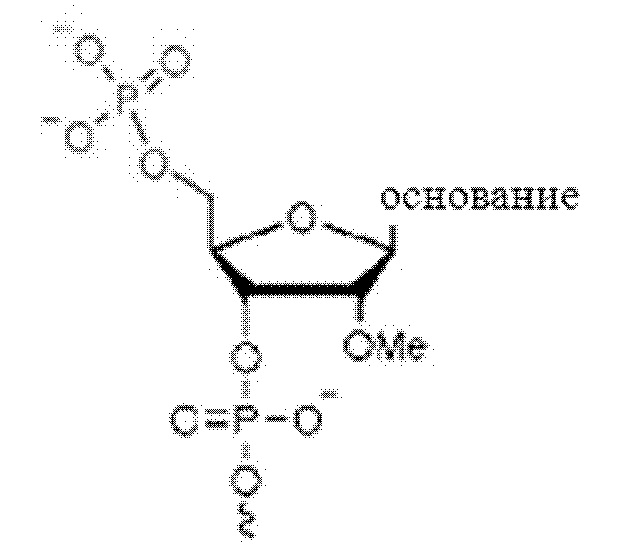
Нуклеотид с природным фосфатом на 5'-конце
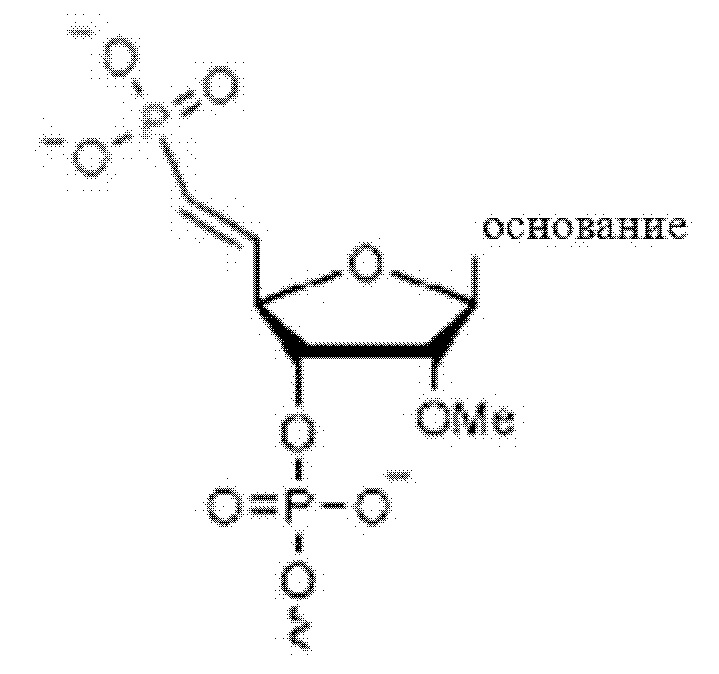
Нуклеотид с Е-винилфосфонатом на 5'-конце
5'-(Е)-винилфосфонат представляет собой миметик 5'-фосфата. Биологический миметик представляет собой молекулу, которая способна выполнять ту же функцию, как и исходная молекула, которую она имитирует, и структурно очень сходна с ней. Применительно к настоящему изобретению 5'-(Е)-винилфосфонат имитирует функцию обычного 5'-фосфата, например, обеспечивая эффективную загрузку RISC. Кроме того, благодаря своей незначительно измененной структуре 5'-(Е)-винилфосфонат способен стабилизировать 5'-концевой нуклеотид, защищая его от дефосфорилирования ферментами, такими как фосфатазы.
Один аспект настоящего изобретения представляет собой нуклеиновую кислоту, раскрытую в настоящей заявке, для ингибирования экспрессии гена-мишени в клетке, содержащую по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, причем указанная первая цепь содержит модифицированные нуклеотиды или немодифицированные нуклеотиды во множестве положений для облегчения процессинга нуклеиновой кислоты под действием RISC.
Согласно одному аспекту «облегчает процессинг под действием RISC» означает, что нуклеиновая кислота может подвергаться процессингу под действием RISC, например, любая присутствующая модификация делает возможным процессинг нуклеиновой кислоты под действием RISC приемлемо таким образом, чтобы могла реализовываться активность миРНК.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, а нуклеотид на второй цепи, который соответствует положению 13 первой цепи, не модифицирован с применением 2'-O-метильной модификации.
Нуклеотид на второй цепи, который «соответствует» положению на первой цепи, приемлемо, является нуклеотидом, который спаривается с указанным нуклеотидом на первой цепи.
Согласно одному аспекту нуклеотид на второй цепи, который соответствует положению 13 первой цепи, представляет собой нуклеотид, который образует пару оснований с положением 13 первой цепи.
Согласно одному аспекту нуклеотид на второй цепи, который соответствует положению 11 первой цепи, представляет собой нуклеотид, который образует пару оснований с положением 11 первой цепи.
Согласно одному аспекту нуклеотид на второй цепи, который соответствует положению 12 первой цепи, представляет собой нуклеотид, который образует пару оснований с положением 12 первой цепи.
Эту номенклатуру можно применять к другим положениям второй цепи. Например, в 19-членной нуклеиновой кислоте, которая является двухцепочечной и имеет тупые концы, положение 13 первой цепи будет спариваться с положением 7 второй цепи. Положение 11 первой цепи будет спариваться с положением 9 второй цепи. Эту номенклатуру можно применять к другим положениям второй цепи.
Нуклеотид, который соответствует положению 13 первой цепи, приемлемо, представляет собой положение 13 второй цепи, при отсчете от 3'-второй цепи, начиная с первого нуклеотид а двухцепочечной области. Аналогичным образом, положение 11 второй цепи, приемлемо, представляет собой 11 нуклеотид с 3'-второй цепи, начиная с первого нуклеотида двухцепочечной области. Эту номенклатуру можно применять к другим положениям второй цепи.
Согласно одному аспекту, в случае частичной комплементарности первой и второй цепей, нуклеотид на второй цепи, который «соответствует» положению на первой цепи, необязательно может образовывать пару оснований, если это положение представляет собой положение, в котором присутствует несоответствие, однако принцип номенклатуры все еще применим.
Предпочтительной является первая и вторая цепи, которые полностью комплементарны на протяжении дуплексной области (не учитывая любые выступающие области), и в двухцепочечной области нуклеиновой кислоты отсутствуют несоответствия.
Также предпочтительными являются:
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, а нуклеотид на второй цепи, который соответствует положению 11 первой цепи, не модифицирован с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, а нуклеотиды на второй цепи, которые соответствуют положениям 11 и 13 первой цепи, не модифицированы с применением 2'-O-метильной модификации.
Согласно одному аспекту нуклеотид на второй цепи, который соответствует положению 12 первой цепи, не модифицирован с применением 2'-O-метильной модификации. Это ограничение на нуклеиновой кислоте может наблюдаться с любым другим ограничением, описанным в настоящей заявке.
Таким образом, другим аспектом настоящего изобретения является нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, а нуклеотиды на второй цепи, которые соответствуют положению 11-13 первой цепи, не модифицированы с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, а нуклеотиды на второй цепи, которые соответствуют положению 11 или 13, или 11 и 13, или 11-13 первой цепи, модифицированы с применением 2'-фтор-модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи модифицированы с применением 2'-фтор-модификации, а нуклеотиды на второй цепи, которые соответствуют положениям 11 или 13, или 11 и 13, или 11-13 первой цепи, не модифицированы с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи модифицированы с применением 2'-фтор-модификации, а нуклеотиды на второй цепи, которые соответствуют положениям 11 или 13, или 11 и 13, или 11-13 первой цепи, модифицированы с применением 2'-фтор-модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой более 50% нуклеотидов первой и/или второй цепей содержат 2'-O-метильную модификацию, например, более 55%, 60%, 65%, 70%, 75%, 80% или 85% или более первой и/или второй цепей содержат 2'-O-метильную модификацию, предпочтительно как измерено в процентах от общего количества нуклеотидов в обеих первой и второй цепях.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой более 50% нуклеотидов первой и/или второй цепей содержат природную модификацию РНК, например, в которой более 55%, 60%, 65%, 70%, 75%, 80% или 85% или более первой и/или второй цепей содержат такую модификацию, предпочтительно как измерено в процентах от общего количества нуклеотидов обеих первой и второй цепей. Подходящие природные модификации включают, наряду с 2-O'-метилом, другие 2'-модификации сахара, в частности, 2'-Н-модификацию, приводящую к получению ДНК-нуклеотида.
Нуклеиновая кислота, раскрытая в настоящей заявке, содержащая не более 20%, например, не более 15%, например, более 10%, нуклеотидов, которые имеют 2'-модификации, которые не являются 2'-O-метильными модификациями, на первой и/или второй цепях, предпочтительно как измерено в процентах от общего количества нуклеотидов обеих первой и второй цепей.
Нуклеиновая кислота, раскрытая в настоящей заявке, содержащая не более 20% (например, не более 15% или не более 10%) 2'-фтор-модификаций на первой и/или второй цепях, предпочтительно как измерено в процентах от общего количества нуклеотидов обеих цепей.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой все нуклеотиды модифицированы с применением 2'-O-метильной модификации, за исключением положений 2 и 14 с 5'-конца первой цепи и нуклеотидов на второй цепи, которые соответствуют положению 11 или 13, или 11 и 13, или 11-13 первой цепи.
Предпочтительно нуклеотиды, которые не модифицированы с применением 2'-O-метила, модифицированы с применением фтора в положении 2'.
Предпочтительной является нуклеиновая кислота, раскрытая в настоящей заявке, в которой все нуклеотиды нуклеиновой кислоты модифицированы в 2'-положении сахара. Предпочтительно эти нуклеотиды модифицированы с применением 2'-фтор-модификации, причем указанная модификация не является 2'-O-метильной модификацией.
Нуклеиновые кислоты согласно настоящему изобретению могут содержать один или более нуклеотидов, модифицированных в 2'-положении с применением 2'-Н, и, следовательно, содержащие ДНК-нуклеотид внутри нуклеиновой кислоты. Нуклеиновые кислоты согласно настоящему изобретению могут содержать ДНК -нуклеотиды в положениях 2 и/или 14 первой цепи, при отсчете от 5'-конца первой цепи. Нуклеиновые кислоты могут содержать ДНК-нуклеотиды на второй цепи, которые соответствуют положению 11 или 13, или 11 и 13, или 11-13 первой цепи.
Согласно одному аспекту присутствует не более одной ДНК на нуклеиновую кислоту согласно настоящему изобретению.
Нуклеиновые кислоты согласно настоящему изобретению могут содержать один или более LNA-нуклеотидов. Нуклеиновые кислоты согласно настоящему изобретению могут содержать LNA-нуклеотиды в положениях 2 и/или 14 первой цепи, при отсчете от 5'-конца первой цепи. Нуклеиновые кислоты могут содержать LNA на второй цепи, которые соответствуют положению 11 или 13, или 11 и 13, или 11-13 первой цепи.
Согласно одному аспекту нуклеиновая кислота модифицирована на первой цепи с применением чередующихся 2-O-метильных модификаций и 2-фтор-модификаций, и положения 2 и 14 (начиная с 5'-конца) модифицированы с применением 2'-фтор. Предпочтительно вторая цепь модифицирована с применением 2'-фтор-модификаций в нуклеотидах на второй цепи, которые соответствуют положению 11 или 13, или 11 и 13, или 11-13 первой цепи. Предпочтительно вторая цепь модифицирована с применением 2'-фтор-модификаций в положениях 11-13, при отсчете от 3'-конца, начиная с первого положения комплементарной (двухцепочечной) области, а остальные модификации представляют собой природные модификации, предпочтительно 2'-O-метил.
Согласно одному аспекту нуклеиновые кислоты согласно настоящему изобретению содержат один или более инвертированных рибонуклеотидов, предпочтительно инвертированный аденин, с применением 5'-5'-связи или 3'-3'-связи, предпочтительно 3'-3'-связи на 3'-конце второй цепи.
Согласно одному аспекту нуклеиновая кислота содержит одну или более фосфодитиоатных связей, таких как 1, 2, 3 или 4 фосфодитиоатные связи. Предпочтительно присутствует до 4 фосфодитиоатных связей, по одной на 5' и 3'-концах первой и второй цепей.
Все признаки нуклеиновых кислот могут быть объединены со всеми другими аспектами настоящего изобретения, раскрытыми в настоящей заявке.
В частности, предпочтительными являются нуклеиновые кислоты, которые представляют собой молекулы миРНК, в которых нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, и нуклеиновая кислота содержит одно или более или все из:
(i) инвертированного нуклеотида, предпочтительно 3'-3'-связь на 3'-конце второй цепи;
(ii) одной или более фосфодитиоатных связей;
(iii) нуклеотид второй цепи, соответствующий положению 11 или 13 первой цепи, не модифицирован с применением 2'-O-метильной модификации, при этом предпочтительно одно или оба из этих положений содержат 2'-фтор-модификацию;
(iv) нуклеиновая кислота содержит по меньшей мере 80% от всех нуклеотидов, содержащих 2'-O-метильную модификацию;
(v) нуклеиновая кислота содержит не более 20% нуклеотидов, которые содержат 2'-фтор-модификации.
Согласно настоящему изобретению также предложена нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи и нуклеотиды в положениях 7 и/или 9 или 7-9 с 5'-конца второй цепи модифицированы с применением 2'-фтор-модификации, и по меньшей мере 90% оставшихся нуклеотидов являются 2'-O-метил-модифицированными или содержат другую природную 2'-модификацию.
Конкретными предпочтительными примерами для 19-членной двухцепочечной нуклеиновой кислоты с тупыми концами и без липкого конца, являются:
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, и нуклеотид в положении 7 с 5'-конца второй цепи не модифицирован с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, и нуклеотид в положении 9 с 5'-конца второй цепи не модифицирован с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, и нуклеотиды в положениях 7 и 9 с 5'-конца второй цепи не модифицированы с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, и нуклеотиды в положениях 7-9 с 5'-конца второй цепи не модифицированы с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи не модифицированы с применением 2'-O-метильной модификации, и нуклеотиды в положениях 7 и/или 9, или 7-9 с 5'-конца второй цепи модифицированы с применением 2'-фтор-модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи модифицированы с применением 2'-фтор-модификации, и нуклеотиды в положениях 7 и/или 9, или 7-9 с 5'-конца второй цепи не модифицированы с применением 2'-O-метильной модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи модифицированы с применением 2'-фтор-модификации, и нуклеотиды в положениях 7 и/или 9, или 7-9 с 5'-конца второй цепи модифицированы с применением 2'-фтор-модификации.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой более 50% нуклеотидов первой и/или второй цепей содержат 2'-O-метильную модификацию, например, более 55%, 60%, 65%, 70%, 75%, 80% или 85% или более первой и/или второй цепей содержат 2'-O-метильную модификацию, предпочтительно как измерено в процентах от общего количества нуклеотидов обеих первой и второй цепей.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой более 50% нуклеотидов первой и/или второй цепей содержат природную модификацию РНК, например, более 55%, 60%, 65%, 70%, 75%, 80% или 85% или более первой и/или второй цепей содержат такую модификацию, предпочтительно как измерено в процентах от общего количества нуклеотидов обеих первой и второй цепей. Подходящие природные модификации включают, наряду с 2-O'-метилом, другие 2'-модификации сахара, в частности, 2'-Н-модификацию, приводящую к получению ДНК-нуклеотида.
Нуклеиновая кислота, раскрытая в настоящей заявке, содержащая не более 20%, например, не более 15%, например, более 10%, нуклеотидов, которые содержат 2'-модификации, которые не являются 2'-O-метильными модификациями, на первой и/или второй цепях, предпочтительно как измерено в процентах от общего количества нуклеотидов обеих первой и второй цепей.
Нуклеиновая кислота, раскрытая в настоящей заявке, содержащая не более 20% (например, не более 15% или не более 10%) 2'-фтор-модификаций на первой и/или второй цепях, предпочтительно как измерено в процентах от общего количества нуклеотидов обеих цепей.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой все нуклеотиды модифицированы с применением 2'-O-метильной модификации, за исключением положений 2 и 14 с 5'-конца первой цепи и нуклеотидов в положениях 7 и/или 9 с 5'-конца второй цепи. Предпочтительно нуклеотиды, которые не модифицированы с применением 2'-O-метила, модифицированы с применением фтора в положении 2'.
Нуклеиновая кислота, раскрытая в настоящей заявке, в которой все нуклеотиды модифицированы с применением 2'-O-метильной модификации, за исключением положений 2 и 14 с 5'-конца первой цепи и нуклеотидов в положениях 7-9 с 5'-конца второй цепи. Предпочтительно нуклеотиды, которые не модифицированы с применением 2'-O-метила, модифицированы с применением фтора в положении 2'.
Для нуклеиновой кислоты, содержащей дуплексную область из 20 пар оснований, вторая цепь предпочтительно не содержит 2'-O-метильную группу в нуклеотидах 8 или 9, или 10, при отсчете от 5'-конца дуплекса, соответствующих положениям 13, 12 и 11 первой цепи, соответственно.
Для нуклеиновой кислоты, содержащей дуплексную область из 21 пары оснований, вторая цепь предпочтительно не содержит 2'-O-метильную группу в нуклеотидах 9 или 10, или 11, при отсчете от 5'-конца дуплекса, соответствующих положениям 13, 12 и 11 первой цепи, соответственно.
Настоящее изобретение также относится к немодифицированным последовательностям всех модифицированных последовательностей, раскрытых в настоящей заявке.
Настоящее изобретение будет далее описано со ссылкой на следующие неограничивающие чертежи и примеры, на которых:
На Фигуре 1 показаны результаты анализа стабильности в сыворотке конъюгатов GalNAc-миРНК, содержащих два фосфотиоата (PS), один PS, два фосфодитиоата (PS2) и один PS2 в концевых положениях;
На Фигуре 2 показаны результаты анализа стабильности в сыворотке конъюгатов GalNAc-миРНК, содержащих два PS, один PS, два PS2 и один PS2 в концевых положениях, но без PS в группе GalNAc;
На Фигуре 3 показаны результаты анализа стабильности в сыворотке конъюгатов GalNAc-миРНК, содержащих один PS2 на отдельных концах;
На Фигуре 4 показана активность конъюгатов GalNAc-миРНК, содержащих один PS2 на отдельных концах;
На Фигуре 5 показаны результаты анализа стабильности в сыворотке конъюгата GalNAc-миРНК, содержащего любой один PS2 на 5'-конце второй цепи и на 3'-конце второй цепи, но без PS в линкерной группе;
На Фигуре 6 показана активность конъюгата GalNAc-миРНК, содержащего любой один PS2 на 5'-конце второй цепи и на 3'-конце второй цепи, но без PS в группе GalNAc;
На Фигуре 7 показаны последовательности конъюгата миРНК, содержащие PS2 на разных концах миРНК вместе с группами GalNAc без внутреннего PS;
На Фигуре 8 показана стабильность в сыворотке конъюгатов GalNAc миРНК с PS2 на разных концах миРНК вместе с группами GalNAc без внутреннего PS;
На Фигуре 9 показана активность в условиях in vitro конъюгатов GalNAc миРНК с PS2 на разных концах миРНК вместе с группами GalNAc без внутреннего PS;
На Фигуре 10 показана блок-схема синтеза олигонуклеотидов, конъюгированных с древовидным трехвалентным GalNAc, содержащих фосфодитиоатную связь;
На Фигуре 11 показана блок-схема синтеза других олигонуклеотидов, конъюгированных с древовидным трехвалентным GalNAc, содержащих фосфодитиоатную связь;
На Фигуре 12 показана активность конъюгатов GalNAc миРНК с PS2 на разных концах миРНК, направленная на уменьшение мРНК, в условиях in vivo;
На Фигуре 13 показана активность конъюгатов GalNAc миРНК с PS2 на разных концах миРНК, направленная на снижение уровня железа в сыворотке, в условиях in vivo;
На Фигуре 14 показана активность конъюгатов GalNAc миРНК с PS2 и PS на разных концах миРНК вместе с группами GalNAc с внутренним PS или без него в условиях in vitro.
На Фигуре 15 показана активность конъюгатов миРНК, содержащих любой один GalNAc, соединенный с серинолом, на 5' и 3' конце второй цепи и с концевыми фосфодитиоатами.
На Фигуре 16 схематически представлены различные варианты реализации нуклеиновых кислот, конъюгированных с лигандами за счет линкеров.
Примеры
Пример 1
Общие процедуры
Модификация миРНК: синтез миРНК с фосфотиоатными (PS) или фосфодитиоатными связями (PS2).
Примерные соединения синтезировали в соответствии со способами, описанными ниже, и способами, известными специалисту в данной области техники. Сборку олигонуклеотидной цепи и линкерных строительных блоков выполняли с помощью твердофазного синтеза с применением фосфоамидитной методологии.
Синтез, удаление защитных групп и очистку олигонуклеотидов проводили в соответствии со стандартными процедурами, известными в данной области техники.
Все олигонуклеотиды синтезировали на синтезаторе АКТА oligopilot с применением стандартных фосфоамидитных реакций. Коммерчески доступную твердую подложку и 2'-O-метил-РНК-фосфоамидиты, 2'-фтор, 2'-дезокси-РНК-фосфоамидиты (все со стандартной защитой) и тиофосфоамидиты (AM Biotech, GlenResearch) применяли в соответствии с процедурами, рекомендованными производителями.
Синтез фосфоамидитных производных ST41 (ST41-phos), а также ST23 (ST23-phos) может быть выполнен, как описано в WO2017/174657:
ST41-phos:
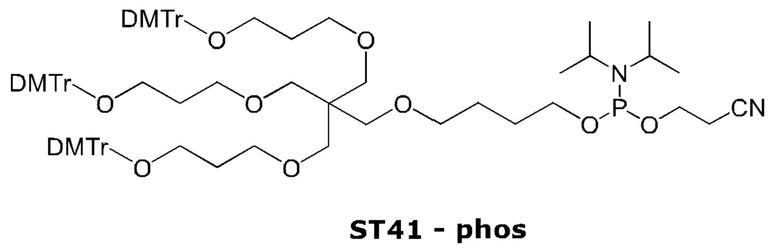
ST23-phos:
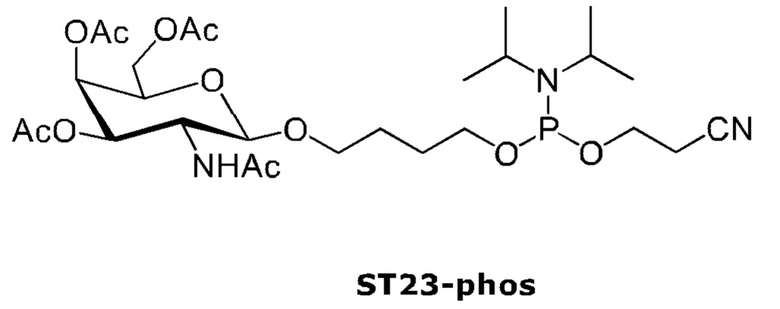
Вспомогательные реагенты приобретали у EMP Biotech. Синтез выполняли с применением 0,1 М раствора фосфоамидита в сухом ацетонитриле и в качестве активатора применяли бензилтиотетразол (БТТ) (0,3 М в ацетонитриле). Время связывания составляло 15 мин. Применяли цикл Сар/ОХ/Сар или Cap/Thio/Cap (Cap: Ac2O/'NMI/лутидин/ацетонитрил, окислитель: 0,1 М I2 в пиридине/Н2О). Фосфотиоаты и фосфодитиоаты вводили с применением 50 мМ EDITH в ацетонитриле. Все остальные реагенты и растворители были доступны коммерчески и использовались при стандартном качестве реагентов.
Отщепление DMT осуществляли с помощью обработки 3% дихлоруксусной кислотой в толуоле. После завершения запрограммированных циклов синтеза выполняли промывку диэтиламином (DEA). Все олигонуклеотиды синтезировали в режиме DMT-off.
Одиночные цепи отщепляли от CPG с помощью обработки 40% водн. метиламином. Полученный неочищенный олигонуклеотид очищали с помощью ионообменной хроматографии (Resource Q, 6 мл, GE Healthcare) на системе для ВЭЖХ АКТА Pure с применением градиента хлорида натрия. Содержащие продукт фракции объединяли, обессоливали на колонке для гель-проникающей хроматографии (Zetadex, EMP Biotech) и лиофилизировали.
Синтез олигонуклеотидов
Все одноцепочечные олигонуклеотиды синтезировали в соответствии с условиями реакции, описанными выше и на Фигуре 10.
Все готовые одноцепочечные продукты анализировали с помощью АХ-ВЭЖХ для подтверждения их чистоты. Чистота представлена в % FLP (% полноразмерного продукта), который представляет собой процент УФ-площади под сигналом заданного продукта на УФ-кривой анализа готового продукта методом АХ-ВЭЖХ. Идентичность соответствующих одноцепочечных продуктов (немодифицированных, амино-модифицированных предшественников или GalNAc-конъюгированных олигонуклеотидов) подтверждали с помощью анализа методом ЖХ/МС.
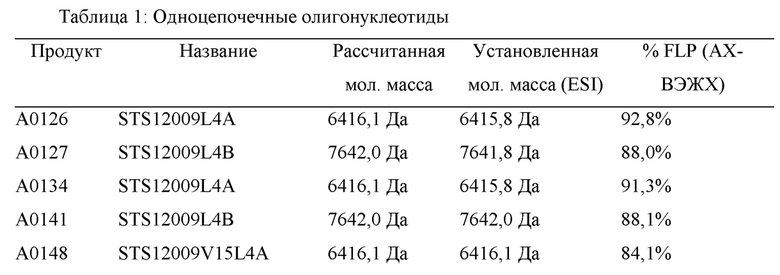

Образование двойной цепи
Отдельные одиночные цепи растворяли в концентрации 60 OD/мл в Н2О. Оба раствора отдельных олигонуклеотидов добавляли вместе в реакционный сосуд. Для более легкого мониторинга реакции выполняли титрование. Первую цепь добавляли с 25% избытком по сравнению со второй цепью, что определяли по УФ-поглощению при 260 нм. Реакционную смесь нагревали до 80°С в течение 5 минут и затем медленно охлаждали до комнатной температуры. Образование двойной цепи контролировали по образованию ионных пар методом ВЭЖХ с обращенной фазой. На основании УФ-площади остаточной одиночной цепи рассчитывали необходимое количество второй цепи и добавляли его к реакционной смеси. Реакционную смесь снова нагревали до 80°С и медленно охлаждали до комнатной температуры. Эту процедуру повторяли до тех пор, пока не было обнаружено менее 10% остаточной одиночной цепи.
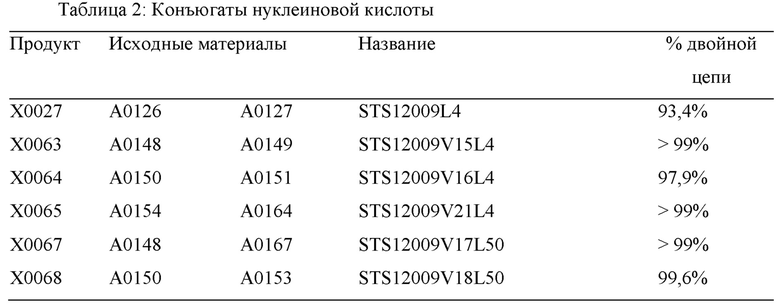
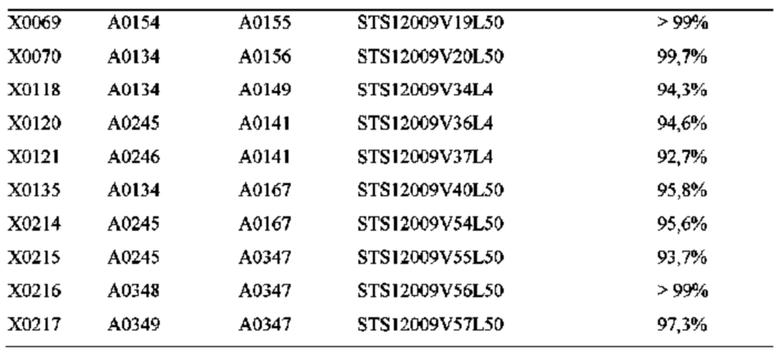
Пример 2
Анализ стабильности в сыворотке конъюгатов GalNAc-миРНК, содержащих два PS (STS12009L4), один PS (STS12009V21L4), два PS2 (STS12009V16L4) и один PS2 (STS12009V15L4) в концевых положениях. GalNAc конъюгировали с 5'-концом второй цепи и стабилизировали внутри с помощью четырех PS. Фосфотиоаты и фосфодитиоаты, соответственно, помещали на 5'-конце первой цепи, 3'-конце первой цепи и 3'-конце второй цепи. 5 мкМ конъюгатов GalNAc-миРНК инкубировали с 50% фетальной бычьей сывороткой (ФБС) в течение 3 дней при 37°С. РНК экстрагировали и анализировали на 20% ТВЕ полиакриламидных гелях, и результаты показаны на Фигуре 1. «UT» обозначает необработанные образцы, «FBS» обозначает обработку ФБС. «Контроль» обозначает менее стабилизированный конъюгат GalNAc-миРНК с другой последовательностью.
Последовательности приведены в таблице 3.

Таблица 3: конъюгаты GalNAc-миРНК, содержащие два PS, один PS, два PS2 и один PS2 на всех неконъюгированных концах.
Пример 3
Анализ стабильности в сыворотке конъюгатов GalNAc-миРНК, содержащих два PS (STS12009L4, STS12009V20L50), один PS (STS12009V19L50), два PS2 (STS12009V18L50) и один PS2 (STS12009V17L50) в концевых положениях. В вариантах -V20, -V19, -V18 и -V17 GalNAc был конъюгирован с 5'-концом второй цепи и не содержит какой-либо PS. Фосфотиоаты и фосфодитиоаты, соответственно, помещали на 5'-конце первой цепи, 3'-конце первой цепи, 5'-конце второй цепи и 3'-конце второй цепи. STS12009L4 содержит два любых концевых PS на 5'-конце первой цепи, 3'-конце первой цепи и 3'-конце второй цепи, тогда как GalNAc присоединен к 5'-концу второй цепи и стабилизирован с помощью четырех внутренних PS. 5 мкМ конъюгатов GalNAc-миРНК инкубировали с 50% ФБС в течение 3 дней при 37°С. РНК экстрагировали и анализировали на 20% ТВЕ полиакриламидных гелях. Результаты показаны на Фигуре 2. «UT» обозначает необработанные образцы, «ФБС» обозначает обработку ФБС.
Последовательности приведены в таблице 4.

Таблица 4: конъюгаты GalNAc-миРНК, содержащие два PS, один PS, два PS2 и один PS2 в концевых положениях.
Пример 4
Анализ стабильности в сыворотке конъюгатов GalNAc-миРНК, содержащих один PS2 на отдельных концах. GalNAc конъюгировали с 5'-концом второй цепи и стабилизировали внутри с помощью четырех PS. Фосфодитиоатные модификации помещали на 5'-конце первой цепи (STS12009V37L4), 3'-конце первой цепи (STS12009V36L4) и 3'-конце второй цепи (STS12009V34L4). Все остальные неконъюгированные концы стабилизировали двумя любыми концевыми PS. STS12009L4 содержит два концевых PS на 5'-конце первой цепи, 3'-конце первой цепи и 3'-конце второй цепи. 5 мкМ конъюгатов GalNAc-миРНК инкубировали с 50% ФБС в течение 3 дней при 37°С. РНК экстрагировали и анализировали на 20% ТВЕ полиакриламидных гелях. Результаты показаны на Фигуре 3. «UT» обозначает необработанные образцы, «ФБС» обозначает обработку ФБС. «Контроль» обозначает менее стабилизированный конъюгат GalNAc-миРНК с другой последовательностью. Последовательности приведены в таблице 5.

Таблица 5: конъюгаты GalNAc-миРНК, содержащие один PS2 на отдельных концах.
Пример 5
Активность конъюгатов GalNAc-миРНК, содержащих один PS2 на отдельных концах. GalNAc конъюгировали с 5'-концом второй цепи и стабилизировали внутри с помощью четырех PS. Фосфодитиоатные модификации помещали на 5'-конце первой цепи (STS12009V37L4), 3'-конце первой цепи (STS12009V36L4) и 3'-конце второй цепи (STS12009V34L4). Все остальные неконъюгированные концы стабилизировали двумя любыми концевыми PS. STS12009L4 содержит два любых концевых PS на 5'-конце первой цепи, 3'-конце первой цепи и 3'-конце второй цепи. Эксперимент проводили на первичных гепатоцитах мыши. Клетки высевали при плотности 250000 клеток на 6-луночный планшет и обрабатывали с применением 100 нМ, 10 нМ и 1 нМ GalNAc-миРНК. Трансфекции с применением 10 нМ GalNAc-миРНК и 1 мкг/мл Atufect использовали в качестве контроля. Клетки лизировали через 24 часа, экстрагировали общую РНК и определяли уровни мРНК Tmprss6 и Pten с помощью количественной ПЦР (R) в режиме реального времени TaqMan®. Результаты показаны на Фигуре 4. Каждый столбик представляет среднее значение ± стандартное отклонение трех технических повторов. Последовательности представлены в таблице 5.
Пример 6
Анализ стабильности в сыворотке конъюгата GalNAc-миРНК (STS12009V40L50), содержащего любой один PS2 на 5'-конце второй цепи и на 3'-конце второй цепи. GalNAc конъюгировали с 5'-концом второй цепи и не стабилизировали каким-либо внутренним PS. STS12009L4 содержит два любых концевых PS на 5'-конце первой цепи, 3'-конце первой цепи и 3'-конце второй цепи, GalNAc присоединен к 5'-концу второй цепи и стабилизирован с помощью четырех внутренних PS. 5 мкМ конъюгатов GalNAc-миРНК инкубировали с 50% ФБС в течение 3 дней при 37°С. РНК экстрагировали и анализировали на 20% ТВЕ полиакриламидных гелях. Результаты показаны на Фигуре 5. «UT» обозначает необработанные образцы, «ФБС» обозначает обработку ФБС.
Последовательности приведены в таблице 6

Таблица 6: конъюгат GalNAc-миРНК (STS12009V40L50), содержащий любой один PS2 на 5'-конце второй и на 3'-конце второй цепи, в комбинации с не содержащим PS GalNAc-линкером.
Пример 7
Активность конъюгата GalNAc-миРНК (STS12009V40L50), содержащего любой один PS2 на 5'-конце второй цепи и на 3'-конце второй цепи. GalNAc был конъюгирован с 5'-концом второй цепи и не стабилизирован каким-либо внутренним PS. STS12009L4 содержит два любых концевых PS на 5'-конце первой цепи, 3'-конце первой цепи и 3'-конце второй цепи. В данном случае GalNAc присоединен к 5'-концу второй цепи и стабилизирован с помощью четырех внутренних PS. Эксперимент проводили на первичных гепатоцитах мыши. Клетки высевали при плотности 250000 клеток на 6-
луночный планшет и обрабатывали с применением 100 нМ, 10 нМ и 1 нМ GalNAc-миРНК. В качестве контроля использовали GalNAc-конъюгат миРНК против люциферазы (GalNAc-Luc). Клетки лизировали через 24 часа, экстрагировали общую РНК и определяли уровни мРНК Tmprss6 и Pten с помощью кПЦР в режиме реального времени TaqMan®. Результаты показаны на Фигуре 6. Каждый столбик представляет среднее значение ± стандартное отклонение трех технических повторов. Последовательности представлены в таблице 6.
Пример 8
Анализ стабильности в сыворотке конъюгатов GalNAc-миРНК с фосфотиоатами, фосфодитиоатами и фосфодиэфирами в концевых положениях и в группе GalNAc. GalNAc был конъюгирован с 5'-концом смысловой цепи и стабилизирован внутри с помощью четырех PS (STS12009L4) или вместо них применяли фосфодиэфирные связи (STS12009V54L50 - V57L50). Фосфодитиоатные модификации помещали во всех концевых положениях дуплекса, кроме 5'-конца первой цепи (-V54L50), только на 3'-концах (-V55L50, -V57L50) или только на 3'-конце второй цепи (-V56L50). В определенных конструкциях фосфодиэфиры применяли в концевых положениях дуплекса миРНК (-V56L50, -V57L50).
5 мкМ конъюгатов GalNAc-миРНК инкубировали с 50% ФБС в течение 3 дней при 37°С. РНК экстрагировали и анализировали на 20% ТВЕ полиакриламидных гелях. «UT» обозначает необработанные образцы, «ФБС» обозначает обработку ФБС. «Контроль» обозначает менее стабилизированный конъюгат GalNAc-миРНК с другой последовательностью.
Последовательности показаны на Фигуре 7, а результаты показаны на Фигуре 8.
Пример 9
GalNAc-конъюгаты миРНК, нацеленные на Tmprss6 и содержащие различные концевые стабилизирующие химические структуры (фосфотиоат, фосфодитиоат, фосфодиэфир), тестировали с помощью опосредуемого рецептором поглощения в первичных гепатоцитах мыши. GalNAc конъюгировали с 5'-концом второй цепи и стабилизировали внутри с помощью четырех PS (STS12009L4) или вместо них применяли фосфодиэфирные связи (STS12009V54L50 - V57L50). Фосфодитиоатные модификации помещали во всех концевых положениях дуплекса, кроме 5'-конца первой цепи (-V54L50), только на 3'-концах (-V55L50, -V57L50) или только на 3'-конце второй цепи (-V56L50). В определенных конструкциях фосфодиэфиры применяли в концевых положениях дуплекса миРНК (-V56L50, -V57L50).
Эксперимент проводили на первичных гепатоцитах мыши. Клетки высевали при плотности 20000 клеток на 96-луночный планшет и обрабатывали с применением от 125 нМ до 0,2 нМ GalNAc-миРНК. Клетки лизировали через 24 часа, экстрагировали общую РНК и определяли уровни мРНК Tmprss6 и Pten с помощью кПЦР в режиме реального времени TaqMan®. Каждый столбик представляет среднее значение ± стандартное отклонение трех технических повторов.
Последовательности показаны на Фигуре 7, а результаты показаны на Фигуре 9.
Пример 10
GalNAc-конъюгаты, нацеленные на TMPRSS6 и содержащие фосфодитиоатные связи на одном или более концах, эффективно снижают уровни железа в сыворотке и мРНК TMPRSS6 в условиях in vivo.
STS12009L4 и STS12009V34L4 содержат группу GalNAc, которая стабилизирована внутри с помощью четырех фосфотиоатных связей. STS12009V54L50 содержит группу GalNAc без внутренних фосфотиоатов. В STS12009L4 все неконъюгированные концы стабилизированы любыми двумя фосфотиоатами. В STS12009V34L4 одна фосфодитиоатная связь присутствует на 3'-конце второй цепи, тогда как все другие неконъюгированные концы стабилизированы любыми двумя фосфотиоатами. В STS12009V54L50 любой один фосфодитиоат присутствует на 3'-конце первой цепи, на 5'-конце второй цепи и на 3'-конце второй цепи. 5'-конец первой цепи стабилизирован двумя фосфотиоатами. Эти конъюгаты миРНК проявляют дозозависимое уменьшение уровней мРНК TMPRSS6 и уровней железа в сыворотке. Содержащие фосфодитиоат конъюгаты STS12009V34L4 и STS12009V54L50 обладают такой же активностью, как и эталонное соединение, которое не содержит фосфодитиоаты. Следовательно, количество фосфотиоатов может быть уменьшено с десяти (STS12009L4) до восьми (STS12009V34L4) и далее до двух (STS12009V54L50) без ухудшения активности. STS12009V57L50 содержит любую одну фосфодитиоатную связь на 3'-конце первой цепи и на 3'-конце второй цепи. 5'-концы обоих цепей содержат фосфодиэфиры, а линкерная группа не содержит внутренние фосфодиэфиры. Активность этого конъюгата миРНК в условиях in vivo сильно уменьшена.
Самцы мышей C57BL/6 (n=6) получали подкожно 3 мг/кг, 1 мг/кг и 0,3 мг/кг конъюгата GalNAc. Срезы печени готовили через семь дней после обработки, из ткани экстрагировали общую РНК и уровни мРНК TMPRSS6 и PTEN определяли с помощью кПЦР в режиме реального времени TaqMan®. Кроме того, анализировали уровни железа в сыворотке.
Последовательности показаны в таблице 7 ниже, и результаты представлены на Фигурах 12 и 13.
Пример 11
GalNAc-конъюгаты с концевыми фосфодитиоатами активны в условиях in vitro.
GalNAc-конъюгаты миРНК, нацеленные на TMPRSS6 и содержащие различные концевые стабилизирующие химические структуры (фосфотиоат, фосфодитиоат, фосфодиэфир), тестировали с помощью опосредуемого рецептором поглощения в первичных гепатоцитах мыши. Трехантенную группу GalNAc конъюгировали с 5' концом второй цепи и стабилизировали внутри с помощью четырех PS в Х0027, Х0346, Х0347. В этом случае фосфотиоат отсутствует на 5'-конце второй цепи. В Х0214 и Х0345 группа GalNAc не содержит фосфотиоаты, а фосфодитиоат присутствует на 5'-конце второй цепи. В Х0214, Х0345, Х0346 и Х0347 фосфодитиоатные модификации присутствуют на 3'-концах первой и второй цепей. 5'-конец первый цепи либо стабилизирован с помощью двух фосфотиоатов (Х0214, Х0346), либо содержит фосфодиэфирные связи (Х0345, Х0347). Все описанные конъюгаты уменьшают уровни целевой мРНК в условиях in vitro. Х0214 и Х0346 показывают уменьшенную активность по сравнению с Х0345 и Х0347. Это свидетельствует о том, что фосфотиоаты на 5'-конце первой цепи отрицательно влияют на активность миРНК в условиях in vitro.
Эксперимент проводили на первичных гепатоцитах мыши. Клетки высевали при плотности 20000 клеток в 96-луночный планшет и обрабатывали с применением 0,1 нМ, 1 нМ, 10 нМ и 100 нМ GalNAc-миРНК. Клетки лизировали через 24 часа, экстрагировали общую РНК и уровни мРНК TMPRSS6 и PTEN определяли с помощью кПЦР в режиме реального времени TaqMan. Каждый столбик представляет среднее значение ± стандартное отклонение трех технических повторов.
Последовательности показаны в таблице 7 ниже, а данные представлены на Фигуре 14.
Пример 12
Конъюгаты миРНК с любым одним GalNAc, соединенным с серинолом, на 5' и 3' конце второй цепи и с концевыми фосфодитиоатами активны в условиях in vitro.
GalNAc-конъюгированные миРНК, нацеленные на TMPRSS6, тестировали с помощью опосредуемого рецептором поглощения в первичных гепатоцитах мыши. В обоих Х0454 и Х0456 любой один GalNAc, соединенный с серинолом, конъюгировали с 5'- и 3'-концами второй цепи. Оба конъюгата содержат (Е)-винилфосфонат на 5'-конце первой цепи. Фосфотиоаты отсутствуют на 5'-конце первой цепи. В Х0454 любые два фосфотиоата присутствуют на 3'-конце первой цепи и на 5'- и 3'-концах второй цепи. Каждая группа GalNAc содержит один фосфотиоат. В Х0456 любой один фосфодитиоат присутствует между двумя последними нуклеотидами на 3'-конце первой цепи и на 5' и 3'-концах второй цепи. В Х0456 отсутствует какой-либо неопределенный стереогенный центр. GalNAc-конъюгированную миРНК, нацеленную на люциферазу, применяли в качестве ненацеливающего контроля при 125 нМ, и она не снижает уровни целевой мРНК. Конъюгаты, нацеленные на TMPRSS6, оба уменьшают уровни целевой мРНК в условиях in vitro. Следовательно, фосфодитиоаты можно применять для стабилизации концов миРНК с применением одиночных групп GalNAc на обоих концах второй цепи.
Эксперимент проводили на первичных гепатоцитах мыши. Клетки высевали при плотности 20000 клеток на 96-луночный планшет и обрабатывали с применением 0,2 нМ, 1 нМ, 5 нМ, 25 нМ и 125 нМ GalNAc-миРНК. Клетки лизировали через 24 часа, экстрагировали общую РНК и уровни мРНК TMPRSS6 и АСТВ определяли с помощью кПЦР в режиме реального времени TaqMan®. Каждый столбик представляет среднее значение ± стандартное отклонение трех технических повторов.
Последовательности представлены в таблице 7 ниже, а данные представлены Фигуре 15.
Изложение сущности изобретения
1. Нуклеиновая кислота для ингибирования экспрессии гена-мишени в клетке, содержащая по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна указанной первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, при этом указанные первая и/или вторая цепи содержат фосфодитиоатную связь между по меньшей мере двумя нуклеотидами.
2. Нуклеиновая кислота по утверждению 1, в которой указанная первая цепь не содержит фосфодитиоатную связь между любыми из двух, трех или четырех концевых нуклеотидов на 5'-конце.
3. Нуклеиновая кислота по утверждению 1 или 2, содержащая фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 3'-конце первой цепи.
4. Нуклеиновая кислота по утверждениям 1-3, содержащая фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 3'-конце второй цепи.
5. Нуклеиновая кислота по любому из утверждений 1-4, содержащая фосфотиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 5'-конце второй цепи или фосфодитиоатную связь между каждым из двух, трех или четыре концевых нуклеотидов на 5'-конце второй цепи.
6. Нуклеиновая кислота по любому из утверждений 1-5, причем указанная нуклеиновая кислота содержит фосфотиоатную связь между каждым из трех концевых У нуклеотидов и/или между каждым из трех концевых 5' нуклеотидов на первой цепи, и/или между каждым из трех 3' концевых нуклеотидов и/или между каждым из трех 5' нуклеотидов второй цепи, если на этом конце не присутствует фосфодитиоатная связь.
7. Нуклеиновая кислота по любому из утверждений 1-6, в которой указанная первая цепь и указанная вторая цепь представляют собой отдельные цепи.
8. Нуклеиновая кислота по любому из утверждений 1-6, содержащая одну цепь, которая содержит указанную первую цепь и указанную вторую цепь.
9. Нуклеиновая кислота по любому из утверждений 1-8, в которой каждая из указанной первой цепи и/или указанной второй цепи содержит 17-35 нуклеотидов в длину.
10. Нуклеиновая кислота по любому из утверждений 1-9, в которой указанная по меньшей мере одна дуплексная область состоит из 17-25 пар нуклеотидных оснований.
11. Нуклеиновая кислота по любому предшествующему утверждению, которая
a). имеет тупые концы на обоих концах; или
b). имеет липкий конец на одном конце и тупой конец на другом; или
c). имеет липкие концы на обоих концах.
12. Нуклеиновая кислота по любому из предшествующих утверждений, в которой один или более нуклеотидов на указанных первой и/или второй цепях модифицированы с образованием модифицированных нуклеотидов.
13. Нуклеиновая кислота по утверждению 12, в которой один или более из нуклеотидов в нечетных положениях первой цепи являются модифицированными.
14. Нуклеиновая кислота по утверждению 13, в которой один или более из нуклеотидов в четных положениях первой цепи модифицированы с применением по меньшей мере второй модификации, причем указанная по меньшей мере вторая модификация отличается от модификации по утверждению 13.
15. Нуклеиновая кислота по утверждению 14, в которой по меньшей мере один из одного или более модифицированных нуклеотидов в четных положениях является смежным с по меньшей мере с одним из одного или более модифицированных нуклеотидов в нечетных положениях.
16. Нуклеиновая кислота по любому из утверждений 13-15, в которой множество нуклеотидов в нечетных положениях являются модифицированными.
17. Нуклеиновая кислота по любому из утверждений 14-16, в которой множество нуклеотидов в четных положениях модифицированы с применением второй модификации.
18. Нуклеиновая кислота по любому из утверждений 12-17, в которой указанная первая цепь содержит смежные нуклеотиды, которые модифицированы с применением общей модификации.
19. Нуклеиновая кислота по любому из утверждений 13-18, в которой указанная первая цепь содержит смежные нуклеотиды, которые модифицированы с применением второй модификации, которая отличается от модификации по утверждению 13.
20. Нуклеиновая кислота по любому из утверждений 13-19, в которой один или более из нуклеотидов в нечетных положениях второй цепи модифицированы с применением модификации, которая отличается от модификации по утверждению 13.
21. Нуклеиновая кислота по любому из утверждений 13-19, в которой один или более из нуклеотидов в четных положениях второй цепи модифицированы с применением модификации по утверждению 13.
22. Нуклеиновая кислота по утверждению 20 или 21, в которой по меньшей мере один из одного или более модифицированных нуклеотидов в четных положениях второй цепи является смежным с одним или более модифицированными нуклеотидами в нечетных положениях.
23. Нуклеиновая кислота по любому из утверждений 20-22, в которой множество нуклеотидов в нечетных положениях второй цепи модифицированы с применением общей модификации.
24. Нуклеиновая кислота по любому из утверждений 20-23, в которой множество нуклеотидов в четных положениях модифицированы с применением модификации по утверждению 13.
25. Нуклеиновая кислота по любому из утверждений 20-24, в которой множество нуклеотидов в нечетных положениях модифицированы с применением второй модификации, причем указанная вторая модификация отличается от модификации по утверждению 13.
26. Нуклеиновая кислота по любому из утверждений 20-25, в которой указанная вторая цепь содержит смежные нуклеотиды, которые модифицированы с применением общей модификации.
27. Нуклеиновая кислота по любому из утверждений 20-26, в которой указанная вторая цепь содержит смежные нуклеотиды, которые модифицированы с применением второй модификации, которая отличается от модификации по утверждению 13.
28. Нуклеиновая кислота по любому из утверждений 12-27, в которой каждый из нуклеотидов в нечетных положениях в первой цепи и каждый из нуклеотидов в четных положениях во второй цепи модифицирован с применением общей модификации.
29. Нуклеиновая кислота по любому из утверждений 13-28, в которой каждый из нуклеотидов в четных положениях в первой цепи модифицирован с применением второй модификации, а каждый из нуклеотидов в нечетных положениях во второй цепи модифицирован с применением второй модификации.
30. Нуклеиновая кислота по любому из утверждений 20-29, в которой указанные модифицированные нуклеотиды указанной первой цепи сдвинуты по меньшей мере на один нуклеотид относительно указанных немодифицированных или по-разному модифицированных нуклеотидов указанной второй цепи.
31. Нуклеиновая кислота по любому из утверждений 1-30, в которой указанная первая цепь содержит последовательность SEQ ID NO: 1.
32. Нуклеиновая кислота по любому из утверждений 1-30, в которой указанная вторая цепь содержит последовательность SEQ ID NO: 2.
33. Нуклеиновая кислота по любому из утверждений 8-32, в которой указанная модификация и/или модификации по отдельности и независимо выбраны из группы, состоящей из 3'-концевого дезокситимина, 2'-O-метил, 2'-дезокси-модификации, 2'-амино-модификации, 2'-алкил-модификации, морфолино-модификации, модификации фосфоамидатом, модификации 5'-фосфотиоатной группой, модификации 5'-фосфатом или миметиком 5'-фосфата, а также модификации производным холестерина или группой бисдециламида додекановой кислоты.
34. Нуклеиновая кислота по любому из утверждений 8-33, в которой указанная модификация представляет собой любой из закрытого нуклеотида, лишенного азотистого основания нуклеотида или нуклеотида, содержащего неприродное основание.
35. Нуклеиновая кислота по любому из утверждений 8-34, в которой по меньшей мере одна модификация представляет собой 2'-O-метил.
36. Нуклеиновая кислота по любому из утверждений 8-35, в которой по меньшей мере одна модификация представляет собой 2'-F.
38. Нуклеиновая кислота по любому из утверждений 1-37, конъюгированная с лигандом.
39. Нуклеиновая кислота по любому из утверждений 1-38, содержащая фосфотиоатную связь между одним, двумя или тремя концевыми 3' нуклеотидами и/или 5' нуклеотидами указанной первой и/или второй цепей, если на этом конце не присутствует фосфодитиоат.
40. Нуклеиновая кислота для ингибирования экспрессии гена-мишени в клетке, содержащая по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна указанной первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, подлежащего ингибированию, и при этом указанные первая и/или вторая цепи содержат фосфодитиоатную связь между по меньшей мере двумя концевыми 3' нуклеотидами, и/или указанная вторая цепь содержит фосфодитиоатную связь между по меньшей мере двумя концевыми 5' нуклеотидами, и при этом указанная молекула нуклеиновой кислоты конъюгирована с лигандом.
41. Нуклеиновая кислота по любому из утверждений 38-40, в которой указанный лиганд содержит один или более лигандов GalNAc и их производных.
42. Нуклеиновая кислота по любому из утверждений 38-41, в которой указанный лиганд содержит (i) одну или более групп N-ацетилгалактозамина (GalNAc) и их производных, и (ii) линкер, причем с помощью указанного линкера конъюгируют группы GalNAc с последовательностью по любому из предшествующих утверждений.
43. Нуклеиновая кислота по утверждению 40, в которой указанные нуклеотиды модифицированы по любому из предшествующих утверждений.
44. Нуклеиновая кислота по любому предшествующему утверждению, в которой указанный лиганд содержит формулу I:
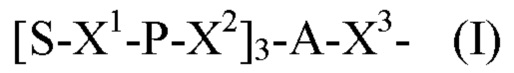
в которой:
S представляет собой сахарид, причем указанный сахарид представляет собой N-ацетилгалактозамин;
X1 представляет собой С3-С6 алкилен или (-СН2-СН2-O)m(-СН2)2-, где m равно 1, 2 или 3;
Р представляет собой фосфат или модифицированный фосфат (предпочтительно тиофосфат);
X2 представляет собой алкилен или простой алкиленовый эфир формулы (-СН2)n-О-СН3-, где n=1-6;
А представляет собой блок разветвления;
X3 представляет собой мостиковый блок;
при этом нуклеиновая кислота в соответствии с настоящим изобретением конъюгирована с X3 за счет фосфата или модифицированного фосфата (предпочтительно тиофосфата).
45. Конъюгированная нуклеиновая кислота, имеющая одну из следующих структур
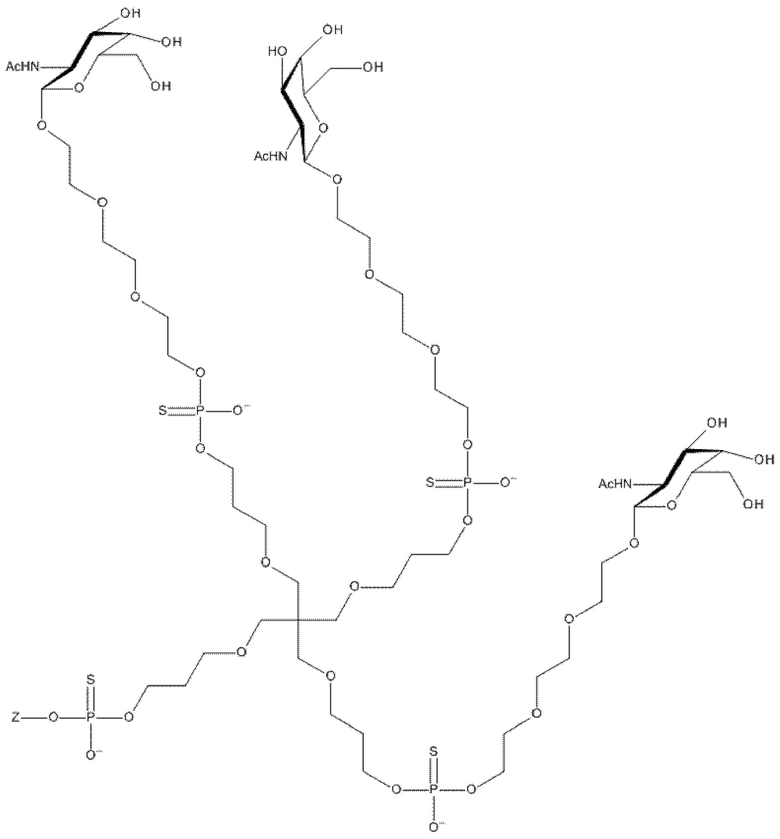
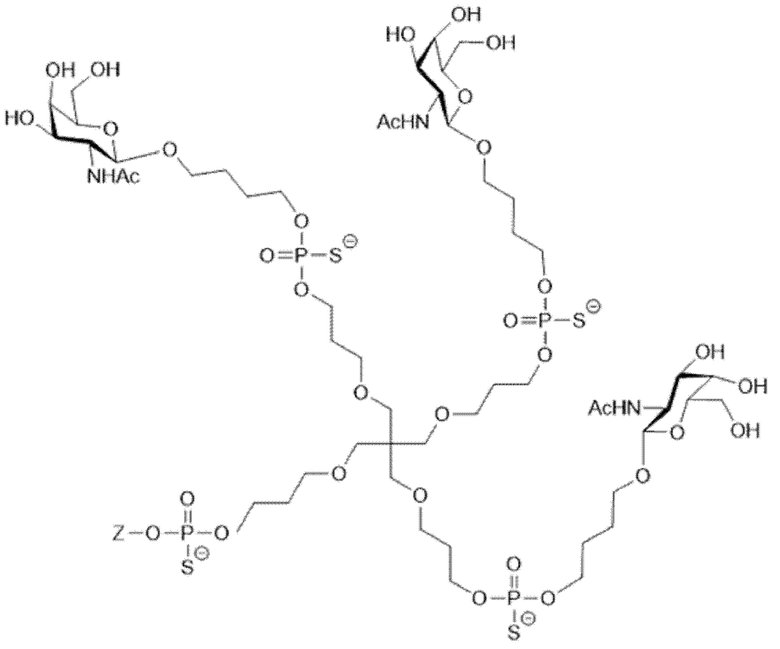
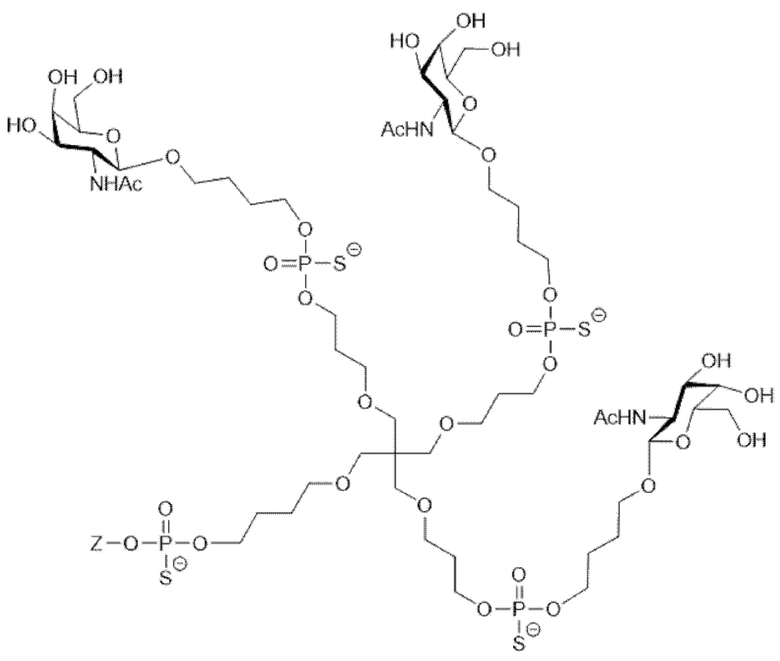
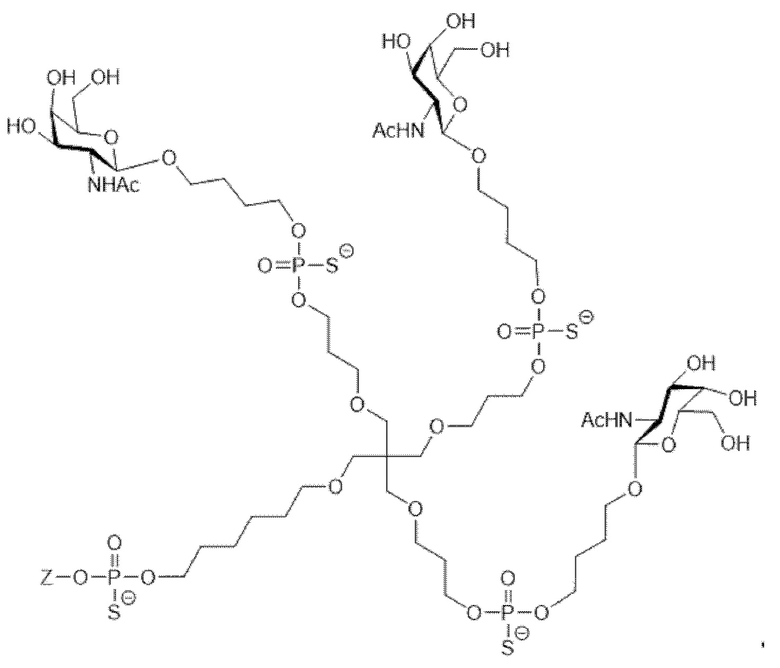
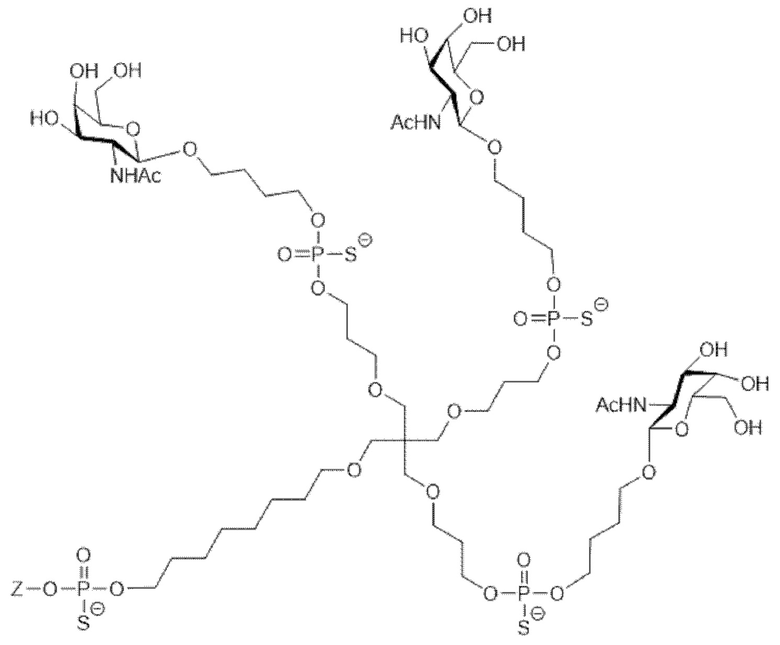
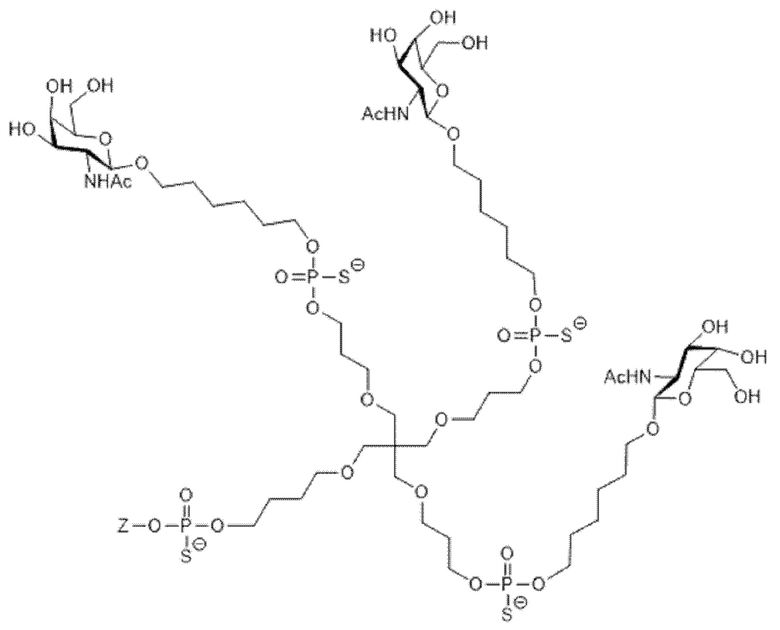
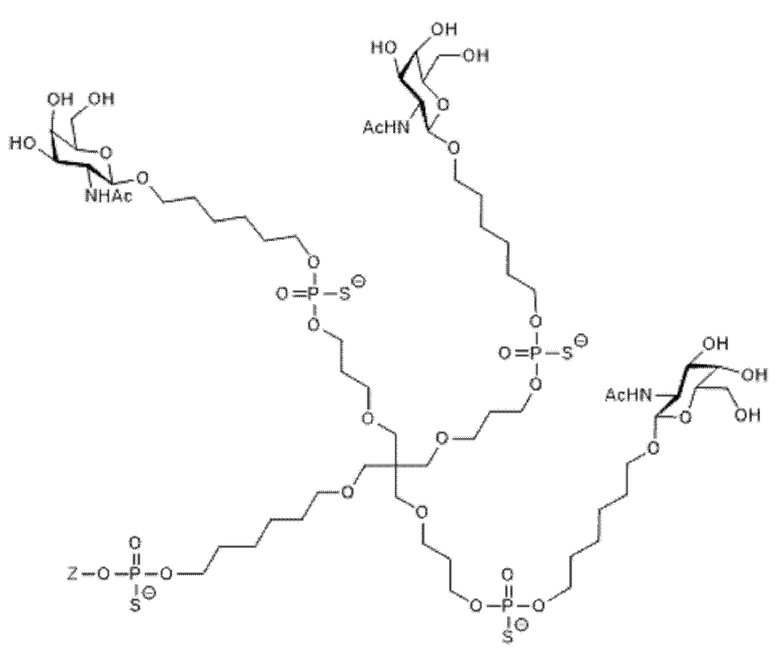
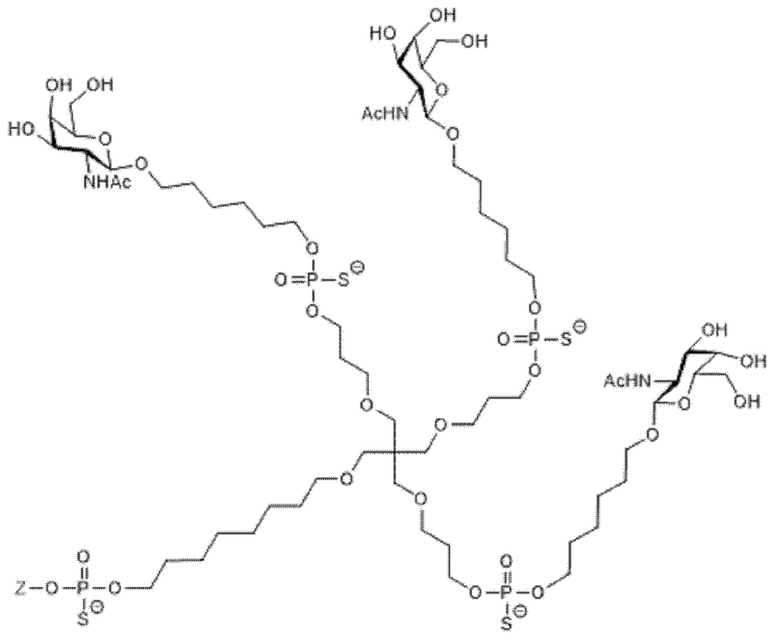
в которых Z представляет собой нуклеиновую кислоту по любому из утверждений 1-39.
46. Нуклеиновая кислота по любому предшествующему утверждению, в которой указанный лиганд содержит:
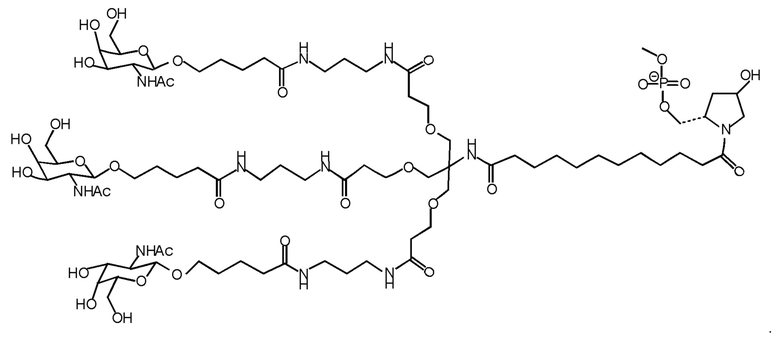
47. Нуклеиновая кислота по любому из утверждений 1-27, 31-32 или 39-43, в которой нуклеотиды в положениях 2 и 14 с 5'-конца первой цепи модифицированы с применением 2'-фтор-модификации, а нуклеотиды на второй цепи, которые соответствуют положению 11 или 13, или 11 и 13, или 11-13 первой цепи, модифицированы с применением 2'-фтор-модификации.
48. Нуклеиновая кислота по любому из утверждений 1-43 или 47, в которой указанная первая цепь РНК представляет собой соединение формулы (XV):
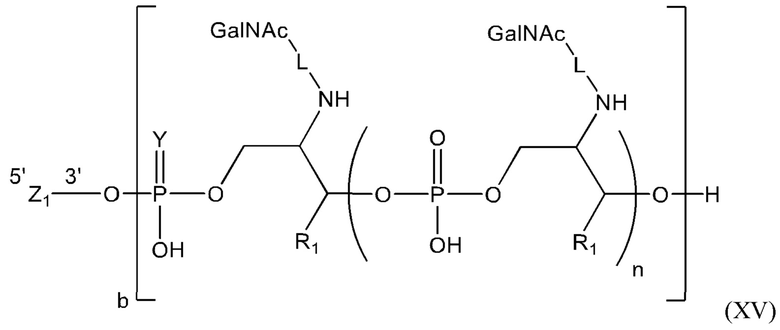
в которой b равно 0 или 1; и
указанная вторая цепь РНК представляет собой соединение формулы (XVI):
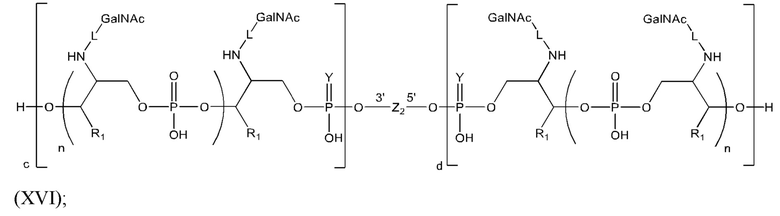
в которой c и d независимо равны 0 или 1;
в которой:
Z1 и Z2 представляют собой части РНК указанных первой и второй цепей РНК, соответственно;
Y представляет собой О или S;
r1 представляет собой Н или метил;
n равно 0, 1, 2 или 3; и
L является одинаковым или различным в формулах (XV) и (XVI) и выбран из группы, состоящей из:
-(CH2)q-, где q=2-12;
-(СН2)r-С(О)-, где r=2-12;
-(CH2-CH2-O)s-CH2-C(O)-, где s=1-5;
-(CH2)t-CO-NH-(CH2)t-NH-C(O)-, где t независимо представляет собой 1-5;
-(CH2)u-CO-NH-(CH2)u-C(O)-, где u независимо представляет собой 1-5; и
-(CH2)v-NH-C(O)-, где v представляет собой 2-12; и
при этом концевой С(O) (если он присутствует) присоединен к группе NH;
и при этом b+с+d равно 2 или 3
49. Нуклеиновая кислота по утверждению 48, в которой b равно 0, с равно 1 и d равно 1.
50. Нуклеиновая кислота по утверждению 48, в которой b равно 1, с равно 0 и d равно 1.
51. Нуклеиновая кислота по утверждению 48, в которой b равно 1, с равно 1 и d равно 0.
52. Нуклеиновая кислота по утверждению 48, в которой b равно 1, с равно 1 и d равно 1.
53. Нуклеиновая кислота по любому из утверждений 48-52, в которой Y представляет собой О.
54. Нуклеиновая кислота по любому из утверждений 48-52, в которой Y представляет собой S.
55. Нуклеиновая кислота по любому из утверждений 48-54, в которой R1 представляет собой Н.
56. Нуклеиновая кислота по любому из утверждений 48-54, в которой R1 представляет собой метил.
57. Нуклеиновая кислота по любому из утверждений 48-56, в которой n равно 0.
58. Нуклеиновая кислота по любому из утверждений 48-57, в которой L представляет собой -(СН2)r-С(O)-, где r=2-12.
59. Нуклеиновая кислота по утверждению 58, в которой r=2-6.
60. Нуклеиновая кислота по утверждению 59, в которой r=4 или 6, например, 4.
61. Композиция, содержащая нуклеиновую кислоту по любому предшествующему утверждению и состав, содержащий:
а. катионный липид или его фармацевтически приемлемую соль;
b. стероид;
с. фосфолипид фосфатидилэтаноламин;
d. пегилированный липид.
62. Композиция по утверждению 61, в которой содержание компонента указанного катионного липида в составе составляет от приблизительно 55 мол.% до приблизительно 65 мол.% от общего содержания липидов липидной композиции, предпочтительно приблизительно 59 мол.% от общего содержания липидов липидной композиции.
63. Композиция по утверждению 62, причем указанный состав содержит:
катионный липид, имеющий структуру;
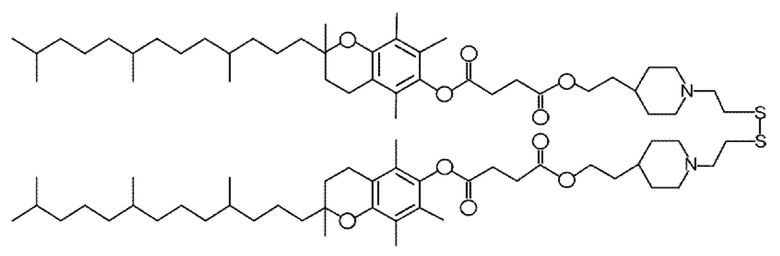
стероид, имеющий структуру;
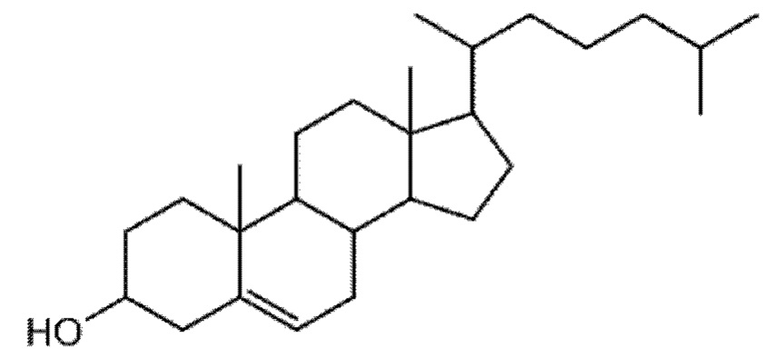
холестерин
фосфолипид фосфатидилэтаноламин, имеющий структуру;
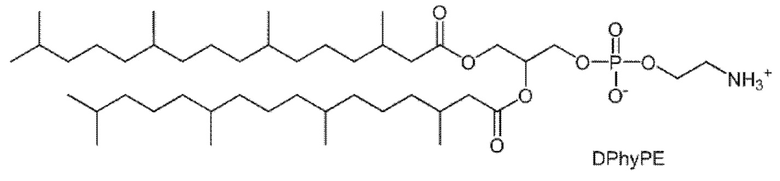
и пегилированныи липид, имеющий структуру;
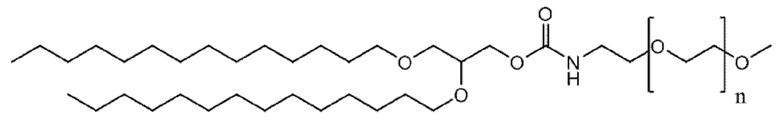
мПЭГ-2000-ДМГ
64. Композиция, содержащая нуклеиновую кислоту или конъюгированную нуклеиновую кислоту по любому предшествующему утверждению и физиологически приемлемое вспомогательное вещество.
65. Нуклеиновая кислота или конъюгированная нуклеиновая кислота по любому предшествующему утверждению для применения при лечении заболевания или нарушения.
66. Применение нуклеиновой кислоты или конъюгированной нуклеиновой кислоты по любому предшествующему утверждению при изготовлении лекарственного средства для лечения заболевания или нарушения.
67. Способ лечения заболевания или нарушения, включающий введение композиции, содержащей нуклеиновую кислоту или конъюгированную нуклеиновую кислоту по любому предшествующему утверждению, индивидууму, нуждающемуся в лечении.
68. Способ по утверждению 67, в котором указанную молекулу нуклеиновой кислоты или конъюгированной нуклеиновой кислоты вводят субъекту подкожно или внутривенно.
69. Способ изготовления нуклеиновой кислоты или конъюгированной нуклеиновой кислоты по любому из утверждений 1-65.
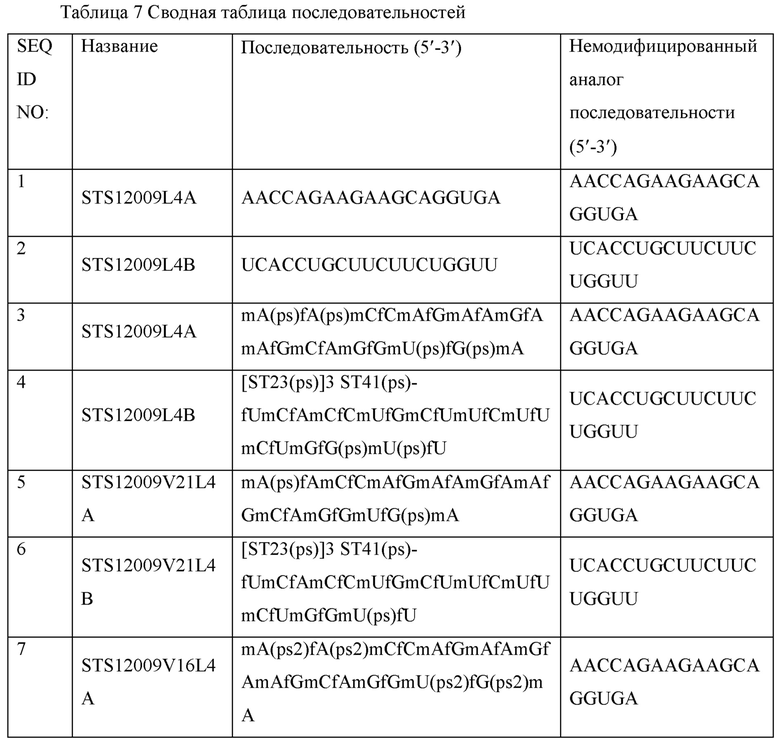
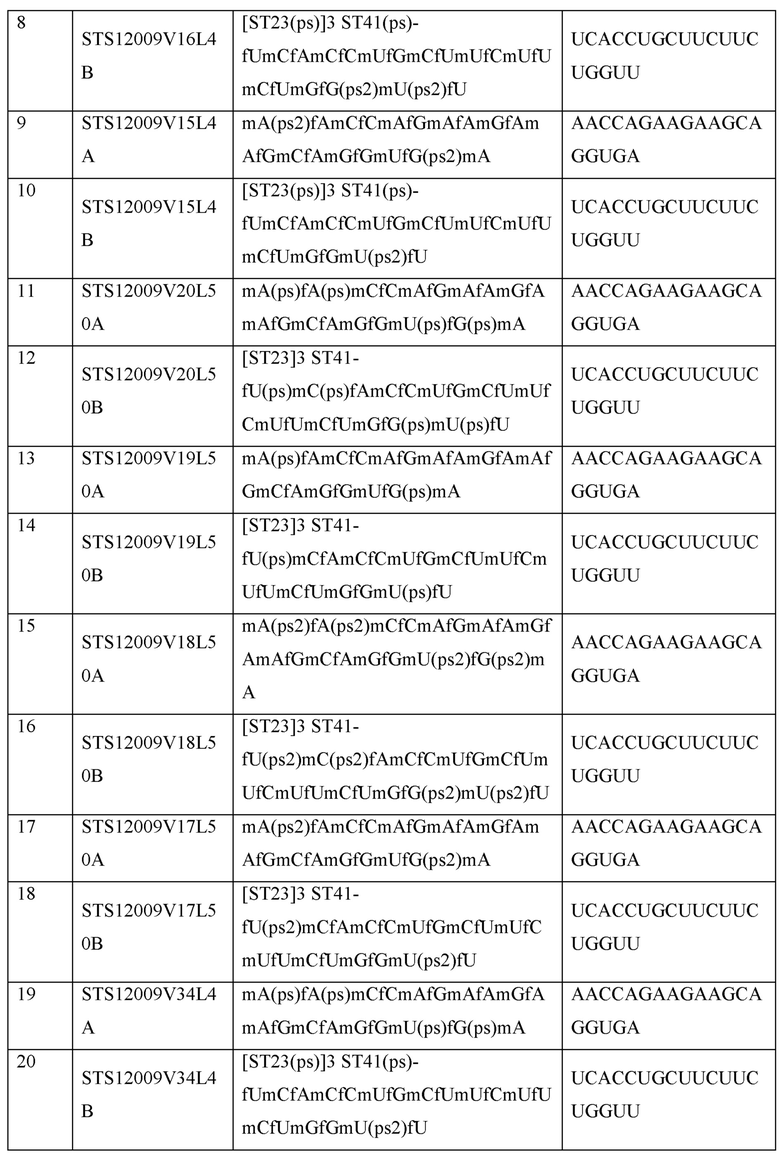
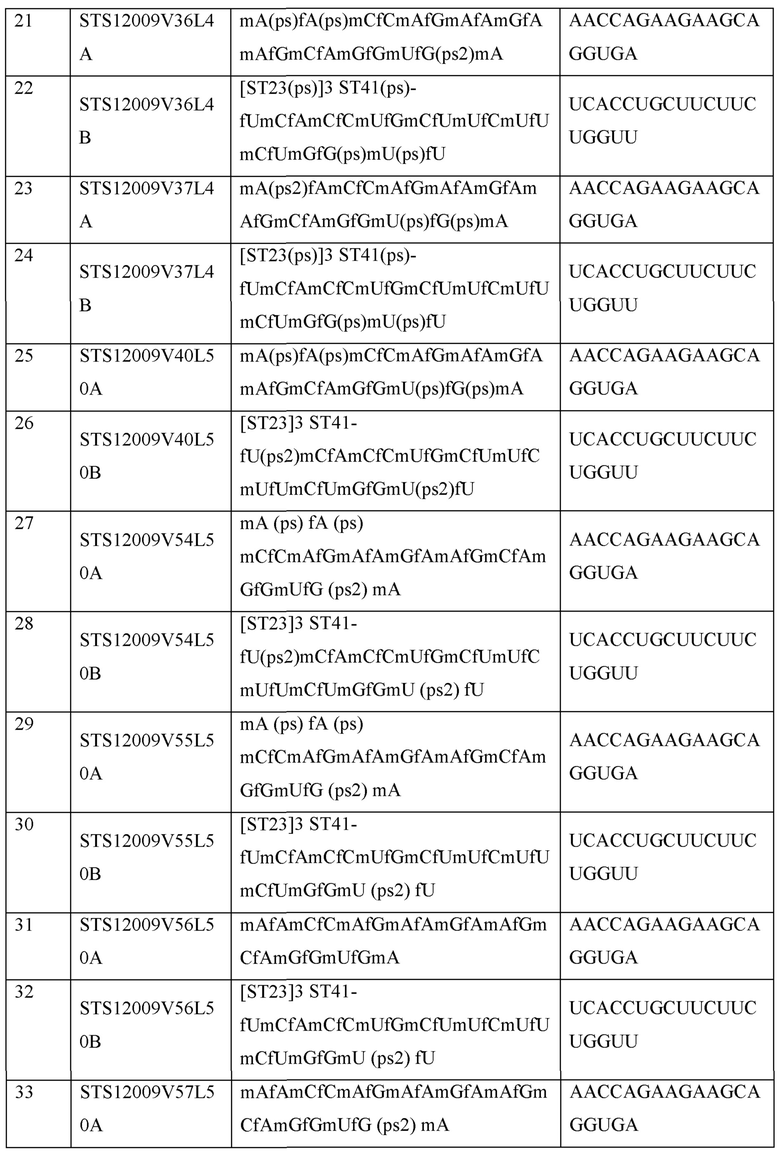
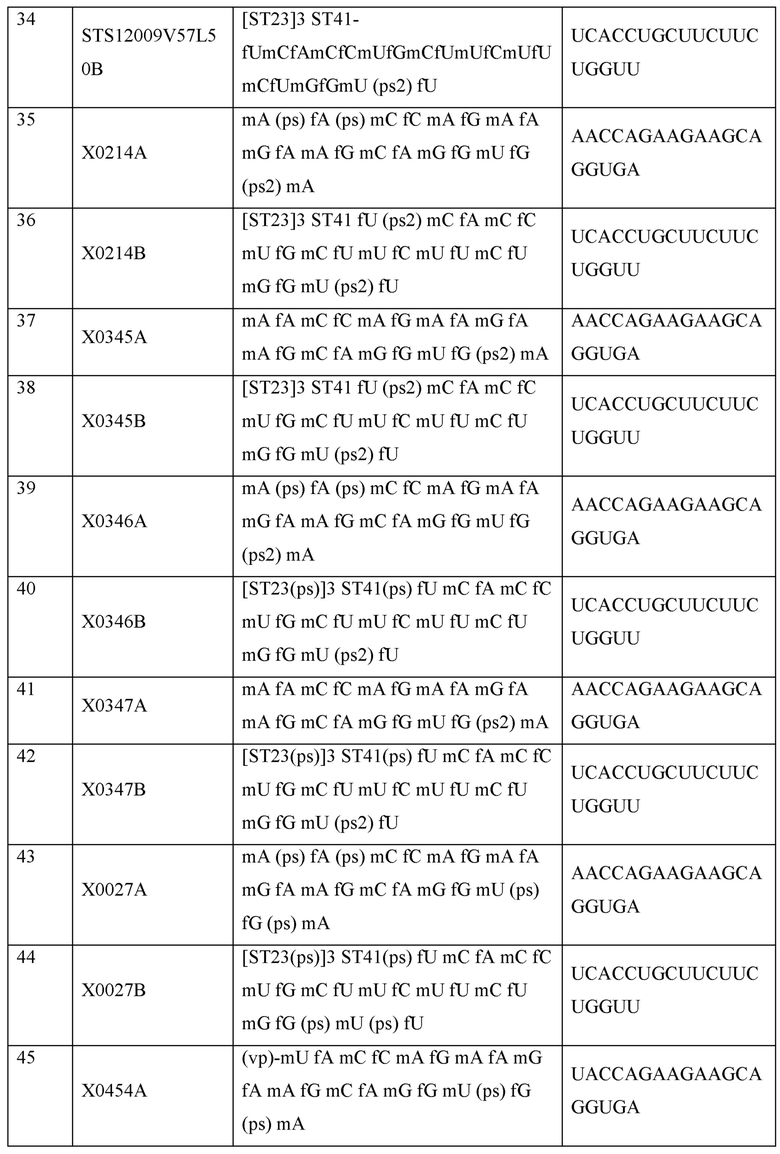

Последовательности, заканчивающиеся на «А» (как в Х0456А), представляют собой последовательности первой цепи, а последовательности, заканчивающиеся на «В» (как в Х0456 В), представляют собой последовательности второй цепи.
mA, mU, mC, mG - 2'-ОМе РНК
fA, fU, fC, fG - 2'-F РНК
(ps) - фосфотиоат
(ps2) - фосфодитиоат
(vp) - винил-(Е)-фосфонат
Перечисленные выше последовательности могут быть раскрыты с линкером или лигандом, таким как GalNAc, или, например, связями (ps) или (ps2). Они образуют необязательную, но предпочтительную, часть последовательности из перечня последовательностей.
В настоящей заявке могут быть использованы следующие сокращения:
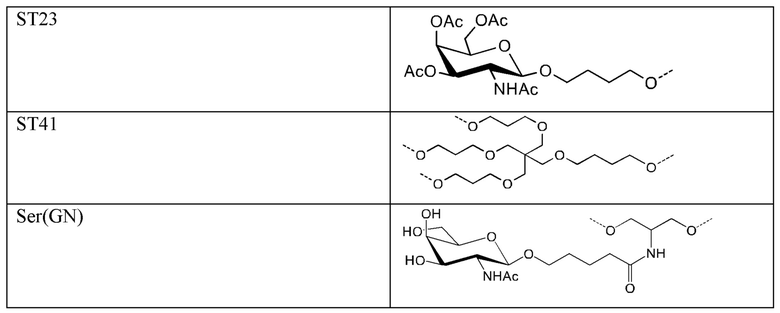
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> САЙЛЕНС ТЕРАПЬЮТИКС ГМБХ
<120> НУКЛЕИНОВЫЕ КИСЛОТЫ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ ГЕНА-МИШЕНИ,
СОДЕРЖАЩИЕ ФОСФОДИТИОАТНЫЕ СВЯЗИ
<130> S111PCT
<150> EP17201408.6
<151> 2017-11-13
<150> GB1800679.1
<151> 2018-01-16
<150> EP18165913.7
<151> 2018-04-05
<160> 48
<170> PatentIn версии 3.5
<210> 1
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 1
aaccagaaga agcagguga 19
<210> 2
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК
<400> 2
ucaccugcuu cuucugguu 19
<210> 3
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 3
aaccagaaga agcagguga 19
<210> 4
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 4
ucaccugcuu cuucugguu 19
<210> 5
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 5
aaccagaaga agcagguga 19
<210> 6
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 6
ucaccugcuu cuucugguu 19
<210> 7
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 7
aaccagaaga agcagguga 19
<210> 8
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 8
ucaccugcuu cuucugguu 19
<210> 9
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 9
aaccagaaga agcagguga 19
<210> 10
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 10
ucaccugcuu cuucugguu 19
<210> 11
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 11
aaccagaaga agcagguga 19
<210> 12
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 12
ucaccugcuu cuucugguu 19
<210> 13
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 13
aaccagaaga agcagguga 19
<210> 14
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 14
ucaccugcuu cuucugguu 19
<210> 15
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 15
aaccagaaga agcagguga 19
<210> 16
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 16
ucaccugcuu cuucugguu 19
<210> 17
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 17
aaccagaaga agcagguga 19
<210> 18
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 18
ucaccugcuu cuucugguu 19
<210> 19
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 19
aaccagaaga agcagguga 19
<210> 20
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 20
ucaccugcuu cuucugguu 19
<210> 21
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 21
aaccagaaga agcagguga 19
<210> 22
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 22
ucaccugcuu cuucugguu 19
<210> 23
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 23
aaccagaaga agcagguga 19
<210> 24
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 24
ucaccugcuu cuucugguu 19
<210> 25
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 25
aaccagaaga agcagguga 19
<210> 26
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 26
ucaccugcuu cuucugguu 19
<210> 27
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 27
aaccagaaga agcagguga 19
<210> 28
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 28
ucaccugcuu cuucugguu 19
<210> 29
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 29
aaccagaaga agcagguga 19
<210> 30
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 30
ucaccugcuu cuucugguu 19
<210> 31
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 31
aaccagaaga agcagguga 19
<210> 32
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 32
ucaccugcuu cuucugguu 19
<210> 33
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 33
aaccagaaga agcagguga 19
<210> 34
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 34
ucaccugcuu cuucugguu 19
<210> 35
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 35
aaccagaaga agcagguga 19
<210> 36
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 36
ucaccugcuu cuucugguu 19
<210> 37
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 37
aaccagaaga agcagguga 19
<210> 38
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 38
ucaccugcuu cuucugguu 19
<210> 39
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 39
aaccagaaga agcagguga 19
<210> 40
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 40
ucaccugcuu cuucugguu 19
<210> 41
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 41
aaccagaaga agcagguga 19
<210> 42
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 42
ucaccugcuu cuucugguu 19
<210> 43
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 43
aaccagaaga agcagguga 19
<210> 44
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 44
ucaccugcuu cuucugguu 19
<210> 45
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 45
uaccagaaga agcagguga 19
<210> 46
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 46
ucaccugcuu cuucuggua 19
<210> 47
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 47
uaccagaaga agcagguga 19
<210> 48
<211> 19
<212> РНК
<213> Искусственная последовательность
<220>
<223> миРНК - с модифицированными основаниями, модифицированная согласно
сводной таблице последовательностей в конце описания заявки
<400> 48
ucaccugcuu cuucuggua 19
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| НУКЛЕИНОВЫЕ КИСЛОТЫ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ LPA В КЛЕТКЕ | 2018 |
|
RU2822093C1 |
| КОНЪЮГАТЫ УГЛЕВОДА И LNA-ОЛИГОНУКЛЕОТИДА | 2014 |
|
RU2649367C2 |
| СРЕДСТВА ДЛЯ РНКи, КОМПОЗИЦИИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, АССОЦИИРОВАННЫХ С ТРАНСТИРЕТИНОМ (TTR) | 2012 |
|
RU2678807C2 |
| Композиция системы доставки на основе конъюгата для доставки полинуклеотида РНК-интерференции в клетку печени и способ ее получения | 2011 |
|
RU2623160C9 |
| НИЗКОМОЛЕКУЛЯРНЫЕ КОНЪЮГАТЫ ДЛЯ ВНУТРИКЛЕТОЧНОЙ ДОСТАВКИ НУКЛЕИНОВЫХ КИСЛОТ | 2011 |
|
RU2582235C2 |
| НИЗКОМОЛЕКУЛЯРНЫЕ КОНЪЮГАТЫ ДЛЯ ВНУТРИКЛЕТОЧНОЙ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ | 2011 |
|
RU2629957C2 |
| КОМПОЗИЦИИ И СПОСОБЫ МОДУЛИРОВАНИЯ ЭКСПРЕССИИ АПОЛИПОПРОТЕИНА C-III | 2014 |
|
RU2650510C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ АССОЦИИРОВАННОГО С SERPINC1 РАССТРОЙСТВА | 2016 |
|
RU2754188C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЯВЛЕНИЯ КРОВОТЕЧЕНИЯ У БОЛЬНОГО ГЕМОФИЛИЕЙ | 2018 |
|
RU2801263C2 |
| КОНЪЮГАТЫ ОЛИГОНУКЛЕОТИДОВ | 2013 |
|
RU2653438C2 |
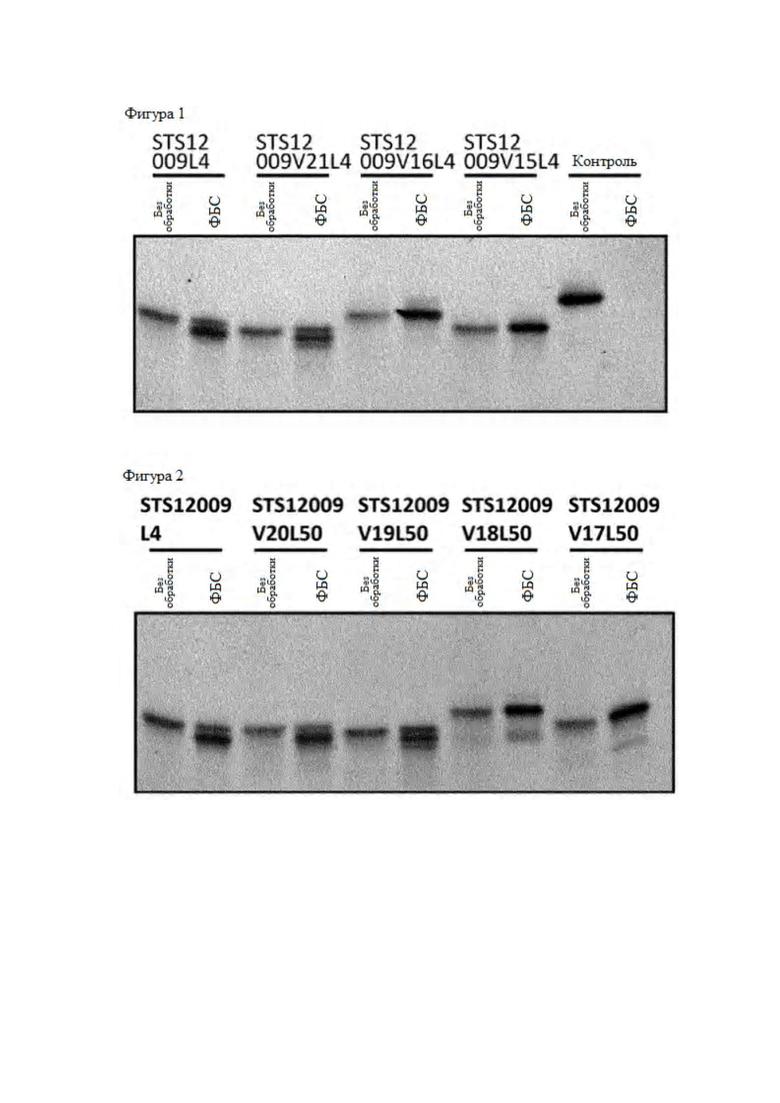
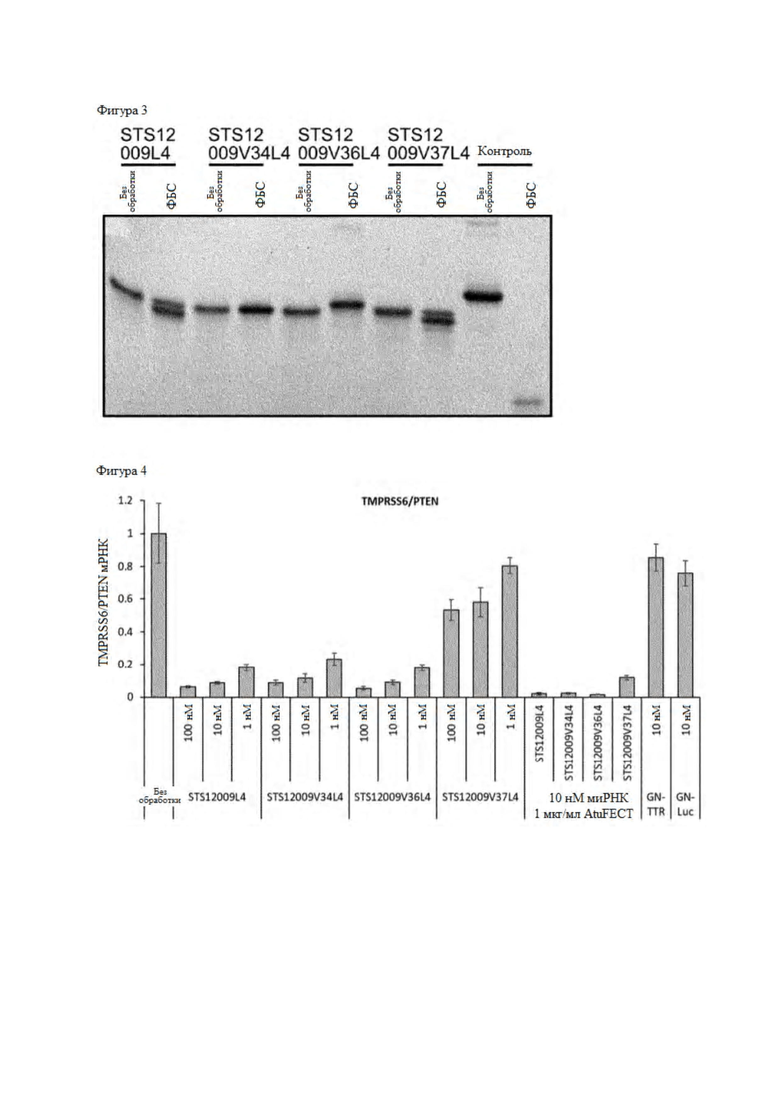
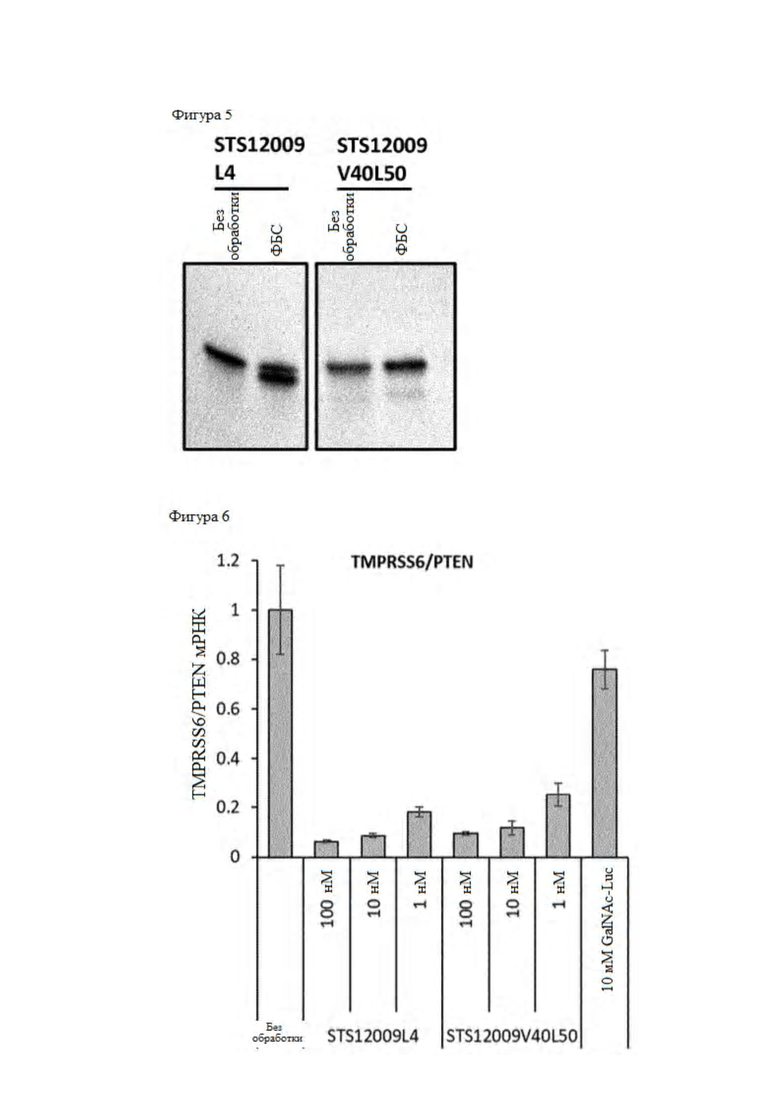
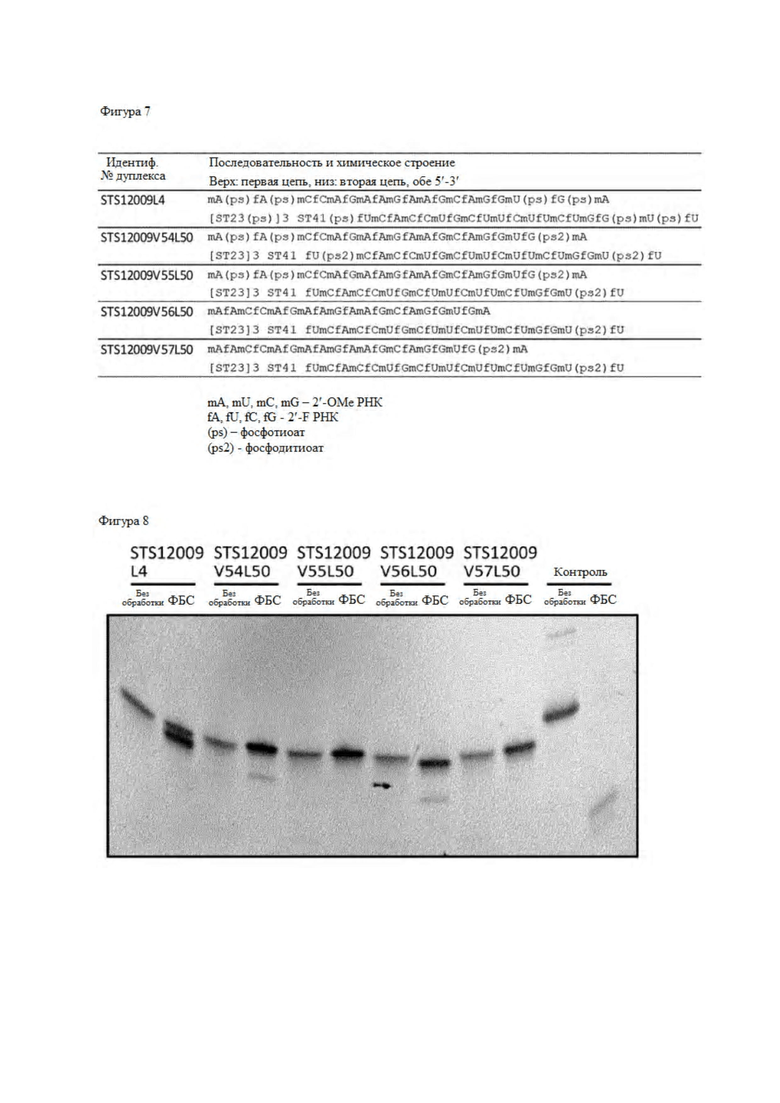
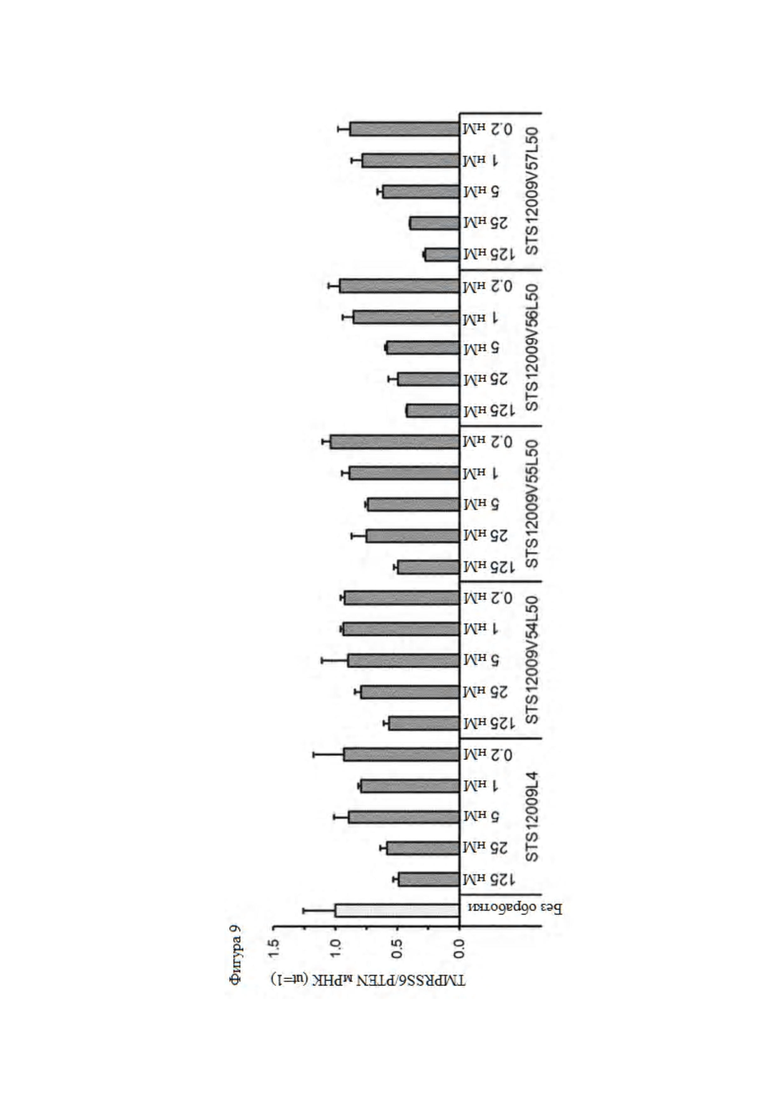

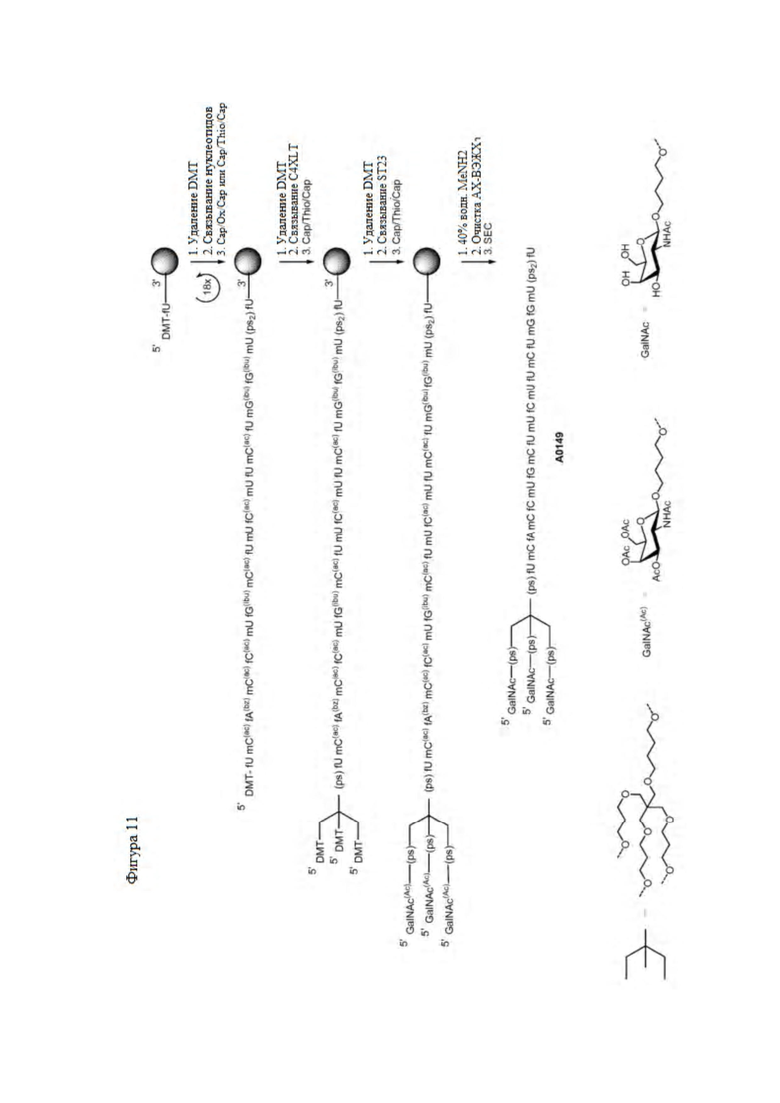
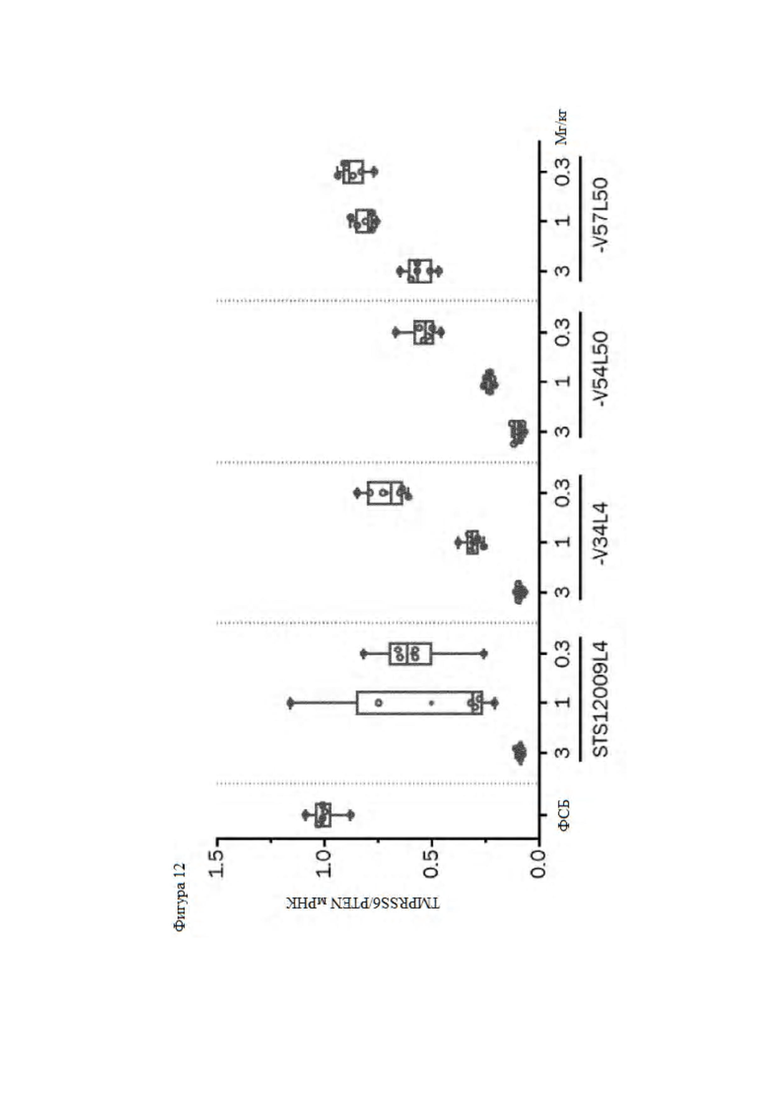

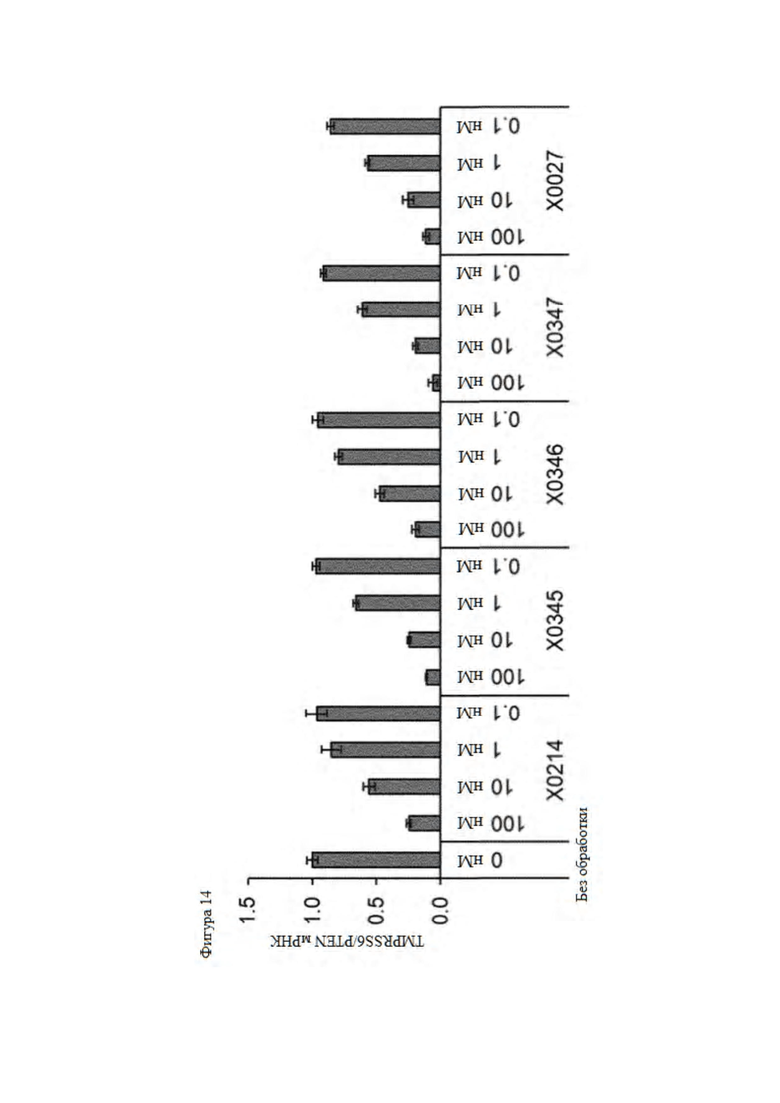
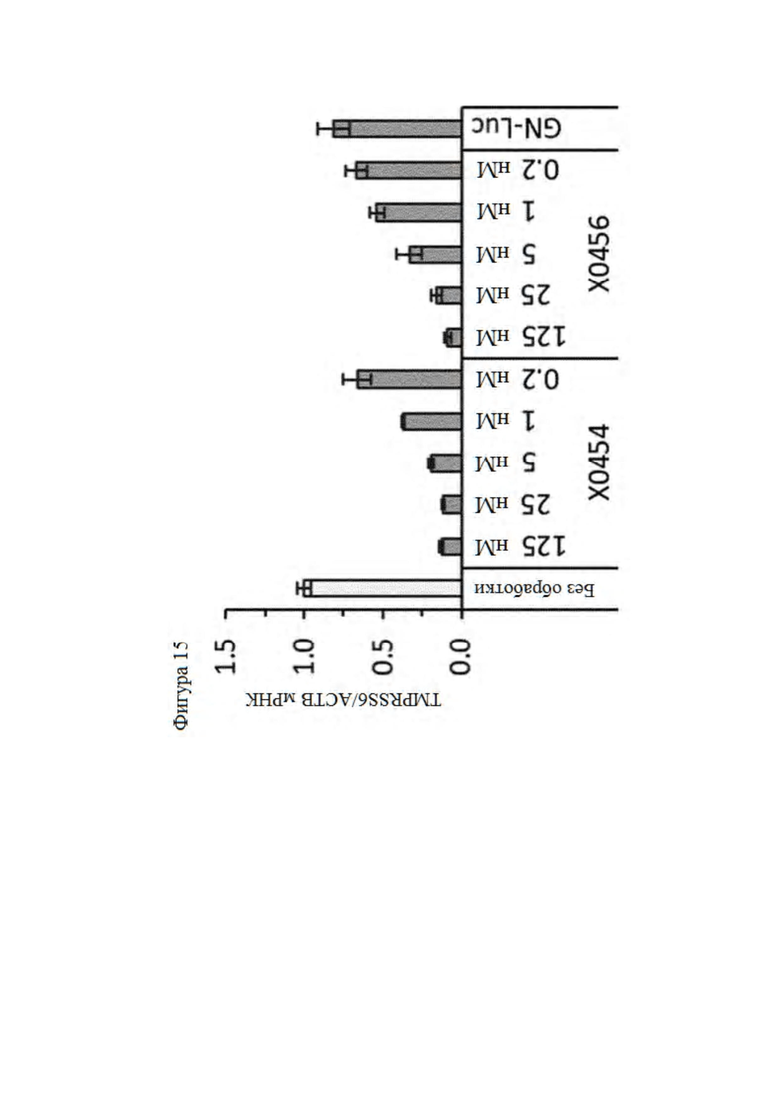
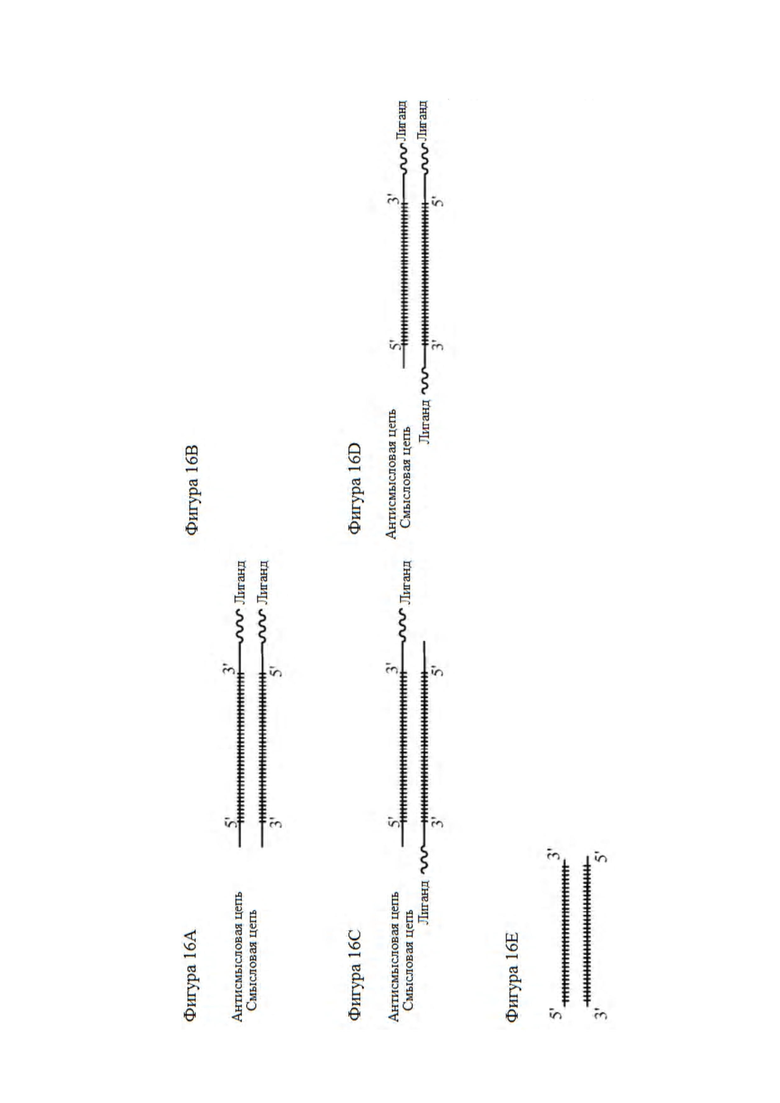
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая нуклеиновую кислоту для ингибирования экспрессии гена-мишени в клетке (варианты), конъюгат для ингибирования экспрессии гена-мишени в клетке (варианты), композицию для применения в качестве лекарственного средства для предотвращения или лечения заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени, фармацевтическую композицию для предотвращения или лечения заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени, применение нуклеиновой кислоты или конъюгата или фармацевтической композиции при предотвращении или лечении заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени и способ предотвращения или лечения заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени. Изобретение расширяет арсенал средств для ингибирования экспрессии гена-мишени в клетке. 9 н. и 17 з.п. ф-лы, 20 ил., 8 табл., 12 пр.
1. Нуклеиновая кислота для ингибирования экспрессии гена-мишени в клетке, содержащая по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна указанной первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени, при этом указанные первая и/или вторая цепи содержат фосфодитиоатную связь между по меньшей мере двумя нуклеотидами и каждая из указанной первой цепи и/или указанной второй цепи содержит 17-35 нуклеотидов в длину.
2. Нуклеиновая кислота по п. 1, отличающаяся тем, что указанная первая цепь не содержит фосфодитиоатную связь между любыми из двух, трех или четырех концевых нуклеотидов на 5'-конце.
3. Нуклеиновая кислота по любому из предшествующих пунктов, содержащая фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 3'-конце указанной первой цепи и/или содержащая фосфодитиоатную связь между каждым из двух, трех или четыре концевых нуклеотидов на 3'-конце указанной второй цепи и/или фосфодитиоатную связь между каждым из двух, трех или четырех концевых нуклеотидов на 5'-конце указанной второй цепи.
4. Нуклеиновая кислота по любому из предшествующих пунктов, отличающаяся тем, что указанная нуклеиновая кислота содержит фосфотиоатную связь между каждым из трех концевых 3' нуклеотидов и/или между каждым из трех концевых 5' нуклеотидов на указанной первой цепи и/или между каждым из трех 3' концевых нуклеотидов и/или между каждым из трех 5' нуклеотидов указанной второй цепи, если на этом конце не присутствует фосфодитиоатная связь.
5. Нуклеиновая кислота по любому из предшествующих пунктов, отличающаяся тем, что указанная первая цепь и указанная вторая цепь представляют собой отдельные цепи.
6. Нуклеиновая кислота по любому из предшествующих пунктов, отличающаяся тем, что указанная по меньшей мере одна дуплексная область состоит из 17-25 пар нуклеотидных оснований.
7. Нуклеиновая кислота по любому из предшествующих пунктов, отличающаяся тем, что один или более нуклеотидов в указанной первой и/или второй цепи модифицированы с образованием модифицированных нуклеотидов.
8. Нуклеиновая кислота по п. 7, отличающаяся тем, что указанная модификация представляет собой любой из закрытого нуклеотида, лишенного азотистого основания нуклеотида или нуклеотида, содержащего неприродное основание.
9. Конъюгат для ингибирования экспрессии гена-мишени в клетке, содержащий нуклеиновую кислоту по любому из предшествующих пунктов и лиганд.
10. Конъюгат по п. 9, отличающийся тем, что указанный лиганд содержит (i) одну или более групп N-ацетилгалактозамина (GalNAc) или их производных, и (ii) линкер, причем с помощью указанного линкера конъюгируют по меньшей мере одну группу GalNAc или ее производное с указанной нуклеиновой кислотой.
11. Конъюгат по любому из пп. 9, 10, отличающийся тем, что указанный лиганд содержит соединение формулы (I):
[S-X1-P-X2]3-A-X3-, (I)
в которой:
S представляет собой сахарид, при этом предпочтительно указанный сахарид представляет собой N-ацетилгалактозамин;
X1 представляет собой C3-C6 алкилен или (-CH2-CH2-O)m(-CH2)2-, где m равно 1, 2 или 3;
P представляет собой фосфат или модифицированный фосфат, предпочтительно незамещенный фосфат;
X2 представляет собой алкилен или простой алкиленовый эфир формулы (-CH2)n-O-CH2-, где n=1-6;
А представляет собой блок разветвления;
X3 представляет собой мостиковый блок;
при этом нуклеиновая кислота по любому из пп. 1-8 конъюгирована с X3 за счет фосфата или модифицированного фосфата, предпочтительно незамещенного фосфата.
12. Конъюгат по любому из пп. 9, 10, отличающийся тем, что указанная первая цепь РНК представляет собой соединение формулы (X):
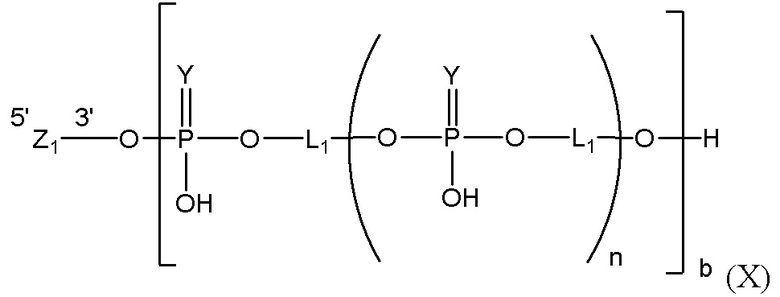
в которой b равно 0 или 1; и
указанная вторая цепь РНК представляет собой соединение формулы (XI):
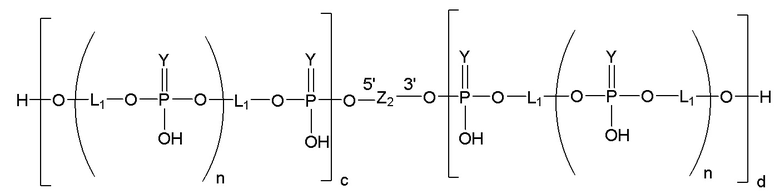 (XI)
(XI)
в которой:
с и d независимо равны 0 или 1;
Z1 и Z2 представляют собой части РНК указанных первой и второй цепей РНК, соответственно;
Y представляет собой O или S, предпочтительно O;
n равно 0, 1, 2 или 3; и
L1 представляет собой линкер, к которому присоединен лиганд; и
при этом b + c + d равно 2 или 3.
13. Нуклеиновая кислота для ингибирования экспрессии гена-мишени в клетке, содержащая по меньшей мере одну дуплексную область, которая содержит по меньшей мере часть первой цепи и по меньшей мере часть второй цепи, которая по меньшей мере частично комплементарна указанной первой цепи, причем указанная первая цепь по меньшей мере частично комплементарна по меньшей мере части РНК, транскрибированной с указанного гена-мишени,
при этом указанная нуклеиновая кислота содержит фосфодитиоатные связи между двумя концевыми нуклеотидами на 3'-конце указанной первой цепи,
при этом указанная нуклеиновая кислота содержит фосфодитиоатную связь между двумя концевыми нуклеотидами на 3'-конце и между двумя концевыми нуклеотидами на 5'-конце указанной второй цепи, и
при этом указанная первая цепь содержит связь, отличную от фосфодитиоатной связи, между двумя, тремя или четырьмя концевыми нуклеотидами на 5'-конце,
при этом каждая из указанной первой цепи и/или указанной второй цепи содержит 17-35 нуклеотидов в длину.
14. Конъюгат для ингибирования экспрессии гена-мишени в клетке, содержащий нуклеиновую кислоту по п. 13 и лиганд, содержащий соединение формулы (I):
[S-X1-P-X2]3-A-X3-, (I)
в которой:
S представляет собой сахарид, при этом предпочтительно указанный сахарид представляет собой N-ацетилгалактозамин;
X1 представляет собой C3-C6 алкилен или (-CH2-CH2-O)m(-CH2)2-, где m равно 1, 2 или 3;
P представляет собой фосфат или модифицированный фосфат, предпочтительно незамещенный фосфат;
X2 представляет собой алкилен или простой алкиленовый эфир формулы (-CH2)n-O-CH2-, где n=1-6;
А представляет собой блок разветвления;
X3 представляет собой мостиковый блок;
при этом нуклеиновая кислота по п. 13 конъюгирована с X3 за счет фосфата или модифицированного фосфата.
15. Конъюгат для ингибирования экспрессии гена-мишени в клетке, содержащий нуклеиновую кислоту по п. 13 и лиганд, причем указанная первая цепь РНК представляет собой соединение формулы (XV):
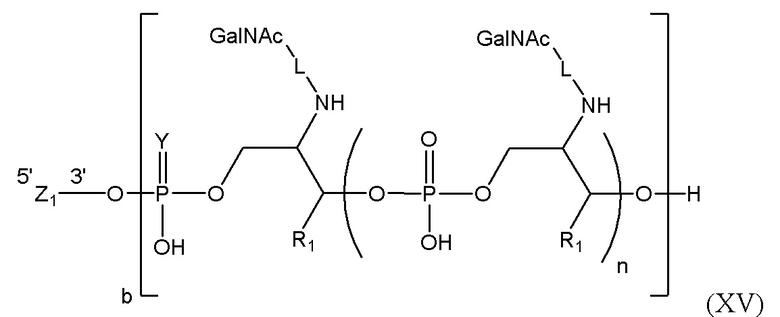
в которой b равно 0 или 1; и
указанная вторая цепь РНК представляет собой соединение формулы (XVI):
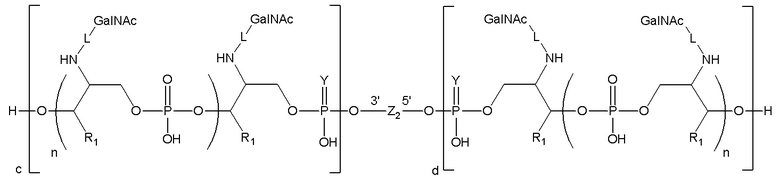 (XVI)
(XVI)
в которой с и d независимо равны 0 или 1;
при этом:
Z1 и Z2 представляют собой части РНК указанных первой и второй цепей РНК, соответственно;
Y представляет собой O или S, предпочтительно O;
R1 представляет собой H или метил;
n равно 0, 1, 2 или 3; и
L является одинаковым или различным в формулах (XV) и (XVI) и выбран из группы, состоящей из:
-(CH2)q, где q=2-12;
-(CH2)r-C(O)-, где r=2-12;
-(CH2-CH2-O)s-CH2-C(O)-, где s=1-5;
-(CH2)t-CO-NH-(CH2)t-NH-C(O)-, где t независимо представляет собой 1-5;
-(CH2)u-CO-NH-(CH2)u-C(O)-, где u независимо представляет собой 1-5; и
-(CH2)v-NH-C(O)-, где v представляет собой 2-12; и
при этом концевой C(O), если он присутствует, присоединен к группе NH;
и при этом b + c + d равно 2 или 3.
16. Нуклеиновая кислота по п. 13 или конъюгат по п. 14 или 15, отличающиеся тем, что указанная первая цепь РНК имеет концевой 5'-(E)-винилфосфонатный нуклеотид на своем 5' конце и при этом указанный концевой 5'-(E)-винилфосфонатный нуклеотид предпочтительно соединен со вторым нуклеотидом в указанной первой цепи за счет фосфодиэфирной связи.
17. Нуклеиновая кислота по п. 13 или 16 или конъюгат по любому из пп. 14-16, отличающиеся тем, что один или более нуклеотидов в указанной первой и/или второй цепи модифицированы с образованием модифицированных нуклеотидов.
18. Нуклеиновая кислота или конъюгат по п. 17, отличающиеся тем, что указанная модификация представляет собой любой из закрытого нуклеотида, лишенного азотистого основания нуклеотида или нуклеотида, содержащего неприродное основание.
19. Нуклеиновая кислота или конъюгат по п. 17, отличающиеся тем, что нуклеотиды указанной первой цепи модифицированы с применением первой модификации на нуклеотидах в нечетных положениях и модифицированы с применением второй модификации на нуклеотидах в четных положениях, а нуклеотиды указанной второй цепи модифицированы на нуклеотидах в нечетных положениях с применением второй модификации и модифицированы с применением первой модификации на нуклеотидах в четных положениях, причем указанная первая цепь пронумерована от 5' к 3', при этом самый крайний 5'-нуклеотид представляет собой нуклеотид номер 1 первой цепи, и вторая цепь пронумерована от 3' к 5', при этом самый крайний 3'-нуклеотид представляет собой нуклеотид номер 1 второй цепи, при этом указанная первая модификация предпочтительно представляет собой 2'OMe, при этом указанная вторая модификация предпочтительно представляет собой 2'-фтор, и при этом указанная нуклеиновая кислота предпочтительно имеет тупые концы на обоих концах.
20. Нуклеиновая кислота или конъюгат по п. 17, отличающиеся тем, что нуклеотиды в положениях 2 и 14 с 5'-конца указанной первой цепи модифицированы с применением 2'-фтор-модификации, и нуклеотиды на указанной второй цепи, которые соответствуют положению 11 или 13, или 11 и 13, или 11-13 указанной первой цепи, модифицированы с применением 2'-фтор-модификации, и при этом предпочтительно остальные нуклеотиды модифицированы с применением 2'-OMe-модификации.
21. Нуклеиновая кислота по любому из пп. 13 и 16-20 или конъюгат по любому из пп. 14-20, отличающиеся тем, что все связи между нуклеотидами обеих цепей, кроме связи между двумя концевыми нуклеотидами на 3'-конце указанной первой цепи и связей между двумя концевыми нуклеотидами на 3'-конце и 5'-конце указанной второй цепи, представляют собой незамещенные фосфатные связи.
22. Композиция для применения в качестве лекарственного средства для предотвращения или лечения заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени, содержащая нуклеиновую кислоту по любому из пп. 1-8, 13 и 16-21 или конъюгат по любому из пп. 9-12 и 14-21 и необязательно носитель для доставки и/или физиологически приемлемое вспомогательное вещество, и/или носитель, и/или разбавитель, и/или буфер, и/или консервант.
23. Фармацевтическая композиция для предотвращения или лечения заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени, содержащая нуклеиновую кислоту по любому из пп. 1-8, 13 и 16-21 или конъюгат по любому из пп. 9-12 и 14-21 и дополнительно содержащая носитель для доставки, предпочтительно липосомы, и/или физиологически приемлемое вспомогательное вещество, и/или носитель, и/или разбавитель.
24. Применение нуклеиновой кислоты по любому из пп. 1-8, 13 и 16-21, или конъюгата по любому из пп. 9-12 и 14-21, или фармацевтической композиции по п. 23 при предотвращении или лечении заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени.
25. Способ предотвращения или лечения заболевания, нарушения или синдрома, при которых целевым является снижение экспрессии продуктов гена-мишени, включающий введение композиции, содержащей нуклеиновую кислоту по любому из пп. 1-8, 13 и 16-21 или конъюгат по любому из пп. 9-12 и 14-21, или композиции по любому из пп. 22, 23, индивидууму, нуждающемуся в лечении.
26. Способ по п. 25, отличающийся тем, что указанную композицию вводят указанному субъекту подкожно, внутривенно, перорально, ректально или внутрибрюшинно.
| WO 1999032619 A1, 01.07.1999 | |||
| WO 2003070910 A2, 28.08.2003 | |||
| WO 2009073809 A2, 11.06.2009 | |||
| WO 2011123621 A2, 06.10.2011 | |||
| ПОЛИКОНЪЮГАТЫ ДЛЯ ВВЕДЕНИЯ IN VIVO ПОЛИНУКЛЕОТИДОВ | 2007 |
|
RU2430740C2 |
| WO 2013176477 A1, 28.11.2013 | |||
| Нуклеиновые кислоты: от А до Я | |||
| /Б | |||
| Аппель [и др.]; под ред | |||
| С | |||
| Мюллер; пер с англ | |||
| - М.: БИНОМ | |||
| Лаборатория знаний, 2013 | |||
| Устройство для избирательного управления двумя реле | 1918 |
|
SU978A1 |
| См | |||
| стр | |||
| Приспособление для подвешивания тележки при подъемках сошедших с рельс вагонов | 1920 |
|
SU216A1 |
Авторы
Даты
2024-02-02—Публикация
2018-11-13—Подача