Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицины, в частности к клинической лабораторной диагностике в области онкоурологии, и может быть использовано для неинвазивной первичной диагностики рака мочевого пузыря, а также для мониторинга рецидивов заболевания.
Уровень техники
Рак мочевого пузыря является наиболее распространенным онкологическим заболеванием мочевого тракта, при этом занимая 9-е место по заболеваемости и 13-е по смертности среди всех типов рака [Antoni S., Ferlay J., Soerjomataram I., Znaor A., Jemal A., Bray F. Bladder Cancer Incidence and Mortality: A Global Overview and Recent Trends //. Eur Urol.. 2017. Vol. 71(1). P. 96-108. DOI: 10.1016/j.eururo.2016.06.010]. Данное заболевание характеризуется высокой частотой рецидивов. Известно, что после трансуретральной резекции опухоли каждый третий пациент сталкивается с рецидивом [Chamie K., Litwin M.S., Bassett J.C., Daskivich T.J., Lai J., Hanley J.M., Konety B.R., Saigal C.S.; Urologic Diseases in America Project. Recurrence of high-risk bladder cancer: a population-based analysis // Cancer. 2013. Vol. 119(17). P. 3219-27. DOI: 10.1002/cncr.28147]. Таким образом, пациентам необходим регулярный мониторинг на протяжении первых 5 лет после удаления опухоли (с частотой 3-6 месяцев), в результате чего рак мочевого пузыря является одним из наиболее дорогих онкологических заболеваний в отношении ведения пациентов [Mariotto A.B., Yabroff K.R., Shao Y., Feuer E.J., Brown M.L. Projections of the cost of cancer care in the United States: 2010-2020 // J Natl Cancer Inst. 2011. Vol. 103(2). P. 117-28. DOI: 10.1093/jnci/djq495].
Из уровня техники известен золотой стандарт диагностики рака мочевого пузыря - цистоскопия с последующими биопсией и гистологическим подтверждением [Клинические рекомендации “Рак мочевого пузыря», 2022 год. (Электронный ресурс). URL: https://oncology-association.ru/wp-content/uploads/2022/03/rak-mochevogo-puzyrya.pdf (дата обращения 31.05.2023)]. Несмотря на то, что цистоскопия является эффективным диагностическим инструментом, ее точность не является абсолютной, что усугубляется высокой стоимостью процедуры и необходимостью в высокой квалификации исполняющего ее персонала. Так, чувствительность и специфичность данного инструментального метода колеблются в диапазонах 62-84% и 43-98%, соответственно, в зависимости от стадии и типа опухоли [Jocham D., Stepp H., Waidelich R. Photodynamic diagnosis in urology: state-of-the-art // Eur Urol. 2008. Vol. 53(6). P. 1138-48. DOI: 10.1016/j.eururo.2007.11.048], что во многом связано с высокой внутри- и межоператорской вариабельностью, ассоциированной с его применением [McCroskey Z., Pambuccian S.E., Kleitherms S., Antic T. Accuracy and Interobserver Variability of the Cytologic Diagnosis of Low-Grade Urothelial Carcinoma in Instrumented Urinary Tract Cytology Specimens // Am J of Clin Pathol. 2015. Vol. 144(6). P. 902-908, DOI: 10.1309/AJCPE1O9YKMRSQKG]. Более того, из-за высокой инвазивности подобного подхода пациенты часто испытывают такие побочные эффекты, как боль при мочеиспускании (50%), частое мочеиспускание (37%), гематурию (17%) и инфекции мочевого тракта (3%) [Biardeau X., Lam O., Ba V., Campeau L., Corcos J. Prospective evaluation of anxiety, pain, and embarrassment associated with cystoscopy and urodynamic testing in clinical practice // Can Urol Assoc J. 2017. Vol. 11(3-4). P. 104-110. DOI: 10.5489/cuaj.4127].
Впрочем, существует и ряд неинвазивных подходов к диагностике рака мочевого пузыря. Большая часть подобных методик основана на изучении мочи в качестве диагностического субстрата.
Так, из уровня техники известен способ диагностики рака мочевого пузыря, основанный на цитологическом исследовании мочи [Pannek J., Rademacher F., Wöllner J. Clinical usefulness of urine cytology in the detection of bladder tumors in patients with neurogenic lower urinary tract dysfunction // Res Rep Urol. 2017. Vol. 9. P. 219-223. DOI: 10.2147/RRU.S148429] и подразумевающий приготовление мазка из осадка мочи, его окраску и изучение под микроскопом. Данный способ весьма чувствителен на поздних стадиях заболевания (до 100%), однако на ранних стадиях и при мониторинге рецидивов чувствительность составляет 4-31%, тогда как его специфичность - 43-98%. Более того, интерпретация результатов цитологического исследования может быть искажена при уролитиазе, инфекциях мочевыводящих путей и низком содержании клеток в моче [Raitanen M.P., Aine R., Rintala E., Kallio J., Rajala P., Juusela H., Tammela T.L. FinnBladder Group. Differences between local and review urinary cytology in diagnosis of bladder cancer. An interobserver multicenter analysis // Eur Urol. 2002. Vol. 41(3). P. 284-9. DOI: 10.1016/s0302-2838(02)00006-4].
Из уровня техники также известен способ диагностики рака мочевого пузыря, заключающийся в применении технологий секвенирования нового поколения с целью обнаружения мутаций в генах ARID1A, ASXL1, ASXL2, ATM, BTG2, CASP8, CCND3, CDKN1A, CDKN2A, CREBBP, CTNNB1, ELF3, EP300, ERBB2, ERBB3, ERCC2, FAT1 , FBXW7, FGFR3, FOXA1, FOXQ1, HRAS, KDM6A, KLF5, KMT2A, KMT2C, KMT2D, KRAS, NFE2L2, NRAS, PIK3CA, PTEN, RB1, RHOA, RHOB, RXRA, SPTAN, STAG2, TERT, TP53, TSC1, TXNIP, ZFP36L1 [Патент WO2019222325A1; Urinary DNA detection for urothelial cancer]. Так как подобные “hotspot” мутации не встречаются в нормальных клетках, то данный способ характеризуется крайне низкой вероятностью ложноположительного результата, тогда как широкая панель анализируемых мишеней позволяет добиться охвата большей части генотипов опухолей мочевого пузыря (чувствительность до 90%). Однако из уровня техники известно, что вышеперечисленные гены мутируют и в клетках широкого спектра других опухолей, например, при раке желудка, поджелудочной железы, глиомах и др. [Tomczak K., Czerwińska P., Wiznerowicz M. The Cancer Genome Atlas (TCGA): an immeasurable source of knowledge // Contemp Oncol (Pozn). 2015. Vol. 19(1A). P. A68-77. DOI: 10.5114/wo.2014.471360]. Таким образом, данный способ не позволяет проводить дифференциальную диагностику с большинством онкологических заболеваний других локализаций, клеточная и внеклеточная опухолевая ДНК, из которых может попадать в мочу из крови. Более того, секвенирование нового поколения характеризуется высокой стоимостью, необходимостью в высококвалифицированном персонале, а также в биоинформатической обработке результатов, что препятствует распространению и внедрению подобных подходов в клиническую практику.
Из уровня техники также известен способ определения вероятности наличия рака мочевого пузыря [Патент RU2718284C1; Способ скринингового определения вероятности наличия рака мочевого пузыря], подразумевающий измерение уровней биомаркеров sVCAM.1, ApoA1, СА19.9, АроА2, CYFRA.21.1, D-димера, АроВ, hsCRP, TTR, В2М в плазме или сыворотке пациента, а также определение пола с последующим включением полученных данных в классификационную модель, позволяющую рассчитать вероятность наличия заболевания. Данный способ характеризуется высокой чувствительностью, впрочем, частота ложноположительных результатов доходит до 5% (следует отметить, что гипердиагностика данного заболевания может привести к назначению избыточного хирургического лечения с частичной или тотальной резекцией мочевого пузыря, что может быть сопряжено с рядом осложнений и снижением качества жизни), а также малой инвазивностью. К недостаткам данного способа следует отнести малый потенциал к дифференциальной диагностике с другими онкологическими заболеваниями, так как из уровня техники известно, что вышеперечисленные биомаркеры повышены и при ряде других онкологических заболеваний [Dymicka-Piekarska V., Guzinska-Ustymowicz K., Kuklinski A., Kemona H. Prognostic significance of adhesion molecules (sICAM-1, sVCAM-1) and VEGF in colorectal cancer patients // Thromb Res. 2012. Vol. 129(4). P. e47-50. DOI: 10.1016/j.thromres.2011.12.004; Ballehaninna U.K., Chamberlain R.S. The clinical utility of serum CA 19-9 in the diagnosis, prognosis and management of pancreatic adenocarcinoma: An evidence-based appraisal // J Gastrointest Oncol. 2012. Vol.3(2). P. 105-19. DOI: 10.3978/j.issn.2078-6891.2011.021], а также отсутствие данных о применимости на ранних стадиях заболевания и при мониторинге рецидивов заболевания.
Таким образом, в настоящее время существует необходимость в разработке способа неинвазивной диагностики рака мочевого пузыря, лишенного всех вышеперечисленных недостатков.
Техническая проблема, решаемая посредством заявляемого изобретения, заключается в необходимости разработки способа диагностики рака мочевого пузыря, отличающегося от аналогов неинвазивностью, потенциалом к дифференциальной диагностике с другими онкологическими заболеваниями (специфичностью в отношении рака мочевого пузыря), отсутствием необходимости в привлечении высококвалифицированного персонала и биоинформатической обработке результатов измерений, применимостью на ранних стадиях заболевания и для мониторинга рецидивов заболевания после хирургического и медикаментозного лечения, а также отсутствием ложноположительных результатов.
Раскрытие изобретения
Техническим результатом заявляемого изобретения является определение в биологической жидкости пациента уровня опухолевой ДНК, несущей мутации энхансера гена GPR126, характерные для клеток опухоли мочевого пузыря, не встречающиеся в нормальных клетках организма, не распространенные в клетках иных опухолей и являющихся ранним событием туморогенеза, таким образом, подходящих для анализа на ранних стадиях заболевания [Garinet S., Pignot G., Vacher S., Le Goux C., et al. High Prevalence of a Hotspot of Noncoding Somatic Mutations in Intron 6 of GPR126 in Bladder Cancer // Mol Cancer Res. 2019 Vol. 17(2). P. 469-475. DOI: 10.1158/1541-7786.MCR-18-0363], на основании чего неинвазивно устанавливается наличие или отсутствие у пациента рака мочевого пузыря вне зависимости от стадии заболевания или рецидива опухоли после хирургического и/или медикаментозного лечения, не требующее привлечения высококвалифицированного персонала и биоинформатической обработки результатов, со специфичностью 100% и чувствительностью 36%, соответствующей распространенности данных мутаций в популяции пациентов с раком мочевого пузыря [Garinet S., Pignot G., Vacher S., Le Goux C., et al. High Prevalence of a Hotspot of Noncoding Somatic Mutations in Intron 6 of GPR126 in Bladder Cancer // Mol Cancer Res. 2019 Vol. 17(2). P. 469-475. DOI: 10.1158/1541-7786.MCR-18-0363].
Техническая проблема решается за счет создания набора реагентов, включающего прямой и обратный олигонуклеотидные праймеры с последовательностями SEQ ID NO: 1 и SEQ ID NO: 2 и комбинацию из трех флуоресцентно меченых олигонуклеотидных зондов, детектирующих две обособленные мутации энхансера гена GPR126 (хромосома 6: нуклеотидная замена G/A в позиции 142.706.206 и нуклеотидная замена С/Т в позиции 142.706.209; сборка генома GRCh37) и факт их одновременного присутствия; одного флуоресцентно меченого зонда, детектирующего соответствующую последовательность ДНК дикого типа; два олигонуклеотидных праймера, позволяющих амплифицировать участок энхансера гена GPR126, содержащий вышеназванные некодирующие мутации (размер ампликона - 121 пар оснований).
При этом олигонуклеотидные флуоресцентно меченый зонд с последовательностью SEQ ID NO: 3 специфичен к нуклеотидной замене G/A (хромосома 6: позиция 142.706.206; сборка генома GRCh37), SEQ ID NO: 4 специфичен к нуклеотидной замене С/Т (хромосома 6: позиция 142.706.209; сборка генома GRCh37), SEQ ID NO: 5 специфичен к одновременному присутствию нуклеотидных замен G/A (хромосома 6: позиция 142.706.206; сборка генома GRCh37) и С/Т (хромосома 6: позиция 142.706.209; сборка генома GRCh37) и один флуоресцентно меченый олигонуклеотидный зонд SEQ ID NO: 6, специфичный к ДНК дикого типа энхансера гена GPR126.
Техническая проблема также решается способом неинвазивной диагностики рака мочевого пузыря с выявлением опухолевой ДНК, включающим:
- выделение нуклеиновых кислот из исследуемого образца любого жидкого биоматериала (например, плазмы, сыворотки, слюны, но предпочтительно цельной мочи, так как она находится в продолжительном контакте с опухолью и может отражать как клеточный, так и внеклеточный компонент опухолевой ДНК, превосходя по содержанию данного аналита прочие биологические жидкости [Ou Z., Li K., Yang T., Dai Y., Chandra M., Ning J., Wang Y., Xu R., Gao T., Xie Y, et al. Detection of bladder cancer using urinary cell-free DNA and cellular DNA // Clin Transl Med. 2020. Vol. 9. 4. DOI: 10.1186/s40169-020-0257-2]) любым известным из уровня техники способом, например, с использованием сорбционной колонки или магнитных частиц [Pandoh P., Corbett R., McDonald H. et al. A high-throughput protocol for isolating cell-free circulating tumor DNA from peripheral blood // Biotechniques. 2019 Vol. 66(2). P. 85-92. DOI: 10.2144/btn-2018-0148];
- проведение любой известной из уровня техники вариации цифровой ПЦР, например, цифровой капельной ПЦР или цифровой ПЦР на чипах [Quan P., Sauzade M., Brouzes E. dPCR: A Technology Review // Sensors. 2018 Vol. 18(4). P. 1271. DOI: 10.3390/s18041271], с количественным определением уровней ДНК дикого типа и опухолевой ДНК, несущей мутации энхансера гена GPR126, с использованием заявляемого в данном документе набора олигонуклеотидных праймеров и флуоресцентно меченых зондов, специфичных к анализируемому фрагменту ДНК;
- расчет значения фракции опухолевой ДНК в соответствии со следующей формулой:
Ф = (Смут / (Сдт+Смут)) - 0,0185) × 100%,
где Ф - фракция опухолевой ДНК, Смут - концентрация ДНК с мутантным аллелем (копии на 1 микролитр раствора ДНК), Сдт - концентрация ДНК с аллелем дикого типа (копии на 1 микролитр раствора ДНК);
- при значении фракции опухолевой ДНК >0% делается вывод о наличии у пациента рака мочевого пузыря или рецидива опухоли после хирургического и/или медикаментозного лечения;
- при значении фракции опухолевой ДНК ≤0% делается вывод об отсутствии у пациента рака мочевого пузыря или рецидива опухоли после хирургического и/или медикаментозного лечения.
Краткое описание чертежей
Изобретение поясняется следующими чертежами.
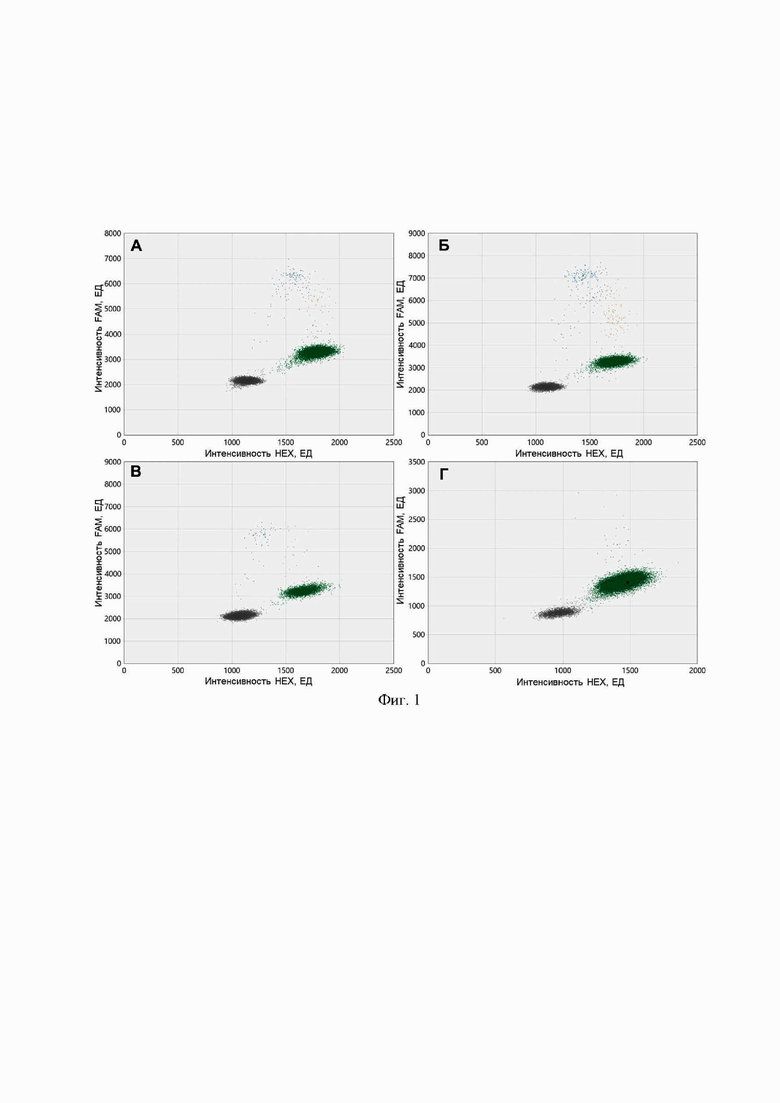
На фиг. 1 представлены примеры 2D точечных диаграмм с результатами цифровой капельной ПЦР с целью количественного анализа уровня синтетических конструкций ДНК, несущих А) нуклеотидную замену G/A (хромосома 6: позиция 142.706.206; сборка генома GRCh37); Б) нуклеотидную замену С/Т (хромосома 6: позиция 142.706.209; сборка генома GRCh37); В) одновременно нуклеотидную замену G/A (хромосома 6: позиция 142.706.206; сборка генома GRCh37) и нуклеотидную замену С/Т (хромосома 6: позиция 142.706.209; сборка генома GRCh37) и добавленных к раствору контрольной ДНК дикого типа, а также Г) раствора контрольной ДНК дикого типа без добавления синтетических конструкций ДНК. По оси X отложена интенсивность флуоресценции по каналу FAM, соответствующему флуоресцентно меченым зондам на мутантные аллели энхансера гена GPR126 по заявляемому способу. По оси Y отложена интенсивность флуоресценции по каналу HEX, соответствующему флуоресцентно меченым зондам на ДНК дикого типа энхансера гена GPR126 по заявляемому способу. Точки на диаграмме соответствуют каплям эмульсии. Кластер точек, смещенный по каналу HEX, соответствует ДНК дикого типа. Кластер точек, смещенный по каналу FAM, соответствует синтетическим конструкциям ДНК, несущим вышеописанные мутации.
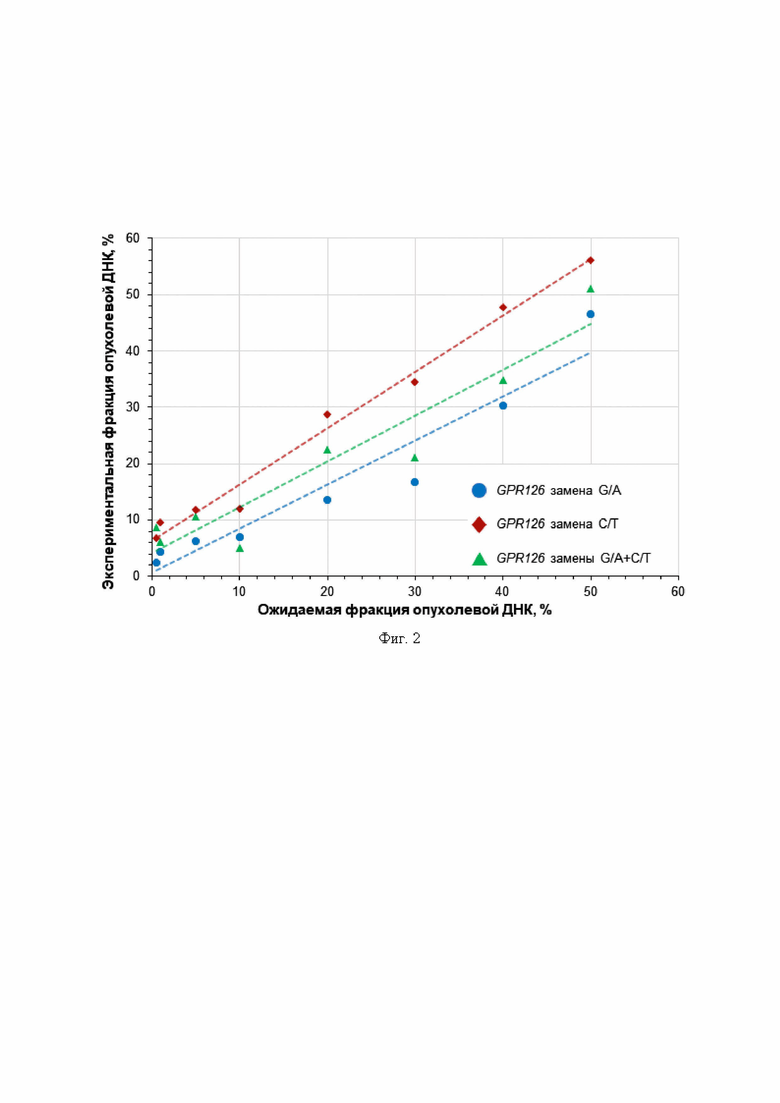
На фиг. 2 представлены результаты определения линейности количественного анализа уровня синтетических конструкций ДНК, несущих мутации энхансера гена GPR126, добавленных к раствору ДНК дикого типа в разных концентрациях. По оси X отложены ожидаемые значения концентрации синтетических конструкций ДНК, полученные в ходе их разведения в растворе ДНК дикого типа. По оси Y отложены экспериментально полученные значения концентрации синтетических конструкций ДНК в заданных разведениях, определенные по заявляемому способу. Пунктирной линией проведены кривые линейной апроксимации. Обозначение «GPR126 замена G/A» соответствует данным от экспериментов по анализу синтетических конструкций ДНК с нуклеотидной заменой G/A (хромосома 6: позиция 142.706.206; сборка генома GRCh37). Обозначение «GPR126 замена С/Т» соответствует данным от экспериментов по анализу синтетических конструкций ДНК с нуклеотидной заменой С/Т (хромосома 6: позиция 142.706.209; сборка генома GRCh37). Обозначение «GPR126 замены G/A + С/Т» соответствует данным от экспериментов по анализу синтетических конструкций ДНК с одновременным присутствием нуклеотидных замен G/A (хромосома 6: позиция 142.706.206; сборка генома GRCh37) и С/Т (хромосома 6: позиция 142.706.209; сборка генома GRCh37).
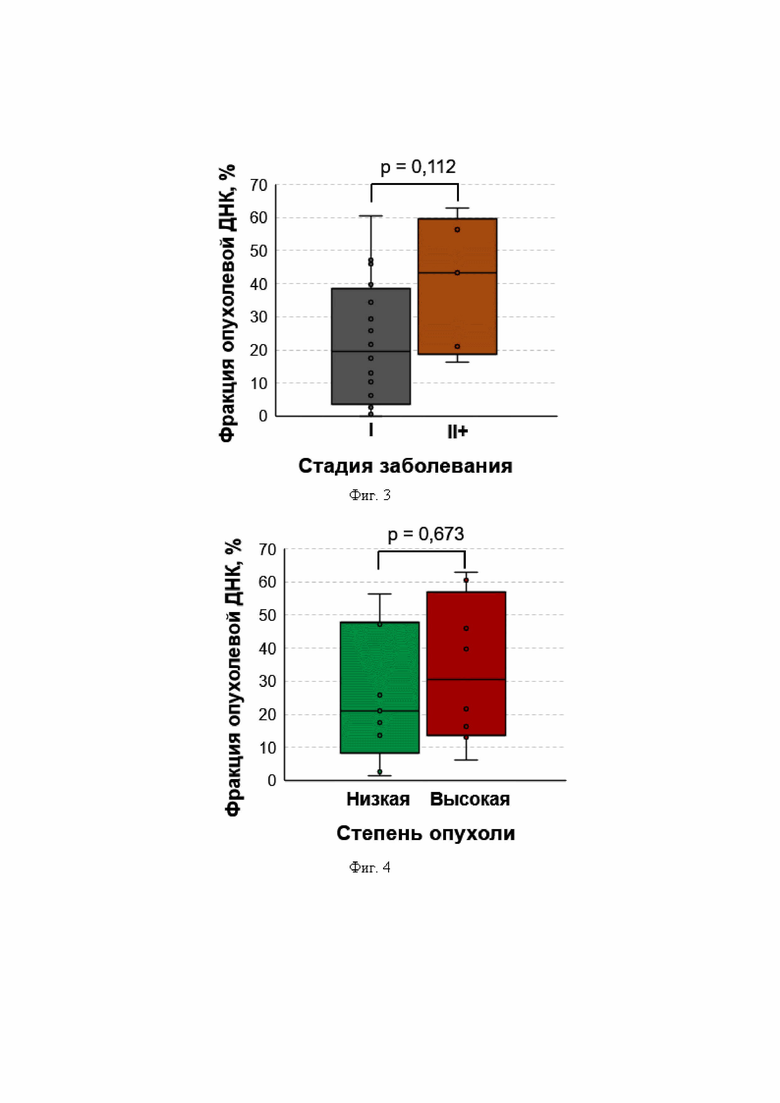
На фиг. 3 представлены диаграммы «ящики с усами» для сравнения фракций опухолевой ДНК, несущей мутации энхансера гена GPR126, по заявляемому способу между пациентами со стадиями заболевания I и II и более (II+). По оси Х отложена принадлежность данных к группе. По оси Y отложена фракция опухолевой ДНК, выраженная в процентах. Показано отсутствие статистически значимых различий; р-значение было рассчитано с использованием U-критерия Манна-Уитни.
На фиг. 4 представлены диаграммы «ящики с усами» для сравнения фракций опухолевой ДНК, несущей мутации энхансера гена GPR126, по заявляемому способу между пациентами со степенью опухоли низкой и высокой. По оси Х отложена принадлежность данных к группе. По оси Y отложена фракция опухолевой ДНК, выраженная в процентах. Показано отсутствие статистически значимых различий; р-значение было рассчитано с использованием U-критерия Манна-Уитни.
Осуществление изобретения
Для реализации способа неинвазивной диагностики рака мочевого пузыря с выявлением опухолевой ДНК в биологических жидкостях был разработан набор реагентов (модифицированных и немодифицированных олигонуклеотидов), позволяющий детектировать ДНК дикого типа и опухолевую ДНК, несущую мутации энхансера гена GPR126, характерные для клеток рака мочевого пузыря и не распространенные в клетках иных опухолей. Данный набор реагентов включает прямой (SEQ ID NO: 1) и обратный (SEQ ID NO: 2) олигонуклеотидные праймеры, амплифицирующие фрагмент энхансера гена GPR126 размером 121 пар оснований; меченые 6-карбоксифлуоресцеином (FAM) и тушителем флуоресценции «Black Hole Quencher 1» (BHQ1) зонд на мутацию G/A (хромосома 6: позиция 142.706.206; сборка генома GRCh37) (SEQ ID NO: 3), зонд на мутацию С/Т (хромосома 6: позиция 142.706.209; сборка генома GRCh37) (SEQ ID NO: 4), зонд на одновременное присутствие мутаций G/A и С/Т (хромосома 6: позиции 142.706.209 и 142.706.209; сборка генома GRCh37) (SEQ ID NO: 5); меченый гексафлуоресцеином (HEX) и тушителем флуоресценции «Black Hole Quencher 1» (BHQ1) зонд на ДНК дикого типа (SEQ ID NO: 6), которые могут быть синтезированы и мечены любым известным из уровня техники способом, например, в ходе прямого синтеза с постсинтетическим конъюгированием флуоресцентной метки [Zearfoss N., Ryder S. End-labeling oligonucleotides with chemical tags after synthesis // Methods Mol Biol. 2012. Vol. 941. P. 181-193. DOI: 10.1007/978-1-62703-113-4_14]. Представленный набор реагентов подходит для применения с любой системой для цифровой ПЦР, например, цифровой капельной ПЦР или цифровой ПЦР на чипах [Quan P., Sauzade M., Brouzes E. dPCR: A Technology Review // Sensors. 2018 Vol. 18(4). P. 1271. DOI: 10.3390/s18041271].
5’-ATGGGAATATTATAATTCTAACTAA-3’ (SEQ ID NO: 1)
5’-CACCGTATAAATGTTCTTG-3’ (SEQ ID NO: 2)
5’-FAM-TTTGTATAAACATACAAAGAGCCTC-BHQ1-3’ (SEQ ID NO: 3)
5’-FAM-TTTGTATGAATATACAAAGAGCCTC-BHQ1-3’ (SEQ ID NO: 4)
5’-FAM-TTTGTATAAATATACAAAGAGCCTC-BHQ1-3’ (SEQ ID NO: 5)
5’-HEX-TTTGTATGAACATACAAAGAGCCTC-BHQ1-3’ (SEQ ID NO: 6)
Доклиническая валидация разработанного набора реагентов проводилась с использованием контрольных образцов ДНК дикого типа, выделенных из клеточной линии Raji (Евроген, Москва, Россия), не несущей некодирующих мутаций в гене GPR126, а также с использованием трех синтетических конструкций, представляющих собой фрагмент гена GPR126 из ДНК клеточной линии Raji, клонированный при помощи pAL2-T вектора (Евроген, Москва, Россия) и подвергнутый сайт-направленному мутагенезу с внесением нуклеотидных замен, имитирующих две обособленные мутации энхансера гена GPR126 (хромосома 6: нуклеотидная замена G/A в позиции 142.706.206 и нуклеотидная замена С/Т в позиции 142.706.209; сборка генома GRCh37) и факт их одновременного присутствия. Для определения линейности анализа с использованием разработанного набора реагентов вышеуказанные синтетические конструкции, несущие некодирующие мутации гена GPR126, вносились в раствор контрольной ДНК дикого типа в широком диапазоне концентраций, имитирующих ожидаемые фракции опухолевой ДНК в жидком биоматериале пациентов на основе предыдущего опыта анализа опухолевой ДНК (0,5-50,0%) [Jain M., Kamalov D., Tivtikyan A. et al. Urine TERT promoter mutations-based tumor DNA detection in patients with bladder cancer: A pilot study // Molecular and Clinical Oncology 2021. Vol. 15 (253). DOI:10.3892/mco.2021.2415]. Пример 2D-точечных диаграмм цифровой капельной ПЦР представлен на фиг. 1. Разработанный набор реагентов позволял проводить количественный анализ синтетических конструкций, несущих искомые некодирующие мутации, с высокой линейностью (фиг. 2). Коэффициенты линейности (R2) для синтетических конструкций, имитирующих обособленную мутацию энхансера гена GPR126 (хромосома 6: нуклеотидная замена G/A в позиции 142.706.206; сборка генома GRCh37), обособленную мутацию энхансера гена GPR126 (хромосома 6: нуклеотидная замена С/Т в позиции 142.706.209; сборка генома GRCh37) и факт их одновременного присутствия, составили 0,923, 0,986, 0,902 соответственно.
При серийном анализе контрольных образцов ДНК дикого типа было установлено, что количество ложноположительных по мутантным аллелям капель при проведении цифровой капельной ПЦР с использованием разработанного набора реагентов коррелировало с общей концентрацией ДНК в растворе (коэффициент корреляции Спирмена составил 0,593; р<0,001). Таким образом, пороговое значение для ложноположительного сигнала при проведении цифровой капельной ПЦР в ходе клинической валидации набора реагентов определялось для фракции опухолевой ДНК (выраженной в %), а не для абсолютного числа копий мутантного аллеля.
Клиническая валидация разработанного набора реагентов проводилась на биоматериале от 70 пациентов с мышечно-неинвазивным раком мочевого пузыря, подтвержденным гистологически (группа рака мочевого пузыря), от 22 пациентов с различными формами цистита (группа цистита), а также от 50 здоровых добровольцев, не имеющих урологических заболеваний и семейного анамнеза рака мочевого пузыря (контрольная группа). В качестве биоматериала использовалась цельная моча. Клинико-демографическая характеристика участников исследования представлена в табл. 1.
(n=70)
(n=22)
(n=50)
- Мужской
- Женский
9 (12,8%)
10 (45,5%)
26 (52%)
- I
- II
- IIIA
- IIIB
- IVA
2 (2,9%)
6 (8,6%)
1 (1,4%)
1 (1,4%)
Н/Д
Н/Д
Н/Д
Н/Д
Н/Д
Н/Д
Н/Д
Н/Д
- Низкая
- Высокая
- Неизвестная
20 (28,6%)
17 (24,3%)
Н/Д
Н/Д
Н/Д
Н/Д
Примечание: Н/Д - нет данных; * - среднее (разброс); ** - медиана [интерквартильный размах].
В ходе количественного анализа опухолевой ДНК, несущей мутации энхансера гена GPR126, в образцах мочи участников исследования из контрольной группы и группы цистита было установлено, что максимальное значение ложноположительной фракции опухолевой ДНК составляло 1,79%. ROC-анализ на общей выборке продемонстрировал, что при пороговом значении 1,85% специфичность анализа составила 100% (отсутствие ложноположительных результатов). Данное значение было внесено в конечную формулу для подсчета фракции опухолевой ДНК. В группе рака мочевого пузыря уровень опухолевой ДНК, несущей мутации энхансера гена GPR126, выше порога наблюдался у 25 пациентов при медианном значении фракции опухолевой ДНК - 21,61 [8,30-44,52] %. Подобная выявляемость (с поправкой на неинвазивную природу анализа, т.е. анализ опухолевых дериватов в биологической жидкости, а не в непосредственном опухолевом материале, полученном при биопсии или хирургическом вмешательстве) согласуется с теоретической распространенностью некодирующих мутаций гена GPR126 в популяции пациентов с раком мочевого пузыря, которая близка к 50% [Garinet S., Pignot G., Vacher S., Le Goux C., et al. High Prevalence of a Hotspot of Noncoding Somatic Mutations in Intron 6 of GPR126 in Bladder Cancer // Mol Cancer Res. 2019 Vol. 17(2). P. 469-475. DOI: 10.1158/1541-7786.MCR-18-0363]. Статистически значимой ассоциации фракции опухолевой ДНК с макрогематурией выявлено не было (p>0,05). Не было обнаружено статистически значимых различий фракции опухолевой ДНК между пациентами со стадиями заболевания I и II-IV (фиг. 3), а также между пациентами с низкой и высокой степенью заболевания (фиг. 4), что подтверждает тот факт, что некодирующие мутации гена GPR126 являются ранними событиями в туморогенезе опухолей мочевого пузыря, а значит, они пригодны для выявления опухолевой ДНК на ранних стадиях заболевания.
Ниже представлено более детальное описание заявляемого способа, которое не ограничивает объем притязаний заявляемого изобретения, а демонстрирует возможность осуществления изобретения с достижением заявляемого технического результата.
1) В качестве субстрата для анализа опухолевой ДНК по заявляемому способу допустимо использовать любой жидкий биоматериал пациента, например, плазму, сыворотку, слюну, но предпочтительно цельную мочу.
2) Выделение нуклеиновых кислот из жидкого биоматериала можно проводить с использованием любого известного из уровня техники набора реагентов и расходуемых материалов при соблюдении всех рекомендаций производителя, например, с использованием сорбционной колонки или магнитных частиц.
3) Количественный анализ опухолевой ДНК, несущей мутации энхансера гена GPR126, характерные для рака мочевого пузыря, можно проводить с использованием любой известной из уровня техники вариации цифровой ПЦР, например, цифровой капельной ПЦР или цифровой ПЦР на чипах.
4) В реакционную смесь для цифровой ПЦР вносить заявляемые олигонуклеотидные праймеры (SEQ ID NO: 1 и SEQ ID NO: 2) в конечной концентрации 0,2-1,2 мкмоль/л, но предпочтительно в концентрации 0,9 мкмоль/л.
5) В реакционную смесь для цифровой ПЦР вносить заявляемые флуоресцентно меченые зонды на мутантные аллели (SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5) в конечной концентрации по 0,05-0,3 мкмоль/л, но предпочтительно 0,083 мкмоль/л, а флуоресцентно меченые зонды на ДНК дикого типа (SEQ ID NO: 6) - в конечной концентрации 0,15-0,9 мкмоль/л, но предпочтительно 0,25 мкмоль/л, что позволит проводить скрининговый анализ на наличие опухолевой ДНК, несущей две мутации энхансера гена GPR126 (хромосома 6: нуклеотидная замена G/A в позиции 142.706.206; нуклеотидная замена С/Т в позиции 142.706.209; сборка генома GRCh37), а также факт их одновременного присутствия, в одной пробирке, без необходимости выполнять 3 отдельные реакции.
6) Предпочтительно для цифровой ПЦР использовать двуступенчатый протокол амплификации (41 цикл), рекомендуемый производителем, с этапом отжига / элонгации при температуре 53,7°С в течение 60 с.
7) Расчет значения значения фракции опухолевой ДНК необходимо проводить в соответствии со следующей формулой:
Ф = ((Смут / (Сдт + Смут)) - 0,0185) × 100%,
где Ф - фракция опухолевой ДНК, Смут - концентрация ДНК с мутантным аллелем (копии на 1 микролитр раствора ДНК), Сдт - концентрация ДНК с аллелем дикого типа (копии на 1 микролитр раствора ДНК);
8) При значении фракции опухолевой ДНК >0% делается вывод о наличии у пациента рака мочевого пузыря или рецидива опухоли после хирургического и/или медикаментозного лечения;
9) При значении фракции опухолевой ДНК ≤0% делается вывод об отсутствии у пациента рака мочевого пузыря или рецидива опухоли после хирургического и/или медикаментозного лечения.
10) В случае возникновения необходимости количественного анализа опухолевой ДНК по каждой из вышеобозначенных мутаций (а также факта их одновременного присутствия) по отдельности в п.5 изменить алгоритм действий, а именно в реакционную смесь для цифровой ПЦР вносить заявляемые флуоресцентно меченые зонды SEQ ID NO: 3 и SEQ ID NO: 6 в конечной концентрации по 0,15-0,9 мкмоль/л, но предпочтительно 0,25 мкмоль/л - для анализа мутации энхансера гена GPR126 (хромосома 6: нуклеотидная замена G/A в позиции 142.706.206; сборка генома GRCh37); SEQ ID NO: 4 и SEQ ID NO: 6 в концентрации по 0,15-0,9 мкмоль/л, но предпочтительно 0,25 мкмоль/л - для анализа мутации энхансера гена GPR126 (хромосома 6: нуклеотидная замена С/Т в позиции 142.706.209; сборка генома GRCh37); SEQ ID NO: 5 и SEQ ID NO: 6 в концентрации по 0,15-0,9 мкмоль/л, но предпочтительно 0,25 мкмоль/л - для анализа одновременного присутствия обеих мутаций энхансера гена GPR126 (хромосома 6: нуклеотидная замена G/A в позиции 142.706.206 и нуклеотидная замена С/Т в позиции 142.706.209; сборка генома GRCh37), тогда как п.6-9 оставить неизменными.
Пример 1
Пациентка К., женщина, 81 год. Обратилась с жалобами на учащенное болезненное мочеиспускание, кровь в моче. У пациента был взят образец цельной мочи. ДНК выделялась из 4 мл биоматериала. В полученных растворах ДНК был проведен количественный анализ опухолевой ДНК, несущей мутации энхансера гена GPR126, методом цифровой капельной ПЦР в соответствии с заявляемым способом.
Концентрация ДНК с мутантным аллелем составила 142 копии/мкл, ДНК дикого типа - 677 копий/мкл. Данные значения для каждого из образцов были подставлены в формулу расчета фракции опухолевой ДНК по заявляемому способу:
Ф = ((142 копии/мкл) / (677 копий/мкл + 142 копии/мкл)) - 0,0185)×100% = 15,49%
Значение фракции опухолевой ДНК оказалось более 0%, был сделан вывод о наличии рака мочевого пузыря.
Параллельно пациенту были выполнены ультразвуковое исследование, цистоскопия с биопсией, а также компьютерная томография органов малого таза. По результатам гистологического исследования был поставлен диагноз папиллярный уротелиальный рак мочевого пузыря, стадия I (T1N0M0). Пациенту было назначено хирургическое и химиотерапевтическое лечение.
Таким образом, результаты неинвазивной диагностики рака мочевого пузыря с выявлением опухолевой ДНК, несущей мутации энхансера гена GPR126, по заявляемому способу совпадали с таковыми при использовании рутинных инструментальных методов с инвазивным забором биоматериала.
Пример 2
Пациент Б., мужчина, 62 года. Прооперирован в связи с раком мочевого пузыря (трансуретральная резекция), прибыл на контрольный осмотр через 3 месяца после операции. У пациента был взят образец цельной мочи. ДНК выделялась из 4 мл биоматериала. В полученных растворах ДНК был проведен количественный анализ опухолевой ДНК, несущей мутации энхансера гена GPR126, методом цифровой капельной ПЦР в соответствии с заявляемым способом.
Концентрация ДНК с мутантным аллелем составила 9 копий/мкл, ДНК дикого типа - 383 копий/мкл. Данные значения для каждого из образцов были подставлены в формулу расчета фракции опухолевой ДНК по заявляемому способу:
Ф = ((9 копии/мкл) / (383 копий/мкл + 9 копии/мкл)) - 0,0185) × 100% = 0,45%
Значение фракции опухолевой ДНК оказалось более 0%, был сделан вывод о рецидиве рака мочевого пузыря.
Параллельно пациенту была выполнена цистоскопия с биопсией. По результатам гистологического исследования рецидив рака мочевого пузыря установлен не был.
Через 3 месяца на следующем контрольном осмотре пациенту вновь были выполнены цистоскопия с биопсией. По результатам гистологического исследования был установлен рецидив рака мочевого пузыря. Было назначено повторное хирургическое лечение.
Таким образом, результаты неинвазивной диагностики рецидива рака мочевого пузыря с выявлением опухолевой ДНК, несущей мутации энхансера гена GPR126, по заявляемому способу совпадали с таковыми при использовании рутинных инструментальных методов с инвазивным забором биоматериала и, более того, опережали их на 3 месяца.
Пример 3
Пациент В., мужчина, 74 года. Обратился с жалобами на учащенное болезненное мочеиспускание, кровь в моче. У пациента был взят образец цельной мочи. ДНК выделялась из 4 мл биоматериала. В полученных растворах ДНК был проведен количественный анализ опухолевой ДНК, несущей мутации энхансера гена GPR126, методом цифровой капельной ПЦР в соответствии с заявляемым способом.
Концентрация ДНК с мутантным аллелем составила 14 копии/мкл, ДНК дикого типа - 802 копии/мкл. Данные значения для каждого из образцов были подставлены в формулу расчета фракции опухолевой ДНК по заявляемому способу:
Ф = ((14 копии/мкл) / (802 копии/мкл + 14 копии/мкл)) - 0,0185) × 100% = минус 0,001%
Значение фракции опухолевой ДНК оказалось ниже 0%, был сделан вывод об отсутствии рака мочевого пузыря.
Параллельно пациенту были выполнены ультразвуковое исследование, цистоскопия с биопсией. По результатам гистологического исследования был поставлен диагноз геморрагический цистит. Пациенту был выполнен бактериальный посев мочи, назначена антибиотикотерапия.
Таким образом, результаты неинвазивной диагностики рака мочевого пузыря с выявлением опухолевой ДНК, несущей мутации энхансера гена GPR126, по заявляемому способу совпадали с таковыми при использовании рутинных инструментальных методов с инвазивным забором биоматериала.
Настоящее изобретение относится к области медицины, в частности к клинической лабораторной диагностике в области онкоурологии, и может быть использовано для неинвазивной диагностики рака мочевого пузыря и рецидива опухоли после хирургического и/или медикаментозного лечения. Изобретение включает способ количественного анализа опухолевой ДНК, несущей мутации энхансера гена GPR126, в биологических жидкостях, а также набор реагентов для цифровой полимеразной цепной реакции, позволяющий его осуществить. Проводят выделение ДНК из биологической жидкости, количественный анализ опухолевой ДНК (Смут), ДНК дикого типа (Сдт), расчет фракции опухолевой ДНК (Ф) по формуле Ф = ((Смут / (Сдт + Смут)) - 0,0185) × 100%. При получении значения Ф более 0% делают вывод о наличии рака мочевого пузыря. В случае, если значение Ф равно или менее 0% делают вывод об отсутствии рака мочевого пузыря. Способ и набор реагентов для его осуществления позволяют проводить неинвазивную диагностику рака мочевого пузыря на ранних стадиях заболевания при низкой вероятности ложноположительных результатов, так как мутации энхансера гена GPR126 не встречаются в здоровых клетках организма. 2 н. и 3 з.п. ф-лы, 4 ил., 1 табл.
1. Набор реагентов для проведения цифровой полимеразной цепной реакции с целью выявления опухолевой ДНК, несущей мутации энхансера гена GPR126, включающий прямой и обратный олигонуклеотидные праймеры с последовательностями SEQ ID NO: 1 и SEQ ID NO: 2, позволяющие амплифицировать фрагмент энхансера гена GPR126, три олигонуклеотидных флуоресцентно меченых зонда с последовательностями SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, специфичных к мутациям энхансера гена GPR126, один флуоресцентно меченый олигонуклеотидный зонд SEQ ID NO: 6, специфичный к ДНК дикого типа энхансера гена GPR126.
2. Способ диагностики рака мочевого пузыря с выявлением опухолевой ДНК, несущей мутации энхансера гена GPR126, в образцах жидкого биоматериала, характеризующийся тем, что включает выделение ДНК, количественный анализ опухолевой ДНК, несущей мутации энхансера гена GPR126 с использованием набора реагентов по п. 1, расчет фракции опухолевой ДНК, при значении фракции опухолевой ДНК, несущей мутации энхансера гена GPR126, более 0% делают вывод о наличии у пациента рака мочевого пузыря или рецидива опухоли, при значении равной или менее 0% делают вывод об отсутствии у пациента рака мочевого пузыря или рецидива опухоли.
3. Способ по п. 2, характеризующийся тем, что для одновременного детектирования двух мутаций энхансера гена GPR126, а также факта их одновременного присутствия в одной реакционной смеси выполняют цифровую полимеразную цепную реакцию, смешивая олигонуклеотидные флуоресцентно меченые зонды с последовательностями SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5 в равном соотношении.
4. Способ по п. 2, характеризующийся тем, что для детектирования мутаций энхансера гена GPR126, а также факта их одновременного присутствия по отдельности в разных реакционных смесях выполняют цифровую полимеразную цепную внося олигонуклеотидные флуоресцентно меченые зонды с последовательностями SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5 отдельно в разные реакционные смеси.
5. Способ по п. 2, характеризующийся тем, что для расчета фракции опухолевой ДНК, несущей мутации энхансера гена GPR126, используют формулу:
Ф = ((Смут / (Сдт + Смут)) – 0,0185) × 100%,
где Ф – фракция опухолевой ДНК, Смут – концентрация ДНК с мутантным аллелем, копии на 1 микролитр раствора ДНК; Сдт – концентрация ДНК с аллелем дикого типа, копии на 1 микролитр раствора ДНК.
Авторы
Даты
2024-02-15—Публикация
2023-07-31—Подача