Изобретение относится к способу получения новых азот-, кислород- или серосодержащих гетероциклических соединений, а именно 6-арил-замещенных 5-ацетил-4-(2,4-дигидроксифенил)-4-метилгексагидропирими-дин-2-онов(тионов), которые могут быть использованы в качестве прекурсоров для синтеза биологически активных веществ и лекарственных препаратов.
Данные соединения являются новыми, и из уровня техники нам не известны способы получения таких соединений.
Техническим результатом изобретения является разработка способа получения 6-арил-замещенных 5-ацетил-4-(2,4-дигидроксифенил)-4-метилгексагидропирими-дин-2-онов(тионов) общей структурной формулы:
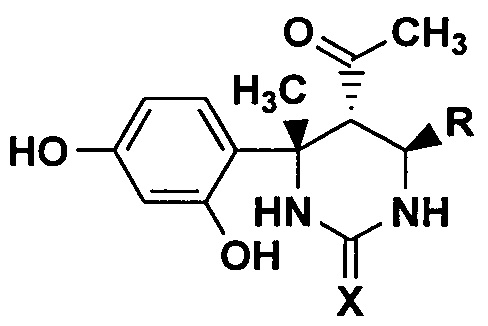
где R=С6Н5 или 4-ClC6H4 или 4-МеС6Н4 или 4-МеОС6Н4, X=О или S
Технический результат достигается тем, что в качестве реагентов для синтеза 6-арилзамещенных 5-ацетил-4-(2,4-дигидроксифенил)-4-метилгекса-гидропиримидин-2-онов(тионов) используют полученные реакцией Биджи-нелли 4-арилзамещенные 5-ацетил-6-метилдигидропиримидин-2-оны(тионы) и бензол-1,3-диол, которые взаимодействуют в растворе четыреххлористого углерода (CCl4) и уксусной (АсОН) кислоты в присутствии метансульфоновой (CH3SO3H) кислоты.
Вышеуказанные соединения получают следующей реакцией:
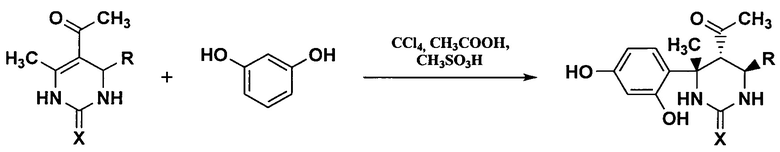
при условиях, описанных ниже.
Реакционную смесь, состоящую из 4-арилзамещенных 5-ацетил-6-метилдигидропиримидин-2-онов(тионов) и бензол-1,3-диола (мольное соотношение 1:2, соответственно), нагревают в CCl4 и АсОН с добавлением CH3SO3H при температуре 30…40°С в течение 24-28 часов. Затем полученную реакционную массу охлаждают и выливают в водный раствор гидрокарбоната натрия (NaHCO3). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из хлороформа. Сушат на воздухе.
Все приведенные признаки являются существенными, и только заявляемая совокупность признаков позволяет достичь технического результата.
Строение полученных соединений подтверждено методами ИК, ЯМР Н1, ЯМР С13, NOESY, НМВС- спектроскопией и масс-спектрометрией.
Изобретение иллюстрируется следующими примерами.
Пример 1. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-фенил-гексагидропиримидин-2-тион:
Смесь 5-ацетил-6-метил-4-фенил-дигидропиримидин-2-тиона (1 ммоль) с бензол-1,3-диолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 30°С в течение 27 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 8 мл хлороформа. Сушат на воздухе. Получают 221 мг (62% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-фенил-гексагидропиримидин-2-тиона - кристаллический осадок желтого цвета, Тпл=201-203°С. ИК спектр, ν/см-1: 3409 (ОН), 3335, 3295 (NH), 1710 (С=O), 1615 (С=С), 1207 (C=S), 1195, 1183, 1125 (С-О-С). Спектр ЯМР 1Н (400 МГц, δ, м.д., J/Гц): 1.43 (с, 3 Н, С(4)СН3), 1.65 (с, 3 Н, С(5)СОСН3), 4.02 (д, 1 Н, С(6)Н, J=4.6), 4.08 (д, 1 Н, С(5)Н, J=4.6), 6.25 (дд, 1 Н, С(5')Н, J=8.5, J=1.6), 6.40 (д, 1 Н, С(3')Н, J=1.6), 6.91 (д, 1 Н, С(6')Н, J=8.5), 7.21-7.37 (м, 5 Н, С(2'', 3'', 4'', 5'', 6'')Н), 8.24 (с, 1 Н, N(l)H), 8.44 (с, 1 Н, N(3)H), 9.31 (уш.с, 1 Н, С(4')ОН), 9.80 (уш.с, 1 Н, С(2')ОН). Спектр ЯМР 13С (100 МГц, δ, м.д.): 22.80, 33.90, 53.45, 53.82, 54.38, 104.20, 106.18, 122.20, 126.56 (2 С), 127.71, 128.51, 128.65 (2 С), 137.89, 153.68, 157.76, 174.12, 206.33. Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 356 [М]+ (0,5), 313 [М-Ас]+ (30), 237 (48), 203 (29), 177 (25), 152 (11), 136 (11), 104 (18), 77 (21), 43 (100). Найдено (%): С, 63.81; Н, 5.64; N, 7.83. C19H20N2O3S. Вычислено (%): С, 64.02; Н, 5.66; N, 7.86.
Пример 2. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-хлорфенил)-гексагидропиримидин-2-тион:
Смесь 5-ацетил-6-метил-4-(4-хлорфенил)-дигидропиримидин-2-тиона (1 ммоль) с бензол-1,3-диолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 40°С в течение 25 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 6 мл хлороформа. Сушат на воздухе. Получают 306 мг (78% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-хлорфенил)-гексагидропиримидин-2-тиона -кристаллический осадок белого цвета, Тпл=207-209°С.ИК спектр, ν/cm-1: 3401 (ОН), 3318, 3240 (NH), 1709 (С=O), 1616 (С=С), 1204 (C=S), 1184, 1123 (С-О-С). Спектр ЯМР 1Н (400 МГц, 5, м.д., J/Гц): 1.44 (с, 3 Н, С(4)СН3), 1.71 (с, 3 Н, С(5)СОСН3), 4.01 (д, 1 Н, С(6)Н, J=4.6), 4.08 (д, 1 Н, С(5)Н, J=4.6), 6.25 (дд, 1 Н, С(5')Н, J=8.6, J=2.2), 6.40 (д, 1 Н, С(3')Н, J=2.2), 6.87 (д, 1 Н, С(6')Н, J=8.6), 7.05 (д, 2 Н, С(3'',5'')Н, J=8.6), 7.37 (д, 2 Н, С(2'',6'')Н, J=8.5), 8.31 (с, 1 Н, N(l)H), 8.42 (с, 1 Н, N(3)H), 9.36 (с, 1 Н, С(4')ОН), 9.80 (с, 1 Н, С(2')ОН). Спектр ЯМР 13С (100 МГц, δ, м.д.): 22.83, 33.95, 53.27, 53.76, 58.26, 104.21, 106.15, 121.97, 128.22 (2 С), 128.26 (2 С), 128.41, 131.95, 136.91, 153.67, 157.77, 177.00, 206.23. Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 390 [М]+ (7), 372 (23), 347 [М-Ас]+ (25), 281 [M-Rezorcin]+ (24), 280 (82), 271 (49), 261 (53), 247 (19), 237 (67), 229 (84), 204 (17), 188 (15), 178 (14), 174 (20), 151 (20), 140 (100), 125 (31), 110 (68), 82 (42), 43 (93). Найдено (%): С, 58.12; Н, 4.88; N, 7.13. C19H19ClN2O3S. Вычислено (%): С, 58.38; Н, 4.90; N, 7.17.
Пример 3. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метилфенил)-гексагидропиримидин-2-тион:
Смесь 5-ацетил-6-метил-4-(4-метилфенил)-дигидропиримидин-2-тиона (1 ммоль) с бензол-1,3-диолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 35°С в течение 28 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 10 мл хлороформа. Сушат на воздухе. Получают 156 мг (42% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метилфенил)-гексагидропиримидин-2-тиона - кристаллический осадок белого цвета, Тпл=213-215°С. ИК спектр, ν/cm-1: 3401 (ОН), 3318, 3240 (N-H), 1709 (С=O), 1616 (С=С), 1204 (C=S), 1184, 1123 (С-О-С). Спектр ЯМР 1H (400 МГц, δ, м.д., J/Гц): 1.42 (с, 3 Н, С(4)СН3), 1.67 (с, 3 Н, С(5)СОСН3), 2.24 (с, 3 Н, С(4'')СН3), 3.98 (д, 1 Н, С(6)Н, J=4.7), 4.05 (д, 1 Н, С(5)Н, J=4.7), 6.24 (дд, 1 Н, С(5')Н, J=8.6, J=2.0), 6.39 (д, 1 Н, С(3')Н, J=2.0), 6.88 (д, 1 Н, С(6')Н, J=8.6), 6.91 (д, 2 Н, С(3'',5'')Н, J=8.0), 7.10 (д, 2 Н, С(2'',6'')Н, J=8.0), 8.29 (с, 1 Н, N(1)H), 8.49 (с, 1 Н, N(3)H), 9.35 (уш.с, 1 Н, С(4')ОН), 9.79 (с, 1 Н, С(2')ОН). Спектр ЯМР 13С (100 МГц, δ, м.д.): 20.60, 22.81, 33.82, 53.48, 54.10, 58.24, 104.19, 106.13, 122.2, 126.13 (2 С), 128.49, 128.84 (2 С), 134.78, 136.62, 153.65, 157.72, 176.92, 206.37. Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 370 [М]+ (0,2), 327 [М-Ас]+ (17), 251 (15), 217 (10), 91 (10), 43 (100). Найдено (%): С, 64.79; Н, 5.96; N, 7.53. C20H22N2O3S. Вычислено (%): С, 64.84; Н, 5.99; N, 7.56.
Пример 4. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метоксифенил)-гексагидропиримидин-2-тион:
Смесь 5-ацетил-6-метил-4-(4-метоксифенил)-дигидропиримидин-2-тиона (1 ммоль) с бензол-1,3-диолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 40°С в течение 24 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 5 мл хлороформа. Сушат на воздухе. Получают 105 мг (27% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метоксифенил)-гексагидропиримидин-2-тиона - кристаллический осадок розового цвета, Тпл=198-200°С. ИК спектр, ν/cm-1: 3454 (ОН), 3311, 3230 (N-H), 1695 (С=O), 1618 (С=С), 1201 (C=S), 1180, 1018 (С-О-С). Спектр ЯМР 1Н (400 МГц, δ, м.д., J/Гц): 1.43 (с, 3 Н, С(4)СН3), 1.69 (с, 3 Н, С(5)СОСН3), 3.71 (с, 3 Н, С(4'')ОСН3), 3.99 (д, 1 Н, С(6)Н, J=4.4), 4.04 (д, 1 Н, С(5)Н, J=4.4), 6.25 (дд, 1 Н, С(5')Н, J=8.6, J=2.0), 6.39 (д, 1 Н, С(3')Н, J=2.0), 6.85 (д, 2 Н, С(3'',5'')Н, J=8.5), 6.89 (д., 1 Н, С(6')Н, J=8.6), 6.95 (д, 2 Н, С(2'',6'')Н, J=8.5), 8.20 (уш.с, 1 Н, N(1)H), 8.42 (уш.с, 1 Н, N(3)H), 9.29 (уш.с, 1 Н, С(4')ОН), 9.74 (уш.с, 1 Н, С(2')ОН). Спектр ЯМР 13С (100 МГц, δ, м.д.): 22.81, 33.96, 53.47, 53.84, 55.07, 58.25, 104.21, 106.13, 113.68 (2 С), 122.26, 127.44 (2 С), 128.51, 129.55, 153.67, 157.72, 158.54, 176.85, 206.58. Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 386 [М]+ (17), 343 [М-Ас]+ (53), 276 [M-Rezorcin]+ (18), 267 (32), 261 (10), 233 (24), 199 (12), 134 (16), 110 (18), 77 (13), 43 (100). Найдено (%): С, 61.92; Н, 5.72; N, 7.22. C20H22N2O4S. Вычислено (%): С, 62.16; Н, 5.74; N, 7.25.
Пример 5. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-фенил-гексагидропиримидин-2(1H)-он:
Смесь 5-ацетил-6-метил-4-фенил-дигидропиримидин-2(1H)-она (1 ммоль) с бензол-1,3-бензолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 30 °С в течение 28 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 8 мл хлороформа. Сушат на воздухе. Получают 123 мг (36% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-фенил-гексагидропиримидин-2(1H)-она - кристаллический осадок белого цвета, Тпл=197-199°С.ИК спектр, ν/см-1: 3417 (ОН), 3304 (N-H), 1710 (С=O), 1645 (С=О), 1599 (С=С), 1172, 1125 (С-О-С). Спектр ЯМР 1H (400 МГц, δ, м.д., J/Гц): 1.38 (с, 3 Н, С(4)СН3), 1.71 (с, 3 Н, С(5)СОСН3), 4.04 (д, 1 Н, С(5)Н, J=4.2), 4.07 (д, 1 Н, С(6)Н, J=4.2), 6.24 (дд, 1 Н, С(5')Н, J=8.6, J=1.7), 6.41 (д, 1 Н, С(3')Н, J=1.7), 6.66 (уш.с, 1 Н, N(1)H), 6.79 (уш.с, 1 Н, N(3)H), 7.01 (д, 1 Н, С(6')Н, J=8.6), 7.07 (д, 2 Н, С(2'',6'')Н, J=7.6), 7.21 (тр, 1 Н, С(4'')Н, J=7.6), 7.29 (д, 2 Н, С(3'',5'')Н, J=7.6), 9.27 (с, 1 Н, С(2')ОН), 9.69 (уш.с, 1 Н, С(4')ОН). Спектр ЯМР 13С (100 МГц, δ, м.д.): 23.73, 32.69, 53.74, 55.14, 57.09 104.09, 106.01, 123.24, 126.10 (2 С), 126.40, 126.91, 128.29 (2 С), 139.26, 154.57, 156.29, 157.68, 206.67. Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 340 [М]+ (0,4), 229 (42), 215 (21), 187 (21), 174 (14), 153 (100), 146 (73), 136 (47), 110 (35), 77 (41), 43 (62). Найдено (%): С, 66.83; Н, 5.90; N, 8.19. C19H20N2O4. Вычислено (%): С, 67.05; Н, 5.92; N, 8.23.
Пример 6. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-хлорфенил)-гексагидропиримидин-2(1H)-он:
Смесь 5-ацетил-6-метил-4-(4-хлорфенил)-дигидропиримидин-2(1H)-она (1 ммоль) с бензол-1,3-диолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 40°С в течение 26 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 7 мл хлороформа. Сушат на воздухе. Получают 237 мг (63% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-хлорфенил)-гексагидропиримидин-2(1H)-она - кристаллический осадок белого цвета, Тпл=200-202°С. ИК спектр, ν/см-1: 3525, 3418 (ОН), 3300 (N-H), 1705 (С=O), 1640 (С=O), 1619 (С=C), 1175, 1127 (С-О-С). Спектр ЯМР 1Н (500 МГц, δ, м.д., J/Гц): 1.42 (с, 3 Н, С(4)СН3), 1.80 (с, 3 Н, С(5)СОСН3), 4.05 (д, 1 Н, С(5)Н, J=4.4), 4.08 (д, 1 Н, С(6)Н, J=4.4), 6.28 (дд, 1 Н, С(5')Н, J=8.6, J=1.9), 6.42 (д, 1 Н, С(3')Н, J=1.9), 6.82 (уш.с, 1 H, N(1)H), 6.92 (уш.с, 1 Н, N(3)H), 7.05 (д, 1 Н, С(6')Н, J=8.6), 7.12 (д, 2 Н, С(2'',6'')Н, J=8.3), 7.37 (д, 2 Н, С(3'',5'')Н, J=8.3), 9.29 (уш.с, 1 Н, С(2')ОН), 9.72 (уш.с, 1 Н, С(4')ОН). Спектр ЯМР 13С (126 МГц, δ, м.д.): 23.78 (С(4)СН3), 33.92 (С(5)СОСН3), 53.24 (С(6)), 55.05 (С(5)), 57.07 (С(4)), 104.14 (С(3')), 106.08 (С(5')), 123.05 (С(1')), 128.05 (2 С, С(2''), С(6'')), 128.24 (3 С, С(3''), С(5''), С(6')), 131.71 (С(4'')), 138.32 (С(1'')), 153.86 (С(4')), 156.27 (С(2)), 157.60 (С(2')), 206.64 (С(5)СОСН3). Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 331 [М-Ас]+ (1), 265 [M-Rezorcin]+ (6), 221 (33), 178 (25), 165 (11), 152 (29), 140 (25), 110 (69), 43 (100). Найдено (%): С, 60.71; Н, 5.09; N, 7.43. C19H19ClN2O4. Вычислено (%): С, 60.88; Н, 5.11; N, 7.47.
Пример 7. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метилфенил)-гексагидропиримидин-2(1H)-он:
Смесь 5-ацетил-6-метил-4-(4-метилфенил)-дигидропиримидин-2(1H)-она (1 ммоль) с бензол-1,3-диолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 35°С в течение 27 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 9 мл хлороформа. Сушат на воздухе. Получают 291 мг (82% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метилфенил)-гексагидропиримидин-2(1H)-она - кристаллический осадок белого цвета, Тпл=211-213°С. ИК спектр, ν/cm-1: 3518, 3410 (ОН), 3304 (N-H), 1705 (С=O), 1645 (С=O), 1612 (С=C), 1256 (С-О-С). Спектр ЯМР 1Н (400 МГц, 8, м.д., J/Гц): 1.37 (с, 3 Н, С(4)СН3), 1.74 (с, 3 Н, С(5)СОСН3), 2.24 (с, 3 Н, С(4'')СН3), 3.98 (д, 1 Н, С(5)Н, J=4.2), 4.02 (д, 1 Н, С(6)Н, J=4.2), 6.24 (дд, 1 Н, С(5')Н, J=8.6, J=1.7), 6.38 (д, 1 Н, С(3')Н, J=1.7), 6.63 (с, 1 Н, N(l)H), 6.79 (с, 1 Н, N(3)H), 6.95 (д, 2 Н, С(3'',5'')Н, J=8.0), 7.02 (д, 1 Н, С(6')Н, J=8.6), 7.09 (д, 2 Н, С(2'',6'')Н, J=8.0), 9.27 (с, 1 Н, С(2')ОН), 9.68 (с, 1 Н, С(4')ОН). Спектр ЯМР 13С (100 МГц, δ, м.д.): 20.62, 23.73, 33.84, 53.45, 55.24, 57.02, 104.09, 106.00, 123.25, 125.98 (2 С), 128.33, 128.85 (2 С), 136.19, 136.34, 153.86, 156.38, 157.54, 206.84. Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 354 [М]+ (3), 336 (58), 321 (72), 278 (11), 280 (82), 271 (49), 251 (36), 243 (17), 229 (22), 229 (84), 204 (17), 201 (100), 188(15), 178 (12), 174(13), 152 (27), 145 (17), 118(17), 110 (22), 91 (33), 42 (35). Найдено (%): С, 67.59; Н, 6.23; N, 7.87. C20H22N2O4. Вычислено (%): С, 67.78; Н, 6.26; N, 7.90.
Пример 8. (4R*,5S*,6R*)-5-Ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метоксифенил)-гексагидропиримидин-2(1Н)-он:
Смесь 5-ацетил-6-метил-4-(4-метоксифенил)-дигидропиримидин-2(1H)-она (1 ммоль) с 1,3-бензолдиолом (2 ммоль) в четыреххлористом углероде (5 мл), уксусной кислоте (1 мл) и MeSO3H 0,230 мл (3,56*10-3 М) нагревают при 40°С в течение 25 часов. Затем охлаждают и выливают в 3%-ный водный раствор NaHCO3 (10 мл). Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из 6 мл хлороформа. Сушат на воздухе. Получают 312 мг (84% от теории) (4R*,5S*,6R*)-5-ацетил-4-(2,4-дигидроксифенил)-4-метил-6-(4-метоксифенил)-гексагидропиримидин-2(1H)-она - кристаллический осадок белого цвета, Тпл=204-206°С. ИК спектр, ν/cm-1: 3515, 3408 (ОН), 3312 (N-H), 1700 (С=O), 1656 (С=O), 1614 (С=С), 1236 (С-О-С). Спектр ЯМР 1Н (400 МГц, δ, м.д., J/Гц): 1.37 (с, 3 Н, С(4)СН3), 1.74 (с, 3 Н, С(5)СОСН3), 3.98 (д, 1 Н, С(5)Н, J=4.4), 4.02 (д, 1 Н, С(6)Н, J=4.4), 6.25 (дд, 1 Н, С(5')Н, J=8.6, J=2.2), 6.38 (д, 1 Н, С(3')Н, J=2.2), 6.57 (с, 1 Н, N(1)H), 6.76 (с, 1 Н, N(3)H), 6.84 (д, 2 Н, С(3'',5'')Н, J=8.5), 6.98 (д, 2 Н, С(2'',6'')Н, J=8.5), 7.02 (д, 1 Н, С(6')Н, J=8.6), 9.23 (с, 1 Н, С(2')ОН), 9.64 (с, 1 Н, С(4')ОН). Спектр ЯМР 13С (100 МГц, δ, м.д.): 23.73, 33.82, 53.13, 55.01, 55.25, 56.97, 104.08, 105.97, 113.62 (2 С), 123.30, 127.15 (2 С), 128.26, 130.97, 153.80, 156.21, 157.46, 158.33, 204.05. Масс-спектр (ЭУ, 70 эВ), m/z (Ioтн, (%)): 352 [М-18]+ (2), 267 (11), 259 (25), 259 (16), 245 (16), 217 (100), 178 (43), 162 (16), 152 (33), 136 (85), 134 (42), 110 (54), 77 (23), 43 (59). Найдено (%): С, 64.61; Н, 5.97; N, 7.53. C20H22N2O5. Вычислено (%): С, 64.85; Н, 5.99; N, 7.56.
Техническим результатом изобретения является получение новых химических соединений достаточной степени чистоты, которые могут быть использованы в качестве прекурсоров для синтеза биологически активных веществ и лекарственных препаратов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения замещенных (4R*,5S*,6R*)-2-тиогексагидропиримидин-5-карбогидразидов | 2021 |
|
RU2776954C1 |
| Способ получения 4-арилзамещенных 8-гидрокси-5,10а-диметил-1,3,4,10а-тетрагидро-2Н-хромено[2.3-d]пиримидин-2-онов(тионов) | 2023 |
|
RU2821110C1 |
| Хиральные S-монотерпенилцистеины | 2018 |
|
RU2689381C1 |
| Способ получения замещенных 8-гидрокси-1,2,3,4,4a,10b-гексагидро-2H-хромено[4,3-d]пиримидин-2,5(1H)-дионов | 2022 |
|
RU2785713C1 |
| Способ получения замещенных O-алкилированных гексагидро-2H-хромено[4,3-d]пиримидин-2,5(1H)-дионов | 2022 |
|
RU2796532C1 |
| 2-АМИНОЗАМЕЩЕННЫЕ 6-МЕТОКСИ-4-ТРИФТОРМЕТИЛ-9Н-ПИРИМИДО[4,5b]ИНДОЛЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ И ПРЕДШЕСТВЕННИКИ | 2016 |
|
RU2625316C1 |
| Способ получения 6-стирил-4-трифторметил-2-тиоксо-1,2-дигидропиридин-3-карбонитрилов | 2023 |
|
RU2827934C1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДРАЗОНОВ 4-R-1,2,5-ОКСАДИАЗОЛ-3-КАРБОНОВОЙ КИСЛОТЫ | 2014 |
|
RU2557659C1 |
| ПРОИЗВОДНЫЕ МАННОЗЫ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2013 |
|
RU2667060C2 |
| АНТАГОНИСТЫ TLR7/8 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2833035C2 |
Изобретение относится к способу получения 6-арилзамещенных 5-ацетил-4-(2,4-дигидроксифенил)-4-метилгексагидропиримидин-2-онов(тионов) структурной формулы
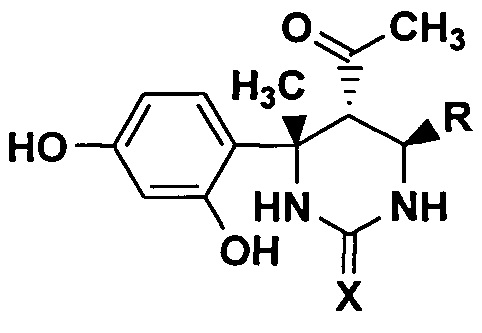
где R=С6Н5, или 4-ClC6H4, или 4-МеС6Н4, или 4-МеОС6Н4, X=О или S, который заключается во взаимодействии 4-арилзамещенных 5-ацетил-6-метилдигидропиримидин-2-онов(тионов) и бензол-1,3-диола. Технический результат: способ получения 6-арилзамещенных 5-ацетил-4-(2,4-дигидроксифенил)-4-метил-гексагидропиримидин-2-онов(тионов) позволяет получать новые ранее неописанные в литературе замещенные гексагидропиримидин-2-оны(тионы), которые могут быть использованы в качестве прекурсоров для синтеза биологически активных веществ и лекарственных препаратов. 8 пр.
Способ получения 6-арилзамещенных 5-ацетил-4-(2,4-дигидроксифенил)-4-метилгексагидропиримидин-2-онов(тионов) общей структурной формулы
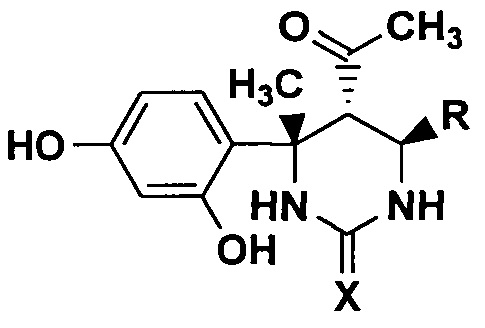
где R=С6Н5, или 4-ClC6H4, или 4-МеС6Н4, или 4-МеОС6Н4, X=О или S, заключающийся в том, что в качестве реагентов для синтеза 6-арилзамещенных 5-ацетил-4-(2,4-дигидроксифенил)-4-метилгексагидропиримидин-2-онов(тионов) используют 4-арилзамещенные 5-ацетил-6-метилдигидропиримидин-2-оны(тионы) и бензол-1,3-диол мольное соотношение 1:2, которые взаимодействуют в растворе четыреххлористого углерода и уксусной кислоты в присутствии метансульфоновой кислоты при температуре 30…40°С в течение 24-28 часов, затем полученную реакционную массу охлаждают и выливают в водный раствор гидрокарбоната натрия, выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из хлороформа, сушат на воздухе.
| Способ получения замещенных 8-гидрокси-1,2,3,4,4a,10b-гексагидро-2H-хромено[4,3-d]пиримидин-2,5(1H)-дионов | 2022 |
|
RU2785713C1 |
| Способ получения замещенных (4R*,5S*,6R*)-2-тиогексагидропиримидин-5-карбогидразидов | 2021 |
|
RU2776954C1 |
| S | |||
| I | |||
| FILIMONOV et al., A Condensation of Biginelli Products with 1,3-Benzenediols: a Facile Access to Diastereomerically Pure Hexahydro-5H-chromeno[4,3-d]pyrimidin-5-ones, CHEMISTRYSELECT, 4, pp | |||
| Прибор для поверки прицельной линии орудия | 1927 |
|
SU9550A1 |
| E | |||
| S | |||
| Makarova, M | |||
| V | |||
| Kabanova, S | |||
| I | |||
| Filimonov, А | |||
| А | |||
| Shetnev, K | |||
| Yu | |||
Авторы
Даты
2024-02-15—Публикация
2023-06-13—Подача